短效苯并二氮杂*盐及其多晶型
本发明涉及短效苯并二氮杂
的盐,和该盐作为药物,尤其是用于镇静或催眠、抗焦虑、肌肉松弛或抗惊厥目的的用途。
欧洲专利号1,183,243描述了包括羧酸酯结构部分的短效苯并二氮杂
并且通过非特异性组织酯酶钝化。器官非依赖性清除机理预测是这些苯并二氮杂
的特性,从而提供更可预测和可再现的药效分布型。该化合物适合于治疗目的,包括镇静催眠、抗焦虑、肌肉松弛和抗惊厥目的。该化合物是短效CNS抑制剂,它们可用于按以下临床设定中静脉内地给药:围手术期事件中的手术前镇静、抗焦虑和遗忘用途;在短期诊断、手术或内窥镜程序期间的清醒性镇静;在施用其它麻醉剂或止痛剂之前和/或同时,作为用于全身麻醉的诱导和维持的组分;ICU镇静。
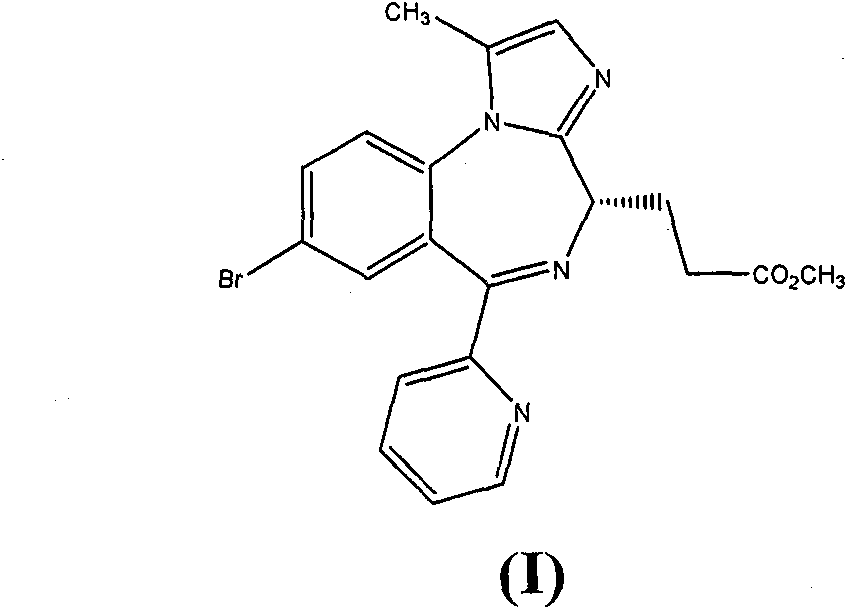
EP 1,183,243中公开的化合物之一(在实施例Ic-8,36页)是3-[(4S)-8-溴-1-甲基-6-(2-吡啶基)-4H-咪唑[1,2-a][1,4]苯并二氮杂
-4-基]丙酸甲酯,如下面通式(I)所示:
虽然通式(I)的游离碱当在5℃下储存时稳定,但是观察到在40℃/75%相对湿度(开放)下储存的样品潮解,颜色变成黄色到橙色,并且相对于初始含量显示显著的含量降低(参见下面实施例1)。
现已令人惊奇地发现,通式(I)的化合物形成高度结晶的单(苯并磺酸)苯磺酸盐,它们容易地从一定范围的药物可接受的溶剂离析并且显示良好的热稳定性、低的吸湿性和高的水溶性。
根据本发明,提供了以下通式(I)的化合物的苯磺酸盐。优选地,该盐是结晶盐。优选地,该结晶盐具有1∶1的通式(I)的化合物:苯磺酸盐的化学计量。苯磺酸盐的多晶型物的制备和表征在下面实施例中描述。
根据本发明,提供了通式(I)的化合物的苯磺酸盐的结晶多晶型物(在此表示为苯磺酸盐1型),它显示在大约7.3、7.8、9.4、12.1、14.1、14.4、14.7或15.6度2θ处包括特征峰的X射线粉末衍射(XRPD)图案。
优选地,该苯磺酸盐1型结晶多晶型物显示在大约7.3、7.8、9.4、12.1、14.1、14.4、14.7和15.6度2θ处包括特征峰的XRPD图案。
更优选,苯磺酸盐1型结晶多晶型物显示XRPD图案,该XRPD图案在:7.25(10.60)、7.84(72.60)、9.36(12.10)、12.13(32.50)、14.06(48.50)、14.41(74.30)、14.70(50.70)、15.60(26.90)[角度2θ度(百分率相对强度)]处包括特征峰。
优选地,苯磺酸盐1型结晶多晶型物在187-204℃、优选大约191-192℃的范围中具有差示扫描量热法(DSC)开起始熔融温度。
1型的晶体结构在190K处解析(R因数为6.3)。I型具有1∶1的化合物:苯磺酸盐的化学计量。它的结晶学不对称单元包含两个独立的化合物分子和两个苯磺酸盐分子。该两个独立的化合物分子在咪唑环上是单质子化的。该晶体结构具有以下单晶尺寸:a=7.6868
b=29.2607
c=12.3756
α=90°,β=97.7880°,γ=90°和P2
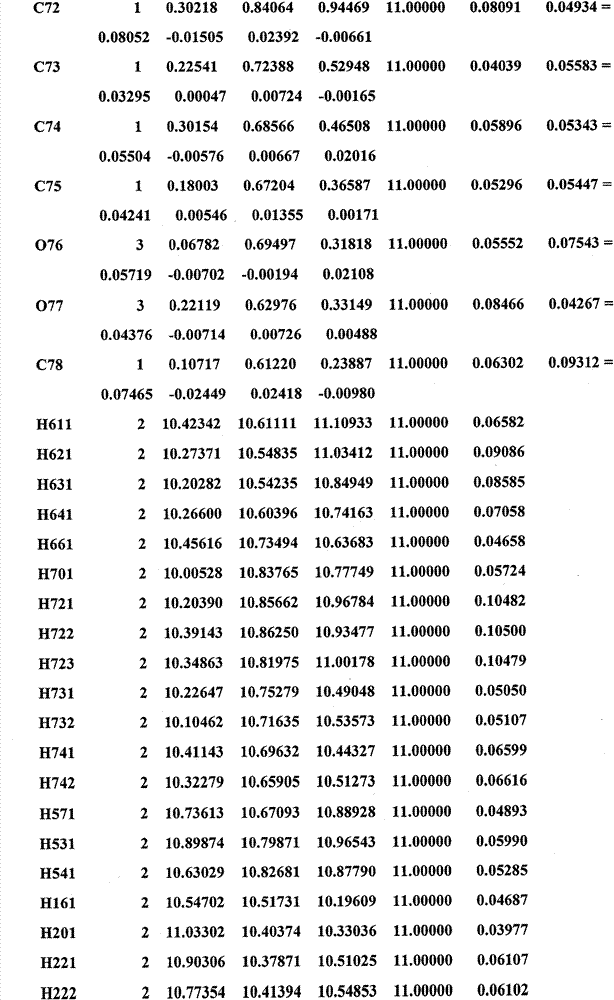
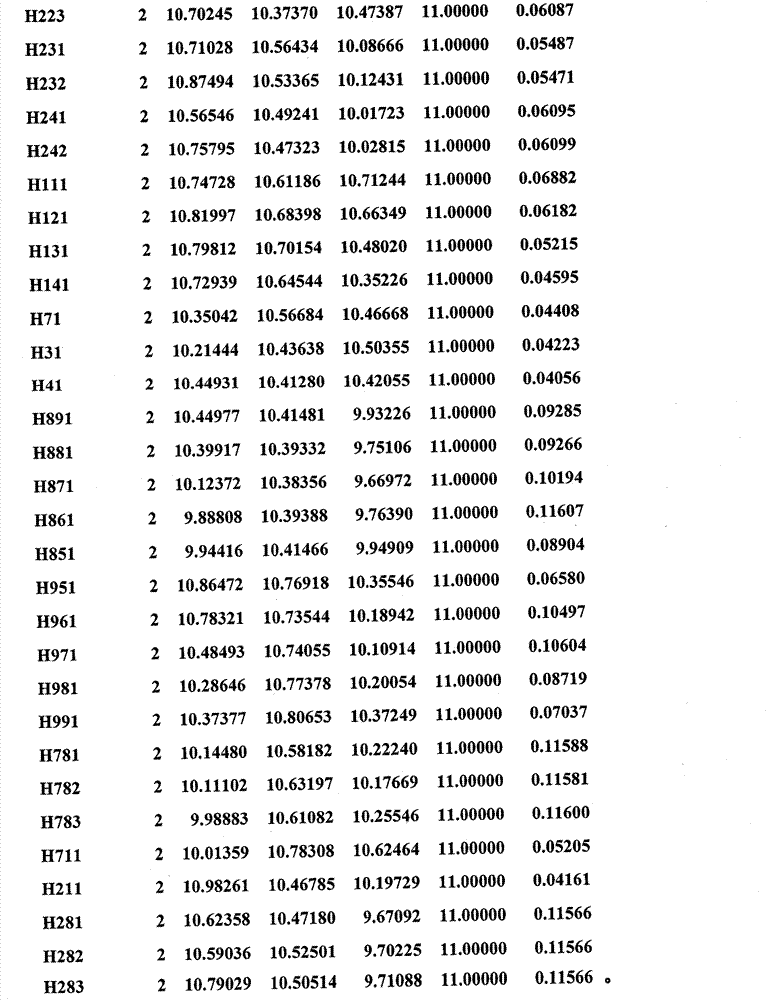
1的空间群。该晶体结构在实施例9中进行了更详细地描述,并且结晶学坐标在表17中给出。1型的键长和角度分别在表19和20中给出。
根据本发明,提供了通式(I)的化合物的苯磺酸盐,它是结晶多晶型物,该结晶多晶型物包含具有以下单晶尺寸的晶体:a=7.6868
b=29.2607
c=12.3756
α=90°,β=97.7880°,γ=90°。
根据本发明还提供了通式(I)的化合物的苯磺酸盐,它是结晶多晶型物,该结晶多晶型物具有由表17所示的结构坐标限定的晶体结构。
根据本发明进一步提供了通式(I)的化合物的苯磺酸盐,它具有分别如表19和20所示的键长和角度。
根据本发明进一步提供了通式(I)的化合物的苯磺酸盐的结晶多晶型物(在此表示为苯磺酸盐2型),它显示在大约8.6、10.5、12.0、13.1、14.4或15.9度2θ处包括特征峰的XRPD图案。
优选地,该苯磺酸盐2型结晶多晶型物显示在大约8.6、10.5、12.0、13.1、14.4和15.9度2θ处包括特征峰的XRPD图案。
更优选,苯磺酸盐2型结晶多晶型物显示XRPD图案,该XRPD图案在:8.64(17.60)、10.46(21.00)、12.03(22.80)、13.14(27.70)、14.42(11.20)、15.91(100.00)[角度2θ度(百分率相对强度)]处包括特征峰。
优选地,苯磺酸盐2型结晶多晶型物在170-200℃的范围中、优选在大约180℃具有差示扫描量热法(DSC)起始熔融温度。
2型的晶体结构在190K处解析(R因数为3.8)。2型具有1∶1化合物:苯磺酸盐的化学计量。它的结晶学不对称单元包含一个化合物分子和一个苯磺酸盐分子。该化合物分子在咪唑环上是单质子化的。该晶体结构具有以下单晶尺寸a=8.92130
b=11.1536
c=25.8345
α=90°,β=90°,γ=90°和P2
12
12
1的空间群。该晶体结构在实施例10中进行了更详细地描述,并且结晶学坐标在表18中给出。2型的键长和角度分别在表21和22中给出。
根据本发明,提供了通式(I)的化合物的苯磺酸盐,它是结晶多晶型物,该结晶多晶型物包含具有以下单晶尺寸的晶体:a=8.92130
b=11.1536
c=25.8345
α=90°,β=90°,γ=90°。
根据本发明还提供了通式(I)的化合物的苯磺酸盐,它是结晶多晶型物,该结晶多晶型物具有由表18所示的结构坐标限定的晶体结构。
根据本发明进一步提供了通式(I)的化合物的苯磺酸盐,它具有分别如表21和22所示的键长和角度。
根据本发明进一步提供了通式(I)的化合物的苯磺酸盐的结晶多晶型物(在此表示为苯磺酸盐3型),它显示在大约7.6、11.2、12.4、14.6、15.2、16.4或17.7度2θ处包括特征峰的X射线粉末衍射(XRPD)图案。
优选地,苯磺酸盐3型结晶多晶型物显示在大约:7.6、11.2、12.4、14.6、15.2、16.4和17.7度2θ处包括特征峰的XRPD图案。
更优选,苯磺酸盐3型结晶多晶型物显示XRPD图案,该XRPD图案在:7.61(65.70)、11.19(33.20)、12.38(48.70)、14.63(30.60)、15.18(33.20)、16.40(29.60)、17.68(51.30)[角度2θ°(百分率相对强度)]处包括特征峰。
优选地,苯磺酸盐3型结晶多晶型物在195-205℃、优选大约200-201℃的范围中具有差示扫描量热法(DSC)起始熔融温度。
根据本发明进一步提供了通式(I)的化合物的苯磺酸盐的结晶多晶型物(在此表示为苯磺酸盐4型),它显示在大约7.6、10.8、15.2、15.9或22.0度2θ处包括特征峰的XRPD图案。
优选地,该苯磺酸盐4型结晶多晶型物显示在大约:7.6、10.8、15.2、15.9和22.0度2θ处包括特征峰的XRPD图案。
优选地,苯磺酸盐4型结晶多晶型物显示XRPD图案,该XRPD图案在:7.62(83.50)、10.75(14.70)、15.17(37.80)、15.85(28.70)、22.03(100)[角度2θ°(百分率相对强度)]处包括特征峰。
优选地,苯磺酸盐4型结晶多晶型物在180-185℃的范围中、优选在大约182℃具有差示扫描量热法(DSC)起始熔融温度。
优选的盐是基于形成的稳固性、产率、纯度和化学和固体形状稳定性的苯磺酸盐1型。
根据本发明还提供了通式(I)的化合物的苯磺酸盐的制造方法,该方法包括使通式(I)的化合物的游离碱与苯磺酸反应。
根据本发明还提供了本发明的盐的制造方法,该方法包括使通式(I)的化合物的游离碱与苯磺酸在溶液中接触以引起该苯磺酸盐的沉淀的形成。优选地,该方法还包括离析该沉淀。
优选地,将游离碱溶于甲苯、乙醇、乙酸乙酯、MtBE、二氯甲烷(DCM)、乙酸异丙酯、甲酸乙酯、甲醇或丙酮。更优选,将游离碱溶于甲苯或乙酸乙酯。优选地,将苯磺酸溶于乙醇。
苯磺酸盐1型可以如下制备:使通式(I)的化合物的游离碱在甲苯、乙酸乙酯、丙酮、乙酸异丙酯或甲酸乙酯中的溶液与苯磺酸在乙醇中的溶液接触以引起该盐的沉淀的形成。
根据本发明还提供可通过上述方法获得的通式(I)的化合物的苯磺酸盐。
苯磺酸盐2型可以如下制备:使通式(I)的化合物的游离碱在甲醇中的溶液与苯磺酸在乙醇中的溶液接触以引起该盐的沉淀的形成。优选地,将该混合物冷却到小于环境温度(例如4℃)。
根据本发明还提供可通过上述方法获得的通式(I)的化合物的苯磺酸盐。
苯磺酸盐3型可以如下制备:用1型为由1型从乙酸乙酯/乙醇的结晶产生的体液播种。优选地,将该液体冷却到小于环境温度(例如4℃)。
在一个实施方案中,苯磺酸盐3型可以如下制备:用通式(I)的化合物的苯磺酸盐1型结晶盐为滤液播种,该滤液是与通过使通式(I)的化合物在乙酸乙酯中的溶液与苯磺酸在乙醇中的溶液接触而形成的沉淀分离的滤液,以制备苯磺酸盐3型结晶多晶型物。
根据本发明还提供可通过上述方法中任一种获得的通式(I)的化合物的苯磺酸盐。
苯磺酸盐4型可以通过使苯磺酸盐1型从乙酸异丙酯/乙醇、优选40%乙酸异丙酯/乙醇重结晶来制备。
根据本发明还提供可通过上述方法获得的通式(I)的化合物的苯磺酸盐。
本发明的盐还可以如下制备:使通式(I)的化合物的苯磺酸盐从适合的溶剂、或从适合的溶剂/反溶剂或溶剂/助溶剂混合物结晶。如果合适,可以将该溶液或混合物冷却和/或蒸发以实现结晶。
已经发现,在其中存在极性(例如乙腈∶水)或亲脂性(正壬烷)或两者(二甲基亚砜:1,2-二氯苯)的极端的条件下观察到2型的结晶。
用于2型结晶的溶剂的实例是:壬烷;甲醇。
用于1型结晶的溶剂/反溶剂混合物的实例是:二甲基乙酰胺/甲基异丁基酮;二甲基乙酰胺/四氯乙烯;乙腈/3-甲基丁-1-醇;乙腈/1,2-二氯苯;乙腈/乙酸戊酯;甲醇/3-甲基丁-1-醇;甲醇/甲基异丁基酮;2,2,2-三氟乙醇/1,4-二甲苯;乙醇/甲基异丁基酮;乙醇/1,4-二甲苯;丙-1-醇/1,2-二氯苯;丙-1-醇/四氯乙烯;丙-2-醇/1,2-二氯苯;丙-2-醇/正壬烷;2-甲氧基乙醇/水;2-甲氧基乙醇/乙酸戊酯;2-甲氧基乙醇/1,4-二甲苯;四氢呋喃/水;四氢呋喃/3-甲基丁-1-醇;四氢呋喃/1,2-二氯苯;四氢呋喃/乙酸乙酯;四氢呋喃/1,3-二甲苯。
用于2型结晶的溶剂/反溶剂混合物的实例是:乙醇/乙酸乙酯;乙醇/甲基异丁基酮;乙醇/对-异丙基苯;二甲亚砜/1,2-二氯苯;乙腈/水;乙醇/1,2-二氯苯;乙醇/四氯乙烯;四氢呋喃/1,2-二氯苯;四氢呋喃/乙酸乙酯。
根据一个优选的实施方案,使1型从2-甲氧基乙醇/乙酸戊酯结晶。
根据一个优选的实施方案,使2型从乙醇/乙酸乙酯结晶。
根据一个优选的实施方案,使2型从甲醇/乙醇结晶(优选通过将通式(I)的化合物的苯磺酸盐在甲醇/乙醇中的溶液冷却到小于环境温度,例如4℃)。
根据一个优选的实施方案,使3型从乙醇/乙酸乙酯结晶(适合地通过将该混合物冷却到小于环境温度,例如4℃)。
根据一个优选的实施方案,使4型从乙酸异丙酯/乙醇结晶(优选通过将通式(I)的化合物的苯磺酸盐在乙酸异丙酯/乙醇中的溶液冷却到环境温度)。
根据本发明还提供可通过上述方法中任一种获得的通式(I)的化合物的苯磺酸盐。
将在下面实施例中详细地描述本发明的盐的制备方法。
本发明的盐可以用作药物,尤其是用于镇静或催眠、抗焦虑、肌肉松弛或抗惊厥目的。
虽然本发明的盐作为本体活性化学品施用是可能的,但是优选为其提供药物可接受的载体、赋形剂或稀释剂以形成药物组合物。所述载体、赋形剂或稀释剂当然必须在一定程度上与组合物的其它成分相容并且不能对接受者有害。
因此,本发明提供包含本发明的盐和药学可接受的载体、赋形剂或稀释剂的药物组合物。
本发明的药物组合物包括适合于口服、直肠、局部、颊粘膜(例如舌下)和非肠道(例如皮下、肌内、皮内或静脉内)给药的那些。
优选地,本发明的盐以用于非肠道给药(例如,通过溶液的静脉内或肌肉注射给药)的药物组合物形式提供。当该药物组合物用于非肠道给药时,该组合物可以是含水或非水溶液或液体的混合物,它们可以包括抑菌剂、抗氧化剂、缓冲物或其它药物可接受的添加剂。
本发明的盐的优选配方在pH值2-4的含水酸性介质中或在环糊精(CD)的水溶液中。可以用于这些配方的环糊精是β-CD、特别是SBE7-β-CD的阴离子带电磺基丁基醚(SBE)衍生物,由CyDex,Inc.以商品名称Captisol销售(Critical Reviews in Therapeutic DrugCarrier Systems,14(1),1-104(1997)),或是羟丙基CD’s。
本发明的盐的另一种优选的配方是冻干配方,它除了该盐之外还包含以下试剂中至少一种:抗坏血酸、柠檬酸、马来酸、磷酸、甘氨酸、甘氨酸盐酸盐、丁二酸或酒石酸。这些试剂认为可用作缓冲、结块或造影剂。在一些情况下,在配方中包括氯化钠、甘露糖醇、聚乙烯吡咯烷酮或其它成分可能是有益的。
配方(即,酸缓冲物或CD基)的优选方法可能取决于特定盐的物理化学性能(例如,水溶性、pKa等)。优选地该盐也可以作为冻干固体存在以便与水(用于注射)或右旋糖或盐溶液重构。此类配方通常以单元剂型例如安瓿或一次性喷射器存在。它们还可以按多剂量剂型例如从中可以取出合适剂量的瓶子存在。所有这些配方应该是无菌的。
根据本发明提供在受试者中产生镇静或催眠状态的方法,该方法包括对该受试者施用镇静或催眠有效量的本发明盐。
根据本发明还提供在受试者中引起抗焦虑的方法,该方法包括对该受试者施用抗焦虑有效量的本发明盐。
根据本发明进一步提供在受试者中引起肌肉松弛的方法,该方法包括对该受试者施用肌肉松弛有效量的本发明盐。
根据本发明进一步提供在受试者中治疗惊厥状态的方法,该方法包括对该受试者施用抗惊厥的有效量的本发明盐。
根据本发明还提供镇静或催眠量的本发明盐在制造药物中的用途,该药物用于在受试者中产生镇静或催眠状态。
根据本发明还提供本发明的用于在受试者中产生镇静或催眠状态的盐。
根据本发明还提供抗焦虑量的本发明盐在制造药物中的用途,该药物用于在受试者中产生抗焦虑状态。
根据本发明还提供本发明的用于在受试者中产生抗焦虑状态的盐。
根据本发明进一步提供肌肉松弛量的本发明盐在制造药物中的用途,该药物用于在受试者中产生肌肉松弛状态。
根据本发明进一步提供本发明的用于在受试者中产生肌肉放松状态的盐。
根据本发明进一步提供抗惊厥量的本发明盐在制造药物中的用途,该药物用于在受试者中治疗惊厥状态。
根据本发明进一步提供本发明的用于在受试者中治疗惊厥状态的盐。
受试者适合地是哺乳动物,优选人类。
用于对人类给药的适合的药物非肠道制剂将优选包含0.1-20mg/ml在溶液中的本发明盐或对于多剂量小瓶它的多倍。
静脉内给药可以采取丸剂注射或,更适当地,连续灌输的形式。每一受试者的剂量可以改变,然而,本发明盐在哺乳动物中获得镇静或催眠状态的适合的静脉内用量或剂量将是0.01-5.0mg/kg体重,更尤其是0.02-0.5mg/kg体重,上述量基于是活性成分的盐的重量。本发明盐在哺乳动物中获得抗焦虑状态的适合的静脉内用量或剂量将是0.01-5.0mg/kg体重,更尤其是0.02-0.5mg/kg体重,上述量基于是活性成分的盐的重量。本发明盐在哺乳动物中获得肌肉松驰状态的适合的静脉内用量或剂量将是0.01-5.0mg/kg体重,更尤其是0.02-0.5mg/kg体重,上述量基于是活性成分的盐的重量。本发明盐在哺乳动物中治疗惊厥状态的适合的静脉内用量或剂量将是0.01-5.0mg/kg体重,更尤其是0.02-0.5mg/kg体重,上述量基于是活性成分的盐的重量。
本发明盐是短效CNS抑制剂,它们可用于按以下临床设定静脉内地给药:围手术期事件中的手术前镇静、抗焦虑和遗忘用途;在短期诊断、手术或内窥镜程序期间的清醒性镇静;在施用其它麻醉剂或止痛剂之前和/或同时,作为用于全身麻醉的诱导和维持的组分;ICU镇静。
在以下实施例中将参照附图描述本发明的优选实施方案,在附图中:
图1示出了通式(I)化合物含量(%相对于初始)对储存温度的曲线图;
图2示出了LJC-039-081-1的差示扫描量热法(DSC);
图3示出了与LJC-039-081-2(虚线)重叠的LJC-039-081-1(实线)的DSC;
图4示出了苯磺酸盐晶型(1型实线,2型阴影线)的DSC;
图5示出了苯磺酸盐晶型(1型实线,3型虚线和阴影线)的DSC;
图6示出了LJC-039-037-1在T0和T4的色谱(并且涉及表10中的结果);
图7示出了比较在4周稳定性研究前后的LJC-039-037-1(苯磺酸盐)的XRPD;
图8A示出了苯磺酸盐1型和2型的XRPD对比;
图8B示出了1型和2型的差示扫描量热法(DSC)覆盖图;
图9A示出了苯磺酸盐1型和3型的XRPD对比,图9B示出了1型和3型的覆盖图;
图10示出了LJC-039-086-1(苯磺酸盐4型)的DSC;
图11示出了苯磺酸盐1型的结果:A)100mg批料LJC-039-037-1的XRPD;B)100mg批料LJC-039-037-1的DSC;C)100mg批料LJC-039-037-1的TGA;D)100mg批料LJC-039-037-1的1H NMR;E)100mg批料LJC-039-037-1的GVS;F)100mg批料LJC-039-037-1的GVS后的XRPD;G)100mg批料LJC-039-037-1在40℃/75%RH下稳定后的XRPD;H)100mg批料LJC-039-037-1的VT;I)100mg批料LJC-039-037-1的光偏振显微镜检查;
图12示出了苯磺酸盐2型的结果:A)100mg批料LJC-039-067-8的XRPD;B)100mg批料LJC-039-067-8的DSC;C)在2℃/分钟的温变率下的DSC;D)LJC-039-067-8的1H NMR;
图13示出了苯磺酸盐3型的结果:A)LJC-039-081-2(LJC-039-081-1的溶液的第二收获物)的XRPD;B)LJC-039-081-2的DSC;C)LJC-039-081-2(2℃/分钟温变率)的DSC;D)LJC-039-081-2的TGA;E)LJC-039-081-2的1H NMR;F)LJC-039-081-2的GVS;G)LJC-039-081-2在GVS后的XRPD;
图14示出了苯磺酸盐4型的结果:A)LJC-039-086-1的XRPD;B)LJC-039-086-1的DSC;C)LJC-039-086-1的1H NMR;
图15示出了苯磺酸盐的释放批料的HPLC色谱,接着AgilentChemStation报道详细结果;
图16示出了LJC-039-081-1和LJC-039-083-1的手性色谱;
图17示出了在通式(I)的化合物苯磺酸的结晶中观察到固体晶型的范例图像(大约4-8mm直径视野);
图18示出了1型中不对称单元的含量;
图19示出了由通式(I)的化合物的苯磺酸盐(1型)的晶体的单晶X射线衍射测定的分子结构,该晶体从具有由热椭圆体表示的原子的2-甲氧基乙醇∶乙酸戊酯溶液生长。仅描绘了特别位于晶体结构中的氢;
图20示出了通过1型中两个独立分子采纳的构象;
图21示出了由1型中一个独立分子采纳的构象(顶部)和2型中的构象(底部)的对比;
图22示出了沿两个不同方向观察的由1型中两个独立苯磺酸盐采纳的构象的对比;
图23示出了由1型中一个独立苯磺酸盐采纳的构象(顶部)和2型中的构象(底部)的对比;
图24示出了沿着结晶学a轴(a)、b轴(b)和c轴(c)观察的由通式(I)的化合物苯磺酸的晶体的单晶X射线衍射测定的晶体结构,该晶体从2-甲氧基乙醇∶乙酸戊酯溶液生长;
图25示出了1型的短接触C-O<3.6
C-C<3.6
和N-O<3.5
图26示出了从1型的单晶X射线衍射数据计算的粉末衍射图案;
图27示出了对通式(I)的化合物的苯磺酸盐2型观察到的板形晶体;
图28示出了2型中的不对称单元的含量;
图29示出了由通式(I)的化合物苯磺酸盐2型的晶体的单晶X射线衍射测定的分子结构,该晶体具有由热椭圆体表示的原子。仅描绘了特别位于晶体结构中的氢;
图30示出了由2型中的独立分子采纳的构象;
图31示出了沿着两个不同方向观察的由2型中的独立苯磺酸盐采纳的构象;
图32示出了沿着结晶学a轴(a)、b轴(b)和c轴(c)观察的由通式(I)的化合物苯磺酸盐2型的晶体的单晶X射线衍射测定的晶体结构;
图33示出了2型的短接触C-O<3.6
C-C<3.6
和N-O<3.5
图34示出了从2型的单晶X射线衍射数据计算的粉末衍射图案;
图35示出了通式(I)的化合物苯磺酸盐1型的原子中心的标记;和
图36示出了通式(I)的化合物苯磺酸盐2型的原子中心的标记。
实施例1
通式(I)的化合物的固态稳定性研究
方法/技术。将精确称重的2mg通式(I)的化合物放入4-mL透明玻璃螺口小瓶中。在最初和在5℃/环境相对湿度(AMRH)封闭、30℃/60%RH封闭、40℃/75%RH开放和60℃/AMRH封闭下储存34天之后测试样品。
视觉上检查样品的外观。通过表1中的HPLC方法测定通式(I)的化合物含量值。相对于通式(I)的化合物批料U12438/79/1的标准样品测量%重量/重量(%w/w)值。通过用通式(I)的化合物峰面积除以总峰面积获得%面积值。
表1.HPLC方法条件
结果
外观。表2列出了外观结果。
表2.通式(I)的化合物外观数据的归纳
|
储存条件 |
时间点 |
外观 |
|
|
天 |
|
|
|
|
|
|
RT |
最初 |
乳膏至淡黄色粉末 |
|
|
|
|
|
5C/AMRH封闭 |
34 |
乳膏至淡黄色粉末 |
|
|
|
|
|
30C/60%RH封闭 |
34 |
乳膏至淡黄色粉末 |
|
|
|
|
|
40C/75%RH开放 |
34 |
小瓶底部上的潮解黄色物质 |
|
|
|
|
|
60C/AMRH封闭 |
34 |
小瓶底部上的潮解暗黄色至橙色物质 |
通式(I)的化合物含量(%w/w)。%w/w含量值(参见表3)显示过多可变性而检测到在初始值和在5℃/AMRH封闭,30℃/60%RH封闭或40℃/75%RH开放下34天之后测量的那些间的差异。对在60℃/AMRH封闭下储存34天的样品测量的平均%w/w显示从初始值降低10%w/w。
通式(I)的化合物含量(%面积)。通式(I)的化合物%面积含量(参见表3和图1)在5℃/AMRH封闭下储存34天后没有显示显著的变化,但是在30℃/60%RH封闭,40℃/75%RH开放或60℃/AMRH封闭下随样品的储存温度提高而稳定地减小。在RRT 0.68、0.87和RRT0.90下观察到主递减峰,但是色谱图(它们甚至在初始时也是较复杂的(23峰))也显示许多新的小递减峰(例如在30℃/60%RH封闭时,7峰;在60℃/AMRH封闭时13-20峰)。这些观察结果暗示多重递减路径。在RRT 0.68处的递减试验性地确定为酯水解产物(通式(I)的化合物的游离酸)。它在40℃/75%RH开放样品中最普遍的,对于水解产物将是预期的。
表3.通式(I)的化合物HPLC数据的归纳
脚注
1.由于自动取样器定序器误差仅试验一个样品。
结论
对于在5℃/AMRH封闭下储存至少34天,通式(I)的化合物在外观和含量方面是稳定的。在30℃/60%RH封闭下没有看出外观变化,但是观察到通式(I)的化合物含量相对于初始%面积的大约0.6%下降。在40℃/75%RH开放或60℃/AMRH封闭下储存的样品潮解,颜色方面变成黄色至橙色并且显示通式(I)的化合物含量相对于初始的显著降低(1.5-8%)。观察到在RRT 0.68、0.87和RRT 0.90处的主递减峰以及许多较小峰,这暗示多重递减路径。在RRT 0.68处的递减峰试验性地确定为酯水解产物。这些结果表明为了长期储存通式(I)的化合物应该冷冻储存。
实施例2
在宽的有机溶剂范围内测定通式(I)的化合物的溶解性。溶解性数据在下表4中示出。
表4
|
溶剂 |
所要求的最少溶剂/mg/ml |
|
甲醇 |
446 |
|
乙醇 |
324 |
|
丙-2-醇 |
454 |
|
丙酮 |
214 |
|
甲苯 |
460 |
|
乙酸乙酯 |
218 |
|
四氢呋喃 |
311 |
|
乙腈 |
362 |
数据清楚地表明通式(I)的化合物在常用的有机溶剂中具有高溶解性。优选的溶剂是乙醇和甲苯。
测量该化合物的游离碱的两种碱性中心的pKa。然而,该吡啶环的碱性中心具有1.99的pKa。该咪唑环的碱性中心的pKa测得为4.53。
使用苯磺酸制备通式(I)的化合物的苯磺酸盐。使用6倍体积溶剂对20mg规模进行实验。用作为在乙醇(1M)中的原料溶液或作为固体(取决于溶解性)加入的酸在环境温度下进行所有反应。
离析的固体在1H NMR中显示显著的峰位移以证实盐的形成。X射线粉末衍射(XRPD)显示盐具有结晶指征。表5归纳了该离析的盐晶型。
表5
|
项目 |
盐 |
溶剂 |
ID |
|
1 |
苯磺酸盐 |
甲苯 |
LJC-039-009-7 |
随后在40℃/75%RH下储存该盐两周,然后通过XRPD和HPLC再分析化学纯度以评价该材料的稳定性。在暴露到该湿度条件中之后该盐保持相同的粉末图案,此外还保持高的化学纯度,支持改进的稳定性。
从该离析盐的T1纯度结果(下表6)可以看出来自甲苯的苯磺酸盐在稳定性研究前后显示高纯度值。
表6在40℃/75%RH保持1周前后的纯度归纳
|
项目 |
盐 |
ID |
纯度T0/% |
纯度T1/% |
|
1 |
苯磺酸盐 |
LJC-039-009-7 |
95.9 |
95.9 |
上面的结果表明该苯磺酸盐晶型显示高纯度和有利的稳定性结果。
实施例3
基于实施例2中的数据将苯磺酸盐按比例放大到100mg。发现甲苯是用于离析苯磺酸盐的优选溶剂。
通式(I)的化合物的苯磺酸盐
将进料按比例放大到50mg以便确认该方法是否将按比例放大,和确认离析的材料是否具有与在前的小规模实验看出的相同结晶形态(1型)。一旦该分析证实该盐是1型并且性能与所预期的一致,就用100mg进料再进行按比例放大以便进行完全表征并将该样品用于在40℃/75%RH下的4周稳定性研究。在甲苯中进行这两个比例增大反应,其中苯磺酸作为在乙醇中的溶液(1M)添加。
苯磺酸盐实验程序
将通式(I)的化合物游离碱(100mg,批料704-17)加入小瓶中并在环境温度下添加甲苯(600μl)。向该溶液中添加苯磺酸(250μl,1M,在乙醇中)并搅拌该反应混合物十五分钟,此后,过滤从该溶液沉淀的固体,用甲苯洗涤并在真空下在40℃烘干。通过XRPD分析表明该固体具有与产生的其它苯磺酸盐相同的粉末图案,并且1HNMR证实由于显著的峰位移而形成了盐。
表7
|
项目 |
ID |
盐 |
GVS摄取/% |
起始熔融/℃ |
TGA重量损失/% |
溶解度mg/ml |
化学纯度/% |
手性纯度/%e.e |
|
1 |
LJC-039-037-1 |
苯磺酸盐 |
2.0 |
201.3 |
4.9 |
8.3 |
97.1 |
94.4 |
LJC-039-037-1的对映异构过量仅是94.4,因此将该结果与在相同条件下离析的苯磺酸盐(LJC-039-081-1)的另一批料对比。这一批料的对映异构过量是99.1%。
方法优化
为了改进进一步苯磺酸盐(1型)的产率,筛选四种溶剂(乙酸异丙酯、甲酸乙酯、甲醇和丙酮)。在这些溶剂中进行总计八个100mg规模反应,其中有关的酸作为在乙醇中的原料溶液添加以便与前述实验对比。
在环境下将通式(I)的化合物(批料704-38,100mg)溶于溶剂(600μl)。添加酸(250μl,在乙醇中的1M原料溶液)并在环境下静置所有反应混合物48小时。结果概括在表8中。
表8方法优化实验的结果
|
表项目 |
实验室工作簿参考 |
盐 |
溶剂 |
XRPD |
产率/% |
纯度/%面积 |
40℃/75%RH保持4周后的纯度 |
|
1 |
LJC-039-067-2 |
苯磺酸盐 |
丙酮 |
1型 |
38 |
98.4 |
98.1 |
|
2 |
LJC-039-067-4 |
苯磺酸盐 |
乙酸异丙酯 |
1型 |
79 |
97.7 |
95.9 |
|
3 |
LJC-039-067-6 |
苯磺酸盐 |
甲酸乙酯 |
1型 |
40 |
98.6 |
98.3 |
|
4 |
LJC-039-067-8 |
苯磺酸盐 |
甲醇 |
单晶,2型 |
没有记录 |
98.1 |
没有记录 |
除了甲醇中的苯磺酸盐形成的所有反应显示1型。该甲醇反应物在4℃下储存。所获得的数据确认无水苯磺酸盐1∶1,并且材料的粉末图案确认新晶型(2型)的存在。
从该研究断定,溶剂例如乙酸异丙酯提高该盐的纯度,然而降低回收率。因为溶剂(乙酸乙酯)的前述选择产生具有高纯度值的高产率盐,所以决定将乙酸乙酯用于最后的按比例放大实验。
苯磺酸盐(1型)1g按比例放大
进行苯磺酸盐的1g形成。这样成功地产生950mg(70%产率)1型。该溶液是高度着色的(黄色)并因此用少量1型播种,以帮助回收。在4℃下储存该溶液16小时。所获得的固体显示新的粉末图案(3型)。通过热分析和可变温度XRPD分析该固体以确认它是否是真实的多晶型物或溶剂合物。分析的判读断定根据1H NMR情况证据它不是溶剂合物,并且DSC显示被高温显微术确认的两个吸热事件(图3)。据解释,1型的种子在187℃熔融,3型在200℃熔融。1型没有被XRPD鉴定的理由是它是不如显微镜检查敏感的技术。
3型在较低温度下沉淀成1型。
对该多晶型物进行表征以提出它们之间的关系。
表9苯磺酸盐晶型的热数据
|
项目 |
ID |
晶型 |
熔融的起始/℃ |
ΔH/Jg-1 |
|
1 |
LJC-039-081-1 |
1 |
201 |
56 |
|
2 |
LJC-039-067-8 |
2 |
180 |
73 |
|
3 |
LJC-039-081-2 |
1,3 |
187,200 |
7.6,37 |
存在于LJC-039-081-2中的少量1型的更低熔点可能归因于更低的纯度(97.2%,较之LJC-039-081-1中的97.9%)。
图4示出了苯磺酸盐1型(实线)和2(阴影线)的DSC。
图5示出了苯磺酸盐1型(实线)和3(虚线和阴影线)的DSC。
实施例4
盐稳定性研究
表10在4周稳定性研究后盐纯度的归纳表
|
样品ID |
盐 |
T0 |
T1 |
T2 |
T3 |
T4 |
|
LJC-039-037-1 |
苯磺酸盐 |
97.1 |
97.3 |
97.4 |
96.7 |
96.7 |
在40℃/75%RH下储存苯磺酸盐的结晶样品总共四周并每七天吸取样品用于HPLC。苯磺酸盐hplc纯度保持一致,直到T3,此时它达到96.7%。然而,这一值保持与T4一致。
苯磺酸盐晶型在时间点零周和四周的hplc色谱在图6中示出。
据怀疑,在母体的峰之前的主峰来自污染物,因为λmax不与该母峰的λmax匹配。T1、T2、T3和T4的杂质分布图中也不存在。
从湿润研究前和后该盐的粉末图案可以看出,晶型方面不存在变化。
图7示出了比较在4周稳定性研究前后的LJC-039-037-1(苯磺酸盐)的XRPD。
实施例5
多晶型现象研究
为了测定苯磺酸盐显示多晶型现象的倾向,使用三十种溶剂(十五种纯加上它们的2.5%含水对应物)建立成熟实验。基于从环境到60℃的加热/冷却循环在各种溶剂(参见表11)中将固体制成浆一周。在一周后,蒸发该浆料并通过XRPD和HPLC分析固体。
表11苯磺酸盐(LJC-039-058-2)的多晶型现象研究的结果
·起始hplc纯度97.7%
|
项目 |
溶剂 |
1周后的XRPD |
HPLC纯度%面积 |
|
1 |
丙酮 |
1型 |
97.5 |
|
2 |
THF |
1型 |
97.6 |
|
3 |
IPA |
粉末 |
97.1 |
|
4 |
MtBE |
1型 |
97.7 |
|
5 |
DCM |
粉末 |
97.4 |
|
6 |
EtOH |
油 |
没有分析 |
|
7 |
MEK |
1型 |
97.2 |
|
8 |
1,4-二噁烷 |
1型 |
97.2 |
|
9 |
iPrOAc |
1型 |
97.5 |
|
10 |
DMF |
油 |
没有分析 |
|
11 |
MeCN |
1型 |
94.3 |
|
12 |
nBuOH |
油 |
没有分析 |
|
13 |
nPrOH |
油 |
没有分析 |
|
14 |
MIBK |
1型 |
97.7 |
|
15 |
MeOH |
油 |
没有分析 |
|
16 |
2.5%丙酮水溶液 |
1型 |
96.8 |
|
17 |
2.5%THF水溶液 |
粉末 |
93.3 |
|
18 |
2.5%IPA水溶液 |
1型 |
76.1 |
|
19 |
2.5%MtBE水溶液 |
油 |
没有分析 |
|
20 |
2.5%DCM水溶液 |
1型 |
97.4 |
|
21 |
2.5%EtOH水溶液 |
油 |
没有分析 |
|
22 |
2.5%MEK水溶液 |
1型 |
93.9 |
|
23 |
2.5%1,4-二噁烷水溶液 |
1型 |
86 |
|
24 |
2.5%iPrOAc水溶液 |
油 |
没有分析 |
|
25 |
2.5%DMF水溶液 |
油 |
没有分析 |
|
26 |
2.5%MeCN水溶液 |
1型 |
93.3 |
|
27 |
2.5%nBuOH水溶液 |
油 |
没有分析 |
|
28 |
2.5%nPrOH水溶液 |
油 |
没有分析 |
|
29 |
2.5%MIBK水溶液 |
1型 |
97.3 |
|
30 |
2.5%MeOH水溶液 |
油 |
没有分析 |
该使用苯磺酸盐的成熟研究揭示没有新的晶型。成熟后的纯度结果表明在乙腈、THF水溶液、IPA水溶液、MEK水溶液、二噁烷水溶液和乙腈水溶液中制浆的那些降低。这表明苯磺酸盐(1型)在纯有机溶剂中在高温下具有良好的溶液稳定性。
研究苯磺酸盐的新晶型
虽然从成熟研究没有看出新的苯磺酸盐晶型,但是当在甲醇中让晶体生长时,看出新的晶型。研磨从甲醇获得的单晶以获得粉末图案。发现该图案不同于1型。进行重复实验以获得2型的另外供应品。仅可能在16小时内从该溶液通过沉淀离析2型,这与允许溶剂蒸发相反,这样产生1型。有趣地存在两种形态;针状体和块体。两者都显示与针状体形态相同的粉末图案,该针状体形态用于单晶结构测定。
对2型进行全分析。已经断定它是真实的多晶型物,因为单晶数据确认无水苯磺酸盐1∶1。
图8A示出了苯磺酸盐1型和2型的XRPD对比。1型(轨迹1)和2型(轨迹2)间存在明显的差异。从这两个粉末图案可以看出,两种晶型非常不同。进行热分析以相比这两种晶型的熔点此外还记录热力学溶解度测量值。
图8B示出了1型和2型的覆盖图。1型和2型示出了吸热事件(熔融)。
当从LJC-039-081-1的溶液(1g按比例放大反应)离析第二收获物时,确认了3型。进行分析以确定它是否是溶剂合物和晶型如何互换。
图9A示出了苯磺酸盐1型和3型的XRPD对比。图9B示出了1型和3型的覆盖图。
1型示出了吸热事件(熔融),而3型显示了两个事件。对3型的高温显微术清楚地显示在彼此的20℃内两个熔点。据假定,存在少量较低熔点多晶型物,因为它在可变温度XRPD中没有被获得,该可变温度XRPD是不太敏感的技术。第一吸热事件代表1型是相当可能的,因为它用来为3型从中离析的溶液播种。
该溶解度数据表明所有三种晶型在pH值3下具有非常相似的7.8-8.3mg/ml的水溶液溶解度。
苯磺酸盐4型
苯磺酸盐1型(LJC-039-083-1)的释放批料具有高纯度(97.6%),但是包含少量从游离碱载入的杂质(0.78%,11.9分钟RT)。在显示吸热转变(在130℃开始)的DSC实验中观察到这种杂质。该峰被确认为具有与母峰无关的λmax。
取100mg样品用于从40%乙酸异丙酯/乙醇进行重结晶试验。通过将盐溶解在最低量的热溶剂中,然后缓慢地冷却到环境以产生沉淀来传统地进行重结晶。通过XRPD分析干固体,该XRPD指示新的晶型,并且采用热分析和1H NMR,确认它是多晶型物并且不是溶剂合物。图10示出了LJC-039-086-1的DSC。
该盐筛选研究已经表明通式(I)的化合物在合适的pKa范围内形成许多盐,并且它们容易地从一定范围的溶剂离析。从该盐的完全表征,已经测定该苯磺酸盐相对于湿度具有良好的稳定性。已经断定存在两种苯磺酸盐的多晶型物。3型来自LJC-039-081-1液体在用1型播种后的第二收获物。在从40%乙酸异丙酯/乙醇进行1型的重结晶后,观察到4型。
在下图11-14中示出了全部分析数据。
实施例2-5的实验方法
实施例2
将通式(I)的化合物(5mg/井)溶于在HPLC小瓶中的溶剂1(30μl)。向该溶液添加苯磺酸(11.4μl,1M,在乙醇中)并在环境下静置该反应混合物一整夜。在40℃在真空下干燥包含固体的那些小瓶,通过蒸发浓缩保持为溶液的那些,然后用庚烷处理。如所提及的那样干燥沉淀的那些,在4℃下储存油化的那些。
苯磺酸盐1型按比例放大
将通式(I)的化合物(100mg)溶于乙酸乙酯(600μl)并添加苯磺酸(250μl,1M,在乙醇中)。沉淀立即产生并在环境下搅拌该反应混合物24小时。过滤固体,用乙酸乙酯洗涤并在真空下在40℃烘干16小时。
分析方法
差示扫描量热法(DSC)
在配备有50位置自动取样器的TA仪器Q1000上收集DSC数据。能量和温度标定标准样品是铟。以10℃/分钟的速度在25和350℃之间加热样品。在样品上方维持30ml/分钟的氮气吹扫。
除非另有说明,使用0.5-3mg样品,并且所有样品在针孔铝盘中运转。
热重分析(TGA)
在TA仪器Q500TGA上收集TGA数据,该仪器用Alumel校准并且以10℃/分钟的扫描速率运转。在样品上方维持60ml/分钟的氮气吹扫。
除非另有说明,通常,将5-10mg样品装载到预称皮重的铂坩埚上。
NMR
在配备有自动取样器的Bruker 400MHz上收集所有光谱。除非另有说明,在d6-DMSO中制备样品。
XRPD(X射线粉末衍射)
bruker AXS C2 GADDS衍射计
在Bruker AXS C2 GADDS衍射计上获得样品的X射线粉末衍射图案,该衍射计使用Cu Kα辐射(40kV,40mA)、自动XYZ台、用于自动样品定位的激光视盘显微镜和HiStar 2-维区域检测器。X射线光学系统由与0.3mm的针孔准直仪耦合的单多层镜子构成。
样品上的X射线束的射束发散度,即有效尺寸是大约4mm。采用θ-θ连续扫描模式,其中样品与检测器的距离为20cm,这产生3.2-29.8°的有效2θ范围。样品的典型暴露时间将是120s。
使用原样没有研磨的粉末制备在环境条件下运转的样品作为平板试样。轻轻地将大约1-2mg样品压制在载玻片上以获得平整表面。将在非环境条件下运转的样品安装在具有导热化合物的硅晶片上。然后以大约20℃/分钟将样品加热到合适的温度,随后等温保持大约1分钟,然后启动数据收集。
纯度分析:
化学方法
在HP1100 Agilent上进行纯度分析:
方法:梯度,反相
方法持续时间/分钟:34
柱:Phenomenex Gemini C18 5μm(2.0×50mm)(保护盒Phenomenex Gemini C18保护盒2×4mm)
柱温/℃:40
注射/μl:5
流速ml/分钟:0.8
检测:UV
波长/nm:255(90nm的带宽),240(80nm的带宽)、254(8nm的带宽)
相A:2mmol NH4HCO3(用NH3溶液调节到pH10)
相B:乙腈
时间表:
| 时间/分钟 |
%A |
%B |
|
0 |
90 |
10 |
|
25 |
10 |
90 |
|
28.8 |
10 |
90 |
|
29 |
90 |
10 |
|
34 |
90 |
10 |
手性方法
在Gilson HPLC系统上进行纯度分析:
方法:等浓度,正常相
方法持续时间/分钟:50
柱:Diacel Chrialcel OJ-H(5μm)4.6×250mm(保护盒DiacelChrialcel OJ-H分析保护盒5μm 4.0×10mm)
柱温/℃:40
注射/μl:10
流速ml/分钟:1.0
检测:UV
波长/nm:225(单波长检测器)
相A:己烷
相B:乙醇
时间表:
重力蒸气吸附(GVS)研究
在运行CFRSorp软件的Hiden IGASorp水分吸附分析器上分析所有样品。样品大小通常是10mg。水分吸附解吸等温线如下面概括的那样进行(2次扫描产生1个完整循环)。在典型的房间湿度和温度(40%RH,25℃)下装载/卸除所有样品。GVS分析后通过XRPD分析所有样品。除非另有说明,在25℃下以10%RH间隔在0-90%RH范围内进行标准等温分析。
溶解度
溶解度如下测量:将足够的化合物悬浮在0.25ml溶剂(水)中以产生该化合物的母体游离型的10mg/ml的最大最终浓度。在25℃下使该悬浮液平衡24小时,接着检测pH值并滤过玻璃纤维C 96井板。然后将滤液稀释101x。通过HPLC参照以大约0.1mg/ml溶于DMSO的标准样品进行定量。注射不同体积的标准、稀释和未稀释的试验物。将在与标准注射剂中峰最大值相同的停留时间下发现的峰面积积分计算溶解度。如果在滤板中存在足够的固体,则对于相变、水合物形成、非晶体化、结晶化等,通常检查XRPD。
表:
|
时间/分钟 |
%相A |
%相B |
|
0.0 |
95 |
5 |
|
1.0 |
80 |
20 |
|
2.3 |
5 |
95 |
|
3.3 |
5 |
95 |
|
3.5 |
95 |
5 |
|
4.4 |
95 |
5 |
pKa测定
在具有D-PAS附件的Sirius GlpKa仪器上进行pka测定。通过在甲醇∶H2O混合物中在25℃下电位滴定进行测量。滴定介质是用0.15MKCl调节的离子强度。经由Yasuda-ShedlovSky外推法将在甲醇∶H2O混合物中发现的值外推到0%助溶剂。
高温显微术
使用与Mettler-Toledo MTFP82HT热台相结合的Leica LM/DM偏振显微镜在25~350℃的温度范围中采用10-20℃/分钟的典型加热速率研究高温显微术。将少量样品分散到载玻片上,让个体颗粒尽可能充分地分离。在正常光线或交叉偏振光(与λ假色滤光片耦合)下用x20物镜观察样品。
手性纯度方法
系统配置
泵:Gilson 322二元泵
检测器:Gilson 152UV/Vis
自动取样器:Gilson 233XL rack+Gilson 402双注射泵
柱温箱:Phenomenex Thermasphere TS-130
软件:Gilson Unipoint LC软件
柱:Daicel Chiralcel OJ-H,5μm,4.6×250mm
保护柱:Daicel Chiralcel OJ-H分析保护盒,5μm,4.6x10mm
HPLC条件
通道A:己烷(93%)
通道B:乙醇(7%)
流速: 1.0ml/分钟
检测器波长225nm
柱温: 40℃
运行时间:50.0分钟
样品条件
将大约0.2mg样品溶于合适体积的己烷∶乙醇1∶1v/v而获得0.2mg/ml溶液。将它封闭并放置在旋涡混合器上以高速保持~15秒。如果将固体保留在此时,然后超声振荡样品小瓶大约10秒接着进一步在旋涡混合器上10-15秒。将10μl注射到HPLC系统上。在初始重复注射己烷∶乙醇1∶1v/v作为空白样品之后,一式二份地注射样品。
实施例5
药理学试验实施例
评价本发明苯磺酸盐1型的麻醉和镇静效果。将苯磺酸(苯并磺酸)盐溶于生理盐水以便将该试验组合物向动物的给药。将试验组合物给予小鼠,该小鼠放在独立的有机玻璃笼子(20×10×10cm)中。通过静脉途径用载体或受试物质注射小鼠。记录潜伏状态到睡眠和麻醉的持续时间(最大值:在受试物质给药后90分钟)。通过翻正反射(LRR)的丧失指示麻醉。一旦该动物似乎镇静就进行翻正反射试验,大约每隔20-30秒。一旦翻正反射不存在,通过此后大致每隔20-30秒测试翻正反射的恢复测量翻正反射丧失的持续时间。每一组研究八个小鼠并盲性地进行试验。研究的结果在下表中给出。
Mann-Whitney U试验:NS=不显著;*=p<0.05;**=p<0.01
Fisher′s精确试验(具有LRR的小鼠的数目):没有指征=不显著;
+=p<0.05;++=p<0.01
(#):如果n<3,则不计算
(##):最大值=在注射后90分钟
上表中的结果表明苯磺酸盐1型到翻正反射丧失具有短的潜伏状态并且因此在动物中具有短的到麻醉的诱导时间。另外,正如翻正反射丧失的短持续时间所示,小鼠从麻醉迅速地恢复。因此,这种化合物可以提供快速诱导和从麻醉的恢复。
实施例6
2型、3和4的结晶的附加条件
对附加条件进行试验以求再现2型、3和4的早先报道的结晶。然而,如下所述,报道的规模显著地降低并因此改进了方法。
2型
将5mg固体溶于25μl乙醇并添加10μl乙醇;然后在4℃下冷藏该溶液3天。
3型
尝试三种变体:
1.将5mg固体溶于50μl乙醇并添加120μl乙酸乙酯;然后在4℃下冷藏该溶液3天。
2.将10.1mg固体溶于300μl甲醇并添加120μl乙酸乙酯;然后在4℃下冷藏该溶液3天。
3.在硅烷化的小瓶中将2.5mg固体溶于50μl乙醇并添加100μl乙酸乙酯;然后在4℃下冷藏该溶液3天。
4型
尝试三种变体:
1.按20μl等分试样将热(70℃)混合物乙酸异丙酯∶乙醇(40%∶60%v/v)添加到5mg热固体中直到固体溶解(总计60μl溶剂混合物);然后在数小时的期间内允许该溶液最初在70℃下在恒温水浴中缓慢地冷却到环境温度。
2.将5mg固体溶于180μl热(50℃)乙酸异丙酯∶乙醇(40%∶60%v/v)溶剂并允许该溶液在恒温水浴中(最初在50℃)在数小时期间内缓慢地冷却到环境温度。
3.在硅烷化的小瓶中将5mg部分固体溶于100μl热(50℃)乙酸异丙酯∶乙醇(40%∶60%v/v)溶剂并允许该溶液在恒温水浴中(最初在50℃)在数小时期间内缓慢地冷却到环境温度。
每种结晶中产生具有叶片和板状形态的固体材料,其中4型结晶还产生针状材料。
实施例7
通式(I)的化合物苯磺酸盐的表征
通式(I)的化合物苯磺酸盐是手性的并且认为具有下面的单对映异构体型式,即S对映异构体(与随后测定的晶体结构一致):
该杂环构造包含在咪唑环中的碱性氮(pKa为大约5),和吡啶基环中的弱碱性氮(pKa为大约2)。该咪唑氮通常在强酸性苯磺酸盐(pKa大约-0.6)存在下在水溶液中将被质子化,其中吡啶基氮在过量苯磺酸盐的条件下也可能被质子化。
该化合物的中性游离碱晶型(即未质子化型)预期是略微亲脂性的(loP辛醇∶水大约4.0)并因此将与水性环境相比更喜欢一定亲脂性的环境。此外,它很可能保持亲脂性程度,即使当被单质子化(logD辛醇∶水大约2,在pH 3)时,但是苯磺酸根反离子的效果很可能经由其固有的亲水性改善这种趋势。对于二质子化型(logD辛醇∶水大约0.6,在pH0),亲脂性的程度进一步减弱。
该化合物还具有过量的氢键受体并且因此将适合地被供氢键溶剂配伍。因此预期该化合物将更喜欢在一定范围的极性有机溶剂例如醇,尤其是提供部分亲脂性、供氢键环境的那些中溶解。这已经由实验证据证实(所使用的溶剂的细节在实施例8中给出):
|
溶剂 |
观察到的溶解度(mg/ml) |
|
甲酰胺 |
350 |
|
水 |
2 |
|
二甲基亚砜 |
500 |
|
二甲基乙酰胺 |
200 |
|
1,2-乙二醇 |
60 |
|
二甲基甲酰胺 |
300 |
|
乙腈 |
>20 |
|
甲醇 |
400 |
|
2-乙氧基乙醇 |
20 |
|
2,2,2-三氟乙醇 |
1000 |
|
乙醇 |
100 |
|
丙酮 |
2 |
|
丙-1-醇 |
15 |
|
丙-2-醇 |
4.8 |
|
2-甲氧基乙醇 |
167 |
|
六氟丙-2-醇 |
>700 |
|
二氯甲烷 |
<<0.3 |
|
四氢呋喃 |
2.5 |
|
苯甲酸甲酯 |
2 |
|
乙酸乙酯 |
0.2 |
|
氯仿 |
<<0.4 |
|
1,4-二噁烷 |
1 |
可溶(>5mg/ml),部分可溶(2.5-5mg/ml),部分不溶(0.5-2.5mg/ml,不溶(<0.5mg/ml).
引用的值是近似的,但是实验上被确认.
这些结果强调了该化合物在各种极性有机溶剂中的良好溶解性。具体来说,2,2,2-三氟乙醇和六氟丙-2-醇都确定为是该化合物的极其良好的溶剂。这与上面讨论的考虑一致,该两种溶剂是强氢键供体。同样地,更显著亲脂性的溶剂确定为不良溶剂,并因此是用于结晶的可能的反溶剂。
实施例8
通式(I)的化合物苯磺酸盐结晶
描述了有助于获得通式(I)的化合物苯磺酸盐1型和2型的结晶材料的各种条件。包括醇或乙腈溶剂作为组分与它们各自相容的反溶剂或助溶剂的结晶条件据认为提供最有希望的条件以产生有用的结晶材料。使用溶剂/反溶剂二元混合物的结晶化是主要使用的。通过在环境温度和降低(4℃)的温度下从该化合物在溶剂/反溶剂混合物中的亚饱和溶液延迟蒸发进行结晶。通常在制备的3-5天内观察结晶。
当允许样品数量时,所有结晶条件一式两份地在玻璃96-井板型式中进行;每一井板的一半用来重复该井板另一半中的条件。通过设计使井间的交叉污染最小化。试验的所有条件以至少一式两份地可再现运转,大多数产生适合于进一步分析的固体材料。
在所有情况下,小心翼翼地用各种溶剂和反应试剂清洗与样品和结晶介质接触的设备,然后浸泡在乙醇之中并使用大量蒸发的氮气吹干。
采用得自商业供应商的高质量溶剂,如表12所述。
表12
|
溶剂 |
供应商 |
产品号 |
批料号 |
等级 |
纯度 |
|
1,2-二氯苯 |
Romil |
H177 |
E558470 |
SpS |
>99.8% |
| 1,4-二甲苯 |
Fluka |
95682 |
429739/1 |
purissp.a. |
>99% |
|
1,4-二噁烷 |
Romil |
H297 |
H540480 |
SpS |
>99.9% |
|
2,2,2-三氟乙醇 |
Romil |
H860 |
M538412 |
SpS |
>99.9% |
|
乙腈 |
Romil |
H049 |
D531490 |
SpS |
>99.9% |
|
二甲基乙酰胺 |
Romil |
H249 |
B540480 |
SpS |
>99.9% |
|
二甲基亚砜 |
Romil |
H280 |
W530480 |
SpS |
>99.9% |
|
乙醇 |
Romil |
H314 |
O533480 |
SpS |
>99.8% |
|
乙酸乙酯 |
Romil |
H346 |
T533480 |
SpS |
>99.9% |
|
甲基异丁基酮 |
Romil |
H446 |
M539430 |
SpS |
>99.9% |
|
正壬烷 |
Romil |
H568 |
O558450 |
SpS |
>99.9% |
| 乙酸戊酯 |
Fluka |
46022 |
13248/1 |
purissp.a. |
>98.5% |
|
丙-1-醇 |
Romil |
H624 |
G531460 |
SpS |
>99.9% |
|
丙-2-醇 |
Romil |
H625 |
O530480 |
SpS |
>99.9% |
|
四氯乙烯 |
Romil |
H702 |
W536450 |
SpS |
>99.9% |
|
四氢呋喃 |
Romil |
H718 |
B532470 |
SpS |
>99.9% |
|
丙酮 |
Romil |
H031 |
E559470 |
SpS |
>99.9% |
|
氯仿 |
Romil |
H135 |
B554470 |
SpS |
>99.9% |
|
二氯甲烷 |
Romil |
H202 |
O554460 |
SpS |
>99.9% |
|
二甲基甲酰胺 |
Romil |
H253 |
T546460 |
SpS |
>99.9% |
|
甲酰胺 |
Romil |
H351 |
Q537480 |
BioPure |
>99.9% |
|
六氟丙-2-醇 |
Romil |
H359 |
H559470 |
SpS |
>99.9% |
|
苯甲酸甲酯 |
Fluka |
12460 |
417868/1 |
purum |
>98% |
|
水 |
Romil |
H950 |
D537480 |
SpS |
>99.9% |
使用附有数字照相机的双目显微镜(大约10x-40x放大率)视觉分析所得的结晶形态,该双目显微镜酌情采用透射和反射光照。
固体材料的视觉表征在下表14中归纳。观察到优势的叶片或表格式/板形态,作为独特的晶体或作为球粒。总体上,在环境温度下进行的结晶和在4℃进行的那些之间几乎没有形态差异,除用乙醇作为溶剂的那些之外,其中球粒和界面类型生长的趋势随温度降低而减弱。值得注意的是,使用反溶剂可以显著地改进结晶材料的质量。
观察到的结晶材料的实施例图像在图17中给出。如该图所示,乙腈具有产生球粒生长的倾向,这通常看作差成核作用的结果并因此从质量差的结晶表面生长。相反,2-甲氧基乙醇具有产生具有叶片/针状形态的独特晶体的倾向。
1型从许多条件结晶似乎是一般优选的。然而,值得注意的是,2型也从一些结晶条件观察到,包括获得3型和4的按比例缩小类似物(在实施例6中进行了描述)。在其中存在极性(例如乙腈∶水)或亲脂性(正壬烷)或两者(二甲基亚砜:1,2-二氯苯)的极端的条件下观察到2型。一般而言,2型的晶体在它们的优等品质和特异的良好成形的板/表格式晶形方面是显著的。
单晶X射线衍射晶胞测定
为了提供所产生的结晶形态的佐证证据,使用单晶X射线衍射测定具有适合质量的许多晶体的晶胞参数。使用Kappa CCD衍射计用Mo辐射测定晶体单晶参数,该晶体安装在含油且保持在260k的玻璃纤维上。已经测定了1型和2型的参数,如表13中所归纳。
表13.对通式(I)的化合物苯磺酸盐的晶体测定的晶胞参数
通式(I)的化合物苯磺酸盐从溶剂/助溶剂和溶剂/反溶剂条件的结晶结果与单晶X射线衍射单晶结果在表14中制表。
表14.通式(I)的化合物苯磺酸盐从溶剂/助溶剂和溶剂/反溶剂条件的实验结晶结果,与单晶X射线衍射单晶结果(除非另有说明,环境结晶的X射线结果)。
对于全部单晶X射线衍射晶体结构测定,获得适合质量的各种晶体,并对于1型和2型,获得全部结构。这些晶体结构在实施例9和10中报道。
实施例9
1型的晶体结构
从2-甲氧基乙醇∶乙酸戊酯溶液生长的通式(I)的化合物苯磺酸盐的晶体(它们具有针状晶形)在图17中成像。
选择单针晶形晶体(尺寸大约0.8×0.04×0.02mm)并且在260K,然后在190K测定它的晶胞参数。当在260-190K之间降温时没有观察到转变。这里分析的结构用于在190K的数据;晶体的参数和X射线衍射细化在表15中给出。
表15.通式(I)的化合物苯磺酸盐1型的2-甲氧基乙醇∶乙酸戊酯生长晶体的数据。
不对称单元的含量在图18中显示出。它由化合物的两个独立的分子和两个独立的苯磺酸根反离子构成。每一化合物的咪唑氮被质子化。
Flack“Enantiopole”参数测定为0.03(1)并因此这里描绘的结构的立体化学良好地建立并且与该化合物的声称的立体化学一致:
结晶学共纵坐标及其它有关数据以SHELX文件形式在表17中制表。
构象无序可以由原子位置的“热椭圆体”表示(大致上),如图19上给出的那样。可以看出,无序的主要区域位于甲基和苯磺酸盐。
两个独立分子间的差异主要来自酯链,如图20所示。一个分子具有与咪唑环共面的酯链,而另一个分子具有是正交的酯链。
酯链的构象不同于2型中采纳的构象(图21)。在1型中观察到的正交构象与2型中发现的构象最相似。
两个独立的苯磺酸盐具有参差构象(图22)。显然键长方面没有相当大的差异。
一个苯磺酸盐采纳对2型中的苯磺酸盐观察到的构象(图23)。
沿着结晶学a、b和c轴观察到的解析的晶体结构分别在图24a、b和c中示出。图25归纳了晶体填充中观察到的最短接触。
每一化合物与两个独立的苯磺酸盐相互作用。具体来说,一个苯磺酸盐的一个氧原子和该化合物的咪唑环的质子化氮间建立了短距离(氢键型)。第二独立的化合物相似地相互作用,但是是与第二独立的苯磺酸盐相互作用。
在该化合物和主要在咪唑和吡啶基环附近的苯磺酸盐间观察到其它紧密接触(C-O,H-O)。在两个化合物本身(Br-N、C-C、O-H)和两个苯磺酸盐本身(O-H接触)间也观察到某种紧密接触,但是后者程度更小。
使用实验上测定的晶体结构,已经使用
(CrystalDiffract是CrystalMaker Ltd的注册商标)计算了1型的粉末衍射图案并在图26中绘出。这一粉末图案与对1型报道的实验性粉末图案匹配。
实施例10
2型的晶体结构
将通式(I)的化合物苯磺酸盐2型(它具有板晶形)的晶体在图27中成像。
选择单板晶形晶体(尺寸大约0.7×0.30×0.25mm)并且在260K,然后在190K测定它的晶胞参数。当在260-190K之间降温时没有观察到转变。这里分析的结构用于在190K的数据;晶体的参数和X射线衍射细化在表16中给出。
表16.通式(I)的化合物苯磺酸盐(2型)的乙醇∶乙酸乙酯生长晶体的数据。
不对称单元的含量在图28中显示出。它由该化合物的一个独立的分子和一个独立的苯磺酸盐构成。该化合物的咪唑氮被质子化。
Flack″Enantiopole″参数被测定为0.011(9)并因此这里描绘的结构的立体化学良好建立并且与该化合物的声称的立体化学一致。结晶学共纵坐标及其它有关数据以SHELX文件形式在表18中制表。
构象无序可以由原子位置的“热椭圆体”表示(大致上),如图29上给出的那样。可以看出,无序的主要区域位于苯磺酸盐。
如上所讨论,2型中的酯链的构象(图30中绘出)不同于1型中采纳的构象。
然而,该苯磺酸盐的构象与对1型中的苯磺酸盐之一观察到的构象(图31)相似。
沿着结晶学a、b和c轴观察的解析晶体结构分别在图32a、b和c中示出,其中图33归纳在晶体填充中观察到的最短接触。该化合物经由咪唑环的质子化氮与该苯磺酸盐的一个氧原子短接触(氢键型)。在该化合物和苯磺酸盐间观察到经由咪唑环的其它短接触(C-C、C-O、H-O)。
在这两种化合物本身(Br-C、C-C、O-C、O-H)之间也观察到某种紧密接触,它们中大部分经由酯链。苯磺酸盐本身之间不存在紧密接触。
使用实验上测定的晶体结构,已经使用
计算出2型的粉末衍射图案(图34)。这一粉末图案与对2型报道的实验性粉末图案匹配。
表17.以SHELX文件形式对通式(I)的化合物苯磺酸盐剂型1制表的结晶学共纵坐标及其它有关数据。
TITL 12161316 化合物 CNS7056
型
CELL 0.71073 7.687 29.261 12.376 90.000 97.788 90.000
ZERR 2 0.0001 0.0005 0.0003 0.0000 0.0008 0.0000
LATT -1
SYMM -X,Y+0.500,-Z
SFAC C 2.3100 20.8439 1.0200 10.2075 1.5886
0.5687 0.8650=
51.6512 0.2156 0.0033 0.0016 1.15
0.7700 12.0110
SFAC H 0.4930 10.5109 0.3229 26.1257 0.1402
3.1424 0.0408=
57.7998 0.0030 0.0000 0.0000 0.06
0.3200 1.0079
SFAC O 3.0485 13.2771 2.2868 5.7011 1.5463
0.3239 0.8670=
32.9089 0.2508 0.0106 0.0060 3.25
0.7700 15.9994
SFAC BR 17.1789 2.1723 5.2358 16.5796 5.6377
0.2609 3.9851=
41.4328 2.9557 -0.2901 2.4595 1000.00
1.1000 79.9040
SFAC N 12.2126 0.0057 3.1322 9.8933 2.0125
28.9975 1.1663=
0.5826 -11.5290 0.0061 0.0033 1.96
0.7700 14.0067
SFAC S 6.9053 1.4679 5.2034 22.2151 1.4379
0.2536 1.5863=
56.1720 0.8669 0.1246 0.1234 53.20
1.1100 32.0660
UNIT 108.100.20.4.16.4.
S80 6 0.23964 0.43139 0.09908 11.00000
0.04634 0.03299=
0.04052 0.00002 0.01880 -0.00340
O81 3 0.16028 0.39374 0.15143 11.00000
0.06864 0.04111=
0.05255 -0.00210 0.02801 0.00002
O82 3 0.14598 0.47435 0.11207 11.00000
0.08099 0.03603=
0.04614 0.00545 0.03373 -0.00236
O83 3 0.42589 0.43401 0.12925 11.00000
0.05754 0.08564=
0.05198 -0.01536 0.01792 -0.00644
C84 1 0.20581 0.41866 -0.04324 11.00000
0.05949 0.04444=
0.02903 0.00359 0.01728 0.00704
C85 1 0.03624 0.41100 -0.09142 11.00000
0.06649 0.10092=
0.05586 0.01088 0.01751 0.00507
C86 1 0.00323 0.39810 -0.20187 11.00000
0.08670 0.14765=
0.05902 -0.02096 -0.03160 -0.00004
C87 1 0.14311 0.39209 -0.25693 11.00000
0.07916 0.11651=
0.06238 -0.01696 0.00195 0.02481
C88 1 0.30473 0.39806 -0.20987 11.00000
0.09246 0.09710=
0.04155 0.00157 0.01795 0.02685
C89 1 0.33456 0.41126 -0.10133 11.00000
0.05999 0.09817=
0.07178 -0.01451 0.00886 0.02173
S90 6 0.68868 0.81145 0.51625 11.00000
0.04072 0.02869=
0.05437 0.00158 0.00214 0.00223
O91 3 0.79129 0.77464 0.57315 11.00000
0.08025 0.03751=
0.04867 -0.00213 -0.00954 0.01626
O92 3 0.52601 0.81933 0.56122 11.00000
0.04778 0.05360=
0.06934 -0.00642 0.01702 0.00039
O93 3 0.78935 0.85213 0.50763 11.00000
0.07515 0.04369=
0.05025 -0.01354 0.01764 -0.01547
C94 1 0.62446 0.78970 0.38130 11.00000
0.04232 0.04028=
0.05049 0.00898 0.00929 0.00525
C95 1 0.74659 0.76959 0.32396 11.00000
0.06194 0.06998=
0.03238 0.00341 -0.00103 0.00990
C96 1 0.69911 0.75023 0.22476 11.00000
0.12417 0.10337=
0.03441 0.01537 0.02421 0.03314
C97 1 0.51941 0.75295 0.17732 11.00000
0.11897 0.11939=
0.02308 -0.01324 -0.00963 -0.00586
C98 1 0.40301 0.77268 0.23169 11.00000
0.06106 0.10242=
0.05463 0.00570 -0.01263 -0.00283
C99 1 0.45446 0.79193 0.33547 11.00000
0.05307 0.07089=
0.04982 0.00728 -0.00426 -0.01944
BR1 4 0.06011 0.52462 0.55140 11.00000
0.04153 0.05204=
0.07369 -0.00524 0.02434 0.00670
C2 1 0.25757 0.50395 0.49005 11.00000
0.02832 0.04536=
0.03350 -0.00752 0.01511 0.00763
C3 1 0.28921 0.45781 0.47911 11.00000
0.03135 0.03107=
0.04579 0.00145 0.00221 -0.00479
C4 1 0.42954 0.44393 0.43174 11.00000
0.03767 0.03461=
0.02980 -0.00320 -0.00151 -0.00125
C5 1 0.54674 0.47556 0.39943 11.00000
0.03535 0.02939=
0.03479 -0.00390 0.00647 0.00183
C6 1 0.51907 0.52242 0.41134 11.00000
0.04226 0.03479=
0.04333 -0.00172 0.00236 0.00188
C7 1 0.37213 0.53602 0.45794 11.00000
0.03598 0.02793=
0.04586 -0.00044 0.01652 0.00336
C8 1 0.64321 0.55824 0.38118 11.00000
0.03964 0.02453=
0.02719 0.00516 0.00457 0.00373
C9 1 0.68998 0.59645 0.46059 11.00000
0.03743 0.03694=
0.04454 -0.00375 0.01588 0.00649
N10 5 0.69097 0.58514 0.56581 11.00000
0.06070 0.03116=
0.04918 -0.00640 0.02020 -0.00054
C11 1 0.74090 0.61847 0.63822 11.00000
0.06804 0.05787=
0.04752 -0.00600 0.01695 -0.00669
C12 1 0.78515 0.66221 0.61053 11.00000
0.05480 0.04458=
0.05526 -0.02125 0.01554 -0.00787
C13 1 0.77550 0.67229 0.50132 11.00000
0.04463 0.03102=
0.05452 0.00407 0.01432 -0.00038
C14 1 0.73186 0.63955 0.42553 11.00000
0.04272 0.03021=
0.04282 -0.00243 0.01499 0.00270
N15 5 0.71451 0.55972 0.29408 11.00000
0.04979 0.02502=
0.03692 0.00975 0.01748 0.00775
C16 1 0.67500 0.52204 0.21324 11.00000
0.04463 0.02346=
0.04948 -0.00464 0.01738 0.00561
C17 1 0.75857 0.47996 0.26673 11.00000
0.04549 0.02673=
0.01954 -0.00693 0.00506 -0.00121
N18 5 0.70009 0.45973 0.35317 11.00000
0.03293 0.02806=
0.02597 -0.00088 0.00321 0.00207
C19 1 0.81334 0.42409 0.39181 11.00000
0.03678 0.02848=
0.03351 -0.00426 0.00585 0.00488
C20 1 0.93968 0.42402 0.32661 11.00000
0.03371 0.02802=
0.03711 0.00202 0.00106 0.00680
N21 5 0.90585 0.45925 0.25315 11.00000
0.04775 0.03416=
0.02231 -0.01051 0.01052 -0.00308
C22 1 0.79597 0.39511 0.48941 11.00000
0.03997 0.03711=
0.04548 0.01039 0.00508 0.00197
C23 1 0.74788 0.53407 0.10940 11.00000
0.05650 0.04712=
0.03514 0.00836 0.00449 0.00605
C24 1 0.68780 0.50047 0.01647 11.00000
0.08242 0.04077=
0.03001 -0.00046 0.01385 0.00523
C25 1 0.71419 0.51690 -0.09234 11.00000
0.06429 0.06543=
0.03392 0.00018 0.00559 -0.00499
O26 3 0.76261 0.55440 -0.11450 11.00000
0.12347 0.08282=
0.04188 0.01501 0.01658 -0.04001
O27 3 0.65910 0.48459 -0.16756 11.00000
0.10340 0.06919=
0.03191 0.00253 0.01824 -0.00449
C28 1 0.66642 0.49760 -0.27953 11.00000
0.19131 0.12699=
0.01390 -0.01417 0.02134 -0.05279
BR51 4 1.06737 0.71057 0.98743 11.00000
0.03812 0.08781=
0.06774 0.00566 -0.00531 0.00447
C52 1 0.84276 0.73306 0.93243 11.00000
0.03132 0.05952=
0.03819 0.00358 0.00226 -0.00263
C53 1 0.81293 0.77906 0.93249 11.00000
0.04627 0.06820=
0.03723 -0.00581 0.00481 -0.00474
C54 1 0.65043 0.79579 0.88269 11.00000
0.04551 0.03939=
0.04858 -0.00084 0.00376 -0.01071
C55 1 0.51946 0.76552 0.84226 11.00000
0.04294 0.03573=
0.03413 0.00062 0.00952 -0.00208
C56 1 0.54512 0.71765 0.84581 11.00000
0.02688 0.03659=
0.04586 -0.00025 0.00561 0.00047
C57 1 0.71139 0.70186 0.88914 11.00000
0.03105 0.04840=
0.04447 -0.00668 -0.00429 0.00504
C58 1 0.40956 0.68443 0.79765 11.00000
0.03348 0.02893=
0.04334 0.00070 0.00351 0.00421
C59 1 0.38048 0.64253 0.86694 11.00000
0.03165 0.03488=
0.04951 0.00002 0.00425 0.00528
N60 5 0.42879 0.64650 0.97247 11.00000
0.03542 0.05694=
0.03178 0.00872 0.00154 0.00467
C61 1 0.38962 0.61026 1.03529 11.00000
0.04457 0.06338=
0.05765 0.01416 0.00707 0.00171
C62 1 0.30187 0.57202 0.98967 11.00000
0.06548 0.04957=
0.11303 0.03456 0.03582 0.00696
C63 1 0.25733 0.56863 0.88018 11.00000
0.07395 0.04664=
0.09803 0.00115 0.01240 -0.01007
C64 1 0.29561 0.60475 0.81590 11.00000
0.08355 0.04152=
0.05459 -0.00010 0.00128 -0.02308
N65 5 0.31344 0.68797 0.70771 11.00000
0.03846 0.03072=
0.04952 -0.00160 0.00032 0.00597
C66 1 0.33129 0.72953 0.64125 11.00000
0.03574 0.02676=
0.05519 0.00406 0.00580 0.00330
C67 1 0.26347 0.76733 0.70231 11.00000
0.03803 0.03316=
0.04166 0.01528 0.00868 0.00029
N68 5 0.35122 0.78274 0.79764 11.00000
0.03387 0.03259=
0.05055 0.00549 0.00427 0.00218
C69 1 0.24763 0.81583 0.84108 11.00000
0.05345 0.03305=
0.04570 0.00005 0.02067 -0.00546
C70 1 0.09873 0.81841 0.77077 11.00000
0.04465 0.03799=
0.06107 0.00794 0.01464 0.00936
N71 5 0.10819 0.78841 0.68720 11.00000
0.03892 0.03266=
0.05306 0.00974 0.01063 0.00803
C72 1 0.30218 0.84064 0.94469 11.00000
0.08091 0.04934=
0.08052 -0.01505 0.02392 -0.00661
C73 1 0.22541 0.72388 0.52948 11.00000
0.04039 0.05583=
0.03295 0.00047 0.00724 -0.00165
C74 1 0.30154 0.68566 0.46508 11.00000
0.05896 0.05343=
0.05504 -0.00576 0.00667 0.02016
C75 1 0.18003 0.67204 0.36587 11.00000
0.05296 0.05447=
0.04241 0.00546 0.01355 0.00171
O76 3 0.06782 0.69497 0.31818 11.00000
0.05552 0.07543=
0.05719 -0.00702 -0.00194 0.02108
O77 3 0.22119 0.62976 0.33149 11.00000
0.08466 0.04267=
0.04376 -0.00714 0.00726 0.00488
C78 1 0.10717 0.61220 0.23887 11.00000
0.06302 0.09312=
0.07465 -0.02449 0.02418 -0.00980
H611 2 10.42342 10.61111 11.10933 11.00000
0.06582
H621 2 10.27371 10.54835 11.03412 11.00000
0.09086
H631 2 10.20282 10.54235 10.84949 11.00000
0.08585
H641 2 10.26600 10.60396 10.74163 11.00000
0.07058
H661 2 10.45616 10.73494 10.63683 11.00000
0.04658
H701 2 10.00528 10.83765 10.77749 11.00000
0.05724
H721 2 10.20390 10.85662 10.96784 11.00000
0.10482
H722 2 10.39143 10.86250 10.93477 11.00000
0.10500
H723 2 10.34863 10.81975 11.00178 11.00000
0.10479
H731 2 10.22647 10.75279 10.49048 11.00000
0.05050
H732 2 10.10462 10.71635 10.53573 11.00000
0.05107
H741 2 10.41143 10.69632 10.44327 11.00000
0.06599
H742 2 10.32279 10.65905 10.51273 11.00000
0.06616
H571 2 10.73613 10.67093 10.88928 11.00000
0.04893
H531 2 10.89874 10.79871 10.96543 11.00000
0.05990
H541 2 10.63029 10.82681 10.87790 11.00000
0.05285
H161 2 10.54702 10.51731 10.19609 11.00000
0.04687
H201 2 11.03302 10.40374 10.33036 11.00000
0.03977
H221 2 10.90306 10.37871 10.51025 11.00000
0.06107
H222 2 10.77354 10.41394 10.54853 11.00000
0.06102
H223 2 10.70245 10.37370 10.47387 11.00000
0.06087
H231 2 10.71028 10.56434 10.08666 11.00000
0.05487
H232 2 10.87494 10.53365 10.12431 11.00000
0.05471
H241 2 10.56546 10.49241 10.01723 11.00000
0.06095
H242 2 10.75795 10.47323 10.02815 11.00000
0.06099
H111 2 10.74728 10.61186 10.71244 11.00000
0.06882
H121 2 10.81997 10.68398 10.66349 11.00000
0.06182
H131 2 10.79812 10.70154 10.48020 11.00000
0.05215
H141 2 10.72939 10.64544 10.35226 11.00000
0.04595
H71 2 10.35042 10.56684 10.46668 11.00000
0.04408
H31 2 10.21444 10.43638 10.50355 11.00000
0.04223
H41 2 10.44931 10.41280 10.42055 11.00000
0.04056
H891 2 10.44977 10.41481 9.93226 11.00000
0.09285
H881 2 10.39917 10.39332 9.75106 11.00000
0.09266
H871 2 10.12372 10.38356 9.66972 11.00000
0.10194
H861 2 9.88808 10.39388 9.76390 11.00000
0.11607
H851 2 9.94416 10.41466 9.94909 11.00000
0.08904
H951 2 10.86472 10.76918 10.35546 11.00000
0.06580
H961 2 10.78321 10.73544 10.18942 11.00000
0.10497
H971 2 10.48493 10.74055 10.10914 11.00000
0.10604
H981 2 10.28646 10.77378 10.20054 11.00000
0.08719
H991 2 10.37377 10.80653 10.37249 11.00000
0.07037
H781 2 10.14480 10.58182 10.22240 11.00000
0.11588
H782 2 10.11102 10.63197 10.17669 11.00000
0.11581
H783 2 9.98883 10.61082 10.25546 11.00000
0.11600
H711 2 10.01359 10.78308 10.62464 11.00000
0.05205
H211 2 10.98261 10.46785 10.19729 11.00000
0.04161
H281 2 10.62358 10.47180 9.67092 11.00000
0.11566
H282 2 10.59036 10.52501 9.70225 11.00000
0.11566
H283 2 10.79029 10.50514 9.71088 11.00000
0.11566
表18.以SHELX文件形式对通式(I)的化合物苯磺酸盐型制表的结晶学共纵坐标及其它有关数据。
TITL 1142055 化合物 CNS7056剂型1
CELL 0.71073 8.921 11.154 25.834 90.000 90.000 90.000
ZERR 4 0.0001 0.0002 0.0004 0.0000 0.0000 0.0000
LATT -1
SYMM X+0.500,-Y+0.500,-Z
SYMM -X,Y+0.500,-Z+0.500
SYMM -X+0.500,-Y,Z+0.500
SFAC C 2.3100 20.8439 1.0200 10.2075 1.5886
0.5687 0.8650=
51.6512 0.2156 0.0033 0.0016 1.15
0.7700 12.0110
SFAC H 0.4930 10.5109 0.3229 26.1257 0.1402
3.1424 0.0408=
57.7998 0.0030 0.0000 0.0000 0.06
0.3200 1.0079
SFAC BR 17.1789 2.1723 5.2358 16.5796 5.6377
0.2609 3.9851=
41.4328 2.9557 -0.2901 2.4595 1000.00
1.1000 79.9040
SFAC N 12.2126 0.0057 3.1322 9.8933 2.0125
28.9975 1.1663=
0.5826 -11.5290 0.0061 0.0033 1.96
0.7700 14.0067
SFAC O 3.0485 13.277 12.2868 5.7011 1.5463
0.3239 0.8670=
32.9089 0.2508 0.0106 0.0060 3.25
0.7700 15.9994
SFAC S 6.9053 1.4679 5.2034 22.2151 1.4379
0.2536 1.5863=
56.1720 0.8669 0.1246 0.1234 53.20
1.1100 32.0660
UNIT 108.100.4.16.20.4.
BR1 3 -0.04819 -0.10880 -0.27710 11.00000
0.07032 0.03277=
0.03090 0.00144 -0.01238 -0.02224
C2 1 -0.15018 -0.21830 -0.32054 11.00000
0.02777 0.02177=
0.02345 -0.00009 -0.00209 -0.00471
C3 1 -0.17401 -0.18875 -0.37205 11.00000
0.02963 0.01861=
0.02702 0.00623 0.00188 -0.00107
C4 1 -0.24491 -0.26965 -0.40362 11.00000
0.02825 0.02442=
0.01718 0.00327 0.00106 -0.00145
C5 1 -0.29275 -0.37943 -0.38401 11.00000
0.02223 0.01822=
0.01875 -0.00067 0.00141 0.00066
C6 1 -0.27139 -0.40894 -0.33163 11.00000
0.02028 0.01967=
0.01926 0.00182 0.00105 -0.00153
C7 1 -0.20042 -0.32532 -0.29979 11.00000
0.02809 0.02763=
0.01685 0.00206 0.00190 -0.00055
C8 1 -0.32197 -0.52600 -0.30927 11.00000
0.01670 0.02233=
0.01945 0.00135 -0.00476 -0.00144
C9 1 -0.39853 -0.52353 -0.25770 11.00000
0.01623 0.02317=
0.01584 0.00259 -0.00384 -0.00281
N10 4 -0.46099 -0.41943 -0.24363 11.00000
0.02251 0.02613=
0.02353 -0.00189 0.00408 0.00155
C11 1 -0.52777 -0.41652 -0.19697 11.00000
0.02617 0.03441=
0.02357 -0.00451 0.00365 0.00346
C12 1 -0.53610 -0.51390 -0.16425 11.00000
0.02740 0.04329=
0.02040 -0.00335 0.00652 -0.00779
C13 1 -0.47518 -0.62062 -0.17997 11.00000
0.03584 0.03200=
0.02405 0.00767 0.00645 -0.00687
C14 1 -0.40334 -0.62685 -0.22730 11.00000
0.02879 0.02223=
0.02565 0.00090 0.00272 -0.00057
N15 4 -0.30040 -0.62781 -0.33049 11.00000
0.02151 0.02416=
0.01713 0.00287 -0.00002 0.00182
C16 1 -0.21928 -0.62991 -0.38036 11.00000
0.02330 0.02286=
0.01602 0.00057 0.00417 0.00450
C17 1 -0.32510 -0.57975 -0.41920 11.00000
0.02824 0.02308=
0.01704 -0.00121 0.00336 -0.00285
N18 4 -0.36294 -0.46298 -0.41818 11.00000
0.02482 0.02037=
0.01483 0.00150 -0.00070 0.00079
C19 1 -0.46920 -0.44117 -0.45641 11.00000
0.03022 0.02725=
0.01634 0.00325 0.00039 -0.00224
C20 1 -0.49445 -0.54753 -0.47911 11.00000
0.03071 0.03401=
0.01669 0.00110 -0.00174 -0.00215
N21 4 -0.40440 -0.63226 -0.45591 11.00000
0.03619 0.02354=
0.02146 -0.00463 0.00147 -0.00154
C22 1 -0.5431 0-0.32298 -0.46595 11.00000
0.03636 0.03429=
0.03074 0.00778 -0.00982 -0.00011
C23 1 -0.15995 -0.75547 -0.39193 11.00000
0.03430 0.02640=
0.01793 -0.00359 0.00177 0.00554
C24 1 -0.06166 -0.79435 -0.34621 11.00000
0.04707 0.03881=
0.02350 0.00041 0.00034 0.01530
C25 1 0.06625 -0.87542 -0.35603 11.00000
0.03182 0.02650=
0.01948 0.00340 -0.00125 -0.00016
O26 5 0.17233 -0.88334 -0.32760 11.00000
0.03778 0.06570=
0.03313 -0.01160 -0.01173 0.00417
O27 5 0.05245 -0.94265 -0.39885 11.00000
0.03130 0.03874=
0.02467 -0.00799 -0.00330 0.01418
C28 1 0.17574 -1.02443 -0.40865 11.00000
0.05622 0.08123=
0.03697 -0.01153 -0.00496 0.04396
S80 6 -0.94275 -0.52899 -0.49624 11.00000
0.03340 0.02679=
0.02442 0.00000 0.00210 -0.00075
O81 5 -0.83867 -0.47114 -0.53020 11.00000
0.05118 0.08336=
0.03575 0.02297 -0.00622 -0.02476
O82 5 -1.08156 -0.46260 -0.49186 11.00000
0.04015 0.07788=
0.05503 -0.01022 -0.00539 0.01721
O83 5 -0.97025 -0.65272 -0.50726 11.00000
0.13945 0.03230=
0.06071 -0.01467 0.01447 -0.00725
C84 1 -0.86288 -0.52210 -0.43343 11.00000
0.02735 0.05893=
0.02832 0.01509 0.00686 -0.00534
C85 1 -0.87781 -0.41462 -0.40588 11.00000
0.03763 0.08695=
0.03855 -0.01799 0.00427 -0.00754
C86 1 -0.81420 -0.39965 -0.35764 11.00000
0.05438 0.16315=
0.04455 -0.02905 0.00147 -0.02905
C87 1 -0.73766 -0.49241 -0.33773 11.00000
0.06202 0.20226=
0.06481 0.03510 -0.02105 -0.05062
C88 1 -0.71885 -0.60444 -0.36221 11.00000
0.04217 0.17120=
0.11388 0.10762 -0.01320 -0.03729
C89 1 -0.78500 -0.61610 -0.41251 11.00000
0.03725 0.08786=
0.07642 0.05538 -0.00772 -0.01074
H891 2 9.22557 9.31210 9.56883 11.00000
0.08027
H881 2 9.33331 9.33306 9.65289 11.00000
0.13097
H851 2 9.06867 9.64846 9.57936 11.00000
0.06577
H861 2 9.17563 9.67239 9.66111 11.00000
0.10509
H161 2 9.86530 9.42517 9.62245 11.00000
0.02469
H111 2 9.42959 9.65626 9.81326 11.00000
0.03383
H121 2 9.41618 9.49292 9.86839 11.00000
0.03606
H131 2 9.51614 9.31066 9.84059 11.00000
0.03697
H141 2 9.64103 9.30191 9.76144 11.00000
0.03108
H231 2 9.89972 9.24922 9.57680 11.00000
0.03066
H232 2 9.75764 9.18723 9.60372 11.00000
0.03099
H241 2 9.87585 9.16237 9.67759 11.00000
0.04434
H242 2 9.97980 9.27746 9.67100 11.00000
0.04489
H281 2 10.15353 8.92912 9.56085 11.00000
0.08666
H282 2 10.18989 8.92278 9.62053 11.00000
0.08723
H283 2 10.26566 9.02166 9.58620 11.00000
0.08710
H201 2 9.44027 9.43682 9.49457 11.00000
0.03327
H221 2 9.36727 9.66624 9.51370 11.00000
0.05146
H222 2 9.52479 9.72860 9.51527 11.00000
0.05104
H223 2 9.43193 9.71611 9.56601 11.00000
0.05131
H41 2 9.73983 9.74902 9.56204 11.00000
0.02807
H31 2 9.85823 9.88568 9.61518 11.00000
0.03001
H71 2 9.81367 9.65791 9.73490 11.00000
0.02870
H871 2 9.30621 9.51762 9.69480 11.00000
0.13226
H211 2 9.59801 9.29339 9.53630 11.00000
0.03270
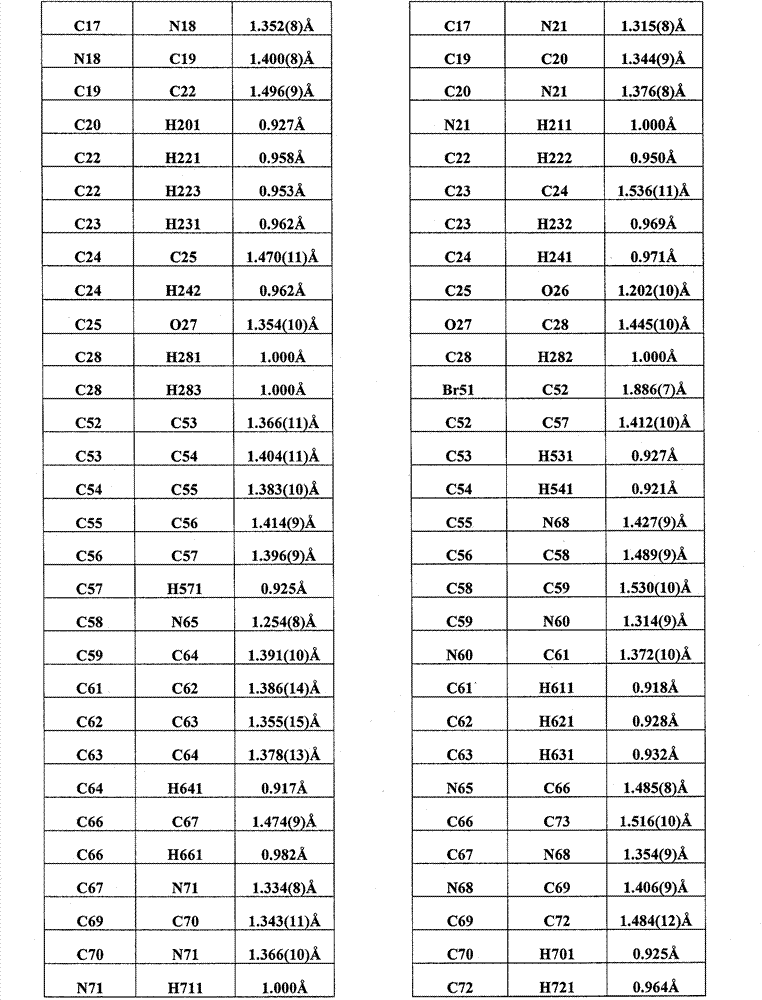
表21.通式(I)的化合物苯磺酸盐型的键长。