WO1999018201A1 - Gankyrin - Google Patents
Gankyrin Download PDFInfo
- Publication number
- WO1999018201A1 WO1999018201A1 PCT/JP1998/004467 JP9804467W WO9918201A1 WO 1999018201 A1 WO1999018201 A1 WO 1999018201A1 JP 9804467 W JP9804467 W JP 9804467W WO 9918201 A1 WO9918201 A1 WO 9918201A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- gankyrin
- polypeptide
- amino acid
- seq
- acid sequence
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/30—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants from tumour cells
- C07K16/303—Liver or Pancreas
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/34—Identification of a linear epitope shorter than 20 amino acid residues or of a conformational epitope defined by amino acid residues
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
Definitions
- the present invention relates to a novel protein gankyrin, its production and its use.
- Hepatocellular carcinoma is one of the most commonly found cancers in the East and South Africa. Significant progress has been made in the diagnosis and treatment of HCC patients over the past 10 years, resulting in an increase in the number of cases that can be resected (Arii, S. et al., Primary liver cancer in Japan, Spain). -Ver 1 ag (1992) 243-255; The liver cancer Study Group of Japan, Primary liver cancer in Japan, Springer-Verlag (1992) 445-453). However, despite its significant progress, survival rates remain low. One of the major obstacles to prolonging survival is recruitment of intrahepatic recurrence after macroscopically eliminating tumor tumors (The Liver Cancer Study Group of Japan, Ann. Surg. (1990) 211, 277-287; Belghi ti, J. et al., Ann. Surg. (1991) 214, 114-117).
- a novel molecular tool for HCC that adds predictive value to traditional clinical prognostic factors such as portal vein involvement, ⁇ -photoprotein (AFP) levels, tumor size, and number of tumors
- AFP ⁇ -photoprotein
- the liver Cancer Study Group of Japan Primary liver Cancer in Japan, Springer-Ver 1 ag (1992) 445-453; The liver Cancer Study Group of Japan, Ann. Surg. (1990 211, 277-287; The liver Cancer Study Group of Japan, Cancer (1994) 74, 2772-2780; Franco, D. et al., Gastroenterology (1990) 98.733-738; Cal vet, X. et al., Hepatology (1990) 12, 753-760). Disclosure of the invention
- the present invention provides a novel gankyrin polypeptide, a gene system encoding the same, a method for producing the polypeptide, an antibody against the polypeptide, and uses thereof.
- the present invention provides an amino acid sequence up to the A1a position at position 14 shown in SEQ ID NO: 2, G1y at position 222, and the like;
- the present invention provides a polypeptide having a biological activity of:
- the present invention also relates to the deletion, addition and deletion of one or more amino acids in the amino acid sequence from A1a at position 14 to G1y at position 2226 shown in SEQ ID NO: 2.
- a polypeptide comprising an amino acid sequence modified by substitution with amino or other amino acids and maintaining the biological activity of gankyrin.
- the present invention also provides a polypeptide having the biological activity of gankyrin, which comprises the amino acid sequence from Met at position 1 to G1y at position 226 shown in SEQ ID NO: 2. provide.
- the present invention also relates to a deletion, addition and / or deletion of one or more amino acids in the amino acid sequence from Met at position 1 to G1y at position 2226 shown in SEQ ID NO: 2.
- a polypeptide consisting of an amino acid sequence modified by substitution with another amino acid and maintaining the biological activity of gankyrin.
- the present invention also relates to a gankyrin organism, which is coded by a DNA having the nucleotide sequence of SEQ ID NO: 1 and a DNA that can hybridize under stringent conditions.
- a gankyrin organism which is coded by a DNA having the nucleotide sequence of SEQ ID NO: 1 and a DNA that can hybridize under stringent conditions.
- the stringent condition is, for example, a condition given by 65 ° C., 0.1 ⁇ SSC and 0.1% SSD.
- the present invention also comprises an amino acid sequence up to A1a at position 14 shown in SEQ ID NO: 2, amino acid sequence up to G1y at position 2226, and has the biological activity of gankyrin.
- DNA encoding the polypeptide, one or more amino acids in the amino acid sequence up to A1a at position 14 and G1y at position 26 shown in SEQ ID NO: 2 A polypeptide consisting of an amino acid sequence modified by deletion, addition and substitution of Z or another amino acid with the amino acid and maintaining the biological activity of gankyrin
- DNA having the nucleotide sequence shown in SEQ ID NO: 1 and a stringent DNA Provides a signal-added polypeptide that is coded by DNA that can be hybridized under conditions and has a signal sequence added to a polypeptide that has the biological properties of gankyrin.
- the stringent conditions are, for example, the conditions given by 65 ° C., 0.1 XSSC and 0.1% SDS.
- the present invention also relates to a polibe comprising the amino acid sequence from A1a at position 14 to Met at position 231, as shown in SEQ ID NO: 4, and having the biological activity of gankyrin. Provide the peptide.
- the present invention also relates to the deletion, addition and / or deletion of one or more amino acids in the amino acid sequence from A1a at position 14 to Met at position 231, as shown in SEQ ID NO: 4.
- the present invention provides a polybeptide comprising an amino acid sequence modified by substitution with another amino acid, and maintaining the biological activity of gankyrin.
- the present invention also relates to a polypeptide having the biological activity of gankyrin, which comprises the amino acid sequence up to the Met position at position 1 shown in SEQ ID NO: 4 and the Met at position 231, and the like. I will provide a.
- the present invention also relates to deletion, addition and Z or other deletion of one or more amino acids in the amino acid sequence from Met at position 1 to Met at position 231 shown in SEQ ID NO: 4.
- the present invention provides a polybeptide comprising an amino acid sequence modified by substitution with an amino acid, and maintaining the biological activity of gankyrin.
- the present invention also relates to a DNA having the nucleotide sequence of SEQ ID NO: 3, which is coded by DXA capable of hybridizing under stringent conditions.
- the stringent condition is, for example, a condition given by 65 ° C., 0.1 XSSC and 0.1% SDS.
- W / 101 The present invention also comprises an amino acid sequence from A1a at position 14 to Met at position 231, as shown in SEQ ID NO: 4, and has the biological activity of gankyrin.
- Polypeptides which consist of an amino acid sequence modified by acid deletion, addition and / or substitution by another amino acid and which maintain the biological activity of gankyrin. It is coded by a coding DNA or a DNA having the base sequence shown in SEQ ID NO: 3 and a DNA capable of hybridizing under stringent conditions, and Signal-added polypeptide with a signal sequence added to a polypeptide having the biological properties of provide .
- the stringent conditions are, for example, the conditions given by 65 ° C., 0.1 XSSC and 0.1% SDS.
- the present invention also relates to a polypeptide comprising an amino acid sequence from A1a at position 14 to Met at position 231, as shown in SEQ ID NO: 6, and having a biological activity of gankyrin. Provide the peptide.
- the present invention also relates to the deletion, addition, and deletion of one or more amino acids in the amino acid sequence from A1a at position 14 to Met at position 231, as shown in SEQ ID NO: 6.
- the present invention provides a polypeptide comprising an amino acid sequence modified by substitution with another amino acid and maintaining the biological activity of gankyrin.
- the present invention also provides a polypeptide comprising an amino acid sequence from Met at position 1 to Met at position 231 shown in SEQ ID NO: 6, and having a biological activity of gankyrin. I do.
- the present invention also relates to the deletion, addition and Z or other deletion of one or more amino acids in the amino acid sequence from Met at position 1 to Met at position 231 shown in SEQ ID NO: 6.
- Amino Acids Modified by Substitution with Amino Acids The present invention provides a polypeptide which is composed of an acid sequence and maintains the biological activity of gankyrin.
- the present invention is also coded by a DNA having the nucleotide sequence of SEQ ID NO: 5 and a DNA capable of hybridizing under stringent conditions, and further comprising a gankyrin biology.
- the stringent condition is, for example, a condition given by 65 ° C., 0.1 X SSC and 0.1% SDS.
- the present invention also provides a polypeptide comprising the amino acid sequence from A1a at position 14 to Met at position 231 as shown in SEQ ID NO: 6, and having the biological activity of gankyrin.
- Deletion of one or more amino acids in the amino acid sequence up to the A1 at position 14 shown in SEQ ID NO: 6, the amino acid sequence up to Met at position 231 shown in SEQ ID NO: 6 Encodes a polypeptide that consists of an amino acid sequence modified by addition and substitution by Z or another amino acid, and that retains the biological activity of gankyrin It is coded by DNA or a DNA having the base sequence of SEQ ID NO: 5 and a DNA that can hybridize under stringent conditions, and is a gankyrin organism.
- the present invention also provides a fusion polypeptide comprising the above-mentioned polypeptide and another peptide or polypeptide.
- the present invention also provides a DNA encoding the above polypeptide.
- the present invention also provides the c-present invention provides a base pin definition one comprising DNA also provides a host transformed by the above vectors I do.
- the present invention also relates to the aforementioned method for producing a polypeptide, comprising culturing a host transformed with an expression vector comprising DNA encoding the polypeptide, and culturing the host.
- a method for producing a polypeptide comprising culturing a host transformed with an expression vector comprising DNA encoding the polypeptide, and culturing the host.
- a target polypeptide is collected from an object.
- the present invention also provides an antibody that specifically reacts with the above-mentioned polypeptide.
- This antibody is preferably a monoclonal or polyclonal antibody.
- the present invention also comprises contacting the above antibody with a sample expected to contain gankyrin polypeptide, and detecting the formation of an immune complex between the antibody and gankyrin polypeptide. Or a method for detecting or measuring a gankyrin polypeptide comprising measuring.
- the present invention also provides an antisense oligonucleotide which hybridizes to any part of the nucleotide sequence shown in SEQ ID NO: 1.
- the present invention also provides antisense oligonucleotides to at least 20 consecutive nucleotides in the nucleotide sequence of SEQ ID NO: 1.
- the antisense oligonucleotides for at least 20 or more consecutive nucleotides preferably include a translation initiation codon.
- the present invention also provides a gankyrin polypeptide expression inhibitor comprising the antisense oligonucleotide as an active ingredient.
- the present invention also provides a method of screening gankyrin polypeptides for binding to gankyrin polypeptides and Rb, the method for screening gankyrin polypeptides or antagonists in the presence of Rb.
- Polypeptide or gankyrin polypeptide content and gankyrin polypeptide A method for contacting a sample suspected of containing gonist or antagonist, and detecting free gankyrin polypeptide or Rb.
- the gankyrin-containing substance is, for example, a lysate of cells expressing gankyrin.
- the present invention also provides a method for screening a ganky lipopeptide agonist or an antagonist for binding of ganky lipopeptide to NFB in the presence of NFB.
- the gankyrin polypeptide or a substance containing gankyrin polypeptide is brought into contact with a sample expected to contain an agonist or antagonist of gankyrin polypeptide, and the free gankyrin polypeptide is contacted.
- a method for detecting a peptide or NF ⁇ B is, for example, a lysate of cells expressing gankyrin.
- Figure 1 is a schematic diagram showing the location of the gankyrin gene on the human X chromosome.
- FIG. 2 is a photograph showing that a gankyrin gene on a chromosome in a human lymphocyte was detected by fluorescent staining using an in situ hybridization method.
- Figure 3 shows the results of Northern RNA detection of mRNA from normal liver tissue (N) and liver cancer tissue (T) of five liver cancer patients (1 to 5) using human gankyrin cDNA as a probe. It is an electrophoretogram.
- FIG. 4 is an electrophoretogram showing the results of detection of mRNAs of various human cell lines by the Northern method using human gankyrin cDNA as a probe.
- Figure 5 is an electrophoretogram showing the results of Northern mRNA detection of mRNA in various normal tissues using human gankyrin cDNA as a probe. is there.
- FIG. 6 shows the results obtained by analyzing gankyrin polypeptide in cell lysates from normal liver tissue (N) and liver cancer tissue (T) of three liver cancer patients (1 to 3) using an anti-gankyrin polypeptide antibody.
- FIG. 4 is an electrophoretogram showing the results of detection by the Western blot method.
- Figure 7 shows the results of Western blot detection of gankyrin polypeptides in cell lysates from various human cell lines using anti-gankyrin polypeptide antibodies. It is an electrophoretogram.
- FIG. 8 shows the results of detection of the in vitro translated gankyrin gene product in the same manner as in Fig. 6, and B shows the in vitro translated gankyrin gene product (unlabeled). 7) is an electrophoretogram showing the results of detecting the same as in FIG.
- FIG. 9 is an electrophoretic diagram showing the results obtained by expressing a fusion polypeptide of gankyrin polypeptide and GST in Escherichia coli and detecting it with various antibodies.
- FIG. I0 is an electrophoretogram showing the results of expression of fusion polypeptides of gankyrin polypeptide and HA in 2993 cells and detection with various antibodies.
- FIG. 11 is an electrophoretogram showing the results of expression of fusion polypeptides of gankyrin polypeptide and HA in 2993 cells, and detection with various antibodies.
- FIG. 12 is an electrophoretogram showing the results of detecting mRXA in various cell cycles of NIH / 3T3 cells by the Northern method using mouse gankyrin cDNA as a probe.
- FIG. 13 is an electrophoretogram showing the results of detecting mRNA of NIHZ 3 T3 cells grown at various concentrations in the same manner as in FIG. Figure 14 shows the liver regeneration process after partial hepatectomy in the mouse.
- FIG. 13 is an electrophoretogram showing the results of detecting mRNA in liver tissue in the same manner as in FIG. 12.
- FIG. 15 shows the positions of ankyrin repeats in various proteins and the number of repeats.
- gankyrin polypeptide refers to a polybeptide having the biological activity of gankyrin.
- the biological activity of gankyrin is carcinogenic, and its specific action is shown in Example 4, which increases the ability of cells to form colonies in soft agar, tumorigenicity in mice and apoptosis. It is suppression of induction.
- the gankyrin gene or its cDNA of the present invention can be screened using hepatoma cells or hepatoma tissue as a source to obtain the gene or its cDNA.
- Methods for screening or isolating the gene or its cDNA include the subtraction method (Nucleic Acids Research (1988) 16, 10937), differential hybridization, and the like. Methods such as the one-shot method (Cell (1979) 16, 443-452) that can selectively screen genes whose expression level changes can be used.
- the gene encoding the gankyrin polypeptide of the present invention may be, for example, a subtraction between a cDNA library prepared from normal liver tissue and a cDNA library prepared from liver cancer tissue. Ri by the ® emission method, is obtained by the this has been transferred to select the c DNA derived from m R lambda tau Alpha that is not transcribed in normal tissues in the liver cancer tissue.
- the subtraction method uses primers to amplify cDNA obtained from liver cancer tissue or normal liver tissue.
- a primer for amplifying normal liver tissue is labeled with a labeling compound, for example, biotin.
- a labeling compound for example, biotin.
- an excess amount of double-stranded cDNA from normal liver tissue and a small amount of liver cancer tissue is mixed with the resulting double-stranded cDNA and heat-denatured to form a single strand, which is then returned to double strand.
- cDNAs derived from liver cancer tissues those that are also expressed in normal liver tissues are almost double-stranded with excess cDNAs derived from normal liver tissues, and become labeled.
- cDNAs derived from liver cancer tissues form a double strand, they have no label.
- removal of the labeled double-stranded DNA can yield cDNA specific to liver cancer tissue.
- cDNA specific to liver cancer tissue can be concentrated. This specific method is described in Example 1. Using the obtained cDNA fragment or full-length cDNA as a probe, cells or tissues expressing gankyrin polypeptide and cells not expressing gankyrin polypeptide or By performing northern blotting on tissue mRNA, it can be confirmed that the mRNA of the selected gene is specifically expressed.
- the gankyrin gene can be obtained from different cells, tissues, organs or species by screening the cDNA library obtained using the cDNA or cDNA fragment obtained as described above as a probe. it can. Furthermore, by determining the nucleotide sequence of the obtained cDNA, the translation region encoding the polypeptide of the gankyrin gene product can be determined, and the amino acid sequence of this polypeptide is determined. Can be obtained. In addition, chromosomal DNA can be isolated by screening the genomic DNA library using the obtained cDNA as a probe.
- DNA libraries such as the cDNA Library and the Genomic DNA Library are described in, for example, Sambrook, J. et al., olecular C1 on ing Co Id Spring Harbor Laboratory Press (1989). Alternatively, a commercially available DNA library may be used.
- the gene or DNA of the present invention can be obtained by using the PCR method as a primer when the nucleotide sequence or a part thereof is clear.
- the gankyrin polypeptide of the present invention is also encoded by a DNA that hybridizes under stringent conditions with a nucleic acid having a base sequence represented by SEQ ID NO: 1, and comprises a gankyrin polypeptide. Includes biologically active polypeptides.
- a low stringent condition As a stringent condition, a low stringent condition can be mentioned. Low stringent conditions are, for example, 50 ° C., 2 ⁇ SSC, 0.1% SDS. More preferably, high stringent conditions are included. High stringent conditions include, for example, 65 ° C, 0.1 X SSC and 0.1% SSD.
- the hybridizing DNA described above may preferably be a naturally occurring DNA, for example, cDNA or dizinomic DNA.
- cDNA or dizinomic DNA For the amino acid sequence shown in SEQ ID NO: 2 and the nucleotide sequence shown in SEQ ID NO: 1, all sequences contained in the known DNA database (GenBank, EMBL) and the protein database (SWISS-PLOT) As a result of a homology search for, no match was found. This has revealed that the gene of the present invention and its gene product, polypeptide, are novel molecules.
- the gene that hybridizes to the cDNA of the novel gankyrin polypeptide of the present invention is also used in animals other than humans such as rats and mice in the present invention. It was found to be widely distributed and also in various tissues of humans. Therefore, the above-mentioned naturally-occurring DNA is, for example, cDNA derived from a tissue in which mRNA that hybridizes with the cDNA of the human gankyrin polypeptide is detected in Example 1, or dinoomic. It may be DNA.
- the present invention also encompasses a DNA that hybridizes with a nucleic acid having the nucleotide sequence of SEQ ID NO: 2 as described above and encodes a polypeptide having gankyrin activity.
- This DNA can also be expressed by the method described above.
- a synthetic oligonucleotide primer can be used to introduce a desired mutation into the nucleotide sequence of the gankyrin gene (Mark, Natl.Acad.Sci. USA (1984) 81, 5662-5666, Zoller, MJ & Smith, M. Nucleic Acids Research (1982) 10, 6487-6500, Wang, A. et al. , Science 224, 1431-1433, Dalbadie-McFarland, G. et al., Proc. Nat 1. Acad. Sci. USA (1982) 79, 6409-6413).
- synthetic DNA may also be used.
- a DNA encoding gankyrin having an amino acid sequence represented by SEQ ID NO: 2 is exemplified.
- a DNA having a base sequence represented by SEQ ID NO: 1 is used.
- These DNAs can also be produced using a genetic technique known per se.
- Escherichia coli carrying the plasmid pBS-t4-U obtained in Example 1 described below was named Escherichia coli DH5a (pBS-t4-11), and was named in 1997. It was deposited with the Institute of Biotechnology and Industrial Technology, Institute of Industrial Science and Technology (Tsukuba-Higashi 1-3-1-3, Ibaraki Prefecture) on February 29 under the deposit number FERM BP-612.
- the gankyrin polypeptide of the present invention includes, for example, a ganky lip having the same or substantially the same amino acid sequence as the amino acid sequence represented by SEQ ID NO: 2. And polypeptides. Specifically, in addition to gankyrin having the amino acid sequence represented by SEQ ID NO: 2, one or more of the amino acid sequences represented by SEQ ID NO: 2 are preferably used. Is a deletion of 2 to 30 amino acids, more preferably 2 to 10 amino acids, and 1 or 2 in the amino acid sequence represented by SEQ ID NO: 2.
- the present invention also includes a polypeptide having a biological activity of gankyrin and having homology to a polypeptide having an amino acid sequence represented by SEQ ID NO: 2.
- a homologous polypeptide is an amino acid sequence of SEQ ID NO: 2 which generally comprises at least 20 and preferably 30 contiguous amino acid residues. At least 70%, preferably at least 80%, more preferably at least 90%, more preferably at least 95%, homology on amino acid sequences Means a polypeptide having The gankyrin polypeptide of the present invention differs in the amino acid sequence, molecular weight, isoelectric point, presence or absence and form of a sugar chain depending on the cell host or the purification method for producing the gankyrin polypeptide described below.
- the present invention is included in the present invention as long as the obtained gankyrin polypeptide has substantially the same activity as natural gankyrin polypeptide.
- Activities substantially equivalent to gankyrin polypeptide include the carcinogenicity described in Example 4 below, such as increased colony forming ability of cells in soft agar, and tumorigenicity in mice. And suppression of apoptosis induction.
- the term “substantially the same quality” means that the carcinogenicity and the like are of the same quality in nature.
- the partial peptides of the gankyrin polypeptide of the present invention include, for example, molecules of gankyrin molecules.
- Partial peptides containing one or more of the hydrophobic region and the hydrophilic region estimated from the hydrophobic plot analysis C may include part or all of one hydrophobic region, or may include part or all of one hydrophilic region.
- the partial peptide of the gankyrin polypeptide of the present invention is produced according to a peptide synthesis method known per se, or by cleaving the gankyrin polypeptide of the present invention with an appropriate peptide. be able to.
- a peptide synthesis method for example, any of a solid phase synthesis method and a liquid phase synthesis method may be used.
- the partial peptide of the present invention can be isolated and purified by a combination of ordinary purification methods such as solvent extraction, distillation, column chromatography, high-performance liquid chromatography, and recrystallization. Can be.
- the DNA constructed as described above can be expressed by a known method to obtain gankyrin polypeptides.
- useful promoters commonly used such as Z enhancers, expressed genes, and DNA containing a functionally linked poly A signal downstream of the 3 'end or vectors containing the same. It can be expressed more.
- the promoter Z enhancer can be mentioned as a human cytomegalovirus immediate ear promoter / enhancer.
- lettuce virus, polymouse virus, adenovirus, and stains can be used as promoters and promoters that can be used for gankyrin polypeptide expression. Promoters such as amphibious 40 (SV40), etc. Promoters from mammalian cells derived from mammalian cells such as promoters of Z-enhancers, hysterogens, etc. 1a (HEF1) You just need to use
- promoters include the lacZ promoter and the araB promoter.
- lacZ promoter the method of Ward et al. (Nature (1098) 341, 544-546; FASEB J. (1992) 6, 2422-2427), and when using the araB promoter, the method of Better et al. (Science (1988) 240, 1041-1043).
- the signal sequence for gankyrin polypeptide secretion is the pelB signal sequence (Lei, SP, et al J. Bacteriol. (1987) 169, 4379) when produced by E. coli periplasm.
- pelB signal sequence As a replication origin, those derived from SV40, Poliovirus, Adenovirus, Dipapipillomavirus (BPV) and the like can be used.
- the expression vector is used as a selectable marker to amplify the number of gene copies in the host cell system, such as the aminoglycoside transferase (APH) gene and thymidine kinase.
- TK Escherichia coli xanthinguanine phosphoribosyltransferase
- dhfr dihydrofolate reductase
- any production system can be used for the production of gankyrin polypeptide.
- Production systems for the production of gankyrin polypeptides include in vitro and in vivo production systems.
- the in vitro production system include a production system using eukaryotic cells and a production system using prokaryotic cells.
- prokaryotic cells When eukaryotic cells are used, there are production systems using animal cells, plant cells, and fungal cells.
- animal cells include (1) mammalian cells, such as CH0 (J. Exp.
- CH0 cells include dhfr-CHO (Pi'oc. Natl. Acad. Sci. USA (1980) 77, 4216-4220) and CHO K-1 (Pro Natl Acad. Sci. USA (1968) 60, 1275) can be preferably used.
- yeast such as the genus Saccharomyces, for example, Saccharomyces 'Saccharomyces cerevisiae', yarn
- the genus Aspergillus such as Aspergillus niger, has been vigorously used.
- E. coli Escherichia coli
- Bacillus subtilis Bacillus subtilis
- gankyrin polypeptides are transformed with the DNA of interest, and the transformed cells are cultured in invitro to obtain gankyrin polypeptides.
- Culture is performed according to a known method.
- DMEM, MEM, RPMI 1640, 1MDM can be used as a culture solution.
- a serum replacement solution such as fetal calf serum (FCS) may be used in combination, or serum-free culture may be performed.
- FCS fetal calf serum
- the pH during the culturing is preferably about 6-8. Culture is usually performed at about 30 to 40 ° C for about 15 to 200 hours, and the medium is replaced, aerated, and agitated as necessary.
- in vivo production systems include production systems using animals and plants. Production systems using The target DNA is introduced into these animals or plants, and gankyrin polypeptide is produced in the animals or plants and collected.
- the “host” in the present invention includes these animals and plants.
- mice When using animals, there are production systems using mammals and insects. Goats, pigs, sheep, mice, and mice can be used as mammals (Vicki Glaser, SPECTRUM Biotechnology Applications, 1993). When a mammal is used, a transgenic animal can be used.
- a DNA of interest is inserted into a gene encoding a protein produced in milk, such as goat 3-casein, to prepare a fusion gene.
- the DNA fragment containing the fusion gene with the inserted DNA is injected into a goat embryo, and the embryo is introduced into a female goat.
- Gankyrin polypeptide is obtained from milk produced by a transgenic jujugian goat born from a goat that has received an embryo or its offspring.
- hormones may be used in the transgenics to increase the amount of milk containing gankyrin polypeptides produced from the transgenics. (Ebert, K.M. et al., Bio / Technology (1994) 12, 699-702) o
- silkworms can be used as insects, for example.
- baculovirus containing the DNA of interest is infected to the silkworm, and a desired gankyrin polypeptide is obtained from the body fluid of the silkworm (Susumu, M. et al. , ature (1985) 315, 592-594
- tobacco when using plants, for example, tobacco can be used.
- the target DNA is introduced into a plant expression vector, for example, pMON530, and the vector is transferred to Agrobacterium tumefaci l 8 Introduce to technology such as ens.
- This bacterium is infected with tobacco, for example, Nicotiana tabacum, to obtain the desired polypeptide from the leaves of this tobacco (Julian, K.-a et al., Eur. J. Immunol. (1994) 24 , 131-138).
- known methods for example, a calcium phosphate method (Virology (1973) 52, 456-467) and an electrophoresis method ( EMBO J.
- gankyrin gene product thus obtained has the biological activity of gankyrin can be confirmed, for example, as follows.
- ganky lipopeptide-producing cells are cultured in soft agar using the method described in Example 4 below.
- Gankyrin polypeptide-expressing cells have an increased ability to form colonies in soft agar.
- cells expressing gankyrin polypeptide are transplanted into mice.
- Gankyrin polypeptide-expressing cells exhibit tumorigenicity in the mouse.
- the cells expressing gankyrin polypeptide are subjected to apoptosis-inducing conditions.
- Gankyrin polypeptide-expressing cells suppress apoptosis induction.
- the gankyrin polypeptide obtained above can be isolated from the inside or outside of a cell or from a host and purified as a substantially pure and homogeneous polypeptide. Separation and purification of gankyrin polypeptide can be performed by the separation and purification methods used in ordinary protein purification, and is not limited at all. For example, chromatographic columns, finolase, ultrafiltration, salting out, solvent precipitation, immunoprecipitation, SDS-polyacrylamide gel electrophoresis, isoelectric focusing, dialysis, etc. Select as appropriate, Chromatography that can separate and purify Gankyrin polypeptides when combined is, for example, affinity chromatography, ion chromatography.
- chromatographs are liquid-phase chromatographs. It can be carried out using a liquid phase chromatography such as HP, C and FPLC.
- the gankyrin polypeptide can be arbitrarily modified or partially removed by the action of an appropriate protein-modifying enzyme before or after purification of the gankyrin polypeptide. it can.
- the protein-modifying enzyme include trypsin, chymotoribcin, lysylendopeptidase, protein kinase, glucosidase, protein kinase, and glucosidase.
- the ganky lipopeptide of the present invention is useful for being used in a screening method. That is, in the presence of Rb (DeCaprio, JA et al., Cell (1989) 58, 1085-1095), a gankyrin polypeptide or a gankyrinpolypeptide-containing substance and a gankyrin Contacting a sample that is expected to contain the agonite or antagonite of the polypeptide and detecting or measuring free gankyrin polypeptide or Rb.
- a method for screening the gankyrin polypeptide agonist or gankyrin antagonist; or NF / B (Baeuerle, PA et al., Cell (1988) 53, 21).
- the gankyrin polypeptide used in these screening methods can be used either in a recombinant form or in a natural form.
- a partial peptide of gankyrin polypeptide may be used as long as the binding to Rb or NFcB is maintained.
- the gankyrin polypeptide-containing substance includes a lysate of cells expressing gankyrin polypeptide.
- the present invention is expected to include gankyrin polypeptide or gankyrin polypeptide-containing substance and agonist or antagonist of gankyrin polypeptide in the presence of Rb.
- the sample is brought into contact with the sample, the sample containing gankyrin polypeptide or gankyrin polypeptide and the sample containing no gankyrin polypeptide agonist or antagonist are brought into contact with each other.
- Screening of an agonite or antagonist of a gankyrin polypeptide comprising comparing the detected or measured free gankyrin polypeptide or Rb Involved in the method.
- the present invention is also expected to include ganky lipopeptide or ganky lipopeptide content and agonist or antagonist of ganky lipopeptide in the presence of NFB.
- a gankyrin polypeptide agonist or antagonist screen consisting of comparing the detected or measured free gankyrin polypeptide or NF ⁇ B Related to the ng method.
- gankyrin polypeptide, Rb or NF / B for example, gankyrin polypeptide, Rb or NFcB is used.
- labeled compound for example bi Ochin, Abidin emissions, radioisotopes, for example [1 2 5 I], [3 5 S], [3 H], [1 4 C], fluorescent substances, enzymes, for example Western Wasabiperu Okishidaze, alk Labeling can be carried out using rephosphatase, which can be detected or measured.
- labeling compounds are already known and can be labeled according to a usual method.
- an antibody against gankyrin polypeptide, Rb or NFB can be used.
- gankyrin polypeptide is fixed to a support, for example, a bead or a plate, and gankyrin polypeptide agonist or antagonis in the presence of Rb or NF / cB. Then, after adding a sample expected to contain Rb, and incubating, Rb or NF / B contained in the solution may be detected or measured with an antibody. In order to detect or measure free Rb or NFB, Rb or NF ⁇ B bound to gankyrin polypeptide immobilized on a plate may be detected or measured.
- a fusion polypeptide in which a ganky polypeptide is fused with another peptide or polypeptide by genetic engineering can be used.
- HA as another peptide or polypeptide attached to the fusion
- gankyrin polypeptide can be detected or measured using antibodies against other peptides or polypeptides attached to these fusions. Can be. Therefore, a fusion polypeptide in which gankyrin polypeptide is fused to another peptide or polypeptide by genetic engineering is useful in the present invention. It is.
- Examples of a sample that is expected to contain agonite or antagonist of gankyrin polypeptide used in the screening method of the present invention include, but are not limited to, peptides, proteins, and non-peptides.
- the screening method of the present invention is useful because an agonist or antagonist of a gankyrin polypeptide having carcinogenicity can be detected or measured.
- Gankyrin polypeptides were found to interact with Rb or NF / cB in the present invention. Because gankyrin polypeptide has carcinogenicity, agonist or antagonist of gankyrin polypeptide that regulates the binding of gankyrin polypeptide to Rb or NFB is a pharmaceutical. Useful as
- the ganky lipopeptide or the ganky lipopeptide-containing substance of the present invention is converted into a buffer solution suitable for screening.
- the buffer may be any buffer as long as it does not inhibit the binding of gankyrin polypeptide, such as a phosphate buffer of pH 6 to 8, a buffer of Tris-HCl, PBS, or HBSS. Used. Further, for the purpose of reducing non-specific binding, a surfactant such as a protein of bovine serum albumin, CHAPS, Tween 80 TM, digitonin and the like can be added. In addition, a proteolytic enzyme inhibitor such as PMSF, pepstatin, or loupeptin can be added to suppress the decomposition of gankyrin polypeptide by the proteolytic enzyme.
- a surfactant such as a protein of bovine serum albumin, CHAPS, Tween 80 TM, digitonin and the like can be added.
- a proteolytic enzyme inhibitor such as PMSF, pepstatin, or loupeptin can be added to suppress the decomposition of gankyrin polypeptide by the proteolytic enzyme.
- Rb or NF / cB labeled with a radioisotope and a sample having an appropriate concentration are simultaneously added to the gankyrin polypeptide preparation, and the mixture is added at about 0 to 50 ° C (preferably, (Approximately 4 to 37 ° C), approximately 0.5 to 24 hours
- the radiation dose remaining in the gankyrin polypeptide preparation is measured using a gamma counter or a liquid scintillation counter.
- a gamma counter or a liquid scintillation counter is used as a negative control.
- the value obtained by subtracting the non-specific binding amount from the residual radiation dose when the sample is included is the specific binding amount.
- a sample that reduces the amount of specific binding can be selected as a candidate substance of gankyrin polypeptide agonist or antagonist.
- the ganky lipopeptide agonist or antagonist obtained by using the screening method of the present invention can be used as a sample, for example, a peptide or protein, by using the screening method.
- a sample for example, a peptide or protein
- gankyrin polypeptide agonists or antagonists are substances that inhibit the binding of gankyrin polypeptide to Rb or NF / cB.
- gankyrin polypeptide agonists or antagonists are substances that inhibit the binding of gankyrin polypeptide to Rb or NF / cB.
- a substance which is converted by addition, deletion or substitution is also included in the ganky lipopeptide agonist or the antagonist obtained by using the screening method of the present invention.
- An agonist or antagonist of ganky lipopeptide obtained by using the screening method of the present invention is a human mammal, such as "mouse, rat, guinea pig, egret, ni ⁇ When used as a medicament for birds, cats, dogs, sheep, pigs, horses, monkeys, baboons, and chimpanzees, it can be carried out in a conventional manner.
- aseptic with orally coated tablets, capsules, elixirs and microcapsules, or with water or other pharmaceutically acceptable liquids can be used parenterally in the form of injectable solutions or suspensions.
- a gankyrin polypeptide agonist or antagonist is generally recognized as a physiologically acceptable substance, flavoring agent, excipient, vehicle, preservative, stabilizer, and binder. It can be manufactured by mixing in the unit dosage form required for the given pharmaceutical practice. The amount of the active ingredient in these preparations is such that an appropriate dose in the specified range can be obtained.
- excipients examples include binders such as' gelatin, corn starch, tragacanth gum, gum arabic, and excipients such as crystalline cellulose.
- Swelling agents such as corn starch, gelatin, alginic acid, lubricants such as magnesium stearate, sweeteners such as sucrose, lactose or saccharin, and peppermint.
- a flavoring agent such as coconut oil or tea is used.
- the preparation unit form is a capsule, the above-mentioned materials can further contain a liquid simple substance such as oil and fat.
- Sterile compositions for injection are formulated normally by dissolving or suspending the active substance in a vehicle, such as distilled water for injection, or naturally occurring vegetable oils such as sesame oil or coconut oil. It can be prescribed according to
- Aqueous solutions for injection include, for example, saline, isotonic solutions containing glucose and other adjuvants, such as D-sorbitol, D-mannose, D-mannitol, Sodium chloride; suitable solubilizers, such as alcohols, specifically ethanol, polyalcohols, such as propylene glycol, polyethylene glycol, nonionic surfactants, such as Polysorbate 80 (TM) and HC 0-50 may be used in combination.
- saline isotonic solutions containing glucose and other adjuvants, such as D-sorbitol, D-mannose, D-mannitol, Sodium chloride
- suitable solubilizers such as alcohols, specifically ethanol, polyalcohols, such as propylene glycol, polyethylene glycol, nonionic surfactants, such as Polysorbate 80 (TM) and HC 0-50 may be used in combination.
- oily liquid examples include sesame oil and soybean oil, and may be used in combination with benzyl benzoate or benzyl alcohol as a solubilizing agent.
- buffering agents such as phosphate buffer, sodium acetate buffer, soothing agents such as benzalkonium chloride, procaine hydrochloride, stabilizers such as benzyl alcohol, phenol And antioxidants.
- the prepared injection solution is usually filled into an appropriate sample.
- the dosage of gankyrin polypeptide agonist or antagonist varies depending on the symptoms, but in the case of oral administration, in general, for adults (with a body weight of 60 kg), It is about 0.1 mg / day, 100 mg / day, preferably about 1.0 kg / day, 50 mg / day, more preferably about 1.0 kg / day.
- the single dose When administered parenterally, the single dose varies depending on the subject, target organs, symptoms, and administration method. For example, in the case of parenteral injection, it is usually used in adults (with a body weight of 60 kg). Is about 0.01 to 30 mg, preferably about 0.1 to 20 mg, more preferably about 0.1 to 10 mg per day by intravenous injection It is convenient to do so. In the case of other animals, the dose can be administered in terms of the weight per 60 kg.
- the anti-gankyrin polypeptide antibody of the present invention can be prepared by known means. It can be obtained as a monoclonal antibody or a polyclonal antibody.
- Monoclonal antibodies are obtained by using gankyrin polypeptide as a sensitizing antigen, immunizing the immunized cells according to a usual immunization method, and immunizing the obtained immune cells by a conventional cell fusion method using a known parental cell fusion method. It can be prepared by screening monoclonal antibody-producing cells by a conventional screening method.
- a monoclonal antibody or a polyclonal antibody may be prepared as follows.
- gankyrin polypeptide used as a sensitizing antigen for obtaining antibodies is not limited to the animal species from which it is derived, but may be derived from mammals, for example, human, mouse, or rat. Polypeptides are preferred. These human, mouse, or rat gankyrin polypeptides can be obtained using the gene sequences disclosed herein.
- gankyrin polypeptides used as sensitizing antigens include gankyrin polypeptides having all the biological activities of gankyrin polypeptide described in this specification. Polypeptides can be used. Also, fragments of gankyrin polypeptide can be used. Examples of gankyrin polypeptide fragments include carboxy (C) terminal fragments of gankyrin polypeptide.
- anti-gankyrin polypeptide antibody means an antibody that specifically reacts with a full-length or fragment of gankyrin polypeptide.
- a gene encoding gankyrin polypeptide or a fragment thereof is inserted into a known expression vector system to transform the host cell described herein, and then into or out of the host cell or from the host.
- the desired gankyrin polypeptide or a fragment thereof may be obtained by a known method, and this gankyrin polypeptide may be used as a sensitizing antigen.
- Gunki Rinpo Rebuchi The cells expressing the host or a lysate thereof may be used as the sensitizing antigen.
- the mammal immunized with the sensitizing antigen is not particularly limited, but may be used for cell fusion. The selection is preferably made in consideration of the compatibility with the parent cell. Generally, rodents, ephedra, and primates are used.
- Egrets are used as egrets.
- monkeys are used as primates.
- monkeys with lower nasal nose old world monkeys
- cynomolgus monkeys lizard monkeys
- baboons baboons
- chimpanzees are used.
- Immunization of an animal with a sensitizing antigen is performed according to a known method.
- a sensitizing antigen is administered intraperitoneally or in a mammal.
- the sensitizing antigen is diluted to an appropriate amount with PBS (Phosphate-Buffered Saline), physiological saline, or the like, and the suspension is suspended in a normal adjuvant, such as Freon. It is advisable to mix a suitable amount of complete adjuvant, emulsify and administer to mammals, and then administer the sensitizing antigen mixed appropriately in Freund's incomplete adjuvant several times every 4 to 21 days. I like it.
- a suitable carrier can be used at the time of immunization with the sensitizing antigen. Immunization is performed in this manner, and it is confirmed by a conventional method that the level of the desired antibody in serum is increased.
- the blood of a mammal sensitized with the antigen is extracted after confirming that the level of the desired antibody in the serum has increased.
- the serum is separated from the blood by a known method.
- Serum containing the polyclonal antibody may be used as the polyclonal antibody, and if necessary, a fraction containing the polyclonal antibody may be further isolated from this serum. Is also good.
- To obtain a monoclonal antibody it is necessary to confirm that the level of the desired antibody is increased in the serum of a mammal sensitized with the above antigen, and then remove immune cells from the mammal and subject them to cell fusion. Good.
- preferred immune cells used for cell fusion include spleen cells in particular.
- Mammalian myeloma cells as the other parent cells fused with the immune cells are preferred.
- Cell fusion of the immune cells and myeloma cells is basically performed by a known method, for example, the method of Milstein et al. (Gal fre, G. and Milstein, C., Methods Enzymol. (1981) 73, 3). -46) etc.
- the cell fusion is performed, for example, in a normal nutrient culture in the presence of a cell fusion promoter.
- a cell fusion promoter for example, polyethylene glycol (PEG), Sendai virus (HVJ) and the like are used, and if necessary, an auxiliary agent such as dimethyl sulfoxide to increase the fusion efficiency. Can also be used.
- the ratio of the use of the immune cells to the myeloma cells is, for example, preferably 1 to 10 times the number of the immune cells to the myeloma cells.
- the culture medium used for the cell fusion include RPMI 1640 culture medium and MEM culture medium suitable for the growth of the myeloma cell line, and other ordinary cultures used for cell culture of this type.
- a fluid can be used, and a serum replacement fluid such as fetal calf serum (FCS) can also be used in combination.
- FCS fetal calf serum
- a predetermined amount of the immune cell and the myeloma cell are mixed well in the culture medium, and a PEG solution previously heated to about 37 ° C., for example, an average molecular weight of 100
- a PEG solution of up to about 600 is added at a concentration of 30 to 60% (wZv) and mixed to form a target fused cell (hybridoma).
- wZv concentration of 30 to 60%
- the hybridoma is selected by culturing it in an ordinary selective culture solution, for example, an HAT culture solution (a culture solution containing hypoxanthine, aminobuterin and thymidine).
- HAT culture solution a culture solution containing hypoxanthine, aminobuterin and thymidine.
- the culturing in the HAT culture solution is continued for a period of time sufficient for cells other than the target hybridoma (non-fused cells) to die, usually for several days to several weeks.
- ordinary limiting dilution is performed, and screening and cloning of the hybridoma producing the desired antibody are performed.
- a human lymphocyte such as a human EB virus-infected human lymphocyte
- a human lymphocyte is in vitro cultured with a cancer cell.
- the sensitized lymphocyte is fused with a human-derived myeloma cell capable of permanently dividing, for example, U266.
- a human-derived myeloma cell capable of permanently dividing, for example, U266.
- a transgenic animal having a human antibody gene receptor immunization is immunized with a gankyrin polypeptide, a gankyrin polypeptide-expressing cell or a lysate thereof as an antigen.
- a hybridoma fused with myeloma cells To obtain anti-gankyrin polypeptide antibody-producing cells, and to obtain human antibodies against gankyrin polypeptide by using a hybridoma fused with myeloma cells.
- Good International Patent Application Publication No. W092 — 03918, W ⁇ 93-2227, W094-02620.W094 — 255985, WO96-33 735 and W096-34096).
- the hybridomas producing monoclonal antibodies produced in this way can be subcultured in ordinary culture medium, and can be stored for a long period in liquid nitrogen. It is possible.
- a method of culturing the hybridoma according to an ordinary method and obtaining the culture supernatant, or transferring the hybridoma to a mammal compatible therewith A method of transplanting, growing, and obtaining ascites is used.
- the former method is suitable for obtaining high-purity antibodies, while the latter method is suitable for mass production of antibodies.
- cells in which immune cells such as sensitized lymphocytes producing antibodies are immortalized by oncogenes may be used.
- the monoclonal antibody thus obtained can also be obtained as a recombinant antibody produced using a genetic recombination technique.
- a recombinant antibody is obtained by cloning an anti-gankyrin polypeptide antibody gene from immune cells such as a hybridoma or a sensitized lymphocyte producing the antibody, and incorporating the gene into an appropriate vector. This is introduced into the host and produced.
- This recombinant antibody can be used in the present invention ( See, for example, Borrebaeck, CAK and Larrick, JW, THERAPEUTIC MONOCLONAL ANTIBODIES, Published in the United Kingdom by AC ILLAN PUBLISHERS LTD, 1990).
- mRNA encoding the variable region (V region) of the anti-gankyrin polypeptide antibody is isolated from the hybridoma producing the anti-gankyrin polypeptide antibody.
- mRNA can be isolated by known methods, for example, guanidine ultracentrifugation (Chirgwin, J.. et al., Biochemistry (1979) 18, 5294-5299), AGPC method (Chomczynski, P. andd. Prepare total RNA using Sacchi, N., Anal. Biochem. (1987) 162, 156-159) and purify mRNA from total RNA using mRNA Purification Kit (Pharmacia).
- mRNA can be directly prepared by using the QuickPrep mRNA Purification Kit (Pharmacia).
- cDNA of the antibody V region is synthesized using reverse transcriptase.
- c DNA can also be synthesized using AMV Reverse Transcriptase First-Strand cDNA Synthesis Kit (Seikagaku Corporation) or the like.
- AMV Reverse Transcriptase First-Strand cDNA Synthesis Kit (Seikagaku Corporation) or the like.
- 5'-RACE using 5'-Ampli FINDER RACE Kit C 1 on tech
- PCR polymerase chain reaction
- DNA encoding the V region of the desired anti-gankyrin polypeptide antibody is obtained, it is ligated to the DNA encoding the desired antibody constant region (C region), and the expression vector is expressed.
- C region the DNA encoding the V region of the antibody
- DNA encoding the V region of the antibody may be incorporated into an expression vector that already contains the DNA of the antibody C region.
- an antibody C region derived from the same animal species as the V region may be used, or an antibody C region derived from an animal species different from the V region may be used.
- an antibody gene is incorporated into an expression vector so as to be expressed under the control of an expression control region, for example, an enhancer or a promoter.
- host cells are transformed with this expression vector to express the antibody.
- the expression of the antibody gene is determined by separately separating the DNA encoding the heavy chain (H chain) or light chain (L chain) of the antibody.
- the host cell may be transformed by incorporating the DNA encoding the H and L chains into a single expression vector, or the host cell may be transformed by incorporating the DNA encoding the H and L chains into a single expression vector. (See International Patent Application Publication No. W ⁇ 94-1-11523).
- the antibody used in the present invention may be an antibody fragment or a modified antibody thereof, as long as it binds to gankyrin polypeptide.
- antibody fragments include Fab, F (ab ') 2, Fv, or a single-chain Fv (scFV) in which the Fv of the H chain and the L chain are linked by an appropriate linker.
- an enzyme for example, pappine or pepsin
- the antibody was treated with an enzyme, for example, pappine or pepsin, to generate an antibody fragment, or a gene encoding these antibody fragments was constructed and introduced into an expression vector. Later, it is expressed in a suitable host cell (for example, Co,. S. et al., J. Immunol.
- scFv can be obtained by linking the H chain V region and L chain V region of the antibody.
- the H chain V region and L chain V region are linked via a linker, preferably a peptide linker (Huston, JS et al., Pro Natl. Acad. Sci. USA (1988) 85, 5 879-5883).
- the H chain V region and L chain V region in scFv may be derived from any of the antibodies described above.
- the peptide linker that connects the V regions for example, any single-chain peptide consisting of 12 to 19 residues of amino acid is used.
- the DNA encoding the sc FV is a type II DNA encoding the H chain or the V region of the H chain and a DNA encoding the L chain or the V region of the L chain of the antibody.
- the DNA portion encoding the desired amino acid sequence is amplified by PCR using a pair of primers defining both ends thereof, and then the DNA encoding a peptide linker portion is further amplified. And by amplifying them by combining a pair of primers such that both ends thereof are linked to an H chain and an L chain, respectively.
- DNAs encoding isc Fv are prepared, expression vectors containing them and hosts transformed with the expression vectors can be obtained according to a conventional method.
- the scFv can be obtained using the host according to a conventional method.
- the antibody fragment may be an antibody fragment in which a part of the sequence has undergone mutation, substitution, deletion or insertion. These antibody fragments can be obtained and expressed in the same manner as described above, and produced by a host. .
- the “antibody” referred to in the claims of the present application also includes these antibody fragments.
- an anti-gankyrin polypeptide antibody conjugated to various molecules such as polyethylene glycol (PEG) can also be used.
- PEG polyethylene glycol
- the “antibody” referred to in the claims of the present application also includes these modified antibodies.
- Such a modified antibody can be obtained by subjecting the obtained antibody to chemical modification. These methods are already established in this field.
- the anti-gankyrin polypeptide antibody of the present invention can be obtained as a chimeric antibody or a humanized antibody using a known technique.
- the antibody gene constructed as described above can be expressed and obtained by a known method.
- a promoter for production of the gankyrin polypeptide described herein can be used.
- any production system can be used, and the production system for producing the gankyrin polypeptide described in the present specification can be used.
- production systems for the production of anti-gankyrin polypeptide antibodies include in Vitro and in vivo production systems.
- in vitro production systems include production systems using eukaryotic cells and production systems using prokaryotic cells.
- in vivo production system include a production system using animals and a production system using plants. When using animals, there are production systems using mammals and insects.
- Goats, pigs, sheep, mice, mice, and their transgenic animals can be used as mammals (Glaser, V., SPECTRUM Biotechnology Applications, 1993).
- silkworms can be used as insects.
- plants for example, tobacco, for example, Nicotiana bacbacum, can be used (Ma, JK et al., Eur. J. Immunol. (1994) 24, 131-138).
- the antibody gene is introduced into these animals or plants as described above, and antibodies are produced in the animals or plants and collected.
- the host When producing an antibody in an in vitro or in vivo production system as described above, the host may be co-transformed by separately incorporating DNA encoding the antibody H chain or L chain into an expression vector. Alternatively, the host may be transformed by incorporating DNAs encoding the H chain and the L chain into a single expression vector (see International Patent Application Publication No. WO94-115253). .
- the antibody expressed and produced as described above can be separated from the host inside and outside the cell and from the host and purified to homogeneity.
- the separation and purification of the antibody used in the present invention may be performed by using the separation and purification methods used for ordinary proteins, and is not limited at all.
- chromatography chromatography such as affinity chromatography, filtration, ultrafiltration, salting out, dialysis, SDS polyacrylamide gel electrophoresis
- Antibodies can be separated and purified by appropriately selecting and combining isoelectric focusing and isoelectric focusing (Antibodies: A Labora tory Manual. Ed Harlow and David Lane, Cold Spring Harbor and a boratory, 1988).
- Columns used for the affinity chromatography include a tine A column and a protein G column.
- a tine A column For example, as a column using a mouth tin A column, Hyper D, POROS, Separose FF (Pharmacia) and the like can be mentioned.
- Chromatographs other than affinity chromatographs include, for example, ion exchange chromatographs and hydrophobic chromatographies. Graphite, gel filtration, reversed-phase chromatography, adsorption chromatography (Strategies for Protein Purification and Characterization: A Laboratory Course Manual. Ed Daniel R. Mar shak et al , Cold Spring Harbor Laboratory Press, 1996). These chromatographies can be performed using a liquid-phase chromatograph such as HPLC or FPLC.
- the concentration of the antibody obtained above can be measured by measuring the absorbance or by enzyme-linked immunosorbent assay (ELISA). That is, when the absorbance is measured, the obtained antibody is appropriately diluted with PBS, and then the absorbance at 280 nm is measured. The extinction coefficient differs depending on the species and subclass. Calculate mg / ml as 1.40D.
- measurement can be performed as follows. That is, goat anti-human IgG antibody 1001, diluted to 1 ig / ml with 0.1 M bicarbonate buffer (pH 9.6), was added to a 96-well plate (Nunc), and Incubate overnight at ° C to immobilize the antibody. After blocking, add appropriately diluted antibody or a sample containing the antibody of the present invention, or add human IgG 100 ⁇ 1 at a known concentration as a concentration standard, and incubate at room temperature for 1 hour. Take a shot.
- BIA c 0 re can be used for measuring the concentration of the antibody.
- the activity of the anti-gankyrin polypeptide antibody of the present invention can be evaluated using a generally known method.
- Was added Gankiri emission port Liberation 1 25 Petit de in the solid boss was playing Bok I-labeled anti Ganki Li down port Liberation Petit de antibody, washed in accordance with known methods, by a child measuring the radioactivity, anti The activity of gankyrin polypeptide antibodies can be evaluated (Antibodies: A Laboratory Manual. Ed Harlow and David Lane, Cold Spring Harbor Laboratory, 1988).
- ELISA Enzyme-linked immunosorbent assay
- RIA radioimmunoassay
- fluorescent antibody assay may be used to measure the antigen-binding activity of the anti-gankyrin polypeptide antibody used in the present invention. Can be used.
- gankyrin polypeptide is added to a plate on which an anti-gankyrin polypeptide antibody is immobilized, and then a sample containing the desired anti-gankyrin polypeptide antibody For example, a culture supernatant of an anti-gankyrin polypeptide antibody-producing cell or a purified antibody is added. After adding a secondary antibody that recognizes an anti-gankyrin polypeptide antibody labeled with an enzyme, for example, alkaline phosphatase, etc., incubate the plate, wash the plate, and then add Antigen binding activity can be evaluated by measuring the absorbance after adding an enzyme substrate such as phenylphosphoric acid.
- an enzyme substrate such as phenylphosphoric acid
- gankyrin polypeptide a fragment of gankyrin polypeptide, for example, a C-terminal fragment or an N-terminal fragment thereof may be used.
- the activity of the anti-gankyrin polypeptide antibody of the present invention can be evaluated using BIAcore (Pharmacia). By using these techniques, the anti-gankyrin polypeptide of the present invention can be used.
- the antibody is contacted with a sample expected to contain gankyrin polypeptide contained in the sample, and the antibody and gankyrin polypeptide are contacted.
- a method for detecting or measuring gankyrin polypeptide which comprises detecting or measuring an immune complex with a peptide can be carried out.
- a sample containing gankyrin polypeptide is added to a plate on which anti-gankyrin polypeptide antibody is immobilized, and then the anti-gankyrin polypeptide is added.
- Add peptide antibody After adding a secondary antibody that recognizes an anti-gankyrin polypeptide antibody labeled with an enzyme, for example, alkaline phosphatase, etc., incubate the plate, wash the plate, and then add p-nitrate.
- the presence of gankyrin polypeptide in a sample can be evaluated by measuring the absorbance by adding an enzyme substrate such as phenylphosphoric acid.
- gankyrin polypeptide for example, a C-terminal fragment or an N′-terminal fragment thereof may be used.
- BIAcore Pharmacia
- the method for detecting or measuring ganky lipopeptide of the present invention uses ganky lipopeptide because ganky lipopeptide can be specifically detected or measured. It is useful for various experiments.
- the present invention includes a nucleotide (related A or RNA) or a nucleotide derivative which can selectively hybridize with the gene of the present invention, for example, antisense oligonucleotide, lipozyme and the like. included.
- the present invention includes, for example, an antisense oligonucleotide which hybridizes at any position in the nucleotide sequence shown in SEQ ID NO: 1.
- the antisense oligonucleotide is preferably an antisense oligonucleotide against at least 20 consecutive nucleotides in the nucleotide sequence shown in SEQ ID NO: 1. Is.
- the antisense oligonucleotide as described above wherein at least 20 or more consecutive nucleotides include a translation initiation codon.
- the antisense oligonucleotide of the present invention has SEQ ID NO: 8.
- the antisense oligonucleotide of the present invention has SEQ ID NO: 9.
- antisense oligonucleotide refers to not only those in which all of the nucleotides corresponding to the nucleotides constituting the predetermined region of DNA or mRNA are complementary, as well as DNA. Alternatively, as long as the mRNA and the oligonucleotide can selectively and stably hybridize to the nucleotide sequence shown in SEQ ID NO: 1, the mismatch of one or more nucleotides may be reduced. May be present.
- Selective and stable hybridization means that at least 20, preferably 30 contiguous nucleotide sequence regions, at least 70%, preferably at least 80%, More preferably, they have a homology of 90% or more, more preferably 95% or more in nucleotide sequence.
- the antisense oligonucleotide has the nucleotide sequence shown in SEQ ID NO: 8. Further, according to one embodiment of the present invention, the antisense oligonucleotide has the nucleotide sequence shown in SEQ ID NO: 9.
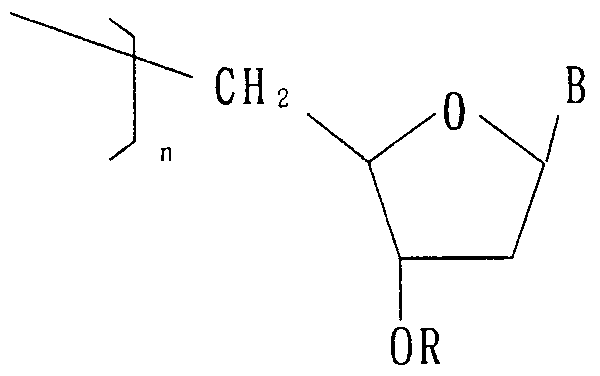
- each structure is as shown in Formula I.
- X may independently be oxygen ( ⁇ ), zeolite (S), a lower alkyl group, or any of a primary amine and a secondary amine.
- Y may independently be either oxygen (0) or zeolite (S).
- B is selected from the group consisting of adenine, guanine, thymine, and cytosine, and is mainly a complementary oligonucleotide of the DNA or mRNA of the human gankyrin gene.
- R is independently hydrogen (H), a dimethoxytrityl group or a lower alkyl group.
- n is 7-28.
- Preferred oligonucleotide derivatives include not only unmodified oligonucleotides but also modified oligonucleotides as shown below.
- a modified product may be, for example, a lower alkyl such as a methylphosphonate type or an ethylphosphonate type. Examples include modified phosphonate, modified phosphorothioate, and modified phospholipid.
- oligonucleotides can be obtained by a conventional method as follows. Oligonucleotides in which X and Y in Chemical Formula 1 are 0 can be easily synthesized by a commercially available DNA synthesizer, for example, manufactured by Applied Biostems. The synthesis method can be obtained by a solid-phase synthesis method using phosphoramidite, a solid-phase synthesis method using di-, i-didiphosphonate, or the like (Atkinson, T. & Smith, M. in Oligonucleotides). Synthesis: A
- the modified phosphoric acid triester in which X is a lower alkoxy group can be prepared by a conventional method, for example, by converting an oligonucleotide obtained by chemical synthesis into a DMF / methanol / 2, This can be enhanced by treatment with a 6-lutidine solution (Moody, HM et al., Nuclein Acids Res. (1989) 17, 4769-4782).
- Modified alkyl phosphonates in which X is an alkyl group can be obtained by a conventional method, for example, using a phosphoamidite (Dorman,. A. et al., Tetrahedron Lett. (1984) 40, 95). -102, Agarwal, KL
- Modified phosphorothioate in which X is S can be obtained by a conventional method, for example, a solid phase synthesis method using thiol (Stein, CA et al., Ucleic Acids Resea rch (1988) 16, 3209-3221) or solid-phase synthesis using tetraethylthiuram dis-norefide (Vu, H. & Hirschbein, BL Tetrahedron Lett. (1991) 32, 3005-3008)
- a modified phosphorodithioate in which X and Y are both S can be obtained by a solid-phase synthesis method by, for example, converting bisamidite into thioamidite and then reacting with thioamide (Brill). , W. KD. J. Am. Che. So (1989) 111, 2321-2322).
- a phosphoramidate-modified product in which X is a primary or secondary amine is obtained by a solid phase synthesis method, for example, by treating a hydrodinin phosphonate with a primary or secondary amine.
- a solid phase synthesis method for example, by treating a hydrodinin phosphonate with a primary or secondary amine.
- it can be obtained by oxidizing the amidite with tert-butyl hydroperoxide (Ozaki, H. et al., Tetrahedron and ett. (1989) 30, 5899-5902).
- Purification and purity confirmation can be performed by high performance liquid chromatography and polyacrylamide gel electrophoresis.
- the molecular weight can be confirmed by Electrospray Ionization Mass Spectrometry or Fast Atom Bonbar dment-Mass Spectrometry.
- the antisense oligonucleotide derivative of the present invention has a sequence that hybridizes to the nucleotide sequence of DNA or mRNA encoding human gankyrin polypeptide, its synthesis method and origin can be any. May be.
- the antisense oligonucleotide derivative of the present invention acts on a human gankyrin polypeptide receptor-producing cell as shown in Example 7 below, and codes for the human gankyrin polypeptide. Binding to DNA or mRNA that inhibits the expression of human gankyrin polypeptide by inhibiting its transcription or translation or promoting mRNA degradation As a result, it has the effect of suppressing the action of human gankyrin polypeptide.
- the action of the human ganky lipopeptide which is inhibited by the antisense oligonucleotide derivative of the present invention includes the activity of the cells in soft agar described in Example 7 described below. Suppression of rhone formation ability.
- the antisense oligonucleotide derivative of the present invention can be used as an external preparation such as a liniment or a poultice by mixing with a suitable base which is inactive against the antisense oligonucleotide derivative.
- excipients may be added to tablets, splinters, granules, capsules, ribosome capsules, injections And freeze-dried preparations such as preparations, solutions, and nasal drops. These can be prepared according to a conventional method.
- the antisense oligonucleotide derivative of the present invention is applied directly to the affected area of the patient, or is applied to the patient so as to be able to reach the affected area as a result of intravenous administration or the like.
- antisense encapsulating materials that enhance durability and membrane permeability can be used.
- liposome, poly-lysine, lipid, cholesterol, ribopectin or derivatives thereof can be mentioned.
- the dosage of the antisense oligonucleotide derivative of the present invention can be appropriately adjusted depending on the condition of the patient, and a preferred amount can be used. For example, it can be administered in the range of 0.1 to 100 mg / kg, preferably in the range of 0.1 to 50 mg / kg.
- the antisense oligonucleotides of the present invention inhibit the expression of gankyrin polypeptides and are therefore useful in suppressing the biological activity of gankyrin polypeptides.
- the invention discloses a gankyrin polypeptide containing the antisense oligonucleotide of the present invention.
- the present inhibitors can suppress the biological activity of gankyrin, ie, carcinogenicity, and are useful as therapeutic agents for cancer and hyperproliferative diseases.
- Example 1 Cloning of cDNA by the subtraction method
- the subtraction method (Nakayama, H. et al., Develop. Growth D if fer. (1996) 38, 141-151) was used. Using this, we cloned the cDNA of a gene specifically expressed in liver cancer.
- RNAs were extracted from each tissue using the TRIS01 reagent (GIBCO BRL).
- TRIS01 reagent GRIS01 reagent
- a double-stranded cDNA was synthesized from the entire RNA using a cDNA synthesis kit (Pharmacia) with o1igo-dT primer. After digestion of this cDNA with the restriction enzyme RsaI, a linker adapter (Nakayama, H. et al., Develop. Growth D if fer. (1996) 38, 141-151) was added, followed by PCR.
- cDNAs were amplified using primers (Nakayama, H. et al., Develop. Growth Differ. (1996) 38, 141-151).
- primers Nakayama, H. et al., Develop. Growth Differ. (1996) 38, 141-151).
- a primer labeled with piotin was used.
- the enriched liver cancer tissue-specific cDNA molecules were amplified using the PCR method, and the same procedure was repeated to perform enrichment a total of five times. In this way, a cDNA fragment of 250 bp specific to liver cancer tissue derived from human liver tissue was obtained.
- cDNA libraries were prepared from human placenta, mouse NIH / 3T3 cell line, and rat placenta according to a standard method, and ⁇ ⁇ ⁇ ⁇ ⁇ It was linked to a phage vector (Strategene). The human placenta cDNA library was screened under high stringent conditions using the above 250 bp human cDNA fragment as a probe.
- PCR amplification of the 678 bp 0RF in this cDNA was used as a probe, and the cDNA library of rat placenta and mouse NIH / 3T3 cell line was used under low stringent conditions.
- the screen was screened. That is, the hybridization solution (5 XSSPE, 50% formamide, 5 ⁇ Denhardt's solution, 0.5% SDS, 100 ⁇ g Z ml denatured DNA, It was hybridized at 37 ° C in 10% dextran sulfate and then washed under the conditions of 1XSSC and 1.0% SDS at 37 ° C (Sambrook, J.
- rat and mouse cDNAs were isolated.
- the nucleotide sequences of these cDNAs were determined by a conventional method, and the amino acid sequence was determined from the nucleotide sequences.
- Table 1 shows the results of a comparison of the putative amino acid sequences of human, rat, and mouse, using single-letter codes.
- the polypeptide having this amino acid sequence was designated as gankyrin.
- the human ganglion gene and the mouse ganquilin gene had 90% homology at the nucleotide sequence level, and had 93% homology at the amino acid sequence level.
- the human gangan killin gene and the rat gankyrin gene had 91% homology at the nucleotide sequence level and 94% homology at the amino acid sequence level.
- the amino acid sequence of the obtained human gankyrin polypeptide was 5.5 ankyrin repeats (Lambert, S. et al., Proc. Natl. Acad. Sci. USA, (1990) 87, 1730-1734). This situation is shown in Table 2 below.
- FIG. 15 shows the location and number of repeats of ankyrin repeats in various proteins.
- lymphocytes isolated from human blood were transferred to a minimum essential medium (MEM) supplemented with 10% fetal serum and glutamicin (PHA) at 37 ° C for 6 hours at 37 ° C.
- MEM minimum essential medium
- PHA glutamicin
- the culture was performed for 8 to 72 hours.
- the cell cycle of the cell population was synchronized by treating the lymphocyte culture with 0.18 mgZml of BrdU (Sigma). The cell cycle-synchronized cells were washed three times with serum-free medium.
- the cell cycle arrest was released and recultured in MEM containing 2.5 g / ml thymidine (manufactured by Sigma) at 37 ° C for 6 hours. Cells were collected and chromosomal slides were prepared using standard methods, including hypotonic treatment, fixation and air drying.
- Phage DNA (Sambrook, J. et al., Moleculor Cloning, supra) containing about 8.0 kb of the gankyrin gene insertion site was purified using a BRL BioNick label kit according to the instructions and followed by dATP and biotin. Biotin labeling was carried out by nick transfer for 1 hour at 15 ° C with 16 — d CTP (Herg et al., Pro atl. A cad. Sci. USA, 89: 9509-9513 (1992)).
- FISH fluorescence in situ hybridization
- the slide was treated at 55 ° C for 1 hour to fix the chromosome to the slide glass.
- the slide was denatured with 70% formamide in 2 x SSC at 70 ° C for 2 minutes, then It was dehydrated with ethanol.
- the probe was denatured at 75 ° C. for 5 minutes in a hybridization mixture containing 50% formamide, 10% dextran sulfate and human cot I DNA. After incubating at 37 ° C. for 15 minutes to suppress repetitive sequences, the probe was added onto the denatured slide. After overnight hybridization--slides were washed at 37 ° C with 50% formamide in 2XSSC and then at 60 ° C in 1XSSC .
- FITC-conjugated avidin After detecting the biotin with fluorescently labeled FITC-conjugated avidin (manufactured by Vector Laboratories), it was stained with DAPI (manufactured by Sigma), a fluorescent reagent that stains DNA, and G / G Q—Band pattern is generated.
- DAPI manufactured by Sigma
- a chromosome-specific shading band pattern can be created with a fluorescent reagent that stains DNA, and chromosome assignment and chromosome mapping (location) can be made.
- the FISH map data was assigned to the chromosome band by superimposing the FISH signal and the DAPI band forming chromosome (Hery et al., Methods in Molecu ar Biology: In situ hybridization protocols (KHA Choo. ed), p.35-49 (1994), Human Press, CI if ton, NJ.
- the hybridization efficiency for this probe was approximately 81%. That is, 80 of the 100 mitotic figures tested showed a signal on a pair of chromosomes. Since DAPI banding was used to identify a particular chromosome, the signal from the probe was assigned to the long arm of the X chromosome. In addition, a more detailed positioning can be achieved by combining 10 photos. Was performed. The results are shown in Figure 1. Because no other loci were detected by FISH detection under the conditions used, probe T411 was mapped to chromosome X region q21.3—q22.2.
- Fig. 2 shows the results (fluorescent staining) of the obtained in situ hybridization.
- liver cancer tissue T
- liver non-cancerous tissue N
- FIG. 3- Sample results from liver cancer tissue (T) and liver non-cancerous tissue (N) are shown in FIG. 3-the lower part shows the results of the internal standard, and the upper part shows the results detected with the human gangan killer cDNA probe.
- Gankyrin mRNA was shown to be overexpressed only in liver cancer tissues.
- R C C (renal cell carcinoma) 0 2 0
- gankyrin mRNA was also overexpressed in gastric cancer tissues among the test cancer tissues.
- FIG. 5 shows the results of the test samples 6), placenta (lane 7), ovaries (lane 8), testes (lane 9), kidneys (lane 10), and lungs (lane 11). As shown in FIG. 5, the expression of gankyrin mRNA in normal human tissues was slight.
- Glu-Gly-Cys-Val-Ser-Asn-Leu-Met-Val-Cys peptide corresponding to the C-terminal region of gankyrin for the preparation of anti-gankyrin polypeptide antibodies -Asn-Leu-Ala-Tyr (SEQ ID NO: 7) was synthesized. This peptide was linked to a keyhole link with mosaicin, and immunized to a egret. 14, 42, and 56 days after immunization The heron was immunized to obtain antiserum.
- Affinity was obtained using the above-mentioned peptide on which the obtained antiserum was immobilized.
- gankyrin polypeptide was obtained by adding a gankyrin gene expression plasmid to a TNT expression system (Promega). At this time, it was synthesized [35 S] by a child added main Chionin the system [35 S] Main Chioni down labeled human Togankiri emission port Ripepuchi de. Unlabeled gankyrin polypeptide was also synthesized using the same conditions.
- the blotting membrane was washed repeatedly in Tris buffer, 0.1% Tween-20 at room temperature. Then, the cells were incubated at room temperature for 1 hour together with anti-pseudoimyoglobulin antibody labeled with horseradish peroxidase as a secondary antibody. After washing, it was developed with an electrochemiluminescent reagent (Amersham).
- FIG. 8A shows the result of the in vitro translated labeled gankyrin gene product.
- Type I (1) (lane 1), positive controls (luciferase cDNA corresponding to ⁇ 60 kDa) (lane 2), gankyrin (lane 3).
- Figure 8B shows the results of analysis of the gankyrin gene product (unlabeled) translated in vitro by Western blot using an anti-gankyrin polypeptide antibody.
- Each lane shows type I (lane 1), positive controls (luciferase cDNA corresponding to ⁇ 60 kDa) (lane 2), and gankyrin (lane 3).
- Fig. 6 shows the results of detection by Western blotting using a receptor antibody. Similar to the mRNA level shown in Example 2, more gankyrin polypeptides were detected in liver cancer tissues than in non-cancerous liver.
- HepG2 (ATCC Catalog 1994 (American Type Culture Collection)) (lane 1), HeLa (ATCC Catalog 1994 (American Type Culture Collection)) (lane 2) ), T24 (ATCC Catalog 1994 (American Type Culture Col 1 ection)) (lane 3), NC65 (Hoehn, W. and Schroeder, FH, Invest. Urol. (1978) 16, 106) (Lane 4), NEC 8 (hi Man Science Research Resource Bank, Cell. Gene Catalog, 2nd ed., 1995 (Lane 5), Jurkat (ATCC Catalog 1994 (American Type Culture Collection)) ( Whole cells of lanes 6), 293 (ATCC catalog 1994 (American Type Culture Collection)) (lane 7) and CS ⁇ 7 (ATCC catalog 1994 (American Type Culture Collection)) (lane 8) FIG.
- FIG. 7 shows the results of detection of the gankyrin polypeptide in the lysate by the Western blot method using an anti-gankyrin polypeptide antibody which was purified in the same manner as described above. As a result, expression of gankyrin polypeptide was confirmed in all cell lines.
- the sample was separated by SDS-polyacrylamide gel electrophoresis (PAGE), and the gel used for SDS-PAGE was immobilized (Immob i 1 on transfer membrane) (manufactured by Mi UIpore). And blotted in a Tris buffer containing 5% ⁇ serum albumin (BSA) . The blotting membrane was then plated with Tris buffer, 0.1% TSA. ween — 1: 2 0 0 0 in 20 and BSA
- the 678 bp cDNA encoding the human cancer lipopeptide (Example 1) was ligated to the pMKIT-NEO mammalian expression vector (a new cytology protocol, P. 259). , Tokyo University of Medical Science, Shujunsha) in the sense direction and antisense direction.
- the SRa promoter in this vector is able to constitutively direct the synthesis of RNA from the inserted DNA.
- the pMKIT-NEO vector has a neomycin resistance gene suitable for selecting a transformant.
- plasmid construct was transferred to NIH 3T3 cells (Jainchi 11, JF et al., J. Virol (1969) 4, 549-553) by the calcium phosphate method. It's a shock. Forty-eight hours after transfection, G418 was added to the medium at a concentration of 1000 ⁇ g / ml. Individual colonies were isolated and expanded for further analysis. In this way, five sense clones, five antisense clones, and five control clones are established, and these clones are subjected to in vitro proliferation, morphology, and detailed analysis. It was characterized by blast cycle and tumorigenicity.
- the doubling time was determined from the growth curve.
- Cells were cultured in two layers of soft agar consisting of a lower layer (DMEM, 10% FCS, 0.6% agar) and an upper layer (DMEM, 10% FCS, 0.3% agar).
- 3 in soft agar plates of 5 flame was inoculated with 5 X 1 0 3 cells, four to five weeks I at 3 7 ° C After incubation, the cells were counted.
- the average of 5 clones in the number of colonies consisting of 15 or more cells was 25 ⁇ 2 for the control clone and 123 ⁇ 1 for the sense clone. Therefore, it was shown that the cells expressing gankyrin polypeptides had an increased ability to form colonies in soft agar.
- the average value of the number of colony focuses obtained from the G418 selection medium in the three transfusion experiments was 56 ⁇ 4 for the control clone and 7 for the sense clone. It was 0 ⁇ 4 and 23 ⁇ 3 for antisense clones. Therefore, it was shown that gankyrin polypeptide acts on cell growth promotion or apoptosis induction suppression.
- each cloned cell was grown on a cover glass for 48 hours until reaching a 60% saturation density, and after removing serum, the apoptotic cell was stained with an ApopTag apoptosis detection kit (manufactured by Oncor). Then, the ratio of apoptotic cells to the total number of adherent cells was measured by light microscopy.
- the extract was treated with 1 mg / ml proteinase K for a further 30 minutes at 37 ° C.
- the extract of 301 was subjected to 1.7% agarose gel electrophoresis in the presence of 0.5 gZ ml of bromide medium.
- the ladder-like electrophoresis pattern due to DNA fragmentation between nucleosomes was reduced in the cells into which the sensane gankyrin gene was introduced, as compared with the control cells. Therefore, these three experiments indicated that the gankyrin gene product functions to suppress apoptosis induction. This is a feature found in several other oncogenes, supporting that the gankyrin gene is a carcinogenic gene.
- PCMV 4 — 3 HA 'vector (Brockman) containing the Z promoter and the base sequence of influenza virus HA (hemogluatinin) epitope , JA et al., Moleculor and Cellulo Biology (1995) 15, 2809-2818), and ligated the human gankyrin cDNA obtained in Example 1 to obtain a fusion consisting of gankyrin and influenza virus HA.
- a plasmid pCMV4-3HA + gankyrin expressing polypeptide was prepared.
- a human gankyrin coding sequence into vector pGEX (manufactured by Pharmacia)
- pGEX human gankyrin coding sequence
- a fusion polypeptide consisting of GST (glutathione, S-transferase) and gankyrin can be obtained.
- Plasmid p GEX-gankyrin to be expressed was produced.
- 2293 cells were temporarily transfected by the calcium phosphate method.
- PGEX-gankyrin was introduced into E. coli, and the production of GST-gankyrin fusion polypeptide was induced by ImM IPTG.
- Cells were harvested by centrifugation at 4 ° C and lysed by sonication in PBS containing Triton-XI00. This cell lysate was mixed with a whole cell extract from a 2993 cell transformant and incubated at 4 ° C for 16 hours.
- the GST fusion polypeptide was collected on glutathione Sepharose 4B (Pharmacia), and anti-Rb antibody, anti-NFB p50 antibody, and anti-NF / cBp65 (all from Santa Crutz) ) was analyzed by the Western blot method.
- HEPES H7.5
- 150 mM NaCl 150 mM NaCl, 2.5 mM EGTA, 1 mM DTT, 0.1% Tween—20, 10% glycerol, protease inhibitors and phos
- IP buffer containing a phosphatase inhibitor, sonicated, and then centrifuged at 10,000 X g for 10 minutes at 4 ° C.
- protein A—Sepharose CL4B Pharmacia pre-coated with anti-HA antibody, anti-Rb antibody, anti-NF / cBp50 antibody or anti-NF / cBp65 antibody
- the supernatant was sedimented at 4 ° C for 16 hours.
- the immunoprecipitated protein on the beads was washed 10 times with IP buffer. 2 Precipitate in XSDS sample buffer was separated by SDS-polyacrylamide gel electrophoresis, and then anti-HA antibody, anti-Rb antibody, anti-NFcBp50 antibody or anti-NF / cB Analysis was performed by the Western blot method using the p65 antibody.
- Figure 9 shows the results of using the cell lysate in vitro. Either GST alone or a fusion polypeptide of GST and gankyrin was expressed in Escherichia coli and recovered. The lysate of human 293 cells and the previously obtained GST alone or GST-gankyrin fusion polypeptide were mixed, sedimented with glutathione-conjugated sepharose, and electrophoresed. .
- FIG. 10 shows an in vivo cell experiment. Lysates of human 293 cells expressing gankyrin fused with HA were immunoprecipitated with (A) anti-Rb antibody, (B) anti-P50 antibody or (C) anti-p65 antibody, Then anti When detected with the HA antibody, the HA-fused gankyrin polypeptide was detected.
- A a lysate of human 293 cells transformed with a vector containing no gankyrin gene was treated with non-specific immunoglobulin (lane 1) or anti-Rb antibody (lane 2). Precipitated, electrophoresed, and detected with anti-HA antibody. Lysate of human 293 cells transformed with a vector containing the gankyrin gene was lysed into non-specific immunoglobulin (lane 3). ) Or anti-Rb antibody (lane 4), and electrophoresed and detected with anti-HA antibody.
- the lane is a lysate of human 293 cells transformed with a vector containing no gankyrin gene, which is obtained by using a non-specific immunoglobulin (lane 1) or an anti-p50 antibody. (Lane 2), which were electrophoresed and detected with an anti-HA antibody. Lysates of human 293 cells transformed with a vector containing the gankyrin gene were used for non-specific immunoassay.
- lane was isolated from lysate of human 293 cells transformed with vector containing no gankyrin gene by non-specific immunoglobulin (lane 1) or anti-p6. 5 Precipitation with antibody (lane 2), electrophoresis, detection with anti-HA antibody, and non-specific lysate of human 293 cells transformed with a vector containing the gankyrin gene. Sedimented with immunoglobulin (lane 3) or anti-p65 antibody (lane 4), electrophoresed and detected with anti-HA antibody, and vectors containing gankyrin gene Lysate of human 293 cells (lane 5) transformed with The result is shown.
- Figure 11 shows the results of the in vivo cell experiment.
- a lysate of human 293 cells expressing a fusion polypeptide consisting of HA and gankyrin was immunoprecipitated with an anti-HA antibody, and (A) an anti-Rb antibody or (B) an anti-p65 antibody.
- Rb or p65 was detected, respectively.
- lane was detected with an anti-Rb antibody (lane 1) by electrophoresis of a lysate of human 293 cells transformed with a vector containing no gankyrin gene. Lysate of human 293 cells transformed with a vector that does not contain the gankyrin gene is precipitated with non-specific immunoglobulin (lane 2) or anti-HA antibody (lane 3). The lysate of human 293 cells transformed with a vector containing the gankyrin gene was purified by electrophoresis and detected with an anti-Rb antibody. Non-specific immunoglobulin (lane 4) Alternatively, the results obtained by sedimentation with an anti-HA antibody (lane 5), electrophoresis, and detection with an anti-Rb antibody are shown.
- the lane shows the lysate of the human 293 cells transformed with the vector containing no gankyrin gene, and the non-specific immunoglobulin (lane 1) or anti-HA antibody.
- Lane 2 which were electrophoresed and detected with an anti-P65 antibody, and the lysate of human 293 cells transformed with a vector containing the gankyrin gene was non-specific.
- Precipitated with munoglobulin (lane 3) or anti-HA antibody (lane 4) electrophoresed and detected with anti-P65 antibody, and transformed with a vector containing the gankyrin gene
- the results obtained by electrophoresis of the lysate of human 293 cells (lane 5) detected with an anti-p65 antibody are shown.
- Example 6 Cell cycle and gankyrin gene expression NIH / 3T3 cells were fixed to the early G1 phase by serum starvation for 72 hours, and cell cycle was synchronized by re-adding serum. Cells were lysed, mRNA was extracted, and detection was performed using gankyrin cDNA as a probe. That is, the cDNA of the coding region of mouse gankyrin was converted into type I, amplified by PCR, and labeled with 32 P using random priming as a probe. MRNA was detected by the kit method.
- Flow cytometry (F10 w Cytometry) was used for cell cycle analysis of each cell means. That is, the cells were washed with C a 2+ and M g 2 + containing no PBS, and subjected to preparative Li busi down process. Next, the cells were washed and recovered with DMEM containing 10% FCS, washed once again with a sample buffer and resuspended, and then fixed with 70% ethanol. This was stained with PI (Propiodiumiodine) and measured with a flow cytometer.
- PI Propiodiumiodine
- Figure 12 shows the results.
- each lane was 1 hour (lane 1), 3 hours (lane 2), 6 hours (lane 3), 9 hours (lane 4), and 12 hours (lane) 5), 15 hours (lane 6), 18 hours (lane 7), 21 hours (lane 8), 24 hours (lane 9), 27 hours (lane 10), The results for 30 hours (lane 11) and 33 hours (lane 12) are shown.
- 1 to 9 hours (lanes 1 to 4) are in G1 phase
- 12 to 18 hours (lanes 5 to 7) are in S phase
- FIG. 13 shows the results of detecting mRNA expressed in cells grown at various cell concentrations.
- FIG. 14 shows the results of detection of mRNA expressed during the liver regeneration process of mice after partial hepatectomy.
- lane 1 1 hour
- lane 2 6 hours
- lane 3 6 hours
- lane 4 24 hours
- lane 4 48 hours after partial hepatectomy
- the results are shown for (lane 5), 72 hours later (lane 6) and 168 hours later (lane 7).
- hepatocyte proliferation of a human gankyrin / antisense oligonucleotide derivative (sequence: CCTGTCGCTTTACCTCCCCA) (SEQ ID NO: 8) and (TACCTCCCCACACACAGAGATT) (SEQ ID NO: 9)
- the inhibitory effect was investigated.
- RPM 164 Nesi
- FCS fetal calf serum
- the gankyrin polypeptide of the present invention exhibits carcinogenicity because it exhibits an effect such as an increase in the ability of cells to form colonies, a tumorigenicity in mice, and suppression of apoptosis induction. .
- Gankyrin polypeptides and the DNA encoding them are useful for elucidating the mechanism of action of carcinogenesis.
- a screening method using gankyrin polypeptide, an antibody against gankyrin polypeptide, a method for detecting or measuring gankyrin polypeptide using the same, and a gankyrin polypeptide are used.
- Antisense oligonucleotides against DNA that binds are also useful for elucidating the mechanism of action of carcinogenesis.
- VN (: ucoid 2i fmn:- ⁇ a ⁇
- VNd MM Co ⁇ IIU: — ⁇ , ⁇ ⁇ : r: mom 3 ⁇ 4 3 ⁇ 4: Co 1 ⁇ 2 2 @ C 69: $ jin 2
- Sequence type nucleic acid
- Sequence type nucleic acid
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Gastroenterology & Hepatology (AREA)
- Biochemistry (AREA)
- Immunology (AREA)
- Toxicology (AREA)
- Cell Biology (AREA)
- Zoology (AREA)
- General Chemical & Material Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Public Health (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Veterinary Medicine (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Description
Claims
Priority Applications (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP52146999A JP4229475B2 (ja) | 1997-10-03 | 1998-10-02 | ガンキリン |
| EP98945595A EP1024190A4 (en) | 1997-10-03 | 1998-10-02 | GANKYRINE |
| CA002305814A CA2305814A1 (en) | 1997-10-03 | 1998-10-02 | Gankyrin |
| AU92829/98A AU9282998A (en) | 1997-10-03 | 1998-10-02 | Gankyrin |
| US11/083,944 US7833988B2 (en) | 1997-10-03 | 2005-03-21 | Gankyrin |
| US11/702,119 US20070148179A1 (en) | 1997-10-03 | 2007-02-05 | Gankyrin |
| US12/372,899 US7939506B2 (en) | 1997-10-03 | 2009-02-18 | Treating hepatoma by inhibiting expression of gankyrin |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP9/286214 | 1997-10-03 | ||
| JP28621497 | 1997-10-03 |
Related Child Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US09509775 A-371-Of-International | 1998-10-02 | ||
| US11/083,944 Division US7833988B2 (en) | 1997-10-03 | 2005-03-21 | Gankyrin |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO1999018201A1 true WO1999018201A1 (en) | 1999-04-15 |
Family
ID=17701459
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP1998/004467 Ceased WO1999018201A1 (en) | 1997-10-03 | 1998-10-02 | Gankyrin |
Country Status (6)
| Country | Link |
|---|---|
| US (3) | US7833988B2 (ja) |
| EP (2) | EP1024190A4 (ja) |
| JP (1) | JP4229475B2 (ja) |
| AU (1) | AU9282998A (ja) |
| CA (1) | CA2305814A1 (ja) |
| WO (1) | WO1999018201A1 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1024190A4 (en) | 1997-10-03 | 2003-06-25 | Jun Fujita | GANKYRINE |
| CN102532313A (zh) * | 2010-12-13 | 2012-07-04 | 中国人民解放军第二军医大学 | 一种p28GANK单克隆抗体及其用途 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1994011523A2 (en) | 1992-11-13 | 1994-05-26 | Idec Pharmaceuticals Corporation | Fully impaired consensus kozac sequences for mammalian expression |
| JPH0975085A (ja) * | 1995-09-13 | 1997-03-25 | Sagami Chem Res Center | ヒト26sプロテアソーム構成成分蛋白質およびそれをコードするdna |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1024190A4 (en) | 1997-10-03 | 2003-06-25 | Jun Fujita | GANKYRINE |
-
1998
- 1998-10-02 EP EP98945595A patent/EP1024190A4/en not_active Withdrawn
- 1998-10-02 EP EP07075163A patent/EP1930437A1/en not_active Withdrawn
- 1998-10-02 WO PCT/JP1998/004467 patent/WO1999018201A1/ja not_active Ceased
- 1998-10-02 JP JP52146999A patent/JP4229475B2/ja not_active Expired - Fee Related
- 1998-10-02 CA CA002305814A patent/CA2305814A1/en not_active Abandoned
- 1998-10-02 AU AU92829/98A patent/AU9282998A/en not_active Abandoned
-
2005
- 2005-03-21 US US11/083,944 patent/US7833988B2/en not_active Expired - Fee Related
-
2007
- 2007-02-05 US US11/702,119 patent/US20070148179A1/en not_active Abandoned
-
2009
- 2009-02-18 US US12/372,899 patent/US7939506B2/en not_active Expired - Fee Related
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1994011523A2 (en) | 1992-11-13 | 1994-05-26 | Idec Pharmaceuticals Corporation | Fully impaired consensus kozac sequences for mammalian expression |
| JPH0975085A (ja) * | 1995-09-13 | 1997-03-25 | Sagami Chem Res Center | ヒト26sプロテアソーム構成成分蛋白質およびそれをコードするdna |
Non-Patent Citations (26)
| Title |
|---|
| "Antibodies: A Laboratory Manual", 1988, COLD SPRING HARBOR LABORATORY |
| "Antibodies: A Laboratory Manual.", 1988, COLD SPRING HARBOR LABORATORY |
| "Primary liver cancer in Japan", 1992, SPRINGER-VERLAG, article "The Liver Cancer Study Group of Japan", pages: 445 - 453 |
| "Strategies for Protein Purification and Characterization: A Laboratory Course Manual", 1986, COLD SPRING HARBOR LABORATORY PRESS |
| "The Liver Cancer Study Group of Japan", ANN. SURG., vol. 211, 1990, pages 277 - 287 |
| "The Liver Cancer Study Group of Japan", CANCER, vol. 74, 1994, pages 2772 - 2780 |
| BAEUERLE P.A. et al., "Activation of DNA-Binding Activity in an Apparently Cytoplasmic Precursor of the NF-kappa B Transcription Factor", CELL, Vol. 53, No. 2, (1988), pp. 211-217. * |
| BAEUERLE, P. A. ET AL., CELL, vol. 53, 1988, pages 211 - 217 |
| CALVET, X. ET AL., HEPATOLOGY, vol. 12, 1990, pages 753 - 760 |
| CELL, vol. 16, 1979, pages 443 - 452 |
| DALBADIE-MCFARLAND, G. ET AL., PROC. NATL. ACAD. SCI. U.S.A., vol. 79, 1982, pages 6409 - 6413 |
| DeCAPRIO J.A. et al., "The Product of the Retinoblastoma Susceptibility Gene Has Properties of a Cell Cycle Regulatory Element", CELL, Vol. 58, No. 6, (1989), pp. 1085-1095. * |
| FASEB J., vol. 6, 1992, pages 2422 - 2427 |
| FRANCO, D. ET AL., GASTROENTEROLOGY, vol. 98, 1990, pages 733 - 738 |
| GLASER V., SPECTRUM BIOTECHNOLOGY APPLICATIONS, 1993 |
| MA, J. K. ET AL., EUR. J. IMMUNOL., vol. 24, 1994, pages 131 - 138 |
| MARK, D. F. ET AL., PROC. NATL. ACAD. SCI. U.S.A., vol. 81, 1984, pages 5662 - 5666 |
| MIZUSHIMA ET AL., NUCLEIC ACIDS RES., vol. 18, 1990, pages 5322 |
| MULLIGAN ET AL., NATURE, vol. 277, 1979, pages 108 |
| NUCLEIC ACIDS RESEARCH, vol. 16, 1988, pages 10937 |
| SAMBROOK, J. ET AL.: "Molecular Cloning", 1989, COLD SPRING HARBOR LABORATORY PRESS |
| See also references of EP1024190A4 * |
| WANG, A. ET AL., SCIENCE, vol. 224, pages 1431 - 1433 |
| WARD, NATURE, vol. 341, pages 544 - 546 |
| WILLARDSON B.M. et al., "Localization of the Ankyrin-Binding Site on Erythrocyte Membrane Protein, Band 3", J. BIOL. CHEM., Vol. 264, No. 27, (1989), pp. 15893-15899. * |
| ZOLLER, M. J., SMITH, M., NUCLEIC ACIDS RESEARCH, vol. 10, 1982, pages 6487 - 6500 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20070148179A1 (en) | 2007-06-28 |
| US7833988B2 (en) | 2010-11-16 |
| CA2305814A1 (en) | 1999-04-15 |
| EP1024190A1 (en) | 2000-08-02 |
| US20050170424A1 (en) | 2005-08-04 |
| US7939506B2 (en) | 2011-05-10 |
| JP4229475B2 (ja) | 2009-02-25 |
| EP1930437A1 (en) | 2008-06-11 |
| AU9282998A (en) | 1999-04-27 |
| US20090163438A1 (en) | 2009-06-25 |
| EP1024190A4 (en) | 2003-06-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2254224T3 (es) | Nueva proteina del receptor de hematopoyetina, nr12. | |
| PT1188830E (pt) | Nova proteína nr10 receptora da hemopoietina | |
| JP2003523207A (ja) | Liv−1関連タンパク質、それをコードするポリヌクレオチド、及び癌の治療へのその利用 | |
| WO2001009316A1 (en) | Novel genes encoding protein kinase/protein phosphatase | |
| WO1999067290A1 (fr) | Nouvelles proteines receptrices d'hemopoïetine | |
| ES2253320T3 (es) | Polipeptido y acido nucleico que lo codifica. | |
| EP0566571A1 (en) | DIAGNOSIS OF METASTATIC CANCER USING THE MTS-1 GENE. | |
| US20090197317A1 (en) | TSG-Like Gene | |
| WO1999018201A1 (en) | Gankyrin | |
| EP1464704B1 (en) | Mouse adhesion molecule occludin | |
| US8242245B2 (en) | Fetal polypeptides from human liver | |
| JP4789822B2 (ja) | ガンキリンの生物学的活性を有するポリペプチドに対する阻害剤を含んでなる癌治療剤 | |
| JPWO1999018201A1 (ja) | ガンキリン | |
| AU2005203194A1 (en) | Gankyrin | |
| ES2242597T3 (es) | Composiciones y procedimientos para el diagnostico y tratamiento de un tumor. | |
| WO1999047671A2 (en) | Dna sequences encoding semaphorin-h and diagnosis of metastatic cancer | |
| JPWO2001062916A1 (ja) | 新規アルマジロリピート含有蛋白質、alex1 | |
| WO2000065047A1 (en) | Tumor suppressor genes | |
| JPWO2000021999A1 (ja) | 新規g蛋白質結合型受容体 | |
| WO2001083738A1 (en) | Sex determinative differentiation regulatory factor | |
| JPH11506342A (ja) | 結腸特異的遺伝子およびタンパク質 | |
| JPWO2001018200A1 (ja) | Tsg様遺伝子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AK | Designated states |
Kind code of ref document: A1 Designated state(s): AL AM AT AU AZ BA BB BG BR BY CA CH CN CU CZ DE DK EE ES FI GB GD GE GH GM HR HU ID IL IS JP KE KG KR KZ LC LK LR LS LT LU LV MD MG MK MN MW MX NO NZ PL PT RO RU SD SE SG SI SK SL TJ TM TR TT UA UG US UZ VN YU ZW |
|
| AL | Designated countries for regional patents |
Kind code of ref document: A1 Designated state(s): GH GM KE LS MW SD SZ UG ZW AM AZ BY KG KZ MD RU TJ TM AT BE CH CY DE DK ES FI FR GB GR IE IT LU MC NL PT SE BF BJ CF CG CI CM GA GN GW ML MR NE SN TD TG |
|
| DFPE | Request for preliminary examination filed prior to expiration of 19th month from priority date (pct application filed before 20040101) | ||
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application | ||
| WWE | Wipo information: entry into national phase |
Ref document number: 92829/98 Country of ref document: AU |
|
| ENP | Entry into the national phase |
Ref document number: 2305814 Country of ref document: CA Ref country code: CA Ref document number: 2305814 Kind code of ref document: A Format of ref document f/p: F |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 09509775 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: KR |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 1998945595 Country of ref document: EP |
|
| WWP | Wipo information: published in national office |
Ref document number: 1998945595 Country of ref document: EP |
|
| REG | Reference to national code |
Ref country code: DE Ref legal event code: 8642 |