WO2004089950A1 - Tricyclische heteroaromatische verbindungen - Google Patents
Tricyclische heteroaromatische verbindungen Download PDFInfo
- Publication number
- WO2004089950A1 WO2004089950A1 PCT/EP2004/003626 EP2004003626W WO2004089950A1 WO 2004089950 A1 WO2004089950 A1 WO 2004089950A1 EP 2004003626 W EP2004003626 W EP 2004003626W WO 2004089950 A1 WO2004089950 A1 WO 2004089950A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- methyl
- quinoline
- alkyl
- compound
- radical
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- 0 C*(C)C=C(*)Nc1ccc(*C(*)(*2)C3CC=CCC3)c2c1 Chemical compound C*(C)C=C(*)Nc1ccc(*C(*)(*2)C3CC=CCC3)c2c1 0.000 description 2
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D513/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00
- C07D513/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00 in which the condensed system contains two hetero rings
- C07D513/04—Ortho-condensed systems
Definitions
- the invention relates to tricyclic heteroaromatic compounds and their salts, their preparation and their use as medicaments, in particular as painkillers.
- Acute pain i.e. short-term, temporary pain
- pain usually subsides quickly after the causes have been eliminated and, if need be, cause negligible damage to tissues.
- pain can also last for a long time.
- chronic pain which is usually associated with tissue damage, inflammation or other ailments.
- Diseases that are accompanied by chronic or chronic recurring pain include migraines, neuralgia, muscle pain and inflammation pain.
- Chronic neuronal pain includes postoperative pain, shingles, phantom pain, diabetic neuropathy, pain after chronic nerve compression, and AIDS and cancer in the final stages.
- first pain also called light pain
- second pain the so-called dark or dull pain
- the first pain is encountered as immediate pain with injuries. It is sent to the brain at high speed (about 20 meters per second). If there is no first pain in injuries, the second pain is observed. It reaches the brain much more slowly (about two meters per second), but is more stable and remains as a dull pain over a long period of time.
- Active substances such as acetylsalicylic acid, paracetamol or ibuprofen are available for the treatment of mild pain or headache. Particularly severe pain is treated with opium-related agents such as codeine, morphine or similar substances. Its main task is to improve the patient's quality of life by suppressing the pain. Opiates and opioids mainly work in the central nervous system. In addition to their pain-relieving effects, they can also sedate (calm), have a euphoric effect, inhibit the respiratory center and dampen the cough. They include substances such as codeine, morphine, tilidine and tramadol.
- Non-opioid pain relievers usually work in the peripheral nervous system and are also antipyretic and anti-inflammatory.
- An active ingredient such as caffeine is often added to the active ingredients.
- Examples of such pain relievers are Double-Gap, Eudorlin, Migraine, Neuralgin, Thomapyrin, Titralgan, and Vivimed.
- N-type Caicium channel antagonists for the treatment and prevention of pain are described in international applications WO 02/36567, WO 02/36568 and WO 02/36569.
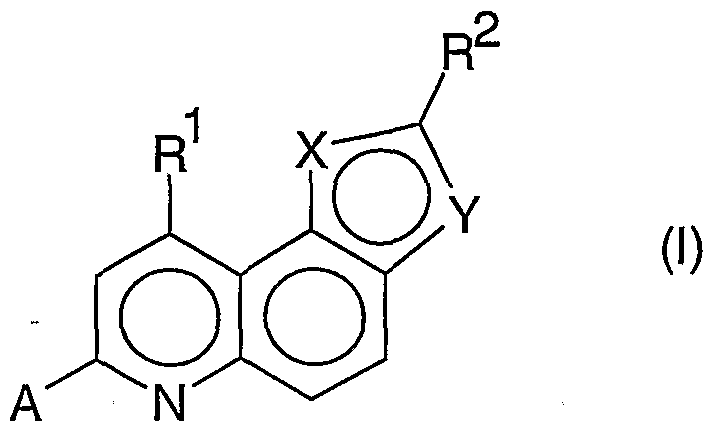
- the present invention provides new compounds and their salts which are useful for relieving pain, particularly chronic pain. These compounds are described by the general formula (I):
- X is a nitrogen atom (N), oxygen atom (O) or sulfur atom (S);
- Y is a nitrogen atom when X represents an oxygen atom or a sulfur atom
- Y is a nitrogen atom with a bonded radical R 3 or a sulfur atom or an oxygen atom when X represents a nitrogen atom;
- A is an unsubstituted or substituted mono-, di- or tricyclic aromatic radical which has either no or 1-3 heteroatoms selected from the group Group contains nitrogen, oxygen and sulfur, at least one of the
- Heteroatoms is a nitrogen atom;
- R 1 is hydroxy, fluorine, chlorine or bromine, amino, (C ⁇ - 6 ) alkylamino, di (C ⁇ -6 ) alkylamino,
- R 2 and R 3 independently of one another are hydrogen (H), (C 1-8 ) alkyl or (C 3 -7) cycloalkyl;
- alkyl describes both saturated and mono- or polyunsaturated aliphatic hydrocarbon radicals.
- (C n -m) alkyl groups are understood to mean those which contain n to m carbon atoms, n and m being integers.
- saturated radicals are preferably (C 1 -C 0 ) alkyl groups
- unsaturated radicals are preferably (C 2 -i 2 ) alkyl groups.
- alkyl encompasses both straight-chain and branched hydrocarbon radicals.
- straight-chain radicals are preferably (C ⁇ -8 ) alkyl groups
- branched radicals are preferably (C 3 - ⁇ o) alkyl groups.
- Hydrogen atoms of alkyl radicals can be partially or completely replaced by halogen atoms.
- halogen atoms are the atoms of fluorine, chlorine, bromine and iodine. If all hydrogen atoms are replaced by halogens, the term "perhalogen alkyl" radical is also used.
- cycloalkyl is used to summarize saturated and mono- or polyunsaturated aliphatic hydrocarbon radicals which form cyclic, ie ring-shaped closed carbon chains which do not represent an aromatic ring system.
- Cycloalkyl groups (C n -m) are those whose ring structure is composed of n until m carbon atoms are formed, where n and m are integers which are greater than 2. Unless otherwise defined, they are preferably monocyclic (C 3 -s) cycloalkyl groups.
- heterocycloalkyl describes cycloalkyl radicals whose closed chain contains one or more heteroatoms in addition to carbon atoms. These heteroatoms can be nitrogen, oxygen or sulfur atoms.
- the (Cn-m) heterocycloalkyl groups are those whose ring structure is formed from n to m atoms , where n and m are integers greater than 3. Unless otherwise defined, monocyclic (C. 8 ) and bicyclic (C 8 -n) heterocycloalkyl groups are preferred. Each ring can usually contain 1 to 4 heteroatoms The residue can be linked to the compound according to the invention via any carbon or heteroatom of the ring system which allows the formation of a stable bond.
- heterocycloalkyl radicals are pyrrolinyl, pyrrolidinyl, pyrazolinyl, pyrazolidinyl, piperidinyl, morpholinyl, thiomorpholinyl, piperazinyl, indolinyl, Azetidinyl, tetrahydropyranyl, tetrahydrothiopyranyl, tetr ahydrofuranyl, hexahydropyrimidinyl, hexahydropyridazinyl, dihydrooxazolyl, 1, 2-thiazinanyl-1, 1-dioxide, 1, 2,6-
- acyl describes both saturated and mono- or polyunsaturated radicals of aliphatic carboxylic acids which are formed by removing the OH group of the carboxy group.
- (C n -m) acyl groups are understood to mean those which contain n to m carbon atoms, where n and m stand for integers.
- saturated radicals are preferably (C ⁇ - ⁇ o) acyl groups
- unsaturated radicals are preferably (C 2 -i 2 ) acyl groups.
- acyl includes both straight-chain and also branched radicals. Straight chain radicals are preferred
- (C ⁇ - 8 ) acyl groups branched radicals preferably (C 3 - ⁇ o) acyl groups. Hydrogen atoms of these radicals can be partially or completely replaced by halogen atoms. Examples of these are the atoms of fluorine, chlorine, bromine and iodine. If all hydrogen atoms have been replaced by halogen atoms, the term "perhaloacyl" radical is used. Terms that consist of syllables or functional groups, the meaning of which is familiar from the specialist literature, and one or more of the syllables defined above, refer to radicals which are composed of the corresponding structural elements.
- alkyloxy and “alkylthio” denote alkyl groups which are bonded to a further structural element via an oxygen or sulfur atom.
- acylamino one of the hydrogen atoms of an amino group is replaced by an acyl group.
- both X and Y stand for a nitrogen atom.
- the radical A is unsubstituted or substituted by the radicals R 4 , R 5 and R 6, phenyl, pyridyl, pyrimidyl, pyridazinyl, pyrazinyl, imidazolyl, pyrazolyl, oxazolyl, isoxazolyl, furazanyl, thiazolyl, isothiazolyl, or pyrrolyl, wherein R 4 , R 5 and R 6 independently of one another for hydrogen (H), (C ⁇ . 8 ) alkyl, monofluoro (C ⁇ .
- radical A is a phenyl or pyridyl group substituted by 1 to 3 substituents.
- the radical R 1 has the meaning of amino, alkylamino, di (C ⁇ - 6) alkylamino, (C ⁇ .
- R 1 are especially those which have properties of an electron donor.
- Preferred radicals R 2 and R 3 are hydrogen, (C ⁇ - 6) AlkyI or (C 3 - 6) cycloalkyl.
- Preferred radicals R 4 , R 5 and R 6 are hydrogen, fluorine, chlorine, bromine, (C ⁇ - 3 ) alkyl, Fluoromethyl, difluoromethyl, trifluoromethyl, fluoromethyloxy, difluoromethyloxy, trifluoromethyloxy, and di (C ⁇ - 3 ) alkylamino.
- the invention also includes pharmaceutically suitable derivatives of the compounds of formula (I).
- a “pharmaceutically suitable derivative” is taken to mean salts and precursors of the compounds of the formula (I) which, after being administered to a patient, are converted directly or indirectly into one of the compounds according to the invention or one of their pharmacologically active metabolites Salts, acids and esters of the compounds according to the invention. Of particular importance are salts which are derived from pharmaceutically suitable inorganic or organic acids or bases.
- Examples are the salts with acids such as hydrochloric acid, hydrobromic acid, sulfuric acid, phosphoric acid, nitric acid, oxalic acid, malonic acid, fumaric acid , Maleic acid, tartaric acid, citric acid, ascorbic acid and methanesulfonic acid.
- acids such as hydrochloric acid, hydrobromic acid, sulfuric acid, phosphoric acid, nitric acid, oxalic acid, malonic acid, fumaric acid , Maleic acid, tartaric acid, citric acid, ascorbic acid and methanesulfonic acid.
- Precursors are compounds which, following simple chemical conversion, give compounds of formula (I) or one of their pharmacologically active metabolites.
- Simple chemical transformations include hydrolysis, oxidation and reduction which e.g. can be done enzymatically or metabolically.
- Compounds of this invention that have one or more asymmetric carbon atoms can exist as racemates or racemic mixtures, as isolated enantiomers, as diastereomeric mixtures, or as individual diastereomers.
- Each stereogenic carbon atom can be in the R or S configuration or in a combination of both configurations.
- Some of the compounds can also be in tautomeric forms.
- the compounds according to the invention can be prepared, for example, according to the following reaction scheme:
- a 3-oxo-propionic acid ester which can be prepared from the corresponding acetyl derivative and whose carbonyl group is bonded to the desired radical A is e.g. reacted with the salt of a primary amine such as N-methylammonium acetate to give the corresponding acrylic ester derivative. The latter is then reacted with the desired amino derivative of benzimidazole, benzoxazole or benzothiazole. The residue introduced by the primary amine is exchanged for the corresponding radical of the benzimidazole, benzoxazole or benzothiazole derivative.
- Phosphorus oxychloride are halogenated at this position before being in a last one Step is reacted with the desired amine to give a compound according to the invention.
- the intermediate products obtained after the individual process steps are, if necessary, purified.
- the compounds produced in this way are active substances of interest, in particular for the preparation of an analgesic for the relief or treatment of pain. This effect can be determined using a simple test procedure in which the pain reactions of animals are observed and quantitatively evaluated.
- the compounds according to the invention are operated as follows:
- mice Male rats (strain: Chbb-THOM; weight: 200 to 300 g) are injected with 20 ⁇ l of a 2% formaldehyde solution in the plantar region of the right hind paw. Immediately afterwards, the number of flinches (twitches of the affected hind paw) and the duration of the licking of the affected paw are recorded for one hour. After five minutes, the values are summarized into epochs and time-effect curves for the flinches and the licking are created from these values. Typically, two phases of formalin action (flinches, licking) are observed: a first phase from 0 to 10 minutes and a second phase from 10 to 60 minutes.
- the number of flinches and the duration of the leak decrease to zero for a short time (interphase).
- the areas under the curves for the first and second phases are determined from the time-effect curves.
- Five animals are usually used for control, placebo and substance dose.
- the results of the substance doses are compared with those of the control, and ED 50 values are determined therefrom.
- the ED 50 is the dose at which the control values are inhibited by 50%.
- the antinociceptive activity of the compounds of this invention is based on blocking voltage-dependent N-type calcium channels.
- the proof of this inhibitory effect is electrophysiologically using patch-clamp technique (see: Improved patch-clamp techniques for high resolution current recording from cells and cell-free membrane patches; Hamill et al .; Pflügers Archiv, 391. 1981, 85 - 100) on recombinant HEK 293 cells expressing the N-type calcium channel.
- patch-clamp technique see: Improved patch-clamp techniques for high resolution current recording from cells and cell-free membrane patches; Hamill et al .; Pflügers Archiv, 391. 1981, 85 - 100
- the compounds of Examples 4 and 6 showed IC 50 values of 3.6 and 2.0 / mol / L, respectively.
- the compounds according to the invention can thus be used in processes which serve to alleviate or treat pain, a patient being administered a therapeutically effective amount of the compound according to the invention.
- These can be acute pain, chronic pain, neuropathic pain or post-operative pain, as well as pain related to migraines, arthralgia, neuropathies, nerve injuries, diabetic neuropathy, neurodegeneration, neurotic skin diseases, stroke, bladder hypersensitivity, irritable bowel syndrome, Respiratory diseases such as asthma or chronic obstructive pulmonary disease, skin, eye or mucous membrane irritation, duodenal and gastric ulcers, stomach inflammation or other inflammatory diseases.
- the compounds according to the invention For the treatment of pain, it can be advantageous to combine the compounds according to the invention with invigorating substances such as caffeine or other pain-relieving active substances. If suitable active substances are available for treating the cause of the pain, these can be combined with the compounds according to the invention. If other medical treatments are indicated regardless of the pain treatment, for example for hypertension or diabetes, the active substances required for this can also be combined with the compounds according to the invention.
- the dose required to achieve an analgesic effect is expediently 0.01 to 3 mg / kg body weight, preferably 0.1 to 1 mg / kg, and 0.1 to 8 mg / kg body weight, preferably 0.5 to 3 mg / kg, respectively, in the case of intravenous administration 1 to 3 times a day.
- the compounds of the formula (I) prepared according to the invention optionally in combination with other active substances, together with one or more inert customary carriers and / or diluents, for example with corn starch, Milk sugar, cane sugar, microcrystalline cellulose, magnesium stearate, polyvinylpyrrolidone, citric acid, tartaric acid, water, water / ethanol, water / glycerin, water / sorbitol, water / polyethylene glycol, propylene glycol, cetylstearyl alcohol, carboxymethyl cellulose or fat-containing substances such as hard fat, or their suitable mixtures Work in galenical preparations such as tablets, coated tablets, capsules, powders, suspensions or suppositories.
- inert customary carriers and / or diluents for example with corn starch, Milk sugar, cane sugar, microcrystalline cellulose, magnesium stearate, polyvinylpyrrolidone, citric acid, tartaric acid, water, water /
- Example 1 3- ef ⁇ y / -9-mei' ⁇ y / am / ⁇ o-7- pyr / d / n-4-y / 3H- / m / / azo / 4 ? 5-f7c ⁇ / no /// 7
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Pain & Pain Management (AREA)
- Rheumatology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Abstract
Die Erfindung betrifft tricyclische heteroaromatische Verbindungen der allgemeinen Formel (I) und ihre Salze wobei die Strukturelemente X, Y, A, R1 und R2 in der Beschreibung definiert sind. Weiter betrifft die Erfindung die Herstellung dieser Verbindungen und ihre Verwendung als Arzneimittel, insbesondere als Schmerzmittel.
Description
Tricyclische Heteroaromatische Verbindungen
Die Erfindung betrifft tricyclische heteroaromatische Verbindungen und deren Salze, ihre Herstellung und ihre Verwendung als Arzneimittel, insbesondere als Schmerzmittel.
Akute Schmerzen, also kurzzeitige, vorübergehen Schmerzen, klingen in der Regel nach Beseitigung der Ursachen schnell wieder ab und verursachen allenfalls vernachlässigbare Schädigungen an Geweben. Daneben können Schmerzen aber auch längere Zeit andauern. Man spricht dann von einem chronischen Schmerz, der in der Regel mit Gewebsschädigungen, Entzündungen oder anderen Leiden verbunden ist. Erkrankungen, die von chronischem bzw. chronisch wiederkehrendem Schmerz begleitet werden, sind unter anderen Migräne, Neuralgien, Muskelschmerzen und Entzündungsschmerzen. Zu den chronisch neuronalen Schmerzen gehören u.a. postoperative Schmerzen, Gürtelrose, Phantomschmerz, diabetische Neuropathie, Schmerz nach chronischer Nervenkompression sowie Aids und Krebs im Finalstadium.
Man unterscheidet zwischen einem Erstschmerz, auch heller Schmerz bezeichnet, und einem Zweitschmerz, dem sogenannten dunklen oder dumpfen Schmerz. Dem Erstschmerz begegnet man als Sofortschmerz bei Verletzungen. Er wird mit hoher Geschwindigkeit (etwa 20 Meter pro Sekunde) zum Gehirn geleitet. Kommt es bei Verletzungen nicht zum Erstschmerz beobachtet man den Zweitschmerz. Er gelangt viel langsamer (etwa zwei Metern pro Sekunde) zum Gehirn, ist dafür aber beständiger und bleibt als dumpfer Schmerz über längere Zeit bestehen.
Für die Behandlung leichter Schmerzen oder Kopfschmerzen stehen Wirkstoffe wie Acetylsalicylsäure, Paracetamol oder Ibuprofen zur Verfügung. Besonders starke Schmerzen werden mit Opium-verwandten Mitteln wie Codein, Morphin oder ähnlichen Substanzen behandelt. Ihre Aufgabe besteht vor allem darin durch Unterdrückung der Schmerzen die Lebensqualität der Patienten zu erhöhen.
Opiate und Opioide wirken überwiegend im Zentralnervensystem. Neben ihrer schmerzhemmenden Wirkung können sie auch sedieren (beruhigen), euphorisierend wirken, das Atemzentrum hemmen und den Husten dämpfen. Zu ihnen zählen Substanzen wie Kodein, Morphin, Tilidin und Tramadol.
Nichtopioide Schmerzmittel wirken in der Regel im peripheren Nervensystem und sind auch fiebersenkend und entzündungshemmend. Häufig wird den Wirkstoffen ein zusätzlich belebender Stoff wie Koffein beigemischt. Beispiele für solche Schmerzmittel sind Doppel-Spalt, Eudorlin, Migränin, Neuralgin, Thomapyrin, Titralgan, und Vivimed.
Antagonisten eines Caicium Kanals vom N-Typ zur Behandlung und Verhütung von Schmerzen werden in den Internationalen Anmeldungen WO 02/36567, WO 02/36568 und WO 02/36569 beschrieben.
Die vorliegende Erfindung stellt neue Verbindungen und ihre Salze bereit, die zur Linderung von Schmerzen, insbesondere chronischen Schmerzen, geeignet sind. Diese Verbindungen werden durch die allgemeine Formel (I) beschrieben:
In dieser Formel (I) bedeuten
X ein Stickstoffatom (N), Sauerstoffatom (O) oder Schwefelatom (S);
Y ein Stickstoffatom, wenn X ein Sauerstoffatom oder Schwefelatom bedeutet;
Y ein Stickstoffatom mit einem gebundenen Rest R3 oder ein Schwefelatom oder ein Sauerstoffatom, wenn X ein Stickstoffatom bedeutet; A einen unsubstituierten oder substituierten mono-, di- oder tricyclischen aromatischen Rest, der entweder kein oder 1-3 Heteroatome ausgewählt aus der
Gruppe Stickstoff, Sauerstoff und Schwefel enthält, wobei wenigstens eines der
Heteroatome ein Stickstoffatom ist; R1 Hydroxy, Fluor, Chlor oder Brom, Amino, (Cι-6)Alkylamino, Di(Cι-6)alkylamino,
(C3-7)Cycloalkylamino, Di(C3-7)cycloalkylamino, (Cι-6)Alkyl-(C3-z)cycloalkylamino, sowie die Heterocycloalkylgruppierungen Acetidin-1-yl, Pyrrolidin-1-yl, Piperidin-
1-yl, Morpholin-4-yl, Thiomorpholin-4-yl, Thiomorpholin-S-oxid-4-yl,
Thiomorpholin-S-dioxid-4-yl, oder Hexamethylenimino; R2 und R3 unabhängig voneinander Wasserstoff (H), (C1-8)Alkyl oder (C3-7)Cycloalkyl; und
Der Begriff „Alkyl" beschreibt sowohl gesättigte als auch ein- oder mehrfach ungesättigte aliphatische Kohlenwasserstoff Radikale. Unter (Cn-m)Alkylgruppen werden solche verstanden, die n bis m Kohlenstoffatome enthalten, wobei n und m ganze Zahlen darstellen. Wenn nicht anders definiert handelt es sich bei gesättigten Radikalen vorzugsweise um (Cι-ι0)Alkylgruppierungen, bei ungesättigte vorzugsweise um (C2-i2)Alkylgruppen.
Gleichzeitig umfasst der Begriff „Alkyl" sowohl geradkettige als auch verzweigte Kohlenwasserstoff Radikale. Wenn nicht anders definiert sind geradkettige Radikale vorzugsweise (Cι-8)Alkylgruppierungen, verzweigte Radikale vorzugsweise (C3-ιo)Alkylgruppen.
Wasserstoffatome von Alkylradikalen können teilweise oder vollständig durch Halogenatome ersetzt sein. Beispiele für solche Halogenatome sind die Atome von Fluor, Chlor, Brom und Jod. Sind alle Wasserstoffatome durch Halogene ersetzt, so wird auch von einem „Perhalogen Alkyl" Radikal gesprochen.
Unter dem Begriff „Cycloalkyl" werden gesättigte und ein- oder mehrfach ungesättigte aliphatische Kohlenwasserstoff Radikale zusammengefasst, die zyklische, d.h. ringförmig geschlossene Kohlenstoffketten bilden, welche kein aromatisches Ringsystem darstellen. Als (Cn-m)Cycloalkylgruppen werden solche bezeichnet, deren Ringstruktur von n bis m Kohlenstoffatomen gebildet wird, wobei n und m ganze Zahlen bedeuten, die grösser als 2 sind. Wenn nicht anders definiert handelt es sich bevorzugt um monocyclische (C3-s)Cycloalkylgruppierungen.
Der Begriff „Heterocycloalkyl" beschreibt Cycloalkyl Radikale deren geschlossene Kette neben Kohlenstoffatomen ein oder mehrere Heteroatome enthält. Diese Heteroatome können Stickstoff-, Sauerstoff- oder Schwefelatome sein. Als (Cn-m)Heterocycloalkylgruppen werden solche bezeichnet, deren Ringstruktur von n bis m Atomen gebildet wird, wobei n und m ganze Zahlen bedeuten, die grösser als 3 sind. Wenn nicht anders definiert sind monocylische (C .8)- und bicyclische (C8-n)Heterocycloalkylgruppierungen bevorzugt. Jeder Ring kann üblicherweise 1 bis 4 Heteroatome enthalten. Die Anknüpfung des Rests an die erfindungsgemässe Verbindung kann über jedes Kohlenstoff oder Heteroatom des Ringsystems erfolgen, das die Ausbildung einer stabilen Bindung erlaubt. Beispiele für „Heterocycloalkyl" Radikale sind Pyrrolinyl, Pyrrolidinyl, Pyrazolinyl, Pyrazolidinyl, Piperidinyl, Morpholinyl, Thiomorpholinyl, Piperazinyl, Indolinyl, Azetidinyl, Tetrahydropyranyl, Tetrahydrothiopyranyl, Tetrahydrofuranyl, Hexahydropyrimidinyl, Hexahydropyridazinyl, Dihydrooxazolyl, 1 ,2-thiazinanyl-1 ,1-dioxid, 1 ,2,6-
Thiadiazinanyl-1 ,1-dioxid, lsothiazolidinyl-1 ,1 -dioxid und lmidazolidinyl-2,4-dion.
Der Begriff „Acyl" beschreibt sowohl gesättigte als auch ein- oder mehrfach ungesättigte Radikale aliphatischer Carbonsäuren, die durch Entfernung der OH- Gruppe der Carboxygruppe entstehen. Unter (Cn-m)Acylgruppen werden solche verstanden, die n bis m Kohlenstoffatome enthalten, wobei n und m für ganze Zahlen stehen. Wenn nicht anders definiert handelt es sich bei gesättigten Radikalen vorzugsweise um (Cι-ιo)Acylgruppierungen, bei ungesättigte vorzugsweise um (C2-i2)Acylgruppen. Gleichzeitig umfasst der Begriff „Acyl" sowohl geradkettige als auch verzweigte Radikale. Geradkettige Radikale sind vorzugsweise
(Cι-8)Acylgruppierungen, verzweigte Radikale vorzugsweise (C3-ιo)Acylgruppen. Wasserstoffatome dieser Radikale können teilweise oder vollständig durch Halogenatome ersetzt sein. Beispiele hierfür sind die Atome des Fluor, Chlor, Brom und Jod. Sind alle Wasserstoffatome durch Halogenatome ersetzt, so wird von einem „PerhalogenAcyl" Radikal gesprochen.
Begriffe, die sich aus Silben bzw. funktioneilen Gruppen, deren Bedeutung aus der Fachliteratur geläufig ist, sowie einer oder mehreren der oben definierten Silben zusammensetzen, beziehen sich auf Radikale, die aus den entsprechenden Strukturelementen aufgebaut sind. So bezeichnen die Begriffe „Alkyloxy" und „Alkylthio" Alkylgruppierungen, die über ein Sauerstoff- bzw. Schwefelatom an ein weiteres Strukturelement gebunden sind. Ein „Alkylcarbonyl" Radikal stellt eine Alkylgruppe dar, die über eine Carbonylgruppe (C=O) an ein anderes Strukturelement gebunden ist. In einer „Acylamino" Gruppe wird eines der Wasserstoffatome einer Aminogruppe durch eine Acylgruppe ersetzt.
In ausgewählten Ausführungsformen der erfindungsgemässen Verbindung stehen sowohl X als auch Y für ein Stickstoffatom.
In anderen Ausführungsformen steht.der Rest A für unsubstituiertes oder mit den Resten R4, R5 und R6 substituiertes Phenyl, Pyridyl, Pyrimidyl, Pyridazinyl, Pyrazinyl, Imidazolyl, Pyrazolyl, Oxazolyl, Isoxazolyl, Furazanyl, Thiazolyl, Isothiazolyl, oder Pyrrolyl, worin R4, R5 und R6 unabhängig voneinander für Wasserstoff (H), (Cι.8)Alkyl, Monofluor(Cι.5)alkyl, Difluor(C1-5)alkyl, Trifluor(Cι-5)alkyl, (C3-7)Cycloalkyl, Hydroxy,
Fluormethyloxy, Difluormethyloxy, Trifluormethyloxy, (C3-6)Cycloalkyloxy, Fluor, Chor, Brom, Carboxy, (C-ι-6)Alkoxycarbonyl, Amino, (Cι-6)Alkylamino, Di(Cι-6)alkylamino, Acetidin-1-yl, Pyrrolidin-1-yl, Piperidin-1-yl, (Cι-4)Acylamino, (C1-6)Alkyl-(Cι.4)Acylamino, Aminocarbonyl, (Cι.6)Alkylaminocarbonyl, Di(Cι-6)alkylaminocarbonyl, Acetidin-1 -yl-carbonyl, Pyrrolidin-1-yl-carbonyl, oder Piperidin-1 -yl-carbonyl stehen. Als Rest A bevorzugt ist eine mit 1 bis 3 Substituenten substituierte Phenyl- oder Pyridyl-Gruppierung. In wieder anderen Ausführungsformen hat der Rest R1 die Bedeutung Amino, (Cι.6)Alkylamino, Di(Cι-6)alkylamino, (C3-7)Cycloalkylamino, Di(C3-7)cycloalkylamino oder (Cι-6)Alkyl-(C3-7)cycloalkylamino. Bevorzugte Reste von R1 sind vor allem solche, die Eigenschaften eines Elektronendonors besitzen. Bevorzugte Reste R2 und R3 sind Wasserstoff, (Cι-6)AlkyI oder (C3-6)Cycloalkyl. Bevorzugte Reste R4, R5 und R6 sind Wasserstoff, Fluor, Chlor, Brom, (Cι-3)Alkyl,
Fluormethyl, Difluormethyl, Trifluormethyl, Fluormethyloxy, Difluormethyloxy, Trifluormethyloxy, und Di(Cι-3)alkylamino.
Die Erfindung schliesst auch pharmazeutisch geeignete Derivate der Verbindungen von Formel (I) mit ein. Unter einem „pharmazeutisch geeigneten Derivat" werden Salze und Vorstufen der Verbindungen von Formel (I) verstanden, die nach Darreichung an einen Patienten, direkt oder indirekt in eine der erfindungsgemässen Verbindungen oder einen ihrer pharmakologisch aktiven Metaboliten umgewandelt werden. Es handelt sich vor allem um Salze, Säuren und Ester der erfindungsgemässen Verbindungen. Von besonderer Bedeutung sind Salze, die sich von pharmazeutisch geeigneten anorganischen oder organischen Säuren oder Basen ableiten. Beispiele sind die Salze mit Säuren wie Salzsäure, Bromwasserstoffsäure, Schwefelsäure, Phosphorsäure, Salpetersäure, Oxalsäure, Malonsäure, Fumarsäure, Maleinsäure, Weinsäure, Zitronensäure, Ascorbinsäure und Methansulfonsäure.
Vorstufen sind Verbindungen, die im Anschluss an eine einfache chemische Umwandlung Verbindungen der Formel (I) oder eines ihrer pharmakologisch aktiven Metaboliten ergeben. Einfache chemische Umwandlungen umfassen Hydrolyse, Oxidation und Reduktion die z.B. enzymatisch oder metabolisch erfolgen können. Für die vorliegende Erfindung bedeutet dies, dass die Darreichung einer Vorstufe der erfindungsgemässen Verbindungen an einen Patienten zur Umwandlung dieser Vorstufe in eine Verbindung der Formel (I) führt, die dann den gewünschten pharmakologischen Effekt hervorruft.
Verbindungen dieser Erfindung, die ein oder mehrere asymmetrische Kohlenstoffatome besitzen, können als Racemate oder racemische Mischungen vorliegen, als isolierte Enantiomere, als diastereomere Mischungen oder als individuelle Diastereomere. Jedes stereogene Kohlenstoffatom kann in der R oder S Konfiguration oder in der Kombination beider Konfigurationen vorliegen. Einige der Verbindungen können auch in tautomerer Formen vorliegen.
Die erfindungsgemässen Verbindungen können beispielsweise nach folgendem Reaktionsschema hergestellt werden:
a .COO-Alkyl
Ein aus dem entsprechenden Acetylderivat herstellbarer 3-oxo-propionsäureester, dessen Carbonylgruppe an den gewünschten Rest A gebunden ist, wird z.B. mit dem Salz eines primären Amins wie N-Methlyammonium-acetat zum entsprechenden Acrylsäureesterderivat umgesetzt. Letzteres wird dann mit dem gewünschten Aminoderivat des Benzimidazols, Benzoxazols oder Benzthiazols umgesetzt. Dabei wird der durch das primäre Amin eingeführte Rest gegen das entsprechende Radikal des Benzimidazol-, Benzoxazol- oder Benzthiazolderivates ausgetauscht. Anschliessend führt man durch Erhitzen in einem geeigneten Lösungsmittel einen Ringschluss zum entsprechenden Derivat des 3H-imidazo[4,5-f]chinolins, 3H- oxazo[4,5-f]chinolins oder 3H-thiazo[4,5-f]chinolins herbei. Die erhaltene Verbindung ist an Position 9 hydroxyliert und kann mit Hilfe von Verbindungen wie
Phorphoroxychlorid an dieser Position halogeniert werden bevor sie in einem letzen
Schritt mit dem gewünschten Amin zu einer erfindungsgemässen Verbindung umgesetzt wird. Die nach den einzelnen Verfahrensschritten erhaltenen Zwischenprodukte werden, falls nötig, aufgereinigt.
Die so hergestellten Verbindungen sind als Arzneimittel Wirkstoffe von Interesse, insbesondere zur Herstellung eines Analgetikums zur Linderung bzw. Behandlung von Schmerzen. Diese Wirkung lässt sich anhand eines einfachen Testverfahrens ermitteln, in dem man die Schmerzreaktionen von Tieren beobachtet und quantitativ auswertet. Hierzu wird mit den erfindungsgemäßen Verbindungen wie folgt verfahren:
Männlichen Ratten (Stamm: Chbb-THOM; Gewicht: 200 bis 300 g) werden 20 μl einer 2%igen Formaldehyd-Lösung in die Plantarregion der rechten Hinterpfote injiziert. Unmittelbar danach werden eine Stunde lang die Anzahl der Flinches (Zuckungen der betroffenen Hinterpfote) und die Dauer des Leckens der betroffenen Pfote registriert. Nach jeweils fünf Minuten werden die Werte zu Epochen zusammengefasst und aus diesen Werten Zeit-Wirkungs-Kurven für die Flinches und das Lecken erstellt. Typischerweise werden dabei zwei Phasen der Formalin- Wirkung (Flinches, Lecken) beobachtet: Eine erste Phase von 0 bis 10 Minuten und eine zweite Phase von 10 bis 60 Minuten. Nach der ersten Phase sinken Anzahl der Flinches und Dauer des Leckens für eine kurze Zeit gegen Null (Interphase). Aus den Zeit-Wirkungs-Kurven werden die Flächen unter den Kurven für die erste und die zweite Phase ermittelt. Für die Kontrolle, Placebogabe und Substanzdosis werden üblicherweise jeweils fünf Tiere eingesetzt. Die Ergebnisse der Substanzdosen werden mit denen der Kontrolle verglichen, und daraus werden ED50-Werte ermittelt. Die ED50 ist die Dosis, bei der die Kontrollwerte um 50% gehemmt sind.
Die antinocizeptive Wirkung der Verbindungen dieser Erfindung beruht auf einer Blockade von spannungsabhängigen N-Typ Kalziumkanälen. Der Nachweis dieser inhibierenden Wirkung wird elektrophysiologisch mittels Patch-Clamp Technik (siehe: Improved patch-clamp techniques for high resolution current recording from cells and cell-free membrane patches ; Hamill et al.; Pflügers Archiv, 391. 1981, 85 - 100) an rekombinanten HEK 293-Zellen, die den N-Typ Kalziumkanal exprimieren, geführt.
So zeigten bei diesen Untersuchungen beispielsweise die Verbindungen der Beispiele 4 und 6 IC50 - Werte von 3.6 bzw. 2.0 /Mol/L.
Somit können die erfindungsgemässen Verbindungen in Verfahren Verwendung finden, die der Linderung oder Behandlung von Schmerzen dienen, wobei einem Patienten eine therapeutisch wirksame Menge der erfindungsgemässen Verbindung dargereicht wird. Dabei kann es sich um akute Schmerzen handeln, um chronische Schmerzen, neuropathische Schmerzen oder post-operative Schmerzen, sowie um Schmerzen in Zusammenhang mit Migräne, Arthralgie, Neuropathien, Nervenverletzungen, diabetischer Neuropathie, Neurodegeneration, neurotischen Hautkrankheiten, Schlaganfall, Harnblasen Übersensitivität, Reizdarm, Atemwegserkrankungen wie Asthma oder chronischer obstruktiver Lungenerkrankung, Irritationen der Haut, Augen oder Schleimhäute, Zwölffingerdarm- und Magengeschwüren, Magenentzündung oder anderen Entzündungserkrankungen.
Zur Behandlung von Schmerzen kann es vorteilhaft sein, die erfindungsgemässen Verbindungen mit belebenden Stoffen wie Koffein oder anderen schmerzlindernden Wirkstoffen zu kombinieren. Stehen zur Behandlung der Ursache der Schmerzen geeignete Wirkstoffe zur Verfügung, so können diese mit den erfindungsgemässen Verbindungen kombiniert werden. Sind unabhängig von der Schmerzbehandlung auch noch weitere medizinische Behandlungen angezeigt, zum Beispiel gegen Bluthochdruck oder Diabetes, so können auch die dafür nötigen Wirkstoffe mit den erfindungsgemässen Verbindungen kombiniert werden.
Die zur Erzielung einer schmerzstillenden Wirkung erforderliche Dosierung beträgt bei intravenöser Gabe zweckmäßigerweise 0.01 bis 3 mg/kg Körpergewicht, vorzugsweise 0.1 bis 1 mg/kg, und bei oraler Gabe 0.1 bis 8 mg/kg Körpergewicht, vorzugsweise 0.5 bis 3 mg/kg, jeweils 1 bis 3 x täglich. Hierzu lassen sich die erfindungsgemäß hergestellten Verbindungen der Formel (I), gegebenenfalls in Kombination mit anderen Wirksubstanzen, zusammen mit einem oder mehreren inerten üblichen Trägerstoffen und/oder Verdünnungsmitteln, z.B. mit Maisstärke,
Milchzucker, Rohrzucker, mikrokristalliner Zellulose, Magnesiumstearat, Polyvinylpyrrolidon, Zitronensäure, Weinsäure, Wasser, Wasser/Ethanol, Wasser/Glycerin, Wasser/Sorbit, Wasser/Polyethylenglykol, Propylenglykol, Cetylstearylalkohol, Carboxymethylcellulose oder fetthaltigen Substanzen wie Hartfett oder deren geeigneten Gemischen, in übliche galenische Zubereitungen wie Tabletten, Dragees, Kapseln, Pulver, Suspensionen oder Zäpfchen einarbeiten.
Erfindungsgemäße Verbindungen werden in den nachfolgenden Beispielen beschrieben. Dem Fachmann ist bewusst, dass diese Beispiele der Veranschaulichung des Erfindungsgegenstandes dienen und nicht der Beschränkung der dargestellten allgemeinen technischen Lehre der Erfindung.
Beispiele
Beispiel 1 : 3- efΛy/-9-mei'Λy/am/πo-7- pyr/d/n-4-y/ 3H-/m/ /azo/4?5-f7cή/no///7
1a. 3-Methylamino-3-foyridin-4-yl)-acrylsäureethylester
Eine Lösung von 17.2g (89 mMol) 3-Oxo-3-(pyridin-4-yl)-propionsäureethylester und 41.0g (450 mMol) N-Methylammonium-acetat in 120 ml Ethanol werden eine Stunde zum Rückfluss erhitzt, danach das Lösungsmittel abgedampft. Der Rückstand wird in
ca. 300 ml Dichlormethan gelöst, diese Lösung zweimal mit ca. 100 ml Wasser gewaschen, über Natriumsulfat getrocknet und dann eingedampft. Das so erhaltene Produkt wird ohne weitere Reinigung weiterverarbeitet. .
Ausbeute: 98% der Theorie. CnH14N202 (206.25)
RrWert: 0.40 (Kieselgel, Petrolether/Essigsäureethylester 1 : 1) Massenspektrum: (M+H)+ = 207 (M-H)~ = 205
1 b. 3-(1 -Methyl-1 -/-benzimidazol-5-yl-amino)-3-(pyridin-4-vπ-acrylsäureethylester
Eine Lösung von 619mg (3.0 mMol) 3-Methylamino-3-(pyridin-4-yl)- acrylsäureethylester und 442mg (3.0 mMol) 5-Amino-1-methyl-benzimidazol in einer Mischung aus 36 ml Dichlormethan und 4 ml Ethanol wird ca. 20 Stunden unter Rückfluss erhitzt. Danach wird zur Trockne eingeengt und das so erhaltene Rohprodukt durch Säulenchromatographie (Kieselgel; Elutionsmittel: Dichlormethan mit 2-5% Ethanol) gereinigt.
Ausbeute: 26% der Theorie. Cι8H18N402 (322.37) RrWert: 0.22 (Kieselgel, Dichlormethan/Ethanol 19 : 1)
1c. 9-Hvdroxy-3-methyl-7-(pyridin-4-yl)-3ry-imidazor4.5-flchinolin
Zu 20 ml Dowtherm (Sigma-Aldrich Chemie GmbH, D-82024 Taufkirchen, Germany), das unter Rühren auf 250°C erhitzt wurde, werden 1.7g (5.27 mMol) 3-(1-Methyl-1 H- benzimidazol-5-yl-amino)-3-(pyridin-4-yl)-acryIsäureethylester portionsweise zugegeben und eine weitere Stunde bei 250°C gerührt. Das Gemisch wird dann auf Raumtemperatur abgekühlt, mit ca. 30 ml Petrolether verdünnt, das ausgefallene Produkt abfiltriert, mit ca. 30 ml Petrolether nachgewaschen und getrocknet.
Ausbeute: 82% der Theorie.
Cι6H12N4O (276.30)
RrWert: 0.13 (Kieselgel; Dichlörmethan/Ethanol 9 : 1)
Massenspektrum: (M+H)+ = 277 (M-H)" = 275 1H-NMR-Spektrum (d6-DMSO): δ = 3.95 (s, 3H); 6.42 (s, 1 H); 7.90 (d, 2H); 8.03 (s,
1 H); 8.30 (s, 1 H); 8.47 (s, 1 H); 8.81 (d, 2H); 11.77 (s, 1 H) ppm.
1d. 9-Chlor-3-methyl-7-(pyridin-4-yl)-3H-imidazor4.5-f1chinolin
1.2g (276 mMol) 9-Hydroxy-3-methyl-7-(pyridin-4-yl)-3H-imidazo[4,5-f]chinolin werden in 15 ml Phosphoroxychlorid eine Stunde bei 50°C gerührt. Dann wird das Phosphoroxychlorid im Vakuum abdestilliert und der Rückstand mit gesättigter
Natriumhydrogencarbonat-Lösung neutralisiert. Der ausgefallene Feststoff wird abgesaugt, in einer Mischung aus Dichlormethan und Ethanol (9 : 1 ) gelöst, die Lösung filtriert und erneut eingeengt. Man erhält das Produkt so als kristallinen Feststoff.
Ausbeute: 23% der Theorie.
Cι6HnCIN4 (294.75)
RrWert: 0.59 (Kieselgel; Dichlormethan/Ethanol 9 : 1 )
1H-NMR-Spektrum (d6-DMSO): δ = 4.04 (s, 3H); 8.31 (d, 2H); 8.36 (s, 1 H); 8.48 (s,
1 H); 8.50 (s, 1 H); 8.16 (s, 1 H); 8.80 (d, 2H) ppm.
1 e. 3-Methyl-9-methylamino-7-(pyridin-4-vO-3H-imidazor4,5-f1chinolin
Eine 33%ige Lösung von Methylamin in Ethanol (3 ml) wird mit 15 ml Ethanol verdünnt, dann werden 270 mg (0.92 mMol) 9-Chlor-3-methyl-7-(pyridin-4-yl)-3H- imidazo[4,5-f]chinolin hinzugefügt und dieses Gemisch 6 Stunden in einer Roth- Bombe auf 120°C erhitzt. Es wird dann bis zur Trockne eingedampft und das so erhaltene Rohprodukt durch Säulenchromatographie (Kieselgel; Elutionsmittel: Dichlormethan mit 2 - 7% Ethanol) gereinigt.
Ausbeute: 17% der Theorie. Cι7Hι5N5 (289.34)
Rf-Wert: 0.51 (Kieselgel; Dichlormethan/Ethanol 9 : 1)
1 H-NMR-Spektrum (d6-DMSO): δ = 3.20 (d, 3H); 4.02 (s, 3H); 7.20 (s, 1 H); 7.82 (d, 1 H); 7.99 (d, 1 H); 8.20 (d, 2H); 8.46 (s, 1 H); 8.72 (d, 2H); 8.92 (s, 1 H) ppm.
Beispiel 2: 7-(3-Fluσrphenyl)-3-methyl-9-methylamino-3H- imidazo[4,5-f]chinolin
Wird analog zu Beispiel 1 hergestellt, wobei im letzten Verfahrenschritt 1e 9-Chlor-7- (3-fluorphenyl)-3-methyl-3H-imidazo[4,5-f]chinolin in ethanolischer Methylamin- Lösung umgesetzt wird.
Ausbeute: 41% der Theorie.
Cι8H15FN4 (306.35)
Massenspektrum: (M+H)+ = 307
1H-NMR-Spektrum (d6-DMSO): δ = 3.20 (d, 3H); 4.01 (s, 3H); 7.12 (s, 1 H); 7.28 (dt,
1 H); 7.55 (q, 1 H); 7.80 (d, 1 H); 7.92 (d, 1 H); 8.08 (dt, 1 H); 8.12 (d, 1 H), 8.41 (s, 1 H);
8.73 (q, 1 H) ppm.
IC50-Wert: 15.2 vM
Beispiel 3: 9-Dimethylamino-7-(3~fluorphenyl)-3-methyl-3H- imidazo[4,5-fjchinolin
Wird analog zu Beispiel 1 hergestellt, wobei in Verfahrensschritt 1 e 9-Chlor-7-(3- fluorphenyl)-3-methyl-3H-imidazo[4,5-f]chinolin in ethanolischer Dimethylamin- Lösung umgesetzt wird.
Ausbeute: 25% der Theorie.
C19H17FN4 (320.37)
Massenspektrum: (M+H)+ = 321
1H-NMR-Spektrum (d6-DMSO): δ = 3.08 (s, 6H); 3.99 (s, 3H); 7.30 (dt, 1 H); 7.50 (s,
1 H); 7.58 (q, 1 H); 7.90 (d, 1 H); 7.99 (d, 1 H); 8.05 - 8.12 (m, 2H); 8.33 (s, 1 H) ppm.
IC5o-Wert: biphasisch
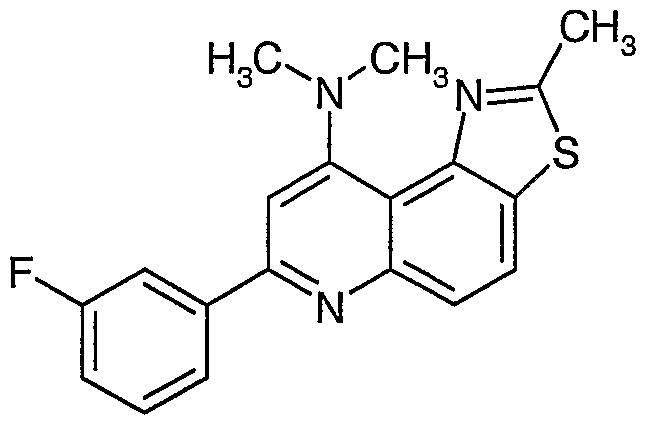
Beispiel 4: 9-Dimethylamino-7-(3-fluorphenyl)-2-methyl-thiazolo[4,5-f]chinolin
Wird analog zu Beispiel 1 hergestellt, wobei in Verfahrensschritt 1e 9-Chlor-7-(3- fluorphenyl)-2-methyl-thiazolo[4,5-f]chinolin in ethanolischer Dimethylamin-Lösung umgesetzt wird.
Ausbeute: 36% der Theorie.
Cι9H16FN3S (337.42)
Massenspektrum: (M+H)+ = 338
1 H-NMR-Spektrum (d6-DMSO): δ = 2.92 (s, 3H); 3.05 (s, 6H); 7.32 (dt, 1 H); 7.51 (s,
1H); 7.59 (q, 1 H); 7.95 (d, 1 H); 8.05 - 8.15 (m, 2H); 8.30 (d, 1 H) ppm.
Beispi el 5 : 9-Dimethylamino-7-(3-fluorphenyl)-thiazolo[5,4-f]chinolϊn
Wird analog zu Beispiel 1 hergestellt, wobei in Verfahrensschritt 1 e 9-Chlor-7-(3- fluorphenyl)-thiazolo[5,4-f]chinolin in ethanolischer Dimethylamin-Lösung umgesetzt wird.
Ausbeute: 52% der Theorie.
Cι8H14FN3S (323.39)
Massenspektrum: (M+H)+ = 324
1H-NMR-Spektrum (d6-DMSO): δ = 2.91 (s, 6H); 7.36 (dt, 1H); 7.61 (q, 1 H); 8.02 (s,
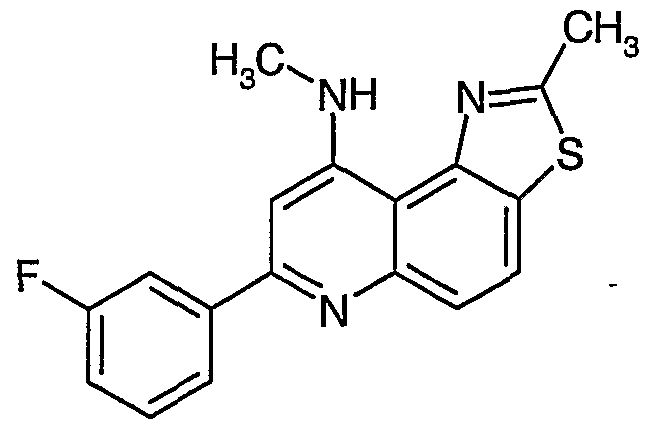
Beispiel 6: 7-(3-Fluorphenyl)-2-methyl-9~methylamino thiazolo[4,5-f]chinolin
Wird analog zu Beispiel 1 hergestellt, wobei in Verfahrensschritt 1e 9-Chlor-7-(3- fluorphenyl)-2-methyl-thiazolo[4,5-f]chinolin in ethanolischer Methylamin-Lösung umgesetzt wird.
Ausbeute: 56% der Theorie.
C18H14FN3S (323.39)
RrWert: 0.48 (Kieselgel; Dichlormethan/Methanol 9 : 1)
Massenspektrum: (M+H)+ = 324
1H-NMR-Spektrum (d6-DMSO): δ = 2.97 (s, 3H); 3.18 (d, 3H), 7.14 (s, 1 H); 7.30 (dt,
1 H); 7.57 (q, 1 H); 7.88 (d, 1 H); 8.05 - 8.15 (m, 2H); 8.23 (d, 1 H); 9.13 (q, 1 H) ppm.
IC50-Wert: 2.0//M
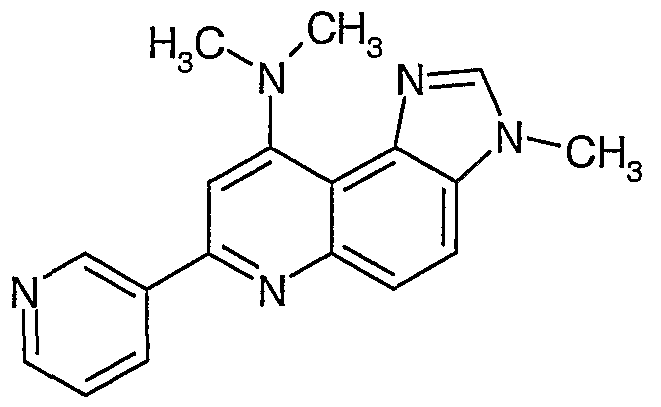
Beispiel 7: 9-Dimethylamino-3~methyl-7-(pyridin-3-yI)~3H-imidazo[4,5- fjchinolin
Wird analog zu Beispiel 1 hergestellt, wobei in Verfahrensschritt 1 e 9-Chlor-3-methyl- 3H-7-(pyridin-3-yl)-imidazo[4,5-f]chinolin in ethanolischer Dimethylamin-Lösung umgesetzt wird.
Ausbeute: 7.6% der Theorie. C18H17N5 (303.37) Massenspektrum: M+ = 303 (M+H)+ = 304
Beispiel 8: 3-Methyl-9'methylamino-7-(pyπdin-3-yl)-3H'imidazo[4,5-f]chinolin
Wird analog zu Beispiel 1 hergestellt, wobei in Verfahrensschritt 1 e 9-Chlor-3-methyl- 7-(pyridin-3-yl)-3H-imidazo[4,5-f]chinolin in ethanolischer Methylamin-Lösung umgesetzt wird.
Ausbeute: 15% der Theorie.
C17H15N5 (289.34)
Massenspektrum: (M+H)+ = 290
1H-NMR-Spektrum (d6-DMSO): δ = 3.20 (d, 3H); 4.01 (s, 3H); 7.15 (s, 1 H); 7.53 (m,
1 H); 7.81 (d, 1 H); 7.94 (d, 1 H); 8.41 (s, 1 H); 8.58 (dt, 1 H); 8.14 (d, 1 H); 8.80 (m, 1 H);
9.41 (s, 1 H) ppm.
Beispiel 9: 2-Methyl-9~methylamino-7-(pyridin-3-yl)-thiazolo[4,5-f]chinolin
Wird analog zu Beispiel 1 hergestellt, wobei in Verfahrensschritt 1e 9-Chlor-2-methyl- 7-(pyridin-3-yl)-thiazolo[4,5-f]chinolin in ethanolischer Methylamin-Lösung umgesetzt wird.
Ausbeute: 19% der Theorie.
C17H14N4S (306.37)
Massenspektrum: (M+H)+ = 307
1 H-NMR-Spektrum "(de-DMSO): δ = 2.99 (s, 3H); 3.20 (d, 3H); 7.20 (s,1H); 7.54 (m,
1H); 7.90 (d, 1H); 8.27 (d, 1H); 8.60 (dt, 1H); 8.65 (d, 1H); 9.20 (m, 1H); 9.42 (s, 1H) ppm.
Beispiel 10: 9-Di ethylamino-2-methyl-7-(pyridin-3-yl)-thiazolo[4,5- hinolin
Wird analog zu Beispiel 1 hergestellt, wobei in Verfahrensschritt 1e 9-Chlor-2-methyl- 7-(pyridin-3-yl)-thiazolo[4,5-f]chinolin in ethanolischer Dimethylamin-Lösung umgesetzt wird.
Ausbeute: 14% der Theorie.
C18Hι6N4S (320.42)
Massenspektrum: (M+H)+ = 321
1H-NMR-Spektrum (d6-DMSO): δ = 2.92 (s, 3H); 3.05 (s, 6H); 7.05 (s, 1H); 7.08 (m,
1H); 7.96 (d, 1H); 8.31 (d, 1H); 8.61 (dt, 1H); 8.68 (m, 1H); 9.43 (s, 1H) ppm.
Claims
1. Verbindung der allgemeinen Formel (I) und ihre Salze,
worin die Elemente X, Y, A, R1, R2 und R3 bedeuten:
X ein Stickstof atom (N), Sauerstoffatom (O) oder Schwefelatom (S); Y ein Stickstoffatom, wenn X ein Sauerstoffatom oder Schwefelatom bedeutet; Y ein Stickstoffatom mit einem gebundenen Rest R3 oder ein. Schwefelatom oder ein Sauerstoffatom, wenn X ein Stickstoffatom bedeutet; A einen unsubstituierten oder substituierten mono-, di- oder tricyclischen aromatischen Rest, der entweder kein oder 1-3 Heteroatome ausgewählt aus der Gruppe Stickstoff, Sauerstoff und Schwefel enthält, wobei wenigstens eines der Heteroatome ein Stickstoffatom ist;
R1 Hydroxy, Fluor, Chlor oder Brom, Amino, (Cι-6)Alkylamino,
Di(Cι-6)alkylamino, (C3-7)Cycloalkylamino, Di(C3-7)cycloalkylamino, (Cι-6)Alkyl-(C3.7)cycloalkylamino, Acetidin-1 -yl, Pyrrolidin-1-yl, Pyrrolin-1-yl, lmidazolidin-1-yl, lmidazolin-1-yl, Pyrazolidin-1-yl, Pyrazolin-1-yl, Piperidin- 1-yl, Piperazin-1-yl, Morpholin-4-yl, Thiomorpholin-4-yl, Thiomorpholin-S- oxid-4-yl, Thiomorpholin-S-dioxid-4-yl, oder Hexamethylenimino; und R2 und R3 unabhängig voneinander Wasserstoff, (Cι-s)Alkyl, oder (C3-7)Cycloalkyl.
2. Die Verbindung von Anspruch 1 , dadurch gekennzeichnet dass der Rest A unsubstituiertes oder mit den Resten R4, R5 und R6 substituiertes Phenyl, Pyridyl, Pyrimidyl, Pyridazinyl, Pyrazinyl, Imidazolyl, Pyrazolyl, Oxazolyl, Isoxazolyl, Furazanyl, Thiazolyl, Isothiazolyl, oder Pyrrolyl bedeutet, worin R4, R5 und R6 unabhängig voneinander für Wasserstoff, (Cι.8)Alkyl, Monofluor(Cι-5)alkyl, Difluor(Cι-5)alkyl, Trifluor(Cι-5)alkyl, (C3-7)Cycloalkyl, Hydroxy, Fluormethyloxy, Difluormethyloxy, Trifluormethyloxy, (C3-e)Cycloalkyloxy, Fluor, Chor, Brom, Carboxy, (Cι-6)Alkoxycarbonyl, Amino, (Cι-6)Alkylamino, Di(C1-6)alkylamino, Acetidin-1-yl, Pyrrolidin-1-yl, Piperidin-1-yl, (Cι-4)Acylamino, (Cι-6)Alkyl-(Cι-4)Acylamino, Aminocarbonyl, (Cι-e)Alkylaminocarbonyl, Di(Cι-6)alkylaminocarbonyl, Acetidin-1 -yl-carbonyl, Pyrrolidin-1 -yl-carbonyl oder Piperidin-1 -yl-carbonyl stehen.
3. Die Verbindung von Anspruch 2, dadurch gekennzeichnet dass der Rest A Pyridyl oder Fluorphenyl bedeutet.
4. Die Verbindung von Anspruch 1 , dadurch gekennzeichnet dass dem Rest R1 die Bedeutung Amino, Methylamino oder Dimethylamino zukommt.
5. Die Verbindung von Anspruch 1 , dadurch gekennzeichnet dass der Rest R2 für Methyl steht.
6. Die Verbindung von Anspruch 1 , dadurch gekennzeichnet dass der Rest R3 für Methyl steht.
7. Verbindung von Anspruch 1 ausgewählt aus der Gruppe der Verbindungen
3-Methyl-9-methylamino-7-(pyridin-4-yl)-3H-imidazo[4,5-f]chinolin; 7-(3-Fluorphenyl)-3-methyl-9-methylamino-3H-imidazo[4,5-f]chinolin;
9-Dimethylamino-7-(3-fluorphenyl)-3-methyl-3H-imidazo[4,5-f]chinolin;
9-Dimethylamino-7-(3-fluorphenyl)-2-methyl-thiazolo[4,5-f]chinolin;
9-Dimethylamino-7-(3-fluorphenyl)-thiazolo[5,4-f]chinolin;
7-(3-Fluorphenyl)-2-methyl-9-methylamino thiazolo[4,5-f]chinolin; 9-Dimethylamino-3-methyl-7-(pyridin-3-yl)-3H-imidazo[4,5-f]chinolin;
3-Methyl-9-methylamino-7-(pyridin-3-yl)-3H-imidazo[4,5-f]chinolin;
2-Methyl-9-methylamino-7-(pyridin-3-yl)-thiazolo[4,5-f]chinolin; und
9-Dimethylamino-2-methyl-7-(pyridin-3-yl)-thiazolo[4,5-f]chinolin.
8. Verfahren zur Herstellung der Verbindung von Anspruch 1 , dadurch gekennzeichnet dass ein 3-Oxo-Propionsäureester, dessen Carbonylgruppe an den gewünschten Rest A gebunden ist, gemäss dem folgenden Reaktionsschema zu einer erfindungsgemässen Verbindung umgesetzt wird, wobei
a .COO-Alkyl
Verfahrensschritt a in Gegenwart eines primären Amins abläuft; Verfahrensschritt b in Gegenwart des gewünschten Aminoderivates von
Benzimidazol, Benzoxazol oder Benzthiazol; Verfahrensschritt c in Gegenwart eines geeigneten Lösungsmittels; Verfahrensschritt d in Gegenwart eines Halogenierungsmittels; und Verfahrensschritt e in Gegenwart des gewünschten Amins.
9. Verwendung der Verbindung von Anspruch 1 als Arzneimittelwirkstoff.
10. Verwendung gemäss Anspruch 8, dadurch gekennzeichnet, dass es sich beim Arzneimittelwirkstoff um ein Analgetikum handelt.
11. Verwendung der Verbindung von Anspruch 1 zur Herstellung eines Arzneimittels zur Linderung oder Behandlung von Schmerzen.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE10316659A DE10316659A1 (de) | 2003-04-11 | 2003-04-11 | Tricyclische Heteroaromatische Verbindungen |
| DE10316659.9 | 2003-04-11 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2004089950A1 true WO2004089950A1 (de) | 2004-10-21 |
Family
ID=33039021
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2004/003626 Ceased WO2004089950A1 (de) | 2003-04-11 | 2004-04-06 | Tricyclische heteroaromatische verbindungen |
Country Status (2)
| Country | Link |
|---|---|
| DE (1) | DE10316659A1 (de) |
| WO (1) | WO2004089950A1 (de) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2008143263A1 (ja) | 2007-05-22 | 2008-11-27 | Astellas Pharma Inc. | 1位置換テトラヒドロイソキノリン化合物 |
| WO2016083490A1 (en) * | 2014-11-27 | 2016-06-02 | Remynd Nv | Compounds for the treatment of amyloid-associated diseases |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3947434A (en) * | 1973-06-06 | 1976-03-30 | Morton-Norwich Products, Inc. | 9-(P-phenylazoanilino)-7-methyl-1H-imidazo[4,5-f]quinolines |
| EP0187705A2 (de) * | 1985-01-08 | 1986-07-16 | Norwich Eaton Pharmaceuticals, Inc. | Imidazo(4,5-f)chinoline brauchbar als Immunomodulatormittel |
| WO2002036567A1 (en) * | 2000-11-06 | 2002-05-10 | Astrazeneca Ab | N-type calcium channel antagonists for the treatment of pain |
-
2003
- 2003-04-11 DE DE10316659A patent/DE10316659A1/de not_active Withdrawn
-
2004
- 2004-04-06 WO PCT/EP2004/003626 patent/WO2004089950A1/de not_active Ceased
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3947434A (en) * | 1973-06-06 | 1976-03-30 | Morton-Norwich Products, Inc. | 9-(P-phenylazoanilino)-7-methyl-1H-imidazo[4,5-f]quinolines |
| EP0187705A2 (de) * | 1985-01-08 | 1986-07-16 | Norwich Eaton Pharmaceuticals, Inc. | Imidazo(4,5-f)chinoline brauchbar als Immunomodulatormittel |
| WO2002036567A1 (en) * | 2000-11-06 | 2002-05-10 | Astrazeneca Ab | N-type calcium channel antagonists for the treatment of pain |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2008143263A1 (ja) | 2007-05-22 | 2008-11-27 | Astellas Pharma Inc. | 1位置換テトラヒドロイソキノリン化合物 |
| US8263607B2 (en) | 2007-05-22 | 2012-09-11 | Astellas Pharma Inc. | 1-substituted tetrahydroisoquinoline compound |
| WO2016083490A1 (en) * | 2014-11-27 | 2016-06-02 | Remynd Nv | Compounds for the treatment of amyloid-associated diseases |
Also Published As
| Publication number | Publication date |
|---|---|
| DE10316659A1 (de) | 2004-10-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0193056B1 (de) | Kombination von Flupirtin und anticholinergisch wirkenden Spasmolytika | |
| EP0683780A1 (de) | Imidazopyridine und ihre anwendung zur behandlung von magen-darm krankheiten | |
| DE2365526A1 (de) | Pharmazeutische zusammensetzung mit entzuendungshemmender, analgetischer, antipyretischer, hustenstillender und die geschwuerbildung hemmender wirkung | |
| DE69908608T2 (de) | Derivate von Imidazo[1,2-a]pyridin zur Behandlung von gastrointestinalen Krankheiten | |
| WO1997031918A1 (de) | Morphin- und diamorphinsalze anionischer nicht-narkotischer analgetika vom typ der substituierten carbonsäuren | |
| DE19831878C2 (de) | Polycyclische Thiazolidin-2-yliden Amine, Verfahren zu ihrer Herstellung und ihre Verwendung als Arzneimittel | |
| EP0006114B1 (de) | 7-Methoxy-5-oxo-5H-thiazolo(2,3-b)chinazolin-2-carbonsäure und deren pharmazeutisch verwendbare Salze. Verfahren zu deren Herstellung und sie enthaltende Arzneimittel | |
| EP0621037B1 (de) | Pyrido-pyrimidindione, Verfahren zu ihrer Herstellung und ihre Verwendung als Arzneimittel | |
| DE10048715A1 (de) | Verwendung von Aminosäure zur Behandlung von Schmerz | |
| WO2000051602A1 (de) | Verwendung von polycyclischen 2-amino-thiazol systemen zur herstellung von medikamenten zur prophylaxe oder behandlung von obesitas | |
| WO2004089950A1 (de) | Tricyclische heteroaromatische verbindungen | |
| DE3007710C2 (de) | 5,6;8,9-Tetrahydro-7H-dibenz(d,f)azonin-derivate, Verfahren zu deren Herstellung und Arzneimittel | |
| EP0027268A2 (de) | Chinazolin-Derivate, Verfahren und Zwischenprodukte zu deren Herstellung, Arzneimittel enthaltend solche Chinazolin-Derivate und deren pharmazeutische Verwendung | |
| EP0576906A1 (de) | Neue Thienothiazinderivate, Verfahren zu ihrer Herstellung und ihre Verwendung als Antiinflammatorium und Analgeticum | |
| DE3844415A1 (de) | Neue 3-piperidincarboxaldehydoxim-derivate, deren herstellungsverfahren und deren verwendung als arzneimittel | |
| DE3026365C2 (de) | ||
| US20040214833A1 (en) | Tricyclic heteroaromatic compounds | |
| DE68924545T2 (de) | Verwendung von Chinolizin- und Chinolizinon-Derivaten zur Herstellung von Arzneimitteln. | |
| DE4218159C2 (de) | 4,4,4-Trifluoracetessigsäureamide, Verfahren zu ihrer Herstellung und Arzneimittel | |
| DE2349493A1 (de) | 2-(2-pyridyl)- omega-phenylalkylamine und verfahren zu ihrer herstellung | |
| DE4124587A1 (de) | Dimethylacetessigsaeureamide, verfahren zu ihrer herstellung und arzneimittel | |
| DE2530005C3 (de) | 6,11-Dihydrodibenzo [b,e] thiepin-Derivate und deren Salze, Verfahren zu ihrer Herstellung und diese Substanzen enthaltende pharmazeutische Zubereitungen | |
| EP0138034A1 (de) | Substituierte Pyrido(1,2-c)imidazo((1,2-a)benzimidazole, Verfahren zu ihrer Herstellung, ihre Verwendung sowie pharmazeutische Präparate auf Basis dieser Verbindungen | |
| DE3310796A1 (de) | Substituierte ethenylderivate von 1h-pyrazolo-(1,5-a)-pyrimidin, verfahren zur herstellung derselben, sowie diese enthaltende pharmazeutische praeparate | |
| EP0001062B1 (de) | Ergolin-Derivate, Verfahren zu ihrer Herstellung, diese enthaltende pharmazeutische Zusammensetzungen und ihre Anwendung bei therapeutischen Behandlungen |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AK | Designated states |
Kind code of ref document: A1 Designated state(s): AE AG AL AM AT AU AZ BA BB BG BR BW BY BZ CA CH CN CO CR CU CZ DK DM DZ EC EE EG ES FI GB GD GE GH GM HR HU ID IL IN IS JP KE KG KP KR KZ LC LK LR LS LT LU LV MA MD MG MK MN MW MX MZ NA NI NO NZ OM PG PH PL PT RO RU SC SD SE SG SK SL SY TJ TM TN TR TT TZ UA UG US UZ VC VN YU ZA ZM ZW |
|
| AL | Designated countries for regional patents |
Kind code of ref document: A1 Designated state(s): BW GH GM KE LS MW MZ SD SL SZ TZ UG ZM ZW AM AZ BY KG KZ MD RU TJ TM AT BE BG CH CY CZ DE DK EE ES FI FR GB GR HU IE IT LU MC NL PL PT RO SE SI SK TR BF BJ CF CG CI CM GA GN GQ GW ML MR NE SN TD TG |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application | ||
| 122 | Ep: pct application non-entry in european phase |