WO2007068325A1 - Konjugierte polymere enthaltend triarylamin-arylvinylen-einheiten, deren darstellung und verwendung - Google Patents
Konjugierte polymere enthaltend triarylamin-arylvinylen-einheiten, deren darstellung und verwendung Download PDFInfo
- Publication number
- WO2007068325A1 WO2007068325A1 PCT/EP2006/011085 EP2006011085W WO2007068325A1 WO 2007068325 A1 WO2007068325 A1 WO 2007068325A1 EP 2006011085 W EP2006011085 W EP 2006011085W WO 2007068325 A1 WO2007068325 A1 WO 2007068325A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- polymers
- units
- mono
- formula
- occurrence
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- QMQWNYRZNHNRPV-UHFFFAOYSA-N C=[Br]c1ccc(CBr)cc1 Chemical compound C=[Br]c1ccc(CBr)cc1 QMQWNYRZNHNRPV-UHFFFAOYSA-N 0.000 description 1
- IPTXXSZUISGKCJ-UHFFFAOYSA-N CCOP(Cc(cc1)ccc1Br)(OCC)=O Chemical compound CCOP(Cc(cc1)ccc1Br)(OCC)=O IPTXXSZUISGKCJ-UHFFFAOYSA-N 0.000 description 1
- XBQPOQVPPGNROQ-UHFFFAOYSA-N Cc1ncc(C(C=C2C3=CC(c4ncc(C)nc4)=C4C3=CC=CC=C4)=C3C2=CC=CC=C3)nc1 Chemical compound Cc1ncc(C(C=C2C3=CC(c4ncc(C)nc4)=C4C3=CC=CC=C4)=C3C2=CC=CC=C3)nc1 XBQPOQVPPGNROQ-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/12—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent materials, e.g. electroluminescent or chemiluminescent
- C09K11/06—Luminescent materials, e.g. electroluminescent or chemiluminescent containing organic luminescent materials
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F5/00—Compounds containing elements of Groups 3 or 13 of the Periodic Table
- C07F5/02—Boron compounds
- C07F5/025—Boronic and borinic acid compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G83/00—Macromolecular compounds not provided for in groups C08G2/00 - C08G81/00
- C08G83/002—Dendritic macromolecules
- C08G83/003—Dendrimers
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L65/00—Compositions of macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain; Compositions of derivatives of such polymers
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/12—Light sources with substantially two-dimensional [2D] radiating surfaces
- H05B33/14—Light sources with substantially two-dimensional [2D] radiating surfaces characterised by the chemical or physical composition or the arrangement of the electroluminescent material, or by the simultaneous addition of the electroluminescent material in or onto the light source
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K30/00—Organic devices sensitive to infrared radiation, light, electromagnetic radiation of shorter wavelength or corpuscular radiation
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/10—Organic polymers or oligomers
- H10K85/111—Organic polymers or oligomers comprising aromatic, heteroaromatic, or aryl chains, e.g. polyaniline, polyphenylene or polyphenylene vinylene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/10—Organic polymers or oligomers
- H10K85/151—Copolymers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/791—Starburst compounds
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1007—Non-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1011—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1022—Heterocyclic compounds bridged by heteroatoms, e.g. N, P, Si or B
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1092—Heterocyclic compounds characterised by ligands containing sulfur as the only heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/18—Metal complexes
- C09K2211/185—Metal complexes of the platinum group, i.e. Os, Ir, Pt, Ru, Rh or Pd
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2102/00—Constructional details relating to the organic devices covered by this subclass
- H10K2102/10—Transparent electrodes, e.g. using graphene
- H10K2102/101—Transparent electrodes, e.g. using graphene comprising transparent conductive oxides [TCO]
- H10K2102/103—Transparent electrodes, e.g. using graphene comprising transparent conductive oxides [TCO] comprising indium oxides, e.g. ITO
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/10—Organic polymers or oligomers
- H10K85/111—Organic polymers or oligomers comprising aromatic, heteroaromatic, or aryl chains, e.g. polyaniline, polyphenylene or polyphenylene vinylene
- H10K85/113—Heteroaromatic compounds comprising sulfur or selene, e.g. polythiophene
- H10K85/1135—Polyethylene dioxythiophene [PEDOT]; Derivatives thereof
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Definitions
- the present invention relates to conjugated polymers and dendrimers containing styryl-triarylamine structural units, their use in electronic components, in particular in polymeric organic
- Light-emitting diodes monomers for their preparation, as well as such polymers and dendrimer-containing components and light-emitting diodes.
- Conjugated polymers are currently being studied intensively as promising materials in PLEDs (Polymer Light Emitting Diodes). Their simple processing in contrast to SMOLEDs (Small Molecule Organic Light Emitting Diodes) promises a more cost-effective production of corresponding light-emitting diodes.
- conjugated polymers based on fluorenes, indenofluorenes, spirobifluorenes, phenanthrenes and dihydrophenanthrenes are synthesized today in order to be able to produce blue-luminescent organic light-emitting diodes.
- conjugated polymers based on fluorenes, indenofluorenes, spirobifluorenes, phenanthrenes and dihydrophenanthrenes are synthesized today in order to be able to produce blue-luminescent organic light-emitting diodes.
- conjugated polymers containing triarylamine units which are substituted by a styryl group have as blue or green emitting unit very good and prior art properties.
- This relates, inter alia, to the photostability, but also to the efficiency of the polymers.
- the incorporation of triphenylamines substituted by a styryl group into the emission layer of a polymer in low concentrations leads to an increase in the lifetime, the efficiency as well as a lowering of the operating voltage with little shift of the emission color.
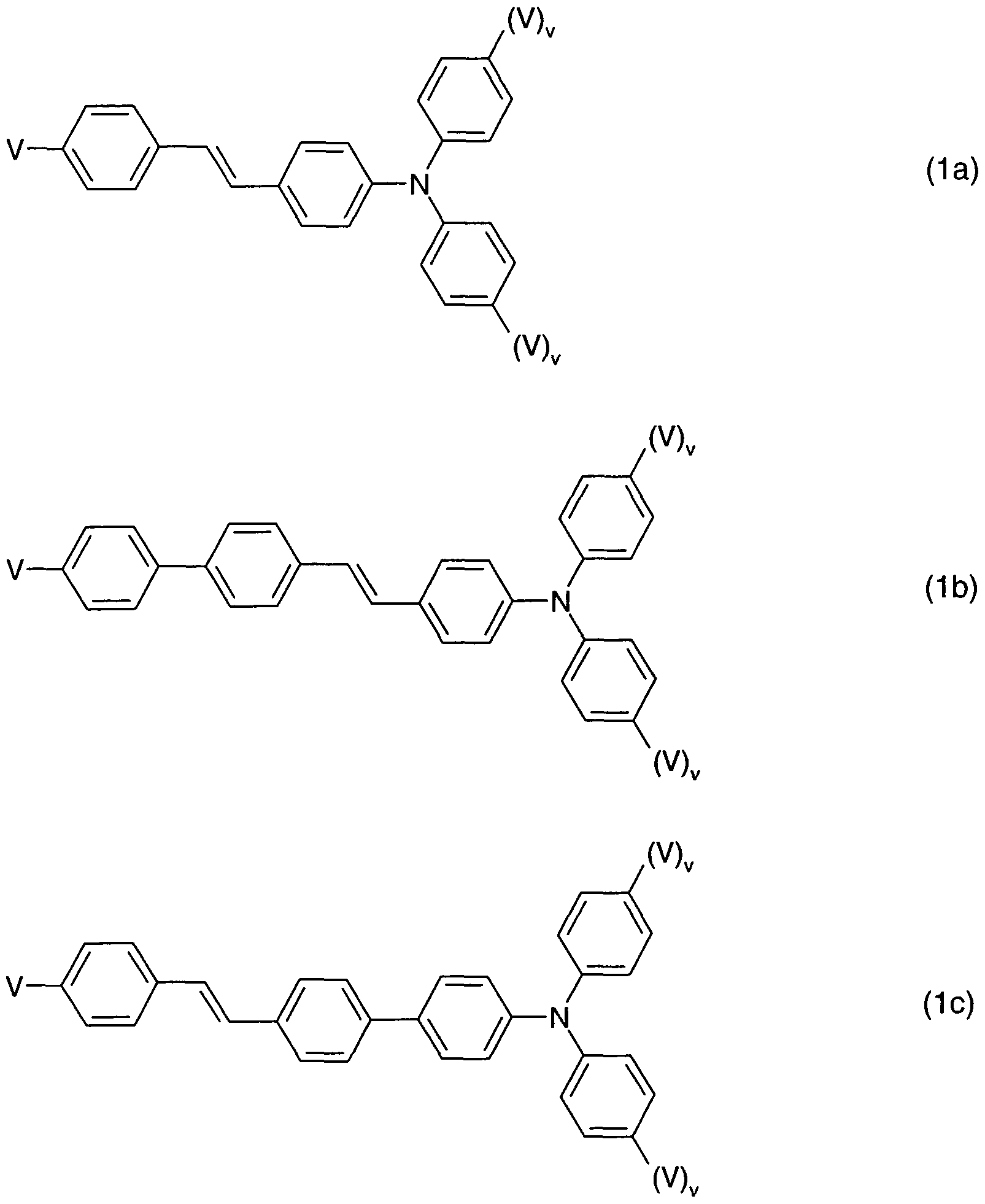
- Polymers for OLEDs containing vinyl and triarylamine groups are disclosed in EP 1 281 745 A1, EP 1 277 824 A1 and US 6,066,712. However, polymers according to the present invention are not shown therein. Geganstand the invention are conjugated polymers and dendrimers, characterized in that they contain one or more units of formula (1)
- Ar 1 is, identically or differently, mono- or polycyclic aryl or heteroaryl at each occurrence, which may be monosubstituted or polysubstituted by R 1 ,
- Ar 2 is identical or different at each occurrence mono or polycyclic aryl or heteroaryl, which may be mono- or polysubstituted by R 2 ,
- Ar 3 is the same or different at each occurrence mono or polycyclic aryl or heteroaryl, which may be mono- or polysubstituted by R 3 ,
- Ar 4 is, identically or differently, mono- or polycyclic aryl or heteroaryl at each occurrence, which may be monosubstituted or polysubstituted by R 4 ,
- Y is the same or different H 1 F, Cl or a carbon or hydrocarbon radical having 1 to 40 carbon atoms, and also two radicals Y, or a radical Y and an adjacent radical
- R 1 , R 4 , Ar 1 or Ar 4 may together form an aliphatic or aromatic, mono- or polycyclic ring system
- R 1 "4 is the same or different H, F, Cl, OH, CN, N (R) 2 , Si (R) 31 B (R) 2 , or a carbon or hydrocarbon radical having 1 to 40 C at each occurrence -Atomen, wherein two or more of the radicals R 1 "4 can form an aliphatic or aromatic, mono- or polycyclic ring system with one another, R 1 , R 2 and R 3 can also be a covalent linkage in the polymer or dendrimer,
- Radicals R 1 can be substituted; also several radicals R, or radicals R with further radicals R 1'4 , form an aromatic or aliphatic, mono- or polycyclic ring system,
- R 0 is identical or different at each occurrence H oer an aliphatic or aromatic hydrocarbon radical having 1 to 20 carbon atoms,
- a is the same or different 1, 2 or 3 at each occurrence,
- b is the same or different 1, 2 or 3 for each occurrence
- c is the same or different O or 1 at each occurrence.
- the linking of the units of the formula (1) to adjacent units in the polymers according to the invention can be effected along the polymer main chain or else in the polymer side chain.
- polymers containing one or more units of the formula (1) preferably in the polymer main chain, in which Ar 2 has a substituent R 2 which is a linkage.
- polymers comprising one or more units of the formula (1) preferably in the polymer side chain, in which Ar 2 and Ar 3 have no substituents R 2 or R 3 which signify a linkage.
- branched polymers comprising one or more units of the formula (1) in which Ar 2 and one or more radicals Ar 3 each have a substituent R 2 or R 3 which denotes a linkage, ie polymers containing at least one unit of the formula (1) as a branch point.
- dendrimers containing one or more units of the formula (1) in which Ar 2 and one or more radicals Ar 3 JeWeUs have a substituent R 2 or R 3 , which signifies a linkage.
- carbon radical above and below means a monovalent or polyvalent organic radical containing at least one carbon atom, which either contains no further atoms (such as -C ⁇ C-), or optionally one or more further atoms such as N 1 O, S, P, Si, Se, As, Te or Ge contains (eg carbonyl, etc.).
- hydrocarbon radical means a carbon radical which additionally contains one or more H atoms and optionally one or more heteroatoms such as, for example, N, O, S 1 P, Si, Se, As, Te or Ge.
- aryl means an aromatic carbon group or a group derived therefrom.
- heteroaryl means "aryl” as defined above containing one or more heteroatoms.
- the carbon or hydrocarbon radical can be a saturated or be unsaturated group. Unsaturated groups are, for example, aryl, alkenyl or alkynyl groups.
- a carbon or hydrocarbon radical having more than 3 C atoms may be straight-chain, branched and / or cyclic, and may also have spiro-linkages or fused rings.
- Particularly preferred carbon and hydrocarbon radicals are straight-chain, branched or cyclic, alkenyl, alkynyl, alkoxy,
- Very particularly preferred carbon and hydrocarbon radicals are C 1 -C 40 alkyl, C 2 -C 40 alkenyl, C 2 -C 40 alkynyl, C 3 -C 40 allyl, C 4 -C 40
- 22 alkyl are particularly preferred 22 alkyl, C 2 -C 22 alkenyl, C 2 -C 22 alkynyl, C 3 -C 22 allyl, C 4 -C 22 alkyl dienyl, C 6 -C 12 aryl, Ce-C 20 arylalkyl and CQ-C 2 O heteroaryl.
- alkyl groups are methyl, ethyl, n-propyl, isopropyl, n-butyl, isobutyl, s-butyl, t-butyl, 2-methylbutyl, n-pentyl, s-pentyl, cyclopentyl, n-hexyl, cyclohexyl, 2- Ethylhexyl, n-heptyl, cycloheptyl, 1, 1, 5-trimethylheptyl, n-octyl, cyclooctyl, dodecanyl, trifluoromethyl, perfluoro-n-butyl, 2,2,2-trifluoroethyl, perfluorooctyl,
- Preferred alkenyl groups are, for example, ethenyl, propenyl, butenyl, pentenyl, cyclopentenyl, hexenyl, cyclohexenyl, heptenyl, cycloheptenyl, octenyl, cyclooctenyl, etc.
- Preferred alkynyl groups are, for example, ethynyl, propynyl, butynyl, pentynyl, hexynyl, octynyl, etc.
- Preferred alkoxy groups are, for example, methoxy, ethoxy, 2-methoxyethoxy, n-propoxy, i-propoxy, n-butoxy, i-butoxy, s-butoxy, t-butoxy, 2-methylbutoxy, n-pentoxy, n-hexoxy, n- Heptoxy, n-octoxy, n-nonoxy, n-decoxy, etc.
- Preferred amino groups are, for example, dimethylamino, methylamino, methylphenylamino, phenylamino, etc.
- Aryl groups can be monocyclic or polycyclic, i. they may have a ring (for example phenyl) or two or more rings, which may also be condensed (for example naphthyl) or covalently linked (for example biphenyl), or a combination of fused and linked rings. Preference is given to fully conjugated aryl groups.
- Preferred aryl groups are, for example, phenyl, biphenyl, triphenyl, [i.i'iS'.V'jTerphenyl ⁇ '- yl, naphthyl, anthracene, binaphthyl, phenanthrene, pyrene, dihydropyrene, chrysene, perylene, tetracene, pentacene, benzopyrene, fluorene, Indene, indenofluorene, spirobifluorene, etc.
- Preferred heteroaryl groups are, for example, 5-membered rings such as pyrrole, pyrazole, imidazole, 1, 2,3-triazole, 1, 2,4-triazole, tetrazole, furan, Thiophene, selenophene, oxazole, isoxazole, 1, 2-thiazole, 1, 3-thiazole, 1, 2,3-oxadiazole, 1, 2,4-oxadiazole, 1, 2,5-oxadiazole, 1, 3,4- Oxadiazole, 1, 2,3-thiadiazole, 1, 2,4-thiadiazole, 1, 2,5-thiadiazole, 1, 3,4-thiadiazole, 6-membered rings such as pyridine, pyridazine, pyrimidine, pyrazine, 1, 3 , 5-triazine, 1, 2,4-triazine, 1, 2,3-triazine, 1, 2,4,5-tetrazine, 1, 2,3,4-tetrazine, 1, 2,3,5-
- heteroaryl groups may also be substituted by alkyl, alkoxy, thioalkyl, fluorine, fluoroalkyl or other aryl or heteroaryl groups.
- the aryl, heteroaryl, carbon and hydrocarbon radicals optionally have one or more substituents, which are preferably selected from the group consisting of SiIyI, sulfo, sulfonyl, formyl, amine, imine, nitrile, mercapto, nitro, halogen, ci- I 2 is alkyl, C 6 -i 2 aryl, Ci -12 alkoxy, hydroxy, or combinations of these groups.
- Preferred substituents are, for example, solubility-promoting groups such as alkyl or alkoxy, electron-withdrawing groups such as fluorine, nitro or nitrile, or substituents for increasing the glass transition temperature (Tg) in the polymer, in particular bulky groups such as e.g. t-butyl or optionally substituted aryl groups.
- alkyl also include polyvalent groups, for example alkylene, arylene, heteroarylene, etc.
- Halogen means F 1 Cl, Br or I.
- Conjugated polymers in the context of this invention are polymers which contain in the main chain mainly sp 2 -hybridized (or optionally also sp-hybridized) carbon atoms, which may also be replaced by corresponding heteroatoms. In the simplest case this means alternating presence of double and single bonds in the main chain, but also polymers with units such as, for example, meta-linked phenylene are to be considered as conjugated polymers for the purposes of this invention. "Mainly” means that naturally (involuntarily) occurring defects that lead to interruptions in conjugation do not invalidate the term "conjugated polymer".
- conjugated if in the main chain, for example, arylamine units, Arylphosphinechen and / or certain heterocycles (ie conjugation of N, O, P or S atoms) and / or organometallic complexes (ie conjugation over the metal atom).
- conjugated dendrimers for example, arylamine units, Arylphosphinechen and / or certain heterocycles (ie conjugation of N, O, P or S atoms) and / or organometallic complexes (ie conjugation over the metal atom).
- the term "dendrimer” is to be understood here as meaning a highly branched compound which is composed of a multifunctional center (core) to which branched monomers are bonded in a regular structure, so that a tree-like structure is obtained. Both the center and the monomers can assume any branched structures consisting of purely organic units as well as organometallic compounds or coordination compounds. "Dendrimer” is to be understood here in general terms as described, for example, by M. Fischer and F. Vögtle (Angew Chem, Int Ed. 1999, 38, 885).
- the units according to formula (1) can be incorporated according to the invention in the main or in the side chain of the polymer. When incorporated into the side chain, there is the possibility that the unit of formula (1) may be in conjugation with the polymer backbone or that it is unconjugated to the polymer backbone.
- the unit according to formula (1) is in conjugation with the polymer main chain. This can be achieved, on the one hand, by incorporating this unit in the main chain of the polymer in such a way that the conjugation of the
- this unit can also be linked in the side chain of the polymer so that there is a conjugation to the main chain of the polymer. This is the case, for example, if the linkage to the main chain only via sp 2 -hybridized (or possibly also via sp-hybridized)
- Carbon atoms which may also be replaced by corresponding heteroatoms takes place.
- the linking is by units such as simple (thio) ether bridges, esters, amides or alkylene chains, the structural unit of formula (1) is defined as non-conjugated to the main chain.
- the attachment of the units of the formula (1) to the main chain can be carried out directly or via one or more additional units.
- radicals R 1 "4 in formula (1) are preferably selected from the abovementioned groups.
- the radicals R 1'4 in formula (1) are preferably selected from the abovementioned groups.
- radicals Ar 1 "3 in formula (1) are preferably phenyl (as a monovalent radical) or phenylene (as a divalent radical), these being
- Groups may be mono- or polysubstituted by R 5 , and R 5 has one of the meanings given in formula (1) for R 4 . If one of the phenylene radicals Ar 1 "3 has a link to an adjacent unit, then this is in the 2-, 3- or 4-position, preferably in the 4-position.
- the radicals Ar 4 in formula (1) are preferably selected from phenylene, in particular 1,4-phenylene, 4,4'-biphenylene, 9,9-disubstituted fluorene-2,7-diyl, or 6,6,12,12 tetrasubstituted indenofluorene-2,8-diyl or spirobifluorene-2,7-diyl, which groups may be mono- or polysubstituted by R 5 as defined above.
- the groups Y in formula (1) are preferably H or form an unsaturated, 5- or 6-membered, optionally substituted ring system with the adjacent group Ar 4 .
- V is a covalent linkage in the polymer or dendrimer and v is 0 or 1
- R 5 has the same or different one of the meanings given for R 4 in formula (1) at each occurrence.
- the phenyl rings can also be mono- or polysubstituted by R 5 .
- the conjugated polymers and dendrimers according to the invention preferably contain at least 0.5 mol%, in particular 1 to 50 mol%, particularly preferably 1 to 30 mol%, very particularly preferably 1 to 10 mol% of one or more units of the formula (1).
- the compounds of the formula I can be prepared by methods known to the person skilled in the art and described in the literature. Other suitable and preferred synthetic methods can be found in the examples.
- the compounds of the formula I can be prepared, for example, by reacting optionally substituted phenyl-4-bromophenyl-4-formylphenylamine, which can be prepared by literature methods, with optionally substituted (4-bromobenzylmethyl) -diethylphosphonate in the presence of a base.
- polymers according to the invention which, in addition to units of the formula (1), also contain further structural elements and are therefore to be referred to as copolymers.
- the other comonomers are necessary for the synthesis of the copolymers of the invention; However, they are not themselves subject of the present invention and are thus to be described by citation.
- These further structural units can come, for example, from the classes described below: Group 1: comonomers which constitute the polymer backbone.
- Group 2 comonomers containing the hole injection and / or
- Group 3 comonomers which significantly increase the electron injection and / or transport properties of the polymers.
- Group 4 comonomers having combinations of single group 2 and group 3 units.
- Group 1 - Comonomers which Represent the Polymer Backbone Preferred Group 1 units are especially those containing aromatic or carbocyclic structures of 6 to 40 carbon atoms. Suitable and preferred units include fluorene derivatives such. In EP 0842208, WO 99/54385, WO 00/22027, WO 00/22026 or WO 00/46321, further spirobifluorene derivatives such. In EP 0707020, EP 0894107 and WO 03/020790, or dihydrophenanthrene derivatives as disclosed in WO 2005/014689. It is also possible to use a combination of two or more of these monomer units, e.g. in WO 02/077060.
- substituted or unsubstituted aromatic structures having 6 to 40 carbon atoms or stilbene or Bisstyrylarylenderivate such as. B. 1, 4-phenylene, 1, 4-naphthylene, 1, 4 or 9,10-anthrylene, 1, 6 or 2,7- or 4,9-pyrenylene,
- Preferred units for the polymer backbone are spirobifluorenes, indenofluorenes, phenanthrene and dihydrophenanthrenes.
- Particularly preferred units of group 1 are divalent units according to the following formulas, wherein the dotted line denotes the link to the adjacent unit:
- YY is Si or Ge and VV is O, S or Se.
- triarylphosphines are also suitable here, as described in the unpublished application EP 03018832.0.
- Particularly preferred group 2 units are two-membered units according to the following formulas, wherein the dashed line represents the link to the adjacent unit:
- R 6 has one of the meanings given for R 5
- the various formulas at the free positions may also be additionally substituted by one or more substituents R 5 and the symbols and indices mean the following:
- n is the same or different at each occurrence O, 1, or 2,
- O, 1 or 2 is identical or different at each occurrence O, 1 or 2, preferably O or 1,
- Ar Ar are identical or different at each occurrence, an aromatic or heteroaromatic ring system having 2 to 40 carbon atoms, which may be monosubstituted or polysubstituted by R 5 or unsubstituted; the possible substituents R 5 can potentially be located at any free position,
- Ar 12 , Ar 14 are the same or different on each occurrence Ar 11 , Ar 13 or a substituted or unsubstituted stilbenylene or tolanylene unit, Ar 15 is identical or different at each occurrence either a system according to Ar 11 or an aromatic or heteroaromatic ring system having 9 to 40 aromatic atoms (C or hetero atoms), which may be mono- or polysubstituted or unsubstituted by R 5 and which at least two condensed rings; the possible substituents R 5 can potentially sit at any free position.
- aromatics or heterocycles such as substituted or unsubstituted pyridines, pyrimidines, pyridazines, pyrazines, anthracenes, oxadiazoles, quinolines, quinoxalines or phenazines , but also compounds such as triarylbor
- Particularly preferred group 3 units are divalent units according to the following formulas, wherein the dotted line represents the link to the adjacent unit:
- the polymers of the invention contain units in which structures which increase hole mobility and which enhance electron mobility are directly bonded to each other. However, some of these units shift the emission color to yellow or red; their use in polymers according to the invention for producing blue or green emission is therefore less preferred.
- Group 4 units are included in the polymers of the invention, they are preferably selected from divalent units according to the following formulas, wherein the dotted line represents the link to the adjacent unit:
- the polymer according to the invention can furthermore likewise contain metal complexes bonded in the main or side chain, which are generally composed of one or more ligands and one or more metal centers.
- polymers according to the invention which, in addition to structural units of the formula (1), additionally contain one or more units selected from groups 1 to 4.
- polymers according to the invention which, in addition to units of the formula (1), also contain units from group 1, particularly preferably at least 50 mol% of these units. It is likewise preferred if the polymers according to the invention contain units which improve the charge transport or the charge injection, ie units from group 2 and / or 3; particularly preferred is a proportion of 1 - 30 mol% of these units; very particular preference is given to a proportion of 1-10 mol% of these units.
- the polymers according to the invention contain units from group 1 and units from group 2 and / or 3, in particular at least 50 mol% units from group 1 and 1-30 mol% units from group 2 and / or 3.
- the polymers according to the invention generally have 10 to 10,000, preferably 20 to 5000, particularly preferably 50 to 2000 repeat units. Corresponding dendrimers may also have fewer repeat units.
- the polymers according to the invention are either homopolymers of units of the formula (1) or copolymers.
- the polymers according to the invention can be linear or branched (crosslinked).
- copolymers according to the invention can potentially have one or more further structures from groups 1 to 4 listed above.
- copolymers according to the invention may have random, alternating or block-like structures or alternatively have several of these structures in turn. How copolymers having block-like structures can be obtained and which further structural elements are particularly preferred for this purpose is described in detail, for example, in WO 2005/014688. This is via quote part of the present Registration. It should also be emphasized at this point that the polymer can also have dendritic structures.
- structural units according to formula (1) can be used as green or blue emitting comonomers for the synthesis of red emitting polymers. Another object of the invention is therefore the use of structural units according to formula (1) for the synthesis of red emitting polymers.
- the polymers of the invention are usually by
- the CC linkages are preferably selected from the groups of the SUZUKI coupling, the YAMAMOTO coupling and the STILLE coupling.
- dendrimers according to the invention can be prepared according to methods known to the person skilled in the art or in analogy thereto. suitable
- Monomers which lead to structural units of the formula (1) in polymers and dendrimers according to the invention are preferably selected from formula (1)
- Ar 1 "4 , a, b and c have the meanings given above, and wherein one of the substituents R 1 to Ar 1 and optionally one of the substituents R 2 and Ar 2 and one of the substituents R 3 to Ar 3 are each independently Reactive group Z, which is suitable for a polymerization reaction.
- Formula (1) in particular new monomers of the formula (1) and their preferred sub-formulas, are also the subject of the present invention.
- Particularly preferred groups Z are selected from halogen, in particular Cl, Br, I, O-tosylate, O-triflate, O-SO 2 R 1 , B (OH) 2 , B (OIT) 2 or
- R 1 is optionally substituted alkyl or aryl and two groups R 1 can form an aromatic or aliphatic, mono- or polycyclic ring system.
- Aryl and “alkyl” preferably have one of the meanings given above.
- the monomers may be prepared by methods known to those skilled in the art and described in standard organic chemistry. Particularly suitable and preferred methods are described in the examples.
- the polymers of the present invention show higher photostability compared with prior art polymers. This is of crucial importance for the application of these polymers, since they must not decompose either by the radiation released by electroluminescence or by radiation incident from the outside. This property is still deficient in polymers of the prior art.
- Energy consumption can be achieved, especially in mobile Applications (displays for cell phones, pagers, PDAs, etc.), which rely on batteries and rechargeable batteries, is very important. Conversely, higher brightness levels are obtained with the same energy consumption, which may be interesting for lighting applications, for example.
- polymer according to the invention may also be preferred not to use the polymer according to the invention as a pure substance but as a mixture (blend) together with further optional polymeric, oligomeric, dendritic or low molecular weight substances. These can for example improve the electronic properties or emit themselves. Such blends are therefore also part of the present invention.
- the invention furthermore relates to solutions and formulations of one or more polymers or blends according to the invention in one or more solvents.
- polymer solutions can be prepared is known to the person skilled in the art and described, for example, in WO 02/072714, WO 03/019694 and the literature cited therein.
- These solutions can be used to prepare thin polymer layers, for example, by area coating methods (eg, spin-coating) or by printing methods (eg, inkjet printing).
- area coating methods eg, spin-coating
- printing methods eg, inkjet printing
- the solutions, formulations, blends or mixtures according to the invention may optionally contain further components or additives, for example one or more additives selected from the group consisting of surface-active substances, lubricants, wetting agents, dispersing agents, adhesion promoters, hydrophobizing agents, flow improvers, defoamers, deaerators, thinners, reactive diluents , Scratch resistance improvers, catalysts, sensitizers, stabilizers, for example, against light, heat and oxidation, inhibitors, chain transfer agents, comonomers, dyes, pigments and nanoparticles.
- the polymers of the invention can be used in PLEDs. How PLEDs can be produced is known to the person skilled in the art and is described in detail, for example, as a general method in WO 2004/070772, which must be adapted accordingly for the individual case.
- the polymers according to the invention are very particularly suitable as electroluminescent materials in PLEDs or displays produced in this way.
- Active layer means that the layer is capable of emitting light (light-emitting layer) upon application of an electric field and / or that it improves the injection and / or transport of the positive and / or negative charges (charge injection or charge transport layer).
- the invention therefore also relates to the use of a polymer or blend of the invention in a PLED, in particular as an electroluminescent material.
- the invention thus likewise provides a PLED having one or more active layers, wherein at least one of these is active
- Layers one or more polymers of the invention contains.
- the active layer may be, for example, a light-emitting layer and / or a transport layer and / or a charge injection layer.
- conjugated dendrimers are therefore also the subject of the present invention.
- reaction mixture is washed twice with water and the organic phase filtered through Celite and concentrated by rotary evaporation. This gives 79.4 g (99% of theory) of the product in the form of a yellow oil.
- the polymers are synthesized by SUZUKI coupling according to WO 03/048225.
- the composition of the synthesized polymers P1 and P2 is summarized in Table 1.
- the comparative polymers V1 and V2 are synthesized which contain the monomer M4 instead of the monomer M1, which leads to units of the formula (1) in the polymer.
- the composition of these comparative polymers is also listed in Table 1.
- the polymers are being investigated for use in PLEDs.
- the PLEDs are each two-layer systems, ie substrate // ITO // PEDOT // polymer // cathode.
- PEDOT is a polythiophene derivative (Baytron P, from HC Starck, Goslar).
- the cathode used is Ba / Ag (Aldrich) in all cases. How PLEDs can be represented is described in detail in WO 04/037887 and the literature cited therein.
- Example 5 Device examples
- the efficiency of the polymers according to the invention is better than that of the comparative polymers.
- the emission color is comparable and the lifetimes are significantly improved considering this. This shows that the polymers according to the invention are more suitable for use in displays than polymers according to the prior art.
Landscapes
- Chemical & Material Sciences (AREA)
- Materials Engineering (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Electromagnetism (AREA)
- Electroluminescent Light Sources (AREA)
- Polyoxymethylene Polymers And Polymers With Carbon-To-Carbon Bonds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
Claims
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008544785A JP5507084B2 (ja) | 2005-12-17 | 2006-11-18 | 共役ポリマー、その調製及びその使用 |
| US12/097,782 US7799875B2 (en) | 2005-12-17 | 2006-11-18 | Triarylamine-arylvinylene moiety-containing conjugated polymers, their production and use |
| EP06818653.5A EP1961016B1 (de) | 2005-12-17 | 2006-11-18 | Konjugierte polymere enthaltend triarylamin-arylvinylen-einheiten, deren darstellung und verwendung |
| KR1020087017396A KR101304153B1 (ko) | 2005-12-17 | 2006-11-18 | 트리아릴아민-아릴비닐렌 부분-함유 공액 중합체, 이의제조와 용도 |
| CN2006800476219A CN101331558B (zh) | 2005-12-17 | 2006-11-18 | 共轭聚合物、其制备和用途 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102005060473A DE102005060473A1 (de) | 2005-12-17 | 2005-12-17 | Konjugierte Polymere, deren Darstellung und Verwendung |
| DE102005060473.0 | 2005-12-17 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2007068325A1 true WO2007068325A1 (de) | 2007-06-21 |
Family
ID=37709521
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2006/011085 Ceased WO2007068325A1 (de) | 2005-12-17 | 2006-11-18 | Konjugierte polymere enthaltend triarylamin-arylvinylen-einheiten, deren darstellung und verwendung |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US7799875B2 (de) |
| EP (2) | EP2273512B1 (de) |
| JP (1) | JP5507084B2 (de) |
| KR (1) | KR101304153B1 (de) |
| CN (1) | CN101331558B (de) |
| DE (1) | DE102005060473A1 (de) |
| TW (1) | TW200736293A (de) |
| WO (1) | WO2007068325A1 (de) |
Cited By (69)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102008017591A1 (de) | 2008-04-07 | 2009-10-08 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008018670A1 (de) | 2008-04-14 | 2009-10-15 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008033943A1 (de) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008050841A1 (de) | 2008-10-08 | 2010-04-15 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009005746A1 (de) | 2009-01-23 | 2010-07-29 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009009277A1 (de) | 2009-02-17 | 2010-08-19 | Merck Patent Gmbh | Organische elektronische Vorrichtung |
| DE102009034625A1 (de) | 2009-07-27 | 2011-02-03 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| WO2011054442A2 (de) | 2009-11-06 | 2011-05-12 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| DE102009052428A1 (de) | 2009-11-10 | 2011-05-12 | Merck Patent Gmbh | Verbindung für elektronische Vorrichtungen |
| DE102009053644A1 (de) | 2009-11-17 | 2011-05-19 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010005697A1 (de) | 2010-01-25 | 2011-07-28 | Merck Patent GmbH, 64293 | Verbindungen für elektronische Vorrichtungen |
| DE102010009903A1 (de) | 2010-03-02 | 2011-09-08 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| DE102010014933A1 (de) | 2010-04-14 | 2011-10-20 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| WO2011157346A1 (de) | 2010-06-18 | 2011-12-22 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| DE102010024542A1 (de) | 2010-06-22 | 2011-12-22 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102010033548A1 (de) | 2010-08-05 | 2012-02-09 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| WO2012048780A1 (de) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2012095143A1 (de) | 2011-01-13 | 2012-07-19 | Merck Patent Gmbh | Verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2012110182A1 (de) | 2011-02-17 | 2012-08-23 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2012139692A1 (de) | 2011-04-13 | 2012-10-18 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2012139693A1 (de) | 2011-04-13 | 2012-10-18 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2012143079A1 (de) | 2011-04-18 | 2012-10-26 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2012149999A1 (de) | 2011-05-05 | 2012-11-08 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2012150001A1 (de) | 2011-05-05 | 2012-11-08 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2013013754A1 (en) | 2011-07-25 | 2013-01-31 | Merck Patent Gmbh | Copolymers with functionalized side chains |
| WO2013017192A1 (de) | 2011-08-03 | 2013-02-07 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2013017189A1 (de) | 2011-07-29 | 2013-02-07 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2013060418A1 (en) | 2011-10-27 | 2013-05-02 | Merck Patent Gmbh | Materials for electronic devices |
| WO2013087142A1 (de) | 2011-12-12 | 2013-06-20 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| DE102012022880A1 (de) | 2011-12-22 | 2013-06-27 | Merck Patent Gmbh | Elektronische Vorrichtungen enthaltend organische Schichten |
| WO2013120577A1 (en) | 2012-02-14 | 2013-08-22 | Merck Patent Gmbh | Spirobifluorene compounds for organic electroluminescent devices |
| DE102012011335A1 (de) | 2012-06-06 | 2013-12-12 | Merck Patent Gmbh | Verbindungen für Organische Elekronische Vorrichtungen |
| WO2014015937A1 (de) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Verbindungen und organische elektrolumineszierende vorrichtungen |
| WO2014015935A2 (de) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Verbindungen und organische elektronische vorrichtungen |
| WO2014015938A1 (de) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Derivate von 2-diarylaminofluoren und diese enthaltnde organische elektronische verbindungen |
| WO2014082705A1 (de) | 2012-11-30 | 2014-06-05 | Merck Patent Gmbh | Elektronische vorrichtung |
| WO2014106522A1 (de) | 2013-01-03 | 2014-07-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2014106524A2 (de) | 2013-01-03 | 2014-07-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2015086108A1 (de) | 2013-12-12 | 2015-06-18 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2016074755A1 (de) | 2014-11-11 | 2016-05-19 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2016119992A1 (en) | 2015-01-30 | 2016-08-04 | Merck Patent Gmbh | Materials for electronic devices |
| WO2017012694A1 (en) | 2015-07-23 | 2017-01-26 | Merck Patent Gmbh | Phenyl derivatives substituted with at least two electron acceptors and at least two electron donors for use in organic electronic devices |
| WO2017012687A1 (en) | 2015-07-22 | 2017-01-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2017028940A1 (en) | 2015-08-14 | 2017-02-23 | Merck Patent Gmbh | Phenoxazine derivatives for organic electroluminescent devices |
| WO2017036573A1 (en) | 2015-08-28 | 2017-03-09 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2017133829A1 (de) | 2016-02-05 | 2017-08-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2017207596A1 (en) | 2016-06-03 | 2017-12-07 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2018007421A1 (en) | 2016-07-08 | 2018-01-11 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2018069167A1 (de) | 2016-10-10 | 2018-04-19 | Merck Patent Gmbh | Elektronische vorrichtung |
| WO2018083053A1 (de) | 2016-11-02 | 2018-05-11 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2018087020A1 (en) | 2016-11-08 | 2018-05-17 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2018095839A1 (de) | 2016-11-22 | 2018-05-31 | Merck Patent Gmbh | Verbrückte triarylamine für elektronische vorrichtungen |
| WO2018095940A1 (en) | 2016-11-25 | 2018-05-31 | Merck Patent Gmbh | Bisbenzofuran-fused indeno[1,2-b]fluorene derivatives and related compounds as materials for organic electroluminescent devices (oled) |
| WO2018095888A1 (en) | 2016-11-25 | 2018-05-31 | Merck Patent Gmbh | Bisbenzofuran-fused 2,8-diaminoindeno[1,2-b]fluorene derivatives and related compounds as materials for organic electroluminescent devices (oled) |
| EP3345984A1 (de) | 2013-12-06 | 2018-07-11 | Merck Patent GmbH | Verbindungen und organische elektronische vorrichtungen |
| WO2018134392A1 (en) | 2017-01-23 | 2018-07-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2018141706A1 (de) | 2017-02-02 | 2018-08-09 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2018157981A1 (de) | 2017-03-02 | 2018-09-07 | Merck Patent Gmbh | Materialien für organische elektronische vorrichtungen |
| EP3378857A1 (de) | 2012-11-12 | 2018-09-26 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| WO2018197447A1 (de) | 2017-04-25 | 2018-11-01 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2018234346A1 (en) | 2017-06-23 | 2018-12-27 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2019002190A1 (en) | 2017-06-28 | 2019-01-03 | Merck Patent Gmbh | MATERIALS FOR ELECTRONIC DEVICES |
| WO2019020654A1 (en) | 2017-07-28 | 2019-01-31 | Merck Patent Gmbh | SPIROBIFLUORENE DERIVATIVES FOR USE IN ELECTRONIC DEVICES |
| WO2019048443A1 (de) | 2017-09-08 | 2019-03-14 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2019101719A1 (de) | 2017-11-23 | 2019-05-31 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2019115577A1 (en) | 2017-12-15 | 2019-06-20 | Merck Patent Gmbh | Substituted aromatic amines for use in organic electroluminescent devices |
| WO2019121483A1 (en) | 2017-12-20 | 2019-06-27 | Merck Patent Gmbh | Heteroaromatic compounds |
| WO2019175149A1 (en) | 2018-03-16 | 2019-09-19 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| EP4236652A2 (de) | 2015-07-29 | 2023-08-30 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10214937A1 (de) * | 2002-04-04 | 2003-10-16 | Basf Ag | Cyclische Verbindungen und ihre Verwendung als Lichtabsorber, Lichtemitter oder Komplexliganden |
| DE102005040411A1 (de) | 2005-08-26 | 2007-03-01 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102007024850A1 (de) | 2007-05-29 | 2008-12-04 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| US8063399B2 (en) * | 2007-11-19 | 2011-11-22 | E. I. Du Pont De Nemours And Company | Electroactive materials |
| DE102008054141A1 (de) | 2008-10-31 | 2010-05-06 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| JP5836935B2 (ja) * | 2009-05-29 | 2015-12-24 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツングMerck Patent Gesellschaft mit beschraenkter Haftung | 共役ポリマーおよび有機半導体としてのそれらの使用 |
| DE102009033371A1 (de) | 2009-07-16 | 2011-05-12 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| EP2737555A2 (de) | 2011-07-25 | 2014-06-04 | Merck Patent GmbH | Polymere und oligomere mit funktionalisierten seitengruppen |
| WO2013156125A1 (de) * | 2012-04-17 | 2013-10-24 | Merck Patent Gmbh | Vernetzbare sowie vernetzte polymere, verfahren zu deren herstellung sowie deren verwendung |
| CN105409022B (zh) | 2013-07-29 | 2018-06-19 | 默克专利有限公司 | 电光器件及其用途 |
| CN107043452A (zh) * | 2017-03-23 | 2017-08-15 | 华南理工大学 | 一种基于二芳胺基团的共轭聚合物及其制备方法与应用 |
| CN110718642B (zh) * | 2018-07-11 | 2022-07-26 | 东莞伏安光电科技有限公司 | 一种基于共混发光层的oled器件及其制备方法 |
| CN110951049A (zh) * | 2018-09-26 | 2020-04-03 | 华南协同创新研究院 | 一类发光聚合物及其制备方法和在制备发光二极管中的应用 |
| US10541506B1 (en) | 2019-04-10 | 2020-01-21 | King Saud University | Conjugated polymer laser with temperature-controlled power output |
| CN113265039B (zh) * | 2020-02-14 | 2022-04-08 | 台州学院 | 一种共轭有机微孔聚合物及其制备方法 |
| CN114181378B (zh) * | 2021-11-25 | 2023-06-16 | 上海科技大学 | 一种三芳基硼类共轭聚合物多孔材料及其制备方法和用途 |
Citations (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0707020A2 (de) | 1994-10-14 | 1996-04-17 | Hoechst Aktiengesellschaft | Konjugierte Polymere mit Spirozentren und ihre Verwendung als Elektrolumineszenzmaterialien |
| DE19532574A1 (de) * | 1995-09-04 | 1997-03-06 | Hoechst Ag | Polymere mit Triarylamin-Einheiten als Elektrolumineszenzmaterialien |
| EP0842208A1 (de) | 1995-07-28 | 1998-05-20 | The Dow Chemical Company | 2,7-aryl-9-substituierte fluorene und 9-substituierte fluorenoligomere und polymere |
| EP0894107A1 (de) | 1996-04-17 | 1999-02-03 | Hoechst Research & Technology Deutschland GmbH & Co. KG | Polymere mit spiroatomen und ihre verwendung als elektrolumineszenzmaterialien |
| WO1999054385A1 (en) | 1998-04-21 | 1999-10-28 | The Dow Chemical Company | Fluorene-containing polymers and electroluminescent devices therefrom |
| WO2000022027A1 (de) | 1998-10-10 | 2000-04-20 | Celanese Ventures Gmbh | Konjugierte polymere enthaltend 2,7-fluorenyleinheiten mit verbesserten eigenschaften |
| WO2000022026A1 (de) | 1998-10-10 | 2000-04-20 | Celanese Ventures Gmbh | Konjugierte polymere, enthaltend spezielle fluoren-bausteine mit verbesserten eigenschaften |
| US6066712A (en) * | 1997-05-09 | 2000-05-23 | Minolta Co., Ltd. | Styryl polymer, production method and use thereof |
| WO2000046321A1 (en) | 1999-02-04 | 2000-08-10 | The Dow Chemical Company | Fluorene copolymers and devices made therefrom |
| WO2002077060A1 (de) | 2001-03-24 | 2002-10-03 | Covion Organic Semiconductors Gmbh | Konjugierte polymere enthaltend spirobifluoren-einheiten und fluoren-einheiten und deren verwendung |
| EP1277824A1 (de) * | 2001-07-19 | 2003-01-22 | Sumitomo Chemical Company, Limited | Polymere fluoreszierende Substanz und Licht emittierende Polymer Vorrichtung, die selbige Substanz verwendet |
| WO2003020790A2 (de) | 2001-09-04 | 2003-03-13 | Covion Organic Semiconductors Gmbh | Konjugierte polymere enthaltend spirobifluoren-einheiten und deren verwendung |
| WO2003020760A1 (en) | 2001-09-03 | 2003-03-13 | Nederlandse Organisatie Voor Toegepast- Natuurwetenschappelijk Onderzoek Tno | Modulation of the expression of toll-like receptors influences neurodegeneration and neuroprotection in the human central nervous system |
| WO2004037887A2 (de) | 2002-10-25 | 2004-05-06 | Covion Organic Semiconductors Gmbh | Arylamin-einheiten enthaltende konjugierte polymere, deren darstellung und verwendung |
| WO2005014688A2 (de) | 2003-08-12 | 2005-02-17 | Covion Organic Semiconductors Gmbh | Konjiugierte block copolymere, deren darstellung und verwendung |
| WO2005014689A2 (de) | 2003-08-12 | 2005-02-17 | Covion Organic Semiconductors Gmbh | Konjugierte polymere enthaltend dihydrophenanthren-einheiten und deren verwendung |
| WO2005030828A1 (de) | 2003-09-20 | 2005-04-07 | Covion Organic Semiconductors Gmbh | Konjugierte polymere, deren darstellung und verwendung |
| WO2005040302A1 (de) | 2003-10-22 | 2005-05-06 | Merck Patent Gmbh | Neue materialien für die elektrolumineszenz und deren verwendung |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US288617A (en) * | 1883-11-20 | Daniel e | ||
| JP3541076B2 (ja) * | 1994-04-06 | 2004-07-07 | 株式会社リコー | ジヒドロキシスチルベン化合物とその製造方法 |
| WO1997009394A1 (de) | 1995-09-04 | 1997-03-13 | Hoechst Research & Technology Deutschland Gmbh & Co. Kg | Polymere mit triarylamin-einheiten als elektrolumineszenzmaterialien |
| JP3416401B2 (ja) * | 1996-06-28 | 2003-06-16 | キヤノン株式会社 | 電子写真感光体、プロセスカートリッジ及び電子写真装置 |
| TW354371B (en) * | 1997-01-09 | 1999-03-11 | Peter B Hutton | A module valve manifold, a valve module and an integral valve manifold/differential pressure transducer/differential pressure transmitter |
| JP3780619B2 (ja) * | 1997-05-09 | 2006-05-31 | コニカミノルタホールディングス株式会社 | 新規スチリル系高分子化合物、その製造方法および用途 |
| JP4045691B2 (ja) * | 1999-04-27 | 2008-02-13 | 住友化学株式会社 | 高分子発光素子 |
| TWI293964B (en) | 2001-02-05 | 2008-03-01 | Sumitomo Chemical Co | Polymeric fluorescent substance, production thereof and polymer light-emitting device |
| GB0104177D0 (en) | 2001-02-20 | 2001-04-11 | Isis Innovation | Aryl-aryl dendrimers |
| WO2002072714A1 (de) | 2001-03-10 | 2002-09-19 | Covion Organic Semiconductors Gmbh | Lösung und dispersionen organischer halbleiter |
| WO2002088223A1 (en) | 2001-04-27 | 2002-11-07 | Sumitomo Chemical Company, Limited | Block copolymer and polymeric luminescent element |
| SG94878A1 (en) | 2001-07-30 | 2003-03-18 | Sumitomo Chemical Co | Polymeric fluorescent substance and polymer light-emitting device using the same |
| DE10141624A1 (de) | 2001-08-24 | 2003-03-06 | Covion Organic Semiconductors | Lösungen polymerer Halbleiter |
| DE10159946A1 (de) | 2001-12-06 | 2003-06-18 | Covion Organic Semiconductors | Prozess zur Herstellung von Aryl-Aryl gekoppelten Verbindungen |
| JP2004107651A (ja) * | 2002-08-26 | 2004-04-08 | Sharp Corp | デンドリック高分子及びこれを用いた電子デバイス素子 |
| JP2004115761A (ja) * | 2002-09-30 | 2004-04-15 | Toyo Ink Mfg Co Ltd | 有機エレクトロルミネッセンス素子の発光材料およびそれを使用した有機エレクトロルミネッセンス素子 |
| DE10304819A1 (de) * | 2003-02-06 | 2004-08-19 | Covion Organic Semiconductors Gmbh | Carbazol-enthaltende konjugierte Polymere und Blends, deren Darstellung und Verwendung |
| KR20110112475A (ko) | 2003-09-12 | 2011-10-12 | 스미또모 가가꾸 가부시키가이샤 | 덴드리머 화합물 및 그것을 사용한 유기 발광 소자 |
| US7619036B2 (en) | 2004-03-19 | 2009-11-17 | University Of Tennessee Research Foundation | Copolymers of fluorinated polydienes and sulfonated polystyrene |
-
2005
- 2005-12-17 DE DE102005060473A patent/DE102005060473A1/de not_active Withdrawn
-
2006
- 2006-11-18 JP JP2008544785A patent/JP5507084B2/ja not_active Expired - Fee Related
- 2006-11-18 EP EP10008590.1A patent/EP2273512B1/de active Active
- 2006-11-18 US US12/097,782 patent/US7799875B2/en not_active Expired - Fee Related
- 2006-11-18 EP EP06818653.5A patent/EP1961016B1/de not_active Not-in-force
- 2006-11-18 WO PCT/EP2006/011085 patent/WO2007068325A1/de not_active Ceased
- 2006-11-18 CN CN2006800476219A patent/CN101331558B/zh not_active Expired - Fee Related
- 2006-11-18 KR KR1020087017396A patent/KR101304153B1/ko not_active Expired - Fee Related
- 2006-12-13 TW TW095146683A patent/TW200736293A/zh unknown
Patent Citations (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0707020A2 (de) | 1994-10-14 | 1996-04-17 | Hoechst Aktiengesellschaft | Konjugierte Polymere mit Spirozentren und ihre Verwendung als Elektrolumineszenzmaterialien |
| EP0842208A1 (de) | 1995-07-28 | 1998-05-20 | The Dow Chemical Company | 2,7-aryl-9-substituierte fluorene und 9-substituierte fluorenoligomere und polymere |
| DE19532574A1 (de) * | 1995-09-04 | 1997-03-06 | Hoechst Ag | Polymere mit Triarylamin-Einheiten als Elektrolumineszenzmaterialien |
| EP0894107A1 (de) | 1996-04-17 | 1999-02-03 | Hoechst Research & Technology Deutschland GmbH & Co. KG | Polymere mit spiroatomen und ihre verwendung als elektrolumineszenzmaterialien |
| US6066712A (en) * | 1997-05-09 | 2000-05-23 | Minolta Co., Ltd. | Styryl polymer, production method and use thereof |
| WO1999054385A1 (en) | 1998-04-21 | 1999-10-28 | The Dow Chemical Company | Fluorene-containing polymers and electroluminescent devices therefrom |
| WO2000022027A1 (de) | 1998-10-10 | 2000-04-20 | Celanese Ventures Gmbh | Konjugierte polymere enthaltend 2,7-fluorenyleinheiten mit verbesserten eigenschaften |
| WO2000022026A1 (de) | 1998-10-10 | 2000-04-20 | Celanese Ventures Gmbh | Konjugierte polymere, enthaltend spezielle fluoren-bausteine mit verbesserten eigenschaften |
| WO2000046321A1 (en) | 1999-02-04 | 2000-08-10 | The Dow Chemical Company | Fluorene copolymers and devices made therefrom |
| WO2002077060A1 (de) | 2001-03-24 | 2002-10-03 | Covion Organic Semiconductors Gmbh | Konjugierte polymere enthaltend spirobifluoren-einheiten und fluoren-einheiten und deren verwendung |
| EP1277824A1 (de) * | 2001-07-19 | 2003-01-22 | Sumitomo Chemical Company, Limited | Polymere fluoreszierende Substanz und Licht emittierende Polymer Vorrichtung, die selbige Substanz verwendet |
| WO2003020760A1 (en) | 2001-09-03 | 2003-03-13 | Nederlandse Organisatie Voor Toegepast- Natuurwetenschappelijk Onderzoek Tno | Modulation of the expression of toll-like receptors influences neurodegeneration and neuroprotection in the human central nervous system |
| WO2003020790A2 (de) | 2001-09-04 | 2003-03-13 | Covion Organic Semiconductors Gmbh | Konjugierte polymere enthaltend spirobifluoren-einheiten und deren verwendung |
| WO2004037887A2 (de) | 2002-10-25 | 2004-05-06 | Covion Organic Semiconductors Gmbh | Arylamin-einheiten enthaltende konjugierte polymere, deren darstellung und verwendung |
| WO2005014688A2 (de) | 2003-08-12 | 2005-02-17 | Covion Organic Semiconductors Gmbh | Konjiugierte block copolymere, deren darstellung und verwendung |
| WO2005014689A2 (de) | 2003-08-12 | 2005-02-17 | Covion Organic Semiconductors Gmbh | Konjugierte polymere enthaltend dihydrophenanthren-einheiten und deren verwendung |
| WO2005030828A1 (de) | 2003-09-20 | 2005-04-07 | Covion Organic Semiconductors Gmbh | Konjugierte polymere, deren darstellung und verwendung |
| WO2005040302A1 (de) | 2003-10-22 | 2005-05-06 | Merck Patent Gmbh | Neue materialien für die elektrolumineszenz und deren verwendung |
Non-Patent Citations (1)
| Title |
|---|
| ROST, HÖRHOLD, KREUDER,SPREITZER: "Novel ight-Emitting Poly(arylene vinylene) Copolymer conatining alternating phenylene and TPD units", SPIE CONFERENCE PROCEEDINGS, vol. 3148, no. 18, 1 August 1997 (1997-08-01) - 1997, pages 373 - 381, XP002419822 * |
Cited By (104)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102008017591A1 (de) | 2008-04-07 | 2009-10-08 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008018670A1 (de) | 2008-04-14 | 2009-10-15 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008033943A1 (de) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008050841A1 (de) | 2008-10-08 | 2010-04-15 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| US8637168B2 (en) | 2008-10-08 | 2014-01-28 | Merck Patent Gmbh | Materials for organic electroluminescence devices |
| DE102008050841B4 (de) | 2008-10-08 | 2019-08-01 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| WO2010083869A2 (de) | 2009-01-23 | 2010-07-29 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US8710284B2 (en) | 2009-01-23 | 2014-04-29 | Merck Patent Gmbh | Materials for organic electroluminescent devices containing substituted 10-benzo[c]phenanthrenes |
| US9006503B2 (en) | 2009-01-23 | 2015-04-14 | Merck Patent Gmbh | Organic electroluminescence devices containing substituted benzo[C]phenanthrenes |
| DE102009005746A1 (de) | 2009-01-23 | 2010-07-29 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009009277A1 (de) | 2009-02-17 | 2010-08-19 | Merck Patent Gmbh | Organische elektronische Vorrichtung |
| WO2010094378A1 (de) | 2009-02-17 | 2010-08-26 | Merck Patent Gmbh | Organische elektronische vorrichtung |
| US9066410B2 (en) | 2009-02-17 | 2015-06-23 | Merck Patent Gmbh | Organic electronic device |
| DE102009009277B4 (de) | 2009-02-17 | 2023-12-07 | Merck Patent Gmbh | Organische elektronische Vorrichtung, Verfahren zu deren Herstellung und Verwendung von Verbindungen |
| DE102009034625A1 (de) | 2009-07-27 | 2011-02-03 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| WO2011012212A1 (de) | 2009-07-27 | 2011-02-03 | Merck Patent Gmbh | Neue materialien für organische elektrolumineszenzvorrichtungen |
| DE102009053191A1 (de) | 2009-11-06 | 2011-05-12 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| WO2011054442A2 (de) | 2009-11-06 | 2011-05-12 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2011057701A1 (de) | 2009-11-10 | 2011-05-19 | Merck Patent Gmbh | Organische verbindungen für elektroluminiszenz vorrichtungen |
| DE102009052428A1 (de) | 2009-11-10 | 2011-05-12 | Merck Patent Gmbh | Verbindung für elektronische Vorrichtungen |
| DE102009053644A1 (de) | 2009-11-17 | 2011-05-19 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| WO2011060859A1 (de) | 2009-11-17 | 2011-05-26 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| DE102009053644B4 (de) | 2009-11-17 | 2019-07-04 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010005697A1 (de) | 2010-01-25 | 2011-07-28 | Merck Patent GmbH, 64293 | Verbindungen für elektronische Vorrichtungen |
| WO2011088877A1 (de) | 2010-01-25 | 2011-07-28 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| DE102010009903A1 (de) | 2010-03-02 | 2011-09-08 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| WO2011107186A2 (de) | 2010-03-02 | 2011-09-09 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| DE102010014933A1 (de) | 2010-04-14 | 2011-10-20 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| WO2011128017A1 (de) | 2010-04-14 | 2011-10-20 | Merck Patent Gmbh | Überbrückte triarylamine und -phosphine als materialien für elektronische vorrichtungen |
| WO2011157346A1 (de) | 2010-06-18 | 2011-12-22 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| DE102010024335A1 (de) | 2010-06-18 | 2011-12-22 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| WO2011160757A1 (de) | 2010-06-22 | 2011-12-29 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| DE102010024542A1 (de) | 2010-06-22 | 2011-12-22 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| WO2012016630A1 (de) | 2010-08-05 | 2012-02-09 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| DE102010033548A1 (de) | 2010-08-05 | 2012-02-09 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| WO2012048780A1 (de) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| DE102010048607A1 (de) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| WO2012095143A1 (de) | 2011-01-13 | 2012-07-19 | Merck Patent Gmbh | Verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2012110182A1 (de) | 2011-02-17 | 2012-08-23 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| DE102011011539A1 (de) | 2011-02-17 | 2012-08-23 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| WO2012139692A1 (de) | 2011-04-13 | 2012-10-18 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2012139693A1 (de) | 2011-04-13 | 2012-10-18 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2012143079A1 (de) | 2011-04-18 | 2012-10-26 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2012149999A1 (de) | 2011-05-05 | 2012-11-08 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2012150001A1 (de) | 2011-05-05 | 2012-11-08 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2013013754A1 (en) | 2011-07-25 | 2013-01-31 | Merck Patent Gmbh | Copolymers with functionalized side chains |
| WO2013017189A1 (de) | 2011-07-29 | 2013-02-07 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2013017192A1 (de) | 2011-08-03 | 2013-02-07 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| EP3439065A1 (de) | 2011-08-03 | 2019-02-06 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| WO2013060418A1 (en) | 2011-10-27 | 2013-05-02 | Merck Patent Gmbh | Materials for electronic devices |
| WO2013087142A1 (de) | 2011-12-12 | 2013-06-20 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| DE102012022880A1 (de) | 2011-12-22 | 2013-06-27 | Merck Patent Gmbh | Elektronische Vorrichtungen enthaltend organische Schichten |
| EP3235892A1 (de) | 2012-02-14 | 2017-10-25 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2013120577A1 (en) | 2012-02-14 | 2013-08-22 | Merck Patent Gmbh | Spirobifluorene compounds for organic electroluminescent devices |
| EP3101088A1 (de) | 2012-02-14 | 2016-12-07 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| DE102012011335A1 (de) | 2012-06-06 | 2013-12-12 | Merck Patent Gmbh | Verbindungen für Organische Elekronische Vorrichtungen |
| WO2013182263A1 (de) | 2012-06-06 | 2013-12-12 | Merck Patent Gmbh | Phenanthrenverbindungen für organische elektronische vorrichtungen |
| WO2014015938A1 (de) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Derivate von 2-diarylaminofluoren und diese enthaltnde organische elektronische verbindungen |
| WO2014015935A2 (de) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Verbindungen und organische elektronische vorrichtungen |
| WO2014015937A1 (de) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Verbindungen und organische elektrolumineszierende vorrichtungen |
| EP3424907A2 (de) | 2012-07-23 | 2019-01-09 | Merck Patent GmbH | Verbindungen und organische elektronische vorrichtungen |
| DE202013012401U1 (de) | 2012-07-23 | 2016-10-12 | Merck Patent Gmbh | Verbindungen und Organische Elektronische Vorrichtungen |
| EP3378857A1 (de) | 2012-11-12 | 2018-09-26 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| WO2014082705A1 (de) | 2012-11-30 | 2014-06-05 | Merck Patent Gmbh | Elektronische vorrichtung |
| WO2014106522A1 (de) | 2013-01-03 | 2014-07-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2014106524A2 (de) | 2013-01-03 | 2014-07-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| EP3345984A1 (de) | 2013-12-06 | 2018-07-11 | Merck Patent GmbH | Verbindungen und organische elektronische vorrichtungen |
| EP3693437A1 (de) | 2013-12-06 | 2020-08-12 | Merck Patent GmbH | Verbindungen und organische elektronische vorrichtungen |
| WO2015086108A1 (de) | 2013-12-12 | 2015-06-18 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2016074755A1 (de) | 2014-11-11 | 2016-05-19 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2016119992A1 (en) | 2015-01-30 | 2016-08-04 | Merck Patent Gmbh | Materials for electronic devices |
| WO2017012687A1 (en) | 2015-07-22 | 2017-01-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2017012694A1 (en) | 2015-07-23 | 2017-01-26 | Merck Patent Gmbh | Phenyl derivatives substituted with at least two electron acceptors and at least two electron donors for use in organic electronic devices |
| EP4236652A2 (de) | 2015-07-29 | 2023-08-30 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2017028940A1 (en) | 2015-08-14 | 2017-02-23 | Merck Patent Gmbh | Phenoxazine derivatives for organic electroluminescent devices |
| WO2017036573A1 (en) | 2015-08-28 | 2017-03-09 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2017133829A1 (de) | 2016-02-05 | 2017-08-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| EP3978477A2 (de) | 2016-06-03 | 2022-04-06 | Merck Patent GmbH | Materialien für organische elektrolumineszente vorrichtungen |
| WO2017207596A1 (en) | 2016-06-03 | 2017-12-07 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2018007421A1 (en) | 2016-07-08 | 2018-01-11 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| EP3792235A1 (de) | 2016-07-08 | 2021-03-17 | Merck Patent GmbH | Materialien für organische elektrolumineszente vorrichtungen |
| EP4255151A2 (de) | 2016-10-10 | 2023-10-04 | Merck Patent GmbH | Spiro[fluoren-9,9'-(thio)xanthen] verbindungen |
| WO2018069167A1 (de) | 2016-10-10 | 2018-04-19 | Merck Patent Gmbh | Elektronische vorrichtung |
| EP4113643A1 (de) | 2016-10-10 | 2023-01-04 | Merck Patent GmbH | Elektronische vorrichtung |
| WO2018083053A1 (de) | 2016-11-02 | 2018-05-11 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2018087020A1 (en) | 2016-11-08 | 2018-05-17 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2018095839A1 (de) | 2016-11-22 | 2018-05-31 | Merck Patent Gmbh | Verbrückte triarylamine für elektronische vorrichtungen |
| WO2018095888A1 (en) | 2016-11-25 | 2018-05-31 | Merck Patent Gmbh | Bisbenzofuran-fused 2,8-diaminoindeno[1,2-b]fluorene derivatives and related compounds as materials for organic electroluminescent devices (oled) |
| WO2018095940A1 (en) | 2016-11-25 | 2018-05-31 | Merck Patent Gmbh | Bisbenzofuran-fused indeno[1,2-b]fluorene derivatives and related compounds as materials for organic electroluminescent devices (oled) |
| WO2018134392A1 (en) | 2017-01-23 | 2018-07-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2018141706A1 (de) | 2017-02-02 | 2018-08-09 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2018157981A1 (de) | 2017-03-02 | 2018-09-07 | Merck Patent Gmbh | Materialien für organische elektronische vorrichtungen |
| WO2018197447A1 (de) | 2017-04-25 | 2018-11-01 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2018234346A1 (en) | 2017-06-23 | 2018-12-27 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2019002190A1 (en) | 2017-06-28 | 2019-01-03 | Merck Patent Gmbh | MATERIALS FOR ELECTRONIC DEVICES |
| WO2019020654A1 (en) | 2017-07-28 | 2019-01-31 | Merck Patent Gmbh | SPIROBIFLUORENE DERIVATIVES FOR USE IN ELECTRONIC DEVICES |
| EP4603562A2 (de) | 2017-07-28 | 2025-08-20 | Merck Patent GmbH | Spirobifluorenderivate zur verwendung in elektronischen vorrichtungen |
| WO2019048443A1 (de) | 2017-09-08 | 2019-03-14 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2019101719A1 (de) | 2017-11-23 | 2019-05-31 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| EP4242286A2 (de) | 2017-11-23 | 2023-09-13 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| WO2019115577A1 (en) | 2017-12-15 | 2019-06-20 | Merck Patent Gmbh | Substituted aromatic amines for use in organic electroluminescent devices |
| WO2019121483A1 (en) | 2017-12-20 | 2019-06-27 | Merck Patent Gmbh | Heteroaromatic compounds |
| EP4451832A2 (de) | 2017-12-20 | 2024-10-23 | Merck Patent GmbH | Heteroaromatische verbindungen |
| WO2019175149A1 (en) | 2018-03-16 | 2019-09-19 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
Also Published As
| Publication number | Publication date |
|---|---|
| EP1961016B1 (de) | 2013-06-05 |
| JP5507084B2 (ja) | 2014-05-28 |
| EP2273512B1 (de) | 2016-07-20 |
| TW200736293A (en) | 2007-10-01 |
| JP2009520045A (ja) | 2009-05-21 |
| CN101331558B (zh) | 2012-10-03 |
| EP2273512A3 (de) | 2011-03-09 |
| KR101304153B1 (ko) | 2013-09-04 |
| KR20080078722A (ko) | 2008-08-27 |
| CN101331558A (zh) | 2008-12-24 |
| US20090005505A1 (en) | 2009-01-01 |
| EP1961016A1 (de) | 2008-08-27 |
| DE102005060473A1 (de) | 2007-06-28 |
| EP2273512A2 (de) | 2011-01-12 |
| US7799875B2 (en) | 2010-09-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2273512B1 (de) | Konjugierte Polymere enthaltend Triarylamin-arylvinylen-einheiten, deren Darstellung und Verwendung | |
| EP2052006B1 (de) | Konjugierte polymere, verfahren zu deren herstellung sowie deren verwendung | |
| EP1741148B1 (de) | Elektrolumineszierende polymere enthaltend planare arylamin-einheiten, deren darstellung und verwendung | |
| EP2315792B1 (de) | Elektrolumineszierende polymere, verfahren zu ihrer herstellung sowie ihre verwendung | |
| WO2010136111A1 (de) | Zusammensetzung, enthaltend mindestens eine emitterverbindung und mindestens ein polymer mit konjugationsunterbrechenden einheiten | |
| EP2046785B1 (de) | 1,4-bis(2-thienylvinyl)benzolderivate und ihre verwendung | |
| DE102009023156A1 (de) | Polymere, die substituierte Indenofluorenderivate als Struktureinheit enthalten, Verfahren zu deren Herstellung sowie deren Verwendung | |
| EP1977432A1 (de) | Elektrolumineszierende materialien und deren verwendung | |
| DE102010007938A1 (de) | Elektrolumineszierende Polymere, Verfahren zu ihrer Herstellung sowie ihre Verwendung | |
| EP1741149A1 (de) | Elektrolumineszierende polymere und deren verwendung | |
| WO2006061181A1 (de) | Teilkonjugierte polymere, deren darstellung und verwendung | |
| EP2601237B1 (de) | Polymere mit struktureinheiten, die elektronen-transport-eigenschaften aufweisen | |
| EP2328950A1 (de) | Neue polymere mit niedriger polydispersität | |
| WO2012007102A1 (de) | Polymere materialien für organische elektrolumineszenzvorrichtungen | |
| WO2011009522A2 (de) | Materialien für elektronische vorrichtungen |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 200680047621.9 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application | ||
| WWE | Wipo information: entry into national phase |
Ref document number: 2006818653 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 12097782 Country of ref document: US Ref document number: 2008544785 Country of ref document: JP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2856/KOLNP/2008 Country of ref document: IN |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 1020087017396 Country of ref document: KR |
|
| WWP | Wipo information: published in national office |
Ref document number: 2006818653 Country of ref document: EP |