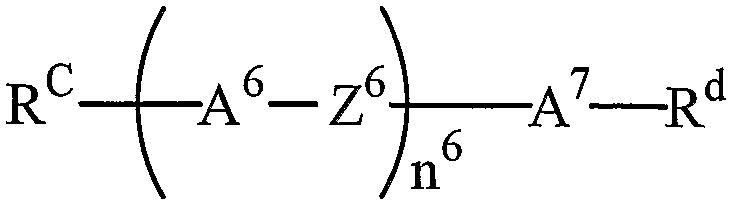' 液晶組成物および液晶素子 技術分野
本発明は、 光学的に等方性の液晶相で駆動させる素子に用いられる光学的に等 方性の液晶組成物およびその組成物を用レ、た液晶素子に関する。 背景技術 明
ネマチック液晶材料をネマチック相が発現している状態から加熱していくと等 糸
方相が発現する。 このようなネマチック液晶材料における等方相 (本明細書中、
「非液晶等方相」 ということがある) では、 電気複屈折値 (等方性媒体に電界を 印加した時に誘起される複屈折値) Δ. n Eが電場 Eの二乗に比例する現象である カー効果 [ Δ η Ε = Κ λ Ε 2 (Κ:カー係数 (カー定数) 、 λ :波長) ] が観測 される。.具体的には、 ネマチック相一等方相転移温度直上において、 大きなカー 係数が観測されている。 このようなカー効果は非液晶等方相中において熱ゆらぎ によ て生じるネマチック的分子配列の短距離秩序の存在に起因するものと考え られている。
液晶材料では、 非液晶等方相だけではなくブルー相においても力一効果が観測 される。 一般的に、 プル一相はキラルネマチック相と非液晶.等方相との間で発現 するが、 その温度範囲は一般に 1〜2 °C程度と極めて狭い。
他方、 高分子とキラル液晶の複合材料において、 比較的広い温度範囲で、 「光 学的に等方性の液晶相 (巨視的には液晶分子配列は等方的であるが微視的には液 晶秩序が存在する相) 」 を発現し、 これらの相では大きなカー係数のカー効果が 観測されている [例えば、 特開 2 0 0 3— 3 2 7 9 6 6号公報、 Nature Materials, 1, 64 - 68 (2002)、 Advanced Materials, 17, 96-98 (2005) 、 Advanced Materials, 17, 2311-2315 (2005)を参照] 。
しかしながら、 このような複合材料では高分子を含有するため、 高電界印加後
に電界を印加しない状態に戻しても複屈折が残存する場合があるという問題点が あった。 また、 高分子を含む複合材料を液晶素子に用いた場合、 駆動電圧の上昇 や長期的信頼性に問題点が生じる可能性があった。 したがって、 表示素子等の液 晶素子では、 高分子との複合材料を用いることができるケースは限られていた。 発明の開示
上記の状況の下、 大きな電気複屈折 (大きなカー係数のカー効果を含む) が観 測できる液晶材料が求められている。 また、 高電界印加後に電界を印加しない状 態に戻しても複屈折が残存しない液晶材料が求められている。 長期的信頼性に優 れた液晶材料が求められている。 また、 高分子を含まない液晶材料が求められて いる。 ' 本発明者等は、 新しい液晶組成物を見出し、 この知見に基づいて本発明を完成 した。 本発明は以下のような液晶組成物および液晶素子等を提供する。 なお、 本明細書において、 特に言及がなければ、 ネマチック相はキラルネマ チック相を含まない、 狭義のネマチック相を意味する。
[ 1 ] 光学的に等方性の液晶相で駆動させる素子に用いられ、 ネマチック相を 発現しない、 光学的に等方性の液晶組成物。 ·
[ 2 ] 光学的に等方性の液晶相が二色以上の回折光を示さない、 請求項 1に記 載の液晶組成物。
[ 3 ] 光学的に等方性の液晶相が二色以上の回折光を示す、 請求項 1に記載の 液晶組成物。
[ 4 ] 透明点 1 の化合物 1と、 透明点 T 2の化合物 2とを含む、 透明点が Τ の液晶組成物であって、 液晶組成物に対して化合物 1を 1 0〜 8 0重量%お よび化合物 2を 2 0〜9 0重量%含み、 透明点 1\と透明点 Τ 2と液晶組成物 の透明点 Τ Xとが、
τ χ > τ 2
T「Tx≥ 1 00°C
を満たす、 [ 2 ] または [ 3 ] に記載の液晶組成物。
[5] 透明点 1\の化合物 1と、 透明点 T2の化合物 2とを含む、 透明点が T Xの液晶組成物であって、 液晶組成物に対して化合物 1を.5〜 70重量%およ び化合物 2を 30〜 9 5重量%含み、 透明点 1\と透明点 Τ2と液晶組成物の透 明点 Τ Xとが、
Τ! > Τ 2'
Τ! -Τ ≥ 1 50°C
を満たす、 [ 2 ] または [ 3 ] に記載の液晶組成物。
[6] 透明点 T\の化合物 1と、 透明点 T2の化合物 2とを含む、 透明点が T の液晶組成物であって、 液晶組成物に対して化合物 1を 5〜 70重量%およ ぴ化合物 2を 30〜9 5重量%含み、 透明点 1\と透明点 Τ2と液晶組成物の透 明点 Τχとが、
ΤΧ>Τ2
T1-Tx≥ 200°C
を満たす、 [ 2 ] または [ 3 ] に記載の液晶組成物。
[7} 透明点 T\の化合物 1と、 透明点 Τ2の化合物 2とを含む、 透明点が Τ Xの液晶組成物であって、 液晶組成物に対して化合物 1を 1 0〜 80重量%およ び化合物 2を 20〜 90重量%含み、 透明点 1\と透明点 Τ2と液晶組成物の透 明点 Τχと力
τχ>τ2
Ί 一 Tx≥ 1 00°C
を満たし、 キラルネマチック相と非液晶等方相とが共存する上限温度と下限温 度との差が 3°C〜1 50°Cである組成物に、 さらにキラル剤を添加して得られる.
[ 2 ] または [ 3 ] に記載の液晶組成物。
[8] 透明点 1\の化合物 1と、 透明点 T2の化合物 2とを含む、 透明点が Τ の液晶組成物であって、 液晶組成物に対して化合物 1を 5〜 70重量%および 化合物 2を 3 0〜 9 5重量%含み、 透明点 と透明点 Τ2と液晶組成物の透明
点 T χと力
τ\>τ2
Τ\一 Tx≥ 1 50°C '
を満たし、 キラルネマチック相と非液晶等方相とが共存する上限温度と下限温 度との差が 3°C〜 1 50°Cである組成物に、 さらにキラル剤を添加して得られる
[ 2 ] または [ 3 ] に記載の液晶組成物。
[9] 液晶組成物に対して化合物 1を 30〜60重量%、 および、 化合物 2を 30〜 70重量%含む、 請求項 7に記載の液晶組成物。
[1 0] 化合物 1が、'下記一般式 ( 1 )
(式中、 Raは水素、 炭素数 1〜 20のアルキルであり、 このアルキル中の任意 の一 CH2_は、 一 O—、 一 一、 一 COO—、 一 OCO—、 - CH= CH-, —CF=CF—または一 C≡C一で置き換えられてもよく、 このアルキル基中の 任意の水素はハロゲンで置き換えられてもよく ; Rbは水素、 ハロゲン、 一 CN _N = C = 0、 一 N = C = S、 _CF3、 一 O C F 3または炭素数 1〜 20のァ ルキルであり、 このアルキル中の任意の一 CH2_は、 一0—、 一 S—、 -CO O—、 一 OCO_、 一 CH=CH―、 一 CF = CF—または一 C≡G—で置き換 えられてもよく、 このアルキル中の任意の水素はハロゲンで置き換えられてもよ く、 このアルキル中の一 CH3は一 CNで置き換えられてもよく ; 八ェ〜 5は独 立に芳香族性あるいは非芳香族性の 3〜 8員環、 または炭素数 9以上の縮合環で あり、 これらの環の任 の水素がハロゲン、 炭素数 1〜3のアルキル、 またはハ ロゲン化アルキルで置き換えられてもよく、 環の一 CH2—は一 O—、 一 S—ま たは一NH—で置き換えられてもよく、 一 CH =は一 N二で置き換えられてもよ いが、 A A5がテトラヒ ドロピラン環であることはなく、 ; Zi Z4は独立
に単結合、 炭素数 1〜 8のアルキレンであり、 このアルキレン中の任意の一 CH 2—は、 一 O—、 — S―、 一 COO—、 一 OCO—、 一 C SO—、 一 OC S—、 — N = N―、 — CH = N―、 一 N = CH—、 一 N (O) =N—、 一 N = N (O) ―、 一CH = CH—、 一CF = CF—または一C≡C一で置き換えられてもよく 任意の水素はハロゲンで置き換えられてもよく ; nェ〜11 3は独立に 0または 1 であり、 Rbが水素またはフッ素の場合は n 2および η 3は 1であり、 ∑4が一。 ΟΟ—である場合は、 η2と η3が 1であり、 A 4または A 5の少なく とも一つ が炭素数 9以上の縮合環である場合のみ!! 1〜 n 3すべてが 0となり うる。 ) で 表され、 透明点が 1 5 0 °C〜 4 0 0 °Cである化合物である、 [ 4 :! 〜
[ 9 ] のいずれか 1項に記載の液晶組成物。
[1 1] Raは炭素数 1〜 1 0のアルキルであり、 このアルキル中の任意の一 CH2—は、 一O—、 一S—、 一 COO—、 一OCO_、 一 CH = CH—または 一 C≡C一で置き換えられてもよく ; Rbはハロゲン、 一 CN、 _N=C = 0、 一 N = C= S、 一 CF3、 一 OC F 3または炭素数:!〜 20のアルキルであり、 このアルキル中の任意の一 CH2—は、 一 O—、 一 CH = CH—または一 C≡C 一で置き換えられてもよく、 このアルキル中の任意の水素はハロゲンで置き換え られてもよく、 このアルキル中の一CH3は一 CNで置き換えられてもよく ; A 〜 5は独立にベンゼン環、 ナフタレン環またはシクロへキサン環であり、 こ れらの環の任意の水素がハロゲン、.炭素数 1〜3のアルキル、 またはハロゲン化 アルキルで置き換えられてもよく、 環の一 CH2—は一 O—または一 S—で置き 換えられてもよく、 一 CH =は一 N==で置き換えられてもよく ; 1〜 4は独 立に単結合、 炭素数 1〜4のアルキレンであり、 このアルキレン中の任意の一 C H2—は、 一〇一、 一 S—、 一 COO—、 一OCO—、 一 C SO—、 一 OC S— 一 CH = CH—、 一 C.F = C F—または一 C≡C—で置き換えられてもよく、 任 意の水素はハロゲンで置き換えられてもよく ; n 3は独立に 0または 1で あり、 Rbが水素またはフッ素の場合は n 2および n 3は 1であり、 A4または A 5の少なく とも一つが炭素数 9以上の縮合環である場合のみ r! 1〜 113すべてが 0となり うる、 [1 0] に記載の液晶組成物。
W 200
[1 2] Raが炭素数 1〜 1 ひのアルキルであり、 このアルキル中の任意の一 CH2—は、 一CH = CH—または一 C三 C—で置き換えられてもよく ; Rbは フッ素、 塩素、 一 CN、 一 N = C = Sまたは炭素数 1〜20のアルキルであり、 このアルキル中の任意の一 CH2—は、 一O—、. 一 CH=CH—または一 Cミ C 一で置き換えられてもよく ; ュ〜 5が独立にベンゼン環、 ナフタレン環また はシクロへキサン環であり、 これらの環の任意の水素がフッ素または塩素、 メチ ル、 またはハロゲン化メチルで置き換えられてもよく、 一 CH2—は一 O—また は一 S—で置き換えられてもよく、 一 CH =は一 N =で置き換えられてもよく ; Zェ〜 4は独立に単結合または一 C≡C一であり ; r! 1〜 n 3は独立に 0または 1であり、 Rbが水素またはフッ素の場合は η 2および n 3は 1であり、 A 4また は A 5の少なく とも一つが炭素数 9以上の縮合環である場合のみ n 3すべ てが 0となり うる、 [1 0] に記載の液晶組成物。
[1 3] Raが炭素数 1〜1 0のアルキルであり、 このアルキル中の任意の一 CH2—は、 一 O—または一 CH=CH—で置き換えられてもよく ; Rbがフッ 素、 塩素、 _CN、 または炭素数 1〜 1 0のアルキルであり、 このアルキル中の 任意の一 CH2—は、 一 O—で置き換えられてもよく ;
Ai〜A5が独立にベンゼン環、 ジォキサン環またはシク口へキサン環であり . ベンゼン環の任意の水素がフッ素で置き換えられてもよく ; Zi〜Z4は独立に 単結合または一 C≡C一であり ; n 1が 1、 n2と n3が 0である、 [1 0] に記 載の液晶組成物。 .
(式中、 は水素、 炭素数 1〜 20のアルキルであり、 このアルキル中の任意 の _CH2—は、 _〇一、 一S—、 一 COO—、 一 OCO—、 _CH=CH—、 一 CF二 CF—または一 C≡C一で置き換えられてもよく、 このアルキル中の任 意の水素はハロゲンで置き換えられてもよく ; Rdはハロゲン、 一 CN、 一 N =
C = 0、 _N = C = S、 一CF3、 一 OCF3、 一 C≡C— CN、 または一 C≡ C一 C F 3であり' ; A6と A7は独立に芳香族性あるいは非芳香族性の 3〜 8員環 または炭素数 9以上の縮合環であり、 この環の任意の水素がハロゲン、 炭素数 1 〜 3のアルキル、 またはハロゲン化アルキルで置き換えられてもよく、 この環の 任意の一 CH2—は一 O—、 一 S—または— NH—で置き換えられてもよく、 一 CH =は—N =で置き換えられてもよく ; Z6は単結合または炭素数 1〜8のァ ルキレンで り、 このアルキレン中の任意の一 CH2—は、 一 O—、 一 S—、 - COO—、 一 OCO—、 一 C SO—、 一 OC S—、 一 N = N—、 一 CH = N—、 一 N=CH―、 -N (0) =N—、 -N = N (O) 一、 —CH = CH—、 - C F =C F—または一 C≡C一で置き換えられてもよく、 このアルキレン中の任意の 水素はハロゲンで置き換えられてもよく ; n6は 0または 1であり、 A7が炭素 数 9以上の縮合環である場合、 n6は 0である。 ) で表される化合物である [ 1 0] 〜 [1 3] のいずれか 1項に記載の液晶組成物。
[1 5] Reは炭素数 1〜1 0のアルキルであり、 このアルキル中の任意の一 CH2 は、 一 O—、 一 S—、 一COO—、 一 OCO—、 一 CH=CH—または — C≡C一で置き換えられてもよく ; Rdはハロゲン、 一 CN、 一 N = C=S、 — CF3、 一 C≡C一 CN、 一 C≡C— CF3であり ; A6と A7は独立にベンゼ ン環、 ナフタレン環、 シクロへキサン環であり、 これらの環の任意の水素がハロ ゲン、 炭素数 1 ~ 3のアルキル、 またはハロゲン化アルキルで置き換えられても よく、 この環の任意の一 CH2—は一 O—または一 S—で置.き換えられてもよく , 一 CH =は—N =で置き換えられてもよく ; Z 6は単結合、 炭素数 1〜4のアル キレンであり、 このアルキレン中の任意の一 CH2—は、 _〇一、 一 S―、 - C 0〇一、 一 OCO—、 一 CSO—、 一 OC S—、 一 CH=CH—、 -C F = C F 一または一 C≡C一で置き換えられてもよく、 このアルキレン中の任意の水素は ハロゲンで置き換えられてもよく ; n6は 0または 1であり、 A7がナフタレン 環である場合、 n6は 0である、 [1 0] 〜 [1 3] のいずれか 1項に記載の液 晶組成物。
[1 6] Rcは炭素数 1〜 1 0のアルキルであり、 このアルキル中の任意の一
CH2—は、 一 CH-CH—または一 C三 C—で置き換えられてもよく ; Rdは ハロゲン、 一 CN、 一 N=C = S、 一 CF3、 一 C≡C一 CN、 一 Cョ C— CF 3であり ; A6と A7は独立にベンゼン環、 ナフタレン環、 シクロへキサン環であ り、 これらの環の任意の水素がフッ素または塩素、 メチル、 またはハロゲン化メ チルで置き換えられてもよく、 この環の任意の一 CH2—は一 O—または一 S— で置き換えられてもよく、 一 CH=は一 N=で置き換えられてもよく ; Z6は単 結合、 一 COO—、 一CF2〇一または一 C≡C一であり ; 11 6は0または 1で あり、 A7がナフタレン環である場合は 0である、 [1 0] 〜 [1 3] のいずれ か 1項に記載の液晶組成物。
[1 7] R。は炭素数 1〜 1 0のアルキルであり、 このアルキル中の任意の一 CH2—は、 一 0—で置き換えられてもよく ; Rdはハロゲン、 一 CNであり ; A 6と A7は独立にベンゼン環、 ジォキサン環またはシクロへキサン環であり、 ベンゼン環の任意の水素がフッ素で置き換えられてもよく ; Z 6は単結合または 一 COO—であり ; n6は 0または 1であり、 [1 0]' 〜 [1 3] のいずれか 1 項に記載の液晶組成物。
[1 8] 化合物 2が、 下記一般式 (3)
(式中、 Reは炭素数 1〜 1 0のアルキルであり、 このアルキル中の任意の一 C H2—は、 一 O—、 一S―、 一 CO〇_、 一OCO—、 一 CH = CH—、 一 CF =C F—または一 C≡C一で置き換えられてもよく、 このアルキル中の任意の水 素はハロゲンで置き換えられてもよく ; Xaはフッ素、 塩素、 一 CN、 -N = C =S、 一 CF3—、 一 C≡C一 CNまたは一 C≡C— CF3であり ; Z 12は単結 合、 一 COO—まだは一 C≡C一であり ; Ls〜Lnは独立して水素またはフッ 素である。 ) で表される化合物である、 [1 0] 〜 [1 3] のいずれか 1項
に記載の液晶組成物。
[1 9] Reは炭素数 1〜 10のアルキルであり、 このアルキル中の任意の一 CH2—は、 一 O—、 一CH=CH—または一 C≡C一で置き換えられてもよ く ;
Xaはフッ素または一CNであり ; Z 12は一 CO〇一であり、 L8〜Lnは独 立して水素またはフッ素であり、 それらの少なくとも 2個以上がフッ素である、 [10] 〜 [1 3] のいずれか 1項に記載の液晶組成物。
[20] キラルネマチック相と非液晶等方相とが共存する上限温度と下限温度 との差が 3°C〜150°Cである組成物に、 さらにキラル剤を添加して得られる、 [ 2 ] または [ 3 ] に記載の液晶組成物。
[21] キラルネマチック相と非液晶等方相とが共存する上限温度と下限瘟度 との差が 5°C〜 1 50である組成物に、 さらにキラル剤を添加して得られる、
[ 2 ] または [ 3 ] に記載の液晶.組成物。
[22] ネマチック相と非液晶等方相とが共存する上限温度と下限温度との差 が 3 °C〜 1 5 0 °Cである組成物に、 さらにキラル剤を添加して得られる、 [ 2 ] または [ 3 ] に記載の液晶組成物。
[2 3] 液晶組成物の全重量に対して、 キラル剤を 1〜 40重量%含む、 [1] 〜 [22] のいずれか 1項に記載の液晶組成物。
[24] 液晶組成物の全重量に対して、 キラル剤を 5〜 1 5重量%含む、 [1] 〜 [22] のいずれか 1項に記載の液晶組成物。 .
[25] ピッチが 700 nm以下である、 [23] または [24] に記載の液 晶組成物。
[26] キラル剤が、 下記式 (K1) 〜 (K5)
(式 (.K l) 〜 (K 5) 中、 RKは独立に、 水素、 ハロゲン、 一 CN、 -N = C =0、 一 N = C = Sまたは炭'素数;!〜 20のァノレキノレであり、 このァノレキル中の 任意の一 CH2 —は、 一0—、 一S—、 一 COO—、 _OCO—、 _CH=CH ―、 一 CF = CF—または一 C≡C一で置き換えられてもよく、 このアルキル中 の任意の水素はハロゲンで置き換えられてもよく ; Aは独立に、 芳香族性あるい は非芳香族性の 3ないし 8員環、 または、 炭素数 9以上の縮合環であり、 これら の環の任意の水素がハロゲン、 炭素数 1〜 3のアルキルまたはハロアルキルで置 き換えられてもよく、 環の一 CH2 —は一 O—、 一 S—または一 NH—で置き換 えられてもよく、 一 CH =は一N =で置き換えられてもよく ; Zは独立に、 単結 合、 炭素数 1〜8のァ レキレンであるが、 任意の一 CH2 —は、 一 O—、 一 S— 一 COO—、 一 OCO—、 一 CSO—、 一 OCS—、 一 N = N—、 一 CH = N— 一 N=CH—、 一 N (O) =N—、 一 N = N (O) 一、 一 CH=CH—、 一 CF =CF—または一 C≡C—で置き換えられてもよく、 任意の水素はハロゲンで置 き換えられてもよく ; Xは単結合、 一 COO—、 一 CH2 O—、 一 CF2 O—、
-CH2 CH2 —であり ; mは;!〜 4である。 )
で表される化合物を 1種以上含む、 [23] 〜 [25] のいずれか 1項に記載の 液晶組成物。
[27] キラル剤が、 下記式 (K2— 1) 〜 (K2— 8) および (K5— 1) 〜 (K 5 _ 3)
(K2-4)
(R
K は独立に、 炭素数 3〜 1 0のアルキルであり、 このアルキル中の環に隣接 する一CH
2—は一 O—で置き換えられてもよく、 任意の一 CH
2 - は、 一 CH
=CH—で置き換えられてもよい。 ) で表される化合物を 1種以上含む、 [2 3] 〜 [25] のいずれか 1項に記載の液晶組成物。
[2 8] 透明点 1\の化合物 1と、 透明点 T2の化合物 2とキラル剤とを含む 透明点が Τ Xの液晶組成物であって、 液晶組成物に対して化合物 1を 20〜40 重量%、 化合物 2を 20〜60重量%およびキラル剤を 5〜20重量%含み、 化合物 1が下記一般式 (1)
(式中、 Raおよび Rbは、 それぞれ独立して炭素数 1〜 1 0のアルキルであり このアルキル中の任意の一 CH2—は、 一 O—で置き換えられてもよく ;八1〜 A4が独立にベンゼン環、 ジォキサン環またはシクロへキサン環であり、 これら の環の任意の水素がフッ素で置き換えられてもよく、 .A 5がベンゼン環であり ; Z 〜 4は独立に単結合または一 C≡C一であり ; n 1が 1、 n2と n 3が 0で ある) で表される化合物であり、
化合物 2が下記一般式 (2)
(式中、 R
eは炭素数 1〜 1 0のアルキルであり、 このアルキル中の任意の一 C H
2—は、 一O—で置き換えられてもよく ; R
dはハロゲン、 一CNであり ; A
6 はベンゼン環またはシクロへキサン環であり、 これらの環の任意の水素がフッ素 で置き換えられてもよ'く、 A
7は独立にベンゼン環であり ; Z
6は単結合または 一 COO—であり ; n
6は 1である。 ) で表される化合物と、 下記一般式 (3)
(式中、 Reは炭素数 1〜1 0のアルキルであり、 このアルキル中の任意の一 C H2—は、 一O—、 一CH=CH—または一 C≡C一で置き換えられてもよく ; Xaはフッ素または一 CNであり'; Z 12は一 COO—であり、 し8〜!^11は独 立して水素またはフッ素であり、 それらの少なくとも 2個以上がフッ素であり、 L1 Qおよび L11のうち少なくとも 1つはフッ素である。 ) で表される化合物と からなり、 キラル剤が、 下記式 (K2 - 5) 〜 (K 2 - 8)
、
(R
Kは独立に、 炭素数 3〜 1 0のアルキルであり、 このアルキル中の環に隣接 する一 CH
2—は一 O—で置き換えられてもよく、 任意の一 CH
2 — は、 一 CH =CH—で置き換えられてもよい。 ) で表される化合物を 1種以上含み、 透明点 T iと透明点 T
2と液晶組成物の透明点 T Xとが、
T1>T2
1\一 Tx≥ 1 00°C
を満たし、 光学的に等方性の液晶相が二色以上の回折光を示さない光学的に等 方性の相を有する液晶組成物。
[2 9] 透明点 1\の化合物 1と、 透明点 T2の化合物 2とキラル剤とを含む 透明点が Τ Xの液晶組成物であって、 液晶組成物に対して化合物 1を 8〜 30重 量%、 化合物 2を 40〜60重量%およびキラル剤を 5〜20重量%含み、 化合物 1が下記一般式 (1)
(式中、 Raは、 炭素数 1〜1 0のアルキルであり、 このアルキル中の任意の一 CH2—は、 一 O—で置き換えられてもよく ; ェ〜 4が独立にベンゼン環、 ジ ォキサン環またはシクロへキサン環であり、 これらベンゼン環の任意の水素がフ ッ素で置き換えられてもよく、 A5がベンゼン環であり ; Zi Z4は独立に単結 合または一 C≡C一であり ; n1と n2が 1、 n3が 0である)
で表される化合物であり、 化合物 2が下記一般式 (3)
(式中、 Reは炭素数 1〜 1 0のアルキルであり、 このアルキル中の任意の一 C H2—は、 _〇一、 一 CH=CH—または一 C≡C—で置き換えられてもよく ; Xaはフッ素または一 CNであり ; Z12は一COO—であり、 L8〜Lnは独 立して水素またはフッ素であり、 それらの少なくとも 2個以上がフッ素であり、 L1 Gおよび L11のうち少なくとも 1つはフッ素である。 ) で表される化合物で あり、 キラル剤が、 下記式 (K2— 5) 〜 (K2— 8)
(RKは独立に、 炭素数 3〜 1 0のアルキルであり、 このアルキル中の環に隣接 する— CH2—は一 O—で置き換えら.れてもよく、 任意の一 CH2―は、 一CH =CH—で置き換えられてもよい。 ) で表される化合物を 1種以上含み、 透明点 1\と透明点 T2と液晶組成物の透明点 Txとが、
τ,>τ2
を満たし、 光学的に等方性の液晶相が二色以上の回折光を示す光学的に等方性 の相を有する液晶組成物。 .
[30] 透明点 の化合物 1と、 透明点 T2の化合物 2とキラル剤とを含む 透明点が Τ Xの液晶組成物であって、 液晶組成物に対して化合物 1を 20〜 40 重量%、 化合物 2を 20〜60重量%およぴキラル剤を 5〜25重量%含み、 化合物 1が下記一般式 (1)
(式中、 R aが炭素数 1〜 1 0のアルキルであり、 このアルキル中の任意の一 C
H2—は、 一O—で置き換えられてもよく ; Rbは、 ハロゲン、 一 CN、 -N = C = 0、 一 N=C=S、 一 C F3、 一OC F3であり ; A 〜A4が独立にベンゼ ン環、 ジォキサン環またはシクロへキサン環であり、 ベンゼン環の任意の水素が フッ素で置き換えられてもよく、 A5がベンゼン環であり ; 1〜?4は独立に単 結合または一 C≡C—であり ; n1が 1、 n2と n3が 0である) で表される化合 物であり、 化合物 2が下記一般式 (2)
(式中、 Rcは炭素数 1〜 1 0のアルキルであり、 このアルキル中の任意の一 C H2—は、 一O—で置き換えられてもよく ; Rdはハロゲン、 一 CNであり ; A6 はベンゼン環またはシクロへキサン環であり、 これらの環の任意の水素がフッ素 で置き換えられてもよく、 A7は独立にベンゼン環であり ; Z 6は単結合または 一 COO—であり ; n6は 1である。 ) で表される化合物と、 下記一般式 (3)
(式中、 R
eは炭素数 1〜 1 0のアルキルであり、 このアルキル中め任意の一 C H
2—は、 一 O—、 一 CH=CH—または一 C≡C—で置き換えられてもよく ; X
aはフッ素または一 CNであり ; Z
12は一 COO—であり、 し
8〜!^
11は独立 して水素またはフッ素であり、 それらの少なくとも 2個以上がフッ素であり、 L 1
0および L
11のうち少なく とも 1つはフッ素である。 ) で表される化合物とか らなり、 キラル剤が、 下記式 (K2— 5) 〜 (K2— 8)
(RKは独立に、 炭素数 3〜 1 0のアルキルであり、 このアルキル中の環に隣接 する _CH2—は一 O—で置き換えられてもよく、 任意の _CH2 - は、 一 CH =CH—で置き換えられてもよい。 ) で表される化合物を 1種以上含み、 透明点 T と透明点 T 2と液晶組成物の透明点 T Xとが、
τ,>τ2
Τ ^-Τ X ≥ 1 0 o°c
を満たし、 光学的に等方性の液晶相が二色以上の回折光を示さない光学的に等 方性の相を有する液晶組成物。 . · [3 1] 一方または両方の面に電極が配置され、 基板間に配置された液晶 組成物、 および電極を介して液晶組成物に電界を印加する電界印加手段を備 えた液晶素子であって、 前記液晶組成物が、 [1] 〜 [3 0] のいずれか 1項に 記載の液晶組成物である液晶素子。
[3 2] —方または両方の面に電極が配置され、 少なくとも一方が透明な一組 の基板、 基板間に配置された液晶組成物、 および基板の外側に配置され た偏光板を有し、 電極を介して液晶組成物に電界を印加する電界印加手段を備え た液晶素子であって、 前記液晶組成物が、 [1] 〜 [30] のいずれか 1項に記 載の液晶組成物である液晶素子。
[33] 一組の基板の少なくとも一方の基板上において、 少なくとも 2方向に 電界を印加できるように電極が構成されている [32] に記載の液晶素子。
[34] 互いに平行に配置された一組の基板の一方または両方に、 少なくとも 2方向に電界を印加できるように電極が構成されている [3.2] に記載の液晶素 子。
[35] 電極がマトリックス状に配置されて、 画素電極を構成し、 各画素がァ クティブ素子を備え、 このアクティブ素子が薄膜トランジスター' (TFT) であ る [3 1] [34] のいずれか 1項に記載の液晶素子。
[36] 透明点 1\の化合物 1と、 透明点 T2の化合物 2とを含む、 透明点が Τ Xの液晶組成物であって、 液晶組成物に対して化合物 1を 1 0〜 80重量%お よび化合物 2を 20〜90重量%含み、 透明点 1\と透明点 Τ2と液晶組成物の 透明点 Τ Xとが、
τχ>τ2
を満たす、 光学的に等方性の液晶相で駆動させる素子に用いられる液 晶組成物。
[ 3 '7 ] キラルネマチック相と非液晶等方相とが共存する上限温度 と下限温度との差が 3 °C〜 1 5 0 °Cである、 光学的に等方性の液晶相 で駆動させる素子に用いられる液晶組成物の成分である液晶組成物。
[ 3 8 ] キラルネマチック相と非液晶等方相とが *存する上限温度 と下限温度との差が 3 °C〜 1 5 0 °Cである、 [ 3 6 ] に記載の液晶組 成物。
[39] 化合物 1が、 下記一般式 ( 1 )
(式中、 R
aは水素、 炭素数 1〜20のアルキルであり、 このアルキル中の任意 の _CH
2—は、 一 O—、 一 S—、 一COO—、 一 OCO—、 一 CH=CH—、 —CF=CF—または一 C≡C一で置き換えられてもよく、 このアルキル基中の 任意の水素はハロゲンで置き換えられてもよく .; R
bは水素、 ハロゲン、 一 CN、 一 N=C =〇、 一 N = C = S、 — C F
3、 一 OC F
3または炭素数:!〜 20のァ ルキルであり、 このアルキル中の任意の一 CH
2—は、 一O—、 一 S―、 一 CO O—、 —OCO—、 一 CH=CH—、 一 CF=CF—または一 C≡C—で置き換 えられてもよく、 このアルキル中の任意の水素はハロゲンで置き換えられてもよ く、 このアルキル中の一 CH
3は一 CNで置き換えられてもよく ; 八 〜八
5は独 立に芳香族性あるいは非芳香族性の 3〜 8員環、 または炭素数 9以上の縮合環で あり、 これらの環の任意の水素がハロゲン、 炭素数 1〜 3のアルキル、 またはハ ロゲン化アルキルで置き換えられてもよく、 環の一 CH
2—は一 O—、 一 S—ま たは一 NH—で置き換えられてもよぐ、 一 CH =は一 N =で置き換えられてもよ いが、 〜
5がテトラヒ ドロピラン環であることはなく、 ;
1〜
4は独立 に単結合、 炭素数 1〜8のアルキレンであり、 このアルキレン中の任意の一 CH
2—は、 一 O—、 一 S—、 _COO_、 _OCO—、 一 C SO—、 一 OC S—、 — N N—、 一 CH = N—、 一 N = CH—、 一 N (O) =N—、 -N = N (O) ―、 _CH=CH—、 一 C F = C F—または一 Cョ C一で置き換えられてもよく、 任意の水素はハロゲンで置き換えられてもよく ; n
3は独立に 0または 1 であり、 R
bが水素またはフッ素の場合は n
2および n
3は 1であり、 Z
4がー C 0〇一である場合は、 n
2と n
3が 1であり、 A4または A 5の少なく とも一つ が炭素数 9以上の縮合環である場合のみ n
3すべてが 0となり うる。 ) で 表され透明点が 1 50°C〜400°Cである化合物である、 [ 3 6 ] または
[ 3 8 ] に記載の液晶組成物。
(式中、 Reは水素、 炭素数 1〜 20のアルキルであり、 このアルキル中の任意 の一 CH2—は、 一 O—、 一 S—、 一COO—、 一 OCO—、 一 CH=CH—、 一 CF = CF—または一 C≡C一で置き換えられてもよく、 このアルキル中の任 意の水素はハロゲンで置き換えられてもよく ; Rdはハロゲン、 CN、 _N = C = 0、 一 N = C = S、 一CF3、 一 OC F3、 一 C≡C一 CN、 または一 C≡ C一 CF3であり ; A6と A7は独立に芳香族性あるいは非芳香族性の 3〜8員環、 または炭素数 9以上の縮合環であり、 この環の任意の水素がハロゲン、 炭素数 1 〜 3のアルキル、 またはハロゲン化アルキルで置き換えられてもよく、 この環の 任意の一 CH2—は一0—、 一 S—または一 NH—で置き換えられてもよく、 一 CH =は一 N =で置き換えられてもよく ; Z 6は単結合または炭素数 1〜8のァ ルキレンであり、 このアルキレン中の任意の一 CH2 は、 一〇_、 一 S—、 一 COO—、 一 OCO—、 一 C SO—、 一 OC S—、 一 N = N—、 一 CH = N—、 _N=CH—、 一 N (O) 二 N―、 一 N = N (〇) 一、 一 CH = CH—、 一 CF =CF—または一 C≡C一で置き換えられてもよく、 このアルキレン中の任意の 水素はハロゲンで置き換えられてもよく ; n6は 0または 1であり、 A7が炭素 数 9以上の縮合環である場合、 n6は 0である。 ) で表される化合物である [3 6] 、 [38] または [3 9] に記載の液晶組成物。
[41] 化合物 2が、 下記一般式 (3) '
(式中、 Reは炭素数 1〜1 0のアルキルであり、 このアルキル中の任意の一 C H。一は、 一 O—、 一 S—、 一 COO—、 一 OCO—、 一 CH = CH—、 一 CF
=C F—または— C≡C—で置き換えられてもよく、 このアルキル中の任意の水 素はハロゲンで置き換えられてもよく ; Xaはフッ素、 塩素、 一 CN、 -N = C =S、 一CF3—、 一 Cョ C— CNまたは一 C≡C— CF3であり ; Z 12は単結 合、 一 COO—または一 C≡ C一であり ; L^^L11は独立して水素またはフッ 素である。 ) で表される化合物である、 [36] または [3 8] 〜 [40] のいずれか 1項に記載の液晶組成物。 本発明の好ましい態様に係る液晶組成物は、 高分子物質を実質的に含まずに、 光学的に等方性の液晶相を広い温度範囲で発現させることができる。 また、 本発 明の好ましい態様に係る液晶組成物は、 大きな電気複屈折 (大きなカー係数の力 一効果を含む) が観測できる。 また、 本発明の好ましい態様に係る液晶組成物は、 応答速度が極めて速く、 また単色化が可能である。 本発明の好ましい態様に係る 液晶組成物は、 高電界印加後に電界を印加しない状態に戻しても残留する複屈折 を軽減できる。 また、 本発明の好ましい態様に係る液晶組成物は、 これらの効果 に基づいて表示素子等の液晶素子等に好適に用いることができる。 図面の簡単な説明
図 1は、 液晶組成物 B— 2の降温過程における偏光顕微鏡像を示す。
図 2は、 実施例 5で用いた櫛型電極基板を示す。
図 3は、 実施例 5で用いた光学系を示す。 . 発明を実施するための最良の形態
本発明の液晶組成物は、 光学的に等方性の液晶相で駆動させる素子に用いられ る光学的に等方性の液晶組成物である。 すなわち、 本発明の液晶組成物は、 液晶 素子に用いられる液晶組成物であって、 光学的に等方性の性質を示す液晶状態 (例えばブルー相) で液晶素子に用いることができる液晶組成物である。
ネマチック相 (キラルネマチック相を除く) を発現する液晶組成物は、 どのよ うな温度でも光学的に等方性の液晶相を発現しない。 したがって、 本発明の液晶
組成物は、 ネマチック相を、 どのような温度でも発現しない組成物である。
また、 ネマチック相とキラルネマチック相は共に光学的に等方性の相ではない。 したがって、 光学的に等方性の液晶相で駆動する素子に用いる本発明の液晶組成 物は、 ネマチック相またはキラルネマチック相で駆動される素子に用いられる液 晶組成物を含まない。
本発明の液晶組成物は、 たとえば、 式 ( 1 ) で表される化合物 1 と、 式 ( 2 ) または式 ( 3 ) で表される化合物 2 とを混合して得られる液 晶組成物 A、 および当該組成物にさ らに一定量のキラル剤を添加して 得られる、 光学的に等方性の液晶相を発現する液晶組成物 Bである。 ただし液晶組成物 Aは光学的に等方性の液晶相を発現しない範囲内で キラル剤を含有していてもよい。
本発明の液晶組成物 Aにおいて、 化合物 1 は、 式 ( 1 ) で表される 1つの化合物でも、 式 ( 1 ) で表される複数の化合物からなるもので もよい。 同様に、 化合物 2は、 式 ( 2 ) または式 ( 3 ) で表される 1 つの化合物でも、 式 ( 2 ) または式 ( 3 ) で表される複数の化合物か らなるものでもよレ、。
また、 本明細書において、 液晶組成物とは液晶相を有する組成物、 ま たは、 液晶材料との混合により液晶相一非液晶等方相転移温度を著しく低下させ ることのないものをいう。
また、 液晶性化合物あるいは液晶性組成物が液晶相を発 しない場合は、 後述 する液晶相一非液晶等方相転移点の外挿法による算出法を適用する。 液晶相一非 液晶等方相転移点が液晶の熱分解温度より高温である化合物、 組成物についても この外揷法を適用してもよい。 1 液晶組成物 A
1 . 1 透明点
本発明の液晶組成物 Aにおいて、 当該液晶組成物 Aに含まれる化合 物 1 の透明点 ( T ) と化合物 2 の透明点 ( T 2 ) と液晶組成物 Aの
透明点 ( T X ) は、
T ! > T 2
T i— T x ^ l O O :
を満たすこ とが好ま しい。 また、 .
T x > T 2
— T x≥ 1 5 0。C
であるこ がさ らに好ま しい。
ここで、 透明点とは、 化合物または組成物が昇温過程で、 非液晶等 方相を発現する点をいう。 透明点の具体例と しては、 ネマチック相か ら非液晶等方相への相転移点である N— I 点等が挙げられる。 また、 本発明の液晶組成物の場合、 非液晶等方相と液晶相の共存状態が発現すること があるが、 この場合は昇温過程において非液晶等方相が最初に発現した温度を透 明点とする。 また液晶相を発現しない化合物、 すなわち K一 I点を有する化合物 の透明点は、 K— I点以下であり、 必要に応じて、 後述の液晶相一非液晶等方相 転移点の外揷法による算出法を適用してもよい。
1. 2 化合物 1
化合物 1 は、 比較的透明点が高い化合物が好ま しい。 具体的には、 化合物 1 は、 式 ( 1 ) で表される化合物である こ とが好ま しい。 式 ( 1 ) 中、 R aは水素、 炭素数 1〜 20のアルキルであり.、 このアルキル中の 任意の一 CH2—は、 一〇_、 _S—、 一 COO—、 一〇CO—、 _CH=CH 一、 一 CF二 CF—または一 C≡C一で置き換えられてもよく、 このアルキル基 中の任意の水素はハロゲンで置き換えられてもよい。 これらの中でも、 Raは、 好ましくは、 炭素数 1〜 1 0のアルキルであり、 このアルキル中の任意の _ CH 2—は、 一 O—、 一 S—、 一 COO—、 一〇CO—、 一 CH=CH—または一 C ≡C一で置き換えられてもよく、 さらに好ましくは、 炭素数 1〜 1 0のアルキル であり、 このアルキル中の任意の一 CH2—は、 一 CH= CH—または一 C≡ C 一で置き換えられてもよい。 これらの中でも、 Raは炭素数 1〜 1 0のアルキル
またはアルコキシが最も好ましい。 ·
式 (1) 中、 Rbは水素、 ハロゲン、 一 CN、 一 N = C =〇、 — N=C=S、 —CF3、 一 OCF3または炭素数 1〜20のアルキルであり、 このアルキル中 の任意の一 CH2—は、 一 O—、 一 S—、 一 CQO—、 -OCO-, — CH = C H—、 一CF = CF—または一 C≡C一で置き換えられてもよく、 このアルキル 中の任意の水素はハロゲンで置き換えられてもよく、 このアルキル中の一 CH3 は一 CNで蚩き換えられてもよい。 これらの中でも、 Rbは好ましくは、 ハロゲ ン、 — CN、 一 N=C =〇、 一 N = C=S、 一 CF3、 一OCF3または炭素数 1〜 20のアルキルであり、 このアルキル中の任意の _ CH2—は、 一 O—、 一 CH=CH—または一 C≡C一で置き換えられてもよく、 このアルキル中の任意 の水素はハロゲンで置き換えられてもよく、 このアルキル中の一 CH3は一 CN で置き換えられてもよく、 さらに好ましくは、 Rbはフッ素、 塩素、 一 CN、 一 N=C = Sまたは炭素数 1〜20のアルキルであり、 このアルキル中の任意の一 CH2—は、 一〇_、 一CH=CH—または一 C≡C一で置き換えられてもよレ、。 式 (.1) 中、 1〜 A5は独立に芳香族性あるいは非芳香族性の 3〜 8員環、 または炭素数 9以上の縮合環であり、 これらの環の任意の水素がハロゲン、 炭素 数 1 3のアルキル、 またはハロゲン化アルキルで置き換えられてもよく、 環の —CH2—は一 O—、 一 S—または一NH—で置き換えられてもよく、 一 CH= は一 N =で置き換えられてもよいが、 ェ〜 5がテトラヒ ドロビラン環である ことはない。 これらの中でも、 〜 5は好ましくは、 独.立にベンゼン環、 ナ フタレン環、 ジォキサン環またはシクロへキサン環であり、 これらの環の任意の 水素がハロゲン、 炭素数 1〜3のアルキル、 またはハロゲン化アルキルで置き換 えられてもよく、 環の一 CH2_は一 O—または一 S—で置き換えられてもよく、 一 CH =は一 N =で置き換えられてもよく、 さらに好ましくは、 〜 5は独 立にベンゼン環、 ナフタレン環、 ジォキサン環またはシクロへキサン環であり、 ベンゼン環またはナフタレン環の任意の水素がフッ素または塩素、 メチル、 また はハロゲン化メチルで置き換えられてもよく、 一 CH2—は一 O—または一 S— で置き換えられてもよく、 一 CH=は一N二で置き換えられてもよい。 これらの
中でも、 Ai A5は、 最も好ましぐは、 独立にベンゼン環、 ジォキサン環また はシク口へキサン環であり、 ベンゼン環の任意の水素がフッ素で置き換えられて もよい。
式 (1) 中、 Z i〜Z4は独立に単結合、 炭素数 1〜 8のアルキレンであり、 このアルキレン中の任意の一 CH2—は、 一O—、 一S―、 一 COO—、 -0 C O—、 一 C SO—、 一 OC S—、 一 N = N—、 _CH = N—、 一 N = CH—、 一 N (O) =N―、 一 N = N (O) 一、 一 CH二 CH—、 一 CF = CF—または一 C≡C—で置き換えられてもよく、 任意の水素はハロゲンで置き換えられてもよ い。 これらの中でも、 Z i~Z4は好ましくは、 独立に単結合、 炭素数 1〜4の アルキレンであり、 このアルキレン中の任意の一 CH2—は、 一〇_、 一 S—、 — COO—、 — OC〇一、 一 C SO—、 _OC S—、 一 CH=CH—、 - C F = CF—または一 C≡C一で置き換えられてもよく、 任意の水素はハロゲンで置き 換えられてもよく、 さらに好ましくは、 Z i~Z4は独立に単結合または一 C≡ C—である。
式 (.1) 中、 1!1〜 n 3は独立に 0または 1であり、 Rbが水素またはフッ素の 場合は n 2および n 3は 1であり、 Z4が一COO—である場合は、 n2と n 3が 1であり、 A 4または A 5の少なくとも一つが炭素数 9以上の縮合環である場合 のみ n 3すべてが 0となり うる。 これらの中でも、 !! 1〜!!3は好ましくは、 独立に 0または 1であり、 R bが水素またはフッ素の場合は n 2および n 3は 1で あり、 A 4または A 5の少なく とも一つが炭素数 9以上の縮合環である場合のみ n丄〜!!3すべてが 0となり うる。 これらの中でも、 !! 1〜!!3は、 さらに好まし くは、 独立に 0または 1であり、 Rbが水素またはフッ素の場合は n 2および n 3 は 1であり、 A 4または A 5の少なく とも一つが炭素数 9以上の縮合環である場 合のみ n 3すべてが 0となり うる。
また、 式 (1) で表される化合物は、 透明点が 1 50°C〜400°Cであること が好ましく、 200°C〜 3 5 0°Cであることがさらに好ましい。 透明点が 1 5 0 °Cより低いと、 化合物 1 の透明点 ( Tェ) と液晶組成物 Aの透明点 ( T X ) の関係式 ( T _ T X ≥ 1 0 0 °C ) を満たす上で不利となる。
透明点が 4 0 0 °Cを超える と、 '組み合わせる他の化合物によっては、 相溶性が悪く なり 、 低温で結晶が析出するなど、 液晶相の下限温度が 高く なることがある。 1. 3 化合物 2
化合物 2は、 透明点が低く 、 誘電率異方性が大きい化合物が好ま し い。 具体的には、 化合物 2 は、 式 ( 2 ) または式 ( 3 ) で表される化 合物であるこ とが好ましい。 1. 3. 1 式 ( 2 ) で表される化合物
式 (2) 中、 Rcは水素、 炭素数 1〜 2 0のアルキルであり、 このアルキル中 の任意の一 CH2—は、 一 0_、 一 S―、 一 COO—、 一OCO—、 一 CH= C H—、 一 C F=CF—または一 C≡C—で置き換えられてもよく、 このアルキル 中の任意の水素はハロゲンで置き換えられてもよい。 'これらの中でも、 Rcは好 ましぐは、 炭素数:!〜 1 0のアルキルであり、 このアルキノレ中の任意の一 CH2 —は、 一 O—、 一 S—、 一 COO—、 一OCO—、 一 CH = CH—または一 C≡ C一で置き換えられてもよく、 Reは、 さらに好ましくは、 炭素数 1〜 1 0のァ ルキルであり、 このアルキル中の任意の _ CH2—は、 一 O—、 一 CH=CH— または一 C≡C—で置き換えられてもよい。 Rcは、 最も好ましくは、 炭素数 1 〜 1 0のアルキルであり、 このアルキル中の任意の一 CH2—は、 一 O—で置き 換えられてもよレ、。
式 (2) 中、 Rdはハロゲン、 一 CN、 _N=C = 0、 一 N = C = S、 一 C F 3—、 一 OC F3—、 一 C≡C_CN、 または一 C≡C— C F3である。 これらの 中でも、 Rdは好ましくは、 ハロゲン、 一 CN、 一 N=C= S、 一 C F 3、 — C ≡C一 CN、 一 C≡C一 CF3である。
式 (2) 中、 A6と A7は独立に芳香族性あるいは非芳香族性の 3〜8員環、 または炭素数 9以上の縮合環であり、 この環の任意の水素がハロゲン、 炭素数 1 〜 3のアルキル、 またはハロゲン化アルキルで置き換えられてもよく、 この環の
任意の一 CH2—は一 O—、 一 S—または一NH—で置き換えられてもよく、 一 CH=は一 N=で置き換えられてもよい。
これらの中でも、 A6と A7は、 さらに好ましくは、 独立にベンゼン環、 ナフタ レン環、 シクロへキサン環であり、 これらの環の任意の水素がハロゲン、 炭素数 :!〜 3のアルキル、 またはハロゲン化アルキルで置き換えられてもよく、 この環 の任意の一 CH2—は一 O—または一 S—で置き換えられてもよく、 一 CH =は 一 N =で置き換えられてもよく、 さらに好ましくは、 A6と A7は独立にベンゼ ン環、 ナフタレン環、 シクロへキサン環であり、 これらの環の任意の水素がフッ 素または塩素、 メチル、 またはハロゲン化メチルで置き換えられてもよく、 この 環の任意の一 CH2—は一 O—または一 S—で置き換えられてもよく、 一 CH = は一 N =で置き換えられてもよい。 A6と A7は、 最も好ましくは、 独立にベン ゼン環、 ジォキサン環またはシクロへキサン環であり、 ベンゼン環の任意の水素 がフッ素で置き換えられてもよい。 - 式 (2) 中、 Z 6は単結合または炭素数 1〜8のアルキレンであり、 このアル キレン中の任意の一 CH2—は、 一〇_、 一 S—、 一 COO_、 一 OCO—、 一 CSO—、 _OC S―、 _N = N—、 一 CH = N—、 一 N = CH—、 一 N (O) =N 、 一 N = N (O) 一、 一CH=CH—、 _C F二 C F—または一 C≡C一 で置き換えられてもよく、 このアルキレン中の任意の水素はハロゲンで置き換え られてもよい。 これらの中でも、 Z 6は好ましくは、 単結合、 炭素数 1〜4のァ ルキレンであり、 このアルキレン中の任意の一CH2—は、 .一 O—、 一S—、 一 COO—、 一 OCO—、 一 C SO—、 一 OC S—、 一 CH = CH—、 - C F = C F—または一 C≡C一で置き換えられてもよく、 このアルキレン中の任意の水素 はハロゲンで置き換えられてもよく、 さらに好ましくは、 Z 6は単結合、 一CO O—、 一 C F 20—または一 C≡ C—である。 最も好ましくは、 Z6は単結合ま たは一 CO O—である。
式 (2) 中、 n6は 0または 1であるが A7が炭素数 9以上の縮合環である場 合、 n6は 0である。 これらの中でも、 n 6は、 好ましくは、 0または 1である が A7がナフタレン環である場合、 n6は 0であり、 さらに好ましくは、 n6は 0
または 1であり、 A7がナフタレン璨である場合は 0である。 n6は、 最も好ま しくは、 n6は 0または 1である。
1. 3. 2 式 ( 3 ) で表される化合物
式 (3) 中、 Reは炭素数 1〜 1 0のアルキルであり、 このアルキル中の任意 の一 CH2—は、 一 O—、 一 S―、 一 COO—、 一 OCO—、 一CH=CH—、 — CF=CF—または一 C≡C—で置き換えられてもよく、 このアルキル中の任 意の水素はハロゲンで置き換えられてもよい。 これらの中でも、 Reは、 好まし くは、 炭素数 1〜 1 0のアルキルであり、 このアルキル中の任意の一 CH2—は —0—、 一 CH=CH—または— C≡C—で置き換えられてもよい。
式 (3) 中、 Xaはフッ素、 塩素、 一 CN、 一 N=C=S、 一 CF3—、 一 C ≡C— CNまたはーC≡C_CF3でぁる。
式 (3) 中、 Z 12は単結合、 一 COO—または一 C≡C一であり、 これらの 中でも _C OO—が好ましい。
式 ('3) 中、 8〜!^11は独立して水素またはフッ素である。 これらの中でも し8〜]^11は、 好ましくは、 独立して水素またはフッ素であり、 それらの少なく とも 2個以上がフッ素である。
1 . 4 重量比
化合物 1の透明点が 1 50〜250°Cである場合、 液晶組成物 Aに対して化合 物 1を 1 0〜8 0重量%および化合物 2を 20〜 90重量%含むことが好ましく . 化合物 1を 30〜6 0重量%および化合物 2を 3 0〜70重量%含むことがさら に好ましい。 また、 化合物 1の透明点が 250〜400°Cである場合、 液晶組成 物 Aに対して化合物 1を 5〜 70重量%および化合物 2を 30〜9 5重量%含む ことが好ましい。 なお、 上述の通り、 本発明の液晶組成物において、 化合 物 1 と して式 ( 1 ) で表される複数の化合物を含んでもよく 、 同様に. 化合物 2 と して式 ( 2 ) で表される複数の化合物 2を含んでもよい。 したがって、 たとえば、 式 (1) で表される化合物が複数含まれている場合
には、 式 (1 ) で表される全ての化合物の合計が 1 0〜8 0重量0 /0 (または 5〜 7 0重量 °/0) ということになる。
1 . 5 (キラル) ネマチック相と非液晶等方相とが共存する温度範 囲
液晶組成物 Aは、 キラル剤を含んでいない場合、 降温過程でネマチック相と非 液晶等方相の共存状態が発現し、 キラル剤を含んでいる場合、 降温過程でキラ ルネマチック相と非液晶等方相の共存状態が発現する液晶組成物であって、 光 学的等方性の液晶相を ¾現しない組成物である。 なお、 (キラル) ネマチック 相と非液晶等方相との共存状態は、 たとえば偏光顕微鏡観察で確認できる。 な お、 この共存状態は液晶組成物にかかる温度勾配によるものではない。
本発明の液晶組成物と しては、 (キラル) ネマチック相と非液晶等 方相とが共存する液晶組成物 Aにおいて、 (キラル) ネマチック相と非 液晶等方相とが共存する温度範囲が広いことが好ましく、 具体的には、 これらの 相が共存する上限温度と下限温度との差が、 3 °C〜 1 5 0 °Cであることがさらに 好ましい。 両者が共存する温度範囲が広いと、 さらにキラル剤を添加して得られ る液晶組成物 Bが、 広い温度範囲で光学的に等方性の液晶相を有するようになり やすいからである。
また、 ネマチック相と非液晶等^^相とが広い温度範囲で共存するキラル剤を 含まない液晶組成物 Aにキラル剤を添加すると、 広い温度範囲でキラルネマチ ック相と非液晶等方相とが共存する液晶組成物 Aを得ることが容易である。 液晶組成物 Aにおいて非液晶等方相と共存しないキラルネマチック相のピッチ が 7 0 0 n m以上であるが、 後述の通り、 さらにキラル剤を添加すると、 ピッチ が短い液晶組成物 Bが得られる。
2 液晶組成物 B
2 . 1 液晶組成物 Bの組成
液晶組成物 Bは、 光学的等方性の液晶相を発現する組成物である。 液晶組成物
Bは、 例えば、 液晶組成物 Aにさらにキラル剤を添加して得ることができる。 当該液晶組成物 Aの組成おょぴさらに添加されるキラル剤の種類等に依存する 力 液晶組成物 Bに含まれるキラル剤が組成物 Bの全重量に対して 1〜40重量、 好ましくは 5〜 1 5重量%となるように添加した液晶組成物は、 光学的に等方性 の液晶相を有するようになりやすく、 好ましい。
液晶組成物 Aにキラル剤を添加することを特徴とする液晶組成物 Bの製造工程 において、 予め液晶組成物 Aが含み得るキラル剤と、 液晶組成物 Bを得るために さらに添加されるキラル剤とは同一でも異なっていてもよい。 2. 2 キラル剤
液晶組成物 Bが含有するキラル剤としては、 ねじり力 (Helical Twisting Power) が大きい化合物が好ましい。 ねじり力が大きい化合物は所望のピッチを 得るために必要な添加量が少なくでき.るので、 駆動電圧の上昇を抑えられ、 実用 上有利である。 具体的には、 上記式 (K 1) 〜 (K5)'で表される化合物が好ま しい。 ' 式 (K 1) 〜 (; K5) 中、 RKは独立に、 水素、 ハロゲン、 一 CN、 -N = C =0、 一 N=C= Sまたは炭素数 1〜 20のアルキルであり、 このアルキル中の 任意の _CH2 —は、 一 O—、 一 S—、 一 COO—、 一OCO—、 -CH=CH —、 一 CF = CF_または一 Cョ C—で置き換えられてもよ.く、 このアルキル中 の任意の水素はハロゲンで置き換えられてもよく ; Aは独立に、 芳香族性あるい は非芳香族性の 3ないし 8員環、 または、 炭素数 9以上の縮合環であり、 これら の環の任意の水素がハロゲン、 炭素数 1〜 3のアルキルまたはハロアルキルで置 き換えられてもよく、 CH2 —は _0—、 一 S—または一 NH—で置き換えら れてもよく、 一 CH =は一N =で置き換えられてもよく ; Zは独立に、 単結合、 炭素数 1〜 8のアルキレンであるが、 任意の一 CH2 —は、 一 0_、 一 S—、 一 COO—、 一 OCO—、 一 C SO—、 一 OC S—、 一 N = N—、 一 CH = N—、 一 N=CH—、 -N (O) =N—、 一 N = N (O) 一、 一 CH二 CH―、 一 CF
=CF—または一 C≡C一で置き換えられてもよく、 任意の水素はハロゲンで置 き換えられてもよく ; Xは単結合、 一 COO—、 一 CH2 O—、 一 CF2 O—、 一 CH2 CH2 一であり ; mは:!〜 4である。
これらの中でも、 液晶組成物 Bに添加されるキラル剤としては、 式 (K2) に 含まれる式 (K 2— 1) 〜式 (K 2— 8) 、 および、 式 (K 5) に含まれる式 (K 5 - 1) 〜式 (K5— 3) が好ましい (式中、 RKは独立に、 炭素数 3〜 1 0のアルキルであり、 このアルキル中の環に隣接する一 CH2—は一 O—で置き 換えられてもよく、 任意の一 CH2 — は、 一CH = CH—で置き換えられても よい。 ) 。
液晶組成物 Bの全重量に対して、 キラル剤を 1〜40重量%含むことが好まし く、 3〜25重量%含むことがさらに好ましく、 5〜 1 5重量%含むことが最も 好ましい。
2. 3 光学的に等方性の液晶相
液晶組成物 Bは、 光学的に等方性の液晶相を有する。 液晶組成物が光学 的等方性を有するとは、 巨視的には液晶分子配列は等方的であるため光学的に等 方性を示すが、 微視的には液晶秩序が存在することをいう。 液晶組成物 Bが微視 的に有する液晶秩序に基づくピッチは 700 nm以下であることが好ましく、 5 00 nm以下であることがさらに好ましく、 350 n m以下であることが最も好 ましい。
ここで、 「非液晶等方相」 とは一般的に定義される等方相、 すなわち、 無秩序 相であり、 局所的な秩序パラメーターがゼロでない領域が生成したとしても、 そ の原因がゆらぎによるものである等方相である。 たとえばネマチック相の高温側 に発現する等方相は、 本明細書では非液晶等方相に該当する。 本明細書における キラルな液晶についても、 同様の定義があてはまるものとする。 そして、 本明細 書において 「光学的に等方性の液晶相」 とは、 ゆらぎではなく光学的に等方性の 液晶相を発現する相を表し、 たとえばプレートレット組織を発現する相 (狭義の ブルー相) はその一例である。
本発明の液晶組成物 Bにおいて、 光学的に等方性の液晶相ではあるが、 偏光顕 微鏡観察下、 ブルー相に典型的なプレートレツト組織が観測されないことがある。 そこで本明細書において、 プレートレット組織を発現する相のみをブルー相 (狭 義のブルー相) と称し、 二色以上の回折光を示さない光学的に等方性の液晶相と は区別する。
一般的に、 ブルー相は 3種類に分類され (ブルー相 I、 ブルー相 I I、 ブルー 相 I I I ) 、 これら 3種類のブルー相はすべて光学活性であり、 かつ、 等方性で ある。 ブルー相 Iやブルー相 I Iのブルー相では異なる格子面からのブラッグ反 射に起因する 2種以上の回折光が観測される。
光学的に等方性の液晶相が二色以上の回折光を示さない状態とは、 ブルー相 I、 ブルー相 I Iに観測されるプレートレツト組織が観測されず、 概ね一面単色'であ ることを意味する。 二色以上の回折光を示さない光学的に等方性の液晶相では、 色の明暗が面内で均一であることまでは不要である。
二色以上の回折光を示さない光学的に等方性の液晶相は、 ブラッグ反射による 反射光強度が抑えられる、 あるいは低波長側にシフトするという利点がある。 また、 可視光の光を反射する液晶材料では、 表示素子として利用する場合に色 味が問題となることがあるが、 二色以上の回折光を示さない液晶では、 反射波長 が低波長シフトするため、 狭義のブルー相 (プレートレツト組織を発現する相) より長いピッチで可視光の反射を消失させることができる。
光学的に等方性の液晶相における電気複屈折はピッチが長くなるほど大きくな るので、 電気複屈折を大きくすることができる。 この状態で液晶組成物 Bに電界 を印加すると残像のない速やかな応答が得られる。
3 その他 .
本発明の液晶組成物は、 その組成物の特性に影響を与えない範囲で、 さ らに高分子物質等の他の化合物が添加されてもよい。 本発明の液晶 組成物は、 高分子物質の他にも、 たとえば二色性色素、 フォ トクロミック 化合物を含有していてもよい。
本発明の液晶組成物の誘電率異方性の正負に関しては、 特に制限されるもので はないが、 正のものが好ましい。,液晶材料の誘電率異方性値 (Δ ε ) の絶対値と 屈折率異方性値 (Δ η) とは大きいほど電気複屈折は大きくなるため、 いずれも 大きいほど好ましい。 実施例
以下、 実施例により本発明さらに具体的に説明するが、 本発明はこれらの実施 例により限定されるものではない。 本明細書の実施例において、 Κは結晶相、 Iは非液晶等方相、 Νはネマチック 相、 Ν*はキラルネマチック相、 BPはブルー相、 B PXは二色以上の回折光が 観測されない光学的に等方性の液晶相を表す。 2相の共存状態は (N*+ I ) 、 (N* + B P X) という形式で表記することがある。 具体的には、 (N*+ I ) は、 それぞれ非液晶等方相とキラルネマチック相がと共存する相を表し、 (N* +B PX) は、 二色以上の回折光が観測されない光学的に等方性の液晶相とキラ ルネマチック相が共存した相を表す。 U nは光学的等方性ではない未確認の相を 表す。'
本明細書において、 I _N相転移点を N— I点ということがある。 I一 N*転 移点を N*— I点ということがある。 I— B P相転移点を B P— I点ということ がある。
本明細書の実施例において、 物性値等の測定 ·算出は特に断らない限り、 日本 亀ナ機械工桌規格 (Standard of Electronic Industries Association of Japan) 、 E I A J · ED— 2521 Aに記載された方法に従った。 具体的な測 定方法、 算出方法等は以下のとおりである。 相転移点
偏光顕微鏡を備えた融点測定装置のホットプレートに試料を置き、 クロスニコ ルの状態で、 まず試料が非液晶等方相になる温度まで昇温した後、 1°CZ分の速
度で降温し、 完全にキラルネマチック相または光学的異方性の相が出現させた。 その過程での相転移温度を測定し、 次いで i°cz分の速度で加熱し、 その過程に おける相転移温度を測定した。 光学的に等方性の液晶相においてクロス-コル下 では暗視野で相転移点の判別が困難な場合は、 偏光板をクロスニコルの状態から 1〜: 10° ずらして相転移温度を測定した。 液晶相一非液晶等方相転移点の外揷法による算出法
ネマチック相を呈する母液晶 85重量%と液晶性化合物あるいは液晶性組成物 15重量%からなるネマチック液晶組成物を調製する。 母液晶の液晶相一非液晶 等方相転移点と後者の液晶相一非液晶等方相転移点から直線外挿し、 液晶性化合 物あるいは液晶性組成物の液晶相一非液晶等方相転移点を求めた。 ネマチック相の下限温度 (TC ;。 C)
ネマチック相を有する試料をガラス瓶に入れ、 0°C、 一 10°C、 _20°C、 一 3 0°C、 および _ 40°Cのフリーザー中に 10日間保管したあと、 液晶相を観察し た。 例えば、 試料が一 20でではネマチック相のままであり、 _ 30 °Cでは結晶 またはスメクチック相に変化したとき、 TC≤- 20°Cと記載した。 ネマチック 相の下限温度を 「下限温度」 と略すことがある。 粘度 (77 ; 20°Cで測定; mP a · s )
粘度の測定には E型粘度計を用いた。 光学異方性 (屈折率異方性; Δ n ; 25°Cで測定) :
波長 589 nmの光によりを用い、 接眼鏡に偏光板を取り付けたアッベ屈折計 により測定した。 主プリズムの表面を一方向にラビングしたあと、 試料を主プリ ズムに滴下した。 屈折率 n IIは偏光の方向がラビングの方向と平行であるときに 測定した。 屈折率 n丄は偏光の方向がラビングの方向と垂直であるときに測定し た。 Δη = η ||— n丄、 の式から計算した。
誘電率異方性 (Δ £ ; 25°Cで測定)
1) 誘電率異方性が正である液晶材料
2枚のガラス基板の間隔 (ギャップ) が約 9 m、 ツイスト角が 80度の TN セルに試料を入れた。 このセルにサイン波 (10V、 1 k H z ) を印加し、 2秒 後に液晶分子の長軸方向における誘電率 (ε II) を測定した。 このセルにサイン 波 (0. 5V、 1 kHz) を印加し、 2秒後に液晶分子の短軸方向における誘電 率 丄) を測定した。 誘電率異方性の値は、 Δ ε = ε II— ε丄、 の式から計算 した。
2) 誘電率異方性が負である液晶材料
2枚のガラス基板の間隔 (ギャップ) が約 9 μπι、 ホメオト口ピック配向に処 理した液晶セルに試料を入れ、 サイン波 (0. 5V、 1 kH z) を印加し、 2秒 後の誘電率 (ε || ) を測定した。 さらに 2枚のガラス基板の間隔 (ギャップ) が 約 9 / m、 ホモジニァス配向に処理した液晶セルに試料を入れ、 サイン波 (0. 5V、 1 k H z ) を印加し、 2秒後の誘電率 (ε丄) を測定した。 誘電率異方性 の値は、 Δ ε = Ε II— ε丄、 の式から計算した。 電圧保持率 (VHR ; 25°Cで測定;%)
測定に用いた TN素子はポリイミ ド配向膜を有し、 そしてセルギャップは 6 μ mである。 この素子は試料を入れたあと紫外線によって重合する接着剤で密閉し た。 この TN素子にパルス電圧 (5Vで 60 /秒) を印加して充電した。 減衰す る電圧を高速電圧計で 1 6. 7m秒のあいだ測定し、 単位周期において電圧曲線 と横軸との間の面積を求めた。 TN素子を取り除いたあと測定した電圧の波形か ら同様にして面積を求めた。 2つの面積の値を比較して電圧保持率を算出した。 ピッチ (P ; 25°Cで測定; nm)
ピッチ長は選択反射を用いて測定した (液晶便覧 196 頁 (2000 年発行、 丸 善) 。 選択反射波長 には、 関係式く η>ρ/λ = 1が成立する。 ここでく η>は平
均屈折率を表し、 次式で与えられる。 く ii>={(n i| 2+ n l2)/2}1/2。 選択反射 波長は顕微分光光度計 (日本電子 (株) 、 商品名 MSV- 350) で測定した。 得られ た反射波長を平均屈折率で除すことにより、 ピッチを求めた。
可視光より長波長領域に反射波長を有するコレステリック液晶のピッチは、 光 学活性化合物濃度が低い領域では光学活性化合物の濃度の逆数に比例することか ら、 可視光領域に選択反射波長を有する液晶のピッチ長を数点測定し、 直線外揷 法により求めた。
[実施例 1 ]
下記式 (a) , (b— 1) 〜 (b— 5) , (c) および (d) で表される化合 物 (以下、 「化合物 a j 等という) を下記に示す重量比で混合してネマチック液 晶組成物 A— 1を調製した。 具体的には、 上記式 (1 ) で表される化合物 1とし て透明点である N— I点が 2 0 2°Cの化合物 a、 上記式 (2) で表される化合物 2として透明点 (N— I点) が 3 5. 5°Cの化合物 c、 上記式 (3) で表される 化合物 2として K一 I点が 4 9. 8°Cの化合物 d、 およびその他の化合物 (化合 物 b— 1〜化合物 b 5) を混合して調整した。 重量比の右に示す値は、 各化合物 の相転移温度である。 化合物 dの透明点は、 7. 7°Cであった。 当該透明点は、 母液晶 Z L I— 1 1 3 2 (メルク社製) に化合物 dを 1 5重量%混合して測定し た N I点の外揷値として求めた。 '
C2H5— -OCH3 (b-1) 5% K73.0
C
3H
7 - -OCH
3 (b-2) 5% K 65.5 (N 62.3)
C4H9 - -OC2H5 (b-4) 5% K 52.9 N 80.3
次に、 液晶組成物 A— 1に、 下記式で表されるキラル剤 I S O— 60 B A 2を 添加して、 液晶組成物 A— 2、 A— 3、 A— 4、 A— 5、 A— 6および A— 7を 得た。
具体的には、 表 1に示すように、 キラル剤の濃度が得られる液晶組成物に対し て 7. 5、 1 0. 0、 1 1. 0、 1 2. 5、 1 6. 6、 20. 0重量0 /0となる液
晶組成物を調製し、 それぞれ液晶組成物 A— 2、 A〜3、 A— 4、 A— 5、 A— 6、 A— 7とした。 そして、 各液晶組成物 A— 1〜 A— 7を配向処理の施されて いない I TO付ガラス 2枚からなるセル (セル厚 1 3マイクロメ一トル) に狭持 し、 偏光顕微鏡を用いて相転移温度を測定した。.
(表 1)
液晶組成物 A— 1〜A— 7の相転移温度は表 1に示すとおりであった。 具体的 には、 ― 1 °C/m i nの降温過程において、 液晶組成物 A— 1ではネマチック相 (N) と非液晶等方相 ( I ) とが共存する上限温度 (77°C) と下限温度 (7 3°C) との差 (以下、 「共存温度範囲」 ともいう) は 4. 0°Cであった。 液晶組 成物 A_2では、 一 1 °C/m i nの降温過程においてキラルネマチック相 (N *) と非液晶等方相 ( I ) とが共存する上限温度 (63. 7°C) と下限温度 (5 6°C) との差 (共存温度範囲) が 7. 7°Cであった。 同様に、 液晶組成物 A— 3 〜A_ 4の共存温度範囲はそれぞれ 1 1. 3、 1 3. 1°Cであった。
また、 液晶組成物 A— 5の 1 °C/m i nの昇温過程において、 光学的に等方性 の液晶相が発現する上限温度 (57°C〜52. 2°C) と下限温度 (42. 4 °C)
との差 (以下、 「B PX温度範囲」 ともいう) は 9. 8°C〜1 4. 6°Cであった 同様に、 液晶組成物 A— 6と A— 7の B PX温度範囲はそれぞれ 20、 2 1 °Cで あった。 このように、 液晶組成物 A— 5と A— 7は昇温過程で、 光学的に当方性 の液晶相を広い温度範囲で発現した。 .
液晶組成物 A— 5〜A— 7の光学的に等方性の液晶相の光学組織において、 プ ルー相 I、 I Iで確認されるプレートレツト組織は観測されず、 二色以上の回折 光は観測されなかった。 また液晶組成物 A_ 7ではクロス-コルでの偏光顕微鏡 観察において、 色味もなく暗視野であった。
化合物 1である化合物 aの透明点である N— I点 (1\) は 20 2°Cであり、 液晶組成物 A— 1の透明点である N— I点 (Tx) は 75. 5°Cであり、 一 Τ X = 1 26. 5°Cであった。
同様に、 化合物 1である化合物 aの透明点である N— I点 (T ) は 202°C であり、 液晶組成物 A— 2の透明点である N*— I点 (T x) は 6 0. 7°Cであ り、 Tx= 141. 3°Cであった。
同様.に、 液晶組成物 A— 3〜A_ 7における Τ^— Τχは以下のとおりであつ た。
液晶組成物 A— 3 : 一 τ X =202。C一 5 5. 4。C = 1 46. 6。C 液晶組成物 A— 4 : 一 τ X =202。C一 52. 2°C = 1 49. 8°C 液晶組成物 A— 5 : 一 τ X =202°C— 5 7°C = 1 45。C
液晶組成物 A— 6 : 一 τ X =202。C_ 48°C = 1 54°C
液晶組成物 A— 7 : — τ X =202°C— 4 1 °C = 1 6 1。C
[比較例 1 ]
実施例 1における液晶組成物 A— 1の成分に含まれる化合物 aを用いずに、 化 合物 b— 1〜化合物 dだけを用いて液晶組成物 E— 1を調製した。 具体的な組成 は以下のとおりであった。
C5H"- (c) 33.3%
次に、 液晶組成物 E_ 1に、 キラル剤 I SO— 60 BA2を混合して、 液晶組 成物 E— 2〜 E— 5を得た。
具体的には、 表 2に示すように、 キラル剤の濃度が 2. 0、 3. 5、 5. 0、 7. 0重量%となる液晶組成物を調製し、 それぞれ液晶組成物 E— 2、 E— 3、 E— 4、 E— 5とした。 そして、 各液晶組成物 E— 1〜E— 5を配向処理の施さ れていない I TO付ガラス 2枚からなるセル (セル厚 1 3マイクロメ'一トル) に 狭持し、 偏光顕微鏡を用いて相転移温度を測定した。
(表 2)
液晶組成物 E—:! 〜 E— 5の相転移温度は表 2に示すとおりであつた。 具体的 には、 液晶組成物 E— 1では、 一 l°CZm i nの降温過程において、 ネマチック 相 (N) と非液晶等方相 (I) とが共存する上限温度 (3 1. 1°C) と下限温度 ( 30. 8 °C) との差 (共存温度範囲) は 0. 3 °Cであった。 液晶組成物 E— 2 では、 一 l°C/m i nの降温過程においてキラルネマチック相 (N*) と非液晶 等方相.(I ) とが共存する上限温度 (28. 3°C) と下限温度 (27. 5°C) と の差 (共存温度範囲) が 0. '8°Cであった。 同様に、 液晶組成物 E— 3〜E_4 の共存温度範囲はそれぞれ 1. 2、 1. 3°Cであった。
また、 液晶組成物 E— 5では降温過程と昇温過程においてブルー相 Iが確認さ れ、 昇温過程におけるブルー相 Iが発現する上限温度と下限温度との差は 2. 0°Cであった。
[実施例 2]
下記式 (e- 1) (e -2) , (f ) 〜 ( i) および (d) で表される化合物 を下記に示す重量比で混合してネマチック液晶組成物 B— 1を調製した。 具体的 には、 上記式 (1) で表される化合物として、 透明点である N_ I点が 250°C 以上であるの化合物 e— 1と化合物 e— 2、 上記式 (3) で表される化合物 2と して、 1^ー 1点が49. 8°Cで透明点 (外挿値) が 7. 7°Cである化合物 d、 お よび、 化合物 f 〜化合物 iを混合して調整した。 重量比の右に示す値は、 各化合
物の相転移温度である ( N >250 N >250
次に、 液晶組成物 B _ 1に、 キラル剤 I SO— 60 BA2を添加して液晶組成 物 B— 2、 B— 3、 B_4および B_ 5を得た。 具体的には、 表 3に示すように, キラル剤の濃度が 2. 9、 5. 0、 8. 1、 1 0. 0重量%となる液晶組成物を 調製し、 それぞれ液晶組成物 B— 2、 B— 3、 B— 4、 B— 5とした。 そして、 各液晶組成物 B— 1〜B— 5を配向処理の施されていない I TO付ガラス 2枚か らなるセル (セル厚 1 3マイクロメートル) に狭持し、 偏光顕微鏡を用いて相転 移温度を測定した。 ■
(表 3)
液晶組成物 B—:!〜 B— 5の相転移温度は表 3に示すとおりであつた。 具体的 には、 液晶組成物 B_ 1では一 l°CZm i nの降温過程においてネマチック相 (N) と非液晶等方相 ( I ) とが共存する上限温度 (60°C) と下限温度 (5 4°C) との差 (共存温度範囲) が 6. 0°Cであった。 液晶組成物 B— 2では、 一 l°CZm i ηの降温過程においてキラルネマチック相 (Ν*) と非液晶等方相 ( I ) とが共存する上限温度 (54. 7°C) と下限温度 (48. 6°C) との差 (共存'温度範囲) が 6. 1°Cであった。
また、 液晶組成物 B— 4の 1 °C/m i nの昇温過程において、 光学的に等方性 の液晶相が発現する上限温度 (4 1. 9°C 44. 9°C) と下限温度 (34. 7°C) との差 (BP温度範囲) は 7. 2°C 10. 2°Cであった。 同様に、 液晶 組成物 B— 5の B P温度範囲は 10°Cであった。 このように、 液晶組成物 B— 4 と B— 5は昇温過程で、 光学的に等方性の液晶相を広い温度範囲で発現した。 また、 液晶組成物 B— 2の降温過程における 54. 5°C 52°C 49°Cにお ける偏光顕微鏡像 (図 1) によれば、 当該液晶組成物において非液晶等方相とキ ラルネマチック相が共存していることがわかった。
化合物 1である化合物 e— 1と化合物 e— 2の等重量混合物の透明点である N 一 I点 (TJ は 270°C以上であり、 液晶組成物 B— 1の透明点である N— I 点 (Tx) は 56. 5 °Cであるから (1\— Tx) は 21 3. 5 °C以上であった, また液晶組成物 B— 2の透明点である N*— I点 (Tx) は 5 1. 5°Cであるか ら、 (Ti— Tx) は 218. 5°C以上であった。
同様に、 液晶組成物 B— 3〜 B— 5における T i一 T Xは以下のとおりであつ た。
液晶組成物 B— 3 : T\— T X = 270。C以上一 5 1. 0°C= 2 1 9. 0°C以 上
液晶組成物 B— 4 : Ti-T X = 270。C以上— 4 1. 9°C= 228. 1 °0以 上
液晶組成物 B - 5 : T1-Tx = 2 70 °C以上— 40 °C = 230 °C以上 [比較例 2]
化合物 j〜化合物 1および化合物 cを用いて、 液晶組成物 C一 1を調製した。 具体的な組成は以下のとおりであった。
次に、 液晶組成物 C— 1に、 キラル剤 I S O— 60 B A 2を添加して、 液晶組 成物 C_ 2〜C— 5を得た。 具体的には、 表 4に示すように、 キラル剤の濃度が 1. 9、 4. 0、 6. 0、 8. 1重量%となる液晶組成物を調製し、 それぞれ液 晶組成物 C一 2、 C_ 3、 C一 4、 C— 5とした。 そして、 各液晶組成物 C _ 1 〜C一 5を配向処理の施されていない I TO付ガラス 2枚からなるセル (セル厚 1 3マイクロメートル) に狭持し、 偏光顕微鏡を用いて相転移温度を測定した。
(表 4)
液晶組成物 C一;!〜 C一 5の相転移温度は表 4に示すとおりであつた。 具体的 には、 液晶組成物 C一 1では一 1 °CZm i nの降温過程において、 ネマチック相 (N) と非液晶等方相 (I) とが共存する上限温度 (62°C) と下限温度 (61. 9°C) との差 (共存温度範囲) は 0. 1°Cであった。
液晶組成物 C一 2では、 一 1 °C/m i nの降温過程においてキラルネマチック 相 (N*) と非液晶等方相 ( I) とが共存する上限温度 (59. 2°C) と下限温 度 (58. 7°C) との差 (共存温度範囲) が 0. 5°Cであった。 同様に、 液晶組 成物 C一 3の共存温度範囲はそれぞれ 1. 2°Cであった。
液晶組成物 C一 4は昇温過程で発現した光学的に等方性の液晶相が発現する上 限温度 (53. 0°C) と下限温度 (5 1. 5°C) との差 ( P温度範囲) は 1. 5°Cであった。 同様に液晶組成物 C一 5の B P温度範囲は 1. 8°Cであった。
[実施例 3]
下記式 (m) , (n) , (c) および (d) で表される化合物を下記に示す重 量比で混合してネマチック液晶組成物 D— 1を調製した。 具体的には、 上記式 (1) で表される化合物 1として透明点である N— I点が 239°Cであるの化合 物 mと、 N_ I点が 222°Cである化合物 n、 上記式 (2) で表される化合物 2 として透明点 (N— I点) が 36. 5°Cの化合物 c、 および、 上記式 (3) で表
される化合物 2として K一 I点が 49. 8°Cで透明点 (外揷値) が 7. 7°Cであ る化合物 dを混合して調整した。 .重量比の右に示す値は、 各化合物の相転移温度 である。
次に、 液晶組成物 D— 1に.、 キラル剤 I SO— 60 BA2を添加して液晶組成 物 D— 2、 D— 3および D— 4を得た。
具体的には、 表 5に示すように、 キラル剤の濃度が 9. 1、 14. 3、 20. 4重量%となる液晶組成物を調製し、 それぞれ液晶組成物 D— 2、 D— 3、 D- 4とした。 そして、 各液晶組成物 D—:!〜 D— 4を配向処理の施されていない I TO付ガラス 2枚からなるセル (セル厚 1 3マイクロメートル) に狭持し、 偏光 顕微鏡を用いて相転移温度を測定した。 (表 5)
液晶組成物 D—:!〜 D— 4の相転移温度は表 5に示すとおりであった。 具体的 には、 液晶組成物 D— 1では一 1 °C/m i nの降温過程においてネマチック相 (N) と非液晶等方相 ( I ) とが共存する上限温度 (1 0 7. 6°C) と下限温度 ( 9 5 °C) との差 (共存温度範囲) が 1 2. 6°Cであった。
液晶組成物 D— 2では、 一 l °C/m i nの降温過程においてキラルネマチック 相 (N*) と非液晶等方相 ( I ) とが共存する上限温度 (9 1. 5°C) と下限温 度 (7 2. 0°C) との差 (共存温度範囲) が 1 9. 5 °Cであった。 同様に、 液晶 組成物 D _ 3の共存温度範囲は 3 0. 8 °Cであった。
また、 液晶組成物 D— 4の 1 °C/m i nの昇温過程において、 光学的に等方性 の液晶相が発現する上限温度 (6 8 °C〜 7 2°C) と下限温度 (3 7°C) との差 (B P X温度範囲) は 3 1 °C〜 3 5°Cであった。 このように、 液晶組成物 D— 4 は昇温過程で、 光学的に当方性の液晶相を広い温度範囲で発現した。
液晶組成物 D— 4における光学的に等方性の液晶相の光学組織はプル一相 I 、 I Iで確認されるプレートレット組織は観測されず、 二色以上の回折光は観測さ れなかった。 また D— 4ではクロスニコルでの偏光顕微鏡観察において、 色味も なく暗視野であった。
化合物 1である化合物 mと化合物 nの等重量混合物の透明点である N— I点 (T は 2 3 0°Cであり、 液晶組成物 D— 1の透明点である N— I点 (T x) は 1 0 3. 7°Cであるから、 (Ti— T x) は 1 2 6. 3 °Cであった。
同様に、 液晶組成物 D— 3〜D— 4における 1 一 T xは以下のとおりであつ
た。
液晶組成物 D— 3 T 1-Ύ χ = 2 3 0°C- 6 5. 3°C= 1 6 4. 7 °C 液晶組成物 D— 4 T ! -T x = 2 3 0°C— 6 8°C= 1 6 2 °C
[実施例 4]
下記式 (o— 1) 、 (o— 2) 、 (o— 3) および (p) で表される化合物を 下記に示す重量比で混合してネマチック液晶組成物 F— 1を調製した。 具体的に は、 上記式 (1) で表される化合物として、 透明点である N— I点が 2 5 0°C以 上であるの化合物 (o - 1 ) 〜 (o— 3) 、 上記式 ( 3) で表される化合物 2と して、 K一 I点が 2 1. 4°Cで透明点 (外挿値) が一 4 1. 6°Cである化合物 p を混合して調整した。 重量比の右に示す値は、 各化合物の相転移温度である。
次に、 液晶組成物 F _ 1に、 キラル剤 I SO— 6 0 BA 2を添加して液晶組成 物 F— 2、 F— 3を得た。 具体的には、 表に示すように、 キラル剤の濃度が 0. 8, 1 0. 0重量 °/
0となる液晶組成物を調製し、 それぞれ液晶組成物 F— 2、 F 一 3とした。 そして、 各液晶組成物 F— 2〜F— 3を配向処理の施されていない
I TO付ガラス 2枚からなるセル (セル厚 1 3マイクロメートル) に狭持し、 偏 光顕微鏡を用いて相転移温度を測定した。 ここで F— 3の透明点は実施例 4で用 いたセルと同様のセルを用い、 偏光顕微鏡を確認しながら、 80V交流正弦波を 印加し、 昇温条件下、 透過率が急激に低下する温度を透明点.とした。
(表 6)
液晶組成物 F— 1〜 F— 3の相転移温度は表 6に示すとおりであった。 具体的 には、 液晶組成物 F— 1では一 l ^Zm i nの降温過程においてネマチック相 (N) と非液晶等方相 ( I ) とが共存する上限温度 (98. 7°C) と下限温度 ( 85 °C) との差 (共存温度範囲) が 13. 7 °Cであつた。 液晶組成物 F— 2で は、 _ 1 °CZm i nの降温過程においてキラルネマチック相 (N*) と非液晶等 方相 ( I ) とが共存する上限温度 · (97. 2°C) と下限温度 (8 1°C) との差 (共存温度範囲) が 16. 2°Cであった。
また、 液晶組成物 F— 3では、 l°CZm i nの昇温過程において、 光学的に等 方性の液晶相が発現する上限温度 (74°C) と下限温度 (54°C) との差 (BP (X) または B P温度範囲) は 20°Cであった。 このように、 液晶組成物 F— 3 は昇温過程で、 光学的に等方性の液晶相を広い温度範囲で発現した。
化合物 1である化合物 o— 1、 化合物 o— 2および化合物 o— 3の等重量混合 物の透明点である N— I点 (Ί\) は 254°Cであり、 液晶組成物 F— 1の透明 点である N_ I点 (T x) は 8 9. 2 °Cであるから (T^— Tx) は 1 64. 8 °C以上であった。 また液晶組成物 F— 2の透明点 N * _ I点 ( T X ) は 84 °C
であるから、 (T\— Tx) は 1.70°Cであった。 [実施例 5 ]
実施例 1の液晶組成物 A— 7を配向処理の施されていない櫛型電極基板 (図 2) と対向ガラス基板 (非電極付与) との間 (セル厚 1 2マイクロメートル) に 狭持し、 組成物を含むこれらの基板 (櫛歯電極セル) を図 3に示した光学系に設 置し、 電気光学特性を測定した。
櫛歯電極セルは、 レーザー光のセルへの入射角度がセル面に対して垂直となる ように、 かつ、 櫛型電極の線方向が Polarizer と Analyzer偏光板に対してそれ ぞれ 45° となるように設置した。 振幅 1 1 0Vの矩形波を印加することで透過 率が飽和した。 フォトディテクターで検出した電界無印加時の透過光強度は 0.
078、 電界印加時の透過光強度は 3 1 0であり、 コントラストは 39 70と算 出された。 このときの応答速度は立ち上がり (透過率光強度が電界印加時の強度 の 1 0%から 90%まで変化するのに要する時間) が 1 50マイクロ秒、 立ち下 がり (透過率光強度が電界印加時の強度の 90%から 1 0%まで変化するのに要 する時間) が 1 1 0マイクロ秒であった。 クロスニコルの偏光顕微鏡下で同様に 電界を印加したところ残像は確認されなかった。 なお、 測定温度は室温の 22°C である。
このように、 液晶組成物 A— 7は電界のオン Zオフで明と喑の 2状態を実現で き、 かつ透過率が飽和するまで電界を印加しても高速応答が実現できた。 産業上の利用可能性
本発明の活用法として、 たとえば、 液晶材料、 および、 液晶材料を用いる液晶 素子が挙げられる。