WO2009104760A1 - 抗ウイルス物質、抗ウイルス繊維及び抗ウイルス繊維構造物 - Google Patents
抗ウイルス物質、抗ウイルス繊維及び抗ウイルス繊維構造物 Download PDFInfo
- Publication number
- WO2009104760A1 WO2009104760A1 PCT/JP2009/053083 JP2009053083W WO2009104760A1 WO 2009104760 A1 WO2009104760 A1 WO 2009104760A1 JP 2009053083 W JP2009053083 W JP 2009053083W WO 2009104760 A1 WO2009104760 A1 WO 2009104760A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- antiviral
- fiber
- maleic acid
- virus
- nonwoven fabric
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D135/00—Coating compositions based on homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a carboxyl radical, and containing at least another carboxyl radical in the molecule, or of salts, anhydrides, esters, amides, imides or nitriles thereof; Coating compositions based on derivatives of such polymers
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N25/00—Biocides, pest repellants or attractants, or plant growth regulators, characterised by their forms, or by their non-active ingredients or by their methods of application, e.g. seed treatment or sequential application; Substances for reducing the noxious effect of the active ingredients to organisms other than pests
- A01N25/34—Shaped forms, e.g. sheets, not provided for in any other sub-group of this main group
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N59/00—Biocides, pest repellants or attractants, or plant growth regulators containing elements or inorganic compounds
- A01N59/16—Heavy metals; Compounds thereof
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N59/00—Biocides, pest repellants or attractants, or plant growth regulators containing elements or inorganic compounds
- A01N59/16—Heavy metals; Compounds thereof
- A01N59/20—Copper
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F222/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a carboxyl radical and containing at least one other carboxyl radical in the molecule; Salts, anhydrides, esters, amides, imides, or nitriles thereof
- C08F222/04—Anhydrides, e.g. cyclic anhydrides
- C08F222/06—Maleic anhydride
-
- D—TEXTILES; PAPER
- D01—NATURAL OR MAN-MADE THREADS OR FIBRES; SPINNING
- D01F—CHEMICAL FEATURES IN THE MANUFACTURE OF ARTIFICIAL FILAMENTS, THREADS, FIBRES, BRISTLES OR RIBBONS; APPARATUS SPECIALLY ADAPTED FOR THE MANUFACTURE OF CARBON FILAMENTS
- D01F6/00—Monocomponent artificial filaments or the like of synthetic polymers; Manufacture thereof
- D01F6/28—Monocomponent artificial filaments or the like of synthetic polymers; Manufacture thereof from copolymers obtained by reactions only involving carbon-to-carbon unsaturated bonds
- D01F6/36—Monocomponent artificial filaments or the like of synthetic polymers; Manufacture thereof from copolymers obtained by reactions only involving carbon-to-carbon unsaturated bonds comprising unsaturated carboxylic acids or unsaturated organic esters as the major constituent
-
- D—TEXTILES; PAPER
- D01—NATURAL OR MAN-MADE THREADS OR FIBRES; SPINNING
- D01F—CHEMICAL FEATURES IN THE MANUFACTURE OF ARTIFICIAL FILAMENTS, THREADS, FIBRES, BRISTLES OR RIBBONS; APPARATUS SPECIALLY ADAPTED FOR THE MANUFACTURE OF CARBON FILAMENTS
- D01F6/00—Monocomponent artificial filaments or the like of synthetic polymers; Manufacture thereof
- D01F6/44—Monocomponent artificial filaments or the like of synthetic polymers; Manufacture thereof from mixtures of polymers obtained by reactions only involving carbon-to-carbon unsaturated bonds as major constituent with other polymers or low-molecular-weight compounds
- D01F6/52—Monocomponent artificial filaments or the like of synthetic polymers; Manufacture thereof from mixtures of polymers obtained by reactions only involving carbon-to-carbon unsaturated bonds as major constituent with other polymers or low-molecular-weight compounds of polymers of unsaturated carboxylic acids or unsaturated esters
-
- A—HUMAN NECESSITIES
- A62—LIFE-SAVING; FIRE-FIGHTING
- A62B—DEVICES, APPARATUS OR METHODS FOR LIFE-SAVING
- A62B23/00—Filters for breathing-protection purposes
Definitions
- the present invention relates to an antiviral substance made of a polymer effective for viruses and a fiber having an antiviral function.
- Patent Document 1 An agent for inactivating such an influenza virus is disclosed in Patent Document 1.
- This influenza virus inactivating agent is a solution containing iodine and ⁇ -cyclodextrin.
- Patent Document 2 discloses a cellulose composition having an ion exchange function comprising a mixture of cellulose and a vinyl acetate-maleic acid copolymer. This cellulosic composition is described as having antibacterial properties against staphylococci and gram-negative bacteria.
- a crosslinked acrylic fiber is used as a fiber having a crosslinked structure and having a carboxyl group in the molecule, and fine particles of metal and / or metal compound that are hardly soluble in water are dispersed in the fiber.
- An antiviral fiber is disclosed.
- this method provides a sufficient virus inactivating effect. It is considered that the effect is reduced unless it is made into a moisture atmosphere.
- JP 2006-328039 A Japanese Patent Laid-Open No. 3-121145 PCT International Publication No. WO2005 / 083171 Republished Gazette
- the inventors of the present invention have studied for many years focusing on the unique properties of the cellulose-based composition disclosed in Patent Document 2, and have found that proteins are denatured.
- the present invention utilizes such characteristics of the cellulosic composition, such as staphylococci and gram-negative bacteria.
- An object is to provide an antiviral substance effective against a virus much smaller than the size of a bacterium, a fiber carrying an antiviral substance, a fiber structure, and a fiber product.
- the antiviral substance of the invention according to claim 1 made to achieve the above object is characterized by comprising a polymer containing a maleic acid component as a monomer unit in a polymer chain.
- the antiviral substance of the invention of claim 2 is the antiviral substance of the invention of claim 1, wherein the polymer is an olefin-maleic acid copolymer, a styrene-maleic acid copolymer, It is characterized by being a vinyl ester-maleic acid copolymer, a vinyl acetate-maleic acid copolymer, or a vinyl chloride-maleic acid copolymer.
- the antiviral substance of the invention according to claim 3 is also the antiviral substance of the invention according to claim 1, wherein the polymer carries ions of a metal selected from copper, silver, zinc and nickel. It is characterized by that.
- the antiviral substance of the invention according to claim 4 is the antiviral substance of the invention according to claim 1, wherein the polymer containing the maleic acid component is a vinyl acetate-maleic acid copolymer polymer carrying copper ions. It is characterized by being.
- the antiviral substance of the invention according to claim 5 is characterized in that cellulose is mixed with at least one copolymer polymer selected from the copolymer polymers containing the maleic acid component according to claim 2. To do.
- the antiviral substance of the invention according to claim 6 is an antiviral substance of the invention according to claim 1, and is effective against avian influenza virus.
- the antiviral substance of the invention of claim 7 is the antiviral substance of the invention of claim 6, wherein the avian influenza virus is A / whistling swan / Shimane / 499/83 (H5N3) strain, and A / Turkey It is characterized by at least one selected from / Wisconsin / 1/66 (H9N2) strain.
- the antiviral substance of the invention according to claim 8 is the antiviral substance of the invention according to claim 1, and is effective against human influenza virus.
- the antiviral substance of the invention according to claim 9 is an antiviral substance of the invention according to claim 1, and is effective against swine influenza virus.
- the antiviral substance of the invention according to claim 10 is an antiviral substance of the invention according to claim 1, and is effective against norovirus.
- the antiviral fiber of the invention according to claim 11 made to achieve the above object comprises an antiviral substance comprising a polymer containing a maleic acid component as a monomer unit in a polymer chain. It is characterized by including as an ingredient.
- the antiviral fiber structure of the invention according to claim 12 made to achieve the above object includes at least a part of the antiviral fiber of the invention according to claim 11, To do.
- an antiviral fiber product of the invention according to claim 13 of the invention made to achieve the above object includes at least a part of the antiviral fiber of the invention of claim 11, and includes clothing, bedding, It is characterized by being formed into a futon, curtain, wallpaper, carpet, mat, sheet, filter, mask, wiper, towel, protective clothing, protective net, waste chicken bag, poultry house supplies, medical sheet.
- the antiviral substance of the present invention is effective for inactivating viruses. Further, the antiviral fiber of the present invention in which the polymer of the antiviral substance of the present invention is spun or supported is effective for inactivating viruses. Furthermore, the antiviral fiber of the present invention is processed into a fiber product to constitute the fiber structure of the present invention. The antiviral fiber structure has a high inactivation effect on the virus in contact.
- the antiviral substance of the present invention is composed of a polymer containing a maleic acid component as a monomer unit in a polymer chain.
- a polymer containing a maleic acid component as a monomer unit in a polymer chain.
- a polymer containing a maleic acid component as a monomer unit in a polymer chain.
- a polymer containing a maleic acid component as a monomer unit in a polymer chain.
- a polymer containing a maleic acid component as a monomer unit in a polymer chain.
- a polymer containing a maleic acid component as a monomer unit in a polymer chain.
- an olefin-maleic acid copolymer for example, an olefin-maleic acid copolymer, a styrene-maleic acid copolymer, a vinyl ester -Maleic acid copolymer, vinyl acetate-maleic acid copolymer, or
- viruses that are the target of the inactivation effect include all viruses regardless of the kind of genome and the presence or absence of an envelope.
- viruses having DNA as a genome include herpes virus, smallpox virus, cowpox virus, chicken pox virus, adenovirus and the like
- viruses having RNA as a genome include measles virus, influenza virus, coxsackie virus, calicivirus. (Norovirus genus), retroviruses (lentivirus genus such as HIV (human immunodeficiency virus)), coronavirus and the like.
- viruses having an envelope include herpes virus, smallpox virus, cowpox virus, chicken pox virus, measles virus, influenza virus, etc.
- viruses having no envelope include adenovirus, Examples include Coxsackie virus and Norovirus.
- this antiviral substance has an inactivating effect on the virus is presumed to be that it inhibits the activity of protuberance HA (hemagglutinin) and NA (neuramitase) on the virus surface against influenza virus. In other viruses, it is presumed to inhibit the activity of protrusions on the surface of the virus or directly destroy virus particles.
- protuberance HA hemagglutinin
- NA neuroamitase
- the antiviral substance has a high inactivation effect on the avian influenza virus, and is particularly effective for highly pathogenic avian influenza viruses such as H5 or H7 subtypes.
- the antiviral effect is proved for the avian influenza virus A / whistling swan / Shimane / 499/83 (H5N3) strain and the avian influenza virus A / Turkey / Wisconsin / 1/66 (H9N2) strain, but H5N1 It is thought to be effective for avian influenza viruses such as types.
- the antiviral substance of the present invention has a high inactivation effect on human influenza virus and is effective for all kinds of influenza viruses. Although the antiviral effect of human influenza virus A / Aichi / 2/68 (H3N2) strain has been proved, it is considered to be effective for other human influenza viruses.
- this antiviral substance has proved antiviral effect on swine influenza virus A / Swine / Iowa / 15/30 / (H1N1) strains.
- this antiviral substance has a high inactivation effect on norovirus.
- the antiviral effect has been demonstrated for calicivirus, which is widely used as a substitute for norovirus, which cannot be cultured in cells.
- a typical example of the polymer containing the maleic acid component is a vinyl acetate-maleic acid copolymer.
- This copolymer can be obtained by subjecting vinyl acetate and maleic anhydride to solution polymerization using a known radical polymerization initiator in the presence of an organic solvent such as benzene, toluene, and acetate. .
- vinyl acetate and maleic acid are approximately equimolar copolymers.
- the molecular weight can range over a wide range depending on the application, but is usually in the range of 10,000 to 2,000,000, preferably 100,000 to 500,000.
- Vinyl acetate and maleic anhydride may be charged at a ratio of 0.9: 1.1 to 1.1: 0.9 when obtaining an equimolar copolymer of both.
- the polymerization temperature is usually about 50 to 120 ° C., and the polymerization time is about 1 to 6 hours.
- radical polymerization initiators include peroxide polymerization initiators such as benzoyl peroxide and acetyl peroxide, and azo polymerization initiators such as azobisisobutyronitrile. It is about 0.05 to 1.0 mass% with respect to the body.
- the solvent can be removed from the obtained copolymer solution to obtain an antiviral substance having a copolymer solid content.
- the polymer containing the maleic acid component can be supported on or mixed with an organic or inorganic carrier.
- the content of the polymer containing the maleic acid component with respect to the carrier is not particularly limited as long as it can be supported on or mixed with the carrier and can exhibit an antiviral effect.
- the maleic acid component with respect to 100 parts by mass of the carrier The polymer containing is preferably 1 to 100 parts by mass.
- a more preferable content of the polymer containing a maleic acid component is 5 to 60 parts by mass.
- the antiviral substance of the present invention is preferably carried on a cellulose material as the organic carrier.
- Cellulose materials tend to exhibit antiviral effects because of their good water absorption.
- a metal ion selected from copper, silver, and zinc, which will be described later, is supported, it is important to hold the carrier in a + ion or -ion state. Is advantageous.
- Cellulose material is processed into the form of a fiber, sponge, etc., for example.
- fibers are particularly preferable. Since the fiber is bulky and has a large surface area, the polymer containing the maleic acid component efficiently contacts the virus in the air.
- fiber materials include cellulosic fibers (cotton, hemp, rayon, pulp, etc.), protein fibers (wool, silk, etc.), polyamide fibers, polyester fibers, polyacrylic fibers, polyvinyl alcohol fibers, polyvinyl chloride. All kinds of natural fibers such as fibers, polyvinylidene chloride fibers, polyolefin fibers and polyurethane fibers, recycled fibers, semi-synthetic fibers and synthetic fibers are used. Among these, cellulosic fibers are advantageous as well as the reason why the cellulose material is preferable. Cellulosic fibers do not accumulate dust due to static electricity unlike synthetic fibers, so that the reaction sites are not blocked by dust, and can exhibit a more antiviral effect. In particular, rayon has good water absorption and can easily adjust the fineness and fiber length, so that it can be applied to various fiber structures and fiber products.
- this vinyl acetate-maleic acid copolymer solution is obtained by spinning a mixed solution of a viscose solution of cellulose obtained by a known method or a metal-containing alkali solution such as a copper ammonia solution of cellulose through a spinning nozzle.
- the antiviral fiber of the present invention can be obtained by discharging into a solution and so-called wet spinning (see, for example, Japanese Patent Publication No. 8-13905).
- the mixing ratio of cellulose and copolymer is preferably about 60 to 99% by mass for the former and about 40 to 1% by mass for the latter.
- the proportion of cellulose used is less than 60% by mass, the resulting cellulose composition may have a sticky feeling on the surface, and disadvantages such as blocking may occur in subsequent steps such as spinning and compounding.
- it exceeds 99% by mass the antiviral effect by using a vinyl acetate-maleic acid copolymer may be lowered.
- the antiviral fiber of the present invention is subjected to processing such as immersion, coating, etc. in a solution containing metal ions selected from copper, silver, zinc, nickel, etc. It is preferable to carry at least one metal ion selected from ions, zinc ions, and nickel ions. As the metal ion, copper ions have a high antiviral effect and are particularly preferable.
- the copper ions can be adsorbed by being immersed in a solution of copper sulfate (CuSO 4 ) or copper nitrate (Cu (NO 3 ) 2 ).
- copper sulfate CuSO 4
- copper nitrate Cu (NO 3 ) 2
- zinc ions can be adsorbed by being immersed in a zinc chloride (ZnCl 2 ) solution.
- the antiviral fiber can be used by adding to, for example, a sheet-like product, a resin molded product, an inorganic molded product, or the like. Moreover, it can adhere
- the cross-sectional shape of the antiviral fiber is not particularly limited, and may be circular, irregular, hollow, or the like.
- the fiber length of the antiviral fiber is not particularly limited, and may be any of long fiber, short fiber, fine fiber, and the like. If it is a long fiber, it can be obtained by winding the fiber around a bobbin or the like after spinning. If it is a short fiber, it can be cut into a predetermined fiber length with a cutter or the like, or if it is a natural fiber, it can be used as it is. If it is a fine fiber, it can be obtained by grinding and grinding with a grind mill or the like, and classifying through a sieve having an arbitrary mesh. The fine fibers ground and cut are moderately curved. Furthermore, the fineness of the antiviral fiber is not particularly limited, and may be appropriately selected depending on the application.
- the antiviral fiber structure of the present invention can be used by forming the antiviral fiber at least in part and forming it into yarn, woven or knitted fabric, web, nonwoven fabric, paper, net or the like. Moreover, it is good also as a lamination sheet laminated
- the antiviral fiber structure of the present invention is obtained with a thread, (1) a polymer containing a maleic acid component as an antiviral substance or a metal acid component such as copper, silver, or zinc previously supported on a maleic acid component A method of producing a fiber that spins or carries a molecule to obtain an antiviral fiber, and then produces a yarn containing at least a part of the antiviral fiber. (2) Spinning a polymer containing a maleic acid component as an antiviral substance.
- the maleic acid component is loaded with a metal ion such as copper, silver, zinc or the like, or (3) a yarn by a known method Then, a method of supporting a polymer containing a maleic acid component on the fiber surface can be employed.
- the above-described yarn can be obtained by a known method for producing spun yarn or multifilament yarn.
- a polymer containing a maleic acid component as an antiviral substance or a metal ion such as copper, silver or zinc is supported on the maleic acid component.
- a method for producing a woven or knitted fabric by obtaining a fiber in which a polymer is spun or supported to obtain an antiviral fiber, and then weaving a yarn containing a predetermined antiviral fiber and dyeing it if necessary.
- Method of supporting metal ions such as copper, silver, zinc, etc. (3) Short fibers previously cut into 5 mm or less of antiviral fibers or finely pulverized fibers are supported on the fiber surface constituting the woven or knitted fabric with a binder. Method, or the like can be adopted.
- the woven or knitted fabric described above can be obtained by a known method for producing woven or knitted fabric.
- the antiviral fiber structure is obtained by web, non-woven fabric, paper, or net, it can be obtained by the same method as the processing of the woven / knitted fabric.
- the antiviral fiber is included at least in part, for example, clothing (including hats, gloves, handkerchiefs), futons, curtains, wallpaper, carpets, mats, sheets, filters, masks, wipers, towels, protective clothing, protective nets. It can be used in everyday life as a textile product such as abandoned chicken bags and poultry house products, and it can destroy viruses that scatter and float in the living space.
- the fiber web may be formed by a card method, an airlaid method, a wet papermaking method, a spunbond method, a melt blown method, a flash spinning method, an electrostatic spinning method, or the like. It can.
- the obtained fiber web is processed into a thermal bond nonwoven fabric such as an air-through nonwoven fabric or a thermocompression bonded nonwoven fabric, a chemical bond nonwoven fabric, a needle punched nonwoven fabric, a hydroentangled nonwoven fabric, a spunbond nonwoven fabric, or a melt blown nonwoven fabric.
- the fiber web may be 100% by mass of the antiviral fiber, but may be mixed with other antiviral fibers or antiviral. You may mix with another fiber within the range in which an effect is acquired.
- the antiviral fiber is preferably at least 20% by mass. More preferably, it is at least 30% by mass. Even more preferably, it is 50 mass% or more.
- the fiber web obtained in this manner can be subjected to predetermined processing to obtain a nonwoven fabric.
- a metal ion can also be carry
- a fiber hereinafter also referred to as a carrier fiber
- a fiber web is prepared, processed into a nonwoven fabric, and then loaded with an antiviral substance
- the fiber web is 100% by mass of the carrier fiber.
- the carrier fibers are preferably at least 20% by mass. More preferably, it is at least 30% by mass. Even more preferably, it is 50 mass% or more.
- a metal ion can also be carry
- the strength of the nonwoven fabric can be greatly increased and the production speed can be increased.
- the handling property at the time of processing such as is good and preferable.
- spunbond nonwoven fabric, melt blown nonwoven fabric, unidirectional stretched array fiber nonwoven fabric in which filaments are aligned and stretched in one direction, background orthogonally laminated fiber nonwoven fabric laminated such that the filament array directions are orthogonal to each other Examples include wet papermaking, nets, films, and woven and knitted fabrics.
- a spunbond nonwoven fabric, a unidirectionally stretched fiber nonwoven fabric, and a history-orthogonal laminated fiber nonwoven fabric are preferably used as a reinforcing layer because the strength of the nonwoven fabric after lamination can be increased.
- antiviral fibers may be used in combination with the antiviral fiber structure of the present invention.
- fibers in which a fiber having an antiviral effect is supported on the fibers include, for example, the following formula I (Wherein M is a metal selected from Fe, Co, Mn, Ti, V, Ni, Cu, Zn, Mo, W, Os, and R 1 , R 2 , R 3 and R 4 are the same or different ⁇ COOH group or —SO 3 H group, and n1, n2, n3 and n4 are positive numbers satisfying 0 to 4 and satisfying 1 ⁇ n1 + n2 + n3 + n4 ⁇ 8).
- Fiber hereinafter also referred to as other antiviral fiber P).
- M in the above formula I is Fe
- R 1 , R 2 , R 3 and R 4 are the same or different —COOH groups
- n1, n2, n3 and n4 are 0-4 and 1
- a metal phthalocyanine derivative represented by a positive number satisfying ⁇ n1 + n2 + n3 + n4 ⁇ 4 is preferable.
- M in the above formula I is Co
- R 1 , R 2 , R 3 and R 4 are the same or different —SO 3 H groups
- n1, n2, n3 and n4 are 0 to 1 and 1 ⁇
- a metal phthalocyanine derivative represented by a positive number satisfying n1 + n2 + n3 + n4 ⁇ 2 has the same effect and is preferable.
- the metal phthalocyanine derivative refers to a metal phthalocyanine compound having the above structure or a salt thereof.
- the salt of the metal phthalocyanine compound include a salt with an inorganic base and a salt with an organic base.
- Preferable examples of the salt with an inorganic base include alkali metal salts such as sodium salt and potassium salt; alkaline earth metal salts such as calcium salt and magnesium salt; and copper (II) salt and ammonium salt.
- Preferable examples of the salt with an organic base include salts with trimethylamine, triethylamine, pyridine, picoline, ethanolamine, diethanolamine, triethanolamine, dicyclohexylamine and the like.
- the antiviral fiber P supports a metal phthalocyanine in which R 1 , R 2 , R 3 and R 4 in the formula I are all H, that is, a structure having no functional group around the metal phthalocyanine ring. It may be a
- the other antiviral fiber P as a method of supporting the metal phthalocyanine derivative on the carrier fiber, a method of immersing the carrier fiber in a metal phthalocyanine derivative solution, or direct dyeing, ion dyeing (such as cotton or rayon)
- a dyeing method such as a method in which a cationic group is bonded to the fiber and the carboxyl group or the anion group of the sulfone group of the dye is ionically bonded), a metal phthalocyanine derivative solution containing a binder component is used as a fiber or
- coating to a fiber structure using printing, spraying, or a coater is mentioned.
- the antiviral fiber structure of the present invention is used by mixing the antiviral fiber of the present invention and another antiviral fiber P in advance, or the antiviral fiber of the present invention and After mixing the carrier fiber, it is contacted with the phthalocyanine derivative solution to obtain another antiviral fiber P, or in addition to the above method, the antiviral fiber of the present invention is contacted with the metal ion solution to obtain the antiviral fiber of the present invention. It can be obtained by a method in which metal ions are supported on each other, or each carrier fiber is prepared and a polymer containing a maleic acid component and a phthalocyanine derivative are added.
- thermal bond nonwoven fabric An example of a thermal bond nonwoven fabric is shown as the antiviral fiber structure of the present invention.
- the antiviral fiber of the present invention, the heat-adhesive fiber, and other antiviral fibers as necessary, and other fibers are mixed to form a fiber web, which is heat-treated at a temperature at which the heat-adhesive fiber is thermally bonded.
- a thermal bond nonwoven fabric can be obtained.
- heat-adhesive fiber examples include polymers such as polyethylene terephthalate, polybutylene terephthalate, polytrimethylene terephthalate, polylactic acid and other polyesters, nylons such as nylon 6 and nylon 66, polypropylenes, polyethylene, polyolefins such as polybutene, Single component fibers or composite fibers in which the polymer is at least partially exposed on the fiber surface can be used.
- polymers such as polyethylene terephthalate, polybutylene terephthalate, polytrimethylene terephthalate, polylactic acid and other polyesters, nylons such as nylon 6 and nylon 66, polypropylenes, polyethylene, polyolefins such as polybutene, Single component fibers or composite fibers in which the polymer is at least partially exposed on the fiber surface can be used.
- an example of a chemical bond nonwoven fabric is shown as an antiviral fiber structure.
- the antiviral fiber of the present invention is mixed with other antiviral fibers and other fibers as necessary to form a fiber web.
- a binder is applied by dipping, spraying (eg, spray bonding), coating (eg, foam bonding), etc., and drying and / or curing It can ring and a chemical bond nonwoven fabric can be obtained.
- a binder an acrylic binder, a urethane binder, or the like can be used.
- the adhesion amount of the binder is not particularly limited as long as the form of the nonwoven fabric can be maintained and the antiviral effect is not inhibited.
- the solid content is preferably 5 to 50% by mass with respect to the mass of the nonwoven fabric.
- hydroentangled nonwoven fabric is shown as an antiviral fiber structure.
- the antiviral fiber of the present invention is mixed with other antiviral fibers and other fibers as necessary to form a fiber web.
- Other sheets can be laminated on the fiber web as required.
- other sheets include spunbonded nonwoven fabrics, meltblown nonwoven fabrics, unidirectionally stretched arrayed fiber nonwoven fabrics, wefted laminated fiber nonwoven fabrics, wet papermaking, nets, films, and woven and knitted fabrics.
- a spunbond nonwoven fabric, a unidirectionally stretched fiber nonwoven fabric, and a history-orthogonal laminated fiber nonwoven fabric are preferably used as a reinforcing layer because the strength of the nonwoven fabric after lamination can be increased.
- an orifice having a hole diameter of 0.05 mm or more and 0.5 mm or less is provided on the fiber web or the laminated sheet from a nozzle provided with an interval of 0.5 mm or more and 1.5 mm or less. It can be obtained by entanglement of fibers 1 to 4 times each from the front and back sides of the web.
- an antiviral fiber structure of the present invention if waterproofness is required, a waterproof film is laminated on the surface of the antiviral fiber structure, or a resin is laminated using an extrusion laminating machine, etc. An antiviral fiber structure having the following can be obtained. Further, when moisture permeability and waterproof properties are required, an antiviral fiber structure having moisture permeability and waterproof properties can be obtained by laminating ultrafine fiber nonwoven fabrics such as melt blown nonwoven fabrics or laminating a resin having moisture permeability. .
- Such an antiviral fiber structure having waterproofness and moisture-permeable waterproofness can be used for medical sheets such as hospital bed sheets, hospital curtains, surgical sheets, and experimental sheets.
- the thermal bond nonwoven fabric, chemical bond nonwoven fabric, and hydroentangled nonwoven fabric can be used, for example, in an air filter.
- the fineness of the constituent fibers is preferably 2 to 50 dtex in the case of a medium and coarse dust filter.
- the basis weight is preferably 10 to 150 g / m 2 .
- the air filter thus obtained can be used as a filter for home appliances such as an air conditioner, an air cleaner, and a vacuum cleaner.
- a filter for an air purifier has a laminated structure of a support such as a chemical bond nonwoven fabric, an antiviral fiber structure, and a high-accuracy filter layer such as an electret nonwoven fabric, HEPA, or ULPA, and is pleated.
- a processed sheet is used.
- the antiviral fiber structure of the present invention can also be used for masks such as sanitary masks, surgical masks, dust masks (for example, N95 compatible masks (Particulate Respirator Type N95), respiratory protection equipment).
- examples of the antiviral fiber structure that can be used for the mask include the thermal bond nonwoven fabric and hydroentangled nonwoven fabric.
- the fineness of the antiviral fiber that can be used for the mask is preferably 1 to 10 dtex. More preferably, it is 2 to 8 dtex.
- the basis weight is preferably 30 to 60 g / m 2 .
- a reinforced nonwoven fabric for example, a spunbond nonwoven fabric, a thermal bond nonwoven fabric
- an antiviral nonwoven fabric of the present invention / an ultrafine fiber nonwoven fabric (for example, a meltblown nonwoven fabric) / a reinforced or flexible nonwoven fabric
- an ultrafine fiber nonwoven fabric for example, a meltblown nonwoven fabric
- a reinforced or flexible nonwoven fabric for example, when a laminated structure of a spunbond nonwoven fabric or a thermal bond nonwoven fabric is used, the antiviral performance can be effectively exhibited.
- the antiviral fiber structure of the present invention a short fiber obtained by cutting an antiviral fiber to 5 mm or less or a fine fiber (hereinafter collectively referred to as fiber powder) supported on another fiber surface is supported.
- fiber powder a fine fiber supported on another fiber surface.
- Non-woven fabric a fine fiber supported on the surface of another fiber with a binder.
- a predetermined amount of antiviral fiber powder and a binder for example, acrylic binder, urethane binder, etc.
- a binder solution can be applied by dipping, spraying (for example, spray bonding), coating (for example, knife coater, gravure coater), etc., and dried and / or cured to obtain an antiviral fiber powder-carrying nonwoven fabric.
- an antiviral fiber powder is prepared by preparing an aqueous dispersion of antiviral fiber powder and immersing, spraying, coating, etc.
- the aqueous dispersion in a fiber structure containing heat-adhesive fibers or wet heat-adhesive fibers After adhering, the antiviral fiber powder-supporting nonwoven fabric can be obtained by heat treatment and adhering the powder with heat-adhesive fibers or wet heat-adhesive fibers.
- a nonwoven fabric such as a thermal bond nonwoven fabric, a spun bond nonwoven fabric, a hydroentangled nonwoven fabric, or a woven or knitted fabric can be used.
- the antiviral fiber powder-supporting nonwoven fabric can be used for protective clothing, for example.
- the non-woven fabric can be cut into a predetermined shape, and the end portions of the non-woven fabric can be overlapped to perform heat sealing, ultrasonic sealing, high-frequency sealing, or sewing.
- the antiviral fiber structure of the present invention is a woven or knitted fabric
- a specific example is shown.
- an antiviral fiber in which a polymer containing a maleic acid component is spun or supported as an antiviral substance is formed, and then a yarn containing a predetermined antiviral fiber is woven.
- the obtained knitted or knitted fabric is used in a dyeing machine such as a zicker dyeing machine, a high-pressure liquid dyeing machine, or a paddle dyeing machine, and 0.05 to 5 parts by weight, ie 0.05 to 5% owf, with respect to 100 parts by weight of fibers.
- a metal ion compound for example, an aqueous copper fiber
- aqueous copper sulfate solution for example, an aqueous copper sulfate solution
- the antiviral woven or knitted fabric thus obtained can be used for, for example, clothing, futons, curtains, carpets, mats, sheets, towels, protective clothing, protective nets, waste chicken bags, poultry house supplies, medical sheet materials, etc. it can.
- Example 1 Production of antiviral fibers-- Example 1 A water-soluble salt of vinyl acetate-maleic anhydride copolymer is added to a viscose solution of cellulose (cellulose concentration 9%) so that the copolymer solid content is 20 parts with respect to 100 parts of cellulose solid content and dissolved. did. Each mixed solution was spun by extrusion from a platinum nozzle in a strongly acidic bath of 130 g / l sulfuric acid, 10 g / l zinc sulfate, and 250 g / l sodium sulfate. A sample of viscose rayon fiber (invention) mixed with vinyl acetate-maleic anhydride copolymer was obtained by desulfurization and scouring bleaching by a conventional method. The fineness was 3.3 dtex, and the fiber length was 51 mm.
- Example 2 The obtained fiber of Example 1 was immersed in a 4% aqueous copper sulfate solution and allowed to stand for 10 minutes, then washed with distilled water and dried at 70 ° C. for 3 hours to obtain a sample of antiviral fiber.
- the amount of copper supported on the antiviral fiber was 1% by mass.
- H5N3 avian influenza virus A / whistling swan / Shimane / 499/83 (H5N3) strain stored in Tottori University Center for Bird Influenza was used.
- This avian influenza virus strain is also referred to as avian influenza virus A / swan / Shimane / 499/83 (H5N3) (hereinafter referred to as H5N3 strain).
- H9N2 strain avian influenza virus A / Turkey / Wisconsin / 1/66 (H9N2) strain
- test virus swine influenza virus A / Swine / Iowa / 15/30 strain
- H1N1 strain swine influenza virus A / Swine / Iowa / 15/30
- the antiviral fibers produced in each of the above examples were cut to a length of about 1.5 cm, 0.2 g was put in a polyethylene bag, and the test virus was diluted 100-fold with phosphate buffered saline (PBS). Each 0.6 ml of virus solution A was dispensed into polyethylene bags, and the virus solution was soaked into the antiviral fiber. The reaction was allowed to stand at 4 ° C for 10 minutes (or 1 minute). The virus solution was collected and further diluted 10-fold with PBS, and 0.2 ml was inoculated into the chorioallantoic cavity in 10-day-old chicken eggs (SPF). After culturing for 2 days, allantoic fluid B was collected and the presence or absence of virus growth was determined by chicken hemagglutination. The virus titer was calculated by the method of Reed & Muench (1938).
- unprocessed rayon fiber was used as a comparative example.
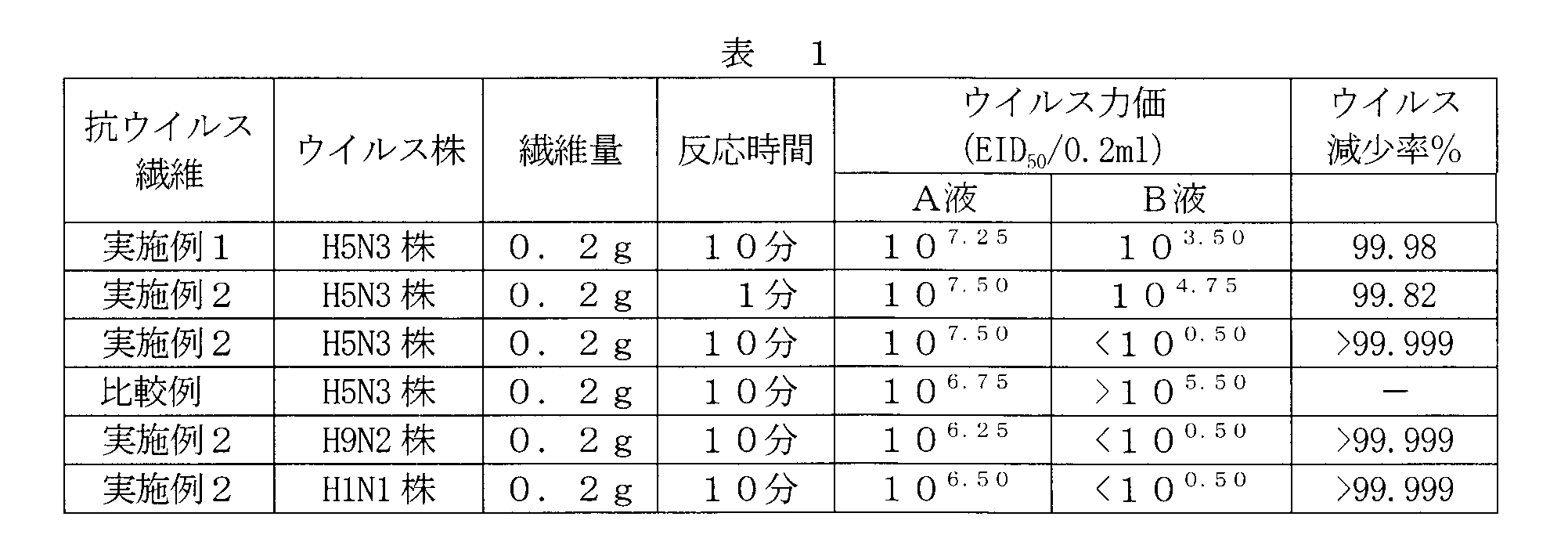
- Table 1 shows the virus titer of each prototype antiviral fiber.
- the allantoic fluid B using the antiviral fibers of Examples 1 and 2 had a significantly reduced virus titer than the virus solution A, and the virus reduction rate was 99% or more.
- the antiviral fibers of Examples 1 and 2 have an antiviral effect against avian influenza virus.
- the virus reduction rate of all virus strains was 99.999% or more. It was.
- the allantoic fluid B of the comparative example using no antiviral fiber under the same conditions had a virus titer decreased as compared with the virus A, but was not sufficient.
- Example 2 100% by mass of the antiviral fiber of Example 2 was mixed to form a fiber web using a parallel card machine, and hydroentangled to prepare an antiviral nonwoven fabric having a basis weight of 40 g / m 2 .
- the obtained antiviral nonwoven fabric is placed on a polypropylene spunbond nonwoven fabric, and a polypropylene meltblown nonwoven fabric and a polypropylene spunbond nonwoven fabric are overlapped, cut into a length of 15 cm and a width of 15 cm, and pleated in three stages.
- An ear strap was provided at the center of the lateral end, and the four sides of the sheet end were heat sealed to produce an antiviral mask.
- the antiviral nonwoven fabric was taken out and the virus titer was measured.
- allantoic fluid B ⁇ 10 1.5 (EID 50 /0.2 ml)
- the virus titer was significantly lower than (10 6.5 (EID 50 /0.2 ml)), and the virus reduction rate was 99.999%. It was confirmed that it can withstand long-term use.
- Example 3 A sample of viscose rayon fiber (invention) mixed with a vinyl acetate-maleic anhydride copolymer having a fineness of 1.7 dtex and a fiber length of 38 mm obtained by spinning in the same manner as in Example 1, and a core component Used was a sheath-core type composite fiber (NBF (H), manufactured by Daiwabo Polytech Co., Ltd.) having a fineness of 2.2 dtex and a fiber length of 51 mm.
- NPF sheath-core type composite fiber
- the sample of the present invention was mixed so that the sample was 60% by mass and the sheath-core composite fiber was 40% by mass, and opened using a parallel card machine to produce a card web.
- the basis weight was 40 g / m 2 .
- the obtained card web was sprayed twice on the surface of the web using a nozzle provided with orifices having a hole diameter of 0.08 mm at intervals of 0.6 mm, and similarly on the opposite surface.
- the fiber was entangled by jetting a columnar water flow with a water pressure of 4 MPa twice. Then, after dewatering in a box-type vacuum suction device, the water flow is fused and dried by a drum-type dryer (set temperature: 140 ° C.) with the sheath component of the sheath-core composite fiber, and is integrated by hydroentanglement.
- a entangled nonwoven fabric was obtained.
- the obtained laminated nonwoven fabric is immersed in a 0.1% aqueous copper sulfate solution at 25 ° C., squeezed with a nip roll, sufficiently washed with a water washing tank, dried at 80 ° C., and a sample of an antiviral nonwoven fabric. Got.
- This antiviral nonwoven fabric had a copper loading of 1% by mass.
- Example 4 A laminated nonwoven fabric comprising the following first to third fiber layers was produced.
- the first fiber layer and the third fiber layer were made of a viscose rayon mixed with a vinyl acetate-maleic anhydride copolymer having a fineness of 1.7 dtex and a fiber length of 38 mm obtained by spinning in the same manner as in Example 1.
- NPF sheath core-type composite fiber
- the sample of the present invention was mixed so that the sample was 60% by mass and the sheath-core composite fiber was 40% by mass, and opened using a parallel card machine to produce a card web.
- the basis weight was 20 g / m 2 for each layer.
- a one-way stretched array nonwoven fabric (trade name: Milife T05, manufactured by Nippon Oil Plast Co., Ltd.) made of polyester fiber and having a basis weight of 5 g / m 2 was prepared.
- a laminated web was prepared by laminating three fiber layers so that the second fiber layer was positioned between the first fiber layer and the third fiber layer. Next, using a nozzle in which orifices having a hole diameter of 0.08 mm are provided at intervals of 0.6 mm, a columnar water flow having a water pressure of 4 MPa is sprayed twice on the surface of the web on the first fiber layer side. The fibers were entangled by injecting a columnar water flow with a water pressure of 4 MPa twice on the surface on the side.
- the obtained laminated nonwoven fabric is immersed in a 0.1% aqueous copper sulfate solution at 25 ° C., squeezed with a nip roll, sufficiently washed with a water washing tank, dried at 80 ° C., and a sample of an antiviral nonwoven fabric. Got. The amount of copper supported on the antiviral nonwoven fabric was 0.7% by mass.
- Table 2 shows the virus titer of avian influenza virus in the samples of Examples 3 to 4.
- the test sample which cut the nonwoven fabric into the length of about 1.5 cm was used for the measurement sample.
- the allantoic fluid B using the samples of Examples 3 to 4 had a significantly reduced virus titer than the virus solution A, and the virus reduction rate was 99% or more. This indicates that the antiviral fiber and antiviral nonwoven fabric of Examples 3 to 4 have an antiviral effect against avian influenza virus.
- H3N2 strain human influenza virus A / Aichi / 2/68 (H3N2) strain (hereinafter referred to as H3N2 strain) was used.
- H3N2 strain human influenza virus A / Aichi / 2/68 (H3N2) strain
- 0.2 g of a test piece cut to a length of about 1.5 cm is taken out, or in the case of fiber, 0.2 g of cotton is prepared by cutting the test piece to a length of about 1.5 cm. Place in a bag and dispense 0.6ml each of virus solution A diluted 100 times with Phosphate Buffered Saline (PBS) into a polyethylene bag so that the virus solution is soaked into the antiviral fiber. It was.
- PBS Phosphate Buffered Saline
- the reaction was allowed to stand at 4 ° C for 10 minutes (or 1 minute).
- the virus solution was collected and further diluted 10-fold with PBS, and 0.2 ml was inoculated into the chorioallantoic cavity in 10-day-old chicken eggs (SPF). After culturing for 2 days, allantoic fluid B was collected and the presence or absence of virus growth was determined by chicken hemagglutination.
- the virus titer was calculated by the method of Reed & Muench (1938).
- Table 3 shows the virus titers of human influenza viruses in the samples of Examples 2 to 4.
- the allantoic fluid B using the samples of Examples 2 to 4 had a greatly reduced virus titer compared to the virus solution A, and the virus reduction rate was 99% or more. This indicates that the antiviral fibers and antiviral nonwoven fabrics of Examples 2 to 4 have an antiviral effect against human influenza virus.
- the laminated nonwoven fabric of Example 4 had better post-processability than the nonwoven fabric of Example 3.
- Feline calicivirus F-9 ATCC VR-782 (hereinafter referred to as feline calicivirus), which is a norovirus substitute virus, was used as a test virus, and antiviral performance was evaluated by the following method. 1. Test method (1) Cells used CRFK cells (Dainippon Pharmaceutical Co., Ltd.) (2) Media used i-cell growth medium An MEM medium “Nissui” i (Nissui Pharmaceutical Co., Ltd.) with 10% fetal calf serum was used.
- ii Cell maintenance medium An MEM medium "Nissui” i with 2% fetal calf serum was used. (3) Preparation of Virus Suspension i Cell Culture Using the cell growth medium, the cells used were cultured in a single layer in a tissue culture flask. ii Virus inoculation After the monolayer culture, the cell growth medium was removed from the flask and the test virus was inoculated. Next, a cell maintenance medium was added and cultured in a carbon dioxide incubator (CO 2 concentration 5%) at 37 ° C. ⁇ 1 ° C. for 1 to 5 days.
- CO 2 concentration 5% carbon dioxide incubator
- iii Preparation of virus suspension After culturing, the morphology of cells was observed using an inverted phase contrast microscope, and it was confirmed that morphological changes (cytopathic effect) occurred in the cells. Next, the culture solution was centrifuged (3000 r / min. 10 minutes), and the resulting supernatant was diluted 10-fold with purified water to obtain a virus suspension. (4) Preparation of sample The nonwoven fabric of Example 3 cut into a size of about 3 cm x 3 cm was used as a sample. (5) Test procedure 0.2 ml of the virus suspension was dropped into the sample and stored at room temperature. (6) Washing out virus After 24 hours of storage, the sample virus suspension was washed out with 2 ml of cell maintenance medium.
- Example 5 Production of waterproof antiviral nonwoven fabric Using an extrusion laminator, low density polyethylene having a melting point of 103 ° C. is laminated on the surface of the antiviral nonwoven fabric of Example 4 so as to have a thickness of 30 ⁇ m. An antiviral nonwoven was prepared.
- Example 6 Preparation of antiviral fiber powder First, a sample of viscose rayon fiber (invention) mixed with a vinyl acetate-maleic anhydride copolymer having a fineness of 3.3 dtex was prepared in the same manner as in Example 1. After obtaining, an antiviral fiber powder was prepared by cutting with a cutter so that the fiber length was 0.1 mm.
- the obtained powder was immersed in a 4% aqueous copper sulfate solution and allowed to stand for 10 minutes, then washed with distilled water and dried at 70 ° C. for 3 hours to obtain a sample of antiviral fiber powder carrying copper ions. .
- This antiviral fiber powder had a copper loading of 1% by mass.
- rayon fibers fineness 2.2 dtex, fiber length 0.1 mm
- rayon fibers fineness 2.2 dtex, fiber length 0.1 mm
- 15 g / L of sodium hydroxide aqueous solution 1 kg was added under the condition of a bath ratio of 1:10 and reacted at 85 ° C. for 45 minutes.
- allantoic fluid B (10 2.75 (EID 50 /0.2 ml)) had a greatly reduced virus titer than virus solution A (10 7.25 (EID 50 /0.2 ml)), with a virus reduction rate of 99.99%.
- a polypropylene spunbonded nonwoven fabric having a basis weight of 40 g / m 2 was prepared as a base fabric.
- an acrylic emulsion binder for adhering the antiviral fiber powder to the base fabric is prepared, and an acrylic emulsion binder, 50% by mass of the antiviral fiber powder of the present invention, and 50% by mass of the antiviral rayon fiber P powder are added.
- a solution was prepared. 3 g / m 2 of fiber powder was applied to the surface of the base fabric using a knife coater. The binder was applied in a solid content of 6 g / m 2 . Next, curing was performed at 150 ° C. for 3 minutes to obtain an antiviral fiber powder-supporting nonwoven fabric.
- Table 4 shows the virus titer of avian influenza virus in the sample of Example 6.
- the allantoic fluid B using the sample of Example 6 had a significantly reduced virus titer than the virus solution A, and the virus reduction rate was 99% or more. This has shown that the antiviral fiber powder carrying
- Example 6 (3) Production of Protective Clothing The nonwoven fabric of Example 6 was cut into a predetermined shape, and the nonwoven fabric ends were overlapped and heat-sealed to produce a protective garment. Since the nonwoven fabric itself is flexible and the fiber powder does not fall off, it was confirmed that it can be used as protective clothing.
- Example 7 Preparation of antiviral nonwoven fabric Viscose rayon fiber mixed with vinyl acetate-maleic anhydride copolymer having a fineness of 7.8 dtex and a fiber length of 51 mm obtained by spinning in the same manner as in Example 1 (this Invention) and a cobalt (II) sodium phthalocyanine monosulfonate and cobalt (II) sodium phthalocyanine disulfonate having a fineness of 15 dtex and a fiber length of 64 mm obtained by processing in the same manner as in Example 6.
- a virus rayon fiber P and a polyester fiber having a fineness of 30 dtex and a fiber length of 64 mm were prepared.
- Example 8 Preparation of antiviral nonwoven fabric Viscose rayon fiber mixed with vinyl acetate-maleic anhydride copolymer having a fineness of 7.8 dtex and a fiber length of 51 mm obtained by spinning in the same manner as in Example 1 (this A sample of (Invention) was prepared.
- allantoic fluid B (10 4.75 (EID 50 /0.2 ml)) had a greatly reduced virus titer than virus solution A (10 6.75 (EID 50 /0.2 ml)), with a virus reduction rate of 99%.
- the sheath-core type composite fiber used in Example 3 was prepared. 30% by mass of a sample of viscose rayon fiber (invention) mixed with vinyl acetate-maleic anhydride copolymer, 40% by mass of antiviral rayon fiber P, and 30% by mass of sheath-core type composite fiber were mixed, and the card A laminated web was produced by cross layering the card web opened using a machine. Subsequently, it heat-processed with the 140 degreeC hot-air processing machine, the sheath component of the sheath-core type composite fiber was melted, and the thermal bond nonwoven fabric was produced. The basis weight was 60 g / m 2 .
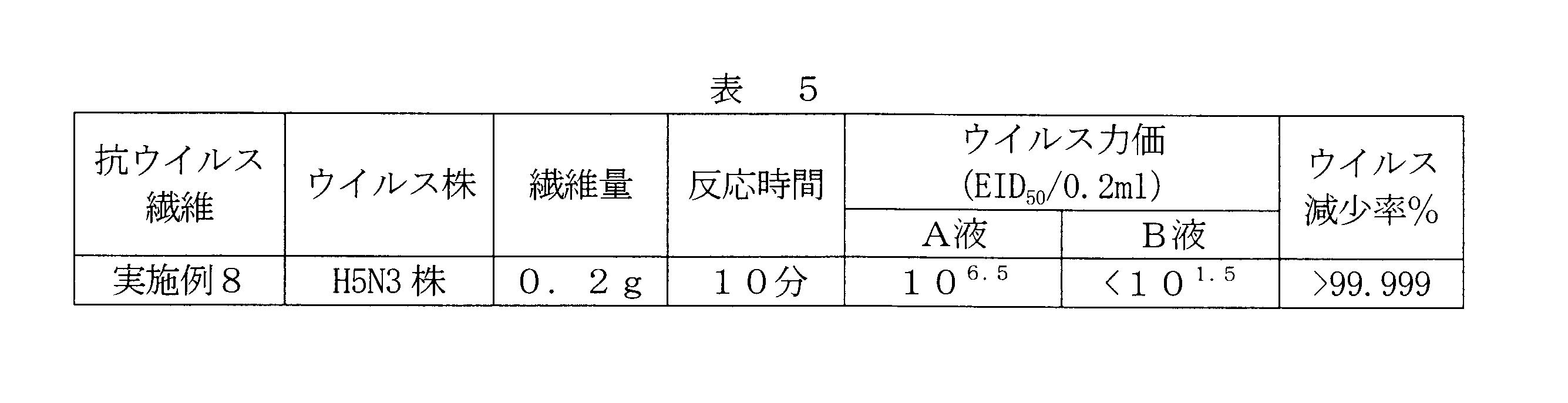
- the virus titer of avian influenza virus in the sample of Example 8 is shown in Table 5.
- the allantoic fluid B using the sample of Example 8 had a significantly reduced virus titer than the virus solution A, and the virus reduction rate was 99% or more. This indicates that the antiviral nonwoven fabric of Example 8 has an antiviral effect against avian influenza virus.
- Example 9 Production of antiviral fabric Viscose rayon fiber mixed with a vinyl acetate-maleic anhydride copolymer having a fineness of 1.4 dtex and a fiber length of 38 mm obtained by spinning in the same manner as in Example 1 Invention) and a recycled polyester fiber (trade name Ecopet, manufactured by Teijin Fibers Limited) having a fineness of 1.45 dtex and a fiber length of 35 mm were used.
- a 14th single yarn (with a coefficient of 4.3 to 4.5) in which 50% by mass of the sample of the present invention and 50% by mass of recycled polyester fiber were blended was produced.
- a warp 89 pieces / inch, a weft 51 pieces / inch, and a 3/1 twill fabric were produced.
- the woven fabric was subjected to metal ion processing using a zicker dyeing machine.
- An aqueous copper sulfate solution of 0.5% owf based on the fiber mass was added to the Zicker dyeing machine, and the fabric was immersed.
- Example 10 A water-soluble salt of vinyl acetate-maleic anhydride copolymer is added to a viscose solution of cellulose (cellulose concentration 9%) so that the copolymer solid content is 20 parts with respect to 100 parts of cellulose solid content and dissolved. did.
- Each mixed solution was spun by extrusion from a platinum nozzle in a strongly acidic bath of 130 g / l sulfuric acid, 10 g / l zinc sulfate, and 250 g / l sodium sulfate.
- a sample of viscose rayon fiber (invention) mixed with vinyl acetate-maleic anhydride copolymer was obtained by desulfurization and scouring bleaching by a conventional method.
- the fineness was 7.8 dtex, and the fiber length was 76 mm.
- the obtained rayon fiber was immersed in a 5% zinc sulfate (ZnSO 4 ⁇ 7H 2 O) aqueous solution and allowed to stand at 60 ° C. for 20 minutes, then washed with distilled water and dried at 70 ° C. for 3 hours. A sample was obtained. The amount of zinc supported by the antiviral fiber was 1% by mass.
- Example 11 The rayon fiber obtained in Example 10 was immersed in a 5% nickel chloride (NiCl 2 ⁇ 6H 2 O) aqueous solution and allowed to stand at 60 ° C. for 20 minutes, then washed with distilled water, and dried at 70 ° C. for 3 hours. A sample of antiviral fiber was obtained. The amount of nickel supported on the antiviral fiber was 1% by mass.
- NiCl 2 ⁇ 6H 2 O nickel chloride
- Table 6 shows the results of evaluating the performance against the avian influenza virus (H5N3) for the antiviral fibers prototyped in Examples 10 and 11 above.
- Example 10 (rayon fiber containing vinyl acetate-maleic acid copolymer polymer carrying zinc ions), Example 11 (containing vinyl acetate-maleic acid copolymer polymer carrying nickel ions)
- the virus titer was significantly reduced as compared with the virus liquid A, and the virus reduction rate was 99% or more. This indicates that the antiviral fibers of Examples 10 and 11 have an antiviral effect against avian influenza virus.
- Example 12 Preparation of antiviral nonwoven fabric
- These fibers were mixed, made into a fiber web using a parallel card machine, and subjected to hydroentanglement treatment to produce an antiviral nonwoven fabric having a basis weight of 50 g / m 2 .
- allantoic fluid B ( ⁇ 10 0.75 (EID 50 /0.2 ml) was found to be virus fluid A (10 6.75 (EID 50 The virus titer was significantly lower than that of 0.2 ml)), and the virus reduction rate was 99.999%.
- antiviral mask The obtained antiviral nonwoven is placed on a polypropylene spunbonded nonwoven fabric, and a polypropylene meltblown nonwoven fabric and a polypropylene spunbonded nonwoven fabric are overlapped and cut into 15 cm in length and 15 cm in width, in three steps.
- the antiviral mask was prepared by folding the pleats, providing an ear strap at the center of the lateral edge, and heat-sealing the four sides of the sheet edge.
- This antiviral mask had a constitution of protective nonwoven fabric (spunbond nonwoven fabric) / non-woven fabric for microfiltration (melt blown nonwoven fabric) / antiviral nonwoven fabric / protective nonwoven fabric (spunbond nonwoven fabric) from the outside toward the inside (mouth side). When this mask was worn, there was no breathing and the wearability was good.
- Example 13 Preparation of Antiviral Nonwoven Fabric
- antiviral fiber P having a fineness of 5.6 dtex and a fiber length of 76 mm obtained by the same method as described above, and a sheath having a fineness of 2.2 dtex and a fiber length of 51 mm consisting of polypropylene as the core component and high-density polyethylene as the sheath component 40% by mass of core-type composite fiber (Niwa (H) manufactured by Daiwabo Polytech Co., Ltd.) was used. These fibers were mixed and a card web opened using a parallel card machine was produced. Next, heat treatment is performed at 140 ° C.
- allantoic fluid B ( ⁇ 10 1.50 (EID 50 /0.2 ml) was found to be viral fluid A (10 6.75 ( The virus titer was significantly lower than EID 50 /0.2 ml)), and the virus reduction rate was 99.999%.
- Air filter production A chemically bonded non-woven fabric mixed with polyester fiber and rayon fiber is used as a support. After spraying a hot melt agent on the support, the resulting antiviral non-woven fabric is laminated and integrated with the hot melt agent. did. Next, after spraying a hot melt agent on the antiviral nonwoven fabric, an electret nonwoven fabric (precision filter layer) having a basis weight of about 150 g / m 2 was laminated and integrated with the hot melt agent. The obtained sheet was pleated by a pleating machine and fitted into a plastic unit to produce an air purifier filter.
- the antiviral substance of the present invention can be used as a raw material for the antiviral fiber of the present invention.
- the antiviral fiber structure containing at least a part of the antiviral fiber of the present invention can be formed into yarn, woven or knitted fabric, web, nonwoven fabric, paper, net, etc. and used in various textile industries.
- the antiviral fiber structure has a high inactivation effect against the virus that comes into contact with it, and is useful for medical treatment.
- the antiviral fiber product containing at least a part of the antiviral fiber includes, for example, clothing, futon, curtain, wallpaper, carpet, mat, bed sheet, filter, mask, wiper, towel, protective clothing, protective net, waste chicken Can be used in the form of bags, poultry house supplies and medical sheets.
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Health & Medical Sciences (AREA)
- Wood Science & Technology (AREA)
- General Health & Medical Sciences (AREA)
- Dentistry (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Agronomy & Crop Science (AREA)
- Plant Pathology (AREA)
- Pest Control & Pesticides (AREA)
- General Chemical & Material Sciences (AREA)
- Inorganic Chemistry (AREA)
- Textile Engineering (AREA)
- Organic Chemistry (AREA)
- Toxicology (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Materials Engineering (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Compositions Of Macromolecular Compounds (AREA)
- Chemical Or Physical Treatment Of Fibers (AREA)
- Artificial Filaments (AREA)
- Materials For Medical Uses (AREA)
- Nonwoven Fabrics (AREA)
Abstract
ウイルスを不活化させるに有効な抗ウイルス物質、抗ウイルス物質を担持した繊維製品、並びに繊維構造物を提供する。
抗ウイルス物質は、重合鎖中にモノマー単位としてのマレイン酸成分を含む高分子からなり、鳥インフルエンザウイルスに有効である。この共重合高分子と、セルロースとを混合し紡糸して抗ウイルス繊維が製造される。
Description
本発明は、ウイルスに有効な高分子からなる抗ウイルス物質、抗ウイルス機能を備えた繊維に関するものである。
近年、SARS(重症急性呼吸器症候群)や鳥インフルエンザなどのウイルス病が世界的に猛威をふるい、特にインフルエンザウイルスは、次々と新種のものが発見され、人類にとって脅威となっている。本来、ウイルスの宿主域は限定され、哺乳類に感染するものは哺乳類だけ、鳥類に感染するものは鳥類だけというのが通常である。しかし、鳥インフルエンザウイルスは、鳥類のみならず哺乳類にも感染することができる広い宿主域をもつウイルスであるため、ヒトに対して感染する恐れがある。現在では、アジアやヨーロッパでもH5N1型インフルエンザが蔓延しており、それをベースにしたヒト新型インフルエンザの出現が危惧されている。
また、鳥インフルエンザウイルスは、渡り鳥により遠隔地まで運搬されるため、食品のように疾病の発生した国からの輸入を停止し、検疫のみにより国内への侵入を阻止することができない。
このようなインフルエンザウイルスを不活化する剤が特許文献1に開示されている。このインフルエンザウイルス不活化剤は、ヨウ素とβ-シクロデキストリンとを包含する溶液である。
一方、特許文献2には、セルロースと酢酸ビニル-マレイン酸共重合体との混合体からなるイオン交換機能を持ったセルロース系組成物が開示されている。このセルロース系組成物は、ブドウ状球菌、グラム陰性菌に対する抗菌性があると記載されている。
また、特許文献3には、架橋構造を有し、且つ分子中にカルボキシル基を有する繊維として、架橋アクリル繊維を用い、その繊維中に水に難溶性の金属および/または金属化合物の微粒子が分散している抗ウイルス性繊維が開示されている。しかし、繊維中に微分散している水に難溶性の金属及び/又は金属化合物の微粒子とウイルスが接触してウイルス不活化効果を得ているが、その方法では十分なウイルス不活化効果が得られず、また水分雰囲気化でないとその効果が低下するものと考えられる。
本発明の発明者は、特許文献2で開示したセルロース系組成物の特異な性質に着目して永年に渡り研究し、蛋白質を変性させることを見出した。前記したとおりインフルエンザの発生を全面的に取り除くことは極めて困難であることに鑑みて、本発明は、セルロース系組成物の持つそのような特性を利用し、ブドウ状球菌、グラム陰性菌のような細菌の大きさよりもはるかに小さいウイルスに有効な抗ウイルス物質、抗ウイルス物質を担持した繊維、繊維構造物、並びに繊維製品を提供することを目的とする。
前記の目的を達成するためになされた、請求の範囲の請求項1に係る発明の抗ウイルス物質は、重合鎖中にモノマー単位としてのマレイン酸成分を含む高分子からなることを特徴とする。
同じく請求項2に係る発明の抗ウイルス物質は、請求項1に係る発明の抗ウイルス物質であって、該高分子が、オレフィン-マレイン酸共重合高分子、スチレン-マレイン酸共重合高分子、ビニルエステル-マレイン酸共重合高分子、酢酸ビニル-マレイン酸共重合高分子、または塩化ビニル-マレイン酸共重合高分子であることを特徴とする。
請求項3に係る発明の抗ウイルス物質は、同じく請求項1に係る発明の抗ウイルス物質であって、該高分子が、銅、銀、亜鉛、ニッケルから選ばれる金属のイオンを担持していることを特徴とする。
請求項4に係る発明の抗ウイルス物質は、請求項1に係る発明の抗ウイルス物質であって、該マレイン酸成分を含む高分子が、銅イオンを担持した酢酸ビニル-マレイン酸共重合高分子であることを特徴とする。
請求項5に係る発明の抗ウイルス物質は、請求項2に記載のマレイン酸成分を含む共重合高分子から選ばれる少なくとも一つの共重合高分子と、セルロースとが混合されていることを特徴とする。
請求項6に係る発明の抗ウイルス物質は、請求項1に係る発明の抗ウイルス物質において、鳥インフルエンザウイルスに有効なことを特徴とする。
請求項7に係る発明の抗ウイルス物質は、請求項6に係る発明の抗ウイルス物質であって、該鳥インフルエンザウイルスがA/whistling swan/Shimane/499/83 (H5N3)株、及びA/Turkey/Wisconsin/1/66 (H9N2)株から選ばれる少なくとも1種類であることを特徴とする。
請求項8に係る発明の抗ウイルス物質は、請求項1に係る発明の抗ウイルス物質において、ヒトインフルエンザウイルスに有効なことを特徴とする。
請求項9に係る発明の抗ウイルス物質は、請求項1に係る発明の抗ウイルス物質において、ブタインフルエンザウイルスに有効なことを特徴とする。
請求項10に係る発明の抗ウイルス物質は、請求項1に係る発明の抗ウイルス物質において、ノロウイルスに有効なことを特徴とする。
また、前記の目的を達成するためになされた、請求の範囲の請求項11に係る発明の抗ウイルス繊維は、重合鎖中にモノマー単位としてのマレイン酸成分を含む高分子からなる抗ウイルス物質を成分として含むことを特徴とする。
さらに前記の目的を達成するためになされた、請求の範囲の請求項12に係る発明の抗ウイルス繊維構造物は、請求項11に係る発明の抗ウイルス繊維を少なくとも一部に含むことを特徴とする。
さらに前記の目的を達成するためになされた、請求の範囲の請求項13に係る発明の抗ウイルス繊維製品は、請求項11に係る発明の抗ウイルス繊維を少なくとも一部に含み、衣類、寝具、布団、カーテン、壁紙、カーペット、マット、シーツ、フィルター、マスク、ワイパー、タオル、防護衣類、防護ネット、廃鶏袋、鶏舎用品、医療用シートに形づくられたことを特徴とする。
本発明の抗ウイルス物質は、ウイルスを不活化させるのに有効である。また、本発明の抗ウイルス物質の高分子を紡糸または担持した本発明の抗ウイルス繊維は、ウイルスを不活化させるのに有効である。さらに、本発明の抗ウイルス繊維は繊維製品に加工され、本発明の繊維構造物を構成する。その抗ウイルス繊維構造物は、接触するウイルスに対して不活化効果が高い。
本発明の抗ウイルス物質は、重合鎖中にモノマー単位としてのマレイン酸成分を含む高分子からなるもので、例えば、オレフィン-マレイン酸共重合高分子、スチレン-マレイン酸共重合高分子、ビニルエステル-マレイン酸共重合高分子、酢酸ビニル-マレイン酸共重合高分子、または塩化ビニル-マレイン酸共重合高分子が挙げられる。
この抗ウイルス物質は、様々なウイルスに対して不活化効果を有する。本発明において不活化効果の対象となるウイルスは、ゲノム種類、及びエンベロープの有無等によらず、全てのウイルスが含まれる。例えば、ゲノムとしてDNAを有するウイルスとしては、ヘルペスウイルス、天然痘ウイルス、牛痘ウイルス、水疱瘡ウイルス、アデノウイルス等が挙げられ、ゲノムとしてRNAを有するウイルスとしては、麻疹ウイルス、インフルエンザウイルス、コクサッキーウイルス、カリシウイルス(ノロウイルス属)、レトロウイルス(レンチウイルス属、例えばHIV(human immunodeficiency virus:ヒト免疫不全ウイルス)等)、コロナウイルス等が挙げられる。また、これらのウイルスのうち、エンベロープを有するウイルスとしては、ヘルペスウイルス、天然痘ウイルス、牛痘ウイルス、水疱瘡ウイルス、麻疹ウイルス、インフルエンザウイルス等が挙げられ、エンベロープを有さないウイルスとしては、アデノウイルス、コクサッキーウイルス、ノロウイルス等が挙げられる。
この抗ウイルス物質がウイルスに対して不活化効果を有する理由は、インフルエンザウイルスに対して、ウイルス表面にある突起HA(ヘマグルチニン)とNA(ノイラミターゼ)の活性を阻害するためと推定される。また、他のウイルスにおいても、ウイルス表面の突起の活性を阻害するか、ウイルス粒子を直接破壊するためと推定される。
抗ウイルス物質は、鳥インフルエンザウイルスに対する不活化効果が高く、特にH5、あるいはH7の亜型のような強毒性のある高病原性鳥インフルエンザウイルスに有効である。本発明では、鳥インフルエンザウイルスA/whistling swan/Shimane/499/83 (H5N3)株、鳥インフルエンザウイルスA/Turkey/Wisconsin/1/66 (H9N2)株について抗ウイルス効果を証明しているが、H5N1型などの鳥インフルエンザウイルスにも効果があると考えられる。
また、本発明の抗ウイルス物質は、ヒトインフルエンザウイルスに対する不活化効果も高く、あらゆる種類のインフルエンザウイルスに有効である。ヒトインフルエンザウイルスA/Aichi/2/68 (H3N2)株について抗ウイルス効果を証明しているが、他のヒトインフルエンザウイルスにも効果があると考えられる。
さらに、この抗ウイルス物質は、ブタインフルエンザウイルスA/Swine/Iowa/15/30 (H1N1) 株について抗ウイルス効果を証明している。
さらに、この抗ウイルス物質は、ノロウイルスに対する不活化効果も高い。本発明では、細胞培養が不可能なノロウイルスの代替ウイルスとして広く使用されているカリシウイルスについて抗ウイルス効果を証明している。
前記マレイン酸成分を含む高分子として代表的には、酢酸ビニル-マレイン酸共重合体である。この共重合体は、酢酸ビニルと無水マレイン酸とを公知のラジカル重合開始剤を使用して、ベンゼン、トルエン、酢酸エステルのような有機溶媒の存在下に、溶液重合させることにより得ることができる。
酢酸ビニルとマレイン酸は、ほぼ等モル共重合体であることが望ましい。分子量は用途に応じて広い範囲に亘り得るが通常1万~200万好ましくは10万~50万の範囲である。
酢酸ビニル及び無水マレイン酸は両者の等モル共重合体を得る場合0.9:1.1~1.1:0.9の割合で仕込めばよい。重合温度は通常50~120℃程度、重合時間は1~6時間程度とする。ラジカル重合開始剤としては、過酸化ベンゾイル、過酸化アセチルなどの過酸化物系重合開始剤、アゾビスイソブチロニトリルなどのアゾ系重合開始剤を例示でき、それらの使用量は通常全単量体に対して0.05~1.0質量%程度とされる。得られた共重合体溶液から溶剤を除去し、共重合体固形分の抗ウイルス物質とすることができる。
前記マレイン酸成分を含む高分子は、有機物、無機物の担体に担持または混合することができる。マレイン酸成分を含む高分子が担体に対する含有量は、担体に担持または混合でき、且つ抗ウイルス効果を発揮し得る範囲であれば特に限定されないが、例えば、担体100質量部に対してマレイン酸成分を含む高分子が1~100質量部であることが好ましい。より好ましいマレイン酸成分を含む高分子の含有量は、5~60質量部である。
本発明の抗ウイルス物質は、前記有機物の担体としてセルロース材料に担持していることが好ましい。セルロース材料は、吸水性が良いため、抗ウイルス効果を発揮しやすい傾向にある。特に、後述する銅、銀、亜鉛から選ばれる金属のイオンを担持させたときに、+イオンまたは-イオンの状態で担体に保持させておくことが重要であり、水分を保持できるセルロース材料の方が有利である。セルロース材料は、例えば、繊維、スポンジ等の形態に加工される。
前記有機物の担体としては、繊維が特に好ましい。繊維は、嵩量があり大きな表面積を持つため、マレイン酸成分を含む高分子が効率よく空気中のウイルスに接触する。
繊維素材は、例えばセルロース系繊維(木綿、麻、レーヨン、パルプなど)、蛋白質系繊維(羊毛、絹など)、ポリアミド系繊維、ポリエステル系繊維、ポリアクリル系繊維、ポリビニルアルコール系繊維、ポリ塩化ビニル系繊維、ポリ塩化ビニリデン系繊維、ポリオレフィン系繊維、ポリウレタン系繊維などあらゆる天然繊維、再生繊維、半合成繊維、合成繊維が使用される。なかでもセルロース系繊維は、上記セルロース材料が好ましい理由と同様に有利である。また、セルロース系繊維は、合成繊維のように静電気がおきて埃がたまることがないので、埃により反応サイトが塞がれることがなく、より抗ウイルス効果を発揮することができる。特にレーヨンは、吸水性が良く、繊度や繊維長を調整しやすいので、様々な繊維構造物および繊維製品に適用することができる。
例えば、この酢酸ビニル-マレイン酸共重合体溶液は、公知の方法により得られるセルロースのビスコース溶液、あるいはセルロースの銅アンモニア溶液などの含金属アルカリ溶液と溶解混合した混合液を、紡糸ノズルを通じて紡糸液に吐き出して、いわゆる湿式紡糸により本発明の抗ウイルス繊維を得ることができる(例えば特公平8-13905号公報参照)。
セルロースと共重合体との混合割合は、前者が60~99質量%、後者が40~1質量%程度が好ましい。セルロースの使用割合が60質量%未満の場合には、得られるセルロース系組成物は表面にべとつき感が生じることがあり、引き続く紡織、複合化などの工程に際してブロッキングなどの不利が生じることがある。また99質量%を越える場合には酢酸ビニル-マレイン酸共重合体を使用することによる抗ウイルス効果が低くなることがある。
本発明の抗ウイルス繊維には、さらに抗ウイルス作用を高めるために、銅、銀、亜鉛、ニッケルから選ばれる金属のイオンを含む溶液などに浸漬、コーティング等の加工を施して、銅イオン、銀イオン、亜鉛イオン、及びニッケルイオンから選ばれる少なくとも一つの金属イオンを担持することが好ましい。金属イオンとしては、銅イオンの抗ウイルス効果が高く、特に好ましい。
前記抗ウイルス繊維に、銅イオンを担持させる方法としては、例えば硫酸銅(CuSO4)あるいは硝酸銅(Cu(NO3)2)などの溶液に浸漬して銅イオンを吸着することができる。亜鉛イオンを担持させる方法としては、塩化亜鉛(ZnCl2)溶液に浸漬して亜鉛イオンを吸着することができる。
前記抗ウイルス繊維は、例えば、シート状物、樹脂成型物、無機成型物などに添加して用いることもできる。また、バインダー等を併用して、シート状物、樹脂成型物、無機成型物などに接着することができる。
前記抗ウイルス繊維の断面形状は特に限定されず、円形、異形、中空等のいずれであってもよい。また、抗ウイルス繊維の繊維長も特に限定されず、長繊維、短繊維、微細繊維等のいずれであってもよい。長繊維であれば、紡糸後そのままボビン等に繊維を巻き付けることにより得ることができる。短繊維であれば、カッターなどで所定の繊維長に切断するか、天然繊維であればそのまま用いることができる。微細繊維であれば、グラインドミルなどですり潰すようにして裁断し、任意のメッシュを有する篩にかけて分級することにより得ることができる。すり潰して裁断した微細繊維は適度に湾曲している。さらに、前記抗ウイルス繊維の繊度は特に限定されず、用途に応じて適宜選定するとよい。
本発明の抗ウイルス繊維構造物は、前記抗ウイルス繊維を少なくとも一部に含み、糸、織編物、ウェブ、不織布、紙、ネット等に成形して用いることができる。また、前記繊維構造物とフィルム等の他のシートと積層した積層シートとしてもよい。
以下、具体的な抗ウイルス繊維構造物について説明する。本発明の抗ウイルス繊維構造物を糸で得る場合、(1)先に抗ウイルス物質としてマレイン酸成分を含む高分子又はマレイン酸成分に銅、銀、亜鉛等の金属のイオンを担持させた高分子を紡糸または担持した繊維を得て、抗ウイルス繊維とした後に、少なくとも一部に抗ウイルス繊維を含む糸を作製する方法、(2)抗ウイルス物質としてマレイン酸成分を含む高分子を紡糸または担持した繊維を得て、少なくとも一部に抗ウイルス繊維を含む糸を作製した後、マレイン酸成分に銅、銀、亜鉛等の金属のイオンを担持させる方法、あるいは(3)公知の方法により糸を作製した後、マレイン酸成分を含む高分子を繊維表面に担持させる方法、等を採ることができる。前記した糸は、公知の紡績糸、マルチフィラメント糸を製造する方法で得ることができる。
本発明の抗ウイルス繊維構造物を織編物で得る場合、(1)先に抗ウイルス物質としてマレイン酸成分を含む高分子又はマレイン酸成分に銅、銀、亜鉛等の金属のイオンを担持させた高分子を紡糸または担持した繊維を得て、抗ウイルス繊維とした後、所定の抗ウイルス繊維を含有する糸を製織し、必要に応じて染色して、織編物を作製する方法、(2)抗ウイルス物質としてマレイン酸成分を含む高分子を紡糸または担持した繊維を得て、少なくとも一部に抗ウイルス繊維を含む糸を作製して製織した後、必要に応じて染色し、マレイン酸成分に銅、銀、亜鉛等の金属のイオンを担持させる方法、(3)先に抗ウイルス繊維を5mm以下に切断した短繊維、または粉砕した微細繊維をバインダーにより織編物を構成する繊維表面に担持させる方法、等を採ることができる。前記した織編物は、公知の織編物を製造する方法で得ることができる。
抗ウイルス繊維構造物をウェブ、不織布、紙、ネットで得る場合も上記織編物の加工と同様の方法で得ることができる。
前記抗ウイルス繊維は、少なくとも一部に含み、例えば、衣類(帽子、手袋、ハンカチを含む)、布団、カーテン、壁紙、カーペット、マット、シーツ、フィルター、マスク、ワイパー、タオル、防護衣類、防護ネット、廃鶏袋、鶏舎用品のごとき繊維製品にして日常の生活に供され、生活空間に飛散浮遊するウイルスをせん滅させることができる。
以下、本発明の抗ウイルス繊維構造物および抗ウイルス繊維製品について、具体的に例示する。本発明の抗ウイルス繊維構造物が不織布の場合、繊維ウェブの形成方法は、カード法、エアレイド法、湿式抄紙法、スパンボンド法、メルトブローン法、フラッシュ紡糸法、静電紡糸法などを用いることができる。得られた繊維ウェブは、エアースルー不織布や熱圧着不織布などのサーマルボンド不織布、ケミカルボンド不織布、ニードルパンチ不織布、水流交絡不織布、スパンボンド不織布、メルトブローン不織布などに加工される。
例えば、予め抗ウイルス物質が混合または担持された抗ウイルス繊維を用いた場合、前記繊維ウェブは、抗ウイルス繊維100質量%であってもよいが、他の抗ウイルス繊維との混合、あるいは抗ウイルス効果が得られる範囲内で他の繊維と混合してもよい。他の繊維と混合する場合は、抗ウイルス繊維が少なくとも20質量%であることが好ましい。より好ましくは、少なくとも30質量%である。さらにより好ましくは、50質量%以上である。このようにして得られた繊維ウェブは、所定の加工が施されて不織布を得ることができる。また、得られた繊維ウェブまたは不織布に金属イオンを上述した方法で担持することもできる。
例えば、担体となる繊維(以下、担体用繊維ともいう)を準備し、繊維ウェブを作製し、不織布に加工した後、抗ウイルス物質を担持させる場合、繊維ウェブは、担体用繊維100質量%であってもよいが、他の抗ウイルス繊維との混合、あるいは抗ウイルス効果が得られる範囲内で他の繊維と混合してもよい。他の繊維と混合する場合は、担体用繊維が少なくとも20質量%であることが好ましい。より好ましくは、少なくとも30質量%である。さらにより好ましくは、50質量%以上である。また、得られた繊維ウェブまたは不織布に金属イオンを上述した方法で担持することもできる。このように、後加工で繊維ウェブまたは不織布に抗ウイルス物質および/または金属イオンを担持させる場合、不織布に他のシートを積層し一体化すると、例えば、不織布強力を大きく生産速度を上げることができるなどの加工時の取り扱い性がよく、好ましい。他のシートとしては、スパンボンド不織布、メルトブローン不織布、フィラメントが1方向に配列され延伸された一方向延伸配列繊維不織布、フィラメントの配列方向が互いに直交するように積層されてなる経緯直交積層繊維不織布、湿式抄紙、ネット、フィルム、織編物などが挙げられる。特に、スパンボンド不織布、一方向延伸配列繊維不織布、および経緯直交積層繊維不織布は、積層した後の不織布強力を大きくすることができるので、補強層として好ましく用いられる。
本発明の抗ウイルス繊維構造物には、他の抗ウイルス繊維を併用してもよい。抗ウイルス効果を有する物質を繊維に担持させた他の繊維としては、例えば、下記I式
(I式中、MはFe、Co、Mn、Ti、V、Ni、Cu、Zn、Mo、W、Osから選択される金属、R1、R2、R3およびR4は同一または異なる-COOH基または-SO3H基であり、n1、n2、n3およびn4は0~4で1≦n1+n2+n3+n4≦8を満たす正数)で示される金属フタロシアニン誘導体を有効成分に含む抗ウイルス剤が担持された繊維(以下、他の抗ウイルス繊維Pともいう)が挙げられる。この繊維Pは、上記I式中のMはFeであり、R1、R2、R3およびR4は同一または異なる-COOH基であり、n1、n2、n3およびn4は0~4で1≦n1+n2+n3+n4≦4を満たす正数で示される金属フタロシアニン誘導体であることが好ましい。また、上記I式中のMはCoであり、R1、R2、R3およびR4は同一または異なる-SO3H基であり、n1、n2、n3およびn4は0~1で1≦n1+n2+n3+n4≦2を満たす正数で示される金属フタロシアニン誘導体であっても同様の効果を有しており、好ましい。前記金属フタロシアニン誘導体とは、上記構造を有する金属フタロシアニン化合物またはその塩をいう。金属フタロシアニン化合物の塩としては、例えば無機塩基との塩、有機塩基との塩等が挙げられる。無機塩基との塩の好適な例としては、例えばナトリウム塩、カリウム塩などのアルカリ金属塩;カルシウム塩、マグネシウム塩などのアルカリ土類金属塩;ならびに銅(II)塩、アンモニウム塩などが挙げられる。有機塩基との塩の好適な例としては、例えばトリメチルアミン、トリエチルアミン、ピリジン、ピコリン、エタノールアミン、ジエタノールアミン、トリエタノールアミン、ジシクロヘキシルアミン等との塩が挙げられる。
或いは抗ウイルス繊維Pは、前記I式におけるR1、R2、R3およびR4がすべてHである金属フタロシアニン、すなわち金属フタロシアニン環の周辺に官能基がない構造のものを、繊維に坦持させたものでもよい。
前記他の抗ウイルス繊維Pとして、担体用繊維に前記金属フタロシアニンの誘導体を担持させる方法としては、担体用繊維を金属フタロシアニン誘導体溶液へ浸漬させる方法、あるいは直接染色、イオン染色(コットンやレーヨンなどの繊維にカチオン基を結合させ、そのカチオン基と染料の持つカルボキシル基やスルホン基のアニオン基をイオン的に結合させて行う染色法)などの染色法、バインダー成分を含む金属フタロシアニン誘導体溶液を繊維または繊維構造物へ印刷、噴霧またはコーターを用いて塗布する方法が挙げられる。
上記他の抗ウイルス繊維Pを併用する場合、本発明の抗ウイルス繊維構造物は、予め本発明の抗ウイルス繊維と他の抗ウイルス繊維Pを混合して用いるか、本発明の抗ウイルス繊維と担体用繊維を混合した後、フタロシアニン誘導体溶液に接触させて他の抗ウイルス繊維Pを得るか、上記方法に加えて本発明の抗ウイルス繊維に金属イオン溶液に接触させて本発明の抗ウイルス繊維に金属イオンを担持させるか、あるいは、それぞれの担体用繊維を用意し、マレイン酸成分を含む高分子とフタロシアニン誘導体を付与するか、などの方法により得ることができる。
本発明の抗ウイルス繊維構造物として、サーマルボンド不織布の一例を示す。本発明の抗ウイルス繊維と、熱接着性繊維と、必要に応じて他の抗ウイルス繊維、他の繊維を混合して繊維ウェブを形成し、熱接着性繊維が熱接着する温度で熱処理されて、サーマルボンド不織布を得ることができる。熱接着性繊維としては、例えば、ポリエチレンテレフタレート、ポリブチレンテレフタレート、ポリトリメチレンテレフタレート、ポリ乳酸等のポリエステル、ナイロン6,ナイロン66等のポリアミド、ポリプロピレン、ポリエチレン、ポリブテン等のポリオレフィン、などのポリマーまたは共重合ポリマーが少なくとも一部が繊維表面に露出した単一成分繊維または複合繊維を用いることができる。
抗ウイルス繊維構造物として、ケミカルボンド不織布の一例を示す。まず、本発明の抗ウイルス繊維と、必要に応じて他の抗ウイルス繊維、他の繊維を混合して繊維ウェブを形成する。必要に応じて、繊維ウェブを不織布(例えば、ニードルパンチ不織布)に成形した後、バインダーを浸漬、噴霧(例えば、スプレーボンド)、コーティング(例えば、フォームボンド)等により付着させ、乾燥及び/またはキュアリングして、ケミカルボンド不織布を得ることができる。バインダーとしては、アクリルバインダー、ウレタンバインダーなどを用いることができる。バインダーの付着量は、不織布の形態を維持することができ、抗ウイルス効果を阻害しない範囲であれば、特に限定されない。例えば、不織布質量に対して、固形分で5~50質量%であることが好ましい。
抗ウイルス繊維構造物として、水流交絡不織布の一例を示す。まず、本発明の抗ウイルス繊維と、必要に応じて他の抗ウイルス繊維、他の繊維を混合して繊維ウェブを形成する。この繊維ウェブには、必要に応じて他のシートを積層することができる。他のシートとしては、例えば、スパンボンド不織布、メルトブローン不織布、一方向延伸配列繊維不織布、経緯直交積層繊維不織布、湿式抄紙、ネット、フィルム、織編物などが挙げられる。特に、スパンボンド不織布、一方向延伸配列繊維不織布、および経緯直交積層繊維不織布は、積層した後の不織布強力を大きくすることができるので、補強層として好ましく用いられる。繊維ウェブまたは積層シートには、例えば、孔径0.05mm以上0.5mm以下のオリフィスが、0.5mm以上1.5mm以下の間隔で設けられたノズルから、水圧1MPa以上10MPa以下の水流を、繊維ウェブの表裏面側からそれぞれ1~4回ずつ噴射して繊維同士を交絡させて得ることができる。
本発明の抗ウイルス繊維構造物において、防水性が必要な場合は、抗ウイルス繊維構造物の表面に防水性のフィルムを積層したり、押出ラミネート機等を用いて樹脂をラミネートして、防水性を有する抗ウイルス繊維構造物を得ることができる。また、透湿防水性が必要な場合は、メルトブローン不織布などの極細繊維不織布を積層したり、透湿性を有する樹脂をラミネートして、透湿防水性を有する抗ウイルス繊維構造物を得ることができる。
このような防水性や透湿防水性を有する抗ウイルス繊維構造物は、例えば、病院用ベッドシーツ、病院用カーテン、手術用シーツ、実験シートなどの医療用シートに用いることができる。
上記サーマルボンド不織布、ケミカルボンド不織布、及び水流交絡不織布は、例えば、エアフィルターに用いることができる。エアフィルターに用いる場合、中粗塵用フィルターであれば、構成する繊維の繊度は、2~50dtexであることが好ましい。目付は10~150g/m2であることが好ましい。このようにして得られたエアフィルターは、エアコン、空気清浄機、掃除機などの家電用フィルターとして用いることができる。例えば空気清浄機用フィルターであれば、ケミカルボンド不織布等の支持体と、抗ウイルス繊維構造物と、エレクトレット不織布やHEPA、ULPA等の高精度フィルター層の積層構造を有し、プリーツ(ひだ折り)加工されたシートが用いられる。
本発明の抗ウイルス繊維構造物は、衛生マスク、サージカルマスク、防塵マスク(例えば、N95対応マスク(Particulate Respirator Type N95)、呼吸用保護具)等のマスクに用いることもできる。マスクに用いることができる抗ウイルス繊維構造物としては、前記サーマルボンド不織布や水流交絡不織布が挙げられる。マスクに用いることができる抗ウイルス繊維の繊度は、1~10dtexであることが好ましい。より好ましくは、2~8dtexである。目付は30~60g/m2であることが好ましい。マスクの構成としては、例えば、外側から口側にかけて、補強不織布(例えば、スパンボンド不織布、サーマルボンド不織布)/本発明の抗ウイルス不織布/極細繊維不織布(例えば、メルトブローン不織布)/補強または柔軟不織布(例えば、スパンボンド不織布、サーマルボンド不織布)の積層構造にすると、抗ウイルス性能を効果的に発揮することができる。
本発明の抗ウイルス繊維構造物の別の一例として、抗ウイルス繊維を5mm以下に切断した短繊維、または粉砕した微細繊維(以下、総称して繊維パウダーともいう)を他の繊維表面に担持させた不織布が挙げられる。このように繊維パウダーにした抗ウイルス繊維は、バインダーにより他の繊維表面に担持することができる。バインダーにより抗ウイルス繊維パウダーを担持する方法としては、例えば、抗ウイルス繊維パウダーと、バインダー(例えば、アクリルバインダー、ウレタンバインダーなど)を所定量添加してバインダー溶液を調製し、繊維基布に対してバインダー溶液を浸漬、噴霧(例えば、スプレーボンド)、コーティング(例えば、ナイフコーター、グラビアコーター)等により付着させ、乾燥及び/またはキュアリングして、抗ウイルス繊維パウダー担持不織布を得ることができる。また、別の方法としては、抗ウイルス繊維パウダーの水分散液を調整し、熱接着性繊維または湿熱接着性繊維を含む繊維構造物に水分散液を浸漬、噴霧、コーティング等により抗ウイルス繊維パウダーを付着させた後、熱処理して熱接着性繊維または湿熱接着性繊維によりパウダーを接着させて、抗ウイルス繊維パウダー担持不織布を得ることもできる。
前記繊維基布としては、例えば、サーマルボンド不織布、スパンボンド不織布、水流交絡不織布等の不織布、織編物などを用いることができる。
前記抗ウイルス繊維パウダー担持不織布は、例えば、防護衣に用いることができる。不織布を所定の形状に裁断し、不織布端部同士を重ねてヒートシール、超音波シール、高周波シールをするか、縫製するか、などの方法で作製することができる。
本発明の抗ウイルス繊維構造物を織編物である場合、具体的な一例を示す。まず、抗ウイルス物質としてマレイン酸成分を含む高分子を紡糸または担持した抗ウイルス繊維とした後、所定の抗ウイルス繊維を含有する糸を製織する。得られた織編物を、ジッカー染色機、高圧液流染色機、パドル染色機等の染色機を用い、繊維100質量部に対して0.05~5質量部、すなわち0.05~5%owf(on weight fiber)の金属イオン化合物を含む溶液(例えば、硫酸銅水溶液)に織編物を浸漬し、水洗処理、乾燥し、必要に応じてアクリル樹脂やウレタン樹脂等をディッピングして風合い加工等を行い、マレイン酸成分に銅、銀、亜鉛等の金属のイオンを担持させた抗ウイルス織編物を得ることができる。
このようにして得られる抗ウイルス織編物は、例えば、衣類、布団、カーテン、カーペット、マット、シーツ、タオル、防護衣類、防護ネット、廃鶏袋、鶏舎用品、医療用シート材などに用いることができる。
以下、本発明の実施例を詳細に説明するが、本発明の範囲はこれらの実施例に限定されるものではない。
--抗ウイルス繊維の作製--
(実施例1)
酢酸ビニル-無水マレイン酸共重合体水溶性塩を、セルロースのビスコース溶液(セルロース濃度9%)に前記共重合体固形分がセルロース固形分100部に対して20部となるよう添加し、溶解した。各々の混合溶液を硫酸130g/l、硫酸亜鉛10g/l、硫酸ナトリウム250g/lの強酸性浴中に白金ノズルから押出して紡糸した。常法により脱硫、精練漂白することにより、酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料を得た。繊度は3.3dtex、繊維長は51mmであった。
(実施例1)
酢酸ビニル-無水マレイン酸共重合体水溶性塩を、セルロースのビスコース溶液(セルロース濃度9%)に前記共重合体固形分がセルロース固形分100部に対して20部となるよう添加し、溶解した。各々の混合溶液を硫酸130g/l、硫酸亜鉛10g/l、硫酸ナトリウム250g/lの強酸性浴中に白金ノズルから押出して紡糸した。常法により脱硫、精練漂白することにより、酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料を得た。繊度は3.3dtex、繊維長は51mmであった。
(実施例2)
得られた実施例1の繊維を4%硫酸銅水溶液に浸漬して10分間放置したのち、蒸留水で洗浄し、70℃で3時間乾燥し、抗ウイルス繊維の試料を得た。この抗ウイルス繊維の銅担持量は1質量%であった。
得られた実施例1の繊維を4%硫酸銅水溶液に浸漬して10分間放置したのち、蒸留水で洗浄し、70℃で3時間乾燥し、抗ウイルス繊維の試料を得た。この抗ウイルス繊維の銅担持量は1質量%であった。
(鳥インフルエンザウイルスに対する抗ウイルス繊維の性能評価)
被検ウイルスは、国立大学法人鳥取大学鳥インフルエンザ研究センターに保管されている鳥インフルエンザウイルスA/whistling swan/Shimane/499/83 (H5N3)株を使用した。この鳥インフルエンザウイルス株は、鳥インフルエンザウイルスA/コハクチョウ/島根/499/83(H5N3)とも称される(以下、H5N3株という)。
被検ウイルスは、国立大学法人鳥取大学鳥インフルエンザ研究センターに保管されている鳥インフルエンザウイルスA/whistling swan/Shimane/499/83 (H5N3)株を使用した。この鳥インフルエンザウイルス株は、鳥インフルエンザウイルスA/コハクチョウ/島根/499/83(H5N3)とも称される(以下、H5N3株という)。
この他、被検ウイルスとして、鳥インフルエンザウイルスA/Turkey/Wisconsin/1/66 (H9N2) 株(以下、H9N2株という)、ブタインフルエンザウイルスA/Swine/Iowa/15/30 (H1N1) 株(以下、H1N1株という)を使用した。
上記各実施例で試作した抗ウイルス繊維を約1.5cm長さに切り揃え、ポリエチレン袋に0.2gを入れ、被検ウイルスを燐酸緩衝生理食塩水(Phosphate Buffered Saline:PBS)で100倍に希釈したウイルス液Aを各0.6mlずつポリエチレン袋に分注し、抗ウイルス繊維にウイルス液を染み込ませた。4℃で反応時間10分間(あるいは1分間)静置した。そのウイルス液を採取しPBSでさらに10倍段階希釈し、10日齢発育鶏卵(SPF)に0.2mlずつ漿尿膜腔内に接種した。2日間培養後、尿膜腔液Bを回収し、鶏赤血球凝集反応によりウイルス増殖の有無を判定した。ウイルス力価はReed & Muench (1938)の方法によって算出した。
比較例として、未加工のレーヨン繊維を用いた。
各試作抗ウイルス繊維のウイルス力価を表1に示してある。
表1から、実施例1、2の抗ウイルス繊維を使用した尿膜腔液Bは、ウイルス液Aよりもウイルス力価が大幅に減少しており、ウイルス減少率が99%以上であった。これは、実施例1、2の抗ウイルス繊維に鳥インフルエンザウイルスに対する抗ウイルス効果があることを示している。特に、実施例2の銅イオンを担持した酢酸ビニル-マレイン酸共重合高分子を含有するレーヨン繊維であったため、総てのウイルス株についてウイルス減少率が99.999%以上の抗ウイルス性を示した。一方、同一条件で抗ウイルス繊維を使用しない比較例の尿膜腔液Bは、ウイルス液Aよりもウイルス力価が減少していたが十分なものではなかった。
また、実施例2の抗ウイルス繊維を100質量%混合し、パラレルカード機を用いて繊維ウェブとし、水流交絡処理して、目付40g/m2の抗ウイルス不織布を作製した。
得られた抗ウイルス不織布を、ポリプロピレンスパンボンド不織布の上に載置し、さらにポリプロピレンメルトブローン不織布とポリプロピレンスパンボンド不織布を重ね合わせて、縦15cm、横15cmに切断し、3段にプリーツ折りして、横方向の端の中央部に耳掛け紐を設け、シート端の四辺をヒートシール加工し、抗ウイルスマスクを作製した。
得られた抗ウイルスマスクを7日間着用した後、前記抗ウイルス不織布を取り出し、ウイルス力価を測定したところ、尿膜腔液B(<101.5(EID50/0.2ml))は、ウイルス液A(106.5(EID50/0.2ml))よりもウイルス力価が大幅に減少し、99.999%のウイルス減少率であった。長時間の使用にも耐え得ることが確認できた。
(実施例3)
実施例1と同様の方法で紡糸して得られた繊度1.7dtex、繊維長38mmの酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料と、芯成分がポリプロピレン、鞘成分が高密度ポリエチレンからなる繊度2.2dtex、繊維長51mmの鞘芯型複合繊維(ダイワボウポリテック(株)製、NBF(H))を用いた。本発明の試料が60質量%と鞘芯型複合繊維が40質量%となるように混合し、パラレルカード機を用いて開繊してカードウェブを作製した。目付は、40g/m2とした。
実施例1と同様の方法で紡糸して得られた繊度1.7dtex、繊維長38mmの酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料と、芯成分がポリプロピレン、鞘成分が高密度ポリエチレンからなる繊度2.2dtex、繊維長51mmの鞘芯型複合繊維(ダイワボウポリテック(株)製、NBF(H))を用いた。本発明の試料が60質量%と鞘芯型複合繊維が40質量%となるように混合し、パラレルカード機を用いて開繊してカードウェブを作製した。目付は、40g/m2とした。
得られたカードウェブは、孔径0.08mmのオリフィスが0.6mm間隔で設けられたノズルを用いて、ウェブの表面に、水圧4MPaの柱状水流を2回噴射し、同様にその反対の表面に、水圧4MPaの柱状水流を2回噴射して繊維を交絡された。その後、ボックス型真空吸引装置にて、脱水後、ドラム型乾燥機(設定温度140℃)にて鞘芯型複合繊維の鞘成分で融着し、乾燥させて、水流交絡により一体化された水流交絡不織布を得た。
得られた積層不織布は、25℃、0.1%の硫酸銅水溶液に浸漬され、ニップロールで絞られた後、水洗槽で十分に水洗されて、80℃で乾燥して、抗ウイルス不織布の試料を得た。この抗ウイルス不織布の銅担持量は1質量%であった。
(実施例4)
下記の第1~第3繊維層から成る積層不織布を作製した。第1繊維層と第3繊維層は、実施例1と同様の方法で紡糸して得られた繊度1.7dtex、繊維長38mmの酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料と、芯成分がポリプロピレン、鞘成分が高密度ポリエチレンからなる繊度2.2dtex、繊維長51mmの鞘芯型複合繊維(ダイワボウポリテック(株)製、NBF(H))を用いた。本発明の試料が60質量%と鞘芯型複合繊維が40質量%となるように混合し、パラレルカード機を用いて開繊してカードウェブを作製した。目付は、各層とも20g/m2とした。
下記の第1~第3繊維層から成る積層不織布を作製した。第1繊維層と第3繊維層は、実施例1と同様の方法で紡糸して得られた繊度1.7dtex、繊維長38mmの酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料と、芯成分がポリプロピレン、鞘成分が高密度ポリエチレンからなる繊度2.2dtex、繊維長51mmの鞘芯型複合繊維(ダイワボウポリテック(株)製、NBF(H))を用いた。本発明の試料が60質量%と鞘芯型複合繊維が40質量%となるように混合し、パラレルカード機を用いて開繊してカードウェブを作製した。目付は、各層とも20g/m2とした。
第2繊維層として、ポリエステル繊維からなる、目付が5g/m2の1方向延伸配列不織布(商品名ミライフT05、新日石プラスト(株)製)を用意した。
第1繊維層と第3繊維層の間に第2繊維層が位置するように、3つの繊維層を積層して積層ウェブを作製した。次いで、孔径0.08mmのオリフィスが0.6mm間隔で設けられたノズルを用いて、ウェブの第1繊維層側の表面に、水圧4MPaの柱状水流を2回噴射し、同様に第3繊維層側の表面に、水圧4MPaの柱状水流を2回噴射することに、繊維を交絡させた。その後、ボックス型真空吸引装置にて、脱水後、ドラム型乾燥機(設定温度140℃)にて鞘芯型複合繊維の鞘成分で融着し、乾燥させて、水流交絡により一体化された積層不織布を得た。
得られた積層不織布は、25℃、0.1%の硫酸銅水溶液に浸漬され、ニップロールで絞られた後、水洗槽で十分に水洗されて、80℃で乾燥して、抗ウイルス不織布の試料を得た。この抗ウイルス不織布の銅担持量は0.7質量%であった。
実施例3~4の試料における鳥インフルエンザウイルスのウイルス力価を表2に示す。なお、測定試料は、不織布を約1.5cmの長さ四方にカットした試験片を使用した。
表2から、実施例3~4の試料を使用した尿膜腔液Bは、ウイルス液Aよりもウイルス力価が大幅に減少しており、ウイルス減少率が99%以上であった。これは、実施例3~4の抗ウイルス繊維および抗ウイルス不織布に鳥インフルエンザウイルスに対する抗ウイルス効果があることを示している。
(ヒトインフルエンザウイルスに対する抗ウイルス繊維の性能評価)
被検ウイルスは、ヒトインフルエンザウイルスA/Aichi/2/68 (H3N2)株(以下、H3N2株という)を使用した。不織布の場合、約1.5cm長さ四方にカットした試験片を0.2g取り出すか、繊維の場合、約1.5cmの長さに切り揃えて0.2gの綿を用意し、それぞれをポリエチレン袋に入れ、被検ウイルスを燐酸緩衝生理食塩水(Phosphate Buffered Saline:PBS)で100倍に希釈したウイルス液Aを各0.6mlずつポリエチレン袋に分注し、抗ウイルス繊維にウイルス液を染み込ませた。4℃で反応時間10分間(あるいは1分間)静置した。そのウイルス液を採取しPBSでさらに10倍段階希釈し、10日齢発育鶏卵(SPF)に0.2mlずつ漿尿膜腔内に接種した。2日間培養後、尿膜腔液Bを回収し、鶏赤血球凝集反応によりウイルス増殖の有無を判定した。ウイルス力価はReed & Muench (1938)の方法によって算出した。
被検ウイルスは、ヒトインフルエンザウイルスA/Aichi/2/68 (H3N2)株(以下、H3N2株という)を使用した。不織布の場合、約1.5cm長さ四方にカットした試験片を0.2g取り出すか、繊維の場合、約1.5cmの長さに切り揃えて0.2gの綿を用意し、それぞれをポリエチレン袋に入れ、被検ウイルスを燐酸緩衝生理食塩水(Phosphate Buffered Saline:PBS)で100倍に希釈したウイルス液Aを各0.6mlずつポリエチレン袋に分注し、抗ウイルス繊維にウイルス液を染み込ませた。4℃で反応時間10分間(あるいは1分間)静置した。そのウイルス液を採取しPBSでさらに10倍段階希釈し、10日齢発育鶏卵(SPF)に0.2mlずつ漿尿膜腔内に接種した。2日間培養後、尿膜腔液Bを回収し、鶏赤血球凝集反応によりウイルス増殖の有無を判定した。ウイルス力価はReed & Muench (1938)の方法によって算出した。
実施例2~4の試料におけるヒトインフルエンザウイルスのウイルス力価を表3に示す。
表3から、実施例2~4の試料を使用した尿膜腔液Bは、ウイルス液Aよりもウイルス力価が大幅に減少しており、ウイルス減少率が99%以上であった。これは、実施例2~4の抗ウイルス繊維および抗ウイルス不織布にヒトインフルエンザウイルスに対する抗ウイルス効果があることを示している。
実施例4の積層不織布は、実施例3の不織布に比べ、後加工性が良好であった。
(ノロウイルスに対する抗ウイルス不織布の性能評価)
被検ウイルスとしてノロウイルスの代替ウイルスであるFeline calicivirus F-9 ATCC VR-782(以下、ネコカリシウイルスという)を使用し、以下の方法で抗ウイルス性能を評価した。
1.試験方法
(1)使用細胞
CRFK細胞(大日本製薬(株))
(2)使用培地
i細胞増殖培地
イーグルMEM培地「ニッスイ」i(日水製薬(株))に牛胎仔血清を10%加えたものを使用した。
ii細胞維持培地
イーグルMEM培地「ニッスイ」iに牛胎仔血清を2%加えたものを使用した。
(3)ウイルス浮遊液の調製
i細胞の培養
細胞増殖培地を用い、使用細胞を組織培養用フラスコ内に単層培養した。
iiウイルスの接種
単層培養後にフラスコ内から細胞増殖培地を除き、被験ウイルスを接種した。次に、細胞維持培地を加えて37℃±1℃の炭酸ガスインキュベーター(CO2濃度5%)内で1~5日間培養した。
iiiウイルス浮遊液の調製
培養後、倒立位相差顕微鏡を用いて細胞の形態を観察し、細胞に形態変化(細胞変性効果)が起こっていることを確認した。次に、培養液を遠心分離(3000r/min. 10分間)し、得られた上澄み液を精製水で10倍に希釈し、ウイルス浮遊液とした。
(4)試料の調製
約3cm×3cmの大きさに切断した実施例3の不織布を試料とした。
(5)試験操作
試料にウイルス浮遊液0.2mlを滴下し、室温で保存した。
(6)ウイルスの洗い出し
保存24時間後、試料のウイルス浮遊液を細胞維持培地2mlで洗い出した。
(7)ウイルス感染価の測定
細胞増殖培地を用い、使用細胞を組織培養用マイクロプレート(96穴)内で単層培養した後、細胞増殖培地を除き細胞維持培地を0.1mlずつ加えた。次に、試料洗い出し液及びその希釈液0.1mlを4穴ずつに接種し、37℃±1℃の炭酸ガスインキュベーター(CO2濃度5%)内で4~7日間培養した。培養後、倒立位相差顕微鏡を用いて細胞の形態変化(細胞変性効果)の有無を観察し、Reed-Muench法により50%組織培養感染量(TCID50)を算出して洗い出し液1ml当たりのウイルス感染価に換算した。
その結果、試料(実施例3の不織布)に接種した24時間後の後Log TCID50/mlは<2.5(検出せず)であるのに対し、対照[標準布(綿)]における接種直後のLog
TCID50/mlは7.0、接種した24時間後のLog TCID50/mlは6.0であった。
この結果から、実施例3の抗ウイルス不織布は、ウイルス感染価が大幅に減少しており、ノロウイルスに対する抗ウイルス効果があることを示している。
(ノロウイルスに対する抗ウイルス不織布の性能評価)
被検ウイルスとしてノロウイルスの代替ウイルスであるFeline calicivirus F-9 ATCC VR-782(以下、ネコカリシウイルスという)を使用し、以下の方法で抗ウイルス性能を評価した。
1.試験方法
(1)使用細胞
CRFK細胞(大日本製薬(株))
(2)使用培地
i細胞増殖培地
イーグルMEM培地「ニッスイ」i(日水製薬(株))に牛胎仔血清を10%加えたものを使用した。
ii細胞維持培地
イーグルMEM培地「ニッスイ」iに牛胎仔血清を2%加えたものを使用した。
(3)ウイルス浮遊液の調製
i細胞の培養
細胞増殖培地を用い、使用細胞を組織培養用フラスコ内に単層培養した。
iiウイルスの接種
単層培養後にフラスコ内から細胞増殖培地を除き、被験ウイルスを接種した。次に、細胞維持培地を加えて37℃±1℃の炭酸ガスインキュベーター(CO2濃度5%)内で1~5日間培養した。
iiiウイルス浮遊液の調製
培養後、倒立位相差顕微鏡を用いて細胞の形態を観察し、細胞に形態変化(細胞変性効果)が起こっていることを確認した。次に、培養液を遠心分離(3000r/min. 10分間)し、得られた上澄み液を精製水で10倍に希釈し、ウイルス浮遊液とした。
(4)試料の調製
約3cm×3cmの大きさに切断した実施例3の不織布を試料とした。
(5)試験操作
試料にウイルス浮遊液0.2mlを滴下し、室温で保存した。
(6)ウイルスの洗い出し
保存24時間後、試料のウイルス浮遊液を細胞維持培地2mlで洗い出した。
(7)ウイルス感染価の測定
細胞増殖培地を用い、使用細胞を組織培養用マイクロプレート(96穴)内で単層培養した後、細胞増殖培地を除き細胞維持培地を0.1mlずつ加えた。次に、試料洗い出し液及びその希釈液0.1mlを4穴ずつに接種し、37℃±1℃の炭酸ガスインキュベーター(CO2濃度5%)内で4~7日間培養した。培養後、倒立位相差顕微鏡を用いて細胞の形態変化(細胞変性効果)の有無を観察し、Reed-Muench法により50%組織培養感染量(TCID50)を算出して洗い出し液1ml当たりのウイルス感染価に換算した。
その結果、試料(実施例3の不織布)に接種した24時間後の後Log TCID50/mlは<2.5(検出せず)であるのに対し、対照[標準布(綿)]における接種直後のLog
TCID50/mlは7.0、接種した24時間後のLog TCID50/mlは6.0であった。
この結果から、実施例3の抗ウイルス不織布は、ウイルス感染価が大幅に減少しており、ノロウイルスに対する抗ウイルス効果があることを示している。
--抗ウイルスマスクの作製--
実施例3,4の不織布を、ポリプロピレンスパンボンド不織布の上に載置し、さらにポリプロピレンメルトブローン不織布とポリプロピレンスパンボンド不織布を重ね合わせて、縦15cm、横15cmに切断し、3段にプリーツ折りして、横方向の端の中央部に耳掛け紐を設け、シート端の四辺をヒートシール加工し、抗ウイルスマスクを作製した。このマスクを装着したところ、息苦しさもなく、装着性も良好であった。
実施例3,4の不織布を、ポリプロピレンスパンボンド不織布の上に載置し、さらにポリプロピレンメルトブローン不織布とポリプロピレンスパンボンド不織布を重ね合わせて、縦15cm、横15cmに切断し、3段にプリーツ折りして、横方向の端の中央部に耳掛け紐を設け、シート端の四辺をヒートシール加工し、抗ウイルスマスクを作製した。このマスクを装着したところ、息苦しさもなく、装着性も良好であった。
(実施例5)
(1)防水性抗ウイルス不織布の作製
実施例4の抗ウイルス不織布の表面に、押出ラミネート機を用いて、融点が103℃の低密度ポリエチレンを厚み30μmとなるようにラミネートして、防水性の抗ウイルス不織布を作製した。
(1)防水性抗ウイルス不織布の作製
実施例4の抗ウイルス不織布の表面に、押出ラミネート機を用いて、融点が103℃の低密度ポリエチレンを厚み30μmとなるようにラミネートして、防水性の抗ウイルス不織布を作製した。
(2)医療用シート、実験シートの作製
この防水性不織布を医療用ベッドシーツや実験シートに用いたところ、防水性と抗ウイルス効果があることを確認できた。
この防水性不織布を医療用ベッドシーツや実験シートに用いたところ、防水性と抗ウイルス効果があることを確認できた。
(実施例6)
(1)抗ウイルス繊維パウダーの作製
まず、実施例1と同様の方法で、繊度が3.3dtexの酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料を得た後、繊維長が0.1mmとなるようにカッターで切断し、抗ウイルス繊維パウダーを作製した。
(1)抗ウイルス繊維パウダーの作製
まず、実施例1と同様の方法で、繊度が3.3dtexの酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料を得た後、繊維長が0.1mmとなるようにカッターで切断し、抗ウイルス繊維パウダーを作製した。
得られたパウダーは、4%硫酸銅水溶液に浸漬されて10分間放置したのち、蒸留水で洗浄し、70℃で3時間乾燥し、銅イオンが担持された抗ウイルス繊維パウダーの試料を得た。この抗ウイルス繊維パウダーの銅担持量は1質量%であった。
次に、イオン染色法により別の抗ウイルスレーヨン繊維を作製した。カチオン化剤として、50g/LのカチオノンUK(一方社製の商品名)と、15g/Lの水酸化ナトリウム水溶液との混合液10Lに、レーヨン繊維(繊度2.2dtex、繊維長0.1mm)1kgを浴比1:10の条件で入れ、85℃で45分間反応させた。得られたカチオン化レーヨン繊維を十分に水にて洗浄した後、濃度1%owfのコバルト(II)フタロシアニンモノスルホン酸及びコバルト(II)フタロシアニンジスルホン酸が混合した水酸化ナトリウム溶液(pH=12)10L中に浸し、80℃で30分間撹拌し、レーヨン繊維を染色した。得られた染色レーヨン繊維を十分に水にて洗浄して乾燥し、コバルト(II)フタロシアニンモノスルホン酸ナトリウム及びコバルト(II)フタロシアニンジスルホン酸ナトリウムが担持された抗ウイルスレーヨン繊維Pパウダーを得た。
得られた抗ウイルス繊維Pについて、鳥インフルエンザウイルス(H5N3株)のウイルス力価(試料量0.2g、反応時間10分)を測定したところ、尿膜腔液B(102.75(EID50/0.2ml))は、ウイルス液A(107.25(EID50/0.2ml))よりもウイルス力価が大幅に減少し、99.99%のウイルス減少率であった。
得られた抗ウイルス繊維Pについて、鳥インフルエンザウイルス(H5N3株)のウイルス力価(試料量0.2g、反応時間10分)を測定したところ、尿膜腔液B(102.75(EID50/0.2ml))は、ウイルス液A(107.25(EID50/0.2ml))よりもウイルス力価が大幅に減少し、99.99%のウイルス減少率であった。
(2)抗ウイルス繊維パウダー担持不織布の作製
基布として、目付が40g/m2のポリプロピレン製スパンボンド不織布を用意した。次に、抗ウイルス繊維パウダーを基布に接着させるアクリルエマルジョンバインダーを用意し、アクリルエマルジョンバインダーと、本発明の抗ウイルス繊維パウダー50質量%と、抗ウイルスレーヨン繊維Pパウダー50質量%を添加したバインダー溶液を調製した。前記基布の表面に、ナイフコーターを用いて、3g/m2の繊維パウダーを塗布した。バインダーは、固形分で6g/m2塗布されていた。次いで、150℃、3分間のキュアリングを施して、抗ウイルス繊維パウダー担持不織布を得た。
実施例6の試料における鳥インフルエンザウイルスのウイルス力価を表4に示す。
基布として、目付が40g/m2のポリプロピレン製スパンボンド不織布を用意した。次に、抗ウイルス繊維パウダーを基布に接着させるアクリルエマルジョンバインダーを用意し、アクリルエマルジョンバインダーと、本発明の抗ウイルス繊維パウダー50質量%と、抗ウイルスレーヨン繊維Pパウダー50質量%を添加したバインダー溶液を調製した。前記基布の表面に、ナイフコーターを用いて、3g/m2の繊維パウダーを塗布した。バインダーは、固形分で6g/m2塗布されていた。次いで、150℃、3分間のキュアリングを施して、抗ウイルス繊維パウダー担持不織布を得た。
実施例6の試料における鳥インフルエンザウイルスのウイルス力価を表4に示す。
表4から、実施例6の試料を使用した尿膜腔液Bは、ウイルス液Aよりもウイルス力価が大幅に減少しており、ウイルス減少率が99%以上であった。これは、実施例6の抗ウイルス繊維パウダー担持不織布に鳥インフルエンザウイルスに対する抗ウイルス効果があることを示している。
(3)防護衣の作製
実施例6の不織布を所定の形状に裁断し、不織布端部同士を重ねて熱融着させて、防護衣を作製した。不織布自体が柔軟であり、繊維パウダーの脱落もないため、防護衣として使用できることを確認できた。
実施例6の不織布を所定の形状に裁断し、不織布端部同士を重ねて熱融着させて、防護衣を作製した。不織布自体が柔軟であり、繊維パウダーの脱落もないため、防護衣として使用できることを確認できた。
(実施例7)
(1)抗ウイルス不織布の作製
実施例1と同様の方法で紡糸して得られた繊度7.8dtex、繊維長51mmの酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料と、実施例6と同様の方法で加工して得られた繊度15dtex、繊維長64mmのコバルト(II)フタロシアニンモノスルホン酸ナトリウム及びコバルト(II)フタロシアニンジスルホン酸ナトリウムが担持された抗ウイルスレーヨン繊維Pと、繊度30dtex、繊維長64mmのポリエステル繊維を用意した。本発明の試料20質量%と、抗ウイルスレーヨン繊維P40質量%と、ポリエステル繊維40質量%を混合し、カード機を用いて開繊したカードウェブをクロスレイヤーで積層ウェブを作製した。次いで、アクリルバインダーを積層ウェブの両面にスプレーして、120℃、1分間乾燥し、150℃、3分間キュアリングして、ケミカルボンド不織布を作製した。アクリルバインダーは固形分で15質量%付着していた。目付は、60g/m2とした。
(1)抗ウイルス不織布の作製
実施例1と同様の方法で紡糸して得られた繊度7.8dtex、繊維長51mmの酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料と、実施例6と同様の方法で加工して得られた繊度15dtex、繊維長64mmのコバルト(II)フタロシアニンモノスルホン酸ナトリウム及びコバルト(II)フタロシアニンジスルホン酸ナトリウムが担持された抗ウイルスレーヨン繊維Pと、繊度30dtex、繊維長64mmのポリエステル繊維を用意した。本発明の試料20質量%と、抗ウイルスレーヨン繊維P40質量%と、ポリエステル繊維40質量%を混合し、カード機を用いて開繊したカードウェブをクロスレイヤーで積層ウェブを作製した。次いで、アクリルバインダーを積層ウェブの両面にスプレーして、120℃、1分間乾燥し、150℃、3分間キュアリングして、ケミカルボンド不織布を作製した。アクリルバインダーは固形分で15質量%付着していた。目付は、60g/m2とした。
(2)エアフィルターの作製
得られたケミカルボンド不織布を所定の大きさに裁断して、プラスチック製ユニットにはめ込んで、空気清浄機用プレフィルターを作製した。
得られたケミカルボンド不織布を所定の大きさに裁断して、プラスチック製ユニットにはめ込んで、空気清浄機用プレフィルターを作製した。
(実施例8)
(1)抗ウイルス不織布の作製
実施例1と同様の方法で紡糸して得られた繊度7.8dtex、繊維長51mmの酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料を用意した。
(1)抗ウイルス不織布の作製
実施例1と同様の方法で紡糸して得られた繊度7.8dtex、繊維長51mmの酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料を用意した。
実施例6のカチオン化レーヨン繊維を十分に水にて洗浄した後、濃度1%owfの鉄(III)フタロシアニンモノスルホン酸及び鉄(III)フタロシアニンジスルホン酸が混合した水酸化ナトリウム溶液(pH=12)10L中に浸し、80℃で30分間撹拌し、レーヨン繊維を染色した。得られた染色レーヨン繊維を十分に水にて洗浄して乾燥し、鉄(III)フタロシアニンモノスルホン酸ナトリウム及び鉄(III)フタロシアニンジスルホン酸ナトリウムが担持された、繊度5.5dtex、繊維長51mmの抗ウイルスレーヨン繊維Pを用意した。
得られた抗ウイルス繊維Pについて、鳥インフルエンザウイルス(H5N3株)のウイルス力価(試料量0.2g、反応時間10分)を測定したところ、尿膜腔液B(104.75(EID50/0.2ml))は、ウイルス液A(106.75(EID50/0.2ml))よりもウイルス力価が大幅に減少し、99%のウイルス減少率であった。
得られた抗ウイルス繊維Pについて、鳥インフルエンザウイルス(H5N3株)のウイルス力価(試料量0.2g、反応時間10分)を測定したところ、尿膜腔液B(104.75(EID50/0.2ml))は、ウイルス液A(106.75(EID50/0.2ml))よりもウイルス力価が大幅に減少し、99%のウイルス減少率であった。
さらに実施例3で用いた鞘芯型複合繊維を用意した。酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料30質量%と、抗ウイルスレーヨン繊維P40質量%と、鞘芯型複合繊維30質量%を混合し、カード機を用いて開繊したカードウェブをクロスレイヤーで積層ウェブを作製した。次いで、140℃の熱風加工機で熱処理して、鞘芯型複合繊維の鞘成分を溶融させて、サーマルボンド不織布を作製した。目付は、60g/m2とした。
実施例8の試料における鳥インフルエンザウイルスのウイルス力価を表5に示す。
実施例8の試料における鳥インフルエンザウイルスのウイルス力価を表5に示す。
表5から、実施例8の試料を使用した尿膜腔液Bは、ウイルス液Aよりもウイルス力価が大幅に減少しており、ウイルス減少率が99%以上であった。これは、実施例8の抗ウイルス不織布に鳥インフルエンザウイルスに対する抗ウイルス効果があることを示している。
(実施例9)
(1)抗ウイルス織物の作製
実施例1と同様の方法で紡糸して得られた繊度1.4dtex、繊維長38mmの酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料と、繊度1.45dtex、繊維長35mmの再生ポリエステル繊維(帝人ファイバー(株)製、商品名エコペット)を用いた。本発明の試料50質量%と再生ポリエステル繊維50質量%が混紡された14番手の単糸(より係数4.3~4.5)を作製した。次に、エアージェット織機を用いて、経糸89本/インチ、緯糸51本/インチ、3/1綾目の織物を作製した。
(1)抗ウイルス織物の作製
実施例1と同様の方法で紡糸して得られた繊度1.4dtex、繊維長38mmの酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料と、繊度1.45dtex、繊維長35mmの再生ポリエステル繊維(帝人ファイバー(株)製、商品名エコペット)を用いた。本発明の試料50質量%と再生ポリエステル繊維50質量%が混紡された14番手の単糸(より係数4.3~4.5)を作製した。次に、エアージェット織機を用いて、経糸89本/インチ、緯糸51本/インチ、3/1綾目の織物を作製した。
次に、上記織物にジッカー染色機を用いて金属イオン加工を施した。繊維質量に対して0.5%owfの硫酸銅水溶液をジッカー染色機に添加し、織物を浸漬した。次いで、ニップロールで絞られた後、水洗槽で十分に水洗されて、120℃で乾燥して、銅イオンが担持した抗ウイルス織物の試料を得た。
(2)作業衣の作製
実施例9の織物を所定の形状に裁断し、織物端部同士を重ねて縫製して、作業衣を作製した。着用性も良好であった。
--抗ウイルス繊維の作製--
実施例9の織物を所定の形状に裁断し、織物端部同士を重ねて縫製して、作業衣を作製した。着用性も良好であった。
--抗ウイルス繊維の作製--
(実施例10)
酢酸ビニル-無水マレイン酸共重合体水溶性塩を、セルロースのビスコース溶液(セルロース濃度9%)に前記共重合体固形分がセルロース固形分100部に対して20部となるよう添加し、溶解した。各々の混合溶液を硫酸130g/l、硫酸亜鉛10g/l、硫酸ナトリウム250g/lの強酸性浴中に白金ノズルから押出して紡糸した。常法により脱硫、精練漂白することにより、酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料を得た。繊度は7.8dtex、繊維長は76mmであった。
得られたレーヨン繊維を5%硫酸亜鉛(ZnSO4・7H2O)水溶液に浸漬して60℃で20分間放置したのち、蒸留水で洗浄し、70℃で3時間乾燥し、抗ウイルス繊維の試料を得た。この抗ウイルス繊維の亜鉛担持量は1質量%であった。
酢酸ビニル-無水マレイン酸共重合体水溶性塩を、セルロースのビスコース溶液(セルロース濃度9%)に前記共重合体固形分がセルロース固形分100部に対して20部となるよう添加し、溶解した。各々の混合溶液を硫酸130g/l、硫酸亜鉛10g/l、硫酸ナトリウム250g/lの強酸性浴中に白金ノズルから押出して紡糸した。常法により脱硫、精練漂白することにより、酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料を得た。繊度は7.8dtex、繊維長は76mmであった。
得られたレーヨン繊維を5%硫酸亜鉛(ZnSO4・7H2O)水溶液に浸漬して60℃で20分間放置したのち、蒸留水で洗浄し、70℃で3時間乾燥し、抗ウイルス繊維の試料を得た。この抗ウイルス繊維の亜鉛担持量は1質量%であった。
(実施例11)
実施例10で得られたレーヨン繊維を5%塩化ニッケル(NiCl2・6H2O)水溶液に浸漬して60℃で20分間放置したのち、蒸留水で洗浄し、70℃で3時間乾燥し、抗ウイルス繊維の試料を得た。この抗ウイルス繊維のニッケル担持量は1質量%であった。
実施例10で得られたレーヨン繊維を5%塩化ニッケル(NiCl2・6H2O)水溶液に浸漬して60℃で20分間放置したのち、蒸留水で洗浄し、70℃で3時間乾燥し、抗ウイルス繊維の試料を得た。この抗ウイルス繊維のニッケル担持量は1質量%であった。
上記実施例10、11で試作した抗ウイルス繊維について、鳥インフルエンザウイルス(H5N3)に対する性能を評価した結果を表6に示す。
表6から、実施例10(亜鉛イオンを担持した酢酸ビニル-マレイン酸共重合高分子を含有するレーヨン繊維)、実施例11(ニッケルイオンを担持した酢酸ビニル-マレイン酸共重合高分子を含有するレーヨン繊維)の抗ウイルス繊維を使用した尿膜腔液Bは、ウイルス液Aよりもウイルス力価が大幅に減少しており、ウイルス減少率が99%以上であった。これは、実施例10,11の抗ウイルス繊維に鳥インフルエンザウイルスに対する抗ウイルス効果があることを示している。
(実施例12)
1.抗ウイルス不織布の作製
(1)抗ウイルス繊維の作製
実施例2と同様の方法で得られた繊度1.7dtex、繊維長38mmの抗ウイルス繊維を用意した。
(2)別の抗ウイルス繊維Pの作製
実施例8と同様の方法で得られた繊度1.7dtex、繊維長38mmの抗ウイルス繊維Pを用意した。
(3)不織布の作製
抗ウイルス繊維を30質量%と、抗ウイルス繊維Pを20質量%と、繊度2.2dtex、繊維長51mmのポリエステル系熱接着性複合繊維(ユニチカ(株)製、商品名メルティ)を50質量%用いた。これらの繊維を混合し、パラレルカード機を用いて繊維ウェブとし、水流交絡処理して、目付50g/m2の抗ウイルス不織布を作製した。
1.抗ウイルス不織布の作製
(1)抗ウイルス繊維の作製
実施例2と同様の方法で得られた繊度1.7dtex、繊維長38mmの抗ウイルス繊維を用意した。
(2)別の抗ウイルス繊維Pの作製
実施例8と同様の方法で得られた繊度1.7dtex、繊維長38mmの抗ウイルス繊維Pを用意した。
(3)不織布の作製
抗ウイルス繊維を30質量%と、抗ウイルス繊維Pを20質量%と、繊度2.2dtex、繊維長51mmのポリエステル系熱接着性複合繊維(ユニチカ(株)製、商品名メルティ)を50質量%用いた。これらの繊維を混合し、パラレルカード機を用いて繊維ウェブとし、水流交絡処理して、目付50g/m2の抗ウイルス不織布を作製した。
前記抗ウイルス不織布について、鳥インフルエンザウイルス(H5N3株)のウイルス力価を測定したところ、尿膜腔液B(<100.75(EID50/0.2ml))は、ウイルス液A(106.75(EID50/0.2ml))よりもウイルス力価が大幅に減少し、99.999%のウイルス減少率であった。
2. 抗ウイルスマスクの作製
得られた抗ウイルス不織布を、ポリプロピレンスパンボンド不織布の上に載置し、さらにポリプロピレンメルトブローン不織布とポリプロピレンスパンボンド不織布を重ね合わせて、縦15cm、横15cmに切断し、3段にプリーツ折りして、横方向の端の中央部に耳掛け紐を設け、シート端の四辺をヒートシール加工し、抗ウイルスマスクを作製した。
この抗ウイルスマスクは、外側から内側(口側)に向けて保護不織布(スパンボンド不織布)/精密濾過用不織布(メルトブローン不織布)/抗ウイルス不織布/保護不織布(スパンボンド不織布)の構成とした。このマスクを装着したところ、息苦しさもなく、装着性も良好であった。
得られた抗ウイルス不織布を、ポリプロピレンスパンボンド不織布の上に載置し、さらにポリプロピレンメルトブローン不織布とポリプロピレンスパンボンド不織布を重ね合わせて、縦15cm、横15cmに切断し、3段にプリーツ折りして、横方向の端の中央部に耳掛け紐を設け、シート端の四辺をヒートシール加工し、抗ウイルスマスクを作製した。
この抗ウイルスマスクは、外側から内側(口側)に向けて保護不織布(スパンボンド不織布)/精密濾過用不織布(メルトブローン不織布)/抗ウイルス不織布/保護不織布(スパンボンド不織布)の構成とした。このマスクを装着したところ、息苦しさもなく、装着性も良好であった。
(実施例13)
1. 抗ウイルス不織布の作製
実施例7の繊度7.8dtex、繊維長76mmの酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料を30質量%と、実施例6と同様の方法で得られた繊度5.6dtex、繊維長76mmの抗ウイルス繊維Pを30質量%と、芯成分がポリプロピレン、鞘成分が高密度ポリエチレンからなる繊度2.2dtex、繊維長51mmの鞘芯型複合繊維(ダイワボウポリテック(株)製、NBF(H))を40質量%用いた。これらの繊維を混合し、パラレルカード機を用いて開繊したカードウェブを作製した。次いで、一対のエンボスロール/フラットロールからなる熱ロール加工機を用いて140℃で熱処理して、鞘芯型複合繊維の鞘成分を溶融し部分的に圧着(エンボス面積率約18%)させて、サーマルボンド不織布(抗ウイルス不織布)2種類を作製した。目付は、それぞれ15g/m2、30g/m2であった。
1. 抗ウイルス不織布の作製
実施例7の繊度7.8dtex、繊維長76mmの酢酸ビニル-無水マレイン酸共重合体が混合されたビスコースレーヨン繊維(本発明)の試料を30質量%と、実施例6と同様の方法で得られた繊度5.6dtex、繊維長76mmの抗ウイルス繊維Pを30質量%と、芯成分がポリプロピレン、鞘成分が高密度ポリエチレンからなる繊度2.2dtex、繊維長51mmの鞘芯型複合繊維(ダイワボウポリテック(株)製、NBF(H))を40質量%用いた。これらの繊維を混合し、パラレルカード機を用いて開繊したカードウェブを作製した。次いで、一対のエンボスロール/フラットロールからなる熱ロール加工機を用いて140℃で熱処理して、鞘芯型複合繊維の鞘成分を溶融し部分的に圧着(エンボス面積率約18%)させて、サーマルボンド不織布(抗ウイルス不織布)2種類を作製した。目付は、それぞれ15g/m2、30g/m2であった。
前記抗ウイルス不織布について、鳥インフルエンザウイルス(H5N3株)のウイルス力価を測定したところ、いずれも尿膜腔液B(<101.50(EID50/0.2ml))は、ウイルス液A(106.75(EID50/0.2ml))よりもウイルス力価が大幅に減少し、99.999%のウイルス減少率であった。
2. エアフィルターの作製
ポリエステル繊維とレーヨン繊維を混合したケミカルボンド不織布を支持体とし、その支持体の上にホットメルト剤を噴霧した後に、得られた抗ウイルス不織布を積層し、ホットメルト剤により一体化した。次いで、その抗ウイルス不織布の上にホットメルト剤を噴霧した後に、目付が約150g/m2のエレクトレット不織布(精密フィルター層)を積層し、ホットメルト剤により一体化した。得られたシートは、プリーツ加工機によりプリーツ折りされて、プラスチック製ユニットにはめ込まれ、空気清浄機用フィルターを作製した。
ポリエステル繊維とレーヨン繊維を混合したケミカルボンド不織布を支持体とし、その支持体の上にホットメルト剤を噴霧した後に、得られた抗ウイルス不織布を積層し、ホットメルト剤により一体化した。次いで、その抗ウイルス不織布の上にホットメルト剤を噴霧した後に、目付が約150g/m2のエレクトレット不織布(精密フィルター層)を積層し、ホットメルト剤により一体化した。得られたシートは、プリーツ加工機によりプリーツ折りされて、プラスチック製ユニットにはめ込まれ、空気清浄機用フィルターを作製した。
本発明の抗ウイルス物質は、本発明の抗ウイルス繊維の原材料として使用できる。
また、本発明の抗ウイルス繊維を少なくとも一部に含む抗ウイルス繊維構造物は、糸、織編物、ウェブ、不織布、紙、ネット等に成形して、様々な繊維産業に使用できる。その抗ウイルス繊維構造物は、接触するウイルスに対して不活化効果が高く、医療に役立つ。
さらに、前記抗ウイルス繊維を少なくとも一部に含む抗ウイルス繊維製品は、例えば、衣類、布団、カーテン、壁紙、カーペット、マット、シーツ、フィルター、マスク、ワイパー、タオル、防護衣類、防護ネット、廃鶏袋、鶏舎用品、医療用シートに形づくられて使用できる。
Claims (13)
- 重合鎖中にモノマー単位としてのマレイン酸成分を含む高分子からなることを特徴とする抗ウイルス物質。
- 該高分子が、オレフィン-マレイン酸共重合高分子、スチレン-マレイン酸共重合高分子、ビニルエステル-マレイン酸共重合高分子、酢酸ビニル-マレイン酸共重合高分子、または塩化ビニル-マレイン酸共重合高分子であることを特徴とする請求項1に記載の抗ウイルス物質。
- 該高分子が、銅、銀、亜鉛、ニッケルから選ばれる金属のイオンを担持していることを特徴とする請求項1に記載の抗ウイルス物質。
- 該マレイン酸成分を含む高分子が、銅イオンを担持した酢酸ビニル-マレイン酸共重合高分子であることを特徴とする請求項1に記載の抗ウイルス物質。
- 請求項2に記載のマレイン酸成分を含む共重合高分子から選ばれる少なくとも一つの共重合高分子と、セルロースとが混合されていることを特徴とする抗ウイルス物質。
- 請求項1に記載の抗ウイルス物質において、鳥インフルエンザウイルスに有効なことを特徴とする抗ウイルス物質。
- 該鳥インフルエンザウイルスがA/whistling swan/Shimane/499/83 (H5N3)株、及びA/Turkey/Wisconsin/1/66 (H9N2)株から選ばれる少なくとも1種類であることを特徴とする請求項6に記載の抗ウイルス物質。
- 請求項1に記載の抗ウイルス物質において、ヒトインフルエンザウイルスに有効なことを特徴とする抗ウイルス物質。
- 請求項1に記載の抗ウイルス物質において、ブタインフルエンザウイルスに有効なことを特徴とする抗ウイルス物質。
- 請求項1に記載の抗ウイルス物質において、ノロウイルスに有効なことを特徴とする抗ウイルス物質。
- 重合鎖中にモノマー単位としてのマレイン酸成分を含む高分子からなる抗ウイルス物質を成分として含むことを特徴とする抗ウイルス繊維。
- 請求項11に記載の抗ウイルス繊維を少なくとも一部に含むことを特徴とする抗ウイルス繊維構造物。
- 請求項11に記載の抗ウイルス繊維を少なくとも一部に含み、衣類、寝具、布団、カーテン、壁紙、カーペット、マット、シーツ、フィルター、マスク、ワイパー、タオル、防護衣類、防護ネット、廃鶏袋、鶏舎用品、医療用シートに形づくられた抗ウイルス繊維製品。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN2009801005391A CN101932237A (zh) | 2008-02-20 | 2009-02-20 | 抗病毒物质,抗病毒纤维及抗病毒纤维结构物 |
| US12/679,211 US20100272668A1 (en) | 2008-02-20 | 2009-02-20 | Antiviral substance, antiviral fiber, and antiviral fiber structure |
| EP09712946A EP2243360A4 (en) | 2008-02-20 | 2009-02-20 | ANTIVIRAL SUBSTANCE, ANTIVIRAL FIBER AND ANTIVIRAL FIBER STRUCTURE |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008-039333 | 2008-02-20 | ||
| JP2008039333 | 2008-02-20 | ||
| JP2008-176178 | 2008-07-04 | ||
| JP2008176178 | 2008-07-04 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2009104760A1 true WO2009104760A1 (ja) | 2009-08-27 |
Family
ID=40985637
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2009/053083 Ceased WO2009104760A1 (ja) | 2008-02-20 | 2009-02-20 | 抗ウイルス物質、抗ウイルス繊維及び抗ウイルス繊維構造物 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20100272668A1 (ja) |
| EP (1) | EP2243360A4 (ja) |
| JP (1) | JP4584339B2 (ja) |
| CN (1) | CN101932237A (ja) |
| TW (2) | TW201008486A (ja) |
| WO (1) | WO2009104760A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013102621A1 (fr) | 2012-01-04 | 2013-07-11 | Rhodia Operations | Procede pour le diagnostic du dysfonctionnement d'un dispositif d'additivation d'un additif dans un carburant pour un vehicule et systeme pour la mise en oeuvre de ce procede |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20120177714A1 (en) * | 2011-01-11 | 2012-07-12 | Philip Khoury | Floor mat for life |
| WO2012122500A1 (en) * | 2011-03-10 | 2012-09-13 | Adc Tech International Ltd. | Air purifier having an electret module |
| JP5673375B2 (ja) * | 2011-06-14 | 2015-02-18 | 住友ベークライト株式会社 | 繊維樹脂複合構造体、成形体の製造方法及び成形体 |
| BR112013033475A2 (pt) | 2011-06-28 | 2017-12-19 | Ctc Bio Inc | composição farmacêutica para tratamento, prevenção ou melhora da ejaculação precoce e método para tratamento, prevenção ou melhora da ejaculação precoce |
| JP6055765B2 (ja) | 2011-07-06 | 2016-12-27 | 株式会社Nbcメッシュテック | 抗ウイルス性樹脂部材 |
| US20140367263A1 (en) | 2011-09-07 | 2014-12-18 | NBC MESHTEC, INC. of Tokyo, Japan | Anti-virus aluminum member and method for producing same |
| JP2013087064A (ja) * | 2011-10-14 | 2013-05-13 | Nbc Meshtec Inc | ウイルス不活化シート |
| WO2015005476A1 (ja) | 2013-07-12 | 2015-01-15 | ロンシール工業株式会社 | 抗ウイルス性塩化ビニル系樹脂組成物、抗ウイルス性塩化ビニル系樹脂製シート、及びその製造方法、内装シート、内装シートの製造方法、ポリ塩化ビニル系樹脂製内装シート、抗ウイルス性壁紙、及び抗ウイルス性壁紙の製造方法 |
| DE102013218412A1 (de) * | 2013-09-13 | 2015-03-19 | Kelheim Fibres Gmbh | Filterhilfsmittel und Filterschicht |
| JP7008914B2 (ja) * | 2015-03-31 | 2022-01-25 | 住化エンバイロメンタルサイエンス株式会社 | 抗ウイルス組成物 |
| US11952510B2 (en) * | 2016-09-23 | 2024-04-09 | Devan Chemicals | Textile coating composition |
| CN108927014A (zh) * | 2018-07-26 | 2018-12-04 | 苏州市天翱特种织绣有限公司 | 一种口罩中pva复合空气过滤膜的制备方法 |
| IL295944A (en) * | 2020-03-04 | 2022-10-01 | Ascend Performance Mat Operations Llc | Antiviral/antimicrobial polymer composites, fibers and products |
| CN111636109A (zh) * | 2020-07-13 | 2020-09-08 | 青岛迦南美地家居用品有限公司 | 一种抗菌消臭粘胶长丝纤维及制造方法 |
| US11849782B2 (en) * | 2020-09-11 | 2023-12-26 | American Biomedical Group Inc. | Facemask |
| US20230329234A1 (en) * | 2020-09-18 | 2023-10-19 | Dai Nippon Printing Co., Ltd. | Antiviral article and antiviral resin composition |
| FR3115380A1 (fr) * | 2020-10-15 | 2022-04-22 | Elmer | Système de gestion de masques réutilisables |
| KR102566091B1 (ko) * | 2021-03-31 | 2023-08-11 | 주식회사 코리아마스크 | 습도를 제어하는 안면마스크 제조용 다층 구조의 부직포 시트 및 이를 이용한 안면마스크 |
| CN113564928A (zh) * | 2021-06-28 | 2021-10-29 | 南京林业大学 | 一种抗菌抗病毒可降解无纺布及其制备方法和应用 |
| WO2023100967A1 (ja) * | 2021-12-03 | 2023-06-08 | 古河電気工業株式会社 | 抗ウイルス性組成物及びその成形体 |
| US20260083122A1 (en) | 2022-08-29 | 2026-03-26 | Nissan Motor Co., Ltd. | Method and agent for inactivating bacteria or viruses, and antiviral base material using same |
Citations (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS59228847A (ja) * | 1983-06-10 | 1984-12-22 | ユニチカ株式会社 | 生理活性を有する成形体の製造方法 |
| JPH03121145A (ja) | 1989-06-23 | 1991-05-23 | Daiwabou Kurieito Kk | イオン交換機能を持ったセルロース系組成物 |
| JPH05132871A (ja) * | 1991-11-13 | 1993-05-28 | Daiwabo Co Ltd | 消臭抗菌性布帛の製造方法 |
| JPH0625998A (ja) * | 1992-03-30 | 1994-02-01 | Sanden Seishi Kk | イオン消臭紙 |
| JPH0813905A (ja) | 1994-06-30 | 1996-01-16 | Shin Nikkei Co Ltd | 天 窓 |
| JPH09225238A (ja) * | 1996-02-26 | 1997-09-02 | Matsushita Electric Ind Co Ltd | 空気清浄機用エアーフィルタ |
| WO1998012924A1 (fr) * | 1996-09-24 | 1998-04-02 | Snd Co., Ltd. | Procede pour preparer des solutions de sterilisation, et solutions et milieu de sterilisation |
| JPH1119238A (ja) * | 1997-06-30 | 1999-01-26 | Kokago Corp Kk | 抗菌効果を有するマスク |
| JP2003205023A (ja) * | 2002-01-11 | 2003-07-22 | Okada Giken:Kk | 消臭抗菌剤 |
| WO2005083171A1 (ja) | 2004-03-02 | 2005-09-09 | Japan Exlan Co., Ltd. | 抗ウイルス性繊維、及び該繊維の製法、並びに該繊維を用いた繊維製品 |
| JP2006291031A (ja) * | 2005-04-11 | 2006-10-26 | Rengo Co Ltd | 微小たんぱく質不活化素材 |
| JP2006328039A (ja) | 2005-04-26 | 2006-12-07 | Nippo Kagaku Kk | 鳥インフルエンザウイルス不活化剤 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20040247690A1 (en) * | 2001-12-27 | 2004-12-09 | Si-Young Yang | Method of preparing functional microcapsule incorporating silver nanoparticles |
| US20040197386A1 (en) * | 2003-04-01 | 2004-10-07 | The Cupron Corporation | Disposable paper-based hospital and operating theater products |
| US20050244365A1 (en) * | 2004-05-03 | 2005-11-03 | Novaflux Biosciences, Inc. | Methods, compositions, formulations, and uses of cellulose and acrylic-based polymers |
| JP4719081B2 (ja) * | 2006-05-24 | 2011-07-06 | ダイワボウホールディングス株式会社 | 湿熱接着性複合繊維及びフィラー固着繊維、繊維構造物 |
| AU2007276218B2 (en) * | 2006-07-18 | 2013-03-21 | Glaxo Group Limited | Anti-viral face mask and filter material |
-
2009
- 2009-02-20 US US12/679,211 patent/US20100272668A1/en not_active Abandoned
- 2009-02-20 WO PCT/JP2009/053083 patent/WO2009104760A1/ja not_active Ceased
- 2009-02-20 JP JP2009038490A patent/JP4584339B2/ja not_active Expired - Fee Related
- 2009-02-20 TW TW098105447A patent/TW201008486A/zh unknown
- 2009-02-20 CN CN2009801005391A patent/CN101932237A/zh active Pending
- 2009-02-20 EP EP09712946A patent/EP2243360A4/en not_active Withdrawn
- 2009-02-20 TW TW099109170A patent/TW201029568A/zh unknown
Patent Citations (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS59228847A (ja) * | 1983-06-10 | 1984-12-22 | ユニチカ株式会社 | 生理活性を有する成形体の製造方法 |
| JPH03121145A (ja) | 1989-06-23 | 1991-05-23 | Daiwabou Kurieito Kk | イオン交換機能を持ったセルロース系組成物 |
| JPH05132871A (ja) * | 1991-11-13 | 1993-05-28 | Daiwabo Co Ltd | 消臭抗菌性布帛の製造方法 |
| JPH0625998A (ja) * | 1992-03-30 | 1994-02-01 | Sanden Seishi Kk | イオン消臭紙 |
| JPH0813905A (ja) | 1994-06-30 | 1996-01-16 | Shin Nikkei Co Ltd | 天 窓 |
| JPH09225238A (ja) * | 1996-02-26 | 1997-09-02 | Matsushita Electric Ind Co Ltd | 空気清浄機用エアーフィルタ |
| WO1998012924A1 (fr) * | 1996-09-24 | 1998-04-02 | Snd Co., Ltd. | Procede pour preparer des solutions de sterilisation, et solutions et milieu de sterilisation |
| JPH1119238A (ja) * | 1997-06-30 | 1999-01-26 | Kokago Corp Kk | 抗菌効果を有するマスク |
| JP2003205023A (ja) * | 2002-01-11 | 2003-07-22 | Okada Giken:Kk | 消臭抗菌剤 |
| WO2005083171A1 (ja) | 2004-03-02 | 2005-09-09 | Japan Exlan Co., Ltd. | 抗ウイルス性繊維、及び該繊維の製法、並びに該繊維を用いた繊維製品 |
| JP2006291031A (ja) * | 2005-04-11 | 2006-10-26 | Rengo Co Ltd | 微小たんぱく質不活化素材 |
| JP2006328039A (ja) | 2005-04-26 | 2006-12-07 | Nippo Kagaku Kk | 鳥インフルエンザウイルス不活化剤 |
Non-Patent Citations (2)
| Title |
|---|
| JOURNAL OF MACROMOLECULAR SCIENCE, CHEMISTRY, vol. A22, no. 5-7, 1985, pages 819 - 832, XP008131175 * |
| See also references of EP2243360A4 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013102621A1 (fr) | 2012-01-04 | 2013-07-11 | Rhodia Operations | Procede pour le diagnostic du dysfonctionnement d'un dispositif d'additivation d'un additif dans un carburant pour un vehicule et systeme pour la mise en oeuvre de ce procede |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2010030984A (ja) | 2010-02-12 |
| EP2243360A1 (en) | 2010-10-27 |
| TW201029568A (en) | 2010-08-16 |
| EP2243360A4 (en) | 2011-06-01 |
| TW201008486A (en) | 2010-03-01 |
| JP4584339B2 (ja) | 2010-11-17 |
| US20100272668A1 (en) | 2010-10-28 |
| CN101932237A (zh) | 2010-12-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4584339B2 (ja) | 抗ウイルス物質、抗ウイルス繊維及び抗ウイルス繊維構造物 | |
| JP4558831B2 (ja) | 抗ウイルス剤、抗ウイルス繊維及び抗ウイルス繊維構造物 | |
| JP5298012B2 (ja) | 抗ウイルスフェイスマスクおよびフィルター材 | |
| TWI762276B (zh) | 具有抗微生物或抗病毒性能的濾材和口罩 | |
| CN101489425A (zh) | 抗病毒面罩和过滤材料 | |
| JP2011042615A (ja) | 抗ウイルス物質、抗ウイルス繊維及び抗ウイルス繊維構造物 | |
| JP6057343B2 (ja) | 砂塵飛来有害物質及び微生物を除去する除去剤、セルロース繊維並びに繊維構造物 | |
| JP4030231B2 (ja) | 空気清浄化フィルター | |
| JP6801954B2 (ja) | 抗菌及び抗ウイルス加工剤及びそれによる加工品 | |
| EP4132309A1 (en) | Article for infection prevention for fomite materials | |
| JP2011042095A (ja) | 抗ウイルス膜材、防水布製品、及びテント | |
| JP2011234867A (ja) | 抗ウィルス性透視カバー | |
| JP7579543B2 (ja) | 抗ウィルス繊維構造体およびその製造方法、抗ウィルス加工製品 | |
| WO2004088029A2 (en) | Disposable, paper-based hospital and operating theater products | |
| CN113558047A (zh) | 杀菌性纳米胶囊、葡萄状微粒集合体、消毒杀菌过滤器和它们的制造方法 | |
| CN113840552A (zh) | 抗病毒纤维产品的制造方法和使用其制成的抗病毒口罩 | |
| JP2023042777A (ja) | 抗ウイルス性不織布 | |
| JP2024142555A (ja) | 抗ウイルスエアフィルター用積層濾材 | |
| JP2021028342A (ja) | 抗菌及び抗ウイルス加工剤及びそれによる加工品 | |
| HK40053504A (en) | Bactericidal nanocapsule, grape-like particle aggregate, disinfection and sterilization filter and their manufacturing method |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 200980100539.1 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 09712946 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2009712946 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 12679211 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |