WO2014092100A1 - 複素環化合物 - Google Patents
複素環化合物 Download PDFInfo
- Publication number
- WO2014092100A1 WO2014092100A1 PCT/JP2013/083140 JP2013083140W WO2014092100A1 WO 2014092100 A1 WO2014092100 A1 WO 2014092100A1 JP 2013083140 W JP2013083140 W JP 2013083140W WO 2014092100 A1 WO2014092100 A1 WO 2014092100A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- optionally substituted
- substituted
- atom
- ring
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D498/08—Bridged systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2013—Organic compounds, e.g. phospholipids, fats
- A61K9/2018—Sugars, or sugar alcohols, e.g. lactose, mannitol; Derivatives thereof, e.g. polysorbates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/4858—Organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/06—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom containing only hydrogen and carbon atoms in addition to the ring nitrogen atom
- C07D213/08—Preparation by ring-closure
- C07D213/09—Preparation by ring-closure involving the use of ammonia, amines, amine salts, or nitriles
- C07D213/12—Preparation by ring-closure involving the use of ammonia, amines, amine salts, or nitriles from unsaturated compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/72—Nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/72—Nitrogen atoms
- C07D213/74—Amino or imino radicals substituted by hydrocarbon or substituted hydrocarbon radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
- C07D239/32—One oxygen, sulfur or nitrogen atom
- C07D239/42—One nitrogen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D451/00—Heterocyclic compounds containing 8-azabicyclo [3.2.1] octane, 9-azabicyclo [3.3.1] nonane, or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane or granatane alkaloids, scopolamine; Cyclic acetals thereof
- C07D451/02—Heterocyclic compounds containing 8-azabicyclo [3.2.1] octane, 9-azabicyclo [3.3.1] nonane, or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane or granatane alkaloids, scopolamine; Cyclic acetals thereof containing not further condensed 8-azabicyclo [3.2.1] octane or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane; Cyclic acetals thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D451/00—Heterocyclic compounds containing 8-azabicyclo [3.2.1] octane, 9-azabicyclo [3.3.1] nonane, or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane or granatane alkaloids, scopolamine; Cyclic acetals thereof
- C07D451/02—Heterocyclic compounds containing 8-azabicyclo [3.2.1] octane, 9-azabicyclo [3.3.1] nonane, or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane or granatane alkaloids, scopolamine; Cyclic acetals thereof containing not further condensed 8-azabicyclo [3.2.1] octane or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane; Cyclic acetals thereof
- C07D451/04—Heterocyclic compounds containing 8-azabicyclo [3.2.1] octane, 9-azabicyclo [3.3.1] nonane, or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane or granatane alkaloids, scopolamine; Cyclic acetals thereof containing not further condensed 8-azabicyclo [3.2.1] octane or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane; Cyclic acetals thereof with hetero atoms directly attached in position 3 of the 8-azabicyclo [3.2.1] octane or in position 7 of the 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/10—Spiro-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/10—Spiro-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/12—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains three hetero rings
- C07D487/18—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/12—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains three hetero rings
- C07D491/18—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/99—Enzyme inactivation by chemical treatment
Definitions
- the present invention relates to a heterocyclic compound having an inhibitory action on cholesterol 24 hydroxylase (sometimes abbreviated as “CH24H” in the present specification), a pharmaceutical composition containing them, and the like.
- CH24H cholesterol 24 hydroxylase
- Alzheimer's disease is a progressive neurodegenerative disease characterized by amyloid ⁇ protein (A ⁇ ) deposition, accumulation of phosphorylated tau (neurofibrillary tangles) in nerve cells, and nerve cell death.
- a ⁇ amyloid ⁇ protein
- phosphorylated tau neuroofibrillary tangles
- nerve cell death an effective treatment has not been developed yet.
- An acetylcholinesterase (AchE) inhibitor is mainly used as a therapeutic agent for Alzheimer's disease currently used in the medical field.
- AchE inhibitors have been confirmed to have certain usefulness
- treatment with AchE inhibitors is only symptomatic treatment because it aims to supplement reduced acetylcholine. For this reason, it is strongly desired to develop a radical treatment method and a preventive drug as soon as possible.
- Non-patent Document 1 Science, 261, 921-923, 1993]. Since this discovery, correlations between multiple polymorphisms responsible for the expression of proteins that control cholesterol metabolism and the incidence of Alzheimer's disease have been shown, suggesting an association between cholesterol metabolism and Alzheimer's disease [Non-Patent Document 2]. : Neurobiology of Aging (Neurobiol.Aging), 24, 421-426, 2003, Non-Patent Document 3: Molecular Psychiatry (8, 635-638, 2003).
- Cyp46 (synonymous with “cholesterol 24 hydroxylase (CH24H)”), a cholesterol oxidase specifically expressed in the brain, is a risk factor for Alzheimer's disease [Non-patent document 4: Neurology]. Science Letters (Neurosci. Lett.), 328, 9-12, 2002]. Cyp46 (CH24H) is expressed around the deposited amyloid of Alzheimer patients [Non-patent document 5: Journal of Biological Chemistry, 279, 34672-34681, 2004.
- 24-HC Its metabolite 24S-hydroxycholesterol (24-HC) is increased in the cerebrospinal fluid (CSF) of Alzheimer's patients
- CSF cerebrospinal fluid
- 24-HC is a human neuroblast cell line SH- Inducing cell death in SY5Y cells
- Patent Document 8 Brain Research, 818, 171-175, 1999
- rats injected with 24-HC into the lateral brain show short-term memory impairment seen in Alzheimer's disease patients, It has been suggested that hippocampal nerves are injured by 24-HC
- Non-patent Document 9 Neuroscience, 164, 398-403, 2009].
- Cyp46 (CH24H) is deeply involved in the pathology of Alzheimer's disease. Therefore, a compound that inhibits the activity of Cyp46 (CH24H) (ie, Cyp46 (CH24H) inhibitor) reduces neuronal 24-HC, thereby causing neuronal cell death, A ⁇ increase, brain activity in Alzheimer's disease. It is promising as a therapeutic or prophylactic agent that suppresses inflammation and has an effect of suppressing progression as well as improving symptoms.
- AchE inhibitors that have already been clinically applied as Alzheimer's disease therapeutic agents have an effect of improving memory impairment in mice caused by A ⁇ [Non-patent Document 10: British Journal of Pharmacology.
- Cyp46 (CH24H) inhibitors are promising as therapeutic agents for Alzheimer's disease.
- traumatic brain injury also referred to herein as TBI
- TBI traumatic brain injury
- Non-Patent Document 15 NeuroReport, 16, 909-913, 2005
- the inflammatory reaction in the brain accompanied by activation of glial cells is a pathological change characteristic of neurodegenerative diseases
- Non-patent document 16 Glia, 50, 427-434, 2005.
- Treatment of neurodegenerative diseases such as Huntington's disease, Parkinson's disease, and amyotrophic lateral sclerosis by suppressing inflammation in the brain
- Neurodegenerative diseases such as Huntington's disease, Parkinson's disease, and amyotrophic lateral sclerosis
- Cyp46 inhibition is a new therapeutic agent for neurodegenerative diseases such as Huntington's disease, Parkinson's disease, cerebral infarction, glaucoma, amyotrophic lateral sclerosis or the like. Promising as a preventive drug.
- Glaucoma is the most common cause of blindness and is considered as a major social problem, but there is no effective treatment for normal intraocular pressure-type visual field constriction, which accounts for most of it.
- the genetic polymorphism of Cyp46 (CH24H) with a high level of 24-HC in the blood has been associated with the risk of developing glaucoma [Non-patent document 18: Investigative Opsalmology and Visual Science (Invest. Opthalmol. Vis. Sci.), 50, 5712-5717, 2009], and Cyp46 (CH24H) inhibitors are promising as therapeutic or prophylactic agents for glaucoma.
- Spasm is a disease that occurs in a seizure with abnormal electrical excitation of nerve cells in the brain.
- Convulsions are one of the characteristic clinical findings of Alzheimer's disease [Non-patent document 19: Epilepsya, 47, 867-872, 2006], and there is also an association between epilepsy and the onset of Alzheimer's disease [Non-patent document 20: Epilepsya, Vol. 52, Appendix 1, pp. 39-46, 2011].
- Non-Patent Document 22 Journal of Neurology (J. Neurol., 65, 652-663, 2006)].
- Carbamazepine a convulsant treatment drug, exhibits a short-term memory improvement effect in a Y maze test in a mouse epileptic model [Non-patent Document 23: Journal of Neurology Neurosurgery Psychiatry (J. Neurol. Neurosurg. Psychiatry), 48 Vol. 459-468, 1985], and in a model animal showing convulsions, a CH24H inhibitor showing a short-term memory improving action is promising as a new therapeutic or prophylactic agent for convulsions or epilepsy. is there.
- ⁇ ⁇ Schizophrenia has various psychological symptoms such as hallucinations, delusions, excitement, and manic-depressive symptoms. Therefore, its therapeutic drugs are being developed from various angles. In recent years, it has been pointed out that changes in cholesterol metabolism are involved in abnormal neuronal activity observed in schizophrenia [Non-patent Document 24: Journal of Psychiatry Neuroscience, Vol. 36, 47-55, 2011]. In addition, since cytotoxic factors such as oxidative stress also contribute to the pathology of schizophrenia, neurocytotoxicity due to 24-HC may be involved in the worsening of symptoms [Non-Patent Document 25: Psychoneuroendo]. Cryology (Vol. 28, 83-96, 2003)]. Accordingly, a Cyp46 (CH24H) inhibitor that inhibits metabolism of cholesterol to 24-HC in the brain is promising as a therapeutic or prophylactic agent for schizophrenia.
- CH24H Cyp46
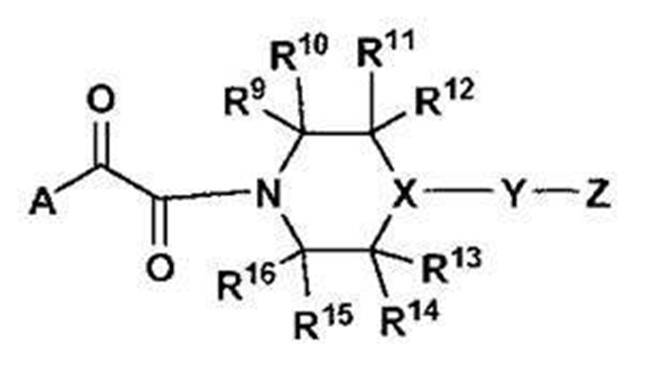
- Patent Document 1 describes the following compounds as therapeutic agents such as HIV and AIDS.
- R 1 represents a hydrogen atom, C 1-4 alkyl or the like
- R 2 represents a hydrogen atom
- R 4 to R 7 independently represent a hydrogen atom, a halogen atom or the like
- X is N or CH
- Y represents a 5- to 7-membered monocyclic aromatic heterocycle and the like
- Z represents an aryl or aromatic heterocyclic group
- R 9 to R 16 are each independently a hydrogen atom, C 1-6 alkyl or the like.
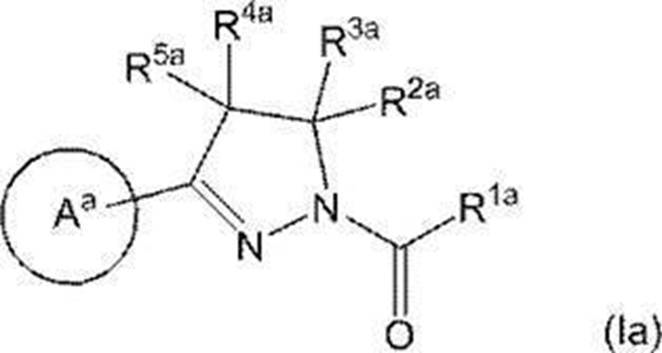
- Patent Document 2 describes the following compounds as a therapeutic agent for neurodegenerative diseases (eg, Alzheimer's disease, mild cognitive impairment, multiple sclerosis, etc.) having a CH24H inhibitory action.
- neurodegenerative diseases eg, Alzheimer's disease, mild cognitive impairment, multiple sclerosis, etc.
- Ring A a represents an optionally substituted ring
- R 1a is (1) Formula: -X 1a -R 6a (Where X 1a represents a C 1-6 alkylene group, a C 2-6 alkenylene group, or a C 3-6 cycloalkylene group, and R 6a represents an optionally substituted C 6-14 aryl group, An optionally substituted C 6-14 aryloxy group, or an optionally substituted heterocyclic group), (2) an optionally substituted C 6-14 aryl group, (3) an optionally substituted C 6-14 aryloxy group, or (4) represents an optionally substituted heterocyclic group;
- R 2a represents a hydrogen atom, an optionally substituted C 1-6 alkyl group, an optionally substituted C 3-6 cycloalkyl group, or an optionally substituted hydroxy group
- R 3a represents an optionally substituted C 1-6 alkyl group, an optionally substituted C 3-6 cycloalkyl group, or an optionally substituted hydroxy group,
- Patent Document 3 describes the following compounds as therapeutic agents for bone diseases (eg, osteoporosis, fractures, etc.) having a calcium sensitive receptor (CaSR) antagonistic action.
- bone diseases eg, osteoporosis, fractures, etc.
- CaSR calcium sensitive receptor
- Ring A a represents an optionally substituted ring;
- R 1a is (1) Formula: —X 1a —R 6a (wherein X 1a represents a C 1-6 alkylene group, a C 2-6 alkenylene group, or a C 3-6 cycloalkylene group, and R 6a is substituted)
- the object of the present invention is to have an excellent CH24H inhibitory action, epilepsy, neurodegenerative diseases (eg, Alzheimer's disease, mild cognitive impairment, Huntington's disease, Parkinson's disease, multiple sclerosis, amyotrophic lateral sclerosis, trauma Cerebral infarction, cerebral infarction, glaucoma, etc.), and a compound useful as a preventive or therapeutic agent for schizophrenia.
- neurodegenerative diseases eg, Alzheimer's disease, mild cognitive impairment, Huntington's disease, Parkinson's disease, multiple sclerosis, amyotrophic lateral sclerosis, trauma Cerebral infarction, cerebral infarction, glaucoma, etc.
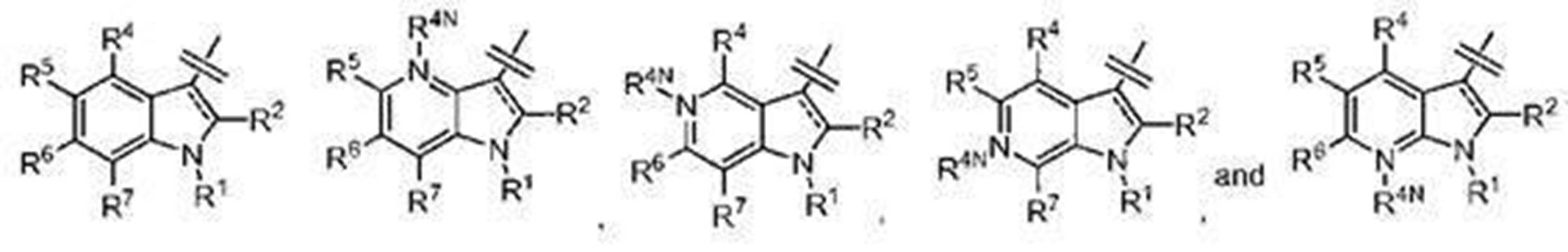
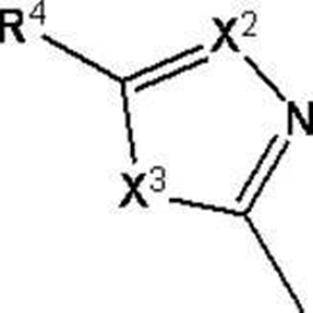
- Rings A may each be further substituted and each may be bridged.
- R 1 is an optionally substituted C 1-6 alkyl group, an optionally substituted hydroxy group, an optionally substituted amino group, an optionally substituted carbocyclic group, or an optionally substituted R 1 may be bonded to an atom on ring A to form a spiro ring or a condensed ring, together with ring A, each substituted with an oxo group and optionally further substituted.
- R 2 represents an optionally substituted C 6-14 aryl group, or an optionally substituted aromatic heterocyclic group
- R 3 represents a hydrogen atom or a substituent when X 1 is a carbon atom, and is absent when X 1 is a nitrogen atom.
- R 1 is optionally substituted C 1-6 alkyl group, optionally substituted C 1-6 alkoxy group, an optionally substituted amino group, optionally C 3 substituted
- the compound according to [1] which is an -8 cycloalkyl group, an optionally substituted C 6-14 aryl group, or an optionally substituted non-aromatic heterocyclic group (provided that tert-butyl 4- (Except 4-phenylpyrimidin-5-yl) piperazine-1-carboxylate) or salts thereof.
- R 1 is (1) (a) a cyano group, (b) a C 6-14 aryl group optionally substituted by 1 to 3 C 1-6 alkoxy groups, (c) a C 6-14 aryloxy group, (d) a C 3-8 cycloalkyl group, (e) a 5- or 6-membered monocyclic aromatic heterocyclic group, (f) 8 to 12 membered fused aromatic heterocyclic group, and (g) 3 to 8 membered monocyclic non-aromatic heterocyclic group optionally substituted by 1 to 3 oxo groups
- R 1 is bonded to an atom on ring A to be substituted with oxo together with ring A, and 1 to 3 C 1-1 Forming a spiro ring optionally further substituted with 6 alkyl groups;
- R 2 is (1) substituted with 1 to 3 substituents selected from (a) a halogen atom, and (b) a C 1-6 alkyl group optionally substituted with 1 to 3 halogen atoms A good C 6-14 aryl group, or (2) (a) a halogen atom, (b) a cyano group, (c) a C 1-6 alkyl group optionally substituted with 1 to 3 halogen atoms, and (d) a substituent substituted with 1 to 3 substituents selected from C 3-8 cycloalkyl group An optionally substituted 5- to 12-membered aromatic heterocyclic group;
- X 1 is a carbon atom or a nitrogen atom;
- R 1 is (1) (a) a cyano group, (b) a C 6-14 aryl group optionally substituted by 1 to 3 C 1-6 alkoxy groups, (c) a C 6-14 aryloxy group, (d) a C 3-8 cycloalkyl group, (e) a 5- or 6-membered monocyclic aromatic heterocyclic group, (f) 8 to 12 membered fused aromatic heterocyclic group, and (g) 3 to 8 membered monocyclic non-aromatic heterocyclic group optionally substituted by 1 to 3 oxo groups
- An optionally substituted 3- to 12-membered non-aromatic heterocyclic group, or R 1 is bonded to an atom on ring A to be substituted with oxo together with ring A, and 1 to 3 C 1-1
- R 1 is (1) (a) a cyano group, (b) a C 6-14 aryl group optionally substituted by 1 to 3 C 1-6 alkoxy groups, (c) a C 6-14 aryloxy group, (d) a C 3-8 cycloalkyl group, (e) a pyrazolyl group, (f) an indazolyl group, and (g) a C 1-6 alkyl group optionally substituted with 1 to 3 substituents selected from dihydropyridyl groups optionally substituted with 1 to 3 oxo groups , (2) a C 1-6 alkoxy group optionally substituted by 1 to 3 C 6-14 aryl groups, (3) (a) (i) a halogen atom, (ii) a cyano group, (iii) a C 3-8 cycloalkyl group, (iv) a C 6-14 aryl group which may be substituted with 1 to 3 substituents selected from a halogen atom and a
- R 1 is on ring A Together with ring A to form a 2,8-diazaspiro [4.5] decane ring substituted with oxo and optionally substituted with 1 to 3 C 1-6 alkyl groups.
- R 2 is (1) substituted with 1 to 3 substituents selected from (a) a halogen atom, and (b) a C 1-6 alkyl group optionally substituted with 1 to 3 halogen atoms A good C 6-14 aryl group, or (2) (a) a halogen atom, (b) a cyano group, (c) a C 1-6 alkyl group optionally substituted with 1 to 3 halogen atoms, and (d) 1 to 3 substituents selected from a C 3-8 cycloalkyl group, An optionally substituted 5- or 6-membered monocyclic aromatic heterocyclic group or an 8- to 12-membered fused aromatic heterocyclic group;
- X 1 is a carbon atom or a nitrogen atom;
- R 3 is (1) a hydrogen atom, or (2) a halogen atom; and
- ring A is (1) (a) a halogen atom, (b) a C 1-6 alkyl group, and (c) 1 to 3 substitu
- R 1 is (1) (a) a cyano group, (b) a C 6-14 aryl group optionally substituted by 1 to 3 C 1-6 alkoxy groups, (c) a C 6-14 aryloxy group, (d) a C 3-8 cycloalkyl group, (e) a pyrazolyl group, (f) an indazolyl group, and (g) a C 1-6 alkyl group optionally substituted with 1 to 3 substituents selected from dihydropyridyl groups optionally substituted with 1 to 3 oxo groups , (2) a C 1-3 alkoxy group optionally substituted by 1 to 3 C 6-14 aryl groups, (3) (a) (i) a halogen atom, (ii) a cyano group, (iii) a C 3-8 cycloalkyl group, (iv) a C 6-14 aryl group which may be substituted with 1 to 3 substituents selected from a halogen atom and a
- R 1 is on ring A Together with ring A to form a 2,8-diazaspiro [4.5] decane ring substituted with oxo and optionally substituted with 1 to 3 C 1-6 alkyl groups , [1], [3], [A] and [B] or a salt thereof.
- R 1 is (a) a halogen atom, (b) a cyano group, (c) a carbamoyl group, (d) 1 to 3 C 1-6 alkoxy group optionally substituted by a C 1-6 alkyl group, and (e) a 3- to 8-membered monocyclic non-aromatic heterocyclic group which may be substituted with 1 to 5 substituents selected from C 1-6 alkoxy groups;
- R 2 is (1) substituted with 1 to 3 substituents selected from (a) a halogen atom, and (b) a C 1-6 alkyl group optionally substituted with 1 to 3 halogen atoms A good C 6-14 aryl group, or (2) a 5- or 6-membered monocyclic aromatic heterocyclic group which may be substituted with 1 to 3 substituents selected from (a) a halogen atom and (b) a C 1-6 alkyl group Is;
- X 1 is a carbon atom;
- R 3 is a hydrogen
- R 1 is (1) (a) a cyano group, (b) a phenyl group optionally substituted by 1 to 3 C 1-6 alkoxy groups, (c) a phenoxy group, (d) a cyclopropyl group, (e) a pyrazolyl group, (f) an indazolyl group, and (g) a C 1-6 alkyl group optionally substituted with 1 to 3 substituents selected from dihydropyridyl groups optionally substituted with 1 to 3 oxo groups , (2) a C 1-6 alkoxy group optionally substituted by 1 to 3 phenyl groups, (3) (a) (i) a halogen atom, (ii) a cyano group, (iii) cyclopropyl group, (iv) a cyclobutyl group, (v) a phenyl group which may be substituted with 1 to 3 substituents selected from a halogen atom and a C 1-6 alk
- R 1 is an atom on ring A In combination with ring A to form a 2,8-diazaspiro [4.5] decane ring substituted with oxo and optionally further substituted with 1 to 3 C 1-6 al
- X 1 is a carbon atom or a nitrogen atom;
- R 3 is (1) a hydrogen atom, or (2) a halogen atom;
- ring A is (1) (a) a halogen atom, (b) a C 1-6 alkyl group, and (c) 1 to 3 substituents selected from an oxo group, each of which may be further substituted.
- R 1 is (1) (a) a cyano group, (b) a phenyl group optionally substituted by 1 to 3 C 1-6 alkoxy groups, (c) a phenoxy group, (d) a cyclopropyl group, (e) a pyrazolyl group, (f) an indazolyl group, and (g) a C 1-6 alkyl group optionally substituted with 1 to 3 substituents selected from dihydropyridyl groups optionally substituted with 1 to 3 oxo groups , (2) a C 1-3 alkoxy group optionally substituted with 1 to 3 phenyl groups, (3) (a) (i) a halogen atom, (ii) a cyano group, (iii) cyclopropyl group, (iv) a cyclobutyl group, (v) a phenyl group which may be substituted with 1 to 3 substituents selected from a halogen atom and a C 1-6 alk
- R 1 is an atom on ring A bonded to together with ring a, is substituted with oxo, and further optionally substituted 2,8-diazaspiro [4.5] to form a decane ring with one
- R 1 is (1) (a) (i) a halogen atom, and (ii) C optionally substituted with 1 to 3 substituents selected from phenyl groups optionally substituted with 1 to 3 halogen atoms 1-6 alkyl groups, (b) a tetrahydropyranyl group, and (c) an amino group optionally mono- or disubstituted with a substituent selected from a tetrahydrofuryl group, or (2) (a) a halogen atom, (b) a cyano group, (c) a carbamoyl group, (d) a C 1-6 alkyl group, and (e) an azetidinyl group or a pyrrolidinyl group, each optionally substituted by 1 to 5 substituents selected from C 1-6 alkoxy groups; R 2 is (1) a phenyl group optionally substituted by 1 to 3 halogen atoms, or (2) (a) a halogen atom, (
- R 1 is (1) (a) (i) a halogen atom, and (ii) C optionally substituted with 1 to 3 substituents selected from phenyl groups optionally substituted with 1 to 3 halogen atoms 1-6 alkyl groups, (b) a tetrahydropyranyl group, and (c) an amino group optionally mono- or disubstituted with a substituent selected from a tetrahydrofuryl group, or (2) an azetidinyl group or a pyrrolidinyl group each optionally substituted with 1 to 5 substituents selected from (a) a halogen atom and (b) a cyano group;
- R 2 is (1) a phenyl group optionally substituted by 1 to 3 halogen atoms, or (2) (a) a halogen atom, (b) a C 1-6 alkyl group, and (c) a pyrazolyl group or a thiazolyl group each optionally substituted
- R 1 is (1) (a) (i) a halogen atom, and (ii) C optionally substituted with 1 to 3 substituents selected from phenyl groups optionally substituted with 1 to 3 halogen atoms 1-6 alkyl groups, (b) a tetrahydropyranyl group, and (c) an amino group optionally mono- or disubstituted with a substituent selected from a tetrahydrofuryl group, or (2) an azetidinyl group or a pyrrolidinyl group each optionally substituted by 1 to 3 halogen atoms;
- R 2 is (1) a phenyl group optionally substituted by 1 to 3 halogen atoms, or (2) (a) a halogen atom, (b) a C 1-6 alkyl group, and (c) a pyrazolyl group or a thiazolyl group each optionally substituted by 1 to 3 substituents selected from a cyclopropyl group;
- R 1 is (a) a halogen atom, (b) a cyano group, (c) a carbamoyl group, (d) 1 to 3 C 1-6 alkoxy group optionally substituted by a C 1-6 alkyl group, and (e) a pyrrolidinyl group optionally substituted with 1 to 5 substituents selected from C 1-6 alkoxy groups;
- R 2 is (1) substituted with 1 to 3 substituents selected from (a) a halogen atom, and (b) a C 1-6 alkyl group optionally substituted with 1 to 3 halogen atoms A good phenyl group, or (2) a pyrazolyl group, a thiadiazolyl group or a pyridyl group each optionally substituted by 1 to 3 substituents selected from (a) a halogen atom and (b) a C 1-6 alkyl group;
- X 1 is a carbon atom;
- R 3 is a hydrogen atom; and
- R 1 is (a) a halogen atom, (b) a cyano group, (c) a carbamoyl group, (d) a C 1-6 alkyl group, and (e) a pyrrolidinyl group optionally substituted with 1 to 5 substituents selected from C 1-6 alkoxy groups;
- R 2 is (a) a halogen atom, and (b) a pyrazolyl group or a thiadiazolyl group each optionally substituted by 1 to 3 substituents selected from C 1-6 alkyl groups;
- X 1 is a carbon atom;
- R 3 is a hydrogen atom; and Ring A is
- R 1 is (a) a halogen atom, and (b) a pyrrolidinyl group optionally substituted with 1 to 5 substituents selected from a cyano group
- R 2 is (a) a halogen atom, and (b) a pyrazolyl group optionally substituted by 1 to 3 substituents selected from C 1-6 alkyl groups
- X 1 is a carbon atom
- R 3 is a hydrogen atom
- Ring A is
- R 1 is (1) a C 1-6 alkyl group optionally substituted with 1 to 3 substituents selected from (a) a cyclopropyl group, and (b) an indazolyl group, (2) a C 1-6 alkoxy group optionally substituted by 1 to 3 phenyl groups, (3) (a) (i) a halogen atom, (ii) a phenyl group optionally substituted by 1 to 3 halogen atoms, (iii) a pyridyl group, and (iv) a C 1 1 -optionally substituted C 1 1 -3 selected from 1 to 3 substituents selected from an oxetanyl group optionally substituted by 1 to 3 C 1-6 alkyl groups.
- X 1 is a carbon atom or a nitrogen atom;
- R 3 is (1) a hydrogen atom, or (2) a halogen atom;
- ring A is (1) (a) a halogen atom, and (b) 1 to 3 substituents selected from a C 1-6 alkyl group, each of which may be further substituted.
- R 1 is (a) a halogen atom, (b) a cyano group, (c) a carbamoyl group, and (d) a pyrrolidinyl group optionally substituted with 1 to 3 substituents selected from C 1-6 alkyl groups optionally substituted with 1 to 3 C 1-6 alkoxy groups;
- R 2 is (a) a halogen atom, and (b) a pyrazolyl group, a thiazolyl group, a thiadiazolyl group or a pyridyl group each optionally substituted by 1 to 3 substituents selected from C 1-6 alkyl groups;
- X 1 is a carbon atom;
- R 3 is a hydrogen atom; and Ring A is
- [15] The compound or salt thereof according to any one of [1] to [10] for use in the prevention or treatment of epilepsy or neurodegenerative diseases.
- [16] The compound or salt thereof according to [15], wherein the neurodegenerative disease is Alzheimer's disease, mild cognitive impairment, Huntington's disease, Parkinson's disease or multiple sclerosis.
- a method for inhibiting cholesterol 24 hydroxylase in a mammal comprising administering an effective amount of the compound or salt thereof according to any one of [1] to [10] to the mammal.
- a method for preventing or treating epilepsy or a neurodegenerative disease in a mammal comprising administering an effective amount of the compound or salt thereof according to any one of [1] to [10] to the mammal.
- neurodegenerative disease is Alzheimer's disease, mild cognitive impairment, Huntington's disease, Parkinson's disease or multiple sclerosis.
- the use according to [20], wherein the neurodegenerative disease is Alzheimer's disease, mild cognitive impairment, Huntington's disease, Parkinson's disease or multiple sclerosis.
- Compound (I) has an excellent CH24H inhibitory action, and is an epilepsy, neurodegenerative disease (eg, Alzheimer's disease, mild cognitive impairment, Huntington's disease, Parkinson's disease, multiple sclerosis, amyotrophic lateral sclerosis, trauma Cerebral injuries, cerebral infarction, glaucoma, etc.) and schizophrenia.
- neurodegenerative disease eg, Alzheimer's disease, mild cognitive impairment, Huntington's disease, Parkinson's disease, multiple sclerosis, amyotrophic lateral sclerosis, trauma Cerebral injuries, cerebral infarction, glaucoma, etc.
- the “halogen atom” represents a fluorine atom, a chlorine atom, a bromine atom, or an iodine atom.
- the “C 1-10 alkyl group” means, for example, methyl, ethyl, propyl, isopropyl, butyl, 2-methylpropyl, 1-methylpropyl, tert-butyl, pentyl, isopentyl, neopentyl, 1-pentyl Examples thereof include ethylpropyl, hexyl, isohexyl, 1,1-dimethylbutyl, 2,2-dimethylbutyl, 3,3-dimethylbutyl, 2-ethylbutyl, peptyl, octyl, nonyl, decyl and the like.
- C 1-6 alkyl (group) means, for example, methyl, ethyl, propyl, isopropyl, butyl, isobutyl, sec-butyl, tert-butyl, pentyl, isopentyl, neopentyl, 1-ethylpropyl. Hexyl, isohexyl, 1,1-dimethylbutyl, 2,2-dimethylbutyl, 3,3-dimethylbutyl, 2-ethylbutyl and the like.
- C 2-10 alkenyl group means, for example, vinyl, 1-propenyl, 2-propenyl, 2-methyl-1-propenyl, 1-butenyl, 2-butenyl, 3-butenyl, 3- Methyl-2-butenyl, 1-pentenyl, 2-pentenyl, 3-pentenyl, 4-pentenyl, 4-methyl-3-pentenyl, 1-hexenyl, 3-hexenyl, 5-hexenyl, 1-peptenyl, 1-octenyl Etc. Of these, a C 2-6 alkenyl group is preferable.
- C 2-6 alkenyl (group) means, for example, vinyl, 1-propenyl, 2-propenyl, 2-methyl-1-propenyl, 1-butenyl, 2-butenyl, 3-butenyl, 3-methyl-2-butenyl, 1-pentenyl, 2-pentenyl, 3-pentenyl, 4-pentenyl, 4-methyl-3-pentenyl, 1-hexenyl, 3-hexenyl, 5-hexenyl and the like are shown.
- C 2-10 alkynyl group means, for example, ethynyl, 1-propynyl, 2-propynyl, 1-butynyl, 2-butynyl, 3-butynyl, 1-pentynyl, 2-pentynyl, 3-pentyl Pentynyl, 4-pentynyl, 1,1-dimethylprop-2-yn-1-yl, 1-hexynyl, 2-hexynyl, 3-hexynyl, 4-hexynyl, 5-hexynyl, 1-peptynyl, 1-octynyl, etc. Indicates.
- C 2-6 alkynyl group is preferable.
- “C 2-6 alkynyl (group)” means, for example, ethynyl, 1-propynyl, 2-propynyl, 1-butynyl, 2-butynyl, 3-butynyl, 1-pentynyl, 2-pentynyl, 3-pentynyl, 4-pentynyl, 1,1-dimethylprop-2-in-1-yl, 1-hexynyl, 2-hexynyl, 3-hexynyl, 4-hexynyl, 5-hexynyl and the like are shown.
- C 1-6 alkoxy (group) means, for example, methoxy, ethoxy, propoxy, isopropoxy, butoxy, isobutoxy, sec-butoxy, tert-butoxy, pentyloxy, isopentyloxy, hexyloxy Etc.
- C 1-3 alkoxy group refers to methoxy, ethoxy, propoxy and isopropoxy.
- C 2-6 alkenyloxy (group) means, for example, vinyloxy, 1-propenyloxy, 2-propenyloxy, 2-methyl-1-propenyloxy, 1-butenyloxy, 2-butenyloxy, 3-butenyloxy, 3-methyl-2-butenyloxy, 1-pentenyloxy, 2-pentenyloxy, 3-pentenyloxy, 4-pentenyloxy, 4-methyl-3-pentenyloxy, 1-hexenyloxy, 3-hexenyloxy , 5-hexenyloxy and the like.
- C 2-6 alkynyloxy (group) means, for example, ethynyloxy, 1-propynyloxy, 2-propynyloxy, 1-butynyloxy, 2-butynyloxy, 3-butynyloxy, 1-pentynyl Oxy, 2-pentynyloxy, 3-pentynyloxy, 4-pentynyloxy, 1,1-dimethylprop-2-yn-1-yloxy, 1-hexynyloxy, 2-hexynyloxy, 3-hexynyloxy, 4-hexynyloxy , 5-hexynyloxy and the like.
- C 1-6 alkylenedioxy (group) means, for example, methylenedioxy, ethylenedioxy and the like.
- C 1-6 alkoxy-carbonyl (group) means, for example, methoxycarbonyl, ethoxycarbonyl, propoxycarbonyl, isopropoxycarbonyl, butoxycarbonyl, isobutoxycarbonyl, tert-butoxycarbonyl and the like.
- C 1-6 alkyl-carbonyl (group) means, for example, acetyl, propanoyl, butanoyl, 2-methylpropanoyl and the like.
- “mono-C 1-6 alkylamino (group)” means, for example, methylamino, ethylamino, propylamino, isopropylamino, butylamino, isobutylamino, tert-butylamino and the like.
- “di-C 1-6 alkylamino (group)” means, for example, dimethylamino, diethylamino, dipropylamino, diisopropylamino, dibutylamino, diisobutylamino, ditert-butylamino and the like.
- C 3-10 cycloalkyl group means, for example, cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl, cycloheptyl, cyclooctyl, cyclononyl, cyclodecyl and the like. Of these, a C 3-6 cycloalkyl group is preferable.
- C 3-8 cycloalkyl (group) refers to, for example, cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl, cycloheptyl, cyclooctyl and the like.
- C 3-6 cycloalkyl (group) means, for example, a C 3-8 cycloalkyl (group) having 3 to 6 carbon atoms.
- C 3-8 cycloalkyloxy (group) means, for example, cyclopropyloxy, cyclobutyloxy, cyclopentyloxy, cyclohexyloxy, cycloheptyloxy, cyclooctyloxy and the like.
- C 3-6 cycloalkyloxy (group)” means, for example, cyclopropyloxy, cyclobutyloxy, cyclopentyloxy, cyclohexyloxy and the like.
- C 3-10 cycloalkenyl (group) means, for example, cyclopropenyl (eg, 2-cyclopropen-1-yl), cyclobutenyl (eg, 2-cyclobuten-1-yl), cyclo Pentenyl (eg, 2-cyclopenten-1-yl, 3-cyclopenten-1-yl), cyclohexenyl (eg, 1-cyclohexen-1-yl, 2-cyclohexen-1-yl, 3-cyclohexen-1-yl) Cycloheptenyl (eg, 1-cyclopenten-1-yl, 2-cyclohepten-1-yl, 2-cyclohepten-1-yl), cyclooctenyl (eg, 1-cyclohepten-1-yl, 2-cyclohepten-1-yl, 3-cyclohepten-1-yl), cyclononenyl (eg, 1-cyclononen-1-yl, 2-cyclononen-1
- C 3-8 cycloalkenyl group is preferable.
- “C 3-8 cycloalkenyl (group)” means, for example, cyclopropenyl (eg, 2-cyclopropen-1-yl), cyclobutenyl (eg, 2-cyclobuten-1-yl), cyclo Pentenyl (eg, 2-cyclopenten-1-yl, 3-cyclopenten-1-yl), cyclohexenyl (eg, 2-cyclohexen-1-yl, 3-cyclohexen-1-yl) and the like are shown.
- C 3-8 cycloalkenyloxy (group) means, for example, cyclopropenyloxy (eg, 2-cyclopropen-1-yloxy), cyclobutenyloxy (eg, 2-cyclobutene-1) -Yloxy), cyclopentenyloxy (eg, 2-cyclopenten-1-yloxy, 3-cyclopenten-1-yloxy), cyclohexenyloxy (eg, 2-cyclohexen-1-yloxy, 3-cyclohexen-1-yloxy), etc. Indicates.
- cyclopropenyloxy eg, 2-cyclopropen-1-yloxy
- cyclobutenyloxy eg, 2-cyclobutene-1) -Yloxy
- cyclopentenyloxy eg, 2-cyclopenten-1-yloxy, 3-cyclopenten-1-yloxy
- cyclohexenyloxy eg, 2-cyclohexen-1-yloxy, 3-cycl
- C 4-10 cycloalkadienyl group means, for example, 1,3-cyclobutadiene-1-yl, 1,3-cyclopentadien-1-yl, 1,4-cyclopentadiene- 1-yl, 2,4-cyclopentadien-1-yl, 1,3-cyclohexadien-1-yl, 1,4-cyclohexadien-1-yl, 1,5-cyclohexadien-1-yl, 2, 4-cyclohexadien-1-yl, 2,5-cyclohexadien-1-yl, 1,3-cyclooctadien-1-yl, 1,4-cyclooctadien-1-yl, 1,5-cycloocta Dien-1-yl, 1,6-cyclooctadien-1-yl, 1,7-cyclooctadien-1-yl, 2,4-cyclooctadien-1-yl, 2,5-cyclo
- C 4-6 cycloalkadienyl group means, for example, 1,3-cyclobutadiene-1-yl, 1,3-cyclopentadien-1-yl, 1,4-cyclopentadiene- 1-yl, 2,4-cyclopentadien-1-yl, 1,3-cyclohexadien-1-yl, 1,4-cyclohexadien-1-yl, 1,5-cyclohexadien-1-yl, 2, 4-cyclohexadien-1-yl, 2,5-cyclohexadien-1-yl and the like are shown.
- the above C 3-10 cycloalkyl group, C 3-10 cycloalkenyl group and C 4-10 cycloalkadienyl group may each be condensed with a benzene ring to form a condensed ring group.
- Examples of the condensed ring group include indanyl, dihydronaphthyl, tetrahydronaphthyl, fluorenyl and the like.
- the C 3-10 cycloalkyl group, the C 3-10 cycloalkenyl group and the C 4-10 cycloalkadienyl group may be a C 7-10 bridged hydrocarbon group.
- Examples of the C 7-10 bridged hydrocarbon group include bicyclo [2.2.1] heptyl (norbornyl), bicyclo [2.2.2] octyl, bicyclo [3.2.1] octyl, bicyclo [3. 2.2] nonyl, bicyclo [3.3.1] nonyl, bicyclo [4.2.1] nonyl, bicyclo [4.3.1] decyl, adamantyl and the like.
- C 3-10 cycloalkyl group, C 3-10 cycloalkenyl group and C 4-10 cycloalkadienyl group are respectively C 3-10 cycloalkane, C 3-10 cycloalkene or C 4-10.
- a cycloalkadiene may form a spiro ring group.
- C 3-10 cycloalkane, C 3-10 cycloalkene and C 4-10 cycloalkadiene the above C 3-10 cycloalkyl group, C 3-10 cycloalkenyl group and C 4-10 cycloalkane are mentioned. Examples include rings corresponding to alkadienyl groups. Examples of such a spiro ring group include spiro [4.5] decan-8-yl.
- C 6-14 aryl (group) means, for example, phenyl, 1-naphthyl, 2-naphthyl and the like.
- C 6-14 aryloxy (group) means, for example, phenoxy, 1-naphthyloxy, 2-naphthyloxy and the like.
- C 7-14 aralkyl (group) means, for example, benzyl, phenethyl and the like.
- C 7-14 aralkyloxy (group)” means, for example, benzyloxy, phenethyloxy and the like.
- C 8-13 arylalkenyl (group)” means, for example, styryl and the like.
- the “hydrocarbon group” means, for example, a C 1-10 alkyl group, a C 2-10 alkenyl group, a C 2-10 alkynyl group, a C 3-10 cycloalkyl group, a C 3-10 cycloalkenyl group.
- the “heterocyclic group” refers to an aromatic heterocyclic group or a non-aromatic heterocyclic group.
- the “aromatic heterocyclic group” refers to a monocyclic aromatic heterocyclic group or a condensed aromatic heterocyclic group. For example, it represents a 5- to 12-membered aromatic heterocyclic group, specifically a 5- to 7-membered monocyclic aromatic heterocyclic group or an 8- to 12-membered condensed aromatic heterocyclic group.
- examples of the “monocyclic aromatic heterocyclic group” include, for example, oxygen atoms, sulfur atoms (which may be oxidized) and nitrogen atoms (which may be oxidized) as ring-constituting atoms in addition to carbon atoms.
- examples of the “fused aromatic heterocyclic group” include an 8- to 12-membered condensed aromatic heterocyclic group, specifically, the 5- to 7-membered monocyclic aromatic heterocyclic group.
- non-aromatic heterocyclic group refers to a monocyclic non-aromatic heterocyclic group or a condensed non-aromatic heterocyclic group.
- it represents a 3- to 12-membered non-aromatic heterocyclic group, specifically, a 3- to 8-membered monocyclic non-aromatic heterocyclic group or an 8- to 12-membered condensed non-aromatic heterocyclic group.
- examples of the “monocyclic non-aromatic heterocyclic group” include, for example, oxygen atoms, sulfur atoms (which may be oxidized) and nitrogen atoms (which are oxidized) as ring-constituting atoms in addition to carbon atoms.
- the “fused non-aromatic heterocyclic group” is, for example, an 8- to 12-membered condensed non-aromatic heterocyclic group, specifically, the above-mentioned 3- to 8-membered monocyclic non-aromatic heterocyclic group.
- non-aromatic heterocyclic group and “fused non-aromatic heterocyclic group” may be bridged, and examples of such a group include 3-oxa-6-azabicyclo [3.1.1]. ] Heptyl, 8-oxa-3-azabicyclo [3.2.1] octyl, 2-oxa-5-azabicyclo [2.2.1] heptyl, 3-oxa-8-azabicyclo [3.2.1] Octyl, 6-oxa-3-azabicyclo [3.1.1] heptyl and the like.
- the “carbocyclic group” refers to a C 6-14 aryl group, a C 3-10 cycloalkyl group, a C 3-10 cycloalkenyl group, or a C 4-10 cycloalkadienyl group.
- the “carbocyclic group” may be condensed with a C 6-14 aromatic hydrocarbon, C 3-10 cycloalkane, C 3-10 cycloalkene or C 4-10 cycloalkadiene, and C 3 A spiro ring may be formed with -10 cycloalkane, C 3-10 cycloalkene or C 4-10 cycloalkadiene, and may be bridged.
- C 6-14 aromatic hydrocarbon refers to, for example, benzene and naphthalene.
- C 3-10 cycloalkane means, for example, cyclopropane, cyclobutane, cyclopentane, cyclohexane, cycloheptane, cyclooctane, cyclononane, cyclodecane and the like.
- C 3-10 cycloalkene refers to, for example, cyclopropene, cyclobutene, cyclopentene, cyclohexene, cyclooctene, cyclononene, cyclodecene and the like.
- C 4-10 cycloalkadiene means, for example, 1,3-cyclobutadiene, 1,3-cyclopentadiene, 1,4-cyclopentadiene, 2,4-cyclopentadiene, 1,3 -Cyclohexadiene, 1,4-cyclohexadiene, 1,5-cyclohexadiene, 2,4-cyclohexadiene, 2,5-cyclohexadiene, 1,3-cyclooctadiene, 1,4-cyclooctadiene, 1, 5-cyclooctadiene, 1,6-cyclooctadiene, 1,7-cyclooctadiene, 2,4-cyclooctadiene, 2,5-cyclooctadiene, 2,6-cyclooctadiene, 2,7- And cyclooctadiene, 3,5-cyclooctadiene, 3,6-cyclooctadiene and the like.
- R 1 in formula (I) is an optionally substituted C 1-6 alkyl group, an optionally substituted hydroxy group, an optionally substituted amino group, an optionally substituted carbocyclic group, Or represents an optionally substituted heterocyclic group, or R 1 is bonded to an atom on ring A, and together with ring A, each is substituted with an oxo group, and may be further substituted. Spiro rings or condensed rings may be formed.
- the “C 1-6 alkyl group” of the “ optionally substituted C 1-6 alkyl group” represented by R 1 is 1 to 5 (preferably 1 to 3) substituents at substitutable positions. You may have. Examples of such a substituent include a substituent selected from the following substituent group A. When a plurality of substituents are present, each substituent may be the same or different.
- Substituent group A (1) a halogen atom; (2) a cyano group; (3) a nitro group; (4) hydroxy group; (5) (a) a halogen atom, (b) a cyano group, (c) a C 1-6 alkyl group optionally substituted with 1 to 3 halogen atoms, And (d) a C 3-8 cycloalkyl group optionally substituted with 1 to 3 substituents selected from C 1-6 alkoxy groups optionally substituted with 1 to 3 halogen atoms; (6) (a) a halogen atom, (b) a cyano group, (c) a C 1-6 alkyl group optionally substituted with 1 to 3 halogen atoms, and (d) a C 1-6 alkoxy group optionally substituted with 1 to 3 halogen atoms.
- 5- or 6-membered monocyclic aromatic heterocyclic group which may be substituted by 1 to 3 substituents such as furyl, thienyl, pyrrolyl, oxazolyl, isoxazolyl, thiazolyl, isothiazolyl, imidazolyl, pyridyl, pyrazolyl Morpholinyl); (62) (a) a halogen atom, (b) a C 1-6 alkyl group optionally substituted with 1 to 3 halogen atoms, and (c) a C 1-6 alkoxy group optionally substituted with 1 to 3 halogen atoms.
- fused non-aromatic heterocyclic groups eg, dihydrobenzofuranyl
- 6-membered monocyclic aromatic heterocyclic oxy groups eg furyloxy, thienyloxy, pyrrolyloxy, oxazolyloxy, isoxazolyloxy, thiazolyloxy, isothiazolyloxy, imidazolyloxy, pyridyl) Oxy, pyrazolyloxy
- 8- to 12-membered condensed aromatic heterocyclic oxy groups eg, benzofuranyloxy, isobenzofuranyloxy, benzothienyloxy, isobenzothienyloxy, indolyloxy, isoindolyloxy, indazolyl) Oxy, benzimidazolyloxy, benzoxazolyloxy
- 3- to 8-membered monocyclic non-aromatic heterocyclic oxy groups eg, oxiranyloxy
- Examples of the “optionally substituted hydroxy group” represented by R 1 include, for example, a C 1-10 alkyl group, a C 2-10 alkenyl group, a C 3-10 cycloalkyl group, each of which may be substituted, A C 3-10 cycloalkenyl group, a C 6-14 aryl group, a C 7-14 aralkyl group, a C 8-13 arylalkenyl group, a C 1-6 alkyl-carbonyl group, a heterocyclic group (eg, an aromatic heterocyclic group) And a hydroxy group which may be substituted with a substituent selected from a non-aromatic heterocyclic group) and the like.
- a C 1-10 alkyl group a C 2-10 alkenyl group
- a C 3-10 cycloalkyl group each of which may be substituted
- a C 3-10 cycloalkenyl group a C 6-14 aryl group, a C 7-14 aralkyl group
- the C 1-10 alkyl group, the C 2-10 alkenyl group, and the C 1-6 alkyl-carbonyl group have 1 to 5 (preferably 1 to 3) substituents at substitutable positions. It may be.
- substituents include a substituent selected from the above substituent group A.
- each substituent may be the same or different.
- the C 3-10 cycloalkyl group, the C 3-10 cycloalkenyl group and the non-aromatic heterocyclic group have 1 to 5 (preferably 1 to 3) substituents at substitutable positions. May be.
- substituents include a substituent selected from the following substituent group B. When a plurality of substituents are present, each substituent may be the same or different.
- Substituent group B (1) the above substituent group A; (2) (a) a halogen atom, (b) a cyano group, (c) a hydroxy group, (d) (i) a halogen atom, (ii) a cyano group; and (iii) a C 3-optionally substituted C 3 -3 selected from a C 1-6 alkyl group optionally substituted with 1 to 3 halogen atoms.
- aryl groups (f) a C 1-6 alkoxy group optionally substituted with 1 to 3 halogen atoms, (g) an amino group optionally mono- or di-substituted with a C 1-6 alkyl group, (h) a 5- or 6-membered monocyclic aromatic heterocyclic group, (i) an 8- to 12-membered fused aromatic heterocyclic group, (j) a 3- to 8-membered monocyclic non-aromatic heterocyclic group, (k) an 8- to 12-membered fused non-aromatic heterocyclic group, (l) a carboxy group, and (m) an optionally substituted C 1-6 alkoxy-carbonyl group optionally substituted with 1 to 3 halogen atoms.
- 1-6 alkyl groups (3) (a) a halogen atom, (b) a hydroxy group, (c) a C 1-6 alkoxy group, (d) an amino group optionally mono- or disubstituted with a C 1-6 alkyl group, (e) a carboxy group, and (f) a C 2-6 alkenyl group optionally substituted with 1 to 3 substituents selected from a C 1-6 alkoxy-carbonyl group; (4) (a) a halogen atom, (b) a hydroxy group, (c) a C 1-6 alkoxy group, and (d) a substituent substituted with 1 to 3 substituents selected from a C 1-6 alkyl group optionally substituted with 1 to 3 halogen atoms.
- the C 6-14 aryl group, the C 7-14 aralkyl group, the C 8-13 arylalkenyl group and the aromatic heterocyclic group may be substituted with 1 to 5 (preferably 1 to 3) substituted positions. It may have a group.
- substituents include a substituent selected from the above-mentioned substituent group B except oxo. When a plurality of substituents are present, each substituent may be the same or different.
- the “amino group” of the “optionally substituted amino group” represented by R 1 is, for example, a C 1-10 alkyl group, a C 2-10 alkenyl group, a C 3-10 which may each be substituted. Cycloalkyl group, C 3-10 cycloalkenyl group, C 6-14 aryl group, C 7-14 aralkyl group, C 8-13 arylalkenyl group, heterocyclic group (eg, aromatic heterocyclic group, non-aromatic heterocyclic group) And an amino group which may be mono- or di-substituted with a substituent selected from an acyl group. In the case of disubstitution, the two substituents may be combined to form a heterocyclic group which may be substituted.
- the C 1-10 alkyl group and the C 2-10 alkenyl group may have 1 to 5 (preferably 1 to 3) substituents at substitutable positions.
- substituents include a substituent selected from the above substituent group A.
- each substituent may be the same or different.
- the C 3-10 cycloalkyl group, the C 3-10 cycloalkenyl group and the non-aromatic heterocyclic group have 1 to 5 (preferably 1 to 3) substituents at substitutable positions. May be.
- substituents include a substituent selected from the above substituent group B. When a plurality of substituents are present, each substituent may be the same or different.
- the C 6-14 aryl group, the C 7-14 aralkyl group, the C 8-13 arylalkenyl group and the aromatic heterocyclic group may be substituted with 1 to 5 (preferably 1 to 3) substituted positions. It may have a group.
- substituents include a substituent selected from the above-mentioned substituent group B except oxo. When a plurality of substituents are present, each substituent may be the same or different.
- acyl group exemplified as the substituent of the “amino group” include, for example, the formula: —COR A , —CO—OR A , —SO 3 R A , —S (O) 2 R A , —SOR A , -CO-NR A 'R B ', -CS-NR A 'R B ', -S (O) 2 NR A 'R B ' [wherein R A is a hydrogen atom, optionally substituted carbon A hydrogen group or an optionally substituted heterocyclic group is shown.
- R A ′ and R B ′ are the same or different and each represents a hydrogen atom, an optionally substituted hydrocarbon group, or an optionally substituted heterocyclic group, or R A ′ and R B ′ are A nitrogen-containing heterocyclic ring which may be substituted with an adjacent nitrogen atom may be formed], and the like.
- Examples of the “hydrocarbon group” in the “optionally substituted hydrocarbon group” represented by R A , R A ′ or R B ′ include, for example, a C 1-10 alkyl group, a C 2-10 alkenyl group, C 2-10 alkynyl group, C 3-10 cycloalkyl group, C 3-10 cycloalkenyl group, C 4-10 cycloalkadienyl group, C 6-14 aryl group, C 7-14 aralkyl group, C 8-13 An arylalkenyl group etc. are mentioned.
- the C 1-10 alkyl group, C 2-10 alkenyl group and C 2-10 alkynyl group exemplified as the “hydrocarbon group” are substituted with 1 to 5 (preferably 1 to 3) substituted positions. It may have a group. Examples of such a substituent include a substituent selected from the above substituent group A. When a plurality of substituents are present, each substituent may be the same or different.
- the C 3-10 cycloalkyl group, the C 3-10 cycloalkenyl group, and the C 4-10 cycloalkadienyl group exemplified as the “hydrocarbon group” may be substituted at 1 to 5 positions (preferably May have 1 to 3 substituents.
- substituents include a substituent selected from the above substituent group B. When a plurality of substituents are present, each substituent may be the same or different.
- the C 6-14 aryl group, C 7-14 aralkyl group, and C 8-13 arylalkenyl group exemplified as the “hydrocarbon group” are 1 to 5 (preferably 1 to 3) at substitutable positions. May be substituted.
- Examples of such a substituent include a substituent selected from the above-mentioned Substituent group B excluding an oxo group. When a plurality of substituents are present, each substituent may be the same or different.
- heterocyclic group of the “optionally substituted heterocyclic group” represented by R A , R A ′ or R B ′ is 1 to 5 (preferably 1 to 3) at substitutable positions. It may have a substituent.
- examples of such a substituent include the above substituent group B excluding an oxo group, and in the case of a non-aromatic heterocyclic group, for example, the above substituent group B. .
- each substituent may be the same or different.
- the “nitrogen-containing heterocycle” in the “optionally substituted nitrogen-containing heterocycle” formed by R A ′ and R B ′ together with the adjacent nitrogen atom includes, for example, at least one ring-constituting atom other than a carbon atom And a 5- to 7-membered nitrogen-containing heterocyclic ring which may contain 1 to 2 heteroatoms selected from oxygen, sulfur and nitrogen atoms.
- the nitrogen-containing heterocycle include pyrrolidine, imidazolidine, pyrazolidine, piperidine, piperazine, morpholine, thiomorpholine and the like.
- the nitrogen-containing heterocycle may have 1 to 5 (preferably 1 to 3) substituents at substitutable positions.
- substituents include a substituent selected from the above substituent group B.
- each substituent may be the same or different.
- acyl group (1) formyl group; (2) a carboxy group; (3) a C 1-6 alkyl-carbonyl group (eg acetyl) optionally substituted by 1 to 3 halogen atoms; (4) a C 1-6 alkoxy-carbonyl group (eg, methoxycarbonyl, ethoxycarbonyl, propoxycarbonyl, tert-butoxycarbonyl) optionally substituted by 1 to 3 halogen atoms; (5) C 3-10 cycloalkyl-carbonyl group (eg, cyclopropylcarbonyl, cyclopentylcarbonyl, cyclohexylcarbonyl); (6) a C 6-14 aryl-carbonyl group (eg, benzoyl, 1-naphthoyl, 2-naphthoyl) optionally substituted with 1 to 3 halogen atoms; (7) (a) a C 1-6 alkyl group which may be substituted with 1 to 3
- the “carbocyclic group” of the “optionally substituted carbocyclic group” represented by R 1 may have 1 to 5 (preferably 1 to 3) substituents at substitutable positions. Good.
- substituents include, in the case of a C 6-14 aryl group, the above substituent group B excluding an oxo group, including a C 3-10 cycloalkyl group, a C 3-10 cycloalkenyl group, and a C 4
- the above substituent group B can be mentioned.
- each substituent may be the same or different.
- heterocyclic group of the “optionally substituted heterocyclic group” represented by R 1 may have 1 to 5 (preferably 1 to 3) substituents at substitutable positions. Good.
- substituents include the above substituent group B excluding an oxo group, and in the case of a non-aromatic heterocyclic group, for example, the above substituent group B. .
- each substituent may be the same or different.
- a “spiro ring or condensed ring” of “a spiro ring or a condensed ring each substituted with an oxo group and further substituted,” which R 1 combines with an atom on ring A to form with ring A Is a spiro ring such as 2,8-diazaspiro [4.5] decane, 2,7-diazaspiro [3.5] nonane, hexahydroimidazo [1,5-a] pyrazine, hexahydropyrrolo [1,2- a] A condensed ring such as pyrazine.
- the “spiro ring or condensed ring” of “a spiro ring or a condensed ring each substituted with an oxo group and optionally further substituted” that R 1 combines with an atom on ring A to form with ring A is , It may have 1 to 5 (preferably 1 to 3) substituents at substitutable positions.
- the said substituent group B is mentioned, for example.
- each substituent may be the same or different.
- R 1 is preferably optionally substituted C 1-6 alkyl group, optionally substituted C 1-6 alkoxy group, an optionally substituted amino group, optionally C 3 substituted An -8 cycloalkyl group, an optionally substituted C 6-14 aryl group, or an optionally substituted non-aromatic heterocyclic group, or R 1 is bonded to an atom on ring A; Together with ring A, it forms a spiro ring that is substituted with oxo and optionally further substituted.
- R 1 is more preferably (1) (a) a cyano group, (b) a C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 C 1-6 alkoxy groups (eg, methoxy), (c) a C 6-14 aryloxy group (eg, phenoxy), (d) a C 3-8 cycloalkyl group (eg, cyclopropyl), (e) a 5- or 6-membered monocyclic aromatic heterocyclic group (eg, pyrazolyl), (f) an 8- to 12-membered fused aromatic heterocyclic group (eg, indazolyl), and (g) a 3- to 8-membered monocyclic non-aromatic heterocycle optionally substituted with 1 to 3 oxo groups Ring group (eg, dihydropyridyl) A C 1-6 alkyl group (eg, methyl, ethyl) optionally substituted with 1 to 3 substituents selected from: (2) a
- R 1 is bonded to an atom on ring A and is substituted with ring A together with oxo and further substituted with 1 to 3 C 1-6 alkyl groups (eg methyl).
- C 1-6 alkyl groups eg methyl.
- R 1 is more preferably (1) (a) a cyano group, (b) a C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 C 1-6 alkoxy groups (eg, methoxy), (c) a C 6-14 aryloxy group (eg, phenoxy), (d) a C 3-8 cycloalkyl group (eg, cyclopropyl), (e) a 5- or 6-membered monocyclic aromatic heterocyclic group (eg, pyrazolyl), (f) an 8- to 12-membered fused aromatic heterocyclic group (eg, indazolyl), and (g) a 3- to 8-membered monocyclic non-aromatic heterocycle optionally substituted with 1 to 3 oxo groups Ring group (eg, dihydropyridyl) A C 1-6 alkyl group (eg, methyl, ethyl) optionally substituted with 1 to 3 substituents selected from:
- R 1 is bonded to an atom on ring A and is substituted with ring A together with oxo and further substituted with 1 to 3 C 1-6 alkyl groups (eg methyl).
- C 1-6 alkyl groups eg methyl
- R 1 is more preferably (1) (a) a C 3-8 cycloalkyl group (eg, cyclopropyl), and (b) an 8- to 12-membered fused aromatic heterocyclic group (eg, indazolyl)
- a C 1-6 alkyl group eg, methyl, ethyl
- R 1 optionally substituted with 1 to 3 substituents selected from: (2) a C 1-6 alkoxy group (preferably a C 1-3 alkoxy group (eg, methoxy)) optionally substituted by 1 to 3 C 6-14 aryl groups (eg, phenyl), (3) (a) (i) a halogen atom (eg, fluorine atom), (ii) a C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 halogen atoms (eg, fluorine atom), (iii) a 5- or 6-membered monocyclic aromatic heterocyclic group (eg, pyri
- R 1 is preferably, optionally substituted C 1-6 alkyl group, optionally substituted C 1-6 alkoxy group, an optionally substituted amino group, substituted An optionally substituted C 3-8 cycloalkyl group, an optionally substituted C 6-14 aryl group, or an optionally substituted non-aromatic heterocyclic group.
- R 1 is more preferably (1) (a) a cyano group, (b) a C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 C 1-6 alkoxy groups (eg, methoxy), (c) a C 6-14 aryloxy group (eg, phenoxy), (d) a C 3-8 cycloalkyl group (eg, cyclopropyl), (e) a 5- or 6-membered monocyclic aromatic heterocyclic group (eg, pyrazolyl), (f) an 8- to 12-membered fused aromatic heterocyclic group (eg, indazolyl), and (g) a 3- to 8-membered monocyclic non-aromatic heterocycle optionally substituted with 1 to 3 oxo groups Ring group (eg, dihydropyridyl) A C 1-6 alkyl group (eg, methyl, ethyl) optionally substituted with 1 to 3 substituents selected from: (2) a
- R 1 is more preferably (a) a halogen atom (eg, fluorine atom), (b) a cyano group, (c) a carbamoyl group, (d) a C 1-6 alkyl group (eg, methyl) optionally substituted with 1 to 3 C 1-6 alkoxy groups (eg, methoxy), and (e) C 1-6 alkoxy group (eg, methoxy)
- a 3- to 8-membered monocyclic non-aromatic heterocyclic group eg, pyrrolidinyl which may be substituted with 1 to 5 substituents selected from
- R 1 is still more preferably (a) a halogen atom (eg, fluorine atom), (b) a cyano group, (c) a carbamoyl group, and (d) a C 1-6 alkyl group (eg, methyl) optionally substituted by 1 to 3 C 1-6 alkoxy groups (eg, methoxy)
- a 3- to 8-membered monocyclic non-aromatic heterocyclic group eg, pyrrolidinyl which may be substituted with 1 to 5 (preferably 1 to 3) substituents selected from
- R 1 is more preferably (1) (a) (i) a halogen atom (eg, fluorine atom), and (ii) a C 6-14 aryl group (eg, optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom)) , Phenyl) A C 1-6 alkyl group (eg, methyl, ethyl) optionally substituted with 1 to 3 substituents selected from: (b) a 3- to 8-membered monocyclic non-aromatic heterocyclic group ( Eg, tetrahydropyranyl, tetrahydrofuryl) An amino group optionally mono- or di-substituted with a substituent selected from (2) (a) a halogen atom (eg, fluorine atom), (b) a cyano group, (c) a carbamoyl group, (d) C 1-6 alkyl group (eg, methyl), and (e) C 1-6
- R 1 is still more preferably (1) (a) (i) a halogen atom (eg, fluorine atom), and (ii) a C 6-14 aryl group (eg, optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom)) , Phenyl) A C 1-6 alkyl group (eg, methyl, ethyl) optionally substituted with 1 to 3 substituents selected from: (b) a 3- to 8-membered monocyclic non-aromatic heterocyclic group ( Eg, tetrahydropyranyl, tetrahydrofuryl) An amino group optionally mono- or di-substituted with a substituent selected from (2) (a) a halogen atom (eg, fluorine atom), and (b) a 3- to 8-membered monocyclic non-aromatic group optionally substituted with 1 to 5 substituents selected from a cyano group A heterocyclic group (e
- R 1 is particularly preferably (1) (a) (i) a halogen atom (eg, fluorine atom), and (ii) a C 6-14 aryl group (eg, optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom)) , Phenyl) A C 1-6 alkyl group (eg, methyl, ethyl) optionally substituted with 1 to 3 substituents selected from: (b) a 3- to 8-membered monocyclic non-aromatic heterocyclic group ( Eg, tetrahydropyranyl, tetrahydrofuryl) An amino group optionally mono- or di-substituted with a substituent selected from (2) A 3- to 8-membered monocyclic non-aromatic heterocyclic group (eg, azetidinyl, pyrrolidinyl) which may be substituted with 1 to 3 halogen atoms (eg, fluorine atom).
- R 1 is more preferably (a) a halogen atom (eg, fluorine atom), (b) a cyano group, (c) a carbamoyl group, (d) a C 1-6 alkyl group (eg, methyl), and (e) C 1-6 alkoxy group (eg, methoxy)
- a 3- to 8-membered monocyclic non-aromatic heterocyclic group eg, pyrrolidinyl which may be substituted with 1 to 5 substituents selected from
- R 1 is still more preferably (a) a halogen atom (eg, a fluorine atom), and (b) a 3- to 8-membered monocyclic non-aromatic heterocyclic group (eg, pyrrolidinyl) optionally substituted with 1 to 5 substituents selected from a cyano group.
- a halogen atom eg, a fluorine atom
- a 3- to 8-membered monocyclic non-aromatic heterocyclic group eg, pyrrolidinyl
- R 2 in the formula (I) represents an optionally substituted C 6-14 aryl group or an optionally substituted aromatic heterocyclic group.
- the “C 6-14 aryl group” of the “ optionally substituted C 6-14 aryl group” represented by R 2 is 1 to 5 (preferably 1 to 3) substituents at substitutable positions. You may have. Examples of such a substituent include the above substituent group B excluding an oxo group. When a plurality of substituents are present, each substituent may be the same or different.
- R 2 is preferably (1) (a) a halogen atom (eg, fluorine atom, chlorine atom), and (b) a C 1-6 alkyl group (eg, optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom)) , Methyl) A C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 substituents selected from: or (2) (a) halogen atoms (eg, chlorine atoms, bromine atoms), (b) a cyano group, (c) a C 1-6 alkyl group (eg, methyl, ethyl) optionally substituted with 1 to 3 halogen atoms (eg, fluorine atom), and (d) a C 3-8 cycloalkyl group (eg, , Cyclopropyl) A 5- to 12-membered aromatic heterocyclic group (preferably a 5- or 6-membered monocyclic aromatic heterocyclic group (
- R 2 is more preferably (1) (a) a halogen atom (eg, fluorine atom, chlorine atom), and (b) a C 1-6 alkyl group (eg, optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom)) , Methyl) A C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 substituents selected from: or (2) (a) a halogen atom (eg, chlorine atom), and (b) a C 1-6 alkyl group (eg, methyl) 5- or 6-membered monocyclic aromatic heterocyclic group optionally substituted by 1 to 3 substituents selected from (eg, pyrazolyl, thiadiazolyl, pyridyl) It is.
- a halogen atom eg, fluorine atom, chlorine atom
- a C 1-6 alkyl group eg, optionally substituted by 1 to 3 halogen
- R 2 is more preferably (1) (a) a halogen atom (eg, fluorine atom), and (b) a C 1-6 alkyl group (eg, methyl) A C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 substituents selected from: or (2) (a) halogen atoms (eg, chlorine atoms, bromine atoms), (b) a cyano group, (c) a C 1-6 alkyl group (eg, methyl) optionally substituted with 1 to 3 halogen atoms (eg, fluorine atom), and (d) a C 3-8 cycloalkyl group (eg, cyclo Propyl) A 5- to 12-membered aromatic heterocyclic group (preferably a 5- or 6-membered monocyclic aromatic heterocyclic group (eg, pyrazolyl, Oxazolyl, thiazolyl, thiadiazolyl, pyridyl), 8-
- R 2 is more preferably (a) a halogen atom (eg, a chlorine atom), and (b) C 1-6 alkyl group (eg, methyl) 5- or 6-membered monocyclic aromatic heterocyclic group (eg, pyrazolyl, thiazolyl, thiadiazolyl, pyridyl (preferably pyrazolyl, thiadiazolyl, Preferably, pyrazolyl)).
- a halogen atom eg, a chlorine atom
- C 1-6 alkyl group eg, methyl
- 5- or 6-membered monocyclic aromatic heterocyclic group eg, pyrazolyl, thiazolyl, thiadiazolyl, pyridyl (preferably pyrazolyl, thiadiazolyl, Preferably, pyrazolyl)
- R 2 is more preferably (1) a C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 halogen atoms (eg, fluorine atom), or (2) (a) halogen atoms (eg, chlorine atoms, bromine atoms), (b) a C 1-6 alkyl group (eg, methyl), and (c) a C 3-8 cycloalkyl group (eg, cyclopropyl).
- halogen atoms eg, chlorine atoms, bromine atom
- a C 1-6 alkyl group eg, methyl
- C 3-8 cycloalkyl group eg, cyclopropyl
- a 5- or 6-membered monocyclic aromatic heterocyclic group eg, pyrazolyl, thiazolyl, thiadiazolyl (preferably pyrazolyl, thiazolyl)
- pyrazolyl, thiazolyl, thiadiazolyl preferably pyrazolyl, thiazolyl
- X 1 in formula (I) represents a carbon atom or a nitrogen atom.
- X 1 is preferably a carbon atom.
- R 3 in formula (I) represents a hydrogen atom or a substituent when X 1 is a carbon atom, and is absent when X 1 is a nitrogen atom.
- an optionally substituted hydrocarbon group an optionally substituted heterocyclic group, an optionally substituted hydroxy group, an optionally substituted sulfanyl group, It means an optionally substituted amino group, acyl group, nitro group, cyano group or halogen atom.
- the C 1-10 alkyl group, C 2-10 alkenyl group and C 2-10 alkynyl group exemplified as the “hydrocarbon group” are substituted with 1 to 5 (preferably 1 to 3) substituted positions. It may have a group. Examples of such a substituent include a substituent selected from the above substituent group A. When a plurality of substituents are present, each substituent may be the same or different.
- the C 3-10 cycloalkyl group, the C 3-10 cycloalkenyl group, and the C 4-10 cycloalkadienyl group exemplified as the “hydrocarbon group” may be substituted at 1 to 5 positions at substitutable positions ( It preferably has 1 to 3 substituents. Examples of such a substituent include a substituent selected from the above substituent group B. When a plurality of substituents are present, each substituent may be the same or different.
- the C 6-14 aryl group, C 7-14 aralkyl group, and C 8-13 arylalkenyl group exemplified as the “hydrocarbon group” are 1 to 5 (preferably 1 to 3) at substitutable positions. May be substituted.
- Examples of such a substituent include a substituent selected from the above-mentioned Substituent group B excluding an oxo group. When a plurality of substituents are present, each substituent may be the same or different.
- Examples of the “optionally substituted heterocyclic group” exemplified as the “substituent” represented by R 3 include the same as the “optionally substituted heterocyclic group” represented by R 1. .
- Examples of the “optionally substituted hydroxy group” exemplified as the “substituent” represented by R 3 include the same as the “optionally substituted hydroxy group” represented by R 1 .
- Examples of the “optionally substituted sulfanyl group” exemplified as the “substituent” represented by R 3 include, for example, a C 1-10 alkyl group, a C 2-10 alkenyl group, each of which may be substituted, C 3-10 cycloalkyl group, C 3-10 cycloalkenyl group, C 6-14 aryl group, C 7-14 aralkyl group, C 8-13 arylalkenyl group, C 1-6 alkyl-carbonyl group, heterocyclic group Examples thereof include a sulfanyl group which may be substituted with a substituent selected from (eg, aromatic heterocyclic group, non-aromatic heterocyclic group) and the like.
- the C 1-10 alkyl group, the C 2-10 alkenyl group, and the C 1-6 alkyl-carbonyl group have 1 to 5 (preferably 1 to 3) substituents at substitutable positions. It may be.
- substituents include a substituent selected from the above substituent group A.
- each substituent may be the same or different.
- the C 3-10 cycloalkyl group, the C 3-10 cycloalkenyl group and the non-aromatic heterocyclic group have 1 to 5 (preferably 1 to 3) substituents at substitutable positions. May be.
- substituents include a substituent selected from the above substituent group B. When a plurality of substituents are present, each substituent may be the same or different.
- the C 6-14 aryl group, the C 7-14 aralkyl group, the C 8-13 arylalkenyl group and the aromatic heterocyclic group may be substituted with 1 to 5 (preferably 1 to 3) substituted positions. It may have a group.
- substituents include a substituent selected from the above-mentioned substituent group B except oxo. When a plurality of substituents are present, each substituent may be the same or different.
- Examples of the “optionally substituted amino group” exemplified as the “substituent” represented by R 3 include the same as the “optionally substituted amino group” represented by R 1 .
- acyl group exemplified as the “substituent” represented by R 3
- the “acyl group” exemplified as the “substituent” represented by R 1 is exemplified as the substituent of the “optionally substituted amino group”. The same thing as “acyl group” is mentioned.
- R 3 is preferably (1) a hydrogen atom, or (2) Halogen atoms (eg, fluorine atoms) It is.
- R 3 is more preferably a hydrogen atom.
- Ring A in formula (I) may be further substituted and each may be bridged.
- Examples thereof include 8-azabicyclo [3.2.1] octane, 2,5-diazabicyclo [2.2.1] heptane, 3-azabicyclo [3.1.0] hexane, and preferably 8- Azabicyclo [3.2.1] octane and 2,5-diazabicyclo [2.2.1] heptane.
- Each ring A may be cross-linked
- Each ring A may be cross-linked
- each substituent may be the same or different.
- Ring A is preferably (a) a halogen atom (eg, fluorine atom), (b) a C 1-6 alkyl group (eg, methyl), and (c) may be further substituted with 1 to 5 (preferably 1 to 3) substituents selected from oxo groups, and each may be bridged;
- a halogen atom eg, fluorine atom
- a C 1-6 alkyl group eg, methyl
- substituents selected from oxo groups and each may be bridged;
- Ring A is more preferably (1) (a) a halogen atom (eg, fluorine atom), (b) a C 1-6 alkyl group (eg, methyl), and (c) 1 to 3 substituents selected from an oxo group, each of which may be further substituted.
- a halogen atom eg, fluorine atom
- a C 1-6 alkyl group eg, methyl
- substituents selected from an oxo group each of which may be further substituted.
- Ring A is more preferably (1) (a) a halogen atom (eg, fluorine atom), and (b) a C 1-6 alkyl group (eg, methyl) Each of which may be further substituted with 1 to 3 substituents selected from:
- Ring A is still more preferably
- Ring A is particularly preferably
- R 1 is optionally substituted C 1-6 alkyl group, optionally substituted C 1-6 alkoxy group, an optionally substituted amino group, optionally C 3-8 cycloalkyl which may be substituted An alkyl group, an optionally substituted C 6-14 aryl group, or an optionally substituted non-aromatic heterocyclic group, or R 1 is bonded to an atom on ring A together with ring A Forming a spiro ring substituted with oxo and optionally further substituted; R 2 is an optionally substituted C 6-14 aryl group, or an optionally substituted aromatic heterocyclic group; X 1 is a carbon atom or a nitrogen atom; R 3 is a hydrogen atom or a substituent when X 1 is a carbon atom, and absent when X 1 is a nitrogen atom; Each ring A may be further substituted and each may be bridged;
- R 1 is optionally substituted C 1-6 alkyl group, optionally substituted C 1-6 alkoxy group, an optionally substituted amino group, optionally C 3-8 cycloalkyl which may be substituted An alkyl group, an optionally substituted C 6-14 aryl group, or an optionally substituted non-aromatic heterocyclic group;
- R 2 is an optionally substituted C 6-14 aryl group, or an optionally substituted aromatic heterocyclic group;
- X 1 is a carbon atom or a nitrogen atom;
- R 3 is a hydrogen atom or a substituent when X 1 is a carbon atom, and absent when X 1 is a nitrogen atom;
- Each ring A may be further substituted and each may be bridged;
- R 1 is (1) (a) a cyano group, (b) a C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 C 1-6 alkoxy groups (eg, methoxy), (c) a C 6-14 aryloxy group (eg, phenoxy), (d) a C 3-8 cycloalkyl group (eg, cyclopropyl), (e) a 5- or 6-membered monocyclic aromatic heterocyclic group (eg, pyrazolyl), (f) an 8- to 12-membered fused aromatic heterocyclic group (eg, indazolyl), and (g) a 3- to 8-membered monocyclic non-aromatic heterocycle optionally substituted with 1 to 3 oxo groups Ring group (eg, dihydropyridyl) A C 1-6 alkyl group (eg, methyl, ethyl) optionally substituted with 1 to 3 substituents selected from: (2)
- R 1 is bonded to an atom on ring A and is substituted with oxo together with ring A, and further substituted with 1 to 3 C 1-6 alkyl groups (eg, methyl).
- R 2 is (1) (a) a halogen atom (eg, fluorine atom, chlorine atom), and (b) a C 1-6 alkyl group (eg, optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom)) , Methyl) A C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 substituents selected from: or (2) (a) halogen atoms (eg, chlorine atoms, bromine atoms), (b) a cyano group, (c) a C 1-6 alkyl group (eg, methyl,
- R 1 is (1) (a) a cyano group, (b) a C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 C 1-6 alkoxy groups (eg, methoxy), (c) a C 6-14 aryloxy group (eg, phenoxy), (d) a C 3-8 cycloalkyl group (eg, cyclopropyl), (e) a 5- or 6-membered monocyclic aromatic heterocyclic group (eg, pyrazolyl), (f) an 8- to 12-membered fused aromatic heterocyclic group (eg, indazolyl), and (g) a 3- to 8-membered monocyclic non-aromatic heterocycle optionally substituted with 1 to 3 oxo groups Ring group (eg, dihydropyridyl) A C 1-6 alkyl group (eg, methyl, ethyl) optionally substituted with 1 to 3 substituents selected from: (2)
- R 1 is bonded to an atom on ring A and is substituted with oxo together with ring A, and further substituted with 1 to 3 C 1-6 alkyl groups (eg, methyl).
- R 2 is (1) (a) a halogen atom (eg, fluorine atom, chlorine atom), and (b) a C 1-6 alkyl group (eg, optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom)) , Methyl) A C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 substituents selected from: or (2) (a) halogen atoms (eg, chlorine atoms, bromine atoms), (b) a cyano group, (c) a C 1-6 alkyl group (eg, methyl, ethyl) optionally substituted with 1 to 3 halogen atoms (eg, fluorine atom), and (d) a C 3-8 cycloalkyl group (eg, , Cyclopropyl) A 5- to 12-
- R 1 is (1) (a) a cyano group, (b) a C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 C 1-6 alkoxy groups (eg, methoxy), (c) a C 6-14 aryloxy group (eg, phenoxy), (d) a C 3-8 cycloalkyl group (eg, cyclopropyl), (e) a 5- or 6-membered monocyclic aromatic heterocyclic group (eg, pyrazolyl), (f) an 8- to 12-membered fused aromatic heterocyclic group (eg, indazolyl), and (g) a 3- to 8-membered monocyclic non-aromatic heterocycle optionally substituted with 1 to 3 oxo groups Ring group (eg, dihydropyridyl) A C 1-6 alkyl group (eg, methyl, ethyl) optionally substituted with 1 to 3 substituents selected from: (2)
- R 1 is bonded to an atom on ring A and is substituted with oxo together with ring A, and further substituted with 1 to 3 C 1-6 alkyl groups (eg, methyl).
- R 2 is (1) (a) a halogen atom (eg, fluorine atom, chlorine atom), and (b) a C 1-6 alkyl group (eg, optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom)) , Methyl) A C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 substituents selected from: or (2) (a) halogen atoms (eg, chlorine atoms, bromine atoms), (b) a cyano group, (c) a C 1-6 alkyl group (eg, methyl, ethyl) optionally substituted with 1 to 3 halogen atoms (eg, fluorine atom), and (d) a C 3-8 cycloalkyl group (eg, , Cyclopropyl) A 5- to 12-
- R 1 is (1) (a) a cyano group, (b) a C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 C 1-6 alkoxy groups (eg, methoxy), (c) a C 6-14 aryloxy group (eg, phenoxy), (d) a C 3-8 cycloalkyl group (eg, cyclopropyl), (e) a pyrazolyl group, (f) an indazolyl group, and (g) a C 1-6 alkyl group optionally substituted with 1 to 3 substituents selected from dihydropyridyl groups optionally substituted with 1 to 3 oxo groups (Eg, methyl, ethyl), (2) a C 1-6 alkoxy group (eg, methoxy, tert-butoxy, preferably a C 1-3 alkoxy group (eg, phenyl) optionally substituted by 1 to 3 C 6-14 aryl groups
- a C 1-6 alkyl group (eg, methyl, ethyl), (b) a C 3-8 cycloalkyl group (eg, cyclopropyl, cyclobutyl, cyclopentyl) optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom), (c) a C 6-14 aryl group (eg, phenyl), and (d) a tetrahydropyranyl group, oxetanyl each optionally substituted with 1 to 3 C 1-6 alkyl groups (eg, methyl)
- An amino group optionally mono- or di-substituted with a substituent selected from the group, a tetrahydrofuryl group or a pyrrolidinyl group, (4) a C 3-8 cycloalkyl group (eg, cyclopropyl) optionally substituted by 1 to 3 C 6-14 aryl groups (eg, phenyl), (5)
- R 1 is (1) (a) a cyano group, (b) a C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 C 1-6 alkoxy groups (eg, methoxy), (c) a C 6-14 aryloxy group (eg, phenoxy), (d) a C 3-8 cycloalkyl group (eg, cyclopropyl), (e) a pyrazolyl group, (f) an indazolyl group, and (g) a C 1-6 alkyl group optionally substituted with 1 to 3 substituents selected from dihydropyridyl groups optionally substituted with 1 to 3 oxo groups (Eg, methyl, ethyl), (2) a C 1-3 alkoxy group (eg, methoxy) optionally substituted with 1 to 3 C 6-14 aryl groups (eg, phenyl), (3) (a) (i) a halogen atom (eg,
- a C 1-6 alkyl group (eg, methyl, ethyl), (b) a C 3-8 cycloalkyl group (eg, cyclopropyl, cyclobutyl, cyclopentyl) optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom), (c) a C 6-14 aryl group (eg, phenyl), and (d) a tetrahydropyranyl group, oxetanyl each optionally substituted with 1 to 3 C 1-6 alkyl groups (eg, methyl)
- An amino group optionally mono- or di-substituted with a substituent selected from the group, a tetrahydrofuryl group or a pyrrolidinyl group, (4) a C 3-8 cycloalkyl group (eg, cyclopropyl) optionally substituted by 1 to 3 C 6-14 aryl groups (eg, phenyl), (5)
- R 1 is (1) (a) a cyano group, (b) a phenyl group optionally substituted by 1 to 3 C 1-6 alkoxy groups (eg, methoxy), (c) a phenoxy group, (d) a cyclopropyl group, (e) a pyrazolyl group, (f) an indazolyl group, and (g) a C 1-6 alkyl group optionally substituted with 1 to 3 substituents selected from dihydropyridyl groups optionally substituted with 1 to 3 oxo groups (Eg, methyl, ethyl), (2) a C 1-6 alkoxy group (eg, methoxy, tert-butoxy, preferably C 1-3 alkoxy group (eg, methoxy)) optionally substituted by 1 to 3 phenyl groups, (3) (a) (i) a halogen atom (eg, fluorine atom), (ii) a cyano group, (ii
- a C 1-6 alkyl group (eg, methyl, ethyl), (b) a cyclopropyl group, a cyclobutyl group or a cyclopentyl group each optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom), (c) a phenyl group, and (d) a tetrahydropyranyl group, an oxetanyl group, a tetrahydrofuryl group, or a pyrrolidinyl group, each of which may be substituted with 1 to 3 C 1-6 alkyl groups (eg, methyl).
- An amino group optionally mono- or di-substituted with selected substituents (4) a cyclopropyl group optionally substituted by 1 to 3 phenyl groups, (5) a phenyl group, or (6) (a) a halogen atom (eg, fluorine atom), (b) a cyano group, (c) a hydroxy group, (d) an oxo group, (e) a carbamoyl group optionally mono- or di-substituted with a C 1-6 alkyl group (eg, methyl), (f) (i) a hydroxy group, and (ii) a C 1-6 alkoxy group (eg, methoxy) A C 1-6 alkyl group (eg, methyl, ethyl, isopropyl) optionally substituted with 1 to 3 substituents selected from: (g) a C 1-6 alkoxy group (eg, methoxy, ethoxy, isopropoxy) optionally
- Each may be substituted with 5 substituents, Azetidinyl group, pyrrolidinyl group, piperidyl group, piperazinyl group, morpholinyl group, 1,1-dioxidethiomorpholinyl group, tetrahydropyranyl group, 3-oxa-6-azabicyclo [3.1.1] heptyl group, 8-oxa-3-azabicyclo [3.2.1] octyl group, 2-oxa-5-azabicyclo [2.2.1] heptyl group, 3-oxa-8-azabicyclo [3.2.1] octyl group 6-oxa-3-azabicyclo [3.1.1] heptyl group or 3,7-dioxa-9-azabicyclo [3.3.1] nonyl group, or R 1 is an atom on ring A combine with with ring a, is substituted with oxo, and 1 to 3 C 1-6 alkyl groups (e.g., methyl) further
- R 1 is (1) (a) a cyano group, (b) a phenyl group optionally substituted by 1 to 3 C 1-6 alkoxy groups (eg, methoxy), (c) a phenoxy group, (d) a cyclopropyl group, (e) a pyrazolyl group, (f) an indazolyl group, and (g) a C 1-6 alkyl group optionally substituted with 1 to 3 substituents selected from dihydropyridyl groups optionally substituted with 1 to 3 oxo groups (Eg, methyl, ethyl), (2) a C 1-3 alkoxy group (eg, methoxy) optionally substituted with 1 to 3 phenyl groups, (3) (a) (i) a halogen atom (eg, fluorine atom), (ii) a cyano group, (iii) cyclopropyl group, (iv) a cyclobutyl group, (
- a C 1-6 alkyl group (eg, methyl, ethyl), (b) a cyclopropyl group, a cyclobutyl group or a cyclopentyl group each optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom), (c) a phenyl group, and (d) a tetrahydropyranyl group, an oxetanyl group, a tetrahydrofuryl group, or a pyrrolidinyl group, each of which may be substituted with 1 to 3 C 1-6 alkyl groups (eg, methyl).
- An amino group optionally mono- or di-substituted with selected substituents (4) a cyclopropyl group optionally substituted by 1 to 3 phenyl groups, (5) a phenyl group, or (6) (a) a halogen atom (eg, fluorine atom), (b) a cyano group, (c) a hydroxy group, (d) an oxo group, (e) a carbamoyl group optionally mono- or di-substituted with a C 1-6 alkyl group (eg, methyl), (f) (i) a hydroxy group, and (ii) a C 1-6 alkoxy group (eg, methoxy) A C 1-6 alkyl group (eg, methyl, ethyl, isopropyl) optionally substituted with 1 to 3 substituents selected from: (g) a C 1-6 alkoxy group (eg, methoxy, ethoxy, isopropoxy) optionally
- Each may be substituted with 5 substituents, Azetidinyl group, pyrrolidinyl group, piperidyl group, piperazinyl group, morpholinyl group, 1,1-dioxidethiomorpholinyl group, tetrahydropyranyl group, 3-oxa-6-azabicyclo [3.1.1] heptyl group, 8-oxa-3-azabicyclo [3.2.1] octyl group, 2-oxa-5-azabicyclo [2.2.1] heptyl group, 3-oxa-8-azabicyclo [3.2.1] octyl group 6-oxa-3-azabicyclo [3.1.1] heptyl group or 3,7-dioxa-9-azabicyclo [3.3.1] nonyl group, or R 1 is an atom on ring A combine with with ring a, is substituted with oxo, and 1 to 3 C 1-6 alkyl groups (e.g., methyl) further
- R 1 is (1) (a) (i) a halogen atom (eg, fluorine atom), and (ii) a C 6-14 aryl group (eg, optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom)) , Phenyl) A C 1-6 alkyl group (eg, methyl, ethyl) optionally substituted with 1 to 3 substituents selected from: (b) a 3- to 8-membered monocyclic non-aromatic heterocyclic group ( Eg, tetrahydropyranyl, tetrahydrofuryl) An amino group optionally mono- or di-substituted with a substituent selected from (2) (a) a halogen atom (eg, fluorine atom), (b) a cyano group, (c) a carbamoyl group, (d) C 1-6 alkyl group (eg, methyl), and (e) C 1-6 al
- a 5- or 6-membered monocyclic aromatic heterocyclic group (eg, pyrazolyl, thiazolyl, thiadiazolyl (preferably pyrazolyl, thiazolyl)) which may be substituted with 1 to 3 substituents selected from ;
- X 1 is a carbon atom or a nitrogen atom;
- R 3 is a hydrogen atom; and
- Ring A is
- R 1 is (1) 1 to 3 selected from (a) (i) a halogen atom (eg, fluorine atom), and (ii) a phenyl group optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom)
- An optionally substituted C 1-6 alkyl group eg, methyl, ethyl
- (b) a tetrahydropyranyl group and (c) an amino group optionally mono- or disubstituted with a substituent selected from a tetrahydrofuryl group, or (2) (a) a halogen atom (eg, fluorine atom), (b) a cyano group, (c) a carbamoyl group, (d) C 1-6 alkyl group (eg, methyl), and (e) C 1-6 alkoxy group (eg, methoxy) An azetidinyl group or a pyrrolidinyl group each optional
- R 1 is (1) (a) (i) a halogen atom (eg, fluorine atom), and (ii) a C 6-14 aryl group (eg, optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom)) , Phenyl) A C 1-6 alkyl group (eg, methyl, ethyl) optionally substituted with 1 to 3 substituents selected from: (b) a 3- to 8-membered monocyclic non-aromatic heterocyclic group ( Eg, tetrahydropyranyl, tetrahydrofuryl) An amino group optionally mono- or di-substituted with a substituent selected from (2) (a) a halogen atom (eg, fluorine atom), and (b) a 3- to 8-membered monocyclic non-aromatic group optionally substituted with 1 to 5 substituents selected from a cyano group A heterocyclic group (
- a 5- or 6-membered monocyclic aromatic heterocyclic group (eg, pyrazolyl, thiazolyl, thiadiazolyl (preferably pyrazolyl, thiazolyl)) which may be substituted with 1 to 3 substituents selected from ;
- X 1 is a carbon atom or a nitrogen atom;
- R 3 is a hydrogen atom; and
- Ring A is
- R 1 is (1) 1 to 3 selected from (a) (i) a halogen atom (eg, fluorine atom), and (ii) a phenyl group optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom)
- An optionally substituted C 1-6 alkyl group eg, methyl, ethyl
- (b) a tetrahydropyranyl group and (c) an amino group optionally mono- or disubstituted with a substituent selected from a tetrahydrofuryl group, or (2) (a) a halogen atom (eg, fluorine atom), and (b) an azetidinyl group or a pyrrolidinyl group each optionally substituted with 1 to 5 substituents selected from a cyano group
- R 2 is (1) a phenyl group optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom),
- R 1 is (1) (a) (i) a halogen atom (eg, fluorine atom), and (ii) a C 6-14 aryl group (eg, optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom)) , Phenyl) A C 1-6 alkyl group (eg, methyl, ethyl) optionally substituted with 1 to 3 substituents selected from: (b) a 3- to 8-membered monocyclic non-aromatic heterocyclic group ( Eg, tetrahydropyranyl, tetrahydrofuryl) An amino group optionally mono- or di-substituted with a substituent selected from (2) a 3- to 8-membered monocyclic non-aromatic heterocyclic group (eg, azetidinyl, pyrrolidinyl) optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom); R
- a 5- or 6-membered monocyclic aromatic heterocyclic group (eg, pyrazolyl, thiazolyl, thiadiazolyl (preferably pyrazolyl, thiazolyl)) which may be substituted with 1 to 3 substituents selected from ;
- X 1 is a carbon atom or a nitrogen atom;
- R 3 is a hydrogen atom; and
- Ring A is
- R 1 is (1) 1 to 3 selected from (a) (i) a halogen atom (eg, fluorine atom), and (ii) a phenyl group optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom)
- An optionally substituted C 1-6 alkyl group eg, methyl, ethyl
- (b) a tetrahydropyranyl group and (c) an amino group optionally mono- or disubstituted with a substituent selected from a tetrahydrofuryl group, or (2) an azetidinyl group or a pyrrolidinyl group each optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom)
- R 2 is (1) a phenyl group optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom), or (2) (a) halogen atoms (eg, chlorine atoms,
- R 1 is (a) a halogen atom (eg, fluorine atom), (b) a cyano group, (c) a carbamoyl group, (d) a C 1-6 alkyl group (eg, methyl), and (e) C 1-6 alkoxy group (eg, methoxy)
- a 3- to 8-membered monocyclic non-aromatic heterocyclic group eg, pyrrolidinyl which may be substituted with 1 to 5 substituents selected from:
- R 2 is (a) a halogen atom (eg, a chlorine atom), and (b) C 1-6 alkyl group (eg, methyl) 5- or 6-membered monocyclic aromatic heterocyclic group (eg, pyrazolyl, thiazolyl, thiadiazolyl, pyridyl (preferably pyrazolyl, thiadiazolyl, Preferably pyrazolyl));
- X 1 is a carbon atom;
- R 1 is (a) a halogen atom (eg, fluorine atom), (b) a cyano group, (c) a carbamoyl group, (d) a C 1-6 alkyl group (eg, methyl), and (e) C 1-6 alkoxy group (eg, methoxy)
- a pyrrolidinyl group optionally substituted with 1 to 5 substituents selected from:
- R 2 is (a) a halogen atom (eg, a chlorine atom), and (b) C 1-6 alkyl group (eg, methyl)
- a pyrazolyl group or a thiadiazolyl group each optionally substituted by 1 to 3 substituents selected from:
- X 1 is a carbon atom;
- R 3 is a hydrogen atom; and Ring A is
- R 1 is (a) a halogen atom (eg, a fluorine atom), and (b) a 3- to 8-membered monocyclic non-aromatic heterocyclic group (eg, pyrrolidinyl) optionally substituted with 1 to 5 substituents selected from a cyano group;
- R 2 is (a) a halogen atom (eg, a chlorine atom), and (b) C 1-6 alkyl group (eg, methyl) 5- or 6-membered monocyclic aromatic heterocyclic group (eg, pyrazolyl, thiazolyl, thiadiazolyl, pyridyl (preferably pyrazolyl, thiadiazolyl, Preferably pyrazolyl));
- X 1 is a carbon atom;
- R 3 is a hydrogen atom; and Ring A is
- R 1 is (a) a halogen atom (eg, a fluorine atom), and (b) a pyrrolidinyl group optionally substituted with 1 to 5 substituents selected from a cyano group;
- R 2 is (a) a halogen atom (eg, a chlorine atom), and (b) C 1-6 alkyl group (eg, methyl)
- a pyrazolyl group optionally substituted by 1 to 3 substituents selected from:
- X 1 is a carbon atom;
- R 3 is a hydrogen atom; and Ring A is
- R 1 is (1) (a) a C 3-8 cycloalkyl group (eg, cyclopropyl), and (b) an 8- to 12-membered fused aromatic heterocyclic group (eg, indazolyl)
- a C 1-6 alkyl group eg, methyl, ethyl
- substituents selected from: (2) a C 1-6 alkoxy group (preferably a C 1-3 alkoxy group (eg, methoxy)) optionally substituted by 1 to 3 C 6-14 aryl groups (eg, phenyl), (3) (a) (i) a halogen atom (eg, fluorine atom), (ii) a C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 halogen atoms (eg, fluorine atom), (iii) a 5- or 6-membered monocyclic aromatic heterocyclic group (eg, pyridyl
- R 2 is (1) (a) a halogen atom (eg, fluorine atom), and (b) a C 1-6 alkyl group (eg, methyl) A C 6-14 aryl group (eg, phenyl) optionally substituted with 1 to 3 substituents selected from: or (2) (a) halogen atoms (eg, chlorine atoms, bromine atoms), (b) a cyano group, (c) a C 1-6 alkyl group (eg, methyl) optionally substituted with 1 to 3 halogen atoms (eg, fluorine atom), and (d) a C 3-8 cycloalkyl group (eg, cyclo Propyl) A 5- to 12-membered aromatic heterocyclic group (preferably a 5- or 6-membered monocyclic aromatic heterocyclic group (eg, pyrazolyl, Oxazolyl)
- a 5- to 12-membered aromatic heterocyclic group preferably a 5- or 6-membered monocyclic aromatic
- R 1 is (1) a C 1-6 alkyl group (eg, methyl, ethyl) optionally substituted with 1 to 3 substituents selected from (a) a cyclopropyl group, and (b) an indazolyl group, (2) a C 1-6 alkoxy group (preferably a C 1-3 alkoxy group (eg, methoxy)) optionally substituted by 1 to 3 phenyl groups, (3) (a) (i) a halogen atom (eg, fluorine atom), (ii) a phenyl group optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom), (iii) substituted with 1 to 3 substituents selected from an oxetanyl group optionally substituted with a pyridyl group, and (iv) 1 to 3 C 1-6 alkyl groups (eg, methyl) A C 1-6 alkyl group (eg, methyl, ethyl) optionally substituted
- R 1 may be bonded to an atom on ring A, together with ring A, substituted with oxo and optionally further substituted with 1 to 3 C 1-6 alkyl groups (eg, methyl) -Forming a diazaspiro [4.5] decane ring;
- R 2 is (1) (a) a halogen atom (eg, fluorine atom), and (b) a C 1-6 alkyl group (eg, methyl) A phenyl group optionally substituted with 1 to 3 substituents selected from: (2) (a) halogen atoms (eg, chlorine atoms, bromine atoms), (b) a cyano group, (c) a C
- R 1 is (a) a halogen atom (eg, fluorine atom), (b) a cyano group, (c) a carbamoyl group, and (d) a C 1-6 alkyl group (eg, methyl) optionally substituted by 1 to 3 C 1-6 alkoxy groups (eg, methoxy)
- a 3- to 8-membered monocyclic non-aromatic heterocyclic group eg, pyrrolidinyl
- R 2 is (a) a halogen atom (eg, a chlorine atom), and (b) C 1-6 alkyl group (eg, methyl) 5- or 6-membered monocyclic aromatic heterocyclic group (eg, pyrazolyl, thiazolyl, thiadiazolyl, pyridyl (preferably pyrazolyl, thiadiazolyl, Preferably pyrazolyl));
- R 1 is (a) a halogen atom (eg, fluorine atom), (b) a cyano group, (c) a carbamoyl group, and (d) a C 1-6 alkyl group (eg, methyl) optionally substituted by 1 to 3 C 1-6 alkoxy groups (eg, methoxy)
- R 2 is (a) a halogen atom (eg, a chlorine atom), and (b) C 1-6 alkyl group (eg, methyl)
- X 1 is a carbon atom
- R 3 is a hydrogen atom
- Ring A is
- R 1 is (a) a halogen atom (eg, fluorine atom), (b) a cyano group, (c) a carbamoyl group, (d) a C 1-6 alkyl group (eg, methyl) optionally substituted with 1 to 3 C 1-6 alkoxy groups (eg, methoxy), and (e) C 1-6 alkoxy group (eg, methoxy)
- a 3- to 8-membered monocyclic non-aromatic heterocyclic group eg, pyrrolidinyl which may be substituted with 1 to 5 substituents selected from:
- R 2 is (1) (a) a halogen atom (eg, fluorine atom, chlorine atom), and (b) a C 1-6 alkyl group (eg, optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom)) , Methyl)
- a C 6-14 aryl group eg, phenyl
- R 1 is (a) a halogen atom (eg, fluorine atom), (b) a cyano group, (c) a carbamoyl group, (d) a C 1-6 alkyl group (eg, methyl) optionally substituted with 1 to 3 C 1-6 alkoxy groups (eg, methoxy), and (e) C 1-6 alkoxy group (eg, methoxy)
- a pyrrolidinyl group optionally substituted with 1 to 5 substituents selected from:
- R 2 is (1) (a) a halogen atom (eg, fluorine atom, chlorine atom), and (b) a C 1-6 alkyl group (eg, optionally substituted by 1 to 3 halogen atoms (eg, fluorine atom)) , Methyl)
- a phenyl group optionally substituted with 1 to 3 substituents selected from: (2) (a) a halogen atom (eg, chlorine atom), and (b
- salts include metal salts, ammonium salts, salts with organic bases, salts with inorganic acids, salts with organic acids, basic or acidic amino acids, and the like.
- examples include salts.
- the metal salt include alkali metal salts such as sodium salt and potassium salt; alkaline earth metal salts such as calcium salt, magnesium salt and barium salt; aluminum salt and the like.
- the salt with organic base include, for example, trimethylamine, triethylamine, pyridine, picoline, 2,6-lutidine, ethanolamine, diethanolamine, triethanolamine, cyclohexylamine, dicyclohexylamine, N, N′-dibenzyl.
- Examples include salts with ethylenediamine and the like.
- Preferable examples of the salt with inorganic acid include salts with hydrochloric acid, hydrobromic acid, nitric acid, sulfuric acid, phosphoric acid and the like.
- Preferable examples of the salt with organic acid include, for example, formic acid, acetic acid, trifluoroacetic acid, phthalic acid, fumaric acid, oxalic acid, tartaric acid, maleic acid, citric acid, succinic acid, malic acid, methanesulfonic acid, benzene Examples thereof include salts with sulfonic acid, p-toluenesulfonic acid and the like.
- salts with basic amino acids include salts with arginine, lysine, ornithine and the like
- salts with acidic amino acids include salts with aspartic acid, glutamic acid and the like. Is mentioned. Of these, pharmaceutically acceptable salts are preferred.
- inorganic salts such as alkali metal salts (eg, sodium salts, potassium salts, etc.), alkaline earth metal salts (eg, calcium salts, magnesium salts, etc.), ammonium salts
- a salt with an inorganic acid such as hydrochloric acid, hydrobromic acid, nitric acid, sulfuric acid, phosphoric acid, or acetic acid, phthalic acid, fumaric acid
- organic acids such as acid, tartaric acid, maleic acid, citric acid, succinic acid, methanesulfonic acid, benzenesulfonic acid, and p-toluenesulfonic acid.
- the compound of the present invention and its starting compound can be produced by a method known per se, for example, by the method shown in the following scheme.
- room temperature usually indicates 0 to 40 ° C.
- each symbol in the chemical structural formula described in the scheme is as defined above unless otherwise specified.
- the compound in a formula also includes the case where it forms the salt, As such a salt, the thing similar to the salt of this invention compound etc. are mentioned, for example.
- the compound obtained in each step can be used in the next reaction as a reaction solution or as a crude product, but can also be isolated from the reaction mixture according to a conventional method, and can be separated by means of separation such as recrystallization, distillation, chromatography, etc. Can be easily purified.
- a commercially available product can be used as it is.
- the ring in formula (I) has a substituent
- the corresponding precursor also has the same substituent.
- the raw material compound has an amino group, a carboxy group, a hydroxy group, or a heterocyclic group
- these groups may be protected with a protecting group that is generally used in peptide chemistry or the like.
- the target compound can be obtained by removing the protecting group as necessary after the reaction.
- Introduction or removal of these protecting groups a method known per se, for example, Wiley-Interscience, Inc. 1999 annual “Protective Groups in Organic Synthesis, 3 rd Ed. " (Theodora W. Greene, Peter GM Wuts Author) The method according to And so on.
- the protecting group include tert-butyl carbamate group, benzyl carbamate group, benzyl group, methyl group, ethyl group, tert-butyl group and the like.
- Examples of the “leaving group” represented by LG 1 to LG 3 include a halogen atom (eg, fluorine atom, chlorine atom, bromine atom, iodine atom), C 1-6 alkylsulfonyloxy (eg, methanesulfonyloxy). Ethanesulfonyloxy, trifluoromethanesulfonyloxy, etc.), C 1-6 alkylsulfonyl (eg, methanesulfonyl, ethanesulfonyl, etc.) and the like.
- a halogen atom eg, fluorine atom, chlorine atom, bromine atom, iodine atom
- C 1-6 alkylsulfonyloxy eg, methanesulfonyloxy
- Ethanesulfonyloxy, trifluoromethanesulfonyloxy, etc. C 1-6 alkylsulfon
- LG 1 to LG 3 also contain a substituent that can be converted to a leaving group, and can be converted to the leaving group by a reaction known per se in a desired step.
- a substituent that can be converted to a leaving group, and can be converted to the leaving group by a reaction known per se in a desired step.
- LG 1 to LG 3 are methylsulfanyl groups, they are converted to methanesulfonyl groups by an oxidation reaction.
- Each step described below can be performed without solvent or by dissolving or suspending the raw material compound in an appropriate solvent before the reaction.
- one type of solvent may be used alone, or two or more types of solvents may be mixed and used at an appropriate ratio.
- Specific examples of the solvent used in the production method of the compound of the present invention include the following.
- Aromatic hydrocarbons such as 1,2-dimethoxyethane: Saturated hydrocarbons such as benzene, chlorobenzene, toluene, xylene: Amides such as cyclohexane and hexane: N, N-dimethylformamide, N, N-dimethylacetamide, hexamethylphosphoric Halogenated hydrocarbons such as triamide and N-methylpyrrolidone: Dinitriles such as dichloromethane, chloroform, carbon tetrachloride and 1,2-dichloroethane: Sulfoxides such as acetonitrile
- Inorganic bases Basic salts such as sodium hydroxide, potassium hydroxide, magnesium hydroxide: Sodium carbonate, potassium carbonate, cesium carbonate, calcium carbonate, sodium bicarbonate, etc.
- Organic bases Triethylamine, diisopropylethylamine, tributylamine, cyclohexyldimethyl Amine, pyridine, lutidine, 4-dimethylaminopyridine, N, N-dimethylaniline, N-methylpiperidine, N-methylpyrrolidine, N-methylmorpholine, 1,5-diazabicyclo [4.3.0] -5-nonene 1,4-diazabicyclo [2.2.2] octane, 1,8-diazabicyclo [5.4.0] -7-undecene, imidazole and other metal alkoxides: sodium methoxide, sodium ethoxide, potassium tert-butoxide Equal al Metallic hydrides: Metal amides such as sodium hydride and potassium hydride: Sodium amide, lithium diisopropylamide, lithium hexamethyldisilazide and other organic lithium reagents: methyllithium, n-buty
- Specific examples of the acid or acid catalyst used in the production method of the compound of the present invention include the following.
- Inorganic acids hydrochloric acid, sulfuric acid, nitric acid, hydrobromic acid, phosphoric acid, etc.
- Organic acids acetic acid, trifluoroacetic acid, oxalic acid, phthalic acid, fumaric acid, tartaric acid, maleic acid, citric acid, succinic acid, methanesulfonic acid, Lewis acids such as p-toluenesulfonic acid, 10-camphorsulfonic acid: boron trifluoride ether complex, zinc iodide, anhydrous aluminum chloride, anhydrous zinc chloride, anhydrous iron chloride, etc.
- each R a represents a hydrogen atom or an optionally substituted C 1-6 alkyl group.
- each R a is an optionally substituted C 1-6 alkyl group
- the two R a are combined together to form 4,4,5,5-tetramethyl-1,3,2-dioxaborolane, etc.
- the ring may be formed.
- R 4 represents an optionally substituted hydrocarbon group, an optionally substituted heterocyclic group, or a hydrogen atom.
- X 2 represents an optionally substituted carbon atom or nitrogen atom.
- X 3 represents an oxygen atom or a sulfur atom.
- optionally substituted C 1-6 alkyl group represented by R a
- R 4 and “optionally substituted hydrocarbon group”, “optionally substituted heterocyclic group", R A it may be "substituted represented by R A 'or R B' Examples thereof include those similar to “hydrocarbon group” and “optionally substituted heterocyclic group”.
- substituent of “optionally substituted carbon atom” for X 2 include the same substituents as the substituent of “optionally substituted aromatic heterocyclic group” for R 2 .
- Compound (6) is produced by reacting Compound (2) and Compound (3), Compound (2) and Compound (4), or Compound (2) and Compound (5). Can do. In the reaction, the compound (2) and the compound (3), the compound (2) and the compound (4), or the compound (2) and the compound (5) are reacted in the presence of an acid catalyst, a base or a metal catalyst.
- an acid catalyst include organic acids. The acid catalyst is used in an amount of about 0.05 to 2 mol per 1 mol of compound (2).
- the base include basic salts, organic bases, alkali metal hydrides, organic lithium reagents and the like. The base is used in an amount of about 1 to 20 mol per 1 mol of compound (2).
- the metal catalyst examples include palladium compounds [eg, palladium (II) acetate, tetrakis (triphenylphosphine) palladium (0), dichlorobis (triphenylphosphine) palladium (II), dichlorobis (triethylphosphine) palladium (II), tris (Dibenzylideneacetone) dipalladium (0), [1,1-bis (diphenylphosphino) ferrocene] dichloropalladium (II), palladium (II) acetate and 1,1′-bis (diphenylphosphino) ferrocene Body, etc.], copper compounds [e.g., copper iodide (I), copper bromide (I), etc.] and the like.
- palladium compounds eg, palladium (II) acetate, tetrakis (triphenylphosphine) palladium (0), dichlorobis
- the metal catalyst is used in an amount of about 0.000001 to 10 mol per 1 mol of compound (2).
- Metal catalysts include phosphine ligands (eg triphenylphosphine, 4,5-bis (diphenylphosphino) -9,9-dimethylxanthene, tri-tert-butylphosphine, tri-tert-butylphosphine tetrafluoroborate. Etc.] or amine ligands (eg, 8-methylquinolin-1-ol, 1,10-phenanthroline, 1,2-diaminocyclohexane, N, N′-dimethyl-1,2-ethanediamine, etc.) Can do.
- phosphine ligands eg triphenylphosphine, 4,5-bis (diphenylphosphino) -9,9-dimethylxanthene, tri-tert-butylphosphine, tri-tert-butyl
- phosphine ligand or an amine ligand When a phosphine ligand or an amine ligand is used, it is used in an amount of about 0.01 to 5 mol per 1 mol of compound (2).
- Compound (3), compound (4) or compound (5) is used in an amount of about 0.8 to 10 mol per 1 mol of compound (2).
- the reaction is performed using a metal catalyst, it is preferable to perform the reaction in the presence of a base.
- the base include inorganic bases and basic salts.
- the base is used in an amount of about 1 to 20 mol per 1 mol of compound (2).
- the reaction is preferably performed in an inert gas stream such as argon gas or nitrogen gas.
- This reaction is advantageously performed using a solvent inert to the reaction.
- a solvent is not particularly limited as long as the reaction proceeds.
- alcohols, ethers, aromatic hydrocarbons, saturated hydrocarbons, amides, halogenated hydrocarbons, nitriles, esters, A sulfoxide, a solvent such as water, or a mixed solvent thereof is preferable.
- the reaction time varies depending on the reagent and solvent to be used, it is generally 1 min to 200 hr.
- the reaction temperature is preferably 0 to 200 ° C.
- microwaves may be irradiated for the purpose of promoting the reaction.
- Compound (2), compound (3), compound (4) and compound (5) may be commercially available products, or can be produced by a method known per se or a method analogous thereto.
- Compound (I) can be produced by reacting compound (6) with compound (7).
- the reaction may be performed according to the same method as in step A-1.
- Compound (7) may be a commercially available product, or can be produced by a method known per se or a method analogous thereto.
- Compound (6) can also be synthesized from compound (8) by a series of reaction steps from Step A-3 to Step A-4.
- Step A-3 Compound (10) can be produced by condensing compound (8) and compound (9).
- the condensation reaction is carried out by reacting compound (8) or a reactive derivative thereof with compound (9).
- the reactive derivative include acid halides such as acid chlorides and acid bromides; acid amides with pyrazole, imidazole, benzotriazole, etc .; mixed acid anhydrides with acetic acid, propionic acid, butyric acid, etc .; acid azides; Acid ester, diphenoxyphosphate ester, p-nitrophenyl ester, 2,4-dinitrophenyl ester, cyanomethyl ester, pentachlorophenyl ester, ester with N-hydroxysuccinimide, ester with N-hydroxyphthalimide, 1-hydroxy Active esters such as esters with benzotriazole, esters with 6-chloro-1-hydroxybenzotriazole, esters with 1-hydroxy-1H-2-pyridone; 2-pyridylthioester, 2-benz
- the compound (8) may be directly reacted with the compound (9) in the presence of a suitable condensing agent.
- the condensing agent include N, N'-disubstituted carbodiimides such as N, N'-dicyclohexylcarbodiimide, 1-ethyl-3- (3-dimethylaminopropyl) carbodiimide (WSC) hydrochloride; Azolides such as'-carbonyldiimidazole; dehydrating agents such as N-ethoxycarbonyl-2-ethoxy-1,2-dihydroquinoline, phosphorus oxychloride, alkoxyacetylene; 2-chloromethylpyridinium iodide, 2-fluoro-1 2-halogenopyridinium salts such as methylpyridinium iodide; phosphorylcyanides such as diethylphosphoryl cyanide; 2- (7-azabenzo
- reaction is considered to proceed via a reactive derivative of compound (8).
- Compound (9) is generally used in an amount of about 0.8 to 5 mol per 1 mol of compound (8) or a reactive derivative thereof.
- This reaction is advantageously performed using a solvent inert to the reaction.
- a solvent is not particularly limited as long as the reaction proceeds.
- a solvent such as a base or a mixed solvent thereof is preferred.
- Examples of such a deoxidizer include basic salts and organic bases.
- basic salts, organic bases, and the like can be used.
- the reaction temperature is preferably 0 to 100 ° C.
- Compound (8) and compound (9) may be commercially available products, or can be produced by a method known per se or a method analogous thereto.
- Step A-4) Compound (6) can be produced by treating compound (10) with an acid or a dehydrating agent.
- the acid include organic acids and inorganic acids.
- the acid is used in an amount of about 1-50 mol per 1 mol of compound (10).
- the dehydrating agent include phosphorus oxychloride, methyl carbamate-N- (triethylammoniumsulfonyl) (Burges reagent), and the like.
- the dehydrating agent is used in an amount of about 1 to 10 mol per 1 mol of compound (10). If desired, the reaction can be performed in the presence of a sulfurizing agent.
- sulfurizing agent examples include 2,4-bis (4-methoxyphenyl) -1,3,2,4-dithiadiphosphetane-2,4-disulfide (Lawsson's reagent).
- the sulfurizing agent is used in an amount of about 1 to 10 mol per 1 mol of compound (10).
- This reaction is advantageously performed using a solvent inert to the reaction.
- a solvent is not particularly limited as long as the reaction proceeds.
- a solvent such as a base or a mixed solvent thereof is preferred.
- the reaction can be performed in the presence of a deoxidizing agent for the purpose of removing them from the reaction system.
- a deoxidizing agent include basic salts and organic bases.
- basic salts, organic bases, and the like can be used.
- the reaction time varies depending on the reagent and solvent to be used, it is generally 1 min to 72 hr.
- the reaction temperature is preferably 0 to 150 ° C.
- compound (Ic) can also be synthesized from compound (Ia) according to production method B described below.
- compound (Ie) can also be synthesized from compound (Id) according to production method B described below.
- R 5 and R 8 each represents an optionally substituted hydrocarbon group.
- R 6 and R 7 are each a hydrogen atom, an optionally substituted C 1-10 alkyl group, a C 2-10 alkenyl group, a C 3-10 cycloalkyl group, a C 3-10 cycloalkenyl group, C 6-14 aryl group, C 7-14 aralkyl group, C 8-13 arylalkenyl group or heterocyclic group (eg, aromatic heterocyclic group, non-aromatic heterocyclic group), or acyl group, in this case
- R 6 , R 6 and R 7 may be combined to form an optionally substituted heterocyclic group.
- a 1 represents a piperidine ring which may be further substituted and may be bridged
- a 2 represents a piperazine ring which may be further substituted and may be bridged.
- Ring A 1 and ring A 2 may have 1 to 5 (preferably 1 to 3) substituents at substitutable positions. Examples of such a substituent include a substituent selected from the above substituent group B. When a plurality of substituents are present, each substituent may be the same or different.
- Examples of “bridged piperidine and piperazine rings” include 8-azabicyclo [3.2.1] octane, 2,5-diazabicyclo [2.2.1] heptane, 3-azabicyclo [3.1.0]. ] Hexane etc. are mentioned.
- the “optionally substituted hydrocarbon group” represented by R 5 or R 8 is the same as the “optionally substituted hydrocarbon group” represented by R A , R A ′ or R B ′. Is mentioned.
- Examples of the “optionally substituted hydrocarbon group” and the “optionally substituted heterocyclic group” represented by R 6 or R 7 include “substituted” represented by R A , R A ′ or R B ′. And the same as the “optionally substituted hydrocarbon group” and “optionally substituted heterocyclic group”.
- the “optionally substituted heterocyclic group” formed by R 6 and R 7 together is the “optionally substituted heterocyclic group” represented by R A , R A ′ or R B ′. And the like.
- Compound (Ib) can be produced by hydrolyzing compound (Ia).
- the hydrolysis reaction can be carried out using an inorganic base or an inorganic acid under reaction conditions generally used as a hydrolysis reaction.
- a method known per se, for example, Wiley-Interscience, Inc. 1999 annual “Protective Groups in Organic Synthesis, 3 rd Ed. " (Theodora W. Greene, Peter G. M. Wuts Author) may be carried out according to such methods described.
- Compound (Ic) can be produced by condensing compound (Ib) with compound (11). The reaction may be performed according to the same method as in step A-3.
- Compound (11) may be a commercially available product, or can be produced by a method known per se or a method analogous thereto.
- Compound (12) can be produced by removing the carbamate group of compound (Id).
- carbamate group of compound (Id) For the removal of the carbamate group, according to methods known per se, for example, Wiley-Interscience, Inc. 1999 annual “Protective Groups in Organic Synthesis, 3 rd Ed. " (Theodora W. Greene, Peter GM Wuts Author) to method described in Just do it.
- condensing agent examples include phosgenes such as phosgene and triphosgene, and azolides such as N, N′-carbonyldiimidazole.
- phosgenes such as phosgene and triphosgene
- azolides such as N, N′-carbonyldiimidazole.
- the reaction is considered to proceed via a reactive derivative of compound (12).
- Compound (11) is generally used in an amount of about 0.8 to 5 mol per mol of compound (12) or a reactive derivative thereof.
- This reaction is advantageously performed using a solvent inert to the reaction.
- a solvent is not particularly limited as long as the reaction proceeds.
- a solvent such as a base or a mixed solvent thereof is preferred.
- the reaction can be performed in the presence of a deoxidizing agent for the purpose of removing them from the reaction system.
- a deoxidizer include basic salts and organic bases.
- basic salts, organic bases, and the like can be used.
- the reaction time varies depending on the reagent and solvent to be used, it is generally 1 min to 72 hr.
- the reaction temperature is preferably 0 to 100 ° C.
- Compound (13) may be a commercially available product, or can be produced by a method known per se or a method analogous thereto.
- the raw material compound and / or production intermediate of compound (I) may form a salt, and is not particularly limited as long as the reaction is achieved.
- a salt that compound (I) or the like may form The same salt or the like is used.
- the configurational isomer (E, Z form) of compound (I) can be isolated and purified by usual separation means such as extraction, recrystallization, distillation, chromatography, etc., when isomerization occurs. Pure compounds can be produced.
- the corresponding pure isomer can also be obtained by proceeding with isomerization of the double bond by an acid catalyst, a transition metal complex, a metal catalyst, a radical species catalyst, light irradiation or a strong base catalyst.
- the compound (I) may have a stereoisomer depending on the kind of the substituent, and this isomer alone or a mixture thereof is also included in the present invention.
- Compound (I) may be a hydrate or non-hydrate.
- each of deprotection reaction, acylation reaction, alkylation reaction, hydrogenation reaction, oxidation reaction, reduction reaction, carbon chain extension reaction and substituent exchange reaction may be carried out alone or in combination of two or more thereof.
- Compound (I) can be synthesized by combining these compounds.
- the desired product When the desired product is obtained in the free state by the above reaction, it may be converted into a salt according to a conventional method. When it is obtained as a salt, it is converted into a free form or other salt according to a conventional method.
- the compound (I) thus obtained can be isolated and purified from the reaction solution by known means such as phase transfer, concentration, solvent extraction, fractional distillation, crystallization, recrystallization, chromatography and the like.
- compound (I) exists as a configurational isomer (configuration isomer), diastereomer, conformer or the like, each can be isolated by the separation and purification means as desired.
- the compound (I) is a racemate, it can be separated into a d-form and an l-form by ordinary optical resolution means.
- a functional group such as an amino group, a hydroxy group, or a carboxy group
- it may be subjected to the reaction after introducing a protecting group generally used in peptide chemistry or the like.
- the target compound can be obtained by removing the protecting group as necessary after the reaction.
- the protecting group include formyl or each optionally substituted C 1-6 alkyl-carbonyl (eg, acetyl, propionyl, etc.), phenylcarbonyl, C 1-6 alkoxy-carbonyl (eg, methoxycarbonyl, ethoxycarbonyl).
- phenyloxycarbonyl C 7-10 aralkyloxy-carbonyl (eg, benzyloxycarbonyl etc.), trityl, phthaloyl and the like.
- substituents halogen atoms (eg, fluorine, chlorine, bromine, iodine, etc.), C 1-6 alkyl-carbonyl (eg, acetyl, propionyl, valeryl, etc.), nitro and the like are used.
- the number of substituents is, for example, about 1 to 3.
- a method for removing the protecting group a method known per se or a method equivalent thereto is used.
- reaction mixture obtained by a method known per se, such as extraction, concentration, neutralization, filtration, distillation, recrystallization, column chromatography, It can be isolated and purified by using means such as layer chromatography, preparative high performance liquid chromatography (preparative HPLC), medium pressure preparative liquid chromatography (medium pressure preparative LC) and the like.
- Compound (I) which is a salt is in accordance with a method known per se, for example, when compound (I) is a basic compound, by adding an inorganic acid or an organic acid, or compound (I) is an acidic compound In some cases, it can be prepared by adding an organic base or an inorganic base.
- compound (I) may have optical isomers, any of these individual optical isomers and mixtures thereof are naturally included in the scope of the present invention. If desired, these isomers are known per se. According to the means, it can be optically divided or manufactured separately.
- compound (I) exists as a configurational isomer (configuration isomer), diastereomer, conformer, etc., each can be isolated by the above-described separation and purification means, if desired.
- the compound (I) is a racemate, it can be separated into an S form and an R form by an ordinary optical resolution means.
- a stereoisomer exists in the compound (I), the case where this isomer is used alone or a mixture thereof is also included in the present invention.
- Compound (I) may be used as a prodrug.
- a prodrug of compound (I) is a compound that is converted to compound (I) by a reaction with an enzyme, gastric acid, or the like under physiological conditions in vivo, that is, compound (I) that is enzymatically oxidized, reduced, hydrolyzed, etc.
- a compound in which the amino of the compound (I) is acylated, alkylated or phosphorylated for example, the amino of the compound (I) is eicosanoylated, alanylated, pentylaminocarbonylated, (5-methyl-2- Oxo-1,3-dioxolen-4-yl) methoxycarbonylation, tetrahydrofuranylation, pyrrolidylmethylation, pivaloyloxymethylation, tert-butylation, ethoxycarbonylation, tert-butoxycarbonylation, acetylation, Cyclopropylcarbonylated compounds, etc.); (2) Compounds in which hydroxy of compound (I) is acylated, alkylated, phosphorylated, borated (eg, hydroxy of compound (I) is acetylated, palmitoylated, propanoylated, pivaloyl
- prodrug of compound (I) changes to compound (I) under physiological conditions as described in Hirokawa Shoten, 1990, “Development of Drugs”, Volume 7, Molecular Design, pages 163 to 198. There may be.
- compound (I) and their prodrugs may be collectively abbreviated as “the compound of the present invention”.
- any one of the isomers and a mixture are included in the compound (I).
- the optical isomer resolved from the racemate is also encompassed in compound (I).
- Each of these isomers can be obtained as a single product by a known synthesis method or separation method (concentration, solvent extraction, column chromatography, recrystallization, etc.).
- Compound (I) may be a crystal, and it is included in compound (I) regardless of whether the crystal form is a single crystal form or a mixture of crystal forms.
- the crystal can be produced by crystallization by applying a crystallization method known per se.
- Compound (I) may be a hydrate, a non-hydrate, a solvate, or a non-solvate.
- Compounds labeled with isotopes eg, 3 H, 11 C, 14 C, 18 F, 35 S, 125 I, etc.
- a deuterium converter obtained by converting 1 H into 2 H (D) is also encompassed in compound (I).
- Compound (I) may be a pharmaceutically acceptable cocrystal or cocrystal salt.
- co-crystals or co-crystal salts are two or more unique at room temperature, each having different physical properties (eg structure, melting point, heat of fusion, hygroscopicity, solubility and stability). It means a crystalline substance composed of a simple solid.
- the cocrystal or cocrystal salt can be produced according to a cocrystallization method known per se.
- Compound (I) may be used as a PET tracer.
- the compound of the present invention has low toxicity and is used as it is or mixed with a pharmacologically acceptable carrier to make a pharmaceutical composition, so that a mammal (eg, human, mouse, rat, rabbit, dog, cat, Cattle, horses, pigs, monkeys) can be used as preventive or therapeutic agents for various diseases described below.
- a mammal eg, human, mouse, rat, rabbit, dog, cat, Cattle, horses, pigs, monkeys
- the pharmacologically acceptable carrier various organic or inorganic carrier substances commonly used as pharmaceutical materials are used, and excipients, lubricants, binders, disintegrants in solid preparations; solvents in liquid preparations , Solubilizing agents, suspending agents, isotonic agents, buffers, soothing agents and the like. If necessary, preparation additives such as preservatives, antioxidants, colorants, sweeteners and the like can also be used.
- excipients include lactose, sucrose, D-mannitol, D-sorbitol, starch, pregelatinized starch, dextrin, crystalline cellulose, low-substituted hydroxypropylcellulose, sodium carboxymethylcellulose, gum arabic, pullulan, light
- excipients include anhydrous silicic acid, synthetic aluminum silicate, and magnesium aluminate metasilicate.
- lubricant examples include magnesium stearate, calcium stearate, talc and colloidal silica.
- Preferred examples of the binder include pregelatinized starch, sucrose, gelatin, gum arabic, methylcellulose, carboxymethylcellulose, sodium carboxymethylcellulose, crystalline cellulose, sucrose, D-mannitol, trehalose, dextrin, pullulan, hydroxypropylcellulose, hydroxy Examples include propylmethylcellulose and polyvinylpyrrolidone.
- disintegrant examples include lactose, sucrose, starch, carboxymethyl cellulose, carboxymethyl cellulose calcium, croscarmellose sodium, carboxymethyl starch sodium, light anhydrous silicic acid, and low-substituted hydroxypropyl cellulose.
- Suitable examples of the solvent include water for injection, physiological saline, Ringer's solution, alcohol, propylene glycol, polyethylene glycol, sesame oil, corn oil, olive oil, and cottonseed oil.
- solubilizer examples include polyethylene glycol, propylene glycol, D-mannitol, trehalose, benzyl benzoate, ethanol, trisaminomethane, cholesterol, triethanolamine, sodium carbonate, sodium citrate, sodium salicylate, sodium acetate. Is mentioned.
- suspending agent examples include surfactants such as stearyltriethanolamine, sodium lauryl sulfate, laurylaminopropionic acid, lecithin, benzalkonium chloride, benzethonium chloride, glyceryl monostearate; polyvinyl alcohol, polyvinylpyrrolidone And hydrophilic polymers such as sodium carboxymethylcellulose, methylcellulose, hydroxymethylcellulose, hydroxyethylcellulose, hydroxypropylcellulose; polysorbates; polyoxyethylene hydrogenated castor oil.
- surfactants such as stearyltriethanolamine, sodium lauryl sulfate, laurylaminopropionic acid, lecithin, benzalkonium chloride, benzethonium chloride, glyceryl monostearate
- polyvinyl alcohol polyvinylpyrrolidone
- hydrophilic polymers such as sodium carboxymethylcellulose, methylcellulose, hydroxymethylcellulose, hydroxyethylcellulose, hydroxy
- Preferable examples of the isotonic agent include sodium chloride, glycerin, D-mannitol, D-sorbitol and glucose.
- buffer solutions such as phosphate, acetate, carbonate, citrate.
- a preferred example of the soothing agent is benzyl alcohol.
- Preferable examples of the preservative include p-hydroxybenzoates, chlorobutanol, benzyl alcohol, phenethyl alcohol, dehydroacetic acid and sorbic acid.
- Preferable examples of the antioxidant include sulfite and ascorbate.
- the colorant examples include water-soluble edible tar dyes (eg, edible dyes such as edible red Nos. 2 and 3, edible yellows Nos. 4 and 5, edible blue Nos. 1 and 2, etc.), water-insoluble lake dyes (Eg, the aluminum salt of the water-soluble edible tar dye) and natural dyes (eg, ⁇ -carotene, chlorophyll, bengara).
- water-soluble edible tar dyes eg, edible dyes such as edible red Nos. 2 and 3, edible yellows Nos. 4 and 5, edible blue Nos. 1 and 2, etc.
- water-insoluble lake dyes Eg, the aluminum salt of the water-soluble edible tar dye
- natural dyes eg, ⁇ -carotene, chlorophyll, bengara
- Suitable examples of sweeteners include saccharin sodium, dipotassium glycyrrhizinate, aspartame, and stevia.
- Examples of the dosage form of the pharmaceutical composition include tablets (including sugar-coated tablets, film-coated tablets, sublingual tablets, orally disintegrating tablets), capsules (including soft capsules and microcapsules), granules, powders, and lozenges.
- Oral preparations such as syrup, emulsion, suspension, film (eg, orally disintegrating film); and injection (eg, subcutaneous injection, intravenous injection, intramuscular injection, intraperitoneal injection, Intravenous preparations, external preparations (eg, transdermal preparations, ointments), suppositories (eg, rectal suppositories, vaginal suppositories), pellets, nasal preparations, pulmonary preparations (inhalants), eye drops, etc. Oral preparations are mentioned. These can be safely administered orally or parenterally (eg, topical, rectal, intravenous administration).
- compositions may be controlled-release preparations (eg, sustained-release microcapsules) such as immediate-release preparations or sustained-release preparations.
- the pharmaceutical composition can be produced by a method commonly used in the field of pharmaceutical technology, for example, a method described in the Japanese Pharmacopoeia.
- the content of the compound of the present invention in the pharmaceutical composition varies depending on the dosage form, the dose of the compound of the present invention, etc., but is, for example, about 0.1 to 100% by weight.
- an oral preparation When manufacturing an oral preparation, it may be coated for the purpose of taste masking, enteric solubility or sustainability, if necessary.
- coating base used for coating examples include sugar coating base, water-soluble film coating base, enteric film coating base and sustained-release film coating base.
- sucrose is used, and one or more selected from talc, precipitated calcium carbonate, gelatin, gum arabic, pullulan, carnauba wax and the like may be used in combination.
- water-soluble film coating base examples include cellulose polymers such as hydroxypropylcellulose, hydroxypropylmethylcellulose, hydroxyethylcellulose, and methylhydroxyethylcellulose; polyvinyl acetal diethylaminoacetate, aminoalkyl methacrylate copolymer E [Eudragit E (trade name) ], Synthetic polymers such as polyvinylpyrrolidone; polysaccharides such as pullulan.
- enteric film coating bases include cellulose polymers such as hydroxypropylmethylcellulose phthalate, hydroxypropylmethylcellulose acetate succinate, carboxymethylethylcellulose, and cellulose acetate phthalate; methacrylic acid copolymer L [Eudragit L (trade name) ] Acrylic acid polymers such as methacrylic acid copolymer LD [Eudragit L-30D55 (trade name)], methacrylic acid copolymer S [Eudragit S (trade name)]; natural products such as shellac.
- cellulose polymers such as hydroxypropylmethylcellulose phthalate, hydroxypropylmethylcellulose acetate succinate, carboxymethylethylcellulose, and cellulose acetate phthalate
- methacrylic acid copolymer L (Eudragit L (trade name) ]
- Acrylic acid polymers such as methacrylic acid copolymer LD [Eudragit L-30D55 (trade name)], methacrylic acid copolymer
- sustained-release film coating base examples include cellulose polymers such as ethyl cellulose; aminoalkyl methacrylate copolymer RS [Eudragit RS (trade name)], ethyl acrylate-methyl methacrylate copolymer suspension [Eudragit Acrylic polymer such as NE (trade name)].
- cellulose polymers such as ethyl cellulose; aminoalkyl methacrylate copolymer RS [Eudragit RS (trade name)], ethyl acrylate-methyl methacrylate copolymer suspension [Eudragit Acrylic polymer such as NE (trade name)].
- the above-mentioned coating bases may be used by mixing two or more of them in an appropriate ratio. Moreover, you may use light-shielding agents, such as a titanium oxide, ferric oxide, etc. in the case of coating.
- the compound of the present invention has low toxicity (eg, acute toxicity, chronic toxicity, genotoxicity, reproductive toxicity, cardiotoxicity, carcinogenicity), few side effects, and mammals (eg, humans, cows, horses, dogs, cats, Monkeys, mice, rats) can be used as preventive or therapeutic agents for various diseases or as diagnostic agents.
- toxicity eg, acute toxicity, chronic toxicity, genotoxicity, reproductive toxicity, cardiotoxicity, carcinogenicity
- mammals eg, humans, cows, horses, dogs, cats, Monkeys, mice, rats
- the compound of the present invention has an excellent CH24H inhibitory action, and can suppress neuronal cell death, A ⁇ increase, brain inflammation and the like. Therefore, the compound of the present invention is useful for prevention, symptom improvement, progression inhibition or treatment of diseases involving hyperfunction of CH24H, for example, neurodegenerative diseases.
- neurodegenerative disease means a disease accompanied by degeneration of neural tissue. Specific examples of neurodegenerative diseases include Alzheimer's disease, mild cognitive impairment, Huntington's disease, Parkinson's disease, multiple sclerosis, amyotrophic lateral sclerosis, traumatic brain injury, cerebral infarction, glaucoma, etc. .
- the compound of the present invention is useful for the prevention, symptom improvement, progression inhibition or treatment of diseases involving hyperfunction of CH24H, such as epilepsy, schizophrenia and convulsions.
- the dose of the compound of the present invention varies depending on the administration subject, administration route, target disease, symptom, etc.
- the dose when administered orally to an adult patient (body weight 60 kg), the dose is usually about 0.01 to 100 mg / kg. kg body weight, preferably 0.05 to 30 mg / kg body weight, more preferably 0.1 to 10 mg / kg body weight, and this amount is desirably administered once to three times a day.
- the compound of the present invention When the compound of the present invention is applied to each of the above-mentioned diseases, it can be appropriately used in combination with drugs or treatment methods usually used for those diseases.
- examples of the drug used in combination with the compound of the present invention include, for example, an acetylcholinesterase inhibitor (eg, donepezil, rivastigmine, galantamine, zanapezil), an anti-dementia drug (eg, memantine), ⁇ -amyloid protein production, secretion, accumulation, aggregation and / or deposition inhibitor, ⁇ -secretase inhibitor (eg, 6- (4-biphenylyl) methoxy-2- [2- (N, N-dimethylamino) ethyl] tetralin, 6- (4-biphenylyl) methoxy-2- (N, N-dimethylamino) methyltetralin, 6- (4-biphenylyl) methoxy
- Brain function stimulants eg, aniracetam, nicergoline
- Parkinson's disease drugs eg, dopamine receptor agonists (eg, L-dopa, bromocriptine, pergolide, talipexol, pramipexole, cabergoline, amantadine), monoamine oxidation Enzyme (MAO) inhibitors (eg, deprenyl, Luzirine (selegiline), remasemide, riluzole), anticholinergic agents (eg, trihexyphenidyl, biperidene), COMT inhibitors (eg, entacapone)], amyotrophic lateral sclerosis drug (eg, riluzole, etc., nerve (Nutrient factors), abnormal behavior associated with the progression of dementia, therapeutic agents such as epilepsy (
- the compound of the present invention may be used in combination with the following concomitant drugs: (1) Diabetes therapeutic agents: For example, insulin preparations (eg, animal insulin preparations extracted from bovine and porcine pancreas; human insulin preparations genetically engineered using E. coli or yeast; insulin zinc; protamine insulin zinc; insulin Fragment or derivative (eg, INS-1), oral insulin preparation), insulin sensitizer (eg, pioglitazone or a salt thereof (preferably hydrochloride), rosiglitazone or a salt thereof (preferably maleate), tessaglitazar (Tesaglitazar), Ragaglitazar, Muraglitazar, Edaglitazone, Metaglidasen, Naveglitazar, AMG-131, THR-0921, ⁇ -glucosidase inhibitors (eg, carboglisose) Migri , Emiglitate), biguanides (eg, metformin, buformin or salts thereof (eg,
- aldose reductase inhibitors eg, tolrestat, epalrestat, zenarestat, zopolrestat, minalrestat, fidarestat, CT-112
- neurotrophic factors and their increasing agents eg, NGF, NT-3, BDNF, neurotrophin production / secretion enhancer described in WO01 / 14372 (for example, 4- (4-chlorophenyl) -2- (2-methyl-1-imidazolyl) -5- [3- (2-methylphenoxy) propyl] oxazole)
- nerve regeneration promoter eg, Y-128
- PKC inhibitor eg, ruboxistaurin mesylate
- AGE inhibitor eg, ALT946, pimagedin
- Pyratoxatin N-phenacylthiazolium bromide (ALT766), ALT-711, EXO-226, pyridoline (Pyridorin), pyridox
- statin compounds eg, pravastatin, simvastatin, lovastatin, atorvastatin, fluvastatin, rosuvastatin, pitavastatin or salts thereof (eg, sodium salt, calcium salt)
- squalene synthase inhibition Agents eg, lapaquistat acetate or salts thereof
- fibrate compounds eg, bezafibrate, clofibrate, simfibrate, clinofibrate
- ACAT inhibitors eg, Avasimibe, eflucimibe
- Anion exchange resins eg, cholestyramine
- ethyl icosapentate plant sterols (eg, soysterol)
- Gamma oryzanol ⁇ -oryzanol
- Antihypertensive agents For example, angiotensin converting enzyme inhibitors (eg, captopril, enalapril, delapril), angiotensin II antagonists (eg, candesartan cilexetil, losartan, eprosartan, valsartan, telmisartan, irbesartan, tasosartan, 1-[[2 '-(2,5-Dihydro-5-oxo-4H-1,2,4-oxadiazol-3-yl) biphenyl-4-yl] methyl] -2-ethoxy-1H-benzimidazole-7-carvone Acid, azilsartan, azilsartan medoxomil), calcium antagonists (eg, manidipine, nifedipine, amlodipine, efonidipine, nicardipine), potassium channel openers (eg, lebucromakalim, L-27152, AL 06
- Anti-obesity agents For example, central anti-obesity agents (eg, dexfenfluramine, fenfluramine, phentermine, sibutramine, ampifepramon, dexamphetamine, mazindol, phenylpropanolamine, clobenzorex; MCH receptor antagonist Drugs (eg, SB-568849; SNAP-7941; compounds described in WO01 / 82925 and WO01 / 87834); neuropeptide Y antagonists (eg, CP-422935); cannabinoid receptor antagonists (eg, SR-141716, SR-147778); ghrelin antagonists; 11 ⁇ -hydroxysteroid dehydrogenase inhibitors (eg, BVT-3498)), pancreatic lipase inhibitors (eg, orlistat, cetiristat), ⁇ 3 agonists (eg, AJ-9677, AZ40140) , Peptide appetite suppressants (eg
- xanthine derivatives eg, sodium salicylate theobromine, calcium salicylate theobromine
- thiazide-based preparations eg, etiazide, cyclopenthiazide, trichloromethiazide, hydrochlorothiazide, hydroflumethiazide, benzylhydrochlorothiazide, pentfurizide, polythiazide , Methiclotiazide
- anti-aldosterone preparations eg, spironolactone, triamterene
- carbonic anhydrase inhibitors eg, acetazolamide
- chlorobenzenesulfonamide preparations eg, chlorthalidone, mefluside, indapamide
- azosemide isosorbide, ethacrynic acid, Piretanide, bumetanide, furosemide and the like
- Chemotherapeutic agents For example, alkylating agents (eg, cyclophosphamide, ifosfamide), antimetabolites (eg, methotrexate, 5-fluorouracil or derivatives thereof), anticancer antibiotics (eg, mitomycin, adriamycin) Plant-derived anticancer agents (eg, vincristine, vindesine, taxol), cisplatin, carboplatin, etopoxide and the like. Of these, 5-fluorouracil derivatives such as flurtulon or neofluturon are preferred.
- Immunotherapeutic agents For example, microorganisms or bacterial components (eg, muramyl dipeptide derivatives, picibanil), immunopotentiating polysaccharides (eg, lentinan, schizophyllan, krestin), cytokines obtained by genetic engineering techniques (eg, , Interferon, interleukin (IL)), colony stimulating factor (eg, granulocyte colony stimulating factor, erythropoietin) and the like, and interleukins such as IL-1, IL-2 and IL-12 are preferred.
- microorganisms or bacterial components eg, muramyl dipeptide derivatives, picibanil
- immunopotentiating polysaccharides eg, lentinan, schizophyllan, krestin
- cytokines obtained by genetic engineering techniques
- IL Interferon, interleukin (IL)
- colony stimulating factor eg, granulocyte colony stimulating factor, ery
- Antithrombotic agents For example, heparin (eg, heparin sodium, heparin calcium, dalteparin sodium), warfarin (eg, warfarin potassium), antithrombin drug (eg, argatroban), thrombolytic agent (eg, urokinase, tisokinase, Andreteplase, nateplase, monteplase, pamiteplase), platelet aggregation inhibitors (eg, ticlopidine hydrochloride, cilostazol, ethyl icosapentate, beraprost sodium, sarpogrelate hydrochloride) and the like.
- heparin eg, heparin sodium, heparin calcium, dalteparin sodium
- warfarin eg, warfarin potassium
- antithrombin drug eg, argatroban
- thrombolytic agent eg, urokinase, t
- Cachexia-improving drugs For example, cyclooxygenase inhibitors (eg, indomethacin) [Cancer Research, 49, 5935-5939, 1989], progesterone derivatives (eg, megesterol acetate) [Journal of Clinical Oncology, Vol.
- carbohydrate steroids eg, dexamethasone
- metoclopramide drugs e.g., metoclopramide drugs
- tetrahydrocannabinol drugs the literature is the same as above
- fat metabolism improvers eg, eicosapentaene
- growth hormone IGF-1
- cachexia-inducing factors TNF- ⁇ , LIF, IL-6
- Oncosta Examples include antibodies to tin M.
- the above concomitant drugs may be used in combination of two or more at an appropriate ratio.
- the compound of the present invention when applied to each of the above-mentioned diseases, it can be used in combination with a biopharmaceutical (eg, antibody, vaccine preparation), and also applied as a combination therapy in combination with a gene therapy method or the like. Is also possible.
- a biopharmaceutical eg, antibody, vaccine preparation
- antibody and vaccine preparation examples include vaccine preparation against angiotensin II, vaccine preparation against CETP, CETP antibody, antibody against TNF ⁇ antibody and other cytokines, amyloid ⁇ vaccine preparation, type 1 diabetes vaccine (eg, DIAPEP-277 from Peptor) )
- type 1 diabetes vaccine eg, DIAPEP-277 from Peptor
- antibodies or vaccine preparations against cytokines, renin / angiotensin enzymes and their products antibodies or vaccine preparations against enzymes and proteins involved in blood lipid metabolism, blood coagulation / Examples include antibodies or vaccines related to enzymes and proteins involved in the fibrinolytic system, antibodies to vaccines related to sugar metabolism and insulin resistance, and vaccine preparations.
- GH growth factor
- IGF insulin growth factor
- Examples of gene therapy methods include cytokines, renin-angiotensin enzymes and their products, G proteins, G protein-coupled receptors, and genes using genes related to the phosphorylase, DNA such as NF ⁇ B decoy, etc.
- organ regeneration methods such as heart regeneration, kidney regeneration, pancreas regeneration, blood vessel regeneration, cell transplantation therapy using bone marrow cells (bone marrow mononuclear cells, bone marrow stem cells), and artificial organs using tissue engineering (eg, artificial blood vessels, It can also be used in combination with a cardiomyocyte sheet).
- bone marrow cells bone marrow mononuclear cells, bone marrow stem cells
- tissue engineering eg, artificial blood vessels, It can also be used in combination with a cardiomyocyte sheet.
- the administration time of the compound of the present invention and the concomitant drug is not limited, and these may be administered to the administration subject at the same time or may be administered with a time difference. Furthermore, the compound of the present invention and the concomitant drug may be administered as two types of preparations containing each active ingredient, or may be administered as a single preparation containing both active ingredients.
- the dose of the concomitant drug can be appropriately selected based on the clinically used dose.
- the compounding ratio of the compound of the present invention and the concomitant drug can be appropriately selected depending on the administration subject, administration route, target disease, symptom, combination and the like. For example, when the administration subject is a human, 0.01 to 100 parts by weight of the concomitant drug may be used per 1 part by weight of the compound of the present invention.
- room temperature usually indicates about 10 ° C. to about 35 ° C.
- the ratio shown in the mixed solvent is a volume ratio unless otherwise specified. % Indicates% by weight unless otherwise specified.
- silica gel column chromatography when described as NH, aminopropylsilane-bonded silica gel was used.
- HPLC high performance liquid chromatography
- octadecyl-bonded silica gel was used.
- the ratio of elution solvent indicates a volume ratio unless otherwise specified.
- THF Tetrahydrofuran
- DME 1,2-Dimethoxyethane
- DMF N, N-dimethylformamide
- DMA N, N-dimethylacetamide
- DMSO Dimethyl sulfoxide
- APCI Electrospray ionization method
- APCI Atmospheric pressure chemical ionization [M + H] + : Molecular ion peak
- M molar concentration
- IPE diisopropyl ether
- WSC 1- [3- (dimethylamino) propyl] -3-ethylcarbodiimide
- HATU 2- (7-azabenzotriazol-1-yl) -1,1,3 , 3-tetramethyluronium hexafluorophosphate
- HOBt 1-hydroxybenzotriazole
- HPLC high performance liquid chromatography
- DIPEA N, N-diisopropylethylamine
- NMP N-methyl-2-pyrrolidone
- a molecular ion peak is observed, but in the case of a compound having a tert-butoxycarbonyl group (-Boc), a peak from which the tert-butoxycarbonyl group or tert-butyl group is eliminated should be observed as a fragment ion. There is also. In the case of a compound having a hydroxyl group (—OH), a peak from which H 2 O is eliminated may be observed as a fragment ion. In the case of a salt, a free molecular ion peak or a fragment ion peak is usually observed.
- the elemental analysis value (Anal.) Is the calculated value (Calcd) and the measured value (Found).
- Example 1 (4- (4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) -N, N-dimethylpiperidine-4-carboxamide A) 4- (4-Chloro-1H-pyrazol-1-yl) -3-fluoropyridine p-toluenesulfonic acid monohydrate (0.58 g), 4-chloro-3-fluoropyridine (2.0 g), 4 A mixture of -chloro-1H-pyrazole (1.7 g) and 2-propanol (10 mL) was microwaved at 130 ° C. for 2 hours. The mixture was cooled to room temperature, saturated aqueous sodium hydrogen carbonate was added, and the mixture was extracted with ethyl acetate.
- Example 13 (3-exo) -N, N-dimethyl-8- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) -8-azabicyclo [3.2.1] octane-3-carboxamide
- the mixture was diluted with ethyl acetate / water and extracted with ethyl acetate.
- the organic layer was separated, washed with water and saturated brine, dried over sodium sulfate, and the solvent was evaporated under reduced pressure.
- the residue was purified by silica gel column chromatography (NH, ethyl acetate / hexane), and the obtained solid was recrystallized from ethyl acetate / hexane to give the title compound (25 mg).
- Example 21 4- (4- (1,3-Benzothiazol-2-yl) pyridin-3-yl) -N, N-dimethylpiperidine-4-carboxamide A) 2,4,6-Tripropyl-1,3 in a mixture of 2- (3-fluoropyridin-4-yl) benzo [d] thiazole 3-fluoroisonicotinic acid (1.0 g) and DIPEA (1.9 mL) , 5,2,4,6-trioxatriphosphorinane-2,4,6-trioxide (1.9 mL, 50% ethyl acetate solution) and 2-aminobenzenethiol (0.76 mL) were added at room temperature and at 70 ° C. Stir overnight.
- Example 43 (4- (4-Bromo-1H-pyrazol-1-yl) pyridin-3-yl) -N, N-dimethylpiperidine-4-carboxamide A) 4- (4-Bromo-1H-pyrazol-1-yl) -3-fluoropyridine p-toluenesulfonic acid monohydrate (0.30 g), 4-chloro-3-fluoropyridine (1.0 g), 4 A mixture of -bromo-1H-pyrazole (1.3 g) and 2-propanol (5.0 mL) was microwaved at 130 ° C. for 2 hours. The mixture was cooled to room temperature, saturated aqueous sodium hydrogen carbonate was added, and the mixture was extracted with ethyl acetate.
- Example 54 (4- (4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) -N-methyl-N- (tetrahydro-2H-pyran-4-yl) piperidine-4-carboxamide 1- ( 4- (4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (0.50 g), N-methyltetrahydro-2H-pyran-4-amine (0.16 g), HATU (0.81 g), a mixture of triethylamine (0.91 mL) and DMF (8.2 mL) was stirred at room temperature for 3 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 58 (4- (4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) -N-cyclopropyl-N-methylpiperidine-4-carboxamide 1- (4- (4-Chloro-1H- A mixture of pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (0.5 g) and DMF (8.2 mL) was added to HATU (0.81 g), triethylamine (0.91 mL) and N-methylcyclopropanamine ( 0.14 g) was added, and the mixture was stirred at room temperature for 3 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 59 (4- (4-Cyclopropyl-1H-pyrazol-1-yl) pyridin-3-yl) -N, N-dimethylpiperidine-4-carboxamide 1- (4- (4-Bromo-1H-pyrazole- 1-yl) pyridin-3-yl) -N, N-dimethylpiperidine-4-carboxamide (80 mg), cyclopropylboronic acid (36 mg), 1,1'-bis (diphenylphosphino) ferrocene-palladium ( II) A mixture of dichloride dichloromethane complex (17 mg), cesium carbonate (210 mg), DME (1.5 mg) and water (0.30 mg) was irradiated with microwave at 100 ° C.
- Example 68 1- (4- (4-Methyl-1H-pyrazol-1-yl) pyridin-3-yl) -N- (tetrahydro-2H-pyran-4-yl) piperidine-4-carboxamide 1- (4- (4 -Methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (1.0 g), tetrahydro-2H-pyran-4-amine (0.36 mL), HATU (1.7 g), triethylamine ( A mixture of 1.9 mL) and DMF (12 mL) was stirred at room temperature for 3 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 70 (2R) -1-((1- (4- (4-Methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) carbonyl) pyrrolidine-2-carbonitrile
- Example 70 (Another production method) (2R) -1-((1- (4- (4-Methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) carbonyl) pyrrolidine-2-carbonitrile
- Example 79 1- (4- (4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) -3,3-difluoro-N- (tetrahydro-2H-pyran-4-yl) piperidine-4-carboxamide A) 3- (4-((Benzyloxy) methyl) -3,3-difluoropiperidin-1-yl) -4-chloropyridine 4-((benzyloxy) methyl) -3,3-difluoropiperidine (560 mg ), 3-bromo-4-chloropyridine (490 mg), palladium acetate (26 mg), Xantphos (140 mg), sodium tert-butoxide (340 mg) and toluene (12 mL) under microwave irradiation.
- Example 82 2-Methyl-8- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) -2,8-diazaspiro [4.5] decan-1-one
- 1-tert-butyl 4-ethyl 4- (cyanomethyl) piperidine-1,4-dicarboxylate Diisopropylamine (4.7 g) and THF (75 mL) in a mixture of n-butyllithium in hexane (1.6 M, 29 mL) was added under ice-cooling, and the mixture was stirred for 30 minutes.
- Example 83 (4- (4-Cyano-1H-pyrazol-1-yl) pyridin-3-yl) -N, N-dimethylpiperidine-4-carboxamide 1- (4- (4-Bromo-1H-pyrazole-1 -Yl) pyridin-3-yl) -N, N-dimethylpiperidine-4-carboxamide (60 mg), Pd 2 (dba) 3 (15 mg), zinc cyanide (56 mg), DPPF (18 mg) and A mixture of anhydrous DMF (1.5 mL) was heated at 100 ° C. for 7 hours under an argon atmosphere.
- Example 86 N-cyclopropyl-N-methyl-1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxamide 1- (4- (4-methyl-1H- A mixture of pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (0.5 g) and DMF (8.2 mL) was added to HATU (0.86 g), triethylamine (0.97 mL) and N-methylcyclopropanamine ( 0.15 g) was added, and the mixture was stirred at room temperature for 3 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 114 1-((1- (4- (4-Methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) carbonyl) -L-prolinamide 1- (4- (4-methyl -1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (100 mg), DIPEA (0.31 mL) and DMF (2.0 mL) in a mixture of HATU (200 mg) and (S)- Pyrrolidine-2-carboxamide (48 mg) was added and stirred at room temperature for 30 minutes. The mixture was diluted with water and saturated brine, and extracted with ethyl acetate / THF.
- Example 118 4,4-difluoro-1-((1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) carbonyl) -L-prolinamide 1-
- (S) -4,4-difluoropyrrolidine-2-carboxamide (240 mg) were added at room temperature and stirred for 1 hour.
- Example 120 (2S) -1-((1- (4- (4-Methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) carbonyl) pyrrolidine-2-carbonitrile 1- (4 HATU (200 mg) in a mixture of-(4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (100 mg), DIPEA (0.31 mL) and DMF (2.0 mL) And (S) -pyrrolidine-2-carbonitrile hydrochloride (56 mg) were added, and the mixture was stirred at room temperature for 30 minutes.
- Example 124 1-((1- (4- (4-Methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) carbonyl) -D-prolinamide 1- (4- (4-methyl -1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (52 mg) and DMF (1.0 mL) in a mixture of HATU (90 mg), triethylamine (0.056 mL) and (R)- Prolineamide (25 mg) was added at room temperature and stirred for 2 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 127 (2R) -2-methyl-1-((1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) carbonyl) pyrrolidine-2-carbonitrile 2-methyl-1-((1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) carbonyl) -D-prolinamide (100 mg) and Trifluoroacetic anhydride (0.039 mL) was added to a mixture of pyridine (2.0 mL) under ice cooling, and the mixture was stirred at room temperature for 30 minutes.
- Example 128 (2R) -2-methyl-1-((1- (4- (5-methyl-1,3,4-thiadiazol-2-yl) pyridin-3-yl) piperidin-4-yl) carbonyl) pyrrolidine- 2-carbonitrile 2-methyl-1-((1- (4- (5-methyl-1,3,4-thiadiazol-2-yl) pyridin-3-yl) piperidin-4-yl) carbonyl) -D -Trifluoroacetic anhydride (0.12 mL) was added to a mixture of -prolinamide (160 mg) and pyridine (2.0 mL) under ice cooling, and the mixture was stirred for 15 minutes under ice cooling under a nitrogen atmosphere.
- Example 133 ((2R) -2- (methoxymethyl) pyrrolidin-1-yl) (1- (4- (5-methyl-1,3,4-thiadiazol-2-yl) pyridin-3-yl) piperidin-4- Yl) methanone 1- (4- (5-methyl-1,3,4-thiadiazol-2-yl) pyridin-3-yl) piperidine-4-carboxylic acid (80 mg), (R) -2- (methoxy HATU (150 mg) and DIPEA (0.14 mL) were added to a mixture of methyl) pyrrolidine (36 mg) and DMF (1.0 mL), and the mixture was stirred at room temperature for 3 hours.
- Example 142 (2R) -1-((1- (2,4′-bipyridin-3′-yl) piperidin-4-yl) carbonyl) pyrrolidine-2-carbonitrile A) 1,3-Dimethyl-2,3-dihydro-2-oxopyridinium sulfate 1,3-dimethylurea (40 g), 1,1,3,3-tetramethoxypropane (55 mL) and methanol (400 Concentrated sulfuric acid (27 mL) was slowly added dropwise to the mixture at room temperature, and the mixture was stirred at 50 ° C. for 30 minutes.
- Example 160 tert-butyl (1S, 4S) -5- (4-phenylpyridin-3-yl) -2,5-diazabicyclo [2.2.1] heptane-2-carboxylate
- Example 161 2-Cyclopropyl-1-((1S, 4S) -5- (4-phenylpyridin-3-yl) -2,5-diazabicyclo [2.2.1] hept-2-yl) ethanone A) (1S, 4S) -2- (4-Phenylpyridin-3-yl) -2,5-diazabicyclo [2.2.1] heptane dihydrochloride tert-butyl (1S, 4S) -5- (4-phenyl To a mixture of pyridin-3-yl) -2,5-diazabicyclo [2.2.1] heptane-2-carboxylate (440 mg) and methanol (5.0 mL) was added 4M hydrogen chloride / ethyl acetate solution (10 mL), Stir at room temperature for 2 hours.
- Example 186 Methyl 4-methyl-1- (4-phenylpyrimidin-5-yl) piperidine-4-carboxylate 5-bromo-4-phenylpyrimidine (600 mg), methyl 4-methylpiperidine-4-carboxylate hydrochloride (520 mg), Pd 2 (dba) 3 (120 mg), Xantphos (150 mg), sodium tert-butoxide (620 mg) and 1,4-dioxane (20 mL) under microwave irradiation under a 110 Stir at 0 ° C. for 9 hours. The mixture was filtered through silica gel (NH, ethyl acetate), and the filtrate was concentrated under reduced pressure.
- silica gel NH, ethyl acetate
- the aqueous solution was made basic by adding 1M aqueous sodium hydroxide solution, saturated brine was added, and the mixture was extracted with a mixed solvent of ethyl acetate and THF. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and the solvent was evaporated under reduced pressure to give the title compound (0.86 g).
- Example 277 N-cyclopropyl-1- (4- (4-fluorophenyl) pyrimidin-5-yl) -N-methylpiperidine-4-carboxamide A) Ethyl 1- (2- (4-fluorophenyl) -2-oxoethyl) piperidine-4-carboxylate Ethyl piperidine-4-carboxylate (5.0 g), potassium carbonate (6.0 g) and acetonitrile (60 mL) A mixture of 2-chloro-1- (4-fluorophenyl) ethanone (5.0 g) and acetonitrile (40 mL) was added dropwise to the mixture at room temperature, and the mixture was stirred at room temperature overnight.
- Example 278 (3-Fluoroazetidin-1-yl) (1- (4- (4-fluorophenyl) pyrimidin-5-yl) piperidin-4-yl) methanone 1- (4- (4-fluorophenyl) pyrimidine-5 -Yl) piperidine-4-carboxylic acid (0.10 g), 3-fluoroazetidine hydrochloride (0.056 g), HATU (0.16 g), DIPEA (0.23 mL) and DMF (2.0 mL) at room temperature for 18 hours Stir. The mixture was diluted with ethyl acetate and water and extracted with ethyl acetate.
- Example 280 (3-Fluoroazetidin-1-yl) (1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) methanone 1- (4- (4 -Methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (60 mg), 3-fluoroazetidine hydrochloride (28 mg), HATU (96 mg), DIPEA (0.091 mL ) And DMF (2.0 mL) were stirred at room temperature for 4 h. Water was added to the mixture and extracted with ethyl acetate.
- Example 281 (1- (4- (4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) (3-fluoroazetidin-1-yl) methanone 1- (4- (4 -Chloro-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (0.060 g), 3-fluoroazetidine hydrochloride (0.026 g), HATU (0.089 g), DIPEA (0.085 mL) ) And DMF (2.0 mL) were stirred at room temperature for 4 h. The mixture was diluted with ethyl acetate and water and extracted with ethyl acetate.
- Example 282 ((3S) -3-Fluoropyrrolidin-1-yl) (1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) methanone 1- (4 -(4-Methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (60 mg), (S) -3-fluoropyrrolidine hydrochloride (32 mg), HATU (96 mg ), DIPEA (0.091 mL) and DMF (2.0 mL) were stirred at room temperature for 4 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 283 ((3R) -3-fluoropyrrolidin-1-yl) (1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) methanone 1- (4 -(4-Methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (60 mg), (R) -3-fluoropyrrolidine hydrochloride (32 mg), HATU (96 mg ), DIPEA (0.091 mL) and DMF (2.0 mL) were stirred at room temperature for 4 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 284 (1- (4- (4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) ((3S) -3-fluoropyrrolidin-1-yl) methanone 1- (4 -(4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (0.060 g), (S) -3-fluoropyrrolidine hydrochloride (0.030 g), HATU (0.089 g ), DIPEA (0.085 mL) and DMF (2.0 mL) were stirred at room temperature for 4 hours.
- the mixture was diluted with ethyl acetate and water and extracted with ethyl acetate.
- the organic layer was washed with water and saturated brine, dried over anhydrous sodium sulfate, and the solvent was evaporated under reduced pressure.
- the residue was purified by silica gel column chromatography (NH, ethyl acetate / hexane) and crystallized from ethyl acetate / heptane to give the title compound (0.064 g).
- Example 285 (1- (4- (4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) ((3R) -3-fluoropyrrolidin-1-yl) methanone 1- (4 -(4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (60 mg), (R) -3-fluoropyrrolidine hydrochloride (30 mg), HATU (89 mg ), DIPEA (0.085 mL) and DMF (2.0 mL) were stirred at room temperature for 2 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 286 (1- (4- (4-Fluorophenyl) pyrimidin-5-yl) piperidin-4-yl) ((3S) -3-fluoropyrrolidin-1-yl) methanone 1- (4- (4-fluorophenyl) Of pyrimidine-5-yl) piperidine-4-carboxylic acid (0.060 g), (S) -3-fluoropyrrolidine hydrochloride (0.030 g), HATU (0.091 g), DIPEA (0.087 mL) and DMF (2.0 mL) The mixture was stirred at room temperature for 4 hours. The mixture was diluted with ethyl acetate and water and extracted with ethyl acetate.
- Example 287 (1- (4- (4-Fluorophenyl) pyrimidin-5-yl) piperidin-4-yl) ((3R) -3-fluoropyrrolidin-1-yl) methanone 1- (4- (4-fluorophenyl) Of pyrimidine-5-yl) piperidine-4-carboxylic acid (60 mg), (R) -3-fluoropyrrolidine hydrochloride (30 mg), HATU (91 mg), DIPEA (0.087 mL) and DMF (2.0 mL) The mixture was stirred at room temperature for 4 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 288 1- (4- (4-Fluorophenyl) pyrimidin-5-yl) -N-methyl-N- (tetrahydro-2H-pyran-4-yl) piperidine-4-carboxamide 1- (4- (4-Fluorophenyl) ) Pyrimidin-5-yl) piperidine-4-carboxylic acid (60 mg), N-methyl-N- (tetrahydro-2H-pyran-4-yl) amine (28 mg), HATU (91 mg), DIPEA (0.087 mL) and DMF (2.0 mL) were stirred at room temperature for 4 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 290 (4- (4-Fluorophenyl) pyrimidin-5-yl) -N-((3S) -tetrahydrofuran-3-yl) piperidine-4-carboxamide 1- (4- (4-fluorophenyl) pyrimidine-5 -Yl) piperidine-4-carboxylic acid (0.30 g), (S) -tetrahydrofuran-3-amine hydrochloride (0.15 g), HATU (0.45 g), DIPEA (0.43 mL) and DMF (5.0 mL) Stir at room temperature for 4 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 291 (4- (4-Fluorophenyl) pyrimidin-5-yl) -N-((3R) -tetrahydrofuran-3-yl) piperidine-4-carboxamide 1- (4- (4-fluorophenyl) pyrimidine-5 -Yl) piperidine-4-carboxylic acid (0.30 g), (R) -tetrahydrofuran-3-amine hydrochloride (0.15 g), HATU (0.45 g), DIPEA (0.43 mL) and DMF (5.0 mL) Stir at room temperature for 4 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 292 (4- (4-Methyl-1H-pyrazol-1-yl) pyridin-3-yl) -N-((3S) -tetrahydrofuran-3-yl) piperidine-4-carboxamide 1- (4- (4 -Methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (1.0 g), (S) -tetrahydrofuran-3-amine hydrochloride (0.43 g), HATU (1.7 g), A mixture of triethylamine (1.9 mL) and DMF (12 mL) was stirred at room temperature for 3 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 293 (4- (4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) -N-((3S) -tetrahydrofuran-3-yl) piperidine-4-carboxamide 1- (4- (4 -Chloro-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (0.50 g), (S) -tetrahydrofuran-3-amine hydrochloride (0.20 g), HATU (0.81 g), A mixture of triethylamine (0.91 mL) and DMF (5.4 mL) was stirred at room temperature for 3 hours.
- Example 294 (4- (4-Methyl-1H-pyrazol-1-yl) pyridin-3-yl) -N-((3R) -tetrahydrofuran-3-yl) piperidine-4-carboxamide 1- (4- (4 -Methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (1.0 g), (R) -tetrahydrofuran-3-amine hydrochloride (0.43 g), HATU (1.7 g), A mixture of triethylamine (1.9 mL) and DMF (12 mL) was stirred at room temperature for 3 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 295 (4- (4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) -N-((3R) -tetrahydrofuran-3-yl) piperidine-4-carboxamide 1- (4- (4 -Chloro-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (0.50 g), (R) -tetrahydrofuran-3-amine hydrochloride (0.20 g), HATU (0.81 g), A mixture of triethylamine (0.91 mL) and DMF (5.4 mL) was stirred at room temperature for 3 hours.
- Example 296 N-methyl-1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) -N- (tetrahydro-2H-pyran-4-yl) piperidine-4-carboxamide 1- ( 4- (4-Methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (80 mg), N-methyl-N- (tetrahydro-2H-pyran-4-yl) amine A mixture of (39 mg), HATU (0.13 g), DIPEA (0.12 mL) and DMF (2.0 mL) was stirred at room temperature for 4 hours. Water was added to the mixture and extracted with ethyl acetate.
- Methyl iodide (0.047 mL) was added to the mixture under ice-cooling, and the mixture was stirred at the same temperature for 30 min. A saturated aqueous ammonium chloride solution, ethyl acetate and pyridine were added to the mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with water and saturated brine, dried over anhydrous sodium sulfate, and the solvent was evaporated under reduced pressure. The residue was purified by silica gel column chromatography (NH, ethyl acetate / hexane) to give the title compound (0.18 g).
- Example 299 (1- (4- (4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) ((3S) -3-methoxypyrrolidin-1-yl) methanone 1- (4 -(4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (0.10 g), (S) -3-methoxypyrrolidine hydrochloride (49 mg), HATU (0.16 g ), Triethylamine (0.18 mL) and DMF (1.1 mL) were stirred at room temperature for 3 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 300 (1- (4- (4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) ((3R) -3-methoxypyrrolidin-1-yl) methanone 1- (4 -(4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (0.10 g), (R) -3-methoxypyrrolidine hydrochloride (49 mg), HATU (0.16 g ), Triethylamine (0.18 mL) and DMF (1.1 mL) were stirred at room temperature for 3 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 301 ((3S) -3-Methoxypyrrolidin-1-yl) (1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) methanone 1- (4 -(4-Methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (0.10 g), (S) -3-methoxypyrrolidine hydrochloride (53 mg), HATU (0.17 g ), Triethylamine (0.20 mL) and DMF (1.2 mL) were stirred at room temperature for 3 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 302 ((3R) -3-methoxypyrrolidin-1-yl) (1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) methanone 1- (4 -(4-Methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (100 mg), (R) -3-methoxypyrrolidine hydrochloride (53 mg), HATU (0.17 g ), Triethylamine (0.20 mL) and DMF (1.2 mL) were stirred at room temperature for 3 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 303 (1- (4- (4-Fluorophenyl) pyrimidin-5-yl) piperidin-4-yl) ((3S) -3-methoxypyrrolidin-1-yl) methanone 1- (4- (4-fluorophenyl) Of pyrimidine-5-yl) piperidine-4-carboxylic acid (0.10 g), (S) -3-methoxypyrrolidine hydrochloride (50 mg), HATU (0.16 g), triethylamine (0.19 mL) and DMF (1.1 mL) The mixture was stirred at room temperature for 3 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 304 (1- (4- (4-Fluorophenyl) pyrimidin-5-yl) piperidin-4-yl) ((3R) -3-methoxypyrrolidin-1-yl) methanone 1- (4- (4-fluorophenyl) Of pyrimidine-5-yl) piperidine-4-carboxylic acid (0.10 g), (R) -3-methoxypyrrolidine hydrochloride (50 mg), HATU (0.16 g), triethylamine (0.19 mL) and DMF (1.1 mL) The mixture was stirred at room temperature for 3 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 305 N-methyl-1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) -N-((3S) -tetrahydrofuran-3-yl) piperidine-4-carboxamide 1- ( 4- (4-Methyl-1H-pyrazol-1-yl) pyridin-3-yl) -N-((3S) -tetrahydrofuran-3-yl) piperidine-4-carboxamide (0.12 g) and DMF (2.0 mL) Sodium hydride (60%, 20 mg) was added to the mixture under ice-cooling and stirred for 30 minutes.
- Methyl iodide (0.032 mL) was added to the mixture, and the mixture was stirred for 1 hour under ice-cooling. A saturated aqueous ammonium chloride solution, ethyl acetate and pyridine were added to the mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with water and saturated brine, dried over anhydrous sodium sulfate, and the solvent was evaporated under reduced pressure. The residue was purified by silica gel column chromatography (NH, ethyl acetate / hexane) and crystallized from ethyl acetate / heptane to give the title compound (0.084 g).
- Example 306 N-methyl-1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) -N-((3R) -tetrahydrofuran-3-yl) piperidine-4-carboxamide 1- ( 4- (4-Methyl-1H-pyrazol-1-yl) pyridin-3-yl) -N-((3R) -tetrahydrofuran-3-yl) piperidine-4-carboxamide (0.12 g) and DMF (2.0 mL) Sodium hydride (60%, 20 mg) was added to the mixture under ice-cooling and stirred for 30 minutes.
- Methyl iodide (0.032 mL) was added to the mixture, and the mixture was stirred for 1 hour under ice-cooling. A saturated aqueous ammonium chloride solution, ethyl acetate and pyridine were added to the mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with water and saturated brine, dried over anhydrous sodium sulfate, and the solvent was evaporated under reduced pressure. The residue was purified by silica gel column chromatography (NH, ethyl acetate / hexane) and crystallized from ethyl acetate / heptane to give the title compound (0.066 g).
- Example 307 (4- (4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) -N-methyl-N-((3S) -tetrahydrofuran-3-yl) piperidine-4-carboxamide 1- ( 4- (4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) -N-((3S) -tetrahydrofuran-3-yl) piperidine-4-carboxamide (0.12 g) and DMF (2.0 mL) Sodium hydride (60%, 19 mg) was added to the mixture under ice-cooling and stirred for 30 minutes.
- Methyl iodide (0.030 mL) was added to the mixture, and the mixture was stirred for 1 hour under ice-cooling. A saturated aqueous ammonium chloride solution, ethyl acetate and pyridine were added to the mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with water and saturated brine, dried over anhydrous sodium sulfate, and the solvent was evaporated under reduced pressure. The residue was purified by silica gel column chromatography (NH, ethyl acetate / hexane) to give the title compound (0.094 g).
- Example 308 1- (4- (4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) -N-methyl-N-((3R) -tetrahydrofuran-3-yl) piperidine-4-carboxamide 1- ( 4- (4-Chloro-1H-pyrazol-1-yl) pyridin-3-yl) -N-((3R) -tetrahydrofuran-3-yl) piperidine-4-carboxamide (0.12 g) and DMF (2.0 mL) Sodium hydride (60%, 19 mg) was added to the mixture under ice-cooling and stirred for 30 minutes.
- Methyl iodide (0.030 mL) was added to the mixture, and the mixture was stirred for 1 hour under ice-cooling. A saturated aqueous ammonium chloride solution, ethyl acetate and pyridine were added to the mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with water and saturated brine, dried over anhydrous sodium sulfate, and the solvent was evaporated under reduced pressure. The residue was purified by silica gel column chromatography (NH, ethyl acetate / hexane) to give the title compound (0.092 g).
- Example 309 (4- (4-Fluorophenyl) pyrimidin-5-yl) -N-methyl-N-((3S) -tetrahydrofuran-3-yl) piperidine-4-carboxamide 1- (4- (4-Fluorophenyl) ) Pyrimidin-5-yl) -N-((3S) -tetrahydrofuran-3-yl) piperidine-4-carboxamide (0.12 g) and DMF (2.0 mL) with sodium hydride (60%, 19 mg). The mixture was added under ice cooling and stirred for 30 minutes.
- Methyl iodide (0.034 mL) was added to the mixture, and the mixture was stirred for 2.5 hours under ice cooling. A saturated aqueous ammonium chloride solution, ethyl acetate and pyridine were added to the mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with water and saturated brine, dried over anhydrous sodium sulfate, and the solvent was evaporated under reduced pressure. The residue was purified by silica gel column chromatography (NH, ethyl acetate / hexane) and crystallized from ethyl acetate / heptane to give the title compound (0.091 g).
- Example 310 (4- (4-Fluorophenyl) pyrimidin-5-yl) -N-methyl-N-((3R) -tetrahydrofuran-3-yl) piperidine-4-carboxamide 1- (4- (4-Fluorophenyl) ) Pyrimidin-5-yl) -N-((3R) -tetrahydrofuran-3-yl) piperidine-4-carboxamide (0.12 g) and DMF (2.0 mL) with sodium hydride (60%, 19 mg). The mixture was added under ice cooling and stirred for 30 minutes.
- Methyl iodide (0.034 mL) was added to the mixture, and the mixture was stirred for 2.5 hours under ice cooling. A saturated aqueous ammonium chloride solution, ethyl acetate and pyridine were added to the mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with water and saturated brine, dried over anhydrous sodium sulfate, and the solvent was evaporated under reduced pressure. The residue was purified by silica gel column chromatography (NH, ethyl acetate / hexane) and crystallized from ethyl acetate / heptane to give the title compound (0.087 g).
- Example 311 N- (2-fluoroethyl) -1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) -N- (tetrahydro-2H-pyran-4-yl) piperidine-4 -Carboxamide 1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) -N- (tetrahydro-2H-pyran-4-yl) piperidine-4-carboxamide (0.12 g) and Sodium hydride (60%, 19 mg) was added to a mixture of DMF (2.0 mL) and stirred for 30 minutes.
- Example 312 N- (2-fluoroethyl) -1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) -N-((3S) -tetrahydrofuran-3-yl) piperidine-4 -Carboxamide 1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) -N-((3S) -tetrahydrofuran-3-yl) piperidine-4-carboxamide (0.12 g) and Sodium hydride (60%, 20 mg) was added to a mixture of DMF (2.0 mL) and stirred for 30 minutes.
- Example 313 N- (2-fluoroethyl) -1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) -N-((3R) -tetrahydrofuran-3-yl) piperidine-4 -Carboxamide 1- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) -N-((3R) -tetrahydrofuran-3-yl) piperidine-4-carboxamide (0.12 g) and Sodium hydride (60%, 20 mg) was added to a mixture of DMF (2.0 mL) and stirred for 30 minutes.
- Example 314 N-benzyl-N- (2-fluoroethyl) -4- (4-phenylpyrimidin-5-yl) piperazine-1-carboxamide N-benzyl-4- (4-phenylpyrimidin-5-yl) piperazine-1- Sodium hydride (16 mg) was added to a mixture of carboxamide (0.11 g), 15-crown 5-ether (0.078 mL) and THF (2.0 mL) under ice cooling, and the mixture was stirred at room temperature for 30 min. To the mixture was added a THF solution (1.0 mL) of 2-fluoroethyl 4-methylbenzenesulfonate (0.12 g), and the mixture was stirred at room temperature for 4 days.
- the reaction was stopped by adding an aqueous ammonium chloride solution, and the mixture was extracted with ethyl acetate.
- the organic layer was washed with water and saturated brine, dried over anhydrous sodium sulfate, and the solvent was evaporated under reduced pressure.
- the residue was purified by silica gel column chromatography (NH, ethyl acetate / hexane and methanol / ethyl acetate) to give the title compound (43 mg).
- Example 315 N- (4-Fluorobenzyl) -N- (2-fluoroethyl) -4- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperazine-1-carboxamide N- ( 4-Fluorobenzyl) -4- (4- (4-methyl-1H-pyrazol-1-yl) pyridin-3-yl) piperazine-1-carboxamide (0.12 g), 15-crown 5-ether (0.079 mL) Sodium hydride (0.016 g) was added to a mixture of THF and THF (2.0 mL) at 0 ° C., and the mixture was stirred at room temperature for 30 minutes.
- Example 316 ((3S) -3-Fluoropyrrolidin-1-yl) (1- (4- (5-methyl-1,3-thiazol-2-yl) pyridin-3-yl) piperidin-4-yl) methanone 1- (4- (5-methyl-1,3-thiazol-2-yl) pyridin-3-yl) piperidine-4-carboxylic acid (0.080 g), (S) -3-fluoropyrrolidine hydrochloride (0.040 g), A mixture of HATU (0.12 g), DIPEA (0.12 mL) and DMF (2.0 mL) was stirred at room temperature for 18 hours.
- the mixture was diluted with ethyl acetate and water and extracted with ethyl acetate.
- the organic layer was washed with water and saturated brine, dried over anhydrous sodium sulfate, and the solvent was evaporated under reduced pressure.
- the residue was purified by silica gel column chromatography (NH, ethyl acetate / hexane) and crystallized from ethyl acetate / heptane to give the title compound (0.075 g).
- Example 317 (3-Fluoroazetidin-1-yl) (1- (4- (5-methyl-1,3-thiazol-2-yl) pyridin-3-yl) piperidin-4-yl) methanone 1- (4- (5-methyl-1,3-thiazol-2-yl) pyridin-3-yl) piperidine-4-carboxylic acid (0.080 g), 3-fluoroazetidine hydrochloride (0.035 g), HATU (0.12 g), A mixture of DIPEA (0.12 mL) and DMF (2.0 mL) was stirred at room temperature for 18 hours. The mixture was diluted with ethyl acetate and water and extracted with ethyl acetate.
- Example 318 (1- (4- (4-Bromo-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) ((3S) -3-fluoropyrrolidin-1-yl) methanone
- Ethyl 1- (4- (4-bromo-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-carboxylate
- 4- (4-bromo-1H-pyrazol-1-yl) -3 A mixture of -fluoropyridine (3.0 g), ethyl piperidine-4-carboxylate (4.2 mL) and NMP (12 mL) was stirred at 180 ° C. for 4 hours.
- the mixture was diluted with ethyl acetate and water and extracted with ethyl acetate.
- the organic layer was washed with water and saturated brine, dried over anhydrous sodium sulfate, and the solvent was evaporated under reduced pressure.
- the residue was purified by silica gel column chromatography (NH, ethyl acetate / hexane) and crystallized from ethyl acetate / heptane to give the title compound (0.31 g).
- Example 319 (1- (4- (4-Bromo-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) (3-fluoroazetidin-1-yl) methanone 1- (4- (4 -Bromo-1H-pyrazol-1-yl) pyridin-3-yl) piperidine-4-carboxylic acid (0.078 g), 3-fluoroazetidine hydrochloride (0.025 g), HATU (0.11 g), triethylamine (0.12 mL) ) And DMF (1.0 mL) were stirred at room temperature for 3 hours. Water was added to the mixture and extracted with ethyl acetate.
- Example 322 (1- (4- (4-Cyclopropyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) ((3S) -3-fluoropyrrolidin-1-yl) methanone (S) -(1- (4- (4-Bromo-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) (3-fluoropyrrolidin-1-yl) methanone (0.10 g), potassium carbonate (0.13 g), bis (di-tert-butyl (4-dimethylaminophenyl) phosphine) dichloropalladium (II) (0.017 g), cyclopropyl trifluoroborate potassium salt (0.11 g), toluene (2.0 mL) and water (0.40 mL) was stirred at 110 ° C.
- Example 323 (1- (4- (4-Cyclopropyl-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) (3-fluoroazetidin-1-yl) methanone (1- (4- (4-Bromo-1H-pyrazol-1-yl) pyridin-3-yl) piperidin-4-yl) (3-fluoroazetidin-1-yl) methanone (0.10 g), potassium carbonate (0.14 g), bis (Di-tert-butyl (4-dimethylaminophenyl) phosphine) dichloropalladium (II) (0.017 g), cyclopropyl trifluoroborate potassium salt (0.11 g), toluene (2.0 mL) and water (0.40 mL) The mixture was stirred at 110 ° C.
- Example compounds produced according to the above methods or methods similar thereto are shown in the following table.
- MS in the table indicates actual measurement.
- Formulation Example 1 (Manufacture of capsules) 1) 30 mg of the compound of Example 1 2) Fine powder cellulose 10 mg 3) Lactose 19 mg 4) Magnesium stearate 1 mg 60 mg total 1), 2), 3) and 4) are mixed and filled into gelatin capsules.
- Formulation Example 2 Manufacture of tablets
- Test Example 1 Construction of human-type CH24H (CYP46) expression vector Plasmid DNA for expressing human-type CH24H in FreeStyle 293 cells was prepared as follows. Using Full-Length Mammalian Gene Collection No.4819975 (Invitrogen) as a template, the following two types of synthetic DNA: 5'-GCCCCGGAGCCATGAGCCCCGGGCTG-3 '(SEQ ID NO: 1), and 5'-GTCCTGCCTGGAGGCCCCCTCAGCAG-3 '(SEQ ID NO: 2) PCR was performed to amplify the 91-1625 bp region of human-type CH24H (BC022539). The obtained fragment was cloned using TOPO TA Cloning Kit (Invitrogen). The obtained fragment was subcloned into pcDNA3.1 (+) cleaved with BamHI and XhoI to obtain human-type CH24H expression plasmid DNA (pcDNA3.1 (+) / hCH24H).
- Test Example 2 Expression of human CH24H and lysate preparation of human CH24H Human CH24H was expressed using FreeStyle 293 Expression System (Invitrogen). According to the manual attached to the FreeStyle 293 Expression System, transient expression by FreeStyle293-F cells was performed using the plasmid DNA for human-type CH24H expression (pcDNA3.1 (+) / hCH24H) constructed in Test Example 1. After transfection, shaking culture was performed at 37 ° C., 8% CO 2 , 125 rpm for 2 days. The cells were collected by centrifugation, and suspended in a suspension buffer (100 mM potassium phosphate (pH 7.4), 0.1 mM EDTA, 1 mM DTT, 20% glycerol).
- a suspension buffer 100 mM potassium phosphate (pH 7.4), 0.1 mM EDTA, 1 mM DTT, 20% glycerol).
- the suspension was crushed with a Polytron homogenizer (manufactured by Kinematica), centrifuged at 9000 ⁇ g for 10 minutes, and the supernatant was recovered. The collected supernatant was stored frozen ( ⁇ 80 ° C.) as a human-type CH24H lysate preparation.
- Test Example 3 Measurement of CH24H inhibitory activity
- CH24H inhibitory activity was measured using the human-type CH24H lysate prepared in Test Example 2, and the amount of 24-HC produced from cholesterol catalyzed by CH24H in the presence of the test compound. The measurement was carried out by comparing with the absence of the test compound. That is, a reaction buffer solution (50 mM potassium phosphate containing 0.1% BSA and Complete, EDTA-free, pH 7.4) and human CH24H lysate were added to the test compound solution at each concentration and mixed. Next, [ 14 C] cholesterol (53 mCi / mmol specific activity) 15 ⁇ M was added, and the CH24H reaction was performed at 37 ° C. for 5 hours.
- a reaction buffer solution 50 mM potassium phosphate containing 0.1% BSA and Complete, EDTA-free, pH 7.4
- human CH24H lysate were added to the test compound solution at each concentration and mixed.
- [ 14 C] cholesterol 53 mCi /
- Test Example 4 Quantitative test of 24-HC Animals used were 6-week-old female C57BL / 6N mice (3 mice in each group). The test compound was suspended at 1 mg / mL in a 0.5% aqueous solution of methylcellulose [133-14255 WAKO], and repeated oral gavage was performed once a day for 3 days after weighing the mice. Half the brain was collected 16 hours after the third administration, and the amount of 24-HC was measured. After weighing the wet weight of the brain, homogenization was performed with 4 volumes of physiological saline, and this solution was used as a brain extract.
- 24-HC contained in the brain extract was extracted with an acetonitrile solution (98% acetonitrile, 1.98% methanol, 0.02% formic acid) and quantified by HPLC. The results were shown as relative values when the average value of 24-HC amount was calculated and the control group was taken as 100%. The results are shown in Table 3 below.
- Test Example 5 Novel object recognition test using APP transgenic (Tg2576) mice Six-week-old Tg2576 mice and their wild-type mice were used (10 mice per group). The test compound was suspended in methylcellulose [133-14255 WAKO] 0.5% aqueous solution at 3 mg / mL, and after weight measurement of mice, repeated oral gavage was performed once a day at 10 mL / kg for 6 weeks. A novel object recognition test was conducted. The novel object recognition test was conducted as follows. The day before the acquisition trial, a mouse in the same cage was placed in an observation box set with an illuminance of 300 lx, acclimated for 30 minutes, and the compound was orally administered after the acclimation was completed.
- the mouse was placed in an observation box in which two identical objects were placed, and the number of contact times and the contact time for the object for 5 minutes were measured under 300 lx.
- the compound was orally administered after the measurement.
- one object was replaced with a novel object, and the number of contact times and contact time for 5 minutes were measured for each object.
- a metal cylinder and a ceramic triangular pyramid were used.
- a control group non-treated group of test compound
- a control group in wild-type mice were placed.
- the ratio of the number of times of contact with a novel object and the time with respect to the total number of times of contact with the object and time was expressed in%.
- Table 4 The results are shown in Table 4 below.
- the compound of the present invention has an excellent CH24H inhibitory action, and is an epilepsy, neurodegenerative disease (eg, Alzheimer's disease, mild cognitive impairment, Huntington's disease, Parkinson's disease, multiple sclerosis, amyotrophic lateral sclerosis, traumatic) (Brain injury, cerebral infarction, glaucoma, etc.) and schizophrenia are useful as preventive or therapeutic agents.
- neurodegenerative disease eg, Alzheimer's disease, mild cognitive impairment, Huntington's disease, Parkinson's disease, multiple sclerosis, amyotrophic lateral sclerosis, traumatic
- Brain injury cerebral infarction, glaucoma, etc.
- schizophrenia are useful as preventive or therapeutic agents.
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Neurosurgery (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Epidemiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- Psychology (AREA)
- Psychiatry (AREA)
- Pain & Pain Management (AREA)
- Hospice & Palliative Care (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Pyridine Compounds (AREA)
- Emergency Medicine (AREA)
- Hydrogenated Pyridines (AREA)
Abstract
Description
アルツハイマー病は、アミロイドβタンパク(Aβ)の沈着、神経細胞内におけるリン酸化タウの蓄積(神経原線維変化)、および神経細胞死を特徴とする進行性の神経変性疾患である。近年、高齢化が進みアルツハイマー患者数が増加する一方で、効果的な治療法は未だ開発されていない。現在医療現場で使われているアルツハイマー病治療薬は、アセチルコリンエステラーゼ(AchE)阻害剤が主流である。しかし、AchE阻害剤は、一定の有用性が確かめられているものの、低下したアセチルコリンの補充を目的としたものであるので、AchE阻害剤による治療は対症療法に過ぎない。このことから、一刻も早く根本治療法および予防薬の開発をすることが強く望まれている。
特許文献1には、HIV、AIDS等の治療薬として以下の化合物が記載されている。
環Aは、
R1は、水素原子、C1-4アルキル等を;
R2は、水素原子を;
R4-R7は、独立して、水素原子、ハロゲン原子等を;
Xは、NまたはCHを;
Yは、5ないし7員の単環式芳香族複素環等を;
Zは、アリールまたは芳香族複素環基を;
R9-R16は、独立して、水素原子、C1-6アルキル等である。]
環Aaは、置換されていてもよい環を示し;
R1aは、
(1) 式:-X1a-R6a
(ここで、X1aは、C1-6アルキレン基、C2-6アルケニレン基、またはC3-6シクロアルキレン基を示し、R6aは、置換されていてもよいC6-14アリール基、置換されていてもよいC6-14アリールオキシ基、または置換されていてもよい複素環基を示す)で表される基、
(2) 置換されていてもよいC6-14アリール基、
(3) 置換されていてもよいC6-14アリールオキシ基、または
(4) 置換されていてもよい複素環基
を示し;
R2aは、水素原子、置換されていてもよいC1-6アルキル基、置換されていてもよいC3-6シクロアルキル基、または置換されていてもよいヒドロキシ基を示し、
R3aは、置換されていてもよいC1-6アルキル基、置換されていてもよいC3-6シクロアルキル基、または置換されていてもよいヒドロキシ基を示すか、あるいは、
R2aとR3aが、一緒になって、オキソ基、C1-3アルキリデン基、または置換されていてもよい環を形成してもよく;そして
R4aおよびR5aは、同一または異なって、それぞれ水素原子、ハロゲン原子、置換されていてもよいC1-6アルキル基、置換されていてもよいC3-6シクロアルキル基、または置換されていてもよいヒドロキシ基を示すか、あるいは、
R4aとR5aが、一緒になって、オキソ基、C1-3アルキリデン基、または置換されていてもよい環を形成してもよい。]
環Aaは、置換されていてもよい環を示し;
R1aは、
(1) 式:-X1a-R6a(式中、X1aは、C1-6アルキレン基、C2-6アルケニレン基、またはC3-6シクロアルキレン基を示し、R6aは、置換されていてもよいC3-6シクロアルキル基、置換されていてもよいC3-6シクロアルキルオキシ基、置換されていてもよいC6-14アリール基、置換されていてもよいC6-14アリールオキシ基、置換されていてもよいC7-14アラルキルオキシ基、置換されていてもよい複素環基、置換されていてもよい複素環オキシ基、または置換されていてもよいアミノ基を示す)で表される基、
(2) 置換されていてもよいC3-6シクロアルキル基、
(3) 置換されていてもよいC3-6シクロアルキルオキシ基、
(4) 置換されていてもよいC6-14アリール基、
(5) 置換されていてもよいC6-14アリールオキシ基、
(6) 置換されていてもよいC7-14アラルキルオキシ基、
(7) 置換されていてもよい複素環基、
(8) 置換されていてもよい複素環オキシ基、または
(9) 置換されていてもよいアミノ基
を示し;
R2aは、水素原子、置換されていてもよいC1-6アルキル基、置換されていてもよいC3-6シクロアルキル基、または置換されていてもよいヒドロキシ基を示し、
R3aは、置換されていてもよいC1-6アルキル基、置換されていてもよいC3-6シクロアルキル基、または置換されていてもよいヒドロキシ基を示すか、あるいは、
R2aとR3aが、一緒になって、C1-3アルキリデン基、または置換されていてもよい環を形成してもよく;そして
R4aおよびR5aは、同一または異なって、それぞれ水素原子、ハロゲン原子、置換されていてもよいC1-6アルキル基、置換されていてもよいC3-6シクロアルキル基、または置換されていてもよいヒドロキシ基を示すか、あるいは、
R4aとR5aが、一緒になって、オキソ基、C1-3アルキリデン基、または置換されていてもよい環を形成してもよい。]
すなわち、本発明は以下の通りである。
[1] 式(I):
X1は、炭素原子または窒素原子を示し;
環Aは、それぞれさらに置換されていてもよく、それぞれ架橋されていてもよい、
R1は、置換されていてもよいC1-6アルキル基、置換されていてもよいヒドロキシ基、置換されていてもよいアミノ基、置換されていてもよい炭素環基、または置換されていてもよい複素環基を示すか、あるいはR1は環A上の原子と結合して、環Aとともに、それぞれ、オキソ基で置換され、かつさらに置換されていてもよい、スピロ環または縮合環を形成してもよく;
R2は、置換されていてもよいC6-14アリール基、または置換されていてもよい芳香族複素環基を示し;
R3は、X1が炭素原子の場合、水素原子または置換基を示し、X1が窒素原子の場合、存在しない。]
で表される化合物(以下、化合物(I)と称す場合もある)(ただし、tert-ブチル 4-(4-フェニルピリミジン-5-イル)ピペラジン-1-カルボキシラートを除く)またはその塩。
[2] R1が、置換されていてもよいC1-6アルキル基、置換されていてもよいC1-6アルコキシ基、置換されていてもよいアミノ基、置換されていてもよいC3-8シクロアルキル基、置換されていてもよいC6-14アリール基、または置換されていてもよい非芳香族複素環基である、[1]に記載の化合物(ただし、tert-ブチル 4-(4-フェニルピリミジン-5-イル)ピペラジン-1-カルボキシラートを除く)またはその塩。
R1が、
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基で置換されていてもよいC6-14アリール基、
(c)C6-14アリールオキシ基、
(d)C3-8シクロアルキル基、
(e)5または6員の単環式芳香族複素環基、
(f)8ないし12員の縮合芳香族複素環基、および
(g)1ないし3個のオキソ基で置換されていてもよい3ないし8員の単環式非芳香族複素環基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(2)1ないし3個のC6-14アリール基で置換されていてもよいC1-6アルコキシ基、
(3)(a)(i)ハロゲン原子、
(ii)シアノ基、
(iii)C3-8シクロアルキル基、
(iv)ハロゲン原子およびC1-6アルコキシ基から選ばれる1ないし3個の置換基で置換されていてもよいC6-14アリール基、
(v) 5または6員の単環式芳香族複素環基、および
(vi)1ないし3個のC1-6アルキル基で置換されていてもよい3ないし8員の単環式非芳香族複素環基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(b)1ないし3個のハロゲン原子で置換されていてもよいC3-8シクロアルキル基、
(c)C6-14アリール基、および
(d)1ないし3個のC1-6アルキル基で置換されていてもよい3ないし8員の単環式非芳香族複素環基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のC6-14アリール基で置換されていてもよいC3-8シクロアルキル基、
(5)C6-14アリール基、または
(6)(a)ハロゲン原子、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)C1-6アルキル基でモノまたはジ置換されていてもよいカルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(g)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルコキシ基、
(h)C1-6アルコキシ-カルボニル基、および
(i)1ないし3個のハロゲン原子で置換されていてもよいC6-14アリール基
から選択される1ないし5個の置換基で置換されていてもよい3ないし12員の非芳香族複素環基であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基でさらに置換されていてもよいスピロ環を形成し;
R2が、
(1)(a)ハロゲン原子、および
(b)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基
から選択される1ないし3個の置換基で置換されていてもよいC6-14アリール基、または
(2)(a)ハロゲン原子、
(b)シアノ基、
(c)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基、および
(d)C3-8シクロアルキル基
から選択される1ないし3個の置換基で置換されていてもよい5ないし12員の芳香族複素環基であり;
X1が、炭素原子または窒素原子であり;
R3が、
(1)水素原子、または
(2)ハロゲン原子であり;かつ
環Aが、
(a)ハロゲン原子、
(b)C1-6アルキル基、および
(c)オキソ基
から選択される1ないし5個の置換基でそれぞれさらに置換されていてもよく、それぞれ架橋されていてもよい、
R1が、
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基で置換されていてもよいC6-14アリール基、
(c)C6-14アリールオキシ基、
(d)C3-8シクロアルキル基、
(e)5または6員の単環式芳香族複素環基、
(f)8ないし12員の縮合芳香族複素環基、および
(g)1ないし3個のオキソ基で置換されていてもよい3ないし8員の単環式非芳香族複素環基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(2)1ないし3個のC6-14アリール基で置換されていてもよいC1-3アルコキシ基、
(3)(a)(i)ハロゲン原子、
(ii)シアノ基、
(iii)C3-8シクロアルキル基、
(iv)ハロゲン原子およびC1-6アルコキシ基から選ばれる1ないし3個の置換基で置換されていてもよいC6-14アリール基、
(v)5または6員の単環式芳香族複素環基、および
(vi)1ないし3個のC1-6アルキル基で置換されていてもよい3ないし8員の単環式非芳香族複素環基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(b)1ないし3個のハロゲン原子で置換されていてもよいC3-8シクロアルキル基、
(c)C6-14アリール基、および
(d)1ないし3個のC1-6アルキル基で置換されていてもよい3ないし8員の単環式非芳香族複素環基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のC6-14アリール基で置換されていてもよいC3-8シクロアルキル基、
(5)C6-14アリール基、または
(6)(a)ハロゲン原子、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)C1-6アルキル基でモノまたはジ置換されていてもよいカルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(g)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルコキシ基、
(h)C1-6アルコキシ-カルボニル基、および
(i)1ないし3個のハロゲン原子で置換されていてもよいC6-14アリール基
から選択される1ないし5個の置換基で置換されていてもよい3ないし12員の非芳香族複素環基であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基でさらに置換されていてもよいスピロ環を形成する、[1]または[A]に記載の化合物またはその塩。
R1が、
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基で置換されていてもよいC6-14アリール基、
(c)C6-14アリールオキシ基、
(d)C3-8シクロアルキル基、
(e)ピラゾリル基、
(f)インダゾリル基、および
(g)1ないし3個のオキソ基で置換されていてもよいジヒドロピリジル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(2)1ないし3個のC6-14アリール基で置換されていてもよいC1-6アルコキシ基、
(3)(a)(i)ハロゲン原子、
(ii)シアノ基、
(iii)C3-8シクロアルキル基、
(iv)ハロゲン原子およびC1-6アルコキシ基から選ばれる1ないし3個の置換基で置換されていてもよいC6-14アリール基、
(v)ピリジル基、および
(vi)1ないし3個のC1-6アルキル基で置換されていてもよいオキセタニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(b)1ないし3個のハロゲン原子で置換されていてもよいC3-8シクロアルキル基、
(c)C6-14アリール基、および
(d)1ないし3個のC1-6アルキル基でそれぞれ置換されていてもよい、テトラヒドロピラニル基、オキセタニル基、テトラヒドロフリル基もしくはピロリジニル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のC6-14アリール基で置換されていてもよいC3-8シクロアルキル基、
(5)C6-14アリール基、または
(6)(a)ハロゲン原子、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)C1-6アルキル基でモノまたはジ置換されていてもよいカルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(g)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルコキシ基、
(h)C1-6アルコキシ-カルボニル基、および
(i)1ないし3個のハロゲン原子で置換されていてもよいC6-14アリール基
から選択される1ないし5個の置換基でそれぞれ置換されていてもよい、3ないし8員の単環式非芳香族複素環基もしくは3,7-ジオキサ-9-アザビシクロ[3.3.1]ノニル基
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基でさらに置換されていてもよい2,8-ジアザスピロ[4.5]デカン環を形成し;
R2が、
(1)(a)ハロゲン原子、および
(b)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基
から選択される1ないし3個の置換基で置換されていてもよいC6-14アリール基、または
(2)(a)ハロゲン原子、
(b)シアノ基、
(c)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基、および
(d)C3-8シクロアルキル基
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、5または6員の単環式芳香族複素環基もしくは8ないし12員の縮合芳香族複素環基であり;
X1が、炭素原子または窒素原子であり;
R3が、
(1)水素原子、または
(2)ハロゲン原子であり;かつ
環Aが、
(1)(a)ハロゲン原子、
(b)C1-6アルキル基、および
(c)オキソ基
から選択される1ないし3個の置換基でそれぞれさらに置換されていてもよい、
(2)8-アザビシクロ[3.2.1]オクタン環、2,5-ジアザビシクロ[2.2.1]ヘプタン環、もしくは3-アザビシクロ[3.1.0]ヘキサン環
である、[1]または[A]に記載の化合物(ただし、tert-ブチル 4-(4-フェニルピリミジン-5-イル)ピペラジン-1-カルボキシラートを除く)またはその塩。
R1が、
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基で置換されていてもよいC6-14アリール基、
(c)C6-14アリールオキシ基、
(d)C3-8シクロアルキル基、
(e)ピラゾリル基、
(f)インダゾリル基、および
(g)1ないし3個のオキソ基で置換されていてもよいジヒドロピリジル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(2)1ないし3個のC6-14アリール基で置換されていてもよいC1-3アルコキシ基、
(3)(a)(i)ハロゲン原子、
(ii)シアノ基、
(iii)C3-8シクロアルキル基、
(iv)ハロゲン原子およびC1-6アルコキシ基から選ばれる1ないし3個の置換基で置換されていてもよいC6-14アリール基、
(v)ピリジル基、および
(vi)1ないし3個のC1-6アルキル基で置換されていてもよいオキセタニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(b)1ないし3個のハロゲン原子で置換されていてもよいC3-8シクロアルキル基、
(c)C6-14アリール基、および
(d)1ないし3個のC1-6アルキル基でそれぞれ置換されていてもよい、テトラヒドロピラニル基、オキセタニル基、テトラヒドロフリル基もしくはピロリジニル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のC6-14アリール基で置換されていてもよいC3-8シクロアルキル基、
(5)C6-14アリール基、または
(6)(a)ハロゲン原子、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)C1-6アルキル基でモノまたはジ置換されていてもよいカルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(g)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルコキシ基、
(h)C1-6アルコキシ-カルボニル基、および
(i)1ないし3個のハロゲン原子で置換されていてもよいC6-14アリール基
から選択される1ないし5個の置換基でそれぞれ置換されていてもよい、3ないし8員の単環式非芳香族複素環基もしくは3,7-ジオキサ-9-アザビシクロ[3.3.1]ノニル基
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基でさらに置換されていてもよい2,8-ジアザスピロ[4.5]デカン環を形成する、[1]、[3]、[A]および[B]の何れかに記載の化合物またはその塩。
R1が、
(a)ハロゲン原子、
(b)シアノ基、
(c)カルバモイル基、
(d)1ないし3個のC1-6アルコキシ基で置換されていてもよいC1-6アルキル基、および
(e)C1-6アルコキシ基
から選択される1ないし5個の置換基で置換されていてもよい3ないし8員の単環式非芳香族複素環基であり;
R2が、
(1)(a)ハロゲン原子、および
(b)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基
から選択される1ないし3個の置換基で置換されていてもよいC6-14アリール基、または
(2)(a)ハロゲン原子、および
(b)C1-6アルキル基
から選択される1ないし3個の置換基で置換されていてもよい5または6員の単環式芳香族複素環基であり;
X1が、炭素原子であり;
R3が、水素原子であり;かつ
環Aが、
R1が、
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基で置換されていてもよいフェニル基、
(c)フェノキシ基、
(d)シクロプロピル基、
(e)ピラゾリル基、
(f)インダゾリル基、および
(g)1ないし3個のオキソ基で置換されていてもよいジヒドロピリジル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(2)1ないし3個のフェニル基で置換されていてもよいC1-6アルコキシ基、
(3)(a)(i)ハロゲン原子、
(ii)シアノ基、
(iii)シクロプロピル基、
(iv)シクロブチル基、
(v)ハロゲン原子およびC1-6アルコキシ基から選ばれる1ないし3個の置換基で置換されていてもよいフェニル基、
(vi)ピリジル基、および
(vii)1ないし3個のC1-6アルキル基で置換されていてもよいオキセタニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(b)1ないし3個のハロゲン原子でそれぞれ置換されていてもよい、シクロプロピル基、シクロブチル基もしくはシクロペンチル基、
(c)フェニル基、および
(d)1ないし3個のC1-6アルキル基でそれぞれ置換されていてもよい、テトラヒドロピラニル基、オキセタニル基、テトラヒドロフリル基もしくはピロリジニル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のフェニル基で置換されていてもよいシクロプロピル基、
(5)フェニル基、または
(6)(a)ハロゲン原子、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)C1-6アルキル基でモノまたはジ置換されていてもよいカルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(g)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルコキシ基、
(h)C1-6アルコキシ-カルボニル基、および
(i)1ないし3個のハロゲン原子で置換されていてもよいフェニル基
から選択される1ないし5個の置換基でそれぞれ置換されていてもよい、
アゼチジニル基、ピロリジニル基、ピペリジル基、ピペラジニル基、モルホリニル基、1,1-ジオキシドチオモルホリニル基、テトラヒドロピラニル基、3-オキサ-6-アザビシクロ[3.1.1]へプチル基、8-オキサ-3-アザビシクロ[3.2.1]オクチル基、2-オキサ-5-アザビシクロ[2.2.1]ヘプチル基、3-オキサ-8-アザビシクロ[3.2.1]オクチル基、6-オキサ-3-アザビシクロ[3.1.1]へプチル基もしくは3,7-ジオキサ-9-アザビシクロ[3.3.1]ノニル基
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基でさらに置換されていてもよい2,8-ジアザスピロ[4.5]デカン環を形成し;
R2が、
(1)(a)ハロゲン原子、および
(b)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基
から選択される1ないし3個の置換基で置換されていてもよいフェニル基、または
(2)(a)ハロゲン原子、
(b)シアノ基、
(c)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基、および
(d)シクロプロピル基
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基、オキサゾリル基、チアゾリル基、チアジアゾリル基、ピリジル基、インダゾリル基もしくはベンゾチアゾリル基であり;
X1が、炭素原子または窒素原子であり;
R3が、
(1)水素原子、または
(2)ハロゲン原子であり;かつ
環Aが、
(1)(a)ハロゲン原子、
(b)C1-6アルキル基、および
(c)オキソ基
から選択される1ないし3個の置換基でそれぞれさらに置換されていてもよい、
(2)8-アザビシクロ[3.2.1]オクタン環、2,5-ジアザビシクロ[2.2.1]ヘプタン環、もしくは3-アザビシクロ[3.1.0]ヘキサン環
である、[1]、[3]および[A]の何れかに記載の化合物(ただし、tert-ブチル 4-(4-フェニルピリミジン-5-イル)ピペラジン-1-カルボキシラートを除く)またはその塩。
R1が、
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基で置換されていてもよいフェニル基、
(c)フェノキシ基、
(d)シクロプロピル基、
(e)ピラゾリル基、
(f)インダゾリル基、および
(g)1ないし3個のオキソ基で置換されていてもよいジヒドロピリジル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(2)1ないし3個のフェニル基で置換されていてもよいC1-3アルコキシ基、
(3)(a)(i)ハロゲン原子、
(ii)シアノ基、
(iii)シクロプロピル基、
(iv)シクロブチル基、
(v)ハロゲン原子およびC1-6アルコキシ基から選ばれる1ないし3個の置換基で置換されていてもよいフェニル基、
(vi)ピリジル基、および
(vii)1ないし3個のC1-6アルキル基で置換されていてもよいオキセタニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(b)1ないし3個のハロゲン原子でそれぞれ置換されていてもよい、シクロプロピル基、シクロブチル基もしくはシクロペンチル基、
(c)フェニル基、および
(d)1ないし3個のC1-6アルキル基でそれぞれ置換されていてもよい、テトラヒドロピラニル基、オキセタニル基、テトラヒドロフリル基もしくはピロリジニル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のフェニル基で置換されていてもよいシクロプロピル基、
(5)フェニル基、または
(6)(a)ハロゲン原子、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)C1-6アルキル基でモノまたはジ置換されていてもよいカルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(g)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルコキシ基、
(h)C1-6アルコキシ-カルボニル基、および
(i)1ないし3個のハロゲン原子で置換されていてもよいフェニル基
から選択される1ないし5個の置換基でそれぞれ置換されていてもよい、
アゼチジニル基、ピロリジニル基、ピペリジル基、ピペラジニル基、モルホリニル基、1,1-ジオキシドチオモルホリニル基、テトラヒドロピラニル基、3-オキサ-6-アザビシクロ[3.1.1]へプチル基、8-オキサ-3-アザビシクロ[3.2.1]オクチル基、2-オキサ-5-アザビシクロ[2.2.1]ヘプチル基、3-オキサ-8-アザビシクロ[3.2.1]オクチル基、6-オキサ-3-アザビシクロ[3.1.1]へプチル基もしくは3,7-ジオキサ-9-アザビシクロ[3.3.1]ノニル基
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基でさらに置換されていてもよい2,8-ジアザスピロ[4.5]デカン環を形成する、[1]、[3]、[4]、[A]、[B]および[D]の何れかに記載の化合物またはその塩。
R1が、
(1)(a)(i)ハロゲン原子、および
(ii)1ないし3個のハロゲン原子で置換されていてもよいフェニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(b) テトラヒドロピラニル基、および
(c) テトラヒドロフリル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、または
(2)(a)ハロゲン原子、
(b)シアノ基、
(c)カルバモイル基、
(d)C1-6アルキル基、および
(e)C1-6アルコキシ基
から選択される1ないし5個の置換基でそれぞれ置換されていてもよい、アゼチジニル基もしくはピロリジニル基であり;
R2が、
(1)1ないし3個のハロゲン原子で置換されていてもよいフェニル基、または
(2)(a)ハロゲン原子、
(b)C1-6アルキル基、および
(c)シクロプロピル基
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基、チアゾリル基もしくはチアジアゾリル基であり;
X1が、炭素原子または窒素原子であり;
R3が、水素原子であり;かつ
環Aが、
R1が、
(1)(a)(i)ハロゲン原子、および
(ii)1ないし3個のハロゲン原子で置換されていてもよいフェニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(b)テトラヒドロピラニル基、および
(c)テトラヒドロフリル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、または
(2)(a)ハロゲン原子、および
(b)シアノ基
から選択される1ないし5個の置換基でそれぞれ置換されていてもよい、アゼチジニル基もしくはピロリジニル基であり;
R2が、
(1)1ないし3個のハロゲン原子で置換されていてもよいフェニル基、または
(2)(a)ハロゲン原子、
(b)C1-6アルキル基、および
(c)シクロプロピル基
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基もしくはチアゾリル基であり;
X1が、炭素原子または窒素原子であり;
R3が、水素原子であり;かつ
環Aが、
R1が、
(1)(a)(i)ハロゲン原子、および
(ii)1ないし3個のハロゲン原子で置換されていてもよいフェニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(b)テトラヒドロピラニル基、および
(c)テトラヒドロフリル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、または
(2)1ないし3個のハロゲン原子でそれぞれ置換されていてもよい、アゼチジニル基もしくはピロリジニル基であり;
R2が、
(1)1ないし3個のハロゲン原子で置換されていてもよいフェニル基、または
(2)(a)ハロゲン原子、
(b)C1-6アルキル基、および
(c)シクロプロピル基
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基もしくはチアゾリル基であり;
X1が、炭素原子または窒素原子であり;
R3が、水素原子であり;かつ
環Aが、
R1が、
(a)ハロゲン原子、
(b)シアノ基、
(c)カルバモイル基、
(d)1ないし3個のC1-6アルコキシ基で置換されていてもよいC1-6アルキル基、および
(e)C1-6アルコキシ基
から選択される1ないし5個の置換基で置換されていてもよいピロリジニル基であり;
R2が、
(1)(a)ハロゲン原子、および
(b)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基
から選択される1ないし3個の置換基で置換されていてもよいフェニル基、または
(2)(a)ハロゲン原子、および
(b)C1-6アルキル基
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基、チアジアゾリル基もしくはピリジル基であり;
X1が、炭素原子であり;
R3が、水素原子であり;かつ
環Aが、
R1が、
(a)ハロゲン原子、
(b)シアノ基、
(c)カルバモイル基、
(d)C1-6アルキル基、および
(e)C1-6アルコキシ基
から選択される1ないし5個の置換基で置換されていてもよいピロリジニル基であり;
R2が、
(a)ハロゲン原子、および
(b)C1-6アルキル基
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基もしくはチアジアゾリル基であり;
X1が、炭素原子であり;
R3が、水素原子であり;かつ
環Aが、
R1が、
(a)ハロゲン原子、および
(b)シアノ基
から選択される1ないし5個の置換基で置換されていてもよいピロリジニル基であり;
R2が、
(a)ハロゲン原子、および
(b)C1-6アルキル基
から選択される1ないし3個の置換基で置換されていてもよいピラゾリル基であり;
X1が、炭素原子であり;
R3が、水素原子であり;かつ
環Aが、
R1が、
(1)(a)シクロプロピル基、および
(b)インダゾリル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(2)1ないし3個のフェニル基で置換されていてもよいC1-6アルコキシ基、
(3)(a)(i)ハロゲン原子、
(ii)1ないし3個のハロゲン原子で置換されていてもよいフェニル基、
(iii)ピリジル基、および
(iv)1ないし3個のC1-6アルキル基で置換されていてもよいオキセタニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(b)シクロプロピル基、
(c)シクロペンチル基、
(d)テトラヒドロピラニル基、
(e)テトラヒドロフリル基、および
(f)フェニル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)シクロプロピル基、または
(5)(a)ハロゲン原子、
(b)シアノ基、
(c)カルバモイル基、
(d)1ないし3個のC1-6アルコキシ基で置換されていてもよいC1-6アルキル基、
(e)C1-6アルコキシ基、および
(f)1ないし3個のハロゲン原子で置換されていてもよいフェニル基
から選択される1ないし5個の置換基でそれぞれ置換されていてもよい、アゼチジニル基、ピロリジニル基、1,1-ジオキシドチオモルホリニル基もしくは3-オキサ-6-アザビシクロ[3.1.1]へプチル基
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基でさらに置換されていてもよい2,8-ジアザスピロ[4.5]デカン環を形成し;
R2が、
(1)(a)ハロゲン原子、および
(b)C1-6アルキル基
から選択される1ないし3個の置換基で置換されていてもよいフェニル基、または
(2)(a)ハロゲン原子、
(b)シアノ基、
(c)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基、および
(d)シクロプロピル基
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基、オキサゾリル基、チアゾリル基、チアジアゾリル基、ピリジル基もしくはベンゾチアゾリル基であり;
X1が、炭素原子または窒素原子であり;
R3が、
(1)水素原子、または
(2)ハロゲン原子
であり;かつ
環Aが、
(1)(a)ハロゲン原子、および
(b)C1-6アルキル基
から選択される1ないし3個の置換基でそれぞれさらに置換されていてもよい、
(2)8-アザビシクロ[3.2.1]オクタン環、もしくは2,5-ジアザビシクロ[2.2.1]ヘプタン環である、[1]、[3]、[A]および[D]の何れかに記載の化合物またはその塩。
R1が、
(a)ハロゲン原子、
(b)シアノ基、
(c)カルバモイル基、および
(d)1ないし3個のC1-6アルコキシ基で置換されていてもよいC1-6アルキル基
から選択される1ないし3個の置換基で置換されていてもよいピロリジニル基であり;
R2が、
(a)ハロゲン原子、および
(b)C1-6アルキル基
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基、チアゾリル基、チアジアゾリル基またはピリジル基であり;
X1が、炭素原子であり;
R3が、水素原子であり;かつ
環Aが、
(2R)-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリルまたはその塩、
(2R)-1-((1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリルまたはその塩、
(2R)-4,4-ジフルオロ-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリルまたはその塩、
(3-フルオロアゼチジン-1-イル)(1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-イル)メタノンまたはその塩、
(1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)(3-フルオロアゼチジン-1-イル)メタノンまたはその塩、
(1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)((3S)-3-フルオロピロリジン-1-イル)メタノンまたはその塩、
(1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-イル)((3S)-3-フルオロピロリジン-1-イル)メタノンまたはその塩、
N-ベンジル-N-(2-フルオロエチル)-4-(4-フェニルピリミジン-5-イル)ピペラジン-1-カルボキサミドまたはその塩、
N-(4-フルオロベンジル)-N-(2-フルオロエチル)-4-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペラジン-1-カルボキサミドまたはその塩、
((3S)-3-フルオロピロリジン-1-イル)(1-(4-(5-メチル-1,3-チアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノンまたはその塩、
(3-フルオロアゼチジン-1-イル)(1-(4-(5-メチル-1,3-チアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノンまたはその塩、
(1-(4-(4-ブロモ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)(3-フルオロアゼチジン-1-イル)メタノンまたはその塩、または
(1-(4-(4-シクロプロピル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)(3-フルオロアゼチジン-1-イル)メタノンまたはその塩。
[9] (2R)-1-((1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリルまたはその塩。
[10] (2R)-4,4-ジフルオロ-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリルまたはその塩。
[11] [1]~[10]の何れかに記載の化合物またはその塩を含有してなる医薬。
[12] コレステロール24ヒドロキシラーゼ阻害剤である、[11]に記載の医薬。
[13] 癲癇または神経変性疾患の予防または治療剤である、[11]に記載の医薬。
[14] 神経変性疾患が、アルツハイマー病、軽度認知障害、ハンチントン病、パーキンソン病または多発性硬化症である、[13]に記載の医薬。
[15] 癲癇または神経変性疾患の予防または治療に使用するための、[1]~[10]の何れかに記載の化合物またはその塩。
[16] 神経変性疾患が、アルツハイマー病、軽度認知障害、ハンチントン病、パーキンソン病または多発性硬化症である、[15]に記載の化合物またはその塩。
[17] [1]~[10]の何れかに記載の化合物またはその塩を哺乳動物に有効量投与することを特徴とする、該哺乳動物におけるコレステロール24ヒドロキシラーゼの阻害方法。
[18] [1]~[10]の何れかに記載の化合物またはその塩を哺乳動物に有効量投与することを特徴とする、該哺乳動物における癲癇または神経変性疾患の予防または治療方法。
[19] 神経変性疾患が、アルツハイマー病、軽度認知障害、ハンチントン病、パーキンソン病または多発性硬化症である、[18]に記載の予防または治療方法。
[20] 癲癇または神経変性疾患の予防または治療剤を製造するための、[1]~[10]の何れかに記載の化合物またはその塩の使用。
[21] 神経変性疾患が、アルツハイマー病、軽度認知障害、ハンチントン病、パーキンソン病または多発性硬化症である、[20]に記載の使用。
本明細書中、「ハロゲン原子」とは、フッ素原子、塩素原子、臭素原子、ヨウ素原子を示す。
本明細書中、「C1-10アルキル基」とは、例えば、メチル、エチル、プロピル、イソプロピル、ブチル、2-メチルプロピル、1-メチルプロピル、tert-ブチル、ペンチル、イソペンチル、ネオペンチル、1-エチルプロピル、ヘキシル、イソヘキシル、1,1-ジメチルブチル、2,2-ジメチルブチル、3,3-ジメチルブチル、2-エチルブチル、ぺプチル、オクチル、ノニル、デシル等を示す。なかでも、C1-6アルキル基が好ましい。
本明細書中、「C1-6アルキル(基)」とは、例えば、メチル、エチル、プロピル、イソプロピル、ブチル、イソブチル、sec-ブチル、tert-ブチル、ペンチル、イソペンチル、ネオペンチル、1-エチルプロピル、ヘキシル、イソヘキシル、1,1-ジメチルブチル、2,2-ジメチルブチル、3,3-ジメチルブチル、2-エチルブチル等を示す。
本明細書中、「C2-10アルケニル基」とは、例えば、ビニル、1-プロペニル、2-プロペニル、2-メチル-1-プロペニル、1-ブテニル、2-ブテニル、3-ブテニル、3-メチル-2-ブテニル、1-ペンテニル、2-ペンテニル、3-ペンテニル、4-ペンテニル、4-メチル-3-ペンテニル、1-ヘキセニル、3-ヘキセニル、5-ヘキセニル、1-ぺプテニル、1-オクテニル等を示す。なかでも、C2-6アルケニル基が好ましい。
本明細書中、「C2-6アルケニル(基)」とは、例えば、ビニル、1-プロペニル、2-プロペニル、2-メチル-1-プロペニル、1-ブテニル、2-ブテニル、3-ブテニル、3-メチル-2-ブテニル、1-ペンテニル、2-ペンテニル、3-ペンテニル、4-ペンテニル、4-メチル-3-ペンテニル、1-ヘキセニル、3-ヘキセニル、5-ヘキセニル等を示す。
本明細書中、「C2-10アルキニル基」とは、例えば、エチニル、1-プロピニル、2-プロピニル、1-ブチニル、2-ブチニル、3-ブチニル、1-ペンチニル、2-ペンチニル、3-ペンチニル、4-ペンチニル、1,1-ジメチルプロプ-2-イン-1-イル、1-ヘキシニル、2-ヘキシニル、3-ヘキシニル、4-ヘキシニル、5-ヘキシニル、1-ぺプチニル、1-オクチニル等を示す。なかでも、C2-6アルキニル基が好ましい。
本明細書中、「C2-6アルキニル(基)」とは、例えば、エチニル、1-プロピニル、2-プロピニル、1-ブチニル、2-ブチニル、3-ブチニル、1-ペンチニル、2-ペンチニル、3-ペンチニル、4-ペンチニル、1,1-ジメチルプロプ-2-イン-1-イル、1-ヘキシニル、2-ヘキシニル、3-ヘキシニル、4-ヘキシニル、5-ヘキシニル等を示す。
本明細書中、「C1-3アルコキシ基」とは、メトキシ、エトキシ、プロポキシおよびイソプロポキシを示す。
本明細書中、「C2-6アルケニルオキシ(基)」とは、例えば、ビニルオキシ、1-プロペニルオキシ、2-プロペニルオキシ、2-メチル-1-プロペニルオキシ、1-ブテニルオキシ、2-ブテニルオキシ、3-ブテニルオキシ、3-メチル-2-ブテニルオキシ、1-ペンテニルオキシ、2-ペンテニルオキシ、3-ペンテニルオキシ、4-ペンテニルオキシ、4-メチル-3-ペンテニルオキシ、1-ヘキセニルオキシ、3-ヘキセニルオキシ、5-ヘキセニルオキシ等を示す。
本明細書中、「C2-6アルキニルオキシ(基)」とは、例えば、エチニルオキシ、1-プロピニルオキシ、2-プロピニルオキシ、1-ブチニルオキシ、2-ブチニルオキシ、3-ブチニルオキシ、1-ペンチニルオキシ、2-ペンチニルオキシ、3-ペンチニルオキシ、4-ペンチニルオキシ、1,1-ジメチルプロプ-2-イン-1-イルオキシ、1-ヘキシニルオキシ、2-ヘキシニルオキシ、3-ヘキシニルオキシ、4-ヘキシニルオキシ、5-ヘキシニルオキシ等を示す。
本明細書中、「C1-6アルキル-カルボニル(基)」とは、例えば、アセチル、プロパノイル、ブタノイル、2-メチルプロパノイル等を示す。
本明細書中、「ジ-C1-6アルキルアミノ(基)」とは、例えば、ジメチルアミノ、ジエチルアミノ、ジプロピルアミノ、ジイソプロピルアミノ、ジブチルアミノ、ジイソブチルアミノ、ジtert-ブチルアミノ等を示す。
本明細書中、「C3-8シクロアルキル(基)」とは、例えば、シクロプロピル、シクロブチル、シクロペンチル、シクロヘキシル、シクロヘプチル、シクロオクチル等を示す。
本明細書中、「C3-6シクロアルキル(基)」とは、例えば、上記C3-8シクロアルキル(基)のうち、炭素数が3ないし6個のものを示す。
本明細書中、「C3-8シクロアルキルオキシ(基)」とは、例えば、シクロプロピルオキシ、シクロブチルオキシ、シクロペンチルオキシ、シクロヘキシルオキシ、シクロヘプチルオキシ、シクロオクチルオキシ等を示す。
本明細書中、「C3-6シクロアルキルオキシ(基)」とは、例えば、シクロプロピルオキシ、シクロブチルオキシ、シクロペンチルオキシ、シクロヘキシルオキシ等を示す。
本明細書中、「C3-8シクロアルケニル(基)」とは、例えば、シクロプロペニル(例、2-シクロプロペン-1-イル)、シクロブテニル(例、2-シクロブテン-1-イル)、シクロペンテニル(例、2-シクロペンテン-1-イル、3-シクロペンテン-1-イル)、シクロヘキセニル(例、2-シクロヘキセン-1-イル、3-シクロヘキセン-1-イル)等を示す。
本明細書中、「C3-8シクロアルケニルオキシ(基)」とは、例えば、シクロプロペニルオキシ(例、2-シクロプロペン-1-イルオキシ)、シクロブテニルオキシ(例、2-シクロブテン-1-イルオキシ)、シクロペンテニルオキシ(例、2-シクロペンテン-1-イルオキシ、3-シクロペンテン-1-イルオキシ)、シクロヘキセニルオキシ(例、2-シクロヘキセン-1-イルオキシ、3-シクロヘキセン-1-イルオキシ)等を示す。
本明細書中、「C4-10シクロアルカジエニル基」とは、例えば、1,3-シクロブタジエン-1-イル、1,3-シクロペンタジエン-1-イル、1,4-シクロペンタジエン-1-イル、2,4-シクロペンタジエン-1-イル、1,3-シクロヘキサジエン-1-イル、1,4-シクロヘキサジエン-1-イル、1,5-シクロヘキサジエン-1-イル、2,4-シクロヘキサジエン-1-イル、2,5-シクロヘキサジエン-1-イル、1,3-シクロオクタジエン-1-イル、1,4-シクロオクタジエン-1-イル、1,5-シクロオクタジエン-1-イル、1,6-シクロオクタジエン-1-イル、1,7-シクロオクタジエン-1-イル、2,4-シクロオクタジエン-1-イル、2,5-シクロオクタジエン-1-イル、2,6-シクロオクタジエン-1-イル、2,7-シクロオクタジエン-1-イル、3,5-シクロオクタジエン-1-イル、3,6-シクロオクタジエン-1-イル等を示す。なかでも、C4-6シクロアルカジエニル基が好ましい。
本明細書中、「C4-6シクロアルカジエニル基」とは、例えば、1,3-シクロブタジエン-1-イル、1,3-シクロペンタジエン-1-イル、1,4-シクロペンタジエン-1-イル、2,4-シクロペンタジエン-1-イル、1,3-シクロヘキサジエン-1-イル、1,4-シクロヘキサジエン-1-イル、1,5-シクロヘキサジエン-1-イル、2,4-シクロヘキサジエン-1-イル、2,5-シクロヘキサジエン-1-イル等を示す。
本明細書中、「C6-14アリールオキシ(基)」とは、例えば、フェノキシ、1-ナフチルオキシ、2-ナフチルオキシ等を示す。
本明細書中、「C7-14アラルキル(基)」とは、例えば、ベンジル、フェネチル等を示す。
本明細書中、「C7-14アラルキルオキシ(基)」とは、例えば、ベンジルオキシ、フェネチルオキシ等を示す。
本明細書中、「C8-13アリールアルケニル(基)」とは、例えば、スチリル等を示す。
本明細書中、「芳香族複素環基」とは、単環式芳香族複素環基または縮合芳香族複素環基を示す。例えば、5ないし12員の芳香族複素環基、具体的には、5ないし7員の単環式芳香族複素環基または8ないし12員の縮合芳香族複素環基を示す。
本明細書中、「単環式芳香族複素環基」としては、例えば、環構成原子として炭素原子以外に酸素原子、硫黄原子(酸化されていてもよい)および窒素原子(酸化されていてもよい)から選ばれるヘテロ原子を1ないし4個含有する、5ないし7員(好ましくは、5または6員)の単環式芳香族複素環基、例えば、フリル(例、2-フリル、3-フリル)、チエニル(例、2-チエニル、3-チエニル)、ピリジル(例、2-ピリジル、3-ピリジル、4-ピリジル)、ピリミジニル(例、2-ピリミジニル、4-ピリミジニル、5-ピリミジニル)、ピリダジニル(例、3-ピリダジニル、4-ピリダジニル)、ピラジニル(例、2-ピラジニル)、ピロリル(例、1-ピロリル、2-ピロリル、3-ピロリル)、イミダゾリル(例、1-イミダゾリル、2-イミダゾリル、4-イミダゾリル、5-イミダゾリル)、ピラゾリル(例、1-ピラゾリル、3-ピラゾリル、4-ピラゾリル)、チアゾリル(例、2-チアゾリル、4-チアゾリル、5-チアゾリル)、イソチアゾリル(例、3-イソチアゾリル、4-イソチアゾリル、5-イソチアゾリル)、オキサゾリル(例、2-オキサゾリル、4-オキサゾリル、5-オキサゾリル)、イソオキサゾリル(例、3-イソオキサゾリル、4-イソオキサゾリル、5-イソオキサゾリル)、オキサジアゾリル(例、1,2,4-オキサジアゾール-5-イル、1,3,4-オキサジアゾール-2-イル)、チアジアゾリル(例、1,3,4-チアジアゾール-2-イル)、トリアゾリル(例、1,2,4-トリアゾール-1-イル、1,2,4-トリアゾール-3-イル、1,2,3-トリアゾール-1-イル、1,2,3-トリアゾール-2-イル、1,2,3-トリアゾール-4-イル)、テトラゾリル(例、テトラゾール-1-イル、テトラゾール-5-イル)、トリアジニル(例、1,2,4-トリアジン-1-イル、1,2,4-トリアジン-3-イル)等が挙げられる。
本明細書中、「単環式非芳香族複素環基」としては、例えば、環構成原子として炭素原子以外に酸素原子、硫黄原子(酸化されていてもよい)および窒素原子(酸化されていてもよい)から選ばれるヘテロ原子を1ないし4個含有する、3ないし8員(好ましくは、5または6員)の単環式非芳香族複素環基、例えば、アゼチジニル(例、1-アゼチジニル、2-アゼチジニル)、ピロリジニル(例、1-ピロリジニル、2-ピロリジニル)、ピペリジル(例、ピペリジノ、2-ピペリジル、3-ピペリジル、4-ピペリジル)、モルホリニル(例、モルホリノ)、チオモルホリニル(例、チオモルホリノ)、ピペラジニル(例、1-ピペラジニル、2-ピペラジニル、3-ピペラジニル)、オキサゾリジニル(例、オキサゾリジン-2-イル)、チアゾリジニル(例、チアゾリジン-2-イル)、ジヒドロチオピラニル(例、ジヒドロチオピラン-3-イル、ジヒドロチオピラン-4-イル)、イミダゾリジニル(例、イミダゾリジン-2-イル、イミダゾリジン-3-イル)、オキサゾリニル(例、オキサゾリン-2-イル)、チアゾリニル(例、チアゾリン-2-イル)、イミダゾリニル(例、イミダゾリン-2-イル、イミダゾリン-3-イル)、ジオキソリル(例、1,3-ジオキソール-4-イル)、ジオキソラニル(例、1,3-ジオキソラン-4-イル)、ジヒドロオキサジアゾリル(例、4,5-ジヒドロ-1,2,4-オキサジアゾール-3-イル)、ピラニル(例、2-ピラニル、4-ピラニル)、テトラヒドロピラニル(例、2-テトラヒドロピラニル、3-テトラヒドロピラニル、4-テトラヒドロピラニル)、チオピラニル(例、4-チオピラニル)、テトラヒドロチオピラニル(例、2-テトラヒドロチオピラニル、3-テトラヒドロチオピラニル、4-テトラヒドロチオピラニル)、1-オキシドテトラヒドロチオピラニル(例、1-オキシドテトラヒドロチオピラン-4-イル)、1,1-ジオキシドテトラヒドロチオピラニル(例、1,1-ジオキシドテトラヒドロチオピラン-4-イル)、テトラヒドロフリル(例、テトラヒドロフラン-3-イル、テトラヒドロフラン-2-イル)、オキセタニル(例、オキセタン-2-イル、オキセタン-3-イル)、ピラゾリジニル(例、ピラゾリジン-1-イル、ピラゾリジン-3-イル)、ピラゾリニル(例、ピラゾリン-1-イル)、テトラヒドロピリミジニル(例、テトラヒドロピリミジン-1-イル)、ジヒドロトリアゾリル(例、2,3-ジヒドロ-1H-1,2,3-トリアゾール-1-イル)、テトラヒドロトリアゾリル(例、2,3,4,5-テトラヒドロ-1H-1,2,3-トリアゾール-1-イル)、アゼパニル(例、1-アゼパニル、2-アゼパニル、3-アゼパニル、4-アゼパニル)、ジヒドロピリジル(例、ジヒドロピリジン-1-イル、ジヒドロピリジン-2-イル、ジヒドロピリジン-3-イル、ジヒドロピリジン-4-イル)、テトラヒドロピリジル(例、1,2,3,4-テトラヒドロピリジン-1-イル、1,2,3,4-テトラヒドロピリジン-2-イル、1,2,3,4-テトラヒドロピリジン-3-イル、1,2,3,4-テトラヒドロピリジン-4-イル)等が挙げられる。
本明細書中、「C3-10シクロアルカン」とは、例えば、シクロプロパン、シクロブタン、シクロペンタン、シクロヘキサン、シクロヘプタン、シクロオクタン、シクロノナン、シクロデカン等を示す。
本明細書中、「C3-10シクロアルケン」とは、例えば、シクロプロペン、シクロブテン、シクロペンテン、シクロヘキセン、シクロオクテン、シクロノネン、シクロデセン等を示す。
本明細書中、「C4-10シクロアルカジエン」とは、例えば、1,3-シクロブタジエン、1,3-シクロペンタジエン、1,4-シクロペンタジエン、2,4-シクロペンタジエン、1,3-シクロヘキサジエン、1,4-シクロヘキサジエン、1,5-シクロヘキサジエン、2,4-シクロヘキサジエン、2,5-シクロヘキサジエン、1,3-シクロオクタジエン、1,4-シクロオクタジエン、1,5-シクロオクタジエン、1,6-シクロオクタジエン、1,7-シクロオクタジエン、2,4-シクロオクタジエン、2,5-シクロオクタジエン、2,6-シクロオクタジエン、2,7-シクロオクタジエン、3,5-シクロオクタジエン、3,6-シクロオクタジエン等を示す。
(1) ハロゲン原子;
(2) シアノ基;
(3) ニトロ基;
(4) ヒドロキシ基;
(5)(a) ハロゲン原子、
(b) シアノ基、
(c) 1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基、
および
(d) 1ないし3個のハロゲン原子で置換されていてもよいC1-6アルコキシ基
から選ばれる1ないし3個の置換基で置換されていてもよいC3-8シクロアルキル基;
(6)(a) ハロゲン原子、
(b) シアノ基、
(c) 1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基、および
(d) 1ないし3個のハロゲン原子で置換されていてもよいC1-6アルコキシ基
から選ばれる1ないし3個の置換基で置換されていてもよいC6-14アリール基;
(7)(a) ハロゲン原子、
(b) シアノ基、
(c) ハロゲン原子を1ないし3個有していてもよいC3-8シクロアルキル基、
(d) ハロゲン原子を1ないし3個有していてもよいC3-8シクロアルケニル基、
(e) ハロゲン原子を1ないし3個有していてもよいC6-14アリール基、および
(f) 5または6員の単環式芳香族複素環基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルコキシ基;
(8) ハロゲン原子を1ないし3個有していてもよいC2-6アルケニルオキシ基(例、ビニルオキシ、プロペニルオキシ、ブテニルオキシ、ペンテニルオキシ、へキセニルオキシ);
(9) ハロゲン原子を1ないし3個有していてもよいC2-6アルキニルオキシ基(例、エチニルオキシ、プロピニルオキシ、ブチニルオキシ、ペンチニルオキシ、ヘキシニルオキシ);
(10) ハロゲン原子を1ないし3個有していてもよいC3-8シクロアルキルオキシ基(例、シクロプロピルオキシ、シクロブチルオキシ、シクロペンチルオキシ、シクロヘキシルオキシ);
(11) ハロゲン原子を1ないし3個有していてもよいC3-8シクロアルケニルオキシ基(例、シクロプロペニルオキシ、シクロブテニルオキシ、シクロペンテニルオキシ、シクロヘキセニルオキシ);
(12) ハロゲン原子を1ないし3個有していてもよいC6-14アリールオキシ基;
(13) ハロゲン原子を1ないし3個有していてもよいC7-14アラルキルオキシ基;
(14)(a) C1-6アルキル基、
(b) C3-6シクロアルキル基、
(c) C6-14アリール基、
(d) C1-6アルコキシ基、
(e) 5または6員の単環式芳香族複素環基、
(f) 8ないし12員の縮合芳香族複素環基、
(g) 3ないし8員の単環式非芳香族複素環基、および
(h) 8ないし12員の縮合非芳香族複素環基
から選ばれる置換基でモノまたはジ置換されていてもよいカルバモイル基;
(15)(a) C1-6アルキル基、
(b) C3-6シクロアルキル基、
(c) C6-14アリール基、
(d) C1-6アルコキシ基、
(e) 5または6員の単環式芳香族複素環基、
(f) 8ないし12員の縮合芳香族複素環基、
(g) 3ないし8員の単環式非芳香族複素環基、および
(h) 8ないし12員の縮合非芳香族複素環基
から選ばれる置換基でモノまたはジ置換されていてもよいスルファモイル基;
(16) ホルミル基;
(17) C1-6アルキル-カルボニル基;
(18) C2-6アルケニル-カルボニル基(例、アクリロイル、ブテノイル、ペンテノイル、ヘキセノイル、ヘプテノイル);
(19) C2-6アルキニル-カルボニル基(例、プロピオロイル、プロピニルカルボニル、ブチニルカルボニル、ペンチニルカルボニル、ヘキシニルカルボニル);
(20) C3-8シクロアルキル-カルボニル基(例、シクロプロピルカルボニル、シクロブチルカルボニル、シクロペンチルカルボニル、シクロヘキシルカルボニル);
(21) C3-8シクロアルケニル-カルボニル基(例、シクロプロペニルカルボニル、シクロブテニルカルボニル、シクロペンテニルカルボニル、シクロヘキセニルカルボニル);
(22) C6-14アリール-カルボニル基(例、ベンゾイル、1-ナフチルカルボニル、2-ナフチルカルボニル);
(23) C3-8シクロアルキル-C1-6アルキル-カルボニル基(例、シクロプロピルアセチル、3-シクロプロピルプロピオニル、シクロブチルアセチル、シクロペンチルアセチル、シクロヘキシルアセチル、シクロヘキシルプロピオニル);
(24) C3-8シクロアルケニル-C1-6アルキル-カルボニル基(例、シクロペンテニルアセチル、シクロヘキセニルアセチル、3-シクロヘキセニルプロピオニル、3-シクロヘキセニルプロピオニル);
(25) C7-14アラルキル-カルボニル基(例、フェニルアセチル、3-フェニルプロピオニル);
(26) 5または6員の単環式芳香族複素環カルボニル基(例、フリルカルボニル、チエニルカルボニル、ピロリルカルボニル、オキサゾリルカルボニル、イソオキサゾリルカルボニル、チアゾリルカルボニル、イソチアゾリルカルボニル、イミダゾリルカルボニル、ピリジルカルボニル、ピラゾリルカルボニル);
(27) 8ないし12員の縮合芳香族複素環カルボニル基(例、ベンゾフラニルカルボニル、イソベンゾフラニルカルボニル、ベンゾチエニルカルボニル、イソベンゾチエニルカルボニル、インドリルカルボニル、イソインドリルカルボニル、インダゾリルカルボニル、ベンズイミダゾリルカルボニル、ベンズオキサゾリルカルボニル);
(28) 3ないし8員の単環式非芳香族複素環カルボニル基(例、オキシラニルカルボニル、アゼチジニルカルボニル、オキセタニルカルボニル、チエタニルカルボニル、ピロリジニルカルボニル、テトラヒドロフリルカルボニル、チオラニルカルボニル、ピペリジルカルボニル);
(29) 8ないし12員の縮合非芳香族複素環カルボニル基(例、ジヒドロベンゾフラニル);
(30)(a) ハロゲン原子を1ないし3個有していてもよいC1-6アルキル基、
(b) ハロゲン原子を1ないし3個有していてもよいC1-6アルキル-カルボニル基、
(c) C3-8シクロアルキル-カルボニル基、
(d) ハロゲン原子を1ないし3個有していてもよいC6-14アリール-カルボニル基、
(e) 5または6員の単環式芳香族複素環カルボニル基、
(f) 8ないし12員の縮合芳香族複素環カルボニル基、
(g) 3ないし8員の単環式非芳香族複素環カルボニル基、および
(h) 8ないし12員の縮合非芳香族複素環カルボニル基
から選ばれる置換基でモノまたはジ置換されていてもよいアミノ基;
(31) スルファニル基;
(32) C1-6アルキルスルファニル基(例、メチルスルファニル、エチルスルファニル);
(33) C2-6アルケニルスルファニル基(例、ビニルスルファニル、プロペニルスルファニル);
(34) C2-6アルキニルスルファニル基(例、エチニルスルファニル、プロピニルスルファニル);
(35) C3-8シクロアルキルスルファニル基(例、シクロプロピルスルファニル、シクロブチルスルファニル);
(36) C3-8シクロアルケニルスルファニル基(例、シクロプロペニルスルファニル、シクロブテニルスルファニル);
(37) C6-14アリールスルファニル基(例、フェニルスルファニル);
(38) C3-8シクロアルキル-C1-6アルキルスルファニル基(例、シクロプロピルメチルスルファニル);
(39) C3-8シクロアルケニル-C1-6アルキルスルファニル基(例、シクロペンテニルメチルスルファニル);
(40) C1-6アルキルスルフィニル基(例、メチルスルフィニル、エチルスルフィニル);
(41) C2-6アルケニルスルフィニル基(例、ビニルスルフィニル、プロペニルスルフィニル);
(42) C2-6アルキニルスルフィニル基(例、エチニルスルフィニル、プロピニルスルフィニル);
(43) C3-8シクロアルキルスルフィニル基(例、シクロプロピルスルフィニル、シクロブチルスルフィニル);
(44) C3-8シクロアルケニルスルフィニル基(例、シクロプロペニルスルフィニル、シクロブテニルスルフィニル);
(45) C6-14アリールスルフィニル基(例、フェニルスルフィニル);
(46) C3-8シクロアルキル-C1-6アルキルスルフィニル基(例、シクロプロピルメチルスルフィニル);
(47) C3-8シクロアルケニル-C1-6アルキルスルフィニル基(例、シクロペンテニルメチルスルフィニル);
(48) C1-6アルキルスルホニル基(例、メチルスルホニル、エチルスルホニル);
(49) C2-6アルケニルスルホニル基(例、ビニルスルホニル、プロペニルスルホニル);
(50) C2-6アルキニルスルホニル基(例、エチニルスルホニル、プロピニルスルホニル);
(51) C3-8シクロアルキルスルホニル基(例、シクロプロピルスルホニル、シクロブチルスルホニル);
(52) C3-8シクロアルケニルスルホニル基(例、シクロプロペニルスルホニル、シクロブテニルスルホニル);
(53) C6-14アリールスルホニル基(例、フェニルスルホニル);
(54) C3-8シクロアルキル-C1-6アルキルスルホニル基(例、シクロプロピルメチルスルホニル);
(55) C3-8シクロアルケニル-C1-6アルキルスルホニル基(例、シクロペンテニルメチルスルホニル);
(56) C6-14アリール-C1-6アルキルスルホニル基(例、ベンジルスルホニル);
(57) 5または6員の単環式芳香族複素環スルホニル基(例、フリルスルホニル、チエニルスルホニル、ピリジルスルホニル);
(58) 8ないし12員の縮合芳香族複素環スルホニル基(例、ベンゾフラニルスルホニル、イソベンゾフラニルスルホニル);
(59) 3ないし8員の単環式非芳香族複素環スルホニル基(例、オキシラニルスルホニル、アゼチジニルスルホニル);
(60) 8ないし12員の縮合非芳香族複素環スルホニル基(例、ジヒドロベンゾフラニルスルホニル);
(61)(a) ハロゲン原子、
(b) 1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基、および
(c) 1ないし3個のハロゲン原子で置換されていてもよいC1-6アルコキシ基
から選ばれる1ないし3個の置換基で置換されていてもよい5または6員の単環式芳香族複素環基(例、フリル、チエニル、ピロリル、オキサゾリル、イソオキサゾリル、チアゾリル、イソチアゾリル、イミダゾリル、ピリジル、ピラゾリル、モルホリニル);
(62)(a) ハロゲン原子、
(b) 1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基、および
(c) 1ないし3個のハロゲン原子で置換されていてもよいC1-6アルコキシ基
から選ばれる1ないし3個の置換基で置換されていてもよい8ないし12員の縮合芳香族複素環基(例、ベンゾフラニル、イソベンゾフラニル、ベンゾチエニル、イソベンゾチエニル、インドリル、イソインドリル、インダゾリル、ベンズイミダゾリル、ベンズオキサゾリル);
(63)(a) ハロゲン原子、
(b) 1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基、
(c) 1ないし3個のハロゲン原子で置換されていてもよいC1-6アルコキシ基、および
(d) オキソ基
から選ばれる1ないし3個の置換基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、オキシラニル、アゼチジニル、オキセタニル、チエタニル、ピロリジニル、テトラヒドロフリル、チオラニル、ピペリジル、ピペラジニル、ジヒドロオキサジアゾリル、チアゾリニル);
(64)(a) ハロゲン原子、
(b) 1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基、
(c) 1ないし3個のハロゲン原子で置換されていてもよいC1-6アルコキシ基、および
(d) オキソ基
から選ばれる1ないし3個の置換基で置換されていてもよい8ないし12員の縮合非芳香族複素環基(例、ジヒドロベンゾフラニル);
(65) 5または6員の単環式芳香族複素環オキシ基(例、フリルオキシ、チエニルオキシ、ピロリルオキシ、オキサゾリルオキシ、イソオキサゾリルオキシ、チアゾリルオキシ、イソチアゾリルオキシ、イミダゾリルオキシ、ピリジルオキシ、ピラゾリルオキシ);
(66) 8ないし12員の縮合芳香族複素環オキシ基(例、ベンゾフラニルオキシ、イソベンゾフラニルオキシ、ベンゾチエニルオキシ、イソベンゾチエニルオキシ、インドリルオキシ、イソインドリルオキシ、インダゾリルオキシ、ベンズイミダゾリルオキシ、ベンズオキサゾリルオキシ);
(67) 3ないし8員の単環式非芳香族複素環オキシ基(例、オキシラニルオキシ、アゼチジニルオキシ、オキセタニルオキシ、チエタニルオキシ、ピロリジニルオキシ、テトラヒドロフリルオキシ、チオラニルオキシ、ピペリジルオキシ);
(68) 8ないし12員の縮合非芳香族複素環オキシ基(例、ジヒドロベンゾフラニルオキシ);
(69) カルボキシ基;
(70) C1-6アルコキシ-カルボニル基;
(71) C2-6アルケニルオキシ-カルボニル基(例、ビニルオキシカルボニル、プロペニルオキシカルボニル、ブテニルオキシカルボニル、ペンテニルオキシカルボニル、へキセニルオキシカルボニル);
(72) C2-6アルキニルオキシ-カルボニル基(例、エチニルオキシカルボニル、プロピニルオキシカルボニル、ブチニルオキシカルボニル、ペンチニルオキシカルボニル、ヘキシニルオキシカルボニル);
(73) C3-8シクロアルキルオキシ-カルボニル基(例、シクロプロピルオキシカルボニル、シクロブチルオキシカルボニル、シクロペンチルオキシカルボニル、シクロヘキシルオキシカルボニル);
(74) C3-8シクロアルケニルオキシ-カルボニル基(例、シクロプロペニルオキシカルボニル、シクロブテニルオキシカルボニル、シクロペンテニルオキシカルボニル、シクロヘキセニルオキシカルボニル);
(75) C6-14アリールオキシ-カルボニル基(例、フェノキシカルボニル、1-ナフチルオキシカルボニル、2-ナフチルオキシカルボニル);
(76) C3-8シクロアルキル-C1-6アルコキシ-カルボニル基(例、シクロプロピルメチルオキシカルボニル、シクロプロピルエチルオキシカルボニル、シクロブチルメチルオキシカルボニル、シクロペンチルメチルオキシカルボニル、シクロヘキシルメチルオキシカルボニル、シクロヘキシルエチルオキシカルボニル);
(77) C3-8シクロアルケニル-C1-6アルコキシ-カルボニル基(例、シクロペンテニルメチルオキシカルボニル、シクロヘキセニルメチルオキシカルボニル、シクロヘキセニルエチルオキシカルボニル、シクロヘキセニルプロピルオキシカルボニル);
(78) C7-14アラルキルオキシ-カルボニル基(例、ベンジルオキシカルボニル、フェネチルオキシカルボニル);
(79) モノ-C1-6アルキルチオカルバモイル基(例、メチルチオカルバモイル、エチルチオカルバモイル、プロピルチオカルバモイル);
(80) ジ-C1-6アルキルチオカルバモイル基(例、ジメチルチオカルバモイル、ジエチルチオカルバモイル、ジプロピルチオカルバモイル);
(81) C1-6アルキル-カルボニルオキシ基(例、アセチルオキシ、プロパノイルオキシ、ブタノイルオキシ、2-メチルプロパノイルオキシ);
(82) ヒドロキシ基で置換されていてもよいイミノ基;および
(83) C1-6アルキレンジオキシ基(例、メチレンジオキシ、エチレンジオキシ)。
(1) 上記置換基A群;
(2)(a) ハロゲン原子、
(b) シアノ基、
(c) ヒドロキシ基、
(d)(i) ハロゲン原子、
(ii) シアノ基、および
(iii) 1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基
から選ばれる1ないし3個の置換基で置換されていてもよいC3-8シクロアルキル基;
(e)(i) ハロゲン原子、
(ii) シアノ基、および
(iii) 1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基
から選ばれる1ないし3個の置換基で置換されていてもよいC6-14アリール基、
(f) 1ないし3個のハロゲン原子で置換されていてもよいC1-6アルコキシ基、
(g) C1-6アルキル基でモノまたはジ置換されていてもよいアミノ基、
(h) 5または6員の単環式芳香族複素環基、
(i) 8ないし12員の縮合芳香族複素環基、
(j) 3ないし8員の単環式非芳香族複素環基、
(k) 8ないし12員の縮合非芳香族複素環基、
(l) カルボキシ基、および
(m) 1ないし3個のハロゲン原子で置換されていてもよいC1-6アルコキシ-カルボニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基;
(3)(a) ハロゲン原子、
(b) ヒドロキシ基、
(c) C1-6アルコキシ基、
(d) C1-6アルキル基でモノまたはジ置換されていてもよいアミノ基、
(e) カルボキシ基、および
(f) C1-6アルコキシ-カルボニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC2-6アルケニル基;
(4)(a) ハロゲン原子、
(b) ヒドロキシ基、
(c) C1-6アルコキシ基、および
(d) 1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基
から選ばれる1ないし3個の置換基で置換されていてもよいC7-14アラルキル基;および
(5) オキソ基。
(1)ホルミル基;
(2)カルボキシ基;
(3)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル-カルボニル基(例、アセチル);
(4)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルコキシ-カルボニル基(例、メトキシカルボニル、エトキシカルボニル、プロポキシカルボニル、tert-ブトキシカルボニル);
(5)C3-10シクロアルキル-カルボニル基(例、シクロプロピルカルボニル、シクロペンチルカルボニル、シクロヘキシルカルボニル);
(6)1ないし3個のハロゲン原子で置換されていてもよいC6-14アリール-カルボニル基(例、ベンゾイル、1-ナフトイル、2-ナフトイル);
(7)(a)ハロゲン原子、C1-6アルコキシ基、C1-6アルコキシ-カルボニル基およびカルボキシ基から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、および
(b)C1-6アルコキシ-カルボニル基でモノまたはジ置換されていてもよいアミノ基
から選ばれる置換基でモノまたはジ置換されていてもよいカルバモイル基;
(8)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキルスルホニル基(例、メチルスルホニル、エチルスルホニル、イソプロピルスルホニル);
(9)C6-14アリールスルホニル基(例、ベンゼンスルホニル);
(10)スルファモイル基;
(11)チオカルバモイル基;
(12)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基から選ばれる1ないし3個の置換基で置換されていてもよい芳香族複素環カルボニル基(例、フリルカルボニル、チエニルカルボニル);
(13)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基から選ばれる1ないし3個の置換基で置換されていてもよい非芳香族複素環カルボニル基(例、テトラヒドロフリルカルボニル、ピロリジノカルボニル);
等が挙げられる。
R1が環A上の原子と結合して環Aとともに形成する「それぞれ、オキソ基で置換され、かつさらに置換されていてもよい、スピロ環または縮合環」の「スピロ環または縮合環」は、置換可能な位置に1ないし5個(好ましくは1ないし3個)の置換基を有していてもよい。このような置換基としては、例えば、上記置換基群Bが挙げられる。置換基が複数存在する場合、各置換基は、同一でも異なっていてもよい。
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいC6-14アリール基(例、フェニル)、
(c)C6-14アリールオキシ基(例、フェノキシ)、
(d)C3-8シクロアルキル基(例、シクロプロピル)、
(e)5または6員の単環式芳香族複素環基(例、ピラゾリル)、
(f)8ないし12員の縮合芳香族複素環基(例、インダゾリル)、および
(g)1ないし3個のオキソ基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、ジヒドロピリジル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(2)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC1-6アルコキシ基(例、メトキシ、tert-ブトキシ、好ましくはC1-3アルコキシ基(例、メトキシ))、
(3)(a)(i)ハロゲン原子(例、フッ素原子)、
(ii)シアノ基、
(iii)C3-8シクロアルキル基(例、シクロプロピル、シクロブチル)、
(iv)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)、
(v) 5または6員の単環式芳香族複素環基(例、ピリジル)、および
(vi)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、オキセタニル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC3-8シクロアルキル基(例、シクロプロピル、シクロブチル、シクロペンチル)、
(c)C6-14アリール基(例、フェニル)、および
(d)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、テトラヒドロピラニル、オキセタニル、テトラヒドロフリル、ピロリジニル)
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC3-8シクロアルキル基(例、シクロプロピル)、
(5)C6-14アリール基(例、フェニル)、または
(6)(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)カルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基(例、メトキシ)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル、イソプロピル)、
(g)C1-6アルコキシ基(例、メトキシ、エトキシ、イソプロポキシ)、
(h)C1-6アルコキシ-カルボニル基(例、メトキシカルボニル)、および
(i)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)
から選択される1ないし5個の置換基で置換されていてもよい3ないし12員の非芳香族複素環基(好ましくは、3ないし8員の単環式非芳香族複素環基(例、アゼチジニル、ピロリジニル、ピペリジル、ピペラジニル、モルホリニル、1,1-ジオキシドチオモルホリニル、テトラヒドロピラニル、3-オキサ-6-アザビシクロ[3.1.1]へプチル、8-オキサ-3-アザビシクロ[3.2.1]オクチル、2-オキサ-5-アザビシクロ[2.2.1]ヘプチル、3-オキサ-8-アザビシクロ[3.2.1]オクチル、6-オキサ-3-アザビシクロ[3.1.1]へプチル))
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基(例、メチル)でさらに置換されていてもよいスピロ環(例、2,8-ジアザスピロ[4.5]デカン)を形成する。
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいC6-14アリール基(例、フェニル)、
(c)C6-14アリールオキシ基(例、フェノキシ)、
(d)C3-8シクロアルキル基(例、シクロプロピル)、
(e)5または6員の単環式芳香族複素環基(例、ピラゾリル)、
(f)8ないし12員の縮合芳香族複素環基(例、インダゾリル)、および
(g)1ないし3個のオキソ基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、ジヒドロピリジル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(2)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC1-6アルコキシ基(例、メトキシ、tert-ブトキシ、好ましくはC1-3アルコキシ基(例、メトキシ))、
(3)(a)(i)ハロゲン原子(例、フッ素原子)、
(ii)シアノ基、
(iii)C3-8シクロアルキル基(例、シクロプロピル、シクロブチル)、
(iv)ハロゲン原子(例、フッ素原子)およびC1-6アルコキシ基(例、メトキシ)から選ばれる1ないし3個の置換基で置換されていてもよいC6-14アリール基(例、フェニル)、
(v)5または6員の単環式芳香族複素環基(例、ピリジル)、および
(vi)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、オキセタニル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC3-8シクロアルキル基(例、シクロプロピル、シクロブチル、シクロペンチル)、
(c)C6-14アリール基(例、フェニル)、および
(d)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、テトラヒドロピラニル、オキセタニル、テトラヒドロフリル、ピロリジニル)
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC3-8シクロアルキル基(例、シクロプロピル)、
(5)C6-14アリール基(例、フェニル)、または
(6)(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)C1-6アルキル基(例、メチル)でモノまたはジ置換されていてもよいカルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基(例、メトキシ)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル、イソプロピル)、
(g)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルコキシ基(例、メトキシ、エトキシ、イソプロポキシ)、
(h)C1-6アルコキシ-カルボニル基(例、メトキシカルボニル)、および
(i)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)
から選択される1ないし5個の置換基で置換されていてもよい3ないし12員の非芳香族複素環基(好ましくは、3ないし8員の単環式非芳香族複素環基(例、アゼチジニル、ピロリジニル、ピペリジル、ピペラジニル、モルホリニル、1,1-ジオキシドチオモルホリニル、テトラヒドロピラニル、3-オキサ-6-アザビシクロ[3.1.1]へプチル、8-オキサ-3-アザビシクロ[3.2.1]オクチル、2-オキサ-5-アザビシクロ[2.2.1]ヘプチル、3-オキサ-8-アザビシクロ[3.2.1]オクチル、6-オキサ-3-アザビシクロ[3.1.1]へプチル)、3,7-ジオキサ-9-アザビシクロ[3.3.1]ノニル)
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基(例、メチル)でさらに置換されていてもよいスピロ環(例、2,8-ジアザスピロ[4.5]デカン)を形成する。
(1)(a)C3-8シクロアルキル基(例、シクロプロピル)、および
(b)8ないし12員の縮合芳香族複素環基(例、インダゾリル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(2)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC1-6アルコキシ基(好ましくはC1-3アルコキシ基(例、メトキシ))、
(3)(a)(i)ハロゲン原子(例、フッ素原子)、
(ii)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)、
(iii)5または6員の単環式芳香族複素環基(例、ピリジル)、および
(iv)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、オキセタニル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(b)C3-8シクロアルキル基(例、シクロプロピル、シクロペンチル)、
(c)3ないし8員の単環式非芳香族複素環基(例、テトラヒドロピラニル、テトラヒドロフリル)、および
(d)C6-14アリール基(例、フェニル)
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)C3-8シクロアルキル基(例、シクロプロピル)、または
(5)(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)カルバモイル基、
(d)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいC1-6アルキル基(例、メチル、イソプロピル)、
(e)C1-6アルコキシ基(例、メトキシ)、および
(f)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)
から選択される1ないし5個の置換基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、アゼチジニル、ピロリジニル、1,1-ジオキシドチオモルホリニル、3-オキサ-6-アザビシクロ[3.1.1]へプチル)
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基(例、メチル)でさらに置換されていてもよいスピロ環(例、2,8-ジアザスピロ[4.5]デカン)を形成する。
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいC6-14アリール基(例、フェニル)、
(c)C6-14アリールオキシ基(例、フェノキシ)、
(d)C3-8シクロアルキル基(例、シクロプロピル)、
(e)5または6員の単環式芳香族複素環基(例、ピラゾリル)、
(f)8ないし12員の縮合芳香族複素環基(例、インダゾリル)、および
(g)1ないし3個のオキソ基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、ジヒドロピリジル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(2)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC1-6アルコキシ基(例、メトキシ、tert-ブトキシ、好ましくはC1-3アルコキシ基(例、メトキシ))、
(3)(a)(i)ハロゲン原子(例、フッ素原子)、
(ii)シアノ基、
(iii)C3-8シクロアルキル基(例、シクロプロピル、シクロブチル)、
(iv)ハロゲン原子(例、フッ素原子)およびC1-6アルコキシ基(例、メトキシ)から選ばれる1ないし3個の置換基で置換されていてもよいC6-14アリール基(例、フェニル)、
(v) 5または6員の単環式芳香族複素環基(例、ピリジル)、および
(vi)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、オキセタニル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC3-8シクロアルキル基(例、シクロプロピル、シクロブチル、シクロペンチル)、
(c)C6-14アリール基(例、フェニル)、および
(d)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、テトラヒドロピラニル、オキセタニル、テトラヒドロフリル、ピロリジニル)
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC3-8シクロアルキル基(例、シクロプロピル)、
(5)C6-14アリール基(例、フェニル)、または
(6)(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)C1-6アルキル基(例、メチル)でモノまたはジ置換されていてもよいカルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基(例、メトキシ)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル、イソプロピル)、
(g)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルコキシ基(例、メトキシ、エトキシ、イソプロポキシ)、
(h)C1-6アルコキシ-カルボニル基(例、メトキシカルボニル)、および
(i)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)
から選択される1ないし5個の置換基で置換されていてもよい3ないし12員の非芳香族複素環基(好ましくは、3ないし8員の単環式非芳香族複素環基(例、アゼチジニル、ピロリジニル、ピペリジル、ピペラジニル、モルホリニル、1,1-ジオキシドチオモルホリニル、テトラヒドロピラニル、3-オキサ-6-アザビシクロ[3.1.1]へプチル、8-オキサ-3-アザビシクロ[3.2.1]オクチル、2-オキサ-5-アザビシクロ[2.2.1]ヘプチル、3-オキサ-8-アザビシクロ[3.2.1]オクチル、6-オキサ-3-アザビシクロ[3.1.1]へプチル)、3,7-ジオキサ-9-アザビシクロ[3.3.1]ノニル)
である。
(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)カルバモイル基、
(d)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいC1-6アルキル基(例、メチル)、および
(e)C1-6アルコキシ基(例、メトキシ)
から選択される1ないし5個の置換基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、ピロリジニル)である。
(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)カルバモイル基、および
(d)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいC1-6アルキル基(例、メチル)
から選択される1ないし5個(好ましくは、1ないし3個)の置換基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、ピロリジニル)である。
(1)(a)(i)ハロゲン原子(例、フッ素原子)、および
(ii)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、および
(b)3ないし8員の単環式非芳香族複素環基(例、テトラヒドロピラニル、テトラヒドロフリル)
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、または
(2)(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)カルバモイル基、
(d)C1-6アルキル基(例、メチル)、および
(e)C1-6アルコキシ基(例、メトキシ)
から選択される1ないし5個の置換基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、アゼチジニル、ピロリジニル)である。
(1)(a)(i)ハロゲン原子(例、フッ素原子)、および
(ii)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、および
(b)3ないし8員の単環式非芳香族複素環基(例、テトラヒドロピラニル、テトラヒドロフリル)
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、または
(2)(a)ハロゲン原子(例、フッ素原子)、および
(b)シアノ基
から選択される1ないし5個の置換基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、アゼチジニル、ピロリジニル)である。
(1)(a)(i)ハロゲン原子(例、フッ素原子)、および
(ii)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、および
(b)3ないし8員の単環式非芳香族複素環基(例、テトラヒドロピラニル、テトラヒドロフリル)
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、または
(2)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、アゼチジニル、ピロリジニル)である。
(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)カルバモイル基、
(d)C1-6アルキル基(例、メチル)、および
(e)C1-6アルコキシ基(例、メトキシ)
から選択される1ないし5個の置換基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、ピロリジニル)である。
(a)ハロゲン原子(例、フッ素原子)、および
(b)シアノ基
から選択される1ないし5個の置換基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、ピロリジニル)である。
(1)(a)ハロゲン原子(例、フッ素原子、塩素原子)、および
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよいC6-14アリール基(例、フェニル)、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)シアノ基、
(c)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、および
(d)C3-8シクロアルキル基(例、シクロプロピル)
から選択される1ないし3個の置換基で置換されていてもよい5ないし12員の芳香族複素環基(好ましくは、5または6員の単環式芳香族複素環基(例、ピラゾリル、オキサゾリル、チアゾリル、チアジアゾリル、ピリジル)、8ないし12員の縮合芳香族複素環基(例、インダゾリル、ベンゾチアゾリル))
である。
(1)(a)ハロゲン原子(例、フッ素原子、塩素原子)、および
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよいC6-14アリール基(例、フェニル)、または
(2)(a)ハロゲン原子(例、塩素原子)、および
(b)C1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよい5または6員の単環式芳香族複素環基(例、ピラゾリル、チアジアゾリル、ピリジル)
である。
(1)(a)ハロゲン原子(例、フッ素原子)、および
(b)C1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよいC6-14アリール基(例、フェニル)、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)シアノ基、
(c)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル)、および
(d)C3-8シクロアルキル基(例、シクロプロピル)
から選択される1ないし3個の置換基で置換されていてもよい5ないし12員の芳香族複素環基(好ましくは、5または6員の単環式芳香族複素環基(例、ピラゾリル、オキサゾリル、チアゾリル、チアジアゾリル、ピリジル)、8ないし12員の縮合芳香族複素環基(例、ベンゾチアゾリル))である。
(a)ハロゲン原子(例、塩素原子)、および
(b)C1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよい5または6員の単環式芳香族複素環基(例、ピラゾリル、チアゾリル、チアジアゾリル、ピリジル(好ましくは、ピラゾリル、チアジアゾリル、より好ましくは、ピラゾリル))である。
(1)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)C1-6アルキル基(例、メチル)、および
(c)C3-8シクロアルキル基(例、シクロプロピル)
から選択される1ないし3個の置換基で置換されていてもよい5または6員の単環式芳香族複素環基(例、ピラゾリル、チアゾリル、チアジアゾリル(好ましくは、ピラゾリル、チアゾリル))である。
X1は、好ましくは炭素原子である。
(1)水素原子、または
(2)ハロゲン原子(例、フッ素原子)
である。
(a)ハロゲン原子(例、フッ素原子)、
(b)C1-6アルキル基(例、メチル)、および
(c)オキソ基
から選択される1ないし5個(好ましくは1ないし3個)の置換基でそれぞれさらに置換されていてもよく、それぞれ架橋されていてもよい、
(1)(a)ハロゲン原子(例、フッ素原子)、
(b)C1-6アルキル基(例、メチル)、および
(c)オキソ基
から選択される1ないし3個の置換基でそれぞれさらに置換されていてもよい、
(2)8-アザビシクロ[3.2.1]オクタン環、2,5-ジアザビシクロ[2.2.1]ヘプタン環、もしくは3-アザビシクロ[3.1.0]ヘキサン環である。
(1)(a)ハロゲン原子(例、フッ素原子)、および
(b)C1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基でそれぞれさらに置換されていてもよい、
(2)8-アザビシクロ[3.2.1]オクタン環、もしくは2,5-ジアザビシクロ[2.2.1]ヘプタン環である。
[化合物A-1]
R1が、置換されていてもよいC1-6アルキル基、置換されていてもよいC1-6アルコキシ基、置換されていてもよいアミノ基、置換されていてもよいC3-8シクロアルキル基、置換されていてもよいC6-14アリール基、または置換されていてもよい非芳香族複素環基であるか、あるいは、R1が環A上の原子と結合して環Aとともに、オキソで置換され、かつさらに置換されていてもよいスピロ環を形成し;
R2が、置換されていてもよいC6-14アリール基、または置換されていてもよい芳香族複素環基であり;
X1が、炭素原子または窒素原子であり;
R3が、X1が炭素原子の場合、水素原子または置換基であり、X1が窒素原子の場合、存在せず;
環Aが、それぞれさらに置換されていてもよく、それぞれ架橋されていてもよい、
化合物(I)
R1が、置換されていてもよいC1-6アルキル基、置換されていてもよいC1-6アルコキシ基、置換されていてもよいアミノ基、置換されていてもよいC3-8シクロアルキル基、置換されていてもよいC6-14アリール基、または置換されていてもよい非芳香族複素環基であり;
R2が、置換されていてもよいC6-14アリール基、または置換されていてもよい芳香族複素環基であり;
X1が、炭素原子または窒素原子であり;
R3が、X1が炭素原子の場合、水素原子または置換基であり、X1が窒素原子の場合、存在せず;
環Aが、それぞれさらに置換されていてもよく、それぞれ架橋されていてもよい、
化合物(I)
R1が、
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいC6-14アリール基(例、フェニル)、
(c)C6-14アリールオキシ基(例、フェノキシ)、
(d)C3-8シクロアルキル基(例、シクロプロピル)、
(e)5または6員の単環式芳香族複素環基(例、ピラゾリル)、
(f)8ないし12員の縮合芳香族複素環基(例、インダゾリル)、および
(g)1ないし3個のオキソ基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、ジヒドロピリジル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(2)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC1-6アルコキシ基(例、メトキシ、tert-ブトキシ、好ましくはC1-3アルコキシ基(例、メトキシ))、
(3)(a)(i)ハロゲン原子(例、フッ素原子)、
(ii)シアノ基、
(iii)C3-8シクロアルキル基(例、シクロプロピル、シクロブチル)、
(iv)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)、
(v) 5または6員の単環式芳香族複素環基(例、ピリジル)、および
(vi)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、オキセタニル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC3-8シクロアルキル基(例、シクロプロピル、シクロブチル、シクロペンチル)、
(c)C6-14アリール基(例、フェニル)、および
(d)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、テトラヒドロピラニル、オキセタニル、テトラヒドロフリル、ピロリジニル)
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC3-8シクロアルキル基(例、シクロプロピル)、
(5)C6-14アリール基(例、フェニル)、または
(6)(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)カルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基(例、メトキシ)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル、イソプロピル)、
(g)C1-6アルコキシ基(例、メトキシ、エトキシ、イソプロポキシ)、
(h)C1-6アルコキシ-カルボニル基(例、メトキシカルボニル)、および
(i)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)
から選択される1ないし5個の置換基で置換されていてもよい3ないし12員の非芳香族複素環基(好ましくは、3ないし8員の単環式非芳香族複素環基(例、アゼチジニル、ピロリジニル、ピペリジル、ピペラジニル、モルホリニル、1,1-ジオキシドチオモルホリニル、テトラヒドロピラニル、3-オキサ-6-アザビシクロ[3.1.1]へプチル、8-オキサ-3-アザビシクロ[3.2.1]オクチル、2-オキサ-5-アザビシクロ[2.2.1]ヘプチル、3-オキサ-8-アザビシクロ[3.2.1]オクチル、6-オキサ-3-アザビシクロ[3.1.1]へプチル))
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基(例、メチル)でさらに置換されていてもよいスピロ環(例、2,8-ジアザスピロ[4.5]デカン)を形成し;
R2が、
(1)(a)ハロゲン原子(例、フッ素原子、塩素原子)、および
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよいC6-14アリール基(例、フェニル)、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)シアノ基、
(c)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、および
(d)C3-8シクロアルキル基(例、シクロプロピル)
から選択される1ないし3個の置換基で置換されていてもよい5ないし12員の芳香族複素環基(好ましくは、5または6員の単環式芳香族複素環基(例、ピラゾリル、オキサゾリル、チアゾリル、チアジアゾリル、ピリジル)、8ないし12員の縮合芳香族複素環基(例、インダゾリル、ベンゾチアゾリル))
であり;
X1が、炭素原子または窒素原子であり;
R3が、
(1)水素原子、または
(2)ハロゲン原子(例、フッ素原子)
であり;かつ
環Aが、
(a)ハロゲン原子(例、フッ素原子)、
(b)C1-6アルキル基(例、メチル)、および
(c)オキソ基
から選択される1ないし5個(好ましくは1ないし3個)の置換基でそれぞれさらに置換されていてもよく、それぞれ架橋されていてもよい、
化合物(I)
R1が、
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいC6-14アリール基(例、フェニル)、
(c)C6-14アリールオキシ基(例、フェノキシ)、
(d)C3-8シクロアルキル基(例、シクロプロピル)、
(e)5または6員の単環式芳香族複素環基(例、ピラゾリル)、
(f)8ないし12員の縮合芳香族複素環基(例、インダゾリル)、および
(g)1ないし3個のオキソ基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、ジヒドロピリジル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(2)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC1-6アルコキシ基(例、メトキシ、tert-ブトキシ、好ましくはC1-3アルコキシ基(例、メトキシ))、
(3)(a)(i)ハロゲン原子(例、フッ素原子)、
(ii)シアノ基、
(iii)C3-8シクロアルキル基(例、シクロプロピル、シクロブチル)、
(iv)ハロゲン原子(例、フッ素原子)およびC1-6アルコキシ基(例、メトキシ)から選ばれる1ないし3個の置換基で置換されていてもよいC6-14アリール基(例、フェニル)、
(v)5または6員の単環式芳香族複素環基(例、ピリジル)、および
(vi)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、オキセタニル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC3-8シクロアルキル基(例、シクロプロピル、シクロブチル、シクロペンチル)、
(c)C6-14アリール基(例、フェニル)、および
(d)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、テトラヒドロピラニル、オキセタニル、テトラヒドロフリル、ピロリジニル)
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC3-8シクロアルキル基(例、シクロプロピル)、
(5)C6-14アリール基(例、フェニル)、または
(6)(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)C1-6アルキル基(例、メチル)でモノまたはジ置換されていてもよいカルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基(例、メトキシ)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル、イソプロピル)、
(g)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルコキシ基(例、メトキシ、エトキシ、イソプロポキシ)、
(h)C1-6アルコキシ-カルボニル基(例、メトキシカルボニル)、および
(i)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)
から選択される1ないし5個の置換基で置換されていてもよい3ないし12員の非芳香族複素環基(好ましくは、3ないし8員の単環式非芳香族複素環基(例、アゼチジニル、ピロリジニル、ピペリジル、ピペラジニル、モルホリニル、1,1-ジオキシドチオモルホリニル、テトラヒドロピラニル、3-オキサ-6-アザビシクロ[3.1.1]へプチル、8-オキサ-3-アザビシクロ[3.2.1]オクチル、2-オキサ-5-アザビシクロ[2.2.1]ヘプチル、3-オキサ-8-アザビシクロ[3.2.1]オクチル、6-オキサ-3-アザビシクロ[3.1.1]へプチル)、3,7-ジオキサ-9-アザビシクロ[3.3.1]ノニル)
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基(例、メチル)でさらに置換されていてもよいスピロ環(例、2,8-ジアザスピロ[4.5]デカン)を形成し;
R2が、
(1)(a)ハロゲン原子(例、フッ素原子、塩素原子)、および
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよいC6-14アリール基(例、フェニル)、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)シアノ基、
(c)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、および
(d)C3-8シクロアルキル基(例、シクロプロピル)
から選択される1ないし3個の置換基で置換されていてもよい5ないし12員の芳香族複素環基(好ましくは、5または6員の単環式芳香族複素環基(例、ピラゾリル、オキサゾリル、チアゾリル、チアジアゾリル、ピリジル)、8ないし12員の縮合芳香族複素環基(例、インダゾリル、ベンゾチアゾリル))
であり;
X1が、炭素原子または窒素原子であり;
R3が、
(1)水素原子、または
(2)ハロゲン原子(例、フッ素原子)
であり;かつ
環Aが、
(a)ハロゲン原子(例、フッ素原子)、
(b)C1-6アルキル基(例、メチル)、および
(c)オキソ基
から選択される1ないし5個(好ましくは1ないし3個)の置換基でそれぞれさらに置換されていてもよく、それぞれ架橋されていてもよい、
化合物(I)
R1が、
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいC6-14アリール基(例、フェニル)、
(c)C6-14アリールオキシ基(例、フェノキシ)、
(d)C3-8シクロアルキル基(例、シクロプロピル)、
(e)5または6員の単環式芳香族複素環基(例、ピラゾリル)、
(f)8ないし12員の縮合芳香族複素環基(例、インダゾリル)、および
(g)1ないし3個のオキソ基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、ジヒドロピリジル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(2)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC1-3アルコキシ基(例、メトキシ)、
(3)(a)(i)ハロゲン原子(例、フッ素原子)、
(ii)シアノ基、
(iii)C3-8シクロアルキル基(例、シクロプロピル、シクロブチル)、
(iv)ハロゲン原子(例、フッ素原子)およびC1-6アルコキシ基(例、メトキシ)から選ばれる1ないし3個の置換基で置換されていてもよいC6-14アリール基(例、フェニル)、
(v)5または6員の単環式芳香族複素環基(例、ピリジル)、および
(vi)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、オキセタニル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC3-8シクロアルキル基(例、シクロプロピル、シクロブチル、シクロペンチル)、
(c)C6-14アリール基(例、フェニル)、および
(d)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、テトラヒドロピラニル、オキセタニル、テトラヒドロフリル、ピロリジニル)
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC3-8シクロアルキル基(例、シクロプロピル)、
(5)C6-14アリール基(例、フェニル)、または
(6)(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)C1-6アルキル基(例、メチル)でモノまたはジ置換されていてもよいカルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基(例、メトキシ)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル、イソプロピル)、
(g)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルコキシ基(例、メトキシ、エトキシ、イソプロポキシ)、
(h)C1-6アルコキシ-カルボニル基(例、メトキシカルボニル)、および
(i)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)
から選択される1ないし5個の置換基で置換されていてもよい3ないし12員の非芳香族複素環基(好ましくは、3ないし8員の単環式非芳香族複素環基(例、アゼチジニル、ピロリジニル、ピペリジル、ピペラジニル、モルホリニル、1,1-ジオキシドチオモルホリニル、テトラヒドロピラニル、3-オキサ-6-アザビシクロ[3.1.1]へプチル、8-オキサ-3-アザビシクロ[3.2.1]オクチル、2-オキサ-5-アザビシクロ[2.2.1]ヘプチル、3-オキサ-8-アザビシクロ[3.2.1]オクチル、6-オキサ-3-アザビシクロ[3.1.1]へプチル)、3,7-ジオキサ-9-アザビシクロ[3.3.1]ノニル)
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基(例、メチル)でさらに置換されていてもよいスピロ環(例、2,8-ジアザスピロ[4.5]デカン)を形成し;
R2が、
(1)(a)ハロゲン原子(例、フッ素原子、塩素原子)、および
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよいC6-14アリール基(例、フェニル)、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)シアノ基、
(c)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、および
(d)C3-8シクロアルキル基(例、シクロプロピル)
から選択される1ないし3個の置換基で置換されていてもよい5ないし12員の芳香族複素環基(好ましくは、5または6員の単環式芳香族複素環基(例、ピラゾリル、オキサゾリル、チアゾリル、チアジアゾリル、ピリジル)、8ないし12員の縮合芳香族複素環基(例、インダゾリル、ベンゾチアゾリル))
であり;
X1が、炭素原子または窒素原子であり;
R3が、
(1)水素原子、または
(2)ハロゲン原子(例、フッ素原子)
であり;かつ
環Aが、
(a)ハロゲン原子(例、フッ素原子)、
(b)C1-6アルキル基(例、メチル)、および
(c)オキソ基
から選択される1ないし5個(好ましくは1ないし3個)の置換基でそれぞれさらに置換されていてもよく、それぞれ架橋されていてもよい、
化合物(I)
R1が、
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいC6-14アリール基(例、フェニル)、
(c)C6-14アリールオキシ基(例、フェノキシ)、
(d)C3-8シクロアルキル基(例、シクロプロピル)、
(e)ピラゾリル基、
(f)インダゾリル基、および
(g)1ないし3個のオキソ基で置換されていてもよいジヒドロピリジル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(2)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC1-6アルコキシ基(例、メトキシ、tert-ブトキシ、好ましくはC1-3アルコキシ基(例、メトキシ))、
(3)(a)(i)ハロゲン原子(例、フッ素原子)、
(ii)シアノ基、
(iii)C3-8シクロアルキル基(例、シクロプロピル、シクロブチル)、
(iv)ハロゲン原子(例、フッ素原子)およびC1-6アルコキシ基(例、メトキシ)から選ばれる1ないし3個の置換基で置換されていてもよいC6-14アリール基(例、フェニル)、
(v)ピリジル基、および
(vi)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよいオキセタニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC3-8シクロアルキル基(例、シクロプロピル、シクロブチル、シクロペンチル)、
(c)C6-14アリール基(例、フェニル)、および
(d)1ないし3個のC1-6アルキル基(例、メチル)でそれぞれ置換されていてもよい、テトラヒドロピラニル基、オキセタニル基、テトラヒドロフリル基もしくはピロリジニル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC3-8シクロアルキル基(例、シクロプロピル)、
(5)C6-14アリール基(例、フェニル)、または
(6)(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)C1-6アルキル基(例、メチル)でモノまたはジ置換されていてもよいカルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基(例、メトキシ)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル、イソプロピル)、
(g)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルコキシ基(例、メトキシ、エトキシ、イソプロポキシ)、
(h)C1-6アルコキシ-カルボニル基(例、メトキシカルボニル)、および
(i)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)
から選択される1ないし5個の置換基でそれぞれ置換されていてもよい、3ないし8員の単環式非芳香族複素環基(例、アゼチジニル、ピロリジニル、ピペリジル、ピペラジニル、モルホリニル、1,1-ジオキシドチオモルホリニル、テトラヒドロピラニル、3-オキサ-6-アザビシクロ[3.1.1]へプチル、8-オキサ-3-アザビシクロ[3.2.1]オクチル、2-オキサ-5-アザビシクロ[2.2.1]ヘプチル、3-オキサ-8-アザビシクロ[3.2.1]オクチル、6-オキサ-3-アザビシクロ[3.1.1]へプチル)もしくは3,7-ジオキサ-9-アザビシクロ[3.3.1]ノニル基
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基(例、メチル)でさらに置換されていてもよい2,8-ジアザスピロ[4.5]デカン環を形成し;
R2が、
(1)(a)ハロゲン原子(例、フッ素原子、塩素原子)、および
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよいC6-14アリール基(例、フェニル)、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)シアノ基、
(c)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、および
(d)C3-8シクロアルキル基(例、シクロプロピル)
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、5または6員の単環式芳香族複素環基(例、ピラゾリル、オキサゾリル、チアゾリル、チアジアゾリル、ピリジル)もしくは8ないし12員の縮合芳香族複素環基(例、インダゾリル、ベンゾチアゾリル)であり;
X1が、炭素原子または窒素原子であり;
R3が、
(1)水素原子、または
(2)ハロゲン原子(例、フッ素原子)であり;かつ
環Aが、
(1)(a)ハロゲン原子(例、フッ素原子)、
(b)C1-6アルキル基(例、メチル)、および
(c)オキソ基
から選択される1ないし3個の置換基でそれぞれさらに置換されていてもよい、
(2)8-アザビシクロ[3.2.1]オクタン環、2,5-ジアザビシクロ[2.2.1]ヘプタン環、もしくは3-アザビシクロ[3.1.0]ヘキサン環である、
化合物(I)
R1が、
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいC6-14アリール基(例、フェニル)、
(c)C6-14アリールオキシ基(例、フェノキシ)、
(d)C3-8シクロアルキル基(例、シクロプロピル)、
(e)ピラゾリル基、
(f)インダゾリル基、および
(g)1ないし3個のオキソ基で置換されていてもよいジヒドロピリジル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(2)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC1-3アルコキシ基(例、メトキシ)、
(3)(a)(i)ハロゲン原子(例、フッ素原子)、
(ii)シアノ基、
(iii)C3-8シクロアルキル基(例、シクロプロピル、シクロブチル)、
(iv)ハロゲン原子(例、フッ素原子)およびC1-6アルコキシ基(例、メトキシ)から選ばれる1ないし3個の置換基で置換されていてもよいC6-14アリール基(例、フェニル)、
(v)ピリジル基、および
(vi)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよいオキセタニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC3-8シクロアルキル基(例、シクロプロピル、シクロブチル、シクロペンチル)、
(c)C6-14アリール基(例、フェニル)、および
(d)1ないし3個のC1-6アルキル基(例、メチル)でそれぞれ置換されていてもよい、テトラヒドロピラニル基、オキセタニル基、テトラヒドロフリル基もしくはピロリジニル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC3-8シクロアルキル基(例、シクロプロピル)、
(5)C6-14アリール基(例、フェニル)、または
(6)(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)C1-6アルキル基(例、メチル)でモノまたはジ置換されていてもよいカルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基(例、メトキシ)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル、イソプロピル)、
(g)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルコキシ基(例、メトキシ、エトキシ、イソプロポキシ)、
(h)C1-6アルコキシ-カルボニル基(例、メトキシカルボニル)、および
(i)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)
から選択される1ないし5個の置換基でそれぞれ置換されていてもよい、3ないし8員の単環式非芳香族複素環基(例、アゼチジニル、ピロリジニル、ピペリジル、ピペラジニル、モルホリニル、1,1-ジオキシドチオモルホリニル、テトラヒドロピラニル、3-オキサ-6-アザビシクロ[3.1.1]へプチル、8-オキサ-3-アザビシクロ[3.2.1]オクチル、2-オキサ-5-アザビシクロ[2.2.1]ヘプチル、3-オキサ-8-アザビシクロ[3.2.1]オクチル、6-オキサ-3-アザビシクロ[3.1.1]へプチル)もしくは3,7-ジオキサ-9-アザビシクロ[3.3.1]ノニル基
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基(例、メチル)でさらに置換されていてもよい2,8-ジアザスピロ[4.5]デカン環を形成し;
R2が、
(1)(a)ハロゲン原子(例、フッ素原子、塩素原子)、および
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよいC6-14アリール基(例、フェニル)、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)シアノ基、
(c)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、および
(d)C3-8シクロアルキル基(例、シクロプロピル)
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、5または6員の単環式芳香族複素環基(例、ピラゾリル、オキサゾリル、チアゾリル、チアジアゾリル、ピリジル)もしくは8ないし12員の縮合芳香族複素環基(例、インダゾリル、ベンゾチアゾリル)であり;
X1が、炭素原子または窒素原子であり;
R3が、
(1)水素原子、または
(2)ハロゲン原子(例、フッ素原子)であり;かつ
環Aが、
(1)(a)ハロゲン原子(例、フッ素原子)、
(b)C1-6アルキル基(例、メチル)、および
(c)オキソ基
から選択される1ないし3個の置換基でそれぞれさらに置換されていてもよい、
(2)8-アザビシクロ[3.2.1]オクタン環、2,5-ジアザビシクロ[2.2.1]ヘプタン環、もしくは3-アザビシクロ[3.1.0]ヘキサン環である、
化合物(I)
R1が、
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいフェニル基、
(c)フェノキシ基、
(d)シクロプロピル基、
(e)ピラゾリル基、
(f)インダゾリル基、および
(g)1ないし3個のオキソ基で置換されていてもよいジヒドロピリジル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(2)1ないし3個のフェニル基で置換されていてもよいC1-6アルコキシ基(例、メトキシ、tert-ブトキシ、好ましくはC1-3アルコキシ基(例、メトキシ))、
(3)(a)(i)ハロゲン原子(例、フッ素原子)、
(ii)シアノ基、
(iii)シクロプロピル基、
(iv)シクロブチル基、
(v)ハロゲン原子(例、フッ素原子)およびC1-6アルコキシ基(例、メトキシ)から選ばれる1ないし3個の置換基で置換されていてもよいフェニル基、
(vi)ピリジル基、および
(vii)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよいオキセタニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(b)1ないし3個のハロゲン原子(例、フッ素原子)でそれぞれ置換されていてもよい、シクロプロピル基、シクロブチル基もしくはシクロペンチル基、
(c)フェニル基、および
(d)1ないし3個のC1-6アルキル基(例、メチル)でそれぞれ置換されていてもよい、テトラヒドロピラニル基、オキセタニル基、テトラヒドロフリル基もしくはピロリジニル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のフェニル基で置換されていてもよいシクロプロピル基、
(5)フェニル基、または
(6)(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)C1-6アルキル基(例、メチル)でモノまたはジ置換されていてもよいカルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基(例、メトキシ)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル、イソプロピル)、
(g)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルコキシ基(例、メトキシ、エトキシ、イソプロポキシ)、
(h)C1-6アルコキシ-カルボニル基(例、メトキシカルボニル)、および
(i)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいフェニル基
から選択される1ないし5個の置換基でそれぞれ置換されていてもよい、
アゼチジニル基、ピロリジニル基、ピペリジル基、ピペラジニル基、モルホリニル基、1,1-ジオキシドチオモルホリニル基、テトラヒドロピラニル基、3-オキサ-6-アザビシクロ[3.1.1]へプチル基、8-オキサ-3-アザビシクロ[3.2.1]オクチル基、2-オキサ-5-アザビシクロ[2.2.1]ヘプチル基、3-オキサ-8-アザビシクロ[3.2.1]オクチル基、6-オキサ-3-アザビシクロ[3.1.1]へプチル基もしくは3,7-ジオキサ-9-アザビシクロ[3.3.1]ノニル基
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基(例、メチル)でさらに置換されていてもよい2,8-ジアザスピロ[4.5]デカン環を形成し;
R2が、
(1)(a)ハロゲン原子(例、フッ素原子、塩素原子)、および
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよいフェニル基、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)シアノ基、
(c)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、および
(d)シクロプロピル基
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基、オキサゾリル基、チアゾリル基、チアジアゾリル基、ピリジル基、インダゾリル基もしくはベンゾチアゾリル基であり;
X1が、炭素原子または窒素原子であり;
R3が、
(1)水素原子、または
(2)ハロゲン原子(例、フッ素原子)であり;かつ
環Aが、
(1)(a)ハロゲン原子(例、フッ素原子)、
(b)C1-6アルキル基(例、メチル)、および
(c)オキソ基
から選択される1ないし3個の置換基でそれぞれさらに置換されていてもよい、
(2)8-アザビシクロ[3.2.1]オクタン環、2,5-ジアザビシクロ[2.2.1]ヘプタン環、もしくは3-アザビシクロ[3.1.0]ヘキサン環である、
化合物(I)
R1が、
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいフェニル基、
(c)フェノキシ基、
(d)シクロプロピル基、
(e)ピラゾリル基、
(f)インダゾリル基、および
(g)1ないし3個のオキソ基で置換されていてもよいジヒドロピリジル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(2)1ないし3個のフェニル基で置換されていてもよいC1-3アルコキシ基(例、メトキシ)、
(3)(a)(i)ハロゲン原子(例、フッ素原子)、
(ii)シアノ基、
(iii)シクロプロピル基、
(iv)シクロブチル基、
(v)ハロゲン原子(例、フッ素原子)およびC1-6アルコキシ基(例、メトキシ)から選ばれる1ないし3個の置換基で置換されていてもよいフェニル基、
(vi)ピリジル基、および
(vii)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよいオキセタニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(b)1ないし3個のハロゲン原子(例、フッ素原子)でそれぞれ置換されていてもよい、シクロプロピル基、シクロブチル基もしくはシクロペンチル基、
(c)フェニル基、および
(d)1ないし3個のC1-6アルキル基(例、メチル)でそれぞれ置換されていてもよい、テトラヒドロピラニル基、オキセタニル基、テトラヒドロフリル基もしくはピロリジニル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のフェニル基で置換されていてもよいシクロプロピル基、
(5)フェニル基、または
(6)(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)C1-6アルキル基(例、メチル)でモノまたはジ置換されていてもよいカルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基(例、メトキシ)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル、イソプロピル)、
(g)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルコキシ基(例、メトキシ、エトキシ、イソプロポキシ)、
(h)C1-6アルコキシ-カルボニル基(例、メトキシカルボニル)、および
(i)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいフェニル基
から選択される1ないし5個の置換基でそれぞれ置換されていてもよい、
アゼチジニル基、ピロリジニル基、ピペリジル基、ピペラジニル基、モルホリニル基、1,1-ジオキシドチオモルホリニル基、テトラヒドロピラニル基、3-オキサ-6-アザビシクロ[3.1.1]へプチル基、8-オキサ-3-アザビシクロ[3.2.1]オクチル基、2-オキサ-5-アザビシクロ[2.2.1]ヘプチル基、3-オキサ-8-アザビシクロ[3.2.1]オクチル基、6-オキサ-3-アザビシクロ[3.1.1]へプチル基もしくは3,7-ジオキサ-9-アザビシクロ[3.3.1]ノニル基
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基(例、メチル)でさらに置換されていてもよい2,8-ジアザスピロ[4.5]デカン環を形成し;
R2が、
(1)(a)ハロゲン原子(例、フッ素原子、塩素原子)、および
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよいフェニル基、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)シアノ基、
(c)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、および
(d)シクロプロピル基
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基、オキサゾリル基、チアゾリル基、チアジアゾリル基、ピリジル基、インダゾリル基もしくはベンゾチアゾリル基であり;
X1が、炭素原子または窒素原子であり;
R3が、
(1)水素原子、または
(2)ハロゲン原子(例、フッ素原子)であり;かつ
環Aが、
(1)(a)ハロゲン原子(例、フッ素原子)、
(b)C1-6アルキル基(例、メチル)、および
(c)オキソ基
から選択される1ないし3個の置換基でそれぞれさらに置換されていてもよい、
(2)8-アザビシクロ[3.2.1]オクタン環、2,5-ジアザビシクロ[2.2.1]ヘプタン環、もしくは3-アザビシクロ[3.1.0]ヘキサン環である、
化合物(I)
R1が、
(1)(a)(i)ハロゲン原子(例、フッ素原子)、および
(ii)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、および
(b)3ないし8員の単環式非芳香族複素環基(例、テトラヒドロピラニル、テトラヒドロフリル)
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、または
(2)(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)カルバモイル基、
(d)C1-6アルキル基(例、メチル)、および
(e)C1-6アルコキシ基(例、メトキシ)
から選択される1ないし5個の置換基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、アゼチジニル、ピロリジニル)であり;
R2が、
(1)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)C1-6アルキル基(例、メチル)、および
(c)C3-8シクロアルキル基(例、シクロプロピル)
から選択される1ないし3個の置換基で置換されていてもよい5または6員の単環式芳香族複素環基(例、ピラゾリル、チアゾリル、チアジアゾリル(好ましくは、ピラゾリル、チアゾリル))であり;
X1が、炭素原子または窒素原子であり;
R3が、水素原子であり;かつ
環Aが、
化合物(I)
R1が、
(1)(a)(i)ハロゲン原子(例、フッ素原子)、および
(ii)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいフェニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(b) テトラヒドロピラニル基、および
(c) テトラヒドロフリル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、または
(2)(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)カルバモイル基、
(d)C1-6アルキル基(例、メチル)、および
(e)C1-6アルコキシ基(例、メトキシ)
から選択される1ないし5個の置換基でそれぞれ置換されていてもよい、アゼチジニル基もしくはピロリジニル基であり;
R2が、
(1)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいフェニル基、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)C1-6アルキル基(例、メチル)、および
(c)シクロプロピル基
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基、チアゾリル基もしくはチアジアゾリル基であり;
X1が、炭素原子または窒素原子であり;
R3が、水素原子であり;かつ
環Aが、
化合物(I)
R1が、
(1)(a)(i)ハロゲン原子(例、フッ素原子)、および
(ii)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、および
(b)3ないし8員の単環式非芳香族複素環基(例、テトラヒドロピラニル、テトラヒドロフリル)
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、または
(2)(a)ハロゲン原子(例、フッ素原子)、および
(b)シアノ基
から選択される1ないし5個の置換基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、アゼチジニル、ピロリジニル)であり;
R2が、
(1)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)C1-6アルキル基(例、メチル)、および
(c)C3-8シクロアルキル基(例、シクロプロピル)
から選択される1ないし3個の置換基で置換されていてもよい5または6員の単環式芳香族複素環基(例、ピラゾリル、チアゾリル、チアジアゾリル(好ましくは、ピラゾリル、チアゾリル))であり;
X1が、炭素原子または窒素原子であり;
R3が、水素原子であり;かつ
環Aが、
化合物(I)
R1が、
(1)(a)(i)ハロゲン原子(例、フッ素原子)、および
(ii)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいフェニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(b)テトラヒドロピラニル基、および
(c)テトラヒドロフリル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、または
(2)(a)ハロゲン原子(例、フッ素原子)、および
(b)シアノ基
から選択される1ないし5個の置換基でそれぞれ置換されていてもよい、アゼチジニル基もしくはピロリジニル基であり;
R2が、
(1)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいフェニル基、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)C1-6アルキル基(例、メチル)、および
(c)シクロプロピル基
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基もしくはチアゾリル基であり;
X1が、炭素原子または窒素原子であり;
R3が、水素原子であり;かつ
環Aが、
化合物(I)
R1が、
(1)(a)(i)ハロゲン原子(例、フッ素原子)、および
(ii)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、および
(b)3ないし8員の単環式非芳香族複素環基(例、テトラヒドロピラニル、テトラヒドロフリル)
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、または
(2)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、アゼチジニル、ピロリジニル)であり;
R2が、
(1)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)C1-6アルキル基(例、メチル)、および
(c)C3-8シクロアルキル基(例、シクロプロピル)
から選択される1ないし3個の置換基で置換されていてもよい5または6員の単環式芳香族複素環基(例、ピラゾリル、チアゾリル、チアジアゾリル(好ましくは、ピラゾリル、チアゾリル))であり;
X1が、炭素原子または窒素原子であり;
R3が、水素原子であり;かつ
環Aが、
化合物(I)
R1が、
(1)(a)(i)ハロゲン原子(例、フッ素原子)、および
(ii)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいフェニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(b)テトラヒドロピラニル基、および
(c)テトラヒドロフリル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、または
(2)1ないし3個のハロゲン原子(例、フッ素原子)でそれぞれ置換されていてもよい、アゼチジニル基もしくはピロリジニル基であり;
R2が、
(1)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいフェニル基、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)C1-6アルキル基(例、メチル)、および
(c)シクロプロピル基
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基もしくはチアゾリル基であり;
X1が、炭素原子または窒素原子であり;
R3が、水素原子であり;かつ
環Aが、
化合物(I)
R1が、
(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)カルバモイル基、
(d)C1-6アルキル基(例、メチル)、および
(e)C1-6アルコキシ基(例、メトキシ)
から選択される1ないし5個の置換基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、ピロリジニル)であり;
R2が、
(a)ハロゲン原子(例、塩素原子)、および
(b)C1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよい5または6員の単環式芳香族複素環基(例、ピラゾリル、チアゾリル、チアジアゾリル、ピリジル(好ましくは、ピラゾリル、チアジアゾリル、より好ましくは、ピラゾリル))であり;
X1が、炭素原子であり;
R3が、水素原子であり;かつ
環Aが、
化合物(I)
R1が、
(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)カルバモイル基、
(d)C1-6アルキル基(例、メチル)、および
(e)C1-6アルコキシ基(例、メトキシ)
から選択される1ないし5個の置換基で置換されていてもよいピロリジニル基であり;
R2が、
(a)ハロゲン原子(例、塩素原子)、および
(b)C1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基もしくはチアジアゾリル基であり;
X1が、炭素原子であり;
R3が、水素原子であり;かつ
環Aが、
化合物(I)
R1が、
(a)ハロゲン原子(例、フッ素原子)、および
(b)シアノ基
から選択される1ないし5個の置換基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、ピロリジニル)であり;
R2が、
(a)ハロゲン原子(例、塩素原子)、および
(b)C1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよい5または6員の単環式芳香族複素環基(例、ピラゾリル、チアゾリル、チアジアゾリル、ピリジル(好ましくは、ピラゾリル、チアジアゾリル、より好ましくは、ピラゾリル))であり;
X1が、炭素原子であり;
R3が、水素原子であり;かつ
環Aが、
化合物(I)
R1が、
(a)ハロゲン原子(例、フッ素原子)、および
(b)シアノ基
から選択される1ないし5個の置換基で置換されていてもよいピロリジニル基であり;
R2が、
(a)ハロゲン原子(例、塩素原子)、および
(b)C1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよいピラゾリル基であり;
X1が、炭素原子であり;
R3が、水素原子であり;かつ
環Aが、
化合物(I)
R1が、
(1)(a)C3-8シクロアルキル基(例、シクロプロピル)、および
(b)8ないし12員の縮合芳香族複素環基(例、インダゾリル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(2)1ないし3個のC6-14アリール基(例、フェニル)で置換されていてもよいC1-6アルコキシ基(好ましくはC1-3アルコキシ基(例、メトキシ))、
(3)(a)(i)ハロゲン原子(例、フッ素原子)、
(ii)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)、
(iii)5または6員の単環式芳香族複素環基(例、ピリジル)、および
(iv)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、オキセタニル)
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(b)C3-8シクロアルキル基(例、シクロプロピル、シクロペンチル)、
(c)3ないし8員の単環式非芳香族複素環基(例、テトラヒドロピラニル、テトラヒドロフリル)、および
(d)C6-14アリール基(例、フェニル)
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)C3-8シクロアルキル基(例、シクロプロピル)、または
(5)(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)カルバモイル基、
(d)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいC1-6アルキル基(例、メチル、イソプロピル)、
(e)C1-6アルコキシ基(例、メトキシ)、および
(f)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC6-14アリール基(例、フェニル)
から選択される1ないし5個の置換基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、アゼチジニル、ピロリジニル、1,1-ジオキシドチオモルホリニル、3-オキサ-6-アザビシクロ[3.1.1]へプチル)
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基(例、メチル)でさらに置換されていてもよいスピロ環(例、2,8-ジアザスピロ[4.5]デカン)を形成し;
R2が、
(1)(a)ハロゲン原子(例、フッ素原子)、および
(b)C1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよいC6-14アリール基(例、フェニル)、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)シアノ基、
(c)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル)、および
(d)C3-8シクロアルキル基(例、シクロプロピル)
から選択される1ないし3個の置換基で置換されていてもよい5ないし12員の芳香族複素環基(好ましくは、5または6員の単環式芳香族複素環基(例、ピラゾリル、オキサゾリル、チアゾリル、チアジアゾリル、ピリジル)、8ないし12員の縮合芳香族複素環基(例、ベンゾチアゾリル))であり;
X1が、炭素原子または窒素原子であり;
R3が、
(1)水素原子、または
(2)ハロゲン原子(例、フッ素原子)
であり;かつ
環Aが、
(1)(a)ハロゲン原子(例、フッ素原子)、および
(b)C1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基でそれぞれさらに置換されていてもよい、
(2)8-アザビシクロ[3.2.1]オクタン環、もしくは2,5-ジアザビシクロ[2.2.1]ヘプタン環である、
化合物(I)
R1が、
(1)(a)シクロプロピル基、および
(b)インダゾリル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(2)1ないし3個のフェニル基で置換されていてもよいC1-6アルコキシ基(好ましくはC1-3アルコキシ基(例、メトキシ))、
(3)(a)(i)ハロゲン原子(例、フッ素原子)、
(ii)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいフェニル基、
(iii)ピリジル基、および
(iv)1ないし3個のC1-6アルキル基(例、メチル)で置換されていてもよいオキセタニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基(例、メチル、エチル)、
(b)シクロプロピル基、
(c)シクロペンチル基、
(d)テトラヒドロピラニル基、
(e)テトラヒドロフリル基、および
(f)フェニル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)シクロプロピル基、または
(5)(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)カルバモイル基、
(d)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいC1-6アルキル基(例、メチル、イソプロピル)、
(e)C1-6アルコキシ基(例、メトキシ)、および
(f)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいフェニル基
から選択される1ないし5個の置換基でそれぞれ置換されていてもよい、アゼチジニル基、ピロリジニル基、1,1-ジオキシドチオモルホリニル基もしくは3-オキサ-6-アザビシクロ[3.1.1]へプチル基
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基(例、メチル)でさらに置換されていてもよい2,8-ジアザスピロ[4.5]デカン環を形成し;
R2が、
(1)(a)ハロゲン原子(例、フッ素原子)、および
(b)C1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよいフェニル基、または
(2)(a)ハロゲン原子(例、塩素原子、臭素原子)、
(b)シアノ基、
(c)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル)、および
(d)シクロプロピル基
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基、オキサゾリル基、チアゾリル基、チアジアゾリル基、ピリジル基もしくはベンゾチアゾリル基であり;
X1が、炭素原子または窒素原子であり;
R3が、
(1)水素原子、または
(2)ハロゲン原子(例、フッ素原子)
であり;かつ
環Aが、
(1)(a)ハロゲン原子(例、フッ素原子)、および
(b)C1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基でそれぞれさらに置換されていてもよい、
(2)8-アザビシクロ[3.2.1]オクタン環、もしくは2,5-ジアザビシクロ[2.2.1]ヘプタン環である、
化合物(I)
R1が、
(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)カルバモイル基、および
(d)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいC1-6アルキル基(例、メチル)
から選択される1ないし5個(好ましくは、1ないし3個)の置換基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、ピロリジニル)であり;
R2が、
(a)ハロゲン原子(例、塩素原子)、および
(b)C1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよい5または6員の単環式芳香族複素環基(例、ピラゾリル、チアゾリル、チアジアゾリル、ピリジル(好ましくは、ピラゾリル、チアジアゾリル、より好ましくは、ピラゾリル))であり;
X1が、炭素原子であり;
R3が、水素原子であり;かつ
環Aが、
化合物(I)
R1が、
(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)カルバモイル基、および
(d)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいC1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよいピロリジニル基であり;
R2が、
(a)ハロゲン原子(例、塩素原子)、および
(b)C1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基、チアゾリル基、チアジアゾリル基またはピリジル基であり;
X1が、炭素原子であり;
R3が、水素原子であり;かつ
環Aが、
化合物(I)
R1が、
(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)カルバモイル基、
(d)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいC1-6アルキル基(例、メチル)、および
(e)C1-6アルコキシ基(例、メトキシ)
から選択される1ないし5個の置換基で置換されていてもよい3ないし8員の単環式非芳香族複素環基(例、ピロリジニル)であり;
R2が、
(1)(a)ハロゲン原子(例、フッ素原子、塩素原子)、および
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよいC6-14アリール基(例、フェニル)、または
(2)(a)ハロゲン原子(例、塩素原子)、および
(b)C1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよい5または6員の単環式芳香族複素環基(例、ピラゾリル、チアジアゾリル、ピリジル)
であり;
X1が、炭素原子であり;
R3が、水素原子であり;かつ
環Aが、
化合物(I)
R1が、
(a)ハロゲン原子(例、フッ素原子)、
(b)シアノ基、
(c)カルバモイル基、
(d)1ないし3個のC1-6アルコキシ基(例、メトキシ)で置換されていてもよいC1-6アルキル基(例、メチル)、および
(e)C1-6アルコキシ基(例、メトキシ)
から選択される1ないし5個の置換基で置換されていてもよいピロリジニル基であり;
R2が、
(1)(a)ハロゲン原子(例、フッ素原子、塩素原子)、および
(b)1ないし3個のハロゲン原子(例、フッ素原子)で置換されていてもよいC1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基で置換されていてもよいフェニル基、または
(2)(a)ハロゲン原子(例、塩素原子)、および
(b)C1-6アルキル基(例、メチル)
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基、チアジアゾリル基もしくはピリジル基であり;
X1が、炭素原子であり;
R3が、水素原子であり;かつ
環Aが、
化合物(I)
(2R)-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル、
(2R)-1-((1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル、
(2R)-4,4-ジフルオロ-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル、
(3-フルオロアゼチジン-1-イル)(1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-イル)メタノン、
(1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)(3-フルオロアゼチジン-1-イル)メタノン、
(1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)((3S)-3-フルオロピロリジン-1-イル)メタノン、
(1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-イル)((3S)-3-フルオロピロリジン-1-イル)メタノン、
N-ベンジル-N-(2-フルオロエチル)-4-(4-フェニルピリミジン-5-イル)ピペラジン-1-カルボキサミド、
N-(4-フルオロベンジル)-N-(2-フルオロエチル)-4-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペラジン-1-カルボキサミド、
((3S)-3-フルオロピロリジン-1-イル)(1-(4-(5-メチル-1,3-チアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノン、
(3-フルオロアゼチジン-1-イル)(1-(4-(5-メチル-1,3-チアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノン、
(1-(4-(4-ブロモ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)(3-フルオロアゼチジン-1-イル)メタノン、および
(1-(4-(4-シクロプロピル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)(3-フルオロアゼチジン-1-イル)メタノン
から選択される化合物(I)
(2R)-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
[化合物K-3]
(2R)-1-((1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
[化合物K-4]
(2R)-4,4-ジフルオロ-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
このうち、薬学的に許容し得る塩が好ましい。例えば、化合物内に酸性官能基を有する場合には、アルカリ金属塩(例、ナトリウム塩、カリウム塩等)、アルカリ土類金属塩(例、カルシウム塩、マグネシウム塩等)等の無機塩、アンモニウム塩等、また、化合物内に塩基性官能基を有する場合には、例えば、塩酸、臭化水素酸、硝酸、硫酸、リン酸等の無機酸との塩、または酢酸、フタル酸、フマル酸、シュウ酸、酒石酸、マレイン酸、クエン酸、コハク酸、メタンスルホン酸、ベンゼンスルホン酸、p-トルエンスルホン酸等の有機酸との塩が挙げられる。
本発明化合物及びその原料化合物は、自体公知の手段を用いて、例えば以下のスキームで示される方法等によって製造できる。以下「室温」は通常0~40℃を示し、スキーム中に記載されている化学構造式中の各記号は、特記しない限り前記と同義である。なお、式中の化合物は、塩を形成している場合も含み、このような塩としては、例えば本発明化合物の塩と同様のもの等が挙げられる。各工程で得られた化合物は反応液のままか粗製物として次の反応に用いることもできるが、常法に従って反応混合物から単離することもでき、再結晶、蒸留、クロマトグラフィー等の分離手段により容易に精製することができる。式中の化合物が市販されている場合には市販品をそのまま用いることもできる。また、式(I)中の各環が置換基を有している場合、対応する前駆体においても同様の置換基を有しているものとする。
アルコール類:メタノール、エタノール、1-プロパノール、2-プロパノール、tert-ブチルアルコール、tert-アミルアルコール、2-メトキシエタノール等
エーテル類:ジエチルエーテル、ジイソプロピルエーテル、ジフェニルエーテル、テトラヒドロフラン、1,4-ジオキサン、1,2-ジメトキシエタン等
芳香族炭化水素類:ベンゼン、クロロベンゼン、トルエン、キシレン等
飽和炭化水素類:シクロヘキサン、ヘキサン等
アミド類:N,N-ジメチルホルムアミド、N,N-ジメチルアセトアミド、ヘキサメチルホスホリックトリアミド、N-メチルピロリドン等
ハロゲン化炭化水素類:ジクロロメタン、クロロホルム、四塩化炭素、1,2-ジクロロエタン等
ニトリル類:アセトニトリル、プロピオニトリル等
スルホキシド類:ジメチルスルホキシド等
有機塩基類:トリエチルアミン、ピリジン、ルチジン等
酸無水物類:無水酢酸等
有機酸類:ギ酸、酢酸、プロピオン酸、トリフルオロ酢酸、メタンスルホン酸等
無機酸類:塩酸、硫酸等
エステル類:酢酸メチル、酢酸エチル、酢酸ブチル等
ケトン類:アセトン、メチルエチルケトン等
水
無機塩基類:水酸化ナトリウム、水酸化カリウム、水酸化マグネシウム等
塩基性塩類:炭酸ナトリウム、炭酸カリウム、炭酸セシウム、炭酸カルシウム、炭酸水素ナトリウム等
有機塩基類:トリエチルアミン、ジイソプロピルエチルアミン、トリブチルアミン、シクロヘキシルジメチルアミン、ピリジン、ルチジン、4-ジメチルアミノピリジン、N,N-ジメチルアニリン、N-メチルピペリジン、N-メチルピロリジン、N-メチルモルホリン、1,5-ジアザビシクロ[4.3.0]-5-ノネン、1,4-ジアザビシクロ[2.2.2]オクタン、1,8-ジアザビシクロ[5.4.0]-7-ウンデセン、イミダゾール等
金属アルコキシド類:ナトリウムメトキシド、ナトリウムエトキシド、カリウムtert-ブトキシド等
アルカリ金属水素化物類:水素化ナトリウム、水素化カリウム等
金属アミド類:ナトリウムアミド、リチウムジイソプロピルアミド、リチウムヘキサメチルジシラジド等
有機リチウム試薬:メチルリチウム、n-ブチルリチウム、sec-ブチルリチウム、tert-ブチルリチウム等
無機酸類:塩酸、硫酸、硝酸、臭化水素酸、リン酸等
有機酸類:酢酸、トリフルオロ酢酸、シュウ酸、フタル酸、フマル酸、酒石酸、マレイン酸、クエン酸、コハク酸、メタンスルホン酸、p-トルエンスルホン酸、10-カンファースルホン酸等
ルイス酸:三フッ化ホウ素エーテル錯体、ヨウ化亜鉛、無水塩化アルミニウム、無水塩化亜鉛、無水塩化鉄等
反応式中の各一般式における記号は、特に記載のない限り、それぞれ、上記と同義である。式中、Raは、それぞれ水素原子または置換されていてもよいC1-6アルキル基を示す。Raがそれぞれ置換されていてもよいC1-6アルキル基の場合において、2つのRa同士が一緒になって、4,4,5,5-テトラメチル-1,3,2-ジオキサボロラン等の環を形成していてもよい。R4は、置換されていてもよい炭化水素基、置換されていてもよい複素環基または水素原子を示す。X2は、置換されていてもよい炭素原子または窒素原子を示す。
X3は、酸素原子または硫黄原子を示す。
Raで示される「置換されていてもよいC1-6アルキル基」としては、R1で示される「置換されていてもよいC1-6アルキル基」と同様のものが挙げられる。
R4で示される「置換されていてもよい炭化水素基」および「置換されていてもよい複素環基」は、RA、RA’またはRB’で示される「置換されていてもよい炭化水素基」および「置換されていてもよい複素環基」と同様のものが挙げられる。
X2で示される「置換されていてもよい炭素原子」の置換基としては、R2で示される「置換されていてもよい芳香族複素環基」の置換基と同様のものが挙げられる。
化合物(6)は、化合物(2)と化合物(3)とを、化合物(2)と化合物(4)とを、または化合物(2)と化合物(5)とを、反応させることによって製造することができる。反応は、化合物(2)と化合物(3)とを、化合物(2)と化合物(4)とを、または化合物(2)と化合物(5)とを、酸触媒、塩基または金属触媒の存在下で行う。該酸触媒としては、例えば、有機酸類等が挙げられる。酸触媒は、化合物(2)1モルに対し約0.05~2モル用いる。該塩基としては、例えば、塩基性塩類、有機塩基類、アルカリ金属水素化物類、有機リチウム試薬等が挙げられる。塩基は、化合物(2)1モルに対し約1~20モル用いる。該金属触媒としては、パラジウム化合物〔例:酢酸パラジウム(II)、テトラキス(トリフェニルホスフィン)パラジウム(0)、ジクロロビス(トリフェニルホスフィン)パラジウム(II)、ジクロロビス(トリエチルホスフィン)パラジウム(II)、トリス(ジベンジリデンアセトン)ジパラジウム(0)、[1,1-ビス(ジフェニルホスフィノ)フェロセン]ジクロロパラジウム(II)、酢酸パラジウム(II)と1,1’-ビス(ジフェニルホスフィノ)フェロセンの複合体等〕、銅化合物〔例:ヨウ化銅(I)、臭化銅(I)等〕等が挙げられる。金属触媒は、化合物(2)1モルに対し約0.000001~10モル用いる。金属触媒は、ホスフィン配位子〔例:トリフェニルホスフィン、4,5-ビス(ジフェニルホスフィノ)-9,9-ジメチルキサンテン、トリ-tert-ブチルホスフィン、トリ-tert-ブチルホスフィンテトラフルオロボラート等〕またはアミン配位子〔例:8-メチルキノリン-1-オール、1,10-フェナントロリン、1,2-ジアミノシクロヘキサン、N,N’-ジメチル-1,2-エタンジアミン等〕とともに用いることができる。ホスフィン配位子またはアミン配位子を用いる場合には、化合物(2)1モルに対し、約0.01~5モル使用する。化合物(3)、化合物(4)または化合物(5)は、化合物(2)1モルに対し約0.8~10モル用いる。金属触媒を用いて反応を行う場合、塩基の存在下で行うことが望ましい。該塩基としては、例えば、無機塩基類、塩基性塩類等が挙げられる。塩基は、化合物(2)1モルに対し約1~20モル用いる。また、これらの反応で酸素に不安定な金属触媒を用いる場合には、例えば、アルゴンガス、窒素ガス等の不活性なガス気流中で反応を行うことが好ましい。本反応は反応に不活性な溶媒を用いて行うのが有利である。このような溶媒としては反応が進行する限り特に限定されないが、例えば、アルコール類、エーテル類、芳香族炭化水素類、飽和炭化水素類、アミド類、ハロゲン化炭化水素類、ニトリル類、エステル類、スルホキシド類、水等の溶媒、またはそれらの混合溶媒等が好ましい。反応時間は用いる試薬や溶媒により異なるが通常1分~200時間である。反応温度は好ましくは、0~200℃である。また、反応を促進させる目的で、マイクロ波を照射してもよい。化合物(2)、化合物(3)、化合物(4)および化合物(5)は市販品をそのまま用いてもよく、また、自体公知の方法あるいはそれに準じた方法により製造することもできる。
化合物(I)は、化合物(6)と化合物(7)とを反応させることによって製造することができる。反応は、工程A-1と同様の方法に従って行えばよい。化合物(7)は市販品をそのまま用いてもよく、また、自体公知の方法あるいはそれに準じた方法により製造することもできる。
化合物(10)は、化合物(8)と化合物(9)とを縮合させることによって製造することができる。縮合反応は化合物(8)もしくはその反応性誘導体と化合物(9)とを反応させることにより行う。該反応性誘導体としては、例えば酸塩化物、酸臭化物等の酸ハロゲン化物;ピラゾール、イミダゾール、ベンゾトリアゾール等との酸アミド;酢酸、プロピオン酸、酪酸等との混合酸無水物;酸アジド;ジエトキシリン酸エステル、ジフェノキシリン酸エステル、p-ニトロフェニルエステル、2,4-ジニトロフェニルエステル、シアノメチルエステル、ペンタクロロフェニルエステル、N-ヒドロキシスクシンイミドとのエステル、N-ヒドロキシフタルイミドとのエステル、1-ヒドロキシベンゾトリアゾールとのエステル、6-クロロ-1-ヒドロキシベンゾトリアゾールとのエステル、1-ヒドロキシ-1H-2-ピリドンとのエステル等の活性エステル;2-ピリジルチオエステル、2-ベンゾチアゾリルチオエステル等の活性チオエステル等が挙げられる。また該反応性誘導体を用いる代わりに、化合物(8)を適当な縮合剤の存在下、直接化合物(9)と反応させてもよい。該縮合剤としては、例えば、N,N’-ジシクロヘキシルカルボジイミド、1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド(WSC)塩酸塩等のN,N’-ジ置換カルボジイミド類;N,N’-カルボニルジイミダゾール等のアゾライド類;N-エトキシカルボニル-2-エトキシ-1,2-ジヒドロキノリン、オキシ塩化リン、アルコキシアセチレン等の脱水剤;2-クロロメチルピリジニウムヨージド、2-フルオロ-1-メチルピリジニウムヨージド等の2-ハロゲノピリジニウム塩;ジエチルホスホリルシアニド等のホスホリルシアニド類;2-(7-アザベンゾトリアゾール-1-イル)-1,1,3,3-テトラメチルウロニウムヘキサフルオロホスフェイト(HATU)、O-(7-アザベンゾトリアゾールー1-イル)-N,N,N’,N’-テトラメチルウロニウムテトラフルオロボレイト(TATU)等が挙げられる。これらの縮合剤を用いた場合、反応は化合物(8)の反応性誘導体を経て進行すると考えられる。化合物(9)は、化合物(8)もしくはその反応性誘導体1モルに対し通常約0.8~5モル用いる。本反応は反応に不活性な溶媒を用いて行うのが有利である。このような溶媒としては反応が進行する限り特に限定されないが、例えば、エーテル類、芳香族炭化水素類、飽和炭化水素類、アミド類、ハロゲン化炭化水素類、ニトリル類、スルホキシド類、芳香族有機塩基類等の溶媒、またはそれらの混合溶媒等が好ましい。また、反応により酸性物質が放出される場合は、それらを反応系内から除去する目的で、脱酸剤の存在下に反応を行うことができる。このような脱酸剤としては、例えば、塩基性塩類、有機塩基類等が使用される。また、反応を促進させる目的で、例えば、塩基性塩類、有機塩基類等を用いることもできる。反応時間は用いる試薬や溶媒により異なるが通常1分~72時間である。反応温度は好ましくは、0~100℃である。化合物(8)および化合物(9)は市販品をそのまま用いてもよく、また、自体公知の方法あるいはそれに準じた方法により製造することもできる。
化合物(6)は、化合物(10)を酸または脱水剤で処理することにより製造することができる。該酸としては、例えば、有機酸類、無機酸類等が挙げられる。酸は、化合物(10)1モルに対し約1~50モル用いる。該脱水剤としては、オキシ塩化リン、カルバミン酸メチル-N-(トリエチルアンモニウムスルホニル)(Burgess reagent)等が挙げられる。脱水剤は、化合物(10)1モルに対し約1~10モル用いる。また、所望により、硫化剤の存在下反応を行うこともできる。該硫化剤としては、2,4-ビス(4-メトキシフェニル)-1,3,2,4-ジチアジホスフェタン-2,4-ジスルフィド(Lawesson’s reagent)等が挙げられる。硫化剤は、化合物(10)1モルに対し約1~10モル用いる。本反応は反応に不活性な溶媒を用いて行うのが有利である。このような溶媒としては反応が進行する限り特に限定されないが、例えば、エーテル類、芳香族炭化水素類、飽和炭化水素類、アミド類、ハロゲン化炭化水素類、ニトリル類、スルホキシド類、芳香族有機塩基類等の溶媒、またはそれらの混合溶媒等が好ましい。また、反応により酸性物質が放出される場合は、それらを反応系内から除去する目的で、脱酸剤の存在下に反応を行うことができる。このような脱酸剤としては、例えば、塩基性塩類、有機塩基類等が使用される。また、反応を促進させる目的で、例えば、塩基性塩類、有機塩基類等を用いることもできる。反応時間は用いる試薬や溶媒により異なるが通常1分~72時間である。反応温度は好ましくは、0~150℃である。
式中、R5およびR8は、それぞれ置換されていてもよい炭化水素基を示す。
R6およびR7は、それぞれ、水素原子、それぞれ置換されていてもよい、C1-10アルキル基、C2-10アルケニル基、C3-10シクロアルキル基、C3-10シクロアルケニル基、C6-14アリール基、C7-14アラルキル基、C8-13アリールアルケニル基または複素環基(例、芳香族複素環基、非芳香族複素環基)、またはアシル基を示し、この場合において、R6とR7とが一緒になって置換されていてもよい複素環基を形成していてもよい。
A1は、さらに置換されていてもよく、架橋されていてもよいピペリジン環を、A2は、さらに置換されていてもよく、架橋されていてもよいピペラジン環を示す。
環A1および環A2は、置換可能な位置に1ないし5個(好ましくは1ないし3個)の置換基を有していてもよい。このような置換基としては、例えば、上記置換基B群から選ばれる置換基が挙げられる。置換基が複数存在する場合、各置換基は、同一でも異なっていてもよい。
「架橋されたピペリジン環およびピペラジン環」の例としては、8-アザビシクロ[3.2.1]オクタン、2,5-ジアザビシクロ[2.2.1]ヘプタン、3-アザビシクロ[3.1.0]ヘキサン等が挙げられる。
R5またはR8で示される「置換されていてもよい炭化水素基」としては、RA、RA’またはRB’で示される「置換されていてもよい炭化水素基」と同様のものが挙げられる。
R6またはR7で示される「置換されていてもよい炭化水素基」および「置換されていてもよい複素環基」としては、RA、RA’またはRB’で示される「置換されていてもよい炭化水素基」および「置換されていてもよい複素環基」と同様のものが挙げられる。
R6とR7とが一緒になって形成する「置換されていてもよい複素環基」としては、RA、RA’またはRB’で示される「置換されていてもよい複素環基」と同様のものが挙げられる。
化合物(Ib)は、化合物(Ia)を加水分解することによって製造することができる。加水分解反応は、無機塩基や無機酸を用い、加水分解反応として一般的に用いられる反応条件により行うことができる。自体公知の方法、例えば、Wiley-Interscience社1999年刊「Protective Groups in Organic Synthesis, 3rdEd.」(Theodora W. Greene, Peter G. M. Wuts著)に記載の方法等に準じて行えばよい。
化合物(Ic)は、化合物(Ib)を化合物(11)と縮合させることによって製造することができる。反応は、工程A-3と同様の方法に従って行えばよい。化合物(11)は市販品をそのまま用いてもよく、また、自体公知の方法あるいはそれに準じた方法により製造することもできる。
化合物(12)は、化合物(Id)のカルバマート基を除去することによって製造することができる。カルバマート基の除去に関しては、自体公知の方法、例えば、Wiley-Interscience社1999年刊「Protective Groups in Organic Synthesis, 3rdEd.」(Theodora W. Greene, Peter G. M. Wuts著)に記載の方法等に準じて行えばよい。
化合物(Ie)は、化合物(12)と化合物(11)(R1=N(R6)(R7)の場合)とを、または化合物(12)と化合物(13)とを、縮合させることによって製造することができる。
化合物(12)と化合物(13)を縮合させる場合、反応は、工程A-3と同様の方法に従って行えばよい。
化合物(12)と化合物(11)を縮合させる場合、化合物(12)の反応性誘導体と化合物(11)を反応させる方法や、適当な縮合剤の存在下、化合物(12)と化合物(11)を直接反応させる方法などがある。該反応性誘導体としては、例えば、イミダゾールなどとのカルボキサミドなどが挙げられる。また、該縮合剤としては、例えば、ホスゲン、トリホスゲンなどのホスゲン類、N,N’-カルボニルジイミダゾールなどのアゾライド類などが挙げられる。これらの縮合剤を用いた場合、反応は化合物(12)の反応性誘導体を経て進行すると考えられる。化合物(11)は、化合物(12)もしくはその反応性誘導体1モルに対し通常約0.8~5モル用いる。本反応は反応に不活性な溶媒を用いて行うのが有利である。このような溶媒としては反応が進行する限り特に限定されないが、例えば、エーテル類、芳香族炭化水素類、飽和炭化水素類、アミド類、ハロゲン化炭化水素類、ニトリル類、スルホキシド類、芳香族有機塩基類等の溶媒、またはそれらの混合溶媒等が好ましい。また、反応により酸性物質が放出される場合は、それらを反応系内から除去する目的で、脱酸剤の存在下に反応を行うことができる。このような脱酸剤としては、例えば、塩基性塩類、有機塩基類等が使用される。また、反応を促進させる目的で、例えば、塩基性塩類、有機塩基類等を用いることもできる。反応時間は用いる試薬や溶媒により異なるが通常1分~72時間である。反応温度は好ましくは、0~100℃である。化合物(13)は市販品をそのまま用いてもよく、また、自体公知の方法あるいはそれに準じた方法により製造することもできる。
化合物(I)の配置異性体(E,Z体)については異性化が生じた時点で、例えば、抽出、再結晶、蒸留、クロマトグラフィー等の通常の分離手段により単離、精製することができ、純粋な化合物を製造することができる。また、新実験化学講座14(日本化学会編)、第251ないし253頁、第4版実験化学講座19(日本化学会編)、第273ないし274頁記載の方法およびそれに準じる方法に従って、加熱、酸触媒、遷移金属錯体、金属触媒、ラジカル種触媒、光照射あるいは強塩基触媒等により二重結合の異性化を進行させ、対応する純粋な異性体を得ることもできる。
化合物(I)は水和物であっても非水和物であってもよい。
いずれの場合にも、さらに所望により、脱保護反応、アシル化反応、アルキル化反応、水素添加反応、酸化反応、還元反応、炭素鎖延長反応、置換基交換反応を各々、単独あるいはその二つ以上を組み合わせて行うことにより化合物(I)を合成することができる。
上記反応によって、目的物が遊離の状態で得られる場合には、常法に従って塩に変換してもよく、また塩として得られる場合には、常法に従って遊離体または他の塩に変換することもできる。かくして得られる化合物(I)は、公知の手段例えば、転溶、濃縮、溶媒抽出、分溜、結晶化、再結晶、クロマトグラフィー等により反応溶液から単離、精製することができる。
なお、化合物(I)が、コンフィギュレーショナル アイソマー(配置異性体)、ジアステレオマー、コンフォーマー等として存在する場合には、所望により、前記分離、精製手段によりそれぞれを単離することができる。また、化合物(I)がラセミ体である場合には、通常の光学分割手段によりd体、l体に分離することができる。
保護基としては、例えば、ホルミルまたはそれぞれ置換されていてもよいC1-6アルキル-カルボニル(例、アセチル、プロピオニル等)、フェニルカルボニル、C1-6アルコキシ-カルボニル(例、メトキシカルボニル、エトキシカルボニル等)、フェニルオキシカルボニル、C7-10アラルキルオキシ-カルボニル(例、ベンジルオキシカルボニル等)、トリチル、フタロイル等が用いられる。これらの置換基としては、ハロゲン原子(例、フッ素、塩素、臭素、ヨウ素等)、C1-6アルキル-カルボニル(例、アセチル、プロピオニル、バレリル等)、ニトロ等が用いられる。置換基の数は例えば1ないし3個程度である。
また、保護基の除去方法としては、自体公知またはそれに準じる方法が用いられるが、例えば、酸、塩基、紫外光、ヒドラジン、フェニルヒドラジン、N-メチルジチオカルバミン酸ナトリウム、テトラブチルアンモニウムフルオリド、酢酸パラジウム等で処理する方法または還元反応が用いられる。
化合物(I)に光学異性体が存在し得る場合、これら個々の光学異性体およびそれら混合物のいずれも当然本発明の範囲に包含されるものであり、所望によりこれらの異性体をそれ自体公知の手段に従い光学分割したり、個別に製造することもできる。
化合物(I)が、コンフィギュレーショナル アイソマー(配置異性体)、ジアステレオマー、コンフォーマー等として存在する場合には、所望により、前記の分離、精製手段によりそれぞれを単離することができる。また、化合物(I)がラセミ体である場合には、通常の光学分割手段によりS体およびR体に分離することができる。
化合物(I)に立体異性体が存在する場合には、この異性体が単独の場合およびそれらの混合物の場合も本発明に含まれる。
(1) 化合物(I)のアミノがアシル化、アルキル化、りん酸化された化合物(例えば、化合物(I)のアミノが、エイコサノイル化、アラニル化、ペンチルアミノカルボニル化、(5-メチル-2-オキソ-1,3-ジオキソレン-4-イル)メトキシカルボニル化、テトラヒドロフラニル化、ピロリジルメチル化、ピバロイルオキシメチル化、tert-ブチル化、エトキシカルボニル化、tert-ブトキシカルボニル化、アセチル化、シクロプロピルカルボニル化された化合物等);
(2) 化合物(I)のヒドロキシが、アシル化、アルキル化、りん酸化、ホウ酸化された化合物(例えば、化合物(I)のヒドロキシが、アセチル化、パルミトイル化、プロパノイル化、ピバロイル化、スクシニル化、フマリル化、アラニル化、ジメチルアミノメチルカルボニル化された化合物等);
(3) 化合物(I)のカルボキシが、エステル化、アミド化された化合物(例えば、化合物(I)のカルボキシが、エチルエステル化、フェニルエステル化、カルボキシメチルエステル化、ジメチルアミノメチルエステル化、ピバロイルオキシメチルエステル化、エトキシカルボニルオキシエチルエステル化、フタリジルエステル化、(5-メチル-2-オキソ-1,3-ジオキソレン-4-イル)メチルエステル化、シクロヘキシルオキシカルボニルエチルエステル化、メチルアミド化された化合物等);
等が挙げられる。これらの化合物は、自体公知の方法によって化合物(I)から製造することができる。
化合物(I)は、水和物、非水和物、溶媒和物、無溶媒和物のいずれであってもよい。
同位元素(例、3H、11C、14C、18F、35S、125I等)等で標識された化合物も、化合物(I)に包含される。
さらに、1Hを2H(D)に変換した重水素変換体も、化合物(I)に包含される。
化合物(I)は、薬学的に許容され得る共結晶または共結晶塩であってもよい。ここで、共結晶または共結晶塩とは、各々が異なる物理的特性(例えば、構造、融点、融解熱、吸湿性、溶解性および安定性等)を持つ、室温で二種またはそれ以上の独特な固体から構成される結晶性物質を意味する。共結晶または共結晶塩は、自体公知の共結晶化法に従い製造することができる。
化合物(I)は、PETトレーサーとして用いてもよい。
無痛化剤の好適な例としては、ベンジルアルコールが挙げられる。
抗酸化剤の好適な例としては、亜硫酸塩、アスコルビン酸塩等が挙げられる。
これらはそれぞれ経口的あるいは非経口的(例、局所、直腸、静脈投与)に安全に投与できる。
従って、本発明化合物は、CH24Hの機能亢進が関与する疾患、例えば、神経変性疾患の予防、症状改善、進展抑制または治療に有用である。
本明細書において、「神経変性疾患」とは、神経組織の変性を伴う疾患を意味する。
神経変性疾患の具体例としては、例えば、アルツハイマー病、軽度認知障害、ハンチントン病、パーキンソン病、多発性硬化症、筋萎縮性側索硬化症、外傷性脳損傷、脳梗塞、緑内障などが挙げられる。
また、本発明化合物は、CH24Hの機能亢進が関与する疾患、例えば、癲癇、統合失調症、痙攣などの予防、症状改善、進展抑制または治療に有用である。
本発明化合物と組み合わせて用いられる薬剤(以下、「併用薬剤」と略記する)としては、例えば、アセチルコリンエステラーゼ阻害剤(例、ドネペジル、リバスチグミン、ガランタミン、ザナペジル)、抗痴呆剤(例、メマンチン)、βアミロイド蛋白産生、分泌、蓄積、凝集および/または沈着抑制剤、βセクレターゼ阻害剤(例、6-(4-ビフェニリル)メトキシ-2-[2-(N,N-ジメチルアミノ)エチル]テトラリン、6-(4-ビフェニリル)メトキシ-2-(N,N-ジメチルアミノ)メチルテトラリン、6-(4-ビフェニリル)メトキシ-2-(N,N-ジプロピルアミノ)メチルテトラリン、2-(N,N-ジメチルアミノ)メチル-6-(4’-メトキシビフェニル-4-イル)メトキシテトラリン、6-(4-ビフェニリル)メトキシ-2-[2-(N,N-ジエチルアミノ)エチル]テトラリン、2-[2-(N,N-ジメチルアミノ)エチル]-6-(4’-メチルビフェニル-4-イル)メトキシテトラリン、2-[2-(N,N-ジメチルアミノ)エチル]-6-(4’-メトキシビフェニル-4-イル)メトキシテトラリン、6-(2’,4’-ジメトキシビフェニル-4-イル)メトキシ-2-[2-(N,N-ジメチルアミノ)エチル]テトラリン、6-[4-(1,3-ベンゾジオキソール-5-イル)フェニル]メトキシ-2-[2-(N,N-ジメチルアミノ)エチル]テトラリン、6-(3’,4’-ジメトキシビフェニル-4-イル)メトキシ-2-[2-(N,N-ジメチルアミノ)エチル]テトラリン、その光学活性体、その塩およびその水和物、OM99-2(国際公開01/00663))、γセクレターゼ阻害作用剤、βアミロイド蛋白凝集阻害作用剤(例、PTI-00703、ALZHEMED(NC-531)、PPI-368(特表平11-514333)、PPI-558(特表2001-500852)、SKF-74652(Biochem.J.(1999),340(1),283-289))、βアミロイドワクチン、βアミロイド分解酵素等、脳機能賦活薬(例、アニラセタム、ニセルゴリン)、他のパーキンソン病治療薬[(例、ドーパミン受容体作動薬(例、L-ドーパ、ブロモクリプチン、パーゴライド、タリペキソール、プラミペキソール、カベルゴリン、アマンタジン)、モノアミン酸化酵素(MAO)阻害薬(例、デプレニル、セルジリン(セレギリン)、レマセミド、リルゾール)、抗コリン剤(例、トリヘキシフェニジル、ビペリデン)、COMT阻害剤(例、エンタカポン)]、筋萎縮性側索硬化症治療薬(例、リルゾール等、神経栄養因子)、痴呆の進行に伴う異常行動、徘徊等の治療薬(例、鎮静剤、抗不安剤)、アポトーシス阻害薬(例、CPI-1189、IDN-6556、CEP-1347)、神経分化・再生促進剤(例、レテプリニム、キサリプローデン(Xaliproden;SR-57746-A)、SB-216763、Y-128、VX-853、prosaptide、5,6-ジメトキシ-2-[2,2,4,6,7-ペンタメチル-3-(4-メチルフェニル)-2,3-ジヒドロ-1-ベンゾフラン-5-イル]イソインドリン、5,6-ジメトキシ-2-[3-(4-イソプロピルフェニル)-2,2,4,6,7-ペンタメチル-2,3-ジヒドロ-1-ベンゾフラン-5-イル]イソインドリン、6-[3-(4-イソプロピルフェニル)-2,2,4,6,7-ペンタメチル-2,3-ジヒドロ-1-ベンゾフラン-5-イル]-6,7-ジヒドロ-5H-[1,3]ジオキソロ[4,5-f]イソインドールおよびその光学活性体、塩、水和物)、抗うつ薬(例、デシプラミン、アミトリプチリン、イミプラミン、トラマドル)、抗癲癇薬(例、ラモトリジン)、抗不安薬(例、ベンゾジアゼピン)、非ステロイド性抗炎症薬(例、メロキシカム、テノキシカム、インドメタシン、イブプロフェン、セレコキシブ、ロフェコキシブ、アスピリン、インドメタシン)、疾患修飾性抗リウマチ薬(DMARDs)、抗サイトカイン薬(例、TNF阻害薬、MAPキナーゼ阻害薬)、ステロイド薬(例、デキサメサゾン、ヘキセストロール、酢酸コルチゾン)、尿失禁・頻尿治療剤(例、塩酸フラボキサート、塩酸オキシブチニン、塩酸プロピベリン)、ホスホジエステラーゼ阻害薬(例、(クエン酸)シルデナフィル)、ドーパミン作動薬(例、アポモルフィン)、抗不整脈薬(例、メキシレチン)、性ホルモンまたはその誘導体(例、プロゲステロン、エストラジオール、安息香酸エストラジオール)、骨粗鬆症治療剤(例、アルファカルシドール、カルシトリオール、エルカトニン、サケカルシトニン、エストリオール、イプリフラボン、パミドロン酸二ナトリウム、アレンドロン酸ナトリウム水和物、インカドロン酸二ナトリウム)、副甲状腺ホルモン(PTH)、カルシウム受容体拮抗薬、不眠症治療薬(例、ベンゾジアゼピン系薬剤、非ベンゾジアゼピン系薬剤、メラトニン作動薬)、統合失調症治療薬(例、ハロペリドールなどの定型抗精神病薬;クロザピン、オランザピン、リスペリドン、アリピプラゾールなどの非定型抗精神病薬;代謝型グルタミン酸受容体またはイオンチャネル共役型グルタミン酸受容体に作用する薬剤;ホスホジエステラーゼ阻害薬)等が挙げられる。
(1)糖尿病治療剤
例えば、インスリン製剤(例、ウシ、ブタの膵臓から抽出された動物インスリン製剤;大腸菌またはイーストを用い、遺伝子工学的に合成したヒトインスリン製剤;インスリン亜鉛;プロタミンインスリン亜鉛;インスリンのフラグメントまたは誘導体(例、INS-1)、経口インスリン製剤)、インスリン抵抗性改善剤(例、ピオグリタゾンまたはその塩(好ましくは塩酸塩)、ロシグリタゾンまたはその塩(好ましくはマレイン酸塩)、テサグリタザール(Tesaglitazar)、ラガグリタザール(Ragaglitazar)、ムラグリタザール(Muraglitazar)、エダグリタゾン(Edaglitazone)、メタグリダセン(Metaglidasen)、ナベグリタザール(Naveglitazar)、AMG-131、THR-0921)、α-グルコシダーゼ阻害剤(例、ボグリボース、アカルボース、ミグリトール、エミグリテート)、ビグアナイド剤(例、メトホルミン、ブホルミンまたはそれらの塩(例、塩酸塩、フマル酸塩、コハク酸塩))、インスリン分泌促進剤[スルホニルウレア剤(例、トルブタミド、グリベンクラミド、グリクラジド、クロルプロパミド、トラザミド、アセトヘキサミド、グリクロピラミド、グリメピリド、グリピザイド、グリブゾール)、レパグリニド、ナテグリニド、ミチグリニドまたはそのカルシウム塩水和物、グルコース依存性インスリン分泌促進薬(例、[(3S)-6-({2',6'-ジメチル-4'-[3-(メチルスルホニル)プロポキシ]ビフェニル-3-イル}メトキシ)-2,3-ジヒドロ-1-ベンゾフラン-3-イル]酢酸またはその塩)]、ジペプチジルペプチダーゼIV阻害剤(例、アログリプチン(Alogliptin)、ヴィルダグリプチン(Vildagliptin)、シタグリプチン(Sitagliptin)、サクサグリプチン(Saxagliptin)、T-6666、TS-021)、β3アゴニスト(例、AJ-9677)、GPR40アゴニスト、GLP-1受容体アゴニスト[例、GLP-1、GLP-1MR剤、NN-2211、AC-2993(exendin-4)、BIM-51077、Aib(8,35)hGLP-1(7,37)NH2、CJC-1131]、アミリンアゴニスト(例、プラムリンチド)、ホスホチロシンホスファターゼ阻害剤(例、バナジン酸ナトリウム)、糖新生阻害剤(例、グリコーゲンホスホリラーゼ阻害剤、グルコース-6-ホスファターゼ阻害剤、グルカゴン拮抗剤)、SGLUT(sodium-glucose cotransporter)阻害剤(例、T-1095)、11β-ヒドロキシステロイドデヒドロゲナーゼ阻害薬(例、BVT-3498)、アジポネクチンまたはその作動薬、IKK阻害薬(例、AS-2868)、レプチン抵抗性改善薬、ソマトスタチン受容体作動薬、グルコキナーゼ活性化薬(例、Ro-28-1675)、GIP(Glucose-dependent insulinotropic peptide)等が挙げられる。
例えば、アルドース還元酵素阻害剤(例、トルレスタット、エパルレスタット、ゼナレスタット、ゾポルレスタット、ミナルレスタット、フィダレスタット、CT-112)、神経栄養因子およびその増加薬(例、NGF、NT-3、BDNF、WO01/14372に記載のニューロトロフィン産生・分泌促進剤(例えば、4-(4-クロロフェニル)-2-(2-メチル-1-イミダゾリル)-5-[3-(2-メチルフェノキシ)プロピル]オキサゾール))、神経再生促進薬(例、Y-128)、PKC阻害剤(例、ルボキシスタウリン メシレート(ruboxistaurin mesylate))、AGE阻害剤(例、ALT946、ピマゲジン、ピラトキサチン、N-フェナシルチアゾリウム ブロマイド(ALT766)、ALT-711、EXO-226、ピリドリン(Pyridorin)、ピリドキサミン)、活性酸素消去薬(例、チオクト酸)、脳血管拡張剤(例、チアプリド、メキシレチン)、ソマトスタチン受容体作動薬(例、BIM23190)、アポトーシスシグナルレギュレーティングキナーゼ-1(ASK-1)阻害薬等が挙げられる。
例えば、スタチン系化合物(例、プラバスタチン、シンバスタチン、ロバスタチン、アトルバスタチン、フルバスタチン、ロスバスタチン、ピタバスタチンまたはそれらの塩(例、ナトリウム塩、カルシウム塩))、スクアレン合成酵素阻害剤(例、ラパキスタットアセテート(lapaquistat acetate)またはその塩)、フィブラート系化合物(例、ベザフィブラート、クロフィブラート、シムフィブラート、クリノフィブラート)、ACAT阻害剤(例、アバシマイブ(Avasimibe)、エフルシマイブ(Eflucimibe))、陰イオン交換樹脂(例、コレスチラミン)、プロブコール、ニコチン酸系薬剤(例、ニコモール(nicomol)、ニセリトロール(niceritrol))、イコサペント酸エチル、植物ステロール(例、ソイステロール(soysterol)、ガンマオリザノール(γ-oryzanol))等が挙げられる。
例えば、アンジオテンシン変換酵素阻害剤(例、カプトプリル、エナラプリル、デラプリル)、アンジオテンシンII拮抗剤(例、カンデサルタン シレキセチル、ロサルタン、エプロサルタン、バルサルタン、テルミサルタン、イルベサルタン、タソサルタン、1-[[2’-(2,5-ジヒドロ-5-オキソ-4H-1,2,4-オキサジアゾール-3-イル)ビフェニル-4-イル]メチル]-2-エトキシ-1H-ベンズイミダゾール-7-カルボン酸、アジルサルタン、アジルサルタン メドキソミル)、カルシウム拮抗剤(例、マニジピン、ニフェジピン、アムロジピン、エホニジピン、ニカルジピン)、カリウムチャンネル開口薬(例、レブクロマカリム、L-27152、AL 0671、NIP-121)、クロニジン等が挙げられる。
例えば、中枢性抗肥満薬(例、デキスフェンフルラミン、フェンフルラミン、フェンテルミン、シブトラミン、アンフェプラモン、デキサンフェタミン、マジンドール、フェニルプロパノールアミン、クロベンゾレックス;MCH受容体拮抗薬(例、SB-568849;SNAP-7941;WO01/82925およびWO01/87834に記載の化合物);ニューロペプチドY拮抗薬(例、CP-422935);カンナビノイド受容体拮抗薬(例、SR-141716、SR-147778);グレリン拮抗薬;11β-ヒドロキシステロイドデヒドロゲナーゼ阻害薬(例、BVT-3498))、膵リパーゼ阻害薬(例、オルリスタット、セティリスタット)、β3アゴニスト(例、AJ-9677、AZ40140)、ペプチド性食欲抑制薬(例、レプチン、CNTF(毛様体神経栄養因子))、コレシストキニンアゴニスト(例、リンチトリプト、FPL-15849)、摂食抑制薬(例、P-57)等が挙げられる。
例えば、キサンチン誘導体(例、サリチル酸ナトリウムテオブロミン、サリチル酸カルシウムテオブロミン)、チアジド系製剤(例、エチアジド、シクロペンチアジド、トリクロルメチアジド、ヒドロクロロチアジド、ヒドロフルメチアジド、ベンチルヒドロクロロチアジド、ペンフルチジド、ポリチアジド、メチクロチアジド)、抗アルドステロン製剤(例、スピロノラクトン、トリアムテレン)、炭酸脱水酵素阻害剤(例、アセタゾラミド)、クロルベンゼンスルホンアミド系製剤(例、クロルタリドン、メフルシド、インダパミド)、アゾセミド、イソソルビド、エタクリン酸、ピレタニド、ブメタニド、フロセミド等が挙げられる。
例えば、アルキル化剤(例、サイクロフォスファミド、イフォスファミド)、代謝拮抗剤(例、メソトレキセート、5-フルオロウラシルまたはその誘導体)、抗癌性抗生物質(例、マイトマイシン、アドリアマイシン)、植物由来抗癌剤(例、ビンクリスチン、ビンデシン、タキソール)、シスプラチン、カルボプラチン、エトポキシド等が挙げられる。なかでも5-フルオロウラシル誘導体であるフルツロンあるいはネオフルツロン等が好ましい。
例えば、微生物または細菌成分(例、ムラミルジペプチド誘導体、ピシバニール)、免疫増強活性のある多糖類(例、レンチナン、シゾフィラン、クレスチン)、遺伝子工学的手法で得られるサイトカイン(例、インターフェロン、インターロイキン(IL))、コロニー刺激因子(例、顆粒球コロニー刺激因子、エリスロポエチン)等が挙げられ、なかでもIL-1、IL-2、IL-12等のインターロイキンが好ましい。
例えば、ヘパリン(例、ヘパリンナトリウム、ヘパリンカルシウム、ダルテパリンナトリウム)、ワルファリン(例、ワルファリンカリウム)、抗トロンビン薬(例、アルガトロバン)、血栓溶解薬(例、ウロキナーゼ、チソキナーゼ、アルテプラーゼ、ナテプラーゼ、モンテプラーゼ、パミテプラーゼ)、血小板凝集抑制薬(例、塩酸チクロピジン、シロスタゾール、イコサペント酸エチル、ベラプロストナトリウム、塩酸サルポグレラート)等が挙げられる。
例えば、シクロオキシゲナーゼ阻害剤(例、インドメタシン)〔Cancer Research、第49巻、5935~5939頁、1989年〕、プロゲステロン誘導体(例、メゲステロールアセテート)〔Journal of Clinical Oncology、第12巻、213~225頁、1994年〕、糖質ステロイド(例、デキサメサゾン)、メトクロプラミド系薬剤、テトラヒドロカンナビノール系薬剤(文献はいずれも上記と同様)、脂肪代謝改善剤(例、エイコサペンタエン酸等)〔British Journal of Cancer、第68巻、314~318頁、1993年〕、成長ホルモン、IGF-1、あるいは悪液質を誘導する因子であるTNF-α、LIF、IL-6、オンコスタチンMに対する抗体等が挙げられる。
以下の実施例中の「室温」は通常約 10 ℃ないし約 35 ℃を示す。混合溶媒において示した比は、特に断らない限り容量比を示す。%は、特に断らない限り重量%を示す。
シリカゲルカラムクロマトグラフィーにおいて、NHと記載した場合は、アミノプロピルシラン結合シリカゲルを用いた。HPLC (高速液体クロマトグラフィー) において、C18と記載した場合は、オクタデシル結合シリカゲルを用いた。溶出溶媒の比は、特に断らない限り容量比を示す。
THF :テトラヒドロフラン
DME :1,2-ジメトキシエタン
DMF :N,N-ジメチルホルムアミド
DMA :N,N-ジメチルアセトアミド
DMSO :ジメチルスルホキシド
ESI :エレクトロスプレーイオン化法
APCI :大気圧化学イオン化
[M+H]+ :分子イオンピーク
M :モル濃度
IPE :ジイソプロピルエーテル
WSC :1-[3-(ジメチルアミノ)プロピル]-3-エチルカルボジイミド
HATU :2-(7-アザベンゾトリアゾール-1-イル)-1,1,3,3-テトラメチルウロニウムヘキサフルオロホスフェイト
HOBt :1-ヒドロキシベンゾトリアゾール
HPLC :高速液体クロマトグラフィー
DIPEA :N,N-ジイソプロピルエチルアミン
NMP :N-メチル-2-ピロリドン
DPPF :1,1'-ビス(ジフェニルホスフィノ)フェロセン
Pd2(dba)3 :トリス(ジベンジリデンアセトン)ジパラジウム(0)
Xantphos :4,5-ビス(ジフェニルホスフィノ)-9,9-ジメチルキサンテン
MS (マススペクトル) は、LC/MS (液体クロマトグラフ質量分析計) により測定した。
大気圧イオン化 (API、Atomospheric Pressure Ionization) 法としては、ESI (ElectroSpray Ionization、エレクトロスプレーイオン化) 法、または、APCI (Atomospheric Pressure Cheimcal Ionization、大気圧化学イオン化) 法を用いた。データは実測値 (found)を記載した。通常、分子イオンピークが観測されるが、tert-ブトキシカルボニル基 (-Boc) を有する化合物の場合、フラグメントイオンとして、tert-ブトキシカルボニル基あるいはtert-ブチル基が脱離したピークが観測されることもある。また、水酸基 (-OH) を有する化合物の場合、フラグメントイオンとして、H2Oが脱離したピークが観測されることもある。塩の場合は、通常、フリー体の分子イオンピークもしくはフラグメントイオンピークが観測される。
元素分析値 (Anal.) は、計算値 (Calcd) と実測値 (Found) を記載した。
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)-N,N-ジメチルピペリジン-4-カルボキサミド
A) 4-(4-クロロ-1H-ピラゾール-1-イル)-3-フルオロピリジン
p-トルエンスルホン酸一水和物 (0.58 g)、4-クロロ-3-フルオロピリジン(2.0 g)、4-クロロ-1H-ピラゾール (1.7 g) および2-プロパノール(10 mL) の混合物を130℃で2時間マイクロウェーブ照射した。混合物を室温まで冷却し、飽和重曹水を加え、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製し、標題化合物 (2.2 g) を得た。
MS (API+), found: 198.2, 200.0.
1-((ベンジルオキシ)カルボニル)ピペリジン-4-カルボン酸 (1.2 g) およびDMF (12 mL) の混合物に、HATU (2.1 g)、 トリエチルアミン(0.83 mL) およびジメチルアミンTHF溶液(2M, 2.73 mL) を室温で加えた。混合物を室温で4時間撹拌し、飽和塩化アンモニウム水溶液を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、標題化合物 (960 mg) を得た。
MS (API+): [M+H]+291.2.
ベンジル 4-(ジメチルカルバモイル)ピペリジン-1-カルボキシラート(960 mg) をエタノール (15 mL) および酢酸エチル (15 mL) に溶解させ、10% パラジウム炭素 (96 mg) を加え、混合物を水素雰囲気下、室温で5時間撹拌した。不溶物を濾去し、濾液を減圧下留去し、標題化合物 (530 mg) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.31-1.57 (4H, m), 2.45 (1H, d, J = 3.0 Hz), 2.63 (1H, tt, J = 11.1, 4.0 Hz), 2.79 (3H, s), 2.91 (2H, dt, J = 12.1, 3.0 Hz), 2.99 (3H, s), 3.29 (2H, brs).
4-(4-クロロ-1H-ピラゾール-1-イル)-3-フルオロピリジン(98 mg), N,N-ジメチルピペリジン-4-カルボキサミド(160 mg), 炭酸カリウム(140 mg) および DMA (0.50 mL)の混合物を200℃で10時間マイクロウェーブ照射した。水を加え、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから結晶化して標題化合物 (39 mg) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.57-1.74 (4H, m), 2.67-2.79 (3H, m), 2.82 (3H, s), 2.86-2.96 (2H, m), 3.02 (3H, s), 7.52 (1H, d, J = 5.3 Hz), 7.96 (1H, s), 8.36 (1H, d, J = 5.3 Hz), 8.48 (1H, s), 8.77 (1H, s).
(3-exo)-N,N-ジメチル-8-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)-8-アザビシクロ[3.2.1]オクタン-3-カルボキサミド
A) tert-ブチル 3-(ジメチルカルバモイル)-8-アザビシクロ[3.2.1]オクタン-8-カルボキシラート
8-(tert-ブトキシカルボニル)-8-アザビシクロ[3.2.1]オクタン-3-カルボン酸 (400 mg)、ジメチルアミン塩酸塩 (260 mg)、HATU (770 mg)、DIPEA (0.96 mL) およびDMF (5.0 mL) の混合物を室温で16時間撹拌した。混合物を酢酸エチル/水で希釈し、酢酸エチルで抽出した。有機層を分離し、水および飽和食塩水で洗浄後、硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサンおよびメタノール/酢酸エチル)で精製し、標題化合物 (440 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.45-1.56 (11H, m), 1.60-1.70 (2H, m), 1.95-2.07 (4H, m), 2.93 (3H, s), 3.00-3.13 (4H, m), 4.20-4.35 (2H, m).
tert-ブチル 3-(ジメチルカルバモイル)-8-アザビシクロ[3.2.1]オクタン-8-カルボキシラート (440 mg) および酢酸エチル (4.0 mL) の混合物に4M 塩化水素/酢酸エチル (10 mL) を加え、室温で16時間撹拌した。混合物を減圧下濃縮して、標題化合物 (340 mg) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.59-1.71 (2H, m), 1.86-2.06 (6H, m), 2.81 (3H, s), 2.99-3.15 (4H, m), 3.86-4.00 (2H, m), 8.68 (1H, brs), 9.39 (1H, brs).
p-トルエンスルホン酸一水和物 (0.83 g)、4-クロロ-3-フルオロピリジン(2.9 g)、4-メチル-1H-ピラゾール (1.9 mL) および2-プロパノール (14 mL) の混合物を130℃で2時間マイクロウェーブ照射した。混合物に飽和重曹水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製し、標題化合物 (3.3 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 2.12 (3H, s), 7.76 (1H, s), 7.93 (1H, dd, J = 7.0, 5.5 Hz), 8.18 (1H, dd, J = 1.9, 0.8 Hz), 8.49 (1H, d, J = 5.3 Hz), 8.74 (1H, d, J = 4.2 Hz).
N,N-ジメチル-8-アザビシクロ[3.2.1]オクタン-3-カルボキサミド塩酸塩 (170 mg)、3-フルオロ-4-(4-メチル-1H-ピラゾール-1-イル)ピリジン (260 mg)、炭酸カリウム (320 mg) およびNMP (2.0 mL) の混合物をマイクロウェーブ照射下、200℃で16時間撹拌した。混合物を酢酸エチル/水で希釈し、酢酸エチルで抽出した。有機層を分離し、水および飽和食塩水で洗浄後、硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン)で精製し、得られた固体を酢酸エチル/ヘキサンから再結晶して標題化合物 (25 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.45-1.55 (2H, m), 1.63-1.72 (2H, m), 1.98-2.13 (4H, m), 2.18 (3H, s), 2.90-3.03 (4H, m), 3.05 (3H, s), 3.59-3.67 (2H, m), 7.36 (1H, d, J = 5.3 Hz), 7.52 (1H, s), 8.03-8.07 (1H, m), 8.20 (1H, d, J = 4.9 Hz), 8.32 (1H, s).
1-(4-(1,3-ベンゾチアゾール-2-イル)ピリジン-3-イル)-N,N-ジメチルピペリジン-4-カルボキサミド
A) 2-(3-フルオロピリジン-4-イル)ベンゾ[d]チアゾール
3-フルオロイソニコチン酸 (1.0 g) およびDIPEA (1.9 mL) の混合物に2,4,6-トリプロピル-1,3,5,2,4,6-トリオキサトリホスホリナン-2,4,6-トリオキシド (1.9 mL, 50%酢酸エチル溶液) および2-アミノベンゼンチオール(0.76 mL) を室温で加え、70 ℃で終夜撹拌した。混合物を水および酢酸エチルを用いて希釈し、60 ℃まで加熱し、不溶物を濾去し、酢酸エチルを用いて抽出した。有機層を飽和食塩水で洗浄した後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製し、標題化合物 (460 mg) を得た。
MS (API+): [M+H]+231.1.
2-(3-フルオロピリジン-4-イル)ベンゾ[d]チアゾール (100 mg)、N,N-ジメチルピペリジン-4-カルボキサミド (81 mg)、炭酸カリウム (90 mg) およびNMP (0.50 mL) の混合物を150 ℃で終夜撹拌した。室温まで冷却した後、混合物を水で希釈し酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから再結晶して標題化合物 (79 mg) を得た。
1H NMR (400 MHz, CDCl3) δ 1.86 (2H, d, J = 13.0 Hz), 2.24-2.37 (2H, m), 2.72 (1H, tt, J = 11.6, 3.6 Hz), 2.93-3.04 (5H, m), 3.12 (3H, s), 3.29 (2H, d, J = 11.7 Hz), 7.41-7.48 (1H, m), 7.52 (1H, td, J = 7.6, 1.2 Hz), 8.00 (1H, d, J = 7.8 Hz), 8.11 (1H, d, J = 8.1 Hz), 8.25 (1H, d, J = 5.1 Hz), 8.52 (1H, d, J = 5.1 Hz),
8.66 (1H, s).
(2R)-1-((1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
A) エチル 1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボキシラート
4-(4-クロロ-1H-ピラゾール-1-イル)-3-フルオロピリジン(3.4 g)、エチル ピペリジン-4-カルボキシラート(13 mL)、炭酸カリウム(7.1 g) および NMP(15 mL)の混合物を180℃で4時間撹拌した。混合物に0℃で水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製し、標題化合物 (5.3 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.16-1.23 (3H, m), 1.56-1.74 (2H, m), 1.80-1.93 (2H, m), 2.37-2.46 (1H, m), 2.66-2.79 (2H, m), 2.89 (2H, dt, J = 12.1, 3.2 Hz), 4.09 (2H, q, J = 7.2 Hz), 7.52 (1H, d, J = 4.9 Hz), 7.96 (1H, s), 8.36 (1H, d, J = 4.9 Hz), 8.48 (1H, s), 8.77 (1H, s).
エチル 1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボキシラート(5.3 g) をTHF(55 mL) および エタノール (20 mL) に溶解させ、混合物に2M 水酸化ナトリウム水溶液(12 mL) を加え、室温で終夜撹拌した。混合物を 1M 塩酸(24 mL)で中和し、沈殿した固体を濾取し、標題化合物 (4.0 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.55-1.71 (2H, m), 1.84 (2H, dd, J = 13.3, 3.0 Hz), 2.25-2.39 (1H, m), 2.64-2.76 (2H, m), 2.89 (2H, dt, J = 12.0, 3.3 Hz), 7.52 (1H, d, J = 5.3 Hz), 7.96 (1H, s), 8.36 (1H, d, J = 5.3 Hz), 8.48 (1H, s), 8.77 (1H, s), 12.27 (1H, brs).
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (300 mg) およびDMF (6.0 mL) の混合物にHATU (480 mg)、トリエチルアミン (0.30 mL)および (R)-ピロリジン-2-カルボニトリル塩酸塩 (160 mg) を室温で加え、2時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから結晶化して標題化合物 (290 mg) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.60-1.84 (4H, m), 1.95-2.31 (4H, m), 2.66-3.04 (5H, m), 3.36-3.59 (1H, m), 3.60-3.75 (1H, m), 4.72 (1H, dd, J = 7.6, 3.8 Hz), 7.52 (1H, d, J = 4.9 Hz), 7.97 (1H, s), 8.36 (1H, d, J = 4.9 Hz), 8.49 (1H, s), 8.78 (1H, s).
1-(4-(4-ブロモ-1H-ピラゾール-1-イル)ピリジン-3-イル)-N,N-ジメチルピペリジン-4-カルボキサミド
A)4-(4-ブロモ-1H-ピラゾール-1-イル)-3-フルオロピリジン
p-トルエンスルホン酸一水和物 (0.30 g)、4-クロロ-3-フルオロピリジン(1.0 g)、4-ブロモ-1H-ピラゾール (1.3 g) および2-プロパノール(5.0 mL) の混合物を130℃で2時間マイクロウェーブ照射した。混合物を室温まで冷却し、飽和重曹水を加え、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製し、標題化合物 (1.5 g) を得た。
MS (API+), found: 242.0, 244.0.
4-(4-ブロモ-1H-ピラゾール-1-イル)-3-フルオロピリジン(700 mg), N,N-ジメチルピペリジン-4-カルボキサミド(680 mg), 炭酸カリウム(800 mg) および NMP (2.5 mL)の混合物を180℃で5時間加熱した。混合物を室温まで冷却し、水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサン/IPEから結晶化して標題化合物 (410 mg) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.49-1.78 (4H, m), 2.64-2.84 (6H, m), 2.86-2.96 (2H, m), 3.02 (3H, s), 7.52 (1H, d, J = 4.9 Hz), 7.96 (1H, s), 8.36 (1H, d, J = 5.3 Hz), 8.48 (1H, s), 8.77 (1H, d, J = 0.8 Hz).
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-メチル-N-(テトラヒドロ-2H-ピラン-4-イル)ピペリジン-4-カルボキサミド
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (0.50 g)、N-メチルテトラヒドロ-2H-ピラン-4-アミン (0.16 g)、HATU (0.81 g)、トリエチルアミン (0.91 mL) およびDMF (8.2 mL) の混合物を室温で3時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー(NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから結晶化して標題化合物 (0.43 g) を得た。
1H NMR (300 MHz, CDCl3) δ1.45-1.65 (2H, m), 1.65-2.11 (6H, m), 2.61 (1H, brs), 2.71-2.97 (5H, m), 3.13 (2H, d, J = 11.7 Hz), 3.37-3.59 (2H, m), 3.94-4.16 (2H, m), 4.66-4.84 (1H, m), 7.59 (1H, s), 7.66 (1H, s), 8.40 (1H, s), 8.46 (1H, s), 8.59 (1H, s).
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-シクロプロピル-N-メチルピペリジン-4-カルボキサミド
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (0.5 g) およびDMF (8.2 mL) の混合物にHATU (0.81 g)、トリエチルアミン (0.91 mL) および N-メチルシクロプロパンアミン (0.14 g) を加え、室温で3時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー(NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから結晶化して標題化合物 (0.40 g) を得た。
1H NMR (300 MHz, CDCl3) δ 0.71-0.99 (4H, m), 1.71-1.85 (2H, m), 1.96 (2H, dd, J = 12.3, 2.8 Hz), 2.64-2.85 (3H, m), 2.94 (3H, s), 3.06-3.22 (3H, m), 7.60 (1H, d, J = 4.9 Hz), 7.66 (1H, s), 8.37 (1H, s), 8.46 (1H, s), 8.62 (1H, s).
1-(4-(4-シクロプロピル-1H-ピラゾール-1-イル)ピリジン-3-イル)-N,N-ジメチルピペリジン-4-カルボキサミド
1-(4-(4-ブロモ-1H-ピラゾール-1-イル)ピリジン-3-イル)-N,N-ジメチルピペリジン-4-カルボキサミド (80 mg)、シクロプロピルボロン酸 (36 mg)、1,1'-ビス(ジフェニルホスフィノ)フェロセン-パラジウム(II)ジクロリド ジクロロメタン錯体(17 mg)、炭酸セシウム (210 mg)、DME(1.5 mg)および水 (0.30 mg) の混合物を100℃で30分間マイクロウェーブ照射した。1,1'-ビス(ジフェニルホスフィノ)フェロセン-パラジウム(II)ジクロリド ジクロロメタン錯体 (17 mg) およびシクロプロピルボロン酸 (36 mg) を加え、100℃で1時間マイクロウェーブ照射した。飽和重曹水を加え、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン)で精製した後、HPLC (C18、移動相:水/アセトニトリル (0.1% TFA含有系) ) にて分取した。得られた画分に飽和炭酸水素ナトリウム水溶液を加え、酢酸エチルで抽出した。無水硫酸ナトリウムで乾燥し、減圧下濃縮後、得られた固体を酢酸エチル/ヘキサンから結晶化し、標題化合物 (15 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 0.56-0.63 (2H, m), 0.88-0.96 (2H, m), 1.73-1.83 (3H, m), 1.86-2.02 (2H, m), 2.56-2.67 (1H, m), 2.73 (2H, td, J = 11.9, 2.3 Hz), 2.98 (3H, s), 3.08 (3H, s), 3.09-3.17 (2H, m), 7.49 (1H, s), 7.60 (1H, d, J = 5.3 Hz), 8.34 (1H, d, J = 5.3 Hz), 8.36 (1H, s), 8.40 (1H, s).
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-(テトラヒドロ-2H-ピラン-4-イル)ピペリジン-4-カルボキサミド
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (1.0 g)、テトラヒドロ-2H-ピラン-4-アミン (0.36 mL)、HATU (1.7 g)、トリエチルアミン (1.9 mL) およびDMF (12 mL) の混合物を室温で3時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから結晶化して標題化合物 (0.78 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.35-1.54 (2H, m), 1.78-1.98 (6H, m), 2.06-2.21 (4H, m), 2.70 (2H, dt, J = 11.7, 7.2 Hz), 3.12 (2H, d, J = 12.1 Hz), 3.48 (2H, td, J = 11.7, 2.3 Hz), 3.88-4.09 (3H, m), 5.37 (1H, d, J = 7.6 Hz), 7.54 (1H, s), 7.60 (1H, d, J = 5.3 Hz), 8.30-8.36 (2H, m), 8.39 (1H, s).
(2R)-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
A) エチル 1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボキシラート
3-フルオロ-4-(4-メチル-1H-ピラゾール-1-イル)ピリジン(2.5 g)、エチル ピペリジン-4-カルボキシラート(4.3 mL)、炭酸カリウム(5.8 g) および NMP(12 mL)の混合物を180℃で7時間撹拌した。混合物にエチル ピペリジン-4-カルボキシラート (2.0 mL) を室温で加え、180℃で2時間撹拌後、室温で終夜撹拌した。0℃で混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製し、標題化合物 (2.8 g) を得た。
MS (API+): [M+H]+315.2.
エチル 1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボキシラート(1.2 g)、THF(15 mL) およびエタノール (5.0 mL) の溶液に2M 水酸化ナトリウム水溶液 (3.0 mL) を加え、室温で終夜撹拌した。混合物を0℃に冷却後、1M 塩酸(6.0 mL)で中和した。沈殿した固体を濾取し、水で洗浄して標題化合物 (0.84 g) を得た。
MS (API+): [M+H]+287.2.
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (0.25 g)およびDMF (6.0 mL)の溶液にHATU (0.43 g)、トリエチルアミン (0.27 mL)および(R)-ピロリジン-2-カルボニトリル塩酸塩(0.14 g) を室温で加え、2時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから結晶化して標題化合物 (0.22 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.64-1.83 (4H, m), 1.97-2.07 (2H, m), 2.10-2.21 (5H, m), 2.54-2.61 (1H, m), 2.69-2.81 (2H, m), 2.89-3.04 (2H, m), 3.49-3.59 (1H, m), 3.63-3.73 (1H, m), 4.72 (1H, dd, J = 7.6, 3.8 Hz), 7.54 (1H, d, J = 5.3 Hz), 7.63 (1H, s), 8.31 (1H, d, J = 5.3 Hz), 8.42 (1H, s), 8.44 (1H, s).
(2R)-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
A) エチル 1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボキシラート
3-フルオロ-4-(4-メチル-1H-ピラゾール-1-イル)ピリジン(0.80 g)、エチル ピペリジン-4-カルボキシラート(1.5 mL) およびNMP(4.5 mL)の混合物を185℃で8.5時間撹拌した。混合物をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製し、標題化合物(1.0 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.19 (3H, t, J = 7.2 Hz), 1.60-1.76 (2H, m), 1.81-1.93 (2H, m), 2.12 (3H, s), 2.37-2.48 (1H, m), 2.65-2.77 (2H, m), 2.88-2.99 (2H, m), 4.09 (2H, q, J = 7.2 Hz), 7.53 (1H, d, J = 4.9 Hz), 7.63 (1H, s), 8.31 (1H, d, J = 5.3 Hz), 8.41 (1H, s), 8.42 (1H, s).
エチル 1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボキシラート(2.8 g)、THF(30 mL) およびエタノール (10 mL) の溶液に2M 水酸化ナトリウム水溶液 (7.0 mL) を加え、室温で終夜撹拌した。混合物に0℃で1M 塩酸 (14 mL) を加え中和した。得られた固体を濾取し、水で洗浄して標題化合物 (2.2 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.54-1.75 (2H, m), 1.78-1.92 (2H, m), 2.12 (3H, s), 2.25-2.41 (1H, m), 2.63-2.75 (2H, m), 2.86-2.98 (2H, m), 7.53 (1H, d, J = 4.9 Hz), 7.63 (1H, s), 8.30 (1H, d, J = 5.3 Hz), 8.39-8.45 (2H, m), 12.33 (1H, brs).
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (80 g) およびアセトニトリル (0.32 L) の懸濁液にDIPEA (0.21 L)、(R)-プロリンアミド (40 g) および2,4,6-トリプロピル-1,3,5,2,4,6-トリオキサトリホスホリナン-2,4,6-トリオキシド (1.7M 酢酸エチル溶液、0.28 L) を0℃で加えた。室温で1時間撹拌した後、混合物に2,4,6-トリプロピル-1,3,5,2,4,6-トリオキサトリホスホリナン-2,4,6-トリオキシド (1.7M 酢酸エチル溶液、0.35 L)を加え、70℃で終夜撹拌した。混合物に飽和炭酸水素ナトリウム水溶液 (1600 mL) を0℃で加えた後、酢酸エチルおよびTHFの混合溶媒で抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥後、溶液をシリカゲルカラムクロマトグラフィー (酢酸エチル)で精製した。溶媒を減圧下留去し、残渣にジイソプロピルエーテルを加え、室温で終夜撹拌した。固体を濾取し、ジイソプロピルエーテルで洗浄して標題化合物 (93 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.57-1.82 (4H, m), 1.89-2.30 (7H, m), 2.53-2.83 (3H, m), 2.86-3.06 (2H, m), 3.41-3.58 (1H, m), 3.62-3.75 (1H, m), 4.72 (1H, dd, J = 7.4, 4.0 Hz), 7.53 (1H, d, J = 5.3 Hz), 7.63 (1H, s), 8.31 (1H, d, J = 5.3 Hz), 8.41 (1H, s), 8.43 (1H, s).
D) (2R)-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
(2R)-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリルの粗結晶 (103 g) をエタノール (620 mL) に70℃で溶解後、ヘプタン (620 mL) を同温度で滴下し1時間撹拌した。ヘプタン (820 mL) をさらに1時間かけて加えた後、室温で終夜撹拌した。結晶を濾取し、ヘプタン (1.0 L) で洗浄して標題化合物 (92 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.59-1.83 (4H, m), 1.89-2.29 (7H, m), 2.53-2.82 (3H, m), 2.88-3.07 (2H, m), 3.43-3.58 (1H, m), 3.66-3.72 (1H, m), 4.72 (1H, dd, J = 7.6, 3.8 Hz), 7.53 (1H, d, J = 4.9 Hz), 7.63 (1H, s), 8.31 (1H, d, J = 5.3 Hz), 8.41 (1H, s), 8.43 (1H, s).
mp: 178℃
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)-3,3-ジフルオロ-N-(テトラヒドロ-2H-ピラン-4-イル)ピペリジン-4-カルボキサミド
A) 3-(4-((ベンジルオキシ)メチル)-3,3-ジフルオロピペリジン-1-イル)-4-クロロピリジン
4-((ベンジルオキシ)メチル)-3,3-ジフルオロピペリジン(560 mg)、3-ブロモ-4-クロロピリジン (490 mg)、酢酸パラジウム (26 mg)、Xantphos (140 mg)、ナトリウム tert-ブトキシド (340 mg) およびトルエン (12 mL) の混合物をマイクロウェーブ照射下、120℃で3時間撹拌した。混合物をNH-シリカゲルパッド (酢酸エチル) にて濾過し、濾液を減圧下濃縮した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン)で精製した後、さらに、シリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し標題化合物 (550 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.74-1.92 (1H, m), 2.13-2.37 (2H, m), 2.83-2.94 (1H, m), 2.98-3.15 (1H, m), 3.44-3.56 (2H, m), 3.59-3.71 (1H, m), 3.94 (1H, dd, J = 9.3, 4.0 Hz), 4.53 (1H, d, J = 12.0 Hz), 4.59 (1H, d, J = 12.0 Hz), 7.27-7.40 (6H, m), 8.21 (1H, d, J = 4.9 Hz), 8.29 (1H, s).
3-(4-((ベンジルオキシ)メチル)-3,3-ジフルオロピペリジン-1-イル)-4-クロロピリジン (1.9 g)、4-クロロ-1H-ピラゾール (0.72 g)、p-トルエンスルホン酸一水和物 (0.21 g) および2-プロパノール (12 mL) の混合物をマイクロウェーブ照射下、150℃で6時間撹拌した。混合物を酢酸エチル/飽和重曹水で希釈し、酢酸エチルで抽出した。有機層を分離し、水および飽和食塩水で洗浄後、硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン)で精製し、標題化合物 (1.5 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.59-1.74 (1H, m), 2.05-2.33 (2H, m), 2.65-2.79 (1H, m), 2.94-3.16 (2H, m), 3.27-3.40 (1H, m), 3.52 (1H, t, J = 8.9 Hz), 3.92 (1H, dd, J = 9.3, 4.0 Hz), 4.53 (1H, d, J = 12.0 Hz), 4.57 (1H, d, J = 12.0 Hz), 7.27-7.40 (5H, m), 7.63 (1H, d, J = 5.3 Hz), 7.67 (1H, s), 8.42 (1H, s), 8.44 (1H, d, J = 4.9 Hz), 8.52 (1H, s).
3-(4-((ベンジルオキシ)メチル)-3,3-ジフルオロピペリジン-1-イル)-4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン (1.5 g) およびアセトニトリル (30 mL) の混合物に氷冷下、ヨウ化トリメチルシリル (5.0 mL) を加え、室温で20時間撹拌した。混合物に氷冷下、水を加え、同温度にて10分間撹拌した。混合物に、ピリジン(15 mL)、チオ硫酸ナトリウム水溶液および飽和重曹水を加え、酢酸エチルで抽出した。有機層を分離し、水および飽和食塩水で洗浄後、硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサンおよびメタノール/酢酸エチル)で精製し、標題化合物(0.91 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.57-1.78 (2H, m), 1.90-2.21 (2H, m), 2.70-2.83 (1H, m), 2.95-3.17 (2H, m), 3.29-3.42 (1H, m), 3.70-3.81 (1H, m), 4.03-4.12 (1H, m), 7.64 (1H, d, J = 5.3 Hz), 7.68 (1H, s), 8.43 (1H, s), 8.46 (1H, d, J = 5.3 Hz), 8.51 (1H, s).
1-メチル-2-アザアダマンタン N-オキシル(1.5 g) および水 (5.0 mL) の混合物に、42%テトラフルオロホウ酸水溶液 (1.9 mL) を室温で30分かけて滴下した。反応液が琥珀色に変化したのを確認後、次亜塩素酸ナトリウム水溶液 (6.1 mL) を氷冷下1時間かけて加え、同温度で更に1時間撹拌した。沈殿物を濾取して、氷冷した5%重曹水 (15 mL)、水 (15 mL) および氷冷したジエチルエーテル (75 mL) で洗浄後、50℃で24時間乾燥し、標題化合物 (850 mg) を得た。
Anal. Calcd for C10H16BF4NO: C, 47.46; H, 6.37; N, 5.49. Found: C, 47.47; H, 6.40; N, 5.50.
(1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)-3,3-ジフルオロピペリジン-4-イル)メタノール (0.91 g) およびアセトニトリル (20 mL)/pH 6.8 リン酸緩衝液 (10 mL) の混合物に、亜塩素酸ナトリウム (1.3 g) および(1r,3s,5R,7S)-1-メチル-2-オキソ-2-アザアダマンタン-2-イウムテトラフルオロホウ酸塩 (42 mg) を順次加えた。室温にて1.5時間撹拌した後、2-メチルブタ-2-エン (6.0 mL) を加えて更に15分間撹拌した。溶媒の大部分を留去した後、水を加え、氷冷下30分間撹拌した。生じた沈殿物を濾取して、水およびジエチルエーテルで洗浄後、乾燥し、標題化合物 (0.85 g) を得た。
1H NMR (400 MHz, DMSO-d6) δ 1.82-2.00 (2H, m), 2.79-2.94 (2H, m), 3.00-3.13 (1H, m), 3.19-3.34 (2H, m), 7.58 (1H, d, J = 5.1 Hz), 7.99 (1H, d, J = 0.5 Hz), 8.43 (1H, d, J = 5.4 Hz), 8.57 (1H, s), 8.63 (1H, d, J = 0.5 Hz), 12.90 (1H, brs).
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)-3,3-ジフルオロピペリジン-4-カルボン酸 (30 mg)、テトラヒドロピラン-4-イルアミン (12 mg)、HATU (43 mg)、DIPEA (20 μL) およびDMF (1.0 mL) の混合物を室温で1時間撹拌した。混合物を酢酸エチル/水で希釈し、酢酸エチルで抽出した。有機層を分離し、水および飽和食塩水で洗浄後、硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサンおよびメタノール/酢酸エチル)で精製し、標題化合物(30 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.43-1.59 (2H, m), 1.87-2.01 (2H, m), 2.05-2.15 (2H, m), 2.64-2.83 (2H, m), 3.02-3.25 (2H, m), 3.41-3.56 (3H, m), 3.90-4.11 (3H, m), 5.80 (1H, d, J = 5.7 Hz), 7.63 (1H, d, J = 5.3 Hz), 7.68 (1H, s), 8.43-8.50 (3H, m).
2-メチル-8-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)-2,8-ジアザスピロ[4.5]デカン-1-オン
A) 1-tert-ブチル 4-エチル 4-(シアノメチル)ピペリジン-1,4-ジカルボキシラート
ジイソプロピルアミン (4.7 g) およびTHF (75 mL) の混合物にn-ブチルリチウムのヘキサン溶液 (1.6 M, 29 mL) を氷冷下で加え、30分間撹拌した。混合物に1-tert-ブチル 4-エチル ピペリジン-1,4-ジカルボキシラート (6.0 g) およびTHF (10 mL) の混合物を氷冷下で加え、氷冷下で3時間撹拌した後、2-ブロモアセトニトリル (5.6 g) を氷冷下で加えた。混合物を12時間撹拌し、溶媒を減圧下留去し、水を加え、酢酸エチルで抽出した。有機層を無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製して標題化合物 (2.6 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.21 (3H, t, J = 7.0 Hz), 1.39 (9H, s), 1.43-1.54 (2H, m), 1.90-2.00 (2H, m), 2.87 (2H, s), 2.96-3.12 (2H, m), 3.57-3.67 (2H, m), 4.11-4.22 (2H, m).
1-tert-ブチル 4-エチル 4-(シアノメチル)ピペリジン-1,4-ジカルボキシラート(2.5 g)、コバルト(II)クロリド六水和物 (1.0 g) およびメタノール (50 mL) の混合物に水素化ホウ素ナトリウム (1.6 g) を氷冷下で加え、氷冷下2時間撹拌し、室温で2日間撹拌し、60 ℃で1時間撹拌した。28%アンモニア水を加えた後、沈殿物を濾過し、濾液を酢酸エチルで抽出した。その有機層を無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル) で精製して標題化合物(1.1 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.25-1.35 (2H, m), 1.40 (9H, s), 1.45-1.58 (2H, m), 1.90-1.98 (2H, m), 2.90 (2H, brs), 3.16 (2H, t, J = 7.2 Hz), 3.76-3.86 (2H, m), 7.56 (1H, brs).
tert-ブチル 1-オキソ-2,8-ジアザスピロ[4.5]デカン-8-カルボキシラート(400 mg)、酢酸エチル (10 mL) およびエタノール(2.0 mL) の混合物に4 M塩化水素/酢酸エチル溶液 (5.0 mL) を室温で加え、60 ℃で2時間撹拌した後、溶媒を減圧下留去した。残渣を酢酸エチルで希釈し、得られた固体をろ取して標題化合物 (240 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.47-1.64 (2H, m), 1.77-1.92 (2H, m), 1.93-2.03 (2H, m), 2.81-3.03 (2H, m), 3.11-3.34 (4H, m), 7.72 (1H, brs), 8.62-9.33 (2H, m).
3-フルオロ-4-(4-メチル-1H-ピラゾール-1-イル)ピリジン (50 mg)、2,8-ジアザスピロ[4.5]デカン-1-オン塩酸塩 (54 mg)、炭酸カリウム (120 mg) およびNMP (0.20 mL) の混合物を160 ℃で1日間撹拌し、180 ℃で7時間撹拌した。室温まで冷却した後、混合物を水で希釈し、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、メタノール/酢酸エチル) で精製して標題化合物 (36 mg) を得た。
MS (API+): [M+H]+312.2.
8-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)-2,8-ジアザスピロ[4.5]デカン-1-オン (35 mg) およびDMF (0.50 mL) の混合物に水素化ナトリウム (60%、6.7 mg) を氷冷下で加えた。窒素雰囲気下、室温で30分間撹拌した後、混合物にヨウ化メチル (7.0 μL) およびDMF (0.50 mL) の混合物を加え、室温で1時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を分離し、飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから再結晶して標題化合物 (18 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.46 (2H, d, J = 13.6 Hz), 1.95-2.12 (4H, m), 2.17 (3H, s), 2.76 (2H, td, J = 12.0, 2.5 Hz), 2.87 (3H, s), 3.08 (2H, dt, J = 12.1, 3.4 Hz), 3.27-3.37 (2H, m), 7.53 (1H, s), 7.60 (1H, d, J = 5.3 Hz), 8.34 (1H, d, J = 5.3 Hz), 8.40 (2H, d, J = 4.9 Hz).
1-(4-(4-シアノ-1H-ピラゾール-1-イル)ピリジン-3-イル)-N,N-ジメチルピペリジン-4-カルボキサミド
1-(4-(4-ブロモ-1H-ピラゾール-1-イル)ピリジン-3-イル)-N,N-ジメチルピペリジン-4-カルボキサミド(60 mg), Pd2(dba)3(15 mg), シアン化亜鉛(56 mg) 、DPPF (18 mg) および無水DMF (1.5 mL) の混合物をアルゴン雰囲気下、100℃で7時間加熱した。混合物を室温まで冷却した後、混合物にPd2(dba)3(7.0 mg) を追加し、アルゴン雰囲気下、100℃で5時間加熱した。混合物を室温まで冷却し、不溶物を濾去し、濾液に酢酸エチルと水を加え、有機層を水および飽和食塩水で洗浄し、無水硫酸ナトリウムで乾燥後減圧濃縮した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製した後、HPLC (C18、移動相:水/アセトニトリル (0.1% TFA含有系) ) にて分取し、得られた画分に飽和炭酸水素ナトリウム水溶液を加え、酢酸エチルで抽出した。無水硫酸ナトリウムで乾燥後、減圧下濃縮し、得られた固体を酢酸エチル/THF/ヘキサンから結晶化し、標題化合物 (17 mg) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.58-1.69 (4H, m), 2.65-2.91 (8H, m), 3.01 (3H, s), 7.54 (1H, d, J = 5.3 Hz), 8.39 (1H, d, J = 4.9 Hz), 8.44 (1H, s), 8.53 (1H, s), 9.32 (1H, s).
N-シクロプロピル-N-メチル-1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボキサミド
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (0.5 g) およびDMF (8.2 mL) の混合物 にHATU (0.86 g)、トリエチルアミン (0.97 mL) および N-メチルシクロプロパンアミン (0.15 g) を加え、室温で3時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー(NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから結晶化して標題化合物 (0.25 g) を得た。
1H NMR (300 MHz, CDCl3) δ 0.68-1.00 (4H, m), 1.77 (2H, s), 1.96 (2H, dd, J = 12.3, 2.8 Hz), 2.17 (3H, s), 2.65-2.83 (3H, m), 2.94 (3H, s), 3.14 (3H, d, J = 11.7 Hz), 7.54 (1H, s), 7.62 (1H, d, J = 5.3 Hz), 8.25-8.50 (3H, m).
(2R)-1-((1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
A) N'-アセチル-3-フルオロイソニコチノヒドラジド
3-フルオロイソニコチン酸 (4.5 g) およびチオニルクロリド (20 mL) の混合物を窒素雰囲気下、4時間加熱還流した。溶媒を減圧下留去した。残渣をトルエンに懸濁させ、溶媒を減圧下留去した。残渣をTHF (20 mL) に懸濁させ、混合物をアセトヒドラジド (2.8 g)、トリエチルアミン (9.8 mL) およびTHF (20 mL) の混合物に氷冷下で滴下し、室温で30分間撹拌した。不溶物を濾去した後、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (メタノール/酢酸エチル) で精製して標題化合物 (3.9 g) を得た。
MS (API+): [M+H]+198.1.
N'-アセチル-3-フルオロイソニコチノヒドラジド (3.8 g) およびトルエン (100 mL) の混合物に2,4-ビス(4-メトキシフェニル)-1,3-ジチア-2,4-ジホスフェタン2,4-ジスルフィド (7.8 g) を加え110 ℃で5時間撹拌した。溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製して標題化合物 (2.6 g) を得た。
MS (API+): [M+H]+196.1.
2-(3-フルオロピリジン-4-イル)-5-メチル-1,3,4-チアジアゾール (1.5 g)、エチル ピペリジン-4-カルボキシラート (1.8 g)、炭酸カリウム (1.6 g) およびNMP (8.0 mL) の混合物を150 ℃で2時間撹拌した。室温まで冷却した後、混合物を水で希釈して酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンで洗浄して標題化合物 (1.5 g) を得た。
MS (API+): [M+H]+333.2.
エチル 1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-カルボキシラート(1.5 g)、THF (10 mL) およびメタノール(3.0 mL) の混合物に2M 水酸化ナトリウム水溶液(2.2 mL) を室温で加え、終夜撹拌した。混合物にさらに2M 水酸化ナトリウム水溶液 (2.2 mL) を加え、室温で15分間撹拌した。1M 塩酸で中和した後、得られた固体を濾取して標題化合物 (1.3 g) を得た。
MS (API+): [M+H]+305.2.
1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (80 mg)、DIPEA (0.23 mL) およびDMF (0.50 mL) の混合物にHATU (150 mg)を加え、(R)-ピロリジン-2-カルボニトリル塩酸塩 (52 mg)およびDMF (0.50 mL)の混合物を加え、室温で終夜撹拌した。混合物を水で希釈し酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから再結晶して標題化合物 (59 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.77-2.01 (2H, m), 2.07-2.41 (6H, m), 2.45-2.63 (1H, m), 2.80-2.88 (3H, m), 2.89-3.08 (2H, m), 3.18 (2H, d, J = 3.4 Hz), 3.44-3.65 (1H, m), 3.68-3.81 (1H, m), 4.66-4.85 (1H, m), 8.20 (1H, d, J = 5.7 Hz), 8.53 (1H, d, J = 4.9 Hz), 8.60-8.68 (1H, m).
1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)-L-プロリンアミド
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (100 mg)、DIPEA (0.31 mL) およびDMF (2.0 mL) の混合物にHATU (200 mg) および(S)-ピロリジン-2-カルボキサミド(48 mg) を加え、室温で30分間撹拌した。混合物を水および飽和食塩水で希釈し、酢酸エチル/THFで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、メタノール/酢酸エチル) で精製して標題化合物 (92 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.74-2.23 (10H, m), 2.36-2.58 (2H, m), 2.65-2.82 (2H, m), 3.05-3.23 (2H, m), 3.49-3.72 (2H, m), 4.61 (1H, dd, J = 8.1, 2.1 Hz), 5.28 (1H, brs), 6.88 (1H, brs), 7.54 (1H, s), 7.58-7.63 (1H, m), 8.30-8.37 (2H, m), 8.37-8.42 (1H, m).
4,4-ジフルオロ-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)-L-プロリンアミド
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (300 mg)およびDMF (6.0 mL) の混合物にHATU (520 mg)、トリエチルアミン (0.32 mL)および (S)-4,4-ジフルオロピロリジン-2-カルボキサミド (240 mg) を室温で加え、1時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体の一部 (53 mg) をエーテルで洗浄し、標題化合物 (39 mg) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.56-1.85 (4H, m), 2.12 (3H, s), 2.25-2.37 (1H, m), 2.62-2.80 (3H, m), 2.88-3.04 (3H, m), 3.86-4.24 (2H, m), 4.44 (1H, dd, J = 9.5, 4.9 Hz), 7.07 (1H, s), 7.38 (1H, brs), 7.53 (1H, d, J = 5.3 Hz), 7.63 (1H, s), 8.31 (1H, d, J = 4.9 Hz), 8.40 (1H, s), 8.43 (1H, s).
(2S)-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (100 mg)、DIPEA (0.31 mL) およびDMF (2.0 mL) の混合物にHATU (200 mg) および(S)-ピロリジン-2-カルボニトリル塩酸塩 (56 mg) を加え、室温で30分間撹拌した。混合物を水および飽和食塩水で希釈し、酢酸エチル/THFで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから再結晶して標題化合物 (86 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.70-2.05 (4H, m), 2.10-2.60 (8H, m), 2.62-2.88 (2H, m), 3.02-3.27 (2H, m), 3.44-3.60 (1H, m), 3.64-3.77 (1H, m), 4.59-4.88 (1H, m), 7.54 (1H, s), 7.61 (1H, d, J = 5.3 Hz), 8.30-8.38 (2H, m), 8.40 (1H, s).
(2S)-4,4-ジフルオロ-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
4,4-ジフルオロ-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)-L-プロリンアミド(380 mg) 、イミダゾール(62 mg)、ピリジン(4.5 mL) の混合物にオキシ塩化リン(0.17 mL) を-40℃で加え、-20℃で1時間撹拌した。混合物に1M 塩酸(30 mL) を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、標題化合物 (290 mg) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.52-1.85 (4H, m), 2.12 (3H, s), 2.61-3.06 (6H, m), 3.92-4.32 (3H, m), 5.04 (1H, dd, J = 9.1, 3.0 Hz), 7.53 (1H, d, J = 5.3 Hz), 7.63 (1H, s), 8.31 (1H, d, J = 4.9 Hz), 8.42 (2H, d, J = 6.8 Hz).
1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)-D-プロリンアミド
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (52 mg)およびDMF (1.0 mL) の混合物にHATU (90 mg)、トリエチルアミン (0.056 mL)および (R)-プロリンアミド (25 mg) を室温で加え、2時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサンおよびメタノール/酢酸エチル) で精製し、標題化合物(62 mg) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.58-1.98 (8H, m), 2.12 (3H, s), 2.62-2.81 (2H, m), 2.87-3.04 (2H, m), 3.40-3.67 (2H, m), 4.15-4.39 (1H, m), 5.74 (1H, s), 6.84 (1H, s), 7.12-7.23 (1H, m), 7.50-7.56 (1H, m), 7.63 (1H, s), 8.30 (1H, d, J = 5.3 Hz), 8.39-8.46 (2H, m).
2-メチル-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)-D-プロリンアミド
A) (R)-メチル2-メチルピロリジン-2-カルボキシラート塩酸塩
(R)-2-メチルピロリジン-2-カルボン酸 (400 mg) およびメタノール (10 mL) の混合物にチオニルクロリド (0.68 mL) を氷冷下で滴下し、室温で終夜撹拌した。溶媒を減圧下留去した。残渣を酢酸エチルに懸濁させ、得られた固体を濾取して標題化合物 (400 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.86 (3H, s), 1.93-2.25 (3H, m), 2.33-2.53 (1H, m), 3.48-3.69 (2H, m), 3.86 (3H, s), 9.47 (1H, brs), 10.48 (1H, brs).
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (200 mg)、(R)-メチル 2-メチルピロリジン-2-カルボキシラート塩酸塩 (150 mg) およびDMF (3.0 mL) の混合物にHATU (400 mg) およびDIPEA (0.61 mL) を加え、室温で終夜撹拌した。混合物を水で希釈し酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製して標題化合物 (190 mg) を得た。
MS (API+): [M+H]+412.3.
(R)-メチル 2-メチル-1-(1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボニル)ピロリジン-2-カルボキシラート(160 mg)、THF (1.0 mL) およびメタノール(0.30 mL)の混合物に2M 水酸化ナトリウム水溶液(0.39 mL)を加え、室温で3時間撹拌し、50 ℃で終夜撹拌した。混合物を1M 塩酸で酸性 (pH=4)にした後、飽和食塩水で希釈し、酢酸エチル/THFで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去して標題化合物 (160 mg) を得た。
MS (API+): [M+H]+398.2.
(R)-2-メチル-1-(1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボニル)ピロリジン-2-カルボン酸 (160 mg)、DIPEA (0.11 mL) およびDMF (2.0 mL) の混合物にHATU (230 mg) を加え、室温で30分間撹拌した。混合物に0.4M アンモニア/THF溶液(1.5 mL)を加え、室温で終夜撹拌した。混合物を水、飽和重曹水および飽和食塩水で希釈し、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、メタノール/酢酸エチル) で精製して標題化合物 (110 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.68 (3H, s), 1.70-2.03 (7H, m), 2.17 (3H, s), 2.43-2.79 (4H, m), 3.09-3.21 (2H, m), 3.55-3.77 (2H, m), 5.25 (1H, brs), 6.91 (1H, s), 7.54 (1H, s), 7.61 (1H, d, J = 5.3 Hz), 8.31-8.38 (2H, m), 8.40 (1H, s).
2-メチル-1-((1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)-D-プロリンアミド
A) (R)-メチル2-メチル-1-(1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-カルボニル)ピロリジン-2-カルボキシラート
1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (200 mg)、(R)-メチル 2-メチルピロリジン-2-カルボキシラート塩酸塩 (130 mg) およびDMF (3.0 mL) の混合物にHATU (380 mg) およびDIPEA (0.57 mL) を加え、室温で終夜撹拌した。混合物を水で希釈し酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製して標題化合物 (250 mg) を得た。
MS (API+): [M+H]+430.1.
(R)-メチル 2-メチル-1-(1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-カルボニル)ピロリジン-2-カルボキシラート(250 mg)、THF (1.5 mL) およびメタノール(0.50 mL) の混合物に2M 水酸化ナトリウム水溶液(1.1 mL) を加え、2時間加熱還流した。混合物に1M 塩酸を加え酸性 (pH=4~5) にした後、飽和食塩水で希釈し、酢酸エチル/THFで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去して標題化合物 (230 mg) を得た。
MS (API+): [M+H]+416.2.
(R)-2-メチル-1-(1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-カルボニル)ピロリジン-2-カルボン酸 (220 mg)、DIPEA (0.14 mL) およびDMF (2.0 mL) の混合物にHATU (300 mg) を加え、窒素雰囲気下、室温で1時間撹拌した。混合物に0.4 M アンモニア/THF溶液(2.0 mL)を加え、室温で終夜撹拌した。混合物を飽和食塩水で希釈し、酢酸エチル/THFで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー(NH、メタノール/酢酸エチル) で精製して標題化合物 (160 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.71 (3H, s), 1.73-2.23 (7H, m), 2.49-2.68 (2H, m), 2.84 (3H, s), 2.89-3.01 (2H, m), 3.11-3.22 (2H, m), 3.60-3.81 (2H, m), 5.29 (1H, brs), 6.83 (1H, brs), 8.20 (1H, d, J = 5.3 Hz), 8.52 (1H, d, J = 5.3 Hz), 8.65 (1H, s).
(2R)-2-メチル-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
2-メチル-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)-D-プロリンアミド(100 mg) およびピリジン (2.0 mL) の混合物にトリフルオロ酢酸無水物 (0.039 mL) を氷冷下で加え、室温で30分間撹拌した。混合物にさらにトリフルオロ酢酸無水物 (0.039 mL) を氷冷下で加え、室温で30分間撹拌した。混合物にトリフルオロ酢酸無水物 (0.078 mL) を加え、室温で30分間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製して標題化合物 (76 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.76 (3H, s), 1.80-2.14 (7H, m), 2.18 (3H, s), 2.36-2.60 (2H, m), 2.71 (2H, t, J = 11.7 Hz), 3.07-3.24 (2H, m), 3.53-3.76 (2H, m), 7.54 (1H, s), 7.61 (1H, d, J = 5.3 Hz), 8.31-8.36 (2H, m), 8.40 (1H, s).
(2R)-2-メチル-1-((1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
2-メチル-1-((1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)-D-プロリンアミド(160 mg) およびピリジン (2.0 mL) の混合物にトリフルオロ酢酸無水物 (0.12 mL) を氷冷下で加え、窒素雰囲気下、氷冷下で15分間撹拌した。混合物に氷冷下で飽和重曹水を加え、飽和食塩水で希釈し、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから再結晶して標題化合物 (87 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.78 (3H, s), 1.82-1.97 (2H, m), 2.03-2.28 (5H, m), 2.44-2.61 (2H, m), 2.86 (3H, s), 2.93 (2H, tt, J = 11.9, 2.5 Hz), 3.11-3.22 (2H, m, J = 5.9, 3.6 Hz), 3.59-3.79 (2H, m), 8.20 (1H, d, J = 4.5 Hz), 8.53 (1H, d, J = 4.9 Hz), 8.64 (1H, s).
(2R)-1-((1-(4-(5-メチル-1,3-チアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
A)3-フルオロ-N-(2-ヒドロキシプロピル)イソニコチンアミド
3-フルオロイソニコチン酸 (4.5 g) と塩化チオニル (20 mL) の混合物を窒素雰囲気下、4時間加熱還流した。混合物を減圧下留去し、残渣に無水THF (20 mL) を加え、混合物に1-アミノプロパン-2-オール (2.9 g)、DIPEA (12 mL) およびTHF (20 mL) の混合物を0℃で滴下し、室温で終夜撹拌した。混合物を減圧下留去し、残渣にTHFを加え、不溶物を濾去し、濾液を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (メタノール/酢酸エチル) で精製し、標題化合物 (4.9 g) を得た。
MS (API+): [M+H]+199.1.
3-フルオロ-N-(2-ヒドロキシプロピル)イソニコチンアミド(4.4 g)、トリエチルアミン(6.2 mL) およびDMSO (70 mL) の混合物に三酸化イオウ-ピリジン錯体 (7.0 g) を室温で加え、終夜撹拌した。混合物を減圧下留去し、残渣に水と酢酸エチルを加え、1M 水酸化ナトリウム水溶液で混合物を塩基性にした後、酢酸エチルおよびTHFで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製し、標題化合物 (1.9 g) を得た。
MS (API+): [M+H]+197.2.
3-フルオロ-N-(2-オキソプロピル)イソニコチンアミド(1.9 g) およびトルエン (30 mL) の混合物に2,4-ビス(4-メトキシフェニル)-1,3-ジチア-2,4-ジホスフェタン2,4-ジスルフィド (4.7 g) を加え、110 ℃ で1時間撹拌した。混合物を減圧下留去し、残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、標題化合物を得た(1.0 g)。
MS (API+): [M+H]+195.1.
2-(3-フルオロピリジン-4-イル)-5-メチルチアゾール(500 mg)、エチル ピペリジン-4-カルボキシラート(610 mg)、炭酸カリウム(530 mg) および NMP(2.0 mL)の混合物を150℃で終夜撹拌した。混合物を室温まで冷却し、エチル ピペリジン-4-カルボキシラート(2.0 mL)加え、180℃で2時間攪拌後、室温で終夜攪拌した。混合物を室温まで冷却し、水を加え、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製し、標題化合物 (780 mg) を得た。
MS (API+): [M+H]+332.2.
エチル 1-(4-(5-メチルチアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-カルボキシラート(770 mg) をTHF(5.0 mL) および メタノール (2.0 mL) に溶解させ、混合物に2M 水酸化ナトリウム水溶液(2.3 mL) を加え、室温で2時間撹拌した。混合物を1M 塩酸(4.7 mL)で中和し、沈殿した固体を濾取し、標題化合物 (480 mg) を得た。
MS (API+): [M+H]+304.1.
1-(4-(5-メチルチアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸およびDMF (1.0 mL) の混合物にHATU (86 mg)、トリエチルアミン (0.053 mL)および (R)-ピロリジン-2-カルボニトリル塩酸塩(28 mg) を室温で加え、2時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから結晶化して標題化合物 (39 mg) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.75-2.30 (8H, m), 2.53 (3H, d, J = 0.8 Hz), 2.61-2.75 (1H, m), 2.91-3.11 (4H, m), 3.52-3.63 (1H, m), 3.68-3.78 (1H, m), 4.75 (1H, dd, J = 7.2, 3.8 Hz), 7.72 (1H, d, J = 1.1 Hz), 8.03 (1H, d, J = 5.3 Hz), 8.44 (1H, d, J = 5.3 Hz), 8.68 (1H, s).
(2R)-4,4-ジフルオロ-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
A) (2R,4R)-1-(tert-ブトキシカルボニル)-4-ヒドロキシピロリジン-2-カルボン酸
(2R,4R)-4-ヒドロキシピロリジン-2-カルボン酸 (5.3 g)、二炭酸ジ-tert-ブチル (19 mL)、トリエチルアミン (10 mL) およびメタノール (90 mL) の混合物を2時間加熱還流した。室温に冷却後、溶媒を減圧留去した。氷冷下、残渣にリン酸二水素ナトリウム (400 mg) および希塩酸を加えてpH2に調節した。混合物を氷冷下30分間撹拌し、酢酸エチル/2-プロパノール (5:1) で抽出した。有機層を分離し、飽和食塩水で洗浄後、硫酸マグネシウムで乾燥し、溶媒を減圧下留去して標題化合物 (9.3 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.31-1.41 (9H, m), 1.75-1.86 (1H, m), 2.23-2.39 (1H, m), 3.03-3.15 (1H, m), 3.43-3.54 (1H, m), 4.03-4.13 (1H, m), 4.15-4.25 (1H, m).
(2R,4R)-1-(tert-ブトキシカルボニル)-4-ヒドロキシピロリジン-2-カルボン酸 (500 mg) とアセトニトリル (6.0 mL) の混合物に氷冷下、WSC塩酸塩(500 mg)およびHOBt一水和物 (400 mg) を加えた。混合物を室温で1.5時間撹拌後、0℃に冷却し、28%アンモニア水(0.60 mL) を加えた。同温度で15分間撹拌後、室温で30分間撹拌した。混合物に硫酸ナトリウムを加え、不溶物をシリカゲル (NH、酢酸エチル) で濾去し、濾液を減圧下濃縮した。残渣をシリカゲルカラムクロマトグラフィー (メタノール/酢酸エチル)で精製し、標題化合物 (320 mg) を得た。
1H NMR (400 MHz, DMSO-d6) δ 1.30-1.43 (9H, m), 1.65-1.75 (1H, m), 2.21-2.35 (1H, m), 3.13-3.22 (1H, m), 3.41-3.50 (1H, m), 3.97-4.17 (2H, m), 5.25 (1H, d, J = 6.8 Hz), 7.04-7.16 (1H, m), 7.39-7.49 (1H, m).
(2R,4R)-tert-ブチル 2-カルバモイル-4-ヒドロキシピロリジン-1-カルボキシラート (4.0 g) および酢酸エチル (40 mL) /水 (40 mL) の混合物に氷冷下、酸化ルテニウム(IV)一水和物(0.13 g)および過ヨウ素酸ナトリウム (11 g) を加えた。混合物を室温で4時間撹拌した後、酢酸エチル/2-プロパノール (5:1) で抽出した。有機層を水および飽和食塩水で洗浄後、硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製し、標題化合物 (2.4 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.36-1.44 (9H, m), 2.24-2.37 (1H, m), 2.93-3.12 (1H, m), 3.63-3.85 (2H, m), 4.44-4.58 (1H, m), 7.04-7.21 (1H, m), 7.58 (1H, brs).
(R)-tert-ブチル 2-カルバモイル-4-オキソピロリジン-1-カルボキシラート (2.4 g) およびジクロロメタン (50 mL) の混合物にビス(2-メトキシエチル)アミノ硫黄 三フッ化物 (5.8 mL) を-5℃で加えた。混合物を同温度で15分間撹拌後、室温で3.5時間撹拌した。混合物を重曹および氷中に注ぎ、40分間撹拌し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン)で精製し、標題化合物 (1.4 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.30-1.46 (9H, m), 2.20-2.42 (1H, m), 2.65-2.88 (1H, m), 3.61-3.83 (2H, m), 4.19-4.32 (1H, m), 7.05-7.19 (1H, m), 7.40-7.53 (1H, m).
(R)-tert-ブチル 2-カルバモイル-4,4-ジフルオロピロリジン-1-カルボキシラート (1.1 g) およびピリジン (10 mL) の混合物に、トリフルオロ酢酸無水物 (0.79 mL) を-5℃で加えた。混合物を同温度で15分間撹拌後、室温で1時間撹拌した。混合物を酢酸エチル/水で希釈し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン)で精製し、標題化合物 (0.82 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.45 (9H, s), 2.67-3.01 (2H, m), 3.63-3.87 (2H, m), 4.96 (1H, dd, J = 9.1, 2.7 Hz).
(R)-tert-ブチル 2-シアノ-4,4-ジフルオロピロリジン-1-カルボキシラート (0.82 g)、p-トルエンスルホン酸一水和物 (1.3 g) およびアセトニトリル (15 mL) の混合物を室温で18時間撹拌した。溶媒を減圧下留去した後、残渣を酢酸エチルに溶解させ、再び減圧下濃縮した。生じた固体にジエチルエーテルおよび酢酸エチルを順次加え、沈殿物を濾過後、冷たい酢酸エチルで洗浄し、標題化合物 (0.67 g) を得た。
1H NMR (300 MHz, CD3OD) δ 2.37 (3H, s), 2.81-3.13 (2H, m), 3.71-3.95 (2H, m), 5.02-5.11 (1H, m), 7.23 (2H, d, J = 8.0 Hz), 7.68-7.74 (2H, m).
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (60 mg)、(R)-4,4-ジフルオロピロリジン-2-カルボニトリル 4-メチルベンゼンスルホナート (96 mg)、HATU (110 mg)、DIPEA (0.11 mL) およびDMF (2.0 mL) の混合物を室温で18時間撹拌した。混合物を酢酸エチル/水で希釈し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン)で精製し、標題化合物 (70 mg) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.60-1.84 (4H, m), 2.12 (3H, s), 2.54-3.04 (7H, m), 4.04-4.30 (2H, m), 5.04 (1H, dd, J = 9.3, 3.2 Hz), 7.53 (1H, d, J = 5.3 Hz), 7.63 (1H, s), 8.31 (1H, d, J = 4.9 Hz), 8.39-8.44 (2H, m).
(2R)-1-((4-フルオロ-1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
A) エチル 4-フルオロ-1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-カルボキシラート
2-(3-フルオロピリジン-4-イル)-5-メチル-1,3,4-チアジアゾール (300 mg)、エチル 4-フルオロピペリジン-4-カルボキシラート (650 mg)、炭酸カリウム (320 mg) およびNMP (1.0 mL) の混合物をマイクロウェーブ照射下、180 ℃で1時間撹拌した。混合物を水で希釈し、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製して標題化合物 (130 mg) を得た。
MS (API+): [M+H]+351.1.
エチル 4-フルオロ-1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-カルボキシラート(120 mg)、THF (1.0 mL) およびメタノール(0.30 mL) の混合物に2M 水酸化ナトリウム水溶液(0.35 mL) を室温で加え、室温で4時間撹拌した。混合物を1M 塩酸で酸性 (pH=4) にし、酢酸エチル/THF/2-プロパノールで抽出し、溶媒を減圧下留去した。残渣をトルエンに懸濁させ、溶媒を減圧下留去した。得られた固体を酢酸エチルで洗浄した。得られた固体、(R)-ピロリジン-2-カルボニトリル塩酸塩 (56 mg) およびDMF (1.0 mL) の混合物にHATU (160 mg) およびDIPEA (0.19 mL) を加え、室温で終夜撹拌した。混合物を飽和食塩水で希釈し酢酸エチルで抽出した。有機層を無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー(NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから再結晶させて標題化合物 (20 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.96-2.76 (8H, m), 2.80-2.91 (3H, m), 2.96-3.11 (2H, m), 3.17-3.39 (2H, m), 3.47-4.03 (2H, m), 4.70-5.21 (1H, m), 8.21 (1H, d, J = 5.3 Hz), 8.55 (1H, d, J = 5.3 Hz), 8.70 (1H, s).
(2R)-4,4-ジフルオロ-1-((1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (60 mg)、(R)-4,4-ジフルオロピロリジン-2-カルボニトリル 4-メチルベンゼンスルホナート (54 mg) およびDMF (1 mL)の混合物にHATU (100 mg) およびDIPEA (0.12 mL) を加え、室温で終夜撹拌した。混合物を飽和食塩水で希釈し酢酸エチル/THFで抽出した。有機層を無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから再結晶して標題化合物 (41 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.80-1.99 (2H, m), 2.08-2.28 (2H, m), 2.37-2.56 (1H, m), 2.72-2.84 (2H, m), 2.86 (3H, s), 2.95 (2H, td, J = 11.9, 2.7 Hz), 3.12-3.25 (2H, m), 3.92-4.11 (2H, m), 5.00 (1H, t, J = 6.6 Hz), 8.21 (1H, d, J = 4.9 Hz), 8.54 (1H, d, J = 5.3 Hz), 8.64 (1H, s).
((2R)-2-(メトキシメチル)ピロリジン-1-イル)(1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノン
1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (80 mg)、(R)-2-(メトキシメチル)ピロリジン (36 mg) およびDMF (1.0 mL) の混合物にHATU (150 mg) およびDIPEA (0.14 mL) を加え、室温で3時間撹拌した。混合物を水で希釈し酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから再結晶して標題化合物 (76 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.73-2.38 (8H, m), 2.46-2.81 (1H, m), 2.84 (3H, s), 2.94 (2H, t, J = 12.1 Hz), 3.08-3.22 (2H, m), 3.27-3.67 (7H, m), 4.08-4.36 (1H, m), 8.20 (1H, d, J = 5.3 Hz), 8.52 (1H, d, J = 5.3 Hz), 8.64 (1H, s).
(2R)-1-((1-(2,4'-ビピリジン-3'-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
A) 1,3-ジメチル-2,3-ジヒドロ-2-オキソピリジニウム スルフェイト
1,3-ジメチル尿素 (40 g)、1,1,3,3-テトラメトキシプロパン (55 mL) およびメタノール (400 mL) の混合物に濃硫酸 (27 mL) を室温でゆっくりと滴下し、50℃で30分間撹拌した。混合物を5℃に冷却し、沈殿物を濾過後、メタノールで洗浄し、標題化合物 (31 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 3.71 (6H, s), 7.05 (1H, t, J = 6.1 Hz), 9.09 (2H, d, J = 6.1 Hz).
1-(3-ブロモピリジン-4-イル)エタノン (1.0 g)、1,3-ジメチル-2,3-ジヒドロ-2-オキソピリジニウム スルフェイト (0.91 g) およびアセトニトリル (4.0 mL) の混合物に氷冷下、トリエチルアミン (1.1 mL) を加え、45℃に昇温した。同温度で1.5時間撹拌後、減圧下濃縮した。残渣に酢酸 (4,0 mL) および酢酸アンモニウム (2.1 g) を加え、混合物を120℃で4時間撹拌した。混合物を室温に冷却後、0℃に冷やした8M 水酸化ナトリウム水溶液 (35 mL) に注ぎ、酢酸エチルで抽出した。有機層を分離し、水および飽和食塩水で洗浄後、硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン)で精製し、標題化合物 (0.55 g) を得た。1H NMR (300 MHz, CDCl3) δ 7.38 (1H, ddd, J = 7.6, 4.9, 1.1 Hz), 7.52 (1H, dd, J = 4.9, 0.8 Hz), 7.66-7.73 (1H, m), 7.78-7.87 (1H, m), 8.61 (1H, d, J = 4.9 Hz), 8.73-8.79 (1H, m), 8.85 (1H, s).
3'-ブロモ-2,4'-ビピリジン (1.1 g)、1,4-ジアザビシクロ[2.2.2]オクタン (0.25 g)、イソニペコチン酸エチル (7.0 mL) およびDIPEA (5.0 mL) の混合物をマイクロウェーブ照射下、200℃で18時間撹拌した。混合物を酢酸エチル/水で希釈し、酢酸エチルで抽出した。有機層を分離し、水および飽和食塩水で洗浄後、硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン)で精製し、標題化合物 (0.44 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.25 (3H, t, J = 7.2 Hz), 1.58-1.75 (1H, m), 1.82-1.93 (2H, m), 2.28-2.40 (1H, m), 2.67-2.78 (2H, m), 3.12-3.22 (2H, m), 4.14 (2H, q, J = 7.2 Hz), 7.25-7.31 (2H, m), 7.50 (1H, d, J = 4.5 Hz), 7.72-7.80 (1H, m), 8.08 (1H, d, J = 8.3 Hz), 8.36-8.40 (2H, m), 8.71-8.76 (1H, m).
エチル 1-([2,4'-ビピリジン]-3'-イル)ピペリジン-4-カルボキシラート(0.44 g) およびTHF (4.0 mL) /エタノール(1.0 mL) の混合物に、2M 水酸化ナトリウム水溶液(1.8 mL) を加え、60℃で1.5時間撹拌した。混合物を氷冷下、2M 塩酸 (1.8 mL) で中和した。沈殿物を濾過後、水で洗浄して標題化合物 (0.40 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.43-1.60 (2H, m), 1.71-1.82 (2H, m), 2.21-2.35 (1H, m), 2.64-2.76 (2H, m), 2.99-3.10 (2H, m), 7.38-7.44 (1H, m), 7.47 (1H, d, J = 4.9 Hz), 7.87-7.95 (1H, m), 8.08-8.14 (1H, m), 8.31 (1H, d, J = 4.9 Hz), 8.38 (1H, s), 8.70-8.74 (1H, m), 12.21 (1H, s).
1-([2,4'-ビピリジン]-3'-イル)ピペリジン-4-カルボン酸 (57 mg)、(R)-ピロリジン-2-カルボニトリル塩酸塩 (32 mg)、HATU (92 mg)、DIPEA (0.11 mL) およびDMF (2.0 mL) の混合物を室温で16時間撹拌した。混合物を酢酸エチル/水で希釈し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサンおよびメタノール/酢酸エチル)で精製し、標題化合物(52 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.67-1.92 (4H, m), 2.09-2.45 (5H, m), 2.66-2.79 (2H, m), 3.18-3.31 (2H, m), 3.45-3.56 (1H, m), 3.63-3.73 (1H, m), 4.61-4.78 (1H, m), 7.27-7.31 (1H, m), 7.52 (1H, d, J = 4.9 Hz), 7.75-7.83 (1H, m), 8.10 (1H, d, J = 8.0 Hz), 8.37-8.41 (2H, m), 8.71-8.75 (1H, m).
(2R,4S)-4-メトキシ-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリル
A)(2R,4S)-1-(tert-ブトキシカルボニル)-4-ヒドロキシピロリジン-2-カルボン酸
(2R,4S)-4-ヒドロキシピロリジン-2-カルボン酸 (7.1 g)、二炭酸ジ-tert-ブチル (25 mL)、 トリエチルアミン (14 mL) および メタノール (130 mL) の混合物を2時間加熱還流した。混合物を室温まで冷却し、溶媒を減圧下留去した。残渣にリン酸二水素一ナトリウム (590 mg) を0℃で加え、希塩酸で酸性 (pH=2) にした。混合物を0℃で30分間撹拌した後、酢酸エチル/2-プロパノール (5:1) で抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去して、標題化合物 (11 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.40-1.52 (9H, m), 2.07-2.43 (2H, m), 3.43-3.68 (2H, m), 4.34-4.57 (2H, m), 5.00 (2H, brs).
(2R,4S)-1-(tert-ブトキシカルボニル)-4-ヒドロキシピロリジン-2-カルボン酸 (11 g) およびアセトニトリル (130 mL) の混合物にWSC塩酸塩 (11 g) とHOBt一水和物(8.7 g) を0℃で加え、室温で2.5時間撹拌した。混合物を0℃まで冷却し、28% アンモニア水(25 mL) を加え、0℃で15 分間撹拌した後、室温で終夜撹拌した。不溶物を濾去し、濾液を減圧下留去した。残渣を酢酸エチル-メタノール (4:1) に溶解し、不溶物を濾去し、濾液を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (メタノール/酢酸エチル) で精製し、標題化合物(7.0 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.31-1.41 (9H, m), 1.73-1.87 (1H, m), 1.93-2.09 (1H, m), 3.20-3.28 (1H, m), 3.33-3.44 (1H, m), 4.02-4.13 (1H, m), 4.21 (1H, d, J = 1.9 Hz), 4.96 (1H, d, J = 3.4 Hz), 6.79-6.93 (1H, m), 7.26-7.39 (1H, m).
(2R,4S)-tert-ブチル 2-カルバモイル-4-ヒドロキシピロリジン-1-カルボキシラート (3.0 g) およびピリジン (30 mL) の混合物に無水トリフルオロ酢酸 (4.6 mL) を0℃で加え、室温で3時間撹拌した。混合物に酢酸エチルおよび飽和重曹水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製し、標題化合物 (2.7 g) を得た。
1H NMR (300 MHz, CD3OD) δ 1.46-1.54 (9H, m), 2.29-2.40 (2H, m), 3.37-3.56 (2H, m), 4.37-4.45 (1H, m), 4.61 (1H, t, J =8.0 Hz).
(2R,4S)-tert-ブチル 2-シアノ-4-ヒドロキシピロリジン-1-カルボキシラート (550 mg)、ヨウ化メチル (3.2 mL)、酸化銀 (1.0 g) およびアセトニトリル (6.0 mL) の混合物を窒素雰囲気下、5時間加熱還流した後、室温で9時間撹拌した。混合物をNH-シリカゲルおよびセライトパッドで濾過し、濾液を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製し、標題化合物 (470 mg) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.43 (9H, s), 2.20-2.35 (1H, m), 2.37-2.47 (1H, m), 3.31 (3H, s), 3.39-3.45 (2H, m), 3.98 (1H, brs), 4.55 (1H, t, J = 7.8 Hz).
(2R,4S)-tert-ブチル 2-シアノ-4-メトキシピロリジン-1-カルボキシラート (85 mg) およびアセトニトリル (1.0 mL) の混合物にp-トルエンスルホン酸一水和物(140 mg) を室温で加え、2時間撹拌した後に、50℃で 2時間加熱した。混合物を減圧留去し、残渣をMP-Carbonate (マクロ多孔質ポリスチレン陰イオン交換レジン) で精製し、標題化合物 (45 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 2.09-2.36 (2H, m), 2.99-3.09 (1H, m), 3.12-3.21 (1H, m), 3.29 (3H, s), 3.97-4.04 (1H, m), 4.10-4.21 (1H, m), 5.25 (1H, brs).
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (52 mg) およびDMF (1.0 mL) の混合物にHATU (90 mg)、トリエチルアミン (0.051 mL) および(2R,4S)-4-メトキシピロリジン-2-カルボニトリル (45 mg) を室温で加え、1.5時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、標題化合物 (32 mg) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.62-1.84 (4H, m), 2.13 (3H, s), 2.22-2.32 (1H, m), 2.37-2.47 (1H, m), 2.67-2.83 (2H, m), 2.90-3.05 (2H, m), 3.25 (3H, s), 3.34-3.40 (1H, m), 3.66-3.76 (2H, m), 4.05-4.11 (1H, m), 4.63 (1H, t, J = 8.0 Hz), 7.53 (1H, d, J = 5.3 Hz), 7.63 (1H, s), 8.31 (1H, d, J = 5.3 Hz), 8.41 (1H, s), 8.43 (1H, s).
tert-ブチル (1S,4S)-5-(4-フェニルピリジン-3-イル)-2,5-ジアザビシクロ[2.2.1]ヘプタン-2-カルボキシラート
A) (1S,4S)-tert-ブチル 5-(4-クロロピリジン-3-イル)-2,5-ジアザビシクロ[2.2.1]ヘプタン-2-カルボキシラート
3-ブロモ-4-クロロピリジン (580 mg)、(1S,4S)-tert-ブチル 2,5-ジアザビシクロ[2.2.1]ヘプタン-2-カルボキシラート (500 mg)、Pd2(dba)3 (69 mg)、Xantphos (130 mg)、ナトリウムtert-ブトキシド (364 mg) およびトルエン (10 mL) の混合物をアルゴン雰囲気下110 ℃で3時間撹拌した。混合物をセライトで濾過し、濾液を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン)およびシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、標題化合物 (590 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.34-1.55 (9H, m), 1.86-2.03 (2H, m), 3.24-3.51 (2H, m), 3.55-3.75 (1H, m), 3.92 (1H, dd, J = 9.4, 2.3 Hz), 4.44-4.66 (2H, m), 7.20 (1H, d, J = 4.5 Hz), 7.95 (1H, d, J = 5.3 Hz), 8.08 (1H, s).
(1S,4S)-tert-ブチル 5-(4-クロロピリジン-3-イル)-2,5-ジアザビシクロ[2.2.1]ヘプタン-2-カルボキシラート (590 mg)、フェニルボロン酸 (260 mg)、テトラキス(トリフェニルホスフィン)パラジウム(0) (110 mg) および炭酸カリウム (790 mg) のDME/水(10/2.0 mL) 混合物をマイクロウェーブ照射下、140 ℃で1時間撹拌した。混合物を水で希釈し、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、NHシリカゲルで濾過 (酢酸エチル) した後、溶媒を減圧下留去した。得られた固体を酢酸エチル/ヘキサンから再結晶して標題化合物 (440 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.39 (9H, s), 1.72-1.89 (2H, m), 2.55 (1H, d, J = 9.4 Hz), 2.87-3.04 (1H, m), 3.25-3.35 (1H, m), 3.51-3.61 (1H, m), 4.17-4.40 (2H, m), 6.98-7.10 (1H, m), 7.29-7.46 (5H, m), 8.03-8.20 (2H, m).
2-シクロプロピル-1-((1S,4S)-5-(4-フェニルピリジン-3-イル)-2,5-ジアザビシクロ[2.2.1]ヘプタ-2-イル)エタノン
A) (1S,4S)-2-(4-フェニルピリジン-3-イル)-2,5-ジアザビシクロ[2.2.1]ヘプタン二塩酸塩
tert-ブチル (1S,4S)-5-(4-フェニルピリジン-3-イル)-2,5-ジアザビシクロ[2.2.1]ヘプタン-2-カルボキシラート (440 mg) とメタノール (5.0 mL) の混合物に4M 塩化水素/酢酸エチル溶液 (10 mL) を加え、室温で2時間撹拌した。混合物を減圧下留去し、残渣にメタノールおよびトルエンを加えた後、さらに減圧下溶媒を留去し、標題化合物 (410 mg) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.85-2.10 (2H, m), 2.81-3.00 (2H, m), 3.08-3.42 (2H, m), 4.22 (1H, brs), 4.63 (1H, s), 7.41-7.61 (5H, m), 7.72 (1H, d, J = 5.7 Hz), 8.34 (1H, d, J = 5.7 Hz), 8.54 (1H, s), 9.14 (1H, brs), 9.82 (1H, brs).
(1S,4S)-2-(4-フェニルピリジン-3-イル)-2,5-ジアザビシクロ[2.2.1]ヘプタン二塩酸塩 (140 mg)、シクロプロピル酢酸 (0.047 mL)、HATU (190 mg)、トリエチルアミン (0.29 mL) およびDMF (3.0 mL) の混合物を室温で3時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから再結晶して標題化合物 (65 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 0.02-0.15 (2H, m), 0.41-0.56 (2H, m), 0.89-1.05 (1H, m), 1.74-2.26 (4H, m), 2.47-2.59 (1H, m), 2.97 (0.6H, dd, J = 9.8, 2.3 Hz), 3.05 (0.4H, dd, J = 9.4, 1.9 Hz), 3.37-3.47 (1H, m), 3.66 (0.6H, d, J = 9.4 Hz), 3.74 (0.4H, dd, J = 11.5, 1.3 Hz), 4.22 (0.4H, s), 4.36 (1H, brs), 4.75 (0.6H, s), 7.00-7.09 (1H, m), 7.30-7.46 (5H, m), 8.06-8.21 (2H, m).
シクロプロピル(4-(5-フルオロ-4-フェニルピリジン-3-イル)ピペラジン-1-イル)メタノン
A) 3-ブロモ-5-フルオロ-4-フェニルピリジン
3-ブロモ-5-フルオロピリジン (2.5 g)、ヨウ化銅 (0.28 g)、塩化リチウム (0.12 g) およびTHF (23 mL) の混合物に-20℃にて、クロロギ酸フェニル (2.0 mL) を滴下し、同温度で30分間撹拌した。混合物に2M フェニルマグネシウム 臭化物 THF溶液(7.9 mL) を滴下し、同温で1.5時間撹拌した。混合物を更に室温で30分間撹拌後、飽和塩化アンモニウム水溶液を加え、酢酸エチルで抽出した。有機層を分離し、水および飽和食塩水で洗浄後、硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。得られた残渣、2,3,5,6-テトラクロロシクロヘキサ-2,5-ジエン-1,4-ジオン (3.6 g) およびトルエン (15 mL) の混合物を6時間加熱還流した。室温に冷却後、2M 水酸化ナトリウム水溶液 (15 mL) で希釈し、室温で10分間撹拌し、セライトで濾過 (酢酸エチル) した。濾液の有機層を分離し、2M 水酸化ナトリウム水溶液および水で洗浄後、硫酸ナトリウムで乾燥した。シリカゲル (NH、酢酸エチル) で濾過し、濾液を減圧下濃縮した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン)で精製し、標題化合物 (1.6 g) を得た。
1H NMR (300 MHz, CDCl3) δ 7.33-7.41 (2H, m), 7.46-7.56 (3H, m), 8.48 (1H, s), 8.67 (1H, s).
3-ブロモ-5-フルオロ-4-フェニルピリジン(600 mg)、tert-ブチル 1-ピペラジンカルボキシラート (490 mg)、Pd2(dba)3(65 mg)、Xantphos (83 mg)、ナトリウムtert-ブトキシド (270 mg) およびトルエン (10 mL) の混合物をマイクロウェーブ照射下、110℃で2時間撹拌した。混合物をシリカゲル (NH、酢酸エチル) で濾過し、濾液を減圧下濃縮した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン)で精製し、標題化合物 (480 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.43 (9H, s), 2.77-2.89 (4H, m), 3.22-3.33 (4H, m), 7.37-7.57 (5H, m), 8.14 (1H, s), 8.27 (1H, s).
tert-ブチル 4-(5-フルオロ-4-フェニルピリジン-3-イル)ピペラジン-1-カルボキシラート (480 mg) および2M 塩化水素/メタノール溶液 (16 mL) の混合物を室温で5時間撹拌した。溶媒を減圧下留去し、標題化合物 (440 mg) を得た。
1H NMR (300 MHz, DMSO-d6) δ 2.84-2.97 (4H, m), 3.02-3.13 (4H, m), 7.45-7.64 (5H, m), 8.33 (1H, s), 8.47 (1H, d, J = 0.8 Hz), 9.33 (2H, brs).
1-(5-フルオロ-4-フェニルピリジン-3-イル)ピペラジン二塩酸塩 (100 mg) およびTHF (2.0 mL) の混合物に氷冷下、DIPEA (0.21 mL) およびシクロプロパンカルボン酸クロリド (0.036 mL) を順次加え、室温で2時間撹拌した。混合物を酢酸エチル/飽和重曹水で希釈し、酢酸エチルで抽出した。有機層を分離し、水および飽和食塩水で洗浄後、硫酸ナトリウムで乾燥し、シリカゲル (NH、酢酸エチル) で濾過し、濾液を減圧下濃縮した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサンおよびメタノール/酢酸エチル)で精製し、標題化合物 (92 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 0.69-0.79 (2H, m), 0.90-1.01 (2H, m), 1.58-1.71 (1H, m), 2.80-2.97 (4H, m), 3.44-3.59 (4H, m), 7.37-7.58 (5H, m), 8.15 (1H, s), 8.28 (1H, s).
ベンジル 4-(4-フェニルピリミジン-5-イル)ピペラジン-1-カルボキシラート
A) ベンジル 4-(2-オキソ-2-フェニルエチル)ピペラジン-1-カルボキシラート
ベンジル ピペラジン-1-カルボキシラート (3.1 g)、炭酸カリウム (2.7 g) およびアセトニトリル (30 mL) の混合物に2-クロロ-1-フェニルエタノン(2.0 g) およびアセトニトリル (20 mL)の混合物を室温で滴下し、室温で終夜撹拌した。溶媒を減圧下留去した後、混合物を水で希釈し、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製して標題化合物 (4.2 g) を得た。
MS (API+): [M+H]+339.1.
ベンジル 4-(2-オキソ-2-フェニルエチル)ピペラジン-1-カルボキシラート (4.2 g) およびN,N-ジメチルホルムアミドジメチルアセタール (40 mL) の混合物を100 ℃で終夜撹拌した。溶媒を減圧下留去した。その残渣、n-ブタノール (50 mL) およびDIPEA (50 mL)の混合物にホルムアミジン アセタート (7.7 g)を加え、110 ℃で終夜撹拌した。溶媒を減圧下留去した後、残渣を水で希釈し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) およびシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン)で精製して標題化合物 (3.1 g) を得た。
1H NMR (300 MHz, CDCl3) δ 2.92 (4H, brs), 3.46-3.59 (4H, m), 5.12 (2H, s), 7.29-7.39 (5H, m), 7.42-7.52 (3H, m), 7.99-8.07 (2H, m), 8.39 (1H, s), 8.95 (1H, s).
N-ベンジル-4-(4-フェニルピリミジン-5-イル)ピペラジン-1-カルボキサミド
A) 4-フェニル-5-(ピペラジン-1-イル)ピリミジン
ベンジル 4-(4-フェニルピリミジン-5-イル)ピペラジン-1-カルボキシラート (3.1 g)、10%パラジウム炭素(約50%水湿潤品、0.30 g) およびエタノール (30 mL)の混合物を水素雰囲気下、50 ℃で3時間撹拌した。触媒を濾去した後、溶媒を減圧下留去して標題化合物 (1.9 g)を得た。
MS (API+): [M+H]+241.1.
4-フェニル-5-(ピペラジン-1-イル)ピリミジン (100 mg) およびTHF (2.0 mL) の混合物にベンジル イソシアナート (0.054 mL) を室温で加え、室温で4時間撹拌した。溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン)で精製し、得られた固体を酢酸エチル/ヘキサンから再結晶させて標題化合物 (120 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 2.85-3.00 (4H, m), 3.28-3.47 (4H, m), 4.42 (2H, d, J = 5.3 Hz), 4.69 (1H, t, J = 5.1 Hz), 7.27-7.37 (5H, m), 7.41-7.51 (3H, m), 7.99-8.07 (2H, m), 8.40 (1H, s), 8.95 (1H, s).
メチル 4-メチル-1-(4-フェニルピリミジン-5-イル)ピペリジン-4-カルボキシラート
5-ブロモ-4-フェニルピリミジン (600 mg)、メチル 4-メチルピペリジン-4-カルボキシラート塩酸塩 (520 mg)、Pd2(dba)3(120 mg)、Xantphos (150 mg)、ナトリウムtert-ブトキシド (620 mg) および1,4-ジオキサン (20 mL) の脱気した混合物をマイクロウェーブ照射下、110℃で9時間撹拌した。混合物をシリカゲル (NH、酢酸エチル) で濾過し、濾液を減圧下濃縮した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン)で精製し、標題化合物(130 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.22 (3H, s), 1.41-1.54 (2H, m), 2.06-2.15 (2H, m), 2.68-2.79 (2H, m), 2.98-3.08 (2H, m), 3.69 (3H, s), 7.39-7.51 (3H, m), 8.01-8.07 (2H, m), 8.39 (1H, s), 8.89 (1H, s).
(2R)-1-((4-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペラジン-1-イル)カルボニル)ピロリジン-2-カルボニトリル
A) tert-ブチル4-(2-(4-フルオロフェニル)-2-オキソエチル)ピペラジン-1-カルボキシラート
tert-ブチル ピペラジン-1-カルボキシラート (5.9 g)、炭酸カリウム (6.0 g) およびアセトニトリル (60 mL) の混合物に2-クロロ-1-(4-フルオロフェニル)エタノン (5.0 g) およびアセトニトリル (40 mL) の混合物を室温で滴下し、室温で終夜撹拌した。溶媒を減圧下留去した後、混合物を水で希釈し、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去して標題化合物 (10 g) を得た。
MS (API+): [M+H]+323.2.
tert-ブチル 4-(2-(4-フルオロフェニル)-2-オキソエチル)ピペラジン-1-カルボキシラート(8.2 g) およびN,N-ジメチルホルムアミドジメチルアセタール(50 mL) の混合物を5時間加熱還流した。溶媒を減圧下留去した。その残渣、n-ブタノール (40 mL) およびDIPEA (40 mL)の混合物にホルムアミジン アセタート (9.3 g)を加え、100 ℃で終夜撹拌した。溶媒を減圧下留去した後、残渣を水で希釈し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製して標題化合物 (5.81 g) を得た。
MS (API+): [M+H]+359.2.
tert-ブチル 4-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペラジン-1-カルボキシラート (5.8 g) および酢酸エチル (50 mL) の混合物に4M 塩化水素/酢酸エチル溶液 (50 mL) を室温で加え、室温で終夜撹拌した。混合物を酢酸エチルで希釈し、析出物を濾取して標題化合物 (5.6 g) を得た。
MS (API+): [M+H]+259.1.
4-(4-フルオロフェニル)-5-(ピペラジン-1-イル)ピリミジン二塩酸塩 (200 mg)、DIPEA (0.74 mL) およびアセトニトリル(2.0 mL) の混合物にビス(トリクロロメチル) カルボナート (72 mg) を室温で加えた。室温で10分間撹拌した後、混合物に(R)-ピロリジン-2-カルボニトリル塩酸塩 (160 mg) を加え、室温で終夜撹拌した。混合物を水で希釈し酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサンおよびメタノール/酢酸エチル) で精製して標題化合物(58 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.83-2.01 (1H, m), 2.01-2.39 (3H, m), 2.87-3.05 (4H, m), 3.27-3.52 (6H, m), 4.73-4.85 (1H, m), 7.12-7.22 (2H, m), 8.07-8.16 (2H, m), 8.42 (1H, s), 8.95 (1H, s).
N-(4-フルオロベンジル)-4-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペラジン-1-カルボキサミド
A) tert-ブチル 4-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペラジン-1-カルボキシラート
tert-ブチル ピペラジン-1-カルボキシラート (0.41 g) およびTHF (5.0 mL) の混合物にn-ブチルリチウムのヘキサン溶液(1.6 M, 1.4 mL) を-78 ℃で加え、窒素雰囲気下30分間撹拌した。混合物に3-フルオロ-4-(4-メチル-1H-ピラゾール-1-イル)ピリジン (0.30 g) のTHF (1.0 mL) 溶液を加え、窒素雰囲気下-78 ℃で15分間撹拌した。温度を室温まで上昇させた後、1時間撹拌した。混合物に飽和塩化アンモニウム水溶液を加え、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製し、標題化合物 (0.26 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.46-1.49 (9H, m), 2.17 (3H, s), 2.81-2.88 (4H, m), 3.45-3.56 (4H, m), 7.55 (1H, s), 7.58 (1H, d, J = 5.3 Hz), 8.29 (1H, s), 8.38 (2H, t, J = 2.7 Hz).
tert-ブチル 4-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペラジン-1-カルボキシラート(1.2 g)、酢酸エチル (10 mL) およびメタノール(5.0 mL) の混合物に4M塩化水素/酢酸エチル溶液 (10 mL) を加え、室温で終夜撹拌した。溶媒を減圧下留去した。残渣に水を加え酢酸エチルで洗浄した。水溶液に1M水酸化ナトリウム水溶液を加えて塩基性にし、飽和食塩水を加えた後、酢酸エチルおよびTHFの混合溶媒で抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去して標題化合物 (0.86 g) を得た。
1H NMR (300 MHz, CDCl3) δ2.17 (3H, s), 2.81-2.90 (4H, m), 2.91-3.00 (4H, m), 7.54 (1H, s), 7.59 (1H, d, J = 4.9 Hz), 8.32-8.43 (3H, m).
ビス(トリクロロメチル) カルボナート (31 mg)、DIPEA (0.11 mL) およびTHF (2.0 mL) の混合物 に(4-フルオロフェニル)メタンアミン(0.035 mL) のTHF (0.5 mL) 溶液を氷冷下加え、10分間撹拌した。混合物に1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペラジン (50 mL) のTHF (0.5 mL) 溶液を加え、室温で30分間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから結晶化して標題化合物 (51 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 2.16 (3H, s), 2.84-2.92 (4H, m), 3.41-3.51 (4H, m), 4.40 (2H, d, J = 5.7 Hz), 4.74 (1H, t, J = 5.3 Hz), 6.97-7.06 (2H, m), 7.27-7.33 (2H, m), 7.53-7.59 (2H, m), 8.24 (1H, d, J = 0.8 Hz), 8.34-8.42 (2H, m).
(5-(メトキシメチル)-2,2-ジメチルピロリジン-1-イル)(1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノン(光学異性体)
(5-(メトキシメチル)-2,2-ジメチルピロリジン-1-イル)(1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノンのラセミ体 (120 mg) をHPLC (カラム:CHIRALPAK AD、50 mmID×500 mmL、移動相:ヘキサン/エタノール/ジエチルアミン = 860/140/1) にて分取し、保持時間の小さい方を標題化合物 (56 mg)として得た。
(5-(メトキシメチル)-2,2-ジメチルピロリジン-1-イル)(1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノン(光学異性体)
(5-(メトキシメチル)-2,2-ジメチルピロリジン-1-イル)(1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノンのラセミ体 (120 mg) をHPLC (カラム:CHIRALPAK AD、50 mmID×500 mmL、移動相:ヘキサン/エタノール/ジエチルアミン = 860/140/1) にて分取し、保持時間の大きい方を標題化合物 (56 mg)として得た。
5,5-ジメチル-1-((1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)プロリンアミド(光学異性体)
5,5-ジメチル-1-((1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)プロリンアミドのラセミ体 (63 mg) をHPLC (カラム:CHIRALPAK AS、50 mmID×500 mmL、移動相:ヘキサン/エタノール/ジエチルアミン = 700/300/1) にて分取し、保持時間の小さい方を標題化合物 (30 mg)として得た。
5,5-ジメチル-1-((1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)プロリンアミド(光学異性体)
5,5-ジメチル-1-((1-(4-(5-メチル-1,3,4-チアジアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)プロリンアミドのラセミ体 (63 mg) をHPLC (カラム:CHIRALPAK AS、50 mmID×500 mmL、移動相:ヘキサン/エタノール/ジエチルアミン = 700/300/1) にて分取し、保持時間の大きい方を標題化合物 (22 mg)として得た。
N-シクロプロピル-1-(4-(4-フルオロフェニル)ピリミジン-5-イル)-N-メチルピペリジン-4-カルボキサミド
A) エチル 1-(2-(4-フルオロフェニル)-2-オキソエチル)ピペリジン-4-カルボキシラート
エチル ピペリジン-4-カルボキシラート (5.0 g)、炭酸カリウム (6.0 g) およびアセトニトリル (60 mL) の混合物に2-クロロ-1-(4-フルオロフェニル)エタノン (5.0 g) およびアセトニトリル (40 mL) の混合物を室温で滴下し、室温で終夜撹拌した。溶媒を減圧下留去した後、混合物を水で希釈し、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去して標題化合物 (8.7 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.19-1.30 (3H, m), 1.75-1.98 (4H, m), 2.15-2.37 (3H, m), 2.92 (2H, dt, J = 11.6, 3.5 Hz), 3.72 (2H, s), 4.13 (2H, q, J = 7.2 Hz), 7.05-7.17 (2H, m), 8.01-8.13 (2H, m).
エチル 1-(2-(4-フルオロフェニル)-2-オキソエチル)ピペリジン-4-カルボキシラート (8.0 g) およびN,N-ジメチルホルムアミドジメチルアセタール (50 mL) の混合物を5時間加熱還流した後、溶媒を減圧下留去した。得られた残渣、n-ブタノール (40 mL) およびDIPEA (40 mL) の混合物にホルムアミジン アセタート (9.9 g) を加え、100 ℃で終夜撹拌した。混合物に1M塩酸を加えた後、溶媒を減圧下留去した。残渣を水で希釈し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから結晶化して標題化合物 (4.7 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.27 (3H, t, J = 7.2 Hz), 1.67-1.84 (2H, m), 1.87-2.00 (2H, m), 2.38 (1H, tt, J = 11.2, 4.0 Hz), 2.68 (2H, td, J = 11.5, 2.7 Hz), 3.21 (2H, dt, J = 12.2, 3.2 Hz), 4.16 (2H, q, J = 7.2 Hz), 7.12-7.21 (2H, m), 8.07-8.18 (2H, m), 8.41 (1H, s), 8.90 (1H, s).
エチル 1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-カルボキシラート (2.2 g) をTHF (20 mL) および メタノール (5.0 mL) に溶解させ、混合物に2M 水酸化ナトリウム水溶液 (6.6 mL) を加え、室温で3.5時間撹拌した。混合物を濃縮した後、2M 塩酸で中和し、沈殿した固体を濾取し、標題化合物 (2.0 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.51-1.68 (2H, m), 1.76-1.88 (2H, m), 2.24-2.38 (1H, m), 2.62-2.75 (2H, m), 3.06-3.18 (2H, m), 7.30-7.41 (2H, m), 8.09-8.20 (2H, m), 8.54 (1H, s), 8.85 (1H, s), 12.25 (1H, brs).
D) N-シクロプロピル-1-(4-(4-フルオロフェニル)ピリミジン-5-イル)-N-メチルピペリジン-4-カルボキサミド
1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-カルボン酸 (0.10 g)、N-メチルシクロプロパンアミン (28 mg)、HATU (0.15 g)、DIPEA (0.15 mL)およびDMF (2.0 mL) の混合物 を室温で4時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘプタンから結晶化して標題化合物 (94 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 0.70-0.81 (2H, m), 0.85-0.96 (2H, m), 1.65-1.77 (2H, m), 1.82-1.99 (2H, m), 2.62-2.75 (3H, m), 2.93 (3H, s), 3.02-3.17 (1H, m), 3.24-3.37 (2H, m), 7.13-7.22 (2H, m), 8.11-8.20 (2H, m), 8.42 (1H, s), 8.90 (1H, s).
(3-フルオロアゼチジン-1-イル)(1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-イル)メタノン
1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-カルボン酸 (0.10 g)、3-フルオロアゼチジン 塩酸塩 (0.056 g)、HATU (0.16 g)、DIPEA (0.23 mL) およびDMF (2.0 mL) の混合物を室温で18時間撹拌した。混合物を酢酸エチルおよび水で希釈し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、ジエチルエーテルで固化して標題化合物 (0.11 g) を得た。
1H NMR (300 MHz, CDCl3) δ1.62-1.94 (4H, m), 2.18-2.31 (1H, m), 2.59-2.73 (2H, m), 3.21-3.34 (2H, m), 4.03-4.49 (4H, m), 5.18-5.46 (1H, m), 7.12-7.21 (2H, m), 8.09-8.17 (2H, m), 8.41 (1H, s), 8.90 (1H, s).
(3-フルオロアゼチジン-1-イル)(1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノン
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (60 mg)、3-フルオロアゼチジン 塩酸塩 (28 mg)、HATU (96 mg)、DIPEA (0.091 mL)およびDMF (2.0 mL) の混合物を室温で4時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘプタンから結晶化して標題化合物 (68 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.67-1.99 (4H, m), 2.17 (3H, s), 2.20-2.33 (1H, m), 2.64-2.78 (2H, m), 3.07-3.19 (2H, m), 4.04-4.52 (4H, m), 5.19-5.48 (1H, m), 7.54 (1H, s), 7.60 (1H, d, J = 5.3 Hz), 8.32-8.36 (2H, m), 8.39 (1H, s).
(1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)(3-フルオロアゼチジン-1-イル)メタノン
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (0.060 g)、3-フルオロアゼチジン 塩酸塩 (0.026 g)、HATU (0.089 g)、DIPEA (0.085 mL) およびDMF (2.0 mL) の混合物を室温で4時間撹拌した。混合物を酢酸エチルおよび水で希釈し酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、酢酸エチル/ヘプタンから結晶化して標題化合物 (0.062 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.69-2.01 (4H, m), 2.21-2.36 (1H, m), 2.68-2.81 (2H, m), 3.05-3.18 (2H, m), 4.03-4.53 (4H, m), 5.19-5.48 (1H, m), 7.59 (1H, d, J = 5.3 Hz), 7.66 (1H, s), 8.39 (1H, d, J = 5.3 Hz), 8.44 (1H, s), 8.56 (1H, s).
((3S)-3-フルオロピロリジン-1-イル)(1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノン
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (60 mg)、(S)-3-フルオロピロリジン 塩酸塩 (32 mg)、HATU (96 mg)、DIPEA (0.091 mL) およびDMF (2.0 mL) の混合物を室温で4時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘプタンから結晶化して標題化合物 (68 mg) を得た。
1H NMR (300 MHz, CDCl3) δ1.68-2.10 (5H, m), 2.17 (3H, s), 2.20-2.56 (2H, m), 2.66-2.79 (2H, m), 3.09-3.20 (2H, m), 3.45-3.99 (4H, m), 5.14-5.44 (1H, m), 7.54 (1H, s), 7.61 (1H, d, J = 5.3 Hz), 8.32-8.37 (2H, m), 8.40 (1H, s).
((3R)-3-フルオロピロリジン-1-イル)(1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノン
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (60 mg)、(R)-3-フルオロピロリジン 塩酸塩 (32 mg)、HATU (96 mg)、DIPEA (0.091 mL) およびDMF (2.0 mL) の混合物を室温で4時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘプタンから結晶化して標題化合物 (64 mg) を得た。
1H NMR (300 MHz, CDCl3) δ1.70-2.15 (5H, m), 2.17 (3H, s), 2.21-2.56 (2H, m), 2.65-2.80 (2H, m), 3.08-3.20 (2H, m), 3.45-4.00 (4H, m), 5.15-5.43 (1H, m), 7.54 (1H, s), 7.61 (1H, d, J = 5.3 Hz), 8.33-8.37 (2H, m), 8.40 (1H, s).
(1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)((3S)-3-フルオロピロリジン-1-イル)メタノン
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (0.060 g)、(S)-3-フルオロピロリジン 塩酸塩 (0.030 g)、HATU (0.089 g)、DIPEA (0.085 mL) およびDMF (2.0 mL) の混合物 を室温で4時間撹拌した。混合物を酢酸エチルおよび水で希釈し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、酢酸エチル/ヘプタンから結晶化して標題化合物 (0.064 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.72-2.58 (7H, m), 2.69-2.84 (2H, m), 3.08-3.20 (2H, m), 3.46-4.01 (4H, m), 5.13-5.44 (1H, m), 7.60 (1H, d, J = 5.3 Hz), 7.66 (1H, s), 8.39 (1H, d, J = 5.3 Hz), 8.45 (1H, s), 8.59 (1H, s).
(1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)((3R)-3-フルオロピロリジン-1-イル)メタノン
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (60 mg)、(R)-3-フルオロピロリジン 塩酸塩 (30 mg)、HATU (89 mg)、DIPEA (0.085 mL) およびDMF (2.0 mL) の混合物 を室温で2時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘプタンから結晶化して標題化合物 (63 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.74-2.59 (7H, m), 2.69-2.84 (2H, m), 3.07-3.20 (2H, m), 3.45-3.99 (4H, m), 5.15-5.44 (1H, m), 7.60 (1H, d, J = 5.3 Hz), 7.66 (1H, s), 8.39 (1H, d, J = 5.3 Hz), 8.46 (1H, s), 8.59 (1H, s).
(1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-イル)((3S)-3-フルオロピロリジン-1-イル)メタノン
1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-カルボン酸 (0.060 g)、(S)-3-フルオロピロリジン 塩酸塩 (0.030 g)、HATU (0.091 g)、DIPEA (0.087 mL) およびDMF (2.0 mL) の混合物を室温で4時間撹拌した。混合物を酢酸エチルおよび水で希釈し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、酢酸エチル/ヘプタンから結晶化して標題化合物 (0.059 g) を得た。
1H NMR (300 MHz, CDCl3) δ1.66-2.54 (7H, m), 2.61-2.74 (2H, m), 3.25-3.36 (2H, m), 3.45-3.98 (4H, m), 5.14-5.41 (1H, m), 7.12-7.22 (2H, m), 8.11-8.18 (2H, m), 8.42 (1H, s), 8.90 (1H, s).
(1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-イル)((3R)-3-フルオロピロリジン-1-イル)メタノン
1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-カルボン酸 (60 mg)、(R)-3-フルオロピロリジン 塩酸塩 (30 mg)、HATU (91 mg)、DIPEA (0.087 mL) およびDMF (2.0 mL) の混合物を室温で4時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘプタンから結晶化して標題化合物 (60 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.64-2.53 (7H, m), 2.61-2.75 (2H, m), 3.24-3.37 (2H, m), 3.46-3.98 (4H, m), 5.13-5.43 (1H, m), 7.12-7.21 (2H, m), 8.10-8.18 (2H, m), 8.42 (1H, s), 8.90 (1H, s).
1-(4-(4-フルオロフェニル)ピリミジン-5-イル)-N-メチル-N-(テトラヒドロ-2H-ピラン-4-イル)ピペリジン-4-カルボキサミド
1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-カルボン酸 (60 mg)、N-メチル-N-(テトラヒドロ-2H-ピラン-4-イル)アミン (28 mg)、HATU (91 mg)、DIPEA (0.087 mL) およびDMF (2.0 mL) の混合物 を室温で4時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘプタンから結晶化して標題化合物 (68 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.46-2.06 (8H, m), 2.48-2.77 (3H, m), 2.81-2.95 (3H, m), 3.21-3.57 (4H, m), 3.96-4.13 (2H, m), 4.62-4.84 (1H, m), 7.12-7.21 (2H, m), 8.10-8.19 (2H, m), 8.42 (1H, s), 8.90 (1H, s).
1-(4-(4-フルオロフェニル)ピリミジン-5-イル)-N-((3S)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド
1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-カルボン酸 (0.30 g)、(S)-テトラヒドロフラン-3-アミン 塩酸塩 (0.15 g)、HATU (0.45 g)、DIPEA (0.43 mL)およびDMF (5.0 mL) の混合物を室温で4時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘプタンから結晶化して標題化合物 (0.32 g) を得た
1H NMR (300 MHz, CDCl3) δ 1.70-1.87 (5H, m), 2.06-2.19 (1H, m), 2.22-2.36 (1H, m), 2.59-2.71 (2H, m), 3.21-3.34 (2H, m), 3.66 (1H, dd, J = 9.4, 2.3 Hz), 3.74-3.85 (2H, m), 3.89-3.99 (1H, m), 4.47-4.60 (1H, m), 5.63 (1H, d, J = 6.4 Hz), 7.12-7.21 (2H, m), 8.08-8.16 (2H, m), 8.41 (1H, s), 8.90 (1H, s).
1-(4-(4-フルオロフェニル)ピリミジン-5-イル)-N-((3R)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド
1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-カルボン酸 (0.30 g)、(R)-テトラヒドロフラン-3-アミン 塩酸塩 (0.15 g)、HATU (0.45 g)、DIPEA (0.43 mL) およびDMF (5.0 mL) の混合物を室温で4時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘプタンから結晶化して標題化合物 (0.34 g) を得た。
1H NMR (300 MHz, CDCl3) δ1.71-1.86 (5H, m), 2.04-2.18 (1H, m), 2.22-2.36 (1H, m), 2.59-2.71 (2H, m), 3.22-3.32 (2H, m), 3.62-3.69 (1H, m), 3.74-3.85 (2H, m), 3.89-3.99 (1H, m), 4.47-4.60 (1H, m), 5.63 (1H, d, J = 7.5 Hz), 7.12-7.22 (2H, m), 8.06-8.17 (2H, m), 8.41 (1H, s), 8.90 (1H, s).
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-((3S)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (1.0 g)、(S)-テトラヒドロフラン-3-アミン 塩酸塩 (0.43 g)、HATU (1.7 g)、トリエチルアミン (1.9 mL) およびDMF (12 mL) の混合物を室温で3時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから結晶化して標題化合物 (0.82 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.72-1.92 (5H, m), 2.07-2.21 (4H, m), 2.22-2.38 (1H, m), 2.69 (2H, dt, J = 11.7, 7.2 Hz), 3.12 (2H, d, J = 12.1 Hz), 3.66 (1H, dd, J = 9.5, 2.7 Hz), 3.74-3.87 (2H, m), 3.88-4.01 (1H, m), 4.47-4.61 (1H, m), 5.73 (1H, d, J = 7.2 Hz), 7.54 (1H, s), 7.60 (1H, d, J = 5.3 Hz), 8.31 (1H, d, J = 0.8 Hz), 8.35 (1H, d, J = 5.3 Hz), 8.39 (1H, s).
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-((3S)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (0.50 g)、(S)-テトラヒドロフラン-3-アミン 塩酸塩 (0.20 g)、HATU (0.81 g)、トリエチルアミン (0.91 mL) およびDMF (5.4 mL) の混合物を室温で3時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから結晶化して標題化合物 (0.51 g) を得た。
1H NMR (300 MHz, CDCl3) δ1.72-1.96 (5H, m), 2.10-2.37 (2H, m), 2.73 (2H, td, J = 10.8, 4.2 Hz), 3.04-3.18 (2H, m), 3.67 (1H, dd, J = 9.5, 2.3 Hz), 3.74-3.87 (2H, m), 3.89-4.00 (1H, m), 4.49-4.62 (1H, m), 5.71 (1H, d, J = 7.2 Hz), 7.59 (1H, d, J = 5.3 Hz), 7.66 (1H, d, J = 0.8 Hz), 8.39 (1H, d, J = 5.3 Hz), 8.44 (1H, s), 8.54 (1H, d, J = 0.8 Hz).
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-((3R)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (1.0 g)、(R)-テトラヒドロフラン-3-アミン 塩酸塩 (0.43 g)、HATU (1.7 g)、トリエチルアミン (1.9 mL) およびDMF (12 mL) の混合物を室温で3時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから結晶化して標題化合物 (0.83 g) を得た。
1H NMR (300 MHz, CDCl3) δ1.67-1.93 (5H, m), 2.05-2.37 (5H, m), 2.69 (2H, dt, J = 12.0, 7.2 Hz), 3.12 (2H, d, J = 11.7 Hz), 3.67 (1H, dd, J = 9.5, 2.3 Hz), 3.73-3.87 (2H, m), 3.88-4.00 (1H, m), 4.55 (1H, dtd, J = 7.6, 4.8, 2.8 Hz), 5.75 (1H, d, J = 7.2 Hz), 7.54 (1H, s), 7.60 (1H, d, J = 4.9 Hz), 8.31 (1H, s), 8.34 (1H, d, J = 5.3 Hz), 8.39 (1H, s).
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-((3R)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (0.50 g)、(R)-テトラヒドロフラン-3-アミン 塩酸塩 (0.20 g)、HATU (0.81 g)、トリエチルアミン (0.91 mL) およびDMF (5.4 mL) の混合物を室温で3時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから結晶化して標題化合物 (0.50 g) を得た。
1H NMR (300 MHz, CDCl3) δ1.69-1.97 (5H, m), 2.10-2.37 (2H, m), 2.73 (2H, td, J = 10.8, 4.2 Hz), 3.05-3.17 (2H, m), 3.67 (1H, dd, J = 9.5, 2.3 Hz), 3.73-3.87 (2H, m), 3.89-4.01 (1H, m), 4.55 (1H, ddt, J = 7.6, 5.1, 2.4 Hz), 5.69 (1H, d, J = 7.2 Hz), 7.59 (1H, d, J = 5.3 Hz), 7.66 (1H, s), 8.39 (1H, d, J = 5.3 Hz), 8.44 (1H, s), 8.54 (1H, d, J = 0.8 Hz).
N-メチル-1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-(テトラヒドロ-2H-ピラン-4-イル)ピペリジン-4-カルボキサミド
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (80 mg)、N-メチル-N-(テトラヒドロ-2H-ピラン-4-イル)アミン (39 mg)、HATU (0.13 g)、DIPEA (0.12 mL) およびDMF (2.0 mL) の混合物を室温で4時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘプタンから結晶化して標題化合物 (73 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.49-2.07 (8H, m), 2.17 (3H, s), 2.52-2.81 (3H, m), 2.84-2.96 (3H, m), 3.08-3.21 (2H, m), 3.38-3.57 (2H, m), 3.97-4.13 (2H, m), 4.67-4.83 (1H, m), 7.54 (1H, s), 7.61 (1H, d, J = 5.3 Hz), 8.33-8.39 (2H, m), 8.40 (1H, s).
N-(4-フルオロベンジル)-N-メチル-4-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペラジン-1-カルボキサミド
N-(4-フルオロベンジル)-4-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペラジン-1-カルボキサミド(0.20 g) およびDMF (3.0 mL) の混合物に水素化ナトリウム (60%、30 mg) を氷冷下加え、同温度で30分間撹拌した。混合物にヨウ化メチル (0.047 mL) を氷冷下加え、同温度で30分間撹拌した。混合物に飽和塩化アンモニウム水溶液、酢酸エチルおよびピリジンを加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、標題化合物 (0.18 g) を得た。
1H NMR (300 MHz, CDCl3) δ2.17 (3H, s), 2.78 (3H, s), 2.88-2.95 (4H, m), 3.30-3.38 (4H, m), 4.38 (2H, s), 6.97-7.07 (2H, m), 7.19-7.26 (2H, m), 7.55 (1H, s), 7.58 (1H, d, J = 5.3 Hz), 8.30 (1H, s), 8.35-8.41 (2H, m).
N-ベンジル-N-メチル-4-(4-フェニルピリミジン-5-イル)ピペラジン-1-カルボキサミド
N-ベンジル-4-(4-フェニルピリミジン-5-イル)ピペラジン-1-カルボキサミド (0.15 g) およびDMF (3.0 mL) の混合物に水素化ナトリウム (60%、24 mg) を氷冷下加え、同温度で30分間撹拌した。混合物にヨウ化メチル (0.038 mL) を加え、氷冷下1.5時間撹拌した。混合物に飽和塩化アンモニウム水溶液、酢酸エチルおよびピリジンを加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、酢酸エチル/ヘプタンから結晶化して標題化合物(0.11 g) を得た。
1H NMR (300 MHz, CDCl3) δ2.75 (3H, s), 2.93-3.02 (4H, m), 3.25-3.33 (4H, m), 4.40 (2H, s), 7.19-7.37 (5H, m), 7.42-7.52 (3H, m), 8.03-8.11 (2H, m), 8.41 (1H, s), 8.94 (1H, s).
(1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)((3S)-3-メトキシピロリジン-1-イル)メタノン
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (0.10 g)、(S)-3-メトキシピロリジン 塩酸塩 (49 mg)、HATU (0.16 g)、トリエチルアミン (0.18 mL) およびDMF (1.1 mL) の混合物 を室温で3時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから結晶化して標題化合物 (0.066 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.73-2.22 (6H, m), 2.37-2.55 (1H, m), 2.69-2.82 (2H, m), 3.06-3.20 (2H, m), 3.34 (3H, d, J = 5.3 Hz), 3.41-3.76 (4H, m), 3.92-4.07 (1H, m), 7.60 (1H, d, J = 5.3 Hz), 7.66 (1H, s), 8.38 (1H, d, J = 5.3 Hz), 8.45 (1H, s), 8.60 (1H, s).
(1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)((3R)-3-メトキシピロリジン-1-イル)メタノン
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (0.10 g)、(R)-3-メトキシピロリジン 塩酸塩 (49 mg)、HATU (0.16 g)、トリエチルアミン (0.18 mL) およびDMF (1.1 mL) の混合物 を室温で3時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、得られた固体を酢酸エチル/ヘキサンから結晶化して標題化合物 (0.076 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.73-2.20 (6H, m), 2.36-2.55 (1H, m), 2.68-2.83 (2H, m), 3.13 (2H, dd, J = 11.4, 3.0 Hz), 3.34 (3H, d, J = 5.3 Hz), 3.41-3.76 (4H, m), 3.92-4.07 (1H, m), 7.60 (1H, d, J = 5.3 Hz), 7.66 (1H, s), 8.39 (1H, d, J = 5.3 Hz), 8.45 (1H, s), 8.60 (1H, s).
((3S)-3-メトキシピロリジン-1-イル)(1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノン
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (0.10 g)、(S)-3-メトキシピロリジン 塩酸塩 (53 mg)、HATU (0.17 g)、トリエチルアミン (0.20 mL) およびDMF (1.2 mL) の混合物を室温で3時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製して標題化合物 (0.050 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.71-2.20 (9H, m), 2.44 (1H, d, J = 17.0 Hz), 2.72 (2H, td, J = 11.9, 2.7 Hz), 3.14 (2H, d, J = 12.1 Hz), 3.34 (3H, d, J = 5.3 Hz), 3.42-3.77 (4H, m), 3.92-4.06 (1H, m), 7.53 (1H, s), 7.61 (1H, d, J = 5.3 Hz), 8.31-8.42 (3H, m).
((3R)-3-メトキシピロリジン-1-イル)(1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノン
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (100 mg)、(R)-3-メトキシピロリジン 塩酸塩 (53 mg)、HATU (0.17 g)、トリエチルアミン (0.20 mL) およびDMF (1.2 mL) の混合物を室温で3時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製して標題化合物 (0.039 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.72-2.21 (9H, m), 2.33-2.55 (1H, m), 2.72 (2H, td, J = 12.0, 2.5 Hz), 3.14 (2H, d, J = 12.1 Hz), 3.34 (3H, d, J = 5.3 Hz), 3.43-3.76 (4H, m), 3.90-4.11 (1H, m), 7.53 (1H, s), 7.61 (1H, d, J = 4.9 Hz), 8.29-8.43 (3H, m).
(1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-イル)((3S)-3-メトキシピロリジン-1-イル)メタノン
1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-カルボン酸 (0.10 g)、(S)-3-メトキシピロリジン 塩酸塩 (50 mg)、HATU (0.16 g)、トリエチルアミン (0.19 mL) およびDMF (1.1 mL) の混合物を室温で3時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製して標題化合物 (0.073 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.65-2.20 (6H, m), 2.34-2.51 (1H, m), 2.67 (2H, td, J = 11.8, 2.5 Hz), 3.21-3.37 (5H, m), 3.41-3.74 (4H, m), 3.89-4.05 (1H, m), 7.09-7.23 (2H, m), 8.07-8.19 (2H, m), 8.41 (1H, s), 8.90 (1H, s).
(1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-イル)((3R)-3-メトキシピロリジン-1-イル)メタノン
1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-カルボン酸 (0.10 g)、(R)-3-メトキシピロリジン 塩酸塩 (50 mg)、HATU (0.16 g)、トリエチルアミン (0.19 mL) およびDMF (1.1 mL) の混合物を室温で3時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製して標題化合物 (0.074 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.66-2.22 (6H, m), 2.31-2.51 (1H, m), 2.58-2.76 (2H, m), 3.21-3.38 (5H, m), 3.39-3.77 (4H, m), 3.90-4.07 (1H, m), 7.16 (2H, t, J = 8.7 Hz), 8.15 (2H, dd, J = 8.7, 5.7 Hz), 8.41 (1H, s), 8.90 (1H, s).
N-メチル-1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-((3S)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-((3S)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド (0.12 g) およびDMF (2.0 mL) の混合物に水素化ナトリウム (60%、20 mg) を氷冷下加え、30分間撹拌した。混合物にヨウ化メチル (0.032 mL) を加え、氷冷下1時間撹拌した。混合物に飽和塩化アンモニウム水溶液、酢酸エチルおよびピリジンを加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、酢酸エチル/ヘプタンから結晶化して標題化合物(0.084 g) を得た。
1H NMR (300 MHz, CDCl3) δ1.69-2.05 (5H, m), 2.17 (3H, s), 2.20-2.35 (1H, m), 2.51-3.03 (6H, m), 3.08-3.20 (2H, m), 3.60-3.85 (3H, m), 4.00-4.13 (1H, m), 5.30-5.43 (1H, m), 7.54 (1H, s), 7.61 (1H, d, J = 5.3 Hz), 8.33-8.37 (2H, m), 8.40 (1H, s).
N-メチル-1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-((3R)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-((3R)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド (0.12 g) およびDMF (2.0 mL) の混合物に水素化ナトリウム (60%、20 mg) を氷冷下加え、30分間撹拌した。混合物にヨウ化メチル (0.032 mL) を加え、氷冷下1時間撹拌した。混合物に飽和塩化アンモニウム水溶液、酢酸エチルおよびピリジンを加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、酢酸エチル/ヘプタンから結晶化して標題化合物(0.066 g) を得た。
1H NMR (300 MHz, CDCl3) δ1.70-2.03 (5H, m), 2.17 (3H, s), 2.20-2.35 (1H, m), 2.51-3.03 (6H, m), 3.09-3.19 (2H, m), 3.61-3.85 (3H, m), 4.01-4.14 (1H, m), 5.30-5.43 (1H, m), 7.54 (1H, s), 7.61 (1H, d, J = 5.3 Hz), 8.33-8.37 (2H, m), 8.40 (1H, s).
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-メチル-N-((3S)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-((3S)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド (0.12 g) およびDMF (2.0 mL) の混合物に水素化ナトリウム (60%、19 mg) を氷冷下加え、30分間撹拌した。混合物にヨウ化メチル (0.030 mL) を加え、氷冷下1時間撹拌した。混合物に飽和塩化アンモニウム水溶液、酢酸エチルおよびピリジンを加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製して標題化合物 (0.094 g) を得た。
1H NMR (300 MHz, CDCl3) δ1.71-2.03 (5H, m), 2.19-2.35 (1H, m), 2.53-3.02 (6H, m), 3.07-3.19 (2H, m), 3.60-3.85 (3H, m), 4.01-4.12 (1H, m), 5.30-5.44 (1H, m), 7.60 (1H, d, J = 5.3 Hz), 7.66 (1H, s), 8.39 (1H, d, J = 4.9 Hz), 8.45 (1H, s), 8.58 (1H, s).
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-メチル-N-((3R)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド
1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-((3R)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド (0.12 g) およびDMF (2.0 mL) の混合物に水素化ナトリウム (60%、19 mg) を氷冷下加え、30分間撹拌した。混合物にヨウ化メチル (0.030 mL) を加え、氷冷下1時間撹拌した。混合物に飽和塩化アンモニウム水溶液、酢酸エチルおよびピリジンを加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製して標題化合物 (0.092 g) を得た。
1H NMR (300 MHz, CDCl3) δ1.70-2.03 (5H, m), 2.18-2.35 (1H, m), 2.53-3.04 (6H, m), 3.08-3.20 (2H, m), 3.60-3.85 (3H, m), 4.01-4.12 (1H, m), 5.31-5.43 (1H, m), 7.60 (1H, d, J = 5.3 Hz), 7.66 (1H, s), 8.39 (1H, d, J = 5.3 Hz), 8.45 (1H, s), 8.58 (1H, s).
1-(4-(4-フルオロフェニル)ピリミジン-5-イル)-N-メチル-N-((3S)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド
1-(4-(4-フルオロフェニル)ピリミジン-5-イル)-N-((3S)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド (0.12 g) およびDMF (2.0 mL) の混合物に水素化ナトリウム (60%、19 mg) を氷冷下加え、30分間撹拌した。混合物にヨウ化メチル (0.034 mL) を加え、氷冷下2.5時間撹拌した。混合物に飽和塩化アンモニウム水溶液、酢酸エチルおよびピリジンを加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、酢酸エチル/ヘプタンから結晶化して標題化合物(0.091 g) を得た。
1H NMR (300 MHz, CDCl3) δ1.66-2.03 (5H, m), 2.17-2.35 (1H, m), 2.46-2.75 (3H, m), 2.83-3.01 (3H, m), 3.23-3.35 (2H, m), 3.60-3.82 (3H, m), 4.00-4.12 (1H, m), 5.27-5.42 (1H, m), 7.12-7.22 (2H, m), 8.09-8.19 (2H, m), 8.42 (1H, s), 8.90 (1H, s).
1-(4-(4-フルオロフェニル)ピリミジン-5-イル)-N-メチル-N-((3R)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド
1-(4-(4-フルオロフェニル)ピリミジン-5-イル)-N-((3R)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド (0.12 g) およびDMF (2.0 mL) の混合物に水素化ナトリウム (60%、19 mg) を氷冷下加え、30分間撹拌した。混合物にヨウ化メチル (0.034 mL) を加え、氷冷下2.5時間撹拌した。混合物に飽和塩化アンモニウム水溶液、酢酸エチルおよびピリジンを加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、酢酸エチル/ヘプタンから結晶化して標題化合物(0.087 g) を得た。
1H NMR (300 MHz, CDCl3) δ1.65-2.02 (5H, m), 2.16-2.36 (1H, m), 2.48-2.77 (3H, m), 2.84-3.02 (3H, m), 3.24-3.35 (2H, m), 3.60-3.81 (3H, m), 4.00-4.11 (1H, m), 5.29-5.41 (1H, m), 7.12-7.21 (2H, m), 8.10-8.19 (2H, m), 8.42 (1H, s), 8.90 (1H, s).
N-(2-フルオロエチル)-1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-(テトラヒドロ-2H-ピラン-4-イル)ピペリジン-4-カルボキサミド
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-(テトラヒドロ-2H-ピラン-4-イル)ピペリジン-4-カルボキサミド (0.12 g) およびDMF (2.0 mL) の混合物に水素化ナトリウム (60%、19 mg) を加え、30分間撹拌した。混合物に2-フルオロエチル 4-メチルベンゼンスルホナート (0.11 g) のDMF (1.0 mL) 溶液を加え、室温で16時間撹拌した。混合物に飽和塩化アンモニウム水溶液を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製して標題化合物 (3.4 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.61-2.04 (8H, m), 2.17 (3H, s), 2.56-2.85 (3H, m), 3.06-3.22 (2H, m), 3.38-3.89 (5H, m), 3.97-4.15 (2H, m), 4.35-4.74 (2H, m), 7.54 (1H, s), 7.61 (1H, d, J = 5.3 Hz), 8.31-8.45 (3H, m).
N-(2-フルオロエチル)-1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-((3S)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-((3S)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド (0.12 g) およびDMF (2.0 mL) の混合物に水素化ナトリウム (60%、20 mg) を加え、30分間撹拌した。混合物に2-フルオロエチル 4-メチルベンゼンスルホナート (0.11 g) のDMF (1.0 mL) 溶液を加え、室温で16時間撹拌した。混合物に飽和塩化アンモニウム水溶液を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製して標題化合物 (12 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.70-2.06 (5H, m), 2.18 (3H, s), 2.23-2.41 (1H, m), 2.62-2.84 (3H, m), 3.06-3.22 (2H, m), 3.51-3.90 (5H, m), 4.03-4.14 (1H, m), 4.42-5.00 (3H, m), 7.54 (1H, s), 7.61 (1H, d, J = 5.3 Hz), 8.31-8.43 (3H, m).
N-(2-フルオロエチル)-1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-((3R)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド
1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)-N-((3R)-テトラヒドロフラン-3-イル)ピペリジン-4-カルボキサミド (0.12 g) およびDMF (2.0 mL) の混合物に水素化ナトリウム (60%、20 mg) を加え、30分間撹拌した。混合物に2-フルオロエチル 4-メチルベンゼンスルホナート (0.11 g) のDMF (1.0 mL) 溶液を加え、室温で16時間撹拌した。混合物に飽和塩化アンモニウム水溶液を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製して標題化合物 (12 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 1.70-2.04 (5H, m), 2.17 (3H, s), 2.22-2.39 (1H, m), 2.62-2.84 (3H, m), 3.07-3.22 (2H, m), 3.50-3.92 (5H, m), 4.03-4.14 (1H, m), 4.43-5.01 (3H, m), 7.54 (1H, s), 7.61 (1H, d, J = 5.3 Hz), 8.31-8.44 (3H, m).
N-ベンジル-N-(2-フルオロエチル)-4-(4-フェニルピリミジン-5-イル)ピペラジン-1-カルボキサミド
N-ベンジル-4-(4-フェニルピリミジン-5-イル)ピペラジン-1-カルボキサミド (0.11 g)、15-クラウン 5-エーテル (0.078 mL) および THF (2.0 mL) の混合物に水素化ナトリウム (16 mg) を氷冷下加え、室温で30分間撹拌した。混合物に2-フルオロエチル 4-メチルベンゼンスルホナート (0.12 g) のTHF溶液 (1.0 mL) を加え、室温で4日間撹拌した。塩化アンモニウム水溶液を加えて反応を停止し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサンおよびメタノール/酢酸エチル) で精製して標題化合物(43 mg) を得た。
1H NMR (300 MHz, CDCl3) δ 2.91-3.01 (4H, m), 3.28-3.50 (6H, m), 4.42-4.65 (4H, m), 7.17-7.38 (5H, m), 7.43-7.52 (3H, m), 8.03-8.10 (2H, m), 8.40 (1H, s), 8.94 (1H, s).
N-(4-フルオロベンジル)-N-(2-フルオロエチル)-4-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペラジン-1-カルボキサミド
N-(4-フルオロベンジル)-4-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペラジン-1-カルボキサミド(0.12 g)、15-クラウン 5-エーテル (0.079 mL) および THF (2.0 mL) の混合物に水素化ナトリウム (0.016 g) を0℃で加え、室温で30分間撹拌した。混合物に2-フルオロエチル 4-メチルベンゼンスルホナート (0.12 g) のTHF溶液 (1.0 mL) を加え、室温で4日間撹拌した。混合物に塩化アンモニウム水溶液を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサンおよびメタノール/酢酸エチル) で精製して標題化合物 (0.072 g) を得た。
1H NMR (300 MHz, CDCl3) δ 2.17 (3H, s), 2.87-2.96 (4H, m), 3.32-3.50 (6H, m), 4.44-4.67 (4H, m), 6.99-7.09 (2H, m), 7.17-7.25 (2H, m), 7.55 (1H, s), 7.58 (1H, d, J = 4.9 Hz), 8.28 (1H, s), 8.36-8.40 (2H, m).
((3S)-3-フルオロピロリジン-1-イル)(1-(4-(5-メチル-1,3-チアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノン
1-(4-(5-メチル-1,3-チアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (0.080 g)、(S)-3-フルオロピロリジン 塩酸塩 (0.040 g)、HATU (0.12 g)、DIPEA (0.12 mL) およびDMF (2.0 mL) の混合物を室温で18時間撹拌した。混合物を酢酸エチルおよび水で希釈し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、酢酸エチル/ヘプタンから結晶化して標題化合物 (0.075 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.78-2.65 (10H, m), 2.87-3.02 (2H, m), 3.17-3.28 (2H, m), 3.49-4.03 (4H, m), 5.16-5.47 (1H, m), 7.60 (1H, d, J = 0.9 Hz), 8.09 (1H, d, J = 5.1 Hz), 8.45 (1H, d, J = 5.1 Hz), 8.59 (1H, s).
(3-フルオロアゼチジン-1-イル)(1-(4-(5-メチル-1,3-チアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノン
1-(4-(5-メチル-1,3-チアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (0.080 g)、3-フルオロアゼチジン 塩酸塩 (0.035 g)、HATU (0.12 g)、DIPEA (0.12 mL) およびDMF (2.0 mL) の混合物を室温で18時間撹拌した。混合物を酢酸エチルおよび水で希釈し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、酢酸エチル/ヘプタンから結晶化して標題化合物 (0.071 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.74-1.92 (2H, m), 2.12-2.28 (2H, m), 2.29-2.41 (1H, m), 2.53 (3H, d, J = 0.9 Hz), 2.86-2.99 (2H, m), 3.15-3.27 (2H, m), 4.07-4.57 (4H, m), 5.22-5.50 (1H, m), 7.60 (1H, d, J = 0.9 Hz), 8.09 (1H, d, J = 5.1 Hz), 8.45 (1H, d, J = 5.1 Hz), 8.58 (1H, s).
(1-(4-(4-ブロモ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)((3S)-3-フルオロピロリジン-1-イル)メタノン
A) エチル 1-(4-(4-ブロモ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボキシラート
4-(4-ブロモ-1H-ピラゾール-1-イル)-3-フルオロピリジン (3.0 g)、エチル ピペリジン-4-カルボキシラート (4.2 mL) およびNMP (12 mL) の混合物を180℃で4時間撹拌した。混合物をシリカゲルカラムクロマトグラフィー (酢酸エチル/ヘキサン) で精製し、酢酸エチル/ヘキサンで洗浄して標題化合物 (2.3 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.28 (3H, t, J = 7.1 Hz), 1.73-1.91 (2H, m), 1.95-2.07 (2H, m), 2.35-2.50 (1H, m), 2.68-2.82 (2H, m), 2.99-3.13 (2H, m), 4.18 (2H, q, J = 7.2 Hz), 7.58 (1H, d, J = 5.1 Hz), 7.70 (1H, s), 8.39 (1H, d, J = 5.1 Hz), 8.44 (1H, s), 8.58 (1H, s).
エチル 1-(4-(4-ブロモ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボキシラート (1.2 g)、2M 水酸化ナトリウム水溶液 (2.4 mL)、THF (4.0 mL) およびエタノール (4.0 mL) の混合物を室温で3時間撹拌した。混合物を濃縮し、残渣を2M 塩酸 (2.4 mL) で中和した。沈殿物を集め、水で洗浄し、減圧下乾燥して標題化合物 (1.1 g) を得た。
1H NMR (300 MHz, DMSO-d6) δ 1.54-1.72 (2H, m), 1.77-1.90 (2H, m), 2.26-2.41 (1H, m), 2.64-2.77 (2H, m), 2.83-2.95 (2H, m), 7.52 (1H, d, J = 5.1 Hz), 7.96 (1H, s), 8.36 (1H, d, J = 5.1 Hz), 8.48 (1H, s), 8.77 (1H, s), 12.26 (1H, s).
1-(4-(4-ブロモ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (0.30 g)、(S)-3-フルオロピロリジン 塩酸塩 (0.13 g)、HATU (0.39 g)、DIPEA (0.37 mL) およびDMF (3.0 mL) の混合物を室温で18時間撹拌した。混合物を酢酸エチルおよび水で希釈し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、酢酸エチル/ヘプタンから結晶化して標題化合物 (0.31 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.73-2.59 (7H, m), 2.68-2.85 (2H, m), 3.06-3.21 (2H, m), 3.47-4.01 (4H, m), 5.14-5.44 (1H, m), 7.59 (1H, d, J = 5.3 Hz), 7.69 (1H, s), 8.39 (1H, d, J = 5.3 Hz), 8.46 (1H, s), 8.61 (1H, s).
(1-(4-(4-ブロモ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)(3-フルオロアゼチジン-1-イル)メタノン
1-(4-(4-ブロモ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-カルボン酸 (0.078g)、3-フルオロアゼチジン 塩酸塩 (0.025 g)、HATU (0.11 g)、トリエチルアミン (0.12 mL) およびDMF (1.0 mL) の混合物を室温で3時間撹拌した。混合物に水を加え、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、溶媒を減圧下留去した。残渣をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) で精製し、酢酸エチル/ヘキサンから結晶化して標題化合物 (0.052 g) を得た。
1H NMR (300 MHz, CDCl3) δ 1.68-2.03 (4H, m), 2.17-2.37 (1H, m), 2.64-2.84 (2H, m), 3.03-3.19 (2H, m), 4.02-4.53 (4H, m), 5.15-5.49 (1H, m), 7.59 (1H, d, J = 5.3 Hz), 7.69 (1H, s), 8.39 (1H, d, J = 5.3 Hz), 8.44 (1H, s), 8.59 (1H, s).
(1-(4-(4-シクロプロピル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)((3S)-3-フルオロピロリジン-1-イル)メタノン
(S)-(1-(4-(4-ブロモ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)(3-フルオロピロリジン-1-イル)メタノン (0.10 g)、炭酸カリウム (0.13 g)、ビス(ジ-tert-ブチル(4-ジメチルアミノフェニル)ホスフィン)ジクロロパラジウム(II) (0.017 g)、シクロプロピル トリフルオロボラート カリウム塩 (0.11 g)、トルエン (2.0 mL) および水 (0.40 mL) の混合物をマイクロウェーブ照射下、110℃で12時間撹拌した。混合物をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) およびHPLC (C18、移動相: 水/アセトニトリル (0.1% TFA含有系))で精製した。得られた画分を濃縮し、炭酸水素ナトリウム水溶液で中和し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去して標題化合物 (0.046 g) を得た。
1H NMR (300 MHz, CDCl3) δ 0.55-0.66 (2H, m), 0.87-0.99 (2H, m), 1.70-2.57 (8H, m), 2.65-2.83 (2H, m), 3.07-3.21 (2H, m), 3.46-4.01 (4H, m), 5.13-5.45 (1H, m), 7.48-7.71 (2H, m), 8.32-8.64 (3H, m).
(1-(4-(4-シクロプロピル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)(3-フルオロアゼチジン-1-イル)メタノン
(1-(4-(4-ブロモ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)(3-フルオロアゼチジン-1-イル)メタノン (0.10 g)、炭酸カリウム (0.14 g)、ビス(ジ-tert-ブチル(4-ジメチルアミノフェニル)ホスフィン)ジクロロパラジウム(II) (0.017 g)、シクロプロピル トリフルオロボラート カリウム塩 (0.11 g)、トルエン (2.0 mL) および水 (0.40 mL) の混合物をマイクロウェーブ照射下、110℃で12時間撹拌した。混合物をシリカゲルカラムクロマトグラフィー (NH、酢酸エチル/ヘキサン) およびHPLC (C18、移動相: 水/アセトニトリル (0.1% TFA含有系))で精製した。得られた画分を濃縮し、炭酸水素ナトリウム水溶液で中和し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、溶媒を減圧下留去して標題化合物 (0.045 g) を得た。
1H NMR (300 MHz, CDCl3) δ 0.56-0.63 (2H, m), 0.88-0.97 (2H, m), 1.67-2.00 (5H, m), 2.21-2.33 (1H, m), 2.63-2.80 (2H, m), 3.05-3.18 (2H, m), 4.04-4.52 (4H, m), 5.18-5.50 (1H, m), 7.46-7.73 (2H, m), 8.30-8.61 (3H, m).
1)実施例1の化合物 30 mg
2)微粉末セルロース 10 mg
3)乳糖 19 mg
4)ステアリン酸マグネシウム 1 mg
計 60 mg
1)、2)、3)および4)を混合して、ゼラチンカプセルに充填する。
1)実施例1の化合物 30 g
2)乳糖 50 g
3)トウモロコシデンプン 15 g
4)カルボキシメチルセルロースカルシウム 44 g
5)ステアリン酸マグネシウム 1 g
1000錠 計 140 g
1)、2)、3)の全量および30gの4)を水で練合し、真空乾燥後、整粒を行う。この整粒末に14gの4)および1gの5)を混合し、打錠機により打錠する。このようにして、1錠あたり実施例1の化合物30mgを含有する錠剤1000錠を得る。
ヒト型CH24HをFreeStyle 293細胞で発現させるためのプラスミドDNAは以下のように作製した。Full-Length Mammalian Gene Collection No.4819975(Invitrogen社)を鋳型として、以下の2種類の合成DNA:
5’-GCCCCGGAGCCATGAGCCCCGGGCTG-3’(配列番号1)、および
5’-GTCCTGCCTGGAGGCCCCCTCAGCAG-3’(配列番号2)
を用いてPCRを行い、ヒト型CH24H(BC022539)の91-1625bpの領域を増幅した。得られた断片をTOPO TA Cloning Kit(Invitrogen社)を用いてクローニングした。得られた断片をBamHIとXhoIで切断したpcDNA3.1(+)にサブクローニングし、ヒト型CH24H発現用プラスミドDNA(pcDNA3.1(+)/hCH24H)とした。
ヒト型CH24Hの発現はFreeStyle 293 Expression System(Invitrogen社)を用いて行った。FreeStyle 293 Expression System添付のマニュアルに従い、試験例1で構築したヒト型CH24H発現用プラスミドDNA(pcDNA3.1(+)/hCH24H)を用いてFreeStyle293-F細胞による一過性発現を行った。トランスフェクションした後、37℃、8% CO2、125rpmで2日間振とう培養を行った。遠心分離により細胞を回収し、懸濁用緩衝液(100mMリン酸カリウム(pH7.4)、0.1mM EDTA、1mM DTT、20%グリセロール)に懸濁した。その懸濁物をポリトロンホモジナイザー(キネマチカ社製)で破砕し、9000×gで10分間遠心分離し、その上清を回収した。回収した上清をヒト型CH24Hライゼート標品として凍結(-80 ℃)保存した。
CH24H阻害活性の測定は、試験例2で調製したヒト型CH24Hライゼートを用い、コレステロールからCH24Hにより触媒されて生成する24-HCの生成量を被験化合物存在下で測定し、被験化合物非存在下と比較することで実施した。すなわち、各濃度の被験化合物溶液に反応緩衝液(0.1% BSAおよびComplete, EDTA-freeを含む50mMリン酸カリウム、pH7.4)およびヒト型CH24Hライゼートを加え混合した。次いで[14C]コレステロール(53mCi/mmol比活性)15μMを加え、37℃、5時間、CH24H反応を行い、反応終了後、クロロホルム/メタノール/蒸留水(2:2:1v/v)からなる停止液を加え、生成した24-HCを振とう抽出した。シリカゲル薄層クロマトグラフィー(酢酸エチル:トルエン=4:6)を行い、得られた14C-24HC画分をBAS2500(富士フイルム)で測定した。
阻害率(%)は被験化合物非存在下での放射活性に対する被験化合物存在下での放射活性比から算出した。結果を以下の表2に示す。
動物は6週齢の雌性C57BL/6Nマウスを使用した(各群3匹)。被験化合物をメチルセルロース[133-14255 WAKO]0.5%水溶液に1 mg/mLにて懸濁させ、マウスの体重測定後、1日1回、3日間強制経口反復投与を行った。3回目投与後16時間後に半脳を回収し、24-HC量を測定した。
脳の湿重量を計量後、4倍容の生理食塩水でホモジナイズを行い、この溶液を脳抽出物とした。脳抽出物に含まれる24-HCはアセトニトリル溶液(98%アセトニトリル、1.98%メタノール、0.02%蟻酸)で抽出し、HPLCにより定量した。結果は、24-HC量の平均値を算出後、コントロール群を100%とした時の相対値として示した。結果を以下の表3に示す。
動物は6週齢のTg2576マウスおよびその野生型マウスを使用した(各群10匹)。被験化合物をメチルセルロース[133-14255 WAKO]0.5%水溶液に3mg/mLにて懸濁させ、マウスの体重測定後、1日1回、10 mL/kgにて6週間強制経口反復投与を行い、その後、新奇物体認知試験を行った。新奇物体認知試験は下記にて実施した。獲得試行を行う前日に、照度を300 lxに設定した観察ボックスに同じケージのマウスを入れ、30分間馴化させ、馴化終了後に化合物を経口投与した。その翌日、獲得試行として同じ物体を2つ置いた観察ボックスにマウスを入れ、300 lx下で5分間の物体に対する接触回数及び接触時間を測定した。測定後に化合物を経口投与した。獲得試行の翌日に片方の物体を新奇物体に置換し、各物体に対する5分間の接触回数及び接触時間を測定した。本試験では金属製の円柱と陶器製三角錐を用いた。比較対象として、コントロール群(被験化合物の非処置群)、および、野生型マウスにおけるコントロール群を置いた。結果は、物体に対する総接触回数および時間に対する新奇物体への接触回数および時間の割合を%にて示した。結果を以下の表4に示す。
Claims (21)
- 式(I):
[式中、
X1は、炭素原子または窒素原子を示し;
環Aは、それぞれさらに置換されていてもよく、それぞれ架橋されていてもよい、
を示し;
R1は、置換されていてもよいC1-6アルキル基、置換されていてもよいヒドロキシ基、置換されていてもよいアミノ基、置換されていてもよい炭素環基、または置換されていてもよい複素環基を示すか、あるいはR1は環A上の原子と結合して、環Aとともに、それぞれ、オキソ基で置換され、かつさらに置換されていてもよい、スピロ環または縮合環を形成してもよく;
R2は、置換されていてもよいC6-14アリール基、または置換されていてもよい芳香族複素環基を示し;
R3は、X1が炭素原子の場合、水素原子または置換基を示し、X1が窒素原子の場合、存在しない。]
で表される化合物(ただし、tert-ブチル 4-(4-フェニルピリミジン-5-イル)ピペラジン-1-カルボキシラートを除く)またはその塩。 - R1が、
置換されていてもよいC1-6アルキル基、置換されていてもよいC1-6アルコキシ基、置換されていてもよいアミノ基、置換されていてもよいC3-8シクロアルキル基、置換されていてもよいC6-14アリール基、または置換されていてもよい非芳香族複素環基
である請求項1記載の化合物(ただし、tert-ブチル 4-(4-フェニルピリミジン-5-イル)ピペラジン-1-カルボキシラートを除く)またはその塩。 - R1が、
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基で置換されていてもよいC6-14アリール基、
(c)C6-14アリールオキシ基、
(d)C3-8シクロアルキル基、
(e)ピラゾリル基、
(f)インダゾリル基、および
(g)1ないし3個のオキソ基で置換されていてもよいジヒドロピリジル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(2)1ないし3個のC6-14アリール基で置換されていてもよいC1-6アルコキシ基、
(3)(a)(i)ハロゲン原子、
(ii)シアノ基、
(iii)C3-8シクロアルキル基、
(iv)ハロゲン原子およびC1-6アルコキシ基から選ばれる1ないし3個の置換基で置換されていてもよいC6-14アリール基、
(v)ピリジル基、および
(vi)1ないし3個のC1-6アルキル基で置換されていてもよいオキセタニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(b)1ないし3個のハロゲン原子で置換されていてもよいC3-8シクロアルキル基、
(c)C6-14アリール基、および
(d)1ないし3個のC1-6アルキル基でそれぞれ置換されていてもよい、テトラヒドロピラニル基、オキセタニル基、テトラヒドロフリル基もしくはピロリジニル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のC6-14アリール基で置換されていてもよいC3-8シクロアルキル基、
(5)C6-14アリール基、または
(6)(a)ハロゲン原子、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)C1-6アルキル基でモノまたはジ置換されていてもよいカルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(g)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルコキシ基、
(h)C1-6アルコキシ-カルボニル基、および
(i)1ないし3個のハロゲン原子で置換されていてもよいC6-14アリール基
から選択される1ないし5個の置換基でそれぞれ置換されていてもよい、3ないし8員の単環式非芳香族複素環基もしくは3,7-ジオキサ-9-アザビシクロ[3.3.1]ノニル基
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基でさらに置換されていてもよい2,8-ジアザスピロ[4.5]デカン環を形成し;
R2が、
(1)(a)ハロゲン原子、および
(b)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基
から選択される1ないし3個の置換基で置換されていてもよいC6-14アリール基、または
(2)(a)ハロゲン原子、
(b)シアノ基、
(c)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルキル基、および
(d)C3-8シクロアルキル基
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、5または6員の単環式芳香族複素環基もしくは8ないし12員の縮合芳香族複素環基であり;
X1が、炭素原子または窒素原子であり;
R3が、
(1)水素原子、または
(2)ハロゲン原子であり;かつ
環Aが、
(1)(a)ハロゲン原子、
(b)C1-6アルキル基、および
(c)オキソ基
から選択される1ないし3個の置換基でそれぞれさらに置換されていてもよい、
、または
(2)8-アザビシクロ[3.2.1]オクタン環、2,5-ジアザビシクロ[2.2.1]ヘプタン環、もしくは3-アザビシクロ[3.1.0]ヘキサン環
である請求項1記載の化合物(ただし、tert-ブチル 4-(4-フェニルピリミジン-5-イル)ピペラジン-1-カルボキシラートを除く)またはその塩。 - R1が、
(1)(a)シアノ基、
(b)1ないし3個のC1-6アルコキシ基で置換されていてもよいC6-14アリール基、
(c)C6-14アリールオキシ基、
(d)C3-8シクロアルキル基、
(e)ピラゾリル基、
(f)インダゾリル基、および
(g)1ないし3個のオキソ基で置換されていてもよいジヒドロピリジル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(2)1ないし3個のC6-14アリール基で置換されていてもよいC1-3アルコキシ基、
(3)(a)(i)ハロゲン原子、
(ii)シアノ基、
(iii)C3-8シクロアルキル基、
(iv)ハロゲン原子およびC1-6アルコキシ基から選ばれる1ないし3個の置換基で置換されていてもよいC6-14アリール基、
(v)ピリジル基、および
(vi)1ないし3個のC1-6アルキル基で置換されていてもよいオキセタニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(b)1ないし3個のハロゲン原子で置換されていてもよいC3-8シクロアルキル基、
(c)C6-14アリール基、および
(d)1ないし3個のC1-6アルキル基でそれぞれ置換されていてもよい、テトラヒドロピラニル基、オキセタニル基、テトラヒドロフリル基もしくはピロリジニル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、
(4)1ないし3個のC6-14アリール基で置換されていてもよいC3-8シクロアルキル基、
(5)C6-14アリール基、または
(6)(a)ハロゲン原子、
(b)シアノ基、
(c)ヒドロキシ基、
(d)オキソ基、
(e)C1-6アルキル基でモノまたはジ置換されていてもよいカルバモイル基、
(f)(i)ヒドロキシ基、および
(ii)C1-6アルコキシ基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(g)1ないし3個のハロゲン原子で置換されていてもよいC1-6アルコキシ基、
(h)C1-6アルコキシ-カルボニル基、および
(i)1ないし3個のハロゲン原子で置換されていてもよいC6-14アリール基
から選択される1ないし5個の置換基でそれぞれ置換されていてもよい、3ないし8員の単環式非芳香族複素環基もしくは3,7-ジオキサ-9-アザビシクロ[3.3.1]ノニル基
であるか、あるいはR1が環A上の原子と結合して環Aとともに、オキソで置換され、かつ1ないし3個のC1-6アルキル基でさらに置換されていてもよい2,8-ジアザスピロ[4.5]デカン環を形成する
請求項3記載の化合物またはその塩。 - R1が、
(1)(a)(i)ハロゲン原子、および
(ii)1ないし3個のハロゲン原子で置換されていてもよいフェニル基
から選ばれる1ないし3個の置換基で置換されていてもよいC1-6アルキル基、
(b) テトラヒドロピラニル基、および
(c) テトラヒドロフリル基
から選択される置換基でモノまたはジ置換されていてもよいアミノ基、または
(2)(a)ハロゲン原子、
(b)シアノ基、
(c)カルバモイル基、
(d)C1-6アルキル基、および
(e)C1-6アルコキシ基
から選択される1ないし5個の置換基でそれぞれ置換されていてもよい、アゼチジニル基もしくはピロリジニル基であり;
R2が、
(1)1ないし3個のハロゲン原子で置換されていてもよいフェニル基、または
(2)(a)ハロゲン原子、
(b)C1-6アルキル基、および
(c)シクロプロピル基
から選択される1ないし3個の置換基でそれぞれ置換されていてもよい、ピラゾリル基、チアゾリル基もしくはチアジアゾリル基であり;
X1が、炭素原子または窒素原子であり;
R3が、水素原子であり;かつ
環Aが、
である請求項1記載の化合物またはその塩。 - (2R)-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリルまたはその塩、
(2R)-1-((1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリルまたはその塩、
(2R)-4,4-ジフルオロ-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリルまたはその塩、
(3-フルオロアゼチジン-1-イル)(1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-イル)メタノンまたはその塩、
(1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)(3-フルオロアゼチジン-1-イル)メタノンまたはその塩、
(1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)((3S)-3-フルオロピロリジン-1-イル)メタノンまたはその塩、
(1-(4-(4-フルオロフェニル)ピリミジン-5-イル)ピペリジン-4-イル)((3S)-3-フルオロピロリジン-1-イル)メタノンまたはその塩、
N-ベンジル-N-(2-フルオロエチル)-4-(4-フェニルピリミジン-5-イル)ピペラジン-1-カルボキサミドまたはその塩、
N-(4-フルオロベンジル)-N-(2-フルオロエチル)-4-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペラジン-1-カルボキサミドまたはその塩、
((3S)-3-フルオロピロリジン-1-イル)(1-(4-(5-メチル-1,3-チアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノンまたはその塩、
(3-フルオロアゼチジン-1-イル)(1-(4-(5-メチル-1,3-チアゾール-2-イル)ピリジン-3-イル)ピペリジン-4-イル)メタノンまたはその塩、
(1-(4-(4-ブロモ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)(3-フルオロアゼチジン-1-イル)メタノンまたはその塩、または
(1-(4-(4-シクロプロピル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)(3-フルオロアゼチジン-1-イル)メタノンまたはその塩。 - (2R)-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリルまたはその塩。
- (2R)-1-((1-(4-(4-クロロ-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリルまたはその塩。
- (2R)-4,4-ジフルオロ-1-((1-(4-(4-メチル-1H-ピラゾール-1-イル)ピリジン-3-イル)ピペリジン-4-イル)カルボニル)ピロリジン-2-カルボニトリルまたはその塩。
- 請求項1記載の化合物またはその塩を含有してなる医薬。
- コレステロール24ヒドロキシラーゼ阻害剤である、請求項11記載の医薬。
- 癲癇または神経変性疾患の予防または治療剤である、請求項11記載の医薬。
- 神経変性疾患が、アルツハイマー病、軽度認知障害、ハンチントン病、パーキンソン病または多発性硬化症である、請求項13記載の医薬。
- 癲癇または神経変性疾患の予防または治療に使用するための、請求項1記載の化合物またはその塩。
- 神経変性疾患が、アルツハイマー病、軽度認知障害、ハンチントン病、パーキンソン病または多発性硬化症である、請求項15記載の化合物またはその塩。
- 請求項1記載の化合物またはその塩を哺乳動物に有効量投与することを特徴とする、該哺乳動物におけるコレステロール24ヒドロキシラーゼの阻害方法。
- 請求項1記載の化合物またはその塩を哺乳動物に有効量投与することを特徴とする、該哺乳動物における癲癇または神経変性疾患の予防または治療方法。
- 神経変性疾患が、アルツハイマー病、軽度認知障害、ハンチントン病、パーキンソン病または多発性硬化症である、請求項18記載の予防または治療方法。
- 癲癇または神経変性疾患の予防または治療剤を製造するための、請求項1記載の化合物またはその塩の使用。
- 神経変性疾患が、アルツハイマー病、軽度認知障害、ハンチントン病、パーキンソン病または多発性硬化症である、請求項20記載の使用。
Priority Applications (22)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| MX2015007495A MX2015007495A (es) | 2012-12-11 | 2013-12-10 | Compuesto heterociclico. |
| UAA201506890A UA115156C2 (uk) | 2012-12-11 | 2013-12-10 | Гетероциклічна сполука |
| CR20150364A CR20150364A (es) | 2012-12-11 | 2013-12-10 | Compuesto heterociclico |
| KR1020157018652A KR20150093240A (ko) | 2012-12-11 | 2013-12-10 | 헤테로시클릭 화합물 |
| AU2013358112A AU2013358112B2 (en) | 2012-12-11 | 2013-12-10 | Heterocyclic compound |
| JP2014552058A JP6224004B2 (ja) | 2012-12-11 | 2013-12-10 | 複素環化合物 |
| EP13862252.7A EP2933247B1 (en) | 2012-12-11 | 2013-12-10 | Heterocyclic compound |
| EA201591122A EA029056B1 (ru) | 2012-12-11 | 2013-12-10 | Гетероциклическое соединение |
| US14/650,429 US9643957B2 (en) | 2012-12-11 | 2013-12-10 | Heterocyclic compounds having cholesterol 24-hydroxylase activity |
| CN201380072647.9A CN104981457B (zh) | 2012-12-11 | 2013-12-10 | 杂环化合物 |
| ES13862252T ES2695350T3 (es) | 2012-12-11 | 2013-12-10 | Compuesto heterocíclico |
| MA38245A MA38245B1 (fr) | 2012-12-11 | 2013-12-10 | Nouveaux composes heterocycliques et leurs compostions pour la prevention et le traitement de maladies telles que l'epilepsie et l’alzheimer |
| HK15111402.2A HK1210769A1 (en) | 2012-12-11 | 2013-12-10 | Heterocyclic compound |
| SG11201504516PA SG11201504516PA (en) | 2012-12-11 | 2013-12-10 | Heterocyclic compound |
| CA2894492A CA2894492A1 (en) | 2012-12-11 | 2013-12-10 | Heterocyclic compound |
| TW103119854A TW201536758A (zh) | 2013-10-07 | 2014-06-09 | 雜環化合物 |
| UY0001035603A UY35603A (es) | 2013-10-07 | 2014-06-10 | Compuesto heterocíclico |
| TNP2015000245A TN2015000245A1 (en) | 2012-12-11 | 2015-06-03 | Heterocyclic compound |
| IL239278A IL239278B (en) | 2012-12-11 | 2015-06-08 | Compound containing pyridine or pyrimidine and non-aryl heterocyclic amine, drug, and compounds for use in the prevention or treatment of epilepsy or neurodegenerative disease |
| PH12015501316A PH12015501316A1 (en) | 2012-12-11 | 2015-06-09 | Heterocyclic compound |
| ZA2015/04980A ZA201504980B (en) | 2012-12-11 | 2015-07-10 | Heterocyclic compound |
| US15/467,548 US10112956B2 (en) | 2012-12-11 | 2017-03-23 | Heterocyclic compounds having cholesterol 24-hydroxylase activity |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012-270445 | 2012-12-11 | ||
| JP2012270445 | 2012-12-11 | ||
| JP2013-210439 | 2013-10-07 | ||
| JP2013210439 | 2013-10-07 |
Related Child Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US14/650,429 A-371-Of-International US9643957B2 (en) | 2012-12-11 | 2013-12-10 | Heterocyclic compounds having cholesterol 24-hydroxylase activity |
| US15/467,548 Continuation US10112956B2 (en) | 2012-12-11 | 2017-03-23 | Heterocyclic compounds having cholesterol 24-hydroxylase activity |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2014092100A1 true WO2014092100A1 (ja) | 2014-06-19 |
Family
ID=50934388
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2013/083140 Ceased WO2014092100A1 (ja) | 2012-12-11 | 2013-12-10 | 複素環化合物 |
Country Status (27)
| Country | Link |
|---|---|
| US (2) | US9643957B2 (ja) |
| EP (1) | EP2933247B1 (ja) |
| JP (1) | JP6224004B2 (ja) |
| KR (1) | KR20150093240A (ja) |
| CN (1) | CN104981457B (ja) |
| AP (1) | AP2015008591A0 (ja) |
| AU (1) | AU2013358112B2 (ja) |
| CA (1) | CA2894492A1 (ja) |
| CL (1) | CL2015001599A1 (ja) |
| CR (1) | CR20150364A (ja) |
| DO (1) | DOP2015000140A (ja) |
| EA (1) | EA029056B1 (ja) |
| EC (1) | ECSP15028917A (ja) |
| ES (1) | ES2695350T3 (ja) |
| GE (1) | GEP201706756B (ja) |
| HK (1) | HK1210769A1 (ja) |
| HU (1) | HUE039922T2 (ja) |
| IL (1) | IL239278B (ja) |
| MX (1) | MX2015007495A (ja) |
| PE (1) | PE20151162A1 (ja) |
| PH (1) | PH12015501316A1 (ja) |
| SG (1) | SG11201504516PA (ja) |
| TN (1) | TN2015000245A1 (ja) |
| TR (1) | TR201814885T4 (ja) |
| UA (1) | UA115156C2 (ja) |
| WO (1) | WO2014092100A1 (ja) |
| ZA (1) | ZA201504980B (ja) |
Cited By (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015190613A1 (en) | 2014-06-09 | 2015-12-17 | Takeda Pharmaceutical Company Limited | Radiolabeled compounds |
| US9598398B2 (en) | 2013-04-04 | 2017-03-21 | Takeda Pharmaceutical Company Limited | Heterocyclic compound |
| US9624184B2 (en) | 2013-04-04 | 2017-04-18 | Takeda Pharmaceutical Company Limited | Heterocyclic compound |
| US9951063B2 (en) | 2014-03-24 | 2018-04-24 | Idorsia Pharmaceuticals Ltd | 8-(piperazin-1-yl)-1,2,3,4-tetrahydro-isoquinoline derivatives |
| US10047080B2 (en) | 2015-01-15 | 2018-08-14 | Idorsia Pharmaceuticals Ltd. | (R)-2-methyl-piperazine derivatives as CXCR3 receptor modulators |
| JP2018522831A (ja) * | 2015-06-01 | 2018-08-16 | リューゲン ホールディングス (ケイマン) リミテッド | Nr2bnmdaレセプターアンタゴニストとしての3,3−ジフルオロピペリジンカルバメート複素環式化合物 |
| US10053457B2 (en) | 2015-01-15 | 2018-08-21 | Idorsia Pharmaceuticals Ltd. | Hydroxyalkyl-piperazine derivatives as CXCR3 receptor modulators |
| US10259807B2 (en) | 2013-07-22 | 2019-04-16 | Idorsia Pharmaceuticals Ltd. | 1-(piperazin-1-yl)-2-([1,2,4]triazol-1-yl)-ethanone derivatives |
| JP2020532508A (ja) * | 2017-08-31 | 2020-11-12 | 武田薬品工業株式会社 | Cns状態の治療 |
| JP2020533303A (ja) * | 2017-09-08 | 2020-11-19 | ピーアイ インダストリーズ リミテッドPi Industries Ltd | 新規な殺菌性複素環化合物 |
| US11000526B2 (en) | 2016-11-22 | 2021-05-11 | Rugen Holdings (Cayman) Limited | Treatment of autism spectrum disorders, obsessive-compulsive disorder and anxiety disorders |
| JP2022533436A (ja) * | 2019-05-24 | 2022-07-22 | セージ セラピューティクス, インコーポレイテッド | 化合物、組成物、および使用方法 |
| WO2022261510A1 (en) | 2021-06-11 | 2022-12-15 | Sage Therapeutics, Inc. | Neuroactive steroid for the treatment of alzheimer's disease |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TWI568722B (zh) | 2012-06-15 | 2017-02-01 | 葛蘭馬克製藥公司 | 作爲mPGES-1抑制劑之三唑酮化合物 |
| PE20151162A1 (es) * | 2012-12-11 | 2015-08-28 | Takeda Pharmaceutical | Compuestos heterociclicos inhibidores del colesterol 24-hidroxilasa (ch24h) |
| WO2020027344A1 (en) | 2018-08-03 | 2020-02-06 | Takeda Pharmaceutical Company Limited | Ch24h inhibitors for mdd use |
| EP3852757A1 (en) * | 2018-09-20 | 2021-07-28 | Takeda Pharmaceutical Company Limited | Ch24h inhibitors for pain use |
| WO2021165927A1 (en) * | 2020-02-21 | 2021-08-26 | Wockhardt Bio Ag | 2-cyanopyrroldines, -piperidines or -dazepines as hyperglycemic agents |
| AU2021324684A1 (en) * | 2020-08-11 | 2023-04-20 | Board Of Trustees Of Michigan State University | Proteasome enhancers and uses thereof |
| US12029718B2 (en) | 2021-11-09 | 2024-07-09 | Cct Sciences, Llc | Process for production of essentially pure delta-9-tetrahydrocannabinol |
| EP4308555A4 (en) * | 2021-03-18 | 2025-07-30 | Sironax Ltd | RECEPTOR-INTERACTING PROTEIN-1 INHIBITORS, PREPARATIONS AND USES THEREOF |
Citations (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH11514333A (ja) | 1995-03-14 | 1999-12-07 | プレーシス ファーマスーティカルズ インコーポレイテッド | アミロイドの凝集の調節剤 |
| WO2001000663A2 (en) | 1999-06-28 | 2001-01-04 | Oklahoma Medical Research Foundation | Catalytically active recombinant memapsin and methods of use thereof |
| JP2001500852A (ja) | 1996-08-27 | 2001-01-23 | プレーシス ファーマスーティカルズ インコーポレイテッド | D―アミノ酸を含むβ―アミロイドペプチド凝集のモジュレーター |
| WO2001082925A1 (en) | 2000-04-28 | 2001-11-08 | Takeda Chemical Industries, Ltd. | Melanin concentrating hormone antagonists |
| WO2001087834A1 (en) | 2000-05-16 | 2001-11-22 | Takeda Chemical Industries, Ltd. | Melanin-concentrating hormone antagonist |
| WO2007127635A2 (en) | 2006-04-25 | 2007-11-08 | Bristol-Myers Squibb Company | Diketo-piperazine and piperidine derivatives as antiviral agents |
| WO2010110400A1 (ja) | 2009-03-26 | 2010-09-30 | 武田薬品工業株式会社 | 複素環化合物 |
| JP2010248183A (ja) | 2009-03-26 | 2010-11-04 | Takeda Chem Ind Ltd | 複素環化合物 |
| WO2011016559A1 (ja) * | 2009-08-07 | 2011-02-10 | 武田薬品工業株式会社 | 複素環化合物およびその用途 |
| WO2013146969A1 (ja) * | 2012-03-29 | 2013-10-03 | 第一三共株式会社 | 新規二置換シクロヘキサン誘導体 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005019200A2 (en) * | 2003-08-14 | 2005-03-03 | Icos Corporation | Aryl piperidine derivatives as vla-1 integrin antagonists and uses thereof |
| GB0325956D0 (en) | 2003-11-06 | 2003-12-10 | Addex Pharmaceuticals Sa | Novel compounds |
| AU2005249494A1 (en) * | 2004-05-28 | 2005-12-15 | Vertex Pharmaceuticals Incorporated | Modulators of muscarinic receptors |
| GB0510143D0 (en) | 2005-05-18 | 2005-06-22 | Addex Pharmaceuticals Sa | Novel compounds A1 |
| CN101432278B (zh) * | 2006-04-25 | 2012-11-28 | 布里斯托尔-迈尔斯斯奎布公司 | 作为抗病毒剂的二酮基哌嗪和哌啶衍生物 |
| PL2763979T3 (pl) | 2011-10-07 | 2019-06-28 | Takeda Pharmaceutical Company Limited | Związki 1-arylokarbonyl-4-oksy-piperydynowe użyteczne do leczenia chorób neurodegeneracyjnych |
| US9296746B2 (en) | 2012-10-16 | 2016-03-29 | Takeda Pharmaceutical Company Limited | Heterocyclic compound |
| PE20151162A1 (es) * | 2012-12-11 | 2015-08-28 | Takeda Pharmaceutical | Compuestos heterociclicos inhibidores del colesterol 24-hidroxilasa (ch24h) |
| JP6272832B2 (ja) | 2013-04-04 | 2018-01-31 | 武田薬品工業株式会社 | 複素環化合物 |
| EP3152198B1 (en) * | 2014-06-09 | 2019-02-27 | Takeda Pharmaceutical Company Limited | Radiolabeled compounds |
-
2013
- 2013-12-10 PE PE2015000884A patent/PE20151162A1/es not_active Application Discontinuation
- 2013-12-10 TR TR2018/14885T patent/TR201814885T4/tr unknown
- 2013-12-10 ES ES13862252T patent/ES2695350T3/es active Active
- 2013-12-10 MX MX2015007495A patent/MX2015007495A/es unknown
- 2013-12-10 HK HK15111402.2A patent/HK1210769A1/en unknown
- 2013-12-10 GE GEAP201313877A patent/GEP201706756B/en unknown
- 2013-12-10 AP AP2015008591A patent/AP2015008591A0/xx unknown
- 2013-12-10 EP EP13862252.7A patent/EP2933247B1/en active Active
- 2013-12-10 UA UAA201506890A patent/UA115156C2/uk unknown
- 2013-12-10 SG SG11201504516PA patent/SG11201504516PA/en unknown
- 2013-12-10 CN CN201380072647.9A patent/CN104981457B/zh not_active Expired - Fee Related
- 2013-12-10 KR KR1020157018652A patent/KR20150093240A/ko not_active Withdrawn
- 2013-12-10 US US14/650,429 patent/US9643957B2/en not_active Expired - Fee Related
- 2013-12-10 AU AU2013358112A patent/AU2013358112B2/en not_active Ceased
- 2013-12-10 CA CA2894492A patent/CA2894492A1/en not_active Abandoned
- 2013-12-10 CR CR20150364A patent/CR20150364A/es unknown
- 2013-12-10 EA EA201591122A patent/EA029056B1/ru not_active IP Right Cessation
- 2013-12-10 WO PCT/JP2013/083140 patent/WO2014092100A1/ja not_active Ceased
- 2013-12-10 HU HUE13862252A patent/HUE039922T2/hu unknown
- 2013-12-10 JP JP2014552058A patent/JP6224004B2/ja active Active
-
2015
- 2015-06-03 TN TNP2015000245A patent/TN2015000245A1/fr unknown
- 2015-06-08 IL IL239278A patent/IL239278B/en not_active IP Right Cessation
- 2015-06-09 PH PH12015501316A patent/PH12015501316A1/en unknown
- 2015-06-09 CL CL2015001599A patent/CL2015001599A1/es unknown
- 2015-06-10 DO DO2015000140A patent/DOP2015000140A/es unknown
- 2015-07-06 EC ECIEPI201528917A patent/ECSP15028917A/es unknown
- 2015-07-10 ZA ZA2015/04980A patent/ZA201504980B/en unknown
-
2017
- 2017-03-23 US US15/467,548 patent/US10112956B2/en active Active
Patent Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH11514333A (ja) | 1995-03-14 | 1999-12-07 | プレーシス ファーマスーティカルズ インコーポレイテッド | アミロイドの凝集の調節剤 |
| JP2001500852A (ja) | 1996-08-27 | 2001-01-23 | プレーシス ファーマスーティカルズ インコーポレイテッド | D―アミノ酸を含むβ―アミロイドペプチド凝集のモジュレーター |
| WO2001000663A2 (en) | 1999-06-28 | 2001-01-04 | Oklahoma Medical Research Foundation | Catalytically active recombinant memapsin and methods of use thereof |
| WO2001082925A1 (en) | 2000-04-28 | 2001-11-08 | Takeda Chemical Industries, Ltd. | Melanin concentrating hormone antagonists |
| WO2001087834A1 (en) | 2000-05-16 | 2001-11-22 | Takeda Chemical Industries, Ltd. | Melanin-concentrating hormone antagonist |
| WO2007127635A2 (en) | 2006-04-25 | 2007-11-08 | Bristol-Myers Squibb Company | Diketo-piperazine and piperidine derivatives as antiviral agents |
| JP2009535352A (ja) * | 2006-04-25 | 2009-10-01 | ブリストル−マイヤーズ スクイブ カンパニー | 抗ウイルス薬としてのジケト−ピペラジンおよびピペリジン誘導体 |
| WO2010110400A1 (ja) | 2009-03-26 | 2010-09-30 | 武田薬品工業株式会社 | 複素環化合物 |
| JP2010248183A (ja) | 2009-03-26 | 2010-11-04 | Takeda Chem Ind Ltd | 複素環化合物 |
| WO2011016559A1 (ja) * | 2009-08-07 | 2011-02-10 | 武田薬品工業株式会社 | 複素環化合物およびその用途 |
| WO2013146969A1 (ja) * | 2012-03-29 | 2013-10-03 | 第一三共株式会社 | 新規二置換シクロヘキサン誘導体 |
Non-Patent Citations (51)
| Title |
|---|
| ""IYAKUHIN no KAIHATSU (Development of Pharmaceuticals)"", vol. 7, 1990, HIROKAWA SHOTEN, article "Design of Molecules,", pages: 163 - 198 |
| "Jikken Kagaku Kouza (Courses in Experimental Chemistry", vol. 14, pages: 251 - 253 |
| "Jikken Kagaku Kouza", vol. 19, pages: 273 - 274 |
| "Journal of Neurotrauma", J. NEUROTRAUMA, vol. 25, 2008, pages 1087 - 1098 |
| "Journal of Psychiatry Neuroscience", J. PSYCHIATRY NEUROSCI, vol. 36, 2011, pages 47 - 55 |
| BIOCHEM. J., vol. 340, no. 1, 1999, pages 283 - 289 |
| BRAIN RES., vol. 818, 1999, pages 171 - 175 |
| BRAIN RESEARCH (BRAIN RES., vol. 818, 1999, pages 171 - 175 |
| BRITISH JOURNAL OF CANCER, vol. 68, 1993, pages 314 - 318 |
| BRITISH JOURNAL OF PHARMACOLOGY, vol. 149, 2006, pages 998 - 1012 |
| CANCER RESEARCH, vol. 49, 1989, pages 5935 - 5939 |
| EPILEPSIA, vol. 47, 2006, pages 867 - 872 |
| EPILEPSIA, vol. 52, no. 1, 2011, pages 39 - 46 |
| GLIA, vol. 50, 2005, pages 427 - 434 |
| INVEST. OPHTHALMOL. VIS. SCI., vol. 50, 2009, pages 5712 - 5717 |
| INVESTIGATIVE OPHTHALMOLOGY & VISUAL SCIENCE (INVEST. OPTHALMOL. VIS. SCI., vol. 50, 2009, pages 5712 - 5717 |
| J. BIOL. CHEM., vol. 279, 2004, pages 34674 - 34681 |
| J. NEUROL. NEUROSURG. PSYCHIATRY, vol. 48, 1985, pages 459 - 468 |
| J. NEUROL., vol. 65, 2006, pages 652 - 663 |
| J. NEUROSCI. RES., vol. 85, 2007, pages 1499 - 1505 |
| J. NEUROSCI., vol. 29, 2012, pages 3453 - 3462 |
| J. NEUROTRAUMA, vol. 25, 2008, pages 1087 - 1098 |
| J. PSYCHIATRY NEUROSCI., vol. 36, 2011, pages 47 - 55 |
| JOURNAL OF CLINICAL ONCOLOGY, vol. 12, 1994, pages 213 - 225 |
| JOURNAL OF NEUROLOGY (J. NEUROL., vol. 65, 2006, pages 652 - 663 |
| JOURNAL OF NEUROLOGY NEUROSURGERY PSYCHIATRY (J. NEUROL. NEUROSURG. PSYCHIATRY, vol. 48, 1985, pages 459 - 468 |
| JOURNAL OF NEUROSCIENCE (J. NEUROSCI., vol. 29, 2012, pages 3453 - 3462 |
| JOURNAL OF NEUROSCIENCE RESEARCH (J. NEUROSCI. RES., vol. 85, 2007, pages 1499 - 1505 |
| JOURNAL OF THE BIOLOGICAL CHEMISTRY (J. BIOL. CHEM., vol. 279, 2004, pages 34674 - 34681 |
| MOL. NEURODEGENERATION, vol. 4, 2009, pages 47 - 59 |
| MOL. PSYCHIATRY, vol. 8, 2003, pages 635 - 638 |
| MOLECULAR NEURODEGENERATION (MOL. NEURODEGENERATION, vol. 4, 2009, pages 47 - 59 |
| MOLECULAR PSYCHIATRY (MOL. PSYCHIATRY, vol. 8, 2003, pages 635 - 638 |
| NEUROBIOL. AGING, vol. 24, 2003, pages 421 - 426 |
| NEUROBIOLOGY OF AGING (NEUROBIOL. AGING, vol. 24, 2003, pages 421 - 426 |
| NEUROREPORT, vol. 16, 2005, pages 909 - 913 |
| NEUROSCI. LETT., vol. 324, 2002, pages 83 - 85 |
| NEUROSCI. LETT., vol. 328, 2002, pages 9 - 12 |
| NEUROSCI. LETT., vol. 331, 2002, pages 163 - 166 |
| NEUROSCI. LETT., vol. 397, 2006, pages 83 - 87 |
| NEUROSCIENCE LETTERS (NEUROSCI. LETT., vol. 324, 2002, pages 83 - 85 |
| NEUROSCIENCE LETTERS (NEUROSCI. LETT., vol. 328, 2002, pages 9 - 12 |
| NEUROSCIENCE LETTERS (NEUROSCI. LETT., vol. 331, 2002, pages 163 - 166 |
| NEUROSCIENCE LETTERS (NEUROSCI. LETT., vol. 397, 2006, pages 83 - 87 |
| NEUROSCIENCE, vol. 164, 2009, pages 398 - 403 |
| PROC. NATL. ACAD. SCI. USA, vol. 102, 2005, pages 8333 - 8338 |
| PROCEEDINGS OF THE NATIONAL ACADEMY OF SCIENCES USA (PROC. NATL. ACAD. SCI. USA, vol. 102, 2005, pages 8333 - 8338 |
| PSYCHONEUROENDOCRINOLOGY, vol. 28, 2003, pages 83 - 96 |
| SCIENCE, vol. 261, 1993, pages 921 - 923 |
| See also references of EP2933247A4 |
| THEODORA W. GREENE; PETER G. M. WUTS: "Protective Groups in Organic Synthesis, 3rd Ed", 1999, JOHN WILEY AND SONS, INC. |
Cited By (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9598398B2 (en) | 2013-04-04 | 2017-03-21 | Takeda Pharmaceutical Company Limited | Heterocyclic compound |
| US9624184B2 (en) | 2013-04-04 | 2017-04-18 | Takeda Pharmaceutical Company Limited | Heterocyclic compound |
| US10259807B2 (en) | 2013-07-22 | 2019-04-16 | Idorsia Pharmaceuticals Ltd. | 1-(piperazin-1-yl)-2-([1,2,4]triazol-1-yl)-ethanone derivatives |
| US9951063B2 (en) | 2014-03-24 | 2018-04-24 | Idorsia Pharmaceuticals Ltd | 8-(piperazin-1-yl)-1,2,3,4-tetrahydro-isoquinoline derivatives |
| US9963443B2 (en) | 2014-06-09 | 2018-05-08 | Takeda Pharmaceutical Company Limited | Radiolabeled compounds |
| WO2015190613A1 (en) | 2014-06-09 | 2015-12-17 | Takeda Pharmaceutical Company Limited | Radiolabeled compounds |
| US10047080B2 (en) | 2015-01-15 | 2018-08-14 | Idorsia Pharmaceuticals Ltd. | (R)-2-methyl-piperazine derivatives as CXCR3 receptor modulators |
| US10053457B2 (en) | 2015-01-15 | 2018-08-21 | Idorsia Pharmaceuticals Ltd. | Hydroxyalkyl-piperazine derivatives as CXCR3 receptor modulators |
| JP2018522831A (ja) * | 2015-06-01 | 2018-08-16 | リューゲン ホールディングス (ケイマン) リミテッド | Nr2bnmdaレセプターアンタゴニストとしての3,3−ジフルオロピペリジンカルバメート複素環式化合物 |
| US11136328B2 (en) | 2015-06-01 | 2021-10-05 | Rugen Holdings (Cayman) Limited | 3,3-difluoropiperidine carbamate heterocyclic compounds as NR2B NMDA receptor antagonists |
| US12527799B2 (en) | 2016-11-22 | 2026-01-20 | Rugen Holdings (Cayman) Limited | Treatment of autism spectrum disorders, obsessive-compulsive disorder and anxiety disorders |
| US11752155B2 (en) | 2016-11-22 | 2023-09-12 | Rugen Holdings (Cayman) Limited | Treatment of autism spectrum disorders, obsessive-compulsive disorder and anxiety disorders |
| US11000526B2 (en) | 2016-11-22 | 2021-05-11 | Rugen Holdings (Cayman) Limited | Treatment of autism spectrum disorders, obsessive-compulsive disorder and anxiety disorders |
| JP7196157B2 (ja) | 2017-08-31 | 2022-12-26 | 武田薬品工業株式会社 | Cns状態の治療 |
| JP2023027267A (ja) * | 2017-08-31 | 2023-03-01 | 武田薬品工業株式会社 | Cns状態の治療 |
| JP7469445B2 (ja) | 2017-08-31 | 2024-04-16 | 武田薬品工業株式会社 | Cns状態の治療 |
| JP2020532508A (ja) * | 2017-08-31 | 2020-11-12 | 武田薬品工業株式会社 | Cns状態の治療 |
| JP2020533303A (ja) * | 2017-09-08 | 2020-11-19 | ピーアイ インダストリーズ リミテッドPi Industries Ltd | 新規な殺菌性複素環化合物 |
| JP2022533436A (ja) * | 2019-05-24 | 2022-07-22 | セージ セラピューティクス, インコーポレイテッド | 化合物、組成物、および使用方法 |
| JP7687964B2 (ja) | 2019-05-24 | 2025-06-03 | セージ セラピューティクス, インコーポレイテッド | 化合物、組成物、および使用方法 |
| WO2022261510A1 (en) | 2021-06-11 | 2022-12-15 | Sage Therapeutics, Inc. | Neuroactive steroid for the treatment of alzheimer's disease |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6224004B2 (ja) | 複素環化合物 | |
| US11174272B2 (en) | 1-arylcarbonyl-4-oxy-piperidine compounds useful for the treatment of neurodegenerative diseases | |
| JP6272832B2 (ja) | 複素環化合物 | |
| EP2927229B1 (en) | Benzene-fused 5-membered nitrogen-containing heteroaromatic compounds useful for prophylaxis or treatment of neurodegenerative diseases or epilepsy | |
| JP6272833B2 (ja) | 複素環化合物 | |
| TW201536758A (zh) | 雜環化合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 139350140003002551 Country of ref document: IR |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 13862252 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2014552058 Country of ref document: JP Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 239278 Country of ref document: IL Ref document number: 14650429 Country of ref document: US |
|
| ENP | Entry into the national phase |
Ref document number: 2894492 Country of ref document: CA |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 12015501316 Country of ref document: PH |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 000884-2015 Country of ref document: PE Ref document number: 2013862252 Country of ref document: EP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: MX/A/2015/007495 Country of ref document: MX |
|
| ENP | Entry into the national phase |
Ref document number: 13877 Country of ref document: GE Kind code of ref document: P |
|
| WWE | Wipo information: entry into national phase |
Ref document number: DZP2015000407 Country of ref document: DZ Ref document number: 15157083 Country of ref document: CO Ref document number: IDP00201504217 Country of ref document: ID Ref document number: 38245 Country of ref document: MA |
|
| WWE | Wipo information: entry into national phase |
Ref document number: CR2015-000364 Country of ref document: CR |
|
| ENP | Entry into the national phase |
Ref document number: 20157018652 Country of ref document: KR Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 201591122 Country of ref document: EA Ref document number: A201506890 Country of ref document: UA |
|
| ENP | Entry into the national phase |
Ref document number: 2013358112 Country of ref document: AU Date of ref document: 20131210 Kind code of ref document: A |
|
| REG | Reference to national code |
Ref country code: BR Ref legal event code: B01A Ref document number: 112015013314 Country of ref document: BR |
|
| ENP | Entry into the national phase |
Ref document number: 112015013314 Country of ref document: BR Kind code of ref document: A2 Effective date: 20150608 |