WO2014094961A1 - Metallkomplexe - Google Patents
Metallkomplexe Download PDFInfo
- Publication number
- WO2014094961A1 WO2014094961A1 PCT/EP2013/003581 EP2013003581W WO2014094961A1 WO 2014094961 A1 WO2014094961 A1 WO 2014094961A1 EP 2013003581 W EP2013003581 W EP 2013003581W WO 2014094961 A1 WO2014094961 A1 WO 2014094961A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- formula
- atoms
- group
- radicals
- substituted
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- 0 *C(c1cnccc11)=C(*)N(C=C2)C1=NC2=O Chemical compound *C(c1cnccc11)=C(*)N(C=C2)C1=NC2=O 0.000 description 11
- SPFNTHHEJJFGJK-UHFFFAOYSA-N CC(C)(C)c1cncc2cccnc12 Chemical compound CC(C)(C)c1cncc2cccnc12 SPFNTHHEJJFGJK-UHFFFAOYSA-N 0.000 description 1
- PKFMOJLTFPGBED-UHFFFAOYSA-N CC(C)(C1C(N)=O)OC(C)(C)C1=O Chemical compound CC(C)(C1C(N)=O)OC(C)(C)C1=O PKFMOJLTFPGBED-UHFFFAOYSA-N 0.000 description 1
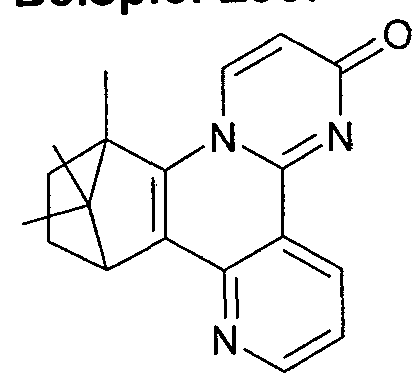
- CCIXHYRORIWPNP-UHFFFAOYSA-N CC(C)Cc1c(C=CN(C(C(C)(C)C)=C2)C3=NC2=O)c3ccn1 Chemical compound CC(C)Cc1c(C=CN(C(C(C)(C)C)=C2)C3=NC2=O)c3ccn1 CCIXHYRORIWPNP-UHFFFAOYSA-N 0.000 description 1
- JZDLCHLLTUUKLU-UHFFFAOYSA-N CC1(C)OC(C)(C)C(N(c(cccc2)c2-c2c3ccc(-c4ccccc4)n2)C3=N2)=C1C2=O Chemical compound CC1(C)OC(C)(C)C(N(c(cccc2)c2-c2c3ccc(-c4ccccc4)n2)C3=N2)=C1C2=O JZDLCHLLTUUKLU-UHFFFAOYSA-N 0.000 description 1
- OXVCHCDTOWTARD-UHFFFAOYSA-N COC1C(CC2)CCC2C1 Chemical compound COC1C(CC2)CCC2C1 OXVCHCDTOWTARD-UHFFFAOYSA-N 0.000 description 1
- HJDLKHXAQXGASW-UHFFFAOYSA-N Clc1nc(cccc2)c2c2c1ccc(-c1ccccc1)n2 Chemical compound Clc1nc(cccc2)c2c2c1ccc(-c1ccccc1)n2 HJDLKHXAQXGASW-UHFFFAOYSA-N 0.000 description 1
- SUOCHTKNURHDDX-UHFFFAOYSA-N O=C1N=C(c2cccnc2C=C2)N2C=C1 Chemical compound O=C1N=C(c2cccnc2C=C2)N2C=C1 SUOCHTKNURHDDX-UHFFFAOYSA-N 0.000 description 1
- FQYQVJRYSJSVLE-UHFFFAOYSA-N O=CCC(Nc1nccc2ncccc12)=O Chemical compound O=CCC(Nc1nccc2ncccc12)=O FQYQVJRYSJSVLE-UHFFFAOYSA-N 0.000 description 1
- BWSIGHHUTNIABV-UHFFFAOYSA-N OC1(C2)C2(C2)C(C3)C2CC3C1 Chemical compound OC1(C2)C2(C2)C(C3)C2CC3C1 BWSIGHHUTNIABV-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table
- C07F15/0006—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table compounds of the platinum group
- C07F15/0033—Iridium compounds
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent materials, e.g. electroluminescent or chemiluminescent
- C09K11/02—Use of particular materials as binders, particle coatings or suspension media therefor
- C09K11/025—Use of particular materials as binders, particle coatings or suspension media therefor non-luminescent particle coatings or suspension media
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent materials, e.g. electroluminescent or chemiluminescent
- C09K11/06—Luminescent materials, e.g. electroluminescent or chemiluminescent containing organic luminescent materials
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/12—Light sources with substantially two-dimensional [2D] radiating surfaces
- H05B33/14—Light sources with substantially two-dimensional [2D] radiating surfaces characterised by the chemical or physical composition or the arrangement of the electroluminescent material, or by the simultaneous addition of the electroluminescent material in or onto the light source
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
- H10K85/342—Transition metal complexes, e.g. Ru(II)polypyridine complexes comprising iridium
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1007—Non-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1059—Heterocyclic compounds characterised by ligands containing three nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/18—Metal complexes
- C09K2211/185—Metal complexes of the platinum group, i.e. Os, Ir, Pt, Ru, Rh or Pd
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Definitions
- iridium complexes are used in phosphorescent OLEDs as triplet emitters in particular.
- iridium complexes are known in which the ligand contains at least one carbonyl group.
- further improvements are desirable in the case of phosphorescent emitters.
- adjacent groups X means that groups X in the structure are directly bonded to each other.
- aryl group or heteroaryl either a simple aromatic cycle, ie benzene, or a simple heteroaromatic cycle, for example pyridine, pyrimidine, thiophene, etc., or a fused aryl or heteroaryl group, for example naphthalene, anthracene, phenanthrene, quinoline, isoquinoline, etc., understood.
- 4,5,9,10-tetraazaperylene pyrazine, phenazine, phenoxazine, phenothiazine, fluorubin, naphthyridine, azacarbazole, benzocarboline, phenanthroline, 1, 2,3-triazole, 1, 2,4-triazole, benzotriazole, 1, 2, 3-oxadiazole, 1, 2,4-oxadiazole, 1, 2,5-oxadiazole, 1, 3,4-oxadiazole, 1, 2,3-thiadiazole, 1, 2,4-thiadiazole, 1, 2,5- Thiadiazole, 1, 3,4-thiadiazole, 1, 3,5-triazine, 1, 2,4-triazine,
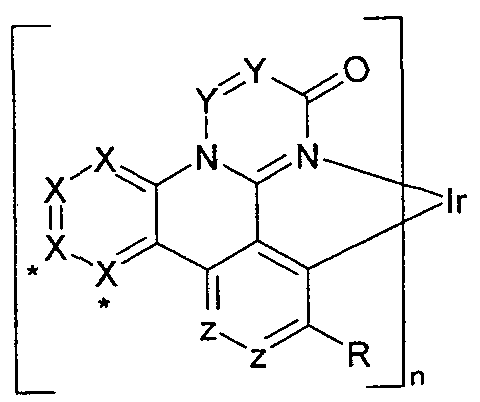
- the complex according to the invention contains a ligand L and two bidentate ligands L '.
- the ligand L ' is an ortho-metalated ligand which coordinates to the iridium via a carbon atom and a nitrogen atom or a carbon atom and an oxygen atom.
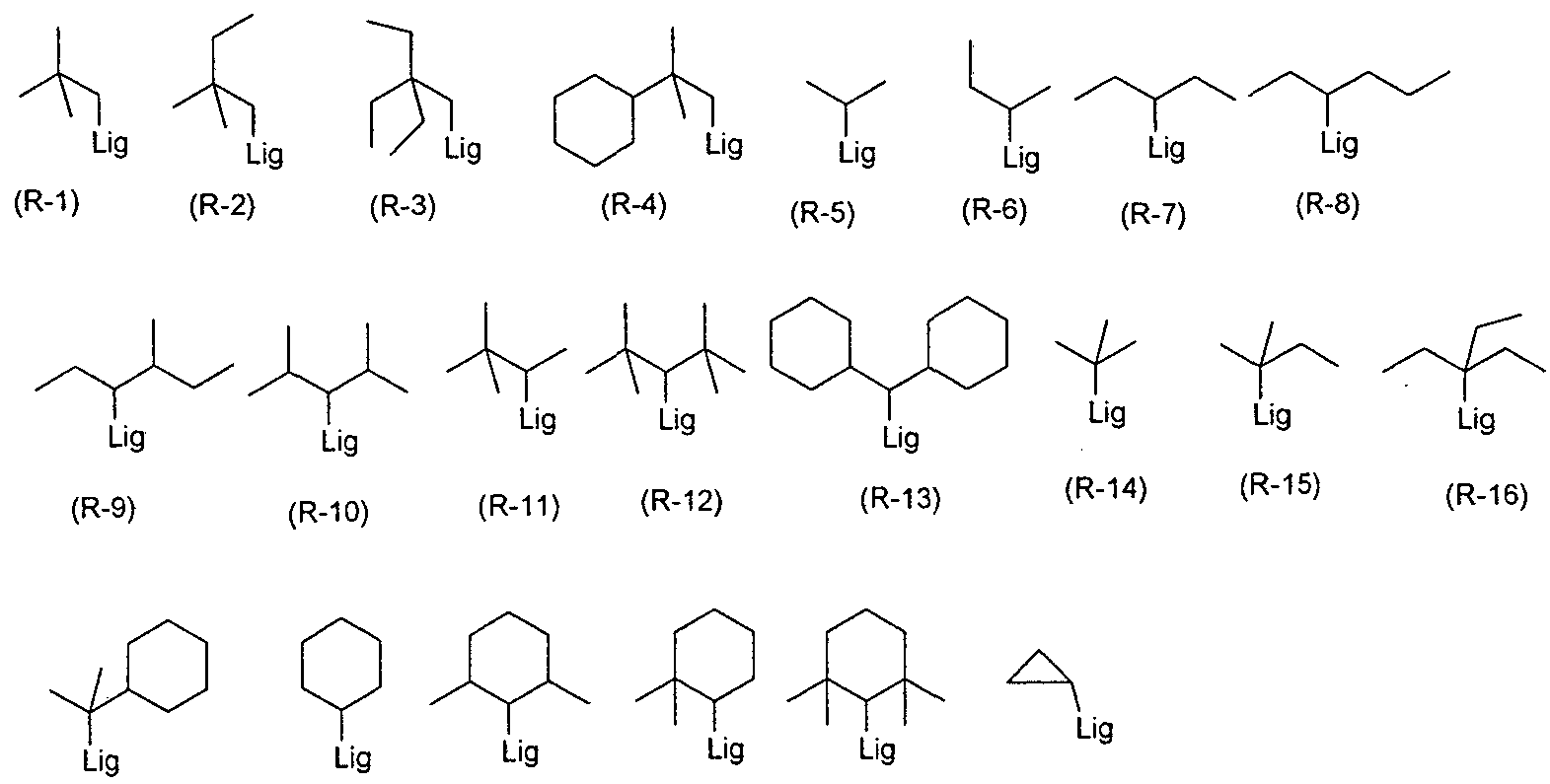
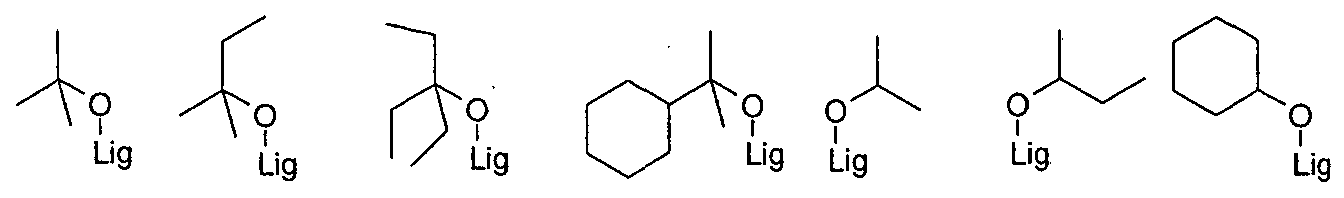
- R-66 (R-67) (R-68) wherein Lig denotes the attachment of the aralkyl group to the ligand and the phenyl groups may each be substituted by one or more radicals R 1 .
- R 1 the radical which is adjacent to a nitrogen atom stands for an aromatic or heteroaromatic ring system
- this aromatic or heteroaromatic ring system preferably has 5 to 30 aromatic ring atoms, more preferably 5 to 24 aromatic ring atoms.
- this aromatic or heteroaromatic ring system preferably contains no aryl or heteroaryl groups in which more than two aromatic six-membered rings are condensed directly to one another.
- Lig denotes the attachment of the heteroaromatic ring system to the ligand and the aromatic and heteroaromatic groups may each be substituted by one or more radicals R 1 .
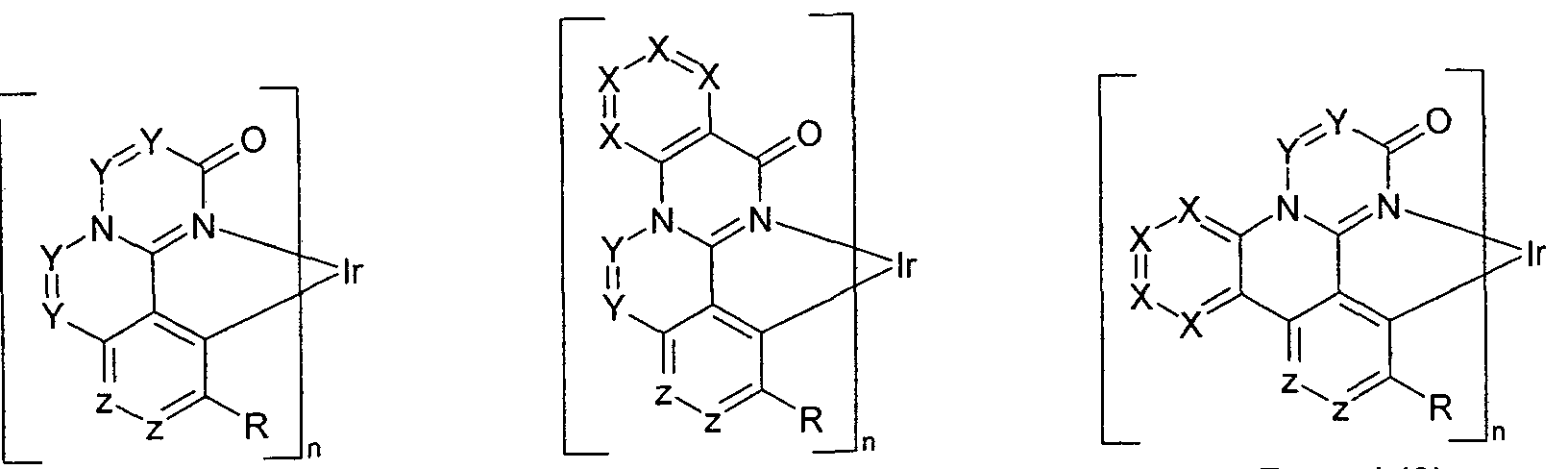
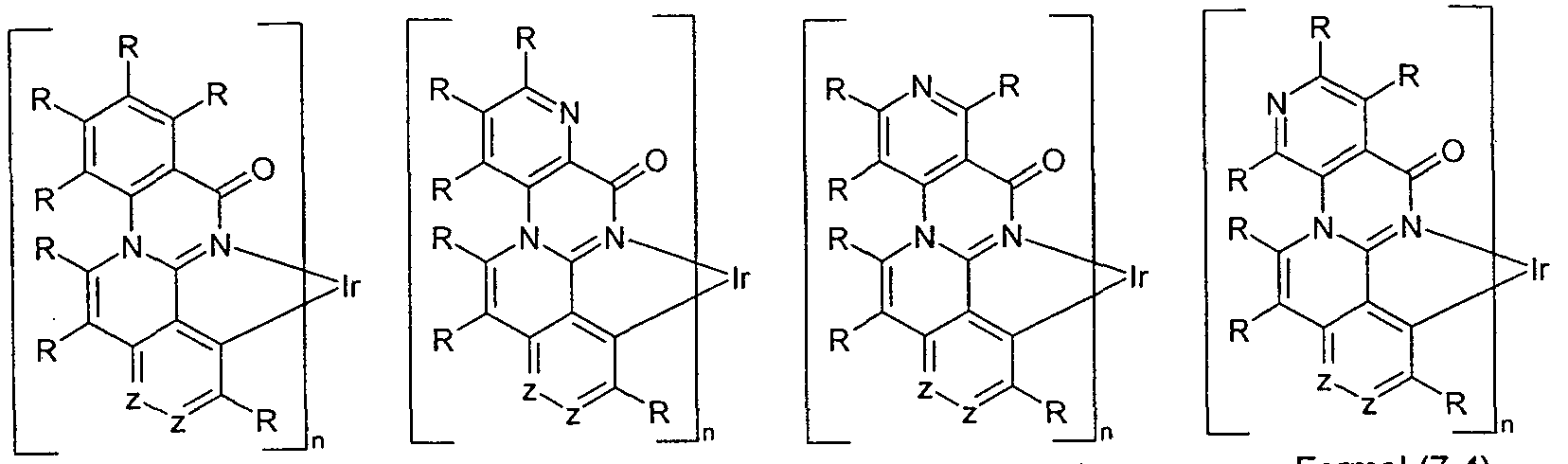
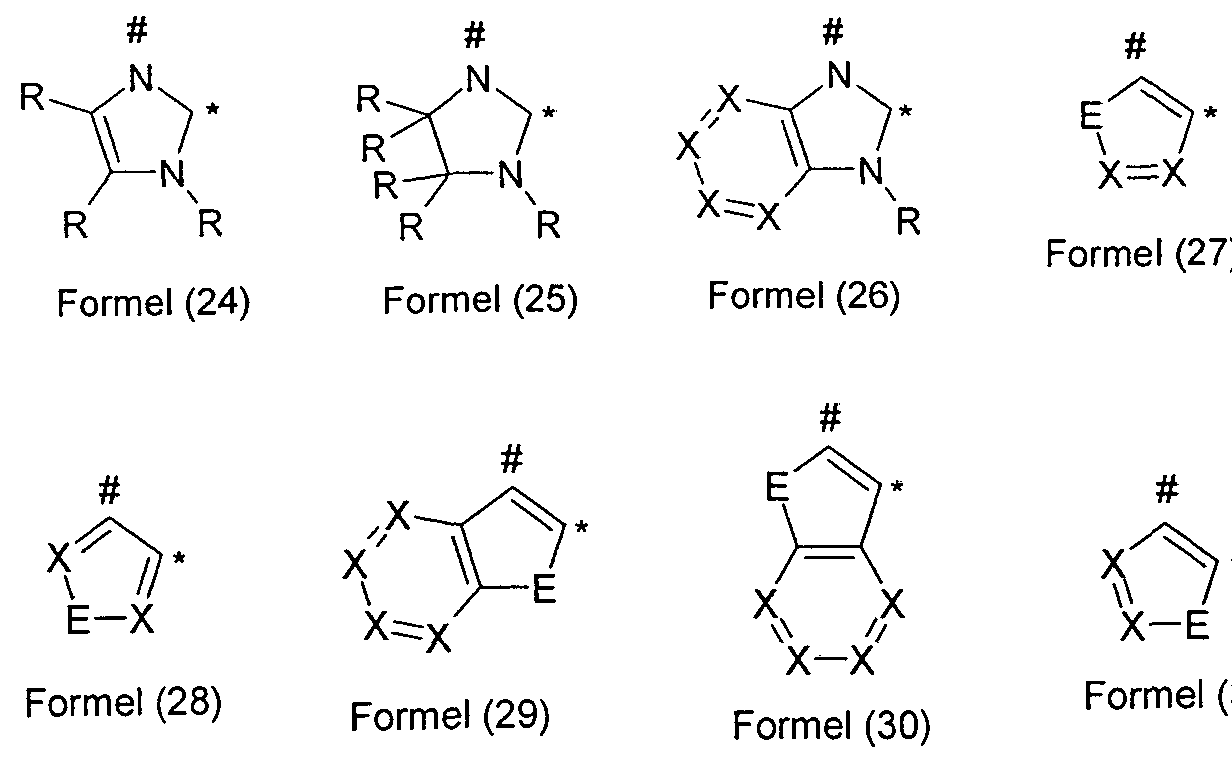
- two adjacent groups Y and / or, if present, two adjacent groups X stand for CR and the respective radicals R together with the C atoms form a fused aliphatic 5-membered ring, Span 6-ring or 7-ring without acidic benzylic protons and / or in the partial structures of the formulas (6-1) to (8-7) or the preferred embodiments two radicals R which bind to directly bonded C atoms, together with the C atoms to which they bind form a fused aliphatic 5-membered ring, 6-membered ring or 7-membered ring with no acidic benzylic protons.
- the groups of formulas (9) to (5) can be present in any position of the partial structure of formula (2) in which two groups Y or, if present, two groups X are directly bonded to one another.
- Preferred positions in which a group of the formula (9) to (15) is present are the partial structures of the following formulas (6 ') to (8 ""),
- benzylic protons protons which bind to a carbon atom which are bound directly to the ligand.
- the absence of acidic benzylic protons is achieved in formulas (9) to (11) and (15) by defining A 1 and A 3 , when they stand for C (R 3 ) 2 , in such a way that R 3 is not hydrogen.
- the absence of acid benzylic protons is achieved in formulas (9) to (11) and (15) by defining A 1 and A 3 , when they stand for C (R 3 ) 2 , in such a way that R 3 is not hydrogen.
- At most one of the groups A, A 2 and A 3 is a heteroatom, in particular O or NR 3 , and the other groups are C (R 3 ) 2 or C (R 1 ) 2 or A 1 and A 3 are the same or different at each
- ligands L 'are described, as may occur in compounds of the formula (1).
- the ligands L 'are preferably neutral, monoanionic, dianionic or trianionic ligands, particularly preferably neutral or monoanionic ligands. Preference is given to bidentate ligands L '.
- Carboxylates such as. Acetate, trifluoroacetate, propionate, benzoate,
- Aryl groups such as. Phenyl, naphthyl, and anionic nitrogen-containing heterocycles such as pyrrolidine, imidazolide, pyrazolide.
- the alkyl groups are preferably Ci-C 2 o alkyl groups, more preferably Ci-Ci 0 alkyl groups in these groups, very particularly preferably Ci-C 4 alkyl groups.
- An aryl group is also understood to mean heteroaryl groups. These groups are as defined above.
- Preferred neutral or mono- or dianionic, bidentate or higher-dentate ligands L ' are selected from diamines, such as. Example, ethylene diamine, ⁇ , ⁇ , ⁇ ', ⁇ ' tetramethylethylenediamine, propylenediamine, ⁇ , ⁇ , ⁇ ', ⁇ ' - tetramethylpropylenediamine, cis- or trans-diaminocyclohexane, cis- or trans-N, N, N ' , N'-tetramethyldiaminocyclohexane, imines, such as. B.
- diphosphines such as.
- 3-ketoesters such as.
- L ' is a bidentate, monoanionic ligand that coordinates to the iridium via two oxygen atoms, two nitrogen atoms, nitrogen and oxygen, carbon and nitrogen, or carbon and oxygen.
- the ligand L ' is a monoanionic ligand formed from two of the groups of the formula (16) to (43), one of these groups having a negatively charged carbon atom and the other these groups coordinated to the iridium via a neutral nitrogen atom.
- the compounds according to the invention can also be made soluble by suitable substitution, for example by longer alkyl groups (about 4 to 20 C atoms), in particular branched alkyl groups, or optionally substituted aryl groups, for example xylyl, mesityl or branched terphenyl or quaterphenyl groups. Such compounds are then soluble in common organic solvents at room temperature in sufficient concentration to process the complexes from solution can, for example by printing.
- the abovementioned preferred embodiments can be combined with one another as desired. In a particularly preferred embodiment of the invention, the abovementioned preferred embodiments apply simultaneously.
- the compounds can also be used as chiral, enantiomerically pure complexes which can emit circularly polarized light. This can have advantages because it can save the polarization filter on the device.
- such complexes are also suitable for use in security labels, since in addition to the emission they also have the polarization of the light as an easily readable feature.
- Another object of the present invention is a process for the preparation of the compounds of formula (1) by reacting the corresponding free ligands with Iridiumalkoholaten of formula (44), with Iridiumketoketonaten of formula (45), with Iridiumhalogeniden of formula (46) or with dimeric iridium complexes of the formula (47) or (48),
- iridium compounds which carry both alcoholate and / or halide and / or hydroxyl and also ketoketonate radicals. These connections can also be loaded.
- Corresponding iridium compounds which are particularly suitable as starting materials are disclosed in WO 2004/085449. Particularly suitable is [IrcI 2 (acac) 2 r, for example Na [IrCl 2 (acac) 2].
- Other particularly suitable iridium educts are iridium (III) tris (acetylacetonate) and iridium (III) tris (2, 2,6,6-tetramethyl-3,5-heptanedionate).
- each A is a non-coordinating anion, such as.
- triflate, tetrafluoroborate, hexafluorophosphate, etc. represents, in dipolar protic solvents such.
- ethylene glycol, propylene glycol, glycerol, diethylene glycol, triethylene glycol, etc. are performed.
- the synthesis of the complexes is preferably carried out as in WO
- Alcohol ethers ethoxyethanol, diethylene glycol, triethylene glycol, polyethylene glycol, etc.
- ethers di- and tri-ethylene glycol dimethyl ether, diphenyl ether, etc.
- aromatic, heteroaromatic and / or aliphatic hydrocarbons toluene, xylene, mesitylene, chlorobenzene, pyridine, Lutidine, quinoline, iso-quinoline, tridecane, hexadecane, etc.
- amides DF, DMAC, etc.
- lactams NMP
- sulfoxides DMSO
- sulfones dimethylsulfone, sulfolane, etc.
- Suitable melting aids are compounds which are solid at room temperature, but melt on heating the reaction mixture and the
- Dissolve reactants to form a homogeneous melt are biphenyl, m-terphenyl, triphenylene, 1, 2-, 1, 3-, 1, 4-bis-phenoxybenzene, triphenylphosphine oxide, 18-crown-6, phenol, naphthol, hydroquinone, etc ..
- An electronic device is understood to mean a device which contains anode, cathode and at least one layer, this layer containing at least one organic or organometallic compound.
- the electronic device according to the invention thus contains anode, cathode and at least one layer which contains at least one compound of the above-mentioned formula (1).
- WO 2012/048781 It may also be preferred to use several different matrix materials as a mixture. Particularly suitable for this are mixtures of at least one electron-transporting matrix material and at least one hole-transporting matrix material or mixtures of at least two electron-transporting matrix materials or mixtures of at least one hole- or electron-transporting matrix material and at least one further material with a large band gap, which is thus largely electrically inert and not or not substantially participate in charge transport, such.
- a preferred combination is, for example, the use of an aromatic ketone or a triazine derivative with a triarylamine derivative or a carbazole derivative as a mixed matrix for the metal complex according to the invention.
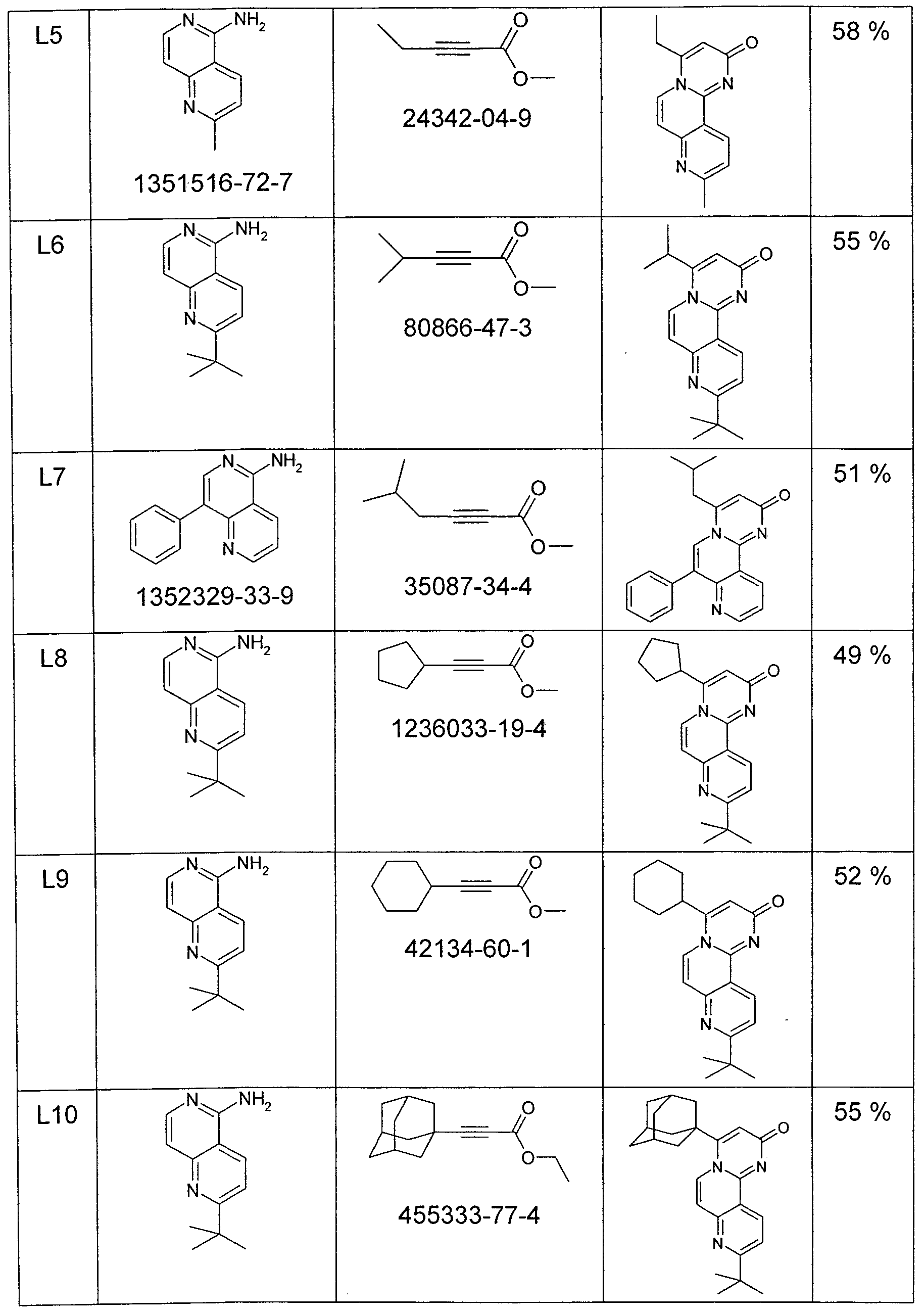
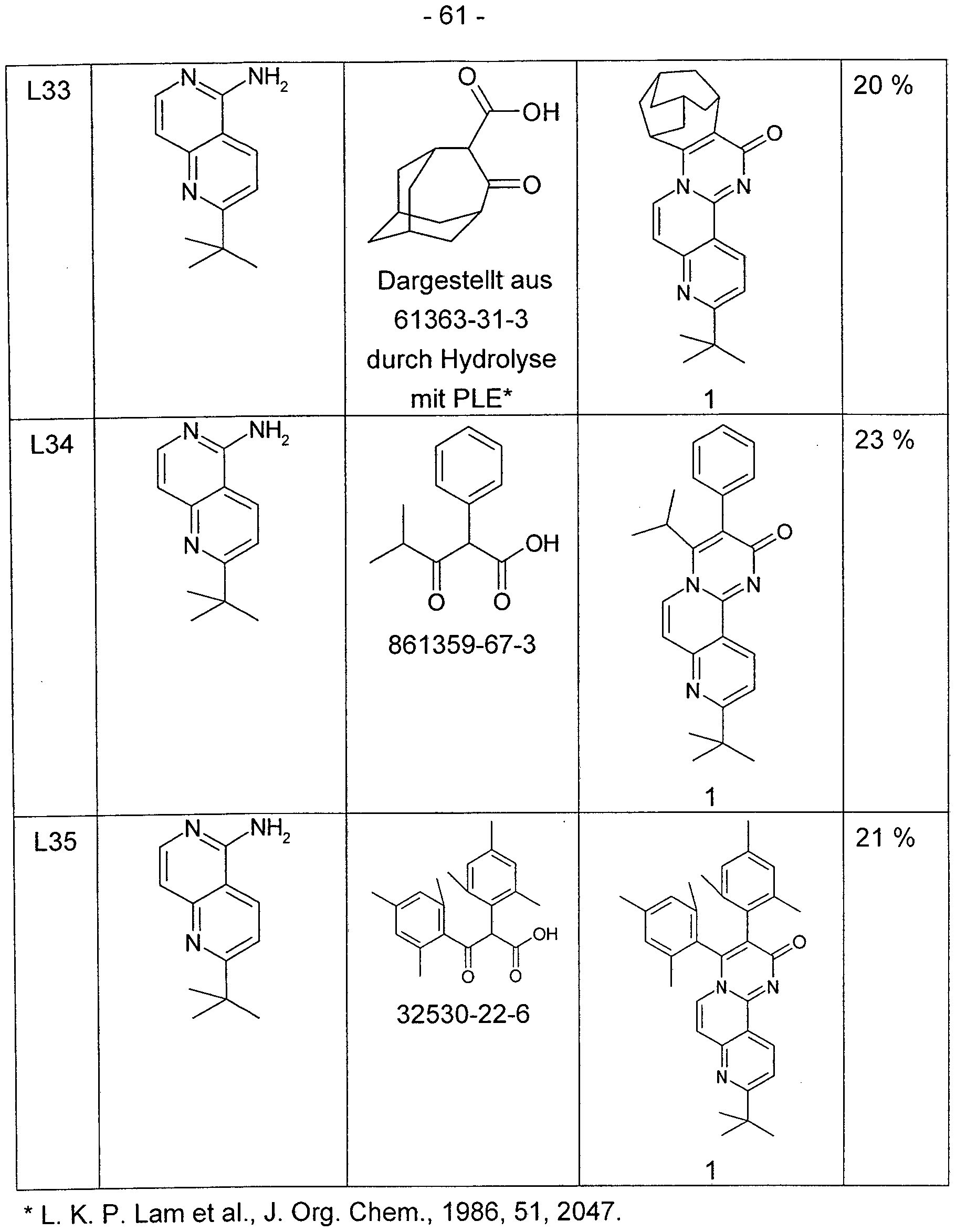
- a cooled to -78 ° C solution of 100 mmol of the ketone is added dropwise with 100 ml of a solution of lithium di-iso-propylamide, 2.0 M in THF, ether, benzene and 15 min. touched. Then added dropwise to a solution of 100 mmol of 2-fluoro-3-cyanopyridine in 100 ml of THF. After removal of the cooling bath and heating to room temperature, the mixture is stirred at room temperature for 3 h. After stripping off the THF in vacuo, the residue is taken up in 200 ml of ethylene glycol, added to 110 mmol of ß-aminoester hydrochloride and heated at 180 ° C for 6 h on a water.
- Naphthyridin-5-ylamines [2,6] naphthyridin-1-ylamines can be used.
- Variant A tris-acetylacetonato-iridium (III) as iridium starting material
- the fine suspension is decanted from the glass beads, the solid is filtered off with suction, washed with 50 ml of the suspension medium and dried in vacuo.
- the dry solid is placed in a continuous hot extractor on a 3-5 cm high Alox Bed (Alox, basic activity level 1) and then placed with a
- the enantiomers ⁇ , the ⁇ Point group C3 generally has a significantly lower solubility in the extractant than the enantiomers of point group C1, which consequently accumulate in the mother liquor, separating the C3 from the C1 diastereomers in this way is often possible, but the diastereomers may also be If ligands of the point group C1 are used in enantiomerically pure form, a pair of diastereomers ⁇ , ⁇ of the point group C3 are formed The diastereomers can be separated by crystallization or chromatography and thus obtained as enantiomerically pure compounds.
- Variant B tris (2,2,6,64etramethyl-3,5-heptanedionato) iridium (III) as
- Extractant concentrated in vacuo to about 100 ml.
- Metal complexes which have too good solubility in the extractant are brought to crystallization by the dropwise addition of 200 ml of methanol.
- the solid of the suspensions thus obtained is filtered off with suction, washed once with about 50 ml of methanol and dried. After drying, the purity of the metal complex is determined by NMR and / or HPLC. If the purity is less than 99.5%, the hot extraction step is repeated, if the purity is 99.5 - 99.9% or better, the metal complex is tempered or sublimed.
- the purification can also be carried out by chromatography on silica gel or Alox.
- Annealing is carried out in a high vacuum (p about 10 ⁇ 6 mbar) in the temperature range of about 200 - 300 ° C.
- the sublimation takes place in the high Vacuum (p about 10 "6 mbar) in the temperature range of about 300-400 ° C, wherein the sublimation is preferably carried out in the form of a fractional sublimation.
- Step 1
- the cathode is formed by a 100 nm thick aluminum layer.
- the emission layer always consists of at least one matrix material (host material, host material) and an emitting dopant (dopant, emitter) which passes through the matrix material or the matrix materials
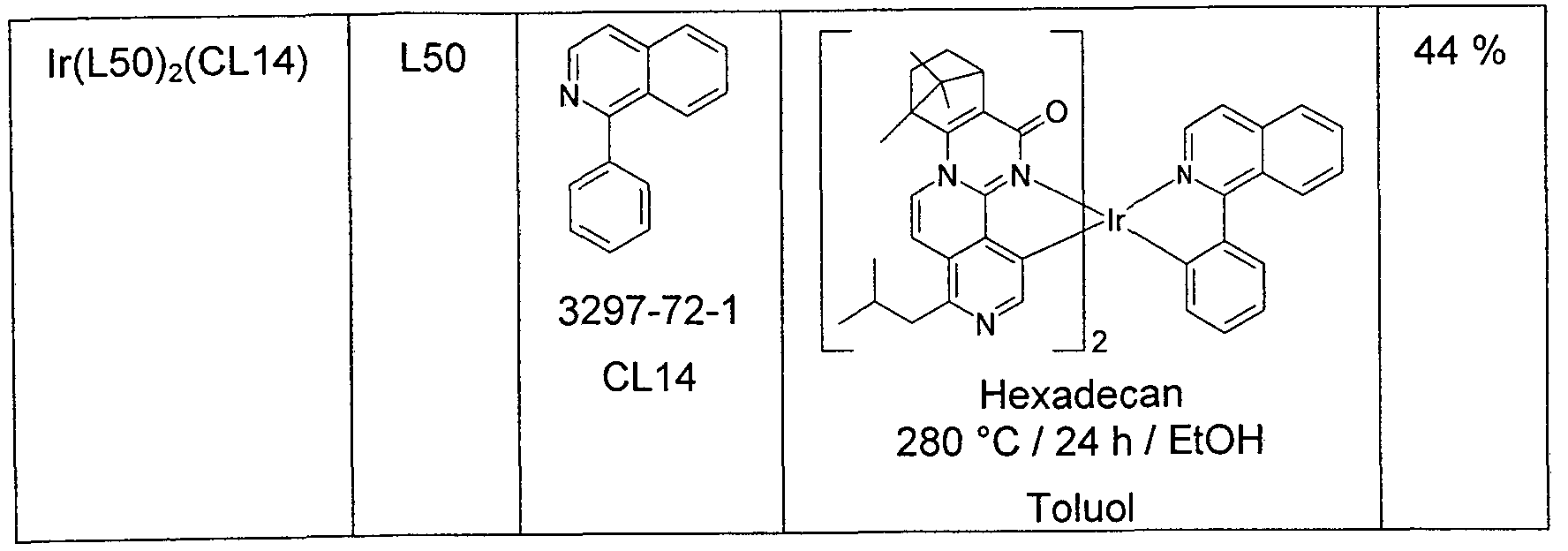
- HTM M1 lr (L29) 2 (CL6) ⁇ 1 ⁇ 2
- M7 M9: lr (L25) 2 (L1) ⁇ 1 ⁇ 2
- M3 M2: lr (L53) 2 (CL2) ⁇ 1 ⁇ 2
- M3 M2: lr (L53) 2 (CL14) ⁇ 1 ⁇ 2
- Polystyrene films are produced side by side on a glass slide by dropping a dichloromethane solution of polystyrene and an emitter (solids content of polystyrene about 10% by weight, solids content of emitter about 0.1% by weight) and evaporating off the solvent.
- a dichloromethane solution of polystyrene and an emitter solids content of polystyrene about 10% by weight, solids content of emitter about 0.1% by weight
- UV lamp commercial lamp for viewing DCs
- Movie 1 polystyrene film containing the reference emitter Ir-Ref, tris [6- (1, 1- dimethylethyl) -benzimidazo [1, 2-c] quinazolin-1-yl-KC 1 K / V 12] iridium,
- Film 2 polystyrene film containing emitter lr (L1) 3 according to the invention.
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Crystallography & Structural Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
Description
Claims
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020157019917A KR102188212B1 (ko) | 2012-12-21 | 2013-11-27 | 금속 착물 |
| CN201380066495.1A CN104870459B (zh) | 2012-12-21 | 2013-11-27 | 金属络合物 |
| EP13805768.2A EP2935292B1 (de) | 2012-12-21 | 2013-11-27 | Metallkomplexe |
| US14/654,187 US20150333280A1 (en) | 2012-12-21 | 2013-11-27 | Metal Complexes |
| JP2015548256A JP6556629B2 (ja) | 2012-12-21 | 2013-11-27 | 金属錯体 |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP12008582 | 2012-12-21 | ||
| EP12008582.4 | 2012-12-21 | ||
| EP13003484 | 2013-07-10 | ||
| EP13003484.6 | 2013-07-10 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| WO2014094961A1 true WO2014094961A1 (de) | 2014-06-26 |
| WO2014094961A8 WO2014094961A8 (de) | 2014-09-04 |
Family
ID=49766023
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2013/003581 Ceased WO2014094961A1 (de) | 2012-12-21 | 2013-11-27 | Metallkomplexe |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20150333280A1 (de) |
| EP (1) | EP2935292B1 (de) |
| JP (1) | JP6556629B2 (de) |
| KR (1) | KR102188212B1 (de) |
| CN (1) | CN104870459B (de) |
| TW (1) | TWI627178B (de) |
| WO (1) | WO2014094961A1 (de) |
Cited By (169)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015104045A1 (de) * | 2014-01-13 | 2015-07-16 | Merck Patent Gmbh | Metallkomplexe |
| WO2015169412A1 (de) | 2014-05-05 | 2015-11-12 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| CN105531347A (zh) * | 2013-09-11 | 2016-04-27 | 默克专利有限公司 | 金属络合物 |
| JP2016108374A (ja) * | 2014-12-02 | 2016-06-20 | セイコーエプソン株式会社 | 成膜用インク、成膜方法、膜付きデバイスおよび電子機器 |
| US9412956B2 (en) | 2013-09-12 | 2016-08-09 | Semiconductor Energy Laboratory Co., Ltd. | Organometallic iridium complex, light-emitting element, light-emitting device, electronic device, and lighting device |
| WO2017148565A1 (de) | 2016-03-03 | 2017-09-08 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2017157983A1 (de) | 2016-03-17 | 2017-09-21 | Merck Patent Gmbh | Verbindungen mit spirobifluoren-strukturen |
| WO2017178311A1 (de) | 2016-04-11 | 2017-10-19 | Merck Patent Gmbh | Heterocyclische verbindungen mit dibenzofuran- und/oder dibenzothiophen-strukturen |
| WO2017186760A1 (en) | 2016-04-29 | 2017-11-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2018050583A1 (de) | 2016-09-14 | 2018-03-22 | Merck Patent Gmbh | Verbindungen mit carbazol-strukturen |
| WO2018050584A1 (de) | 2016-09-14 | 2018-03-22 | Merck Patent Gmbh | Verbindungen mit spirobifluoren-strukturen |
| WO2018060218A1 (de) | 2016-09-30 | 2018-04-05 | Merck Patent Gmbh | Carbazole mit diazadibenzofuran- oder diazadibenzothiophen-strukturen |
| WO2018060307A1 (de) | 2016-09-30 | 2018-04-05 | Merck Patent Gmbh | Verbindungen mit diazadibenzofuran- oder diazadibenzothiophen-strukturen |
| WO2018087022A1 (de) | 2016-11-09 | 2018-05-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018087346A1 (de) | 2016-11-14 | 2018-05-17 | Merck Patent Gmbh | Verbindungen mit einer akzeptor- und einer donorgruppe |
| WO2018091435A1 (en) | 2016-11-17 | 2018-05-24 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2018099846A1 (de) | 2016-11-30 | 2018-06-07 | Merck Patent Gmbh | Verbindungen mit valerolaktam-strukturen |
| WO2018104195A1 (de) | 2016-12-05 | 2018-06-14 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen zur verwendung in oleds |
| WO2018104194A1 (de) | 2016-12-05 | 2018-06-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018104193A1 (de) | 2016-12-05 | 2018-06-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018114883A1 (de) | 2016-12-22 | 2018-06-28 | Merck Patent Gmbh | Mischungen umfassend mindestens zwei organisch funktionelle verbindungen |
| WO2018127465A1 (de) | 2017-01-04 | 2018-07-12 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018138306A1 (de) | 2017-01-30 | 2018-08-02 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018138039A1 (de) | 2017-01-25 | 2018-08-02 | Merck Patent Gmbh | Carbazolderivate |
| WO2018149769A1 (de) | 2017-02-14 | 2018-08-23 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018166934A1 (de) | 2017-03-15 | 2018-09-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018166932A1 (de) | 2017-03-13 | 2018-09-20 | Merck Patent Gmbh | Verbindungen mit arylamin-strukturen |
| WO2018189134A1 (de) | 2017-04-13 | 2018-10-18 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2018206526A1 (en) | 2017-05-11 | 2018-11-15 | Merck Patent Gmbh | Organoboron complexes for organic electroluminescent devices |
| WO2018206537A1 (en) | 2017-05-11 | 2018-11-15 | Merck Patent Gmbh | Carbazole-based bodipys for organic electroluminescent devices |
| CN108886168A (zh) * | 2017-01-23 | 2018-11-23 | 株式会社Lg化学 | 用于非水电解质溶液的添加剂、用于锂二次电池的非水电解质溶液以及包括该非水电解质溶液的锂二次电池 |
| WO2018215318A1 (de) | 2017-05-22 | 2018-11-29 | Merck Patent Gmbh | Hexazyklische heteroaromatische verbindungen für elektronische vorrichtungen |
| WO2018234346A1 (en) | 2017-06-23 | 2018-12-27 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2019007867A1 (de) | 2017-07-05 | 2019-01-10 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2019007866A1 (de) | 2017-07-05 | 2019-01-10 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2019052933A1 (de) | 2017-09-12 | 2019-03-21 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2019068679A1 (en) | 2017-10-06 | 2019-04-11 | Merck Patent Gmbh | MATERIALS FOR ORGANIC ELECTROLUMINESCENT DEVICES |
| WO2019081391A1 (de) | 2017-10-24 | 2019-05-02 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2019096717A2 (de) | 2017-11-14 | 2019-05-23 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2019121458A1 (de) | 2017-12-19 | 2019-06-27 | Merck Patent Gmbh | Heterocyclische verbindung zur verwendung in electronischen vorrichtungen |
| WO2019145316A1 (de) | 2018-01-25 | 2019-08-01 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2019175149A1 (en) | 2018-03-16 | 2019-09-19 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2019229011A1 (de) | 2018-05-30 | 2019-12-05 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2019233904A1 (de) | 2018-06-07 | 2019-12-12 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen |
| WO2020011686A1 (de) | 2018-07-09 | 2020-01-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020016264A1 (en) | 2018-07-20 | 2020-01-23 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2020053314A1 (de) | 2018-09-12 | 2020-03-19 | Merck Patent Gmbh | Elektrolumineszierende vorrichtungen |
| WO2020053150A1 (en) | 2018-09-12 | 2020-03-19 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2020053315A1 (de) | 2018-09-12 | 2020-03-19 | Merck Patent Gmbh | Elektrolumineszierende vorrichtungen |
| WO2020064662A2 (de) | 2018-09-27 | 2020-04-02 | Merck Patent Gmbh | Verfahren zur herstellung von sterisch gehinderten stickstoffhaltigen heteroaromatischen verbindungen |
| WO2020064666A1 (de) | 2018-09-27 | 2020-04-02 | Merck Patent Gmbh | Verbindungen, die in einer organischen elektronischen vorrichtung als aktive verbindungen einsetzbar sind |
| WO2020094542A1 (de) | 2018-11-06 | 2020-05-14 | Merck Patent Gmbh | 5,6-diphenyl-5,6-dihydro-dibenz[c,e][1,2]azaphosphorin- und 6-phenyl-6h-dibenzo[c,e][1,2]thiazin-5,5-dioxid-derivate und ähnliche verbindungen als organische elektrolumineszenzmaterialien für oleds |
| WO2020094539A1 (de) | 2018-11-05 | 2020-05-14 | Merck Patent Gmbh | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| WO2020099307A1 (de) | 2018-11-15 | 2020-05-22 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020099349A1 (de) | 2018-11-14 | 2020-05-22 | Merck Patent Gmbh | Zur herstellung einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| WO2020127165A1 (de) | 2018-12-19 | 2020-06-25 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020148303A1 (de) | 2019-01-17 | 2020-07-23 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020148243A1 (en) | 2019-01-16 | 2020-07-23 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2020169241A1 (de) | 2019-02-18 | 2020-08-27 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2020178230A1 (en) | 2019-03-04 | 2020-09-10 | Merck Patent Gmbh | Ligands for nano-sized materials |
| WO2020182779A1 (de) | 2019-03-12 | 2020-09-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020187865A1 (de) | 2019-03-20 | 2020-09-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020193447A1 (de) | 2019-03-25 | 2020-10-01 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020208051A1 (en) | 2019-04-11 | 2020-10-15 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2020212296A1 (de) | 2019-04-15 | 2020-10-22 | Merck Patent Gmbh | Metallkomplexe |
| WO2021013775A1 (de) | 2019-07-22 | 2021-01-28 | Merck Patent Gmbh | Verfahren zur herstellung ortho-metallierter metallverbindungen |
| WO2021037401A1 (de) | 2019-08-26 | 2021-03-04 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021043703A1 (de) | 2019-09-02 | 2021-03-11 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021043755A1 (de) | 2019-09-03 | 2021-03-11 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021053046A1 (de) | 2019-09-20 | 2021-03-25 | Merck Patent Gmbh | Peri-kondensierte heterozyklische verbindungen als materialien für elektronische vorrichtungen |
| WO2021052924A1 (en) | 2019-09-16 | 2021-03-25 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021052921A1 (de) | 2019-09-19 | 2021-03-25 | Merck Patent Gmbh | Mischung von zwei hostmaterialien und organische elektrolumineszierende vorrichtung damit |
| WO2021078831A1 (de) | 2019-10-25 | 2021-04-29 | Merck Patent Gmbh | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| WO2021078710A1 (en) | 2019-10-22 | 2021-04-29 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021089447A1 (de) | 2019-11-04 | 2021-05-14 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2021089450A1 (en) | 2019-11-04 | 2021-05-14 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021094269A1 (en) | 2019-11-12 | 2021-05-20 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021110741A1 (en) | 2019-12-04 | 2021-06-10 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021110720A1 (de) | 2019-12-04 | 2021-06-10 | Merck Patent Gmbh | Metallkomplexe |
| WO2021122538A1 (de) | 2019-12-18 | 2021-06-24 | Merck Patent Gmbh | Aromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021122535A1 (de) | 2019-12-17 | 2021-06-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021122740A1 (de) | 2019-12-19 | 2021-06-24 | Merck Patent Gmbh | Polycyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021151922A1 (de) | 2020-01-29 | 2021-08-05 | Merck Patent Gmbh | Benzimidazol-derivate |
| WO2021170522A1 (de) | 2020-02-25 | 2021-09-02 | Merck Patent Gmbh | Verwendung von heterocyclischen verbindungen in einer organischen elektronischen vorrichtung |
| WO2021175706A1 (de) | 2020-03-02 | 2021-09-10 | Merck Patent Gmbh | Verwendung von sulfonverbindungen in einer organischen elektronischen vorrichtung |
| WO2021180614A1 (de) | 2020-03-11 | 2021-09-16 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2021180625A1 (de) | 2020-03-11 | 2021-09-16 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2021185712A1 (de) | 2020-03-17 | 2021-09-23 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021185829A1 (de) | 2020-03-17 | 2021-09-23 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021191183A1 (de) | 2020-03-26 | 2021-09-30 | Merck Patent Gmbh | Cyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021191058A1 (en) | 2020-03-23 | 2021-09-30 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021191117A1 (de) | 2020-03-24 | 2021-09-30 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2021198213A1 (de) | 2020-04-02 | 2021-10-07 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021204646A1 (de) | 2020-04-06 | 2021-10-14 | Merck Patent Gmbh | Polycyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021239772A1 (de) | 2020-05-29 | 2021-12-02 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2021254984A1 (de) | 2020-06-18 | 2021-12-23 | Merck Patent Gmbh | Indenoazanaphthaline |
| WO2021259824A1 (de) | 2020-06-23 | 2021-12-30 | Merck Patent Gmbh | Verfahren zur herstellung einer mischung |
| WO2022002771A1 (de) | 2020-06-29 | 2022-01-06 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022002772A1 (de) | 2020-06-29 | 2022-01-06 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022029096A1 (de) | 2020-08-06 | 2022-02-10 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022034046A1 (de) | 2020-08-13 | 2022-02-17 | Merck Patent Gmbh | Metallkomplexe |
| WO2022038066A1 (de) | 2020-08-19 | 2022-02-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022038065A1 (de) | 2020-08-18 | 2022-02-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022069422A1 (de) | 2020-09-30 | 2022-04-07 | Merck Patent Gmbh | Verbindungen zur strukturierung von funktionalen schichten organischer elektrolumineszenzvorrichtungen |
| WO2022069421A1 (de) | 2020-09-30 | 2022-04-07 | Merck Patent Gmbh | Zur strukturierung von funktionalen schichten organischer elektrolumineszenzvorrichtungen einsetzbare verbindungen |
| WO2022079067A1 (de) | 2020-10-16 | 2022-04-21 | Merck Patent Gmbh | Verbindungen mit heteroatomen für organische elektrolumineszenzvorrichtungen |
| WO2022079068A1 (de) | 2020-10-16 | 2022-04-21 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022101171A1 (de) | 2020-11-10 | 2022-05-19 | Merck Patent Gmbh | Schwefelhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022117473A1 (de) | 2020-12-02 | 2022-06-09 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022122682A2 (de) | 2020-12-10 | 2022-06-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022129113A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Stickstoffhaltige heteroaromaten für organische elektrolumineszenzvorrichtungen |
| WO2022129116A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Indolo[3.2.1-jk]carbazole-6-carbonitril-derivate als blau fluoreszierende emitter zur verwendung in oleds |
| WO2022129114A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Stickstoffhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022148717A1 (de) | 2021-01-05 | 2022-07-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022157343A1 (de) | 2021-01-25 | 2022-07-28 | Merck Patent Gmbh | Stickstoffhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022194799A1 (de) | 2021-03-18 | 2022-09-22 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022200638A1 (de) | 2021-07-06 | 2022-09-29 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022229126A1 (de) | 2021-04-29 | 2022-11-03 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022229298A1 (de) | 2021-04-29 | 2022-11-03 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022229234A1 (de) | 2021-04-30 | 2022-11-03 | Merck Patent Gmbh | Stickstoffhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022243403A1 (de) | 2021-05-21 | 2022-11-24 | Merck Patent Gmbh | Verfahren zur kontinuierlichen aufreinigung von mindestens einem funktionalen material und vorrichtung zur kontinuierlichen aufreinigung von mindestens einem funktionalen material |
| WO2023036976A1 (en) | 2021-09-13 | 2023-03-16 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2023041454A1 (de) | 2021-09-14 | 2023-03-23 | Merck Patent Gmbh | Borhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023052314A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052313A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052275A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052272A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023072799A1 (de) | 2021-10-27 | 2023-05-04 | Merck Patent Gmbh | Bor- und stickstoffhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023094412A1 (de) | 2021-11-25 | 2023-06-01 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023099543A1 (en) | 2021-11-30 | 2023-06-08 | Merck Patent Gmbh | Compounds having fluorene structures |
| WO2023110742A1 (de) | 2021-12-13 | 2023-06-22 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2023117837A1 (de) | 2021-12-21 | 2023-06-29 | Merck Patent Gmbh | Verfahren zur herstellung von deuterierten organischen verbindungen |
| WO2023152346A1 (de) | 2022-02-14 | 2023-08-17 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023152063A1 (de) | 2022-02-09 | 2023-08-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2023161168A1 (de) | 2022-02-23 | 2023-08-31 | Merck Patent Gmbh | Aromatische heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2023161167A1 (de) | 2022-02-23 | 2023-08-31 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2023213837A1 (de) | 2022-05-06 | 2023-11-09 | Merck Patent Gmbh | Cyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023222559A1 (de) | 2022-05-18 | 2023-11-23 | Merck Patent Gmbh | Verfahren zur herstellung von deuterierten organischen verbindungen |
| WO2023247663A1 (de) | 2022-06-24 | 2023-12-28 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2023247662A1 (de) | 2022-06-24 | 2023-12-28 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2024013004A1 (de) | 2022-07-11 | 2024-01-18 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2024033282A1 (en) | 2022-08-09 | 2024-02-15 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2024061942A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2024061948A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024094592A2 (de) | 2022-11-01 | 2024-05-10 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024105066A1 (en) | 2022-11-17 | 2024-05-23 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2024132993A1 (de) | 2022-12-19 | 2024-06-27 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2024132892A1 (en) | 2022-12-19 | 2024-06-27 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2024133048A1 (en) | 2022-12-20 | 2024-06-27 | Merck Patent Gmbh | Method for preparing deuterated aromatic compounds |
| WO2024149694A1 (de) | 2023-01-10 | 2024-07-18 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024153568A1 (de) | 2023-01-17 | 2024-07-25 | Merck Patent Gmbh | Heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024184050A1 (de) | 2023-03-07 | 2024-09-12 | Merck Patent Gmbh | Cyclische stickstoffverbindungen für organische elektrolumineszenzvorrichtungen |
| WO2024194264A1 (de) | 2023-03-20 | 2024-09-26 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2024218109A1 (de) | 2023-04-20 | 2024-10-24 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2024240725A1 (de) | 2023-05-25 | 2024-11-28 | Merck Patent Gmbh | Tris[1,2,4]triazolo[1,5-a:1',5'-c:1'',5''-e][1,3,5]triazin-derivate zur verwendung in organischen elektrolumineszenzvorrichtungen |
| EP4486099A1 (de) | 2023-06-30 | 2025-01-01 | Merck Patent GmbH | Verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2025021855A1 (de) | 2023-07-27 | 2025-01-30 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen und organische sensoren |
| WO2025045842A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025045843A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025045851A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025109056A1 (de) | 2023-11-24 | 2025-05-30 | Merck Patent Gmbh | Sauerstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2025132551A1 (de) | 2023-12-22 | 2025-06-26 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US12402531B2 (en) | 2014-04-08 | 2025-08-26 | Dupont Specialty Materials Korea Ltd. | Multi-component host material and organic electroluminescent device comprising the same |
| WO2025181124A1 (de) | 2024-03-01 | 2025-09-04 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2025181097A1 (de) | 2024-02-29 | 2025-09-04 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2025181044A1 (de) | 2024-02-29 | 2025-09-04 | Merck Patent Gmbh | Stickstoffenthaltende verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2026008710A1 (de) | 2024-07-05 | 2026-01-08 | Merck Patent Gmbh | Cyclische siliciumverbindungen für organische elektrolumineszenzvorrichtungen |
| WO2026022016A1 (de) | 2024-07-22 | 2026-01-29 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2026041632A1 (de) | 2024-08-21 | 2026-02-26 | Merck Patent Gmbh | Heterocyclische materialien für organische lichtemittierende vorrichtungen |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2935291B1 (de) * | 2012-12-21 | 2019-10-16 | Merck Patent GmbH | Iridiumkomplexe und deren verwendung in oligomeren, polymeren oder dendrimeren in elektronischen vorrichtungen |
| US11393988B2 (en) | 2014-02-05 | 2022-07-19 | Merck Patent Gmbh | Metal complexes |
| WO2017080324A1 (zh) * | 2015-11-12 | 2017-05-18 | 广州华睿光电材料有限公司 | 含无机纳米材料的印刷组合物及其应用 |
| JP6617966B2 (ja) | 2016-06-24 | 2019-12-11 | 国立研究開発法人産業技術総合研究所 | ハロゲン架橋イリジウムダイマーの製造方法 |
| EP3583111B1 (de) * | 2017-02-14 | 2020-12-23 | Merck Patent GmbH | Verfahren zur herstellung ortho-metallierter metallverbindungen |
| US11773320B2 (en) * | 2019-02-21 | 2023-10-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12486296B2 (en) | 2019-10-02 | 2025-12-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| CN112592371A (zh) * | 2019-10-02 | 2021-04-02 | 环球展览公司 | 有机电致发光材料和装置 |
| CN116200187B (zh) * | 2023-02-09 | 2025-09-30 | 中国科学院化学研究所 | 一种离子型金属铱配合物及其制备方法与应用 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011044988A1 (de) * | 2009-10-16 | 2011-04-21 | Merck Patent Gmbh | Metallkomplexe |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4307000B2 (ja) * | 2001-03-08 | 2009-08-05 | キヤノン株式会社 | 金属配位化合物、電界発光素子及び表示装置 |
| JP2004161661A (ja) * | 2002-11-12 | 2004-06-10 | Takasago Internatl Corp | イリジウム錯体の製造方法 |
| WO2005113563A1 (de) * | 2004-05-19 | 2005-12-01 | Merck Patent Gmbh | Metallkomplexe |
| DE102009007038A1 (de) * | 2009-02-02 | 2010-08-05 | Merck Patent Gmbh | Metallkomplexe |
| KR20130087499A (ko) * | 2010-06-15 | 2013-08-06 | 메르크 파텐트 게엠베하 | 금속 착물 |
| WO2012147896A1 (en) * | 2011-04-29 | 2012-11-01 | Semiconductor Energy Laboratory Co., Ltd. | Organometallic complex, light-emitting element, light-emitting device, electronic device, and lighting device |
| EP2935291B1 (de) * | 2012-12-21 | 2019-10-16 | Merck Patent GmbH | Iridiumkomplexe und deren verwendung in oligomeren, polymeren oder dendrimeren in elektronischen vorrichtungen |
| JP6556630B2 (ja) * | 2012-12-21 | 2019-08-07 | メルク パテント ゲーエムベーハー | 金属錯体 |
-
2013
- 2013-11-27 KR KR1020157019917A patent/KR102188212B1/ko active Active
- 2013-11-27 EP EP13805768.2A patent/EP2935292B1/de active Active
- 2013-11-27 CN CN201380066495.1A patent/CN104870459B/zh active Active
- 2013-11-27 WO PCT/EP2013/003581 patent/WO2014094961A1/de not_active Ceased
- 2013-11-27 JP JP2015548256A patent/JP6556629B2/ja active Active
- 2013-11-27 US US14/654,187 patent/US20150333280A1/en not_active Abandoned
- 2013-12-18 TW TW102146913A patent/TWI627178B/zh active
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011044988A1 (de) * | 2009-10-16 | 2011-04-21 | Merck Patent Gmbh | Metallkomplexe |
Cited By (189)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105531347A (zh) * | 2013-09-11 | 2016-04-27 | 默克专利有限公司 | 金属络合物 |
| CN105531347B (zh) * | 2013-09-11 | 2018-09-11 | 默克专利有限公司 | 金属络合物 |
| US9831448B2 (en) | 2013-09-11 | 2017-11-28 | Merck Patent Gmbh | Metal complexes |
| US9412956B2 (en) | 2013-09-12 | 2016-08-09 | Semiconductor Energy Laboratory Co., Ltd. | Organometallic iridium complex, light-emitting element, light-emitting device, electronic device, and lighting device |
| CN105916868A (zh) * | 2014-01-13 | 2016-08-31 | 默克专利有限公司 | 金属络合物 |
| US11005050B2 (en) | 2014-01-13 | 2021-05-11 | Merck Patent Gmbh | Metal complexes |
| WO2015104045A1 (de) * | 2014-01-13 | 2015-07-16 | Merck Patent Gmbh | Metallkomplexe |
| CN105916868B (zh) * | 2014-01-13 | 2020-06-23 | 默克专利有限公司 | 金属络合物 |
| US12402531B2 (en) | 2014-04-08 | 2025-08-26 | Dupont Specialty Materials Korea Ltd. | Multi-component host material and organic electroluminescent device comprising the same |
| WO2015169412A1 (de) | 2014-05-05 | 2015-11-12 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10526500B2 (en) | 2014-12-02 | 2020-01-07 | Seiko Epson Corporation | Film-forming ink, film formation method, device with film, and electronic apparatus |
| JP2016108374A (ja) * | 2014-12-02 | 2016-06-20 | セイコーエプソン株式会社 | 成膜用インク、成膜方法、膜付きデバイスおよび電子機器 |
| WO2017148564A1 (de) | 2016-03-03 | 2017-09-08 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2017148565A1 (de) | 2016-03-03 | 2017-09-08 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2017157983A1 (de) | 2016-03-17 | 2017-09-21 | Merck Patent Gmbh | Verbindungen mit spirobifluoren-strukturen |
| WO2017178311A1 (de) | 2016-04-11 | 2017-10-19 | Merck Patent Gmbh | Heterocyclische verbindungen mit dibenzofuran- und/oder dibenzothiophen-strukturen |
| WO2017186760A1 (en) | 2016-04-29 | 2017-11-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2018050583A1 (de) | 2016-09-14 | 2018-03-22 | Merck Patent Gmbh | Verbindungen mit carbazol-strukturen |
| WO2018050584A1 (de) | 2016-09-14 | 2018-03-22 | Merck Patent Gmbh | Verbindungen mit spirobifluoren-strukturen |
| WO2018060307A1 (de) | 2016-09-30 | 2018-04-05 | Merck Patent Gmbh | Verbindungen mit diazadibenzofuran- oder diazadibenzothiophen-strukturen |
| WO2018060218A1 (de) | 2016-09-30 | 2018-04-05 | Merck Patent Gmbh | Carbazole mit diazadibenzofuran- oder diazadibenzothiophen-strukturen |
| WO2018087022A1 (de) | 2016-11-09 | 2018-05-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018087346A1 (de) | 2016-11-14 | 2018-05-17 | Merck Patent Gmbh | Verbindungen mit einer akzeptor- und einer donorgruppe |
| EP4271163A2 (de) | 2016-11-14 | 2023-11-01 | Merck Patent GmbH | Verbindungen mit einer akzeptor- und einer donorgruppe |
| WO2018091435A1 (en) | 2016-11-17 | 2018-05-24 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2018099846A1 (de) | 2016-11-30 | 2018-06-07 | Merck Patent Gmbh | Verbindungen mit valerolaktam-strukturen |
| WO2018104194A1 (de) | 2016-12-05 | 2018-06-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018104193A1 (de) | 2016-12-05 | 2018-06-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018104195A1 (de) | 2016-12-05 | 2018-06-14 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen zur verwendung in oleds |
| EP3978491A1 (de) | 2016-12-05 | 2022-04-06 | Merck Patent GmbH | Stickstoffhaltige heterocyclen zur verwendung in oleds |
| WO2018114883A1 (de) | 2016-12-22 | 2018-06-28 | Merck Patent Gmbh | Mischungen umfassend mindestens zwei organisch funktionelle verbindungen |
| WO2018127465A1 (de) | 2017-01-04 | 2018-07-12 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10923768B2 (en) | 2017-01-23 | 2021-02-16 | Lg Chem, Ltd. | Alkynyl-containing compound additive for non-aqueous electrolyte solution, and non-aqueous electrolyte solution for lithium secondary battery and lithium secondary battery which include the same |
| CN108886168A (zh) * | 2017-01-23 | 2018-11-23 | 株式会社Lg化学 | 用于非水电解质溶液的添加剂、用于锂二次电池的非水电解质溶液以及包括该非水电解质溶液的锂二次电池 |
| EP3419099A4 (de) * | 2017-01-23 | 2019-05-08 | LG Chem, Ltd. | Additiv für wasserfreien elektrolyt, wasserfreier elektrolyt einer lithiumsekundärbatterie damit und lithiumsekundärbatterie |
| WO2018138039A1 (de) | 2017-01-25 | 2018-08-02 | Merck Patent Gmbh | Carbazolderivate |
| WO2018138306A1 (de) | 2017-01-30 | 2018-08-02 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018149769A1 (de) | 2017-02-14 | 2018-08-23 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018166932A1 (de) | 2017-03-13 | 2018-09-20 | Merck Patent Gmbh | Verbindungen mit arylamin-strukturen |
| WO2018166934A1 (de) | 2017-03-15 | 2018-09-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018189134A1 (de) | 2017-04-13 | 2018-10-18 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2018206526A1 (en) | 2017-05-11 | 2018-11-15 | Merck Patent Gmbh | Organoboron complexes for organic electroluminescent devices |
| WO2018206537A1 (en) | 2017-05-11 | 2018-11-15 | Merck Patent Gmbh | Carbazole-based bodipys for organic electroluminescent devices |
| WO2018215318A1 (de) | 2017-05-22 | 2018-11-29 | Merck Patent Gmbh | Hexazyklische heteroaromatische verbindungen für elektronische vorrichtungen |
| WO2018234346A1 (en) | 2017-06-23 | 2018-12-27 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2019007867A1 (de) | 2017-07-05 | 2019-01-10 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2019007866A1 (de) | 2017-07-05 | 2019-01-10 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| EP4186898A1 (de) | 2017-07-05 | 2023-05-31 | Merck Patent GmbH | Zusammensetzung für organische elektronische verbindungen |
| WO2019052933A1 (de) | 2017-09-12 | 2019-03-21 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2019068679A1 (en) | 2017-10-06 | 2019-04-11 | Merck Patent Gmbh | MATERIALS FOR ORGANIC ELECTROLUMINESCENT DEVICES |
| WO2019081391A1 (de) | 2017-10-24 | 2019-05-02 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2019096717A2 (de) | 2017-11-14 | 2019-05-23 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2019121458A1 (de) | 2017-12-19 | 2019-06-27 | Merck Patent Gmbh | Heterocyclische verbindung zur verwendung in electronischen vorrichtungen |
| WO2019145316A1 (de) | 2018-01-25 | 2019-08-01 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2019175149A1 (en) | 2018-03-16 | 2019-09-19 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2019229011A1 (de) | 2018-05-30 | 2019-12-05 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2019233904A1 (de) | 2018-06-07 | 2019-12-12 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen |
| WO2020011686A1 (de) | 2018-07-09 | 2020-01-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020016264A1 (en) | 2018-07-20 | 2020-01-23 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2020053314A1 (de) | 2018-09-12 | 2020-03-19 | Merck Patent Gmbh | Elektrolumineszierende vorrichtungen |
| DE202019005923U1 (de) | 2018-09-12 | 2023-06-27 | MERCK Patent Gesellschaft mit beschränkter Haftung | Elektrolumineszierende Vorrichtungen |
| WO2020053150A1 (en) | 2018-09-12 | 2020-03-19 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| DE202019005924U1 (de) | 2018-09-12 | 2023-05-10 | MERCK Patent Gesellschaft mit beschränkter Haftung | Elektrolumineszierende Vorrichtungen |
| WO2020053315A1 (de) | 2018-09-12 | 2020-03-19 | Merck Patent Gmbh | Elektrolumineszierende vorrichtungen |
| EP4601449A2 (de) | 2018-09-27 | 2025-08-13 | Merck Patent GmbH | Verbindungen, die in einer organischen elektronischen vorrichtung als aktive verbindungen einsetzbar sind |
| WO2020064666A1 (de) | 2018-09-27 | 2020-04-02 | Merck Patent Gmbh | Verbindungen, die in einer organischen elektronischen vorrichtung als aktive verbindungen einsetzbar sind |
| WO2020064662A2 (de) | 2018-09-27 | 2020-04-02 | Merck Patent Gmbh | Verfahren zur herstellung von sterisch gehinderten stickstoffhaltigen heteroaromatischen verbindungen |
| US12178124B2 (en) | 2018-09-27 | 2024-12-24 | Merck Kgaa | Compounds that can be used in an organic electronic device as active compounds |
| EP4190880A1 (de) | 2018-09-27 | 2023-06-07 | Merck Patent GmbH | Verbindungen, die in einer organischen elektronischen vorrichtung als aktive verbindungen einsetzbar sind |
| WO2020094539A1 (de) | 2018-11-05 | 2020-05-14 | Merck Patent Gmbh | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| WO2020094542A1 (de) | 2018-11-06 | 2020-05-14 | Merck Patent Gmbh | 5,6-diphenyl-5,6-dihydro-dibenz[c,e][1,2]azaphosphorin- und 6-phenyl-6h-dibenzo[c,e][1,2]thiazin-5,5-dioxid-derivate und ähnliche verbindungen als organische elektrolumineszenzmaterialien für oleds |
| WO2020099349A1 (de) | 2018-11-14 | 2020-05-22 | Merck Patent Gmbh | Zur herstellung einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| WO2020099307A1 (de) | 2018-11-15 | 2020-05-22 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020127165A1 (de) | 2018-12-19 | 2020-06-25 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020148243A1 (en) | 2019-01-16 | 2020-07-23 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2020148303A1 (de) | 2019-01-17 | 2020-07-23 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020169241A1 (de) | 2019-02-18 | 2020-08-27 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2020178230A1 (en) | 2019-03-04 | 2020-09-10 | Merck Patent Gmbh | Ligands for nano-sized materials |
| WO2020182779A1 (de) | 2019-03-12 | 2020-09-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020187865A1 (de) | 2019-03-20 | 2020-09-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020193447A1 (de) | 2019-03-25 | 2020-10-01 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020208051A1 (en) | 2019-04-11 | 2020-10-15 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2020212296A1 (de) | 2019-04-15 | 2020-10-22 | Merck Patent Gmbh | Metallkomplexe |
| WO2021013775A1 (de) | 2019-07-22 | 2021-01-28 | Merck Patent Gmbh | Verfahren zur herstellung ortho-metallierter metallverbindungen |
| WO2021037401A1 (de) | 2019-08-26 | 2021-03-04 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US12108665B2 (en) | 2019-09-02 | 2024-10-01 | Merck Kgaa | Materials for organic electroluminescent devices |
| WO2021043703A1 (de) | 2019-09-02 | 2021-03-11 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021043755A1 (de) | 2019-09-03 | 2021-03-11 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021052924A1 (en) | 2019-09-16 | 2021-03-25 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| EP4697919A2 (de) | 2019-09-19 | 2026-02-18 | Merck Patent GmbH | Organische elektrolumineszierende vorrichtung |
| WO2021052921A1 (de) | 2019-09-19 | 2021-03-25 | Merck Patent Gmbh | Mischung von zwei hostmaterialien und organische elektrolumineszierende vorrichtung damit |
| WO2021053046A1 (de) | 2019-09-20 | 2021-03-25 | Merck Patent Gmbh | Peri-kondensierte heterozyklische verbindungen als materialien für elektronische vorrichtungen |
| WO2021078710A1 (en) | 2019-10-22 | 2021-04-29 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021078831A1 (de) | 2019-10-25 | 2021-04-29 | Merck Patent Gmbh | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| WO2021089447A1 (de) | 2019-11-04 | 2021-05-14 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2021089450A1 (en) | 2019-11-04 | 2021-05-14 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021094269A1 (en) | 2019-11-12 | 2021-05-20 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021110720A1 (de) | 2019-12-04 | 2021-06-10 | Merck Patent Gmbh | Metallkomplexe |
| WO2021110741A1 (en) | 2019-12-04 | 2021-06-10 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021122535A1 (de) | 2019-12-17 | 2021-06-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021122538A1 (de) | 2019-12-18 | 2021-06-24 | Merck Patent Gmbh | Aromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021122740A1 (de) | 2019-12-19 | 2021-06-24 | Merck Patent Gmbh | Polycyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021151922A1 (de) | 2020-01-29 | 2021-08-05 | Merck Patent Gmbh | Benzimidazol-derivate |
| WO2021170522A1 (de) | 2020-02-25 | 2021-09-02 | Merck Patent Gmbh | Verwendung von heterocyclischen verbindungen in einer organischen elektronischen vorrichtung |
| WO2021175706A1 (de) | 2020-03-02 | 2021-09-10 | Merck Patent Gmbh | Verwendung von sulfonverbindungen in einer organischen elektronischen vorrichtung |
| WO2021180614A1 (de) | 2020-03-11 | 2021-09-16 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2021180625A1 (de) | 2020-03-11 | 2021-09-16 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2021185829A1 (de) | 2020-03-17 | 2021-09-23 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021185712A1 (de) | 2020-03-17 | 2021-09-23 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021191058A1 (en) | 2020-03-23 | 2021-09-30 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021191117A1 (de) | 2020-03-24 | 2021-09-30 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2021191183A1 (de) | 2020-03-26 | 2021-09-30 | Merck Patent Gmbh | Cyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021198213A1 (de) | 2020-04-02 | 2021-10-07 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021204646A1 (de) | 2020-04-06 | 2021-10-14 | Merck Patent Gmbh | Polycyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021239772A1 (de) | 2020-05-29 | 2021-12-02 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2021254984A1 (de) | 2020-06-18 | 2021-12-23 | Merck Patent Gmbh | Indenoazanaphthaline |
| WO2021259824A1 (de) | 2020-06-23 | 2021-12-30 | Merck Patent Gmbh | Verfahren zur herstellung einer mischung |
| WO2022002771A1 (de) | 2020-06-29 | 2022-01-06 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022002772A1 (de) | 2020-06-29 | 2022-01-06 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022029096A1 (de) | 2020-08-06 | 2022-02-10 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022034046A1 (de) | 2020-08-13 | 2022-02-17 | Merck Patent Gmbh | Metallkomplexe |
| WO2022038065A1 (de) | 2020-08-18 | 2022-02-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022038066A1 (de) | 2020-08-19 | 2022-02-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022069421A1 (de) | 2020-09-30 | 2022-04-07 | Merck Patent Gmbh | Zur strukturierung von funktionalen schichten organischer elektrolumineszenzvorrichtungen einsetzbare verbindungen |
| WO2022069422A1 (de) | 2020-09-30 | 2022-04-07 | Merck Patent Gmbh | Verbindungen zur strukturierung von funktionalen schichten organischer elektrolumineszenzvorrichtungen |
| WO2022079068A1 (de) | 2020-10-16 | 2022-04-21 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022079067A1 (de) | 2020-10-16 | 2022-04-21 | Merck Patent Gmbh | Verbindungen mit heteroatomen für organische elektrolumineszenzvorrichtungen |
| WO2022101171A1 (de) | 2020-11-10 | 2022-05-19 | Merck Patent Gmbh | Schwefelhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022117473A1 (de) | 2020-12-02 | 2022-06-09 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022122682A2 (de) | 2020-12-10 | 2022-06-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| EP4676208A2 (de) | 2020-12-18 | 2026-01-07 | Merck Patent GmbH | Stickstoffhaltige heteroaromaten für organische elektrolumineszenzvorrichtungen |
| WO2022129113A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Stickstoffhaltige heteroaromaten für organische elektrolumineszenzvorrichtungen |
| WO2022129114A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Stickstoffhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022129116A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Indolo[3.2.1-jk]carbazole-6-carbonitril-derivate als blau fluoreszierende emitter zur verwendung in oleds |
| WO2022148717A1 (de) | 2021-01-05 | 2022-07-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022157343A1 (de) | 2021-01-25 | 2022-07-28 | Merck Patent Gmbh | Stickstoffhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022194799A1 (de) | 2021-03-18 | 2022-09-22 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022229298A1 (de) | 2021-04-29 | 2022-11-03 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022229126A1 (de) | 2021-04-29 | 2022-11-03 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022229234A1 (de) | 2021-04-30 | 2022-11-03 | Merck Patent Gmbh | Stickstoffhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022243403A1 (de) | 2021-05-21 | 2022-11-24 | Merck Patent Gmbh | Verfahren zur kontinuierlichen aufreinigung von mindestens einem funktionalen material und vorrichtung zur kontinuierlichen aufreinigung von mindestens einem funktionalen material |
| WO2022200638A1 (de) | 2021-07-06 | 2022-09-29 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2023036976A1 (en) | 2021-09-13 | 2023-03-16 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2023041454A1 (de) | 2021-09-14 | 2023-03-23 | Merck Patent Gmbh | Borhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023052313A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052272A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052275A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052314A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023072799A1 (de) | 2021-10-27 | 2023-05-04 | Merck Patent Gmbh | Bor- und stickstoffhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023094412A1 (de) | 2021-11-25 | 2023-06-01 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023099543A1 (en) | 2021-11-30 | 2023-06-08 | Merck Patent Gmbh | Compounds having fluorene structures |
| WO2023110742A1 (de) | 2021-12-13 | 2023-06-22 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2023117837A1 (de) | 2021-12-21 | 2023-06-29 | Merck Patent Gmbh | Verfahren zur herstellung von deuterierten organischen verbindungen |
| WO2023152063A1 (de) | 2022-02-09 | 2023-08-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2023152346A1 (de) | 2022-02-14 | 2023-08-17 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023161168A1 (de) | 2022-02-23 | 2023-08-31 | Merck Patent Gmbh | Aromatische heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2023161167A1 (de) | 2022-02-23 | 2023-08-31 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2023213837A1 (de) | 2022-05-06 | 2023-11-09 | Merck Patent Gmbh | Cyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023222559A1 (de) | 2022-05-18 | 2023-11-23 | Merck Patent Gmbh | Verfahren zur herstellung von deuterierten organischen verbindungen |
| WO2023247662A1 (de) | 2022-06-24 | 2023-12-28 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2023247663A1 (de) | 2022-06-24 | 2023-12-28 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| WO2024013004A1 (de) | 2022-07-11 | 2024-01-18 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2024033282A1 (en) | 2022-08-09 | 2024-02-15 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2024061948A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024061942A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2024094592A2 (de) | 2022-11-01 | 2024-05-10 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024105066A1 (en) | 2022-11-17 | 2024-05-23 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2024132892A1 (en) | 2022-12-19 | 2024-06-27 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2024132993A1 (de) | 2022-12-19 | 2024-06-27 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2024133048A1 (en) | 2022-12-20 | 2024-06-27 | Merck Patent Gmbh | Method for preparing deuterated aromatic compounds |
| WO2024149694A1 (de) | 2023-01-10 | 2024-07-18 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024153568A1 (de) | 2023-01-17 | 2024-07-25 | Merck Patent Gmbh | Heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024184050A1 (de) | 2023-03-07 | 2024-09-12 | Merck Patent Gmbh | Cyclische stickstoffverbindungen für organische elektrolumineszenzvorrichtungen |
| WO2024194264A1 (de) | 2023-03-20 | 2024-09-26 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2024218109A1 (de) | 2023-04-20 | 2024-10-24 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2024240725A1 (de) | 2023-05-25 | 2024-11-28 | Merck Patent Gmbh | Tris[1,2,4]triazolo[1,5-a:1',5'-c:1'',5''-e][1,3,5]triazin-derivate zur verwendung in organischen elektrolumineszenzvorrichtungen |
| EP4486099A1 (de) | 2023-06-30 | 2025-01-01 | Merck Patent GmbH | Verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2025021855A1 (de) | 2023-07-27 | 2025-01-30 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen und organische sensoren |
| WO2025045843A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025045842A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025045851A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025109056A1 (de) | 2023-11-24 | 2025-05-30 | Merck Patent Gmbh | Sauerstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2025132551A1 (de) | 2023-12-22 | 2025-06-26 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2025181097A1 (de) | 2024-02-29 | 2025-09-04 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2025181044A1 (de) | 2024-02-29 | 2025-09-04 | Merck Patent Gmbh | Stickstoffenthaltende verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2025181124A1 (de) | 2024-03-01 | 2025-09-04 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2026008710A1 (de) | 2024-07-05 | 2026-01-08 | Merck Patent Gmbh | Cyclische siliciumverbindungen für organische elektrolumineszenzvorrichtungen |
| WO2026022016A1 (de) | 2024-07-22 | 2026-01-29 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2026041632A1 (de) | 2024-08-21 | 2026-02-26 | Merck Patent Gmbh | Heterocyclische materialien für organische lichtemittierende vorrichtungen |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2014094961A8 (de) | 2014-09-04 |
| EP2935292A1 (de) | 2015-10-28 |
| TWI627178B (zh) | 2018-06-21 |
| JP6556629B2 (ja) | 2019-08-07 |
| KR102188212B1 (ko) | 2020-12-08 |
| CN104870459B (zh) | 2018-06-26 |
| CN104870459A (zh) | 2015-08-26 |
| TW201437216A (zh) | 2014-10-01 |
| JP2016507491A (ja) | 2016-03-10 |
| US20150333280A1 (en) | 2015-11-19 |
| KR20150096805A (ko) | 2015-08-25 |
| EP2935292B1 (de) | 2019-04-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2935292B1 (de) | Metallkomplexe | |
| EP2935291B1 (de) | Iridiumkomplexe und deren verwendung in oligomeren, polymeren oder dendrimeren in elektronischen vorrichtungen | |
| EP3044284B1 (de) | Metallkomplexe | |
| EP3174890B1 (de) | Metallkomplexe | |
| DE112011102008B4 (de) | Metallkomplexe | |
| DE112011102366B4 (de) | Metallkomplexe | |
| EP2726490B1 (de) | Metallkomplexe | |
| EP3478698A1 (de) | Verfahren zur auftrennung von enantiomerenmischungen von metallkomplexen | |
| WO2014094962A2 (de) | Metallkomplexe | |
| EP3526228A1 (de) | Metallkomplexe | |
| WO2018041769A1 (de) | Bl- und trinukleare metallkomplexe aufgebaut aus zwei miteinander verknüpften tripodalen hexadentaten liganden zur verwendung in elektrolumineszenzvorrichtungen | |
| EP3526227A1 (de) | Binukleare metallkomplexe sowie elektronische vorrichtungen, insbesondere organische elektrolumineszenzvorrichtungen, enthaltend diese metallkomplexe | |
| EP2906575A1 (de) | Metallkomplexe | |
| WO2014023377A2 (de) | Metallkomplexe | |
| EP3160976A1 (de) | Metallkomplexe | |
| EP3094638A1 (de) | Metallkomplexe | |
| EP3046927A1 (de) | Polycyclische phenyl-pyridin iridiumkomplexe und derivate davon für oled | |
| EP3507294A1 (de) | Bl- und trinukleare metallkomplexe aufgebaut aus zwei miteinander verknüpften tripodalen hexadentaten liganden zur verwendung in elektrolumineszenzvorrichtungen | |
| EP2714704A1 (de) | Metallkomplexe | |
| WO2010086089A1 (de) | Metallkomplexe | |
| WO2017016634A1 (de) | Elektrolumineszierende überbrückte metallkomplexe zur verwendung in elektronischen vorrichtungen | |
| WO2014044347A1 (de) | Metallkomplexe | |
| WO2020212296A1 (de) | Metallkomplexe | |
| EP4069709A1 (de) | Metallkomplexe |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 13805768 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2013805768 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 14654187 Country of ref document: US |
|
| ENP | Entry into the national phase |
Ref document number: 2015548256 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 20157019917 Country of ref document: KR Kind code of ref document: A |