WO2018105198A1 - ミックスモードアフィニティクロマトグラフィー用担体 - Google Patents
ミックスモードアフィニティクロマトグラフィー用担体 Download PDFInfo
- Publication number
- WO2018105198A1 WO2018105198A1 PCT/JP2017/033642 JP2017033642W WO2018105198A1 WO 2018105198 A1 WO2018105198 A1 WO 2018105198A1 JP 2017033642 W JP2017033642 W JP 2017033642W WO 2018105198 A1 WO2018105198 A1 WO 2018105198A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- amino acid
- side chain
- carrier
- acid residue
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/281—Sorbents specially adapted for preparative, analytical or investigative chromatography
- B01J20/286—Phases chemically bonded to a substrate, e.g. to silica or to polymers
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/26—Selective adsorption, e.g. chromatography characterised by the separation mechanism
- B01D15/30—Partition chromatography
- B01D15/305—Hydrophilic interaction chromatography [HILIC]
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/26—Selective adsorption, e.g. chromatography characterised by the separation mechanism
- B01D15/36—Selective adsorption, e.g. chromatography characterised by the separation mechanism involving ionic interaction, e.g. ion-exchange, ion-pair, ion-suppression or ion-exclusion
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/26—Selective adsorption, e.g. chromatography characterised by the separation mechanism
- B01D15/36—Selective adsorption, e.g. chromatography characterised by the separation mechanism involving ionic interaction, e.g. ion-exchange, ion-pair, ion-suppression or ion-exclusion
- B01D15/361—Ion-exchange
- B01D15/362—Cation-exchange
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/26—Selective adsorption, e.g. chromatography characterised by the separation mechanism
- B01D15/38—Selective adsorption, e.g. chromatography characterised by the separation mechanism involving specific interaction not covered by one or more of groups B01D15/265 and B01D15/30 - B01D15/36, e.g. affinity, ligand exchange or chiral chromatography
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/26—Selective adsorption, e.g. chromatography characterised by the separation mechanism
- B01D15/38—Selective adsorption, e.g. chromatography characterised by the separation mechanism involving specific interaction not covered by one or more of groups B01D15/265 and B01D15/30 - B01D15/36, e.g. affinity, ligand exchange or chiral chromatography
- B01D15/3804—Affinity chromatography
- B01D15/3809—Affinity chromatography of the antigen-antibody type, e.g. protein A, G or L chromatography
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/26—Selective adsorption, e.g. chromatography characterised by the separation mechanism
- B01D15/38—Selective adsorption, e.g. chromatography characterised by the separation mechanism involving specific interaction not covered by one or more of groups B01D15/265 and B01D15/30 - B01D15/36, e.g. affinity, ligand exchange or chiral chromatography
- B01D15/3847—Multimodal interactions
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/281—Sorbents specially adapted for preparative, analytical or investigative chromatography
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/30—Processes for preparing, regenerating, or reactivating
- B01J20/32—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating
- B01J20/3202—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating characterised by the carrier, support or substrate used for impregnation or coating
- B01J20/3206—Organic carriers, supports or substrates
- B01J20/3208—Polymeric carriers, supports or substrates
- B01J20/321—Polymeric carriers, supports or substrates consisting of a polymer obtained by reactions involving only carbon to carbon unsaturated bonds
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/30—Processes for preparing, regenerating, or reactivating
- B01J20/32—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating
- B01J20/3202—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating characterised by the carrier, support or substrate used for impregnation or coating
- B01J20/3206—Organic carriers, supports or substrates
- B01J20/3208—Polymeric carriers, supports or substrates
- B01J20/3212—Polymeric carriers, supports or substrates consisting of a polymer obtained by reactions otherwise than involving only carbon to carbon unsaturated bonds
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/30—Processes for preparing, regenerating, or reactivating
- B01J20/32—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating
- B01J20/3231—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating characterised by the coating or impregnating layer
- B01J20/3242—Layers with a functional group, e.g. an affinity material, a ligand, a reactant or a complexing group
- B01J20/3268—Macromolecular compounds
- B01J20/3272—Polymers obtained by reactions otherwise than involving only carbon to carbon unsaturated bonds
- B01J20/3274—Proteins, nucleic acids, polysaccharides, antibodies or antigens
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/30—Processes for preparing, regenerating, or reactivating
- B01J20/32—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating
- B01J20/3231—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating characterised by the coating or impregnating layer
- B01J20/3242—Layers with a functional group, e.g. an affinity material, a ligand, a reactant or a complexing group
- B01J20/3285—Coating or impregnation layers comprising different type of functional groups or interactions, e.g. different ligands in various parts of the sorbent, mixed mode, dual zone, bimodal, multimodal, ionic or hydrophobic, cationic or anionic, hydrophilic or hydrophobic
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J39/00—Cation exchange; Use of material as cation exchangers; Treatment of material for improving the cation exchange properties
- B01J39/26—Cation exchangers for chromatographic processes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K1/00—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length
- C07K1/14—Extraction; Separation; Purification
- C07K1/16—Extraction; Separation; Purification by chromatography
- C07K1/165—Extraction; Separation; Purification by chromatography mixed-mode chromatography
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K1/00—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length
- C07K1/14—Extraction; Separation; Purification
- C07K1/16—Extraction; Separation; Purification by chromatography
- C07K1/22—Affinity chromatography or related techniques based upon selective absorption processes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/06—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies from serum
- C07K16/065—Purification, fragmentation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K17/00—Carrier-bound or immobilised peptides; Preparation thereof
- C07K17/02—Peptides being immobilised on, or in, an organic carrier
- C07K17/08—Peptides being immobilised on, or in, an organic carrier the carrier being a synthetic polymer
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K17/00—Carrier-bound or immobilised peptides; Preparation thereof
- C07K17/02—Peptides being immobilised on, or in, an organic carrier
- C07K17/10—Peptides being immobilised on, or in, an organic carrier the carrier being a carbohydrate
- C07K17/12—Cellulose or derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/50—Cyclic peptides containing at least one abnormal peptide link
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/64—Cyclic peptides containing only normal peptide links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/10—Immunoglobulins specific features characterized by their source of isolation or production
- C07K2317/14—Specific host cells or culture conditions, e.g. components, pH or temperature
Definitions
- the present invention relates to a carrier for mixed mode affinity chromatography.
- antibody pharmaceuticals using the functions of antibodies.
- antibody drugs work more specifically for target molecules, and are expected to reduce side effects and achieve high therapeutic effects. It contributes to the improvement.
- antibody pharmaceuticals are administered in large quantities to living bodies, their purity has a large effect on quality when compared to other recombinant protein pharmaceuticals.
- antibody drugs are produced by purifying antibodies expressed in host cells by genetic recombination, contamination of host cells and impurities derived from the production process becomes a problem.
- host cell protein (HCP) that remains as an impurity in antibody drugs is suspected to be related to the development of anaphylaxis during administration of antibody drugs, thus improving purification purity and reducing impurities. Is required.
- Patent Document 1 describes a mixed mode antibody affinity separation matrix having an antibody affinity ligand and a cation exchange group in the same separation matrix (Claim 1). Further, it is described that the antibody affinity ligand is at least one selected from protein A, protein G, protein L, protein H, protein D, protein Arp, protein Fc ⁇ R, antibody-binding synthetic ligand, and related substances. (Claim 5).
- Patent Document 2 describes a mixed-mode carrier characterized in that it has a group containing an acidic group and an affinity ligand on a synthetic polymer support (claim 11). Furthermore, protein A, protein G, protein L, protein H, protein D, protein Arp, protein Fc ⁇ R, antibody-binding synthetic peptide ligands and related substances are described as antibody affinity ligands ( ⁇ 0043>).
- Patent Document 3 describes a separating agent in which an interactive functional group is introduced into surface-modified porous crosslinked particles ( ⁇ 0011>), and an ion-exchange group; an affinity ligand as the interactive functional group
- a hydrophobic group such as an alkyl group, a phenyl group and a polyalkyl ether group is preferable, and a separating agent into which such an interactive functional group is introduced is particularly used as an adsorbent for a polymer substance such as a protein, particularly for chromatography. It describes that it can be used effectively as a separating agent ( ⁇ 0026>).
- protein A is a protein derived from Staphylococcus aureus and has high immunogenicity to the human body, it is expected to be expected when mixed with purified antibodies and administered to the human body. May cause an immune response. Since protein A is produced by genetic engineering using Escherichia coli, LPS (Lipopolysaccharide, Lipopolysaccharide; Lipid A, Lipid A) derived from Escherichia coli is mixed in the purified antibody. There is also a fear. Therefore, protein A is required to have a high degree of purification, which is one of the factors that increase the cost of antibody purification.
- the inventor conceived of using an antibody-binding peptide that can be produced at a lower cost than protein A as an affinity ligand used for a carrier for mixed mode affinity chromatography. The chemical resistance was examined.
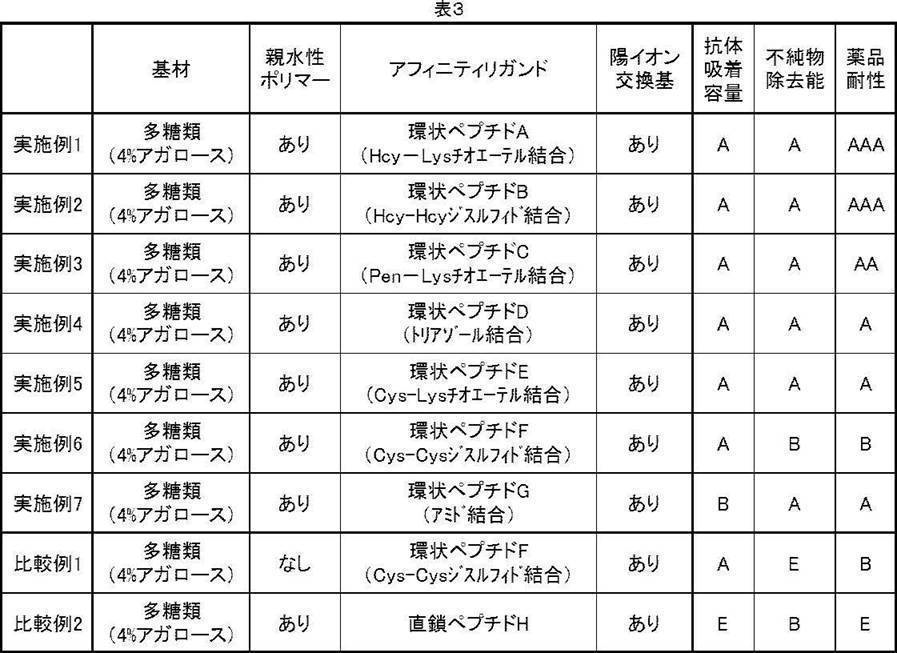
- the present inventors have found that there is room for improvement in any one or more of antibody adsorption capacity, impurity removal ability, and chemical resistance in a mixed mode affinity chromatography carrier using a linear peptide as an affinity ligand. I found out. For example, in Comparative Example 2 described later, a linear peptide is used as the affinity ligand, but the antibody adsorption capacity and chemical resistance are insufficient, and it is indicated that improvement is necessary.
- an object of the present invention is to provide a carrier for mixed mode affinity chromatography which is excellent in all of antibody adsorption capacity, impurity removal ability and chemical resistance.
- the present inventor has found that a carrier for mixed mode affinity chromatography having a substrate, a hydrophilic polymer, a cyclic peptide, and a cation exchange group is adsorbed to an antibody. It was learned that the capacity, the ability to remove impurities and the chemical resistance were all excellent, and the present invention was completed.
- a carrier for mixed mode affinity chromatography having a base material, a hydrophilic polymer, an antibody-binding cyclic peptide, and a cation exchange group.
- the intramolecular bridge includes at least one selected from the group consisting of a disulfide bond, a thioether bond, a triazole bond, and an amide bond.
- the side chain thiol group of the first amino acid residue derived from an amino acid having a thiol group in the side chain selected from the group consisting of cysteine, homocysteine and penicillamine, and cysteine, homocysteine and penicillamine A disulfide bond formed between the side chain thiol group of the second amino acid residue derived from an amino acid having a thiol group in the side chain selected from the group consisting of cysteine and homocysteine
- a side chain thiol group of a first amino acid residue derived from an amino acid having a thiol group in a side chain selected from the group consisting of penicillamine and a second amino acid residue derived from an amino acid having a haloacetyl group in the side chain [4] A thioether bond formed with a side chain haloacetyl group.
- the disulfide bond is selected from the group consisting of the side chain thiol group of the first amino acid residue derived from an amino acid having a thiol group in the side chain selected from the group consisting of homocysteine and penicillamine, and homocysteine and penicillamine.
- a side chain thiol group of a first amino acid residue derived from an amino acid having a thiol group in the selected side chain and a side chain haloacetyl group of a second amino acid residue derived from an amino acid having a haloacetyl group in the side chain Any one of the above-mentioned [4] to [6], which is a thioether bond formed between Support for Cusmode affinity chromatography.
- the disulfide bond is a disulfide bond formed between the side chain thiol group of the first amino acid residue derived from homocysteine and the side chain thiol group of the second amino acid residue derived from homocysteine.
- the thioether bond is formed between the side chain thiol group of the first amino acid residue derived from homocysteine and the side chain haloacetyl group of the second amino acid residue derived from an amino acid having a haloacetyl group in the side chain
- [10] The carrier for mixed mode affinity chromatography according to any one of [2] to [9] above, wherein the number of amino acid residues in the cyclic portion is 8 to 14 residues.
- the linear part includes an amino acid residue having at least one selected from the group consisting of a hydroxy group and a carboxy group in the side chain.
- Carrier for affinity chromatography [15] The carrier for mixed mode affinity chromatography according to any one of [1] to [14], wherein the substrate is at least one selected from the group consisting of agarose and cellulose.
- the present invention it is possible to provide a carrier for mixed mode affinity chromatography which is excellent in all of antibody adsorption capacity, impurity removal ability and chemical resistance.
- the carrier for mixed mode affinity chromatography of the present invention has a substrate, a hydrophilic polymer, an antibody-binding cyclic peptide, and a cation exchange group.
- the carrier for mixed mode affinity chromatography of the present invention has such a structure, it is considered that it has excellent antibody adsorption capacity, impurity removal ability, and chemical resistance when applied to affinity chromatography for antibody purification. .
- the reason is not limited, it is estimated that the reason is as follows.
- both ligands act in concert and have specific adsorption ability and aggregate removal ability, so that the antibody adsorption capacity and impurity removal It was excellent in both performance and chemical resistance.
- the impurity removal ability is the ratio of the HCP amount before purification (ppm) to the HCP amount after purification (ppm) HCP purification factor [HCP amount before purification (ppm) / HCP amount after purification (Ppm)], which is a measure of the impurity removal performance of the chromatographic support.
- the substrate used for the carrier for mixed mode affinity chromatography of the present invention is not particularly limited, but is preferably at least one selected from the group consisting of polysaccharides, acrylate polymers, methacrylate polymers, and styrene polymers. More preferably, it is at least one selected from the group consisting of polysaccharides, acrylate polymers and methacrylate polymers, and more preferably at least one selected from the group consisting of agarose and cellulose.
- a base material may be used individually by 1 type, and may be used in combination of 2 or more type.
- the polysaccharide is not particularly limited, and examples thereof include natural polysaccharides such as cellulose, agarose, dextran, chitosan, and glucomannan, and cross-linked polysaccharides in which a cross-linked structure is introduced into these natural polysaccharides.
- Cross-linked polysaccharides are produced, for example, by introducing a cross-linked structure to the hydroxyl groups of natural polysaccharides using a cross-linking agent such as epichlorohydrin, (poly) alkylene glycol diglycidyl ether, and alkylene diisocyanate. can do.
- the polysaccharide is preferably at least one selected from cellulose, crosslinked cellulose, agarose and crosslinked agarose, more preferably at least one selected from agarose and crosslinked agarose.
- the acrylate polymer is not particularly limited.
- a polymer obtained by polymerizing one kind of acrylate ester such as monoacrylate, glycidyl acrylate, 4,5-epoxybutyl acrylate, and 9,10-epoxystearyl acrylate, and two or more kinds of acrylate esters are copolymerized.
- a copolymer obtained by copolymerizing at least one acrylic ester and at least one vinyl group-containing compound other than the acrylic ester for example, ethylene and monovinyl compounds such as propylene, aromatic polyvinyl compounds such as divinylbenzene and trivinylbenzene, and butadiene, methylenebisacrylamide, And polyvinyl compounds such as triallyl isocyanurate.
- a crosslinked structure may be introduced into these polymers or copolymers using a crosslinking agent such as epichlorohydrin, (poly) alkylene glycol diglycidyl ether, and alkylene diisocyanate.
- the methacrylate polymer is not particularly limited.
- the methacrylate polymer is not particularly limited.
- Examples of the vinyl group-containing compound other than the methacrylic acid ester include the compounds exemplified for the vinyl group-containing compound other than the acrylic acid ester described above. You may introduce
- the styrene polymer is not particularly limited.
- a polymer obtained by polymerizing one kind of styrene compound such as styrene, methylstyrene, ethylstyrene, hydroxystyrene, and chlorostyrene, styrene
- a copolymer obtained by polymerizing two or more kinds of styrene compounds, a copolymer obtained by copolymerizing one or more kinds of styrene compounds and one or more kinds of vinyl group-containing compounds other than styrene compounds, and the like Can be mentioned.
- Examples of the vinyl group-containing compound other than the styrene compound include the compounds exemplified for the vinyl group-containing compound other than the acrylate ester described above. You may introduce
- the substrate is preferably a porous particle or a porous membrane.
- the substrate is a porous particle or a porous film, the surface area is increased, and the processing capacity per unit time can be increased.
- the pore volume when the substrate is a porous particle or a porous membrane is not particularly limited, but the pore volume measured with a mercury porosimeter is preferably 0.2 mL / g to 10 mL / g, more preferably 0. Within the range of 2 mL / g to 5.0 mL / g. When the pore volume is within this range, the antibody adsorption capacity increases. Further, the mechanical strength does not decrease.
- the specific surface area when the substrate is a porous particle or a porous film is not particularly limited, but the specific surface area (BET specific surface area) measured by the BET (Brunauer, Emmett, Teller) method is preferably 2 m 2 / g. It is in the range of ⁇ 1500 m 2 / g, more preferably 5 m 2 / g to 1000 m 2 / g. When the specific surface area is within this range, the antibody adsorption capacity increases.
- the average particle diameter when the substrate is porous particles is not particularly limited, but is preferably in the range of 0.5 ⁇ m to 1000 ⁇ m, more preferably 1 ⁇ m to 250 ⁇ m, and still more preferably 2 ⁇ m to 150 ⁇ m. When the average particle diameter is within this range, the pressure loss when the column is filled and passed is small, the flow rate can be increased, the processing efficiency is improved, and the antibody adsorption capacity is increased.
- the average particle diameter of the porous particles can be measured by a known method. For example, the average particle diameter can be obtained by measuring the particle diameter of 100 or more porous particles with an optical microscope and calculating the median diameter from the distribution.
- Specific examples of substrate> Specific examples of the base material include, for example, Sepharose series (manufactured by GE Healthcare) (“SEPHAROSE” is a registered trademark) which is an agarose-based carrier, Cellfine series (manufactured by JNC) which is a cellulose-based cross-linking carrier ( “CELLUFINE” is a registered trademark), Sephacryl series (manufactured by GE Healthcare) which is a cross-linked polymer of allyl dextran and N, N′-methylenebisacrylamide (“SEPHACRYL” is a registered trademark), and an acrylate carrier
- a commercial product such as a certain Toyopearl HW series (manufactured by Tosoh Corporation) (“Toyopearl” and “TOYOPEARL” are registered trademarks) is mentioned, but is not limited thereto.
- a material obtained by introducing a functional group capable of covalently bonding with a hydroxyl group such as an epoxy group into a commercially available substrate may be used as the substrate.
- a carrier in which an agarose hydroxy group is glycidylated by treating an agarose-based carrier with 2-chloromethyloxirane (also known as epichlorohydrin) and an epoxy group is introduced on the surface can be used.
- ⁇ Hydrophilic polymer> By coating the substrate with a hydrophilic polymer, the hydrophilicity of the surface of the carrier for mixed mode affinity chromatography of the present invention is increased, and the adsorption of non-specific adsorbents is suppressed, so that the purification purity is improved. .
- the hydrophilic polymer used for the carrier for mixed mode affinity chromatography of the present invention is not particularly limited, but is preferably at least one selected from the group consisting of hydrophilic polysaccharides, more preferably dextran, carboxymethyldextran, It is at least one selected from the group consisting of pullulan, hydroxyethyl cellulose, and carboxymethyl cellulose, and more preferably at least one selected from the group consisting of dextran, carboxymethyl dextran, and pullulan.
- hydrophilic polymer one kind may be used alone, or two or more kinds may be used in combination.
- the hydrophilic polymer is fixed to the substrate by a covalent bond.
- the substrate is a porous particle, it preferably has a functional group that can be covalently bonded to a hydroxy group on the surface.
- the functional group capable of covalently bonding to a hydroxy group include an epoxy group and a glycidyl group; a hydroxy group activated by cyanogen bromide, N, N-disuccinimidyl carbonate (DSC), etc .; an aldehyde And reactive functional groups such as activated carboxylic acid groups such as N-hydroxysuccinimide ester and carbonyldiimidazole activated ester.
- hydrophilic polysaccharide is not particularly limited, but is preferably at least one selected from dextran, carboxymethyl dextran, and pullulan, and more preferably dextran because of its high effect of improving purification purity.
- the molecular weight of the hydrophilic polymer is not particularly limited, but is an intrinsic viscosity, preferably 0.10 dL / g or more, more preferably 0.10 dL / g to 0.90 dL / g, and still more preferably 0.12 dL / g to 0. .40 dL / g, more preferably in the range of 0.15 dL / g to 0.30 dL / g, even more preferably in the range of 0.15 dL / g to 0.25 dL / g.
- the intrinsic viscosity is within this range, the purification purity is further improved.
- the intrinsic viscosity is determined by determining the viscosity of several polymer solutions having different concentrations according to the viscosity measurement method in the general measurement method listed in the 16th revised Japanese Pharmacopoeia, the first method “capillary viscometer method”. Can be obtained by measuring the concentration dependence of the curve and extrapolating the obtained straight line concentration to zero.
- ⁇ Dextran intrinsic viscosity
- Mw Dextran weight average molecular weight
- the coating amount of the hydrophilic polymer (hereinafter sometimes simply referred to as “hydrophilic polymer coating amount”) is not particularly limited, but is preferably 3 mg / g-dry gel to 450 mg / g-dry gel, more preferably 3 mg. / G-dry gel to 250 mg / g-dry gel, more preferably 3 mg / g-dry gel to 230 mg / g-dry gel, more preferably 10 mg / g-dry gel to 230 mg / g-dry gel, more preferably Is 20 mg / g-dry gel to 230 mg / g-dry gel.
- the hydrophilic polymer coating amount is within this range, the hydrophilicity of the surface of the carrier for mixed mode affinity chromatography of the present invention is moderately increased to suppress the adsorption of non-specific adsorbents, and the antibody is supported on the substrate. Since there is a lot of room for diffusion and penetration and the antibody adsorption capacity is increased, the purification purity is improved and the purification cost is reduced.
- the hydrophilic polymer does not need to cover the entire surface of the base material, and may cover at least a part of the base material.
- the hydrophilic polymer coating amount [unit: mg / g-dry gel] is the dry mass (W P ) [unit: mg] of the coated hydrophilic polymer, and the dry mass (W 0) of the substrate before coating. ) [Unit: g-dry gel]. Further, the dry weight (W P ) of the hydrophilic polymer is the difference (W 1 ⁇ W 0 ) [unit: mg] between the dry weight (W 1 ) of the total amount of the carrier and the dry weight (W 0 ) of the substrate before coating. is there. Therefore, the hydrophilic polymer coating amount can be obtained by the following formula.
- the carrier the total amount of the dry weight (W 1) can also be calculated in the same manner.
- the hydrophilicity of the polymer or polysaccharide means that it contains at least one kind of hydrophilic group.
- the hydrophilic group is preferably a carboxy group, an alkali metal salt of a carboxy group, a sulfonic acid group, an alkali metal salt of a sulfonic acid group, a hydroxy group, an amide group, a carbamoyl group, a sulfonamide group, a sulfamoyl group, a phosphoric acid group, Functional groups such as alkali metal salts of phosphoric acid groups, oxyphosphoric acid groups, and alkali metal salts of oxyphosphoric acid groups may be mentioned.
- These hydrophilic groups may be present at any position in the polymer, and may be bonded, for example, directly or via a linking group to the polymer main chain end and / or side chain. A plurality of hydrophilic groups are preferably present in one molecule.
- the antibody-binding cyclic peptide used for the carrier for mixed mode affinity chromatography of the present invention is not particularly limited, but preferably has a cyclic portion cyclized by intramolecular crosslinking between side chains.
- the intramolecular bridge preferably includes at least one selected from the group consisting of a disulfide bond, a thioether bond, a triazole bond, and an amide bond, and more preferably a group consisting of a disulfide bond, a thioether bond, and a triazole bond. And more preferably a disulfide bond or a thioether bond.
- the antibody-binding cyclic peptide may be simply referred to as “cyclic peptide” or “affinity ligand”.
- the disulfide bond is not particularly limited as long as it is an “SS” bond, and examples thereof include an SS bond formed between two thiol groups (also referred to as “mercapto groups”).
- the disulfide bond is preferably such that the side chain thiol group of the first amino acid residue derived from an amino acid having a thiol group in the side chain and the second amino acid residue derived from an amino acid having a thiol group in the side chain It is a disulfide bond formed between the side chain thiol groups of the group.
- the disulfide bond is more preferably the side chain thiol group of the first amino acid residue derived from an amino acid having a thiol group in the side chain other than L-cysteine and D-cysteine, and L-cysteine and D- It is a disulfide bond formed between the side chain thiol group of the second amino acid residue derived from an amino acid having a thiol group in the side chain other than cysteine.
- the disulfide bond is more preferably a side chain thiol group of a first amino acid residue derived from an amino acid having a thiol group in a side chain selected from the group consisting of cysteine, homocysteine and penicillamine, and cysteine, It is a disulfide bond formed between the side chain thiol group of the second amino acid residue derived from an amino acid having a thiol group in the side chain selected from the group consisting of homocysteine and penicillamine.
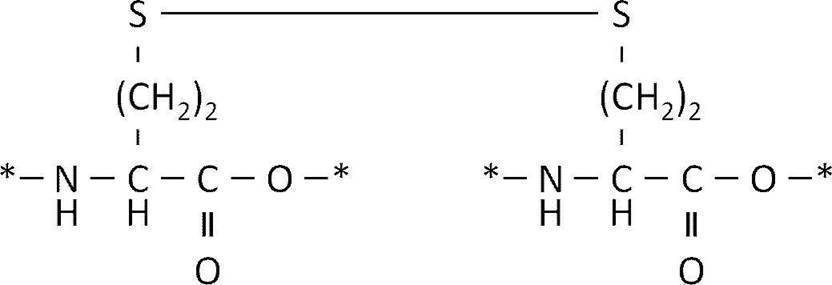
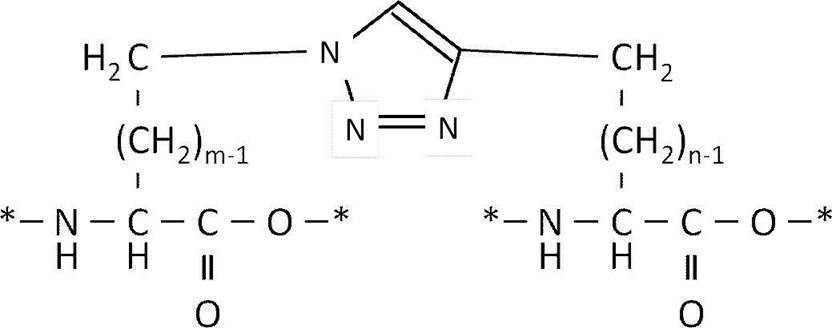
- Examples of such disulfide bonds include those represented by the following formula.
- the disulfide bond is more preferably the side chain thiol group of the first amino acid residue derived from an amino acid having a thiol group in the side chain selected from the group consisting of homocysteine and penicillamine, homocysteine and penicillamine
- Examples of such disulfide bonds include those represented by the following formula.
- the disulfide bond is more preferably formed between the side chain thiol group of the first amino acid residue derived from homocysteine and the side chain thiol group of the second amino acid residue derived from homocysteine. Disulfide bond.
- Examples of such disulfide bonds include those represented by the following formula.
- * represents a point of attachment to another amino acid residue or another substituent.
- disulfide bond Since the disulfide bond has a high alkali resistance, the support for mixed mode affinity chromatography can maintain the antibody binding property even when repeated washing with alkali is performed, thereby reducing the antibody purification cost.
- a disulfide bond other than a disulfide bond formed between two cysteine residues is preferable, and a disulfide formed between amino acid residues derived from an amino acid having a thiol group in a side chain other than cysteine A bond is more preferred, and a disulfide bond formed between two homocysteine residues is particularly preferred.
- the thioether bond is not particularly limited as long as it is an “—S—” bond in which the oxygen atom of the ether bond “—O—” is substituted with a sulfur atom.
- An —S— bond formed with a haloacetyl group can be mentioned.
- the haloacetyl group is preferably a chloroacetyl group or a bromoacetyl group, and more preferably a chloroacetyl group.
- the haloacetyl group is preferably one introduced into an amino acid in the form of replacing a hydrogen atom of the side chain amino group.
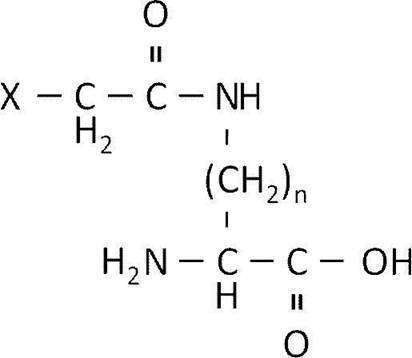
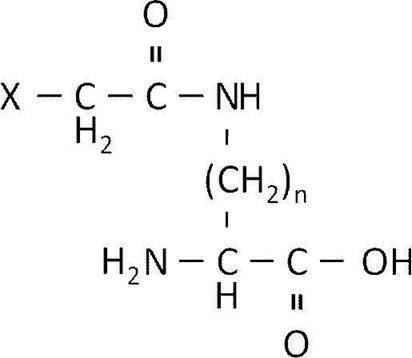
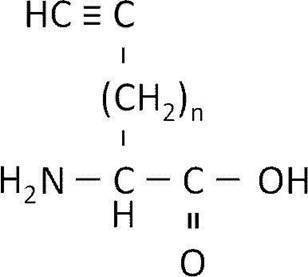
- amino acids having a haloacetyl group in the side chain include those represented by the following formulae.
- n is an integer greater than or equal to 1
- X is a halogen atom.
- n is an integer that preferably satisfies 1 ⁇ n ⁇ 4
- X is preferably a chlorine atom or a bromine atom, and more preferably a chlorine atom.
- the thioether bond is preferably such that the side chain thiol group of the first amino acid residue derived from an amino acid having a thiol group in the side chain and the second amino acid residue derived from an amino acid having a haloacetyl group in the side chain It is a thioether bond formed with the side chain haloacetyl group of the group.
- the thioether bond is more preferably a side chain thiol group of the first amino acid residue derived from an amino acid having a thiol group on the side chain other than L-cysteine and D-cysteine and a haloacetyl group on the side chain. It is a thioether bond formed with the side chain haloacetyl group of the second amino acid residue derived from the amino acid having it.
- the thioether bond is more preferably the side chain thiol group and side chain of the first amino acid residue derived from an amino acid having a thiol group in the side chain selected from the group consisting of cysteine, homocysteine and penicillamine It is a thioether bond formed with the side chain haloacetyl group of the second amino acid residue derived from an amino acid having a haloacetyl group.
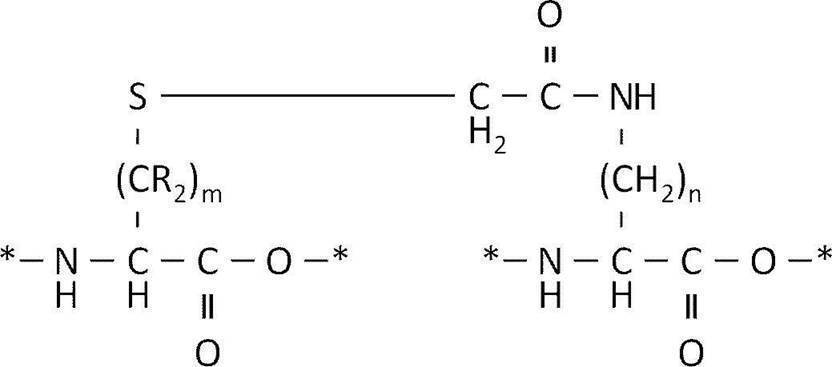
- Examples of such a thioether bond include those represented by the following formula.
- N is preferably an integer satisfying 1 ⁇ n ⁇ 4.
- the thioether bond is more preferably a side chain thiol group of a first amino acid residue derived from an amino acid having a thiol group in a side chain selected from the group consisting of homocysteine and penicillamine and a haloacetyl group in the side chain It is a thioether bond formed with a side chain haloacetyl group of a second amino acid residue derived from an amino acid having a group.
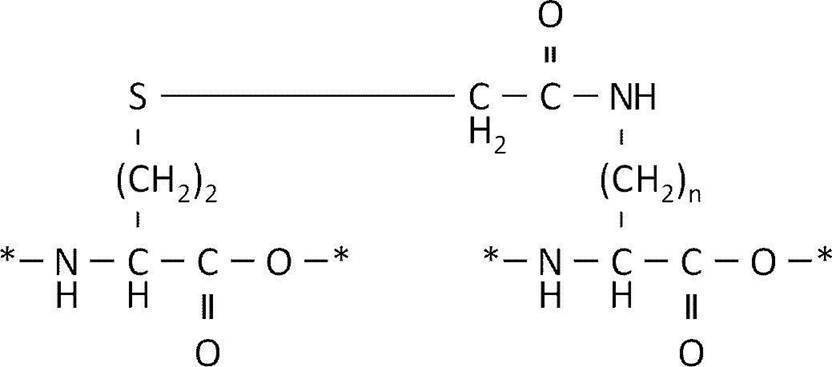
- Examples of such a thioether bond include those represented by the following formula.
- N is preferably an integer satisfying 1 ⁇ n ⁇ 4.
- the thioether bond is more preferably a side chain thioacetyl group of a first amino acid residue derived from homocysteine and a side chain haloacetyl of a second amino acid residue derived from an amino acid having a haloacetyl group in the side chain.
- Examples of such a thioether bond include those represented by the following formula.
- n is an integer of 1 or more, and * represents a point of attachment to another amino acid residue or another substituent.
- N is preferably an integer satisfying 1 ⁇ n ⁇ 4.
- thioether bond Since the thioether bond has a high alkali resistance, the support for mixed mode affinity chromatography can maintain the antibody binding property even if the washing with alkali is repeatedly performed, and the antibody purification cost can be reduced.
- a thioether bond a thioether bond formed between a homocysteine residue and an N- ⁇ -chloroacetyllysine residue is particularly preferable.
- the triazole bond is not particularly limited, but is preferably a second amino acid derived from an amino acid having a side chain azide group of the first amino acid residue derived from an amino acid having an azide group in the side chain and an amino acid having an alkynyl group in the side chain.
- * is a bonding point with other amino acid residues or other substituents
- m and n are each independently an integer of 1 or more, preferably each independently an integer of 1 or more. And at least one is an integer of 2 or more.
- the amino acid residue derived from an amino acid having an azide group in the side chain is an amino acid residue derived from ⁇ -azido-L-alanine or ⁇ -azido-D-alanine, preferably ⁇ An amino acid residue derived from azido-L-alanine.
- the amino acid residue derived from an amino acid having an azide group in the side chain is an amino acid residue derived from ⁇ -azido-L-homoalanine or ⁇ -azido-D-homoalanine, preferably ⁇ -azido-L-homoalanine.
- the amino acid residue derived from an amino acid having an azide group in the side chain is an amino acid residue derived from ⁇ -azido-L-ornithine or ⁇ -azido-D-ornithine, preferably ⁇ -Azido-L-ornithine.
- the amino acid residue derived from an amino acid having an azide group in the side chain is an amino acid residue derived from ⁇ -azido-L-lysine or ⁇ -azido-D-lysine, preferably ⁇ -Azido-L-lysine.
- an amino acid residue derived from an amino acid having an alkynyl group in the side chain is 2-propargyl-L-glycine [(2S) -2-amino-4-pentynoic acid] or D-propargylglycine [ (2R) -2-amino-4-pentynoic acid], preferably an amino acid residue derived from 2-propargyl-L-glycine [(2S) -2-amino-4-pentynoic acid] It is a group.
- the amino acid residue derived from an amino acid having an alkynyl group in the side chain is 2-propargyl-L-alanine (L-homopropargylglycine) [(2S) -2-amino-5-hexynoic acid ]
- 2-propargyl-L-alanine (L -Homopropargylglycine) [(2S) -2-amino-5-hexynoic acid].
- the amino acid residue derived from an amino acid having an alkynyl group in the side chain is 2-propargyl-L-homoalanine (2-propargyl-L-bishomoglycine) [(2S) -2-amino- 6-heptynoic acid] or 2-propargyl-D-homoalanine (2-propargyl-D-bishomoglycine) [(2R) -2-amino-6-heptynoic acid], preferably 2 -An amino acid residue derived from propargyl-L-homoalanine (2-propargyl-L-bishomoglycine) [(2S) -2-amino-6-heptynoic acid].
- triazole bond Since triazole bonds have high alkali resistance, mixed mode affinity chromatography supports maintain antibody binding properties even when repeated washing with alkali reduces the cost of antibody purification if triazole bonds are included in the intramolecular crosslinks. be able to.
- a triazole bond is particularly preferably a triazole bond formed between a ⁇ -azidohomoalanine residue or ⁇ -azidricine residue and a homopropargylglycine residue or bishomopropargylglycine residue.
- the amide bond is not particularly limited, but preferably a second amino acid derived from an amino acid having a side chain amino group of a first amino acid residue derived from an amino acid having an amino group in the side chain and an amino acid having a carboxy group in the side chain It is an amide bond formed with the side chain carboxy group of the residue.
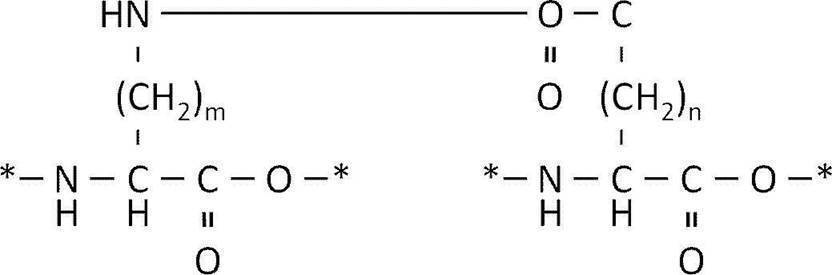
- amide bond formed Between the side chain amino group of the first amino acid residue derived from an amino acid having an amino group in the side chain and the side chain carboxy group of a second amino acid residue derived from an amino acid having a carboxy group in the side chain Examples of the amide bond formed include those represented by the following formula.
- * is a point of attachment with other amino acid residues or other substituents
- an amino acid residue derived from an amino acid having an amino group in the side chain is L-2,3-diaminopropanoic acid [(2S) -2,3-diaminopropanoic acid] or D-2, It is an amino acid residue derived from 3-diaminopropanoic acid [(2R) -2,3-diaminopropanoic acid], preferably L-2,3-diaminopropanoic acid [(2S) -2-aminopropanoic acid]. It is an amino acid residue derived from.
- the amino acid residue derived from the amino acid having an amino group in the side chain is L-lysine [(2S) -2,6-diaminohexanoic acid] or D-lysine [(2R) -2, Amino acid residues derived from 6-diaminohexanoic acid], preferably amino acid residues derived from L-lysine [(2S) -2,6-diaminohexanoic acid].
- the amino acid residue derived from an amino acid having a carboxy group in the side chain is an amino acid residue derived from L-aspartic acid or D-aspartic acid, and preferably derived from L-aspartic acid An amino acid residue.
- the amino acid residue derived from an amino acid having a carboxy group in the side chain is an amino acid residue derived from L-glutamic acid or D-glutamic acid, preferably an amino acid residue derived from L-glutamic acid It is.
- the amino acid residue derived from the amino acid having a carboxy group in the side chain is L-homoglutamic acid [(2S) -2-aminoadipic acid] or D-homoglutamic acid [(2R) -2- Amino acid residues derived from [amino adipic acid], preferably amino acid residues derived from L-homoglutamic acid [(2S) -2-aminoadipic acid].
- amide bond (Particularly preferred amide bond) Since the amide bond has a high alkali resistance, the carrier for mixed mode affinity chromatography can maintain the antibody binding property even if the washing with alkali is repeatedly performed, and the antibody purification cost can be reduced.
- an amide bond formed between a lysine residue and a glutamic acid residue is particularly preferable.
- the number of amino acid residues in the cyclic portion is not particularly limited as long as it is equal to or less than the total number of amino acid residues in the cyclic peptide, preferably 8 to 14 residues, more preferably 9 to 13 residues, Preferably it is 10-12 residues, more preferably 11 residues.
- the cyclic peptide may have a linear part.
- a linear part means the part which is not contained in a cyclic part among the polypeptide chains of the said cyclic peptide.
- the linear part may contain an amino acid residue having at least one selected from the group consisting of a hydroxy group and a carboxy group in the side chain.
- the amino acid residue having at least one selected from the group consisting of a hydroxy group and a carboxy group in the side chain will be described later.
- the linear part may contain an amino acid residue derived from an amino acid having an immobilized functional group in the side chain.
- the immobilized functional group and the amino acid having the immobilized functional group will be described later.
- the cyclic peptide is preferably bonded to at least one of the base material and the hydrophilic polymer via a covalent bond.
- a covalent bond includes (a) a covalent bond between the amino acid residue side chain of the cyclic peptide linear chain portion and at least one of the substrate and the hydrophilic polymer, or (b) the polypeptide chain of the cyclic peptide. Examples include a covalent bond between the N-terminal or C-terminal and at least one of the substrate and the hydrophilic polymer.
- the immobilized functional group of the amino acid residue side chain and at least one reactive functional group of the substrate and the hydrophilic polymer can react with the immobilized functional group to form a covalent bond).
- the immobilized functional group and reactive functional group in this case will be described later.
- Examples of the covalent bond in (b) above include a bond between or without a linker between the N-terminal or C-terminal of the polypeptide chain and at least one polymer main chain or side chain of the base material and the hydrophilic polymer. Is mentioned.
- the linker in this case include a PEG (Polyethylene glycol) linker. The number of ethylene glycol units in the PEG linker is not particularly limited as long as it is 1 or more, but is preferably 1 to 24, more preferably 1 to 12, and further preferably 4 to 8.
- the molecular weight of the cyclic peptide is not particularly limited, but is preferably 10,000 or less from the viewpoint of synthesis cost, and preferably 5000 or less from the viewpoint of antigenicity.
- the molecular weight of the cyclic peptide is more preferably about 4000 or less, still more preferably about 3000 or less, and most preferably about 2000 or less.
- “about” means including a range of ⁇ 2%.
- the molecular weight of the cyclic peptide is the combined molecular weight of the cyclic part and the linear part. When the molecular weight is less than 5,000, the antigenicity is reduced and substantially no antigenicity is exhibited.
- the number of amino acid residues of the cyclic peptide is not particularly limited, but is preferably 100 residues or less, more preferably 50 residues or less, still more preferably 40 residues or less, and even more preferably 30 There are no more than residues, even more preferably no more than 20 residues.
- the number of amino acid residues of the cyclic peptide is the number of amino acid residues in which the cyclic part and the linear part are combined.
- antibody binding refers to binding to an antibody and / or antibody derivative.
- An antibody refers to an immunoglobulin or an analog, fragment or fusion thereof.
- Immunoglobulins include IgG (Immunoglobulin G), IgM (Immunoglobulin M; Immunoglobulin M), IgA (Immunoglobulin A; Immunoglobulin A), IgD (Immunoglobulin D; Immunoglobulin D) and IgE (Immunoglobulin; Immunoglobulin; Any of the five classes (isotypes) of globulin E) is preferred, but IgG or IgM is preferred, and IgG is more preferred.
- An analog also refers to a natural or artificially produced protein or protein conjugate in which the structure or function of the immunoglobulin is at least partially retained.
- a fragment refers to a protein having a partial structure of an immunoglobulin produced by enzymatic treatment or genetic engineering design.
- a fusion refers to a protein produced by genetically fusing a functional part of a protein having biological activity, such as various cytokines and cytokine receptors, with all or part of an immunoglobulin.
- a derivative is a chimeric antibody in which the Fc region of human immunoglobulin and the Fab region of non-human mammalian immunoglobulin are fused, some Fc regions of human immunoglobulin and some of non-human mammalian immunoglobulins
- amino acids are, in principle, a joint naming committee by the International Union of Pure and Applied Chemistry and the International Union of Biochemistry and Molecular Biology. It is expressed using names, abbreviations, etc. adopted in Commission on Biochemical Nomenclature (JCBN)).
- An amino acid residue is expressed using an abbreviation of the amino acid from which the amino acid residue is derived.
- the amino acid residue includes an N-terminal amino acid (N-terminal residue) and a C-terminal amino acid (C-terminal residue).
- the amino acid sequence of a peptide or protein (also referred to as “primary structure”) represents amino acid residues arranged one-dimensionally from the N-terminus to the C-terminus from the left end to the right end.
- a number indicating the number of the amino acid residue from the N-terminal side is attached to the right side of the abbreviation of the amino acid residue. May be expressed.
- the second L-lysine from the N-terminus may be expressed as Lys2.
- amino acids when expressed using their names and there are isomers in the enantiomeric relationship, that is, L-form and D-form, the distinction between L-form and D-form is explicitly shown. Except for the case, it shall represent L body in principle.
- isoleucine represents “L-isoleucine”
- the enantiomer of “isoleucine” represents “D-isoleucine”. The same applies to amino acid residues.
- Diastereomers are treated as different types of amino acids using the prefix “Allo”. For example, “threonine” and “L-threonine” do not include “L-allthreonine”, and “D-threonine” does not include “D-allthreonine”. The same applies to amino acid residues.
- Table 1 shows amino acid names and abbreviations (one-letter abbreviation, three-letter abbreviation) in which one-letter abbreviation and three-letter abbreviation are officially recognized.
- amino acids are not limited to those listed in Table 1, and amino acids called abnormal amino acids can also be used. Examples of abnormal amino acids are listed in Table 2 below, but are not limited thereto.
- the cyclic peptide is preferably a cyclic peptide represented by the following formula (I).
- Xn intends that n Xs are linked. In other words, it can be said to be-(X) n- .
- the definitions of X g , X i , X m , X j , and X h are the same as those of X n above.
- cyclic part In the cyclic peptide used for the carrier for mixed mode affinity chromatography of the present invention, the part of the ring closed by crosslinking in the polypeptide chain is called the cyclic part, and the part not included in the cyclic part is called the linear part.
- the portion forming the intramolecular cross-linked structure of the cyclic peptide of the present invention is referred to as a cross-linked portion, and the portion that strongly contributes to the antibody binding property of the cyclic peptide of the present invention is referred to as an antibody binding portion.
- the cyclic part of the cyclic peptide represented by the formula (I) is the “X a -X m -X 1 -X 2 -X 3 -X n -X b ” part, and the linear part is “X g ”, “ X h ”,“ X i ”, and“ X j ”, the cross-linking portions are“ X a ”and“ X b ”, and the antibody binding portion is“ X 1 -X 2 -X 3 ”.
- [X i -X a -X m -X 1 -X 2 -X 3 -X n -X b -X j ] may be referred to as a repeating part.
- X 1 is an L-leucine residue, an L-isoleucine residue, an L-methionine residue, an L-lysine residue, or an L-arginine residue, preferably an L-leucine residue Group or L-isoleucine residue, more preferably L-leucine residue.
- X 2 is an L-valine residue or an L-isoleucine residue, preferably an L-valine residue.
- X 3 is an L-tryptophan residue or an L-phenylalanine residue, preferably an L-tryptophan residue.
- Xa and Xb are any one of the following (a) to (d).
- Xa and Xb are cross-linked by a disulfide bond.
- X a and X b are preferably each independently an amino acid residue derived from an amino acid having a thiol group in the side chain, and more preferably at least one of X a and X b is L-cysteine and D- It is an amino acid residue derived from an amino acid having a thiol group in a side chain other than cysteine, and more preferably, both X a and X b are amino acids having a thiol group in a side chain other than L-cysteine and D-cysteine. It is an amino acid residue derived from.
- a disulfide bond between X a and X b is preferably a disulfide bond between the two amino acid residues from an amino acid having a thiol group in a side chain, more preferably, L- cysteine and D- cysteine A disulfide bond between an amino acid residue derived from an amino acid having a thiol group in the side chain and an amino acid residue derived from an amino acid having a thiol group in the side chain, and more preferably L-cysteine and D-cysteine It is a disulfide bond between two amino acid residues having a thiol group in the side chain other than.
- Chemical resistance of X a and X b between cyclic peptide composed is crosslinked by a disulfide bond is usually compared to the case both X a and X b is an amino acid residue derived from a L- cysteine or D- cysteine , X a and X b are higher when one is an amino acid residue derived from an amino acid having a thiol group in the side chain other than L-cysteine and D-cysteine, and both X a and X b Is even higher when the amino acid residue is derived from an amino acid having a thiol group in the side chain other than L-cysteine and D-cysteine.
- the disulfide bond is more preferably a disulfide bond other than a disulfide bond between two amino acid residues derived from L-cysteine or D-cysteine, and a side other than L-cysteine and D-cysteine.
- a disulfide bond between two amino acid residues derived from an amino acid having a thiol group in the chain is more preferred, and a disulfide bond between two amino acid residues derived from homocysteine is particularly preferred.
- amino acids having a thiol group in the side chain examples include L-cysteine, D-cysteine, L-homocysteine, D-homocysteine, L-penicillamine, D-penicillamine, and the like.
- An amino acid selected from the group consisting of penicillamine is preferred.
- amino acids having a thiol group in the side chain other than L-cysteine and D-cysteine include L-homocysteine, D-homocysteine, L-penicillamine, and D-penicillamine.
- amino acids selected from the group consisting of penicillamine examples include L-cysteine, D-cysteine, L-homocysteine, D-penicillamine, and D-penicillamine.
- X a and X b are cross-linked by thioether bonds.
- X a and X b are preferably amino acid residues derived from an amino acid having one side chain having a thiol group and the other side derived from an amino acid having a side chain having a haloacetyl group.
- the amino acid having a thiol group in the side chain is preferably an amino acid having a thiol group in a side chain other than L-cysteine and D-cysteine.
- the amino acid having a thiol group in the side chain is preferably an amino acid having a thiol group in the side chain selected from the group consisting of cysteine, homocysteine and penicillamine.
- the amino acid having a thiol group in the side chain is more preferably an amino acid having a thiol group in the side chain selected from the group consisting of homocysteine and penicillamine, and more preferably homocysteine.
- the amino acid having a haloacetyl group in the side chain is preferably an amino acid represented by the following formula.
- n is an integer greater than or equal to 1
- X is a halogen atom.
- n is an integer that preferably satisfies 1 ⁇ n ⁇ 4
- X is preferably a chlorine atom or a bromine atom, and more preferably a chlorine atom.
- the amino acid having a haloacetyl group in the side chain is particularly preferably N- ⁇ -chloroacetyl-L-lysine, N- ⁇ -chloroacetyl-D-lysine, N- ⁇ -chloroacetyl-L-ornithine, or N- ⁇ -chloroacetyl-D-ornithine, particularly preferably N- ⁇ -chloroacetyl-L-lysine or N- ⁇ -chloroacetyl-L-ornithine, most preferably N- ⁇ -chloroacetyl-L- Ornithine.
- X a and X b are cross-linked by a triazole bond.
- X a and X b are preferably amino acid residues derived from an amino acid having one side chain having an azide group, and the other being an amino acid residue derived from an amino acid having an alkynyl group in the side chain.
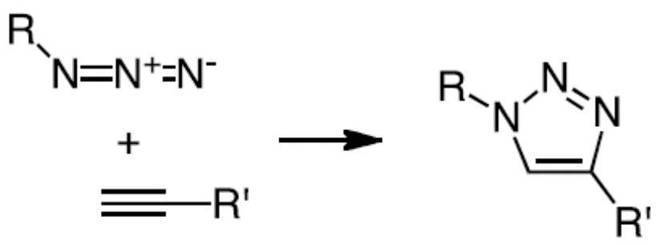
- the triazole bond is a bond formed by an azide group and an alkynyl group by the Huisgen reaction represented by the following formula.
- R represents a portion other than the azide group of the amino acid residue having an azide group in the side chain
- R ′ represents a portion other than the ethynyl group of the amino acid residue having an alkynyl group in the side chain.
- amino acid having an azido group in the side chain examples include those represented by the following formula. However, in the following formula, m is an integer of 1 or more.
- the amino acid having an azide group in the side chain represented by the above formula is ⁇ -azido-L-homoalanine or ⁇ -azido-D-homoalanine, preferably ⁇ -azido-L-homoalanine It is.
- the amino acid having an azide group in the side chain represented by the above formula is ⁇ -azido-L-ornithine or ⁇ -azido-D-ornithine, preferably ⁇ -azido-L-ornithine It is.
- the amino acid having an azide group in the side chain represented by the above formula is ⁇ -azido-L-lysine or ⁇ -azido-D-lysine, preferably ⁇ -azido-L-lysine. It is.
- the amino acid having an azide group in the side chain is particularly preferably ⁇ -azido-L-lysine, ⁇ -azido-L-ornithine, or ⁇ -azido-L-homoalanine, particularly preferably ⁇ -azido-L- Lysine or ⁇ -azido-L-ornithine, most preferably ⁇ -azido-L-lysine.
- amino acids having an alkynyl group in the side chain include those represented by the following formula. However, in the following formula, n is an integer of 1 or more.
- n 1, the amino acid having an alkynyl group in the side chain represented by the above formula is 2-propargyl-L-glycine or 2-propargyl-D-glycine, preferably 2-propargyl-L-glycine It is.
- the amino acid having an alkynyl group in the side chain represented by the above formula is 2-propargyl-L-alanine (2-propargyl-L-homoglycine) or 2-propargyl-D-alanine (2- Propargyl-D-homoglycine), preferably 2-propargyl-L-alanine (2-propargyl-L-homoglycine).
- the amino acid having an alkynyl group in the side chain represented by the above formula is 2-propargyl-L-homoalanine (2-propargyl-L-bishomoglycine) or 2-propargyl-D-homoalanine ( 2-propargyl-D-bishomoglycine), preferably 2-propargyl-L-homoalanine (2-propargyl-L-bishomoglycine).
- the amino acid having an alkynyl group in the side chain is particularly preferably 2-propargyl-L-alanine (2-propargyl-L-homoglycine) or 2-propargyl-L-homoalanine (2-propargyl-L-bishomoglycine). Particularly preferred is 2-propargyl-L-homoalanine (2-propargyl-L-bishomoglycine).
- Xa and Xb are cross-linked by an amide bond.
- X a and X b are preferably an amino acid residue derived from an amino acid having one amino group in the side chain and the other derived from an amino acid having a carboxy group in the side chain.
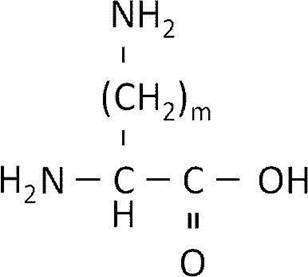
- amino acid having an amino group in the side chain examples include those represented by the following formula. However, in the following formula, m is an integer of 1 or more.
- the amino acid having an amino group in the side chain represented by the above formula is L-2,3-diaminopropanoic acid [(2S) -2,3-diaminopropanoic acid] or D-2, 3-Diaminopropanoic acid [(2R) -2,3-diaminopropanoic acid], preferably L-2,3-diaminopropanoic acid [(2S) -2,3-diaminopropanoic acid].
- the amino acid having an amino group in the side chain represented by the above formula is L-2,4-diaminobutanoic acid [(2S) -2,4-diaminobutanoic acid] or D-2, 4-Diaminobutanoic acid [(2R) -2,4-diaminobutanoic acid], preferably L-2,4-diaminobutanoic acid [(2S) -2,4-diaminobutanoic acid].
- the amino acid having an amino group in the side chain represented by the above formula is L-ornithine or D-ornithine, preferably L-ornithine.
- the amino acid having an amino group in the side chain represented by the above formula is L-lysine or D-lysine, preferably L-lysine.
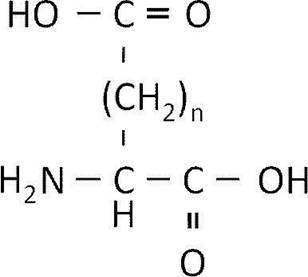
- amino acid having a carboxy group in the side chain examples include those represented by the following formula. However, in the following formula, n is an integer of 1 or more.
- X represents an amino acid residue, and when X is plural, the plural Xs may be the same or different from each other.
- X is not particularly limited as long as it is an amino acid residue, and an amino acid derived from an amino acid selected from the group consisting of the amino acids shown in Table 1 (excluding B, Z and X) and the amino acids shown in Table 2 It is preferably a residue, and more preferably an amino acid residue derived from an amino acid selected from the group consisting of the amino acids shown in Table 1 (excluding B, Z and X). Further, when present, it may be an amino acid residue derived from an enantiomer or diastereomer of these amino acids.
- R N represents an N terminal group.
- Examples of the N-terminal group include an amino group, and the amino group may be subjected to N-terminal modification such as N-acetylation, N-formylation, or N-acylation.
- R C represents a C-terminal group.
- the C-terminal group include a carboxy group, and the carboxy group may be C-terminal modified such as amidation.
- g and h are each independently an integer of 0 or more.
- g preferably satisfies 0 ⁇ g ⁇ 20, more preferably satisfies 0 ⁇ g ⁇ 10, and still more preferably satisfies 0 ⁇ g ⁇ 5.
- h preferably satisfies 0 ⁇ h ⁇ 20, more preferably satisfies 0 ⁇ h ⁇ 10, and still more preferably satisfies 0 ⁇ h ⁇ 5.
- i and j are each independently an integer of 0 or more.
- i preferably satisfies 0 ⁇ i ⁇ 20, more preferably satisfies 0 ⁇ i ⁇ 10, and still more preferably satisfies 0 ⁇ i ⁇ 5.
- j preferably satisfies 0 ⁇ j ⁇ 20, more preferably satisfies 0 ⁇ j ⁇ 10, and still more preferably satisfies 0 ⁇ j ⁇ 5.
- m and n are integers satisfying 0 ⁇ m ⁇ 9 and 0 ⁇ n ⁇ 9, respectively. Furthermore, m and n satisfy 3 ⁇ m + n ⁇ 9, preferably satisfy 4 ⁇ m + n ⁇ 8, and more preferably satisfy 5 ⁇ m + n ⁇ 7.
- the number of amino acid residues [(m + n + 5) residues] in the cyclic part [X a -X m -X 1 -X 2 -X 3 -X n -X b ] is 8 to 14 acid groups It is preferably 9 to 13 residues, more preferably 10 to 12 residues. If the number of amino acid residues in the cyclic part is within this range, the intramolecular strain of the cyclic peptide does not become too large, and higher-order structures such as ⁇ -helices are stabilized. Excellent.
- the number of repeating units is not particularly limited, but the larger the number of repeating units, the greater the number of repeating units, so that more cyclic parts can be included. Therefore, there is a possibility that the antibody binding property of the cyclic peptide can be improved. Since the total number of amino acid residues can be reduced as the number of units decreases, the antigenicity of the cyclic peptide may be suppressed. From the viewpoint of the synthesis cost of the cyclic peptide, it is preferable that the number of amino acid residues is small, and it is preferable that the number of repeating units is small.
- the cyclic peptide represented by the formula (I) is a repeating unit [X i -X a -X m -X 1 -X 2 -X 3 -X n -X b -X j ] or more, X 1 , X 2 , X 3 , X a , X b , X i , X j , X m , and X n in the repeating unit are the same among the repeating units. Or may be different.
- the total number of amino acid residues of the cyclic peptide is preferably 8 to 50 residues, more preferably 9 to 40 residues, still more preferably 10 to 30 residues. More preferably, it is 10 to 20 residues.
- g, h, j, j, m, n, and k preferably satisfy 8 ⁇ g + h + (i + j + m + n + 5) ⁇ k ⁇ 50, and more preferably 9 ⁇ g + h + (i + j + m + n + 5) ⁇ k ⁇ 40, more preferably 10 ⁇ g + h + (i + j + m + n + 5) ⁇ k ⁇ 30, and more preferably 10 ⁇ g + h + (i + j + m + n + 5) ⁇ k ⁇ 20.
- the greater the number of amino acid residues the higher the synthesis cost. From the economical viewpoint, it is preferable that the total number of amino acid residues is small.
- the cyclic peptide is more preferably a cyclic peptide represented by the following formula (IA).
- R N, R C, X 1, X 2, X 3, X a, X b, X g, X h, X m, X n, X, g, h, m, n, and k is as defined in the above formula (I).
- X n is intended to connect n X as in the case of X n in Formula (I).
- X m , X p1 , X p2 , X q1 , and X q2 are intended to mean that r is connected to r of X 4 and s are connected to s of X 5 , respectively.
- the linear portion of the cyclic peptide represented by the formula (IA) is “X g ”, “X h ”, “X p2 -X 4 r -X p1 ”, and “X q1 -X 5 s -X q2 ”. is there.
- crosslinking part, and an antibody binding part are the same as that of the cyclic peptide represented by Formula (I).
- the repeating unit [X p2 -X 4 r -X p1 -X a -X m -X 1 -X 2 -X 3 -X n -X b -X q1 -X 5 s - X q2 ].
- X 4 and X 5 each independently represent an amino acid residue derived from an amino acid having a carboxy group in the side chain or an amino acid residue derived from an amino acid having a hydroxy group in the side chain.
- amino acid having a carboxy group in the side chain examples include L-aspartic acid, D-aspartic acid, L-glutamic acid, D-glutamic acid, L-homoglutamic acid, D-homoglutamic acid and the like.
- Examples of the amino acid having a hydroxy group in the side chain include L-serine, D-serine, L-homoserine, D-homoserine, L-tyrosine, D-tyrosine, L-threonine, D-threonine, and L-allothreonine. , And D-allothreonine.
- X 4 and X 5 are preferably independently selected from L-serine residue, D-serine residue, L-homoserine residue, D-homoserine residue, L-aspartic acid residue, D-aspartic acid Residue, L-glutamic acid residue, D-glutamic acid residue, L-homoglutamic acid residue, D-homoglutamic acid residue, L-tyrosine residue, D-tyrosine residue, L-homotyrosine residue, D-homotyrosine An amino acid residue selected from the group consisting of a residue, an L-threonine residue, a D-threonine residue, an L-allothreonine residue, and a D-allothreonine residue, more preferably each independently An amino acid residue selected from the group consisting of L-aspartic acid residue, D-aspartic acid residue, L-threonine residue and D-threonine residue, more preferably X 4 is L- as
- X 4 and X 5 are each independently an amino acid residue derived from an amino acid having a carboxy group in the side chain or an amino acid residue derived from an amino acid having a hydroxy group in the side chain, antibody binding in the cyclic part It is considered that the antibody and the antibody can be more strongly interacted with each other by hydrogen bonding and / or electrostatic interaction, and the antibody binding property is improved.
- p1, p2, q1, and q2 are each independently an integer of 0 or more.
- p1 preferably satisfies 0 ⁇ p1 ⁇ 20, more preferably satisfies 0 ⁇ p1 ⁇ 10, further preferably satisfies 0 ⁇ p1 ⁇ 5, and more preferably satisfies 0 ⁇ p1 ⁇ 2.
- p2 preferably satisfies 0 ⁇ p2 ⁇ 20, more preferably satisfies 0 ⁇ p2 ⁇ 10, further preferably satisfies 0 ⁇ p2 ⁇ 5, and more preferably satisfies 0 ⁇ p2 ⁇ 2.
- q1 preferably satisfies 0 ⁇ q1 ⁇ 20, more preferably satisfies 0 ⁇ q1 ⁇ 10, further preferably satisfies 0 ⁇ q1 ⁇ 5, and more preferably satisfies 0 ⁇ q1 ⁇ 2.
- q2 preferably satisfies 0 ⁇ q2 ⁇ 20, more preferably satisfies 0 ⁇ q2 ⁇ 10, further preferably satisfies 0 ⁇ q2 ⁇ 5, and more preferably satisfies 0 ⁇ q2 ⁇ 2.
- r and s are integers satisfying 0 ⁇ r ⁇ 5, 0 ⁇ s ⁇ 5, and 1 ⁇ Max (r, s) ⁇ 5, respectively, preferably 0 ⁇ r ⁇ 4, 0 ⁇ s ⁇ 4, and 1 ⁇ Max (r, s) ⁇ 4, more preferably 0 ⁇ r ⁇ 3, 0 ⁇ s ⁇ 3, and 1 ⁇ Max (r, s) An integer satisfying ⁇ 3.
- the number of amino acid residues [(m + n + 5) residues] in the cyclic part [X a -X m -X 1 -X 2 -X 3 -X n -X b ] is defined by the formula (I) In the same manner as above, it is an 8 to 14 acid group, preferably 9 to 13 residues, more preferably 10 to 12 residues. If the number of amino acid residues in the cyclic part is within this range, the intramolecular strain of the cyclic peptide does not become too large, and higher-order structures such as ⁇ -helices are stabilized. Excellent.
- the total number of amino acid residues of the cyclic peptide is preferably 8 to 50 residues, more preferably 9 to 40 residues, and further preferably 10 to 30 residues. More preferably, it is 10 to 20 residues.
- g, h, m, n, p1, p2, q1, q2, r, s, and k preferably satisfy 8 ⁇ g + h + (m + n + p1 + p2 + q1 + q2 + r + s + 5) ⁇ k ⁇ 50, more preferably 9 ⁇ g + h + (m + n + p1 + p2 + q1 + q2 + r + s + 5) ⁇ k ⁇ 40 is satisfied, more preferably 10 ⁇ g + h + (m + n + p1 + p2 + q1 + q2 + r + s + 5) ⁇ k ⁇ 30 is satisfied, and more preferably 10 ⁇ g + h + (m + n + p + q + q + q + q + q + q + q + q + q + q + q + q + q + q + q +
- the cyclic peptide is more preferably a cyclic peptide represented by the following formula (IB).
- R N, R C, X 1, X 2, X 3, X a, X b, X i, X j, X m, X n, X, i, j, m, n, and k is as defined in the above formula (I).
- X n is intended to connect n X in the same manner as X n in Formula (I). The same applies to X m , X v1 , X v2 , X w1 , and X w2 .
- X 6 t and X 7 u are intended to mean that t 6 of X 6 are connected and u of X 7 are connected, respectively.
- the linear portion of the cyclic peptide represented by formula (IB) is “X i ”, “X j ”, “X v1 -X 6 t -X v2 ”, and “X w2 -X 7 u -X w1 ”. is there.
- crosslinking part, and an antibody binding part are the same as that of the cyclic peptide represented by Formula (I).
- the repeating unit is [X i -X a -X m -X 1 -X 1 -X 2 -X 3 -X n -X b -X j ] as in the formula (I). .
- X 6 and X 7 each independently represent amino acid residues from an amino acid with immobilized functional groups in the side chain, if X 6 or X 7 is plural, X 6 or X 7 may be the same as or different from each other.
- the “immobilized functional group” is a functional group capable of forming a covalent bond by reacting with a functional group on a substrate and / or a hydrophilic polymer (sometimes referred to as “reactive functional group”).
- immobilized functional group include an amino group, a carboxy group, a hydroxy group, a thiol group, a formyl group (aldehyde group), a carbamoyl group, an azide group, and an alkynyl group.
- the combination of the immobilized functional group of the cyclic peptide and the functional group on the base material and / or hydrophilic polymer includes an amino group and a carboxy group (amide bond forming reaction), an amino group and a formyl group (reductive amination reaction). ), Amino group and epoxy group, carboxy group and hydroxy group (ester bond formation reaction), thiol group and thiol group (disulfide bond), thiol group and epoxy group, and azide group and alkynyl group (Husgen cycloaddition reaction) Etc.
- the cyclic peptide is immobilized on a carrier by reacting the immobilized functional group of the cyclic peptide with a functional group on the base material and / or hydrophilic polymer to form a covalent bond.
- the immobilized functional group is preferably at least one selected from the group consisting of an amino group, a thiol group and an aldehyde group, more preferably an amino group and a thiol group. At least one selected from the group consisting of:
- the amino acid having an immobilized functional group on the side chain is preferably at least one selected from the group consisting of L-lysine, D-lysine, L-cysteine, D-cysteine, L-homocysteine and D-homocysteine.
- a kind of amino acid is preferably at least one selected from the group consisting of L-lysine, D-lysine, L-cysteine, D-cysteine, L-homocysteine and D-homocysteine.
- an amino group as an immobilization functional group, it can be bound to a carboxy group on a carrier via an amide bond, and the cyclic peptide of the present invention as an affinity ligand can be easily immobilized.
- a thiol group as an immobilization functional group, it can be bonded to an epoxy group on a carrier via a covalent bond, and the cyclic peptide of the present invention as an affinity ligand can be easily immobilized.
- Amino acids having an amino group in the side chain include L-lysine and D-lysine, and amino acids having a thiol group in the side chain include L-cysteine and D-cysteine, which are relatively inexpensive. Therefore, the synthesis cost of the cyclic peptide of the present invention can be suppressed, which is preferable from an economical viewpoint.
- t and u are integers satisfying 0 ⁇ t ⁇ 5, 0 ⁇ u ⁇ 5, and 1 ⁇ Max (t, u) ⁇ 5, preferably 0 ⁇ t ⁇ 4. , 0 ⁇ u ⁇ 4, 1 ⁇ Max (t, u) ⁇ 4, more preferably 0 ⁇ t ⁇ 3, 0 ⁇ u ⁇ 3, 1 ⁇ Max (t, u) ⁇ 3 It is an integer.
- v1, v2, w1 and w2 are each independently an integer of 0 or more.
- v1 preferably satisfies 0 ⁇ v1 ⁇ 20, more preferably satisfies 0 ⁇ v1 ⁇ 10, further preferably satisfies 0 ⁇ v1 ⁇ 5, and more preferably satisfies 0 ⁇ v1 ⁇ 2.
- v2 preferably satisfies 0 ⁇ v2 ⁇ 20, more preferably satisfies 0 ⁇ v2 ⁇ 10, further preferably satisfies 0 ⁇ v2 ⁇ 5, and more preferably satisfies 0 ⁇ v2 ⁇ 2.
- w1 preferably satisfies 0 ⁇ w1 ⁇ 20, more preferably satisfies 0 ⁇ w1 ⁇ 10, further preferably satisfies 0 ⁇ w1 ⁇ 5, and more preferably satisfies 0 ⁇ w1 ⁇ 2.
- w2 preferably satisfies 0 ⁇ w2 ⁇ 20, more preferably satisfies 0 ⁇ w2 ⁇ 10, further preferably satisfies 0 ⁇ w2 ⁇ 5, and more preferably satisfies 0 ⁇ w2 ⁇ 2.
- the cyclic peptide represented by the formula (IB) is a repeating unit [X i -X a -X m -X 1 -X 2 -X 3 -X n -X b -X j ]] or more, X 1 , X 2 , X 3 , X a , X b , X m , X n , X i , and X j in the repeating unit are the same among the repeating units. Or may be different.
- the total number of amino acid residues of the cyclic peptide is preferably 8 to 50 residues, more preferably 9 to 40 residues, still more preferably 10 to 30 residues. More preferably, it is 10 to 20 residues.
- i, j, m, n, t, u, v1, v2, w1, w2, and k preferably satisfy 8 ⁇ (i + j + m + n + 5) ⁇ k + t + u + v1 + v2 + w1 + w2 ⁇ 50, more preferably ( i + j + m + n + 5) ⁇ k + t + u + v1 + v2 + w1 + w2 ⁇ 40, more preferably 10 ⁇ (i + j + m + n + 5) ⁇ k + t + u + v1 + v2 + w1 + w2 ⁇ 30, and more preferably 10 ⁇ (i + j + m + n + 5) ⁇ k + v + 2 + w + 1
- the greater the number of amino acid residues the higher the synthesis cost. From the economical viewpoint, it is preferable that the greater the number of amino acid residues, the
- the cyclic peptide is more preferably a cyclic peptide represented by the following formula (IC).
- IC cyclic peptide represented by the following formula (IC).
- X m, X p1, X p2 , X q1, X q2, X v1, X v2, X w1, for and X w2 is the same. Furthermore, in the formula (IC), X 4 r , X 5 s , X 6 t , and X 7 u are respectively connected to r that X 4 is connected to, s that X 5 is connected to, that X 6 is t pieces connected, and that X 7 is u pieces connected contemplates.
- the linear portion of the cyclic peptide represented by the formula (IC) is “X v1 -X 6 t -X v2 ”, “X w2 -X 7 u -X w1 ”, “X p2 -X 4 r -X p1 ”. , And “X q1 -X 5 s -X q2 ”.
- crosslinking part, and an antibody binding part are the same as that of the cyclic peptide represented by Formula (I).
- repeating units are as for formula (IA), [X p2 -X 4 r -X p1 -X a -X m -X 1 -X 2 -X 3 -X n -X b -X q1 -X 5 s -X q2 ].
- the total number of amino acid residues of the cyclic peptide is preferably 8 to 50 residues, more preferably 9 to 40 residues, still more preferably 10 to 30 residues. More preferably, it is 10 to 20 residues.
- m, n, p1, p2, q1, q2, r, s, t, u, v1, v2, w1, w2, and k are preferably 8 ⁇ (m + n + p1 + p2 + q1 + q2 + r + s + 5) ⁇ k + t + u + v1 + v2 + w1 + w2 ⁇ met 50, more preferably satisfies the 9 ⁇ (m + n + p1 + p2 + q1 + q2 + r + s + 5) ⁇ k + t + u + v1 + v2 + w1 + w2 ⁇ 40, more preferably satisfies 10 ⁇ (m + n + p1 + p2 + q1 + q2 + r + s + 5) ⁇ k + t + u + v1 + v2 + w2 + w2 + w
- X m -X 1 -X 2 -X 3 -X n amino acid partial sequence X m -X 1 -X 2 -X 3 -X n in the above formula (I), (IA), (IB), or (IC) is represented by the following formula (1).
- AYH-L 1 -GEL 2 -VW (1) AYH-R-G-E-L 2 -VW (2)
- A represents an L-alanine residue or a D-alanine residue
- Y represents an L-tyrosine residue or a D-tyrosine residue
- H represents an L-histidine residue.
- D-histidine residue L 1 represents L-leucine residue or D-leucine residue
- R represents L-arginine residue or D-arginine residue
- G represents glycine residue
- E represents an L-glutamic acid residue or a D-glutamic acid residue
- L 2 represents an L-leucine residue
- V represents an L-valine residue
- W represents an L-tryptophan residue.
- sequence homology between two amino acid sequences is determined as follows.
- (Ii) Calculate sequence homology Based on the obtained alignment, sequence homology is calculated by the following equation. Sequence homology [%] (number of matching positions / number of all positions) ⁇ 100 [%] The total number of positions is the length of the alignment, and the number of matching positions is the number of positions where the amino acid types match.
- the judgment of whether or not the types of amino acid residues are identical is based on whether or not the structures of the side chains (amino acid side chains) of the amino acids that are the basis of the amino acid residues are the same.
- sequence homology For example, consider the following amino acid sequence. Sequence A AYHRGELVW Sequence B AWHGELVW When this is aligned under the above-mentioned conditions, it is as follows. Here, a homology string “
- the number of repeating units is one, the total length of the cyclic peptide can be shortened, and synthesis becomes easy. Moreover, it is possible to avoid the formation of a cross-link at an unintended location by the Huisgen reaction during cyclization.
- the cyclic peptide is particularly preferably a cyclic peptide represented by the following formula (II).
- X a , X b , X, R N , and R C are the same as those in the above formula (I).
- Xe0 intends that e0 pieces of X are linked in the same manner as Xn in formula (I). The same applies to X f0 , X p0 , X q0 , X v0 , and X w0 .
- the cyclic part of the cyclic peptide represented by the formula (II) is “X a -AYHX 8 -GELVWX b ”, and the linear part is “X v0 -X 6 t0 -X e0 -X 4 r0 -X p0 - "and” an X q0 -X 5 s0 -X f0 -X 7 u0 -X w0 "bridge section” X a "and” X b " And the antibody binding site is “LVV”.
- e0 and f0 are integers satisfying 0 ⁇ e0 ⁇ 10 and 0 ⁇ f0 ⁇ 10, respectively.
- e0 preferably satisfies 0 ⁇ e0 ⁇ 5, more preferably satisfies 0 ⁇ e0 ⁇ 3, and more preferably satisfies 0 ⁇ e0 ⁇ 2.
- f0 preferably satisfies 0 ⁇ f0 ⁇ 5, more preferably satisfies 0 ⁇ f0 ⁇ 3, and more preferably satisfies 0 ⁇ f0 ⁇ 2.
- p0 and q0 are integers satisfying 0 ⁇ p0 ⁇ 5 and 0 ⁇ q0 ⁇ 5, respectively.
- p0 preferably satisfies 0 ⁇ p0 ⁇ 3, and more preferably satisfies 0 ⁇ p0 ⁇ 2.
- q0 preferably satisfies 0 ⁇ q0 ⁇ 3, and more preferably satisfies 0 ⁇ q0 ⁇ 2.
- r0 and s0 are integers satisfying 0 ⁇ r0 ⁇ 5 and 0 ⁇ s0 ⁇ 5, respectively.
- r0 preferably satisfies 0 ⁇ r0 ⁇ 3, and more preferably satisfies 0 ⁇ r0 ⁇ 2.
- s0 preferably satisfies 0 ⁇ s0 ⁇ 3, and more preferably satisfies 0 ⁇ s0 ⁇ 2.
- t0 and u0 are integers that satisfy 0 ⁇ t0 ⁇ 5 and 0 ⁇ u0 ⁇ 5, respectively.
- t0 preferably satisfies 0 ⁇ t0 ⁇ 3, and more preferably satisfies 0 ⁇ t0 ⁇ 2.
- s0 preferably satisfies 0 ⁇ s0 ⁇ 3, and more preferably satisfies 0 ⁇ s0 ⁇ 2.
- v0 and w0 are integers satisfying 0 ⁇ v0 ⁇ 5 and 3 ⁇ w0 ⁇ 5, respectively.
- v0 preferably satisfies 0 ⁇ v0 ⁇ 3, and more preferably satisfies 0 ⁇ v0 ⁇ 2.
- w0 preferably satisfies 0 ⁇ w0 ⁇ 3, and more preferably satisfies 0 ⁇ w0 ⁇ 2.
- A represents an L-alanine residue or D-alanine residue
- Y represents an L-tyrosine residue or D-tyrosine residue
- H represents an L-histidine residue or D -Represents a histidine residue
- L 1 represents an L-leucine residue or a D-leucine residue
- G represents a glycine residue
- E represents an L-glutamic acid residue or a D-glutamic acid residue
- L 2 represents an L-leucine residue
- V represents an L-valine residue
- W represents an L-tryptophan residue.
- the total number of amino acid residues of the cyclic peptide is 11 to 50 residues, preferably 11 to 40 residues, more preferably 11 to 30 residues, still more preferably. Is 11-20 residues. That is, in the formula (II), e0, f0, p0, q0, r0, s0, t0, u0, v0, and w0 satisfy 0 ⁇ e0 + f0 + p0 + q0 + r0 + s0 + t0 + u0 + v0 + w0 ⁇ 39, preferably satisfy 0 ⁇ e0 + f0 + p0 + q0 + 0 + w0 Satisfies 0 ⁇ e0 + f0 + p0 + q0 + r0 + s0 + t0 + u0 + v0 + w0 ⁇ 19, more preferably 0 ⁇ e0 + f0 + f0 + q0 + r
- Xaa1 is an amino acid residue derived from L-homocysteine
- Xaa11 is an amino acid residue derived from N- ⁇ -chloroacetyl-L-lysine
- Xaa1 and Xaa11 are L- A thioether bond is formed between the thiol group on the side chain of homocysteine and the chloroacetyl group on the side chain of N- ⁇ -chloroacetyl-L-lysine (SEQ ID NO: 3).
- Xaa1 is an amino acid residue derived from N- ⁇ -chloroacetyl-L-lysine
- Xaa11 is an amino acid residue derived from L-homocysteine
- Xaa1 and Xaa11 are N- A thioether bond is formed between the chloroacetyl group of the side chain of ⁇ -chloroacetyl-L-lysine and the thiol group of the side chain of L-homocysteine to form a bridge (SEQ ID NO: 4).
- Xaa1 is an amino acid residue derived from L-cysteine
- Xaa11 is an amino acid residue derived from N- ⁇ -chloroacetyl-L-lysine
- Xaa1 and Xaa11 are L-cysteine.
- a thioether bond is formed between the thiol group of the side chain and the chloroacetyl group of the side chain of N- ⁇ -chloroacetyl-L-lysine (SEQ ID NO: 5).
- Xaa1 is an amino acid residue derived from N- ⁇ -chloroacetyl-L-lysine
- Xaa11 is an amino acid residue derived from L-penicillamine
- Xaa1 and Xaa11 are N- ⁇ -Crosslinked by forming a thioether bond between the chloroacetyl group of the side chain of chloroacetyl-L-lysine and the thiol group of the side chain of L-cysteine (SEQ ID NO: 6).
- Xaa1 and Xaa11 are both amino acid residues derived from L-homocysteine, which are crosslinked by forming a disulfide bond between thiol groups in the side chains of L-homocysteine ( SEQ ID NO: 7).
- Xaa1 and Xaa11 are both amino acid residues derived from L-penicillamine and are crosslinked by forming a disulfide bond between the thiol groups of the side chains of L-cysteine (SEQ ID NO: 8).
- Xaa1 is an amino acid residue derived from 2-propargyl-L-homoglycine
- Xaa11 is an amino acid residue derived from ⁇ -azido-L-alanine
- Xaa1 and Xaa11 are represented by 2- The propargyl-L-homoglycine side chain propargyl group and the ⁇ azide-L-alanine side chain azide group form a triazole bond and are crosslinked (SEQ ID NO: 9).
- Xaa1 is an amino acid residue derived from ⁇ -azido-L-alanine
- Xaa11 is an amino acid residue derived from 2-propargyl-L-homoglycine
- Xaa1 and Xaa11 are ⁇ azide
- a triazole bond is formed between the azide group of the side chain of -L-alanine and the propargyl group of the side chain of 2-propargyl-L-homoglycine to form a bridge (SEQ ID NO: 10).
- Xaa1 is an amino acid residue derived from L-lysine
- Xaa11 is an amino acid residue derived from L-glutamic acid
- An amide bond is formed with the carboxy group of each other to crosslink (SEQ ID NO: 11).
- Xaa1 is an amino acid residue derived from L-glutamic acid
- Xaa11 is an amino acid residue derived from L-lysine
- the carboxy group of the side chain of L-glutamic acid and the side chain of L-lysine An amide bond is formed with the amino group of the compound to crosslink (SEQ ID NO: 12).
- affinity ligand introduced amount The amount of affinity ligand introduced into the carrier for mixed mode affinity chromatography of the present invention (hereinafter sometimes simply referred to as “affinity ligand introduced amount”) is not particularly limited, but is preferably 0.01 mmol / L-gel to 100 mmol. / L-gel, more preferably 0.05 mmol / L-gel to 50 mmol / L-gel, still more preferably 0.10 mmol / L-gel to 10 mmol / L-gel, still more preferably 0.10 mmol / L-gel to 5.0 mmol / L-gel, more preferably 0.10 mmol / L-gel to 2.5 mmol / L-gel.
- the method for synthesizing the cyclic peptide is not particularly limited, and can be synthesized by, for example, an organic synthetic chemical peptide synthesis method or a genetic engineering peptide synthesis method.
- an organic synthetic chemical peptide synthesis method either a liquid phase synthesis method or a solid phase synthesis method can be used.
- a method for synthesizing the polypeptide of the present invention a solid phase synthesis method using an automatic peptide synthesizer is simple and preferable.
- the genetic engineering peptide synthesis method is a method of synthesizing a peptide by introducing a gene into a cell.
- bacteria bacteria, nematode cells, insect cells, mammalian cells, animal cells and the like are used.
- it can be synthesized by introducing an unnatural amino acid using a 4-base codon method.
- the peptide can be synthesized by cyclization by synthesizing a linear peptide and reacting with a crosslinkable functional group on the side chain of the amino acid residue introduced into the cyclic part.
- a side-chain thiol group between homocysteine residues or a side-chain thiol group of a homocysteine residue and a side-chain thiol group of an amino acid residue having a longer methylene chain than homocysteine It can be reacted under oxidizing conditions to form disulfide bonds.
- a thioether bond for example, a lysine residue or ornithine residue obtained by chloroacetylating a side chain amino group and a side chain thiol group of a homocysteine residue may be reacted to form a thioether bond. it can.
- the side chain amino group of the lysine residue is chloroacetylated (—NH—C ( ⁇ O) —CH 2 —Cl; number of methylene units 1) or 3-chloropropion oxidation (—NH
- the compound used in the chlorination is exemplified here because it is chlorinated by —C ( ⁇ O) — (CH 2 ) 2 —Cl; the number of methylene units 2) and then reacted with a thiol group.
- the number of methylene units is small, that is, the shorter the methylene chain is, the higher the cyclization efficiency is, and it is preferable.
- an azide group and an alkynyl group are used as the crosslinkable functional group.
- a method of incorporating an amino acid introduced with an azide group or alkynyl group into the polypeptide chain during peptide synthesis or There is a method of introducing an azido group or an alkynyl group into the side chain of a desired amino acid residue after synthesis. Any method may be used.
- an addition reaction between the alkynyl group and the azide group is caused by a Huisgen reaction to bridge the amino acid residues.
- the azide group and alkynyl group are inert to many functional groups and biomolecules, and the reaction that forms a triazole ring from both is an exothermic thermodynamically advantageous reaction. It is preferable to use a copper catalyst since the Huisgen reaction accelerates dramatically in the presence of a copper catalyst.
- the cation exchange group acts in concert with the antibody-binding cyclic peptide and has specific adsorption ability and aggregate removal ability, thereby improving the impurity removal ability of the carrier for mixed mode affinity chromatography of the present invention. it is conceivable that.
- the cation exchange group used in the carrier for mixed mode affinity chromatography of the present invention is not particularly limited, but is preferably a carboxy group or a sulfoxy group, and more preferably a carboxy group. Both the carboxy group and the sulfoxy group are excellent in the ability to remove aggregates, but the carboxy group is particularly advantageous because it has a lower ionic strength than the sulfonic acid group and can suppress nonspecific adsorption.
- cation exchange group introduction amount The amount of cation exchange groups introduced into the carrier for mixed mode affinity chromatography of the present invention (hereinafter sometimes simply referred to as “cation exchange group introduction amount”) is not particularly limited, but is preferably an ion exchange capacity, 15 mmol / L-gel to 60 mmol / L-gel, more preferably 15 mmol / L-gel to 55 mmol / L-gel, and still more preferably 15 mmol / L-gel to 40 mmol / L-gel.
- the introduction amount of the cation exchange group is within this range, the introduction amount of the affinity ligand can be within an appropriate range, and the adsorption of the nonspecific adsorbate can be suppressed.
- the carrier for mixed mode affinity chromatography of the present invention is produced by coating a substrate with a hydrophilic polymer, introducing a cation exchange group, and further introducing an affinity ligand into at least one of the substrate and the hydrophilic polymer. be able to.
- the base material, hydrophilic polymer and affinity ligand are as already described in “Carrier for Mixed Mode Affinity Chromatography”.
- the method of coating the substrate with a hydrophilic polymer is not particularly limited as long as the hydrophilic polymer can be bonded to the substrate by covalent bonding.
- a method in which 2-chloromethyloxirane (also known as epichlorohydrin) is reacted with a substrate to introduce an epoxy group and a hydrophilic polymer is reacted with the substrate, in a solvent in the presence of alkali Is reacted with a crosslinking agent such as 2-chloromethyloxirane (also known as epichlorohydrin), and the resulting reaction product is reacted with a hydrophilic polymer, or a halogen group such as a chloro group (chlorine atom) (halogen) Atom) is introduced into the substrate using a halogenating agent, and a hydrophilic polymer is immobilized using Williamson's ether synthesis method.
- the amount of the hydrophilic polymer coated is preferably 3 mg / g-dry gel to 450 mg / g-dry gel, more preferably 3 mg / g-dry gel to 250 mg / g- dry gel, more preferably 3 mg / g-dry gel to 230 mg / g-dry gel, more preferably 10 mg / g-dry gel to 230 mg / g-dry gel, more preferably 20 mg / g-dry gel to 230 mg / g. -Try to be dry gel.
- a substrate immediately before coating with a hydrophilic polymer is referred to as a “substrate before coating”, and a substrate coated with a hydrophilic polymer may be referred to as a “coated carrier”.
- the method of introducing a cation exchange group into a coated carrier is particularly suitable as long as it can bind a compound having a cation exchange group to the coated carrier by a covalent bond.
- a method in which chloroacetic acid is reacted with a coated carrier under alkaline conditions to introduce a carboxymethyl group into a part of the hydroxy group on the surface of the coated carrier, or a formyl group is introduced into the coated carrier.
- a method of introducing a cation exchange group into a formyl group by a reductive amination method through a cation exchange group such as an amino acid and an amino group of a compound having an amino group such as an amino acid and an amino group of a compound having an amino group.
- the amount of cation exchange group introduced is 15 mmol / L-gel to 60 mmol / L-gel, preferably 15 mmol / L-gel to 55 mmol / L-gel. And more preferably 15 mmol / L-gel to 40 mmol / L-gel.
- a product obtained by introducing a cation exchange group into a coated carrier may be referred to as a “cation exchange group-introduced carrier”.
- a carrier having a carboxy group introduced therein may be referred to as a “carboxy group-introducing carrier”, and a carrier having a sulfoxy group introduced therein may be referred to as a “sulfoxy group-introducing carrier”.
- EDC N- (3-dimethylaminopropyl) -N′-ethylcarbodiimide; N- (3-dimethylaminopropyl)- N'-ethylcarbodiimide) / NHS (N-hydroxysuccinimide)
- NHS N-hydroxysuccinimide
- the ligand is to protect the cation exchange groups, by introducing a formyl group, and a method of introducing the affinity ligands formyl group by reductive amination via an amino group.
- the amount of the affinity ligand introduced is preferably 0.01 mmol / L-gel to 100 mmol / L-gel, more preferably 0.05 mmol / L-gel to 50 mmol / L-gel, more preferably 0.10 mmol / L-gel to 10 mmol / L-gel, even more preferably 0.10 mmol / L-gel to 5.0 mmol / L-gel, even more preferably 0.10 mmol / L-gel ⁇ 2.5 mmol / L-gel.
- the amount of cation exchange group introduced into the carrier for mixed mode affinity chromatography when the affinity ligand is bound to a part of the cation exchange group of the cation exchange group introduction carrier is as follows. It is expressed as “exchange group introduction amount ⁇ affinity ligand introduction amount of the carrier for mixed mode affinity chromatography”.
- the biological material purified by the carrier for mixed mode affinity chromatography of the present invention is not particularly limited, but is preferably an antibody or an antibody derivative, more preferably an immunoglobulin G or a derivative thereof. These are used as raw materials for antibody drugs.
- the purification of biological materials (especially antibodies) using a mixed mode affinity chromatography carrier is largely comprised of four steps: an adsorption step, a washing step, an ionic strength adjustment step, and an elution step, and subsequent regeneration.
- a process for reuse such as a process and / or a CIP (cleaning-in-place) process, a re-equilibration process, and the like may be included.
- a general affinity chromatography purification method can be used. That is, in one example, after adjusting the pH of the protein solution containing immunoglobulin G to be near neutral, the solution is passed through a column packed with the carrier for mixed mode affinity chromatography of the present invention, and the affinity ligand The immunoglobulin G is specifically adsorbed on a carrier for mixed mode affinity chromatography via
- its loading pH that is, the pH at the time of addition of a biological substance is preferably 5.0 to 9.0, more preferably 5.3 to 9.0, More preferably, it is 5.5 to 9.0, and more preferably 6.0 to 8.5.
- the preparation of ionic strength is not particularly required, and nonspecific adsorption can be further suppressed by increasing the ionic strength in advance.
- the washing step an appropriate amount of a buffer solution in a condition range in which the affinity ligand functions is passed through to wash the inside of the column. That is, the preferable range of the pH of the buffer solution may be the same as that at the time of loading, for example, preferably pH 5.0 to 9.0.
- the preferable range of the pH of the buffer solution may be the same as that at the time of loading, for example, preferably pH 5.0 to 9.0.
- immunoglobulin G is adsorbed on the carrier for mixed mode affinity chromatography of the present invention.
- impurities may be effectively removed by ionic strength and / or composition optimization at a pH near neutral.
- a condition in which the cation exchange group does not function is preferable, that is, it is preferable to use a washing solution having a pH close to neutral and an ionic strength of a certain level, and in this process, a carrier for mixed mode affinity chromatography and / or Impurities remaining on the column non-specifically through the immunoglobulin G can be washed.
- the ionic strength is, for example, preferably 0.2M or more, and more preferably 0.5M or more.
- the column is replaced with a buffer solution having a low ionic strength in the vicinity of neutrality to prepare for the expression of an ionic strength-dependent elution function by the cation exchange group during elution.
- a combination of acidic pH and ionic strength allows the cation exchange separation mode to function during elution from affinity ligands, and the high monomer content fraction is eluted at a low ionic strength through the concerted action of both ligands. It can be collected in fractions.
- the pH of the eluate the elution pH of immunoglobulin G from the affinity ligand can be applied. Since this pH is determined centering on the separation conditions determined by the type of carrier for mixed mode affinity chromatography and immunoglobulin G, no special condition setting is required.
- the pH during elution is preferably set to 2.0 to 5.0.
- the pH is more preferably 2.8 or more, further preferably pH 3.0 or more, and still more preferably pH 3.2 or more.
- the pH is preferably 5.0 or less, more preferably 4.8 or less.
- the pH during elution is generally preferably set to 3.2 to 4.0, but is not limited thereto.
- the elution ionic strength depends not only on the introduction ratio of affinity ligand and cation exchange group, but also on the amount of immunoglobulin G loaded per unit volume. ⁇ can be set easily.
- Antibody elution from a carrier for mixed mode affinity chromatography prepared according to the present invention can be applied by salt concentration gradient elution or stepwise elution. However, for the purpose of reducing the amount of eluate, stepping by ionic strength is possible. Wise elution is preferred. Furthermore, in order to simplify the operation, it is preferable to set conditions that can achieve antibody recovery and high purification purity by one-step elution.
- the ionic strength adjustment step can be omitted if aggregates remain in the column and are not mixed into the elution fraction even with a combination of ionic strength and acidic pH in the washing step.
- the biological material purified by the purification method of the present invention does not change its own structure and properties before and after purification, but has a high purification purity. However, how high it is depends on the solution before purification, etc., so it cannot be generally stated.
- Immunoglobulin G purified using the mixed-mode affinity chromatography carrier prepared according to the present invention exhibits a higher monomer selectivity than the affinity chromatography carrier based on a single separation mode. High monomer content.
- the carboxylated carrier is taken out, transferred to a 100 mL beaker, suspended in 40 mL of 0.1 mol / L saline solution, and 0.1 mol / L of water using an automatic titrator “COM-1600” (manufactured by Hiranuma Sangyo Co., Ltd.). Titrated with aqueous sodium oxide.
- Chromatography system AKTA york 25 (manufactured by GE Healthcare) ("AKTAAVANT” is a registered trademark)
- Buffer 20 mM phosphate buffer, 150 mM NaCl, pH 7.4
- Flow rate 0.5 mL / min
- a stationary cleaning (CIP; cleaning in place) solution (0.1 M sodium hydroxide aqueous solution) was allowed to flow at the same flow rate, and then a re-equilibration solution (20 mM phosphate buffer, 150 mM NaCl, pH 7.4). At a flow rate of 5 mL.
- a re-equilibration solution (20 mM phosphate buffer, 150 mM NaCl, pH 7.4).
- the antibody elution amount of the eluate in each fraction was calculated from the IgG elution peak obtained by monitoring the absorbance at 280 nm.
- the amount of antibody eluted from the pre-elution washing solution to the CIP solution was calculated as the antibody adsorption capacity.
- IgG and HCP amount After equilibrating the column with an equilibration solution (20 mM phosphate buffer, 150 mM NaCl, pH 7.4), IgG and CHO-S (Chinese Hamster Over S) cell-derived HCPs were 1.6 mg / mL, 0.00%, respectively.
- the IgG / HCP mixture prepared using a standard buffer (20 mM phosphate buffer, 150 mM NaCl, pH 7.4) to a concentration of 32 mg / mL is 80% of the antibody adsorption capacity obtained in C above. Was added at a flow rate of 0.21 mL / min.
- eluate 1 100 mM citrate buffer, pH 3.2
- eluate 2 100 mM citrate buffer, 50 mM NaCl, pH 3.2
- eluate 3 100 mM citrate
- eluent 4 100 mM citrate buffer, 500 mM
- the eluate of each fraction was collected, the pH of each eluate was adjusted to 5-6 using 1M Tris-HCl solution, and then a host cell-derived protein detection kit “CHO HCP 3rd Generation ELISA kit” (manufactured by Cygnus Technologies) The amount of HCP in the eluate in each fraction was calculated by the ELISA method using
- HCP contamination in eluates 1 to 3 (ppm) total HCP in eluates 1 to 3 / total IgG in eluates 1 to 3 HCP contamination in eluates (ppm) and loaded IgG / HCP mixture
- HCP purification factor was calculated from the HCP contamination amount (ppm) in the following formula.
- HCP purification factor HCP contamination in the loaded IgG / HCP mixture (ppm) / HCP contamination in eluates 1 to 3 (ppm)
- HCP purification factor exceeds 5000 ... Evaluation "A" HCP purification factor is more than 1500 and less than 5000 ... Evaluation "B” HCP purification factor is 1500 or less ... Evaluation "E” Evaluations A and B indicate that the impurity removal ability is sufficient, and evaluation E indicates that the impurity removal ability is not sufficient.
- the carrier for mixed mode affinity chromatography of the present invention having sufficient impurity removal capability is used for antibody purification, the purity of the antibody can be increased, and the purity of the antibody can be further improved.
- the human IgG antibody was adjusted to 5 mg / mL with a standard buffer (20 mM phosphate buffer, 150 mM NaCl, pH 7.4). 15 mL of the solution was added at a flow rate of 0.21 mL / min. Thereafter, after washing by washing 5 mL of post-loading washing solution (20 mM phosphate buffer, 150 mM NaCl, pH 7.4) at the same flow rate, 5 mL of washing solution before elution (20 mM phosphate buffer, 1 M NaCl, pH 7.4) at the same flow rate. Washed away.
- Example 1 Production of carrier for mixed mode affinity chromatography (1) Preparation of wet gel Cross-linked agarose base material “Sepharose 4 Fast Flow” (manufactured by GE Healthcare) (“SEPHAROSE” is a registered trademark) Was washed by repeating suspension and filtration using pure water on a glass filter to obtain a base slurry. Pure water was removed from the substrate slurry by suction filtration to obtain a wet gel.
- the EDC solution was prepared by dissolving 0.2 g of EDC in 2 mL of DMSO (dimethyl sulfoxide), and the NHS solution was prepared by dissolving 0.2 g of NHS in 2 mL of DMSO. is there.
- the reaction gel solution was transferred to a disposable column and washed with 6 mL of ice-cold 1 mM hydrochloric acid to obtain an EDC / NHS activated carboxylated carrier.
- Xaa5 is an amino acid residue derived from N- ⁇ -chloroacetyl-L-lysine
- Xaa15 is an amino acid residue derived from L-homocysteine
- Xaa5 and Xaa15 are: The chloroacetyl group on the side chain of N- ⁇ -chloroacetyl-L-lysine and the thiol group on the side chain of L-homocysteine form a thioether bond and crosslink.
- Cyclic Peptide Immobilization amount (affinity ligand introduction amount) of the obtained cyclic peptide-immobilized carboxylated carrier was measured according to the above-mentioned “Method for measuring affinity ligand introduction amount (peptide immobilization amount)”. . As a result, the amount of cyclic peptide immobilized was 1.7 mmol / L-gel.
- Example 2 Production of carrier for mixed mode affinity chromatography
- cyclic peptide B represented by the following formula (B) (SEQ ID NO: 14)
- B SEQ ID NO: 14
- Xaa5 and Xaa15 are both amino acid residues derived from L-homocysteine, and Xaa5 and Xaa15 have a disulfide bond between the thiol groups in the side chains of L-homocysteine. Formed and cross-linked.
- Cyclic Peptide Immobilization amount (affinity ligand introduction amount) of the obtained cyclic peptide-immobilized carboxylated carrier was measured according to the above-mentioned “Method for measuring affinity ligand introduction amount (peptide immobilization amount)”. As a result, the amount of cyclic peptide introduced was 1.6 mmol / L-gel.
- Example 3 Production of carrier for mixed mode affinity chromatography Carboxylation was carried out in the same manner as in Example 1 except that the amount of sodium chloroacetate was changed to 6.1 g in “Preparation of carboxylated carrier-introduction of cation exchange group”. A carrier was prepared.
- Xaa5 is an amino acid residue derived from N- ⁇ -chloroacetyl-L-lysine
- Xaa15 is an amino acid residue derived from L-penicillamine
- Xaa5 and Xaa15 are N
- the ⁇ -chloroacetyl-L-lysine side chain chloroacetyl group and the L-penicillamine side chain thiol group are cross-linked to form a thioether bond.
- Cyclic Peptide Immobilization amount (affinity ligand introduction amount) of the obtained cyclic peptide-immobilized carboxylated carrier was measured according to the above-mentioned “Method for measuring affinity ligand introduction amount (peptide immobilization amount)”. . As a result, the amount of cyclic peptide immobilized was 2.0 mmol / L-gel.
- Example 4 Production of carrier for mixed mode affinity chromatography
- carboxylated carrier prepared as described above was used, and the following formula was used instead of cyclic peptide A.
- a cyclic peptide-immobilized carboxylated carrier was prepared in the same manner as in Example 3 except that the cyclic peptide D (SEQ ID NO: 16) represented by (D) was used.
- Xaa5 is an amino acid residue derived from 2-propargyl-L-homoglycine
- Xaa15 is an amino acid residue derived from ⁇ -azide-L-alanine
- Xaa5 and Xaa15 are: Crosslinking is performed by forming a triazole bond between the propargyl group of the side chain of 2-propargyl-L-homoglycine and the azide group of the side chain of ⁇ -azide-L-alanine.
- Cyclic Peptide Immobilization amount (affinity ligand introduction amount) of the obtained cyclic peptide-immobilized carboxylated carrier was measured according to the above-mentioned “Method for measuring affinity ligand introduction amount (peptide immobilization amount)”. . As a result, the amount of cyclic peptide immobilized was 1.7 mmol / L-gel.
- Example 5 Production of carrier for mixed mode affinity chromatography
- carboxylated carrier prepared as described above was used, and the following formula was used instead of cyclic peptide A.
- a cyclic peptide-immobilized carboxylated carrier was prepared in the same manner as in Example 3 except that the cyclic peptide E (SEQ ID NO: 17) represented by (E) was used.
- Xaa5 is an amino acid residue derived from N- ⁇ -chloroacetyl-L-lysine
- Xaa15 is an amino acid residue derived from cysteine
- Xaa5 and Xaa15 are N- The chloroacetyl group in the side chain of ⁇ -chloroacetyl-L-lysine and the thiol group in the side chain of cysteine are crosslinked by forming a thioether bond.
- Cyclic Peptide Immobilization amount (affinity ligand introduction amount) of the obtained cyclic peptide-immobilized carboxylated carrier was measured according to the above-mentioned “Method for measuring affinity ligand introduction amount (peptide immobilization amount)”. . As a result, the cyclic peptide immobilization amount was 1.9 mmol / L-gel.
- Example 6 Production of carrier for mixed mode affinity chromatography
- cyclic peptide F represented by the following formula (F) (SEQ ID NO: 18)
- F cyclic peptide-immobilized carboxylated carrier
- Xaa5 and Xaa15 are both amino acid residues derived from L-cysteine, and Xaa5 and Xaa15 form a disulfide bond between the thiol groups in the side chains of L-cysteine. Are cross-linked.
- Cyclic Peptide Immobilization amount (affinity ligand introduction amount) of the obtained cyclic peptide-immobilized carboxylated carrier was measured according to the above-mentioned “Method for measuring affinity ligand introduction amount (peptide immobilization amount)”. . As a result, the cyclic peptide immobilization amount was 1.8 mmol / L-gel.
- Example 7 Production of carrier for mixed mode affinity chromatography
- the point using the carboxylated carrier prepared as described above, and the above 5 mg / mL cyclic peptide A solution 1 Example except that 1.5 mL of 10 mg / mL cyclic peptide G solution prepared by dissolving cyclic peptide G (SEQ ID NO: 19) represented by the following formula (G) in DMSO was used instead of 5 mL
- a cyclic peptide-immobilized carboxylated carrier was prepared.
- Xaa5 is an amino acid residue derived from L-lysine
- Xaa15 is an amino acid residue derived from L-glutamic acid
- the amino group of the side chain of L-lysine and L-glutamic acid It is crosslinked by forming an amide bond with the side chain carboxy group.
- Cyclic Peptide Immobilization amount (affinity ligand introduction amount) of the obtained cyclic peptide-immobilized carboxylated carrier was measured according to the above-mentioned “Method for measuring affinity ligand introduction amount (peptide immobilization amount)”. . As a result, the amount of cyclic peptide immobilized was 1.2 mmol / L-gel.
- Cyclic Peptide Immobilization amount (affinity ligand introduction amount) of the obtained cyclic peptide-immobilized carboxylated carrier was measured according to the above-mentioned “Method for measuring affinity ligand introduction amount (peptide immobilization amount)”. . As a result, the cyclic peptide immobilization amount was 1.1 mmol / L-gel.
- the carrier for mixed mode affinity chromatography of Comparative Example 1 which does not contain a hydrophilic polymer had an impurity removal ability of “E” evaluation and did not have sufficient impurity removal ability.
- the carrier for mixed mode affinity chromatography of Comparative Example 2 containing a hydrophilic polymer had an impurity removal ability of “B” evaluation, and had a sufficient impurity removal ability.
- the cyclic peptide cross-linked structure includes a thioether bond between a homocysteine residue and a haloacetyl group-containing amino acid residue (which means an amino acid residue having a haloacetyl group in the side chain) and a homocysteine residue.
- a disulfide bond is particularly preferred, a thioether bond between a penicillamine residue and a haloacetyl group-containing amino acid residue is next preferred, and a thioether bond, a triazole bond and an amide bond between cysteine and a haloacetyl group-containing amino acid residue are further preferred. It can be seen that it is preferable.
- the carrier for mixed mode affinity chromatography of the present invention comprises all of a base material, a hydrophilic polymer, an antibody-binding cyclic peptide, and a cation exchange group, so that the antibody adsorption capacity, impurity removal ability and chemical resistance can be obtained. Both are excellent.
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Analytical Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Molecular Biology (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Medicinal Chemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Immunology (AREA)
- Peptides Or Proteins (AREA)
- Solid-Sorbent Or Filter-Aiding Compositions (AREA)
Abstract
Description
[1] 基材と、親水性ポリマーと、抗体結合性環状ペプチドと、陽イオン交換基と、を有するミックスモードアフィニティクロマトグラフィー用担体。
[2] 上記抗体結合性環状ペプチドは側鎖間の分子内架橋により環化した環状部を有する、上記[1]に記載のミックスモードアフィニティクロマトグラフィー用担体。
[3] 上記分子内架橋が、ジスルフィド結合、チオエーテル結合、トリアゾール結合、およびアミド結合からなる群から選択される少なくとも1つを含む、上記[2]に記載のミックスモードアフィニティクロマトグラフィー用担体。
[4] 上記分子内架橋が、ジスルフィド結合、チオエーテル結合、およびトリアゾール結合からなる群から選択される少なくとも1つを含む、上記[2]または[3]に記載のミックスモードアフィニティクロマトグラフィー用担体。
[5] 上記ジスルフィド結合が、L-システインおよびD-システイン以外の側鎖にチオール基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖チオール基とL-システインおよびD-システイン以外の側鎖にチオール基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖チオール基との間で形成されたジスルフィド結合であり、上記チオエーテル結合が、L-システインおよびD-システイン以外の側鎖にチオール基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖チオール基と側鎖にハロアセチル基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖ハロアセチル基との間で形成されたチオエーテル結合である、上記[4]に記載のミックスモードアフィニティクロマトグラフィー用担体。
[6] 上記ジスルフィド結合が、システイン、ホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖チオール基とシステイン、ホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖チオール基との間で形成されたジスルフィド結合であり、上記チオエーテル結合が、システイン、ホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖チオール基と側鎖にハロアセチル基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖ハロアセチル基との間で形成されたチオエーテル結合である、上記[4]に記載のミックスモードアフィニティクロマトグラフィー用担体。
[7] 上記ジスルフィド結合が、ホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖チオール基とホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖チオール基との間で形成されたジスルフィド結合であり、上記チオエーテル結合が、ホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖チオール基と側鎖にハロアセチル基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖ハロアセチル基との間で形成されたチオエーテル結合である、上記[4]~[6]のいずれか1つに記載のミックスモードアフィニティクロマトグラフィー用担体。
[8] 上記分子内架橋が、ホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖チオール基とホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖チオール基との間で形成されたジスルフィド結合、またはホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖チオール基と側鎖にハロアセチル基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖ハロアセチル基との間で形成されたチオエーテル結合である、上記[2]または[3]に記載のミックスモードアフィニティクロマトグラフィー用担体。
[9] 上記ジスルフィド結合がホモシステインに由来する第1のアミノ酸残基の側鎖チオール基とホモシステインに由来する第2のアミノ酸残基の側鎖チオール基との間で形成されたジスルフィド結合であり、上記チオエーテル結合がホモシステインに由来する第1のアミノ酸残基の側鎖チオール基と側鎖にハロアセチル基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖ハロアセチル基との間で形成されたチオエーテル結合である、上記[8]に記載のミックスモードアフィニティクロマトグラフィー用担体。
[10] 上記環状部のアミノ酸残基数が8~14残基である、上記[2]~[9]のいずれか1つに記載のミックスモードアフィニティクロマトグラフィー用担体。
[11] 上記抗体結合性環状ペプチドは直鎖部を有する、上記[1]~[10]のいずれか1つに記載のミックスモードアフィニティクロマトグラフィー用担体。
[12] 上記直鎖部は側鎖にヒドロキシ基およびカルボキシ基からなる群から選択される少なくとも1つを有するアミノ酸残基を含む、上記[11]に記載のミックスモードアフィニティクロマトグラフィー用担体。
[13] 上記基材が多糖類、アクリレート系重合体、メタクリレート系重合体およびスチレン系重合体からなる群から選択される少なくとも1種である、上記[1]~[12]のいずれか1つに記載のミックスモードアフィニティクロマトグラフィー用担体。
[14] 上記基材が多糖類、アクリレート系重合体およびメタクリレート系重合体からなる群から選択される少なくとも1種である、上記[1]~[13]のいずれか1つに記載のミックスモードアフィニティクロマトグラフィー用担体。
[15] 上記基材がアガロースおよびセルロースからなる群から選択される少なくとも1種である、上記[1]~[14]のいずれか1つに記載のミックスモードアフィニティクロマトグラフィー用担体。
[16] 上記親水性ポリマーが親水性多糖類である、上記[1]~[15]のいずれか1つに記載のミックスモードアフィニティクロマトグラフィー用担体。
[17] 上記親水性多糖類がデキストラン、カルボキシメチルデキストラン、プルラン、ヒドロキシエチルセルロース、およびカルボキシメチルセルロースからなる群から選択される少なくとも1種である、上記[16]に記載のミックスモードアフィニティクロマトグラフィー用担体。
[18] 上記親水性多糖類が、デキストラン、カルボキシメチルデキストランおよびプルランからなる群から選択される少なくとも1種である、上記[16]または[17]に記載のミックスモードアフィニティクロマトグラフィー用担体。
[19] 上記抗体結合性環状ペプチドの分子量が5000未満である、上記[1]~[18]のいずれか1つに記載のミックスモードアフィニティクロマトグラフィー用担体。
[20] 上記陽イオン交換基がカルボキシ基またはスルホキシ基である、上記[1]~[19]のいずれか1つに記載のミックスモードアフィニティクロマトグラフィー用担体。
[21] 上記陽イオン交換基がカルボキシ基である、上記[1]~[20]のいずれか1つに記載のミックスモードアフィニティクロマトグラフィー用担体。
なお、本発明において、範囲を「~」を用いて表現した場合は、その範囲は「~」の両側を含むものとする。
本発明のミックスモードアフィニティクロマトグラフィー用担体は、基材と、親水性ポリマーと、抗体結合性環状ペプチドと、陽イオン交換基と、を有する。
本発明のミックスモードアフィニティクロマトグラフィー用担体に用いる基材は、特に限定されないが、好ましくは多糖類、アクリレート系重合体、メタクリレート系重合体およびスチレン系重合体からなる群から選択される少なくとも1種であり、より好ましくは多糖類、アクリレート系重合体およびメタクリレート系重合体からなる群から選択される少なくとも1種であり、さらに好ましくはアガロースおよびセルロースからなる群から選択される少なくとも1種である。
基材は1種を単独で用いてもよいし、2種以上を組み合わせて用いてもよい。
上記多糖類は、特に限定されないが、例えば、セルロース、アガロース、デキストラン、キトサン、および、グルコマンナン等の天然多糖類、ならびに、これら天然多糖類に架橋構造を導入した架橋多糖類等が挙げられる。架橋多糖類は、例えば、天然多糖類が有する水酸基に対して、エピクロロヒドリン、(ポリ)アルキレングリコールジグリシジルエーテル、および、アルキレンジイソシアネート等の架橋剤を用いて架橋構造を導入することにより製造することができる。
上記アクリレート系重合体は、特に限定されないが、例えば、アクリル酸メチル、アクリル酸エチル、アクリル酸ヒドロキシエチル、アクリル酸ヒドロキシプロピル、アクリル酸ブチル、アクリル酸ステアリル、アクリル酸2-エチルヘキシル、シクロヘキシルアクリレート、グリセリンモノアクリレート、グリシジルアクリレート、4,5-エポキシブチルアクリレート、および、9,10-エポキシステアリルアクリレート等のアクリル酸エステルの1種を重合してなる重合体、アクリル酸エステルの2種以上を共重合してなる共重合体、ならびに、アクリル酸エステルの1種以上とアクリル酸エステル以外のビニル基含有化合物の1種以上とを共重合してなる共重合体等が挙げられる。ここで、アクリル酸エステル以外のビニル基含有化合物としては、例えば、エチレン、および、プロピレン等のモノビニル化合物、ジビニルベンゼン、および、トリビニルベンゼン等の芳香族ポリビニル化合物、ならびに、ブタジエン、メチレンビスアクリルアミド、および、イソシアヌル酸トリアリル等のポリビニル化合物が挙げられる。これらの重合体または共重合体に対して、エピクロロヒドリン、(ポリ)アルキレングリコールジグリシジルエーテル、および、アルキレンジイソシアネート等の架橋剤を用いて架橋構造を導入してもよい。
上記メタクリレート系重合体は、特に限定されるものではないが、例えば、メタクリル酸メチル、メタクリル酸エチル、メタクリル酸ヒドロキシエチル、メタクリル酸ヒドロキシプロピル、メタクリル酸ブチル、メタクリル酸ステアリル、メタクリル酸2-エチルヘキシル、シクロヘキシルメタクリレート、グリセリンモノメタクリレート、グリシジルメタクリレート、4,5-エポキシブチルメタクリレート、および、9,10-エポキシステアリルメタクリレート等のメタクリル酸エステルの1種を重合してなる重合体、メタクリル酸エステルの2種以上を共重合してなる共重合体、ならびに、メタクリル酸エステルの1種以上とメタクリル酸エステル以外のビニル基含有化合物の1種以上とを共重合してなる共重合体等が挙げられる。メタクリル酸エステル以外のビニル基含有化合物としては、例えば、上述したアクリル酸エステル以外のビニル基含有化合物で例示した化合物が挙げられる。これらの重合体または共重合体に対して、アクリレート系重合体で用いられ得る上述した架橋剤を用いて架橋構造を導入してもよい。
上記スチレン系重合体は、特に限定されるものではないが、例えば、スチレン、メチルスチレン、エチルスチレン、ヒドロキシスチレン、および、クロロスチレン等のスチレン系化合物の1種を重合してなる重合体、スチレン系化合物の2種以上を重合してなる共重合体、ならびに、スチレン系化合物の1種以上とスチレン系化合物以外のビニル基含有化合物の1種以上とを共重合してなる共重合体等が挙げられる。スチレン系化合物以外のビニル基含有化合物としては、例えば、上述したアクリル酸エステル以外のビニル基含有化合物で例示した化合物が挙げられる。これらの重合体または共重合体に対して、アクリレート系重合体で用いられ得る架橋剤を用いて架橋構造を導入してもよい。
基材は多孔質粒子または多孔質膜であることが好ましい。基材が多孔質粒子または多孔質膜であることにより、表面積が大きくなり、単位時間あたりの処理容量を大きくすることができる。
基材が多孔質粒子または多孔質膜である場合の細孔容積は、特に限定されないが、水銀ポロシメーターにより測定した細孔容積が、好ましくは0.2mL/g~10mL/g、より好ましくは0.2mL/g~5.0mL/gの範囲内である。細孔容積がこの範囲内であると、抗体吸着容量が大きくなる。また、機械的強度が低下しない。
基材が多孔質粒子または多孔質膜である場合の比表面積は、特に限定されないが、BET(Brunauer、Emmett、Teller)法により測定した比表面積(BET比表面積)が、好ましくは2m2/g~1500m2/g、より好ましくは5m2/g~1000m2/gの範囲内である。比表面積がこの範囲内であると、抗体吸着容量が大きくなる。
基材が多孔質粒子である場合の平均粒子径は、特に限定されないが、好ましくは0.5μm~1000μm、より好ましくは1μm~250μm、さらに好ましくは2μm~150μmの範囲内である。平均粒子径がこの範囲内であると、カラムに充填して通液した時の圧力損失が小さく、通液速度を高くでき、処理効率が向上するとともに、抗体吸着容量が大きくなる。なお、多孔質粒子の平均粒子径は、既知の方法で測定することができる。例えば、光学顕微鏡にて、100個以上の多孔質粒子の粒子径を測定し、その分布からメジアン径を算出することで平均粒子径が得られる。
基材の具体例として、例えば、アガロース系の担体であるセファローズシリーズ(GEヘルスケア社製)(“SEPHAROSE”は登録商標)、セルロース系の架橋担体であるセルファインシリーズ(JNC社製)(“CELLUFINE”は登録商標)、アリルデキストランとN,N’-メチレンビスアクリルアミドの架橋ポリマーであるセファクリルシリーズ(GEヘルスケア社製)(“SEPHACRYL”は登録商標)、ならびに、アクリレート系の担体であるトヨパールHWシリーズ(東ソー社製)(“トヨパール”および“TOYOPEARL”は登録商標)等の市販品が挙げられるが、これらに限定されるものではない。
基材を親水性ポリマーで被覆することで、本発明のミックスモードアフィニティクロマトグラフィー用担体表面の親水性が増し、非特異的吸着物の吸着が抑制されるため、精製純度が改善する効果がある。
上記基材が多孔質粒子である場合、表面にヒドロキシ基と共有結合しうる官能基を有することが好ましい。ここで、ヒドロキシ基と共有結合しうる官能基としては、例えば、エポキシ基およびグリシジル基;臭化シアン、N,N-ジスクシンイミジル炭酸塩(DSC)などで活性化されるヒドロキシ基;アルデヒド基(ホルミル基);ならびに、N-ヒドロキシスクシンイミドエステルおよびカルボニルジイミダゾール活性化エステル等の活性化カルボン酸基;などの反応性官能基等を挙げることができる。
親水性多糖類は、特に限定されないが、精製純度を改善する効果が高いことから、好ましくはデキストラン、カルボキシメチルデキストランおよびプルランから選択される少なくとも1種であり、より好ましくはデキストランである。
親水性ポリマーの分子量は、特に限定されないが、極限粘度で、好ましくは0.10dL/g以上、より好ましくは0.10dL/g~0.90dL/g、さらに好ましくは0.12dL/g~0.40dL/g、いっそう好ましくは0.15dL/g~0.30dL/g、よりいっそう好ましくは0.15dL/g~0.25dL/gの範囲内である。
極限粘度がこの範囲内であると、精製純度がさらに向上する。なお、極限粘度は、第16改正日本薬局方に収載された一般測定法における粘度測定法、第1法「毛細管粘度計法」に従って、数個の異なる濃度の高分子溶液の粘度を求めて粘度の濃度依存性を測定し、得られた直線の濃度を0に外挿することにより求めることができる。
ところで、高分子の極限粘度ηと分子量Mとの間には、下記マーク-ホウィンク-桜田の式(Mark-Houwink-Sakurada equation)が成立することから、直接的な測定法でいくつかの試料の分子量を求め、分子量とそれぞれの極限粘度の値とからKとαを決めておけば、同じ種類の高分子については、極限粘度ηを測定することによって分子量Mが、分子量Mを測定することによって極限粘度ηが、それぞれ、求められる。
η=KMα
ここで、Kおよびαは高分子の種類、溶媒の種類および温度によって定まる定数である。
ηDextran[dL/g]=9×10-4×MwDextran 0.5[dL/g]
親水性ポリマーの被覆量(以下、単に「親水性ポリマー被覆量」という場合がある。)は、特に限定されないが、好ましくは3mg/g-dry gel~450mg/g-dry gel、より好ましくは3mg/g-dry gel~250mg/g-dry gel、さらに好ましくは3mg/g-dry gel~230mg/g-dry gel、いっそう好ましくは10mg/g-dry gel~230mg/g-dry gel、よりいっそう好ましくは20mg/g-dry gel~230mg/g-dry gelである。
従って、親水性ポリマー被覆量は以下の式により求めることができる。
親水性ポリマー被覆量(mg/g-dry gel)=WP/W0=(W1-W0)/W0
上記被覆前基材の乾燥質量(W0)は、次のようにして算出することができる。
W0=W0,xg×w0/x
ここで、
W0,xg:被覆前基材の湿ゲルxgの乾燥質量
w0:親水性ポリマー被覆反応に用いた被覆前基材の湿ゲル質量
x:乾燥に用いた被覆前基材の湿ゲル質量(xg)
である。
上記担体全量の乾燥質量(W1)も、同様にして算出することができる。
まず、被覆前基材の湿ゲル5gを50℃で質量変化がなくなるまで減圧乾燥して質量を測定し、親水性ポリマー被覆反応に用いた被覆前基材の湿ゲル質量との積より、被覆前基材の乾燥質量とする。
次いで、被覆前基材に親水性ポリマーを被覆して得た担体の湿ゲル5gを50℃で質量変化がなくなるまで減圧乾燥して質量を測定し、親水性ポリマー被覆反応後に得られた担体の湿ゲル質量との積より、担体の乾燥質量とする。
さらに、担体の乾燥質量と被覆前基材の乾燥質量との差を、被覆前基材を被覆している親水性ポリマーの乾燥質量とする。
最後に、親水性ポリマー被覆量を、被覆前基材の乾燥質量あたりの親水性ポリマーの乾燥質量として算出する。
なお、本発明では、ポリマーまたは多糖類について親水性とは、少なくとも1種類の親水性基を含むことをいう。親水性基とは、好ましくはカルボキシ基、カルボキシ基のアルカリ金属塩、スルホン酸基、スルホン酸基のアルカリ金属塩、ヒドロキシ基、アミド基、カルバモイル基、スルホンアミド基、スルファモイル基、リン酸基、リン酸基のアルカリ金属塩、オキシリン酸基、および、オキシリン酸基のアルカリ金属塩等の官能基が挙げられる。これらの親水性基は、ポリマー中のどの位置に存在してもよく、例えば、ポリマー主鎖末端および/または側鎖に、直接または連結基を介して結合していてもよい。また、親水性基は1分子中に、好ましくは複数個が存在する。
本発明のミックスモードアフィニティクロマトグラフィー用担体に用いる抗体結合性環状ペプチドは、特に限定されないが、好ましくは側鎖間の分子内架橋により環化した環状部を有する。
ジスルフィド結合は「S-S」結合であれば特に限定されず、例えば、2個のチオール基(「メルカプト基」ともいう。)間で形成されるS-S結合が挙げられる。
mおよびnは、それぞれ独立に、1または2であり;
m=1であるとき、R1は水素原子またはメチル基であり;
m=2であるとき、R1は水素原子であり;
n=1であるとき、R2は水素原子またはメチル基であり;
n=2であるとき、R2は水素原子であり;
*は他のアミノ酸残基または他の置換基との結合点を表す。
mおよびnは、それぞれ独立に、1または2であり;
m=1であるとき、R1はメチル基であり;
m=2であるとき、R1は水素原子であり;
n=1であるとき、R2はメチル基であり;
n=2であるとき、R2は水素原子であり;
*は他のアミノ酸残基または他の置換基との結合点を表す。
ジスルフィド結合はアルカリ耐性が高いことから、ミックスモードアフィニティクロマトグラフィー用担体は、アルカリによる洗浄を繰り返し行っても抗体結合性が維持され、抗体精製コストを低減することができる。このようなジスルフィド結合としては、2つのシステイン残基間で形成されたジスルフィド結合以外のジスルフィド結合が好ましく、システイン以外の側鎖にチオール基を有するアミノ酸に由来するアミノ酸残基間で形成されたジスルフィド結合がより好ましく、2つのホモシステイン残基間で形成されたジスルフィド結合が特に好ましい。
チオエーテル結合は、エーテル結合「-O-」の酸素原子を硫黄原子で置換した形の「-S-」結合であれば特に限定されず、例えば、チオール基(「メルカプト基」ともいう。)とハロアセチル基との間で形成される-S-結合が挙げられる。ここで、ハロアセチル基は、好ましくはクロロアセチル基またはブロモアセチル基であり、より好ましくはクロロアセチル基である。また、ハロアセチル基は、側鎖アミノ基の水素原子を置換する形でアミノ酸に導入されたものが好ましい。
なお、nは、好ましくは1≦n≦4を満たす整数であり、Xは、好ましくは塩素原子または臭素原子であり、より好ましくは塩素原子である。
n=1であるとき、N3-ハロアセチル-L-2,3-ジアミノプロパン酸〔(2S)-2-アミノ-3-[(2-ハロアセチル)アミノ]プロパン酸〕またはN3-ハロアセチル-D-2,3-ジアミノプロパン酸〔(2R)-2-アミノ-3-[(2-ハロアセチル)アミノ]プロパン酸〕であり、
n=2であるとき、N4-ハロアセチル-L-2,4-ジアミノブタン酸〔(2S)-2-アミノ-4-[(2-ハロアセチル)アミノ]ブタン酸〕またはN4-ハロアセチル-D-2,4-ジアミノブタン酸〔(2R)-2-アミノ-4-[(2-ハロアセチル)アミノ]ブタン酸〕であり、
n=3であるとき、N-δ-ハロアセチル-L-オルニチン〔(2S)-2-アミノ-5-[(2-ハロアセチル)アミノ]ペンタン酸〕またはN-δ-ハロアセチル-D-オルニチン〔(2R)-2-アミノ-5-[(2-ハロアセチル)アミノ]ペンタン酸〕であり、
n=4であるとき、N-ε-ハロアセチル-L-リシン〔(2S)-2-アミノ-6-[(2-ハロアセチル)アミノ]ヘキサン酸〕またはN-ε-ハロアセチル-D-リシン〔(2R)-2-アミノ-6-[(2-ハロアセチル)アミノ]ヘキサン酸〕である。
mは1または2であり;
nは1以上の整数であり;
m=1であるとき、Rは水素原子またはメチル基であり;
m=2であるとき、Rは水素原子であり;
*は他のアミノ酸残基または末端基との結合点を表す。
また、nは、好ましくは、1≦n≦4を満たす整数である。
mは1または2であり;
nは1以上の整数であり;
m=1であるとき、Rはメチル基であり;
m=2であるとき、Rは水素原子であり;
*は他のアミノ酸残基または他の基との結合点を表す。
また、nは、好ましくは、1≦n≦4を満たす整数である。
チオエーテル結合はアルカリ耐性が高いことから、ミックスモードアフィニティクロマトグラフィー用担体は、アルカリによる洗浄を繰り返し行っても抗体結合性が維持され、抗体精製コストを低減することができる。このようなチオエーテル結合としては、ホモシステイン残基とN-ε-クロロアセチルリシン残基との間で形成されたチオエーテル結合が特に好ましい。
上記トリアゾール結合は、特に限定されないが、好ましくは側鎖にアジド基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖アジド基と側鎖にアルキニル基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖アルキニル基との間で形成されたトリアゾール結合である。
m-=2であるとき、側鎖にアジド基を有するアミノ酸に由来するアミノ酸残基は、γ-アジド-L-ホモアラニンまたはγ-アジド-D-ホモアラニンに由来するアミノ酸残基であり、好ましくはγ-アジド-L-ホモアラニンである。
m=3であるとき、側鎖にアジド基を有するアミノ酸に由来するアミノ酸残基は、δ-アジド-L-オルニチンまたはδ-アジド-D-オルニチンに由来するアミノ酸残基であり、好ましくはδ-アジド-L-オルニチンである。
m=4であるとき、側鎖にアジド基を有するアミノ酸に由来するアミノ酸残基は、ε-アジド-L-リシンまたはε-アジド-D-リシンに由来するアミノ酸残基であり、好ましくはε-アジド-L-リシンである。
n=2であるとき、側鎖にアルキニル基を有するアミノ酸に由来するアミノ酸残基は、2-プロパルギル-L-アラニン(L-ホモプロパルギルグリシン)〔(2S)-2-アミノ-5-ヘキシン酸〕または2-プロパルギル-D-アラニン(D-ホモプロパルギルグリシン)〔(2R)-2-アミノ-5-ヘキシン酸〕に由来するアミノ酸残基であり、好ましくは2-プロパルギル-L-アラニン(L-ホモプロパルギルグリシン)〔(2S)-2-アミノ-5-ヘキシン酸〕に由来するアミノ酸残基である。
n=3であるとき、側鎖にアルキニル基を有するアミノ酸に由来するアミノ酸残基は、2-プロパルギル-L-ホモアラニン(2-プロパルギル-L-ビスホモグリシン)〔(2S)-2-アミノ-6-ヘプチン酸〕または2-プロパルギル-D-ホモアラニン(2-プロパルギル-D-ビスホモグリシン)〔(2R)-2-アミノ-6-ヘプチン酸〕に由来するアミノ酸残基であり、好ましくは2-プロパルギル-L-ホモアラニン(2-プロパルギル-L-ビスホモグリシン)〔(2S)-2-アミノ-6-ヘプチン酸〕に由来するアミノ酸残基である。
トリアゾール結合はアルカリ耐性が高いことから、分子内架橋にトリアゾール結合を含むと、ミックスモードアフィニティクロマトグラフィー用担体は、アルカリによる洗浄を繰り返し行っても抗体結合性が維持され、抗体精製コストを低減することができる。このようなトリアゾール結合としては、とりわけ、γ-アジドホモアラニン残基またはε-アジドリシン残基とホモプロパルギルグリシン残基またはビスホモプロパルギルグリシン残基との間で形成されるトリアゾール結合が好ましい。
上記アミド結合は、特に限定されないが、好ましくは側鎖にアミノ基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖アミノ基と側鎖にカルボキシ基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖カルボキシ基との間で形成されたアミド結合である。
m=2であるとき、側鎖にアミノ基を有するアミノ酸に由来するアミノ酸残基は、L-2,4-ジアミノブタン酸〔(2S)-2,4-ジアミノブタン酸〕またはD-2,4-ジアミノブタン酸〔(2R)-2,4-ジアミノブタン酸〕に由来するアミノ酸残基であり、好ましくはL-2,4-ジアミノブタン酸〔(2S)-2,4-ジアミノブタン酸〕に由来するアミノ酸残基である。
m=3であるとき、側鎖にアミノ基を有するアミノ酸に由来するアミノ酸残基は、L-オルニチン〔(2S)-2,5-ジアミノペンタン酸〕またはD-オルニチン〔(2R)-2,5-ジアミノペンタン酸〕に由来するアミノ酸残基であり、好ましくはL-オルニチン〔(2S)-2,5-ジアミノペンタン酸〕に由来するアミノ酸残基である。
m=4であるとき、側鎖にアミノ基を有するアミノ酸に由来するアミノ酸残基は、L-リシン〔(2S)-2,6-ジアミノヘキサン酸〕またはD-リシン〔(2R)-2,6-ジアミノヘキサン酸〕に由来するアミノ酸残基であり、好ましくはL-リシン〔(2S)-2,6-ジアミノヘキサン酸〕に由来するアミノ酸残基である。
n=2であるとき、側鎖にカルボキシ基を有するアミノ酸に由来するアミノ酸残基は、L-グルタミン酸またはD-グルタミン酸に由来するアミノ酸残基であり、好ましくはL-グルタミン酸に由来するアミノ酸残基である。
n=3であるとき、側鎖にカルボキシ基を有するアミノ酸に由来するアミノ酸残基は、L-ホモグルタミン酸〔(2S)-2-アミノアジピン酸〕またはD-ホモグルタミン酸〔(2R)-2-アミノアジピン酸〕に由来するアミノ酸残基であり、好ましくはL-ホモグルタミン酸〔(2S)-2-アミノアジピン酸〕に由来するアミノ酸残基である。
アミド結合はアルカリ耐性が高いことから、ミックスモードアフィニティクロマトグラフィー用担体は、アルカリによる洗浄を繰り返し行っても抗体結合性が維持され、抗体精製コストを低減することができる。このようなアミド結合としては、とりわけ、リシン残基とグルタミン酸残基との間で形成されたアミド結合が好ましい。
上記環状部のアミノ酸残基数は、上記環状ペプチドの全アミノ酸残基数以下であれば特に限定されないが、好ましくは8~14残基であり、より好ましくは9~13残基であり、さらに好ましくは10~12残基であり、いっそう好ましくは11残基である。
上記環状ペプチドは直鎖部を有してもよい。直鎖部とは上記環状ペプチドのポリペプチド鎖のうち、環状部に含まれない部分をいう。
上記環状ペプチドは基材および親水性ポリマーの少なくとも一方と共有結合を介して結合していることが好ましい。
このような共有結合としては、(a)環状ペプチド直鎖部のアミノ酸残基側鎖と基材および親水性ポリマーの少なくとも一方との間の共有結合、または(b)環状ペプチドのポリペプチド鎖のN末端またはC末端と基材および親水性ポリマーの少なくとも一方との間の共有結合等が挙げられる。
上記(a)の共有結合としては、アミノ酸残基側鎖の固定化官能基と基材および親水性ポリマーの少なくとも一方の反応性官能基(固定化官能基と反応して共有結合を形成しうる官能基をいう。)との間で形成される結合等が挙げられる。この場合の固定化官能基および反応性官能基については後述する。
上記(b)の共有結合としては、ポリペプチド鎖のN末端またはC末端と基材および親水性ポリマーの少なくとも一方のポリマー主鎖または側鎖との間のリンカーを介した、または介さない結合等が挙げられる。
この場合のリンカーとしては、PEG(Polyethylene glycol;ポリエチレングリコール)リンカー等が挙げられる。PEGリンカーのエチレングリコール単位数は、1個以上であれば特に限定されないが、好ましくは1~24個、より好ましくは1~12個、さらに好ましくは4~8個である。
上記環状ペプチドの分子量は、特に限定されるものではないが、合成コストの観点から10000以下が好ましく、抗原性の観点から5000以下が好ましい。上記環状ペプチドの分子量は、より好ましくは約4000以下であり、さらに好ましくは約3000以下であり、最も好ましくは約2000以下である。ここで、「約」は±2%の範囲を含むことを意味する。
なお、ここで、環状ペプチドの分子量は、環状部と直鎖部とを合わせた分子量である。
分子量が5000未満であると、抗原性が低減され、実質的に抗原性を示さなくなる。
また、上記環状ペプチドのアミノ酸残基数は、特に限定されないが、好ましくは100残基以下であり、より好ましくは50残基以下であり、さらに好ましくは40残基以下であり、いっそう好ましくは30残基以下であり、よりいっそう好ましくは20残基以下である。
なお、ここで、環状ペプチドのアミノ酸残基数は、環状部と直鎖部とを合わせたアミノ酸残基数である。
本発明において、抗体結合性とは、抗体および/または抗体誘導体との結合性をいう。
抗体結合性が高いほど、アフィニティクロマトグラフィー用担体のアフィニティリガンドとして使用した際に、抗体の吸着力が高く、洗浄時でも脱離しにくくなる。
抗体とは、免疫グロブリンまたはその類縁体、フラグメントもしくは融合体をいう。
免疫グロブリンは、IgG(Immunoglobulin G;免疫グロブリンG)、IgM(Immunoglobulin M;免疫グロブリンM)、IgA(Immunoglobulin A;免疫グロブリンA)、IgD(Immunoglobulin D;免疫グロブリンD)およびIgE(Immunoglobulin E;免疫グロブリンE)の5種類のクラス(アイソタイプ)のいずれでもよいが、IgGまたはIgMが好ましく、IgGがより好ましい。
また、類縁体とは、免疫グロブリンの構造または機能が少なくとも部分的に保持された、天然の、または人工的に作製された、タンパク質またはタンパク質コンジュゲートをいう。
また、フラグメントとは、酵素的な処理または遺伝子工学的な設計によって作製された、免疫グロブリンの部分構造を有するタンパク質をいう。
また、融合体とは、各種サイトカイン、サイトカイン受容体等の生物活性を有するタンパク質の機能部分を、免疫グロブリンの全体または一部と遺伝子工学的に融合させて作製したタンパク質をいう。
抗体としては、モノクローナル抗体または免疫グロブリンのFc領域を有する融合体が好ましく、モノクローナル抗体がより好ましい。
上記環状ペプチドをより具体的に説明する。
なお、ここでは、本発明のミックスモードアフィニティクロマトグラフィー用担体にアフィニティリガンドとして導入する前の環状ペプチドについて説明する。
特に明示しない限り、ペプチドまたはタンパク質のアミノ酸配列(「1次構造」ともいう。)は、左端から右端にかけてN末端からC末端となるようにアミノ酸残基を1次元に並べて表す。ペプチドまたはタンパク質のアミノ酸配列中のアミノ酸残基を位置も含めて特定する場合には、アミノ酸残基の略号の右側にN末端側からの何番目のアミノ酸残基であるかを示す数字を付して表す場合がある。例えば、N末端から2番目のL-リシンをLys2と表す場合がある。
上記環状ペプチドは、好ましくは下記式(I)によって表される環状ペプチドである。
RN-Xg-[Xi-Xa-Xm-X1―X2-X3-Xn-Xb-Xj]k-Xh-RC ・・・(I)
本発明のミックスモードアフィニティクロマトグラフィー用担体に用いる環状ペプチドにおいて、ポリペプチド鎖のうち、架橋によって閉じた環の部分を環状部、環状部に含まれない部分を直鎖部という。また、環状部のうち、本発明の環状ペプチドの分子内架橋構造を形成している部分を架橋部といい、本発明の環状ペプチドの抗体結合性に強く寄与する分を抗体結合部という。
式(I)によって表される環状ペプチドの環状部は「Xa-Xm-X1―X2-X3-Xn-Xb」部分であり、直鎖部は「Xg」、「Xh」、「Xi」、および「Xj」であり、架橋部は「Xa」および「Xb」であり、抗体結合部は「X1―X2-X3」である。
また、式(1)中、[Xi-Xa-Xm-X1―X2-X3-Xn-Xb-Xj]を繰返し部という場合がある。
上記式(1)において、X1は、L-ロイシン残基、L-イソロイシン残基、L-メチオニン残基、L-リジン残基、またはL-アルギニン残基であり、好ましくはL-ロイシン残基またはL-イソロイシン残基であり、より好ましくはL-ロイシン残基である。
また、上記式(1)において、X2は、L-バリン残基またはL-イソロイシン残基であり、好ましくはL-バリン残基である。
また、上記式(1)において、X3は、L-トリプトファン残基またはL-フェニルアラニン残基であり、好ましくはL-トリプトファン残基である。
式(I)中、XaおよびXbは、以下の(a)~(d)のうち、いずれか1つである。
XaおよびXbは、好ましくは、それぞれ独立に、側鎖にチオール基を有するアミノ酸に由来するアミノ酸残基であり、より好ましくは、XaおよびXbの少なくとも一方がL-システインおよびD-システイン以外の側鎖にチオール基を有するアミノ酸に由来するアミノ酸残基であり、さらに好ましくは、XaおよびXbの両方がL-システインおよびD-システイン以外の側鎖にチオール基を有するアミノ酸に由来するアミノ酸残基である。
また、上記L-システインおよびD-システイン以外の側鎖にチオール基を有するアミノ酸としては、例えば、L-ホモシステイン、D-ホモシステイン、L-ペニシラミン、およびD-ペニシラミン等が挙げられ、ホモシステインおよびペニシラミンからなる群から選択されるアミノ酸が好ましい。
XaおよびXbは、好ましくは、一方が側鎖にチオール基を有するアミノ酸に由来するアミノ酸残基であり、他方が側鎖にハロアセチル基を有するアミノ酸に由来するアミノ酸残基である。
また、上記側鎖にチオール基を有するアミノ酸は、好ましくは、システイン、ホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸である。
さらに、上記側鎖にチオール基を有するアミノ酸は、より好ましくは、ホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸であり、さらに好ましくは、ホモシステインである。
なお、nは、好ましくは1≦n≦4を満たす整数であり、Xは、好ましくは塩素原子または臭素原子であり、より好ましくは塩素原子である。
n=1であるとき、N3-ハロアセチル-L-2,3-ジアミノプロパン酸〔(2S)-2-アミノ-3-[(2-ハロアセチル)アミノ]プロパン酸〕またはN3-ハロアセチル-D-2,3-ジアミノプロパン酸〔(2R)-2-アミノ-3-[(2-ハロアセチル)アミノ]プロパン酸〕を表し、
n=2であるとき、N4-ハロアセチル-L-2,4-ジアミノブタン酸〔(2S)-2-アミノ-4-[(2-ハロアセチル)アミノ]ブタン酸〕またはN4-ハロアセチル-D-2,4-ジアミノブタン酸〔(2R)-2-アミノ-4-[(2-ハロアセチル)アミノ]ブタン酸〕を表し、
n=3であるとき、N-δ-ハロアセチル-L-オルニチン〔(2S)-2-アミノ-5-[(2-ハロアセチル)アミノ]ペンタン酸〕またはN-δ-ハロアセチル-D-オルニチン〔(2R)-2-アミノ-5-[(2-ハロアセチル)アミノ]ペンタン酸〕を表し、
n=4であるとき、N-ε-ハロアセチル-L-リシン〔(2S)-2-アミノ-6-[(2-ハロアセチル)アミノ]ヘキサン酸〕またはN-ε-ハロアセチル-D-リシン〔(2R)-2-アミノ-6-[(2-ハロアセチル)アミノ]ヘキサン酸〕を表す。
XaおよびXbは、好ましくは、一方が側鎖にアジド基を有するアミノ酸に由来するアミノ酸残基であり、他方が側鎖にアルキニル基を有するアミノ酸に由来するアミノ酸残基である。
m=1であるとき、上記式で表される側鎖にアジド基を有するアミノ酸は、β-アジド-L-アラニンまたはβ-アジド-D-アラニンであり、好ましくはβ-アジド-L-アラニンである。
m=2であるとき、上記式で表される側鎖にアジド基を有するアミノ酸は、γ-アジド-L-ホモアラニンまたはγ-アジド-D-ホモアラニンであり、好ましくはγ-アジド-L-ホモアラニンである。
m=3であるとき、上記式で表される側鎖にアジド基を有するアミノ酸は、δ-アジド-L-オルニチンまたはδ-アジド-D-オルニチンであり、好ましくはδ-アジド-L-オルニチンである。
m=4であるとき、上記式で表される側鎖にアジド基を有するアミノ酸は、ε-アジド-L-リシンまたはε-アジド-D-リシンであり、好ましくはε-アジド-L-リシンである。
n=1であるとき、上記式で表される側鎖にアルキニル基を有するアミノ酸は、2-プロパルギル-L-グリシンまたは2-プロパルギル-D-グリシンであり、好ましくは2-プロパルギル-L-グリシンである。
n=2であるとき、上記式で表される側鎖にアルキニル基を有するアミノ酸は、2-プロパルギル-L-アラニン(2-プロパルギル-L-ホモグリシン)または2-プロパルギル-D-アラニン(2-プロパルギル-D-ホモグリシン)であり、好ましくは2-プロパルギル-L-アラニン(2-プロパルギル-L-ホモグリシン)である。
n=3であるとき、上記式で表される側鎖にアルキニル基を有するアミノ酸は、2-プロパルギル-L-ホモアラニン(2-プロパルギル-L-ビスホモグリシン)または2-プロパルギル-D-ホモアラニン(2-プロパルギル-D-ビスホモグリシン)であり、好ましくは2-プロパルギル-L-ホモアラニン(2-プロパルギル-L-ビスホモグリシン)である。
XaおよびXbは、好ましくは、一方が側鎖にアミノ基を有するアミノ酸に由来するアミノ酸残基であり、他方が側鎖にカルボキシ基を有するアミノ酸に由来するアミノ酸残基である。
m=1であるとき、上記式で表される側鎖にアミノ基を有するアミノ酸は、L-2,3-ジアミノプロパン酸〔(2S)-2,3-ジアミノプロパン酸〕またはD-2,3-ジアミノプロパン酸〔(2R)-2,3-ジアミノプロパン酸〕であり、好ましくはL-2,3-ジアミノプロパン酸〔(2S)-2,3-ジアミノプロパン酸〕である。
m=2であるとき、上記式で表される側鎖にアミノ基を有するアミノ酸は、L-2,4-ジアミノブタン酸〔(2S)-2,4-ジアミノブタン酸〕またはD-2,4-ジアミノブタン酸〔(2R)-2,4-ジアミノブタン酸〕であり、好ましくはL-2,4-ジアミノブタン酸〔(2S)-2,4-ジアミノブタン酸〕である。
m=3であるとき、上記式で表される側鎖にアミノ基を有するアミノ酸は、L-オルニチンまたはD-オルニチンであり、好ましくはL-オルニチンである。
m=4であるとき、上記式で表される側鎖にアミノ基を有するアミノ酸は、L-リシンまたはD-リシンであり、好ましくはL-リシンである。
n=1であるとき、上記式で表される側鎖にカルボキシ基を有するアミノ酸は、L-アスパラギン酸またはD-アスパラギン酸であり、好ましくはL-アスパラギン酸である。
n=2であるとき、上記式で表される側鎖にカルボキシ基を有するアミノ酸は、L-グルタミン酸またはD-グルタミン酸であり、好ましくはL-グルタミン酸である。
n=3であるとき、上記式で表される側鎖にカルボキシ基を有するアミノ酸は、L-ホモグルタミン酸またはD-ホモグルタミン酸であり、好ましくはL-ホモグルタミン酸である。
式(I)中、Xは、アミノ酸残基を表し、Xが複数である場合は、複数のXは互いに同一であっても異なっていてもよい。
上記Xは、アミノ酸残基であればよく、特に限定されないが、表1に示すアミノ酸(B、ZおよびXを除く。)および表2に示すアミノ酸からなる群から選択されるアミノ酸に由来するアミノ酸残基であることが好ましく、表1に示すアミノ酸(B、ZおよびXを除く。)からなる群から選択されるアミノ酸に由来するアミノ酸残基であることがより好ましい。また、存在する場合には、これらのアミノ酸のエナンチオマーまたはジアステレオマーに由来するアミノ酸残基であってもよい。
式(I)中、RNは、N末端基を表す。
上記N末端基としては、例えば、アミノ基が挙げられ、当該アミノ基は、N-アセチル化、N-ホルミル化、またはN-アシル化等のN末端修飾がされていてもよい。
上記C末端基としては、例えば、カルボキシ基が挙げられ、当該カルボキシ基は、アミド化等のC末端修飾がされていてもよい。
式(I)中、gおよびhは、それぞれ独立に、0以上の整数である。
gは、好ましくは0≦g≦20を満たし、より好ましくは0≦g≦10を満たし、さらに好ましくは0≦g≦5を満たす。
hは、好ましくは0≦h≦20を満たし、より好ましくは0≦h≦10を満たし、さらに好ましくは0≦h≦5を満たす。
式(I)中、iおよびjは、それぞれ独立に、0以上の整数である。
iは、好ましくは0≦i≦20を満たし、より好ましくは0≦i≦10を満たし、さらに好ましくは0≦i≦5を満たす。
jは、好ましくは0≦j≦20を満たし、より好ましくは0≦j≦10を満たし、さらに好ましくは0≦j≦5を満たす。
式(I)中、mおよびnは、それぞれ、0≦m≦9、および、0≦n≦9を満たす整数である。
さらに、mおよびnは、3≦m+n≦9を満たし、好ましくは4≦m+n≦8を満たし、より好ましくは5≦m+n≦7を満たす。
上記式(I)において、環状部[Xa-Xm-X1―X2-X3-Xn-Xb]のアミノ酸残基数[(m+n+5)残基]は、8~14酸基であり、好ましくは9~13残基であり、より好ましくは10~12残基である。
環状部のアミノ酸残基数がこの範囲内であると、環状ペプチドの分子内ひずみが大きくなり過ぎず、αヘリックス等の高次構造が安定化するため、本発明の環状ペプチドの抗体結合性が優れる。
kは、k≧1を満たす整数であり、好ましくは1≦k≦3であり、より好ましくは1≦k≦2であり、さらに好ましくはk=1である。
繰返し単位の数は、特に限定されるものではないが、繰返し単位の数が多いほど環状部を多く含むことができるため、環状ペプチドの抗体結合性を向上させることができる可能性があり、繰返し単位の数が少ないほど総アミノ酸残基数を少なくできるため、環状ペプチドの抗原性を抑制することができる可能性がある。環状ペプチドの合成コストの観点からは、アミノ酸残基数が少ない方が好ましく、繰返し単位の数の少ないことが好ましい。
また、k≧2である場合、すなわち、式(I)によって表される環状ペプチドが繰返し単位[Xi-Xa-Xm-X1―X2-X3-Xn-Xb-Xj]を2個以上含む場合は、繰返し単位中のX1、X2、X3、Xa、Xb、Xi、Xj、Xm、およびXnは、それぞれ、繰返し単位間で同一であってもよいし、相違していてもよい。
さらに、上記式(I)において、環状ペプチドの総アミノ酸残基数は、好ましくは8~50残基であり、より好ましくは9~40残基であり、さらに好ましくは10~30残基であり、いっそう好ましくは10~20残基である。
すなわち式(I)中、g、h、j、j、m、n、およびkは、好ましくは8≦g+h+(i+j+m+n+5)×k≦50を満たし、より好ましくは9≦g+h+(i+j+m+n+5)×k≦40を満たし、さらに好ましくは10≦g+h+(i+j+m+n+5)×k≦30を満たし、いっそう好ましくは10≦g+h+(i+j+m+n+5)×k≦20を満たす。
通常、アミノ酸残基数が多くなるほど合成コストが高くなるため、経済的な観点からは、アミノ酸残基の総数は少ない方が好ましい。
また、上記環状ペプチドは、より好ましくは、下記式(IA)によって表される環状ペプチドである。
RN-Xg-[Xp2-X4 r-Xp1-Xa-Xm-X1―X2-X3-Xn-Xb-Xq1-X5 s-Xq2]k-Xh-RC ・・・(IA)
また、式(IA)中、Xnは、式(I)中のXnと同様に、Xがn個連結していることを意図する。Xm、Xp1、Xp2、Xq1、およびXq2についても同様である。
さらに、式(IA)中、X4 rおよびX5 sは、それぞれ、X4がr個連結していること、および、X5がs個連結していること、を意図する。
式(IA)によって表される環状ペプチドの直鎖部は「Xg」、「Xh」、「Xp2-X4 r-Xp1」、および「Xq1-X5 s-Xq2」である。環状部、架橋部、および抗体結合部は式(I)で表される環状ペプチドと同様である。
また、式(IA)中、繰返し単位は[Xp2-X4 r-Xp1-Xa-Xm-X1-X2-X3-Xn-Xb-Xq1-X5 s-Xq2]である。
式(IA)中、X4およびX5は、それぞれ独立に、側鎖にカルボキシ基を有するアミノ酸に由来するアミノ酸残基または側鎖にヒドロキシ基を有するアミノ酸に由来するアミノ酸残基を表す。
式(IA)中、p1、p2、q1、およびq2は、それぞれ独立に、0以上の整数である。
p1は、好ましくは0≦p1≦20を満たし、より好ましくは0≦p1≦10を満たし、さらに好ましくは0≦p1≦5を満たし、いっそう好ましくは0≦p1≦2を満たす。
p2は、好ましくは0≦p2≦20を満たし、より好ましくは0≦p2≦10を満たし、さらに好ましくは0≦p2≦5を満たし、いっそう好ましくは0≦p2≦2を満たす。
q1は、好ましくは0≦q1≦20を満たし、より好ましくは0≦q1≦10を満たし、さらに好ましくは0≦q1≦5を満たし、いっそう好ましくは0≦q1≦2を満たす。
q2は、好ましくは0≦q2≦20を満たし、より好ましくは0≦q2≦10を満たし、さらに好ましくは0≦q2≦5を満たし、いっそう好ましくは0≦q2≦2を満たす。
式(IA)中、rおよびsは、それぞれ、0≦r≦5、0≦s≦5、および、1≦Max(r,s)≦5を満たす整数であり、好ましくは、0≦r≦4、0≦s≦4、および、1≦Max(r,s)≦4を満たす整数であり、より好ましくは、0≦r≦3、0≦s≦3、および、1≦Max(r,s)≦3を満たす整数である。
ただし、Max(r,s)は、r≠sであるとき、rとsの2数のうち大きい方を表し、r=sであるとき、rまたはsを表す。
上記式(IA)において、環状部[Xa-Xm-X1―X2-X3-Xn-Xb]のアミノ酸残基数[(m+n+5)残基]は、上記式(I)と同様に、8~14酸基であり、好ましくは9~13残基であり、より好ましくは10~12残基である。
環状部のアミノ酸残基数がこの範囲内であると、環状ペプチドの分子内ひずみが大きくなり過ぎず、αヘリックス等の高次構造が安定化するため、本発明の環状ペプチドの抗体結合性が優れる。
また、k≧2である場合、すなわち、式(IA)によって表される環状ペプチドが繰返し単位[Xp2-X4 r-Xp1-Xa-Xm-X1―X2-X3-Xn-Xb-Xq1-X5 s-Xq2]を2個以上含む場合は、繰返し単位中のX1、X2、X3、Xa、Xb、X4 r、X5 s、Xm、Xn、Xp2、Xp1、Xq1、およびXq2は、それぞれ、繰返し単位間で同一であってもよいし、相違していてもよい。
さらに、上記式(IA)において、環状ペプチドの総アミノ酸残基数は、好ましくは8~50残基であり、より好ましくは9~40残基であり、さらに好ましくは10~30残基であり、いっそう好ましくは10~20残基である。
すなわち、式(IA)中、g、h、m、n、p1、p2、q1、q2、r、s、およびkは、好ましくは8≦g+h+(m+n+p1+p2+q1+q2+r+s+5)×k≦50を満たし、より好ましくは9≦g+h+(m+n+p1+p2+q1+q2+r+s+5)×k≦40を満たし、さらに好ましくは10≦g+h+(m+n+p1+p2+q1+q2+r+s+5)×k≦30を満たし、いっそう好ましくは10≦g+h+(m+n+p1+p2+q1+q2+r+s+5)×k≦20を満たす。
通常、アミノ酸残基数が多くなるほど合成コストが高くなるため、経済的な観点からは、アミノ酸残基の総数は少ない方が好ましい。
また、上記環状ペプチドは、より好ましくは下記式(IB)によって表される環状ペプチドである。
RN-Xv1-X6 t-Xv2-[Xi-Xa-Xm-X1―X2-X3-Xn-Xb-Xj]k-Xw2-X7 u-Xw1-RC ・・・(IB)
また、式(IB)中、Xnは、式(I)中のXnと同様に、Xがn個連結していることを意図する。Xm、Xv1、Xv2、Xw1、およびXw2についても同様である。
さらに、式(IB)中、X6 tおよびX7 uは、それぞれ、X6がt個連結していること、および、X7がu個連結していること、を意図する。
式(IB)によって表される環状ペプチドの直鎖部は「Xi」、「Xj」、「Xv1-X6 t-Xv2」、および「Xw2-X7 u-Xw1」である。環状部、架橋部、および抗体結合部は式(I)で表される環状ペプチドと同様である。
また、式(IB)中、繰返し単位は、式(I)と同様に、[Xi-Xa-Xm-X1-X2-X3-Xn-Xb-Xj]である。
式(IB)中、X6およびX7は、それぞれ独立に、側鎖に固定化官能基を有するアミノ酸に由来するアミノ酸残基を表し、X6またはX7が複数である場合は、複数のX6またはX7は互いに同一であっても異なっていてもよい。
このような固定化官能基としては、例えば、アミノ基、カルボキシ基、ヒドロキシ基、チオール基、ホルミル基(アルデヒド基)、カルバモイル基、アジド基、および、アルキニル基等が挙げられる。
上記環状ペプチドが有する固定化官能基と基材および/または親水性ポリマー上の官能基の組合せとしては、アミノ基とカルボキシ基(アミド結合形成反応)、アミノ基とホルミル基(還元的アミノ化反応)、アミノ基とエポキシ基、カルボキシ基とヒドロキシ基(エステル結合形成反応)、チオール基とチオール基(ジスルフィド結合)、チオール基とエポキシ基、および、アジド基とアルキニル基(ヒュスゲン環化付加反応)等が挙げられる。
上記環状ペプチドが有する固定化官能基と基材および/または親水性ポリマー上の官能基とが反応して共有結合を形成することにより、上記環状ペプチドが担体に固定化される。なお、上記環状ペプチドが有する固定化官能基の少なくとも一部が基材および/または親水性ポリマー上の官能基と反応して共有結合を形成すればよく、すべての固定化官能基が基材および/または親水性ポリマー上の官能基と反応しなくてもよい。
式(IB)中、tおよびuは、それぞれ、0≦t≦5、0≦u≦5、および、1≦Max(t,u)≦5を満たす整数であり、好ましくは0≦t≦4、0≦u≦4、1≦Max(t,u)≦4を満たす整数であり、より好ましくは0≦t≦3、0≦u≦3、1≦Max(t,u)≦3を満たす整数である。
ただし、Max(t,u)は、t≠uであるとき、tとuの2数のうち大きい方を表し、t=uであるとき、tまたはuを表す。
式(IB)中、v1、v2、w1、およびw2は、それぞれ独立に、0以上の整数である。
v1は、好ましくは0≦v1≦20を満たし、より好ましくは0≦v1≦10を満たし、さらに好ましくは0≦v1≦5を満たし、いっそう好ましくは0≦v1≦2を満たす。
v2は、好ましくは0≦v2≦20を満たし、より好ましくは0≦v2≦10を満たし、さらに好ましくは0≦v2≦5を満たし、いっそう好ましくは0≦v2≦2を満たす。
w1は、好ましくは0≦w1≦20を満たし、より好ましくは0≦w1≦10を満たし、さらに好ましくは0≦w1≦5を満たし、いっそう好ましくは0≦w1≦2を満たす。
w2は、好ましくは0≦w2≦20を満たし、より好ましくは0≦w2≦10を満たし、さらに好ましくは0≦w2≦5を満たし、いっそう好ましくは0≦w2≦2を満たす。
また、上記式(IB)において、環状部[Xa-Xm-X1―X2-X3-Xn-Xb]のアミノ酸残基数[(m+n+5)残基]は、上記式(I)と同様に、8~14酸基であり、好ましくは9~13残基であり、より好ましくは10~12残基である。
環状部のアミノ酸残基数がこの範囲内であると、環状ペプチドの分子内ひずみが大きくなり過ぎず、αヘリックス等の高次構造が安定化するため、本発明の環状ペプチドの抗体結合性が優れる。
また、k≧2である場合、すなわち、式(IB)によって表される環状ペプチドが繰返し単位[Xi-Xa-Xm-X1―X2-X3-Xn-Xb-Xj]を2個以上含む場合は、繰返し単位中のX1、X2、X3、Xa、Xb、Xm、Xn、Xi、およびXjは、それぞれ、繰返し単位間で同一であってもよいし、相違していてもよい。
さらに、上記式(IB)において、環状ペプチドの総アミノ酸残基数は、好ましくは8~50残基であり、より好ましくは9~40残基であり、さらに好ましくは10~30残基であり、いっそう好ましくは10~20残基である。
すなわち、式(IB)中、i、j、m、n、t、u、v1、v2、w1、w2、およびkは、好ましくは8≦(i+j+m+n+5)×k+t+u+v1+v2+w1+w2≦50を満たし、より好ましくは(i+j+m+n+5)×k+t+u+v1+v2+w1+w2≦40を満たし、さらに好ましくは10≦(i+j+m+n+5)×k+t+u+v1+v2+w1+w2≦30を満たし、いっそう好ましくは10≦(i+j+m+n+5)×k+t+u+v1+v2+w1+w2≦20を満たす。
通常、アミノ酸残基数が多くなるほど合成コストが高くなるため、経済的な観点からは、アミノ酸残基の総数は少ない方が好ましい。
さらに、上記環状ペプチドは、さらに好ましくは下記式(IC)によって表される環状ペプチドである。
RN-Xv1-X6 t-Xv2-[Xp2-X4 r-Xp1-Xa-Xm-X1―X2-X3-Xn-Xb-Xq1-X5 s-Xq2]k-Xw2-X7 u-Xw1-RC ・・・(IC)
また、式(IC)中、Xnは、式(I)中のXnと同様に、Xがn個連結していることを意図する。Xm、Xp1、Xp2、Xq1、Xq2、Xv1、Xv2、Xw1、およびXw2についても同様である。
さらに、式(IC)中、X4 r、X5 s、X6 t、およびX7 uは、それぞれ、X4がr個連結していること、X5がs個連結していること、X6がt個連結していること、および、X7がu個連結していること、を意図する。
式(IC)によって表される環状ペプチドの直鎖部は「Xv1-X6 t-Xv2」、「Xw2-X7 u-Xw1」、「Xp2-X4 r-Xp1」、および「Xq1-X5 s-Xq2」である。環状部、架橋部、および抗体結合部は式(I)で表される環状ペプチドと同様である。
また、式(IC)中、繰返し単位は、式(IA)と同様に、[Xp2-X4 r-Xp1-Xa-Xm-X1―X2-X3-Xn-Xb-Xq1-X5 s-Xq2]である。
また、上記式(IC)において、環状部[Xa-Xm-X1-X2-X3-Xn-Xb]のアミノ酸残基数[(m+n+5)残基]は、上記式(I)と同様に、8~14酸基であり、好ましくは9~13残基であり、より好ましくは10~12残基である。
環状部のアミノ酸残基数がこの範囲内であると、環状ペプチドの分子内ひずみが大きくなり過ぎず、αヘリックス等の高次構造が安定化するため、本発明の環状ペプチドの抗体結合性が優れる。
また、k≧2である場合、すなわち、式(IC)によって表される環状ペプチドが繰返し単位[Xp2-X4 r-Xp1-Xa-Xm-X1-X2-X3-Xn-Xb-Xq1-X5 s-Xq2]を2個以上含む場合は、繰返し単位中のX1、X2、X3、Xa、Xb、X4 r、X5 s、Xm、Xn、Xp2、Xp1、Xq1、およびXq2は、それぞれ、繰返し単位間で同一であってもよいし、相違していてもよい。
さらに、上記式(IC)において、環状ペプチドの総アミノ酸残基数は、好ましくは8~50残基であり、より好ましくは9~40残基であり、さらに好ましくは10~30残基であり、いっそう好ましくは10~20残基である。
すなわち、式(IC)中、m、n、p1、p2、q1、q2、r、s、t、u、v1、v2、w1、w2、およびkは、好ましくは8≦(m+n+p1+p2+q1+q2+r+s+5)×k+t+u+v1+v2+w1+w2≦50を満たし、より好ましくは9≦(m+n+p1+p2+q1+q2+r+s+5)×k+t+u+v1+v2+w1+w2≦40を満たし、さらに好ましくは10≦(m+n+p1+p2+q1+q2+r+s+5)×k+t+u+v1+v2+w1+w2≦30を満たし、いっそう好ましくは10≦(m+n+p1+p2+q1+q2+r+s+5)×k+t+u+v1+v2+w1+w2≦20を満たす。
通常、アミノ酸残基数が多くなるほど合成コストが高くなるため、経済的な観点からは、アミノ酸残基の総数が少ない方が好ましい。
さらには、上記式(I)、(IA)、(IB)、または(IC)中のアミノ酸部分配列Xm-X1-X2-X3-Xnは、下記式(1)で表されるアミノ酸配列(配列番号1)または下記式(2)で表されるアミノ酸配列(配列番号2)と、好ましくは70%以上の、より好ましくは75%以上の、さらに好ましくは85%以上の、いっそう好ましくは90%以上の配列相同性を有する。
A-Y-H-L1-G-E-L2-V-W ・・・(1)
A-Y-H-R-G-E-L2-V-W ・・・(2)
(i)2つのアミノ酸配列のアラインメントを行う
一致(マッチ)は+1、不一致(ミスマッチ)は-1、ギャップは-1のスコアを与え、アラインメント・スコアが最大となるようにアラインメントを行う。
(ii)配列相同性を計算する
得られたアラインメントに基づいて、次式により配列相同性を計算する。
配列相同性[%]=(一致ポジション数/全ポジション数)×100[%]
全ポジション数はアラインメントの長さであり、一致ポジション数はアミノ酸の種類が一致するポジションの数である。
ここで、アミノ酸残基の種類が一致するか否かの判断は、そのアミノ酸残基の元になるアミノ酸の側鎖(アミノ酸側鎖)の構造が同一であるか否かによるものとする。なお、エナンチオマーの関係にあるアミノ酸の側鎖の構造は同一ではない。
(iii)配列相同性の計算例
例えば、次のアミノ酸配列を考える。
配列A AYHRGELVW
配列B AWHGELVW
これを、上記した条件の下でアラインメントすると、次のようになる。ここで、配列A、B間でアミノ酸(残基)の種類が一致する箇所には、見やすくするため、ホモロジー・ストリング「|」を付けている。また、「-」はギャップである。
配列A AYHRGELVW
| | |||||
配列B AWHLGELVW
このアラインメントのスコアは、一致(+1)×7+不一致(-1)×1+ギャップ(-1)×1=5である。
この例では、全ポジション数は9であり、一致ポジション数は7であるから、上記式に従って算出した配列相同性は、7/9×100=77.8%である。
RN-Xv0-X6 t0-Xe0-X4 r0-Xp0-Xa-A-Y-H-X8-G-E-L―V-W-Xb-Xq0-X5 s0-Xf0-X7 u0-Xw0-RC ・・・(II)
式(II)中、Xa、Xb、X、RN、およびRCは、上記式(I)中におけるものと同義である。
また、式(II)中、Xe0は、式(I)中のXnと同様に、Xがe0個連結していることを意図する。Xf0、Xp0、Xq0、Xv0、およびXw0についても同様である。
式(II)中、X6およびX7は、上記式(IB)中におけるものと同義である。
e0は、好ましくは0≦e0≦5を満たし、より好ましくは0≦e0≦3を満たし、さらに好ましくは0≦e0≦2を満たす。
f0は、好ましくは0≦f0≦5を満たし、より好ましくは0≦f0≦3を満たし、さらに好ましくは0≦f0≦2を満たす。
p0は、好ましくは0≦p0≦3を満たし、より好ましくは0≦p0≦2を満たす。
q0は、好ましくは0≦q0≦3を満たし、より好ましくは0≦q0≦2を満たす。
r0は、好ましくは0≦r0≦3を満たし、より好ましくは0≦r0≦2を満たす。
s0は、好ましくは0≦s0≦3を満たし、より好ましくは0≦s0≦2を満たす。
t0は、好ましくは0≦t0≦3を満たし、より好ましくは0≦t0≦2を満たす。
s0は、好ましくは0≦s0≦3を満たし、より好ましくは0≦s0≦2を満たす。
v0は、好ましくは0≦v0≦3を満たし、より好ましくは0≦v0≦2を満たす。
w0は、好ましくは0≦w0≦3を満たし、より好ましくは0≦w0≦2を満たす。
すなわち、式(II)中、e0、f0、p0、q0、r0、s0、t0、u0、v0、およびw0は、0≦e0+f0+p0+q0+r0+s0+t0+u0+v0+w0≦39を満たし、好ましくは0≦e0+f0+p0+q0+r0+s0+t0+u0+v0+w0≦29を満たし、より好ましくは0≦e0+f0+p0+q0+r0+s0+t0+u0+v0+w0≦19を満たし、さらに好ましくは0≦e0+f0+p0+q0+r0+s0+t0+u0+v0+w0≦9を満たす。
上記環状ペプチド環状部の例を以下に示すが、これらに限定されるものではない。
-Xaa1-Ala-Tyr-His-Leu-Gly-Glu-Leu-Val-Trp-Xaa11- ・・・(i)
式(i)中、Xaa1はL-ホモシステインに由来するアミノ酸残基であり、Xaa11はN-ε-クロロアセチル-L-リシンに由来するアミノ酸残基であり、Xaa1とXaa11とは、L-ホモシステインの側鎖のチオール基とN-ε-クロロアセチル-L-リシンの側鎖のクロロアセチル基との間でチオエーテル結合を形成して架橋している(配列番号3)。
式(ii)中、Xaa1はN-ε-クロロアセチル-L-リシンに由来するアミノ酸残基であり、Xaa11はL-ホモシステインに由来するアミノ酸残基であり、Xaa1とXaa11とは、N-ε-クロロアセチル-L-リシンの側鎖のクロロアセチル基とL-ホモシステインの側鎖のチオール基との間でチオエーテル結合を形成して架橋している(配列番号4)。
式(iii)中、Xaa1はL-システインに由来するアミノ酸残基であり、Xaa11はN-ε-クロロアセチル-L-リシンに由来するアミノ酸残基であり、Xaa1とXaa11とは、L-システインの側鎖のチオール基とN-ε-クロロアセチル-L-リシンの側鎖のクロロアセチル基との間でチオエーテル結合を形成して架橋している(配列番号5)。
式(iv)中、Xaa1はN-ε-クロロアセチル-L-リシンに由来するアミノ酸残基であり、Xaa11はL-ペニシラミンに由来するアミノ酸残基であり、Xaa1とXaa11とは、N-ε-クロロアセチル-L-リシンの側鎖のクロロアセチル基とL-システインの側鎖のチオール基との間でチオエーテル結合を形成して架橋している(配列番号6)。
-Xaa1-Ala-Tyr-His-Leu-Gly-Glu-Leu-Val-Trp-Xaa11- ・・・(v)
式(v)中、Xaa1およびXaa11は、いずれも、L-ホモシステインに由来するアミノ酸残基であり、L-ホモシステインの側鎖のチオール基間でジスルフィド結合を形成して架橋している(配列番号7)。
式(vi)中、Xaa1およびXaa11は、いずれも、L-ペニシラミンに由来するアミノ酸残基であり、L-システインの側鎖のチオール基間でジスルフィド結合を形成して架橋している(配列番号8)。
-Xaa1-Ala-Tyr-His-Leu-Gly-Glu-Leu-Val-Trp-Xaa11- ・・・(vii)
式(vii)中、Xaa1は2-プロパルギル-L-ホモグリシンに由来するアミノ酸残基であり、Xaa11はβ-アジド-L-アラニンに由来するアミノ酸残基であり、Xaa1とXaa11とは、2-プロパルギル-L-ホモグリシンの側鎖のプロパルギル基とβアジド-L-アラニンの側鎖のアジド基との間でトリアゾール結合を形成して架橋している(配列番号9)。
式(viii)中、Xaa1はβ-アジド-L-アラニンに由来するアミノ酸残基であり、Xaa11は2-プロパルギル-L-ホモグリシンに由来するアミノ酸残基であり、Xaa1とXaa11とは、βアジド-L-アラニンの側鎖のアジド基と2-プロパルギル-L-ホモグリシンの側鎖のプロパルギル基との間でトリアゾール結合を形成して架橋している(配列番号10)。
-Xaa1-Ala-Tyr-His-Leu-Gly-Glu-Leu-Val-Trp-Xaa11- ・・・(ix)
式(ix)中、Xaa1はL-リシンに由来するアミノ酸残基であり、Xaa11はL-グルタミン酸に由来するアミノ酸残基であり、L-リシンの側鎖のアミノ基とL-グルタミン酸の側鎖のカルボキシ基との間でアミド結合を形成して架橋している(配列番号11)。
式(ix)中、Xaa1はL-グルタミン酸に由来するアミノ酸残基であり、Xaa11はL-リシンに由来するアミノ酸残基であり、L-グルタミン酸の側鎖のカルボキシ基とL-リシンの側鎖のアミノ基との間でアミド結合を形成して架橋している(配列番号12)。
本発明のミックスモードアフィニティクロマトグラフィー用担体のアフィニティリガンドの導入量(以下、単に「アフィニティリガンド導入量」という場合がある。)は、特に限定されないが、好ましくは0.01mmol/L-gel~100mmol/L-gel、より好ましくは0.05mmol/L-gel~50mmol/L-gel、さらに好ましくは0.10mmol/L-gel~10mmol/L-gel、いっそう好ましくは0.10mmol/L-gel~5.0mmol/L-gel、よりいっそう好ましくは0.10mmol/L-gel~2.5mmol/L-gelである。
上記環状ペプチドの合成方法は特に限定されるものではないが、例えば、有機合成化学的ペプチド合成方法または遺伝子工学的ペプチド合成方法によって合成することができる。
有機合成化学的ペプチド合成方法としては、液相合成法、固相合成法のいずれも用いることができる。本発明のポリペプチドの合成方法としては、自動ペプチド合成装置を用いた固相合成法が簡便であり好ましい。
遺伝子工学的ペプチド合成方法は、細胞に遺伝子導入し、ペプチドを合成する方法である。細胞としては、細菌、線虫細胞、昆虫細胞、哺乳類細胞、および、動物細胞等が用いられる。
例えば、4塩基コドン法を用いて、非天然アミノ酸を導入して合成することが可能である。また、直鎖ペプチドを合成し、環状部に導入されたアミノ酸残基の側鎖の架橋性官能基を反応させることにより環化し、合成できる。
ジスルフィド結合を形成する場合は、例えば、ホモシステイン残基同士の側鎖チオール基、またはホモシステイン残基の側鎖チオール基とホモシステインよりもメチレン鎖の長いアミノ酸残基の側鎖チオール基とを酸化条件下で反応させてジスルフィド結合を形成することができる。
チオエーテル結合を形成する場合は、例えば、側鎖のアミノ基をクロロアセチル化したリシン残基またはオルニチン残基と、ホモシステイン残基の側鎖チオール基とを反応させてチオエーテル結合を形成することができる。
なお、チオエーテル結合形成は、リシン残基の側鎖アミノ基をクロロアセチル化(-NH-C(=O)-CH2-Cl;メチレン単位の数1)、または3-クロロプロピオン酸化(-NH-C(=O)-(CH2)2-Cl;メチレン単位の数2)等によるクロロ化をした後、チオール基と反応させるものであるため、クロロ化に用いられる化合物は、ここに例示したものに限定されないが、メチレン単位の数が少ない、すなわちメチレン鎖が短いものほど環化効率が高まり、好ましい。
陽イオン交換基は、抗体結合性環状ペプチドと協奏的に作用し、特異的な吸着能と凝集体除去能をもつことにより、本発明のミックスモードアフィニティクロマトグラフィー用担体の不純物除去能を向上させると考えられる。
本発明のミックスモードアフィニティクロマトグラフィー用担体の陽イオン交換基の導入量(以下、単に「陽イオン交換基導入量」という場合がある。)は、特に限定されないが、イオン交換容量で、好ましくは15mmol/L-gel~60mmol/L-gelであり、より好ましくは15mmol/L-gel~55mmol/L-gelであり、さらに好ましくは15mmol/L-gel~40mmol/L-gelである。
本発明のミックスモードアフィニティクロマトグラフィー用担体は、基材を親水性ポリマーで被覆し、陽イオン交換基を導入し、さらにアフィニティリガンドを基材および親水性ポリマーの少なくとも一方に導入することにより製造することができる。
基材を親水性ポリマーで被覆する方法は、親水性ポリマーを基材に共有結合によって結合させることができるものであれば特に限定されるものではないが、例えば、基材に2-クロロメチルオキシラン(別名:エピクロロヒドリン)を反応させてエポキシ基を導入し、これに親水性ポリマーを反応させる方法、溶媒中、アルカリの存在下、基材を2-クロロメチルオキシラン(別名:エピクロロヒドリン)のような架橋剤と反応させ、得られた反応生成物を親水性ポリマーと反応させる方法、クロロ基(塩素原子)等のハロゲン基(ハロゲン原子)をハロゲン化剤を用いて基材に導入し、および、ウィリアムソンのエーテル合成法を用いて親水性ポリマーを固定化する方法等が挙げられる。
被覆担体に陽イオン交換基を導入する方法は、陽イオン交換基を有する化合物を被覆担体に共有結合によって結合させることができるものであれば特に限定されるものではないが、例えば、アルカリ条件下で被覆担体にクロロ酢酸を反応させて、被覆担体表面のヒドロキシ基の一部にカルボキシメチル基を導入する方法、被覆担体にホルミル基を導入し、アミノ酸等の陽イオン交換基およびアミノ基を有する化合物のアミノ基を介して還元的アミノ化法でホルミル基に陽イオン交換基を導入する方法等が挙げられる。
陽イオン交換基導入担体にアフィニティリガンドを導入(固定化)する方法は、アフィニティリガンドを陽イオン交換基導入担体に共有結合によって結合させることができるものであれば特に限定されないが、例えば、陽イオン交換基の一部をEDC(N-(3-dimethylaminopropyl)-N’-ethylcarbodiimide;N‐(3‐ジメチルアミノプロピル)-N’‐エチルカルボジイミド)/NHS(N-hydroxysuccinimide;N‐ヒドロキススクシンイミド)化し、アフィニティリガンドと反応させ、反応後に未反応のEDC/NHS化された陽イオン交換基を再生する方法、アミノ基を有するアフィニティリガンドの場合には、陽イオン交換基を保護して、ホルミル基を導入し、アミノ基を介して還元的アミノ化法でホルミル基にアフィニティリガンドを導入する方法等が挙げられる。
本発明のミックスモードアフィニティクロマトグラフィー用担体により精製される生体物質は、特に限定されるものではないが、好ましくは抗体または抗体誘導体、より好ましくは免疫グロブリンGまたはその誘導体である。
これらは抗体医薬品の原料として利用される。
A.陽イオン交換基導入量の測定方法
カルボキシ化担体1gを3mLの純水に懸濁し、内径15mmのディスポーザブルカラムに注ぎ、吸引ろ過で溶媒を除去した。0.2mol/Lの塩酸3mLで4回洗浄し、その後純水4mLで洗浄を繰返した。洗浄後、ベッド(カラムに堆積した担体部分)高を測定することで、カルボキシ化担体の体積を算出した。カルボキシ化担体を取り出し、100mL容ビーカーに移し、40mLの0.1mol/Lの食塩水に懸濁し、自動滴定装置「COM-1600」(平沼産業社製)を用い、0.1mol/Lの水酸化ナトリウム水溶液で滴定した。終点までの滴定液量からカルボキシ化担体1Lあたりのイオン交換容量(meq/L-gel)を算出した。さらに、単位を「mmol/L-gel」に換算した(1meq/L-gel=1mmol/L-gel)。陽イオン交換基導入量はイオン交換容量で表した。
ペプチド固定化反応後のペプチド液、反応液および洗浄液を、それぞれ、ゲルろ過クロマトグラフィー(下記)にかけ、280nmにおける吸光度のピーク面積値より、各溶液に含まれるペプチド量を算出した。
ペプチド固定化反応前のペプチド液、反応液および洗浄液に含まれるペプチド量との差より、ペプチド固定化量を算出した。
(ゲルろ過クロマトグラフィーの条件)
クロマトシステム:アクタアヴァント25(AKTA avant 25)(GEヘルスケア社製)
(“AKTAAVANT”は登録商標)
カラム:ペプチド精製用ゲルろ過クロマトグラフィーカラム「Superdex Peptide 10/300 GL(GEヘルスケア社製)」
バッファー:20mM リン酸バッファー、150mM NaCl、pH7.4
流速:0.5mL/min
(a)抗体吸着容量の測定
実施例または比較例で製造したミックスモードアフィニティクロマトグラフィー用担体1mLをガラスカラム「トリコーン 10/20 カラム(Tricorn 10/20 column)」(GEヘルスケア社製)(“TRICORN”は登録商標)に充填し、クロマトシステム「アクタアヴァント25(AKTA avant 25)」(GEヘルスケア社製)(“AKTAAVANT”は登録商標)に接続し、抗体吸着容量の測定を行った。
カラムを平衡化液(20mMリン酸バッファー、150mM NaCl、pH7.4)で平衡化した後に、ヒトIgG抗体(Immunoglobulin G:免疫グロブリンG)を標準バッファー(20mMリン酸バッファー、150mM NaCl、pH7.4)で5mg/mLに調整した溶液15mLを流速0.42mL/minにて添加した。その後、負荷後洗浄液(20mMリン酸バッファー、150mM NaCl、pH7.4)を同じ流速で5mL流して洗浄した後に、溶出前洗浄液(20mMリン酸バッファー、1M NaCl、pH7.4)を同じ流速で5mL流した。その後、溶出液(100mMクエン酸バッファー、500mM NaCl、pH3.2)を同じ流速で5mL流した。さらに連続して、定置洗浄(CIP;cleaning in place)液(0.1M水酸化ナトリウム水溶液)を同じ流速で5mL流し、その後、再平衡化液(20mMリン酸バッファー、150mM NaCl、pH7.4)を、同じ流速で5mL流した。このとき、280nmの吸光度をモニタリングして得られたIgG溶出ピークより、各分画における溶出液の抗体溶出量を算出した。溶出前洗浄液からCIP液までに溶出した抗体量を抗体吸着容量として算出した。
抗体吸着容量の評価は以下の基準に従って行った。
抗体吸着容量が30g/L超・・・評価「A」
抗体吸着容量が3.5g/L超、30g/L以下・・・評価「B」
抗体吸着容量が3.5g/L以下・・・評価「E」
評価AおよびBは抗体吸着容量が十分であることを表し、評価Eは抗体吸着容量が十分でないことを表す。
十分な抗体吸着容量を持つ本発明のミックスモードアフィニティクロマトグラフィー用担体を抗体の精製に用いると、抗体の精製効率を高めることができ、抗体精製コストをより低減することができる。
(a)HCP精製ファクターの算出
実施例または比較例で製造したミックスモードアフィニティクロマトグラフィー用担体1mLをガラスカラム「トリコーン 10/20 カラム(Tricorn 10/20 column)」(GEヘルスケア社製)(“TRICORN”は登録商標)に充填し、クロマトシステム「アクタアヴァント25(AKTA avant 25)」(GEヘルスケア社製)(“AKTAAVANT”は登録商標)に接続し、各分画で溶出されるHCP(host cell protein;宿主細胞由来タンパク質)量およびIgG(Immunoglobulin G;免疫グロブリンG)量の測定を行った。
カラムを平衡化液(20mMリン酸バッファー、150mM NaCl、pH7.4)で平衡化した後に、IgG、CHO-S(Chinese Hamster Ovary S)細胞由来HCPが、それぞれ、1.6mg/mL、0.32mg/mLになるように標準バッファー(20mMリン酸バッファー、150mM NaCl、pH7.4)を用いて調製したIgG/HCP混合液を、上述したCで得られた抗体吸着容量の8割の抗体量が負荷されるような溶液量を流速0.21mL/minにて添加した。その後、負荷後洗浄液(20mMリン酸バッファー、150mM NaCl、pH7.4)を同じ流速で5mL流して洗浄した後に、溶出前洗浄液(20mMリン酸バッファー、1M NaCl、pH7.4)を流速0.42mL/minで5mL流した。その後、イオン強度調節液(20mMリン酸バッファー、pH7.4)を同じ流速で5mL流した。その後、溶出液1(100mMクエン酸バッファー、pH3.2)を同じ流速で5mL流し、さらに連続して溶出液2(100mMクエン酸バッファー、50mM NaCl、pH3.2)、溶出液3(100mMクエン酸バッファー、75mM NaCl、pH3.2)、溶出液4(100mMクエン酸バッファー、500mM)を同じ流速で5mLずつ流した。さらに連続して、CIP液(0.1M水酸化ナトリウム水溶液)を同じ流速で5mL流し、その後再平衡化液(20mMリン酸バッファー、150mM NaCl、pH7.4)を同じ流速で5mL流した。
280nmの吸光度をモニタリングして得られたIgG溶出ピークより、各分画における溶出液のIgG溶出量を算出した。
各分画の溶出液を回収し、1M Tris-HCl溶液を用いて各溶出液のpHを5~6とした後、宿主細胞由来タンパク質検出キット「CHO HCP 3rd Generation ELISA kit」(シグナステクノロジーズ社製)を用いたELISA法により、各分画における溶出液のHCP量を算出した。
算出した溶出液のIgG量およびHCP量を用いて、溶出液におけるHCP混入量を溶出液中のIgG量あたりのHCP量として、以下の式により算出した。
溶出液1~3のHCP混入量(ppm)=溶出液1~3の総HCP量/溶出液1~3の総IgG量
この溶出液のHCP混入量(ppm)と負荷したIgG/HCP混合液のHCP混入量(ppm)からHCP精製ファクターを、以下の式により算出した。
HCP精製ファクター=負荷したIgG/HCP混合液のHCP混入量(ppm)/溶出液1~3のHCP混入量(ppm)
不純物除去能の評価は以下の基準に従って行った。
HCP精製ファクターが5000超・・・評価「A」
HCP精製ファクターが1500超、5000以下・・・評価「B」
HCP精製ファクターが1500以下・・・評価「E」
評価AおよびBは不純物除去能が十分であることを表し、評価Eは不純物除去能が十分でないことを表す。
十分な不純物除去能を持つ本発明のミックスモードアフィニティクロマトグラフィー用担体を抗体の精製に用いると、抗体の精製純度を高めることができ、抗体の精製純度をより改善することができる。
(a)結合量変化率の算出
実施例または比較例で製造したミックスモードアフィニティクロマトグラフィー用担体1mLをガラスカラム「トリコーン 10/20 カラム(Tricorn 10/20 column)」(GEヘルスケア社製)(“TRICORN”は登録商標)に充填し、クロマトシステム「アクタアヴァント25(AKTA avant 25)」(GEヘルスケア社製)(“AKTAAVANT”は登録商標)に接続し、抗体結合容量の測定を行った。カラムを平衡化液(20mMリン酸バッファー、150mM NaCl、pH7.4)で平衡化した後に、ヒトIgG抗体を標準バッファー(20mMリン酸バッファー、150mM NaCl、pH7.4)で5mg/mLに調整した溶液15mLを流速0.21mL/minにて添加した。その後、負荷後洗浄液(20mMリン酸バッファー、150mM NaCl、pH7.4)を同じ流速で5mL流して洗浄した後に、溶出前洗浄液(20mMリン酸バッファー、1M NaCl、pH7.4)を同じ流速で5mL流した。その後、溶出液(100mMクエン酸バッファー、pH3.2)を同じ流速で5mL流した。さらに連続して、CIP(cleaning in place;定置洗浄)液(0.1M水酸化ナトリウム)を同じ流速で5mLを流し、その後再平衡化液(20mMリン酸バッファー、150mM NaCl、pH7.4)を同じ流速で5mL流した。このとき、280nmの吸光度をモニタリングして得られたIgG(Immunoglobulin G;免疫グロブリンG)溶出ピークより、抗体原液の10%が担体から漏れ出すまでに担体に抗体が結合した量を抗体結合容量として測定した。次に、ミックスモードアフィニティクロマトグラフィー用担体を0.2M NaOH水溶液に25℃で6時間満たして静置した後、同様に担体の抗体結合容量を測定し、アルカリ処理前後の抗体結合量から結合量変化率を算出した。
薬品耐性の評価は以下の基準に従って行った。
結合量変化率が75%超・・・・・・・・・・・・・・・AAA
結合量変化率が65%超、75%以下・・・・・・・・・AA
結合量変化率が40%超、65%以下・・・・・・・・・A
結合量変化率が15%超、40%以下・・・・・・・・・B
結合量変化率が15%以下・・・・・・・・・・・・・・E
評価AAA、AA、AおよびBは薬品耐性が十分であることを表し、評価Eは薬品耐性が十分でないことを表す。
十分な薬品耐性を持つ本発明のミックスモードアフィニティクロマトグラフィー用担体を抗体の精製に用いると、洗浄後も抗体と特異的に繰り返し結合することができ、長期間、抗体を精製することが可能となり、抗体の精製コストをより低減することができる。
抗原性リガンド混入の評価は以下の基準に従って行った。
導入したアフィニティリガンドが低抗原性(分子量4,000未満)・・・評価「A」
導入したアフィニティリガンドが低抗原性(分子量5,000未満)・・・評価「B」
導入したアフィニティリガンドが抗原性(分子量5,000以上)・・・評価「E」
評価AおよびBは精製した抗体に抗原性リガンドが実質的に混入しないことを表し、評価Eは精製した抗体に抗原性リガンドが混入するおそれがあることを表す。
抗原性リガンドが混入した抗体を生体に投与すると、意図しない免疫応答を誘導する場合があり、好ましくない副作用を生ずるおそれがある。
1.ミックスモードアフィニティクロマトグラフィー用担体の製造
(1)湿ゲルの調製
架橋アガロース系基材「セファローズ4 ファスト・フロー(Sepharose 4 Fast Flow)」(GEヘルスケア社製)(“SEPHAROSE”は登録商標)を、グラスフィルター上で、純水を用いて懸濁およびろ過を繰り返すことによって洗浄し、基材スラリーを得た。この基材スラリーから、吸引ろ過によって純水を除去して、湿ゲルを得た。
得られた湿ゲル50g、純水76mLおよび2-クロロメチルオキシラン25gを、300mL容の三口フラスコに入れ、45℃の温浴中で、フラスコ内容物の撹拌を開始した。フラスコ内の温度が45℃になるまで撹拌を行った。45℃の温浴中で、フラスコ内の温度を約45℃に維持しながら、50%(w/w)水酸化ナトリウム水溶液20.4gを2時間かけてフラスコ内に滴下した。水酸化ナトリウム水溶液の全量を滴下した後、さらに1時間反応し、グラスフィルター上で、純水を用いて懸濁およびろ過を繰り返すことによって洗浄し、被覆前基材の湿ゲルを得た。
デキストラン40(重量平均分子量約40,000)31gおよび純水72mLを、300mL容の三口フラスコに入れ、室温で、フラスコ内容物の撹拌を開始した。デキストラン40が完全に溶解するまで撹拌した。溶解後、被覆前基材の湿ゲル42gをこの三口フラスコに加え、室温で、さらに撹拌した。三口フラスコ内の混合液が均一なってから、50%(w/w)水酸化ナトリウム水溶液2.0gを加えた。水酸化ナトリウム水溶液を加えた後、室温で16時間反応し、グラスフィルター上で、純水を用いて懸濁およびろ過を繰り返すことによって洗浄し、担体の湿ゲルを得た。
得られた担体の湿ゲル15g、クロロ酢酸ナトリウム5.1gおよび純水31mLを、100mL容の三口フラスコに入れ、50℃の温浴中で、フラスコ内容物の撹拌を開始した。クロロ酢酸ナトリウムが完全に溶解するまで撹拌した。溶解後、50℃の温浴中で、フラスコ内温度を約50℃に維持しながら、50%(w/w)水酸化ナトリウム水溶液11gを1時間かけて滴下した。水酸化ナトリウム水溶液の全量を滴下した後、さらに3時間反応し、グラスフィルター上で、純水を用いて懸濁およびろ過を繰り返すことによって洗浄し、カルボキシ化担体の湿ゲルを得た。
得られたカルボキシ化担体を、湿潤体積として2.5mL分、ディスポーザブルカラムに入れ、純水を用いて懸濁およびろ過を繰り返すことによって洗浄し、担体スラリーを得た。この担体スラリーから、吸引ろ過によって純水を除去して、湿ゲルを得た。
得られた湿ゲル2.0gを反応容器にとり、EDC(N-(3-dimethylaminopropyl)-N’-ethylcarbodiimide;N-(3-ジメチルアミノプロピル)-N’ -エチルカルボジイミド)溶液2mLを加え、室温で、10分間、転倒撹拌した。その後、反応容器にNHS(N-hydroxysuccinimide;N‐ヒドロキススクシンイミド)溶液2mLを加え、室温で、30分間、転倒撹拌した。ここで、EDC溶液は、DMSO(dimethyl sulfoxide;ジメチルスルホキシド)2mLにEDC 0.2gを溶解して調製したものであり、NHS溶液は、DMSO 2mLにNHS 0.2gを溶解して調製したものである。
反応ゲル溶液をディスポーザブルカラムに移し、氷冷した1mM塩酸6mLで洗浄し、EDC/NHS活性化されたカルボキシ化担体を得た。
ここで、上記5mg/mL環状ペプチドA容液は、下記式(A)で表される環状ペプチドA(配列番号13)をDMSOに溶解して調製したものである。
Lys-Lys-Lys-Asp-Xaa5-Ala-Tyr-His-Leu-Gly-Glu-Leu-Val-Trp-Xaa15-Thr ・・・(A)
ただし、式(A)中、Xaa5はN-ε-クロロアセチル-L-リシンに由来するアミノ酸残基であり、Xaa15はL-ホモシステインに由来するアミノ酸残基であり、Xaa5とXaa15とは、N-ε-クロロアセチル-L-リシンの側鎖のクロロアセチル基とL-ホモシステインの側鎖のチオール基との間でチオエーテル結合を形成して架橋している。
得られたカルボキシ化担体のカルボキシ基導入量を、上述した「陽イオン交換基導入量の測定方法」に従って測定した。その結果、カルボキシ基導入量は30mmol/L-gelであった。
得られた環状ペプチド固定カルボキシ化担体の環状ペプチド固定化量(アフィニティリガンド導入量)を、上述した「アフィニティリガンド導入量(ペプチド固定化量)の測定方法」に従って測定した。その結果、環状ペプチド固定化量は1.7mmol/L-gelであった。
得られた環状ペプチド固定カルボキシ化担体の抗体吸着容量を、上述した「抗体吸着容量の評価方法」に従って評価した。評価結果を表3の「抗体吸着容量」欄に示す。
得られた環状ペプチド固定カルボキシ化担体の不純物除去能を、上述した「不純物除去能の評価方法」に従って評価した。評価結果を表3の「不純物除去能」欄に示す。
得られた環状ペプチド固定カルボキシ化担体の薬品耐性を、上述した「薬品耐性の評価方法」に従って評価した。評価結果を表3の「薬品耐性」欄に示す。
得られた環状ペプチド固定カルボキシ化担体の抗原性リガンド混入を、上述した「抗原性リガンド混入の評価方法」に従って評価した。その結果、抗原性リガンド混入の評価は「A」であった。
1.ミックスモードアフィニティクロマトグラフィー用担体の製造
「環状ペプチド固定カルボキシ化担体の調製 - 環状ペプチドの導入」において、上記環状ペプチドAに代えて下記式(B)で表される環状ペプチドB(配列番号14)を用いた点を除き、実施例1と同様にして環状ペプチド固定カルボキシ化担体を調製した。
Lys-Lys-Lys-Asp-Xaa5-Ala-Tyr-His-Leu-Gly-Glu-Leu-Val-Trp-Xaa15-Thr ・・・(B)
ただし、式(B)中、Xaa5およびXaa15は、いずれも、L-ホモシステインに由来するアミノ酸残基であり、Xaa5とXaa15とは、L-ホモシステインの側鎖のチオール基間でジスルフィド結合を形成して架橋している。
得られた環状ペプチド固定カルボキシ化担体の環状ペプチド固定化量(アフィニティリガンド導入量)を上述した「アフィニティリガンド導入量(ペプチド固定化量)の測定方法」に従って測定した。その結果、環状ペプチド導入量は1.6mmol/L-gelであった。
得られた環状ペプチド固定カルボキシ化担体の抗体吸着容量、不純物除去能および薬品耐性を、実施例1と同様にして評価した。評価結果を、それぞれ、表3の「抗体吸着容量」欄、「不純物除去能」欄および「薬品耐性」欄に示す。
得られた環状ペプチド固定カルボキシ化担体の抗原性リガンド混入を、上述した「抗原性リガンド混入の評価方法」に従って評価した。その結果、抗原性リガンド混入の評価は「A」であった。
1.ミックスモードアフィニティクロマトグラフィー用担体の製造
「カルボキシ化担体の調製 - 陽イオン交換基の導入」において、クロロ酢酸ナトリウム量を6.1gに変更した点を除き、実施例1と同様にして、カルボキシ化担体を調製した。
Lys-Lys-Lys-Asp-Xaa5-Ala-Tyr-His-Leu-Gly-Glu-Leu-Val-Trp-Xaa15-Thr ・・・(C)
ただし、式(C)中、Xaa5はN-ε-クロロアセチル-L-リシンに由来するアミノ酸残基であり、Xaa15はL-ペニシラミンに由来するアミノ酸残基であり、Xaa5とXaa15とは、N-ε-クロロアセチル-L-リシンの側鎖のクロロアセチル基とL-ペニシラミンの側鎖のチオール基との間でチオエーテル結合を形成して架橋している。
得られたカルボキシ化担体のカルボキシ基導入量を、上述した「陽イオン交換基導入量の測定方法」に従って測定した。その結果、カルボキシ基導入量は36mmol/L-gelであった。
得られた環状ペプチド固定カルボキシ化担体の環状ペプチド固定化量(アフィニティリガンド導入量)を、上述した「アフィニティリガンド導入量(ペプチド固定化量)の測定方法」に従って測定した。その結果、環状ペプチド固定化量は2.0mmol/L-gelであった。
得られた環状ペプチド固定カルボキシ化担体の抗体吸着容量、不純物除去能および薬品耐性を、実施例1と同様にして評価した。評価結果を、それぞれ、表3の「抗体吸着容量」欄、「不純物除去能」欄および「薬品耐性」欄に示す。
得られた環状ペプチド固定カルボキシ化担体の抗原性リガンド混入を、上述した「抗原性リガンド混入の評価方法」に従って評価した。その結果、抗原性リガンド混入の評価は「A」であった。
1.ミックスモードアフィニティクロマトグラフィー用担体の製造
「環状ペプチド固定カルボキシ化担体の調製 - 環状ペプチドの導入」において、上述のとおり調製したカルボキシ化担体を用いた点、および、上記環状ペプチドAに代えて下記式(D)で表される環状ペプチドD(配列番号16)を用いた点を除き、実施例3と同様にして環状ペプチド固定カルボキシ化担体を調製した。
Lys-Lys-Lys-Asp-Xaa5-Ala-Tyr-His-Leu-Gly-Glu-Leu-Val-Trp-Xaa15-Thr ・・・(D)
ただし、式(D)中、Xaa5は2-プロパルギル-L-ホモグリシンに由来するアミノ酸残基であり、Xaa15は、βアジド-L-アラニンに由来するアミノ酸残基であり、Xaa5とXaa15とは、2-プロパルギル-L-ホモグリシンの側鎖のプロパルギル基とβアジド-L-アラニンの側鎖のアジド基との間でトリアゾール結合を形成して架橋している。
得られた環状ペプチド固定カルボキシ化担体の環状ペプチド固定化量(アフィニティリガンド導入量)を、上述した「アフィニティリガンド導入量(ペプチド固定化量)の測定方法」に従って測定した。その結果、環状ペプチド固定化量は1.7mmol/L-gelであった。
得られた環状ペプチド固定カルボキシ化担体の抗体吸着容量、不純物除去能および薬品耐性を、実施例1と同様にして評価した。評価結果を、それぞれ、表3の「抗体吸着容量」欄、「不純物除去能」欄および「薬品耐性」欄に示す。
得られた環状ペプチド固定カルボキシ化担体の抗原性リガンド混入を、上述した「抗原性リガンド混入の評価方法」に従って評価した。その結果、抗原性リガンド混入の評価は「A」であった。
1.ミックスモードアフィニティクロマトグラフィー用担体の製造
「環状ペプチド固定カルボキシ化担体の調製 - 環状ペプチドの導入」において、上述のとおり調製したカルボキシ化担体を用いた点、および、上記環状ペプチドAに代えて下記式(E)で表される環状ペプチドE(配列番号17)を用いた点を除き、実施例3と同様にして環状ペプチド固定カルボキシ化担体を調製した。
Lys-Lys-Lys-Asp-Xaa5-Ala-Tyr-His-Leu-Gly-Glu-Leu-Val-Trp-Xaa15-Thr ・・・(E)
ただし、式(E)中、Xaa5はN-ε-クロロアセチル-L-リシンに由来するアミノ酸残基であり、Xaa15は、システインに由来するアミノ酸残基であり、Xaa5とXaa15とは、N-ε-クロロアセチル-L-リシンの側鎖のクロロアセチル基とシステインの側鎖のチオール基との間でチオエーテル結合を形成して架橋している。
得られた環状ペプチド固定カルボキシ化担体の環状ペプチド固定化量(アフィニティリガンド導入量)を、上述した「アフィニティリガンド導入量(ペプチド固定化量)の測定方法」に従って測定した。その結果、環状ペプチド固定化量は1.9mmol/L-gelであった。
得られた環状ペプチド固定カルボキシ化担体の抗体吸着容量、不純物除去能および薬品耐性を、実施例1と同様にして評価した。評価結果を、それぞれ、表3の「抗体吸着容量」欄、「不純物除去能」欄および「薬品耐性」欄に示す。
得られた環状ペプチド固定カルボキシ化担体の抗原性リガンド混入を、上述した「抗原性リガンド混入の評価方法」に従って評価した。その結果、抗原性リガンド混入の評価は「A」であった。
1.ミックスモードアフィニティクロマトグラフィー用担体の製造
「環状ペプチド固定カルボキシ化担体の調製 - 環状ペプチドの導入」において、上記環状ペプチドAに代えて下記式(F)で表される環状ペプチドF(配列番号18)を用いた点を除き、実施例1と同様にして環状ペプチド固定カルボキシ化担体を調製した。
Lys-Lys-Lys-Asp-Xaa5-Ala-Tyr-His-Leu-Gly-Glu-Leu-Val-Trp-Xaa15-Thr ・・・(F)
ただし、式(F)中、Xaa5およびXaa15は、いずれも、L-システインに由来するアミノ酸残基であり、Xaa5とXaa15とは、L-システインの側鎖のチオール基間でジスルフィド結合を形成して架橋している。
得られた環状ペプチド固定カルボキシ化担体の環状ペプチド固定化量(アフィニティリガンド導入量)を、上述した「アフィニティリガンド導入量(ペプチド固定化量)の測定方法」に従って測定した。その結果、環状ペプチド固定化量は1.8mmol/L-gelであった。
得られた環状ペプチド固定カルボキシ化担体の抗体吸着容量、不純物除去能および薬品耐性を、実施例1と同様にして評価した。評価結果を、それぞれ、表3の「抗体吸着容量」欄、「不純物除去能」欄および「薬品耐性」欄に示す。
得られた環状ペプチド固定カルボキシ化担体の抗原性リガンド混入を、上述した「抗原性リガンド混入の評価方法」に従って評価した。その結果、抗原性リガンド混入の評価は「A」であった。
1.ミックスモードアフィニティクロマトグラフィー用担体の製造
「環状ペプチド固定カルボキシ化担体の調製 - 環状ペプチドの導入」において、上述のとおり調製したカルボキシ化担体を用いた点、および、上記5mg/mL環状ペプチドA溶液1.5mLに代えて、下記式(G)で表される環状ペプチドG(配列番号19)をDMSOに溶解して調製した10mg/mL環状ペプチドG溶液1.5mLを用いた点を除き、実施例3と同様にして環状ペプチド固定カルボキシ化担体を調製した。
Lys-Lys-Lys-Asp-Xaa5-Ala-Tyr-His-Leu-Gly-Glu-Leu-Val-Trp-Xaa15-Thr ・・・(G)
ただし、式(G)中、Xaa5はL-リシンに由来するアミノ酸残基であり、Xaa15はL-グルタミン酸に由来するアミノ酸残基であり、L-リシンの側鎖のアミノ基とL-グルタミン酸の側鎖のカルボキシ基との間でアミド結合を形成して架橋している。
得られた環状ペプチド固定カルボキシ化担体の環状ペプチド固定化量(アフィニティリガンド導入量)を、上述した「アフィニティリガンド導入量(ペプチド固定化量)の測定方法」に従って測定した。その結果、環状ペプチド固定化量は1.2mmol/L-gelであった。
得られた環状ペプチド固定カルボキシ化担体の抗体吸着容量、不純物除去能および薬品耐性を、実施例1と同様にして評価した。評価結果を、それぞれ、表3の「抗体吸着容量」欄、「不純物除去能」欄および「薬品耐性」欄に示す。
得られた環状ペプチド固定カルボキシ化担体の抗原性リガンド混入を、上述した「抗原性リガンド混入の評価方法」に従って評価した。その結果、抗原性リガンド混入の評価は「A」であった。
1.ミックスモードアフィニティクロマトグラフィー用担体の製造
(1)湿ゲルの調製
架橋アガロース系基材「セファローズ4 ファスト・フロー(Sepharose 4
Fast Flow)」(GEヘルスケア社製)を、グラスフィルター上で、純水を用いて懸濁およびろ過を繰り返すことによって洗浄し、基材スラリーを得た。この基材スラリーから、吸引ろ過によって純水を除去して、湿ゲルを得た。
得られた湿ゲル15g、クロロ酢酸ナトリウム11.7gおよび純水31mLを100mL容の三口フラスコに入れ、50℃の温浴中で、フラスコ内容物の撹拌を開始した。クロロ酢酸ナトリウムが完全に溶解するまで撹拌した。溶解後、50℃の温浴中で、フラスコ内温度を約50℃に維持しながら、50%(w/w)水酸化ナトリウム水溶液11gを1時間かけて滴下した。水酸化ナトリウム水溶液の全量を滴下した後、さらに3時間反応し、グラスフィルター上で、純水を用いて懸濁およびろ過を繰り返すことによって洗浄し、カルボキシ化担体の湿ゲルを得た。
上述のとおり調製したカルボキシ化担体を用いた点を除き、実施例6と同様にして環状ペプチド固定カルボキシ化担体を調製した。
得られたカルボキシ化担体のカルボキシ基導入量を、上述した「陽イオン交換基導入量の測定方法」に従って測定した。その結果、カルボキシ基導入量は26mmol/L-gelであった。
得られた環状ペプチド固定カルボキシ化担体の環状ペプチド固定化量(アフィニティリガンド導入量)を、上述した「アフィニティリガンド導入量(ペプチド固定化量)の測定方法」に従って測定した。その結果、環状ペプチド固定化量は1.1mmol/L-gelであった。
得られた環状ペプチド固定カルボキシ化担体の抗体吸着容量、不純物除去能および薬品耐性を、実施例1と同様にして評価した。評価結果を、それぞれ、表3の「抗体吸着容量」欄、「不純物除去能」欄および「薬品耐性」欄に示す。
得られた環状ペプチド固定カルボキシ化担体の抗原性リガンド混入を、上述した「抗原性リガンド混入の評価方法」に従って評価した。その結果、抗原性リガンド混入の評価は「A」であった。
1.ミックスモードアフィニティクロマトグラフィー用担体の製造
「環状ペプチド固定カルボキシ化担体の調製 - 環状ペプチドの導入」において、上述のとおり調製したカルボキシ化担体を用いた点、および、上記5mg/mL環状ペプチドA溶液1.5mLに代えて、下記式(H)で表される直鎖ペプチドH(配列番号20)を50mM炭酸水素ナトリウムバッファーに溶解して調製した10mg/mL直鎖ペプチドH溶液1.5mLを用いた点を除き、実施例3と同様にして直鎖ペプチド固定カルボキシ化担体を調製した。
Lys-Lys-Lys-Lys-Lys-Glu-Gln-Gln-Asn-Ala-Phe-Tyr-Glu-Ile-Leu-His-Leu-Pro-Asn-Leu-Thr-Glu-Glu-Gln-Arg-Asn-Ala-Phe-Ile-Gln-Ser-Leu-Arg-Asp ・・・(H)
得られた直鎖ペプチド固定カルボキシ化担体の直鎖ペプチド固定化量(アフィニティリガンド導入量)を、上述した「アフィニティリガンド導入量(ペプチド固定化量)の測定方法」に従って測定した。その結果、直鎖ペプチド固定化量は4.6mmol/L-gelであった。
得られた直鎖ペプチド固定カルボキシ化担体の抗体吸着容量、不純物除去能および薬品耐性を、実施例1と同様にして評価した。評価結果を、それぞれ、表3の「抗体吸着容量」欄、「不純物除去能」欄および「薬品耐性」欄に示す。
得られた直鎖ペプチド固定カルボキシ化担体の抗原性リガンド混入を、上述した「抗原性リガンド混入の評価方法」に従って評価した。その結果、抗原性リガンド混入の評価は「B」であった。
(抗体吸着容量)
実施例1~7のミックスモードアフィニティクロマトグラフィー用担体は、いずれも抗体吸着容量が「A」または「B」評価であり、十分な抗体吸着容量を有していた。
また、比較例1のミックスモードアフィニティクロマトグラフィー用担体も、抗体吸着容量が「A」評価であり、十分な抗体吸着容量を有していた。これは、アフィニティリガンドとして環状ペプチドを用いたことによるものと考えられる。
一方、実施例1~7および比較例2のミックスモードアフィニティクロマトグラフィー用担体は、いずれも親水性ポリマーを含むが、抗体吸着容量が前者は「A」または「B」評価、後者は「E」評価であり、十分な抗体吸着容量を有していなかった。これは、アフィニティリガンドが前者は環状ペプチドであるのに対し、後者は直鎖ペプチドであることから、直鎖ペプチドと親水性ポリマーとの組み合わせがよくないためと考えられるが、抗体吸着容量が異なるメカニズムについては現在のところ明確な説明をすることができない。
実施例1~7のミックスモードアフィニティクロマトグラフィー用担体は、いずれも不純物除去能が「A」または「B」評価であり、十分な不純物除去能を有していた。
これに対し、親水性ポリマーを含まない比較例1のミックスモードアフィニティクロマトグラフィー用担体は、不純物除去能が「E」評価であり、十分な不純物除去能を有していなかった。
一方、親水性ポリマーを含む比較例2のミックスモードアフィニティクロマトグラフィー用担体は、不純物除去能が「B」評価であり、十分な不純物除去能を有していた。
これらの結果は、不純物除去能が親水性ポリマーと陽イオン交換基が共存することにより改善されることによるのではないかと考えられる。
実施例1~7および比較例1のミックスモードアフィニティクロマトグラフィー用担体は、薬品耐性が「B」評価以上であり、十分な薬品耐性を有していた。
これに対し、アフィニティリガンドとして直鎖ペプチドを用いた比較例2では、薬品耐性が「E」評価であり、十分な薬品耐性を有していなかった。
これらの結果は、薬品耐性において、直鎖ペプチドが環状ペプチドに劣ることによると考えられる。
また、実施例1~7および比較例1の中でも、実施例1および実施例2は評価が「AAA」であり、特に優れていた。薬剤耐性の観点からは、環状ペプチドの架橋構造としては、ホモシステイン残基とハロアセチル基含有アミノ酸残基(側鎖にハロアセチル基を有するアミノ酸残基をいう。)間のチオエーテル結合およびホモシステイン残基間のジスルフィド結合が特に好ましく、ペニシラミン残基とハロアセチル基含有アミノ酸残基間のチオエーテル結合がその次に好ましく、システインとハロアセチル基含有アミノ酸残基間のチオエーテル結合、トリアゾール結合およびアミド結合がさらにその次に好ましいことがわかる。
本発明のミックスモードアフィニティクロマトグラフィー用担体は、基材と、親水性ポリマーと、抗体結合性環状ペプチドと、陽イオン交換基と、をすべて備えることにより、抗体吸着容量、不純物除去能および薬品耐性のいずれにも優れたものとなっている。
Claims (21)
- 基材と、親水性ポリマーと、抗体結合性環状ペプチドと、陽イオン交換基と、を有するミックスモードアフィニティクロマトグラフィー用担体。
- 前記抗体結合性環状ペプチドは側鎖間の分子内架橋により環化した環状部を有する、請求項1に記載のミックスモードアフィニティクロマトグラフィー用担体。
- 前記分子内架橋が、ジスルフィド結合、チオエーテル結合、トリアゾール結合、およびアミド結合からなる群から選択される少なくとも1つを含む、請求項2に記載のミックスモードアフィニティクロマトグラフィー用担体。
- 前記分子内架橋が、ジスルフィド結合、チオエーテル結合、およびトリアゾール結合からなる群から選択される少なくとも1つを含む、請求項2または3に記載のミックスモードアフィニティクロマトグラフィー用担体。
- 前記ジスルフィド結合が、L-システインおよびD-システイン以外の側鎖にチオール基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖チオール基と、L-システインおよびD-システイン以外の側鎖にチオール基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖チオール基との間で形成されたジスルフィド結合であり、
前記チオエーテル結合が、L-システインおよびD-システイン以外の側鎖にチオール基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖チオール基と、側鎖にハロアセチル基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖ハロアセチル基との間で形成されたチオエーテル結合である、請求項4に記載のミックスモードアフィニティクロマトグラフィー用担体。 - 前記ジスルフィド結合が、システイン、ホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖チオール基と、システイン、ホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖チオール基との間で形成されたジスルフィド結合であり、
前記チオエーテル結合が、システイン、ホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖チオール基と、側鎖にハロアセチル基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖ハロアセチル基との間で形成されたチオエーテル結合である、請求項4に記載のミックスモードアフィニティクロマトグラフィー用担体。 - 前記ジスルフィド結合が、ホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖チオール基と、ホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖チオール基との間で形成されたジスルフィド結合であり、
前記チオエーテル結合が、ホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖チオール基と、側鎖にハロアセチル基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖ハロアセチル基との間で形成されたチオエーテル結合である、請求項4~6のいずれか1項に記載のミックスモードアフィニティクロマトグラフィー用担体。 - 前記分子内架橋が、ホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖チオール基と、ホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖チオール基との間で形成されたジスルフィド結合、または、ホモシステインおよびペニシラミンからなる群から選択される側鎖にチオール基を有するアミノ酸に由来する第1のアミノ酸残基の側鎖チオール基と、側鎖にハロアセチル基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖ハロアセチル基との間で形成されたチオエーテル結合である、請求項2~4のいずれか1項に記載のミックスモードアフィニティクロマトグラフィー用担体。
- 前記ジスルフィド結合が、ホモシステインに由来する第1のアミノ酸残基の側鎖チオール基と、ホモシステインに由来する第2のアミノ酸残基の側鎖チオール基との間で形成されたジスルフィド結合であり、
前記チオエーテル結合がホモシステインに由来する第1のアミノ酸残基の側鎖チオール基と側鎖にハロアセチル基を有するアミノ酸に由来する第2のアミノ酸残基の側鎖ハロアセチル基との間で形成されたチオエーテル結合である、請求項8に記載のミックスモードアフィニティクロマトグラフィー用担体。 - 前記環状部のアミノ酸残基数が8~14残基である、請求項2~9のいずれか1項に記載のミックスモードアフィニティクロマトグラフィー用担体。
- 前記抗体結合性環状ペプチドは直鎖部を有する、請求項1~10のいずれか1項に記載のミックスモードアフィニティクロマトグラフィー用担体。
- 前記直鎖部は側鎖にヒドロキシ基およびカルボキシ基からなる群から選択される少なくとも1つを有するアミノ酸残基を含む、請求項11に記載のミックスモードアフィニティクロマトグラフィー用担体。
- 前記基材が、多糖類、アクリレート系重合体、メタクリレート系重合体およびスチレン系重合体からなる群から選択される少なくとも1種である、請求項1~12のいずれか1項に記載のミックスモードアフィニティクロマトグラフィー用担体。
- 前記基材が、多糖類、アクリレート系重合体およびメタクリレート系重合体からなる群から選択される少なくとも1種である、請求項1~13のいずれか1項に記載のミックスモードアフィニティクロマトグラフィー用担体。
- 前記基材が、アガロースおよびセルロースからなる群から選択される少なくとも1種である、請求項1~14のいずれか1項に記載のミックスモードアフィニティクロマトグラフィー用担体。
- 前記親水性ポリマーが親水性多糖類である、請求項1~15のいずれか1項に記載のミックスモードアフィニティクロマトグラフィー用担体。
- 前記親水性多糖類が、デキストラン、カルボキシメチルデキストラン、プルラン、ヒドロキシエチルセルロース、およびカルボキシメチルセルロースからなる群から選択される少なくとも1種である、請求項16に記載のミックスモードアフィニティクロマトグラフィー用担体。
- 前記親水性多糖類が、デキストラン、カルボキシメチルデキストランおよびプルランからなる群から選択される少なくとも1種である、請求項16または17に記載のミックスモードアフィニティクロマトグラフィー用担体。
- 前記抗体結合性環状ペプチドの分子量が5000未満である、請求項1~18のいずれか1項に記載のミックスモードアフィニティクロマトグラフィー用担体。
- 前記陽イオン交換基が、カルボキシ基またはスルホキシ基である、請求項1~19のいずれか1項に記載のミックスモードアフィニティクロマトグラフィー用担体。
- 前記陽イオン交換基がカルボキシ基である、請求項1~20のいずれか1項に記載のミックスモードアフィニティクロマトグラフィー用担体。
Priority Applications (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CA3044645A CA3044645A1 (en) | 2016-12-09 | 2017-09-19 | Mixed mode affinity chromatography carrier |
| EP17879511.8A EP3553073A4 (en) | 2016-12-09 | 2017-09-19 | AFFINITY CHROMATOGRAPHY SUPPORT IN MIXED MODE |
| KR1020197013217A KR20190061062A (ko) | 2016-12-09 | 2017-09-19 | 믹스모드 어피니티 크로마토그래피용 담체 |
| BR112019009485A BR112019009485A2 (pt) | 2016-12-09 | 2017-09-19 | veículo de cromatografia por afinidade de modo misto |
| CN201780070910.9A CN109983026B (zh) | 2016-12-09 | 2017-09-19 | 混合模式亲和层析用载体 |
| JP2018554831A JP6906547B2 (ja) | 2016-12-09 | 2017-09-19 | ミックスモードアフィニティクロマトグラフィー用担体 |
| US16/402,447 US11565240B2 (en) | 2016-12-09 | 2019-05-03 | Mixed mode affinity chromatography carrier |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016239536 | 2016-12-09 | ||
| JP2016-239536 | 2016-12-09 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US16/402,447 Continuation US11565240B2 (en) | 2016-12-09 | 2019-05-03 | Mixed mode affinity chromatography carrier |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2018105198A1 true WO2018105198A1 (ja) | 2018-06-14 |
Family
ID=62490943
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2017/033642 Ceased WO2018105198A1 (ja) | 2016-12-09 | 2017-09-19 | ミックスモードアフィニティクロマトグラフィー用担体 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US11565240B2 (ja) |
| EP (1) | EP3553073A4 (ja) |
| JP (1) | JP6906547B2 (ja) |
| KR (1) | KR20190061062A (ja) |
| CN (1) | CN109983026B (ja) |
| BR (1) | BR112019009485A2 (ja) |
| CA (1) | CA3044645A1 (ja) |
| WO (1) | WO2018105198A1 (ja) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SG11201902818PA (en) * | 2016-09-30 | 2019-05-30 | Fujifilm Corp | Cyclic peptide, affinity chromatography support, labeled antibody, antibody drug conjugate, and pharmaceutical preparation |
| JP2023536366A (ja) * | 2020-08-07 | 2023-08-24 | エフ. ホフマン-ラ ロシュ アーゲー | タンパク質組成物を製造するための方法 |
| CN117169393B (zh) * | 2023-11-03 | 2024-03-19 | 杭州湃肽生化科技有限公司 | 一种植物组织中环肽的检测方法 |
Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1992000997A1 (en) * | 1990-07-09 | 1992-01-23 | Biochem Pharma Inc. | Synthetic peptides and mixtures thereof for detecting hiv antibodies |
| WO2007027139A1 (en) * | 2005-08-31 | 2007-03-08 | Ge Healthcare Bio-Sciences Ab | Manufacture of chromatography matrices |
| JP2010133734A (ja) * | 2008-12-02 | 2010-06-17 | Tosoh Corp | アフィニティークロマトグラフィー用カルボキシル化担体、及びそれを用いたアフィニティークロマトグラフィー用分離剤 |
| WO2013027796A1 (ja) * | 2011-08-24 | 2013-02-28 | 大塚化学株式会社 | IgG結合性ペプチド及びそれによるIgGの検出および精製方法 |
| WO2013081037A1 (ja) * | 2011-11-30 | 2013-06-06 | 国立大学法人鹿児島大学 | IgA結合性ペプチド及びそれによるIgAの精製 |
| WO2014034457A1 (ja) * | 2012-09-03 | 2014-03-06 | 株式会社カネカ | ミックスモード抗体アフィニティー分離マトリックスとそれを用いた精製方法および標的分子 |
| WO2017069269A1 (ja) * | 2015-10-23 | 2017-04-27 | 富士フイルム株式会社 | 環状ペプチド、アフィニティクロマトグラフィー担体、標識化抗体、抗体薬物複合体、および医薬製剤 |
| WO2017069254A1 (ja) * | 2015-10-23 | 2017-04-27 | 富士フイルム株式会社 | アフィニティクロマトグラフィ担体および生体物質の精製方法 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2008200795A1 (en) * | 2007-12-31 | 2009-07-16 | University Of Basel | Monoclonal antibodies and binding fragments thereof directed to the melanocortin-4 receptor and their use in the treatment of cachexia and related conditions and diseases |
| EP3680251A1 (en) * | 2011-09-30 | 2020-07-15 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecules for promoting elimination of antigens |
| JP5891703B2 (ja) | 2011-10-21 | 2016-03-23 | 三菱化学株式会社 | 多孔質架橋粒子および分離剤の製造方法ならびに分離方法 |
| TWI787670B (zh) * | 2011-12-28 | 2022-12-21 | 日商中外製藥股份有限公司 | 具有環狀部之胜肽化合物及其醫藥組成物 |
| KR101609840B1 (ko) * | 2012-07-12 | 2016-04-07 | 한국생명공학연구원 | 항체의 Fc 부위 결합 펩타이드를 이용한 항체 정제용 흡착 칼럼 |
| KR101450182B1 (ko) | 2012-09-12 | 2014-10-13 | 주식회사 메즈파 | 평탄도 확보를 위한 파이프 벤딩기 |
| EP3010550B1 (en) * | 2013-06-20 | 2021-10-27 | California Institute of Technology | Cyclic peptides as protein targeting agents |
| JP6630036B2 (ja) | 2014-09-30 | 2020-01-15 | Jsr株式会社 | 標的物の精製方法、及び、ミックスモード用担体 |
-
2017
- 2017-09-19 CN CN201780070910.9A patent/CN109983026B/zh active Active
- 2017-09-19 BR BR112019009485A patent/BR112019009485A2/pt not_active IP Right Cessation
- 2017-09-19 KR KR1020197013217A patent/KR20190061062A/ko not_active Withdrawn
- 2017-09-19 CA CA3044645A patent/CA3044645A1/en not_active Abandoned
- 2017-09-19 WO PCT/JP2017/033642 patent/WO2018105198A1/ja not_active Ceased
- 2017-09-19 EP EP17879511.8A patent/EP3553073A4/en active Pending
- 2017-09-19 JP JP2018554831A patent/JP6906547B2/ja active Active
-
2019
- 2019-05-03 US US16/402,447 patent/US11565240B2/en active Active
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1992000997A1 (en) * | 1990-07-09 | 1992-01-23 | Biochem Pharma Inc. | Synthetic peptides and mixtures thereof for detecting hiv antibodies |
| WO2007027139A1 (en) * | 2005-08-31 | 2007-03-08 | Ge Healthcare Bio-Sciences Ab | Manufacture of chromatography matrices |
| JP2010133734A (ja) * | 2008-12-02 | 2010-06-17 | Tosoh Corp | アフィニティークロマトグラフィー用カルボキシル化担体、及びそれを用いたアフィニティークロマトグラフィー用分離剤 |
| WO2013027796A1 (ja) * | 2011-08-24 | 2013-02-28 | 大塚化学株式会社 | IgG結合性ペプチド及びそれによるIgGの検出および精製方法 |
| WO2013081037A1 (ja) * | 2011-11-30 | 2013-06-06 | 国立大学法人鹿児島大学 | IgA結合性ペプチド及びそれによるIgAの精製 |
| WO2014034457A1 (ja) * | 2012-09-03 | 2014-03-06 | 株式会社カネカ | ミックスモード抗体アフィニティー分離マトリックスとそれを用いた精製方法および標的分子 |
| WO2017069269A1 (ja) * | 2015-10-23 | 2017-04-27 | 富士フイルム株式会社 | 環状ペプチド、アフィニティクロマトグラフィー担体、標識化抗体、抗体薬物複合体、および医薬製剤 |
| WO2017069254A1 (ja) * | 2015-10-23 | 2017-04-27 | 富士フイルム株式会社 | アフィニティクロマトグラフィ担体および生体物質の精製方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN109983026B (zh) | 2023-09-19 |
| CN109983026A (zh) | 2019-07-05 |
| KR20190061062A (ko) | 2019-06-04 |
| JPWO2018105198A1 (ja) | 2019-10-24 |
| EP3553073A4 (en) | 2020-01-08 |
| US20190247827A1 (en) | 2019-08-15 |
| JP6906547B2 (ja) | 2021-07-21 |
| US11565240B2 (en) | 2023-01-31 |
| EP3553073A1 (en) | 2019-10-16 |
| BR112019009485A2 (pt) | 2019-07-30 |
| CA3044645A1 (en) | 2018-06-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6554452B2 (ja) | 環状ペプチド、アフィニティクロマトグラフィー担体、標識化抗体、抗体薬物複合体、および医薬製剤 | |
| JP6630036B2 (ja) | 標的物の精製方法、及び、ミックスモード用担体 | |
| JP2019034963A (ja) | 陽イオン交換基を用いた新規抗体精製法(Novel Antibody Purification method using Cation Exchanger) | |
| JP4685294B2 (ja) | 新規ペプチド、生産方法、新規吸着体、吸着器および吸着方法 | |
| CN104645949B (zh) | 一种以四肽为功能配基的亲和层析介质及其制备方法 | |
| US10888841B2 (en) | Affinity chromatography carrier and method for purifying biological substance | |
| WO2011118599A1 (ja) | アフィニティークロマトグラフィー用充填剤およびイムノグロブリンを単離する方法 | |
| US11565240B2 (en) | Mixed mode affinity chromatography carrier | |
| CN104603144A (zh) | 混合模式抗体亲和分离基质和使用其的纯化方法及靶分子 | |
| CN109790202B (zh) | 环肽、亲和层析载体、标记抗体、抗体药物复合体及药物制剂 | |
| WO2017069269A1 (ja) | 環状ペプチド、アフィニティクロマトグラフィー担体、標識化抗体、抗体薬物複合体、および医薬製剤 | |
| US8034785B2 (en) | Adsorbent adsorbing antibody against β1 adrenoreceptor |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 17879511 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 20197013217 Country of ref document: KR Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 2018554831 Country of ref document: JP Kind code of ref document: A |
|
| REG | Reference to national code |
Ref country code: BR Ref legal event code: B01A Ref document number: 112019009485 Country of ref document: BR |
|
| ENP | Entry into the national phase |
Ref document number: 3044645 Country of ref document: CA |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2019116741 Country of ref document: RU |
|
| ENP | Entry into the national phase |
Ref document number: 2017879511 Country of ref document: EP Effective date: 20190709 |
|
| ENP | Entry into the national phase |
Ref document number: 112019009485 Country of ref document: BR Kind code of ref document: A2 Effective date: 20190509 |