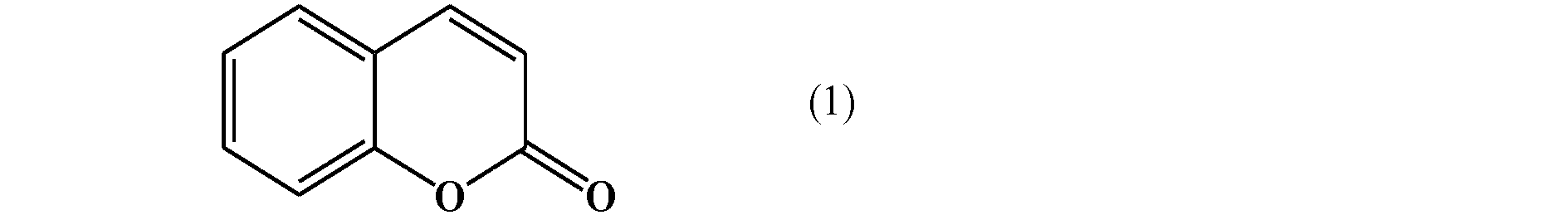WO2019069853A1 - 放射線線量測定ゾル又はゲル、及びそれを放射線線量の計測材料として備える放射線線量計 - Google Patents
放射線線量測定ゾル又はゲル、及びそれを放射線線量の計測材料として備える放射線線量計 Download PDFInfo
- Publication number
- WO2019069853A1 WO2019069853A1 PCT/JP2018/036694 JP2018036694W WO2019069853A1 WO 2019069853 A1 WO2019069853 A1 WO 2019069853A1 JP 2018036694 W JP2018036694 W JP 2018036694W WO 2019069853 A1 WO2019069853 A1 WO 2019069853A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- radiation
- sodium
- sol
- gel
- water
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent materials, e.g. electroluminescent or chemiluminescent
- C09K11/02—Use of particular materials as binders, particle coatings or suspension media therefor
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01T—MEASUREMENT OF NUCLEAR OR X-RADIATION
- G01T1/00—Measuring X-radiation, gamma radiation, corpuscular radiation, or cosmic radiation
- G01T1/02—Dosimeters
- G01T1/10—Luminescent dosimeters
- G01T1/105—Read-out devices
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent materials, e.g. electroluminescent or chemiluminescent
- C09K11/06—Luminescent materials, e.g. electroluminescent or chemiluminescent containing organic luminescent materials
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01T—MEASUREMENT OF NUCLEAR OR X-RADIATION
- G01T1/00—Measuring X-radiation, gamma radiation, corpuscular radiation, or cosmic radiation
- G01T1/02—Dosimeters
- G01T1/04—Chemical dosimeters
-
- G—PHYSICS
- G21—NUCLEAR PHYSICS; NUCLEAR ENGINEERING
- G21K—HANDLING OF PARTICLES OR IONISING RADIATION NOT OTHERWISE PROVIDED FOR; IRRADIATION DEVICES; GAMMA RAY OR X-RAY MICROSCOPES
- G21K4/00—Conversion screens for the conversion of the spatial distribution of X-rays or particle radiation into visible images, e.g. fluoroscopic screens
-
- G—PHYSICS
- G21—NUCLEAR PHYSICS; NUCLEAR ENGINEERING
- G21K—HANDLING OF PARTICLES OR IONISING RADIATION NOT OTHERWISE PROVIDED FOR; IRRADIATION DEVICES; GAMMA RAY OR X-RAY MICROSCOPES
- G21K4/00—Conversion screens for the conversion of the spatial distribution of X-rays or particle radiation into visible images, e.g. fluoroscopic screens
- G21K2004/08—Conversion screens for the conversion of the spatial distribution of X-rays or particle radiation into visible images, e.g. fluoroscopic screens with a binder in the phosphor layer
Definitions
- the present invention relates to a radiation dosimetry sol or gel, and a radiation dosimeter including the same as a measurement material of radiation dose. More specifically, the present invention relates to a radiation dosimetry sol or gel used for measurement of a three-dimensional dose distribution, and a radiation dosimeter equipped with it as a measurement material of radiation dose.
- Gel dosimeters are three-dimensional dosimeters that use radiation-induced chemical reactions.
- the reaction product retained in the gel after irradiating the gel dosimeter with radiation is read by a three-dimensional scanner such as nuclear magnetic resonance imaging (MRI) or optical CT (OCT) and converted to dose distribution Be done. Since most of the gel is water and has a composition close to that of a living body, it is expected to be used as a verification tool for the complicated three-dimensional dose distribution planned particularly in radiation therapy.
- MRI nuclear magnetic resonance imaging
- OCT optical CT
- the FLICKE gel dosimeter is a gelation of a solution (an aqueous solution containing ferrous sulfate) of a FLICKE dosimeter known as a liquid chemical dosimeter, and the oxidation reaction of iron from divalent to trivalent with radiation ( Coloring) is utilized in proportion to the absorbed dose.
- a polymer gel dosimeter is one in which a monomer is dispersed in a gel, and utilizing radiation generation (polymerization reaction) of a polymer in proportion to a dose (non-patent document 1).
- the main components of the gel dosimeter are radiation sensitive compounds, gelling agents and water (solvent). Since water accounts for 70% to 90% of the whole gel dosimeter, looking at the radiation-induced chemical reaction in the gel, it begins with the radiolysis of water. The hydrolytic radicals generated at this time become species that cause oxidation reaction and polymerization reaction. The generation concentration of water-splitting radicals is only about several ⁇ M for an absorbed dose of 10 Gy, and in the above-mentioned gel dosimeter, sensitivity is improved by the progress of a chain reaction from one water-splitting radical.
- Non-patent Document 2 Non-patent Document 2
- Non-patent Document 4 those containing an organic gel such as gelatin do not have expected high sensitivity results.
- gel dosimeters have been reported that use a radiation fading reaction of a fluorescent substance such as rhodamine, but a dose as high as several hundred Gy is required for measurement (Non-patent Document 5).
- Watanabe Y, Warmington L, Gopishankar N Three-dimensional radiation dose using polymer gel and solid radiochromic polymer: From basics to clinical applications.
- International Journal of Applied Radiation and Isotopes 33: 1159-70, 1982 Place Delft University of Technology: Delft University of Technology; 2017. (https://pure.tudelft.nl/portal/files/9767609/thesis.pdf#search % Yao T, 3D Radiation Dosimetry Using a Radio-Fluorogenic gel.
- the radiation dosimeter using a conventional fluorescent probe has a problem that the sensitivity to radiation irradiation is low and it is difficult to obtain high sensitivity characteristics. Therefore, the present invention provides a sol or gel which can be used as a radiation dose measuring material, and has a good sensitivity to radiation irradiation.
- the present inventor differs from the organic gelling agent on the premise that the reaction between the radiation sensitive compound and the water splitting radical is hindered by the trapping of the water splitting radical by the organic gelling agent (such as gelatin or agarose),
- the organic gelling agent such as gelatin or agarose
- an inorganic gelling agent or an organic-inorganic hybrid gelling agent having low reactivity with hydrolytic radicals is used, a compound in which the fluorescence characteristic by excitation light is changed by a radiation decomposition product of water and the inorganic gelling agent or organic inorganic
- the radiation dosimeter which applied the sol or gel containing a composite gelling agent to the measurement material of radiation dose discovered that it was extremely sensitive to radiation irradiation, and completed the present invention.
- a radiation dose measurement sol characterized by comprising a compound (A) and a silicate (B) in which the fluorescence characteristics by excitation light are changed by radiolysis products of water. Or a gel.
- the compound (A) whose fluorescence characteristics are changed by excitation light due to the radioactive decomposition product of water is one or more selected from the group consisting of coumarin derivatives, aromatic carboxylic acid derivatives, oxazole derivatives and rhodamines
- the present invention relates to a radiation dosimetry sol or gel according to the first aspect, which is two or more kinds.
- the first aspect or the second aspect wherein the silicate (B) is at least one water-swellable silicate particle selected from the group consisting of smectite, bentonite, vermiculite and mica.
- the radiation dose measurement sol or gel according to As a fourth aspect a water-soluble organic polymer (C) having an organic acid salt structure or an organic acid anion structure and a dispersant (D) for a silicate (B) are further included, the first aspect The radiation dosimetry sol or gel according to any one of the third aspects.
- the present invention relates to the radiation dosimetry sol or gel according to the fourth aspect, wherein the water-soluble organic polymer (C) is a completely neutralized or partially neutralized polyacrylate.
- the dispersant (D) is sodium orthophosphate, sodium pyrophosphate, sodium tripolyphosphate, sodium tetraphosphate, sodium hexametaphosphate, sodium polyphosphate, sodium poly (meth) acrylate, poly (meth) acrylic acid Ammonium, sodium acrylate / sodium maleate copolymer, ammonium acrylate / ammonium maleate copolymer, sodium hydroxide, hydroxylamine, sodium carbonate, sodium silicate, polyethylene glycol, polypropylene glycol, sodium humate and lignin sulfone It relates to the radiation dosimetry sol or gel according to the fourth or fifth aspect, which is one or more selected from the group consisting of sodium acid.
- a seventh aspect relates to the radiation dosimetry sol or gel according to the fourth or
- An eighth aspect relates to a radiation dosimeter including the radiation dose measurement sol or gel according to any one of the first to seventh aspects as a measurement material of a radiation dose.
- the present invention relates to the radiation dosimeter according to the eighth aspect, wherein the radiation dosimeter is a radiation dosimeter for an optical CT apparatus.
- the radiation dosimetry sol or gel of the present invention has excellent sensitivity to radiation as compared with gelatin, agarose and the like widely used in conventional radiation dosimeters.
- the radiation dosimetry sol or gel of the present invention has a constant quality because it can be manufactured only by mixing at room temperature using industrially readily available raw materials without the need for heating. It can also be used as a material for measuring radiation doses in radiation dosimeters, as injectable sols or gels.
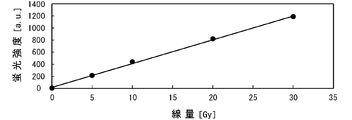
- FIG. 1 is a view showing the results of the irradiation test in Example 2.
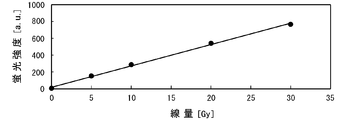
- FIG. 2 is a diagram showing the results of the irradiation test in Example 7.
- FIG. 3 is a diagram showing the results of the irradiation test in Example 11.
- FIG. 4 is a diagram showing the results of the irradiation test in Example 14.
- FIG. 5 is a diagram showing the results of the irradiation test in Example 14.
- FIG. 6 is a diagram showing the results of the irradiation test in Example 16.
- FIG. 7 is a photograph of each sample after radiation irradiation in the diffusion evaluation test in Example 19 (a) Sample 1 month after radiation irradiation in Example 17, (b) Sample 2 days after radiation irradiation in Example 18 ].
- FIG. 19 is a photograph of each sample after radiation irradiation in the diffusion evaluation test in Example 19 (a) Sample 1 month after radiation irradiation in Example 17, (b) Sample 2 days after radiation irradiation in
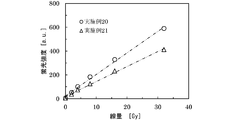
- FIG. 8 is a diagram showing the results of the irradiation test in Example 22.
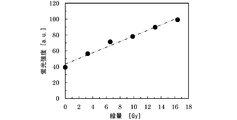
- FIG. 9 is a diagram showing the results of the irradiation test in Example 25.
- FIG. 10 is an image obtained from the fluorescent gel scanner in Example 26.
- FIG. 11 is a diagram showing the results of the irradiation test in Example 26.
- FIG. 12 is an image after radiation irradiation (after 73 days) in the diffusion evaluation test in Example 27.
- FIG. 13 is a diagram showing the results of spectrometry in Example 28.
- [Radiation dosimetry sol or gel] As a component of the radiation dosimetry sol or gel of the present invention, a compound (A) and a silicate (B) whose fluorescence characteristics are changed by excitation light due to a radiolysis product of water, or a radiolysis product of water, Dispersing agent for compound (A), silicate (B), water-soluble organic polymer (C) having organic acid salt structure or organic acid anion structure, and silicate (B), whose fluorescence properties are changed by excitation light ((A) D) may be mentioned, but in addition to the above components, other components may be optionally blended as needed, as long as the intended effects of the present invention are not impaired.
- the compound (A) whose fluorescence characteristics are changed by excitation light by radiation decomposition products of water is excited by a compound which emits fluorescence by excitation light by radiation decomposition products of water, or by radiation decomposition products of water It is a compound in which the fluorescence by light fades.
- the radiation dosimetry sol or gel of the present invention comprises a compound (A) in which the fluorescence characteristic by excitation light is changed by the radiolysis product of water, whereby the radiation dosimetry sol or gel of the present invention measures radiation dose
- the radiation dosimeter provided as a material functions as a fluorescent sol or gel dosimeter.
- Compound (A) whose fluorescence characteristics are changed by excitation light by radiation decomposition products of water irradiates water with radiation, and is excited by reaction with active oxygen species such as hydroxy radical and superoxide radical generated thereby.
- a compound whose fluorescence characteristics change due to light such as a compound that emits fluorescence due to excitation light due to a radiation decomposition product of water or a compound that causes fluorescence due to excitation light to fade due to a radiation decomposition product of water.
- a fluorescent probe that emits fluorescence due to excitation light due to the radiation decomposition product of water can be used as a compound that emits fluorescence due to excitation light due to the radiolysis product of water.
- a fluorescent dye can be used as a compound whose fluorescence due to excitation light is discolored.
- compounds (A) whose fluorescence characteristics by excitation light are changed by such a radiolysis product of water coumarin derivatives, aromatic carboxylic acid derivatives, oxazole derivatives, rhodamines, acridines, coumestrols, fluoresceins And pyrenes, stilbenes, resorufins, eosins, xanthans, naphthalimides and polymethines, among which coumarin derivatives, aromatic carboxylic acid derivatives, oxazole derivatives and rhodamines are preferable.
- compounds (A) whose fluorescence characteristics are changed by excitation light due to a radiolysis product of water can be used singly or in combination of two or more.
- the coumarin derivative is a compound having a coumarin skeleton represented by the following formula (1).
- the coumarin derivative is not particularly limited, but coumarin, coumarin-3-carboxylic acid, 3-aminocoumarin, umbelliferone (7-hydroxycoumarin) and umbelliferone-3-carboxylic acid (7-hydroxycoumarin-3-carboxylone) Acid) and the like.
- the aromatic carboxylic acid derivative is not particularly limited, and examples thereof include benzoic acid, terephthalic acid, pyromellitic acid, trimellitic acid, 3- (4-hydroxyphenyl) propionic acid, 1-naphthalic acid and 2-naphthalic acid. .
- the oxazole derivative is not particularly limited, and examples thereof include 2,5-diphenyloxazole and 2- (1-naphthyl) -5-phenyloxazole.
- the rhodamines are not particularly limited, and include rhodamine B, rhodamine 6G, rhodamine 123 and the like.
- the following compounds which are widely known as compounds in which the fluorescence characteristics by excitation light are changed due to the products of radiolysis of water may be used.
- the following compounds include compounds classified into the above-mentioned coumarin derivatives, aromatic carboxylic acid derivatives, oxazole derivatives and rhodamines, which means that the compounds do not fall under the above-mentioned coumarin derivatives etc.
- the content of the compound (A) whose fluorescence characteristics are changed by excitation light due to the radiolysis product of water is 0.1 ⁇ M to 1000 ⁇ M, preferably the radiation decomposition product of water causes the fluorescence due to the excitation light to fade
- the concentration is 0.1 ⁇ M to 5 ⁇ M for the compound, and 50 ⁇ M to 500 ⁇ M for the compound that emits fluorescence due to excitation light due to the radiolysis product of water.
- silicate (B) examples include water-swellable silicate particles such as smectite, bentonite, vermiculite, and mica, and those forming a colloid using water or a water-containing liquid as a dispersion medium are preferable.
- smectite is a general term for swelling clay minerals such as montmorillonite, beidellite, hectorite, saponite and stevensite.
- the silicate (B) can be used singly or in combination of two or more.
- Examples of the shape of primary particles of silicate particles include disk, plate, sphere, particle, cubic, needle, rod and amorphous, and for example, a disk or plate having a diameter of 5 nm to 1000 nm. Is preferred.
- silicates include layered silicates.
- Examples of readily available commercially available products include Laponite XLG (synthetic hectorite) manufactured by Rockwood Additives, and XLS (synthetic hectorite).
- Lucentite SWN synthetic smectite
- SWF synthetic smectite manufactured by Coop Chemical Co., Ltd., micro mica (synthetic mica), and soma sif (synthetic mica); Kunipia (montmorillonite) manufactured by Kuninine Industrial Co., Ltd. Smecton SA (synthetic saponite); Etc. Formula Company Hojun made Wenger (natural bentonite purified product) and the like.
- the content of the silicate (B) is 0.01% by mass to 20% by mass, preferably 0.1% by mass to 10% by mass, in 100% by mass of the radiation dosimetry sol or gel.
- Examples of the salt having an organic acid group salt include salts of the above-mentioned organic acid group (sodium salt, ammonium salt, potassium salt, lithium salt and the like) and the like. Moreover, as what has an organic acid anion structure, what has a structure which the cation dissociated from the salt of said organic acid group, etc. are mentioned.
- (meth) acrylic acid means both acrylic acid and methacrylic acid.
- the water-soluble organic polymer (C) is preferably a linear structure having no branched or chemically crosslinked structure, and the water-soluble organic polymer (C) is a completely neutralized product or organic acid salt structure consisting only of an organic acid salt structure Either a partially neutralized product in which the acid and the organic acid structure are mixed or a mixture of a completely neutralized product and a partially neutralized product can be used.
- the weight average molecular weight of the water-soluble organic polymer (C) is preferably 1,000,000 or more and 10,000,000 or less, more preferably 2.5,000,000 or more and 5,000,000 or less, in terms of polyethylene glycol by gel permeation chromatography (GPC).
- the water-soluble organic polymer (C) is preferably a completely neutralized or partially neutralized polyacrylate, more preferably a completely or partially neutralized linear polyacrylate, and having a weight average molecular weight of at least 1,000,000. Particularly preferred is a completely neutralized or partially neutralized linear polyacrylic acid sodium having a molecular weight of up to 10,000,000, and a completely or partially neutralized linear polyacrylic acid sodium having a weight average molecular weight of not less than 2.5 million and not more than 5,000,000. More preferable.
- the degree of neutralization of partial neutralization is 10% to 90%, preferably 30% to 80%.
- the content of the water-soluble organic polymer (C) is 0.01% by mass to 20% by mass, preferably 0.03% by mass to 10% by mass, in 100% by mass of the radiation dosimetry sol or gel.
- Dispersant for silicate (B) a dispersant or a peptizer used for the purpose of improving the dispersibility of the silicate or exfoliating the layered silicate can be used.
- phosphate dispersants, carboxylate dispersants, those acting as alkalis and organic peptizers can be used.
- sodium pyrophosphate as a phosphate dispersant
- sodium etidronate sodium poly (meth) acrylate as a carboxylate dispersant
- polyethylene glycol such as PEG 900
- sodium poly (meth) acrylate is more preferable, and low-polymerized sodium polyacrylate having a weight average molecular weight of 1,000 or more and 20,000 or less is particularly preferable.
- the low-polymerized sodium polyacrylate interacts with the silicate particles to generate a negative charge derived from the carboxy anion on the particle surface, and acts as a dispersing agent by a mechanism such as dispersing the silicate by repulsion of charge.
- the content of the dispersant (D) is 0.001% by mass to 20% by mass, preferably 0.01% by mass to 10% by mass, in 100% by mass of the radiation dosimetry sol or gel.
- the dispersant may or may not be further added.
- the component (A) is a preferable combination of the compound (A) and the silicate dispersant (B) in which the fluorescence characteristics by excitation light are changed by radiolysis products of water.
- 100% by mass of the gel a combination of 0.1% by mass to 10% by mass of water-swellable smectite or saponite as the component (B) can be mentioned.
- the radiation dosimetry sol or gel of the present invention contains the component (C) and the component (D), the compound (A) in which the fluorescence characteristic by excitation light is changed by the radiolysis product of water
- a radiation decomposition product of water as the component (A) causes fluorescence by excitation light
- the radiation dosimetry sol or gel of the present invention can also contain pH adjusters such as glucono- ⁇ -lactone, perchloric acid, sulfuric acid and sodium chloride.
- the method for producing the radiation dosimetry sol or gel of the present invention is not particularly limited, but the component (A) and the component (B) and, if necessary, the component (C) and the component (D) to be added
- a method of gelling by mixing, or a mixture of at least two of components (A) to (D) or an aqueous solution or a water-containing solution thereof, a remaining component or a mixture of the remaining components or an aqueous solution or its solution
- Examples of such a method include gelation by mixing with a water-containing solution.
- ultrasonication may be used in addition to mechanical or manual stirring.
- mechanical stirring is particularly preferred.
- a magnetic stirrer, propeller stirrer, rotation / revolution mixer, disper, homogenizer, shaker, vortex mixer, ball mill, kneader, ultrasonic oscillator, etc. can be used.
- mixing by a rotation / revolution mixer is preferable.
- the temperature for mixing is a freezing point to a boiling point of the aqueous solution or aqueous dispersion, preferably -5 ° C to 50 ° C, more preferably 0 ° C to 30 ° C.
- the strength is weak and it is in the form of sol, but it gels when left to stand.
- the standing time is preferably 2 hours to 100 hours.
- the standing temperature is ⁇ 5 ° C. to 100 ° C., preferably 0 ° C. to 30 ° C.
- the container can be filled with the radiation dosimetry sol or gel into a radiation dosimeter, for example, a phantom.
- the container is not particularly limited as long as it transmits radiation and has solvent resistance and airtightness, and the material is preferably glass, acrylic resin, polyester, ethylene-vinyl alcohol copolymer, or the like. Further, after filling the container, it may be replaced with nitrogen gas or the like.
- the radiation dosimeter of the present invention has excellent sensitivity to radiation irradiation and has high linearity in the amount of increase in fluorescence intensity or the amount of increase in absorbance with respect to the absorbed dose, so that fluorescence intensity or absorbance can be measured.
- the apparatus and conditions used for analysis of the sample are as follows.
- X-ray irradiation device Industrial X-ray device (Radioflex 250 CG, RIGAKU)
- Irradiation conditions 250 kVp, 8 mA, 1 mm aluminum filter, and the dose rate is 1.72 Gy / min.
- the sample was placed and illuminated on a circumference of 18 cm ⁇ .
- Fluorescence intensity measurement apparatus Spectrofluorometer F-4500 (Hitachi High-Technologies Corporation)
- Absorbance measurement apparatus UV-visible photodiode array spectrophotometer MultiSpec-1500 (Shimadzu Corporation)
- Example 1 Production of a radiation dosimeter equipped with radiation dose measurement sol or gel as a measurement material of radiation dose]
- 2.5 g of Laponite XLG was added to 97.5 mL of ultrapure water and stirred to prepare a dispersion of 2.5 wt%.
- 5 mg of coumarin-3-carboxylic acid (CCA) as a fluorescent probe was placed in a 100 mL flask to prepare a 0.267 mM fluorescent probe aqueous solution. Thereafter, 37.5 mL of a fluorescent probe aqueous solution and 2.5 mL of ultrapure water are added to 60 mL of Laponite XLG dispersion, and the mixture is stirred until it becomes uniform.
- CCA coumarin-3-carboxylic acid
- the final concentrations of Laponite XLG and the fluorescent probe are 1.5 wt% and 0.
- a mixture of 100 ml of 1 mM was obtained.
- the resulting mixture was loaded into a spectrometry cell to obtain a sample for irradiation test.
- Comparative Example 1 Production of a radiation dosimeter equipped with gelatin as a measuring material for radiation dose 2.5 g of gelatin was added to 97.5 mL of ultrapure water, and the mixture was heated to about 50 ° C. to dissolve, and an aqueous gelatin solution of 2.5 wt% was prepared. Then, the procedure of Example 1 is repeated except that gelatin aqueous solution is used instead of the Laponite XLG dispersion, and the cell is allowed to stand overnight in a refrigerator after filling in a cell for spectrometry, gelatin at 0.1 mM CCA Samples for three types of irradiation tests were obtained with 5 wt%, 0.1 wt% and 0.01 wt%.
- Example 2 Irradiation Test
- Each sample obtained in Example 1 and Comparative Example 1 was irradiated with radiation (X-ray).
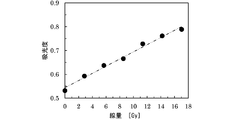
- the results are shown in FIG.
- FIG. 1 shows the dose dependency of the fluorescence intensity when the type of gelling agent and the concentration thereof are changed with respect to 0.1 mM coumarin-3-carboxylic acid.
- the samples using 0.1 wt% or 0.01 wt% gelatin were substantially liquid, and it was found that application of gelatin to a radiation dosimeter is difficult.
- silicate Liaponite XLG
- the sol or gel for radiation measurement of the present invention has excellent sensitivity to radiation irradiation and is high in the amount of increase in fluorescence intensity relative to the absorbed dose, as compared with gelatin widely used in conventional gel dosimeters. It is clear that it has linearity.
- Example 3 Production of a radiation dosimeter
- benzoic acid is used as the fluorescent probe in place of the coumarin-3-carboxylic acid used in Example 1
- final concentrations of Laponite XLG and the fluorescent probe are respectively 1.
- a mixture of 5 wt% and 0.1 mM in 100 mL was obtained.
- the resulting mixture was loaded into a spectrometry cell to obtain a sample for irradiation test.
- Example 4 Production of a radiation dosimeter
- terephthalic acid was used as the fluorescent probe in place of coumarin-3-carboxylic acid used in Example 1
- final concentrations of Laponite XLG and the fluorescent probe were 1.
- a mixture of 5 wt% and 0.1 mM in 100 mL was obtained.
- the resulting mixture was loaded into a spectrometry cell to obtain a sample for irradiation test.
- Example 5 Production of Radiation Dosimeter
- trimellitic acid was used as the fluorescent probe instead of the coumarin-3-carboxylic acid used in Example 1
- the final concentrations of Laponite XLG and the fluorescent probe were 1 each.
- a mixture of 5 wt% and 0.1 mM in 100 mL was obtained.
- the resulting mixture was loaded into a spectrometry cell to obtain a sample for irradiation test.
- Example 6 Production of a radiation dosimeter
- pyromellitic acid was used as the fluorescent probe instead of the coumarin-3-carboxylic acid used in Example 1
- the final concentrations of Laponite XLG and the fluorescent probe were respectively 1
- a mixture of 5 wt% and 0.1 mM in 100 mL was obtained.
- the resulting mixture was loaded into a spectrometry cell to obtain a sample for irradiation test.
- Example 7 Irradiation Test
- slit width excitation side 10 nm
- fluorescence side 10 nm
- photomultiplier voltage 700V.
- the excitation wavelength (Ex) and the peak wavelength (Em) of readout fluorescence are coumarin-3-carboxylic acid (Ex: 370 nm, Em: 448 nm), benzoic acid (Ex: 300 nm, Em: 409 nm), terephthalic acid (Ex) It was: 320 nm, Em: 425 nm), trimellitic acid (Ex: 310 nm, Em: 409 nm) and pyromellitic acid (Ex: 310 nm, Em: 433 nm). As shown in FIG.
- Example 8 Production of Radiation Dosimeter
- rhodamine 6G was used as the fluorescent dye in place of the coumarin-3-carboxylic acid used in Example 1
- final concentrations of Laponite XLG and the fluorescent dye were 1.
- a mixture of 5 wt% and 1 ⁇ M in 100 mL was obtained.
- the resulting mixture was loaded into a spectrometry cell to obtain a sample for irradiation test.
- Example 9 Production of Radiation Dosimeter
- coumarin-3-carboxylic acid used in Example 1, the procedure was carried out except using umbelliferone-3-carboxylic acid (7-hydroxycoumarin-3-carboxylic acid: 7OH-CCA) as a fluorescent dye.
- umbelliferone-3-carboxylic acid 7-hydroxycoumarin-3-carboxylic acid: 7OH-CCA
- the resulting mixture was loaded into a spectrometry cell to obtain a sample for irradiation test.
- Example 10 Manufacture of a radiation dosimeter
- umbelliferone-3-carboxylic acid was used as the fluorescent dye in place of the coumarin-3-carboxylic acid used in Example 1
- Laponite XLG and the fluorescent dye were used.
- a mixture of 100 mL final concentration of 1.5 wt% and 0.25 ⁇ M respectively was obtained.
- the resulting mixture was loaded into a spectrometry cell to obtain a sample for irradiation test.
- Example 11 Irradiation Test
- X-ray X-ray
- fluorescence intensity was evaluated by a spectrofluorimeter. The results are shown in FIG. FIG. 3 shows the dose dependency of the decrease in fluorescence intensity due to irradiation.
- the measurement conditions of the spectrofluorimeter are 1 ⁇ M Rhodamine 6G (Ex: 500 nm, Em: 561 nm, Slit width Excitation side: 2.5 nm, Fluorescence side: 5 nm, Photomal voltage: 700 V), 1 ⁇ M umbelliferone-3 -Carboxylic acid (Ex: 370 nm, Em: 446 nm, slit width excitation side: 2.5 nm, fluorescence side: 5 nm, photomars voltage: 700 V) and 0.25 ⁇ M umbelliferone 3-carboxylic acid (Ex: 370 nm, Em: The slit width at 446 nm, excitation side: 5 nm, fluorescence side: 5 nm, photo-mars voltage: 700 V).
- Both fluorescent dyes decreased in fluorescence intensity in proportion to the radiation dose.
- the measurement conditions of the spectrofluorometer are different, and when the initial fluorescence intensity is small, the slit width is taken large. Therefore, although the sensitivity characteristics of radiation dosimeters can not simply be compared, in the case of umbelliferone-3-carboxylic acid, it is thought that the decrease rate of the fluorescence intensity can be increased by decreasing the initial concentration. . That is, it is inferred that the decomposition amount of the fluorescent dye by the irradiation of radiation does not depend on the initial concentration of the fluorescent dye. It is also speculated that many fluorescent dyes are applicable to the radiation dosimeter of the present invention.
- Example 12 Production of a Radiation Dosimeter 1.5 g of Laponite XLG and 0.4 g of a 40% aqueous solution of sodium polyacrylate (molecular weight: 6,000) were added to 48.1 g of ultrapure water and stirred to prepare a 3.0 wt% Laponite XLG dispersion. On the other hand, 0.4 g of partially neutralized sodium polyacrylate (degree of neutralization 35 mol%) is added to 39.6 g of ultrapure water and stirred to obtain an aqueous solution of partially neutralized sodium polyacrylate having a solid content of 1.0 wt% Was produced.
- coumarin-3-carboxylic acid (CCA) was placed in a 100 mL flask to prepare a 1.0 mM fluorescent probe aqueous solution. Thereafter, 4.0 g of a fluorescent probe aqueous solution and 1.6 g of a 1.0 wt% sodium polyacrylate partially neutralized aqueous solution are added to 32.8 g of ultrapure water and stirred, and then 1.6 g of 3.0 wt% Laponite XLG dispersion liquid is added. Add and stir until uniform to obtain 40 mL of mixture. The resulting mixture was loaded into a spectrophotometer cell (1 ⁇ 1 ⁇ 4 cm, four-sided transparent) to obtain a sample for the irradiation test.
- CCA coumarin-3-carboxylic acid
- Example 13 Production of a Radiation Dosimeter After adding 4.0 g of the fluorescent probe aqueous solution prepared in Example 12 and 4.0 g of a 1.0 wt% sodium polyacrylate partially neutralized aqueous solution prepared in Example 12 to 28.0 g of ultrapure water and stirring, Example 4.0 g of the 3.0 wt% Laponite XLG dispersion prepared in 12 was added and stirred until uniform to obtain 40 mL of a mixture. The resulting mixture was loaded into a spectrophotometer cell (1 ⁇ 1 ⁇ 4 cm, four-sided transparent) to obtain a sample for the irradiation test.
- Example 14 Irradiation Test
- a spectrofluorimeter The results of the sample of Example 12 are shown in FIG. 4, and the results of the sample of Example 13 are shown in FIG.
- the measurement conditions of the spectrofluorimeter were: slit width excitation side: 10 nm, fluorescence side: 10 nm, photomultiplier voltage: 700V.
- the excitation wavelength (Ex) and the peak wavelength (Em) of readout fluorescence were Ex: 370 nm and Em: 446 nm, respectively.
- FIG. 1 FIG. 1
- the sol or gel for radiation measurement of the present invention containing a water-soluble organic polymer (C) having a water-soluble organic polymer (C) and a dispersant (D) of a silicate (B) is compared to gelatin widely used in conventional gel dosimeters.
- a water-soluble organic polymer (C) having a water-soluble organic polymer (C) and a dispersant (D) of a silicate (B) is compared to gelatin widely used in conventional gel dosimeters.
- Example 15 Manufacture of a radiation dosimeter Final concentration of Laponite XLG and fluorescent dye in the same manner as in Example 1 except that 2,5-diphenyloxazole is used as a fluorescent dye in place of coumarin-3-carboxylic acid used in Example 1. There were obtained 100 mL mixtures of 1.5 wt% and 0.5 ⁇ M respectively. The resulting mixture was loaded into a spectrometry cell to obtain a sample for irradiation test.
- Example 16 Irradiation Test
- the sample obtained in Example 15 was irradiated with X-rays, and the fluorescence intensity was evaluated by a spectrofluorimeter.
- the results are shown in FIG. FIG. 6 shows the dose dependency of the decrease in fluorescence intensity due to irradiation.
- the measurement conditions of the spectrofluorimeter were Ex: 310 nm, Em: 378 nm, slit width excitation side: 2.5 nm, fluorescence side: 5 nm, and photomultiplier voltage: 700V.
- the fluorescence intensity decreased in proportion to the absorbed dose.
- Example 17 Production of Radiation Dosimeter
- rhodamine 6G was used as the fluorescent dye in place of the coumarin-3-carboxylic acid used in Example 1
- final concentrations of Laponite XLG and the fluorescent dye were respectively 2.
- a mixture of 5 wt% and 1 ⁇ M in 100 mL was obtained.
- the resulting mixture was loaded into a spectrometry cell to obtain a sample for irradiation test.
- Example 18 Production of Radiation Dosimeter
- 7-diethylamino-4-methylcoumarin was used instead of coumarin-3-carboxylic acid used in Example 1
- final concentrations of Laponite XLG and a fluorescent probe were respectively different.
- a mixture of 2.5 wt% and 1 ⁇ M in 100 mL was obtained.
- the resulting mixture was loaded into a spectrometry cell to obtain a sample for irradiation test.
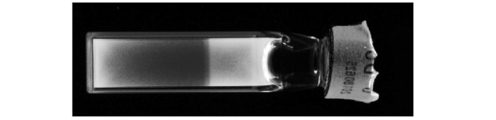
- Example 19 Diffusion Evaluation Test In the radiation dosimeter of the present invention, in order to confirm the diffusion state of the compound (A) -derived compound upon irradiation, the sample obtained in Example 17 one month after irradiation was obtained in Example 18 The samples obtained were photographed two days after irradiation. The results are shown in FIG. 7 ((a) in FIG. 7 is a sample one month after irradiation with radiation in Example 17, (b) a sample two days after irradiation with radiation in Example 18). The radiation dose for the sample obtained in Example 17 was 140 Gy, and the radiation dose for the sample obtained in Example 18 was 100 Gy. In all cases, the samples after irradiation were placed in a dark box and a 365 nm LED light was used.
- Example 20 Manufacture of a radiation dosimeter After adding 4.0 g of the fluorescent probe aqueous solution prepared in Example 12 and 6.0 g of a 1.0 wt% sodium polyacrylate partially neutralized aqueous solution prepared in Example 12 to 24.0 g of ultrapure water and stirring, Example 6.0 g of the 3.0 wt% Laponite XLG dispersion prepared in 12 was added and stirred until uniform to obtain 40 mL of a mixture. The resulting mixture was loaded into a spectrophotometer cell (1 ⁇ 1 ⁇ 4 cm, four-sided transparent) to obtain a sample for the irradiation test.
- Example 21 Manufacture of a radiation dosimeter
- a radiation dosimeter After adding 4.0 g of the fluorescent probe aqueous solution prepared in Example 12 and 8.0 g of the 1.0 wt% sodium polyacrylate partially neutralized aqueous solution prepared in Example 12 to 20.0 g of ultrapure water and stirring, Example 8.0 g of the 3.0 wt% Laponite XLG dispersion prepared in 12 was added and stirred until uniform to obtain 40 mL of a mixture. The resulting mixture was loaded into a spectrophotometer cell (1 ⁇ 1 ⁇ 4 cm, four-sided transparent) to obtain a sample for the irradiation test.
- Example 22 Irradiation Test Each sample obtained in Example 20 and Example 21 was irradiated with radiation (X-ray), and the fluorescence intensity was evaluated by a spectrofluorimeter. The results are shown in FIG. FIG. 8 shows the dose dependency of the fluorescence intensity when changing the concentration of the sodium polyacrylate partially neutralized to 15 wt% or 20 wt%. The value in the vicinity of the maximum wavelength of 446.8 nm of the fluorescence spectrum of the radiation dosimeter obtained in Example 20 and Example 21 was read, and the increase in fluorescence intensity due to irradiation was plotted. The results shown in FIG.
- the difference in each slope means the difference in sensitivity characteristics.
- the sol or gel for radiation measurement of the present invention to which sodium polyacrylate partially neutralized is added is irradiated compared to gelatin which is widely used in conventional gel dosimeters. It is apparent that the compound has excellent sensitivity to H and has high linearity in the amount of increase in fluorescence intensity with respect to the absorbed dose.
- Example 23 Manufacture of a radiation dosimeter equipped with a radiation dosimetry sol or gel as a measurement material of radiation dose
- dihydrorhodamine 123 hydrochloride manufactured by Fujifilm Wako Pure Chemical Industries, Ltd., hereinafter also referred to as DHR
- the final concentration of Laponite XLG and DHR was a mixture of 1.5 wt% and 0.1 mM.
- the resulting mixture was filled into 5 mL vials and a spectrometric cell, respectively, to obtain a sample for irradiation test.
- Example 24 Manufacture of a radiation dosimeter equipped with radiation dose measurement sol or gel as a measurement material of radiation dose]
- DHR dihydrorhodamine hydrochloride
- final concentrations of Laponite XLG and DHR were , A mixture of 2.5 wt% and 0.1 mM.
- the obtained mixture was filled in a cell for spectrometry and a container for 2D distribution analysis (100 mm ⁇ 100 mm ⁇ 5 mm) to obtain a sample for an irradiation test.
- Example 25 Irradiation Test
- Each sample obtained in Example 23 and Example 24 was irradiated with radiation (X-ray), and the fluorescence intensity was evaluated by a spectrofluorimeter.
- the results are shown in FIG. FIG. 9 shows the dose dependency of fluorescence intensity when the concentration of silicate (Laponite XLG) is changed to 1.5 wt% or 2.5 wt% using a fluorescent probe (DHR).
- DHR fluorescent probe
- the values in the vicinity of the maximum wavelength of 539 nm of the fluorescence spectra of the radiation dosimeters obtained in Example 23 and Example 24 were read, and the increase in fluorescence intensity due to irradiation was plotted.
- the sol or gel for radiation measurement of the present invention has excellent sensitivity to radiation irradiation and high linearity in the amount of increase in fluorescence intensity with respect to the absorbed dose. . Further, as shown in FIG. 9, it is apparent that the sol or gel for radiation measurement of the present invention can be used as a sol or gel for radiation measurement regardless of the concentration of the gelling agent.
- Example 26 Irradiation Test
- the sample filled in the container for 2D distribution analysis obtained in Example 24 was irradiated with radiation (X-ray), and the fluorescence intensity was evaluated by a fluorescent gel scanner (manufactured by Pacific Image Electronics, model number: Glite 900 BW).
- the results are shown in FIG. 10 and FIG. FIG. 10 is an image obtained from a fluorescent gel scanner after X-ray irradiation.
- FIG. 11 is a graph in which the average value of the fluorescence intensity for each irradiation area of the sample irradiated with X-rays is read by a fluorescent gel scanner, and the increase in the fluorescence intensity according to the irradiation dose is plotted.
- the sol or gel for radiation measurement of the present invention has excellent sensitivity to radiation also in a two-dimensional image, and has high linearity in the amount of increase in fluorescence intensity with respect to the absorbed dose. It is clear.
- Example 27 Diffusion evaluation test
- the sample filled in the cell for spectrometry obtained in Example 24 was taken 73 days after radiation irradiation did. The results are shown in FIG. The sample was irradiated to the upper half on the cap side with a radiation dose of 7 Gy. Moreover, imaging was performed using a fluorescent gel scanner. As shown in FIG. 12, for the sample of Example 24, the boundary line (contrast) between the irradiated area and the non-irradiated area by radiation irradiation is maintained after the irradiation, and the diffusion of the compound (A) is suppressed with time. It can be seen that the diffusion effect of the compound (A) can be ignored.
- Example 28 Irradiation Test (Reading by Spectrophotometer)
- the sample obtained in Example 23 was irradiated with radiation (X-ray), and the absorbance was evaluated by a spectrophotometer.
- the results are shown in FIG. In FIG. 13, the absorbance at a wavelength of 400 nm to 600 nm of the irradiated sample was measured with a spectrophotometer, the value near the maximum absorbance of 511 nm was read, and the increase in absorbance due to the radiation dose was plotted.
- the absorbance of the sol or gel for radiation measurement of the present invention increases in proportion to the radiation dose, and can also be quantified in light absorption measurement. That is, the sol or gel for radiation measurement of the present invention can also be used, for example, as a radiation dosimeter for an optical CT apparatus.
Landscapes
- Health & Medical Sciences (AREA)
- Physics & Mathematics (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Physics & Mathematics (AREA)
- High Energy & Nuclear Physics (AREA)
- Molecular Biology (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Organic Chemistry (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Pathology (AREA)
- Analytical Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Engineering & Computer Science (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Investigating Or Analysing Materials By The Use Of Chemical Reactions (AREA)
Abstract
【課題】 放射線線量測定ゾル又はゲル、及びそれを放射線線量の計測材料として備える放射線線量計の提供。 【解決手段】 水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)及びケイ酸塩(B)を含むことを特徴とする、放射線線量測定ゾル又はゲル。 水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)、ケイ酸塩(B)、有機酸塩構造又は有機酸アニオン構造を有する水溶性有機高分子(C)及びケイ酸塩(B)の分散剤(D)を含む、放射線線量測定ゾル又はゲル。 上記の放射線線量測定ゾル又はゲルを放射線線量の計測材料として備える放射線線量計。
Description
本発明は、放射線線量測定ゾル又はゲル、及びそれを放射線線量の計測材料として備える放射線線量計に関する。より詳しくは、本発明は、3次元線量分布の測定に用いられる放射線線量測定ゾル又はゲル、及びそれを放射線線量の計測材料として備える放射線線量計に関する。
ゲル線量計は放射線誘起の化学反応を利用した3次元線量計である。ゲル線量計に放射線を照射した後にゲル中に保持される反応生成物は核磁気共鳴画像診断装置(MRI)や光学的CT装置(OCT)などの3次元スキャナーにて読み取られ、線量分布へ換算される。ゲルの大部分は水であり、生体に近い組成を持つことから、特に放射線治療において計画される複雑な3次元線量分布の検証ツールとしての利用が期待される。
代表的な3次元線量分布の測定が可能なゲル線量計としては、フリッケゲル線量計やポリマーゲル線量計などが知られている。フリッケゲル線量計は、液体化学線量計として知られるフリッケ線量計の溶液(硫酸第一鉄を含む水溶液)をゲル化したものであり、放射線照射に伴う2価から3価への鉄の酸化反応(着色)が、吸収線量に比例して増加することを利用している。一方、ポリマーゲル線量計は、モノマーをゲル中に分散させたものであり、放射線照射すると線量に比例してポリマーが生成すること(重合反応)を利用している(非特許文献1)。
ゲル線量計の主な構成要素は、放射線感受性化合物、ゲル化剤及び水(溶媒)である。水はゲル線量計全体の7割から9割近くを占めるため、ゲル中の放射線誘起の化学反応を見てみると、水の放射線分解から始まる。この時に生じる水分解ラジカルが酸化反応や重合反応を引き起こす種となる。水分解ラジカルの生成濃度は10Gyの吸収線量に対して数μM程度しかなく、前述のゲル線量計では1つの水分解ラジカルから連鎖的な反応が進行することで感度が向上している。特に、数Gyからの検出が可能であるポリマーゲル線量計では、少なくとも、数マイクロ秒以内に終わる水分解ラジカルとの反応に対して、重合の連鎖反応は放射線照射後から約1日間進行する。そのため、安定した線量分布情報の読み取りをすぐに行うことができない。
そこで、近年、より取扱やすく、かつ高感度なゲル線量計として、蛍光プローブを利用した高感度なゲル線量計の開発が試みられている。蛍光プローブは蛍光分光光度計により数nMでも定量可能である。OCTの測定で用いる吸光度測定法がμMオーダーでの生成物の定量に用いられるので、単純に1000倍の高感度化が期待できる。実際に、蛍光プローブを用いた水溶液線量計では数ミリGyからの検出が可能であることが報告されている(非特許文献2)。
一方、蛍光測定法を用いるゲル線量計の開発では、重合反応後に蛍光物質を生成するradio-fluorogenic(RFG)ゲル線量計が報告されているものの、同じ重合反応を利用したポリマーゲル線量計と同様に放射線の線量率に依存することが報告されている(非特許文献3)。また、クマリン誘導体を利用した蛍光ゲル線量計が報告されている。クマリン誘導体は水の放射線分解により生じるOHラジカルとの反応後に強い蛍光物質を生成するので、クマリン誘導体を利用した蛍光ゲル線量計は水溶液線量計としては最も高感度な化学線量計として確立されているものの、ゼラチンなどの有機ゲルを含むものは、期待した高感度な結果が得られていない(非特許文献4)。同様に、ローダミンなどの蛍光物質の放射線による退色反応を利用したゲル線量計も報告されているが、数百Gyと高い線量が測定に必要とされる(非特許文献5)。
Watanabe Y, Warmington L, Gopishankar N: Three-dimensional radiation dosimetry using polymer gel and solid radiochromic polymer: From basics to clinical applications. World journal of radiology 9: 112-25, 2017
Matthews RW: Aqueous Chemical Dosimetry. International Journal of Applied Radiation and Isotopes 33: 1159-70, 1982
Yao T, 3D Radiation Dosimetry Using a Radio-Fluorogenic gel. Place Delft University of Technology: Delft University of Technology; 2017.(https://pure.tudelft.nl/portal/files/9767609/thesis.pdf#search=%27%E2%80%9DYao+T%2C+3D+Radiation+Dosimetry+Using+a+RadioFluorogenic+gel%E2%80%9D%27)
Sandwall PA, Spitz HB, Elson HR, et al.: Measuring the photon depth dose distribution produced by a medical linear accelerator in a water-equivalent radio-fluorogenic gel. Journal of Radioanalytical and Nuclear Chemistry 307: 2505-08, 2016
Benevides CA, Duarte de Menezes F, de Araujo RE: Evaluation of fluorescent dye degradation indirectly induced by x-ray ionizing radiation. Appl. Opt. 54: 6935-9, 2015
従来の蛍光プローブを用いた放射線線量計では、放射線照射に対する感度が低く、高感度特性が得られ難いという問題があった。
したがって、本発明は、放射線線量の計測材料として使用可能なゾル又はゲルであって、放射線照射に対する感度が良好な放射線線量測定ゾル又はゲルを提供するものである。
したがって、本発明は、放射線線量の計測材料として使用可能なゾル又はゲルであって、放射線照射に対する感度が良好な放射線線量測定ゾル又はゲルを提供するものである。
本発明者は、有機ゲル化剤(ゼラチンやアガロース等)が水分解ラジカルを捕捉することで、放射線感受性化合物と水分解ラジカルとの反応が妨げられることを前提に、有機ゲル化剤と異なり、水分解ラジカルとの反応性が低い無機ゲル化剤又は有機無機複合ゲル化剤を用いたところ、水の放射線分解生成物により、励起光による蛍光特性が変化する化合物と無機ゲル化剤又は有機無機複合ゲル化剤とを含むゾル又はゲルを放射線線量の計測材料に適用した放射線線量計は、放射線照射に対して極めて感度が高いことを見出し、本発明を完成させた。
すなわち、本発明は、第1観点として、水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)及びケイ酸塩(B)を含むことを特徴とする、放射線線量測定ゾル又はゲルに関する。
第2観点として、前記水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)がクマリン誘導体、芳香族カルボン酸誘導体、オキサゾール誘導体及びローダミン類からなる群より選ばれる1種又は2種以上である、第1観点に記載の放射線線量測定ゾル又はゲルに関する。
第3観点として、前記ケイ酸塩(B)がスメクタイト、ベントナイト、バーミキュライト及び雲母からなる群より選ばれる1種又は2種以上の水膨潤性ケイ酸塩粒子である、第1観点又は第2観点に記載の放射線線量測定ゾル又はゲルに関する。
第4観点として、有機酸塩構造又は有機酸アニオン構造を有する水溶性有機高分子(C)及びケイ酸塩(B)の分散剤(D)を更に含むことを特徴とする、第1観点乃至第3観点のいずれか1項に記載の放射線線量測定ゾル又はゲルに関する。
第5観点として、前記水溶性有機高分子(C)が完全中和又は部分中和ポリアクリル酸塩である、第4観点に記載の放射線線量測定ゾル又はゲルに関する。
第6観点として、前記分散剤(D)がオルトリン酸ナトリウム、ピロリン酸ナトリウム、トリポリリン酸ナトリウム、テトラリン酸ナトリウム、ヘキサメタリン酸ナトリウム、ポリリン酸ナトリウム、ポリ(メタ)アクリル酸ナトリウム、ポリ(メタ)アクリル酸アンモニウム、アクリル酸ナトリウム/マレイン酸ナトリウム共重合体、アクリル酸アンモニウム/マレイン酸アンモニウム共重合体、水酸化ナトリウム、ヒドロキシルアミン、炭酸ナトリウム、ケイ酸ナトリウム、ポリエチレングリコール、ポリプロピレングリコール、フミン酸ナトリウム及びリグニンスルホン酸ナトリウムからなる群から選ばれる1種又は2種以上である、第4観点又は第5観点に記載の放射線線量測定ゾル又はゲルに関する。
第7観点として、pH調整剤を更に含む、第1観点乃至第6観点のいずれか1項に記載の放射線線量測定ゾル又はゲルに関する。
第2観点として、前記水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)がクマリン誘導体、芳香族カルボン酸誘導体、オキサゾール誘導体及びローダミン類からなる群より選ばれる1種又は2種以上である、第1観点に記載の放射線線量測定ゾル又はゲルに関する。
第3観点として、前記ケイ酸塩(B)がスメクタイト、ベントナイト、バーミキュライト及び雲母からなる群より選ばれる1種又は2種以上の水膨潤性ケイ酸塩粒子である、第1観点又は第2観点に記載の放射線線量測定ゾル又はゲルに関する。
第4観点として、有機酸塩構造又は有機酸アニオン構造を有する水溶性有機高分子(C)及びケイ酸塩(B)の分散剤(D)を更に含むことを特徴とする、第1観点乃至第3観点のいずれか1項に記載の放射線線量測定ゾル又はゲルに関する。
第5観点として、前記水溶性有機高分子(C)が完全中和又は部分中和ポリアクリル酸塩である、第4観点に記載の放射線線量測定ゾル又はゲルに関する。
第6観点として、前記分散剤(D)がオルトリン酸ナトリウム、ピロリン酸ナトリウム、トリポリリン酸ナトリウム、テトラリン酸ナトリウム、ヘキサメタリン酸ナトリウム、ポリリン酸ナトリウム、ポリ(メタ)アクリル酸ナトリウム、ポリ(メタ)アクリル酸アンモニウム、アクリル酸ナトリウム/マレイン酸ナトリウム共重合体、アクリル酸アンモニウム/マレイン酸アンモニウム共重合体、水酸化ナトリウム、ヒドロキシルアミン、炭酸ナトリウム、ケイ酸ナトリウム、ポリエチレングリコール、ポリプロピレングリコール、フミン酸ナトリウム及びリグニンスルホン酸ナトリウムからなる群から選ばれる1種又は2種以上である、第4観点又は第5観点に記載の放射線線量測定ゾル又はゲルに関する。
第7観点として、pH調整剤を更に含む、第1観点乃至第6観点のいずれか1項に記載の放射線線量測定ゾル又はゲルに関する。
第8観点として、第1観点乃至第7観点のいずれか1項に記載の放射線線量測定ゾル又はゲルを放射線線量の計測材料として備える放射線線量計に関する。
第9観点として、前記放射線線量計が、光学CT装置用の放射線線量計である、第8観点に記載の放射線線量計に関する。
第9観点として、前記放射線線量計が、光学CT装置用の放射線線量計である、第8観点に記載の放射線線量計に関する。
本発明の放射線線量測定ゾル又はゲルは、従来の放射線線量計で広く使用されているゼラチンやアガロースなどと比べて、放射線照射に対して優れた感度を有する。
また、本発明の放射線線量測定ゾル又はゲルは、工業的に入手容易な原料を用いて、加熱を必要とすることなく、室温で混合するだけで製造することができるので、一定品質を有し、またインジェクタブルなゾル又はゲルとして、放射線線量計における放射線線量の計測材料に使用することができる。
[放射線線量測定ゾル又はゲル]
本発明の放射線線量測定ゾル又はゲルの成分として、水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)及びケイ酸塩(B)、又は水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)、ケイ酸塩(B)、有機酸塩構造又は有機酸アニオン構造を有する水溶性有機高分子(C)及びケイ酸塩(B)の分散剤(D)が挙げられるが、上記成分の他に、本発明の所期の効果を損なわない範囲で、必要に応じて、他の成分を任意に配合してもよい。
水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)とは、水の放射線分解生成物により、励起光による蛍光を発光する化合物、又は水の放射線分解生成物により、励起光による蛍光が退色する化合物、である。
本発明の放射線線量測定ゾル又はゲルの成分として、水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)及びケイ酸塩(B)、又は水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)、ケイ酸塩(B)、有機酸塩構造又は有機酸アニオン構造を有する水溶性有機高分子(C)及びケイ酸塩(B)の分散剤(D)が挙げられるが、上記成分の他に、本発明の所期の効果を損なわない範囲で、必要に応じて、他の成分を任意に配合してもよい。
水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)とは、水の放射線分解生成物により、励起光による蛍光を発光する化合物、又は水の放射線分解生成物により、励起光による蛍光が退色する化合物、である。
<成分(A):水の放射線分解生成物により、励起光による蛍光特性が変化する化合物>
本発明の放射線線量測定ゾル又はゲルは水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)を含み、これにより、本発明の放射線線量測定ゾル又はゲルを放射線線量の計測材料として備える放射線線量計は蛍光ゾル又はゲル線量計として機能する。
本発明の放射線線量測定ゾル又はゲルは水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)を含み、これにより、本発明の放射線線量測定ゾル又はゲルを放射線線量の計測材料として備える放射線線量計は蛍光ゾル又はゲル線量計として機能する。
水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)は、水に放射線を照射し、それにより生じる、ヒドロキシラジカル及びスーパーオキシドラジカル等の活性酸素種との反応によって、励起光による蛍光特性が変化する化合物であって、水の放射線分解生成物により、励起光による蛍光を発光する化合物及び水の放射線分解生成物により、励起光による蛍光が退色する化合物等が挙げられる。
水の放射線分解生成物により、励起光による蛍光を発光する化合物として、水の放射線分解生成物により、励起光による蛍光を発光する蛍光プローブを使用することができ、また水の放射線分解生成物により、励起光による蛍光が退色する化合物として、蛍光色素を使用することができる。
水の放射線分解生成物により、励起光による蛍光を発光する化合物として、水の放射線分解生成物により、励起光による蛍光を発光する蛍光プローブを使用することができ、また水の放射線分解生成物により、励起光による蛍光が退色する化合物として、蛍光色素を使用することができる。
そのような水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)としては、クマリン誘導体、芳香族カルボン酸誘導体、オキサゾール誘導体、ローダミン類、アクリジン類、クメストロール類、フルオレセイン類、ピレン類、スチルベン類、レゾルフィン類、エオシン類、キサンタン類、ナフタルイミド類及びポリメチン類等が挙げられ、その中でもクマリン誘導体、芳香族カルボン酸誘導体、オキサゾール誘導体及びローダミン類が好ましい。
本発明では、水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)は1種単独で、又は2種以上を組み合わせて使用することができる。
本発明では、水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)は1種単独で、又は2種以上を組み合わせて使用することができる。
クマリン誘導体としては特に限定されないが、クマリン、クマリン-3-カルボン酸、3-アミノクマリン、ウンベリフェロン(7-ヒドロキシクマリン)及びウンベリフェロン-3-カルボン酸(7-ヒドロキシクマリン-3-カルボン酸)等が挙げられる。
芳香族カルボン酸誘導体としては特に限定されないが、安息香酸、テレフタル酸、ピロメリット酸、トリメリット酸、3-(4-ヒドロキシフェニル)プロピオン酸、1-ナフタレン酸及び2-ナフタレン酸等が挙げられる。
オキサゾール誘導体としては特に限定されないが、2,5-ジフェニルオキサゾール及び2-(1-ナフチル)-5-フェニルオキサゾール等が挙げられる。
ローダミン類としては特に限定されないが、ローダミンB、ローダミン6G及びローダミン123等が挙げられる。
また、本発明では、上記例示の化合物以外に、水の放射線分解生成物により、励起光による蛍光特性が変化する化合物として広く知られる以下の化合物も用いられうる。なお以下の化合物には、上記のクマリン誘導体、芳香族カルボン酸誘導体、オキサゾール誘導体及びローダミン類に分類される化合物も含まれているが、このことは該化合物が上記のクマリン誘導体等に該当しないことを意味するものではない:2-ヒドロキシビフェニル、フルラム、フルオレセインアミン、アントラセン、1,2-ビス(2-アミノフェノキシ)エタン-N,N,N’,N’-四酢酸四ナトリウム塩、フェナントレン、アントラセン-9-カルボン酸、フタルジアルデヒド、2’,7’-ジクロロフルオレセインジアセテート、1-エチルナフタレン、9-フルオレニルメチルカルバゼート、トリフェニレン、ナフタレン、フェナントリジン、ジヒドロフルオレセインジアセテート、p-ターフェニル、3-(4-ヒドロキシフェニル)プロピオン酸、1,2-ビス(2-アミノフェノキシ)エタン-N,N,N’,N’-四酢酸、1-アルギニン-4-メチル-7-クマリニルアミド塩酸、トリオキサレン、p-クォーターフェニル、5(6)-カルボキシフルオレセインジアセテートN-スクシンイミジルエステル、フルオレセインジアセテート、5(6)-カルボキシフルオレセインジアセテート、5(6)-カルボキシ-2’,7’-ジクロロフルオレセインジアセテートn-スクシンイミジルエステル、2-エチルナフタレン、4-ニトロフェニルリン酸二ナトリウム塩、5-メトキシソラレン、3,3-ジメチル-2-(4-ジメチルアミノスチリル)-1-オクタデシルインドリウムパークロレート、4-メチルウンベリフェリルパルミテート、4-メチルウンベリフェリルエナンテート、4-メチルウンベリフェリルオレアート、4-メチルウンベリフェリルアセテート、4-メチルウンベリフェリルブチレート、4-メチルウンベリフェリル-n-アセチル-アルファ-d-ノイラミン酸ナトリウム塩二水和物、N,N’-ビス(サリチリデン)エチレンジアミン、4-メチルウンベリフェリル-ベータ-d-ガラクトピラノシド、4-メチルウンベリフェリル-ベータ-d-グルクロニド三水和物、4-メチルウンベリフェリル-ベータ-d-グルコピラノシド、4-メチルウンベリフェリル-n-アセチル-ベータ-d-グルコサミニド二水和物、4-メチルウンベリフェリル-アルファ-d-グルコピラノシド、4-メチルウンベリフェリル-アルファ-d-ガラクトピラノシド、8-ノナノイルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、6-(p-トルイジノ)-2-ナフタレンスルホン酸、6-(p-トルイジノ)-2-ナフタレンスルホン酸ナトリウム塩、4-メチルウンベリフェリルホスフェート、4-メチルウンベリフェリルホスフェート二ナトリウム塩、2-ナフトール、7-ヒドロキシ-4-メチル-2(1H)-キノロン、塩キニーネ二水和物、カルセインブルー、N-スクシンイミジル-7-ヒドロキシ-4-クマリニルアセテート、塩酸4-メチルウンベリフェリル-4-グアニジノベンゾエート一水和物、7-エトキシクマリン、4-ヘプタデシルウンベリフェロン、グルタリル-1-フェニルアラニン-4-メチル-7-クマリニルアミド、4-(トリフルオロメチル)ウンベリフェリル-ベータ-d-グルコピラノシド、4-(トリフルオロメチル)ウンベリフェリル-ベータ-d-ガラクトピラノシド、ウンベリフェロン、1-アラニン-4-メチル-7-クマリニルアミドトリフルオロアセテート、3,4-ジメチルウンベリフェロン、塩酸1-ロイシン-4-メチル-7-クマリニルアミド、N-スクシンイミジル-7-ヒドロキシ-4-メチル-3-クマリニルアセテート、ホタルルシフェリンナトリウム塩、ホタルルシフェリン、トランス,トランス-1,4-ジフェニル-1,3-ブタジエン、4-ベンジルアミノ-7-ニトロベンゾフラザン、4-ブロモメチル-7-メトキシクマリン、1,4-ジアセトキシ-2,3-ジシアノベンゼン、7-メトキシ-4-メチルクマリン、7-エトキシ-4-メチルクマリン、3-カルボキシウンベリフェリル-ベータ-d-ガラクトピラノシド、1-ナフトール、1,5-ジアミノナフタレン、4-メチルウンベリフェリル-N,N’-ジアセチル-ベータ-d-キトビオシド一水和物、3-カルボキシウンベリフェリル-ベータ-d-ガラクトピラノシドN-スクシンイミジルエステル、3-(2-ベンゾチアゾリル)ウンベリフェロン、3-フェニルウンベリフェリルホスフェートヘミピリジン塩、7-エトキシ-4-(トリフルオロメチル)クマリン、
2-(4,4,4-トリフルオロアセトアセチル)ナフタレン、7-メトキシ-4-(トリフルオロメチル)クマリン、4-メチルウンベリフェリルサルフェートカリウム塩、ダンシルカダベリン、9,10-ビス-N-(2-ジメチルアミノエチル)メチルアミノメチルアントラセンビス-塩化亜鉛錯体、11-(5-ジメチルアミノナフタレン-1-スルホニルアミノ)ウンデカン酸、ソラレン、ダンシルヒドラジン、N-(ヨードアセトアミノエチル)-1-ナフチルアミン-5-スルホン酸、4-クロロ-7-ニトロベンゾフラザン、ダンシル-1-チロシル-1-バリル-グリシントリフルオロアセテート、3-(ダンシルアミノ)フェニルボロン酸、ビスベンズイミド、3-フェニルウンベリフェロン、4-メチルウンベリフェリル-N,N’,N’’-トリアセチル-ベータ-キトトリオシド、ビスベンズイミド、7-メトキシクマリン、1-メチルピレン、2-4-(ヨードアセトアミド)フェニル-6-メチルベンゾチアゾール、キサントキシン、6,7-ジエトキシ-4-メチルクマリン、2,3-ジアミノナフタレン、1-ピレン酪酸、4,4’-ジイソチオシアネートスチルベン-2,2’-ジスルホン酸二ナトリウム塩、6-(1-ピレニル)ヘキサン酸、1-ピレンドデカン酸、1-ピレンデカン酸、7-ヒドロキシクマリン-3-カルボン酸、ピレン-1-カルボン酸、4-ジメチルアミノ-1-ナフチルイソチオシアネート、硫酸キニーネ二水和物、6-メトキシ-1-(3-スルホプロピル)キノリニウム一水和物、ピレン-1-スルホン酸ナトリウム塩、ピレン-1-カルボキシアルデヒド、3-ブロモメチル-7-メトキシ-1,4-ベンゾオキサジン-2-オン、キニーネ無水物、2-アミノ-5-(6-カルボキシインドール-2-イル)フェノール-N,N,O-四酢酸カリウム塩、4-(6-メチル-2-ベンゾチアゾリル)フェニルイソシアネート、4-メチルウンベリフェリル-アルファ-d-マンノピラノシド、3-(2-ベンゾオキサゾリル)ウンベリフェリルオクタノエート、2-(2-アミノ-5-メチルフェノキシ)メチル-6-メトキシ-8-アミノキノリン-N,N,N’,N’-四酢酸テトラキス(アセトキシメチルエステル)、コレステリルピレン-l-カルボキシレート、1,6-ジフェニル-1,3,5-ヘキサトリエン-4’-プロピオン酸、6,7-ジメトキシ-4-(トリフルオロメチル)クマリン、3-(2-ベンゾオキサゾリル)ウンベリフェリルアセテート、n-ヘキサデシルピレン-1-スルホンアミド、1,6-ジフェニル-1,3,5-ヘキサトリエン、7-アミノ-4-メチル-3-クマリニル酢酸、ピレン、フタロシアニン、7-アミノ-4-メチルクマリン、4-ブロモメチル-6,7-ジメトキシクマリン、ジヒドロエチジウム、1-(エトキシカルボニルメチル)-6-メトキシキノリニウムブロミド、1,6-ジフェニル-1,3,5-ヘキサトリエン-4’-トリメチルアンモニウムトシレート、5-ジメチルアミノナフタレン-1-スルホニルフルオリド、1,8-ジアミノナフタレン、8-アミノナフタレン-1,3,6-トリスルホン酸二ナトリウム塩、1,4-ビス(5-フェニル-2-オキサゾリル)ベンゼン、N-スクシンイミジル-7-メトキシクマリン-3-カルボキシレート、7-ヒドロキシ-n-オクタデシルクマリン-3-カルボキサミド、4-(4-ジメチルアミノスチリル)-1-オクタデシルピリジニウムパークロレート、4-クロロ-7-スルホベンゾフラザンアンモニウム塩、3-オクタデカノイルウンベリフェロン、7-メトキシクマリン-3-カルボン酸、7-ヒドロキシ-4-メチル-3-クマリニル酢酸、6,7-ジヒドロキシ-4-メチルクマリン、アントラセン-9-カルボニルシアニド、ヒドロキシスチルバミジン-ビス-メタンスルホネート、N,N-ジメチル-6-プロピオニル-2-ナフチルアミン、フラ-2、N,N-ジメチル-6-ドデカノイル-2-ナフチルアミン、6,8-ジアセトオキシピレン-1,3-ジスルホン酸二ナトリウム塩、2-(4-ジメチルアミノスチリル)-3-オクタデシルベンゾチアゾリウムパークロレート、7-ヒドロキシ-4-クマリニル酢酸、6,7-ジヒドロキシ-4-(トリフルオロメチル)クマリン、8-ヘキサデカノイルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、8-ドデカノイルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、コレステリルアントラセン-9-カルボキシレート、5,6-ベンゾクマリン-3-カルボニルクロリド、3-アセチルウンベリフェロン、5-ジメチルアミノナフタレン-1-スルホニルクロリド、8-アニリノナフタレン-1-スルホン酸アンモニウム塩、4-メチルウンベリフェロン(ベータ)、11-(ピレン-1-スルホニルアミノ)ウンデカン酸、3,3’-ジエチルチアカルボシアニンヨージド、モノクロロビマン、トランス-4’-ヒドラジノ-2-スチルバゾールジヒドロクロリド、3,6,8-トリス(ジメチルアミノスルホニル)-1-ピレニルホスフェートピリジン塩、1-(4-メトキシフェニル)-6-フェニルヘキサトリエン、9,10-アントラセンジイル-ビス-(メチレン)-ジマロン酸、12-(アントラセン-9-カルボニルオキシ)ステアリン酸、8-オレオイルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、8-オクタノイルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、8-ブチリルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、8-ブチリルオキシ-N,N,N’,N’,N’’,N’’-ヘキサメチルピレン-1,3,6-トリスルホンアミド、12-オキソ-12-(1-ピレニル)ドデカン酸、4-(トリフルオロメチル)ウンベリフェロン、6,7-ジヒドロキシ-4-クマリニル酢酸、3,3’-ジオクチルチアカルボシアニンヨージド、7-オクタデシルオキシ-3-3-(3-スルホプロピル)-2-ベンゾチアゾリリオクマリン、3-(2-ベンゾチアゾリル)-7-オクタデシルオキシクマリン、3-メチル-2-7-オクタデシルオキシ-3-クマリニルベンゾチアゾリウムメトサルフェート、8-テトラデシルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、ジブロモビマン、8-アセトキシ-N,N,N’,N’,N’’,N’’-ヘキサメチルピレン-1,3,6-トリスルホンアミド、n-(7-ジメチルアミノ-4-メチル-3-クマリニル)マレイミド、7-(ジエチルアミノ)クマリン-3,4-ジカルボン酸、モノブロモビマン、N-(l-ロイシル)-2-アミノアクリドン、N-(s-ベンジル-l-システイニル)-2-アミノアクリドン、n-(n-スクシニル-1-フェニルアラニル)-2-アミノアクリドン、n-(n-グルタリル-1-フェニルアラニル)-2-アミノアクリドン、n-(n-トシル-l-フェニルアラニル)-2-アミノアクリドン、ベンゾフルオランテン、ペリレン、オクタデシル-7-ヒドロキシクマリン-3-カルボキシレート、8-ヘキサデシルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、8-ドデシルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、8-ヒドロキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、7-アセトキシ-1-メチルキノリニウムヨージド、8-オクタデシルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、8-デシルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、8-メトキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、1-(4-ニトロフェニル)-6-フェニルヘキサトリエン、6,8-ジヒドロキシピレン-1,3-ジスルホン酸二ナトリウム塩、7-ヒドロキシ-1-メチルキノリニウムヨージド、プロトポルフィリン、プロトポルフィリン-ジメチルエステル、7-(ジエチルアミノ)クマリン-3-カルボン酸、N-スクシンイミジル-3-(2-ベンゾチアゾリル)ウンベリフェロン-4-カルボキシレート、3-(5-クロロ-2-ベンゾオキサゾリル)-4-シアノウンベリフェリルホスフェートピリジン塩、チオフラビン、10-(3-スルホプロピル)アクリジニウムベタイン、10-(3-スルホプロピル)アクリジニウムベタイン、3-(5-クロロ-2-ベンゾオキサゾリル)-4-シアノウンベリフェロン、N-スクシンイミジル-7-ヒドロキシクマリン-3-カルボキシレート、7-(ジエチルアミノ)クマリン-3-カルボヒドラジド、8-(ベータ-d-ガラクトピラノシルオキシ)-N,N,N’,N’,N’’,N’’-ヘキサメチルピレン-1,3,6-トリスルホンアミド、アクチノマイシン、2-(4-ジメチルアミノスチリル)-3-メチルベンゾアゾリウムパークロレート、8-アミノピレン-1,3,6-トリスルホン酸三ナトリウム塩、2-アミノアクリドン、フェナジン、ルシファーイエロージカリウム塩、ルシファーイエロージリチウム塩、N-スクシンイミジル-7-(ジエチルアミノ)クマリン-3-カルボキシレート、7-(ジエチルアミノ)クマリン-3-カルボニルアジド、8-イソチオシアネートピレン-1,3,6-トリスルホン酸三ナトリウム塩、9-(2-カルボキシ-2-シアンビニル)-ジュロリジン-N-スクシンイミジルエステル、9-(2,2-ジシアンビニル)-ジュロリジン、9-(2-カルボキシ-2-シアンビニル)-ジュロリジン、4-ニトロ-4’-(オクタデシルアミノ)スチルベン、4-(ジオクタデシルアミノ)-4’-ニトロスチルベン、プロフラビンヘミサルフェート二水和物、
3-(2-ベンゾチアゾリル)-7-(ジエチルアミノ)クマリン-4-カルボン酸、ベンゾニンヒドリン一水和物、8-ヒドロキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、N,N’-ジメチル-9,9’-ビアクリジニウムジニトレート、N,N’-ジメチル-9,9’-ビアクリジニウムジニトレート、トリス(4,7-ジフェニルフェナントロリン)ルテニウム(ii)ビス-錯体、3-(2-ベンゾチアゾリル)-7-(ジエチルアミノ)クマリン、2-(4-ジメチルアミノスチリル)-1-メチルキノリニウムヨージド、11-(7-ニトロベンゾフラザン-4-イルアミノ)ウンデカン酸、6-(7-ニトロベンゾフラザン-4-イルアミノ)ヘキサン酸、12-(7-ニトロベンゾフラザン-4-イルアミノ)ドデカン酸、レゾルフィン-ベータ-d-ガラクトピラノシド、レゾルフィンホスフェートピリジン塩、レゾルフィン-ベータ-d-グルコピラノシド、4-フルオロ-7-ニトロベンゾフラザン、1,3’-ジエチル-4,2’-キノリルチアシアニンヨージド、塩酸ドキソルビシン、4-(4-ジペンタデシルアミノスチリル)-1-メチルピリジニウムヨージド、2-(4-ジエチルアミノスチリル)-1-メチルピリジニウムヨージド、ジミジウムブロミド、エチジウムブロミド溶液、エチジウムブロミド、フルオレセイン-5(6)-カルボキサミドカプロン酸、2’,7’-ビス(2-カルボキシエチル)-5(6)-カルボキシフルオレセイン、プロピジウムヨージド、2-(4-ジメチルアミノスチリル)-1-メチルピリジニウムヨージド、3,3’-ジヘプチルオキサカルボシアニンヨージド、3,3’-ジエチルオキサカルボシアニンヨージド、3,3’-ジプロピルオキサカルボシアニンヨージド、3,3’-ジペンチルオキサカルボシアニンヨージド、3,3’-ジオクタデシルオキサカルボシアニンパークロレート、3,3’-ジヘキシルオキサカルボシアニンヨージド、3,3’-ジブチルオキサカルボシアニンヨージド、4-(4-ジエチルアミノスチリル)-1-メチルピリジニウムヨージド、フルオレセインイソチオシアネートデキストラン、5(6)-カルボキシフルオレセイン、フルオレセインナトリウム、フルオレセイン(遊離酸)、フルオレセイン-5(6)-カルボキサミドカプロン酸n-スクシンイミジルエステル、5-カルボキシ-フルオレセインn-スクシンイミジルエステル、5-カルボキシ-フルオレセイン、6-カルボキシフルオレセイン、6-カルボキシ-フルオレセインN-スクシンイミジルエステル、フルオレセイン-5-チオセミカルバジド、5-(ヨードアセトアミド)フルオレセイン、エチジウムホモダイマー、10-ドデシルアクリジンオレンジブロミド、10-オクタデシルアクリジンオレンジブロミド、カルセイン二ナトリウム塩、10-ノニルアクリジンオレンジブロミド、フルオレセイン酢酸第二水銀、ローダミン110クロリド、N’-オクタデシルフルオレセイン-5-チオ尿素、フルオ3、5(6)-カルボキシ-2’,7’-ジクロロフルオレセイン、3-(2-ベンゾオキサゾリル)-4-シアノウンベリフェロン、9-(2-カルボキシフェニル)-6-ジメチルアミノ-3-キサンテノンサルフェート、ローダミン16パークロレート、ローダミン640パークロレート、ローダミン590クロリド、エオシン、ローダミン5-3(4)-(アミノカルボニル)-4(3)-カルボキシベンゼンスルホニルフルオリド、ローダミンB 5-3(4)-(アミノカルボニル)-4(3)-カルボキシベンゼンスルホニルフルオリド、エオシンイエローイッシュ、5,10,15,20-テトラキス(1-メチル-4-ピリジニオ)ポルフィリンテトラ(トルエン-4-スルホネート)、エオシン5-イソチオシアネート、ローダミン19パークロレート、ローダミン6G、ローダミン6Gテトラフルオロボレート、ローダミン800、3,3’-ジオクタデシルチアカルボシアニンパークロレート、レゾルフィンブチレート、レゾルフィンアセテート、5(6)-カルボキシテトラメチルローダミン、テトラメチルローダミンBイソチオシアネート、ローダミンBイソチオシアネート、6-カルボキシ-テトラメチルローダミンN-スクシンイミジルエステル、5-カルボキシ-テトラメチルローダミンN-スクシンイミジルエステル、6-カルボキシ-テトラメチルローダミン、5-カルボキシ-テトラメチルローダミン、n-オクタデカノイル-ナイルブルー、ストレプトアビジン-B-フィコエリトリン、ビオチン-B-フィコエリトリン、1,1’-ジオクチル-3,3,3’,3’-テトラメチルインドカルボシアニンヨージド、3,3’-ジヘキシルチアカルボシアニンヨージド、1,1’-ジヘキシル-3,3,3’,3’-テトラメチルインドカルボシアニンヨージド、ベンガルローズb、テトラメチルローダミンメチルエステルパークロレート、1,1’-ジプロピル-3,3,3’,3’-テトラメチルインドカルボシアニンヨージド、1,1’-ジペンチル-3,3,3’,3’-テトラメチルインドカルボシアニンヨージド、1,1’-ジブチル-3,3,3’,3’-テトラメチルインドカルボシアニンヨージド、テトラメチルローダミンエチルエステルパークロレート、2-(4-ジメチルアミノスチリル)-1-オクタデシルピリジニウムパークロレート、1,1’-ジオクタデシル-3,3,3’,3’-テトラメチルインドカルボシアニンパークロレート、
ローダミンB、ローダミンBオクタデシルエステルパークロレート、メロシアニン540、3,3’-ジプロピルチアカルボシアニンヨージド、スルホローダミンb5-酸フルオリド、3,3’-ジペンチルチアカルボシアニンヨージド、1,1’-ジエチル-3,3,3’,3’-テトラメチルインドカルボシアニンヨージド、3,3’-ジブチルチアカルボシアニンヨージド、スルホローダミンB 2-酸フルオリド、3,3’-ジヘプチルチアカルボシアニンヨージド、スルホローダミンB酸クロリド、スルホローダミンBモノナトリウム塩、ローダミン101、5(6)-カルボキシ-x-ローダミン、スルホローダミンQ 5-酸フルオリド、6-カルボキシ-X-ローダミン-N-スクシンイミジルエステル、5-カルボキシ-x-ローダミン-n-スクシンイミジルエステル、5-カルボキシ-X-ローダミン(5-ROX)、6-カルボキシ-X-ローダミン(6-Rox)、5(6)-カルボキシ-X-ローダミンN-スクシンイミジルエステル、3,3’-ジエチルオキサジカルボシアニンヨージド、スルホローダミンQ 2-酸フルオリド、スルホローダミン101酸クロリド、スルホローダミン101遊離酸、ナフトフルオレセイン、ビオチン-c-フィコシアニン、クレジルバイオレットパークロレート、5(6)-カルボキシナフトフルオレセインN-スクシンイミジルエステル、オクタエチルポルフィン、アズールA、フルオレセントレッド646、1,1’-ジオクタデシル-3,3,3’,3’-テトラメチルインドジカルボシアニンパークロレート、メソテトラフェニルポルフィリン、アズールB、3,3’-ジプロピルチアジカルボシアニンヨージド、3,3’-ジエチルチアジカルボシアニンヨージド、4,5-ベンゾ-5’-(n-スクシンイミジル-オキシカルボニル-メチル)-1’-エチル-3,3,3’,3’-テトラメチル-1-(4-スルホブチル)インドジカルボシアニン、4,5-ベンゾ-5’-(インドアセトアミノメチル)-1’,3,3,3’,3’-ペンタメチル-l-(4-スルホブチル)インドジカルボシアニン、1,1’-ビス(4-スルホブチル)-11-(4-イソチオシアネートフェニルチオ)-3,3,3’,3’-テトラメチル-10,12-トリメチレンインドトリカルボシアニンモノナトリウム塩、3,3’-ジエチルオキサトリカルボシアニンヨージド、3,3’-ジエチルチアトリカルボシアニンヨージド、1,1’-ジエチル-4,4’-カルボシアニンヨージド、2,5-ビス(4-ビフェニリル)-1,3,4-オキサジアゾール、無水1-ナフチル酢酸、5-ジメチルアミノナフタレン-1-スルホンアミド、無水ジフェニルマレイン酸、カルバゾール-9-カルボニルクロリド、n-(3-フルオランチル)マレイミド、n-4-(2-ベンズイミダゾリル)フェニルマレイミド、6-ヒドロキシ-2-ナフチルジスルフィド、2-(2-アミノ-5-メチルフェノキシ)メチル-6-メトキシ-8-アミノキノリン-N,N,N’,N’-テトラ酢酸テトラカリウム塩、1,2-フェニレンジアミンジヒドロクロリド、1,2-フェニレンジアミン、2-(4-マレイミドフェニル)-6-メチルベンゾチアゾール、メソ-1,2-ビス(4-メトキシフェニル)エチレンジアミン、N-(l-ピレニル)マレイミド、1,2-ジアセチルベンゼン、4’,6-ジアミジノ-2-フェニルインドールジヒドロクロリド、4-メチルウンベリフェリル-アルファ-1-フコピラノシド、イソニコチンヒドラジド、4-ヒドロキシベンズヒドラジド、9-クロロメチル-アントラセン、4-メチルウンベリフェリル-ベータ-d-ラクトシド、ジフェニルボリン無水物、4,5-メチレンジオキシ-1,2-フェニレンジアミンジヒドロクロリド、マロンアミド、Z-グリシル-l-プロリン-4-メチル-7-クマリニルアミド、1,3-シクロヘキサンジオン、8-エトキシ-N,N,N’,N’,N’’,N’’-ヘキサメチルピレン-1,3,6-トリスルホンアミド、4-(トリフルオロメチル)ウンベリフェリルホスフェート二ナトリウム塩、4-(トリフルオロメチル)ウンベリフェリルエナンテート、4-(トリフルオロメチル)ウンベリフェリルオレアート、7-フルオロベンゾフラザン-4-スルホン酸アンモニウム塩、4-(トリフルオロメチル)ウンベリフェリルブチレート、2-メトキシ-2,4-ジフェニル-3(2H)-フラノン、4-(トリフルオロメチル)ウンベリフェリルアセテート、8-メトキシ-N,N,N’,N’,N’’,N’’-ヘキサメチルピレン-1,3,6-トリスルホンアミド、8-アセトオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、4-ヒドラジノ-7-ニトロベンゾフラザン、5(6)-カルボキシ-2’,7’-ジクロロフルオレセインジアセテート、4’,5’-ビスN,N-ジ(カルボキシメチル)アミノメチルフルオレセイン、2’,7’-ビス(2-カルボキシエチル)-5(6)-カルボキシフルオレセインテトラキス(アセトメチル)エステル、フルオレセインジラウレート、フルオレセインジブチレート、フルオレセインジアセテート-5-イソチオシアネート、5(6)-カルボキシエオシンジアセテート、5-マレイミド-エオシン、ナフトフルオレセインジアセテート、5(6)-カルボキシナフトフルオレセインジアセテートN-スクシンイミジルエステル、4-ジメチルアミノ-4’-ニトロスチルベン、1,4-ビス(2-メチルスチリル)ベンゼン、1,4-ビス(4-メチル-5-フェニル-2-オキサゾリル)ベンゼン、2-(4-ビフェニリル)-5-フェニル-1,3,4-オキサジアゾール、2-(4-tert-ブチルフェニル)-5-(4-ビフェニリル)-1,3,4-オキサジアゾール、2-(p-トリル)ベンゾオキサゾール、2-(4-ビフェニリル)-6-フェニルベンゾオキサゾール、4-ヒドロキシクマリン、2,5-ジフェニル-1,3,4-オキサジアゾール、1,4-ビス-2-(5-フェニルオキサゾリル)ベンゼン、1,4-ビス-2-(4-メチル-5-フェニルオキサゾリル)ベンゼン、オーラミンO、サフラニン、ベーシックブルー12、クリスタルバイオレット、3,6-アクリジンジアミン及び7-ジエチルアミノ-4-メチルクマリン。
2-(4,4,4-トリフルオロアセトアセチル)ナフタレン、7-メトキシ-4-(トリフルオロメチル)クマリン、4-メチルウンベリフェリルサルフェートカリウム塩、ダンシルカダベリン、9,10-ビス-N-(2-ジメチルアミノエチル)メチルアミノメチルアントラセンビス-塩化亜鉛錯体、11-(5-ジメチルアミノナフタレン-1-スルホニルアミノ)ウンデカン酸、ソラレン、ダンシルヒドラジン、N-(ヨードアセトアミノエチル)-1-ナフチルアミン-5-スルホン酸、4-クロロ-7-ニトロベンゾフラザン、ダンシル-1-チロシル-1-バリル-グリシントリフルオロアセテート、3-(ダンシルアミノ)フェニルボロン酸、ビスベンズイミド、3-フェニルウンベリフェロン、4-メチルウンベリフェリル-N,N’,N’’-トリアセチル-ベータ-キトトリオシド、ビスベンズイミド、7-メトキシクマリン、1-メチルピレン、2-4-(ヨードアセトアミド)フェニル-6-メチルベンゾチアゾール、キサントキシン、6,7-ジエトキシ-4-メチルクマリン、2,3-ジアミノナフタレン、1-ピレン酪酸、4,4’-ジイソチオシアネートスチルベン-2,2’-ジスルホン酸二ナトリウム塩、6-(1-ピレニル)ヘキサン酸、1-ピレンドデカン酸、1-ピレンデカン酸、7-ヒドロキシクマリン-3-カルボン酸、ピレン-1-カルボン酸、4-ジメチルアミノ-1-ナフチルイソチオシアネート、硫酸キニーネ二水和物、6-メトキシ-1-(3-スルホプロピル)キノリニウム一水和物、ピレン-1-スルホン酸ナトリウム塩、ピレン-1-カルボキシアルデヒド、3-ブロモメチル-7-メトキシ-1,4-ベンゾオキサジン-2-オン、キニーネ無水物、2-アミノ-5-(6-カルボキシインドール-2-イル)フェノール-N,N,O-四酢酸カリウム塩、4-(6-メチル-2-ベンゾチアゾリル)フェニルイソシアネート、4-メチルウンベリフェリル-アルファ-d-マンノピラノシド、3-(2-ベンゾオキサゾリル)ウンベリフェリルオクタノエート、2-(2-アミノ-5-メチルフェノキシ)メチル-6-メトキシ-8-アミノキノリン-N,N,N’,N’-四酢酸テトラキス(アセトキシメチルエステル)、コレステリルピレン-l-カルボキシレート、1,6-ジフェニル-1,3,5-ヘキサトリエン-4’-プロピオン酸、6,7-ジメトキシ-4-(トリフルオロメチル)クマリン、3-(2-ベンゾオキサゾリル)ウンベリフェリルアセテート、n-ヘキサデシルピレン-1-スルホンアミド、1,6-ジフェニル-1,3,5-ヘキサトリエン、7-アミノ-4-メチル-3-クマリニル酢酸、ピレン、フタロシアニン、7-アミノ-4-メチルクマリン、4-ブロモメチル-6,7-ジメトキシクマリン、ジヒドロエチジウム、1-(エトキシカルボニルメチル)-6-メトキシキノリニウムブロミド、1,6-ジフェニル-1,3,5-ヘキサトリエン-4’-トリメチルアンモニウムトシレート、5-ジメチルアミノナフタレン-1-スルホニルフルオリド、1,8-ジアミノナフタレン、8-アミノナフタレン-1,3,6-トリスルホン酸二ナトリウム塩、1,4-ビス(5-フェニル-2-オキサゾリル)ベンゼン、N-スクシンイミジル-7-メトキシクマリン-3-カルボキシレート、7-ヒドロキシ-n-オクタデシルクマリン-3-カルボキサミド、4-(4-ジメチルアミノスチリル)-1-オクタデシルピリジニウムパークロレート、4-クロロ-7-スルホベンゾフラザンアンモニウム塩、3-オクタデカノイルウンベリフェロン、7-メトキシクマリン-3-カルボン酸、7-ヒドロキシ-4-メチル-3-クマリニル酢酸、6,7-ジヒドロキシ-4-メチルクマリン、アントラセン-9-カルボニルシアニド、ヒドロキシスチルバミジン-ビス-メタンスルホネート、N,N-ジメチル-6-プロピオニル-2-ナフチルアミン、フラ-2、N,N-ジメチル-6-ドデカノイル-2-ナフチルアミン、6,8-ジアセトオキシピレン-1,3-ジスルホン酸二ナトリウム塩、2-(4-ジメチルアミノスチリル)-3-オクタデシルベンゾチアゾリウムパークロレート、7-ヒドロキシ-4-クマリニル酢酸、6,7-ジヒドロキシ-4-(トリフルオロメチル)クマリン、8-ヘキサデカノイルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、8-ドデカノイルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、コレステリルアントラセン-9-カルボキシレート、5,6-ベンゾクマリン-3-カルボニルクロリド、3-アセチルウンベリフェロン、5-ジメチルアミノナフタレン-1-スルホニルクロリド、8-アニリノナフタレン-1-スルホン酸アンモニウム塩、4-メチルウンベリフェロン(ベータ)、11-(ピレン-1-スルホニルアミノ)ウンデカン酸、3,3’-ジエチルチアカルボシアニンヨージド、モノクロロビマン、トランス-4’-ヒドラジノ-2-スチルバゾールジヒドロクロリド、3,6,8-トリス(ジメチルアミノスルホニル)-1-ピレニルホスフェートピリジン塩、1-(4-メトキシフェニル)-6-フェニルヘキサトリエン、9,10-アントラセンジイル-ビス-(メチレン)-ジマロン酸、12-(アントラセン-9-カルボニルオキシ)ステアリン酸、8-オレオイルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、8-オクタノイルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、8-ブチリルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、8-ブチリルオキシ-N,N,N’,N’,N’’,N’’-ヘキサメチルピレン-1,3,6-トリスルホンアミド、12-オキソ-12-(1-ピレニル)ドデカン酸、4-(トリフルオロメチル)ウンベリフェロン、6,7-ジヒドロキシ-4-クマリニル酢酸、3,3’-ジオクチルチアカルボシアニンヨージド、7-オクタデシルオキシ-3-3-(3-スルホプロピル)-2-ベンゾチアゾリリオクマリン、3-(2-ベンゾチアゾリル)-7-オクタデシルオキシクマリン、3-メチル-2-7-オクタデシルオキシ-3-クマリニルベンゾチアゾリウムメトサルフェート、8-テトラデシルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、ジブロモビマン、8-アセトキシ-N,N,N’,N’,N’’,N’’-ヘキサメチルピレン-1,3,6-トリスルホンアミド、n-(7-ジメチルアミノ-4-メチル-3-クマリニル)マレイミド、7-(ジエチルアミノ)クマリン-3,4-ジカルボン酸、モノブロモビマン、N-(l-ロイシル)-2-アミノアクリドン、N-(s-ベンジル-l-システイニル)-2-アミノアクリドン、n-(n-スクシニル-1-フェニルアラニル)-2-アミノアクリドン、n-(n-グルタリル-1-フェニルアラニル)-2-アミノアクリドン、n-(n-トシル-l-フェニルアラニル)-2-アミノアクリドン、ベンゾフルオランテン、ペリレン、オクタデシル-7-ヒドロキシクマリン-3-カルボキシレート、8-ヘキサデシルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、8-ドデシルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、8-ヒドロキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、7-アセトキシ-1-メチルキノリニウムヨージド、8-オクタデシルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、8-デシルオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、8-メトキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、1-(4-ニトロフェニル)-6-フェニルヘキサトリエン、6,8-ジヒドロキシピレン-1,3-ジスルホン酸二ナトリウム塩、7-ヒドロキシ-1-メチルキノリニウムヨージド、プロトポルフィリン、プロトポルフィリン-ジメチルエステル、7-(ジエチルアミノ)クマリン-3-カルボン酸、N-スクシンイミジル-3-(2-ベンゾチアゾリル)ウンベリフェロン-4-カルボキシレート、3-(5-クロロ-2-ベンゾオキサゾリル)-4-シアノウンベリフェリルホスフェートピリジン塩、チオフラビン、10-(3-スルホプロピル)アクリジニウムベタイン、10-(3-スルホプロピル)アクリジニウムベタイン、3-(5-クロロ-2-ベンゾオキサゾリル)-4-シアノウンベリフェロン、N-スクシンイミジル-7-ヒドロキシクマリン-3-カルボキシレート、7-(ジエチルアミノ)クマリン-3-カルボヒドラジド、8-(ベータ-d-ガラクトピラノシルオキシ)-N,N,N’,N’,N’’,N’’-ヘキサメチルピレン-1,3,6-トリスルホンアミド、アクチノマイシン、2-(4-ジメチルアミノスチリル)-3-メチルベンゾアゾリウムパークロレート、8-アミノピレン-1,3,6-トリスルホン酸三ナトリウム塩、2-アミノアクリドン、フェナジン、ルシファーイエロージカリウム塩、ルシファーイエロージリチウム塩、N-スクシンイミジル-7-(ジエチルアミノ)クマリン-3-カルボキシレート、7-(ジエチルアミノ)クマリン-3-カルボニルアジド、8-イソチオシアネートピレン-1,3,6-トリスルホン酸三ナトリウム塩、9-(2-カルボキシ-2-シアンビニル)-ジュロリジン-N-スクシンイミジルエステル、9-(2,2-ジシアンビニル)-ジュロリジン、9-(2-カルボキシ-2-シアンビニル)-ジュロリジン、4-ニトロ-4’-(オクタデシルアミノ)スチルベン、4-(ジオクタデシルアミノ)-4’-ニトロスチルベン、プロフラビンヘミサルフェート二水和物、
3-(2-ベンゾチアゾリル)-7-(ジエチルアミノ)クマリン-4-カルボン酸、ベンゾニンヒドリン一水和物、8-ヒドロキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、N,N’-ジメチル-9,9’-ビアクリジニウムジニトレート、N,N’-ジメチル-9,9’-ビアクリジニウムジニトレート、トリス(4,7-ジフェニルフェナントロリン)ルテニウム(ii)ビス-錯体、3-(2-ベンゾチアゾリル)-7-(ジエチルアミノ)クマリン、2-(4-ジメチルアミノスチリル)-1-メチルキノリニウムヨージド、11-(7-ニトロベンゾフラザン-4-イルアミノ)ウンデカン酸、6-(7-ニトロベンゾフラザン-4-イルアミノ)ヘキサン酸、12-(7-ニトロベンゾフラザン-4-イルアミノ)ドデカン酸、レゾルフィン-ベータ-d-ガラクトピラノシド、レゾルフィンホスフェートピリジン塩、レゾルフィン-ベータ-d-グルコピラノシド、4-フルオロ-7-ニトロベンゾフラザン、1,3’-ジエチル-4,2’-キノリルチアシアニンヨージド、塩酸ドキソルビシン、4-(4-ジペンタデシルアミノスチリル)-1-メチルピリジニウムヨージド、2-(4-ジエチルアミノスチリル)-1-メチルピリジニウムヨージド、ジミジウムブロミド、エチジウムブロミド溶液、エチジウムブロミド、フルオレセイン-5(6)-カルボキサミドカプロン酸、2’,7’-ビス(2-カルボキシエチル)-5(6)-カルボキシフルオレセイン、プロピジウムヨージド、2-(4-ジメチルアミノスチリル)-1-メチルピリジニウムヨージド、3,3’-ジヘプチルオキサカルボシアニンヨージド、3,3’-ジエチルオキサカルボシアニンヨージド、3,3’-ジプロピルオキサカルボシアニンヨージド、3,3’-ジペンチルオキサカルボシアニンヨージド、3,3’-ジオクタデシルオキサカルボシアニンパークロレート、3,3’-ジヘキシルオキサカルボシアニンヨージド、3,3’-ジブチルオキサカルボシアニンヨージド、4-(4-ジエチルアミノスチリル)-1-メチルピリジニウムヨージド、フルオレセインイソチオシアネートデキストラン、5(6)-カルボキシフルオレセイン、フルオレセインナトリウム、フルオレセイン(遊離酸)、フルオレセイン-5(6)-カルボキサミドカプロン酸n-スクシンイミジルエステル、5-カルボキシ-フルオレセインn-スクシンイミジルエステル、5-カルボキシ-フルオレセイン、6-カルボキシフルオレセイン、6-カルボキシ-フルオレセインN-スクシンイミジルエステル、フルオレセイン-5-チオセミカルバジド、5-(ヨードアセトアミド)フルオレセイン、エチジウムホモダイマー、10-ドデシルアクリジンオレンジブロミド、10-オクタデシルアクリジンオレンジブロミド、カルセイン二ナトリウム塩、10-ノニルアクリジンオレンジブロミド、フルオレセイン酢酸第二水銀、ローダミン110クロリド、N’-オクタデシルフルオレセイン-5-チオ尿素、フルオ3、5(6)-カルボキシ-2’,7’-ジクロロフルオレセイン、3-(2-ベンゾオキサゾリル)-4-シアノウンベリフェロン、9-(2-カルボキシフェニル)-6-ジメチルアミノ-3-キサンテノンサルフェート、ローダミン16パークロレート、ローダミン640パークロレート、ローダミン590クロリド、エオシン、ローダミン5-3(4)-(アミノカルボニル)-4(3)-カルボキシベンゼンスルホニルフルオリド、ローダミンB 5-3(4)-(アミノカルボニル)-4(3)-カルボキシベンゼンスルホニルフルオリド、エオシンイエローイッシュ、5,10,15,20-テトラキス(1-メチル-4-ピリジニオ)ポルフィリンテトラ(トルエン-4-スルホネート)、エオシン5-イソチオシアネート、ローダミン19パークロレート、ローダミン6G、ローダミン6Gテトラフルオロボレート、ローダミン800、3,3’-ジオクタデシルチアカルボシアニンパークロレート、レゾルフィンブチレート、レゾルフィンアセテート、5(6)-カルボキシテトラメチルローダミン、テトラメチルローダミンBイソチオシアネート、ローダミンBイソチオシアネート、6-カルボキシ-テトラメチルローダミンN-スクシンイミジルエステル、5-カルボキシ-テトラメチルローダミンN-スクシンイミジルエステル、6-カルボキシ-テトラメチルローダミン、5-カルボキシ-テトラメチルローダミン、n-オクタデカノイル-ナイルブルー、ストレプトアビジン-B-フィコエリトリン、ビオチン-B-フィコエリトリン、1,1’-ジオクチル-3,3,3’,3’-テトラメチルインドカルボシアニンヨージド、3,3’-ジヘキシルチアカルボシアニンヨージド、1,1’-ジヘキシル-3,3,3’,3’-テトラメチルインドカルボシアニンヨージド、ベンガルローズb、テトラメチルローダミンメチルエステルパークロレート、1,1’-ジプロピル-3,3,3’,3’-テトラメチルインドカルボシアニンヨージド、1,1’-ジペンチル-3,3,3’,3’-テトラメチルインドカルボシアニンヨージド、1,1’-ジブチル-3,3,3’,3’-テトラメチルインドカルボシアニンヨージド、テトラメチルローダミンエチルエステルパークロレート、2-(4-ジメチルアミノスチリル)-1-オクタデシルピリジニウムパークロレート、1,1’-ジオクタデシル-3,3,3’,3’-テトラメチルインドカルボシアニンパークロレート、
ローダミンB、ローダミンBオクタデシルエステルパークロレート、メロシアニン540、3,3’-ジプロピルチアカルボシアニンヨージド、スルホローダミンb5-酸フルオリド、3,3’-ジペンチルチアカルボシアニンヨージド、1,1’-ジエチル-3,3,3’,3’-テトラメチルインドカルボシアニンヨージド、3,3’-ジブチルチアカルボシアニンヨージド、スルホローダミンB 2-酸フルオリド、3,3’-ジヘプチルチアカルボシアニンヨージド、スルホローダミンB酸クロリド、スルホローダミンBモノナトリウム塩、ローダミン101、5(6)-カルボキシ-x-ローダミン、スルホローダミンQ 5-酸フルオリド、6-カルボキシ-X-ローダミン-N-スクシンイミジルエステル、5-カルボキシ-x-ローダミン-n-スクシンイミジルエステル、5-カルボキシ-X-ローダミン(5-ROX)、6-カルボキシ-X-ローダミン(6-Rox)、5(6)-カルボキシ-X-ローダミンN-スクシンイミジルエステル、3,3’-ジエチルオキサジカルボシアニンヨージド、スルホローダミンQ 2-酸フルオリド、スルホローダミン101酸クロリド、スルホローダミン101遊離酸、ナフトフルオレセイン、ビオチン-c-フィコシアニン、クレジルバイオレットパークロレート、5(6)-カルボキシナフトフルオレセインN-スクシンイミジルエステル、オクタエチルポルフィン、アズールA、フルオレセントレッド646、1,1’-ジオクタデシル-3,3,3’,3’-テトラメチルインドジカルボシアニンパークロレート、メソテトラフェニルポルフィリン、アズールB、3,3’-ジプロピルチアジカルボシアニンヨージド、3,3’-ジエチルチアジカルボシアニンヨージド、4,5-ベンゾ-5’-(n-スクシンイミジル-オキシカルボニル-メチル)-1’-エチル-3,3,3’,3’-テトラメチル-1-(4-スルホブチル)インドジカルボシアニン、4,5-ベンゾ-5’-(インドアセトアミノメチル)-1’,3,3,3’,3’-ペンタメチル-l-(4-スルホブチル)インドジカルボシアニン、1,1’-ビス(4-スルホブチル)-11-(4-イソチオシアネートフェニルチオ)-3,3,3’,3’-テトラメチル-10,12-トリメチレンインドトリカルボシアニンモノナトリウム塩、3,3’-ジエチルオキサトリカルボシアニンヨージド、3,3’-ジエチルチアトリカルボシアニンヨージド、1,1’-ジエチル-4,4’-カルボシアニンヨージド、2,5-ビス(4-ビフェニリル)-1,3,4-オキサジアゾール、無水1-ナフチル酢酸、5-ジメチルアミノナフタレン-1-スルホンアミド、無水ジフェニルマレイン酸、カルバゾール-9-カルボニルクロリド、n-(3-フルオランチル)マレイミド、n-4-(2-ベンズイミダゾリル)フェニルマレイミド、6-ヒドロキシ-2-ナフチルジスルフィド、2-(2-アミノ-5-メチルフェノキシ)メチル-6-メトキシ-8-アミノキノリン-N,N,N’,N’-テトラ酢酸テトラカリウム塩、1,2-フェニレンジアミンジヒドロクロリド、1,2-フェニレンジアミン、2-(4-マレイミドフェニル)-6-メチルベンゾチアゾール、メソ-1,2-ビス(4-メトキシフェニル)エチレンジアミン、N-(l-ピレニル)マレイミド、1,2-ジアセチルベンゼン、4’,6-ジアミジノ-2-フェニルインドールジヒドロクロリド、4-メチルウンベリフェリル-アルファ-1-フコピラノシド、イソニコチンヒドラジド、4-ヒドロキシベンズヒドラジド、9-クロロメチル-アントラセン、4-メチルウンベリフェリル-ベータ-d-ラクトシド、ジフェニルボリン無水物、4,5-メチレンジオキシ-1,2-フェニレンジアミンジヒドロクロリド、マロンアミド、Z-グリシル-l-プロリン-4-メチル-7-クマリニルアミド、1,3-シクロヘキサンジオン、8-エトキシ-N,N,N’,N’,N’’,N’’-ヘキサメチルピレン-1,3,6-トリスルホンアミド、4-(トリフルオロメチル)ウンベリフェリルホスフェート二ナトリウム塩、4-(トリフルオロメチル)ウンベリフェリルエナンテート、4-(トリフルオロメチル)ウンベリフェリルオレアート、7-フルオロベンゾフラザン-4-スルホン酸アンモニウム塩、4-(トリフルオロメチル)ウンベリフェリルブチレート、2-メトキシ-2,4-ジフェニル-3(2H)-フラノン、4-(トリフルオロメチル)ウンベリフェリルアセテート、8-メトキシ-N,N,N’,N’,N’’,N’’-ヘキサメチルピレン-1,3,6-トリスルホンアミド、8-アセトオキシピレン-1,3,6-トリスルホン酸三ナトリウム塩、4-ヒドラジノ-7-ニトロベンゾフラザン、5(6)-カルボキシ-2’,7’-ジクロロフルオレセインジアセテート、4’,5’-ビスN,N-ジ(カルボキシメチル)アミノメチルフルオレセイン、2’,7’-ビス(2-カルボキシエチル)-5(6)-カルボキシフルオレセインテトラキス(アセトメチル)エステル、フルオレセインジラウレート、フルオレセインジブチレート、フルオレセインジアセテート-5-イソチオシアネート、5(6)-カルボキシエオシンジアセテート、5-マレイミド-エオシン、ナフトフルオレセインジアセテート、5(6)-カルボキシナフトフルオレセインジアセテートN-スクシンイミジルエステル、4-ジメチルアミノ-4’-ニトロスチルベン、1,4-ビス(2-メチルスチリル)ベンゼン、1,4-ビス(4-メチル-5-フェニル-2-オキサゾリル)ベンゼン、2-(4-ビフェニリル)-5-フェニル-1,3,4-オキサジアゾール、2-(4-tert-ブチルフェニル)-5-(4-ビフェニリル)-1,3,4-オキサジアゾール、2-(p-トリル)ベンゾオキサゾール、2-(4-ビフェニリル)-6-フェニルベンゾオキサゾール、4-ヒドロキシクマリン、2,5-ジフェニル-1,3,4-オキサジアゾール、1,4-ビス-2-(5-フェニルオキサゾリル)ベンゼン、1,4-ビス-2-(4-メチル-5-フェニルオキサゾリル)ベンゼン、オーラミンO、サフラニン、ベーシックブルー12、クリスタルバイオレット、3,6-アクリジンジアミン及び7-ジエチルアミノ-4-メチルクマリン。
水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)の含有量は、0.1μM乃至1000μMであり、好ましくは水の放射線分解生成物により、励起光による蛍光が退色する化合物では0.1μM乃至5μMであり、水の放射線分解生成物により、励起光による蛍光を発光する化合物では50μM乃至500μMである。
<成分(B):ケイ酸塩>
ケイ酸塩(B)としては、例えば、スメクタイト、ベントナイト、バーミキュライト及び雲母等の水膨潤性ケイ酸塩粒子が挙げられ、水又は含水液体を分散媒としたコロイドを形成するものが好ましい。
なお、スメクタイトとは、モンモリロナイト、バイデライト、ヘクトライト、サポナイト及びスチブンサイト等の膨潤性を有する粘土鉱物の総称である。
本発明では、ケイ酸塩(B)は1種単独で、又は2種以上を組み合わせて使用することができる。
ケイ酸塩(B)としては、例えば、スメクタイト、ベントナイト、バーミキュライト及び雲母等の水膨潤性ケイ酸塩粒子が挙げられ、水又は含水液体を分散媒としたコロイドを形成するものが好ましい。
なお、スメクタイトとは、モンモリロナイト、バイデライト、ヘクトライト、サポナイト及びスチブンサイト等の膨潤性を有する粘土鉱物の総称である。
本発明では、ケイ酸塩(B)は1種単独で、又は2種以上を組み合わせて使用することができる。
ケイ酸塩粒子の一次粒子の形状としては、円盤状、板状、球状、粒状、立方状、針状、棒状及び無定形等が挙げられ、例えば直径5nm乃至1000nmの円盤状又は板状のものが好ましい。
ケイ酸塩の好ましい具体的としては、層状ケイ酸塩が挙げられ、市販品として容易に入手可能な例として、ロックウッド・アディティブズ社製のラポナイトXLG(合成ヘクトライト)、XLS(合成ヘクトライト、分散剤としてピロリン酸ナトリウム含有)、XL21(ナトリウム・マグネシウム・フルオロシリケート)、RD(合成ヘクトライト)、RDS(合成ヘクトライト、分散剤として無機ポリリン酸塩含有)、及びS482(合成ヘクトライト、分散剤含有);コープケミカル株式会社製のルーセンタイトSWN(合成スメクタイト)及びSWF(合成スメクタイト)、ミクロマイカ(合成雲母)、及びソマシフ(合成雲母);クニミネ工業株式会社製のクニピア(モンモリロナイト)、スメクトンSA(合成サポナイト);株式会社ホージュン製のベンゲル(天然ベントナイト精製品)等が挙げられる。
ケイ酸塩(B)の含有量は、放射線線量測定ゾル又はゲル100質量%中に0.01質量%乃至20質量%であり、好ましくは0.1質量%乃至10質量%である。
<成分(C):有機酸塩構造又は有機酸アニオン構造を有する水溶性有機高分子>
有機酸塩構造又は有機酸アニオン構造を有する水溶性有機高分子(C)としては、有機高分子の側鎖として、カルボキシル基、スルホニル基及びホスホニル基等の有機酸基の塩構造又は有機酸アニオン構造を有し、水に自由に溶解する高分子等が挙げられる。
有機酸塩構造又は有機酸アニオン構造を有する水溶性有機高分子(C)としては、有機高分子の側鎖として、カルボキシル基、スルホニル基及びホスホニル基等の有機酸基の塩構造又は有機酸アニオン構造を有し、水に自由に溶解する高分子等が挙げられる。
有機酸基の塩構造を有するものとしては、上記の有機酸基の塩(ナトリウム塩、アンモニウム塩、カリウム塩及びリチウム塩等)等が挙げられる。
また、有機酸アニオン構造を有するものとしては、上記の有機酸基の塩からカチオンが解離した構造を有するもの等が挙げられる。
また、有機酸アニオン構造を有するものとしては、上記の有機酸基の塩からカチオンが解離した構造を有するもの等が挙げられる。
そのような水溶性有機高分子としては、例えば、カルボキシル基を有するものとして、ポリ(メタ)アクリル酸塩、カルボキシビニルポリマーの塩、カルボキシメチルセルロースの塩;スルホニル基を有するものとして、ポリスチレンスルホン酸塩;ホスホニル基を有するものとして、ポリビニルホスホン酸塩等が挙げられる。
なお、本発明では、(メタ)アクリル酸とは、アクリル酸とメタクリル酸の両方を意味する。
なお、本発明では、(メタ)アクリル酸とは、アクリル酸とメタクリル酸の両方を意味する。
水溶性有機高分子(C)は分岐及び化学架橋構造を持たない直鎖型構造が好ましく、また水溶性有機高分子(C)は有機酸塩構造のみからなる完全中和物若しくは有機酸塩構造と有機酸構造とが混在する部分中和物又は完全中和物と部分中和物との混合物のいずれも使用できる。
水溶性有機高分子(C)の重量平均分子量は、ゲル浸透クロマトグラフィー(GPC)によるポリエチレングリコール換算で、好ましくは100万以上1000万以下であり、より好ましくは250万以上500万以下である。
水溶性有機高分子(C)としては、完全中和又は部分中和ポリアクリル酸塩が好ましく、完全中和又は部分中和の直鎖型ポリアクリル酸塩がより好ましく、重量平均分子量100万以上1000万以下の完全中和又は部分中和の直鎖型ポリアクリル酸ナトリウムが特に好ましく、重量平均分子量250万以上500万以下の完全中和又は部分中和の直鎖型ポリアクリル酸ナトリウムが特により好ましい。部分中和の中和度としては10%乃至90%であり、好ましくは30%乃至80%である。
水溶性有機高分子(C)の含有量は、放射線線量測定ゾル又はゲル100質量%中に0.01質量%乃至20質量%であり、好ましくは0.03質量%乃至10質量%である。
<成分(D):ケイ酸塩(B)の分散剤>
ケイ酸塩(B)の分散剤(D)として、ケイ酸塩の分散性の向上や、層状ケイ酸塩を層剥離させる目的で使用される分散剤又は解膠剤を使用することができる。例えば、リン酸塩系分散剤、カルボン酸塩系分散剤、アルカリとして作用するもの及び有機解膠剤を使用することができる。
ケイ酸塩(B)の分散剤(D)として、ケイ酸塩の分散性の向上や、層状ケイ酸塩を層剥離させる目的で使用される分散剤又は解膠剤を使用することができる。例えば、リン酸塩系分散剤、カルボン酸塩系分散剤、アルカリとして作用するもの及び有機解膠剤を使用することができる。
例えば、リン酸塩系分散剤として、オルトリン酸ナトリウム、ピロリン酸ナトリウム、トリポリリン酸ナトリウム、テトラリン酸ナトリウム、ヘキサメタリン酸ナトリウム、ポリリン酸ナトリウム、エチドロン酸ナトリウム;カルボン酸塩系分散剤として、ポリ(メタ)アクリル酸ナトリウム、ポリ(メタ)アクリル酸アンモニウム、アクリル酸ナトリウム/マレイン酸ナトリウム共重合体、アクリル酸アンモニウム/マレイン酸アンモニウム共重合体;アルカリとして作用するものとして、水酸化ナトリウム、ヒドロキシルアミン;多価カチオンと反応し不溶性塩又は錯塩を形成するものとして、炭酸ナトリウム、ケイ酸ナトリウム;有機解膠剤として、ポリエチレングリコール、ポリプロピレングリコール、フミン酸ナトリウム、リグニン、スルホン酸ナトリウム等が挙げられる。
好ましくは、リン酸塩系分散剤としてピロリン酸ナトリウム、エチドロン酸ナトリウム、カルボン酸塩系分散剤としてポリ(メタ)アクリル酸ナトリウム、有機解膠剤としてポリエチレングリコール(PEG900等)である。
これらの中でも、ポリ(メタ)アクリル酸ナトリウムがより好ましく、重量平均分子量1000以上2万以下の低重合ポリアクリル酸ナトリウムが特に好ましい。
好ましくは、リン酸塩系分散剤としてピロリン酸ナトリウム、エチドロン酸ナトリウム、カルボン酸塩系分散剤としてポリ(メタ)アクリル酸ナトリウム、有機解膠剤としてポリエチレングリコール(PEG900等)である。
これらの中でも、ポリ(メタ)アクリル酸ナトリウムがより好ましく、重量平均分子量1000以上2万以下の低重合ポリアクリル酸ナトリウムが特に好ましい。
低重合ポリアクリル酸ナトリウムはケイ酸塩粒子と相互作用して粒子表面にカルボキシアニオン由来の負電荷を生じさせ、電荷の反発によりケイ酸塩を分散させる等の機構により分散剤として作用することが知られている。
分散剤(D)の含有量は、放射線線量測定ゾル又はゲル100質量%中に0.001質量%乃至20質量%であり、好ましくは0.01質量%乃至10質量%である。
なお、本発明では、分散剤を含有するケイ酸塩を使用する場合は、分散剤をさらに添加しても、添加しなくてもよい。
なお、本発明では、分散剤を含有するケイ酸塩を使用する場合は、分散剤をさらに添加しても、添加しなくてもよい。
本発明の放射線線量測定ゾル又はゲルにおいて、水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)及びケイ酸塩の分散剤(B)の好ましい組合せとしては、成分(A)として水の放射線分解生成物により、励起光による蛍光が退色する化合物0.1μM乃至5μM又は水の放射線分解生成物により、励起光による蛍光を発光する化合物50μM乃至500μM、及び放射線線量測定ゾル又はゲル100質量%中、成分(B)として水膨潤性スメクタイト又はサポナイト0.1質量%乃至10質量%の組合せが挙げられる。
また、本発明の放射線線量測定ゾル又はゲルが成分(C)及び成分(D)を含む場合、水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)、ケイ酸塩の分散剤(B)、水溶性有機高分子(C)及びケイ酸塩(B)の分散剤(D)の好ましい組合せとしては、成分(A)として水の放射線分解生成物により、励起光による蛍光が退色する化合物0.1μM乃至5μM又は水の放射線分解生成物により、励起光による蛍光を発光する化合物50μM乃至500μM、放射線線量測定ゾル又はゲル100質量%中、成分(B)として水膨潤性スメクタイト又はサポナイト0.1質量%乃至10質量%、成分(C)として重量平均分子量250万以上500万以下の完全中和又は部分中和の直鎖型ポリアクリル酸ナトリウム0.03質量%乃至10質量%、及び成分(D)としてピロリン酸ナトリウム0.01質量%乃至10質量%、又は重量平均分子量1000以上2万以下の低重合ポリアクリル酸ナトリウム0.01質量%乃至10質量%の組合せが挙げられる。
また、本発明の放射線線量測定ゾル又はゲルは、グルコノ-δ-ラクトン、過塩素酸、硫酸及び食塩等のpH調整剤を含むことができる。
[放射線線量測定ゾル又はゲルの製造方法]
本発明の放射線線量測定ゾル又はゲルの製造方法は特に限定されるものではないが、成分(A)及び成分(B)、並びに必要に応じて、添加する成分(C)及び成分(D)を混合することによってゲル化させる方法、又は成分(A)乃至成分(D)のうちの少なくとも2種の成分の混合物若しくはその水溶液又は含水溶液と、残りの成分若しくは残りの成分の混合物又はその水溶液若しくは含水溶液とを混合することによってゲル化させる方法等が挙げられる。
本発明の放射線線量測定ゾル又はゲルの製造方法は特に限定されるものではないが、成分(A)及び成分(B)、並びに必要に応じて、添加する成分(C)及び成分(D)を混合することによってゲル化させる方法、又は成分(A)乃至成分(D)のうちの少なくとも2種の成分の混合物若しくはその水溶液又は含水溶液と、残りの成分若しくは残りの成分の混合物又はその水溶液若しくは含水溶液とを混合することによってゲル化させる方法等が挙げられる。
成分(A)及び成分(B)、並びに必要に応じて、添加する成分(C)及び成分(D)を混合する方法としては、機械式又は手動による撹拌の他、超音波処理を用いることができるが、特に機械式撹拌が好ましい。機械式撹拌には、例えば、マグネチックスターラー、プロペラ式撹拌機、自転・公転式ミキサー、ディスパー、ホモジナイザー、振とう機、ボルテックスミキサー、ボールミル、ニーダー、超音波発振器等を使用することができる。その中でも、好ましくは自転・公転式ミキサーによる混合である。
混合する際の温度は、水溶液又は水分散液の凝固点乃至沸点、好ましくは-5℃乃至50℃であり、より好ましくは0℃乃至30℃である。
混合直後は強度が弱くゾル状であるが、静置することでゲル化する。静置時間は2時間乃至100時間が好ましい。静置温度は-5℃乃至100℃であり、好ましくは0℃乃至30℃である。また、混合直後のゲル化する前に型に流し込んだり、押出成型したりすることにより、任意形状の放射線線量測定ゲルを作製することができる。
また、放射線線量測定能を失わない範囲で、ゾル状のままでもよい。
また、放射線線量測定能を失わない範囲で、ゾル状のままでもよい。
<放射線線量計>
本発明の放射線線量測定ゾル又はゲルは放射線線量の計測材料に適するため、当該放射線線量測定ゾル又はゲルを容器に充填して放射線線量計、例えばファントムとすることができる。容器は放射線を透過し、耐溶剤性及び気密性等を有していれば特に限定されず、その材質はガラス、アクリル樹脂、ポリエステル及びエチレン-ビニルアルコール共重合体等が好ましい。また、容器に充填した後、窒素ガス等で置換してもよい。
また、本発明の放射線線量計は、放射線照射に対して優れた感度を有し、かつ吸収線量に対する蛍光強度増加量又は吸光度増加量において、高い線形性を有するので、蛍光強度又は吸光度を測定可能な装置に使用できる。例えば光CT装置用の放射線線量計として使用することができる。
本発明の放射線線量測定ゾル又はゲルは放射線線量の計測材料に適するため、当該放射線線量測定ゾル又はゲルを容器に充填して放射線線量計、例えばファントムとすることができる。容器は放射線を透過し、耐溶剤性及び気密性等を有していれば特に限定されず、その材質はガラス、アクリル樹脂、ポリエステル及びエチレン-ビニルアルコール共重合体等が好ましい。また、容器に充填した後、窒素ガス等で置換してもよい。
また、本発明の放射線線量計は、放射線照射に対して優れた感度を有し、かつ吸収線量に対する蛍光強度増加量又は吸光度増加量において、高い線形性を有するので、蛍光強度又は吸光度を測定可能な装置に使用できる。例えば光CT装置用の放射線線量計として使用することができる。
次に実施例を挙げ本発明の内容を具体的に説明するが、本発明はこれらに限定されるものではない。
実施例において、試料の分析に用いた装置及び条件は、以下の通りである。
(1)X線照射
装置:工業用X線装置(ラジオフレックス250CG、リガク)
照射条件:250kVp,8mA,1mmアルミフィルターであり、線量率は1.72Gy/分である。18cmΦの円周上にサンプルを配置して照射した。
(2)蛍光強度測定
装置:分光蛍光光度計F-4500(株式会社日立ハイテクノロジーズ)
(3)吸光度測定
装置:紫外可視フォトダイオードアレイ分光光度計 MultiSpec-1500(株式会社 島津製作所)
(1)X線照射
装置:工業用X線装置(ラジオフレックス250CG、リガク)
照射条件:250kVp,8mA,1mmアルミフィルターであり、線量率は1.72Gy/分である。18cmΦの円周上にサンプルを配置して照射した。
(2)蛍光強度測定
装置:分光蛍光光度計F-4500(株式会社日立ハイテクノロジーズ)
(3)吸光度測定
装置:紫外可視フォトダイオードアレイ分光光度計 MultiSpec-1500(株式会社 島津製作所)
[実施例1:放射線線量測定ゾル又はゲルを放射線線量の計測材料として備える放射線線量計の製造]
超純水97.5mLにラポナイトXLG 2.5gを加えて撹拌し、2.5wt%となる分散液を作製した。また、蛍光プローブとなるクマリン-3-カルボン酸(CCA)5mgを100mLのフラスコに入れ0.267mMの蛍光プローブ水溶液を作製した。その後に、ラポナイトXLG分散液60mLに蛍光プローブ水溶液37.5mL及び超純水2.5mLを加え、均一になるまで攪拌し、ラポナイトXLGと蛍光プローブとの最終濃度がそれぞれ1.5wt%と0.1mMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
超純水97.5mLにラポナイトXLG 2.5gを加えて撹拌し、2.5wt%となる分散液を作製した。また、蛍光プローブとなるクマリン-3-カルボン酸(CCA)5mgを100mLのフラスコに入れ0.267mMの蛍光プローブ水溶液を作製した。その後に、ラポナイトXLG分散液60mLに蛍光プローブ水溶液37.5mL及び超純水2.5mLを加え、均一になるまで攪拌し、ラポナイトXLGと蛍光プローブとの最終濃度がそれぞれ1.5wt%と0.1mMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
[比較例1:ゼラチンを放射線線量の計測材料として備える放射線線量計の製造]
超純水97.5mLにゼラチン2.5gを加えて50℃程度まで加温して溶解し、2.5wt%となるゼラチン水溶液を作製した。そして、ラポナイトXLG分散液の替りにゼラチン水溶液を用いたこと及び分光測定用セルに充填後、一晩冷蔵庫に静置したこと以外は実施例1と同様の操作で、CCAが0.1mM、ゼラチンが5wt%、0.1wt%及び0.01wt%となる3種類の照射試験用の試料を得た。
超純水97.5mLにゼラチン2.5gを加えて50℃程度まで加温して溶解し、2.5wt%となるゼラチン水溶液を作製した。そして、ラポナイトXLG分散液の替りにゼラチン水溶液を用いたこと及び分光測定用セルに充填後、一晩冷蔵庫に静置したこと以外は実施例1と同様の操作で、CCAが0.1mM、ゼラチンが5wt%、0.1wt%及び0.01wt%となる3種類の照射試験用の試料を得た。
[実施例2:放射線照射試験]
実施例1及び比較例1で得られた各試料に放射線(X線)を照射した。その結果を図1に示す。
図1はクマリン-3-カルボン酸0.1mMに対して、ゲル化剤の種類及びその濃度を変化させた場合の蛍光強度の線量依存性を示す。ゲル化剤として、ケイ酸塩(ラポナイトXLG)1.5wt%、ゼラチン0.01wt%、0.1wt%及び5wt%を用いた放射線線量計の蛍光スペクトルの最大波長448nm近辺の値を読み取り、放射線照射による蛍光強度の増加量をプロットした。図1に示した結果は、同じ分光蛍光光度計の測定条件(スリット幅 励起側:2.5nm、蛍光側:10nm、ホトマル電圧:700V)で得られた試験結果であり、それぞれの傾きの違いが感度特性の違いを意味する。
ゼラチン5wt%を用いた試料では、25Gy未満の線量を照射しても蛍光強度の変化を観測することができなかった。また、ゼラチンの量を0.1wt%と0.01wt%に減らすことによって、線量に対する蛍光強度の増加を観測した。0.1wt%や0.01wt%のゼラチンを用いた試料は実質的に液体であり、放射線線量計へのゼラチンの適用は困難であることがわかった。これに対して、ケイ酸塩(ラポナイトXLG)は、1.5wt%の使用量でも高い線量応答性を有することがわかった。
本発明の放射線測定用ゾル又はゲルは、従来のゲル線量計で広く使用されているゼラチンに比べて、放射線照射に対して優れた感度を有し、かつ吸収線量に対する蛍光強度増加量において、高い線形性を有することが明らかである。
実施例1及び比較例1で得られた各試料に放射線(X線)を照射した。その結果を図1に示す。
図1はクマリン-3-カルボン酸0.1mMに対して、ゲル化剤の種類及びその濃度を変化させた場合の蛍光強度の線量依存性を示す。ゲル化剤として、ケイ酸塩(ラポナイトXLG)1.5wt%、ゼラチン0.01wt%、0.1wt%及び5wt%を用いた放射線線量計の蛍光スペクトルの最大波長448nm近辺の値を読み取り、放射線照射による蛍光強度の増加量をプロットした。図1に示した結果は、同じ分光蛍光光度計の測定条件(スリット幅 励起側:2.5nm、蛍光側:10nm、ホトマル電圧:700V)で得られた試験結果であり、それぞれの傾きの違いが感度特性の違いを意味する。
ゼラチン5wt%を用いた試料では、25Gy未満の線量を照射しても蛍光強度の変化を観測することができなかった。また、ゼラチンの量を0.1wt%と0.01wt%に減らすことによって、線量に対する蛍光強度の増加を観測した。0.1wt%や0.01wt%のゼラチンを用いた試料は実質的に液体であり、放射線線量計へのゼラチンの適用は困難であることがわかった。これに対して、ケイ酸塩(ラポナイトXLG)は、1.5wt%の使用量でも高い線量応答性を有することがわかった。
本発明の放射線測定用ゾル又はゲルは、従来のゲル線量計で広く使用されているゼラチンに比べて、放射線照射に対して優れた感度を有し、かつ吸収線量に対する蛍光強度増加量において、高い線形性を有することが明らかである。
[実施例3:放射線線量計の製造]
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光プローブとして、安息香酸を用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光プローブとの最終濃度がそれぞれ1.5wt%と0.1mMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光プローブとして、安息香酸を用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光プローブとの最終濃度がそれぞれ1.5wt%と0.1mMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
[実施例4:放射線線量計の製造]
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光プローブとして、テレフタル酸を用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光プローブとの最終濃度がそれぞれ1.5wt%と0.1mMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光プローブとして、テレフタル酸を用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光プローブとの最終濃度がそれぞれ1.5wt%と0.1mMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
[実施例5:放射線線量計の製造]
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光プローブとして、トリメリット酸を用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光プローブとの最終濃度がそれぞれ1.5wt%と0.1mMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光プローブとして、トリメリット酸を用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光プローブとの最終濃度がそれぞれ1.5wt%と0.1mMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
[実施例6:放射線線量計の製造]
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光プローブとして、ピロメリット酸を用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光プローブとの最終濃度がそれぞれ1.5wt%と0.1mMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光プローブとして、ピロメリット酸を用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光プローブとの最終濃度がそれぞれ1.5wt%と0.1mMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
[実施例7:放射線照射試験]
実施例1及び実施例3乃至実施例6で得られた各試料に1~5GyのX線を照射し、分光蛍光光度計により蛍光強度を評価した。その結果を図2に示す。
なお、分光蛍光光度計の測定条件は、スリット幅 励起側:10nm、蛍光側:10nm、ホトマル電圧:700Vであった。励起波長(Ex)と読み取りの蛍光のピーク波長(Em)はそれぞれ、クマリン-3-カルボン酸(Ex:370nm、Em:448nm)、安息香酸(Ex:300nm、Em:409nm)、テレフタル酸(Ex:320nm、Em:425nm)、トリメリット酸(Ex:310nm、Em:409nm)及びピロメリット酸(Ex:310nm、Em:433nm)であった。
図2に示すように、クマリン-3-カルボン酸、安息香酸、テレフタル酸、トリメリット酸及びピロメリット酸のすべての蛍光プローブにおいて、1~5Gyの低い線量での吸収線量に対する蛍光強度増加量の線形性が確認できた。特に、本試験条件ではテレフタル酸が最も高い感度を有することが分かった。
実施例1及び実施例3乃至実施例6で得られた各試料に1~5GyのX線を照射し、分光蛍光光度計により蛍光強度を評価した。その結果を図2に示す。
なお、分光蛍光光度計の測定条件は、スリット幅 励起側:10nm、蛍光側:10nm、ホトマル電圧:700Vであった。励起波長(Ex)と読み取りの蛍光のピーク波長(Em)はそれぞれ、クマリン-3-カルボン酸(Ex:370nm、Em:448nm)、安息香酸(Ex:300nm、Em:409nm)、テレフタル酸(Ex:320nm、Em:425nm)、トリメリット酸(Ex:310nm、Em:409nm)及びピロメリット酸(Ex:310nm、Em:433nm)であった。
図2に示すように、クマリン-3-カルボン酸、安息香酸、テレフタル酸、トリメリット酸及びピロメリット酸のすべての蛍光プローブにおいて、1~5Gyの低い線量での吸収線量に対する蛍光強度増加量の線形性が確認できた。特に、本試験条件ではテレフタル酸が最も高い感度を有することが分かった。
[実施例8:放射線線量計の製造]
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光色素として、ローダミン6Gを用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光色素との最終濃度がそれぞれ1.5wt%と1μMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光色素として、ローダミン6Gを用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光色素との最終濃度がそれぞれ1.5wt%と1μMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
[実施例9:放射線線量計の製造]
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光色素として、ウンベリフェロン-3-カルボン酸(7-ヒドロキシクマリン-3-カルボン酸:7OH-CCA)を用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光色素との最終濃度がそれぞれ1.5wt%と1μMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光色素として、ウンベリフェロン-3-カルボン酸(7-ヒドロキシクマリン-3-カルボン酸:7OH-CCA)を用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光色素との最終濃度がそれぞれ1.5wt%と1μMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
[実施例10:放射線線量計の製造]
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光色素として、ウンベリフェロン-3-カルボン酸を用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光色素との最終濃度がそれぞれ1.5wt%と0.25μMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光色素として、ウンベリフェロン-3-カルボン酸を用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光色素との最終濃度がそれぞれ1.5wt%と0.25μMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
[実施例11:放射線照射試験]
実施例8乃至実施例10で得られた各試料にX線を照射し、分光蛍光光度計により蛍光強度を評価した。その結果を図3に示す。
図3は放射線照射による蛍光強度の減少量の線量依存性を示す。
なお、分光蛍光光度計の測定条件はそれぞれ、1μM ローダミン6G(Ex:500nm、Em:561nm、スリット幅 励起側:2.5nm、蛍光側:5nm、ホトマル電圧:700V)、1μM ウンベリフェロン-3-カルボン酸(Ex:370nm、Em:446nm、スリット幅 励起側:2.5nm、蛍光側:5nm、ホトマル電圧:700V)及び0.25μM ウンベリフェロン-3-カルボン酸(Ex:370nm、Em:446nm、スリット幅 励起側:5nm、蛍光側:5nm、ホトマル電圧:700V)であった。
どちらの蛍光色素も放射線量に比例して蛍光強度が減少した。分光蛍光光度計の測定条件は異なり、初期の蛍光強度が少ない場合はスリット幅を大きくとっている。そのため、単純に放射線線量計の感度特性の比較ができないものの、ウンベリフェロン-3-カルボン酸の場合はその初期濃度を少なくすることで、蛍光強度の減少率を大きくすることができると考えられる。つまり、放射線照射による蛍光色素の分解量が初期の蛍光色素濃度に依存していないと推察される。また、多くの蛍光色素が本発明の放射線線量計に適用可能であることが推測される。
実施例8乃至実施例10で得られた各試料にX線を照射し、分光蛍光光度計により蛍光強度を評価した。その結果を図3に示す。
図3は放射線照射による蛍光強度の減少量の線量依存性を示す。
なお、分光蛍光光度計の測定条件はそれぞれ、1μM ローダミン6G(Ex:500nm、Em:561nm、スリット幅 励起側:2.5nm、蛍光側:5nm、ホトマル電圧:700V)、1μM ウンベリフェロン-3-カルボン酸(Ex:370nm、Em:446nm、スリット幅 励起側:2.5nm、蛍光側:5nm、ホトマル電圧:700V)及び0.25μM ウンベリフェロン-3-カルボン酸(Ex:370nm、Em:446nm、スリット幅 励起側:5nm、蛍光側:5nm、ホトマル電圧:700V)であった。
どちらの蛍光色素も放射線量に比例して蛍光強度が減少した。分光蛍光光度計の測定条件は異なり、初期の蛍光強度が少ない場合はスリット幅を大きくとっている。そのため、単純に放射線線量計の感度特性の比較ができないものの、ウンベリフェロン-3-カルボン酸の場合はその初期濃度を少なくすることで、蛍光強度の減少率を大きくすることができると考えられる。つまり、放射線照射による蛍光色素の分解量が初期の蛍光色素濃度に依存していないと推察される。また、多くの蛍光色素が本発明の放射線線量計に適用可能であることが推測される。
[実施例12:放射線線量計の製造]
超純水48.1gにラポナイトXLG 1.5g、及び40%ポリアクリル酸ナトリウム水溶液(分子量6,000)0.4gを加えて攪拌し、3.0wt%ラポナイトXLG分散液を作製した。一方、超純水39.6gにポリアクリル酸ナトリウム部分中和物(中和度35モル%)0.4gを加えて攪拌し、固形分1.0wt%のポリアクリル酸ナトリウム部分中和物水溶液を作製した。
また、クマリン-3-カルボン酸(CCA)19mgを100mLのフラスコに入れ1.0mMの蛍光プローブ水溶液を作製した。
その後、超純水32.8gに蛍光プローブ水溶液4.0g及び1.0wt%ポリアクリル酸ナトリウム部分中和物水溶液1.6gを加え攪拌した後、3.0wt%ラポナイトXLG分散液1.6gを加え、均一になるまで撹拌し、40mLの混合物を得た。得られた混合物を分光測定セル(1×1×4cmの四面透明)に充填し、照射試験用の試料を得た。
超純水48.1gにラポナイトXLG 1.5g、及び40%ポリアクリル酸ナトリウム水溶液(分子量6,000)0.4gを加えて攪拌し、3.0wt%ラポナイトXLG分散液を作製した。一方、超純水39.6gにポリアクリル酸ナトリウム部分中和物(中和度35モル%)0.4gを加えて攪拌し、固形分1.0wt%のポリアクリル酸ナトリウム部分中和物水溶液を作製した。
また、クマリン-3-カルボン酸(CCA)19mgを100mLのフラスコに入れ1.0mMの蛍光プローブ水溶液を作製した。
その後、超純水32.8gに蛍光プローブ水溶液4.0g及び1.0wt%ポリアクリル酸ナトリウム部分中和物水溶液1.6gを加え攪拌した後、3.0wt%ラポナイトXLG分散液1.6gを加え、均一になるまで撹拌し、40mLの混合物を得た。得られた混合物を分光測定セル(1×1×4cmの四面透明)に充填し、照射試験用の試料を得た。
[実施例13:放射線線量計の製造]
超純水28.0gに実施例12で作製した蛍光プローブ水溶液4.0g及び実施例12で作製した1.0wt%ポリアクリル酸ナトリウム部分中和物水溶液4.0gを加え攪拌した後、実施例12で作製した3.0wt%ラポナイトXLG分散液4.0gを加え、均一になるまで撹拌し、40mLの混合物を得た。得られた混合物を分光測定セル(1×1×4cmの四面透明)に充填し、照射試験用の試料を得た。
超純水28.0gに実施例12で作製した蛍光プローブ水溶液4.0g及び実施例12で作製した1.0wt%ポリアクリル酸ナトリウム部分中和物水溶液4.0gを加え攪拌した後、実施例12で作製した3.0wt%ラポナイトXLG分散液4.0gを加え、均一になるまで撹拌し、40mLの混合物を得た。得られた混合物を分光測定セル(1×1×4cmの四面透明)に充填し、照射試験用の試料を得た。
[実施例14:放射線照射試験]
実施例12及び実施例13で得られた各試料にX線を照射し、分光蛍光光度計により蛍光強度を評価した。実施例12の試料の結果を図4に、また実施例13の試料の結果を図5にそれぞれ示す。
なお、分光蛍光光度計の測定条件は、スリット幅 励起側:10nm、蛍光側:10nm、ホトマル電圧:700Vであった。励起波長(Ex)と読み取りの蛍光のピーク波長(Em)はそれぞれ、Ex:370nm、Em:446nmであった。
図1、図4及び図5に示すように、水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)、ケイ酸塩(B)、有機酸塩構造又は有機酸アニオン構造を有する水溶性有機高分子(C)及びケイ酸塩(B)の分散剤(D)を含む本発明の放射線測定用ゾル又はゲルは、従来のゲル線量計で広く使用されているゼラチンに比べて、放射線照射に対して優れた感度を有し、かつ吸収線量に対する蛍光強度増加量において、高い線形性を有することが明らかである。
実施例12及び実施例13で得られた各試料にX線を照射し、分光蛍光光度計により蛍光強度を評価した。実施例12の試料の結果を図4に、また実施例13の試料の結果を図5にそれぞれ示す。
なお、分光蛍光光度計の測定条件は、スリット幅 励起側:10nm、蛍光側:10nm、ホトマル電圧:700Vであった。励起波長(Ex)と読み取りの蛍光のピーク波長(Em)はそれぞれ、Ex:370nm、Em:446nmであった。
図1、図4及び図5に示すように、水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)、ケイ酸塩(B)、有機酸塩構造又は有機酸アニオン構造を有する水溶性有機高分子(C)及びケイ酸塩(B)の分散剤(D)を含む本発明の放射線測定用ゾル又はゲルは、従来のゲル線量計で広く使用されているゼラチンに比べて、放射線照射に対して優れた感度を有し、かつ吸収線量に対する蛍光強度増加量において、高い線形性を有することが明らかである。
[実施例15:放射線線量計の製造]
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光色素として、2,5-ジフェニルオキサゾールを用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光色素との最終濃度がそれぞれ1.5wt%と0.5μMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光色素として、2,5-ジフェニルオキサゾールを用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光色素との最終濃度がそれぞれ1.5wt%と0.5μMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
[実施例16:放射線照射試験]
実施例15で得られた試料にX線を照射し、分光蛍光光度計により蛍光強度を評価した。その結果を図6に示す。
図6は放射線照射による蛍光強度の減少量の線量依存性を示す。
なお、分光蛍光光度計の測定条件は、Ex:310nm、Em:378nm、スリット幅 励起側:2.5nm、蛍光側:5nm、ホトマル電圧:700Vであった。
図6に示すように、蛍光色素である2,5-ジフェニルオキサゾールにおいて、吸収線量に比例して蛍光強度が減少した。
実施例15で得られた試料にX線を照射し、分光蛍光光度計により蛍光強度を評価した。その結果を図6に示す。
図6は放射線照射による蛍光強度の減少量の線量依存性を示す。
なお、分光蛍光光度計の測定条件は、Ex:310nm、Em:378nm、スリット幅 励起側:2.5nm、蛍光側:5nm、ホトマル電圧:700Vであった。
図6に示すように、蛍光色素である2,5-ジフェニルオキサゾールにおいて、吸収線量に比例して蛍光強度が減少した。
[実施例17:放射線線量計の製造]
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光色素として、ローダミン6Gを用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光色素との最終濃度がそれぞれ2.5wt%と1μMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光色素として、ローダミン6Gを用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光色素との最終濃度がそれぞれ2.5wt%と1μMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
[実施例18:放射線線量計の製造]
実施例1で用いたクマリン-3-カルボン酸の替りに、7-ジエチルアミノ-4-メチルクマリンを用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光プローブとの最終濃度がそれぞれ2.5wt%と1μMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
実施例1で用いたクマリン-3-カルボン酸の替りに、7-ジエチルアミノ-4-メチルクマリンを用いた以外は、実施例1と同様の操作で、ラポナイトXLGと蛍光プローブとの最終濃度がそれぞれ2.5wt%と1μMの100mLの混合物を得た。得られた混合物を分光測定用セルに充填し、照射試験用の試料を得た。
[実施例19:拡散評価試験]
本発明の放射線線量計において、放射線照射による化合物(A)由来の化合物の拡散状況を確認するため、実施例17で得られた試料については放射線照射1ヶ月後のものを、実施例18で得られた試料については放射線照射2日後のものをそれぞれ撮影した。その結果を図7に示す[図7中(a)は実施例17における放射線照射1ヶ月後の試料、(b)実施例18における放射線照射2日後の試料]。
なお、実施例17で得られた試料に対する放射線量は140Gyであり、実施例18で得られた試料に対する放射線量は100Gyであった。また撮影はいずれも暗箱中に放射線照射後の試料を置き、365nm LEDライトを利用して行った。
図7に示すように、実施例17及び実施例18の試料それぞれについて、放射線照射によるコントラストは放射線照射後も維持されており、放射線照射による化合物(A)由来の化合物の拡散が抑制されていることを確認できた。
本発明の放射線線量計において、放射線照射による化合物(A)由来の化合物の拡散状況を確認するため、実施例17で得られた試料については放射線照射1ヶ月後のものを、実施例18で得られた試料については放射線照射2日後のものをそれぞれ撮影した。その結果を図7に示す[図7中(a)は実施例17における放射線照射1ヶ月後の試料、(b)実施例18における放射線照射2日後の試料]。
なお、実施例17で得られた試料に対する放射線量は140Gyであり、実施例18で得られた試料に対する放射線量は100Gyであった。また撮影はいずれも暗箱中に放射線照射後の試料を置き、365nm LEDライトを利用して行った。
図7に示すように、実施例17及び実施例18の試料それぞれについて、放射線照射によるコントラストは放射線照射後も維持されており、放射線照射による化合物(A)由来の化合物の拡散が抑制されていることを確認できた。
[実施例20:放射線線量計の製造]
超純水24.0gに実施例12で作製した蛍光プローブ水溶液4.0g及び実施例12で作製した1.0wt%ポリアクリル酸ナトリウム部分中和物水溶液6.0gを加え攪拌した後、実施例12で作製した3.0wt%ラポナイトXLG分散液6.0gを加え、均一になるまで撹拌し、40mLの混合物を得た。得られた混合物を分光測定セル(1×1×4cmの四面透明)に充填し、照射試験用の試料を得た。
超純水24.0gに実施例12で作製した蛍光プローブ水溶液4.0g及び実施例12で作製した1.0wt%ポリアクリル酸ナトリウム部分中和物水溶液6.0gを加え攪拌した後、実施例12で作製した3.0wt%ラポナイトXLG分散液6.0gを加え、均一になるまで撹拌し、40mLの混合物を得た。得られた混合物を分光測定セル(1×1×4cmの四面透明)に充填し、照射試験用の試料を得た。
[実施例21:放射線線量計の製造]
超純水20.0gに実施例12で作製した蛍光プローブ水溶液4.0g及び実施例12で作製した1.0wt%ポリアクリル酸ナトリウム部分中和物水溶液8.0gを加え攪拌した後、実施例12で作製した3.0wt%ラポナイトXLG分散液8.0gを加え、均一になるまで撹拌し、40mLの混合物を得た。得られた混合物を分光測定セル(1×1×4cmの四面透明)に充填し、照射試験用の試料を得た。
超純水20.0gに実施例12で作製した蛍光プローブ水溶液4.0g及び実施例12で作製した1.0wt%ポリアクリル酸ナトリウム部分中和物水溶液8.0gを加え攪拌した後、実施例12で作製した3.0wt%ラポナイトXLG分散液8.0gを加え、均一になるまで撹拌し、40mLの混合物を得た。得られた混合物を分光測定セル(1×1×4cmの四面透明)に充填し、照射試験用の試料を得た。
[実施例22:放射線照射試験]
実施例20及び実施例21で得られた各試料に放射線(X線)を照射し、分光蛍光光度計により蛍光強度を評価した。その結果を図8に示す。
図8はポリアクリル酸ナトリウム部分中和物の濃度を15wt%又は20wt%に変化させた場合の蛍光強度の線量依存性を示す。実施例20及び実施例21で得られた放射線線量計の蛍光スペクトルの最大波長446.8nm近辺の値を読み取り、放射線照射による蛍光強度の増加量をプロットした。図8に示した結果は、同じ分光蛍光光度計の測定条件(励起波長:270.0nm、スリット幅 励起側:5.0nm、蛍光側:5.0nm、ホトマル電圧:700V)で得られた試験結果であり、それぞれの傾きの違いが感度特性の違いを意味する。
図1及び図8に示すように、ポリアクリル酸ナトリウム部分中和物を添加した本発明の放射線測定用ゾル又はゲルは、従来のゲル線量計で広く使用されているゼラチンに比べて、放射線照射に対して優れた感度を有し、かつ吸収線量に対する蛍光強度増加量において、高い線形性を有することが明らかである。
実施例20及び実施例21で得られた各試料に放射線(X線)を照射し、分光蛍光光度計により蛍光強度を評価した。その結果を図8に示す。
図8はポリアクリル酸ナトリウム部分中和物の濃度を15wt%又は20wt%に変化させた場合の蛍光強度の線量依存性を示す。実施例20及び実施例21で得られた放射線線量計の蛍光スペクトルの最大波長446.8nm近辺の値を読み取り、放射線照射による蛍光強度の増加量をプロットした。図8に示した結果は、同じ分光蛍光光度計の測定条件(励起波長:270.0nm、スリット幅 励起側:5.0nm、蛍光側:5.0nm、ホトマル電圧:700V)で得られた試験結果であり、それぞれの傾きの違いが感度特性の違いを意味する。
図1及び図8に示すように、ポリアクリル酸ナトリウム部分中和物を添加した本発明の放射線測定用ゾル又はゲルは、従来のゲル線量計で広く使用されているゼラチンに比べて、放射線照射に対して優れた感度を有し、かつ吸収線量に対する蛍光強度増加量において、高い線形性を有することが明らかである。
[実施例23:放射線線量測定ゾル又はゲルを放射線線量の計測材料として備える放射線線量計の製造]
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光プローブとしてジヒドロローダミン123塩酸塩(富士フィルム和光純薬製、以下DHRともいう)を使用した以外は、実施例1と同様の操作で、ラポナイトXLGとDHRとの最終濃度が、1.5wt%と0.1mMの混合物を得た。得られた混合物を5mLのバイアル及び分光測定用セルに夫々充填し、照射試験用の試料を得た。
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光プローブとしてジヒドロローダミン123塩酸塩(富士フィルム和光純薬製、以下DHRともいう)を使用した以外は、実施例1と同様の操作で、ラポナイトXLGとDHRとの最終濃度が、1.5wt%と0.1mMの混合物を得た。得られた混合物を5mLのバイアル及び分光測定用セルに夫々充填し、照射試験用の試料を得た。
[実施例24:放射線線量測定ゾル又はゲルを放射線線量の計測材料として備える放射線線量計の製造]
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光プローブとしてジヒドロローダミン塩酸塩(DHR)を使用した以外は、実施例1と同様の操作で、ラポナイトXLGとDHRとの最終濃度が、2.5wt%と0.1mMの混合物を得た。得られた混合物を分光測定用セル及び2D分布解析用容器(100mm×100mm×5mm)に夫々充填し、照射試験用の試料を得た。
実施例1で用いたクマリン-3-カルボン酸の替りに、蛍光プローブとしてジヒドロローダミン塩酸塩(DHR)を使用した以外は、実施例1と同様の操作で、ラポナイトXLGとDHRとの最終濃度が、2.5wt%と0.1mMの混合物を得た。得られた混合物を分光測定用セル及び2D分布解析用容器(100mm×100mm×5mm)に夫々充填し、照射試験用の試料を得た。
[実施例25:放射線照射試験]
実施例23及び実施例24で得られた各試料に放射線(X線)を照射し、分光蛍光光度計により蛍光強度を評価した。その結果を図9に示す。
図9は蛍光プロープ(DHR)を用い、ケイ酸塩(ラポナイトXLG)の濃度を1.5wt%又は2.5wt%に変化させた場合の蛍光強度の線量依存性を示す。実施例23及び実施例24で得られた放射線線量計の蛍光スペクトルの最大波長539nm近辺の値を読み取り、放射線照射による蛍光強度の増加量をプロットした。図9に示した結果は、同じ分光蛍光光度計の測定条件(励起波長:480.0nm、スリット幅 励起側:1.0nm、蛍光側:20.0nm、ホトマル電圧:700V)で得られた試験結果であり、それぞれの傾きの違いが感度特性の違いを意味する。
図9に示すように、本発明の放射線測定用ゾル又はゲルは、放射線照射に対して優れた感度を有し、かつ吸収線量に対する蛍光強度増加量において、高い線形性を有することが明らかである。
また、図9に示す様に、本発明の放射線測定用ゾル又はゲルは、ゲル化剤の濃度によらず、放射線測定用ゾル又はゲルとして使用できることが明らかである。
実施例23及び実施例24で得られた各試料に放射線(X線)を照射し、分光蛍光光度計により蛍光強度を評価した。その結果を図9に示す。
図9は蛍光プロープ(DHR)を用い、ケイ酸塩(ラポナイトXLG)の濃度を1.5wt%又は2.5wt%に変化させた場合の蛍光強度の線量依存性を示す。実施例23及び実施例24で得られた放射線線量計の蛍光スペクトルの最大波長539nm近辺の値を読み取り、放射線照射による蛍光強度の増加量をプロットした。図9に示した結果は、同じ分光蛍光光度計の測定条件(励起波長:480.0nm、スリット幅 励起側:1.0nm、蛍光側:20.0nm、ホトマル電圧:700V)で得られた試験結果であり、それぞれの傾きの違いが感度特性の違いを意味する。
図9に示すように、本発明の放射線測定用ゾル又はゲルは、放射線照射に対して優れた感度を有し、かつ吸収線量に対する蛍光強度増加量において、高い線形性を有することが明らかである。
また、図9に示す様に、本発明の放射線測定用ゾル又はゲルは、ゲル化剤の濃度によらず、放射線測定用ゾル又はゲルとして使用できることが明らかである。
[実施例26:放射線照射試験]
実施例24で得られた2D分布解析用容器に充填した試料に放射線(X線)を照射し、蛍光ゲルスキャナー(パシフィックイメージエレクトロニクス社製、型番:Glite 900 BW)により蛍光強度を評価した。その結果を図10及び図11に示す。図10はX線照射後に蛍光ゲルスキャナーから得られる画像である。図11は、蛍光ゲルスキャナーによりX線照射した試料の照射領域毎の蛍光強度の平均値を読み取り、放射線照射量による蛍光強度の増加量をプロットしたものである。図11に示すように、本発明の放射線測定用ゾル又はゲルは、2次元画像においても放射線照射に対して優れた感度を有し、かつ吸収線量に対する蛍光強度増加量において、高い線形性を有することが明らかである。
実施例24で得られた2D分布解析用容器に充填した試料に放射線(X線)を照射し、蛍光ゲルスキャナー(パシフィックイメージエレクトロニクス社製、型番:Glite 900 BW)により蛍光強度を評価した。その結果を図10及び図11に示す。図10はX線照射後に蛍光ゲルスキャナーから得られる画像である。図11は、蛍光ゲルスキャナーによりX線照射した試料の照射領域毎の蛍光強度の平均値を読み取り、放射線照射量による蛍光強度の増加量をプロットしたものである。図11に示すように、本発明の放射線測定用ゾル又はゲルは、2次元画像においても放射線照射に対して優れた感度を有し、かつ吸収線量に対する蛍光強度増加量において、高い線形性を有することが明らかである。
[実施例27:拡散評価試験]
本発明の放射線線量計において、放射線照射による化合物(A)由来の化合物の拡散状況を確認するため、実施例24で得られた分光測定用セルに充填した試料について放射線照射73日後のものを撮影した。その結果を図12に示す。
試料に対して放射線量7Gyでキャップ側上部半分に照射を行った。また、撮影は蛍光ゲルスキャナーを利用して行った。
図12に示すように、実施例24の試料について、放射線照射による照射領域と未照射領域の境界線(コントラスト)は放射線照射後も維持されており、時間と共に化合物(A)の拡散は抑制されており、化合物(A)の拡散の影響は無視できることがわかる。
本発明の放射線線量計において、放射線照射による化合物(A)由来の化合物の拡散状況を確認するため、実施例24で得られた分光測定用セルに充填した試料について放射線照射73日後のものを撮影した。その結果を図12に示す。
試料に対して放射線量7Gyでキャップ側上部半分に照射を行った。また、撮影は蛍光ゲルスキャナーを利用して行った。
図12に示すように、実施例24の試料について、放射線照射による照射領域と未照射領域の境界線(コントラスト)は放射線照射後も維持されており、時間と共に化合物(A)の拡散は抑制されており、化合物(A)の拡散の影響は無視できることがわかる。
[実施例28:放射線照射試験(分光光度計による読み取り)]
実施例23で得られた試料に放射線(X線)を照射し、分光光度計により吸光度を評価した。その結果を図13に示す。
図13は放射線照射した試料の400nm乃至600nmの波長の吸光度を分光光度計により測定し、最大吸光度511nm付近の値を読み取り、放射線照射量による吸光度の増加量をプロットした。
図13に示す様に、本発明の放射線測定用ゾル又はゲルの吸光度は、放射線量に比例して増加しており、光吸収測定においても定量可能であることが明らかである。つまり、本発明の放射線測定用ゾル又はゲルは、例えば光CT装置用の放射線線量計としても用いることができる。
実施例23で得られた試料に放射線(X線)を照射し、分光光度計により吸光度を評価した。その結果を図13に示す。
図13は放射線照射した試料の400nm乃至600nmの波長の吸光度を分光光度計により測定し、最大吸光度511nm付近の値を読み取り、放射線照射量による吸光度の増加量をプロットした。
図13に示す様に、本発明の放射線測定用ゾル又はゲルの吸光度は、放射線量に比例して増加しており、光吸収測定においても定量可能であることが明らかである。つまり、本発明の放射線測定用ゾル又はゲルは、例えば光CT装置用の放射線線量計としても用いることができる。
Claims (9)
- 水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)及びケイ酸塩(B)を含むことを特徴とする、放射線線量測定ゾル又はゲル。
- 前記水の放射線分解生成物により、励起光による蛍光特性が変化する化合物(A)がクマリン誘導体、芳香族カルボン酸誘導体、オキサゾール誘導体及びローダミン類からなる群より選ばれる1種又は2種以上である、請求項1に記載の放射線線量測定ゾル又はゲル。
- 前記ケイ酸塩(B)がスメクタイト、ベントナイト、バーミキュライト及び雲母からなる群より選ばれる1種又は2種以上の水膨潤性ケイ酸塩粒子である、請求項1又は請求項2に記載の放射線線量測定ゾル又はゲル。
- 有機酸塩構造又は有機酸アニオン構造を有する水溶性有機高分子(C)及びケイ酸塩(B)の分散剤(D)を更に含むことを特徴とする、請求項1乃至請求項3のいずれか1項に記載の放射線線量測定ゾル又はゲル。
- 前記水溶性有機高分子(C)が完全中和又は部分中和ポリアクリル酸塩である、請求項4に記載の放射線線量測定ゾル又はゲル。
- 前記分散剤(D)がオルトリン酸ナトリウム、ピロリン酸ナトリウム、トリポリリン酸ナトリウム、テトラリン酸ナトリウム、ヘキサメタリン酸ナトリウム、ポリリン酸ナトリウム、ポリ(メタ)アクリル酸ナトリウム、ポリ(メタ)アクリル酸アンモニウム、アクリル酸ナトリウム/マレイン酸ナトリウム共重合体、アクリル酸アンモニウム/マレイン酸アンモニウム共重合体、水酸化ナトリウム、ヒドロキシルアミン、炭酸ナトリウム、ケイ酸ナトリウム、ポリエチレングリコール、ポリプロピレングリコール、フミン酸ナトリウム及びリグニンスルホン酸ナトリウムからなる群から選ばれる1種又は2種以上である、請求項4又は請求項5に記載の放射線線量測定ゾル又はゲル。
- pH調整剤を更に含む、請求項1乃至請求項6のいずれか1項に記載の放射線線量測定ゾル又はゲル。
- 請求項1乃至請求項7のいずれか1項に記載の放射線線量測定ゾル又はゲルを放射線線量の計測材料として備える放射線線量計。
- 前記放射線線量計が、光CT装置用の放射線線量計である、請求項8に記載の放射線線量計。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019546696A JPWO2019069853A1 (ja) | 2017-10-02 | 2018-10-01 | 放射線線量測定ゾル又はゲル、及びそれを放射線線量の計測材料として備える放射線線量計 |
| EP18864654.1A EP3686632A4 (en) | 2017-10-02 | 2018-10-01 | SOL OR GEL FOR RADIATION DOSIMETRY AND RADIATION DOSIMETER PROVIDED WITH SUCH SOL OR GEL AS A MATERIAL FOR RADIATION DOSIMETRY |
| US16/753,244 US11150358B2 (en) | 2017-10-02 | 2018-10-01 | Radiation dosimetry sol or gel and radiation dosimeter comprising same as material for radiation dosimetry |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017-193001 | 2017-10-02 | ||
| JP2017193001 | 2017-10-02 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2019069853A1 true WO2019069853A1 (ja) | 2019-04-11 |
Family
ID=65994350
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2018/036694 Ceased WO2019069853A1 (ja) | 2017-10-02 | 2018-10-01 | 放射線線量測定ゾル又はゲル、及びそれを放射線線量の計測材料として備える放射線線量計 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US11150358B2 (ja) |
| EP (1) | EP3686632A4 (ja) |
| JP (1) | JPWO2019069853A1 (ja) |
| WO (1) | WO2019069853A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPWO2020241354A1 (ja) * | 2019-05-24 | 2020-12-03 |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11971510B2 (en) * | 2020-11-27 | 2024-04-30 | Riken | Gel dosimeter for measuring radiation dose |
| CN113933889A (zh) * | 2021-10-13 | 2022-01-14 | 散裂中子源科学中心 | 一种组合式Fricke凝胶剂量计的制备和数据读取方法 |
| CN114280015A (zh) * | 2021-11-30 | 2022-04-05 | 苏州科技大学 | 石墨炔/血红素复合材料的应用及采用该材料对还原型小分子检测的方法 |
| CN115291268B (zh) * | 2022-07-28 | 2025-06-20 | 苏州大学 | 一种电离辐射凝胶剂量计及其制备方法 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2016016261A1 (fr) * | 2014-07-29 | 2016-02-04 | Areva Nc | Formulations de gels pour la detection et la localisation d'une contamination radioactive en surface de substrats solides et procede de detection, de localisation utilisant ces gels |
| WO2016098888A1 (ja) * | 2014-12-19 | 2016-06-23 | 国立研究開発法人理化学研究所 | 放射線線量測定ゲル、及びそれを放射線線量の計測材料として備える放射線線量計 |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2321426A4 (en) * | 2008-07-30 | 2011-12-14 | Dana Farber Cancer Inst Inc | COMPOSITIONS FOR DETECTING CELL DEATH AND USE METHOD |
| US20160089316A1 (en) * | 2014-09-26 | 2016-03-31 | Genesis Laboratories Inc. | Compound, Composition, Polymer, Mylar Film and Method for Indicating Maximum Exposure to the Sun and UV Radiation |
-
2018
- 2018-10-01 US US16/753,244 patent/US11150358B2/en not_active Expired - Fee Related
- 2018-10-01 WO PCT/JP2018/036694 patent/WO2019069853A1/ja not_active Ceased
- 2018-10-01 JP JP2019546696A patent/JPWO2019069853A1/ja not_active Withdrawn
- 2018-10-01 EP EP18864654.1A patent/EP3686632A4/en not_active Withdrawn
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2016016261A1 (fr) * | 2014-07-29 | 2016-02-04 | Areva Nc | Formulations de gels pour la detection et la localisation d'une contamination radioactive en surface de substrats solides et procede de detection, de localisation utilisant ces gels |
| WO2016098888A1 (ja) * | 2014-12-19 | 2016-06-23 | 国立研究開発法人理化学研究所 | 放射線線量測定ゲル、及びそれを放射線線量の計測材料として備える放射線線量計 |
Non-Patent Citations (8)
| Title |
|---|
| BENEVIDES CADUARTE DE MENEZES FDE ARAUJO RE: "Evaluation of fluorescent dye degradation indirectly induced by x-ray ionizing radiation", APPL. OPT., vol. 54, 2015, pages 6935 - 9 |
| HAYASHI SHINICHIRO: "Polymer Gel Dosimeter", RADIATION CHEMISTRY, no. 93, 31 March 2012 (2012-03-31), pages 23 - 30, XP009520060, ISSN: 0286-6722 * |
| K. PAPADOPOULOS ET AL.: "Radiochemiluminescence of acridones and alkyl acridines", JOURNAL OF PHOTOCHEMISTRY AND PHOTOBIOLOGY A:CHEMISTRY, vol. 115, 27 January 1998 (1998-01-27), pages 137 - 142, XP055589627 * |
| MATTHEWS RW: "Aqueous Chemical Dosimetry", INTERNATIONAL JOURNAL OF APPLIED RADIATION AND ISOTOPES, vol. 33, 1982, pages 1159 - 70, XP024718074, DOI: 10.1016/0020-708X(82)90241-1 |
| SANDWALL PASPITZ HBELSON HR ET AL.: "Measuring the photon depth dose distribution produced by a medical linear accelerator in a water-equivalent radio-fluorogenic gel", JOURNAL OF RADIOANALYTICAL AND NUCLEAR CHEMISTRY, vol. 307, 2016, pages 2505 - 08, XP035921021, DOI: 10.1007/s10967-015-4563-x |
| See also references of EP3686632A4 |
| WATANABE YWARMINGTON LGOPISHANKAR N: "Three-dimensional radiation dosimetry using polymer gel and solid radiochromic polymer: From basics to clinical applications", WORLD JOURNAL OF RADIOLOGY, vol. 9, 2017, pages 112 - 25 |
| YAO T: "3D Radiation Dosimetry Using a Radio-Fluorogenic gel", 2017, PLACE DELFT UNIVERSITY OF TECHNOLOGY |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPWO2020241354A1 (ja) * | 2019-05-24 | 2020-12-03 | ||
| WO2020241354A1 (ja) * | 2019-05-24 | 2020-12-03 | 国立研究開発法人理化学研究所 | 放射線線量測定ゲル、及びそれを放射線線量の計測材料として備える放射線線量計 |
| JP7414241B2 (ja) | 2019-05-24 | 2024-01-16 | 国立研究開発法人理化学研究所 | 放射線線量測定ゲル、及びそれを放射線線量の計測材料として備える放射線線量計 |
| US11960038B2 (en) | 2019-05-24 | 2024-04-16 | Riken | Radiation dosimetry gel and radiation dosimeter comprising same as material for measuring radiation dose |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3686632A1 (en) | 2020-07-29 |
| US20200333474A1 (en) | 2020-10-22 |
| JPWO2019069853A1 (ja) | 2021-06-17 |
| EP3686632A4 (en) | 2020-10-14 |
| US11150358B2 (en) | 2021-10-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2019069853A1 (ja) | 放射線線量測定ゾル又はゲル、及びそれを放射線線量の計測材料として備える放射線線量計 | |
| Hayashi et al. | Novel radiochromic gel dosimeter based on a polyvinyl alcohol–Iodide complex | |
| Breukers et al. | Transparent lithium loaded plastic scintillators for thermal neutron detection | |
| Zhou et al. | Red-emitting carbon dots as luminescent agent in wide-range water detection in organic solvents and polarity-selective zebrafish imaging | |
| Nsubuga et al. | Investigating the reactive oxygen species production of Rose Bengal and Merocyanine 540-loaded radioluminescent nanoparticles | |
| WO2016098888A1 (ja) | 放射線線量測定ゲル、及びそれを放射線線量の計測材料として備える放射線線量計 | |
| Liu et al. | Significantly enhanced afterglow brightness via intramolecular energy transfer | |
| Qiao et al. | MOF matrix doped with rare earth ions to realize ratiometric fluorescent sensing of 2, 4, 6-trinitrophenol: synthesis, characterization and performance | |
| Maeyama et al. | Nanoclay gel-based radio-fluorogenic gel dosimeters using various fluorescence probes | |
| Liang et al. | Effects of a nanoscale silica matrix on the fluorescence quantum yield of encapsulated dye molecules | |
| Zhou et al. | Quantum yield measurements of photochemical reaction-based afterglow luminescence materials | |
| Rabaeh et al. | High optical stability of reusable radiochromic polyvinyl alcohol-iodine gel dosimeter for radiotherapy | |
| Iwata et al. | Leuco-based composite resin dosimeter film | |
| Xu et al. | Polarized resonance synchronous spectroscopy as a powerful tool for studying the kinetics and optical properties of aggregation-induced emission | |
| Mochizuki et al. | Sensitivity enhancement of DHR123 radio-fluorogenic nanoclay gel dosimeter by incorporating surfactants and halogenides | |
| Salas-Juárez et al. | Persistent luminescence of ZrO2: Tb3+ after beta particle irradiation for dosimetry applications | |
| JP2021032856A (ja) | 放射線線量測定用組成物及びその製造方法、並びに放射線線量計 | |
| Duan et al. | Dual-emission LaF3: Tb@ DPA-Eu nanoparticles as a ratiometric fluorescence probe for the detection of marbofloxacin | |
| Maity | Photophysical detection of singlet oxygen | |
| Zhang et al. | A time-resolved ratiometric luminescent anthrax biomarker nanosensor based on an Ir (III) complex-doped coordination polymer network | |
| US9234081B2 (en) | Method of manufacturing a nitro blue tetrazolium and polyvinyl butyral based dosimeter film | |
| Akhtar et al. | Improved performance of radiochromic films for high-dose dosimetry | |
| Krysiak-Smułek et al. | Assessing the effects of luminescently labelled and non-labelled PET nanoparticles on environmental bacteria | |
| JP4820963B2 (ja) | 機能性シリカ粒子及びその用途 | |
| Arık et al. | Molecular aggregates of pyronin dyes with polyelectrolyte polystyrene sulfonate (PSS) in aqueous solution |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 18864654 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2019546696 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2018864654 Country of ref document: EP Effective date: 20200420 |