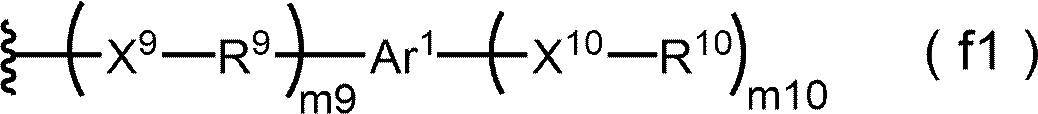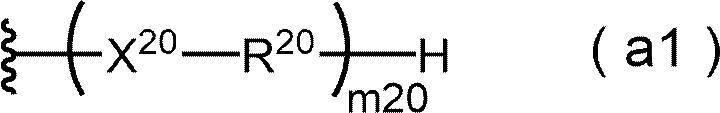WO2021049552A1 - ペプチド化合物の製造方法、保護基形成用試薬、及び、ヒドラジン誘導体 - Google Patents
ペプチド化合物の製造方法、保護基形成用試薬、及び、ヒドラジン誘導体 Download PDFInfo
- Publication number
- WO2021049552A1 WO2021049552A1 PCT/JP2020/034194 JP2020034194W WO2021049552A1 WO 2021049552 A1 WO2021049552 A1 WO 2021049552A1 JP 2020034194 W JP2020034194 W JP 2020034194W WO 2021049552 A1 WO2021049552 A1 WO 2021049552A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- terminal
- peptide compound
- aliphatic hydrocarbon
- ring
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K1/00—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length
- C07K1/06—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length using protecting groups or activating agents
- C07K1/061—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length using protecting groups or activating agents using protecting groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K1/00—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length
- C07K1/06—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length using protecting groups or activating agents
- C07K1/061—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length using protecting groups or activating agents using protecting groups
- C07K1/062—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length using protecting groups or activating agents using protecting groups for alpha- or omega-carboxy functions
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C243/00—Compounds containing chains of nitrogen atoms singly-bound to each other, e.g. hydrazines, triazanes
- C07C243/24—Hydrazines having nitrogen atoms of hydrazine groups acylated by carboxylic acids
- C07C243/26—Hydrazines having nitrogen atoms of hydrazine groups acylated by carboxylic acids with acylating carboxyl groups bound to hydrogen atoms or to acyclic carbon atoms
- C07C243/28—Hydrazines having nitrogen atoms of hydrazine groups acylated by carboxylic acids with acylating carboxyl groups bound to hydrogen atoms or to acyclic carbon atoms to hydrogen atoms or to carbon atoms of a saturated carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K1/00—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length
- C07K1/02—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length in solution
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/55—Design of synthesis routes, e.g. reducing the use of auxiliary or protecting groups
Definitions
- the present disclosure relates to a method for producing a peptide compound, a reagent for forming a protecting group, and a hydrazine derivative.
- Examples of the peptide production method include a solid phase method and a liquid phase method.
- the solid-phase method is advantageous in that the isolation and purification after the reaction can be performed only by washing the resin. However, it is essentially a heterogeneous phase reaction, requiring the use of excess amounts of reaction reagents or reagents to compensate for the low reactivity. In addition, it was difficult to track the reaction and analyze the reaction product while being supported on the carrier.
- the liquid phase method has good reactivity, and the intermediate peptide can be purified by extraction washing, isolation, etc. after the condensation reaction. However, the liquid phase method still has problems in each step of coupling reaction and deprotection.
- the separation carrier described in Patent Document 1 As a separation carrier used for conventional peptide synthesis, the separation carrier described in Patent Document 1 is known. Further, as conventional reagents for forming a protecting group, a compound having a diphenylmethane structure described in Patent Document 2 and a compound having a fluorene structure described in Patent Document 3 are known.
- Patent Document 1 International Publication No. 2007/034812
- Patent Document 2 International Publication No. 2010/1133939
- Patent Document 3 International Publication No. 2010/104169
- An object to be solved by one embodiment of the present invention is to provide a method for producing a peptide compound having an excellent yield at the time of deprotection.
- Another problem to be solved by another embodiment of the present invention is to provide a reagent for forming a protecting group, which has an excellent yield at the time of deprotection.
- a problem to be solved by yet another embodiment of the present invention is to provide a novel hydrazine derivative.
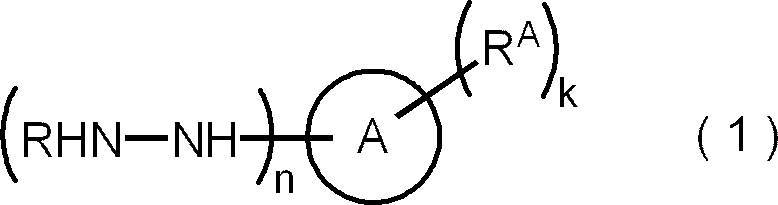
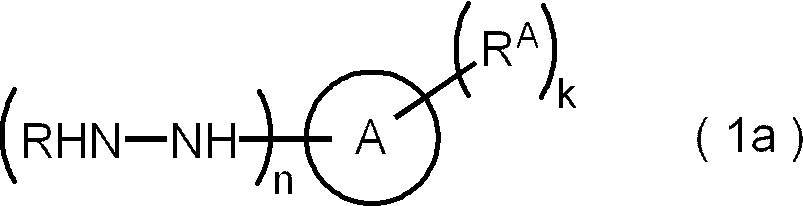
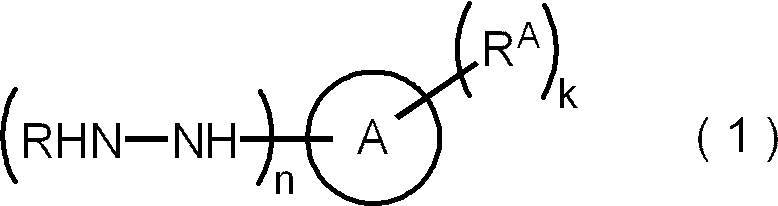
- Means for solving the above problems include the following aspects. ⁇ 1> A method for producing a peptide compound, which comprises a step of using a hydrazine derivative represented by the following formula (1).
- ring A represents an aromatic hydrocarbon ring or an aromatic heterocycle
- R represents a hydrogen atom, an amino-protecting group, an amino acid residue, or a peptide residue
- k represents 1 to 1 to 1.
- n is 1 or 2
- R a is independently an aliphatic hydrocarbon group, or represents an organic group having an aliphatic hydrocarbon group, at least one of the k R a
- One aliphatic hydrocarbon group has 13 or more carbon atoms.
- the step of using the hydrazine derivative represented by the above formula (1) is a C-terminal protection step of protecting the carboxy group of the amino acid compound or the peptide compound by the hydrazine derivative represented by the above formula (1).
- N-terminal deprotection step for deprotecting the N-terminal of the N-terminal protected C-terminal protected amino acid compound or N-terminal protected C-terminal protected peptide compound obtained in the C-terminal protection step, and the N-terminal deprotection step.
- the peptide compound according to ⁇ 3> further comprising a peptide chain extension step of condensing the N-terminal protected amino acid compound or N-terminal protected peptide compound with the N-terminal of the C-terminal protected amino acid compound or C-terminal protected peptide compound obtained in Production method.
- ⁇ 5> The method for producing a peptide compound according to ⁇ 4>, further comprising a precipitation step of precipitating the N-terminal protected C-terminal protected peptide compound obtained in the peptide chain extension step.
- ⁇ 6> The method for producing a peptide compound according to ⁇ 4>, further comprising an extraction step of adding water to the N-terminal protected C-terminal protected peptide compound obtained in the peptide chain extension step and extracting and separating impurities into the aqueous phase. ..
- a step of deprotecting the N-terminal of the obtained N-terminal protected C-terminal protected peptide compound, and an N-terminal protected amino acid compound at the N-terminal of the obtained C-terminal protected peptide compound After the precipitation step or extraction step, a step of deprotecting the N-terminal of the obtained N-terminal protected C-terminal protected peptide compound, and an N-terminal protected amino acid compound at the N-terminal of the obtained C-terminal protected peptide compound.
- the peptide compound according to ⁇ 5> or ⁇ 6> further comprising a step of condensing the N-terminal protected peptide compound and a step of precipitating the obtained N-terminal protected C-terminal protected peptide compound at least once in this order. Production method.
- ⁇ 8> The method for producing a peptide compound according to any one of ⁇ 1> to ⁇ 7>, which further comprises a C-terminal deprotection step of deprotecting a C-terminal protecting group.
- ⁇ 9> The method for producing a peptide compound according to any one of ⁇ 1> to ⁇ 8>, wherein the ring A is a benzene ring, a naphthalene ring, or a pyridine ring.
- ⁇ 11> The method for producing a peptide compound according to any one of ⁇ 1> to ⁇ 10>, wherein n is 1.
- ⁇ 12> The method for producing a peptide compound according to any one of ⁇ 1> to ⁇ 11>, wherein k is 1.
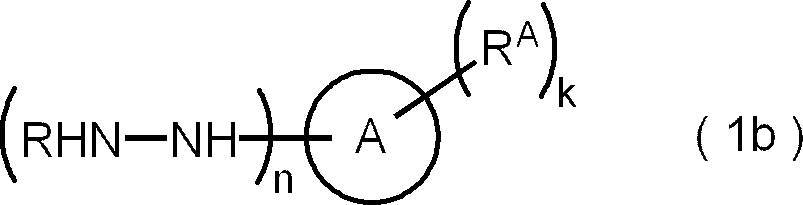
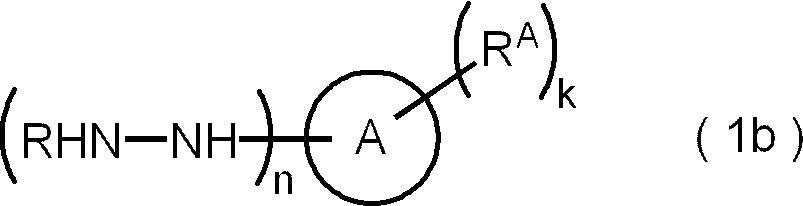
- ⁇ 13> A reagent for forming a protecting group containing a hydrazine derivative represented by the following formula (1a).
- ring A represents an aromatic hydrocarbon ring or an aromatic heterocycle
- R represents a hydrogen atom or an amino-protecting group
- k represents an integer of 1 to 5
- n represents an integer of 1 to 5.
- R a is independently an aliphatic hydrocarbon group, or represents an organic group having an aliphatic hydrocarbon group, the carbon of the at least one aliphatic hydrocarbon group in the k R a
- the number is 13 or more.
- reagent for forming a protecting group according to ⁇ 13> wherein the reagent for forming a protecting group is a reagent for forming a protecting group of a carboxy group.
- reagent for forming a protecting group according to ⁇ 13> or ⁇ 14> wherein the reagent for forming a protecting group is a reagent for forming a carboxy group of an amino acid compound or a reagent for forming a C-terminal protecting group of a peptide compound.
- ⁇ 16> The reagent for forming a protecting group according to any one of ⁇ 13> to ⁇ 15>, wherein the ring A is a benzene ring, a naphthalene ring, or a pyridine ring.
- ⁇ 18> The reagent for forming a protecting group according to any one of ⁇ 13> to ⁇ 17>, wherein n is 1.
- ⁇ 19> The reagent for forming a protecting group according to any one of ⁇ 13> to ⁇ 18>, wherein k is 1.
- ring A represents an aromatic hydrocarbon ring or an aromatic heterocycle
- R represents a hydrogen atom or an amino-protecting group
- k represents an integer of 1 to 5
- n represents an integer of 1 to 5.
- R a is independently an aliphatic hydrocarbon group, or represents an organic group having an aliphatic hydrocarbon group, the carbon of at least two aliphatic hydrocarbon groups in the k R a The number is 13 or more.
- ⁇ 21> The hydrazine derivative according to ⁇ 20>, wherein the ring A is a benzene ring, a naphthalene ring, or a pyridine ring.
- ⁇ 22> The hydrazine derivative according to ⁇ 20> or ⁇ 21>, wherein n is 1.
- ⁇ 23> The hydrazine derivative according to any one of ⁇ 20> to ⁇ 22>, wherein k is 1.
- a method for producing a peptide compound having an excellent yield at the time of deprotection it is possible to provide a reagent for forming a protecting group having an excellent yield at the time of deprotection.
- a novel hydrazine derivative can be provided.
- the numerical range represented by using "-" in the present specification means a range including the numerical values before and after "-" as the lower limit value and the upper limit value.
- the upper limit value or the lower limit value described in one numerical range may be replaced with the upper limit value or the lower limit value of another numerical range described stepwise. Good.
- the upper limit value or the lower limit value of the numerical range may be replaced with the value shown in the examples.
- the term "process” is included in this term not only as an independent process but also as long as the intended purpose of the process is achieved even when it cannot be clearly distinguished from other processes.
- the notation that does not describe substitution and non-substitution includes those having no substituent as well as those having a substituent.
- the "alkyl group” includes not only an alkyl group having no substituent (unsubstituted alkyl group) but also an alkyl group having a substituent (substituted alkyl group).
- the chemical structural formula in the present specification may be described by a simplified structural formula in which a hydrogen atom is omitted.
- “% by mass” and “% by weight” are synonymous, and “parts by mass” and “parts by weight” are synonymous.
- a combination of two or more preferred embodiments is a more preferred embodiment.
- the "organic group having an aliphatic hydrocarbon group” is a monovalent (one bond) organic group having an aliphatic hydrocarbon group in its molecular structure.
- the "aliphatic hydrocarbon group” is preferably a linear, branched, or cyclic saturated or unsaturated aliphatic hydrocarbon group having 5 or more carbon atoms, and also has a carbon number (also referred to as "carbon atom number”).
- An aliphatic hydrocarbon group having 5 to 60 carbon atoms is more preferable, an aliphatic hydrocarbon group having 5 to 40 carbon atoms is further preferable, and an aliphatic hydrocarbon group having 10 to 30 carbon atoms is particularly preferable.
- the site of the aliphatic hydrocarbon group in the organic group having an aliphatic hydrocarbon group is not particularly limited, and may be present at the terminal (monovalent group) or at another site (for example, divalent).
- the "aliphatic hydrocarbon group” includes a monovalent group such as an alkyl group, a cycloalkyl group, an alkenyl group, and an alkynyl group, and a divalent group derived from them (a hydrogen atom is selected from the monovalent group described above). Divalent groups excluding one), groups excluding hydroxy groups from various steroid groups, and the like.
- alkyl group for example, an alkyl group having 1 to 30 carbon atoms is preferable, and for example, a methyl group, an ethyl group, a propyl group, an isopropyl group, a butyl group, a sec-butyl group, an isobutyl group, a tert-butyl group and the like are preferable.
- Pentyl group isopentyl group, 2-methylbutyl group, 2-pentyl group, 3-pentyl group, hexyl group, octyl group, 2-ethylhexyl group, decyl group, hexadecyl group, octadecyl group, icosyl group, docosyl group, tetracosyl group.
- Lauryl group tridecyl group, myristyl group, isostearyl group and the like.
- alkyl group in the above aliphatic hydrocarbon group an octadecyl group, an icosyl group, a docosyl group or a tetracosyl group is preferable, and an icosyl group, a docosyl group or a tetracosyl group is more preferable.
- alkyl group in the aliphatic hydrocarbon group an alkyl group having 5 to 40 carbon atoms is preferable, and an alkyl group having 10 to 30 carbon atoms is more preferable.
- the "alkyl group” in the present disclosure may be a linear alkyl group or a branched alkyl group unless otherwise specified.
- the alkenyl group and the alkynyl group are the same as those of the alkyl group.
- a cycloalkyl group for example, a cycloalkyl group having 3 to 30 carbon atoms is preferable, and examples thereof include a cyclopentyl group, a cyclohexyl group, an isobornyl group, a tricyclodecanyl group and the like. Further, these may be repeatedly connected, or may have a condensed ring structure of two or more rings. Further, as the cycloalkyl group in the above aliphatic hydrocarbon group, a cycloalkyl group having 5 to 30 carbon atoms is more preferable.
- alkenyl group for example, an alkenyl group having 2 to 30 carbon atoms is preferable, and examples thereof include a pentenyl group, a hexenyl group, an oleyl group and the like. Further, as the “alkenyl group”, an alkenyl group having 5 to 30 carbon atoms is more preferable.
- alkynyl group for example, an alkynyl group having 2 to 30 carbon atoms is preferable, and examples thereof include a 4-pentynyl group and a 5-hexenyl group. Further, as the "alkynyl group”, an alkynyl group having 5 to 30 carbon atoms is more preferable.
- steroid group for example, a group having a cholesterol structure, a group having an estradiol structure, or the like is preferable.
- aryl group for example, an aryl group having 6 to 14 carbon atoms is preferable, and examples thereof include a phenyl group, a 1-naphthyl group, a 2-naphthyl group, a biphenylyl group, a 2-anthryl group and the like.
- amino protecting group protecting group of amino group
- examples of the "amino protecting group (protecting group of amino group)” include a formyl group, an acyl group having 1 to 6 carbon atoms (eg, an acetyl group and a propionyl group), and an alkoxycarbonyl group having 2 to 6 carbon atoms (eg, an alkoxycarbonyl group).
- These groups consist of a halogen atom (eg, fluorine atom, chlorine atom, bromine atom, iodine atom), an alkoxy group having 1 to 6 carbon atoms (eg, methoxy group, ethoxy group, propoxy group), and a nitro group. It may be substituted with 1 to 3 substituents selected from the group.
- a halogen atom eg, fluorine atom, chlorine atom, bromine atom, iodine atom
- an alkoxy group having 1 to 6 carbon atoms eg, methoxy group, ethoxy group, propoxy group
- a nitro group e.g, 1,3-butanethoxycarbonyl group
- an alkoxycarbonyl group having 1 to 6 carbon atoms and an arylalkyloxycarbonyl group having 7 to 20 carbon atoms are preferable.
- hydroxy group protecting group examples include an alkyl group having 1 to 6 carbon atoms, a phenyl group, a trityl group, a formyl group, an acyl group having 1 to 6 carbon atoms, a benzoyl group, and an arylalkyl group having 7 to 10 carbon atoms.
- examples thereof include a carbonyl group, a 2-tetrahydropyranyl group, a 2-tetrahydrofuranyl group, a silyl group, and an alkenyl group having 2 to 6 carbon atoms. Even if these groups are substituted with 1 to 3 substituents selected from the group consisting of halogen atoms, alkyl groups having 1 to 6 carbon atoms, alkoxy groups having 1 to 6 carbon atoms, and nitro groups. Good.
- Examples of the "carboxyl protecting group” include an alkyl group having 1 to 6 carbon atoms, an arylalkyl group having 7 to 10 carbon atoms, a phenyl group, a trityl group, a silyl group, an alkenyl group having 2 to 6 carbon atoms, and the like. Can be mentioned. These groups may be substituted with 1 to 3 substituents selected from the group consisting of halogen atoms, alkoxy groups having 1 to 6 carbon atoms, and nitro groups.
- Examples of the "carbonyl group protecting group” include cyclic acetals (eg, 1,3-dioxane), acyclic acetals (eg, di (alkyl having 1 to 6 carbon atoms) acetals) and the like.
- Examples of the “guanidyl protecting group” include 2,2,4,6,7-pentamethyldihydrobenzofuran-5-sulfonyl group, 2,3,4,5,6-pentamethylbenzenesulfonyl group and tosyl group. , Nitro group and the like.
- protecting group of the mercapto group include a trityl group, a 4-methylbenzyl group, an acetylaminomethyl group, a t-butyl group, a t-butylthio group and the like.
- the method for producing a peptide compound according to the present disclosure includes a step of using a hydrazine derivative represented by the following formula (1).
- Ring A represents an aromatic hydrocarbon ring or an aromatic heterocycle.
- R represents a hydrogen atom, an amino protecting group, an amino acid residue, or a peptide residue.
- k represents an integer from 1 to 5 and represents n represents 1 or 2 RA independently represent an aliphatic hydrocarbon group or an organic group having an aliphatic hydrocarbon group. At least one aliphatic hydrocarbon group in k RA has 13 or more carbon atoms.
- the hydrazine derivative represented by the above formula (1) has not been known at all. Since the hydrazine derivative represented by the above formula (1) has a hydradino group bonded to an aromatic hydrocarbon ring or an aromatic heterocycle, it is oxidized at the time of deprotection without subjecting the reaction system to acidic conditions. Deprotection can be performed by the reaction, deprotection in a uniform system, which has been difficult in the past, can be easily performed, and the yield of the substitution reaction with a nucleophile is excellent. I presume that it is excellent.
- the loading yield (yield at the time of protection) is excellent, and the bond with the C-terminal of the peptide compound is a stable amide bond. It is presumed that the by-product of hydrazine can be suppressed.
- the hydrazine derivative represented by the above formula (1) has a carbon number of at least one aliphatic hydrocarbon group in the k R A from being 13 or more, after the condensation completed, to change the composition of the solvent Thereby, the condensate can be precipitated and isolated, and the yield of the obtained peptide compound is also excellent. Furthermore, since the hydrazine derivative represented by the formula (1) according to the present disclosure has the above structure, side reactions can be suppressed and a peptide compound can be synthesized in a high yield.
- a poorly synthesized peptide compound such as an unnatural peptide containing an unnatural amino acid that easily causes a side reaction suppresses the side reaction and has high purity.
- a poorly synthesized peptide compound such as an unnatural peptide containing an unnatural amino acid that easily causes a side reaction suppresses the side reaction and has high purity.
- the diketopiperazine compound described later may be produced as a by-product, the by-product of the diketopiperazine compound can be suppressed, and the peptide compound can be obtained in a high yield.
- the hydrazine derivative represented by the formula (1) not only forms a protecting group, but also modifies the peptide compound, adjusts the solubility in water or an organic solvent, and crystallizes. It can be used for improvement, multimerization, etc.
- the hydrazine derivative represented by the formula (1) is preferably used for forming a protecting group, and more preferably used for forming a C-terminal protecting group in an amino acid compound or a peptide compound.
- Ring A represents an aromatic hydrocarbon ring or an aromatic heterocycle.
- R represents a hydrogen atom, an amino protecting group, an amino acid residue, or a peptide residue.
- k represents an integer from 1 to 5 and represents n represents 1 or 2 RA independently represent an aliphatic hydrocarbon group or an organic group having an aliphatic hydrocarbon group. At least one aliphatic hydrocarbon group in k RA has 13 or more carbon atoms.
- the ring A in the formula (1) represents an aromatic hydrocarbon ring or an aromatic heterocycle, and the ring A may further have a substituent in addition to RA and -NH-NHR.
- the aromatic hydrocarbon ring and the aromatic heterocycle in the ring A may be a monocyclic ring or a fused ring having two or more rings.
- the fused rings include two or more fused polycyclic aromatic hydrocarbon rings, two or more fused polycyclic aromatic heterocycles, one or more aromatic hydrocarbon rings, and one or more aromatic heterocycles. The fused ring of.
- Ring A is more likely to be monocyclic or bicyclic from the viewpoint of deprotection rate, by-product inhibitory property of diketopiperazine compound, yield at the time of peptide compound synthesis, and yield at the time of deprotection. It is preferable, and it is particularly preferable that it is a single ring. Further, the ring A is preferably an aromatic hydrocarbon ring from the viewpoint of crystallization property, deprotection rate, and yield at the time of deprotection.
- Ring A includes a benzene ring, a naphthalene ring, an anthracene ring, and a phenanthrene ring from the viewpoints of deprotection rate, by-product inhibitory property of diketopiperazine compound, yield at the time of peptide compound synthesis, and yield at the time of deprotection.
- Tetracene ring triphenylene ring, pyrene ring, chrysene ring, pyridine ring, quinoline ring, isoquinoline ring, benzothiophene ring, furan ring, benzofuran ring, pyrrole ring, indole ring, carbazole ring, pyrazole ring, indazole ring, or thiophene. It is preferably a ring, more preferably a benzene ring, a naphthalene ring, or a pyridine ring, further preferably a benzene ring or a pyridine ring, and particularly preferably a benzene ring.
- the ring A may have a ring structure in which two or more substituents are bonded to each other, and the ring A has a structure in which an aliphatic hydrocarbon ring, an aliphatic heterocycle, or the like is further condensed. It may be.
- the substituent which may be contained on the ring A is not particularly limited, but is an alkyl group having 1 to 10 carbon atoms (preferably 1 to 4 carbon atoms).
- R st- CO-NR st- , -CON (R st ) 2 dialkylamino group with 1 to 10 carbon atoms, alkylarylamino group with 6 to 20 carbon atoms, diarylamino group with 12 to 30 carbon atoms, and these Examples include a group in which two or more of the above are combined.
- R st represents a hydrogen atom, an alkyl group having 1 to 10 carbon atoms, or an aryl group having 6 to 20 carbon atoms.
- the amino protecting group of R the above-mentioned amino protecting group can be used, but an alkoxycarbonyl group having 2 to 6 carbon atoms and an arylalkyloxycarbonyl group having 8 to 20 carbon atoms are preferable.
- the amino acid residue or peptide residue which is R means that the hydroxy group is removed from the amino acid or peptide and can bind to -NH-NH-.
- R is an amino acid residue or a peptide residue, it is also a protected amino acid compound or peptide compound.
- the types of amino acid residues and peptide residues are not particularly limited, but those described in Examples are preferable.
- the amino acid residue the amino acid residue described in the C-terminal protection step described later is preferably mentioned, and as the peptide residue, the residue obtained by removing the hydroxy group from the peptide compound described in the C-terminal protection step described later.
- R is a hydrogen atom, a Boc group, an Fmoc group, a benzyloxycarbonyl group (Cbz group), a 2,2,2-trichloroethoxycarbonyl group (Troc group), or an allyloxycarbonyl from the viewpoint of synthetic suitability.
- a group (Alloc group) it is more preferably a Boc group, an Fmoc group, a Cbz group, a Troc group, or an Alloc group, and a Boc group or an Fmoc group. It is more preferably present, and particularly preferably it is a Boc group. Further, from the viewpoint of reactivity, a hydrogen atom is particularly preferable as R.
- k in the formula (1) is preferably an integer of 1 to 4, more preferably an integer of 1 to 3, and particularly preferably 1.
- N in the formula (1) is preferably 1 from the viewpoint of the yield at the time of peptide compound synthesis and the yield at the time of deprotection.
- R A is independently an aliphatic hydrocarbon group, or represents an organic group having an aliphatic hydrocarbon group, the number of carbon atoms of at least one aliphatic hydrocarbon group in the k R A is 13 or more.
- RA is preferably an organic group having an aliphatic hydrocarbon group independently from the viewpoint of crystallization and solubility, and is an organic having two or more aliphatic hydrocarbon groups having 13 or more carbon atoms. It is more preferably a group, more preferably an organic group having 2 to 6 aliphatic hydrocarbon groups having 13 or more carbon atoms, and 2 or 3 aliphatic hydrocarbon groups having 13 or more carbon atoms. It is particularly preferable that the organic group has.
- the aliphatic hydrocarbon group having 13 or more carbon atoms preferably has 13 or more carbon atoms, and more preferably 14 or more carbon atoms, from the viewpoint of solvent solubility, crystallization, and yield. It is more preferable that the number of carbon atoms is 16 or more, and it is particularly preferable that the number of carbon atoms is 18 or more.
- the organic group may be further substituted with a silyl group, a hydrocarbon group having a silyloxy structure, or an organic group having a perfluoroalkyl structure.
- silyl group a trialkylsilyl group is preferable, and a silyl group having three alkyl groups having 1 to 6 carbon atoms is more preferable.
- the silyloxy structure of the hydrocarbon group having a silyloxy structure is preferably a trialkylsilyloxy structure, and more preferably a silyloxy structure having three alkyl groups having 1 to 6 carbon atoms.
- the hydrocarbon group having a silyloxy structure preferably has 1 to 6 silyloxy structures.
- the number of carbon atoms of the hydrocarbon group having a silyloxy structure is preferably 10 or more, more preferably 10 to 100, and particularly preferably 16 to 50.
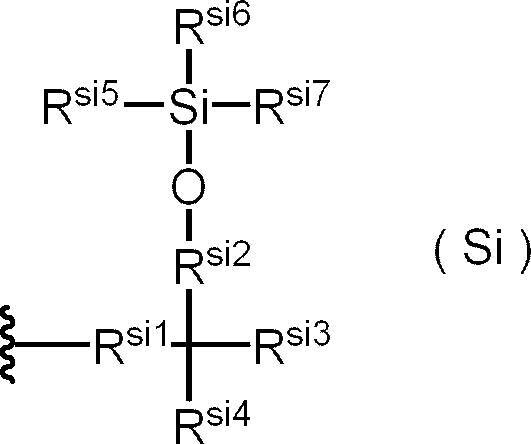
- hydrocarbon group having the silyloxy structure a group represented by the following formula (Si) is preferably mentioned.
- R si1 is a single bond, or represents an alkylene group having 1 to 3 carbon atoms
- R si2 represents an alkylene group having 1 to 3 carbon atoms
- R si3 and R si4 are each independently , Hydrogen atom, alkyl group having 1 to 6 carbon atoms, or -OSiR si5 R si6 R si7
- R si5 to R si7 independently represent an alkyl group or an aryl group having 1 to 6 carbon atoms. ..
- Each of R si5 to R si7 in the formula (Si) is preferably an alkyl group having 1 to 6 carbon atoms or a phenyl group independently, and more preferably an alkyl group having 1 to 6 carbon atoms.
- the perfluoroalkyl structure in the organic group having a perfluoroalkyl structure is preferably a perfluoroalkyl structure having 1 to 20 carbon atoms, more preferably a perfluoroalkyl structure having 5 to 20 carbon atoms, and carbon. It is particularly preferable to have a perfluoroalkyl structure of the number 7 to 16. Further, the perfluoroalkyl structure may be linear, may have a branch, or may have a ring structure.
- the organic group having a perfluoroalkyl structure is preferably a perfluoroalkyl group, an alkyl group having a perfluoroalkyl structure, or an alkyl group having a perfluoroalkyl structure and an amide bond in the alkyl chain.
- the number of carbon atoms of the organic group having a perfluoroalkyl structure is preferably 5 or more, more preferably 10 or more, further preferably 10 to 100, and particularly preferably 16 to 50. ..
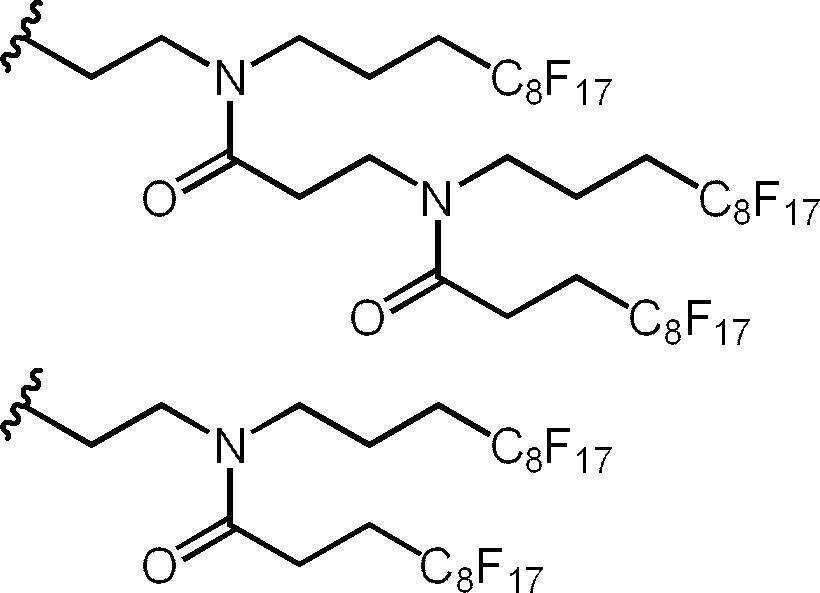
- the organic group having the perfluoroalkyl structure for example, the groups shown below are preferably mentioned.
- the site other than the aliphatic hydrocarbon group in the organic group having an aliphatic hydrocarbon group can be arbitrarily set. For example, even if it has a site such as an ether bond, a thioether bond, an ester bond, a sulfonamide bond, an amide bond, or a hydrocarbon group (monovalent group or divalent group) other than the "aliphatic hydrocarbon group". Good.
- the hydrocarbon group other than the aliphatic hydrocarbon group include an aliphatic hydrocarbon group having 1 to 4 carbon atoms, an aromatic hydrocarbon group and the like, and specifically, for example, having 1 to 4 carbon atoms.
- a monovalent group such as an alkyl group and an aryl group, and a divalent group derived from them are used.
- an aryl group having 6 to 10 carbon atoms is more preferable, and a phenyl group is particularly preferable.
- the hydrocarbon group other than the above-mentioned aliphatic hydrocarbon group and the above-mentioned aliphatic hydrocarbon group may be substituted with a substituent selected from a halogen atom, an oxo group and the like.
- binding to the ring A of the organic group having an aliphatic hydrocarbon group (substituted) may be via an aliphatic hydrocarbon group or the hydrocarbon group present in the R A, i.e., direct carbon -It may be bonded by a carbon bond or may be via a site such as an ether bond, a thioether bond, an ester bond, an amide bond, or a sulfonamide bond existing in the above RA.
- the organic group having an aliphatic hydrocarbon group preferably has at least an ester bond, an amide bond or a sulfonamide bond, and may have at least an ester bond or an amide bond from the viewpoint of easiness of synthesizing the compound. More preferred.
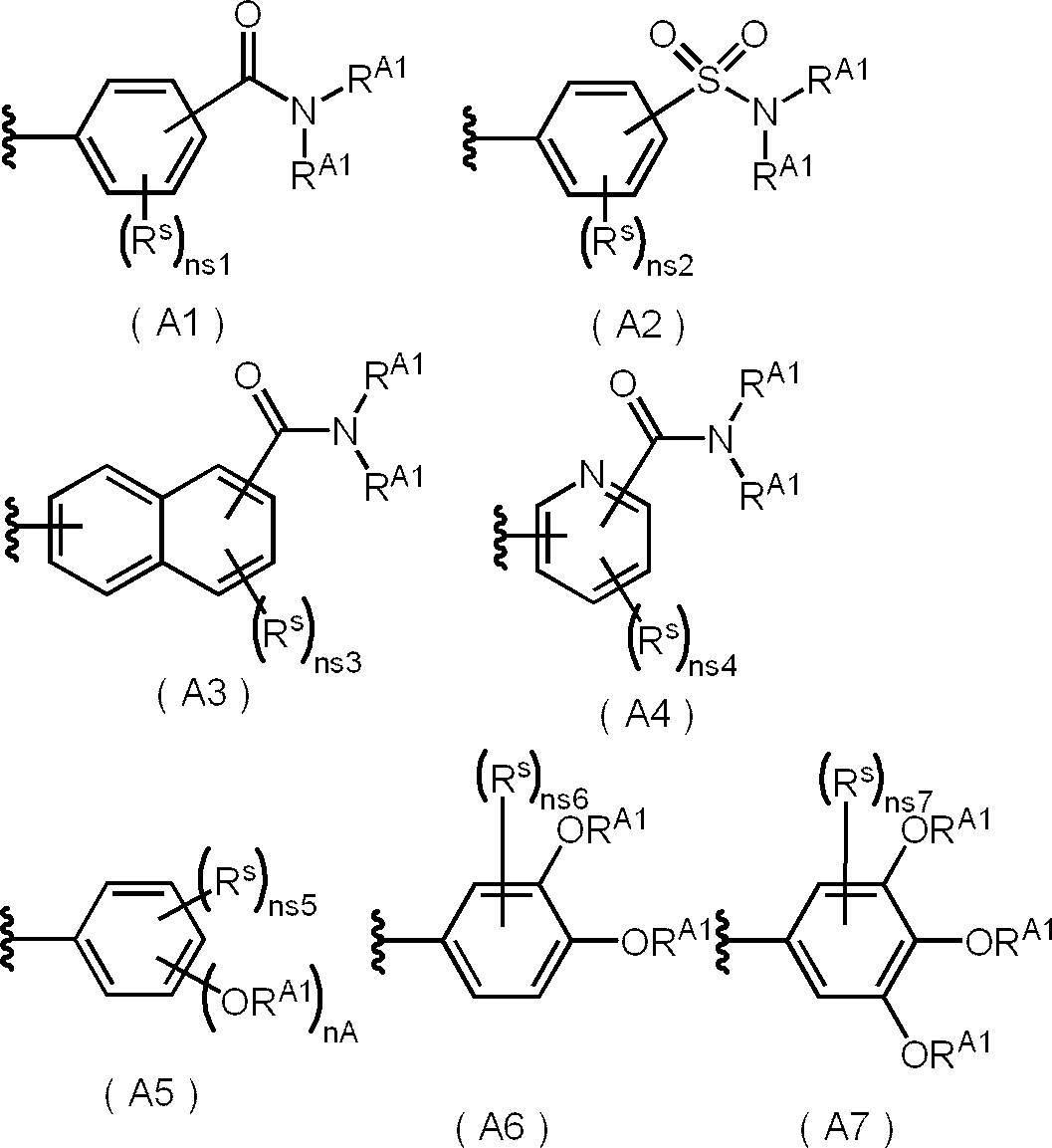
- the organic group having an aliphatic hydrocarbon group preferably has a group represented by the following formulas (A1) to (A5) from the viewpoint of synthetic suitability, crystallization property and solubility.
- a group represented by the following formulas (A1) to (A4) and further preferably to have a group represented by the following formula (A1) or formula (A2).
- a group represented by the following formula (A1) is particularly preferable to have a group represented by the following formula (A1).
- the group represented by the following formula (A5) is preferably a group represented by the following formula (A6) or formula (A7) from the viewpoint of crystallization and solubility.
- R A1 is independently an aliphatic hydrocarbon group having 13 or more carbon atoms
- nA represents an integer of 1 to 5
- each R s is independently a substituted group
- Ns1 and ns2 independently represent an integer of 0 to 4
- ns3 represents an integer of 0 to 6
- ns4 represents an integer of 0 to 3
- ns5 represents an integer of 0 to (5-nA).
- Ns6 represents an integer of 0 to 3
- ns7 represents an integer of 0 to 2
- the wavy line portion represents a connection position with another structure.
- each R A1 independently in Formula (A1) ⁇ formula (A7) in terms of yield and availability of raw materials at the time of peptide compounds synthesis, is preferably an aliphatic hydrocarbon group having a carbon number of 16-40, carbon It is more preferably an aliphatic hydrocarbon group having a number of 18 to 36, further preferably an alkyl group having 18 to 32 carbon atoms, and particularly preferably a linear alkyl group having 18 to 22 carbon atoms.
- R A1 in the formula (A1) ⁇ formula (A7) from the viewpoint of synthesis suitability, it is preferable that all of them are the same group.
- nA in the formula (A5) is preferably an integer of 1 to 4, more preferably an integer of 2 to 4, and particularly preferably 2 or 3. .
- ns1 and ns2 in the formula (A1) or the formula (A2) are preferably integers of 0 to 2, more preferably 0 or 1, and particularly preferably 0.
- the ns3 in the formula (A3) is preferably an integer of 0 to 4, more preferably an integer of 0 to 2, and particularly preferably 0.
- Ns4 in the formula (A4) is preferably an integer of 0 to 2, more preferably 0 or 1, and particularly preferably 0.
- ns5 to ns7 in the formulas (A5) to (A7) are preferably 0 or 1, and more preferably 0.
- the total number of carbon atoms in all the aliphatic hydrocarbon group having all of R A, solvent solubility, crystal segregation, deprotection speed, by-production of diketopiperazine compounds is preferably 26 or more, more preferably 26 to 200, and even more preferably 32 to 100. , 34-80, most preferably 44-66.
- the hydrazine derivative represented by the formula (1) has a carbon number of at least one aliphatic hydrocarbon group in the k R A is a compound is several 13 or more carbon atoms, solubility in solvents, crystallization segregation From the viewpoint, it is preferable that at least two aliphatic hydrocarbon groups in k RA have 13 or more carbon atoms, and one or more RA having two or more aliphatic hydrocarbon groups having 13 or more carbon atoms. It is more preferable to have. For example, in the case where " at least two aliphatic hydrocarbon groups in k RA have 13 or more carbon atoms", the hydrazine derivative represented by the formula (1) is an aliphatic hydrocarbon having 13 or more carbon atoms.
- a R a having a group of two or more may be a mode having at least one, to the R a to only one have a number 13 or more aliphatic hydrocarbon group having a carbon may be an embodiment having two or more , Both aspects may be used.
- the hydrazine derivative represented by the formula (1) is more preferably a compound having at least one aliphatic hydrocarbon group having 13 to 100 carbon atoms from the viewpoint of solubility and crystallization.
- a compound having at least one aliphatic hydrocarbon group of 18 to 40 is more preferable, and a compound having at least one aliphatic hydrocarbon group having 20 to 36 carbon atoms is particularly preferable.
- Hydrazine derivatives represented by the formula (1) has a carbon number of at least one aliphatic hydrocarbon group in the k R A is preferably 14 or more, more preferably 16 or more, more preferably 18 or more, particularly preferably When is 20 or more, a better effect is exhibited. The reason is that as the number of carbon atoms increases, the contribution of hydrophobicity to the entire molecule increases, making it easier to dissolve in hydrophobic solvents, and for hydrophilic solvents, the increase in carbon number causes cohesion. This is thought to be because the force increases and crystallization becomes easier.
- the aliphatic hydrocarbon group is preferably an alkyl group, more preferably a linear alkyl group, from the viewpoint of crystallization property.
- each carbon number of one R A independently, be a solvent soluble, from the viewpoint of crystal segregation, preferably 13 to 200, more preferably from 18 to 150, a 18-100 Is more preferable, and 20 to 80 is particularly preferable.
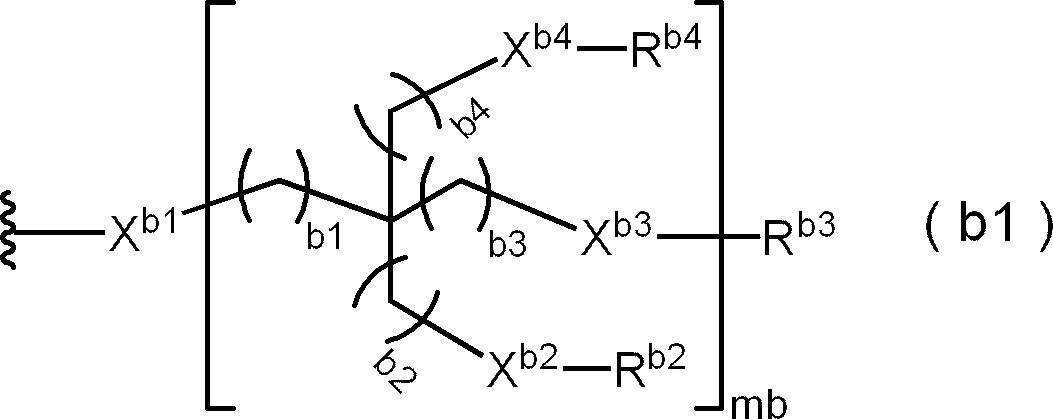
- At least one RA is of the following formula (f1), formula (a1), formula (b1) or formula (e1) from the viewpoint of solvent solubility, crystallization and yield. It is preferably a group represented by any of the following, more preferably a group represented by the following formula (f1) or (a1), and particularly preferably a group represented by the following formula (f1). preferable.
- the wavy line portion represents the coupling position with other structures
- m9 represents an integer of 1 to 3
- X 9 independently represents a single coupling, -O-, -S-, and -COO-.
- R 9 independently represents a divalent aliphatic hydrocarbon group
- Ar 1 is (m10 + 1). It represents a valent aromatic group or a (m10 + 1) valent heteroaromatic group
- m10 represents an integer of 1 to 3
- X 10 are independently single-bonded, -O-, -S-,-, respectively.
- each R 10 is independently, represents a monovalent aliphatic hydrocarbon group, at least one of R 10 One is a monovalent aliphatic hydrocarbon group having 5 or more carbon atoms.
- the wavy line portion represents the bonding position with other structures
- m20 represents an integer of 1 to 10
- X 20 is independently single-bonded, -O-, -S-, and -COO.
- R 20 each independently represents a divalent aliphatic hydrocarbon group, at least one of R 20 Is a divalent aliphatic hydrocarbon group having 5 or more carbon atoms.
- the wavy line portion represents the coupling position with another structure
- mb represents 1 or 2
- b1 to b4 each independently represent an integer of 0 to 2
- X b1 to X b4 represent an integer of 0 to 2.
- Each independently represents a single bond, -O-, -S-, -COO-, -OCONH-, or -CONH-
- R b2 and R b4 independently represent a hydrogen atom, a methyl group, or a carbon. It represents an aliphatic hydrocarbon group having 5 or more carbon atoms
- R b3 represents an aliphatic hydrocarbon group having 5 or more carbon atoms.
- the wavy line portion represents a bond position with another structure
- X e1 represents a single bond, -O-, -S-, -NHCO-, or -CONH-
- me is 0 to 0 to.
- e1 represents an integer of 0 to 11
- e2 represents an integer of 0 to 5
- X e2 independently represent single bonds, -O-, -S-, -COO-, and -OCONH.
- R e2 each independently represents a hydrogen atom, a methyl group, an organic group having an aliphatic hydrocarbon group having 5 or more carbon atoms.
- the m9 in the formula (f1) is preferably 1 or 2, and more preferably 1.
- X 9 and X 10 in the formula (f1) are preferably -O-, -S-, -COO-, -OCONH-, or -CONH-, and more preferably -O-. preferable.
- Each of R 9 in the formula (f1) is preferably an alkylene group having 1 to 10 carbon atoms, more preferably an alkylene group having 1 to 4 carbon atoms, and particularly preferably a methylene group.
- Each of R 10 in the formula (f1) is preferably a monovalent aliphatic hydrocarbon group having 5 to 60 carbon atoms, and more preferably a monovalent aliphatic hydrocarbon group having 12 to 50 carbon atoms.
- a monovalent aliphatic hydrocarbon group having 18 to 40 carbon atoms is more preferable, and a monovalent aliphatic hydrocarbon group having 20 to 32 carbon atoms is particularly preferable.
- each of R 10 is preferably a linear alkyl group or a branched alkyl group independently, and more preferably a linear alkyl group.
- the m10 in the formula (f1) is preferably 2 or 3, and more preferably 2.
- Ar 1 in the formula (f1) is preferably an aromatic group having a (m10 + 1) valence, and is a group obtained by removing (m10 + 1) hydrogen atoms from benzene, or removing (m10 + 1) hydrogen atoms from naphthalene. It is more preferable that it is a naphthalene group, and it is particularly preferable that it is a group obtained by removing (m10 + 1) hydrogen atoms from benzene.
- the group represented by the above formula (f1) is preferably a group represented by the following formula (f2) from the viewpoint of solvent solubility, crystallization and yield.
- the wavy line portion represents the connection position with other structures
- m10 represents an integer of 1 to 3
- m11 represents an integer of 1 to 3
- X 10 is an independent single bond.
- R 10 is an independent one with 5 or more carbon atoms.
- m10 in formula (f2), X 10 and R 10 has the same meaning as m10, X 10 and R 10 in the formula (f1), preferable embodiments thereof are also the same.
- M11 in the formula (f2) is preferably 1 or 2, and more preferably 1.
- the m20 in the formula (a1) is preferably 1 or 2.
- To X 20 are each independently of formula (a1), -O -, - S -, - COO -, - OCONH-, or preferably from -CONH-, more preferably -O-.
- R 20 in the formula (a1) is preferably 5 or more divalent aliphatic hydrocarbon group having a carbon, more preferably a divalent aliphatic hydrocarbon group having 5 to 60 carbon atoms, carbon It is more preferably a divalent aliphatic hydrocarbon group having a number of 8 to 40, and particularly preferably a divalent aliphatic hydrocarbon group having 12 to 32 carbon atoms.
- R 20 is preferably a linear alkylene group.
- the mb in the formula (b1) is preferably 1.
- b1 to b4 in the formula (b1) are preferably 1 or 2, and more preferably 1.
- X b1 to X b4 in the formula (b1) are preferably -O-, -S-, -COO-, -OCONH-, or -CONH-, and more preferably -O-. preferable.
- R b2 and R b4 in the formula (b1) are preferably hydrogen atoms, methyl groups, or aliphatic hydrocarbon groups having 5 to 60 carbon atoms, respectively, and are hydrogen atoms, methyl groups, or carbon atoms.
- R b3 in the formula (b1) is preferably a monovalent aliphatic hydrocarbon group having 5 to 60 carbon atoms, and more preferably a monovalent aliphatic hydrocarbon group having 5 to 60 carbon atoms.
- a monovalent aliphatic hydrocarbon group having 8 to 40 carbon atoms is more preferable, and a monovalent aliphatic hydrocarbon group having 12 to 32 carbon atoms is particularly preferable.
- R b3 is preferably a linear alkyl group.
- the organic group having an aliphatic hydrocarbon group having a branch is used as the organic group having an aliphatic hydrocarbon group.
- the groups shown below are more preferred.
- the wavy line portion represents a bonding position with another structure
- nt2 represents an integer of 3 or more
- nt3 represents an integer set so that the total carbon number of the following groups is 14 to 300.
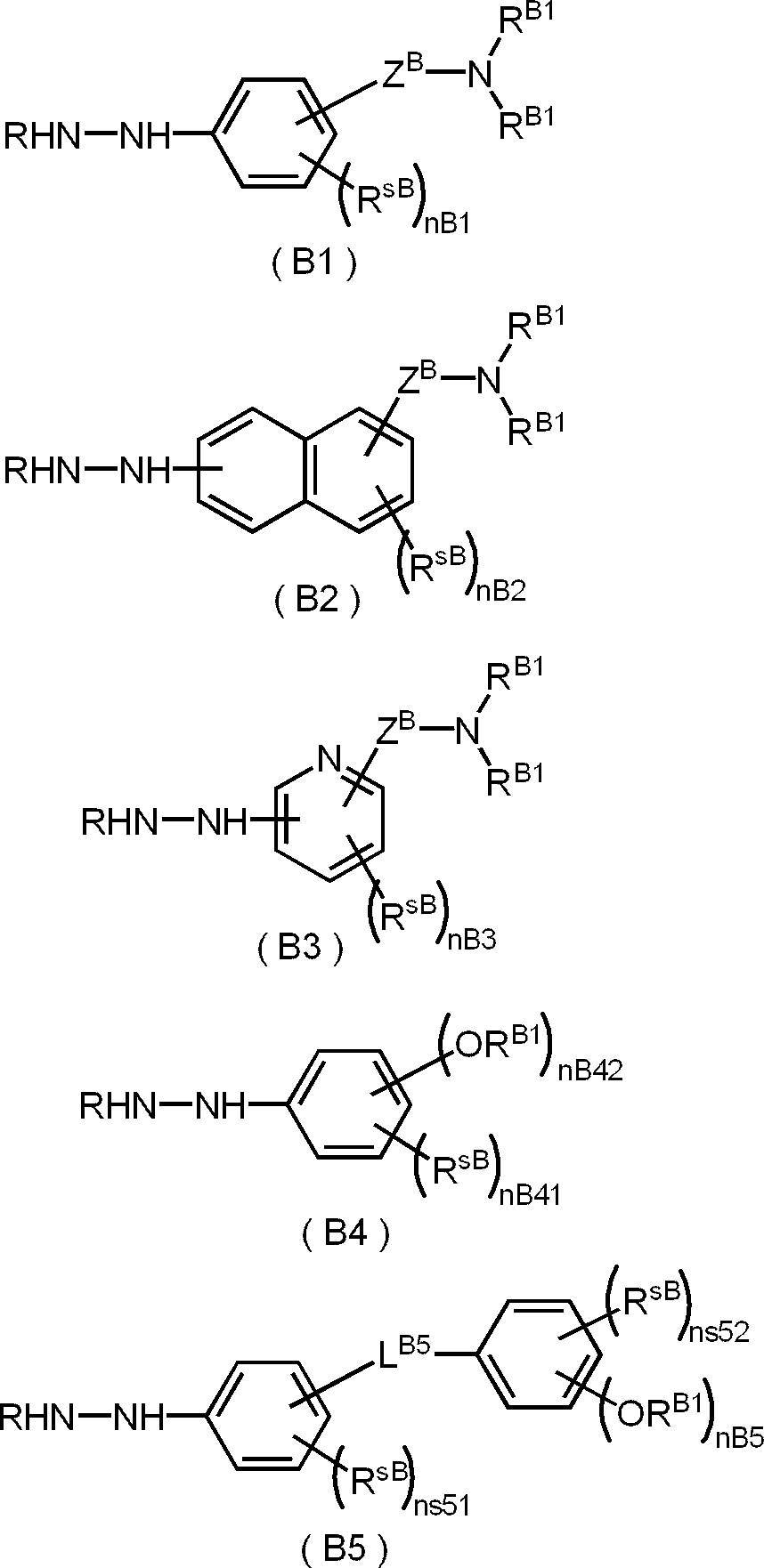
- the hydrazine derivative represented by the formula (1) may be a compound represented by any of the following formulas (B1) to (B5) from the viewpoint of synthetic suitability and yield at the time of deprotection. It is preferable that the compound is represented by any of the formulas (B1) to (B4), and the compound represented by the formula (B1) is particularly preferable.
- R B1 independently represents an aliphatic hydrocarbon group having 13 or more carbon atoms
- Z B represents a carbonyl group or a sulfonyl group
- R sB independently represents a carbonyl group or a sulfonyl group.
- nB1 independently represents an integer of 0 to 4
- nB2 represents an integer of 0 to 6
- nB3 represents an integer of 0 to 3
- nB41 represents an integer of 0 to 4
- nB42 independently represents an aliphatic hydrocarbon group having 13 or more carbon atoms
- Z B represents a carbonyl group or a sulfonyl group
- R sB independently represents a carbonyl group or a sulfonyl group.
- Ns51 represents an integer of 0 to 4
- ns52 represents an integer of 0 to 4
- nB5 + ns52 an integer of 1 to 5 is satisfied.
- R in the formulas (B1) to (B5) is synonymous with R in the formula (1), and the preferred embodiment is also the same.
- the R B1 independently in Formula (B1) ⁇ formula (B5) is preferably an aliphatic hydrocarbon group having a carbon number of 16-40, carbon It is more preferably an aliphatic hydrocarbon group having a number of 18 to 36, further preferably an alkyl group having 18 to 32 carbon atoms, and particularly preferably a linear alkyl group having 18 to 22 carbon atoms.
- R B1 in the formula (B1) ⁇ formula (B5) from the viewpoint of synthesis suitability, it is preferable that all of them are the same group.
- nB5 in the formula (B5) is preferably an integer of 1 to 4, more preferably an integer of 2 to 4, and particularly preferably 2 or 3. .
- R sB in the formulas (B1) to (B5) a substituent similar to the substituent which may be contained on the ring A is preferably mentioned.
- nB1 in the formula (B1) is preferably an integer of 0 to 2, more preferably 0 or 1, and particularly preferably 0.
- NB2 in the formula (B2) is preferably an integer of 0 to 4, more preferably an integer of 0 to 2, and particularly preferably 0.
- NB3 in the formula (B3) is preferably an integer of 0 to 2, more preferably 0 or 1, and particularly preferably 0.
- NB41 in the formula (B4) is preferably 0 or 1, more preferably 0. NB42 in the formula (B4) is preferably an integer of 2 to 5, more preferably 2 to 4, and particularly preferably 2 or 3.
- the group may be a combination of at least one bond selected from the group consisting of an ester bond, an amide bond, a sulfonamide bond, an ether bond, a urethane bond and a urea bond and one or more alkylene groups. More preferred It is more preferable that the group is a combination of at least one bond selected from the group consisting of an ester bond, an amide bond and a sulfonamide bond and one or more alkylene groups. It is particularly preferable that the group is a combination of one or two bonds of at least one selected from the group consisting of ester bonds, amide bonds and sulfonamide bonds and one or two alkylene groups.
- substitution positions on the benzene ring of -OR B1 in the formula (B5) is not particularly limited, the substitution position of L B5 to (position 1) is preferably 3-position and 5-position.
- the ns51 in the formula (B5) is preferably an integer of 0 to 2, more preferably 0 or 1, and particularly preferably 0.
- the ns52 in the formula (B5) is preferably an integer of 0 to 2, more preferably 0 or 1, and particularly preferably 0.
- the molecular weight of the hydrazine derivative represented by the formula (1) is not particularly limited, but is deprotection rate, crystallization property, solvent solubility, by-product inhibitory property of diketopiperazine compound, yield at the time of peptide compound synthesis, From the viewpoint of the yield at the time of deprotection, it is preferably 340 to 3,000, more preferably 400 to 2,000, further preferably 500 to 1,500, and 800 to 1 , 300 is particularly preferable.
- the molecular weight is 3,000 or less, the proportion of the hydrazine derivative represented by the formula (1) in the target product is appropriate, and the hydrazine derivative represented by the formula (1) can be deprotected. Since the proportion of the compound does not decrease, the productivity is excellent.
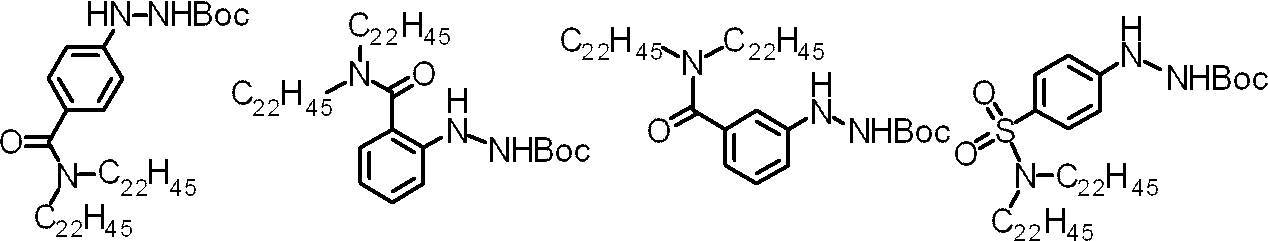
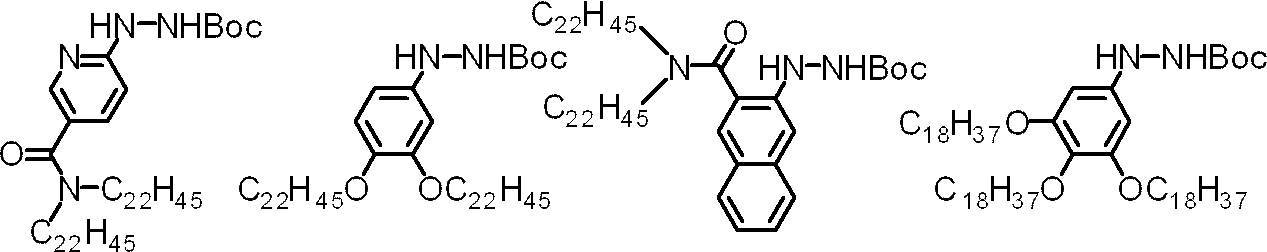
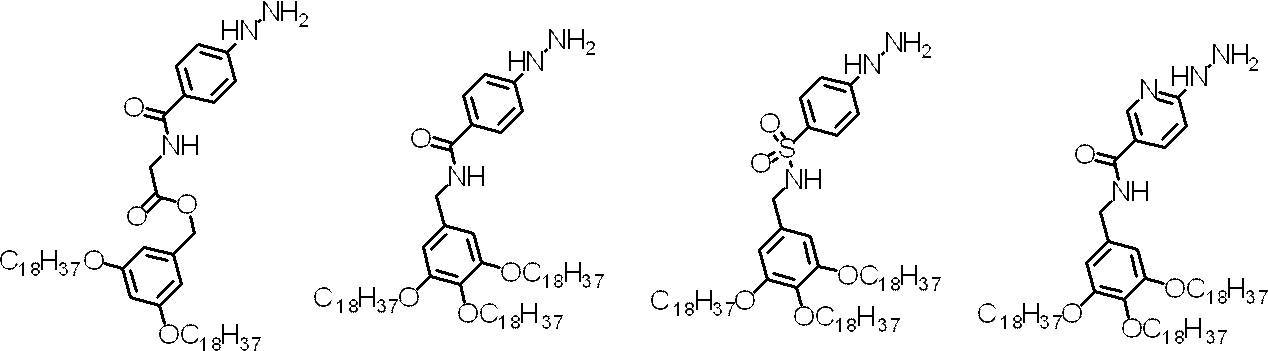
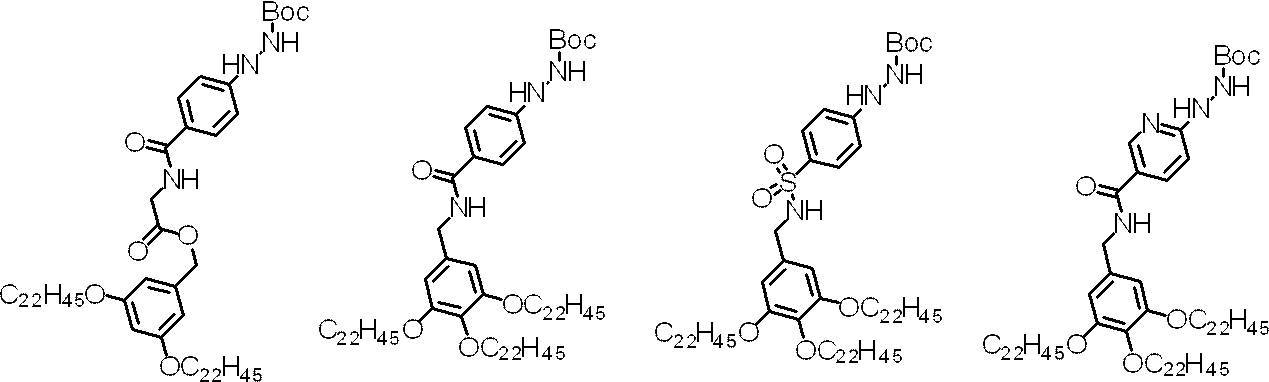
- hydrazine derivative represented by the formula (1) include, but needless to say, the compounds shown below.
- the method for producing the hydrazine derivative represented by the formula (1) is not particularly limited, but it can be produced by referring to a known method.
- the raw material compound used for producing the hydrazine derivative represented by the formula (1) may be a commercially available compound, or may be produced according to a method known per se or a method similar thereto. You can also.
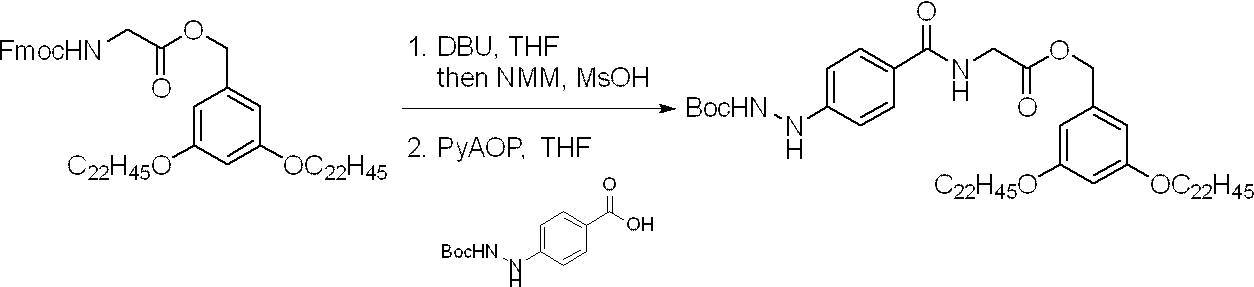
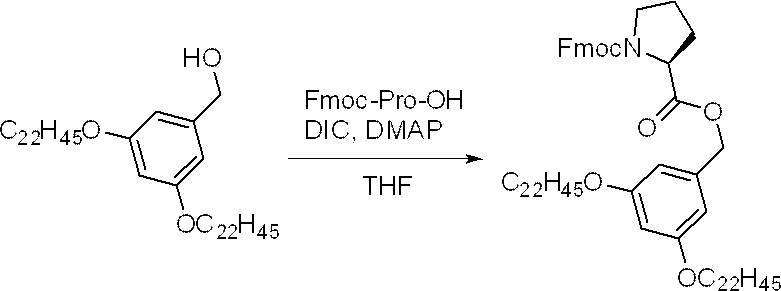
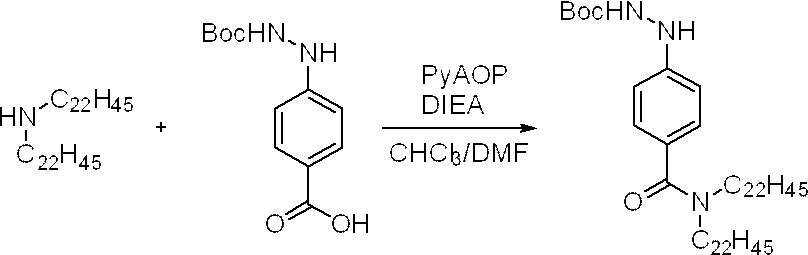
- a group having an aliphatic hydrocarbon group having 13 or more carbon atoms into an aromatic hydrazine derivative such as tert-butoxycarbonylhydrazinelbenzoic acid, it is preferably represented by the formula (1). Hydrazine derivatives can be made.
- the produced hydrazine derivative represented by the formula (1) may be purified by a known purification method.
- a method of isolating and purifying by recrystallization, column chromatography, or the like, a method of purifying by reprecipitation by means for changing the solution temperature, a means for changing the solution composition, or the like can be performed.
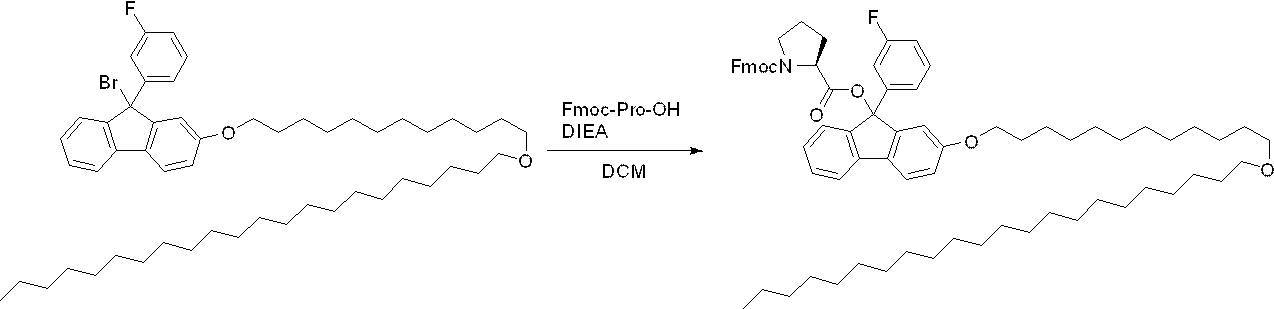
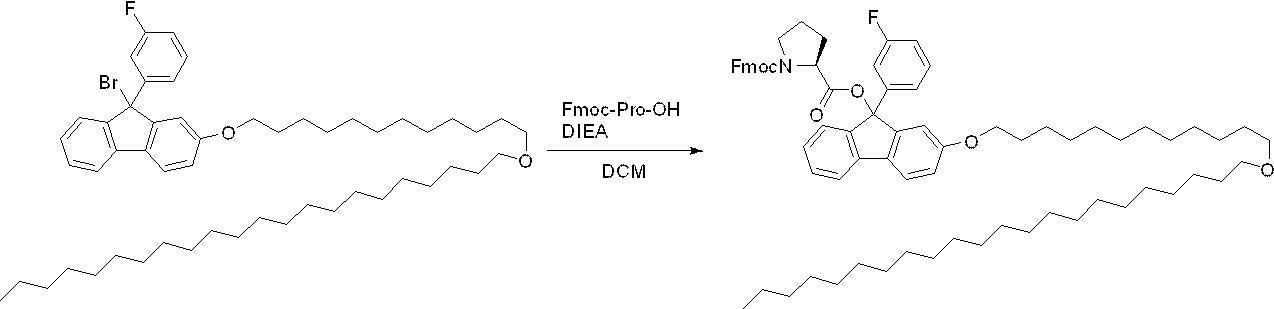
- the step of using the hydrazine derivative represented by the above formula (1) protects the carboxy group of the amino acid compound or the peptide compound by the hydrazine derivative represented by the above formula (1). It is preferably a C-terminal protection step. Further, in the method for producing a peptide compound according to the present disclosure, the carboxy group of the amino acid compound or the peptide compound is protected by the hydrazine derivative represented by the above formula (1) from the viewpoint of ease of synthesis of the peptide compound and yield.
- the N-terminal deprotection step for deprotecting the N-terminal of the N-terminal protected C-terminal protected amino acid compound or the N-terminal protected C-terminal protected peptide compound obtained in the C-terminal protection step and the above-mentioned
- the peptide chain extension step of condensing the N-terminal protected amino acid compound or the N-terminal protected peptide compound at the N-terminal of the C-terminal protected amino acid compound or the C-terminal protected peptide compound obtained in the N-terminal deprotection step may be further included.
- More preferred Water is added to the precipitation step of precipitating the N-terminal protected C-terminal protected peptide compound obtained in the peptide chain extension step, or the N-terminal protected C-terminal protected peptide compound obtained in the peptide chain extension step to remove impurities. It is more preferable to further include an extraction step of extracting and separating into the aqueous phase.
- the method for producing a peptide compound according to the present disclosure preferably further includes a dissolution step of dissolving the hydrazine derivative represented by the above formula (1) in a solvent before the C-terminal protection step.
- R in the hydrazine derivative represented by the above formula (1) is an amino acid residue or a peptide residue, it is used as a reaction substrate in the N-terminal deprotection step or the peptide chain extension step. , Can be preferably used.
- each step and the like described above will be described in detail.
- the method for producing a peptide compound according to the present disclosure preferably includes a dissolution step of dissolving the hydrazine derivative represented by the above formula (1) in a solvent before the C-terminal protection step.
- a solvent a general organic solvent can be used for the reaction, but the higher the solubility in the above solvent, the better the reactivity can be expected. Therefore, the solvent having a high solubility of the hydrazine derivative represented by the formula (1). It is preferable to select.
- halogenated hydrocarbons such as chloroform and dichloromethane
- non-polar organic solvents such as 1,4-dioxane, tetrahydrofuran, cyclopentyl methyl ether and 4-methyltetrahydropyran. Two or more of these solvents may be mixed and used in an appropriate ratio.
- aromatic hydrocarbons such as benzene, toluene and xylene
- nitriles such as acetonitrile and propionitrile
- ketones such as acetone and 2-butanone
- N N.
- -Amids such as dimethylformamide and N-methylpyrrolidone; sulfoxides such as dimethyl sulfoxide and esters such as isopropyl acetate and ethyl acetate in an appropriate ratio as long as the hydrazine derivative represented by the formula (1) can be dissolved. May be mixed and used in.
- the solvent described in Organic Process Research & Development, 2017, 21, 3, 365-369 may be used.
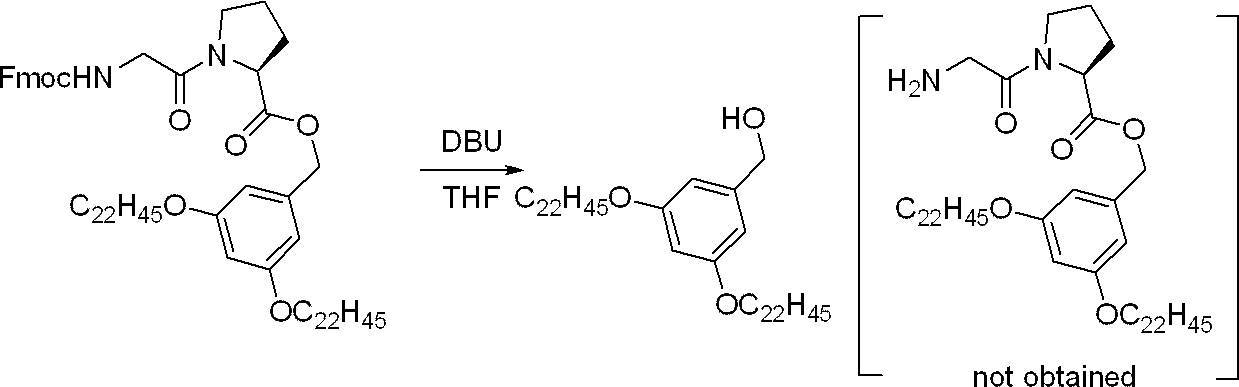
- ⁇ Amino protecting group deprotection step on hydrazino group> when a compound in which R in the hydrazine derivative represented by the above formula (1) is an amino protecting group is used, the amino protection of R in the hydrazine derivative represented by the formula (1) is used. It is preferred to include an amino protecting group deprotection step on the hydrazino group that deprotects the group. Further, the amino protecting group deprotection step on the hydradino group may be performed before or at the same time as the C-terminal protection step described later. Further, the hydrazine derivative represented by the formula (1) in which the amino-protecting group is deprotected and R is a hydrogen atom may be isolated, or may be used as it is in the C-terminal protection step described later without isolation. Good.
- the deprotection conditions are appropriately selected depending on the type of the amino protecting group described above, but a group capable of deprotecting under conditions different from the removal of the protecting group at the N-terminal described later is preferable.
- a group capable of deprotecting under conditions different from the removal of the protecting group at the N-terminal described later is preferable.
- an Fmoc group it is carried out by treating with a base
- a Boc group it is carried out by treating with an acid.
- the reaction is carried out in a solvent that does not affect the reaction.
- the base secondary amines such as dimethylamine and diethylamine, 1,8-diazabicyclo [5.4.0] -7-undecene (DBU), and 1,4-diazabicyclo [2.2.2] octane ( Examples include non-nucleophilic organic bases such as DABCO) and 1,5-diazabicyclo [4.3.0] -5-nonen (DBN).
- the above-mentioned solvent can be preferably used in the above-mentioned dissolution step.
- the method for producing a peptide compound according to the present disclosure preferably includes a C-terminal protection step of protecting the carboxy group of the amino acid compound or the peptide compound with the hydrazine derivative represented by the above formula (1).
- the amino acid compound or peptide compound used in the C-terminal protection step is not particularly limited, and known ones can be used, but the N-terminal protected amino acid compound or the N-terminal protected peptide compound may be used. More preferably, it is an Fmoc-protected amino acid compound or an Fmoc-protected peptide compound.
- the method for producing a peptide compound according to the present disclosure can suppress the by-product of the diketopiperazine compound, and therefore, from the viewpoint of exerting the above effect more, the proline residue, which is a peptide compound in which the diketopiperazine compound is likely to be by-produced Peptide compounds having at least one residue selected from the group consisting of groups, glycine residues, N-alkyl amino acid residues, peptoids, and D-amino acid residues are preferably used, with proline residues or glycine residues. It is more preferable to use a peptide compound having a residue, and a peptide compound having a proline residue is particularly preferable.
- the positions and numbers of the proline residue, glycine residue, N-alkyl amino acid residue, peptoid, and D-amino acid residue in the peptide compound are not particularly limited, but the C-terminal amino acid residue, Alternatively, the amino acid residue next to the C-terminal amino acid residue is preferably at least a proline residue, a glycine residue, an N-alkyl amino acid residue, a peptoid, or a D-amino acid residue, and is a C-terminal amino acid. More preferably, the residue is at least a proline residue, a glycine residue, an N-methyl amino acid residue, or a D-amino acid residue.
- the amino acid compound used in the C-terminal protection step or the hydroxy group, amino group, carbonyl group, amide group, imidazole group, indol group, guanidyl group, mercapto group and the like other than the C-terminal portion of the peptide compound are described above. It is preferably protected by a known protective group.
- the amount of the amino acid compound or peptide compound used as the reaction substrate is preferably 1 molar equivalent to 10 molar equivalents, preferably 1 molar equivalent to 5 molar equivalents, relative to 1 molar equivalent of the hydrazine derivative represented by the above formula (1). Equivalents are more preferred, 1 molar equivalents to 2 molar equivalents are even more preferred, and 1 molar equivalents to 1.5 molar equivalents are particularly preferred.
- a condensing agent in the presence of a condensation additive (condensation activator) in a solvent that does not affect the reaction, or to react in an acid catalyst.
- the amount of the condensation additive used is preferably 0.05 molar equivalent to 1.5 molar equivalent with respect to 1 molar equivalent of the hydrazine derivative represented by the above formula (1).
- a condensing agent generally used in peptide synthesis can be used without limitation in the present disclosure, and is not limited to this, for example, 4- (4,6-dimethoxy-1,3,5).
- -Triazine-2-yl) -4-methylmorphonium chloride DTMMM
- O- (benzotriazole-1-yl) -1,1,3,3-tetramethyluronium hexafluorophosphate HBTU
- O- (6-chlorobenzotriazole-1-yl) -1,1, 3,3-Tetramethyluronium hexafluorophosphate HBTU (6-Cl)
- O- (benzotriazole-1-yl) -1,1,3,3-tetramethyluronium tetrafluorobolate TBTU
- the amount of the condensing agent used is preferably 1 molar equivalent to 10 molar equivalents, preferably 1 molar equivalent to 5 molar equivalents, relative to 1 molar equivalent of the hydrazine derivative represented by the above formula (1). preferable.
- an acid catalyst generally used in peptide synthesis can be used without limitation, and for example, trifluoroacetic acid (TFA), hydrochloric acid, trifluoroethanol (TFE), hexafluoroisopropanol (HFIP) can be used. ), Acetic acid, methanesulfonic acid, trifluoromethanesulfonic acid, p-toluenesulfonic acid and the like. Of these, trifluoroacetic acid is preferable.
- the amount of the acid catalyst used is preferably more than 0 molar equivalent and 4.0 molar equivalent with respect to 1 molar equivalent of the hydrazine derivative represented by the above formula (1), and is 0.05 molar equivalent to 1.5 molar equivalent. It is more preferably a molar equivalent, and even more preferably 0.1 molar equivalent to 0.3 molar equivalent.
- condensation activator in the present disclosure is a reagent that, in coexistence with a condensing agent, leads an amino acid to a corresponding active ester, symmetric acid anhydride, or the like to facilitate the formation of a peptide bond (amide bond).
- a condensation activator generally used in peptide synthesis can be used without limitation, and for example, 4-dimethylaminopyridine, N-methylimidazole, boronic acid derivative, 1-hydroxybenzotriazole (1-hydroxybenzotriazole).
- HOBt ethyl 1-hydroxytriazole-4-carboxylate
- HACt 1-hydroxy-7-azabenzotriazole
- HONb 3-hydroxy-1,2,3-benzotriazodin-4 (3H)- On
- HOOBt N-Hydroxysuccinimide
- HPht N-Hydroxyphthalimide
- HONb N-Hydroxy-5-norbornene-2,3-dicarboxyimide
- pentafluorophenol ethyl (hydroxyimino) cyanoacetate (Oxyma) and the like can be mentioned.
- the amount of the activator used is preferably more than 0 molar equivalent and 4.0 molar equivalent, more preferably 0.1 molar equivalent to 1.5 molar equivalent, relative to the amino acid compound or peptide compound. ..
- a base generally used in peptide synthesis can be used without limitation, and examples thereof include a tertiary amine such as diisopropylethylamine.
- the solvent the above-mentioned solvent can be preferably used in the above-mentioned dissolution step.
- the reaction temperature is not particularly limited, but is preferably ⁇ 10 ° C. to 80 ° C., more preferably 0 ° C. to 40 ° C.
- the reaction time is not particularly limited, but is preferably 1 hour to 30 hours.
- a method similar to that of a general liquid phase organic synthesis reaction can be applied. That is, the reaction can be traced using thin layer silica gel chromatography, high performance liquid chromatography, NMR or the like.
- the N-terminal protected C-terminal protected amino acid compound or the N-terminal protected C-terminal protected peptide compound obtained by the above C-terminal protection step may be purified.
- the N-terminal is used in order to isolate the product obtained after dissolving the obtained N-terminal protected C-terminal protected amino acid compound or N-terminal protected C-terminal protected peptide compound in a solvent and carrying out the desired organic synthesis reaction.
- a method of changing the solvent in which the protected C-terminal protected amino acid compound or the N-terminal protected C-terminal protected peptide compound is dissolved eg, changing the solvent composition, changing the type of solvent
- reprecipitating is preferably mentioned.
- the reaction is carried out under conditions such that the N-terminal protected C-terminal protected amino acid compound or the N-terminal protected C-terminal protected peptide compound is dissolved, and after the reaction, the solvent is distilled off and then the solvent is replaced. After the reaction, the agglomerates are precipitated and impurities are eliminated by adding a polar solvent to the reaction system without distilling off the solvent.
- polar organic solvents such as methanol, acetonitrile and water are used alone or in combination.
- the reaction is carried out under conditions such that the N-terminal protected C-terminal protected amino acid compound or the N-terminal protected C-terminal protected peptide compound is dissolved, and after the reaction, the solvent substitution is, for example, a halogenated solvent, THF or the like for dissolution.
- a polar organic solvent such as methanol, acetonitrile or water, or a mixed solvent thereof is used.
- the method for producing a peptide compound according to the present disclosure includes an N-terminal deprotection step of deprotecting the N-terminal of the N-terminal protected C-terminal protected amino acid compound or the N-terminal protected C-terminal protected peptide compound obtained in the above C-terminal protection step. It is preferable to include it.
- the N-terminal protecting group the above-mentioned amino group protecting group generally used in technical fields such as peptide chemistry can be used, but in the present disclosure, the Boc group, Cbz group, or Fmoc group is used. It is preferably used.
- the deprotection conditions are appropriately selected depending on the type of the temporary protecting group, but are different from the removal of the protecting group derived from the hydrazine derivative represented by the above formula (1) (amino protecting group deprotecting step on the hydrazino group).
- a group that can be deprotected depending on the conditions is preferable.
- an Fmoc group it is carried out by treating with a base
- a Boc group it is carried out by treating with an acid.
- the reaction is carried out in a solvent that does not affect the reaction.
- the base the above-mentioned base can be preferably used in the step of deprotecting the amino protecting group on the hydrazino group.
- the solvent the above-mentioned solvent can be preferably used in the above-mentioned dissolution step.
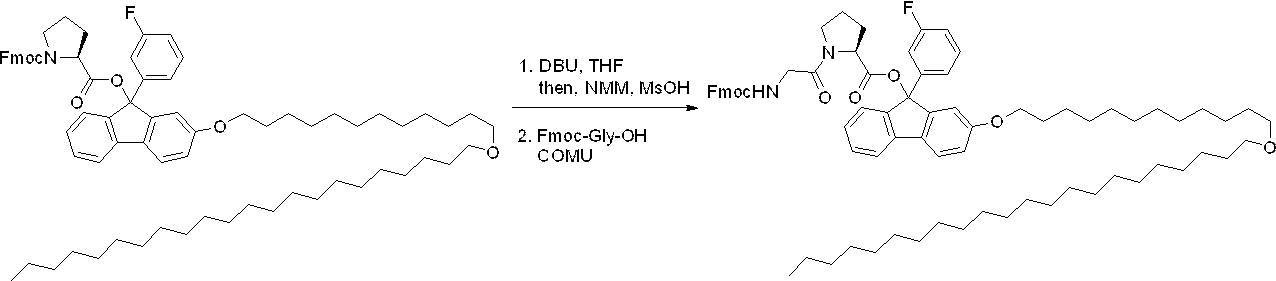
- the method for producing a peptide compound according to the present disclosure is a method for producing an N-terminal protected amino acid compound or an N-terminal protected peptide compound at the N-terminal of the C-terminal protected amino acid compound or C-terminal protected peptide compound obtained in the above N-terminal deprotection step. It is preferable to include a peptide chain extension step of condensing.
- the peptide chain extension step is preferably performed under peptide synthesis conditions generally used in the field of peptide chemistry, using the above-mentioned condensing agent, condensation additive and the like.
- the N-terminal protected amino acid compound or N-terminal protected peptide compound is not particularly limited, and any desired one can be used, but an Fmoc-protected amino acid compound or Fmoc-protected peptide compound can be preferably used.
- the hydroxy group, amino group, carbonyl group, amide group, imidazole group, indol group, guanidyl group, mercapto group and the like other than the C-terminal portion of the N-terminal protected amino acid compound or the N-terminal protected peptide compound are protective groups described later. It is preferable that it is protected by a known protective group such as.
- the method for producing a peptide compound according to the present disclosure preferably further includes a precipitation step of precipitating the N-terminal protected C-terminal protected peptide compound obtained in the peptide chain extension step.
- the precipitation step can be carried out in the same manner as the precipitation method in purification which may be carried out after the above-mentioned C-terminal protection step.
- the method for producing a peptide compound according to the present disclosure preferably further includes an extraction step of adding water to the N-terminal protected C-terminal protected peptide compound obtained in the peptide chain extension step and extracting and separating impurities into the aqueous phase. ..
- the extraction step for example, water is added to the N-terminal protected C-terminal protected peptide compound obtained in the peptide chain extension step or an organic solvent added thereto, and a liquid separation operation is performed to remove impurities from the aqueous phase.
- the aqueous phase and the oil phase or the N-terminal protected C-terminal protected peptide compound are separated from each other, and if necessary, the organic solvent is removed from the oil phase to obtain a purified N-terminal protected C-terminal protected peptide compound.
- the organic solvent the above-mentioned organic solvent can be used in the above-mentioned dissolution step.
- the extraction conditions and extraction operations in the above extraction step are not particularly limited, and can be performed using known extraction conditions and extraction operations.
- the method for producing a peptide compound according to the present disclosure is a step of deprotecting the N-terminal of the obtained N-terminal protected C-terminal protected peptide compound after the precipitation step, and the N-terminal of the obtained C-terminal protected peptide compound. It is preferable that the step of condensing the N-terminal protected amino acid compound or the N-terminal protected peptide compound and the step of precipitating the obtained N-terminal protected C-terminal protected peptide compound are further included once or more in this order. By repeating the above three steps, the chain extension of the obtained peptide compound can be easily performed. Each step in the above three steps can be performed in the same manner as each corresponding step described above.
- the method for producing a peptide compound according to the present disclosure preferably further includes a C-terminal deprotection step of deprotecting a C-terminal protecting group.
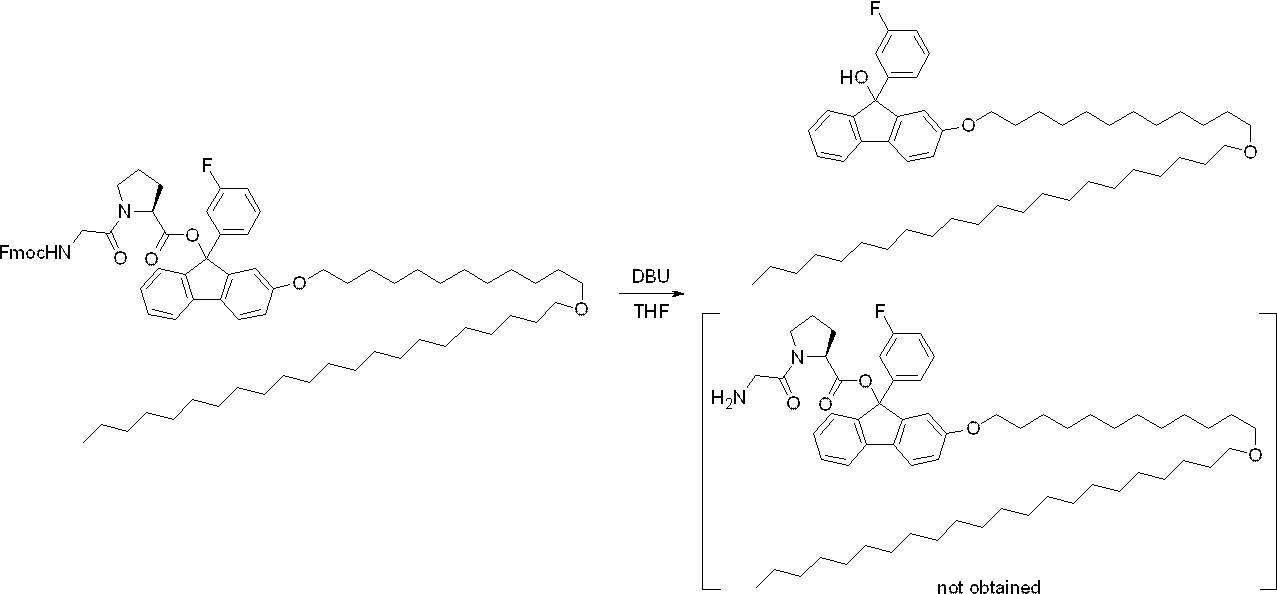
- the final object is obtained by removing the C-terminal protecting group formed by the hydrazine derivative represented by the above formula (1) in the C-terminal protected peptide compound having a desired number of amino acid residues. Can be obtained as a peptide compound.
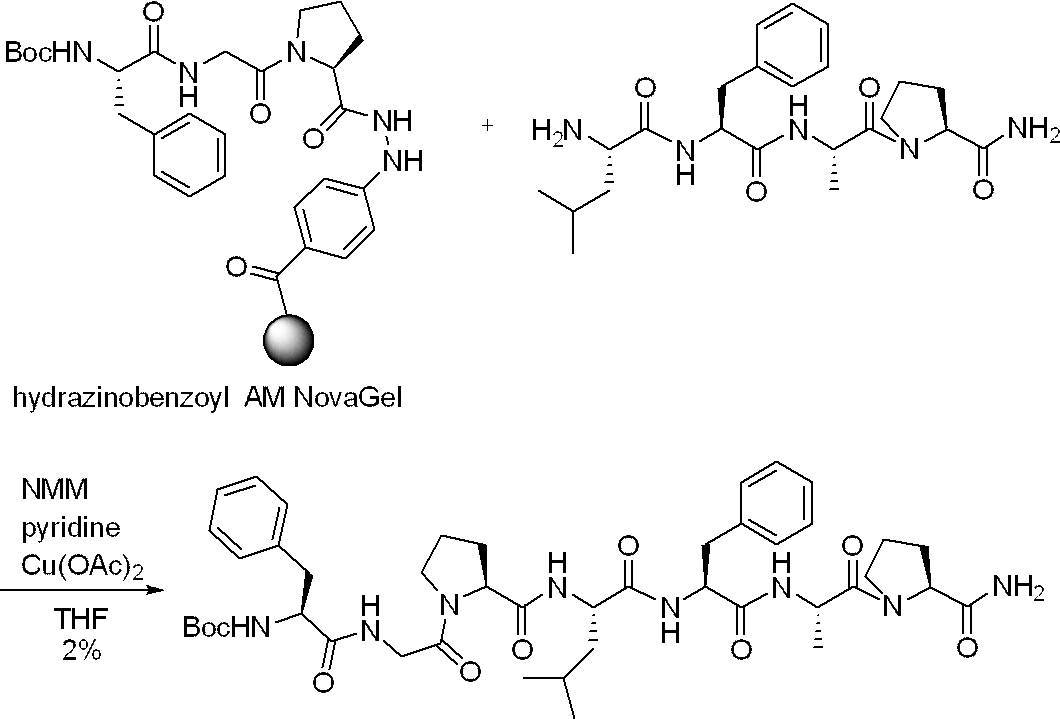
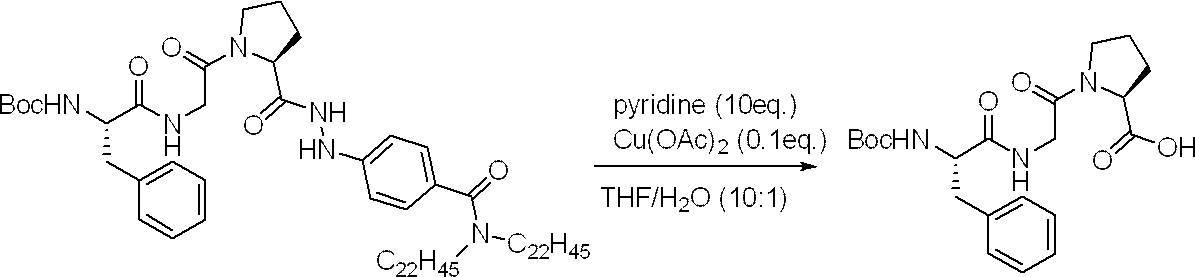
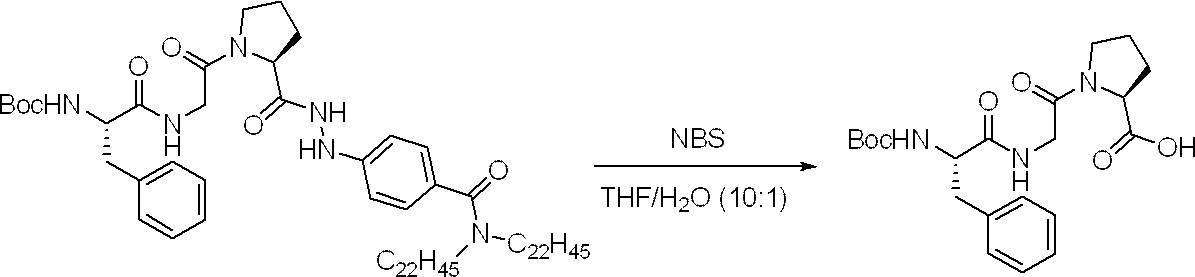
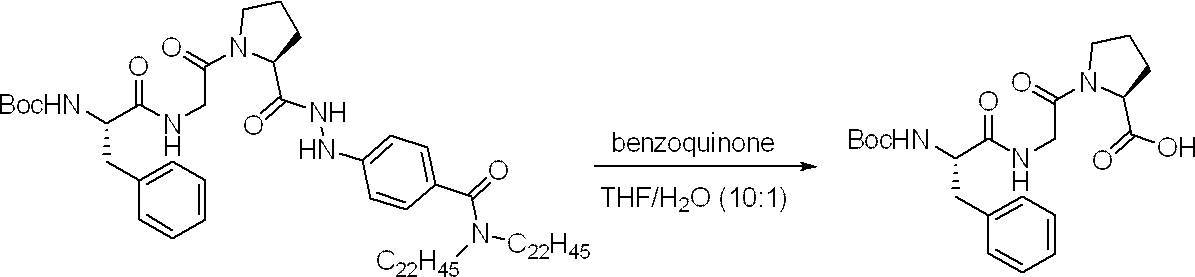
- a method for removing the C-terminal protecting group a deprotection method using an oxidizing agent is preferably mentioned.
- the oxidizing agent either an inorganic oxidizing agent or an organic oxidizing agent can be used, and a known oxidizing agent can be used.
- a metal hydrochloric acid agent is preferable, a copper hydrochloric acid agent is more preferable, and a divalent copper salt is particularly preferable.
- the divalent copper salt include copper bromide, copper chloride, copper fluoride, copper hydroxide, copper phosphate, copper acetate, copper dimethyldithiocarbamate, copper methoxide, copper ethoxydo, copper isopropoxyside, and copper ethylacetate acetate.
- 2-Ethylhexanate copper gluconate copper, hexafluoroacetylacetonate copper, isobutyrate copper, phthalate copper, trifuoloacetylacetonate copper, trifluoromethanesulfonate copper and the like.
- organic oxidizing agent quinones, hypervalent iodine, organic peroxide, or a compound having a nitrogen-halogen bond is preferable.
- N-halogenated nitrogen-containing compound examples include N-chlorosuccinimide, N-bromosuccinimide, N-iodosuccinimide, N-chlorophthalimide, N-bromophthalimide, N-iodophthalimide, N-chloroacetimide, and N-bromoacetate.
- Imide compounds such as imide and N-iodoacetimide, 1,3-dichloro-2,5-dimethylhydranthin, 1,3-dibromo-2,5-dimethylhydranthin, 1,3-diiodo-2,5-dimethylhydranthin
- Hydantin compounds such as 1,3,5-trichloroisocyanuric acid, 1,3,5-tribromoisocyanic acid, isocyanuric acid compounds such as 1,3,5-triiodoisocyanuric acid and the like can be mentioned.
- divalent copper salts, quinones, or N-halogenated nitrogen-containing compounds are preferable, and divalent copper halides, divalent carboxylic acid copper salts, benzoquinones, and N-halogenated imides are preferable.
- divalent copper acetate, 1,4-benzoquinone, or N-bromosuccinimide is particularly preferred.
- the above-mentioned solvent in the above-mentioned dissolution step a polar solvent such as water, an alcohol compound and acetonitrile, and a mixed solvent thereof can be preferably used.
- the reaction temperature is not particularly limited, but is preferably ⁇ 10 ° C. to 80 ° C., more preferably 0 ° C. to 40 ° C.
- the reaction time is not particularly limited, but is preferably 0.1 hour to 30 hours.
- the final target peptide compound obtained by the method for producing a peptide compound according to the present disclosure can be isolated and purified according to a method commonly used in peptide chemistry.
- the final target peptide compound can be isolated and purified by extracting and washing the reaction mixture, crystallization, chromatography and the like.
- the type of peptide produced by the method for producing a peptide compound according to the present disclosure is not particularly limited, but the number of amino acid residues of the peptide compound is preferably, for example, about several tens or less.
- the peptides obtained by the method for producing a peptide compound according to the present disclosure are similar to existing or unknown synthetic peptides and natural peptides, and are used in various fields such as, but not limited to, pharmaceuticals, foods, cosmetics, electronic materials, and biosensors. It can be used in fields such as sensors.
- the precipitation step can be appropriately omitted as long as it does not affect the reaction in the next step.
- amino acid compound used in the method for producing the peptide compound according to the present disclosure and the peptide compound have a hydroxy group, an amino group, a carboxy group, a carbonyl group, a guadinyl group, a mercapto group, etc.
- these groups are subjected to peptide chemistry or the like.
- a commonly used protective group may be introduced, and the target compound can be obtained by removing the protective group if necessary after the reaction. Examples of these protecting groups include those described above.
- the method for removing these protecting groups may be carried out according to a method known per se, for example, the method described in Greene's Protective Groups in Organic Synthesis (2014).
- a method using an acid, a base, ultraviolet light, hydrazine, phenylhydrazine, sodium N-methyldithiocarbamate, tetrabutylammonium fluoride, palladium acetate, trialkylsilyl halide (for example, trimethylsilyl iodide, trimethylsilyl bromide, etc.) and the like. , Reduction method, etc. are used.
- the reagent for forming a protecting group according to the present disclosure contains a hydrazine derivative represented by the following formula (1a).
- Ring A represents an aromatic hydrocarbon ring or an aromatic heterocycle.
- R represents a hydrogen atom or an amino protecting group.
- k represents an integer from 1 to 5 and represents n represents 1 or 2 RA independently represent an aliphatic hydrocarbon group or an organic group having an aliphatic hydrocarbon group. At least one aliphatic hydrocarbon group in k RA has 13 or more carbon atoms.
- the protecting group forming reagent according to the present disclosure is preferably a carboxy group protecting group forming reagent, and more preferably a C-terminal protecting group forming reagent of an amino acid compound or a peptide compound.
- a preferred embodiment of the hydrazine derivative represented by the formula (1a) in the protecting group-forming reagent according to the present disclosure is in the method for producing a peptide compound according to the present disclosure, except that R is a hydrogen atom or an amino protecting group. This is the same as the preferred embodiment of the hydrazine derivative represented by the above formula (1).
- a preferred embodiment of R of the hydrazine derivative represented by the formula (1a) in the protecting group forming reagent according to the present disclosure is the hydrazine represented by the above formula (1) in the method for producing a peptide compound according to the present disclosure. It is the same as the embodiment in which the amino acid residue and the peptide residue are removed from the preferred embodiment of R of the derivative.
- the reagent for forming a protecting group according to the present disclosure may be a solid reagent or a liquid reagent.
- the content of the hydrazine derivative represented by the formula (1a) in the protecting group forming reagent according to the present disclosure is not particularly limited, but is 0.1% by mass to 100% by mass with respect to the total mass of the protecting group forming reagent. %, More preferably 1% by mass to 100% by mass, and even more preferably 3% by mass to 100% by mass.
- the reagent for forming a protecting group according to the present disclosure may contain components other than the hydrazine derivative represented by the formula (1a).
- Other components may include known components. For example, water, an organic solvent, an antioxidant, a pH adjuster and the like can be mentioned.
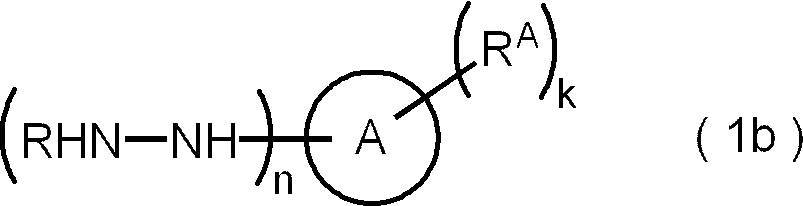
- Ring A represents an aromatic hydrocarbon ring or an aromatic heterocycle.
- R represents a hydrogen atom or an amino protecting group.
- k represents an integer from 1 to 5 and represents n represents 1 or 2 RA independently represent an aliphatic hydrocarbon group or an organic group having an aliphatic hydrocarbon group. At least two aliphatic hydrocarbon groups in k RA have 13 or more carbon atoms.
- the hydrazine derivative represented by the formula (1b), which is the compound according to the present disclosure, is a novel compound and can be suitably used for the production of a peptide compound.
- it can be suitably used as a reagent for forming a protecting group, more preferably as a reagent for forming a protecting group for a carboxy group, and particularly preferably used as a reagent for forming a C-terminal protecting group of an amino acid compound or a peptide compound. be able to.
- R is a hydrogen atom, or an amino protecting group
- the carbon number of at least two aliphatic hydrocarbon groups in the k R A Is the same as the hydrazine derivative represented by the above-mentioned formula (1) in the method for producing a peptide compound according to the present disclosure, except that the number is 13 or more, and the preferred embodiment is also the same.
- the preferred embodiment of R in the compound according to the present disclosure is the same as the preferred embodiment of R of the hydrazine derivative represented by the above-mentioned formula (1) according to the present disclosure, in which amino acid residues and peptide residues are removed. is there.
- hydrazine derivative represented by the above formula (1b) can be synthesized in the same manner as the hydrazine derivative represented by the above formula (1).
- purification by silica gel column chromatography is performed by an automatic purification device ISOLERA (manufactured by Biotage) or a medium-pressure liquid chromatograph YFLC-Wprep2XY. N (manufactured by Yamazen Corporation) was used.
- SNAPKP-Sil Cartridge manufactured by Biotage
- high flash columns W001, W002, W003, W004 or W005 manufactured by Yamazen Corporation
- the MS spectrum was measured using ACQUITY SQD LC / MS System (manufactured by Waters) or LC-MS2020 (manufactured by Shimadzu Corporation), ionization method: ESI (ElectroSpray Ionization, electrospray ionization).
- the NMR spectrum was measured using Bruker AV300 (Made by Bruker, 300 MHz) or Bruker AV400 (manufactured by Bruker, 400 MHz) using tetramethylsilane as an internal reference, and the total ⁇ value was shown in ppm.
- 3,5-bis (docosyloxy) benzyl (((9H-fluorene-9-yl) methoxy) carbonyl) diazabicycloundecene (DBU, DBU, 215 ⁇ L (1.43 mmol) was added, and the mixture was stirred at room temperature for 1 hour.
- N-Methylmorpholine (NMM, 158 ⁇ L, 1.43 mmol) and methanesulfonic acid (MsOH, 96.1 ⁇ L, 1.47 mmol) were added, and the mixture was stirred at room temperature for 10 minutes.
- tert-Butyl 2-(4-((2- (3,5-bis (docosyloxy) benzyloxy) -2-oxoethyl) carbamoyl) phenyl) hydrazine-1-carboxylate (356 mg, 0.340 mmol) in dichloromethane Trifluoroacetic acid (TFA, 6.6 mL) was added to (DCM, 6.6 mL), and the mixture was stirred at room temperature for 1 hour and 30 minutes. The solvent was distilled off under reduced pressure, and tetrahydrofuran (6.8 mL) was added to the obtained white solid.
- TFA Trifluoroacetic acid
- N-Methylmorpholine (48.7 ⁇ L, 0.442 mmol) and methanesulfonic acid (44.2 ⁇ L, 0.674 mmol) were added, and the mixture was stirred at room temperature for 10 minutes.
- N-Methylmorpholine (48.3 ⁇ L, 0.438 mmol) and methanesulfonic acid (29.4 ⁇ L, 0.449 mmol) were added, and the mixture was stirred at room temperature for 10 minutes.
- COMPU 117 mg, 0.274 mmol
- tert-butyl ((S) -1-((2-((S) -2-(((S) -1-(((S) -1-((S) ) -1-((S) -1-((S) 2-carbamoylpyrrolidine-1-yl) -1-oxopropan-2-yl) amino) -1-oxo-3-phenylpropane-2-yl) Amino) -4-methyl-1-oxopentan-2-yl) carbamoyl) pyrrolidine-1-yl) -2-oxoethyl) amino) -1-oxo-3-phenylpropan-2-yl) carbamate (2.19 mg) , 0.00259 mmol).
- tetrahydrofuran 660 ⁇ L
- 3,5-bis (docosyloxy) phenyl) methanol 25.0 mg, 0.0330 mmol.
- 7 mg, 0.0495 mmol N, N'-diisopropylcarbodiimide (7.75 ⁇ L, 0.0495 mmol) and N, N-dimethyl-4-aminopyridine (0.81 mg, 0.0066 mmol) were added and stirred overnight at room temperature. did.
- N-[(9H-fluorene-9-ylmethoxy) carbonyl] glycine (10.4 mg, 0.0348 mmol), cyano-2-ethoxy-2-oxoethylideneamineoxy) dimethylamino-moriholino-carbenium hexafluorophosphate in the mixture (14.9 mg, 0.0348 mmol) was added, and the mixture was stirred at room temperature for 1 hour. By adding acetonitrile, the precipitated solid was recovered by centrifugation and 3,5-bis (docosyloxy) benzyl (((9H-fluorene-9-yl) methoxy) carbonyl) glycyl-L-prolinete (23). 0.0 mg, 0.0203 mmol) was obtained.
- Solid-phase peptide synthesis was performed using an automatic peptide synthesizer (SYRO I, manufactured by biotage).
- SYRO I automatic peptide synthesizer
- 4-Fmoc-hydrazinobenzoyl AM NovaGel (246 mg, 0.61 mmol / g, black spheres represent the binding position to the solid phase)
- N-methylpyrrolidone of Fmoc amino acid 0.5 mol / L
- Set NMP NMP solution
- NMP solution of cyano-hydroxyimino-acetate ethyl ester 1.0 mol / L
- NMP solution of diisopropylcarbodiimide 1.0 mol / L
- NMP solution of piperidine (40% v / v).
- tert-butyl ((S) -1-((2-((S) -2-(((S) -1-(((S) -1-((S) ) -1-((S) -1-((S) -2-carbamoylpyrrolidine-1-yl) -1-oxopropan-2-yl) amino) -1-oxo-3-phenylpropane-2-yl ) Amino) -4-methyl-1-oxopentan-2-yl) carbamoyl) pyrrolidine-1-yl) -2-oxoethyl) amino) -1-oxo-3-phenylpropan-2-yl) carbamate (0. 33 mg, 0.00039 mmol) was obtained.
- Fluorene-9-ylmethoxy) carbonyl] -L-proline (59.7 mg, 0.177 mmol) and diisopropylethylamine (DIEA, 61.7 ⁇ L, 0.354 mmol) were added at room temperature and then stirred overnight at room temperature. By adding acetonitrile, the precipitated solid was recovered by centrifugation and NMR was confirmed. As a result, the target product was 2-((12- (docosyloxy) dodecyl) oxy) -9- (3-fluorophenyl)-. No formation of 9H-fluorene-9-yl (((9H-fluorene-9-yl) methoxy) carbonyl) -L-prolinete was observed.
- DIEA diisopropylethylamine
- N-[(9H-fluorene-9-ylmethoxy) carbonyl] -L-proline (199 mg, 0.59 mmol) and diisopropylethylamine (103 ⁇ L, 0.59 mmol) were added at room temperature and then stirred at 50 ° C. for 4 hours.
- the precipitated solid was recovered by centrifugation and NMR was confirmed.
- the target compound was 2-((12- (docosyloxy) dodecyl) oxy) -9- (3-fluorophenyl)-.
- N-Methylmorpholine (11.1 ⁇ L, 0.101 mmol) and methanesulfonic acid (6.78 ⁇ L, 0.103 mmol) were added, and the mixture was stirred at room temperature for 30 minutes.
- tert-butyl 2- (4- (didocosylcarbamoyl) phenyl) hydrazine-1-carboxylate (3.78 g, 4.914 mmol). It was.
- NMM 140 ⁇ L, 1.27 mmol
- methanesulfonic acid 85 ⁇ L, 1.30 mmol
- Fmoc-Gly-OH 235 mg, 0.791 mmol
- COMU 339 mg, 0.791 mmol
- tert-Butyl ((S) -1-((2-((S) -2-(2- (4- (didocosylcarbamoyl) phenyl) hydrazine-1-carbonyl) pyrrolidine-1-yl) -2- Water (340 ⁇ L), pyridine (69.1 ⁇ L, 0.855 mmol) in tetrahydrofuran solution (3.4 mL) of oxoethyl) amino) -1-oxo-3-phenylpropane-2-yl) carbamate (100 mg, 0.0854 mmol).
- tert-Butyl ((S) -1-((2-((S) -2-(2- (4- (didocosylcarbamoyl) phenyl) hydrazine-1-carbonyl) pyrrolidine-1-yl) -2- Oxoethyl) amino) -1-oxo-3-phenylpropane-2-yl) carbamate (50 mg, 0.0427 mmol) in tetrahydrofuran (1.7 mL) with water (170 ⁇ L), N-bromosuccinimide (NBS, 15. 2 mg (0.0855 mmol) was added, and the mixture was stirred at room temperature for 2 hours.
- N-bromosuccinimide N-bromosuccinimide
- tert-Butyl ((S) -1-((2-((S) -2-(2- (4- (didocosylcarbamoyl) phenyl) hydrazine-1-carbonyl) pyrrolidine-1-yl) -2- Oxoethyl) amino) -1-oxo-3-phenylpropan-2-yl) carbamate (50 mg, 0.0427 mmol) in tetrahydrofuran (1.7 mL) with water (170 ⁇ L), phenyliododiacetate (PIDA, 27. 5 mg (0.0855 mmol) was added, and the mixture was stirred at room temperature for 2 hours.
- PIDA phenyliododiacetate
- tert-Butyl ((S) -1-((2-((S) -2-(2- (4- (didocosylcarbamoyl) phenyl) hydrazine-1-carbonyl) pyrrolidine-1-yl) -2- Oxoethyl) Amino) -1-oxo-3-phenylpropan-2-yl) Carbamate (50 mg, 0.0427 mmol) in tetrahydrofuran (1.7 mL) with water (170 ⁇ L), N-broiodosuccinimide (NIS, 19). .2 mg (0.0855 mmol) was added, and the mixture was stirred at room temperature for 2 hours.
- N-broiodosuccinimide N-broiodosuccinimide
- the method for producing a peptide compound in this example using the hydrazine derivative represented by the formula (1) is superior in yield at the time of deprotection as compared with the method for producing a peptide compound in Comparative Example. Met.
- the method for producing a peptide compound in this example using the hydrazine derivative represented by the formula (1) synthesizes a peptide compound in high yield even during protection and peptide chain extension. In addition, it was possible to suppress the by-product of the diketopiperazine compound. It was also confirmed that the protection of C-terminal amino acids proceeded in good yield without residual raw materials.
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Medicinal Chemistry (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Analytical Chemistry (AREA)
- Peptides Or Proteins (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
式(1)で表されるヒドラジン誘導体を用いる工程を含むペプチド化合物の製造方法、上記化合物を含む保護基形成用試薬、及び、ヒドラジン誘導体。式(1)中、環Aは、芳香族炭化水素環又は芳香族ヘテロ環を表し、Rは、水素原子、アミノ保護基、アミノ酸残基、又は、ペプチド残基を表し、kは、1~5の整数を表し、nは、1又は2を表し、RAはそれぞれ独立に、脂肪族炭化水素基、又は、脂肪族炭化水素基を有する有機基を表す。
Description
本開示は、ペプチド化合物の製造方法、保護基形成用試薬、及び、ヒドラジン誘導体に関する。
ペプチドの製造方法としては、固相法、液相法などがある。
固相法は、反応後の単離及び精製をレジンの洗浄だけで行える点で有利である。しかし、本質的に不均一相の反応であり、低い反応性を補うために反応試剤又は試薬を過剰量用いる必要があった。また、反応の追跡、及び、担体に担持された状態での反応生成物の解析が困難であった。
一方、液相法は、反応性が良好で、縮合反応の後に抽出洗浄、単離等により中間体ペプチドの精製ができる。しかし、液相法には、カップリング反応及び脱保護の各工程における課題が未だ存在する。
固相法は、反応後の単離及び精製をレジンの洗浄だけで行える点で有利である。しかし、本質的に不均一相の反応であり、低い反応性を補うために反応試剤又は試薬を過剰量用いる必要があった。また、反応の追跡、及び、担体に担持された状態での反応生成物の解析が困難であった。
一方、液相法は、反応性が良好で、縮合反応の後に抽出洗浄、単離等により中間体ペプチドの精製ができる。しかし、液相法には、カップリング反応及び脱保護の各工程における課題が未だ存在する。
従来のペプチド合成に用いられる分離用担体としては、特許文献1に記載された分離用担体が知られている。
また、従来の保護基形成用試薬としては、特許文献2に記載されたジフェニルメタン構造を有する化合物、及び、特許文献3に記載されたフルオレン構造を有する化合物が知られている。
また、従来の保護基形成用試薬としては、特許文献2に記載されたジフェニルメタン構造を有する化合物、及び、特許文献3に記載されたフルオレン構造を有する化合物が知られている。
特許文献1:国際公開第2007/034812号
特許文献2:国際公開第2010/113939号
特許文献3:国際公開第2010/104169号
特許文献2:国際公開第2010/113939号
特許文献3:国際公開第2010/104169号
本発明の一実施形態が解決しようとする課題は、脱保護時の収率に優れるペプチド化合物の製造方法を提供することである。
また、本発明の他の一実施形態が解決しようとする課題は、脱保護時の収率に優れる保護基形成用試薬を提供することである。
また、本発明の更に他の一実施形態が解決しようとする課題は、新規なヒドラジン誘導体を提供することである。
また、本発明の他の一実施形態が解決しようとする課題は、脱保護時の収率に優れる保護基形成用試薬を提供することである。
また、本発明の更に他の一実施形態が解決しようとする課題は、新規なヒドラジン誘導体を提供することである。
上記課題を解決するための手段には、以下の態様が含まれる。
<1> 下記式(1)で表されるヒドラジン誘導体を用いる工程を含むペプチド化合物の製造方法。
<1> 下記式(1)で表されるヒドラジン誘導体を用いる工程を含むペプチド化合物の製造方法。
式(1)中、環Aは、芳香族炭化水素環又は芳香族ヘテロ環を表し、Rは、水素原子、アミノ保護基、アミノ酸残基、又は、ペプチド残基を表し、kは、1~5の整数を表し、nは、1又は2を表し、RAはそれぞれ独立に、脂肪族炭化水素基、又は、脂肪族炭化水素基を有する有機基を表し、k個のRAにおける少なくとも1つの脂肪族炭化水素基の炭素数が13以上である。
<2> 上記式(1)で表されるヒドラジン誘導体を用いる工程が、上記式(1)で表されるヒドラジン誘導体により、アミノ酸化合物又はペプチド化合物のカルボキシ基を保護するC末端保護工程である<1>に記載のペプチド化合物の製造方法。
<3> 上記C末端保護工程におけるアミノ酸化合物又はペプチド化合物が、N末端保護アミノ酸化合物又はN末端保護ペプチド化合物である<2>に記載のペプチド化合物の製造方法。
<4> 上記C末端保護工程で得られたN末端保護C末端保護アミノ酸化合物又はN末端保護C末端保護ペプチド化合物のN末端を脱保護するN末端脱保護工程、及び、上記N末端脱保護工程で得られたC末端保護アミノ酸化合物又はC末端保護ペプチド化合物のN末端に、N末端保護アミノ酸化合物又はN末端保護ペプチド化合物を縮合させるペプチド鎖延長工程を更に含む<3>に記載のペプチド化合物の製造方法。
<5> 上記ペプチド鎖延長工程で得られたN末端保護C末端保護ペプチド化合物を沈殿させる沈殿工程を更に含む<4>に記載のペプチド化合物の製造方法。
<6> 上記ペプチド鎖延長工程で得られたN末端保護C末端保護ペプチド化合物に水を添加し、不純物を水相に抽出分離する抽出工程を更に含む<4>に記載のペプチド化合物の製造方法。
<7> 上記沈殿工程又は抽出工程の後に、得られたN末端保護C末端保護ペプチド化合物のN末端を脱保護する工程、得られたC末端保護ペプチド化合物のN末端に、N末端保護アミノ酸化合物又はN末端保護ペプチド化合物を縮合させる工程、及び、得られたN末端保護C末端保護ペプチド化合物を沈殿する工程をこの順で1回以上更に含む<5>又は<6>に記載のペプチド化合物の製造方法。
<8> C末端保護基を脱保護するC末端脱保護工程を更に含む<1>~<7>のいずれか1つに記載のペプチド化合物の製造方法。
<9> 上記環Aが、ベンゼン環、ナフタレン環、又は、ピリジン環である<1>~<8>のいずれか1つに記載のペプチド化合物の製造方法。
<10> 上記式(1)において、k個のRAにおける少なくとも2つの脂肪族炭化水素基の炭素数が13以上である<1>~<9>のいずれか1つに記載のペプチド化合物の製造方法。
<11> 上記nが、1である<1>~<10>のいずれか1つに記載のペプチド化合物の製造方法。
<12> 上記kが、1である<1>~<11>のいずれか1つに記載のペプチド化合物の製造方法。
<13> 下記式(1a)で表されるヒドラジン誘導体を含む保護基形成用試薬。
<3> 上記C末端保護工程におけるアミノ酸化合物又はペプチド化合物が、N末端保護アミノ酸化合物又はN末端保護ペプチド化合物である<2>に記載のペプチド化合物の製造方法。
<4> 上記C末端保護工程で得られたN末端保護C末端保護アミノ酸化合物又はN末端保護C末端保護ペプチド化合物のN末端を脱保護するN末端脱保護工程、及び、上記N末端脱保護工程で得られたC末端保護アミノ酸化合物又はC末端保護ペプチド化合物のN末端に、N末端保護アミノ酸化合物又はN末端保護ペプチド化合物を縮合させるペプチド鎖延長工程を更に含む<3>に記載のペプチド化合物の製造方法。
<5> 上記ペプチド鎖延長工程で得られたN末端保護C末端保護ペプチド化合物を沈殿させる沈殿工程を更に含む<4>に記載のペプチド化合物の製造方法。
<6> 上記ペプチド鎖延長工程で得られたN末端保護C末端保護ペプチド化合物に水を添加し、不純物を水相に抽出分離する抽出工程を更に含む<4>に記載のペプチド化合物の製造方法。
<7> 上記沈殿工程又は抽出工程の後に、得られたN末端保護C末端保護ペプチド化合物のN末端を脱保護する工程、得られたC末端保護ペプチド化合物のN末端に、N末端保護アミノ酸化合物又はN末端保護ペプチド化合物を縮合させる工程、及び、得られたN末端保護C末端保護ペプチド化合物を沈殿する工程をこの順で1回以上更に含む<5>又は<6>に記載のペプチド化合物の製造方法。
<8> C末端保護基を脱保護するC末端脱保護工程を更に含む<1>~<7>のいずれか1つに記載のペプチド化合物の製造方法。
<9> 上記環Aが、ベンゼン環、ナフタレン環、又は、ピリジン環である<1>~<8>のいずれか1つに記載のペプチド化合物の製造方法。
<10> 上記式(1)において、k個のRAにおける少なくとも2つの脂肪族炭化水素基の炭素数が13以上である<1>~<9>のいずれか1つに記載のペプチド化合物の製造方法。
<11> 上記nが、1である<1>~<10>のいずれか1つに記載のペプチド化合物の製造方法。
<12> 上記kが、1である<1>~<11>のいずれか1つに記載のペプチド化合物の製造方法。
<13> 下記式(1a)で表されるヒドラジン誘導体を含む保護基形成用試薬。
式(1a)中、環Aは、芳香族炭化水素環又は芳香族ヘテロ環を表し、Rは、水素原子、又は、アミノ保護基を表し、kは、1~5の整数を表し、nは、1又は2を表し、RAはそれぞれ独立に、脂肪族炭化水素基、又は、脂肪族炭化水素基を有する有機基を表し、k個のRAにおける少なくとも1つの脂肪族炭化水素基の炭素数が13以上である。
<14> 上記保護基形成用試薬が、カルボキシ基の保護基形成用試薬である<13>に記載の保護基形成用試薬。
<15> 上記保護基形成用試薬が、アミノ酸化合物のカルボキシ基又はペプチド化合物のC末端保護基形成用試薬である<13>又は<14>に記載の保護基形成用試薬。
<16> 上記環Aが、ベンゼン環、ナフタレン環、又は、ピリジン環である<13>~<15>のいずれか1つに記載の保護基形成用試薬。
<17> 上記式(1a)において、k個のRAにおける少なくとも2つの脂肪族炭化水素基の炭素数が13以上である<13>~<16>のいずれか1つに記載の保護基形成用試薬。
<18> 上記nが、1である<13>~<17>のいずれか1つに記載の保護基形成用試薬。
<19> 上記kが、1である<13>~<18>のいずれか1つに記載の保護基形成用試薬。
<20> 下記式(1b)で表されるヒドラジン誘導体。
<15> 上記保護基形成用試薬が、アミノ酸化合物のカルボキシ基又はペプチド化合物のC末端保護基形成用試薬である<13>又は<14>に記載の保護基形成用試薬。
<16> 上記環Aが、ベンゼン環、ナフタレン環、又は、ピリジン環である<13>~<15>のいずれか1つに記載の保護基形成用試薬。
<17> 上記式(1a)において、k個のRAにおける少なくとも2つの脂肪族炭化水素基の炭素数が13以上である<13>~<16>のいずれか1つに記載の保護基形成用試薬。
<18> 上記nが、1である<13>~<17>のいずれか1つに記載の保護基形成用試薬。
<19> 上記kが、1である<13>~<18>のいずれか1つに記載の保護基形成用試薬。
<20> 下記式(1b)で表されるヒドラジン誘導体。
式(1b)中、環Aは、芳香族炭化水素環又は芳香族ヘテロ環を表し、Rは、水素原子、又は、アミノ保護基を表し、kは、1~5の整数を表し、nは、1又は2を表し、RAはそれぞれ独立に、脂肪族炭化水素基、又は、脂肪族炭化水素基を有する有機基を表し、k個のRAにおける少なくとも2つの脂肪族炭化水素基の炭素数が13以上である。
<21> 上記環Aが、ベンゼン環、ナフタレン環、又は、ピリジン環である<20>に記載のヒドラジン誘導体。
<22> 上記nが、1である<20>又は<21>に記載のヒドラジン誘導体。
<23> 上記kが、1である<20>~<22>のいずれか1つに記載のヒドラジン誘導体。
<22> 上記nが、1である<20>又は<21>に記載のヒドラジン誘導体。
<23> 上記kが、1である<20>~<22>のいずれか1つに記載のヒドラジン誘導体。
本発明の一実施形態によれば、脱保護時の収率に優れるペプチド化合物の製造方法を提供することができる。
また、本発明の他の一実施形態によれば、脱保護時の収率に優れる保護基形成用試薬を提供することができる。
また、本発明の更に他の一実施形態によれば、新規なヒドラジン誘導体を提供することができる。
また、本発明の他の一実施形態によれば、脱保護時の収率に優れる保護基形成用試薬を提供することができる。
また、本発明の更に他の一実施形態によれば、新規なヒドラジン誘導体を提供することができる。
以下において、本開示の内容について詳細に説明する。以下に記載する構成要件の説明は、本開示の代表的な実施態様に基づいてなされることがあるが、本開示はそのような実施態様に限定されるものではない。
また、本明細書において「~」を用いて表される数値範囲は、「~」の前後に記載される数値を下限値及び上限値として含む範囲を意味する。
本明細書中に段階的に記載されている数値範囲において、一つの数値範囲で記載された上限値又は下限値は、他の段階的な記載の数値範囲の上限値又は下限値に置き換えてもよい。また、本明細書中に記載されている数値範囲において、その数値範囲の上限値又は下限値は、実施例に示されている値に置き換えてもよい。
本明細書において「工程」との語は、独立した工程だけでなく、他の工程と明確に区別できない場合であっても工程の所期の目的が達成されれば、本用語に含まれる。
本明細書における基(原子団)の表記において、置換及び無置換を記していない表記は、置換基を有さないものと共に置換基を有するものをも包含するものである。例えば「アルキル基」とは、置換基を有さないアルキル基(無置換アルキル基)のみならず、置換基を有するアルキル基(置換アルキル基)をも包含するものである。
また、本明細書における化学構造式は、水素原子を省略した簡略構造式で記載する場合もある。
本開示において、「質量%」と「重量%」とは同義であり、「質量部」と「重量部」とは同義である。
また、本開示において、2以上の好ましい態様の組み合わせは、より好ましい態様である。
また、本明細書において「~」を用いて表される数値範囲は、「~」の前後に記載される数値を下限値及び上限値として含む範囲を意味する。
本明細書中に段階的に記載されている数値範囲において、一つの数値範囲で記載された上限値又は下限値は、他の段階的な記載の数値範囲の上限値又は下限値に置き換えてもよい。また、本明細書中に記載されている数値範囲において、その数値範囲の上限値又は下限値は、実施例に示されている値に置き換えてもよい。
本明細書において「工程」との語は、独立した工程だけでなく、他の工程と明確に区別できない場合であっても工程の所期の目的が達成されれば、本用語に含まれる。
本明細書における基(原子団)の表記において、置換及び無置換を記していない表記は、置換基を有さないものと共に置換基を有するものをも包含するものである。例えば「アルキル基」とは、置換基を有さないアルキル基(無置換アルキル基)のみならず、置換基を有するアルキル基(置換アルキル基)をも包含するものである。
また、本明細書における化学構造式は、水素原子を省略した簡略構造式で記載する場合もある。
本開示において、「質量%」と「重量%」とは同義であり、「質量部」と「重量部」とは同義である。
また、本開示において、2以上の好ましい態様の組み合わせは、より好ましい態様である。
本明細書中、「脂肪族炭化水素基を有する有機基」とは、その分子構造中に脂肪族炭化水素基を有する一価(結合手が1つ)の有機基である。
「脂肪族炭化水素基」とは、直鎖状、分岐状、若しくは環状の飽和又は不飽和の炭素数5以上の脂肪族炭化水素基であることが好ましく、炭素数(「炭素原子数」ともいう。)5~60の脂肪族炭化水素基がより好ましく、炭素数5~40の脂肪族炭化水素基が更に好ましく、炭素数10~30の脂肪族炭化水素基が特に好ましい。
脂肪族炭化水素基を有する有機基における脂肪族炭化水素基の部位は、特に限定されず、末端に存在しても(一価基)、それ以外の部位に存在してもよい(例えば二価基)。
「脂肪族炭化水素基」としては、アルキル基、シクロアルキル基、アルケニル基、アルキニル基等の一価の基、及び、それらから誘導される二価の基(上記一価の基から水素原子を1つ除いた二価の基)、各種ステロイド基からヒドロキシ基などを除外した基などが挙げられる。
「アルキル基」としては、例えば、炭素数1~30のアルキル基等が好ましく、例えば、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、sec-ブチル基、イソブチル基、tert-ブチル基、ペンチル基、イソペンチル基、2-メチルブチル基、2-ペンチル基、3-ペンチル基、ヘキシル基、オクチル基、2-エチルヘキシル基、デシル基、ヘキサデシル基、オクタデシル基、イコシル基、ドコシル基、テトラコシル基、ラウリル基、トリデシル基、ミリスチル基、イソステアリル基等が挙げられる。
上記脂肪族炭化水素基におけるアルキル基としては、オクタデシル基、イコシル基、ドコシル基、又は、テトラコシル基が好ましく、イコシル基、ドコシル基、又は、テトラコシル基がより好ましい。
また、上記脂肪族炭化水素基におけるアルキル基としては、炭素数5~40のアルキル基が好ましく、炭素数10~30のアルキル基がより好ましい。
また、本開示における「アルキル基」は、特に言及していない場合、直鎖アルキル基であっても、分岐アルキル基であってもよい。また、アルケニル基、及び、アルキニル基についても、アルキル基と同様である。
「シクロアルキル基」としては、例えば、炭素数3~30のシクロアルキル基等が好ましく、例えば、シクロペンチル基、シクロヘキシル基、イソボルニル基、トリシクロデカニル基等が挙げられる。また、これらが繰り返し連結してもよく、2環以上の縮環構造であってもよい。
また、上記脂肪族炭化水素基におけるシクロアルキル基としては、炭素数5~30のシクロアルキル基がより好ましい。
「アルケニル基」としては、例えば、炭素数2~30のアルケニル基等が好ましく、例えば、ペンテニル基、ヘキセニル基、オレイル基等が挙げられる。また、「アルケニル基」としては、炭素数5~30のアルケニル基がより好ましい。
「アルキニル基」としては、例えば、炭素数2~30のアルキニル基等が好ましく、例えば、4-ペンチニル基、5-ヘキセニル基等が挙げられる。また、「アルキニル基」としては、炭素数5~30のアルキニル基がより好ましい。
「ステロイド基」としては、例えば、コレストロール構造を有する基やエストラジオール構造を有する基等が好ましい。
「アリール基」としては、例えば、炭素数6~14のアリール基等が好ましく、例えば、フェニル基、1-ナフチル基、2-ナフチル基、ビフェニリル基、2-アンスリル基等が挙げられる。
「脂肪族炭化水素基」とは、直鎖状、分岐状、若しくは環状の飽和又は不飽和の炭素数5以上の脂肪族炭化水素基であることが好ましく、炭素数(「炭素原子数」ともいう。)5~60の脂肪族炭化水素基がより好ましく、炭素数5~40の脂肪族炭化水素基が更に好ましく、炭素数10~30の脂肪族炭化水素基が特に好ましい。
脂肪族炭化水素基を有する有機基における脂肪族炭化水素基の部位は、特に限定されず、末端に存在しても(一価基)、それ以外の部位に存在してもよい(例えば二価基)。
「脂肪族炭化水素基」としては、アルキル基、シクロアルキル基、アルケニル基、アルキニル基等の一価の基、及び、それらから誘導される二価の基(上記一価の基から水素原子を1つ除いた二価の基)、各種ステロイド基からヒドロキシ基などを除外した基などが挙げられる。
「アルキル基」としては、例えば、炭素数1~30のアルキル基等が好ましく、例えば、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、sec-ブチル基、イソブチル基、tert-ブチル基、ペンチル基、イソペンチル基、2-メチルブチル基、2-ペンチル基、3-ペンチル基、ヘキシル基、オクチル基、2-エチルヘキシル基、デシル基、ヘキサデシル基、オクタデシル基、イコシル基、ドコシル基、テトラコシル基、ラウリル基、トリデシル基、ミリスチル基、イソステアリル基等が挙げられる。
上記脂肪族炭化水素基におけるアルキル基としては、オクタデシル基、イコシル基、ドコシル基、又は、テトラコシル基が好ましく、イコシル基、ドコシル基、又は、テトラコシル基がより好ましい。
また、上記脂肪族炭化水素基におけるアルキル基としては、炭素数5~40のアルキル基が好ましく、炭素数10~30のアルキル基がより好ましい。
また、本開示における「アルキル基」は、特に言及していない場合、直鎖アルキル基であっても、分岐アルキル基であってもよい。また、アルケニル基、及び、アルキニル基についても、アルキル基と同様である。
「シクロアルキル基」としては、例えば、炭素数3~30のシクロアルキル基等が好ましく、例えば、シクロペンチル基、シクロヘキシル基、イソボルニル基、トリシクロデカニル基等が挙げられる。また、これらが繰り返し連結してもよく、2環以上の縮環構造であってもよい。
また、上記脂肪族炭化水素基におけるシクロアルキル基としては、炭素数5~30のシクロアルキル基がより好ましい。
「アルケニル基」としては、例えば、炭素数2~30のアルケニル基等が好ましく、例えば、ペンテニル基、ヘキセニル基、オレイル基等が挙げられる。また、「アルケニル基」としては、炭素数5~30のアルケニル基がより好ましい。
「アルキニル基」としては、例えば、炭素数2~30のアルキニル基等が好ましく、例えば、4-ペンチニル基、5-ヘキセニル基等が挙げられる。また、「アルキニル基」としては、炭素数5~30のアルキニル基がより好ましい。
「ステロイド基」としては、例えば、コレストロール構造を有する基やエストラジオール構造を有する基等が好ましい。
「アリール基」としては、例えば、炭素数6~14のアリール基等が好ましく、例えば、フェニル基、1-ナフチル基、2-ナフチル基、ビフェニリル基、2-アンスリル基等が挙げられる。
「アミノ保護基(アミノ基の保護基)」としては、例えば、ホルミル基、炭素数1~6のアシル基(例、アセチル基、プロピオニル基)、炭素数2~6のアルコキシカルボニル基(例、メトキシカルボニル基、エトキシカルボニル基、tert-ブトキシカルボニル基(Boc基))、ベンゾイル基、炭素数8~20のアリールアルキルオキシカルボニル基(例、ベンジルオキシカルボニル基、9-フルオレニルメトキシカルボニル基(Fmoc基))、トリチル基、モノメトキシトリチル基、1-(4,4-Dimethyl-2,6-dioxocyclohex-1-ylidene)-3-methylbutyl基、フタロイル基、N,N-ジメチルアミノメチレン基、シリル基(例、トリメチルシリル基、トリエチルシリル基、ジメチルフェニルシリル基、tert-ブチルジメチルシリル基、tert-ブチルジエチルシリル基)、炭素数2~6のアルケニル基等が挙げられる。これらの基は、ハロゲン原子(例、フッ素原子、塩素原子、臭素原子、ヨウ素原子)、炭素数1~6のアルコキシ基(例、メトキシ基、エトキシ基、プロポキシ基)、及び、ニトロ基よりなる群から選ばれる1個~3個の置換基で置換されていてもよい。
アミノ保護基としては、炭素数1~6のアルコキシカルボニル基、及び、炭素数7~20のアリールアルキルオキシカルボニル基が好ましい。
アミノ保護基としては、炭素数1~6のアルコキシカルボニル基、及び、炭素数7~20のアリールアルキルオキシカルボニル基が好ましい。
「ヒドロキシ基の保護基」としては、例えば、炭素数1~6のアルキル基、フェニル基、トリチル基、ホルミル基、炭素数1~6のアシル基、ベンゾイル基、炭素数7~10のアリールアルキルカルボニル基、2-テトラヒドロピラニル基、2-テトラヒドロフラニル基、シリル基、炭素数2~6のアルケニル基等が挙げられる。これらの基は、ハロゲン原子、炭素数1~6のアルキル基、炭素数1~6のアルコキシ基、及び、ニトロ基よりなる群から選ばれる1個~3個の置換基で置換されていてもよい。
「カルボキシ基の保護基」としては、例えば、炭素数1~6のアルキル基、炭素数7~10のアリールアルキル基、フェニル基、トリチル基、シリル基、炭素数2~6のアルケニル基等が挙げられる。これらの基は、ハロゲン原子、炭素数1~6のアルコキシ基、及び、ニトロ基よりなる群から選ばれる1個~3個の置換基で置換されていてもよい。
「カルボニル基の保護基」としては、例えば、環状アセタール(例、1,3-ジオキサン)、非環状アセタール(例、ジ(炭素数1~6のアルキル)アセタール)等が挙げられる。
「グアニジル基の保護基」としては、例えば、2,2,4,6,7-ペンタメチルジヒドロベンゾフラン-5-スルホニル基、2,3,4,5,6-ペンタメチルベンゼンスルホニル基、トシル基、ニトロ基等が挙げられる。
「メルカプト基(スルフヒドリル基)の保護基」としては、例えば、トリチル基、4-メチルベンジル基、アセチルアミノメチル基、t-ブチル基、t-ブチルチオ基等が挙げられる。
「グアニジル基の保護基」としては、例えば、2,2,4,6,7-ペンタメチルジヒドロベンゾフラン-5-スルホニル基、2,3,4,5,6-ペンタメチルベンゼンスルホニル基、トシル基、ニトロ基等が挙げられる。
「メルカプト基(スルフヒドリル基)の保護基」としては、例えば、トリチル基、4-メチルベンジル基、アセチルアミノメチル基、t-ブチル基、t-ブチルチオ基等が挙げられる。
(ペプチド化合物の製造方法)
本開示に係るペプチド化合物の製造方法は、下記式(1)で表されるヒドラジン誘導体を用いる工程を含む。
本開示に係るペプチド化合物の製造方法は、下記式(1)で表されるヒドラジン誘導体を用いる工程を含む。
式(1)中、
環Aは、芳香族炭化水素環又は芳香族ヘテロ環を表し、
Rは、水素原子、アミノ保護基、アミノ酸残基、又は、ペプチド残基を表し、
kは、1~5の整数を表し、
nは、1又は2を表し、
RAはそれぞれ独立に、脂肪族炭化水素基、又は、脂肪族炭化水素基を有する有機基を表し、
k個のRAにおける少なくとも1つの脂肪族炭化水素基の炭素数が13以上である。
環Aは、芳香族炭化水素環又は芳香族ヘテロ環を表し、
Rは、水素原子、アミノ保護基、アミノ酸残基、又は、ペプチド残基を表し、
kは、1~5の整数を表し、
nは、1又は2を表し、
RAはそれぞれ独立に、脂肪族炭化水素基、又は、脂肪族炭化水素基を有する有機基を表し、
k個のRAにおける少なくとも1つの脂肪族炭化水素基の炭素数が13以上である。
特許文献1~3に記載されていような従来のアミノ酸又はペプチドの保護基として用いられる化合物としては、上記式(1)で表されるヒドラジン誘導体は何ら知られていなかった。
上記式(1)で表されるヒドラジン誘導体は、芳香族炭化水素環又は芳香族ヘテロ環に結合したヒドラジノ基を有することから、脱保護時において、反応系中を酸性条件とすることなく、酸化反応により脱保護することができ、また、従来困難であった均一系での脱保護を容易に行うことができ、求核剤による置換反応の収率に優れるため、脱保護時の収率に優れると推定している。また、ヒドラジン構造の高い求核性のため、ローディング収率(保護時の収率)に優れ、また、ペプチド化合物におけるC末端との結合が安定なアミド結合であるため、後述するジケトピぺラジン化合物の副生を抑制できると推定される。
上記式(1)で表されるヒドラジン誘導体は、芳香族炭化水素環又は芳香族ヘテロ環に結合したヒドラジノ基を有することから、脱保護時において、反応系中を酸性条件とすることなく、酸化反応により脱保護することができ、また、従来困難であった均一系での脱保護を容易に行うことができ、求核剤による置換反応の収率に優れるため、脱保護時の収率に優れると推定している。また、ヒドラジン構造の高い求核性のため、ローディング収率(保護時の収率)に優れ、また、ペプチド化合物におけるC末端との結合が安定なアミド結合であるため、後述するジケトピぺラジン化合物の副生を抑制できると推定される。
また、上記式(1)で表されるヒドラジン誘導体は、k個のRAにおける少なくとも1つの脂肪族炭化水素基の炭素数が13以上であることから、縮合完了後、溶媒の組成を変更することにより、縮合物を沈殿及び単離することができ、得られるペプチド化合物の収率にも優れる。
更に、本開示に係る式(1)で表されるヒドラジン誘導体は、上記構造であることにより、副反応を抑制し、高収率でペプチド化合物を合成することができる。
更に、本開示に係る式(1)で表されるヒドラジン誘導体を用いることにより、副反応が生じ易い非天然アミノ酸を含む非天然ペプチドのような難合成ペプチド化合物でも、副反応を抑制し高純度で合成できる。特に、後述するジケトピペラジン化合物が副生する可能性のある場合であっても、ジケトピペラジン化合物の副生を抑制でき、高収率でペプチド化合物を得ることができる。
更に、本開示に係る式(1)で表されるヒドラジン誘導体は、上記構造であることにより、副反応を抑制し、高収率でペプチド化合物を合成することができる。
更に、本開示に係る式(1)で表されるヒドラジン誘導体を用いることにより、副反応が生じ易い非天然アミノ酸を含む非天然ペプチドのような難合成ペプチド化合物でも、副反応を抑制し高純度で合成できる。特に、後述するジケトピペラジン化合物が副生する可能性のある場合であっても、ジケトピペラジン化合物の副生を抑制でき、高収率でペプチド化合物を得ることができる。
以下、本開示に係るペプチド化合物の製造方法について、詳細に説明する。
本開示に係るペプチド化合物の製造方法において、式(1)で表されるヒドラジン誘導体は、保護基の形成だけでなく、ペプチド化合物の変性、水又は有機溶媒等への溶解度の調整、結晶化性の改良、多量体化等に用いることができる。
中でも、式(1)で表されるヒドラジン誘導体は、保護基の形成に用いることが好ましく、アミノ酸化合物又はペプチド化合物におけるC末端保護基の形成に用いることがより好ましい。
中でも、式(1)で表されるヒドラジン誘導体は、保護基の形成に用いることが好ましく、アミノ酸化合物又はペプチド化合物におけるC末端保護基の形成に用いることがより好ましい。
<式(1)で表されるヒドラジン誘導体>
本開示における式(1)で表されるヒドラジン誘導体(以下、単に「式(1)で表される化合物」ともいう。)を、以下に示す。
本開示における式(1)で表されるヒドラジン誘導体(以下、単に「式(1)で表される化合物」ともいう。)を、以下に示す。
式(1)中、
環Aは、芳香族炭化水素環又は芳香族ヘテロ環を表し、
Rは、水素原子、アミノ保護基、アミノ酸残基、又は、ペプチド残基を表し、
kは、1~5の整数を表し、
nは、1又は2を表し、
RAはそれぞれ独立に、脂肪族炭化水素基、又は、脂肪族炭化水素基を有する有機基を表し、
k個のRAにおける少なくとも1つの脂肪族炭化水素基の炭素数が13以上である。
環Aは、芳香族炭化水素環又は芳香族ヘテロ環を表し、
Rは、水素原子、アミノ保護基、アミノ酸残基、又は、ペプチド残基を表し、
kは、1~5の整数を表し、
nは、1又は2を表し、
RAはそれぞれ独立に、脂肪族炭化水素基、又は、脂肪族炭化水素基を有する有機基を表し、
k個のRAにおける少なくとも1つの脂肪族炭化水素基の炭素数が13以上である。
式(1)における環Aは、芳香族炭化水素環又は芳香族ヘテロ環を表し、また、環Aは、RA及び-NH-NHRに加えて更に置換基を有していてもよい。
環Aにおける芳香族炭化水素環、及び、芳香族ヘテロ環は、単環であっても、2環以上の縮合環であってもよい。上記縮合環としては、2環以上の縮合多環芳香族炭化水素環、2環以上の縮合多環芳香族ヘテロ環、1環以上の芳香族炭化水素環と1環以上の芳香族ヘテロ環との縮合環が挙げられる。
環Aは、脱保護速度、ジケトピペラジン化合物の副生抑制性、ペプチド化合物合成時の収率、及び、脱保護時の収率の観点から、単環、又は、2環であることがより好ましく、単環であることが特に好ましい。
また、環Aは、晶析性、脱保護速度、及び、脱保護時の収率の観点から、芳香族炭化水素環であることが好ましい。
環Aとしては、脱保護速度、ジケトピペラジン化合物の副生抑制性、ペプチド化合物合成時の収率、及び、脱保護時の収率の観点から、ベンゼン環、ナフタレン環、アントラセン環、フェナントレン環、テトラセン環、トリフェニレン環、ピレン環、クリセン環、ピリジン環、キノリン環、イソキノリン環、ベンゾチオフェン環、フラン環、ベンゾフラン環、ピロール環、インドール環、カルバゾール環、ピラゾール環、インダゾール環、又は、チオフェン環であることが好ましく、ベンゼン環、ナフタレン環、又は、ピリジン環であることがより好ましく、ベンゼン環、又は、ピリジン環であることが更に好ましく、ベンゼン環であることが特に好ましい。
更に、環Aは、後述するように、2以上の置換基が結合して環構造を形成していてもよく、環Aに脂肪族炭化水素環、脂肪族複素環等が更に縮環した構造であってもよい。
環Aにおける芳香族炭化水素環、及び、芳香族ヘテロ環は、単環であっても、2環以上の縮合環であってもよい。上記縮合環としては、2環以上の縮合多環芳香族炭化水素環、2環以上の縮合多環芳香族ヘテロ環、1環以上の芳香族炭化水素環と1環以上の芳香族ヘテロ環との縮合環が挙げられる。
環Aは、脱保護速度、ジケトピペラジン化合物の副生抑制性、ペプチド化合物合成時の収率、及び、脱保護時の収率の観点から、単環、又は、2環であることがより好ましく、単環であることが特に好ましい。
また、環Aは、晶析性、脱保護速度、及び、脱保護時の収率の観点から、芳香族炭化水素環であることが好ましい。
環Aとしては、脱保護速度、ジケトピペラジン化合物の副生抑制性、ペプチド化合物合成時の収率、及び、脱保護時の収率の観点から、ベンゼン環、ナフタレン環、アントラセン環、フェナントレン環、テトラセン環、トリフェニレン環、ピレン環、クリセン環、ピリジン環、キノリン環、イソキノリン環、ベンゾチオフェン環、フラン環、ベンゾフラン環、ピロール環、インドール環、カルバゾール環、ピラゾール環、インダゾール環、又は、チオフェン環であることが好ましく、ベンゼン環、ナフタレン環、又は、ピリジン環であることがより好ましく、ベンゼン環、又は、ピリジン環であることが更に好ましく、ベンゼン環であることが特に好ましい。
更に、環Aは、後述するように、2以上の置換基が結合して環構造を形成していてもよく、環Aに脂肪族炭化水素環、脂肪族複素環等が更に縮環した構造であってもよい。
RA及び-NH-NHRに加えて、環A上に有していてもよい置換基としては、特に制限はないが、炭素数1~10のアルキル基(好ましい炭素数は1~4)、炭素数1~10のアルコキシ基、炭素数6~20のアリールオキシ基、ハロゲン原子、炭素数1~10のハロゲン化アルキル基、炭素数6~20のアリール基、炭素数1~20のアシル基、炭素数6~20のアシルオキシ基、炭素数1~10のアルコキシカルボニル基、炭素数6~20のアリールオキシカルボニル基、炭素数6~20のアルキルチオ基、炭素数6~20のアリールチオ基、Rst-CO-NRst-、-CON(Rst)2、炭素数1~10のジアルキルアミノ基、炭素数6~20のアルキルアリールアミノ基、炭素数12~30のジアリールアミノ基、及び、これらを2以上組み合わせた基等が挙げられる。なお、Rstは、水素原子、炭素数1~10のアルキル基又は炭素数6~20のアリール基を表す。
Rであるアミノ保護基としては、上述したアミノ保護基が使用できるが、炭素数2~6のアルコキシカルボニル基、及び、炭素数8~20のアリールアルキルオキシカルボニル基が好ましい。
Rであるアミノ酸残基又はペプチド残基としては、アミノ酸又はペプチドからヒドロキシ基が除去され、-NH-NH-と結合できるものを意味する。また、Rがアミノ酸残基又はペプチド残基である場合は、保護されたアミノ酸化合物又はペプチド化合物でもある。アミノ酸残基及びペプチド残基の種類は特に限定されないが、実施例に記載されているものが好ましい。
また、アミノ酸残基としては、後述するC末端保護工程に記載のアミノ酸残基が好ましく挙げられ、ペプチド残基としては、後述するC末端保護工程に記載のペプチド化合物からヒドロキシ基を除去した残基が好ましく挙げられる。
中でも、Rとしては、合成適性の観点から、水素原子、Boc基、Fmoc基、ベンジルオキシカルボニル基(Cbz基)、2,2,2-トリクロロエトキシカルボニル基(Troc基)、又は、アリルオキシカルボニル基(Alloc基)であることが好ましく、保存安定性の観点からは、Boc基、Fmoc基、Cbz基、Troc基、又は、Alloc基であることがより好ましく、Boc基、又は、Fmoc基であることが更に好ましく、Boc基であることが特に好ましい。
また、反応性の観点からは、Rとしては、水素原子が特に好ましい。
Rであるアミノ酸残基又はペプチド残基としては、アミノ酸又はペプチドからヒドロキシ基が除去され、-NH-NH-と結合できるものを意味する。また、Rがアミノ酸残基又はペプチド残基である場合は、保護されたアミノ酸化合物又はペプチド化合物でもある。アミノ酸残基及びペプチド残基の種類は特に限定されないが、実施例に記載されているものが好ましい。
また、アミノ酸残基としては、後述するC末端保護工程に記載のアミノ酸残基が好ましく挙げられ、ペプチド残基としては、後述するC末端保護工程に記載のペプチド化合物からヒドロキシ基を除去した残基が好ましく挙げられる。
中でも、Rとしては、合成適性の観点から、水素原子、Boc基、Fmoc基、ベンジルオキシカルボニル基(Cbz基)、2,2,2-トリクロロエトキシカルボニル基(Troc基)、又は、アリルオキシカルボニル基(Alloc基)であることが好ましく、保存安定性の観点からは、Boc基、Fmoc基、Cbz基、Troc基、又は、Alloc基であることがより好ましく、Boc基、又は、Fmoc基であることが更に好ましく、Boc基であることが特に好ましい。
また、反応性の観点からは、Rとしては、水素原子が特に好ましい。
式(1)におけるkは、晶析性、溶剤溶解性、の観点から、1~4の整数であることが好ましく、1~3の整数であることがより好ましく、1であることが特に好ましい。
式(1)におけるnは、ペプチド化合物合成時の収率、及び、脱保護時の収率の観点から、1であることが好ましい。
式(1)におけるnは、ペプチド化合物合成時の収率、及び、脱保護時の収率の観点から、1であることが好ましい。
RAはそれぞれ独立に、脂肪族炭化水素基、又は、脂肪族炭化水素基を有する有機基を表し、k個のRAにおける少なくとも1つの脂肪族炭化水素基の炭素数が13以上である。
中でも、RAはそれぞれ独立に、晶析性及び溶解性の観点から、脂肪族炭化水素基を有する有機基であることが好ましく、炭素数13以上の脂肪族炭化水素基を2つ以上有する有機基であることがより好ましく、炭素数13以上の脂肪族炭化水素基を2つ~6つ有する有機基であることがより好ましく、炭素数13以上の脂肪族炭化水素基を2つ又は3つ有する有機基であることが特に好ましい。
中でも、RAはそれぞれ独立に、晶析性及び溶解性の観点から、脂肪族炭化水素基を有する有機基であることが好ましく、炭素数13以上の脂肪族炭化水素基を2つ以上有する有機基であることがより好ましく、炭素数13以上の脂肪族炭化水素基を2つ~6つ有する有機基であることがより好ましく、炭素数13以上の脂肪族炭化水素基を2つ又は3つ有する有機基であることが特に好ましい。
また、上記炭素数13以上の脂肪族炭化水素基は、溶剤溶解性、晶析性、及び、収率の観点から、炭素数13以上であることが好ましく、炭素数14以上であることがより好ましく、炭素数16以上であることが更に好ましく、炭素数18以上であることが特に好ましい。
上記有機基は更にシリル基、シリルオキシ構造を有する炭化水素基、パーフルオロアルキル構造を有する有機基で置換されてもよい。
上記有機基は更にシリル基、シリルオキシ構造を有する炭化水素基、パーフルオロアルキル構造を有する有機基で置換されてもよい。
上記シリル基としては、トリアルキルシリル基が好ましく、炭素数1~6のアルキル基を3つ有するシリル基であることがより好ましい。
上記シリルオキシ構造を有する炭化水素基におけるシリルオキシ構造としては、トリアルキルシリルオキシ構造であることが好ましく、炭素数1~6のアルキル基を3つ有するシリルオキシ構造であることがより好ましい。
また、上記シリルオキシ構造を有する炭化水素基は、シリルオキシ構造を1~6個有することが好ましい。
更に、上記シリルオキシ構造を有する炭化水素基の炭素数は、10以上であることが好ましく、10~100であることがより好ましく、16~50であることが特に好ましい。
上記シリルオキシ構造を有する炭化水素基におけるシリルオキシ構造としては、トリアルキルシリルオキシ構造であることが好ましく、炭素数1~6のアルキル基を3つ有するシリルオキシ構造であることがより好ましい。
また、上記シリルオキシ構造を有する炭化水素基は、シリルオキシ構造を1~6個有することが好ましい。
更に、上記シリルオキシ構造を有する炭化水素基の炭素数は、10以上であることが好ましく、10~100であることがより好ましく、16~50であることが特に好ましい。
上記シリルオキシ構造を有する炭化水素基としては、下記式(Si)で表される基が好ましく挙げられる。
式(Si)中、Rsi1は、単結合、又は、炭素数1~3のアルキレン基を表し、Rsi2は、炭素数1~3のアルキレン基を表し、Rsi3及びRsi4はそれぞれ独立に、水素原子、炭素数1~6のアルキル基、又は、-OSiRsi5Rsi6Rsi7を表し、Rsi5~Rsi7はそれぞれ独立に、炭素数1~6のアルキル基、又は、アリール基を表す。
式(Si)におけるRsi5~Rsi7はそれぞれ独立に、炭素数1~6のアルキル基、又はフェニル基であることが好ましく、炭素数1~6のアルキル基であることがより好ましい。
上記パーフルオロアルキル構造を有する有機基におけるパーフルオロアルキル構造は、炭素数1~20のパーフルオロアルキル構造であることが好ましく、炭素数5~20のパーフルオロアルキル構造であることがより好ましく、炭素数7~16のパーフルオロアルキル構造であることが特に好ましい。また、上記パーフルオロアルキル構造は、直鎖状であっても、分岐を有していても、環構造を有していてもよい。
上記パーフルオロアルキル構造を有する有機基は、パーフルオロアルキル基、パーフルオロアルキル構造を有するアルキル基、又は、パーフルオロアルキル構造及びアルキル鎖中にアミド結合を有するアルキル基であることが好ましい。
上記パーフルオロアルキル構造を有する有機基の炭素数は、5以上であることが好ましく、10以上であることがより好ましく、10~100であることが更に好ましく、16~50であることが特に好ましい。
上記パーフルオロアルキル構造を有する有機基としては、例えば、下記に示す基が好ましく挙げられる。
上記パーフルオロアルキル構造を有する有機基は、パーフルオロアルキル基、パーフルオロアルキル構造を有するアルキル基、又は、パーフルオロアルキル構造及びアルキル鎖中にアミド結合を有するアルキル基であることが好ましい。
上記パーフルオロアルキル構造を有する有機基の炭素数は、5以上であることが好ましく、10以上であることがより好ましく、10~100であることが更に好ましく、16~50であることが特に好ましい。
上記パーフルオロアルキル構造を有する有機基としては、例えば、下記に示す基が好ましく挙げられる。
脂肪族炭化水素基を有する有機基中の脂肪族炭化水素基以外の部位は任意に設定することができる。例えば、エーテル結合、チオエーテル結合、エステル結合、スルホンアミド結合、アミド結合、「脂肪族炭化水素基」以外の炭化水素基(一価の基又は二価の基)等の部位を有していてもよい。
脂肪族炭化水素基以外の炭化水素基としては、例えば、炭素数1~4の脂肪族炭化水素基、芳香族炭化水素基等が挙げられ、具体的には、例えば、炭素数1~4のアルキル基及びアリール基等の一価の基、並びに、それらから誘導される二価の基が用いられる。中でも、炭素数6~10のアリール基がより好ましく、フェニル基が特に好ましい。
また、上記脂肪族炭化水素基、上記脂肪族炭化水素基以外の炭化水素基は、ハロゲン原子、オキソ基等から選択される置換基で置換されていてもよい。
脂肪族炭化水素基以外の炭化水素基としては、例えば、炭素数1~4の脂肪族炭化水素基、芳香族炭化水素基等が挙げられ、具体的には、例えば、炭素数1~4のアルキル基及びアリール基等の一価の基、並びに、それらから誘導される二価の基が用いられる。中でも、炭素数6~10のアリール基がより好ましく、フェニル基が特に好ましい。
また、上記脂肪族炭化水素基、上記脂肪族炭化水素基以外の炭化水素基は、ハロゲン原子、オキソ基等から選択される置換基で置換されていてもよい。
上記RAにおいて、脂肪族炭化水素基を有する有機基の環Aへの結合(置換)は、上記RA中に存在する脂肪族炭化水素基又は上記炭化水素基を介するもの、すなわち、直接炭素-炭素結合で結合しているものであっても、上記RA中に存在するエーテル結合、チオエーテル結合、エステル結合、アミド結合、スルホンアミド結合等の部位を介するものであってもよい。中でも、脂肪族炭化水素基を有する有機基は、化合物の合成のし易さの点から、エステル結合、アミド結合又はスルホンアミド結合を少なくとも有することが好ましく、エステル結合又はアミド結合を少なくとも有することがより好ましい。
また、上記脂肪族炭化水素基を有する有機基は、合成適性、晶析性及び溶解性の観点から、下記式(A1)~式(A5)で表される基を有していることが好ましく、下記式(A1)~式(A4)で表される基を有していることがより好ましく、下記式(A1)又は式(A2)で表される基を有していることが更に好ましく、下記式(A1)で表される基を有していることが特に好ましい。
また、下記式(A5)で表される基は、晶析性及び溶解性の観点から、下記式(A6)又は式(A7)で表される基であることが好ましい。
また、下記式(A5)で表される基は、晶析性及び溶解性の観点から、下記式(A6)又は式(A7)で表される基であることが好ましい。
式(A1)~式(A7)中、RA1はそれぞれ独立に、炭素数13以上の脂肪族炭化水素基を表し、nAは1~5の整数を表し、Rsはそれぞれ独立に、置換基を表し、ns1及びns2はそれぞれ独立に、0~4の整数を表し、ns3は0~6の整数を表し、ns4は0~3の整数を表し、ns5は0~(5-nA)の整数を表し、ns6は0~3の整数を表し、ns7は0~2の整数を表し、波線部分は他の構造との結合位置を表す。
式(A1)~式(A7)におけるRA1はそれぞれ独立に、ペプチド化合物合成時の収率及び原料入手性の観点から、炭素数16~40の脂肪族炭化水素基であることが好ましく、炭素数18~36の脂肪族炭化水素基であることがより好ましく、炭素数18~32のアルキル基であることが更に好ましく、炭素数18~22の直鎖アルキル基であることが特に好ましい。
また、式(A1)~式(A7)におけるRA1は、合成適性の観点から、全て同じ基であることが好ましい。
式(A5)におけるnAは、溶解性及び晶析性の観点から、1~4の整数であることが好ましく、2~4の整数であることがより好ましく、2又は3であることが特に好ましい。
また、式(A1)~式(A7)におけるRA1は、合成適性の観点から、全て同じ基であることが好ましい。
式(A5)におけるnAは、溶解性及び晶析性の観点から、1~4の整数であることが好ましく、2~4の整数であることがより好ましく、2又は3であることが特に好ましい。
式(A1)~式(A7)におけるRsとしては、上記「環A上に有していてもよい置換基」と同様の置換基が好ましく挙げられる。
式(A1)又は式(A2)におけるns1及びns2はそれぞれ独立に、0~2の整数であることが好ましく、0又は1であることがより好ましく、0であることが特に好ましい。
式(A3)におけるns3は、0~4の整数であることが好ましく、0~2の整数であることがより好ましく、0であることが特に好ましい。
式(A4)におけるns4は、0~2の整数であることが好ましく、0又は1であることがより好ましく、0であることが特に好ましい。
式(A5)~式(A7)におけるns5~ns7はそれぞれ独立に、0又は1であることが好ましく、0であることがより好ましい。
式(A1)又は式(A2)におけるns1及びns2はそれぞれ独立に、0~2の整数であることが好ましく、0又は1であることがより好ましく、0であることが特に好ましい。
式(A3)におけるns3は、0~4の整数であることが好ましく、0~2の整数であることがより好ましく、0であることが特に好ましい。
式(A4)におけるns4は、0~2の整数であることが好ましく、0又は1であることがより好ましく、0であることが特に好ましい。
式(A5)~式(A7)におけるns5~ns7はそれぞれ独立に、0又は1であることが好ましく、0であることがより好ましい。
式(1)で表されるヒドラジン誘導体において、全てのRAが有する全ての脂肪族炭化水素基の合計炭素数が、溶剤溶解性、晶析性、脱保護速度、ジケトピペラジン化合物の副生抑制性、ペプチド化合物合成時の収率、及び、脱保護時の収率の観点から、26以上であることが好ましく、26~200であることがより好ましく、32~100であることが更に好ましく、34~80であることが特に好ましく、44~66であることが最も好ましい。
また、式(1)で表されるヒドラジン誘導体は、k個のRAにおける少なくとも1つの脂肪族炭化水素基の炭素数が炭素数13以上である化合物であり、溶剤溶解性、晶析性の観点から、k個のRAにおける少なくとも2つの脂肪族炭化水素基の炭素数が13以上であることが好ましく、炭素数13以上の脂肪族炭化水素基を2つ以上有するRAを1つ以上有することがより好ましい。
例えば、「k個のRAにおける少なくとも2つの脂肪族炭化水素基の炭素数が13以上である」場合では、式(1)で表されるヒドラジン誘導体は、炭素数13以上の脂肪族炭化水素基を2つ以上有するRAを1つ以上有する態様であってもよいし、炭素数13以上の脂肪族炭化水素基を1つのみ有するRAを2つ以上有する態様であってもよいし、その両方の態様であってもよい。
更に、式(1)で表されるヒドラジン誘導体は、溶解性及び晶析性の観点から、炭素数13~100の脂肪族炭化水素基を少なくとも1つ有する化合物であることがより好ましく、炭素数18~40の脂肪族炭化水素基を少なくとも1つ有する化合物であることが更に好ましく、炭素数20~36の脂肪族炭化水素基を少なくとも1つ有する化合物であることが特に好ましい。
式(1)で表されるヒドラジン誘導体は、k個のRAにおける少なくとも1つの脂肪族炭化水素基の炭素数が、好ましくは14以上、より好ましくは16以上、更に好ましくは18以上、特に好ましくは20以上であると、より優れた効果を発揮する。その理由は炭素数が増加することで分子全体に占める疎水性の寄与率が大きくなり、疎水性溶剤に溶解しやすくなり、また、親水性溶媒に対しては、炭素数が増加することで凝集力がより増加し、晶析しやすくなるためと考えられる。
更に、上記脂肪族炭化水素基は、晶析性の観点から、アルキル基であることが好ましく、直鎖アルキル基であることがより好ましい。
また、1つのRAの炭素数はそれぞれ独立に、溶剤溶解性、晶析性の観点から、13~200であることが好ましく、18~150であることがより好ましく、18~100であることが更に好ましく、20~80であることが特に好ましい。
また、式(1)で表されるヒドラジン誘導体は、k個のRAにおける少なくとも1つの脂肪族炭化水素基の炭素数が炭素数13以上である化合物であり、溶剤溶解性、晶析性の観点から、k個のRAにおける少なくとも2つの脂肪族炭化水素基の炭素数が13以上であることが好ましく、炭素数13以上の脂肪族炭化水素基を2つ以上有するRAを1つ以上有することがより好ましい。
例えば、「k個のRAにおける少なくとも2つの脂肪族炭化水素基の炭素数が13以上である」場合では、式(1)で表されるヒドラジン誘導体は、炭素数13以上の脂肪族炭化水素基を2つ以上有するRAを1つ以上有する態様であってもよいし、炭素数13以上の脂肪族炭化水素基を1つのみ有するRAを2つ以上有する態様であってもよいし、その両方の態様であってもよい。
更に、式(1)で表されるヒドラジン誘導体は、溶解性及び晶析性の観点から、炭素数13~100の脂肪族炭化水素基を少なくとも1つ有する化合物であることがより好ましく、炭素数18~40の脂肪族炭化水素基を少なくとも1つ有する化合物であることが更に好ましく、炭素数20~36の脂肪族炭化水素基を少なくとも1つ有する化合物であることが特に好ましい。
式(1)で表されるヒドラジン誘導体は、k個のRAにおける少なくとも1つの脂肪族炭化水素基の炭素数が、好ましくは14以上、より好ましくは16以上、更に好ましくは18以上、特に好ましくは20以上であると、より優れた効果を発揮する。その理由は炭素数が増加することで分子全体に占める疎水性の寄与率が大きくなり、疎水性溶剤に溶解しやすくなり、また、親水性溶媒に対しては、炭素数が増加することで凝集力がより増加し、晶析しやすくなるためと考えられる。
更に、上記脂肪族炭化水素基は、晶析性の観点から、アルキル基であることが好ましく、直鎖アルキル基であることがより好ましい。
また、1つのRAの炭素数はそれぞれ独立に、溶剤溶解性、晶析性の観点から、13~200であることが好ましく、18~150であることがより好ましく、18~100であることが更に好ましく、20~80であることが特に好ましい。
式(1)において、少なくとも1つのRAが、溶剤溶解性、晶析性、及び、収率の観点から、下記式(f1)、式(a1)、式(b1)又は式(e1)のいずれかで表される基であることが好ましく、下記式(f1)又は式(a1)で表される基であることがより好ましく、下記式(f1)で表される基であることが特に好ましい。
式(f1)中、波線部分は他の構造との結合位置を表し、m9は1~3の整数を表し、X9はそれぞれ独立に、単結合、-O-、-S-、-COO-、-OCO-、-OCONH-、-NHCONH-、-NHCO-、又は、-CONH-を表し、R9はそれぞれ独立に、二価の脂肪族炭化水素基を表し、Ar1は、(m10+1)価の芳香族基、又は、(m10+1)価の複素芳香族基を表し、m10は、1~3の整数を表し、X10はそれぞれ独立に、単結合、-O-、-S-、-COO-、-OCO-、-OCONH-、-NHCONH-、-NHCO-、又は、-CONH-を表し、R10はそれぞれ独立に、一価の脂肪族炭化水素基を表し、R10の少なくとも1つは、炭素数5以上の一価の脂肪族炭化水素基である。
式(a1)中、波線部分は他の構造との結合位置を表し、m20は、1~10の整数を表し、X20はそれぞれ独立に、単結合、-O-、-S-、-COO-、-OCO-、-OCONH-、-NHCONH-、-NHCO-、又は、-CONH-を表し、R20はそれぞれ独立に、二価の脂肪族炭化水素基を表し、R20の少なくとも1つは、炭素数5以上の二価の脂肪族炭化水素基である。
式(b1)中、波線部分は他の構造との結合位置を表し、mbは、1又は2を表し、b1~b4はそれぞれ独立に、0~2の整数を表し、Xb1~Xb4はそれぞれ独立に、単結合、-O-、-S-、-COO-、-OCONH-、又は、-CONH-を表し、Rb2及びRb4はそれぞれ独立に、水素原子、メチル基、又は、炭素数5以上の脂肪族炭化水素基を表し、Rb3は、炭素数5以上の脂肪族炭化水素基を表す。
式(e1)中、波線部分は他の構造との結合位置を表し、Xe1は、単結合、-O-、-S-、-NHCO-、又は、-CONH-を表し、meは0~15の整数を表し、e1は0~11の整数を表し、e2は0~5の整数を表し、Xe2はそれぞれ独立に、単結合、-O-、-S-、-COO-、-OCONH-、-NHCO-、又は、-CONH-を表し、Re2はそれぞれ独立に、水素原子、メチル基、炭素数5以上の脂肪族炭化水素基を有する有機基を表す。
式(f1)におけるm9は、1又は2であることが好ましく、1であることがより好ましい。
式(f1)におけるX9及びX10はそれぞれ独立に、-O-、-S-、-COO-、-OCONH-、又は、-CONH-であることが好ましく、-O-であることがより好ましい。
式(f1)におけるR9はそれぞれ独立に、炭素数1~10のアルキレン基であることが好ましく、炭素数1~4のアルキレン基であることがより好ましく、メチレン基であることが特に好ましい。
式(f1)におけるR10はそれぞれ独立に、炭素数5~60の一価の脂肪族炭化水素基であることが好ましく、炭素数12~50の一価の脂肪族炭化水素基がより好ましく、炭素数18~40の一価の脂肪族炭化水素基が更に好ましく、炭素数20~32の一価の脂肪族炭化水素基であることが特に好ましい。また、R10はそれぞれ独立に、直鎖アルキル基、又は、分岐アルキル基であることが好ましく、直鎖アルキル基であることがより好ましい。
式(f1)におけるm10は、2又は3であることが好ましく、2であることがより好ましい。
式(f1)におけるAr1は、(m10+1)価の芳香族基であることが好ましく、ベンゼンから(m10+1)個の水素原子を除いた基、又は、ナフタレンから(m10+1)個の水素原子を除いた基であることがより好ましく、ベンゼンから(m10+1)個の水素原子を除いた基であることが特に好ましい。
式(f1)におけるX9及びX10はそれぞれ独立に、-O-、-S-、-COO-、-OCONH-、又は、-CONH-であることが好ましく、-O-であることがより好ましい。
式(f1)におけるR9はそれぞれ独立に、炭素数1~10のアルキレン基であることが好ましく、炭素数1~4のアルキレン基であることがより好ましく、メチレン基であることが特に好ましい。
式(f1)におけるR10はそれぞれ独立に、炭素数5~60の一価の脂肪族炭化水素基であることが好ましく、炭素数12~50の一価の脂肪族炭化水素基がより好ましく、炭素数18~40の一価の脂肪族炭化水素基が更に好ましく、炭素数20~32の一価の脂肪族炭化水素基であることが特に好ましい。また、R10はそれぞれ独立に、直鎖アルキル基、又は、分岐アルキル基であることが好ましく、直鎖アルキル基であることがより好ましい。
式(f1)におけるm10は、2又は3であることが好ましく、2であることがより好ましい。
式(f1)におけるAr1は、(m10+1)価の芳香族基であることが好ましく、ベンゼンから(m10+1)個の水素原子を除いた基、又は、ナフタレンから(m10+1)個の水素原子を除いた基であることがより好ましく、ベンゼンから(m10+1)個の水素原子を除いた基であることが特に好ましい。
また、上記式(f1)で表される基は、溶剤溶解性、晶析性、及び、収率の観点から、下記式(f2)で表される基であることが好ましい。
式(f2)中、波線部分は他の構造との結合位置を表し、m10は、1~3の整数を表し、m11は、1~3の整数を表し、X10はそれぞれ独立に、単結合、-O-、-S-、-COO-、-OCO-、-OCONH-、-NHCONH-、-NHCO-、又は、-CONH-を表し、R10はそれぞれ独立に、炭素数5以上の一価の脂肪族炭化水素基を表す。
式(f2)におけるm10、X10及びR10はそれぞれ、式(f1)におけるm10、X10及びR10と同義であり、好ましい態様も同様である。
式(f2)におけるm11は、1又は2であることが好ましく、1であることがより好ましい。
式(f2)におけるm11は、1又は2であることが好ましく、1であることがより好ましい。
式(a1)におけるm20は、1又は2であることが好ましい。
式(a1)におけるX20はそれぞれ独立に、-O-、-S-、-COO-、-OCONH-、又は、-CONH-であることが好ましく、-O-であることがより好ましい。
式(a1)におけるR20は、炭素数5以上の二価の脂肪族炭化水素基であることが好ましく、炭素数5~60の二価の脂肪族炭化水素基であることがより好ましく、炭素数8~40の二価の脂肪族炭化水素基であることが更に好ましく、炭素数12~32の二価の脂肪族炭化水素基であることが特に好ましい。また、R20は、直鎖アルキレン基であることが好ましい。
式(a1)におけるX20はそれぞれ独立に、-O-、-S-、-COO-、-OCONH-、又は、-CONH-であることが好ましく、-O-であることがより好ましい。
式(a1)におけるR20は、炭素数5以上の二価の脂肪族炭化水素基であることが好ましく、炭素数5~60の二価の脂肪族炭化水素基であることがより好ましく、炭素数8~40の二価の脂肪族炭化水素基であることが更に好ましく、炭素数12~32の二価の脂肪族炭化水素基であることが特に好ましい。また、R20は、直鎖アルキレン基であることが好ましい。
式(b1)におけるmbは、1であることが好ましい。
式(b1)におけるb1~b4はそれぞれ独立に、1又は2であることが好ましく、1であることがより好ましい。
式(b1)におけるXb1~Xb4はそれぞれ独立に、-O-、-S-、-COO-、-OCONH-、又は、-CONH-であることが好ましく、-O-であることがより好ましい。
式(b1)におけるRb2及びRb4はそれぞれ独立に、水素原子、メチル基、又は、炭素数5~60の脂肪族炭化水素基であることが好ましく、水素原子、メチル基、又は、炭素数8~40のアルキル基であることが好ましく、水素原子、メチル基、又は、炭素数12~32のアルキル基であることが特に好ましい。
式(b1)におけるRb3は、炭素数5~60の、一価の脂肪族炭化水素基であることが好ましく、炭素数5~60の一価の脂肪族炭化水素基であることがより好ましく、炭素数8~40の一価の脂肪族炭化水素基であることが更に好ましく、炭素数12~32の一価の脂肪族炭化水素基であることが特に好ましい。また、Rb3は、直鎖アルキル基であることが好ましい。
式(b1)におけるb1~b4はそれぞれ独立に、1又は2であることが好ましく、1であることがより好ましい。
式(b1)におけるXb1~Xb4はそれぞれ独立に、-O-、-S-、-COO-、-OCONH-、又は、-CONH-であることが好ましく、-O-であることがより好ましい。
式(b1)におけるRb2及びRb4はそれぞれ独立に、水素原子、メチル基、又は、炭素数5~60の脂肪族炭化水素基であることが好ましく、水素原子、メチル基、又は、炭素数8~40のアルキル基であることが好ましく、水素原子、メチル基、又は、炭素数12~32のアルキル基であることが特に好ましい。
式(b1)におけるRb3は、炭素数5~60の、一価の脂肪族炭化水素基であることが好ましく、炭素数5~60の一価の脂肪族炭化水素基であることがより好ましく、炭素数8~40の一価の脂肪族炭化水素基であることが更に好ましく、炭素数12~32の一価の脂肪族炭化水素基であることが特に好ましい。また、Rb3は、直鎖アルキル基であることが好ましい。
また、本開示に係る式(1)で表される化合物は、溶剤溶解性の観点からは、上記脂肪族炭化水素基を有する有機基として、分岐を有する脂肪族炭化水素基を有する有機基が好ましく挙げられ、以下に示す基がより好ましく挙げられる。なお、波線部分は他の構造との結合位置を表し、nt2は3以上の整数を表し、nt3は、下記基の総炭素数が14~300となるように設定される整数を表す。
また、式(1)で表されるヒドラジン誘導体は、合成適性及び、脱保護時の収率の観点から、下記式(B1)~式(B5)のいずれかで表される化合物であることが好ましく、式(B1)~式(B4)のいずれかで表される化合物であることがより好ましく、式(B1)で表される化合物であることが特に好ましい。
式(B1)~式(B5)中、RB1はそれぞれ独立に、炭素数13以上の脂肪族炭化水素基を表し、ZBは、カルボニル基又はスルホニル基を表し、RsBはそれぞれ独立に、置換基を表し、nB1はそれぞれ独立に、0~4の整数を表し、nB2は0~6の整数を表し、nB3は0~3の整数を表し、nB41は0~4の整数を表し、nB42は1~5の整数を表し、nB5は1~5の整数を表し、LB5は、二価の連結基を表し、Rは、水素原子、アミノ保護基、アミノ酸残基、又は、ペプチド残基を表し、ns51は0~4の整数を表し、ns52は0~4の整数を表し、nB5+ns52=1~5の整数を満たす。
式(B1)~式(B5)におけるRはそれぞれ、式(1)におけるRと同義であり、好ましい態様も同様である。
式(B1)~式(B5)におけるRB1はそれぞれ独立に、ペプチド化合物合成時の収率及び原料入手性の観点から、炭素数16~40の脂肪族炭化水素基であることが好ましく、炭素数18~36の脂肪族炭化水素基であることがより好ましく、炭素数18~32のアルキル基であることが更に好ましく、炭素数18~22の直鎖アルキル基であることが特に好ましい。
また、式(B1)~式(B5)におけるRB1は、合成適性の観点から、全て同じ基であることが好ましい。
式(B5)におけるnB5は、溶解性及び晶析性の観点から、1~4の整数であることが好ましく、2~4の整数であることがより好ましく、2又は3であることが特に好ましい。
式(B1)~式(B5)におけるRsBとしては、上記環A上に有していてもよい置換基と同様の置換基が好ましく挙げられる。
式(B1)におけるnB1はそれぞれ独立に、0~2の整数であることが好ましく、0又は1であることがより好ましく、0であることが特に好ましい。
式(B2)におけるnB2は、0~4の整数であることが好ましく、0~2の整数であることがより好ましく、0であることが特に好ましい。
式(B3)におけるnB3は、0~2の整数であることが好ましく、0又は1であることがより好ましく、0であることが特に好ましい。
式(B4)におけるnB41は、0又は1であることが好ましく、0であることがより好ましい。
式(B4)におけるnB42は、2~5の整数であることが好ましく、2~4であることがより好ましく、2又は3であることが特に好ましい。
式(B1)~式(B5)におけるRB1はそれぞれ独立に、ペプチド化合物合成時の収率及び原料入手性の観点から、炭素数16~40の脂肪族炭化水素基であることが好ましく、炭素数18~36の脂肪族炭化水素基であることがより好ましく、炭素数18~32のアルキル基であることが更に好ましく、炭素数18~22の直鎖アルキル基であることが特に好ましい。
また、式(B1)~式(B5)におけるRB1は、合成適性の観点から、全て同じ基であることが好ましい。
式(B5)におけるnB5は、溶解性及び晶析性の観点から、1~4の整数であることが好ましく、2~4の整数であることがより好ましく、2又は3であることが特に好ましい。
式(B1)~式(B5)におけるRsBとしては、上記環A上に有していてもよい置換基と同様の置換基が好ましく挙げられる。
式(B1)におけるnB1はそれぞれ独立に、0~2の整数であることが好ましく、0又は1であることがより好ましく、0であることが特に好ましい。
式(B2)におけるnB2は、0~4の整数であることが好ましく、0~2の整数であることがより好ましく、0であることが特に好ましい。
式(B3)におけるnB3は、0~2の整数であることが好ましく、0又は1であることがより好ましく、0であることが特に好ましい。
式(B4)におけるnB41は、0又は1であることが好ましく、0であることがより好ましい。
式(B4)におけるnB42は、2~5の整数であることが好ましく、2~4であることがより好ましく、2又は3であることが特に好ましい。
式(B5)におけるLB5の炭素数は、合成適性及び晶析性の観点から、炭素数1~30であることが好ましく、炭素数1~20であることがより好ましく、炭素数1~8であることが特に好ましい。
式(B5)におけるLB5は、合成適性及び晶析性の観点から、アルキレン基、又は、エステル結合、アミド結合、スルホンアミド結合、エーテル結合、ウレタン結合及びウレア結合よりなる群から選ばれた少なくとも1種の結合を1つ以上とアルキレン基を1つ以上とを組み合わせた基であることが好ましく、
エステル結合、アミド結合、スルホンアミド結合、エーテル結合、ウレタン結合及びウレア結合よりなる群から選ばれた少なくとも1種の結合を1つ以上とアルキレン基を1つ以上とを組み合わせた基であることがより好ましく、
エステル結合、アミド結合及びスルホンアミド結合よりなる群から選ばれた少なくとも1種の結合を1つ以上とアルキレン基を1つ以上とを組み合わせた基であることが更に好ましく、
エステル結合、アミド結合及びスルホンアミド結合よりなる群から選ばれた少なくとも1種の結合を1つ又は2つとアルキレン基を1つ又は2つとを組み合わせた基であることが特に好ましい。
更に、式(B5)における-ORB1のベンゼン環上の置換位置は、特に制限はないが、LB5の置換位置(1位)に対し、3位~5位であることが好ましい。
式(B5)におけるns51は、0~2の整数であることが好ましく、0又は1であることがより好ましく、0であることが特に好ましい。
式(B5)におけるns52は、0~2の整数であることが好ましく、0又は1であることがより好ましく、0であることが特に好ましい。
式(B5)におけるLB5は、合成適性及び晶析性の観点から、アルキレン基、又は、エステル結合、アミド結合、スルホンアミド結合、エーテル結合、ウレタン結合及びウレア結合よりなる群から選ばれた少なくとも1種の結合を1つ以上とアルキレン基を1つ以上とを組み合わせた基であることが好ましく、
エステル結合、アミド結合、スルホンアミド結合、エーテル結合、ウレタン結合及びウレア結合よりなる群から選ばれた少なくとも1種の結合を1つ以上とアルキレン基を1つ以上とを組み合わせた基であることがより好ましく、
エステル結合、アミド結合及びスルホンアミド結合よりなる群から選ばれた少なくとも1種の結合を1つ以上とアルキレン基を1つ以上とを組み合わせた基であることが更に好ましく、
エステル結合、アミド結合及びスルホンアミド結合よりなる群から選ばれた少なくとも1種の結合を1つ又は2つとアルキレン基を1つ又は2つとを組み合わせた基であることが特に好ましい。
更に、式(B5)における-ORB1のベンゼン環上の置換位置は、特に制限はないが、LB5の置換位置(1位)に対し、3位~5位であることが好ましい。
式(B5)におけるns51は、0~2の整数であることが好ましく、0又は1であることがより好ましく、0であることが特に好ましい。
式(B5)におけるns52は、0~2の整数であることが好ましく、0又は1であることがより好ましく、0であることが特に好ましい。
式(1)で表されるヒドラジン誘導体の分子量は、特に制限はないが、脱保護速度、晶析性、溶剤溶解性、ジケトピペラジン化合物の副生抑制性、ペプチド化合物合成時の収率、及び、脱保護時の収率の観点から、340~3,000であることが好ましく、400~2,000であることがより好ましく、500~1,500であることが更に好ましく、800~1,300であることが特に好ましい。また、分子量が3,000以下であると、目的物に占める式(1)で表されるヒドラジン誘導体の割合が適度であり、式(1)で表されるヒドラジン誘導体を脱保護して得られる化合物の割合が少なくならないため、生産性に優れる。
式(1)で表されるヒドラジン誘導体の具体例としては、下記に示す化合物が好ましく挙げられるが、これらに限定されないことは言うまでもない。
<式(1)で表されるヒドラジン誘導体の製造方法>
式(1)で表されるヒドラジン誘導体の製造方法としては、特に限定されないが、公知の方法を参照して製造することができる。
式(1)で表されるヒドラジン誘導体の製造に用いる原料化合物は、特に述べない限り、市販されているものを用いてもよいし、自体公知の方法、又は、これらに準ずる方法に従って製造することもできる。例えば、tert-ブトキシカルボニルヒドラジニル安息香酸のような、芳香族ヒドラジン誘導体に、炭素数13以上の脂肪族炭化水素基を有する基を導入することにより、好適に式(1)で表されるヒドラジン誘導体を作製することができる。
また、必要に応じ、製造した式(1)で表されるヒドラジン誘導体を公知の精製方法により、精製してもよい。例えば、再結晶、カラムクロマトグラフィー等によって単離及び精製する方法、及び、溶液温度を変化させる手段や溶液組成を変化させる手段等によって再沈殿により精製する方法等を行うことができる。
式(1)で表されるヒドラジン誘導体の製造方法としては、特に限定されないが、公知の方法を参照して製造することができる。
式(1)で表されるヒドラジン誘導体の製造に用いる原料化合物は、特に述べない限り、市販されているものを用いてもよいし、自体公知の方法、又は、これらに準ずる方法に従って製造することもできる。例えば、tert-ブトキシカルボニルヒドラジニル安息香酸のような、芳香族ヒドラジン誘導体に、炭素数13以上の脂肪族炭化水素基を有する基を導入することにより、好適に式(1)で表されるヒドラジン誘導体を作製することができる。
また、必要に応じ、製造した式(1)で表されるヒドラジン誘導体を公知の精製方法により、精製してもよい。例えば、再結晶、カラムクロマトグラフィー等によって単離及び精製する方法、及び、溶液温度を変化させる手段や溶液組成を変化させる手段等によって再沈殿により精製する方法等を行うことができる。
本開示に係るペプチド化合物の製造方法において、上記式(1)で表されるヒドラジン誘導体を用いる工程が、上記式(1)で表されるヒドラジン誘導体によりアミノ酸化合物又はペプチド化合物のカルボキシ基を保護するC末端保護工程であることが好ましい。
また、本開示に係るペプチド化合物の製造方法は、ペプチド化合物の合成容易性、及び、収率の観点から、上記式(1)で表されるヒドラジン誘導体によりアミノ酸化合物又はペプチド化合物のカルボキシ基を保護するC末端保護工程に加え、上記C末端保護工程で得られたN末端保護C末端保護アミノ酸化合物又はN末端保護C末端保護ペプチド化合物のN末端を脱保護するN末端脱保護工程、及び、上記N末端脱保護工程で得られたC末端保護アミノ酸化合物又はC末端保護ペプチド化合物のN末端に、N末端保護アミノ酸化合物、又は、N末端保護ペプチド化合物を縮合させるペプチド鎖延長工程を更に含むことがより好ましく、
上記ペプチド鎖延長工程で得られたN末端保護C末端保護ペプチド化合物を沈殿させる沈殿工程、又は、上記ペプチド鎖延長工程で得られたN末端保護C末端保護ペプチド化合物に水を添加し、不純物を水相に抽出分離する抽出工程を更に含むことが更に好ましく、
上記沈殿工程又は上記抽出工程の後に、得られたN末端保護C末端保護ペプチド化合物のN末端を脱保護する工程、得られたC末端保護ペプチド化合物のN末端に、N末端保護アミノ酸化合物、又は、N末端保護ペプチド化合物を縮合させる工程、及び、得られたN末端保護C末端保護ペプチド化合物を沈殿する工程をこの順で1回以上更に含むことが特に好ましい。
また、本開示に係るペプチド化合物の製造方法は、C末端保護基を脱保護するC末端脱保護工程を更に含むことが好ましい。
更に、本開示に係るペプチド化合物の製造方法は、上記C末端保護工程の前に、上記式(1)で表されるヒドラジン誘導体を溶媒に溶解する溶解工程を更に含むことが好ましい。
また更に、上記式(1)で表されるヒドラジン誘導体におけるRが、アミノ酸残基、又は、ペプチド残基である場合は、上記N末端脱保護工程、又は、上記ペプチド鎖延長工程における反応基質として、好適に用いることができる。
以下、上述した各工程等について詳細に説明する。
また、本開示に係るペプチド化合物の製造方法は、ペプチド化合物の合成容易性、及び、収率の観点から、上記式(1)で表されるヒドラジン誘導体によりアミノ酸化合物又はペプチド化合物のカルボキシ基を保護するC末端保護工程に加え、上記C末端保護工程で得られたN末端保護C末端保護アミノ酸化合物又はN末端保護C末端保護ペプチド化合物のN末端を脱保護するN末端脱保護工程、及び、上記N末端脱保護工程で得られたC末端保護アミノ酸化合物又はC末端保護ペプチド化合物のN末端に、N末端保護アミノ酸化合物、又は、N末端保護ペプチド化合物を縮合させるペプチド鎖延長工程を更に含むことがより好ましく、
上記ペプチド鎖延長工程で得られたN末端保護C末端保護ペプチド化合物を沈殿させる沈殿工程、又は、上記ペプチド鎖延長工程で得られたN末端保護C末端保護ペプチド化合物に水を添加し、不純物を水相に抽出分離する抽出工程を更に含むことが更に好ましく、
上記沈殿工程又は上記抽出工程の後に、得られたN末端保護C末端保護ペプチド化合物のN末端を脱保護する工程、得られたC末端保護ペプチド化合物のN末端に、N末端保護アミノ酸化合物、又は、N末端保護ペプチド化合物を縮合させる工程、及び、得られたN末端保護C末端保護ペプチド化合物を沈殿する工程をこの順で1回以上更に含むことが特に好ましい。
また、本開示に係るペプチド化合物の製造方法は、C末端保護基を脱保護するC末端脱保護工程を更に含むことが好ましい。
更に、本開示に係るペプチド化合物の製造方法は、上記C末端保護工程の前に、上記式(1)で表されるヒドラジン誘導体を溶媒に溶解する溶解工程を更に含むことが好ましい。
また更に、上記式(1)で表されるヒドラジン誘導体におけるRが、アミノ酸残基、又は、ペプチド残基である場合は、上記N末端脱保護工程、又は、上記ペプチド鎖延長工程における反応基質として、好適に用いることができる。
以下、上述した各工程等について詳細に説明する。
<溶解工程>
本開示に係るペプチド化合物の製造方法は、上記C末端保護工程の前に、上記式(1)で表されるヒドラジン誘導体を溶媒に溶解する溶解工程を含むことが好ましい。
溶媒としては、一般的な有機溶媒を反応に用いることができるが、上記溶媒における溶解度が高い程、優れた反応性が期待できるため、式(1)で表されるヒドラジン誘導体の溶解度の高い溶媒を選択することが好ましい。具体的にはクロロホルム、ジクロロメタン等のハロゲン化炭化水素類;1,4-ジオキサン、テトラヒドロフラン、シクロペンチルメチルエーテル、4-メチルテトラヒドロピラン等の非極性有機溶媒等が挙げられる。これらの溶媒は2種以上を適宜の割合で混合して用いてもよい。また、上記ハロゲン化炭素類や非極性有機溶媒に、ベンゼン、トルエン、キシレン等の芳香族炭化水素類;アセトニトリル、プロピオニトリル等のニトリル類;アセトン、2-ブタノン等のケトン類;N,N-ジメチルホルムアミド、N-メチルピロリドン等のアミド類;ジメチルスルホキシド等のスルホキシド類、酢酸イソプロピル、酢酸エチル等のエステル類を、式(1)で表されるヒドラジン誘導体が溶解し得る限り、適宜の割合で混合して用いてもよい。
また、Organic Process Research & Development、2017、21、3、365-369に記載の溶剤を使用してもよい。
本開示に係るペプチド化合物の製造方法は、上記C末端保護工程の前に、上記式(1)で表されるヒドラジン誘導体を溶媒に溶解する溶解工程を含むことが好ましい。
溶媒としては、一般的な有機溶媒を反応に用いることができるが、上記溶媒における溶解度が高い程、優れた反応性が期待できるため、式(1)で表されるヒドラジン誘導体の溶解度の高い溶媒を選択することが好ましい。具体的にはクロロホルム、ジクロロメタン等のハロゲン化炭化水素類;1,4-ジオキサン、テトラヒドロフラン、シクロペンチルメチルエーテル、4-メチルテトラヒドロピラン等の非極性有機溶媒等が挙げられる。これらの溶媒は2種以上を適宜の割合で混合して用いてもよい。また、上記ハロゲン化炭素類や非極性有機溶媒に、ベンゼン、トルエン、キシレン等の芳香族炭化水素類;アセトニトリル、プロピオニトリル等のニトリル類;アセトン、2-ブタノン等のケトン類;N,N-ジメチルホルムアミド、N-メチルピロリドン等のアミド類;ジメチルスルホキシド等のスルホキシド類、酢酸イソプロピル、酢酸エチル等のエステル類を、式(1)で表されるヒドラジン誘導体が溶解し得る限り、適宜の割合で混合して用いてもよい。
また、Organic Process Research & Development、2017、21、3、365-369に記載の溶剤を使用してもよい。
<ヒドラジノ基上のアミノ保護基脱保護工程>
本開示に係るペプチド化合物の製造方法は、上記式(1)で表されるヒドラジン誘導体におけるRがアミノ保護基である化合物を用いる場合、式(1)で表されるヒドラジン誘導体におけるRのアミノ保護基を脱保護するヒドラジノ基上のアミノ保護基脱保護工程を含むことが好ましい。
また、上記ヒドラジノ基上のアミノ保護基脱保護工程は、後述するC末端保護工程と前に行っても、同時に行ってもよい。
更に、上記アミノ保護基が脱保護されたRが水素原子である式(1)で表されるヒドラジン誘導体は、単離してもよいし、単離せずそのまま後述するC末端保護工程に用いてもよい。
本開示に係るペプチド化合物の製造方法は、上記式(1)で表されるヒドラジン誘導体におけるRがアミノ保護基である化合物を用いる場合、式(1)で表されるヒドラジン誘導体におけるRのアミノ保護基を脱保護するヒドラジノ基上のアミノ保護基脱保護工程を含むことが好ましい。
また、上記ヒドラジノ基上のアミノ保護基脱保護工程は、後述するC末端保護工程と前に行っても、同時に行ってもよい。
更に、上記アミノ保護基が脱保護されたRが水素原子である式(1)で表されるヒドラジン誘導体は、単離してもよいし、単離せずそのまま後述するC末端保護工程に用いてもよい。
脱保護条件は、上記アミノ保護基の種類により適宜選択されるが、後述するN末端における保護基の除去とは異なる条件により脱保護できる基が好ましい。例えば、Fmoc基の場合は、塩基で処理することにより行われ、Boc基の場合は、酸で処理することにより行われる。当該反応は、反応に影響を及ぼさない溶媒中で行われる。
塩基としては、ジメチルアミン、ジエチルアミンなどの第二級アミンや、1,8-ジアザビシクロ[5.4.0]-7-ウンデセン(DBU)、1,4-ジアザビシクロ[2.2.2]オクタン(DABCO)、1,5-ジアザビシクロ[4.3.0]-5-ノネン(DBN)などの求核性のない有機塩基等が挙げられる。
溶媒としては、上記溶解工程において上述した溶剤を好適に用いることができる。
塩基としては、ジメチルアミン、ジエチルアミンなどの第二級アミンや、1,8-ジアザビシクロ[5.4.0]-7-ウンデセン(DBU)、1,4-ジアザビシクロ[2.2.2]オクタン(DABCO)、1,5-ジアザビシクロ[4.3.0]-5-ノネン(DBN)などの求核性のない有機塩基等が挙げられる。
溶媒としては、上記溶解工程において上述した溶剤を好適に用いることができる。
<C末端保護工程>
本開示に係るペプチド化合物の製造方法は、上記式(1)で表されるヒドラジン誘導体によりアミノ酸化合物又はペプチド化合物のカルボキシ基を保護するC末端保護工程を含むことが好ましい。
上記C末端保護工程に用いられるアミノ酸化合物、又は、ペプチド化合物としては、特に制限はなく、公知のものを用いることができるが、N末端保護アミノ酸化合物、又は、N末端保護ペプチド化合物であることが好ましく、Fmoc保護アミノ酸化合物、又は、Fmoc保護ペプチド化合物であることがより好ましい。
本開示に係るペプチド化合物の製造方法は、ジケトピペラジン化合物の副生を抑制することができるためより上記効果を発揮する観点から、ジケトピペラジン化合物が副生しやすいペプチド化合物である、プロリン残基、グリシン残基、N-アルキルアミノ酸残基、ペプトイド、及び、D-アミノ酸残基よりなる群から選ばれた少なくとも1種の残基を有するペプチド化合物を用いることが好ましく、プロリン残基又はグリシン残基を有するペプチド化合物を用いることがより好ましく、プロリン残基を有するペプチド化合物が特に好ましい。
また、上記ペプチド化合物における上記プロリン残基、グリシン残基、N-アルキルアミノ酸残基、ペプトイド、及び、D-アミノ酸残基の位置及び数は、特に制限はないが、C末端のアミノ酸残基、又は、C末端アミノ酸残基の隣のアミノ酸残基が少なくとも、プロリン残基、グリシン残基、N-アルキルアミノ酸残基、ペプトイド、又は、D-アミノ酸残基であることが好ましく、C末端のアミノ酸残基が少なくとも、プロリン残基、グリシン残基、N-メチルアミノ酸残基、又は、D-アミノ酸残基であることがより好ましい。
また、上記C末端保護工程に用いられるアミノ酸化合物、又は、ペプチド化合物におけるC末端部分以外のヒドロキシ基、アミノ基、カルボニル基、アミド基、イミダゾール基、インドール基、グアニジル基、メルカプト基等は上述した公知の保護基により保護されていることが好ましい。
反応基質であるアミノ酸化合物又はペプチド化合物の使用量は、上記式(1)で表されるヒドラジン誘導体1モル当量に対し、1モル当量~10モル当量であることが好ましく、1モル当量~5モル当量であることがより好ましく、1モル当量~2モル当量であることが更に好ましく、1モル当量~1.5モル当量であることが特に好ましい。
本開示に係るペプチド化合物の製造方法は、上記式(1)で表されるヒドラジン誘導体によりアミノ酸化合物又はペプチド化合物のカルボキシ基を保護するC末端保護工程を含むことが好ましい。
上記C末端保護工程に用いられるアミノ酸化合物、又は、ペプチド化合物としては、特に制限はなく、公知のものを用いることができるが、N末端保護アミノ酸化合物、又は、N末端保護ペプチド化合物であることが好ましく、Fmoc保護アミノ酸化合物、又は、Fmoc保護ペプチド化合物であることがより好ましい。
本開示に係るペプチド化合物の製造方法は、ジケトピペラジン化合物の副生を抑制することができるためより上記効果を発揮する観点から、ジケトピペラジン化合物が副生しやすいペプチド化合物である、プロリン残基、グリシン残基、N-アルキルアミノ酸残基、ペプトイド、及び、D-アミノ酸残基よりなる群から選ばれた少なくとも1種の残基を有するペプチド化合物を用いることが好ましく、プロリン残基又はグリシン残基を有するペプチド化合物を用いることがより好ましく、プロリン残基を有するペプチド化合物が特に好ましい。
また、上記ペプチド化合物における上記プロリン残基、グリシン残基、N-アルキルアミノ酸残基、ペプトイド、及び、D-アミノ酸残基の位置及び数は、特に制限はないが、C末端のアミノ酸残基、又は、C末端アミノ酸残基の隣のアミノ酸残基が少なくとも、プロリン残基、グリシン残基、N-アルキルアミノ酸残基、ペプトイド、又は、D-アミノ酸残基であることが好ましく、C末端のアミノ酸残基が少なくとも、プロリン残基、グリシン残基、N-メチルアミノ酸残基、又は、D-アミノ酸残基であることがより好ましい。
また、上記C末端保護工程に用いられるアミノ酸化合物、又は、ペプチド化合物におけるC末端部分以外のヒドロキシ基、アミノ基、カルボニル基、アミド基、イミダゾール基、インドール基、グアニジル基、メルカプト基等は上述した公知の保護基により保護されていることが好ましい。
反応基質であるアミノ酸化合物又はペプチド化合物の使用量は、上記式(1)で表されるヒドラジン誘導体1モル当量に対し、1モル当量~10モル当量であることが好ましく、1モル当量~5モル当量であることがより好ましく、1モル当量~2モル当量であることが更に好ましく、1モル当量~1.5モル当量であることが特に好ましい。
また、上記C末端保護工程において、反応に影響を及ぼさない溶媒中、縮合添加剤(縮合活性化剤)存在下、縮合剤を添加するか、酸触媒中で反応させることが好ましく挙げられる。
縮合添加剤の使用量は、上記式(1)で表されるヒドラジン誘導体1モル当量に対して、0.05モル当量~1.5モル当量であることが好ましい。
縮合添加剤の使用量は、上記式(1)で表されるヒドラジン誘導体1モル当量に対して、0.05モル当量~1.5モル当量であることが好ましい。
縮合剤としては、ペプチド合成において一般的に用いられる縮合剤が、本開示においても制限なく用いることができ、これに限定されないが、例えば、4-(4,6-ジメトキシ-1,3,5-トリアジン-2-イル)-4-メチルモルホニウムクロリド(DMTMM)、O-(ベンゾトリアゾール-1-イル)-1,1,3,3-テトラメチルウロニウムヘキサフルオロホスフェート(HBTU)、O-(7-アザベンゾトリアゾール-1-イル)-1,1,3,3-テトラメチルウロニウムヘキサフルオロホスフェート(HATU)、O-(6-クロロベンゾトリアゾール-1-イル)-1,1,3,3-テトラメチルウロニウムヘキサフルオロホスフェート(HBTU(6-Cl))、O-(ベンゾトリアゾール-1-イル)-1,1,3,3-テトラメチルウロニウムテトラフルオロボレート(TBTU)、O-(6-クロロベンゾトリアゾール-1-イル)-1,1,3,3-テトラメチルウロニウムテトラフルオロボレート(TCTU)、(1-シアノ-2-エトキシ-2-オキソエチリデンアミノオキシ)ジメチルアミノモルホリノカルベニウムヘキサフルオロリン酸塩(COMU)、ジシクロヘキシルカルボジイミド(DCC)、ジイソプロピルカルボジイミド(DIC)、1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド(EDC)、その塩酸塩(EDC・HCl)、ヘキサフルオロリン酸(7-アザベンゾトリアゾール-1-イルオキシ)トリピロリジノホスホニウム(PyAOP)、及び、ヘキサフルオロリン酸(ベンゾトリアゾール-1-イルオキシ)トリピロリジノホスホニウム(PyBop)等を挙げることができる。
中でも、DIC、EDC、EDC・HCl、DMT-MM、HBTU、HATU、COMU、又は、PyAOPが好ましい。
縮合剤の使用量は、上記式(1)で表されるヒドラジン誘導体1モル当量に対して、1モル当量~10モル当量であることが好ましく、1モル当量~5モル当量であることがより好ましい。
中でも、DIC、EDC、EDC・HCl、DMT-MM、HBTU、HATU、COMU、又は、PyAOPが好ましい。
縮合剤の使用量は、上記式(1)で表されるヒドラジン誘導体1モル当量に対して、1モル当量~10モル当量であることが好ましく、1モル当量~5モル当量であることがより好ましい。
縮合反応に用いる酸触媒としては、ペプチド合成において一般的に用いられる酸触媒を制限なく用いることができ、例えば、トリフルオロ酢酸(TFA)、塩酸、トリフルオロエタノール(TFE)、ヘキサフルオロイソプロパノール(HFIP)、酢酸、メタンスルホン酸、トリフルオロメタンスルホン酸、p-トルエンスルホン酸等を挙げることができる。
中でも、トリフルオロ酢酸が好ましい。
酸触媒の使用量は、上記式(1)で表されるヒドラジン誘導体1モル当量に対して、0モル当量を超え4.0モル当量であることが好ましく、0.05モル当量~1.5モル当量であることがより好ましく、0.1モル当量~0.3モル当量であることが更に好ましい。
中でも、トリフルオロ酢酸が好ましい。
酸触媒の使用量は、上記式(1)で表されるヒドラジン誘導体1モル当量に対して、0モル当量を超え4.0モル当量であることが好ましく、0.05モル当量~1.5モル当量であることがより好ましく、0.1モル当量~0.3モル当量であることが更に好ましい。
上記C末端保護工程において、反応を促進する、又はラセミ化などの副反応を抑制するため、縮合活性化剤を添加することが好ましい。
本開示における縮合活性化剤とは、縮合剤との共存化で、アミノ酸を、対応する活性エステル、対称酸無水物などに導いて、ペプチド結合(アミド結合)を形成させやすくする試薬である。
縮合活性化剤としては、ペプチド合成において一般的に用いられる縮合活性化剤を制限なく用いることができ、例えば、4-ジメチルアミノピリジン、N-メチルイミダゾール、ボロン酸誘導体、1-ヒドロキシベンゾトリアゾール(HOBt)、エチル 1-ヒドロキシトリアゾール-4-カルボキシレート(HOCt)、1-ヒドロキシ-7-アザベンゾトリアゾール(HOAt)、3-ヒドロキシ-1,2,3-ベンゾトリアゾジン-4(3H)-オン(HOOBt)、N-ヒドロキシスクシンイミド(HOSu)、N-ヒドロキシフタルイミド(HOPht)、N-ヒドロキシ-5-ノルボルネン-2,3-ジカルボキシイミド(HONb)、ペンタフルオロフェノール、エチル(ヒドロキシイミノ)シアノアセタート(Oxyma)等を挙げることができる。中でも、4-ジメチルアミノピリジン、HOBt、HOCt、HOAt、HOOBt、HOSu、HONb、又は、Oxymaが好ましい。
活性化剤の使用量は、アミノ酸化合物又はペプチド化合物に対して、0モル当量を超え4.0モル当量であることが好ましく、0.1モル当量~1.5モル当量であることがより好ましい。
本開示における縮合活性化剤とは、縮合剤との共存化で、アミノ酸を、対応する活性エステル、対称酸無水物などに導いて、ペプチド結合(アミド結合)を形成させやすくする試薬である。
縮合活性化剤としては、ペプチド合成において一般的に用いられる縮合活性化剤を制限なく用いることができ、例えば、4-ジメチルアミノピリジン、N-メチルイミダゾール、ボロン酸誘導体、1-ヒドロキシベンゾトリアゾール(HOBt)、エチル 1-ヒドロキシトリアゾール-4-カルボキシレート(HOCt)、1-ヒドロキシ-7-アザベンゾトリアゾール(HOAt)、3-ヒドロキシ-1,2,3-ベンゾトリアゾジン-4(3H)-オン(HOOBt)、N-ヒドロキシスクシンイミド(HOSu)、N-ヒドロキシフタルイミド(HOPht)、N-ヒドロキシ-5-ノルボルネン-2,3-ジカルボキシイミド(HONb)、ペンタフルオロフェノール、エチル(ヒドロキシイミノ)シアノアセタート(Oxyma)等を挙げることができる。中でも、4-ジメチルアミノピリジン、HOBt、HOCt、HOAt、HOOBt、HOSu、HONb、又は、Oxymaが好ましい。
活性化剤の使用量は、アミノ酸化合物又はペプチド化合物に対して、0モル当量を超え4.0モル当量であることが好ましく、0.1モル当量~1.5モル当量であることがより好ましい。
塩基としては、ペプチド合成において一般的に用いられる塩基を制限なく用いることができ、例えば、ジイソプロピルエチルアミンなどの第三級アミン等が挙げられる。
溶媒としては、上記溶解工程において上述した溶剤を好適に用いることができる。
反応温度は、特に制限はないが、-10℃~80℃であることが好ましく、0℃~40℃であることがより好ましい。反応時間は、特に制限はないが、1時間~30時間であることが好ましい。
反応の進行の確認は、一般的な液相有機合成反応と同様の方法を適用できる。すなわち、薄層シリカゲルクロマトグラフィー、高速液体クロマトグラフィー、NMR等を用いて反応を追跡することができる。
溶媒としては、上記溶解工程において上述した溶剤を好適に用いることができる。
反応温度は、特に制限はないが、-10℃~80℃であることが好ましく、0℃~40℃であることがより好ましい。反応時間は、特に制限はないが、1時間~30時間であることが好ましい。
反応の進行の確認は、一般的な液相有機合成反応と同様の方法を適用できる。すなわち、薄層シリカゲルクロマトグラフィー、高速液体クロマトグラフィー、NMR等を用いて反応を追跡することができる。
また、上記C末端保護工程により得られたN末端保護C末端保護アミノ酸化合物又はN末端保護C末端保護ペプチド化合物は、精製を行ってもよい。
例えば、得られたN末端保護C末端保護アミノ酸化合物又はN末端保護C末端保護ペプチド化合物を溶媒に溶解させ、所望の有機合成反応を行った後に得られる生成物を単離するために、N末端保護C末端保護アミノ酸化合物又はN末端保護C末端保護ペプチド化合物が溶解している溶媒を変化させ(例、溶媒組成の変更、溶媒の種類の変更)、再沈殿させる方法が好ましく挙げられる。
具体的には例えば、N末端保護C末端保護アミノ酸化合物又はN末端保護C末端保護ペプチド化合物が溶解するような条件下にて反応を行い、反応後、溶媒を留去後、溶媒置換するか、反応後、溶媒を留去せずに、反応系へ極性溶媒を添加することによって凝集物を沈殿化し不純物を淘汰する。置換溶媒としては、メタノール、アセトニトリル、水等の極性有機溶媒を単独又は混合して用いる。すなわち、N末端保護C末端保護アミノ酸化合物又はN末端保護C末端保護ペプチド化合物が溶解するような条件下にて反応を行い、反応後、溶媒置換としては、例えば溶解にはハロゲン化溶媒、THF等を用いて、沈殿化にはメタノール、アセトニトリルや水等の極性有機溶媒、又は、それらの混合溶媒を用いる。
例えば、得られたN末端保護C末端保護アミノ酸化合物又はN末端保護C末端保護ペプチド化合物を溶媒に溶解させ、所望の有機合成反応を行った後に得られる生成物を単離するために、N末端保護C末端保護アミノ酸化合物又はN末端保護C末端保護ペプチド化合物が溶解している溶媒を変化させ(例、溶媒組成の変更、溶媒の種類の変更)、再沈殿させる方法が好ましく挙げられる。
具体的には例えば、N末端保護C末端保護アミノ酸化合物又はN末端保護C末端保護ペプチド化合物が溶解するような条件下にて反応を行い、反応後、溶媒を留去後、溶媒置換するか、反応後、溶媒を留去せずに、反応系へ極性溶媒を添加することによって凝集物を沈殿化し不純物を淘汰する。置換溶媒としては、メタノール、アセトニトリル、水等の極性有機溶媒を単独又は混合して用いる。すなわち、N末端保護C末端保護アミノ酸化合物又はN末端保護C末端保護ペプチド化合物が溶解するような条件下にて反応を行い、反応後、溶媒置換としては、例えば溶解にはハロゲン化溶媒、THF等を用いて、沈殿化にはメタノール、アセトニトリルや水等の極性有機溶媒、又は、それらの混合溶媒を用いる。
<N末端脱保護工程>
本開示に係るペプチド化合物の製造方法は、上記C末端保護工程で得られたN末端保護C末端保護アミノ酸化合物又はN末端保護C末端保護ペプチド化合物のN末端を脱保護するN末端脱保護工程を含むことが好ましい。
N末端の保護基としては、ペプチド化学等の技術分野で一般的に用いられる上述のアミノ基の保護基が使用可能であるが、本開示においては、Boc基、Cbz基、又は、Fmoc基が好適に用いられる。
本開示に係るペプチド化合物の製造方法は、上記C末端保護工程で得られたN末端保護C末端保護アミノ酸化合物又はN末端保護C末端保護ペプチド化合物のN末端を脱保護するN末端脱保護工程を含むことが好ましい。
N末端の保護基としては、ペプチド化学等の技術分野で一般的に用いられる上述のアミノ基の保護基が使用可能であるが、本開示においては、Boc基、Cbz基、又は、Fmoc基が好適に用いられる。
脱保護条件は、当該一時保護基の種類により適宜選択されるが、上記式(1)で表されるヒドラジン誘導体由来の保護基の除去(ヒドラジノ基上のアミノ保護基脱保護工程)とは異なる条件により脱保護できる基が好ましい。例えば、Fmoc基の場合は、塩基で処理することにより行われ、Boc基の場合は、酸で処理することにより行われる。当該反応は、反応に影響を及ぼさない溶媒中で行われる。
塩基としては、上記ヒドラジノ基上のアミノ保護基脱保護工程おいて上述した塩基を好適に用いることができる。
溶媒としては、上記溶解工程において上述した溶剤を好適に用いることができる。
塩基としては、上記ヒドラジノ基上のアミノ保護基脱保護工程おいて上述した塩基を好適に用いることができる。
溶媒としては、上記溶解工程において上述した溶剤を好適に用いることができる。
<ペプチド鎖延長工程>
本開示に係るペプチド化合物の製造方法は、上記N末端脱保護工程で得られたC末端保護アミノ酸化合物又はC末端保護ペプチド化合物のN末端に、N末端保護アミノ酸化合物、又は、N末端保護ペプチド化合物を縮合させるペプチド鎖延長工程を含むことが好ましい。
上記ペプチド鎖延長工程は、上述した縮合剤、縮合添加剤等を使用し、ペプチド化学の分野において一般的に用いられるペプチド合成条件下で好適に行われる。
N末端保護アミノ酸化合物、又は、N末端保護ペプチド化合物としては、特に制限はなく、所望のものを用いることができるが、Fmoc保護アミノ酸化合物、又は、Fmoc保護ペプチド化合物を好適に用いることができる。
また、N末端保護アミノ酸化合物、又は、N末端保護ペプチド化合物におけるC末端部分以外のヒドロキシ基、アミノ基、カルボニル基、アミド基、イミダゾール基、インドール基、グアニジル基、メルカプト基等は後述する保護基等の公知の保護基により保護されていることが好ましい。
本開示に係るペプチド化合物の製造方法は、上記N末端脱保護工程で得られたC末端保護アミノ酸化合物又はC末端保護ペプチド化合物のN末端に、N末端保護アミノ酸化合物、又は、N末端保護ペプチド化合物を縮合させるペプチド鎖延長工程を含むことが好ましい。
上記ペプチド鎖延長工程は、上述した縮合剤、縮合添加剤等を使用し、ペプチド化学の分野において一般的に用いられるペプチド合成条件下で好適に行われる。
N末端保護アミノ酸化合物、又は、N末端保護ペプチド化合物としては、特に制限はなく、所望のものを用いることができるが、Fmoc保護アミノ酸化合物、又は、Fmoc保護ペプチド化合物を好適に用いることができる。
また、N末端保護アミノ酸化合物、又は、N末端保護ペプチド化合物におけるC末端部分以外のヒドロキシ基、アミノ基、カルボニル基、アミド基、イミダゾール基、インドール基、グアニジル基、メルカプト基等は後述する保護基等の公知の保護基により保護されていることが好ましい。
<沈殿工程>
本開示に係るペプチド化合物の製造方法は、上記ペプチド鎖延長工程で得られたN末端保護C末端保護ペプチド化合物を沈殿させる沈殿工程を更に含むことが好ましい。
上記沈殿工程は、上述した上記C末端保護工程の後に行ってもよい精製における沈殿方法と同様にして行うことができる。
本開示に係るペプチド化合物の製造方法は、上記ペプチド鎖延長工程で得られたN末端保護C末端保護ペプチド化合物を沈殿させる沈殿工程を更に含むことが好ましい。
上記沈殿工程は、上述した上記C末端保護工程の後に行ってもよい精製における沈殿方法と同様にして行うことができる。
<抽出工程>
本開示に係るペプチド化合物の製造方法は、上記ペプチド鎖延長工程で得られたN末端保護C末端保護ペプチド化合物に水を添加し、不純物を水相に抽出分離する抽出工程を更に含むことが好ましい。
上記抽出工程は、例えば、上記ペプチド鎖延長工程で得られたN末端保護C末端保護ペプチド化合物又はこれに有機溶媒を添加したものに、水を添加し、分液操作を行い、不純物を水相に抽出し、水相と油相又はN末端保護C末端保護ペプチド化合物とを分離し、油相から必要に応じて、有機溶媒を除去し、精製されたN末端保護C末端保護ペプチド化合物を得ることができる。
有機溶媒としては、上記溶解工程において上述した有機溶媒を用いることができる。
上記抽出工程における抽出条件及び抽出操作としては、特に制限はなく、公知の抽出条件及び抽出操作を用いて行うことができる。
本開示に係るペプチド化合物の製造方法は、上記ペプチド鎖延長工程で得られたN末端保護C末端保護ペプチド化合物に水を添加し、不純物を水相に抽出分離する抽出工程を更に含むことが好ましい。
上記抽出工程は、例えば、上記ペプチド鎖延長工程で得られたN末端保護C末端保護ペプチド化合物又はこれに有機溶媒を添加したものに、水を添加し、分液操作を行い、不純物を水相に抽出し、水相と油相又はN末端保護C末端保護ペプチド化合物とを分離し、油相から必要に応じて、有機溶媒を除去し、精製されたN末端保護C末端保護ペプチド化合物を得ることができる。
有機溶媒としては、上記溶解工程において上述した有機溶媒を用いることができる。
上記抽出工程における抽出条件及び抽出操作としては、特に制限はなく、公知の抽出条件及び抽出操作を用いて行うことができる。
<鎖延長>
本開示に係るペプチド化合物の製造方法は、上記沈殿工程の後に、得られたN末端保護C末端保護ペプチド化合物のN末端を脱保護する工程、得られたC末端保護ペプチド化合物のN末端に、N末端保護アミノ酸化合物、又は、N末端保護ペプチド化合物を縮合させる工程、及び、得られたN末端保護C末端保護ペプチド化合物を沈殿する工程をこの順で1回以上更に含むことが好ましい。
上記3工程を繰り返し行うことにより、得られるペプチド化合物の鎖延長を容易に行うことができる。
上記3工程における各工程は、上述した対応する各工程と同様に行うことができる。
本開示に係るペプチド化合物の製造方法は、上記沈殿工程の後に、得られたN末端保護C末端保護ペプチド化合物のN末端を脱保護する工程、得られたC末端保護ペプチド化合物のN末端に、N末端保護アミノ酸化合物、又は、N末端保護ペプチド化合物を縮合させる工程、及び、得られたN末端保護C末端保護ペプチド化合物を沈殿する工程をこの順で1回以上更に含むことが好ましい。
上記3工程を繰り返し行うことにより、得られるペプチド化合物の鎖延長を容易に行うことができる。
上記3工程における各工程は、上述した対応する各工程と同様に行うことができる。
<C末端脱保護工程>
本開示に係るペプチド化合物の製造方法は、C末端保護基を脱保護するC末端脱保護工程を更に含むことが好ましい。
上記C末端脱保護工程において、所望のアミノ酸残基数を有するC末端保護ペプチド化合物における上記式(1)で表されるヒドラジン誘導体により形成されたC末端保護基を除去することによって、最終目的物であるペプチド化合物を得ることができる。
C末端保護基の除去方法としては、酸化剤を用いた脱保護方法が好ましく挙げられる。
酸化剤としては、無機酸化剤、有機酸化剤のいずれを用いることができ、公知の酸化剤を用いることができる。
無機酸化剤としては、金属塩酸化剤が好ましく、銅塩酸化剤がより好ましく、二価の銅塩が特に好ましい。
二価の銅塩としては、例えば、臭化銅、塩化銅、フッ化銅、水酸化銅、燐酸銅、酢酸銅、ジメチルジチオカルバミン酸銅、銅メトキサイド、銅エトキシド、銅イソプロポキサイド、エチルアセト酢酸銅、2-エチルヘキサン酸銅、グルコン酸銅、ヘキサフルオロアセチルアセトナート銅、イソ酪酸銅、フタル酸銅、トリフオロアセチルアセトナート銅、トリフルオロメタンスルホン酸銅等を挙げることができる。
有機酸化剤としては、キノン類、超原子価ヨウ素、有機過酸化物、又は、窒素-ハロゲン結合を有する化合物が好ましい。
N-ハロゲン化含窒素化合物としては、N-クロロスクシンイミド、N-ブロモスクシンイミド、N-ヨードスクシンイミド、N-クロロフタルイミド、N-ブロモフタルイミド、N-ヨードフタルイミド、N-クロロアセトイミド、N-ブロモアセトイミド、N-ヨードアセトイミド等のイミド化合物、1,3-ジクロロ-2,5-ジメチルヒダントイン、1,3-ジブロモ-2,5-ジメチルヒダントイン、1,3-ジヨード-2,5-ジメチルヒダントイン等のヒダントイン化合物、1,3,5-トリクロロイソシアヌル酸、1,3,5-トリブロモイソシアヌル酸、1,3,5-トリヨードイソシアヌル酸等のイソシアヌル酸化合物等を挙げることができる。
中でも、酸化剤としては、二価の銅塩、キノン類、又は、N-ハロゲン化含窒素化合物が好ましく、二価のハロゲン化銅、二価のカルボン酸銅塩、ベンゾキノン、N-ハロゲン化イミド化合物がより好ましく、二価の酢酸銅、1,4-ベンゾキノン又は、N-ブロモスクシンイミドが特に好ましい。
本開示に係るペプチド化合物の製造方法は、C末端保護基を脱保護するC末端脱保護工程を更に含むことが好ましい。
上記C末端脱保護工程において、所望のアミノ酸残基数を有するC末端保護ペプチド化合物における上記式(1)で表されるヒドラジン誘導体により形成されたC末端保護基を除去することによって、最終目的物であるペプチド化合物を得ることができる。
C末端保護基の除去方法としては、酸化剤を用いた脱保護方法が好ましく挙げられる。
酸化剤としては、無機酸化剤、有機酸化剤のいずれを用いることができ、公知の酸化剤を用いることができる。
無機酸化剤としては、金属塩酸化剤が好ましく、銅塩酸化剤がより好ましく、二価の銅塩が特に好ましい。
二価の銅塩としては、例えば、臭化銅、塩化銅、フッ化銅、水酸化銅、燐酸銅、酢酸銅、ジメチルジチオカルバミン酸銅、銅メトキサイド、銅エトキシド、銅イソプロポキサイド、エチルアセト酢酸銅、2-エチルヘキサン酸銅、グルコン酸銅、ヘキサフルオロアセチルアセトナート銅、イソ酪酸銅、フタル酸銅、トリフオロアセチルアセトナート銅、トリフルオロメタンスルホン酸銅等を挙げることができる。
有機酸化剤としては、キノン類、超原子価ヨウ素、有機過酸化物、又は、窒素-ハロゲン結合を有する化合物が好ましい。
N-ハロゲン化含窒素化合物としては、N-クロロスクシンイミド、N-ブロモスクシンイミド、N-ヨードスクシンイミド、N-クロロフタルイミド、N-ブロモフタルイミド、N-ヨードフタルイミド、N-クロロアセトイミド、N-ブロモアセトイミド、N-ヨードアセトイミド等のイミド化合物、1,3-ジクロロ-2,5-ジメチルヒダントイン、1,3-ジブロモ-2,5-ジメチルヒダントイン、1,3-ジヨード-2,5-ジメチルヒダントイン等のヒダントイン化合物、1,3,5-トリクロロイソシアヌル酸、1,3,5-トリブロモイソシアヌル酸、1,3,5-トリヨードイソシアヌル酸等のイソシアヌル酸化合物等を挙げることができる。
中でも、酸化剤としては、二価の銅塩、キノン類、又は、N-ハロゲン化含窒素化合物が好ましく、二価のハロゲン化銅、二価のカルボン酸銅塩、ベンゾキノン、N-ハロゲン化イミド化合物がより好ましく、二価の酢酸銅、1,4-ベンゾキノン又は、N-ブロモスクシンイミドが特に好ましい。
溶媒としては、上記溶解工程において上述した溶剤、並びに、水、アルコール化合物及びアセトニトリル等の極性溶媒、並びに、それらの混合溶媒を好適に用いることができる。
反応温度は、特に制限はないが、-10℃~80℃であることが好ましく、0℃~40℃であることがより好ましい。反応時間は、特に制限はないが、0.1時間~30時間であることが好ましい。
反応温度は、特に制限はないが、-10℃~80℃であることが好ましく、0℃~40℃であることがより好ましい。反応時間は、特に制限はないが、0.1時間~30時間であることが好ましい。
本開示に係るペプチド化合物の製造方法により得られた最終目的物であるペプチド化合物は、ペプチド化学で常用される方法に従って、単離精製することができる。例えば、反応混合物を抽出洗浄、晶析、クロマトグラフィーなどによって、最終目的物であるペプチド化合物を単離精製することができる。
本開示に係るペプチド化合物の製造方法により製造されるペプチドの種類は特に限定されないが、ペプチド化合物のアミノ酸残基数が、例えば、数十以下程度であることが好ましい。本開示に係るペプチド化合物の製造方法によって得られるペプチドは、既存の又は未知の合成ペプチドや天然ペプチドと同様に、様々な分野、例えばこれに限定されないが、医薬、食品、化粧品、電子材料、バイオセンサー等の分野に利用できる。
本開示に係るペプチド化合物の製造方法は、次工程の反応に影響を及ぼさない範囲で上記沈殿工程を適宜省略することも可能である。
本開示に係るペプチド化合物の製造方法に用いられるアミノ酸化合物、及び、ペプチド化合物がヒドロキシ基、アミノ基、カルボキシ基、カルボニル基、グアジニル基、メルカプト基等を有する場合、これらの基にペプチド化学等で一般的に用いられるような保護基が導入されていてもよく、反応後に必要に応じて保護基を除去することにより目的化合物を得ることができる。
これら保護基としては、上述したものが挙げられる。
これら保護基としては、上述したものが挙げられる。
また、これらの保護基の除去方法は、自体公知の方法、例えば、Greene‘s Protective Groups in Organic Synthesis(2014)に記載の方法等に準じて行えばよい。例えば、酸、塩基、紫外光、ヒドラジン、フェニルヒドラジン、N-メチルジチオカルバミン酸ナトリウム、テトラブチルアンモニウムフルオリド、酢酸パラジウム、トリアルキルシリルハライド(例えば、トリメチルシリルヨージド、トリメチルシリルブロミド等)等を使用する方法、還元法等が用いられる。
(保護基形成用試薬)
本開示に係る保護基形成用試薬は、下記式(1a)で表されるヒドラジン誘導体を含む。
本開示に係る保護基形成用試薬は、下記式(1a)で表されるヒドラジン誘導体を含む。
式(1a)中、
環Aは、芳香族炭化水素環又は芳香族ヘテロ環を表し、
Rは、水素原子、又は、アミノ保護基を表し、
kは、1~5の整数を表し、
nは、1又は2を表し、
RAはそれぞれ独立に、脂肪族炭化水素基、又は、脂肪族炭化水素基を有する有機基を表し、
k個のRAにおける少なくとも1つの脂肪族炭化水素基の炭素数が13以上である。
環Aは、芳香族炭化水素環又は芳香族ヘテロ環を表し、
Rは、水素原子、又は、アミノ保護基を表し、
kは、1~5の整数を表し、
nは、1又は2を表し、
RAはそれぞれ独立に、脂肪族炭化水素基、又は、脂肪族炭化水素基を有する有機基を表し、
k個のRAにおける少なくとも1つの脂肪族炭化水素基の炭素数が13以上である。
本開示に係る保護基形成用試薬は、カルボキシ基の保護基形成用試薬であることが好ましく、アミノ酸化合物又はペプチド化合物のC末端保護基形成用試薬であることがより好ましい。
本開示に係る保護基形成用試薬における式(1a)で表されるヒドラジン誘導体の好ましい態様は、Rが水素原子、又は、アミノ保護基であること以外、本開示に係るペプチド化合物の製造方法において上述した式(1)で表されるヒドラジン誘導体の好ましい態様と同様である。
また、本開示に係る保護基形成用試薬における式(1a)で表されるヒドラジン誘導体のRの好ましい態様は、本開示に係るペプチド化合物の製造方法において上述した式(1)で表されるヒドラジン誘導体のRの好ましい態様からアミノ酸残基及びペプチド残基を除いた態様と同様である。
本開示に係る保護基形成用試薬は、固体状の試薬であっても、液体状の試薬であってもよい。
本開示に係る保護基形成用試薬における式(1a)で表されるヒドラジン誘導体の含有量は、特に制限はないが、保護基形成用試薬の全質量に対し、0.1質量%~100質量%であることが好ましく、1質量%~100質量%であることがより好ましく、3質量%~100質量%であることが更に好ましい。
また、本開示に係る保護基形成用試薬における式(1a)で表されるヒドラジン誘導体のRの好ましい態様は、本開示に係るペプチド化合物の製造方法において上述した式(1)で表されるヒドラジン誘導体のRの好ましい態様からアミノ酸残基及びペプチド残基を除いた態様と同様である。
本開示に係る保護基形成用試薬は、固体状の試薬であっても、液体状の試薬であってもよい。
本開示に係る保護基形成用試薬における式(1a)で表されるヒドラジン誘導体の含有量は、特に制限はないが、保護基形成用試薬の全質量に対し、0.1質量%~100質量%であることが好ましく、1質量%~100質量%であることがより好ましく、3質量%~100質量%であることが更に好ましい。
本開示に係る保護基形成用試薬は、式(1a)で表されるヒドラジン誘導体以外の他の成分を含んでいてもよい。
他の成分としては、公知の成分を含むことができる。例えば、水、有機溶媒、酸化防止剤、pH調整剤等が挙げられる。
他の成分としては、公知の成分を含むことができる。例えば、水、有機溶媒、酸化防止剤、pH調整剤等が挙げられる。
(式(1b)で表されるヒドラジン誘導体)
本開示に係る化合物は、下記式(1b)で表されるヒドラジン誘導体である。
本開示に係る化合物は、下記式(1b)で表されるヒドラジン誘導体である。
式(1b)中、
環Aは、芳香族炭化水素環又は芳香族ヘテロ環を表し、
Rは、水素原子、又は、アミノ保護基を表し、
kは、1~5の整数を表し、
nは、1又は2を表し、
RAはそれぞれ独立に、脂肪族炭化水素基、又は、脂肪族炭化水素基を有する有機基を表し、
k個のRAにおける少なくとも2つの脂肪族炭化水素基の炭素数が13以上である。
環Aは、芳香族炭化水素環又は芳香族ヘテロ環を表し、
Rは、水素原子、又は、アミノ保護基を表し、
kは、1~5の整数を表し、
nは、1又は2を表し、
RAはそれぞれ独立に、脂肪族炭化水素基、又は、脂肪族炭化水素基を有する有機基を表し、
k個のRAにおける少なくとも2つの脂肪族炭化水素基の炭素数が13以上である。
本開示に係る化合物である式(1b)で表されるヒドラジン誘導体は、新規な化合物であり、ペプチド化合物の製造に好適に用いることができる。中でも、保護基形成用試薬として好適に用いることができ、カルボキシ基の保護基形成用試薬としてより好適に用いることができ、アミノ酸化合物又はペプチド化合物のC末端保護基形成用試薬として特に好適に用いることができる。
本開示に係る化合物における式(1b)で表されるヒドラジン誘導体は、Rが水素原子、又は、アミノ保護基であり、かつ、k個のRAにおける少なくとも2つの脂肪族炭化水素基の炭素数が13以上であること以外、本開示に係るペプチド化合物の製造方法において上述した式(1)で表されるヒドラジン誘導体と同様であり、好ましい態様も同様である。
また、本開示に係る化合物におけるRの好ましい態様は、上述した本開示に係る式(1)で表されるヒドラジン誘導体のRの好ましい態様からアミノ酸残基及びペプチド残基を除いた態様と同様である。
また、本開示に係る化合物におけるRの好ましい態様は、上述した本開示に係る式(1)で表されるヒドラジン誘導体のRの好ましい態様からアミノ酸残基及びペプチド残基を除いた態様と同様である。
また、上記式(1b)で表されるヒドラジン誘導体は、上記式(1)で表されるヒドラジン誘導体と同様にして、合成することができる。
以下に実施例を挙げて本発明の実施形態を更に具体的に説明する。以下の実施例に示す材料、使用量、割合、処理内容、及び、処理手順等は、本発明の実施形態の趣旨を逸脱しない限り、適宜、変更することができる。したがって、本発明の実施形態の範囲は以下に示す具体例に限定されない。なお、特に断りのない限り、「部」、「%」は質量基準である。
特に記載のない場合、シリカゲルカラムクロマトグラフィーによる精製は、自動精製装置ISOLERA(Biotage社製)又は中圧液体クロマトグラフYFLC-Wprep2XY.N(山善(株)製)を使用した。
特に記載のない場合、高速液体クロマトグラフィー(HPLC)による精製はAgilent社製1260InfinityバイナリLCシステム、カラム:Agilent社製PREP-C18(50mm×21.2mm)、グラジエント条件:H2O(0.1%HCO2H)/アセトニトリル(0.1%HCO2H)=90/10→30/70、流速:20.0ml/min)により精製した。
特に記載のない場合、シリカゲルカラムクロマトグラフィーにおける担体は、SNAPKP-Sil Cartridge(Biotage社製)、ハイフラッシュカラムW001、W002、W003、W004又はW005(山善(株)製)を使用した。
MSスペクトルは、ACQUITY SQD LC/MS System(Waters社製)又はLC-MS2020((株)島津製作所製)、イオン化法:ESI(ElectroSpray Ionization、エレクトロスプレーイオン化)法を用いて測定した。
NMRスペクトルは、内部基準としてテトラメチルシランを用い、Bruker AV300(Bruker社製、300MHz)、又は、Bruker AV400(Bruker社製、400MHz)を用いて測定し、全δ値をppmで示した。
特に記載のない場合、高速液体クロマトグラフィー(HPLC)による精製はAgilent社製1260InfinityバイナリLCシステム、カラム:Agilent社製PREP-C18(50mm×21.2mm)、グラジエント条件:H2O(0.1%HCO2H)/アセトニトリル(0.1%HCO2H)=90/10→30/70、流速:20.0ml/min)により精製した。
特に記載のない場合、シリカゲルカラムクロマトグラフィーにおける担体は、SNAPKP-Sil Cartridge(Biotage社製)、ハイフラッシュカラムW001、W002、W003、W004又はW005(山善(株)製)を使用した。
MSスペクトルは、ACQUITY SQD LC/MS System(Waters社製)又はLC-MS2020((株)島津製作所製)、イオン化法:ESI(ElectroSpray Ionization、エレクトロスプレーイオン化)法を用いて測定した。
NMRスペクトルは、内部基準としてテトラメチルシランを用い、Bruker AV300(Bruker社製、300MHz)、又は、Bruker AV400(Bruker社製、400MHz)を用いて測定し、全δ値をppmで示した。
<3,5-ビス(ドコシルオキシ)ベンジル=(((9H-フルオレン-9-イル)メトキシ)カルボニル)グリシナートの合成>
(3,5-ビス(ドコシルオキシ)フェニル)メタノール(600mg、0.792mmol)のテトラヒドロフラン(THF)溶液(15.9mL)に、N-[(9H-フルオレン-9-イルメトキシ)カルボニル]グリシン(Fmoc-Gly-OH、353mg、1.188mmol)、N,N’-ジイソプロピルカルボジイミド(DIC、186μL、1.188mmol)及びN,N―ジメチル-4-アミノピリジン(DMAP、19.4mg、0.159mmol)を加え、室温(25℃、以下同様)で1時間攪拌した。アセトニトリルを添加することで析出させた固体をろ取、減圧乾燥させることで、3,5-ビス(ドコシルオキシ)ベンジル=(((9H-フルオレン-9-イル)メトキシ)カルボニル)グリシナート(741mg、0.715mmol)を得た。
1H-NMR(CDCl3)δ:7.76(2H,d,J=7.9Hz),7.60(2H,d,J=7.9Hz),7.46-7.30(4H,m),6.47(2H,d,J=2.0Hz),6.40(1H,s),5.11(2H,s),4.41(2H,d,J=6.6Hz),4.29-4.18(1H,m),4.06(2H,d,J=5.3Hz),3.96-3.85(4H,m),1.83-1.19(80H,m),0.88(6H,t,J=6.6Hz).
1H-NMR(CDCl3)δ:7.76(2H,d,J=7.9Hz),7.60(2H,d,J=7.9Hz),7.46-7.30(4H,m),6.47(2H,d,J=2.0Hz),6.40(1H,s),5.11(2H,s),4.41(2H,d,J=6.6Hz),4.29-4.18(1H,m),4.06(2H,d,J=5.3Hz),3.96-3.85(4H,m),1.83-1.19(80H,m),0.88(6H,t,J=6.6Hz).
<tert-ブチル=2-(4-((2-(3,5-ビス(ドコシルオキシ)ベンジルオキシ)-2-オキソエチル)カルバモイル)フェニル)ヒドラジン-1-カルボキシレートの合成>
3,5-ビス(ドコシルオキシ)ベンジル=(((9H-フルオレン-9-イル)メトキシ)カルボニル)グリシナート(741mg、0.715mmol)のテトラヒドロフラン溶液(14.3mL)にジアザビシクロウンデセン(DBU、215μL、1.43mmol)を加え、室温で1時間撹拌した。N-メチルモルホリン(NMM、158μL、1.43mmol)、メタンスルホン酸(MsOH、96.1μL、1.47mmol)を加え、室温で10分撹拌した。4-(2-(tert-ブトキシカルボニル)ヒドラジニル)安息香酸(225mg、0.894mmol)及び7-アザベンゾトリアゾール-1-イルオキシ)トリピロリジノホスホニウムヘキサフルオロホスフェート(PyAOP、466mg、0.894mmol)を加え、室温で2時間30分撹拌した。アセトニトリルを添加することで析出させた固体をろ取、減圧乾燥させることで、tert-ブチル=2-(4-((2-(3,5-ビス(ドコシルオキシ)ベンジルオキシ)-2-オキソエチル)カルバモイル)フェニル)ヒドラジン-1-カルボキシレート(356mg、0.340mmol)を得た。
1H-NMR(CDCl3)δ:7.71(2H,d,J=8.6Hz),6.82(2H,d,J=8.6Hz),6.63-6.33(5H,m),6.04-5.94(1H,m),5.13(2H,s),4.27(2H,t,J=4.6Hz),3.92(4H,t,J=6.6Hz),1.86-1.19(89H,m),0.88(6H,t,J=6.6Hz).
1H-NMR(CDCl3)δ:7.71(2H,d,J=8.6Hz),6.82(2H,d,J=8.6Hz),6.63-6.33(5H,m),6.04-5.94(1H,m),5.13(2H,s),4.27(2H,t,J=4.6Hz),3.92(4H,t,J=6.6Hz),1.86-1.19(89H,m),0.88(6H,t,J=6.6Hz).
(実施例1)
<(9H-フルオレン-9-イル)メチル=(S)-2-(2-(4-((2-((3,5-ビス(ドコシルオキシ)ベンジル)オキシ)-2-オキソエチル)カルバモイル)フェニル)フェニル)ヒドラジン)-1-カルボニル)ピロリジン-1-カルボキシレートの合成>
<(9H-フルオレン-9-イル)メチル=(S)-2-(2-(4-((2-((3,5-ビス(ドコシルオキシ)ベンジル)オキシ)-2-オキソエチル)カルバモイル)フェニル)フェニル)ヒドラジン)-1-カルボニル)ピロリジン-1-カルボキシレートの合成>
tert-ブチル=2-(4-((2-(3,5-ビス(ドコシルオキシ)ベンジルオキシ)-2-オキソエチル)カルバモイル)フェニル)ヒドラジン-1-カルボキシレート(356mg、0.340mmol)のジクロロメタン溶液(DCM、6.6mL)に、トリフルオロ酢酸(TFA、6.6mL)を加え、室温で1時間30分撹拌した。減圧下溶媒を留去し、得られた白色固体にテトラヒドロフラン(6.8mL)を添加した。混合物にN-[(9H-フルオレン-9-イルメトキシ)カルボニル]-L-プロリン(Fmoc-Pro-OH、172mg、0.509mmol)、7-アザベンゾトリアゾール-1-イルオキシ)トリピロリジノホスホニウムヘキサフルオロホスフェート(266mg、0.509mmol)、N-メチルモルホリン(337μL、3.06mmol)を加え、室温で30分撹拌した。アセトニトリルを添加することで析出させた固体をろ取することで、(9H-フルオレン-9-イル)メチル=(S)-2-(2-(4-((2-((3,5-ビス(ドコシルオキシ)ベンジル)オキシ)-2-オキソエチル)カルバモイル)フェニルヒドラジン)-1-カルボニル)ピロリジン-1-カルボキシレート(282mg、0.222mmol)を得た。
ESI-MS(-)=1,266.00
なお、縮合時に原料の残存は観測されなかった。
ESI-MS(-)=1,266.00
なお、縮合時に原料の残存は観測されなかった。
<3,5-ビス(ドコシルオキシ)ベンジル=(4-(2-((((9H-フルオレン-9-イル)メトキシ)カルボニル)グリシル-L-プロリル)ヒドラジニル)ベンゾイル)グリシネートの合成>
(9H-フルオレン-9-イル)メチル=(S)-2-(2-(4-((2-((3,5-ビス(ドコシルオキシ)ベンジル)オキシ)-2-オキソエチル)カルバモイル)フェニルヒドラジン)-1-カルボニル)ピロリジン-1-カルボキシレート(280mg、0.221mmol)のテトラヒドロフラン溶液(7.4mL)にジアザビシクロウンデセン(101μL、0.674mmol)を加え、室温で30分撹拌した。N-メチルモルホリン(48.7μL、0.442mmol)、メタンスルホン酸(44.2μL、0.674mmol)を加え、室温で10分撹拌した。混合物にN-[(9H-フルオレン-9-イルメトキシ)カルボニル]-グリシン(125mg、0.420mmol)、シアノ-2-エトキシ-2-オキソエチリデンアミンオキシ)ジメチルアミノ-モリホリノ-カルベニウムヘキサフルオロホスフェート(180mg、0.42mmol)を加え、室温で30分撹拌した。アセトニトリルを添加することで析出させた固体をろ取することで、3,5-ビス(ドコシルオキシ)ベンジル=(4-(2-((((9H-フルオレン-9-イル)メトキシ)カルボニル)グリシル-L-プロリル)ヒドラジニル)ベンゾイル)グリシネート(293mg、0.220mmol)を得た。
ESI-MS(-)=1,322.85
ESI-MS(-)=1,322.85
<3,5-ビス(ドコシルオキシ)ベンジル(4-(2-((tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリル)ヒドラジニル)ベンゾイル)グリシネートの合成>
3,5-ビス(ドコシルオキシ)ベンジル=(4-(2-((((9H-フルオレン-9-イル)メトキシ)カルボニル)グリシル-L-プロリル)ヒドラジニル)ベンゾイル)グリシネート(290mg、0.219mmol)のテトラヒドロフラン溶液(5.0mL)にジアザビシクロウンデセン(65.8μL、0.438mmol)を加え、室温で40分撹拌した。N-メチルモルホリン(48.3μL、0.438mmol)、メタンスルホン酸(29.4μL、0.449mmol)を加え、室温で10分撹拌した。混合物にN-(tert-ブトキシカルボニル)-L-フェニルアラニン(Boc-Phe-OH、72.6mg、0.274mmol)、シアノ-2-エトキシ-2-オキソエチリデンアミンオキシ)ジメチルアミノ-モリホリノ-カルベニウムヘキサフルオロホスフェート(COMU、117mg、0.274mmol)を加え、室温で50分撹拌した。アセトニトリルを添加することで析出させた固体をろ取することで、3,5-ビス(ドコシルオキシ)ベンジル=(4-(2-((tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリル)ヒドラジニル)ベンゾイル)グリシネート(216mg、0.160mmol)を得た。
なお、DBU処理時におけるジケトピペラジン化合物の生成は確認されなかった。
ESI-MS(-)=1,347.85
なお、DBU処理時におけるジケトピペラジン化合物の生成は確認されなかった。
ESI-MS(-)=1,347.85
<tert-ブチル=((S)-1-((2-((S)-2-(ベンジルカルバモイル)ピロリジン-1-イル)-2-オキソエチル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)カルバメートの合成(脱保護反応)>
3,5-ビス(ドコシルオキシ)ベンジル=(4-(2-((tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリル)ヒドラジニル)ベンゾイル)グリシネート(25.0mg、0.0185mmol)のテトラヒドロフラン溶液(740μL)に、ベンジルアミン(benzylamine、3.30μL)、ピリジン(pyridine、15μL、0.185mmol)、酢酸銅一水和物(Cu(OAc)2、0.37mg、0.00185mmol)を加え、室温で2時間撹拌した。メタノールを添加することで析出させた固体を遠心分離でさせ除去し、目的のペプチド化合物を含んだ上澄みを得た。減圧下溶媒を留去し、シリカパッドによる前処理、HPLCによる精製を行うことで、(tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリン(3.57mg、0.00683mmol)を得た。
ESI-MS(+)=509.3
ESI-MS(+)=509.3
(実施例2)
<(tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリンの合成>
<(tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリンの合成>
3,5-ビス(ドコシルオキシ)ベンジル=(4-(2-((tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリル)ヒドラジニル)ベンゾイル)グリシネート(25.0mg、0.0185mmol)のテトラヒドロフラン溶液(740μL)に、水(74μL)、ピリジン(15μL、0.185mmol)、酢酸銅一水和物(0.37mg、0.00185mmol)を加え、室温で2時間撹拌した。メタノールを添加することで析出させた固体を遠心分離でさせ除去し、目的のペプチド化合物を含んだ上澄みを得た。減圧下溶媒を留去し、シリカパッドによる前処理、HPLCによる精製を行うことで、(tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリン(3.44mg、0.00820mmol)を得た。
ESI-MS(+)=420.3
ESI-MS(+)=420.3
(実施例3)
<tert-ブチル=((S)-1-((2-((S)-2-(((S)-1-(((S)-1-((S)-1-((S)2-カルバモイルピロリジン-1-イル)-1-オキソプロパン-2-イル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)アミノ)-4-メチル-1-オキソペンタン-2-イル)カルバモイル)ピロリジン-1-イル)-2-オキソエチル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)カルバメートの合成>
<tert-ブチル=((S)-1-((2-((S)-2-(((S)-1-(((S)-1-((S)-1-((S)2-カルバモイルピロリジン-1-イル)-1-オキソプロパン-2-イル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)アミノ)-4-メチル-1-オキソペンタン-2-イル)カルバモイル)ピロリジン-1-イル)-2-オキソエチル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)カルバメートの合成>
3,5-ビス(ドコシルオキシ)ベンジル=(4-(2-((tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリル)ヒドラジニル)ベンゾイル)グリシネート(25.0mg、0.0185mmol)のテトラヒドロフラン溶液(740μL)に、(S)-1-(L-ロイシル-L-フェニルアラニル-L-アラニル)ピロリジン-2-カルボキサミドのTFA塩(12.0mg、0.0215mmol)、ピリジン(15μL、0.185mmol)、N-メチルモルホリン(10.2μL、0.0244mmol)、酢酸銅一水和物(0.37mg、0.00185mmol)を加え、室温で2時間撹拌した。メタノールを添加することで析出させた固体を遠心分離で沈殿させ除去し、目的のペプチドを含んだ上澄みを得た。減圧下溶媒を留去し、HPLCによる精製を行うことで、tert-ブチル=((S)-1-((2-((S)-2-(((S)-1-(((S)-1-((S)-1-((S)2-カルバモイルピロリジン-1-イル)-1-オキソプロパン-2-イル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)アミノ)-4-メチル-1-オキソペンタン-2-イル)カルバモイル)ピロリジン-1-イル)-2-オキソエチル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)カルバメート(2.19mg、0.00259mmol)を得た。
ESI-MS(―)=845.4
ESI-MS(―)=845.4
(比較例1:ジケトピペラジン化合物の生成)
<1-((9H-フルオレン-9-イル)メチル)=2-(3,5-ビス(ドコシルオキシ)ベンジル)=(S)-ピロリジン-1,2-ジカルボキシラートの合成>
<1-((9H-フルオレン-9-イル)メチル)=2-(3,5-ビス(ドコシルオキシ)ベンジル)=(S)-ピロリジン-1,2-ジカルボキシラートの合成>
(3,5-ビス(ドコシルオキシ)フェニル)メタノール(25.0mg、0.0330mmol)のテトラヒドロフラン溶液(660μL)に、N-[(9H-フルオレン-9-イルメトキシ)カルボニル]-L-プロリン(16.7mg、0.0495mmol)、N,N’-ジイソプロピルカルボジイミド(7.75μL、0.0495mmol)およびN,N-ジメチル-4-アミノピリジン(0.81mg、0.0066mmol)を加え、室温で終夜撹拌した。アセトニトリルを添加することで、析出させた固体を遠心分離で回収し、1-((9H-フルオレン-9-イル)メチル)=2-(3,5-ビス(ドコシルオキシ)ベンジル)=(S)-ピロリジン-1,2-ジカルボキシラート(33.3mg、0.0309mmol)を得た。目的物の含有率は、NMR換算で約95モル%であり、プロリンが導入されず、残存した原料が約5モル%混入していた。
<3,5-ビス(ドコシルオキシ)ベンジル=(((9H-フルオレン-9-イル)メトキシ)カルボニル)グリシル-L-プロリネートの合成>
1-((9H-フルオレン-9-イル)メチル)=2-(3,5-ビス(ドコシルオキシ)ベンジル)=(S)-ピロリジン-1,2-ジカルボキシラート(30.0mg、0.0279mmol)のテトラヒドロフラン溶液(557μL)にジアザビシクロウンデセン(65.8μL、0.438mmol)を加え、室温で30分撹拌した。N-メチルモルホリン(6.15μL、0.0557mmol)、メタンスルホン酸(3.74μL、0.0571mmol)を加え、室温で10分撹拌した。混合物にN-[(9H-フルオレン-9-イルメトキシ)カルボニル]グリシン(10.4mg、0.0348mmol)、シアノ-2-エトキシ-2-オキソエチリデンアミンオキシ)ジメチルアミノ-モリホリノ-カルベニウムヘキサフルオロホスフェート(14.9mg、0.0348mmol)を加え、室温で1時間撹拌した。アセトニトリルを添加することで、析出させた固体を遠心分離で回収し、3,5-ビス(ドコシルオキシ)ベンジル=(((9H-フルオレン-9-イル)メトキシ)カルボニル)グリシル-L-プロリネート(23.0mg、0.0203mmol)を得た。
<3,5-ビス(ドコシルオキシ)ベンジル=グリシル-L-プロリネートの合成((S)-ヘキサヒドロピロロ[1,2-a]ピラジン-1,4-ジオンが得られた。)>
3,5-ビス(ドコシルオキシ)ベンジル=(((9H-フルオレン-9-イル)メトキシ)カルボニル)グリシル-L-プロリネート(23.0mg、0.0203mmol)のテトラヒドロフラン溶液(405μL)にジアザビシクロウンデセン(6.10μL、0.0406mmol)を加え、室温で1時間撹拌した。アセトニトリルを添加することで、析出させた固体を遠心分離で回収したところ、3,5-ビス(ドコシルオキシ)ベンジル=グリシル-L-プロリネートの環化反応(ジケトピペラジン形成)により生成した(3,5-ビス(ドコシルオキシ)フェニル)メタノール(14.2mg、0.0188mmol)が得られ、目的とする3,5-ビス(ドコシルオキシ)ベンジル=グリシル-L-プロリネートは得られなかった。
(比較例2:固相中でのペプチドによる求核置換反応)
<(tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリンのC末端に樹脂が結合したhydrazinobenzoyl AM NovaGelの合成>
<(tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリンのC末端に樹脂が結合したhydrazinobenzoyl AM NovaGelの合成>
ペプチド自動合成装置(SYRO I,biotage社製)を用いてペプチド固相合成(SPPS)を行った。合成装置に4-Fmoc-hydrazinobenzoyl AM NovaGel(246mg、0.61mmol/g、なお、黒球は固相への結合位置を表す。)、Fmocアミノ酸(0.5mol/L)のN-メチルピロリドン(NMP)溶液、シアノ-ヒドロキシイミノ-酢酸エチルエステル(1.0mol/L)のNMP溶液、ジイソプロピルカルボジイミド(1.0mol/L)のNMP溶液、ピペリジン(40%v/v)のNMP溶液をセットし、マニュアルに従い合成を行った。Fmoc脱保護(室温、20分)、NMPによる洗浄、Fmocアミノ酸の縮合(40℃、1時間)、NMPによる洗浄を1サイクルとし、このサイクルを繰り返すことで、ペプチド鎖を伸長させた。伸長終了後、レジンをジクロロメタンで洗浄したのち、減圧下溶媒を留去し、265mgの樹脂を得た。
<tert-ブチル=((S)-1-((2-((S)-2-(((S)-1-(((S)-1-((S)-1-((S)-2-カルバモイルピロリジン-1-イル)-1-オキソプロパン-2-イル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)アミノ)-4-メチル-1-オキソペンタン-2-イル)カルバモイル)ピロリジン-1-イル)-2-オキソエチル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)カルバメートの合成>
(tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリンのC末端に樹脂が結合したhydrazinobenzoyl AM NovaGel(32.7mg、0.0185mmol、based on resin loading)にテトラヒドロフラン(740μL)、(S)-1-(L-ロイシル-L-フェニルアラニル-L-アラニル)ピロリジン-2-カルボキサミドのTFA塩(12.0mg、0.0215mmol)、ピリジン(15μL、0.185mmol)、N-メチルモルホリン(10.2μL、0.0244mmol)、酢酸銅一水和物(0.37mg、0.00185mmol)を加え、室温で2時間撹拌した。レジンを濾別し、樹脂をメタノールで2回洗浄し、ペプチド溶液を回収した。減圧下溶媒を留去し、HPLCによる精製を行うことで、tert-ブチル=((S)-1-((2-((S)-2-(((S)-1-(((S)-1-((S)-1-((S)-2-カルバモイルピロリジン-1-イル)-1-オキソプロパン-2-イル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)アミノ)-4-メチル-1-オキソペンタン-2-イル)カルバモイル)ピロリジン-1-イル)-2-オキソエチル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)カルバメート(0.33mg、0.00039mmol)を得た。
(比較例3:フルオレン型リンカーへのアミノ酸のローディング)
<2-((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレン-9-イル(((9H-フルオレン-9-イル)メトキシ)カルボニル)-L-プロリネートの合成>
<2-((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレン-9-イル(((9H-フルオレン-9-イル)メトキシ)カルボニル)-L-プロリネートの合成>
国際公開第2010/104169号明細書に記載の方法により合成した9-ブロモ-2-((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレンを使用した。
9-ブロモ-2-((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレン(100mg、0.118mmol)のジクロロメタン溶液(590μL)にN-[(9H-フルオレン-9-イルメトキシ)カルボニル]-L-プロリン(59.7mg、0.177mmol)、ジイソプロピルエチルアミン(DIEA、61.7μL、0.354mmol)を室温で加えた後、室温で終夜撹拌した。アセトニトリルを添加することで、析出させた固体を遠心分離で回収しNMRを確認したところ、目的物である2-((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレン-9-イル(((9H-フルオレン-9-イル)メトキシ)カルボニル)-L-プロリネートの生成は見られなかった。
9-ブロモ-2-((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレン(100mg、0.118mmol)のジクロロメタン溶液(590μL)にN-[(9H-フルオレン-9-イルメトキシ)カルボニル]-L-プロリン(59.7mg、0.177mmol)、ジイソプロピルエチルアミン(DIEA、61.7μL、0.354mmol)を室温で加えた後、室温で終夜撹拌した。アセトニトリルを添加することで、析出させた固体を遠心分離で回収しNMRを確認したところ、目的物である2-((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレン-9-イル(((9H-フルオレン-9-イル)メトキシ)カルボニル)-L-プロリネートの生成は見られなかった。
(比較例4:フルオレン型リンカーへのアミノ酸のローディング、加熱条件、試薬増量)
<2-((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレン-9-イル=(((9H-フルオレン-9-イル)メトキシ)カルボニル)-L-プロリネートの合成>
<2-((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレン-9-イル=(((9H-フルオレン-9-イル)メトキシ)カルボニル)-L-プロリネートの合成>
9-ブロモ-2-((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレン(500mg、0.59mmol)のジクロロメタン溶液(6.0mL)にN-[(9H-フルオレン-9-イルメトキシ)カルボニル]-L-プロリン(398mg、1.18mmol)、ジイソプロピルエチルアミン(206μL、1.18mmol)を室温で加えた後、50℃で3時間30分撹拌した。N-[(9H-フルオレン-9-イルメトキシ)カルボニル]-L-プロリン(199mg、0.59mmol)、ジイソプロピルエチルアミン(103μL、0.59mmol)を室温で加えた後50℃で4時間撹拌した。アセトニトリルを添加することで、析出させた固体を遠心分離で回収しNMRを確認したところ、目的物である2-((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレン-9-イル(((9H-フルオレン-9-イル)メトキシ)カルボニル)-L-プロリネートの生成が見られたが、原料及びその分解体と思われる化合物も観測された。そのためシリカゲルカラムクロマトグラフィーによる分離を行い、2-((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレン-9-イル=(((9H-フルオレン-9-イル)メトキシ)カルボニル)-L-プロリネート(73.0mg)を得た。
<2-((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレン-9-イル=(((9H-フルオレン-9-イル)メトキシ)カルボニル)グリシル-L-プロリネートの合成>
2-((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレン-9-イル=(((9H-フルオレン-9-イル)メトキシ)カルボニル)-L-プロリネート(55.7mg、0.0504mmol)のテトラヒドロフラン溶液(504μL)にジアザビシクロウンデセン(15.2μL、0.101mmol)を加え、室温で20分撹拌した。N-メチルモルホリン(11.1μL、0.101mmol)、メタンスルホン酸(6.78μL、0.103mmol)を加え、室温で30分撹拌した。混合物にN-[(9H-フルオレン-9-イルメトキシ)カルボニル]-グリシン(18.7mg、0.0630mmol)、シアノ-2--エトキシ-2--オキソエチリデンアミンオキシ)ジメチルアミノ-モリホリノ-カルベニウムヘキサフルオロホスフェート(27.0mg、0.0630mmol)を加え、室温で30分攪拌した。アセトニトリルを添加することで、析出させた固体を遠心分離で回収することで、2―((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレン-9-イル=(((9H-フルオレン-9-イル)メトキシ)カルボニル)グリシル-L-プロリネート(24.3mg、0.0209mmol)を得た。
2-((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレン-9-イル=(((9H-フルオレン-9-イル)メトキシ)カルボニル)グリシル-L-プロリネート(18.5mg、0.0159mmol)のテトラヒドロフラン溶液(320μL)にジアザビシクロウンデセン(4.8μL、0.0319mmol)を加え、室温で20分攪拌した。アセトニトリルを添加することで、析出させた固体を遠心分離で回収したところ、2-((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレン-9-イル=グリシル-L-プロリネートの環化反応(ジケトピペラジン形成)により生成した2-((12-(ドコシルオキシ)ドデシル)オキシ)-9-(3-フルオロフェニル)-9H-フルオレン-9-オール(8.5mg、0.0108mmol)のみが得られた。
(実施例4)
<tert-ブチル=2-(4-(ジドコシルカルバモイル)フェニル)ヒドラジン-1-カルボキシラートの合成>
<tert-ブチル=2-(4-(ジドコシルカルバモイル)フェニル)ヒドラジン-1-カルボキシラートの合成>
ジオクタデシルアミン(2.61g、5.00mmol)及び4-(2-(tert-ブトキシカルボニル)ヒドラジニル)安息香酸(2.52g、10.0mmol)のクロロホルム溶液(50mL)にヘキサフルオロリン酸(7-アザベンゾトリアゾール-1-イルオキシ)トリピロリジノホスホニウム(PyAOP、5.21g、10.0mmol)及びDIEA(3.49mL、20.0mmol)を室温下加え、1.5時間撹拌した。アセトニトリルを添加することで析出させた固体をろ取することで、tert-ブチル=2-(4-(ジドコシルカルバモイル)フェニル)ヒドラジン-1-カルボキシラート(3.78g、4.914mmol)を得た。
<(9H-フルオレン-9-イル)メチル=(S)-2-(1-(2-(4-(ジドコシルカルバモイル)フェニル)ヒドラジニル)ピロリジン-2-イル)-2-オキソアセテートの合成>
tert-ブチル=2-(4-(ジドコシルカルバモイル)フェニル)ヒドラジン-1-カルボキシラート(1.25g、1.436mmol)に水(623μL)、クロロホルム(12.5mL)及び塩化水素の酢酸エチル溶液(4mol/L、18.7mL)を室温下加え、30分攪拌しBoc基を除去した。減圧下溶媒を留去し、白色固体を得た。テトラヒドロフラン(28.7mL)、Fmoc-Pro-OH(606mg、1.80mmol)、NMM(317μL、2.87mmol)及びCOMU(769mg、1.80mmol)を加え、室温で30分撹拌した。アセトニトリルを添加することで析出させた固体をろ取することで、(9H-フルオレン-9-イル)メチル=(S)-2-(1-(2-(4-(ジドコシルカルバモイル)フェニル)ヒドラジニル)ピロリジン-2-イル)-2-オキソアセテート(1.56g、1.28mmol)を得た。
<(9H-フルオレン-9-イル)メチル=(S)-(2-(2-(2-(2-(4-(ジドコシルカルバモイル)フェニル)ヒドラジン-1-カルボニル)ピロリジン-1-イル)-2-オキソエチル)カルバメートの合成>
(9H-フルオレン-9-イル)メチル=(S)-2-(1-(2-(4-(ジドコシルカルバモイル)フェニル)ヒドラジニル)ピロリジン-2-イル)-2-オキソアセテート(688mg、0.633mmol)のテトラヒドロフラン溶液(12.7mL)にジアザビシクロウンデセン(190μL、1.27mmol)を加え、室温で20分攪拌した。NMM(140μL、1.27mmol)、メタンスルホン酸(85μL、1.30mmol)を加え、室温で10分撹拌した。混合物にFmoc-Gly-OH(235mg、0.791mmol)及びCOMU(339mg、0.791mmol)を加え、30分室温で撹拌した。5%含水アセトニトリルを添加することで析出させた固体をろ取することで、(9H-フルオレン-9-イル)メチル=(S)-(2-(2-(2-(2-(4-(ジドコシルカルバモイル)フェニル)ヒドラジン-1-カルボニル)ピロリジン-1-イル)-2-オキソエチル)カルバメート(668mg、0.584mmol)を得た。
<tert-ブチル=((S)-1-((2-((S)-2-(2-(4-(ジドコシルカルバモイル)フェニル)ヒドラジン-1-カルボニル)ピロリジン-1-イル)-2-オキソエチル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)カルバメートの合成>
(9H-フルオレン-9-イル)メチル=(S)-(2-(2-(2-(2-(4-(ジドコシルカルバモイル)フェニル)ヒドラジン-1-カルボニル)ピロリジン-1-イル)-2-オキソエチル)カルバメート(1.25g、1.09mmol)のテトラヒドロフラン溶液(14.6mL)にDBU(329μL、2.19mmol)を加え、室温で20分攪拌した。NMM(241μL、2.19mmol)、メタンスルホン酸(147μL、2.24mmol)を加え、室温で10分撹拌した。混合物にBoc-Phe-OH(362mg、1.37mmol)及びCOMU(585mg、1.37mmol)を加え、30分室温で撹拌した。アセトニトリルを添加することで析出させた固体をろ取することで、tert-ブチル=((S)-1-((2-((S)-2-(2-(4-(ジドコシルカルバモイル)フェニル)ヒドラジン-1-カルボニル)ピロリジン-1-イル)-2-オキソエチル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)カルバメート(1.20g、1.02mmol)を得た。
<(tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリンの合成>
tert-ブチル=((S)-1-((2-((S)-2-(2-(4-(ジドコシルカルバモイル)フェニル)ヒドラジン-1-カルボニル)ピロリジン-1-イル)-2-オキソエチル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)カルバメート(100mg、0.0854mmol)のテトラヒドロフラン溶液(3.4mL)に、水(340μL)、ピリジン(69.1μL、0.855mmol)、酢酸銅一水和物(Cu(OAc)2、1.62mg、0.00855mmol)を加え、室温で2時間撹拌した。メタノールを添加することで析出させた固体を遠心分離でさせ除去し、目的のペプチド化合物を含んだ上澄みを得た。減圧下溶媒を留去し、HPLCによる精製を行うことで、(tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリン(6.33mg)を得た。
ESI-MS(+)=420.3
ESI-MS(+)=420.3
tert-ブチル=((S)-1-((2-((S)-2-(2-(4-(ジドコシルカルバモイル)フェニル)ヒドラジン-1-カルボニル)ピロリジン-1-イル)-2-オキソエチル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)カルバメート(50mg、0.0427mmol)のテトラヒドロフラン溶液(1.7mL)に、水(170μL)、N-ブロモスクシンイミド(NBS、15.2mg、0.0855mmol)を加え、室温で2時間撹拌した。メタノールを添加することで析出させた固体を遠心分離でさせ除去し、目的のペプチド化合物を含んだ上澄みを得た。減圧下溶媒を留去し、HPLCによる精製を行うことで、(tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリン(0.72mg)を得た。
ESI-MS(+)=420.3
ESI-MS(+)=420.3
tert-ブチル=((S)-1-((2-((S)-2-(2-(4-(ジドコシルカルバモイル)フェニル)ヒドラジン-1-カルボニル)ピロリジン-1-イル)-2-オキソエチル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)カルバメート(50mg、0.0427mmol)のテトラヒドロフラン溶液(1.7mL)に、水(170μL)、フェニルヨードジアセテート(PIDA、27.5mg、0.0855mmol)を加え、室温で2時間撹拌した。メタノールを添加することで析出させた固体を遠心分離でさせ除去し、目的のペプチド化合物を含んだ上澄みを得た。減圧下溶媒を留去し、HPLCによる精製を行うことで、(tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリン(6.57mg)を得た。
ESI-MS(+)=420.3
ESI-MS(+)=420.3
tert-ブチル=((S)-1-((2-((S)-2-(2-(4-(ジドコシルカルバモイル)フェニル)ヒドラジン-1-カルボニル)ピロリジン-1-イル)-2-オキソエチル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)カルバメート(50mg、0.0427mmol)のテトラヒドロフラン溶液(1.7mL)に、水(170μL)、N-ブロヨードスクシンイミド(NIS、19.2mg、0.0855mmol)を加え、室温で2時間撹拌した。メタノールを添加することで析出させた固体を遠心分離でさせ除去し、目的のペプチド化合物を含んだ上澄みを得た。減圧下溶媒を留去し、HPLCによる精製を行うことで、(tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリン(4.82mg)を得た。
ESI-MS(+)=420.3
ESI-MS(+)=420.3
tert-ブチル((S)-1-((2-((S)-2-(2-(4-(ジドコシルカルバモイル)フェニル)ヒドラジン-1-カルボニル)ピロリジン-1-イル)-2-オキソエチル)アミノ)-1-オキソ-3-フェニルプロパン-2-イル)カルバメート(100mg、0.0854mmol)のテトラヒドロフラン溶液(3.4mL)に、水(340μL)、ベンゾキノン(11.1mg、0.103mmol)を加え、室温で2時間撹拌した。亜硫酸ナトリウム(4.9mg)を添加したのち、10%含水アセトニトリルを添加することで析出させた固体を遠心分離でさせ除去し、目的のペプチド化合物を含んだ上澄みを得た。減圧下溶媒を留去し、HPLCによる精製を行うことで、(tert-ブトキシカルボニル)-L-フェニルアラニルグリシル-L-プロリン(3.78mg)を得た。
ESI-MS(+)=420.3
ESI-MS(+)=420.3
上記に示すように、式(1)で表されるヒドラジン誘導体を使用した本実施例におけるペプチド化合物の製造方法は、比較例のペプチド化合物の製造方法に比べ、脱保護時の収率に優れるものであった。
また、上記に示すように、式(1)で表されるヒドラジン誘導体を使用した本実施例におけるペプチド化合物の製造方法は、保護時及びペプチド鎖延長時においても高収率でペプチド化合物を合成することができ、また、ジケトピペラジン化合物の副生を抑制できた。また、C末端アミノ酸の保護も、原料の残留なく収率良く進行することが確認できた。
また、上記に示すように、式(1)で表されるヒドラジン誘導体を使用した本実施例におけるペプチド化合物の製造方法は、保護時及びペプチド鎖延長時においても高収率でペプチド化合物を合成することができ、また、ジケトピペラジン化合物の副生を抑制できた。また、C末端アミノ酸の保護も、原料の残留なく収率良く進行することが確認できた。
2019年9月12日に出願された日本国特許出願第2019-165967号の開示は、その全体が参照により本明細書に取り込まれる。
本明細書に記載された全ての文献、特許出願、及び、技術規格は、個々の文献、特許出願、及び、技術規格が参照により取り込まれることが具体的かつ個々に記された場合と同程度に、本明細書中に参照により取り込まれる。
本明細書に記載された全ての文献、特許出願、及び、技術規格は、個々の文献、特許出願、及び、技術規格が参照により取り込まれることが具体的かつ個々に記された場合と同程度に、本明細書中に参照により取り込まれる。
Claims (16)
- 前記式(1)で表されるヒドラジン誘導体を用いる工程が、前記式(1)で表されるヒドラジン誘導体により、アミノ酸化合物又はペプチド化合物のカルボキシ基を保護するC末端保護工程である請求項1に記載のペプチド化合物の製造方法。
- 前記C末端保護工程におけるアミノ酸化合物又はペプチド化合物が、N末端保護アミノ酸化合物又はN末端保護ペプチド化合物である請求項2に記載のペプチド化合物の製造方法。
- 前記C末端保護工程で得られたN末端保護C末端保護アミノ酸化合物又はN末端保護C末端保護ペプチド化合物のN末端を脱保護するN末端脱保護工程、及び、
前記N末端脱保護工程で得られたC末端保護アミノ酸化合物又はC末端保護ペプチド化合物のN末端に、N末端保護アミノ酸化合物、又は、N末端保護ペプチド化合物を縮合させるペプチド鎖延長工程を更に含む請求項3に記載のペプチド化合物の製造方法。 - 前記ペプチド鎖延長工程で得られたN末端保護C末端保護ペプチド化合物を沈殿させる沈殿工程を更に含む請求項4に記載のペプチド化合物の製造方法。
- 前記ペプチド鎖延長工程で得られたN末端保護C末端保護ペプチド化合物に水を添加し、不純物を水相に抽出分離する抽出工程を更に含む請求項4に記載のペプチド化合物の製造方法。
- 前記沈殿工程又は抽出工程の後に、
得られたN末端保護C末端保護ペプチド化合物のN末端を脱保護する工程、
得られたC末端保護ペプチド化合物のN末端に、N末端保護アミノ酸化合物又はN末端保護ペプチド化合物を縮合させる工程、及び、
得られたN末端保護C末端保護ペプチド化合物を沈殿する工程
をこの順で1回以上更に含む請求項5又は請求項6に記載のペプチド化合物の製造方法。 - C末端保護基を脱保護するC末端脱保護工程を更に含む請求項1~請求項7のいずれか1項に記載のペプチド化合物の製造方法。
- 前記環Aが、ベンゼン環、ナフタレン環、又は、ピリジン環である請求項1~請求項8のいずれか1項に記載のペプチド化合物の製造方法。
- 前記式(1)において、k個のRAにおける少なくとも2つの脂肪族炭化水素基の炭素数が13以上である請求項1~請求項9のいずれか1項に記載のペプチド化合物の製造方法。
- 前記保護基形成用試薬が、カルボキシ基の保護基形成用試薬である請求項11に記載の保護基形成用試薬。
- 前記保護基形成用試薬が、アミノ酸化合物のカルボキシ基又はペプチド化合物のC末端保護基形成用試薬である請求項11又は請求項12に記載の保護基形成用試薬。
- 前記環Aが、ベンゼン環、ナフタレン環、又は、ピリジン環である請求項11~請求項13のいずれか1項に記載の保護基形成用試薬。
- 前記式(1a)において、k個のRAにおける少なくとも2つの脂肪族炭化水素基の炭素数が13以上である請求項11~請求項14のいずれか1項に記載の保護基形成用試薬。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP20863826.2A EP4011902A4 (en) | 2019-09-12 | 2020-09-09 | METHOD FOR PREPARING A PEPTIDE COMPOUND, PROTECTING REAGENT AND HYDRAZINE DERIVATIVE |
| JP2021545579A JP7459121B2 (ja) | 2019-09-12 | 2020-09-09 | ペプチド化合物の製造方法、保護基形成用試薬、及び、ヒドラジン誘導体 |
| US17/654,060 US20220185841A1 (en) | 2019-09-12 | 2022-03-08 | Method for producing peptide compound, reagent for forming protective group, and hydrazine derivative |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019-165967 | 2019-09-12 | ||
| JP2019165967 | 2019-09-12 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US17/654,060 Continuation US20220185841A1 (en) | 2019-09-12 | 2022-03-08 | Method for producing peptide compound, reagent for forming protective group, and hydrazine derivative |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2021049552A1 true WO2021049552A1 (ja) | 2021-03-18 |
Family
ID=74866988
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2020/034194 Ceased WO2021049552A1 (ja) | 2019-09-12 | 2020-09-09 | ペプチド化合物の製造方法、保護基形成用試薬、及び、ヒドラジン誘導体 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20220185841A1 (ja) |
| EP (1) | EP4011902A4 (ja) |
| JP (1) | JP7459121B2 (ja) |
| TW (1) | TW202124408A (ja) |
| WO (1) | WO2021049552A1 (ja) |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005148108A (ja) * | 2003-11-11 | 2005-06-09 | Konica Minolta Medical & Graphic Inc | 熱現像画像記録材料 |
| WO2007034812A1 (ja) | 2005-09-20 | 2007-03-29 | National University Corporation, Tokyo University Of Agriculture And Technology | 分離用担体、化合物の分離方法、及びこれを用いたペプチド合成方法 |
| JP2008127331A (ja) * | 2006-11-21 | 2008-06-05 | Fujifilm Corp | タンパク質を固定化した粒子 |
| WO2010104169A1 (ja) | 2009-03-12 | 2010-09-16 | 味の素株式会社 | フルオレン化合物 |
| WO2010113939A1 (ja) | 2009-03-30 | 2010-10-07 | 味の素株式会社 | ジフェニルメタン化合物 |
| JP2019165967A (ja) | 2018-03-23 | 2019-10-03 | 株式会社サンセイアールアンドディ | 遊技機 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4204870A (en) * | 1978-07-25 | 1980-05-27 | Eastman Kodak Company | Photographic products and processes employing novel nondiffusible heterocyclyazonaphthol dye-releasing compounds |
| CA1196912A (en) * | 1982-05-21 | 1985-11-19 | Eastman Kodak Company | Photographic products and processes employing novel nondiffusible magenta dye-releasing compounds and precursors thereof |
| RU2073011C1 (ru) * | 1993-10-20 | 1997-02-10 | Российско-германское совместное предприятие "Константа" | Линкер для твердофазного синтеза пептидов |
| JP6011528B2 (ja) * | 2011-05-31 | 2016-10-19 | 味の素株式会社 | ペプチドの製造方法 |
| CN113508103A (zh) * | 2019-02-28 | 2021-10-15 | 富士胶片株式会社 | 肽化合物的制造方法、保护基形成用试药及稠合多环芳香族烃化合物 |
| JP7628073B2 (ja) * | 2019-02-28 | 2025-02-07 | 富士フイルム株式会社 | ペプチド化合物の製造方法、保護基形成用試薬、及び、芳香族複素環化合物 |
-
2020
- 2020-09-09 EP EP20863826.2A patent/EP4011902A4/en active Pending
- 2020-09-09 JP JP2021545579A patent/JP7459121B2/ja active Active
- 2020-09-09 WO PCT/JP2020/034194 patent/WO2021049552A1/ja not_active Ceased
- 2020-09-10 TW TW109131061A patent/TW202124408A/zh unknown
-
2022
- 2022-03-08 US US17/654,060 patent/US20220185841A1/en not_active Abandoned
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005148108A (ja) * | 2003-11-11 | 2005-06-09 | Konica Minolta Medical & Graphic Inc | 熱現像画像記録材料 |
| WO2007034812A1 (ja) | 2005-09-20 | 2007-03-29 | National University Corporation, Tokyo University Of Agriculture And Technology | 分離用担体、化合物の分離方法、及びこれを用いたペプチド合成方法 |
| JP2008127331A (ja) * | 2006-11-21 | 2008-06-05 | Fujifilm Corp | タンパク質を固定化した粒子 |
| WO2010104169A1 (ja) | 2009-03-12 | 2010-09-16 | 味の素株式会社 | フルオレン化合物 |
| WO2010113939A1 (ja) | 2009-03-30 | 2010-10-07 | 味の素株式会社 | ジフェニルメタン化合物 |
| JP2019165967A (ja) | 2018-03-23 | 2019-10-03 | 株式会社サンセイアールアンドディ | 遊技機 |
Non-Patent Citations (2)
| Title |
|---|
| ORGANIC PROCESS RESEARCH & DEVELOPMENT, vol. 21, no. 3, 2017, pages 365 - 369 |
| See also references of EP4011902A4 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20220185841A1 (en) | 2022-06-16 |
| JPWO2021049552A1 (ja) | 2021-03-18 |
| JP7459121B2 (ja) | 2024-04-01 |
| TW202124408A (zh) | 2021-07-01 |
| EP4011902A1 (en) | 2022-06-15 |
| EP4011902A4 (en) | 2022-10-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US12325727B2 (en) | Method for producing peptide compound, protective group-forming reagent, and aromatic heterocyclic compound | |
| JP7139511B2 (ja) | ペプチド化合物の製造方法、保護基形成用試薬、及び、縮合多環芳香族炭化水素化合物 | |
| JP7238123B2 (ja) | ペプチド化合物の製造方法、保護基形成用試薬、及び、縮合多環芳香族炭化水素化合物 | |
| US20240317796A1 (en) | Method for producing peptide compound, protective group-forming reagent, and substituted benzyl compound | |
| US12227542B2 (en) | Method for producing peptide compound, protective group-forming reagent, and condensed polycyclic compound | |
| WO2022138605A1 (ja) | ペプチドの製造方法、保護基形成用試薬、及び、縮合多環化合物 | |
| JP7459121B2 (ja) | ペプチド化合物の製造方法、保護基形成用試薬、及び、ヒドラジン誘導体 | |
| WO2022196797A1 (ja) | アミノ酸又はペプチドの製造方法、保護基形成用試薬、及び、化合物 | |
| WO2025229966A1 (ja) | Fmoc基の除去方法、ペプチドの製造方法、および化合物の製造方法 | |
| WO2025063265A1 (ja) | ペプチド化合物の製造方法、保護基形成用試薬、およびジナフチルメチル化合物 | |
| WO2025229967A1 (ja) | ペプチドの製造方法 | |
| WO2025154779A1 (ja) | ペプチドの製造方法、化合物、及びペプチド合成試薬 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 20863826 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2021545579 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2020863826 Country of ref document: EP Effective date: 20220316 |