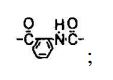CAMPO TÉCNICO
[001] A presente invenção diz respeito a um novo derivado de quinazolino-2,4-diona da fórmula (I)
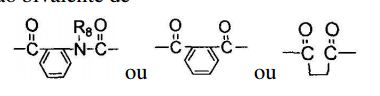
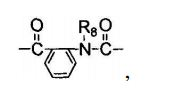
em que R1 é hidrogênio ou alquila; cada um de R2 e R3 é independentemente selecionado de hidrogênio, alquila, -COR6, -SO2R7, ou fenila ou benzila substituídos ou não substituídos, em que R6 é alquila, alcóxi, fenila, fenilóxi ou benzilóxi, cada um dos quais é não substituído ou substituído com halogênio, hidróxi, metóxi, etóxi ou nitro, e R7 é alquila inferior ou arila não substituído ou substituído; A é -(CH2)n- ou -CH2CH=CHCH2-, em que n é um número inteiro selecionado de 2 a 4; R4 é hidrogênio e R5 é hidrogênio ou benzoíla não substituído ou substituído com um ou mais de halogênio, hidróxi, alcóxi ou nitro em anel de benzeno ou quando R4 e R5 juntos com N formam um anel , R4 e R5 formam uma porção bivalente de

em que R8 é hidrogênio ou alquila; cada um de l e m é independentemente um número inteiro selecionado de 2 a 4; e p é um número inteiro de 0 ou 1, ou um sal deste farmaceuticamente aceitável, e uma composição farmacêutica que compreende o composto da fórmula (I) como um ingrediente ativo para prevenir ou tratar doenças cerebrais neurológicas
[002] O progresso das doenças cerebrais neurológicas pela morte das células nervosas por um tempo curto ou logo e resulta em perda fatal da função cerebral. Derrame é uma das doenças cerebrovascular mais frequentemente geradas. Porque os distúrbios de nervo craniano em pacientes no grupo de idade vigorosa dos quarenta aos cinquenta têm acentuadamente aumentado, é indicado como não apenas um problema individual mas também um problema nacional.
[003] Existem amplamente dois tipos de derrame: o infarto cerebral e a hemorragia cerebral. O infarto cerebral resulta da necrose de tecido cerebral causada por um bloqueio do fornecimento de sangue para o tecido cerebral causado por trombo e assim por diante. A hemorragia cerebral, por outro lado, resulta da perda de sangue devido aos vasos sanguíneos rompidos no cérebro. Embora a patogênese do infarto cerebral e da hemorragia cerebral sejam diferentes, seus sintomas são frequentemente similares.
[004] O método padrão para tratar o período agudo de infarto é correntemente a trombólise. O período de tempo antes do tratamento de partida e depois do início do infarto cerebral é muito importante, e é conhecido que a situação funcional do paciente pode ser melhorada quando um agente trombolítico é administrado dentro de 3 horas depois do início do infarto cerebral.
[005] A causa da necrose da célula cerebral devido à isquemia foi elucidada por muitos pesquisadores, e o caminho principal é sugerido como toxicidade excitável pela toxicidade oxidativa de neurotransmissor excessiva, pelo estresse, toxicidade de zinco, apoptose e assim por diante.
[006] O glutamato, que é uma das substâncias tóxicas excitáveis, é um neurotransmissor excitável do sistema nervoso central, e ele reage com o receptor de NMDA (N-metil-D-aspartato). A morte das células nervosas é induzida quando o glutamato é excessivamente produzido pela isquemia. É recentemente relatado que estas toxicidades excitáveis podem ser o mecanismo principal da morte das células nervosas pelo derrame isquêmico assim como da epilepsia. Se o fornecimento de oxigênio-glicose para o tecido nervoso depois da isquemia é reduzido, o glutamato que é um neurotransmissor excitável, é acumulado na junção entre os neurônios. E depois, a morte das células nervosas pela atividade excessiva do receptor de glutamato NMDA principalmente ocorre. Portanto, a morte das células nervosas pelo derrame isquêmico pode ser suprimida pelo uso de antagonistas do receptor de glutamato NMDA.
[007] Os radicais livres também são um dos mecanismos principais da morte das células nervosas. Um aumento de radicais livres pela isquemia e outros nas células nervosas induz a destruição do lipídeo da membrana pela peroxidação de lipídeo, dano de ácido nucléico pelos radicais de oxigênio, desnaturação de proteína e outros. Isto resulta em dano fatal aos fatores essenciais para a sobrevivência de célula. Muitos pesquisadores têm relatado que a isquemia leva a aumentos do oxigênio ativo no cérebro, espécies de oxigênio reativo na doença de Parkinson, doença de Huntington e doença de Alzheimer, catalase (uma enzima descontaminante de radical), atividade de Cu/Zn superóxido dismutase (SOD) e Fe2+.
[008] Como mencionado acima, embora muitos mecanismos sejam revelados tratar os distúrbios de nervo craniano, o desenvolvimento de novos medicamentos é demorado por causa de problemas a cerca da eficácia e toxicidade.
[009] Os presentes inventores descobriram que substâncias naturais são liberadas de EISENIA ANDREI e EISENIA FETIDA vivas dada eletroestimulação enquanto nós as estudamos a partir de remédios populares a muito tempo usados no Oriente. E nós descobrimos que compostos específicos destas substâncias mostram a proteção válida dos nervos cranianos. Muitos compostos derivados incluindo novos compostos isolados a partir de produtos naturais foram sintetizados com base nesta descoberta. Foi aprendido que o composto derivado da quinazolino-2,4-diona da fórmula (I) e um sal deste têm um efeito superior na proteção da atividade das células nervosas, e nós completamos a presente invenção.
DESCRIÇÃO DETALHADA DA INVENÇÃO
PROPÓSITO DA INVENÇÃO
[0010] O propósito da presente invenção é fornecer um composto da fórmula (I) ou um sal deste farmaceuticamente aceitável, e uma composição farmacêutica que compreenda o dito composto como um ingrediente ativo para prevenir ou tratar doenças cerebrais neurológicas.
MEIOS TÉCNICOS
[0011] A presente invenção fornece um novo derivado de quinazolino-2,4-diona da fórmula (I)
em que R1 é hidrogênio ou alquila; cada um de R2 e R3 é independentemente selecionado de hidrogênio, alquila, -COR6, -SO2R7, ou fenila ou benzila substituído ou não substituído, em que R6 é alquila, alcóxi, fenila, fenilóxi ou benzilóxi, cada um dos quais é não substituído ou substituído com halogênio, hidróxi, metóxi, etóxi ou nitro, e R7 é alquila inferior ou arila não substituído ou substituído; A é -(CH2)n- ou -CH2CH=CHCH2-, em que n é um número inteiro selecionado de 2 a 4; R4 é hidrogênio e R5 é hidrogênio ou benzoíla não substituído ou substituído com um ou mais de halogênio, hidróxi, alcóxi ou nitro em anel de benzeno ou quando R4 e R5 juntos com N formam um anel, R4 e R5 formam uma porção bivalente de
em que R8 é hidrogênio ou alquila; cada um de l e m é independentemente um número inteiro selecionado de 2 a 4; e p é um número inteiro de 0 ou 1, ou um sal deste farmaceuticamente aceitável.
[0012] Como aqui usado, o termo “alquila” refere-se a alquila tendo de 1 a 6 átomos de carbono, por exemplo, uma cadeia de hidrocarboneto alifático incluindo cadeia de partida, cadeia ramificada ou forma cíclica tal como metila, etila, n-propila, isopropila, n-butila, sec-butila, isobutila, terc- butila, n-pentila, 2-metilpentila, hexila e cicloexila.
[0013] O termo “alquila inferior” refere-se a uma cadeia de hidrocarboneto reta ou ramificada tendo de 1 a 4 átomos de carbono.
[0014] O termo “alcóxi” refere-se a -O-alquila, em que “alquila” refere-se a uma cadeia de hidrocarboneto reta ou ramificada tendo de 1 a 4 átomos de carbono.
[0015] O compostos da fórmula (I) podem ser usados nas formas de sais farmaceuticamente aceitáveis destes e os sais farmaceuticamente aceitáveis incluem sais de adição de ácido convencionalmente conhecidos ou sais de metal alcalino na técnica.
[0016] Os exemplos típicos da fórmula (I) de acordo com a presente invenção são como segue: 3-{3-[4-(3-aminopropilamino)butilamino]propil}-1H- quinazolino-2,4-diona; 3-(3-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propilamino]butil-amino}propil)-1H-quinazolino-2,4-diona; N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-{4- [3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propilamino]butil}acetamida; N-(4-{acetil-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]amino}-butil)-N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]acetamida; Éster etílico do ácido [3-(2,4-dioxo-1,4-diidro-2H-quinazolin- 3-il)propil]-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propilamino]- butil}carbâmico; N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-(4- {[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]metilamino}butil) acetamida; 3-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propilamino]butil}-1H-quinazolino-2,4-diona; N-(3-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propilamino]butil-amino}propil)-4-hidroxibenzamida; 3-{3-[4-({N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]-N-benzil}amino)butilamino]propil}-1H-quinazolino-2,4-diona; N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-{4- [3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propilamino]butil}benzamida; Éster terc-butílico do ácido [3-(2,4-dioxo-1,4-diidro-2H- quinazolin-3-il)propil]-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propilamino]-butil}carbâmico; N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-{4- [3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propilamino]butil}metano- sulfonamida; N-(4-{benzil-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]amino}-butil)-N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]acetamida; Éster etílico do ácido (4-{acetil-[3-(2,4-dioxo-1,4-diidro-2H- quinazolin-3-il)propil]amino}-butil)-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin- 3-il)propil]carbâmico; 3-{[3-(4-{N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]-N-benzilamino}butil)-N-benzilamino]propil}-1H-quinazolino-2,4- diona; Éster etílico do ácido [3-(2,4-dioxo-1,4-diidro-2H-quinazolin- 3-il)propil]-(4-{[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil] etoxicarboníl-amino}butil)carbâmico; Éster terc-butílico do ácido (4-{terc-butoxicarbonil-[3-(2,4- dioxo-1,4-diidro-2H-quinazolin-3-il)propil]amino}butil)-[3-(2,4-dioxo-1,4- diidro-2H-quinazolin-3-il)propil]carbâmico; N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-(4- {[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]metanossulfonilamino}butil)-metanossulfonamida; N-[3-(acetil-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil-amino]butil}amino)propil]-4-hidroxibenzamida; N-[3-(4-{acetil-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]-amino}butilamino)propil]-4-hidroxibenzamida; N-{3-[acetil-(4-{acetil-[3-(2,4-dioxo-1,4-diidro-2H- quinazolin-3-il)propil]amino}butil)amino]propil}-4-hidroxibenzamida; N-[4-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)butil]-N-[3- (2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]acetamida; 3-(2-{3-[2-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)etilamino] propil-amino}etil)-1H-quinazolino-2,4-diona; 3-(3-{3-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propilamino]propil-amino}propil)-1H-quinazolino-2,4-diona; 3-(3-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propilamino]-2-butenilamino}propil)-1H-quinazolino-2,4-diona; Éster terc-butílico do ácido (4-{terc-butoxicarbonil-[3-(1- metil-2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]amino}butil)-[3-(1- metil-2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]carbâmico; 1-metil-3-(3-{4-[3-(1-metil-2,4-dioxo-1,4-diidro-2H- quinazolin-3-il)-propilamino]butilamino}propil)-1H-quinazolino-2,4-diona; 3-(3-{4-[3-(1,3-dioxo-1,3-diidro-isoindol-2-il)propilamino] butilamino}-propil)-1H-quinazolino-2,4-diona; 3-(3-{2-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propilamino]etil-amino}propil)-1H-quinazolino-2,4-diona; Éster terc-butílico do ácido [3-(2,4-dioxo-1,4-diidro-2H- quinazolin-3-il)propil]-(4-{[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]hexil-amino}butil)carbâmico; 3-[3-(4-{N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]-N-hexilamino}butilamino)propil]-1H-quinazolino-2,4-diona; Éster terc-butílico do ácido (4-{terc-butoxicarbonil-[3-(1- hexil-2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]amino}butil)-[3-(1- hexil-2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]carbâmico; 1-hexil-3-(3-{4-[3-(1-hexil-2,4-dioxo-1,4-diidro-2H- quinazolin-3-il)-propilamino]butilamino}propil)-1H-quinazolino-2,4-diona; Éster terc-butílico do ácido [3-(2,4-dioxo-1,4-diidro-2H- quinazolin-3-il)propil]-(4-{[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]heptanoilamino}butil)carbâmico; Amida do ácido [3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propilamino]butil}- heptanoíco; N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-{4- [3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propilamino]butil}-2,2,2- trifluoro-acetamida; N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-{4- [[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-(2,2,2-trifluoroacetil)- amino]butil}-2,2,2-trifluoroacetamida; N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-{4- [3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propilamino]butil}-2-metóxi- acetamida; Éster benzílico do ácido; [3-(2,4-dioxo-1,4-diidro-2H- quinazolin-3-il)propil]-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propilamino]-butil}carbâmico N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-{4- [3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propilamino]butil}-4- metilbenzeno-sulfonamida; N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-(4- {[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-4-metilbenzenossulfonil- amino}butil)-4-metilbenzenossulfonamida; ou 3-(3-{4-[3-(2,5-dioxo-pirrolidino-1-il)propilamino] butilamino}propil)-1H-quinazolino-2,4-diona.
[0017] O composto da fórmula (1) pode ser preparado pelas reações como descritas nas seguintes esquemas de reação de I a III. Portanto, é um outro objetivo da presente invenção para fornecer tais processos de preparação.
[0018] Entretanto, os seguintes esquemas de reação ilustram os processos de ilustração mais gerais da presente invenção. Os processos para preparar o composto da fórmula (1) de acordo com a presente invenção não são limitados aos seguintes esquemas de reação ilustrados. O composto da fórmula (1) pode ser preparado pelos vários processos conhecidos nas técnicas. Esquema de reação I
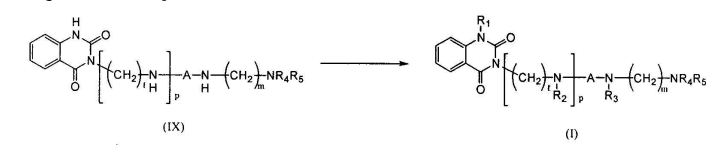
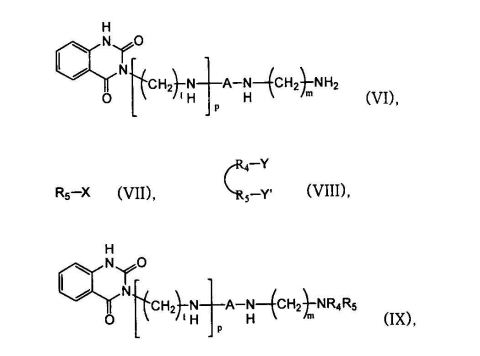
[0019] Pela reação do composto derivado do ácido benzóico (IV) tendo um substituinte de alcoxicarbonilamino na posição 2 com o composto de amina (V) em que A é adequadamente selecionado para formar um anel sob a existência ou a ausência de solvente, um derivado de quinazolina 2,4- diona de composto de amina primária (IX) tendo uma estrutura de esqueleto de quinazolina 2,4-diona pode ser obtido, em que R4 e R5 são hidrogênio. Alternativamente, aumentando-se as quantidades estequiométricas do composto (IV), um derivado de quinazolina 2,4-diona dos compostos (IX) em que R4 e R5 formam quinazolino-2,4-diona cíclica com o átomo N pode ser obtido. A reação de fusão do anel sob a ausência de solventes deve ser realizada em uma temperatura suficiente para fundir dois reagentes.
[0020] No esquema de reação acima, A, I, m e p são os mesmos como definidos acima, R4 e R5 representam hidrogênio, ou quando R4 e R5 juntos com N formam um anel, R4 e R5 formam uma porção bivalente de
e Alk representa alquila. L representa um grupo de partida que é preferivelmente hidróxi, alcóxi ou halogênio. Esquema de reação II
[0021] Pela reação do composto (VI) com o composto (VII) ou (VIII) tendo substituintes R4 e R5, um derivado de quinazolino-2,4-diona do composto (IX) em que R4 e R5 são adequadamente introduzidos na amina primária terminal pode ser obtido, em que a reação pode ser realizada sob a existência de solventes, a reação de fusão pode ser realizada sob a ausência de solventes ou a reação de condensação pode ser realizada, se X é hidróxi.
[0022] A reação de condensação pode ser realizada usando-se DCC (dicicloexila carbodiimida) ou EDC (1-(3-dimetilaminopropil)-3-etil- carbodiimida). Alternativamente, o composto (IX) pode ser obtido pela conversão do grupo carboxila em grupo mais reativo tal como anidrido ácido ou cloreto ácido e depois reagindo-o com o composto (VI).
[0023] No esquema de reação acima, A, R4, R5, I, m e p são os mesmos como definidos acima, R5 não é H, X representa hidróxi, halogênio, alcóxi ou -OR5. Cada um de Y e Y’ é hidróxi, halogênio, alcóxi ou quando Y e Y’ formam um anel, Y e Y’ formam -O-. Esquema de reação III
[0024] Pela substituição de pelo menos um hidrogênio do composto da fórmula (IX) com R2 e/ou R3, um derivado de quinazolino-2,4-diona do composto (I) pode ser obtido, em que R2 e R3 são adequadamente introduzidos na posição amina, R1 é hidrogênio, e pelo menos um de R2 e R3 não é hidrogênio. No caso de obter o composto em que R2 e R3 são os mesmos substituintes, os substituintes R2 e R3 podem ser introduzidos de uma vez.
[0025] No caso de obter o composto em que R2 e R3 são substituintes diferentes, o substituinte R2 pode ser primeiro introduzido no composto (IX) para obter o derivado de quinazolino-2,4-diona do composto (I) que R1 e R3 são hidrogênio, e depois o substituinte R3 pode ser introduzido na presença de solvente orgânico e base. Por outro lado, o substituinte R3 pode ser primeiro introduzido nos compostos (IX) e depois o substituinte R2 pode ser introduzido no composto substituído em R3 para obter o derivado de quinazolino-2,4-diona do composto (I) em que R2 e R3 são adequadamente substituídos e R1 é hidrogênio.
[0026] Também, depois que os substituintes desejados são introduzidos na posição de amina secundária do composto (IX), o derivado de quinazolino-2,4-diona do composto (I), em que R1 é alquila e os substituintes desejados são introduzidos, pode ser obtido pela alquilação da posição 1 no anel de quinazolina com um agente de alquilação sob a existência de base ou desproteção adicional subsequente à alquilação. O haleto de alquila, sulfato de dialquila ou sulfonato de alquila podem ser usados como o agente de alquilação acima.
[0027] No esquema de reação acima, A, R1, R2, R3, R4, R5, l, m e p são os mesmos como definidos acima, e R5 não é H. condições de reação mais específicas são descritas nos seguintes Exemplos de 1 a 42.
[0028] Por outro lado, o composto da fórmula (1) de acordo com a presente invenção preparado pelos processos acima podem ser submetidos a outra isolação e purificação pelos métodos de pós tratamento convencionais ou podem ser preparados como um sal farmaceuticamente aceitável correspondente pelos métodos convencionais. O sal, como no geral conhecido pelos técnicos habilitados, devem ser farmaceuticamente aceitáveis e não tóxicos. Vários sais podem ser usados para produzir o composto da presente invenção e um sal deste não tóxico farmaceuticamente aceitável.
[0029] O sal farmaceuticamente aceitável do composto de acordo com a presente invenção inclui sais de adição de ácido ou sais de metal alcalino. Tais sais de adição de ácido podem ser, mas não são limitados a estes, um sal com o ácido clorídrico, ácido bromídrico, ácido iodídrico, ácido sulfúrico, ácido acético, ácido benzenossulfônico, ácido metano-sulfônico, ácido fosfórico, ácido nítrico, ácido fórmico, ácido propiônico, ácido succínico, ácido glicólico, ácido láctico, ácido málico, ácido orótico, ácido nicotínico, ácido adípico, ácido tartárico, ácido cítrico, ácido ascórbico, ácido maléico, ácido benzóico, ácido salicílico, ácido fumárico, ácido cansílico ou ácido carboxílico, e tal sal de metal alcalino pode ser, mas não é limitado a estes, um sal de sódio, potássio, lítio, magnésio ou cálcio.
[0030] Adicionalmente, a presente invenção fornece uma composição farmacêutica que é útil para prevenir ou tratar doenças cerebrais neurológicas como acima mencionadas pela combinação do composto derivado de quinazolino-2,4-diona da fórmula (I) e o sal deste farmaceuticamente aceitável com um carregador farmaceuticamente aceitável.
[0031] O composto da fórmula (I) de acordo com a presente invenção é útil para tratar uma doença causada pela degeneração normal ou anormal do sistema cerebral neurológico ou proteger as células nervosas da mesma, como provado pelos resultados dos exemplos que seguem.
[0032] A presente invenção fornece uma composição farmacêutica que compreende o composto da fórmula (I) ou um sal deste farmaceuticamente aceitável como um ingrediente ativo com um carregador farmaceuticamente aceitável, para prevenir ou tratar distúrbio do sistema cerebral neurológico, doença cerebral neurológica degenerativa ou disfunção do sistema nervoso. Mais especificamente, uma composição farmacêutica de acordo com a presente invenção é útil para prevenir ou tratar a doença que é selecionada de disfunção neurológica, falta de memória, insuficiência cerebrovascular, lesão cerebral local, trauma cerebral focal, trauma cerebral difuso, lesão da medula espinhal, isquemia cerebral, hemorragia cerebral, derrame isquêmico, derrame hemorrágico, demência, infarto cerebral, oclusão embólica, oclusão trombótica, reperfusão a seguir da isquemia aguda, ataque isquêmico transitório, lesão hipóxica-isquêmica perinatal, parada cardíaca, hemorragia intracraniana, hemorragia subaracnoidal, aneurisma cerebral, aneurisma de Willis, hemiplegia infantil aguda, lesão do pescoço, síndrome da criança sacudida, doença de Alzheimer, doença de Pick, doença de corpo de Lewy difusa, paralisia supranuclear progressiva (síndrome de Steel- Richardson), degeneração de sistema múltiplo (síndrome de Shy-Drager), condições epilépticas crônicas associadas com neurodegeneração, doenças neuronais motoras, esclerose lateral amiotrófica, esclerose lateral primária, ataxias degenerativas, degeneração basal cortical, panencefalite esclerosante subaguda, doença de Huntington, doença de Parkinson, sinucleinopatias, afasia progressiva primária, atrofia muscular espinal e atrofia muscular espinobulbar (doença de Kennedy), esclerose múltipla, doença de Tay-Sach, paraplegia espástica, doença priônica, doença de Creutzfeldt-Jakob, epilepsia, plexopatia ou neuropatia; e para a melhora da memória.
[0033] A composição farmacêutica da presente invenção pode ser preparada combinando-se um composto da presente invenção com um carregador inativo farmaceuticamente aceitável na forma de sólido ou líquido e pode ser formulada em uma forma farmaceuticamente aceitável apropriada para a administração. A formulação acima pode ser preparada na forma de liberação imediata ou liberação prolongada, que são bem conhecidas pelo técnico habilitado. A composição farmacêutica pode ser formulada em tabletes, pílulas, grânulos, pós, cápsulas, suspensões, xaropes, elixires, soluções, emulsões ou injeções para a administração oral, intravenosa ou parenteral. A composição farmacêutica pode ser formulada em tabletes, cápsulas, pós, microgrânulos, soluções ou suspensões esterilizadas para a administração retal ou na forma de supositórios.
[0034] O carregador farmaceuticamente aceitável acima pode incluir lactose, dextrose, sacarose, sorbitol, manitol, xilitol, eritritol, malditol, amido, goma acácia, alginato, gelatina, fosfato de cálcio, silicato de cálcio, celulose, metil-celulose, celulose microcristalina, polivinilpirrolidona, água, hidroxibenzoato de metila, hidroxibenzoato de propila, talco, estearato de magnésio ou óleos minerais. Adicionalmente, o carregador farmaceuticamente aceitável acima pode incluir diluentes ou aditivos tais como enchedores, extensores, agentes de aglutinação, agentes de umectação, desintegrantes, tensoativos, etc.
[0035] A formulação sólida para a administração oral pode estar na forma de tabletes, pílulas, pós, grânulos, cápsulas, etc. e pode incluir pelo menos um aditivo, por exemplo, tal como amido, carbonato de cálcio, sacarose, lactose e gelatina, ou lubrificantes tais como estearato de magnésio, talco, etc. A formulação líquida para a administração oral pode estar na forma de suspensões, soluções, emulsões, xaropes, etc. e podem incluir diluentes tais como água e parafina líquida, agentes umectantes, adoçantes, aromáticos ou preservantes. A formulação para a administração parenteral pode estar na forma de soluções esterilizadas, solventes não aquosos, suspensões, emulsões, liofilizações ou supositórios. Os solventes não aquosos e as suspensões incluem propileno glicol, polietileno glicol, óleos vegetais tais como óleo de oliva, ésteres injetáveis tais como oleato de etila, etc. Witepsol, macrogol, tween 61, óleo de cacau, óleo de laurina, glicerogelatina e outros como um carregador para supositórios podem ser usados.
[0036] A dose desejável do composto da fórmula (I) ou do sal deste farmaceuticamente aceitável incluídos na composição farmacêutica da presente invenção varia dependendo da condição, peso, idade e gênero do paciente, severidade da doença, forma medicamentosa, e via e período de administração, e pode ser escolhida por aqueles habilitados na técnica. Por exemplo, é no geral recomendado administrar na quantidade variando de 0,01 a 500 mg/kg, preferivelmente, de 0,1 a 100 mg/kg em peso/dia do composto da fórmula (I) ou o sal deste farmaceuticamente aceitável, mas o mesmo não é limitado a este escopo. Uma dose única pode ser administrada ou a mesma pode ser dividida em várias vezes ao dia ou semanalmente.
[0037] Adicionalmente, a composição farmacêutica da presente invenção pode incluir 0,001 a 50 % em peso, preferivelmente de 0,1 a 50 % em peso do composto da fórmula (I) ou o sal deste farmaceuticamente aceitável, com base no peso total da composição, mas a mesma não é limitada ao seu escopo.
EFEITOS VANTAJOSOS
[0038] Um derivado de quinazolino-2,4-diona, um sal deste farmaceuticamente aceitável e uma composição que compreende o derivado de quinazolino-2,4-diona e o sal deste farmaceuticamente aceitável de acordo com a presente invenção têm efeitos sobre a supressão da morte celular no cérebro, proteção das células nervosas, anti-oxidação, anti-convulsão e relaxação dos vasos sanguíneos, e assim são úteis para prevenir ou tratar as várias doenças anteriormente mencionadas por exemplo, derrame, doença de Alzheimer e epilepsia assim como realçar a memória.
DESCRIÇÃO DOS DESENHOS
[0039] A Figura 1 mostra o efeito anti-derrame do composto 3 em um modelo de oclusão da artéria cerebral central (MCAO). A cor vermelha (tingida) representa a área cerebral normal e a cor branca (não tingida) representa a área de oclusão. 100 mg/kg de composto 3 e 2000 mg/kg de citicolina foram administrados em 1 hora e exatamente antes de induzir o derrame (oito camundongos foram usados em cada grupo experimental).
[0040] A Figura 2 mostra um efeito do composto 3 sobre a supressão do estresse oxidativo induzido pelo NMDA de células cerebrais em camundongos. “Controle normal” é células normais sem qualquer tratamento, e “controle negativo” é células cerebrais com tratamento de 300 μM de NMDA. 125 μg/ml e 250 μg/ml de composto 3 foram administrados (grupos tratados com composto). As marcas de #, * e ** são intencionadas a mostrar a diferença significante de P<0,05, quando comparada com cada controle correspondente, nos casos de realização dos testes de ANOVA e t de Student (#;comparar controle normal com controle negativo; e * e **; comparar grupos tratados com compostos com controle negativo). FORMAS DE REALIZAÇÃO CONCRETAS PARA REALIZAR A INVENÇÃO
[0041] A presente invenção será mais especificamente explicada por referência aos seguintes exemplos, que são fornecidos por via de ilustração e não são intencionados como limitantes. Exemplo 1 3-{3-[4-(3-aminopropilamino)butilamino]propil}-1H-quinazolino-2,4-diona (Composto 1) 1) Preparação de 2-etoxicarbonilamino benzoato de etila:
[0042] 2-amino benzoato de etila (20 g, 0,12 mol) foi dissolvido em 140 ml de xileno e cloroformiato de etila (13,8 ml, 0,15 mol) foi adicionado a este. Depois de reagir sob refluxo por 3 horas, o solvente foi removido pela destilação sob pressão reduzida. 30 ml de éter de petróleo foram adicionados ao resíduo e esfriado. O composto do título de sólido branco (26 g, 90,5 %) foi obtido pela coleta do sólido formado através do processo de filtração e pela concentração e cristalização da solução filtrada.
[0043] 1H RMN (CDCl3) : 10,51 (s, 1H), 8,43 (dd, 1H), 8,01 (dd 1H), 7,51 (t, 1 H), 7,01 (t, 1H), 4,37 (q, 2H), 4,22 (q, 2H), 1,40 (t, 3H), 1,32 (t, 3H); 2) Preparação do 3-{3-[4-(3-aminopropilamino)butilamino]-propil}-1H- quinazolino-2,4-diona:
[0044] 2-etoxicarbonilamino benzoato de etila (8,0 g, 33,7 mmol) e N,N’-bis-(3-aminopropil)butano-1,4-diamina (8,87 g, 43,8 mmol) foram fundidos com aquecimento. Depois de agitar por 4 horas de 125 a 135OC, isopropil-álcool foi adicionado a este e o ácido clorídrico concentrado foi adicionado para formar sólido.
[0045] O sólido obtido pelo processo de filtração foi dissolvido em água e neutralizado com solução aquosa de hidróxido de sódio. Depois da remoção da água pela destilação sob pressão reduzida, a cromatografia de coluna em gel de sílica do resíduo remanescente foi realizado para dar o composto do título na forma oleosa (5,0 g, 43 %).
[0046] 1H RMN (D2O) : 7,48 (dd, 1H), 7,30 (t, 1H), 6,83 (m, 2H), 3,73 (t, 2H), 2,59 (t, 2H), 2,52 (t, 2H), 2,46 (t 6H), 1,66 (m, 2H), 1,56 ((m, 2H), 1,37 (m, 4H): Exemplo 2 3-(3-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propilamino]butilamino}-propil)-1H-quinazolino-2,4-diona (Composto 2) (Processo 1)
[0047] 2-etoxicarbonilamino benzoato de etila (4,9 g, 20,6 mmol) e N,N’-bis-(3-aminopropil)butano-1,4-diamina (2,1 g, 10,3 mmol) foram fundidos com aquecimento. Depois de agitar por 5 horas de 125 a 135OC, 25 ml de álcool isopropílico foi adicionado a este para fabricar um sólido e secado sob pressão reduzida depois da filtração para dar o composto do título de sólido branco (3,3g, 64 %).
[0048] 1H RMN (CDCl3) : 8,05 (d, 2H), 7,62 (t, 2H), 7,22 (t, 2H), 7,15 (d, 2H), 4,11 (t, 4H), 2,62 (m, 8H), 1,94 (m, 4H), 1,55 (s, 4H) (Processo 2)
[0049] 3-{3-[4-(3-aminopropilamino)butilamino]propil}-1H- quinazolino-2,4-diona (2,1 g, 6,0 mmol) e 2-etoxicarbonilamino benzoato de etila (1,6g, 6,6 mmol) foram fundidos de 125 ~ 135C. Depois de 5 horas, 20 ml de álcool isopropílico foi adicionado a este para fabricar um sólido e secado sob pressão reduzida depois da filtração para dar o composto do título do sólido branco (2,2 g, 74 %) que é o mesmo como o composto obtido pelo Processo 1. Exemplo 3 O sal do ácido clorídrico de N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]-N-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)- propilamino]butil}acetamida (Composto 3)
[0050] Depois de 3-(3-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)-propilamino]butilamino}propil)-1H-quinazolino-2,4-diona (3g, 6,1 mmol) foi dissolvido em 60 ml de piridina, anidrido acético (0,7 ml, 7,3 mmol) foi adicionado a este. Depois de 2 horas, a piridina foi removida pela destilação sob pressão reduzida. O diclorometano e água foram adicionados ao resíduo remanescente, e cada camada foi separada na solução depois do sólido formado foi removido pelo processo de filtração. O ácido clorídrico concentrado foi adicionado à camada aquosa, e o pH foi ajustado até 2 a 3. Depois da remoção da água pela destilação sob pressão reduzida, a cromatografia de coluna em gel de sílica do resíduo remanescente foi realizada para dar o composto do título (1,1 g, 32 %).
[0051] 1H RMN (MeOD) : 7,97 (m, 2H), 7,61 (m, 2H), 7,17 (m, 4H), 4,14 (m, 2H), 4,02 (m, 2H), 3,47 (m, 4H), 3,07 (m, 4H), 2,12 (s, 5H), 1,96 (m, 2H), 1,73 (m, 4H)
[0052] Tratando-se o composto 1,0 g do Exemplo acima 3 com resina de troca iônica, composto na forma de base, N-[3-(2,4-dioxo-1,4-diidro-2H- quinazolin-3-il)propil]-N-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)- propilamino]butil}acetamida (0,65g) foi obtido.
[0053] 1H RMN (MeOD) : 7,89 (m, 2H), 7,53 (m, 2H), 7,15 (m, 4H), 3,97 (m, 4H), 3,40 (t, 2H), 3,32 (q, 2H), 2,54 (m, 4H), 2,05 (d, 3H), 1,94 - 1,83 (m, 4H), 1,61 - 1,44 (m, 4H) Exemplo 4 N-(4-{acetil-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il) propil]amino}butil)-N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il) propil]acetamida (Composto 4)
[0054] Depois de 3-(3-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)-propilamino]butilamino}propil)-1H-quinazolino-2,4-diona (2 g, 4,1 mmol) foi dissolvida em 50 ml de piridina, anidrido acético (1,0 ml, 10,2 mmol) foi adicionado. Depois de 2 horas, a piridina foi removida pela destilação sob pressão reduzida, e a cromatografia de coluna em gel de sílica do resíduo remanescente foi realizado para dar o composto do título (2,1 g, 90 %).
[0055] 1H RMN (DMSO) : 11,40 (s, 2H), 7,91 (m, 2H), 7,63 (m, 2H), 7,17 (m, 4H), 3,86 (m, 4H), 3,27 (m, 8H), 1,95 (m, 6H), 1,08 (m, 4H), 1,43 (m, 4H); Exemplo 5 O sal do ácido clorídrico do éster etílico do ácido [3-(2,4-dioxo-1,4-diidro- 2H-quinazolin-3-il)propil]-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil-amino]butil}carbâmico (Composto 5)
[0056] 3-(3-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil- amino]butilamino}propil)-1H-quinazolino-2,4-diona (2 g, 4,1 mmol) foi dissolvida em 20 ml de hexametilfosforamida com aquecimento, esfriado e cloroformiato de etila (0,4 ml, 4,1 mmol) foi adicionado a este. Depois de 2 horas, a cromatografia de coluna em gel de sílica da mistura de reação foi realizada para dar o composto do título do sólido amarelo (0,48 g, 20 %)
[0057] 1H RMN (MeOD) : 8,00 (t, 2H), 7,63 (q, 2H), 7,21 (q, 2H), 7,14 (m, 2H), 4,15 (t, 2H), 4,09 (q, 2H), 4,02 (t, 2H), 3,36 (m, 4H), 3,05 (m, 4H), 2,10 (m, 2H), 1,95 (m, 2H), 1,71 (t, 4H), 1,21 (bs, 3H) Exemplo 6 N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-(4-{[3-(2,4-dioxo- 1,4-diidro-2H-quinazolin-3-il)propil]metilamino}butil) acetamida (Composto 6)
[0058] O sal do ácido clorídrico de N-[3-(2,4-dioxo-1,4-diidro-2H- quinazolin-3-il)propil]-N-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)- propilamino]butil}acetamida (2 g, 3,5 mmol) foi dissolvido em 80 ml de diclorometano e 10 ml de metanol. A trietilamina (0,45 g, 4,5 mmol) e paraformaldeído (0,14 g, 4,5 mmol) foram adicionados a este e agitados por 2 horas na temperatura ambiente. Depois da concentração do solvente, 40 ml de metanol e boroidreto de sódio (0,76 g, 20,2 mmol) foram adicionados a este e agitados por 15 horas. Depois da remoção do metanol pela destilação sob pressão reduzida, a cromatografia de coluna em gel de sílica do resíduo remanescente foi realizada para dar o composto do título do sólido branco (1,2 g, 62 %).
[0059] 1H RMN (MeOD) : 7,98 (m, 2H), 7,60 (m, 2H), 7,19 (m, 2H), 7,11 (m, 2H), 4,02 (m, 4H), 3,46 - 3,36 (m, 4H), 2,69 - 2,52 (m, 4H), 2,41 - 2,34 (s, 3H), 1,10 (d, 3H), 1,98 - 1,90 (m, 4H), 1,63 1,51 (m, 4H); Exemplo 7 3-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propilamino] butil}-1H- quinazolino-2,4-diona (Composto 7)
[0060] 2-etoxicarbonilamino benzoato de etila (7 g, 29,5 mmol) e N- (3-aminopropil)butano-1,4-diamina 2,1g (14,8 mmol) foram fundidos de 140OC a. Depois de 3 horas, 50 ml de álcool isopropílico foram adicionados a este para a formação dos sólido, filtrados e secados sob pressão reduzida. O composto do título do sólido amarelo foi obtido (3,2 g, 50 %).
[0061] 1H RMN (MeOD) : 7,91 (m, 2H), 7,63 (m, 2H), 7,18 (m, 4H), 3,90 (m, 4H), 2,50 (m, 4H), 2,69 (m, 2H), 1,58 (m, 2H), 1,39 (m, 2H) Exemplo 8 Sal do ácido diclorídrico N-(3-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propilamino]butilamino}propil)-4-hidroxibenzamida (Composto 8)
[0062] Ácido 4-hidroxibenzílico (1,13 g, 8,2 mmol), 1-hidroxibenzo- triazol (1,27 g, 9,4 mmol), 1,3-dicicloexilcarbodiimida (1,94 g, 9,4 mmol) e N,N’-diisopropiletilamina (1,64 ml, 9,4 mmol) foram adicionados em 20 ml de sulfóxido de dimetila e agitados por 15 minutos. 3-{3-[4-(3-aminopropil- amino)butilamino]propil}-1H-quinazolino-2,4-diona (2,18 g, 6,3 mmol) dissolvida em sulfóxido de dimetila 10 ml foi adicionado a este e agitado a 50 C com agitação. Depois de 5 horas, sulfóxido de dimetila foi removido, a solução remanescente foi dissolvida em metanol com o ácido clorídrico concentrado. Depois da remoção do metanol, a cromatografia de coluna em gel de sílica do resíduo remanescente foi realizada para dar o composto do título do sólido branco (1,6 g, 47 %).
[0063] 1H RMN (D2O) : 7,91 (m, 1H), 7,74 (t, 1H), 7,63 (m, 2H), 7,33 (t, 1H), 7,16 (d, 1H), 6,87 (d, 2H), 4,07 (t, 2H), 3,53 (t, 2H), 3,20 (m, 8H), 2,11 (m, 4H), 1,91 (s, 4H); Exemplo 9 3-{3-[4-({N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-benzil}- amino)butilamino]propil}-1H-quinazolino-2,4-diona (Composto 9)
[0064] 3-(3-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il) propilamino]butilamino}-propil)-1H-quinazolino-2,4-diona (2 g, 4,1 mmol) foi dissolvida em 60 ml tetraidrofurano e solução aquosa de hidróxido de sódio (0,3 g, 8,1 mol) 60 ml e foi esfriada. O brometo de benzila (0,48 ml, 4,1 mmol) foi adicionado às gotas a este. Depois de 25 horas, os sólidos formados foi filtrados e o filtrado foi destilado sob pressão reduzida. A cromatografia de coluna em gel de sílica do resíduo remanescente foi realizada para dar o composto do título do sólido branco (0,28 g, 12 %).
[0065] 1H RMN (D2O) : 7,91 (m, 1H), 7,74 (t, 1H), 7,63 (m, 2H), 7,33 (t, 1H), 7,16 (d, 1H), 6,87 (d, 2H), 4,07 (t, 2H), 3,53 (t, 2H), 3,20 (m, 8H), 2,11 (m, 4H), 1,91 (s, 4H); Exemplo 10 O sal do ácido clorídrico de N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]-N-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)- propilamino]butil}benzamida (Composto 10)
[0066] No Exemplo 5 acima, cloreto de benzoíla (0,69 g, 4,9 mmol) foi usado ao invés de cloroformiato de etila. O mesmo procedimento descrito no Exemplo 5 acima foi realizado para dar o composto do título do sólido branco (0,2 g, 7,8%).
[0067] 1H RMN (DMSO-d6) : 7,94 - 7,84 (m, 2H), 7,65 (m, 2H), 7,38 (m, 2H), 7,22 - 7,01 (m, 7H), 3,96 - 3,72 (m, 4H), 3,48 - 3,16 (, 4H), 2,89 - 2,64 (m, 4H), 1,96 - 1,82 (m, 4H), 1,62 - 1,34 (m, 4H); Exemplo 11 Éster terc-butílico do ácido [3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)- propil]-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propilamino]butil}- carbâmico (Composto 11)
[0068] 3-(3-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il) propilamino]butilamino}-propil)-1H-quinazolino-2,4-diona (2 g, 4,1 mmol) foi dissolvida em piridina 20 ml e depois esfriada. 0,93 g di-terc-butila dicarbonato (4,3 mmol) foi adicionado a este. Depois de 3 horas, a piridina foi removida sob pressão reduzida, e cromatografia de coluna em gel de sílica foi realizada para dar o composto do título do sólido amarelo (0,25 g, 10,4 %).
[0069] 1H RMN (MeOD) : 7,99 (m, 2H), 7,60 (m, 2H), 7,22 - 7,09 (m, 4H), 4,04 (m, 4H), 3,25 (t, 4H), 2,59 (m, 4H), 1,90 (m, 4H), 1,60 - 1,48 (m, 4H), 1,40 (s, 2H) Exemplo 12 O sal do ácido clorídrico de N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]-N-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)- propilamino]butil}metanossulfonamida (Composto 12)
[0070] 3-(3-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il) propilamino]butilamino}-propil)-1H-quinazolino-2,4-diona (2 g, 4,1 mmol) foi dissolvida em hexametilfosforamida 10 ml com aquecimento. O diclorometano 30 ml foi adicionado a este e esfriado, e depois cloreto de metanossulfonila (0,5 g, 4,3 mmol) foi adicionado a este. Depois de 2 horas, diclorometano foi removido sob pressão reduzida e a cromatografia de coluna em gel de sílica do resíduo remanescente foi realizada para dar o composto do título do sólido branco (0,67 g, 27 %).
[0071] 1H RMN (DMSO-d6) : 7,93 (m, 2H), 7,64 (m, 2H), 7,20 (m, 4H), 3,97 (t, 2H), 3,17 (m, 4H), 290 (s, 3H), 2,89 (m, 4H), 1,97 (m, 2H), 1,85 (m, 2H), 1,61 (s, 4H); Exemplo 13 N-(4-{benzil-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il) propil]amino}butil)-N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il) propil]acetamida (Composto 13)
[0072] 3-3-[4-({N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il) propil]-N-benzil}-amino)butilamino]propil-1H-quinazolino-2,4-diona (0,28 g, 0,48 mmol) foi dissolvida em 5 ml de diclorometano. A trietilamina (0,13 ml, 0,96 mmol) e anidrido acético (0,06 ml, 0,58 mmol) foram adicionados a este e agitados por 1 hora. A camada orgânica foi separada pela adição de água e secada com sulfato de magnésio. Depois da filtração e concentração, a cromatografia de coluna em gel de sílica do resíduo remanescente foi realizada para dar o composto do título do forma oleosa (0,12 g, 40 %).
[0073] 1H RMN (MeOD) : 7,96 (t, 2H), 7,58 (m, 2H), 7,32 (d, 2H), 7,25 - 7,06 (m, 7H), 4,01 (m, 4H), 3,64 - 3,59 (s, 2H), 3,41 (m, 4H), 3,29 (s, 2H), 2,54 (m, 4H), 2,09 - 2,04 (s, 3H), 1,98 - 1,85 (m, 4H), 1,63 - 1,49 (m, 4H); Exemplo 14 Éster etílico do ácido (4-{acetil-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]amino}butil)-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]- carbâmico (Composto 14)
[0074] No Exemplo 4 acima, o sal do ácido clorídrico de N-[3-(2,4- dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-{4-[3-(2,4-dioxo-1,4-diidro- 2H -quinazolin-3-il)propilamino]butil}acetamida 3 g (5,3 mmol) e cloroformiato de etila 0,6 ml (6,3 mmol) foi usado, ao invés do 3-(3-4-[3-(2,4- dioxo-1,4-diidro-2H-quinazolin-3-il)propilamino]butilaminopropil)-1H- quinazolino-2,4-diona e anidrido acético. O mesmo procedimento do Exemplo 4 acima foi realizado para dar o composto do título do sólido branco (1,1 g, 34 %) no solvente misto de piridina e diclorometano.
[0075] 1H RMN (CDCl3) : 10,40 (d, 2H), 8,06 (m, 2H), 7,56 (m, 2H), 7,17 (m, 4H), 4,10 (m, 6H), 3,50 - 3,30 (m, 8H), 2,10 (s, 3H), 1,97 (m, 4H), 1,55 (d, 4H), 1,21 (s, 3H); Exemplo 15 3-[3-(4-{N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-benzil- amino}butil)-N-benzilamino]propil-1H-quinazolino-2,4-diona (Composto 15)
[0076] No Exemplo 9 acima, o composto do título (0,4 g, 15 %) foi obtido pela filtração sólidos brancos formados pela reação de 15 horas.
[0077] 1H RMN (DMSO-d6) : 7,88 (d, 2H), 7,61 (t, 2H), 7,27 - 7,13 (m, 14H), 3,88 (t, 4H), 3,46 (s, 4H), 2,39 (t, 4H), 2,99 (s, 4H), 1,72 (m, 4H), 1,36 (s, 4H); Exemplo 16 Éster etílico do ácido [3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-(4- {[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil] etoxicarbonilamino}- butil)carbâmico (Composto 16)
[0078] 3-(3-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propilamino]butilamino}-propil)-1H-quinazolino-2,4-diona (2 g, 4,1 mmol) foi dissolvida em 40 ml de piridina e cloroformiato de etila (0,46 ml , 4,9 mmol) foi adicionada a este. Depois de 2 horas, a piridina foi removida sob pressão reduzida e o diclorometano e água foram adicionados ao resíduo remanescente. Depois cada camada foi separada, diclorometano foi removido e a cromatografia de coluna em gel de sílica do resíduo remanescente foi realizada para dar o composto do título do sólido amarelo (0,61 g, 24 %).
[0079] 1H RMN (DMSO-d6) : 8,09 (d, 2H), 7,58 (t, 2H), 7,20 (t, 2H), 7,12 (d, 2H), 4,09 (m, 8H), 3,35 - 3,25 (m, 8H), 1,96 (m, 4H), 1,52 (s, 4H), 1,21 (t, 6H); Exemplo 17 Éster terc-butílico do ácido (4-{terc-butoxicarbonil-[3-(2,4-dioxo-1,4-diidro- 2H-quinazolin-3-il)propil]-amino}butil)-[3-(2,4-dioxo-1,4-diidro-2H- quinazolin-3-il)propil]carbâmico (Composto 17)
[0080] No Exemplo 11 acima, o composto do título do sólido branco (0,3 g, 11 %) foi obtido tomando-se uma outra fração da cromatografia de coluna em gel de sílica.
[0081] 1H RMN (CDCl3) : 10,08 (bs, 2H), 8,09 (d, 2H), 7,56 (t, 2H), 7,19 (t, 2H), 7,12 (d, 2H), 4,05 (m, 4H), 3,30 - 3,20 (m, 8H), 1,94 (t, 4H), 1,51 (s, 4H), 1,42 (t, 18H); Exemplo 18 N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-(4-{[3-(2,4-dioxo- 1,4-diidro-2H-quinazolin-3-il)propil]metanossulfonilamino} butil)metano- sulfonamida (Composto 18)
[0082] No Exemplo 12 acima, o composto do título do sólido branco (0,24 g, 9,1 %) foi obtido tomando-se uma outra fração da cromatografia de coluna em gel de sílica.
[0083] 1H RMN (DMSO-d6) : 11,36 (s, 2H), 7,90 (d, 2H), 7,62 (t, 2H), 7,16 (m, 4H), 3,90 (t, 4H), 3,21 - 3,13 (m, 8H), 2,88 (s, 6H), 1,84 (m, 4H), 1,56 (t, 4H); Exemplo 19 N-[3-(acetil-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propilamino]- butil}amino)propil]-4-hidroxibenzamida (Composto 19)
[0084] N-(3-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il) propilamino]butil-amino}propil)-4-hidroxibenzamida (1,27 g, 2,72 mmol) foi dissolvida em 10 ml de piridina e anidrido acético (0,4 ml , 4,07 mmol) foi adicionado a este. Depois de 2 horas, a piridina foi removida pela destilação sob pressão reduzida e o diclorometano e água foram adicionados a este. A camada orgânica foi separada e removida. Depois da concentração sob pressão reduzida, o resíduo remanescente foi tratado pela cromatografia de coluna em gel de sílica e resina de troca iônica para dar o composto do título da forma oleosa (0,06 g, 4,3 %).
[0085] 1H RMN (MeOD) : 8,00 (d, 1H), 7,70 (d, 2H), 7,63 (t, 1H), 7,21 (t, 1H), 7,16 (d, 1H), 6,08 (d, 2H), 4,09 (t, 2H), 3,39 (m, 6H), 2,77 (m, 4H), 2,12 - 2,09 (s, 3H), 1,99 - 1,82 (m, 4H), 1,59 (m, 4H); Exemplo 20 N-[3-(4-{acetil-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]amino}- butilamino)propil]-4-hidroxibenzamida (Composto 20)
[0086] No Exemplo 19 acima, o composto do título da forma oleosa (0,06 g, 4,0 %) foi obtido tomando-se uma outra fração da cromatografia de coluna em gel de sílica e tratando a fração com a resina de troca iônica CG- 50.
[0087] 1H RMN (MeOD) : 7,99 (m, 1H), 7,70 (d, 2H), 7,61 (m, 1H), 7,17 (m, 2H), 6,80 (d, 2H), 4,01 (m, 2H), 3,42 (m, 6H), 2,87 (m, 4H), 2,10 (s, 3H), 1,97 - 1,90 (m, 4H), 1,64 (m, 4H); Exemplo 21 N-{3-[acetil-(4-{acetil-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]- amino}butil)amino]propil}-4-hidroxibenzamida (Composto 21)
[0088] No Exemplo 19 acima, o composto do título do sólido branco (0,53 g, 35,4 %) foi obtido tomando-se uma outra fração da cromatografia de coluna em gel de sílica.
[0089] 1H RMN (MeOD) : 7,98 (t, 1H), 7,70 (dd, 2H), 7,60 (m, 1H), 7,15 (m, 2H), 3,99 (m, 2H), 3,42 - 3,30 (m, 10H), 2,09 (t, 3H), 2,07 ®t, 3H) 1,92 - 1,78 (m, 4H), 1,55 (m, 4H); Exemplo 22 N-[4-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)butil]-N-[3-(2,4-dioxo-1,4- diidro-2H-quinazolin-3-il)propil]acetamida (Composto 22)
[0090] No Exemplo 4 acima, 3-{4-[3-(2,4-dioxo-1,4-diidro-2H-quina- zolin-3-il)propilamino]butil}-1H-quinazolino-2,4-diona (1 g, 2,3 mmol) foi usada ao invés da 3-(3-4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil- amino]butilaminopropil)-1H-quinazolino-2,4-diona. O mesmo procedimento do Exemplo 4 acima foi realizado para dar o composto do título do sólido branco (0,89 g, 81 %) no solvente misto de piridina e diclorometano.
[0091] 1H RMN (MeOD) : 7,98 (m, 2H), 7,60 (m, 2H), 7,16 (m, 4H),4,02 (m, 4H), 3,42 (m, 4H), 2,09 (d, 3H), 1,95 (m, 2H), 1,64 (m, 4H); Exemplo 23 3-(2-{3-[2-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il) etilamino]propilamino}- etil)-1H-quinazolino-2,4-diona (Composto 23)
[0092] No Exemplo 7 acima, N,N’-bis(2-aminoetil)-1,3- propanodiamina 2,4 g (14,8 mmol) foi usada ao invés de N-(3-aminopropil) butano-1,4-diamina. O mesmo procedimento do Exemplo 7 acima foi realizado para dar o composto do título do sólido amarelo (3,7 g, 55 %).
[0093] 1H RMN (DMSO-d6) : 7,88 (d, 2H), 7,59 (t, 2H), 7,14 (m, 4H), 3,92 (t, 4H), 2,65 (t, 4H), 2,47 (m, 4H), 1,92 - 1,78 (m, 4H), 1,43 (m, 2H); Exemplo 24 3-(3-{3-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propilamino]propil- amino}propil)-1H-quinazolino-2,4-diona (Composto 24)
[0094] No Exemplo 7 acima, N,N’-bis(3-aminopropil)-1,3-propano- diamina 2,8 g (14,8 mmol) foi usada ao invés de N-(3-aminopropil)butano- 1,4-diamina. O mesmo procedimento do Exemplo 7 acima foi realizado para dar o composto do título do sólido branco (2,9 g, 41 %).
[0095] 1H RMN (DMSO-d6) : 7,91 (d, 2H), 7,63 (t, 2H), 7,17 (m, 4H), 3,92 (t, 4H), 2,49 (t, 8H), 1,70 (m, 4H), 1,49 (m, 2H); Exemplo 25 3-(3-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propilamino]-2-butenil- amino}propil)-1H-quinazolino-2,4-diona (Composto 25)
[0096] No Exemplo 7 acima, N,N’-bis(3-aminopropil)-2-buteno-1,4- diamina 2,96 g (14,8 mmol) foi usada ao invés de N-(3-aminopropil)butano- 1,4-diamina. O mesmo procedimento do Exemplo 7 acima foi realizado para dar o composto do título do sólido branco (4,5 g, 62 %).
[0097] 1H RMN (DMSO-d6) : 7,91 (d, 2H), 7,63 (t, 2H), 7,17 (m, 4H), 5,51 (s, 2H), 3,91 (t, 4H), 3,06 (s, 4H), 2,47 (m, 4H), 1,68 (m, 4H); Exemplo 26 Éster terc-butílico do ácido (4-{terc-butoxicarbonil-[3-(1-metil-2,4-dioxo-1,4- diidro-2H-quinazolin-3-il)propil]amino}butil)-[3-(1-metil-2,4-dioxo-1,4- diidro-2H-quinazolin-3-il)-propil]carbâmico (Composto 26)
[0098] Éster terc-butílico do ácido (4-{terc-butoxicarbonil-[3-(2,4- dioxo-1,4-diidro-2H-quinazolin-3-il)propil]amino}butil)-[3-(2,4-dioxo-1,4- diidro-2H-quinazolin-3-il)propil]carbâmico (2 g, 2,9 mmol) foi dissolvido em 10 ml de tetraidrofurano e 10 ml de diclorometano e esfriado. O Hidreto de sódio (0,2 g, 8,3 mmol) e iodeto de metila (0,6 ml , 9,6 mmol) foram adicionados a este e agitados por 2 horas. Depois que o solvente foi concentrado sob pressão reduzida, a cromatografia de coluna em gel de sílica do resíduo remanescente foi realizada para dar o composto do título do forma oleosa (1,9 g, 91 %).
[0099] 1H RMN (CDCl3) : 8,21 (d, 2H), 7,66 (t, 2H), 7,24 (t, 2H), 7,18 (d, 2H), 4,09 (t, 4H), 3,59 (s, 6H), 3,26 - 3,19 (m, 8H), 1,91 (m, 4H),1,48 (s, 4H), 1,40 (s, 1H); Exemplo 27 Sal do ácido diclorídrico de 1-metil-3-(3-{4-[3-(1-metil-2,4-dioxo-1,4-diidro- 2H-quinazolin-3-il)propilamino]butilamino}propil)-1H-quinazolino-2,4-diona (Composto 27)
[00100] Éster terc-butílico do ácido (4-{terc-butoxicarbonil-[3-(1- metil-2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]amino}butil)-[3-(1- metil-2,4-dioxo-1,4-di-hidro-2H-quinazolin-3-il)propil]carbâmico (1,8 g, 2,5 mmol) foi dissolvido em 20 ml de metanol, o ácido clorídrico concentrado foi adicionado a este e agitado. Depois metanol foi concentrado, o composto do título do sólido branco (1,3 g, 88 %) foi obtido pelo cristalização.
[00101] 1H RMN (D2O) : 7,81 (d, 2H), 7,71 (t, 2H), 7,25 (t, 2H), 7,19 (d, 2H), 4,07 (t, 4H), 3,34 (s, 6H), 3,13 (m, 8H), 2,10 (m, 4H), 1,89 (s, 4H); Exemplo 28 Sal do ácido diclorídrico do 3-(3-{4-[3-(1,3-dioxo-1,3-diidro-isoindol-2-il)- propilamino]butilamino}propil)-1H-quinazolino-2,4-diona (Composto 28)
[00102] 3-{3-[4-(3-aminopropilamino)butilamino]propil}-1H- quinazolino-2,4-diona (1,06 g, 3,1 mmol) e ftalato de dietila (0,68 g, 3,1 mmol) foram adicionados e agitados de 125 ~ 130oC. Depois de 3 horas, 25 ml do álcool isopropílico e o ácido clorídrico concentrado foram adicionados a este para formar um sólido. A cromatografia de coluna em gel de sílica do sólido obtido pela filtração foi realizada para dar o composto do título do sólido branco (0,25 g, 15 %).
[00103] 1H RMN (D2O) : 7,77 (d, 1H), 7,71 (m, 4H), 7,61 (m, 1H), 7,19 (t, 1H), 6,99 (d, 1H), 3,98 (t, 2H), 3,71 (t, 2H), 3,10 M, 8H), (2,06 (m, 4H), 1,81 (s, 4H); Exemplo 29 Sal do ácido diclorídrico do 3-(3-{2-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin- 3-il)propilamino]etilamino}propil)-1H-quinazolino-2,4-diona (Composto 29)
[00104] No Exemplo 7 acima, N,N’-bis(3-aminopropil)etilenodiamina (2,5 g, 14,3 mmol) foi usada ao invés de N-(3-aminopropil)butano-1,4- diamina. O mesmo procedimento do Exemplo 7 acima foi realizado para formar um sólido e o ácido clorídrico concentrado foi depois tratado para dar o composto do título do sólido branco (1,5 g, 9,5 %) em metanol.
[00105] 1H RMN (D2O) : 7,91 (d, 2H), 7,64 (m, 2H), 7,25 (m, 2H), 7,07 (d, 2H), 4,07 (t, 4H), 3,48 (s, 4H), 3,21 (t, 4H), 2,12 (m, 4H); Exemplo 30 Éster terc-butílico do ácido [3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]-(4-{[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il) propil]hexilamino}-butil)carbâmico (Composto 30)
[00106] Éster terc-butílico do ácido [3-(2,4-dioxo-1,4-diidro-2H- quinazolin-3-il)propil]-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propilamino]butil}-carbâmico (2 g, 3,4 mmol) foi dissolvido em 40 ml de tetraidrofurano. O hidreto de sódio (0,16 g, 6,7 mmol) e 1-bromo-hexano (0,67 g, 4,0 mmol) foram adicionados a este e agitados sob o refluxo. O solvente foi concentrado sob pressão reduzida, e a cromatografia de coluna em gel de sílica do resíduo remanescente foi realizada para dar o composto do título do sólido branco (0,52 g, 23 %).
[00107] 1H RMN (MeOD) : 7,99 (m, 2H), 7,61 (m, 2H), 7,20 (m, 2H), 7,12 (dd, 2H), 4,04 (m, 4H), 3,26 (m, 4H), 2,74 (m, 6H), 1,93 (m, 4H), 1,54 (m, 6H), - 1,40 (s, 9H), 1,29 (s 6H), 0,88 (t, 3H); Exemplo 31 Sal do ácido diclorídrico do 3-[3-(4-{N-[3-(2,4-dioxo-1,4-diidro-2H- quinazolin-3-il)propil]-N-hexilamino}butilamino)propil]-1H-quinazolino-2,4- diona (Composto 31)
[00108] Éster terc-butílico do ácido [3-(2,4-dioxo-1,4-diidro-2H- quinazolin-3-il)-propil](4-{[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il) propil]hexil-amino}-butil)carbâmico 0,4 g (0,6 mmol) foi desprotegido pelo mesmo procedimento do exemplo 27 acima e separado pela cromatografia para dar o composto do título do sólido branco (0,1 g, 26 %).
[00109] 1H RMN (MeOD) : 7,97 (m, 2H), 7,60 (m, 2H), 7,20 (m, 2H), 7,11 (t, 2H), 4,13 (t, 2H), 4,04 (t, 2H), 3,04 (m, 4H), 2,75 (t, 2H), 2,67 (m, 4H), 2,10 (m, 2H) 1,91 (m, 2H), 1,79 (m, 2H), 1,70 (m, 2H), 1,55 (m, 2H), 1,30 (m, 6H), 0,88 (t, 3H); Exemplo 32 Éster terc-butílico do ácido (4-{terc-butoxicarbonil-[3-(1-hexil-2,4-dioxo-1,4- diidro-2H-quinazolin-3-il)propil]amino}butil)-[3-(1-hexil-2,4-dioxo-1,4-di- hidro-2H-quinazolin-3-il)propil]carbâmico (Composto 32)
[00110] Éster terc-butílico do ácido (4-{terc-butoxicarbonil-[3-(2,4- dioxo-1,4-diidro-2H-quinazolin-3-il)propil]amino}butil)-[3-(2,4-dioxo-1,4- diidro-2H-quinazolin-3-il)propil]carbâmico (3 g, 4,3 mmol) foi dissolvido em 120 ml de acetonitrila. Carbonato de potássio (3,45 g, 25,0 mmol) e 1- bromoexano (3,5 g, 21,1 mmol) foram adicionados a este e agitados por 3 horas sob refluxo. O solvente foi concentrado sob pressão reduzida, e a cromatografia de coluna em gel de sílica do resíduo remanescente foi realizada para dar o composto do título da forma oleosa incolor (3,7 g, 99 %).
[00111] 1H RMN (CDCl3) : 8,13 (d, 2H), 7,57 (t, 2H), 7,14 (t, 2H), 7,09 (d, 2H), 4,01 (m, 8H), 3,13 (m, 8H), 1,84 (m, 4H), 1,64 (m, 4H), 1,36 (s, 18H), 1,41 - 1,25 (m, 16H) 0,82 (t, 6H); Exemplo 33 Sal do ácido diclorídrico do 1-hexil-3-(3-{4-[3-(1-hexil-2,4-dioxo-1,4-diidro- 2H-quinazolin-3-il)propilamino]butilamino}propil)-1H-quinazolino-2,4-diona (Composto 33)
[00112] Éster terc-butílico do ácido (4-{terc-butoxicarbonil-[3-(1- hexil-2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]amino}butil)-[3-(1- hexil-2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]carbâmico (2 g, 2,3 mmol) foi desprotegido pelo mesmo procedimento como o do Exemplo 27 acima e cristalizado em etanol para dar o composto do título do sólido branco (1,07 g, 63 %).
[00113] 1H RMN (MeOD) : 8,15 (d, 2H), 7,78 (m, 2H), 7,43 (d, 2H), 7,30 (t, 2H), 4,17 (m, 8H), 3,09 (t, 8H), 2,12 (m, 4H), 1,84 (s, 4H), 1,72 (m, 4H), 1,45 - 1,35 (m, 12H), 0,91 (t, 6H); Exemplo 34 Éster terc-butílico do ácido [3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)- propil]-(4-{[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il) propil]heptanoil- amino}butil)carbâmico (Composto 34)
[00114] Éster terc-butílico do ácido [3-(2,4-dioxo-1,4-diidro-2H- quinazolin-3-il)propil]-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propilamino]butil}-carbâmico (0,4 g, 0,7 mmol) foi reagido com anidrido heptanóico (0,2 g, 0,8 mmol) ao invés de anidrido acético do Exemplo 4 acima. O composto do título do sólido branco (0,37 g, 88 %) foi obtido pelo mesmo procedimento como o Exemplo 4 acima.
[00115] 1H RMN (CDCl3) : 8,10 (m, 2H), 7,58 (m, 2H), 7,26 - 7,10 (m, 4H), 4,08 (m, 4H), 3,49 - 3,23 (m, 8H), 2,28 (t, 2H), 1,95 (m, 4H), 1,66 - 1,05 (m, 6H), 1,43 (d, 9H), 1,27 (m, 6H), 0,87 (m, 3H); Exemplo 35 O sal do ácido clorídrico da amida do ácido [3-(2,4-dioxo-1,4-diidro-2H- quinazolin-3-il)propil]-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propilamino]butil}-heptanoíco (Composto 35)
[00116] Usando éster terc-butílico do ácido [3-(2,4-dioxo-1,4-diidro- 2H-quinazolin-3-il)propil]-(4-{[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)- propil]heptanoilamino}butil)carbâmico (0,36 g, 0,5 mmol), o composto do título do sólido branco (0,2 g, 61 %) foi obtido pelo mesmo procedimento como o Exemplo 31 acima.
[00117] 1H RMN (MeOD) : 8,01 (m, 2H), 7,63 (m, 2H), 7,23 - 7,13 (m, 4H), 4,14 (t, 2H), 4,05 (m, 2H), 3,45 (m, 4H), 3,02 (m, 4H), 2,35 (m, 2H), 2,10 - 1,95 (m, 4H), 1,76 - 1,55 (m, 6H), 1,27 (m, 6H), 0,87 (m, 3H); Exemplo 36 O sal do ácido clorídrico da N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]-N-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)- propilamino]butil}-2,2,2-trifluoroacetamida (Composto 36)
[00118] No Exemplo 3 acima, trifluoroanidrido acético 1,5 g (7,3 mmol) foi usado ao invés de anidrido acético, e o composto do título do sólido amarelo (0,6 g, 15,8 %) foi obtido pelo mesmo procedimento como o Exemplo 3 acima.
[00119] 1H RMN (MeOD) : 8,00 (m, 2H), 7,63 (m, 2H), 7,25 7,13 (m, 4H), 4,14 (m, 2H), 4,06 (m, 2H), 3,54 (m, 4H), 3,01 (m, 4H), 2,07 (m, 4H), 1,74 (m, 4H); Exemplo 37 N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-{4-[[3-(2,4-dioxo- 1,4-diidro-2H-quinazolin-3-il)propil]-(2,2,2-trifluoroacetil)amino]butil}- 2,2,2-trifluoroacetamida (Composto 37)
[00120] O composto do título do sólido branco (1,1 g, 26,4 %) foi obtido tomando-se uma outra fração da cromatografia de coluna em gel de sílica e sólido formado no Exemplo 36 acima.
[00121] 1H RMN (MeOD) : 8,01 (m, 2H), 7,62 (m, 2H), 7,23 - 7,12 (m, 4H), 4,03 (m, 4H), 3,50 (m, 8H), 2,01 (m, 4H), 1,65 (m, 4H); Exemplo 38 O sal do ácido clorídrico da N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propil]-N-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)- propilamino]butil}-2-metoxiacetamida (Composto 38)
[00122] O material de partida do Exemplo 5 acima 0,5 g (1,0 mmol) e cloreto de metoxiacetila (0,12 g, 1,1 mmol) ao invés de cloroformiato de etila foi usado. O mesmo procedimento do Exemplo 5 acima foi realizado para dar o composto do título do sólido branco (0,1 g, 16,4 %).
[00123] 1H RMN (MeOD) : 8,00 (m, 2H), 7,63 (m, 2H), 7,23 - 7,12 (m, 4H), 4,14 (m, 4H), 4,05 (m, 2H), 3,48 - 3,32 (m, 7H), 3,01 (m, 4H), 2,12201 (m, 4H), 1,70 (m, 4H); Exemplo 39 O sal do ácido clorídrico do éster benzílico do ácido [3-(2,4-dioxo-1,4-diidro- 2H-quinazolin-3-il)propil]-{4-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3- il)propilamino]butil}carbâmico (Composto 39)
[00124] O cloroformiato de benzila 1,05 g (6,1 mmol) ao invés de anidrido acético do Exemplo 3 acima foi usado, e o mesmo procedimento do Exemplo 3 acima foi realizado para dar o composto do título do sólido amarelo (0,34 g, 8,4 %).
[00125] 1H RMN (MeOD) : 8,00 (m, 2H), 7,63 (m, 2H), 7,33 - 7,19 (m, 7H), 7,13 (t, 2H), 5,08 (s, 2H), 4,13 (t, 2H), 4,00 (m, 2H), 3,41 (m, 4H), 3,00 - 2,92 (m, 4H), 2,06 (m, 2H), 1,96 (m, 2H), 1,69 (bs, 4H); Exemplo 40 N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-{4-[3-(2,4-dioxo- 1,4-diidro-2H-quinazolin-3-il)propilamino]butil}-4- metilbenzenossulfonamida (Composto 40)
[00126] Ao invés de cloreto de metanossulfonila do Exemplo 12 acima, cloreto de p-toluenossulfonila 1,4 g (7,3 mmol) foi usado. O mesmo procedimento do Exemplo 12 acima foi realizado em metanol e depois resina de troca iônica CG-50 foi tratada para dar o composto do título do sólido branco (0,3 g, 8 %).
[00127] 1H RMN (MeOD) : 8,95 (d, 2H), 7,64 (d, 2H), 7,58 (m, 2H), 7,33 (d, 2H), 7,18 - 7,08 (m, 4H), 4,02 (t, 4H), 3,23 (t, 2H), 3,15 (t, 2H), 2,55 (q, 4H), 2,39 (s, 3H), 1,89 (m, 4H), 1,63 (m, 2H), 1,532(m, 2H); Exemplo 41 N-[3-(2,4-dioxo-1,4-diidro-2H-quinazolin-3-il)propil]-N-(4-{[3-(2,4-dioxo- 1,4-diidro-2H-quinazolin-3-il)propil]-4-metilbenzenossulfonilamino}butil)-4- metilbenzonossulfonamida (Composto 41)
[00128] No Exemplo 40 acima, o composto do título do sólido branco (1,27 g, 26 %) foi obtido tomando-se uma outra fração da cromatografia de coluna em gel de sílica.
[00129] 1H RMN (DMSO-d6) : 11,40 (s, 2H), 7,90 (d, 2H), 7,62 (m, 6H), 7,32 (m, 4H), 7,17 (m, 4H), 3,86 (t, 4H), 3,08 (m, 8H), 2,35 (s, 6H), 1,75 (m, 4H), 1,42 (s, 4H); Exemplo 42 Sal do ácido diclorídrico do 3-(3-{4-[3-(2,5-dioxo-pirrolidino-1- il)propilamino]butilamino}propil)-1H-quinazolino-2,4-diona (Composto 42)
[00130] O material de partida 1,5 g (4,3 mmol) do Exemplo 28 acima foi usado, e o anidrido succínico (0,43 g, 4,33 mmol) ao invés de ftalato de dietila foi usado. O mesmo procedimento do Exemplo 28 acima foi realizado para dar o composto do título do sólido amarelo (0,23 g, 11 %).
[00131] Será explicado em detalhes que o composto da fórmula (I) acima de acordo com a presente invenção tem excelentes efeitos como um agente neuro-protetor, pelos Exemplos que seguem usando os compostos preparados pelos Exemplos acima.
[00132] Os Exemplos Experimentais que seguem são apresentados para ajudar no entendimento da invenção, e não devem ser interpretados como limitando de nenhum modo a invenção apresentada nas reivindicações que seguem a seguir. <Exemplo Experimental 1> Experimento do efeito anti-derrame no modelo da oclusão da artéria cerebral média (MCAO)
[00133] Ratos machos da espécie SD com 290 a 300 g de peso corporal foram usados como animais de laboratório, e 8 ratos foram usados em cada grupo experimental. A operação foi realizada usando-se o método de Nagasawa ET AL. (Nagasawa, H. e Gogure, K. 1989, Stroke, 20: 1037-1043).
[00134] Os ratos foram anestesiados por Cetamina, e a operação foi realizada conforme a temperatura corporal foi mantida usando termoplaca. A região cerebral foi incisada a seguir da linha mediana do pescoço, e a artéria carótida comum esquerda, a artéria carótida interna e a artéria carótida externa foram separadas, tomando o cuidado para não danificar o nervo vago. A artéria carótida comum e a artéria carótida externa foram ligadas, e uma sonda foi inserida na artéria carótida interna a partir do ponto de ramificação das artérias carótidas interna e externa. E depois o fundo da artéria cerebral mediana foi ocluído pela ligadura exatamente no lado superior da região de inserção. Uma sonda foi fabricada aquecendo-se a extremidade de uma sutura cirúrgica de náilon 4-0 (Dafilon, B. Braun, Alemanha) e cortada em 30 mm. A extremidade de 7 a 9 mm da sonda foi revestida com a mistura de silício (Xantopren VL plus, Heraeus Kulzer, Alemanha) e agente de cura (Optosil- Xantopren VL plus, Heraeus Kulzer, Alemanha), e a espessura foi para ser de 0,3 a 0,4 mm. Depois da intervenção da inserção de sonda e os animais saíram do anestésico, indivíduos em que o sintoma de déficit neurológico (circular na direção certa) foi observado foram incluídos no grupo de isquemia.
[00135] Depois de 3 horas de isquemia, a sonda inserida foi removida para reperfusar a circulação sanguínea. O cérebro foi extraído depois de 24 horas, seguido por tingimento histológico.
[00136] O composto 3 foi administrado em um tempo programado antes ou depois da inserção da sonda com a administração oral ou intravenosa. O tingimento com TTC (cloreto de 2,3,5-trifeniltetrazólio) foi realizado para estimar o dano de tecido cerebral pela isquemia. O procéfalo do cérebro extraído foi fatiado em 2 mm de fatias sequenciais usando-se matriz cerebral (ASI instrument, Warren, MI, USA). As fatias foram colocadas em 2 % de solução de TTC e incubadas a 37° por 60 minutos para tingimento. As fatias de cérebro tingido com TTC foi fixada em 10 % de tampão de formalina e a frente de cada fatia foi fotografada com uma câmara digital. As áreas infartadas (cm2) que não foram tingidas com vermelho profundo em cada imagem adquirida foi medida usando um analisador de imagem, e o volume infartado total (cm3) foi calculado multiplicando-se a espessura das fatias.
[00137] Como um resultado, a administração oral (100 mg/kg) de composto 3 mostrou o efeito inibidor que a porcentagem de volume cerebral infartado foi de 22,3 % e 69,8 % comparado com o controle negativo pela administração oral feita por uma hora e exatamente antes da indução do derrame. Citicolina (2 g/kg) administrada como um controle positivo foi observada 51,1 e 37,8 % cada um (Tabela 1 e Figura 1).
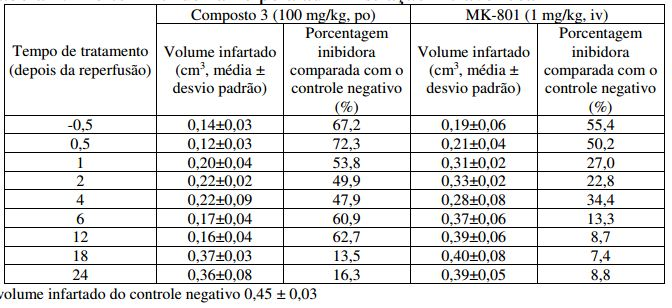
[00138] No experimento, a sonda foi removida depois da indução do derrame de modo que a circulação foi reperfusada. O Composto 3 foi depois administrado em um tempo dividido com 5 mg/kg de dose, o efeito inibidor do volume de necrose de 62,7 % foi observado mesmo que a administração foi realizada 12 horas depois da reperfusão. Por outro lado, MK-801 administrado como um controle positivo mostrou o efeito máximo em 30 minutos depois da reperfusão (Tabela 2). Portanto, o Composto 3 tem efeitos óbvios sobre a prevenção e tratamento de derrame, e também pode ser aplicado aos pacientes cujo tratamento foi demorado depois do início do derrame. Tabela 1. Efeito anti-derrame pela administração oral
Tabela 2. Efeito Anti-derrame pela administração intravenosa
<Exemplo Experimental 2> Efeito inibidor da neurotoxicidade excitável em cultura mista das células nervosas-células gliais
[00139] A isolação e cultura das células nervosas foi realizada pelo método de Choi (Choi, D. W. 1985, Neurosci. Lett., 58: 293-297). Isto é, o córtex foi isolado no feto de camundongo ICR que foi 14 dias prenhe, e depois células únicas foram obtidas do tecido usando pipeta. As células foram aliquotadas na densidade de 2 x 105/reservatório em uma placa de 24 reservatórios (Falcon) em que as células gliais do córtex cerebral foram cultivadas em um incubador mantido a 37° com 5 % de CO2 por mais de 3 semanas. O meio de cultura foi suplementado com MEM (meio essencial mínimo, Sigma), 2 mM de glutamina, 21 mM de glicose, 26,5 mM de bicarbonato, 10 % de soro bovino fetal (FBS). Em 3 a 5 dias depois da alíquota, 10 μM de Ara-C (citosina arabinosida) foi tratada para suprimir a proliferação de neuroglia. E a mesma foi tratada com 100 μM de NMDA e 1^/ml ou 2^/ml de cada amostra (composto) para induzir a morte das células nervosas devido à toxicidade excitável por 20 minutos, em 12 a 15 dias depois da alíquota. Por causa da morte das células nervosas, a lactato desidrogenase (LDH) acumulou em proporção a várias células mortas. Em 24 horas depois do tratamento com medicamento, a quantidade de desidrogenase (LDH) liberada fora das células foi medida usando-se um kit de medição de LDA (CytoTox 96, Promega). Depois que a reação foi completada, a mudança da absorbância dependendo da quantidade de LDH foi medida usando-se um espectrofotômetro de microplaca.
[00140] O efeito inibidor sobre a morte de célula comparado com o controle negativo foi mostrado na Tabela 3, e mostrou um efeito significante. Tabela 3. Efeito protetivo sobre a morte das células nervosas induzida por NMDA em cultura mista das células nervosas-células gliais
<Exemplo Experimental 3> Efeito inibidor sobre a citotoxicidade mediada pelo H2O2 em células SH-SY5Y
[00141] As células SH-SY5Y que são orientadas pela linhagem de célula nervosa de seres humanos foi cultivada com concentração de 3 x 104 células em placas de 96 reservatórios, e a amostra foi tratada. Depois de 30 minutos, 200 μM de peróxido de hidrogênio foi tratado para induzir a toxicidade por 24 horas. Depois que a reação foi completada, a taxa de sobrevivência das células foi medida pelo ensaio de MTT.
[00142] Como um resultado, foi identificado que a taxa de sobrevivência de células SH-SY5Y foi positivamente correlacionada com a concentração do Composto 4, e isto mostrou cerca de 35 % do efeito protetivo sobre as células na concentração de 100 μg/ml (Tabela 4). Tabela 4. Efeito inibidor sobre a toxicidade oxidativa induzida pelo hidroperóxido Concentração Porcentagem Inibidora (%)
<Exemplo Experimental 4> Efeito inibidor sobre a toxicidade mediada pelo ZnSO4 em células SH-SY5Y
[00143] As células SH-SY5Y foram cultivadas com concentração de 3 x 104 células em placas de 96 reservatórios, e o composto (50 μg/ml) foram tratadas. Depois de 30 minutos, 600 μM de sulfato de zinco foi tratado para induzir citotoxicidade por 24 horas e a taxa de sobrevivência das células foi medida pelo ensaio de MTT. O resultado mostrou um efeito inibidor de 9,1 a 21,7 % sobre a toxicidade (Tabela 5). Tabela 5. Efeito inibidor sobre a toxicidade induzida pelo zinco Composto Porcentagem Inibidora
<Exemplo Experimental 5> Efeito inibidor sobre a produção de ROS em células cerebrais
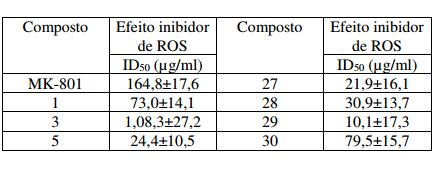
[00144] O estresse oxidativo foi medido para testar os efeitos inibidores sobre a produção de espécie de oxigênio reativo (ROS) pelo uso de DCF-DA, que é uma sonda fluorescente. As células cerebrais foram obtidas a partir do córtex cerebral de camundongo para preparar solução de célula com 2 x 106 células/ml. Cada célula cerebral foi tratada com 11 μM de DCF-DA seguido pela reação em incubador a 37°, 5 % de CO2 por uma hora. Depois de lavar duas vezes, O composto 3 foi tratado com uma concentração de 125 μ/ml e 250 μ/ml. Ao mesmo tempo, 300 μM de NMDA foram tratados e os mesmos foram incubados em incubador a 37°, 5 % de CO2 por 24 horas. Depois que a reação foi completada, a fluorescência quer mostrou oxigênio reativo em solução de reação foi medida usando-se espectrofotômetro de fluorescência (excitação 480 nm/emissão, 535 nm). Como um resultado, o Composto 3 suprime o estresse oxidativo induzido por NMDA das células nervosas em uma maneira dependente da dose (Figura 2).
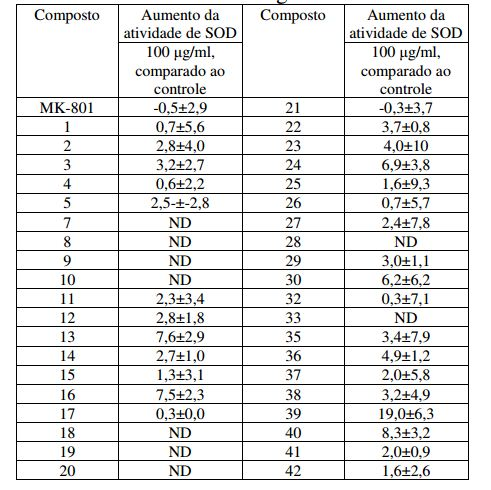
[00145] O efeito inibidor de ROS dos compostos foi representado para a dose que suprime 50 % da produção de oxigênio reativo comparada com o controle. Foi observado aumentar a atividade da superóxido dismutase (SOD), uma enzima que desempenha um papel chave na produção de oxigênio reativo, e uma taxa de aumento foi representada comparada ao controle. A atividade da superóxido dismutase (SOD) foi medida usando-se um kit adquirido na Sigma. Como um resultado, a maioria dos compostos apresentaram doses mais baixas de ID50 comparada com MK-801, que é controle positivo. Isto indica que eles têm um efeito superior com doses mais baixas do que MK-801. Tabela 6. Efeito inibidor sobre a produção de ROS em células de cérebro de camundongo
Tabela 7. Efeito sobre o aumento da atividade de superóxido dismutase (SOD) em células de cérebro de camundongo
[00146] Efeitos antagonísticos dos compostos sobre o receptor de NMDA examinado nos Exemplos Experimentais 2 a 5 demonstraram que os compostos da presente invenção podem ser usados como um medicamento não apenas para tratar derrame isquêmico mas também para prevenir e tratar doença cerebral degenerativa relacionada com este receptor, tal como epilepsia, esclerose lateral amiotrófica (ALS), doença de Parkinson, doença de Huntington, doença de Alzheimer, e lesão cerebral traumática ou lesão da medula espinhal. Este também pode ser usado para melhorar a memória. <Exemplo Experimental 6> Experimento de efeito anti-convulsivo
[00147] Um experimento foi realizado pelo método de Ali ET AL. (Ali, A. ET AL. 2006, Pharmacological Reports, 58: 242-245). Uma dose de 10 mg/kg de composto foi intraperitonealmente administrada para identificar o efeito anti-convulsivo e o efeito foi observado (Tabela 8). Pesquisando o processo de atividade foi realizado pelo Programa de Desenvolvimento de Medicamento Anti-epiléptico (ADD) da NIH durante o desenvolvimento do medicamento anti-convulsivo. Um dos itens tratados de atividade anti- convulsiva na primeira etapa deste programa é o teste do pentilentetrazol (PTZ). Depois da administração do medicamento de teste, 80 mg/kg de dose de PTZ foram subcutaneamente administrados e foi observado por pelo menos 30 minutos. Depois que 20 mg/kg do medicamento de teste foram administrados, a avaliação foi realizada estimando-se o tempo de início da convulsão, duração até que a convulsão completamente desapareceu e taxa de mortalidade. O mesmo foi avaliado como tendo um efeito anti-convulsivo quando um único episódio de espasmo clônico não foi mostrado em 5 segundos no pelo menos um dos 4 animais de laboratório depois da administração de PTZ.


<Exemplo Experimental 7> Efeito relaxante sobre a aorta toráxica em ratos
[00148] Depois ratos machos da espécie SD (250 a 300 g) foram anestesiados pela inalação de éter, as suas aortas toráxicas foram extraídas e colocadas em tampão de Krebs (mM; NaCl 118, NaHCO3 27,3, KCl 4,8, MgSO4 1,2, KH2PO4 1,0, CaCl2 1,25, glicose 11,1). 2 mm de anel aórtico foram fabricados sob microscópio de dissecação e cultivados em um banho de órgão para medir a tensão dos vasos sanguíneos. O banho de órgão foi enchido com tampão de Krebs e saturado com 95 % de O2, 5 % de CO2 para manter o oxigênio dissolvido e o pH fisiológico. A mudança de tensão foi medida por um tensiômetro (Hugo-sachs, modelo K30) e registrada pelo registrador fisiológico (polígrafo Coulbourn). O comprimento dos vasos sanguíneos foi aumentado passo a passo para fazer 1,0 g de tensão basal por 90 minutos. O vaso sanguíneo equilibrado foi contraído pela fenilefrina (0,5 μM). Quando a ruga de contração atingiu o equilíbrio, os compostos foram adicionados, seguidos por observação da resposta de relaxação.
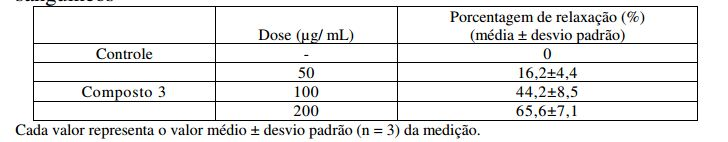
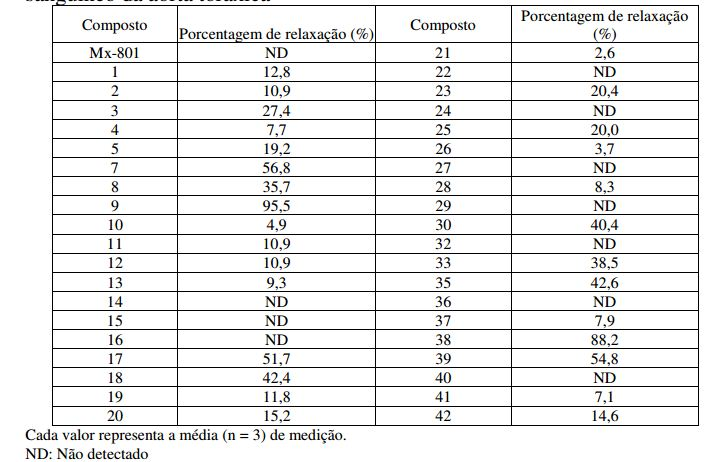
[00149] Um resultado que o Composto 3 foi adicionado com a dose de 50μg/ml, 100/gg/nil e 200gg/nil foi listado na Tabela 9, e o Composto 3 relaxou dependentemente da dose a aorta toráxica de ratos contraídas pela fenilefrina (Tabela 9). O resultado que cada composto foi administrado com uma dose de 67gg/ml foi listado na Tabela 10, e este resultado pode ser presumido retardar a morte da célula e induzir a restauração de células mortas devido ao aumento da corrente sanguínea pela expansão de um vaso sanguíneo em um corpo. Tabela 9. Efeito relaxante dependente da dose sobre os músculos dos vasos
Tabela 10. Efeito relaxante sobre os compostos sobre os músculos do vaso sanguíneo da aorta toráxica
[00150] Um efeito relaxante superior de músculos do vaso sanguíneo foi observado, comparado com controle na maioria dos compostos. APLICABILIDADE INDUSTRIAL
[00151] Como mencionado acima nos exemplos, os compostos da presente invenção mostram um efeito anti-derrame, efeito antagonístico sobre o receptor de NMDA, efeito inibidor sobre a toxicidade de H2O2 e toxicidade de ZnSO4 em células nervosas, efeito antioxidante nas células nervosas, efeito anti-convulsivo e efeito relaxante da aorta toráxica. Portanto, eles podem ser usados como um medicamento para impedir e tratar as várias doenças anteriormente mencionadas tais como derrame, distúrbio funcional do sistema nervoso, perda de memória, disfunção cerebrovascular, dano do cérebro e medula espinhal, isquemia cerebral, demência, doença de Alzheimer, doença de Parkinson e epilepsia.