BRPI0908417B1 - Composto, e, uso do composto - Google Patents
Composto, e, uso do composto Download PDFInfo
- Publication number
- BRPI0908417B1 BRPI0908417B1 BRPI0908417-7A BRPI0908417A BRPI0908417B1 BR PI0908417 B1 BRPI0908417 B1 BR PI0908417B1 BR PI0908417 A BRPI0908417 A BR PI0908417A BR PI0908417 B1 BRPI0908417 B1 BR PI0908417B1
- Authority
- BR
- Brazil
- Prior art keywords
- alkyl
- compound
- substituted
- optionally
- hydroxy
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D495/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4365—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system having sulfur as a ring hetero atom, e.g. ticlopidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/12—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains three hetero rings
- C07D471/14—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/04—Ortho-condensed systems
- C07D491/044—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring
- C07D491/048—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring the oxygen-containing ring being five-membered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D498/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D513/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00
- C07D513/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00 in which the condensed system contains two hetero rings
- C07D513/04—Ortho-condensed systems
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Oncology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Hematology (AREA)
- Epidemiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
Abstract
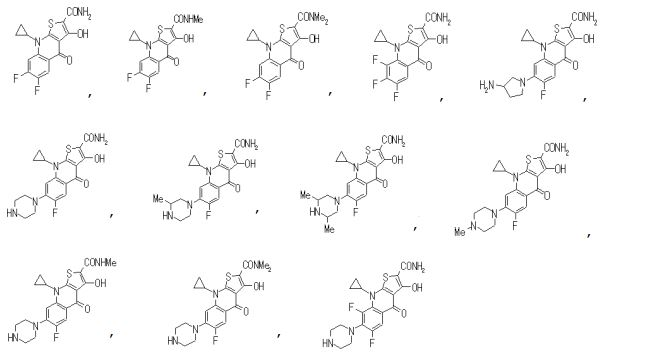
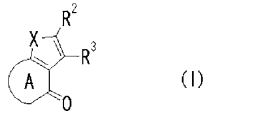
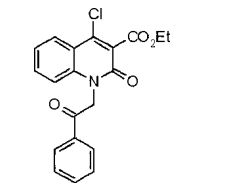
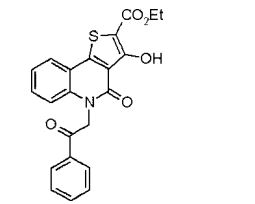
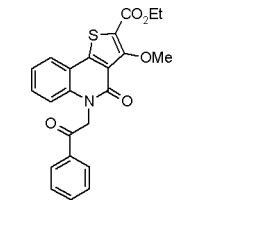
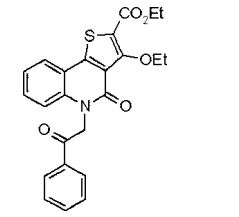
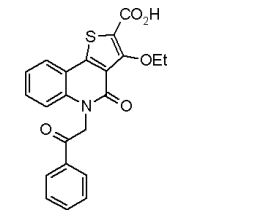
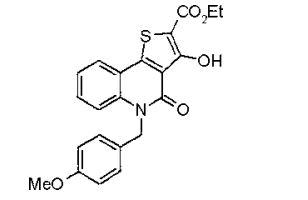
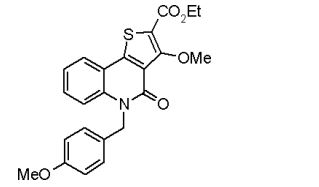
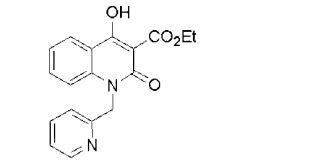
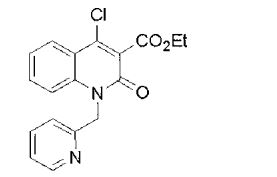
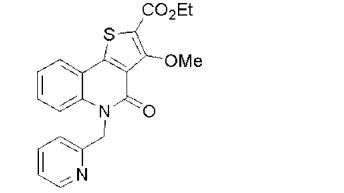
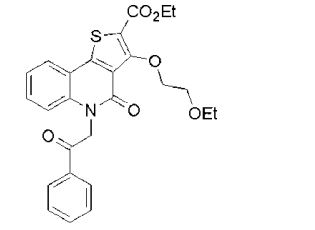
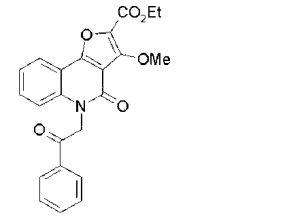
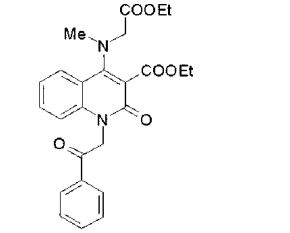
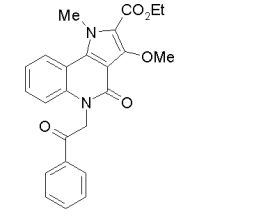
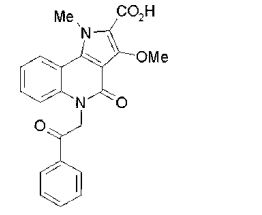
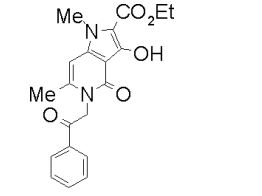
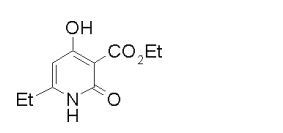
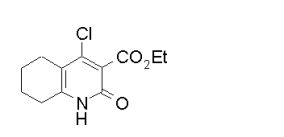
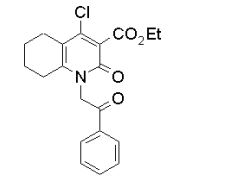
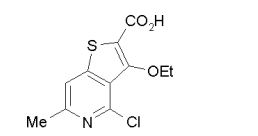
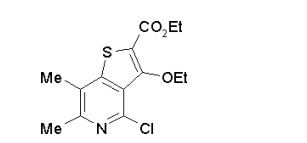
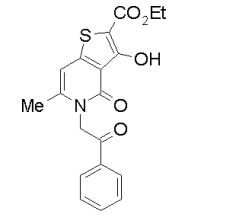
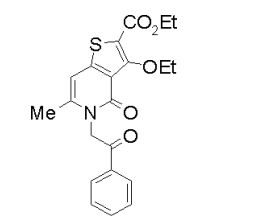
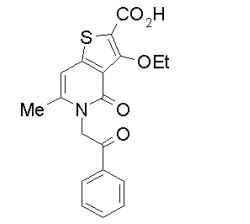
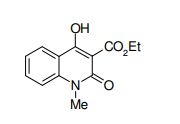
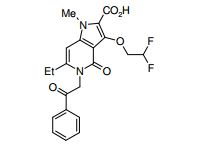
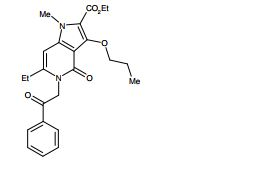
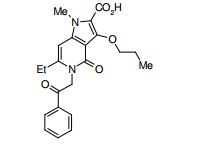
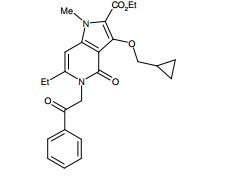
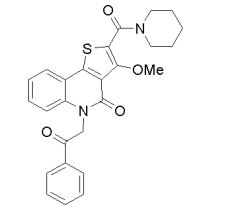
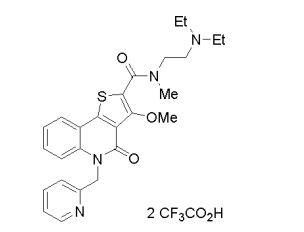
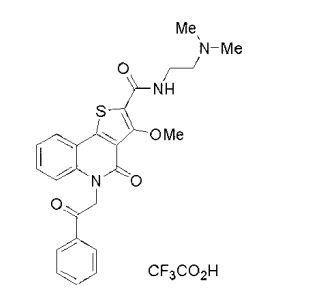
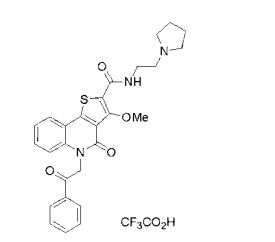
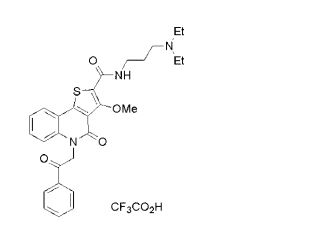
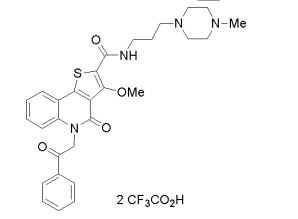
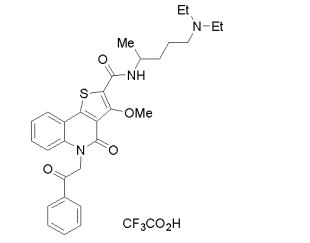
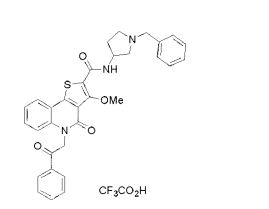
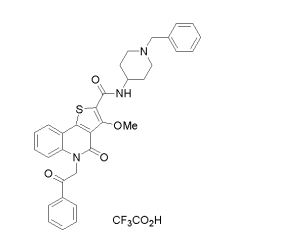
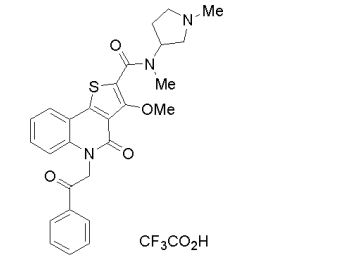
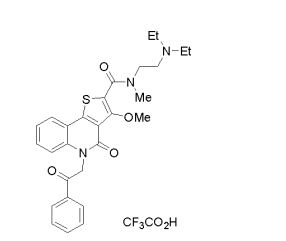
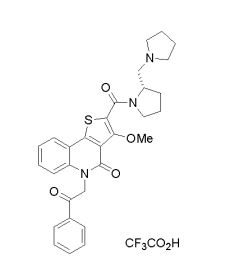
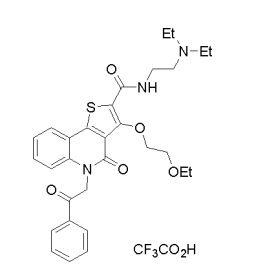
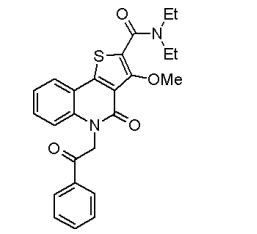
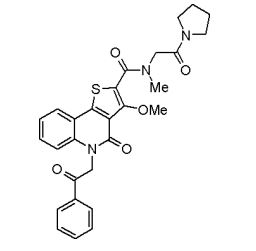
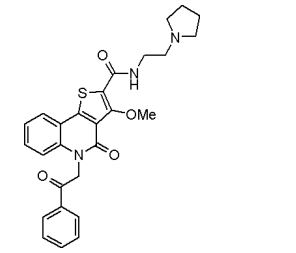
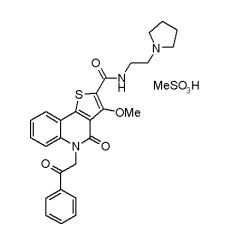
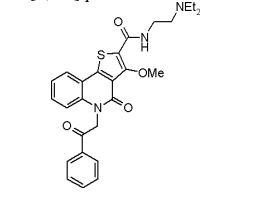
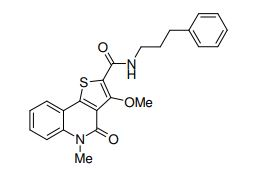
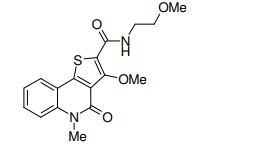
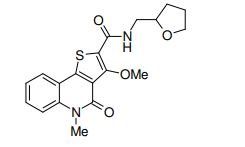
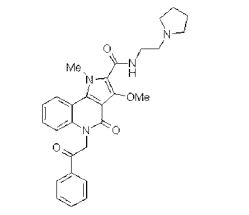
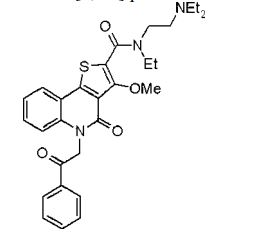
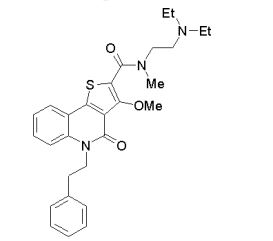
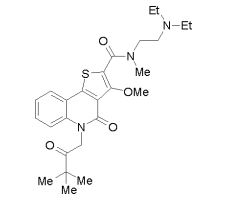
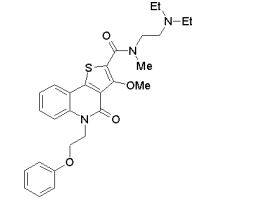
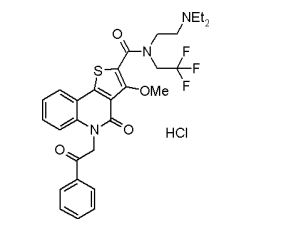
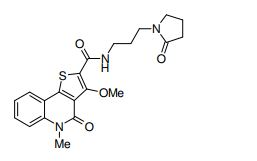
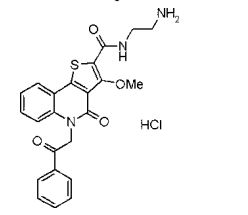
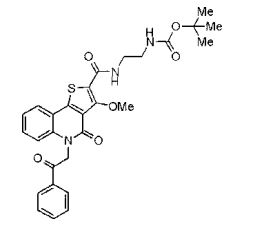
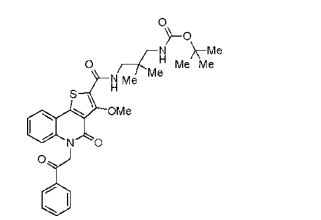
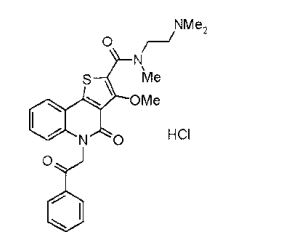
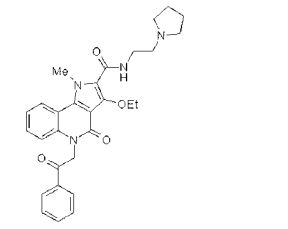
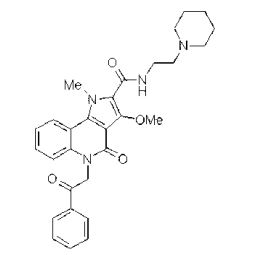
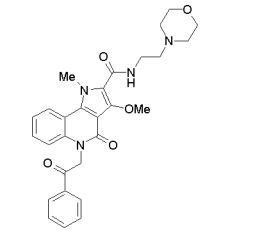
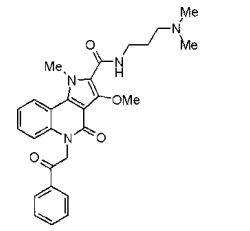
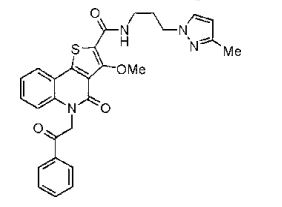
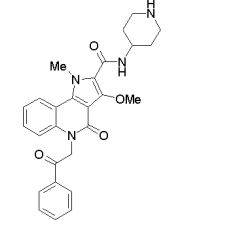
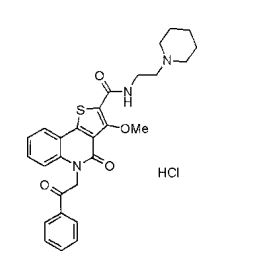
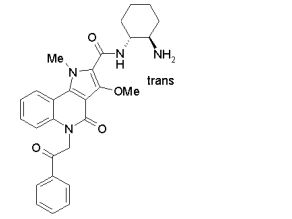
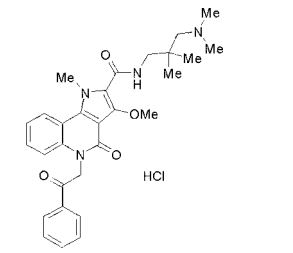
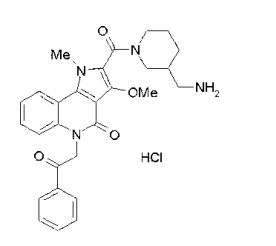
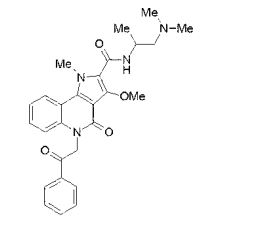
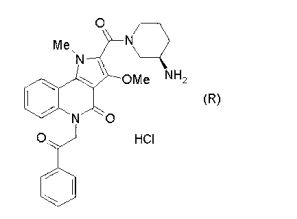
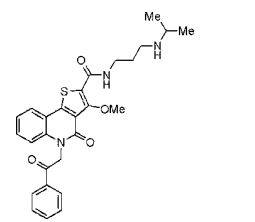
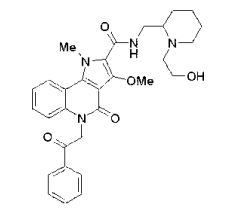
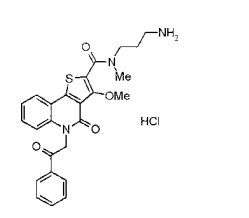
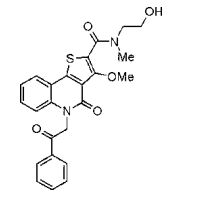
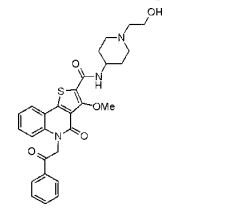
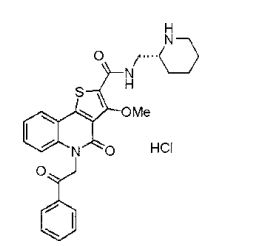
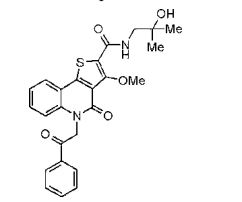
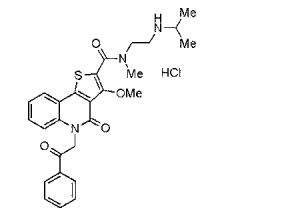
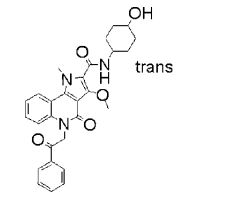
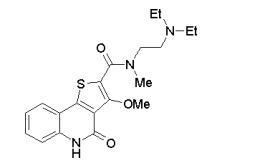
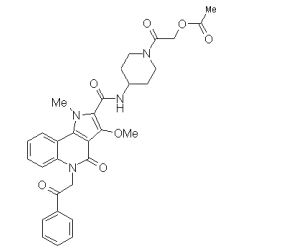
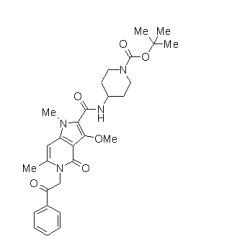
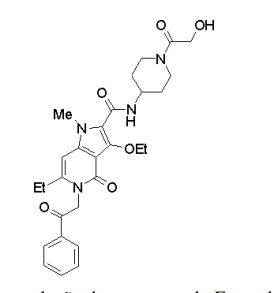
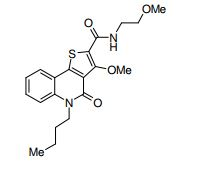
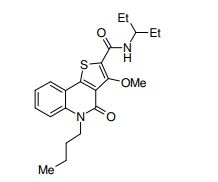
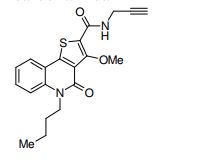
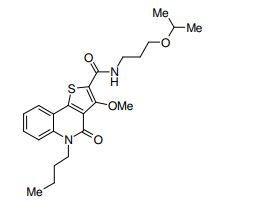
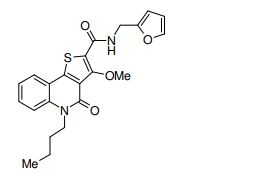
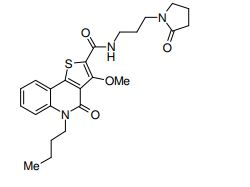
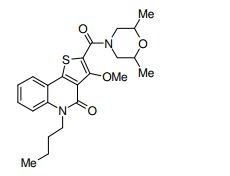
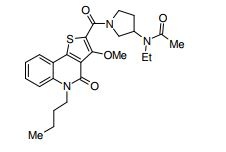
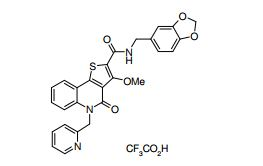
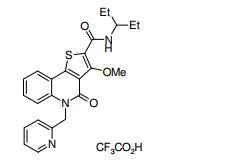
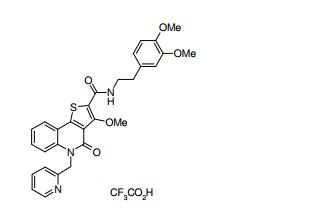
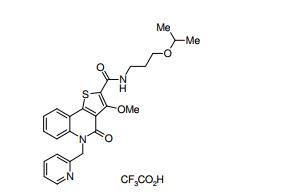
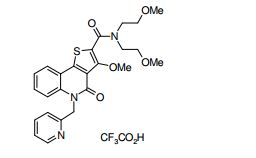
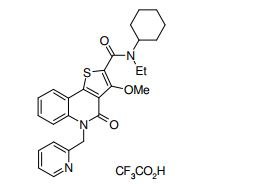
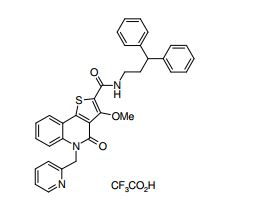
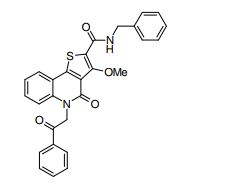
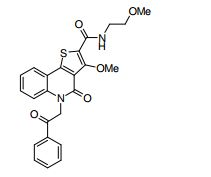
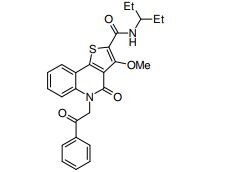
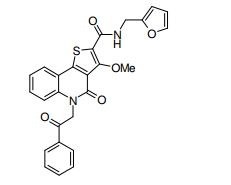
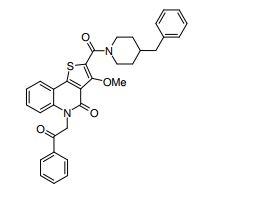
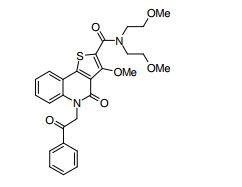
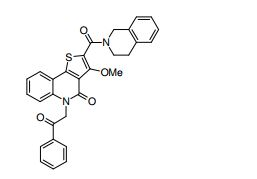
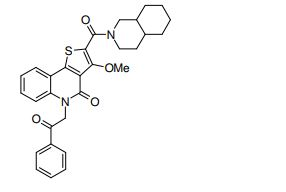
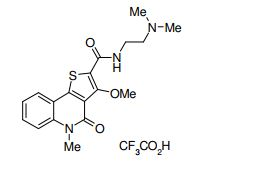
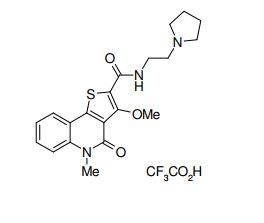
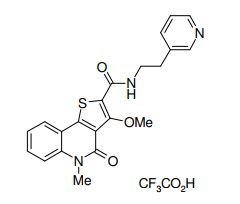
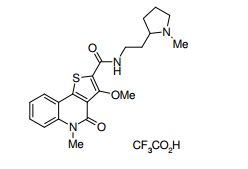
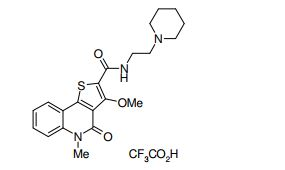
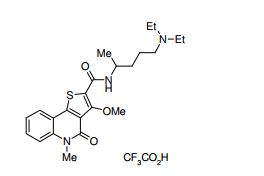
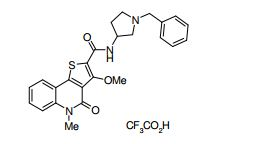
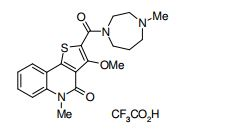
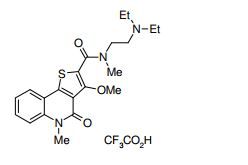
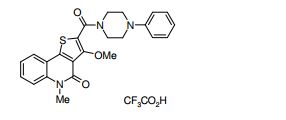
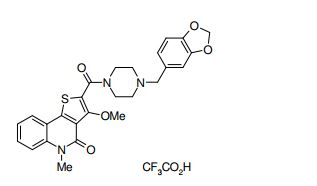
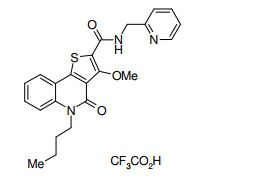
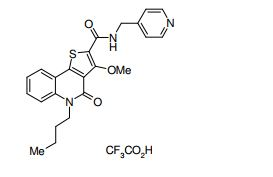
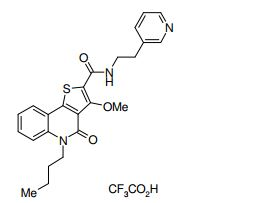
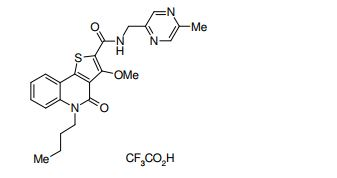
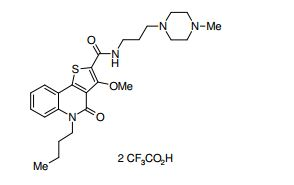
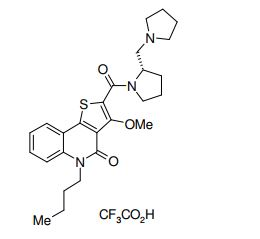
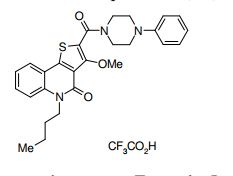
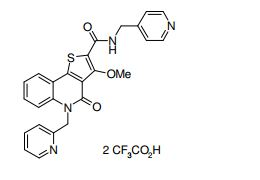
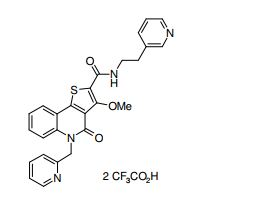
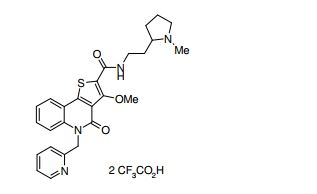
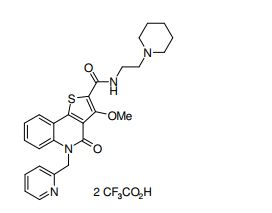
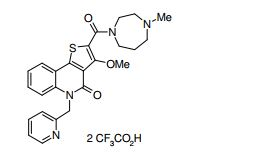
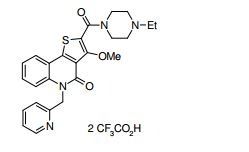
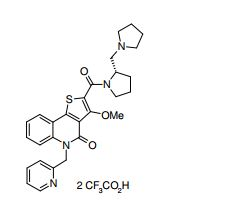
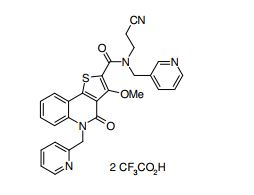
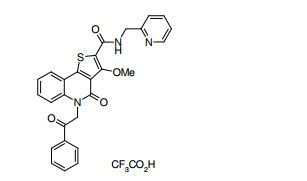
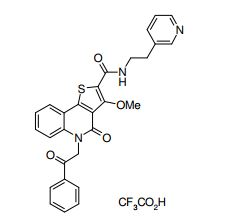
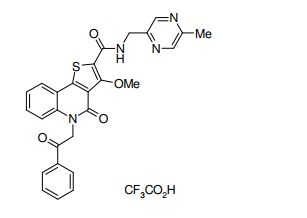
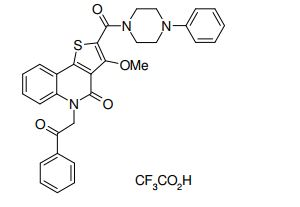
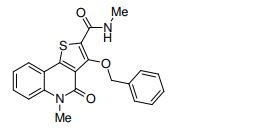
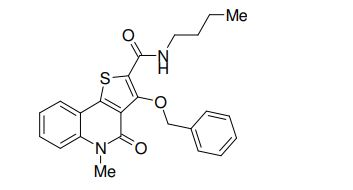
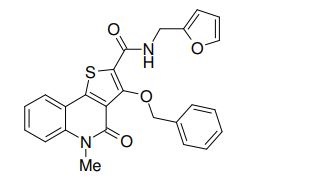
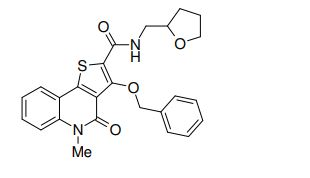
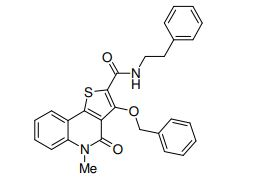
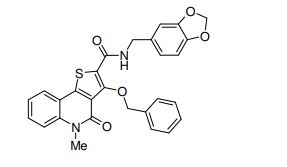
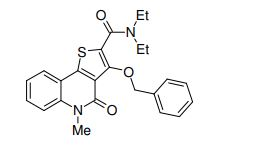
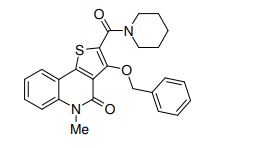
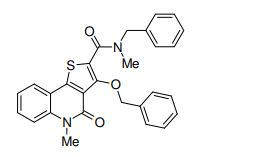
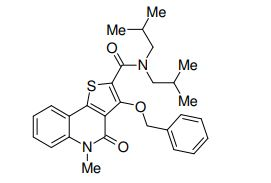
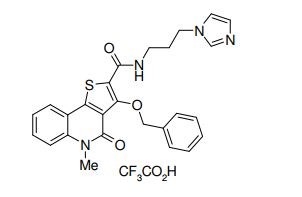
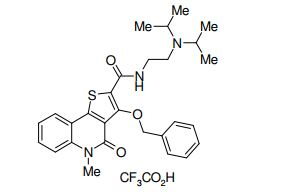
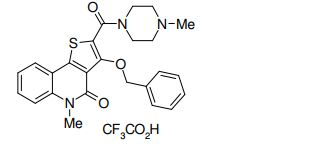
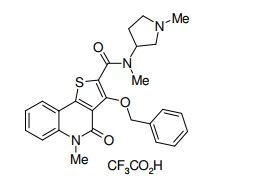
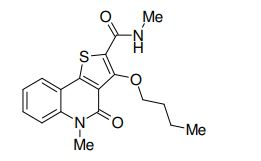
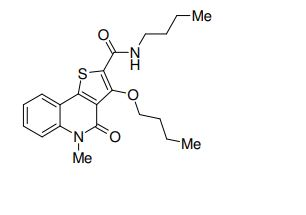
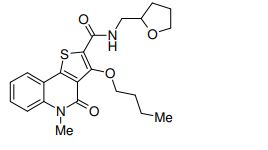
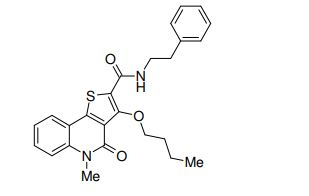
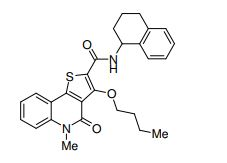
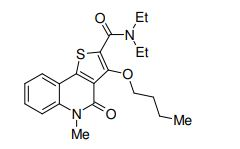
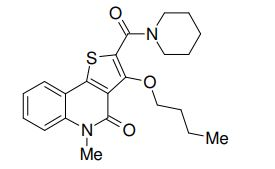
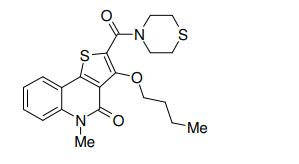
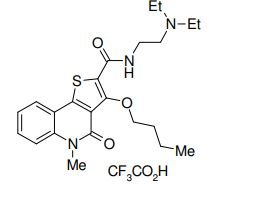
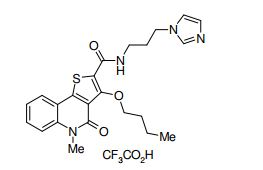
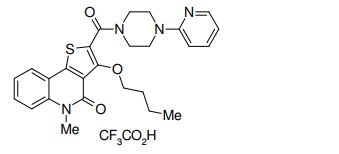
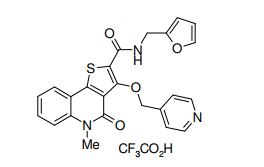
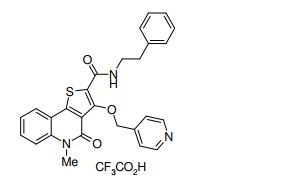
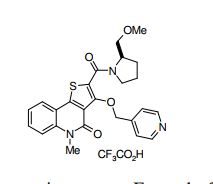
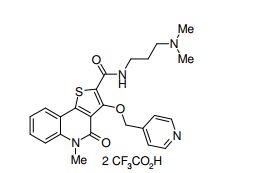
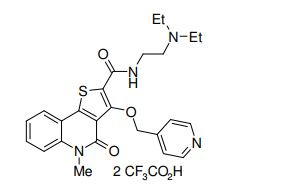
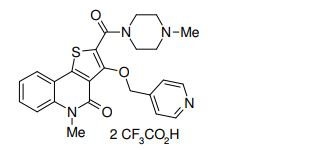
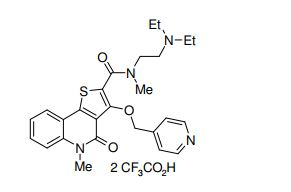
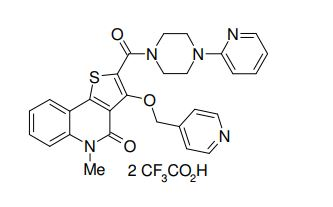
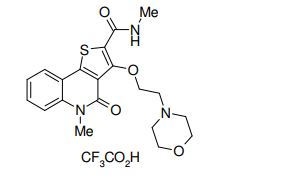
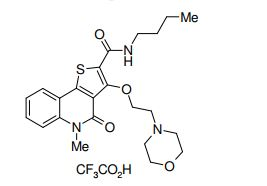
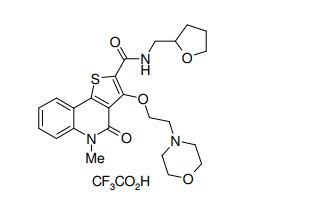
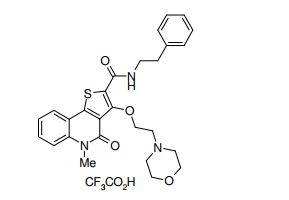
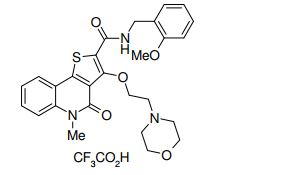
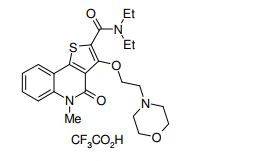
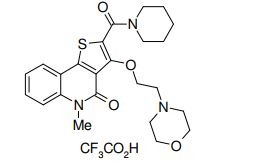
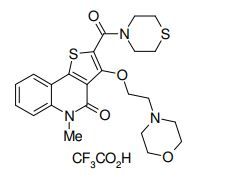
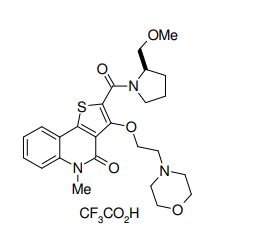
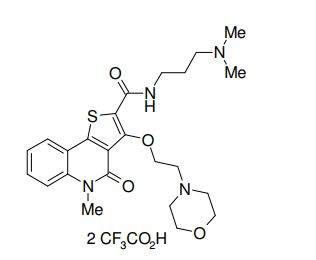
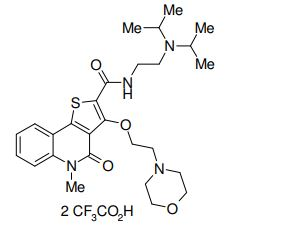
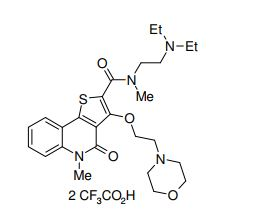
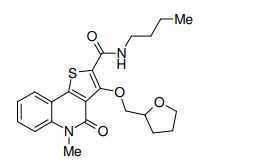
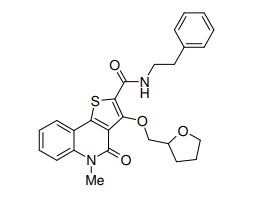
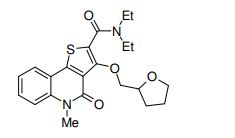
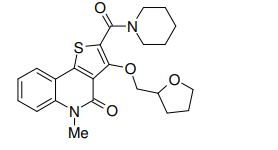
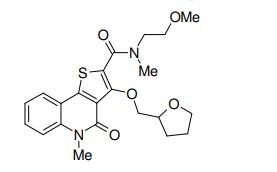
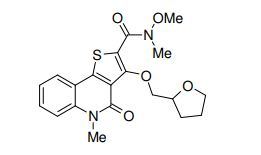
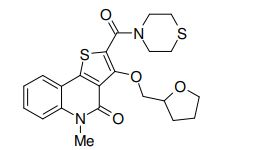
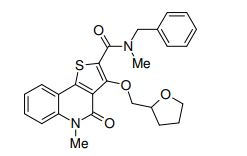
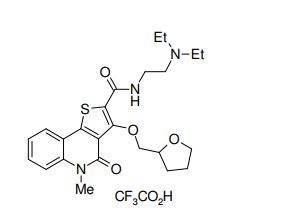
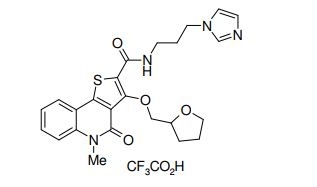
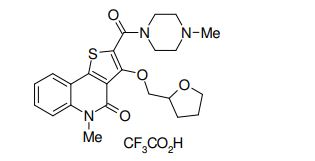
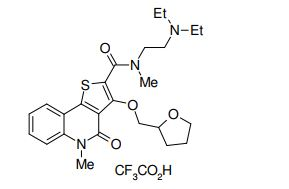
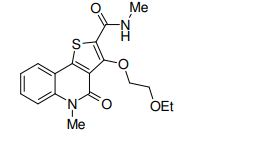
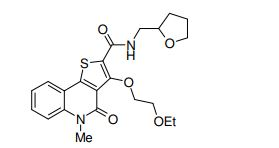
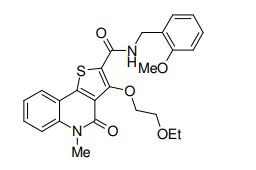
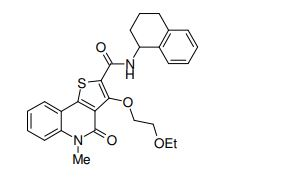
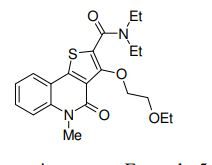
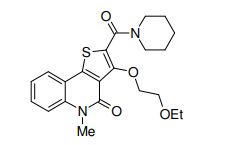
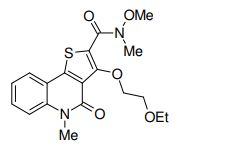
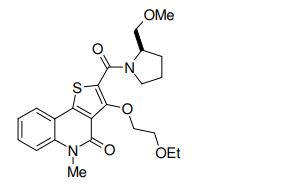
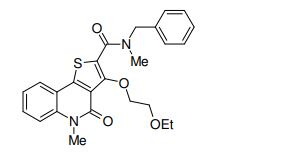
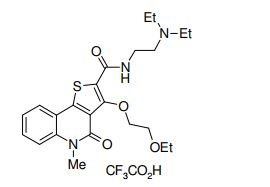
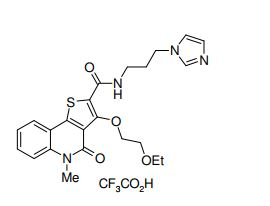
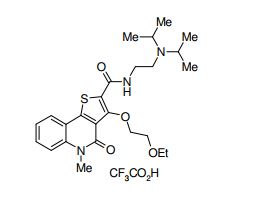
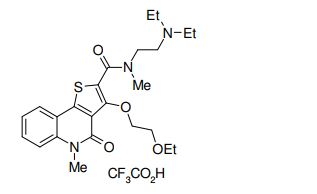
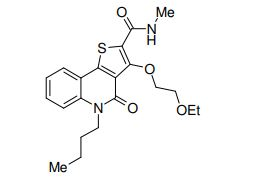
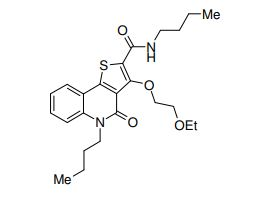
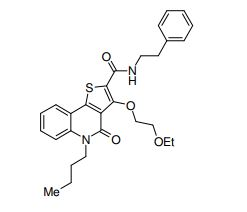
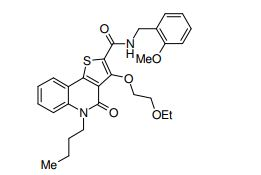
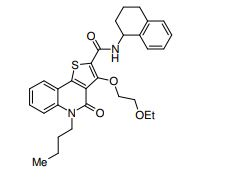
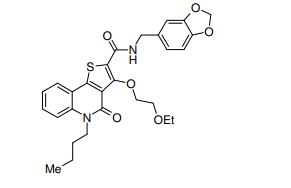
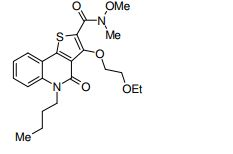
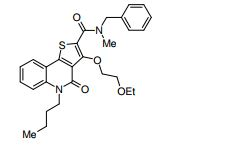
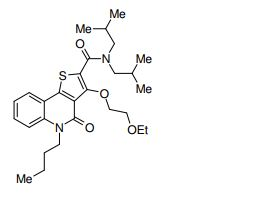
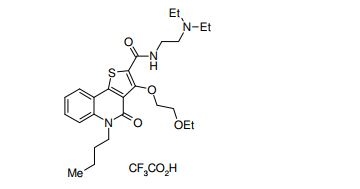
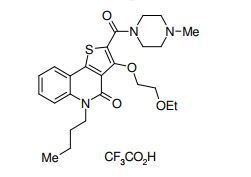
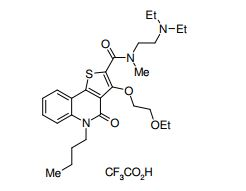
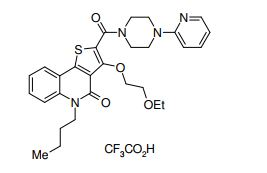
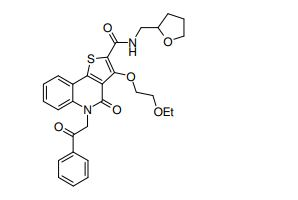
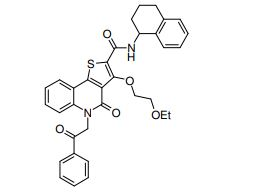
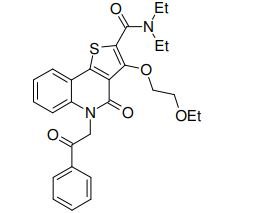
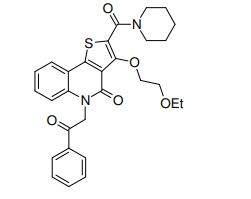
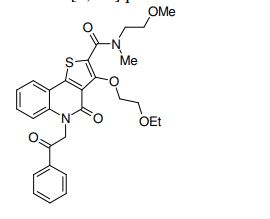
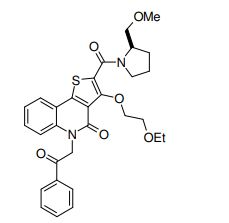
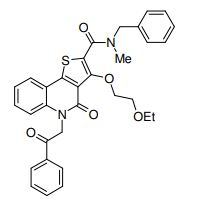
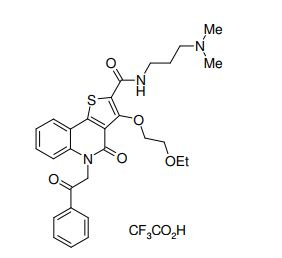
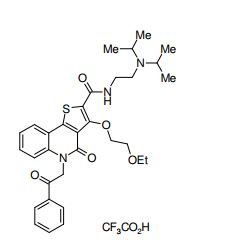
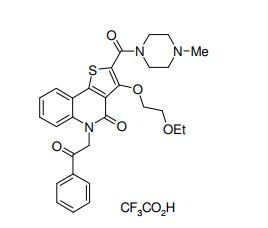
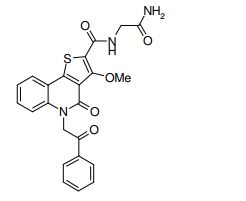
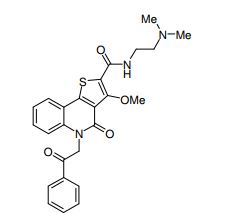
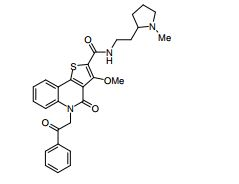
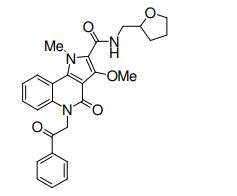
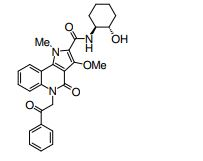
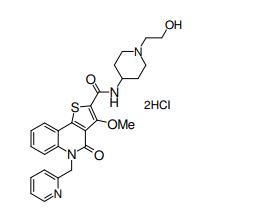
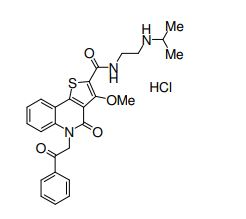
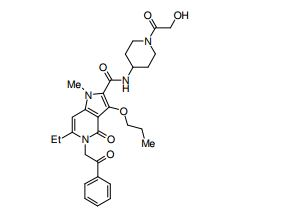
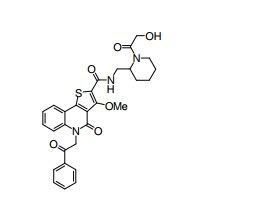
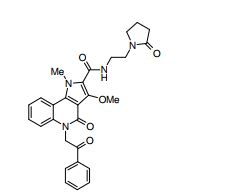
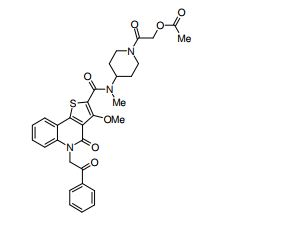
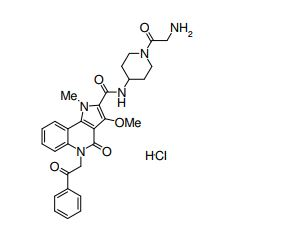
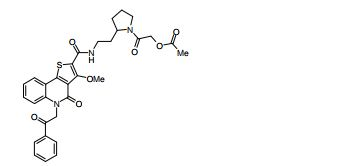
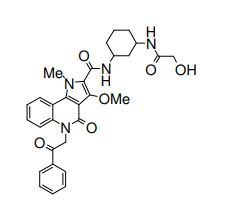
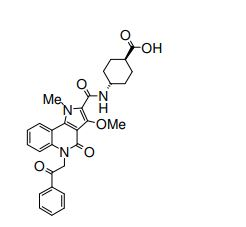
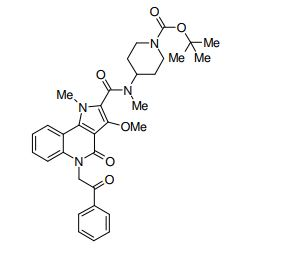
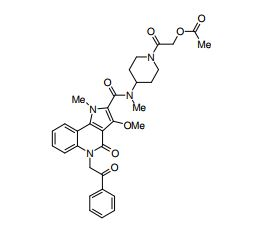
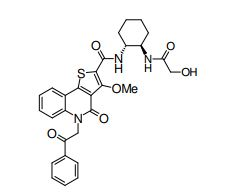
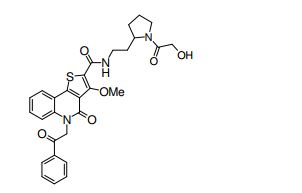
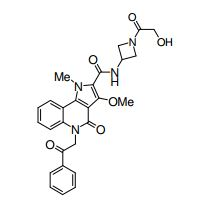
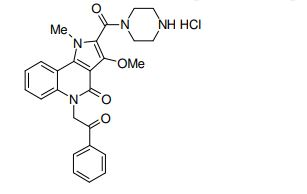
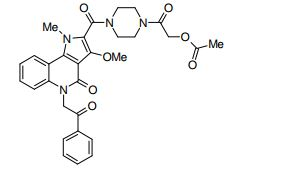
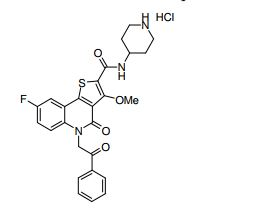
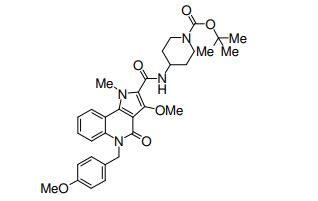
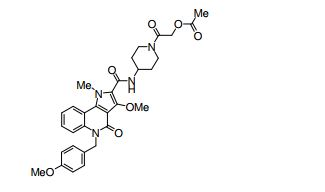
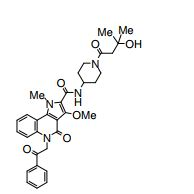
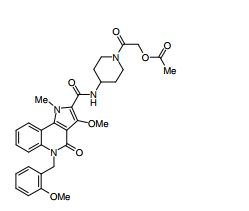
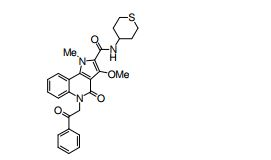
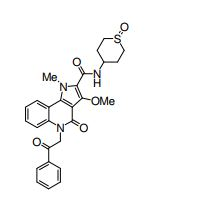
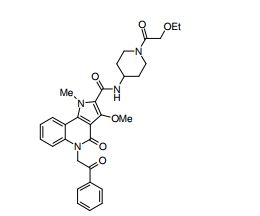
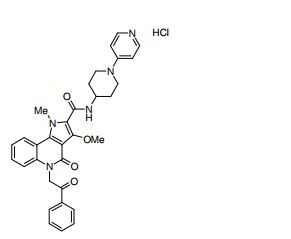
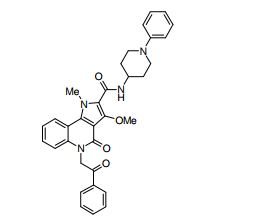
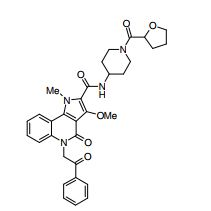
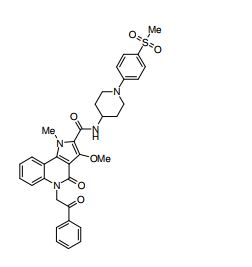
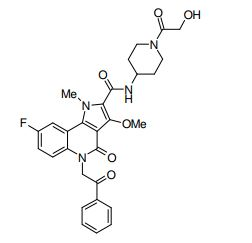
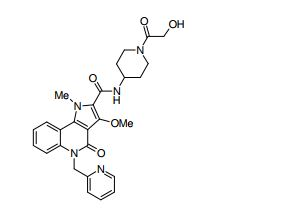
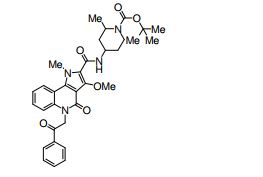
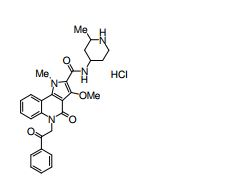
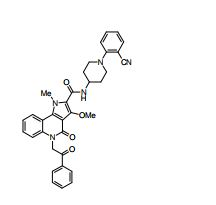
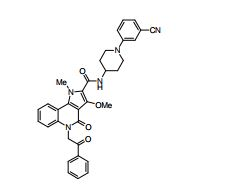
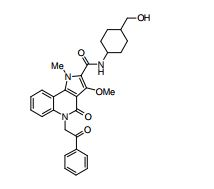
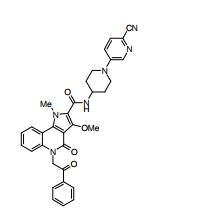
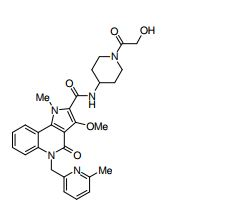
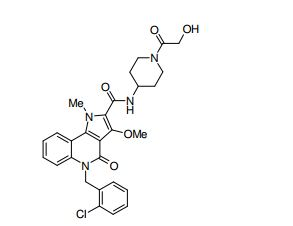
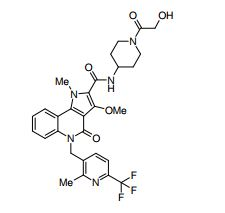
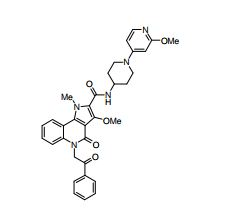
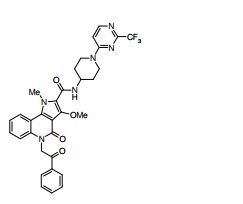
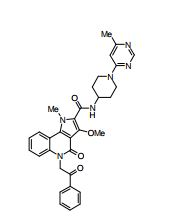
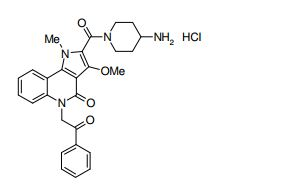
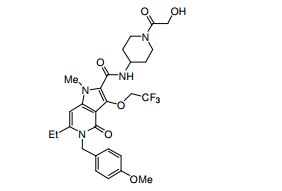
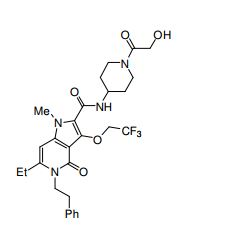
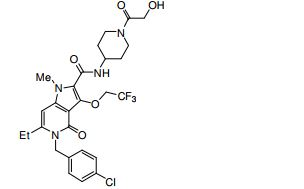
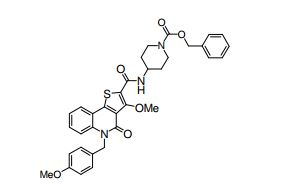
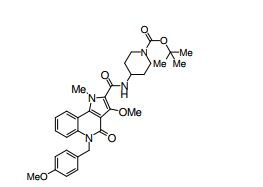
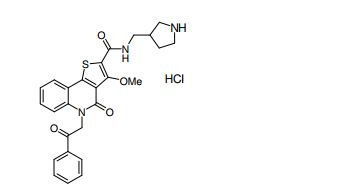
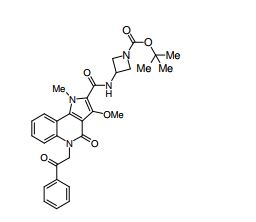
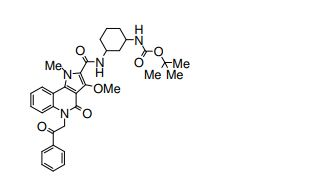
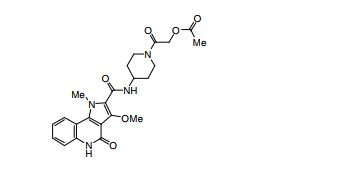
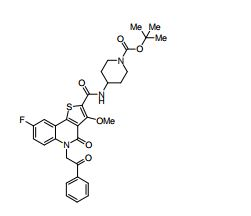
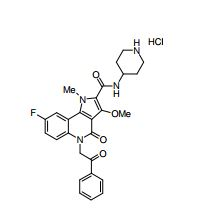
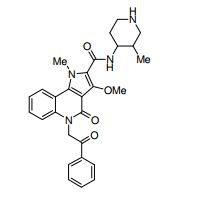
composto, pró-droga, agente farmacêutico, e, uso do composto. a presente invenção proporciona um composto apresentando uma superior atividade inibidora de smo e menor toxicidade, que é suficientemente satisfatório como um produto farmacêutico. a presente invenção proporciona um composto representado pela fórmula (l) (l) sendo que anel a é anel com de 5 a 7 membros apresentando opcionalmente substituinte(s), sendo que substituintes são opcionalmente ligados entre si para formar um anel; x é o, s ou nr¹ (r¹ é um átomo de hidrogênio ou um grupo hidrocarboneto apresentando opcionalmente substituinte(s)); r² é hidróxi apresentando opcionalmente substituinte(s), ou um sal do mesmo.
Description
[001] A presente invenção refere-se a um derivado heterocíclicofundido e uso do mesmo. Mais particularmente, a presente invenção refere-se a um composto apresentando uma forte atividade inibidora de Smo e útil para a profilaxia ou tratamento de câncer e análogos, e uso do mesmo.
[002] O estudo da morfogênese durante o estágio dedesenvolvimento foi realizado com base na seleção de variante usando Drosophila. Verificou-se que o gene do porco-espinho (hh, Hedgehog) é um dos genes que causam anormalidade morfológica do embrião de Drosophila devido à mutação do mesmo. Produto gênico de porco-espinho (Hh, Hedgehog gene product) é uma proteína secretora, que é produzido como um precursor com cerca de 45 kDa e então dividido, devido à autólise, em um domínio lateral N-terminal com 20 kDa, que é um princípio ativo principal, e um domínio lateral C-terminal com 25 kDa. O domínio lateral N-terminal com 20 kDa, que é um princípio ativo principal, é modificado por ácido graxo na ponta N e colesterol na ponta C do mesmo. O sistema de transdução de sina do porco-espinho é formado pelo grupo de proteínas descrito abaixo. O receptor de Hh é Patched (Ptch), que é uma proteína de tipo transmembrana doze. Ptch atua sobre Smoothened (Smo), que é uma proteína de tipo transmembrana sete, e suprime a função de Smo na ausência de Hh. Quando Hh é ligado ao receptor Ptch, a supressão de Smo é liberada e Smo é ativado. O sinal produzido pela ativação de Smo ativa o fator de transcrição Ci, que regula a expressão do grupo de genes envolvido na morfogênese (documento não-patente 1).
[003] Uma via que corresponde ao sistema de transdução de sinalDrosophila Hedgehog também foi confirmada em mamíferos. No humano, por exemplo, sabe-se que três tipos de produtos gênicos, porco-espinho Sonic (Shh, sonic hedgehog), porco-espinho da Índia (Ihh, indian hedgehog) e porco-espinho do deserto (Dhh, desert hedgehog), correspondem a Drosophila Hh, e sofrem modificação pós-tradução como em Drosophila Hh (documento não-patente 2). No Shh humano, um princípio ativo com 19 kDa é clivado de uma proteína precursora com 45 kDa por meio de autólise, e adicionou-foi agitada e colesterol a suas pontas N-terminal e C-terminal, respectivamente (documento não-patente 3). Referida modificação é considerada essencial para a manutenção da atividade de Shh e, por exemplo, obteve-se atividade aumentada de 40 vezes por meio da adição de ácido palmítico a Shh humano recombinante de Escherichia coli livre de modificação N-terminal com ácido graxo, e obteve-se atividade 160 vezes aumentada por meio da adição de ácido mirístico a isto (documento não-patente 4). Por outro lado, como um gene humano correspondente a Drosophila Smo, conhece-se Smo humano, e como um gene humano correspondente a Drosophila Ptch, conhece-se 2 tipos [de] Ptch1 e Ptch2. Adicionalmente, um fator de transcrição correspondente a Drosophila Ci é considerado como sendo Gli em humano, e conhece-se 3 tipos de Gli1, Gli2 e Gli3 (documento não-patente 5). Shh/Ihh/Dhh são ligados, cada um, a Ptch1 e ativam Smo inibindo a ligação entre Ptch1 e Smo. Shh/Ihh/Dhh também são ligados a Ptch2, Hip1, Gas1 e Cdo/Boc, além de Ptch1, e regulam a ativação de Smo. Uma transdução de sinal de Smo induz a localização nuclear de Gli1 e Gli2, e ativa a transcrição de Gli1 (documento não-patente 6).
[004] O sinal de porco-espinho está envolvido na morfogênese nosestágios do desenvolvimento também em mamíferos. No humano, por exemplo, pacientes com holoprosencefalia, que é uma anormalidade desenvolvimental congênita, apresentaram mutação em Shh (documento não- patente 7). Além disso, confirmou-se que um composto natural Ciclopamina derivada do heléboro branco conhecido como um composto que induz Ciclopus em ovelhas (documento não-patente 8) inibe Smo como mecanismo de ação do mesmo (documento não-patente 9). Adicionalmente, preparou-se um camundongo inibidor de Shh, e verificou-se que seu fenótipo inclui Ciclopia, má formação de extremidades (documento não-patente 10), e má formação da placa neural (documento não-patente 11).
[005] Sinal de porco-espinho é inerentemente um sinal dedesenvolvimento, que é promovido em tecidos de tumor e funciona como um sinal de crescimento de células de câncer e de sobrevida. Considera-se que o sinal de porco-espinho funciona para o crescimento e a sobrevida de células de câncer em um modo autócrino, ou funciona entre células de câncer e células intersticiais de câncer em um modo parácrino, em tecidos de tumor (documento não-patente 12). Em um modo autócrino, ele atua para o crescimento e a manutenção de células de câncer, via ativação de transcrição por Gli-1, pelo controle do ciclo de células anormais devido a expressão incrementada de Ciclina D e expressão diminuída de p21, promoção do sinal de proliferação pela ativação da via do EGFR e análogos. Por outro lado, em um modo parácrino, porque Shh expresso em células de câncer atua sobre Smo em células intersticiais de câncer, fatores de crescimento, como fator de crescimento 1 similar a insulina, fator de crescimento de fibroblastos, fator de crescimento derivado de plaquetas e análogos são transmitidos de células intersticiais de câncer para células de câncer, e funciona para o crescimento e sobrevida de células de câncer. Considera-se que a promoção do VEGF, via do PDGF e análogos por Gli-1 promove a angiogênese de tumor (documento não-patente 13). Quanto ao mecanismo de promoção do sinal de porco- espinho, reportou-se que um câncer em que o sinal de porco-espinho é promovido devido à mutação de Ptch1 e um câncer que é promovido pela superexpressão de Shh, que é um dos ligantes (documento não-patente 14). Quanto a um câncer em que o sinal de porco-espinho é promovido devido a mutação, câncer de células basais e meduloblastoma são conhecidos, e a mutação de Ptch1 observada nestes cânceres ativa o sinal de porco-espinho de uma maneira independente de ligante (documento não-patente 15). Quanto a um câncer em que o sinal de porco-espinho é promovido por meio de superexpressão de Shh, reportou-se sobre câncer pancreático (documento não- patente 16) e análogos. Em um camundongo transgênico em que Shh é expresso forçosamente no pâncreas, sugere-se que o sinal de porco-espinho está envolvido não só no crescimento e na manutenção de câncer, mas também em processo carcinogênico, porque se encontrou no pâncreas uma lesão similar a PanIN nos estágios iniciais de câncer (documento não-patente 17). Adicionalmente, considera-se que o sinal de porco-espinho funciona para o crescimento e a sobrevida de células indiferenciadas de câncer, e desempenha um papel-chave na metástase ou recorrência pós-operativa de tumor e análogos (documento não-patente 18).
[006] Como o inibidor de sinal de porco-espinho, conhece-se osseguintes. Reportou-se que a ciclopamina, que é um composto inibidor de Smo naturalmente ocorrente, apresenta um efeito supressivo do crescimento de tumor sobre o glioma (documento não-patente 19) e análogos. Como um composto sintético com baixo peso molecular que inibe Smo, reportou-se CUR-61414 (documento não-patente 20) e SANT-1, 2, 3, 4 (documento não- patente 21). Com relação ao anticorpo inibidor de sinal de porco-espinho reportou-se que a administração de um anticorpo anti-Shh a um camundongo pelado portador de câncer transplantado com a linha de células de câncer colorretal HT-29 resultou em regressão do câncer (documento de patente 1).
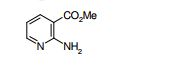
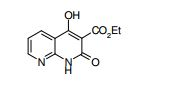
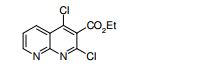
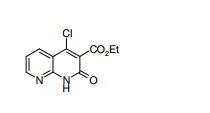
[007] Como um composto similar ao composto descrito na presentedescrição, o documento de patente 2 revela os métodos a seguir apresentando uma atividade antibacteriana.Como um composto apresentando uma atividadeantibacteriana, o documento de patente 3 revela os seguintes compostos. documento de patente 1: WO2004/020599documento de patente 2: JP-A-3-223289documento de patente 3: WO93/13664documento não-patente 1: Curr. Opin. Genet. Dev., vol. 12, páginas 503-511 (2002)documento não-patente 2: Cell, vol. 103, páginas 371-374 (2000)documento não-patente 3: J. Biol. Chem., vol. 273, páginas 14037-14045 (1998)documento não-patente 4: Biochemistry, vol. 40, páginas4359-4371 (2001)documento não-patente 5: Nature Rev. Cancer, vol. 2, páginas 361-372 (2002)documento não-patente 6: Curr. Opin. Cell Biol., vol. 19, páginas 159-165 (2007)documento não-patente 7: Nat. Genet., vol. 14, páginas 357360 (1996)documento não-patente 8: Am. J. Vet. Res., vol. 24, páginas 1164-1175 (1963)documento não-patente 9: Development, vol. 125, páginas 3553-3562 (1998)documento não-patente 10: Nature, vol. 383, páginas 407-413 (1996)documento não-patente 11: Cell, vol. 111, páginas 63-75 (2002)documento não-patente 12: Nat. Rev. Drug Discov., vol. 5, páginas 1026-1033 (2006)documento não-patente 13: Clin Cancer Res., vol. 12, páginas 5924-5928 (2006)documento não-patente 14: Nature Rev. Cancer, vol. 3, páginas 903-911 (2003)documento não-patente 15: Am. J. Med. Gen., vol. 123A, páginas 5-28 (2003)documento não-patente 16: Nature, vol. 425, páginas 846-851 (2003)documento não-patente 17: Nature, vol. 425, páginas 851-856 (2003)documento não-patente 18: Trends Cell Biol., vol. 17, páginas 438-227 (2007)documento não-patente 19: Development, vol. 128, páginas 5201-5212 (2001) documento não-patente 20: Proc. Natl. Acad. Sci. U.S.A., vol.100, páginas 4616-4621 (2003)documento não-patente 21: Proc. Natl. Acad. Sci. U.S.A., vol.99, páginas 14071-14076 (2002)
[008] Um objeto da presente invenção consiste em proporcionar umcomposto apresentando uma superior atividade inibidora de Smo, baixa toxicidade e suficientemente satisfatório como um produto farmacêutico.
[009] Os presentes inventores conduziram estudos intensivos numatentativa de resolver os problemas mencionados acima e verificaram que um composto representado pela fórmula a seguir e um sal do mesmo apresenta uma superior atividade inibidora de Smo, que resultou no completamento da presente invenção.
[0010] Assim, a presente invenção proporciona o seguinte.
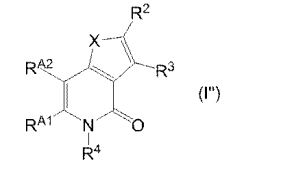
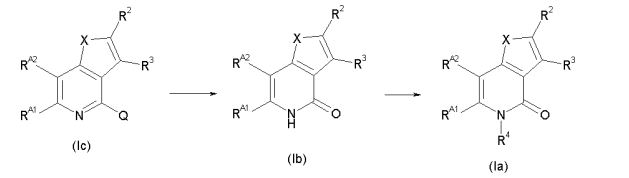
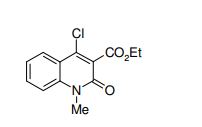
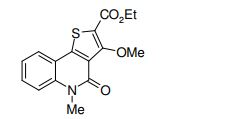
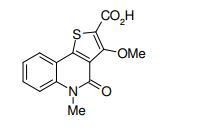
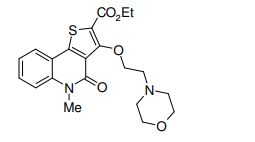
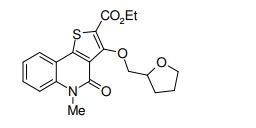
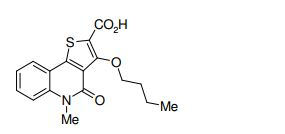
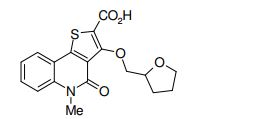
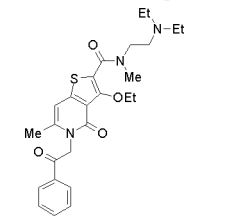
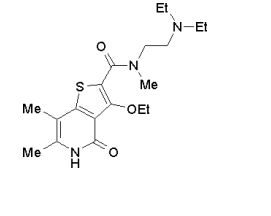
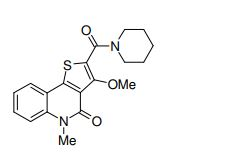
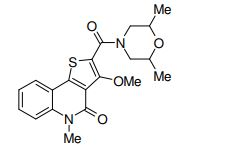
[0011] [1] Um composto representado pela fórmula(I)sendo queanel A é um anel com de 5 a 7 membros apresentandoopcionalmente substituinte(s), sendo que substituintes são opcionalmente ligados entre si para formar um anel;X é O, S ou NR1 (R1 é um átomo de hidrogênio ou um grupo hidrocarboneto apresentando opcionalmente substituinte(s));R2 é carbamoíla apresentando opcionalmente substituinte(s); e R3 é hidróxi apresentando opcionalmente substituinte(s), exceto os seguintes compostos; (abreviado a seguir, por vezes, como composto (I)) ou um saldo mesmo.
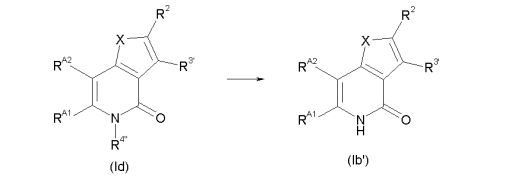
[0012] [2] O composto do [1] indicado acima, que é representado pelafórmulasendo queX, R2 e R3 são como definido no [1] indicado acima,RAA1 e RAA2 são iguais ou diferentes e cada um é um átomo de hidrogênio ou um substituinte, ou RAA1 e RAA2 são opcionalmente ligados entre si para formar um anel com de 5 a 7 membros apresentando opcionalmente substituinte(s), e R4 é um átomo de hidrogênio ou um grupo hidrocarboneto apresentando opcionalmente substituinte(s)(abreviado a seguir, por vezes, como composto (I”’).
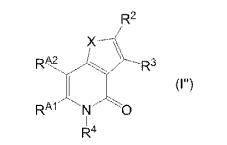
[0013] [3] O composto do [2] indicado acima, que é representado pelafórmulasendo queX, R2 e R3 são como definido no [1] indicado acima,RA1 e RA2 são iguais ou diferentes e cada um é um átomo de hidrogênio ou um substituinte, eR4 é um átomo de hidrogênio ou um grupo hidrocarboneto apresentando opcionalmente substituinte(s)(abreviado a seguir, por vezes, como composto (I”)).
[0014] [4] O composto do [3] indicado acima, sendo que X é O, S ouN(C1-6 alquila),R2 é carbamoíla apresentando opcionalmente substituinte(s),R3 é hidróxi opcionalmente apresentando C1-6 alquila apresentando opcionalmente substituinte(s),RA1 é um átomo de hidrogênio ou um grupo C1-6 alquila,RA2 é um átomo de hidrogênio ou um grupo C1-6 alquila, eR4 é um átomo de hidrogênio ou C1-6 alquila apresentando opcionalmente substituinte(s).
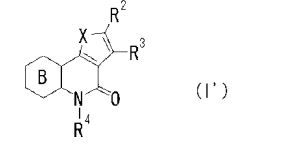
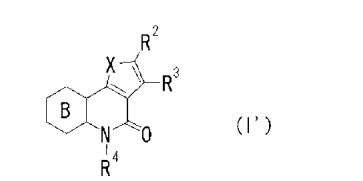
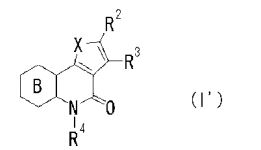
[0015] [5] O composto do [1] indicado acima, que é representado pelafórmula sendo queX, R2 e R3 são como definido no [1] indicado acima,anel B é um anel com 6 membros apresentando opcionalmente substituinte(s); eR4 é um átomo de hidrogênio ou um grupo hidrocarboneto apresentando opcionalmente substituinte(s)(abreviado a seguir, por vezes, como composto (I’)).
[0016] [6] O composto do [5] indicado acima, sendo que anel B é umanel com 6 membros apresentando opcionalmente substituinte(s),X é O, S ou N(C1-6 alquila),R2 é carbamoíla apresentando opcionalmente substituinte(s),R3 é hidróxi opcionalmente apresentando C1-6 alquila apresentando opcionalmente substituinte(s), eR4 é um átomo de hidrogênio ou C1-6 alquila apresentando opcionalmente substituinte(s).
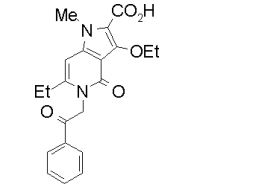
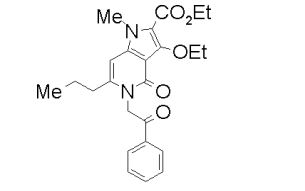
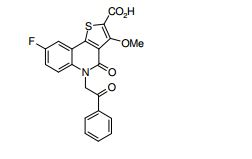
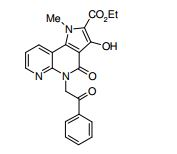
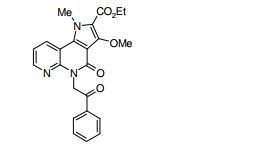
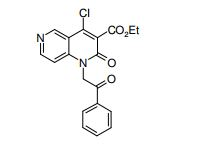
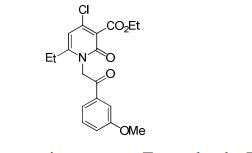
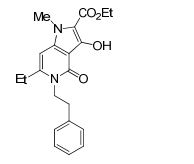
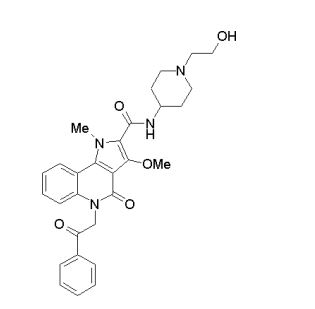
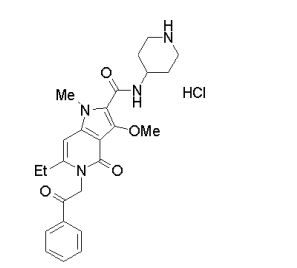
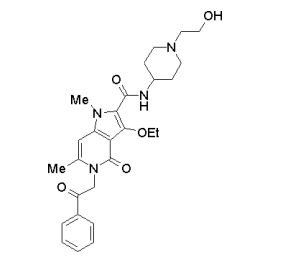
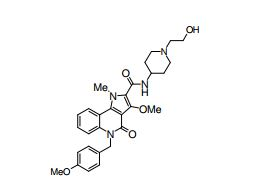
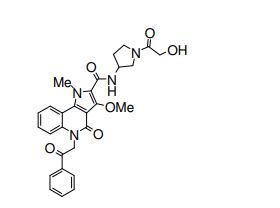
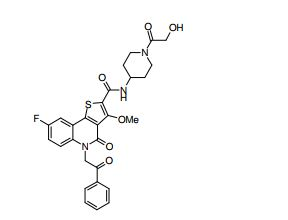
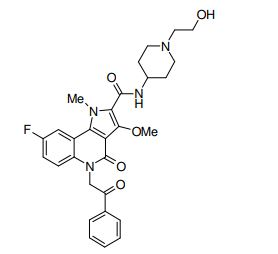
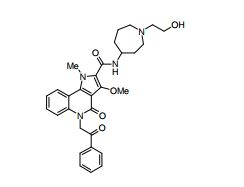
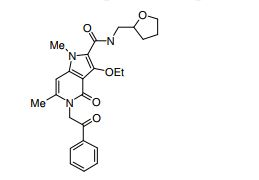
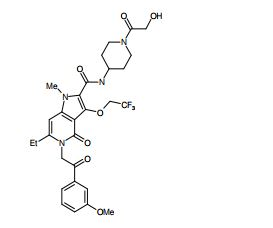
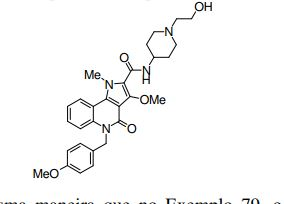
[0017] [7] N-[1-(2-Hidroxietil)piperidin-4-il]-3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamida ou um sal do mesmo.
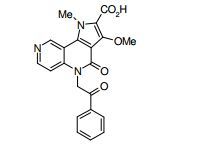
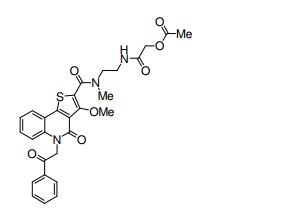
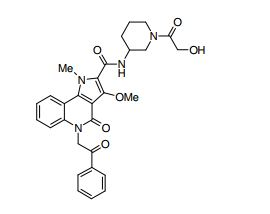
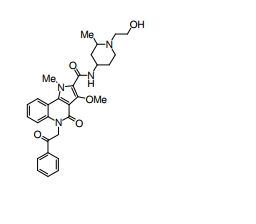
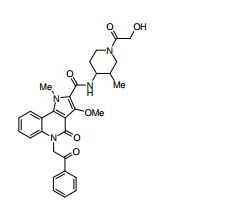
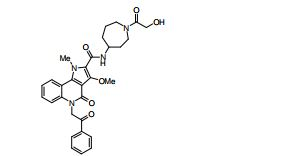
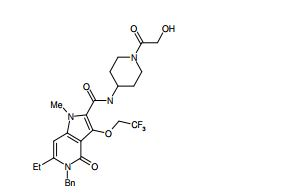
[0018] [8] N-[1-(Hidroxiacetil)piperidin-4-il]-3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamida ou um sal do mesmo.
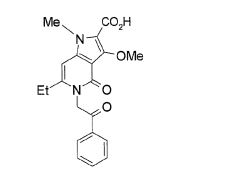
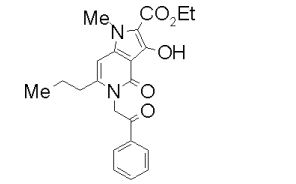
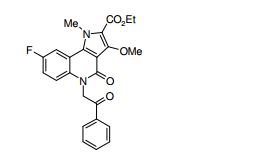
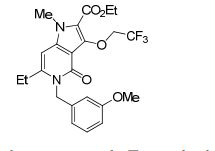
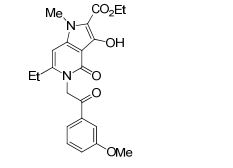
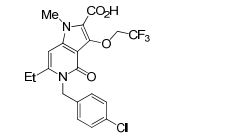
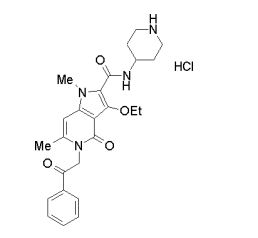
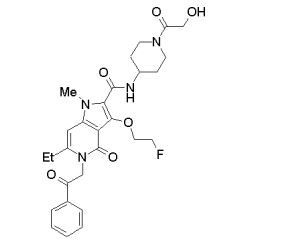
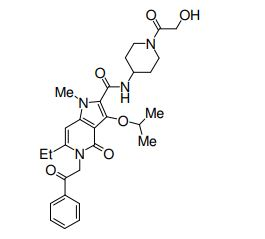
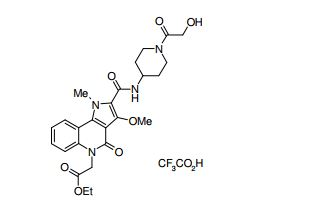
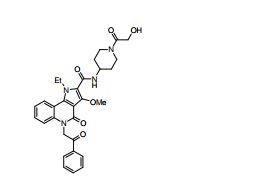
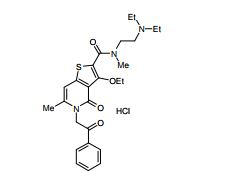
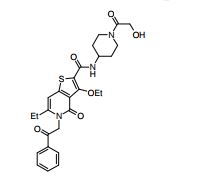
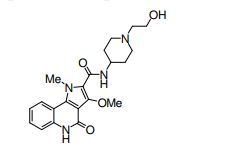
[0019] [9] 3-Etóxi-6-etil-N-[1-(hidroxiacetil)piperidin-4-il]-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxamida ou um sal do mesmo.
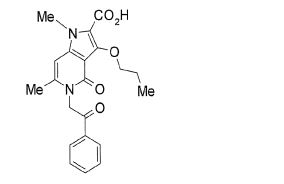
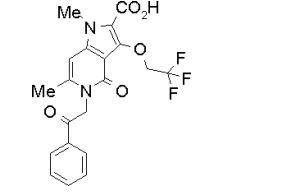
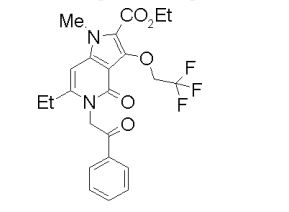
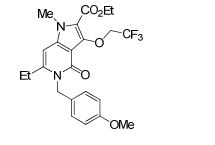
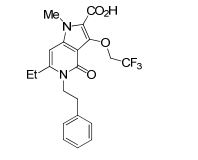
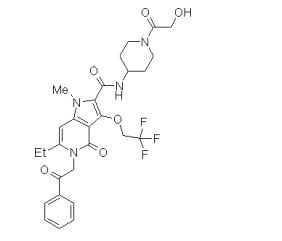
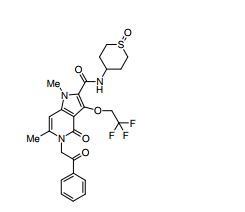
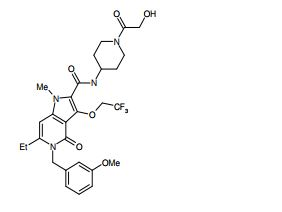
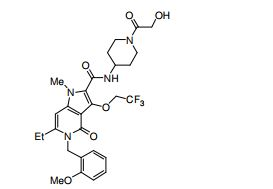
[0020] [10] N-[1-(Hidroxiacetil)piperidin-4-il]-1,6-dimetil-4-oxo-5- (2-oxo-2-feniletil)-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina- 2-carboxamida ou um sal do mesmo.
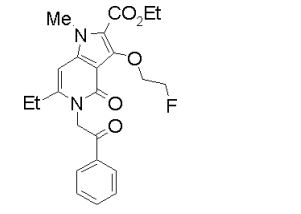
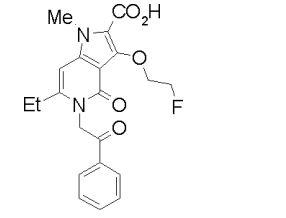
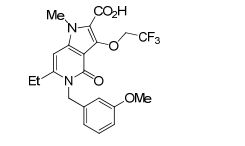
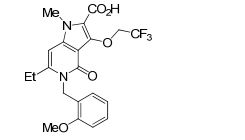
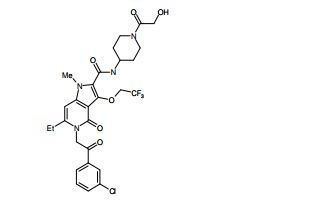
[0021] [11] 6-Etil-N-[1-(hidroxiacetil)piperidin-4-il]-1-metil-4-oxo-5-(2-oxo-2-feniletil)-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina- 2-carboxamida ou um sal do mesmo.
[0022] [12] Uma pró-droga do composto do [1] indicado acima.
[0023] [13] Um agente farmacêutico compreendendo o composto doindicado acima ou uma pró-droga do mesmo.
[0024] [14] O agente farmacêutico do [13] indicado acima, que é uminibidor de Smo.
[0025] [15] O agente farmacêutico do [13] indicado acima, que é umagente para a profilaxia ou tratamento de câncer.
[0026] [16] Um método para inibir Smo em um mamífero, quecompreende administrar uma quantidade efetiva do composto do [1] indicado acima ou uma pró-droga do mesmo ao mamífero.
[0027] [17] Um método para a profilaxia ou tratamento de câncer emum mamífero, que compreende administrar uma quantidade efetiva do composto do [1] indicado acima ou uma pró-droga do mesmo ao mamífero.
[0028] [18] Uso do composto do [1] indicado acima ou uma pró-droga do mesmo para a produção de um inibidor de Smo.
[0029] [19] Uso do composto do [1] indicado acima ou uma pró-droga do mesmo para a produção de um agente para a profilaxia ou tratamento de câncer.
[0030] Na presente descrição, composto (I) compreende composto (I’), composto (I”) e composto (I”’).
[0031] Como o composto da presente invenção apresenta uma forte ação inibidora de Smo, ele pode proporcionar um agente clinicamente útil para a profilaxia ou tratamento de câncer, um inibidor de crescimento de câncer e um agente supressor de metástase do câncer.
[0032] A presente invenção é explicada detalhadamente a seguir.
[0033] No composto (I), X é O, S ou NR1 (R1 é um átomo de hidrogênio ou um grupo hidrocarboneto apresentando opcionalmente substituinte(s)).
[0034] Exemplos do “grupo hidrocarboneto apresentando opcionalmente substituinte(s)” para R1 incluem alquila apresentando opcionalmente substituinte(s), alquenila apresentando opcionalmente substituinte(s), alquinila apresentando opcionalmente substituinte(s), cicloalquila apresentando opcionalmente substituinte(s), arila apresentando opcionalmente substituinte(s) e análogos.
[0035] Exemplos do “alquila" do “alquila apresentando opcionalmente substituinte(s)” indicado acima incluem C1-6 alquila (p. ex., metila, etila, propila, isopropila, butila, isobutila, s-butila, t-butila, pentila, hexila) e análogos.
[0036] Exemplos do substituinte que o “alquila apresentando opcionalmente substituinte(s)” indicado acima pode apresentam incluem o seguinte “grupo substituinte A” e análogos, e de 1 a 5 (de preferência, de 1 a 3) substituintes podem estar presentes em posição substituível ou posições substituíveis: Grupo substituinte Aátomo de halogênio (p. ex., átomo de flúor, átomo de cloro, átomo de bromo, átomo de iodo),ciano,C1-6 alquila (p. ex., metila, etila, propila, isopropila, butila, isobutila, s-butila, t-butila, pentila, hexila) opcionalmente apresentando de 1 a 3 substituintes selecionados dentre(1’) C6-10 arila (p. ex., fenila, naftila), (2’) amina,(3’) C1-6 alcóxi-carbonilamina (p. ex., metoxicarbonilamina, etoxicarbonilamina, propoxicarbonilamina),(4’) hidróxi,(5’) C1-6 alcóxi (p. ex., metóxi, etóxi, propóxi), e(6’) grupo heterocíclico (p. ex., pirrolidinila, benzodioxolila),C2-6 alquenila (p. ex., vinila, alila),C2-6 alquiila (p. ex., etinila, propargila),C3-6 cicloalquila (p. ex., ciclopropila, ciclobutila, ciclopentila, cicloexila) opcionalmente apresentando um hidróxi,C6-10 arila (p. ex., fenila, naftila) opcionalmente apresentando de 1 a 3 substituintes selecionados dentreátomo de halogênio (p. ex., átomo de flúor, átomo de cloro),hidróxi,ciano,C1-6 alquil-sulfonila (p. ex., metilsulfonila), eC1-6 alcóxi (p. ex., metóxi, etóxi, propóxi) opcionalmente apresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor),C1-6 alquil-carbonila (p. ex., acetila, etilcarbonila, propilcarbonila, butilcarbonila) opcionalmente apresentando de 1 a 3 substituintes selecionados dentre(1’) hidróxi,(2’) C1-6 alcóxi (p. ex., metóxi, etóxi),(3’) amina,(4’) C1-6 alquilamina (p. ex., metilamina, etilamina, propilamina, isopropilamina),(5’) C1-6 alquil-sulfonila (p. ex., metilsulfonila), e(6’) C1-6 alquil-carbonilóxi (p. ex., metilcarbonilóxi), C6-10 aril-carbonila (p. ex., benzoila, naftoíla) opcionalmente apresentando de 1 a 3 substituintes selecionados dentreátomo de halogênio (p. ex., átomo de cloro), eC1-6 alcóxi (p. ex., metóxi),carbamoíla,C1-6 alquil-carbamoíla (p. ex., metilcarbamoíla, etilcarbamoíla) opcionalmente apresentando um hidróxi,di-C1-6 alquil-carbamoíla (p. ex., dimetilcarbamoíla, dietilcarbamoíla),C6-10 aril-carbamoíla (p. ex., fenilcarbamoíla, naphtilcarbamoíla),carbamoíla cíclica com de 5 a 7 membros (p. ex., 1- pirrolidinilcarbonila, 1 -piperidilcarbonila, 1 —piperazinilcarbonila, 4- morfolinilcarbonila, 4-tiomorfolinilcarbonila, 1-homopiperazinilcarbonila),carboxila,C1-6 alcóxi-carbonila (p. ex., metoxicarbonila, etoxicarbonila, butoxicarbonila),C6-10 arilóxi-carbonila (p. ex., fenoxicarbonila),amina opcionalmente apresentando 1 ou 2 substituintes selecionados dentreC1-6 alcóxi-carbonila (p. ex., t-butoxicarbonila), eC1-6 alquil-carbonila (p. ex., metilcarbonila) opcionalmente apresentando um hidróxi ou C1-6 alquil-carbonilóxi (p. ex., metilcarbonilóxi),C1-6 alquilamina (p. ex., metilamina, etilamina, propilamina, isopropilamina, butilamina),di-C1-6 alquilamina (p. ex., dimetilamina, dietilamina, dipropilamina) opcionalmente apresentando um hidróxi,C1-6 alquil-carbonilamina (p. ex., acetilamina, etilcarbonilamina) opcionalmente apresentando de 1 a 3 substituintes selecionados dentreC1-6 alquil-carbonil-óxi (p. ex., metilcarbonilóxi),C1-6 alcóxi (p. ex., metóxi), ehidróxi,di-(C1-6 alquil-carbonil)amina (p. ex., di-(acetil)amina, di- (etilcarbonil)amina, di-(propilcarbonil)amina),C1-6 alcóxi-carbonilamina (p. ex., metoxicarbonilamina, etoxicarbonilamina, propoxicarbonilamina, t-butoxicarbonilamina),N-C1-6 alquila-N-(C1-6 alquil-carbonil)amina (p. ex., N- acetil-N-metilamina, N-acetil-N-etilamina),ureído,C1-6 alquila-ureído (p. ex., metilureído, etilureído),hidróxi,C1-6 alcóxi (p. ex., metóxi, etóxi, propóxi, isopropóxi, butóxi, isobutóxi, s-butóxi, t-butóxi) opcionalmente apresentando de 1 a 3 C610 arila (p. ex., fenila),C6-10 arilóxi (p. ex., fenóxi, naftóxi),grupo heterocíclico (p. ex., grupo heterocíclico aromático com 5 ou 6 membros, como 1-pirrolila, 2-piridila, 3-piridila, 4-piridila, 1- pirazolila, 1-imidazolila, 2-imidazolila, 2-pirazinila, 2-furila, 2-tiazolila, 4- pirimidinila e análogos; grupo heterocíclico não-aromático com de 3 a 8 membros, como 3-azetidinila, 1-pirrolidinila, 2-pirrolidinila, 3-pirrolidinila, 1- piperidila, 2-piperidila, 3-piperidila, 4-piperidila, 1-piperazinila, 1- morfolinila, morfolina, 2-tetraidrofurila, tetraidrotiopiran-4-ila, tetraidropiran- 4-ila, 3-azepanila, 4-azepanila e análogos; um grupo obtido por meio de fusão de um grupo heterocíclico não-aromático, como 1,3-benzodioxol-5-ila e análogos e um anel de benzeno) opcionalmente apresentando de 1 a 3 (de preferência 1 ou 2) substituintes selecionados dentre(1’) C1-6 alquila (p. ex., metila, etila, propila) opcionalmente apresentando de 1 a 3 substituintes selecionados dentreátomo de halogênio (p. ex., átomo de flúor), ehidróxi,(2’) hidróxi,(3’) oxo,(4’) ciano,(5’) carbamoíla,(6’) C1-6 alcóxi (p. ex., metóxi),(7’) C1-6 alquil-carbamoíla (p. ex., metilcarbamoíla),(8’) C1-6 alcóxi-carbonila (p. ex., t-butoxicarbonila), e(9’) C1-6 alquil-carbonila (p. ex., acetila, propionila) opcionalmente apresentando de 1 a 3 substituintes selecionados dentrehidróxi,C1-6 alcóxi (p. ex., metóxi, etóxi, propóxi),amina,C1-6 alquilamina (p. ex., metilamina, etilamina,propilamina, isopropilamina),di-C1-6 alquilamina (p. ex., dimetilamina), eC1-6 alquil-carbonilóxi (p. ex., metilcarbonilóxi),oxo,tioxo,C1-6 alquil-sulfonila (p. ex., metilsulfonila),heterociclil-carbonila (p. ex., pirrolidinilcarbonila, tetraidrofurilcarbonila).
[0037] Exemplos do “alquenila" do “alquenila apresentando opcionalmente substituinte(s)” indicado acima incluem C2-6 alquenila (p. ex., vinila, alila) e análogos.
[0038] Exemplos do substituinte do “alquenila apresentando opcionalmente substituinte(s)” indicado acima incluem o Grupo substituinte A indicado acima e análogos, e de 1 a 5 (de preferência, de 1 a 3) substituintes podem estar presentes na posição substituível ou posições substituíveis.
[0039] Exemplos do “alquinila" do “alquinila apresentando opcionalmente substituinte(s)” indicado acima incluem C2-6 alquinila (p. ex., etinila, propargila) e análogos.
[0040] Exemplos do substituinte que o “alquinila apresentando opcionalmente substituinte(s)” indicado acima pode apresentar incluem o Grupo substituinte A indicado acima e análogos, e de 1 a 5 (de preferência, de 1 a 3) substituintes podem estar presentes na posição substituível ou posições substituíveis.
[0041] Exemplos do “cicloalquila" do “cicloalquila apresentando opcionalmente substituinte(s)” indicado acima incluem C3-6 cicloalquila (p. ex., ciclopropila, ciclobutila, ciclopentila, cicloexila) e análogos.
[0042] Exemplos do substituinte que o “cicloalquila apresentando opcionalmente substituinte(s)” indicado acima pode apresentar incluem
[0043] (1) o Grupo substituinte A indicado acima,
[0044] (2) C1-6 alquila opcionalmente apresentando de 1 a 3substituintes selecionados do Grupo substituinte A indicado acima e análogos, e de 1 a 5 (de preferência, de 1 a 3) substituintes podem estar presentes na posição substituível ou posições substituíveis.
[0045] Além disso, o “cicloalquila apresentando opcionalmente substituinte(s)” pode ser um grupo obtido por meio de fusão de C3-6 cicloalquila e um anel de benzeno (p. ex., 1,2,3,4-tetraidronaftalen-1-ila).
[0046] Exemplos do “arila" do “arila apresentando opcionalmente substituinte(s)” indicado acima incluem C6-10 arila (p. ex., fenila, naftila) e análogos.
[0047] Exemplos do substituinte que o “arila apresentando opcionalmente substituinte(s)” indicado acima pode apresentar incluem(1) o Grupo substituinte A indicado acima (exceto oxo e tioxo),(2) C1-6 alquila opcionalmente apresentando de 1 a 3 substituintes selecionados do Grupo substituinte A indicado acima e análogos, e de 1 a 5 (de preferência, de 1 a 3) substituintes podem estar presentes na posição substituível ou posições substituíveis.
[0048] X é, de preferência, O, S ou NR1’ (R1’ é alquila apresentando opcionalmente substituinte(s)), e, de forma particularmente preferível, O, S ou N(C1-6 alquila) (particularmente, N(metila)).
[0049] R2 é carbamoíla apresentando opcionalmente substituinte(s).Exemplos do “carbamoíla apresentando opcionalmente substituinte(s)” para R2 incluem(1) carbamoíla opcionalmente apresentando 1 ou 2 substituinte(s) selecionado(s) dentre “grupo hidrocarboneto apresentando opcionalmente substituinte(s)” e “grupo heterocíclico apresentando opcionalmente substituinte(s)”,(2) carbamoíla cíclico apresentando opcionalmente substituinte(s)e análogos.
[0050] Exemplos do “grupo hidrocarboneto apresentando opcionalmente substituinte(s)” indicado acima incluem aqueles similares ao “grupo hidrocarboneto apresentando opcionalmente substituinte(s)” indicado acima para R1.
[0051] Exemplos do “grupo heterocíclico” do “grupo heterocíclico apresentando opcionalmente substituinte(s)” indicado acima, e o “grupo heterocíclico” indicado como um exemplo do substituinte que o “alquila apresentando opcionalmente substituinte(s)” indicado acima pode apresentar e análogos incluem grupo heterocíclico aromático e grupo heterocíclico não- aromático saturado ou insaturado (grupo heterocíclico alifático), cada um contendo, como um átomo constituinte do sistema de anel (átomo de anel), de 1 a 3 tipos (de preferência, 1 ou 2 tipos) de pelo menos um (de preferência, de 1 a 4, mais preferivelmente 1 ou 2) heteroátomo selecionado dentre átomo de oxigênio, átomo de enxofre (o átomo de enxofre pode ser oxidado) e átomo de nitrogênio, e um grupo apresentando uma ligação no átomo de carbono e análogos são usados.
[0052] Exemplos do “grupo heterocíclico aromático” incluem(1) grupo heterocíclico aromático monocíclico com 5 ou 6 membros, como furila, tienila, pirrolila, oxazolila, isoxazolila, tiazolila, isotiazolila, imidazolila, pirazolila, 1,2,3-oxadiazolila, 1,2,4-oxadiazolila, 1,3,4-oxadiazolila, furazanila, 1,2,3-tiadiazolila, 1,2,4-tiadiazolila, 1,3,4- tiadiazolila, 1,2,3-triazolila, 1,2,4-triazolila, tetrazolila, piridila, piridazinila, pirimidinila, pirazinila, triazinila e análogos, e(2) grupo heterocílico aromático policíclico condensado com de 8 a 12 membros, como benzofuranila, isobenzofuranila, benzo[b]tienila, indolila, isoindolila, 1H-indazolila, benzimidazolila, benzoxazolila, 1,2- benzoisooxazolila, benzotiazolila, benzopiranila, 1,2-benzoisotiazolila, 1H- benzotriazolila, quinolila, isoquinolila, cinolinila, quinazolinila, quinoxalinila, ftalazinila, naftiridinila, purinila, pteridinila, carbazolila, α-carbolinila, β- carbolinila, Y-carbolinila, acrydinila, fenoxazinila, fenotiazinila, fenazinila, fenoxatiinila, tiantrenila, fenantridinila, fenatrolinila, indolizinila, pirrol[1,2- b]piridazinila, pirazolo[1,5-a]piridila, imidazo[1,2-a]piridila, imidazo[1,5- a]piridila, imidazo[1,2-b]piridazinila, imidazo[1,2-a]pirimidinila, 1,2,4- triazolo[4,3-a]piridila, 1,2,4-triazolo[4,3-b]piridazinila e análogos, e análogos.
[0053] Exemplos do “grupo heterocíclico não-aromático” incluemgrupo heterocíclico não-aromático saturado ou não- saturado (de preferência, saturado) com de 3 a 8 membros (de preferência, com 5 ou 6 membros) (grupo heterocíclico alifático), como oxiranila, azepanila, azetidinila, oxetanila, tietanila, pirrolidinila, tetraidrofurila, tioranila, piperidila, tetraidropiranila, tetraidrotiopiranila, morfolinila, tiomorfolinila, piperazinila e análogos,grupo heterocíclico não-aromático sendo que a dupla ligação no grupo heterocíclico aromático monocíclico indicado acima ou grupo heterocíclico aromático condensado policíclico é parcialmente ou totalmente saturado, como 1,2,3,4-tetraidroquinolila, 1,2,3,4- tetraidroisoquinolila e análogos, eum grupo em que grupo heterocíclico não-aromático, como benzodioxolila e análogos e anel de benzeno são fundidose análogos.
[0054] Exemplos do “substituinte” do “grupo heterocíclico apresentando opcionalmente substituinte(s)” indicado acima incluem(1) o Grupo substituinte A indicado acima,(2) aqueles similares ao “grupo hidrocarboneto apresentando opcionalmente substituinte(s)” indicado acima (de preferência C1-6 alquila opcionalmente apresentando de 1 a 3 substituintes selecionados do Grupo substituinte A indicado acima)e análogos, e substituintes em um número substituível podem estar presentes na posição substituível ou posições substituíveis.Como carbamoíla cíclica da “carbamoíla cíclica apresentando opcionalmente substituinte(s)”, usa-substância carbamoíla cíclica com de 5 a 7 membros, e exemplos da mesma incluem pirrolidin-1-ilcarbonila, piperidin- 1-ilcarbonila, piperazin-1-ilcarbonila, morfolin-4-ilcarbonila, tiomorfolin-4- ilcarbonila, homopiperazin-1-ilcarbonila e análogos.
[0055] Exemplos do “substituinte” da “carbamoíla cíclica apresentando opcionalmente substituinte(s)” incluem o Grupo substituinte A indicado acima e análogos, e de 1 a 3 substituintes podem estar presentes na posição substituível ou posições substituíveis.Adicionalmente, os substituintes da carbamoíla cíclica apresentando opcionalmente substituinte(s) podem ser ligados entre si para formar um anel com de 5 a 7 membros. Em outras palavras, o anel com de 5 a 7 membros e carbamoíla cíclica pode formar um sistema de anel fundido. O sistema de anel fundido inclui um sistema spiro de anel fundido.
[0056] Exemplos do anel com de 5 a 7 membros incluem(1) anel homocíclico com de 5 a 7 membros (p. ex., cicloexano, cicloexeno, cicloexanodieno, cicloeptano, benzeno), e(2) heterociclo com de 5 a 7 membros (p. ex., piperidina, piperazina, morfolina, tiomorfolina, piridina, pirazina, pirimidina, piridazina, triazina, pirano, diidropirano, tetraidropirano, 1,3-dioxol). Entre estes são preferíveis anel de cicloexano, anel de benzeno e anel 1,3-dioxol.Como R2,(A) carbamoíla opcionalmente apresentando 1 ou 2 substituintes selecionados dentreC1-6 alquila opcionalmente apresentando 1 ou 2 (de preferência 1) substituintes selecionados dentre(1’) átomo de halogênio,(2’) ciano,(3’) amina,(4’) C1-6 alquilamina,(5’) di-C1-6 alquilamina opcionalmente apresentando um hidróxi,(6’) C1-6 alcóxi-carbonilamina,(7’) hidróxi,(8’) di-C1-6 alquil-carbamoíla,(9’) carbamoíla cíclica com de 5 a 7 membros,(10’) grupo heterocíclico opcionalmente apresentando de 1 a 3 (de preferência 1) substituintes selecionados dentrehidróxi, C1-6 alquila opcionalmente apresentando um hidróxi,oxo,C1-6 alcóxi-carbonila, eC1-6 alquil-carbonila opcionalmente apresentando de 1 a 3(de preferência 1) substituintes selecionados dentre C1-6 alquil-carbonilóxi e hidróxi,(11’) C1-6 alcóxi-carbonila,(12’) C3-6 cicloalquila opcionalmente apresentando um hidróxi,(13’) C1-6 alcóxi,(14’) C2-6 alquinila,(15’) C6-10 arila opcionalmente apresentando de 1 a 3 (depreferência 1 ou 2) C1-6 alcóxi,(16’) carbamoíla, e(17’) C1-6 alquil-carbonil-amina opcionalmente apresentandode 1 a 3 (de preferência 1) substituintes selecionados dentreC1-6 alquil-carbonilóxi,C1-6 alcóxi, ehidróxi,C3-6 cicloalquila ou 1,2,3,4-tetraidronaftalenilaopcionalmente apresentando 1 ou 2 substituintes selecionados dentre(1’) amina opcionalmente apresentando um substituinte selecionado deC1-6 alcóxi-carbonila, eC1-6 alquil-carbonila opcionalmente apresentando de 1 a 3(de preferência 1) substituintes selecionados dentre hidróxi e C1-6 alquil- carbonilóxi,(2’) hidróxi, (3’) carbóxi, (4’) C1-6 alcóxi-carbonila, (5’) C1-6 alquil-carbamoíla opcionalmente apresentando um hidróxi,(6’) C1-6 alquila opcionalmente apresentando um hidróxi, e(7’) C1-6 alcóxi-carbonilamina (p. ex., t-butoxicarbonilamina),C6-10 arila, egrupo heterocíclico opcionalmente apresentando de 1 a 4 (de preferência 1) substituintes selecionados dentre(1’) C1-6 alquila opcionalmente apresentando de 1 a 5 substituintes selecionados dentreC6-10 arila,hidróxi, eátomo de halogênio,(2’) C1-6 alquil-carbonila opcionalmente apresentando de 1 a 3(de preferência 1) substituintes selecionados dentreC1-6 alquil-carbonilóxi,hidróxi,C1-6 alcóxi,C1-6 alquil-sulfonila, eamina,(3’) C1-6 alcóxi-carbonila, e(4’) grupo heterocíclico aromático com 5 ou 6 membros opcionalmente apresentando de 1 a 3 (de preferência 1) substituintes selecionados dentreC1-6 alquila opcionalmente apresentando de 1 a 3 átomos de halogênio,ciano,carbamoíla,C1-6 alcóxi, eC1-6 alquil-carbamoíla, (5’) oxo,(6’) C1-6 alquil-carbamoíla,(7’) C1-6 alquil-sulfonila,(8’) C6-10 arila opcionalmente apresentando de 1 a 3 (de preferência 1) substituintes selecionados dentrehidróxi,ciano, eC1-6 alquil-sulfonila,(9’) heterociclil-carbonila, e(10’) C6-10 arilóxi-carbonila (p. ex., fenoxicarbonila),(B) carbamoíla cíclica com de 5 a 7 membros opcionalmente apresentando de 1 a 3 (de preferência 1) substituintes selecionados dentreC1-6 alquila opcionalmente apresentando de 1 a 3 (de preferência 1) substituintes selecionados dentregrupo heterocíclico,amina,C1-6 alcóxi, eC6-10 arila,amina opcionalmente apresentando um C1-6 alquil- carbonila,N-C1-6 alquila-N-(C1-6 alquil-carbonil)amina,grupo heterocíclico,C1-6 alquil-carbonila opcionalmente apresentando um substituinte selecionado dehidróxi,C1-6 alcóxi,amina,C1-6 alquilamina,di-C1-6 alquilamina, e C1-6 alquil-carbonilóxi,C6-10 arila, eoxo, ou(C) carbamoíla cíclica com de 5 a 7 membros fundida com anel de 5 a 7 membrosé preferível.
[0057] R3 é hidróxi apresentando opcionalmente substituinte(s).Como o “substituinte” do “hidróxi apresentando opcionalmente substituinte(s)” para R3, o “grupo hidrocarboneto apresentando opcionalmente substituinte(s)” indicado acima para R1, o “grupo heterocíclico apresentando opcionalmente substituinte(s)” indicado acima e análogos podem ser indicados.
[0058] Como R3, hidróxi opcionalmente apresentando alquila apresentando opcionalmente substituinte(s) é preferível, hidróxi opcionalmente apresentandoC1-6 alquila opcionalmente apresentando um C1-6 alcóxi,C1-6 alquila opcionalmente apresentando de 1 a 5 (de preferência, de 1 a 3) átomos de halogênio,C1-6 alquila opcionalmente apresentando um C6-10 arila, ouC1-6 alquila opcionalmente apresentando um grupo heterocíclico é mais preferível, ehidróxi substituído porC1-6 alquila opcionalmente apresentando um C1-6 alcóxi,C1-6 alquila opcionalmente apresentando de 1 a 5 (de preferência, de 1 a 3) átomos de halogênio,C1-6 alquila opcionalmente apresentando um C6-10 arila, ougrupo C1-6 alquila opcionalmente apresentando um heterocíclicoé ainda mais preferível.
[0059] Anel A é um anel com de 5 a 7 membros apresentando opcionalmente substituinte(s). Como o “anel de 5 a 7 membros” do “anel com de 5 a 7 membros apresentando opcionalmente substituinte(s)” para anel A,(1) anel homocíclico com de 5 a 7 membros (p. ex., cicloexano, cicloexeno, cicloexanodieno, cicloeptano, benzeno), e(2) heterociclo com de 5 a 7 membros (p. ex., piperidina, piperazina, morfolina, tiomorfolina, piridina, pirazina, pirimidina, piridazina, triazina, pirano, diidropirano, tetraidropirano, 1,3-dioxol)podem ser indicados.
[0060] Exemplos do “substituinte” que o “anel com de 5 a 7 membros” do “anel com de 5 a 7 membros apresentando opcionalmente substituinte(s)” para anel A podem apresentar, incluem(1) o Grupo substituinte A indicado acima,(2) aqueles similares ao “grupo hidrocarboneto apresentando opcionalmente substituinte(s)” indicado acima (de preferência, C1-6 alquila opcionalmente apresentando de 1 a 3 substituintes selecionados do Grupo substituinte A) indicado acimae análogos, e substituintes em um número substituível podem estar presentes na posição substituível ou posições substituíveis.
[0061] Adicionalmente, quanto ao “substituinte” que o “anel com de 5 a 7 membros” do “anel com de 5 a 7 membros apresentando opcionalmente substituinte(s)” para anel A pode apresentar, dois substituintes são opcionalmente ligados entre si para formar um anel. Como o anel formado por referidos “substituintes” ligados entre si,(1) anel homocíclico com de 5 a 7 membros (p. ex., cicloexano, cicloexeno, cicloexanodieno, cicloeptano, benzeno), e(2) heterociclo com de 5 a 7 membros (p. ex., piperidina, piperazina, morfolina, tiomorfolina, piridina, pirazina, pirimidina, piridazina, triazina, pirano, diidropirano, tetraidropirano, 1,3-dioxol) podem ser indicados.
[0062] O anel formado pelos substituintes do anel A, que são ligados entre si, pode apresentar substituinte(s) e exemplos do substituinte incluemo Grupo substituinte A indicado acima,aqueles similares ao “grupo hidrocarboneto apresentando opcionalmente substituinte(s)” indicado acima (de preferência, C1-6 alquila opcionalmente apresentando de 1 a 3 substituintes selecionados do Grupo substituinte A) indicado acima e análogos, e substituintes em um número substituível podem estar presentes na posição substituível ou posições substituíveis.
[0063] Composto (I) apresenta especificamente uma estruturarepresentada pela fórmula a seguir.sendo que anel A1 - anel A20 apresenta opcionalmente maissubstituinte(s), os substituintes são opcionalmente ligados entre si para formar um anel, parte -CH2-CH2- constituindo o anel no anel A1, anel A7, anel A8, anel A9, anel A10, anel A11, anel A12, anel A14, anel A15, anel A16, anel A17, anel A18, anel A19 e anel A20 é opcionalmente convertido o -CH=CH-, parte - NH-CH2- constituindo o anel no anel A2, anel A5, anel A8, anel A11, anel A13, anel A15, anel A18 e anel A20 é opcionalmente convertido a -N=CH-, e outros símbolos são como definido acima.
[0064] Como o substituinte que anel A1 - anel A20 pode apresentar, aqueles similares ao “substituinte” que o “anel de 5 a 7 membros” do “anel com de 5 a 7 membros apresentando opcionalmente substituinte(s)” para anel A pode apresentar, podem ser indicados.
[0065] Como composto (I), um composto representado pela fórmula sendo que cada símbolo é como definido acima, é preferível.
[0066] Dos compostos indicados acima, composto (I”’) representado pela fórmulasendo que X, R2 e R3 são como definido acima, RAA1 e RAA2 são iguais ou diferentes e cada um é um átomo de hidrogênio ou um substituinte, ou RAA1 e RAA2 são opcionalmente ligados entre si para formar um anel com de 5 a 7 membros apresentando opcionalmente substituinte(s), e R4 é um átomo de hidrogênio ou um grupo hidrocarboneto apresentando opcionalmente substituinte(s), é preferível.
[0067] Composto (I”’) é explicado detalhadamente a seguir.
[0068] X, R2 e R3 são como definido acima.
[0069] R4 é um átomo de hidrogênio ou um grupo hidrocarbonetoapresentando opcionalmente substituinte(s). Como o “grupo hidrocarboneto apresentando opcionalmente substituinte(s)” para R4, é possível indicar aqueles similares ao “grupo hidrocarboneto apresentando opcionalmente substituinte(s)” indicado acima para R1 podem ser indicados.
[0070] Como R4, um átomo de hidrogênio ou alquila apresentando opcionalmente substituinte(s) é preferível. Particularmente, são preferíveis (1) átomo de hidrogênio,(2) C1-6 alquila opcionalmente apresentando um substituinte selecionado de(1’) C3-6 cicloalquila,(2’) C6-10 arila opcionalmente apresentando (i) 1 ou 2 C1-6 alcóxi opcionalmente apresentando de 1 a 3 átomos de halogênio ou (ii) de 1 a 3 átomos de halogênio,(3’) C1-6 alquil-carbonila,(4’) C6-10 aril-carbonila opcionalmente apresentando um átomo de halogênio ou C1-6 alcóxi,(5’) C1-6 alcóxi-carbonila,(6’) C6-10 aril-carbamoíla,(7’) grupo heterocíclico opcionalmente apresentando 1 ou 2 C1-6 alquila opcionalmente apresentando de 1 a 3 átomos de halogênio,(8’) C6-10 arilóxi,(9’) carbóxi,(10’) ciano, e(11’) C1-6 alcóxi opcionalmente apresentando um C6-10 arila,C1-6 alquila opcionalmente apresentando de 1 a 3 átomos de halogênio e análogos.(1) RAA1 e RAA2 são iguais ou diferentes e cada um é um átomo de hidrogênio ou um substituinte. Como o substituinte, é possível indicar aqueles similares ao substituinte indicado acima para anel A.Como RAA1, é preferível um átomo de hidrogênio ou grupo C16 alquila.Como RAA2, um átomo de hidrogênio ou grupo C1-6 alquila é preferível.
[0071] Alternativamente,(2) RAA1 e RAA2 são ligados entre si para formar um anel com de 5 a 7 membros apresentando opcionalmente substituinte(s). Como o “anel com de 5 a 7 membros apresentando opcionalmente substituinte(s)”, é possível indicar aqueles similares ao “anel com de 5 a 7 membros apresentando opcionalmente substituinte(s)” indicado acima para anel A. O anel com de 5 a 7 membros opcionalmente apresenta um número substituível de substituintes em posições substituíveis.
[0072] Em uma concretização, composto (I’) representado pela fórmulasendo que X, R2 e R3 são como definido acima, anel B é um anel com 6 membros apresentando opcionalmente substituinte(s), e R4 é um átomo de hidrogênio ou um grupo hidrocarboneto apresentando opcionalmente substituinte(s), em que RAA1 e RAA2 são ligados entre si para formar um anel com 6 membros apresentando opcionalmente substituinte(s), é preferível dentre os compostos (I”’) indicados acima.
[0073] Composto (I’) é explicado detalhadamente a seguir.
[0074] X, R2, R3 e R4 são como definido acima.Na fórmula (I’), exemplos preferíveis de R2 incluem(A) carbamoíla opcionalmente apresentando 1 ou 2 substituintes selecionados dentreC1-6 alquila (p. ex., metila, etila, propila, isopropila, n- butila, 2-metilpropila, 2,2-dimetilpropila, 1-metilbutila, 1-etilpropila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentre(1’) átomo de halogênio (p. ex., átomo de flúor),(2’) ciano,(3’) amina,(4’) C1-6 alquilamina (p. ex., isopropilamina),(5’) di-C1-6 alquilamina (p. ex., dimetilamina, dietilamina, di-i- propilamina) opcionalmente apresentando um hidróxi,(6’) C1-6 alcóxi-carbonilamina (p. ex., t-butoxicarbonilamina),(7’) hidróxi,(8’) di-C1-6 alquil-carbamoíla (p. ex., dietilcarbamoíla),(9’) carbamoíla cíclica com de 5 a 7 membros (p. ex., 1- pirrolidinilcarbonila),(10’) grupo heterocíclico (p. ex., 1-pirrolidinila, 2-pirrolidinila, 3-pirrolidinila, 1-pirazolila, 1-imidazolila, 1-piperidila, 2-piperidila, 3- piperidila, 4-piperidila, 1-piperazinila, 1-morfolinila, morfolina, 2-piridila, 3- piridila, 4-piridila, 2-pirazinila, 2-furila, 2-tetraidrofurila, 1,3-benzodioxol-5- ila) opcionalmente apresentando umhidróxi,C1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um hidróxi,oxo,C1-6 alcóxi-carbonila (p. ex., t-butoxicarbonila), ou C1-6 alquil-carbonila (p. ex., metilcarbonila) opcionalmente apresentando um substituinte selecionado de C1-6 alquil-carbonilóxi (p. ex., metilcarbonilóxi) e hidróxi,(11’) C1-6 alcóxi-carbonila (p. ex., etoxicarbonila),(12’) C3-6 cicloalquila (p. ex., ciclopropila, cicloexila) opcionalmente apresentando um hidróxi,(13’) C1-6 alcóxi (p. ex., metóxi, i-propóxi),(14’) C2-6 alquinila (p. ex., etinila),(15’) C6-10 arila (p. ex., fenila) opcionalmente apresentando 1 ou 2 C1-6 alcóxi (p. ex., metóxi),(16’) carbamoíla, e(17’) C1-6 alquil-carbonil-amina (p. ex., metilcarbonilamina) opcionalmente apresentando um substituinte selecionado dentreC1-6 alquil-carbonil-óxi (p. ex., metilcarbonilóxi),C1-6 alcóxi (p. ex., metóxi), ehidróxi,C3-6 cicloalquila (p. ex., ciclopropila, cicloexila) ou 1,2,3,4- tetraidronaftalenila (p. ex., 1,2,3,4-tetraidronaftalen-1-ila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentre(1’) amina opcionalmente apresentando um substituinte selecionado dentreC1-6 alcóxi-carbonila (p. ex., t-butoxicarbonila), eC1-6 alquil-carbonila (p. ex., metilcarbonila) opcionalmente apresentando um hidróxi ou C1-6 alquil-carbonilóxi (p. ex., metilcarbonilóxi),(2’) hidróxi,(3’) carbóxi,(4’) C1-6 alcóxi-carbonila (p. ex., metoxicarbonila),(5’) C1-6 alquil-carbamoíla (p. ex., etilcarbamoíla)opcionalmente apresentando um hidróxi, (6’) C1-6 alquila (p. ex., metila) opcionalmente apresentando um hidróxi, e(7’) C1-6 alcóxi-carbonilamina (p. ex., t-butoxicarbonilamina),C6-10 arila (p. ex., fenila), egrupo heterocíclico (p. ex., 3-azetidinila, 3-pirrolidinila, 4- piperidila, 2-tetraidrofurila, 3-azepanila, 4-azepanila, tetraidrotiopiran-4-ila, tetraidropiran-4-ila) opcionalmente apresentando de 1 a 4 substituintes selecionados dentre(1’) C1-6 alquila (p. ex., metila, etila, n-propila) opcionalmente apresentando de 1 a 5 substituintes selecionados dentreC6-10 arila (p. ex., fenila),hidróxi, eátomo de halogênio,(2’) C1-6 alquil-carbonila (p. ex., metilcarbonila, etilcarbonila, i-propilcarbonila, i-butilcarbonila) opcionalmente apresentando um substituinte selecionado dentreC1-6 alquil-carbonilóxi (p. ex., metilcarbonilóxi),hidróxi,C1-6 alcóxi (p. ex., metóxi),C1-6 alquil-sulfonila (p. ex., metilsulfonila), eamina,(3’) C1-6 alcóxi-carbonila (p. ex., t-butoxicarbonila),(4’) grupo heterocíclico aromático com 5 ou 6 membros (p. ex., 2-piridila, 3-piridila, 4-piridila, 2-tiazolila, 4-pirimidinila) opcionalmente apresentando um substituinte selecionado dentreC1-6 alquila (p. ex., metila) opcionalmente apresentando de1 a 3 átomos de halogênio (p. ex., átomo de flúor),ciano,carbamoíla, C1-6 alcóxi (p. ex., metóxi), eC1-6 alquil-carbamoíla (p. ex., metilcarbamoíla),(5’) oxo,(6’) C1-6 alquil-carbamoíla (p. ex., etilcarbamoíla),(7’) C1-6 alquil-sulfonila (p. ex., metilsulfonila),) C6-10 arila (p. ex., fenila) opcionalmente apresentando um substituinte selecionado dentrehidróxi,ciano, eC1-6 alquil-sulfonila (p. ex., metilsulfonila),) heterociclil-carbonila (p. ex., 2-pirrolidinilcarbonila, 2- tetraidrofurilcarbonila), e(10’) C6-10 arilóxi-carbonila (p. ex., fenoxicarbonila),carbamoíla cíclica com de 5 a 7 membros (p. ex., 1- pirrolidinilcarbonila, 1-piperidilcarbonila, 1-piperazinilcarbonila, 1- homopiperazinilcarbonila, morfolinocarbonila, tiomorfolinocarbonila) opcionalmente apresentando um substituinte selecionado dentreC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um substituinte selecionado dentregrupo heterocíclico (p. ex., 1-pirrolidinila, benzodioxol-5- ila),amina,C1-6 alcóxi (p. ex., metóxi), eC6-10 arila (p. ex., fenila),amina opcionalmente apresentando um C1-6 alquil- carbonila (p. ex., acetila),N-C1-6 alquila-N-(C1-6 alquil-carbonil)amina (p. ex., N- acetil-N-etilamina),grupo heterocíclico (p. ex., 1-pirrolidinila, 2-piridila), C1-6 alquil-carbonila (p. ex., acetila, propionila)opcionalmente apresentando um substituinte selecionado dentrehidróxi,C1-6 alcóxi (p. ex., metóxi, etóxi),amina,C1-6 alquilamina (p. ex., isopropilamina),di-C1-6 alquilamina (p. ex., dimetilamina), eC1-6 alquil-carbonilóxi (p. ex., metilcarbonilóxi),C6-10 arila (p. ex., fenila), eoxo, e(C) carbamoíla cíclica com de 5 a 7 membros fundida com anel com de 5 a 7 membros (p. ex., anel cicloexano, anel benzeno, anel 1,3- dioxol) (p. ex., 1-piperidilcarbonila).Na fórmula (I’), exemplos preferíveis de R3 incluem hidróxi opcionalmente apresentandoC1-6 alquila (p. ex., metila, etila, n-butila) opcionalmente apresentando umC1-6 alcóxi (p. ex., etóxi),C6-10 arila (p. ex., fenila), ougrupo heterocíclico (p. ex., 4-piridila, morfolina, 2- tetraidrofurila), ouC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor)[de preferência, hidróxi substituído porC1-6 alquila (p. ex., metila, etila, n-butila) opcionalmente apresentando umC1-6 alcóxi (p. ex., etóxi),C6-10 arila (p. ex., fenila), ougrupo heterocíclico (p. ex., 4-piridila, morfolina, 2- tetraidrofurila), ouC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor)].Na fórmula (I’), exemplos preferíveis de R4 incluemátomo de hidrogênio,C1-6 alquila (p. ex., metila, etila, n-propila, n-butila, n- pentila, i-pentila, 2-etilbutila) opcionalmente apresentando um substituinte selecionado dentre(1’) C3-6 cicloalquila (p. ex., ciclopropila, cicloexila),(2’) C6-10 arila (p. ex., fenila) opcionalmente apresentando (i) um C1-6 alcóxi (p. ex., metóxi) opcionalmente apresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor) ou (ii) de 1 a 3 átomos de halogênio (p. ex., átomo de flúor, átomo de cloro),(3’) C1-6 alquil-carbonila (p. ex., metilcarbonila, t-butilcarbonila),(4’) C6-10 aril-carbonila (p. ex., benzoila),(5’) C1-6 alcóxi-carbonila (p. ex., metoxicarbonila, etoxicarbonila, t-butoxicarbonila),(6’) C6-10 aril-carbamoíla (p. ex., fenilcarbamoíla),(7’) grupo heterocíclico (p. ex., 2-piridila, 3-piridila, 4-piridila, 1-pirrolila, 2-imidazolila, 2-furila, 2-tetraidrofurila) opcionalmente apresentando 1 ou 2 C1-6 alquila (p. ex., metila) opcionalmente apresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor),(8’) C6-10 arilóxi (p. ex., fenóxi),(9’) carbóxi,(10’) ciano, e(11’) C1-6 alcóxi (p. ex., metóxi) opcionalmente apresentando um C6-10 arila (p. ex., fenila), eC1-6 alquila (p. ex., etila) opcionalmente apresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor).
[0075] Anel B é um anel com 6 membros apresentando opcionalmente substituinte(s). Como o “anel com 6 membros” do “anel com 6 membros apresentando opcionalmente substituinte(s)”, é possível indicar(1) anel homocíclico (p. ex., cicloexano, cicloexeno, cicloexanodieno, benzeno), e(2) heterociclo (p. ex., piperidina, piperazina, morfolina, tiomorfolina, piridina, pirazina, pirimidina, piridazina, triazina, pirano, diidropirano, tetraidropirano).
[0076] Exemplos do substituinte que o anel B pode apresentar incluemo Grupo substituinte A indicado acima,C1-6 alquila opcionalmente apresentando de 1 a 3 substituintes selecionados do Grupo substituinte Ae análogos, e substituintes em um número substituível podem estar presentes na posição substituível ou posições substituíveis.
[0077] Como anel B, anel cicloexeno apresentando opcionalmente substituinte(s), anel de benzeno apresentando opcionalmente substituinte(s), ou anel piridina apresentando opcionalmente substituinte(s) é preferível, e anel cicloexeno, anel de benzeno opcionalmente apresentando um átomo de halogênio (p. ex., átomo de flúor), ou anel piridina é mais preferível. Particularmente, anel de benzeno e anel piridina são preferíveis.
[0078] Dentre compostos (I’), um composto em queanel B é um anel com 6 membros apresentando opcionalmente substituinte(s),X é O, S ou N(C1-6 alquila),R2 é carbamoíla apresentando opcionalmente substituinte(s),R3 é hidróxi opcionalmente apresentando C1-6 alquila apresentando opcionalmente substituinte(s), e R4 é um átomo de hidrogênio ou C1-6 alquila apresentando opcionalmente substituinte(s)é preferível.
[0079] Exemplos específicos de composto (I’) preferível incluem os seguintes.Composto (I’-1)Composto (I’) em queX é O, S ou N(C1-6 alquila) (particularmente N(metila));R2 écarbamoíla opcionalmente apresentando 1 ou 2 substituintes selecionados dentreC1-6 alquila (p. ex., metila, etila, propila, isopropila, 2,2- dimetilpropila, 1-metilbutila) opcionalmente apresentando um substituinte selecionado dentre(1’) átomo de halogênio (p. ex., átomo de flúor),(2’) ciano,(3’) amina,(4’) C1-6 alquilamina (p. ex., isopropilamina),(5’) di-C1-6 alquilamina (p. ex., dimetilamina, dietilamina) opcionalmente apresentando um hidróxi,(6’) C1-6 alcóxi-carbonilamina (p. ex., t-butoxicarbonilamina),(7’) hidróxi,(8’) di-C1-6 alquil-carbamoíla (p. ex., dietilcarbamoíla),(9’) carbamoíla cíclica com de 5 a 7 membros (p. ex., 1- pirrolidinilcarbonila),(10’) grupo heterocíclico (p. ex., 1-pirrolidinila, 2-pirrolidinila, 3-pirrolidinila, 1-pirazolila, 1-imidazolila, 1-piperidila, 2-piperidila, 3- piperidila, 4-piperidila, 1-piperazinila, 1-morfolinila, 2-piridila, 3-piridila) opcionalmente apresentando um hidróxi, ouC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um hidróxi, e(11’) C1-6 alcóxi-carbonila (p. ex., etoxicarbonila),C3-6 cicloalquila (p. ex., cicloexila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentre(1’) amina, e(2’) hidróxi,C6-10 arila (p. ex., fenila), egrupo heterocíclico (p. ex., 3-pirrolidinila, 4-piperidila) opcionalmente apresentando um C1-6 alquila (p. ex., metila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentreC6-10 arila (p. ex., fenila), ehidróxi, oucarbamoíla cíclica com de 5 a 7 membros (p. ex., 1- pirrolidinilcarbonila, 1-piperidilcarbonila, 1-homopiperazinilcarbonila) opcionalmente apresentando um substituinte selecionado dentreC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um substituinte selecionado dentregrupo heterocíclico (p. ex., 1-pirrolidinila, benzodioxol-5- ila), eamina,amina,N-C1-6 alquila-N-(C1-6 alquil-carbonil)amina (p. ex., N- acetil-N-etilamina),grupo heterocíclico (p. ex., 1-pirrolidinila), eC1-6 alquil-carbonila (p. ex., acetila, propionila)opcionalmente apresentando um substituinte selecionado dentrehidróxi, C1-6 alcóxi (p. ex., metóxi),amina, eC1-6 alquilamina (p. ex., isopropilamina);R3 é hidróxi opcionalmente apresentando C1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um C1-6 alcóxi (p. ex., etóxi);R4 éátomo de hidrogênio, ouC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um substituinte selecionado dentre(1’) C3-6 cicloalquila (p. ex., ciclopropila),(2’) C6-10 arila (p. ex., fenila) opcionalmente apresentando umC1-6 alcóxi (p. ex., metóxi),(3’) C1-6 alquil-carbonila (p. ex., t-butilcarbonila),(4’) C6-10 aril-carbonila (p. ex., benzoila),(5’) C1-6 alcóxi-carbonila (p. ex., etoxicarbonila),(6’) C6-10 aril-carbamoíla (p. ex., fenilcarbamoíla),(7’) grupo heterocíclico (p. ex., 2-piridila),(8’) C6-10 arilóxi (p. ex., fenóxi), e(9’) carbóxi; eanel B é anel de benzeno.Composto (I’-2)Composto (I’) em queX é O, S ou N(C1-6 alquila) (particularmente N(metila));R2 écarbamoíla opcionalmente apresentando 1 ou 2 substituintes selecionados dentreC1-6 alquila (p. ex., metila, etila, propila, isopropila, 2- metilpropila, 2,2-dimetilpropila, 1-metilbutila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentre (1’) átomo de halogênio (p. ex., átomo de flúor),(2’) ciano,(3’) amina,(4’) C1-6 alquilamina (p. ex., isopropilamina),(5’) di-C1-6 alquilamina (p. ex., dimetilamina, dietilamina) opcionalmente apresentando um hidróxi,(6’) C1-6 alcóxi-carbonilamina (p. ex., t-butoxicarbonilamina),(7’) hidróxi,(8’) di-C1-6 alquil-carbamoíla (p. ex., dietilcarbamoíla),(9’) carbamoíla cíclica com de 5 a 7 membros (p. ex., 1- pirrolidinilcarbonila),(10’) grupo heterocíclico (p. ex., 1-pirrolidinila, 2-pirrolidinila, 3-pirrolidinila, 1-pirazolila, 1-imidazolila, 1-piperidila, 2-piperidila, 3- piperidila, 4-piperidila, 1-piperazinila, 1-morfolinila, 2-piridila, 3-piridila) opcionalmente apresentando um (a) hidróxi, ou (b) C1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um hidróxi,(11’) C1-6 alcóxi-carbonila (p. ex., etoxicarbonila), e(12’) C3-6 cicloalquila (p. ex., cicloexila),C3-6 cicloalquila (p. ex., cicloexila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentre(1’) amina, e(2’) hidróxi,C6-10 arila (p. ex., fenila), egrupo heterocíclico (p. ex., 3-pirrolidinila, 4-piperidila) opcionalmente apresentando um substituinte selecionado dentre(1’) C1-6 alquila (p. ex., metila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentreC6-10 arila (p. ex., fenila), ehidróxi, (2’) C1-6 alquil-carbonila (p. ex., metilcarbonila)opcionalmente apresentando um substituinte selecionado dentreC1-6 alquil-carbonilóxi (p. ex., metilcarbonilóxi), ehidróxi,(3’) C1-6 alcóxi-carbonila (p. ex., t-butoxicarbonila), e(4’) grupo heterocíclico aromático com 5 ou 6 membros (p. ex., 4-piridila), oucarbamoíla cíclica com de 5 a 7 membros (p. ex., 1- pirrolidinilcarbonila, 1-piperidilcarbonila, 1-homopiperazinilcarbonila) opcionalmente apresentando um substituinte selecionado dentreC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um substituinte selecionado dentregrupo heterocíclico (p. ex., 1-pirrolidinila, benzodioxol-5- ila), eamina,amina,N-C1-6 alquila-N-(C1-6 alquil-carbonil)amina (p. ex., N- acetil-N-etilamina),grupo heterocíclico (p. ex., 1-pirrolidinila), eC1-6 alquil-carbonila (p. ex., acetila, propionila) opcionalmente apresentando um substituinte selecionado dentrehidróxi,C1-6 alcóxi (p. ex., metóxi),amina, eC1-6 alquilamina (p. ex., isopropilamina);R3 é hidróxi opcionalmente apresentando(1) C1-6 alquila (p. ex., metila, etila) opcionalmenteapresentando um C1-6 alcóxi (p. ex., etóxi), ou(2) C1-6 alquila (p. ex., metila, etila) opcionalmente apresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor)[de preferência, hidroxila substituído por(1) C1-6 alquila (p. ex., metila, etila) opcionalmenteapresentando um C1-6 alcóxi (p. ex., etóxi), ou(2) C1-6 alquila (p. ex., metila, etila) opcionalmenteapresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor)];R4 é(1) átomo de hidrogênio, ou(2) C1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um substituinte selecionado dentre(1’) C3-6 cicloalquila (p. ex., ciclopropila),(2’) C6-10 arila (p. ex., fenila) opcionalmente apresentando umC1-6 alcóxi (p. ex., metóxi),(3’) C1-6 alquil-carbonila (p. ex., t-butilcarbonila),(4’) C6-10 aril-carbonila (p. ex., benzoila),(5’) C1-6 alcóxi-carbonila (p. ex., etoxicarbonila),(6’) C6-10 aril-carbamoíla (p. ex., fenilcarbamoíla),(7’) grupo heterocíclico (p. ex., 2-piridila),(8’) C6-10 arilóxi (p. ex., fenóxi), e(9’) carbóxi; eanel B é anel cicloexeno ou anel de benzeno (particularmente, anel de benzeno).Composto (I’-3)Composto (I’) em queX é O, S ou N(C1-6 alquila) (particularmente N(metila));R2 é(A) carbamoíla opcionalmente apresentando 1 ou 2 substituintes selecionados dentreC1-6 alquila (p. ex., metila, etila, propila, isopropila, n- butila, 2-metilpropila, 2,2-dimetilpropila, 1-metilbutila, 1-etilpropila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentre(1’) átomo de halogênio (p. ex., átomo de flúor),(2’) ciano,(3’) amina,(4’) C1-6 alquilamina (p. ex., isopropilamina),(5’) di-C1-6 alquilamina (p. ex., dimetilamina, dietilamina, di-i- propilamina) opcionalmente apresentando um hidróxi,(6’) C1-6 alcóxi-carbonilamina (p. ex., t-butoxicarbonilamina),(7’) hidróxi,(8’) di-C1-6 alquil-carbamoíla (p. ex., dietilcarbamoíla),(9’) carbamoíla cíclica com de 5 a 7 membros (p. ex., 1- pirrolidinilcarbonila),(10’) grupo heterocíclico (p. ex., 1-pirrolidinila, 2-pirrolidinila, 3-pirrolidinila, 1-pirazolila, 1-imidazolila, 1-piperidila, 2-piperidila, 3- piperidila, 4-piperidila, 1-piperazinila, 1-morfolinila, morfolina, 2-piridila, 3- piridila, 4-piridila, 2-pirazinila, 2-furila, 2-tetraidrofurila, 1,3-benzodioxol-5- ila) opcionalmente apresentando umhidróxi,C1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um hidróxi,oxo,C1-6 alcóxi-carbonila (p. ex., t-butoxicarbonila), ouC1-6 alquil-carbonila (p. ex., metilcarbonila) opcionalmente apresentando um substituinte selecionado dentre C1-6 alquil-carbonilóxi (p. ex., metilcarbonilóxi) e hidróxi,(11’) C1-6 alcóxi-carbonila (p. ex., etoxicarbonila),(12’) C3-6 cicloalquila (p. ex., ciclopropila, cicloexila) opcionalmente apresentando um hidróxi, (13’) C1-6 alcóxi (p. ex., metóxi, i-propóxi),(14’) C2-6 alquinila (p. ex., etinila),(15’) C6-10 arila (p. ex., fenila) opcionalmente apresentando 1 ou 2 C1-6 alcóxi (p. ex., metóxi),(16’) carbamoíla, e(17’) C1-6 alquil-carbonil-amina (p. ex., metilcarbonilamina) opcionalmente apresentando um substituinte selecionado dentreC1-6 alquil-carbonil-óxi (p. ex., metilcarbonilóxi),C1-6 alcóxi (p. ex., metóxi), ehidróxi,C3-6 cicloalquila (p. ex., ciclopropila, cicloexila) ou 1,2,3,4- tetraidronaftalenila (p. ex., 1,2,3,4-tetraidronaftalen-1-ila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentre(1’) amina opcionalmente apresentando um substituinte selecionado dentreC1-6 alcóxi-carbonila (p. ex., t-butoxicarbonila), eC1-6 alquil-carbonila (p. ex., metilcarbonila) opcionalmente apresentando um hidróxi ou C1-6 alquil-carbonilóxi (p. ex., metilcarbonilóxi),(2’) hidróxi,(3’) carbóxi,(4’) C1-6 alcóxi-carbonila (p. ex., metoxicarbonila),(5’) C1-6 alquil-carbamoíla (p. ex., etilcarbamoíla)opcionalmente apresentando um hidróxi,(6’) C1-6 alquila (p. ex., metila) opcionalmente apresentando um hidróxi, e(7’) C1-6 alcóxi-carbonilamina (p. ex., t-butoxicarbonilamina),C6-10 arila (p. ex., fenila), egrupo heterocíclico (p. ex., 3-azetidinila, 3-pirrolidinila, 4- piperidila, 2-tetraidrofurila, 3-azepanila, 4-azepanila, tetraidrotiopiran-4-ila, tetraidropiran-4-ila) opcionalmente apresentando de 1 a 4 substituintes selecionados dentre(1’) C1-6 alquila (p. ex., metila, etila, n-propila) opcionalmente apresentando de 1 a 5 substituintes selecionados dentreC6-10 arila (p. ex., fenila),hidróxi, eátomo de halogênio,(2’) C1-6 alquil-carbonila (p. ex., metilcarbonila, etilcarbonila, i-propilcarbonila, i-butilcarbonila) opcionalmente apresentando um substituinte selecionado dentreC1-6 alquil-carbonilóxi (p. ex., metilcarbonilóxi),hidróxi,C1-6 alcóxi (p. ex., metóxi),C1-6 alquil-sulfonila (p. ex., metilsulfonila), eamina,(3’) C1-6 alcóxi-carbonila (p. ex., t-butoxicarbonila),(4’) grupo heterocíclico aromático com 5 ou 6 membros (p. ex., 2-piridila, 3-piridila, 4-piridila, 2-tiazolila, 4-pirimidinila) opcionalmente apresentando um substituinte selecionado dentreC1-6 alquila (p. ex., metila) opcionalmente apresentando de1 a 3 átomos de halogênio (p. ex., átomo de flúor),ciano,carbamoíla,C1-6 alcóxi (p. ex., metóxi), eC1-6 alquil-carbamoíla (p. ex., metilcarbamoíla),(5’) oxo,(6’) C1-6 alquil-carbamoíla (p. ex., etilcarbamoíla),(7’) C1-6 alquil-sulfonila (p. ex., metilsulfonila),) C6-10 arila (p. ex., fenila) opcionalmente apresentando um substituinte selecionado dentrehidróxi,ciano, eC1-6 alquil-sulfonila (p. ex., metilsulfonila),) heterociclil-carbonila (p. ex., 2-pirrolidinilcarbonila, 2- tetraidrofurilcarbonila), e(10’) C6-10 arilóxi-carbonila (p. ex., fenoxicarbonila),carbamoíla cíclica com de 5 a 7 membros (p. ex., 1- pirrolidinilcarbonila, 1-piperidilcarbonila, 1-piperazinilcarbonila, 1- homopiperazinilcarbonila, morfolinocarbonila, tiomorfolinocarbonila) opcionalmente apresentando um grupo selecionado dentreC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um substituinte selecionado dentregrupo heterocíclico (p. ex., 1-pirrolidinila, benzodioxol-5- ila),amina,C1-6 alcóxi (p. ex., metóxi), eC6-10 arila (p. ex., fenila),amina opcionalmente apresentando um C1-6 alquil- carbonila (p. ex., acetila),N-C1-6 alquila-N-(C1-6 alquil-carbonil)amina (p. ex., N- acetil-N-etilamina),grupo heterocíclico (p. ex., 1-pirrolidinila, 2-piridila),C1-6 alquil-carbonila (p. ex., acetila, propionila)opcionalmente apresentando um substituinte selecionado dentrehidróxi,C1-6 alcóxi (p. ex., metóxi, etóxi),amina,C1-6 alquilamina (p. ex., isopropilamina), di-C1-6 alquilamina (p. ex., dimetilamina), eC1-6 alquil-carbonilóxi (p. ex., metilcarbonilóxi),C6-10 arila (p. ex., fenila), eoxo, ou(C) carbamoíla cíclica com de 5 a 7 membros (p. ex., 1- piperidilcarbonila) fundido com anel com de 5 a 7 membros (p. ex., anel cicloexano, anel de benzeno, anel 1,3-dioxol);R3 é hidróxi opcionalmente apresentandoC1-6 alquila (p. ex., metila, etila, n-butila) opcionalmente apresentando umC1-6 alcóxi (p. ex., etóxi),C6-10 arila (p. ex., fenila), ougrupo heterocíclico (p. ex., 4-piridila, morfolina, 2- tetraidrofurila), ouC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor)[de preferência, hidróxi substituído porC1-6 alquila (p. ex., metila, etila, n-butila) opcionalmente apresentando umC1-6 alcóxi (p. ex., etóxi),C6-10 arila (p. ex., fenila), ougrupo heterocíclico (p. ex., 4-piridila, morfolina, 2- tetraidrofurila), ouC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor)];R4 éátomo de hidrogênio,C1-6 alquila (p. ex., metila, etila, n-propila, n-butila, n- pentila, i-pentila, 2-etilbutila) opcionalmente apresentando um substituinte selecionado dentre(1’) C3-6 cicloalquila (p. ex., ciclopropila, cicloexila),(2’) C6-10 arila (p. ex., fenila) opcionalmente apresentando (i) um C1-6 alcóxi (p. ex., metóxi) opcionalmente apresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor) ou (ii) de 1 a 3 átomos de halogênio (p. ex., átomo de flúor, átomo de cloro),(3’) C1-6 alquil-carbonila (p. ex., metilcarbonila, t- butilcarbonila),(4’) C6-10 aril-carbonila (p. ex., benzoila),(5’) C1-6 alcóxi-carbonila (p. ex., metoxicarbonila,etoxicarbonila, t-butoxicarbonila),(6’) C6-10 aril-carbamoíla (p. ex., fenilcarbamoíla),(7’) grupo heterocíclico (p. ex., 2-piridila, 3-piridila, 4-piridila, 1-pirrolila, 2-imidazolila, 2-furila, 2-tetraidrofurila) opcionalmente apresentando 1 ou 2 C1-6 alquila (p. ex., metila) opcionalmente apresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor),(8’) C6-10 arilóxi (p. ex., fenóxi),(9’) carbóxi,(10’) ciano, e(11’) C1-6 alcóxi (p. ex., metóxi) opcionalmente apresentando um C6-10 arila (p. ex., fenila), ouC1-6 alquila (p. ex., etila) opcionalmente apresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor); eanel B é anel cicloexeno, anel de benzeno opcionalmente apresentando um átomo de halogênio (p. ex., átomo de flúor), ou anel piridina (particularmente, anel de benzeno e anel piridina).Composto (I’-4)N-[1-(2-hidroxietil)piperidin-4-il]-3-metóxi-1-metil-4-oxo-5- (2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamida; N-[1-(hidroxiacetil)piperidin-4-il]-3-metóxi-1-metil-4-oxo-5- (2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamida;ou um sal do mesmo.Em outra concretização dos compostos (I”’) indicados acima, prefere-se um composto (I”) representado pela fórmulasendo que X, R2, R3 e R4 são como definido acima, e RA1 e RA2 são iguais ou diferentes e cada um é um átomo de hidrogênio ou um substituinte.
[0080] A seguir, composto (I”) é descrito detalhadamente.
[0081] X, R2, R3 e R4 são como definido acima.
[0082] Na fórmula (I”), exemplos preferíveis de R2 écarbamoíla opcionalmente apresentando 1 ou 2 substituintes selecionados dentreC1-6 alquila (p. ex., metila, etila, propila, isopropila, 2- metilpropila, 2,2-dimetilpropila, 1-metilbutila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentre(1’) átomo de halogênio (p. ex., átomo de flúor),(2’) ciano,(3’) amina,(4’) C1-6 alquilamina (p. ex., isopropilamina),(5’) di-C1-6 alquilamina (p. ex., dimetilamina, dietilamina) opcionalmente apresentando um hidróxi,(6’) C1-6 alcóxi-carbonilamina (p. ex., t-butoxicarbonilamina),(7’) hidróxi, (8’) di-C1-6 alquil-carbamoíla (p. ex., dietilcarbamoíla),(9’) carbamoíla cíclica com de 5 a 7 membros (p. ex., 1- pirrolidinilcarbonila),(10’) grupo heterocíclico (p. ex., 1-pirrolidinila, 2-pirrolidinila, 3-pirrolidinila, 1-pirazolila, 1-imidazolila, 1-piperidila, 2-piperidila, 3- piperidila, 4-piperidila, 1-piperazinila, 1-morfolinila, 2-piridila, 3-piridila, 2- tetraidrofurila) opcionalmente apresentando umhidróxi, ouC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um hidróxi,(11’) C1-6 alcóxi-carbonila (p. ex., etoxicarbonila), e(12’) C3-6 cicloalquila (p. ex., cicloexila),C3-6 cicloalquila (p. ex., cicloexila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentre(1’) amina, e(2’) hidróxi,C6-10 arila (p. ex., fenila), egrupo heterocíclico (p. ex., 3-pirrolidinila, 4-piperidila, S- óxido-tetraidrotiopiran-4-ila) opcionalmente apresentando um substituinte selecionado dentre(1’) C1-6 alquila (p. ex., metila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentreC6-10 arila (p. ex., fenila), ehidróxi,(2’) C1-6 alquil-carbonila (p. ex., metilcarbonila) opcionalmente apresentando um substituinte selecionado dentreC1-6 alquil-carbonilóxi (p. ex., metilcarbonilóxi), ehidróxi,(3’) C1-6 alcóxi-carbonila (p. ex., t-butoxicarbonila), e (4’) grupo heterocíclico aromático com 5 ou 6 membros (p. ex., 4-piridila), oucarbamoíla cíclica com de 5 a 7 membros (p. ex., 1- pirrolidinilcarbonila, 1-piperidilcarbonila, 1-homopiperazinilcarbonila) opcionalmente apresentando um substituinte selecionado dentreC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um substituinte selecionado dentregrupo heterocíclico (p. ex., 1-pirrolidinila, benzodioxol-5- ila), eamina,amina,N-C1-6 alquila-N-(C1-6 alquil-carbonil)amina (p. ex., N- acetil-N-etilamina),grupo heterocíclico (p. ex., 1-pirrolidinila), eC1-6 alquil-carbonila (p. ex., acetila, propionila) opcionalmente apresentando um substituinte selecionado dentrehidróxi,C1-6 alcóxi (p. ex., metóxi),amina, eC1-6 alquilamina (p. ex., isopropilamina).Na fórmula (I”), exemplos preferíveis de R3 é[] hidróxi opcionalmente apresentando(1) C1-6 alquila (p. ex., metila, etila, n-propila, i-propila) opcionalmente apresentando um C1-6 alcóxi (p. ex., etóxi), ou(2) C1-6 alquila (p. ex., metila, etila, n-propila, i-propila) opcionalmente apresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor)[de preferência, hidroxila substituído por(1) C1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um C1-6 alcóxi (p. ex., etóxi), ou(2) C1-6 alquila (p. ex., metila, etila) opcionalmente apresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor)].Na fórmula (I”), exemplos preferíveis de R4 éátomo de hidrogênio, ouC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um substituinte selecionado dentre(1’) C3-6 cicloalquila (p. ex., ciclopropila),(2’) C6-10 arila (p. ex., fenila) opcionalmente apresentando (i) 1 ou 2 C1-6 alcóxi (p. ex., metóxi), ou (ii) de 1 a 3 átomos de halogênio (p. ex., átomo de cloro),(3’) C1-6 alquil-carbonila (p. ex., t-butilcarbonila),(4’) C6-10 aril-carbonila (p. ex., benzoila) opcionalmente apresentando um átomo de halogênio (p. ex., átomo de cloro) ou C1-6 alcóxi (p. ex., metóxi),(5’) C1-6 alcóxi-carbonila (p. ex., etoxicarbonila),(6’) C6-10 aril-carbamoíla (p. ex., fenilcarbamoíla),(7’) grupo heterocíclico (p. ex., 2-piridila),(8’) C6-10 arilóxi (p. ex., fenóxi), e(9’) carbóxi; eRA1 é um átomo de hidrogênio ou um grupo C1-6 alquila (p. ex., metila, etila, n-propila).RA1 e RA2 são iguais ou diferentes e cada um é um átomo de hidrogênio ou um substituinte. Como o substituinte, é possível indicar aqueles similares ao substituinte do anel A previamente indicado.Como RA1, um átomo de hidrogênio ou grupo C1-6 alquila é preferível.Como RA2, um átomo de hidrogênio ou grupo C1-6 alquila é preferível. Dentre compostos (I”), é preferível um composto em queX é O, S ou N(C1-6 alquila),R2 é carbamoíla apresentando opcionalmente substituinte(s),R3 é hidróxi opcionalmente apresentando C1-6 alquila apresentando opcionalmente substituinte(s),RA1 é um átomo de hidrogênio ou um grupo C1-6 alquila (p. ex., metila, etila, n-propila),RA2 é um átomo de hidrogênio ou um grupo C1-6 alquila (p. ex., metila), eR4 é um átomo de hidrogênio ou C1-6 alquila apresentando opcionalmente substituinte(s).Exemplos específicos de composto (I”) preferível incluem os seguintes.Composto (I”-1)Composto (I”) em queX é O, S ou N(C1-6 alquila) (particularmente N(metila));R2 écarbamoíla opcionalmente apresentando 1 ou 2 substituintes selecionados dentreC1-6 alquila (p. ex., metila, etila, propila, isopropila, 2- metilpropila, 2,2-dimetilpropila, 1-metilbutila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentre(1’) átomo de halogênio (p. ex., átomo de flúor),(2’) ciano,(3’) amina,(4’) C1-6 alquilamina (p. ex., isopropilamina),(5’) di-C1-6 alquilamina (p. ex., dimetilamina, dietilamina) opcionalmente apresentando um hidróxi,(6’) C1-6 alcóxi-carbonilamina (p. ex., t-butoxicarbonilamina), (7’) hidróxi,(8’) di-C1-6 alquil-carbamoíla (p. ex., dietilcarbamoíla),(9’) carbamoíla cíclica com de 5 a 7 membros (p. ex., 1- pirrolidinilcarbonila),(10’) grupo heterocíclico (p. ex., 1-pirrolidinila, 2-pirrolidinila, 3-pirrolidinila, 1-pirazolila, 1-imidazolila, 1-piperidila, 2-piperidila, 3- piperidila, 4-piperidila, 1-piperazinila, 1-morfolinila, 2-piridila, 3-piridila) opcionalmente apresentando umhidróxi, ouC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um hidróxi,(11’) C1-6 alcóxi-carbonila (p. ex., etoxicarbonila), e(12’) C3-6 cicloalquila (p. ex., cicloexila),C3-6 cicloalquila (p. ex., cicloexila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentre(1’) amina, e(2’) hidróxi,C6-10 arila (p. ex., fenila), egrupo heterocíclico (p. ex., 3-pirrolidinila, 4-piperidila) opcionalmente apresentando um substituinte selecionado dentre(1’) C1-6 alquila (p. ex., metila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentreC6-10 arila (p. ex., fenila), ehidróxi,(2’) C1-6 alquil-carbonila (p. ex., metilcarbonila) opcionalmente apresentando um substituinte selecionado dentreC1-6 alquil-carbonilóxi (p. ex., metilcarbonilóxi), ehidróxi,(3’) C1-6 alcóxi-carbonila (p. ex., t-butoxicarbonila), e (4’) grupo heterocíclico aromático com 5 ou 6 membros (p. ex., 4-piridila), oucarbamoíla cíclica com de 5 a 7 membros (p. ex., 1- pirrolidinilcarbonila, 1-piperidilcarbonila, 1-homopiperazinilcarbonila) opcionalmente apresentando um grupo selecionado dentreC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um substituinte selecionado dentregrupo heterocíclico (p. ex., 1-pirrolidinila, benzodioxol-5- ila), eamina,amina,N-C1-6 alquila-N-(C1-6 alquil-carbonil)amina (p. ex., N- acetil-N-etilamina),grupo heterocíclico (p. ex., 1-pirrolidinila), eC1-6 alquil-carbonila (p. ex., acetila, propionila) opcionalmente apresentando um substituinte selecionado dentrehidróxi,C1-6 alcóxi (p. ex., metóxi),amina, eC1-6 alquilamina (p. ex., isopropilamina);R3 é hidróxi opcionalmente apresentando(1) C1-6 alquila (p. ex., metila, etila) opcionalmenteapresentando um C1-6 alcóxi (p. ex., etóxi), ou(2) C1-6 alquila (p. ex., metila, etila) opcionalmenteapresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor)[de preferência, hidróxi substituído por(1) C1-6 alquila (p. ex., metila, etila) opcionalmenteapresentando um C1-6 alcóxi (p. ex., etóxi), ou(2) C1-6 alquila (p. ex., metila, etila) opcionalmente apresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor)];R4 é(1) átomo de hidrogênio, ou(2) C1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um substituinte selecionado dentre(1’) C3-6 cicloalquila (p. ex., ciclopropila),(2’) C6-10 arila (p. ex., fenila) opcionalmente apresentando umC1-6 alcóxi (p. ex., metóxi),(3’) C1-6 alquil-carbonila (p. ex., t-butilcarbonila),(4’) C6-10 aril-carbonila (p. ex., benzoila),(5’) C1-6 alcóxi-carbonila (p. ex., etoxicarbonila),(6’) C6-10 aril-carbamoíla (p. ex., fenilcarbamoíla),(7’) grupo heterocíclico (p. ex., 2-piridila),(8’) C6-10 arilóxi (p. ex., fenóxi), e(9’) carbóxi;RA1 é um átomo de hidrogênio ou um grupo C1-6 alquila (p. ex., metila, etila, n-propila); eRA2 é um átomo de hidrogênio ou um grupo C1-6 alquila (p. ex., metila).Composto (I”-2)Composto (I”) em queX é O, S ou N(C1-6 alquila) (particularmente N(metila));R2 é(A) carbamoíla opcionalmente apresentando 1 ou 2 substituintes selecionados dentreC1-6 alquila (p. ex., metila, etila, propila, isopropila, 2- metilpropila, 2,2-dimetilpropila, 1-metilbutila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentre(1’) átomo de halogênio (p. ex., átomo de flúor), (2’) ciano,(3’) amina,(4’) C1-6 alquilamina (p. ex., isopropilamina),(5’) di-C1-6 alquilamina (p. ex., dimetilamina, dietilamina) opcionalmente apresentando um hidróxi,(6’) C1-6 alcóxi-carbonilamina (p. ex., t-butoxicarbonilamina),(7’) hidróxi,(8’) di-C1-6 alquil-carbamoíla (p. ex., dietilcarbamoíla),(9’) carbamoíla cíclica com de 5 a 7 membros (p. ex., 1- pirrolidinilcarbonila),(10’) grupo heterocíclico (p. ex., 1-pirrolidinila, 2-pirrolidinila, 3-pirrolidinila, 1-pirazolila, 1-imidazolila, 1-piperidila, 2-piperidila, 3- piperidila, 4-piperidila, 1-piperazinila, 1-morfolinila, 2-piridila, 3-piridila, 2- tetraidrofurila) opcionalmente apresentando umhidróxi, ouC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um hidróxi,(11’) C1-6 alcóxi-carbonila (p. ex., etoxicarbonila), e(12’) C3-6 cicloalquila (p. ex., cicloexila),C3-6 cicloalquila (p. ex., cicloexila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentre(1’) amina, e(2’) hidróxi,C6-10 arila (p. ex., fenila), egrupo heterocíclico (p. ex., 3-pirrolidinila, 4-piperidila, S- óxido-tetraidrotiopiran-4-ila) opcionalmente apresentando um substituinte selecionado dentre(1’) C1-6 alquila (p. ex., metila) opcionalmente apresentando 1 ou 2 substituintes selecionados dentre C6-10 arila (p. ex., fenila), ehidróxi,(2’) C1-6 alquil-carbonila (p. ex., metilcarbonila) opcionalmente apresentando um substituinte selecionado dentreC1-6 alquil-carbonilóxi (p. ex., metilcarbonilóxi), ehidróxi,(3’) C1-6 alcóxi-carbonila (p. ex., t-butoxicarbonila), e(4’) grupo heterocíclico aromático com 5 ou 6 membros (p. ex., 4-piridila), ou(B) carbamoíla cíclica com de 5 a 7 membros (p. ex., 1- pirrolidinilcarbonila, 1-piperidilcarbonila, 1-homopiperazinilcarbonila) opcionalmente apresentando um substituinte selecionado dentreC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um substituinte selecionado dentregrupo heterocíclico (p. ex., 1-pirrolidinila, benzodioxol-5- ila), eamina,amina,N-C1-6 alquila-N-(C1-6 alquil-carbonil)amina (p. ex., N- acetil-N-etilamina),grupo heterocíclico (p. ex., 1-pirrolidinila), eC1-6 alquil-carbonila (p. ex., acetila, propionila)opcionalmente apresentando um substituinte selecionado dentrehidróxi,C1-6 alcóxi (p. ex., metóxi),amina, eC1-6 alquilamina (p. ex., isopropilamina);R3 é hidróxi opcionalmente apresentando(1) C1-6 alquila (p. ex., metila, etila, n-propila, i-propila) opcionalmente apresentando um C1-6 alcóxi (p. ex., etóxi), ou(2) C1-6 alquila (p. ex., metila, etila, n-propila, i-propila) opcionalmente apresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor)[de preferência, hidroxila substituído por(1) C1-6 alquila (p. ex., metila, etila) opcionalmenteapresentando um C1-6 alcóxi (p. ex., etóxi), ou(2) C1-6 alquila (p. ex., metila, etila) opcionalmenteapresentando de 1 a 3 átomos de halogênio (p. ex., átomo de flúor)];R4 éátomo de hidrogênio, ouC1-6 alquila (p. ex., metila, etila) opcionalmente apresentando um substituinte selecionado dentre(1’) C3-6 cicloalquila (p. ex., ciclopropila),(2’) C6-10 arila (p. ex., fenila) opcionalmente apresentando (i) 1 ou 2 C1-6 alcóxi (p. ex., metóxi) ou (ii) de 1 a 3 átomos de halogênio (p. ex., átomo de cloro),(3’) C1-6 alquil-carbonila (p. ex., t-butilcarbonila),(4’) C6-10 aril-carbonila (p. ex., benzoila) opcionalmente apresentando um átomo de halogênio (p. ex., átomo de cloro) ou C1-6 alcóxi (p. ex., metóxi),(5’) C1-6 alcóxi-carbonila (p. ex., etoxicarbonila),(6’) C6-10 aril-carbamoíla (p. ex., fenilcarbamoíla),(7’) grupo heterocíclico (p. ex., 2-piridila),(8’) C6-10 arilóxi (p. ex., fenóxi), e(9’) carbóxi;RA1 é um átomo de hidrogênio ou um grupo C1-6 alquila (p. ex., metila, etila, n-propila); eRA2 é um átomo de hidrogênio ou um grupo C1-6 alquila (p. ex., metila).Composto (I”-3)3-etóxi-6-etil-N-[1-(hidroxiacetil)piperidin-4-il]-1-metil-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxamida;N-[1-(hidroxiacetil)piperidin-4-il]-1,6-dimetil-4-oxo-5-(2-oxo- 2-feniletil)-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2- carboxamida;6-etil-N-[1-(hidroxiacetil)piperidin-4-il]-1-metil-4-oxo-5-(2- oxo-2-feniletil)-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2- carboxamida;ou um sal do mesmo.
[0083] Quando composto (I) é um sal, exemplos de referido sal incluem sal metálico, sal de amônio, um sal com base orgânica, um sal com ácido inorgânico, um sal com ácido orgânico, um sal com aminoácido básico ou ácido e análogos. Exemplos preferíveis do sal metálico incluem sal de metal alcalino, como sal de sódio, sal de potássio e análogos; sal de metal alcalino-terroso, como sal de cálcio, sal de magnésio, sal de bário e análogos; sal de alumínio e análogos. Exemplos preferíveis do sal com base orgânica incluem um sal com trimetilamina, trietilamina, piridina, picolina, 2,6- lutidina, etanolamina, dietanolamina, trietanolamina, cicloexilamina, dicicloexilamina, N,N’-dibenziletilenodiamina e análogos. Exemplos preferíveis do sal com ácido inorgânico incluem um sal com ácido clorídrico, ácido bromídrico, ácido nítrico, ácido sulfúrico, ácido fosfórico e análogos. Exemplos preferíveis do sal com ácido orgânico incluem um sal com ácido fórmico, ácido acético, ácido trifluoroacético, ácido ftálico, ácido fumárico, ácido oxálico, ácido tartárico, ácido maleico, ácido cítrico, ácido succínico, ácido málico, ácido metanossulfônico, benzenossulfônico, p- toluenossulfônico e análogos. Exemplos preferíveis do sal com aminoácido basico incluem um sal com arginina, lisina, ornitina e análogos, e exemplos preferíveis do sal com aminoácido ácido incluem um sal com ácido aspártico, ácido glutâmico e análogos.
[0084] Destes, um sal farmaceuticamente aceitável é preferível. Por exemplo, quando um composto apresenta um grupo funcional ácido, é possível indicar um sal inorgânico, como sal de metal alcalino (p. ex., sal de sódio, sal de potássio etc.), sal de metal alcalino-terroso (p. ex., sal de cálcio, sal de magnésio etc.) e análogos, sal de amônio etc., e quando um composto apresenta um grupo funcional básico, por exemplo, um sal com ácido inorgânico, como ácido clorídrico, ácido bromídrico, ácido nítrico, ácido sulfúrico, ácido fosfórico e análogos, ou um sal com ácido orgânico, como ácido acético, ácido ftálico, ácido fumárico, ácido oxálico, ácido tartárico, ácido maleico, ácido cítrico, ácido succínico, ácido metanossulfônico, benzenossulfônico, ácido p-toluenossulfônico e análogos.
[0085] O método de produção do composto da presente invenção é descrito a seguir.
[0086] Em cada um dos métodos de produção a seguir, quando se realiza reação de alquilação, reação de amidação (reação de condensação), reação de esterificação, reação de redução, reação de aminação redutiva, reação de aminação, reação de halogenação, reação de oxidação e análogos, estas reações são realizadas de acordo com métodos conhecidos. Exemplos de referidos métodos incluem os métodos descritos em Organic Functional Group Preparations, 2a edição, Academic Press, Inc. (1989), Comprehensive Organic Transformations, VCH Publishers Inc. (1989) e análogos, e análogos. Reações de proteção e desproteção são realizadas de acordo com métodos conhecidos, por exemplo, os métodos descritos em Protective Groups in Organic Synthesis, 3a edição, John Wiley e Sons, Inc. (1999) ou um método análogo aos mesmos.
[0087] Os solventes indicados em termos genéricos, que são usados nas reações a seguir são explicadas a seguir.
[0088] Exemplos dos “alcoóis” incluem metanol, etanol, 1-propanol, 2-propanol, t-butila e análogos.
[0089] Exemplos dos “éteres” incluem éter de dietila, éter de diisopropila, éter de difenila, tetraidrofurano, 1,4-dioxano, 1,2-dimetoxietano e análogos.
[0090] Exemplos dos “ésteres” incluem acetato de etila, acetato de metila, acetato de t-butila e análogos.
[0091] Exemplos dos “hidrocarbonetos” incluem benzeno, tolueno, xileno, cicloexano, hexano, pentano e análogos.
[0092] Exemplos das “amidas” incluem N,N-dimetilformamida, N,N- dimetilacetamida, triamida hexametilfosfórica e análogos.
[0093] Exemplos dos “hidrocarbonetos halogenados” incluem diclorometano, clorofórmio, tetracloreto de carbono, 1,2-dicloroetano, tetracloroetileno, clorobenzeno e análogos.
[0094] Exemplos dos “nitrilas” incluem acetonitrila, propionitrila e análogos.
[0095] Exemplos das “cetonas” incluem acetona, 2-butanona eanálogos.
[0096] Exemplos dos “ácidos orgânicos” incluem ácido fórmico,ácido acético, ácido propiônico, ácido trifluoroacético, ácido metanossulfônico e análogos.
[0097] Exemplos das “aminas aromáticas” incluem piridina, 2,6- lutidina, quinolina e análogos.
[0098] Exemplos dos “sulfóxidos” incluem sulfóxido de dimetila e análogos.
[0099] Nos presentes métodos de produção, um composto de material de partia e um intermediário de produção podem ser sais. Como referido sal, é possível indicar aqueles similares aos sais do composto (I) previamente indicado.
[00100] Composto (I) pode ser produzido, por exemplo, por meio do Método A mostrado abaixo ou um método análogo ao mesmo.Método AComposto (III) é hidrolisado e o composto (II) obtido é condensado com amina, com o que se pode produzir composto (I).sendo que R5 é C1-6 alquila ou benzila, e outros símbolos são como definido acima.
[00101] Exemplos de C1-6 alquila para R5 incluem metila, etila e análogos, de preferência, etila.
[00102] Composto (III) pode ser produzido de acordo com os métodos de produção do composto (IIIa) e composto (IIIb) mostrados abaixo.
[00103] Composto (III) pode ser convertido a composto (II) por meio de hidrólise em condições ácidas ou básicas em um solvente que não influência adversamente a reação. Particularmente, quando R5 é benzila, é possível usar uma reação de hidrogenação catalítica em um solvente que não influência adversamente a reação.
[00104] Como o ácido usado para hidrólise, é possível indicar ácido clorídrico, ácido sulfúrico e análogos, e, como a base, é possível indicar hidróxido de sódio, hidróxido de potássio, hidróxido de lítio e análogos. A quantidade do mesmo é geralmente de 1 a 20 equivalentes molares, de preferência, de 1 a 10 equivalentes molares, por 1 mol de composto (III).
[00105] Exemplos do catalisador usado para a reação de hidrogenação catalítica incluem níquel Raney, óxido de platina, ou paládio, rutênio, ródio, irídio e análogos sobre carvão ativado, sulfato de bário, carbonato de cálcio e análogos. A quantidade do mesmo é geralmente de 0,01 a 1 equivalente molar, de preferência, de 0,05 a 0,5 equivalente molar, por 1 mol de composto (III).
[00106] Como a fonte de hidrogênio, usa-se hidrogênio, cicloexeno, hidrazina, formiato de amônio e análogos.
[00107] Exemplos do solvente que não influenciam adversamente a reação incluem éteres, alcoóis, hidrocarbonetos, cetonas, nitrilas, amidas, ésteres, água e análogos, dando-se preferência a alcoóis, éteres e água. Dois ou mais tipos dos solventes indicados acima podem ser usados em uma mistura numa relação apropriada.
[00108] A temperatura de reação é geralmente de 0 a 100°C, de preferência, de 20 a 60°C.
[00109] O tempo de reação é geralmente de 0,5 a 100 h, de preferência, de 1 a 48 h.
[00110] A reação de condensação do composto (II) e amina pode ser realizada em um solvente que não influência adversamente a reação e usando, por exemplo, um agente de condensação.
[00111] A amina a ser usada nesta reação pode ser condensada com grupo carbóxi do composto (II) para formar um “carbamoíla apresentando opcionalmente substituinte(s)” para R2. Referida amina pode ser uma comercialmente obtenível, ou pode ser produzida a partir do composto de material de partida correspondente por meio de um método conhecido per se.
[00112] Exemplos do agente de condensação incluem carbodiimida (p. ex., dicicloexilcarbodiimida (DCCD), carbodiimida solúvel em água (WSCD) e análogos), éster de fosfato (p. ex., cianofosfonato de dietila, clorofosfonato de dietila, fosforoazida de difenila e análogos), reagente BOP (hexafluorofosfato de 1H-benzotriazol-1-iloxitripirrolidinofosfônio (PyBOP)), 2-etóxi-1-etoxicarbonil-1,2-diidroquinolina (EEDQ), carbonildiimidazol e análogos, dando-se preferência a WSCD.
[00113] A quantidade de cada um, amina e agente de condensação, a ser usada é geralmente de 1 a 10 equivalentes molares, de preferência, de 1 a 2 equivalentes molares, por 1 mol de composto (II).
[00114] Exemplos do solvente que não influenciam adversamente a reação incluem éteres, hidrocarbonetos, cetonas, nitrilas, amidas, ésteres e análogos, dando-se preferência a éteres e amidas. Dois ou mais tipos dos solventes indicados acima podem ser usados em uma mistura, numa relação apropriada.
[00115] A temperatura de reação é geralmente de 0 a 100°C, de preferência, de 20 a 60°C.
[00116] O tempo de reação é geralmente de 0,5 a 100 h, de preferência, de 1 a 48 h.
[00117] Em compostos (III), é possível produzir composto (IIIa) sendo que R3 é hidróxi, por exemplo, Método B mostrado abaixo ou um método análogo ao mesmo.
[00118] Composto (V) é reagido com composto (1) e o composto (IV) obtido é tratado com uma base dando composto (IIIa).(V) (iv) (|l!a) ,
[00119] sendo que Q é um grupo de saída, R6 é C1-6 alquila, e outros símbolos são como definido acima.
[00120] Exemplos do grupo de saída para Q incluem átomo de halogênio (p. ex., cloro, bromo, iodo), C1-6 alquilsulfonilóxi opcionalmente halogenado (p. ex., metilsulfonilóxi, etilsulfonilóxi, trifluorometilsulfonilóxi), C6-10 arilsulfonilóxi opcionalmente apresentando C1-6 alquila (p. ex., benzenossulfonilóxi, 4-toluenossulfonilóxi), metilmercapto, metanossulfonila e análogos, dando-se preferência a átomo de halogênio.
[00121] Exemplos do C1-6 alquila para R6 incluem metila, etila e análogos.
[00122] Composto (V) pode ser produzido de acordo com os métodos de produção do composto (Va) e composto (Va-2) mostrados abaixo.
[00123] A reação de composto (V) e composto (1) pode ser realizada na presença de uma base conforme necessário e em um solvente que não influência adversamente a reação.
[00124] Composto (1) pode ser um comercialmente obtenível, ou pode ser produzido a partir do composto de material de partida correspondente por meio de um método conhecido per se.
[00125] A quantidade de composto (1) a ser usada é geralmente de 1 a 20 equivalentes molares, de preferência, de 1 a 10 equivalentes molares, por 1 mol de composto (V). Exemplos da base a ser usada conforme necessário incluem hidreto de sódio, metóxido de sódio, etóxido de sódio, carbonato de sódio, hidrogenocarbonato de sódio, hidróxido de sódio, trietilamina, diisopropiletilamina, piridina, 4-dimetilaminapiridina e análogos. A quantidade do mesmo a ser usada é geralmente de 1 a 20 equivalentes molares, de preferência, de 2 a 10 equivalentes molares, por 1 mol de composto (V).
[00126] Exemplos do solvente que não influenciam adversamente a reação incluem éteres, hidrocarbonetos, alcoóis, amidas, ésteres e análogos, dando-se preferência a éteres e amidas. Dois ou mais tipos dos solventes indicados acima podem ser usados em uma mistura, numa relação apropriada.
[00127] A temperatura de reação é geralmente de 0 a 100°C, de preferência, de 20 a 90°C.
[00128] O tempo de reação é geralmente de 0,5 a 100 h, de preferência, de 1 a 48 h.
[00129] Composto (IV) pode ser convertido a composto (IIIa) usando- se uma base em um solvente que não influencia adversamente a reação.
[00130] Exemplos da base incluem metóxido de sódio, etóxido de sódio, hidróxido de sódio, trietilamina e análogos e a quantidade dos mesmos a ser usada é geralmente de 1 a 20 equivalentes molares, de preferência, de 2 a 10 equivalentes molares, por 1 mol de composto (IV).
[00131] Exemplos do solvente que não influenciam adversamente a reação incluem éteres, hidrocarbonetos, alcoóis, amidas, ésteres e análogos, dando-se preferência a éteres e amidas. Dois ou mais tipos dos solventes indicados acima podem ser usados em uma mistura, numa relação apropriada.
[00132] A temperatura de reação é geralmente de 0 a 100°C, de preferência, de 20 a 90°C.
[00133] O tempo de reação é geralmente de 0,5 a 100 h, de preferência, de 1 a 48 h.
[00134] Composto (V) pode ser convertido diretamente a composto (IIIa) sem isolar composto (IV).
[00135] No composto (III), é possível produzir composto (IIIb) sendo que R3 é alcóxi apresentando opcionalmente substituinte(s), por exemplo, por meio do Método C mostrado abaixo ou um método análogo ao mesmo.
[00136] Composto (IIIa) é reagido com alquila halogenada, éster de sulfato, éster de metanossulfonato opcionalmente substituído por átomo de halogênio(s) e análogos dando o composto (IIIb).(ma) (|]|b)sendo que R3’ é alcóxi apresentando opcionalmente substituinte(s), e outros símbolos são como definido acima.
[00137] O “alcóxi apresentando opcionalmente substituinte(s)” para R3’ significa “hidróxi substituído por alquila apresentando opcionalmente substituinte(s)” compreendido no “hidróxi apresentando opcionalmente substituinte(s)” para R3.
[00138] A reação entre composto (IIIa) e alquila halogenada, éster de sulfato, éster de metanossulfonato opcionalmente substituído por átomo de halogênio(s) e análogos pode ser realizada na presença de uma base em um solvente que não influencia adversamente a reação.
[00139] A alquila halogenada, éster de sulfato e éster de metanossulfonato opcionalmente substituído por átomo de halogênio(s) usados nesta reação pode alquilar o grupo hidroxila do composto (IIIa) para formar “alcóxi apresentando opcionalmente substituinte(s)” para R3’. Referida alquila halogenada, éster de sulfato, éster de sulfato e éster de metanossulfonato opcionalmente substituído por átomo de halogênio(s) podem ser comercialmente obteníveis, ou podem ser produzidos a partir do composto de material de partida correspondente por meio de um método conhecido per se.
[00140] A quantidade de alquila halogenada e análogos a ser usada é geralmente de 1 a 3 equivalentes molares, de preferência, de 1 a 2 equivalentes molares, por 1 mol de composto (IIIa). Exemplos da base a ser usada incluem metóxido de sódio, etóxido de sódio, carbonato de césio, carbonato de sódio, hidrogenocarbonato de sódio, hidróxido de sódio, trietilamina, diisopropiletilamina, piridina, 4-dimetilaminapiridina, 1,8- diazabiciclo[5.4.0]undec-7-eno (DBU) e análogos, e a quantidade a ser usada dos mesmos é geralmente de 1 a 5 equivalentes molares, de preferência, de 1 a 3 equivalentes molares, por 1 mol de composto (IIIa).
[00141] Exemplos do solvente que não influenciam adversamente a reação incluem éteres, hidrocarbonetos, alcoóis, cetonas, nitrilas, amidas, ésteres e análogos, dando-se preferência a éteres e amidas. Dois ou mais tipos dos solventes indicados acima podem ser usados em uma mistura, numa relação apropriada.
[00142] A temperatura de reação é geralmente de 0 a 100°C, de preferência, de 20 a 90°C.
[00143] O tempo de reação é geralmente de 0,5 a 100 h, de preferência, de 1 a 48 h.
[00144] Dos compostos (V), é possível produzir éster de 2- oxonicotinato (Va) sendo que anel A é anel piridina ou anel piridina fundido, por exemplo, por meio do Método D mostrado abaixo ou um método análogo ao mesmo.
[00145] Composto (VII) é reagido com éster de malonato (3) e hidróxi do composto (VI) obtido é convertido a um grupo de saída Q dando composto (Va).(VII) (vi) (Va)sendo que R4’ é grupo hidrocarboneto apresentando opcionalmente substituinte(s), e outros símbolos são como definido acima.
[00146] Como o “grupo hidrocarboneto apresentando opcionalmente substituinte(s)” para R4’, é possível indicar aqueles similares ao “grupo hidrocarboneto apresentando opcionalmente substituinte(s)” para R4.
[00147] A reação do composto (VII) e éster de malonato (3) pode ser realizada na presença de uma base em um solvente que não influencia adversamente a reação.
[00148] Éster de malonato (3) pode ser um comercialmente obtenível, ou pode ser produzido a partir do composto de material de partida correspondente por meio de um método conhecido per se.
[00149] A quantidade de éster de malonato (3) a ser usada é geralmente de 1 a 2 equivalentes molares, de preferência, de 1 a 1,5 equivalentes molares, por 1 mol de composto (VII). Exemplos da base a ser usada incluem hidreto de sódio, metóxido de sódio, etóxido de sódio, carbonato de sódio, hidrogenocarbonato de sódio, hidróxido de sódio, trietilamina, diisopropiletilamina, piridina, 4-dimetilaminapiridina, DBU e análogos e a quantidade a ser usada dos mesmos é geralmente de 1 a 10 equivalentes molares, de preferência, de 1 a 5 equivalentes molares, por 1 mol de composto (VII).
[00150] Exemplos do solvente que não influenciam adversamente a reação incluem éteres, hidrocarbonetos, cetonas, nitrilas, amidas e análogos, dando-se preferência a éteres e amidas. Dois ou mais tipos dos solventes indicados acima podem ser usados em uma mistura, numa relação apropriada.
[00151] A temperatura de reação é geralmente de 0 a 100°C, de preferência, de 0 a 80°C.
[00152] O tempo de reação é geralmente de 0,5 a 100 h, de preferência, de 1 a 48 h.
[00153] Conversão de hidróxi do composto (VI) a grupo de saída Q pode ser realizada, por exemplo, por meio do uso de um reagente halogenador e um reagente de sulfonilação em um solvente que não influencia adversamente a reação ou sem solvente e na presença de uma base, conforme necessário.
[00154] Exemplos do reagente halogenador incluem cloreto de tionila, cloreto de fosforila, pentacloreto de fósforo, tribrometo de fósforo e análogos.
[00155] A quantidade do reagente halogenador a ser usada é geralmente de 1 a 20 equivalentes molares, de preferência, de 2 a 10 equivalentes molares, por 1 mol de composto (VI).
[00156] A temperatura de reação é geralmente de 0 a 130°C, de preferência, de 20 a 130°C.
[00157] O tempo de reação é geralmente de 0,5 a 100 h, de preferência, de 1 a 48 h.
[00158] Exemplos do reagente de sulfonilação incluem anidrido de ácido trifluorometanossulfônico, halogeneto de metanossulfonila, halogeneto de benzenossulfonila e análogos e a quantidade a ser usada dos mesmos é geralmente de 1 a 2 equivalentes molares, de preferência, de 1 a 1,5 equivalentes molares, por 1 mol de composto (VI). Exemplos da base a ser usada conforme necessário incluem trietilamina, diisopropiletilamina, piridina, 4-dimetilaminapiridina e análogos e a quantidade a ser usada dos mesmos é geralmente de 2 a 5 equivalentes molares, de preferência, de 2 a 3 equivalentes molares, por 1 mol de composto (VI).
[00159] Exemplos do solvente que não influenciam adversamente a reação incluem éteres, hidrocarbonetos, alcoóis, amidas, ésteres e análogos, dando-se preferência a éteres e amidas. Dois ou mais tipos dos solventes indicados acima podem ser usados em uma mistura, numa relação apropriada.
[00160] A temperatura de reação é geralmente de -10 a 100°C, de preferência, de 0 a 60°C.
[00161] O tempo de reação é geralmente de 0,5 a 100 h, de preferência, de 1 a 48 h.
[00162] Composto (VII) a ser o material de partida no Método D pode ser sintetizado por meio de um método conhecido, por exemplo, o método descrito no Journal of Heterocyclic Chemistry, vol. 12, páginas 565-572 (1975).
[00163] O composto (Va) também pode ser produzida, por exemplo, por meio do Método E mostrado abaixo ou um método análogo ao mesmo.
[00164] O hidróxi do composto (VIII-2) é convertido ao grupo de saída Q, e o composto (VIII) obtido é hidrolisado dando composto (Va-2). Este composto (Va-2) é reagido com hidrocarboneto halogenado e análogos dando composto (Va).(VIII-2) (VIII) (Va-2) (Va)sendo que cada símbolo é como definido acima.
[00165] Composto (VIII) pode ser produzido de acordo com o método de método do composto (Va) no Método D previamente indicado. A quantidade do reagente de halogenação e do reagente de sulfonilação a ser usada pode ser incrementada conforme necessário.
[00166] A hidrólise do composto (VIII) pode ser realizada, por exemplo, após substituir uma vez grupo de saída Q por acetóxi ou alcóxi ou diretamente em condições alcalinas ou condições ácidas, em um solvente que não influencia adversamente a reação.
[00167] Quando o grupo de saída Q é substituído uma vez por acetóxi ou alcóxi, por exemplo, é possível usar acetato de sódio, metóxido de sódio, etóxido de sódio e análogos, e a quantidade a ser usada dos mesmos é geralmente de 1 a 20 equivalentes molares, de preferência, de 1 a 5 equivalentes molares, por 1 mol de composto (VIII).
[00168] Para hidrólise direta em condições ácidas, por exemplo, é possível usar ácido acético, ácido clorídrico, ácido sulfúrico, ácido metanossulfônico e análogos como um ácido.
[00169] Para hidrólise direta em condições alcalinas, por exemplo, é possível usar solução aquosa de hidróxido de sódio, solução aquosa de hidróxido de potássio, solução aquosa de hidróxido de lítio e análogos, como uma base.
[00170] Exemplos do solvente que não influenciam adversamente a reação incluem éteres, hidrocarbonetos, alcoóis, cetonas, nitrilas, amidas, água e análogos, dando-se preferência a éteres, amidas e água. Dois ou mais tipos dos solventes indicados acima podem ser usados em uma mistura, numa relação apropriada.
[00171] A temperatura de reação é geralmente de 0 a 130°C, de preferência, de 20 a 130°C.
[00172] O tempo de reação é geralmente de 0,5 a 100 h, de preferência, de 1 a 48 h.
[00173] Composto (Va-2) pode ser convertido a composto (Va) reagindo-se composto (Va-2) com um composto representado pela fórmula R4’-Q’ sendo que R4’ é como definido acima e Q’ é um grupo de saída, em um solvente que não influencia adversamente a reação ou sem solvente na presença de uma base conforme necessário.
[00174] Exemplos do grupo de saída para Q’ incluem átomo de halogênio (p. ex., cloro, bromo, iodo), C1-6 alquilsulfonilóxi opcionalmente halogenado (p. ex., metilsulfonilóxi, etilsulfonilóxi, trifluorometilsulfonilóxi), C6-10 arilsulfonilóxi opcionalmente apresentando C1-6 alquila (p. ex., benzenossulfonilóxi, 4-toluenossulfonilóxi), metilmercapto, metanossulfonila e análogos, dando-se preferência a átomo de halogênio.
[00175] A quantidade do composto representado pela fórmula R4’-Q’ a ser usada é geralmente de 1 a 20 equivalentes molares, de preferência, de 2 a 10 equivalentes molares, por 1 mol de composto (Va-2).
[00176] Exemplos da base a ser usada conforme necessário incluem trietilamina, diisopropiletilamina, piridina, 4-dimetilaminapiridina, hidreto de sódio, carbonato de potássio, carbonato de césio, t-butóxido de potássio, t- butóxido de sódio e análogos, dando-se preferência a t-butóxido de sódio, e a quantidade a ser usada dos mesmos é geralmente de 2 a 5 equivalentes molares, de preferência, de 2 a 3 equivalentes molares, por 1 mol de composto (Va-2).
[00177] De preferência, adiciona-se brometo de tetrabutilamônio ou análogo à reação.
[00178] Exemplos do solvente que não influenciam adversamente a reação incluem éteres, hidrocarbonetos, alcoóis, amidas, ésteres e análogos, de preferência, éteres e amidas. Dois ou mais tipos dos solventes indicados acima podem ser usados em uma mistura, numa relação apropriada.
[00179] A temperatura de reação é geralmente de -10 a 100°C, de preferência, de 0 a 60°C.
[00180] O tempo de reação é geralmente de 0,5 a 100 h, de preferência, de 1 a 48 h.
[00181] Composto (VIII-2) a ser o material de partida no Método E pode ser sintetizado por meio de um método conhecido, por exemplo, o método descrito no Journal of Organic Chemistry, vol. 46, páginas 3040-3048 (1981).
[00182] Em compostos (I), é possível usar composto (Ia) e composto (Ib), por exemplo, Método F mostrado abaixo ou um método análogo ao mesmo.
[00183] Composto (Ib) e composto (Ia) podem ser produzidos a partir de composto (Ic) por meio de reações de acordo com [Método E].sendo que cada símbolo é como definido acima.
[00184] A reação do composto (Ic) a composto (Ib) pode ser realizada de acordo com a reação do composto (VIII) a composto (Va-2) no Método E.
[00185] A reação do composto (Ib) a composto (Ia) pode ser realizada de acordo com a reação do composto (Va-2) a composto (Va) no Método E.
[00186] Composto (Ic) pode ser produzido de acordo com o método de produção do composto (Ica) e composto (Icb) mostrado abaixo.
[00187] Nos compostos (Ic), é possível produzir composto (Ica) sendo que R3 é hidróxi e composto (Icb) sendo que R3 é alcóxi apresentando opcionalmente substituinte(s) (mostrado por R3’ na fórmula (Icb) a seguir), por exemplo, por meio do Método G mostrado abaixo ou um método análogo ao mesmo.Método G
[00188] Composto (Ica) e composto (Icb) podem ser produzidos do composto (VIII) por meio de reações de acordo com [Método A], [Método B] e [Método C].(Vlll> (Illa1) (lea) (|cb)sendo que cada símbolo é como definido acima.
[00189] A reação do composto (VIII) a composto (IIIa’) pode ser realizada de acordo com Método B.
[00190] A reação do composto (IIIa’) a composto (Ica) pode ser realizada de acordo com Método A.
[00191] A reação do composto (Ica) a composto (Icb) pode ser realizada de acordo com o Método C.
[00192] O composto (Ib) também pode ser produzido, por exemplo, o Método H mostrado abaixo ou um método análogo ao mesmo.
[00193] Dos compostos (Ib), o composto (Ib’), sendo que R3 é alcóxi apresentando opcionalmente substituinte(s) (mostrado por R3’ na seguinte fórmula (Ib’)) pode ser produzido removendo-se R4” do composto (Id), sendo que R3 é alcóxi apresentando opcionalmente substituinte(s) (mostrado por R3’ na fórmula (Id)) a seguir e R4 é fenacila apresentando opcionalmente substituinte(s), metoximetila, 4-metoxibenzila ou 2,4-dimetoxibenzilasendo que R4” é fenacila apresentando opcionalmente substituinte(s), metoximetila, 4-metoxibenzila ou 2,4-dimetoxibenzila, e outros símbolos são como definido acima.
[00194] Quando R4” é fenacila apresentando opcionalmente substituinte(s), a conversão do composto (Id) a composto (Ib’) pode ser realizada, por exemplo, na presença de metal, como zinco e análogos em condições ácidas em um solvente que não influencia adversamente a reação. A quantidade de zinco a ser usada é geralmente de 1 a 20 equivalentes molares, de preferência, de 1 a 10 equivalentes molares, por 1 mol de composto (Id). Como ácido, é possível usar ácido clorídrico, ácido sulfúrico e análogos.
[00195] Exemplos do solvente que não influenciam adversamente a reação incluem éteres, hidrocarbonetos, alcoóis, cetonas, nitrilas, amidas, água e análogos, dando-se preferência a éteres, amidas e água. Dois ou mais tipos dos solventes indicados acima podem ser usados em uma mistura, numa relação apropriada.
[00196] A temperatura de reação é geralmente de 20 a 120°C, de preferência, de 20 a 100°C.
[00197]de 1 a 24 h.
[00198]composto (Ib’) pode ser realizada em condições ácidas em um solvente que não influencia adversamente a reação. Como ácido, é possível usar ácido clorídrico, ácido sulfúrico e análogos.
[00199] Exemplos do solvente que não influenciam adversamente a reação incluem éteres, hidrocarbonetos, alcoóis, cetonas, nitrilas, amidas, água e análogos, dando-se preferência a éteres, amidas e água. Dois ou mais tipos dos solventes indicados acima podem ser usados em uma mistura, numa relação apropriada.
[00200] A temperatura de reação é geralmente de 0 a 120°C, de preferência, de 20 a 60°C.
[00201] O tempo de reação é geralmente de 0,5 a 100 h, de preferência, de 1 a 24 h.
[00202] Quando R4” é 4-metoxibenzila, a conversão do composto (Id) a composto (Ib’) pode ser realizada em fortes condições ácidas em um solvente que não influencia adversamente a reação. Como ácido, é possível usar ácido trifluoroacético, ácido trifluorometanossulfônico e análogos. Neste caso, é possível usar anisol como um aglutinador de cátions, numa quantidade, geralmente, de 1 a 20 equivalentes molares, de preferência, de 1 a 5 equivalentes molares, por 1 mol de composto (Id).
[00203] Exemplos do solvente que não influenciam adversamente a reação incluem éteres, hidrocarbonetos, alcoóis, cetonas, nitrilas, amidas, e análogos, de preferência, éteres e amidas. Dois ou mais tipos dos solventes indicados acima podem ser usados em uma mistura, numa relação apropriada.
[00204] A temperatura de reação é geralmente de 0 a 120°C, de preferência, de 20 a 60°C.
[00205] O tempo de reação é geralmente de 0,5 a 100 h, de preferência, de 1 a 24 h.
[00206] Quando R4” é 2,4-dimetoxibenzila, a conversão do composto (Id) a composto (Ib’) pode ser realizada na presença de um oxidante, como diamônio nitrato de cério (IV) (CAN), 2,3-dicloro-5,6-diciano-1,4- benzoquinona (DDQ) e análogos em um solvente que não influencia adversamente a reação.
[00207] A quantidade do oxidante a ser usada é geralmente de 1 a 20 equivalentes molares, de preferência, de 1 a 5 equivalentes molares, por 1 mol de composto (Id).
[00208] Exemplos do solvente que não influenciam adversamente a reação incluem éteres, hidrocarbonetos, alcoóis, cetonas, nitrilas, amidas, água e análogos, dando-se preferência a éteres, nitrilas, amidas e água. Dois ou mais tipos dos solventes indicados acima podem ser usados em uma mistura, numa relação apropriada.
[00209] A temperatura de reação é geralmente de 0 a 120°C, de preferência, de 20 a 60°C.
[00210] O tempo de reação é geralmente de 0,5 a 100 h, de preferência, de 1 a 24 h.
[00211] O composto (IIIa) também pode ser produzido, por exemplo, por meio do Método I mostrado abaixo ou um método análogo ao mesmo.
[00212] Composto (Vb) é reagido com composto (4) dando composto (IIIa).(Vb) (llla)sendo que Q’ é um grupo de saída, e outros símbolos são como definido acima.
[00213] Exemplos do grupo de saída para Q’ incluem aqueles similares ao grupo de saída para o Q previamente indicado, dando-se preferência a átomo de halogênio.
[00214] Composto (4) pode ser um reagente comercialmente obtenível, ou pode ser sintetizado por meio de um método conhecido per se.
[00215] Composto (Vb), por exemplo, derivado 6-amina-2,4-dioxo- 1,2,3,4-tetraidropirimidina-5-carboxilato e análogos, a ser o material de partida no Método I pode ser sintetizado por meio de um método conhecido, por exemplo, o método descrito no Journal of Chemical Society of Japan, vol. 46, páginas 3849-3853 (1973). Por exemplo, derivado 2-mercapto-4-oxo-1,4- diidroquinolina-3-carboxilato e análogos pode ser sintetizado por meio de um método conhecido, por exemplo, o método descrito no Journal of Heterocyclic Chemistry, vol. 27, páginas 839-843 (1990).
[00216] A reação entre composto (Vb) e composto (4) pode ser realizada na presença de uma base em um solvente que não influencia adversamente a reação.
[00217] A quantidade de composto (4) a ser usada é geralmente de 1 a 3 equivalentes molares, de preferência, de 1 a 2 equivalentes molares, por 1 mol de composto (Vb). Exemplos da base incluem metóxido de sódio, etóxido de sódio, carbonato de sódio, hidrogenocarbonato de sódio, hidróxido de sódio, trietilamina, diisopropiletilamina, piridina, 4-dimetilaminapiridina e análogos e a quantidade a ser usada dos mesmos é geralmente de 2 a 5 equivalentes molares, de preferência, de 2 a 3 equivalentes molares, por 1 mol de composto (Vb).
[00218] Exemplos do solvente que não influenciam adversamente a reação incluem éteres, hidrocarbonetos, alcoóis, cetonas, nitrilas, amidas, água e análogos, dando-se preferência a éteres, amidas e água. Dois ou mais tipos dos solventes indicados acima podem ser usados em uma mistura, numa relação apropriada.
[00219] A temperatura de reação é geralmente de 20 a 120°C, de preferência, de 20 a 100°C.
[00220] O tempo de reação é geralmente de 0,5 a 100 h, de preferência, de 1 a 24 h.
[00221] Um composto no escopo da presente invenção também pode ser produzido aplicando-se um meio conhecidos per se ao composto (I) para a introdução de substituintes e a conversão de grupos funcionais. Para a conversão de substituintes, é possível usar um método convencional conhecido. Por exemplo, pode-se indicar a conversão a carbóxi por meio de hidrólise de éster, conversão a carbamoíla por meio de amidação de carbóxi, conversão a hidroximetila por meio de redução de carbóxi, conversão a composto de álcool por meio de redução ou alquilação de carbonila, aminação redutiva de carbonila, oximação de carbonila, acilação, ureação, sulfonilação ou alquilação de amina, substituição e aminação de halogênio ativo por meio de amina, aminação de nitro por meio de redução, alquilação de hidróxi, substituição e aminação de hidróxi e análogos. Quando um substituinte reativo que causa reação não-objetiva está presente durante a introdução de substituintes e a conversão de grupos funcionais, introduz-se um grupo protetor antecipadamente conforme necessário no substituinte reativo através de um meio conhecido per se, e o grupo protetor é removido através de um meio conhecido per se após a reação objetiva, com o que o composto no escopo da presente invenção também pode ser produzido.
[00222] No método de produção indicado acima, quando o composto de partida ou o composto da presente invenção apresenta um grupo amina, um grupo carboxila, um grupo hidróxi ou um grupo mercapto como um substituinte, é possível introduzir nestes grupos um grupo protetor geralmente usado na química dos peptídeos e análogos. O grupo protetor pode ser removido de acordo com um método convencional em qualquer etapa em cada Esquema.
[00223] O Composto (I) pode ser isolado e purificado através de um meio conhecido per se, como transferência de fase, concentração, extração com solvente, fracionamento, conversão líquida, cristalização, recristalização, cromatografia e análogos. Quando o composto (I) é obtido como um composto livre, ele pode ser convertido a um sal desejado por meio de um método conhecido per se ou um método análogo ao mesmo. Inversamente, quando o composto é obtido como um sal, ele pode ser convertido a uma forma livre ou outro sal desejado por meio de um método conhecido per se ou um método análogo ao mesmo.
[00224] O Composto (I) pode ser usado como uma pró-droga. Uma pró-droga do composto (I) significa um composto convertido a composto (I) por meio de uma reação devida a uma enzima, um ácido gástrico, etc. na condição fisiológica no corpo vivo, ou seja, um composto convertido a composto (I) por meio de oxidação, redução, hidrólise, etc. devido a uma enzima, um composto convertido a composto (I) por meio de hidrólise etc. devido a ácido gástrico, e análogos.
[00225] Uma pró-droga do composto (I) pode ser um composto obtido submetendo-se um amina no composto (I) a uma acilação, alquilação ou fosforilação (p. ex., um composto obtido submetendo-se um amina no composto (I) a eicosanoilação, alanilação, pentilaminacarbonilação, (5-metil- 2-oxo-1,3-dioxolen-4-il)metoxicarbonilação, tetraidrofuranilação,pirrolidilmetilação, pivaloiloximetilação ou t-butilação); um composto obtido submetendo-se hidróxi no composto (I) a acilação, alquilação, fosforilação ou boração (p. ex., um composto obtido submetendo-se hidróxi no composto (I) da presente invenção a acetilação, palmitoilação, propanoilação, pivaloilação, succinilação, fumarilação, alanilação ou dimetilaminametilcarbonilação); um composto obtido submetendo-se carbóxi no composto (I) a esterificação ou amidação (p. ex., um composto obtido submetendo-se carbóxi no composto (I) a esterificação com etila, esterificação com fenila, esterificação com carboximetila, esterificação com dimetilaminametila, esterificação com pivaloiloximetila, esterificação com etoxicarboniloxietila, esterificação com ftalidila, esterificação com (5-metil-2-oxo-1,3-dioxolen-4-il)metila, esterificação com cicloexiloxicarboniletila ou metilamidação) e análogos. Qualquer um destes compostos pode ser produzido do composto (I) por meio de um método conhecido per se.
[00226] Uma pró-droga do composto (I) também pode ser um composto convertido a composto (I) em condições fisiológicas, como aquelas descritas em IYAKUHIN no KAIHATSU (Development of Pharmaceuticals), Vol. 7, Design of Molecules, p. 163-198, publicada por HIROKAWA SHOTEN (1990).
[00227] Quando o composto (I) apresenta um isômero, como isômero óptico, estereoisômero, isômero posicional, isômero rotacional e análogos, qualquer isômero e uma mistura dos mesmos são compreendidos no composto (I). Por exemplo, quando o composto (I) apresenta um isômero óptico, um isômero óptico separado de um racemizado também é compreendido no composto (I). Referidos isômeros podem ser obtidos como produtos independentes por meio uma via de síntese ou um meio de separação (concentração, extração com solvente, cromatografia de coluna, recristalização e análogos) conhecido per se.
[00228] Composto (I) pode ser um cristal, e ambos, um cristal simples e misturas de cristais, são compreendidos no composto (I). Cristais podem ser produzidos por meio de cristalização de acordo com métodos de cristalização conhecidos per se.
[00229] Composto (I) também pode ser um co-cristal.
[00230] Composto (I) pode ser um hidrato, um não-hidrato, um solvatoou um não-solvato, sendo que ambos são compreendidos no composto (I) e análogos.
[00231] Um composto marcado com um isótopo (p. ex., 2H, 3H, 14C, 35S, 125I etc.) também é compreendido no composto (I).
[00232] Composto (I) da presente invenção, ou um sal do mesmo, ou uma pró-droga do mesmo (por vezes abreviado como “o composto da presente invenção” na presente descrição) interage, por exemplo, com proteína Smo humana e altera sua estrutura estérica, com o que a formação de um complexo com uma proteína envolvida na transdução de sinal no citoplasma é inibida e o sistema de transdução de sinal do porco-espinho é inibido. Alternativamente, o composto da presente invenção interage com proteína de Smo humana e inibe diretamente a formação de um complexo de proteína de Smo humana com uma proteína envolvida no sistema de transdução de sinal do porco-espinho no citoplasma, com o que o sistema de transdução de sinal do porco-espinho é inibido. Alternativamente, o composto da presente invenção interage com um sítio de uma proteína Smo, por exemplo, sítio de fosforilação e análogos, que é modificado por meio de uma proteína envolvida no Sistema de transdução de sinal do porco-espinho, com o que a modificação, como fosforilação de Smo e análogos é inibida e o sistema de transdução de sinal do porco-espinho é inibido.
[00233] A inibição do sistema de transdução de sinal do porco-espinho pode ser medida, por exemplo, quantificando-se uma diminuição do nível de expressão de um gene repórter conectado a jusante do sítio de ligação de Gli baseado em intensidade de fluorescência de acordo com o Exemplo Experimental 1. Alternativamente, ela pode ser medida quantificando-se a expressão de Gli-1 mRNA em um extrato de células por meio do método de PCR quantitativa e análogos. Um composto que inibe sinal de porco-espinho objetiva Smo, o que pode ser confirmado, por exemplo, ligando-se ciclopamina marcada com fluorescência e um composto de teste a células expressando Smo, medindo-se o nível de fluorescência da célula, e comparando-se o valor com aquele, sem adição de um composto de teste para verificar uma diminuição.
[00234] Assim, o composto da presente invenção é útil como um inibidor de Smo para mamíferos (p. ex., camundongo, rato, hâmster, coelho, gato, cão, bovina, ovelha, macaco, humano, etc.). O composto da presente invenção é usado como um agente farmacêutico, como um agente para a profilaxia ou tratamento de doenças possivelmente influenciadas por Smo, por exemplo, câncer [p. ex., câncer colorretal (p. ex., câncer do colo, câncer retal, câncer anal, câncer colorretal familiar, câncer colorretal de não-polipose hereditária, tumor estromal gastrintestinal, etc.), câncer do pulmão (p. ex., câncer do pulmão de células não-pequenas, câncer do pulmão de células pequenas, mesotelioma maligno, etc.), mesotelioma, câncer pancreático (p. ex., câncer do duto pancreático, tumor endócrino pancreático, etc.), câncer da faringe, câncer da laringe, câncer do esôfago, câncer gástrico (p. ex., adenocarcinoma papilar, adenocarcinoma mucinoso, câncer adenoescamoso, etc.), câncer duodenal, câncer do intestino delgado, câncer de mama (p. ex., carcinoma de mama ductal invasivo, câncer ductal in situ, câncer de mama inflamatório, etc.), câncer do ovário (p. ex., câncer epitelial ovariano, tumor de células germinativas extragonadais, tumor de células germinativas ovarianas, tumor ovariano com baixo potencial maligno, etc.), tumor testicular, câncer da próstata (p. ex., câncer da próstata dependente de hormônio, câncer da próstata não-dependente de hormônio, etc.), câncer de fígado (p. ex., carcinoma hepatocelular, câncer de fígado primário, câncer de duto biliar extra-hepático, etc.), câncer da tireóide (p. ex., câncer da tireóide medular, etc.), câncer de rim (p. ex., carcinoma de células renais, câncer da pélvis renal e câncer de células transicionais da uretra, etc.), câncer do útero (p. ex., câncer cervical, câncer do corpo uterino, sarcoma uterino, etc.), tumor do cérebro (p. ex., meduloblastoma, glioma, astrocitoma pineal, astrocitoma pilocítico, astrocitoma difuso, astrocitoma anaplásico, adenoma da pituitária, etc.), retinoblastoma, câncer de pele (p. ex., carcinoma de células basais, melanoma maligno, etc.), sarcoma (p. ex., rabdomiosarcoma, leiomiosarcoma, sarcoma dos tecidos moles, etc.), tumor ósseo maligno, câncer da bexiga urinária, câncer do sangue (p. ex., mieloma múltiplo, leucemia, linfoma maligno, doença de Hodgkin, desordem mieloproliferativa crônica, etc.), câncer primário desconhecido etc.], um inibidor de crescimento de câncer, um inibidor da metástase do câncer, um promotor de apoptose e análogos. Entre estes, o composto da presente invenção é efetivo, por exemplo, para tumor do cérebro, câncer de pele, câncer do pulmão, câncer pancreático, câncer do duto biliar, câncer da próstata, câncer do esôfago, câncer gástrico, câncer colorretal, sarcoma e câncer de mama. Particularmente, o composto da presente invenção é efetivo para glioma, meduloblastoma, tumor de células basais, câncer do pulmão de células pequenas, câncer pancreático, câncer do duto biliar, câncer da próstata, câncer do esôfago, câncer gástrico, câncer colorretal, rabdomiosarcoma e câncer de mama.
[00235] O composto da presente invenção pode ser administrado oralmente ou parenteralmente tal qual é ou em uma mistura com um veículo farmacologicamente aceitável.
[00236] A forma de dosagem do composto da presente invenção para administração oral é, por exemplo, de tablete (incluindo tablete revestido com açúcar, tablete revestido com película), pílula, grânulo, pó, cápsula (incluindo cápsula mole, microcápsula), xarope, emulsão, suspensão e análogos, e a forma de dosagem para administração parenteral é, por exemplo, injeção, agente de injeção, instilação, supositório e análogos. Adicionalmente, ela é efetiva para preparar uma preparação de liberação prolongada por meio da combinação do composto com uma base vantajosa (p. ex., polímero de ácido butírico, polímero de ácido glicólico, copolímero de ácido butírico-ácido glicólico, uma mistura de um polímero de ácido butírico e um polímero de ácido glicólico, éster de ácido graxo de poliglicerol etc.).
[00237] Como um método para produzir o composto da presente invenção na forma de dosagem indicada acima, é possível usar um método de produção conhecido geralmente usado no campo pertinente. Quando a forma de dosagem indicado acima é produzida, usa-se geralmente quantidades vantajosas de aditivos, como excipiente, aglutinante, desintegrante, lubrificante, agente adoçante, tensoativo, agente de suspensão, emulsificante e análogos, geralmente usados no campo farmacêutico, [e que] são adicionados de maneira apropriada conforme necessário para a produção.
[00238] Quando o composto da presente invenção é preparado em um tablete, por exemplo, ele pode ser produzido adicionando-se um excipiente, um aglutinante, um desintegrante, um lubrificante e análogos, e quando se deseja preparar uma pílula ou um grânulo, ele pode ser produzido adicionando-se um excipiente, um ligante, um desintegrante e análogos. Quando se deseja preparar um pó ou uma cápsula, isto pode ser produzido adicionando-se um excipiente e análogos, quando se deseja preparar um xarope, isto pode ser produzido adicionando-se um adoçante e análogos, e quando se deseja preparar uma emulsão ou uma suspensão, isto pode ser produzido adicionando-se um agente de suspensão, um tensoativo, um emulsificante e análogos.
[00239] Exemplos do excipiente incluem lactose, sacarose, glicose, amido, sacarose, celulose microcristalina, glicirriza em pó, manitol, hidrogenocarbonato de sódio, fosfato de cálcio, sulfato de cálcio e análogos.
[00240] Exemplos do aglutinante incluem pasta de amido líquido a 5 - 10 % em peso, solução de goma arábica ou solução de gelatina a 10 - 20 % em peso, solução de tragacanto a 1 - 5 % em peso, sol de carboximetil celulose solução, solução de alginato de sódio, glicerina e análogos.
[00241] Exemplos do desintegrante incluem amido, carbonato decálcio e análogos.
[00242] Exemplos do lubrificante incluem estearato de magnésio,ácido esteárico, estearato de cálcio, talco purificado e análogos.
[00243] Exemplos do adoçante incluem glicose, frutose, açúcarinvertido, sorbitol, xilitol, glicerina, xarope simples e análogos.
[00244] Exemplos do tensoativo incluem lauril sulfato de sódio,polissorbato 80, éster de ácido monograxo de sorbitol, estearato de polioxila 40 e análogos.
[00245] Exemplos do agente de suspensão incluem goma arábica, alginato de sódio, carboximetil celulose de sódio, metil celulose, bentonita e análogos.
[00246] Exemplos do emulsificante incluem goma arábica, tragacanto, gelatina, polissorbato 80 e análogos.
[00247] Adicionalmente, quando o composto da presente invenção é produzido na forma de dosagem indicada acima, uma quantidade vantajosa de um corante, um conservante, um aromático, um corretor, um estabilizante, um agente espessante e análogos, usados tipicamente no campo da preparação, pode ser adicionada conforme a necessidade.
[00248] Como a injeção, é possível indicar injeção intravenosa e também injeção subcutânea, injeção intracutânea, injeção intramuscular, instilação e análogos, e como a preparação de liberação prolongada é possível indicar um agente transdérmico de iontoforese.
[00249] Referidas injeções são preparadas por meio de métodos conhecidos per se, ou por meio de dissolução, suspensão ou emulsificação do composto da presente invenção em um líquido oleoso ou aquoso esterilizado. Como um liquido aquoso para injeção, é possível indicar solução salina fisiológica, soluções isotônicas contendo glicose ou outras drogas auxiliares (p. ex., D-sorbitol, D-manitol, cloreto de sódio e análogos) e análogos, e elas podem ser usadas em combinação com agentes solubilizantes vantajosos, como alcoóis (p. ex., etanol), polialcoóis (p. ex., propileno glicol, polietileno glicol), tensoativos não-iônicos (p. ex., polissorbato 80, HCO-50) e análogos. Como um líquido oleoso, é possível usar óleo de gergelim, óleo de soja e análogos, que podem ser usados em combinação com agentes solubilizantes, como benzoato de benzila, álcool de benzila e análogos. Adicionalmente, é possível combinar tamponadores (p. ex., tamponador de fosfato, tamponador de acetato de sódio), agentes acalmadores (p. ex., cloreto de benzalcônio, cloridrato de procaína e análogos), estabilizadores (p. ex., albumina de soro humano, polietileno glicol e análogos), conservantes (p. ex., álcool de benzila, fenol e análogos) e análogos. Uma injeção preparada é geralmente envasada em uma ampola.
[00250] Embora o teor do composto da presente invenção no agente farmacêutico da presente invenção varie dependendo da forma da preparação farmacêutica, ele é geralmente de cerca de 0,01 a 100 % em peso, de preferência, de cerca de 2 a 85 % em peso, mais preferivelmente de cerca de 5 a 70 % em peso, relativa à preparação como um todo.
[00251] Embora o teor do aditivo no agente farmacêutico da presente invenção varie dependendo da forma da preparação farmacêutica, ele é geralmente de cerca de 1 a 99,9 % em peso, de preferência, de cerca de 10 a 90 % em peso, relativamente à preparação como um todo.
[00252] O composto da presente invenção é estável e pouco tóxico, e pode ser usado seguramente. Embora a dose diária varie dependendo da condição e do peso corporal de pacientes, do tipo de composto, da via de administração e análogos, no caso de, por exemplo, administração oral a pacientes para o tratamento de câncer, a dose diária a um adulto (peso corporal de cerca de 60 kg) é de cerca de 1 a 1000 mg, de preferência, de cerca de 3 a 300 mg, mais preferivelmente de cerca de 10 a 200 mg, como um ingrediente ativo (o composto da presente invenção), que pode ser dada em uma única administração ou administrada em 2 ou 3 porções por dia.
[00253] Quando o composto da presente invenção é administrado parenteralmente, ele é geralmente administrado em forma de um líquido (p. ex., injeção). Embora a dose varie dependendo do sujeito da administração, órgão-alvo, sintoma, método de administração e análogos, ela é, por exemplo, de cerca de 0,01 mg a cerca de 100 mg, de preferência, de cerca de 0,01 a cerca de 50 mg, mais preferivelmente de cerca de 0,01 a cerca de 20 mg, na forma de uma injeção, relativamente a 1 kg de peso corporal, e é dada, de preferência, por injeção intravenosa.
[00254] O composto da presente invenção pode ser usado concorrentemente com outras drogas. Para ser específico, o composto da presente invenção pode ser usado juntamente com drogas, como agentes terapêuticos hormonais, agentes quimioterápicos, agentes imunoterápicos, agentes farmacêuticos que inibem a ação de fatores de crescimento celular ou receptores de fator de crescimento celular e análogos. A seguir, as drogas que podem ser usadas em combinação com o composto da presente invenção são abreviadas como drogas concomitantes.
[00255] Exemplos dos “agentes terapêuticos hormonais” incluem fosfestrol, dietilestilbestrol, clorotrianiseno, acetato de medroxiprogesterona acetato, acetato de megestrol, acetato de clormandinona, acetato de ciproterona, danazol, alilestrenol, gestrinona, mepartricina, raloxifeno, oumeloxifeno, levormeloxifeno, anti-estrógenos (p. ex., citrato de tamoxifeno, citrato de toremifeno, e análogos), preparações de pílulas, mepitiostano, testrolactona, aminaglutetimida, agonistas de LH-RH (p. ex., acetato de goserelina, buserelina, leuprorelina, e análogos), droloxifeno, epitiostanol, sulfonato de etinilestradiol, inibidores de aromatase (p. ex., cloridrato de fadrozol, anastrozol, retrozol, exemestano, vorozol, formestano, e análogos), anti-andrógenos (p. ex., flutamida, bicartamida, nilutamida, e análogos), inibidores de 5α-redutase (p. ex., finasterida, epristerida, e análogos), drogas do hormônio do córtex adrenal (p. ex., dexametasona, prednisolona, betametasona, triamcinolona, e análogos), inibidores da síntese de andrógeno (p. ex., abiraterona, e análogos), retinóide e drogas que retardam o metabolismo dos retinóides (p. ex., liarozol, e análogos), hormônio da tireóide, e preparações de Sistemas de Fornecimento de Drogas DDS (Drug Delivery System) dos mesmos, e análogos.
[00256] Exemplos dos “agentes quimioterápicos” incluem agentes de alquilação, antimetabólitos, antibióticos anticâncer, agentes anticâncer derivados de plantas, e análogos.
[00257] Exemplos dos “agentes alquiladores” incluem mostarda de nitrogênio, cloridrato de N-óxido de mostarda de nitrogênio, clorambutila, ciclofosfamida, ifosfamida, tiotepa, carboquona, tosilato de improsulfano, busulfano, cloridrato de nimustina, mitobronitol, melfalano, dacarbazina, ranimustina, fosfato de estramustina de sódio, trietilenomelamina, carmustina, lomustina, estreptozocina, pipobromano, etoglucida, carboplatina, cisplatina, miboplatina, nedaplatina, oxaliplatina, altretamina, ambamustina, cloridrato de dibrospídio, fotemustina, prednimustina, pumitepa, ribomustina, temozolomida, treosulfano, trofosfamida, zinostatina estimalâmero, adozelesina, cistemustina, bizelesina, preparações de DDS (Drug Delivery System) dos mesmos, e análogos.
[00258] Exemplos dos “antimetabólitos” incluem mercaptopurina, 6- mercaptopurina ribosida, tioinosina, metotrexato, pemetrexed, enocitabina, citarabina, ocfosfato de citarabina, cloridrato de ancitabina, drogas 5-FU (p. ex., fluorouracila, tegafur, UFT, doxifluridina, carmofur, galocitabina, emitefur, capecitabina, e análogos), aminapterina, nelzarabina, leucovorina cálcio, tabloid, butocina, folinato de cálcio, levofolinato cálcio, cladribina, emitefur, fludarabina, gemcitabina, hidroxicarbamida, pentostatina, piritrexima, idoxuridina, mitoguazona, tiazofrina, ambamustina, bendamustina, preparações de DDS dos mesmos, e análogos.
[00259] Exemplos dos “antibióticos anticâncer” incluem actinomicina- D, actinomicina-C, mitomicina-C, cromomicina-A3, cloridrato de bleomicina, sulfato de bleomicina, sulfato de peplomicina, cloridrato de daunorubicina, cloridrato de doxorubicina, cloridrato de aclarubicina, cloridrato de pirarubicina, cloridrato de epirubicina, neocarzinostatina, mitramicina, sarcomicina, carzinofilina, mitotano, cloridrato de zorubicina, cloridrato de mitoxantrona, cloridrato de idarubicina, preparações DDS dos mesmos, e análogos.
[00260] Exemplos do “agentes anticâncer derivados de plantas” incluem etoposida, fosfato de etoposida, sulfato de vinblastina, sulfato de vincristina, sulfato de vindesina, teniposida, paclitaxel, docetaxel, vinorelbina, preparações de DDS, e análogos.
[00261] Exemplos dos “agentes imunoterápicos (BRM)” incluem picibanil, krestin, sizofirano, lentinano, ubenimex, interferons, interleucinas, fator estimulador de colônia de macrófagos, fator estimulador de colônia de granulócitos, eritropoietina, linfotoxina, vacina BCG, Corynebacterium parvum, levamisol, polissacarídeo K, procodazol, anticorpo anti-CTLA4, e análogos.
[00262] Exemplo do “fatores de crescimento celular” nos “agentes farmacêuticos que inibem a ação de fatores de crescimento celular ou receptores de fator de crescimento celular” incluem quaisquer substâncias que promovam proliferação de células, que são normalmente peptídeos apresentando peso molecular não superior a 20.000 e que são capazes de apresentar sua atividade em baixas concentrações por meio de ligação a um receptor, incluindo (1) fator de crescimento epidérmico (EGF, epidermal growth factor) ou substâncias que apresentam substancialmente a mesma atividade que EGF [p. ex., TGFα, e análogos], (2) insulina ou substâncias que apresentam substancialmente a mesma atividade que insulina [p. ex., insulina, fator de crescimento similar a insulina (IGF, insulin-like growth factor) IGF- 1, IGF-2, e análogos], (3) fator de crescimento de fibroblastos FGF (fibroblast growth factor) ou substâncias que apresentam substancialmente a mesma atividade que FGF [p. ex., FGF ácido, FGF básico, fator de crescimento de queratinócitos KGF (keratinocyte growth factor), FGF-10, e análogos], e (4) outros fatores de crescimento de células [p. ex., fator estimulador de colônias CSF (colony stimulating factor), EPO (eritropoietina), IL-2 (interleucina-2), fator de crescimento de nervos (NGF, nerve growth factor), fator de crescimento derivado de plaquetas PDGF (platelet-derived growth factor), fator de transformação do crescimento TGFβ (transforming growth factor β), fator de crescimento de hepatócitos (HGF, hepatocyte growth factor), fator de crescimento endotelial vascular (VEGF, vascular endothelial growth factor), heregulina, angiopoietina, e análogos].
[00263] Exemplos dos “receptores de fator de crescimento de células” incluem quaisquer receptores capazes de ligação com os fatores de crescimento de células previamente indicados, incluindo receptor de EGF, receptor de heregulina (HER3, etc.), receptor de insulina, receptor de IGF-1, receptor de IGF-2, receptor de FGF-1 ou receptor de FGF-2, receptor de VEGF, receptor de angiopoietina (Tie2 etc.), receptor de PDGF, e análogos.
[00264] Como os “agentes farmacêuticos que inibem a ação de fatores de crescimento celular ou receptores de fator de crescimento celular”, usa-se inibidor de EGF, inibidor de TGFα, inibidor de heregulina, inibidor de insulina, inibidor de IGF, inibidor de FGF, inibidor de KGF, inibidor de CSF, inibidor de EPO, inibidor de IL-2, inibidor de NGF, inibidor de PDGF, inibidor de TGFβ, inibidor de HGF, inibidor de VEGF, inibidor de angiopoietina, inibidor de receptor de EGF, inibidor de HER2, inibidor de HER4, inibidor de receptor de insulina, inibidor de receptor de IGF-1, inibidor de receptor de IGF-2, inibidor de receptor de FGF-1, inibidor de receptor de FGF-2, inibidor de receptor de FGF-3, inibidor de receptor de FGF-4, inibidor de receptor de VEGF, inibidor de Tie-2, inibidor de recetor de PDGF, inibidor de Abl, inibidor de Raf, inibidor de FLT3, inibidor de c- Kit, inibidor de Src, inibidor de PKC, inibidor de Trk, inibidor de Ret, inibidor de mTOR, inibidor de Aurora, inibidor de PLK, inibidor de MEK(MEK1/2), inibidor de MET, inibidor de CDK, inibidor de Akt, inibidor de ERK e análogos. Mais especificamente, usa-se anticorpo anti-VEGF (Bevacizumab etc.), anticorpo anti-HER2 (Trastuzumab, Pertuzumab etc.), anticorpo anti-EGFR (Cetuximab, Panitumumab, Matuzumab, Nimotuzumab etc.), anticorpo anti-VEGFR, anticorpo anti-HGF, mesilato de Imatinib, Erlotinib, Gefitinib, Sorafenib, Sunitinib, Dasatinib, Lapatinib, Vatalanib, 4- (4-fluoro-2-metil-1H-indol-5-ilóxi)-6-metóxi-7-[3-(1-pirrolidinil)propóxi] quinazolina (AZD-2171), Lestaurtinib, Pazopanib, Canertinib, Tandutinib, 3- (4-bromo-2,6-difluorobenzilóxi)-5-[3-[4-(1-pirrolidinil)butil]ureído]isotiazol- 4-carboxamida (CP-547632), Axitinib, N-(3,3-dimetil-2,3-diidro-1H-indol-6- il)-2-(piridin-4-ilmetilamina)piridina-3-carboxamida (AMG-706), Nilotinib, 6-[4-(4-etilpiperazin-1-ilmetil)fenil]-N-[1(R)-feniletil]-7H-pirrol[2,3- d]pirimidin-4-amina (AEE-788), Vandetanib, Temsirolimus, Everolimus, Enzastaurin, N-[4-[4-(4-metilpiperazin-1-il)-6-(3-metil-1H-pirazol-5-ilamina)pirimidin-2-ilsulfanil]fenil]ciclopropanocarboxamida (VX-680), 2- [N-[3-[4-[5-[N-(3-fluorofenil)carbamoilmetil]-1H-pirazol-3-ilamina] quinazolin-7-ilóxi]propil]-N-etilamina]etil éster do ácido fosfórico (AZD- 1152), ácido 4-[9-cloro-7-(2,6-difluorofenil)-5H-pirimido[5,4- d][2]benzazepin-2-ilamina]benzóico (MLN-8054), sal de sódio de N-[2- metóxi-5-[(E)-2-(2,4,6-trimetoxifenil)vinilsulfonilmetil]fenil]glicina (ON- 1910Na), 4-[8-ciclopentil-7(R)-etil-5-metil-6-oxo-5,6,7,8-tetraidropteridin-2- ilamina]-3-metóxi-N-(1-metilpiperidin-4-il)benzamida (BI-2536), 2-hidroxietil éster do ácido 5-(4-bromo-2-clorofenilamina)-4-fluoro-1-metil-1H- benzimidazol-6-carboidroxâmico (AZD-6244), N-[2(R),3-diidroxipropóxi]- 3,4-difluoro-2-(2-fluoro-4-iodofenilamina)benzamida (PD-0325901),Everolimus (RAD001) e análogos.
[00265] Adicionalmente às drogas previamente indicadas, também é possível usar L-asparaginase, aceglatona, cloridrato de procarbazina, sal de complexo de protoporfirina-cobalto, hematoporfirina mercúrica-sódio, inibidores de topoisomerase I (p. ex., irinotecano, topotecano, e análogos), inibidores de topoisomerase II (p. ex., sobuzoxano, e análogos), indutores de diferenciação (p. ex., retinóide, vitamina D, e análogos), outros inibidores de angiogênese (p. ex., humagilina, extrato de tubarão, inibidor de COX-2, e análogos), α-bloqueadores (p. ex., cloridrato de tamsulosina, e análogos), ácidos bisfosfônicos (p. ex., pamidronato, zoledronato, e análogos), talidomida, 5-azacitidina, decitabina, inibidor de proteasoma (p. ex., bortezomib, e análogos), anticorpo antitumor, como anticorpo anti-CD20 e análogos, anticorpo marcado com toxina e análogos.
[00266] Combinando-se o composto da presente invenção e uma droga concomitante, é possível obter um efeito superior, comoa dose pode ser reduzida em comparação com a administração simples do composto da presente invenção ou uma droga concomitante,a droga a ser combinada com o composto da presente invenção pode ser selecionada de acordo com a condição de pacientes (caso brando, caso grave e análogos),o período de tratamento pode ser ajustado mais prolongado,é possível projetar um efeito de tratamento sustentado,é possível proporcionar um efeito sinérgico por meio do uso combinado do composto da presente invenção e uma droga concomitante, e análogos.
[00267] Na presente descrição, o composto da presente invenção e uma droga concomitante usados em combinação são referidos como o “agente de combinação da presente invenção”.
[00268] Para uso do agente de combinação da presente invenção, o tempo de administração do composto da presente invenção e da droga concomitante não é restrito, e o composto da presente invenção e a droga concomitante podem ser administrados a um sujeito de administração simultaneamente, ou podem ser administrados em momentos diferentes. A dosagem da droga concomitante pode ser determinada de acordo com a dose determinada clinicamente, e pode ser selecionada vantajosamente dependendo do sujeito da administração, via de administração, doença, combinação e análogos.
[00269] Exemplos do modo de administração do uso combinado do composto da presente invenção e da droga concomitante incluem os seguintes métodos: (1) O composto da presente invenção e a droga concomitante são produzidos simultaneamente dando uma preparação simples, que é então administrada. (2) O composto da presente invenção e a droga concomitante são produzidos separadamente dando dois tipos de preparações que são administradas simultaneamente pela mesma via de administração. (3) O composto da presente invenção e a droga concomitante são produzidos separadamente dando dois tipos de preparações que são administradas pela mesma via de administração em diferentes momentos. (4) O composto da presente invenção e a droga concomitante são produzidos separadamente dando dois tipos de preparações que são administradas simultaneamente por diferentes vias de administração. (5) O composto da presente invenção e a droga concomitante são produzidos separadamente dando dois tipos de preparações que são administradas por vias de administração diferentes em momentos diferentes (p. ex., o composto da presente invenção e a droga concomitante são administrados nesta ordem, ou na ordem invertida). A dose da droga concomitante é determinada vantajosamente de acordo com sua dose clínica, e a relação do composto da presente invenção e a droga concomitante é determinada vantajosamente dependendo do sujeito da administração, via de administração, doença-alvo, sintoma, combinação, e análogos. Por exemplo, quando o sujeito da administração é humano, a droga concomitante é usada em de 0,01 a 100 (partes em peso), relativamente a 1 parte em peso do composto da presente invenção.
[00270] O agente de combinação da presente invenção apresenta baixa toxicidade e, por exemplo, o composto da presente invenção e/ou a droga concomitante indicada acima podem ser misturados, de acordo com um método conhecido per se, com um veículo farmacologicamente aceitável dando composições farmacêuticas, como tabletes (incluindo tablete revestido com açúcar, tablete revestido com película), pós, grânulos, cápsulas (incluindo cápsula mole), soluções, injeções, supositórios, agentes de liberação prolongada e análogos, que podem ser administrados com segurança oralmente ou parenteralmente (p. ex., local, retal, venosa, e análogos). Uma injeção pode ser administrada por via intravenosa, intramuscular, subcutânea ou intra-órgão, ou diretamente na lesão.
[00271] Como um veículo farmacologicamente aceitável que pode ser usado para a preparação do agente de combinação da presente invenção, pode-se indicar aqueles similares aos veículos farmacologicamente aceitáveis indicados acima, que podem ser usados para a produção do agente farmacêutico da presente invenção. Onde necessário, também é possível usar os aditivos previamente indicados para a produção do agente farmacêutico da presente invenção, como conservantes, antioxidantes, colorantes, agente adoçantes, adsorventes, agentes umectantes e análogos em quantidades apropriadas.
[00272] A relação de composição do composto da presente invenção para a droga concomitante no agente de combinação da presente invenção pode ser ajustada vantajosamente dependendo do sujeito da administração, via de administração, doenças e análogos.
[00273] Por exemplo, o teor do composto da presente invenção no agente de combinação da presente invenção varia dependendo da forma de dosagem, e é usualmente de cerca de 0,01 a 100 % em peso, de preferência, de cerca de 0,1 a 50 % em peso, ainda mais preferivelmente de cerca de 0,5 a 20 % em peso, com base na preparação como um todo.
[00274] O teor da droga concomitante no agente de combinação da presente invenção varia dependendo da forma de dosagem, e é usualmente de cerca de 0,01 a 90 % em peso, de preferência, de cerca de 0,1 a 50 % em peso, ainda mais preferivelmente de cerca de 0,5 a 20 % em peso, com base na preparação como um todo.
[00275] O teor de aditivos no agente de combinação da presente invenção varia dependendo da forma de dosagem, e é usualmente de cerca de 1 a 99,99 % em peso, de preferência, de cerca de 10 a 90 % em peso, com base na preparação como um todo.
[00276] Quando o composto da presente invenção e a droga concomitante são preparados separadamente, é possível usar todo o conteúdo.
[00277] Estas preparações podem ser produzidas por meio de um método conhecido per se, que é geralmente usado no processo de preparação.
[00278] Por exemplo, o composto da presente invenção e a droga concomitante podem ser preparados em uma injeção aquosa juntamente com um agente dispersante (p. ex., Tween 80 (fabricado pela Atlas Powder, US), HCO 60 (fabricado pela Nikko Chemicals), polietileno glicol, carboximetilcelulose, alginato de sódio, hidroxipropilmetilcelulose, dextrina e análogos), um estabilizante (p. ex., ácido ascórbico, pirossulfito de sódio, e análogos), um tensoativo (p. ex., Polissorbato 80, macrogol e análogos), um solubilizador (p. ex., glicerina, etanol e análogos), um tamponador (p. ex., ácido fosfórico e sal de metal alcalino do mesmo, ácido cítrico e sal de metal alcalino do mesmo, e análogos), um agente isotonizador (p. ex., cloreto de sódio, cloreto de potássio, manitol, sorbitol, glicose e análogos), um ajustador de pH (p. ex., ácido clorídrico, hidróxido de sódio e análogos), um conservante (p. ex., paraoxibenzoato de etila, ácido benzóico, metilparabeno, propilparabeno, álcool de benzila e análogos), um agente de dissolução (p. ex., glicerina conc., meglumina e análogos), um agente solubilizador (p. ex., propileno glicol, sacarose e análogos), um agente acalmador (p. ex., glicose, álcool de benzila e análogos), e análogos, ou podem ser dissolvidos, suspensos ou emulsificados em um óleo vegetal, como óleo de oliva, óleo de gergelim, óleo de semente de algodão, óleo de milho e análogos ou um agente solubilizador, como propileno glicol e análogos e preparados em uma injeção oleosa, com o que se proporciona a injeção.
[00279] Adicionalmente, um excipiente (p. ex., lactose, sacarose, amido e análogos), um agente desintegrador (p. ex., amido, carbonato de cálcio e análogos), um ligante (p. ex., amido, goma arábica, carboximetilcelulose, polivinilpirrolidona, hidroxipropilcelulose e análogos), um lubrificante (p. ex., talco, estearato de magnésio, polietileno glicol 6000 e análogos) e análogos podem ser adicionados ao composto da presente invenção ou à droga concomitante, e a mistura pode ser moldada por compressão, de acordo com um método conhecido per se, então, se desejável, o produto moldado pode ser revestido por meio de um método conhecido per se com o fim de mascarar o sabor, propriedade entérica ou durabilidade, dando uma preparação para administração oral. Como o agente de revestimento é possível usar, por exemplo, hidroxipropilmetilcelulose, etilcelulose, hidroximetilcelulose, hidroxipropilcelulose, polioxietileno glicol, Tween 80, Pluronic F68, ftalato de acetato de celulose, ftalato de hidroxipropilmetilcelulose, succinato de acetato de hidroximetilcelulose, Eudoragit (copolímero de ácido metacílico-ácido acílico, fabricado pela Rohm, DE), pigmento (p. ex., vermelho de óxido de ferro, dióxido de titânio, etc.) e análogos. A preparação para administração oral pode ser qualquer uma dentre uma preparação de liberação imediata e uma preparação de liberação prolongada.
[00280] Além disso, o composto da presente invenção e a droga concomitante podem ser preparados formando um supositório sólido, semissólido ou líquido oleoso ou aquoso de acordo com um método conhecido per se, por meio de mistura dos mesmo com um substrato oleoso, substrato aquoso ou substrato de gel aquoso. Como o substrato oleoso indicado acima indica-se, por exemplo, glicerídeos de ácido graxo superior [p. ex., manteiga de cacau, Witepsols (fabricado pela Dynamit Nobel, Alemanha), etc.], glicerídeos de ácido graxo de cadeia média [p. ex., Miglyols (fabricado pela Dynamit Nobel, Alemanha), etc.], ou óleos vegetais (p. ex., óleo de gergelim, óleo de soja, óleo de semente de algodão e análogos), e análogos. Adicionalmente, como o substrato aquoso indica-se, por exemplo, polietileno glicol, propileno glicol e análogos, e, como o substrato de gel aquoso, por exemplo, gomas naturais, derivados de celulose, polímeros de vinila, polímeros de ácido acrílico e análogos.
[00281] Como a preparação de liberação prolongada indicada acima, indica-se microcápsulas de liberação prolongada e análogos. A microcápsula de liberação prolongada pode ser produzida por meio de um método conhecido per se, por exemplo, um método mostrado no tópico [2] a seguir.
[00282] De preferência, o composto da presente invenção é moldado em uma preparação para administração oral, como uma preparação sólida (p. ex., pó, grânulo, tablete, cápsula) e análogos, ou moldado em uma preparação para administração retal, como um supositório e análogos. Particularmente, uma preparação para administração oral é preferível.
[00283] A droga concomitante pode ser preparada na droga indicada acima dependendo do tipo da droga.
[00284] [1] Uma injeção do composto da presente invenção ou dadroga concomitante, e preparação dos mesmos, [2] uma preparação de liberação prolongada ou preparação de liberação imediata do composto da presente invenção ou da droga concomitante, e preparação dos mesmos, [3] um agente de desintegração rápida sublingual, bucal ou intraoral do composto da presente invenção ou da droga concomitante, e preparação dos mesmos, serão descritos especificamente abaixo.
[00285] Uma injeção preparada por meio de dissolução do composto da presente invenção ou da droga concomitante em água é preferível. Esta injeção pode ser deixada conter um benzoato e/ou salicilato.
[00286] A injeção é obtida dissolvendo-se o composto da presente invenção ou a droga concomitante, e se desejável, um benzoato e/ou salicilato, em água.
[00287] Como os sais de ácido benzóico e ácido salicílico indicados acima lista-se, por exemplo, sais de metais alcalinos, como sódio, potássio e análogos, sais de metais alcalino-terrosos, como cálcio, magnésio e análogos, sais de amônio, sais de meglumina, sais com bases orgânicas, como trometamol e análogos, etc..
[00288] A concentração do composto da presente invenção ou a droga concomitante em uma injeção é de 0,5 a 50 % em peso/volume, de preferência, de cerca de 3 a 20 % em peso/volume. A concentração de um benzoato ou/e salicilato é de 0,5 a 50 % em peso/volume, de preferência, de cerca de 3 a 20 % em peso/volume.
[00289] A injeção da presente invenção contém vantajosamente aditivos usualmente empregados em uma injeção, por exemplo, um estabilizante (p. ex., ácido ascórbico, pirossulfito de sódio e análogos), um tensoativo (p. ex., Polissorbato 80, macrogol e análogos), um solubilizador (p. ex., glicerina, etanol e análogos), um tamponador (p. ex., ácido fosfórico e sal de metal alcalino do mesmo, ácido cítrico e sal de metal alcalino do mesmo, e análogos), um agente isotonizador (p. ex., cloreto de sódio, cloreto de potássio e análogos), um agente dispersante (p. ex., hidroxipropilmetilcelulose, dextrina), um regulador de pH (p. ex., ácido clorídrico, hidróxido de sódio e análogos), um conservante (p. ex., paraidroxibenzoato de etila, ácido benzóico e análogos), um agente de dissolução (p. ex., glicerina conc., meglumina e análogos), um agente solubilizador (p. ex., propileno glicol, sacarose e análogos), um agente calmante (p. ex., glicose, álcool de benzila e análogos), e análogos. Estes aditivos são geralmente combinados numa proporção usualmente empregada em uma injeção.
[00290] É vantajoso que o pH de uma injeção seja controlado de pH de 2 a 12, de preferência, de pH 2,5 a 8,0, por meio de adição de um regulador de pH.
[00291] Uma injeção é obtida dissolvendo-se o composto da presente invenção ou a droga concomitante e, se desejável, um benzoato e/ou um salicilato, e, se necessário, os aditivos indicados acima em água. Estes podem ser dissolvidos em quaisquer ordem, e podem ser dissolvidos vantajosamente da mesma maneira que em um método convencional de produzir uma injeção.
[00292] Vantajosamente, uma solução aquosa para injeção pode ser aquecida, alternativamente é possível realizar, por exemplo, esterilização com filtração, esterilização com calor a alta pressão e análogos da mesma maneira que para uma injeção usual, para proporcionar uma injeção.
[00293] Pode ser vantajoso que uma solução aquosa para injeção seja submetida a esterilização com calor a alta pressão a de 100 a 121°C durante de 5 a 30 min.
[00294] Adicionalmente, uma preparação dotada com uma propriedade antibacteriana de uma solução também pode ser produzida de forma que possa ser usada como uma preparação que é dividida e administrada múltiplas vezes.Preparação de liberação prolongada ou preparação de liberação imediata, e preparação das mesmas
[00295] Uma preparação de liberação prolongada é, de preferência, aquela que é obtida, se desejável, por meio de revestimento de um núcleo contendo o composto da presente invenção ou a droga concomitante com um agente de película, como uma substância insolúvel em água, polímero intumescível e análogos. Por exemplo, uma preparação de liberação prolongada para administração oral de uma administração por dia é preferível.
[00296] Como a substância insolúvel em água usada em um agente de película lista-se, por exemplo, éteres de celulose, como etilcelulose, butilcelulose e análogos, ésteres de celulose, como acetato e celulose, propionato de celulose e análogos, ésteres de polivinila, como acetato de polivinila, butirato de polivinila e análogos, copolímeros de ácido acrílico/ácido metacrílico, copolímeros de metil metacrilato, copolímeros de etoxietil metacrilato/cinamoetil metacrilato/aminaalquil metacrilato, ácido policacrílico, ácido polimetacrílico, copolímeros de ácido metacrílico alquilamida, poli(metil metacrilato), polimetacrilato, polimetacrilamida, copolímeros de aminaalquil metacrilato, poli(anidrido metacrílico), copolímero de glicidil metacrilato, particularmente, polímeros à base de ácido acrílico, como Eudoragit (fabricado pela Rohm Pharma), como Eudoragit RS100, RL-100, RS-30D, RL-30D, RL-PO, RS-PO (copolímero de etil acrilato/metil metacrilato/trimetilcloreto metacrilato/etil amônio), Eudoragit NE-30D (copolímero de metil metacrilato/etil acrilato), e análogos, óleos hidrogenados, como óleo de mamona hidrogenado (p. ex., cera Lubri (fabricado pela Freund Corporation) e análogos), ceras, como cera de carnaúba, éster de glicerina de ácido graxo, parafina e análogos, ésteres de ácido graxo poliglicerina, e análogos.
[00297] Como o polímero intumescível, são preferíveis polímeros apresentando um grupo de dissociação ácida e apresentando intumescimento dependente do pH, e são preferíveis polímeros apresentando um grupo de dissociação ácida, que manifesta pequeno intumescimento em regiões ácidas, como no estômago, e intumescimento grande em regiões neutras, como no intestino delgado e no intestino grosso.
[00298] Como referido polímero apresentando um grupo de dissociação ácida e apresentando intumescimento dependente do pH, lista-se polímeros de ácido poliacrílico reticuláveis, como por exemplo, Carbomer 934P, 940, 941, 974P, 980, 1342 e análogos, policarbofil, policarbofil cálcio (todos estes fabricados pela BF Goodrich), Hiviswako 103, 104, 105, 304 (todos fabricados pela Wako Pure Chemical Industries, Ltd.), e análogos.
[00299] O agente de película usado em uma preparação de liberação prolongada pode conter adicionalmente uma substância hidrofílica.
[00300] Como a substância hidrofílica é possível indicar, por exemplo, polissacarídeos que podem conter um grupo sulfato, como pululano, dextrina, alginato de metal alcalino e análogos, polissacarídeos apresentando um hidroxialquila ou carboxialquila, como hidroxipropilcelulose, hidroxipropilmetilcelulose, carboximetilcelulose sódio e análogos, metilcelulose, polivinilpirrolidona, álcool de polivinila, polietileno glicol e análogos.
[00301] O teor de uma substância insolúvel em água no agente de película de uma preparação de liberação prolongada é de cerca de 30 a cerca de 90 % (peso/peso), de preferência, de cerca de 35 a cerca de 80 % (peso/peso), ainda mais preferivelmente de cerca de 40 a cerca de 75 % (peso/peso), o teor de um polímero intumescível é de cerca de 3 a cerca de 30 % (peso/peso), de preferência, de cerca de 3 a cerca de 15 % (peso/peso). O agente de película pode conter adicionalmente uma substância hidrofílica, e sendo que neste caso o teor de uma substância hidrofílica no agente de película é de cerca de 50 % (peso/peso) ou menos, de preferência, de cerca de 5 a cerca de 40 % (peso/peso), ainda mais preferivelmente de cerca de 5 a cerca de 35 % (peso/peso). Este % (peso/peso) indica o % em peso baseado em uma composição de agente de película que é obtida removendo-se um solvente (p. ex., água, alcoóis inferiores, como metanol, etanol e análogos) de uma solução de agente de película.
[00302] A preparação de liberação prolongada é produzida preparando- se um núcleo contendo uma droga como exemplificado abaixo, depois, revestindo-se o núcleo resultante com uma solução de agente de película preparada dissolvendo-se com calor uma substância insolúvel em água, polímero intumescível e análogos ou dissolvendo-se ou dispersando-se o mesmo em um solvente.
[00303] I. Preparação de núcleo contendo droga
[00304] A forma de núcleo contendo uma droga a ser revestida com um agente de película (a seguir, referidos por vezes como um núcleo) não é particularmente restrita, e, de preferência, o núcleo é formado em partículas, como um grânulo ou partícula fina.
[00305] Quando o núcleo é constituído de grânulos ou partículas finas, o tamanho médio das partículas é, de preferência, de cerca de 150 a cerca de 2000 μm, ainda mais preferivelmente, de cerca de 500 a cerca de 1400 μm.
[00306] Preparação do núcleo pode ser realizada por meio de um método de produção usual. Por exemplo, um excipiente vantajoso, agente de ligação, agente desintegrador, lubrificante, estabilizante e análogos são misturados com uma droga, e a mistura é submetida a um método de granulação com extrusão úmida, método de granulação de leito fluidizado ou análogo, para preparar um núcleo.
[00307] O teor de drogas em um núcleo é de cerca de 0,5 a cerca de 95 % (peso/peso), de preferência, de cerca de 5,0 a cerca de 80 % (peso/peso), ainda mais preferivelmente de cerca de 30 a cerca de 70 % (peso/peso).
[00308] Como o excipiente contido no núcleo usa-se, por exemplo, sacarídeos, como sacarose, lactose, manitol, glicose e análogos, amido, celulose cristalina, fosfato de cálcio, amido de milho e análogos. Entre estes, são preferíveis a celulose cristalina, amido de milho.
[00309] Como o agente de ligação usa-se, por exemplo, álcool de polivinila, hidroxipropilcelulose, polietileno glicol, polivinil pirrolidona, Pluronic F68, goma arábica, gelatina, amido e análogos. Como o agente desintegrante usa-se, por exemplo, carboximetilcelulose cálcio (ECG505), croscarmelose sódio (Ac-Di-Sol), polivinilpirrolidona reticulada (Crospovidona), hidroxipropilcelulose pouco substituída (L-HPC) e análogos. Entre estes são preferíveis a hidroxipropilcelulose, polivinilpirrolidona, hidroxipropilcelulose pouco substituída. Como o lubrificante e inibidor de coagulação usa-se, por exemplo, talco, estearato de magnésio e sais inorgânicos dos mesmos, e como o lubrificante usa-se polietileno glicol e análogos. Como o estabilizante usa-se ácidos, como ácido tartárico, ácido cítrico, ácido succínico, ácido fumárico, ácido maleico e análogos.
[00310] Um núcleo também pode ser preparado, adicionalmente ao método de produção indicado acima, por exemplo, por meio de um método de granulação com rolamento em que uma droga ou uma mistura de uma droga com um excipiente, lubrificante e análogos é adicionada em frações sobre uma partícula-veículo inerte que é o coração do núcleo, enquanto se pulveriza um ligante dissolvido em um solvente vantajoso, como água, álcool inferior (p. ex., metanol, etanol e análogos) e análogos, um método de revestimento com vasilha, um método de revestimento com leito fluidizado ou um método de granulação com fusão. Como a partícula-veículo inerte é possível usar, por exemplo, aquelas constituídas de sacarose, lactose, amido, celulose cristalina ou ceras, e o seu tamanho médio das partículas é, de preferência, de cerca de 100 μm a cerca de 1500 μm.
[00311] Para a separação de uma droga contida em um núcleo e um agente de película, a superfície do núcleo pode ser revestida com um agente protetor. Como o agente protetor usa-se, por exemplo, as substâncias hidrofílicas indicadas acima, substâncias insolúveis em água e análogos. Como o agente protetor usa-se, de preferência, polietileno glicol, e polissacarídeos apresentando um hidroxialquila ou carboxialquila, mais preferivelmente, usa-se hidroxipropilmetilcelulose e hidroxipropilcelulose. O agente protetor pode conter, como estabilizante, ácidos, como ácido tartárico, ácido cítrico, ácido succínico, ácido fumárico, ácido maleico e análogos, e lubrificantes, como talco e análogos. Quando se usa o agente protetor, a quantidade de revestimento é de cerca de 1 a cerca de 15 % (peso/peso), de preferência, de cerca de 1 a cerca de 10 % (peso/peso), ainda mais preferivelmente de cerca de 2 a cerca de 8 % (peso/peso), baseado no núcleo.
[00312] O agente protetor pode ser revestido com um método de revestimento usual e, especificamente, o agente protetor pode ser revestido por meio de revestimento com pulverização do núcleo, por exemplo, por meio de um método de revestimento com leito fluidizado, método de revestimento com vasilha e análogos.
[00313] Um núcleo obtido na etapa I indicada acima é revestido com uma solução de agente de película obtida por meio de dissolução com calor da substância insolúvel em água indicada acima e polímero intumescível dependente do pH, e uma substância hidrofílica, ou por meio de dissolução ou dispersão dos mesmos em um solvente, para dar uma preparação de liberação prolongada.
[00314] Como o método para revestir um núcleo com uma solução de agente de película lista-se, por exemplo, um método com pulverização com spray e análogos.
[00315] A razão na composição de uma substância insolúvel em água, polímero intumescível ou substância hidrofílica em uma solução de agente de película, é selecionada vantajosamente de tal forma que o conteúdo destes componentes em uma película revestida seja dos teores indicados acima, respectivamente.
[00316] A quantidade de revestimento de um agente de película é de cerca de 1 a cerca de 90 % (peso/peso), de preferência, de cerca de 5 a cerca de 50 % (peso/peso), ainda mais preferivelmente de cerca de 5 a cerca de 35 % (peso/peso), baseado em um núcleo (não incluindo a quantidade de revestimento de agente protetor).
[00317] Como o solvente em uma solução de agente de película é possível usar água ou um solvente orgânico sozinho ou em mistura dos mesmos. No caso do uso em mistura, a relação de mistura de água para um solvente orgânico (água/solvente orgânico: em peso) pode ser variada na faixa de 1 a 100 %, e, de preferência, de 1 a cerca de 30 %. O solvente orgânico não é particularmente restrito desde que dissolva uma substância insolúvel em água, e usa-se, por exemplo, alcoóis inferiores, como álcool de metila, álcool de etila, álcool de isopropila, álcool de n-butila e análogos, alcanona inferior, como acetona e análogos, acetonitrila, clorofórmio, cloreto de metileno e análogos. Entre estes, alcoóis inferiores são preferíveis, e álcool de etila e álcool de isopropila são particularmente preferíveis. Água, e uma mistura de água com um solvente orgânico são usados, de preferência, como um solvente para um agente de película. Neste caso, também é possível adicionar, se necessário, um ácido, como ácido tartárico, ácido cítrico, ácido succínico, ácido fumárico, ácido maleico e análogos, em uma solução de agente de película para estabilizar a solução de agente de película.
[00318] Uma operação de revestimento por revestimento com pulverização pode ser realizada por meio de um método de revestimento usual, e, especificamente, ela pode ser realizada aplicando-se um revestimento de uma solução de agente de película sobre um núcleo por meio de um método de revestimento de leito fluidizado, método de revestimento com vasilha e análogos. Neste caso, se necessário, também é possível adicionar talco, óxido de titânio, estearato de magnésio, estearato de cálcio, ácido salicílico anidro leve e análogos como um lubrificante, e também é possível adicionar éster de ácido graxo de glicerina, óleo de mamona hidrogenado, citrato de trietila, álcool de cetila, álcool de estearila e análogos como um plastificante.
[00319] Após revestimento com um agente de película é possível misturar, se necessário, um agente antiestática, como talco e análogos.
[00320] A preparação de liberação imediata pode ser líquida (solução, suspensão, emulsão e análogos) ou sólida (partícula, pílula, tablete e análogos). Como a preparação de liberação imediata usa-se agentes para administração oral e agentes para administração parenteral, como uma injeção e análogos, e agentes para administração oral são preferíveis.
[00321] A preparação de liberação imediata pode conter usualmente, adicionalmente a uma droga de componente ativo, também veículos, aditivos e excipientes convencionalmente usados no campo farmacêutico (a seguir, abreviado por vezes como excipiente). O excipiente usado não é particularmente restrito desde que seja um excipiente usado ordinariamente como um excipiente de preparação. Por exemplo, como o excipiente para uma preparação sólida oral, lista-se preparação sólida oral, lactose, amido, amido de milho, celulose cristalina (Avicel PH101, fabricado pela Asahi Kasei Corporation, e análogos), açúcar em pó, açúcar granulado, manitol, ácido silícico anidro leve, carbonato de magnésio, carbonato de cálcio, L-cisteína e análogos, e, de preferência, amido de milho e manitol e análogos. Estes excipientes podem ser usados sozinhos ou em combinação de dois ou mais. O teor do excipiente é, por exemplo, de cerca de 4,5 a cerca de 99,4 % em peso/peso, de preferência, de cerca de 20 a cerca de 98,5 % em peso/peso, ainda mais preferivelmente de cerca de 30 a cerca de 97 % em peso/peso, baseado na quantidade total da preparação de liberação imediata.
[00322] O teor de uma droga na preparação de liberação imediata pode ser selecionado vantajosamente na faixa de cerca de 0,5 a cerca de 95 % em peso/peso, de preferência, de cerca de 1 a cerca de 60 % em peso/peso baseado na quantidade total da quantidade de liberação imediata.
[00323] Quando a preparação de liberação imediata é uma preparação sólida oral, ela contém usualmente, adicionalmente aos componentes indicados acima, também um agente desintegrante. Como este agente desintegrante usa-se, por exemplo, carboximetilcelulose cálcio (ECG-505, fabricado pela Gotoku Yakuhin), croscarmelose sódio (p. ex., Actisol, fabricado pela Asahi Kasei Corporation), crospovidona (p. ex., Kollidon CL, fabricado pela BASF), hidroxipropilcelulose pouco substituída (fabricado pela Shin-Etsu Chemical Co., Ltd.), carboximetilamido (fabricado pela Matsutani Kagaku K.K.), carboximetilamido sódio (Exprotab, fabricado pela Kimura Sangyo), amido parcialmente pré-gelatinizado (PCS, fabricado pela Asahi Kasei Corporation), e análogos, e, por exemplo, aqueles que desintegram um grânulo por meio de absorção de água em contato com água, causando intumescimento, ou ocasionando um canal entre um ingrediente efetivo e um excipiente que constitui o núcleo. Estes agentes desintegrantes podem ser usados sozinhos ou em combinação de dois ou mais. A quantidade do agente destintegrante usado é selecionada vantajosamente dependendo do tipo e da quantidade de mistura de uma droga usada, projeto da propriedade de liberação, e análogos, e por exemplo, de cerca de 0,05 a cerca de 30 % em peso/peso, de preferência, de cerca de 0,5 a cerca de 15 % em peso/peso, baseado na quantidade total da preparação de liberação imediata.
[00324] Quando a preparação de liberação imediata é uma preparação sólida oral, ela pode conter adicionalmente, além da composição indicada acima, se desejado, aditivos convencionai9s em preparações sólidas. Como um aditivo do tipo referido usa-se, por exemplo, um ligante (p. ex., sacarose, gelatina, pó de goma arábica, metilcelulose, hidroxipropilcelulose, hidroxipropilmetilcelulose, carboximetilcelulose, polivinilpirrolidona, pululano, dextrina e análogos), um lubrificante (p. ex., polietileno glicol, estearato de magnésio, talco, ácido silícico anidro leve (p. ex., Aerosil (fabricado pela Nippon Aerosil))), um tensoativo (p. ex., tensoativos aniônicos, como alquilsulfato de sódio e análogos, tensoativos não-iônicos, como éster de ácido graxo de polioxietileno e éster de ácido graxo polioxietileno sorbitol, derivados de óleo de mamona de polioxietileno e análogos), um corante (p. ex., matéria corante de alcatrão, vermelho óxido de ferro, óxido de titânio, riboflavinas), se necessário, um agente estimulador do apetite (p. ex., agente adoçante, agente aromatizante e análogos), um adsorvente, conservante, agente umectante, agentes antiestática, e análogos. Adicionalmente também é possível adicionar como o estabilizante, um ácido orgânico, como ácido tartárico, ácido cítrico, ácido succínico, ácido fumárico e análogos.
[00325] Como o ligante indicado acima usa-se, de preferência, hidroxipropilcelulose, polietileno glicol e polivinilpirrolidona e análogos.
[00326] A preparação de liberação imediata pode ser preparada com base numa tecnologia usual de produzir preparações, por meio de mistura dos componentes indicados acima, e, se necessário, amassando-se adicionalmente a mistura, e moldando a mesma. A mistura indicada acima é realizada por meio de métodos usados geralmente, por exemplo, mistura, amassamento e análogos. Especificamente, quando uma preparação de liberação imediata é formada, por exemplo, em uma partícula, ela pode preparada de acordo com o mesmo meio que no método indicado acima para a preparação de um núcleo de uma preparação de liberação prolongada, por meio de mistura dos componentes usando um granulador vertical, amassador universal (fabricado pela Hata Tekkosho), granulador de leito fluidizado FD-5S (fabricado pela Powrex Corporation), e análogos, e então, granulando-se a mistura por meio de um método de granulação com extrusão, método de granulação com leito fluidizado e análogos.
[00327] A preparação de liberação imediata e preparação de liberação prolongada assim obtidas podem ser preparadas, elas próprias, em produtos ou preparadas em produtos vantajosamente em conjunto com excipientes de preparação e análogos, separadamente, por meio de um método ordinário, depois, podem ser administradas simultaneamente ou podem ser administradas em combinação em qualquer intervalo de administração, ou elas podem ser preparadas, elas próprias, em uma preparação para administração oral (p. ex., grânulo, grânulo fino, tablete, cápsula e análogos) ou preparadas em uma preparação para administração oral vantajosamente em conjunto com excipientes de preparação e análogos. Também pode ser permissível que elas sejam preparadas em grânulos ou partículas finas, e envasadas na mesma cápsula a ser usada como uma preparação para administração oral.Agente de desintegração rápida sublingual, bucal ou intraoral, e preparação do mesmo
[00328] Agentes de desintegração rápida sublingual, bucal ou intraoral podem ser uma preparação sólida, como tablete e análogos, ou podem ser um adesivo (película) de membrana para a mucosa oral.
[00329] Como o agente de desintegração rápida sublingual, bucal ou intraoral é preferível uma preparação contendo o composto da presente invenção ou a droga concomitante e um excipiente. Ele também pode conter agentes auxiliares, como um lubrificante, agente isotonizador, veículo hidrofílico, polímero dietil éter do ácido, estabilizante e análogos. Adicionalmente, para fácil absorção e maior eficiência de uso in vivo, também pode estar contida β-ciclodextrina ou derivados de β-ciclodextrina (p. ex., hidroxipropil-β-ciclodextrina e análogos) e análogos.
[00330] Como o excipiente indicado acima lista-se lactose, sacarose, D-manitol, amido, celulose cristalina, ácido silícico anidro leve e análogos. Como o lubrificante lista-se estearato de magnésio, estearato de cálcio, talco, sílica coloidal e análogos, e, particularmente, estearato de magnésio e sílica coloidal são preferíveis. Como o agente isotonizador lista-se cloreto de sódio, glicose, frutose, manitol, sorbitol, lactose, sacarose, glicerina, uréia e análogos, e particularmente, manitol é preferível. Como o veículo hidrofílico lista-se veículos hidrofílicos intumescíveis, como celulose cristalina, etilcelulose, polivinilpirrolidona reticulável, ácido silícico anidro leve, ácido silícico, fosfato de dicálcio, carbonato de cálcio e análogos, e particularmente, celulose cristalina (p. ex., celulose microcristalina e análogos) é preferível. Como o polímero dispersável em água lista-se gomas (p. ex., goma tragacanto, goma acácia, goma cyamopsis), alginatos (p. ex., alginato de sódio), derivados de celulose (p. ex., metilcelulose, carboximetilcelulose, hidroximetilcelulose, hidroxipropilcelulose, hidroxipropilmetilcelulose), gelatina, amido solúvel em água, ácidos poliacrílicos (p. ex., Carbomer), ácido polimetacílico, álcool de polivinila, polietileno glicol, polivinilpirrolidona, policarbofil, ácido ascórbico, palmitatos e análogos, e hidroxipropilmetilcelulose, ácido poliacrílico, alginato, gelatina, carboximetilcelulose, polivinilpirrolidona, polietileno glicol e análogos são preferíveis. Particularmente, hidroxipropilmetilcelulose é preferível. Como o estabilizante lista-se cisteína, tiossorbitol, ácido tartárico, ácido cítrico, carbonato de sódio, ácido ascórbico, glicina, sulfito de sódio e análogos, e particularmente, ácido cítrico e ácido ascórbico são preferíveis.
[00331] O agente de desintegração rápida sublingual, bucal ou intraoral pode ser produzido misturando-se o composto da presente invenção ou a droga concomitante e um excipiente por meio de um método conhecido per se. Adicionalmente, se desejado, os agentes auxiliares indicados acima, como um lubrificante, agente isotonizador, veículo hidrofílico, polímero dispersável em água, estabilizante, corante, agente adoçante, conservante e análogos podem ser misturados. O agente de desintegração rápida sublingual, bucal ou intraoral é obtido por meio de mistura dos componentes indicados acima simultaneamente ou com intervalo de tempo, depois, submetendo-se a mistura a moldagem de formação de tabletes com pressão. Para obter dureza vantajosa, também pode ser permissível que os materiais sejam umedecidos com o uso de um solvente, como água, álcool e análogos, se desejado antes e após o processo de formação de tablete, e após a moldagem, os materiais são secados para ser obter um produto.
[00332] No caso da moldagem em um adesivo (película) de membrana da mucosa, o composto da presente invenção ou a droga concomitante e o polímero dispersável em água indicado acima (de preferência, hidroxipropilcelulose, hidroxipropilmetilcelulose), excipiente e análogos são dissolvidos em um solvente, como água e análogos, e a solução resultante é vertida dando uma película. Adicionalmente, também é possível adicionar aditivos, como um plastificante, estabilizante, antioxidante, conservante, corante, tamponador, agente adoçante e análogos. Para conferir elasticidade vantajosa à película, podem estar contidos glicóis, como polietileno glicol, propileno glicol e análogos, ou, para incrementar a adesão da película sobre um revestimento de membrana da mucosa intraoral, também pode estar contido um polímero bio-adesivo (p. ex., policarbofil, carbopol). Na moldagem, a solução é despejada sobre a superfície não-adesiva, espalhada com espessura uniforme (de preferência, de cerca de 10 a 1000 mícrons) com uma ferramenta de aplicação, como um bisturi e análogos, depois a solução é secada para formar uma película. Pode ser vantajoso que a película assim formada seja secada à temperatura ambiente ou com calor, e cortada em uma área desejada.
[00333] Como o agente de desintegração rápida intraoral preferível, lista-se agentes sólidos de dose de espalhamento rápido constituídos de um corpo reticulado compreendendo o composto da presente invenção ou a droga concomitante, e um veículo solúvel em água ou difundível em água que é inerte para o composto da presente invenção ou droga concomitante. Este corpo reticulado é obtido sublimando-se um solvente da composição sólida constituído de uma solução preparada dissolvendo-se o composto da presente invenção ou a droga concomitante em um solvente vantajoso.
[00334] É preferível que a composição o um agente de desintegração rápida intraoral contém um agente formador de matriz e um componente secundário, adicionalmente ao composto da presente invenção ou a droga concomitante.
[00335] Exemplos do agente formador de matriz incluem gelatinas, dextrinas, proteínas animais ou proteínas vegetais, como proteína de semente de soja, trigo e psyllium e análogos; substâncias de borracha, como goma arábica, goma guar, agar, xantano e análogos; polissacarídeos; ácidos algínicos; carboximetilceluloses; carrageninas; dextranos; pectinas; polímeros sintéticos, como polivinilpirrolidona e análogos; substâncias derivadas de um complexo de gelatina-goma arábica, e análogos. Adicionalmente estão contidos sacarídeos, como manitol, dextrose, lactose, galactose, trealose e análogos; sacarídeos cíclicos, como ciclodextrina e análogos; sais inorgânicos, como fosfato de sódio, cloreto de sódio e silicato de alumínio e análogos; aminoácidos apresentando de 2 a 12 átomos de carbono, como glicina, L-alanina, ácido L-aspártico, ácido L-glutâmico, L-hidroxiprolina, L- isoleucina, L-leucina, L-fenilalanina e análogos.
[00336] Um ou mais dos agentes formadores de matriz podem ser introduzidos em uma solução ou suspensão antes da solidificação. Um agente formador de matriz do tipo referido pode estar presente adicionalmente a um tensoativo, ou pode estar presente enquanto um tensoativo é excluído. Os agentes formadores de matriz auxiliam a manter o composto da presente invenção ou a droga concomitante na solução ou suspensão em condição difundida, adicionalmente à formação da matriz.
[00337] A composição pode conter componentes secundários, como um conservante, antioxidante, tensoativo, agente espessante, corante, agente controlador de pH, agente aromatizante, agente adoçante, agente mascarador de sabor alimentício e análogos. Como o corante vantajoso lista-se óxidos de ferro vermelho, preto e amarelo, e corantes FD & C, como azul FD & C Blue 2, vermelho FD & C Red 40 e análogos fabricados pela Ellis e Everard. Exemplos do agente aromatizante vantajoso incluem aroma de hortelã, framboesa, alcaçuz, laranja, limão, toranja, caramelo, baunilha, cereja, uva e combinações dos mesmos. Exemplos do agente controlador de pH vantajoso incluem ácido cítrico, ácido tartárico, ácido fosfórico, ácido clorídrico e ácido maleico. Exemplos do agente adoçante vantajoso incluem aspartame, acesulfame K e taumatina e análogos. Exemplos do agente mascarador de sabor de alimentos vantajoso incluem bicarbonato de sódio, resina de troca de íon, compostos de inclusão de ciclodextrina, substâncias adsorventes e apomorfina microencapsulada.
[00338] A preparação contém o composto da presente invenção ou a droga concomitante em uma quantidade usualmente de cerca de 0,1 a cerca de 50 % em peso, de preferência, de cerca de 0,1 a cerca de 30 % em peso, e prefere-se preparações (como o agente sublingual, bucal e análogos indicado acima) que pode dissolver 90 % ou mais do composto da presente invenção ou a droga concomitante (em água) dentro da faixa de tempo de cerca de 1 a cerca de 60 min, de preferência, de cerca de 1 a cerca de 15 min, mais preferivelmente de cerca de 2 a cerca de 5 min, e preparações de desintegração rápida intraoral que são desintegradas dentro da faixa de 1 a 60 s, de preferência, de 1 a 30 s, ainda mais preferivelmente de 1 a 10 s, após ser colocada em uma cavidade oral.
[00339] O teor do excipiente indicado acima na preparação como um todo é de cerca de 10 a cerca de 99 % em peso, de preferência, de cerca de 30 a cerca de 90 % em peso. O teor de β-ciclodextrina ou derivado de β- ciclodextrina na preparação como um todo é de 0 a cerca de 30 % em peso. O teor do lubrificante na preparação como um todo é de cerca de 0,01 a cerca de 10 % em peso, de preferência, de cerca de 1 a cerca de 5 % em peso. O teor do agente isotonizador na preparação como um todo é de cerca de 0,1 a cerca de 90 % em peso, de preferência, de cerca de 10 a cerca de 70 % em peso. O conteúdo do veículo hidrofílico na preparação como um todo é de cerca de 0,1 a cerca de 50 % em peso, de preferência, de cerca de 10 a cerca de 30 % em peso. O teor do polímero dispersável em água na preparação como um todo é de cerca de 0,1 a cerca de 30 % em peso, de preferência, de cerca de 10 a cerca de 25 % em peso. O teor do estabilizante na preparação como um todo é de cerca de 0,1 a cerca de 10 % em peso, de preferência, de cerca de 1 a 5 % em peso. A preparação indicada acima pode conter adicionalmente aditivos, como um corante, agente adoçante, conservante e análogos, se necessário.
[00340] A dosagem de um agente de combinação da presente invenção difere dependendo do tipo de um composto da presente invenção, idade, peso corporal, condição, forma de droga, método de administração, período de administração e análogos, e por exemplo, para um paciente de câncer (adulto, peso corporal: cerca de 60 kg), o agente de combinação é administrado intravenosamente, a uma dose de cerca de 0,01 a cerca de 1000 mg/kg/dia, de preferência, de cerca de 0,01 a cerca de 100 mg/kg/dia, mais preferivelmente de cerca de 0,1 a cerca de 100 mg/kg/dia, particularmente de cerca de 0,1 a cerca de 50 mg/kg/dia, particularmente cerca de 1,5 a cerca de 30 mg/kg/dia, em termos do composto da presente invenção ou da droga concomitante, respectivamente, uma vez ou várias vezes divididas ao longo de um dia. Evidentemente, como a dose conforme descrita varia dependendo de várias condições, quantidades menores que a dosagem indicada acima podem ser suficientes, adicionalmente, pode ser preciso administrar, por vezes, quantidades acima daquela faixa.
[00341] A quantidade da droga concomitante pode ser ajustada em qualquer valor, exceto que efeitos secundários são problemáticos. A dosagem diária em termos da droga concomitante difere dependendo da gravidade do sintoma, idade, sexo, peso corporal, diferença de sensibilidade do sujeito da administração, período de administração, intervalo, e natureza, fármaco, tipo da preparação farmacêutica, tipo do ingrediente efetivo, e não é particularmente restrita, e a quantidade de uma droga é, no caso de administração oral, por exemplo, usualmente de cerca de 0,001 a 2000 mg, de preferência, de cerca de 0,01 a 500 mg, ainda mais preferivelmente de cerca de 0,1 a 100 mg, por 1 kg de peso corporal de um mamífero, que é administrada usualmente uma vez até 4 vezes divididas ao longo do dia.
[00342] Na administração de um agente de combinação da presente invenção, o composto da presente invenção pode ser administrado após a administração da droga concomitante, ou a droga concomitante pode ser administrada após a administração do composto da presente invenção, embora ela possa ser administrada simultaneamente. Quando administrada em um intervalo de tempo, o intervalo difere dependendo do ingrediente efetivo a ser administrado, forma de droga e método de administração, e, por exemplo, quando a droga concomitante é administrada primeiro, exemplifica-se um método em que o composto da presente invenção é administrado dentro de uma faixa de tempo de 1 min a 3 dias, de preferência, de 10 min a 1 dia, mais preferivelmente de 15 min a 1 h após a administração da droga concomitante. Quando o composto da presente invenção é administrado primeira, exemplifica-se um método em que a droga concomitante é administrada dentro de uma faixa de tempo de 1 min a 1 dia, de preferência, de 10 min a 6 h, mais preferivelmente de 15 min a 1 h após a administração do composto da presente invenção.
[00343] Em uma método de administração preferível, por exemplo, a droga concomitante que fora moldada em uma preparação de administração oral é administrada oralmente numa dose diária de cerca de 0,001 a 200 mg/kg, e cerca de 15 min mais tarde, o composto da presente invenção que fora moldado em uma preparação de administração oral é administrado oralmente a uma dose diária de cerca de 0,005 a 100 mg/kg.
[00344] Adicionalmente, o composto da presente invenção ou o agente de combinação da presente invenção pode ser usado concorrentemente com uma terapia não envolvendo droga. Para ser preciso, o composto da presente invenção ou o agente de combinação da presente invenção pode ser combinado com uma terapia não envolvendo droga, como (1) cirurgia, (2) quimioterapia hipertensiva usando angiotensina II etc., (3) terapia gênica, (4) termoterapia, (5) crioterapia, (6) cauterização com laser, (7) radioterapia, e análogos.
[00345] Por exemplo, usando-se o composto da presente invenção ou o agente de combinação da presente invenção antes ou após uma cirurgia e análogos, ou antes ou após um tratamento combinado de dois ou três tipos do mesmo, pode-se proporcionar efeitos, como prevenção da emergência de resistência, prolongamento da sobrevida livre de doença, supressão da metástase do câncer ou da recorrência, prolongamento da vida e análogos.
[00346] Adicionalmente, é possível combinar um tratamento com o composto da presente invenção ou o agente de combinação da presente invenção com uma terapia de suporte [(i) administração de antibiótico (p. ex., tipo β-lactama, como pansporina e análogos, tipo macrólido, como claritromicina e análogos etc.) para a complicação com várias doenças infecciosas, (ii) administração de transfusão com altas calorias, preparação de aminoácidos ou preparação geral de vitaminas para o melhoramento da subnutrição, (iii) administração de morfina para mitigação da dor, (iv) administração de um agente farmacêutico para melhorar efeitos secundários, como náusea, vômitos, anorexia, diarréia, leucopenia, trombocitopenia, concentração diminuída de hemoglobina, perda de cabelo, hepatopatia, renopatia, DIC, febre e análogos e (v) administração de um agente farmacêutico para suprimir resistência a múltiplas drogas de câncer e análogos].
[00347] De preferência, o composto da presente invenção ou o agente de combinação da presente invenção é administrado oralmente (incluindo preparações de liberação prolongada), intravenosamente (incluindo bolus, infusões e clatratos), subcutaneamente e intramuscularmente (incluindo bolus, infusões e preparações de liberação prolongada), transdermicamente, intratumoralmente ou proximalmente ou após a realização do tratamento descrito acima.
[00348] Como um período para administrar o composto da presente invenção ou o agente de combinação da presente invenção antes da cirurgia, etc., por exemplo, ele pode ser administrado de 1 vez a cerca de 30 min até 24 h antes da cirurgia, etc., ou em 1 a 3 ciclos durante cerca de 3 meses a 6 meses antes da cirurgia, etc. Desta maneira, a cirurgia, etc. pode ser realizada facilmente porque, por exemplo, um tecido de câncer poderia ser reduzido por meio da administração do composto da presente invenção ou o agente de combinação da presente invenção antes da cirurgia, e análogos.
[00349] Como um período para administração do composto da presente invenção ou do agente de combinação da presente invenção após a cirurgia, etc., por exemplo, pode-se administrado repetidamente durante algumas poucas semanas até 3 meses, de cerca de 30 min a 24 h após a cirurgia, e análogos. Desta maneira, ele incrementa o efeito da cirurgia, etc. por meio da administração do composto da presente invenção ou do agente de combinação da presente invenção após a cirurgia, e análogos.
[00350] A presente invenção é explicada detalhadamente a seguir com referência aos Exemplos de Referência, Exemplos, Exemplos de Formulação e Exemplos Experimentais, que não devem ser interpretados como limitantes.
[00351] Nos Exemplos de Referência e Exemplos, a pureza dos compostos foi medida nas seguintes condições de HPLC.
[00352] dispositivo de medição: sistema SHIMADZU Corporation LC- 10 Avpcoluna: CAPSEL PAK C18UG120 S-3 μm, 2,0 X 50 mmsolvente: Solução A; água contendo 0,1 % de ácido trifluoroacético,Solução B; ciclo de gradiente de acetonitrila contendo 0,1 % de ácido trifluoroacético: 0,00 min (Solução A/Solução B=90/10), 4,00 min (Solução A/Solução B=5/95), 5,50 min (Solução A/Solução B=5/95), 5,51 min (Solução A/Solução B=90/10), 8,00 min (Solução A/Solução B=90/10) volume de injeção: 2 μl taxa de fluxo: 0.5 ml/min método de detecção: UV 220 nm
[00353] Nos Exemplos de Referência e Exemplos, a purificação dos compostos por meio de HPLC preparativa foi realizada nas seguintes condições.
[00354] 1) dispositivo de medição: sistema de puficicação de altavazão da Gilson Company Inc.,coluna: YMC CombiPrep ODS-A, S-5 μm, 50 X 20 mmmétodo de detecção: UV 220 nmsolvente: Solução A; água contendo 0,1 % de ácido trifluoroacético,Solução B; acetonitrila contendo 0,1 % de ácidotrifluoroacéticociclo do gradiente: exemplo representativo 0,00 min (Solução A/Solução B=98/2), 1,00 min (Solução A/Solução B=98/2), 5,20 min (Solução A/Solução B=0/100), 6,40 min (Solução A/Solução B=0/100), 6,50 min (Solução A/Solução B=98/2), 6,60 min (Solução A/Solução B=98/2), taxa de fluxo: 25 ml/min, ou 0,00 min (Solução A/Solução B= 90/10), 1,00 min (Solução A/Solução B= 90/10), 4,00 min (Solução A/Solução B= 10/95), 8,50 min (Solução A/Solução B= 10/95), 8,60 min (Solução A/Solução B= 90/10), 8,70 min (Solução A/Solução B= 90/10)taxa de fluxo: 20 ml/min2) dispositivo de medição: sistema de purificação de alta vazão da Gilson Company Inc.
[00355] coluna: YMC CombiPrep, ProC18 RS, S-5 μm, 20 X 50 mm (YMC)solvente: SOLUÇÃO A; água contendo carbonato de amônio 10 mM,SOLUÇÃO B; acetonitrilaciclo do gradiente: 0,00 min (SOLUÇÃO A/SOLUÇÃO B=95/5), 2,00 min (SOLUÇÃO A/SOLUÇÃO B=95/5), 4,02 min(SOLUÇÃO A/SOLUÇÃO B=5/95), 6,40 min (SOLUÇÃO A/SOLUÇÃO B=5/95), 6,50 min (SOLUÇÃO A/SOLUÇÃO B=95/5), 8,00 min(SOLUÇÃO A/SOLUÇÃO B=95/5) 3) dispositivo de medição: sistema de purificação de alta vazão da Gilson Company Inc.,coluna: YMC CombiPrep, ProC18 RS, S-5 μm, 20 X 50 mm (YMC)solvente: SOLUÇÃO A; água contendo 0,1 % de ácido trifluoroacético,SOLUÇÃO B; acetonitrila contendo 0,1 % de ácido trifluoroacéticociclo do gradiente: 0.00 min (SOLUÇÃO A/SOLUÇÃO B=98/2), 1.00 min (SOLUÇÃO A/SOLUÇÃO B=98/2), 5.20 min(SOLUÇÃO A/SOLUÇÃO B=60/40), 5.40 min (SOLUÇÃO A/SOLUÇÃO B=5/95), 6.40 min (SOLUÇÃO A/SOLUÇÃO B=5/95), 6.50 min(SOLUÇÃO A/SOLUÇÃO B=98/2), 6.60 min (SOLUÇÃO A/SOLUÇÃO B=98/2)volume de injeção: 500 μl, taxa de fluxo: 20 ml/min, método de detecção: UV 220 nm, 254 nmNos Exemplos de Referência e Exemplos, o espectro da massa (MS) foi medido nas seguintes condições.
[00356] dispositivo de medição: plataforma Micromass II ou Waters ZMDmétodo de ionização: Ionização Química a Pressão Atmosférica: APCI [Atmospheric Pressure Chemical Ionization] ou método de ionização com impacto de elétrons (ESI, Electron Spray Ionization))Nos Exemplos de Referência e Exemplos, o espectro de massa-HPLC (LC-MS) foi medido nas seguintes condições.
[00357] 1) dispositivo de medição: Micromass ZMD, AgilentTechnologies HP1100 e 1200 LC/MSDcoluna: CAPCELL PAK C18UG120, S-3 μm, 1,5 X 35 mmsolvente: SOLUÇÃO A; água contendo ácido trifluoroacético a 0,05 %,SOLUÇÃO B; acetonitrila contendo ácido trifluoroacético a 0,04 %ciclo do gradiente: 0,00 min (Solução A/Solução B=90/10), 2,00 min (Solução A/Solução B=5/95), 2,75 min (Solução A/Solução B=5/95), 2,76 min (Solução A/Solução B=90/10), 3,45 min (Solução A/Solução B=90/10)volume de injeção: 2 μltaxa de fluxo: 0.5 ml/minmétodo de detecção: UV 220 nmmétodo de ionização: método de ionização por impacto de elétrons (Electron Spray Ionization: ESI)2) dispositivo de medição: sistema Waters, 4-ch LC/MS com MUXcoluna: CAPCELL PAK C18 UG-120, S-3 μm, 1,5 X 35 mm (Shiseido Co., Ltd.)solvente: SOLUÇÃO A; água contendo acetato de amônio 5 mM,SOLUÇÃO B; acetonitrila contendo acetato de amônio 5 mMciclo do gradiente: gradiente: 0,00 min (SOLUÇÃO A/SOLUÇÃO B=100/0), 2,00 min (SOLUÇÃO A/SOLUÇÃO B=0/100), 3,00 min (SOLUÇÃO A/SOLUÇÃO B=0/100), 3,01 min (SOLUÇÃO A/SOLUÇÃO B=100/0), 3,30 min (SOLUÇÃO A/SOLUÇÃO B=100/0)volume de injeção: 2 ml, taxa de fluxo: 0,5 ml/min, método de detecção: UV 220 nmmétodo de ionização: método de ionização por spray de elétrons (ESI)modo de medição: varredura completa (íons positivos+negativos) faixa de valor de massa medida: m/z=150 - 750O espectro de RMN 1H foi medido usando-se tetrametilsilano como o padrão interno, usando BRUKER AVANCE DPX-300 (300 MHz), AV300 (300MHz), AV400 (400 MHz) e VARIAN Mercury-300 (300 MHz), e todos os valores de δ são expressos em ppm.
[00358] Como o aparelho de reação de microondas usou-se EmrysOptimizer, Biotage Japan Ltd..
[00359] Exceto se especificado de outra forma, o valor numérico dosolvente misto mostra uma taxa de mistura volumétrica de cada solvente. Exceto se especificado de outra forma, % significa % em peso. Embora a temperatura do recinto (temperatura ambiente) na presente descrição signifique uma temperatura de cerca de 10°C a cerca de 35°C, ela não é limitada de forma particularmente estrita.
[00360] Outras abreviaturas usadas na descrição significam o seguinte:s: singletod: dubletot: tripletoq: quartetom: multipletosext: sextetobr: largoJ: constante de acoplamentoHz: HertzCDCl3: clorofórmio deuteradoDMSO-d6: sulfóxido de dimetila-d6CD3OD: metanol deuteradoRMN 1H: ressonância magnética nuclear do prótonLC/MS: espectro de cromatografia líquida-espectrometria demassa DMF: N,N-dimetilformamidaDMSO: sulfóxido de dimetilaTHF: tetraidrofuranoWSCD: cloridrato de carbodiimida (1-etil-3-(3-dimetilaminapropil)carbodiimida) solúvel em águaHOBt: 1-hidroxibenzotriazolBoc: t-butoxicarbonilaK2CO3: carbonato de potássioM: concentração molarExemplo de Referência 1Produção de 4-hidróxi-2-oxo-1,2-diidroquinolina-3- carboxilato de etilaA uma solução de antranilato de metila (121 g, 0,8 mol) e dietil malonato (128 g, 0,8 mol) em etanol (900 ml) adicionou-se uma solução a 20 % (274 g) de etóxido de sódio em etanol, e a mistura foi agitada à temperatura ambiente durante 30 min. Etanol foi evaporado, e a mistura foi agitada a 140°C durante 12 h. Após resfriamento, o sólido obtido foi lavado com éter de dietila, e dissolvido em água. Materiais insolúveis foram removidos por filtração, o filtrado foi acidificado com ácido clorídrico 5N, e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água, e secado sob pressão reduzida dando o composto titular (161 g, 86 %) como um pó amarelo claro.
[00361] RMN 1H (300 MHz, DMSO-d6) δ:1,31 (3H, t, J = 7,1 Hz),4,34 (2H, q, J = 7,1 Hz), 7,19-7,29 (2H, m), 7,63 (1H, td, J = 7,8, 1,2 Hz), 7,94 (1H, d, J = 8,1 Hz), 11,51 (1H, br s), 13,40 (1H, br s).Exemplo de Referência 2
[00362] Produção de 2,4-dicloroquinolina-3-carboxilato de etila Uma mistura do composto do Exemplo de Referência 1 (75 g, 0,32 mol) e oxicloreto de fósforo (200 ml) foi agitada a 110°C durante 6 h. Após resfriamento, a reação mistura foi concentrada sob pressão reduzida, o resíduo foi dissolvido em uma pequena quantidade de acetato de etila e a mistura foi despejada em água gelada. A mistura obtida foi extraída com acetato de etila, e o extrato foi lavado sucessivamente com solução aquosa de hidróxido de sódio 1N, água e salmoura, secada sobre sulfato de magnésio, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=1/5) dando o composto titular (68 g, 79 %) como um sólido branco.
[00363] RMN 1H (300 MHz, CDCl3) δ:1,47 (3H, t, J = 7,2 Hz), 4,54 (2H, q, J = 7,2 Hz), 7,71 (1H, t, J = 7,5 Hz), 7,85 (1H, t, J = 7,5 Hz), 8,06 (1H, d, J = 8,2 Hz), 8,24 (1H, d, J = 8,2 Hz).Exemplo de Referência 3
[00364] Produção de 4-cloro-2-oxo-1,2-diidroquinolina-3-carboxilato de etilaUma mistura do composto do Exemplo de Referência 2 (68,0 g, 0,25 mol) e acetato de sódio (21,7 g, 0,26 mol) em ácido acético (200 ml) foi agitada a 120°C durante 20 h. Após resfriamento, a mistura de reação foi adicionada a água, e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água, e secado sob pressão reduzida dando o composto titular (58,8 g, 94 %) como um sólido branco.
[00365] RMN 1H (300 MHz, CDCl3) δ:1,46 (3H, t, J = 7,2 Hz), 4,53 (2H, q, J = 7,2 Hz), 7,34 (1H, t, J = 7,8 Hz), 7,43 (1H, d, J = 8,1 Hz), 7,63 (1H, t, J = 7,8 Hz), 8,00 (1H, d, J = 8,1 Hz), 12,41 (1H, br s).Exemplo de Referência 4
[00366] Produção de 4-cloro-2-oxo-1-(2-oxo-2-feniletil)-1,2-diidroquinolina-3-carboxilato de etilaA uma solução do composto do Exemplo de Referência 3 (10,0 g, 39,7 mmol) em DMF (160 ml) adicionou-se hidreto de sódio (60 % em óleo, 1,7 g, 41,7 mmol) sob resfriamento com gelo, e a mistura foi agitada durante 15 min. Adicionou-se brometo de fenacila (8,7 g, 43,7 mmol) à mistura obtida sob resfriamento com gelo, e a mistura foi agitada durante 1 h. A mistura de reação foi adicionada a água (1,5 l), e a mistura foi extraída com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em sílica-gel (eluado; acetato de etila/hexano=1/2 - 1/1) dando o composto titular (10,5 g, 71 %) como um sólido amarelo claro.
[00367] RMN 1H (300 MHz, CDCl3) δ:1,42 (3H, t, J = 7,2 Hz), 4,47 (2H, q, J = 7,2 Hz), 5,80 (2H, s), 7,02 (1H, d, J = 8,1 Hz), 7,34 (1H, t, J = 7,8 Hz), 7,53-7,60 (3H, m), 7,65-7,70 (1H, m), 8,06-8,13 (3H, m).Exemplo de Referência 5
[00368] Produção de 3-hidróxi-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrotieno[3,2-c]quinolina-2-carboxilato de etilaUma solução a 20 % (17,2 g, 50,5 mmol) de etóxido de sódio em etanol foi diluída com etanol (50 ml), tioglicolato de etila (6,1 g, 50,5 mmol) foi adicionada à solução obtida, e a mistura foi agitada à temperatura ambiente durante 5 min. O composto do Exemplo de Referência 4 (9,3 g, 25,3 mmol) foi adicionado à mistura, e a mistura foi agitada à temperatura ambiente durante 18 h. A mistura de reação foi diluída com água gelada (50 ml), adicionou-se ácido clorídrico 2N (30 ml) e a mistura foi agitada durante 30 min. O sólido precipitado foi recolhido por meio de filtração, lavado com água e éter de dietila, e secado sob pressão reduzida dando o composto titular (10,0 g, 96 %) como um pó branco.
[00369] RMN 1H (300 MHz, DMSO-d6) δ:1,32 (3H, t, J = 7,0 Hz), 4,25-4,35 (2H, m), 6,01 (2H, s), 7,40 (1H, t, J = 7,2 Hz), 7,55-7,67 (4H, m), 7,77 (1H, t, J = 7,5 Hz), 8,00-8,07 (1H, m), 8,07-8,19 (2H, m), 10,40-10,65 (1H, br).Exemplo de Referência 6
[00370] Produção de 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrotieno[3,2-c]quinolina-2-carboxilato de etilaUma mistura do composto do Exemplo de Referência 5 (7,0 g, 17,1 mmol) e DBU (4,3 g, 18,3 mmol) em DMF (150 ml) foi agitada à temperatura ambiente durante 10 min, e adicionou-se iodometano (4,0 g, 28,0 mmol). A mistura foi agitada à temperatura ambiente durante 4 h, e concentrada sob pressão reduzida. O resíduo foi diluído com água, e extraído duas vezes com solução mista de acetato de etila-THF. O extrato foi combinado, lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi lavado com solução mista de acetato de etila-éter de dietila, e secado sob pressão reduzida dando o composto titular (5,7 g, 79 %) como um pó verde claro.
[00371] RMN 1H (300 MHz, DMSO-d6) δ:1,34 (3H, t, J = 7,1 Hz), 3,95 (3H, s), 4,34 (2H, q, J = 7,1 Hz), 5,98 (2H, s), 7,37 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,7 Hz), 7,57-7,67 (3H, m), 7,76 (1H, t, J = 7,5 Hz), 8,06 (1H, d, J = 7,8 Hz), 8,16-8,19 (2H, m).Exemplo de Referência 7
[00372] Produção de ácido 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrotieno[3,2-c]quinolina-2-carboxílicoUma solução mista do composto do Exemplo de Referência 6 (5,7 g, 13,5 mmol) e solução aquosa 2N de hidróxido de sódio (60 ml) em THF (200 ml)-etanol (100 ml) foi agitada à temperatura ambiente durante 18 h. A mistura de reação foi neutralizada com ácido clorídrico 2N (60 ml), e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado sucessivamente com água e éter de dietila, e secado sob pressão reduzida dando o composto titular (4,2 g, 79 %) como um pó rosa claro.
[00373] RMN 1H (300 MHz, DMSO-d6) δ:3,93 (3H, s), 5,98 (2H, s), 7,35 (1H, t, J = 7,8 Hz), 7,48 (1H, d, J = 8,7 Hz), 7,56-7,67 (3H, m), 7,77 (1H, t, J = 7,2 Hz), 8,04 (1H, dd, J = 8,1, 1,2 Hz), 8,16-8,19 (2H, m).Exemplo de Referência 8
[00374] Produção de 3-etóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrotieno[3,2-c]quinolina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 6, o composto titular (461 mg, 87 %) foi obtido como um pó branco do composto (500 mg, 1,22 mmol) do Exemplo de Referência 5, DBU (280 mg, 1,84 mmol) e iodoetano (302 mg, 1,84 mmol).
[00375] RMN 1H (300 MHz, DMSO-d6) δ:1,34 (6H, t, J = 7,0 Hz), 4,21 (2H, q, J = 7,0 Hz), 4,34 (2H, q, J = 7,0 Hz), 5,98 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,4 Hz), 7,57-7,67 (3H, m), 7,76 (1H, t, J = 7,2 Hz), 8,06 (1H, dd, J = 7,8, 1,2 Hz), 8,16-8,19 (2H, m).Exemplo de Referência 9
[00376] Produção de ácido 3-etóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrotieno[3,2-c]quinolina-2-carboxílico
[00377] Da mesma maneira que no Exemplo de Referência 7, o composto titular (392 mg, 95 %) foi obtido como um pó rosa claro a partir do composto (440 mg, 1,01 mmol) do Exemplo de Referência 8.
[00378] RMN 1H (300 MHz, DMSO-d6) δ: 1,33 (3H, t, J = 7,0 Hz), 4,20 (2H, q, J = 7,0 Hz), 6,00 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,47 (1H, d, J = 8,4 Hz), 7,56-7,67 (3H, m), 7,77 (1H, t, J = 7,5 Hz), 8,04 (1H, dd, J = 7,8, 1,2Hz), 8,16-8,19 (2H, m).Exemplo de Referência 10
[00379] Produção de 4-cloro-1-(4-metoxibenzil)-2-oxo-1,2-diidroquinolina-3-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 4, o composto titular (10,8 g, 79 %) foi obtido como um pó branco a partir do composto (10,0 g, 39,8 mmol) do Exemplo de Referência 3 e cloreto de 4- metoxibenzila (7,48 ml, 47,8 mmol).
[00380] RMN 1H (300 MHz, DMSO-d6) δ: 1,34 (3H, t, J = 7,1 Hz), 3,70 (3H, s), 4,40 (2H, q, J = 7,1 Hz), 5,48 (2H, s), 6,89 (2H, d, J = 8,7 Hz), 7,19 (2H, d, J = 8,7 Hz), 7,42 (1H, t, J = 7,8 Hz), 7,61 (1H, d, J = 8,7 Hz), 7,69-7,75 (1H, m), 8,04 (1H, dd, J = 7,8, 1,2 Hz). Exemplo de Referência 11
[00381] Produção diidrotieno[3,2-c]quinolina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 5, o composto titular (10,4 g, 88 %) foi obtido como um pó branco a partir do composto (10,6 g, 31,0 mmol) do Exemplo de Referência 10.
[00382] RMN 1H (300 MHz, DMSO-d6) δ:1,32 (3H, t, J = 7,0 Hz), 3,70 (3H, s), 4,32 (2H, q, J = 7,0 Hz), 5,53 (2H, s), 6,87 (2H, d, J = 8,9 Hz), 7,23 (2H, d, J = 8,9 Hz), 7,34-7,39 (1H, m), 7,58-7,66 (2H, m), 8,00-8,03 (1H, m), 10,77 (1H, s).Exemplo de Referência 12
[00383] Produção de 3-metóxi-5-(4-metoxibenzil)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxilato de etila
[00384] Da mesma maneira que no Exemplo de Referência 6, o composto titular (5,2 g, 64 %) foi obtido como um pó branco a partir do composto (7,5 g, 19,8 mmol) do Exemplo de Referência 11.
[00385] RMN 1H (300 MHz, DMSO-d6) δ:1,34 (3H, t, J = 7,1 Hz), 3,70 (3H, s), 4,01 (3H, s), 4,34 (2H, q, J = 7,1 Hz), 5,50 (2H, s), 6,87 (2H, d, J = 8,7 Hz), 7,20 (2H, d, J = 8,7 Hz), 7,27-7,32 (1H, m), 7,48-7,60 (2H, m), 8,01 (1H, dd, J = 7,7, 1,4 Hz).Exemplo de Referência 13
[00386] Produção de ácido 3-metóxi-5-(4-metoxibenzil)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 7, o composto titular (4,75 g, 98 %) foi obtido como um pó branco a partir do composto (5,0 g, 12,3 mmol) do Exemplo de Referência 12.
[00387] RMN 1H (300 MHz, DMSO-d6) δ:3,70 (3H, s), 3,93 (3H, s), 5,51 (2H, s), 6,87 (2H, d, J = 8,7 Hz), 7,20 (2H, d, J = 8,7 Hz), 7,27-7,32 (1H, m), 7,48-7,59 (2H, m), 7,99 (1H, dd, J = 7,8, 1,2 Hz), 13,40 (1H, s).Exemplo de Referência 14
[00388] Produção de 1-(piridin-2-ilmetil)-2H-3,1-benzooxazina-2,4(1H)-dionaA uma solução de anidrido isatóico (25,4 g, 0,156 mol) em DMF (300 ml) adicionou-se cloridrato de 2-(clorometil)piridina (28,1 g, 0,171 mol) e hidreto de sódio (66 % em óleo, 12,5 g, 0,34 mol) sob resfriamento com gelo. A mistura obtida foi agitada à temperatura ambiente durante 42 h. Adicionou-se água (750 ml) à mistura de reação e a mistura foi resfriada com gelo. O sólido precipitado foi recolhido por meio de filtração, e recristalizado de acetona-éter de diisopropila dando o composto titular (13,4 g, 34 %).
[00389] RMN 1H (300 MHz, DMSO-d6) δ:5,36 (2H, s), 7,24-7,34 (3H, m), 7,49 (1H, d, J = 8,1 Hz), 7,73 (1H, ddd, J = 8,6, 7,2, 1,5 Hz), 7,77 (1H, td, J = 7,7, 1,6 Hz), 8,03 (1H, dd, J = 7,8, 1,8 Hz), 8,50 (1H, ddd, J = 4,9, 1,7, 1,0 Hz).Exemplo de Referência 15
[00390] Produção de 4-hidróxi-2-oxo-1-(piridin-2-ilmetil)-1,2-diidroquinolina-3-carboxilato de etila A uma solução de dietil malonato (15,6 g, 97,4 mmol) em DMF (90 ml) adicionou-se hidreto de sódio (66 % em óleo, 2,60 g, 72 mmol) sob resfriamento com gelo, e a mistura foi agitada à mesma temperatura durante 10 min. O composto do Exemplo de Referência 14 (16,5 g, 64,9 mmol) foi adicionado à mistura obtida em pequenas porções, e a mistura foi agitada a 120°C durante 6 h. A mistura de reação foi concentrada sob pressão reduzida, adicionou-se água gelada ao resíduo e a mistura foi lavada com éter de dietila. A camada aquosa foi basificada fracamente com ácido clorídrico 5N (8 ml) sob resfriamento com gelo. Os cristais precipitados foram recolhidos por meio de filtração, lavados com água, e recristalizados de acetato de etila-éter de diisopropila dando o composto titular (12,8 g, 60 %).
[00391] RMN 1H (300 MHz, CDCl3) δ:1,50 (3H, t, J = 7,1 Hz), 4,53 (2H, q, J = 7,1 Hz), 5,61 (2H, br s), 7,12-7,18 (2H, m), 7,18-7,25 (1H, m), 7,36 (1H, d, J = 8,7 Hz), 7,51-7,59 (2H, m), 8,18 (1H, dd, J = 8,3, 1,7 Hz), 8,56 (1H, dd, J = 5,3, 2,0 Hz), 14,53 (1H, s). Exemplo de Referência 16
[00392] Produção de 4-cloro-2-oxo-1-(piridin-2-ilmetil)-1,2-diidroquinolina-3-carboxilato de etilaA uma mistura do composto do Exemplo de Referência 15 (16,1 g, 49,6 mmol) e tolueno (50 ml) adicionou-se oxicloreto de fósforo (12 ml, 0,13 mol), e a mistura foi agitada a 110°C durante 1 h. A mistura de reação foi deixada resfriar, e o solvente foi removido por decantação. Adicionou-se água ao resíduo e a mistura foi lavada com éter de dietila. A camada aquosa foi neutralizada com carbonato de sódio e extraída duas vezes com clorofórmio. A camada orgânica combinada foi lavada com água e salmoura, secada sobre sulfato de sódio, filtrada, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia de coluna em sílica-gel (eluado; acetato de etila/hexano=1/1 - 3/1) e cristalizado de acetato de etila-hexano dando o composto titular (2,54 g, 15 %).
[00393] RMN 1H (300 MHz, CDCl3) δ:1,44 (3H, t, J = 7,2 Hz), 4,50 (2H, q, J = 7,2 Hz), 5,64 (2H, br s), 7,15-7,26 (2H, m), 7,31 (1H, ddd, J = 8,2, 5,9, 2,3 Hz), 7,52-7,63 (3H, m), 8,06 (1H, dt, J = 7,8, 0,8 Hz), 8,56 (1H, ddd, J = 4,7, 1,9, 0,8 Hz).Exemplo de Referência 17
[00394] Produção de 3-hidróxi-4-oxo-5-(piridin-2-ilmetil)-4,5- diidrotieno[3,2-c]quinolina-2-carboxilato de etilaUma solução a 20 % (4,51 g, 13 mmol) de etóxido de sódio em etanol foi diluída com etanol (15 ml), e adicionou-se tioglicolato de etila (1,74 ml, 15,9 mmol) à solução obtida. A mistura foi agitada à temperatura ambiente durante 10 min. O composto do Exemplo de Referência 16 (2,27 g, 6,62 mmol) foi adicionado à mistura, e a mistura foi agitada à temperatura ambiente durante 5,5 h. A mistura de reação foi neutralizada com água gelada e ácido clorídrico 2N (3,2 ml) sob resfriamento com gelo, e extraída duas vezes com clorofórmio. A camada orgânica combinada foi lavada com água e salmoura, secada sobre sulfato de sódio, filtrada, e concentrada sob pressão reduzida. O sólido obtido foi lavado com etanol dando o composto titular (2,50 g, 99 %).
[00395] RMN 1H (300 MHz, CDCl3) δ:1,43 (3H, t, J = 7,1 Hz), 4,43 (2H, q, J = 7,1 Hz), 5,69 (2H, br s), 7,16-7,24 (2H, m), 7,25-7,32 (1H, m), 7,49 (1H, ddd, J = 8,6, 7,1, 1,5 Hz), 7,57 (1H, d, J = 8,1 Hz), 7,60 (1H, td, J = 7,7, 1,8 Hz), 7,82 (1H, dd, J = 8,1, 1,5 Hz), 8,57 (1H, ddd, J = 4,9, 1,6, 0,8 Hz), 10,68 (1H, s).Exemplo de Referência 18
[00396] Produção de 3-metóxi-4-oxo-5-(piridin-2-ilmetil)-4,5- diidrotieno[3,2-c]quinolina-2-carboxilato de etilaA uma suspensão do composto do Exemplo de Referência 17 (2,26 g, 5,94 mmol) em DMF (20 ml) adicionou-se DBU (1,06 ml, 7,09 mmol), e adicionou-se iodometano (0,74 ml, 12 mmol) à solução obtida. A mistura obtida foi agitada à temperatura ambiente durante 14 h, adicionou-se água, e a mistura foi extraída duas vezes com acetato de etila. A camada orgânica combinada foi lavada com água, solução de hidróxido de sódio 0,5N e água, secada por meio de passagem através de sílica-gel básico (eluído com acetato de etila), e concentrada sob pressão reduzida. O resíduo foi cristalizado de acetato de etila-éter de diisopropila dando o composto titular (1,16 g, 50 %).
[00397] RMN 1H (300 MHz, CDCl3) δ:1,43 (3H, t, J = 7,1 Hz), 4,17 (3H, s), 4,41 (2H, q, J = 7,1 Hz), 5,70 (2H, br s), 7,14-7,26 (3H, m), 7,45 (1H, ddd, J = 8,6, 7,0, 1,6 Hz), 7,51 (1H, dd, J = 8,6, 0,8 Hz), 7,57 (1H, td, J = 7,7, 1,8 Hz), 7,83 (1H, ddd, J = 7,7, 1,5, 0,3 Hz), 8,57 (1H, ddd, J = 5,0, 2,0, 0,9Hz).Exemplo de Referência 19
[00398] Produção de ácido 3-metóxi-4-oxo-5-(piridin-2-ilmetil)-4,5- diidrotieno[3,2-c]quinolina-2-carboxílicoA uma suspensão do composto do Exemplo de Referência 18 (1,21 g, 3,07 mmol) em THF (10 ml) e etanol (10 ml) adicionou-se solução aquosa de hidróxido de sódio 5N (1,2 ml, 6,0 mmol). A mistura obtida foi agitada à temperatura ambiente durante 45 min, adicionou-se etanol (5 ml) e a mistura foi agitada adicionalmente durante 135 min. A mistura de reação foi resfriada com gelo, neutralizada com ácido clorídrico 1N (6,0 ml), e adicionou-se clorofórmio e água. A camada orgânica foi separada, e a camada aquosa foi extraída duas vezes com clorofórmio. A camada orgânica combinada foi lavada com água e salmoura, secada sobre sulfato de sódio, filtrada, e concentrada sob pressão reduzida. O resíduo foi recristalizado de clorofórmio-éter de diisopropila dando o composto titular (1,11 g, 99 %).
[00399] RMN 1H (300 MHz, DMSO-d6) δ:3,96 (3H, s), 5,65 (2H, s), 7,23-7,33 (3H, m), 7,43 (1H, d, J = 8,7 Hz), 7,54 (1H, ddd, J = 8,6, 7,3, 1,4 Hz), 7,73 (1H, td, J = 7,7, 1,9 Hz), 7,97-8,02 (1H, m), 8,45-8,48 (1H, m), 13,38 (1H, br s).Exemplo de Referência 20
[00400] Produção de 3-(2-etoxietóxi)-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrotieno[3,2-c]quinolina-2-carboxilato de etilaA uma suspensão do composto do Exemplo de Referência 5 (1,35 g, 3,31 mmol) em DMF (20 ml) adicionou-se DBU (1,48 ml, 9,90 mmol) e 2-bromoetiletiléter (1,12 ml, 9,93 mmol), e a mistura foi agitada a 60°C durante 30 h. Adicionou-se clorofórmio e água à mistura de reação, a camada orgânica foi separada e a camada aquosa foi extraída com clorofórmio. A camada orgânica combinada foi lavada com solução de hidróxido de sódio 0,5N e água, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia de coluna em sílica-gel (eluado; acetato de etila/hexano=1/3 - 2/3) e recristalizado de diclorometano- éter de diisopropila dando o composto titular (1,36 g, 86 %).
[00401] RMN 1H (300 MHz, CDCl3) δ:1,17 (3H, t, J = 7,1 Hz), 1,43 (3H, t, J = 7,1 Hz), 3,56 (2H, q, J = 7,1 Hz), 3,89 (2H, dd, J = 5,5, 4,6 Hz), 4,40 (2H, q, J = 7,1 Hz), 4,45 (2H, dd, J = 5,5, 4,6 Hz), 5,85 (2H, s), 6,97 (1H, d, J = 8,1 Hz), 7,21-7,28 (1H, m), 7,45 (1H, ddd, J = 8,7, 7,2, 1,4 Hz), 7,517,58 (2H, m), 7,63-7,69 (1H, m), 7,86 (1H, dd, J = 7,8, 1,5 Hz), 8,07-8,12 (2H, m).Exemplo de Referência 21
[00402] Produção de ácido 3-(2-etoxietóxi)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxílicoA uma suspensão do composto do Exemplo de Referência 20 (1,20 g, 2,50 mmol) em THF (16 ml) e etanol (16 ml) adicionou-se solução aquosa de hidróxido de sódio 5N (1,0 ml, 5,0 mmol). A mistura obtida foi agitada à temperatura ambiente durante 3 h. A mistura de reação foi acidificada com ácido clorídrico 1N, e adicionou-se água. Os cristais precipitados foram recolhidos por meio de filtração e lavados com água dando o composto titular (1,09 g, 97 %).
[00403] RMN 1H (300 MHz, DMSO-d6) δ:1,01 (3H, t, J = 6,9 Hz), 3,40 (2H, q, J = 6,9 Hz), 3,71 (2H, t, J = 5,0 Hz), 4,30 (2H, t, J = 5,0 Hz), 5,97 (2H, s), 7,33 (1H, t, J = 7,7 Hz), 7,46 (1H, d, J = 8,7 Hz), 7,54-7,66 (3H, m), 7,76 (1H, t, J = 7,2 Hz), 8,02 (1H, d, J = 7,8 Hz), 8,16 (2H, d, J = 7,5 Hz), 13,27 (1H, br s).Exemplo de Referência 22
[00404] Produção de 3-hidróxi-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrofuro[3,2-c]quinolina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 5, o composto titular (1,10 g, 69 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 4 (1,50 g, 4,06 mmol), uma solução a 20 % (2,76 g, 8,11 mmol) de etóxido de sódio em etanol e glicolato de etila (1,01 g, 9,73 mmol).
[00405] RMN 1H (300 MHz, DMSO-d6) δ:1,34 (3H, t, J = 7,1 Hz), 4,35 (2H, q, J = 7,1 Hz), 5,96 (2H, s), 7,39 (1H, t, J = 7,7 Hz), 7,51 (1H, d, J = 8,4 Hz), 7,60-7,67 (3H, m), 7,74-7,79 (1H, m), 8,05 (1H, dd, J = 7,7, 1,4 Hz), 8,15-8,18 (2H, m), 9,80-11,10 (1H, br).Exemplo de Referência 23
[00406] Produção de 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrofuro[3,2-c]quinolina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 6, o composto titular (250 mg, 23 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 22 (1,05 g, 2,68 mmol), DBU (612 mg, 4,02 mmol) e iodometano (250 ml, 4,02 mmol).
[00407] RMN 1H (300 MHz, DMSO-d6) δ:1,35 (3H, t, J = 7,1 Hz), 4,14 (3H, s), 4,37 (2H, q, J = 7,1 Hz), 5,99 (2H, s), 7,39-7,45 (1H, m), 7,55 (1H, d, J = 8,7 Hz), 7,62-7,68 (3H, m), 7,74-7,80 (1H, m), 8,09 (1H, dd, J = 7,8, 1,5 Hz), 8,16-8,18 (2H, m).Exemplo de Referência 24
[00408] Produção de ácido 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrofuro[3,2-c]quinolina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 7, o composto titular (160 mg, 72 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 23 (240 mg, 0,592 mmol), solução aquosa de hidróxido de sódio 8N (1,0 ml) e etanol (14 ml).
[00409] RMN 1H (300 MHz, DMSO-d6) δ:4,12 (3H, s), 5,99 (2H, s), 7,42 (1H, t, J = 7,6 Hz), 7,54 (1H, d, J = 7,8 Hz), 7,62-7,67 (3H, m), 7,77 (1H, t, J = 7,8 Hz), 8,07 (1H, dd, J = 7,6, 1,5 Hz), 8,16-8,18 (2H, m), 12,60-14,10 (1H, br).Exemplo de Referência 25
[00410] Produção de 4-[(2-etóxi-2-oxoetil)(metil)amina]-2-oxo-1-(2- oxo-2-feniletil)-1,2-diidroquinolina-3-carboxilato de etilaUma mistura do composto do Exemplo de Referência 4 (24,1 g, 65,2 mmol), cloridrato de etil éster de sarcosina (12,0 g, 78,2 mmol), trietilamina (18,1 ml, 130 mmol) e etanol (200 ml) foi agitada a 85°C durante 15 h, adicionou-se mais cloridrato de etil éster de sarcosina (3,00 g, 19,6 mmol) e trietilamina (18,1 ml, 130 mmol), e a mistura foi agitada a 85°C durante 7 h. Após resfriamento, adicionou-se água à mistura de reação, e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água, e secado sob pressão reduzida dando o composto titular (24,6 g, 84 %) como um pó branco.
[00411] RMN 1H (300 MHz, DMSO-d6) δ:1,21-1,31 (6H, m), 2,93 (3H, s), 3,95 (2H, s), 4,15-4,31 (4H, m), 5,87 (2H, s), 7,31 (1H, t, J = 7,8 Hz), 7,40 (1H, d, J = 8,4 Hz), 7,55-7,65 (3H, m), 7,72-7,78 (1H, m), 8,05 (1H, dd, J = 7,8, 1,5 Hz), 8,12-8,15 (2H, m).Exemplo de Referência 26
[00412] Produção de 3-hidróxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidro-1H-pirrol[3,2-c]quinolina-2-carboxilato de etilaUma mistura do composto do Exemplo de Referência 25 (1,25 g, 2,77 mmol), uma solução a 20 % (1,23 g, 3,33 mmol) de etóxido de sódio em etanol e etanol (25 ml) foi agitada a 55°C durante 15 h. A mistura de reação foi diluída com água, adicionou-se ácido clorídrico 1N (5 ml) e a mistura foi agitada durante 30 min. O sólido precipitado foi recolhido por meio de filtração, lavado com água, etanol e acetato de etila, e recristalizado de dimetilformamida-etanol dando o composto titular (760 mg, 68 %) como um pó branco.
[00413] RMN 1H (300 MHz, DMSO-d6) δ:1,33 (3H, t, J = 7,2 Hz), 4,30-4,38 (5H, m), 5,93 (2H, s), 7,30-7,40 (2H, m), 7,48-7,53 (1H, m), 7,617,66 (2H, m), 7,73-7,79 (1H, m), 8,15-8,18 (2H, m), 8,34-8,37 (1H, m), 9,00 (1H, s).Exemplo de Referência 27
[00414] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidro-1H-pirrol[3,2-c]quinolina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 6, o composto titular (420 mg, 55 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 26 (740 mg, 1,83 mmol), DBU (410 ml, 2,74 mmol) e iodometano (171 ml, 2,74 mmol).
[00415] RMN 1H (300 MHz, DMSO-d6) δ:1,35 (3H, t, J = 7,1 Hz), 3,89 (3H, s), 4,29-4,37 (5H, m), 5,96 (2H, s), 7,30-7,40 (2H, m), 7,48-7,53 (1H, m), 7,61-7,66 (2H, m), 7,73-7,78 (1H, m), 8,15-8,18 (2H, m), 8,38 (1H, dd, J = 8,3, 1,4 Hz).Exemplo de Referência 28
[00416] Produção de ácido 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 7, o composto titular (345 mg, 91 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 27 (405 mg, 0,968 mmol), solução aquosa de hidróxido de sódio 8N (1,5 ml) e etanol (15 ml).
[00417] RMN 1H (300 MHz, DMSO-d6) δ:3,88 (3H, s), 4,31 (3H, s), 5,95 (2H, s), 7,29-7,39 (2H, m), 7,46-7,52 (1H, m), 7,61-7,66 (2H, m), 7,737,78 (1H, m), 8,16-8,18 (2H, m), 8,38 (1H, dd, J = 8,3, 1,1 Hz), 12,92 (1H, s). Exemplo de Referência 29
[00418] Produção de 3-etóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidro-1H-pirrol[3,2-c]quinolina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 6, ocomposto titular (2,10 g, quant.) foi obtido como um pó branco a partir do composto (1,90 g, 4,70 mmol) do Exemplo de Referência 26, DBU (1,05 ml, 7,05 mmol) e iodoetano (564 ml, 7,05 mmol).
[00419] RMN 1H (300 MHz, DMSO-d6) δ:1,27-1,37 (6H, m), 4,16 (2H, q, J = 6,9 Hz), 4,29-4,36 (5H, m), 5,95 (2H, s), 7,27-7,39 (2H, m), 7,50 (1H, t, J = 8,0 Hz), 7,63 (2H, t, J = 7,3 Hz), 7,76 (1H, t, J = 7,4 Hz), 8,17 (2H, d, J = 7,3 Hz), 8,38 (1H, d, J = 8,1 Hz).Exemplo de Referência 30
[00420] Produção de ácido 3-etóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 7, ocomposto titular (1,62 g, 89 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 29 (1,95 g, 4,51 mmol), solução aquosa de hidróxido de sódio 8N (2,0 ml) e etanol (14 ml).
[00421] RMN 1H (300 MHz, DMSO-d6) δ:1,27 (3H, t, J = 7,0 Hz), 4,16 (2H, q, J = 7,0 Hz), 4,31 (3H, s), 5,95 (2H, s), 7,27-7,39 (2H, m), 7,49 (1H, t, J = 7,4 Hz), 7,63 (2H, t, J = 7,4 Hz), 7,76 (1H, t, J = 7,4 Hz), 8,15-8,18 (2H, m), 8,38 (1H, d, J = 7,2 Hz), 12,83 (1H, s).Exemplo de Referência 31
[00422] Produção de 4-cloro-6-metil-2-oxo-1,2-diidropiridina-3- carboxilato de etilaUma mistura de 4-hidróxi-6-metil-2-oxo-1,2-diidropiridina-3- carboxilato de etila (3,00 g, 15,2 mmol), oxicloreto de fósforo (7,75 ml), cloreto de n-butiltrietilamônio (13,8 g, 60,8 mmol) e acetonitrila (60 ml) foi agitada a 40°C durante 30 min e em condições de refluxo durante 30 min. Após resfriamento, a mistura de reação foi concentrada sob pressão reduzida, adicionou-se água ao resíduo e a mistura foi extraída com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi lavado com solução mista de acetato de etila-hexano, e secado sob pressão reduzida dando o composto titular (1,45 g, 44 %) como um pó branco.
[00423] RMN 1H (300 MHz, DMSO-d6) δ:1,26 (3H, t, J = 7,0 Hz), 2,20 (3H, s), 4,25 (2H, q, J = 7,0 Hz), 6,26 (1H, s), 12,29 (1H, s).Exemplo de Referência 32
[00424] Produção de 4-cloro-6-metil-2-oxo-1-(2-oxo-2-feniletil)-1,2- diidropiridina-3-carboxilato de etilaUma mistura do composto do Exemplo de Referência 31 (9,00g, 41,7 mmol), carbonato de potássio (17,3 g, 125 mmol), brometo de fenacila (16,6 g, 83,5 mmol) e DMF (100 ml) foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi despejada em água (100 ml), e a mistura foi extraída com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=1/9 - 7/3) dando o composto titular (3,18 g, 23 %) como um pó branco.
[00425] RMN 1H (300 MHz, DMSO-d6) δ:1,25 (3H, t, J = 7,0 Hz), 2,30 (3H, s), 4,25 (2H, q, J = 7,0 Hz), 5,63 (2H, s), 6,54 (1H, d, J = 0,6 Hz), 7,61 (2H, t, J = 7,5 Hz), 7,72-7,78 (1H, m), 8,07-8,10 (2H, m).Exemplo de Referência 33
[00426] Produção de 3-hidróxi-1,6-dimetil-4-oxo-5-(2-oxo-2-feniletil)- 4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaUma mistura do composto do Exemplo de Referência 32 (2,00g, 5,99 mmol), cloridrato de etil éster de sarcosina (1,84 g, 12,0 mmol), trietilamina (4,98 ml, 36,0 mmol) e etanol (20 ml) foi agitada a 80°C durante 15 h, adicionou-se uma solução a 20 % (3,5 ml) de etóxido de sódio em etanol, e a mistura foi agitada a 100°C durante 24 h. Após resfriamento, a mistura de reação foi diluída com água (50 ml), adicionou-se ácido clorídrico 6N para ajustar o pH em de 3 a 4, e a mistura foi agitada durante 30 min. O sólido precipitado foi recolhido por meio de filtração, e lavado com água e acetato de etila/THF dando o composto titular (1,50 g, 68 %) como um pó branco.
[00427] RMN 1H (300 MHz, DMSO-d6) δ:1,31 (3 H, t, J=7,1 Hz), 2,26 (3 H, s), 3,77 (3 H, s), 4,30 (2 H, q, J=7,0 Hz), 5,57 (2 H, s), 6,52 (1 H, s), 7,54-7,67 (2 H, m), 7,69-7,79 (1 H, m), 8,03-8,18 (2 H, m), 8,90 (1 H, s).Exemplo de Referência 34
[00428] Produção de 3-metóxi-1,6-dimetil-4-oxo-5-(2-oxo-2-feniletil)- 4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 6, o composto titular (390 mg, 26 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 33 (1,45 g, 3,94 mmol), DBU (882 ml, 5,90 mmol) e iodometano (367 ml, 5,90 mmol).
[00429] RMN 1H (300 MHz, DMSO-d6) δ:1,30 (3 H, t, J=7,1 Hz), 2,28 (3 H, s), 3,81 (3 H, s), 3,86 (3 H, s), 4,27 (2 H, q, J=7,0 Hz), 5,60 (2 H, s), 6,59 (1 H, s), 7,54-7,66 (2 H, m), 7,69-7,79 (1 H, m), 8,05-8,16 (2 H, m).Exemplo de Referência 35
[00430] Produção de ácido 3-metóxi-1,6-dimetil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 7, o composto titular (305 mg, 89 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 34 (370 mg, 0,968 mmol), solução aquosa de hidróxido de sódio 8N (1 ml) e etanol (7 ml).
[00431] RMN 1H (300 MHz, DMSO-d6) δ:2,28 (3 H, s), 3,81 (3 H, s), 3,86 (3 H, s), 5,60 (2 H, s), 6,58 (1 H, s), 7,61 (2 H, t, J=7,4 Hz), 7,74 (1 H, t, J=7,3 Hz), 8,11 (2 H, d, J=7,7 Hz), 12,50 (1 H, br s).Exemplo de Referência 36
[00432] Produção de (2Z)-3-aminapenta-2-enoato de metilaUma mistura de 3-oxovalerato de metila (75,0 g, 576 mmol), acetato de amônio (222 g, 2,88 mol) e metanol (750 ml) foi agitada à temperatura ambiente durante 3 dias. A mistura foi concentrada sob pressão reduzida, adicionou-se água (500 ml) ao resíduo e a mistura foi extraída com acetato de etila (200 ml). O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, concentrado sob pressão reduzida, e secado dando o composto titular (68,5 g, 92 %) como um óleo amarelo claro.
[00433] RMN 1H (300 MHz, DMSO-d6) δ:1,06 (3 H, t, J=7,6 Hz), 2,09(2 H, q, J=7,6 Hz), 3,49 (3 H, s), 4,34 (1 H, s), 6,94 (1 H, s), 7,72 (1 H, br s). Exemplo de Referência 37
[00434] Produção de carboxilato de etilaA uma solução do composto do Exemplo de Referência 36 (50,0 g, 387 mmol) e dietil malonato (58,8 ml, 387 mmol) em etanol (400 ml) adicionou-se uma solução a 20 % (133 g) de etóxido de sódio em etanol, e a mistura foi agitada a 150°C durante 15 h enquanto se evaporava etanol. Após resfriamento, o sólido obtido foi recolhido por meio de filtração, lavado com acetato de etila, e dissolvido em água. Material insolúvel foi removido por filtração, o filtrado foi acidificado com ácido clorídrico 5N, e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água e acetato de etila-hexano dando o composto titular (36,4 g, 45 %) como um pó branco.
[00435] RMN 1H (300 MHz, DMSO-d6) δ: 1,12 (3 H, t, J=7,6 Hz), 1,26 (3 H, t, J=7,1 Hz), 2,42 (2 H, q, J=7,6 Hz), 4,25 (2 H, q, J=7,0 Hz), 5,79 (1 H, s), 11,37 (1 H, brs), 12,57 (1 H, s).Exemplo de Referência 38
[00436] Produção de carboxilato de etilaUma mistura do composto do Exemplo de Referência 37 (15,0 g, 71,0 mmol) e oxicloreto de fósforo (19,9 ml, 213 mmol) foi agitada a 80°C durante 30 min. A mistura foi concentrada sob pressão reduzida, adicionou-se água gelada ao resíduo, e o sólido precipitado foi recolhido por meio de filtração, e lavado com água e acetato de etila dando o composto titular (9,80 g, 60 %) como um sólido branco.
[00437] RMN 1H (300 MHz, DMSO-d6) δ: 1,15 (3 H, t, J=7,5 Hz), 1,26 (3 H, t, J=7,0 Hz), 2,44-2,55 (2 H, m), 4,25 (2 H, q, J=7,1 Hz), 6,26 (1 H, s), 12,28 (1 H, s).Exemplo de Referência 39
[00438] Produção de 4-cloro-6-etil-2-oxo-1-(2-oxo-2-feniletil)-1,2- diidropiridina-3-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 32, o composto titular (1,00 g, 7 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 38 (9,50 g, 41,4 mmol), carbonato de potássio (13,7 g, 99,2 mmol), brometo de fenacila (9,88 g, 49,6 mmol) e DMF (100 ml).
[00439] RMN 1H (300 MHz, DMSO-d6) δ:1,14 (3 H, t, J=7,4 Hz), 1,24 (3 H, t, J=7,1 Hz), 2,62 (2 H, q, J=7,4 Hz), 4,25 (2 H, q, J=7,1 Hz), 5,61 (2 H, s), 6,44 (1 H, s), 7,54-7,66 (2 H, m), 7,70-7,79 (1 H, m), 8,05-8,13 (2 H, m).Exemplo de Referência 40
[00440] Produção de 6-etil-3-hidróxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaUma mistura do composto do Exemplo de Referência 39 (950 mg, 2,73 mmol), cloridrato de etil éster de sarcosina (839 mg, 5,46 mmol), trietilamina (2,27 ml, 16,4 mmol) e etanol (10 ml) foi agitada a 80°C durante 10 h, adicionou-se mais trietilamina (2,27 ml, 16,4 mmol), e a mistura foi agitada a 100°C durante 15 h. Após resfriamento, adicionou-se água à mistura de reação, e a mistura foi acidificada com ácido clorídrico 1N e extraída com acetato de etila. O extrato foi lavado sucessivamente com água e salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em sílica-gel (eluado; acetato de etila/metanol=10/1) dando o composto titular (698 mg, 67 %) como um sólido castanho.
[00441] RMN 1H (300 MHz, DMSO-d6) δ:1,18 (3 H, t, J=7,4 Hz), 1,31 (3 H, t, J=7,1 Hz), 2,56 (2 H, q, J=7,6 Hz), 3,80 (3 H, s), 4,30 (2 H, q, J=7,2 Hz), 5,55 (2 H, s), 6,43 (1 H, s), 7,60 (2 H, t, J=7,6 Hz), 7,68-7,79 (1 H, m), 8,00-8,21 (2 H, m), 8,90 (1 H, s).Exemplo de Referência 41
[00442] Produção de 6-etil-3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etila Da mesma maneira que no Exemplo de Referência 6, o composto titular (156 mg, 23 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 40 (650 mg, 1,70 mmol).
[00443] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3 H, t, J=7,3 Hz), 1,30 (3 H, t, J=7,1 Hz), 2,58 (2 H, q, J=7,4 Hz), 3,84 (3 H, s), 3,85 (3 H, s), 4,27 (2 H, q, J=7,0 Hz), 5,58 (2 H, s), 6,50 (1 H, s), 7,61 (2 H, t, J=7,6 Hz), 7,67-7,82 (1 H, m), 8,03-8,19 (2 H, m).Exemplo de Referência 42
[00444] Produção de ácido 6-etil-3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 7, o composto titular (110 mg, 79 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 41 (150 mg, 0,378 mmol).
[00445] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3 H, t, J=7,3 Hz), 2,57 (2 H, q, J=7,3 Hz), 3,84 (3 H, s), 3,85 (3 H, s), 5,58 (2 H, s), 6,48 (1 H, s), 7,61 (2 H, t, J=7,6 Hz), 7,67-7,86 (1 H, m), 7,97-8,31 (2 H, m), 12,51 (1 H, br s).Exemplo de Referência 43
[00446] Produção de 3-etóxi-1,6-dimetil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 6, o composto titular (560 mg, 52 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 33 (1,00 g, 2,71 mmol) e iodoetano (326 ml, 4,07 mmol).
[00447] RMN 1H (300 MHz, DMSO-d6) δ:1,24 (3 H, t, J=7,0 Hz), 1,30 (3 H, t, J=7,1 Hz), 2,28 (3 H, s), 3,81 (3 H, s), 4,15 (2 H, q, J=7,0 Hz), 4,26 (2 H, q, J=7,1 Hz), 5,60 (2 H, s), 6,58 (1 H, s), 7,61 (2 H, t, J=7,6 Hz), 7,69-7,78 (1 H, m), 8,06-8,14 (2 H, m).Exemplo de Referência 44
[00448] Produção de ácido 3-etóxi-1,6-dimetil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílico Me CO2HDa mesma maneira que no Exemplo de Referência 7, o composto titular (380 mg, 74 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 43 (550 mg, 1,39 mmol).
[00449] RMN 1H (300 MHz, DMSO-d6) δ:1,22 (3 H, t, J=7,0 Hz), 2,28 (3 H, s), 3,81 (3 H, s), 4,16 (2 H, q, J=7,0 Hz), 5,60 (2 H, s), 6,57 (1 H, s), 7,61 (2 H, t, J=7,6 Hz), 7,69-7,79 (1 H, m), 8,03-8,16 (2 H, m), 12,38 (1 H, br s).Exemplo de Referência 45
[00450] Produção de 1,6-dimetil-4-oxo-5-(2-oxo-2-feniletil)-3-propóxi-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 6, o composto titular (152 mg, 18 %) foi obtido como um pó branco a partir do composto (750 mg, 2,04 mmol) do Exemplo de Referência 33 e 1- bromopropano (277 ml, 3,05 mmol).
[00451] RMN 1H (300 MHz, DMSO-d6) δ:0,94 (3 H, t, J=7,5 Hz), 1,30(3 H, t, J=7,1 Hz), 1,57-1,73 (2 H, m), 2,28 (3 H, s), 3,80 (3 H, s), 4,08 (2 H, t, J=6,5 Hz), 4,26 (2 H, q, J=7,1 Hz), 5,60 (2 H, s), 6,58 (1 H, s), 7,56-7,66 (2H, m), 7,69-7,78 (1 H, m), 8,06-8,15 (2 H, m).Exemplo de Referência 46
[00452] Produção de ácido 1,6-dimetil-4-oxo-5-(2-oxo-2-feniletil)-3-propóxi-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 7, o composto titular (105 mg, 81 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 45 (140 mg, 0,341 mmol).
[00453] RMN 1H (300 MHz, DMSO-d6) δ:0,88-0,94 (3 H, m), 1,581,67 (2 H, m), 2,27 (3 H, s), 3,81 (3 H, s), 4,08 (2 H, t, J=6,6 Hz), 5,60 (2 H, s), 6,57 (1 H, s), 7,55-7,65 (2 H, m), 7,69-7,77 (1 H, m), 8,06-8,14 (2 H, m).Exemplo de Referência 47
[00454] Produção de 6-etil-3-etóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaUma mistura do composto do Exemplo de Referência 40 (330 mg, 0,863 mmol), carbonato de potássio (715 mg, 5,18 mmol), iodoetano (138 ml, 1,73 mmol) e DMF (5 ml) foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com água, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura saturada, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi recolhido por meio de filtração, e secado dando o composto titular (189 mg, 46 %) como um pó branco.
[00455] RMN 1H (300 MHz, DMSO-d6) δ:1,13-1,35 (9 H, m), 2,57 (2 H, q, J=7,2 Hz), 3,84 (3 H, s), 4,10-4,19 (2 H, m), 4,26 (2 H, q, J=7,2 Hz), 5,58 (2 H, s), 6,49 (1 H, s), 7,61 (2 H, t, J=7,6 Hz), 7,70-7,77 (1 H, m), 8,078,14 (2 H, m).Exemplo de Referência 48
[00456] Produção de ácido 3-etóxi-6-etil-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoUma solução do composto do Exemplo de Referência 47 (160 mg, 0,390 mmol) e solução aquosa de hidróxido de sódio 8N (1 ml) em etanol (7 ml) foi agitada a 60°C durante 1 h. A mistura de reação foi diluída com água, acidificada com ácido clorídrico 6N, e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água, e secado sob pressão reduzida dando o composto titular (74,0 mg, 50 %) como um pó branco.
[00457] RMN 1H (300 MHz, DMSO-d6) δ:1,13-1,25 (6 H, m), 2,57 (2 H, q, J=7,3 Hz), 3,84 (3 H, s), 4,15 (2 H, q, J=7,0 Hz), 5,57 (2 H, s), 6,47 (1 H, s), 7,61 (2 H, t, J=7,5 Hz), 7,69-7,78 (1 H, m), 8,08-8,15 (2 H, m), 12,35 (1 H, br s).Exemplo de Referência 49
[00458] Produção de 1,6-dimetil-4-oxo-5-(2-oxo-2-feniletil)-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaUma mistura do composto do Exemplo de Referência 33 (750 mg, 2,04 mmol), 1,1,1-trifluoro-2-iodoetano (603 ml, 6,12 mmol), fluoreto de potássio (119 mg, 2,04 mmol) e sulfóxido de dimetila (10 ml) foi agitada a 100°C durante 15 h. A mistura de reação foi diluída com água, e a mistura foi extraída com acetato de etila. O extrato foi lavado com salmoura saturada, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila) dando o composto titular (125 mg, 14 %) como um sólido branco.
[00459] RMN 1H (300 MHz, DMSO-d6) δ:1,28 (3 H, t, J=7,2 Hz), 2,30 (3 H, s), 3,83 (3 H, s), 4,19-4,31 (2 H, m), 4,84 (2 H, q, J=9,3 Hz), 5,64 (2 H, s), 6,66 (1 H, s), 7,57-7,66 (2 H, m), 7,69-7,79 (1 H, m), 8,07-8,15 (2 H, m). Exemplo de Referência 50
[00460] Produção de ácido 1,6-dimetil-4-oxo-5-(2-oxo-2-feniletil)-3- (2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoUma solução do composto do Exemplo de Referência 49 (110 mg, 0,244 mmol) e solução aquosa de hidróxido de sódio 8N (1 ml) em etanol (7 ml) foi agitada a 60°C durante 1 h. A mistura de reação foi diluída com água e acidificada com ácido clorídrico 6N, e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água, e secado sob pressão reduzida dando o composto titular (78,0 mg, 76 %) como um pó branco.
[00461] RMN 1H (300 MHz, DMSO-d6) δ:2,29 (3 H, s), 3,83 (3 H, s), 4,82 (2 H, q, J=9,3 Hz), 5,63 (2 H, s), 6,64 (1 H, s), 7,61 (2 H, t, J=7,6 Hz), 7,70-7,78 (1 H, m), 8,07-8,15 (2 H, m), 12,57 (1 H, br s).Exemplo de Referência 51
[00462] Produção de (2Z)-3-aminahex-2-enoato de etilaDa mesma maneira que no Exemplo de Referência 36, o composto titular (109 g, quant.) foi obtido como um óleo amarelo claro de 3- oxoexanoato de etila (100 g, 632 mmol), acetato de amônio (244 g, 3,16 mmol) e metanol (750 ml).
[00463] RMN 1H (300 MHz, DMSO-d6) δ:0,87 (3 H, t, J=7,4 Hz), 1,11-1,17 (3 H, m), 1,42-1,58 (2 H, m), 2,00-2,07 (2 H, m), 3,96 (2 H, q, J=7,2 Hz), 4,30 (1 H, s), 6,90 (1 H, br s), 7,73 (1 H, br s).Exemplo de Referência 52
[00464] Produção de 4-hidróxi-2-oxo-6-n-propil-1,2-diidropiridina-3- carboxilato de etilaDa mesma maneira que no Exemplo de Referência 37, o composto titular (27,5 g, 34 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 51 (50,0 g, 0,387 mmol), dietil malonato (58,8 ml, 387 mmol) e etanol (400 ml).
[00465] RMN 1H (300 MHz, DMSO-d6) δ:0,87 (3 H, t, J=7,4 Hz), 1,26 (3 H, t, J=7,2 Hz), 1,49-1,65 (2 H, m), 2,38 (2 H, t), 4,25 (2 H, q, J=7,0 Hz), 5,79 (1 H, s), 11,37 (1 H, s), 12,56 (1 H, s).Exemplo de Referência 53
[00466] Produção de 4-cloro-2-oxo-6-propil-1,2-diidropiridina-3-carboxilato de etilaUma mistura do composto do Exemplo de Referência 52 (37,0 g, 164 mmol) e oxicloreto de fósforo (45,9 ml, 493 mmol) foi agitada a 80°C durante 30 min. A mistura foi concentrada sob pressão reduzida, e adicionou- se água gelada ao resíduo. O sólido precipitado foi recolhido por meio de filtração, e lavado com água e acetato de etila dando o composto titular (17,6 g, 44 %) como um sólido branco.
[00467] RMN 1H (300 MHz, DMSO-d6) δ:0,87 (3 H, t, J=7,4 Hz), 1,26 (3 H, t, J=7,1 Hz), 1,52-1,65 (2 H, m), 2,40-2,48 (2 H, m), 4,25 (2 H, q, J=7,1 Hz), 6,27 (1 H, s), 12,17 (1 H, br s).Exemplo de Referência 54
[00468] Produção de 4-cloro-2-oxo-1-(2-oxo-2-feniletil)-6-propil-1,2- diidropiridina-3-carboxilato de etila Da mesma maneira que no Exemplo de Referência 4, o composto titular (7,15 g, 28 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 53 (17,0 g, 69,8 mmol), hidreto de sódio (60 % em óleo, 3,07 g, 76,7 mmol), brometo de fenacila (16,7 g, 83,8 mmol) e DMF (150 ml).
[00469] RMN 1H (300 MHz, DMSO-d6) δ:0,91 (3 H, t, J=7,3 Hz), 1,24 (3 H, t, J=7,1 Hz), 1,47-1,64 (2 H, m), 2,55-2,66 (2 H, m), 4,24 (2 H, q, J=7,1 Hz), 5,59 (2 H, s), 6,47 (1 H, s), 7,61 (2 H, t, J=7,6 Hz), 7,70-7,80 (1 H, m), 8,06-8,17 (2 H, m).Exemplo de Referência 55
[00470] Produção de 3-hidróxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-6- propil-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaUma mistura do composto do Exemplo de Referência 54 (7,00 g, 19,3 mmol), cloridrato de etil éster de sarcosina (5,94 g, 38,7 mmol), trietilamina (29,7 ml, 193 mmol) e etanol (100 ml) foi agitada durante 2 dias em condições de refluxo. A mistura foi concentrada sob pressão reduzida, adicionou-se água (200 ml) ao resíduo, e a mistura foi acidificada com ácido clorídrico 5N (3 ml). O sólido precipitado foi recolhido por meio de filtração, e lavado com água e hexano-acetato de etila dando o composto titular (5,70 g, 74 %) como um sólido branco.
[00471] RMN 1H (300 MHz, DMSO-d6) δ:0,92 (3 H, t, J=7,3 Hz), 1,31 (3 H, t, J=7,1 Hz), 1,50-1,65 (2 H, m), 2,49-2,57 (2 H, m), 3,78 (3 H, s), 4,30 (2 H, q, J=7,1 Hz), 5,52 (2 H, s), 6,45 (1 H, s), 7,60 (2 H, t, J=7,5 Hz), 7,687,78 (1 H, m), 8,07-8,15 (2 H, m), 8,90 (1 H, br s).Exemplo de Referência 56
[00472] Produção de 3-etóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-6- propil-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaUma mistura do composto do Exemplo de Referência 55 (1,00 g, 8,08 mmol), dietila sulfato (397 ml, 3,03 mmol), carbonato de potássio (1,05 g, 7,57 mmol) e acetona (20 ml) foi agitada durante 15 h em condições de refluxo. Adicionou-se água (30 ml) à mistura, e o sólido precipitado foi recolhido por meio de filtração, e lavado com água e acetato de etila-hexano dando o composto titular (876 mg, 82 %) como um sólido branco.
[00473] RMN 1H (300 MHz, DMSO-d6) δ:0,93 (3 H, t, J=7,4 Hz), 1,23 (3 H, t, J=7,0 Hz), 1,30 (3 H, t, J=7,1 Hz), 1,52-1,66 (2 H, m), 2,51-2,58 (2 H, m), 3,83 (3 H, s), 4,14 (2 H, q, J=7,1 Hz), 4,26 (2 H, q, J=7,1 Hz), 5,54 (2 H, s), 6,51 (1 H, s), 7,61 (2 H, t, J=7,6 Hz), 7,69-7,77 (1 H, m), 8,08-8,15 (2 H, m).Exemplo de Referência 57Produção de ácido 3-etóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-6-propil-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílico
[00474] Uma solução do composto do Exemplo de Referência 56 (850 mg, 2,00 mmol) e solução aquosa de hidróxido de sódio 8N (2 ml) em etanol (14 ml) foi agitada a 60°C durante 30 min. A mistura de reação foi diluída com água, acidificada com ácido clorídrico 5N, e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água, e secado sob pressão reduzida dando o composto titular (705 mg, 89 %) como um pó branco.
[00475] RMN 1H (300 MHz, DMSO-d6) δ:0,93 (3 H, t, J=7,4 Hz), 1,21 (3 H, t, J=7,0 Hz), 1,50-1,66 (2 H, m), 2,50-2,58 (2 H, m), 3,83 (3 H, s), 4,15 (2 H, q, J=7,1 Hz), 5,54 (2 H, s), 6,50 (1 H, s), 7,61 (2 H, t, J=7,6 Hz), 7,697,78 (1 H, m), 8,08-8,16 (2 H, m), 12,42 (1 H, br s).Exemplo de Referência 58
[00476] Produção de 6-etil-3-(2-fluoroetóxi)-1-metil-4-oxo-5-(2-oxo- 2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 6, o composto titular (649 mg, 77 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 40 (750 mg, 1,96 mmol), DBU (440 ml, 2,94 mmol) e 1-fluoro-2-iodoetano (512 mg, 2,94 mmol).
[00477] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3 H, t, J=7,3 Hz), 1,30 (3 H, t, J=7,1 Hz), 2,58 (2 H, q, J=7,3 Hz), 3,85 (3 H, s), 4,26 (2 H, q, J=7,1 Hz), 4,32-4,36 (1 H, m), 4,42-4,47 (1 H, m), 4,53-4,59 (1 H, m), 4,69-4,75 (1 H, m), 5,58 (2 H, s), 6,51 (1 H, s), 7,61 (2 H, t, J=7,6 Hz), 7,70-7,77 (1 H, m), 8,08-8,14 (2 H, m).Exemplo de Referência 59
[00478] Produção de ácido 6-etil-3-(2-fluoroetóxi)-1-metil-4-oxo-5-(2- oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoUma solução do composto do Exemplo de Referência 58 (620 mg, 1,45 mmol) e solução aquosa de hidróxido de sódio 8N (1 ml) em etanol (7 ml) foi agitada a 60°C durante 30 min. A mistura de reação foi diluída com água, acidificado com ácido clorídrico 5N, e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água, e secado sob pressão reduzida dando o composto titular (470 mg, 56 %) como um pó branco.
[00479] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3 H, t, J=7,4 Hz), 2,58 (2 H, q, J=7,4 Hz), 3,85 (3 H, s), 4,32-4,36 (1 H, m), 4,42-4,47 (1 H, m), 4,544,59 (1 H, m), 4,70-4,74 (1 H, m), 5,58 (2 H, s), 6,50 (1 H, s), 7,61 (2 H, t, J=7,6 Hz), 7,70-7,77 (1 H, m), 8,09-8,15 (2 H, m), 12,48 (1 H, br s).Exemplo de Referência 60
[00480] Produção de 6-etil-1-metil-4-oxo-5-(2-oxo-2-feniletil)-3- (2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaUma mistura do composto do Exemplo de Referência 40 (1,00 g, 2,61 mmol), 1,1,1-trifluoro-2-iodoetano (1,29 ml, 13,1 mmol), carbonato de césio (4,27 g, 13,1 mmol) e sulfóxido de dimetila (10 ml) foi agitada a 100°C durante 5 h. A mistura de reação foi filtrada, o filtrado foi diluída com ácido clorídrico 1N (30 ml), e a mistura foi extraída com acetato de etila. O extrato foi lavado com água e salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; hexano/acetato de etila=9/1 - 0/10) dando o composto titular (278 mg, 23 %) como um sólido branco.
[00481] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3 H, t, J=7,4 Hz), 1,28 (3 H, t, J=7,1 Hz), 2,59 (2 H, q, J=7,4 Hz), 3,86 (3 H, s), 4,26 (2 H, q, J=7,1 Hz), 4,83 (2 H, q, J=9,3 Hz), 5,62 (2 H, s), 6,56 (1 H, s), 7,61 (2 H, t, J=7,5 Hz), 7,70-7,78 (1 H, m), 8,08-8,14 (2 H, m).Exemplo de Referência 61
[00482] Produção de ácido 6-etil-1-metil-4-oxo-5-(2-oxo-2-feniletil)-3- (2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoUma solução do composto do Exemplo de Referência 60 (270 mg, 0,581 mmol) e solução aquosa de hidróxido de sódio 8N (1 ml) em etanol (7 ml) foi agitada a 60°C durante 1 h. A mistura de reação foi diluída com água, acidificada com ácido clorídrico 5N, e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água, e secado sob pressão reduzida dando o composto titular (235 mg, 93 %) como um pó branco.
[00483] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3 H, t, J=7,4 Hz), 2,58 (2 H, q, J=7,4 Hz), 3,86 (3 H, s), 4,82 (2 H, q, J=9,2 Hz), 5,61 (2 H, s), 6,54 (1 H, s), 7,61 (2 H, t, J=7,6 Hz), 7,70-7,77 (1 H, m), 8,07-8,16 (2 H, m), 12,74 (1 H, br s).Exemplo de Referência 62
[00484] Produção de 4-cloro-2-oxo-1,2,5,6,7,8-hexaidroquinolina-3- carboxilato de etilaUma mistura de 4-hidróxi-2-oxo-1,2,5,6,7,8- hexaidroquinolina-3-carboxilato de etila (26,0 g, 110 mmol) e oxicloreto de fósforo (51,3 ml) foi agitada a 130°C durante 1,5 h. Após resfriamento, a mistura de reação foi concentrada sob pressão reduzida, e adicionou-se gelo ao resíduo. A mistura foi neutralizada com solução saturada de hidrogenocarbonato de sódio, e extraída com acetato de etila. O extrato foi lavado sucessivamente com solução saturada de hidrogenocarbonato de sódio, água e salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi recolhido por meio de filtração, e lavado com acetato de etila-hexano dando o composto titular (4,65 g, 17 %) como um sólido branco.
[00485] RMN 1H (300 MHz, DMSO-d6) δ:1,25 (3 H, t, J=7,1 Hz),1,61-1,74 (4 H, m), 2,37-2,45 (2 H, m), 2,51-2,57 (2 H, m), 4,24 (2 H, q, J=7,2 Hz), 12,09 (1 H, s).Exemplo de Referência 63
[00486] Produção de 4-cloro-2-oxo-1-(2-oxo-2-feniletil)-1,2,5,6,7,8- hexaidroquinolina-3-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 4, o composto titular (710 mg, 16 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 62 (3,00 g, 11,7 mmol), hidreto de sódio (60 % em óleo, 516 mg, 12,9 mmol) e brometo de fenacila (2,57 g, 12,9 mmol).
[00487] RMN 1H (300 MHz, DMSO-d6) δ:1,25 (3H, t, J = 7,1 Hz), 1,60-1,80 (4H, m), 2,50-2,65 (4H, m), 4,26 (2H, q, J = 7,1 Hz), 5,66 (2H, s), 7,61 (2H, t, J = 7,4 Hz), 7,74 (1H, t, J = 7,4 Hz), 8,09 (2H, d, J = 7,4 Hz).Exemplo de Referência 64
[00488] Produção de 3-hidróxi-4-oxo-5-(2-oxo-2-feniletil)-4,5,6,7,8,9- hexaidrotieno[3,2-c]quinolina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 5, o composto titular (751 mg, 100 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 63 (690 mg, 1,85 mmol), solução a 20 % (1,26 g, 3,69 mmol) de etóxido de sódio em etanol, tioglicolato de etila (486 ml, 4,43 mmol) e etanol (15 ml).
[00489] RMN 1H (300 MHz, DMSO-d6) δ:1,29 (3H, t, J = 7,0 Hz), 1,65-1,85 (4H, m), 2,50-2,65 (4H, m), 4,28 (2H, q, J = 7,0 Hz), 5,72 (2H, s), 7,62 (2H, t, J = 7,7 Hz), 7,73-7,78 (1H, m), 8,10-8,13 (2H, m), 10,39 (1H, s).Exemplo de Referência 65
[00490] Produção de 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5,6,7,8,9- hexaidrotieno[3,2-c]quinolina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 6, o composto titular (238 mg, 31 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 64 (740 mg, 1,80 mmol), iodometano (168 ml, 2,70 mmol), DBU (404 ml, 2,70 mmol) e DMF (15 ml).
[00491] RMN 1H (300 MHz, DMSO-d6) δ:1,31 (3H, t, J = 7,0 Hz), 1,65-1,85 (4H, m), 2,45-2,65 (4H, m), 3,89 (3H, s), 4,29 (2H, q, J = 7,0 Hz),5,67 (2H, s), 7,62 (2H, t, J = 7,4 Hz), 7,75 (1H, t, J = 7,4 Hz), 8,11 (2H, d, J = 7,4 Hz).Exemplo de Referência 66
[00492] Produção de ácido 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5,6,7,8,9-hexaidrotieno[3,2-c]quinolina-2-carboxílicoUma solução do composto do Exemplo de Referência 65 (220mg, 0,517 mmol) e solução aquosa de hidróxido de sódio 8N (1 ml) em etanol (7 ml) foi agitada a 60°C durante 1 h. A mistura de reação foi acidificada com ácido clorídrico 6N (1,5 ml), e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água, e secado sob pressão reduzida dando o composto titular (162 mg, 79 %) como um pó branco.
[00493] RMN 1H (300 MHz, DMSO-d6) δ:1,66-1,88 (4H, m), 2,522,61 (4H, m), 3,86 (3H, s), 5,66 (2H, s), 7,62 (2H, t, J = 7,6 Hz), 7,70-7,79 (1H, m), 8,03-8,11 (2H, m), 13,12 (1H, s).Exemplo de Referência 67
[00494] Produção de 4-cloro-3-hidróxi-6-metiltieno[3,2-c]piridina-2- carboxilato de etilaA uma suspensão de 2,4-dicloro-6-metilpiridina-3-carboxilato de etila (10,0 g, 42,7 mmol) em acetonitrila (45 ml) adicionou-se carbonato de potássio (8,85 g, 64,1 mmol) e tioglicolato de etila (4,68 ml, 42,7 mmol), e a mistura foi agitada durante 15 h em condições de refluxo. A mistura de reação foi diluída com água (150 ml), adicionou-se ácido clorídrico 6N (15 ml) e a mistura foi agitada durante 30 min. O sólido precipitado foi recolhido por meio de filtração, lavado com água e etanol-éter de diisopropila (1/1), e secado sob pressão reduzida dando o composto titular (10,9 g, 94 %) como um pó branco.
[00495] RMN 1H (300 MHz, DMSO-d6) δ:1,32 (3H, t, J = 7,1 Hz), 2,54 (3H, s), 4,36 (2H, q, J = 7,1 Hz), 7,87 (1H, s), 10,75 (1H, s).Exemplo de Referência 68
[00496] Produção de 4-cloro-3-etóxi-6-metiltieno[3,2-c]piridina-2- carboxilato de etilaDa mesma maneira que no Exemplo de Referência 6, o composto titular (4,30 g, 78 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 67 (4,97 g, 18,3 mmol), DBU (4,10 ml, 27,4 mmol) e iodoetano (2,19 ml, 27,4 mmol).
[00497] RMN 1H (300 MHz, DMSO-d6) δ:1,33 (3H, t, J = 7,2 Hz), 1,43 (3H, t, J = 7,1 Hz), 2,54 (3H, s), 4,25 (2H, q, J = 7,0 Hz), 4,34 (2H, q, J = 7,1 Hz), 7,92 (1H, s).Exemplo de Referência 69
[00498] Produção de ácido 4-cloro-3-etóxi-6-metiltieno[3,2-c]piridina- 2-carboxílicoUma solução mista do composto do Exemplo de Referência 68 (4,30 g, 14,3 mmol) e solução aquosa de hidróxido de sódio 8N (15 ml) em THF (22 ml)-etanol (22 ml) foi agitada durante 5 h em condições de refluxo. A mistura de reação foi acidificada com ácido clorídrico 6N (22 ml) e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água, e secado sob pressão reduzida dando o composto titular (3,80 g, 97 %) como um pó branco.
[00499] RMN 1H (300 MHz, DMSO-d6) δ:1,40 (3H, t, J = 6,9 Hz), 2,54 (3H, s), 4,26 (2H, q, J = 6,9 Hz), 7,90 (1H, s), 13,65 (1H, s).Exemplo de Referência 70
[00500] Produção de 4-cloro-N-[2-(dietilamina)etil]-3-etóxi-N,6- dimetiltieno[3,2-c]piridina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular(800 mg, 59 %) foi obtido como um óleo incolor a partir do composto do Exemplo de Referência 69 (1,00 g, 3,68 mmol) e N,N-dietil-N’-metiletano- 1,2-diamina (773 ml, 4,78 mmol).
[00501] RMN 1H (300 MHz, DMSO-d6) δ:0,65-1,10 (6H, m), 1,33 (3H, t, J = 6,9 Hz), 2,20-2,70 (6H, m), 2,53 (3H, s), 3,04 (3H, s), 3,35-3,65 (2H, m), 4,05-4,20 (2H, m), 7,89 (1H, s).Exemplo de Referência 71
[00502] Produção de 4-cloro-3-hidróxi-6,7-dimetiltieno[3,2-c]piridina- 2-carboxilato de etilaUma solução a 20 % (1,73 g, 5,08 mmol) de etóxido de sódio em etanol foi diluída com etanol (5 ml), e adicionou-se tioglicolato de etila (610 mg, 5,08 mmol). Adicionou-se 2,4-dicloro-5,6-dimetilpiridina-3- carboxilato de etila (630 mg, 2,54 mmol) à mistura, e a mistura foi agitada à temperatura ambiente durante 18 h. Adicionou-se ácido clorídrico 2N (3 ml) à mistura de reação e a mistura foi repartida entre salmoura e acetato de etila. A camada orgânica foi secada sobre sulfato de magnésio e concentrada. O sólido obtido foi lavado com diisopropil éter-hexano, e secado sob pressão reduzida dando o composto titular (374 mg, 52 %) como um pó branco.
[00503] RMN 1H (300 MHz, CDCl3) δ:1,43 (3H, t, J = 7,2 Hz), 2,40 (3H, s), 2,61 (3H, s), 4,44 (2H, q, J = 7,2 Hz), 10,63 (1H, s).Exemplo de Referência 72
[00504] Produção de 4-cloro-3-etóxi-6,7-dimetiltieno[3,2-c]piridina-2- carboxilato de etilaDa mesma maneira que no Exemplo de Referência 6, o composto titular (350 mg, 91 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 71 (350 mg, 1,22 mmol), DBU (380 mg, 2,02 mmol) e iodoetano (315 mg, 2,02 mmol).
[00505] RMN 1H (300 MHz, CDCl3) δ:1,43 (3H, t, J = 7,2 Hz), 1,54 (3H, t, J = 7,2 Hz), 2,42 (3H, s), 2,60 (3H, s), 4,31 (2H, q, J = 7,2 Hz), 4,41 (2H, q, J = 7,2 Hz).Exemplo de Referência 73
[00506] Produção de ácido 4-cloro-3-etóxi-6,7-dimetiltieno[3,2- c]piridina-2-carboxílicoUma solução mista do composto do Exemplo de Referência 72 (250 mg, 0,80 mmol) e solução aquosa de hidróxido de sódio 4N (2 ml) em THF (2 ml)-etanol (1 ml) foi agitada à temperatura ambiente durante 18 h. A mistura de reação foi repartida entre ácido clorídrico 1N e acetato de etila, e a camada orgânica foi secada sobre sulfato de magnésio e concentrada sob pressão reduzida dando o composto titular (210 mg, 92 %) como um sólido branco.
[00507] RMN 1H (300 MHz, DMSO-d6) δ:1,40 (3H, t, J= 7,1 Hz), 2,40 (3H, s), 2,53 (3H, s), 4,25 (2H, q, J = 7,0 Hz).Exemplo de Referência 74
[00508] Produção de 4-cloro-N-[2-(dietilamina)etil]-3-etóxi-N,6,7- trimetiltieno[3,2-c]piridina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (230 mg, 79 %) foi obtido como um óleo incolor a partir do composto do Exemplo de Referência 73 (210 mg, 0,73 mmol) e N,N-dietil-N’-metiletano- 1,2-diamina (144 mg, 1,10 mmol).
[00509] RMN 1H (300 MHz, CDCl3) δ:0,80-1,10 (6H, m), 1,42 (3H, t, J = 6,9 Hz), 2,30-2,50 (5H, m), 2,60-2,80 (7H, m), 3,19 (3H, s), 3,45-3,70 (2H, m), 4,18 (2H, q, J = 7,0 Hz).Exemplo de Referência 75
[00510] Produção de 3-hidróxi-6-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrotieno[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 5, o composto titular (8,31 g, 88 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 32 (8,50 g, 25,5 mmol), tioglicolato de etila (6,70 ml, 61,1 mmol), uma solução a 20 % (17,4 g, 51,0 mmol) de etóxido de sódio em etanol e etanol (100 ml).
[00511] RMN 1H (300 MHz, DMSO-d6) δ:1,28 (3H, t, J=7,2 Hz), 2,33 (3H, s), 4,27 (2H, q, J=7,1 Hz), 5,71 (2H, s), 6,93 (1H, d, J=0,9 Hz), 7,62 (2H, t, J=7,5 Hz), 7,69-7,83 (1H, m), 8,01-8,21 (2H, m), 10,34 (1H, s).Exemplo de Referência 76
[00512] Produção de 3-metóxi-6-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]piridina-2-carboxilato de etilaUma mistura do composto do Exemplo de Referência 75 (3,00 g, 8,08 mmol), sulfato de dimetila (4,58 ml, 48,4 mmol), carbonato de potássio (3,35 g, 24,2 mmol) e acetona (60 ml) foi agitada durante 3 dias em condições de refluxo. Adicionou-se água (120 ml) à mistura, e o sólido precipitado foi recolhido por meio de filtração, e lavado com água, etanol e acetato de etila dando o composto titular (2,45 g, 79 %) como um sólido branco.
[00513] RMN 1H (300 MHz, DMSO-d6) δ:1,30 (3H, t, J=7,1 Hz), 2,31 (3H, s), 3,88 (3H, s), 4,28 (2H, q, J=7,2 Hz), 5,66 (2H, s), 6,85 (1H, d, J=0,8 Hz), 7,58-7,67 (2H, m), 7,70-7,80 (1H, m), 8,06-8,15 (2H, m).Exemplo de Referência 77
[00514] Produção de 3-etóxi-6-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrotieno[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 6, o composto titular (585 mg, 54 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 75 (1,00 g, 2,69 mmol), DBU (604 ml, 4,04 mmol) e iodoetano (323 ml, 4,04 mmol).
[00515] RMN 1H (300 MHz, DMSO-d6) δ:1,23-1,35 (6H, m), 2,31 (3H, s), 4,14 (2H, q, J=7,0 Hz), 4,27 (2H, q, J=7,1 Hz), 5,67 (2H, s), 6,84 (1H, d, J=0,8 Hz), 7,57-7,67 (2H, m), 7,71-7,79 (1H, m), 8,07-8,15 (2H, m).Exemplo de Referência 78
[00516] Produção de ácido 3-metóxi-6-metil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidrotieno[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 7, o composto titular (1,25 g, 67 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 76 (2,00 g, 5,19 mmol), solução aquosa de hidróxido de sódio 8N (3 ml) e etanol (21 ml).
[00517] RMN 1H (300 MHz, DMSO-d6) δ:2,31 (3H, m), 3,86 (3H, s), 5,66 (2H, s), 6,83 (1H, d, J=0,8 Hz), 7,58-7,68 (2H, m), 7,71-7,80 (1H, m), 8,08-8,17 (2H, m), 13,07 (1H, br s).Exemplo de Referência 79
[00518] Produção de ácido 3-etóxi-6-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 7, o composto titular (311 mg, 67 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 77 (500 mg, 1,25 mmol), solução aquosa de hidróxido de sódio 8N (1 ml) e etanol (7 ml).
[00519] RMN 1H (300 MHz, DMSO-d6) δ:1,27 (3H, t, J=7,0 Hz), 2,30 (3H, s), 4,14 (2H, q, J=7,0 Hz), 5,66 (2H, s), 6,82 (1H, s), 7,58-7,66 (2H, m), 7,71-7,79 (1H, m), 8,08-8,17 (2H, m), 13,05 (1H, br s).Exemplo de Referência 80
[00520] Produção de 4-hidróxi-1-metil-2-oxo-1,2-diidroquinolina-3- carboxilato de etilaA uma solução de dietil malonato (68,0 g, 0,425 mol) em DMF (400 ml) adicionou-se hidreto de sódio (66 % em óleo, 10,8 g, 0,30 mol) sob resfriamento com gelo, e a mistura foi agitada à mesma temperatura durante 5 min e à temperatura ambiente durante 15 min. Adicionou-se N- anidrido metilisatóico (50,8 g, 0,287 mol) à mistura obtida em pequenas porções, e a mistura foi agitada a 120°C durante 3 h. Adicionou-se diisopropil éter (500 ml) à mistura de reação, e o sólido precipitado foi recolhido por meio de filtração e lavado com diisopropil éter. O sólido obtido foi suspenso em uma mistura de metanol (250 ml) e água (500 ml), adicionou-se ácido clorídrico 5N (60 ml) por gotejamento, e a mistura foi extraída duas vezes com acetato de etila. A camada orgânica combinada foi lavada com água, e concentrada sob pressão reduzida. O resíduo foi lavado com diisopropil éter dando o composto titular (41,4 g, 58 %).
[00521] RMN 1H (300 MHz, CDCl3) δ:1,49 (3H, t, J = 7,1 Hz), 3,66 (3H, s), 4,51 (2H, q, J = 7,1 Hz), 7,23-7,30 (1H, m), 7,32 (1H, d, J = 8,7 Hz), 7,69 (1H, ddd, J = 8,7, 7,1, 1,6 Hz), 8,19 (1H, dd, J = 8,0, 1,6 Hz), 14,21 (1H, s).Exemplo de Referência 81
[00522] Produção de 4-cloro-1-metil-2-oxo-1,2-diidroquinolina-3- carboxilato de etilaUma mistura do composto do Exemplo de Referência 80 (58,0 g, 0,235 mol) e oxicloreto de fósforo (33 ml, 0,35 mol) foi agitada a 110°C durante 30 min. A mistura de reação foi concentrada sob pressão reduzida, e adicionou-se água gelada e acetato de etila. A camada orgânica foi separada, e a camada aquosa foi extraída com acetato de etila. A camada orgânica combinada foi lavada com água, solução de hidróxido de sódio 1N (3 vezes) e água, e concentrada sob pressão reduzida. O resíduo foi cristalizado de acetato de etila-éter de diisopropila dando o composto titular (47,7 g, 76 %).
[00523] RMN 1H (300 MHz, CDCl3) δ:1,42 (3H, t, J = 7,1 Hz), 3,73(3H, s), 4,48 (2H, q, J = 7,1 Hz), 7,35 (1H, ddd, J = 8,7, 7,1, 1,0 Hz), 7,40 (1H, d, J = 8,7 Hz), 7,68 (1H, ddd, J = 8,7, 7,1, 1,4 Hz), 8,07 (1H, dd, J = 8,0, 1,4 Hz).Exemplo de Referência 82
[00524] Produção de 3-hidróxi-5-metil-4-oxo-4,5-diidrotieno[3,2- c]quinolina-2-carboxilato de etilaUma solução a 20 % (23,2 g, 68 mmol) de etóxido de sódio em etanol foi diluída com etanol (70 ml), tioglicolato de etila (9,0 ml, 82 mmol) foi adicionada à solução obtida, e a mistura foi agitada à temperatura ambiente durante 10 min. O composto do Exemplo de Referência 81 (9,04 g, 34,0 mmol) foi adicionado a esta mistura, e a mistura foi agitada à temperatura ambiente durante 4 h. A mistura de reação foi neutralizada com água gelada e ácido clorídrico 2N (40 ml) sob resfriamento com gelo, e a mistura foi extraída duas vezes com clorofórmio. A camada orgânica combinada foi lavada com água e salmoura, secada sobre sulfato de sódio, filtrada, e concentrada sob pressão reduzida. O resíduo foi recristalizado de THF-éter de diisopropila dando o composto titular (9,12 g, 88 %).
[00525] RMN 1H (300 MHz, CDCl3) δ:1,42 (3H, t, J = 7,2 Hz), 3,76 (3H, s), 4,41 (2H, q, J = 7,2 Hz), 7,34 (1H, ddd, J = 7,9, 7,2, 0,8 Hz), 7,447,49 (1H, m), 7,63 (1H, ddd, J = 8,6, 7,2, 1,4 Hz), 7,83 (1H, dd, J = 7,9, 1,4 Hz), 10,76 (1H, s).Exemplo de Referência 83
[00526] Produção de 3-metóxi-5-metil-4-oxo-4,5-diidrotieno[3,2- c]quinolina-2-carboxilato de etilaA uma suspensão do composto do Exemplo de Referência 82 (3,04 g, 10,0 mmol) em DMF (30 ml) adicionou-se DBU (1,65 ml, 11 mmol), e adicionou-se iodometano (0,81 ml, 13 mmol) à solução obtida sob resfriamento com gelo. A mistura obtida foi agitada à temperatura ambiente durante 21 h, adicionou-se água e o sólido precipitado foi recolhido por meio de filtração. Isto foi dissolvido em etanol por meio de aquecimento, tratado com carvão ativado, filtrado, e concentrado sob pressão reduzida. O resíduo foi dissolvido em acetato de etila, e a mistura foi lavada com água e solução de hidróxido de sódio 0,5N, filtrada através de Celite (nome comercial), lavada adicionalmente duas vezes com água, e concentrada sob pressão reduzida. O resíduo foi recristalizado de etanol-éter de diisopropila dando o composto titular (1,51 g, 48 %).
[00527] RMN 1H (300 MHz, CDCl3) δ:1,42 (3H, t, J = 7,2 Hz), 3,76 (3H, s), 4,14 (3H, s), 4,40 (2H, q, J = 7,2 Hz), 7,24-7,31 (1H, m), 7,41 (1H, d, J = 8,7 Hz), 7,59 (1H, ddd, J = 8,7, 7,3, 1,5 Hz), 7,84 (1H, dd, J = 8,1, 1,5 Hz).Exemplo de Referência 84
[00528] Produção de ácido 3-metóxi-5-metil-4-oxo-4,5-diidrotieno [3,2-c]quinolina-2-carboxílicoA uma suspensão do composto do Exemplo de Referência 83 (1,90 g, 5,99 mmol) em THF (20 ml) e etanol (20 ml) adicionou-se solução de hidróxido de sódio 5N (2,4 ml, 12 mmol). A mistura obtida foi agitada à temperatura ambiente durante 1,5 h. Adicionou-se ácido clorídrico 1N (13 ml) à mistura de reação, e o sólido precipitado foi recolhido por meio de filtração, e recristalizado de metanol dando o composto titular (1,14 g, 66 %).
[00529] RMN 1H (300 MHz, DMSO-d6) δ:3,66 (3H, d, J = 1,1 Hz), 3,95 (3H, s), 7,30-7,37 (1H, m), 7,58-7,71 (2H, m), 7,94-8,00 (1H, m).Exemplo de Referência 85
[00530] Produção de 3-(benzilóxi)-5-metil-4-oxo-4,5-diidrotieno[3,2- c]quinolina-2-carboxilato de etilaA uma suspensão do composto do Exemplo de Referência 82 (1,00 g, 3,30 mmol) em DMF (10 ml) adicionou-se DBU (0,592 ml, 3,96 mmol), e adicionou-se brometo de benzila (0,510 ml, 4,29 mmol) à solução obtida. A mistura obtida foi agitada à temperatura ambiente durante 15 h. Adicionou-se acetato de etila e água à mistura de reação e a camada orgânica foi separada. A camada aquosa foi extraída duas vezes com acetato de etila. A camada orgânica combinada foi lavada com água e solução de hidróxido de sódio 0,5N, filtrada através de Celite (nome comercial), lavada adicionalmente com água, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia de coluna em sílica-gel (eluado; acetato de etila/hexano=1/4 - 1/2 - 2/1) dando o composto titular (980 mg, 75 %).
[00531] RMN 1H (300 MHz, CDCl3) δ:1,36 (3H, t, J = 7,2 Hz), 3,78 (3H, s), 4,36 (2H, q, J = 7,2 Hz), 5,34 (2H, s), 7,24-7,44 (5H, m), 7,59 (1H, ddd, J = 8,6, 7,1, 1,4 Hz), 7,63-7,69 (2H, m), 7,85 (1H, dd, J = 7,8, 1,4 Hz). Exemplo de Referência 86
[00532] Produção de 3-butóxi-5-metil-4-oxo-4,5-diidrotieno[3,2- c]quinolina-2-carboxilato de etilaA uma suspensão do composto do Exemplo de Referência 82 (1,00 g, 3,30 mmol) em DMF (10 ml) adicionou-se DBU (0,592 ml, 3,96 mmol), e adicionou-se 1-iodobutano (0,488 ml, 4,29 mmol) à solução obtida. A mistura obtida foi agitada à temperatura ambiente durante 15 h. Adicionou- se acetato de etila e água à mistura de reação, a camada orgânica foi separada, e a camada aquosa foi extraída duas vezes com acetato de etila. A camada orgânica combinada foi lavada com água e solução aquosa de hidróxido de sódio 0,5N, filtrada através de Celite (nome comercial), lavada adicionalmente com água, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia de coluna em sílica-gel (eluado; acetato de etila/hexano=1/4 - 1/2 - 2/1) dando o composto titular (1,05 g, 89 %).
[00533] RMN 1H (300 MHz, CDCl3) δ:1,01 (3H, t, J = 7,5 Hz), 1,42 (3H, t, J = 7,2 Hz), 1,50-1,66 (2H, m), 1,87-1,99 (2H, m), 3,74 (3H, s), 4,28 (2H, t, J = 6,6 Hz), 4,39 (2H, q, J = 7,2 Hz), 7,27 (1H, ddd, J = 8,0, 7,1, 0,9 Hz), 7,40 (1H, d, J = 8,1 Hz), 7,58 (1H, ddd, J = 8,6, 7,1, 1,4 Hz), 7,81-7,86 (1H, m).Exemplo de Referência 87
[00534] Produção de 5-metil-4-oxo-3-(piridin-4-ilmetóxi)-4,5- diidrotieno[3,2-c]quinolina-2-carboxilato de etilaA uma suspensão do composto do Exemplo de Referência 82 (1,00 g, 3,30 mmol) em DMF (20 ml) adicionou-se DBU (1,18 ml, 7,89 mmol), e adicionou-se cloridrato de 4-(clorometil)piridina (704 mg, 4,29 mmol) à solução obtida. A mistura obtida foi agitada à temperatura ambiente durante 18 h, a 45°C durante 2 h, e a 60°C durante 18 h. Adicionou-se DBU (1,18 ml, 7,89 mmol) e cloridrato de 4-(clorometil)piridina (704 mg, 4,29 mmol), e a mistura foi agitada a 60°C durante 10 h. Adicionou-se clorofórmio e água à mistura de reação, a camada orgânica foi separada, e a camada aquosa foi extraída com clorofórmio. A camada orgânica combinada foi lavada com água, e concentrada sob pressão reduzida. O resíduo foi cristalizado de acetato de etila-éter de diisopropila dando o composto titular (678 mg, 53 %).
[00535] RMN 1H (300 MHz, CDCl3) δ:1,35 (3H, t, J = 7,2 Hz), 3,77 (3H, s), 4,37 (2H, q, J = 7,2 Hz), 5,36 (2H, s), 7,27-7,34 (1H, m), 7,43 (1H, d, J = 8,4 Hz), 7,58-7,65 (3H, m), 7,86 (1H, dd, J = 7,8, 1,2 Hz), 8,61-8,65 (2H, m).Exemplo de Referência 88
[00536] Produção de 5-metil-3-(2-morfolin-4-iletóxi)-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxilato de etilaA uma suspensão do composto do Exemplo de Referência 82 (1,00 g, 3,30 mmol) em DMF (20 ml) adicionou-se DBU (1,18 ml, 7,89 mmol), e adicionou-se cloridrato de 4-(2-cloroetil)morfolina (798 mg, 4,29 mmol) à solução obtida. A mistura obtida foi agitada à temperatura ambiente durante 17 h. Adicionou-se clorofórmio e água à mistura de reação e a camada orgânica foi separada. A camada aquosa foi extraída com clorofórmio. A camada orgânica combinada foi lavada com água, e concentrada sob pressão reduzida. O resíduo foi recristalizado de acetato de etila-éter de diisopropila dando o composto titular (2,16 g, 85 %).
[00537] RMN 1H (300 MHz, CDCl3) δ:1,41 (3H, t, J = 7,1 Hz), 2,63 (4H, br t, J = 4,7 Hz), 2,96 (2H, t, J = 5,7 Hz), 3,72 (4H, br t, J = 4,7 Hz), 3,74 (3H, s), 4,38 (2H, q, J = 7,1 Hz), 4,43 (2H, t, J = 5,7 Hz), 7,24-7,31 (1H, m), 7,40 (1H, d, J = 8,5 Hz), 7,58 (1H, ddd, J = 8,5, 7,2, 1,5 Hz), 7,81-7,86 (1H, m).Exemplo de Referência 89
[00538] Produção de 5-metil-4-oxo-3-(tetraidrofuran-2-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxilato de etilaA uma suspensão do composto do Exemplo de Referência 82 (1,00 g, 3,30 mmol) em DMF (20 ml) adicionou-se DBU (0,740 ml, 4,95 mmol), e adicionou-se 2-(bromometil)tetraidrofurano (contendo 90 %) (0,617 ml, 4,9 mmol) à solução obtida. A mistura obtida foi agitada a 40°C durante 19 h e a 80°C durante 23 h, adicionou-se DBU (0,740 ml, 4,95 mmol) e 2- (bromometil)tetraidrofurano (contendo 90 %) (0,617 ml, 4,9 mmol), e a mistura foi agitada a 80°C durante 66 h. Adicionou-se acetato de etila e água à mistura de reação e a camada orgânica foi separada. A camada aquosa foi extraída com acetato de etila. A camada orgânica combinada foi lavada com solução aquosa de hidróxido de sódio 0,5N, filtrada através de Celite (nome comercial), lavada com água, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia de coluna em sílica-gel (eluado; acetato de etila/hexano=3/17 - 2/1) e cristalizado de acetato de etila-éter de diisopropila dando o composto titular (821 mg, 64 %).
[00539] RMN 1H (300 MHz, CDCl3) δ:1,42 (3H, t, J = 7,2 Hz), 1,842,19 (4H, m), 3,74 (3H, s), 3,76-3,85 (1H, m), 3,89-3,98 (1H, m), 4,22-4,49 (5H, m), 7,27 (1H, ddd, J = 8,0, 7,1, 1,0 Hz), 7,39 (1H, d, J = 8,1 Hz), 7,58 (1H, ddd, J = 8,6, 7,1, 1,4 Hz), 7,81-7,86 (1H, m).Exemplo de Referência 90
[00540] Produção de 3-(2-etoxietóxi)-5-metil-4-oxo-4,5-diidrotieno [3,2-c]quinolina-2-carboxilato de etila A uma suspensão do composto do Exemplo de Referência 82 (1,00 g, 3,30 mmol) em DMF (20 ml) adicionou-se DBU (1,48 ml, 9,90 mmol), e adicionou-se 1-bromo-2-etoxietano (1,12 ml, 9,93 mmol) à solução obtida. A mistura obtida foi agitada a 60°C durante 24 h. Adicionou-se acetato de etila e água à mistura de reação, a camada orgânica foi separada, e a camada aquosa foi extraída com acetato de etila. A camada orgânica combinada foi lavada com solução aquosa de hidróxido de sódio 0,5N, filtrada através de Celite (nome comercial), lavada adicionalmente com água, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia de coluna em sílica-gel (eluado; acetato de etila/hexano=1/4 - 1/1) e cristalizado de acetato de etila-hexano dando o composto titular (986 mg, 80 %).
[00541] RMN 1H (300 MHz, CDCl3) δ:1,19 (3H, t, J = 7,0 Hz), 1,43 (3H, t, J = 7,1 Hz), 3,59 (2H, q, J = 7,0 Hz), 3,74 (3H, s), 3,93 (2H, t, J = 5,0 Hz), 4,40 (2H, q, J = 7,1 Hz), 4,46 (2H, t, J = 5,0 Hz), 7,26-7,31 (1H, m), 7,40 (1H, d, J = 8,5 Hz), 7,58 (1H, ddd, J = 8,5, 7,2, 1,4 Hz), 7,84 (1H, dd, J = 8,0, 1,4 Hz).Exemplo de Referência 91
[00542] Produção de ácido 3-(benzilóxi)-5-metil-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxílicoA uma solução do composto do Exemplo de Referência 85 (867 mg, 2,20 mmol) em THF (7 ml) e etanol (7 ml) adicionou-se solução aquosa de hidróxido de sódio 5N (0,88 ml, 4,4 mmol). A mistura obtida foi agitada à temperatura ambiente durante 3 h. Adicionou-se ácido clorídrico 1N (5,0 ml) à mistura de reação, e o sólido precipitado foi recolhido por meio de filtração, lavado com água, e secado ao ar dando o composto titular (665 mg, 83 %).
[00543] RMN 1H (300 MHz, DMSO-d6) δ:3,69 (3H, s),5,22 (2H, s), 7,30-7,41 (4H, m), 7,57-7,72 (4H, m), 7,98 (1H, d, J = 8,1 Hz), 13,31 (1H, br s).Exemplo de Referência 92
[00544] Produção de ácido 3-butóxi-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxílicoA uma solução do composto do Exemplo de Referência 86(923 mg, 2,57 mmol) em THF (7 ml) e etanol (7 ml) adicionou-se solução aquosa de hidróxido de sódio 5N (1,0 ml, 5,0 mmol). A mistura obtida foi agitada à temperatura ambiente durante 3 h. Adicionou-se ácido clorídrico 1N (6,0 ml) à mistura de reação, e o sólido precipitado foi recolhido por meio de filtração, lavado com água, e secado ao ar dando o composto titular (872 mg, quantitativo).
[00545] RMN 1H (300 MHz, DMSO-d6) δ:0,94 (3H, t, J = 7,5 Hz), 1,41-1,55 (2H, m), 1,71-1,82 (2H, m), 3,65 (3H, s), 4,16 (2H, t, J = 6,6 Hz), 7,32 (1H, t, J = 7,2 Hz), 7,54-7,70 (2H, m), 7,91-7,98 (1H, m), 13,21 (1H, br s).Exemplo de Referência 93
[00546] Produção de ácido 5-metil-4-oxo-3-(piridin-4-ilmetóxi)-4,5- diidrotieno[3,2-c]quinolina-2-carboxílico A uma suspensão do composto do Exemplo de Referência 87 (723 mg, 1,83 mmol) em THF (6 ml) e etanol (6 ml) adicionou-se solução aquosa de hidróxido de sódio 5N (0,74 ml, 3,7 mmol). A mistura obtida foi agitada à temperatura ambiente durante 4 h. Adicionou-se ácido clorídrico 1N (3,7 ml) à mistura de reação e a mistura foi diluída com água. O sólido precipitado foi recolhido por meio de filtração, lavado com água, e secado ao ar dando o composto titular (424 mg, 63 %).
[00547] RMN 1H (300 MHz, DMSO-d6) δ:3,67 (3H, s), 5,28 (2H, s), 7,32-7,38 (1H, m), 7,59-7,72 (4H, m), 7,98 (1H, dd, J = 7,8, 1,2 Hz), 8,59 (2H, dd, J = 4,5, 1,5 Hz).Exemplo de Referência 94
[00548] Produção de ácido 5-metil-3-(2-morfolin-4-iletóxi)-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxílicoA uma suspensão do composto do Exemplo de Referência 88 (832 mg, 2,00 mmol) em THF (7 ml) e etanol (7 ml) adicionou-se solução aquosa de hidróxido de sódio 5N (0,80 ml, 4,0 mmol). A mistura obtida foi agitada à temperatura ambiente durante 4 h. Adicionou-se ácido clorídrico 1N (4,0 ml) à mistura de reação e a mistura foi diluída com água, e concentrada sob pressão reduzida. Adicionou-se metanol ao resíduo e a mistura foi concentrada sob pressão reduzida, e cristalizada de água-metanol dando o composto titular (477 mg, 61 %).
[00549] RMN 1H (300 MHz, DMSO-d6) δ:3,00-3,20 (6H, m), 3,67 (3H, s), 3,84 (4H, br t, J = 4,4 Hz), 4,53 (2H, br t, J = 5,0 Hz), 7,31 (1H, ddd, J = 8,0, 6,3, 1,8 Hz), 7,55-7,67 (2H, m), 7,88-7,91 (1H, m).Exemplo de Referência 95Produção de ácido 5-metil-4-oxo-3-(tetraidrofuran-2-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxílicoA uma suspensão do composto do Exemplo de Referência 89 (728 mg, 1,88 mmol) em THF (6 ml) e etanol (6 ml) adicionou-se solução aquosa de hidróxido de sódio 5N (0,76 ml, 3,8 mmol). A mistura obtida foi agitada à temperatura ambiente durante 4 h. Adicionou-se ácido clorídrico 1N (3,8 ml) à mistura de reação e a mistura foi diluída com água e a mistura foi extraída 3 vezes com clorofórmio. A camada orgânica combinada foi lavada com solução aquosa de cloreto de sódio, secada sobre sulfato de sódio, filtrada, e concentrada sob pressão reduzida. O sólido obtido foi lavado com diisopropil éter dando o composto titular (659 mg, 97 %).
[00550] RMN 1H (300 MHz, DMSO-d6) δ:1,73-2,04 (4H, m), 3,563,78 (2H, m), 3,65 (3H, s), 4,02-4,10 (1H, m), 4,19-4,30 (2H, m), 7,29-7,37 (1H, m), 7,57-7,71 (2H, m), 7,92-7,99 (1H, m), 13,20 (1H, br s).Exemplo de Referência 96
[00551] Produção de ácido 3-(2-etoxietóxi)-5-metil-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxílicoA uma suspensão do composto do Exemplo de Referência 90(826 mg, 2,20 mmol) em THF (7 ml) e etanol (7 ml) adicionou-se solução aquosa de hidróxido de sódio 5N (0,88 ml, 4,4 mmol). A mistura obtida foi agitada à temperatura ambiente durante 2,5 h, adicionou-se solução aquosa de hidróxido de sódio 5N (4,4 ml, 22 mmol), e a mistura foi agitada a 50°C durante 3,5 h. A mistura de reação foi acidificada com ácido clorídrico 1N e diluída com água, e o sólido precipitado foi recolhido por meio de filtração, lavado com água, e secado ao ar dando o composto titular (719 mg, 94 %).
[00552] RMN 1H (300 MHz, DMSO-d6) δ:1,03 (3H, t, J = 6,9 Hz), 3,44 (2H, q, J = 6,9 Hz), 3,66 (3H, s), 3,75 (2H, t, J = 5,0 Hz), 4,33 (2H, t, J = 5,0 Hz), 7,33 (1H, t, J = 7,4 Hz), 7,58-7,71 (2H, m), 7,96 (1H, d, J = 8,1 Hz), 13,21 (1H, br s).Exemplo de Referência 97
[00553] Produção de 1-butil-2H-3,1-benzoxazina-2,4(1H)-dionaA uma solução de anidrido isatóico (8,16 g, 50,0 mmol) emDMF (100 ml) adicionou-se hidreto de sódio (66 % em óleo, 2,00 g, 55 mmol) sob resfriamento com gelo, e a mistura foi agitada à mesma temperatura durante 10 min. Adicionou-se 1-iodobutano (8,5 ml, 75 mmol) à mistura obtida e a mistura foi agitada à temperatura ambiente durante 64 h. Adicionou-se água gelada à mistura de reação e a mistura foi extraída duas vezes com acetato de etila. A camada orgânica combinada foi lavada duas vezes com água e concentrada sob pressão reduzida dando o composto titular (10,5 g), que foi usado para a reação seguinte sem purificação.
[00554] RMN 1H (300 MHz, CDCl3) δ:1,01 (3H, t, J = 7,4 Hz), 1,48 (2H, sext, J = 7,4 Hz), 1,69-1,81 (2H, m), 4,02-4,10 (2H, m), 7,17 (1H, d, J = 8,6 Hz), 7,25-7,32 (1H, m), 7,75 (1H, ddd, J = 8,6, 7,4, 1,7 Hz), 8,16 (1H, dd, J = 7,8, 1,7 Hz).Exemplo de Referência 98
[00555] Produção de 1-butil-4-hidróxi-2-oxo-1,2-diidroquinolina-3- carboxilato de etilaA uma solução de dietil malonato (12,0 g, 74,9 mmol) em DMF (70 ml) adicionou-se hidreto de sódio (66 % em óleo, 2,00 g, 55 mmol) sob resfriamento com gelo, e a mistura foi agitada à mesma temperatura durante 10 min. Uma solução do composto do Exemplo de Referência 97 (10,5 g) em DMF (20 ml) foi adicionada por gotejamento à mistura obtida, e a mistura foi agitada a 120°C durante 6 h. A mistura de reação foi concentrada sob pressão reduzida, adicionou-se água gelada ao resíduo e a camada aquosa obtida foi lavada com éter de dietila. A camada aquosa foi fracamente acidificada com ácido clorídrico 5N (12 ml) sob resfriamento com gelo, e extraída duas vezes com acetato de etila. A camada orgânica combinada foi lavada com água, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia de coluna em sílica-gel (eluado; acetato de etila/hexano=1/9 - 1/2) dando o composto titular (9,96 g, 69 %, 2 etapas) como um sólido.
[00556] RMN 1H (300 MHz, CDCl3) δ:0,99 (3H, t, J = 7,4 Hz), 1,482 (2H, sext, J = 7,4 Hz), 1,485 (3H, t, J = 7,1 Hz), 1,64-1,76 (2H, m), 4,17-4,26 (2H, m), 4,50 (2H, q, J = 7,1 Hz), 7,20-7,26 (1H, m), 7,29 (1H, d, J = 8,4 Hz), 7,66 (1H, ddd, J = 8,6, 7,4, 1,6 Hz), 8,18 (1H, dd, J = 8,3, 1,6 Hz), 14,20 (1H, s).Exemplo de Referência 99
[00557] Produção de 1-butil-4-cloro-2-oxo-1,2-diidroquinolina-3- carboxilato de etilaUma mistura do composto do Exemplo de Referência 98 (9,73 g, 33,6 mmol) e oxicloreto de fósforo (4,7 ml, 50 mmol) foi agitada a 110°C durante 30 min. A mistura de reação foi concentrada sob pressão reduzida, e adicionou-se água gelada e acetato de etila. A camada orgânica foi separada, e a camada aquosa foi extraída com acetato de etila. A camada orgânica combinada foi lavada com água, solução saturada de hidrogenocarbonato de sódio e água (duas vezes), e concentrada sob pressão reduzida. O resíduo foi submetido a cromatografia de coluna em sílica-gel (eluado; acetato de etila/hexano=1/9 - 1/3), e as frações contendo o produto desejado foram combinadas, e lavadas com solução de hidróxido de sódio 1N e água (duas vezes). O material insolúvel foi removido por filtração e o filtrado foi concentrado sob pressão reduzida. O resíduo foi cristalizado de acetato de etila-éter de diisopropila dando o composto titular (6,07 g, 59 %).
[00558] RMN 1H (300 MHz, CDCl3) δ:1,00 (3H, t, J = 7,4 Hz), 1,42 (3H, t, J = 7,2 Hz), 1,42-1,56 (2H, m), 1,67-1,79 (2H, m), 4,23-4,31 (2H, m), 4,47 (2H, q, J = 7,2 Hz), 7,33 (1H, ddd, J = 8,1, 7,2, 0,9 Hz), 7,37-7,41 (1H, m), 7,66 (1H, ddd, J = 8,7, 7,2, 1,4 Hz), 8,07 (1H, dd, J = 8,1, 1,4 Hz).Exemplo de Referência 100
[00559] Produção de 5-butil-3-hidróxi-4-oxo-4,5-diidrotieno[3,2- c]quinolina-2-carboxilato de etilaUma solução a 20 % (16,0 g, 47 mmol) de etóxido de sódio em etanol foi diluída com etanol (45 ml), adicionou-se tioglicolato de etila (6,2 ml, 55 mmol) à solução obtida, e a mistura foi agitada à temperatura ambiente durante 10 min. O composto do Exemplo de Referência 99 (7,21 g, 23,4 mmol) foi adicionado a esta mistura, e a mistura foi agitada à temperatura ambiente durante 5 h. A mistura de reação foi neutralizada com água gelada e ácido clorídrico 2N (25 ml) sob resfriamento com gelo, e a mistura foi extraída duas vezes com acetato de etila. A camada orgânica combinada foi lavada duas vezes com água, e concentrada sob pressão reduzida. O resíduo foi cristalizado de acetato de etila-éter de diisopropila dando o composto titular (6,44 g, 80 %).
[00560] RMN 1H (300 MHz, CDCl3) δ:1,02 (3H, t, J = 7,4 Hz), 1,42 (3H, t, J = 7,2 Hz), 1,44-1,58 (2H, m), 1,71-1,83 (2H, m), 4,29-4,36 (2H, m), 4,41 (2H, q, J = 7,2 Hz), 7,32 (1H, ddd, J = 8,0, 7,2, 0,9 Hz), 7,43-7,48 (1H, m), 7,61 (1H, ddd, J = 8,6, 7,3, 1,6 Hz), 7,81-7,86 (1H, m), 10,81 (1H, s).Exemplo de Referência 101
[00561] Produção de 5-butil-3-metóxi-4-oxo-4,5-diidrotieno[3,2- c]quinolina-2-carboxilato de etila A uma suspensão do composto do Exemplo de Referência 100 (3,11 g, 9,00 mmol) em DMF (30 ml) adicionou-se DBU (1,62 ml, 10,8 mmol), e adicionou-se iodometano (1,12 ml, 18,0 mmol) à solução obtida. A mistura obtida foi agitada à temperatura ambiente durante 14 h, adicionou-se água e a mistura foi extraída duas vezes com acetato de etila. A camada orgânica combinada foi lavada com água e solução aquosa de hidróxido de sódio 0,5N, filtrada através de Celite (nome comercial), lavada adicionalmente duas vezes com água, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia de coluna em sílica-gel (eluado; acetato de etila/hexano=1/4 - 1/1) e recristalizado de acetato de etila- hexano dando o composto titular (1,03 g, 32 %).
[00562] RMN 1H (300 MHz, CDCl3) δ:1,01 (3H, t, J = 7,4 Hz), 1,401,60 (2H, m), 1,42 (3H, t, J = 7,2 Hz), 1,69-1,81 (2H, m), 4,14 (3H, s), 4,284,36 (2H, m), 4,40 (2H, q, J = 7,2 Hz), 7,22-7,29 (1H, m), 7,39 (1H, d, J = 8,5 Hz), 7,57 (1H, ddd, J = 8,5, 7,1, 1,4 Hz), 7,84 (1H, dd, J = 8,0, 1,4 Hz).Exemplo de Referência 102
[00563] Produção de 5-butil-3-(2-etoxietóxi)-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxilato de etila A uma suspensão do composto do Exemplo de Referência 100 (1,14 g, 3,30 mmol) em DMF (20 ml) adicionou-se DBU (1,48 ml, 9,90 mmol), e adicionou-se 1-bromo-2-etoxietano (1,12 ml, 9,93 mmol) à solução obtida. A mistura obtida foi agitada a 60°C durante 30 h e adicionou-se acetato de etila e água à mistura de reação. A camada orgânica foi separada, e a camada aquosa foi extraída com acetato de etila. A camada orgânica combinada foi lavada com solução aquosa de hidróxido de sódio 0,5N e água, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia de coluna em sílica-gel (eluado; acetato de etila/hexano=1/4 - 1/2) dando o composto titular (1,28 g, 93 %) como um sólido.
[00564] RMN 1H (300 MHz, CDCl3) δ:1,01 (3H, t, J = 7,4 Hz), 1,18 (3H, t, J = 7,0 Hz), 1,42 (3H, t, J = 7,2 Hz), 1,43-1,57 (2H, m), 1,65-1,79 (2H, m), 3,58 (2H, q, J = 7,0 Hz), 3,92 (2H, dd, J = 5,6, 4,7 Hz), 4,30 (2H, br t, J = 7,8 Hz), 4,39 (2H, q, J = 7,2 Hz), 4,47 (2H, t, J = 5,1 Hz), 7,21-7,28 (1H, m), 7,37 (1H, d, J = 8,5 Hz), 7,56 (1H, ddd, J = 8,5, 7,1, 1,4 Hz), 7,83 (1H, dd, J = 8,1, 1,4 Hz).Exemplo de Referência 103
[00565] Produção de ácido 5-butil-3-metóxi-4-oxo-4,5-diidrotieno[3,2- c]quinolina-2-carboxílico A uma suspensão do composto do Exemplo de Referência 101 (1,81 g, 5,04 mmol) em THF (15 ml) e etanol (15 ml) adicionou-se solução aquosa de hidróxido de sódio 5N (2,0 ml, 10 mmol). A mistura obtida foi agitada à temperatura ambiente durante 1,5 h. A mistura de reação foi resfriada com gelo, ácido clorídrico 1N (15 ml) e adicionou-se acetato de etila, e o sólido precipitado foi recolhido por meio de filtração, e lavado com água e acetato de etila dando um sólido. O filtrado foi separado, e a camada aquosa foi extraída com acetato de etila. A camada orgânica combinada foi lavada com água, e concentrada sob pressão reduzida. O resíduo e o sólido obtido antes foram combinados, e a mistura foi recristalizado de metanol-éter de diisopropila dando o composto titular (1,43 g, 86 %).
[00566] RMN 1H (300 MHz, DMSO-d6) δ:0,95 (3H, t, J = 7,3 Hz), 1,43 (2H, sext, J = 7,3 Hz), 1,56-1,68 (2H, m), 3,95 (3H, s), 4,29 (2H, t, J =7,5 Hz), 7,29-7,36 (1H, m), 7,60-7,71 (2H, m), 7,95-8,00 (1H, m).Exemplo de Referência 104
[00567] Produção de ácido 5-butil-3-(2-etoxietóxi)-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxílico A uma solução do composto do Exemplo de Referência 102 (1,16 g, 2,78 mmol) em THF (9 ml) e etanol (9 ml) adicionou-se solução aquosa de hidróxido de sódio 5N (1,12 ml, 5,6 mmol). A mistura obtida foi agitada à temperatura ambiente durante 2,5 h, adicionou-se solução aquosa de hidróxido de sódio 5N (4,48 ml, 22 mmol), e a mistura foi agitada a 50°C durante 3 h. A mistura de reação foi acidificada com ácido clorídrico 1N, e extraída duas vezes com clorofórmio. A camada orgânica combinada foi lavada com água, e concentrada sob pressão reduzida. O resíduo foi cristalizado de acetato de etila-éter de diisopropila dando o composto titular (965 mg, 89 %).
[00568] RMN 1H (300 MHz, DMSO-d6) δ:0,95 (3H, t, J = 7,3 Hz), 1,02 (3H, t, J = 7,0 Hz), 1,43 (2H, sext, J = 7,3 Hz), 1,56-1,68 (2H, m), 3,43 (2H, q, J = 7,0 Hz), 3,74 (2H, t, J = 5,0 Hz), 4,24-4,40 (2H, m), 4,30 (2H, t, J = 5,0 Hz), 7,32 (1H, t, J = 7,4 Hz), 7,59-7,71 (2H, m), 7,97 (1H, d, J = 7,5 Hz), 13,20 (1H, br s).Exemplo de Referência 105
[00569] Produção de 3-hidróxi-5-(4-metoxibenzil)-1-metil-4-oxo-4,5- diidro-1H-pirrol[3,2-c]quinolina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 25, 4-[(2- etóxi-2-oxoetil)(metil)amina]-1-(4-metoxibenzil)-2-oxo-1,2-diidroquinolina- 3-carboxilato de etila (14,7 g, 63 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 10 (19,2 g, 51,6 mmol).
[00570] Da mesma maneira que no Exemplo de Referência 26, o composto titular (10,35 g, 49 %) foi obtido como um sólido branco a partir do 4-[(2-etóxi-2-oxoetil)(metil)amina]-1-(4-metoxibenzil)-2-oxo-1,2- diidroquinolina-3-carboxilato de etila (14,73 g).
[00571] RMN 1H (300 MHz, CDCl3) δ:1,33 (3H, t, J = 7,1 Hz), 3,69 (3H, s), 4,27 (3H, s), 4,34 (2H, q, J = 7,1 Hz), 5,47 (2H, s), 6,86 (2H, d, J = 8,7 Hz), 7,16 (2H, d, J = 8,7 Hz), 7,27-7,30 (1H, m), 7,48 (2H, d, J = 3,3 Hz), 8,32 (1H, d, J = 8,1 Hz), 9,10 (1H, s).Exemplo de Referência 106
[00572] Produção de 3-metóxi-5-(4-metoxibenzil)-1-metil-4-oxo-4,5- diidro-1H-pirrol[3,2-c]quinolina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 6, o composto titular (6,51 g, 61 %) foi obtido como um sólido amarelo claro a partir do composto do Exemplo de Referência 105 (10,4 g, 25,5 mmol).
[00573] RMN 1H (300 MHz, DMSO-d6) δ:1,35 (3H, t, J = 7,1 Hz), 3,69 (3H, s), 3,94 (3H, s), 4,26 (3H, s), 4,34 (2H, q, J = 7,1 Hz), 5,51 (2H, br s), 6,86 (2H, d, J = 8,7 Hz), 7,15 (1H, d, J = 8,4 Hz), 7,25-7,31 (1H, m), 7,47 (2H, d, J = 3,6 Hz), 8,34 (1H, d, J = 8,1 Hz).Exemplo de Referência 107
[00574] Produção de ácido 3-metóxi-5-(4-metoxibenzil)-1-metil-4- oxo-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 28, o composto titular (5,67 g, 96 %) foi obtido como um sólido amarelo claro a partir do composto do Exemplo de Referência 106 (6,50 g, 15,5 mmol).
[00575] RMN 1H (300 MHz, DMSO-d6) δ:3,70 (3H, s), 3,94 (3H, s), 4,28 (3H, s), 5,51 (2H, br s), 6,86 (2H, d, J = 8,7 Hz), 7,15 (1H, d, J = 8,4 Hz), 7,25-7,30 (1H, m), 7,46 (2H, d, J = 3,9 Hz), 8,34 (1H, d, J = 8,4 Hz), 12,90 (1H, br s).Exemplo de Referência 110
[00576] Produção de 6-fluoro-4-hidróxi-2-oxo-1,2-diidroquinolina-3- carboxilato de etilano Exemplo de Referência 1, o composto titular (8,60 g, 56 %) foi obtido como um sólido amarelo claro a partir de 2-amina-5-fluorobenzoato de etila (10,3 g, 61,0 mmol), dietil malonato (9,2 ml, 61,0 mmol), uma solução a 20 % (21,0 g, 61,0 mmol) de etóxido de sódio em etanol e etanol (70 ml).
[00577] RMN 1H (300 MHz, CDCl3) δ:1,52 (3H, t, J = 7,2 Hz), 4,54 (2H, q, J = 7,1 Hz), 7,20-7,29 (1H, m), 7,31-7,42 (1H, m), 7,75 (1H, dd, J = 8,6, 2,7 Hz), 11,02 (1H, br s), 14,31 (1H, s).Exemplo de Referência 111
[00578] Produção de 2,4-dicloro-6-fluoroquinolina-3-carboxilato deetila no Exemplo de Referência 2, o composto titular (2,2 g, 96 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 110 (2,0 g, 7,8 mmol) e oxicloreto de fósforo (9,0 ml).
[00579] RMN 1H (300 MHz, CDCl3) δ:1,46 (3H, t, J = 7,1 Hz), 4,54 (2H, q, J = 7,2 Hz), 7,54-7,68 (1H, m), 7,86 (1H, dd, J = 9,1, 2,8 Hz), 8,07 (1H, dd, J = 9,2, 5,2 Hz).Exemplo de Referência 112
[00580] Produção de 4-cloro-6-fluoro-2-oxo-1,2-diidroquinolina-3- carboxilato de etilaDa mesma maneira que no Exemplo de Referência 3, o composto titular (1,6 g, 79 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 111 (2,2 g, 7,5 mmol), acetato de sódio (615 mg, 7,5 mmol) e ácido acético (20 ml).
[00581] RMN 1H (300 MHz, CDCl3) δ:1,40-1,51 (3H, m), 4,46-4,57 (2H, m), 7,36-7,46 (2H, m), 7,69 (1H, dd, J = 9,1, 1,9 Hz), 12,36 (1H, br s).Exemplo de Referência 113
[00582] Produção de 4-cloro-6-fluoro-2-oxo-1-(2-oxo-2-feniletil)-1,2- diidroquinolina-3-carboxilato de etila no Exemplo de Referência 4, o composto titular (1,3 g, 57 %) foi obtido como um sólido amarelo claro a partir do composto do Exemplo de Referência 112 (1,6 g, 5,9 mmol), hidreto de sódio (60 % em óleo, 248 mg, 6,2 mmol), brometo de fenacila (1,3 g, 6,5 mmol) e DMF (20 ml).
[00583] RMN 1H (300 MHz, CDCl3) δ:1,42 (3H, t, J = 7,1 Hz), 4,47 (2H, q, J = 7,1 Hz), 5,79 (2H, s), 7,00 (1H, dd, J = 9,3, 4,2 Hz), 7,27-7,38 (1H, m), 7,49-7,61 (2H, m), 7,63-7,73 (1H, m), 7,80 (1H, dd, J = 9,1, 2,8 Hz), 8,02-8,12 (2H, m).Exemplo de Referência 114
[00584] Produção de 8-fluoro-3-hidróxi-4-oxo-5-(2-oxo-2-feniletil)- 4,5-diidrotieno[3,2-c]quinolina-2-carboxilato de etila no Exemplo de Referência 5, o composto titular (1,3 g, 94 %) foi obtido como um sólido amarelo a partir do composto do Exemplo de Referência 113 (1,3 g, 3,3 mmol), uma solução a 20 % (2,3 g, 6,7 mmol) de etóxido de sódio em etanol, tioglicolato de etila (0,97 g, 8,0 mmol) e etanol (14 ml).
[00585] RMN 1H (300 MHz, DMSO-d6) δ:1,32 (3H, t, J = 7,1 Hz),4,32 (2H, q, J = 7,2 Hz), 6,02 (2H, s), 7,47-7,58 (1H, m), 7,59-7,70 (3H, m), 7,72-7,82 (1H, m), 8,00 (1H, dd, J = 8,7, 2,8 Hz), 8,11-8,21 (2H, m), 10,52 (1H, br s).Exemplo de Referência 115
[00586] Produção de 8-fluoro-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 6, ocomposto titular (880 mg, 65 %) foi obtido como um sólido amarelo a partir do composto do Exemplo de Referência 114 (1,3 g, 3,1 mmol), iodometano (0,31 ml, 5,0 mmol), DBU (0,75 ml, 5,0 mmol) e DMF (40 ml).
[00587] RMN 1H (300 MHz, CDCl3) δ:1,43 (3H, t, J = 7,5 Hz), 4,12 (3H, s), 4,42 (2H, q, J = 7,2 Hz), 5,84 (2H, s), 6,98 (1H, dd, J = 9,3, 4,2 Hz), 7,16-7,25 (1H, m), 7,49-7,60 (3H, m), 7,64-7,72 (1H, m), 8,03-8,15 (2H, m).Exemplo de Referência 116
[00588] Produção de ácido 8-fluoro-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 7, o composto titular (602 mg, 73 %) foi obtido como um sólido castanho claro a partir do composto do Exemplo de Referência 115 (880 mg, 2,0 mmol), solução aquosa de hidróxido de sódio 8N (5,7 ml), etanol (32 ml) e THF (9,1 ml).
[00589] RMN 1H (300 MHz, DMSO-d6) δ:3,92 (3H, s), 5,98 (2H, s), 7,39-7,60 (2H, m), 7,60-7,69 (2H, m), 7,72-7,81 (1H, m), 7,91-8,01 (1H, m), 8,12-8,23 (2H, m).Exemplo de Referência 117
[00590] Produção de 8-fluoro-3-hidróxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 25, ocomposto titular (4,1 g, 83 %) foi obtido como um sólido castanho claro a partir do composto do Exemplo de Referência 113 (4,6 g, 12 mmol), cloridrato de etil éster de sarcosina (4,5 g, 30 mmol), trietilamina (6,0 ml, 43 mmol), etanol (35 ml), uma solução a 20 % (3,4 g, 9,9 mmol) de etóxido de sódio em etanol e etanol (35 ml).
[00591] RMN 1H (300 MHz, DMSO-d6) δ:1,33 (3H, t, J = 8,9 Hz), 4,26-4,42 (5H, m), 5,94 (2H, s), 7,33-7,50 (2H, m), 7,58-7,69 (2H, m), 7,717,80 (1H, m), 8,03-8,23 (3H, m), 9,01 (1H, br s).Exemplo de Referência 118
[00592] Produção de 8-fluoro-3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxilato de etilaUma solução do composto do Exemplo de Referência 117 (3,4g, 8,0 mmol), ácido dimetilsulfúrico (1,1 ml, 12 mmol) e DBU (2,4 ml, 16 mmol) em DMF (100 ml) foi agitada à temperatura ambiente durante 2,5 h. Adicionou-se ácido dimetilsulfúrico (1,1 ml, 12 mmol) e DBU (2,4 ml, 16 mmol) à mistura de reação, e a mistura foi agitada à temperatura ambiente durante 1 dia. Adicionou-se mais ácido dimetilsulfúrico (0,75 ml, 8,0 mmol) e DBU (1,8 ml, 11 mmol), e a mistura foi agitada à temperatura ambiente durante 21 h e diluída com água, e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água, e secado sob pressão reduzida dando o composto titular (2,8 g, 80 %) como um sólido branco.
[00593] RMN 1H (300 MHz, DMSO-d6) δ:1,35 (3H, t, J = 7,1 Hz), 3,88 (3H, s), 4,21-4,42 (5H, m), 5,96 (2H, s), 7,28-7,51 (2H, m), 7,55-7,69 (2H, m), 7,71-7,81 (1H, m), 7,98-8,39 (3H, m).Exemplo de Referência 119
[00594] Produção de ácido 8-fluoro-3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 7, ocomposto titular (2,4 g, 90 %) foi obtido como um sólido amarelo claro a partir do composto do Exemplo de Referência 118 (2,8 g, 6,4 mmol).
[00595] RMN 1H (300 MHz, DMSO-d6) δ:3,85 (3H, s), 4,30 (3H, s), 5,95 (2H, s), 7,19-7,49 (2H, m), 7,53-7,69 (2H, m), 7,70-7,82 (1H, m), 7,978,26 (3H, m).Exemplo de Referência 120
[00596] Produção de ácido 1-etil-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxílicoUma solução do composto do Exemplo de Referência 4 (1,0 g, 2,7 mmol), cloridrato de etil éster de N-etilglicina (499 mg, 3,0 mmol) e trietilamina (3,8 ml, 27 mmol) em 1-butanol (10 ml) foi aquecida em refluxo durante 6 h. Adicionou-se cloridrato de etil éster de N-etilglicina (499 mg, 3,0 mmol) e a mistura foi aquecida em refluxo durante 17 h. Adicionou-se cloridrato de etil éster de N-etilglicina (499 mg, 3,0 mmol) e trietilamina (0,41 ml, 3,0 mmol), e a mistura foi aquecida em refluxo durante 6 h, e cloridrato de etil éster de N-etilglicina (499 mg, 3,0 mmol) e trietilamina (0,41 ml, 3,0 mmol), e a mistura foi aquecida em refluxo durante 6 h. Adicionou-se água à mistura de reação, e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água, e secado sob pressão reduzida. Uma mistura do sólido obtido, uma solução a 20 % (777 mg, 2,3 mmol) de etóxido de sódio em etanol e etanol (150 ml) foi agitada à temperatura ambiente durante 5 h. Adicionou-se uma solução a 20 % (777 mg, 2,3 mmol) de etóxido de sódio em etanol, e a mistura de reação foi agitada à temperatura ambiente durante 1 h. A mistura de reação foi diluída com água, neutralizada com ácido clorídrico 5N, e a mistura foi agitada durante 30 min. O sólido precipitado foi recolhido por meio de filtração, lavado com água, secado sob pressão reduzida, e recristalizado de DMF-éter de dietila. A uma solução do sólido obtido e DBU (0,19 ml, 1,3 mmol) em DMF (8,0 ml) adicionou-se ácido dimetilsulfúrico (0,092 ml, 0,97 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 14 h. Adicionou-se mais DBU (0,19 ml, 1,3 mmol) e ácido dimetilsulfúrico (0,092 ml, 0,97 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 4 h, e diluída com água. O sólido precipitado foi recolhido por meio de filtração, o sólido obtido foi lavado com água, e secado sob pressão reduzida. Uma solução mista do sólido obtido e solução de hidróxido de sódio 8N (1,4 ml) em THF (2,3 ml)-etanol (8,0 ml) foi agitada à temperatura ambiente durante 15 h. Adicionou-se solução de hidróxido de sódio 8N (0,70 ml), e a mistura foi agitada à temperatura ambiente durante 3,5 h. Adicionou-se mais solução de hidróxido de sódio 8N (0,14 ml), e a mistura foi agitada à temperatura ambiente durante 3 h. A mistura de reação foi neutralizada com ácido clorídrico 1N e concentrada sob pressão reduzida, e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água, e secado sob pressão reduzida dando o composto titular (180 mg, 16 %) como um sólido branco.
[00597] RMN 1H (300 MHz, DMSO-d6) δ:1,51 (3H, t, J = 6,5 Hz), 3,86 (3H, s), 4,85 (2H, q, J = 7,0 Hz), 5,97 (2H, s), 7,27-7,43 (2H, m), 7,447,54 (1H, m), 7,58-7,69 (2H, m), 7,71-7,83 (1H, m), 8,01-8,45 (3H, m), 12,89 (1H, br s).Exemplo de Referência 121
[00598] Produção de (1-benzilazepan-4-il)carbamato de t-butila BnA uma solução de 1-benzilazepan-4-amina (400 mg, 2,0 mmol) e trietilamina (0,82 ml, 5,9 mmol) em THF (5,0 ml) adicionou-se dicarboneto de di-t-butila (591 mg, 2,7 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 4 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=10/90 - 100/0) dando o composto titular (447 mg, quant.) como um óleo incolor.
[00599] RMN 1H (300 MHz, CDCl3) δ:1,45 (9H, s), 1,53-1,77 (5H, m), 1,78-1,93 (1H, m), 2,37-2,58 (2H, m), 2,61-2,83 (2H, m), 3,61 (2H, s), 3,734,00 (1H, m), 4,92-5,27 (1H, m), 7,07-7,44 (5H, m).Exemplo de Referência 122
[00600] Produção de azepan-4-ilcarbamato de t-butila HUma solução do composto do Exemplo de Referência 121 (447 mg, 1,5 mmol) e paládio-carbono (65 mg) em etanol (10 ml) foi agitada à temperatura ambiente durante 4,5 h sob uma atmosfera de hidrogênio. Paládio-carbono foi removido por filtração, e o filtrado foi concentrado sob pressão reduzida. O resíduo foi dissolvido em metanol (10 ml), adicionou-se paládio-carbono (120 mg), e a mistura foi agitada à temperatura ambiente durante 4,5 h sob uma atmosfera de hidrogênio. Paládio-carbono foi removido por filtração, e o filtrado foi concentrado sob pressão reduzida dando o composto titular (315 mg, quant.) como um óleo incolor.
[00601] RMN 1H (300 MHz, CDCl3) δ:1,34-1,76 (13H, m), 1,78-2,07 (2H, m), 2,39-2,70 (1H, m), 2,71-3,04 (4H, m), 3,66-3,94 (1H, m), 4,60-5,01 (1H, m).Exemplo de Referência 123
[00602] Produção de acetato de 2-{4-[(t-butoxicarbonil)amina]azepan- 1-il}-2-oxoetilaDa mesma maneira que no Exemplo 544, o composto titular(220 mg, 96 %) foi obtido como um sólido branco a partir do composto doExemplo de Referência 122 (157 mg, 0,73 mmol).
[00603] RMN 1H (300 MHz, CDCl3) δ:1,37-1,55 (11H, m), 1,61-2,00(4H, m), 2,07-2,23 (4H, m), 3,21-3,77 (4H, m), 4,35-4,59 (1H, m), 4,59-4,81(2H, m).Exemplo de Referência 124
[00604] Produção de 2-aminapiridina-3-carboxilato de metilaA uma solução de ácido 2-aminapiridina-3-carboxílico (4,3 g, 31 mmol) em metanol (62 ml) adicionou-se, por gotejamento, ácido sulfúrico (31 ml) sob resfriamento com gelo, e a mistura de reação foi agitada à temperatura ambiente durante 30 min. A mistura de reação foi agitada a 70°C durante 15 h, e neutralizada com bicarbonato de sódio sob resfriamento com gelo. A mistura de reação foi extraída duas vezes com acetato de etila, e os extratos foram combinados, e lavados com salmoura. O extrato foi secado sobre sulfato de magnésio, e concentrado sob pressão reduzida dando o composto titular (4,3 g, 90 %) como um sólido branco.
[00605] RMN 1H (300 MHz, CDCl3) δ:3,89 (3H, s), 6,38 (2H, br s), 6,63 (1H, dd, J = 7,8, 4,8 Hz), 8,13 (1H, dd, J = 7,7, 1,9 Hz), 8,22 (1H, dd, J = 4,7, 1,9 Hz).Exemplo de Referência 125
[00606] Produção de 4-hidróxi-2-oxo-1,2-diidro-1,8-naftiridino-3- carboxilato de etilaDa mesma maneira que no Exemplo de Referência 1, o composto titular (2,6 g, 53 %) foi obtido como um sólido vermelho claro a partir do composto do Exemplo de Referência 124 (3,1 g, 21 mmol).
[00607] RMN 1H (300 MHz, DMSO-d6) δ:1,30 (3H, t, J = 7,1 Hz), 4,32 (2H, q, J = 7,1 Hz), 7,27 (1H, dd, J = 7,9, 4,7 Hz), 8,22-8,38 (1H, m), 8,60 (1H, dd, J = 4,6, 1,8 Hz), 11,86 (1H, s), 13,29 (1H, br s).Exemplo de Referência 126
[00608] Produção de 2,4-dicloro-1,8-naftiridino-3-carboxilato de etila CLDa mesma maneira que no Exemplo de Referência 2, o composto titular (2,3 g, 77 %) foi obtido como um sólido amarelo claro a partir do composto do Exemplo de Referência 125 (2,6 g, 11 mmol).
[00609] RMN 1H (300 MHz, CDCI3) δ:1,47 (3H, t, J = 7,2 Hz), 4,56 (2H, q, J = 7,2 Hz), 7,67 (1H, dd, J = 8,4, 4,2 Hz), 8,62 (1H, dd, J = 8,3, 1,9 Hz), 9,21 (1H, dd, J = 4,2, 1,9 Hz).
[00610] Exemplo de Referência 127
[00611] Produção de 4-cloro-2-oxo-1,2-diidro-1,8-naftiridino-3-carboxilato de etilade 4-cloro-2-oxo-1,2-diidro-1,8-naftiridino-3-Da mesma maneira que no Exemplo de Referência 3, ocomposto titular (1,5 g, 71 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 126 (2,2 g, 8,3 mmol).
[00612] RMN 1H (300 MHz, DMSO-d6) δ:1,31 (3H, t, J = 7,1 Hz), 4,37 (2H, q, J = 7,1 Hz), 7,43 (1H, dd, J = 8,1, 4,7 Hz), 8,33 (1H, dd, J = 8,1, 1,7 Hz), 8,69 (1H, dd, J = 4,7, 1,7 Hz), 12,88 (1H, br s).Exemplo de Referência 128
[00613] Produção de 4-cloro-2-oxo-1-(2-oxo-2-feniletil)-1,2-diidro-1,8-naftiridino-3-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 4, o composto titular (1,1 g, 51 %) foi obtido como um óleo amarelo claro a partir do composto do Exemplo de Referência 127 (1,5 g, 5,7 mmol).
[00614] RMN 1H (300 MHz, CDCl3) δ:1,42 (3H, t, J = 7,1 Hz), 4,48 (2H, q, J = 7,1 Hz), 5,98 (2H, s), 7,27-7,33 (1H, m), 7,48-7,58 (2H, m), 7,597,69 (1H, m), 8,02-8,12 (2H, m), 8,36 (1H, dd, J = 8,0, 1,8 Hz), 8,54 (1H, dd, J = 4,7, 1,7 Hz).Exemplo de Referência 129
[00615] Produção de 3-hidróxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidro-1H-pirrol[3,2-c][1,8]naftiridino-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 33, o composto titular (653 mg, 55 %) foi obtido como um sólido amarelo claro a partir do composto do Exemplo de Referência 128 (1,1 g, 2,9 mmol).
[00616] RMN 1H (300 MHz, CDCl3) δ:1,45 (3H, t, J = 7,1 Hz), 4,36 (3H, s), 4,46 (2H, q, J = 7,2 Hz), 6,00 (2H, s), 7,20 (1H, dd, J = 7,9, 4,7 Hz), 7,45-7,58 (2H, m), 7,58-7,69 (1H, m), 8,02-8,15 (2H, m), 8,33-8,51 (2H, m), 8,70 (1H, s).Exemplo de Referência 130
[00617] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c][1,8]naftiridino-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 115, o composto titular (420 mg, 79 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 129 (512 mg, 1,3 mmol).
[00618] RMN 1H (300 MHz, DMSO-d6) δ:1,35 (3H, t, J = 7,1 Hz), 3,91 (3H, s), 4,24-4,44 (5H, m), 5,97 (2H, s), 7,36 (1H, dd, J = 8,1, 4,5 Hz), 7,55-7,69 (2H, m), 7,68-7,82 (1H, m), 8,06-8,24 (2H, m), 8,46 (1H, dd, J = 4,6, 1,4 Hz), 8,75 (1H, dd, J = 8,1, 1,5 Hz).Exemplo de Referência 131
[00619] Produção de ácido 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c][1,8]naftiridino-2-carboxílicoDa mesma maneira que no Exemplo de Referência 7, o composto titular (264 mg, 75 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 130 (380 mg, 0,91 mmol).
[00620] RMN 1H (300 MHz, DMSO-d6) δ:3,90 (3H, s), 4,32 (3H, s), 5,97 (2H, s), 7,35 (1H, dd, J = 8,1, 4,7 Hz), 7,54-7,68 (2H, m), 7,69-7,81 (1H, m), 8,03-8,27 (2H, m), 8,33-8,56 (1H, m), 8,75 (1H, d, J = 7,2 Hz), 13,04 (1H, br s).Exemplo de Referência 132
[00621] Produção de 4-aminapiridina-3-carboxilato de metilaDa mesma maneira que no Exemplo de Referência 124, o composto titular (4,9 g, 89 %) foi obtido como um sólido amarelo claro de ácido 4-aminapiridina-3-carboxílico (5,0 g, 36 mmol), ácido sulfúrico (36 ml) e metanol (72 ml).
[00622] RMN 1H (300 MHz, CDCl3) δ:3,91 (3H, s), 6,20 (2H, br s), 6,51 (1H, d, J = 5,9 Hz), 8,20 (1H, d, J = 6,0 Hz), 8,90 (1H, s).Exemplo de Referência 133
[00623] Produção de 4-hidróxi-2-oxo-1,2-diidro-1,6-naftiridino-3- carboxilato de etilaDa mesma maneira que no Exemplo de Referência 1, o composto titular (3,5 g, 49 %) foi obtido como um pó amarelo claro a partir do composto do Exemplo de Referência 132 (4,7 g, 31 mmol).
[00624] RMN 1H (300 MHz, DMSO-d6) δ:1,28 (3H, t, J = 7,1 Hz), 4,26 (2H, q, J = 7,0 Hz), 7,20 (1H, d, J = 6,0 Hz), 8,50 (1H, d, J = 6,0 Hz), 8,92-9,09 (1H, m), 11,66 (1H, br s).Exemplo de Referência 134
[00625] Produção de 2,4-dicloro-1,6-naftiridino-3-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 2, o composto titular (2,7 g, 66 %) foi obtido como um sólido amarelo claro a partir do composto do Exemplo de Referência 133 (3,5 g, 15 mmol).
[00626] RMN 1H (300 MHz, CDCl3) δ:1,47 (3H, t, J = 7,2 Hz), 4,56 (2H, q, J = 7,1 Hz), 7,87 (1H, dd, J = 5,9, 0,8 Hz), 8,92 (1H, d, J = 5,9 Hz), 9,66 (1H, d, J = 0,9 Hz).Exemplo de Referência 135
[00627] Produção de 4-cloro-2-oxo-1,2-diidro-1,6-naftiridino-3- carboxilato de etila Da mesma maneira que no Exemplo de Referência 3, o composto titular (733 mg, 30 %) foi obtido como um sólido castanho claro a partir do composto do Exemplo de Referência 134 (2,6 g, 9,7 mmol).
[00628] RMN 1H (300 MHz, DMSO-d6) δ:1,31 (3H, t, J = 7,1 Hz), 4,36 (2H, q, J = 7,1 Hz), 7,29 (1H, d, J = 5,7 Hz), 8,63 (1H, d, J = 5,7 Hz), 9,06 (1H, s), 12,72 (1H, br s).Exemplo de Referência 136
[00629] Produção de 4-cloro-2-oxo-1-(2-oxo-2-feniletil)-1,2-diidro- 1,6-naftiridino-3-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 4, o composto titular (344 mg, 33 %) foi obtido como um sólido amarelo claro a partir do composto do Exemplo de Referência 135 (710 mg, 2,8 mmol).
[00630] RMN 1H (300 MHz, CDCl3) δ:1,42 (3H, t, J = 7,2 Hz), 4,48 (2H, q, J = 7,2 Hz), 5,73 (2H, s), 6,86 (1H, d, J = 5,9 Hz), 7,49-7,63 (2H, m), 7,64-7,79 (1H, m), 7,95-8,19 (2H, m), 8,64 (1H, br s), 9,30 (1H, br s).Exemplo de Referência 137
[00631] Produção de 3-hidróxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidro-1H-pirrol[3,2-c][1,6]naftiridino-2-carboxilato de etilaUma mistura do composto do Exemplo de Referência 136 (574 mg, 1,6 mmol), cloridrato de etil éster de sarcosina (286 mg, 1,9 mmol), trietilamina (0,65 ml, 4,7 mmol), e etanol (29 ml) foi aquecida em refluxo durante 2,5 h. Adicionou-se mais cloridrato de etil éster de sarcosina (286 mg, 1,9 mmol) e trietilamina (0,43 ml, 3,1 mmol) e a mistura foi aquecida em refluxo durante 5,5 h. Adicionou-se cloridrato de etil éster de sarcosina (286 mg, 1,9 mmol) e trietilamina (0,65 ml, 4,7 mmol) e a mistura foi aquecida em refluxo durante 46 h. Adicionou-se trietilamina (0,65 ml, 4,7 mmol), e a mistura foi aquecida em refluxo durante 3 h. Adicionou-se trietilamina (0,65 ml, 4,7 mmol) e a mistura foi aquecida em refluxo durante 64 h. Adicionou-se mais trietilamina (0,65 ml, 4,7 mmol) e a mistura foi aquecida em refluxo durante 3 h. Adicionou-se mais trietilamina (0,65 ml, 4,7 mmol) e a mistura foi aquecida em refluxo durante 3 h. A mistura de reação foi concentrada sob pressão reduzida, adicionou-se água ao resíduo, e a mistura foi acidificada com solução aquosa de ácido cítrico a 20 % e agitada durante 30 min sob resfriamento com gelo. O sólido precipitado foi recolhido por meio de filtração, o sólido obtido foi lavado com água, e secado sob pressão reduzida. O sólido foi lavado com solvente misto de acetato de etila-hexano e hexano dando o composto titular (485 mg, 77 %) como um pó castanho claro.
[00632] RMN 1H (300 MHz, DMSO-d6) δ:1,34 (3H, t, J = 7,1 Hz), 4,27-4,43 (5H, m), 5,91 (2H, s), 7,42 (1H, d, J = 6,0 Hz), 7,58-7,69 (2H, m), 7,71-7,82 (1H, m), 8,08-8,23 (2H, m), 8,50 (1H, d, J = 5,9 Hz), 9,07 (1H, br s), 9,49 (1H, s). Exemplo de Referência 138
[00633] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c][1,6]naftiridino-2-carboxilato de etila ME ,CO2EtDa mesma maneira que no Exemplo de Referência 115, ocomposto titular (313 mg, 64 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 137 (471 mg, 1,2 mmol).
[00634] RMN 1H (300 MHz, DMSO-d6) δ:1,35 (3H, t, J = 6,0 Hz), 3,88 (3H, s), 4,28-4,40 (5H, m), 5,94 (2H, s), 7,43 (1H, d, J = 6,0 Hz), 7,597,69 (2H, m), 7,72-7,82 (1H, m), 8,11-8,22 (2H, m), 8,51 (1H, d, J = 6,0 Hz), 9,52 (1H, s).Exemplo de Referência 139
[00635] Produção de ácido 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c][1,6]naftiridino-2-carboxílicoDa mesma maneira que no Exemplo de Referência 7, ocomposto titular (259 mg, 92 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 138 (301 mg, 0,72 mmol).
[00636] RMN 1H (300 MHz, DMSO-d6) δ:3,87 (3H, s), 4,36 (3H, s), 5,94 (2H, s), 7,42 (1H, d, J = 6,0 Hz), 7,57-7,70 (2H, m), 7,71-7,83 (1H, m), 8,07-8,26 (2H, m), 8,49 (1H, d, J = 5,9 Hz), 9,51 (1H, s), 13,01 (1H, br s).Exemplo de Referência 140
[00637] Produção de 6-etil-3-hidróxi-1-metil-4-oxo-4,5-diidro-1H- pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 40, o composto titular (4,87 g, 85 %) foi obtido como um pó castanho a partir do composto do Exemplo de Referência 38 (5,00 g, 21,8 mmol).
[00638] RMN 1H (300 MHz, DMSO-d6) δ:1,18 (3H, t, J = 7,6 Hz), 1,30 (3H, t, J = 7,1 Hz), 2,39-2,49 (2H, m), 3,73 (3H, s), 4,29 (2H, q, J = 7,1 Hz), 6,25 (1H, s), 8,87 (1H, br s), 10,81 (1H, br s).Exemplo de Referência 141
[00639] Produção de 6-etil-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5- diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaUma mistura do composto do Exemplo de Referência 140 (200 mg, 0,757 mmol), carbonato de césio (271 mg, 0,832 mmol), trifluorometanossulfonato de 2,2,2-trifluoroetila (0,109 ml, 0,757 mmol), sulfóxido de dimetila (2,0 ml) e DMF (2,0 ml) foi agitada a 60°C durante 2 h. A mistura de reação foi diluída com água, e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água e diisopropil éter, e secado sob pressão reduzida dando o composto titular (161 mg, 61 %) como um sólido branco.
[00640] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3H, t, J = 7,5 Hz), 1,27 (3H, t, J = 7,0 Hz), 2,51-2,56 (2H, m), 3,79 (3H, s), 4,24 (2H, q, J = 7,0 Hz), 4,97 (2H, q, J = 9,3 Hz), 6,38 (1H, s), 11,06 (1H, br s).Exemplo de Referência 142
[00641] Produção de 6-etil-5-(3-metoxibenzil)-1-metil-4-oxo-3-(2,2,2- trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaUma mistura do composto do Exemplo de Referência 141 (500 mg, 1,44 mmol), t-butóxido de sódio (180 mg, 1,87 mmol), brometo de lítio (250 mg, 2,88 mmol), 1-(clorometil)-3-metoxibenzeno (0,313 ml, 2,16 mmol), DME (8,0 ml) e DMF (2,0 ml) foi agitada a 60°C durante 13 h. Adicionou-se água (50 ml) à mistura de reação, e a mistura foi extraída com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de sódio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em sílica-gel (eluado; acetato de etila/hexano=3/97 - 70/30) dando o composto titular (508 mg, 76 %) como um óleo amarelo.
[00642] RMN 1H (300 MHz, DMSO-d6) δ:1,14-1,36 (6H, m), 2,60 (2H, q, J = 7,2 Hz), 3,70 (3H, s), 3,85 (3H, s), 4,26 (2H, q, J = 7,2 Hz), 4,89 (2H, q, J = 9,3 Hz), 5,28 (2H, br s), 6,44-6,67 (3H, m), 6,74-6,95 (1H, m), 7,22 (1H, t, J = 7,9 Hz).Exemplo de Referência 143
[00643] Produção de ácido 6-etil-5-(3-metoxibenzil)-1-metil-4-oxo-3- (2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 49, o composto titular (333 mg, 66 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 142 (508 mg, 1,09 mmol).
[00644] RMN 1H (300 MHz, DMSO-d6) δ:1,17 (3H, t, J = 7,3 Hz), 2,60 (2H, q, J = 7,3 Hz), 3,70 (3H, s), 3,85 (3H, s), 4,87 (2H, q, J = 9,4 Hz), 5,30 (2H, br s), 6,43-6,67 (3H, m), 6,81 (1H, dd, J = 7,9, 2,3 Hz), 7,22 (1H, t, J = 7,9 Hz), 12,70 (1H, br s).Exemplo de Referência 144
[00645] Produção de 5-benzil-6-etil-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 142, o composto titular (312 mg, 62 %) foi obtido como um óleo amarelo a partir do composto do Exemplo de Referência 141 (400 mg, 1,16 mmol) e brometo de benzila (0,207 ml, 1,74 mmol).
[00646] RMN 1H (300 MHz, DMSO-d6) δ:1,16 (3H, t, J = 7,3 Hz), 1,29 (3H, t, J = 7,1 Hz), 2,61 (2H, q, J = 7,3 Hz), 3,85 (3H, s), 4,26 (2H, q, J = 7,1 Hz), 4,89 (2H, q, J = 9,3 Hz), 5,34 (2H, br s), 6,54 (1H, s), 7,03-7,09 (2H, m), 7,20-7,27 (1H, m), 7,28-7,36 (2H, m).Exemplo de Referência 145
[00647] Produção de ácido 5-benzil-6-etil-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 49, o composto titular (213 mg, 73 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 144 (312 mg, 0,715 mmol).
[00648] RMN 1H (300 MHz, DMSO-d6) δ:1,16 (3H, t, J = 7,3 Hz), 2,60 (2H, q, J = 7,3 Hz), 3,85 (3H, s), 4,87 (2H, q, J = 9,3 Hz), 5,34 (2H, br s), 6,52 (1H, s), 7,01-7,10 (2H, m), 7,17-7,39 (3H, m), 12,73 (1H, br s).Exemplo de Referência 146
[00649] Produção de 5-(2,5-dimetoxibenzil)-6-etil-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 142, o composto titular (121 mg, 21 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 141 (400 mg, 1,16 mmol) e 2- (clorometil)-1,4-dimetoxibenzeno (325 mg, 1,74 mmol).
[00650] RMN 1H (300 MHz, DMSO-d6) δ:1,17 (3H, t, J = 7,3 Hz), 1,29 (3H, t, J = 7,2 Hz), 2,53-2,61 (2H, m), 3,56 (3H, s), 3,83 (3H, s), 3,86 (3H, s), 4,26 (2H, q, J = 7,2 Hz), 4,87 (2H, q, J = 9,3 Hz), 5,19 (2H, br s), 5,93 (1H, d, J = 3,0 Hz), 6,58 (1H, s), 6,79 (1H, dd, J = 8,9, 3,0 Hz), 6,97 (1H, d, J = 8,9 Hz).Exemplo de Referência 147
[00651] Produção de ácido 5-(2,5-dimetoxibenzil)-6-etil-1-metil-4- oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 49, o composto titular (82,7 mg, 72 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 146 (121 mg, 0,244 mmol).
[00652] RMN 1H (300 MHz, DMSO-d6) δ:1,17 (3H, t, J = 7,3 Hz), 2,52-2,60 (2H, m), 3,56 (3H, s), 3,83 (3H, s), 3,86 (3H, s), 4,85 (2H, q, J = 9,3 Hz), 5,19 (2H, br s), 5,92 (1H, d, J = 3,0 Hz), 6,56 (1H, s), 6,79 (1H, dd, J =9,0, 3,0 Hz), 6,97 (1H, d, J = 9,0 Hz), 12,74 (1H, br s).Exemplo de Referência 148
[00653] Produção de 4-cloro-6-etil-1-[2-(3-metoxifenil)-2-oxoetil]-2-oxo-1,2-diidropiridina-3-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 142, o composto titular (879 mg, 53 %) foi obtido como um óleo amarelo a partir do composto do Exemplo de Referência 38 (1,00 g, 4,35 mmol) e 2-bromo-1-(3- metoxifenil)etanona (1,99 g, 8,71 mmol).
[00654] RMN 1H (300 MHz, DMSO-d6) δ:1,13 (3H, t, J = 7,4 Hz), 1,24 (3H, t, J = 7,1 Hz), 2,61 (2H, q, J = 7,4 Hz), 3,85 (3H, s), 4,25 (2H, q, J = 7,1 Hz), 5,60 (2H, s), 6,44 (1H, s), 7,28-7,35 (1H, m), 7,48-7,59 (2H, m), 7,66-7,74 (1H, m).Exemplo de Referência 149
[00655] Produção de 6-etil-3-hidróxi-5-[2-(3-metoxifenil)-2-oxoetil]-1- metil-4-oxo-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 40, o composto titular (526 mg, 55 %) foi obtido como um pó verde a partir do composto do Exemplo de Referência 148 (879 mg, 2,33 mmol).
[00656] RMN 1H (300 MHz, DMSO-d6) δ:1,18 (3H, t, J = 7,4 Hz), 1,31 (3H, t, J = 7,1 Hz), 2,52-2,61 (2H, m), 3,80 (3H, s), 3,85 (3H, s), 4,30 (2H, q, J = 7,1 Hz), 5,54 (2H, s), 6,43 (1H, s), 7,26-7,36 (1H, m), 7,48-7,60 (2H, m), 7,68-7,76 (1H, m), 8,89 (1H, br s).Exemplo de Referência 150
[00657] Produção de 6-etil-5-[2-(3-metoxifenil)-2-oxoetil]-1-metil-4- oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaUma mistura do composto do Exemplo de Referência 149 (470 mg, 1,14 mmol), carbonato de césio (446 mg, 1,37 mmol), trifluorometanossulfonato de 2,2,2-trifluoroetila (0,197 ml, 1,37 mmol) e DMF (4,7 ml) foi agitada à temperatura ambiente durante 1 h. A mistura de reação foi diluída com água, e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água, diisopropil éter e etanol, e secado sob pressão reduzida dando o composto titular (423 mg, 75 %) como um pó verde.
[00658] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3H, t, J = 7,3 Hz), 1,28 (3H, t, J = 7,2 Hz), 2,59 (2H, q, J = 7,3 Hz), 3,83-3,90 (6H, m), 4,26 (2H, q, J = 7,2 Hz), 4,83 (2H, q, J = 9,3 Hz), 5,61 (2H, s), 6,55 (1H, s), 7,27-7,34 (1H, m), 7,48-7,61 (2H, m), 7,68-7,76 (1H, m).Exemplo de Referência 151
[00659] Produção de ácido 6-etil-5-[2-(3-metoxifenil)-2-oxoetil]-1- metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2- carboxílicoDa mesma maneira que no Exemplo de Referência 49, ocomposto titular (300 mg, 86 %) foi obtido como um pó castanho a partir do composto do Exemplo de Referência 150 (370 mg, 0,748 mmol).
[00660] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3H, t, J = 7,3 Hz), 2,58 (2H, q, J = 7,3 Hz), 3,83-3,91 (6H, m), 4,82 (2H, q, J = 9,3 Hz), 5,60 (2H, s), 6,54 (1H, s), 7,26-7,37 (1H, m), 7,47-7,62 (2H, m), 7,67-7,83 (1H, m), 12,70 (1H, br s).Exemplo de Referência 152
[00661] Produção de 4-cloro-1-[2-(3-clorofenil)-2-oxoetil]-6-etil-2-oxo-1,2-diidropiridina-3-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 142, ocomposto titular (486 mg, 29 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 38 (1,50 g, 6,53 mmol) e 2-bromo-1-(3- clorofenil)etanona (2,02 g, 8,65 mmol).
[00662] RMN 1H (300 MHz, DMSO-d6) δ:1,14 (3H, t, J = 7,4 Hz), 1,24 (3H, t, J = 7,1 Hz), 2,63 (2H, q, J = 7,4 Hz), 4,25 (2H, q, J = 7,1 Hz), 5,61 (2H, s), 6,45 (1H, s), 7,59-7,70 (1H, m), 7,77-7,86 (1H, m), 8,00-8,07 (1H, m), 8,08-8,17 (1 H, m).Exemplo de Referência 153
[00663] Produção de 5-[2-(3-clorofenil)-2-oxoetil]-6-etil-3-hidróxi-1- metil-4-oxo-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etila Me CO2EtDa mesma maneira que no Exemplo de Referência 40, o composto titular (460 mg, 87 %) foi obtido como um pó verde a partir do composto do Exemplo de Referência 152 (486 mg, 1,27 mmol).
[00664] RMN 1H (300 MHz, DMSO-d6) δ:1,18 (3H, t, J = 7,4 Hz), 1,31 (3H, t, J = 7,0 Hz), 2,57 (2H, q, J = 7,4 Hz), 3,80 (3H, s), 4,30 (2H, q, J = 7,0 Hz), 5,53 (2H, s), 6,44 (1H, s), 7,61-7,68 (1H, m), 7,80 (1H, ddd, J = 7,8, 2,0, 0,9 Hz), 8,05 (1H, dt, J = 7,8, 0,9 Hz), 8,13 (1H, t, J = 2,0 Hz), 8,90 (1H, s).Exemplo de Referência 154
[00665] Produção de 5-[2-(3-clorofenil)-2-oxoetil]-6-etil-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 150, o composto titular (348 mg, 63 %) foi obtido como um pó verde a partir do composto do Exemplo de Referência 153 (460 mg, 1,10 mmol).
[00666] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3H, t, J = 7,3 Hz), 1,28 (3H, t, J = 7,1 Hz), 2,60 (2H, q, J = 7,3 Hz), 3,86 (3H, s), 4,26 (2H, q, J = 7,1 Hz), 4,83 (2H, q, J = 9,3 Hz), 5,61 (2H, s), 6,56 (1H, s), 7,61-7,69 (1H, m), 7,78-7,84 (1H, m), 8,03-8,09 (1H, m), 8,14 (1H, t, J = 1,7 Hz). Exemplo de Referência 155
[00667] Produção de ácido 5-[2-(3-clorofenil)-2-oxoetil]-6-etil-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 49, o composto titular (192 mg, 59 %) foi obtido como um pó castanho a partir do composto do Exemplo de Referência 154 (348 mg, 0,698 mmol).
[00668] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3H, t, J = 7,3 Hz), 2,60 (2H, q, J = 7,3 Hz), 3,86 (3H, s), 4,81 (2H, q, J = 9,2 Hz), 5,60 (2H, s), 6,55 (1H, s), 7,58-7,71 (1H, m), 7,76-7,86 (1H, m), 8,00-8,10 (1H, m), 8,14 (1H, t, J = 1,7 Hz), 12,72 (1H, br s).Exemplo de Referência 156
[00669] Produção de 6-etil-5-(2-metoxibenzil)-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 142, o composto titular (138 mg, 26 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 141 (400 mg, 1,16 mmol) e 1- (clorometil)-2-metoxibenzeno (272 mg, 1,74 mmol).
[00670] RMN 1H (300 MHz, DMSO-d6) δ:1,17 (3H, t, J = 7,4 Hz), 1,29 (3H, t, J = 7,1 Hz), 2,53-2,61 (2H, m), 3,86 (3H, s), 3,88 (3H, s), 4,26 (2H, q, J = 7,1 Hz), 4,86 (2H, q, J = 9,3 Hz), 5,22 (2H, br s), 6,41 (1H, dd, J = 7,5, 1,2 Hz), 6,57 (1H, s), 6,82 (1H, td, J = 7,5, 0,9 Hz), 7,01-7,09 (1H, m), 7,18-7,28 (1H, m).Exemplo de Referência 157
[00671] Produção de ácido 6-etil-5-(2-metoxibenzil)-1-metil-4-oxo-3- (2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 49, o composto titular (104 mg, 80 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 156 (138 mg, 0,296 mmol).
[00672] RMN 1H (300 MHz, DMSO-d6) δ:1,17 (3H, t, J = 7,3 Hz), 2,53-2,60 (2H, m), 3,86 (3H, s), 3,88 (3H, s), 4,84 (2H, q, J = 9,3 Hz), 5,22 (2H, br s), 6,40 (1H, dd, J = 7,5, 1,3 Hz), 6,55 (1H, s), 6,82 (1H, td, J = 7,5, 0,9 Hz), 7,00-7,11 (1H, m), 7,16-7,31 (1H, m), 12,72 (1H, br s).Exemplo de Referência 158
[00673] Produção de 6-etil-5-(4-metoxibenzil)-1-metil-4-oxo-3-(2,2,2- trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 142, o composto titular (175 mg, 43 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 141 (300 mg, 0,866 mmol) e 1- (clorometil)-4-metoxibenzeno (0,175 ml, 1,30 mmol).
[00674] RMN 1H (300 MHz, DMSO-d6) δ:1,16 (3H, t, J = 7,2 Hz), 1,29 (3H, t, J = 7,2 Hz), 2,62 (2H, q, J = 7,2 Hz), 3,71 (3H, s), 3,84 (3H, s), 4,26 (2H, q, J = 7,2 Hz), 4,90 (2H, q, J = 9,3 Hz), 5,26 (2H, br s), 6,51 (1H, s), 6,82-6,92 (2H, m), 6,97-7,08 (2H, m).Exemplo de Referência 159
[00675] Produção de ácido 6-etil-5-(4-metoxibenzil)-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 49, o composto titular (157 mg, 96 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 158 (175 mg, 0,375 mmol).
[00676] RMN 1H (300 MHz, DMSO-d6) δ:1,16 (3H, t, J = 7,3 Hz), 2,62 (2H, q, J = 7,3 Hz), 3,71 (3H, s), 3,84 (3H, s), 4,88 (2H, q, J = 9,3 Hz), 5,26 (2H, br s), 6,49 (1H, s), 6,81-6,92 (2H, m), 6,96-7,09 (2H, m), 12,70 (1H, br s).Exemplo de Referência 160
[00677] Produção de 5-(2-clorobenzil)-6-etil-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 142, o composto titular (163 mg, 30 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 141 (400 mg, 1,16 mmol) e 1-cloro-2- (clorometil)benzeno (0,226 ml, 1,74 mmol).
[00678] RMN 1H (300 MHz, DMSO-d6) δ:1,18 (3H, t, J = 7,4 Hz), 1,29 (3H, t, J = 7,1 Hz), 2,53-2,62 (2H, m), 3,87 (3H, s), 4,27 (2H, q, J = 7,1 Hz), 4,86 (2H, q, J = 9,3 Hz), 5,32 (2H, s), 6,55 (1H, dd, J = 7,6, 1,5 Hz), 6,62 (1H, s), 7,21-7,33 (2H, m), 7,52 (1H, dd, J = 7,7, 1,3 Hz).Exemplo de Referência 161
[00679] Produção de ácido 5-(2-clorobenzil)-6-etil-1-metil-4-oxo-3- (2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 49, o composto titular (138 mg, 90 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 160 (163 mg, 0,346 mmol).
[00680] RMN 1H (300 MHz, DMSO-d6) δ:1,18 (3H, t, J = 7,4 Hz), 2,52-2,62 (2H, m), 3,87 (3H, s), 4,83 (2H, q, J = 9,3 Hz), 5,32 (2H, s), 6,50 (1H, dd, J = 7,7, 1,6 Hz), 6,60 (1H, s), 7,22-7,33 (2H, m), 7,52 (1H, dd, J = 7,7, 1,3 Hz), 12,76 (1H, br s).Exemplo de Referência 162
[00681] Produção de 4-cloro-6-etil-2-oxo-1-(2-feniletil)-1,2-diidropiridina-3-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 142, o composto titular (480 mg, 16 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 38 (2,00 g, 8,71 mmol) e (2- bromoetil)benzeno (1,77 ml, 11,3 mmol).
[00682] RMN 1H (300 MHz, DMSO-d6) δ:1,14 (3H, t, J = 7,4 Hz), 1,28 (3H, t, J = 7,1 Hz), 2,63 (2H, q, J = 7,4 Hz), 2,85-2,93 (2H, m), 4,07-4,15 (2H, m), 4,29 (2H, q, J = 7,1 Hz), 6,30 (1H, s), 7,19-7,28 (3H, m), 7,28-7,38 (2H, m).Exemplo de Referência 163
[00683] Produção de 6-etil-3-hidróxi-1-metil-4-oxo-5-(2-feniletil)-4,5- diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 40, o composto titular (481 mg, 80 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 162 (480 mg, 1,44 mmol).
[00684] RMN 1H (300 MHz, DMSO-d6) δ:1,20 (3H, t, J = 7,3 Hz), 1,31 (3H, t, J = 7,1 Hz), 2,63 (2H, q, J = 7,3 Hz), 2,80-2,94 (2H, m), 3,75 (3H, s), 4,01-4,16 (2H, m), 4,30 (2H, q, J = 7,1 Hz), 6,34 (1H, s), 7,11-7,41 (5H, m), 8,94 (1H, br s).Exemplo de Referência 164
[00685] Produção de 6-etil-1-metil-4-oxo-5-(2-feniletil)-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 150, o composto titular (185 mg, 31 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 163 (482 mg, 1,31 mmol).
[00686] RMN 1H (300 MHz, DMSO-d6) δ:1,22 (3H, t, J = 7,3 Hz), 1,29 (3H, t, J = 7,2 Hz), 2,67 (2H, q, J = 7,3 Hz), 2,82-2,94 (2H, m), 3,82 (3H, s), 4,10-4,20 (2H, m), 4,26 (2H, q, J = 7,2 Hz), 4,90 (2H, q, J = 9,3 Hz), 6,46 (1H, s), 7,15-7,38 (5H, m).Exemplo de Referência 165
[00687] Produção de ácido 6-etil-1-metil-4-oxo-5-(2-feniletil)-3-(2,2,2- trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 49, o composto titular (143 mg, 83 %) foi obtido como um pó castanho a partir do composto do Exemplo de Referência 164 (185 mg, 0,411 mmol).
[00688] RMN 1H (300 MHz, DMSO-d6) δ:1,21 (3H, t, J = 7,2 Hz), 2,66 (2H, q, J = 7,2 Hz), 2,81-2,94 (2H, m), 3,81 (3H, s), 4,05-4,30 (2H, m), 4,89 (2H, q, J = 9,3 Hz), 6,44 (1H, s), 7,09-7,48 (5H, m), 12,67 (1H, br s).Exemplo de Referência 166
[00689] Produção de 5-(3-clorobenzil)-6-etil-1-metil-4-oxo-3-(2,2,2- trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 142, o composto titular (325 mg, 60 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 141 (400 mg, 1,16 mmol) e 1-cloro-3- (clorometil)benzeno (357 mg, 1,74 mmol).
[00690] RMN 1H (300 MHz, DMSO-d6) δ:1,17 (3H, t, J = 7,4 Hz), 1,29 (3H, t, J = 7,1 Hz), 2,60 (2H, q, J = 7,1 Hz), 3,85 (3H, s), 4,26 (2H, q, J = 7,4 Hz), 4,88 (2H, q, J = 9,3 Hz), 5,33 (2H, br s), 6,56 (1H, s), 6,96-7,05 (1H, m), 7,10-7,18 (1H, m), 7,27-7,43 (2H, m).Exemplo de Referência 167
[00691] Produção de ácido 5-(3-clorobenzil)-6-etil-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 49, o composto titular (281 mg, 92 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 166 (325 mg, 0,690 mmol).
[00692] RMN 1H (300 MHz, DMSO-d6) δ:1,17 (3H, t, J = 7,2 Hz), 2,60 (2H, q, J = 7,2 Hz), 3,85 (3H, s), 4,86 (2H, q, J = 9,3 Hz), 5,34 (2H, br s), 6,54 (1H, s), 6,95-7,05 (1H, m), 7,10-7,18 (1H, m), 7,26-7,43 (2H, m), 12,74 (1H, s).Exemplo de Referência 168
[00693] Produção de 5-(4-clorobenzil)-6-etil-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 142, o composto titular (213 mg, 39 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 141 (400 mg, 1,16 mmol) e 1-cloro-4- (clorometil)benzeno (357 mg, 1,74 mmol).
[00694] RMN 1H (300 MHz, DMSO-d6) δ:1,16 (3H, t, J = 7,3 Hz), 1,29 (3H, t, J = 7,1 Hz), 2,60 (2H, q, J = 7,1 Hz), 3,85 (3H, s), 4,26 (2H, q, J = 7,3 Hz), 4,88 (2H, q, J = 9,3 Hz), 5,32 (2H, br s), 6,55 (1H, s), 7,03-7,16 (2H, m), 7,66-7,43 (2H, m).Exemplo de Referência 169
[00695] Produção de ácido 5-(4-clorobenzil)-6-etil-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 49, o composto titular (188 mg, 94 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 168 (213 mg, 0,452 mmol).
[00696] RMN 1H (300 MHz, DMSO-d6) δ:1,16 (3H, t, J = 7,3 Hz), 2,59 (2H, q, J = 7,3 Hz), 3,84 (3H, s), 4,86 (2H, q, J = 9,3 Hz), 5,32 (2H, br s), 6,53 (1H, s), 7,01-7,20 (2H, m), 7,28-7,49 (2H, m), 12,75 (1H, br s).Exemplo de Referência 170
[00697] Produção de 3-etóxi-6-etil-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrotieno[3,2-c]piridina-2-carboxilato de etila Da mesma maneira que no Exemplo de Referência 5, 6-etil-3- hidróxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]piridina-2- carboxilato de etila foi obtido a partir do composto do Exemplo de Referência 39 (3,6 g, 10,3 mmol), tioglicolato de etila (14,4 ml, 103 mmol) e trietilamina (2,3 ml, 20,6 mmol). O composto titular (900 mg, 47 %) foi obtido como um sólido branco a partir do assim-obtido 6-etil-3-hidróxi-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidrotieno[3,2-c]piridina-2-carboxilato de etila (1,8 g, 4,7 mmol) por meio de um método similar àquele no Exemplo de Referência 43.
[00698] RMN 1H (300 MHz, DMSO-d6) δ:1,17 (3H, t, J = 7,4 Hz), 1,23-1,36 (6H, m), 2,61 (2H, q, J = 7,4 Hz), 4,14 (2H, q, J = 7,1 Hz), 4,28 (2H, q, J = 7,0 Hz), 5,65 (2H, s), 6,83 (1H, s), 7,62 (2H, t, J = 7,6 Hz), 7,707,79 (1H, m), 8,12 (2H, d, J = 7,2 Hz).Exemplo de Referência 171
[00699] Produção de ácido 3-(2,2-difluoroetóxi)-6-etil-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílico ME ZCOH AAo FDa mesma maneira que no Exemplo de Referência 56, 3-(2,2- difluoroetóxi)-6-etil-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H- pirrol[3,2-c]piridina-2-carboxilato de etila foi obtido a partir do composto do Exemplo de Referência 40 (500 mg, 1,31 mmol), trifluorometanossulfonato de 2,2-difluoroetila (336 mg, 1,57 mmol) e carbonato de césio (554 mg, 1,70 mmol). O composto titular (314 mg, 83 %) foi obtido como um pó branco a partir do assim-obtido 3-(2,2-difluoroetóxi)-6-etil-1-metil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etila (400 mg, 0,90 mmol) por meio de um método similar àquele no Exemplo de Referência 59.
[00700] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3H, t, J = 7,2 Hz), 2,58 (2H, q, J = 7,3 Hz), 3,85 (3H, s), 4,40 (2H, td, J = 14,6, 1,2 Hz), 5,60 (2H, s), 6,26 (1H, tt, J = 55,0, 3,9 Hz), 6,77 (1H, s), 7,58-7,76 (3H, m), 8,12 (2H, d, J = 7,5 Hz), 12,50-12,70 (1H, br).Exemplo de Referência 172
[00701] Produção de 6-etil-1-metil-4-oxo-5-(2-oxo-2-feniletil)-3-propóxi-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 56, o composto titular (177 mg, 83 %) foi obtido como um pó castanho a partir do composto do Exemplo de Referência 40 (191 mg, 0,50 mmol), sulfato de dipropila (364 mg, 2,0 mmol), carbonato de potássio (414 mg, 3,0 mmol) e acetona (20 ml).
[00702] RMN 1H (300 MHz, CDCl3) δ:1,01 (3 H, t, J = 7,5 Hz), 1,28 (3H, t, J = 7,3 Hz), 1,40 (3H, t, J = 7,5 Hz), 1,75-1,89 (2H, m), 2,51 (2 H, q, J = 7,2 Hz), 3,88 (3 H, s), 4,21 (2 H, t, J = 6,7 Hz), 4,36 (2H, q, J = 7,2 Hz), 5,59 (2 H, s), 6,19 (1 H, s), 7,47-7,56 (2 H, m), 7,59-7,67 (1 H, m), 8,02-8,09 (2H, m).Exemplo de Referência 173
[00703] Produção de ácido 6-etil-1-metil-4-oxo-5-(2-oxo-2-feniletil)-3- propóxi-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 59, o composto titular (237 mg, 93 %) foi obtido como um pó amarelo claro a partir do composto do Exemplo de Referência 172 (274 mg, 0,65 mmol). RMN 1H (300 MHz, DMSO-d6) δ:0,91 (3 H, t, J = 7,5 Hz), 1,18 (3H, t, J = 7,3 Hz), 1,55-1,70 (2H, m), 2,57 (2 H, q, J = 7,4 Hz), 3,84 (3 H, s), 4,07 (2 H, t, J = 6,5 Hz), 5,58 (2 H, s), 6,47 (1 H, s), 7,56-7,66 (2 H, m), 7,69-7,78 (1 H, m), 8,078,16 (2H, m), 12,42 (1 H, s).Exemplo de Referência 174
[00704] Produção de ácido 6-etil-1-metil-3-(1-metiletóxi)-4-oxo-5-(2- oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 56, 6-etil- 1-metil-3-(1-metiletóxi)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2- c]piridina-2-carboxilato de etila (291 mg, 46 %) foi obtido como um pó púrpura claro a partir do composto do Exemplo de Referência 40 (574 mg, 1,50 mmol), carbonato de potássio (1,04 g, 7,5 mmol) e sulfato de diisopropila (1,37 g, 7,5 mmol). O composto titular (242 mg, 97 %) foi obtido como um pó incolor a partir do assim-obtido 6-etil-1-metil-3-(1-metiletóxi)-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etila (267 mg, 0,63 mmol) por meio de um método similar àquele no Exemplo de Referência 59.
[00705] RMN 1H (300 MHz, DMSO-d6) δ:1,13-1,23 (9 H, m), 2,57 (2 H, q, J = 7,5 Hz), 3,84 (3 H, s), 4,65-4,80 (1H, m), 5,58 (2 H, s), 6,47 (1 H, s), 7,56-7,66 (2 H, m), 7,69-7,78 (1 H, m), 8,07-8,16 (2H, m), 12,29 (1 H, s). Exemplo de Referência 175
[00706] Produção de ácido 6-etil-1-metil-4-oxo-5-(2-oxo-2-feniletil)-3- (2,2,3,3-tetrafluoropropóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 150, 6-etil- 1-metil-4-oxo-5-(2-oxo-2-feniletil)-3-(2,2,3,3-tetrafluoropropóxi)-4,5-diidro- 1H-pirrol[3,2-c]piridina-2-carboxilato de etila (460 mg, 93 %) foi obtido como um pó cinza a partir do composto do Exemplo de Referência 40 (382 mg, 1,00 mmol), trifluorometanossulfonato de 2,2,3,3-tetrafluoropropila (913 mg, 3,46 mmol), carbonato de césio (391 mg, 1,20 mmol) e DMF (10 ml). O composto titular (310 mg, 95 %) foi obtido como um pó cinza a partir do assim-obtido 6-etil-1-metil-4-oxo-5-(2-oxo-2-feniletil)-3-(2,2,3,3-tetrafluoropropóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etila (348 mg, 0,70 mmol) por meio de um método similar àquele no Exemplo de Referência 59.
[00707] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3 H, t, J = 7,3 Hz), 2,58 (2 H, q, J = 7,3 Hz), 3,86 (3 H, s), 4,70 (2H, t, J = 13,1 Hz), 5,62 (2 H, s), 6,54 (1 H, s), 6,73 (1H, tt, J = 52,6, 6,1 Hz), 7,56-7,66 (2H, m), 7,69-7,79 (1H, m), 8,07-8,17 (2H, m), 12,93 (1H, br s).Exemplo de Referência 176
[00708] Produção de 3-(ciclopropilmetóxi)-6-etil-1-metil-4-oxo-5-(2- oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxilato de etilaDa mesma maneira que no Exemplo de Referência 150, o composto titular (65 mg, 15 %) foi obtido como um pó amarelo a partir do composto do Exemplo de Referência 40 (382 mg, 1,00 mmol), carbonato de césio (358 mg, 1,10 mmol), metanossulfonato de ciclopropilmetila (750 mg, 5,00 mmol) e DMF (10 ml).
[00709] RMN 1H (300 MHz, CDCl3) δ:0,29-0,36 (2 H, m), 0,49-0,57 (2H, m), 1,24-1,37 (1H, m), 1,28 (3H, t, J = 7,3 Hz), 1,41 (3H, t, J = 7,1 Hz), 2,51 (2 H, q, J = 7,4 Hz), 3,88 (3 H, s), 4,10 (2 H, d, J = 7,2 Hz), 4,37 (2H, q, J = 7,1 Hz), 5,59 (2H, s), 6,19 (1H, s), 7,47-7,55 (2H, m), 7,59-7,67 (1H, m), 8,02-8,10 (2H, m).Exemplo de Referência 177
[00710] Produção de ácido 3-(ciclopropilmetóxi)-6-etil-1-metil-4-oxo- 5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxílicoDa mesma maneira que no Exemplo de Referência 59, o composto titular (112 mg, 83 %) foi obtido como um pó incolor a partir do composto do Exemplo de Referência 176 (144 mg, 0,33 mmol).
[00711] RMN 1H (300 MHz, DMSO-d6) δ:0,17-0,27 (2H, m), 0,390,48 (2H, m), 1,03-1,22 (1H, m), 1,18 (3H, t, J = 7,3 Hz), 2,56 (2 H, q, J = 7,3 Hz), 3,84 (3 H, s), 3,94 (2H, d, J = 7,0 Hz), 5,58 (2 H, s), 6,46 (1H, s), 7,567,65 (2H, m), 7,69-7,77 (1H, m), 8,07-8,15 (2H, m), 12,43 (1H, br s).Exemplo 1
[00712] Produção de 3-metóxi-5-(2-oxo-2-feniletil)-2-(piperidin-1-ilcarbonil)tieno[3,2-c]quinolin-4(5H)-onaUma solução (0,10 M, 0,600 ml, 60 μmol) do composto do Exemplo de Referência 7 em DMF foi diluída com DMF (0,200 ml), e adicionou-se uma solução (1,0 M, 0,063 ml, 63 mmol) de piperidina em DMF e uma solução (0,50 M, 0,126 ml, 63 mmol) de HOBt e WSCD em mistura a 1:1 em DMF. A mistura obtida foi agitada à temperatura ambiente durante 13 h. Adicionou-se diclorometano (2 ml) e solução aquosa saturada de hidrogenocarbonato de sódio (1 ml) à mistura de reação, e a camada orgânica foi filtrada através de um filtro de Teflon (marca comercial registrada) para separação da camada aquosa, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de HPLC preparativa dando o composto titular (8,5 mg, 31 %).
[00713] LC/MS 461 (M+H).Exemplo 2
[00714] Produção de N-etil-N-(1-{[3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}pirrolidin-3-il) acetamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e N-etil-N- pirrolidin-3-ilacetamida.
[00715] LC/MS 532 (M+H).Exemplo 3
[00716] Produção de ditrifluoroacetato de N-[2-(dietilamina)etil]-3-metóxi-N-metil-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaA uma solução (0,12 M, 0,40 ml, 48 μmol) do composto doExemplo de Referência 19 em DMF adicionou-se uma solução (0,66 M, 0,10 ml, 63 mmol) de N,N-dietil-N’-metiletano-1,2-diamina em DMF e uma solução (0,39 M, 0,20 ml, 78 mmol) de HOBt e WSCD numa mistura a 1:1 em DMF. A mistura obtida foi agitada à temperatura ambiente durante 14 h. Adicionou-se diclorometano (2 ml) e solução aquosa saturada de hidrogenocarbonato de sódio (1 ml) à mistura de reação, e a camada orgânica foi filtrada através de um filtro de Teflon (marca comercial registrada) para separação da camada aquosa, e o filtrado foi concentrado sob pressão reduzida. O resíduo foi purificado por meio de HPLC preparativa dando o composto titular (33,2 mg, 98 %).
[00717] LC/MS 479 (M+H).Exemplo 4
[00718] Produção de ditrifluoroacetato de 2-{[4-(1,3-benzodioxol-5- ilmetil)piperazin-1-il]carbonil}-3-metóxi-5-(piridin-2-ilmetil)tieno[3,2-c]quinolin-4(5H)-ona Da mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 1-(1,3- benzodioxol-5-ilmetil)piperazina.
[00719] LC/MS 569 (M+H).Exemplo 5
[00720] Produção de trifluoroacetato de N-[2-(dimetilamina)etil]-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaA uma solução (0,15 M, 0,40 ml, 60 μmol) do composto do Exemplo de Referência 7 em DMF adicionou-se uma solução (0,66 M, 0,10 ml, 63 mmol) de N,N-dimetiletano-1,2-diamina em DMF e uma solução (0,39 M, 0,20 ml, 78 mmol) de HOBt e WSCD numa mistura a 1:1 em DMF. A mistura obtida foi agitada à temperatura ambiente durante 14 h. Adicionou-se diclorometano (2 ml) e solução aquosa saturada de hidrogenocarbonato de sódio (1 ml) à mistura de reação, e a camada orgânica foi filtrada através de um filtro de Teflon (marca comercial registrada) para separação da camada aquosa, e o filtrado foi concentrado sob pressão reduzida. O resíduo foi purificado por meio de HPLC preparativa dando o composto titular (25,2 mg, 73 %).
[00721] LC/MS 464 (M+H). Exemplo 6
[00722] Produção de trifluoroacetato de 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-N-(2-pirrolidin-1-iletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foiobtido a partir do composto do Exemplo de Referência 7 e 2-pirrolidin-1- iletanamina.
[00723] LC/MS 490 (M+H).Exemplo 7
[00724] Produção de trifluoroacetato de N-[3-(1H-imidazol-1-il)propil]-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c] quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 3-(1H-imidazol-1- il)propan-1-amina.
[00725] LC/MS 501 (M+H).Exemplo 8
[00726] Produção de trifluoroacetato de 3-metóxi-N-[2-(1- metilpirrolidin-2-il)etil]-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foiobtido a partir do composto do Exemplo de Referência 7 e 2-(1- metilpirrolidin-2-il)etanamina.
[00727] LC/MS 504 (M+H).Exemplo 9
[00728] Produção de trifluoroacetato de 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-N-(2-piperidin-1-iletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 2-piperidin-1- iletanamina.
[00729] LC/MS 504 (M+H). Exemplo 10
[00730] Produção de trifluoroacetato de N-[3-(dietilamina)propil]-3- metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e N,N-dietilpropano- 1,3-diamina.
[00731] LC/MS 506 (M+H).Exemplo 11
[00732] Produção de trifluoroacetato de 3-metóxi-N-(3-morfolin-4-ilpropil)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foiobtido a partir do composto do Exemplo de Referência 7 e 3-morfolin-4- ilpropan-1-amina.
[00733] LC/MS 520 (M+H). Exemplo 12
[00734] Produção de ditrifluoroacetato de 3-metóxi-N-[3-(4- metilpiperazin-1-il)propil]-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 3-(4- metilpiperazin-1-il)propan-1-amina.
[00735] LC/MS 533 (M+H).Exemplo 13
[00736] Produção de trifluoroacetato de N-[4-(dietilamina)-1-metilbutil]-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e N1,N1- dietilpentano-1,4-diamina.
[00737] LC/MS 534 (M+H).Exemplo 14
[00738] Produção de trifluoroacetato de N-(1-benzilpirrolidin-3-il)-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 1-benzilpirrolidin- 3-amina.
[00739] LC/MS 552 (M+H).Exemplo 15
[00740] Produção de trifluoroacetato de N-(1-benzilpiperidin-4-il)-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 1-benzilpiperidin- 4-amina.
[00741] LC/MS 566 (M+H). Exemplo 16
[00742] Produção de trifluoroacetato de 3-metóxi-N-metil-N-(1- metilpirrolidin-3-il)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e N,1- dimetilpirrolidin-3-amina.
[00743] LC/MS 490 (M+H).Exemplo 17
[00744] Produção de trifluoroacetato de 3-metóxi-2-[(4-metil-1,4-diazepan-1-il)carbonil]-5-(2-oxo-2-feniletil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 1-metil-1,4- diazepano.
[00745] LC/MS 490 (M+H).Exemplo 18
[00746] Produção de trifluoroacetato de 2-[(4-etilpiperazin-1- il)carbonil]-3-metóxi-5-(2-oxo-2-feniletil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foiobtido a partir do composto do Exemplo de Referência 7 e 1-etilpiperazina.
[00747] LC/MS 490 (M+H).Exemplo 19
[00748] Produção de trifluoroacetato de N-[2-(dietilamina)etil]-3- metóxi-N-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e N,N-dietil-N’- metiletano-1,2-diamina.
[00749] LC/MS 506 (M+H).Exemplo 20
[00750] Produção de trifluoroacetato de 3-metóxi-5-(2-oxo-2-feniletil)- 2-{[(2S)-2-(pirrolidin-1-ilmetil)pirrolidin-1-il]carbonil}tieno[3,2-c]quinolin-4(5H)-ona Da mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 1-[(2S)-pirrolidin- 2-ilmetil]pirrolidina.
[00751] LC/MS 530 (M+H).Exemplo 21
[00752] Produção de trifluoroacetato de 3-metóxi-5-(2-oxo-2-feniletil)-2-[(4-pirrolidin-1-ilpiperidin-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 4-pirrolidin-1- ilpiperidina.
[00753] LC/MS 530 (M+H).Exemplo 22
[00754] Produção de trifluoroacetato de N-(2-cianoetil)-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-N-(piridin-3-ilmetil)-4,5-diidrotieno[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 3-[(piridin-3- ilmetil)amina]propanonitrila.
[00755] LC/MS 537 (M+H).Exemplo 23
[00756] Produção de trifluoroacetato de 2-{[4-(1,3-benzodioxol-5-ilmetil)piperazin-1-il]carbonil}-3-metóxi-5-(2-oxo-2-feniletil)tieno[3,2- c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 1-(1,3- benzodioxol-5-ilmetil)piperazina.
[00757] LC/MS 596 (M+H).Exemplo 24
[00758] Produção de trifluoroacetato de N-[2-(dietilamina)etil]-3-(2- etoxietóxi)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e N,N-dietiletano- 1,2-diamina.
[00759] LC/MS 550 (M+H).Exemplo 25
[00760] Produção de N,N-dietil-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaA uma solução do composto do Exemplo de Referência 7 (130 mg, 0,33 mmol), dietilamina (36 mg, 0,49 mmol) e HOBt (67 mg, 0,49 mmol) em DMF (4 ml) adicionou-se WSCD (94 mg, 0,49 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 18 h. A mistura de reação foi diluída com solução aquosa saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura saturada, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em sílica-gel (eluado; acetato de etila), e o óleo obtido foi recristalizado de acetato de etila-éter de dietila dando o composto titular (104 mg, 70 %) como cristais brancos.
[00761] RMN 1H (300 MHz, DMSO-d6) δ:1,15 (6H, t, J = 7,1 Hz), 3,39-3,50 (4H, m), 3,87 (3H, s), 5,98 (2H, s), 7,33 (1H, t, J = 7,5 Hz), 7,48 (1H, d, J = 7,8 Hz), 7,56 (1H, td, J = 8,7, 1,2 Hz), 7,64 (2H, t, J = 7,5 Hz), 7,75 (1H, d, J = 7,5 Hz), 7,96 (1H, dd, J = 7,8, 1,2 Hz), 8,18 (2H, d, J = 7,5 Hz).Exemplo 26
[00762] Produção de 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-N-phenil- 4,5-diidrotieno[3,2-c]quinolina-2-carboxamida Da mesma maneira que no Exemplo 25, o composto titular (163 mg, 63 %) foi obtido como cristais laranja claros a partir do composto do Exemplo de Referência 7 (200 mg, 0,51 mmol) e anilina (48 ml, 0,51 mmol).
[00763] RMN 1H (300 MHz, DMSO-d6) δ:4,15 (3H, s), 6,02 (2H, s), 7,12-7,21 (1H, m), 7,32-7,44 (3H, m), 7,48-7,55 (1H, m), 7,56-7,70 (3H, m), 7,71-7,82 (3H, m), 8,09 (1H, dd, J = 7,9, 1,3 Hz), 8,14-8,24 (2H, m), 9,74 (1H, s).
[00764] Produção de 3-metóxi-N-metil-4-oxo-5-(2-oxo-2-feniletil)-N- (2-oxo-2-pirrolidin-1-iletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaUma solução mista do composto do Exemplo 120 (400 mg, 0,81 mmol) e uma solução aquosa 2N de hidróxido de sódio (10 ml) em THF (10 ml)-etanol (5 ml) foram agitadas à temperatura ambiente durante 2 h. A mistura de reação foi neutralizada com ácido clorídrico 2N (10 ml), e concentrada sob pressão reduzida. O resíduo foi repartido entre salmoura saturada e acetato de etila, e a fase aquosa extraída com acetato de etila. A fase orgânica foi combinada, secada sobre sulfato de magnésio, e concentrada sob pressão reduzida dando N-{[3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrotieno[3,2-c]quinolin-2-il]carbonil}-N-metilglicina (380 mg, 100 %) como um sólido branco.
[00765] O composto titular (84 mg, 40 %) foi obtido como cristais brancos a partir do assim-obtido N-{[3-metóxi-4-oxo-5-(2-oxo-2-feniletil)- 4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}-N-metilglicina (190 mg, 0,41 mmol) e pirrolidina (44 mg, 0,61 mmol) por meio de um método similar àquele no Exemplo 25.
[00766] RMN 1H (300 MHz, CDCl3) δ:1,75-2,05 (4H, m), 3,20 (1H, s), 3,27 (2H, s), 3,45-3,56 (4H, m), 4,01 (1H, s), 4,13 (2H, s), 4,23 (0,6H, br s), 4,29 (1,4H, s), 5,86 (2H, s), 7,03 (1H, d, J = 8,4 Hz), 7,23-7,28 (1H, m), 7,45 (1H, t, J = 8,0 Hz), 7,55 (2H, t, J = 7,5 Hz), 7,67 (1H, t, J = 7,2 Hz), 7,82 (1H, dd, J = 8,1, 1,2 Hz), 8,10-8,12 (2H, m). Exemplo 28
[00767] Produção de 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-N-(2-pirrolidin-1-iletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (1,54 g, 67 %) foi obtido como cristais brancos a partir do composto do Exemplo de Referência 7 (1,85 g, 4,69 mmol) e 1-(2-aminaetil)pirrolidina (642 mg, 5,63 mmol).
[00768] RMN 1H (300 MHz, DMSO-d6) δ:1,72 (4H, br s), 2,45-2,60 (4H, br), 2,64 (2H, t, J = 6,3 Hz), 3,44 (2H, t, J = 5,9 Hz), 4,01 (3H, s), 6,00 (2H, s), 7,35 (1H, t, J = 7,8 Hz), 7,49 (1H, d, J = 8,1 Hz), 7,55-7,67 (3H, m), 7,70 (1H, t, J = 7,5 Hz), 8,05 (1H, dd, J = 8,1, 1,5 Hz), 8,16-8,19 (3H, m).Exemplo 29
[00769] Produção de N-[2-(dietilamina)-2-oxoetil]-3-metóxi-N-metil- 4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidano Exemplo 25, o composto titular (124 mg, 58 %) foi obtido como cristais brancos a partir de N-{[3-metóxi-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}-N- metilglicina (190 mg, 0,41 mmol) obtido no Exemplo 27 e dietilamina (45 mg, 0,61 mmol).
[00770] RMN 1H (300 MHz, CDCl3) δ:1,05-1,31 (6H, m), 3,18 (1,2H, s), 3,26 (1,8H, s), 3,34-3,47 (4H, m), 4,01 (1,2H, s), 4,10 (1,8H, s), 4,30 (0,8H, s), 4,36 (1,2H, s), 5,85 (2H, s), 7,03 (1H, d, J = 8,4 Hz), 7,23-7,28 (1H, m), 7,46 (1H, t, J = 7,4 Hz), 7,55 (2H, t, J = 7,5 Hz), 7,67 (1H, t, J = 7,4 Hz), 7,82 (1H, d, J = 6,9 Hz), 8,11 (2H, d, J = 7,2 Hz).Exemplo 30
[00771] Produção de cloridrato de 3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-N-(2-pirrolidin-1-iletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaA uma solução do composto do Exemplo 28 (200 mg, 0,41 mmol) em acetato de etila (25 ml) adicionou-se solução 4N cloreto de hidrogênio acetato de etila (0,11 ml). O precipitado foi recolhido por meio de filtração, lavado com acetato de etila, e secado sob pressão reduzida dando o composto titular (162 mg, 75 %) como um pó branco.
[00772] RMN 1H (300 MHz, DMSO-d6) δ:1,77-2,10 (4H, m), 2,95- 3,10 (2H, br), 3,29-3,40 (2H, m), 3,55-3,75 (4H, m), 4,07 (3H, s), 6,00 (2H, s), 7,36 (1H, t, J = 7,4 Hz), 7,51 (1H, d, J = 8,4 Hz), 7,57-7,67 (3H, m), 7,78 (1H, t, J = 7,4 Hz), 8,06 (1H, dd, J = 7,8, 1,2 Hz), 8,16-8,19 (2H, m), 8,31 (1H, t, J = 6,0 Hz), 10,33 (1H, br s). Exemplo 31
[00773] Produção de metanossulfonato de 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-N-(2-pirrolidin-1-iletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaA uma solução do composto do Exemplo 28 (200 mg, 0,41 mmol) em acetato de etila (25 ml) adicionou-se uma solução de ácido metanossulfônico (39 mg, 0,41 mmol) em acetato de etila (5 ml). O precipitado foi recolhido por meio de filtração, lavado com acetato de etila, e secado sob pressão reduzida dando o composto titular (197 mg, 82 %) como um pó branco.
[00774] RMN 1H (300 MHz, DMSO-d6) δ:1,65-2,10 (4H, m), 2,30 (3H, s), 3,00-3,20 (2H, br), 3,35-3,45 (2H, br), 3,60-3,75 (4H, m), 4,06 (3H, s), 6,00 (2H, s), 7,36 (1H, t, J = 7,2 Hz), 7,51 (1H, d, J = 8,4 Hz), 7,57-7,67 (3H, m), 7,78 (1H, t, J = 7,5 Hz), 8,06 (1H, dd, J = 7,8, 1,2 Hz), 8,16-8,19 (2H, m), 8,29 (1H, t, J = 5,9 Hz), 9,30-9,45 (1H, br).Exemplo 32
[00775] Produção de N-(2-hidroxietil)-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (65,8 mg, 67 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (89,0 mg, 0,226 mmol) e 2-aminaetanol (16,3 ml, 0,271 mmol).
[00776] RMN 1H (300 MHz, DMSO-d6) δ:3,40-3,46 (2H, m), 3,543,59 (2H, m), 4,03 (3H, s), 4,87 (1H, t, J = 5,3 Hz), 5,99 (2H, s), 7,32-7,38 (1H, m), 7,48-7,67 (4H, m), 7,74-7,79 (1H, m), 8,00-8,06 (2H, m), 8,16-8,19 (2H, m).Exemplo 33
[00777] Produção de N-ciclopropil-3-metóxi-5-metil-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e ciclopropanamina.
[00778] LC/MS 329 (M+H).Exemplo 34
[00779] Produção de N-[2-(dietilamina)etil]-3-metóxi-4-oxo-5-(2-oxo- 2-femletil)-4,5-diidrotieno[3,2-c]qumolma-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (500 mg, 80 %) foi obtido como cristais brancos a partir do composto do Exemplo de Referência 7 (500 mg, 1,27 mmol) e N,N-dietiletilenodiamina (220 mg, 1,90 mmol).
[00780] RMN 1H (300 MHz, DMSO-d6) δ:1,00 (6H, t, J = 7,1 Hz), 2,50-2,62 (6H, m), 3,37-3,42 (2H, m), 4,03 (3H, s), 6,00 (2H, s), 7,35 (1H, t, J = 7,4 Hz), 7,49 (1H, d, J = 8,4 Hz), 7,55-7,67 (3H, m), 7,77 (1H, t, J = 7,5 Hz), 8,05 (1H, dd, J = 7,8, 1,5 Hz), 8,12 (1H, t, J = 5,1 Hz), 8,16-8,19 (2H, m).Exemplo 35
[00781] Produção de N-benzil-3-metóxi-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 1- fenilmetanamina.
[00782] LC/MS 379 (M+H).Exemplo 36
[00783] Produção de 3-metóxi-5-metil-4-oxo-N-(3-fenilpropil)-4,5- diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 3-fenilpropan-1- amina.
[00784] LC/MS 407 (M+H).Exemplo 37
[00785] Produção de 3-metóxi-N-(2-metoxietil)-5-metil-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 2- metoxietanamina.
[00786] LC/MS 347 (M+H).Exemplo 38
[00787] Produção de 3-metóxi-5-metil-4-oxo-N-(tetraidrofuran-2- ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 1-(tetraidrofuran- 2-il)metanamina.
[00788] LC/MS 373 (M+H).Exemplo 39
[00789] Produção de 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-N-(2-pirrolidin-1-iletil)-4,5-diidrofuro[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (125 mg, 66 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 24 (150 mg, 0,397 mmol) e 1-(2-aminaetil)pirrolidina (65,4 ml, 0,516 mmol).
[00790] RMN 1H (300 MHz, DMSO-d6) δ:1,69-1,73 (4H, m), 2,492,51 (4H, m), 2,61 (2H, t, J = 6,6 Hz), 3,40-3,46 (2H, m), 4,15 (3H, s), 6,00 (2H, s), 7,43 (1H, t, J = 8,1 Hz), 7,54 (1H, d, J = 8,4 Hz), 7,60-7,67 (3H, m), 7,74-7,79 (1H, m), 8,06 (1H, t, J = 8,6 Hz), 8,15-8,19 (3H, m).Exemplo 40
[00791] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N- (2-pirrolidin-1-iletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (145 mg, 78 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (150 mg, 0,384 mmol) e 1-(2-aminaetil)pirrolidina (63,3 ml, 0,499 mmol).
[00792] RMN 1H (300 MHz, DMSO-d6) δ:1,65-1,75 (4H, m), 2,482,55 (4H, m), 2,62 (2H, t, J = 6,2 Hz), 3,39-3,45 (2H, m), 3,97 (3H, s), 4,37 (3H, s), 5,97 (2H, s), 7,29-7,39 (2H, m), 7,45-7,50 (1H, m), 7,61-7,66 (2H, m), 7,73-7,78 (1H, m), 8,16-8,18 (3H, m), 8,39 (1H, dd, J = 8,1, 1,2 Hz).Exemplo 41
[00793] Produção de 5-(ciclopropilmetil)-N-[2-(dietilamina)etil]-3- metóxi-N-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaA uma solução do composto do Exemplo 121 (400 mg, 1,03 mmol) em DMF (5 ml) adicionou-se hidreto de sódio (60 % em óleo, 45,4 mg, 1,14 mmol) sob resfriamento com gelo, e a mistura foi agitada durante 15 min. Adicionou-se ciclopropilmetilbrometo (120 ml, 1,24 mmol) à mistura obtida sob resfriamento com gelo, e a mistura foi agitada durante 15 h. A mistura de reação foi adicionada a água, e a mistura foi extraída com acetato de etila. O extrato foi lavado com salmoura saturada, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=3/7) dando o composto titular (320 mg, 70 %) como um óleo incolor.
[00794] RMN 1H (300 MHz, DMSO-d6) δ:0,45-0,50 (4H, m), 0,701,05 (6H, br), 1,23-1,31 (1H, m), 2,25-2,70 (6H, br), 3,06 (3H, s), 3,40-3,60 (2H, br), 3,89 (3H, s), 4,27 (2H, d, J = 6,9 Hz), 7,30-7,35 (1H, m), 7,62-7,68 (1H, m), 7,76 (1H, d, J = 8,4 Hz), 7,91 (1H, dd, J = 7,8, 1,2 Hz).Exemplo 42
[00795] Produção de N-[2-(dietilamina)etil]-3-metóxi-N-metil-4-oxo- 5-(2-oxo-2-femletil)-4,5-diidrofuro[3,2-c]qumolma-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (130 mg, 80 %) foi obtido como um óleo incolor a partir do composto do Exemplo de Referência 24 (130 mg, 0,344 mmol) e N,N-dietil-N’- metiletilenodiamina (72,3 ml, 0,477 mmol).
[00796] RMN 1H (300 MHz, DMSO-d6) δ:0,75-0,90 (3H, br), 0,901,05 (3H, br), 2,25-2,40 (2H, br), 2,45-2,70 (4H, br), 2,95-3,30 (3H, br), 3,52 (2H, t, J = 6,5 Hz), 4,04 (3H, s), 5,99 (2H, s), 7,37-7,42 (1H, m), 7,52 (1H, d, J = 8,7 Hz), 7,57-7,67 (3H, m), 7,74-7,79 (1H, m), 8,04 (1H, d, J = 7,5 Hz), 8,16-8,19 (2H, m).Exemplo 43
[00797] Produção de 3-etóxi-4-oxo-5-(2-oxo-2-feniletil)-N-(2-pirrolidin-1-iletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (126 mg, 67 %) foi obtido como cristais brancos a partir do composto do Exemplo de Referência 9 (150 mg, 0,37 mmol) e 1-(2-aminaetil)pirrolidina (63 mg,0,55 mmol).
[00798] RMN 1H (300 MHz, DMSO-d6) δ:1,39 (3H, t, J = 7,0 Hz), 1,72 (4H, br s), 2,40-2,60 (4H, br), 2,63 (2H, t, J = 6,0 Hz), 3,40-3,47 (2H, m), 4,31 (2H, q, J = 7,0 Hz), 5,99 (2H, s), 7,35 (1H, t, J = 7,8 Hz), 7,48 (1H, d, J = 8,4 Hz), 7,56 (1H, dd, J = 7,2, 1,5 Hz), 7,64 (2H, t, J = 8,4 Hz), 7,77 (1H, t, J = 7,2 Hz), 8,05 (1H, dd, J = 8,1, 1,5 Hz), 8,10 (1H, br t), 8,16-8,19 (2H, m).Exemplo 44
[00799] Produção de N-[2-(dietilamina)etil]-N-etil-3-metóxi-4-oxo-5-(2-oxo-2-femletil)-4,5-diidrotieno[3,2-c]qumolma-2-carboxamidano Exemplo 25, o composto titular(150 mg, 56 %) foi obtido como cristais brancos a partir do composto do Exemplo de Referência 7 (200 mg, 0,51 mmol) e N,N,N’-trietiletilenodiamina (110 mg, 0,76 mmol).
[00800] RMN 1H (300 MHz, DMSO-d6) δ:0,70-1,10 (6H, br), 1,14 (3H, br t), 2,20-2,70 (6H, br), 3,40-3,60 (4H, br), 3,87 (3H, s), 5,98 (2H, s), 7,33 (1H, t, J = 7,5 Hz), 7,47 (1H, d, J = 8,1 Hz), 7,55 (1H, td, J = 7,8, 1,5 Hz), 7,64 (2H, t, J = 7,5 Hz), 7,77 (1H, t, J = 7,5 Hz), 7,95 (1H, dd, J = 7,8, 1,5 Hz), 8,16-8,19 (2H, m).Exemplo 45
[00801] Produção de cloridrato de N-[2-(dietilamina)etil]-3-etóxi-N- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaA uma solução do composto do Exemplo de Referência 9 (150 mg, 0,37 mmol), N,N-dietil-N’-metiletilenodiamina (72 mg, 0,55 mmol) e HOBt (74 mg, 0,55 mmol) em DMF (5 ml) adicionou-se WSCD (105 mg, 0,55 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 18 h. A mistura de reação foi diluída com solução aquosa saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura saturada, secado sobre sulfato de magnésio, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em sílica-gel (eluado; acetato de etila/hexano=1/1) dando um sólido não-cristalino branco (180 mg).
[00802] A uma solução do sólido não-cristalino branco (180 mg) em acetato de etila (5 ml) adicionou-se solução 4N cloreto de hidrogênio acetato de etila (0,1 ml). O precipitado foi recolhido por meio de filtração, lavado com acetato de etila, e seca sob pressão reduzida dando o composto titular (173 mg, 83 %) como um pó branco.
[00803] RMN 1H (300 MHz, DMSO-d6) δ:1,15-1,35 (9H, m), 3,123,40 (9H, br), 3,84 (2H, t, J = 7,2 Hz), 4,14 (2H, q, J = 7,0 Hz), 5,99 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,1 Hz), 7,55-7,67 (3H, m), 7,75-7,80 (1H, m), 7,98 (1H, dd, J = 8,1, 1,5 Hz), 8,16-8,19 (2H, m), 9,85-10,10 (1H, br).Exemplo 46
[00804] Produção de cloridrato de N-[2-(dietilamina)etil]-3-metóxi-N- (1-metiletil)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 45, o composto titular (164 mg, 56 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (200 mg, 0,51 mmol) e N,N-dietil-N’- isopropiletilenodiamina (120 mg, 0,76 mmol).
[00805] RMN 1H (300 MHz, DMSO-d6) δ:1,20-1,35 (12H, m), 3,153,40 (6H, br), 3,65-3,80 (2H, m), 3,89 (3H, s), 4,10-4,30 (1H, br), 5,99 (2H, s), 7,33 (1H, t, J = 7,5 Hz), 7,49-7,67 (4H, m), 7,77 (1H, t, J = 7,5 Hz), 7,97 (1H, dd, J = 7,2, 1,2 Hz), 8,16-8,19 (2H, m), 9,95-10,10 (1H, br).Exemplo 47
[00806] Produção de N-(1-etilpropil)-3-metóxi-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e pentan-3-amina.
[00807] LC/MS 359 (M+H).Exemplo 48
[00808] Produção de cloridrato de N-[2-(dietilamina)etil]-3-metóxi-5-(4-metoxibenzil)-N-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 25, N-[2-(dietilamina)etil]-3-metóxi-5-(4-metoxibenzil)-N-metil-4-oxo-4,5-diidrotieno [3,2-c]quinolina-2-carboxamida (4,90 g, 85 %) foi obtido como um óleo incolor a partir do composto do Exemplo de Referência 13 (4,50 g, 11,4 mmol) e N,N-dietil-N’-metiletilenodiamina (2,40 ml, 14,8 mmol).
[00809] O composto titular (490 mg, 91 %) foi obtido como um pó branco a partir do assim-obtido N-[2-(dietilamina)etil]-3-metóxi-5-(4- metoxibenzil)-N-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamida (500 mg, 0,985 mmol) por meio de um método similar àquele no Exemplo 30.
[00810] RMN 1H (300 MHz, DMSO-d6) δ:1,15-1,35 (6H, br), 3,13 (3H, s), 3,10-3,40 (6H, br), 3,70 (3H, s), 3,87 (2H, t, J = 6,6 Hz), 3,96 (3H, s), 5,52 (2H, s), 6,87 (2H, d, J = 8,6 Hz), 7,20 (2H, d, J = 8,6 Hz), 7,30 (1H, t, J = 7,2 Hz), 7,49-7,58 (2H, m), 7,92 (1H, d, J = 7,8 Hz), 10,55 (1H, s).Exemplo 49
[00811] Produção de N-[2-(dietilamina)etil]-3-metóxi-N-metil-4-oxo- 5-(2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 41, o composto titular (45,1 mg, 28 %) foi obtido como um óleo incolor a partir do composto do Exemplo 121 (125 mg, 0,323 mmol) e (2-bromoetil)benzeno (53,5 ml, 0,387 mmol).
[00812] RMN 1H (300 MHz, DMSO-d6) δ:0,75-1,05 (6H, br), 2,25- 2,70 (6H, br), 2,92-2,97 (2H, m), 3,05 (3H, s), 3,40-3,55 (2H, br), 3,88 (3H, s), 4,50 (2H, t, J = 6,5 Hz), 7,20-7,26 (1H, m), 7,30-7,36 (5H, m), 7,63-7,75 (2H, m), 7,92 (1H, dd, J = 7,8, 1,5 Hz).Exemplo 50
[00813] Produção de N-[2-(dietilamina)etil]-5-(3,3-dimetil-2-oxobutil)-3-metóxi-N-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 41, o composto titular (45,1 mg, 28 %) foi obtido como um óleo incolor a partir do composto do Exemplo 121 (125 mg, 0,323 mmol) e 1-bromo-3,3-dimetilbutan-2-ona (57,9 ml, 0,441 mmol).
[00814] RMN 1H (300 MHz, DMSO-d6) δ:0,70-1,10 (6H, br), 1,30 (9H, s), 2,20-2,40 (6H, br), 3,06 (3H, s), 3,40-3,60 (2H, br), 3,87 (3H, s), 5,47 (2H, s), 7,28-7,34 (2H, m), 7,55-7,61 (1H, m), 7,92 (1H, dd, J = 7,8, 1,2 Hz).Exemplo 51
[00815] Produção de N-[2-(dietilamina)etil]-3-metóxi-N-metil-4-oxo- 5-(2-fenoxietil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 41, o composto titular (75,1 mg, 43 %) foi obtido como um óleo incolor a partir do composto do Exemplo 121 (135 mg, 0,348 mmol) e (2-bromoetóxi)benzeno (105 mg, 0,522 mmol).
[00816] RMN 1H (300 MHz, DMSO-d6) δ:0,70-1,10 (6H, br), 2,20- 2,70 (6H, br), 3,05 (3H, s), 3,40-3,60 (2H, br), 3,91 (3H, s), 4,30 (2H, t, J = 5,9 Hz), 4,73 (2H, t, J = 5,9 Hz), 6,88-6,93 (3H, m), 7,22-7,36 (3H, m), 7,65 (1H, t, J = 8,0 Hz), 7,83 (1H, d, J = 8,7 Hz), 7,91 (1H, d, J = 7,8 Hz).Exemplo 52
[00817] Produção de cloridrato de N-[2-(dietilamina)etil]-3-metóxi-N- metil-4-oxo-5-[2-oxo-2-(fenilamina)etil]-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaA uma solução do composto do Exemplo 122 (150 mg, 0,336 mmol), anilina (39,8 mg, 0,437 mmol) e HOBt (68,2 mg, 0,505 mmol) em DMF (3 ml) adicionou-se WSCD (96,8 mg, 0,505 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com solução aquosa saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura saturada, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=1/1) dando N-[2-(dietilamina)etil]-3-metóxi-N-metil-4-oxo-5- [2-oxo-2-(fenilamina)etil]-4,5-diidrotieno[3,2-c]quinolina-2-carboxamida como um óleo incolor.
[00818] O composto titular (65,2 mg, 35 %) foi obtido como um pó branco a partir do assim-obtido N-[2-(dietilamina)etil]-3-metóxi-N-metil-4- oxo-5-[2-oxo-2-(fenilamina)etil]-4,5-diidrotieno[3,2-c]quinolina-2- carboxamida por meio de um método similar àquele no Exemplo 30.
[00819] RMN 1H (300 MHz, DMSO-d6) δ:1,10-1,35 (6H, br), 3,12 (3H, s), 3,15-3,40 (6H, br), 3,75-3,90 (2H, br), 3,92 (3H, s), 5,22 (2H, s), 7,07 (1H, t, J = 7,5 Hz), 7,29-7,38 (3H, m), 7,53-7,66 (4H, m), 7,96 (1H, dd, J =7,5, 1,4 Hz), 9,76 (1H, s), 10,51 (1H, s).Exemplo 53
[00820] Produção de [2-{[2-(dietilamina)etil](metil)carbamoil}-3-metóxi-4-oxotieno[3,2-c]quinolin-5(4H)-il]acetato de etilaDa mesma maneira que no Exemplo 41, o composto titular (680 mg, 83 %) foi obtido como um óleo incolor a partir do composto do Exemplo 121 (670 mg, 1,73 mmol) e bromoacetato de etila (229 ml, 2,08 mmol).
[00821] RMN 1H (300 MHz, DMSO-d6) δ:0,70-1,10 (6H, br), 1,23 (3H, t, J = 7,1 Hz), 2,25-2,70 (6H, m), 3,06 (3H, s), 3,40-3,60 (2H, br), 3,89 (3H, s), 4,18 (2H, q, J = 7,1 Hz), 5,16 (2H, s), 7,34 (1H, t, J = 7,7 Hz), 7,51 (1H, d, J = 8,1 Hz), 7,61 (1H, t, J = 8,1 Hz), 7,94 (1H, d, J = 7,7 Hz).Exemplo 54
[00822] Produção de 3-metóxi-5-metil-4-oxo-N-prop-2-in-1-il-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e prop-2-in-1- amina.
[00823] LC/MS 327 (M+H).Exemplo 55
[00824] Produção de N-[2-(dimetilamina)etil]-3-metóxi-1-metil-4-oxo-5-(2-oxo-2-femletil)-4,5-diidro-1H-pirrol[3,2-c]quinolma-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (65,0 mg, 61 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (90,0 mg, 0,231 mmol) e N,N- dimetiletilenodiamina (25,2 ml, 0,300 mmol).
[00825] RMN 1H (300 MHz, DMSO-d6) δ:2,22 (6H, s), 2,44 (2H, t, J = 6,2 Hz), 3,37-3,43 (2H, m), 3,98 (3H, s), 4,38 (3H, s), 5,97 (2H, s), 7,29-7,39 (2H, m), 7,45-7,51 (1H, m), 7,63 (2H, t, J = 7,7 Hz), 7,73-7,79 (1H, m), 8,118,19 (3H, m), 8,38 (1H, dd, J = 8,4, 1,2 Hz).Exemplo 56
[00826] Produção de cloridrato de N-[2-(dietilamina)etil]-3-metóxi- N,1-dimetil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina- 2-carboxamidaDa mesma maneira que no Exemplo 25, N-[2-(dietilamina)etil]-3-metóxi-N,1-dimetil-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidro-1H-pirrol[3,2-c]quinolina-2-carboxamida foi obtido como um óleo incolor a partir do composto do Exemplo de Referência 28 (90,0 mg, 0,231 mmol) e N,N-dietil-N’-metiletilenodiamina (48,6 ml, 0,300 mmol).
[00827] O composto titular (75,1 mg, 60 %) foi obtido como um pó branco a partir do assim-obtido N-[2-(dietilamina)etil]-3-metóxi-N,1-dimetil- 4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamida por meio de um método similar àquele no Exemplo 30.
[00828] RMN 1H (300 MHz, DMSO-d6) δ:1,15-1,31 (6H, br), 2,953,40 (9H, br), 3,80-3,95 (5H, m), 4,03 (3H, s), 5,98 (2H, s), 7,29-7,50 (3H, m), 7,64 (2H, t, J = 7,5 Hz), 7,73-7,79 (1H, m), 8,16-8,19 (2H, m), 8,34 (1H, dd, J = 8,3, 1,1 Hz), 9,80-10,15 (1H, br).Exemplo 57
[00829] Produção de N-[2-(3,4-dimetoxifenil)etil]-3-metóxi-5-metil-4- oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 2-(3,4- dimetoxifenil)etanamina.
[00830] LC/MS 453 (M+H).Exemplo 58
[00831] Produção de cloridrato de N-[2-(dietilamina)etil]-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-N-(2,2,2-trifluoroetil)-4,5-diidrotieno[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 45, o composto titular (12 mg, 7 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (116 mg, 0,29 mmol) e N,N-dietil-N’-(2,2,2-trifluoroetil)etilenodiamina (70 mg, 0,35 mmol).
[00832] RMN 1H (300 MHz, CDCl3) δ:0,80-1,10 (6H, br), 2,30-2,70 (6H, br), 3,75 (2H, t, J = 5,6 Hz), 4,02 (3H, s), 4,44 (2H, br d, J = 7,8 Hz), 5,86 (2H, s), 7,04 (1H, d, J = 8,4 Hz), 7,26 (1H, t, J = 7,8 Hz), 7,47 (1H, td, J = 8,7, 1,5 Hz), 7,56 (2H, t, J = 7,5 Hz), 7,65-7,70 (1H, m), 7,83 (1H, dd, J = 7,8, 1,5 Hz), 8,11 (2H, d, J = 7,2 Hz).Exemplo 59
[00833] Produção de 3-metóxi-5-metil-N-[3-(1-metiletóxi)propil]-4- oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 3-(1- metiletóxi)propan-1-amina.
[00834] LC/MS 389 (M+H).Exemplo 60
[00835] Produção de 3-metóxi-5-metil-4-oxo-N-[3-(2-oxopirrolidin-1- il)propil]-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 1-(3- aminapropil)pirrolidin-2-ona.
[00836] LC/MS 414 (M+H).Exemplo 61
[00837] Produção de cloridrato de N-(2-aminaetil)-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaUma solução do composto do Exemplo 64 (90 mg, 0,17 mmol) e solução 4N cloreto de hidrogênio acetato de etila (10 ml) em acetato de etila (20 ml) foi agitada à temperatura ambiente durante 5 h. O precipitado foi recolhido por meio de filtração, lavado com acetato de etila e éter de dietila, e secado sob pressão reduzida dando o composto titular (78 mg, 97 %) como um pó branco.
[00838] RMN 1H (300 MHz, DMSO-d6) δ:3,02 (2H, t, J = 6,0 Hz),3,62 (2H, q, J = 6,0 Hz), 4,06 (3H, s), 6,00 (2H, s), 7,36 (1H, t, J = 7,4 Hz), 7,50 (1H, d, J = 8,4 Hz), 7,57-7,59 (3H, m), 7,65 (1H, t, J = 7,5 Hz), 7,94 (3H, br s), 8,06 (1H, dd, J = 8,1, 1,5 Hz), 8,16-8,23 (3H, m). Exemplo 62
[00839] Produção de cloridrato de N-(3-aminapropil)-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 61, o composto titular (121 mg, 100 %) foi obtido como um pó branco a partir do composto do Exemplo 65 (130 mg, 0,24 mmol).
[00840] RMN 1H (300 MHz, DMSO-d6) δ:1,80-1,90 (2H, m), 2,85 (2H, t, J = 7,4 Hz), 3,33-3,49 (2H, m), 4,04 (3H, s), 6,00 (2H, s), 7,36 (1H, t, J = 7,4 Hz), 7,50 (1H, d, J = 8,1 Hz), 7,56-7,67 (3H, m), 7,75-7,80 (4H, m), 8,05 (1H, dd, J = 7,8, 1,2 Hz), 8,16-8,23 (3H, m).Exemplo 63
[00841] Produção de cloridrato de N-(3-amina-2,2-dimetilpropil)-3- metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 61, o composto titular (123 mg, 92 %) foi obtido como um pó branco a partir do composto do Exemplo 66 (150 mg, 0,26 mmol).
[00842] RMN 1H (300 MHz, DMSO-d6) δ:1,01 (6H, s), 2,69 (2H, q, J = 6,0 Hz), 3,32 (2H, d, J = 6,6 Hz), 4,08 (3H, s), 6,01 (2H, s), 7,34 (1H, t, J = 7,8 Hz), 7,51 (1H, d, J = 8,1 Hz), 7,57-7,67 (3H, m), 7,78 (1H, t, J = 7,2 Hz), 7,90 (3H, br s), 8,06 (1H, dd, J = 8,1, 1,5 Hz), 8,17-8,19 (3H, m).Exemplo 64
[00843] Produção de [2-({[3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrotieno[3,2-c]quinolin-2-il]carbonil}amina)etil]carbamato de t-butilaDa mesma maneira que no Exemplo 25, o composto titular (136 mg, 50 %) foi obtido como cristais brancos a partir do composto do Exemplo de Referência 7 (200 mg, 0,51 mmol) e N-(2-aminaetil)carbamato de t-butila (122 mg, 0,76 mmol).
[00844] RMN 1H (300 MHz, DMSO-d6) δ:1,37 (9H, s), 3,10-3,20 (2H, m), 3,37-3,41 (2H, m), 4,04 (3H, s), 6,00 (2H, s), 6,99 (1H, br t), 7,35 (1H, t, J = 7,4 Hz), 7,49 (1H, d, J = 8,4 Hz), 7,55-7,67 (3H, m), 7,77 (1H, t, J = 7,5 Hz), 8,04-8,07 (2H, m), 8,16-8,19 (2H, m).Exemplo 65
[00845] Produção de [3-({[3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrotieno[3,2-c]quinolin-2-il]carbonil}amina)propil]carbamato de t-butilaDa mesma maneira que no Exemplo 25, o composto titular (136 mg, 50 %) foi obtido como cristais brancos a partir do composto do Exemplo de Referência 7 (200 mg, 0,51 mmol) e N-(3-aminapropil)carbamato de t-butila (133 mg, 0,76 mmol).
[00846] RMN 1H (300 MHz, DMSO-d6) δ:1,32 (9H, s), 1,60-1,70 (2H, m), 2,90-3,00 (2H, m), 3,25-3,35 (2H, m), 4,05 (3H, s), 6,00 (2H, s), 6,91 (1H, br t), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,4 Hz), 7,55-7,67 (3H, m), 7,77 (1H, t, J = 7,2 Hz), 8,05 (1H, dd, J = 7,8, 1,2 Hz), 8,17-8,19 (3H, m). Exemplo 66
[00847] Produção de [3-({[3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrotieno[3,2-c]quinolin-2-il]carbonil}amina)-2,2-dimetilpropil]carbamato de t-butilaDa mesma maneira que no Exemplo 25, o composto titular (205 mg, 69 %) foi obtido como cristais brancos a partir do composto do Exemplo de Referência 7 (200 mg, 0,51 mmol) e 1-Boc-amina-2,2-dimetil- 1,3-propanodiamina (154 mg, 0,76 mmol).
[00848] RMN 1H (300 MHz, DMSO-d6) δ:1,42 (9H, s), 2,81 (2H, d, J = 6,3 Hz), 3,13 (2H, d, J = 6,3 Hz), 4,09 (3H, s), 6,00 (2H, s), 7,11 (1H, br t), 7,35 (1H, t, J = 7,5 Hz), 7,50 (1H, d, J = 8,4 Hz), 7,56-7,67 (3H, m), 7,77 (1H, t, J = 7,5 Hz), 8,05 (1H, dd, J = 8,1, 1,5 Hz), 8,16-8,19 (2H, m), 8,37 (1H, br t).Exemplo 67
[00849] Produção de cloridrato de N-[2-(dimetilamina)etil]-3-metóxi- N-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaA uma solução do composto do Exemplo de Referência 7 (200 mg, 0,51 mmol), N,N,N’-trimetiletilenodiamina (78 mg, 0,76 mmol) e HOBt (103 mg, 0,76 mmol) em DMF (5 ml) adicionou-se WSCD (145 mg, 0,76 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 24 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em sílica-gel (eluado; acetato de etila/hexano=2/1) dando N-[2-(dimetilamina)etil]-3-metóxi-N-metil-4-oxo-5-(2-oxo-2-feniletil)- 4,5-diidrotieno[3,2-c]quinolina-2-carboxamida (180 mg) como uma substância amorfa incolor.
[00850] A uma solução da N-[2-(dimetilamina)etil]-3-metóxi-N-metil- 4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamida (180 mg, 0,38 mmol) em acetato de etila (10 ml) adicionou-se solução 4N cloreto de hidrogênio acetato de etila (0,1 ml), e o precipitado obtido foi recolhido por meio de filtração, lavado com éter de dietila, e secado sob pressão reduzida dando o composto titular (144 mg, 55 %) como um pó branco.
[00851] RMN 1H (300 MHz, DMSO-d6) δ:1,15 (6H, t, J = 7,1 Hz), 3,10 (3H, s), 3,39-3,50 (4H, m), 3,87 (3H, s), 5,98 (2H, s), 7,33 (1H, t, J = 7,5 Hz), 7,48 (1H, d, J = 7,8 Hz), 7,56 (1H, td, J = 8,7, 1,2 Hz), 7,64 (2H, t, J = 7,5 Hz), 7,75 (1H, d, J = 7,5 Hz), 7,96 (1H, dd, J = 7,8, 1,2 Hz), 8,18 (2H, d, J = 7,5 Hz).Exemplo 68
[00852] Produção de 3-etóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N-(2- pirrolidin-1-iletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (44,0 mg, 18 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 30 (200 mg, 0,495 mmol) e 1-(2-aminaetil)pirrolidina (82,1 ml, 0,644 mmol).
[00853] RMN 1H (300 MHz, DMSO-d6) δ:1,32 (3H, t, J = 7,0 Hz), 1,65-1,75 (4H, br), 2,40-2,55 (4H, br), 2,62 (2H, t, J = 6,0 Hz), 3,05-3,47 (2H, m), 4,29 (2H, q, J = 7,0 Hz), 4,39 (3H, s), 5,96 (2H, s), 7,29-7,39 (2H, m), 7,48 (1H, t, J = 7,8 Hz), 7,63 (2H, t, J = 7,7 Hz), 7,76 (1H, t, J = 7,4 Hz), 8,12-8,19 (3H, m), 8,38 (1H, d, J = 8,4 Hz).Exemplo 69
[00854] Produção de N-[2-(4-hidroxipiperidin-1-il)etil]-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (210 mg, 79 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e 4-(2-aminaetil)cicloexanol (96,0 mg, 0,606 mmol).
[00855] RMN 1H (300 MHz, DMSO-d6) δ:1,35-1,50 (2H, br), 1,701,80 (2H, br), 2,00-2,15 (2H, br), 2,45-2,55 (2H, br), 2,70-2,85 (2H, br), 3,353,50 (3H, m), 4,01 (3H, s), 4,38 (3H, s), 4,56 (1H, d, J = 4,5 Hz), 5,97 (2H, s), 7,29-7,40 (2H, m), 7,48 (1H, t, J = 7,8 Hz), 7,64 (2H, t, J = 7,7 Hz), 7,76 (1H, t, J = 7,2 Hz), 8,12-8,19 (3H, m), 8,38 (1H, d, J = 8,4 Hz).Exemplo 70
[00856] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N- (2-piperidin-1-iletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular(230 mg, 90 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e 1-(2-aminaetil)piperidina (94,9 ml, 0,666 mmol).
[00857] RMN 1H (300 MHz, DMSO-d6) δ:1,30-1,65 (6H, br), 2,302,60 (6H, br), 3,40-3,45 (2H, m), 4,01 (3H, s), 4,38 (3H, s), 5,97 (2H, s), 7,297,39 (2H, m), 7,45-7,51 (1H, m), 7,63 (2H, t, J = 7,5 Hz), 7,73-7,78 (1H, m), 8,11-8,19 (3H, m), 8,38 (1H, dd, J = 8,4, 1,2 Hz).Exemplo 71
[00858] Produção de 3-metóxi-1-metil-N-(2-morfolin-4-iletil)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular(210 mg, 82 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e 1-(2-aminaetil)morfolina (87,4 ml, 0,666 mmol).
[00859] RMN 1H (300 MHz, DMSO-d6) δ:2,40-2,55 (6H, br), 3,403,50 (2H, br), 3,61 (4H, t, J = 4,2 Hz), 4,01 (3H, s), 4,37 (3H, s), 5,97 (2H, s), 7,29-7,40 (2H, m), 7,48 (1H, t, J = 7,7 Hz), 7,64 (2H, t, J = 7,4 Hz), 7,76 (1H, t, J = 7,4 Hz), 8,12-8,19 (3H, m), 8,38 (1H, d, J = 8,4 Hz).Exemplo 72
[00860] Produção de N-[3-(dimetilamina)propil]-3-metóxi-1-metil-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (163 mg, 67 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e N,N-dimetilpropano-1,3- diamina (80,0 ml, 0,666 mmol).
[00861] RMN 1H (300 MHz, DMSO-d6) δ:1,75-1,84 (2H, m), 2,43 (6H, s), 2,65 (2H, t, J = 7,2 Hz), 3,34-3,41 (2H, m), 4,00 (3H, s), 4,32 (3H, s), 5,97 (2H, s), 7,29-7,40 (2H, m), 7,45-7,51 (1H, m), 7,63 (2H, t, J = 7,7 Hz), 7,74-7,78 (1H, m), 8,11-8,19 (3H, m), 8,37 (1H, dd, J = 8,4, 1,2 Hz).Exemplo 73
[00862] Produção de cloridrato de 2-{[2-(aminametil)piperidin-1- il]carbonil}-3-metóxi-5-(2-oxo-2-feniletil)tieno[3,2-c]quinolin-4(5H)-onaA uma solução do composto do Exemplo de Referência 7 (150 mg, 0,38 mmol), 2-(Boc-aminametil)piperidina (122 mg, 0,58 mmol) e HOBt (77 mg, 0,58 mmol) em DMF (5 ml) adicionou-se WSCD (109 mg, 0,58 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 3 dias. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em sílica-gel (eluado; acetato de etila/hexano=1/1 to 2/1) dando [(1-{[3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2- c]quinolin-2-il]carbonil}piperidin-2-il)metil]carbamato de t-butila (150 mg) como um óleo incolor.
[00863] Uma solução do [(1-{[3-metóxi-4-oxo-5-(2-oxo-2-feniletil)- 4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}piperidin-2-il)metil]carbamato de t-butila obtido (150 mg) e solução 4N cloreto de hidrogênio acetato de etila (8 ml) em acetato de etila (15 ml) foi agitada à temperatura ambiente durante 18 h. O precipitado obtido foi recolhido por meio de filtração, lavado com éter de dietila, e secado sob pressão reduzida dando o composto titular (133 mg, 67 %) como um pó branco.
[00864] RMN 1H (300 MHz, DMSO-d6) δ:1,40-1,90 (6H, m), 3,003,15 (2H, m), 3,20-3,30 (1H, m), 3,60-3,80 (1H, m), 3,90 (3H, s), 4,75-4,90 (1H, br), 5,99 (2H, s), 7,35 (1H, t, J = 7,4 Hz), 7,48-7,67 (4H, m), 7,77 (1H, t, J = 7,4 Hz), 7,85-8,00 (4H, m), 8,16-8,19 (2H, m). Exemplo 74
[00865] Produção de cloridrato de 3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-N-(piperidin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 73, o composto titular (95 mg, 53 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (150 mg, 0,38 mmol) e 2-aminametil-N-Boc-piperidina (122 mg, 0,57 mmol).
[00866] RMN 1H (300 MHz, DMSO-d6) δ:1,44-1,91 (6H, m), 2,85 (1H, q, J = 12,0 Hz), 3,26 (2H, d, J = 12,0 Hz), 3,47-3,55 (1H, m), 3,62-3,69 (1H, m), 4,06 (3H, s), 6,01 (2H, s), 7,36 (1H, t, J = 7,5 Hz), 7,51 (1H, d, J = 8,1 Hz), 7,57-7,67 (3H, m), 7,78 (1H, t, J = 7,4 Hz), 8,07 (1H, dd, J = 7,8, 1,2 Hz), 8,18 (2H, d, J = 8,4 Hz), 8,27 (1H, t, J = 6,2 Hz), 8,50-8,70 (1H, m), 8,70-8,85 (1H, m).Exemplo 75
[00867] Produção de cloridrato de 3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-N-(pirrolidin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 73, o composto titular (126 mg, 65 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (150 mg, 0,38 mmol) e 2-aminametil-N-Boc- pirrolidina (122 mg, 0,57 mmol).
[00868] RMN 1H (300 MHz, DMSO-d6) δ:1,63-1,75 (1H, m), 1,83- 2,10 (3H, m), 3,11-3,27 (2H, m), 3,61-3,76 (3H, m), 4,08 (3H, s), 6,01 (2H, s), 7,36 (1H, t, J = 7,5 Hz), 7,51 (1H, d, J = 8,4 Hz), 7,57-7,67 (3H, m), 7,78 (1H, t, J = 7,5 Hz), 8,07 (1H, dd, J = 7,8, 1,2 Hz), 8,16-8,19 (2H, m), 8,40 (1H, t, J = 5,9 Hz), 8,80-9,20 (2H, br).Exemplo 76
[00869] Produção de 3-metóxi-N-[3-(3-metil-1H-pirazol-1-il)propil]-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamida oDa mesma maneira que no Exemplo 25, o composto titular (113 mg, 58 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (150 mg, 0,38 mmol) e (3-metilpirazol-1- il)propanamina (79 mg, 0,57 mmol).
[00870] RMN 1H (300 MHz, DMSO-d6) δ:2,02 (2H, t, J = 6,9 Hz), 2,15 (3H, s), 3,26-3,35 (2H, m), 4,04 (3H, s), 4,09 (2H, t, J = 6,9 Hz), 5,99 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,4 Hz), 7,55-7,67 (4H, m), 7,77 (1H, t, J = 7,5 Hz), 8,05 (1H, dd, J = 8,1, 1,2 Hz), 8,03-8,19 (4H, m).Exemplo 77
[00871] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N-piperidin-4-il-4,5-diidro-1 H-pirrol [3,2-c] quinolma-2-carboxamidano Exemplo 25, 4-({[3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2- il]carbonil}amina)piperidina-1-carboxilato de t-butila (615 mg) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (404 mg, 1,00 mmol) e 4-amina-1-Boc-piperidina (260 mg, 1,33 mmol).O 4-({[3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina)piperidina-1-carboxilato de t-butila assim-obtido (610 mg) e ácido trifluoroacético (5 ml) foram agitados à temperatura ambiente durante 2 h. A mistura de reação foi concentrada sob pressão reduzida, adicionou-se solução saturada de hidrogenocarbonato de sódio, e a mistura foi extraída com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/metanol=20/1), e o sólido obtido foi recristalizado de acetato de etil-etanol dando o composto titular (430 mg, 85 %) como cristais brancos.
[00872] RMN 1H (300 MHz, DMSO-d6) δ:1,34-1,46 (2H, m), 1,781,84 (2H, m), 1,90-2,20 (1H, br), 2,50-2,60 (2H, m), 2,85-3,00 (2H, br), 3,803,95 (1H, m), 3,98 (3H, s), 4,32 (3H, s), 5,97 (2H, s), 7,29-7,39 (2H, m), 7,457,50 (1H, m), 7,63 (2H, t, J = 7,5 Hz), 7,76 (1H, t, J = 7,5 Hz), 7,86 (1H, d, J = 7,8 Hz), 8,16-8,18 (2H, m), 8,37 (1H, dd, J = 8,4, 1,2 Hz).Exemplo 78
[00873] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N- piridin-3-il-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaUma mistura do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol), 3-aminapiridina (60,6 mg, 0,644 mmol), HATU (245 mg, 0,644 mmol), N,N’-diisopropiletilamina (336 ml, 1,93 mmol), e DMF (5 ml) foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com água, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila), e o sólido obtido foi recristalizado de THF dando o composto titular (83,0 mg, 36 %) como cristais brancos.
[00874] RMN 1H (300 MHz, DMSO-d6) δ:4,07 (3H, s), 4,33 (3H, s), 6,00 (2H, s), 7,32-7,44 (3H, m), 7,49-7,54 (1H, m), 7,64 (2H, t, J = 7,5 Hz), 7,77 (1H, t, J = 7,5 Hz), 8,17-8,22 (3H, m), 8,33 (1H, dd, J = 8,3, 1,1 Hz), 8,41 (1H, dd, J = 8,3, 1,1 Hz), 8,91 (1H, d, J = 2,1 Hz), 10,31 (1H, s). Exemplo 79
[00875] Produção de N-[1-(2-hidroxietil)piperidin-4-il]-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamida1) Uma mistura do composto do Exemplo 77 (200 mg, 0,399 mmol), 2-bromoetanol (42,5 ml, 0,599 mmol), carbonato de potássio (248 mg, 1,80 mmol) e DMF (5 ml) foi agitada a 100°C durante 15 h. A mistura de reação foi diluída com água, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila), e o sólido obtido foi recristalizado de acetato de etil-etanol dando o composto titular (68,0 mg, 33 %) como cristais brancos.
[00876] RMN 1H (300 MHz, DMSO-d6) δ:1,51-1,62 (2H, m), 1,751,90 (2H, br), 2,18 (2H, t, J = 10, 5 Hz), 2,40 (2H, t, J = 5,9 Hz), 2,70-2,85 (2H, br), 3,47-3,52 (2H, m), 3,75-3,90 (1H, br), 3,98 (3H, s), 4,32-4,38 (4H, m), 5,97 (2H, s), 7,29-7,39 (2H, m), 7,47 (1H, t, J = 7,6 Hz), 7,63 (2H, t, J = 7,6 Hz), 7,76 (1H, t, J = 7,1 Hz), 7,87 (1H, d, J = 7,5 Hz), 8,17 (2H, d, J = 7,6 Hz), 8,37 (1H, d, J = 8,4 Hz).
[00877] 2) O pó branco foi recristalizado de etanol-água dando ocomposto titular como cristais brancos. ponto de fusão: 202°C Exemplo 80
[00878] Produção de cloridrato de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-N-(piridin-2-ilmetil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 25, 3-metóxi-1-metil-4- oxo-5-(2-oxo-2-feniletil)-N-(piridin-2-ilmetil)-4,5-diidro-1H-pirrol[3,2- c]quinolina-2-carboxamida foi obtida como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e 2- (aminametil)piridina (69,6 mg, 0,644 mmol).
[00879] O composto titular (222 mg, 87 %) foi obtido como um pó branco a partir da assim-obtida 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)- N-(piridin-2-ilmetil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamida por meio de um método similar àquele no Exemplo 30.
[00880] RMN 1H (300 MHz, DMSO-d6) δ:4,08 (3H, s), 4,34 (3H, s), 4,85 (2H, d, J = 5,7 Hz), 5,98 (2H, s), 7,30-7,42 (2H, m), 7,47-7,52 (1H, m), 7,64 (2H, t, J = 7,5 Hz), 7,74-7,85 (3H, m), 8,16-8,19 (2H, m), 8,31-8,40 (2H, m), 8,77-8,84 (2H, m).Exemplo 81
[00881] Produção de cloridrato de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-N-(piperidin-2-ilmetil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 73, o composto titular (230 mg, 89 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e 2-(aminametil)-1-N-Boc- piperidina (138 mg, 0,644 mmol).
[00882] RMN 1H (300 MHz, DMSO-d6) δ:1,40-1,95 (6H, br), 2,702,95 (1H, br), 3,15-3,35 (2H, br), 3,46-3,69 (2H, m), 4,03 (3H, s), 4,36 (3H, s), 5,98 (2H, s), 7,30-7,41 (2H, m), 7,47-7,52 (1H, m), 7,64 (2H, t, J = 7,7 Hz), 7,76 (1H, t, J = 7,5 Hz), 8,16-8,25 (3H, m), 8,39 (1H, dd, J = 8,3, 1,1 Hz), 8,55-8,75 (1H, br), 8,75-8,90 (1H, br).Exemplo 82
[00883] Produção de cloridrato de 3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-N-(2-pirrolidin-1-iletil)-4,5-diidrotieno[3,2-c]quinolin-2- il]carboxamidaDa mesma maneira que no Exemplo 73, o composto titular (114 mg, 47 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (150 mg, 0,38 mmol) e 2-aminaetil-N-Boc- pirrolidina (122 mg, 0,57 mmol).
[00884] RMN 1H (300 MHz, DMSO-d6) δ:1,50-1,65 (1H, m), 1,802,10 (5H, m), 2,14-2,25 (1H, m), 3,10-3,20 (2H, m), 3,35-3,60 (2H, m), 4,05 (3H, s), 6,00 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,50 (1H, d, J = 8,7 Hz), 7,567,67 (3H, m), 7,77 (1H, t, J = 7,5 Hz), 8,05 (1H, dd, J = 7,8, 1,2 Hz), 8,168,20 (3H, m), 8,50-9,50 (2H, br).Exemplo 83
[00885] Produção de cloridrato de 3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-N-(2-piperidin-1-iletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 67, o composto titular (147 mg, 53 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (200 mg, 0,51 mmol) e 1-(2-aminaetil)piperidina (98 mg, 0,76 mmol).
[00886] RMN 1H (300 MHz, DMSO-d6) δ:1,30-1,50 (1H, m), 1,651,80 (5H, m), 2,85-3,00 (2H, m), 3,26 (2H, br d, J = 5,1 Hz), 3,53 (2H, br d, J = 11,1 Hz), 3,73 (2H, q, J = 5,7 Hz), 4,06 (3H, s), 6,00 (2H, s), 7,36 (1H, t, J = 7,5 Hz), 7,50 (1H, d, J = 8,4 Hz), 7,57-7,67 (3H, m), 7,77 (1H, t, J = 7,5 Hz), 8,06 (1H, dd, J = 8,1, 1,5 Hz), 8,16 (1H, d, J = 1,5 Hz), 8,19 (1H, s), 8,40 (1H, t, J = 5,7 Hz), 9,80-9,90 (1H, br).Exemplo 84
[00887] Produção de cloridrato de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-N-piperidin-3-il-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 73, o composto titular (67,1 mg, 27 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e 3-amina-1-N-Boc- piperidina (129 mg, 0,644 mmol).
[00888] RMN 1H (300 MHz, DMSO-d6) δ:1,55-2,05 (4H, m), 2,753,00 (2H, m), 3,20 (1H, d, J = 13,2 Hz), 3,25-3,40 (1H, br), 3,99 (3H, s), 4,204,30 (1H, br), 4,31 (3H, s), 5,98 (2H, s), 7,30-7,41 (2H, m), 7,46-7,52 (1H, m), 7,64 (2H, t, J = 7,7 Hz), 7,73-7,79 (1H, m), 8,05 (1H, d, J = 8,1 Hz), 8,168,19 (2H, m), 8,38 (1H, dd, J = 8,3, 1,4 Hz), 8,85-9,05 (2H, br).Exemplo 85
[00889] Produção de N-[trans-2-aminacicloexil]-3-metóxi-1-metil-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 73, cloridrato de N-[trans-2-aminacicloexil]-3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro- 1H-pirrol[3,2-c]quinolina-2-carboxamida foi obtido a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e N-Boc-trans-1,2- diaminacicloexano (138 mg, 0,644 mmol).
[00890] Ao assim-obtido cloridrato de N-[trans-2-aminacicloexil]-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamida adicionou-se solução saturada de hidrogenocarbonato de sódio, e a mistura foi extraída com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/metanol=20/1), e o sólido obtido foi recristalizado de acetato de etil-etanol dando o composto titular (80,0 mg, 33 %) como cristais brancos.
[00891] RMN 1H (300 MHz, DMSO-d6) δ:1,10-1,40 (4H, br), 1,501,75 (4H, br), 1,70-1,90 (1H, br), 1,90-2,05 (1H, br), 2,45-2,60 (1H, br), 3,453,60 (1H, br), 3,97 (3H, s), 4,30 (3H, s), 5,97 (2H, s), 7,29-7,39 (2H, m), 7,47 (1H, t, J = 7,7 Hz), 7,63 (2H, t, J = 7,7 Hz), 7,76 (1H, t, J = 7,4 Hz), 7,90 (1H, d, J = 7,8 Hz), 8,17 (2H, d, J = 7,7 Hz), 8,37 (1H, d, J = 8,1 Hz).Exemplo 86
[00892] Produção de cloridrato de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-N-pirrolidin-3-il-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 73, o composto titular (122 mg, 50 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e 3-amina-1-N-Boc- pirrolidina (120 mg, 0,644 mmol).
[00893] RMN 1H (300 MHz, DMSO-d6) δ:1,94-2,05 (1H, m), 2,202,32 (1H, m), 3,17-3,49 (4H, m), 4,00 (3H, s), 4,30 (3H, s), 4,58-4,69 (1H, m), 5,98 (2H, s), 7,30-7,40 (2H, m), 7,46-7,52 (1H, m), 7,64 (2H, t, J = 7,5 Hz), 7,73-7,79 (1H, m), 8,16-8,19 (2H, m), 8,26 (1H, d, J = 6,9 Hz), 8,38 (1H, dd, J = 8,3, 1,1 Hz), 9,10-9,30 (2H, br).Exemplo 87
[00894] Produção de cloridrato de N-[3-(dimetilamina)-2,2- dimetilpropil]-3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H- pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, N-[3-(dimetilamina)- 2,2-dimetilpropil]-3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro- 1H-pirrol[3,2-c]quinolina-2-carboxamida foi obtida como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol).
[00895] O composto titular (203 mg, 76 %) foi obtido como um pó branco a partir do assim-obtido N-[3-(dimetilamina)-2,2-dimetilpropil]-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2- c]quinolina-2-carboxamida por meio de um método similar àquele no Exemplo 30.
[00896] RMN 1H (300 MHz, DMSO-d6) δ:1,12 (6H, s), 2,86 (3H, s), 2,87 (3H, s), 3,03-3,07 (2H, br), 3,33-3,40 (2H, br), 4,04 (3H, s), 4,30 (3H, s), 5,99 (2H, s), 7,30-7,41 (2H, m), 7,46-7,52 (1H, m), 7,64 (2H, t, J = 7,5 Hz), 7,76 (1H, t, J = 7,4 Hz), 8,16-8,21 (3H, m), 8,38 (1H, dd, J = 8,3, 1,1 Hz), 9,50-9,70 (1H, br).Exemplo 88
[00897] Produção de cloridrato de N-(4-aminacicloexil)-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 73, o composto titular (121 mg, 47 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e (4- aminacicloexil)carbamato de t-butila (138 mg, 0,644 mmol).
[00898] RMN 1H (300 MHz, DMSO-d6) δ:1,18-1,34 (1H, br), 1,551,75 (1H, br), 1,75-1,90 (2H, br), 1,95-2,20 (1H, br), 2,60-2,81 (2H, m), 3,153,45 (3H, m), 4,01 (3H, s), 4,30 (3H, s), 5,98 (2H, s), 7,30-7,40 (2H, m), 7,467,51 (1H, m), 7,64 (2H, t, J = 7,5 Hz), 7,74-7,79 (1H, m), 8,16-8,20 (3H, m), 8,38 (1H, dd, J = 8,3, 1,4 Hz), 8,65-8,95 (2H, br).Exemplo 89
[00899] Produção de cloridrato de 2-{[(3R)-3-aminapirrolidin-1- il]carbonil}-3-metóxi-1-metil-5-(2-oxo-2-feniletil)-1,5-diidro-4H-pirrol[3,2- c]quinolin-4-onaDa mesma maneira que no Exemplo 73, o composto titular (190 mg, 78 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e (3R)-pirrolidin-3- ilcarbamato de t-butila (120 mg, 0,644 mmol).
[00900] RMN 1H (300 MHz, DMSO-d6) δ:1,95-2,15 (1H, m), 2,152,40 (1H, m), 3,57-3,92 (8H, m), 4,03-4,10 (3H, br), 5,98 (2H, s), 7,28-7,40 (2H, m), 7,44-7,49 (1H, m), 7,63 (2H, t, J = 7,5 Hz), 7,76 (1H, t, J = 7,4 Hz), 8,16-8,19 (2H, m), 8,30-8,50 (4H, br).Exemplo 90
[00901] Produção de cloridrato de 2-{[(3S)-3-aminapiperidin-1- il]carbonil}-3-metóxi-1-metil-5-(2-oxo-2-feniletil)-1,5-diidro-4H-pirrol[3,2- c]quinolin-4-onaDa mesma maneira que no Exemplo 73, o composto titular (190 mg, 78 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e (3S)-piperidin-3- ilcarbamato de t-butila (120 mg, 0,644 mmol).
[00902] RMN 1H (300 MHz, DMSO-d6) δ:1,45-2,00 (3H, br), 2,00- 2,15 (1H, br), 2,75-3,30 (4H, br), 3,65-3,85 (0,5H, br), 3,91 (3H, s), 4,03 (3H, s), 4,40-4,75 (0,5H, br), 5,97 (2H, s), 7,29-7,40 (2H, m), 7,44-7,49 (1H, m), 7,64 (2H, t, J = 7,5 Hz), 7,76 (1H, t, J = 7,4 Hz), 8,10-8,20 (5H, br), 8,34 (1H, d, J = 7,8 Hz).Exemplo 91
[00903] Produção de cloridrato de 2-{[3-(aminametil)piperidin-1- il]carbonil}-3-metóxi-1-metil-5-(2-oxo-2-feniletil)-1,5-diidro-4H-pirrol[3,2- c]quinolin-4-onaDa mesma maneira que no Exemplo 73, o composto titular (170 mg, 66 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e t-butila (piperidin-3- ilmetil)carbamato (143 mg, 0,644 mmol).
[00904] RMN 1H (300 MHz, DMSO-d6) δ:1,20-1,60 (2H, br), 1,602,00 (3H, br), 2,55-3,05 (3H, br), 3,10-3,30 (1H, br), 3,60-3,80 (1H, br), 3,90 (3H, s), 4,01 (3H, s), 4,25-4,60 (1H, br), 5,98 (2H, s), 7,28-7,39 (2H, m), 7,46 (1H, t, J = 7,7 Hz), 7,64 (2H, t, J = 7,7 Hz), 7,76 (1H, t, J = 7,1 Hz), 7,90-8,25 (5H, br), 8,33 (1H, d, J = 8,1 Hz).Exemplo 92
[00905] Produção de N-[2-(dimetilamina)-1-metiletil]-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (67,0 mg, 29 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (440 mg, 1,01 mmol) e 1-(dimetilamina)isopropilamina (68,1 mg, 0,666 mmol).
[00906] RMN 1H (300 MHz, DMSO-d6) δ:1,20 (3H, d, J = 6,0 Hz), 2,20 (6H, s), 2,20-2,27 (1H, m), 2,39-2,46 (1H, m), 3,97 (3H, s), 3,98-4,10 (1H, m), 4,36 (3H, s), 5,97 (2H, s), 7,29-7,39 (2H, m), 7,45-7,51 (1H, m), 7,63 (2H, t, J = 7,5 Hz), 7,73-7,79 (1H, m), 7,96 (1H, d, J = 6,6 Hz), 8,16-8,19 (2H, m), 8,38 (1H, dd, J = 8,1, 1,2 Hz).Exemplo 93
[00907] Produção de cloridrato de 2-{[(3R)-3-aminapiperidin-1- il]carbonil}-3-metóxi-1-metil-5-(2-oxo-2-feniletil)-1,5-diidro-4H-pirrol[3,2- c]quinolin-4-onaDa mesma maneira que no Exemplo 73, o composto titular %) foi obtido como um pó branco a partir do composto do Referência 28 (200 mg, 0,512 mmol) e (3R)-piperidin-3-
[00908] RMN 1H (300 MHz, DMSO-d6) δ:1,45-2,00 (3H, br), 2,002,15 (1H, br), 2,75-3,30 (4H, br), 3,65-3,85 (0,5H, br), 3,91 (3H, s), 4,03 (3H, s), 4,40-4,75 (0,5H, br), 5,97 (2H, s), 7,29-7,40 (2H, m), 7,44-7,49 (1H, m), 7,64 (2H, t, J = 7,7 Hz), 7,76 (1H, t, J = 7,4 Hz), 8,10-8,30 (5H, br), 8,34 (1H, d, J = 8,1 Hz).Exemplo 94
[00909] Produção de cloridrato de 3-metóxi-N-metil-4-oxo-5-(2-oxo-2- feniletil)-N-(2-piperidin-1-iletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 67, o composto titular (154 mg, 73 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (150 mg, 0,38 mmol) e 1-(2-N’- metilaminaetil)piperidina (108 mg, 0,76 mmol).
[00910] RMN 1H (300 MHz, CDCl3) δ:1,25-1,45 (1H, m), 1,60-1,90 (4H, m), 2,80-3,00 (2H, br), 3,11 (3H, s), 3,35-3,40 (2H, m), 3,40-3,65 (2H, br), 3,80-3,90 (5H, m), 5,99 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,48-7,67 (4H, m), 7,77 (1H, t, J = 7,5 Hz), 7,98 (1H, dd, J = 7,8, 1,2 Hz), 8,16-8,19 (3H, m), 9,75-9,90 (1H, br).Exemplo 95
[00911] Produção de cloridrato de 3-metóxi-N-metil-4-oxo-5-(2-oxo-2- feniletil)-N-(2-pirrolidin-1-iletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 67, o composto titular (153 mg, 74 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (150 mg, 0,38 mmol) e 1-(2-N’- metilaminaetil)pirrolidina (98 mg, 0,76 mmol).
[00912] RMN 1H (300 MHz, CDCl3) δ:1,75-2,10 (4H, m), 2,90-3,15 (5H, m), 3,35-3,50 (2H, m), 3,50-3,80 (2H, br), 3,83-3,90 (5H, m), 5,99 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,48-7,67 (4H, m), 7,77 (1H, t, J = 7,5 Hz), 7,97 (1H, dd, J = 7,8, 1,2 Hz), 8,16-8,19 (2H, m), 10,35-10,65 (1H, br).Exemplo 96
[00913] Produção de cloridrato de 3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-N-[(2S)-piperidina-2-ilmetil]-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 73, o composto titular (80 mg, 57 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (107 mg, 0,27 mmol) e (S)-2-(Boc-aminametil)piperidina (58 mg, 0,27 mmol).
[00914] RMN 1H (300 MHz, CDCl3) δ:1,35-1,90 (6H, m), 3,00-3,40 (4H, m), 3,90 (3H, s), 4,70-4,90 (1H, br), 5,99 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,48-7,67 (4H, m), 7,77 (1H, t, J = 7,5 Hz), 7,95-8,19 (6H, m).Exemplo 97
[00915] Produção de 3-metóxi-N-{2-[(1-metiletil)amina]etil}-4-oxo-5- (2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaA uma solução mista do composto do Exemplo 61 (150 mg, 0,32 mmol) e acetona (0,2 ml) em metanol (5 ml)-DMF (5 ml) adicionou-se cianoboroidreto de sódio (20 mg, 0,32 mmol), e a mistura foi agitada à temperatura ambiente durante 24 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila), e o sólido branco obtido foi recristalizado de acetato de etila-hexano dando o composto titular (69 mg, 45 %) como cristais brancos.
[00916] RMN 1H (300 MHz, CDCl3) δ:1,09 (6H, d, J = 6,3 Hz), 2,832,89 (3H, m), 3,57 (2H, q, J = 5,7 Hz), 4,16 (3H, s), 5,87 (2H, s), 7,02 (1H, d, J = 8,4 Hz), 7,26-7,28 (1H, m), 7,44-7,50 (1H, m), 7,56 (2H, t, J = 7,5 Hz), 7,66 (1H, t, J = 7,5 Hz), 7,91 (1H, dd, J = 8,1, 1,2 Hz), 8,10-8,13 (3H, m).Exemplo 98
[00917] Produção de 3-metóxi-N-{3-[(1-metiletil)amina]propil}-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 97, o composto titular (9 mg, 5 %) foi obtido como um pó branco a partir do composto do Exemplo 62 (190 mg, 0,38 mmol).
[00918] RMN 1H (300 MHz, CDCl3) δ:1,08 (6H, d, J = 6,3 Hz), 1,751,88 (2H, m), 2,73 (2H, t, J = 6,9 Hz), 2,76-2,85 (1H, m), 3,58 (2H, q, J = 6,4 Hz), 4,14 (3H, s), 5,87 (2H, s), 7,02 (1H, d, J = 8,7 Hz), 7,20-7,28 (1H, m), 7,44-7,50 (1H, m), 7,56 (2H, t, J = 7,5 Hz), 7,65-7,68 (1H, m), 7,80 (1H, br t), 7,91 (1H, dd, J = 7,8, 1,2 Hz), 8,10-8,13 (2H, m).Exemplo 99
[00919] Produção de cloridrato de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-N-(piperidin-3-ilmetil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 73, o composto titular (190 mg, 75 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e 3-(aminametil)piperidina- 1-carboxilato de t-butila (143 mg, 0,666 mmol).
[00920] RMN 1H (300 MHz, DMSO-d6) δ:1,15-1,35 (1H, br), 1,50- 1,90 (3H, br), 1,95-2,15 (1H, br), 2,64 (1H, t, J = 6,2 Hz), 2,78 (1H, t, J = 5,7 Hz), 3,15-3,45 (4H, br), 4,01 (3H, s), 4,30 (3H, s), 5,98 (2H, s), 7,29-7,41 (2H, m), 7,48 (1H, t, J = 7,6 Hz), 7,64 (2H, t, J = 7,6 Hz), 7,76 (1H, t, J = 7,4 Hz), 8,16-8,19 (3H, m), 8,37 (1H, d, J = 8,1 Hz), 8,55-8,85 (2H, br).Exemplo 100
[00921] Produção de cloridrato de N-[(1-aminacicloexil)metil]-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 73, o composto titular (80,0 mg, 30 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e [1- (aminametil)cicloexil]carbamato de t-butila (147 mg, 0,644 mmol).
[00922] RMN 1H (300 MHz, DMSO-d6) δ:1,25-1,70 (10H, br), 3,61 (2H, d, J = 6,3 Hz), 4,04 (3H, s), 4,34 (3H, s), 5,98 (2H, s), 7,31-7,42 (2H, m), 7,50 (1H, t, J = 7,6 Hz), 7,64 (2H, t, J = 7,6 Hz), 7,77 (1H, t, J = 7,5 Hz), 7,80-8,00 (3H, br), 8,16-8,22 (3H, m), 8,39 (1H, d, J = 8,4 Hz).Exemplo 101
[00923] Produção de N-{[1-(2-hidroxietil)piperidin-2-il]metil}-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2- c]quinolina-2-carboxamidaExemplo 79, o composto titular (47,1 mg, 39 %) foi obtido como um pó branco a partir do composto do Exemplo 81 (200 mg, 0,399 mmol) e 2-bromoetanol (24,2 ml, 0,341 mmol).
[00924] RMN 1H (300 MHz, DMSO-d6) δ:1,20-1,75 (6H, br), 2,203,10 (5H, br), 3,40-3,65 (4H, br), 3,98-4,05 (3H, br), 4,15-4,50 (4H, br), 5,98 (2H, s), 7,29-7,40 (2H, m), 7,45-7,51 (1H, m), 7,64 (2H, t, J = 7,7 Hz), 7,76 (1H, t, J = 7,5 Hz), 8,00-8,20 (3H, m), 8,39 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 102
[00925] Produção de N-{[1-(2-hidroxietil)piperidin-3-il]metil}-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 79, o composto titular (85,2 mg, 50 %) foi obtido como um pó branco a partir do composto do Exemplo 99 (160 mg, 0,306 mmol) e 2-bromoetanol (65,0 ml, 0,918 mmol).
[00926] RMN 1H (300 MHz, DMSO-d6) δ:0,90-1,10 (1H, br), 1,351,55 (1H, br), 1,55-1,90 (4H, br), 1,96 (1H, t, J = 7,1 Hz), 2,36 (2H, t, J = 6,3 Hz), 2,72 (1H, d, J = 9,9 Hz), 2,83 (1H, d, J = 7,5 Hz), 3,15-3,30 (2H, br), 3,45-3,51 (2H, m), 3,99 (3H, s), 4,30-4,34 (4H, m), 5,97 (2H, s), 7,29-7,39 (2H, m), 7,47 (1H, t, J = 7,7 Hz), 7,63 (2H, t, J = 7,7 Hz), 7,76 (1H, t, J = 7,5 Hz), 8,02 (1H, t, J = 6,0 Hz), 8,17 (2H, d, J = 7,7 Hz), 8,37 (1H, d, J = 8,1 Hz).Exemplo 103
[00927] Produção de cloridrato de N-(2-aminaetil)-3-metóxi-N-metil- 4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamida. A uma solução do composto do Exemplo de Referência 7 (300 mg, 0,760 mmol), cloridrato de 1-Boc-amina-2-metilaminaetano (321 mg, 1,52 mmol), trietilamina (154 mg, 1,52 mmol) e HOBt (206 mg, 1,52 mmol) em DMF (10 ml) adicionou-se WSCD (290 mg, 1,52 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 18 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em sílica-gel (eluado; acetato de etila/hexano=2/1) dando {2-[{[3-metóxi-4-oxo- 5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}(metil)amina]etil}carbamato de t-butila (230 mg) como um óleo incolor.
[00928] Uma solução do {2-[{[3-metóxi-4-oxo-5-(2-oxo-2-feniletil)- 4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}(metil)amina]etil}carbamato de t- butila obtido (230 mg) e solução 4N cloreto de hidrogênio acetato de etila (8 ml) em acetato de etila (15 ml) foi agitada à temperatura ambiente durante 2 h. O precipitado obtido foi recolhido por meio de filtração, lavado com éter de dietila, e secado sob pressão reduzida dando o composto titular (178 mg, 48 %) como um pó branco.
[00929] RMN 1H (300 MHz, DMSO-d6) δ:3,00-3,10 (5H, m), 3,603,75 (2H, m), 3,89 (3H, s), 5,99 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,7 Hz), 7,56 (1H, d, J=7,2 Hz), 7,64 (2H, t, J = 7,5 Hz), 7,77 (1H, t, J = 7,2 Hz), 7,80-7,98 (4H, m), 8,17 (2H, d, J = 7,5 Hz).Exemplo 104
[00930] Produção de cloridrato de N-(3-aminapropil)-3-metóxi-N- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaA uma solução do composto do Exemplo de Referência 7 (300 mg, 0,760 mmol), 1-Boc-amina-3-metilaminapropano (286 mg, 1,52 mmol) e HOBt (206 mg, 1,52 mmol) em DMF (10 ml) adicionou-se WSCD (290 mg, 1,52 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 18 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em sílica-gel (eluado; acetato de etila/hexano=2/1) dando {3-[{[3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2- c]quinolin-2-il]carbonil}(metil)amina]propil}carbamato de t-butila (230 mg) como um sólido não-cristalino branco.
[00931] Uma solução {3-[{[3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrotieno[3,2-c]quinolin-2-il]carbonil}(metil)amina]propil}carbamato de t- butila obtido (230 mg) e solução 4N cloreto de hidrogênio acetato de etila (8 ml) em acetato de etila (15 ml) foi agitada à temperatura ambiente durante 2 h. O precipitado obtido foi recolhido por meio de filtração, lavado com éter de dietila, e secado sob pressão reduzida dando o composto titular (216 mg, 54 %) como um pó branco.
[00932] RMN 1H (300 MHz, CDCl3) δ:1,80-2,00 (2H, m), 2,70-2,90 (2H, br), 3,06 (3H, s), 3,45-3,60 (2H, m), 3,89 (3H, s), 5,99 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,48-7,67 (4H, m), 7,75-7,79 (4H, m), 7,97 (1H, d, J = 7,8 Hz), 8,17-8,19 (2H, m).Exemplo 105
[00933] Produção de cloridrato de 3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-N-piperidin-4-il-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 73, o composto titular (222 mg, 57 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (300 mg, 0,760 mmol) e 4-amina-1-Boc-piperidina (305 mg, 1,52 mmol).
[00934] RMN 1H (300 MHz, DMSO-d6) δ:1,70-1,95 (2H, m), 2,05 (2H, d, J = 11,1 Hz), 3,04 (2H, t, J = 11,1 Hz), 3,29 (2H, d, J = 14,7 Hz), 4,034,12 (4H, m), 6,00 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,4 Hz), 7,59-7,67 (3H, m), 7,77 (1H, t, J = 7,5 Hz), 7,90 (1H, d, J = 7,2 Hz), 8,05 (1H, dd, J = 8,1, 1,2 Hz), 8,18 (2H, d, J = 7,5 Hz), 8,70-8,85 (2H, br). Exemplo 106
[00935] Produção de N-(2-hidroxietil)-3-metóxi-N-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (1,16 g, 68 %) foi obtido como cristais brancos a partir do composto do Exemplo de Referência 7 (1,50 g, 3,80 mmol) e N-metil-2-aminaetanol (428 mg, 5,70 mmol).
[00936] RMN 1H (300 MHz, CDCl3) δ:3,00-3,10 (1H, br), 3,21 (3H, s), 3,65-3,80 (2H, br), 3,80-4,00 (2H, br), 4,04 (3H, s), 5,86 (2H, s), 7,03 (1H, d, J = 8,4 Hz), 7,26 (1H, t, J = 7,5 Hz), 7,47 (1H, td, J = 7,8, 1,5 Hz), 7,53-7,59 (2H, m), 7,65-7,71 (1H, m), 7,83 (1H, dd, J = 9,0, 1,2 Hz), 8,10-8,13 (2H, m). Exemplo 107
[00937] Produção de N-{[1-(2-hidroxietil)piperidin-2-il]metil}-3- metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 101, o composto titular (29 mg, 29 %) foi obtido como um pó branco a partir do composto do Exemplo 74 (100 mg, 0,19 mmol).
[00938] RMN 1H (300 MHz, DMSO-d6) δ:1,20-1,50 (3H, m), 1,501,80 (3H, m), 2,27 (1H, t, J = 9,5 Hz), 2,35-2,60 (3H, m), 2,75-2,90 (1H, m), 2,95 (2H, d, J = 12,0 Hz), 3,45-3,60 (4H, m), 4,44 (1H, t, J = 5,4 Hz), 6,00 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,4 Hz), 7,57 (1H, d, J = 7,2 Hz), 7,64 (2H, t, J = 7,5 Hz), 7,77 (1H, t, J = 7,5 Hz), 8,05 (1H, d, J = 7,2 Hz), 8,10 (1H, t, J = 4,2 Hz), 8,18 (2H, d, J = 7,2 Hz).Exemplo 108
[00939] Produção de N-[1-(2-hidroxietil)piperidin-4-il]-3-metóxi-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 101, o composto titular (41 mg, 27 %) foi obtido como um pó branco a partir do composto do Exemplo 105 (150 mg, 0,29 mmol).
[00940] RMN 1H (300 MHz, DMSO-d6) δ:1,55-1,75 (2H, m), 1,84 (2H, d, J = 9,6 Hz), 2,18 (2H, t, J = 10,2 Hz), 2,37-2,44 (2H, m), 2,77 (2H, d, J = 10,8 Hz), 3,46-3,52 (2H, m), 3,75-3,85 (1H, m), 4,04 (3H, s), 4,38 (1H, t, J = 5,4 Hz), 6,00 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,4 Hz), 7,57 (1H, dd, J = 7,2, 1,5 Hz), 7,64 (2H, t, J = 7,5 Hz), 7,71-7,80 (2H, m), 8,05 (1H, dd, J = 7,2, 1,2 Hz), 8,16-8,19 (2H, m).Exemplo 109
[00941] Produção de N-(3-hidróxi-2,2-dimetilpropil)-3-metóxi-1-metil- 4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamida Da mesma maneira que no Exemplo 25, o composto titular (190 mg, 62 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e 3-amina-2,2-dimetil-1- propanol (66,4 mg, 0,644 mmol).
[00942] RMN 1H (300 MHz, DMSO-d6) δ:0,88 (6H, s), 3,22-3,24 (4H, m), 4,02 (3H, s), 4,34 (3H, s), 4,78 (1H, t, J = 8,3 Hz), 5,98 (2H, s), 7,29-7,40 (2H, m), 7,45-7,51 (1H, m), 7,63 (2H, t, J = 7,5 Hz), 7,73-7,79 (1H, m), 8,108,19 (3H, m), 8,38 (1H, dd, J = 8,4, 1,2 Hz).Exemplo 110
[00943] Produção de N-(3-hidróxi-2,2-dimetilpropil)-3-metóxi-4-oxo- 5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (251 mg, 69 %) foi obtido como cristais brancos a partir do composto do Exemplo de Referência 7 (300 mg, 0,76 mmol) e 3-amina-2,2-dimetil-1- propanol (118 mg, 1,14 mmol).
[00944] RMN 1H (300 MHz, CDCl3) δ:0,89 (6H, s), 3,25-3,35 (4H, m), 4,04 (3H, s), 4,99 (1H, t, J = 4,8 Hz), 6,00 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,4 Hz), 7,57 (1H, dd, J = 7,2, 1,2 Hz), 7,64 (2H, t, J = 7,5 Hz), 7,77 (1H, t, J = 7,5 Hz), 8,05 (1H, dd, J = 7,2, 1,2 Hz), 8,16-8,19 (2H, m), 8,29 (1H, t, J = 5,7 Hz).Exemplo 111
[00945] Produção de cloridrato de N-[1-(2-hidroxietil)piperidin-4-il]-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2- c]quinolina-2-carboxamidaA uma solução do composto do Exemplo 79 (150 mg, 0,290 mmol) em acetato de etila (4 ml)/etanol (6 ml) adicionou-se solução 4N cloreto de hidrogênio acetato de etila (80,0 ml). O precipitado foi recolhido por meio de filtração, lavado com acetato de etila, e seca sob pressão reduzida dando o composto titular (72 mg, 45 %) como um pó branco.
[00946] RMN 1H (300 MHz, DMSO-d6) δ:1,88-2,20 (4H, br), 3,05- 3,65 (6H, br), 3,74-3,82 (2H, br), 3,90-4,15 (4H, br), 4,28 (3H, s), 5,30-5,45 (1H, m), 5,98 (2H, s), 7,29-7,40 (2H, m), 7,46-7,51 (1H, m), 7,64 (2H, t, J = 7,5 Hz), 7,76 (1H, t, J = 7,4 Hz), 8,09-8,19 (3H, m), 8,37 (1H, d, J = 7,5 Hz), 9,75-10,10 (1H, br).Exemplo 112
[00947] Produção de cloridrato de N-[2-(dietilamina)etil]-3-metóxi-N- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 30, o composto titular (289 mg, 82 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (330 mg, 0,65 mmol) e N,N-dietil-N’- metiletilenodiamina (149 mg, 1,14 mmol).
[00948] RMN 1H (300 MHz, DMSO-d6) δ:1,20-1,40 (6H, br), 3,103,40 (6H, m), 3,58 (3H, s), 3,84-3,90 (5H, m), 5,99 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,4 Hz), 7,56 (1H, dd, J = 7,2, 1,2 Hz), 7,60-7,67 (2H, m), 7,77 (1H, t, J = 7,5 Hz), 7,97 (1H, dd, J = 7,2, 1,2 Hz), 8,16-8,19 (2H, m), 10,35-10,60 (1H, br).Exemplo 113
[00949] Produção de cloridrato de 3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-N-[(2R)-piperidin-2-ilmetil]-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 73, o composto titular (166 mg, 60 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (200 mg, 0,51 mmol) e (R)-2-aminametil-1-N-Boc- piperidina (163 mg, 0,76 mmol).
[00950] RMN 1H (300 MHz, DMSO-d6) δ:1,40-1,95 (6H, m), 2,753,00 (1H, m), 3,25 (2H, d, J = 10,8 Hz), 3,49-3,57 (1H, m), 3,63-3,70 (1H, m), 4,07 (3H, s), 6,01 (2H, s), 7,36 (1H, t, J = 7,5 Hz), 7,50 (1H, d, J = 8,7 Hz), 7,57-7,67 (3H, m), 7,77 (1H, t, J = 7,5 Hz), 8,06 (1H, dd, J = 7,2, 1,2 Hz), 8,16-8,19 (2H, m), 8,27 (1H, t, J = 6,0 Hz), 8,70-8,90 (2H, m).Exemplo 114
[00951] Produção de N-(2-hidróxi-2-metilpropil)-3-metóxi-4-oxo-5-(2- oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamida Da mesma maneira que no Exemplo 73, o composto titular (108 mg, 47 %) foi obtido como cristais brancos a partir do composto do Exemplo de Referência 7 (200 mg, 0,51 mmol) e 1-amina-2-metil-2-propanol (68 mg, 0,76 mmol).
[00952] RMN 1H (300 MHz, DMSO-d6) δ:1,16 (6H, s), 3,31 (2H, s), 4,06 (3H, s), 4,77 (1H, s), 6,00 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,50 (1H, d, J = 8,4 Hz), 7,57-7,67 (3H, m), 7,77 (1H, t, J = 7,5 Hz), 7,98 (1H, t, J = 2,4 Hz), 8,05 (1H, d, J = 7,8 Hz), 8,18 (2H, d, J = 7,2 Hz).Exemplo 115
[00953] Produção de cloridrato de 3-metóxi-N-metil-N-{2-[(1- metiletil)amina]etil}-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2- c]quinolina-2-carboxamidaA uma solução do composto do Exemplo 103 (130 mg, 0,27 mmol), acetona (155 mg, 2,67 mmol) e ácido acético (0,1 ml) em THF (5 ml) adicionou-se triacetoxiboroidreto de sódio (113 mg, 0,54 mmol), e a mistura foi agitada à temperatura ambiente durante 18 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila) dando um óleo incolor (0,09 g). A uma solução do óleo incolor obtido em acetato de etila (5 ml) adicionou-se solução 4N cloreto de hidrogênio acetato de etila (0,1 ml). O precipitado foi recolhido por meio de filtração, lavado com acetato de etila, e secado sob pressão reduzida dando o composto titular (73,0 mg, 52 %) como um pó branco.
[00954] RMN 1H (300 MHz, DMSO-d6) δ:1,15-1,35 (6H, br), 3,053,25 (5H, m), 3,30-3,40 (1H, m), 3,76 (2H, br t, J = 6,6 Hz), 3,90 (3H, s), 5,99 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, t, J = 8,1 Hz), 7,56 (1H, dd, J =7,2, 1,2 Hz), 7,60-7,67 (2H, m), 7,77 (1H, t, J = 7,5 Hz), 7,98 (1H, dd, J = 7,2, 1,2 Hz), 8,16-8,19 (2H, m), 8,50-8,80 (2H, br).Exemplo 116
[00955] Produção de cloridrato de 3-metóxi-N-metil-N-{3-[(1- metiletil)amina]propil}-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 115, o composto titular (118 mg, 73 %) foi obtido como um pó branco a partir do composto do Exemplo 104 (150 mg, 0,30 mmol).
[00956] RMN 1H (300 MHz, DMSO-d6) δ:1,10-1,35 (6H, br), 1,852,05 (2H, br), 2,70-3,00 (2H, br), 3,07 (3H, s), 3,20-3,40 (1H, m), 3,45-3,60 (2H, m), 3,90 (3H, s), 5,99 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,4 Hz), 7,56 (1H, dd, J = 6,9, 1,2 Hz), 7,62-7,67 (2H, m), 7,77 (1H, t, J = 7,5 Hz), 7,97 (1H, dd, J = 7,2, 1,2 Hz), 8,16-8,19 (2H, m), 8,65-8,80 (2H, br).Exemplo 117
[00957] Produção de cloridrato de N-{2-[etil(2-hidroxietil)amina]etil}- 3-metóxi-N-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina- 2-carboxamidasolução do composto do Exemplo 106 (1,0 g, 2,21 (269 mg, 2,66 mmol) em diclorometano (20 ml) de metanossulfonila (279 mg, 2,44 mmol) sobresfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 18 h. A mistura de reação foi diluída com água, e extraída com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida dando N-(2-cloroetil)-3-metóxi-N-metil-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamida (1,01 g) como um sólido não-cristalino branco.
[00958] Uma solução da N-(2-cloroetil)-3-metóxi-N-metil-4-oxo-5-(2- oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamida obtida (200 mg, 0,43 mmol), N-etilaminaetanol (228 mg, 2,55 mmol), diisopropiletilamina (330 mg, 2,55 mmol) e iodeto de sódio (64 mg, 0,43 mmol) em 1-butanol (5 ml) foi agitada a 110°C durante 18 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila para acetato de etila/metanol=20/1) dando N-{2-[etil(2-hidroxietil)amina]etil}-3-metóxi-N-metil-4-oxo-5-(2-oxo- 2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamida (0,08 g) como um sólido não-cristalino branco.
[00959] RMN 1H (300 MHz, CDCl3) δ:1,00-1,15 (0,75H, br), 1,201,35 (2,25H, m), 2,20-2,9 0 (4H, m), 3,16 (0,75H, s), 3,20 (2,25H, s), 3,503,95 (6H, m), 4,02-4,04 (3H, m), 5,85 (2H, s), 7,03 (1H, d, J = 8,4 Hz), 7,237,28 (1H, m), 7,45 (1H, t, J = 7,5 Hz), 7,55 (2H, t, J =7,5 Hz), 7,64-7,69 (1H, m), 7,80-7,84 (1H, m), 8,09-8,12 (2H, m).
[00960] A uma solução do sólido não-cristalino branco obtido em acetato de etila (5 ml) adicionou-se solução 4N cloreto de hidrogênio acetato de etila (0,1 ml). O precipitado foi recolhido por meio de filtração, lavado com acetato de etila, e secado sob pressão reduzida dando o composto titular (7 mg, 5 %) como um pó branco.Exemplo 118
[00961] Produção de N-(trans-4-hidroxicicloexil)-3-metóxi-1-metil-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular(230 mg, 95 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e trans-4-aminacicloexanol (74,2 mg, 0,644 mmol).
[00962] RMN 1H (300 MHz, DMSO-d6) δ:1,22-1,44 (4H, m), 1,831,92 (4H, m), 3,40-3,55 (1H, br), 3,68-3,85 (1H, br), 3,96 (3H, s), 4,30 (3H, s), 4,57 (1H, d, J = 4,2 Hz), 5,96 (2H, s), 7,28-7,38 (2H, m), 7,44-7,50 (1H, m), 7,63 (2H, t, J = 7,5 Hz), 7,73-7,79 (2H, m), 8,15-8,18 (2H, m), 8,36 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 119
[00963] Produção de N-(1-benzilpiperidin-4-il)-3-metóxi-5-(4-metoxibenzil)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular(1,17 g, 82 %) foi obtido como cristais brancos a partir do composto do Exemplo de Referência 13 (1,0 g, 2,52 mmol) e 4-amina-1-benzilpiperidina (720 mg, 3,78 mmol).
[00964] RMN 1H (300 MHz, DMSO-d6) δ:1,55-1,75 (2H, m), 1,801,95 (2H, br d), 2,17 (2H, t, J = 10,2 Hz), 2,65-2,80 (2H, br d), 3,50 (2H, s), 3,70 (3H, s), 3,80-3,90 (1H, br), 4,08 (3H, s), 5,53 (2H, br s), 6,85-6,88 (2H, m), 7,20 (2H, d, J = 8,7 Hz), 7,25-7,34 (5H, m), 7,49-7,56 (2H, m), 7,74 (1H, d, J = 7,8 Hz), 8,00 (1H, dd, J = 8,1, 1,2 Hz).Exemplo 120
[00965] Produção de etil éster de N-{[3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}-N-metilglicinaDa mesma maneira que no Exemplo 25, o composto titular (400 mg, 91 %) foi obtido como um sólido branco a partir do composto do Exemplo 7 (350 mg, 0,89 mmol) e cloridrato de etil éster de sarcosina (204 mg, 1,33 mmol).
[00966] RMN 1H (300 MHz, CDCl3) δ:1,24-1,35 (3H, m), 3,19 (1,2H, br s), 3,24 (1,8H, s), 3,98 (1,2H, br s), 4,08 (1,8H, s), 4,15-4,30 (4H, m), 5,86 (2H, s), 7,03 (1H, d, J = 8,7 Hz), 7,24-7,29 (1H, m), 7,43-7,49 (1H, m), 7,537,58 (2H, m), 7,65-7,70 (1H, m), 7,83 (1H, dd, J = 7,8, 1,2 Hz), 8,10-8,13 (2H, m).Exemplo 121
[00967] Produção de N-[2-(dietilamina)etil]-3-metóxi-N-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaUma mistura do composto do Exemplo 48 (4,10 g, 8,08 mol),ácido trifluoroacético (34 ml) e ácido trifluorometanossulfônico (6,6 ml) foi agitada à temperatura ambiente durante 5 h e a 80°C durante 2,5 h. Após resfriamento, a mistura de reação foi concentrada sob pressão reduzida, e acetato de etila e solução aquosa 1N de hidróxido de sódio foram adicionados ao resíduo. A mistura foi extraída com acetato de etila e o extrato foi lavado sucessivamente com água e salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=1/2) dando o composto titular (1,50 g, 48 %) como um pó branco.
[00968] RMN 1H (300 MHz, DMSO-d6) δ:0,70-1,10 (6H, br), 2,202,70 (6H, br), 3,05 (3H, s), 3,40-3,60 (2H, br), 3,91 (3H, s), 7,21-7,26 (1H, m), 7,38-7,41 (1H, m), 7,49-7,55 (1H, m), 7,82-7,85 (1H, m), 11,75 (1H, s).Exemplo 122
[00969] Produção de ácido [2-{[2-(dietilamina)etil](metil)carbamoil}- 3-metóxi-4-oxotieno[3,2-c]quinolin-5(4H)-il]acéticoUma solução do composto do Exemplo 53 (670 mg, 1,41mmol) e solução aquosa de hidróxido de sódio 8N (1,0 ml) em etanol (7,0 ml) foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi neutralizada com ácido clorídrico 1N, e concentrada sob pressão reduzida. Adicionou-se THF ao resíduo e, após filtração, o filtrado foi concentrado sob pressão reduzida dando o composto titular (580 mg, 92 %) como um sólido amarelo claro.
[00970] RMN 1H (300 MHz, DMSO-d6) δ:1,10-1,35 (6H, br), 2,703,30 (9H, m), 3,70-3,85 (2H, br), 3,91 (3H, s), 5,06 (2H, s), 7,34 (1H, t, J = 7,7 Hz), 7,48 (1H, d, J = 8,2 Hz), 7,62 (1H, t, J = 8,2 Hz), 7,94 (1H, d, J = 7,7 Hz).Exemplo 123
[00971] Produção de acetato de 2-[4-({[3-metóxi-1-metil-4-oxo-5-(2- oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina) piperidin-1-il]-2-oxoetilaA uma mistura do composto do Exemplo 77 (200 mg, 0,423 mmol), trietilamina (122 ml, 0,880 mmol) e THF (10 ml) adicionou-se cloreto de acetoxiacetila (47,3 ml, 0,440 mmol) a 0°C, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com acetato de etila, lavada com água e salmoura saturada, secada sobre sulfato de magnésio, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila), e o sólido obtido foi recristalizado de acetato de etila-THF dando o composto titular (171 mg, 75 %) como um pó branco.
[00972] RMN 1H (300 MHz, DMSO-d6) δ:1,35-1,70 (2H, m), 1,80- 2,00 (2H, m), 2,08 (3H, s), 2,80-3,00 (1H, m), 3,10-3,25 (1H, m), 3,60-3,80 (1H, m), 3,97 (3H, s), 4,00-4,25 (2H, m), 4,31 (3H, s), 4,80 (2H, d, J = 1,8 Hz), 5,97 (2H, s), 7,29-7,39 (2H, m), 7,45-7,50 (1H, m), 7,63 (2H, t, J = 7,5 Hz), 7,73-7,79 (1H, m), 7,98 (1H, d, J = 7,8 Hz), 8,16-8,18 (2H, m), 8,37 (1H, dd, J = 8,4, 1,2 Hz).Exemplo 124
[00973] Produção de N-[1-(hidroxiacetil)piperidin-4-il]-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidat, J = 7,4 Hz), 7,95 (1H, d, J = 8,4 Hz), 8,17 (2H, d, J = 7,6 Hz), 8,37 (1H, d, J = 8,1 Hz).
[00974] RMN 1H (300 MHz, DMSO-d6) δ:1,35-1,65 (2H, m), 1,802,00 (2H, m), 2,85-3,00 (1H, m), 3,05-3,25 (1H, m), 3,60-3,75 (1H, m), 3,97 (3H, s), 4,00-4,30 (4H, m), 4,31 (3H, s), 4,51 (1H, t, J = 5,3 Hz), 5,97 (2H, s), 7,29-7,39 (2H, m), 7,48 (1H, t, J = 7,6 Hz), 7,63 (2H, t, J = 7,6 Hz), 7,76 (1H,
[00975] 2) O pó branco foi recristalizado de etanol-água dando ocomposto titular como cristais brancos. ponto de fusão: 224°CExemplo 125
[00976] Produção de 4-({[3-metóxi-1,6-dimetil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridin-2-il]carbonil}amina)piperidina-1- carboxilato de t-butilaDa mesma maneira que no Exemplo 25, o composto titular (315 mg, 72 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 35 (290 mg, 0,818 mmol) e 4-amina-1-Boc-piperidina (212 mg, 1,06 mmol).
[00977] RMN 1H (300 MHz, DMSO-d6) δ:1,29-1,51 (11H, m), 1,751,90 (2H, m), 2,28 (3H, s), 2,86-3,05 (2H, m), 3,77-3,90 (5H, m), 3,92-4,04 (4H, m), 5,62 (2H, s), 6,58 (1H, s), 7,55-7,66 (3H, m), 7,73 (1H, d, J = 6,6 Hz), 8,11 (2H, d, J = 7,7 Hz).Exemplo 126
[00978] Produção de cloridrato de 3-metóxi-1,6-dimetil-4-oxo-5-(2- oxo-2-feniletil)-N-piperidin-4-il-4,5-diidro-1H-pirrol[3,2-c]piridina-2- carboxamidaA uma mistura do composto do Exemplo 125 (300 mg, 0,559 mmol) e acetato de etila (4 ml) adicionou-se solução 4N cloreto de hidrogênio acetato de etila (4 ml), e a mistura foi agitada à temperatura ambiente durante 2 h. O sólido precipitado foi recolhido por meio de filtração, e lavado com acetato de etila dando o composto titular (240 mg, 91 %) como um pó branco.
[00979] RMN 1H (300 MHz, DMSO-d6) δ:1,61-1,84 (2H, m), 1,952,11 (2H, m), 2,28 (3H, s), 2,92-3,12 (2H, m), 3,20-3,32 (2H, m), 3,83 (3H, s), 3,94-4,15 (4H, m), 5,62 (2H, s), 6,59 (1H, s), 7,61 (2H, t, J = 7,6 Hz), 7,68-7,81 (2H, m), 8,04-8,19 (2H, m), 8,64 (1H, br s), 8,87 (1H, br s).Exemplo 127
[00980] Produção de acetato de 2-[4-({[3-metóxi-1,6-dimetil-4-oxo-5- (2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridin-2-il]carbonil}amina) piperidin-1-il]-2-oxoetilaDa mesma maneira que no Exemplo 123, o composto titular(210 mg, 82 %) foi obtido como um pó branco a partir do composto do Exemplo 126 (225 mg, 0,476 mmol) e cloreto de acetoxiacetila (61,4 ml, 0,571 mmol).
[00981] RMN 1H (300 MHz, DMSO-d6) δ:1,26-1,64 (2H, m), 1,781,97 (2H, m), 2,09 (3H, s), 2,28 (3H, s), 2,79-2,97 (1H, m), 3,09-3,25 (1H, m), 3,58-3,74 (1H, m), 3,86 (3H, s), 3,95-4,20 (5H, m), 4,79 (2H, s), 5,62 (2H, s), 6,58 (1H, s), 7,55-7,68 (3H, m), 7,69-7,78 (1H, m), 8,06-8,15 (2H, m).Exemplo 128
[00982] Produção de N-[1-(hidroxiacetil)piperidin-4-il]-3-metóxi-1,6- dimetil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2- carboxamida O OHDa mesma maneira que no Exemplo 124, o composto titular (156 mg, 85 %) foi obtido como um pó branco a partir do composto do Exemplo 127 (200 mg, 0,373 mmol), solução aquosa de hidróxido de sódio 8N (0,5 ml), THF (2,5 ml) e etanol (5 ml).
[00983] RMN 1H (300 MHz, DMSO-d6) δ:1,32-1,61 (2H, m), 1,791,93 (2H, m), 2,28 (3H, s), 2,82-2,98 (1H, m), 3,04-3,20 (1H, m), 3,57-3,71 (1H, m), 3,86 (3H, s), 3,96-4,25 (7H, m), 4,50 (1H, d, J = 5,3 Hz), 5,61 (2H, s), 6,58 (1H, s), 7,55-7,67 (3H, m), 7,69-7,78 (1H, m), 8,07-8,16 (2H, m).Exemplo 129
[00984] Produção de 4-({[6-etil-3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridin-2-il]carbonil}amina)piperidina-1- carboxilato de t-butilaDa mesma maneira que no Exemplo 25, o composto titular (126 mg, 84 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 42 (100 mg, 0,271 mmol) e 4-amina-1-Boc-piperidina (70,7 mg, 0,353 mmol).
[00985] RMN 1H (300 MHz, DMSO-d6) δ:1,18 (3H, t, J = 7,3 Hz), 1,32-1,51 (11H, m), 1,74-1,89 (2H, m), 2,58 (2H, q, J = 7,5 Hz), 2,85-3,04 (2H, m), 3,77-3,91 (5H, m), 3,91-4,05 (4H, m), 5,59 (2H, s), 6,49 (1H, s), 7,55-7,67 (3H, m), 7,69-7,79 (1H, m), 8,06-8,16 (2H, m).Exemplo 130
[00986] Produção de cloridrato de 6-etil-3-metóxi-1-metil-4-oxo-5-(2- oxo-2-feniletil)-N-piperidin-4-il-4,5-diidro-1H-pirrol[3,2-c]piridina-2- carboxamidaUma solução do composto do Exemplo 129 (115 mg, 0,209 mmol) e solução 4N cloreto de hidrogênio acetato de etila (4 ml) em acetato de etila (4 ml) foi agitada à temperatura ambiente durante 3 h. O sólido precipitado foi recolhido por meio de filtração, e lavado com acetato de etila dando o composto titular.Exemplo 131
[00987] Produção de 6-etil-N-[1-(hidroxiacetil)piperidin-4-il]-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2- c]piridina-2-carboxamidaA uma mistura do composto do Exemplo 130 (90,0 mg, 0,185 mmol), trietilamina (76,9 ml, 0,555 mmol) e THF (5 ml) adicionou-se cloreto de acetoxiacetila (23,8 ml, 0,221 mmol) a 0°C, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com acetato de etila, lavada com água e salmoura saturada, secada sobre sulfato de magnésio, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila), e o sólido obtido foi dissolvido em THF (1,2 ml)-etanol (2,5 ml). Adicionou-se solução aquosa de hidróxido de sódio 8N (250 ml), e a mistura foi agitada à temperatura ambiente durante 2 h. A mistura de reação foi diluída com água, acidificada com ácido clorídrico 6N (0,5 ml), e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura saturada, secado sobre sulfato de magnésio e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/metanol=10/0 - 9/1), e o sólido obtido foi recristalizado de acetato de etila dando o composto titular (61,2 mg, 65 %) como cristais brancos.
[00988] RMN 1H (300 MHz, DMSO-d6) δ:1,13-1,23 (3H, m), 1,311,59 (2H, m), 1,80-1,94 (2H, m), 2,58 (2H, q, J = 7,4 Hz), 2,83-2,99 (1H, m), 3,04-3,21 (1H, m), 3,59-3,70 (1H, m), 3,89 (3H, s), 3,97-4,26 (7H, m), 4,49 (1H, t, J = 5,4 Hz), 5,59 (2H, s), 6,49 (1H, s), 7,56-7,67 (3H, m), 7,70-7,78 (1H, m), 8,06-8,15 (2H, m).Exemplo 132
[00989] Produção de 3-etóxi-N-(2-hidróxi-2-metilpropil)-1,6-dimetil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (65,8 mg, 67 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 44 (100 mg, 0,271 mmol) e 1-amina-2-metilpropan-2- ol (31,5 mg, 0,353 mmol).
[00990] RMN 1H (300 MHz, DMSO-d6) δ:1,13 (6H, s), 1,31 (3H, t, J = 7,0 Hz), 2,28 (3H, s), 3,24 (2H, d, J = 5,5 Hz), 3,90 (3H, s), 4,35 (2H, q, J = 7,0 Hz), 4,66 (1H, s), 5,61 (2H, s), 6,59 (1H, s), 7,61 (2H, t, J = 7,6 Hz), 7,69-7,79 (1H, m), 7,93 (1H, t, J = 5,6 Hz), 8,06-8,15 (2H, m).Exemplo 133
[00991] Produção de cloridrato de 3-etóxi-1,6-dimetil-4-oxo-5-(2-oxo- 2-feniletil)-N-piperidin-4-il-4,5-diidro-1H-pirrol[3,2-c]piridina-2- carboxamidaDa mesma maneira que no Exemplo 73, o composto titular (303 mg, 95 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 44 (250 mg, 0,679 mmol) e 4-amina-1-Boc-piperidina (177 mg, 0,882 mmol).
[00992] RMN 1H (300 MHz, DMSO-d6) δ:1,28 (3H, t, J = 7,1 Hz), 1,61-1,81 (2H, m), 1,97-2,12 (2H, m), 2,28 (3H, s), 2,94-3,10 (2H, m), 3,213,32 (2H, m), 3,85 (3H, s), 3,97-4,14 (1H, m), 4,34 (2H, q, J = 7,0 Hz), 5,62 (2H, s), 6,59 (1H, s), 7,61 (2H, t, J = 7,6 Hz), 7,69-7,81 (2H, m), 8,04-8,17 (2H, m), 8,85 (2H, br s).Exemplo 134
[00993] Produção de N-(2-hidróxi-2-metilpropil)-3-metóxi-1,6-dimetil- 4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxamida Da mesma maneira que no Exemplo 25, o composto titular (201 mg, 84 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 35 (200 mg, 0,564 mmol) e 1-amina-2-metilpropan-2- ol (65,4 mg, 0,734 mmol).
[00994] RMN 1H (300 MHz, DMSO-d6) δ:1,13 (6H, s), 2,29 (3H, s), 3,24 (2H, d, J = 5,7 Hz), 3,89 (3H, s), 4,02 (3H, s), 4,65 (1H, s), 5,62 (2H, s), 6,59 (1H, s), 7,56-7,66 (2H, m), 7,69-7,78 (1H, m), 7,85 (1H, t, J = 5,7 Hz), 8,06-8,15 (2H, m).Exemplo 135
[00995] Produção de 3-metóxi-1,6-dimetil-4-oxo-5-(2-oxo-2-feniletil)-N-(1-piridin-4-ilpiperidin-4-il)-4,5-diidro-1H-pirrol[3,2-c]piridina-2- carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (656 mg, 91 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 35 (500 mg, 1,41 mmol) e 1-piridin-4-ilpiperidin-4- amina (388 mg, 1,55 mmol).
[00996] RMN 1H (300 MHz, DMSO-d6) δ:1,48-1,65 (2H, m), 1,851,97 (2H, m), 2,28 (3H, s), 2,98-3,14 (2H, m), 3,77-3,90 (5H, m), 3,98 (3H, s), 4,01-4,15 (1H, m), 5,61 (2H, s), 6,58 (1H, s), 6,82 (2H, d, J = 1,5 Hz), 7,56-7,68 (3H, m), 7,70-7,78 (1H, m), 8,05-8,20 (4H, m).Exemplo 136
[00997] Produção de 3-etóxi-N-[1-(hidroxiacetil)piperidin-4-il]-1,6- dimetil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2- carboxamidaA uma mistura do composto do Exemplo 133 (200 mg, 0,423 mmol), trietilamina (122 ml, 0,880 mmol) e THF (10 ml) adicionou-se cloreto de acetoxiacetila (47,3 ml, 0,440 mmol) a 0°C, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com acetato de etila, lavada com água e salmoura, secada sobre sulfato de magnésio, e concentrada sob pressão reduzida. O resíduo foi dissolvido em etanol (7 ml) e THF (2 ml), adicionou-se solução aquosa de hidróxido de sódio 8N (1 ml), e a mistura foi agitada à temperatura ambiente durante 2 h. A mistura de reação foi diluída com água, acidificada com ácido clorídrico 6N (1,5 ml), e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura, secado sobre sulfato de magnésio e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila), e o sólido obtido foi recristalizado de acetato de etila-hexano dando o composto titular (102 mg, 65 %) como cristais brancos.
[00998] RMN 1H (300 MHz, DMSO-d6) δ:1,25 (3H, t, J = 7,1 Hz), 1,31-1,57 (2H, m), 1,82-1,96 (2H, m), 2,28 (3H, s), 2,80-2,95 (1H, m), 3,033,19 (1H, m), 3,87 (3H, s), 3,95-4,13 (3H, m), 4,18-4,28 (1H, m), 4,34 (2H, q, J = 7,0 Hz), 4,50 (1H, t, J = 5,4 Hz), 5,61 (2H, s), 6,58 (1H, s), 7,55-7,78 (4H, m), 8,06-8,14 (2H, m).Exemplo 137Produção de N-[1-(hidroxiacetil)piperidin-4-il]-1,6-dimetil-4-oxo-5-(2-oxo-2- feniletil)-3-propóxi-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxamida OHDa mesma maneira que no Exemplo 25, o composto titular (45,2 mg, 33 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 46 (100 mg, 0,262 mmol), cloridrato de 2-(4- aminapiperidin-1-il)-2-oxoetanol (61,1 mg, 0,314 mmol) e trietilamina (43,5 ml, 0,314 mmol).
[00999] RMN 1H (300 MHz, DMSO-d6) δ:0,92 (3H, t, J = 7,4 Hz), 1,22-1,53 (2H, m), 1,60-1,75 (2H, m), 1,85-1,95 (2H, m), 2,27 (3H, s), 2,772,92 (1H, m), 3,00-3,17 (1H, m), 3,60-3,74 (1H, m), 3,86 (3H, s), 3,95-4,13 (3H, m), 4,25 (3H, t, J = 6,7 Hz), 4,50 (1H, t, J = 5,4 Hz), 5,62 (2H, s), 6,57 (1H, s), 7,55-7,67 (3H, m), 7,69-7,78 (1H, m), 8,05-8,16 (2H, m).Exemplo 138
[001000] Produção de 3-etóxi-N-[1-(2-hidroxietil)piperidin-4-il]-1,6- dimetil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2- carboxamidaDa mesma maneira que no Exemplo 79, o composto titular (78,5 mg, 57 %) foi obtido como um pó branco a partir do composto do Exemplo 133 (135 mg, 0,277 mmol) e 2-bromoetanol (58,9 ml, 0,832 mmol).
[001001] RMN H (300 MHz, DMSO-d6) δ:1,28 (3H, t, J = 7,1 Hz), 1,39-1,57 (2H, m), 1,78-1,91 (2H, m), 2,09-2,22 (2H, m), 2,28 (3H, s), 2,38 (2H, t, J = 6,3 Hz), 2,67-2,81 (2H, m,), 3,48 (2H, q, J = 6,2 Hz), 3,70-3,83 (1H, m), 3,87 (3H, s), 4,29-4,41 (3H, m), 5,61 (2H, s), 6,58 (1H, s), 7,56-7,68 (3H, m), 7,70-7,78 (1H, m), 8,06-8,15 (2H, m).Exemplo 139
[001002] Produção de 3-etóxi-6-etil-N-[1-(hidroxiacetil)piperidin-4-il]- 1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2- carboxamida(49,1 mg, 0,252 mmol), HOBt (39,2 mg, 0,290 mmol) e trietilamina (34,9 ml, 0,252 mmol) em DMF (3 ml) adicionou-se WSCD (55,6 mg, 0,290 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com água, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com água e salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila), e o sólido obtido foi recristalizado de acetato de etila dando o composto titular (61,2 mg, 60 %) como cristais brancos.
[001003] RMN H (300 MHz, DMSO-d6) δ:1,13-1,29 (6H, m), 1,321,56 (2H, m), 1,83-1,96 (2H, m), 2,57 (2H, q, J = 7,4 Hz), 2,80-2,94 (1H, m), 3,04-3,19 (1H, m), 3,59-3,72 (1H, m), 3,90 (3H, s), 3,95-4,14 (3H, m), 4,174,27 (1H, m), 4,34 (2H, q, J = 7,2 Hz), 4,51 (1H, t, J = 5,4 Hz), 5,59 (2H, s), 6,49 (1H, s), 7,56-7,65 (2H, m), 7,66-7,77 (2H, m), 8,07-8,14 (2H, m).
[001004] 2) Os cristais brancos foram recristalizados de etanol-águadando o composto titular como cristais brancos. ponto de fusão: 204°C Exemplo 140
[001005] Produção de N-[1-(hidroxiacetil)piperidin-4-il]-1,6-dimetil-4- oxo-5-(2-oxo-2-feniletil)-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2- c]piridina-2-carboxamida(70,0 mg, 0,166 mmol), cloridrato de 2-(4-aminapiperidin-1-il)-2-oxoetanol (42,0 mg, 0,216 mmol), HOBt (33,6 mg, 0,249 mmol) e trietilamina (29,9 ml, 0,216 mmol) em DMF (3 ml) adicionou-se WSCD (55,6 mg, 0,290 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com água, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com água e salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila), e o sólido obtido foi recristalizado de acetato de etila dando o composto titular (51,3 mg, 55 %) como cristais brancos.
[001006] RMN 1H (300 MHz, DMSO-d6) δ:1,22-1,50 (2H, m), 1,811,94 (2H, m), 2,29 (3H, s), 2,74-2,91 (1H, m), 3,01-3,16 (1H, m), 3,63-3,75 (1H, m), 3,83 (3H, s), 3,95-4,13 (3H, m), 4,20-4,32 (1H, m), 4,53 (1H, t, J = 5,5 Hz), 5,06 (2H, q, J = 9,3 Hz), 5,65 (2H, s), 6,64 (1H, s), 7,51 (1H, d, J = 7,7 Hz), 7,57-7,66 (2H, m), 7,70-7,79 (1H, m), 8,07-8,15 (2H, m).
[001007] 2) Os cristais brancos foram recristalizados de etanol-águadando o composto titular como cristais brancos. ponto de fusão: 132°C Exemplo 141
[001008] Produção de 3-etóxi-N-[1-(hidroxiacetil)piperidin-4-il]-1- metil-4-oxo-5-(2-oxo-2-feniletil)-6-propil-4,5-diidro-1H-pirrol[3,2-c]piridina- 2-carboxamidaA uma solução do composto do Exemplo de Referência 57 (200 mg, 0,504 mmol), cloridrato de 2-(4-aminapiperidin-1-il)-2-oxoetanol (128 mg, 0,656 mmol), HOBt (102 mg, 0,757 mmol) e trietilamina (90,8 ml, 0,656 mmol) em DMF (5 ml) adicionou-se WSCD (145 mg, 0,757 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com água, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com água e salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila), e o sólido obtido foi recristalizado de THF-acetato de etila dando o composto titular (224 mg, 83 %) como cristais brancos.
[001009] RMN 1H (300 MHz, DMSO-d6) δ:0,93 (3H, t, J = 7,3 Hz), 1,25 (3H, t, J = 7,1 Hz), 1,31-1,66 (4H, m), 1,84-1,95 (2H, m), 2,51-2,59 (2H, m), 2,81-2,95 (1H, m), 3,04-3,18 (1H, m), 3,61-3,71 (1H, m), 3,89 (3H, s), 3,96-4,14 (3H, m), 4,18-4,27 (1H, m), 4,33 (2H, q, J = 7,0 Hz), 4,51 (1H, t, J = 5,1 Hz), 5,55 (2H, s), 6,51 (1H, s), 7,56-7,77 (4H, m), 8,08-8,14 (2H, m). Exemplo 142
[001010] Produção de 6-etil-3-(2-fluoroetóxi)-N-[1-(hidroxiacetil) piperidin-4-il]-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2- c]piridina-2-carboxamidaA uma solução do composto do Exemplo de Referência 59 (202 mg, 0,504 mmol), cloridrato de 2-(4-aminapiperidin-1-il)-2-oxoetanol (128 mg, 0,656 mmol), HOBt (102 mg, 0,757 mmol) e trietilamina (90,8 ml, 0,656 mmol) em DMF (5 ml) adicionou-se WSCD (145 mg, 0,757 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com água, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com água e salmoura saturada, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila), e o sólido obtido foi recristalizado de THF-acetato de etila dando o composto titular (219 mg, 80 %) como cristais brancos.
[001011] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3H, t, J = 7,4 Hz), 1,26-1,48 (2H, m), 1,87 (2H, s), 2,59 (2H, q, J = 7,4 Hz), 2,76-2,91 (1H, m), 3,01-3,17 (1H, m), 3,57-3,73 (1H, m), 3,92 (3H, s), 3,97-4,13 (3H, m), 4,184,32 (1H, m), 4,45-4,81 (5H, m), 5,59 (2H, s), 6,49-6,56 (1H, m), 7,55-7,66 (3H, m), 7,69-7,78 (1H, m), 8,06-8,16 (2H, m).Exemplo 143
[001012] Produção de 6-etil-N-[1-(hidroxiacetil)piperidin-4-il]-1-metil- 4-oxo-5-(2-oxo-2-feniletil)-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2- c]piridina-2-carboxamida1) A uma solução do composto do Exemplo de Referência 61(230 mg, 0,527 mmol), cloridrato de 2-(4-aminapiperidin-1-il)-2-oxoetanol (133 mg, 0,685 mmol), HOBt (107 mg, 0,791 mmol) e trietilamina (95,0 ml, 0,685 mmol) em DMF (4 ml) adicionou-se WSCD (152 mg, 0,791 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com água, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com água e salmoura saturada, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=1/3 - 1/0), e o sólido obtido foi recristalizado de acetato de etila-hexano dando o composto titular (146 mg, 48 %) como cristais brancos.
[001013] RMN 1H (300 MHz, DMSO-d6) δ:1,13-1,49 (5H, m), 1,821,94 (2H, m), 2,59 (2H, q, J = 7,2 Hz), 2,76-2,88 (1H, m), 3,023-3,15 (1H, m), 3,64-3,75 (1H, m), 3,86 (3H, s), 3,96-4,16 (3H, m), 4,20-4,33 (1H, m), 4,53 (1H, t, J = 5,4 Hz), 5,05 (2H, q, J = 9,3 Hz), 5,63 (2H, s), 6,54 (1H, s), 7,51 (1H, d, J = 7,7 Hz), 7,61 (2H, t, J = 7,6 Hz), 7,70-7,78 (1H, m), 8,08-8,14 (2H, m).
[001014] 2) Os cristais brancos foram recristalizados de etanol-águadando o composto titular como cristais brancos. ponto de fusão:159°C Exemplo 144
[001015] Produção de N-[2-(dietilamina)etil]-3-metóxi-N-metil-4-oxo- 5-(2-oxo-2-feniletil)-4,5,6,7,8,9-hexaidrotieno[3,2-c]quinolina-2-carboxamida EtvDa mesma maneira que no Exemplo 25, o composto titular (54,0 mg, 28 %) foi obtido como um óleo incolor a partir do composto do Exemplo de Referência 66 (150 mg, 0,377 mmol) e N,N-dietil-N’-metiletano- 1,2-diamina (79,3 ml, 0,490 mmol).
[001016] RMN 1H (300 MHz, DMSO-d6) δ:0,74-1,05 (6H, m), 1,671,85 (4H, m), 2,19-2,65 (10H, m), 3,03 (3H, s), 3,40-3,56 (2H, m), 3,82 (3H, s), 5,65 (2H, s), 7,61 (2H, t, J = 7,6 Hz), 7,70-7,78 (1H, m), 8,07-8,16 (2H, m).Exemplo 145
[001017] Produção de N-[2-(dietilamina)etil]-3-etóxi-N,6-dimetil-4-oxo-4,5-diidrotieno[3,2-c]piridina-2-carboxamidaUma mistura do composto do Exemplo de Referência 70 (2,50 g, 6,51 mmol), ácido clorídrico 6N (15 ml) e DMF (15 ml) foi agitada durante 15 h em condições de refluxo. Após resfriamento, a mistura de reação foi concentrada sob pressão reduzida, e adicionou-se água (20 ml) ao resíduo. A mistura foi neutralizada com solução saturada de hidrogenocarbonato de sódio, e extraída com acetato de etila. O extrato foi lavado sucessivamente com água e salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila) dando o composto titular (568 mg, 24 %) como um óleo incolor.
[001018] RMN 1H (300 MHz, DMSO-d6) δ:0,70-1,05 (6H, m), 1,21 (3H, t, J = 7,0 Hz), 2,21 (3H, s), 2,25-2,65 (6H, m), 3,01 (3H, s), 3,40-3,55 (2H, m), 4,13 (2H, q, J = 7,0 Hz), 6,54 (1H, s), 11,41 (1H, s).Exemplo 146
[001019] Produção de N-[2-(dietilamina)etil]-3-etóxi-N,6-dimetil-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]piridina-2-carboxamida Uma mistura do composto do Exemplo 145 (300 mg, 0,821 mmol), brometo de fenacila (196 mg, 0,985 mmol), carbonato de potássio (272 mg, 1,97 mmol) e DMF (5 ml) foi agitada a 60°C durante 15 h. Após resfriamento, a mistura foi diluída com água (10 ml), e extraída com acetato de etila. O extrato foi lavado sucessivamente com água e salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano = 1/9 to 10/0) dando o composto titular (51,2 mg, 13 %) como um óleo incolor.
[001020] RMN 1H (300 MHz, DMSO-d6) δ:0,70-1,05 (6H, m), 1,151,20 (3H, m), 2,25-2,65 (9H, m), 3,02 (3H, br s), 3,40-3,55 (2H, m), 4,05 (2H, q, J = 6,9 Hz), 5,66 (2H, s), 6,80-6,81 (1H, m), 7,62 (2H, t, J = 7,7 Hz), 7,727,78 (1H, m), 8,10-8,13 (2H, m).Exemplo 147
[001021] Produção de N-[2-(dietilamina)etil]-3-etóxi-N,6,7-trimetil-4- oxo-4,5-diidrotieno[3,2-c]piridina-2-carboxamidaDa mesma maneira que no Exemplo 145, o composto titular (60 mg, 29 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 74 (220 mg, 0,55 mmol).
[001022] RMN 1H (300 MHz, DMSO-d6) δ:0,80-1,10 (6H, m), 1,37 (3H, t, J = 6,9 Hz), 2,17 (3H, s), 2,41 (3H, s), 2,48-2,73 (6H, m), 3,17 (3H, s), 3,61 (2H, br s), 4,27 (2H, q, J = 7,1 Hz), 12,31 (1H, br s).Exemplo 148
[001023] Produção de N-[2-(dietilamina)etil]-3-etóxi-N,6,7-trimetil-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]piridina-2-carboxamidaDa mesma maneira que no Exemplo 146, o composto titular (10 mg, 12 %) foi obtido como um óleo amarelo claro a partir do composto do Exemplo 147 (60 mg, 0,16 mmol) e brometo de fenacila (196 mg, 0,985 mmol).
[001024] RMN 1H (300 MHz, CDCl3) δ: 0,80-1,15 (6H, m), 1,34 (3H, t,J = 7,1 Hz), 2,21-2,80 (12H, m), 3,16 (3H, s), 3,62 (2H, br s), 4,22 (2H, q, J= 7,1 Hz), 5,67 (2H, s), 7,54 (2H, t, J = 7,5 Hz), 7,66 (1H, t, J = 7,5 Hz), 8,08 (2H, dd, J = 8,1, 1,5 Hz).Exemplo 149
[001025] Produção de N-[1-(hidroxiacetil)piperidin-4-il]-3-metóxi-6- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]piridina-2- carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (224 mg, 80 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 78 (200 mg, 0,560 mmol), cloridrato de 2-(4- aminapiperidin-1-il)-2-oxoetanol (142 mg, 0,727 mmol) e trietilamina (101 ml, 0,727 mmol).
[001026] RMN 1H (300 MHz, DMSO-d6) δ: 1,38-1,66 (2H, m), 1,791,92 (2H, m), 2,26-2,35 (3H, m), 2,78-2,94 (1H, m), 3,03-3,18 (1H, m), 3,583,71 (1H, m), 3,94-4,14 (6H, m), 4,18-4,30 (1H, m), 4,51 (1H, t, J = 5,3 Hz), 5,68 (2H, s), 6,86 (1H, s), 7,56-7,69 (3H, m), 7,71-7,80 (1H, m), 8,07-8,16 (2H, m).Exemplo 150
[001027] Produção de 3-etóxi-N-[1-(hidroxiacetil)piperidin-4-il]-6- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]piridina-2- carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (178 mg, 65 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 79 (200 mg, 0,538 mmol), cloridrato de 2-(4- aminapiperidin-1-il)-2-oxoetanol (142 mg, 0,727 mmol) e trietilamina (101 ml, 0,727 mmol).
[001028] RMN 1H (300 MHz, DMSO-d6) δ: 1,30 (3 H, t, J=7,1 Hz), 1,37-1,61 (2 H, m), 1,84-1,95 (2 H, m), 2,30 (3 H, s), 2,76-2,91 (1 H, m), 3,02-3,18 (1 H, m), 3,59-3,73 (1 H, m), 3,95-4,13 (3 H, m), 4,21-4,33 (3 H, m), 4,51 (1 H, t, J=5,4 Hz), 5,68 (2 H, s), 6,86 (1 H, s), 7,57-7,70 (3 H, m), 7,71-7,79 (1 H, m), 8,07-8,17 (2 H, m).Exemplo 151
[001029] Produção de 3-metóxi-5-metil-2-(piperidin-1-ilcarbonil)tieno [3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e piperidina.
[001030] LC/MS 357 (M+H).Exemplo 152
[001031] Produção de 2-[(2,6-dimetilmorfolin-4-il)carbonil]-3-metóxi-5-metiltieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 2,6- dimetilmorfolina.
[001032] LC/MS 387 (M+H). Exemplo 153
[001033] Produção de 2-[(4-benzilpiperidin-1-il)carbonil]-3-metóxi-5-metiltieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 4- benzilpiperidina.
[001034] LC/MS 447 (M+H).Exemplo 154
[001035] Produção de N-[2-(3,4-dimetoxifenil)etil]-3-metóxi-N,5-dimetil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 2-(3,4- dimetoxifenil)-N-metiletanamina.
[001036] LC/MS 467 (M+H).Exemplo 155
[001037] Produção de 3-metóxi-N,N-bis(2-metoxietil)-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 2-metóxi-N-(2- metoxietil)etanamina.
[001038] LC/MS 405 (M+H).Exemplo 156
[001039] Produção de 3-metóxi-5-metil-2-(octaidroisoquinolina-2(1H)-ilcarbonil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e decaidroisoquinolina.
[001040] LC/MS 411 (M+H).Exemplo 157
[001041] Produção de N-etil-N-{1-[(3-metóxi-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolin-2-il)carbonil]pirrolidin-3-il}acetamidaDa mesma maneira que no Exemplo 1, o composto titular foiobtido a partir do composto do Exemplo de Referência 84 e N-etil-N- pirrolidin-3-ilacetamida.
[001042] LC/MS 428 (M+H).Exemplo 158
[001043] Produção de N-{1-[(3-metóxi-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolin-2-il)carbonil]pirrolidin-3-il}acetamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e N-pirrolidin-3- ilacetamida.
[001044] LC/MS 400 (M+H).Exemplo 159
[001045] Produção de N-cicloexil-N-etil-3-metóxi-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e N- etilcicloexanamina.
[001046] LC/MS 399 (M+H).Exemplo 160
[001047] Produção de N-(3,3-difenilpropil)-3-metóxi-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaUma solução do composto do Exemplo de Referência 84 em DMF (0,10 M, 0,601 ml, 60 μmol) foi diluída com DMF (0,200 ml), e adicionou-se uma solução de 3,3-difenilpropan-1-amina em DMF (1,0 M, 0,062 ml, 62 μmol) e uma solução de HOBt e WSCD numa mistura a 1:1 em DMF (0,50 M, 0,134 ml, 67 μmol). A mistura obtida foi agitada à temperatura ambiente durante 16 h. Adicionou-se diclorometano (2 ml) e água (1 ml) à mistura de reação. Após agitar durante 2,5 h, adicionou-se hidrogenocarbonato de sódio (7 mg) e a mistura foi agitada. A camada orgânica foi filtrada através de um filtro de Teflon (marca comercial registrada) para separar a camada aquosa, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de HPLC preparativa dando o composto titular (21,9 mg, 76 %).
[001048] LC/MS 483 (M+H).Exemplo 161
[001049] Produção de 5-butil-N-ciclopropil-3-metóxi-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e ciclopropanamina.
[001050] LC/MS 371 (M+H).Exemplo 162
[001051] Produção de N-benzil-5-butil-3-metóxi-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamida Da mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 1- fenilmetanamina.
[001052] LC/MS 421 (M+H).Exemplo 163
[001053] Produção de N-(1,3-benzodioxol-5-ilmetil)-5-butil-3-metóxi-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 1-(1,3- benzodioxol-5-il)metanamina.
[001054] LC/MS 465 (M+H).Exemplo 164
[001055] Produção de 5-butil-3-metóxi-4-oxo-N-(3-fenilpropil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 3-fenilpropan-1- amina.
[001056] LC/MS 449 (M+H).Exemplo 165
[001057] Produção de 5-butil-3-metóxi-N-(2-metoxietil)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 2- metoxietanamina.
[001058] LC/MS 389 (M+H).Exemplo 166
[001059] Produção de 5-butil-3-metóxi-4-oxo-N-(tetraidrofuran-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 1- (tetraidrofuran-2-il)metanamina.
[001060] LC/MS 415 (M+H).Exemplo 167
[001061] Produção de 5-butil-N-(1-etilpropil)-3-metóxi-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e pentan-3-amina.
[001062] LC/MS 401 (M+H).Exemplo 168
[001063] Produção de 5-butil-3-metóxi-4-oxo-N-prop-2-in-1-il-4,5- diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e prop-2-in-1- amina.
[001064] LC/MS 369 (M+H).Exemplo 169
[001065] Produção de 5-butil-N-[2-(3,4-dimetoxifenil)etil]-3-metóxi-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 2-(3,4- dimetoxifenil)etanamina.
[001066] LC/MS 495 (M+H).Exemplo 170
[001067] Produção de 5-butil-3-metóxi-N-[3-(1-metiletóxi)propil]-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 3-(1- metiletóxi)propan-1-amina.
[001068] LC/MS 431 (M+H).Exemplo 171
[001069] Produção de 5-butil-N-(furan-2-ilmetil)-3-metóxi-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 1-furan-2- ilmetanamina.
[001070] LC/MS 411 (M+H).Exemplo 172
[001071] Produção de 5-butil-3-metóxi-4-oxo-N-[3-(2-oxopirrolidin-1-il)propil]-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 1-(3- aminapropil)pirrolidin-2-ona.
[001072] LC/MS 456 (M+H).Exemplo 173
[001073] Produção de 5-butil-3-metóxi-2-(piperidin-1-ilcarbonil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e piperidina.
[001074] LC/MS 399 (M+H).Exemplo 174
[001075] Produção de 5-butil-2-[(2,6-dimetilmorfolin-4-il)carbonil]-3- metoxitieno[3,2-c]quinolin-4(5H)-ona Da mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 2,6- dimetilmorfolina.
[001076] LC/MS 429 (M+H).Exemplo 175
[001077] Produção de 2-[(4-benzilpiperidin-1-il)carbonil]-5-butil-3-metoxitieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 4- benzilpiperidina.
[001078] LC/MS 489 (M+H).Exemplo 176
[001079] Produção de 5-butil-N-[2-(3,4-dimetoxifenil)etil]-3-metóxi-N-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 2-(3,4- dimetoxifenil)-N-metiletanamina.
[001080] LC/MS 509 (M+H).Exemplo 177
[001081] Produção de 5-butil-3-metóxi-N,N-bis(2-metoxietil)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamida Da mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 2-metóxi-N-(2- metoxietil)etanamina.
[001082] LC/MS 447 (M+H).Exemplo 178
[001083] Produção de 5-butil-3-metóxi-2-(octaidroisoquinolina-2(1H)- ilcarbonil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e decaidroisoquinolina.
[001084] LC/MS 453 (M+H).Exemplo 179
[001085] Produção de N-{1-[(5-butil-3-metóxi-4-oxo-4,5-diidrotieno[3,2-c]quinolin-2-il)carbonil]pirrolidin-3-il}-N-etilacetamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e N-etil-N- pirrolidin-3-ilacetamida.
[001086] LC/MS 470 (M+H).Exemplo 180
[001087] Produção de N-{1-[(5-butil-3-metóxi-4-oxo-4,5-diidrotieno[3,2-c]quinolin-2-il)carbonil]pirrolidin-3-il}acetamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e N-pirrolidin-3- ilacetamida.
[001088] LC/MS 442 (M+H).Exemplo 181
[001089] Produção de 5-butil-N-cicloexil-N-etil-3-metóxi-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e N- etilcicloexanamina.
[001090] LC/MS 441 (M+H).Exemplo 182
[001091] Produção de 5-butil-N-(3,3-difenilpropil)-3-metóxi-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 160, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 3,3- difenilpropan-1-amina.
[001092] LC/MS 525 (M+H).Exemplo 183
[001093] Produção de trifluoroacetato de N-benzil-3-metóxi-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 1- fenilmetanamina.
[001094] LC/MS 456 (M+H).Exemplo 184
[001095] Produção de trifluoroacetato de N-(1,3-benzodioxol-5-ilmetil)-3-metóxi-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 1-(1,3- benzodioxol-5-il)metanamina.
[001096] LC/MS 500 (M+H).Exemplo 185
[001097] Produção de trifluoroacetato de 3-metóxi-4-oxo-N-(3-fenilpropil)-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 3-fenilpropan-1- amina.
[001098] LC/MS 484 (M+H).Exemplo 186
[001099] Produção de trifluoroacetato de 3-metóxi-N-(2-metoxietil)-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 2- metoxietanamina.
[001100] LC/MS 424 (M+H).Exemplo 187
[001101] Produção de trifluoroacetato de 3-metóxi-4-oxo-5-(piridin-2-ilmetil)-N-(tetraidrofuran-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 1-(tetraidrofuran- 2-il)metanamina.
[001102] LC/MS 450 (M+H).Exemplo 188
[001103] Produção de trifluoroacetato de N-(1-etilpropil)-3-metóxi-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e pentan-3-amina.
[001104] LC/MS 436 (M+H).Exemplo 189
[001105] Produção de trifluoroacetato de N-cicloexil-3-metóxi-4-oxo-5- (piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e cicloexanamina.
[001106] LC/MS 448 (M+H).Exemplo 190
[001107] Produção de trifluoroacetato de 3-metóxi-4-oxo-N-prop-2-in- 1-il-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e prop-2-in-1- amina.
[001108] LC/MS 404 (M+H).Exemplo 191
[001109] Produção de trifluoroacetato de N-[2-(3,4-dimetoxifenil)etil]- 3-metóxi-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 2-(3,4- dimetoxifenil)etanamina.
[001110] LC/MS 530 (M+H).Exemplo 192
[001111] Produção de trifluoroacetato de 3-metóxi-N-[3-(1-metiletóxi)propil]-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina- 2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 3-(1- metiletóxi)propan-1-amina.
[001112] LC/MS 466 (M+H).Exemplo 193
[001113] Produção de trifluoroacetato de 3-metóxi-4-oxo-N-(2- oxoazepan-3-il)-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 3-aminaazepan-2- ona.
[001114] LC/MS 477 (M+H).Exemplo 194
[001115] Produção de trifluoroacetato de 3-metóxi-4-oxo-N-[3-(2-oxopirrolidin-1-il)propil]-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 1-(3- aminapropil)pirrolidin-2-ona.
[001116] LC/MS 491 (M+H).Exemplo 195
[001117] Produção de trifluoroacetato de 3-metóxi-2-(piperidin-1-ilcarbonil)-5-(piridin-2-ilmetil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e piperidina.
[001118] LC/MS 434 (M+H).Exemplo 196
[001119] Produção de trifluoroacetato de 2-[(2,6-dimetilmorfolin-4-il)carbonil]-3-metóxi-5-(piridin-2-ilmetil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 2,6- dimetilmorfolina.
[001120] LC/MS 464 (M+H).Exemplo 197
[001121] Produção de trifluoroacetato de 2-[(4-benzilpiperidin-1-il)carbonil]-3-metóxi-5-(piridin-2-ilmetil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 4- benzilpiperidina.
[001122] LC/MS 524 (M+H).Exemplo 198
[001123] Produção de trifluoroacetato de N-[2-(3,4-dimetoxifenil)etil]-3-metóxi-N-metil-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina- 2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 2-(3,4- dimetoxifenil)-N-metiletanamina.
[001124] LC/MS 544 (M+H).Exemplo 199
[001125] Produção de trifluoroacetato de 3-metóxi-N,N-bis(2-metoxietil)-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 2-metóxi-N-(2- metoxietil)etanamina.
[001126] LC/MS 482 (M+H).Exemplo 200
[001127] Produção de trifluoroacetato de 3-metóxi-2- (octaidroisoquinolin-2(1H)-ilcarbonil)-5-(piridin-2-ilmetil)tieno[3,2-c] quinolin-4(5H)-onaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e decaidroisoquinolina.
[001128] LC/MS 488 (M+H).Exemplo 201
[001129] Produção de trifluoroacetato de N-etil-N-(1-{[3-metóxi-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}pirrolidin-3- il)acetamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e N-etil-N- pirrolidin-3-ilacetamida.
[001130] LC/MS 505 (M+H).Exemplo 202
[001131] Produção de trifluoroacetato de N-(1-{[3-metóxi-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}pirrolidin-3- il)acetamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e N-pirrolidin-3- ilacetamida.
[001132] LC/MS 477 (M+H).Exemplo 203
[001133] Produção de trifluoroacetato de N-cicloexil-N-etil-3-metóxi-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e N- etilcicloexanamina.
[001134] LC/MS 476 (M+H).Exemplo 204
[001135] Produção de trifluoroacetato de N-(3,3-difenilpropil)-3-metóxi-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 160, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 3,3- difenilpropan-1-amina.
[001136] LC/MS 560 (M+H).Exemplo 205
[001137] Produção de N-benzil-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 1- fenilmetanamina.
[001138] LC/MS 483 (M+H).Exemplo 206
[001139] Produção de N-(1,3-benzodioxol-5-ilmetil)-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 1-(1,3- benzodioxol-5-il)metanamina.
[001140] LC/MS 527 (M+H).Exemplo 207
[001141] Produção de 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-N-(3- fenilpropil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 3-fenilpropan-1- amina.
[001142] LC/MS 511 (M+H).Exemplo 208
[001143] Produção de 3-metóxi-N-(2-metoxietil)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 2- metoxietanamina.
[001144] LC/MS 451 (M+H).Exemplo 209
[001145] Produção de N-(1-etilpropil)-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e pentan-3-amina.
[001146] LC/MS 463 (M+H).Exemplo 210
[001147] Produção de N-cicloexil-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e cicloexanamina.
[001148] LC/MS 475 (M+H).Exemplo 211
[001149] Produção de 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-N-prop-2-in-1-il-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e prop-2-in-1-amina.
[001150] LC/MS 431 (M+H).Exemplo 212
[001151] Produção de 3-metóxi-N-[3-(1-metiletóxi)propil]-4-oxo-5-(2- oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 3-(1- metiletóxi)propan-1-amina.
[001152] LC/MS 493 (M+H).Exemplo 213
[001153] Produção de 3-metóxi-4-oxo-N-(2-oxoazepan-3-il)-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 3-aminaazepan-2- ona.
[001154] LC/MS 504 (M+H).Exemplo 214
[001155] Produção de N-(furan-2-ilmetil)-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 1-furan-2- ilmetanamina.
[001156] LC/MS 473 (M+H).Exemplo 215
[001157] Produção de 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-N-[3-(2-oxopirrolidin-1-il)propil]-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 1-(3- aminapropil)pirrolidin-2-ona.
[001158] LC/MS 518 (M+H).Exemplo 216
[001159] Produção de 2-[(2,6-dimetilmorfolin-4-il)carbonil]-3-metóxi-5-(2-oxo-2-feniletil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 2,6- dimetilmorfolina.
[001160] LC/MS 491 (M+H).Exemplo 217
[001161] Produção de 2-[(4-benzilpiperidin-1-il)carbonil]-3-metóxi-5-(2-oxo-2-feniletil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 4-benzilpiperidina.
[001162] LC/MS 551 (M+H).Exemplo 218
[001163] Produção de N-[2-(3,4-dimetoxifenil)etil]-3-metóxi-N-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaque no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 2-(3,4- dimetoxifenil)-N-metiletanamina.
[001164] LC/MS 571 (M+H).Exemplo 219
[001165] Produção de 3-metóxi-N,N-bis(2-metoxietil)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 2-metóxi-N-(2- metoxietil)etanamina.
[001166] LC/MS 509 (M+H).Exemplo 220
[001167] Produção de 2-(3,4-diidroisoquinolin-2(1H)-ilcarbonil)-3-metóxi-5-(2-oxo-2-feniletil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 1,2,3,4- tetraidroisoquinolina.
[001168] LC/MS 509 (M+H).Exemplo 221
[001169] Produção de 3-metóxi-2-(octaidroisoquinolin-2(1H)- ilcarbonil)-5-(2-oxo-2-feniletil)tieno[3,2-c]quinolin-4(5H)-ona Da mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e decaidroisoquinolina.
[001170] LC/MS 515 (M+H).Exemplo 222
[001171] Produção de N-(1-{[3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}pirrolidin-3-il)acetamida Da mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e N-pirrolidin-3- ilacetamida.
[001172] LC/MS 504 (M+H).Exemplo 223
[001173] Produção de N-cicloexil-N-etil-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 1, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e N- etilcicloexanamina.
[001174] LC/MS 503 (M+H).Exemplo 224
[001175] Produção de N-(3,3-difenilpropil)-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamida Da mesma maneira que no Exemplo 160, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 3,3- difenilpropan-1-amina.
[001176] LC/MS 587 (M+H).Exemplo 225
[001177] Produção de trifluoroacetato de N-[2-(dimetilamina)etil]-3- metóxi-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e N,N- dimetiletano-1,2-diamina.
[001178] LC/MS 360 (M+H).Exemplo 226
[001179] Produção de trifluoroacetato de 3-metóxi-5-metil-4-oxo-N-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 1-piridin-2- ilmetanamina.
[001180] LC/MS 380 (M+H).Exemplo 227
[001181] Produção de trifluoroacetato de 3-metóxi-5-metil-4-oxo-N-(piridin-4-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 1-piridin-4- ilmetanamina.
[001182] LC/MS 380 (M+H).Exemplo 228
[001183] Produção de trifluoroacetato de 3-metóxi-5-metil-4-oxo-N-(2-pirrolidin-1-iletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 2-pirrolidin-1- iletanamina.
[001184] LC/MS 386 (M+H).Exemplo 229
[001185] Produção de trifluoroacetato de 3-metóxi-5-metil-4-oxo-N-(2-piridin-3-iletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 2-piridin-3- iletanamina.
[001186] LC/MS 394 (M+H).Exemplo 230
[001187] Produção de trifluoroacetato de 3-metóxi-5-metil-N-[(5- metilpirazin-2-il)metil]-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 1-(5-metilpirazin- 2-il)metanamina.
[001188] LC/MS 395 (M+H). Exemplo 231
[001189] Produção de trifluoroacetato de N-[3-(1H-imidazol-1- il)propil]-3-metóxi-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 3-(1H-imidazol- 1-il)propan-1-amina.
[001190] LC/MS 397 (M+H).Exemplo 232
[001191] Produção de trifluoroacetato de 3-metóxi-5-metil-N-[2-(1-metilpirrolidin-2-il)etil]-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 2-(1- metilpirrolidin-2-il)etanamina.
[001192] LC/MS 400 (M+H).Exemplo 233
[001193] Produção de trifluoroacetato de 3-metóxi-5-metil-4-oxo-N-(2-piperidin-1-iletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 2-piperidin-1- iletanamina.
[001194] LC/MS 400 (M+H).Exemplo 234
[001195] Produção de trifluoroacetato de N-[3-(dietilamina)propil]-3- metóxi-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foiobtido a partir do composto do Exemplo de Referência 84 e N,N- dietilpropano-1,3-diamina.LC/MS 402 (M+H).Exemplo 235
[001196] Produção de trifluoroacetato de 3-metóxi-5-metil-N-(3- morfolin-4-ilpropil)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 3-morfolin-4- ilpropan-1-amina.
[001197] LC/MS 416 (M+H).Exemplo 236
[001198] Produção de ditrifluoroacetato de 3-metóxi-5-metil-N-[3-(4-metilpiperazin-1-il)propil]-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 3-(4- metilpiperazin-1-il)propan-1-amina.
[001199] LC/MS 429 (M+H).Exemplo 237
[001200] Produção de trifluoroacetato de N-[4-(dietilamina)-1-metilbutil]-3-metóxi-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e N1,N1- dietilpentano-1,4-diamina.
[001201] LC/MS 430 (M+H). Exemplo 238
[001202] Produção de trifluoroacetato de N-(1-benzilpirrolidin-3-il)-3- metóxi-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 1- benzilpirrolidin-3-amina.
[001203] LC/MS 448 (M+H).Exemplo 239
[001204] Produção de trifluoroacetato de N-(1-benzilpiperidin-4-il)-3- metóxi-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 1-benzilpiperidin- 4-amina.
[001205] LC/MS 462 (M+H).Exemplo 240
[001206] Produção de trifluoroacetato de 3-metóxi-N,5-dimetil-N-(1-metilpirrolidin-3-il)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e N,1- dimetilpirrolidin-3-amina.
[001207] LC/MS 386 (M+H).Exemplo 241
[001208] Produção de trifluoroacetato de 3-metóxi-5-metil-2-[(4-metil- 1,4-diazepan-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 1-metil-1,4- diazepano.
[001209] LC/MS 386 (M+H).Exemplo 242
[001210] Produção de trifluoroacetato de 2-[(4-etilpiperazin-1- il)carbonil]-3-metóxi-5-metiltieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 1-etilpiperazina.
[001211] LC/MS 386 (M+H). Exemplo 243
[001212] Produção de trifluoroacetato de N-[2-(dietilamina)etil]-3- metóxi-N,5-dimetil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e N,N-dietil-N’- metiletano-1,2-diamina.
[001213] LC/MS 402 (M+H).Exemplo 244
[001214] Produção de trifluoroacetato de 3-metóxi-5-metil-2-{[(2S)-2-(pirrolidin-1-ilmetil)pirrolidin-1-il]carbonil}tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 1-[(2S)- pirrolidin-2-ilmetil]pirrolidina.
[001215] LC/MS 426 (M+H).Exemplo 245
[001216] Produção de trifluoroacetato de 3-metóxi-5-metil-2-[(4-pirrolidin-1-ilpiperidin-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 4-pirrolidin-1- ilpiperidina.
[001217] LC/MS 426 (M+H).Exemplo 246
[001218] Produção de trifluoroacetato de 3-metóxi-5-metil-2-[(4- fenilpiperazin-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 1-fenilpiperazina.
[001219] LC/MS 434 (M+H).Exemplo 247
[001220] Produção de trifluoroacetato de N-(2-cianoetil)-3-metóxi-5-metil-4-oxo-N-(piridin-3-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 3-[(piridin-3- ilmetil)amina]propanonitrila.
[001221] LC/MS 433 (M+H).Exemplo 248
[001222] Produção de trifluoroacetato de 2-{[4-(1,3-benzodioxol-5-ilmetil)piperazin-1-il]carbonil}-3-metóxi-5-metiltieno[3,2-c]quinolin-4(5H)- onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 84 e 1-(1,3- benzodioxol-5-ilmetil)piperazina.
[001223] LC/MS 492 (M+H).Exemplo 249
[001224] Produção de trifluoroacetato de 5-butil-N-[2- (dimetilamina)etil]-3-metóxi-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e N,N- dimetiletano-1,2-diamina.
[001225] LC/MS 402 (M+H).Exemplo 250
[001226] Produção de trifluoroacetato de 5-butil-3-metóxi-4-oxo-N- (piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 1-piridin-2- ilmetanamina.
[001227] LC/MS 422 (M+H).Exemplo 251
[001228] Produção de trifluoroacetato de 5-butil-3-metóxi-4-oxo-N-(piridin-4-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 1-piridin-4- ilmetanamina.
[001229] LC/MS 422 (M+H).Exemplo 252
[001230] Produção de trifluoroacetato de 5-butil-3-metóxi-4-oxo-N-(2-pirrolidin-1-iletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 2-pirrolidin-1- iletanamina.
[001231] LC/MS 428 (M+H).Exemplo 253
[001232] Produção de trifluoroacetato de 5-butil-3-metóxi-4-oxo-N-(2- piridin-3-iletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 2-piridin-3- iletanamina.
[001233] LC/MS 436 (M+H).Exemplo 254
[001234] Produção de trifluoroacetato de 5-butil-3-metóxi-N-[(5-metilpirazin-2-il)metil]-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 1-(5- metilpirazin-2-il)metanamina.
[001235] LC/MS 437 (M+H).Exemplo 255
[001236] Produção de trifluoroacetato de 5-butil-N-[3-(1H-imidazol-1-il)propil]-3-metóxi-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 3-(1H-imidazol- 1-il)propan-1-amina.
[001237] LC/MS 439 (M+H).Exemplo 256
[001238] Produção de trifluoroacetato de 5-butil-3-metóxi-N-[2-(1-metilpirrolidin-2-il)etil]-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 2-(1- metilpirrolidin-2-il)etanamina.
[001239] LC/MS 442 (M+H).Exemplo 257
[001240] Produção de trifluoroacetato de 5-butil-3-metóxi-4-oxo-N-(2-piperidin-1-iletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 2-piperidin-1- iletanamina.
[001241] LC/MS 442 (M+H).Exemplo 258
[001242] Produção de trifluoroacetato de 5-butil-N-[3-(dietilamina) propil]-3-metóxi-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e N,N- dietilpropano-1,3-diamina.
[001243] LC/MS 444 (M+H).Exemplo 259
[001244] Produção de trifluoroacetato de 5-butil-3-metóxi-N-(3- morfolin-4-ilpropil)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 3-morfolin-4- ilpropan-1-amina.
[001245] LC/MS 458 (M+H).Exemplo 260
[001246] Produção de ditrifluoroacetato de 5-butil-3-metóxi-N-[3-(4-metilpiperazin-1-il)propil]-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 3-(4- metilpiperazin-1-il)propan-1-amina.
[001247] LC/MS 471 (M+H).Exemplo 261
[001248] Produção de trifluoroacetato de 5-butil-N-[4-(dietilamina)-1- metilbutil]-3-metóxi-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e N1,N1- dietilpentano-1,4-diamina.
[001249] LC/MS 472 (M+H).Exemplo 262
[001250] Produção de trifluoroacetato de N-(1-benzilpirrolidin-3-il)-5-butil-3-metóxi-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 1- benzilpirrolidin-3-amina.
[001251] LC/MS 490 (M+H).Exemplo 263
[001252] Produção de trifluoroacetato de N-(1-benzilpiperidin-4-il)-5- butil-3-metóxi-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 1- benzilpiperidin-4-amina.
[001253] LC/MS 504 (M+H).Exemplo 264
[001254] Produção de trifluoroacetato de 5-butil-3-metóxi-N-metil-N-(1-metilpirrolidin-3-il)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e N,1- dimetilpirrolidin-3-amina.
[001255] LC/MS 428 (M+H).Exemplo 265
[001256] Produção de trifluoroacetato de 5-butil-3-metóxi-2-[(4-metil- 1,4-diazepan-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 1-metil-1,4- diazepano.
[001257] LC/MS 428 (M+H).Exemplo 266
[001258] Produção de trifluoroacetato de 5-butil-2-[(4-etilpiperazin-1- il)carbonil]-3-metoxitieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 1-etilpiperazina.
[001259] LC/MS 428 (M+H).Exemplo 267
[001260] Produção de trifluoroacetato de 5-butil-N-[2-(dietilamina)etil]-3-metóxi-N-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e N,N-dietil-N’- metiletano-1,2-diamina.
[001261] LC/MS 444 (M+H).Exemplo 268
[001262] Produção de trifluoroacetato de 5-butil-3-metóxi-2-{[(2S)-2-(pirrolidin-1-ilmetil)pirrolidin-1-il]carbonil}tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 1-[(2S)- pirrolidin-2-ilmetil]pirrolidina.
[001263] LC/MS 468 (M+H).Exemplo 269
[001264] Produção de trifluoroacetato de 5-butil-3-metóxi-2-[(4- pirrolidin-1-ilpiperidin-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)-ona Da mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 4-pirrolidin-1- ilpiperidina.
[001265] LC/MS 468 (M+H).Exemplo 270
[001266] Produção de trifluoroacetato de 5-butil-3-metóxi-2-[(4- fenilpiperazin-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)-ona Da mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 1- fenilpiperazina.
[001267] LC/MS 476 (M+H).Exemplo 271
[001268] Produção de trifluoroacetato de 5-butil-N-(2-cianoetil)-3-metóxi-4-oxo-N-(piridin-3-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 3-[(piridin-3- ilmetil)amina]propanonitrila.
[001269] LC/MS 475 (M+H).Exemplo 272
[001270] Produção de trifluoroacetato de 2-{[4-(1,3-benzodioxol-5-ilmetil)piperazin-1-il]carbonil}-5-butil-3-metoxitieno[3,2-c]quinolin-4(5H)- onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 103 e 1-(1,3- benzodioxol-5-ilmetil)piperazina.
[001271] LC/MS 534 (M+H).Exemplo 273
[001272] Produção de ditrifluoroacetato de N-[2-(dimetilamina)etil]-3-metóxi-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e N,N- dimetiletano-1,2-diamina.
[001273] LC/MS 437 (M+H).Exemplo 274
[001274] Produção de ditrifluoroacetato de 3-metóxi-4-oxo-N,5-bis(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 1-piridin-2- ilmetanamina.
[001275] LC/MS 457 (M+H).Exemplo 275
[001276] Produção de ditrifluoroacetato de 3-metóxi-4-oxo-5-(piridin-2- ilmetil)-N-(piridin-4-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 1-piridin-4- ilmetanamina.
[001277] LC/MS 457 (M+H).Exemplo 276
[001278] Produção de ditrifluoroacetato de 3-metóxi-4-oxo-5-(piridin-2-ilmetil)-N-(2-pirrolidin-1-iletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 2-pirrolidin-1- iletanamina.
[001279] LC/MS 463 (M+H).Exemplo 277
[001280] Produção de ditrifluoroacetato de 3-metóxi-4-oxo-N-(2-piridin-3-iletil)-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 2-piridin-3- iletanamina.
[001281] LC/MS 471 (M+H).Exemplo 278
[001282] Produção de ditrifluoroacetato de 3-metóxi-N-[(5-metilpirazin-2-il)metil]-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 1-(5-metilpirazin- 2-il)metanamina.
[001283] LC/MS 472 (M+H).Exemplo 279
[001284] Produção de ditrifluoroacetato de N-[3-(1H-imidazol-1-il)propil]-3-metóxi-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 3-(1H-imidazol- 1-il)propan-1-amina.
[001285] LC/MS 474 (M+H).Exemplo 280
[001286] Produção de ditrifluoroacetato de 3-metóxi-N-[2-(1-metilpirrolidin-2-il)etil]-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 2-(1- metilpirrolidin-2-il)etanamina.
[001287] LC/MS 477 (M+H).Exemplo 281
[001288] Produção de ditrifluoroacetato de 3-metóxi-4-oxo-N-(2-piperidin-1-iletil)-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 2-piperidin-1- iletanamina.
[001289] LC/MS 477 (M+H). Exemplo 282
[001290] Produção de ditrifluoroacetato de N-[3-(dietilamina)propil]-3- metóxi-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e N,N- dietilpropano-1,3-diamina.
[001291] LC/MS 479 (M+H).Exemplo 283
[001292] Produção de ditrifluoroacetato de 3-metóxi-N-(3-morfolin-4-ilpropil)-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 3-morfolin-4- ilpropan-1-amina.
[001293] LC/MS 493 (M+H).Exemplo 284
[001294] Produção de ditrifluoroacetato de 3-metóxi-N-[3-(4- metilpiperazin-1-il)propil]-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 3-(4- metilpiperazin-1-il)propan-1-amina.Exemplo 285
[001295] Produção de ditrifluoroacetato de N-[4-(dietilamina)-1- metilbutil]-3-metóxi-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-Da mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e N1,N1- dietilpentano-1,4-diamina.
[001296] LC/MS 507 (M+H).Exemplo 286
[001297] Produção de ditrifluoroacetato de N-(1-benzilpirrolidin-3-il)-3-metóxi-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 1- benzilpirrolidin-3-amina.
[001298] LC/MS 525 (M+H).Exemplo 287
[001299] Produção de ditrifluoroacetato de N-(1-benzilpiperidin-4-il)-3-metóxi-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 1-benzilpiperidin- 4-amina.
[001300] LC/MS 539 (M+H).Exemplo 288
[001301] Produção de ditrifluoroacetato de 3-metóxi-N-metil-N-(1-metilpirrolidin-3-il)-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 3, o composto titular foiobtido a partir do composto do Exemplo de Referência 19 e N,1- dimetilpirrolidin-3-amina.Exemplo 289Produção de ditrifluoroacetato de 3-metóxi-2-[(4-metil-1,4-diazepan-1- il)carbonil]-5-(piridin-2-ilmetil)tieno[3,2-c]quinolin-4(5H)-ona Da mesma maneira que no Exemplo 3, o composto titular foiobtido a partir do composto do Exemplo de Referência 19 e 1-metil-1,4- diazepano.Exemplo 290
[001302] Produção de ditrifluoroacetato de 2-[(4-etilpiperazin-1- il)carbonil]-3-metóxi-5-(piridin-2-ilmetil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 1-etilpiperazina. Exemplo 291
[001303] Produção de ditrifluoroacetato de 3-metóxi-5-(piridin-2- ilmetil)-2-{[(2S)-2-(pirrolidin-1-ilmetil)pirrolidin-1-il]carbonil}tieno[3,2- c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 1-[(2S)- pirrolidin-2-ilmetil]pirrolidina.
[001304] LC/MS 503 (M+H).Exemplo 292
[001305] Produção de ditrifluoroacetato de 3-metóxi-5-(piridin-2- ilmetil)-2-[(4-pirrolidin-1-ilpiperidin-1-il)carbonil]tieno[3,2-c]quinolin- 4(5H)-onaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 4-pirrolidin-1- ilpiperidina.
[001306] LC/MS 503 (M+H).Exemplo 293
[001307] Produção de ditrifluoroacetato de 3-metóxi-2-[(4-fenilpiperazin-1-il)carbonil]-5-(piridin-2-ilmetil)tieno[3,2-c]quinolin-4(5H)- onaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 1-fenilpiperazina.
[001308] LC/MS 511 (M+H).Exemplo 294
[001309] Produção de ditrifluoroacetato de N-(2-cianoetil)-3-metóxi-4-oxo-5-(piridin-2-ilmetil)-N-(piridin-3-ilmetil)-4,5-diidrotieno[3,2-c]quinolina- 2-carboxamidaDa mesma maneira que no Exemplo 3, o composto titular foi obtido a partir do composto do Exemplo de Referência 19 e 3-[(piridin-3- ilmetil)amina]propanonitrila.
[001310] LC/MS 510 (M+H).Exemplo 295
[001311] Produção de trifluoroacetato de 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-N-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 1-piridin-2- ilmetanamina.
[001312] LC/MS 484 (M+H).Exemplo 296
[001313] Produção de trifluoroacetato de 3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-N-(piridin-4-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 1-piridin-4- ilmetanamina.
[001314] LC/MS 484 (M+H).Exemplo 297
[001315] Produção de trifluoroacetato de 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-N-(2-piridin-3-iletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 2-piridin-3- iletanamina.
[001316] LC/MS 498 (M+H).Exemplo 298
[001317] Produção de trifluoroacetato de 3-metóxi-N-[(5-metilpirazin-2-il)metil]-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 1-(5-metilpirazin- 2-il)metanamina.
[001318] LC/MS 499 (M+H).Exemplo 299
[001319] Produção de trifluoroacetato de 3-metóxi-5-(2-oxo-2-feniletil)-2-[(4-fenilpiperazin-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 7 e 1-fenilpiperazina.
[001320] LC/MS 538 (M+H).Exemplo 300
[001321] Produção de 3-(benzilóxi)-N,5-dimetil-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxamidaA uma solução (0,15 M, 0,40 ml, 60 μmol) do composto do Exemplo de Referência 91 em DMF adicionou-se uma solução (0,66 M, 0,10 ml, 66 mmol) de metanamina (solução em THF 2,0 M) em DMF e uma solução (0,39 M, 0,20 ml, 78 mmol) de HOBt e WSCD numa mistura a 1:1 em DMF. A mistura obtida foi agitada à temperatura ambiente durante 14 h. Adicionou-se diclorometano (2 ml) e solução aquosa saturada de hidrogenocarbonato de sódio (1 ml) à mistura de reação, a camada orgânica foi filtrada através de um filtro de Teflon (marca comercial registrada) para separar a camada aquosa, e o filtrado foi concentrado sob pressão reduzida. O resíduo foi purificado por meio de HPLC preparativa dando o composto titular (12,4 mg, 55 %).
[001322] LC/MS 379 (M+H).Exemplo 301
[001323] Produção de 3-(benzilóxi)-N-butil-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e butan-1-amina.
[001324] LC/MS 421 (M+H).Exemplo 302
[001325] Produção de 3-(benzilóxi)-N-(furan-2-ilmetil)-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e 1-furan-2- ilmetanamina.
[001326] LC/MS 445 (M+H).Exemplo 303
[001327] Produção de 3-(benzilóxi)-5-metil-4-oxo-N-(tetraidrofuran-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamida Da mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e 1-(tetraidrofuran- 2-il)metanamina.
[001328] LC/MS 449 (M+H).Exemplo 304
[001329] Produção de 3-(benzilóxi)-5-metil-4-oxo-N-(2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e 2-feniletanamina.
[001330] LC/MS 469 (M+H).Exemplo 305
[001331] Produção de 3-(benzilóxi)-N-(2-metoxibenzil)-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do metoxifenil)metanamina.
[001332] LC/MS 485 (M+H).Exemplo 306
[001333] Produção de tetraidronaftalen-1-il)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e 1,2,3,4- tetraidronaftalen-1-amina.
[001334] LC/MS 495 (M+H).Exemplo 307
[001335] Produção de N-(1,3-benzodioxol-5-ilmetil)-3-(benzilóxi)-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e 1-(1,3- benzodioxol-5-il)metanamina.
[001336] LC/MS 499 (M+H).Exemplo 308
[001337] Produção de 3-(benzilóxi)-N,N-dietil-5-metil-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e N-etiletanamina.
[001338] LC/MS 421 (M+H).Exemplo 309
[001339] Produção de 3-(benzilóxi)-5-metil-2-(piperidin-1-ilcarbonil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e piperidina.
[001340] LC/MS 433 (M+H).Exemplo 310
[001341] Produção de 3-(benzilóxi)-N-(2-metoxietil)-N,5-dimetil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e 2-metóxi-N- metiletanamina.
[001342] LC/MS 437 (M+H).Exemplo 311
[001343] Produção de 3-(benzilóxi)-N-metóxi-N,5-dimetil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamida
[001344] Da mesma maneira que no Exemplo 335, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e cloridrato de N-metoximetanamina.
[001345] LC/MS 409 (M+H).Exemplo 312
[001346] Produção de 3-(benzilóxi)-5-metil-2-(tiomorfolin-4-ilcarbonil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e tiomorfolina.
[001347] LC/MS 451 (M+H).Exemplo 313
[001348] Produção de 3-(benzilóxi)-2-{[(2R)-2-(metoximetil)pirrolidin-1-il]carbonil}-5-metiltieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e (2R)-2- (metoximetil)pirrolidina.
[001349] LC/MS 463 (M+H).Exemplo 314
[001350] Produção de N-benzil-3-(benzilóxi)-N,5-dimetil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e N-metil-1- fenilmetanamina.
[001351] LC/MS 469 (M+H).Exemplo 315
[001352] Produção de 3-(benzilóxi)-5-metil-N,N-bis(2-metilpropil)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 335, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e cloridrato de 2-metil-N-(2-metilpropil)propan-1-amina.
[001353] LC/MS 477 (M+H).Exemplo 316
[001354] Produção de trifluoroacetato de 3-(benzilóxi)-N-[3-(dimetilamina)propil]-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e N,N- dimetilpropano-1,3-diamina.
[001355] LC/MS 450 (M+H).Exemplo 317
[001356] Produção de trifluoroacetato de 3-(benzilóxi)-N-[2-(dietilamina)etil]-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e N,N-dietiletano- 1,2-diamina.
[001357] LC/MS 464 (M+H).Exemplo 318
[001358] Produção de trifluoroacetato de 3-(benzilóxi)-N-[3-(1H-imidazol-1-il)propil]-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e 3-(1H-imidazol- 1-il)propan-1-amina.
[001359] LC/MS 473 (M+H).Exemplo 319
[001360] Produção de trifluoroacetato de 3-(benzilóxi)-N-{2-[bis(1-metiletil)amina]etil}-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e N,N-bis(1- metiletil)etano-1,2-diamina.
[001361] LC/MS 492 (M+H).Exemplo 320
[001362] Produção de trifluoroacetato de 3-(benzilóxi)-5-metil-2-[(4- metilpiperazin-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e 1- metilpiperazina.
[001363] LC/MS 448 (M+H).Exemplo 321
[001364] Produção de trifluoroacetato de 3-(benzilóxi)-N,5-dimetil-N-(1-metilpirrolidin-3-il)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e N,1- dimetilpirrolidin-3-amina.
[001365] LC/MS 462 (M+H).Exemplo 322
[001366] Produção de trifluoroacetato de 3-(benzilóxi)-N-[2-(dietilamina)etil]-N,5-dimetil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e N,N-dietil-N’- metiletano-1,2-diamina.
[001367] LC/MS 478 (M+H).Exemplo 323
[001368] Produção de trifluoroacetato de 3-(benzilóxi)-5-metil-2-[(4-piridin-2-ilpiperazin-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 91 e 1-piridin-2- ilpiperazina.
[001369] LC/MS 511 (M+H).Exemplo 324
[001370] Produção de 3-butóxi-N,5-dimetil-4-oxo-4,5-diidrotieno[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 300, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e metanamina (solução em THF 2,0 M).
[001371] LC/MS 345 (M+H).Exemplo 325
[001372] Produção de 3-butóxi-N-butil-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e butan-1-amina.
[001373] LC/MS 387 (M+H).Exemplo 326
[001374] Produção de 3-butóxi-N-(furan-2-ilmetil)-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e 1-furan-2- ilmetanamina.
[001375] LC/MS 411 (M+H).Exemplo 327
[001376] Produção de 3-butóxi-5-metil-4-oxo-N-(tetraidrofuran-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e 1-(tetraidrofuran- 2-il)metanamina.
[001377] LC/MS 415 (M+H).Exemplo 328
[001378] Produção de 3-butóxi-5-metil-4-oxo-N-(2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e 2-feniletanamina.
[001379] LC/MS 435 (M+H).Exemplo 329
[001380] Produção de 3-butóxi-N-(2-metoxibenzil)-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e 1-(2- metoxifenil)metanamina.
[001381] LC/MS 451 (M+H).Exemplo 330
[001382] Produção de 3-butóxi-5-metil-4-oxo-N-(1,2,3,4- tetraidronaftalen-1-il)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e 1,2,3,4- tetraidronaftalen-1-amina.
[001383] LC/MS 461 (M+H).Exemplo 331
[001384] Produção de N-(1,3-benzodioxol-5-ilmetil)-3-butóxi-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e 1-(1,3- benzodioxol-5-il)metanamina.
[001385] LC/MS 465 (M+H).Exemplo 332
[001386] Produção de 3-butóxi-N,N-dietil-5-metil-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e N-etiletanamina.
[001387] LC/MS 387 (M+H).Exemplo 333
[001388] Produção de 3-butóxi-5-metil-2-(piperidin-1-ilcarbonil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e piperidina.
[001389] LC/MS 399 (M+H).Exemplo 334
[001390] Produção de 3-butóxi-N-(2-metoxietil)-N,5-dimetil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e 2-metóxi-N- metiletanamina.
[001391] LC/MS 403 (M+H).Exemplo 335
[001392] Produção de 3-butóxi-N-metóxi-N,5-dimetil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaA uma solução (0,15 M, 0,40 ml, 60 μmol) do composto do Exemplo de Referência 92 em DMF adicionou-se uma mistura de uma suspensão (0,66 M, 0,111 ml, 73 mmol) de cloridrato de N- metoximetanamina em DMF e trietilamina (10,9 ml, 78 μmol), e uma solução (0,39 M, 0,20 ml, 78 mmol) de HOBt e WSCD numa mistura a 1:1 em DMF. A mistura obtida foi agitada à temperatura ambiente durante 14 h. Adicionou- se diclorometano (2 ml) e solução aquosa saturada de hidrogenocarbonato de sódio (1 ml) à mistura de reação, a camada orgânica foi filtrada através de um filtro de Teflon (marca comercial registrada) para separar a camada aquosa, e o filtrado foi concentrado sob pressão reduzida. O resíduo foi purificado por meio de HPLC preparativa dando o composto titular (16,6 mg, 74 %).
[001393] LC/MS 375 (M+H).Exemplo 336
[001394] Produção de 3-butóxi-5-metil-2-(tiomorfolin-4-ilcarbonil)tieno[3,2-c]quinolin-4(5H)-ona Da mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e tiomorfolina.
[001395] LC/MS 417 (M+H).Exemplo 337
[001396] Produção de 3-butóxi-2-{[(2R)-2-(metoximetil)pirrolidin-1-il]carbonil}-5-metiltieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e (2R)-2- (metoximetil)pirrolidina.
[001397] LC/MS 429 (M+H).Exemplo 338
[001398] Produção de N-benzil-3-butóxi-N,5-dimetil-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e N-metil-1- fenilmetanamina.
[001399] LC/MS 435 (M+H).Exemplo 339
[001400] Produção de 3-butóxi-5-metil-N,N-bis(2-metilpropil)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 335, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e cloridrato de 2-metil-N-(2-metilpropil)propan-1-amina.
[001401] LC/MS 443 (M+H).Exemplo 340
[001402] Produção de trifluoroacetato de 3-butóxi-N-[3-(dimetilamina)propil]-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e N,N- dimetilpropano-1,3-diamina.
[001403] LC/MS 416 (M+H).Exemplo 341
[001404] Produção de trifluoroacetato de 3-butóxi-N-[2-(dietilamina) etil]-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e N,N-dietiletano- 1,2-diamina.
[001405] LC/MS 430 (M+H).Exemplo 342
[001406] Produção de trifluoroacetato de 3-butóxi-N-[3-(1H-imidazol-1-il)propil]-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e 3-(1H-imidazol- 1-il)propan-1-amina.
[001407] LC/MS 439 (M+H).Exemplo 343
[001408] Produção de trifluoroacetato de N-{2-[bis(1-metiletil)amina]etil}-3-butóxi-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e N,N-bis(1- metiletil)etano-1,2-diamina.
[001409] LC/MS 458 (M+H).Exemplo 344
[001410] Produção de trifluoroacetato de 3-butóxi-5-metil-2-[(4-metilpiperazin-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e 1- metilpiperazina.
[001411] LC/MS 414 (M+H).Exemplo 345
[001412] Produção de trifluoroacetato de 3-butóxi-N,5-dimetil-N-(1- metilpirrolidin-3-il)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e N,1- dimetilpirrolidin-3-amina.
[001413] LC/MS 428 (M+H).Exemplo 346
[001414] Produção de trifluoroacetato de 3-butóxi-N-[2-(dietilamina) etil]-N,5-dimetil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e N,N-dietil-N’- metiletano-1,2-diamina.
[001415] LC/MS 444 (M+H).Exemplo 347
[001416] Produção de trifluoroacetato de 3-butóxi-5-metil-2-[(4-piridin-2-ilpiperazin-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 92 e 1-piridin-2- ilpiperazina.
[001417] LC/MS 477 (M+H).Exemplo 348
[001418] Produção de trifluoroacetato de N,5-dimetil-4-oxo-3-(piridin-4-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaA uma solução (0,10 M, 0,40 ml, 40 μmol) do composto do Exemplo de Referência 93 em DMF adicionou-se uma solução (0,66 M, 0,10 ml, 66 mmol) de metanamina (solução em THF 2,0 M) em DMF e uma solução (0,39 M, 0,20 ml, 78 mmol) de HOBt e WSCD numa mistura a 1:1 em DMF. A mistura obtida foi agitada à temperatura ambiente durante 14 h. Adicionou-se diclorometano (2 ml) e solução aquosa saturada de hidrogenocarbonato de sódio (1 ml) à mistura de reação, a camada orgânica foi filtrada através de um filtro de Teflon (marca comercial registrada) para separar a camada aquosa, e o filtrado foi concentrado sob pressão reduzida. O resíduo foi purificado por meio de HPLC preparativa dando o composto titular (13,2 mg, 67 %).
[001419] LC/MS 380 (M+H).Exemplo 349
[001420] Produção de trifluoroacetato de N-butil-5-metil-4-oxo-3-(piridin-4-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaA uma solução (0,10 M, 0,40 ml, 40 μmol) do composto do Exemplo de Referência 93 em DMF adicionou-se uma solução (0,66 M, 0,10 ml, 66 mmol) de butan-1-amina em DMF e uma solução (0,39 M, 0,20 ml, 78 mmol) de HOBt e WSCD numa mistura a 1:1 em DMF. A mistura obtida foi agitada à temperatura ambiente durante 14 h. Adicionou-se diclorometano (2 ml) e solução aquosa saturada de hidrogenocarbonato de sódio (1 ml) à mistura de reação, a camada orgânica foi filtrada através de um filtro de Teflon (marca comercial registrada) para separar a camada aquosa, e o filtrado foi concentrado sob pressão reduzida. O resíduo foi purificado por meio de HPLC preparativa dando o composto titular (13,5 mg, 63 %).
[001421] LC/MS 422 (M+H).Exemplo 350
[001422] Produção de trifluoroacetato de N-(furan-2-ilmetil)-5-metil-4-oxo-3-(piridin-4-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e 1-furan-2- ilmetanamina.
[001423] LC/MS 446 (M+H).Exemplo 351
[001424] Produção de trifluoroacetato de 5-metil-4-oxo-3-(piridin-4-ilmetóxi)-N-(tetraidrofuran-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e 1- (tetraidrofuran-2-il)metanamina.
[001425] LC/MS 450 (M+H).Exemplo 352
[001426] Produção de trifluoroacetato de 5-metil-4-oxo-N-(2-feniletil)-3-(piridin-4-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e 2- feniletanamina.
[001427] LC/MS 470 (M+H).Exemplo 353
[001428] Produção de trifluoroacetato de N-(2-metoxibenzil)-5-metil-4- oxo-3-(piridin-4-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e 1-(2- metoxifenil)metanamina.
[001429] LC/MS 486 (M+H).Exemplo 354
[001430] Produção de trifluoroacetato de 5-metil-4-oxo-3-(piridin-4-ilmetóxi)-N-(1,2,3,4-tetraidronaftalen-1-il)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e 1,2,3,4- tetraidronaftalen-1-amina.
[001431] LC/MS 496 (M+H).Exemplo 355
[001432] Produção de trifluoroacetato de N-(1,3-benzodioxol-5-ilmetil)-5-metil-4-oxo-3-(piridin-4-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e 1-(1,3- benzodioxol-5-il)metanamina.
[001433] LC/MS 500 (M+H).Exemplo 356
[001434] Produção de trifluoroacetato de N,N-dietil-5-metil-4-oxo-3-(piridin-4-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e N- etiletanamina.
[001435] LC/MS 422 (M+H).Exemplo 357
[001436] Produção de trifluoroacetato de 5-metil-2-(piperidin-1- ilcarbonil)-3-(piridin-4-ilmetóxi)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e piperidina.
[001437] LC/MS 434 (M+H).Exemplo 358
[001438] Produção de trifluoroacetato de N-(2-metoxietil)-N,5-dimetil- 4-oxo-3-(piridin-4-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e 2-metóxi-N- metiletanamina.
[001439] LC/MS 438 (M+H).Exemplo 359
[001440] Produção de trifluoroacetato de N-metóxi-N,5-dimetil-4-oxo-3-(piridin-4-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaA uma solução (0,10 M, 0,40 ml, 40 μmol) do composto do Exemplo de Referência 93 em DMF adicionou-se uma mistura de uma suspensão (0,66 M, 0,111 ml, 73 mmol) de cloridrato de N- metoximetanamina em DMF e trietilamina (10,9 ml, 78 μmol), e uma solução (0,39 M, 0,20 ml, 78 mmol) de HOBt e WSCD numa mistura a 1:1 em DMF. A mistura obtida foi agitada à temperatura ambiente durante 14 h. Adicionou- se diclorometano (2 ml) e solução aquosa saturada de hidrogenocarbonato de sódio (1 ml) à mistura de reação, a camada orgânica foi filtrada através de um filtro de Teflon (marca comercial registrada) para separar a camada aquosa, e o filtrado foi concentrado sob pressão reduzida. O resíduo foi purificado por meio de HPLC preparativa dando o composto titular (12,3 mg, 59 %).
[001441] LC/MS 410 (M+H).Exemplo 360
[001442] Produção de trifluoroacetato de 5-metil-3-(piridin-4-ilmetóxi)- 2-(tiomorfolin-4-ilcarbonil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e tiomorfolina.
[001443] LC/MS 452 (M+H).Exemplo 361
[001444] Produção de trifluoroacetato de 2-{[(2R)-2- (metoximetil)pirrolidin-1-il]carbonil}-5-metil-3-(piridin-4-ilmetóxi)tieno[3,2- c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e (2R)-2- (metoximetil)pirrolidina.
[001445] LC/MS 464 (M+H).Exemplo 362
[001446] Produção de trifluoroacetato de N-benzil-N,5-dimetil-4-oxo-3-(piridin-4-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e N-metil-1- fenilmetanamina.
[001447] LC/MS 470 (M+H).Exemplo 363
[001448] Produção de trifluoroacetato de 5-metil-N,N-bis(2- metilpropil)-4-oxo-3-(piridin-4-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 359, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e cloridrato de 2-metil-N-(2-metilpropil)propan-1-amina.
[001449] LC/MS 478 (M+H).Exemplo 364
[001450] Produção de ditrifluoroacetato de N-[3-(dimetilamina)propil]-5-metil-4-oxo-3-(piridin-4-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e N,N- dimetilpropano-1,3-diamina.
[001451] LC/MS 451 (M+H).Exemplo 365
[001452] Produção de ditrifluoroacetato de N-[2-(dietilamina)etil]-5-metil-4-oxo-3-(piridin-4-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e N,N- dietiletano-1,2-diamina.
[001453] LC/MS 465 (M+H).Exemplo 366
[001454] Produção de ditrifluoroacetato de N-[3-(1H-imidazol-1-il)propil]-5-metil-4-oxo-3-(piridin-4-ilmetóxi)-4,5-diidrotieno[3,2-c]Da mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e 3-(1H- imidazol-1-il)propan-1-amina.
[001455] LC/MS 474 (M+H).Exemplo 367
[001456] Produção de ditrifluoroacetato de N-{2-[bis(1-metiletil)amina]etil}-5-metil-4-oxo-3-(piridin-4-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e N,N-bis(1- metiletil)etano-1,2-diamina.
[001457] LC/MS 493 (M+H).Exemplo 368
[001458] Produção de ditrifluoroacetato de 5-metil-2-[(4-metilpiperazin- 1-il)carbonil]-3-(piridin-4-ilmetóxi)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e 1- metilpiperazina.Exemplo 369
[001459] Produção de ditrifluoroacetato de N,5-dimetil-N-(1- metilpirrolidin-3-il)-4-oxo-3-(piridin-4-ilmetóxi)-4,5-diidrotieno[3,2-c] quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e N,1- dimetilpirrolidin-3-amina.Exemplo 370
[001460] Produção de ditrifluoroacetato de N-[2-(dietilamina)etil]-N,5- dimetil-4-oxo-3-(piridin-4-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e N,N-dietil-N’- metiletano-1,2-diamina.Exemplo 371
[001461] Produção de 2 trifluoroacetato de 5-metil-3-(piridin-4- ilmetóxi)-2-[(4-piridin-2-ilpiperazin-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)- onaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 93 e 1-piridin-2- ilpiperazina.
[001462] LC/MS 512 (M+H).Exemplo 372
[001463] Produção de trifluoroacetato de N,5-dimetil-3-(2-morfolin-4- iletóxi)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e metanamina (solução em THF 2,0 M).
[001464] LC/MS 402 (M+H).Exemplo 373
[001465] Produção de trifluoroacetato de N-butil-5-metil-3-(2-morfolin-4-iletóxi)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e butan-1- amina.
[001466] LC/MS 444 (M+H). Exemplo 374
[001467] Produção de trifluoroacetato de N-(furan-2-ilmetil)-5-metil-3- (2-morfolin-4-iletóxi)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e 1-furan-2- ilmetanamina.
[001468] LC/MS 468 (M+H).Exemplo 375
[001469] Produção de trifluoroacetato de 5-metil-3-(2-morfolin-4- iletóxi)-4-oxo-N-(tetraidrofuran-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e 1- (tetraidrofuran-2-il)metanamina.
[001470] LC/MS 472 (M+H).Exemplo 376
[001471] Produção de trifluoroacetato de 5-metil-3-(2-morfolin-4-iletóxi)-4-oxo-N-(2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e 2- feniletanamina.
[001472] LC/MS 492 (M+H).Exemplo 377
[001473] Produção de trifluoroacetato de N-(2-metoxibenzil)-5-metil-3- (2-morfolin-4-iletóxi)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e 1-(2- metoxifenil)metanamina.
[001474] LC/MS 508 (M+H).Exemplo 378
[001475] Produção de trifluoroacetato de 5-metil-3-(2-morfolin-4-iletóxi)-4-oxo-N-(1,2,3,4-tetraidronaftalen-1-il)-4,5-diidrotieno[3,2-c] quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e 1,2,3,4- tetraidronaftalen-1-amina.
[001476] LC/MS 518 (M+H).Exemplo 379
[001477] Produção de trifluoroacetato de N-(1,3-benzodioxol-5-ilmetil)- 5-metil-3-(2-morfolin-4-iletóxi)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e 1-(1,3- benzodioxol-5-il)metanamina.
[001478] LC/MS 522 (M+H).Exemplo 380
[001479] Produção de trifluoroacetato de N,N-dietil-5-metil-3-(2-morfolin-4-iletóxi)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e N- etiletanamina.
[001480] LC/MS 444 (M+H).Exemplo 381
[001481] Produção de trifluoroacetato de 5-metil-3-(2-morfolin-4- iletóxi)-2-(piperidin-1-ilcarbonil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e piperidina.
[001482] LC/MS 456 (M+H).Exemplo 382
[001483] Produção de trifluoroacetato de N-(2-metoxietil)-N,5-dimetil- 3-(2-morfolin-4-iletóxi)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e 2-metóxi-N- metiletanamina.
[001484] LC/MS 460 (M+H).Exemplo 383
[001485] Produção de trifluoroacetato de N-metóxi-N,5-dimetil-3-(2- morfolin-4-iletóxi)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 359, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e cloridrato de N-metoximetanamina.
[001486] LC/MS 432 (M+H).Exemplo 384
[001487] Produção de trifluoroacetato de 5-metil-3-(2-morfolin-4- iletóxi)-2-(tiomorfolin-4-ilcarbonil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e tiomorfolina.
[001488] LC/MS 474 (M+H).Exemplo 385
[001489] Produção de trifluoroacetato de 2-{[(2R)-2-(metoximetil) pirrolidin-1-il]carbonil}-5-metil-3-(2-morfolin-4-iletóxi)tieno[3,2-c]quinolin- 4(5H)-onaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e (2R)-2- (metoximetil)pirrolidina.
[001490] LC/MS 486 (M+H).Exemplo 386
[001491] Produção de trifluoroacetato de N-benzil-N,5-dimetil-3-(2-morfolin-4-iletóxi)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e N-metil-1- fenilmetanamina.
[001492] LC/MS 492 (M+H).Exemplo 387
[001493] Produção de trifluoroacetato de 5-metil-N,N-bis(2-metilpropil)-3-(2-morfolin-4-iletóxi)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 359, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e cloridrato de 2-metil-N-(2-metilpropil)propan-1-amina.
[001494] LC/MS 500 (M+H).Exemplo 388
[001495] Produção de ditrifluoroacetato de N-[3-(dimetilamina)propil]-5-metil-3-(2-morfolin-4-iletóxi)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e N,N- dimetilpropano-1,3-diamina.
[001496] LC/MS 473 (M+H).Exemplo 389
[001497] Produção de ditrifluoroacetato de N-[2-(dietilamina)etil]-5-metil-3-(2-morfolin-4-iletóxi)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e N,N- dietiletano-1,2-diamina.
[001498] LC/MS 487 (M+H).Exemplo 390
[001499] Produção de ditrifluoroacetato de N-[3-(1H-imidazol-1-il)propil]-5-metil-3-(2-morfolin-4-iletóxi)-4-oxo-4,5-diidrotieno[3,2-c] quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e 3-(1H- imidazol-1-il)propan-1-amina.
[001500] LC/MS 496 (M+H).Exemplo 391
[001501] Produção de ditrifluoroacetato de N-{2-[bis(1-metiletil)amina]etil}-5-metil-3-(2-morfolin-4-iletóxi)-4-oxo-4,5-diidrotieno[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e N,N-bis(1- metiletil)etano-1,2-diamina.
[001502] LC/MS 515 (M+H).Exemplo 392
[001503] Produção de ditrifluoroacetato de 5-metil-2-[(4-metilpiperazin- 1-il)carbonil]-3-(2-morfolin-4-iletóxi)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e 1- metilpiperazina.Exemplo 393
[001504] Produção de ditrifluoroacetato de N,5-dimetil-N-(1- metilpirrolidin-3-il)-3-(2-morfolin-4-iletóxi)-4-oxo-4,5-diidrotieno[3,2-c] quinolina-2-carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e N,1- dimetilpirrolidin-3-amina.
[001505] LC/MS 485 (M+H).Exemplo 394
[001506] Produção de ditrifluoroacetato de N-[2-(dietilamina)etil]-N,5-dimetil-3-(2-morfolin-4-iletóxi)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e N,N-dietil-N’- metiletano-1,2-diamina.
[001507] LC/MS 501 (M+H).Exemplo 395
[001508] Produção de ditrifluoroacetato de 5-metil-3-(2-morfolin-4-iletóxi)-2-[(4-piridin-2-ilpiperazin-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)- ona Da mesma maneira que no Exemplo 349, o composto titular foi obtido a partir do composto do Exemplo de Referência 94 e 1-piridin-2- ilpiperazina.
[001509] LC/MS 534 (M+H).Exemplo 396
[001510] Produção de N,5-dimetil-4-oxo-3-(tetraidrofuran-2-ilmetóxi)- 4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 300, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e metanamina (solução em THF 2,0 M).
[001511] LC/MS 373 (M+H).Exemplo 397
[001512] Produção de N-butil-5-metil-4-oxo-3-(tetraidrofuran-2- ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e butan-1-amina.
[001513] LC/MS 415 (M+H).Exemplo 398
[001514] Produção de N-(furan-2-ilmetil)-5-metil-4-oxo-3-(tetraidrofuran-2-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e 1-furan-2- ilmetanamina.
[001515] LC/MS 439 (M+H).Exemplo 399
[001516] Produção de 5-metil-4-oxo-3-(tetraidrofuran-2-ilmetóxi)-N-(tetraidrofuran-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e 1-(tetraidrofuran- 2-il)metanamina.
[001517] LC/MS 443 (M+H).Exemplo 400
[001518] Produção de 5-metil-4-oxo-N-(2-feniletil)-3-(tetraidrofuran-2-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamida Da mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e 2-feniletanamina.
[001519] LC/MS 463 (M+H).Exemplo 401
[001520] Produção de N-(2-metoxibenzil)-5-metil-4-oxo-3- (tetraidrofuran-2-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e 1-(2- metoxifenil)metanamina.
[001521] LC/MS 479 (M+H).Exemplo 402
[001522] Produção de 5-metil-4-oxo-3-(tetraidrofuran-2-ilmetóxi)-N- (1,2,3,4-tetraidronaftalen-1-il)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamida
[001523] Da mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e 1,2,3,4- tetraidronaftalen-1-amina.
[001524] LC/MS 489 (M+H).Exemplo 403
[001525] Produção de N-(1,3-benzodioxol-5-ilmetil)-5-metil-4-oxo-3-(tetraidrofuran-2-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e 1-(1,3- benzodioxol-5-il)metanamina.
[001526] LC/MS 493 (M+H).Exemplo 404
[001527] Produção de N,N-dietil-5-metil-4-oxo-3-(tetraidrofuran-2-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e N-etiletanamina.
[001528] LC/MS 415 (M+H).Exemplo 405
[001529] Produção de 5-metil-2-(piperidin-1-ilcarbonil)-3-(tetraidrofuran-2-ilmetóxi)tieno[3,2-c]quinolin-4(5H)-ona Da mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e piperidina.
[001530] LC/MS 427 (M+H).Exemplo 406
[001531] Produção de N-(2-metoxietil)-N,5-dimetil-4-oxo-3-(tetraidrofuran-2-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e 2-metóxi-N- metiletanamina.
[001532] LC/MS 461 (M+H).Exemplo 407
[001533] Produção de N-metóxi-N,5-dimetil-4-oxo-3-(tetraidrofuran-2-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 335, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e cloridrato de N-metoximetanamina.
[001534] LC/MS 403 (M+H).Exemplo 408
[001535] Produção de 5-metil-3-(tetraidrofuran-2-ilmetóxi)-2- (tiomorfolin-4-ilcarbonil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e tiomorfolina.
[001536] LC/MS 445 (M+H).Exemplo 409
[001537] Produção de 2-{[(2R)-2-(metoximetil)pirrolidin-1-il]carbonil}-5-metil-3-(tetraidrofuran-2-ilmetóxi)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e (2R)-2- (metoximetil)pirrolidina.
[001538] LC/MS 457 (M+H).Exemplo 410
[001539] Produção de N-benzil-N,5-dimetil-4-oxo-3-(tetraidrofuran-2-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e N-metil-1- fenilmetanamina.
[001540] LC/MS 463 (M+H).Exemplo 411
[001541] Produção de 5-metil-N,N-bis(2-metilpropil)-4-oxo-3- (tetraidrofuran-2-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 335, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e cloridrato de 2-metil-N-(2-metilpropil)propan-1-amina.
[001542] LC/MS 471 (M+H).Exemplo 412
[001543] Produção de trifluoroacetato de N-[3-(dimetilamina)propil]-5-metil-4-oxo-3-(tetraidrofuran-2-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e N,N- dimetilpropano-1,3-diamina.
[001544] LC/MS 444 (M+H).Exemplo 413
[001545] Produção de trifluoroacetato de N-[2-(dietilamina)etil]-5-metil-4-oxo-3-(tetraidrofuran-2-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e N,N-dietiletano- 1,2-diamina.
[001546] LC/MS 458 (M+H).Exemplo 414
[001547] Produção de trifluoroacetato de N-[3-(1H-imidazol-1-il)propil]-5-metil-4-oxo-3-(tetraidrofuran-2-ilmetóxi)-4,5-diidrotieno[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e 3-(1H-imidazol- 1-il)propan-1-amina.
[001548] LC/MS 467 (M+H).Exemplo 415
[001549] Produção de trifluoroacetato de N-{2-[bis(1-metiletil)amina]etil}-5-metil-4-oxo-3-(tetraidrofuran-2-ilmetóxi)-4,5-diidrotieno[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e N,N-bis(1- metiletil)etano-1,2-diamina.
[001550] LC/MS 486 (M+H).Exemplo 416
[001551] Produção de trifluoroacetato de 5-metil-2-[(4-metilpiperazin-1-il)carbonil]-3-(tetraidrofuran-2-ilmetóxi)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e 1- metilpiperazina.
[001552] LC/MS 442 (M+H).Exemplo 417
[001553] Produção de trifluoroacetato de N,5-dimetil-N-(1-metilpirrolidin-3-il)-4-oxo-3-(tetraidrofuran-2-ilmetóxi)-4,5-diidrotieno[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e N,1- dimetilpirrolidin-3-amina.
[001554] LC/MS 456 (M+H).Exemplo 418
[001555] Produção de trifluoroacetato de N-[2-(dietilamina)etil]-N,5-dimetil-4-oxo-3-(tetraidrofuran-2-ilmetóxi)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e N,N-dietil-N’- metiletano-1,2-diamina.
[001556] LC/MS 472 (M+H).Exemplo 419
[001557] Produção de trifluoroacetato de 5-metil-2-[(4-piridin-2-ilpiperazin-1-il)carbonil]-3-(tetraidrofuran-2-ilmetóxi)tieno[3,2-c]quinolin- 4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 95 e 1-piridin-2- ilpiperazina.
[001558] LC/MS 505 (M+H).Exemplo 420
[001559] Produção de 3-(2-etoxietóxi)-N,5-dimetil-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 300, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e metanamina (solução em THF 2,0 M).
[001560] LC/MS 361 (M+H).Exemplo 421
[001561] Produção de N-butil-3-(2-etoxietóxi)-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e butan-1-amina.
[001562] LC/MS 403 (M+H).Exemplo 422
[001563] Produção de 3-(2-etoxietóxi)-N-(furan-2-ilmetil)-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e 1-furan-2- ilmetanamina.
[001564] LC/MS 427 (M+H).Exemplo 423
[001565] Produção de 3-(2-etoxietóxi)-5-metil-4-oxo-N-(tetraidrofuran-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e 1-(tetraidrofuran- 2-il)metanamina.
[001566] LC/MS 431 (M+H).Exemplo 424
[001567] Produção de 3-(2-etoxietóxi)-5-metil-4-oxo-N-(2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e 2-feniletanamina.
[001568] LC/MS 451 (M+H).Exemplo 425
[001569] Produção de 3-(2-etoxietóxi)-N-(2-metoxibenzil)-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e 1-(2- metoxifenil)metanamina.
[001570] LC/MS 467 (M+H).Exemplo 426
[001571] Produção de 3-(2-etoxietóxi)-5-metil-4-oxo-N-(1,2,3,4- tetraidronaftalen-1-il)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e 1,2,3,4- tetraidronaftalen-1-amina.
[001572] LC/MS 477 (M+H).Exemplo 427
[001573] Produção de N-(1,3-benzodioxol-5-ilmetil)-3-(2-etoxietóxi)-5- metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e 1-(1,3- benzodioxol-5-il)metanamina.
[001574] LC/MS 481 (M+H).Exemplo 428
[001575] Produção de 3-(2-etoxietóxi)-N,N-dietil-5-metil-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e N-etiletanamina.
[001576] LC/MS 403 (M+H).Exemplo 429
[001577] Produção de 3-(2-etoxietóxi)-5-metil-2-(piperidin-1-ilcarbonil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e piperidina.
[001578] LC/MS 415 (M+H).Exemplo 430
[001579] Produção de 3-(2-etoxietóxi)-N-(2-metoxietil)-N,5-dimetil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e 2-metóxi-N- metiletanamina.
[001580] LC/MS 419 (M+H).Exemplo 431
[001581] Produção de 3-(2-etoxietóxi)-N-metóxi-N,5-dimetil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 335, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e cloridrato de N-metoximetanamina.
[001582] LC/MS 391 (M+H).Exemplo 432
[001583] Produção de 3-(2-etoxietóxi)-5-metil-2-(tiomorfolin-4- ilcarbonil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e tiomorfolina.
[001584] LC/MS 433 (M+H).Exemplo 433
[001585] Produção de 3-(2-etoxietóxi)-2-{[(2R)-2-(metoximetil) pirrolidin-1-il]carbonil}-5-metiltieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e (2R)-2- (metoximetil)pirrolidina.
[001586] LC/MS 445 (M+H).Exemplo 434
[001587] Produção de N-benzil-3-(2-etoxietóxi)-N,5-dimetil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e N-metil-1- fenilmetanamina.
[001588] LC/MS 451 (M+H).Exemplo 435
[001589] Produção de 3-(2-etoxietóxi)-5-metil-N,N-bis(2-metilpropil)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 335, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e cloridrato de 2-metil-N-(2-metilpropil)propan-1-amina.
[001590] LC/MS 459 (M+H).Exemplo 436
[001591] Produção de trifluoroacetato de N-[3-(dimetilamina)propil]-3-(2-etoxietóxi)-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e N,N- dimetilpropano-1,3-diamina.
[001592] LC/MS 432 (M+H).Exemplo 437
[001593] Produção de trifluoroacetato de N-[2-(dietilamina)etil]-3-(2-etoxietóxi)-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e N,N-dietiletano- 1,2-diamina.
[001594] LC/MS 446 (M+H).Exemplo 438
[001595] Produção de trifluoroacetato de 3-(2-etoxietóxi)-N-[3-(1H-imidazol-1-il)propil]-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e 3-(1H-imidazol- 1-il)propan-1-amina.
[001596] LC/MS 455 (M+H).Exemplo 439
[001597] Produção de trifluoroacetato de N-{2-[bis(1-metiletil)amina]etil}-3-(2-etoxietóxi)-5-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e N,N-bis(1- metiletil)etano-1,2-diamina.
[001598] LC/MS 474 (M+H).Exemplo 440
[001599] Produção de trifluoroacetato de 3-(2-etoxietóxi)-5-metil-2-[(4- metilpiperazin-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e 1- metilpiperazina.
[001600] LC/MS 430 (M+H).Exemplo 441
[001601] Produção de trifluoroacetato de 3-(2-etoxietóxi)-N,5-dimetil-N-(1-metilpirrolidin-3-il)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e N,1- dimetilpirrolidin-3-amina.
[001602] LC/MS 444 (M+H).Exemplo 442
[001603] Produção de trifluoroacetato de N-[2-(dietilamina)etil]-3-(2-etoxietóxi)-N,5-dimetil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e N,N-dietil-N’- metiletano-1,2-diamina.
[001604] LC/MS 460 (M+H).Exemplo 443
[001605] Produção de trifluoroacetato de 3-(2-etoxietóxi)-5-metil-2-[(4-piridin-2-ilpiperazin-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 96 e 1-piridin-2- ilpiperazina.
[001606] LC/MS 493 (M+H).Exemplo 444
[001607] Produção de 5-butil-3-(2-etoxietóxi)-N-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 300, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e metanamina (solução em THF 2,0 M).
[001608] LC/MS 403 (M+H).Exemplo 445
[001609] Produção de N,5-dibutil-3-(2-etoxietóxi)-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e butan-1-amina.
[001610] LC/MS 445 (M+H).Exemplo 446
[001611] Produção de 5-butil-3-(2-etoxietóxi)-N-(furan-2-ilmetil)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e 1-furan-2- ilmetanamina.
[001612] LC/MS 469 (M+H).Exemplo 447
[001613] Produção de 5-butil-3-(2-etoxietóxi)-4-oxo-N-(tetraidrofuran-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e 1- (tetraidrofuran-2-il)metanamina.
[001614] LC/MS 473 (M+H).Exemplo 448
[001615] Produção de 5-butil-3-(2-etoxietóxi)-4-oxo-N-(2-feniletil)-4,5- diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e 2- feniletanamina.
[001616] LC/MS 493 (M+H).Exemplo 449
[001617] Produção de 5-butil-3-(2-etoxietóxi)-N-(2-metoxibenzil)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e 1-(2- metoxifenil)metanamina.
[001618] LC/MS 509 (M+H).Exemplo 450
[001619] Produção de 5-butil-3-(2-etoxietóxi)-4-oxo-N-(1,2,3,4- tetraidronaftalen-1-il)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e 1,2,3,4- tetraidronaftalen-1-amina.
[001620] LC/MS 519 (M+H).Exemplo 451
[001621] Produção de N-(1,3-benzodioxol-5-ilmetil)-5-butil-3-(2-etoxietóxi)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e 1-(1,3- benzodioxol-5-il)metanamina.
[001622] LC/MS 523 (M+H).Exemplo 452
[001623] Produção de 5-butil-3-(2-etoxietóxi)-N,N-dietil-4-oxo-4,5- diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e N-etiletanamina.
[001624] LC/MS 445 (M+H).Exemplo 453
[001625] Produção de 5-butil-3-(2-etoxietóxi)-2-(piperidin-1- ilcarbonil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e piperidina.
[001626] LC/MS 457 (M+H).Exemplo 454
[001627] Produção de 5-butil-3-(2-etoxietóxi)-N-(2-metoxietil)-N-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e 2-metóxi-N- metiletanamina.
[001628] LC/MS 461 (M+H).Exemplo 455
[001629] Produção de 5-butil-3-(2-etoxietóxi)-N-metóxi-N-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 335, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e cloridrato de N-metoximetanamina.
[001630] LC/MS 433 (M+H).Exemplo 456
[001631] Produção de 5-butil-3-(2-etoxietóxi)-2-(tiomorfolin-4- ilcarbonil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e tiomorfolina.
[001632] LC/MS 475 (M+H).Exemplo 457
[001633] Produção de 5-butil-3-(2-etoxietóxi)-2-{[(2R)-2-(metoximetil)pirrolidin-1-il]carbonil}tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e (2R)-2- (metoximetil)pirrolidina.
[001634] LC/MS 487 (M+H).Exemplo 458
[001635] Produção de N-benzil-5-butil-3-(2-etoxietóxi)-N-metil-4-oxo- 4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e N-metil-1- fenilmetanamina.LC/MS 493 (M+H).Exemplo 459
[001636] Produção de 5-butil-3-(2-etoxietóxi)-N,N-bis(2-metilpropil)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 335, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e cloridrato de 2-metil-N-(2-metilpropil)propan-1-amina.
[001637] LC/MS 501 (M+H).Exemplo 460
[001638] Produção de trifluoroacetato de 5-butil-N-[3-(dimetilamina)propil]-3-(2-etoxietóxi)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e N,N- dimetilpropano-1,3-diamina.
[001639] LC/MS 474 (M+H). Exemplo 461
[001640] Produção de trifluoroacetato de 5-butil-N-[2-(dietilamina)etil]-3-(2-etoxietóxi)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e N,N-dietiletano- 1,2-diamina.
[001641] LC/MS 488 (M+H).Exemplo 462
[001642] Produção de trifluoroacetato de 5-butil-3-(2-etoxietóxi)-N-[3-(1H-imidazol-1-il)propil]-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e 3-(1H-imidazol- 1-il)propan-1-amina.
[001643] LC/MS 497 (M+H).Exemplo 463
[001644] Produção de trifluoroacetato de N-{2-[bis(1-metiletil)amina]etil}-5-butil-3-(2-etoxietóxi)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e N,N-bis(1- metiletil)etano-1,2-diamina.
[001645] LC/MS 516 (M+H).Exemplo 464
[001646] Produção de trifluoroacetato de 5-butil-3-(2-etoxietóxi)-2-[(4- metilpiperazin-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e 1- metilpiperazina.
[001647] LC/MS 472 (M+H).Exemplo 465
[001648] Produção de trifluoroacetato de 5-butil-3-(2-etoxietóxi)-N-metil-N-(1-metilpirrolidin-3-il)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e N,1- dimetilpirrolidin-3-amina.
[001649] LC/MS 486 (M+H).Exemplo 466
[001650] Produção de trifluoroacetato de 5-butil-N-[2-(dietilamina)etil]-3-(2-etoxietóxi)-N-metil-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e N,N-dietil-N’- metiletano-1,2-diamina.
[001651] LC/MS 502 (M+H).Exemplo 467
[001652] Produção de trifluoroacetato de 5-butil-3-(2-etoxietóxi)-2-[(4-(piridin-2-il)piperazin-1-il)carbonil]tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 104 e 1-(piridin-2- il)piperazina.
[001653] LC/MS 535 (M+H).Exemplo 468
[001654] Produção de 3-(2-etoxietóxi)-N-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 300, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e metanamina (solução em THF 2,0 M).
[001655] LC/MS 465 (M+H).Exemplo 469
[001656] Produção de N-butil-3-(2-etoxietóxi)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidano Exemplo 5, o composto titular foiobtido a partir do composto do Exemplo de Referência 21 e butan-1-amina.
[001657] LC/MS 507 (M+H).Exemplo 470
[001658] Produção de 3-(2-etoxietóxi)-N-(furan-2-ilmetil)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e 1-furan-2- ilmetanamina.
[001659] LC/MS 531 (M+H).Exemplo 471
[001660] Produção de 3-(2-etoxietóxi)-4-oxo-5-(2-oxo-2-feniletil)-N-(tetraidrofuran-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e 1-(tetraidrofuran- 2-il)metanamina.
[001661] LC/MS 535 (M+H).Exemplo 472
[001662] Produção de 3-(2-etoxietóxi)-4-oxo-5-(2-oxo-2-feniletil)-N-(2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e 2-feniletanamina.
[001663] LC/MS 555 (M+H).Exemplo 473
[001664] Produção de 3-(2-etoxietóxi)-N-(2-metoxibenzil)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e 1-(2- metoxifenil)metanamina.
[001665] LC/MS 571 (M+H).Exemplo 474
[001666] Produção de 3-(2-etoxietóxi)-4-oxo-5-(2-oxo-2-feniletil)-N-(1,2,3,4-tetraidronaftalen-1-il)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e 1,2,3,4- tetraidronaftalen-1-amina.
[001667] LC/MS 581 (M+H).Exemplo 475
[001668] Produção de N-(1,3-benzodioxol-5-ilmetil)-3-(2-etoxietóxi)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e 1-(1,3- benzodioxol-5-il)metanamina.
[001669] LC/MS 585 (M+H).Exemplo 476
[001670] Produção de 3-(2-etoxietóxi)-N,N-dietil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e N-etiletanamina.
[001671] LC/MS 507 (M+H).Exemplo 477
[001672] Produção de 3-(2-etoxietóxi)-5-(2-oxo-2-feniletil)-2- (piperidin-1-ilcarbonil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e piperidina.
[001673] LC/MS 519 (M+H).Exemplo 478
[001674] Produção de 3-(2-etoxietóxi)-N-(2-metoxietil)-N-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e 2-metóxi-N- metiletanamina.
[001675] LC/MS 523 (M+H).Exemplo 479
[001676] Produção de 3-(2-etoxietóxi)-N-metóxi-N-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 335, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e cloridrato de N-metoximetanamina.
[001677] LC/MS 495 (M+H).Exemplo 480
[001678] Produção de 3-(2-etoxietóxi)-5-(2-oxo-2-feniletil)-2-(tiomorfolin-4-ilcarbonil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e tiomorfolina.
[001679] LC/MS 537 (M+H).Exemplo 481
[001680] Produção de 3-(2-etoxietóxi)-2-{[(2R)-2-(metoximetil) pirrolidin-1-il]carbonil}-5-(2-oxo-2-feniletil)tieno[3,2-c]quinolin-4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e (2R)-2- (metoximetil)pirrolidina.
[001681] LC/MS 549 (M+H).Exemplo 482
[001682] Produção de N-benzil-3-(2-etoxietóxi)-N-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e N-metil-1- fenilmetanamina.
[001683] LC/MS 555 (M+H).Exemplo 483
[001684] Produção de 3-(2-etoxietóxi)-N,N-bis(2-metilpropil)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 335, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e cloridrato de 2-metil-N-(2-metilpropil)propan-1-amina.
[001685] LC/MS 563 (M+H).Exemplo 484
[001686] Produção de trifluoroacetato de N-[3-(dimetilamina)propil]-3-(2-etoxietóxi)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e N,N- dimetilpropano-1,3-diamina.
[001687] LC/MS 536 (M+H).Exemplo 485
[001688] Produção de trifluoroacetato de 3-(2-etoxietóxi)-N-[3-(1H- imidazol-1-il)propil]-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c] quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e 3-(1H-imidazol- 1-il)propan-1-amina.
[001689] LC/MS 559 (M+H).Exemplo 486
[001690] Produção de trifluoroacetato de N-{2-[bis(1-metiletil)amina]etil}-3-(2-etoxietóxi)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c] quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e N,N-bis(1- metiletil)etano-1,2-diamina.
[001691] LC/MS 578 (M+H).Exemplo 487
[001692] Produção de trifluoroacetato de 3-(2-etoxietóxi)-2-[(4- metilpiperazin-1-il)carbonil]-5-(2-oxo-2-feniletil)tieno[3,2-c]quinolin-4(5H)- onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e 1- metilpiperazina.
[001693] LC/MS 534 (M+H).Exemplo 488
[001694] Produção de trifluoroacetato de 3-(2-etoxietóxi)-N-metil-N-(1-metilpirrolidin-3-il)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c] quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e N,1- dimetilpirrolidin-3-amina.
[001695] LC/MS 548 (M+H). Exemplo 489
[001696] Produção de trifluoroacetato de N-[2-(dietilamina)etil]-3-(2-etoxietóxi)-N-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c] quinolina-2-carboxamidaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e N,N-dietil-N’- metiletano-1,2-diamina.
[001697] LC/MS 564 (M+H).Exemplo 490
[001698] Produção de trifluoroacetato de 3-(2-etoxietóxi)-5-(2-oxo-2-feniletil)-2-[(4-(piridin-2-il)piperazin-1-il)carbonil]tieno[3,2-c]quinolin- 4(5H)-onaDa mesma maneira que no Exemplo 5, o composto titular foi obtido a partir do composto do Exemplo de Referência 21 e 1-(piridin-2- il)piperazina.
[001699] LC/MS 597 (M+H). Exemplo 491
[001700] Produção de N-(2-amina-2-oxoetil)-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaA uma solução do composto do Exemplo de Referência 7 (175 mg, 0,44 mmol), glicina amida (56 mg, 0,51 mmol), HOBt (89 mg, 0,66 mmol) e WSCD (126 mg, 0,66 mmol) em DMF (5,0 ml) adicionou-se trietilamina (0,16 ml, 1,2 mmol), e a mistura foi agitada à temperatura ambiente durante 25 h. Adicionou-se água à mistura de reação, e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água, etanol e éter de dietila, e recristalizado de DMF dando o composto titular (124 mg, 54 %) como cristais brancos.
[001701] RMN 1H (300 MHz, DMSO-d6) δ:3,95 (2H, d, J = 5,3 Hz), 4,06 (3H, s), 6,00 (2H, s), 7,19 (1H, s), 7,30-7,40 (1H, m), 7,45-7,69 (5H, m), 7,73-7,82 (1H, m), 8,06 (1H, dd, J = 7,9, 1,3 Hz), 8,13-8,22 (2H, m), 8,28 (1H, t, J = 5,3 Hz).Exemplo 492
[001702] Produção de N-[2-(dimetilamina)etil]-3-metóxi-4-oxo-5-(2- oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (124 mg, 81 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (130 mg, 0,33 mmol) e N,N-dimetiletilenodiamina (44 mg, 0,49 mmol).
[001703] RMN 1H (300 MHz, DMSO-d6) δ:2,23 (6H, s), 2,45 (2H, d, J = 6,2 Hz), 3,42 (2H, q, J = 5,9 Hz), 4,02 (3H, s), 6,00 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,48 (1H, d, J = 8,7 Hz), 7,57 (1H, dd, J = 7,2, 1,5 Hz), 7,64 (2H, t, J = 7,5 Hz), 7,76 (1H, t, J = 7,5 Hz), 8,05 (1H, dd, J = 8,1, 1,5 Hz), 8,13-8,19 (3H, m).Exemplo 493
[001704] Produção de 3-metóxi-N-[2-(1-metilpirrolidin-2-il)etil]-4-oxo- 5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (86 mg, 52 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (130 mg, 0,33 mmol) e 2-(2-aminaetil)-1-metilpirrolidina (63 mg, 0,49 mmol).
[001705] RMN 1H (300 MHz, DMSO-d6) δ:1,45-1,70 (4H, m), 1,78- 2,15 (4H, m), 2,23 (3H, s), 2,90-2,97 (1H, m), 3,35-3,50 (2H, m), 4,01 (3H, s), 5,99 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,1 Hz), 7,56 (1H, dd, J = 7,2, 1,5 Hz), 7,60-7,67 (2H, m), 7,77 (1H, t, J = 7,5 Hz), 8,04 (1H, dd, J = 7,8, 1,5 Hz), 8,16-8,22 (3H, m).Exemplo 494
[001706] Produção de 2-[({[3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5- diidrotieno[3,2-c]quinolin-2-il]carbonil}amina)metil]piperidina-1-carboxilato de t-butilaDa mesma maneira que no Exemplo 25, o composto titular (190 mg, 85 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (150 mg, 0,38 mmol) e 2-aminametil-N-Boc- piperidina (122 mg, 0,57 mmol).
[001707] RMN 1H (300 MHz, CDCl3) δ:1,39 (9H, s), 1,40-1,60 (1H, m),1,60-1,80 (5H, m), 2,94 (1H, t, J = 12,6 Hz), 3,51-3,57 (1H, m), 3,70-3,90 (1H, br), 4,03 (1H, d, J = 14,4 Hz), 4,15 (3H, s), 4,45-4,60 (1H, m), 5,86 (2H, s), 7,01 (1H, d, J = 8,4 Hz), 7,26-7,28 (1H, m), 7,47 (1H, td, J = 8,1, 1,5 Hz), 7,59 (2H, t, J = 7,4 Hz), 7,65-7,70 (2H, m), 7,90 (1H, dd, J = 7,8, 1,2 Hz), 8,10-8,13 (2H, m).Exemplo 495
[001708] Produção de N-(2-hidróxi-2-metilpropil)-3-metóxi-1-metil-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (215 mg, 91 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e 1-amina-2-metilpropan-2- ol (59,3 mg, 0,666 mmol).
[001709] RMN 1H (300 MHz, DMSO-d6) δ:1,16 (6H, s), 3,29 (2H, d, J = 5,7 Hz), 4,02 (3H, s), 4,38 (3H, s), 4,69 (1H, s), 5,98 (2H, s), 7,29-7,40 (2H, m), 7,46-7,51 (1H, m), 7,64 (2H, t, J = 7,4 Hz), 7,73-7,79 (1H, m), 8,03 (1H, t, J = 5,7 Hz), 8,16-8,19 (2H, m), 8,39 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 496
[001710] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N- (tetraidrofuran-2-ilmetil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (199 mg, 82 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e 1-(tetraidrofuran-2- il)metanamina (68,7 ml, 0,666 mmol).
[001711] RMN 1H (300 MHz, DMSO-d6) δ:1,56-1,67 (1H, m), 1,761,99 (3H, m), 3,36-3,48 (2H, m), 3,63-3,71 (1H, m), 3,79-3,86 (1H, m), 3,96- 4,04 (4H, m), 4,36 (3H, s), 5,97 (2H, s), 7,29-7,40 (2H, m), 7,45-7,51 (1H, m), 7,63 (2H, t, J = 7,5 Hz), 7,73-7,79 (1H, m), 8,03 (1H, t, J = 5,7 Hz), 8,16-8,19 (2H, m), 8,38 (1H, dd, J = 8,4, 1,2 Hz).Exemplo 497
[001712] Produção de N-[trans-2-hidroxicicloexil]-3-metóxi-1-metil-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (168 mg, 67 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e cloridrato de trans-2- aminacicloexanol (101 mg, 0,666 mmol).
[001713] RMN 1H (300 MHz, DMSO-d6) δ:1,15-1,36 (4H, m), 1,551,70 (2H, m), 1,80-1,95 (1H, m), 1,95-2,10 (1H, m), 3,30-3,45 (1H, m), 3,553,70 (1H, m), 3,98 (3H, s), 4,36 (3H, s), 4,78 (1H, d, J = 5,4 Hz), 5,97 (2H, s), 7,29-7,39 (2H, m), 7,45-7,50 (1H, m), 7,63 (2H, t, J = 7,5 Hz), 7,73-7,79 (1H, m), 7,87 (1H, d, J = 7,5 Hz), 8,16-8,19 (2H, m), 8,38 (1H, dd, J = 8,4, 1,2 Hz). Exemplo 498
[001714] Produção de dicloridrato de N-[1-(2-hidroxietil)piperidin-4-il]- 3-metóxi-4-oxo-5-(piridin-2-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaUma mistura do composto do Exemplo 667 (60 mg, 0,15 mmol), cloridrato de 2-(clorometil)piridina (37 mg, 0,22 mmol), carbonato de potássio (52 mg, 0,37 mmol) e DMF (2 ml) foi agitada à temperatura ambiente durante 3 h e a 40°C durante 1 h. A mistura de reação foi diluída com solução aquosa saturada de hidrogenocarbonato de sódio, e extraída com acetato de etila. O extrato foi lavado com salmoura saturada, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila, acetato de etila/metanol=50/1 a 50/2) dando um sólido branco. A uma solução do sólido branco em acetato de etila (2 ml) adicionou-se solução 4N cloreto de hidrogênio acetato de etila (0,1 ml), e coletou-se precipitado por meio de filtração, lavado com éter de dietila, e secado sob pressão reduzida dando o composto titular (4,2 mg, 5 %) como um sólido branco.
[001715] RMN 1H (300 MHz, DMSO-d6) δ:1,91-2,27 (4H, m), 3,053,30 (4H, m), 3,60-3,80 (4H, m), 4,07-4,10 (4H, m), 5,69 (2H, s), 7,28-7,34 (3H, m), 7,41-7,58 (2H, m), 7,77 (1H, t, J = 8,6 Hz), 7,88 (1H, d, J = 7,5 Hz), 8,02 (1H, d, J = 8,1 Hz), 8,50 (1H, d, J = 2,7 Hz), 9,40-9,55 (2H, br), 9,609,70 (1H, br).Exemplo 499
[001716] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N- [1-(3,3,3-trifluoro-2-hidroxipropil)piperidin-4-il]-4,5-diidro-1H-pirrol[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 79, o composto titular (150 mg, 64 %) foi obtido como um pó branco a partir do composto do Exemplo 77 (200 mg, 0,400 mmol), 3-bromo-1,1,1-trifluoropropan-2-ol (62,2 ml, 0,600 mmol) e carbonato de potássio (249 mg, 1,80 mmol).
[001717] RMN 1H (300 MHz, DMSO-d6) δ:1,50-1,70 (2H, m), 1,801,95 (2H, m), 2,15-2,35 (2H, m), 2,45-2,60 (2H, m), 2,75-2,90 (2H, m), 3,753,90 (1H, m), 3,98 (3H, s), 4,05-4,20 (1H, m), 4,31 (3H, s), 5,97 (2H, s), 6,096,16 (1H, m), 7,28-7,39 (2H, m), 7,45-7,50 (1H, m), 7,63 (2H, t, J = 7,7 Hz), 7,73-7,79 (1H, m), 7,90 (1H, d, J = 8,1 Hz), 8,16-8,18 (2H, m), 8,37 (1H, dd, J = 8,3, 1,4 Hz).Exemplo 500
[001718] Produção de cloridrato de 3-metóxi-N-{2-[(1-metiletil)amina] etil}-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaA uma solução do composto do Exemplo 97 (150 mg, 0,30mmol) em acetato de etila (10 ml) adicionou-se solução 4N cloreto de hidrogênio acetato de etila (0,1 ml), e o precipitado resultante foi coletado por meio de filtração, lavado com acetato de etila, e secado sob pressão reduzida dando o composto titular (107 mg, 69 %) como um pó branco.
[001719] RMN 1H (300 MHz, DMSO-d6) δ:1,25 (6H, d, J = 6,6 Hz), 3,13 (2H, br s), 3,30-3,45 (1H, m), 3,68 (2H, q, J = 5,9 Hz), 4,07 (3H, s), 6,00 (2H, s), 7,36 (1H, t, J = 7,5 Hz), 7,50 (1H, d, J = 8,4 Hz), 7,57-7,67 (3H, m), 7,78 (1H, t, J = 7,4 Hz), 8,06 (1H, dd, J = 7,8, 1,2 Hz), 8,18 (2H, d, J = 8,4 Hz), 8,29 (1H, t, J = 5,9 Hz), 8,77 (2H, br s).Exemplo 501
[001720] Produção de N-[1-(2-hidroxietil)piperidin-4-il]-3-metóxi-5-(4- metoxibenzil)-1-metil-4-oxo-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 79, o composto titular (1,91 g, 75 %) foi obtido como cristais brancos a partir do composto do Exemplo 681 (2,50 g, 4,89 mmol).
[001721] RMN 1H (300 MHz, DMSO-d6) δ:1,58 (2H, q, J = 9,9 Hz), 1,85 (2H, d, J = 9,6 Hz), 2,18 (2H, t, J = 9,9 Hz), 2,40 (2H, t, J = 6,3 Hz), 2,78 (2H, d, J = 11,4 Hz), 3,50 (2H, q, J = 6,0 Hz), 3,69 (3H, s), 3,70-3,85 (1H, br), 4,04 (3H, s), 4,29 (3H, s), 4,35-4,40 (1H, m), 5,40-5,65 (2H, br), 6,86 (2H, d, J = 8,7 Hz), 7,14 (2H, d, J = 8,4 Hz), 7,24-7,30 (1H, m), 7,42-7,49 (2H, m), 7,91 (1H, d, J = 7,8 Hz), 8,33 (1H, d, J = 8,1 Hz).Exemplo 502
[001722] Produção de N-[(1-hidroxiciclopropil)metil]-3-metóxi-1-metil- 4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (219 mg, 93 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e 1-(aminametil)ciclopropanol (58,0 mg, 0,666 mmol).
[001723] RMN 1H (300 MHz, DMSO-d6) δ:0,55-0,65 (4H, m), 3,46 (2H, d, J = 5,8 Hz), 4,01 (3H, s), 4,37 (3H, s), 5,50 (1H, s), 5,97 (2H, s), 7,297,40 (2H, m), 7,45-7,51 (1H, m), 7,64 (2H, t, J = 7,5 Hz), 7,73-7,79 (1H, m), 8,10 (1H, t, J = 5,8 Hz), 8,16-8,19 (2H, m), 8,38 (1H, dd, J = 8,1, 1,2 Hz).Exemplo 503
[001724] Produção de N-[(1-hidroxicicloexil)metil]-3-metóxi-1-metil-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (235 mg, 92 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,512 mmol) e 1-(aminametil)cicloexanol (110 mg, 0,666 mmol).
[001725] RMN 1H (300 MHz, DMSO-d6) δ:1,20-1,70 (10H, m), 3,25- 3,40 (2H, m), 4,01 (3H, s), 4,38 (3H, s), 4,50 (1H, s), 5,97 (2H, s), 7,29-7,40 (2H, m), 7,45-7,51 (1H, m), 7,63 (2H, t, J = 7,7 Hz), 7,73-7,79 (1H, m), 8,02 (1H, t, J = 5,6 Hz), 8,16-8,19 (2H, m), 8,38 (1H, dd, J = 8,4, 1,2 Hz).Exemplo 504
[001726] Produção de acetato de 2-({2-[{[3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}(metil)amina]etil} amina)-2-oxoetilaA uma solução do composto do Exemplo 103 (150 mg, 0,31 mmol) e trietilamina (69 mg, 0,68 mmol) em THF (10 ml) adicionou-se cloreto de acetoxiacetila (46 mg, 0,34 mmol) sob resfriamento com gelo. Após agitação à temperatura ambiente durante 1 h, a mistura de reação foi diluída com solução aquosa saturada de hidrogenocarbonato de sódio, e extraída com acetato de etila. O extrato foi lavado com salmoura saturada, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em sílica-gel (eluado; acetato de etila para acetato de etila/metanol=50/1) dando um sólido branco. Recristalização do sólido branco de acetato de etila-hexano deu o composto titular (140 mg, 82 %) como cristais brancos.
[001727] RMN 1H (300 MHz, CDCl3) δ:2,28 (3H, s), 3,19 (3H, s), 3,62 (2H, br s), 3,77 (2H, br s), 4,02 (3H, s), 4,60 (2H, s), 5,87 (2H, s), 7,04 (1H, d, J = 8,4 Hz), 7,20-7,28 (1H, m), 7,45-7,50 (2H, m), 7,56 (2H, t, J = 7,5 Hz), 7,67 (1H, dd, J = 7,5, 1,5 Hz), 7,84 (1H, dd, J = 8,1, 1,2 Hz), 8,10-8,13 (2H, m). Exemplo 505
[001728] Produção de acetato de 2-[4-({[3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina)piperidin-1-il]-1,1-dimetil-2-oxoetilaDa mesma maneira que no Exemplo 504, o composto titular foi obtido como um óleo incolor a partir do composto do Exemplo 77 (200 mg, 0,423 mmol) e acetato de 2-cloro-1,1-dimetil-2-oxoetila (63,0 ml, 0,440 mmol).
[001729] RMN 1H (300 MHz, DMSO-d6) δ:1,36-1,50 (10H, m), 1,801,95 (2H, m), 2,07 (3H, s), 2,75-3,40 (2H, m), 3,96 (3H, s), 4,00-4,25 (1H, m), 4,29 (3H, s), 5,97 (2H, s), 7,29-7,39 (2H, m), 7,45-7,50 (1H, m), 7,63 (2H, t, J = 7,5 Hz), 7,73-7,79 (1H, m), 7,98 (1H, d, J = 7,8 Hz), 8,16-8,18 (2H, m), 8,37 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 506
[001730] Produção de N-[1-(2-hidróxi-2-metilpropanoil)piperidin-4-il]- 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 508, o composto titular (123 mg, 55 %) foi obtido como um pó branco a partir do composto do Exemplo 505, solução aquosa de hidróxido de sódio 8N (1,5 ml) e etanol (12 ml).
[001731] RMN 1H (300 MHz, DMSO-d6) δ:1,33 (6 H, s), 1,40-1,60 (2 H, m), 1,80-1,95 (2 H, m), 2,75-3,45 (2 H, m), 3,97 (3 H, s), 4,00-4,20 (1 H, m), 4,31 (3H, s), 4,20-4,80 (2H, m), 5,39 (1 H, s), 5,97 (2 H, s), 7,29-7,39 (2 H, m), 7,45-7,50 (1 H, m), 7,63 (2 H, t, J = 7,5 Hz), 7,73-7,79 (1 H, m), 7,93 (1 H, d, J = 8,1 Hz), 8,15-8,18 (2 H, m), 8,37 (1 H, d, J = 8,3, 1,4 Hz).Exemplo 507
[001732] Produção de 3-metóxi-N-{2-[(metoxiacetil)amina]etil}-N- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaA uma solução do composto do Exemplo 103 (100 mg, 0,21 mmol) e trietilamina (46 mg, 0,45 mmol) em THF (10 ml) adicionou-se cloreto de metoxiacetila (25 mg, 0,23 mmol) sob resfriamento com gelo. Após agitação à temperatura ambiente durante 2 h, a mistura de reação foi diluída com solução aquosa saturada de hidrogenocarbonato de sódio, e extraída com acetato de etila. O extrato foi lavado com salmoura saturada, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em sílica-gel (eluado; acetato de etila to acetato de etila/metanol=50/1) dando um sólido branco. Recristalização do sólido branco de acetato de etila-hexano deu o composto titular (61 mg, 56 %) como um pó branco.
[001733] RMN 1H (300 MHz, DMSO-d6) δ:3,06 (3H, s), 3,30-3,50 (5H, m), 3,50-3,65 (2H, br), 3,70-3,95 (5H, m), 5,98 (2H, s), 7,34 (1H, t, J = 7,4 Hz), 7,46-7,96 (7H, m), 8,18 (2H, d, J = 7,5 Hz).Exemplo 508
[001734] Produção de N-{2-[(hidroxiacetil)amina]etil}-3-metóxi-N- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaUma solução mista do composto do Exemplo 504 (120 mg, 0,22 mmol) e solução aquosa de hidróxido de sódio 4N (2 ml) em THF (4 ml)-metanol (4 ml) foi agitada à temperatura ambiente durante 2 h, a mistura de reação foi diluída com solução aquosa saturada de hidrogenocarbonato de sódio, e a mistura foi extraída com acetato de etila. O extrato foi lavado com salmoura saturada, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. Recristalização do sólido bruto de acetato de etila-hexano deu o composto titular (65 mg, 58 %) como cristais brancos.
[001735] RMN 1H (300 MHz, DMSO-d6) δ:3,06 (3H, s), 3,20-3,40 (2H, m), 3,45-3,60 (2H, br), 3,70-3,86 (5H, m), 5,40-5,55 (1H, br), 5,98 (2H, s), 7,34 (1H, t, J = 7,5 Hz), 7,47 (1H, d, J = 8,4 Hz), 7,55 (1H, t, J = 7,2 Hz), 7,64 (2H, t, J = 7,5 Hz), 7,77 (1H, t, J = 7,5 Hz), 7,87-7,96 (2H, m), 8,16-8,19 (2H, m).Exemplo 509
[001736] Produção de acetato de 2-[4-({[3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}amina)piperidin-1-il]-2- oxoetilaDa mesma maneira que no Exemplo 123, o composto titular (429 mg, 56 %) foi obtido como um sólido branco a partir do composto do Exemplo 105 (620 mg, 1,20 mmol).
[001737] RMN 1H (300 MHz, CDCl3) δ:1,44-1,64 (2H, m), 2,01-2,28 (5H, m), 2,88-3,05 (1H, m), 3,17-3,34 (1H, m), 3,59-3,75 (1H, m), 4,15 (3H, s), 4,19-4,35 (1H, m), 4,41-4,54 (1H, m), 4,65-4,84 (2H, m), 5,87 (2H, s), 7,03 (1H, d, J = 8,5 Hz), 7,28-7,35 (1H, m), 7,43-7,52 (1H, m), 7,52-7,63 (3H, m), 7,65-7,74 (1H, m), 7,91 (1H, dd, J = 7,9, 1,3 Hz), 8,06-8,18 (2H, m). Exemplo 510
[001738] Produção de 6-etil-N-[1-(hidroxiacetil)piperidin-4-il]-1-metil- 4-oxo-5-(2-oxo-2-feniletil)-3-propóxi-4,5-diidro-1H-pirrol[3,2-c]piridina-2- carboxamidaDa mesma maneira que no Exemplo 140, o composto titular (199 mg, 74 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 173 (198 mg, 0,50 mmol).
[001739] RMN 1H (300 MHz, DMSO-d6) δ:0,92 (3H, t, J = 7,4 Hz), 1,18 (3H, t, J = 7,3 Hz), 1,26-1,55 (2H, m), 1,59-1,75 (2H, m), 1,83-1,97 (2H, m), 2,57 (2H, q, J = 7,4 Hz), 2,77-2,91 (1H, m), 3,01-3,18 (1H, m), 3,60-3,75 (1H, m), 3,89 (3H, s), 3,97-4,14 (3H, m), 4,20-4,34 (3H, m), 4,51 (1H, t, J = 5,4 Hz), 5,59 (2H, s), 6,48 (1H, s), 7,56-7,68 (3H, m), 7,69-7,78 (1H, m), 8,07-8,15 (2H, m).Exemplo 511
[001740] Produção de N-[1-(hidroxiacetil)piperidin-4-il]-3-metóxi-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaA uma solução mista do composto do Exemplo 509 (200 mg, 0,35 mmol) em THF (3,2 ml)-etanol (11 ml) adicionou-se solução aquosa de hidróxido de sódio 8N (1,6 ml, 13 mmol), e a mistura foi agitada à temperatura ambiente durante 30 min. A mistura de reação foi neutralizada com ácido clorídrico 2N, e extraída com solvente misto de acetato de etila- THF. O extrato foi combinado, lavado com salmoura saturada, secado sobre sulfato de magnésio, e submetido a filtração por gel de aminassílica. O filtrado foi concentrado sob pressão reduzida, o resíduo foi recristalizado de THF-acetato de etila dando o composto titular (93 mg, 50 %) como um sólido branco.
[001741] RMN 1H (300 MHz, CDCl3) δ:1,43-1,64 (2H, m), 2,07-2,24 (2H, m), 2,98-3,24 (2H, m), 3,44-3,58 (1H, m), 3,62 (1H, t, J = 4,3 Hz), 4,15 (3H, s), 4,19 (2H, d, J = 4,3 Hz), 4,22-4,35 (1H, m), 4,44-4,57 (1H, m), 5,86 (2H, s), 7,03 (1H, d, J = 8,5 Hz), 7,28-7,34 (1H, m), 7,44-7,63 (4H, m), 7,647,73 (1H, m), 7,91 (1H, dd, J = 7,8, 1,4 Hz), 8,06-8,16 (2H, m).Exemplo 512
[001742] Produção de acetato de 2-{2-[({[3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}amina)metil]piperidin- 1-il}-2-oxoetilaDa mesma maneira que no Exemplo 123, o composto titularfoi obtido como um óleo incolor a partir do composto do Exemplo 84 (500 mg, 0,95 mmol) e cloreto de acetoxiacetila (142 mg, 1,04 mmol).
[001743] RMN 1H (300 MHz, DMSO-d6) δ:1,10-1,80 (6H, m), 2,00 (3H, s), 2,81 (0,5H, t, J = 13,1 Hz), 3,20-3,90 (3H, m), 3,99-4,04 (3,5H, m), 4,24 (0,5H, d, J = 10,5 Hz), 4,65 (0,5H, d, J = 14,7 Hz), 4,80-4,82 (2H, m), 5,99 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,7 Hz), 7,56-7,67 (3H, m), 7,77 (1H, t, J = 7,2 Hz), 7,89 (0,5H, br t), 8,04 (1H, d, J = 8,1 Hz), 8,178,19 (2H, m), 8,26 (0,5H, br s).Exemplo 513
[001744] Produção de N-{[1-(hidroxiacetil)piperidin-2-il]metil}-3- metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 508, o composto titular (109 mg, 58 %) foi obtido como um pó branco a partir do composto do Exemplo 512 (200 mg, 0,34 mmol).
[001745] RMN 1H (300 MHz, DMSO-d6) δ:1,10-1,80 (6H, m), 2,86 (0,5H, t, J = 12,9 Hz), 3,26 (0,5H, t, J = 15,0 Hz), 3,35-3,48 (1,5H, m), 3,703,90 (0,5H, m), 3,90-4,05 (4H, m), 4,05-4,15 (1,5H, m), 4,25-4,40 (1,5H, m), 4,75-4,90 (0,5H, m), 5,99 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,4 Hz), 7,56-7,67 (3H, m), 7,77 (1H, t, J = 7,5 Hz), 7,85-7,95 (0,5H, br), 8,04 (1H, dd, J = 7,8, 1,2 Hz), 8,16-8,19 (2,5H, m).Exemplo 514
[001746] Produção de 3-metóxi-N-[1-(metoxiacetil)piperidin-4-il]-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamida Da mesma maneira que no Exemplo 507, o composto titular foi obtido (159 mg, 73 %) como um pó branco a partir do composto do Exemplo 77 (200 mg, 0,423 mmol) e cloreto de metoxiacetila (40,3 ml, 0,440 mmol).
[001747] RMN 1H (300 MHz, DMSO-d6) δ: 1,35-1,65 (2 H, m), 1,802,00 (2 H, m), 2,80-2,95 (1 H, m), 3,05-3,25 (1 H, m), 3,30 (3 H, s), 3,65-3,85 (1 H, m), 3,97 (3 H, s), 4,00-4,25 (4 H, m), 4,31 (3 H, s), 5,97 (2 H, s), 7,297,39 (2 H, m), 7,45-7,50 (1 H, m), 7,63 (2 H, t, J = 7,7 Hz), 7,73-7,79 (1 H, m), 7,95 (1 H, d, J = 8,1 Hz), 8,15-8,18 (2 H, m), 8,37 (1 H, dd, J = 8,3, 1,1 Hz).Exemplo 515
[001748] Produção de N-[1-(etilcarbamoil)piperidin-4-il]-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaA uma mistura do composto do Exemplo 77 (200 mg, 0,423 mmol) e THF (10 ml) adicionou-se isocianato de etila (101 ml, 1,27 mmol) a 0°C, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com acetato de etila, lavada com água e salmoura saturada, secada sobre sulfato de magnésio, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila). Recristalização do sólido obtido de acetato de etila-THF deu o composto titular (172 mg, 75 %) como um pó branco.
[001749] RMN 1H (300 MHz, DMSO-d6) δ: 1,01 (3H, t, J = 7,1 Hz), 1,35-1,50 (2H, m), 1,75-1,90 (2H, m), 2,80-3,10 (4H, m), 3,80-3,95 (2H, m), 3,96 (3H, s), 3,95-4,10 (1H, m), 4,30 (3H, s), 5,97 (2H, s), 6,48 (1H, t, J = 5,4 Hz), 7,28-7,39 (2H, m), 7,44-7,50 (1H, m), 7,63 (2H, t, J = 7,5 Hz), 7,73-7,79 (1H, m), 7,93 (1H, d, J = 8,1 Hz), 8,15-8,18 (2H, m), 8,36 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 516
[001750] Produção de 3-metóxi-1-metil-N-[1-(metilsulfonil)piperidin-4- il]-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaA uma mistura do composto do Exemplo 77 (200 mg, 0,423 mmol), trietilamina (423 ml, 3,18 mmol) e THF (10 ml) adicionou-se cloreto de metanossulfonila (98,3 ml, 1,27 mmol) a 0°C, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com acetato de etila, lavada com água e salmoura saturada, secada sobre sulfato de magnésio, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila). Recristalização do sólido obtido de acetato de etila deu o composto titular (141 mg, 61 %) como um pó branco.
[001751] RMN 1H (300 MHz, DMSO-d6) δ: 1,60-1,75 (2H, m), 1,902,05 (2H, m), 2,85-3,05 (5H, m), 3,45-3,60 (2H, m), 3,90-4,05 (1H, m), 3,98 (3H, s), 4,30 (3H, s), 5,97 (2H, s), 7,29-7,39 (2H, m), 7,45-7,50 (1H, m), 7,63 (2H, t, J = 7,5 Hz), 7,73-7,79 (1H, m), 8,00 (1H, d, J = 7,8 Hz), 8,16-8,18 (2H, m), 8,37 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 517
[001752] Produção de N-[1-(3-hidroxipropanoil)piperidin-4-il]-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c] quinolina-2-carboxamida A uma mistura do composto do Exemplo 77 (200 mg, 0,423 mmol), trietilamina (423 ml, 3,18 mmol) e THF (10 ml) adicionou-se β- propiolactona (39,9 ml, 0,635 mmol) a 0°C, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com acetato de etila, lavada com água e salmoura saturada, secada sobre sulfato de magnésio, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila). Recristalização do sólido obtido de acetato de etila deu o composto titular (70,0 mg, 30 %) como um pó branco.
[001753] RMN 1H (300 MHz, DMSO-d6) δ: 1,30-1,60 (2 H, m), 1,802,00 (2 H, m), 2,45-2,55 (2 H, m), 2,80-2,90 (1 H, m), 3,15-3,25 (1 H, m), 3,61-3,70 (2 H, m), 3,80-3,95 (1 H, m), 3,97 (3 H, s), 4,00-4,15 (1 H, m), 4,15-4,35 (1 H, m), 4,31 (3H, s), 4,51 (1 H, t, J=5,4 Hz), 5,97 (2 H, s), 7,29-7,39 (2 H, m), 7,45-7,50 (1 H, m), 7,63 (2 H, t, J =7,5 Hz), 7,73-7,79 (1 H, m), 7,94 (1 H, d, J = 7,8 Hz), 8,15-8,22 (2 H, m), 8,37 (1 H, dd, J = 8,4, 1,2 Hz).Exemplo 518
[001754] Produção de 3-metóxi-1-metil-N-{1-[(metilsulfonil)acetil] piperidin-4-il}-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c] quinolina-2-carboxamidaA uma solução do composto do Exemplo 77 (200 mg, 0,423 mmol), ácido (metilsulfonil)acético (76,0 mg, 0,550 mmol) e HOBt (85,8 mg, 0,635 mmol) em DMF (4 ml) adicionou-se WSCD (122 mg, 0,635 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com solução aquosa saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura saturada, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila). Recristalização do sólido obtido de acetato de etila deu o composto titular (60,3 mg, 24 %) como cristais brancos.
[001755] RMN 1H (300 MHz, DMSO-d6) δ: 1,35-1,70 (2H, m), 1,852,00 (2H, m), 2,90-3,05 (1H, m), 3,10 (3H, s), 3,20-3,35 (1H, m), 3,90-4,20 (5H, m), 4,20-4,35 (1H, m), 4,30 (3H, s), 4,50 (2H, s), 5,97 (2H, s), 7,29-7,39 (2H, m), 7,45-7,50 (1H, m), 7,63 (2H, t, J = 7,7 Hz), 7,73-7,79 (1H, m), 7,98(1H, d, J = 7,8 Hz), 8,16-8,18 (2H, m), 8,37 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 519
[001756] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N-[2-(2-oxopirrolidin-1-il)etil]-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (153 mg, 60 %) foi obtido como um sólido amarelo claro a partir do composto do Exemplo de Referência 28 (200 mg, 0,51 mmol), 1-(2-aminaetil)pirrolidin- 2-ona (72 mg, 0,56 mmol), HOBt (89 mg, 0,66 mmol), WSCD (127 mg, 0,66 mmol) e DMF (6,0 ml).
[001757] RMN 1H (300 MHz, CDCl3) δ:1,97-2,14 (2H, m), 2,40 (2H, t, J = 8,1 Hz), 3,44-3,59 (4H, m), 3,60-3,70 (2H, m), 4,18 (3H, s), 4,47 (3H, s), 5,88 (2H, s), 7,00-7,09 (1H, m), 7,21-7,33 (1H, m), 7,35-7,45 (1H, m), 7,49-7,59 (2H, m), 7,62-7,71 (1H, m), 7,81 (1H, t, J = 5,4 Hz), 8,07-8,16 (2H, m), 8,25 (1H, dd, J = 8,3, 1,3 Hz).Exemplo 520
[001758] Produção de acetato de 2-{4-[{[3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}(metil)amina]piperidin- 1-il}-2-oxoetilaDa mesma maneira que no Exemplo 73, cloridrato de N-metil- 3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-N-piperidin-4-il-4,5-diidrotieno[3,2- c]quinolina-2-carboxamida foi obtido a partir do composto do Exemplo de Referência 7 (500 mg, 1,3 mmol) e 4-(metilamina)piperidina-1-carboxilato de t-butila (327 mg, 1,5 mmol), e seguido dos mesmos procedimentos que no Exemplo 500 e 130 o composto titular (182 mg, 24 %) foi obtido como um sólido branco.
[001759] RMN 1H (300 MHz, DMSO-d6) δ:1,59-1,91 (4H, m), 2,08 (3H, s), 2,57-2,77 (1H, m), 2,91 (3H, s), 2,99-3,17 (1H, m), 3,32 (1H, m), 3,69-3,90 (4H, m), 4,29-4,50 (1H, m), 4,78 (2H, s), 5,98 (2H, s), 7,30-7,38 (1H, m), 7,43-7,70 (4H, m), 7,73-7,82 (1H, m), 7,97 (1H, dd, J = 7,9, 1,3 Hz), 8,11-8,22 (2H, m).Exemplo 521
[001760] Produção de N-[1-(hidroxiacetil)piperidin-4-il]-3-metóxi-N- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 511, o composto titular (115 mg, 66 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 520 (187 mg, 0,32 mmol), solução aquosa de hidróxido de sódio 8N (1,6 ml), THF (3,2 ml) e etanol (11 ml).
[001761] RMN 1H (300 MHz, CDCl3) δ:1,64-1,98 (4H, m), 2,67-2,89 (1H, m), 3,00 (3H, s), 3,05-3,19 (1H, m), 3,52-3,66 (2H, m), 4,01 (3H, s), 4,10-4,26 (3H, m), 4,66-4,85 (1H, m), 5,87 (2H, s), 7,04 (1H, d, J = 8,5 Hz), 7,23-7,32 (1H, m), 7,42-7,51 (1H, m), 7,52-7,62 (2H, m), 7,63-7,75 (1H, m), 7,84 (1H, dd, J = 7,9, 1,3 Hz), 7,99-8,20 (2H, m).Exemplo 522
[001762] Produção de 6-etil-N-[1-(hidroxiacetil)piperidin-4-il]-1-metil- 3-(1-metiletóxi)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxamida Da mesma maneira que no Exemplo 140, o composto titularfoi obtido como um pó incolor a partir do composto do Exemplo de Referência 174 (188 mg, 0,50 mmol).
[001763] RMN 1H (300 MHz, DMSO-d6) δ:1,12-1,26 (9H, m), 1,261,57 (2H, m), 1,84-1,97 (2H, m), 2,57 (2H, q, J = 7,4 Hz), 2,76-2,94 (1H, m), 3,02-3,20 (1H, m), 3,59-3,76 (1H, m), 3,91 (3H, s), 3,96-4,19 (3H, m), 4,214,34 (1H, m), 4,50 (1H, t, J = 5,5 Hz), 4,94-5,09 (1H, m), 5,59 (2H, s), 6,48 (1H, s), 7,56-7,69 (3H, m), 7,69-7,78 (1H, m), 8,06-8,16 (2H, m).Exemplo 523
[001764] Produção de 3-({[3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina) pirrolidino- 1-carboxilato de t-butila Da mesma maneira que no Exemplo 25, o composto titular foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (400 mg, 1,02 mmol) e 3-aminapirrolidino-1-carboxilato de t-butila (248 mg, 1,33 mmol).
[001765] RMN 1H (300 MHz, DMSO-d6) δ: 1,41 (9 H, s), 1,87-2,02 (1 H, m), 2,05-2,19 (1 H, m, J = 14,7 Hz), 3,19-3,46 (3 H, m), 3,48-3,61 (1 H, m), 3,95 (3 H, s), 4,30 (3 H, s), 4,40-4,52 (1 H, m), 5,97 (2 H, s), 7,27-7,41 (2 H, m), 7,44-7,53 (1 H, m), 7,63 (2 H, t, J =7,6 Hz), 7,72-7,80 (1 H, m), 8,118,22 (3 H, m), 8,37 (1 H, dd, J = 8,3, 1,1 Hz).Exemplo 524
[001766] Produção de [4-({[3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina)cicloexil] carbamato de t-butila Da mesma maneira que no Exemplo 25, o composto titular foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (400 mg, 1,02 mmol) e (4-aminacicloexil)carbamato de t-butila (285 mg, 1,33 mmol).
[001767] RMN 1H (300 MHz, DMSO-d6) δ: 1,16-1,69 (13H, m), 1,721,96 (4H, m), 3,16-3,29 (1H, m), 3,65-3,80 (1H, m, J = 11,1 Hz), 3,95 (2,5H, s), 4,07 (0,5H, s), 4,30 (2,5H, s), 4,39 (0,5H, s), 5,97 (2H, s), 6,70-6,81 (0,8H, m), 6,85-6,94 (0,2H, m), 7,25-7,42 (2H, m), 7,43-7,53 (1H, m), 7,58-7,68 (2H, m), 7,72-7,86 (2H, m), 8,14-8,22 (2H, m), 8,36 (1H, dd, J = 8,3, 1,1 Hz). Exemplo 525
[001768] Produção de N-[1-(hidroxiacetil)pirrolidin-3-il]-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaUma mistura do composto do Exemplo 523, acetato de etila (2 ml) e solução 4N cloreto de hidrogênio acetato de etila (2 ml) foi agitada à temperatura ambiente durante 1 h. A mistura foi concentrada sob pressão reduzida, solução aquosa saturada de hidrogenocarbonato de sódio foi adicionada ao resíduo, e a mistura foi extraída com acetato de etila. O extrato foi combinado, lavado com salmoura saturada, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida dando 3-metóxi-1-metil-4-oxo- 5-(2-oxo-2-feniletil)-N-pirrolidin-3-il-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamida (153 mg, 27 %) como um pó branco.
[001769] A uma mistura da assim-obtida 3-metóxi-1-metil-4-oxo-5-(2- oxo-2-feniletil)-N-pirrolidin-3-il-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamida (153 mg, 0,327 mmol), adicionou-se trietilamina (99,7 ml, 0,720 mmol) e THF (3 ml) cloreto de acetoxiacetila (38,7 ml, 0,360 mmol) a 0°C, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com acetato de etila, lavada com água e salmoura saturada, secada sobre sulfato de magnésio, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila). O óleo obtido foi dissolvido em THF (4 ml) e etanol (12 ml), adicionou-se solução aquosa de hidróxido de sódio 8N (1 ml) e a mistura foi agitada à temperatura ambiente durante 1,5 h. A mistura de reação foi diluída com água, acidificada com ácido clorídrico 1N (8,5 ml), e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura saturada, secado sobre sulfato de magnésio e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/metanol=10/0 - 9/1). Recristalização do sólido obtido de acetato de etila-THF deu o composto titular (121 mg, 72 %) como um pó branco.
[001770] RMN 1H (300 MHz, DMSO-d6) δ: 1,86-2,31 (2H, m), 3,333,56 (3H, m), 3,58-3,72 (1H, m), 3,94 (3H, s), 4,02 (2H, dd, J = 10,2, 5,7 Hz), 4,29 (3H, d, J = 2,1 Hz), 4,40-4,64 (2H, m), 5,97 (2H, s), 7,27-7,41 (2H, m), 7,43-7,52 (1H, m), 7,63 (2H, t, J = 7,6 Hz), 7,72-7,81 (1H, m), 8,12-8,23 (3H, m), 8,37 (1H, d, J = 7,9 Hz).Exemplo 526
[001771] Produção de N-{4-[(hidroxiacetil)amina]cicloexil}-3-metóxi- 1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaA uma mistura do composto do Exemplo 88 (190 mg, 0,363 mmol), trietilamina (151 ml, 1,09 mmol) e THF (7 ml) adicionou-se cloreto de acetoxiacetila (46,9 ml, 0,436 mmol) a 0°C, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com acetato de etila, lavada com água e salmoura saturada, secada sobre sulfato de magnésio, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila). O óleo obtido foi dissolvido em THF (2,5 ml) e etanol (5 ml), adicionou-se solução aquosa de hidróxido de sódio 8N (0,5 ml) e a mistura foi agitada à temperatura ambiente durante 1,5 h. A mistura de reação foi diluída com água, acidificada com ácido clorídrico 1N (4,5 ml), e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura saturada, secado sobre sulfato de magnésio e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/THF=10/0 - 0/10). Recristalização do sólido obtido de acetato de etila-THF deu o composto titular (91,1 mg, 46 %) como um pó branco.
[001772] RMN 1H (300 MHz, DMSO-d6) δ:1,44 (4H, t, J = 10,1 Hz), 1,67-1,85 (2H, m), 1,88-2,02 (2H, m), 3,55-3,84 (4H, m), 3,96 (3H, s), 4,30 (3H, s), 5,43 (1H, t, J = 5,8 Hz), 5,97 (2H, s), 7,23-7,40 (2H, m), 7,43-7,55 (2H, m), 7,63 (2H, t, J = 7,6 Hz), 7,71-7,89 (2H, m), 8,11-8,23 (2H, m), 8,36(1H, dd, J = 8,3, 1,1 Hz).Exemplo 527
[001773] Produção de cloridrato de N-(1-glicilpiperidin-4-il)-3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaA uma solução do composto do Exemplo 77 (250 mg, 0,529 mmol), N-Boc-glicina (111 mg, 0,635 mmol) e HOBt (107 mg, 0,794 mmol) em DMF (5 ml) adicionou-se WSCD (152 mg, 0,794 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com solução aquosa saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura saturada, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi dissolvido em acetato de etila (2 ml), adicionou-se solução 4N cloreto de hidrogênio acetato de etila (2 ml), e a mistura foi agitada à temperatura ambiente durante 1 h. O sólido precipitado foi recolhido por meio de filtração, lavado com acetato de etila, e recristalizado de etanol-acetato de etila dando o composto titular (236 mg, 79 %) como cristais brancos.
[001774] RMN 1H (300 MHz, DMSO-d6) δ:1,35-1,70 (2H, m), 1,852,00 (2H, m), 2,95-3,10 (1H, m), 3,15-3,30 (1H, m), 3,60-3,75 (1H, m), 3,803,95 (2H, m), 3,97 (3H, s), 4,05-4,30 (2H, m), 4,31 (3H, s), 5,97 (2H, s), 7,297,40 (2H, m), 7,45-7,51 (1H, m), 7,63 (2H, t, J = 7,5 Hz), 7,73-7,79 (1H, m), 7,99 (1H, d, J = 7,8 Hz), 8,08-8,21 (5H, m), 8,37 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 528
[001775] Produção de acetato de 2-{2-[2-({[3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}amina)etil]pirrolidin-1- il}-2-oxoetilaDa mesma maneira que no Exemplo 504, o composto titular(200 mg, 89 %) foi obtido como um sólido branco a partir do composto do Exemplo 82 (200 mg, 0,38 mmol) e cloreto de acetoxiacetila (57 mg, 0,42 mmol).
[001776] RMN 1H (300 MHz, DMSO-d6) δ:1,50-2,00 (6H, m), 2,08 (3H, s), 2,90-3,10 (1H, m), 3,38-3,49 (2H, m), 3,50-3,65 (1H, m), 4,05 (3H, s), 4,10-4,20 (1H, m), 4,73 (2H, s), 5,99 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,4 Hz), 7,57 (1H, d, J = 7,2 Hz), 7,64 (2H, t, J = 7,5 Hz), 7,77 (1H, t, J = 7,5 Hz), 8,04 (1H, d, J = 7,8 Hz), 8,18 (2H, d, J = 7,5 Hz), 8,45 (1H, t, J = 6,0 Hz).Exemplo 529
[001777] Produção de acetato de 2-{3-[({[3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}amina)metil]pirrolidin- 1-il}-2-oxoetilaDa mesma maneira que no Exemplo 504, o composto titular (160 mg, 71 %) foi obtido como um sólido branco a partir do composto do Exemplo 669 (200 mg, 0,39 mmol) e cloreto de acetoxiacetila (87 mg, 0,86 mmol).
[001778] RMN 1H (300 MHz, DMSO-d6) δ:1,60-1,78 (2H, m), 1,841,95 (1H, m), 2,07 (3H, s), 2,50-2,70 (1H, m), 3,07-3,57 (6H, m), 4,03 (1,5H, m), 4,04 (1,5H, s), 4,65 (2H, m), 6,00 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,4 Hz), 7,58-7,67 (3H, m), 7,77 (1H, t, J = 7,5 Hz), 8,05 (1H, d, J = 7,8 Hz), 8,16-8,23 (2H, m).Exemplo 530
[001779] Produção de acetato de 2-{[trans-2-({[3-metóxi-1-metil-4-oxo- 5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil} amina)cicloexil]amina}-2-oxoetilaDa mesma maneira que no Exemplo 504, o composto titular (190 mg, 85 %) foi obtido como um sólido branco a partir do composto do Exemplo 85 (200 mg, 0,38 mmol) e cloreto de acetoxiacetila (63 mg, 0,46 mmol).
[001780] RMN 1H (300 MHz, DMSO-d6) δ:1,20-1,41 (4H, m), 1,71 (2H, br s), 1,80-1,90 (1H, br d), 2,04 (3H, s), 2,41-2,45 (1H, m), 3,72-3,85 (2H, m), 3,95 (3H, s), 4,26 (3H, s), 4,40 (2H, s), 5,97 (2H, s), 7,29-7,40 (2H, m), 7,48 (1H, t, J = 7,8 Hz), 7,64 (2H, t, J = 7,5 Hz), 7,74-7,82 (2H, m), 7,95 (1H, d, J = 8,1 Hz), 8,16-8,19 (2H, m), 8,38 (1H, d, J = 6,9 Hz).Exemplo 531
[001781] Produção de acetato de 2-[3-({[3-metóxi-1-metil-4-oxo-5-(2- oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina) azetidin-1-il]-2-oxoetilaDa mesma maneira que no Exemplo 123, cloridrato de N- azetidin-3-il-3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H- pirrol[3,2-c]quinolina-2-carboxamida (600 mg) foi obtido como um pó branco a partir do composto do Exemplo de Referência 670 (610 mg, 1,12 mmol). O composto titular (121 mg, 17 %) foi obtido como um sólido branco a partir do assim-obtido pó branco por meio de um método similar àquele no Exemplo 504.
[001782] RMN 1H (300 MHz, DMSO-d6) δ:2,09 (3H, s), 3,30-3,50 (2H, m), 3,86 (3H, s), 4,16 (1H, s), 4,36 (3H, s), 4,40-4,42 (2H, m), 4,48 (2H, m), 5,97 (2H, s), 7,30-7,40 (2H, m), 7,48 (1H, d, J = 8,3 Hz), 7,64 (2H, t, J = 7,5 Hz), 7,76 (1H, t, J = 7,5 Hz), 8,16-8,23 (3H, m), 8,40 (1H, d, J = 7,5 Hz).Exemplo 532
[001783] Produção de [3-({[3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina)cicloexil] carbamato de t-butilaDa mesma maneira que no Exemplo 25, o composto titular (395 mg, 66 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (400 mg, 1,02 mmol) e (3-aminacicloexil)carbamato de t-butila (285 mg, 1,33 mmol).
[001784] RMN 1H (300 MHz, DMSO-d6) δ: 0,98-1,46 (13H, m), 1,651,90 (3H, m), 2,00-2,12 (1H, m), 3,23-3,42 (1H, m), 3,73-3,88 (1H, m), 3,96 (2H, s), 4,04 (1H, s), 4,30 (2H, s), 4,35 (1H, s), 5,97 (2H, s), 6,76-6,94 (1H, m), 7,24-7,42 (2H, m), 7,43-7,53 (1H, m), 7,63 (2H, t, J = 7,6 Hz), 7,71-7,80 (1H, m), 7,86 (1H, d, J = 7,9 Hz), 8,12-8,22 (2H, m), 8,31-8,42 (1H, m).Exemplo 533
[001785] Produção de cloridrato de N-(3-aminacicloexil)-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaA uma mistura do composto do Exemplo 532 (380 mg, 0,648) e acetato de etila (4 ml) adicionou-se solução 4N cloreto de hidrogênio acetato de etila (4 ml), e a mistura foi agitada à temperatura ambiente durante 2 h. O sólido precipitado foi recolhido por meio de filtração, e lavado com acetato de etila dando o composto titular (305 mg, 90 %) como um pó branco.
[001786] RMN 1H (300 MHz, DMSO-d6) δ:1,09-2,03 (7H, m), 2,172,32 (1H, m), 3,05-3,24 (1H, m), 3,80-4,10 (4H, m), 4,28 (2,5H, s), 4,32 (0,5H, s), 5,97 (2H, s), 7,26-7,53 (3H, m), 7,63 (2H, t, J = 7,4 Hz), 7,76 (1H, t, J = 7,4 Hz), 7,95-8,22 (6H, m), 8,37 (1H, d, J = 8,3 Hz).Exemplo 534
[001787] Produção de acetato de 2-{[3-({[3-metóxi-1-metil-4-oxo-5-(2- oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina) cicloexil]amina}-2-oxoetilaDa mesma maneira que no Exemplo 504, o composto titular (223 mg, 70 %) foi obtido como um sólido branco a partir do composto do Exemplo 533 (285 mg, 0,546 mmol) e cloreto de acetoxiacetila (70,4 ml, 0,655 mmol).
[001788] RMN 1H (300 MHz, DMSO-d6) δ:1,06-1,48 (4H, m), 1,671,93 (3H, m), 2,00-2,12 (4H, m), 3,59-3,76 (1H, m), 3,78-3,91 (1H, m), 3,95 (2,7H, s), 4,03 (0,3H, s), 4,29 (2,7H, s), 4,35 (0,3H, s), 4,41 (1,8H, s), 4,45 (0,2H, s), 5,97 (2H, s), 7,26-7,40 (2H, m), 7,43-7,52 (1H, m), 7,63 (2H, t, J = 7,6 Hz), 7,72-7,80 (1H, m), 7,85-7,99 (2H, m), 8,11-8,23 (2H, m), 8,36 (1H, dd, J = 8,4, 1,2 Hz).Exemplo 535
[001789] Produção de N-{3-[(hidroxiacetil)amina]cicloexil}-3-metóxi- 1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamida Da mesma maneira que no Exemplo 508, o composto titular (173 mg, 93 %) foi obtido como um pó branco a partir do composto do Exemplo 534 (200 mg, 0,34 mmol), solução aquosa de hidróxido de sódio 8N (0,5 ml), THF (2,5 ml) e etanol (5 ml).
[001790] RMN 1H (300 MHz, DMSO-d6) δ:1,12-1,50 (4H, m), 1,661,82 (2H, m), 1,84-1,94 (1H, m), 1,98-2,10 (1H, m), 3,65-3,91 (4H, m), 3,95 (2,7H, s), 4,06 (0,3H, s), 4,30 (2,7H, s), 4,35 (0,3H, s), 5,39 (1H, d, J = 5,1 Hz), 5,98 (2H, s), 7,24-7,41 (2H, m), 7,46 (1H, d, J = 7,8 Hz), 7,54-7,69 (3H, m), 7,76 (1H, t, J =.3 Hz), 7,87 (1H, d, J = 7,9 Hz), 8,17 (2H, d, J = 7,7 Hz), 8,37 (1H, d, J = 8,3 Hz).Exemplo 536
[001791] Produção de trans-4-({[3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina) cicloexanocarboxilato de metilaDa mesma maneira que no Exemplo 25, o composto titular (535 mg, 79 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (500 mg, 1,28 mmol), trietilamina (230 ml, 1,66 mmol) e cloridrato de metil trans-4-aminacicloexanocarboxilato (321 mg, 1,66 mmol).
[001792] RMN 1H (300 MHz, DMSO-d6) δ: 1,27-1,60 (4H, m), 1,872,07 (4H, m), 2,25-2,41 (1H, m), 3,60 (3H, s), 3,69-3,86 (1H, m), 3,96 (3H, s), 4,30 (3H, s), 5,96 (2H, s), 7,25-7,41 (2H, m), 7,43-7,53 (1H, m), 7,63 (2H, t, J = 7,6 Hz), 7,71-7,88 (2H, m), 8,11-8,23 (2H, m), 8,36 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 537
[001793] Produção de ácido trans-4-({[3-metóxi-1-metil-4-oxo-5-(2- oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina) cicloexanocarboxílicoUma mistura do composto do Exemplo 536 (300 mg, 0,566 mmol), solução aquosa de hidróxido de sódio 8N (1 ml) e etanol (7 ml) foi agitada à temperatura ambiente durante 6 h. A mistura de reação foi acidificada com ácido clorídrico 6N (1,5 ml), e o sólido precipitado foi recolhido por meio de filtração. O sólido obtido foi lavado com água, e secado sob pressão reduzida dando o composto titular (225 mg, 81 %) como um pó branco.
[001794] RMN 1H (300 MHz, DMSO-d6) δ:1,25-1,57 (4H, m), 1,852,05 (4H, m), 2,10-2,26 (1H, m), 3,67-3,85 (1H, m), 3,98 (3H, s), 4,29 (3H, s), 5,97 (2H, s), 7,25-7,41 (2H, m), 7,42-7,52 (1H, m), 7,63 (2H, t, J = 7,6 Hz), 7,71-7,88 (2H, m), 8,12-8,24 (2H, m), 8,37 (1H, dd, J = 8,3, 1,1 Hz), 12,23 (1H, br s).Exemplo 538
[001795] Produção de N-{trans-4-[(2-hidroxietil)carbamoíla]cicloexil}- 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c] quinolina-2-carboxamidaA uma solução do composto do Exemplo 537 (215 mg, 0,417 mmol), 2-aminaetanol (32,5 ml, 0,542 mmol) e HOBt (84,6 mg, 0,626 mmol) em DMF (5 ml) adicionou-se WSCD (120 mg, 0,626 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com solução aquosa saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura saturada, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/metanol=10/0 - 8/2). Recristalização do sólido obtido de acetato de etila- THF deu o composto titular (131 mg, 56 %) como um pó branco.
[001796] RMN 1H (300 MHz, DMSO-d6) δ:1,22-1,58 (4H, m), 1,711,86 (2H, m), 1,90-2,03 (2H, m), 2,05-2,20 (1H, m), 3,03-3,18 (2H, m), 3,343,44 (2H, m), 3,65-3,84 (1H, m), 3,98 (3H, s), 4,30 (3H, s), 4,63 (1H, t, J = 5,6 Hz), 5,97 (2H, s), 7,25-7,41 (2H, m), 7,47 (1H, t, J = 7,7 Hz), 7,58-7,68 (2H, m), 7,70-7,88 (3H, m), 8,17 (2H, d, J = 7,6 Hz), 8,37 (1H, d, J = 8,1 Hz). Exemplo 539
[001797] Produção de acetato de 2-[3-({[3-metóxi-1-metil-4-oxo-5-(2- oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina) piperidin-1-il]-2-oxoetilaDa mesma maneira que no Exemplo 25, o composto titular(284 mg, 39 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 28 (500 mg, 1,3 mmol), 3-aminapiperidina-1- carboxilato de t-butila (257 mg, 1,3 mmol), HOBt (203 mg, 1,5 mmol), WSCD (294 mg, 1,5 mmol), DMF (15 ml), solução 4N cloreto de hidrogênio acetato de etila (4,0 ml), THF (4,0 ml), metanol (4,0 ml), cloreto de acetoxiacetila (0,098 ml, 0,91 mmol), trietilamina (0,28 ml, 2,0 mmol) e THF (16 ml).
[001798] RMN 1H (300 MHz, CDCl3) δ:1,64-1,88 (3H, m), 1,93-2,09 (1H, m), 2,16 (3H, s), 3,24-3,59 (2H, m), 3,67-3,82 (2H, m), 4,04-4,24 (4H, m), 4,47 (3H, s), 4,67-4,88 (2H, m), 5,79-5,97 (2H, m), 7,05 (1H, d, J = 7,9 Hz), 7,20-7,34 (1H, m), 7,37-7,46 (1H, m), 7,55 (2H, t, J = 7,6 Hz), 7,61-7,71 (1H, m), 7,82 (1H, d, J = 7,0 Hz), 8,07-8,16 (2H, m), 8,26 (1H, dd, J = 8,2, 1,4 Hz).Exemplo 540
[001799] Produção de 4-[({[3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina)metil] piperidina-1-carboxilato de t-butilaDa mesma maneira que no Exemplo 25, o composto titular (521 mg, 69 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 28 (500 mg, 1,3 mmol), 4-(aminametil)piperidina-1- carboxilato de t-butila (302 mg, 1,4 mmol), HOBt (208 mg, 1,5 mmol), WSC (294 mg, 1,5 mmol) e DMF (15 ml).
[001800] RMN 1H (300 MHz, CDCl3) δ:1,14-1,33 (2H, m), 1,41-1,51 (9H, m), 1,70-1,85 (3H, m), 2,63-2,80 (2H, m), 3,37 (2H, t, J = 6,1 Hz), 4,034,25 (5H, m), 4,47 (3H, s), 5,89 (2H, s), 7,05 (1H, d, J = 8,5 Hz), 7,21-7,31 (1H, m), 7,36-7,46 (1H, m), 7,50-7,60 (2H, m), 7,62-7,70 (1H, m), 7,76 (1H, t, J = 5,9 Hz), 8,05-8,16 (2H, m), 8,26 (1H, dd, J = 8,3, 1,3 Hz).Exemplo 541
[001801] Produção de 4-[{[3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}(metil)amina] piperidina-1-carboxilato de t-butilaDa mesma maneira que no Exemplo 25, o composto titular (565 mg, 75 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 28 (500 mg, 1,3 mmol), 4-(metilamina)piperidina-1- carboxilato de t-butila (274 mg, 1,3 mmol), HOBt (208 mg, 1,5 mmol), WSCD (294 mg, 1,5 mmol) e DMF (15 ml).
[001802] RMN 1H (300 MHz, CDCl3) δ:1,42-1,52 (9 H, m), 1,65-1,86 (4H, m), 2,56-2,97 (2H, m), 3,03 (3H, s), 3,97-4,20 (7H, m), 4,22-4,37 (1H, m), 4,61-4,81 (1H, m), 5,89 (2H, s), 7,05 (1H, d, J = 8,5 Hz), 7,19-7,30 (1H, m), 7,33-7,43 (1H, m), 7,49-7,59 (2H, m), 7,60-7,70 (1H, m), 8,05-8,15 (2H, m), 8,18 (1H, d, J = 7,4 Hz).Exemplo 542
[001803] Produção de cloridrato de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-N-(piperidin-4-ilmetil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaUma solução mista do composto do Exemplo 540 (500 mg, 0,85 mmol) e solução 4N cloreto de hidrogênio acetato de etila (4,0 ml) em THF (4,0 ml)-metanol (4,0 ml) foi agitada à temperatura ambiente durante 2 h. Adicionou-se solução 4N cloreto de hidrogênio acetato de etila (4,0 ml) e metanol (8,0 ml), e a mistura foi agitada à temperatura ambiente durante 1,5 h. A mistura de reação foi concentrada sob pressão reduzida, e recristalizada de metanol-éter de dietila dando o composto titular (356 mg, 80 %) como um sólido amarelo claro.
[001804] RMN 1H (300 MHz, DMSO-d6) δ:1,29-1,48 (2H, m), 1,75- 1,95 (3H, m), 2,78-2,94 (2H, m), 3,18-3,38 (4H, m), 4,00 (3H, s), 4,31 (3H, s), 5,98 (2H, s), 7,27-7,42 (2H, m), 7,44-7,53 (1H, m), 7,59-7,69 (2H, m), 7,72-7,81 (1H, m), 8,07-8,22 (3H, m), 8,38 (1H, dd, J = 8,4, 1,2 Hz), 8,51 (2H, br s).Exemplo 543
[001805] Produção de N-[1-(hidroxiacetil)piperidin-3-il]-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 511, o composto titular (69 mg, 43 %) foi obtido como um sólido branco a partir do composto do Exemplo 539 (174 mg, 0,30 mmol), solução aquosa de hidróxido de sódio 8N (1,6 ml), THF (3,2 ml) e etanol (11 ml).
[001806] RMN 1H (300 MHz, DMSO-d6) δ:1,44-1,81 (3H, m), 1,841,96 (1H, m), 3,29-3,61 (3H, m), 3,80-3,90 (1H, m), 3,91-4,02 (4H, m), 4,044,17 (2H, m), 4,35 (3H, s), 4,54 (1H, t, J = 5,4 Hz), 5,97 (2H, s), 7,27-7,42 (2H, m), 7,44-7,53 (1H, m), 7,59-7,69 (2H, m), 7,71-7,81 (1H, m), 7,89-8,01 (1H, m), 8,12-8,21 (2H, m), 8,38 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 544
[001807] Produção de acetato de 2-{4-[({[3-metóxi-1-metil-4-oxo-5-(2- oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina) metil]piperidin-1-il}-2-oxoetilaA uma solução do composto do Exemplo 542 (400 mg, 0,76 mmol) e trietilamina (0,29 ml, 2,1 mmol) em THF (17 ml) adicionou-se cloreto de acetoxiacetila (0,10 ml, 0,95 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 4 h. A mistura de reação foi diluída com solução aquosa saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura saturada, secado sobre sulfato de magnésio, e filtrado através gel de aminassílica. O filtrado foi concentrado, e o resíduo foi recristalizado de etanol-hexano dando o composto titular (321 mg, 71 %) como um sólido branco.
[001808] RMN 1H (300 MHz, CDCl3) δ:1,16-1,37 (2H, m), 1,78-1,99 (3H, m), 2,18 (3H, s), 2,58-2,71 (1H, m), 2,99-3,15 (1H, m), 3,31-3,43 (2H, m), 3,63-3,76 (1H, m), 4,17 (3H, s), 4,47 (3H, s), 4,57-4,66 (1H, m), 4,73 (2H, s), 5,89 (2H, s), 7,01-7,08 (1H, m), 7,20-7,33 (1H, m), 7,37-7,47 (1H, m), 7,50-7,60 (2H, m), 7,62-7,71 (1H, m), 7,79 (1H, t, J = 5,9 Hz), 8,07-8,17 (2H, m), 8,26 (1H, dd, J = 8,3, 1,3 Hz).Exemplo 545
[001809] Produção de acetato de 2-{4-[{[3-metóxi-1-metil-4-oxo-5-(2- oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}(metil) amina]piperidin-1-il}-2-oxoetilaDa mesma maneira que no Exemplo 123, o composto titular (226 mg, 40 %) foi obtido como um sólido branco a partir do composto do Exemplo 541 (565 mg, 0,96 mmol), solução 4N cloreto de hidrogênio acetato de etila (4,0 ml), THF (4,0 ml), metanol (4,0 ml), cloreto de acetoxiacetila (0,077 ml, 0,71 mmol), trietilamina (0,22 ml, 1,6 mmol) e THF (13 ml).
[001810] RMN 1H (300 MHz, CDCl3) δ:1,70-1,97 (4H, m), 2,15-2,24 (3H, m), 2,50-2,83 (1H, m), 3,03 (3H, s), 3,10-3,33 (1H, m), 3,63-3,86 (1H, m), 4,02 (3H, s), 4,04-4,11 (3H, m), 4,60-4,87 (4H, m), 5,89 (2H, s), 7,027,10 (1H, m), 7,17-7,32 (1H, m), 7,35-7,44 (1H, m), 7,47-7,60 (2H, m), 7,617,71 (1H, m), 8,07-8,15 (2H, m), 8,19 (1H, dd, J = 8,1, 1,3 Hz).Exemplo 546
[001811] Produção de N-{[1-(hidroxiacetil)piperidin-4-il]metil}-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]Da mesma maneira que no Exemplo 511, o composto titular(77 mg, 41 %) foi obtido como um sólido branco a partir do composto do Exemplo 544 (200 mg, 0,34 mmol), solução aquosa de hidróxido de sódio 8N (1,8 ml), THF (3,6 ml) e etanol (13 ml).
[001812] RMN 1H (300 MHz, DMSO-d6) δ:0,99-1,26 (2H, m), 1,651,93 (3H, m), 2,57-2,71 (1H, m), 2,87-3,01 (1H, m), 3,18-3,27 (2H, m), 3,653,75 (1H, m), 3,98 (3H, s), 4,07 (2H, t, J = 5,4 Hz), 4,27-4,40 (4H, m), 4,414,50 (1H, m), 5,97 (2H, s), 7,25-7,42 (2H, m), 7,44-7,53 (1H, m), 7,59-7,68 (2H, m), 7,71-7,81 (1H, m), 8,07 (1H, t, J = 6,0 Hz), 8,13-8,21 (2H, m), 8,37 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 547
[001813] Produção de N-[1-(hidroxiacetil)piperidin-4-il]-3-metóxi-N,1- dimetil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 511, o composto titular (117 mg, 62 %) foi obtido como um sólido branco a partir do composto do Exemplo 545 (205 mg, 0,35 mmol), solução aquosa de hidróxido de sódio 8N (1,8 ml), THF (3,6 ml) e etanol (13 ml).
[001814] RMN 1H (300 MHz, CDCl3) δ:1,65-2,01 (4H, m), 2,78-2,92 (1H, m), 2,99-3,09 (3H, m), 3,12-3,27 (1H, m), 3,48-3,69 (2H, m), 3,99-4,04 (3H, m), 4,04-4,11 (3H, m), 4,14-4,30 (2H, m), 4,61-4,88 (2H, m), 5,89 (2H, s), 7,06 (1H, d, J = 8,7 Hz), 7,22-7,32 (1H, m), 7,35-7,44 (1H, m), 7,54 (2H, t, J = 7,6 Hz), 7,62-7,72 (1H, m), 8,11 (2H, d, J = 7,6 Hz), 8,19 (1H, dd, J = 8,3, 1,3 Hz).Exemplo 548
[001815] Produção de N-{trans-2-[(hidroxiacetil)amina]cicloexil}-3- metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 508, o composto titular (88 mg, 58 %) foi obtido como cristais brancos a partir do composto do Exemplo 530 (150 mg, 0,26 mmol).
[001816] RMN 1H (300 MHz, DMSO-d6) δ:1,20-1,50 (6H, m), 1,70 (2H, br s), 1,87 (1H, d, J = 11,1 Hz), 2,05 (1H, d, J = 9,6 Hz), 3,72-3,94 (7H, m), 4,31 (3H, s), 5,48 (1H, t, J = 5,7 Hz), 5,97 (2H, s), 7,28-7,39 (2H, m), 7,47 (1H, t, J = 7,8 Hz), 7,61-7,67 (3H, m), 7,76 (1H, t, J = 7,5 Hz), 7,83 (1H, d, J = 7,8 Hz), 8,15-8,18 (2H, m), 8,137 (1H, d, J = 7,2 Hz).Exemplo 549
[001817] Produção de N-{2-[1-(hidroxiacetil)pirrolidin-2-il]etil}-3- metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 508, o composto titular (70 mg, 51 %) foi obtido como cristais brancos a partir do composto do Exemplo 528 (150 mg, 0,25 mmol).
[001818] RMN 1H (300 MHz, DMSO-d6) δ:1,50-2,00 (7H, m), 3,00- 3,15 (1H, m), 3,30-3,45 (1H, m), 3,55-3,70 (1H, m), 4,02-4,25 (7H, m), 4,52 (1H, t, J = 5,3 Hz), 6,00 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,4 Hz), 7,56-7,67 (2H, m), 7,77 (1H, t, J = 7,2 Hz), 8,05 (1H, d, J = 7,8 Hz), 8,18 (2H, d, J = 7,8 Hz), 8,46 (1H, t, J = 5,3 Hz).Exemplo 550
[001819] Produção de N-{[1-(hidroxiacetil)pirrolidin-3-il]metil}-3- metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 508, o composto titular(31 mg, 29 %) foi obtido como cristais brancos a partir do composto do Exemplo 529 (120 mg, 0,20 mmol).
[001820] RMN 1H (300 MHz, DMSO-d6) δ:1,58-1,76 (1H, m), 1,902,10 (1H, m), 2,50-2,65 (1H, m), 3,11-3,17 (1H, m), 3,30-3,65 (5H, m), 3,99 (2H, d, J = 4,2 Hz), 4,03 (3H, d, J = 0,9 Hz), 4,46 (1H, t, J = 4,8 Hz), 6,00 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49 (1H, d, J = 8,4 Hz), 7,56-7,67 (3H, m), 7,77 (1H, t, J = 7,5 Hz), 8,05 (1H, d, J = 7,5 Hz), 8,18 (3H, d, J = 7,5 Hz).Exemplo 551
[001821] Produção de N-[1-(hidroxiacetil)azetidin-3-il]-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 508, o composto titular (58 mg, 64 %) foi obtido como cristais brancos a partir do composto do Exemplo 531 (100 mg, 0,18 mmol).
[001822] RMN 1H (300 MHz, DMSO-d6) δ:3,28-3,44 (2H, m), 3,843,86 (5H, tm), 4,22 (1H, t, J = 6,3 Hz), 4,36 (3H, s), 4,39-4,43 (2H, m), 5,55 (1H, t, J = 5,7 Hz), 5,96 (2H, s), 7,30-7,40 (2H, m), 7,48 (1H, t, J = 7,5 Hz), 7,63 (2H, t, J = 7,5 Hz), 7,76 (1H, t, J = 7,5 Hz), 7,90 (1H, t, J = 6,2 Hz), 8,16-8,19 (2H, m), 8,40 (1H, dd, J = 8,1, 0,9 Hz).Exemplo 552
[001823] Produção de 2-(1,4-dioxa-8-azaspiro[4,5]dec-8-ilcarbonil)-3- metóxi-1-metil-5-(2-oxo-2-feniletil)-1,5-diidro-4H-pirrol[3,2-c]quinolin-4- onaDa mesma maneira que no Exemplo 25, o composto titular (279 mg, 60 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 28 (350 mg, 0,90 mmol), 1,4-dioxa-8- azaspiro[4,5]decano (154 mg, 1,1 mmol), HOBt (146 mg, 1,1 mmol), WSCD (206 mg, 1,1 mmol) e DMF (10 ml).
[001824] RMN 1H (300 MHz, CDCl3) δ:1,72-1,88 (4H, m), 3,64-3,77 (2H, m), 3,82-3,96 (2H, m), 3,98-4,02 (4H, m), 4,03 (3H, s), 4,09 (3H, s), 5,89 (2H, br s), 7,01-7,10 (1H, m), 7,19-7,30 (1H, m), 7,34-7,42 (1H, m), 7,49-7,58 (2H, m), 7,61-7,69 (1H, m), 8,06-8,14 (2H, m), 8,19 (1H, dd, J = 8,3, 1,3 Hz).Exemplo 553
[001825] Produção de cloridrato de 3-metóxi-1-metil-5-(2-oxo-2- feniletil)-2-(piperazin-1-ilcarbonil)-1,5-diidro-4H-pirrol[3,2-c]quinolin-4-onaDa mesma maneira que no Exemplo 542, o composto titular (478 mg, 95 %) foi obtido como um sólido amarelo claro a partir do composto do Exemplo 680 (571 mg, 1,0 mmol), solução 4N ácido clorídrico acetato de etila (11 ml), acetato de etila (8,0 ml) e metanol (8,0 ml).
[001826] RMN 1H (300 MHz, DMSO-d6) δ:3,07-3,27 (4H, m), 3,653,78 (2H, m), 3,81-3,96 (5H, m), 4,05 (3H, s), 5,98 (2H, s), 7,24-7,52 (3H, m), 7,57-7,68 (2H, m), 7,71-7,81 (1H, m), 8,08-8,24 (2H, m), 8,35 (1H, dd, J = 8,2, 1,0 Hz), 9,20 (2H, br s).Exemplo 554
[001827] Produção de acetato de 2-(4-{[3-metóxi-1-metil-4-oxo-5-(2- oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}piperazin-1- il)-2-oxoetila Da mesma maneira que no Exemplo 544, o composto titular (34 mg, 10 %) foi obtido como um sólido branco a partir do composto do Exemplo 553 (300 mg, 0,61 mmol), cloreto de acetoxiacetila (0,081 ml, 0,76 mmol), trietilamina (0,23 ml, 1,7 mmol) e THF (13 ml).
[001828] RMN 1H (300 MHz, DMSO-d6) δ:2,09 (3H, s), 3,43-3,79 (8H, m), 3,91 (3H, s), 4,03 (3H, s), 4,76-4,88 (2H, m), 5,98 (2H, s), 7,25-7,51 (3H, m), 7,59-7,68 (2H, m), 7,71-7,80 (1H, m), 8,13-8,22 (2H, m), 8,30-8,38 (1H, m).Exemplo 555
[001829] Produção de cloridrato de 8-fluoro-3-metóxi-4-oxo-5-(2-oxo- 2-feniletil)-N-piperidin-4-il-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 542, o composto titular (335 mg, 83 %) foi obtido como um sólido branco a partir do composto do Exemplo 673 (452 mg, 0,76 mmol), solução 4N cloreto de hidrogênio acetato de etila (6,0 ml), THF (4,0 ml) e metanol (4,0 ml).
[001830] RMN 1H (300 MHz, DMSO-d6) δ:1,70-1,91 (2H, m), 1,952,12 (2H, m), 2,93-3,13 (2H, m), 3,19-3,52 (2H, m), 3,95-4,22 (4H, m), 6,00 (2H, s), 7,41-7,52 (1H, m), 7,53-7,71 (3H, m), 7,72-7,84 (1H, m), 7,86-8,03(2H, m), 8,11-8,25 (2H, m), 8,63 (2H, br s).Exemplo 556
[001831] Produção de acetato de 2-[4-({[8-fluoro-3-metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}amina)piperidin- 1-il]-2-oxoetilaDa mesma maneira que no Exemplo 544, o composto titular(161 mg, 80 %) foi obtido como um sólido branco a partir do composto do Exemplo 555 (180 mg, 0,34 mmol), cloreto de acetoxiacetila (0,046 ml, 0,42 mmol), trietilamina (0,13 ml, 0,93 mmol) e THF (7,5 ml).
[001832] RMN 1H (300 MHz, CDCl3) δ:1,45-1,64 (2H, m), 2,01-2,26 (5H, m), 2,89-3,05 (1H, m), 3,15-3,34 (1H, m), 3,60-3,77 (1H, m), 4,15 (3H, s), 4,20-4,34 (1H, m), 4,41-4,54 (1H, m), 4,67-4,84 (2H, m), 5,85 (2H, s), 6,95-7,04 (1H, m), 7,16-7,24 (1H, m), 7,51-7,62 (4H, m), 7,64-7,74 (1H, m), 8,06-8,14 (2H, m).Exemplo 557
[001833] Produção de acetato de 2-[4-({[5-(cicloexilmetil)-3-metóxi-1- metil-4-oxo-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina) piperidin-1-il]-2-oxoetilaUma mistura do composto do Exemplo 672 (110 mg, 0,24 mmol), bromometilcicloexano (108 mg, 0,60 mmol), carbonato de potássio (72 mg, 0,60 mmol) e DMF (3 ml) foi agitada a 80°C durante 24 h. Após resfriar à temperatura ambiente, a mistura de reação foi diluída com solução aquosa saturada de hidrogenocarbonato de sódio e extraída com acetato de etila. O extrato foi lavado com salmoura saturada, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em sílica-gel (eluado: acetato de etila) dando o composto titular (34 mg, 16 %) como um óleo incolor.
[001834] RMN 1H (300 MHz, DMSO-d6) δ:1,05-1,20 (5H, m), 1,352,00 (9H, m), 2,09 (3H, s), 2,90 (1H, t, J = 11,4 Hz), 3,19 (1H, t, J = 12,2 Hz), 3,70 (1H, d, J = 13,5 Hz), 3,97 (3H, s), 4,10-4,40 (8H, m), 4,80 (2H, d, J = 2,1 Hz), 7,30 (1H, t, J = 7,5 Hz), 7,54-7,62 (2H, m), 7,96 (1H, d, J = 7,8 Hz), 8, 32 (1H, d, J = 7,8 Hz).Exemplo 558
[001835] Produção de 4-({[3-metóxi-5-(4-metoxibenzil)-1-metil-4-oxo- 4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina)piperidina-1- carboxilato de t-butilaDa mesma maneira que no Exemplo 25, o composto titular (6,09 g, 74 %) foi obtido como cristais brancos a partir do composto do Exemplo de Referência 107 (5,65 g, 14,4 mmol) e 1-Boc-4-aminapiperidina (5,77 g, 28,80 mmol).
[001836] RMN 1H (300 MHz, DMSO-d6) δ:1,32-1,53 (11H, m), 1,85 (2H, d, J = 10,2 Hz), 2,85-3,10 (2H, m), 3,69 (3H, s), 3,88 (2H, d, J = 13,2 Hz), 3,95-4,05 (4H, m), 4,27 (3H, s), 5,52 (2H, br s), 6,85 (2H, d, J = 8,7 Hz), 7,14 (2H, d, J = 8,7 Hz), 7,27 (1H, t, J = 7,1 Hz), 7,41-7,48 (2H, m), 7,96 (1H, d, J = 7,8 Hz), 8,32 (1H, d, J = 8,1 Hz).Exemplo 559
[001837] Produção de acetato de 2-[4-({[3-metóxi-5-(4-metoxibenzil)-1- metil-4-oxo-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina) piperidin-1-il]-2-oxoetilaDa mesma maneira que no Exemplo 123, o composto titular (360 mg, 73 %) foi obtido como um sólido branco a partir do composto do Exemplo 681 (440 mg, 0,87 mmol).
[001838] RMN 1H (300 MHz, DMSO-d6) δ:1,35-1,65 (2H, m), 1,721,95 (2H, m), 2,09 (3H, s), 2,91 (1H, t, J = 11,7 Hz), 3,20 (1H, t, J = 12,0 Hz), 3,58-3,75 (4H, m), 4,00-4,20 (5H, m), 4,27 (3H, s), 4,80 (2H, d, J = 2,4 Hz), 5,40-5,60 (2H, br), 6,86 (2H, d, J = 8,7 Hz), 7,14 (2H, d, J = 8,7 Hz), 7,27 (1H, td, J = 7,1, 2,1 Hz), 7,41-7,49 (2H, m), 8,00 (1H, d, J = 8,1 Hz), 8,33 (1H, d, J = 8,1 Hz).Exemplo 560
[001839] Produção de N-[1-(3-hidróxi-3-metilbutanoil)piperidin-4-il]-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 518, o composto titular (109 mg, 60 %) foi obtido como um pó branco a partir do composto do Exemplo 77 (150 mg, 0,317 mmol) e ácido 3-hidróxi-3-metilbutanóico (45,0 mg, 0,381 mmol).
[001840] RMN 1H (300 MHz, DMSO-d6) δ:1,18 (6H, s), 1,33-1,63 (2H, m), 1,79-1,97 (2H, m), 2,43-2,52 (2H, m), 2,81-2,96 (1H, m), 3,14-3,29 (1H, m), 3,90-4,00 (4H, m), 4,02-4,16 (1H, m), 4,22-4,36 (4H, m), 4,89 (1H, s), 5,97 (2H, s), 7,26-7,41 (2H, m), 7,48 (1H, t, J = 7,6 Hz), 7,63 (2H, t, J = 7,5 Hz), 7,72-7,81 (1H, m), 7,95 (1H, d, J = 7,9 Hz), 8,17 (2H, d, J = 7,7 Hz), 8,37 (1H, d, J = 8,3 Hz).Exemplo 561
[001841] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N- (1-propanoilpiperidin-4-il)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 123, o composto titular (90,2, 81 %) foi obtido como um pó branco a partir do composto do Exemplo 77 (100 mg, 0,212 mmol) e cloreto de propionila (20,2 ml, 0,233 mmol).
[001842] RMN 1H (300 MHz, DMSO-d6) δ:1,00 (3H, t, J = 7,5 Hz), 1,31-1,61 (2H, m), 1,77-1,96 (2H, m), 2,34 (2H, q, J = 7,4 Hz), 2,77-2,92 (1H, m), 3,10-3,25 (1H, m), 3,76-3,88 (1H, m), 3,97 (3H, s), 4,01-4,14 (1H, m), 4,19-4,29 (1H, m), 4,31 (3H, s), 5,97 (2H, s), 7,26-7,41 (2H, m), 7,437,52 (1H, m), 7,63 (2H, t, J = 7,6 Hz), 7,71-7,81 (1H, m), 7,94 (1H, d, J = 7,7 Hz), 8,12-8,22 (2H, m), 8,37 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 562
[001843] Produção de 8-fluoro-N-[1-(hidroxiacetil)piperidin-4-il]-3- metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 511, o composto titular (59 mg, 39 %) foi obtido como um sólido amarelo claro a partir do composto do Exemplo 556 (164 mg, 0,28 mmol).
[001844] RMN 1H (300 MHz, CDCl3) δ:1,42-1,63 (2H, m), 2,08-2,25 (2H, m), 2,97-3,26 (2H, m), 3,47-3,59 (1H, m), 3,62 (1H, t, J = 4,2 Hz), 4,14 (3H, s), 4,20 (2H, d, J = 4,0 Hz), 4,23-4,34 (1H, m), 4,45-4,58 (1H, m), 5,85 (2H, s), 6,94-7,04 (1H, m), 7,15-7,25 (1H, m), 7,50-7,63 (4H, m), 7,64-7,77 (1H, m), 8,04-8,15 (2H, m).Exemplo 563
[001845] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N- (1-piridin-4-ilpiperidin-4-il)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaA uma solução do composto do Exemplo de Referência 28 (200 mg, 0,51 mmol), cloridrato de 1-piridin-4-ilpiperidin-4-amina (128 mg, 0,51 mmol) e HOBt (83 mg, 0,61 mmol) em DMF (5,0 ml) adicionou-se WSCD (118 mg, 0,61 mmol) e trietilamina (0,23 ml, 1,6 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 67 h. A mistura de reação foi diluída com salmoura, e extraída 4 vezes com acetato de etila. Os extratos foram combinados e extraídos sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=40/60 - 100/0) e recristalizado de THF dando o composto titular (121 mg, 43 %) como um sólido púrpura claro.
[001846] RMN 1H (300 MHz, DMSO-d6) δ:1,52-1,68 (2H, m), 1,871,98 (2H, m), 3,08 (2H, m), 3,89 (2H, m), 3,95 (3H, s), 4,04-4,17 (1H, m), 4,31 (3H, s), 5,97 (2H, s), 6,85 (2H, d, J = 6,4 Hz), 7,26-7,41 (2H, m), 7,43- 7,53 (1H, m), 7,63 (2H, m), 7,71-7,80 (1H, m), 7,98 (1H, d, J = 7,7 Hz), 8,108,21 (4H, m), 8,37 (1H, d, J = 7,4 Hz).Exemplo 564
[001847] Produção de N-[1-(hidroxiacetil)piperidin-4-il]-3-metóxi-5-(3-metoxibenzil)-1-metil-4-oxo-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaUma mistura do composto do Exemplo 672 (110 mg, 0,24 mmol), cloreto de 3-metoxibenzila (150 mg, 0,96mmol), carbonato de potássio (55 mg, 0,40 mmol) e DMF (5 ml) foi agitada a 80°C durante 5 h. Após resfriar à temperatura ambiente, adicionou-se solução aquosa 2N de hidróxido de sódio (1 ml), e a mistura foi agitada à temperatura ambiente durante 1 h. A mistura de reação foi diluída com solução aquosa saturada de hidrogenocarbonato de sódio e extraída com acetato de etila. O extrato foi lavado com salmoura saturada, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em sílica-gel (eluado:etila acetato - acetato de etila/metanol=10/1) e precipitado de acetato de etila-hexano dando o composto titular (14 mg, 10 %) como um pó branco.
[001848] RMN 1H (300 MHz, DMSO-d6) δ:1,40-1,65 (2H, m), 1,90 (2H, d, J = 10,2 Hz), 2,93 (1H, t, J = 10,2 Hz), 3,19 (1H, t, J = 14,3 Hz), 3,603,70 (4H, m), 4,00-4,04 (4H, m), 4,04-4,10 (2H, m), 4,30-4,36 (4H, m), 4,52 (1H, t, J = 5,4 Hz), 5,58 (2H, br s), 6,69 (1H, d, J = 8,4 Hz), 6,79 (2H, d, J = 6,3 Hz), 7,20 (1H, t, J = 8,4 Hz), 7,28 (1H, t, J = 6,3 Hz), 7,34-7,48 (2H, m), 7,89 (1H, d, J = 8,1 Hz), 8, 34 (1H, d, J = 8,4 Hz).Exemplo 565
[001849] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N-(2,2,6,6-tetrametilpiperidin-4-il)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (410 mg, 76 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 28 (400 mg, 1,02 mmol) e 4-amina-2,2,6,6- tetrametilpiperidina (320 mg, 2,04 mmol).
[001850] RMN 1H (300 MHz, DMSO-d6) δ: 0,86-1,24 (14H, m), 1,78 (2H, dd, J = 12,6, 2,4 Hz), 3,96 (3H, s), 4,28-4,31 (4H, m), 5,97 (2H, s), 7,297,47 (3H, m), 7,63 (2H, t, J = 7,5 Hz), 7,76 (2H, t, J = 6,9 Hz), 8,17 (2H, d, J = 7,5 Hz), 8,37 (1H, d, J = 8,4 Hz).Exemplo 566
[001851] Produção de 3-metóxi-1-metil-5-(2-oxo-2-feniletil)-2-[(4- oxopiperidin-1-il)carbonil]-1,5-diidro-4H-pirrol[3,2-c]quinolin-4-onaUma solução do composto do Exemplo 552 (285 mg, 0,55 mmol) e ácido clorídrico 5N (3,0 ml) em THF (6,0 ml) foi agitada à temperatura ambiente durante 2 h. Adicionou-se ácido clorídrico 5N (1,5 ml), e a mistura foi agitada à temperatura ambiente durante 2 h. Adicionou-se ácido clorídrico 5N (1,5 ml), e a mistura foi agitada à temperatura ambiente durante 3,5 h e concentrada sob pressão reduzida. O resíduo foi basificado com solução saturada de hidrogenocarbonato de sódio e extraído duas vezes com acetato de etila. Os extratos foram combinados, lavados com salmoura, e concentrados sob pressão reduzida. O resíduo foi lavado com água, e recristalizado de metanol-éter de dietila dando o composto titular (123 mg, 47 %) como um sólido branco.
[001852] RMN 1H (300 MHz, CDCl3) δ:1,78-1,93 (3H, m), 1,95-1,99 (1H, m), 3,58-3,73 (2H, m), 3,79-3,94 (2H, m), 4,03 (3H, s), 4,07-4,11 (3H, m), 5,90 (2H, s), 7,02-7,11 (1H, m), 7,19-7,30 (1H, m), 7,34-7,43 (1H, m), 7,49-7,58 (2H, m), 7,61-7,70 (1H, m), 8,07-8,14 (2H, m), 8,16-8,26 (1H, m). Exemplo 567
[001853] Produção de N-[1-(N,N-dimetilglicil)piperidin-4-il]-3-metóxi- 1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (125 mg, 57 %) foi obtido como um sólido púrpura claro a partir do composto do Exemplo 77 (200 mg, 0,39 mmol) e N,N-dimetilglicina (49 mg, 0,47 mmol).
[001854] RMN 1H (300 MHz, CDCl3) δ:1,40-1,64 (2H, m), 1,99-2,17 (2H, m), 2,31 (6H, s), 2,90-3,05 (1H, m), 3,08-3,21 (2H, m), 3,22-3,36 (1H, m), 3,99-4,11 (1H, m), 4,14 (3H, s), 4,18-4,29 (1H, m), 4,36-4,45 (1H, m), 4,47 (3H, s), 5,88 (2H, d, J = 4,2 Hz), 7,05 (1H, d, J = 7,7 Hz), 7,20-7,32 (1H, m), 7,37-7,46 (1H, m), 7,50-7,59 (2H, m), 7,62-7,73 (2H, m), 8,06-8,16 (2H, m), 8,26 (1H, dd, J = 8,3, 1,3 Hz).Exemplo 568
[001855] Produção de N-[1-(3-etoxipropanoil)piperidin-4-il]-3-metóxi- 1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (159 mg, 70 %) foi obtido como um sólido púrpura claro a partir do composto do Exemplo 77 (200 mg, 0,39 mmol) e ácido 3-etoxipropanóico (56 mg, 0,47 mmol).
[001856] RMN 1H (300 MHz, DMSO-d6) δ:1,09 (3H, t, J = 7,0 Hz), 1,36-1,60 (2H, m), 1,80-1,96 (2H, m), 2,54-2,63 (2H, m), 2,78-2,92 (1H, m), 3,13-3,26 (1H, m), 3,42 (2H, q, J = 6,9 Hz), 3,59 (2H, t, J = 6,7 Hz), 3,81-3,91 (1H, m), 3,96 (3H, s), 4,02-4,14 (1H, m), 4,18-4,27 (1H, m), 4,31 (3H, s), 5,97 (2H, s), 7,26-7,41 (2H, m), 7,44-7,53 (1H, m), 7,58-7,68 (2H, m), 7,727,80 (1H, m), 7,94 (1H, d, J = 7,9 Hz), 8,12-8,21 (2H, m), 8,37 (1H, dd, J = 8,3, 1,3 Hz).Exemplo 569
[001857] Produção de N-[1-(hidroxiacetil)piperidin-4-il]-3-metóxi-5-(2- metoxibenzil)-1-metil-4-oxo-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaA uma solução do composto do Exemplo 570 (40 mg, 0,07 mmol) em THF (1 ml)-metanol (1 ml) adicionou-se solução de hidróxido de sódio 2N (1 ml), e a mistura foi agitada à temperatura ambiente durante 1 h. A mistura de reação foi diluída com água, e extraída com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. Recristalização de acetato de etila-hexano deu o composto titular (30 mg, 80 %) como cristais brancos.
[001858] RMN 1H (300 MHz, DMSO-d6) δ:1,50-1,60 (2H, m), 1,90 (2H, d, J = 10,2 Hz), 2,93 (1H, t, J = 12,5 Hz), 3,15 (1H, t, J = 12,5 Hz), 3,67 (1H, d, J = 13,2 Hz), 3,95 (3H, s), 4,00 (3H, s), 4,05-4,20 (3H, m), 4,20-4,30 (4H, m), 4,51 (1H, t, J = 5,4 Hz), 5,47 (2H, s), 6,50 (1H, d, J = 7,5 Hz), 6,75 (1H, t, J = 7,5 Hz), 7,09 (1H, d, J = 8,4 Hz), 7,21-7,31 (3H, m), 7,44 (1H, t, J = 7,8 Hz), 7,97 (1H, d, J = 7,8 Hz), 8, 36 (1H, d, J = 8,1 Hz).Exemplo 570
[001859] Produção de acetato de 2-[4-({[3-metóxi-5-(2-metoxibenzil)-1- metil-4-oxo-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina) piperidin-1-il]-2-oxoetila Da mesma maneira que no Exemplo 557, um sólido amorfo (90 mg) foi obtido a partir do composto do Exemplo 672 (120 mg, 0,24 mmol), cloreto de 2-metoxibenzila (solução em diclorometano a 50 %; 0,1 ml, 0,79 mmol) e carbonato de potássio (110 mg, 0,79 mmol). Recristalização de acetato de etil-éter de diisopropila deu o composto titular (44 mg, 29 %) como cristais brancos.
[001860] RMN 1H (300 MHz, DMSO-d6) δ:1,50-1,70 (2H, m), 2,072,28 (5H, m), 3,04 (1H, t, J = 11,1 Hz), 3,29 (1H, t, J = 11,1 Hz), 3,70 (1H, d, J = 14,4 Hz), 3,99 (3H, s), 4,21-4,28 (4H, m), 4,40-4,56 (4H, m), 4,78 (2H, s), 5,62 (2H, br s), 6,77 (2H, d, J = 4,2 Hz), 6,95 (1H, d, J = 10,8 Hz), 7,19-7,42 (4H, m), 7,77 (1H, d, J = 7,8 Hz), 8, 25 (1H, dd, J = 8,4, 1,2 Hz).Exemplo 571
[001861] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N- (tetraidro-2H-tiopiran-4-il)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamida Da mesma maneira que no Exemplo 25, o composto titular (2,51 g, 90 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 28 (2,22 g, 5,69 mmol) e tetraidrotiopiran-4-ilamina (1,0 g, 8,53 mmol).
[001862] RMN 1H (300 MHz, DMSO-d6) δ:1,63-1,77 (2H, m), 1,992,17 (2H, m), 2,66-2,78 (4H, m), 3,87-3,97 (4H, m), 4,30 (3H, s), 5,97 (2H, s), 7,28-7,39 (2H, m), 7,47 (1H, td, J = 7,8, 1,2 Hz), 7,63 (2H, t, J = 7,5 Hz), 7,76 (1H, t, J = 8,1 Hz), 7,97 (1H, d, J = 8,1 Hz), 8,16-8,18 (2H, m), 8,36 (1H, dd, J = 8,4, 1,2 Hz).Exemplo 572
[001863] Produção de 3-metóxi-1-metil-N-(1-oxidotetraidro-2H- tiopiran-4-il)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c] quinolina-2-carboxamidaUma solução do composto do Exemplo 571 (200 mg, 0,41 mmol) e mCPBA (água contendo 70 %; 106 mg, 0,43 mmol) em acetato de etila (25 ml) foi agitada a 0°C durante 1 h. A mistura de reação foi diluída com solução aquosa saturada de hidrogenocarbonato de sódio, e extraída com acetato de etila. O extrato foi lavado com salmoura saturada, secado sobre sulfato de magnésio e concentrado sob pressão reduzida. Recristalização do resíduo de acetato de etila-hexano deu o composto titular (54 mg, 26 %) como cristais brancos.
[001864] RMN 1H (300 MHz, DMSO-d6) δ: 1,88 (2H, d, J = 12,9 Hz), 2,20 (2H, q, J = 12,7 Hz), 2,70-3,00 (4H, m), 3,97-4,06 (4H, m), 4,29 (3H, s), 5,97 (2H, s), 7,29-7,40 (2H, m), 7,48 (1H, t, J = 7,5 Hz), 7,63 (2H, t, J = 7,5 Hz), 7,76 (1H, t, J = 7,5 Hz), 8,05 (1H, d, J = 8,1 Hz), 8,16-8,19 (2H, m), 8,37 (1H, d, J = 7,5 Hz).Exemplo 573
[001865] Produção de N-[1-(etoxiacetil)piperidin-4-il]-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (134 mg, 61 %) foi obtido como um sólido branco a partir do composto do Exemplo 77 (200 mg, 0,39 mmol) e ácido etoxiacético (0,045 ml, 0,47 mmol).
[001866] RMN 1H (300 MHz, DMSO-d6) δ:1,14 (3H, t, J = 7,0 Hz), 1,35-1,64 (2H, m), 1,81-1,97 (2H, m), 2,81-2,95 (1H, m), 3,09-3,24 (1H, m), 3,42-3,55 (2H, m), 3,73-3,85 (1H, m), 3,96 (3H, s), 4,02-4,25 (4H, m), 4,31 (3H, s), 5,97 (2H, s), 7,26-7,41 (2H, m), 7,43-7,53 (1H, m), 7,58-7,68 (2H, m), 7,71-7,81 (1H, m), 7,95 (1H, d, J = 7,7 Hz), 8,12-8,22 (2H, m), 8,37 (1H, dd, J = 8,2, 1,2 Hz).Exemplo 574
[001867] Produção de cloridrato de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-N-(1-piridin-4-ilpiperidin-4-il)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaUma solução do composto do Exemplo 563 (250 mg, 0,46 mmol) e solução 4N cloreto de hidrogênio acetato de etila (0,114 ml, 0,46 mmol) em metanol (3,0 ml)-acetato de etila (3,0 ml) foi agitada à temperatura ambiente durante 10 min. A mistura de reação foi concentrada sob pressão reduzida, e o resíduo foi recristalizado de metanol-éter de dietila dando o composto titular (45 mg, 17 %) como um sólido branco.
[001868] RMN 1H (300 MHz, DMSO-d6) δ:1,54-1,74 (2H, m), 1,952,10 (2H, m), 3,36-3,48 (2H, m), 3,96 (3H, s), 4,11-4,36 (6H, m), 5,97 (2H, s), 7,17-7,27 (2H, m), 7,28-7,42 (2H, m), 7,43-7,53 (1H, m), 7,58-7,69 (2H, m), 7,71-7,82 (1H, m), 8,00 (1H, d, J = 7,7 Hz), 8,12-8,19 (2H, m), 8,21-8,28 (2H, m), 8,38 (1H, dd, J = 8,3, 1,1 Hz), 13,40 (1H, br s).Exemplo 575
[001869] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N- (1-fenilpiperidin-4-il)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaUma solução do composto do Exemplo 77 (200 mg, 0,42 mmol), iodobenzeno (0,50 ml), tris(dibenzilidenoacetona)dipaládio (0) (38 mg, 0,042 mmol), x-fós (40 mg, 0,085 mmol) e t-butóxido de sódio (102 mg, 1,1 mmol) em t-butanol (4,0 ml) foi agitada sob irradiação de microondas a 130oC durante 35 min. A mistura de reação foi diluída com água, e extraída duas vezes com acetato de etila. Os extratos foram combinados, secados sobre sulfato de magnésio, e concentrados sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=30/70 - 100/0) e recristalizado de acetato de etila dando o composto titular (70 mg, 30 %) como um sólido branco.
[001870] RMN 1H (300 MHz, CDCl3) δ:1,67-1,85 (2H, m), 2,09-2,25 (2H, m), 2,92-3,08 (2H, m), 3,53-3,69 (2H, m), 4,06-4,25 (4H, m), 4,48 (3H, s), 5,88 (2H, s), 6,82-6,92 (1H, m), 6,94-7,09 (3H, m), 7,20-7,32 (3H, m), 7,35-7,46 (1H, m), 7,49-7,59 (2H, m), 7,61-7,81 (2H, m), 8,03-8,16 (2H, m), 8,26 (1H, dd, J = 8,3, 1,3 Hz).Exemplo 576
[001871] Produção de cloridrato de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-N-(1-prolilpiperidin-4-il)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaA uma solução do composto do Exemplo 77 (300 mg, 0,59 mmol), 1-(t-butoxicarbonil)prolina (152 mg, 0,71 mmol) e HOBt (96 mg, 0,71 mmol) em DMF (7,5 ml) adicionou-se WSCD (136 mg, 0,71 mmol) e trietilamina (0,18 ml, 1,3 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 17 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. Os extratos foram combinados, secados sobre sulfato de magnésio, e concentrados sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=20/80 - 100/0). O composto obtido foi dissolvido em metanol (4,5 ml), adicionou-se solução 4N cloreto de hidrogênio acetato de etila (4,5 ml), e a mistura foi agitada à temperatura ambiente durante 7 h. A mistura de reação foi concentrada sob pressão reduzida e recristalizado de metanol-éter de dietila dando o composto titular (234 mg, 65 %) como um sólido branco.
[001872] RMN 1H (300 MHz, DMSO-d6) δ:1,37-1,69 (2H, m), 1,691,84 (1H, m), 1,84-2,05 (4H, m), 2,29-2,46 (1H, m), 2,91-3,27 (4H, m), 3,753,91 (1H, m), 3,97 (3H, d, J = 1,5 Hz), 4,06-4,29 (2H, m), 4,32 (3H, d, J = 3,2 Hz), 4,48-4,67 (1H, m), 5,97 (2H, s), 7,27-7,43 (2H, m), 7,44-7,54 (1H, m), 7,56-7,70 (2H, m), 7,70-7,83 (1H, m), 7,97 (1H, dd, J = 11,8, 7,8 Hz), 8,088,26 (2H, m), 8,38 (1H, dd, J = 8,3, 1,1 Hz), 8,93 (2H, br s).Exemplo 577
[001873] Produção de metanossulfonato de 3-metóxi-1-metil-4-oxo-5- (2-oxo-2-feniletil)-N-(1-piridin-4-ilpiperidin-4-il)-4,5-diidro-1H-pirrol[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 574, o composto titular (142 mg, 36 %) foi obtido como um sólido amarelo claro a partir do composto do Exemplo 563 (333 mg, 0,61 mmol), ácido metanossulfônico (0,041 ml, 0,64 mmol).
[001874] RMN 1H (300 MHz, DMSO-d6) δ:1,55-1,73 (2H, m), 1,962,09 (2H, m), 2,30 (3H, s), 3,36-3,49 (2H, m), 3,96 (3H, s), 4,14-4,37 (6H, m), 5,97 (2H, s), 7,17-7,27 (2H, m), 7,28-7,42 (2H, m), 7,43-7,52 (1H, m), 7,57-7,68 (2H, m), 7,71-7,81 (1H, m), 8,00 (1H, d, J = 7,9 Hz), 8,11-8,19 (2H, m), 8,21-8,28 (2H, m), 8,38 (1H, dd, J = 8,2, 1,2 Hz), 13,22 (1H, br s).Exemplo 578
[001875] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N- [1-(1,3-tiazol-2-il)piperidin-4-il]-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 25, o composto titular(152 mg, 53 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,51 mmol) e cloridrato de 1-(1,3-tiazol- 2-il)piperidin-4-amina (124 mg, 0,56 mmol).
[001876] RMN 1H (300 MHz, DMSO-d6) δ:1,58-1,79 (2H, m), 1,902,04 (2H, m), 3,15-3,28 (2H, m), 3,81-3,92 (2H, m), 3,96 (3H, s), 4,03-4,18 (1H, m), 4,31 (3H, s), 5,97 (2H, s), 6,83 (1H, d, J = 3,6 Hz), 7,16 (1H, d, J = 3,6 Hz), 7,27-7,41 (2H, m), 7,44-7,52 (1H, m), 7,58-7,68 (2H, m), 7,70-7,82 (1H, m), 8,00 (1H, d, J = 7,9 Hz), 8,10-8,23 (2H, m), 8,37 (1H, dd, J = 8,3, 1,3 Hz).Exemplo 579
[001877] Produção de 8-fluoro-N-[1-(2-hidroxietil)piperidin-4-il]-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]Uma solução do composto do Exemplo 675 (300 mg, 0,57 mmol), carbonato de potássio (629 mg, 4,6 mmol) e trietilamina (0,11 ml, 0,76 mmol) em DMF (13 ml) foi agitada a 100°C durante 5 min, e adicionou- se 2-bromoetanol (0,16 ml, 2,3 mmol). Após agitar a 100°C durante 1,5 h, a mistura de reação foi concentrada sob pressão reduzida. A mistura de reação foi diluída com água, e extraída 3 vezes com acetato de etila. Os extratos foram combinados, lavados com salmoura saturada, secados sobre sulfato de magnésio, e concentrados sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; metanol/acetato de etila=0/100 - 5/95) e recristalizado de THF-éter de dietila dando o composto titular (205 mg, 51 %) como um sólido branco.
[001878] RMN 1H (300 MHz, DMSO-d6) δ:1,47-1,67 (2H, m), 1,751,89 (2H, m), 2,08-2,25 (2H, m), 2,40 (2H, t, J = 6,3 Hz), 2,70-2,86 (2H, m), 3,49 (2H, q, J = 6,1 Hz), 3,74-3,89 (1H, m), 3,97 (3H, s), 4,31 (3H, s), 4,38 (1H, t, J = 5,4 Hz), 5,97 (2H, s), 7,28-7,40 (1H, m), 7,40-7,49 (1H, m), 7,587,68 (2H, m), 7,71-7,82 (1H, m), 7,92 (1H, d, J = 7,7 Hz), 8,05-8,23 (3H, m).Exemplo 580
[001879] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N- [1-(tetraidrofuran-2-ilcarbonil)piperidin-4-il]-4,5-diidro-1H-pirrol[3,2-c] quinolina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (41 mg, 17 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 77 (200 mg, 0,42 mmol) e tetraidrofurano - ácido 2- carboxílico (0,049 ml, 0,51 mmol).
[001880] RMN 1H (300 MHz, DMSO-d6) δ:1,34-1,63 (2H, m), 1,741,95 (4H, m), 1,96-2,12 (2H, m), 2,78-2,97 (1H, m), 3,09-3,28 (1H, m), 3,683,86 (2H, m), 3,88-4,02 (4H, m), 4,03-4,27 (2H, m), 4,28-4,35 (3H, m), 4,68 (1H, dd, J = 7,4, 5,9 Hz), 5,97 (2H, s), 7,26-7,41 (2H, m), 7,43-7,53 (1H, m), 7,58-7,68 (2H, m), 7,71-7,81 (1H, m), 7,89-8,03 (1H, m), 8,12-8,22 (2H, m), 8,37 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 581
[001881] Produção de 3-metóxi-1-metil-N-{1-[4-(metilsulfonil)fenil] piperidin-4-il}-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 575, o composto titular (28 mg, 8,0 %) foi obtido como um sólido branco a partir do composto do Exemplo 77 (260 mg, 0,55 mmol) e 1-bromo-4-(metilsulfonil)benzeno (259 mg, 1,1 mmol).
[001882] RMN 1H (300 MHz, DMSO-d6) δ:1,54-1,72 (2H, m), 1,882,04 (2H, m), 3,05-3,20 (5H, m), 3,85-3,99 (5H, m), 4,04-4,22 (1H, m), 4,31 (3H, s), 5,97 (2H, s), 7,06-7,17 (2H, m), 7,26-7,41 (2H, m), 7,43-7,52 (1H, m), 7,57-7,71 (4H, m), 7,72-7,82 (1H, m), 7,99 (1H, d, J = 7,9 Hz), 8,14-8,23 (2H, m), 8,37 (1H, dd, J = 8,1, 1,1 Hz).Exemplo 582
[001883] Produção de 3-metóxi-1-metil-N-[1-(2-metilpiridin-4-il)piperidin-4-il]-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 575, o composto titular (51 mg, 14 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 77 (300 mg, 0,64 mmol) e 4-bromo-2-metilpiridina (0,15 ml, 1,3 mmol).
[001884] RMN 1H (300 MHz, DMSO-d6) δ:1,48-1,68 (2H, m), 1,841,98 (2H, m), 2,32 (3H, s), 2,95-3,14 (2H, m), 3,80-3,91 (2H, m), 3,95 (3H, s), 4,02-4,18 (1H, m), 4,31 (3H, s), 5,97 (2H, s), 6,62-6,70 (1H, m), 6,71-6,75 (1H, m), 7,24-7,41 (2H, m), 7,43-7,52 (1H, m), 7,58-7,67 (2H, m), 7,70-7,81 (1H, m), 7,92-8,06 (2H, m), 8,12-8,22 (2H, m), 8,37 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 583
[001885] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N- (1-pirimidin-4-ilpiperidin-4-il)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaUma solução do composto do Exemplo 77 (200 mg, 0,42 mmol), 4-cloropirimidina (58 mg, 0,51 mmol) e trietilamina (0,12 ml, 0,85 mmol) em 2-propanol (4,0 ml) foi aquecida em refluxo durante 23 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com um solvente misto de acetato de etila- metanol. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/metanol=0/100 - 5/95) e recristalizado de THF dando o composto titular (97 mg, 42 %) como um sólido branco.
[001886] RMN 1H (300 MHz, DMSO-d6) δ:1,44-1,65 (2H, m), 1,882,02 (2H, m), 3,10-3,24 (2H, m), 3,95 (3H, s), 4,08-4,23 (1H, m), 4,25-4,39 (5H, m), 5,97 (2H, s), 6,88 (1H, dd, J = 6,4, 1,1 Hz), 7,26-7,41 (2H, m), 7,437,52 (1H, m), 7,58-7,68 (2H, m), 7,72-7,81 (1H, m), 7,97 (1H, d, J = 7,9 Hz), 8,11-8,23 (3H, m), 8,37 (1H, dd, J = 8,3, 1,1 Hz), 8,49 (1H, s).Exemplo 584
[001887] Produção de 8-fluoro-N-[1-(hidroxiacetil)piperidin-4-il]-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-Da mesma maneira que no Exemplo 511, o composto titular (103 mg, 38 %) foi obtido como um sólido branco a partir do composto do Exemplo 676 (293 mg, 0,50 mmol).
[001888] RMN 1H (300 MHz, DMSO-d6) δ:1,36-1,63 (2H, m), 1,811,96 (2H, m), 2,84-2,99 (1H, m), 3,06-3,20 (1H, m), 3,61-3,74 (1H, m), 3,95 (3H, s), 4,03-4,15 (3H, m), 4,17-4,27 (1H, m), 4,30 (3H, s), 4,52 (1H, t, J = 5,5 Hz), 5,97 (2H, s), 7,30-7,40 (1H, m), 7,41-7,49 (1H, m), 7,58-7,68 (2H, m), 7,71-7,80 (1H, m), 8,01 (1H, d, J = 7,7 Hz), 8,07-8,21 (3H, m).Exemplo 585
[001889] Produção de N-[1-(hidroxiacetil)piperidin-4-il]-3-metóxi-1- metil-4-oxo-5-(piridin-2-ilmetil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaA uma suspensão do composto do Exemplo 672 (300 mg, 0,66 mmol) em DMF (5 ml) adicionou-se hidreto de sódio (60 % em óleo; 79 mg, 1,98 mmol), e a mistura foi agitada à temperatura ambiente durante 30 min. Adicionou-se cloridrato de 2-clorometilpiridina (238 mg, 1,46 mmol) à mistura, e a mistura foi agitada a 60°C durante 16 h. Após resfriamento, a mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila) dando acetato de 2-[4-({[3-metóxi-1- metil-4-oxo-5-(piridin-2-ilmetil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2- il]carbonil}amina)piperidin-1-il]-2-oxoetila (60 mg).
[001890] A uma solução de acetato de 2-[4-({[3-metóxi-1-metil-4-oxo- 5-(piridin-2-ilmetil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil} amina)piperidin-1-il]-2-oxoetila (60 mg) em THF (2 ml)-metanol (2 ml) adicionou-se solução de hidróxido de sódio 2N (2 ml), e a mistura foi agitada à temperatura ambiente durante 1 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. Recristalização de acetato de etila-éter de diisopropila deu o composto titular (25 mg, 45 %) como cristais bege.
[001891] RMN 1H (300 MHz, DMSO-d6) δ:1,40-1,60 (2H, m), 1,90 (2H, d, J = 11,4 Hz), 2,93 (1H, t, J = 11,2 Hz), 3,15 (1H, t, J = 11,9 Hz), 3,67 (1H, d, J = 13,8 Hz), 4,01-4,29 (10H, m), 4,52 (1H, t, J = 5,4 Hz), 5,66 (2H, s), 7,11 (1H, d, J = 7,8 Hz), 7,24-7,31 (2H, m), 7,40-7,44 (2H, m), 7,71 (1H, td, J = 7,5, 1,8 Hz), 7,97 (1H, d, J = 7,8 Hz), 8,34 (1H, d, J = 8,1 Hz), 8,49-8,51 (1H, m).Exemplo 586
[001892] Produção de N-[1-(hidroxiacetil)piperidin-4-il]-3-metóxi-1- metil-4-oxo-5-(piridin-4-ilmetil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 585, o composto titular (14 mg, 5 %) foi obtido como cristais bege a partir do composto do Exemplo 672 (300 mg, 0,66 mmol) e cloridrato de 4-clorometilpiridina (130 mg, 0,80 mmol).
[001893] RMN 1H (300 MHz, DMSO-d6) δ:1,35-1,60 (2H, m), 1,90 (2H, d, J = 11,4 Hz), 2,93 (1H, t, J = 12,4 Hz), 3,14 (1H, t, J = 14,2 Hz), 3,603,75 (1H, m), 4,10-4,29 (10H, m), 4,45-4,60 (1H, br), 5,63 (2H, s), 7,16 (2H, d, J = 5,1 Hz), 7,28-7,36 (2H, m), 7,46 (1H, t, J = 8,1 Hz), 7,99 (1H, d, J = 7,8 Hz), 8,36 (1H, d, J = 8,4 Hz), 8,48 (2H, d, J = 4,8 Hz).Exemplo 587
[001894] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N- (tetraidro-2H-piran-4-il)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamida Da mesma maneira que no Exemplo 25, o composto titular (204 mg, 84 %) foi obtido como cristais brancos a partir do composto do Exemplo de Referência 28 (200 mg, 0,51 mmol) e 4-aminatetraidropirano (62 mg, 0,61 mmol).
[001895] RMN 1H (300 MHz, DMSO-d6) δ:1,59 (2H, q, J = 10,0 Hz), 1,84 (2H, d, J = 13,5 Hz), 3,44 (2H, t, J = 11,0 Hz), 3,86 (2H, d, J = 11,4 Hz), 3,97 (3H, s), 4,00-4,10 (1H, m), 4,31 (3H, s), 5,97 (2H, s), 7,29-7,39 (2H, m), 7,48 (1H, t, J = 7,5 Hz), 7,63 (2H, t, J = 7,5 Hz), 7,76 (1H, t, J = 7,1 Hz), 7,96 (1H, d, J = 7,8 Hz), 8,17 (2H, d, J = 7,5 Hz), 8,37 (1H, d, J = 8,1 Hz).Exemplo 588
[001896] Produção de 4-({[3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina)-2- metilpiperidina-1-carboxilato de t-butilaDa mesma maneira que no Exemplo 25, o composto titular (220 mg, 75 %) foi obtido como cristais brancos a partir do composto do Exemplo de Referência 28 (200 mg, 0,51 mmol) e 1-Boc-4-amina-2- metilpiperidina (131 mg, 0,61 mmol).
[001897] RMN 1H (300 MHz, DMSO-d6) δ:1,24 (3H, d, J = 6,9 Hz), 1,41 (9H, s), 1,65-1,95 (4H, m), 3,13 (1H, t, J = 10,7 Hz), 3,73 (1H, d, J = 13,2 Hz), 4,02 (3H, s), 4,10-4,20 (2H, m), 4,35 (3H, s), 5,98 (2H, s), 7,30-7,41 (2H, m), 7,48 (1H, t, J = 7,2 Hz), 7,63 (2H, t, J = 7,5 Hz), 7,76 (1H, t, J = 7,5 Hz), 8,02 (1H, d, J = 6,6 Hz), 8,16-8,19 (2H, m), 8,38 (1H, d, J = 7,2 Hz). Exemplo 589
[001898] Produção de cloridrato de 3-metóxi-1-metil-N-(2- metilpiperidin-4-il)-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 61, o composto titular(163 mg, 100 %) foi obtido como cristais brancos a partir do composto do Exemplo 588 (200 mg, 0,34 mmol).
[001899] RMN 1H (300 MHz, DMSO-d6) δ:1,26 (3H, d, J = 6,3 Hz), 1,45-1,90 (3H, m), 2,08 (2H, t, J = 14,1 Hz), 3,04 (1H, t, J = 11,9 Hz), 3,96 (3H, s), 4,04-4,14 (1H, m), 4,28 (3H, s), 5,98 (2H, s), 7,29-7,40 (2H, m), 7,48 (1H, d, J = 7,8 Hz), 7,64 (2H, t, J = 7,5 Hz), 7,76 (1H, t, J = 7,5 Hz), 8,09 (1H, d, J = 7,8 Hz), 8,16-8,19 (2H, m), 8,37 (1H, d, J = 8,4 Hz), 8,50-8,90 (2H, br). Exemplo 590
[001900] Produção de N-[1-(2-hidroxietil)-2-metilpiperidin-4-il]-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c] quinolina-2-carboxamida Da mesma maneira que no Exemplo 79, o composto titular (25 mg, 36 %) foi obtido como cristais brancos a partir do composto do Exemplo 589 (70 mg, 0,13 mmol).
[001901] RMN 1H (300 MHz, DMSO-d6) δ:1,06 (3H, d, J = 6,3 Hz), 1,23 (1H, q, J = 11,6 Hz), 1,40-1,60 (1H, m), 1,85 (2H, d, J = 10,8 Hz), 2,212,32 (3H, m), 2,74-2,83 (1H, m), 2,96 (1H, t, J = 12,3 Hz), 3,45-3,51 (2H, m), 3,70-3,90 (1H, m), 3,98 (3H, s), 4,30-4,38 (4H, m), 5,97 (2H, s), 7,29-7,45 (2H, m), 7,48 (1H, d, J = 7,5 Hz), 7,63 (2H, t, J = 7,5 Hz), 7,74-7,84 (2H, m), 8,17 (2H, d, J = 7,8 Hz), 8,37 (1H, d, J = 8,4 Hz).Exemplo 591
[001902] Produção de N-[1-(hidroxiacetil)-2-metilpiperidin-4-il]-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c] quinolina-2-carboxamida Da mesma maneira que no Exemplo 130, o composto titular (35 mg, 40 %) foi obtido como cristais brancos a partir do composto do Exemplo 589 (80 mg, 0,15 mmol).
[001903] RMN 1H (300 MHz, DMSO-d6) δ:1,28 (3H, d, J = 6,9 Hz), 1,70-1,95 (4H, m), 3,10-3,25 (1H, m), 4,03-4,15 (7H, m), 4,30-4,34 (4H, m), 4,50 (1H, t, J = 5,4 Hz), 5,98 (2H, s), 7,30-7,41 (2H, m), 7,49 (1H, t, J = 8,1 Hz), 7,63 (2H, t, J = 7,5 Hz), 7,76 (1H, t, J = 7,2 Hz), 8,07 (1H, d, J = 6,6 Hz), 8,17 (2H, d, J = 7,2 Hz), 8,38 (1H, d, J = 7,5 Hz).Exemplo 592
[001904] Produção de N-[1-(4-cianofenil)piperidin-4-il]-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaUma solução do composto do Exemplo 77 (300 mg, 0,64 mmol), 4-fluorobenzonitrila (115 mg, 0,95 mmol) e carbonato de potássio (176 mg, 1,3 mmol) em N-metilpirrolidona (3,0 ml) foi agitada a 120oC durante 16,5 h. A mistura de reação foi diluída com água, e extraída duas vezes com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=30/70 - 100/0) e recristalizado de THF-éter de dietila dando o composto titular (73 mg, 20 %) como um sólido amarelo claro.
[001905] RMN 1H (300 MHz, DMSO-d6) δ:1,52-1,70 (2H, m), 1,872,03 (2H, m), 3,02-3,20 (2H, m), 3,81-4,00 (5H, m), 4,03-4,20 (1H, m), 4,31 (3H, s), 5,97 (2H, s), 6,98-7,12 (2H, m), 7,26-7,41 (2H, m), 7,43-7,52 (1H, m), 7,53-7,69 (4H, m), 7,71-7,82 (1H, m), 7,98 (1H, d, J = 7,9 Hz), 8,12-8,22 (2H, m), 8,37 (1H, dd, J = 8,4, 1,2 Hz).Exemplo 593
[001906] Produção de N-[1-(hidroxiacetil)piperidin-4-il]-3-metóxi-1- metil-4-oxo-5-[3-(trifluorometóxi)benzil]-4,5-diidro-1H-pirrol[3,2-c] quinolina-2-carboxamidaDa mesma maneira que no Exemplo 570, acetato de 2-{4-[({3- metóxi-1-metil-4-oxo-5-[3-(trifluorometóxi)benzil]-4,5-diidro-1H-pirrol[3,2- c]quinolin-2-il}carbonil)amina]piperidin-1-il}-2-oxoetila (70 mg) foi obtido como um sólido amorfo incolor a partir do composto do Exemplo 672 (500 mg, 1,10 mmol) e 3-trifluorometoxibrometo de benzila (1,0 g, 3,92 mmol).
[001907] Uma solução de acetato de 2-{4-[({3-metóxi-1-metil-4-oxo-5- [3-(trifluorometóxi)benzil]-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il} carbonil)amina]piperidin-1-il}-2-oxoetila (70 mg) e carbonato de potássio (77 mg, 0,55 mmol) em THF (2 ml)-metanol (1 ml)-água (1 ml) foi agitada à temperatura ambiente durante 3 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi recristalizado de acetato de etila-hexano dando o composto titular (23 mg, 4 %) como cristais brancos.
[001908] RMN 1H (300 MHz, DMSO-d6) δ:1,35-1,65 (2H, m), 1,851,95 (2H, m), 2,93 (1H, t, J = 11,7 Hz), 3,15 (1H, t, J = 11,7 Hz), 3,68 (1H, d, J = 12,3 Hz), 4,01-4,29 (10H, m), 4,53 (1H, t, J = 5,4 Hz), 5,50-5,70 (2H, br), 7,16-7,33 (4H, m), 7,41-7,47 (3H, m), 8,00 (1H, d, J = 8,1 Hz), 8,36 (1H, d, J = 8,1 Hz).Exemplo 594
[001909] Produção de trifluoroacetato de N-[1-(2-hidroxietil)piperidin- 4-il]-3-metóxi-4-oxo-5-[2-(1H-pirrol-1-il)etil]-4,5-diidrotieno[3,2-c] quinolina-2-carboxamidaA uma solução em DMF 0,2M do composto do Exemplo 667 (500 ml, 100 μmol) adicionou-se carbonato de sódio (1 mmol, 138 mg), e adicionou-se a isto uma solução em DMF 0,3M (500 ml, 150 mmol) de 1-(2- bromoetil)-1H-pirrol, por gotejamento. A mistura de reação foi agitada a 40°C de um dia para o outro. Adicionou-se a isto acetato de etila (3 ml) e água (2 ml), e a mistura foi extraída e a camada orgânica foi separada. O acetato de etila foi evaporado sob pressão reduzida e o resíduo foi dissolvido em acetonitrila (500 μl), purificado (tipo ácido trifluoroacético) por meio de HPLC preparativa dando o composto titular.
[001910] rendimento: 6,9 mganálise de LC-MS: pureza de 84 %MS(ESI+): 495 (M+H)Exemplo 595 - Exemplo 602
[001911] Da mesma maneira que no Exemplo 594 obteve-se os compostos na Tabela 1 a partir do composto do Exemplo 667 ou Exemplo 683 e halogeneto correspondente.
[001913] Produção de (2-{[1-(hidroxiacetil)piperidin-4-il]carbamoil}-3- metóxi-1-metil-4-oxo-1,4-diidro-5H-pirrol[3,2-c]quinolin-5-il)acetato de etilaA uma solução em DMF 0,2 M do composto do Exemplo 672 (500 ml, 100 μmol) adicionou-se carbonato de sódio (1 mmol, 138 mg), e adicionou-se a isto uma solução em DMF 2M (500 ml, 1 mmol) de bromoacetato de etila por gotejamento. A mistura de reação foi agitada a 80°C de um dia para o outro. Após o completamento da reação, DMF foi evaporado usando-se um concentrador de vácuo centrífugo com aquecimento a 60°C. Adicionou-se acetonitrila-DMSO (1:1, 500 μl) ao resíduo, e o material insolúvel foi removido por filtração. O filtrado foi purificado (tipo carbonato de amônio) por meio de HPLC preparativa dando o composto titular.
[001914] rendimento: 2,9 mganálise de LC-MS: pureza de 97 %MS(ESI+): 499 (M+H)Exemplo 604 - Exemplo 618
[001915] Da mesma maneira que no Exemplo 594, os compostos mostrados na Tabela 2 foram obtidos a partir do composto do Exemplo 672 ehalogeneto correspondente.Tabela 2
Exemplo 619
[001916] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N- (1-piridin-3-ilpiperidin-4-il)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 575, o composto titular (19 mg, 5,4 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 77 (300 mg, 0,64 mmol) e 3-bromopiridina (0,50 ml, 5,2 mmol).
[001917] RMN 1H (300 MHz, DMSO-d6) δ:1,58-1,81 (2H, m), 1,892,04 (2H, m), 2,90-3,04 (2H, m), 3,64-3,77 (2H, m), 3,97 (3H, s), 4,00-4,13 (1H, m), 4,32 (3H, s), 5,97 (2H, s), 7,15-7,25 (1H, m), 7,27-7,41 (3H, m), 7,42-7,52 (1H, m), 7,57-7,68 (2H, m), 7,71-7,82 (1H, m), 7,93-8,04 (2H, m), 8,11-8,21 (2H, m), 8,30-8,43 (2H, m).Exemplo 620
[001918] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N- (1-piridin-2-ilpiperidin-4-il)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaUma solução do composto do Exemplo 77 (284 mg, 0,60 mmol), 2-iodopiridina (0,13 ml, 1,2 mmol) e carbonato de potássio (208 mg, 1,5 mmol) em DMF (3,0 ml) foi agitada a 90°C durante 5,5 h. Adicionou-se 2-bromopiridina (0,23 ml, 2,5 mmol) e trietilamina (0,49 ml, 3,5 mmol) à mistura de reação, e a mistura foi agitada sob irradiação de microondas a 165°C durante 1 h. A mistura de reação foi diluída com água, e extraída duas vezes com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=30/70 - 100/0) e recristalizado de THF-éter de dietila dando o composto titular (38 mg, 12 %) como um sólido branco.
[001919] RMN 1H (300 MHz, DMSO-d6) δ:1,45-1,65 (2H, m), 1,862,00 (2H, m), 2,99-3,14 (2H, m), 3,95 (3H, s), 4,03-4,14 (1H, m), 4,16-4,26 (2H, m), 4,31 (3H, s), 5,97 (2H, s), 6,61 (1H, dd, J = 6,8, 5,1 Hz), 6,87 (1H, d, J = 8,7 Hz), 7,26-7,42 (2H, m), 7,43-7,57 (2H, m), 7,59-7,68 (2H, m), 7,707,81 (1H, m), 7,97 (1H, d, J = 7,9 Hz), 8,08-8,21 (3H, m), 8,37 (1H, d, J = 7,7 Hz).Exemplo 621
[001920] Produção de N-[1-(2-cianofenil)piperidin-4-il]-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaUma solução do composto do Exemplo 77 (300 mg, 0,59 mmol), 2-fluorobenzonitrila (0,50 ml, 4,6 mmol) e trietilamina (0,50 ml, 3,6 mmol) em DMF (3,5 ml) foi agitada sob irradiação de microondas a 130°C durante 30 min. Adicionou-se 2-bromobenzonitrila (143 mg, 1,2 mmol) e carbonato de potássio (208 mg, 1,5 mmol) à mistura de reação, e a mistura foi agitada sob irradiação de microondas a 165°C durante 30 min. A mistura de reação foi diluída com água, e extraída duas vezes com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=50/50 - 100/0) e recristalizado de acetato de etila-hexano dando o composto titular (74 mg, 22 %) como um sólido amarelo claro.
[001921] RMN 1H (300 MHz, DMSO-d6) δ:1,72-1,89 (2H, m), 1,972,10 (2H, m), 2,94-3,08 (2H, m), 3,43-3,54 (2H, m), 3,95-4,14 (4H, m), 4,32 (3H, s), 5,98 (2H, s), 7,05-7,13 (1H, m), 7,22 (1H, d, J = 8,1 Hz), 7,28-7,42 (2H, m), 7,44-7,52 (1H, m), 7,56-7,81 (5H, m), 8,06 (1H, d, J = 7,9 Hz), 8,148,23 (2H, m), 8,38 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 622
[001922] Produção de N-[1-(3-cianofenil)piperidin-4-il]-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaUma solução do composto do Exemplo 77 (300 mg, 0,59 mmol), 3-bromobenzonitrila (143 mg, 1,2 mmol), tris(dibenzilidenoacetona) dipaládio (0) (54 mg, 0,059 mmol), x-fós (56 mg, 0,12 mmol), t-butóxido de sódio (142 mg, 1,5 mmol) e trietilamina (0,082 ml, 0,59 mmol) em 2- butanona (4,0 ml) foi agitada sob irradiação de microondas a 130oC durante 40 min. A mistura de reação foi diluída com água, e extraída duas vezes com acetato de etila. O extrato foi secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=40/60 - 100/0) e recristalizar de acetato de etila-hexano dando o composto titular (25 mg, 7,4 %) como um sólido branco.
[001923] RMN 1H (300 MHz, DMSO-d6) δ:1,58-1,74 (2H, m), 1,882,01 (2H, m), 2,94-3,07 (2H, m), 3,71-3,83 (2H, m), 3,96 (3H, s), 4,00-4,12 (1H, m), 4,31 (3H, s), 5,97 (2H, s), 7,10-7,16 (1H, m), 7,27-7,42 (5H, m), 7,44-7,52 (1H, m), 7,58-7,68 (2H, m), 7,71-7,80 (1H, m), 7,99 (1H, d, J = 7,9 Hz), 8,11-8,22 (2H, m), 8,38 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 623
[001924] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N- {1-[2-(trifluorometil)piridin-4-il]piperidin-4-il}-4,5-diidro-1H-pirrol[3,2-c] quinolina-2-carboxamidaUma solução do composto do Exemplo 77 (300 mg, 0,59 mmol), carbonato de potássio (204 mg, 1,5 mmol) e trietilamina (0,082 ml, 0,59 mmol) em DMF (3,0 ml) foi aquecida a 80°C, adicionou-se 4-bromo-2- (trifluorometil)piridina (133 mg, 0,59 mmol), e a mistura foi agitada a 100°C durante 23 h. A mistura de reação foi diluída com água, e extraída 3 vezes com acetato de etila. O extrato foi secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=50/50 - 100/0) e recristalizar de acetato de etila-hexano dando o composto titular (126 mg, 35 %) como um sólido branco.
[001925] RMN 1H (300 MHz, DMSO-d6) δ:1,52-1,70 (2H, m), 1,892,02 (2H, m), 3,11-3,25 (2H, m), 3,90-4,07 (5H, m), 4,10-4,24 (1H, m), 4,31 (3H, s), 5,97 (2H, s), 7,08 (1H, dd, J = 6,1, 2,5 Hz), 7,21-7,27 (1H, m), 7,27-7,41 (2H, m), 7,43-7,52 (1H, m), 7,57-7,67 (2H, m), 7,72-7,80 (1H, m), 7,98 (1H, d, J = 7,9 Hz), 8,13-8,21 (2H, m), 8,27 (1H, d, J = 5,9 Hz), 8,37 (1H, dd, J = 8,2, 1,2 Hz).Exemplo 624
[001926] Produção de N-[1-(2-cianopiridin-4-il)piperidin-4-il]-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c] quinolina-2-carboxamidaDa mesma maneira que no Exemplo 623, o composto titular (70 mg, 21 %) foi obtido como um sólido branco a partir do composto do Exemplo 77 (300 mg, 0,59 mmol) e 4-iodopiridina-2-carbonitrila (136 mg, 0,59 mmol).
[001927] RMN 1H (300 MHz, DMSO-d6) δ:1,50-1,69 (2H, m), 1,861,98 (2H, m), 3,10-3,25 (2H, m), 3,90-4,05 (5H, m), 4,08-4,24 (1H, m), 4,31 (3H, s), 5,97 (2H, s), 7,10 (1H, dd, J = 6,1, 2,7 Hz), 7,25-7,42 (2H, m), 7,437,55 (2H, m), 7,58-7,68 (2H, m), 7,71-7,80 (1H, m), 7,97 (1H, d, J = 7,7 Hz), 8,11-8,27 (3H, m), 8,37 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 625
[001928] Produção de N-[4-(hidroximetil)cicloexil]-3-metóxi-1-metil-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamida Da mesma maneira que no Exemplo 25, o composto titular (165 mg, 64 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 28 (200 mg, 0,51 mmol) e (4-aminacicloexil)metanol (130 mg, 1,0 mmol).
[001929] RMN 1H (300 MHz, DMSO-d6) δ:0,92-1,10 (2H, m), 1,211,43 (3H, m), 1,72-1,86 (2H, m), 1,89-2,02 (2H, m), 3,24 (2H, t, J = 5,8 Hz), 3,66-3,83 (1H, m), 3,96 (3H, s), 4,31 (3H, s), 4,42 (1H, t, J = 5,3 Hz), 5,97 (2H, s), 7,25-7,41 (2H, m), 7,42-7,53 (1H, m), 7,58-7,68 (2H, m), 7,71-7,85 (2H, m), 8,10-8,22 (2H, m), 8,37 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 626
[001930] Produção de N-[1-(6-cianopiridin-3-il)piperidin-4-il]-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c] quinolina-2-carboxamidaDa mesma maneira que no Exemplo 623, o composto titular (52 mg, 15 %) foi obtido como um sólido amarelo claro a partir do composto do Exemplo 77 (300 mg, 0,59 mmol) e 5-bromopiridina-2-carbonitrila (119 mg, 0,65 mmol).
[001931] RMN 1H (300 MHz, DMSO-d6) δ:1,56-1,74 (2H, m), 1,88- 2,02 (2H, m), 3,10-3,25 (2H, m), 3,91-4,04 (5H, m), 4,06-4,22 (1H, m), 4,31 (3H, s), 5,97 (2H, s), 7,25-7,52 (4H, m), 7,58-7,68 (2H, m), 7,71-7,81 (2H, m), 7,98 (1H, d, J = 7,9 Hz), 8,12-8,21 (2H, m), 8,37 (1H, dd, J = 8,3, 1,1 Hz), 8,46 (1H, d, J = 2,8 Hz).Exemplo 627
[001932] Produção de N-[1-(hidroxiacetil)piperidin-4-il]-3-metóxi-1- metil-5-[(6-metilpiridin-2-il)metil]-4-oxo-4,5-diidro-1H-pirrol[3,2-c] quinolina-2-carboxamidaDa mesma maneira que no Exemplo 570, acetato de 2-{4-[({3- metóxi-1-metil-5-[(6-metilpiridin-2-il)metil]-4-oxo-4,5-diidro-1H-pirrol[3,2- c]quinolin-2-il}carbonil)amina]piperidin-1-il}-2-oxoetila (80 mg) foi obtido como um sólido amorfo incolor a partir do composto do Exemplo 672 (300 mg, 0,66 mmol), cloridrato de 2-(clorometil)-6-metilpiridina (940 mg, 5,28 mmol) e carbonato de césio (2,18 g, 6,60 mmol).
[001933] Uma solução de acetato de 2-{4-[({3-metóxi-1-metil-5-[(6- metilpiridin-2-il)metil]-4-oxo-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il}carbonil)amina]piperidin-1-il}-2-oxoetila (80 mg) e carbonato de potássio (100 mg, 0,71 mmol) em THF (2 ml)-metanol (1 ml)-água (1 ml) foi agitada à temperatura ambiente durante 3 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi recristalizado de acetato de etila-hexano dando o composto titular (37 mg, 11 %) como cristais brancos.
[001934] RMN 1H (300 MHz, DMSO-d6) δ:1,40-1,60 (2H, m), 1,90 (2H, d, J = 9,6 Hz), 2,47 (3H, s), 2,93 (1H, t, J = 11,7 Hz), 3,14 (1H, t, J = 11,6 Hz), 3,67 (1H, d, J = 12,9 Hz), 3,99-4,29 (10H, m), 4,52 (1H, t, J = 5,4 Hz), 5,59 (2H, s), 6,71 (1H, d, J = 7,8 Hz), 7,12 (1H, d, J = 7,8 Hz), 7,29 (1H, t, J = 7,5 Hz), 7,37-7,48 (2H, m), 7,55 (1H, t, J = 7,8 Hz), 7,98 (1H, d, J = 7,8 Hz), 8,35 (1H, d, J = 7,2 Hz).Exemplo 628
[001935] Produção de 5-(2-clorobenzil)-N-[1-(hidroxiacetil)piperidin-4- il]-3-metóxi-1-metil-4-oxo-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 570, acetato de 2-[4-({[5- (2-clorobenzil)-3-metóxi-1-metil-4-oxo-4,5-diidro-1H-pirrol[3,2-c]quinolin- 2-il]carbonil}amina)piperidin-1-il]-2-oxoetila (80 mg) foi obtido como um sólido amorfo incolor a partir do composto do Exemplo 672 (300 mg, 0,66 mmol), cloreto de 2-clorobenzila (1,06 g, 6,60 mmol) e carbonato de césio (2,18 g, 6,60 mmol).
[001936] Uma solução de acetato de 2-[4-({[5-(2-clorobenzil)-3-metóxi- 1-metil-4-oxo-4,5-diidro-1H-pirrol[3,2-c]quinolin-2- il]carbonil}amina)piperidin-1-il]-2-oxoetila (80 mg) e carbonato de potássio (100 mg, 0,71 mmol) em THF (2 ml)-metanol (1 ml)-água (1 ml) foi agitada à temperatura ambiente durante 3 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi recristalizado de acetato de etila-hexano dando o composto titular (8 mg, 2 %) como cristais brancos.
[001937] RMN 1H (300 MHz, DMSO-d6) δ:1,40-1,60 (2H, m), 1,90 (2H, d, J = 12,3 Hz), 2,93 (1H, t, J = 11,0 Hz), 3,15 (1H, t, J = 11,6 Hz), 3,68 (1H, d, J = 13,5 Hz), 3,99-4,34 (10H, m), 4,52 (1H, t, J = 5,4 Hz), 5,58 (2H, s), 6,59 (1H, d, J = 7,5 Hz), 7,14-7,20 (2H, m), 7,27-7,34 (2H, m), 7,47 (1H, t, J = 7,8 Hz), 7,57 (1H, d, J = 8,1 Hz), 7,99 (1H, d, J = 7,8 Hz), 8,39 (1H, d, J = 8,4 Hz).Exemplo 629
[001938] Produção de N-[1-(hidroxiacetil)piperidin-4-il]-3-metóxi-1- metil-5-{[2-metil-6-(trifluorometil)piridin-3-il]metil}-4-oxo-4,5-diidro-1H- pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 570, acetato de 2-(4-{[(3- metóxi-1-metil-5-{[2-metil-6-(trifluorometil)piridin-3-il]metil}-4-oxo-4,5- diidro-1H-pirrol[3,2-c]quinolin-2-il)carbonil]amina}piperidin-1-il)-2-oxoetila (50 mg) foi obtido como um sólido amorfo incolor a partir do composto do Exemplo 672 (300 mg, 0,66 mmol), 3-clorometil-2-metil-6-trifluorometilpiridina (980 mg, 4,68 mmol) e carbonato de césio (1,09 g, 3,30 mmol).
[001939] Uma solução de acetato de 2-(4-{[(3-metóxi-1-metil-5-{[2- metil-6-(trifluorometil)piridin-3-il]metil}-4-oxo-4,5-diidro-1H-pirrol[3,2- c]quinolin-2-il)carbonil]amina}piperidin-1-il)-2-oxoetila (50 mg) e carbonato de potássio (55 mg, 0,40 mmol) em THF (2 ml)-metanol (1 ml)-água (1 ml) foi agitada à temperatura ambiente durante 3 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi recristalizado de acetato de etila-hexano dando o composto titular (19 mg, 5 %) como cristais brancos.
[001940] RMN 1H (300 MHz, DMSO-d6) δ:1,40-1,60 (2H, m), 1,89 (2H, d, J = 13,5 Hz), 2,77 (3H, s), 2,92 (1H, t, J = 9,9 Hz), 3,14 (1H, t, J = 11,4 Hz), 3,68 (1H, d, J = 12,9 Hz), 3,98 (3H, s), 4,00-4,33 (7H, m), 4,52 (1H, t, J = 5,4 Hz), 5,62 (2H, s), 6,99 (1H, d, J = 7,8 Hz), 7,29-7,36 (2H, m), 7,47 (1H, t, J = 7,5 Hz), 7,54 (1H, d, J = 8,1 Hz), 7,99 (1H, d, J = 7,5 Hz), 8,40 (1H, d, J = 6,9 Hz).Exemplo 630
[001941] Produção de 5-(4-clorobenzil)-N-[1-(hidroxiacetil)piperidin-4- il]-3-metóxi-1-metil-4-oxo-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 570, acetato de 2-[4-({[5- (4-clorobenzil)-3-metóxi-1-metil-4-oxo-4,5-diidro-1H-pirrol[3,2-c]quinolin- 2-il]carbonil}amina)piperidin-1-il]-2-oxoetila (60 mg) foi obtido como um sólido branco a partir do composto do Exemplo 672 (200 mg, 0,44 mmol), cloreto de 4-clorobenzila (708 mg, 4,40 mmol) e carbonato de césio (572 g, 1,76 mmol).
[001942] Uma solução de acetato de 2-[4-({[5-(4-clorobenzil)-3-metóxi- 1-metil-4-oxo-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina) piperidin-1-il]-2-oxoetila (60 mg) e carbonato de potássio (72 mg, 0,52 mmol) em THF (2 ml)-metanol (1 ml)-água (1 ml) foi agitada à temperatura ambiente durante 3 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi recristalizado de acetato de etila-hexano dando o composto titular (7 mg, 2 %) como cristais brancos.
[001943] RMN 1H (300 MHz, DMSO-d6) δ:1,40-1,60 (2H, m), 1,90 (2H, d, J = 10,8 Hz), 2,93 (1H, t, J = 12,0 Hz), 3,15 (1H, t, J = 12,0 Hz), 3,68 (1H, d, J = 13,5 Hz), 4,01-4,34 (10H, m), 4,52 (1H, t, J = 5,4 Hz), 5,59 (2H, br s), 7,20-7,49 (7H, m), 7,99 (1H, d, J = 5,4 Hz), 8,35 (1H, d, J = 8,1 Hz).Exemplo 631
[001944] Produção de N-[1-(2-carbamoilpiridin-4-il)piperidin-4-il]-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c] quinolina-2-carboxamidaDa mesma maneira que no Exemplo 623, o composto titular (58 mg, 17 %) foi obtido como um sólido vermelho claro a partir do composto do Exemplo 77 (300 mg, 0,59 mmol) e 4-bromopiridina-2- carboxamida (119 mg, 0,59 mmol).
[001945] RMN 1H (300 MHz, DMSO-d6) δ:1,52-1,72 (2H, m), 1,882,05 (2H, m), 3,07-3,24 (2H, m), 3,86-4,03 (5H, m), 4,07-4,22 (1H, m), 4,31 (3H, s), 5,96 (2H, s), 6,93-7,08 (1H, m), 7,25-7,41 (2H, m), 7,43-7,54 (3H, m), 7,56-7,68 (2H, m), 7,70-7,82 (1H, m), 7,91-8,04 (2H, m), 8,10-8,25 (3H, m), 8,37 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 632
[001946] Produção de 3-metóxi-N-[1-(2-metoxipiridin-4-il)piperidin-4- il]-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 575, o composto titular (51 mg, 15 %) foi obtido como um sólido branco a partir do composto do Exemplo 77 (300 mg, 0,59 mmol) e 4-bromo-2-metoxipiridina (122 mg, 0,65 mmol).
[001947] RMN 1H (300 MHz, DMSO-d6) δ:1,49-1,70 (2H, m), 1,852,00 (2H, m), 2,98-3,12 (2H, m), 3,73-3,88 (5H, m), 3,95 (3H, s), 4,03-4,18 (1H, m), 4,31 (3H, s), 5,97 (2H, s), 6,15 (1H, d, J = 2,3 Hz), 6,59 (1H, dd, J = 6,2, 2,3 Hz), 7,26-7,41 (2H, m), 7,43-7,52 (1H, m), 7,57-7,68 (2H, m), 7,717,84 (2H, m), 7,96 (1H, d, J = 7,9 Hz), 8,09-8,23 (2H, m), 8,37 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 633
[001948] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N-{1-[6-(trifluorometil)piridin-3-il]piperidin-4-il}-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 623, o composto titular (51 mg, 14 %) foi obtido como um sólido amarelo claro a partir do composto do Exemplo 77 (300 mg, 0,59 mmol) e 5-bromo-2-(trifluorometil)piridina (147 mg, 0,65 mmol).
[001949] RMN 1H (300 MHz, DMSO-d6) δ:1,59-1,77 (2H, m), 1,912,02 (2H, m), 3,07-3,20 (2H, m), 3,86-4,00 (5H, m), 4,05-4,20 (1H, m), 4,31 (3H, s), 5,97 (2H, s), 7,27-7,41 (2H, m), 7,43-7,52 (2H, m), 7,58-7,67 (3H, m), 7,72-7,80 (1H, m), 7,98 (1H, d, J = 7,9 Hz), 8,13-8,20 (2H, m), 8,37 (1H, dd, J = 8,2, 1,0 Hz), 8,46 (1H, d, J = 2,8 Hz).Exemplo 634
[001950] Produção de 3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-N- {1-[2-(trifluorometil)pirimidin-4-il]piperidin-4-il}-4,5-diidro-1H-pirrol[3,2- c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 623, o composto titular (210 mg, 58 %) foi obtido como um sólido vermelho claro a partir do composto do Exemplo 77 (300 mg, 0,59 mmol) e 4-cloro-2- (trifluorometil)pirimidina (129 mg, 0,71 mmol).
[001951] RMN 1H (300 MHz, DMSO-d6) δ:1,48-1,69 (2H, m), 1,912,07 (2H, m), 3,17-3,30 (2H, m), 3,96 (3H, s), 4,10-4,52 (6H, m), 5,97 (2H, s), 7,12 (1H, d, J = 6,4 Hz), 7,26-7,41 (2H, m), 7,43-7,52 (1H, m), 7,57-7,68 (2H, m), 7,71-7,81 (1H, m), 7,97 (1H, d, J = 7,9 Hz), 8,11-8,22 (2H, m), 8,278,45 (2H, m).Exemplo 635
[001952] Produção de 3-metóxi-1-metil-N-{1-[2-(metilcarbamoil) piridin-4-il]piperidin-4-il}-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol [3,2-c]quinolina-2-carboxamidaA uma solução de ácido 4-cloropiridina-2-carboxílico (200 mg, 1,3 mmol), cloridrato de metilamina (103 mg, 1,5 mmol), HOBt (205 mg, 1,5 mmol) e trietilamina (0,42 ml, 3,0 mmol) em DMF (3,0 ml) adicionou-se WSCD (292 mg, 1,5 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 5 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. Os extratos foram combinados, lavados com salmoura, secados sobre sulfato de magnésio, filtrados através de gel de aminassílica, e o filtrado foi concentrado sob pressão reduzida. O resíduo foi dissolvido em DMF (3,0 ml), o composto do Exemplo 77 (300 mg, 0,59 mmol), carbonato de potássio (204 mg, 1,5 mmol) e adicionou-se trietilamina (0,082 ml, 0,59 mmol), e a mistura foi agitada a 100°C durante 16 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com um solvente misto de acetato de etila-THF. O extrato foi secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=40/60 - 100/0) e recristalizado de acetato de etila-hexano dando o composto titular (40 mg, 11 %) como um sólido amarelo claro.
[001953] RMN 1H (300 MHz, DMSO-d6) δ:1,52-1,72 (2H, m), 1,902,05 (2H, m), 2,79 (3H, d, J = 4,9 Hz), 3,09-3,22 (2H, m), 3,88-4,02 (5H, m), 4,07-4,22 (1H, m), 4,31 (3H, s), 5,96 (2H, s), 7,01 (1H, dd, J = 6,0, 2,8 Hz), 7,25-7,41 (2H, m), 7,43-7,52 (2H, m), 7,57-7,68 (2H, m), 7,70-7,81 (1H, m), 7,98 (1H, d, J = 7,9 Hz), 8,11-8,24 (3H, m), 8,37 (1H, dd, J = 8,3, 1,1 Hz), 8,53-8,70 (1H, m).Exemplo 636
[001954] Produção de N-[1-(hidroxiacetil)-3-metilpiperidin-4-il]-3- metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c] quinolina-2-carboxamidaDa mesma maneira que no Exemplo 130, o composto titular (21 mg, 22 %) foi obtido como um sólido branco a partir do composto do Exemplo 678 (83 mg, 0,17 mmol).
[001955] RMN 1H (300 MHz, DMSO-d6) δ:0,82-1,02 (3H, m), 1,552,40 (3H, m), 3,14-3,77 (4H, m), 3,93-4,05 (3H, m), 4,07-4,17 (2H, m), 4,204,41 (4H, m), 4,45-4,57 (1H, m), 5,98 (2H, s), 7,25-7,42 (2H, m), 7,43-7,53 (1H, m), 7,58-7,68 (2H, m), 7,71-7,80 (1H, m), 7,85-8,05 (1H, m), 8,10-8,24 (2H, m), 8,38 (1H, dd, J = 8,4, 1,2 Hz).Exemplo 637
[001956] Produção de 3-metóxi-1-metil-N-[1-(2-metilpirimidin-4-il)piperidin-4-il]-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c] Da mesma maneira que no Exemplo 623, o composto titular (130 mg, 59 %) foi obtido como um sólido castanho claro a partir do composto do Exemplo 77 (200 mg, 0,39 mmol) e 4-cloro-2-metilpirimidina (61 mg, 0,47 mmol).
[001957] RMN 1H (300 MHz, DMSO-d6) δ:1,44-1,62 (2H, m), 1,852,01 (2H, m), 2,36 (3H, s), 3,06-3,23 (2H, m), 3,96 (3H, s), 4,06-4,23 (1H, m), 4,24-4,41 (5H, m), 5,97 (2H, s), 6,68 (1H, d, J = 6,4 Hz), 7,25-7,42 (2H, m), 7,43-7,53 (1H, m), 7,57-7,69 (2H, m), 7,71-7,82 (1H, m), 7,96 (1H, d, J = 7,9 Hz), 8,08 (1H, d, J = 6,2 Hz), 8,13-8,22 (2H, m), 8,37 (1H, d, J = 7,6 Hz).Exemplo 638
[001958] Produção de 3-metóxi-1-metil-N-[1-(6-metilpirimidin-4-il) piperidin-4-il]-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 623, o composto titular(137 mg, 62 %) foi obtido como um sólido castanho claro a partir do composto do Exemplo 77 (200 mg, 0,39 mmol) e 4-cloro-6-metilpirimidina (61 mg, 0,47 mmol).
[001959] RMN 1H (300 MHz, DMSO-d6) δ:1,44-1,64 (2H, m), 1,852,01 (2H, m), 2,26 (3H, s), 3,05-3,23 (2H, m), 3,95 (3H, s), 4,07-4,23 (1H, m), 4,24-4,39 (5H, m), 5,97 (2H, s), 6,77 (1H, s), 7,25-7,42 (2H, m), 7,437,53 (1H, m), 7,57-7,69 (2H, m), 7,70-7,82 (1H, m), 7,96 (1H, d, J = 7,9 Hz), 8,11-8,23 (2H, m), 8,32-8,45 (2H, m).Exemplo 639
[001960] Produção de 1-etil-N-[1-(hidroxiacetil)piperidin-4-il]-3- metóxi-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 140, o composto titular (42 mg, 22 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 120 (140 mg, 0,35 mmol) e cloridrato de 2-(4- aminapiperidin-1-il)-2-oxoetanol (81 mg, 0,42 mmol).
[001961] RMN 1H (300 MHz, DMSO-d6) δ:1,39-1,61 (5H, m), 1,821,98 (2H, m), 2,84-3,01 (1H, m), 3,06-3,21 (1H, m), 3,59-3,74 (1H, m), 3,96 (3H, s), 4,03-4,14 (3H, m), 4,16-4,28 (1H, m), 4,51 (1H, t, J = 5,4 Hz), 4,82 (2H, q, J = 7,1 Hz), 5,98 (2H, s), 7,30-7,42 (2H, m), 7,43-7,52 (1H, m), 7,597,68 (2H, m), 7,71-7,81 (1H, m), 8,03 (1H, d, J = 7,7 Hz), 8,12-8,25 (3H, m).Exemplo 640
[001962] Produção de N-[1-(hidroxiacetil)azepan-4-il]-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaUma solução mista do composto do Exemplo de Referência 123 (220 mg, 0,70 mmol) e solução aquosa de hidróxido de sódio 8N (0,36 ml) em etanol (3,0 ml)-água (3,0 ml) foi agitada durante 30 min sob resfriamento com gelo. A mistura de reação foi neutralizada com ácido clorídrico 1N, agitada durante 10 min sob resfriamento com gelo e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi dissolvido em acetato de etila (2,0 ml), e adicionou-se solução 4N cloreto de hidrogênio acetato de etila (2,0 ml). A mistura foi agitada à temperatura ambiente durante 2 h, e concentrada sob pressão reduzida. A uma solução do resíduo, o composto do Exemplo de Referência 28 (200 mg, 0,51 mmol), HOBt (90 mg, 0,67 mol) e trietilamina (0,22 ml, 1,6 mmol) em DMF (5,0 ml) adicionou-se WSCD (128 mg, 0,67 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 62 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura, secado sobre sulfato de magnésio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=80/20 - 100/0) e recristalizar de THF-éter de dietila dando o composto titular (122 mg, 44 %) como um sólido branco.
[001963] RMN 1H (300 MHz, DMSO-d6) δ:1,55-1,92 (5H, m), 1,932,11 (1H, m), 3,25-3,45 (2H, m), 3,47-3,55 (1H, m), 3,63-3,80 (1H, m), 3,924,06 (4H, m), 4,07-4,18 (2H, m), 4,25-4,36 (3H, m), 4,43 (1H, t, J = 4,7 Hz), 5,97 (2H, s), 7,24-7,42 (2H, m), 7,43-7,52 (1H, m), 7,58-7,67 (2H, m), 7,71-7,81 (1H, m), 7,94 (1H, d, J = 8,1 Hz), 8,12-8,22 (2H, m), 8,37 (1 H, d, J = 7,9 Hz).Exemplo 641
[001964] Produção de N-[1-(2-hidroxietil)azepan-4-il]-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaUma solução do composto do Exemplo de Referência 122 (157 mg, 0,73 mmol) e carbonato de potássio (607 mg, 4,4 mmol) em DMF (6,0 ml) foi agitada a 100°C durante 5 min, adicionou-se 2-bromoetanol (0,16 ml, 2,2 mmol) à mistura de reação, e a mistura foi agitada a 100°C durante 1 h. A mistura de reação foi diluída com água, adicionou-se salmoura, e a mistura foi extraída 4 vezes com acetato de etila. Os extratos foram combinados, secados sobre sulfato de magnésio, e concentrados sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; metanol/acetato de etila=0/100 - 5/95). O resíduo foi dissolvido em acetato de etila (2,0 ml), e adicionou-se solução 4N cloreto de hidrogênio acetato de etila (2,0 ml). A mistura de reação foi agitada à temperatura ambiente durante 30 min, e concentrada sob pressão reduzida. A uma solução do resíduo, o composto do Exemplo de Referência 28 (200 mg, 0,51 mmol) e trietilamina (0,27 ml, 1,9 mmol) em DMF (5,0 ml) adicionou-se DMT-MM (167 mg, 0,61 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 62 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio e água, e extraída duas vezes com acetato de etila. Os extratos foram combinados, lavados com salmoura, secados sobre sulfato de magnésio, e concentrados sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=50/50 - 100/0) e recristalizado de etanol-hexano dando o composto titular (75 mg, 28 %) como um sólido amarelo claro.
[001965] RMN 1H (300 MHz, DMSO-d6) δ:1,49-2,01 (6H, m), 2,532,84 (6H, m), 3,44-3,56 (2H, m), 3,90-4,03 (3H, m), 4,14-4,41 (5H, m), 5,97 (2H, s), 7,25-7,42 (2H, m), 7,43-7,53 (1 H, m), 7,57-7,69 (2H, m), 7,71-7,82 (1H, m), 8,04 (1H, d, J = 8,3 Hz), 8,11-8,23 (2H, m), 8,37 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 642
[001966] Produção de cloridrato de 2-[(4-aminapiperidin-1-il)carbonil]- 3-metóxi-1-metil-5-(2-oxo-2-feniletil)-1,5-diidro-4H-pirrol[3,2-c]quinolina-4- onaDa mesma maneira que no Exemplo 542, o composto titular(119 mg, 79 %) foi obtido como um sólido branco a partir do composto do Exemplo 679 (170 mg, 0,30 mmol).
[001967] RMN 1H (300 MHz, DMSO-d6) δ:1,36-1,73 (2H, m), 1,842,15 (2H, m), 2,83-3,04 (1H, m), 3,08-3,30 (2H, m), 3,77-3,95 (4H, m), 4,00 (3H, s), 4,45-4,68 (1H, m), 5,98 (2H, s), 7,24-7,52 (3H, m), 7,58-7,70 (2H, m), 7,71-7,81 (1H, m), 8,00 (3H, br s), 8,13-8,23 (2H, m), 8,33 (1H, dd, J = 8,2, 1,0 Hz).Exemplo 643
[001968] Produção de N-[1-(hidroxiacetil)piperidin-4-il]-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c][1,8]naftiridino- 2-carboxamida Da mesma maneira que no Exemplo 141, o composto titular (141 mg, 69 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 131 (150 mg, 0,38 mmol).
[001969] RMN 1H (300 MHz, DMSO-d6) δ:1,32-1,65 (2H, m), 1,811,97 (2H, m), 2,81-3,01 (1H, m), 3,04-3,22 (1H, m), 3,63-3,74 (1H, m), 3,98 (3H, s), 4,04-4,16 (3H, m), 4,17-4,28 (1H, m), 4,32 (3H, s), 4,51 (1H, t, J = 5,4 Hz), 5,99 (2H, s), 7,35 (1H, dd, J = 8,1, 4,7 Hz), 7,54-7,68 (2H, m), 7,697,80 (1H, m), 8,00 (1H, d, J = 7,9 Hz), 8,08-8,22 (2H, m), 8,44 (1H, dd, J = 4,7, 1,5 Hz), 8,73 (1H, dd, J = 8,3, 1,5 Hz).Exemplo 644
[001970] Produção de N-[1-(hidroxiacetil)piperidin-4-il]-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c][1,6]naftiridino- 2-carboxamidaDa mesma maneira que no Exemplo 141, o composto titular(97 mg, 48 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 139 (150 mg, 0,38 mmol).
[001971] RMN 1H (300 MHz, DMSO-d6) δ:1,34-1,63 (2H, m), 1,791,97 (2H, m), 2,83-3,01 (1H, m), 3,05-3,22 (1H, m), 3,59-3,74 (1H, m), 3,95 (3H, s), 4,01-4,17 (3H, m), 4,17-4,28 (1H, m), 4,35 (3H, s), 4,50 (1H, t, J = 5,4 Hz), 5,95 (2H, s), 7,42 (1H, d, J = 6,2 Hz), 7,57-7,69 (2H, m), 7,71-7,82 (1H, m), 7,99 (1H, d, J = 7,7 Hz), 8,10-8,22 (2H, m), 8,48 (1H, d, J = 6,0 Hz), 9,51 (1H, s).Exemplo 645
[001972] Produção de cloridrato de N-[2-(dietilamina)etil]-3-etóxi-N,6- dimetil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]piridina-2- carboxamidaA uma solução do composto do Exemplo 146 (150 mg, 0,310 mmol) em acetato de etila (20 ml) adicionou-se solução 4N cloreto de hidrogênio acetato de etila (93,0 ml, 0,372 mmol). A mistura foi concentrada sob pressão reduzida, e o resíduo foi dissolvido em acetato de etila (30 ml) e etanol (5 ml). Adicionou-se hexano (10 ml), e a mistura foi agitada à temperatura ambiente durante 15 h. O sólido precipitado foi recolhido por meio de filtração, e lavado com acetato de etila dando o composto titular (90,0 mg, 56 %) como um sólido branco.
[001973] RMN 1H (300 MHz, DMSO-d6) δ: 1,10-1,35 (9H, m), 2,30 (3H, s), 3,08 (3H, s), 3,00-3,40 (6H, m), 3,79 (2H, t, J = 7,2 Hz), 4,08 (2H, q, J = 7,0 Hz), 5,67 (2H, s), 6,84 (1H, d, J = 0,6 Hz), 7,62 (2H, t, J = 7,5 Hz), 7,72-7,78 (1H, m), 8,10-8,13 (2H, m), 10,03 (1H, s).Exemplo 646
[001974] Produção de 3-etóxi-N-(4-hidroxicicloexil)-1,6-dimetil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (106 mg, 60 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 44 (140 mg, 0,380 mmol) e 4-aminacicloexanol (53 mg, 0,456 mmol).
[001975] RMN 1H (300 MHz, DMSO-d6) δ:1,19-1,35 (7H, m), 1,86 (4H, d, J = 12,8 Hz), 2,27 (3H, s), 3,45 (1H, br s), 3,71 (1H, br s), 3,86 (3H, s), 4,33 (2H, q, J = 6,9 Hz), 4,56 (1H, d, J = 4,3 Hz), 5,61 (2H, s), 6,57 (1H, s), 7,48-7,67 (3H, m), 7,72 (1H, d, J = 7,2 Hz), 8,10 (2H, d, J = 7,4 Hz).Exemplo 647
[001976] Produção de 3-etóxi-1,6-dimetil-4-oxo-5-(2-oxo-2-feniletil)-N- (tetraidrofuran-2-ilmetil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (114 mg, 66 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 35 (140 mg, 0,380 mmol) e 2-tetraidrofurfurilamina (47 μl, 0,456 mmol).
[001977] RMN 1H (300 MHz, DMSO-d6) δ:1,29 (3H, t, J = 6,8 Hz), 1,48-1,62 (1H, m), 1,78-1,99 (3H, m), 2,28 (3H, s), 3,41-3,52 (1H, m), 3,603,71 (1H, m), 3,75-3,84 (1H, m), 3,89 (3H, s), 3,91-4,02 (2 H, m), 4,35 (2H, t, J = 7,0 Hz), 5,61 (2H, s), 6,59 (1H, s), 7,61 (2H, t, J = 7,4 Hz), 7,73 (1H, m), 7,88 (1H, br s), 8,11 (2H, d, J = 7,6 Hz).Exemplo 648
[001978] Produção de 3-etóxi-6-etil-N-(trans-4-hidroxicicloexil)-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2- carboxamidaDa mesma maneira que no Exemplo 25, o composto titular (76mg, 79 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 42 (77 mg, 0,20 mmol) e trans-4-aminacicloexanol (28 mg, 0,24 mmol).
[001979] RMN 1H (300 MHz, DMSO-d6) δ:1,18 (3H, t, J = 7,4 Hz), 1,22-1,36 (7H, m), 1,75-1,96 (4H, m), 2,57 (2H, q, J = 7,3 Hz), 3,44 (1H, br s), 3,71 (1H, br s), 3,89 (3H, s), 4,32 (2H, q, J = 7,1 Hz), 4,57 (1H, d, J = 4,2 Hz), 5,58 (2H, s), 6,48 (1H, s), 7,51-7,66 (3H, m), 7,67-7,78 (1H, m), 8,11 (2H, d, J = 7,2 Hz).Exemplo 649
[001980] Produção de N-[1-(hidroxiacetil)piperidin-4-il]-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c][1,6]naftiridino- 2-carboxamida Da mesma maneira que no Exemplo 140, o composto titular (132 mg, 54 %) foi obtido como cristais brancos a partir do composto do Exemplo de Referência 50 (200 mg, 0,47 mmol) e 4-aminacicloexanol (82 mg, 0,71 mmol).
[001981] RMN 1H (300 MHz, DMSO-d6) δ:1,25 (4H, t, J = 9,6 Hz), 1,80-1,90 (4H, m), 2,29 (3H, s), 3,30-3,45 (1H, br), 3,60-3,80 (1H, br), 3,83 (3H, s), 4,57 (1H, t, J = 4,5 Hz), 5,06 (2H, q, J = 9,3 Hz), 5,65 (2H, s), 6,64 (1H, s), 7,31 (1H, d, J = 7,8 Hz), 7,61 (1H, t, J = 7,5 Hz), 7,74 (1H, t, J = 7,5 Hz), 8,09-8,12 (2H, m).Exemplo 650
[001982] Produção de 3-etóxi-6-etil-N-[1-(hidroxiacetil)piperidin-4-il]- 4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]piridina-2-carboxamida Da mesma maneira que no Exemplo de Referência 7, ácido 3- etóxi-6-etil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]piridina-2- carboxílico (700 mg, 83 %) foi obtido como um pó púrpura a partir do composto do Exemplo de Referência 170 (900 mg, 2,25 mmol). 4-({[3-Etóxi- 6-etil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]piridin-2-il]carbonil} amina)piperidina-1-carboxilato de t-butila (125 mg, 15 %) foi obtido como um pó branco a partir do assim-obtido ácido 3-etóxi-6-etil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidrotieno[3,2-c]piridina-2-carboxílico (550 mg, 1,4 mmol) e 4- amina-1-Boc-piperidina (361 mg, 1,8 mmol). 3-Etóxi-6-etil-4-oxo-5-(2-oxo- 2-feniletil)-N-piperidin-4-il-4,5-diidrotieno[3,2-c]piridina-2-carboxamida (94 mg, 85 %) foi obtida como um pó branco a partir do assim-obtido 4-({[3- etóxi-6-etil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]piridin-2-il] carbonil}amina)piperidina-1-carboxilato de t-butila (125 mg, 0,22 mmol) por meio de um método similar àquele no Exemplo 126. Acetato de 2-[4-({[3- etóxi-6-etil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]piridin-2- il]carbonil}amina)piperidin-1-il]-2-oxoetila (80 mg, 78 %) foi obtido como um sólido branco a partir da assim-obtida 3-etóxi-6-etil-4-oxo-5-(2-oxo-2- feniletil)-N-piperidin-4-il-4,5-diidrotieno[3,2-c]piridina-2-carboxamida (90 mg, 0,18 mmol) por meio de um método similar àquele no Exemplo 127.
[001983] Uma solução mista de acetato de 2-[4-({[3-etóxi-6-etil-4-oxo- 5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]piridin-2-il]carbonil}amina) piperidin-1-il]-2-oxoetila (90 mg, 0,18 mmol) e carbonato de potássio (39 mg, 0,28 mmol) em THF (8 ml)-metanol (2 ml)-água (2 ml) foi agitada à temperatura ambiente durante 1 h. A mistura de reação foi concentrada, e o resíduo foi repartido entre acetato de etila e solução saturada de hidrogenocarbonato de sódio. A camada orgânica foi lavada com salmoura, secada sobre sulfato de magnésio, e concentrada sob pressão reduzida. O resíduo foi recristalizado de acetato de etila-hexano dando o composto titular (64 mg, 69 %) como cristais brancos.
[001984] RMN 1H (300 MHz, DMSO-d6) δ:1,17 (3H, t, J = 7,4 Hz), 1,30 (3H, t, J = 7,1 Hz), 1,35-1,60 (2H, m), 1,90 (2H, d, J = 9,9 Hz), 2,60 (2H, q, J = 7,4 Hz), 2,84 (1H, t, J = 12,0 Hz), 3,10 (1H, t, J = 14,0 Hz), 3,66 (1H, d, J = 13,5 Hz), 4,00-4,09 (3H, m), 4,28 (3H, q, J = 7,1 Hz), 4,50 (1H, t, J = 5,4 Hz), 5,66 (2H, s), 6,84 (1H, s), 7,60-7,68 (2H, m), 7,75 (1H, t, J = 7,5 Hz), 8,10-8,13 (2H, m). Exemplo 651
[001985] Produção de 1,6-dimetil-N-(1-oxidotetraidro-2H-tiopiran-4-il)- 4-oxo-5-(2-oxo-2-feniletil)-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2- c]piridina-2-carboxamidaDa mesma maneira que no Exemplo 571, 1,6-dimetil-4-oxo-5- (2-oxo-2-feniletil)-N-(tetraidro-2H-tiopiran-4-il)-3-(2,2,2-trifluoroetóxi)-4,5- diidro-1H-pirrol[3,2-c]piridina-2-carboxamida (150 mg) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 50 (200 mg, 0,47 mmol). O composto titular (131 mg, 51 %) foi obtido como cristais brancos a partir da assim-obtida 1,6-dimetil-4-oxo-5-(2-oxo-2-feniletil)-N- (tetraidro-2H-tiopiran-4-il)-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2- c]piridina-2-carboxamida (150 mg) por meio de um método similar àquele no Exemplo 571.
[001986] RMN 1H (300 MHz, DMSO-d6) δ:1,60-1,75 (1H, m), 1,83 (1H, d, J = 10,2 Hz), 2,06-2,29 (5H, m), 2,70-2,85 (2H, m), 2,93 (1H, d, J = 12,9 Hz), 3,81 (3H, d, J = 6,3 Hz), 3,90-4,10 (1H, m), 5,00-5,13 (2H, m), 5,65 (2H, s), 6,64 (1H, s), 7,61 (3H, t, J = 7,8 Hz), 7,74 (1H, t, J = 7,2 Hz), 8,108,12 (2H, m).Exemplo 652
[001987] Produção de 3-(2,2-difluoroetóxi)-6-etil-N-[1-(hidroxiacetil) piperidin-4-il]-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2- c]piridina-2-carboxamidaDa mesma maneira que no Exemplo 140, o composto titular (340 mg, 84 %) foi obtido como um sólido amorfo branco a partir do composto do Exemplo de Referência 171 (300 mg, 0,72 mmol).
[001988] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3H, t, J = 7,4 Hz), 1,20-1,50 (2H, m), 1,90 (2H, d, J = 9,9 Hz), 2,59 (2H, q, J = 7,4 Hz), 2,83 (1H, t, J = 12,2 Hz), 3,09 (1H, t, J = 11,7 Hz), 3,68 (1H, d, J = 12,9 Hz), 3,90 (3H, s), 3,95-4,20 (3H, m), 4,26 (1H, d, J = 11,7 Hz), 4,51 (1H, t, J = 5,4 Hz), 4,67 (2H, td, J = 16,1, 3,0 Hz), 5,23 (1H, s), 5,61 (2H, s), 6,33 (1H, tt, J = 54,2, 3,0 Hz), 7,49 (1H, d, J = 7,8 Hz), 7,61 (2H, t, J = 7,5 Hz), 7,73 (1H, t, J = 7,5 Hz), 8,10-8,12 (2H, m).Exemplo 653
[001989] Produção de 6-etil-N-[1-(hidroxiacetil)piperidin-4-il]-5-(3- metoxibenzil)-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol [3,2-c]piridina-2-carboxamidaUma mistura do composto do Exemplo de Referência 143 (200 mg, 0,456 mmol), cloridrato de 2-(4-aminapiperidin-1-il)-2-oxoetanol (115 mg, 0,593 mmol), HOBt (92,4 mg, 0,684 mmol), WSCD (131 mg, 0,684 mmol), trietilamina (0,126 ml, 0,912 mmol) e DMF (4,0 ml) foi agitada à temperatura ambiente durante 16 h. A mistura de reação foi diluída com água, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com água e salmoura, secado sobre sulfato de sódio, e concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila). Recristalização do sólido obtido de acetato de etila deu o composto titular (162 mg, 61 %) como um pó branco.
[001990] RMN 1H (300 MHz, DMSO-d6) δ:1,16 (3H, t, J = 7,3 Hz), 1,24-1,50 (2H, m), 1,81-1,95 (2H, m), 2,60 (2H, q, J = 7,3 Hz), 2,76-2,91 (1H, m), 3,01-3,18 (1H, m), 3,64-3,74 (4H, m), 3,84 (3H, s), 3,95-4,14 (3H, m), 4,20-4,33 (1H, m), 4,52 (1H, t, J = 5,4 Hz), 5,11 (2H, q, J = 9,3 Hz), 5,32 (2H, br s), 6,49-6,64 (3H, m), 6,81 (1H, dd, J = 8,0, 2,2 Hz), 7,22 (1H, t, J = 8,0 Hz), 7,53 (1H, d, J = 7,6 Hz).Exemplo 654
[001991] Produção de 5-benzil-6-etil-N-[1-(hidroxiacetil)piperidin-4-il]- 1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2- carboxamidaDa mesma maneira que no Exemplo 653, o composto titular (182 mg, 75 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 145 (180 mg, 0,441 mmol).
[001992] RMN 1H (300 MHz, DMSO-d6) δ:1,16 (3H, t, J = 7,2 Hz), 1,25-1,48 (2 H, m), 1,83-1,95 (2H, m), 2,60 (2H, q, J = 7,2 Hz), 2,77-2,90 (1H, m), 3,02-3,17 (1H, m), 3,63-3,75 (1H, m), 3,84 (3H, s), 3,96-4,14 (3H, m), 4,20-4,33 (1H, m), 4,52 (1H, t, J = 5,5 Hz), 5,10 (2H, q, J = 9,4 Hz), 5,36 (2H, br s), 6,52 (1H, s), 7,00-7,09 (2H, m), 7,19-7,36 (3H, m), 7,53 (1H, d, J = 7,7 Hz).Exemplo 655
[001993] Produção de 5-(2,5-dimetoxibenzil)-6-etil-N-[1-(hidroxiacetil)piperidin-4-il]-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol [3,2-c]piridina-2-carboxamidaDa mesma maneira que no Exemplo 653, o composto titular (86,0 mg, 80 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 147 (82,7 mg, 0,177 mmol).
[001994] RMN 1H (300 MHz, DMSO-d6) δ:1,17 (3H, t, J = 7,3 Hz), 1,24-1,48 (2H, m), 1,84-1,93 (2H, m), 2,52-2,61 (2H, m), 2,77-2,90 (1H, m), 3,03-3,16 (1H, m), 3,55 (3H, s), 3,64-3,74 (1H, m), 3,83 (3H, s), 3,86 (3H, s), 3,97-4,14 (3H, m), 4,20-4,32 (1H, m), 4,52 (1H, t, J = 5,3 Hz), 5,08 (2H, q, J = 9,2 Hz), 5,21 (2H, br s), 5,89 (1H, d, J = 3,0 Hz), 6,56 (1H, s), 6,79 (1H, dd, J = 8,9, 3,0 Hz), 6,97 (1H, d, J = 8,9 Hz), 7,53 (1H, d, J = 7,9 Hz).Exemplo 656
[001995] Produção de 6-etil-N-[1-(hidroxiacetil)piperidin-4-il]-5-[2-(3- metoxifenil)-2-oxoetil]-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H- pirrol[3,2-c]piridina-2-carboxamidaDa mesma maneira que no Exemplo 653, o composto titular (65,1 mg, 29 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 151 (170 mg, 0,364 mmol).
[001996] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3H, t, J = 7,3 Hz), 1,25-1,48 (2H, m), 1,82-1,95 (2H, m), 2,54-2,64 (2H, m), 2,76-2,90 (1H, m), 3,01-3,15 (1H, m), 3,62-3,74 (1H, m), 3,82-3,90 (6H, m), 3,95-4,13 (3H, m), 4,20-4,35 (1H, m), 4,52 (1H, t, J = 5,5 Hz), 5,05 (2H, q, J = 9,3 Hz), 5,62 (2H, s), 6,54 (1H, s), 7,26-7,35 (1H, m), 7,46-7,62 (3H, m), 7,69-7,76 (1H, m).Exemplo 657
[001997] Produção de 5-[2-(3-clorofenil)-2-oxoetil]-6-etil-N-[1- (hidroxiacetil)piperidin-4-il]-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5- diidro-1H-pirrol[3,2-c]piridina-2-carboxamidaDa mesma maneira que no Exemplo 653, o composto titular (160 mg, 64 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 155 (192 mg, 0,408 mmol).
[001998] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3H, t, J = 7,3 Hz), 1,25-1,49 (2H, m), 1,82-1,95 (2H, m), 2,60 (2H, q, J = 7,3 Hz), 2,76-2,90 (1H, m), 3,01-3,17 (1H, m), 3,62-3,74 (1H, m), 3,86 (3H, s), 3,96-4,15 (3H, m), 4,20-4,32 (1H, m), 4,52 (1H, t, J = 5,4 Hz), 5,05 (2H, q, J = 9,2 Hz), 5,62 (2H, s), 6,55 (1H, s), 7,50 (1H, d, J = 7,6 Hz), 7,61-7,69 (1H, m), 7,77-7,84 (1H, m), 8,03-8,09 (1H, m), 8,14 (1H, t, J = 1,8 Hz).Exemplo 658
[001999] Produção de 6-etil-N-[1-(hidroxiacetil)piperidin-4-il]-5-(2- metoxibenzil)-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol [3,2-c]piridina-2-carboxamida O OHDa mesma maneira que no Exemplo 653, o composto titular (120 mg, 86 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 157 (104 mg, 0,237 mmol).
[002000] RMN 1H (300 MHz, DMSO-d6) δ:1,16 (3H, t, J = 7,4 Hz), 1,26-1,49 (2H, m), 1,81-1,95 (2H, m), 2,52-2,61 (2H, m), 2,77-2,91 (1H, m), 3,00-3,19 (1H, m), 3,56-3,77 (1H, m), 3,86 (3H, s), 3,88 (3H, s), 3,97-4,14 (3H, m), 4,19-4,33 (1H, m), 4,52 (1H, t, J = 5,4 Hz), 5,08 (2H, q, J = 9,2 Hz), 5,23 (2H, br s), 6,32-6,40 (1H, m), 6,56 (1H, s), 6,76-6,85 (1H, m), 7,01-7,09 (1H, m), 7,17-7,28 (1H, m), 7,52 (1H, d, J = 7,6 Hz).Exemplo 659
[002001] Produção de 6-etil-N-[1-(hidroxiacetil)piperidin-4-il]-5-(4- metoxibenzil)-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol [3,2-c]piridina-2-carboxamidaDa mesma maneira que no Exemplo 653, o composto titular (147 mg, 71 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 159 (157 mg, 0,358 mmol).
[002002] RMN 1H (300 MHz, DMSO-d6) δ:1,16 (3H, t, J = 7,3 Hz), 1,24-1,48 (2H, m), 1,83-1,96 (2H, m), 2,62 (2H, q, J = 7,3 Hz), 2,76-2,91 (1H, m), 3,02-3,17 (1H, m), 3,63-3,76 (4H, m), 3,83 (3H, s), 3,95-4,14 (3H, m), 4,20-4,33 (1H, m), 4,52 (1H, t, J = 5,4 Hz), 5,11 (2H, q, J = 9,4 Hz), 5,28 (2H, br s), 6,50 (1H, s), 6,83-6,90 (2H, m), 6,96-7,05 (2H, m), 7,52 (1H, d, J = 7,7 Hz).Exemplo 660
[002003] Produção de 5-(2-clorobenzil)-6-etil-N-[1-(hidroxiacetil) piperidin-4-il]-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol [3,2-c]piridina-2-carboxamida O OH Da mesma maneira que no Exemplo 653, o composto titular (119 mg, 66 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 161 (138 mg, 0,312 mmol).
[002004] RMN 1H (300 MHz, DMSO-d6) δ:1,18 (3H, t, J = 7,3 Hz), 1,26-1,47 (2H, m), 1,82-1,94 (2H, m), 2,53-2,61 (2H, m), 2,76-2,90 (1H, m), 3,02-3,17 (1H, m), 3,61-3,76 (1H, m), 3,86 (3H, s), 3,95-4,14 (3H, m), 4,19-4,33 (1H, m), 4,46-4,56 (1H, m), 5,06 (2H, q, J = 9,4 Hz), 5,33 (2H, s), 6,45-6,55 (1H, m), 6,60 (1H, s), 7,21-7,32 (2H, m), 7,45-7,60 (2H, m).Exemplo 661
[002005] Produção de 6-etil-N-[1-(hidroxiacetil)piperidin-4-il]-1-metil- 4-oxo-5-(2-feniletil)-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c] piridina-2-carboxamida Da mesma maneira que no Exemplo 653, o composto titular (123 mg, 65 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 165 (143 mg, 0,339 mmol).
[002006] RMN 1H (300 MHz, DMSO-d6) δ:1,21 (3H, t, J = 7,2 Hz), 1,25-1,49 (2H, m), 1,82-1,94 (2H, m), 2,66 (2H, q, J = 7,2 Hz), 2,77-2,95 (3H, m), 3,02-3,17 (1H, m), 3,62-3,75 (1H, m), 3,82 (3H, s), 3,95-4,35 (6H, m), 4,52 (1H, t, J = 5,5 Hz), 5,12 (2H, q, J = 9,4 Hz), 6,44 (1H, s), 7,16-7,35 (5H, m), 7,49 (1H, d, J = 7,6 Hz).Exemplo 662
[002007] Produção de 5-(3-clorobenzil)-6-etil-N-[1-(hidroxiacetil) piperidin-4-il]-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol [3,2-c]piridina-2-carboxamida Da mesma maneira que no Exemplo 653, o composto titular (261 mg, 71 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 167 (281 mg, 0,635 mmol).
[002008] RMN 1H (300 MHz, DMSO-d6) δ:1,17 (3H, t, J = 7,2 Hz), 1,23-1,50 (2H, m), 1,81-1,95 (2H, m), 2,60 (2H, q, J = 7,2 Hz), 2,76-2,92 (1H, m), 3,02-3,17 (1H, m), 3,64-3,76 (1H, m), 3,85 (3H, s), 3,95-4,15 (3H, m), 4,19-4,36 (1H, m), 4,52 (1H, t, J = 5,4 Hz), 5,09 (2H, q, J = 9,4 Hz), 5,35 (2H, br s), 6, 55 (1H, s), 6,95-7,03 (1H, m), 7,07-7,15 (1H, m), 7,25-7,40 (2H, m), 7,55 (1H, d, J = 7,6 Hz).Exemplo 663
[002009] Produção de 5-(4-clorobenzil)-6-etil-N-[1-(hidroxiacetil) piperidin-4-il]-1-metil-4-oxo-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol [3,2-c]piridina-2-carboxamidaDa mesma maneira que no Exemplo 653, o composto titular (160 mg, 65 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 169 (188 mg, 0,425 mmol).
[002010] RMN 1H (300 MHz, DMSO-d6) δ:1,16 (3H, t, J = 7,2 Hz), 1,23-1,49 (2H, m), 1,82-1,95 (2H, m), 2,59 (2H, q, J = 7,2 Hz), 2,77-2,90 (1H, m), 3,00-3,17 (1H, m), 3,62-3,76 (1H, m), 3,84 (3H, s), 3,95-4,14 (3H, m), 4,21-4,34 (1H, m), 4,52 (1H, t, J = 5,5 Hz), 5,09 (2H, q, J = 9,4 Hz), 5,33 (2H, br s), 6, 53 (1H, s), 7,03-7,12 (2H, m), 7,34-7,42 (2H, m), 7,53 (1H, d, J = 7,6 Hz).Exemplo 664
[002011] Produção de 4-({[3-metóxi-5-(4-metoxibenzil)-4-oxo-4,5- diidrotieno[3,2-c]quinolin-2-il]carbonil}amina)piperidina-1-carboxilato de benzilaDa mesma maneira que no Exemplo 25, o composto titular (3,07 g, 79 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 13 (2,5 g, 6,31 mmol) e cloridrato de benzil 4- aminapiperidina-1-carboxilato (2,56 g, 9,46 mmol).
[002012] RMN 1H (300 MHz, DMSO-d6) δ:1,15-1,64 (2H, m), 1,87 (2H, br d, J = 9,6 Hz), 2,90-3,10 (2H, br), 3,69 (3H, s), 4,00 (2H, d, J = 11,4 Hz), 4,09 (4H, s), 5,10 (2H, s), 5,53 (2H, br s), 6,87 (2H, d, J = 8,7 Hz), 7,20 (2H, d, J = 8,7 Hz), 7,28-7,40 (6H, m), 7,49-7,56 (2H, m), 7,80 (1H, d, J = 8,1 Hz), 8,00 (1H, d, J = 8,4 Hz).Exemplo 665
[002013] Produção de 3-metóxi-5-(4-metoxibenzil)-4-oxo-N-piperidin- 4-il-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaUma mistura do composto do Exemplo 664 (300 mg, 0,49 mmol), 10 % Pd-C (60 mg) e THF (20 ml)-metanol (10 ml) foi agitada à temperatura ambiente durante 24 h sob uma atmosfera de hidrogênio. O catalisador foi removido por filtração, e o filtrado foi concentrado e recristalizado de metanol-éter de dietila dando o composto titular (154 mg, 66 %) como cristais amarelos claros.
[002014] RMN 1H (300 MHz, DMSO-d6) δ:1,48 (2H, q, J = 11,0 Hz),1,82 (2H, d, J = 9,6 Hz), 1,95-2,15 (1H, br), 2,56 (2H, t, J = 8,4 Hz), 2,93 (2H, d, J = 12,6 Hz), 3,33 (3H, s), 3,70 (3H, s), 3,80-4,00 (1H, br), 4,10 (3H, s), 5,53 (2H, br s), 6,86 (2H, d, J = 8,7 Hz), 7,20 (2H, d, J = 8,4 Hz), 7,30 (1H, t, J = 7,1 Hz), 7,49-7,58 (2H, m), 7,72 (1H, d, J = 8,1 Hz), 8,00 (1H, d, J = 7,8 Hz).Exemplo 666
[002015] Produção de N-[1-(2-hidroxietil)piperidin-4-il]-3-metóxi-5-(4- metoxibenzil)-4-oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaDa mesma maneira que no Exemplo 79, o composto titular (110 mg, 68 %) foi obtido como um sólido branco a partir do composto do Exemplo 665 (150 mg, 0,31 mmol).
[002016] RMN 1H (300 MHz, CDCl3) δ:1,55-1,74 (2H, m), 2,00-2,11 (2H, m), 2,36 (2H, t, J = 11,6 Hz), 2,58 (2H, t, J = 5,4 Hz), 2,84 (3H, br s), 3,65 (2H, t, J = 5,4 Hz), 3,75 (3H, s), 4,05-4,20 (1H, br), 4,20 (3H, s), 5,53 (2H, br s), 6,83 (2H, dd, J = 6,9, 1,8 Hz), 7,17-7,26 (3H, m), 7,35 (1H, d, J = 8,1 Hz), 7,41-7,46 (1H, m), 7,64 (1H, d, J = 7,8 Hz), 7,85 (1H, dd, J = 7,8, 1,5 Hz).Exemplo 667
[002017] Produção de N-[1-(2-hidroxietil)piperidin-4-il]-3-metóxi-4- oxo-4,5-diidrotieno[3,2-c]quinolina-2-carboxamidaUma solução do composto do Exemplo 666 (110 mg, 0,21 mmol), anisol (91 mg, 0,84 mmol) e ácido trifluorometanossulfônico (0,5 ml) em ácido trifluoroacético (2 ml) foi agitada a 80°C durante 1 h. Após resfriamento, a mistura de reação foi concentrada, e o resíduo foi repartido entre acetato de etila e solução saturada de hidrogenocarbonato de sódio. A fase orgânica foi lavada com salmoura, secada sobre sulfato de magnésio, e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em sílica-gel (eluado; acetato de etila/hexano=1/1 to 2/1) dando o composto titular (60 mg, 71 %) como um sólido branco.
[002018] RMN 1H (300 MHz, CDCl3) δ:1,60-1,76 (2H, m), 2,07 (2H, d, J = 14,4 Hz), 2,36 (2H, t, J = 10,1 Hz), 2,59 (2H, t, J = 5,4 Hz), 2,88 (2H, d, J = 11,4 Hz), 3,65 (2H, t, J = 5,4 Hz), 3,70-3,80 (2H, br), 4,00-4,15 (1H, m), 4,22 (3H, s), 6,76-6,85 (1H, m), 7,32 (1H, t, J = 8,1 Hz), 7,51 (1H, t, J = 8,4 Hz), 7,85 (1H, d, J = 8,1 Hz), 10,20-10,50 (1H, br).Exemplo 668
[002019] Produção de 4-({[3-metóxi-5-(4-metoxibenzil)-1-metil-4-oxo- 4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina)piperidina-1- carboxilato de t-butila Da mesma maneira que no Exemplo 25, o composto titular (3,45 g, 95 %) foi obtido como um sólido bege a partir do composto do Exemplo de Referência 107 (2,49 g, 6,35 mmol) e 4-aminapiperidina-1- carboxilato de t-butila (2,54 g, 12,69 mmol).
[002020] RMN 1H (300 MHz, DMSO-d6) δ:1,35-1,49 (11H, m), 1,85 (2H, dd, J = 12,6, 2,7 Hz), 2,89-2,96 (2H, m), 3,69 (3H, s), 3,88 (2H, d, J = 13,5 Hz), 3,96-4,09 (4H, m), 4,27 (3H, s), 5,40-5,60 (2H, br), 6,83-6,88 (2H, m), 7,14 (2H, d, J = 8,7 Hz), 7,24-7,30 (1H, m), 7,41-7,49 (2H, m), 7,97 (1H, d, J = 8,1 Hz), 8,33 (1H, d, J = 8,1 Hz).Exemplo 669
[002021] Produção de cloridrato de 3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-N-(pirrolidin-3-ilmetil)-4,5-diidrotieno[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 25, 3-[({[3-metóxi-4-oxo- 5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}amina)metil]pirrolidino-1-carboxilato de t-butila (530 mg, 72 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (500 mg, 1,27 mmol) e 3-(aminametil)-1-Boc-pirrolidina (381 mg, 1,90 mmol).
[002022] Da mesma maneira que no Exemplo 500, o composto titular (456 mg, 97 %) foi obtido como um pó branco a partir de 3-[({[3-metóxi-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidrotieno[3,2-c]quinolin-2- il]carbonil}amina)metil]pirrolidino-1-carboxilato de t-butila (530 mg, 0,92 mmol).
[002023] RMN 1H (300 MHz, DMSO-d6) δ:1,55-1,73 (1H, m), 1,902,10 (1H, m), 2,55-2,70 (1H, m), 2,85-3,00 (1H, br), 3,10-3,45 (5H, m), 4,05 (3H, s), 6,00 (2H, s), 7,35 (1H, t, J = 7,5 Hz), 7,49-7,67 (5H, m), 7,77 (1H, t, J = 7,4 Hz), 8,05 (1H, d, J = 7,8, Hz), 8,16-8,19 (2H, m), 8,25 (1H, t, J =5,9 Hz), 9,04 (2H, br s).Exemplo 670
[002024] Produção de 3-({[3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina)azetidino-1- carboxilato de t-butila Da mesma maneira que no Exemplo 25, o composto titular (610 mg, 88 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 28 (500 mg, 1,27 mmol) e 3-amina-1-Boc-azetidina (330 mg, 1,92 mmol).
[002025] RMN 1H (300 MHz, DMSO-d6) δ:1,40 (9H, m), 3,85-3,95 (2H, m), 3,99 (3H, s), 4,14 (2H, t, J = 7,8 Hz), 4,27 (3H, s), 4,62-4,74 (1H, m), 5,97 (2H, s), 7,31 (1H, t, J = 7,5 Hz), 7,38 (1H, d, J = 8,1 Hz), 7,48 (1H, t, J = 7,5 Hz), 7,64 (2H, t, J = 7,5 Hz), 7,76 (1H, t, J = 7,5 Hz), 8,16-8,19 (2H, m), 8,37 (1H, d, J = 8,1 Hz), 8,56 (1H, d, J = 7,2 Hz).Exemplo 671
[002026] Produção de [3-({[3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina)cicloexil] carbamato de t-butilaDa mesma maneira que no Exemplo 25, o composto titular (395 mg, 66 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 7 (400 mg, 1,02 mmol) e (3-aminacicloexil) carbamato de t-butila (285 mg, 1,33 mmol).
[002027] RMN 1H (300 MHz, DMSO-d6) δ:0,98-1,46 (13 H, m), 1,651,90 (3 H, m), 2,00-2,12 (1 H, m), 3,23-3,42 (1 H, m), 3,73-3,88 (1 H, m), 3,96 (2 H, s), 4,04 (1 H, s), 4,30 (2 H, s), 4,35 (1 H, s), 5,97 (2 H, s), 6,766,94 (1 H, m), 7,24-7,42 (2 H, m), 7,43-7,53 (1 H, m), 7,63 (2 H, t, J = 7,6 Hz), 7,71-7,80 (1 H, m), 7,86 (1 H, d, J = 7,9 Hz), 8,12-8,22 (2 H, m), 8,318,42 (1 H, m).Exemplo 672
[002028] Produção de acetato de 2-(4-{[(3-metóxi-1-metil-4-oxo-4,5- diidro-1H-pirrol[3,2-c]quinolin-2-il)carbonil]amina}piperidin-1-il)-2-oxoetilaO composto do Exemplo 558 (500 mg, 0,87 mmol), anisol(376 mg, 3,48 mmol) e ácido trifluorometanossulfônico (2 ml) foram dissolvidos em ácido trifluoroacético (9 ml), e a mistura foi agitada a 80°C durante 2 h. Após resfriar à temperatura ambiente, a mistura foi concentrada sob pressão reduzida. O resíduo foi diluído com solução aquosa saturada de hidrogenocarbonato de sódio, e extraído com THF-acetato de etila. O extrato foi concentrado dando 3-metóxi-1-metil-4-oxo-N-piperidin-4-il-4,5-diidro- 1H-pirrol[3,2-c]quinolina-2-carboxamida (1,10 g) como um sólido bege.
[002029] A uma solução de 3-metóxi-1-metil-4-oxo-N-piperidin-4-il- 4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamida (300 mg, 0,87 mmol) e trietilamina (88 mg, 0,87 mmol) em THF (30 ml) adicionou-se cloreto de acetoxiacetila (119 mg, 0,87 mmol) sob resfriamento com gelo, e a mistura foi agitada durante 2 h. A mistura de reação foi diluída com solução aquosa saturada de hidrogenocarbonato de sódio, e extraída com acetato de etila. O extrato foi secado sobre sulfato de magnésio e concentrado. O sólido obtido foi lavado com éter de dietila-hexano dando o composto titular (221 mg, 56 %) como um sólido branco.
[002030] RMN 1H (300 MHz, DMSO-d6) δ:1,30-1,65 (2H, m), 1,802,00 (2H, m), 2,09 (3H, s), 2,90 (2H, t, J = 11,4 Hz), 3,19 (2H, t, J = 11,4 Hz), 3,70 (2H, d, J = 13,5 Hz), 4,02-4,19 (4H, m), 4,28 (3H, s), 7,22 (1H, t, J = 7,5 Hz), 7,40-7,48 (2H, m), 7,93 (1H, d, J = 7,5 Hz), 8,24 (1H, d, J = 8,4 Hz), 11,34 (1H, s).Exemplo 673
[002031] Produção de 4-({[8-fluoro-3-metóxi-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidrotieno[3,2-c]quinolin-2-il]carbonil}amina)piperidina-1-carboxilato de t-butilaDa mesma maneira que no Exemplo 25, o composto titular (486 mg, 84 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 116 (400 mg, 0,97 mmol) e 4-aminapiperidina-1- carboxilato de t-butila (234 mg, 1,2 mmol).
[002032] RMN 1H (300 MHz, CDCl3) δ:1,40-1,53 (11H, m), 1,96-2,11 (2H, m), 2,92-3,10 (2H, m), 3,95-4,08 (2H, m), 4,10-4,24 (4H, m), 5,85 (2H, s), 6,99 (1H, dd, J = 9,3, 4,3 Hz), 7,15-7,25 (1H, m), 7,50-7,62 (4H, m), 7,65-7,74 (1H, m), 8,05-8,16 (2H, m).Exemplo 674
[002033] Produção de 4-({[8-fluoro-3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}amina) piperidina- 1-carboxilato de t-butilaDa mesma maneira que no Exemplo 25, o composto titular (2,5 g, 87 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 119 (2,0 g, 4,9 mmol) e 4-aminapiperidina-1- carboxilato de t-butila (1,2 g, 5,9 mmol).
[002034] RMN 1H (300 MHz, CDCl3) δ:1,34-1,53 (11H, m), 1,89-2,13 (2H, m), 2,94-3,14 (2H, m), 3,89-4,07 (2H, m), 4,08-4,24 (4H, m), 4,46 (3H, s), 5,87 (2H, s), 6,93-7,04 (1H, m), 7,08-7,21 (1H, m), 7,48-7,60 (2H, m), 7,62-7,75 (2H, m), 7,94 (1H, dd, J = 10,0, 2,8 Hz), 8,04-8,20 (2H, m).Exemplo 675
[002035] Produção de cloridrato de 8-fluoro-3-metóxi-1-metil-4-oxo-5- (2-oxo-2-feniletil)-N-piperidin-4-il-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaDa mesma maneira que no Exemplo 542, o composto titular (1,6 g, 72 %) foi obtido como um sólido amarelo claro a partir do composto do Exemplo 674 (2,5 g, 4,3 mmol).
[002036] RMN 1H (300 MHz, DMSO-d6) δ:1,62-1,86 (2H, m), 1,962,13 (2H, m), 2,95-3,14 (2H, m), 3,21-3,47 (2H, m), 3,95 (3H, s), 4,02-4,18 (1H, m), 4,27 (3H, s), 5,98 (2H, s), 7,23-7,51 (2H, m), 7,57-7,68 (2H, m), 7,71-7,84 (1H, m), 8,04-8,26 (4H, m), 8,64 (2H, br s).Exemplo 676
[002037] Produção de acetato de 2-[4-({[8-fluoro-3-metóxi-1-metil-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil} amina)piperidin-1-il]-2-oxoetilaDa mesma maneira que no Exemplo 544, o composto titular (293 mg, 87 %) foi obtido como um sólido branco a partir do composto do Exemplo 675 (300 mg, 0,57 mmol).
[002038] RMN 1H (300 MHz, DMSO-d6) δ:1,30-1,65 (2H, m), 1,821,96 (2H, m), 2,08 (3H, s), 2,80-2,96 (1H, m), 3,08-3,26 (1H, m), 3,65-3,78 (1H, m), 3,96 (3H, s), 4,02-4,22 (2H, m), 4,30 (3H, s), 4,74-4,85 (2H, m), 5,97 (2H, s), 7,29-7,50 (2H, m), 7,57-7,68 (2H, m), 7,72-7,81 (1H, m), 7,988,06 (1H, m), 8,07-8,21 (3H, m).Exemplo 677
[002039] Produção de N-(1-benzil-3-metilpiperidin-4-il)-3-metóxi-1- metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaA uma solução de 1-benzil-3-metilpiperidin-4-ona (227 mg, 1,1 mmol) e acetato de amônio (861 mg, 11 mmol) em metanol (9,0 ml) adicionou-se triacetoxiboroidreto de sódio (750 mg, 3,5 mol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 2 h. A mistura de reação foi diluída com acetato de etila, lavada com solução de hidróxido de sódio 1N, e a camada aquosa foi extraída duas vezes com acetato de etila. Os extratos foram combinados, secados sobre sulfato de magnésio, e concentrados sob pressão reduzida. A uma solução do resíduo, o composto do Exemplo de Referência 28 (396 mg, 1,0 mmol) e HOBt (151 mg, 1,1 mol) em DMF (7,0 ml) adicionou-se WSCD (215 mg, 1,1 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 15 h. A mistura de reação foi diluída com solução saturada de hidrogenocarbonato de sódio, e extraída duas vezes com acetato de etila. O extrato foi combinado, lavado com salmoura, secado sobre sulfato de magnésio, e passado através de um gel de aminassílica. O filtrado foi concentrado sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; acetato de etila/hexano=30/70 - 100/0) e recristalizar de acetato de etila- hexano dando o composto titular (373 mg, 64 %) como um sólido branco.
[002040] RMN 1H (300 MHz, DMSO-d6) δ:0,83-1,01 (3H, m), 1,492,40 (5H, m), 2,56-2,89 (1H, m), 3,22-3,59 (3H, m), 3,94-4,04 (3H, m), 4,074,20 (1H, m), 4,25-4,41 (3H, m), 5,98 (2H, s), 7,16-7,42 (7H, m), 7,43-7,54 (1H, m), 7,58-7,69 (2H, m), 7,72-7,81 (1H, m), 7,82-7,94 (1H, m), 8,10-8,23 (2H, m), 8,28-8,45 (1H, m).Exemplo 678
[002041] Produção de 3-metóxi-1-metil-N-(3-metilpiperidin-4-il)-4- oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamidaA uma solução do composto do Exemplo 677 (373 mg, 0,65 mmol) em THF (40 ml) adicionou-se cloroformiato de 1-cloroetila (0,67 ml, 6,5 mol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 3 h. Adicionou-se cloroformiato de 1-cloroetila (0,67 ml, 6,5 mol) e diisopropiletilamina (0,30 ml, 3,2 mmol) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente durante 20 h. A mistura de reação foi concentrada sob pressão reduzida, e o resíduo foi lavado com éter de dietila. O resíduo foi dissolvido em metanol (50 ml), e a mistura foi agitada à temperatura ambiente durante 7 h e concentrada sob pressão reduzida. O resíduo foi purificado por meio de cromatografia em gel de aminassílica (eluado; metanol/acetato de etila=0/100 - 10/90) e recristalizado de acetato de etila-hexano dando o composto titular (90 mg, 29 %) como um sólido castanho claro.
[002042] RMN 1H (300 MHz, DMSO-d6) δ:0,83-0,95 (3H, m), 1,212,35 (5H, m), 2,60-3,01 (3H, m), 3,94-4,08 (3H, m), 4,11-4,22 (1H, m), 4,264,41 (3H, m), 5,98 (2H, s), 7,22-7,42 (2H, m), 7,43-7,53 (1H, m), 7,59-7,69 (2H, m), 7,71-8,00 (2H, m), 8,12-8,22 (2H, m), 8,32-8,45 (1H, m).Exemplo 679
[002043] Produção de (1-{[3-metóxi-1-metil-4-oxo-5-(2-oxo-2- feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}piperidin-4-il) carbamato de t-butilaDa mesma maneira que no Exemplo 25, o composto titular (440 mg, 86 %) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 28 (350 mg, 0,90 mmol) e piperidin-4-ilcarbamato de t-butila (198 mg, 0,99 mmol).
[002044] RMN 1H (300 MHz, DMSO-d6) δ:1,25-1,51 (11H, m), 1,681,94 (2H, m), 2,91-3,07 (1H, m), 3,10-3,27 (1H, m), 3,47-3,65 (1H, m), 3,67- 3,82 (1H, m), 3,88 (3H, s), 3,95-4,06 (3H, m), 4,29-4,48 ( 1H, m), 5,97 (2H, s), 6,93 (1H, d, J = 6,2 Hz), 7,24-7,51 (3H, m), 7,57-7,69 (2H, m), 7,70-7,83 (1H, m), 8,11-8,23 (2H, m), 8,32 (1H, dd, J = 8,3, 1,1 Hz).Exemplo 680
[002045] Produção de 4-{[3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)- 4,5-diidro-1H-pirrol[3,2-c]quinolin-2-il]carbonil}piperazina-1-carboxilato de t-butilaDa mesma maneira que no Exemplo 25, o composto titular (571 mg, quant.) foi obtido como um sólido branco a partir do composto do Exemplo de Referência 28 (400 mg, 1,0 mmol) e piperazina-1-carboxilato de t-butila (210 mg, 1,1 mmol).
[002046] RMN 1H (300 MHz, CDCl3) δ:1,49 (9H, s), 3,43-3,88 (8H, m),4,05 (3H, s), 4,08-4,12 (3H, m), 5,89 (2H, s), 7,01-7,10 (1H, m), 7,20-7,31 (1H, m), 7,35-7,44 (1H, m), 7,50-7,59 (2H, m), 7,62-7,71 (1H, m), 8,07-8,14 (2H, m), 8,20 (1H, dd, J = 8,2, 1,2 Hz).Exemplo 681
[002047] Produção de cloridrato de 3-metóxi-5-(4-metoxibenzil)-1- metil-4-oxo-N-piperidin-4-il-4,5-diidro-1H-pirrol[3,2-c]quinolina-2- carboxamidaA uma solução do composto do Exemplo 558 (500 mg, 0,87 mmol) em acetato de etila (15 ml) adicionou-se solução 4N cloreto de hidrogênio acetato de etila (5 ml), e a mistura foi agitada à temperatura ambiente durante 4 h. O precipitado foi recolhido por meio de filtração, lavado com éter de dietila, e seca sob pressão reduzida dando o composto titular (440 mg, 99 %) como um pó rosa claro.
[002048] RMN 1H (300 MHz, DMSO-d6) δ:1,78 (2H, q, J = 10,3 Hz), 2,05 (2H, d, J = 10,8 Hz), 3,06 (2H, t, J = 10,7 Hz), 3,26-3,33 (2H, m), 3,63 (3H, s), 4,02 (3H, s), 4,09-4,13 (1H, m), 4,24 (3H, s), 5,40-5,60 (2H, br), 6,86 (2H, d, J = 8,7 Hz), 7,14 (2H, d, J = 8,7 Hz), 7,25-7,30 (1H, m), 7,42-7,49 (2H, m), 8,15 (1H, d, J = 7,5 Hz), 8,33 (1H, d, J = 7,8 Hz), 8,60-8,90 (2H, br). Exemplo 682Produção de N-[1-(2-hidroxietil)piperidin-4-il]-3-metóxi-5-(4-metoxibenzil)- 1-metil-4-oxo-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamida Da mesma maneira que no Exemplo 79, o composto titular (1,91 g, 75 %) foi obtido como cristais brancos a partir do composto do Exemplo 681 (2,50 g, 4,89 mmol).
[002049] RMN 1H (300 MHz, DMSO-d6) δ:1,58 (2H, q, J = 9,9 Hz), 1,85 (2H, d, J = 9,6 Hz), 2,18 (2H, t, J = 9,9 Hz), 2,40 (2H, t, J = 6,3 Hz), 2,78 (2H, d, J = 11,4 Hz), 3,50 (2H, q, J = 6,0 Hz), 3,69 (3H, s), 3,70-3,85 (1H, br), 4,04 (3H, s), 4,29 (3H, s), 4,35-4,40 (1H, m), 5,40-5,65 (2H, br), 6,86 (2H, d, J = 8,7 Hz), 7,14 (2H, d, J = 8,4 Hz), 7,24-7,30 (1H, m), 7,42-7,49 (2H, m), 7,91 (1H, d, J = 7,8 Hz), 8,33 (1H, d, J = 8,1 Hz).Exemplo 683
[002050] Produção de N-[1-(2-hidroxietil)piperidin-4-il]-3-metóxi-1-metil-4-oxo-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamida Da mesma maneira que no Exemplo 672, o composto titular (457 mg, 33 %) foi obtido como cristais brancos a partir do composto do Exemplo 682 (1,79 g, 3,45 mmol).
[002051] RMN 1H (300 MHz, DMSO-d6) δ:1,50-1,60 (2H, m), 1,83 (2H, d, J = 10,2 Hz), 2,18 (2H, t, J = 10,4 Hz), 2,40 (2H, t, J = 6,3 Hz), 2,652,85 (2H, m), 3,50 (2H, q, J = 6,0 Hz), 3,75-3,90 (1H, m), 4,03 (3H, s), 4,29 (3H, s), 4,38 (1H, t, J = 5,4 Hz), 7,22 (1H, t, J = 7,5 Hz), 7,40-7,45 (2H, m), 7,84 (1H, d, J = 7,8 Hz), 8,24 (1H, d, J = 8,1 Hz), 11,33 (1H, s).Exemplo 684
[002052] Produção de 6-etil-N-[1-(hidroxiacetil)piperidin-4-il]-1-metil- 4-oxo-5-(2-oxo-2-feniletil)-3-(2,2,3,3-tetrafluoropropóxi)-4,5-diidro-1H- pirrol[3,2-c]piridina-2-carboxamidaDa mesma maneira que no Exemplo 140, o composto titular (224 mg, 74 %) foi obtido como um pó branco a partir do composto do Exemplo de Referência 175 (234 mg, 0,50 mmol).
[002053] RMN 1H (300 MHz, DMSO-d6) δ:1,19 (3H, t, J = 7,4 Hz), 1,48 (2H, m), 1,82-1,95 (2H, m), 2,58 (2H, q, J = 7,4 Hz), 2,70-2,89 (1H, m), 3,00-3,16 (1H, m), 3,62-3,78 (1H, m), 3,87 (3H, s), 3,96-4,15 (3H, m), 4,23-4,38 (1H, m), 4,53 (1H, t, J = 5,4 Hz), 4,94 (2H, t, J = 14,7 Hz), 5,63 (2H, s), 6,53 (1H, s), 6,66 (1H, tt, J = 52,0, 5,2 Hz), 7,52 (1H, d, J = 7,7 Hz), 7,57-7,66 (2H, m), 7,70-7,78 (1H, m), 8,08-8,16 (2H, m).Exemplo 685
[002054] Produção de 3-(ciclopropilmetóxi)-6-etil-N-[1-(hidroxiacetil) piperidin-4-il]-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2- c]piridina-2-carboxamidaDa mesma maneira que no Exemplo 140, o composto titular (100 mg, 76 %) foi obtido como um pó incolor a partir do composto do Exemplo de Referência 177 (98 mg, 0,24 mmol).
[002055] RMN 1H (300MHz, DMSO-d6) δ:0,19-0,27 (2H, m), 0,46-0,55(2H, m), 1,06-1,20 (1H, m), 1,18 (3H, t, J = 7,4 Hz), 1,25-1,56 (2H, m), 1,842,00 (2H, m), 2,57 (2H, q, J = 7,3 Hz), 2,77-2,94 (1H, m), 3,04-3,20 (1H, m), 3,60-3,75 (1H, m), 3,91 (3H, s), 3,96-4,13 (3H, m), 4,17 (2H, d, J = 7,2 Hz), 4,20-4,32 (1H, m), 4,51 (1H, t, J = 5,5 Hz), 5,59 (2H, s), 6,48 (1H, s), 7,567,66 (2H, m), 7,69-7,81 (2H, m), 8,07-8,15 (2H, m).
[002056] Exemplo de Formulação 1
[002057] Um agente farmacêutico contendo o composto da presente invenção como um ingrediente ativo pode ser produzido, por exemplo, com base na composição a seguir.
[002058] 1. Cápsula (1) composto obtido no Exemplo 25 40 mg (2) lactose 70 mg (3) celulose microcristalina 9 mg (4) estearato de magnésio 1 mg 1 cápsula 120 mg(1), (2), (3) e 1/2 de (4) são misturados e granulados. A istoadiciona-se o resto de (4) e a quantidade total é envasada em uma cápsula degelatina.
[002059] 2. Tablete (1) composto obtido no Exemplo 25 40 mg (2) lactose 58 mg (3) amido de milho 18 mg (4) celulose microcristalina 3,5 mg (5) estearato de magnésio 0,5 mg 1 tablete 120 mg (1), (2), (3), 2/3 de (4) e 1/2 de (5) são misturados egranulados. A isto adiciona-se o resto de (4) e (5) e a mistura é formada por compressão dando um tablete.Exemplo de Formulação 2
[002060] O composto obtido no Exemplo 25 (50 mg) é dissolvido na água para injeção da Farmacopéia Japonesa (50 ml), e a água destilada para injeção da Farmacopéia Japonesa é adicionada a 100 ml. A solução é filtrada em condições estéreis, e 1 ml da solução é envasado em um frasco para injeção em condições estéreis e secado por congelamento e fechado hermeticamente.Exemplo Experimental
[002061] Métodos de operação genética descritos nos Exemplos Experimentais abaixo baseiam-se nos métodos descritos em um livro (Maniatis et al., Molecular Cloning, Cold Spring Harbor Laboratory, 1989), e o protocolo anexo do reagente.Exemplo Experimental 1. Construção do plasmídeo repórter de Gli
[002062] O plasmídeo repórter de Gli foi construído inserindo-se 8 x sítio de ligação de Gli e promotor cristalino δ de frango a montante do luc+ de pGL3 (Promega).
[002063] O promotor cristalino δ foi clonado com método de PCR usando-se, como um conjunto de iniciadores, DNAs sintéticos5’-GAAGATCTGCCAGCCCAGGCTCCGGGGC-3’ (SEQ ID NO: 1) 5’-CCCAAGCTTCTGCCCGCACAGCCCTGCTC-3’ (SEQ ID NO: 2) preparados com referência à sequência de bases descrita no acesso GenBank n° X02187, e DNA do genoma de frango (Clontech) como um modelo. A reação PCR foi realizada usando Pfu Turbo (Stratagene) e seguindo o protocolo anexo. O fragmento de 108 pares de bases obtido foi digerido com enzimas de restrição BglII e HindIII, e inserido no sítio BglII-HindIII do pGL3 dando plasmídeo pGL3/promotor ry δ.
[002064] Como sítio de ligação Gli 8 x, uma sequência contendo oito sequências consenso ligadas a Gli com 9 pares de bases (GACCACCCA) descrita por Yoon et al., J. Biol. Chem., vol. 273, páginas de 3496 a 3501 (1998) foi preparada a partir de DNA sintético. Ou seja, dois DNAs sintéticos, 5’-GGGGTACCGACCACCCAGACCACCCAGACCACCCACACCACCC AGACCACCCAGACCACCCAGACCACCCAGACCACCCAAGATCTTC- 3’ (SEQ ID NO: 3)5’-GAAGATCTTGGGTGGTCTGGGTGGTCTGGGTGGTCTGGGTGGTC TGGGTGGTGTGGGTGGTCTGGGTGGTCTGGGTGGTCGGTACCCC-3’ (SEQ ID NO: 4)foram tratados com calor a 95°C durante 2 minutos, e incubados a 37°C durante 1 h para recombinação dando um DNA de filamento duplo dos dois DNAs sintéticos indicados acima. O DNA de filamento duplo obtido foi digerido com enzimas de restrição BglII e KpnI, e o fragmento de DNA obtido foi inserido no sítio BglII-KpnI do pGL3/promotor cry δ para construir o plasmídeo pGL3/promotor cry δ, sítio de ligação de Gli 8 x, i.e., plasmídeo repórter de Gli.Exemplo Experimental 2. Construção do plasmídeo para expressão do fragmento Shh da ponta N de camundongo
[002065] Como um material para construção de plasmídeo para expressão do fragmento Shh da ponta N, clonou-se primeiramente cDNA de Shh de camundongo.
[002066] O cDNA de Shh de camundongo foi clonado por meio do método de PCR embutido usando cDNA de feto de mouse com 11 dias de vida (Clontech) como um modelo. A sequência de iniciador foi preparada com referência à sequência de bases descrita no acesso GenBank n° NM_009170.
[002067] Como o conjunto de iniciadores para a 1a PCR, usou-se 5’-CTGGGTGGGGATCGGAGACA-3’ (SEQ ID NO: 5) 5’-GCGCTTTCCCATCAGTTCCTTATT-3’ (SEQ ID NO: 6), e como o conjunto de iniciadores para a 2a PCR, usou-se 5’-GGGGTACCATGCTGCTGCTGCTGGCCA-3’ (SEQ IDNO: 7)5’-GCTCTAGATCAGCTGGACTTGACCGCCA-3’ (SEQ ID NO: 8).A reação PCR foi realizada usando Pfu Turbo (Stratagene) e de acordo com o protocolo anexo. O produto de PCR resultante foi clonado por meio de pcDNA3.1 (+) (Invitrogen), e a sequência de bases inserida foi confirmada.
[002068] Usando-se a sequência de cDNA de Shh de camundongo obtida como indicado acima como um modelo, uma sequência de cDNA parcial em que o códon de interrupção (TGA) foi adicionado à ponta 3’ da sequência de cDNA codificando da 1a à 198a sequência de aminoácidos de Shh de camundongo foi obtido por meio do método de PCR. Como o conjunto de iniciadores usou-se,5’-ATGCTGCTGCTGCTGGCCAG-3’ (SEQ ID NO: 9) 5’-TCAGCCGCCGGATTTGGCCG-3’ (SEQ ID NO: 10). Realizou-se reação PCR usando Pfu Turbo (Stratagene) e de acordo com o protocolo anexo. O produto de PCR obtido foi clonado por meio de pcDNA3.1 (+) (Invitrogen), e a sequência de bases inserida foi confirmada.
[002069] Da maneira indicada acima, construiu-se um plasmídeo para a expressão do fragmento Shh na ponta N de camundongo, pcDNA3.1/mShh-N. Exemplo Experimental 3. Produção de fragmento Shh na ponta N de camundongo de tipo recombinante
[002070] Células HEK293 foram desenvolvidas em meio D-MEM (Invitrogen) contendo 10 % de soro bovino fetal em um disco de 10 cm e introduziu-se pcDNA3.1/mShh-N nas células usando FuGENE6 (Roche Applied Science). Em seguida, as células HEK293 foram cultivadas em um incubador com gás de dióxido de carbono a 37°C durante 24 horas, e o meio foi substituído por meio D-MEM (Invitrogen) contendo 2 % de soro bovino fetal. Após cultivo durante 48 h obteve-se um sobrenadante de cultura contendo fragmento Shh na ponta N de camundongo de tipo recombinante, por meio de filtração usando um filtro (0,22 μM).Exemplo Experimental 4. Introdução de plasmídeo para expressão de Gli-1 e plasmídeo repórter em células NIH-3T3 e produção de células de expressão
[002071] Usando D-MEM (Invitrogen) contendo 10 % de soro bovino fetal, plasmídeo de expressão pcDNA3.1 e plasmídeo repórter Gli (pGL3/promotor cry δ, 8 x sítio de ligação de Gli) produzido por meio do método do Exemplo Experimental 1 foram introduzidos em células NIH-3T3 desenvolvidas em um disco de 10 cm por meio do uso de FuGENE6 (Roche Applied Science).
[002072] Após cultivo durante 24 h, as células foram recuperadas, suspensas em meio D-MEM contendo 10 % de soro bovino fetal e suplementado com Geneticina (Life Technologies Oriental, Inc.) a uma concentração final de 500 μg/ml, diluído a 104 células/ml, plaqueado em uma placa com 96 poços, e cultivado em um incubador com gás dióxido de carbono a 37°C dando linha de células transformada resistente a Geneticina.
[002073] A linha de células transformada obtida foi cultivada em uma placa de 96 poços, adicionou-se fragmento Shh na ponta N de camundongo obtido no Exemplo Experimental 3, e selecionou-se a célula repórter NIH- 3T3/Gli, que é uma linha de células capaz de indução da expressão de luciferase.Exemplo Experimental 5. Avaliação do composto
[002074] Células repórter NIH-3T3/Gli cultivadas em D-MEM (Invitrogen) contendo 10 % de soro bovino fetal foram plaqueadas em uma placa branca de 96 poços a 1x104 células/poço, e cultivadas de um dia para o outro em um incubador com gás dióxido de carbono a 37°C. O meio foi removido, adicionou-se um composto (50 μl) e sobrenadante de cultura de HEK293 expressando fragmento Shh na ponta N de camundongo (meio D- MEM contendo 2 % de soro bovino fetal, 50 μl), e as células foram cultivadas durante 48 h em um incubador com gás dióxido de carbono a 37°C. Adicionou-se Bright-Glo (Promega, 50 μl), e a mistura foi agitada, após o que a atividade de luciferase foi medida com EnVision (PerkinElmer). A taxa de inibição foi calculada com base na atividade de luciferase do controle sem adição do composto como sendo de 100. Os resultados são mostrados nas Tabelas abaixo. A concentração do composto e a taxa de inibição foram analisadas com PRISM3.00 (programa [software] da GraphPad), com base em que calculou-se o valor de IC50 (concentração de composto necessária para obter 50 % do valor máximo da taxa de inibição) do composto.
[002075] Valores de IC50 dos compostos dos Exemplos 2, 3, 9, 13, 16, 17, 22, 27, 32, 41, 43, 45, 48, 50, 51, 52, 53, 56, 69, 71, 73, 74, 79, 92, 102, 109 e 115 não foram maiores que 1 μM.Tabela 3
[002076] De acordo com a descrição em Sasaki, K. et al., (2006) Cancer Res. 66: 4215-4222, avaliou-se um efeito anti-tumor de um composto usando um modelo de transplante alogênico de meduloblastoma de camundongo. Para ser preciso, camundongo com gene mutante Patched 1 (nome da linhagem: Ptch1tm1Mps/J) foi adquirido do The Jackson Laboratory e camundongo com gene mutante p53 (nome da linhagem: P53N4-M, nomenclatura: B6.129-Trp53tm/BrdN4) foi adquirido da Taconic, e um camundongo de fenótipo Patched 1(+/-), p53(-/-) foi preparado por meio de acasalamento. O tecido tumoroso de meduloblastoma ocorreu espontaneamente no cerebelo de camundongo Patched 1(+/-), p53(-/-) com de 7 a 9 semanas de vida foi recolhido e transplantado subcutaneamente em um camundongo pelado (nome da linhagem: CAnN.Cg-Foxn1<nu>/CrlCrlj).
[002077] Realizou-se um teste anti-tumor usando um tumor passado por transplante subcutâneo. Uma massa de tumor foi isolada com um separador de células 40 μm (BD Biosciences, n° de catálogo 352340), uma suspensão de tumor foi preparadas com meio L-15 Leibovitz (GIBCO, n° de catálogo 11415-114) numa quantidade de 2 vezes relativamente ao peso da massa de tumor, misturada com uma quantidade equivalente de matrigel (BD Biosciences, n° de catálogo 356237), e transplantada subcutaneamente para um camundongo a 100 μl por sítio de transplante. Mediu-se o diâmetro do tumor após o transplante e, quando o tamanho do tumor atingiu de 150 - 250 mm3, iniciou-se o teste anti-tumor usando 5 camundongos por grupo.
[002078] O composto de teste foi preparado de forma a ser obter uma dose de 6,25 mg/kg com uma suspensão de metilcelulose a 0,5 % (Shin-Etsu Chemical Co., Ltd., n° de catálogo SM-100), e administrado oralmente duas vezes por dia durante 2 semanas. O tamanho do tumor foi calculado com base no diâmetro mais longo e diâmetro mais curto do tumor medidos com um calibre vernier eletrônico. Após o início do teste, o tamanho do tumor foi medido a cada 2 ou 3 dias e calculou-se a taxa de crescimento do tamanho do tumor. Um efeito inibidor do crescimento do tumor de 95 % ou acima foi confirmado em cada grupo de administração que recebeu composto de teste. A taxa de crescimento do tamanho do tumor proporcionada por cada composto de teste ao término do teste é mostrada na tabela a seguir.
[002079] A taxa de crescimento do tumor e os resultados de um teste de diferença significativa por meio da administração de cada composto de teste são mostrados na Tabela. A taxa de crescimento do tamanho do tumor (T/C) foi calculada de acordo com:
[002080] taxa de crescimento (T/C) = ((tamanho do tumor do grupo de administração de composto no término da administração)-(tamanho do tumor do grupo de administração de composto no início da administração))/((tamanho do tumor do grupo de controle no término da administração)-(tamanho do tumor do grupo de controle no início da administração))X100.Tabela 4Os resultados indicados acima confirmam que o composto da presente invenção mostra um efeito anti-tumor.
[002081] Como o composto da presente invenção mostra uma ação inibidora superior de Smo, é possível proporcionar um agente clinicamente útil para a profilaxia ou tratamento de doenças relacionadas com Smo (p. ex., câncer etc.). Adicionalmente, como o composto da presente invenção também é superior em termos de eficácia [] expressão, farmacocinética, solubilidade, interação com outros produtos farmacêuticos, segurança e estabilidade, ele é útil como agente farmacêutico.
[002082] Este pedido baseia-se nos pedidos números 2008-045134 e 2008-256755 depositados no Japão, cujos teores são incorporados aqui por referência.
Claims (11)
1.Composto, caracterizado pelo fato de que é representado pela fórmula (I’’’):sendo queX é O, S ou NR1, em que R1 é C1-C6 alquila, R2 écarbamoíla substituído com zero, um ou dois grupos selecionados de C1-C6 alquila, C3-C6 cicloalquila, C6-C10 arila, 3- pirrolidinila, e 4-piperidinila,em que a C1-C6 alquila e C3-C6 cicloalquila é não substituído ou substituído com um ou dois substituintes que podem ser iguais ou diferentes selecionados de halogênio, ciano, amino, C1-C6 alquilamina, di- C1-C6 alquilamina, di-C1-C6 alquilamina substituída com hidróxi, C1-C6 alcóxi-carbonila, hidróxi, di-C1-C6 alquil-carbamoíla, C1-C6 alcóxi-carbonila e C3-C6 cicloalquila, eem que o 3-pirrolidinila ou 4-piperidinila é não substituído ou é substituído com um substituinte selecionado de C1-C6 alquila não substituído, C1-C6 alquila substituído com um ou dois substituintes que podem ser iguais ou diferentes selecionados de C6-C10 arila e hidróxi, C1-C6 alquil-carbonila não substituído, C1-C6 alquil-carbonila substituído com um grupo selecionado de C1-C6 alquil-carbonilóxi e hidróxi, e C1-C6 alcóxi- carbonila; ou1-pirrolidinilcarbonila, 1-piperidilcarbonila, ou 1- homopiperazinilcarbonila, não substituído ou substituído com um de C1-C6 alquila não substituído; C1-C6 alquila substituído com amino; amino; N-(C1- C6 alquil)-N-(C1-C6 alquil-carbonil)amino; C1-C6 alquil-carbonila não substituído; C1-C6 alquil-carbonila substituído com um de hidróxi, C1-C6 alcóxi, amino e C1-C6 alquilamina;R3 é hidróxi não substituído ou hidróxi substituído com um de:C1-C6 alquila não substituído, C1-C6 alquila substituído com C1-C6 alcóxi, e C1-C6 alquila substituída com 1-3 átomos de halogênio;RAA1 é hidrogênio ou C1-C6 alquila;RAA2 é hidrogênio ou C1-C6 alquila;ou RAA1 e RAA2 estão ligados um ao outro para formar um anel arila ou heteroarila de 6 membros tendo um N como um heteroátomo, cujo arila ou heteroarila é não substituído ou substituído com um átomo de halogênio; eR4 é hidrogênio, C1-C6 alquila não substituído, ou C1-C6 alquila substituído com C3-C6 cicloalquila; C6-C10 arila não substituído; C6C10 arila substituído com 1 ou 2 C1-C6 alcóxi ou com 1, 2 ou 3 átomos de halogênio; C1-C6 alquil-carbonila; C6-C10 aril-carbonila não substituído ou substituído com 1 átomo de halogênio ou C1-C6 alcóxi; C1-C6 alcóxi- carbonila; C6-C10 aril-carbamoíla; C6-C10 arilóxi; ou carbóxi;ou um sal dos mesmos.
3.Composto de acordo com a reivindicação 2, caracterizado pelo fato de que X é O, S ou N(C1-6 alquila),R2 é carbamoíla apresentando opcionalmente substituinte(s),R3 é hidróxi opcionalmente apresentando C1-6 alquila apresentando opcionalmente substituinte(s),RA1 é hidrogênio ou um grupo C1-6 alquila,RA2 é hidrogênio ou um grupo C1-6 alquila, eR4 é hidrogênio ou C1-6 alquila apresentando opcionalmente substituinte(s).
4.Composto de acordo com a reivindicação 1, caracterizado pelo fato de que é representado pela fórmula (I’):sendo queX é O, S ou NR1, em que R1 é C1-C6 alquila,R2 é(A) carbamoíla não substituído;(B) carbamoíla substituído com um ou dois gruposselecionados de(1) C1-C6 alquila não substituído, ou C1-C6 alquilasubstituído com um ou dois substituintes que podem ser iguais ou diferentesselecionados de halogênio, ciano, amino, C1-C6 alquilamina, di-C1-C6alquilamina, di-C1-C6 alquilamina substituído com hidróxi, C1-C6 alcóxicarbonila, hidróxi, di-C1-C6 alquil-carbamoíla, C1-C6 alcóxi-carbonila, 1-pirrolidinilcarbonila, C1-C6 alcóxi-carbonila, C3-C6 cicloalquila nãosubstituído, C3-C6 cicloalquila substituído com hidróxi, C1-C6 alcóxi, C2-C6alquinila, C6-C10 arila não substituído, C6-C10 arila substituído com 1 ou 2 C1-C6 alcóxi, carbamoíla, C1-C6 alquil-carbonil-amina não substituído, e C1-C6alquil-carbonil-amino substituído com um de C1-C6 alquil-carbonil-óxi, C1-C6alcóxi, e hidróxi;(2) C3-C6 cicloalquila não substituído, 1,2,3,4-tetraidronaftalenila não substituído ou C3-C6 cicloalquila ou 1,2,3,4-tetraidronaftalenila substituído com um ou dois de amino, amino substituídocom C1-C6 alcóxi-carbonila, amino substituído com C1-C6 alquil-carbonila,amino substituído com C1-C6 alquil-carbonila substituído com um de hidróxie C1-C6 alquil-carbonilóxi, hidróxi, carbóxi, C1-C6 alcóxi-carbonila, C1-C6alquil-carbamoíla, C1-C6 alquil-carbamoíla substituido com um hidróxi, C1-C6alquila, C1-C6 alquila substituido com um hidróxi e C1-C6 alcóxicarbonilamina;(3) C6-C10 arila; e(4) 3-pirrolidinila não substituído, 4-piperidinila nãosubstituíd,o ou 3-pirrolidinila ou 4-piperidinila substituído com C1-C6 alquila;C1-C6 alquila substituído com 1-5 substituintes que podem ser iguais oudiferentes selecionados de C6-C10 arila, hidróxi e halogênio; C1-C6 alquilcarbonila; C1-C6 alquil-carbonila substituído com um de C1-C6 alquilcarbonilóxi, hidróxi, C1-C6 alcóxi, C1-C6 alquil-sulfonila e amino; C1-C6alcóxi-carbonila; oxo; C1-C6 alquil-carbamoíla; C1-C6 alquil-sulfonila; C6-C10arila não substituído; C6-C10 arila substituído com um de halogênio, ciano, eC1-C6 alquil-sulfonila; e C6-C10 arilóxi-carbonila;(C) 1-pirrolidinilcarbonila não substituído, 1-piperidilcarbonilanão substituído, ou 1-homopiperazinilcarbonila não substituído; ou(D) 1-pirrolidinilcarbonila, 1-piperidilcarbonila, ou 1-homopiperazinilcarbonila substituído com um grupo selecionado de C1-C6alquila; C1-C6 alquila substituído com um amino; C1-C6 alquila substituídocom um C1-C6 alcóxi; C1-C6 alquila substituído com um C6-C10 arila; amino;amino substituído com um C1-C6 alquil-carbonila; N-(C1-C6 alquil)-N-(C1-C6-alquil-carbonil)amino; C1-C6 alquil-carbonila; C1-C6 alquil-carbonilasubstituído com um de hidróxi, C1-C6 alcóxi, amino, C1-C6 alquilamino, diC1-C6 alquilamina, e C1-C6 alquil-carbonilóxi; C6-C10 arila; e oxo;R3 é hidróxi, ou hidróxi substituído com C1-C6 alquila nãosubstituído, C1-C6 alquila substituído com C1-C6 alcóxi, C1-C6 alquilasubstituído com C6-C10 arila, C1-C6 alquila substituído com 1-3 átomos dehalogênio;R4 é(A) hidrogênio;(B) C1-6 alquila não substituído;(C) C1-6 alquila substituído com um de C3-C6 cicloalquila, C6-C10 arila não substituído, C6-C10 arila substituído com C1-C6 alcóxi, C6-C10arila substituído com C1-C6 alcóxi tendo 1-3 átomos de halogênio; C6-C10arila com 1-3 átomos de halogéneo; C1-C6 alquil-carbonila; C6-C10 arilcarbamoíla; 2-piridinila não substituído; 2-piridinila substituído com 1 ou 2C1-C6 alquila, em que o C1-C6 alquila é não substituído ou substituído com 1-3 átomos de halogênio; C6-C10 arilóxi; carbóxi; ciano; C1-C6 alcóxi nãosubstituído; ou C1-C6 alcóxi substituído com C6-C10 arila; eem que o Anel B é ciclohexeno, benzeno não substituído,benzeno substituído com um halogênio e piridina;ou um sal dos mesmos.
5. Composto, caracterizado pelo fato de ser N-[1-(2-Hidroxietil)piperidin-4-il]-3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamida ou um sal do mesmo.
6. Composto, caracterizado pelo fato de ser N-[1-(Hidroxiacetil)piperidin-4-il]-3-metóxi-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]quinolina-2-carboxamida ou um sal do mesmo.
7. Composto, caracterizado pelo fato de ser 3-Etóxi-6-etil-N-[1-(hidroxiacetil)piperidin-4-il]-1-metil-4-oxo-5-(2-oxo-2-feniletil)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxamida ou um sal do mesmo.
8. Composto, caracterizado pelo fato de ser N-[1-(Hidroxiacetil)piperidin-4-il]-1,6-dimetil-4-oxo-5-(2-oxo-2-feniletil)-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxamida ou um saldo mesmo.
9. Composto, caracterizado pelo fato de ser 6-Etil-N-[1-(hidroxiacetil)piperidin-4-il]-1-metil-4-oxo-5-(2-oxo-2-feniletil)-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxamida ou um saldo mesmo.
10. Composto de acordo com a reivindicação 9, caracterizadopelo fato de ser 6-Etil-N-[1-(hidroxiacetil)piperidin-4-il]-1-metil-4-oxo-5-(2-oxo-2-feniletil)-3-(2,2,2-trifluoroetóxi)-4,5-diidro-1H-pirrol[3,2-c]piridina-2-carboxamida.
11. Uso do composto como definido na reivindicação 1, caracterizado pelo fato de que é para preparar um medicamento para o tratamento do câncer.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008045134 | 2008-02-26 | ||
| JP2008-045134 | 2008-02-26 | ||
| JP2008256755 | 2008-10-01 | ||
| JP2008-256755 | 2008-10-01 | ||
| PCT/JP2009/054007 WO2009107850A2 (en) | 2008-02-26 | 2009-02-25 | Fused heterocyclic derivative and use thereof |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI0908417A2 BRPI0908417A2 (pt) | 2020-08-18 |
| BRPI0908417B1 true BRPI0908417B1 (pt) | 2022-01-11 |
Family
ID=40905094
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0908417-7A BRPI0908417B1 (pt) | 2008-02-26 | 2009-02-25 | Composto, e, uso do composto |
Country Status (27)
| Country | Link |
|---|---|
| US (2) | US8217176B2 (pt) |
| EP (1) | EP2247588B1 (pt) |
| JP (2) | JP4719317B2 (pt) |
| KR (1) | KR101569949B1 (pt) |
| CN (1) | CN102015705B (pt) |
| AR (1) | AR070479A1 (pt) |
| AU (1) | AU2009217982B2 (pt) |
| BR (1) | BRPI0908417B1 (pt) |
| CA (1) | CA2716773C (pt) |
| CL (1) | CL2009000429A1 (pt) |
| CO (1) | CO6321277A2 (pt) |
| CR (1) | CR11661A (pt) |
| DO (1) | DOP2010000260A (pt) |
| EA (1) | EA020144B1 (pt) |
| EC (1) | ECSP10010496A (pt) |
| ES (1) | ES2586252T3 (pt) |
| GE (1) | GEP20125664B (pt) |
| IL (1) | IL207735A (pt) |
| JO (1) | JO3259B1 (pt) |
| MA (1) | MA32164B1 (pt) |
| MX (1) | MX2010009372A (pt) |
| MY (1) | MY150379A (pt) |
| NZ (1) | NZ587719A (pt) |
| PE (1) | PE20091556A1 (pt) |
| TW (1) | TWI480282B (pt) |
| WO (1) | WO2009107850A2 (pt) |
| ZA (1) | ZA201006063B (pt) |
Families Citing this family (27)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| MY150379A (en) * | 2008-02-26 | 2013-12-31 | Takeda Pharmaceutical | Fused heterocyclic derivative and use thereof |
| US20160016982A1 (en) | 2009-07-31 | 2016-01-21 | Thar Pharmaceuticals, Inc. | Crystallization method and bioavailability |
| US20120277238A1 (en) * | 2009-07-31 | 2012-11-01 | Shionogi & Co., Ltd | Pharmaceutical composition containing fused hetero-ring derivative |
| DK2459176T3 (en) | 2009-07-31 | 2017-12-04 | Gruenenthal Gmbh | Crystallization process and bioavailability |
| US9169279B2 (en) | 2009-07-31 | 2015-10-27 | Thar Pharmaceuticals, Inc. | Crystallization method and bioavailability |
| EP2471789B9 (en) * | 2009-08-26 | 2015-03-25 | Takeda Pharmaceutical Company Limited | Fused heterocyclic ring derivative and use thereof |
| EP2471793B1 (en) * | 2009-08-26 | 2016-10-05 | Takeda Pharmaceutical Company Limited | Fused heterocyclic ring derivative and use thereof |
| JP5599802B2 (ja) * | 2009-08-26 | 2014-10-01 | 武田薬品工業株式会社 | 縮合複素環誘導体およびその用途 |
| US8927718B2 (en) | 2009-08-26 | 2015-01-06 | Takeda Pharmaceutical Company Limited | Fused heterocyclic ring derivative and use thereof |
| US9340565B2 (en) | 2010-11-24 | 2016-05-17 | Thar Pharmaceuticals, Inc. | Crystalline forms |
| WO2012154731A1 (en) * | 2011-05-08 | 2012-11-15 | Vanderbilt University | Substituted 1h-pyrrolo[3,2-c]quinolin-4(5h)-one analogs as positive allosteric modulators of the muscarinic acetylcholine receptor m4 |
| US8975398B2 (en) | 2012-05-11 | 2015-03-10 | Abbvie Inc. | NAMPT inhibitors |
| ES2732445T3 (es) * | 2013-12-03 | 2019-11-22 | Celestra Life Science Llc | Diseño basado en la racionalidad de una terapia específica para el cáncer |
| JP6353031B2 (ja) | 2014-03-19 | 2018-07-04 | 株式会社東芝 | 電池用電極材料、非水電解質電池、電池パック及び車 |
| CN106459071A (zh) * | 2014-03-31 | 2017-02-22 | 波士顿生物技术公司 | 新的三环醌衍生物 |
| KR20180011843A (ko) | 2015-06-11 | 2018-02-02 | 바실리어 파마슈티카 인터내셔널 리미티드 | 유출-펌프 억제제 및 이의 치료적 용도 |
| AU2015101598A4 (en) * | 2015-09-17 | 2015-12-03 | Macau University Of Science And Technology | Novel ros1 inhibitor and its use |
| CN108884094B (zh) | 2016-02-01 | 2021-09-21 | 武田药品工业株式会社 | 共晶体 |
| US10195218B2 (en) | 2016-05-31 | 2019-02-05 | Grunenthal Gmbh | Crystallization method and bioavailability |
| JP7106563B2 (ja) | 2016-11-29 | 2022-07-26 | スミトモ ファーマ オンコロジー, インコーポレイテッド | ナフトフラン誘導体、その調製、および使用方法 |
| JP7091201B2 (ja) | 2018-09-14 | 2022-06-27 | 株式会社東芝 | 活物質、電極、二次電池、電池パック、及び車両 |
| RU2711968C1 (ru) * | 2018-11-22 | 2020-01-24 | федеральное государственное бюджетное образовательное учреждение высшего образования "Пермский национальный исследовательский политехнический университет" | Анальгезирующее средство |
| WO2020243745A1 (en) * | 2019-05-29 | 2020-12-03 | Nelum Corporation | Methods and uses for treating cancer |
| CN110172068A (zh) * | 2019-06-05 | 2019-08-27 | 河南龙湖生物技术有限公司 | 具有抗肿瘤活性的苯并噻唑类化合物及其制备方法和应用 |
| EP4173639A4 (en) | 2020-06-26 | 2024-03-13 | RaQualia Pharma Inc. | METHOD FOR SELECTING A CANCER PATIENT FOR WHICH COMBINATION THERAPY OF A RETINOID AND A CANCER TREATMENT AGENT WILL BE EFFECTIVE, AND COMBINATION DRUG OF A RETINOID AND A CANCER TREATMENT AGENT |
| CN113292477B (zh) * | 2021-06-01 | 2023-06-02 | 四川大学 | 一种铱催化的碳氢活化反应合成异吲哚-1-酮类化合物的方法 |
| CN113429422B (zh) * | 2021-07-26 | 2022-05-10 | 中国人民解放军军事科学院军事医学研究院 | 一种噻吩并喹诺酮类化合物及其制备方法和应用 |
Family Cites Families (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3012684B2 (ja) | 1989-12-08 | 2000-02-28 | 大日本製薬株式会社 | チエノキノリン誘導体、チエノナフチリジン誘導体およびそれらの塩 |
| WO1993013664A2 (en) | 1992-01-11 | 1993-07-22 | Schering Agrochemicals Limited | Biheterocyclic fungicidal compounds |
| FR2695126B1 (fr) * | 1992-08-27 | 1994-11-10 | Sanofi Elf | Dérivés d'acide thiényl ou pyrrolyl carboxyliques, leur préparation et médicaments les contenant. |
| JP3223289B2 (ja) | 1992-10-22 | 2001-10-29 | 東洋アルミニウム株式会社 | 肉類調理器具および肉類調理方法 |
| CA2333770A1 (en) | 1998-06-04 | 1999-12-09 | Abbott Laboratories | Cell adhesion-inhibiting antinflammatory compounds |
| WO2000075145A1 (en) | 1999-06-03 | 2000-12-14 | Abbott Laboratories | Cell adhesion-inhibiting antiinflammatory compounds |
| EP1217000A1 (en) | 2000-12-23 | 2002-06-26 | Aventis Pharma Deutschland GmbH | Inhibitors of factor Xa and factor VIIa |
| WO2003059884A1 (en) | 2001-12-21 | 2003-07-24 | X-Ceptor Therapeutics, Inc. | Modulators of lxr |
| AU2003265853A1 (en) | 2002-08-29 | 2004-03-19 | Curis, Inc. | Hedgehog antagonists, methods and uses related thereto |
| JP2006151810A (ja) * | 2002-12-26 | 2006-06-15 | Daiichi Asubio Pharma Co Ltd | ジヒドロチエノキノリン誘導体及びそれを含む細胞接着阻害剤 |
| US20050043346A1 (en) | 2003-08-08 | 2005-02-24 | Pharmacia Italia S.P.A. | Pyridylpyrrole derivatives active as kinase inhibitors |
| JPWO2005035516A1 (ja) | 2003-10-10 | 2006-12-21 | 小野薬品工業株式会社 | 新規縮合複素環化合物およびその用途 |
| EP1698335A4 (en) | 2003-12-26 | 2007-08-01 | Ono Pharmaceutical Co | AGENT FOR PREVENTING AND / OR TREATING DISEASES INVOLVING A MITOCHONDRIAL BENZODIAZEPINE RECEPTOR |
| BRPI0509745A (pt) | 2004-04-08 | 2007-09-25 | Topotarget As | compostos de difenil ox-indol-2-ona e seu uso no tratamento de cáncer |
| GB0420722D0 (en) | 2004-09-17 | 2004-10-20 | Addex Pharmaceuticals Sa | Novel allosteric modulators |
| MX2008002165A (es) | 2005-08-16 | 2008-04-29 | Irm Llc | Compuestos y composiciones como inhibidores de la proteina cinasa. |
| AR056560A1 (es) * | 2005-10-06 | 2007-10-10 | Astrazeneca Ab | Pirrolopiridinonas como moduladores cb1 |
| MX2008009557A (es) * | 2006-01-27 | 2009-01-07 | Shanghai Hengrui Pharm Co Ltd | Inhibidores de la cinasa de proteina de la pirrolo [3,2-c] piridin-4-ona-2-indolinona. |
| EP2010170A2 (en) * | 2006-04-14 | 2009-01-07 | Novartis AG | Use of biarylcarboxamides in the treatment of hedgehog pathway-related disorders |
| CN101679308B (zh) * | 2007-03-14 | 2014-05-07 | 埃克塞里艾克西斯公司 | Hedgehog途径抑制剂 |
| PE20090188A1 (es) * | 2007-03-15 | 2009-03-20 | Novartis Ag | Compuestos heterociclicos como moduladores de la senda de hedgehog |
| MY150379A (en) | 2008-02-26 | 2013-12-31 | Takeda Pharmaceutical | Fused heterocyclic derivative and use thereof |
-
2009
- 2009-02-25 MY MYPI2010004006A patent/MY150379A/en unknown
- 2009-02-25 ES ES09714922.3T patent/ES2586252T3/es active Active
- 2009-02-25 GE GEAP200911952A patent/GEP20125664B/en unknown
- 2009-02-25 JO JOP/2009/0079A patent/JO3259B1/ar active
- 2009-02-25 US US12/392,640 patent/US8217176B2/en active Active
- 2009-02-25 NZ NZ587719A patent/NZ587719A/en unknown
- 2009-02-25 BR BRPI0908417-7A patent/BRPI0908417B1/pt active IP Right Grant
- 2009-02-25 AU AU2009217982A patent/AU2009217982B2/en active Active
- 2009-02-25 CL CL2009000429A patent/CL2009000429A1/es unknown
- 2009-02-25 CN CN2009801148111A patent/CN102015705B/zh active Active
- 2009-02-25 EA EA201070994A patent/EA020144B1/ru unknown
- 2009-02-25 TW TW098105923A patent/TWI480282B/zh active
- 2009-02-25 CA CA2716773A patent/CA2716773C/en active Active
- 2009-02-25 MX MX2010009372A patent/MX2010009372A/es active IP Right Grant
- 2009-02-25 EP EP09714922.3A patent/EP2247588B1/en active Active
- 2009-02-25 US US12/919,413 patent/US8399449B2/en active Active
- 2009-02-25 AR ARP090100644A patent/AR070479A1/es active IP Right Grant
- 2009-02-25 JP JP2010533355A patent/JP4719317B2/ja active Active
- 2009-02-25 WO PCT/JP2009/054007 patent/WO2009107850A2/en not_active Ceased
- 2009-02-25 KR KR1020107021331A patent/KR101569949B1/ko active Active
- 2009-02-25 PE PE2009000279A patent/PE20091556A1/es active IP Right Grant
-
2010
- 2010-08-22 IL IL207735A patent/IL207735A/en active IP Right Grant
- 2010-08-25 ZA ZA2010/06063A patent/ZA201006063B/en unknown
- 2010-08-26 DO DO2010000260A patent/DOP2010000260A/es unknown
- 2010-08-31 CR CR11661A patent/CR11661A/es unknown
- 2010-09-21 MA MA33195A patent/MA32164B1/fr unknown
- 2010-09-23 CO CO10117653A patent/CO6321277A2/es active IP Right Grant
- 2010-09-23 EC EC2010010496A patent/ECSP10010496A/es unknown
-
2011
- 2011-02-03 JP JP2011022188A patent/JP5490030B2/ja active Active
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4719317B2 (ja) | 縮合複素環誘導体およびその用途 | |
| EP2471791B1 (en) | Fused heterocyclic ring derivative and use thereof | |
| JP5659159B2 (ja) | 縮合複素環誘導体およびその用途 | |
| EP2471790B1 (en) | Fused heterocyclic ring derivative and use thereof | |
| UA101021C2 (uk) | Конденсована гетероциклічна похідна та її застосування | |
| HK1150274B (en) | Fused heterocyclic derivative and use thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] |
Free format text: DE ACORDO COM O ARTIGO 229-C DA LEI NO 10196/2001, QUE MODIFICOU A LEI NO 9279/96, A CONCESSAO DA PATENTE ESTA CONDICIONADA A ANUENCIA PREVIA DA ANVISA. CONSIDERANDO A APROVACAO DOS TERMOS DO PARECER NO 337/PGF/EA/2010, BEM COMO A PORTARIA INTERMINISTERIAL NO 1065 DE 24/05/2012, ENCAMINHA-SE O PRESENTE PEDIDO PARA AS PROVIDENCIAS CABIVEIS. |
|
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] | ||
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B350 | Update of information on the portal [chapter 15.35 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 25/02/2009, OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF, QUE DETERMINA A ALTERACAO DO PRAZO DE CONCESSAO. |