BRPI0909535A2 - "4-(3-alquilsulfinilbenzoil)pirazol da formula ou seu sal, composição herbicida, método de controle de plantas indesejadas, uso de um composto da fórmula e composto" - Google Patents
"4-(3-alquilsulfinilbenzoil)pirazol da formula ou seu sal, composição herbicida, método de controle de plantas indesejadas, uso de um composto da fórmula e composto" Download PDFInfo
- Publication number
- BRPI0909535A2 BRPI0909535A2 BRPI0909535-7A BRPI0909535A BRPI0909535A2 BR PI0909535 A2 BRPI0909535 A2 BR PI0909535A2 BR PI0909535 A BRPI0909535 A BR PI0909535A BR PI0909535 A2 BRPI0909535 A2 BR PI0909535A2
- Authority
- BR
- Brazil
- Prior art keywords
- och
- ome
- alkyl
- formula
- oet
- Prior art date
Links
- 0 C[n]1nc(*)c(C(c2c(*)c(S(*)=O)c(*)cc2)=O)c1O Chemical compound C[n]1nc(*)c(C(c2c(*)c(S(*)=O)c(*)cc2)=O)c1O 0.000 description 2
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C317/00—Sulfones; Sulfoxides
- C07C317/44—Sulfones; Sulfoxides having sulfone or sulfoxide groups and carboxyl groups bound to the same carbon skeleton
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/48—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with two nitrogen atoms as the only ring hetero atoms
- A01N43/56—1,2-Diazoles; Hydrogenated 1,2-diazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/02—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings
- C07D231/10—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D231/14—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D231/18—One oxygen or sulfur atom
- C07D231/20—One oxygen atom attached in position 3 or 5
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Dentistry (AREA)
- Plant Pathology (AREA)
- Environmental Sciences (AREA)
- Pest Control & Pesticides (AREA)
- Agronomy & Crop Science (AREA)
- General Chemical & Material Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Medicinal Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Urology & Nephrology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
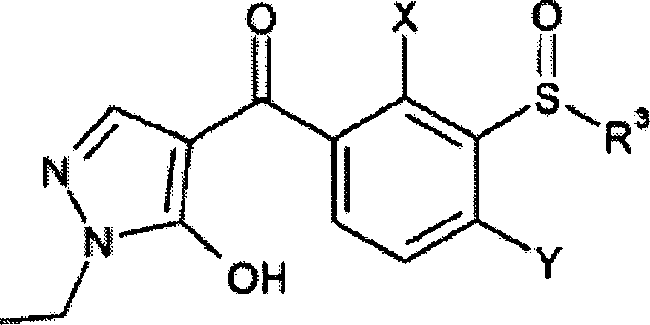
"4-(3-alquilsulfinilbenzoil)pirazol da formula ou seu sal, composição herbicida, método de controle de plantas indesejadas, uso de um composto da fórmula e composto" 4-(3-aiquilsulfinilbenzoil)pirazóis da fórmula (i) são descritos como herbicidas. nesta fórmula (1), r1 a r4 , x e y são radicais tais como hidrogênio, radicais orgânicos tais como alquila e outros radicais, tais como halogênio.
Description
“4-(3-ALQUILSULFINILBENZOIL)PIRAZOL, COMPOSIÇÃO HERBICIDA, MÉTODO DE CONTROLE DE PLANTAS INDESEJADAS, USO DE UM COMPOSTO DE FÓRMULA (I) OU DE UMA COMPOSIÇÃO HERBICIDA E COMPOSTO”
Campo Da Invenção
A presente invenção refere-se ao campo técnico dos herbicidas, particuíarmente ao campo dos herbicidas para o controle seletivo de folhas latifoliadas e plantas daninhas gramíneas em culturas de plantas úteis.
Antecedentes Da Invenção
Já foi descrito em diversas publicações que certos 4benzoilpirazóis substituídos por radicais que contêm enxofre na posição 3 do anel fenila possuem propriedades herbicidas. Desta forma, a patente EP 0.352.543 e o pedido de patente WO 97/41106 mencionam benzoilpirazóis que podem ser substituídos no anel fenila, entre outros, por um radical alquisulfinila. Os pedidos de patente WO 00/03993 e WO 2008/15179 descrevem, entre outros, 3-ciclopropil-4-(3alquilsulfinilbenzoil)pirazóis.
Entretanto, os compostos conhecidos a partir dessas publicações, frequentemente não exibem atividade herbicida suficiente. É, portanto, um objeto da presente invenção fornecer compostos ativos como herbicida alternativos.
Revelou-se agora que certos 4-benzoilpirazóis cujo anel fenila traz um radical alquilsulfinila na posição 3 são especialmente apropriados como herbicidas.
Descrição Da Invenção
A presente invenção refere-se a 4-(3alquílsulfinilbenzoil)pirazóis de fórmula (I) ou um sal do mesmo:
em que:
R1 é alquila (C1-C4);
R2 é hidrogênio ou alquila (C1-C4);
R3 é alquila (Ci-Cg);
R4 é hidrogênio, alquilsulfonila (Ci-Ce), alcóxi (C1-C4)alquilsulfonila (C-i-Ce), ou é fenilsulfonila, tiofenil-2-sulfonila, benzoíla, benzoilalquila (Ci-C6) ou benzila, cada um dos quais é substituído por m radicais idênticos ou diferentes a partir do grupo que consiste em halogênio, alquila (C1-C4) e alcóxi (C1-C4);
X é hidrogênio, mercapto, nitro, halogênio, ciano, tiocianato, alquila (Ci-Ce), haloalquila (Ci-Ce), alquenila (C2-Ce), haloalquenila (C2-C6), alquinila (C2-C6), haloalquinila (C3-C6), cicloalquila (C3-C6), OR5, OCOR5, OSO2R5, S(O)nR5, SO2OR5, SO2N(R5)2, NR5SO2R5, NR5COR5, alquila (CrC6)-S(O)nR5, alquila (Ci-C6)-OR5, alquila (CrCej-OCOR5, alquila (C^Ce)OSO2R5, alquila (CrC6)-SO2OR5, alquila (C1-C6)-SO2N(R5)2 ou alquila (C^Ce)NR5COR5;
Y é flúor, cloro, bromo, iodo, nitro ou o grupo SO2R7;
R5 é hidrogênio, alquila (Ci-C5), alquenila (C2-C6), alquinila (C2-C6), cicloalquila (C3-C6), fenila ou fenilalquila (Ci-C6), em que os seis radicais mencionados por último são substituídos por s radicais do grupo que consiste em hidróxi, mercapto, amino, ciano, nitro, tiocianato, OR6, SR6, N(R6)2, NOR6, OCOR6, SCOR6, NR6COR6, CO2R6, COSR6, CON(R6)2, alquilimino-óxi (C1-C4), alquilcarbonila (C1-C4), alcóxi (Ci-C4)-alcoxicarbonila (C2-Ce) e alquilsulfonila (C1-C4);
R6 é hidrogênio, alquila (Ci-C6), alquenila (C2-Ce) ou alquinila (C2-C6);
R7 é alquila (C1-C4);
m é 0, 1, 2, 3, 4 ou 5;
n é 0, 1 ou 2;
s é 0, 1,2 ou 3.
Na fórmula (I) e em todas as fórmulas fornecidas abaixo, radicais alquila que contêm mais de dois átomos de carbono podem possuir cadeia linear ou ramificada. Radicais alquila são, por exemplo, metila, etila, n ou ipropila, n, i, t ou 2-butila, pentilas e hexilas, tais como n-hexila, i-hexila e 1,3dimetilbutila. Halogênio é flúor, cloro, bromo ou iodo.
Caso um grupo seja polissubstituído por radicais, deve-se compreender isso como indicando que esse grupo é substituído por um ou mais dos radicais mencionados acima que são idênticos ou diferentes.
Devido ao centro de quiralidade do grupo sulfinila, os compostos de fórmula (I) estão presentes como enantiômeros. Além disso, dependendo da natureza dos substituintes e como eles são ligados, pode haver estereoisômeros adicionais, tal como no caso de átomos de carbono assimetricamente substituídos. Estereoisômeros, se já não forem obtidos em forma pura na síntese, podem ser obtidos a partir das misturas geradas no processo de preparação utilizando métodos de separação costumeiros, tais como métodos de separação cromatográfica. Igualmente, estereoisômeros podem ser preparados seletivamente, utilizando reações estéreo-seletivas e empregando materiais de partida e/ou auxiliares oticamente ativos. A presente invenção também se refere a todos os estereoisômeros e suas misturas que são englobados pela fórmula (I), mas não são especificamente definidos.
Dá-se preferência a compostos de fórmula (I), nos quais:
R1 é metila, etila, n-propila ou isopropila;
R2 é hidrogênio, metila, etila, n-propila ou isopropila;
R3 é alquila (C-1-C4);
R4 é hidrogênio, alquilsulfonila (C1-C3), alcóxi (C1-C2)alquilsulfonila (C1-C4) ou é fenilsulfonila, tiofenil-2-sulfonila, benzoíla, benzoilalquila (Ch-Ce) ou benzila, cada um dos quais são substituídos por m grupos metila;
X é nitro, halogênio, alquila (C1-C4), trifluorometila, alcóxi (C1-C4), metilsulfonila, metoximetila, metoximetoximetila, etoxietoximetila, etoximetoximetila, metoxietoximetila, metoxipropoximetila, metilsulfonilmetila, metilsulfoniletoximetila, metoxietilsulfonilmetila ou metilsulfoniletilsulfonilmetila;
Y é flúor, cloro, bromo, iodo ou o grupo SO2R7;
R7 é metila, etila, n-propila ou isopropila;
m é 0, 1, 2 ou 3.
Dá-se preferência específica a compostos de fórmula (I), nos quais:
R1 é metila ou etila;
R2 é hidrogênio, metila ou etila;
R3 é metila, etila, n-propila ou isopropila;
R4 é hidrogênio;
X é nitro, halogênio, alquila (C1-C4), trifluorometila, alcóxi (C1-C4), metilsulfonila, metoximetila, metoximetoximetila, etoxietoximetila, etoximetoximetila, metoxietoximetila, metoxipropoximetila, metilsulfonilmetila, metilsulfoniletoximetila, metoxietilsulfonilmetila ou metilsulfoniletilsulfonilmetila;
Y é flúor, cloro, bromo, iodo ou o grupo SO2R7;
R7 é metila ou etila.
A menos que definido em contrário, os substituintes e os símbolos em todas as fórmulas mencionadas abaixo possuem 0 mesmo significado descrito na fórmula (I).
Os compostos de acordo com a presente invenção nos quais
R4 é hidrogênio podem ser preparados, por exemplo, por meio do processo exibido no Esquema 1 e conhecido a partir do pedido de patente WO 5 2005/122768 por reação de um ácido benzoico de fórmula (II) com um pirazol de fórmula (III) na presença de um agente condensador tal como cloridrato de N-(3dimetilaminopropil)-N’-etilcarbodi-imida, seguido por redisposição catalisada por cianeto.
Esquema 1
(II) (III) (Ia)
Os compostos de fórmula (I) podem ser preparados, por exemplo, por meio do processo exibido no Esquema 2 e descrito no pedido de patente
WO 2005/122768 por meio da reação de um composto de fórmula (Ia) com compostos de fórmula (IV) em que E é um grupo residual nucleofílico. Esquema 2
(la) (IV) (I)
Os compostos de acordo com a presente invenção nos quais R4 é hidrogênio podem também ser preparados, por exemplo, por meio do processo exibido no Esquema 3 por meio de substituição aromática nucleofílica a partir de compostos de fórmula (V) em que L2 é, por exemplo, um átomo de flúor ou cloro utilizando um tiolato (VI) em que M é um cátion metálico, seguido por oxidação.
Esquema 3
2. Oxidação
Os compostos de fórmula (II) podem ser preparados, por exemplo, por meio do processo exibido no Esquema 4 a partir de ácidos benzoicos de 5 fórmula (VII) por meio de introdução do substituinte X, seguido por substituição aromática nucleofílica e oxidação em seguida. Reações apropriadas para introdução do substituinte X são conhecidas, por exemplo, por meio de J. Chem. Soc. Perkin Trans. 1 1995, pág. 1265 e seguintes, J. Heterocyclic Chem. 1999, 36, pág. 1453 e seguintes., Angew. Chem. 2005, 117, 380-398, J. Org. Chem. 2003, 10 68, 2030-2033 e J. Org. Chem. 1994, 59, 4042-4044.
Esquema 4 o
HO (VII)
HO (VIII) (IX) (II)
Os compostos de fórmula (II) são inovadores e também fazem parte do objeto da presente invenção.
Coleções de compostos de fórmula (I) e/ou seus sais que podem ser sintetizados de acordo com as reações mencionadas acima podem também ser preparadas de forma paralela, o que pode ser efetuado manualmente ou de forma total ou parcialmente automática. Neste ponto, é possível, por exemplo, automatizar o procedimento da reação, o trabalho ou a purificação dos produtos ou intermediários. No total, compreende-se que isso significa um procedimento conforme descrito, por exemplo, por D. Tiebes em Combinatorial Chemistry - Synthesis, Analysis, Screening (editor: Günther Jung), Wiley 1999, págs. 1 a 34.
Podem ser utilizados diversos aparelhos disponíveis comercialmente para o procedimento de reação paralela e trabalho, tais como blocos de reação Calpyso da Barnstead International, Dubuque, Iowa 520040797, Estados Unidos, ou amostras de reação da Radleys, Shirehill, Saffron Walden, Essex CB 11 3AZ, Inglaterra, ou Estações de Trabalho Automatizadas MultiPROBE da Perkin Elmer, Waltham, Massachusetts 02451, Estados Unidos. Aparelhos cromatográficos, tais como da ISCO, Inc., 4700 Superior Street, Lincoln NE 68504, Estados Unidos, são disponíveis, entre outros, para a purificação paralela de compostos de fórmula (I) e sais do mesmo ou intermediário gerado no transcurso da preparação.
Os aparelhos relacionados geram um procedimento modular no qual as passagens individuais são automatizadas, mas operações manuais devem ser conduzidas entre as passagens. Isso pode ser superado pelo uso de sistemas de automação total ou parcialmente integrados, em que os módulos de automação relevantes são operados, por exemplo, por robôs. Esses sistemas de automação podem ser obtidos, por exemplo, por meio da Caliper, Hopkinton MA 01748, Estados Unidos.
O desempenho de etapas de sínteses individuais ou de uma série delas pode ser auxiliado pelo uso de resinas extratoras e reagentes sustentados por polímero. A literatura especializada descreve uma série de protocolos experimentais, tais como em ChemFiles, vol. 4, n° 1, PolymerSupported Scavengers and Reagents for Solution-Phase Synthesis (SigmaAldrich).
Além dos métodos descritos no presente, a preparação de compostos de fórmula (I) e sais do mesmo pode ser efetuada, no todo ou em parte, por métodos sustentados por fase sólida. Com este propósito, intermediários individuais ou todos os intermediários da síntese ou de uma síntese adaptada ao procedimento relevante são ligados a uma resina de síntese. Métodos de síntese sustentada por fase sólida são descritos de forma suficiente na literatura especializada, tal como em Barry A. Bunin em The Combinatorial Index, Academic Press, 1998 e Combinatorial Chemistry Synthesis, Analysis, Screening (editor Günther Jung), Wiley, 1999. O uso de métodos de síntese sustentada por fase sólida permite novamente a condução manual ou automática de uma série de protocolos conhecidos na literatura. As reações podem ser conduzidas, por exemplo, por meio de tecnologia IRORI em microrreatores da Nexus Biosystems, 12140 Community Road, Poway CA 92064, Estados Unidos.
A condução de uma ou mais etapas de síntese, tanto sobre uma fase sólida quanto líquida, pode ser auxiliada pelo uso de tecnologia de microondas. Diversos protocolos experimentais são descritos na literatura especializada, tal como em Microwaves in Organic and Medicinal Chemistry (editores C. O. Kappe e A. Stadler), Wiley, 2005.
A preparação de acordo com os processos descritos no presente gera compostos de fórmula (I) e sais do mesmo na forma de coleções de substâncias, que são denominadas bibliotecas. A presente invenção também se refere a bibliotecas que compreendem pelo menos dois compostos de fórmula (I) e sais do mesmo.
Os compostos de fórmula (I) de acordo com a presente invenção (e/ou seus sais), denominados em conjunto a seguir “compostos de acordo com a presente invenção”, possuem atividade herbicida notável contra um amplo espectro de plantas daninhas anuais monocotiledôneas e dicotiledôneas de importância econômica. As substâncias ativas também agem eficientemente sobre plantas daninhas perenes que produzem brotos de rizomas, raízes ou outros órgãos perenes e que são de difícil controle.
A presente invenção também se refere, portanto, a um método de controle de plantas indesejadas ou regulagem do crescimento de plantas, preferencialmente em culturas de plantas, em que um ou mais compostos de acordo com a invenção é(são) aplicados às plantas (tais como plantas daninhas, como ervas monocotiledôneas ou dicotiledôneas, ou plantas de cultura indesejadas), às sementes (tais como grãos, sementes ou propágulos vegetais como tubérculos ou partes de brotos com botões) ou à área na qual as plantas crescem (tal como a área sob cultivo). Neste contexto, os compostos de acordo com a presente invenção podem ser aplicados, por exemplo, antes do plantio (se apropriado, também por meio de incorporação ao solo), antes da emergência ou após a emergência. Serão mencionados exemplos de representantes individuais da flora de ervas monocotiledôneas e dicotiledôneas que podem ser controladas pelos compostos de acordo com a presente invenção, sem que a menção destine-se a limitação a certas espécies.
Plantas daninhas monocotiledôneas dos gêneros: Aegilops, Agropyron, Agrostis, Alopecurus, Apera, Avena, Brachiaria, Bromus, Cenchrus, Commelina, Cynodon, Cyperus, Dactyloctenium, Digitaria, Echinochloa, Eleocharis, Eleusine, Eragrostis, Eriochloa, Festuca, Fimbristylis, Heteranthera, Imperata, Ischaemum, Leptochloa, Lolium, Monochoria, Panicum, Paspalum,
Phalaris, Phleum, Poa, Rottboellia, Sagittaria, Scirpus, Setaria, Sorghum.
Ervas dicotiledôneas dos gêneros: Abutilon, Amaranthus, Ambrosia, Anoda, Anthemis, Aphanes, Artemisia, Atriplex, Bellis, Bidens, Capsella, Carduus, Cassia, Centaurea, Chenopodium, Cirsium, Convolvulus, Datura, Desmodium, Emex, Erysimum, Euphorbia, Galeopsis, Galinsoga, Galium, Hibiscus, Ipomoea, Kochia, Lamium, Lepidium, Lindernia, Matricaria, Mentha, Mercurialis, Mullugo, Myosotis, Papaver, Pharbitis, Plantago, Polygonum, Portulaca, Ranunculus, Raphanus, Rorippa, Rotala, Rumex, Salsola, Senecio, Sesbania, Sida, Sinapis, Solanum, Sonchus, Sphenoclea, Stellaria, Taraxacum, Thlaspi, Trifolium, Urtica, Veronica, Viola, Xanthium.
Caso os compostos de acordo com a presente invenção sejam aplicados à superfície do solo antes da germinação, a emergência das mudas de ervas é completamente evitada ou as ervas crescem até que atinjam o estágio de cotilédone, mas suspendem em seguida o seu crescimento e, por fim, morrem completamente depois de decorridas três a quatro semanas.
Quando as substâncias ativas forem aplicadas após a emergência às partes de plantas verdes, o crescimento é suspenso após o tratamento e as plantas daninhas permanecem no estágio de crescimento a partir do momento da aplicação ou morrem completamente após certo período de tempo, de tal forma que a concorrência das ervas, que é prejudicial às plantas de cultura, seja eliminada precocemente e de forma sustentada.
Embora os compostos de acordo com a presente invenção exibam atividade herbicida notável contra ervas monocotiledôneas e dicotiledôneas, plantas de culturas economicamente importantes, tais como culturas dicotiledôneas dos gêneros Arachis, Beta, Brassica, Cucumis, Cucurbita, Helianthus, Daucus, Glycine, Gossypium, Ipomoea, Lactuca, Linum, Lycopersicon, Nicotiana, Phaseolus, Pisum, Solanum, Vicia ou culturas monocotiledôneas dos gêneros Allium, Ananas, Asparagus, Avena, Hordeum,
Oryza, Panicum, Saccharum, Secale, Sorghum, Triticale, Triticum, Zea, particularmente Zea e Triticum, são danificadas apenas até um ponto insignificante ou não são danificadas, dependendo da estrutura do composto correspondente de acordo com a presente invenção e sua taxa de aplicação. É por isso que os compostos do presente são altamente apropriados para o controle seletivo do crescimento de plantas indesejadas em culturas vegetais, tais como plantas úteis na agricultura ou plantas ornamentais.
Além disso, os compostos de acordo com a presente invenção (dependendo da sua estrutura correspondente e taxa de aplicação) possuem propriedades reguladoras do crescimento notáveis em plantas de culturas. Eles se concentram no metabolismo das plantas de forma reguladora e podem, portanto, ser empregados para influenciar, de forma dirigida, componentes vegetais e facilitar a colheita, por exemplo, acionando a dissecação e retardando o crescimento. Além disso, eles também são apropriados para controlar e inibir, de forma geral, o crescimento de plantas indesejadas sem destruir as plantas no processo. A inibição do crescimento vegetal desempenha um papel importante em muitas culturas monocotiledôneas e dicotiledôneas, pois o alojamento, por exemplo, pode ser reduzido ou completamente evitado pelo presente.
Devido às suas propriedades herbicidas e reguladoras do crescimento vegetal, as substâncias ativas podem também ser empregadas para controle de plantas daninhas em culturas de plantas geneticamente modificadas ou plantas que tenham sido modificadas por meio de mutagênese convencional. Via de regra, as plantas transgênicas são diferenciadas por propriedades especialmente vantajosas, tal como por meio da resistência a certos pesticidas, principalmente certos herbicidas, resistência a doenças das plantas ou organismos causadores de doenças das plantas, tais como certos insetos ou micro-organismos tais como fungos, bactérias ou vírus. Outras propriedades especiais referem-se, por exemplo, ao material colhido com relação à quantidade, qualidade, capacidade de armazenagem, composição e componentes específicos. Desta forma, são conhecidas plantas transgênicas com teor de amido mais alto ou qualidade de amido modificada, ou com uma composição de ácido graxo diferente do material colhido.
Prefere-se utilizar os compostos de acordo com a presente invenção ou seus sais em culturas transgênicas economicamente importantes de plantas úteis e ornamentais, tais como de cereais tais como trigo, cevada, centeio, aveia, sorgo, milho, arroz, mandioca, milho branco ou culturas de beterraba, algodão, soja, canola, batata, tomate, ervilhas e outros legumes. Prefere-se empregar os compostos de acordo com a presente invenção como herbicidas em culturas de plantas úteis que sejam resistentes ou tenham se tornado resistentes por meios recombinantes aos efeitos fitotóxicos dos herbicidas.
Meios convencionais de geração de plantas inovadoras que, em comparação com os métodos existentes, possuem propriedades modificadas são, por exemplo, métodos de cultivo tradicionais e a geração de mutantes. Alternativamente, plantas inovadoras com propriedades modificadas podem ser geradas com o auxílio de métodos recombinantes (vide, por exemplo, patentes EP-A-0221044 e EP-A-0131624). Os seguintes, por exemplo, foram descritos em diversos casos:
modificações recombinantes de plantas de culturas com o propósito de modificar o amido sintetizado nas plantas (tais como os pedidos de patente WO 92/11376, WO 92/14827 e WO 91/19806);
plantas de culturas transgênicas que são resistentes a certos herbicidas do tipo glufosinato (conforme, por exemplo, as patentes EPA-0242236 e EP-A-242246), do tipo glifosato (pedido de patente WO 92/00377) ou do tipo sulfonilureia (patentes EP-A-0257993 e US-A-5013659);
plantas de culturas transgênicas, tais como algodão, que são capazes de produzir toxinas de Bacillus thuringiensis (toxinas Bt), que tornam as plantas resistentes a certas pragas (patentes EP-A-0142924 e EP-A0193259);
plantas de culturas transgênicas com uma composição de ácido graxo modificado (pedido de patente WO 91/13972);
plantas de culturas geneticamente modificadas com componentes inovadores ou metabólitos secundários, tais como fitoalexinas inovadoras, que causam maior resistência à doença (patentes EPA 309862 e EPA 0464461);
plantas geneticamente modificadas com fotorrespiração reduzida que apresentam rendimentos mais altos e maior tolerância à tensão (patente EPA 0305398);
plantas de culturas transgênicas que produzem proteínas com importância farmacêutica ou em diagnóstico (“farmácias moleculares”);
plantas de culturas transgênicas que são diferenciadas por rendimentos mais altos ou melhor qualidade;
plantas de culturas transgênicas que são diferenciadas por uma combinação, por exemplo, das propriedades inovadoras mencionadas acima (“empilhamento genético”).
É conhecida, em princípio, uma grande quantidade de métodos de biologia molecular por meio dos quais podem ser geradas plantas transgênicas inovadoras com propriedades modificadas; vide, por exemplo, I. Potrykus e G. Spangenberg (Eds.), Gene Transfer to Plants, Springer Lab Manual (1995), Springer Verlag Berlin, Heidelberg ou Christou, Trends in Plant Science 1 (1996) 423-431.
Para conduzir essas manipulações recombinantes, é possível introduzir moléculas de ácido nucleico em plasmídeos, que permitem mutagênese ou modificação de sequências por meio de recombinação de sequências de DNA. Podem ser conduzidas, por exemplo, substituições base, sequências parciais podem ser removidas ou sequências naturais ou sintéticas podem ser adicionadas com o auxílio de métodos padrão. Para ligar os fragmentos de DNA entre si, é possível adicionar adaptadores ou ligantes aos fragmentos; vide, por exemplo, Sambrook et al, 1989, Molecular Cloning, A Laboratory Manual, segunda edição, Cold Spring Harbor Laboratory Press, Cold Spring Harbor NY; ou Winnacker, Gene und Klone, VCH Weinheim, segunda edição, 1996.
A geração de células vegetais com uma atividade reduzida para um produto genético pode ser atingida, por exemplo, por meio da expressão de pelo menos um RNA sem sentido correspondente, um RNA com sentido para atingir um efeito de cossupressão ou por meio da expressão de pelo menos uma ribozima construída de forma correspondente, que divide especificamente os transcritos do produto genético mencionado acima. Para fazê-lo, é possível, em primeiro lugar, utilizar moléculas de DNA que compreendem toda a sequência de codificação de um produto genético, incluindo quaisquer sequências laterais que possam estar presentes, ou moléculas de DNA que compreendem apenas partes da sequência de codificação, em que é necessário que essas partes sejam suficientemente longas para causar um efeito sem sentido nas células. Também é possível utilizar sequências de DNA que possuem um alto grau de homologia com as sequências de codificação de um produto genético, mas que não são totalmente idênticas.
Ao expressar moléculas de ácido nucléico em plantas, a proteína sintetizada pode estar localizada em qualquer compartimento da célula vegetal. A fim de atingir a localização em um compartimento específico, entretanto, é possível, por exemplo, ligar a região de codificação a sequências de DNA que garantam a localização em um compartimento específico. Essas sequências são conhecidas dos técnicos no assunto (vide, por exemplo, Braun et al, EMBO J. 11 (1992), 3219-3227; Wolter et al, Proc. Natl. Acad. Sei. U. S. A. 85 (1988), 846-850; Sonnewald et al, Plant J. 1 (1991), 95-106). As moléculas de ácidos nucleicos podem também ser expressas nas organelas das células vegetais.
As células de plantas transgênicas podem ser regeneradas por meio de métodos conhecidos para gerar plantas intactas. Em princípio, as plantas transgênicas podem ser plantas de qualquer espécie vegetal, ou seja, plantas monocotiledôneas e dicotiledôneas.
Desta forma, podem ser obtidas plantas transgênicas que apresentam propriedades modificadas como resultado da sobre-expressão, supressão ou inibição de sequências genéticas ou genes homólogos (= naturais) ou da expressão de sequências genéticas ou genes heterólogos (= exógenos).
Prefere-se empregar os compostos de acordo com a presente invenção em culturas transgênicas que sejam resistentes a reguladores do crescimento, tais como dicamba, ou contra herbicidas que inibem enzimas vegetais essenciais, tais como acetolactato sintases (ALS), EPSP sintases, glutamina sintases (GS) ou hidroxifenilpiruvato dioxigenases (HPPD), ou contra herbicidas do grupo das sulfonilureias, glifosato, glufosinato ou benzoilisoxazóis e substâncias ativas análogas.
Quando as substâncias ativas de acordo com a presente invenção forem utilizadas em plantas transgênicas, são frequentemente observados efeitos (além dos efeitos sobre plantas daninhas que podem ser observados em outras culturas) que são específicos para aplicação na cultura transgênica em questão, tal como um espectro modificado ou especificamente ampliado de ervas que podem ser controladas, taxas de aplicação modificadas que podem ser empregadas para aplicação, preferencialmente boa capacidade de combinação com os herbicidas aos quais a cultura transgênica é resistente e um efeito sobre o crescimento e o rendimento das plantas de culturas transgênicas.
A presente invenção também se refere, portanto, ao uso dos compostos de acordo com a presente invenção como herbicidas para o controle de plantas daninhas em plantas de culturas transgênicas.
Os compostos de acordo com a presente invenção podem ser empregados nas preparações costumeiras, na forma de pós molháveis, concentrados emulsionáveis, soluções pulverizáveis, pós ou grânulos. A presente invenção também se refere, portanto, a composições herbicidas e reguladoras do crescimento das plantas que compreendem os compostos de acordo com a presente invenção.
Os compostos de acordo com a presente invenção podem ser formulados de diversas maneiras, dependendo dos parâmetros biológicos e/ou físico-químicos vigentes. Exemplos de possíveis formulações são: pós molháveis (WP), pós hidrossolúveis (SP), concentrados hidrossolúveis, concentrados emulsionáveis (EC), emulsões (EW), tais como emulsões de óleo em água e água em óleo, soluções pulverizáveis, concentrados em suspensão (SC), dispersões com base em óleo ou água, soluções miscíveis em óleo, suspensões de cápsulas (CS), pós (DP), produtos de revestimento de sementes, grânulos para aplicação por meio de difusão e sobre o solo, grânulos (GR) na forma de microgrânulos, grânulos de pulverização, grânulos revestidos e grânulos de adsorção, grânulos dispersíveis em água (WG), grânulos hidrossolúveis (SG), formulações ULV, microcápsulas e ceras.
Esses tipos individuais de formulação são conhecidos em princípio e descritos, por exemplo, em: Winnacker-Küchler, Chemische Technologie [Tecnologia Química], volume 7, C. Hanser Verlag Munich, quarta edição, 1986; Wade van Valkenburg, Pesticide Formulations, Marcel Dekker, Nova Iorque, 1973; K. Martens, Spray Drying Handbook, terceira edição, 1979,
G. Goodwin Ltd., Londres.
Os auxiliares de formulação necessários, tais como materiais inertes, tensoativos, solventes e aditivos adicionais, também são conhecidos e descritos, por exemplo, em: Watkins, Handbook of Insecticide Dust Diluents and Carriers, segunda edição, Darland Books, Caldwell NJ, H. v. Olphen, Introduction to Clay Colloid Chemistry·, segunda edição, J. Wiley & Sons, Nova Iorque; C. Marsden, Solvents Guide; segunda edição, Interscience, Nova Iorque, 1963; McCutcheon's Detergents and Emulsifiers Annual, MC Publ. Corp., Ridgewood NJ; Sisley e Wood, Encyclopedia of Surface Active Agents, Chem. Publ. Co. Inc., Nova lorque, 1964; Schõnfeldt, Grenzflâchenaktive Ãthylenoxidaddukte [Adutos de Óxido de Etileno Ativos na Interface], Wiss. Verlagsgesell, Stuttgart 1976; Winnacker-Küchler, Chemische Technologie [Tecnologia Química], volume 7, C. Hanser Verlag Munich, quarta edição, 1986.
Com base nessas formulações, também é possível preparar combinações com outras substâncias ativas como pesticidas, tais como inseticidas, acaricidas, herbicidas, fungicidas e com agentes de segurança, fertilizantes e/ou reguladores do crescimento, tal como na forma de mistura pronta ou mistura de tanque.
Pós molháveis são preparações que são uniformemente dispersíveis em água e que, além da substância ativa, também compreendem tensoativos iônicos e/ou não iônicos (umectantes, dispersantes), tais como alquilfenóis polioxietilados, álcoois graxos polioxietilados, aminas graxas polioxietilados, poliglicol éter sulfatos de álcool graxo, alcanossulfonatos, alquilbenzenossulfonatos, lignossulfonato de sódio, 2,2’-dinaftilmetano-6,6’dissulfonato de sódio, dibutilnaftalenossulfonato de sódio ou oleoilmetiltaurinato de sódio, além de um diluente ou substância inerte. Para preparar os pós molháveis, as substâncias ativas como herbicidas são moídas finamente, tal como em aparelhos costumeiros como moinhos martelo, moinhos de sopro e moinhos a jato de ar, e misturadas com os auxiliares de formulação, seja simultânea ou subsequentemente.
Concentrados emulsionáveis são preparados por meio da dissolução da substância ativa em um solvente orgânico, tal como butanol, ciclo-hexanona, dimetilformamida, xileno ou aromáticos com ebulição mais alta, hidrocarbonetos ou misturas dos solventes orgânicos com adição de um ou mais tensoativos iônicos e/ou não iônicos (emulsificantes). Exemplos de emulsificantes que podem ser utilizados são: alquilarilsulfonatos de cálcio tais como dodecilbenzenossulfonato de cálcio ou emulsificantes não iônicos, tais como poliglicol ésteres de ácidos graxos, alquilarilpoliglicol éteres, poliglicol éteres de álcool graxo, condensados de óxido de propileno e óxido de etileno, alquil poliéteres, ésteres de sorbitano tais como ésteres de ácidos graxos de sorbitano ou polioxietileno ésteres de sorbitano, tais como polioxietileno ésteres de ácidos graxos de sorbitano.
Os pós são obtidos por meio de moagem da substância ativa com materiais sólidos finamente divididos, tais como talco, argilas naturais tais como caulim, bentonita e pirofilita, ou terra diatomácea.
Concentrados em suspensão podem ser com base em água ou óleo. Eles podem ser preparados, por exemplo, por meio de moagem úmida por moinhos de esferas disponíveis comercialmente, se apropriado com a adição de tensoativos conforme já relacionado acima, por exemplo, no caso dos outros tipos de formulação.
Emulsões, tais como emulsões de óleo em água (EW), podem ser preparadas, por exemplo, por meio de agitadores, moinhos coloidais e/ou misturadores estáticos utilizando solventes orgânicos aquosos e, se apropriado, tensoativos, conforme já mencionado acima, por exemplo, para os outros tipos de formulação.
Os grânulos podem ser preparados por meio de pulverização da substância ativa sobre material inerte granulado de adsorção ou por meio da aplicação de concentrados de substância ativa à superfície de veículos tais como areia, caulinitas ou material inerte granulado com auxílio de adesivos, tais como álcool polivinílico, poliacrilato de sódio ou outros óleos minerais. Substâncias ativas apropriadas podem também ser granuladas da forma que é costumeira para a produção de grânulos fertilizantes, se desejado, como uma mistura com fertilizantes.
Grânulos díspersíveis em água são geralmente preparados por meio de métodos costumeiros tais como secagem por pulverização, granulação de leito fluido, granulação de disco, mistura com agitadores em alta velocidade e extrusão sem material inerte sólido.
Para preparar grânulos de disco, grânulos de leito fluidificado, grânulos extrusores e grânulos de pulverização, vide, por exemplo, os métodos em Spray-Drying Handbook, terceira edição, 1979, G. Goodwin Ltd., Londres; J. E. Browning, Agglomeration, Chemical and Engineering 1967, págs. 147 e seguintes; Perry's Chemical Engineer's Handbook, quinta edição, McGraw-Hill, Nova lorque, 1973, págs. 8-57.
Para detalhes adicionais de produtos de proteção de culturas, vide, por exemplo, G. C. Klingman, Weed Control as a Science, John Wiley and Sons, Inc., Nova lorque, 1961, págs. 81-96 e J. D. Freyer, S. A. Evans, l/l/eed Control Handbook, quinta edição, Blackwell Scientific Publications, Oxford, 1968, págs. 101-103.
Via de regra, as preparações agroquímicas compreendem de 0,1 a 99% em peso, particularmente de 0,1 a 95% em peso, de compostos de acordo com a presente invenção.
Em pós molháveis, a concentração de substância ativa é, por exemplo, de cerca de 10 a 90% em peso, em que o restante até 100% é composto de componentes de formulação costumeiros. No caso de concentrados emulsionáveis, a concentração de substância ativa pode representar cerca de 1 a 90, preferencialmente de 5 a 80% em peso. Formulações na forma de pós compreendem de 1 a 30% em peso de substância ativa, preferencialmente, na maior parte dos casos, de 5 a 20% em peso de substância ativa e soluções pulverizáveis compreendem cerca de 0,05 a 80, preferencialmente de 2 a 50% em peso de substância ativa. No caso de grânulos dispersíveis em água, o teor de substância ativa depende, em parte, de se o composto ativo encontra-se em forma líquida ou sólida e dos auxiliares de granulação, cargas e similares que estão sendo utilizados. No caso dos grânulos dispersíveis em água, por exemplo, o teor de substância ativa é de 1 a 95% em peso, preferencialmente de 10 a 80% em peso.
Além disso, as formulações de substância ativa mencionadas compreendem, se apropriado, os auxiliares que são convencionais em cada caso, tais como adesivos, umectantes, dispersantes, ernulsificantes, penetrantes, conservantes, agentes anticongelamento, solventes, cargas, veículos, corantes, antiespumantes, inibidores da evaporação e reguladores do pH e da viscosidade.
Com base nessas formulações, também é possível preparar combinações com outras substâncias ativas como pesticidas, tais como inseticidas, acaricidas, herbicidas, fungicidas e com agentes de segurança, fertilizantes e/ou reguladores do crescimento, tal como na forma de mistura pronta ou mistura de tanque.
Substâncias ativas que podem ser empregadas em combinação com os compostos de acordo com a presente invenção em formulações misturadas ou na mistura de tanque são, por exemplo, substâncias ativas conhecidas que são baseadas na inibição de, por exemplo, acetolactato sintase, acetil-CoA carboxilase, celulose sintase, enolpiruvilshikimate-3-fosfato sintase, glutamina sintetase, p-hidroxifenilpiruvato dioxigenase, fitoen dessaturase, fotossistema I, fotossistema II, protoporfirinogênio oxidase, conforme descrito, por exemplo, em Weed Research 26 (1986) 441-445 ou The Pesticide Manual, 14a edição, The British Crop Protection Council e The Royal Society of Chemistry, 2003, e na literatura ali mencionada. Herbicidas ou reguladores do crescimento vegetal conhecidos que podem ser combinados com os compostos de acordo com a presente invenção são, por exemplo, as substâncias ativas a seguir (os compostos são designados pelo nome comum de acordo com a Organização Internacional de Padronização (ISO) ou por um nome químico, se apropriado, junto com o número de código) e sempre compreendem todas as formas de uso tais como ácidos, sais, ésteres e isômeros, tais como estereoisômeros e isômeros óticos. Neste contexto, uma e, em alguns casos, várias formas de uso são mencionadas como forma de exemplo.
Acetoclor, acibenzolar, acibenzolar-S-metil, acifluorfen, acifluorfen sódio, aclonifen, alaclor, alidoclor, aloxidim, aloxidim sódio, ametrina, amicarbazona, amidoclor, amidossulfuron, aminociclopiraclor, aminopiralid, amitrol, sulfamato de amônio, ancimidol, anilofós, asulam, atrazina, azafenidin, azimsulfuron, aziprotrina, BAH-043, BAS-140H, BAS-693H, BAS-714H, BAS762H, BAS-776H, BAS-800H, beflubutamid, benazolin, benazolinetil, bencarbazona, benfluralin, benfuresato, bensulida, bensulfuron metil, bentazona, benzofendizona, benzobiciclon, benzofenap, benzofluor, benzoilprop, bifenox, bilanafós, bilanafós-sódio, bispiribac, bispiribac sódio, bromacil, bromobutida, bromofenoxim, bromoxinil, bromuron, buminafós, busoxinona, butaclor, butafenacil, butamifós, butenaclor, butralin, butroxidim, butilato, cafenstrol, carbetamida, carfentrazona, carfentrazona etil, clometoxifen, cloramben, clorazifop, clorazifop butil, clorbromuron, clorbufam, clorfenac, clorfenac sódio, clorfenprop, clorflurenol, clorflurenol metil, cloridazon, clorimuron, clorimuron etil, cloreto de clormequat, clornitrofen, cloroftalim, clortaldimetil, clorotoluron, clorsulfuron, cinidon, cinidon etil, cinmetilin, cinossulfuron, cletodim, clodinafop, clodinafop propargil, clofencet, clomazone, clomeprop, cloprop, clopiralid, cloransulam, cloransulam metil, cumiluron, cianamida, cianazina, ciclanilida, cicloato, ciclossulfamuron, cicloxidim, cicluron, ci-halofop, ci-halofop butil, ciperquat, ciprazina, ciprazol, 2,4-D, 2,4-DB, daimuron/dimron, dalapon, daminozida, dazomet, n-decanol, desmedifam, desmetrin, detosilpirazolato (DTP), dialato, dicamba, diclobenil, diclorprop, diclorprop-P, diclofop, diclofopmetil, diclofop-P-metil, diclossulam, 10 dietatil, dietatiletil, difenoxuron, difenzoquat, diflufenican, diflufenzopir, diflufenzopir sódio, dimefuron, diquegulac sódio, dimefuron, dimepiperato, dimetaclor, dimetametrin, dimetenamid, dimetenamid-P, dimetipin, dimetrassulfuron, dinitramina, dinoseb, dinoterb, difenamid, dipropetrin, diquat, dibrometo de diquat, ditiopir, diuron, DNOC, eglinazinaetil, endotal, EPTC, 15 esprocarb, etalfluralin, etametsulfuron metil, etefon, etidimuron, etiozin, etofumesato, etoxifen, etoxifenetil, etoxissulfuron, etobenzanid, F-5331, ou seja, N-[2-cloro-4-fluoro-5-[4-(3-fluoropropil)-4,5-di-hidro-5-oxo-1H-tetrazol-1il]fenil]etanossulfonamida, fenoprop, fenoxaprop, fenoxaprop-P, fenoxaprop etil, fenoxaprop-P-etil, fentrazamida, fenuron, flamprop, flamprop-M-isopropil, flamprop-M-metil, flazassulfuron, florassulam, fluazifop, fluazifop-P, fluazifop butil, fluazifop-P-butil, fluazolato, flucarbazona, flucarbazona sódio, flucetossulfuron, flucloralin, flufenacet (tiafluamida), flufempir, flufempiretil, flumetralin, flumetsulam, flumiclorac, flumiclorac pentil, flumioxazin, flumipropin, fluometuron, fluorodifen, fluoroglicofen, fluoroglicofen etil, flupoxam, flupropacil, 25 flupropanato, flupirsulfuron, flupirsulfuron metilsódio, flurenol, flurenolbutil, fluridona, flurocloridona, fluroxipir, fluroxipir metil, flurprimidol, flurtamona, flutiacet, flutiacet metil, flutiamida, fomesafen, foramsulfuron, forclorfenuron, fosamina, furiloxifen, ácido giberélico, glufosinato, L-glufosinato, L-glufosinato probenazol, profluazol, prociazina, prodiamina, prifluralina, profoxidim, próhexadiona, pró-hexadiona cálcio, pró-hidrojasmona, prometon, prometrin, propaclor, propanil, propaquizafop, propazina, profam, propisoclor, propoxicarbazona, propoxicarbazona sódio, propizamida, prossulfalin, prossulfocarb, prosulfuron, prinaclor, piraclonil, piraflufen, piraflufen etil, pirassulfotole, pirazolinato (pirazolato), pirazossulfuron etil, pirazoxifen, piribambenz, piribambenz isopropil, piribenzoxim, piributicarb, piridafol, piridato, piriftalid, piriminobac, piriminobac metil, pirimissulfan, piritiobac, piritiobac sódio, piroxassulfona, piroxsulam, quinclorac, quinmerac, quinoclamina, quizalofop, 10 quizalofop etil, quizalofop-P, quizalofop-P-etil, quizalofop-P-tefuril, rimsulfuron, saflufenacil, secbumeton, setoxidim, siduron, simazina, simetrin, SN-106279, sulcotriona, sulf-alate (CDEC), sulfentrazona, sulfometuron, sulfometuron metil, sulfosato (glifosato trimésio), sulfossulfuron, SIN-523, SIP-249, SIP-298, SIP300, tebutam, tebutiuron, tecnazeno, tefuriltriona, tembotriona, tepraloxidim, 15 terbacil, terbucarb, terbuclor, terbumeton, terbutilazina, terbutrina, T-547, tenilclor, tiafluamida, tiazafluron, tiazopir, tidiazimin, tidiazuron, tiencarbazona, tiencarbazona metil, tifensulfuron, tifensulfuron metil, tiobencarb, tiocarbazil, topramezona, tralcoxidim, trialato, triassulfuron, triaziflam, triazofenamida, tribenuron, tribenuron metil, ácido tricloroacético (TCA), triclopir, tridifano, 20 trietazin, trifloxissulfuron, trifloxissulfuron sódio, trifluralin, triflusulfuron, triflusulfuron metil, trimeturon, trinexapac, trinexapac etil, tritossulfuron, tsitodef, uniconazol, uniconazol-P, vernolato, ZJ-0166, ZJ-0270, ZJ-0543, ZJ-0862 e os
amônio, glufosinato amônio, glifosato, glifosatoisopropil amônio, H-9201, halossafen, halossulfuron, halossulfuron metil, haloxifop, haloxifop-P, haloxifop etoxietil, haloxifop-P-etoxietil, haloxifop metil, haloxifop-P-metil, hexazinona, HNPC-9908, HOK-201, HW-02, imazametabenzo, imazametabenzometil, imazamox, imazapic, imazapir, imazaquin, imazetapir, imazossulfuron, inabenfida, indanofan, ácido indoloacético (IAA), ácido 4-indol-3-ilbutírico (IBA), iodossulfuron, iodossulfuron metilsódio, ioxinil, isocarbamid, isopropalin, isoproturon, isouron, isoxaben, isoxaclortol, isoxaflutol, isoxapirifop, KUH-043, KUH-071, carbutilato, cetospiradox, lactofen, lenacil, linuron, hidrazida maleica, MCPA, MCPB, MCPB-metil, etil e sódio, mecoprop, mecoprop sódio, mecoprop butotil, mecoprop-P-butotil, mecoprop-P-dimetilamônio, mecoprop-P-2-etil-hexil, mecoprop-P-potássio, mefenacet, mefluideto, cloreto de mepiquat, mesossulfuron, mesossulfuron metil, mesotriona, metabenzotiazuron, metam, metamifop, metamitron, metazaclor, metazol, metoxifenona, metildimron, 1-metilciclopropeno, isotiocianato de metila, metobenzuron, metobromuron, metolaclor, S-metolaclor, metossulam, metoxuron, metribuzin, metsulfuron, metsulfuron metil, molinato, monalida, monocarbamida, di-hidrogênio sulfato de monocarbamida, monolinuron, monossulfuron, monuron, MT 128, MT-5950, ou seja, N-[3-cloro-4-(1-metiletil)fenil]-2-metilpentanamida, NGGC-011, naproanilida, napropamida, naptalam, NC-310, ou seja, 4-(2,4-diclorobenzoil)1-metil-5-benziloxipirazol, neburon, nicosulfuron, nipiraclofen, nitralin, nitrofen, nitrofenolat sódio (mistura de isôrneros), nitrofluorfen, ácido nonanoico, norflurazon, orbencarb, ortossulfamuron, orízalin, oxadiargil, oxadiazon, oxassulfuron, oxaziclomefona, oxifluorfen, paclobutrazol, paraquat, dicloreto de paraquat, ácido pelargônico (ácido nonanoico), pendimetalin, pendralin, penoxsulam, pentanoclor, pentoxazona, perfluidona, petoxamid, fenissofam, fenmedifam, fenmedifam etil, picloram, picolinafen, pinoxaden, piperofós, pirifenop, pirifenop butil, pretilaclor, primissulfuron, primissulfuron metil,
Para uso, as formulações, que estão presentes em forma disponível comercialmente, se apropriado, são diluídas da forma costumeira, utilizando, por exemplo, água no caso de pós umectáveis, concentrados emulsionáveis, dispersões e grânulos dispersíveis em água. Preparações na 5 forma de pós, grânulos de solo, grânulos para difusão e soluções pulverizáveis normalmente não são novamente diluídas com sustâncias inertes adicionais antes do uso.
A taxa de aplicação necessária dos compostos de fórmula (I) varia em função das condições externas tais como temperatura, umidade, natureza do herbicida utilizado e similares. Ela pode variar dentro de amplos limites, tais como de 0,001 a 1,0 kg/ha e mais de substância ativa, mas é preferencialmente de 0,005 a 750 g/ha.
Os exemplos a seguir destinam-se a ilustrar a presente invenção.
A. Exemplos químicos:
1. Preparação de 4-(4-cloro-3-etilsulfinil-2-metilbenzoil)-5-hidróxi1 ,3-dimetilpirazol (n° 3-238 da Tabela 3):
Etapa 1: Síntese de 4-cloro-3-(dimetilaminotiocarbonilóxi)-2metilbenzoato de metila.
Sob atmosfera de nitrogênio, 12,3 g (109,7 mmol) de 1,4diazabiciclo[2.2.2]octano e, em seguida, 13,6 g (109,7 mmol) de cloreto de dimetilaminotiocarbonila foram adicionados a 11,0 g (54,8 mmol) de 4-cloro-3hidróxi-2-metilbenzoato de metila em 200 ml de Ν,Ν-dimetilformamida. A mistura foi agitada à temperatura ambiente (RT) por dezesseis horas e, para trabalho, despejada sobre água com gelo. O produto precipitou-se e foi removido por meio de filtragem. O resíduo foi lavado com 1 M HCI. Isso gerou
14,7 g de produto limpo.
Etapa 2: Síntese de 4-cloro-3-(dimetilaminocarboniltio)-2metilbenzoato de metila.
Sob atmosfera de nitrogênio, 12,1 g (42,0 mmol) de 4-cloro-3(dimetilaminotiocarbonilóxi)-2-metilbenzoato de metila em 30 ml de 1,3dimetoxibenzeno foram aquecidos a 220 °C por seis horas. Para trabalho, a mistura de reação foi resfriada e concentrada sob pressão reduzida. Após purificação cromatográfica do resíduo, foram isolados 5,2 g de produto limpo.
Etapa 3: Síntese de ácido 4-cloro-3-mercapto-2metilbenzoico.
6,61 g (85% em peso puro, 100,1 mmol) de hidróxido de potássio foram adicionados a 4,80 g (16,7 mmol) de 4-cloro-3-(dimetilaminocarboniltio)2-metilbenzoato de metila em 150 ml de metanol e a mistura foi agitada sob refluxo por dois dias. A mistura de reação foi liberada do solvente, adicionou-se água ao resíduo, a mistura foi acidificada com 1 M HCI e o sólido foi removido por meio de filtragem. Isso gerou 3,2 g de produto limpo.
Etapa 4: síntese de ácido 4-cloro-3-etiltio-2-metilbenzoico.
3,71 g (11,3 mmol) de carbonato de césio foram adicionados a 1,10 g (5,42 mmol) de ácido 4-cloro-3-mecapto-2-metilbenzoico em 20 ml de acetonitrila. A mistura de reação foi agitada à temperatura ambiente por dez minutos e 1,02 g (6,51 mmol) de iodoetano foram lentamente adicionados em gotas. A mistura de reação foi agitada em seguida à temperatura ambiente por dezesseis horas. O solvente foi removido em seguida e adicionou-se uma mistura de 20 ml de metanol e 2 ml de solução aquosa com resistência de 20% de hidróxido de sódio à mistura de reação. Para hidrólise do etil éster formado, a mistura foi agitada à temperatura ambiente por dezesseis horas e liberada em seguida dos solventes. O resíduo foi absorvido em água, acidificado com HCI diluído e a mistura foi agitada à temperatura ambiente por dez minutos e filtrada em seguida. O resíduo foi lavado com água e sugado seco. Foram isolados 1,15 g de produto limpo.
Etapa 5: síntese de ácido 4-cloro-3-etilsulfinil-2-metilbenzoico (n° 4-238)
1,15 g (4,98 mmol) de ácido 4-cloro-3-etiltio-2-metilbenzoico em 10 ml de ácido acético glacial foram aquecidos a uma temperatura de 50 °C a 60 °C. Sob essa temperatura, foram adicionados em gotas 484 mg (35% de resistência, 4,98 mmol) de uma solução aquosa de peróxido de hidrogênio. A mistura foi agitada a essa temperatura por cinco horas. A mistura de reação foi resfriada, lavada com uma solução aquosa saturada de bissulfito de sódio e, após prova analítica da ausência de peróxidos, liberada dos solventes. Adicionou-se água ao resíduo e a mistura foi acidificada com 6 M de HCI. A mistura foi extraída com acetato de etila e as fases orgânicas combinadas foram secas, filtradas e, sob pressão reduzida, liberadas do solvente. Foram isolados 1,24 g do produto (purificado a cerca de 95% em peso).
Etapa 6: síntese de 4-(4-cloro-3-etilsulfinil-2-metilbenzoil)5-h id róxi-1,3-dimetilpirazol.
128 mg (1,14 mmol) de 5-hidróxi-1,3-dimetilpirazol foram adicionados a 270 mg (95% de pureza em peso; 1,04 mmol) de ácido 4cloro-3-etilsulfinil-2-metilbenzoico em 20 ml de diclorometano (CH2CI2).
Foram adicionados 239 mg (1,24 mmol) de cloridrato de 1-(3'dimetilaminopropil)-3-etilcarbodi-imida e a mistura foi agitada à temperatura ambiente por dezesseis horas. Para trabalho, foram adicionados 3 ml de 1 M HCI e a fase orgânica foi liberada do solvente.
Foram adicionados 210 mg (2,07 mmol) de trietilamina, dez gotas de acetona ciano-hidrina e uma ponta de espátula de cianeto de potássio ao resíduo em 20 ml de acetonintrila. A mistura de reação foi agitada à temperatura ambiente por dezesseis horas e liberada do solvente em seguida. O resíduo foi agitado à temperatura ambiente com 25 ml de uma 10 mistura de solução aquosa saturada de bicarbonato de sódio e dietil éter por dez minutos. As fases foram separadas e a fase aquosa foi acidificada com HCI diluído e extraída em seguida com CH2CI2. A fase orgânica foi liberada do solvente e o resíduo foi purificado cromatograficamente em seguida. Isso gerou 100 mg de produto limpo.
2. Preparação de 5-hidróxi-1 -metil-4-(2-metil-3-metilsulfinil)-4IVIETILSULFONILBENZOIL)PIRAZOL (N° 1-9 DA TABELA 1):
Etapa 1: Síntese de ácido 2-metil-3-metilsulfinil-4metilsulfonilbenzoico (n° 4-9)
900 mg (3,45 mmol) de ácido 2-metil-4-metilsulfonil-320 metiltiobenzoico em 10 ml de ácido acético glacial foram aquecidos a uma temperatura de 50 °C a 60 °C. Sob essa temperatura, foram adicionados em gotas 336 mg (35% de resistência, 3,45 mmol) de uma solução aquosa de peróxido de hidrogênio. A mistura é agitada a 60 °C por cinco horas. A mistura de reação foi resfriada, lavada com uma solução aquosa de 25 bissulfito de sódio com 10% de resistência e, após prova analítica da ausência de peróxidos, liberada dos solventes. Adicionou-se água ao resíduo e a fase aquosa foi extraída por três vezes com acetato de etila. As fases orgânicas combinadas foram secas, filtradas e, sob pressão reduzida, liberadas do solvente. Foram isolados 950 mg de produto limpo.
Etapa 2: síntese de 5-hidróxi-1-metil-4-(2-metil-3metilsulfinil)-4-metilsulfonilbenzoil)pirazol.
mg (0,91 mmol) de 5-hidróxi-1-metilpirazol e uma ponta de espátula de 4-(dimetilamino)piridina foram adicionados a 230 mg (0,83 mmol) de ácido 2-metil-3-metilsulfinil-4-metilsulfonilbenzoico em 20 ml de CH2CI2. Foram adicionados 191 mg (0,99 mmol) de cloridrato de 1-(3’dimetilaminopropil)-3-etilcarbodi-imida e a mistura foi agitada à temperatura ambiente por noventa minutos. Foram adicionados em seguida 3 ml de 1 M HCI e a fase orgânica foi liberada do solvente. Foram adicionados 168 mg (1,66 mmol) de trietilamina, dez gotas de acetona ciano-hidrina e uma ponta de espátula de cianeto de potássio ao resíduo em 15 ml de acetonitrila. A mistura de reação foi agitada à temperatura ambiente por dezesseis horas e liberada do solvente em seguida. Foram adicionados 15 ml de CH2CI2 ao resíduo e, em seguida, foram adicionados 2 ml de 1 M HCI. Após a separação de fases, a fase orgânica foi liberada do solvente. O resíduo foi agitado com 25 ml de uma mistura de solução aquosa saturada de bicarbonato de sódio e dietil éter à temperatura ambiente por dez minutos. As fases foram separadas, a fase aquosa foi acidificada com HCI diluído e extraída em seguida por três vezes com CH2CI2. As fases orgânicas combinadas foram liberadas do solvente. Isso gerou 171 mg de produto limpo.
Os exemplos relacionados nas tabelas abaixo foram preparados de forma análoga aos métodos mencionados acima ou podem ser obtidos de forma análoga aos métodos mencionados acima. Estes compostos são mais especificamente preferidos.
As abreviações utilizadas são:
Et = Etila Me = metila Pr = propila Ph = fenila
Tabela 1
Compostos de Fórmula (I) de Acordo com a Presente Invenção em que R1 é
Metila e R2 e R4 são Hidrogênio
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-1 | Cl | Me | SO2Me | |
| 1-2 | Cl | Et | SO2Me | 8,23 (d, 1H), 7,66 (d, 1H), 7,32 (s, 1H), 3,92 (m, 1H), 3,73 (s, 3H), 3,45 (s, 3H), 3,28 (m, 1H), 1,53 (t, 3H) |
| 1-3 | Cl | n-Pr | SO2Me | |
| 1-4 | Cl | i-Pr | SO2Me | |
| 1-5 | Br | Me | SO2Me | |
| 1-6 | Br | Et | SO2Me | |
| 1-7 | Br | n-Pr | SO2Me | |
| 1-8 | Br | i-Pr | SO2Me | |
| 1-9 | Me | Me | SO2Me | 8,08 (d, 1H), 7,62 (d, 1H), 7,27 (s, 1H), 3,72 (s, 3H), 3,38 (s, 3H), 3,18 (s, 3H), 2,87 (s, 3H) |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-10 | Me | Et | SO2Me | 8,08 (d, 1H), 7,61 (d, 1H), 7,27 (s, 1H), 3,72 (s, 3H), 3,52 (m, 1H), 3,38 (s, 3H), 3,28 (m, 1H), 2,82 (s, 3H), 1,52 (t, 3H) |
| 1-11 | Me | n-Pr | SO2Me | |
| 1-12 | Me | i-Pr | SO2Me | |
| 1-13 | Et | Me | SO2Me | |
| 1-14 | Et | Et | SO2Me | |
| 1-15 | Et | n-Pr | SO2Me | |
| 1-16 | Et | i-Pr | SO2Me | |
| 1-17 | cf3 | Me | SO2Me | |
| 1-18 | cf3 | Et | SO2Me | |
| 1-19 | cf3 | n-Pr | SO2Me | |
| 1-20 | cf3 | i-Pr | SO2Me | |
| 1-21 | OMe | Me | SO2Me | |
| 1-22 | OMe | Et | SO2Me | |
| 1-23 | OMe | n-Pr | SO2Me | |
| 1-24 | OMe | i-Pr | SO2Me | |
| 1-25 | OEt | Me | SO2Me | |
| 1-26 | OEt | Et | SO2Me | |
| 1-27 | OEt | n-Pr | SO2Me | |
| 1-28 | OEt | i-Pr | SO2Me |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-29 | no2 | Me | SO2Me | |
| 1-30 | no2 | Et | SO2Me | |
| 1-31 | no2 | n-Pr | SO2Me | |
| 1-32 | no2 | i-Pr | SO2Me | |
| 1-33 | SO2Me | Me | SO2Me | |
| 1-34 | SO2Me | Et | SO2Me | |
| 1-35 | SO2Me | n-Pr | SO2Me | |
| 1-36 | SO2Me | i-Pr | SO2Me | |
| 1-37 | CH2OMe | Me | SO2Me | |
| 1-38 | CH2OMe | Et | SO2Me | |
| 1-39 | CH2OMe | n-Pr | SO2Me | |
| 1-40 | CH2OMe | i-Pr | SO2Me | |
| 1-41 | CH2SO2Me | Me | SO2Me | |
| 1-42 | CH2SO2Me | Et | SO2Me | |
| 1-43 | CH2SO2Me | n-Pr | SO2Me | |
| 1-44 | CH2SO2Me | i-Pr | SO2Me | |
| 1-45 | CH2OCH2CH2OMe | Me | SO2Me | 8,21 (d, 1H), 7,67 (d, 1H), 7,37 (s, 1H), 5,57 - 5,32 (br, signal, 1H), 5,00 (d, 1H), 3,72 (s, 3H), 3,63 - 3,58 (m, 1H), 3,56-3,50 (m, 1H), 3,42 - 3,25 (m, 2H), 3,37 (s, 3H), 3,32 (s, 3H), 3,23 (s, 3H) |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCl3] |
| 1-46 | CH2OCH2CH2OMe | Et | SO2Me | |
| 1-47 | CH2OCH2CH2OMe | n-Pr | SO2Me | |
| 1-48 | CH2OCH2CH2OMe | i-Pr | SO2Me | |
| 1-49 | CH2OCH2CH2OEt | Me | SO2Me | |
| 1-50 | CH2OCH2CH2OEt | Et | SO2Me | |
| 1-51 | CH2OCH2CH2OEt | n-Pr | SO2Me | |
| 1-52 | CH2OCH2CH2OEt | i-Pr | SO2Me | |
| 1-53 | CH2OCH2CH2CH2 OMe | Me | SO2Me | |
| 1-54 | CH2OCH2CH2CH2 OMe | Et | SO2Me | |
| 1-55 | CH2OCH2CH2CH2 OMe | n-Pr | SO2Me | |
| 1-56 | CH2OCH2CH2CH2 OMe | i-Pr | SO2Me | |
| 1-57 | CH2OCH2OMe | Me | SO2Me | |
| 1-58 | CH2OCH2OMe | Et | SO2Me | |
| 1-59 | CH2OCH2OMe | n-Pr | SO2Me | |
| 1-60 | CH2OCH2OMe | i-Pr | SO2Me | |
| 1-61 | CH2OCH2OEt | Me | SO2Me | |
| 1-62 | CH2OCH2OEt | Et | SO2Me | |
| 1-63 | CH2OCH2OEt | n-Pr | SO2Me | |
| 1-64 | CH2OCH2OEt | i-Pr | SO2Me | |
| 1-65 | CH2OCH2CH2SO2 Me | Me | SO2Me |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-66 | CH2OCH2CH2SO2 Me | Et | SO2Me | |
| 1-67 | CH2OCH2CH2SO2 Me | n-Pr | SC^Me | |
| 1-68 | CH2OCH2CH2SO2 Me | i-Pr | SO2Me | |
| 1-69 | CH2SO2CH2CH2O Me | Me | SO2Me | |
| 1-70 | CH2SO2CH2CH2O Me | Et | SC^Me | |
| 1-71 | CH2SO2CH2CH2O Me | n-Pr | SC^Me | |
| 1-72 | CH2SO2CH2CH2O Me | i-Pr | SO2Me | |
| 1-73 | CH2SO2CH2CH2S C^Me | Me | SO2Me | |
| 1-74 | CH2SO2CH2CH2S O2Me | Et | SO2Me | |
| 1-75 | CH2SO2CH2CH2S O2Me | n-Pr | SO2Me | |
| 1-76 | CH2SO2CH2CH2S C^Me | i-Pr | SO2Me | |
| 1-77 | Cl | Me | SO2Et | |
| 1-78 | Cl | Et | SO2Et | |
| 1-79 | Cl | n-Pr | SO2Et |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-80 | Cl | i-Pr | SO2Et | |
| 1-81 | Br | Me | SO2Et | |
| 1-82 | Br | Et | SO2Et | |
| 1-83 | Br | n-Pr | SO2Et | |
| 1-84 | Br | i-Pr | SO2Et | |
| 1-85 | Me | Me | SO2Et | |
| 1-86 | Me | Et | SO2Et | |
| 1-87 | Me | n-Pr | SO2Et | |
| 1-88 | Me | i-Pr | SO2Et | |
| 1-89 | Et | Me | SO2Et | |
| 1-90 | Et | Et | SO2Et | |
| 1-91 | Et | n-Pr | SO2Et | |
| 1-92 | Et | i-Pr | SO2Et | |
| 1-93 | cf3 | Me | SO2Et | |
| 1-94 | cf3 | Et | SO2Et | |
| 1-95 | cf3 | n-Pr | SO2Et | |
| 1-96 | cf3 | i-Pr | SO2Et | |
| 1-97 | OMe | Me | SO2Et | |
| 1-98 | OMe | Et | SO2Et | |
| 1-99 | OMe | n-Pr | SO2Et | |
| 1-100 | OMe | i-Pr | SO2Et | |
| 1-101 | OEt | Me | SO2Et | |
| 1-102 | OEt | Et | SO2Et | |
| 1-103 | OEt | n-Pr | SO2Et | |
| 1-104 | OEt | i-Pr | SO2Et |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-105 | no2 | Me | SO2Et | |
| 1-106 | no2 | Et | SO2Et | |
| 1-107 | no2 | n-Pr | SO2Et | |
| 1-108 | no2 | i-Pr | SO2Et | |
| 1-109 | SO2Me | Me | SO2Et | |
| 1-110 | SO2Me | Et | SO2Et | |
| 1-111 | SO2Me | n-Pr | SO2Et | |
| 1-112 | SO2Me | i-Pr | SO2Et | |
| 1-113 | CH2OMe | Me | SO2Et | |
| 1-114 | CH2OMe | Et | SO2Et | |
| 1-115 | CH2OMe | n-Pr | SO2Et | |
| 1-116 | CH2OMe | i-Pr | SO2Et | |
| 1-117 | CH2SO2Me | Me | SO2Et | |
| 1-118 | CH2SO2Me | Et | SO2Et | |
| 1-119 | CH2SO2Me | n-Pr | SO2Et | |
| 1-120 | CH2SO2Me | i-Pr | SO2Et | |
| 1-121 | CH2OCH2CH2OMe | Me | SO2Et | |
| 1-122 | CH2OCH2CH2OMe | Et | SO2Et | |
| 1-123 | CH2OCH2CH2OMe | n-Pr | SO2Et | |
| 1-124 | CH2OCH2CH2OMe | i-Pr | SO2Et | |
| 1-125 | CH2OCH2CH2OEt | Me | SO2Et | |
| 1-126 | CH2OCH2CH2OEt | Et | SO2Et | |
| 1-127 | CH2OCH2CH2OEt | n-Pr | SO2Et | |
| 1-128 | CH2OCH2CH2OEt | i-Pr | SO2Et | |
| 1-129 | CH2OCH2CH2CH2 | Me | SO2Et |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| OMe | ||||
| 1-130 | CH2OCH2CH2CH2 OMe | Et | SO2Et | |
| 1-131 | CH2OCH2CH2CH2 OMe | n-Pr | SO2Et | |
| 1-132 | CH2OCH2CH2CH2 OMe | i-Pr | SO2Et | |
| 1-133 | CH2OCH2OMe | Me | SO2Et | |
| 1-134 | CH2OCH2OMe | Et | SO2Et | |
| 1-135 | CH2OCH2OMe | n-Pr | SO2Et | |
| 1-136 | CH2OCH2OMe | i-Pr | SO2Et | |
| 1-137 | CH2OCH2OEt | Me | SO2Et | |
| 1-138 | CH2OCH2OEt | Et | SO2Et | |
| 1-139 | CH2OCH2OEt | n-Pr | SO2Et | |
| 1-140 | CH2OCH2OEt | i-Pr | SO2Et | |
| 1-141 | CH2OCH2CH2SO2 Me | Me | SO2Et | |
| 1-142 | CH2OCH2CH2SO2 Me | Et | SO2Et | |
| 1-143 | CH2OCH2CH2SO2 Me | n-Pr | SO2Et | |
| 1-144 | CH2OCH2CH2SO2 Me | i-Pr | SO2Et | |
| 1-145 | CH2SO2CH2CH2O Me | Me | SO2Et |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-146 | CH2SO2CH2CH2O Me | Et | SO2Et | |
| 1-147 | CH2SO2CH2CH2O Me | n-Pr | SO2Et | |
| 1-148 | CH2SO2CH2CH2O Me | i-Pr | SO2Et | |
| 1-149 | CH2SO2CH2CH2S O2Me | Me | SO2Et | |
| 1-150 | CH2SO2CH2CH2S O2Me | Et | SO2Et | |
| 1-151 | CH2SO2CH2CH2S O2Me | n-Pr | SO2Et | |
| 1-152 | CH2SO2CH2CH2S O2Me | i-Pr | SO2Et | |
| 1-153 | Cl | Me | F | |
| 1-154 | Cl | Et | F | |
| 1-155 | Cl | n-Pr | F | |
| 1-156 | Cl | i-Pr | F | |
| 1-157 | Br | Me | F | |
| 1-158 | Br | Et | F | |
| 1-159 | Br | n-Pr | F | |
| 1-160 | Br | i-Pr | F | |
| 1-161 | Me | Me | F | |
| 1-162 | Me | Et | F | |
| 1-163 | Me | n-Pr | F |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-164 | Me | i-Pr | F | |
| 1-165 | Et | Me | F | |
| 1-166 | Et | Et | F | |
| 1-167 | Et | n-Pr | F | |
| 1-168 | Et | i-Pr | F | |
| 1-169 | cf3 | Me | F | |
| 1-170 | cf3 | Et | F | |
| 1-171 | cf3 | n-Pr | F | |
| 1-172 | cf3 | i-Pr | F | |
| 1-173 | OMe | Me | F | |
| 1-174 | OMe | Et | F | |
| 1-175 | OMe | n-Pr | F | |
| 1-176 | OMe | i-Pr | F | |
| 1-177 | OEt | Me | F | |
| 1-178 | OEt | Et | F | |
| 1-179 | OEt | n-Pr | F | |
| 1-180 | OEt | i-Pr | F | |
| 1-181 | no2 | Me | F | |
| 1-182 | no2 | Et | F | |
| 1-183 | no2 | n-Pr | F | |
| 1-184 | no2 | i-Pr | F | |
| 1-185 | SO2Me | Me | F | |
| 1-186 | SO2Me | Et | F | |
| 1-187 | SO2Me | n-Pr | F | |
| 1-188 | SO2Me | i-Pr | F |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCh] |
| 1-189 | CH2OMe | Me | F | |
| 1-190 | CH2OMe | Et | F | |
| 1-191 | CH2OMe | n-Pr | F | |
| 1-192 | CH2OMe | i-Pr | F | |
| 1-193 | CH2SO2Me | Me | F | |
| 1-194 | CH2SO2Me | Et | F | |
| 1-195 | CH2SO2Me | n-Pr | F | |
| 1-196 | CH2SO2Me | i-Pr | F | |
| 1-197 | CH2OCH2CH2OMe | Me | F | |
| 1-198 | CH2OCH2CH2OMe | Et | F | |
| 1-199 | CH2OCH2CH2OMe | n-Pr | F | |
| 1-200 | CH2OCH2CH2OMe | i-Pr | F | |
| 1-201 | CH2OCH2CH2OEt | Me | F | |
| 1-202 | CH2OCH2CH2OEt | Et | F | |
| 1-203 | CH2OCH2CH2OEt | n-Pr | F | |
| 1-204 | CH2OCH2CH2OEt | i-Pr | F | |
| 1-205 | CH2OCH2CH2CH2 OMe | Me | F | |
| 1-206 | CH2OCH2CH2CH2 OMe | Et | F | |
| 1-207 | CH2OCH2CH2CH2 OMe | n-Pr | F | |
| 1-208 | CH2OCH2CH2CH2 OMe | i-Pr | F | |
| 1-209 | CH2OCH2OMe | Me | F |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-210 | CH2OCH2OMe | Et | F | |
| 1-211 | CH2OCH2OMe | n-Pr | F | |
| 1-212 | CH2OCH2OMe | i-Pr | F | |
| 1-213 | CH2OCH2OEt | Me | F | |
| 1-214 | CH2OCH2OEt | Et | F | |
| 1-215 | CH2OCH2OEt | n-Pr | F | |
| 1-216 | CH2OCH2OEt | i-Pr | F | |
| 1-217 | CH2OCH2CH2SO2 Me | Me | F | |
| 1-218 | CH2OCH2CH2SO2 Me | Et | F | |
| 1-219 | CH2OCH2CH2SO2 Me | n-Pr | F | |
| 1-220 | CH2OCH2CH2SO2 Me | i-Pr | F | |
| 1-221 | CH2SO2CH2CH2O Me | Me | F | |
| 1-222 | CH2SO2CH2CH2O Me | Et | F | |
| 1-223 | CH2SO2CH2CH2O Me | n-Pr | F | |
| 1-224 | CH2SO2CH2CH2O Me | i-Pr | F | |
| 1-225 | CH2SO2CH2CH2S O2Me | Me | F |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-226 | CH2SO2CH2CH2S Ü2Me | Et | F | |
| 1-227 | CH2SO2CH2CH2S Ü2Me | n-Pr | F | |
| 1-228 | CH2SO2CH2CH2S O2Me | i-Pr | F | |
| 1-229 | Cl | Me | Cl | |
| 1-230 | Cl | Et | Cl | |
| 1-231 | Cl | n-Pr | Cl | |
| 1-232 | Cl | i-Pr | Cl | |
| 1-233 | Br | Me | Cl | |
| 1-234 | Br | Et | Cl | |
| 1-235 | Br | n-Pr | Cl | |
| 1-236 | Br | i-Pr | Cl | |
| 1-237 | Me | Me | Cl | 7,41 (d, 1H), 7,36 (d, 1H), 7,32 (s, 1H), 3,71 (s, 3H), 3,02 (s, 3H), 2,74 (s, 3H) |
| 1-238 | Me | Et | Cl | 7,41 (d, 1H), 7,36 (d, 1H), 7,31 (s, 1H), 3,71 (s, 3H), 3,38 (m, 1H), 3,16 (m, 1H), 2,72 (s, 3H), 1,41 (t, 3H) |
| 1-239 | Me | n-Pr | Cl | |
| 1-240 | Me | i-Pr | Cl |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-241 | Et | Me | Cl | |
| 1-242 | Et | Et | Cl | |
| 1-243 | Et | n-Pr | Cl | |
| 1-244 | Et | i-Pr | Cl | |
| 1-245 | cf3 | Me | Cl | |
| 1-246 | cf3 | Et | Cl | |
| 1-247 | cf3 | n-Pr | Cl | |
| 1-248 | cf3 | i-Pr | Cl | |
| 1-249 | OMe | Me | Cl | |
| 1-250 | OMe | Et | Cl | |
| 1-251 | OMe | n-Pr | Cl | |
| 1-252 | OMe | i-Pr | Cl | |
| 1-253 | OEt | Me | Cl | |
| 1-254 | OEt | Et | Cl | |
| 1-255 | OEt | n-Pr | Cl | |
| 1-256 | OEt | i-Pr | Cl | |
| 1-257 | no2 | Me | Cl | |
| 1-258 | no2 | Et | Cl | |
| 1-259 | no2 | n-Pr | Cl | |
| 1-260 | no2 | i-Pr | Cl | |
| 1-261 | SO2Me | Me | Cl | |
| 1-262 | SO2Me | Et | Cl | |
| 1-263 | SO2Me | n-Pr | Cl | |
| 1-264 | SO2Me | i-Pr | Cl | |
| 1-265 | CH2OMe | Me | Cl |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-266 | CH2OMe | Et | Cl | |
| 1-267 | CH2OMe | n-Pr | Cl | |
| 1-268 | CH2OMe | i-Pr | Cl | |
| 1-269 | CH2SO2Me | Me | Cl | |
| 1-270 | CH2SO2Me | Et | Cl | |
| 1-271 | CH2SO2Me | n-Pr | Cl | |
| 1-272 | CH2SO2Me | i-Pr | Cl | |
| 1-273 | CH2OCH2CH2OMe | Me | Cl | |
| 1-274 | CH2OCH2CH2OMe | Et | Cl | |
| 1-275 | CH2OCH2CH2OMe | n-Pr | Cl | |
| 1-276 | CH2OCH2CH2OMe | i-Pr | Cl | |
| 1-277 | CH2OCH2CH2OEt | Me | Cl | |
| 1-278 | CH2OCH2CH2OEt | Et | Cl | |
| 1-279 | CH2OCH2CH2OEt | n-Pr | Cl | |
| 1-280 | CH2OCH2CH2OEt | i-Pr | Cl | |
| 1-281 | CH2OCH2CH2CH2 OMe | Me | Cl | |
| 1-282 | CH2OCH2CH2CH2 OMe | Et | Cl | |
| 1-283 | CH2OCH2CH2CH2 OMe | n-Pr | Cl | |
| 1-284 | CH2OCH2CH2CH2 OMe | i-Pr | Cl | |
| 1-285 | CH2OCH2OMe | Me | Cl | |
| 1-286 | CH2OCH2OMe | Et | Cl |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-287 | CH2OCH2OMe | n-Pr | Cl | |
| 1-288 | CH2OCH2OMe | i-Pr | Cl | |
| 1-289 | CH2OCH2OEt | Me | Cl | |
| 1-290 | CH2OCH2OEt | Et | Cl | |
| 1-291 | CH2OCH2OEt | n-Pr | Cl | |
| 1-292 | CH2OCH2OEt | i-Pr | Cl | |
| 1-293 | CH2OCH2CH2SO2 Me | Me | Cl | |
| 1-294 | CH2OCH2CH2SO2 Me | Et | Cl | |
| 1-295 | CH2OCH2CH2SO2 Me | n-Pr | Cl | |
| 1-296 | CH2OCH2CH2SO2 Me | i-Pr | Cl | |
| 1-297 | CH2SO2CH2CH2O Me | Me | Cl | |
| 1-298 | CH2SO2CH2CH2O Me | Et | Cl | |
| 1-299 | CH2SO2CH2CH2O Me | n-Pr | Cl | |
| 1-300 | CH2SO2CH2CH2O Me | i-Pr | Cl | |
| 1-301 | CH2SO2CH2CH2S O2Me | Me | Cl | |
| 1-302 | CH2SO2CH2CH2S | Et | Cl |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| O2Me | ||||
| 1-303 | CH2SO2CH2CH2S O2Me | n-Pr | Cl | |
| 1-304 | CH2SO2CH2CH2S O2Me | i-Pr | Cl | |
| 1-305 | Cl | Me | Br | |
| 1-306 | Cl | Et | Br | |
| 1-307 | Cl | n-Pr | Br | |
| 1-308 | Cl | i-Pr | Br | |
| 1-309 | Br | Me | Br | |
| 1-310 | Br | Et | Br | |
| 1-311 | Br | n-Pr | Br | |
| 1-312 | Br | i-Pr | Br | |
| 1-313 | Me | Me | Br | 7,55 (d, 1H), 7,32 (s, 1H), 7,30 (d, 1H), 3,72 (s, 3H), 3,01 (s, 3H), 2,77 (s, 3H) |
| 1-314 | Me | Et | Br | |
| 1-315 | Me | n-Pr | Br | |
| 1-316 | Me | i-Pr | Br | |
| 1-317 | Et | Me | Br | |
| 1-318 | Et | Et | Br | |
| 1-319 | Et | n-Pr | Br | |
| 1-320 | Et | i-Pr | Br | |
| 1-321 | cf3 | Me | Br |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-322 | cf3 | Et | Br | |
| 1-323 | cf3 | n-Pr | Br | |
| 1-324 | cf3 | i-Pr | Br | |
| 1-325 | OMe | Me | Br | |
| 1-326 | OMe | Et | Br | |
| 1-327 | OMe | n-Pr | Br | |
| 1-328 | OMe | i-Pr | Br | |
| 1-329 | OEt | Me | Br | |
| 1-330 | OEt | Et | Br | |
| 1-331 | OEt | n-Pr | Br | |
| 1-332 | OEt | i-Pr | Br | |
| 1-333 | no2 | Me | Br | |
| 1-334 | no2 | Et | Br | |
| 1-335 | no2 | n-Pr | Br | |
| 1-336 | no2 | i-Pr | Br | |
| 1-337 | SO2Me | Me | Br | |
| 1-338 | SO2Me | Et | Br | |
| 1-339 | SO2Me | n-Pr | Br | |
| 1-340 | SO2Me | i-Pr | Br | |
| 1-341 | CH2OMe | Me | Br | |
| 1-342 | CH2OMe | Et | Br | |
| 1-343 | CH2OMe | n-Pr | Br | |
| 1-344 | CH2OMe | i-Pr | Br | |
| 1-345 | CH2SO2Me | Me | Br | |
| 1-346 | CH2SO2Me | Et | Br |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-347 | CH2SO2Me | n-Pr | Br | |
| 1-348 | CH2SO2Me | i-Pr | Br | |
| 1-349 | CH2OCH2CH2OMe | Me | Br | |
| 1-350 | CH2OCH2CH2OMe | Et | Br | |
| 1-351 | CH2OCH2CH2OMe | n-Pr | Br | |
| 1-352 | CH2OCH2CH2OMe | i-Pr | Br | |
| 1-353 | CH2OCH2CH2OEt | Me | Br | |
| 1-354 | CH2OCH2CH2OEt | Et | Br | |
| 1-355 | CH2OCH2CH2OEt | n-Pr | Br | |
| 1-356 | CH2OCH2CH2OEt | i-Pr | Br | |
| 1-357 | CH2OCH2CH2CH2 OMe | Me | Br | |
| 1-358 | CH2OCH2CH2CH2 OMe | Et | Br | |
| 1-359 | CH2OCH2CH2CH2 OMe | n-Pr | Br | |
| 1-360 | CH2OCH2CH2CH2 OMe | i-Pr | Br | |
| 1-361 | CH2OCH2OMe | Me | Br | |
| 1-362 | CH2OCH2OMe | Et | Br | |
| 1-363 | CH2OCH2OMe | n-Pr | Br | |
| 1-364 | CH2OCH2OMe | i-Pr | Br | |
| 1-365 | CH2OCH2OEt | Me | Br | |
| 1-366 | CH2OCH2OEt | Et | Br | |
| 1-367 | CH2OCH2OEt | n-Pr | Br |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-368 | CH2OCH2OEt | i-Pr | Br | |
| 1-369 | CH2OCH2CH2SO2 Me | Me | Br | |
| 1-370 | CH2OCH2CH2SO2 Me | Et | Br | |
| 1-371 | CH2OCH2CH2SO2 Me | n-Pr | Br | |
| 1-372 | CH2OCH2CH2SO2 Me | i-Pr | Br | |
| 1-373 | CH2SO2CH2CH2O Me | Me | Br | |
| 1-374 | CH2SO2CH2CH2O Me | Et | Br | |
| 1-375 | CH2SO2CH2CH2O Me | n-Pr | Br | |
| 1-376 | CH2SO2CH2CH2O Me | i-Pr | Br | |
| 1-377 | CH2SO2CH2CH2S O2Me | Me | Br | |
| 1-378 | CH2SO2CH2CH2S O2Me | Et | Br | |
| 1-379 | CH2SO2CH2CH2S O2Me | n-Pr | Br | |
| 1-380 | CH2SO2CH2CH2S O2Me | i-Pr | Br |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-381 | Cl | Me | I | |
| 1-382 | Cl | Et | I | |
| 1-383 | Cl | n-Pr | I | |
| 1-384 | Cl | i-Pr | I | |
| 1-385 | Br | Me | I | |
| 1-386 | Br | Et | I | |
| 1-387 | Br | n-Pr | I | |
| 1-388 | Br | i-Pr | I | |
| 1-389 | Me | Me | I | 7,86 (d, 1H), 7,31 (s, 1H), 7,11 (d, 1H), 3,71 (s, 3H), 2,98 (s, 3H), 2,76 (s, 3H) |
| 1-390 | Me | Et | I | |
| 1-391 | Me | n-Pr | I | |
| 1-392 | Me | i-Pr | I | |
| 1-393 | Et | Me | I | |
| 1-394 | Et | Et | | | |
| 1-395 | Et | n-Pr | I | |
| 1-396 | Et | i-Pr | I | |
| 1-397 | cf3 | Me | I | |
| 1-398 | cf3 | Et | | | |
| 1-399 | cf3 | n-Pr | I | |
| 1-400 | cf3 | i-Pr | I | |
| 1-401 | OMe | Me | I | |
| 1-402 | OMe | Et | I |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-403 | OMe | n-Pr | I | |
| 1-404 | OMe | i-Pr | I | |
| 1-405 | OEt | Me | I | |
| 1-406 | OEt | Et | I | |
| 1-407 | OEt | n-Pr | I | |
| 1-408 | OEt | i-Pr | I | |
| 1-409 | no2 | Me | I | |
| 1-410 | no2 | Et | I | |
| 1-411 | no2 | n-Pr | I | |
| 1-412 | no2 | i-Pr | I | |
| 1-413 | SO2Me | Me | | | |
| 1-414 | SO2Me | Et | I | |
| 1-415 | SO2Me | n-Pr | I | |
| 1-416 | SO2Me | i-Pr | I | |
| 1-417 | CH2OMe | Me | I | |
| 1-418 | CH2OMe | Et | I | |
| 1-419 | CH2OMe | n-Pr | | | |
| 1-420 | CH2OMe | i-Pr | | | |
| 1-421 | CH2SO2Me | Me | I | |
| 1-422 | CH2SO2Me | Et | I | |
| 1-423 | CH2SO2Me | n-Pr | I | |
| 1-424 | CH2SO2Me | i-Pr | | | |
| 1-425 | CH2OCH2CH2OMe | Me | I | |
| 1-426 | CH2OCH2CH2OMe | Et | I | |
| 1-427 | CH2OCH2CH2OMe | n-Pr | I |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-428 | CH2OCH2CH2OMe | i-Pr | I | |
| 1-429 | CH2OCH2CH2OEt | Me | I | |
| 1-430 | CH2OCH2CH2OEt | Et | I | |
| 1-431 | CH2OCH2CH2OEt | n-Pr | I | |
| 1-432 | CH2OCH2CH2OEt | i-Pr | I | |
| 1-433 | CH2OCH2CH2CH2 OMe | Me | | | |
| 1-434 | CH2OCH2CH2CH2 OMe | Et | I | |
| 1-435 | CH2OCH2CH2CH2 OMe | n-Pr | I | |
| 1-436 | CH2OCH2CH2CH2 OMe | i-Pr | I | |
| 1-437 | CH2OCH2OMe | Me | I | |
| 1-438 | CH2OCH2OMe | Et | I | |
| 1-439 | CH2OCH2OMe | n-Pr | I | |
| 1-440 | CH2OCH2OMe | i-Pr | I | |
| 1-441 | CH2OCH2OEt | Me | I | |
| 1-442 | CH2OCH2OEt | Et | I | |
| 1-443 | CH2OCH2OEt | n-Pr | I | |
| 1-444 | CH2OCH2OEt | i-Pr | I | |
| 1-445 | CH2OCH2CH2SO2 Me | Me | I | |
| 1-446 | CH2OCH2CH2SO2 Me | Et | I |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-447 | CH2OCH2CH2SO2 Me | n-Pr | I | |
| 1-448 | CH2OCH2CH2SO2 Me | i-Pr | I | |
| 1-449 | CH2SO2CH2CH2O Me | Me | I | |
| 1-450 | CH2SO2CH2CH2O Me | Et | I | |
| 1-451 | CH2SO2CH2CH2O Me | n-Pr | I | |
| 1-452 | CH2SO2CH2CH2O Me | i-Pr | I | |
| 1-453 | CH2SO2CH2CH2S O2Me | Me | | | |
| 1-454 | CH2SO2CH2CH2S O2Me | Et | I | |
| 1-455 | CH2SO2CH2CH2S O2Me | n-Pr | I | |
| 1-456 | CH2SO2CH2CH2S O2Me | i-Pr | I | |
| 1-457 | Cl | Me | NO2 | |
| 1-458 | Cl | Et | NO2 | |
| 1-459 | Cl | n-Pr | NO2 | |
| 1-460 | Cl | i-Pr | NO2 | |
| 1-461 | Br | Me | NO2 |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-462 | Br | Et | no2 | |
| 1-463 | Br | n-Pr | no2 | |
| 1-464 | Br | i-Pr | no2 | |
| 1-465 | Me | Me | no2 | |
| 1-466 | Me | Et | no2 | |
| 1-467 | Me | n-Pr | no2 | |
| 1-468 | Me | i-Pr | no2 | |
| 1-469 | Et | Me | no2 | |
| 1-470 | Et | Et | no2 | |
| 1-471 | Et | n-Pr | no2 | |
| 1-472 | Et | i-Pr | no2 | |
| 1-473 | cf3 | Me | no2 | |
| 1-474 | cf3 | Et | no2 | |
| 1-475 | cf3 | n-Pr | no2 | |
| 1-476 | cf3 | i-Pr | no2 | |
| 1-477 | OMe | Me | no2 | |
| 1-478 | OMe | Et | no2 | |
| 1-479 | OMe | n-Pr | no2 | |
| 1-480 | OMe | i-Pr | no2 | |
| 1-481 | OEt | Me | no2 | |
| 1-482 | OEt | Et | no2 | |
| 1-483 | OEt | n-Pr | no2 | |
| 1-484 | OEt | i-Pr | no2 | |
| 1-485 | no2 | Me | no2 | |
| 1-486 | no2 | Et | no2 |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-487 | no2 | n-Pr | no2 | |
| 1-488 | no2 | i-Pr | no2 | |
| 1-489 | SO2Me | Me | no2 | |
| 1-490 | SO2Me | Et | no2 | |
| 1-491 | SO2Me | n-Pr | no2 | |
| 1-492 | SO2Me | i-Pr | no2 | |
| 1-493 | CH2OMe | Me | no2 | |
| 1-494 | CH2OMe | Et | no2 | |
| 1-495 | CH2OMe | n-Pr | no2 | |
| 1-496 | CH2OMe | i-Pr | no2 | |
| 1-497 | CH2SO2Me | Me | no2 | |
| 1-498 | CH2SO2Me | Et | no2 | |
| 1-499 | CH2SO2Me | n-Pr | no2 | |
| 1-500 | CH2SO2Me | i-Pr | no2 | |
| 1-501 | CH2OCH2CH2OMe | Me | no2 | |
| 1-502 | CH2OCH2CH2OMe | Et | no2 | |
| 1-503 | CH2OCH2CH2OMe | n-Pr | no2 | |
| 1-504 | CH2OCH2CH2OMe | i-Pr | no2 | |
| 1-505 | CH2OCH2CH2OEt | Me | no2 | |
| 1-506 | CH2OCH2CH2OEt | Et | no2 | |
| 1-507 | CH2OCH2CH2OEt | n-Pr | no2 | |
| 1-508 | CH2OCH2CH2OEt | i-Pr | no2 | |
| 1-509 | CH2OCH2CH2CH2 OMe | Me | no2 | |
| 1-510 | CH2OCH2CH2CH2 | Et | no2 |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| OMe | ||||
| 1-511 | CH2OCH2CH2CH2 OMe | n-Pr | NO2 | |
| 1-512 | CH2OCH2CH2CH2 OMe | i-Pr | NO2 | |
| 1-513 | CH2OCH2OMe | Me | NO2 | |
| 1-514 | CH2OCH2OMe | Et | NO2 | |
| 1-515 | CH2OCH2OMe | n-Pr | NO2 | |
| 1-516 | CH2OCH2OMe | i-Pr | NO2 | |
| 1-517 | CH2OCH2OEt | Me | NO2 | |
| 1-518 | CH2OCH2OEt | Et | NO2 | |
| 1-519 | CH2OCH2OEt | n-Pr | NO2 | |
| 1-520 | CH2OCH2OEt | i-Pr | NO2 | |
| 1-521 | CH2OCH2CH2SO2 Me | Me | NO2 | |
| 1-522 | CH2OCH2CH2SO2 Me | Et | NO2 | |
| 1-523 | CH2OCH2CH2SO2 Me | n-Pr | NO2 | |
| 1-524 | CH2OCH2CH2SO2 Me | i-Pr | NO2 | |
| 1-525 | CH2SO2CH2CH2O Me | Me | NO2 | |
| 1-526 | CH2SO2CH2CH2O Me | Et | NO2 |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1-527 | CH2SO2CH2CH2O Me | n-Pr | NO2 | |
| 1-528 | CH2SO2CH2CH2O Me | i-Pr | NO2 | |
| 1-529 | CH2SO2CH2CH2S O2Me | Me | NO2 | |
| 1-530 | CH2SO2CH2CH2S O2Me | Et | NO2 | |
| 1-531 | CH2SO2CH2CH2S O2Me | n-Pr | NO2 | |
| 1-532 | CH2SO2CH2CH2S O2Me | i-Pr | NO2 |
Tabela 2
Compostos de Fórmula (I) de Acordo com a Presente Invenção em que R1 é
Etila e R2e R4 são Hidrogênio
H3C
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-1 | Cl | Me | SO2Me | |
| 2-2 | Cl | Et | SO2Me | |
| 2-3 | Cl | n-Pr | SO2Me | |
| 2-4 | Cl | i-Pr | SO2Me | |
| 2-5 | Br | Me | SO2Me |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCh] |
| 2-6 | Br | Et | SO2Me | |
| 2-7 | Br | n-Pr | SO2Me | |
| 2-8 | Br | i-Pr | SO2Me | |
| 2-9 | Me | Me | SO2Me | 8,08 (d, 1H), 7,62 (d, 1H), 7,28 (s, 1H), 4,09 (q, 2H), 3,38 (s, 3H), 3,18 (s, 3H), 2,88 (s, 3H), 1,46 (t, 3H) |
| 2-10 | Me | Et | SO2Me | 8,10 (d, 1H), 7,62 (d, 1H), 7,28 (s, 1H), 4,08 (q, 2H), 3,52 (m, 1H), 3,38 (s, 3H), 3,28 (m, 1H), 2,82 (s, 3H), 1,52 (t, 3H), 1,47 (t, 3H) |
| 2-11 | Me | n-Pr | SO2Me | 8,08 (d, 1H), 7,61 (d, 1H), 7,27 (s, 1H), 4,08 (q, 2H), 3,52 (m, 1H), 3,37 (s, 3H), 3,16 (m, 1H), 2,83 (s, 3H), 2,02 (m, 2H), 1,47 (t, 3H), 1,17 (t, 3H) |
| 2-12 | Me | i-Pr | SO2Me | 8,17 (m, 1H), 7,62 (d, 1H), 7,26 (s, 1H), 4,08 (q, 2H), 3,74 (m, 1H), 3,37 (s, 3H), 2,87 (s, 3H), 1,55 (d, 3H), 1,47 (t, 3H), 1,27 (m, 3H) |
| 2-13 | Et | Me | SO2Me |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-14 | Et | Et | SO2Me | |
| 2-15 | Et | n-Pr | SO2Me | |
| 2-16 | Et | i-Pr | SO2Me | |
| 2-17 | cf3 | Me | SO2Me | |
| 2-18 | cf3 | Et | SO2Me | |
| 2-19 | cf3 | n-Pr | SO2Me | |
| 2-20 | cf3 | i-Pr | SO2Me | |
| 2-21 | OMe | Me | SO2Me | |
| 2-22 | OMe | Et | SO2Me | |
| 2-23 | OMe | n-Pr | SO2Me | |
| 2-24 | OMe | i-Pr | SO2Me | |
| 2-25 | OEt | Me | SO2Me | |
| 2-26 | OEt | Et | SO2Me | |
| 2-27 | OEt | n-Pr | SO2Me | |
| 2-28 | OEt | i-Pr | SO2Me | |
| 2-29 | no2 | Me | SO2Me | |
| 2-30 | no2 | Et | SO2Me | |
| 2-31 | no2 | n-Pr | SO2Me | |
| 2-32 | no2 | i-Pr | SO2Me | |
| 2-33 | SO2Me | Me | SO2Me | |
| 2-34 | SO2Me | Et | SO2Me | |
| 2-35 | SO2Me | n-Pr | SO2Me | |
| 2-36 | SO2Me | i-Pr | SO2Me | |
| 2-37 | CH2OMe | Me | SO2Me | |
| 2-38 | CH2OMe | Et | SO2Me |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-39 | CH2OMe | n-Pr | SO2Me | |
| 2-40 | CH2OMe | i-Pr | SO2Me | |
| 2-41 | CH2SO2Me | Me | SO2Me | |
| 2-42 | CH2SO2Me | Et | SO2Me | |
| 2-43 | CH2SO2Me | n-Pr | SO2Me | |
| 2-44 | CH2SO2Me | i-Pr | SO2Me | |
| 2-45 | CH2OCH2CH2OMe | Me | SO2Me | |
| 2-46 | CH2OCH2CH2OMe | Et | SO2Me | |
| 2-47 | CH2OCH2CH2OMe | n-Pr | SO2Me | |
| 2-48 | CH2OCH2CH2OMe | i-Pr | SO2Me | |
| 2-49 | CH2OCH2CH2OEt | Me | SO2Me | 8,22 (d, 1H), 7,67 (d, 1H), 7,38 (s, 1H), 5,60 - 5,10 (br, signal, 1H), 4,97 (d, 1H), 4,09 (q, 2H), 3,62 3,56 (m, 1H), 3,56 - 3,49 (m, 1H), 3,47 - 3,32 (m, 4H), 3,37 (s, 3H), 3,33 (s, 3H), 1,46 (t, 3H), 1,12 (t, 3H) |
| 2-50 | CH2OCH2CH2OEt | Et | SO2Me | |
| 2-51 | CH2OCH2CH2OEt | n-Pr | SO2Me | |
| 2-52 | CH2OCH2CH2OEt | i-Pr | SO2Me | |
| 2-53 | CH2OCH2CH2CH2O Me | Me | SO2Me | |
| 2-54 | CH2OCH2CH2CH2O | Et | SO2Me |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| Me | ||||
| 2-55 | CH2OCH2CH2CH2O Me | n-Pr | SO2Me | |
| 2-56 | CH2OCH2CH2CH2O Me | i-Pr | SO2Me | |
| 2-57 | CH2OCH2OMe | Me | SO2Me | |
| 2-58 | CH2OCH2OMe | Et | SO2Me | |
| 2-59 | CH2OCH2OMe | n-Pr | SO2Me | |
| 2-60 | CH2OCH2OMe | i-Pr | SO2Me | |
| 2-61 | CH2OCH2OEt | Me | SO2Me | |
| 2-62 | CH2OCH2OEt | Et | SO2Me | |
| 2-63 | CH2OCH2OEt | n-Pr | SO2Me | |
| 2-64 | CH2OCH2OEt | i-Pr | SO2Me | |
| 2-65 | CH2OCH2CH2SO2Me | Me | SO2Me | |
| 2-66 | CH2OCH2CH2SO2Me | Et | SO2Me | |
| 2-67 | CH2OCH2CH2SO2Me | n-Pr | SO2Me | |
| 2-68 | CH2OCH2CH2SO2Me | i-Pr | SO2Me | |
| 2-69 | CH2SO2CH2CH2OMe | Me | SO2Me | |
| 2-70 | CH2SO2CH2CH2OMe | Et | SO2Me | |
| 2-71 | CH2SO2CH2CH2OMe | n-Pr | SO2Me | |
| 2-72 | CH2SO2CH2CH2OMe | i-Pr | SO2Me | |
| 2-73 | CH2SO2CH2CH2SO2 Me | Me | SO2Me | |
| 2-74 | CH2SO2CH2CH2SO2 Me | Et | SO2Me |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-75 | CH2SO2CH2CH2SO2 Me | n-Pr | SO2Me | |
| 2-76 | CH2SO2CH2CH2SO2 Me | i-Pr | SO2Me | |
| 2-77 | Cl | Me | SO2Et | |
| 2-78 | Cl | Et | SO2Et | |
| 2-79 | Cl | n-Pr | SO2Et | |
| 2-80 | Cl | i-Pr | SO2Et | |
| 2-81 | Br | Me | SO2Et | |
| 2-82 | Br | Et | SO2Et | |
| 2-83 | Br | n-Pr | SO2Et | |
| 2-84 | Br | i-Pr | SO2Et | |
| 2-85 | Me | Me | SO2Et | |
| 2-86 | Me | Et | SO2Et | |
| 2-87 | Me | n-Pr | SO2Et | |
| 2-88 | Me | i-Pr | SO2Et | |
| 2-89 | Et | Me | SO2Et | |
| 2-90 | Et | Et | SO2Et | |
| 2-91 | Et | n-Pr | SO2Et | |
| 2-92 | Et | i-Pr | SO2Et | |
| 2-93 | cf3 | Me | SO2Et | |
| 2-94 | cf3 | Et | SO2Et | |
| 2-95 | cf3 | n-Pr | SO2Et | |
| 2-96 | cf3 | i-Pr | SO2Et | |
| 2-97 | OMe | Me | SO2Et |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-98 | OMe | Et | SO2Et | |
| 2-99 | OMe | n-Pr | SO2Et | |
| 2-100 | OMe | i-Pr | SO2Et | |
| 2-101 | OEt | Me | SO2Et | |
| 2-102 | OEt | Et | SO2Et | |
| 2-103 | OEt | n-Pr | SO2Et | |
| 2-104 | OEt | i-Pr | SO2Et | |
| 2-105 | no2 | Me | SO2Et | |
| 2-106 | no2 | Et | SO2Et | |
| 2-107 | no2 | n-Pr | SO2Et | |
| 2-108 | no2 | i-Pr | SO2Et | |
| 2-109 | SO2Me | Me | SO2Et | |
| 2-110 | S02Me | Et | SO2Et | |
| 2-111 | SO2Me | n-Pr | SO2Et | |
| 2-112 | SO2Me | i-Pr | SO2Et | |
| 2-113 | CH2OMe | Me | SO2Et | |
| 2-114 | CH2OMe | Et | SO2Et | |
| 2-115 | CH2OMe | n-Pr | SO2Et | |
| 2-116 | CH2OMe | i-Pr | SO2Et | |
| 2-117 | CH2SO2Me | Me | SO2Et | |
| 2-118 | CH2SO2Me | Et | SO2Et | |
| 2-119 | CH2SO2Me | n-Pr | SO2Et | |
| 2-120 | CH2SO2Me | i-Pr | SO2Et | |
| 2-121 | CH2OCH2CH2OMe | Me | SO2Et | |
| 2-122 | CH2OCH2CH2OMe | Et | SO2Et |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-123 | CH2OCH2CH2OMe | n-Pr | SO2Et | |
| 2-124 | CH2OCH2CH2OMe | i-Pr | SO2Et | |
| 2-125 | CH2OCH2CH2OEt | Me | SO2Et | |
| 2-126 | CH2OCH2CH2OEt | Et | SO2Et | |
| 2-127 | CH2OCH2CH2OEt | n-Pr | SO2Et | |
| 2-128 | CH2OCH2CH2OEt | i-Pr | SO2Et | |
| 2-129 | CH2OCH2CH2CH2O Me | Me | SO2Et | |
| 2-130 | CH2OCH2CH2CH2O Me | Et | SO2Et | |
| 2-131 | CH2OCH2CH2CH2O Me | n-Pr | SO2Et | |
| 2-132 | CH2OCH2CH2CH2O Me | i-Pr | SO2Et | |
| 2-133 | CH2OCH2OMe | Me | SO2Et | |
| 2-134 | CH2OCH2OMe | Et | SO2Et | |
| 2-135 | CH2OCH2OMe | n-Pr | SO2Et | |
| 2-136 | CH2OCH2OMe | i-Pr | SO2Et | |
| 2-137 | CH2OCH2OEt | Me | SO2Et | |
| 2-138 | CH2OCH2OEt | Et | SO2Et | |
| 2-139 | CH2OCH2OEt | n-Pr | SO2Et | |
| 2-140 | CH2OCH2OEt | i-Pr | SO2Et | |
| 2-141 | CH2OCH2CH2SO2Me | Me | SO2Et | |
| 2-142 | CH2OCH2CH2SO2Me | Et | SO2Et | |
| 2-143 | CH2OCH2CH2SO2Me | n-Pr | SO2Et |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-144 | CH2OCH2CH2SO2Me | i-Pr | SO2Et | |
| 2-145 | CH2SO2CH2CH2OMe | Me | SO2Et | |
| 2-146 | CH2SO2CH2CH2OMe | Et | SO2Et | |
| 2-147 | CH2SO2CH2CH2OMe | n-Pr | SO2Et | |
| 2-148 | CH2SO2CH2CH2OMe | i-Pr | SO2Et | |
| 2-149 | CH2SO2CH2CH2SO2 Me | Me | SO2Et | |
| 2-150 | CH2SO2CH2CH2SO2 Me | Et | SO2Et | |
| 2-151 | CH2SO2CH2CH2SO2 Me | n-Pr | SO2Et | |
| 2-152 | CH2SO2CH2CH2SO2 Me | i-Pr | SO2Et | |
| 2-153 | Cl | Me | F | |
| 2-154 | Cl | Et | F | |
| 2-155 | Cl | n-Pr | F | |
| 2-156 | Cl | i-Pr | F | |
| 2-157 | Br | Me | F | |
| 2-158 | Br | Et | F | |
| 2-159 | Br | n-Pr | F | |
| 2-160 | Br | i-Pr | F | |
| 2-161 | Me | Me | F | |
| 2-162 | Me | Et | F | |
| 2-163 | Me | n-Pr | F | |
| 2-164 | Me | i-Pr | F |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-165 | Et | Me | F | |
| 2-166 | Et | Et | F | |
| 2-167 | Et | n-Pr | F | |
| 2-168 | Et | i-Pr | F | |
| 2-169 | cf3 | Me | F | |
| 2-170 | cf3 | Et | F | |
| 2-171 | cf3 | n-Pr | F | |
| 2-172 | cf3 | i-Pr | F | |
| 2-173 | OMe | Me | F | |
| 2-174 | OMe | Et | F | |
| 2-175 | OMe | n-Pr | F | |
| 2-176 | OMe | i-Pr | F | |
| 2-177 | OEt | Me | F | |
| 2-178 | OEt | Et | F | |
| 2-179 | OEt | n-Pr | F | |
| 2-180 | OEt | i-Pr | F | |
| 2-181 | no2 | Me | F | |
| 2-182 | no2 | Et | F | |
| 2-183 | no2 | n-Pr | F | |
| 2-184 | no2 | i-Pr | F | |
| 2-185 | SO2Me | Me | F | |
| 2-186 | SO2Me | Et | F | |
| 2-187 | SO2Me | n-Pr | F | |
| 2-188 | SO2Me | i-Pr | F | |
| 2-189 | CH2OMe | Me | F |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-190 | CH2OMe | Et | F | |
| 2-191 | CH2OMe | n-Pr | F | |
| 2-192 | CH2OMe | i-Pr | F | |
| 2-193 | CH2SO2Me | Me | F | |
| 2-194 | CH2SO2Me | Et | F | |
| 2-195 | CH2SO2Me | n-Pr | F | |
| 2-196 | CH2SO2Me | i-Pr | F | |
| 2-197 | CH2OCH2CH2OMe | Me | F | |
| 2-198 | CH2OCH2CH2OMe | Et | F | |
| 2-199 | CH2OCH2CH2OMe | n-Pr | F | |
| 2-200 | CH2OCH2CH2OMe | i-Pr | F | |
| 2-201 | CH2OCH2CH2OEt | Me | F | |
| 2-202 | CH2OCH2CH2OEt | Et | F | |
| 2-203 | CH2OCH2CH2OEt | n-Pr | F | |
| 2-204 | CH2OCH2CH2OEt | i-Pr | F | |
| 2-205 | CH2OCH2CH2CH2O Me | Me | F | |
| 2-206 | CH2OCH2CH2CH2O Me | Et | F | |
| 2-207 | CH2OCH2CH2CH2O Me | n-Pr | F | |
| 2-208 | CH2OCH2CH2CH2O Me | i-Pr | F | |
| 2-209 | CH2OCH2OMe | Me | F | |
| 2-210 | CH2OCH2OMe | Et | F |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-211 | CH2OCH2OMe | n-Pr | F | |
| 2-212 | CH2OCH2OMe | i-Pr | F | |
| 2-213 | CH2OCH2OEt | Me | F | |
| 2-214 | CH2OCH2OEt | Et | F | |
| 2-215 | CH2OCH2OEt | n-Pr | F | |
| 2-216 | CH2OCH2OEt | i-Pr | F | |
| 2-217 | CH2OCH2CH2SO2Me | Me | F | |
| 2-218 | CH2OCH2CH2SO2Me | Et | F | |
| 2-219 | CH2OCH2CH2SO2Me | n-Pr | F | |
| 2-220 | CH2OCH2CH2SO2Me | i-Pr | F | |
| 2-221 | CH2SO2CH2CH2OMe | Me | F | |
| 2-222 | CH2SO2CH2CH2OMe | Et | F | |
| 2-223 | CH2SO2CH2CH2OMe | n-Pr | F | |
| 2-224 | CH2SO2CH2CH2OMe | i-Pr | F | |
| 2-225 | CH2SO2CH2CH2SO2 Me | Me | F | |
| 2-226 | CH2SO2CH2CH2SO2 Me | Et | F | |
| 2-227 | CH2SO2CH2CH2SO2 Me | n-Pr | F | |
| 2-228 | CH2SO2CH2CH2SO2 Me | i-Pr | F | |
| 2-229 | Cl | Me | Cl | |
| 2-230 | Cl | Et | Cl | |
| 2-231 | Cl | n-Pr | Cl |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-232 | Cl | i-Pr | Cl | |
| 2-233 | Br | Me | Cl | |
| 2-234 | Br | Et | Cl | |
| 2-235 | Br | n-Pr | Cl | |
| 2-236 | Br | i-Pr | Cl | |
| 2-237 | Me | Me | Cl | 7,43 (d, 1H), 7,37 (d, 1H), 7,33 (s, 1H), 4,08 (q, 2H), 3,03 (s, 3H), 2,73 (s, 3H), 1,45 (t, 3H) |
| 2-238 | Me | Et | Cl | 7,41 (d, 1H), 7,36 (d, 1H), 7,32 (s, 1H), 4,07 (q, 2H), 3,38 (m, 1H), 3,17 (m, 1H), 2,72 (s, 3H), 1,46 (t, 3H), 1,41 (t, 3H) |
| 2-239 | Me | n-Pr | Cl | |
| 2-240 | Me | i-Pr | Cl | |
| 2-241 | Et | Me | Cl | |
| 2-242 | Et | Et | Cl | |
| 2-243 | Et | n-Pr | Cl | |
| 2-244 | Et | i-Pr | Cl | |
| 2-245 | cf3 | Me | Cl | |
| 2-246 | cf3 | Et | Cl | |
| 2-247 | cf3 | n-Pr | Cl | |
| 2-248 | cf3 | i-Pr | Cl | |
| 2-249 | OMe | Me | Cl |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-250 | OMe | Et | Cl | |
| 2-251 | OMe | n-Pr | Cl | |
| 2-252 | OMe | i-Pr | Cl | |
| 2-253 | OEt | Me | Cl | |
| 2-254 | OEt | Et | Cl | |
| 2-255 | OEt | n-Pr | Cl | |
| 2-256 | OEt | i-Pr | Cl | |
| 2-257 | no2 | Me | Cl | |
| 2-258 | no2 | Et | Cl | |
| 2-259 | no2 | n-Pr | Cl | |
| 2-260 | no2 | i-Pr | Cl | |
| 2-261 | SO2Me | Me | Cl | |
| 2-262 | SO2Me | Et | Cl | |
| 2-263 | SO2Me | n-Pr | Cl | |
| 2-264 | SO2Me | i-Pr | Cl | |
| 2-265 | CH2OMe | Me | Cl | |
| 2-266 | CH2OMe | Et | Cl | |
| 2-267 | CH2OMe | n-Pr | Cl | |
| 2-268 | CH2OMe | i-Pr | Cl | |
| 2-269 | CH2SO2Me | Me | Cl | |
| 2-270 | CH2SO2Me | Et | Cl | |
| 2-271 | CH2SO2Me | n-Pr | Cl | |
| 2-272 | CH2SO2Me | i-Pr | Cl | |
| 2-273 | CH2OCH2CH2OMe | Me | Cl | |
| 2-274 | CH2OCH2CH2OMe | Et | Cl |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-275 | CH2OCH2CH2OMe | n-Pr | Cl | |
| 2-276 | CH2OCH2CH2OMe | i-Pr | Cl | |
| 2-277 | CH2OCH2CH2OEt | Me | Cl | |
| 2-278 | CH2OCH2CH2OEt | Et | Cl | |
| 2-279 | CH2OCH2CH2OEt | n-Pr | Cl | |
| 2-280 | CH2OCH2CH2OEt | i-Pr | Cl | |
| 2-281 | CH2OCH2CH2CH2O Me | Me | Cl | |
| 2-282 | CH2OCH2CH2CH2O Me | Et | Cl | |
| 2-283 | CH2OCH2CH2CH2O Me | n-Pr | Cl | |
| 2-284 | CH2OCH2CH2CH2O Me | i-Pr | Cl | |
| 2-285 | CH2OCH2OMe | Me | Cl | |
| 2-286 | CH2OCH2OMe | Et | Cl | |
| 2-287 | CH2OCH2OMe | n-Pr | Cl | |
| 2-288 | CH2OCH2OMe | i-Pr | Cl | |
| 2-289 | CH2OCH2OEt | Me | Cl | |
| 2-290 | CH2OCH2OEt | Et | Cl | |
| 2-291 | CH2OCH2OEt | n-Pr | Cl | |
| 2-292 | CH2OCH2OEt | i-Pr | Cl | |
| 2-293 | CH2OCH2CH2SO2Me | Me | Cl | |
| 2-294 | CH2OCH2CH2SO2Me | Et | Cl | |
| 2-295 | CH2OCH2CH2SO2Me | n-Pr | Cl |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-296 | CH2OCH2CH2SO2Me | i-Pr | Cl | |
| 2-297 | CH2SO2CH2CH2OMe | Me | Cl | |
| 2-298 | CH2SO2CH2CH2OMe | Et | Cl | |
| 2-299 | CH2SO2CH2CH2OMe | n-Pr | Cl | |
| 2-300 | CH2SO2CH2CH2OMe | i-Pr | Cl | |
| 2-301 | CH2SO2CH2CH2SO2 Me | Me | Cl | |
| 2-302 | CH2SO2CH2CH2SO2 Me | Et | Cl | |
| 2-303 | CH2SO2CH2CH2SO2 Me | n-Pr | Cl | |
| 2-304 | CH2SO2CH2CH2SO2 Me | i-Pr | Cl | |
| 2-305 | Cl | Me | Br | |
| 2-306 | Cl | Et | Br | |
| 2-307 | Cl | n-Pr | Br | |
| 2-308 | Cl | i-Pr | Br | |
| 2-309 | Br | Me | Br | |
| 2-310 | Br | Et | Br | |
| 2-311 | Br | n-Pr | Br | |
| 2-312 | Br | i-Pr | Br | |
| 2-313 | Me | Me | Br | 7,56 (d, 1H), 7,35 (s, 1H), 7,33 (d, 1H), 4,09 (q, 2H), 3,03 (s, 3H), 2,77 (s, 3H), 1,46 (t, 3H) |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-314 | Me | Et | Br | |
| 2-315 | Me | n-Pr | Br | |
| 2-316 | Me | i-Pr | Br | |
| 2-317 | Et | Me | Br | |
| 2-318 | Et | Et | Br | |
| 2-319 | Et | n-Pr | Br | |
| 2-320 | Et | i-Pr | Br | |
| 2-321 | cf3 | Me | Br | |
| 2-322 | cf3 | Et | Br | |
| 2-323 | cf3 | n-Pr | Br | |
| 2-324 | cf3 | i-Pr | Br | |
| 2-325 | OMe | Me | Br | |
| 2-326 | OMe | Et | Br | |
| 2-327 | OMe | n-Pr | Br | |
| 2-328 | OMe | i-Pr | Br | |
| 2-329 | OEt | Me | Br | |
| 2-330 | OEt | Et | Br | |
| 2-331 | OEt | n-Pr | Br | |
| 2-332 | OEt | i-Pr | Br | |
| 2-333 | no2 | Me | Br | |
| 2-334 | no2 | Et | Br | |
| 2-335 | no2 | n-Pr | Br | |
| 2-336 | no2 | i-Pr | Br | |
| 2-337 | SO2Me | Me | Br | |
| 2-338 | SO2Me | Et | Br |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-339 | SO2Me | n-Pr | Br | |
| 2-340 | SO2Me | i-Pr | Br | |
| 2-341 | CH2OMe | Me | Br | |
| 2-342 | CH2OMe | Et | Br | |
| 2-343 | CH2OMe | n-Pr | Br | |
| 2-344 | CH2OMe | i-Pr | Br | |
| 2-345 | CH2SO2Me | Me | Br | |
| 2-346 | CH2SO2Me | Et | Br | |
| 2-347 | CH2SO2Me | n-Pr | Br | |
| 2-348 | CH2SO2Me | i-Pr | Br | |
| 2-349 | CH2OCH2CH2OMe | Me | Br | |
| 2-350 | CH2OCH2CH2OMe | Et | Br | |
| 2-351 | CH2OCH2CH2OMe | n-Pr | Br | |
| 2-352 | CH2OCH2CH2OMe | i-Pr | Br | |
| 2-353 | CH2OCH2CH2OEt | Me | Br | |
| 2-354 | CH2OCH2CH2OEt | Et | Br | |
| 2-355 | CH2OCH2CH2OEt | n-Pr | Br | |
| 2-356 | CH2OCH2CH2OEt | i-Pr | Br | |
| 2-357 | CH2OCH2CH2CH2O Me | Me | Br | |
| 2-358 | CH2OCH2CH2CH2O Me | Et | Br | |
| 2-359 | CH2OCH2CH2CH2O Me | n-Pr | Br | |
| 2-360 | CH2OCH2CH2CH2O | i-Pr | Br |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| Me | ||||
| 2-361 | CH2OCH2OMe | Me | Br | |
| 2-362 | CH2OCH2OMe | Et | Br | |
| 2-363 | CH2OCH2OMe | n-Pr | Br | |
| 2-364 | CH2OCH2OMe | i-Pr | Br | |
| 2-365 | CH2OCH2OEt | Me | Br | |
| 2-366 | CH2OCH2OEt | Et | Br | |
| 2-367 | CH2OCH2OEt | n-Pr | Br | |
| 2-368 | CH2OCH2OEt | i-Pr | Br | |
| 2-369 | CH2OCH2CH2SO2Me | Me | Br | |
| 2-370 | CH2OCH2CH2SO2Me | Et | Br | |
| 2-371 | CH2OCH2CH2SO2Me | n-Pr | Br | |
| 2-372 | CH2OCH2CH2SO2Me | i-Pr | Br | |
| 2-373 | CH2SO2CH2CH2OMe | Me | Br | |
| 2-374 | CH2SO2CH2CH2OMe | Et | Br | |
| 2-375 | CH2SO2CH2CH2OMe | n-Pr | Br | |
| 2-376 | CH2SO2CH2CH2OMe | i-Pr | Br | |
| 2-377 | CH2SO2CH2CH2SO2 Me | Me | Br | |
| 2-378 | CH2SO2CH2CH2SO2 Me | Et | Br | |
| 2-379 | CH2SO2CH2CH2SO2 Me | n-Pr | Br | |
| 2-380 | CH2SO2CH2CH2SO2 Me | i-Pr | Br |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCl3] |
| 2-381 | Cl | Me | I | |
| 2-382 | Cl | Et | I | |
| 2-383 | Cl | n-Pr | I | |
| 2-384 | Cl | i-Pr | I | |
| 2-385 | Br | Me | I | |
| 2-386 | Br | Et | I | |
| 2-387 | Br | n-Pr | I | |
| 2-388 | Br | i-Pr | I | |
| 2-389 | Me | Me | I | 7,87 (d, 1H), 7,31 (s, 1H), 7,12 (d, 1H), 4,08 (q, 2H), 2,97 (s, 3H), 2,77 (s, 3H), 1,45 (t, 3H) |
| 2-390 | Me | Et | I | |
| 2-391 | Me | n-Pr | I | |
| 2-392 | Me | i-Pr | I | |
| 2-393 | Et | Me | I | |
| 2-394 | Et | Et | I | |
| 2-395 | Et | n-Pr | I | |
| 2-396 | Et | i-Pr | I | |
| 2-397 | cf3 | Me | I | |
| 2-398 | cf3 | Et | I | |
| 2-399 | cf3 | n-Pr | I | |
| 2-400 | cf3 | i-Pr | I | |
| 2-401 | OMe | Me | | | |
| 2-402 | OMe | Et | | |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-403 | OMe | n-Pr | I | |
| 2-404 | OMe | i-Pr | I | |
| 2-405 | OEt | Me | | | |
| 2-406 | OEt | Et | | | |
| 2-407 | OEt | n-Pr | | | |
| 2-408 | OEt | i-Pr | I | |
| 2-409 | no2 | Me | I | |
| 2-410 | no2 | Et | I | |
| 2-411 | no2 | n-Pr | I | |
| 2-412 | no2 | i-Pr | I | |
| 2-413 | SO2Me | Me | | | |
| 2-414 | SO2Me | Et | I | |
| 2-415 | SO2Me | n-Pr | I | |
| 2-416 | SO2Me | i-Pr | I | |
| 2-417 | CH2OMe | Me | I | |
| 2-418 | CH2OMe | Et | I | |
| 2-419 | CH2OMe | n-Pr | I | |
| 2-420 | CH2OMe | i-Pr . | I | |
| 2-421 | CH2SO2Me | Me | I | |
| 2-422 | CH2SO2Me | Et | I | |
| 2-423 | CH2SO2Me | n-Pr | | | |
| 2-424 | CH2SO2Me | i-Pr | I | |
| 2-425 | CH2OCH2CH2OMe | Me | I | |
| 2-426 | CH2OCH2CH2OMe | Et | I | |
| 2-427 | CH2OCH2CH2OMe | n-Pr | I |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-428 | CH2OCH2CH2OMe | i-Pr | I | |
| 2-429 | CH2OCH2CH2OEt | Me | I | |
| 2-430 | CH2OCH2CH2OEt | Et | I | |
| 2-431 | CH2OCH2CH2OEt | n-Pr | | | |
| 2-432 | CH2OCH2CH2OEt | i-Pr | I | |
| 2-433 | CH2OCH2CH2CH2O Me | Me | I | |
| 2-434 | CH2OCH2CH2CH2O Me | Et | I | |
| 2-435 | CH2OCH2CH2CH2O Me | n-Pr | I | |
| 2-436 | CH2OCH2CH2CH2O Me | i-Pr | I | |
| 2-437 | CH2OCH2OMe | Me | I | |
| 2-438 | CH2OCH2OMe | Et | I | |
| 2-439 | CH2OCH2OMe | n-Pr | I | |
| 2-440 | CH2OCH2OMe | i-Pr | I | |
| 2-441 | CH2OCH2OEt | Me | I | |
| 2-442 | CH2OCH2OEt | Et | I | |
| 2-443 | CH2OCH2OEt | n-Pr | I | |
| 2-444 | CH2OCH2OEt | i-Pr | | | |
| 2-445 | CH2OCH2CH2SO2Me | Me | I | |
| 2-446 | CH2OCH2CH2SO2Me | Et | I | |
| 2-447 | CH2OCH2CH2SO2Me | n-Pr | I | |
| 2-448 | CH2OCH2CH2SO2Me | i-Pr | I |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCh] |
| 2-449 | CH2SO2CH2CH2OMe | Me | I | |
| 2-450 | CH2SO2CH2CH2OMe | Et | I | |
| 2-451 | CH2SO2CH2CH2OMe | n-Pr | I | |
| 2-452 | CH2SO2CH2CH2OMe | i-Pr | I | |
| 2-453 | CH2SO2CH2CH2SO2 Me | Me | I | |
| 2-454 | CH2SO2CH2CH2SO2 Me | Et | I | |
| 2-455 | CH2SO2CH2CH2SO2 Me | n-Pr | I | |
| 2-456 | CH2SO2CH2CH2SO2 Me | i-Pr | I | |
| 2-457 | Cl | Me | no2 | |
| 2-458 | Cl | Et | no2 | |
| 2-459 | Cl | n-Pr | no2 | |
| 2-460 | Cl | i-Pr | no2 | |
| 2-461 | Br | Me | no2 | |
| 2-462 | Br | Et | no2 | |
| 2-463 | Br | n-Pr | no2 | |
| 2-464 | Br | i-Pr | no2 | |
| 2-465 | Me | Me | no2 | |
| 2-466 | Me | Et | no2 | |
| 2-467 | Me | n-Pr | no2 | |
| 2-468 | Me | i-Pr | no2 | |
| 2-469 | Et | Me | no2 |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-470 | Et | Et | no2 | |
| 2-471 | Et | n-Pr | no2 | |
| 2-472 | Et | i-Pr | no2 | |
| 2-473 | cf3 | Me | no2 | |
| 2-474 | cf3 | Et | no2 | |
| 2-475 | cf3 | n-Pr | no2 | |
| 2-476 | cf3 | i-Pr | no2 | |
| 2-477 | OMe | Me | no2 | |
| 2-478 | OMe | Et | no2 | |
| 2-479 | OMe | n-Pr | no2 | |
| 2-480 | OMe | i-Pr | no2 | |
| 2-481 | OEt | Me | no2 | |
| 2-482 | OEt | Et | no2 | |
| 2-483 | OEt | n-Pr | no2 | |
| 2-484 | OEt | i-Pr | no2 | |
| 2-485 | no2 | Me | no2 | |
| 2-486 | no2 | Et | no2 | |
| 2-487 | no2 | n-Pr | no2 | |
| 2-488 | no2 | i-Pr | no2 | |
| 2-489 | SO2Me | Me | no2 | |
| 2-490 | SO2Me | Et | no2 | |
| 2-491 | SO2Me | n-Pr | no2 | |
| 2-492 | SO2Me | i-Pr | no2 | |
| 2-493 | CH2OMe | Me | no2 | |
| 2-494 | CH2OMe | Et | no2 |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-495 | CH2OMe | n-Pr | no2 | |
| 2-496 | CH2OMe | i-Pr | no2 | |
| 2-497 | CH2SO2Me | Me | no2 | |
| 2-498 | CH2SO2Me | Et | no2 | |
| 2-499 | CH2SO2Me | n-Pr | no2 | |
| 2-500 | CH2SO2Me | i-Pr | no2 | |
| 2-501 | CH2OCH2CH2OMe | Me | no2 | |
| 2-502 | CH2OCH2CH2OMe | Et | no2 | |
| 2-503 | CH2OCH2CH2OMe | n-Pr | no2 | |
| 2-504 | CH2OCH2CH2OMe | i-Pr | no2 | |
| 2-505 | CH2OCH2CH2OEt | Me | no2 | |
| 2-506 | CH2OCH2CH2OEt | Et | no2 | |
| 2-507 | CH2OCH2CH2OEt | n-Pr | no2 | |
| 2-508 | CH2OCH2CH2OEt | i-Pr | no2 | |
| 2-509 | CH2OCH2CH2CH2O Me | Me | no2 | |
| 2-510 | CH2OCH2CH2CH2O Me | Et | no2 | |
| 2-511 | CH2OCH2CH2CH2O Me | n-Pr | no2 | |
| 2-512 | CH2OCH2CH2CH2O Me | i-Pr | no2 | |
| 2-513 | CH2OCH2OMe | Me | no2 | |
| 2-514 | CH2OCH2OMe | Et | no2 | |
| 2-515 | CH2OCH2OMe | n-Pr | no2 |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 2-516 | CH2OCH2OMe | i-Pr | no2 | |
| 2-517 | CH2OCH2OEt | Me | no2 | |
| 2-518 | CH2OCH2OEt | Et | no2 | |
| 2-519 | CH2OCH2OEt | n-Pr | no2 | |
| 2-520 | CH2OCH2OEt | i-Pr | no2 | |
| 2-521 | CH2OCH2CH2SO2Me | Me | no2 | |
| 2-522 | CH2OCH2CH2SO2Me | Et | no2 | |
| 2-523 | CH2OCH2CH2SO2Me | n-Pr | no2 | |
| 2-524 | CH2OCH2CH2SO2Me | i-Pr | no2 | |
| 2-525 | CH2SO2CH2CH2OMe | Me | no2 | |
| 2-526 | CH2SO2CH2CH2OMe | Et | no2 | |
| 2-527 | CH2SO2CH2CH2OMe | n-Pr | no2 | |
| 2-528 | CH2SO2CH2CH2OMe | i-Pr | no2 | |
| 2-529 | CH2SO2CH2CH2SO2 Me | Me | no2 | |
| 2-530 | CH2SO2CH2CH2SO2 Me | Et | no2 | |
| 2-531 | CH2SO2CH2CH2SO2 Me | n-Pr | no2 | |
| 2-532 | CH2SO2CH2CH2SO2 Me | i-Pr | no2 |
Tabela 3
Compostos de Fórmula (I) de Acordo com a Presente Invenção em que R4 é
Hidrogênio e R1 e R2 são Metila
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-1 | Cl | Me | SO2Me | |
| 3-2 | Cl | Et | SO2Me | |
| 3-3 | Cl | n-Pr | SO2Me | |
| 3-4 | Cl | i-Pr | SO2Me | |
| 3-5 | Br | Me | SO2Me | |
| 3-6 | Br | Et | SO2Me | |
| 3-7 | Br | n-Pr | SO2Me | |
| 3-8 | Br | i-Pr | SO2Me | |
| 3-9 | Me | Me | SO2Me | 8,09 (d, 1H), 7,49 (d, 1H), 3,64 (s, 3H), 3,38 (s, 3H), 3,18 (s, 3H), 2,81 (s, 3H), 1,69 (s, 3H) |
| 3-10 | Me | Et | SO2Me | |
| 3-11 | Me | n-Pr | SO2Me | |
| 3-12 | Me | i-Pr | SO2Me | |
| 3-13 | Et | Me | SO2Me | |
| 3-14 | Et | Et | SO2Me | |
| 3-15 | Et | n-Pr | SO2Me |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-16 | Et | i-Pr | SO2Me | |
| 3-17 | cf3 | Me | SO2Me | |
| 3-18 | cf3 | Et | SO2Me | |
| 3-19 | cf3 | n-Pr | SO2Me | |
| 3-20 | cf3 | i-Pr | SO2Me | |
| 3-21 | OMe | Me | SO2Me | |
| 3-22 | OMe | Et | SO2Me | |
| 3-23 | OMe | n-Pr | SO2Me | |
| 3-24 | OMe | i-Pr | SO2Me | |
| 3-25 | OEt | Me | SO2Me | |
| 3-26 | OEt | Et | SO2Me | |
| 3-27 | OEt | n-Pr | SO2Me | |
| 3-28 | OEt | i-Pr | SO2Me | |
| 3-29 | no2 | Me | SO2Me | |
| 3-30 | no2 | Et | SO2Me | |
| 3-31 | no2 | n-Pr | SO2Me | |
| 3-32 | no2 | i-Pr | SO2Me | |
| 3-33 | SO2Me | Me | SO2Me | |
| 3-34 | SO2Me | Et | SO2Me | |
| 3-35 | SO2Me | n-Pr | SO2Me | |
| 3-36 | SO2Me | i-Pr | SO2Me | |
| 3-37 | CH2OMe | Me | SO2Me | |
| 3-38 | CH2OMe | Et | SO2Me | |
| 3-39 | CH2OMe | n-Pr | SO2Me | |
| 3-40 | CH2OMe | i-Pr | SO2Me |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-41 | CH2SO2Me | Me | SO2Me | |
| 3-42 | CH2SO2Me | Et | SO2Me | |
| 3-43 | CH2SO2Me | n-Pr | SO2Me | |
| 3-44 | CH2SO2Me | i-Pr | SO2Me | |
| 3-45 | CH2OCH2CH2OMe | Me | SO2Me | |
| 3-46 | CH2OCH2CH2OMe | Et | SO2Me | |
| 3-47 | CH2OCH2CH2OMe | n-Pr | SO2Me | |
| 3-48 | CH2OCH2CH2OMe | i-Pr | SO2Me | |
| 3-49 | CH2OCH2CH2OEt | Me | SO2Me | |
| 3-50 | CH2OCH2CH2OEt | Et | SO2Me | |
| 3-51 | CH2OCH2CH2OEt | n-Pr | SO2Me | |
| 3-52 | CH2OCH2CH2OEt | i-Pr | SO2Me | |
| 3-53 | CH2OCH2CH2CH2O Me | Me | SO2Me | |
| 3-54 | CH2OCH2CH2CH2O Me | Et | SO2Me | |
| 3-55 | CH2OCH2CH2CH2O Me | n-Pr | SO2Me | |
| 3-56 | CH2OCH2CH2CH2O Me | i-Pr | SO2Me | |
| 3-57 | CH2OCH2OMe | Me | SO2Me | |
| 3-58 | CH2OCH2OMe | Et | SO2Me | |
| 3-59 | CH2OCH2OMe | n-Pr | SO2Me | |
| 3-60 | CH2OCH2OMe | i-Pr | SO2Me | |
| 3-61 | CH2OCH2OEt | Me | SO2Me |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-62 | CH2OCH2OEt | Et | SO2Me | |
| 3-63 | CH2OCH2OEt | n-Pr | SO2Me | |
| 3-64 | CH2OCH2OEt | i-Pr | SO2Me | |
| 3-65 | CH2OCH2CH2SO2Me | Me | SO2Me | |
| 3-66 | CH2OCH2CH2SO2Me | Et | SO2Me | |
| 3-67 | CH2OCH2CH2SO2Me | n-Pr | SO2Me | |
| 3-68 | CH2OCH2CH2SO2Me | i-Pr | SO2Me | |
| 3-69 | CH2SO2CH2CH2OMe | Me | SO2Me | |
| 3-70 | CH2SO2CH2CH2OMe | Et | SO2Me | |
| 3-71 | CH2SO2CH2CH2OMe | n-Pr | SO2Me | |
| 3-72 | CH2SO2CH2CH2OMe | i-Pr | SO2Me | |
| 3-73 | CH2SO2CH2CH2SO2 Me | Me | SO2Me | |
| 3-74 | CH2SO2CH2CH2SO2 Me | Et | SO2Me | |
| 3-75 | CH2SO2CH2CH2SO2 Me | n-Pr | SO2Me | |
| 3-76 | CH2SO2CH2CH2SO2 Me | i-Pr | SO2Me | |
| 3-77 | Cl | Me | SO2Et | |
| 3-78 | Cl | Et | SO2Et | |
| 3-79 | Cl | n-Pr | SO2Et | |
| 3-80 | Cl | i-Pr | SO2Et | |
| 3-81 | Br | Me | SO2Et | |
| 3-82 | Br | Et | SO2Et |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-83 | Br | n-Pr | SO2Et | |
| 3-84 | Br | i-Pr | SO2Et | |
| 3-85 | Me | Me | SO2Et | |
| 3-86 | Me | Et | SO2Et | |
| 3-87 | Me | n-Pr | SO2Et | |
| 3-88 | Me | i-Pr | SO2Et | |
| 3-89 | Et | Me | SO2Et | |
| 3-90 | Et | Et | SO2Et | |
| 3-91 | Et | n-Pr | SO2Et | |
| 3-92 | Et | i-Pr | SO2Et | |
| 3-93 | cf3 | Me | SO2Et | |
| 3-94 | cf3 | Et | SO2Et | |
| 3-95 | cf3 | n-Pr | SO2Et | |
| 3-96 | cf3 | i-Pr | SO2Et | |
| 3-97 | OMe | Me | SO2Et | |
| 3-98 | OMe | Et | SO2Et | |
| 3-99 | OMe | n-Pr | SO2Et | |
| 3-100 | OMe | i-Pr | SO2Et | |
| 3-101 | OEt | Me | SO2Et | |
| 3-102 | OEt | Et | SO2Et | |
| 3-103 | OEt | n-Pr | SO2Et | |
| 3-104 | OEt | i-Pr | SO2Et | |
| 3-105 | no2 | Me | SO2Et | |
| 3-106 | no2 | Et | SO2Et | |
| 3-107 | no2 | n-Pr | SO2Et |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-108 | no2 | i-Pr | SO2Et | |
| 3-109 | SO2Me | Me | SO2Et | |
| 3-110 | SO2Me | Et | SO2Et | |
| 3-111 | SO2Me | n-Pr | SO2Et | |
| 3-112 | SO2Me | i-Pr | SO2Et | |
| 3-113 | CH2OMe | Me | SO2Et | |
| 3-114 | CH2OMe | Et | SO2Et | |
| 3-115 | CH2OMe | n-Pr | SO2Et | |
| 3-116 | CH2OMe | i-Pr | SO2Et | |
| 3-117 | CH2SO2Me | Me | SO2Et | |
| 3-118 | CH2SO2Me | Et | SO2Et | |
| 3-119 | CH2SO2Me | n-Pr | SO2Et | |
| 3-120 | CH2SO2Me | i-Pr | SO2Et | |
| 3-121 | CH2OCH2CH2OMe | Me | SO2Et | |
| 3-122 | CH2OCH2CH2OMe | Et | SO2Et | |
| 3-123 | CH2OCH2CH2OMe | n-Pr | SO2Et | |
| 3-124 | CH2OCH2CH2OMe | i-Pr | SO2Et | |
| 3-125 | CH2OCH2CH2OEt | Me | SO2Et | |
| 3-126 | CH2OCH2CH2OEt | Et | SO2Et | |
| 3-127 | CH2OCH2CH2OEt | n-Pr | SO2Et | |
| 3-128 | CH2OCH2CH2OEt | i-Pr | SO2Et | |
| 3-129 | CH2OCH2CH2CH2O Me | Me | SO2Et | |
| 3-130 | CH2OCH2CH2CH2O Me | Et | SO2Et |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-131 | CH2OCH2CH2CH2O Me | n-Pr | SO2Et | |
| 3-132 | CH2OCH2CH2CH2O Me | i-Pr | SO2Et | |
| 3-133 | CH2OCH2OMe | Me | SO2Et | |
| 3-134 | CH2OCH2OMe | Et | SO2Et | |
| 3-135 | CH2OCH2OMe | n-Pr | SO2Et | |
| 3-136 | CH2OCH2OMe | i-Pr | SO2Et | |
| 3-137 | CH2OCH2OEt | Me | SO2Et | |
| 3-138 | CH2OCH2OEt | Et | SO2Et | |
| 3-139 | CH2OCH2OEt | n-Pr | SO2Et | |
| 3-140 | CH2OCH2OEt | i-Pr | SO2Et | |
| 3-141 | CH2OCH2CH2SO2Me | Me | SO2Et | |
| 3-142 | CH2OCH2CH2SO2Me | Et | SO2Et | |
| 3-143 | CH2OCH2CH2SO2Me | n-Pr | SO2Et | |
| 3-144 | CH2OCH2CH2SO2Me | i-Pr | SO2Et | |
| 3-145 | CH2SO2CH2CH2OMe | Me | SO2Et | |
| 3-146 | CH2SO2CH2CH2OMe | Et | SO2Et | |
| 3-147 | CH2SO2CH2CH2OMe | n-Pr | SO2Et | |
| 3-148 | CH2SO2CH2CH2OMe | i-Pr | SO2Et | |
| 3-149 | CH2SO2CH2CH2SO2 Me | Me | SO2Et | |
| 3-150 | CH2SO2CH2CH2SO2 Me | Et | SO2Et | |
| 3-151 | CH2SO2CH2CH2SO2 | n-Pr | SO2Et |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| Me | ||||
| 3-152 | CH2SO2CH2CH2SO2 Me | i-Pr | SO2Et | |
| 3-153 | Cl | Me | F | |
| 3-154 | Cl | Et | F | |
| 3-155 | Cl | n-Pr | F | |
| 3-156 | Cl | i-Pr | F | |
| 3-157 | Br | Me | F | |
| 3-158 | Br | Et | F | |
| 3-159 | Br | n-Pr | F | |
| 3-160 | Br | i-Pr | F | |
| 3-161 | Me | Me | F | |
| 3-162 | Me | Et | F | |
| 3-163 | Me | n-Pr | F | |
| 3-164 | Me | i-Pr | F | |
| 3-165 | Et | Me | F | |
| 3-166 | Et | Et | F | |
| 3-167 | Et | n-Pr | F | |
| 3-168 | Et | i-Pr | F | |
| 3-169 | cf3 | Me | F | |
| 3-170 | cf3 | Et | F | |
| 3-171 | cf3 | n-Pr | F | |
| 3-172 | cf3 | i-Pr | F | |
| 3-173 | OMe | Me | F | |
| 3-174 | OMe | Et | F |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCh] |
| 3-175 | OMe | n-Pr | F | |
| 3-176 | OMe | i-Pr | F | |
| 3-177 | OEt | Me | F | |
| 3-178 | OEt | Et | F | |
| 3-179 | OEt | n-Pr | F | |
| 3-180 | OEt | i-Pr | F | |
| 3-181 | no2 | Me | F | |
| 3-182 | no2 | Et | F | |
| 3-183 | no2 | n-Pr | F | |
| 3-184 | no2 | i-Pr | F | |
| 3-185 | SO2Me | Me | F | |
| 3-186 | SO2Me | Et | F | |
| 3-187 | SO2Me | n-Pr | F | |
| 3-188 | SO2Me | i-Pr | F | |
| 3-189 | CH2OMe | Me | F | |
| 3-190 | CH2OMe | Et | F | |
| 3-191 | CH2OMe | n-Pr | F | |
| 3-192 | CH2OMe | i-Pr | F | |
| 3-193 | CH2SO2Me | Me | F | |
| 3-194 | CH2SO2Me | Et | F | |
| 3-195 | CH2SO2Me | n-Pr | F | |
| 3-196 | CH2SO2Me | i-Pr | F | |
| 3-197 | CH2OCH2CH2OMe | Me | F | |
| 3-198 | CH2OCH2CH2OMe | Et | F | |
| 3-199 | CH2OCH2CH2OMe | n-Pr | F |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-200 | CH2OCH2CH2OMe | i-Pr | F | |
| 3-201 | CH2OCH2CH2OEt | Me | F | |
| 3-202 | CH2OCH2CH2OEt | Et | F | |
| 3-203 | CH2OCH2CH2OEt | n-Pr | F | |
| 3-204 | CH2OCH2CH2OEt | i-Pr | F | |
| 3-205 | CH2OCH2CH2CH2O Me | Me | F | |
| 3-206 | CH2OCH2CH2CH2O Me | Et | F | |
| 3-207 | CH2OCH2CH2CH2O Me | n-Pr | F | |
| 3-208 | CH2OCH2CH2CH2O Me | i-Pr | F | |
| 3-209 | CH2OCH2OMe | Me | F | |
| 3-210 | CH2OCH2OMe | Et | F | |
| 3-211 | CH2OCH2OMe | n-Pr | F | |
| 3-212 | CH2OCH2OMe | i-Pr | F | |
| 3-213 | CH2OCH2OEt | Me | F | |
| 3-214 | CH2OCH2OEt | Et | F | |
| 3-215 | CH2OCH2OEt | n-Pr | F | |
| 3-216 | CH2OCH2OEt | i-Pr | F | |
| 3-217 | CH2OCH2CH2SO2Me | Me | F | |
| 3-218 | CH2OCH2CH2SO2Me | Et | F | |
| 3-219 | CH2OCH2CH2SO2Me | n-Pr | F | |
| 3-220 | CH2OCH2CH2SO2Me | i-Pr | F |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-221 | CH2SO2CH2CH2OMe | Me | F | |
| 3-222 | CH2SO2CH2CH2OMe | Et | F | |
| 3-223 | CH2SO2CH2CH2OMe | n-Pr | F | |
| 3-224 | CH2SO2CH2CH2OMe | i-Pr | F | |
| 3-225 | CH2SO2CH2CH2SO2 Me | Me | F | |
| 3-226 | CH2SO2CH2CH2SO2 Me | Et | F | |
| 3-227 | CH2SO2CH2CH2SO2 Me | n-Pr | F | |
| 3-228 | CH2SO2CH2CH2SO2 Me | i-Pr | F | |
| 3-229 | Cl | Me | Cl | |
| 3-230 | Cl | Et | Cl | |
| 3-231 | Cl | n-Pr | Cl | |
| 3-232 | Cl | i-Pr | Cl | |
| 3-233 | Br | Me | Cl | |
| 3-234 | Br | Et | Cl | |
| 3-235 | Br | n-Pr | Cl | |
| 3-236 | Br | i-Pr | Cl | |
| 3-237 | Me | Me | Cl | 7,37 (d, 1H), 7,23 (d, 1H), 3,63 (s, 3H), 3,01 (s, 3H), 2,68 (s, 3H), 1,72 (s, 3H) |
| 3-238 | Me | Et | Cl | 7,37 (d, 1H), 7,23 (d, |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 1H), 3,63 (s, 3H), 3,36 (m, 1H), 3,16 (m, 1H), 2,63 (s, 3H), 1,72 (s, 3H), 1,40 (t, 3H) | ||||
| 3-239 | Me | n-Pr | Cl | |
| 3-240 | Me | i-Pr | Cl | |
| 3-241 | Et | Me | Cl | |
| 3-242 | Et | Et | Cl | |
| 3-243 | Et | n-Pr | Cl | |
| 3-244 | Et | i-Pr | Cl | |
| 3-245 | cf3 | Me | Cl | |
| 3-246 | cf3 | Et | Cl | |
| 3-247 | cf3 | n-Pr | Cl | |
| 3-248 | cf3 | i-Pr | Cl | |
| 3-249 | OMe | Me | Cl | |
| 3-250 | OMe | Et | Cl | |
| 3-251 | OMe | n-Pr | Cl | |
| 3-252 | OMe | i-Pr | Cl | |
| 3-253 | OEt | Me | Cl | |
| 3-254 | OEt | Et | Cl | |
| 3-255 | OEt | n-Pr | Cl | |
| 3-256 | OEt | i-Pr | Cl | |
| 3-257 | no2 | Me | Cl | |
| 3-258 | no2 | Et | Cl | |
| 3-259 | no2 | n-Pr | Cl |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-260 | no2 | i-Pr | Cl | |
| 3-261 | SO2Me | Me | Cl | |
| 3-262 | SO2Me | Et | Cl | |
| 3-263 | SO2Me | n-Pr | Cl | |
| 3-264 | SO2Me | i-Pr | Cl | |
| 3-265 | CH2OMe | Me | Cl | |
| 3-266 | CH2OMe | Et | Cl | |
| 3-267 | CH2OMe | n-Pr | Cl | |
| 3-268 | CH2OMe | i-Pr | Cl | |
| 3-269 | CH2SO2Me | Me | Cl | |
| 3-270 | CH2SO2Me | Et | Cl | |
| 3-271 | CH2SO2Me | n-Pr | Cl | |
| 3-272 | CH2SO2Me | i-Pr | Cl | |
| 3-273 | CH2OCH2CH2OMe | Me | Cl | |
| 3-274 | CH2OCH2CH2OMe | Et | Cl | |
| 3-275 | CH2OCH2CH2OMe | n-Pr | Cl | |
| 3-276 | CH2OCH2CH2OMe | i-Pr | Cl | |
| 3-277 | CH2OCH2CH2OEt | Me | Cl | |
| 3-278 | CH2OCH2CH2OEt | Et | Cl | |
| 3-279 | CH2OCH2CH2OEt | n-Pr | Cl | |
| 3-280 | CH2OCH2CH2OEt | i-Pr | Cl | |
| 3-281 | CH2OCH2CH2CH2O Me | Me | Cl | |
| 3-282 | CH2OCH2CH2CH2O Me | Et | Cl |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-283 | CH2OCH2CH2CH2O Me | n-Pr | Cl | |
| 3-284 | CH2OCH2CH2CH2O Me | i-Pr | Cl | |
| 3-285 | CH2OCH2OMe | Me | Cl | |
| 3-286 | CH2OCH2OMe | Et | Cl | |
| 3-287 | CH2OCH2OMe | n-Pr | Cl | |
| 3-288 | CH2OCH2OMe | i-Pr | Cl | |
| 3-289 | CH2OCH2OEt | Me | Cl | |
| 3-290 | CH2OCH2OEt | Et | Cl | |
| 3-291 | CH2OCH2OEt | n-Pr | Cl | |
| 3-292 | CH2OCH2OEt | i-Pr | Cl | |
| 3-293 | CH2OCH2CH2SO2Me | Me | Cl | |
| 3-294 | CH2OCH2CH2SO2Me | Et | Cl | |
| 3-295 | CH2OCH2CH2SO2Me | n-Pr | Cl | |
| 3-296 | CH2OCH2CH2SO2Me | i-Pr | Cl | |
| 3-297 | CH2SO2CH2CH2OMe | Me | Cl | |
| 3-298 | CH2SO2CH2CH2OMe | Et | Cl | |
| 3-299 | CH2SO2CH2CH2OMe | n-Pr | Cl | |
| 3-300 | CH2SO2CH2CH2OMe | i-Pr | Cl | |
| 3-301 | CH2SO2CH2CH2SO2 Me | Me | Cl | |
| 3-302 | CH2SO2CH2CH2SO2 Me | Et | Cl | |
| 3-303 | CH2SO2CH2CH2SO2 | n-Pr | Cl |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| Me | ||||
| 3-304 | CH2SO2CH2CH2SO2 Me | i-Pr | Cl | |
| 3-305 | Cl | Me | Br | |
| 3-306 | Cl | Et | Br | |
| 3-307 | Cl | n-Pr | Br | |
| 3-308 | Cl | i-Pr | Br | |
| 3-309 | Br | Me | Br | |
| 3-310 | Br | Et | Br | |
| 3-311 | Br | n-Pr | Br | |
| 3-312 | Br | i-Pr | Br | |
| 3-313 | Me | Me | Br | 7,57 (d, 1H), 7,16 (d, 1H), 3,67 (s, 3H), 3,02 (s, 3H), 2,69 (s, 3H), 1,75 (s, 3H) |
| 3-314 | Me | Et | Br | |
| 3-315 | Me | n-Pr | Br | |
| 3-316 | Me | i-Pr | Br | |
| 3-317 | Et | Me | Br | |
| 3-318 | Et | Et | Br | |
| 3-319 | Et | n-Pr | Br | |
| 3-320 | Et | i-Pr | Br | |
| 3-321 | cf3 | Me | Br | |
| 3-322 | cf3 | Et | Br | |
| 3-323 | cf3 | n-Pr | Br |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-324 | cf3 | i-Pr | Br | |
| 3-325 | OMe | Me | Br | |
| 3-326 | OMe | Et | Br | |
| 3-327 | OMe | n-Pr | Br | |
| 3-328 | OMe | i-Pr | Br | |
| 3-329 | OEt | Me | Br | |
| 3-330 | OEt | Et | Br | |
| 3-331 | OEt | n-Pr | Br | |
| 3-332 | OEt | i-Pr | Br | |
| 3-333 | no2 | Me | Br | |
| 3-334 | no2 | Et | Br | |
| 3-335 | no2 | n-Pr | Br | |
| 3-336 | no2 | i-Pr | Br | |
| 3-337 | SO2Me | Me | Br | |
| 3-338 | SO2Me | Et | Br | |
| 3-339 | SO2Me | n-Pr | Br | |
| 3-340 | SO2Me | i-Pr | Br | |
| 3-341 | CH2OMe | Me | Br | |
| 3-342 | CH2OMe | Et | Br | |
| 3-343 | CH2OMe | n-Pr | Br | |
| 3-344 | CH2OMe | i-Pr | Br | |
| 3-345 | CH2SO2Me | Me | Br | |
| 3-346 | CH2SO2Me | Et | Br | |
| 3-347 | CH2SO2Me | n-Pr | Br | |
| 3-348 | CH2SO2Me | i-Pr | Br |
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-349 | CH2OCH2CH2OMe | Me | Br | |
| 3-350 | CH2OCH2CH2OMe | Et | Br | |
| 3-351 | CH2OCH2CH2OMe | n-Pr | Br | |
| 3-352 | CH2OCH2CH2OMe | i-Pr | Br | |
| 3-353 | CH2OCH2CH2OEt | Me | Br | |
| 3-354 | CH2OCH2CH2OEt | Et | Br | |
| 3-355 | CH2OCH2CH2OEt | n-Pr | Br | |
| 3-356 | CH2OCH2CH2OEt | i-Pr | Br | |
| 3-357 | CH2OCH2CH2CH2O Me | Me | Br | |
| 3-358 | CH2OCH2CH2CH2O Me | Et | Br | |
| 3-359 | CH2OCH2CH2CH2O Me | n-Pr | Br | |
| 3-360 | CH2OCH2CH2CH2O Me | i-Pr | Br | |
| 3-361 | CH2OCH2OMe | Me | Br | |
| 3-362 | CH2OCH2OMe | Et | Br | |
| 3-363 | CH2OCH2OMe | n-Pr | Br | |
| 3-364 | CH2OCH2OMe | i-Pr | Br | |
| 3-365 | CH2OCH2OEt | Me | Br | |
| 3-366 | CH2OCH2OEt | Et | Br | |
| 3-367 | CH2OCH2OEt | n-Pr | Br | |
| 3-368 | CH2OCH2OEt | i-Pr | Br | |
| 3-369 | CH2OCH2CH2SO2Me | Me | Br |
100
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-370 | CH2OCH2CH2SO2Me | Et | Br | |
| 3-371 | CH2OCH2CH2SO2Me | n-Pr | Br | |
| 3-372 | CH2OCH2CH2SO2Me | i-Pr | Br | |
| 3-373 | CH2SO2CH2CH2OMe | Me | Br | |
| 3-374 | CH2SO2CH2CH2OMe | Et | Br | |
| 3-375 | CH2SO2CH2CH2OMe | n-Pr | Br | |
| 3-376 | CH2SO2CH2CH2OMe | i-Pr | Br | |
| 3-377 | CH2SO2CH2CH2SO2 Me | Me | Br | |
| 3-378 | CH2SO2CH2CH2SO2 Me | Et | Br | |
| 3-379 | CH2SO2CH2CH2SO2 Me | n-Pr | Br | |
| 3-380 | CH2SO2CH2CH2SO2 Me | i-Pr | Br | |
| 3-381 | Cl | Me | I | |
| 3-382 | Cl | Et | I | |
| 3-383 | Cl | n-Pr | I | |
| 3-384 | Cl | i-Pr | I | |
| 3-385 | Br | Me | I | |
| 3-386 | Br | Et | I | |
| 3-387 | Br | n-Pr | I | |
| 3-388 | Br | i-Pr | I | |
| 3-389 | Me | Me | I | 7,68 (d, 1H), 6,96 (d, 1H), 3,65 (s, 3H), 2,96 |
101
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| (s, 3H), 2,68 (s, 3H), 1,74 (s, 3H) | ||||
| 3-390 | Me | Et | I | |
| 3-391 | Me | n-Pr | I | |
| 3-392 | Me | i-Pr | I | |
| 3-393 | Et | Me | I | |
| 3-394 | Et | Et | | | |
| 3-395 | Et | n-Pr | I | |
| 3-396 | Et | i-Pr | I | |
| 3-397 | cf3 | Me | I | |
| 3-398 | cf3 | Et | I | |
| 3-399 | cf3 | n-Pr | I | |
| 3-400 | cf3 | i-Pr | I | |
| 3-401 | OMe | Me | I | |
| 3-402 | OMe | Et | I | |
| 3-403 | OMe | n-Pr | I | |
| 3-404 | OMe | i-Pr | I | |
| 3-405 | OEt | Me | I | |
| 3-406 | OEt | Et | I | |
| 3-407 | OEt | n-Pr | I | |
| 3-408 | OEt | i-Pr | I | |
| 3-409 | no2 | Me | I | |
| 3-410 | no2 | Et | I | |
| 3-411 | no2 | n-Pr | | | |
| 3-412 | no2 | i-Pr | I |
102
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-413 | SO2Me | Me | I | |
| 3-414 | SO2Me | Et | I | |
| 3-415 | SO2Me | n-Pr | I | |
| 3-416 | SO2Me | i-Pr | I | |
| 3-417 | CH2OMe | Me | | | |
| 3-418 | CH2OMe | Et | I | |
| 3-419 | CH2OMe | n-Pr | I | |
| 3-420 | CH2OMe | i-Pr | I | |
| 3-421 | CH2SO2Me | Me | I | |
| 3-422 | CH2SO2Me | Et | I | |
| 3-423 | CH2SO2Me | n-Pr | I | |
| 3-424 | CH2SO2Me | i-Pr | I | |
| 3-425 | CH2OCH2CH2OMe | Me | I | |
| 3-426 | CH2OCH2CH2OMe | Et | I | |
| 3-427 | CH2OCH2CH2OMe | n-Pr | I | |
| 3-428 | CH2OCH2CH2OMe | i-Pr | I | |
| 3-429 | CH2OCH2CH2OEt | Me | I | |
| 3-430 | CH2OCH2CH2OEt | Et | I | |
| 3-431 | CH2OCH2CH2OEt | n-Pr | | | |
| 3-432 | CH2OCH2CH2OEt | i-Pr | I | |
| 3-433 | CH2OCH2CH2CH2O Me | Me | I | |
| 3-434 | CH2OCH2CH2CH2O Me | Et | I | |
| 3-435 | CH2OCH2CH2CH2O | n-Pr | | |
103
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| Me | ||||
| 3-436 | CH2OCH2CH2CH2O Me | i-Pr | I | |
| 3-437 | CH2OCH2OMe | Me | I | |
| 3-438 | CH2OCH2OMe | Et | I | |
| 3-439 | CH2OCH2OMe | n-Pr | I | |
| 3-440 | CH2OCH2OMe | i-Pr | I | |
| 3-441 | CH2OCH2OEt | Me | I | |
| 3-442 | CH2OCH2OEt | Et | I | |
| 3-443 | CH2OCH2OEt | n-Pr | I | |
| 3-444 | CH2OCH2OEt | i-Pr | I | |
| 3-445 | CH2OCH2CH2SO2Me | Me | I | |
| 3-446 | CH2OCH2CH2SO2Me | Et | | | |
| 3-447 | CH2OCH2CH2SO2Me | n-Pr | I | |
| 3-448 | CH2OCH2CH2SO2Me | i-Pr | | | |
| 3-449 | CH2SO2CH2CH2OMe | Me | I | |
| 3-450 | CH2SO2CH2CH2OMe | Et | I | |
| 3-451 | CH2SO2CH2CH2OMe | n-Pr | I | |
| 3-452 | CH2SO2CH2CH2OMe | i-Pr | I | |
| 3-453 | CH2SO2CH2CH2SO2 Me | Me | I | |
| 3-454 | CH2SO2CH2CH2SO2 Me | Et | I | |
| 3-455 | CH2SO2CH2CH2SO2 Me | n-Pr | I |
104
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-456 | CH2SO2CH2CH2SO2 Me | i-Pr | I | |
| 3-457 | Cl | Me | no2 | |
| 3-458 | Cl | Et | no2 | |
| 3-459 | Cl | n-Pr | no2 | |
| 3-460 | Cl | i-Pr | no2 | |
| 3-461 | Br | Me | no2 | |
| 3-462 | Br | Et | no2 | |
| 3-463 | Br | n-Pr | no2 | |
| 3-464 | Br | i-Pr | no2 | |
| 3-465 | Me | Me | no2 | |
| 3-466 | Me | Et | no2 | |
| 3-467 | Me | n-Pr | no2 | |
| 3-468 | Me | i-Pr | no2 | |
| 3-469 | Et | Me | no2 | |
| 3-470 | Et | Et | no2 | |
| 3-471 | Et | n-Pr | no2 | |
| 3-472 | Et | i-Pr | no2 | |
| 3-473 | cf3 | Me | no2 | |
| 3-474 | cf3 | Et | no2 | |
| 3-475 | cf3 | n-Pr | no2 | |
| 3-476 | cf3 | i-Pr | no2 | |
| 3-477 | OMe | Me | no2 | |
| 3-478 | OMe | Et | no2 | |
| 3-479 | OMe | n-Pr | no2 |
105
| Ν° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-480 | OMe | i-Pr | no2 | |
| 3-481 | OEt | Me | no2 | |
| 3-482 | OEt | Et | no2 | |
| 3-483 | OEt | n-Pr | no2 | |
| 3-484 | OEt | i-Pr | no2 | |
| 3-485 | no2 | Me | no2 | |
| 3-486 | no2 | Et | no2 | |
| 3-487 | no2 | n-Pr | no2 | |
| 3-488 | no2 | i-Pr | no2 | |
| 3-489 | SO2Me | Me | no2 | |
| 3-490 | SO2Me | Et | no2 | |
| 3-491 | SO2Me | n-Pr | no2 | |
| 3-492 | SO2Me | i-Pr | no2 | |
| 3-493 | CH2OMe | Me | no2 | |
| 3-494 | CH2OMe | Et | no2 | |
| 3-495 | CH2OMe | n-Pr | no2 | |
| 3-496 | CH2OMe | i-Pr | no2 | |
| 3-497 | CH2SO2Me | Me | no2 | |
| 3-498 | CH2SO2Me | Et | no2 | |
| 3-499 | CH2SO2Me | n-Pr | no2 | |
| 3-500 | CH2SO2Me | i-Pr | no2 | |
| 3-501 | CH2OCH2CH2OMe | Me | no2 | |
| 3-502 | CH2OCH2CH2OMe | Et | no2 | |
| 3-503 | CH2OCH2CH2OMe | n-Pr | no2 | |
| 3-504 | CH2OCH2CH2OMe | i-Pr | no2 |
106
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-505 | CH2OCH2CH2OEt | Me | no2 | |
| 3-506 | CH2OCH2CH2OEt | Et | no2 | |
| 3-507 | CH2OCH2CH2OEt | n-Pr | no2 | |
| 3-508 | CH2OCH2CH2OEt | i-Pr | no2 | |
| 3-509 | CH2OCH2CH2CH2O Me | Me | no2 | |
| 3-510 | CH2OCH2CH2CH2O Me | Et | no2 | |
| 3-511 | CH2OCH2CH2CH2O Me | n-Pr | no2 | |
| 3-512 | CH2OCH2CH2CH2O Me | i-Pr | no2 | |
| 3-513 | CH2OCH2OMe | Me | no2 | |
| 3-514 | CH2OCH2OMe | Et | no2 | |
| 3-515 | CH2OCH2OMe | n-Pr | no2 | |
| 3-516 | CH2OCH2OMe | i-Pr | no2 | |
| 3-517 | CH2OCH2OEt | Me | no2 | |
| 3-518 | CH2OCH2OEt | Et | no2 | |
| 3-519 | CH2OCH2OEt | n-Pr | no2 | |
| 3-520 | CH2OCH2OEt | i-Pr | no2 | |
| 3-521 | CH2OCH2CH2SO2Me | Me | no2 | |
| 3-522 | CH2OCH2CH2SO2Me | Et | no2 | |
| 3-523 | CH2OCH2CH2SO2Me | n-Pr | no2 | |
| 3-524 | CH2OCH2CH2SO2Me | i-Pr | no2 | |
| 3-525 | CH2SO2CH2CH2OMe | Me | no2 |
107
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 3-526 | CH2SO2CH2CH2OMe | Et | no2 | |
| 3-527 | CH2SO2CH2CH2OMe | n-Pr | no2 | |
| 3-528 | CH2SO2CH2CH2OMe | i-Pr | no2 | |
| 3-529 | CH2SO2CH2CH2SO2 Me | Me | no2 | |
| 3-530 | CH2SO2CH2CH2SO2 Me | Et | no2 | |
| 3-531 | CH2SO2CH2CH2SO2 Me | n-Pr | no2 | |
| 3-532 | CH2SO2CH2CH2SO2 Me | i-Pr | no2 |
Tabela 4
Compostos de Fórmula (II) de Acordo com a Presente Invenção
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-1 | Cl | Me | SO2Me | |
| 4-2 | Cl | Et | SO2Me | |
| 4-3 | Cl | n-Pr | SO2Me | |
| 4-4 | Cl | i-Pr | SO2Me | |
| 4-5 | Br | Me | SO2Me | |
| 4-6 | Br | Et | SO2Me | |
| 4-7 | Br | n-Pr | SO2Me |
108
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-8 | Br | i-Pr | SO2Me | |
| 4-9 | Me | Me | SO2Me | (DMSO-d6): 7,93 (s, 2H), 3,46 (s, 3H), 3,08 (s, 3H), 2,87 (s, 3H) |
| 4-10 | Me | Et | SO2Me | (DMSO-d6): 7,93 (s, 2H), 3,47 (m, 1H), 3,46 (s, 3H), 3,08 (m, 1H), 2,82 (s, 3H), 1,33 (t, 3H) |
| 4-11 | Me | n-Pr | SO2Me | |
| 4-12 | Me | i-Pr | SO2Me | |
| 4-13 | Et | Me | SO2Me | |
| 4-14 | Et | Et | SO2Me | |
| 4-15 | Et | n-Pr | SO2Me | |
| 4-16 | Et | i-Pr | SO2Me | |
| 4-17 | cf3 | Me | SO2Me | |
| 4-18 | cf3 | Et | SO2Me | |
| 4-19 | cf3 | n-Pr | SO2Me | |
| 4-20 | cf3 | i-Pr | SO2Me | |
| 4-21 | OMe | Me | SO2Me | |
| 4-22 | OMe | Et | SO2Me | |
| 4-23 | OMe | n-Pr | SO2Me | |
| 4-24 | OMe | i-Pr | SO2Me | |
| 4-25 | OEt | Me | SO2Me | |
| 4-26 | OEt | Et | SO2Me |
109
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-27 | OEt | n-Pr | SO2Me | |
| 4-28 | OEt | i-Pr | SO2Me | |
| 4-29 | no2 | Me | SO2Me | |
| 4-30 | no2 | Et | SO2Me | |
| 4-31 | no2 | n-Pr | SO2Me | |
| 4-32 | no2 | i-Pr | SO2Me | |
| 4-33 | SO2Me | Me | SO2Me | |
| 4-34 | SO2Me | Et | SO2Me | |
| 4-35 | SO2Me | n-Pr | SO2Me | |
| 4-36 | SO2Me | i-Pr | SO2Me | |
| 4-37 | CH2OMe | Me | SO2Me | |
| 4-38 | CH2OMe | Et | SO2Me | |
| 4-39 | CH2OMe | n-Pr | SO2Me | |
| 4-40 | CH2OMe | i-Pr | SO2Me | |
| 4-41 | CH2SO2Me | Me | SO2Me | |
| 4-42 | CH2SO2Me | Et | SO2Me | |
| 4-43 | CH2SO2Me | n-Pr | SO2Me | |
| 4-44 | CH2SO2Me | i-Pr | SO2Me | |
| 4-45 | CH2OCH2CH2OMe | Me | SO2Me | |
| 4-46 | CH2OCH2CH2OMe | Et | SO2Me | |
| 4-47 | CH2OCH2CH2OMe | n-Pr | SO2Me | |
| 4-48 | CH2OCH2CH2OMe | i-Pr | SO2Me | |
| 4-49 | CH2OCH2CH2OEt | Me | SO2Me | |
| 4-50 | CH2OCH2CH2OEt | Et | SO2Me | |
| 4-51 | CH2OCH2CH2OEt | n-Pr | SO2Me |
110
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-52 | CH2OCH2CH2OEt | i-Pr | SO2Me | |
| 4-53 | CH2OCH2CH2CH2OMe | Me | SO2Me | |
| 4-54 | CH2OCH2CH2CH2OMe | Et | SO2Me | |
| 4-55 | CH2OCH2CH2CH2OMe | n-Pr | SO2Me | |
| 4-56 | CH2OCH2CH2CH2OMe | i-Pr | SO2Me | |
| 4-57 | CH2OCH2OMe | Me | SO2Me | |
| 4-58 | CH2OCH2OMe | Et | SO2Me | |
| 4-59 | CH2OCH2OMe | n-Pr | SO2Me | |
| 4-60 | CH2OCH2OMe | i-Pr | SO2Me | |
| 4-61 | CH2OCH2OEt | Me | SO2Me | |
| 4-62 | CH2OCH2OEt | Et | SO2Me | |
| 4-63 | CH2OCH2OEt | n-Pr | SO2Me | |
| 4-64 | CH2OCH2OEt | i-Pr | SO2Me | |
| 4-65 | CH2OCH2CH2SO2Me | Me | SO2Me | |
| 4-66 | CH2OCH2CH2SO2Me | Et | SO2Me | |
| 4-67 | CH2OCH2CH2SO2Me | n-Pr | SO2Me | |
| 4-68 | CH2OCH2CH2SO2Me | i-Pr | SO2Me | |
| 4-69 | CH2SO2CH2CH2OMe | Me | SO2Me | |
| 4-70 | CH2SO2CH2CH2OMe | Et | SO2Me | |
| 4-71 | CH2SO2CH2CH2OMe | n-Pr | SO2Me | |
| 4-72 | CH2SO2CH2CH2OMe | i-Pr | SO2Me | |
| 4-73 | CH2SO2CH2CH2SO2Me | Me | SO2Me | |
| 4-74 | CH2SO2CH2CH2SO2Me | Et | SO2Me | |
| 4-75 | CH2SO2CH2CH2SO2Me | n-Pr | SO2Me | |
| 4-76 | CH2SO2CH2CH2SO2Me | i-Pr | SO2Me |
111
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-77 | Cl | Me | SO2Et | |
| 4-78 | Cl | Et | SO2Et | |
| 4-79 | Cl | n-Pr | SO2Et | |
| 4-80 | Cl | i-Pr | SO2Et | |
| 4-81 | Br | Me | SO2Et | |
| 4-82 | Br | Et | SO2Et | |
| 4-83 | Br | n-Pr | SO2Et | |
| 4-84 | Br | i-Pr | SO2Et | |
| 4-85 | Me | Me | SO2Et | |
| 4-86 | Me | Et | SO2Et | |
| 4-87 | Me | n-Pr | SO2Et | |
| 4-88 | Me | i-Pr | SO2Et | |
| 4-89 | Et | Me | SO2Et | |
| 4-90 | Et | Et | SO2Et | |
| 4-91 | Et | n-Pr | SO2Et | |
| 4-92 | Et | i-Pr | SO2Et | |
| 4-93 | cf3 | Me | SO2Et | |
| 4-94 | cf3 | Et | SO2Et | |
| 4-95 | cf3 | n-Pr | SO2Et | |
| 4-96 | cf3 | i-Pr | SO2Et | |
| 4-97 | OMe | Me | SO2Et | |
| 4-98 | OMe | Et | SO2Et | |
| 4-99 | OMe | n-Pr | SO2Et | |
| 4-100 | OMe | i-Pr | SO2Et | |
| 4-101 | OEt | Me | SO2Et |
112
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-102 | OEt | Et | SO2Et | |
| 4-103 | OEt | n-Pr | SO2Et | |
| 4-104 | OEt | i-Pr | SO2Et | |
| 4-105 | no2 | Me | SO2Et | |
| 4-106 | no2 | Et | SO2Et | |
| 4-107 | no2 | n-Pr | SO2Et | |
| 4-108 | no2 | i-Pr | SO2Et | |
| 4-109 | S02Me | Me | SO2Et | |
| 4-110 | S02Me | Et | SO2Et | |
| 4-111 | S02Me | n-Pr | SO2Et | |
| 4-112 | S02Me | i-Pr | SO2Et | |
| 4-113 | CH20Me | Me | SO2Et | |
| 4-114 | CH20Me | Et | SO2Et | |
| 4-115 | CH20Me | n-Pr | SO2Et | |
| 4-116 | CH20Me | i-Pr | SO2Et | |
| 4-117 | CH2SO2Me | Me | SO2Et | |
| 4-118 | CH2SO2Me | Et | SO2Et | |
| 4-119 | CH2SO2Me | n-Pr | SO2Et | |
| 4-120 | CH2SO2Me | i-Pr | SO2Et | |
| 4-121 | CH2OCH2CH2OMe | Me | SO2Et | |
| 4-122 | CH2OCH2CH2OMe | Et | SO2Et | |
| 4-123 | CH2OCH2CH2OMe | n-Pr | SO2Et | |
| 4-124 | CH2OCH2CH2OMe | i-Pr | SO2Et | |
| 4-125 | CH2OCH2CH2OEt | Me | SO2Et | |
| 4-126 | CH2OCH2CH2OEt | Et | SO2Et |
113
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-127 | CH2OCH2CH2OEt | n-Pr | SO2Et | |
| 4-128 | CH2OCH2CH2OEt | i-Pr | SO2Et | |
| 4-129 | CH2OCH2CH2CH2OMe | Me | SO2Et | |
| 4-130 | CH2OCH2CH2CH2OMe | Et | SO2Et | |
| 4-131 | CH2OCH2CH2CH2OMe | n-Pr | SO2Et | |
| 4-132 | CH2OCH2CH2CH2OMe | i-Pr | SO2Et | |
| 4-133 | CH2OCH2OMe | Me | SO2Et | |
| 4-134 | CH2OCH2OMe | Et | SO2Et | |
| 4-135 | CH2OCH2OMe | n-Pr | SO2Et | |
| 4-136 | CH2OCH2OMe | i-Pr | SO2Et | |
| 4-137 | CH2OCH2OEt | Me | SO2Et | |
| 4-138 | CH2OCH2OEt | Et | SO2Et | |
| 4-139 | CH2OCH2OEt | n-Pr | SO2Et | |
| 4-140 | CH2OCH2OEt | i-Pr | SO2Et | |
| 4-141 | CH2OCH2CH2SO2Me | Me | SO2Et | |
| 4-142 | CH2OCH2CH2SO2Me | Et | SO2Et | |
| 4-143 | CH2OCH2CH2SO2Me | n-Pr | SO2Et | |
| 4-144 | CH2OCH2CH2SO2Me | i-Pr | SO2Et | |
| 4-145 | CH2SO2CH2CH2OMe | Me | SO2Et | |
| 4-146 | CH2SO2CH2CH2OMe | Et | SO2Et | |
| 4-147 | CH2SO2CH2CH2OMe | n-Pr | SO2Et | |
| 4-148 | CH2SO2CH2CH2OMe | i-Pr | SO2Et | |
| 4-149 | CH2SO2CH2CH2SO2Me | Me | SO2Et | |
| 4-150 | CH2SO2CH2CH2SO2Me | Et | SO2Et | |
| 4-151 | CH2SO2CH2CH2SO2Me | n-Pr | SO2Et |
114
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-152 | CH2SO2CH2CH2SO2Me | i-Pr | SO2Et | |
| 4-153 | Cl | Me | F | |
| 4-154 | Cl | Et | F | |
| 4-155 | Cl | n-Pr | F | |
| 4-156 | Cl | i-Pr | F | |
| 4-157 | Br | Me | f | |
| 4-158 | Br | Et | f | |
| 4-159 | Br | n-Pr | f | |
| 4-160 | Br | i-Pr | F | |
| 4-161 | Me | Me | F | |
| 4-162 | Me | Et | F | |
| 4-163 | Me | n-Pr | F | |
| 4-164 | Me | i-Pr | F | |
| 4-165 | Et | Me | F | |
| 4-166 | Et | Et | F | |
| 4-167 | Et | n-Pr | F | |
| 4-168 | Et | i-Pr | f | |
| 4-169 | cf3 | Me | F | |
| 4-170 | cf3 | Et | F | |
| 4-171 | cf3 | n-Pr | F | |
| 4-172 | cf3 | i-Pr | f | |
| 4-173 | OMe | Me | F | |
| 4-174 | OMe | Et | F | |
| 4-175 | OMe | n-Pr | f | |
| 4-176 | OMe | i-Pr | F |
115
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-177 | OEt | Me | F | |
| 4-178 | OEt | Et | F | |
| 4-179 | OEt | n-Pr | F | |
| 4-180 | OEt | i-Pr | F | |
| 4-181 | no2 | Me | F | |
| 4-182 | no2 | Et | F | |
| 4-183 | no2 | n-Pr | F | |
| 4-184 | no2 | i-Pr | F | |
| 4-185 | SO2Me | Me | F | |
| 4-186 | SO2Me | Et | F | |
| 4-187 | SO2Me | n-Pr | F | |
| 4-188 | S02Me | i-Pr | F | |
| 4-189 | CH20Me | Me | F | |
| 4-190 | CH2OMe | Et | F | |
| 4-191 | CH20Me | n-Pr | F | |
| 4-192 | CH2OMe | i-Pr | F | |
| 4-193 | CH2SO2Me | Me | F | |
| 4-194 | CH2SO2Me | Et | F | |
| 4-195 | CH2SO2Me | n-Pr | F | |
| 4-196 | CH2SO2Me | i-Pr | F | |
| 4-197 | CH2OCH2CH2OMe | Me | F | |
| 4-198 | CH2OCH2CH2OMe | Et | F | |
| 4-199 | CH2OCH2CH2OMe | n-Pr | F | |
| 4-200 | CH2OCH2CH2OMe | i-Pr | F | |
| 4-201 | CH2OCH2CH2OEt | Me | F |
116
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-202 | CH2OCH2CH2OEt | Et | F | |
| 4-203 | CH2OCH2CH2OEt | n-Pr | F | |
| 4-204 | CH2OCH2CH2OEt | i-Pr | F | |
| 4-205 | CH2OCH2CH2CH2OMe | Me | F | |
| 4-206 | CH2OCH2CH2CH2OMe | Et | F | |
| 4-207 | CH2OCH2CH2CH2OMe | n-Pr | F | |
| 4-208 | CH2OCH2CH2CH2OMe | i-Pr | F | |
| 4-209 | CH2OCH2OMe | Me | F | |
| 4-210 | CH2OCH2OMe | Et | F | |
| 4-211 | CH2OCH2OMe | n-Pr | F | |
| 4-212 | CH2OCH2OMe | i-Pr | F | |
| 4-213 | CH2OCH2OEt | Me | F | |
| 4-214 | CH2OCH2OEt | Et | F | |
| 4-215 | CH2OCH2OEt | n-Pr | F | |
| 4-216 | CH2OCH2OEt | i-Pr | F | |
| 4-217 | CH2OCH2CH2SO2Me | Me | F | |
| 4-218 | CH2OCH2CH2SO2Me | Et | F | |
| 4-219 | CH2OCH2CH2SO2Me | n-Pr | F | |
| 4-220 | CH2OCH2CH2SO2Me | i-Pr | F | |
| 4-221 | CH2SO2CH2CH2OMe | Me | F | |
| 4-222 | CH2SO2CH2CH2OMe | Et | F | |
| 4-223 | CH2SO2CH2CH2OMe | n-Pr | F | |
| 4-224 | CH2SO2CH2CH2OMe | i-Pr | F | |
| 4-225 | CH2SO2CH2CH2SO2Me | Me | F | |
| 4-226 | CH2SO2CH2CH2SO2Me | Et | F |
117
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-227 | CH2SO2CH2CH2SO2Me | n-Pr | F | |
| 4-228 | CH2SO2CH2CH2SO2Me | i-Pr | F | |
| 4-229 | Cl | Me | Cl | |
| 4-230 | Cl | Et | Cl | |
| 4-231 | Cl | n-Pr | Cl | |
| 4-232 | Cl | i-Pr | Cl | |
| 4-233 | Br | Me | Cl | |
| 4-234 | Br | Et | Cl | |
| 4-235 | Br | n-Pr | Cl | |
| 4-236 | Br | i-Pr | Cl | |
| 4-237 | Me | Me | Cl | (DMSO-d6): 7,77 (d, 1H), 7,47 (d, 1H), 3,01 (s, 3H), 2,78 (s, 3H) |
| 4-238 | Me | Et | Cl | 7,92 (d, 1H), 7,35 (d, 1H), 3,39 (m, 1H), 3,16 (m, 1H), 2,92 (s, 3H), 1,38 (t, 3H) |
| 4-239 | Me | n-Pr | Cl | |
| 4-240 | Me | i-Pr | Cl | |
| 4-241 | Et | Me | Cl | |
| 4-242 | Et | Et | Cl | |
| 4-243 | Et | n-Pr | Cl | |
| 4-244 | Et | i-Pr | Cl | |
| 4-245 | cf3 | Me | Cl | |
| 4-246 | cf3 | Et | Cl |
118
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-247 | cf3 | n-Pr | Cl | |
| 4-248 | cf3 | i-Pr | Cl | |
| 4-249 | OMe | Me | Cl | |
| 4-250 | OMe | Et | Cl | |
| 4-251 | OMe | n-Pr | Cl | |
| 4-252 | OMe | i-Pr | Cl | |
| 4-253 | OEt | Me | Cl | |
| 4-254 | OEt | Et | Cl | |
| 4-255 | OEt | n-Pr | Cl | |
| 4-256 | OEt | i-Pr | Cl | |
| 4-257 | no2 | Me | Cl | |
| 4-258 | no2 | Et | Cl | |
| 4-259 | no2 | n-Pr | Cl | |
| 4-260 | no2 | i-Pr | Cl | |
| 4-261 | SO2Me | Me | Cl | |
| 4-262 | SO2Me | Et | Cl | |
| 4-263 | SO2Me | n-Pr | Cl | |
| 4-264 | SO2Me | i-Pr | Cl | |
| 4-265 | CH2OMe | Me | Cl | |
| 4-266 | CH2OMe | Et | Cl | |
| 4-267 | CH2OMe | n-Pr | Cl | |
| 4-268 | CH2OMe | i-Pr | Cl | |
| 4-269 | CH2SO2Me | Me | Cl | |
| 4-270 | CH2SO2Me | Et | Cl | |
| 4-271 | CH2SO2Me | n-Pr | Cl |
119
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-272 | CH2SO2Me | i-Pr | Cl | |
| 4-273 | CH2OCH2CH2OMe | Me | Cl | |
| 4-274 | CH2OCH2CH2OMe | Et | Cl | |
| 4-275 | CH2OCH2CH2OMe | n-Pr | Cl | |
| 4-276 | CH2OCH2CH2OMe | i-Pr | Cl | |
| 4-277 | CH2OCH2CH2OEt | Me | Cl | |
| 4-278 | CH2OCH2CH2OEt | Et | Cl | |
| 4-279 | CH2OCH2CH2OEt | n-Pr | Cl | |
| 4-280 | CH2OCH2CH2OEt | i-Pr | Cl | |
| 4-281 | CH2OCH2CH2CH2OMe | Me | Cl | |
| 4-282 | CH2OCH2CH2CH2OMe | Et | Cl | |
| 4-283 | CH2OCH2CH2CH2OMe | n-Pr | Cl | |
| 4-284 | CH2OCH2CH2CH2OMe | i-Pr | Cl | |
| 4-285 | CH2OCH2OMe | Me | Cl | |
| 4-286 | CH2OCH2OMe | Et | Cl | |
| 4-287 | CH2OCH2OMe | n-Pr | Cl | |
| 4-288 | CH2OCH2OMe | i-Pr | Cl | |
| 4-289 | CH2OCH2OEt | Me | Cl | |
| 4-290 | CH2OCH2OEt | Et | Cl | |
| 4-291 | CH2OCH2OEt | n-Pr | Cl | |
| 4-292 | CH2OCH2OEt | i-Pr | Cl | |
| 4-293 | CH2OCH2CH2SO2Me | Me | Cl | |
| 4-294 | CH2OCH2CH2SO2Me | Et | Cl | |
| 4-295 | CH2OCH2CH2SO2Me | n-Pr | Cl | |
| 4-296 | CH2OCH2CH2SO2Me | i-Pr | Cl |
120
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-297 | CH2SO2CH2CH2OMe | Me | Cl | |
| 4-298 | CH2SO2CH2CH2OMe | Et | Cl | |
| 4-299 | CH2SO2CH2CH2OMe | n-Pr | Cl | |
| 4-300 | CH2SO2CH2CH2OMe | i-Pr | Cl | |
| 4-301 | CH2SO2CH2CH2SO2Me | Me | Cl | |
| 4-302 | CH2SO2CH2CH2SO2Me | Et | Cl | |
| 4-303 | CH2SO2CH2CH2SO2Me | n-Pr | Cl | |
| 4-304 | CH2SO2CH2CH2SO2Me | i-Pr | Cl | |
| 4-305 | Cl | Me | Br | |
| 4-306 | Cl | Et | Br | |
| 4-307 | Cl | n-Pr | Br | |
| 4-308 | Cl | i-Pr | Br | |
| 4-309 | Br | Me | Br | |
| 4-310 | Br | Et | Br | |
| 4-311 | Br | n-Pr | Br | |
| 4-312 | Br | i-Pr | Br | |
| 4-313 | Me | Me | Br | (DMSO-d6): 7,66 (d, 1H), 7,64 (d, 1H), 2,99 (s, 3H), 2,80 (s, 3H) |
| 4-314 | Me | Et | Br | |
| 4-315 | Me | n-Pr | Br | |
| 4-316 | Me | i-Pr | Br | |
| 4-317 | Et | Me | Br | |
| 4-318 | Et | Et | Br | |
| 4-319 | Et | n-Pr | Br |
121
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-320 | Et | i-Pr | Br | |
| 4-321 | cf3 | Me | Br | |
| 4-322 | cf3 | Et | Br | |
| 4-323 | cf3 | n-Pr | Br | |
| 4-324 | cf3 | i-Pr | Br | |
| 4-325 | OMe | Me | Br | |
| 4-326 | OMe | Et | Br | |
| 4-327 | OMe | n-Pr | Br | |
| 4-328 | OMe | i-Pr | Br | |
| 4-329 | OEt | Me | Br | |
| 4-330 | OEt | Et | Br | |
| 4-331 | OEt | n-Pr | Br | |
| 4-332 | OEt | i-Pr | Br | |
| 4-333 | no2 | Me | Br | |
| 4-334 | no2 | Et | Br | |
| 4-335 | no2 | n-Pr | Br | |
| 4-336 | no2 | i-Pr | Br | |
| 4-337 | SO2Me | Me | Br | |
| 4-338 | SO2Me | Et | Br | |
| 4-339 | SO2Me | n-Pr | Br | |
| 4-340 | SO2Me | i-Pr | Br | |
| 4-341 | CH2OMe | Me | Br | |
| 4-342 | CH2OMe | Et | Br | |
| 4-343 | CH2OMe | n-Pr | Br | |
| 4-344 | CH2OMe | i-Pr | Br |
122
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-345 | CH2SO2Me | Me | Br | |
| 4-346 | CH2SO2Me | Et | Br | |
| 4-347 | CH2SO2Me | n-Pr | Br | |
| 4-348 | CH2SO2Me | i-Pr | Br | |
| 4-349 | CH2OCH2CH2OMe | Me | Br | |
| 4-350 | CH2OCH2CH2OMe | Et | Br | |
| 4-351 | CH2OCH2CH2OMe | n-Pr | Br | |
| 4-352 | CH2OCH2CH2OMe | i-Pr | Br | |
| 4-353 | CH2OCH2CH2OEt | Me | Br | |
| 4-354 | CH2OCH2CH2OEt | Et | Br | |
| 4-355 | CH2OCH2CH2OEt | n-Pr | Br | |
| 4-356 | CH2OCH2CH2OEt | i-Pr | Br | |
| 4-357 | CH2OCH2CH2CH2OMe | Me | Br | |
| 4-358 | CH2OCH2CH2CH2OMe | Et | Br | |
| 4-359 | CH2OCH2CH2CH2OMe | n-Pr | Br | |
| 4-360 | CH2OCH2CH2CH2OMe | i-Pr | Br | |
| 4-361 | CH2OCH2OMe | Me | Br | |
| 4-362 | CH2OCH2OMe | Et | Br | |
| 4-363 | CH2OCH2OMe | n-Pr | Br | |
| 4-364 | CH2OCH2OMe | i-Pr | Br | |
| 4-365 | CH2OCH2OEt | Me | Br | |
| 4-366 | CH2OCH2OEt | Et | Br | |
| 4-367 | CH2OCH2OEt | n-Pr | Br | |
| 4-368 | CH2OCH2OEt | i-Pr | Br | |
| 4-369 | CH2OCH2CH2SO2Me | Me | Br |
123
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-370 | CH2OCH2CH2SO2Me | Et | Br | |
| 4-371 | CH2OCH2CH2SO2Me | n-Pr | Br | |
| 4-372 | CH2OCH2CH2SO2Me | i-Pr | Br | |
| 4-373 | CH2SO2CH2CH2OMe | Me | Br | |
| 4-374 | CH2SO2CH2CH2OMe | Et | Br | |
| 4-375 | CH2SO2CH2CH2OMe | n-Pr | Br | |
| 4-376 | CH2SO2CH2CH2OMe | i-Pr | Br | |
| 4-377 | CH2SO2CH2CH2SO2Me | Me | Br | |
| 4-378 | CH2SO2CH2CH2SO2Me | Et | Br | |
| 4-379 | CH2SO2CH2CH2SO2Me | n-Pr | Br | |
| 4-380 | CH2SO2CH2CH2SO2Me | i-Pr | Br | |
| 4-381 | Cl | Me | I | |
| 4-382 | Cl | Et | | | |
| 4-383 | Cl | n-Pr | I | |
| 4-384 | Cl | i-Pr | I | |
| 4-385 | Br | Me | I | |
| 4-386 | Br | Et | I | |
| 4-387 | Br | n-Pr | I | |
| 4-388 | Br | i-Pr | I | |
| 4-389 | Me | Me | I | 7,87 (d, 1H), 7,61 (d, 1H), 2,99 (s, 3H), 2,98 (s, 3H) |
| 4-390 | Me | Et | I | |
| 4-391 | Me | n-Pr | | | |
| 4-392 | Me | i-Pr | I | |
| 4-393 | Et | Me | I |
124
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-394 | Et | Et | I | |
| 4-395 | Et | n-Pr | I | |
| 4-396 | Et | i-Pr | I | |
| 4-397 | cf3 | Me | I | |
| 4-398 | cf3 | Et | I | |
| 4-399 | cf3 | n-Pr | I | |
| 4-400 | cf3 | i-Pr | I | |
| 4-401 | OMe | Me | I | |
| 4-402 | OMe | Et | I | |
| 4-403 | OMe | n-Pr | I | |
| 4-404 | OMe | i-Pr | I | |
| 4-405 | OEt | Me | I | |
| 4-406 | OEt | Et | I | |
| 4-407 | OEt | n-Pr | I | |
| 4-408 | OEt | i-Pr | I | |
| 4-409 | no2 | Me | I | |
| 4-410 | no2 | Et | I | |
| 4-411 | no2 | n-Pr | I | |
| 4-412 | no2 | i-Pr | I | |
| 4-413 | SO2Me | Me | I | |
| 4-414 | SO2Me | Et | I | |
| 4-415 | SO2Me | n-Pr | I | |
| 4-416 | SO2Me | i-Pr | I | |
| 4-417 | CH2OMe | Me | | | |
| 4-418 | CH2OMe | Et | I |
125
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-419 | CH2OMe | n-Pr | | | |
| 4-420 | CH2OMe | i-Pr | I | |
| 4-421 | CH2SO2Me | Me | I | |
| 4-422 | CH2SO2Me | Et | I | |
| 4-423 | CH2SO2Me | n-Pr | I | |
| 4-424 | CH2SO2Me | i-Pr | I | |
| 4-425 | CH2OCH2CH2OMe | Me | I | |
| 4-426 | CH2OCH2CH2OMe | Et | I | |
| 4-427 | CH2OCH2CH2OMe | n-Pr | I | |
| 4-428 | CH2OCH2CH2OMe | i-Pr | I | |
| 4-429 | CH2OCH2CH2OEt | Me | I | |
| 4-430 | CH2OCH2CH2OEt | Et | I | |
| 4-431 | CH2OCH2CH2OEt | n-Pr | I | |
| 4-432 | CH2OCH2CH2OEt | i-Pr | I | |
| 4-433 | CH2OCH2CH2CH2OMe | Me | I | |
| 4-434 | CH2OCH2CH2CH2OMe | Et | I | |
| 4-435 | CH2OCH2CH2CH2OMe | n-Pr | I | |
| 4-436 | CH2OCH2CH2CH2OMe | i-Pr | | | |
| 4-437 | CH2OCH2OMe | Me | I | |
| 4-438 | CH2OCH2OMe | Et | I | |
| 4-439 | CH2OCH2OMe | n-Pr | I | |
| 4-440 | CH2OCH2OMe | i-Pr | I | |
| 4-441 | CH2OCH2OEt | Me | I | |
| 4-442 | CH2OCH2OEt | Et | I | |
| 4-443 | CH2OCH2OEt | n-Pr | I |
126
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-444 | CH2OCH2OEt | i-Pr | I | |
| 4-445 | CH2OCH2CH2SO2Me | Me | | | |
| 4-446 | CH2OCH2CH2SO2Me | Et | I | |
| 4-447 | CH2OCH2CH2SO2Me | n-Pr | | | |
| 4-448 | CH2OCH2CH2SO2Me | i-Pr | I | |
| 4-449 | CH2SO2CH2CH2OMe | Me | I | |
| 4-450 | CH2SO2CH2CH2OMe | Et | I | |
| 4-451 | CH2SO2CH2CH2OMe | n-Pr | I | |
| 4-452 | CH2SO2CH2CH2OMe | i-Pr | I | |
| 4-453 | CH2SO2CH2CH2SO2Me | Me | I | |
| 4-454 | CH2SO2CH2CH2SO2Me | Et | I | |
| 4-455 | CH2SO2CH2CH2SO2Me | n-Pr | I | |
| 4-456 | CH2SO2CH2CH2SO2Me | i-Pr | I | |
| 4-457 | Cl | Me | no2 | |
| 4-458 | Cl | Et | no2 | |
| 4-459 | Cl | n-Pr | no2 | |
| 4-460 | Cl | i-Pr | no2 | |
| 4-461 | Br | Me | no2 | |
| 4-462 | Br | Et | no2 | |
| 4-463 | Br | n-Pr | no2 | |
| 4-464 | Br | i-Pr | no2 | |
| 4-465 | Me | Me | no2 | |
| 4-466 | Me | Et | no2 | |
| 4-467 | Me | n-Pr | no2 | |
| 4-468 | Me | i-Pr | no2 |
127
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-469 | Et | Me | no2 | |
| 4-470 | Et | Et | no2 | |
| 4-471 | Et | n-Pr | no2 | |
| 4-472 | Et | i-Pr | no2 | |
| 4-473 | cf3 | Me | no2 | |
| 4-474 | cf3 | Et | no2 | |
| 4-475 | cf3 | n-Pr | no2 | |
| 4-476 | cf3 | i-Pr | no2 | |
| 4-477 | OMe | Me | no2 | |
| 4-478 | OMe | Et | no2 | |
| 4-479 | OMe | n-Pr | no2 | |
| 4-480 | OMe | i-Pr | no2 | |
| 4-481 | OEt | Me | no2 | |
| 4-482 | OEt | Et | no2 | |
| 4-483 | OEt | n-Pr | no2 | |
| 4-484 | OEt | i-Pr | no2 | |
| 4-485 | no2 | Me | no2 | |
| 4-486 | no2 | Et | no2 | |
| 4-487 | no2 | n-Pr | no2 | |
| 4-488 | no2 | i-Pr | no2 | |
| 4-489 | SO2Me | Me | no2 | |
| 4-490 | SO2Me | Et | no2 | |
| 4-491 | SO2Me | n-Pr | no2 | |
| 4-492 | SO2Me | i-Pr | no2 | |
| 4-493 | CH2OMe | Me | no2 |
128
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-494 | CH2OMe | Et | no2 | |
| 4-495 | CH2OMe | n-Pr | no2 | |
| 4-496 | CH2OMe | i-Pr | no2 | |
| 4-497 | CH2SO2Me | Me | no2 | |
| 4-498 | CH2SO2Me | Et | no2 | |
| 4-499 | CH2SO2Me | n-Pr | no2 | |
| 4-500 | CH2SO2Me | i-Pr | no2 | |
| 4-501 | CH2OCH2CH2OMe | Me | no2 | |
| 4-502 | CH2OCH2CH2OMe | Et | no2 | |
| 4-503 | CH2OCH2CH2OMe | n-Pr | no2 | |
| 4-504 | CH2OCH2CH2OMe | i-Pr | no2 | |
| 4-505 | CH2OCH2CH2OEt | Me | no2 | |
| 4-506 | CH2OCH2CH2OEt | Et | no2 | |
| 4-507 | CH2OCH2CH2OEt | n-Pr | no2 | |
| 4-508 | CH2OCH2CH2OEt | i-Pr | no2 | |
| 4-509 | CH2OCH2CH2CH2OMe | Me | no2 | |
| 4-510 | CH2OCH2CH2CH2OMe | Et | no2 | |
| 4-511 | CH2OCH2CH2CH2OMe | n-Pr | no2 | |
| 4-512 | CH2OCH2CH2CH2OMe | i-Pr | no2 | |
| 4-513 | CH2OCH2OMe | Me | no2 | |
| 4-514 | CH2OCH2OMe | Et | no2 | |
| 4-515 | CH2OCH2OMe | n-Pr | no2 | |
| 4-516 | CH2OCH2OMe | i-Pr | no2 | |
| 4-517 | CH2OCH2OEt | Me | no2 | |
| 4-518 | CH2OCH2OEt | Et | no2 |
129
| N° | X | R3 | Y | Dados físicos: 1H-NMR: δ [CDCI3] |
| 4-519 | CH2OCH2OEt | n-Pr | no2 | |
| 4-520 | CH2OCH2OEt | i-Pr | no2 | |
| 4-521 | CH2OCH2CH2SO2Me | Me | no2 | |
| 4-522 | CH2OCH2CH2SO2Me | Et | no2 | |
| 4-523 | CH2OCH2CH2SO2Me | n-Pr | no2 | |
| 4-524 | CH2OCH2CH2SO2Me | i-Pr | no2 | |
| 4-525 | CH2SO2CH2CH2OMe | Me | no2 | |
| 4-526 | CH2SO2CH2CH2OMe | Et | no2 | |
| 4-527 | CH2SO2CH2CH2OMe | n-Pr | no2 | |
| 4-528 | CH2SO2CH2CH2OMe | i-Pr | no2 | |
| 4-529 | CH2SO2CH2CH2SO2Me | Me | no2 | |
| 4-530 | CH2SO2CH2CH2SO2Me | Et | no2 | |
| 4-531 | CH2SO2CH2CH2SO2Me | n-Pr | no2 | |
| 4-532 | CH2SO2CH2CH2SO2Me | i-Pr | no2 |
Tabela 5
Compostos de Fórmula (I) de Acordo com a Presente Invenção em que R1 é
Metila e R2 é Hidrogênio
130
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 5-1 | Cl | Me | SO2Me | - SO2-n-Pr | |
| 5-2 | Cl | Et | SO2Me | - SO2-n-Pr | |
| 5-3 | Me | Me | SO2Me | - SO2-n-Pr | |
| 5-4 | Me | Et | SO2Me | - SO2-n-Pr | |
| 5-5 | cf3 | Me | SO2Me | - SO2-n-Pr | |
| 5-6 | cf3 | Et | SO2Me | - SO2-n-Pr | |
| 5-7 | OMe | Me | SO2Me | - SO2-n-Pr | |
| 5-8 | OMe | Et | SO2Me | - SO2-n-Pr | |
| 5-9 | no2 | Me | SO2Me | - SO2-n-Pr | |
| 5-10 | no2 | Et | SO2Me | - SO2-n-Pr | |
| 5-11 | SO2Me | Me | SO2Me | - SO2-n-Pr | |
| 5-12 | SO2Me | Et | SO2Me | - SO2-n-Pr | |
| 5-13 | CH2OMe | Me | SO2Me | - SO2-n-Pr | |
| 5-14 | CH2OMe | Et | SO2Me | - SO2-n-Pr | |
| 5-15 | CH2SO2Me | Me | SO2Me | - SO2-n-Pr | |
| 5-16 | CH2SO2Me | Et | SO2Me | - SO2-n-Pr | |
| 5-17 | CH2OCH2CH2OMe | Me | SO2Me | - SO2-n-Pr | |
| 5-18 | CH2OCH2CH2OMe | Et | SO2Me | - SO2-n-Pr | |
| 5-19 | Cl | Me | Cl | - SO2-n-Pr | |
| 5-20 | Cl | Et | Cl | - SO2-n-Pr | |
| 5-21 | Me | Me | Cl | - SO2-n-Pr | |
| 5-22 | Me | Et | Cl | - SO2-n-Pr | |
| 5-23 | cf3 | Me | Cl | - SO2-n-Pr |
131
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 5-24 | cf3 | Et | Cl | - SO2-n-Pr | |
| 5-25 | OMe | Me | Cl | - SO2-n-Pr | |
| 5-26 | OMe | Et | Cl | - SO2-n-Pr | |
| 5-27 | no2 | Me | Cl | - SO2-n-Pr | |
| 5-28 | no2 | Et | Cl | - SO2-n-Pr | |
| 5-29 | SO2Me | Me | Cl | - SO2-n-Pr | |
| 5-30 | SO2Me | Et | Cl | - SO2-n-Pr | |
| 5-31 | CH2OMe | Me | Cl | - SO2-n-Pr | |
| 5-32 | CH2OMe | Et | Cl | - SO2-n-Pr | |
| 5-33 | CH2SO2Me | Me | Cl | - SO2-n-Pr | |
| 5-34 | CH2SO2Me | Et | Cl | - SO2-n-Pr | |
| 5-35 | CH2OCH2CH2OMe | Me | Cl | - SO2-n-Pr | |
| 5-36 | CH2OCH2CH2OMe | Et | Cl | - SO2-n-Pr | |
| 5-37 | Cl | Me | Br | - SO2-n-Pr | |
| 5-38 | Cl | Et | Br | - SO2-n-Pr | |
| 5-39 | Me | Me | Br | - SO2-n-Pr | |
| 5-40 | Me | Et | Br | - SO2-n-Pr | |
| 5-41 | cf3 | Me | Br | - SO2-n-Pr | |
| 5-42 | cf3 | Et | Br | - SO2-n-Pr | |
| 5-43 | OMe | Me | Br | - SO2-n-Pr | |
| 5-44 | OMe | Et | Br | - SO2-n-Pr | |
| 5-45 | no2 | Me | Br | - SO2-n-Pr | |
| 5-46 | no2 | Et | Br | - SO2-n-Pr |
132
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 5-47 | SO2Me | Me | Br | - SO2-n-Pr | |
| 5-48 | SO2Me | Et | Br | - SO2-n-Pr | |
| 5-49 | CH2OMe | Me | Br | - SO2-n-Pr | |
| 5-50 | CH2OMe | Et | Br | - SO2-n-Pr | |
| 5-51 | CH2SO2Me | Me | Br | - SO2-n-Pr | |
| 5-52 | CH2SO2Me | Et | Br | - SO2-n-Pr | |
| 5-53 | CH2OCH2CH2OMe | Me | Br | - SO2-n-Pr | |
| 5-54 | CH2OCH2CH2OMe | Et | Br | - SO2-n-Pr | |
| 5-55 | Cl | Me | I | - SO2-n-Pr | |
| 5-56 | Cl | Et | I | - SO2-n-Pr | |
| 5-57 | Me | Me | | | - SO2-n-Pr | |
| 5-58 | Me | Et | | | - SO2-n-Pr | |
| 5-59 | cf3 | Me | I | - SO2-n-Pr | |
| 5-60 | cf3 | Et | I | - SO2-n-Pr | |
| 5-61 | OMe | Me | I | - SO2-n-Pr | |
| 5-62 | OMe | Et | I | - SO2-n-Pr | |
| 5-63 | no2 | Me | I | - SO2-n-Pr | |
| 5-64 | no2 | Et | I | - SO2-n-Pr | |
| 5-65 | SO2Me | Me | | | - SO2-n-Pr | |
| 5-66 | SO2Me | Et | I | - SO2-n-Pr | |
| 5-67 | CH2OMe | Me | I | - SO2-n-Pr | |
| 5-68 | CH2OMe | Et | I | - SO2-n-Pr | |
| 5-69 | CH2SO2Me | Me | I | - SO2-n-Pr |
133
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 5-70 | CH2SO2Me | Et | I | - SO2-n-Pr | |
| 5-71 | CH2OCH2CH2OMe | Me | I | - SO2-n-Pr | |
| 5-72 | CH2OCH2CH2OMe | Et | | | - SO2-n-Pr | |
| 5-73 | Cl | Me | no2 | - SO2-n-Pr | |
| 5-74 | Cl | Et | no2 | - SO2-n-Pr | |
| 5-75 | Me | Me | no2 | - SO2-n-Pr | |
| 5-76 | Me | Et | no2 | - SO2-n-Pr | |
| 5-77 | cf3 | Me | no2 | - SO2-n-Pr | |
| 5-78 | cf3 | Et | no2 | - SO2-n-Pr | |
| 5-79 | OMe | Me | no2 | - SO2-n-Pr | |
| 5-80 | OMe | Et | no2 | - SO2-n-Pr | |
| 5-81 | no2 | Me | no2 | - SO2-n-Pr | |
| 5-82 | no2 | Et | no2 | - SO2-n-Pr | |
| 5-83 | SO2Me | Me | no2 | - SO2-n-Pr | |
| 5-84 | SO2Me | Et | no2 | - SO2-n-Pr | |
| 5-85 | CH2OMe | Me | no2 | - SO2-n-Pr | |
| 5-86 | CH2OMe | Et | no2 | - SO2-n-Pr | |
| 5-87 | CH2SO2Me | Me | no2 | - SO2-n-Pr | |
| 5-88 | CH2SO2Me | Et | no2 | - SO2-n-Pr | |
| 5-89 | CH2OCH2CH2OMe | Me | no2 | - SO2-n-Pr | |
| 5-90 | CH2OCH2CH2OMe | Et | no2 | - SO2-n-Pr | |
| 5-91 | Cl | Me | SO2Me | - CO-Ph | |
| 5-92 | Cl | Et | SO2Me | - CO-Ph |
134
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 5-93 | Me | Me | SO2Me | - CO-Ph | |
| 5-94 | Me | Et | SO2Me | - CO-Ph | |
| 5-95 | cf3 | Me | SO2Me | - CO-Ph | |
| 5-96 | cf3 | Et | SO2Me | - CO-Ph | |
| 5-97 | OMe | Me | SO2Me | - CO-Ph | |
| 5-98 | OMe | Et | SO2Me | - CO-Ph | |
| 5-99 | no2 | Me | SO2Me | - CO-Ph | |
| 5-100 | no2 | Et | SO2Me | - CO-Ph | |
| 5-101 | SO2Me | Me | SO2Me | - CO-Ph | |
| 5-102 | SO2Me | Et | SO2Me | - CO-Ph | |
| 5-103 | CH2OMe | Me | SO2Me | - CO-Ph | |
| 5-104 | CH2OMe | Et | SO2Me | - CO-Ph | |
| 5-105 | CH2SO2Me | Me | SO2Me | - CO-Ph | |
| 5-106 | CH2SO2Me | Et | SO2Me | - CO-Ph | |
| 5-107 | CH2OCH2CH2OMe | Me | SO2Me | - CO-Ph | |
| 5-108 | CH2OCH2CH2OMe | Et | SO2Me | - CO-Ph | |
| 5-109 | Cl | Me | Cl | - CO-Ph | |
| 5-110 | Cl | Et | Cl | - CO-Ph | |
| 5-111 | Me | Me | Cl | - CO-Ph | |
| 5-112 | Me | Et | Cl | - CO-Ph | |
| 5-113 | cf3 | Me | Cl | - CO-Ph | |
| 5-114 | cf3 | Et | Cl | - CO-Ph | |
| 5-115 | OMe | Me | Cl | - CO-Ph |
135
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 5-116 | OMe | Et | Cl | - CO-Ph | |
| 5-117 | no2 | Me | Cl | - CO-Ph | |
| 5-118 | no2 | Et | Cl | - CO-Ph | |
| 5-119 | SO2Me | Me | Cl | - CO-Ph | |
| 5-120 | SO2Me | Et | Cl | - CO-Ph | |
| 5-121 | CH2OMe | Me | Cl | - CO-Ph | |
| 5-122 | CH2OMe | Et | Cl | - CO-Ph | |
| 5-123 | CH2SO2Me | Me | Cl | - CO-Ph | |
| 5-124 | CH2SO2Me | Et | Cl | - CO-Ph | |
| 5-125 | CH2OCH2CH2OMe | Me | Cl | - CO-Ph | |
| 5-126 | CH2OCH2CH2OMe | Et | Cl | - CO-Ph | |
| 5-127 | Cl | Me | Br | - CO-Ph | |
| 5-128 | Cl | Et | Br | - CO-Ph | |
| 5-129 | Me | Me | Br | - CO-Ph | |
| 5-130 | Me | Et | Br | - CO-Ph | |
| 5-131 | cf3 | Me | Br | - CO-Ph | |
| 5-132 | cf3 | Et | Br | - CO-Ph | |
| 5-133 | OMe | Me | Br | - CO-Ph | |
| 5-134 | OMe | Et | Br | - CO-Ph | |
| 5-135 | NO2 | Me | Br | - CO-Ph | |
| 5-136 | no2 | Et | Br | - CO-Ph | |
| 5-137 | SO2Me | Me | Br | - CO-Ph | |
| 5-138 | SO2Me | Et | Br | - CO-Ph |
136
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 5-139 | CH2OMe | Me | Br | - CO-Ph | |
| 5-140 | CH2OMe | Et | Br | - CO-Ph | |
| 5-141 | CH2SO2Me | Me | Br | - CO-Ph | |
| 5-142 | CH2SO2Me | Et | Br | - CO-Ph | |
| 5-143 | CH2OCH2CH2OMe | Me | Br | - CO-Ph | |
| 5-144 | CH2OCH2CH2OMe | Et | Br | - CO-Ph | |
| 5-145 | Cl | Me | I | - CO-Ph | |
| 5-146 | Cl | Et | | | - CO-Ph | |
| 5-147 | Me | Me | I | - CO-Ph | |
| 5-148 | Me | Et | I | - CO-Ph | |
| 5-149 | cf3 | Me | I | - CO-Ph | |
| 5-150 | cf3 | Et | I | - CO-Ph | |
| 5-151 | OMe | Me | | | - CO-Ph | |
| 5-152 | OMe | Et | I | - CO-Ph | |
| 5-153 | NO2 | Me | I | - CO-Ph | |
| 5-154 | no2 | Et | I | - CO-Ph | |
| 5-155 | SO2Me | Me | I | - CO-Ph | |
| 5-156 | SO2Me | Et | | | - CO-Ph | |
| 5-157 | CH2OMe | Me | I | - CO-Ph | |
| 5-158 | CH2OMe | Et | I | - CO-Ph | |
| 5-159 | CH2SO2Me | Me | I | - CO-Ph | |
| 5-160 | CH2SO2Me | Et | | | - CO-Ph | |
| 5-161 | CH2OCH2CH2OMe | Me | I | - CO-Ph |
137
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 5-162 | CH2OCH2CH2OMe | Et | I | - CO-Ph | |
| 5-163 | Cl | Me | no2 | - CO-Ph | |
| 5-164 | Cl | Et | no2 | - CO-Ph | |
| 5-165 | Me | Me | no2 | - CO-Ph | |
| 5-166 | Me | Et | no2 | - CO-Ph | |
| 5-167 | cf3 | Me | no2 | - CO-Ph | |
| 5-168 | cf3 | Et | no2 | - CO-Ph | |
| 5-169 | OMe | Me | no2 | - CO-Ph | |
| 5-170 | OMe | Et | no2 | - CO-Ph | |
| 5-171 | no2 | Me | no2 | - CO-Ph | |
| 5-172 | no2 | Et | no2 | - CO-Ph | |
| 5-173 | SO2Me | Me | no2 | - CO-Ph | |
| 5-174 | SO2Me | Et | no2 | - CO-Ph | |
| 5-175 | CH2OMe | Me | no2 | - CO-Ph | |
| 5-176 | CH2OMe | Et | no2 | - CO-Ph | |
| 5-177 | CH2SO2Me | Me | no2 | - CO-Ph | |
| 5-178 | CH2SO2Me | Et | no2 | - CO-Ph | |
| 5-179 | CH2OCH2CH2OMe | Me | no2 | - CO-Ph | |
| 5-180 | CH2OCH2CH2OMe | Et | no2 | - CO-Ph | |
| 5-181 | Cl | Me | SO2Me | - ch2-co- (4-Me-Ph) | |
| 5-182 | Cl | Et | SO2Me | - ch2-co- (4-Me-Ph) |
138
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 5-183 | Me | Me | SO2Me | - ch2-co- (4-Me-Ph) | |
| 5-184 | Me | Et | SO2Me | - ch2-co- (4-Me-Ph) | |
| 5-185 | cf3 | Me | SO2Me | - ch2-co- (4-Me-Ph) | |
| 5-186 | cf3 | Et | SO2Me | - CH2-CO- (4-Me-Ph) | |
| 5-187 | OMe | Me | SO2Me | - ch2-co- (4-Me-Ph) | |
| 5-188 | OMe | Et | SO2Me | - CH2-CO- (4-Me-Ph) | |
| 5-183 | NO2 | λ Λ — ivie | a a ~ | - ch2-co- (4-Me-Ph) | |
| 5-190 | NO2 | Et | SO2Me | - ch2-co- (4-Me-Ph) | |
| 5-191 | SO2Me | Me | SO2Me | - CH2-CO- (4-Me-Ph) | |
| 5-192 | SO2Me | Et | SO2Me | - ch2-co- (4-Me-Ph) | |
| 5-193 | CH2OMe | Me | SO2Me | - ch2-co- (4-Me-Ph) | |
| 5-194 | CH2OMe | Et | SO2Me | - ch2-co- |
139
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| (4-Me-Ph) | |||||
| 5-195 | CH2SO2Me | Me | SO2Me | - ch2-co- (4-Me-Ph) | |
| 5-196 | CH2SO2Me | Et | SO2Me | - CH2-CO- (4-Me-Ph) | |
| 5-197 | CH2OCH2CH2OMe | Me | SO2Me | - ch2-co- (4-Me-Ph) | |
| 5-198 | CH2OCH2CH2OMe | Et | SO2Me | - ch2-co- (4-Me-Ph) | |
| 5-199 | Cl | Me | Cl | - CH2-CO- (4-Me-Ph) | |
| 5-200 | Cl | Et | Cl | - ch2-co- (4-Me-Ph) | |
| 5-201 | Me | Me | Cl | - CH2-CO- (4-Me-Ph) | |
| 5-202 | Me | Et | Cl | - ch2-co- (4-Me-Ph) | |
| 5-203 | cf3 | Me | Cl | - ch2-co- (4-Me-Ph) | |
| 5-204 | cf3 | Et | Cl | - ch2-co- (4-Me-Ph) | |
| 5-205 | OMe | Me | Cl | - ch2-co- (4-Me-Ph) |
140
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 5-206 | OMe | Et | Cl | - ch2-co- (4-Me-Ph) | |
| 5-207 | no2 | Me | Cl | - CH2-CO- (4-Me-Ph) | |
| 5-208 | no2 | Et | Cl | - ch2-co- (4-Me-Ph) | |
| 5-209 | SO2Me | Me | Cl | - ch2-co- (4-Me-Ph) | |
| 5-210 | SO2Me | Et | Cl | - ch2-co- (4-Me-Ph) | |
| 5-211 | CH2OMe | Me | Cl | - ch2-co- (4-Me-Ph) | |
| 5-212 | CH2OMe | Et | Cl | - CH2-CO- (4-Me-Ph) | |
| 5-213 | CH2SO2Me | Me | Cl | - ch2-co- (4-Me-Ph) | |
| 5-214 | CH2SO2Me | Et | Cl | - ch2-co- (4-Me-Ph) | |
| 5-215 | CH2OCH2CH2OMe | Me | Cl | - CH2-CO- (4-Me-Ph) | |
| 5-216 | CH2OCH2CH2OMe | Et | Cl | - CH2-CO- (4-Me-Ph) | |
| 5-217 | Cl | Me | Br | - ch2-co- |
141
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| (4-Me-Ph) | |||||
| 5-218 | Cl | Et | Br | - CH2-CO- (4-Me-Ph) | |
| 5-219 | Me | Me | Br | - CH2-CO(4-Me-Ph) | |
| 5-220 | Me | Et | Br | - CH2-CO- (4-Me-Ph) | |
| 5-221 | cf3 | Me | Br | - ch2-co- (4-Me-Ph) | |
| 5-222 | cf3 | Et | Br | - ch2-co- (4-Me-Ph) | |
| 5-223 | OMe | Me | Br | - CH2-CO- (4-Me-Ph) | |
| 5-224 | OMe | Et | Br | - CH2-CO- (4-Me-Ph) | |
| 5-225 | no2 | Me | Br | - CH2-CO- (4-Me-Ph) | |
| 5-226 | no2 | Et | Br | - CH2-CO- (4-Me-Ph) | |
| 5-227 | SO2Me | Me | Br | - CH2-CO- (4-Me-Ph) | |
| 5-228 | SO2Me | Et | Br | - CH2-CO- (4-Me-Ph) |
142
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 5-229 | CH2OMe | Me | Br | - ch2-co- (4-Me-Ph) | |
| 5-230 | CH2OMe | Et | Br | - CH2-CO- (4-Me-Ph) | |
| 5-231 | CH2SO2Me | Me | Br | - ch2-co- (4-Me-Ph) | |
| 5-232 | CH2SO2Me | Et | Br | - ch2-co- (4-Me-Ph) | |
| 5-233 | CH2OCH2CH2OMe | Me | Br | - ch2-co- (4-Me-Ph) | |
| 5-234 | CH2OCH2CH2OMe | Et | Br | - CH2-CO- (4-Me-Ph) | |
| 5-235 | Cl | Me | I | - ch2-co- (4-Me-Ph) | |
| 5-236 | Cl | Et | | | - CH2-CO- (4-Me-Ph) | |
| 5-237 | Me | Me | | | - CH2-CO- (4-Me-Ph) | |
| 5-238 | Me | Et | I | - CH2-CO- (4-Me-Ph) | |
| 5-239 | cf3 | Me | | | - CH2-CO- (4-Me-Ph) | |
| 5-240 | cf3 | Et | I | - CH2-CO- |
143
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| (4-Me-Ph) | |||||
| 5-241 | OMe | Me | I | - ch2-co- (4-Me-Ph) | |
| 5-242 | OMe | Et | I | - ch2-co- (4-Me-Ph) | |
| 5-243 | no2 | Me | | | - CH2-CO- (4-Me-Ph) | |
| 5-244 | no2 | Et | I | - ch2-co- (4-Me-Ph) | |
| 5-245 | SO2Me | Me | I | - ch2-co(4-Me-Ph) | |
| 5-246 | SO2Me | Et | I | - ch2-co- (4-Me-Ph) | |
| 5-247 | CH2OMe | Me | I | - CH2-CO- (4-Me-Ph) | |
| 5-248 | CH2OMe | Et | I | - ch2-co- (4-Me-Ph) | |
| 5-249 | CH2SO2Me | Me | I | - ch2-co- (4-Me-Ph) | |
| 5-250 | CH2SO2Me | Et | | | - CH2-CO- (4-Me-Ph) | |
| 5-251 | CH2OCH2CH2OMe | Me | I | - ch2-co- (4-Me-Ph) |
144
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 5-252 | CH2OCH2CH2OMe | Et | | | - CH2-CO- (4-Me-Ph) | |
| 5-253 | Cl | Me | NO2 | - CH2-CO- (4-Me-Ph) | |
| 5-254 | Cl | Et | no2 | - ch2-co- (4-Me-Ph) | |
| 5-255 | Me | Me | no2 | - ch2-co- (4-Me-Ph) | |
| 5-256 | Me | Et | no2 | - CH2-CO- (4-Me-Ph) | |
| 5-257 | cf3 | Me | no2 | - ch2-co- (4-Me-Ph) | |
| 5-258 | cf3 | Et | no2 | - CH2-CO- (4-Me-Ph) | |
| 5-259 | OMe | Me | no2 | - ch2-co- (4-Me-Ph) | |
| 5-260 | OMe | Et | no2 | - ch2-co- (4-Me-Ph) | |
| 5-261 | no2 | Me | no2 | - CH2-CO- (4-Me-Ph) | |
| 5-262 | no2 | Et | no2 | - CH2-CO(4-Me-Ph) | |
| 5-263 | SO2Me | Me | no2 | - CH2-CO- |
145
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| (4-Me-Ph) | |||||
| 5-264 | SO2Me | Et | NO2 | - CH2-CO- (4-Me-Ph) | |
| 5-265 | CH2OMe | Me | no2 | - CH2-CO- (4-Me-Ph) | |
| 5-266 | CH2OMe | Et | no2 | - ch2-co- (4-Me-Ph) | |
| 5-267 | CH2SO2Me | Me | no2 | - ch2-co- (4-Me-Ph) | |
| 5-268 | CH2SO2Me | Et | no2 | - ch2-co- (4-Me-Ph) | |
| 5-269 | CH2OCH2CH2OMe | Me | no2 | - ch2-co- (4-Me-Ph) | |
| 5-270 | CH2OCH2CH2OMe | Et | no2 | - CH2-CO- (4-Me-Ph) |
Tabela 6
Compostos de Fórmula (I) de Acordo com a Presente Invenção em que R1 é
146
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 6-1 | Cl | Me | SO2Me | - SO2-n-Pr | |
| 6-2 | Cl | Et | SO2Me | - SO2-n-Pr | |
| 6-3 | Me | Me | SO2Me | - SO2-n-Pr | |
| 6-4 | Me | Et | SO2Me | - SO2-n-Pr | |
| 6-5 | cf3 | Me | SO2Me | - SO2-n-Pr | |
| 6-6 | cf3 | Et | SO2Me | - SO2-n-Pr | |
| 6-7 | OMe | Me | SO2Me | - SO2-n-Pr | |
| 6-8 | OMe | Et | SO2Me | - SO2-n-Pr | |
| 6-9 | no2 | Me | SO2Me | - SO2-n-Pr | |
| 6-10 | no2 | Et | SO2Me | - SO2-n-Pr | |
| 6-11 | SO2Me | Me | SO2Me | - SO2-n-Pr | |
| 6-12 | SO2Me | Et | SO2Me | - SO2-n-Pr | |
| 6-13 | CH2OMe | Me | SO2Me | - SO2-n-Pr | |
| 6-14 | CH2OMe | Et | SO2Me | - SO2-n-Pr | |
| 6-15 | CH2SO2Me | Me | SO2Me | - SO2-n-Pr | |
| 6-16 | CH2SO2Me | Et | SO2Me | - SO2-n-Pr | |
| 6-17 | CH2OCH2CH2OMe | Me | SO2Me | - SO2-n-Pr | |
| 6-18 | CH2OCH2CH2OMe | Et | SO2Me | - SO2-n-Pr | |
| 6-19 | Cl | Me | Cl | - SO2-n-Pr | |
| 6-20 | Cl | Et | Cl | - SO2-n-Pr | |
| 6-21 | Me | Me | Cl | - SO2-n-Pr | |
| 6-22 | Me | Et | Cl | - SO2-n-Pr | |
| 6-23 | cf3 | Me | Cl | - SO2-n-Pr |
147
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 6-24 | cf3 | Et | Cl | - SO2-n-Pr | |
| 6-25 | OMe | Me | Cl | - SO2-n-Pr | |
| 6-26 | OMe | Et | Cl | - SO2-n-Pr | |
| 6-27 | no2 | Me | Cl | - SO2-n-Pr | |
| 6-28 | no2 | Et | Cl | - SO2-n-Pr | |
| 6-29 | SO2Me | Me | Cl | - SO2-n-Pr | |
| 6-30 | SO2Me | Et | Cl | - SO2-n-Pr | |
| 6-31 | CH2OMe | Me | Cl | - SO2-n-Pr | |
| 6-32 | CH2OMe | Et | Cl | - SO2-n-Pr | |
| 6-33 | CH2SO2Me | Me | Cl | - SO2-n-Pr | |
| 6-34 | CH2SO2Me | Et | Cl | - SO2-n-Pr | |
| 6-35 | CH2OCH2CH2OMe | Me | Cl | - SO2-n-Pr | |
| 6-36 | CH2OCH2CH2OMe | Et | Cl | - SO2-n-Pr | |
| 6-37 | Cl | Me | Br | - SO2-n-Pr | |
| 6-38 | Cl | Et | Br | - SO2-n-Pr | |
| 6-39 | Me | Me | Br | - SO2-n-Pr | |
| 6-40 | Me | Et | Br | - SO2-n-Pr | |
| 6-41 | cf3 | Me | Br | - SO2-n-Pr | |
| 6-42 | cf3 | Et | Br | - SO2-n-Pr | |
| 6-43 | OMe | Me | Br | - SO2-n-Pr | |
| 6-44 | OMe | Et | Br | - SO2-n-Pr | |
| 6-45 | no2 | Me | Br | - SO2-n-Pr | |
| 6-46 | no2 | Et | Br | - SO2-n-Pr |
148
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 6-47 | SO2Me | Me | Br | - SO2-n-Pr | |
| 6-48 | SO2Me | Et | Br | - SO2-n-Pr | |
| 6-49 | CH2OMe | Me | Br | - SO2-n-Pr | |
| 6-50 | CH2OMe | Et | Br | - SO2-n-Pr | |
| 6-51 | CH2SO2Me | Me | Br | - SO2-n-Pr | |
| 6-52 | CH2SO2Me | Et | Br | - SO2-n-Pr | |
| 6-53 | CH2OCH2CH2OMe | Me | Br | - SO2-n-Pr | |
| 6-54 | CH2OCH2CH2OMe | Et | Br | - SO2-n-Pr | |
| 6-55 | Cl | Me | I | - SO2-n-Pr | |
| 6-56 | Cl | Et | I | - SO2-n-Pr | |
| 6-57 | Me | Me | I | - SO2-n-Pr | |
| 6-58 | Me | Et | I | - SO2-n-Pr | |
| 6-59 | cf3 | Me | | | - SO2-n-Pr | |
| 6-60 | cf3 | Et | I | - SO2-n-Pr | |
| 6-61 | OMe | Me | I | - SO2-n-Pr | |
| 6-62 | OMe | Et | I | - SO2-n-Pr | |
| 6-63 | no2 | Me | I | - SO2-n-Pr | |
| 6-64 | no2 | Et | I | - SO2-n-Pr | |
| 6-65 | SO2Me | Me | I | - SO2-n-Pr | |
| 6-66 | SO2Me | Et | I | - SO2-n-Pr | |
| 6-67 | CH2OMe | Me | I | - SO2-n-Pr | |
| 6-68 | CH2OMe | Et | I | - SO2-n-Pr | |
| 6-69 | CH2SO2Me | Me | - SO2-n-Pr |
149
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 6-70 | CH2SO2Me | Et | I | - SO2-n-Pr | |
| 6-71 | CH2OCH2CH2OMe | Me | I | - SO2-n-Pr | |
| 6-72 | CH2OCH2CH2OMe | Et | I | - SO2-n-Pr | |
| 6-73 | Cl | Me | no2 | - SO2-n-Pr | |
| 6-74 | Cl | Et | no2 | - SO2-n-Pr | |
| 6-75 | Me | Me | no2 | - SO2-n-Pr | |
| 6-76 | Me | Et | no2 | - SO2-n-Pr | |
| 6-77 | cf3 | Me | no2 | - SO2-n-Pr | |
| 6-78 | cf3 | Et | no2 | - SO2-n-Pr | |
| 6-79 | OMe | Me | no2 | - SO2-n-Pr | |
| 6-80 | OMe | Et | no2 | - SO2-n-Pr | |
| 6-81 | no2 | Me | no2 | - SO2-n-Pr | |
| 6-82 | no2 | Et | no2 | - SO2-n-Pr | |
| 6-83 | SO2Me | Me | no2 | - SO2-n-Pr | |
| 6-84 | SO2Me | Et | no2 | - SO2-n-Pr | |
| 6-85 | CH2OMe | Me | no2 | - SO2-n-Pr | |
| 6-86 | CH2OMe | Et | no2 | - SO2-n-Pr | |
| 6-87 | CH2SO2Me | Me | no2 | - SO2-n-Pr | |
| 6-88 | CH2SO2Me | Et | no2 | - SO2-n-Pr | |
| 6-89 | CH2OCH2CH2OMe | Me | no2 | - SO2-n-Pr | |
| 6-90 | CH2OCH2CH2OMe | Et | no2 | - SO2-n-Pr | |
| 6-91 | Cl | Me | SO2Me | - CO-Ph | |
| 6-92 | Cl | Et | SO2Me | - CO-Ph |
150
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 6-93 | Me | Me | SO2Me | - CO-Ph | |
| 6-94 | Me | Et | SO2Me | - CO-Ph | |
| 6-95 | cf3 | Me | SO2Me | - CO-Ph | |
| 6-96 | cf3 | Et | SO2Me | - CO-Ph | |
| 6-97 | OMe | Me | SO2Me | - CO-Ph | |
| 6-98 | OMe | Et | SO2Me | - CO-Ph | |
| 6-99 | no2 | Me | SO2Me | - CO-Ph | |
| 6-100 | no2 | Et | SO2Me | - CO-Ph | |
| 6-101 | SO2Me | Me | SO2Me | - CO-Ph | |
| 6-102 | SO2Me | Et | SO2Me | - CO-Ph | |
| 6-103 | CH2OMe | Me | SO2Me | - CO-Ph | |
| 6-104 | CH2OMe | Et | SO2Me | - CO-Ph | |
| 6-105 | CH2SO2Me | Me | SO2Me | - CO-Ph | |
| 6-106 | CH2SO2Me | Et | SO2Me | - CO-Ph | |
| 6-107 | CH2OCH2CH2OMe | Me | SO2Me | - CO-Ph | |
| 6-108 | CH2OCH2CH2OMe | Et | SO2Me | - CO-Ph | |
| 6-109 | Cl | Me | Cl | - CO-Ph | |
| 6-110 | Cl | Et | Cl | - CO-Ph | |
| 6-111 | Me | Me | Cl | - CO-Ph | |
| 6-112 | Me | Et | Cl | - CO-Ph | |
| 6-113 | cf3 | Me | Cl | - CO-Ph | |
| 6-114 | cf3 | Et | Cl | - CO-Ph | |
| 6-115 | OMe | Me | Cl | - CO-Ph |
151
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 6-116 | OMe | Et | Cl | - CO-Ph | |
| 6-117 | no2 | Me | Cl | - CO-Ph | |
| 6-118 | no2 | Et | Cl | - CO-Ph | |
| 6-119 | SO2Me | Me | Cl | - CO-Ph | |
| 6-120 | SO2Me | Et | Cl | - CO-Ph | |
| 6-121 | CH2OMe | Me | Cl | - CO-Ph | |
| 6-122 | CH2OMe | Et | Cl | - CO-Ph | |
| 6-123 | CH2SO2Me | Me | Cl | - CO-Ph | |
| 6-124 | CH2SO2Me | Et | Cl | - CO-Ph | |
| 6-125 | CH2OCH2CH2OMe | Me | Cl | - CO-Ph | |
| 6-126 | CH2OCH2CH2OMe | Et | Cl | - CO-Ph | |
| 6-127 | Cl | Me | Br | - CO-Ph | |
| 6-128 | Cl | Et | Br | - CO-Ph | |
| 6-129 | Me | Me | Br | - CO-Ph | |
| 6-130 | Me | Et | Br | - CO-Ph | |
| 6-131 | cf3 | Me | Br | - CO-Ph | |
| 6-132 | cf3 | Et | Br | - CO-Ph | |
| 6-133 | OMe | Me | Br | - CO-Ph | |
| 6-134 | OMe | Et | Br | - CO-Ph | |
| 6-135 | no2 | Me | Br | - CO-Ph | |
| 6-136 | no2 | Et | Br | - CO-Ph | |
| 6-137 | SO2Me | Me | Br | - CO-Ph | |
| 6-138 | SO2Me | Et | Br | - CO-Ph |
152
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 6-139 | CH2OMe | Me | Br | - CO-Ph | |
| 6-140 | CH2OMe | Et | Br | - CO-Ph | |
| 6-141 | CH2SO2Me | Me | Br | - CO-Ph | |
| 6-142 | CH2SO2Me | Et | Br | - CO-Ph | |
| 6-143 | CH2OCH2CH2OMe | Me | Br | - CO-Ph | |
| 6-144 | CH2OCH2CH2OMe | Et | Br | - CO-Ph | |
| 6-145 | Cl | Me | I | - CO-Ph | |
| 6-146 | Cl | Et | I | - CO-Ph | |
| 6-147 | Me | Me | I | - CO-Ph | |
| 6-148 | Me | Et | I | - CO-Ph | |
| 6-149 | cf3 | Me | I | - CO-Ph | |
| 6-150 | cf3 | Et | | | - CO-Ph | |
| 6-151 | OMe | Me | I | - CO-Ph | |
| 6-152 | OMe | Et | I | - CO-Ph | |
| 6-153 | no2 | Me | I | - CO-Ph | |
| 6-154 | no2 | Et | I | - CO-Ph | |
| 6-155 | SO2Me | Me | I | - CO-Ph | |
| 6-156 | SO2Me | Et | I | - CO-Ph | |
| 6-157 | CH2OMe | Me | I | - CO-Ph | |
| 6-158 | CH2OMe | Et | I | - CO-Ph | |
| 6-159 | CH2SO2Me | Me | I | - CO-Ph | |
| 6-160 | CH2SO2Me | Et | I | - CO-Ph | |
| 6-161 | CH2OCH2CH2OMe | Me | I | - CO-Ph |
153
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 6-162 | CH2OCH2CH2OMe | Et | I | - CO-Ph | |
| 6-163 | Cl | Me | no2 | - CO-Ph | |
| 6-164 | Cl | Et | no2 | - CO-Ph | |
| 6-165 | Me | Me | no2 | - CO-Ph | |
| 6-166 | Me | Et | no2 | - CO-Ph | |
| 6-167 | cf3 | Me | no2 | - CO-Ph | |
| 6-168 | cf3 | Et | no2 | - CO-Ph | |
| 6-169 | OMe | Me | no2 | - CO-Ph | |
| 6-170 | OMe | Et | no2 | - CO-Ph | |
| 6-171 | no2 | Me | no2 | - CO-Ph | |
| 6-172 | no2 | Et | no2 | - CO-Ph | |
| 6-173 | SO2Me | Me | no2 | - CO-Ph | |
| 6-174 | SO2Me | Et | no2 | - CO-Ph | |
| 6-175 | CH2OMe | Me | no2 | - CO-Ph | |
| 6-176 | CH2OMe | Et | no2 | - CO-Ph | |
| 6-177 | CH2SO2Me | Me | no2 | - CO-Ph | |
| 6-178 | CH2SO2Me | Et | no2 | - CO-Ph | |
| 6-179 | CH2OCH2CH2OMe | Me | no2 | - CO-Ph | |
| 6-180 | CH2OCH2CH2OMe | Et | no2 | - CO-Ph | |
| 6-181 | Cl | Me | SO2Me | - CH2-CO(4-Me-Ph) | |
| 6-182 | Cl | Et | SO2Me | - CH2-CO(4-Me-Ph) |
154
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 6-183 | Me | Me | SO2Me | - ch2-co(4-Me-Ph) | |
| 6-184 | Me | Et | SO2Me | - CH2-CO- (4-Me-Ph) | |
| 6-185 | cf3 | Me | SO2Me | - ch2-co(4-Me-Ph) | |
| 6-186 | cf3 | Et | SO2Me | - ch2-co- (4-Me-Ph) | |
| 6-187 | OMe | Me | SO2Me | - ch2-co(4-Me-Ph) | |
| 6-188 | OMe | Et | SO2Me | - CH2-CO(4-Me-Ph) | |
| 6-189 | no2 | Me | SO2Me | - CH2-CO- (4-Me-Ph) | |
| 6-190 | no2 | Et | SO2Me | - ch2-co- (4-Me-Ph) | |
| 6-191 | SO2Me | Me | SO2Me | - ch2-co(4-Me-Ph) | |
| 6-192 | SO2Me | Et | SO2Me | - CH2-CO(4-Me-Ph) | |
| 6-193 | CH2OMe | Me | SO2Me | - ch2-co- (4-Me-Ph) |
155
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 6-194 | CH2OMe | Et | SO2Me | - ch2-co(4-Me-Ph) | |
| 6-195 | CH2SO2Me | Me | SO2Me | - ch2-co- (4-Me-Ph) | |
| 6-196 | CH2SO2Me | Et | SO2Me | - CH2-CO(4-Me-Ph) | |
| 6-197 | CH2OCH2CH2OMe | Me | SO2Me | - ch2-co(4-Me-Ph) | |
| 6-198 | CH2OCH2CH2OMe | Et | SO2Me | - ch2-co- (4-Me-Ph) | |
| 6-199 | Cl | Me | Cl | - ch2-co- (4-Me-Ph) | |
| 6-200 | Cl | Et | Cl | - ch2-co- (4-Me-Ph) | |
| 6-201 | Me | Me | Cl | - ch2-co(4-Me-Ph) | |
| 6-202 | Me | Et | Cl | - CH2-CO- (4-Me-Ph) | |
| 6-203 | cf3 | Me | Cl | - CH2-CO- (4-Me-Ph) | |
| 6-204 | cf3 | Et | Cl | - ch2-co- (4-Me-Ph) | |
| 6-205 | OMe | Me | Cl | - ch2-co- |
156
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| (4-Me-Ph) | |||||
| 6-206 | OMe | Et | Cl | - ch2-co(4-Me-Ph) | |
| 6-207 | no2 | Me | Cl | - ch2-co(4-Me-Ph) | |
| 6-208 | no2 | Et | Cl | - CH2-CO- (4-Me-Ph) | |
| 6-209 | SO2Me | Me | Cl | - ch2-co- (4-Me-Ph) | |
| 6-210 | SO2Me | Et | Cl | - ch2-co(4-Me-Ph) | |
| 6-211 | CH2OMe | Me | Cl | - ch2-co(4-Me-Ph) | |
| 6-212 | CH2OMe | Et | Cl | - ch2-co- (4-Me-Ph) | |
| 6-213 | CH2SO2Me | Me | Cl | - ch2-co- (4-Me-Ph) | |
| 6-214 | CH2SO2Me | Et | Cl | - ch2-co(4-Me-Ph) | |
| 6-215 | CH2OCH2CH2OMe | Me | Cl | - CH2-CO(4-Me-Ph) | |
| 6-216 | CH2OCH2CH2OMe | Et | Cl | - ch2-co(4-Me-Ph) |
157
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 6-217 | Cl | Me | Br | - CH2-CO- (4-Me-Ph) | |
| 6-218 | Cl | Et | Br | - ch2-co(4-Me-Ph) | |
| 6-219 | Me | Me | Br | - ch2-co- (4-Me-Ph) | |
| 6-220 | Me | Et | Br | - CH2-CO- (4-Me-Ph) | |
| 6-221 | cf3 | Me | Br | - CH2-CO- (4-Me-Ph) | |
| 6-222 | cf3 | Et | Br | - ch2-co(4-Me-Ph) | |
| 6-223 | OMe | Me | Br | - CH2-CO- (4-Me-Ph) | |
| 6-224 | OMe | Et | Br | - ch2-co(4-Me-Ph) | |
| 6-225 | no2 | Me | Br | - CH2-CO- (4-Me-Ph) | |
| 6-226 | no2 | Et | Br | - CH2-CO(4-Me-Ph) | |
| 6-227 | SO2Me | Me | Br | - ch2-co(4-Me-Ph) | |
| 6-228 | SO2Me | Et | Br | - ch2-co- |
158
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| (4-Me-Ph) | |||||
| 6-229 | CH2OMe | Me | Br | - ch2-co- (4-Me-Ph) | |
| 6-230 | CH2OMe | Et | Br | - CH2-CO- (4-Me-Ph) | |
| 6-231 | CH2SO2Me | Me | Br | - ch2-co- (4-Me-Ph) | |
| 6-232 | CH2SO2Me | Et | Br | - ch2-co- (4-Me-Ph) | |
| 6-233 | CH2OCH2CH2OMe | Me | Br | - ch2-co- (4-Me-Ph) | |
| 6-234 | CH2OCH2CH2OMe | Et | Br | - ch2-co- (4-Me-Ph) | |
| 6-235 | Cl | Me | I | - ch2-co- (4-Me-Ph) | |
| 6-236 | Cl | Et | I | - ch2-co- (4-Me-Ph) | |
| 6-237 | Me | Me | I | - ch2-co- (4-Me-Ph) | |
| 6-238 | Me | Et | I | - ch2-co- (4-Me-Ph) |
159
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 6-239 | cf3 | Me | I | - ch2-co(4-Me-Ph) | |
| 6-240 | cf3 | Et | I | - ch2-co- (4-Me-Ph) | |
| 6-241 | OMe | Me | I | - ch2-co- (4-Me-Ph) | |
| 6-242 | OMe | Et | I | - ch2-co- (4-Me-Ph) | |
| 6-243 | no2 | Me | I | - ch2-co- (4-Me-Ph) | |
| 6-244 | no2 | Et | I | - CH2-CO- (4-Me-Ph) | |
| 6-245 | SO2Me | Me | I | - ch2-co- (4-Me-Ph) | |
| 6-246 | SO2Me | Et | I | - ch2-co- (4-Me-Ph) | |
| 6-247 | CH2OMe | Me | I | - CH2-CO- (4-Me-Ph) | |
| 6-248 | CH2OMe | Et | I | - ch2-co- (4-Me-Ph) | |
| 6-249 | CH2SO2Me | Me | I | - ch2-co(4-Me-Ph) | |
| 6-250 | CH2SO2Me | Et | | | - CH2-CO- |
160
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| (4-Me-Ph) | |||||
| 6-251 | CH2OCH2CH2OMe | Me | I | - ch2-co(4-Me-Ph) | |
| 6-252 | CH2OCH2CH2OMe | Et | I | - CH2-CO- (4-Me-Ph) | |
| 6-253 | Cl | Me | no2 | - ch2-co- (4-Me-Ph) | |
| 6-254 | Cl | Et | no2 | - ch2-co- (4-Me-Ph) | |
| 6-255 | Me | Me | no2 | - ch2-co(4-Me-Ph) | |
| 6-256 | Me | Et | no2 | - CH2-CO(4-Me-Ph) | |
| 6-257 | cf3 | Me | no2 | - CH2-CO(4-Me-Ph) | |
| 6-258 | cf3 | Et | no2 | - CH2-CO- (4-Me-Ph) | |
| 6-259 | OMe | Me | no2 | - CH2-CO- (4-Me-Ph) |
161
| N° | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCh] |
| 6-260 | OMe | Et | no2 | - ch2-co- (4-Me-Ph) | |
| 6-261 | no2 | Me | no2 | - ch2-co- (4-Me-Ph) | |
| 6-262 | no2 | Et | no2 | - ch2-co(4-Me-Ph) | |
| 6-263 | SO2Me | Me | no2 | - ch2-co- (4-Me-Ph) | |
| 6-264 | SO2Me | Et | no2 | - ch2-co- (4-Me-Ph) | |
| 6-265 | CH2OMe | Me | no2 | - CH2-CO- (4-Me-Ph) | |
| 6-266 | CH2OMe | Et | no2 | - ch2-co- (4-Me-Ph) | |
| 6-267 | CH2SO2Me | Me | no2 | - ch2-co- (4-Me-Ph) | |
| 6-268 | CH2SO2Me | Et | no2 | - CH2-CO- (4-Me-Ph) | |
| 6-269 | CH2OCH2CH2OMe | Me | no2 | - CH2-CO- (4-Me-Ph) | |
| 6-270 | CH2OCH2CH2OMe | Et | no2 | - ch2-co- (4-Me-Ph) |
162
Tabela 7
Compostos de Fórmula (I) de Acordo com a Presente Invenção em que R1 e
| No. | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 7-1 | Cl | Me | SO2Me | - SO2-n-Pr | |
| 7-2 | Cl | Et | SO2Me | - SO2-n-Pr | |
| 7-3 | Me | Me | SO2Me | - SO2-n-Pr | |
| 7-4 | Me | Et | SO2Me | - SO2-n-Pr | |
| 7-5 | cf3 | Me | SO2Me | - SO2-n-Pr | |
| 7-6 | cf3 | Et | SO2Me | - SO2-n-Pr | |
| 7-7 | OMe | Me | SO2Me | - SO2-n-Pr | |
| 7-8 | OMe | Et | SO2Me | - SO2-n-Pr | |
| 7-9 | no2 | Me | SO2Me | - SO2-n-Pr | |
| 7-10 | no2 | Et | SO2Me | - SO2-n-Pr | |
| 7-11 | SO2Me | Me | SO2Me | - SO2-n-Pr | |
| 7-12 | SO2Me | Et | SO2Me | - SO2-n-Pr | |
| 7-13 | CH2OMe | Me | SO2Me | - SO2-n-Pr | |
| 7-14 | CH2OMe | Et | SO2Me | - SO2-n-Pr | |
| 7-15 | CH2SO2Me | Me | SO2Me | - SO2-n-Pr | |
| 7-16 | CH2SO2Me | Et | SO2Me | - SO2-n-Pr | |
| 7-17 | CH2OCH2CH2OMe | Me | SO2Me | - SO2-n-Pr |
163
| No. | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 7-18 | CH2OCH2CH2OMe | Et | SO2Me | - SO2-n-Pr | |
| 7-19 | Cl | Me | Cl | - SO2-n-Pr | |
| 7-20 | Cl | Et | Cl | - SO2-n-Pr | |
| 7-21 | Me | Me | Cl | - SO2-n-Pr | |
| 7-22 | Me | Et | Cl | - SO2-n-Pr | |
| 7-23 | cf3 | Me | Cl | - SO2-n-Pr | |
| 7-24 | cf3 | Et | Cl | - SO2-n-Pr | |
| 7-25 | OMe | Me | Cl | - SO2-n-Pr | |
| 7-26 | OMe | Et | Cl | - SO2-n-Pr | |
| 7-27 | no2 | Me | Cl | - SO2-n-Pr | |
| 7-28 | no2 | Et | Cl | - SO2-n-Pr | |
| 7-29 | SO2Me | Me | Cl | - SO2-n-Pr | |
| 7-30 | SO2Me | Et | Cl | - SO2-n-Pr | |
| 7-31 | CH2OMe | Me | Cl | - SO2-n-Pr | |
| 7-32 | CH2OMe | Et | Cl | - SO2-n-Pr | |
| 7-33 | CH2SO2Me | Me | Cl | - SO2-n-Pr | |
| 7-34 | CH2SO2Me | Et | Cl | - SO2-n-Pr | |
| 7-35 | CH2OCH2CH2OMe | Me | Cl | - SO2-n-Pr | |
| 7-36 | CH2OCH2CH2OMe | Et | Cl | - SO2-n-Pr | |
| 7-37 | Cl | Me | Br | - SO2-n-Pr | |
| 7-38 | Cl | Et | Br | - SO2-n-Pr | |
| 7-39 | Me | Me | Br | - SO2-n-Pr | |
| 7-40 | Me | Et | Br | - SO2-n-Pr | |
| 7-41 | cf3 | Me | Br | - SO2-n-Pr |
164
| No. | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 7-42 | cf3 | Et | Br | - SO2-n-Pr | |
| 7-43 | OMe | Me | Br | - SO2-n-Pr | |
| 7-44 | OMe | Et | Br | - SO2-n-Pr | |
| 7-45 | no2 | Me | Br | - SO2-n-Pr | |
| 7-46 | no2 | Et | Br | - SO2-n-Pr | |
| 7-47 | SO2Me | Me | Br | - SO2-n-Pr | |
| 7-48 | SO2Me | Et | Br | - SO2-n-Pr | |
| 7-49 | CH2OMe | Me | Br | - SO2-n-Pr | |
| 7-50 | CH2OMe | Et | Br | - SO2-n-Pr | |
| 7-51 | CH2SO2Me | Me | Br | - SO2-n-Pr | |
| 7-52 | CH2SO2Me | Et | Br | - SO2-n-Pr | |
| 7-53 | CH2OCH2CH2OMe | Me | Br | - SO2-n-Pr | |
| 7-54 | CH2OCH2CH2OMe | Et | Br | - SO2-n-Pr | |
| 7-55 | Cl | Me | I | - SO2-n-Pr | |
| 7-56 | Cl | Et | I | - SO2-n-Pr | |
| 7-57 | Me | Me | I | - SO2-n-Pr | |
| 7-58 | Me | Et | I | - SO2-n-Pr | |
| 7-59 | cf3 | Me | I | - SO2-n-Pr | |
| 7-60 | cf3 | Et | I | - SO2-n-Pr | |
| 7-61 | OMe | Me | I | - SO2-n-Pr | |
| 7-62 | OMe | Et | | | - SO2-n-Pr | |
| 7-63 | NO2 | Me | I | - SO2-n-Pr | |
| 7-64 | no2 | Et | I | - SO2-n-Pr | |
| 7-65 | SO2Me | Me | I | - SO2-n-Pr |
165
| No. | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 7-66 | SO2Me | Et | I | - SO2-n-Pr | |
| 7-67 | CH2OMe | Me | I | - SO2-n-Pr | |
| 7-68 | CH2OMe | Et | I | - SO2-n-Pr | |
| 7-69 | CH2SO2Me | Me | I | - SO2-n-Pr | |
| 7-70 | CH2SO2Me | Et | I | - SO2-n-Pr | |
| 7-71 | CH2OCH2CH2OMe | Me | I | - SO2-n-Pr | |
| 7-72 | CH2OCH2CH2OMe | Et | I | - SO2-n-Pr | |
| 7-73 | Cl | Me | no2 | - SO2-n-Pr | |
| 7-74 | Cl | Et | no2 | - SO2-n-Pr | |
| 7-75 | Me | Me | no2 | - SO2-n-Pr | |
| 7-76 | Me | Et | no2 | - SO2-n-Pr | |
| 7-77 | cf3 | Me | no2 | - SO2-n-Pr | |
| 7-78 | cf3 | Et | no2 | - SO2-n-Pr | |
| 7-79 | OMe | Me | no2 | - SO2-n-Pr | |
| 7-80 | OMe | Et | no2 | - SO2-n-Pr | |
| 7-81 | NO2 | Me | no2 | - SO2-n-Pr | |
| 7-82 | no2 | Et | no2 | - SO2-n-Pr | |
| 7-83 | SO2Me | Me | no2 | - SO2-n-Pr | |
| 7-84 | SO2Me | Et | no2 | - SO2-n-Pr | |
| 7-85 | CH2OMe | Me | no2 | - SO2-n-Pr | |
| 7-86 | CH2OMe | Et | no2 | - SO2-n-Pr | |
| 7-87 | CH2SO2Me | Me | no2 | - SO2-n-Pr | |
| 7-88 | CH2SO2Me | Et | no2 | - SO2-n-Pr | |
| 7-89 | CH2OCH2CH2OMe | Me | no2 | - SO2-n-Pr |
166
| No. | X | R3 | Y | R4 | Dados físicos: |
| 1H-NMR: [CDCI3] | δ | ||||
| 7-90 | CH2OCH2CH2OMe | Et | no2 | - SO2-n-Pr | |
| 7-91 | Cl | Me | SO2Me | - CO-Ph | |
| 7-92 | Cl | Et | SO2Me | - CO-Ph | |
| 7-93 | Me | Me | SO2Me | - CO-Ph | |
| 7-94 | Me | Et | SO2Me | - CO-Ph | |
| 7-95 | cf3 | Me | SO2Me | - CO-Ph | |
| 7-96 | cf3 | Et | SO2Me | - CO-Ph | |
| 7-97 | OMe | Me | SO2Me | - CO-Ph | |
| 7-98 | OMe | Et | SO2Me | - CO-Ph | |
| 7-99 | no2 | Me | SO2Me | - CO-Ph | |
| 7-100 | no2 | Et | SO2Me | - CO-Ph | |
| 7-101 | SO2Me | Me | SO2Me | - CO-Ph | |
| 7-102 | SO2Me | Et | SO2Me | - CO-Ph | |
| 7-103 | CH2OMe | Me | SO2Me | - CO-Ph | |
| 7-104 | CH2OMe | Et | SO2Me | - CO-Ph | |
| 7-105 | CH2SO2Me | Me | SO2Me | - CO-Ph | |
| 7-106 | CH2SO2Me | Et | SO2Me | - CO-Ph | |
| 7-107 | CH2OCH2CH2OMe | Me | SO2Me | - CO-Ph | |
| 7-108 | CH2OCH2CH2OMe | Et | SO2Me | - CO-Ph | |
| 7-109 | Cl | Me | Cl | - CO-Ph | |
| 7-110 | Cl | Et | Cl | - CO-Ph | |
| 7-111 | Me | Me | Cl | - CO-Ph | |
| 7-112 | Me | Et | Cl | - CO-Ph | |
| 7-113 | cf3 | Me | Cl | - CO-Ph |
167
| No. | X | R3 | Y | R4 | Dados físicos: |
| 1H-NMR: [CDCI3] | δ | ||||
| 7-114 | cf3 | Et | Cl | - CO-Ph | |
| 7-115 | OMe | Me | Cl | - CO-Ph | |
| 7-116 | OMe | Et | Cl | - CO-Ph | |
| 7-117 | no2 | Me | Cl | - CO-Ph | |
| 7-118 | no2 | Et | Cl | - CO-Ph | |
| 7-119 | SO2Me | Me | Cl | - CO-Ph | |
| 7-120 | SO2Me | Et | Cl | - CO-Ph | |
| 7-121 | CH2OMe | Me | Cl | - CO-Ph | |
| 7-122 | CH2OMe | Et | Cl | - CO-Ph | |
| 7-123 | CH2SO2Me | Me | Cl | - CO-Ph | |
| 7-124 | CH2SO2Me | Et | Cl | - CO-Ph | |
| 7-125 | CH2OCH2CH2OMe | Me | Cl | - CO-Ph | |
| 7-126 | CH2OCH2CH2OMe | Et | Cl | - CO-Ph | |
| 7-127 | Cl | Me | Br | - CO-Ph | |
| 7-128 | Cl | Et | Br | - CO-Ph | |
| 7-129 | Me | Me | Br | - CO-Ph | |
| 7-130 | Me | Et | Br | - CO-Ph | |
| 7-131 | cf3 | Me | Br | - CO-Ph | |
| 7-132 | cf3 | Et | Br | - CO-Ph | |
| 7-133 | OMe | Me | Br | - CO-Ph | |
| 7-134 | OMe | Et | Br | - CO-Ph | |
| 7-135 | no2 | Me | Br | - CO-Ph | |
| 7-136 | no2 | Et | Br | - CO-Ph | |
| 7-137 | SO2Me | Me | Br | - CO-Ph |
168
| No. | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 7-138 | SO2Me | Et | Br | - CO-Ph | |
| 7-139 | CH2OMe | Me | Br | - CO-Ph | |
| 7-140 | CH2OMe | Et | Br | - CO-Ph | |
| 7-141 | CH2SO2Me | Me | Br | - CO-Ph | |
| 7-142 | CH2SO2Me | Et | Br | - CO-Ph | |
| 7-143 | CH2OCH2CH2OMe | Me | Br | - CO-Ph | |
| 7-144 | CH2OCH2CH2OMe | Et | Br | - CO-Ph | |
| 7-145 | Cl | Me | I | - CO-Ph | |
| 7-146 | Cl | Et | I | - CO-Ph | |
| 7-147 | Me | Me | I | - CO-Ph | |
| 7-148 | Me | Et | I | - CO-Ph | |
| 7-149 | cf3 | Me | I | - CO-Ph | |
| 7-150 | cf3 | Et | I | - CO-Ph | |
| 7-151 | OMe | Me | I | - CO-Ph | |
| 7-152 | OMe | Et | I | - CO-Ph | |
| 7-153 | no2 | Me | I | - CO-Ph | |
| 7-154 | no2 | Et | I | - CO-Ph | |
| 7-155 | SO2Me | Me | I | - CO-Ph | |
| 7-156 | SO2Me | Et | I | - CO-Ph | |
| 7-157 | CH2OMe | Me | I | - CO-Ph | |
| 7-158 | CH2OMe | Et | I | - CO-Ph | |
| 7-159 | CH2SO2Me | Me | I | - CO-Ph | |
| 7-160 | CH2SO2Me | Et | I | - CO-Ph | |
| 7-161 | CH2OCH2CH2OMe | Me | I | - CO-Ph |
169
| No. | X | R3 | Y | R4 | Dados físicos: |
| 1H-NMR: [CDCI3] | δ | ||||
| 7-162 | CH2OCH2CH2OMe | Et | I | - CO-Ph | |
| 7-163 | Cl | Me | no2 | - CO-Ph | |
| 7-164 | Cl | Et | no2 | - CO-Ph | |
| 7-165 | Me | Me | no2 | - CO-Ph | |
| 7-166 | Me | Et | no2 | - CO-Ph | |
| 7-167 | cf3 | Me | no2 | - CO-Ph | |
| 7-168 | cf3 | Et | no2 | - CO-Ph | |
| 7-169 | OMe | Me | no2 | - CO-Ph | |
| 7-170 | OMe | Et | no2 | - CO-Ph | |
| 7-171 | no2 | Me | no2 | - CO-Ph | |
| 7-172 | no2 | Et | no2 | - CO-Ph | |
| 7-173 | SO2Me | Me | no2 | - CO-Ph | |
| 7-174 | SO2Me | Et | no2 | - CO-Ph | |
| 7-175 | CH2OMe | Me | no2 | - CO-Ph | |
| 7-176 | CH2OMe | Et | no2 | - CO-Ph | |
| 7-177 | CH2SO2Me | Me | no2 | - CO-Ph | |
| 7-178 | CH2SO2Me | Et | no2 | - CO-Ph | |
| 7-179 | CH2OCH2CH2OMe | Me | no2 | - CO-Ph | |
| 7-180 | CH2OCH2CH2OMe | Et | no2 | - CO-Ph | |
| 7-181 | Cl | Me | SO2Me | - CH2-CO- (4-Me-Ph) | |
| 7-182 | Cl | Et | SO2Me | - CH2-CO- (4-Me-Ph) | |
| 7-183 | Me | Me | SO2Me | - ch2-co- |
170
| No. | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| (4-Me-Ph) | |||||
| 7-184 | Me | Et | SO2Me | - ch2-co- (4-Me-Ph) | |
| 7-185 | cf3 | Me | SO2Me | - ch2-co- (4-Me-Ph) | |
| 7-186 | cf3 | Et | SO2Me | - CH2-CO- (4-Me-Ph) | |
| 7-187 | OMe | Me | SO2Me | - CH2-CO- (4-Me-Ph) | |
| 7-188 | OMe | Et | SO2Me | - CH2-CO- (4-Me-Ph) | |
| 7-189 | no2 | Me | SO2Me | - CH2-CO- (4-Me-Ph) | |
| 7-190 | no2 | Et | SO2Me | - CH2-CO- (4-Me-Ph) | |
| 7-191 | SO2Me | Me | SO2Me | - CH2-CO- (4-Me-Ph) | |
| 7-192 | SO2Me | Et | SO2Me | - CH2-CO- (4-Me-Ph) | |
| 7-193 | CH2OMe | Me | SO2Me | - CH2-ÇO- (4-Me-Ph) | |
| 7-194 | CH2OMe | Et | SO2Me | - CH2-CO- (4-Me-Ph) | |
| 7-195 | CH2SO2Me | Me | SO2Me | - CH2-CO- |
171
| No. | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| (4-Me-Ph) | |||||
| 7-196 | CH2SO2Me | Et | SO2Me | - ch2-co- (4-Me-Ph) | |
| 7-197 | CH2OCH2CH2OMe | Me | SO2Me | - ch2-co- (4-Me-Ph) | |
| 7-198 | CH2OCH2CH2OMe | Et | SO2Me | - ch2-co- (4-Me-Ph) | |
| 7-199 | Cl | Me | Cl | - ch2-co- (4-Me-Ph) | |
| 7-200 | Cl | Et | Cl | - ch2-co- (4-Me-Ph) | |
| 7-201 | Me | Me | Cl | - ch2-co- (4-Me-Ph) | |
| 7-202 | R A — ivie | Et | Ci | - ch2-co- (4-Me-Ph) | |
| 7-203 | cf3 | Me | Cl | - ch2-co(4-Me-Ph) | |
| 7-204 | cf3 | Et | Cl | - CH2-CO- (4-Me-Ph) | |
| 7-205 | OMe | Me | Cl | - CH2-CO- (4-Me-Ph) | |
| 7-206 | OMe | Et | Cl | - ch2-co- (4-Me-Ph) |
172
| No. | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 7-207 | no2 | Me | Cl | - ch2-co- (4-Me-Ph) | |
| 7-208 | no2 | Et | Cl | - CH2-CO- (4-Me-Ph) | |
| 7-209 | SO2Me | Me | Cl | - ch2-co(4-Me-Ph) | |
| 7-210 | SO2Me | Et | Cl | - CH2-CO- (4-Me-Ph) | |
| 7-211 | CH2OMe | Me | Cl | - ch2-co- (4-Me-Ph) | |
| 7-212 | CH2OMe | Et | Cl | - ch2-co- (4-Me-Ph) | |
| 7-213 | CH2SO2Me | Me | Cl | - CH2-CO- (4-Me-Ph) | |
| 7-214 | CH2SO2Me | Et | Cl | - ch2-co(4-Me-Ph) | |
| 7-215 | CH2OCH2CH2OMe | Me | Cl | - CH2-CO- (4-Me-Ph) | |
| 7-216 | CH2OCH2CH2OMe | Et | Cl | - ch2-co(4-Me-Ph) | |
| 7-217 | Cl | Me | Br | - ch2-co- (4-Me-Ph) | |
| 7-218 | Cl | Et | Br | - ch2-co- (4-Me-Ph) |
173
| No. | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 7-219 | Me | Me | Br | - CH2-CO- (4-Me-Ph) | |
| 7-220 | Me | Et | Br | - CH2-CO- (4-Me-Ph) | |
| 7-221 | cf3 | Me | Br | - ch2-co- (4-Me-Ph) | |
| 7-222 | cf3 | Et | Br | - ch2-co- (4-Me-Ph) | |
| 7-223 | OMe | Me | Br | - ch2-co(4-Me-Ph) | |
| 7-224 | OMe | Et | Br | - ch2-co(4-Me-Ph) | |
| 7-225 | no2 | Me | Br | - ch2-co- (4-Me-Ph) | |
| 7-226 | no2 | Et | Br | - ch2-co- (4-Me-Ph) | |
| 7-227 | SO2Me | Me | Br | - ch2-co- (4-Me-Ph) | |
| 7-228 | SO2Me | Et | Br | - ch2-co- (4-Me-Ph) | |
| 7-229 | CH2OMe | Me | Br | - CH2-CO- (4-Me-Ph) | |
| 7-230 | CH2OMe | Et | Br | - CH2-CO- (4-Me-Ph) |
174
| No. | X | R3 | Y | R4 | Dados físicos: |
| 1H-NMR: [CDCI3] | δ | ||||
| 7-231 | CH2SO2Me | Me | Br | - CH2-CO- (4-Me-Ph) | |
| 7-232 | CH2SO2Me | Et | Br | - CH2-CO- (4-Me-Ph) | |
| 7-233 | CH2OCH2CH2OMe | Me | Br | - CH2-CO- (4-Me-Ph) | |
| 7-234 | CH2OCH2CH2OMe | Et | Br | - CH2-CO- (4-Me-Ph) | |
| 7-235 | Cl | Me | I | - CH2-CO- (4-Me-Ph) | |
| 7-236 | Cl | Et | I | - CH2-CO- (4-Me-Ph) | |
| 7-237 | Me | Me | I | - CH2-CO- (4-Me-Ph) | |
| 7-238 | Me | Et | I | - CH2-CO- (4-Me-Ph) | |
| 7-239 | cf3 | Me | I | - CH2-CO(4-Me-Ph) | |
| 7-240 | cf3 | Et | I | - CH2-CO- (4-Me-Ph) | |
| 7-241 | OMe | Me | I | - CH2-CO- (4-Me-Ph) | |
| 7-242 | OMe | Et | I | - CH2-CO- (4-Me-Ph) |
175
| No. | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDChl |
| 7-243 | no2 | Me | | | - ch2-co- (4-Me-Ph) | |
| 7-244 | no2 | Et | I | - ch2-co- (4-Me-Ph) | |
| 7-245 | SO2Me | Me | I | - ch2-co- (4-Me-Ph) | |
| 7-246 | SO2Me | Et | I | - ch2-co- (4-Me-Ph) | |
| 7-247 | CH2OMe | Me | | | - ch2-co- (4-Me-Ph) | |
| 7-248 | CH2OMe | Et | I | - CH2-CO- (4-Me-Ph) | |
| 7-249 | CH2SO2Me | Me | I | - ch2-co- (4-Me-Ph) | |
| 7-250 | CH2SO2Me | Et | I | - ch2-co- (4-Me-Ph) | |
| 7-251 | CH2OCH2CH2OMe | Me | I | - ch2-co- (4-Me-Ph) | |
| 7-252 | CH2OCH2CH2OMe | Et | I | - CH2-CO- (4-Me-Ph) | |
| 7-253 | Cl | Me | no2 | - CH2-CO- (4-Me-Ph) | |
| 7-254 | Cl | Et | no2 | - CH2-CO- (4-Me-Ph) |
176
| No. | X | R3 | Y | R4 | Dados físicos: 1H-NMR: δ [CDCI3] |
| 7-255 | Me | Me | no2 | - ch2-co- (4-Me-Ph) | |
| 7-256 | Me | Et | no2 | - ch2-co- (4-Me-Ph) | |
| 7-257 | cf3 | Me | no2 | - ch2-co- (4-Me-Ph) | |
| 7-258 | cf3 | Et | no2 | - CH2-CO- (4-Me-Ph) | |
| 7-259 | OMe | Me | no2 | - ch2-co- (4-Me-Ph) | |
| 7-260 | OMe | Et | no2 | - ch2-co- (4-Me-Ph) | |
| 7-261 | no2 | Me | no2 | - ch2-co- (4-Me-Ph) | |
| 7-262 | no2 | Et | no2 | - CH2-CO- (4-Me-Ph) | |
| 7-263 | SO2Me | Me | no2 | - ch2-co- (4-Me-Ph) | |
| 7-264 | SO2Me | Et | no2 | - ch2-co- (4-Me-Ph) | |
| 7-265 | CH2OMe | Me | no2 | - ch2-co- (4-Me-Ph) | |
| 7-266 | CH2OMe | Et | no2 | - ch2-co- (4-Me-Ph) |
177
| No. | X | R3 | Y | R4 | Dados físicos: |
| 1H-NMR: [CDCI3] | δ | ||||
| 7-267 | CH2SO2Me | Me | NO2 | - ch2-co- (4-Me-Ph) | |
| 7-268 | CH2SO2Me | Et | no2 | - ch2-co(4-Me-Ph) | |
| 7-269 | CH2OCH2CH2OMe | Me | no2 | - ch2-co(4-Me-Ph) | |
| 7-270 | CH2OCH2CH2OMe | Et | no2 | - ch2-co- (4-Me-Ph) |
B. Exemplos de Formulação
a. É obtido um pó por meio de mistura de dez partes em peso de um composto de fórmula (I) e/ou seus sais e noventa partes em peso de talco como substância inerte e particulação da mistura em um moinho martelo.
b. Pó molhável que é facilmente dispersível em água é obtido por meio da mistura de 25 partes em peso de um composto de fórmula (I) e/ou seus sais, 64 partes em peso de quartzo que contém caulim como substância inerte, dez partes em peso de lignossulfonato de potássio e uma parte em peso de oleoilmetiltaurinato de sódio como umectante e dispersante e moagem da 10 mistura em um moinho com disco aparafusado.
c. Concentrado em dispersão que é facilmente dispersível em água é obtido por meio de mistura de vinte partes em peso de um composto de fórmula (I) e/ou seus sais com seis partes em peso de alquilfenol poliglicol éter (Triton® x 207), três partes em peso de isotridecanol poliglicol éter (8 EO) e 71 15 partes em peso de óleo mineral parafínico (faixa de ebulição de, por exemplo,
178 cerca de 255 até mais de 277 °C) e moagem da mistura em um moinho de tigela até granulometria de menos de 5 micra.
d. Um concentrado emulsionável é obtido a partir de 15 partes em peso de um composto de fórmula (I) e/ou seus sais, 75 partes em peso de ciclo-hexanona como solvente e 10 partes em peso de nonilfenol oxietilado como emulsificante.
e. Grânulos dispersíveis em água são obtidos por meio da mistura de:
partes em peso de um composto de fórmula (I) e/ou seus sais;
partes em peso de lignossulfonato de cálcio;
partes em peso de lauril sulfato de sódio;
partes em peso de álcool polivinílico; e partes em peso de caulim;
moagem da mistura em um moinho com disco aparafusado e granulação do pó em leito fluidificado por meio de pulverização sobre água na forma de líquido de granulação.
f. Grânulos dispersíveis em água também são obtidos por meio de homogeneização e fragmentação prévia em um moinho coloidal de:
partes em peso de um composto de fórmula (I) e/ou seus sais;
partes em peso de 2,2’-dinaftilmetano-6,6’-dissulfonato de sódio;
partes em peso de oleoilmetiltaurinato de sódio;
parte em peso de álcool polivinílico;
partes em peso de carbonato de cálcio; e partes em peso de água;
moagem subsequente da mistura em um moinho de esferas,
179 atomização e secagem da suspensão resultante em uma torre de pulverização por meio de um bocal de substância única.
C. Exemplos biológicos:
1. Efeito pré-emergência herbicida contra plantas daninhas:
Sementes de ervas monocotiledôneas ou dicotiledôneas ou plantas de culturas são colocadas em solo de lodo arenoso em vasos de fibra de madeira e cobertas com solo. Os compostos de acordo com a presente invenção, formulados como pós molháveis (WP) ou concentrados emulsionáveis (EC), são aplicados em seguida à superfície da cobertura de solo na forma de suspensão aquosa ou emulsão em uma taxa de aplicação de água de 600 a 800 l/ha (convertida), com adição de 0,2% de umectante. Após o tratamento, os vasos são colocados na estufa e mantidos sob boas condições de crescimento para as plantas de teste. Os danos às plantas de teste são avaliados visualmente em comparação com controles não tratados após um período experimental de três semanas (atividade herbicida em percentual (%): 100% de atividade = as plantas morreram, 0% de atividade = similar a plantas controle). Neste ponto, por exemplo, os compostos n° 1-2, 2-9, 2-10, 2-11 e 3238 exibem, em uma taxa de aplicação de 80 g/ha, atividade de resistência de pelo menos 90% contra Amaranthus retroflexus e Veronica pérsica.
Os compostos n° 1-237, 1-238, 2-9, 2-10, 2-237 e 2-238 exibem, em uma taxa de aplicação de 80 g/ha, atividade de resistência de pelo menos 90% contra Abutilon theophrasti, Amaranthus retroflexus e Echinochloa crus galli. Os compostos n° 1-10, 2-9 e 2-238 exibem, em uma taxa de aplicação de 80 g/ha, atividade de resistência de pelo menos 90% contra Abutilon theophrasti e Matricaria inodora.
2. Atividade herbicida pós-emergência contra plantas daninhas:
Sementes de ervas monocotiledôneas ou dicotiledôneas ou plantas de culturas são colocadas em solo de lodo arenoso em vasos de fibra
180 de madeira, cobertas com solo e cultivadas em estufa sob boas condições de crescimento. Duas a três semanas após o cultivo, as plantas de teste são tratadas no estágio de uma folha. Os compostos de acordo com a presente invenção, formulados como pós molháveis (WP) ou concentrados emulsionáveis (EC), são pulverizados em seguida sobre as partes de planta verde na forma de suspensão aquosa ou emulsão em uma taxa de aplicação de água de 600 a 800 l/ha (convertida), com adição de 0,2% de umectante. Após manter-se as plantas de teste em repouso sob condições ideais de crescimento na estufa por cerca de três semanas, a atividade das preparações é avaliada visualmente em comparação com controles não tratados (atividade herbicida em percentual (%): 100% de atividade = as plantas morreram, 0% de atividade = similar a plantas controle).
Neste ponto, por exemplo, os compostos n° 1-10, 1-237 e 2-9 exibem, em uma taxa de aplicação de 80 g/ha, pelo menos 90% de atividade de resistência contra Stellaria media e Veronica pérsica. Os compostos n° 1238, 2-10 e 2-238 exibem, em uma taxa de aplicação de 80 g/ha, atividade de resistência de pelo menos 90% contra Setaria viridis e Viola tricolor. Os compostos n° 1-2, 1-237, 1-238 e 2-11 exibem, em uma taxa de aplicação de 80 g/ha, atividade de resistência de pelo menos 90% contra Abutilon theophrasti e Echinochloa crus galli.
Claims (11)
- Reivindicações1. 4-(3-ALQUILSULFINILBENZOIL)PIRAZOL, caracterizado pelo fato de ser de formula (I) ou um sal do mesmo:r2 oxo \ II I IIem que:R1 é alquila (C1-C4);R2 é hidrogênio ou alquila (C-1-C4);R3 é alquila (C-i-Ce);R4 é hidrogênio, alquilsulfonila (C-i-Ce), alcóxi (C1-C4)alquilsulfonila (C-i-Ce), ou é fenilsulfonila, tiofenil-2-sulfonila, benzoíla, benzoilalquila (Ci-C6) ou benzila, cada um dos quais é substituído por m radicais idênticos ou diferentes a partir do grupo que consiste em halogênio, alquila (C1-C4) e alcóxi (C1-C4);X é hidrogênio, mercapto, nitro, halogênio, ciano, tiocianato, alquila (Ci-C6), haloalquila (C-i-Ce), alquenila (C2-C6), haloalquenila (C2-C6), alquinila (C2-C6), haloalquinila (C3-C6), cicloalquila (C3-C6), OR5, OCOR5, OSO2R5, S(O)nR5, SO2OR5, SO2N(R5)2, NR5SO2R5, NR5COR5, alquila (Ci-C6)-S(O)nR5, alquila (Ci-C6)-OR5, alquila (Ci-C6)-OCOR5, alquila (Ci-C6)OSO2R5, alquila (C1-C6)-SO2OR5, alquila (Ci-C6)-SO2N(R5)2 ou alquila (Ci-C6)NR5COR5;Y é flúor, cloro, bromo, iodo, nitro ou o grupo SO2R7;R5 é hidrogênio, alquila (C-i-C6), alquenila (C2-C6), alquinila (C2-C6), cicloalquila (C3-C6), fenila ou fenilalquila (Cfi-Ce), em que os seis radicais mencionados por último são substituídos por s radicais do grupo que consiste em hidróxi, mercapto, amino, ciano, nitro, tiocianato, OR6, SR6, N(R6)2,NOR6, OCOR6, SCOR6, NR6COR6, CO2R6, COSR6, CON(R6)2, alquilimino-óxi (C1-C4), alquilcarbonila (C1-C4), alcóxi (Ci-C4)-alcoxicarbonila (C2-Ce) e alquilsulfonila (C-1-C4);R6 é hidrogênio, alquila (Ci-C6), alquenila (C2-C6) ou alquinila (C2-Ce);R7 é alquila (C1-C4);m é 0, 1,2, 3, 4 ou 5;n é 0, 1 ou 2;s é 0, 1, 2 ou 3.
- 2. 4-(3-ALQUILSULFINILBENZOIL)PIRAZOL, de acordo com a reivindicação 1, caracterizado pelo fato de que:R1 é metila, etila, n-propila ou isopropila;R2 é hidrogênio, metila, etila, n-propila ou isopropila;R3 é alquila (C1-C4);R4 é hidrogênio, alquilsulfonila (C1-C3), alcóxi (CrC2)alquilsulfonila (C1-C4), ou é fenilsulfonila, tiofenil-2-sulfonila, benzoíla, benzoilalquila (Ci-Ce) ou benzila, cada um dos quais é substituído por m grupos metila;X é nitro, halogênio, alquila (C1-C4), trifluorometila, alcóxi (C1-C4), metilsulfonila, metoximetila, metoximetoximetila, etoxietoximetila, etoximetoximetila, metoxietoximetila, metoxipropoximetila, metilsulfonilmetila, metilsulfoniletoximetila, metoxietilsulfonilmetila ou metilsulfoniletilsulfonilmetila;Y é flúor, cloro, bromo, iodo ou 0 grupo SO2R7;R7 é metila, etila, n-propila ou isopropila;m é 0, 1,2 ou 3.
- 3. 4-(3-ALQUILSULFINILBENZOIL)PIRAZOL, de acordo com a reivindicação 1 ou 2, caracterizado pelo fato de que:R1 é metila ou etila;R2 é hidrogênio, metila ou etila;R3 é metila, etila, n-propila ou isopropila;R4 é hidrogênio;X é nitro, halogênio, alquila (C1-C4), trifluorometila, alcóxi (C1-C4), metilsulfonila, metoximetila, metoximetoximetila, etoxietoximetila, etoximetoximetila, metoxietoximetila, metoxipropoximetila, metilsulfonilmetila, metilsulfoniletoximetila, metoxietilsulfonilmetila, metilsulfoniletilsulfonilmetila;Y é flúor, cloro, bromo, iodo ou o grupo SO2R7;R7 é metila ou etila.
- 4. COMPOSIÇÃO HERBICIDA, caracterizada pelo fato de que compreende uma quantidade ativa como herbicida de pelo menos um composto de fórmula (I) conforme definido em uma das reivindicações 1 a 3.
- 5. COMPOSIÇÃO HERBICIDA, de acordo com a reivindicação 4, caracterizada pelo fato de que é uma mistura com auxiliares de formulação.
- 6. MÉTODO DE CONTROLE DE PLANTAS INDESEJADAS, caracterizado pelo fato de que compreende a aplicação de uma quantidade eficaz de pelo menos um composto de fórmula (I), conforme definido em uma das reivindicações 1 a 3, ou de uma composição herbicida, conforme definida em uma das reivindicações 4 ou 5, às plantas ou ao local de crescimento da planta indesejada.
- 7. USO DE UM COMPOSTO DE FÓRMULA (I), conforme definido em uma das reivindicações 1 a 3, caracterizado pelo fato de ser para o controle de plantas indesejadas.
- 8. USO DE UMA COMPOSIÇÃO HERBICIDA, conforme definida em uma das reivindicações 4 ou 5, caracterizado pelo fato de ser para 0 controle de plantas indesejadas.
- 9. USO, de acordo com a reivindicação 7 ou 8, caracterizado pelo fato de que os compostos de fórmula (I) ou as composições herbicidas são empregados para o controle de plantas indesejadas em culturas de plantas úteis.
- 10. USO, de acordo com a reivindicação 9, caracterizado pelo 5 fato de que as plantas úteis são plantas úteis transgênicas.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP08009758A EP2127521A1 (de) | 2008-05-29 | 2008-05-29 | Herbizid wirksame 4-(3-Alkylsulfinylbenzoyl)pyrazole |
| EP08009758.7 | 2008-05-29 | ||
| PCT/EP2009/003474 WO2009149806A2 (de) | 2008-05-29 | 2009-05-15 | Herbizid wirksame 4- (3-alkylsulfinylbenzoyl) pyrazole |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI0909535A2 true BRPI0909535A2 (pt) | 2019-09-10 |
| BRPI0909535B1 BRPI0909535B1 (pt) | 2021-01-19 |
Family
ID=39865612
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0909535-7A BRPI0909535B1 (pt) | 2008-05-29 | 2009-05-15 | 4-(3-alquilsulfinilbenzoil)pirazol, composição herbicida, método de controle de plantasindesejadas, uso de um composto de fórmula (i) ou de uma composição herbicida e composto |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US8114816B2 (pt) |
| EP (2) | EP2127521A1 (pt) |
| CN (1) | CN102065690B (pt) |
| AR (1) | AR071902A1 (pt) |
| AU (1) | AU2009256968A1 (pt) |
| BR (1) | BRPI0909535B1 (pt) |
| CA (1) | CA2725980C (pt) |
| CL (1) | CL2009001235A1 (pt) |
| DK (1) | DK2296473T3 (pt) |
| TW (1) | TW201010609A (pt) |
| WO (1) | WO2009149806A2 (pt) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1980556A1 (de) * | 2007-04-12 | 2008-10-15 | Bayer CropScience AG | 4-(4-Trifluormethyl-3-thiobenzoyl)pyrazole und ihre Verwendung als Herbizide |
| US20100129641A1 (en) * | 2008-11-25 | 2010-05-27 | Lopez Leonardo C | Polymer carbon composites |
| US20100127434A1 (en) * | 2008-11-25 | 2010-05-27 | Rene Broos | Extruding organic polymers |
| US8440297B2 (en) * | 2008-11-25 | 2013-05-14 | Dow Global Technologies Llc | Polymer organoclay composites |
| EA201270088A1 (ru) * | 2009-07-29 | 2012-09-28 | Байер Кропсайенс Аг | 4-(3-алкилтиобензоил)пиразолы и их применение в качестве гербицидов |
| US8455657B2 (en) * | 2010-12-28 | 2013-06-04 | Bayer Cropscience Ag | Process for the preparation of 3-alkylsulfinylbenzoyl derivatives |
| WO2013124230A1 (de) | 2012-02-21 | 2013-08-29 | Bayer Intellectual Property Gmbh | Herbizid wirksame sulfinimidoyl- und sulfonimidoylbenzoylderivate |
| CN103304480A (zh) * | 2013-07-09 | 2013-09-18 | 黑龙江胜农科技开发有限公司 | 苯甲酰吡唑类化合物及其合成方法和以该类化合物作为除草剂的应用 |
| TWI741040B (zh) * | 2016-10-20 | 2021-10-01 | 德商拜耳作物科學公司 | 製備3-烷基硫基-2-氯-n-(1-烷基-1h-四唑-5-基)-4-三氟甲基苯甲醯胺之方法 |
| CN111808024B (zh) * | 2019-04-11 | 2023-06-27 | 郑州手性药物研究院有限公司 | 一种苯基吡唑酮类化合物或其盐、制备方法和应用 |
| BR112022019738A2 (pt) * | 2020-04-07 | 2022-11-16 | Bayer Ag | Isoftalamidas substituídas e seu uso como herbicidas |
Family Cites Families (26)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US629168A (en) * | 1898-06-27 | 1899-07-18 | William Thompson Brown Mcdonald | Umbrella-repairing device. |
| EP0131624B1 (en) | 1983-01-17 | 1992-09-16 | Monsanto Company | Plasmids for transforming plant cells |
| BR8404834A (pt) | 1983-09-26 | 1985-08-13 | Agrigenetics Res Ass | Metodo para modificar geneticamente uma celula vegetal |
| BR8600161A (pt) | 1985-01-18 | 1986-09-23 | Plant Genetic Systems Nv | Gene quimerico,vetores de plasmidio hibrido,intermediario,processo para controlar insetos em agricultura ou horticultura,composicao inseticida,processo para transformar celulas de plantas para expressar uma toxina de polipeptideo produzida por bacillus thuringiensis,planta,semente de planta,cultura de celulas e plasmidio |
| EP0221044B1 (en) | 1985-10-25 | 1992-09-02 | Monsanto Company | Novel plant vectors |
| ES2018274T5 (es) | 1986-03-11 | 1996-12-16 | Plant Genetic Systems Nv | Celulas vegetales resistentes a los inhibidores de glutamina sintetasa, preparadas por ingenieria genetica. |
| IL83348A (en) | 1986-08-26 | 1995-12-08 | Du Pont | Nucleic acid fragment encoding herbicide resistant plant acetolactate synthase |
| US5013659A (en) | 1987-07-27 | 1991-05-07 | E. I. Du Pont De Nemours And Company | Nucleic acid fragment encoding herbicide resistant plant acetolactate synthase |
| IL85659A (en) * | 1987-03-17 | 1992-03-29 | Nissan Chemical Ind Ltd | 4-benzoylpyrazole derivatives,method for their preparation and herbicidal compositions containing them |
| US4885022A (en) * | 1987-03-17 | 1989-12-05 | Nissan Chemical Industries Ltd. | Herbicidal pyrazole derivatives |
| JPS6452759A (en) * | 1987-05-01 | 1989-02-28 | Nissan Chemical Ind Ltd | Pyrazole derivative and selective herbicide |
| DE3733017A1 (de) | 1987-09-30 | 1989-04-13 | Bayer Ag | Stilbensynthase-gen |
| US4986845A (en) | 1988-07-15 | 1991-01-22 | Nissan Chemical Industries Ltd. | Pyrazole derivatives and herbicides containing them |
| CA2077896C (en) | 1990-03-16 | 2008-02-19 | Gregory A. Thompson | Plant desaturases - compositions and uses |
| DE69132916T2 (de) | 1990-06-18 | 2002-10-31 | Monsanto Technology Llc, St. Louis | Erhöhter stärkegehalt in pflanzen |
| ATE213774T1 (de) | 1990-06-25 | 2002-03-15 | Monsanto Technology Llc | Glyphosattolerante pflanzen |
| DE4107396A1 (de) | 1990-06-29 | 1992-01-02 | Bayer Ag | Stilbensynthase-gene aus weinrebe |
| SE467358B (sv) | 1990-12-21 | 1992-07-06 | Amylogene Hb | Genteknisk foeraendring av potatis foer bildning av staerkelse av amylopektintyp |
| DE4104782B4 (de) | 1991-02-13 | 2006-05-11 | Bayer Cropscience Gmbh | Neue Plasmide, enthaltend DNA-Sequenzen, die Veränderungen der Karbohydratkonzentration und Karbohydratzusammensetzung in Pflanzen hervorrufen, sowie Pflanzen und Pflanzenzellen enthaltend dieses Plasmide |
| DE19532312A1 (de) * | 1995-09-01 | 1997-03-06 | Basf Ag | Pyrazol-4-yl-benzoylderivate |
| AR006793A1 (es) | 1996-04-26 | 1999-09-29 | Ishihara Sangyo Kaisha | Compuestos pirazol o sus sales y herbicidas conteniendo los mismos |
| AU4652499A (en) | 1998-07-16 | 2000-02-07 | Ishihara Sangyo Kaisha Ltd. | Pyrazole-type compounds, process for producing the same and herbicides containing the same |
| EP1135385A1 (de) * | 1998-12-04 | 2001-09-26 | Basf Aktiengesellschaft | Thiochromanoylpyrazolon-derivate |
| DE102004029308A1 (de) | 2004-06-17 | 2005-12-29 | Bayer Cropscience Gmbh | Substituierte Benzoylpyrazole als Herbiszide |
| AR056889A1 (es) * | 2005-12-15 | 2007-10-31 | Ishihara Sangyo Kaisha | Compuestos benzoilpirazol y herbicidas que los contienen |
| DE102007026875A1 (de) | 2007-06-11 | 2008-12-24 | Bayer Cropscience Ag | 3-Cyclopropyl-4-(3-thiobenzoyl)pyrazole und ihre Verwendung als Herbizide |
-
2008
- 2008-05-29 EP EP08009758A patent/EP2127521A1/de not_active Withdrawn
-
2009
- 2009-05-15 CA CA2725980A patent/CA2725980C/en not_active Expired - Fee Related
- 2009-05-15 DK DK09761369.9T patent/DK2296473T3/da active
- 2009-05-15 WO PCT/EP2009/003474 patent/WO2009149806A2/de not_active Ceased
- 2009-05-15 CN CN2009801197777A patent/CN102065690B/zh active Active
- 2009-05-15 BR BRPI0909535-7A patent/BRPI0909535B1/pt not_active IP Right Cessation
- 2009-05-15 EP EP09761369A patent/EP2296473B1/de active Active
- 2009-05-15 AU AU2009256968A patent/AU2009256968A1/en not_active Abandoned
- 2009-05-19 CL CL2009001235A patent/CL2009001235A1/es unknown
- 2009-05-26 AR ARP090101870A patent/AR071902A1/es not_active Application Discontinuation
- 2009-05-26 TW TW098117461A patent/TW201010609A/zh unknown
- 2009-05-27 US US12/472,682 patent/US8114816B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| CN102065690B (zh) | 2013-11-06 |
| CA2725980C (en) | 2016-08-09 |
| CA2725980A1 (en) | 2009-12-17 |
| US20100004129A1 (en) | 2010-01-07 |
| AU2009256968A1 (en) | 2009-12-17 |
| CL2009001235A1 (es) | 2009-10-09 |
| EP2296473A2 (de) | 2011-03-23 |
| EP2127521A1 (de) | 2009-12-02 |
| WO2009149806A2 (de) | 2009-12-17 |
| EP2296473B1 (de) | 2012-07-11 |
| CN102065690A (zh) | 2011-05-18 |
| TW201010609A (en) | 2010-03-16 |
| US8114816B2 (en) | 2012-02-14 |
| AR071902A1 (es) | 2010-07-21 |
| BRPI0909535B1 (pt) | 2021-01-19 |
| WO2009149806A3 (de) | 2011-04-14 |
| DK2296473T3 (da) | 2012-10-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US8481749B2 (en) | N-(tetrazol-5-yl)- and N-(triazol-5-yl)arylcarboxamides and their use as herbicides | |
| US9101141B2 (en) | N-(1,3,4-oxadiazol-2-yl)arylcarboxamides and use thereof as herbicides | |
| US8114816B2 (en) | Herbicidally active 4-(3-alkylsulfinylbenzoyl)pyrazoles | |
| US8288319B2 (en) | 4-(3-alkylthiobenzoyl)pyrazoles and their use as herbicides | |
| AU2018241490B2 (en) | Substituted N-(-1,3,4-oxadiazole-2-yl)aryl carboxamides and the use thereof as herbicides | |
| US8962529B2 (en) | Substituted picolinic acids, salts and acid derivatives thereof, and use thereof as herbicides | |
| US8193121B2 (en) | 2-(3-alkylthiobenzoyl)cyclohexanediones and their use as herbicides | |
| CA2695325A1 (en) | Herbicide triazolylpyridine ketones | |
| EA040923B1 (ru) | Замещенные n-(1,3,4-оксадиазол-2-ил)арилкарбоксамиды и их применение в качестве гербицидов |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B25A | Requested transfer of rights approved |
Owner name: BAYER INTELLECTUAL PROPERTY GMBH (DE) |
|
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 10 (DEZ) ANOS CONTADOS A PARTIR DE 19/01/2021, OBSERVADAS AS CONDICOES LEGAIS. |
|
| B25G | Requested change of headquarter approved |
Owner name: BAYER INTELLECTUAL PROPERTY GMBH (DE) |
|
| B25A | Requested transfer of rights approved |
Owner name: BAYER CROPSCIENCE AKTIENGESELLSCHAFT (DE) |
|
| B21F | Lapse acc. art. 78, item iv - on non-payment of the annual fees in time |
Free format text: REFERENTE A 17A ANUIDADE. |