BRPI0920351B1 - Composição farmacêutica para prevenção e tratamento de diabetes ou obesidade - Google Patents
Composição farmacêutica para prevenção e tratamento de diabetes ou obesidade Download PDFInfo
- Publication number
- BRPI0920351B1 BRPI0920351B1 BRPI0920351-6A BRPI0920351A BRPI0920351B1 BR PI0920351 B1 BRPI0920351 B1 BR PI0920351B1 BR PI0920351 A BRPI0920351 A BR PI0920351A BR PI0920351 B1 BRPI0920351 B1 BR PI0920351B1
- Authority
- BR
- Brazil
- Prior art keywords
- acid
- composition according
- compound
- preparation example
- amino
- Prior art date
Links
- 239000008194 pharmaceutical composition Substances 0.000 title claims abstract description 43
- 206010012601 diabetes mellitus Diseases 0.000 title claims abstract description 27
- 208000008589 Obesity Diseases 0.000 title claims abstract description 16
- 235000020824 obesity Nutrition 0.000 title claims abstract description 16
- 230000002265 prevention Effects 0.000 title claims abstract description 11
- 150000001875 compounds Chemical class 0.000 claims abstract description 192
- 101000930822 Giardia intestinalis Dipeptidyl-peptidase 4 Proteins 0.000 claims abstract description 39
- 150000003839 salts Chemical class 0.000 claims abstract description 25
- 230000003178 anti-diabetic effect Effects 0.000 claims abstract description 22
- 239000003472 antidiabetic agent Substances 0.000 claims abstract description 22
- 239000000883 anti-obesity agent Substances 0.000 claims abstract description 20
- 229940125708 antidiabetic agent Drugs 0.000 claims abstract description 20
- 229940125710 antiobesity agent Drugs 0.000 claims abstract description 20
- 239000004480 active ingredient Substances 0.000 claims abstract description 12
- 239000000203 mixture Substances 0.000 claims description 114
- XZWYZXLIPXDOLR-UHFFFAOYSA-N metformin Chemical group CN(C)C(=N)NC(N)=N XZWYZXLIPXDOLR-UHFFFAOYSA-N 0.000 claims description 65
- 229960003105 metformin Drugs 0.000 claims description 65
- -1 t-butoxy methyl Chemical group 0.000 claims description 47
- 102100025012 Dipeptidyl peptidase 4 Human genes 0.000 claims description 38
- YASAKCUCGLMORW-UHFFFAOYSA-N Rosiglitazone Chemical compound C=1C=CC=NC=1N(C)CCOC(C=C1)=CC=C1CC1SC(=O)NC1=O YASAKCUCGLMORW-UHFFFAOYSA-N 0.000 claims description 36
- JZCPYUJPEARBJL-UHFFFAOYSA-N rimonabant Chemical compound CC=1C(C(=O)NN2CCCCC2)=NN(C=2C(=CC(Cl)=CC=2)Cl)C=1C1=CC=C(Cl)C=C1 JZCPYUJPEARBJL-UHFFFAOYSA-N 0.000 claims description 24
- 229960003015 rimonabant Drugs 0.000 claims description 24
- 229940122820 Cannabinoid receptor antagonist Drugs 0.000 claims description 22
- 239000003536 cannabinoid receptor antagonist Substances 0.000 claims description 22
- 239000003112 inhibitor Substances 0.000 claims description 20
- FZNCGRZWXLXZSZ-CIQUZCHMSA-N Voglibose Chemical compound OCC(CO)N[C@H]1C[C@](O)(CO)[C@@H](O)[C@H](O)[C@H]1O FZNCGRZWXLXZSZ-CIQUZCHMSA-N 0.000 claims description 19
- 229960001729 voglibose Drugs 0.000 claims description 19
- 229960004586 rosiglitazone Drugs 0.000 claims description 18
- 229940122355 Insulin sensitizer Drugs 0.000 claims description 16
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 claims description 15
- 229940122199 Insulin secretagogue Drugs 0.000 claims description 15
- 229940125904 compound 1 Drugs 0.000 claims description 15
- 229940077274 Alpha glucosidase inhibitor Drugs 0.000 claims description 13
- 229960004346 glimepiride Drugs 0.000 claims description 13
- WIGIZIANZCJQQY-RUCARUNLSA-N glimepiride Chemical compound O=C1C(CC)=C(C)CN1C(=O)NCCC1=CC=C(S(=O)(=O)NC(=O)N[C@@H]2CC[C@@H](C)CC2)C=C1 WIGIZIANZCJQQY-RUCARUNLSA-N 0.000 claims description 13
- 229940123208 Biguanide Drugs 0.000 claims description 12
- HYAFETHFCAUJAY-UHFFFAOYSA-N pioglitazone Chemical compound N1=CC(CC)=CC=C1CCOC(C=C1)=CC=C1CC1C(=O)NC(=O)S1 HYAFETHFCAUJAY-UHFFFAOYSA-N 0.000 claims description 11
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 claims description 9
- XNCOSPRUTUOJCJ-UHFFFAOYSA-N Biguanide Chemical compound NC(N)=NC(N)=N XNCOSPRUTUOJCJ-UHFFFAOYSA-N 0.000 claims description 8
- 125000004063 butyryl group Chemical group O=C([*])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 claims description 8
- ZOBPZXTWZATXDG-UHFFFAOYSA-N 1,3-thiazolidine-2,4-dione Chemical compound O=C1CSC(=O)N1 ZOBPZXTWZATXDG-UHFFFAOYSA-N 0.000 claims description 7
- 229960004580 glibenclamide Drugs 0.000 claims description 7
- ZNNLBTZKUZBEKO-UHFFFAOYSA-N glyburide Chemical compound COC1=CC=C(Cl)C=C1C(=O)NCCC1=CC=C(S(=O)(=O)NC(=O)NC2CCCCC2)C=C1 ZNNLBTZKUZBEKO-UHFFFAOYSA-N 0.000 claims description 7
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 claims description 6
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 claims description 6
- XUFXOAAUWZOOIT-SXARVLRPSA-N (2R,3R,4R,5S,6R)-5-[[(2R,3R,4R,5S,6R)-5-[[(2R,3R,4S,5S,6R)-3,4-dihydroxy-6-methyl-5-[[(1S,4R,5S,6S)-4,5,6-trihydroxy-3-(hydroxymethyl)-1-cyclohex-2-enyl]amino]-2-oxanyl]oxy]-3,4-dihydroxy-6-(hydroxymethyl)-2-oxanyl]oxy]-6-(hydroxymethyl)oxane-2,3,4-triol Chemical group O([C@H]1O[C@H](CO)[C@H]([C@@H]([C@H]1O)O)O[C@H]1O[C@@H]([C@H]([C@H](O)[C@H]1O)N[C@@H]1[C@@H]([C@@H](O)[C@H](O)C(CO)=C1)O)C)[C@@H]1[C@@H](CO)O[C@@H](O)[C@H](O)[C@H]1O XUFXOAAUWZOOIT-SXARVLRPSA-N 0.000 claims description 5
- 229960002632 acarbose Drugs 0.000 claims description 5
- XUFXOAAUWZOOIT-UHFFFAOYSA-N acarviostatin I01 Natural products OC1C(O)C(NC2C(C(O)C(O)C(CO)=C2)O)C(C)OC1OC(C(C1O)O)C(CO)OC1OC1C(CO)OC(O)C(O)C1O XUFXOAAUWZOOIT-UHFFFAOYSA-N 0.000 claims description 5
- 239000003888 alpha glucosidase inhibitor Substances 0.000 claims description 5
- 150000004283 biguanides Chemical class 0.000 claims description 5
- 238000009472 formulation Methods 0.000 claims description 5
- 229960005095 pioglitazone Drugs 0.000 claims description 5
- GHOKWGTUZJEAQD-ZETCQYMHSA-N (D)-(+)-Pantothenic acid Chemical compound OCC(C)(C)[C@@H](O)C(=O)NCCC(O)=O GHOKWGTUZJEAQD-ZETCQYMHSA-N 0.000 claims description 4
- HMXDWDSNPRNUKI-UHFFFAOYSA-N 5-(4-bromophenyl)-1-(2,4-dichlorophenyl)-4-ethyl-N-(1-piperidinyl)-3-pyrazolecarboxamide Chemical compound CCC=1C(C(=O)NN2CCCCC2)=NN(C=2C(=CC(Cl)=CC=2)Cl)C=1C1=CC=C(Br)C=C1 HMXDWDSNPRNUKI-UHFFFAOYSA-N 0.000 claims description 4
- RGHNJXZEOKUKBD-SQOUGZDYSA-N D-gluconic acid Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C(O)=O RGHNJXZEOKUKBD-SQOUGZDYSA-N 0.000 claims description 4
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 claims description 4
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 claims description 4
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 claims description 4
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 claims description 4
- 239000002253 acid Substances 0.000 claims description 4
- WNLRTRBMVRJNCN-UHFFFAOYSA-N adipic acid Chemical compound OC(=O)CCCCC(O)=O WNLRTRBMVRJNCN-UHFFFAOYSA-N 0.000 claims description 4
- 125000000217 alkyl group Chemical group 0.000 claims description 4
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 claims description 4
- 229960001381 glipizide Drugs 0.000 claims description 4
- ZJJXGWJIGJFDTL-UHFFFAOYSA-N glipizide Chemical compound C1=NC(C)=CN=C1C(=O)NCCC1=CC=C(S(=O)(=O)NC(=O)NC2CCCCC2)C=C1 ZJJXGWJIGJFDTL-UHFFFAOYSA-N 0.000 claims description 4
- NSJYMFYVNWVGON-UHFFFAOYSA-N glisentide Chemical compound COC1=CC=CC=C1C(=O)NCCC1=CC=C(S(=O)(=O)NC(=O)NC2CCCC2)C=C1 NSJYMFYVNWVGON-UHFFFAOYSA-N 0.000 claims description 4
- 229950008402 glisentide Drugs 0.000 claims description 4
- 125000005842 heteroatom Chemical group 0.000 claims description 4
- SUMDYPCJJOFFON-UHFFFAOYSA-N isethionic acid Chemical compound OCCS(O)(=O)=O SUMDYPCJJOFFON-UHFFFAOYSA-N 0.000 claims description 4
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 claims description 4
- 235000011090 malic acid Nutrition 0.000 claims description 4
- 229960000698 nateglinide Drugs 0.000 claims description 4
- OELFLUMRDSZNSF-BRWVUGGUSA-N nateglinide Chemical compound C1C[C@@H](C(C)C)CC[C@@H]1C(=O)N[C@@H](C(O)=O)CC1=CC=CC=C1 OELFLUMRDSZNSF-BRWVUGGUSA-N 0.000 claims description 4
- UNAZAADNBYXMIV-UHFFFAOYSA-N otenabant Chemical compound C1CC(NCC)(C(N)=O)CCN1C1=NC=NC2=C1N=C(C=1C(=CC=CC=1)Cl)N2C1=CC=C(Cl)C=C1 UNAZAADNBYXMIV-UHFFFAOYSA-N 0.000 claims description 4
- 229950005009 otenabant Drugs 0.000 claims description 4
- 229950003174 surinabant Drugs 0.000 claims description 4
- 235000002906 tartaric acid Nutrition 0.000 claims description 4
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 claims description 4
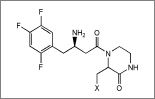
- AKVGPVSDFURZKX-FZKQIMNGSA-N (3r)-4-[(3r)-3-amino-4-(2,4,5-trifluorophenyl)butanoyl]-3-(cyclopentyloxymethyl)piperazin-2-one Chemical compound C([C@@H]1C(=O)NCCN1C(=O)C[C@H](N)CC=1C(=CC(F)=C(F)C=1)F)OC1CCCC1 AKVGPVSDFURZKX-FZKQIMNGSA-N 0.000 claims description 3
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 claims description 3
- BOVGTQGAOIONJV-BETUJISGSA-N 1-[(3ar,6as)-3,3a,4,5,6,6a-hexahydro-1h-cyclopenta[c]pyrrol-2-yl]-3-(4-methylphenyl)sulfonylurea Chemical compound C1=CC(C)=CC=C1S(=O)(=O)NC(=O)NN1C[C@H]2CCC[C@H]2C1 BOVGTQGAOIONJV-BETUJISGSA-N 0.000 claims description 3
- MVDXXGIBARMXSA-PYUWXLGESA-N 5-[[(2r)-2-benzyl-3,4-dihydro-2h-chromen-6-yl]methyl]-1,3-thiazolidine-2,4-dione Chemical compound S1C(=O)NC(=O)C1CC1=CC=C(O[C@@H](CC=2C=CC=CC=2)CC2)C2=C1 MVDXXGIBARMXSA-PYUWXLGESA-N 0.000 claims description 3
- FAEKWTJYAYMJKF-QHCPKHFHSA-N GlucoNorm Chemical compound C1=C(C(O)=O)C(OCC)=CC(CC(=O)N[C@@H](CC(C)C)C=2C(=CC=CC=2)N2CCCCC2)=C1 FAEKWTJYAYMJKF-QHCPKHFHSA-N 0.000 claims description 3
- IBAQFPQHRJAVAV-ULAWRXDQSA-N Miglitol Chemical compound OCCN1C[C@H](O)[C@@H](O)[C@H](O)[C@H]1CO IBAQFPQHRJAVAV-ULAWRXDQSA-N 0.000 claims description 3
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 claims description 3
- JLRGJRBPOGGCBT-UHFFFAOYSA-N Tolbutamide Chemical compound CCCCNC(=O)NS(=O)(=O)C1=CC=C(C)C=C1 JLRGJRBPOGGCBT-UHFFFAOYSA-N 0.000 claims description 3
- 235000011054 acetic acid Nutrition 0.000 claims description 3
- 235000011037 adipic acid Nutrition 0.000 claims description 3
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 claims description 3
- 239000005557 antagonist Substances 0.000 claims description 3
- 229960004111 buformin Drugs 0.000 claims description 3
- XSEUMFJMFFMCIU-UHFFFAOYSA-N buformin Chemical compound CCCC\N=C(/N)N=C(N)N XSEUMFJMFFMCIU-UHFFFAOYSA-N 0.000 claims description 3
- 229960003362 carbutamide Drugs 0.000 claims description 3
- VDTNNGKXZGSZIP-UHFFFAOYSA-N carbutamide Chemical compound CCCCNC(=O)NS(=O)(=O)C1=CC=C(N)C=C1 VDTNNGKXZGSZIP-UHFFFAOYSA-N 0.000 claims description 3
- YZFWTZACSRHJQD-UHFFFAOYSA-N ciglitazone Chemical compound C=1C=C(CC2C(NC(=O)S2)=O)C=CC=1OCC1(C)CCCCC1 YZFWTZACSRHJQD-UHFFFAOYSA-N 0.000 claims description 3
- 229950009226 ciglitazone Drugs 0.000 claims description 3
- 235000015165 citric acid Nutrition 0.000 claims description 3
- 229950000269 emiglitate Drugs 0.000 claims description 3
- 229950002375 englitazone Drugs 0.000 claims description 3
- NWWORXYTJRPSMC-QKPAOTATSA-N ethyl 4-[2-[(2r,3r,4r,5s)-3,4,5-trihydroxy-2-(hydroxymethyl)piperidin-1-yl]ethoxy]benzoate Chemical compound C1=CC(C(=O)OCC)=CC=C1OCCN1[C@H](CO)[C@@H](O)[C@H](O)[C@@H](O)C1 NWWORXYTJRPSMC-QKPAOTATSA-N 0.000 claims description 3
- 229960000346 gliclazide Drugs 0.000 claims description 3
- 229950005319 glisolamide Drugs 0.000 claims description 3
- GZKDXUIWCNCNBJ-UHFFFAOYSA-N glisolamide Chemical compound O1C(C)=CC(C(=O)NCCC=2C=CC(=CC=2)S(=O)(=O)NC(=O)NC2CCCCC2)=N1 GZKDXUIWCNCNBJ-UHFFFAOYSA-N 0.000 claims description 3
- 239000001630 malic acid Substances 0.000 claims description 3
- 229940099690 malic acid Drugs 0.000 claims description 3
- 229960001110 miglitol Drugs 0.000 claims description 3
- 229960003243 phenformin Drugs 0.000 claims description 3
- ICFJFFQQTFMIBG-UHFFFAOYSA-N phenformin Chemical compound NC(=N)NC(=N)NCCC1=CC=CC=C1 ICFJFFQQTFMIBG-UHFFFAOYSA-N 0.000 claims description 3
- 229960002354 repaglinide Drugs 0.000 claims description 3
- 239000011975 tartaric acid Substances 0.000 claims description 3
- 229960002277 tolazamide Drugs 0.000 claims description 3
- OUDSBRTVNLOZBN-UHFFFAOYSA-N tolazamide Chemical compound C1=CC(C)=CC=C1S(=O)(=O)NC(=O)NN1CCCCCC1 OUDSBRTVNLOZBN-UHFFFAOYSA-N 0.000 claims description 3
- 229960005371 tolbutamide Drugs 0.000 claims description 3
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 claims description 3
- GXPHKUHSUJUWKP-UHFFFAOYSA-N troglitazone Chemical group C1CC=2C(C)=C(O)C(C)=C(C)C=2OC1(C)COC(C=C1)=CC=C1CC1SC(=O)NC1=O GXPHKUHSUJUWKP-UHFFFAOYSA-N 0.000 claims description 3
- 229960001641 troglitazone Drugs 0.000 claims description 3
- GXPHKUHSUJUWKP-NTKDMRAZSA-N troglitazone Natural products C([C@@]1(OC=2C(C)=C(C(=C(C)C=2CC1)O)C)C)OC(C=C1)=CC=C1C[C@H]1SC(=O)NC1=O GXPHKUHSUJUWKP-NTKDMRAZSA-N 0.000 claims description 3
- QBYIENPQHBMVBV-HFEGYEGKSA-N (2R)-2-hydroxy-2-phenylacetic acid Chemical compound O[C@@H](C(O)=O)c1ccccc1.O[C@@H](C(O)=O)c1ccccc1 QBYIENPQHBMVBV-HFEGYEGKSA-N 0.000 claims description 2
- WHTXKYSPHZDQKQ-QMTHXVAHSA-N (3r)-4-[(3r)-3-amino-4-(2,4,5-trifluorophenyl)butanoyl]-3-(methoxymethyl)piperazin-2-one Chemical compound C1CNC(=O)[C@@H](COC)N1C(=O)C[C@H](N)CC1=CC(F)=C(F)C=C1F WHTXKYSPHZDQKQ-QMTHXVAHSA-N 0.000 claims description 2
- UNMSUDXXSSQFQK-MLGOLLRUSA-N (3r)-4-[(3r)-3-amino-4-(2,4,5-trifluorophenyl)butanoyl]-3-(propan-2-yloxymethyl)piperazin-2-one Chemical compound C1CNC(=O)[C@@H](COC(C)C)N1C(=O)C[C@H](N)CC1=CC(F)=C(F)C=C1F UNMSUDXXSSQFQK-MLGOLLRUSA-N 0.000 claims description 2
- HZSCESFYCFULOF-WBMJQRKESA-N (3r)-4-[(3r)-3-amino-4-(2,4,5-trifluorophenyl)butanoyl]-3-(tert-butylsulfanylmethyl)piperazin-2-one Chemical compound C1CNC(=O)[C@H](CSC(C)(C)C)N1C(=O)C[C@H](N)CC1=CC(F)=C(F)C=C1F HZSCESFYCFULOF-WBMJQRKESA-N 0.000 claims description 2
- ALUVOKDKZXZDMM-MLGOLLRUSA-N (3r)-4-[(3r)-3-amino-4-(2,4,5-trifluorophenyl)butanoyl]-3-[[ethyl(methyl)amino]methyl]piperazin-2-one Chemical compound C1CNC(=O)[C@@H](CN(C)CC)N1C(=O)C[C@H](N)CC1=CC(F)=C(F)C=C1F ALUVOKDKZXZDMM-MLGOLLRUSA-N 0.000 claims description 2
- MIOPJNTWMNEORI-GMSGAONNSA-N (S)-camphorsulfonic acid Chemical compound C1C[C@@]2(CS(O)(=O)=O)C(=O)C[C@@H]1C2(C)C MIOPJNTWMNEORI-GMSGAONNSA-N 0.000 claims description 2
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 claims description 2
- 239000005711 Benzoic acid Substances 0.000 claims description 2
- GHOKWGTUZJEAQD-UHFFFAOYSA-N Chick antidermatitis factor Natural products OCC(C)(C)C(O)C(=O)NCCC(O)=O GHOKWGTUZJEAQD-UHFFFAOYSA-N 0.000 claims description 2
- RKWGIWYCVPQPMF-UHFFFAOYSA-N Chloropropamide Chemical compound CCCNC(=O)NS(=O)(=O)C1=CC=C(Cl)C=C1 RKWGIWYCVPQPMF-UHFFFAOYSA-N 0.000 claims description 2
- RGHNJXZEOKUKBD-UHFFFAOYSA-N D-gluconic acid Natural products OCC(O)C(O)C(O)C(O)C(O)=O RGHNJXZEOKUKBD-UHFFFAOYSA-N 0.000 claims description 2
- DSLZVSRJTYRBFB-UHFFFAOYSA-N Galactaric acid Natural products OC(=O)C(O)C(O)C(O)C(O)C(O)=O DSLZVSRJTYRBFB-UHFFFAOYSA-N 0.000 claims description 2
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 claims description 2
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 claims description 2
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 claims description 2
- IWYDHOAUDWTVEP-UHFFFAOYSA-N R-2-phenyl-2-hydroxyacetic acid Natural products OC(=O)C(O)C1=CC=CC=C1 IWYDHOAUDWTVEP-UHFFFAOYSA-N 0.000 claims description 2
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 claims description 2
- 239000001361 adipic acid Substances 0.000 claims description 2
- 229910000147 aluminium phosphate Inorganic materials 0.000 claims description 2
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 claims description 2
- 229940092714 benzenesulfonic acid Drugs 0.000 claims description 2
- 235000010233 benzoic acid Nutrition 0.000 claims description 2
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 claims description 2
- 229960001761 chlorpropamide Drugs 0.000 claims description 2
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 claims description 2
- 239000001530 fumaric acid Substances 0.000 claims description 2
- DSLZVSRJTYRBFB-DUHBMQHGSA-N galactaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)[C@@H](O)[C@H](O)C(O)=O DSLZVSRJTYRBFB-DUHBMQHGSA-N 0.000 claims description 2
- 229960001764 glibornuride Drugs 0.000 claims description 2
- RMTYNAPTNBJHQI-LLDVTBCESA-N glibornuride Chemical compound C1=CC(C)=CC=C1S(=O)(=O)NC(=O)N[C@H]1[C@H](C2(C)C)CC[C@@]2(C)[C@H]1O RMTYNAPTNBJHQI-LLDVTBCESA-N 0.000 claims description 2
- 229960003236 glisoxepide Drugs 0.000 claims description 2
- ZKUDBRCEOBOWLF-UHFFFAOYSA-N glisoxepide Chemical compound O1C(C)=CC(C(=O)NCCC=2C=CC(=CC=2)S(=O)(=O)NC(=O)NN2CCCCCC2)=N1 ZKUDBRCEOBOWLF-UHFFFAOYSA-N 0.000 claims description 2
- 239000000174 gluconic acid Substances 0.000 claims description 2
- 235000012208 gluconic acid Nutrition 0.000 claims description 2
- 239000004220 glutamic acid Substances 0.000 claims description 2
- 235000013922 glutamic acid Nutrition 0.000 claims description 2
- BEBCJVAWIBVWNZ-UHFFFAOYSA-N glycinamide Chemical compound NCC(N)=O BEBCJVAWIBVWNZ-UHFFFAOYSA-N 0.000 claims description 2
- 229960000443 hydrochloric acid Drugs 0.000 claims description 2
- 229940045996 isethionic acid Drugs 0.000 claims description 2
- 239000004310 lactic acid Substances 0.000 claims description 2
- 235000014655 lactic acid Nutrition 0.000 claims description 2
- 229960000448 lactic acid Drugs 0.000 claims description 2
- 229960002510 mandelic acid Drugs 0.000 claims description 2
- 229940098779 methanesulfonic acid Drugs 0.000 claims description 2
- 229910017604 nitric acid Inorganic materials 0.000 claims description 2
- WLJNZVDCPSBLRP-UHFFFAOYSA-N pamoic acid Chemical compound C1=CC=C2C(CC=3C4=CC=CC=C4C=C(C=3O)C(=O)O)=C(O)C(C(O)=O)=CC2=C1 WLJNZVDCPSBLRP-UHFFFAOYSA-N 0.000 claims description 2
- 239000011713 pantothenic acid Substances 0.000 claims description 2
- 229940055726 pantothenic acid Drugs 0.000 claims description 2
- 235000019161 pantothenic acid Nutrition 0.000 claims description 2
- MMUOIYIFYYHXAR-CXAGYDPISA-N (3r)-4-[(3r)-3-amino-4-(2,4,5-trifluorophenyl)butanoyl]-3-(diethylaminomethyl)piperazin-2-one Chemical compound C1CNC(=O)[C@@H](CN(CC)CC)N1C(=O)C[C@H](N)CC1=CC(F)=C(F)C=C1F MMUOIYIFYYHXAR-CXAGYDPISA-N 0.000 claims 1
- IDSXRFKNAHVHRL-CXAGYDPISA-N (3r)-4-[(3r)-3-amino-4-(2,4,5-trifluorophenyl)butanoyl]-3-(morpholin-4-ylmethyl)piperazin-2-one Chemical compound C([C@@H]1C(=O)NCCN1C(=O)C[C@H](N)CC=1C(=CC(F)=C(F)C=1)F)N1CCOCC1 IDSXRFKNAHVHRL-CXAGYDPISA-N 0.000 claims 1
- LLJFMFZYVVLQKT-UHFFFAOYSA-N 1-cyclohexyl-3-[4-[2-(7-methoxy-4,4-dimethyl-1,3-dioxo-2-isoquinolinyl)ethyl]phenyl]sulfonylurea Chemical compound C=1C(OC)=CC=C(C(C2=O)(C)C)C=1C(=O)N2CCC(C=C1)=CC=C1S(=O)(=O)NC(=O)NC1CCCCC1 LLJFMFZYVVLQKT-UHFFFAOYSA-N 0.000 claims 1
- 102000018208 Cannabinoid Receptor Human genes 0.000 claims 1
- 108050007331 Cannabinoid receptor Proteins 0.000 claims 1
- 229960003468 gliquidone Drugs 0.000 claims 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 abstract description 103
- 239000008103 glucose Substances 0.000 abstract description 102
- 210000004369 blood Anatomy 0.000 abstract description 63
- 239000008280 blood Substances 0.000 abstract description 63
- 230000000694 effects Effects 0.000 abstract description 41
- 230000002401 inhibitory effect Effects 0.000 abstract description 5
- 239000012453 solvate Substances 0.000 abstract description 5
- 102000016622 Dipeptidyl Peptidase 4 Human genes 0.000 abstract 2
- 238000002360 preparation method Methods 0.000 description 190
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 101
- 230000005764 inhibitory process Effects 0.000 description 53
- 239000003814 drug Substances 0.000 description 51
- 235000001727 glucose Nutrition 0.000 description 48
- 230000002195 synergetic effect Effects 0.000 description 47
- 229940079593 drug Drugs 0.000 description 45
- 238000002474 experimental method Methods 0.000 description 33
- 241000699670 Mus sp. Species 0.000 description 28
- 239000011541 reaction mixture Substances 0.000 description 24
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 21
- 229920000609 methyl cellulose Polymers 0.000 description 21
- 239000001923 methylcellulose Substances 0.000 description 21
- 235000010981 methylcellulose Nutrition 0.000 description 21
- 238000002156 mixing Methods 0.000 description 20
- 239000000243 solution Substances 0.000 description 20
- 230000002829 reductive effect Effects 0.000 description 19
- 239000000725 suspension Substances 0.000 description 19
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 16
- 230000006872 improvement Effects 0.000 description 16
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 15
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 15
- 238000000034 method Methods 0.000 description 15
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 14
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 14
- 238000005259 measurement Methods 0.000 description 14
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 12
- 229940095064 tartrate Drugs 0.000 description 12
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 12
- 238000006243 chemical reaction Methods 0.000 description 11
- 230000001976 improved effect Effects 0.000 description 11
- 239000012044 organic layer Substances 0.000 description 11
- DTHNMHAUYICORS-KTKZVXAJSA-N Glucagon-like peptide 1 Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1N=CNC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 DTHNMHAUYICORS-KTKZVXAJSA-N 0.000 description 10
- 241001465754 Metazoa Species 0.000 description 10
- 238000013116 obese mouse model Methods 0.000 description 10
- IWELDVXSEVIIGI-UHFFFAOYSA-N piperazin-2-one Chemical compound O=C1CNCCN1 IWELDVXSEVIIGI-UHFFFAOYSA-N 0.000 description 10
- 238000005160 1H NMR spectroscopy Methods 0.000 description 9
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 9
- 101710198884 GATA-type zinc finger protein 1 Proteins 0.000 description 9
- 102100040918 Pro-glucagon Human genes 0.000 description 9
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 9
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 8
- LCDDAGSJHKEABN-MLGOLLRUSA-N Evogliptin Chemical compound C1CNC(=O)[C@@H](COC(C)(C)C)N1C(=O)C[C@H](N)CC1=CC(F)=C(F)C=C1F LCDDAGSJHKEABN-MLGOLLRUSA-N 0.000 description 8
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 8
- 230000002411 adverse Effects 0.000 description 8
- 238000011161 development Methods 0.000 description 8
- YROXIXLRRCOBKF-UHFFFAOYSA-N sulfonylurea Chemical class OC(=N)N=S(=O)=O YROXIXLRRCOBKF-UHFFFAOYSA-N 0.000 description 8
- 102000004877 Insulin Human genes 0.000 description 7
- 108090001061 Insulin Proteins 0.000 description 7
- 229930006000 Sucrose Natural products 0.000 description 7
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 7
- 230000000996 additive effect Effects 0.000 description 7
- 230000008859 change Effects 0.000 description 7
- 229940125396 insulin Drugs 0.000 description 7
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 7
- 235000019341 magnesium sulphate Nutrition 0.000 description 7
- 238000011160 research Methods 0.000 description 7
- 239000005720 sucrose Substances 0.000 description 7
- SYOKIDBDQMKNDQ-XWTIBIIYSA-N vildagliptin Chemical compound C1C(O)(C2)CC(C3)CC1CC32NCC(=O)N1CCC[C@H]1C#N SYOKIDBDQMKNDQ-XWTIBIIYSA-N 0.000 description 7
- 229960001254 vildagliptin Drugs 0.000 description 7
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 6
- 229940100389 Sulfonylurea Drugs 0.000 description 6
- 235000005911 diet Nutrition 0.000 description 6
- 230000037213 diet Effects 0.000 description 6
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 6
- 238000001647 drug administration Methods 0.000 description 6
- 239000000463 material Substances 0.000 description 6
- MFFMDFFZMYYVKS-SECBINFHSA-N sitagliptin Chemical compound C([C@H](CC(=O)N1CC=2N(C(=NN=2)C(F)(F)F)CC1)N)C1=CC(F)=C(F)C=C1F MFFMDFFZMYYVKS-SECBINFHSA-N 0.000 description 6
- 238000003756 stirring Methods 0.000 description 6
- 229940124597 therapeutic agent Drugs 0.000 description 6
- 210000003462 vein Anatomy 0.000 description 6
- 102000004190 Enzymes Human genes 0.000 description 5
- 108090000790 Enzymes Proteins 0.000 description 5
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 5
- 230000009471 action Effects 0.000 description 5
- 238000007792 addition Methods 0.000 description 5
- 238000004440 column chromatography Methods 0.000 description 5
- 230000003247 decreasing effect Effects 0.000 description 5
- 238000002347 injection Methods 0.000 description 5
- 239000007924 injection Substances 0.000 description 5
- 238000007410 oral glucose tolerance test Methods 0.000 description 5
- 230000009467 reduction Effects 0.000 description 5
- 229960004034 sitagliptin Drugs 0.000 description 5
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide Chemical compound CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 4
- VZSRBBMJRBPUNF-UHFFFAOYSA-N 2-(2,3-dihydro-1H-inden-2-ylamino)-N-[3-oxo-3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propyl]pyrimidine-5-carboxamide Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C(=O)NCCC(N1CC2=C(CC1)NN=N2)=O VZSRBBMJRBPUNF-UHFFFAOYSA-N 0.000 description 4
- OKKJLVBELUTLKV-MZCSYVLQSA-N Deuterated methanol Chemical compound [2H]OC([2H])([2H])[2H] OKKJLVBELUTLKV-MZCSYVLQSA-N 0.000 description 4
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 239000000556 agonist Substances 0.000 description 4
- 239000003708 ampul Substances 0.000 description 4
- 230000037396 body weight Effects 0.000 description 4
- 239000012267 brine Substances 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- 235000011167 hydrochloric acid Nutrition 0.000 description 4
- 230000003914 insulin secretion Effects 0.000 description 4
- 210000004185 liver Anatomy 0.000 description 4
- 230000007246 mechanism Effects 0.000 description 4
- 239000012528 membrane Substances 0.000 description 4
- 231100000252 nontoxic Toxicity 0.000 description 4
- 230000003000 nontoxic effect Effects 0.000 description 4
- BNYHRGTXRPWASY-UHFFFAOYSA-N nonylsulfonylurea Chemical compound CCCCCCCCCS(=O)(=O)NC(N)=O BNYHRGTXRPWASY-UHFFFAOYSA-N 0.000 description 4
- 210000000496 pancreas Anatomy 0.000 description 4
- 210000000813 small intestine Anatomy 0.000 description 4
- 235000017557 sodium bicarbonate Nutrition 0.000 description 4
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 4
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 4
- 239000002904 solvent Substances 0.000 description 4
- 208000024891 symptom Diseases 0.000 description 4
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 4
- CONKBQPVFMXDOV-QHCPKHFHSA-N 6-[(5S)-5-[[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]methyl]-2-oxo-1,3-oxazolidin-3-yl]-3H-1,3-benzoxazol-2-one Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)C[C@H]1CN(C(O1)=O)C1=CC2=C(NC(O2)=O)C=C1 CONKBQPVFMXDOV-QHCPKHFHSA-N 0.000 description 3
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 3
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 3
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 3
- 241000699666 Mus <mouse, genus> Species 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- 229940126033 PPAR agonist Drugs 0.000 description 3
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 229920002472 Starch Polymers 0.000 description 3
- 229940123464 Thiazolidinedione Drugs 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 238000010521 absorption reaction Methods 0.000 description 3
- 229940024606 amino acid Drugs 0.000 description 3
- 239000011230 binding agent Substances 0.000 description 3
- 210000004027 cell Anatomy 0.000 description 3
- 201000010099 disease Diseases 0.000 description 3
- 208000035475 disorder Diseases 0.000 description 3
- 239000002552 dosage form Substances 0.000 description 3
- 238000011156 evaluation Methods 0.000 description 3
- 239000004615 ingredient Substances 0.000 description 3
- 239000010410 layer Substances 0.000 description 3
- 239000011777 magnesium Substances 0.000 description 3
- 229910052749 magnesium Inorganic materials 0.000 description 3
- 230000010534 mechanism of action Effects 0.000 description 3
- 239000002307 peroxisome proliferator activated receptor agonist Substances 0.000 description 3
- 239000006187 pill Substances 0.000 description 3
- 230000000291 postprandial effect Effects 0.000 description 3
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 3
- 108090000765 processed proteins & peptides Proteins 0.000 description 3
- 235000018102 proteins Nutrition 0.000 description 3
- 108090000623 proteins and genes Proteins 0.000 description 3
- 102000004169 proteins and genes Human genes 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- 102000005962 receptors Human genes 0.000 description 3
- 108020003175 receptors Proteins 0.000 description 3
- 238000010992 reflux Methods 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 241000894007 species Species 0.000 description 3
- 239000003381 stabilizer Substances 0.000 description 3
- 235000019698 starch Nutrition 0.000 description 3
- 239000008107 starch Substances 0.000 description 3
- 238000012360 testing method Methods 0.000 description 3
- 210000001519 tissue Anatomy 0.000 description 3
- 230000004584 weight gain Effects 0.000 description 3
- 235000019786 weight gain Nutrition 0.000 description 3
- HMUNWXXNJPVALC-UHFFFAOYSA-N 1-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]-2-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)C(CN1CC2=C(CC1)NN=N2)=O HMUNWXXNJPVALC-UHFFFAOYSA-N 0.000 description 2
- GTZJUBQWCWZING-VUUHIHSGSA-N 1-o-benzyl 2-o-methyl (2r)-aziridine-1,2-dicarboxylate Chemical compound COC(=O)[C@H]1CN1C(=O)OCC1=CC=CC=C1 GTZJUBQWCWZING-VUUHIHSGSA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- WZFUQSJFWNHZHM-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)CC(=O)N1CC2=C(CC1)NN=N2 WZFUQSJFWNHZHM-UHFFFAOYSA-N 0.000 description 2
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 2
- 210000002237 B-cell of pancreatic islet Anatomy 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- 108010016626 Dipeptides Proteins 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 101000908391 Homo sapiens Dipeptidyl peptidase 4 Proteins 0.000 description 2
- 241000725303 Human immunodeficiency virus Species 0.000 description 2
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 2
- 206010022489 Insulin Resistance Diseases 0.000 description 2
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 2
- 150000001200 N-acyl ethanolamides Chemical class 0.000 description 2
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 2
- 102000003728 Peroxisome Proliferator-Activated Receptors Human genes 0.000 description 2
- 108090000029 Peroxisome Proliferator-Activated Receptors Proteins 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 2
- 241000700159 Rattus Species 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- 210000001744 T-lymphocyte Anatomy 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 235000001014 amino acid Nutrition 0.000 description 2
- 150000001413 amino acids Chemical class 0.000 description 2
- INJTVQFGKWBLEN-CQSZACIVSA-N benzyl (2r)-2-[(2-methylpropan-2-yl)oxymethyl]-3-oxopiperazine-1-carboxylate Chemical compound C1CNC(=O)[C@@H](COC(C)(C)C)N1C(=O)OCC1=CC=CC=C1 INJTVQFGKWBLEN-CQSZACIVSA-N 0.000 description 2
- HSDAJNMJOMSNEV-UHFFFAOYSA-N benzyl chloroformate Chemical compound ClC(=O)OCC1=CC=CC=C1 HSDAJNMJOMSNEV-UHFFFAOYSA-N 0.000 description 2
- 125000001584 benzyloxycarbonyl group Chemical group C(=O)(OCC1=CC=CC=C1)* 0.000 description 2
- 150000001576 beta-amino acids Chemical class 0.000 description 2
- 230000005587 bubbling Effects 0.000 description 2
- RYYVLZVUVIJVGH-UHFFFAOYSA-N caffeine Chemical compound CN1C(=O)N(C)C(=O)C2=C1N=CN2C RYYVLZVUVIJVGH-UHFFFAOYSA-N 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 239000007963 capsule composition Substances 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 239000007884 disintegrant Substances 0.000 description 2
- 239000003995 emulsifying agent Substances 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 239000002621 endocannabinoid Substances 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- YMTINGFKWWXKFG-UHFFFAOYSA-N fenofibrate Chemical compound C1=CC(OC(C)(C)C(=O)OC(C)C)=CC=C1C(=O)C1=CC=C(Cl)C=C1 YMTINGFKWWXKFG-UHFFFAOYSA-N 0.000 description 2
- 229960002297 fenofibrate Drugs 0.000 description 2
- 235000012631 food intake Nutrition 0.000 description 2
- 239000004459 forage Substances 0.000 description 2
- 230000004153 glucose metabolism Effects 0.000 description 2
- KWIUHFFTVRNATP-UHFFFAOYSA-N glycine betaine Chemical compound C[N+](C)(C)CC([O-])=O KWIUHFFTVRNATP-UHFFFAOYSA-N 0.000 description 2
- 239000003316 glycosidase inhibitor Substances 0.000 description 2
- 229910052739 hydrogen Inorganic materials 0.000 description 2
- 239000001257 hydrogen Substances 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 150000007529 inorganic bases Chemical class 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- 230000037356 lipid metabolism Effects 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- QGSITPKXYQEFIR-CILPGNKCSA-N methyl (2r)-1-tritylaziridine-2-carboxylate Chemical compound COC(=O)[C@H]1CN1C(C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 QGSITPKXYQEFIR-CILPGNKCSA-N 0.000 description 2
- IOSDXAFCRZNJCL-LLVKDONJSA-N methyl (2r)-3-[(2-methylpropan-2-yl)oxy]-2-[2-[(2-methylpropan-2-yl)oxycarbonylamino]ethylamino]propanoate Chemical compound CC(C)(C)OC[C@H](C(=O)OC)NCCNC(=O)OC(C)(C)C IOSDXAFCRZNJCL-LLVKDONJSA-N 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 150000007530 organic bases Chemical class 0.000 description 2
- 238000007911 parenteral administration Methods 0.000 description 2
- 230000002093 peripheral effect Effects 0.000 description 2
- 230000003285 pharmacodynamic effect Effects 0.000 description 2
- UYWQUFXKFGHYNT-UHFFFAOYSA-N phenylmethyl ester of formic acid Natural products O=COCC1=CC=CC=C1 UYWQUFXKFGHYNT-UHFFFAOYSA-N 0.000 description 2
- 235000011007 phosphoric acid Nutrition 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 239000011591 potassium Substances 0.000 description 2
- 229910052700 potassium Inorganic materials 0.000 description 2
- 230000003389 potentiating effect Effects 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 238000012827 research and development Methods 0.000 description 2
- 230000000580 secretagogue effect Effects 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 159000000000 sodium salts Chemical class 0.000 description 2
- 239000007858 starting material Substances 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 230000001629 suppression Effects 0.000 description 2
- 239000000375 suspending agent Substances 0.000 description 2
- 239000007916 tablet composition Substances 0.000 description 2
- YAPQBXQYLJRXSA-UHFFFAOYSA-N theobromine Chemical compound CN1C(=O)NC(=O)C2=C1N=CN2C YAPQBXQYLJRXSA-UHFFFAOYSA-N 0.000 description 2
- UFTFJSFQGQCHQW-UHFFFAOYSA-N triformin Chemical compound O=COCC(OC=O)COC=O UFTFJSFQGQCHQW-UHFFFAOYSA-N 0.000 description 2
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 2
- 239000000080 wetting agent Substances 0.000 description 2
- VGKWGAIVTGJOKZ-HSHFZTNMSA-N (2R)-2-amino-3-hydroxypropanoic acid chloromethane Chemical compound CCl.N[C@H](CO)C(=O)O VGKWGAIVTGJOKZ-HSHFZTNMSA-N 0.000 description 1
- LCDDAGSJHKEABN-WBMJQRKESA-N (3s)-4-[(3r)-3-amino-4-(2,4,5-trifluorophenyl)butanoyl]-3-[(2-methylpropan-2-yl)oxymethyl]piperazin-2-one Chemical compound C1CNC(=O)[C@H](COC(C)(C)C)N1C(=O)C[C@H](N)CC1=CC(F)=C(F)C=C1F LCDDAGSJHKEABN-WBMJQRKESA-N 0.000 description 1
- NGJOFQZEYQGZMB-KTKZVXAJSA-N (4S)-5-[[2-[[(2S,3R)-1-[[(2S)-1-[[(2S,3R)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[2-[[(2S)-5-amino-1-[[(2S)-1-[[(2S)-1-[[(2S)-6-amino-1-[[(2S)-1-[[(2S)-1-[[(2S,3S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-6-amino-1-[[2-[[(1S)-4-carbamimidamido-1-carboxybutyl]amino]-2-oxoethyl]amino]-1-oxohexan-2-yl]amino]-3-methyl-1-oxobutan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-3-(1H-indol-3-yl)-1-oxopropan-2-yl]amino]-1-oxopropan-2-yl]amino]-3-methyl-1-oxopentan-2-yl]amino]-1-oxo-3-phenylpropan-2-yl]amino]-4-carboxy-1-oxobutan-2-yl]amino]-1-oxohexan-2-yl]amino]-1-oxopropan-2-yl]amino]-1-oxopropan-2-yl]amino]-1,5-dioxopentan-2-yl]amino]-2-oxoethyl]amino]-4-carboxy-1-oxobutan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-3-(4-hydroxyphenyl)-1-oxopropan-2-yl]amino]-3-hydroxy-1-oxopropan-2-yl]amino]-3-hydroxy-1-oxopropan-2-yl]amino]-3-methyl-1-oxobutan-2-yl]amino]-3-carboxy-1-oxopropan-2-yl]amino]-3-hydroxy-1-oxopropan-2-yl]amino]-3-hydroxy-1-oxobutan-2-yl]amino]-1-oxo-3-phenylpropan-2-yl]amino]-3-hydroxy-1-oxobutan-2-yl]amino]-2-oxoethyl]amino]-4-[[(2S)-2-[[(2S)-2-amino-3-(1H-imidazol-4-yl)propanoyl]amino]propanoyl]amino]-5-oxopentanoic acid Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 NGJOFQZEYQGZMB-KTKZVXAJSA-N 0.000 description 1
- NWUYHJFMYQTDRP-UHFFFAOYSA-N 1,2-bis(ethenyl)benzene;1-ethenyl-2-ethylbenzene;styrene Chemical compound C=CC1=CC=CC=C1.CCC1=CC=CC=C1C=C.C=CC1=CC=CC=C1C=C NWUYHJFMYQTDRP-UHFFFAOYSA-N 0.000 description 1
- OHVLMTFVQDZYHP-UHFFFAOYSA-N 1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)-2-[4-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidin-5-yl]piperazin-1-yl]ethanone Chemical compound N1N=NC=2CN(CCC=21)C(CN1CCN(CC1)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)=O OHVLMTFVQDZYHP-UHFFFAOYSA-N 0.000 description 1
- ASOKPJOREAFHNY-UHFFFAOYSA-N 1-Hydroxybenzotriazole Chemical compound C1=CC=C2N(O)N=NC2=C1 ASOKPJOREAFHNY-UHFFFAOYSA-N 0.000 description 1
- GAVMRTMJEVMRGR-UHFFFAOYSA-N 2,3,5,6-tetrahydro-1h-triazolo[4,5-b]pyrazine Chemical compound N1CCNC2=C1N=NN2 GAVMRTMJEVMRGR-UHFFFAOYSA-N 0.000 description 1
- LDXJRKWFNNFDSA-UHFFFAOYSA-N 2-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)-1-[4-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidin-5-yl]piperazin-1-yl]ethanone Chemical compound C1CN(CC2=NNN=C21)CC(=O)N3CCN(CC3)C4=CN=C(N=C4)NCC5=CC(=CC=C5)OC(F)(F)F LDXJRKWFNNFDSA-UHFFFAOYSA-N 0.000 description 1
- JQMFQLVAJGZSQS-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]-N-(2-oxo-3H-1,3-benzoxazol-6-yl)acetamide Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)CC(=O)NC1=CC2=C(NC(O2)=O)C=C1 JQMFQLVAJGZSQS-UHFFFAOYSA-N 0.000 description 1
- MSWZFWKMSRAUBD-IVMDWMLBSA-N 2-amino-2-deoxy-D-glucopyranose Chemical compound N[C@H]1C(O)O[C@H](CO)[C@@H](O)[C@@H]1O MSWZFWKMSRAUBD-IVMDWMLBSA-N 0.000 description 1
- IHBAVXVTGLANPI-QMMMGPOBSA-N 2-amino-3-methyl-1-pyrrolidin-1-yl-butan-1-one Chemical compound CC(C)[C@H](N)C(=O)N1CCCC1 IHBAVXVTGLANPI-QMMMGPOBSA-N 0.000 description 1
- BFSVOASYOCHEOV-UHFFFAOYSA-N 2-diethylaminoethanol Chemical compound CCN(CC)CCO BFSVOASYOCHEOV-UHFFFAOYSA-N 0.000 description 1
- 229940013085 2-diethylaminoethanol Drugs 0.000 description 1
- YLZOPXRUQYQQID-UHFFFAOYSA-N 3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)-1-[4-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidin-5-yl]piperazin-1-yl]propan-1-one Chemical compound N1N=NC=2CN(CCC=21)CCC(=O)N1CCN(CC1)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F YLZOPXRUQYQQID-UHFFFAOYSA-N 0.000 description 1
- HVCNXQOWACZAFN-UHFFFAOYSA-N 4-ethylmorpholine Chemical compound CCN1CCOCC1 HVCNXQOWACZAFN-UHFFFAOYSA-N 0.000 description 1
- 208000030507 AIDS Diseases 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical class [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 1
- 241000024188 Andala Species 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- KZMGYPLQYOPHEL-UHFFFAOYSA-N Boron trifluoride etherate Chemical compound FB(F)F.CCOCC KZMGYPLQYOPHEL-UHFFFAOYSA-N 0.000 description 1
- 102000009132 CB1 Cannabinoid Receptor Human genes 0.000 description 1
- 108010073366 CB1 Cannabinoid Receptor Proteins 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 208000017667 Chronic Disease Diseases 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- 229930195711 D-Serine Natural products 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 206010012735 Diarrhoea Diseases 0.000 description 1
- 108010067722 Dipeptidyl Peptidase 4 Proteins 0.000 description 1
- 208000032928 Dyslipidaemia Diseases 0.000 description 1
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- CWYNVVGOOAEACU-UHFFFAOYSA-N Fe2+ Chemical compound [Fe+2] CWYNVVGOOAEACU-UHFFFAOYSA-N 0.000 description 1
- 239000004606 Fillers/Extenders Substances 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 102000051325 Glucagon Human genes 0.000 description 1
- 108060003199 Glucagon Proteins 0.000 description 1
- 101800004295 Glucagon-like peptide 1(7-36) Proteins 0.000 description 1
- 102000004366 Glucosidases Human genes 0.000 description 1
- 108010056771 Glucosidases Proteins 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 229940122069 Glycosidase inhibitor Drugs 0.000 description 1
- 102000001554 Hemoglobins Human genes 0.000 description 1
- 108010054147 Hemoglobins Proteins 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 206010021518 Impaired gastric emptying Diseases 0.000 description 1
- LPHGQDQBBGAPDZ-UHFFFAOYSA-N Isocaffeine Natural products CN1C(=O)N(C)C(=O)C2=C1N(C)C=N2 LPHGQDQBBGAPDZ-UHFFFAOYSA-N 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 1
- 238000008214 LDL Cholesterol Methods 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 208000017170 Lipid metabolism disease Diseases 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 239000012359 Methanesulfonyl chloride Substances 0.000 description 1
- MKYBYDHXWVHEJW-UHFFFAOYSA-N N-[1-oxo-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propan-2-yl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C(C(C)NC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 MKYBYDHXWVHEJW-UHFFFAOYSA-N 0.000 description 1
- NIPNSKYNPDTRPC-UHFFFAOYSA-N N-[2-oxo-2-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethyl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C(CNC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 NIPNSKYNPDTRPC-UHFFFAOYSA-N 0.000 description 1
- AFCARXCZXQIEQB-UHFFFAOYSA-N N-[3-oxo-3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propyl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C(CCNC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 AFCARXCZXQIEQB-UHFFFAOYSA-N 0.000 description 1
- UEEJHVSXFDXPFK-UHFFFAOYSA-N N-dimethylaminoethanol Chemical compound CN(C)CCO UEEJHVSXFDXPFK-UHFFFAOYSA-N 0.000 description 1
- HTLZVHNRZJPSMI-UHFFFAOYSA-N N-ethylpiperidine Chemical compound CCN1CCCCC1 HTLZVHNRZJPSMI-UHFFFAOYSA-N 0.000 description 1
- MBBZMMPHUWSWHV-BDVNFPICSA-N N-methylglucamine Chemical compound CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO MBBZMMPHUWSWHV-BDVNFPICSA-N 0.000 description 1
- 206010028813 Nausea Diseases 0.000 description 1
- 206010030113 Oedema Diseases 0.000 description 1
- 206010033307 Overweight Diseases 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- 101000886298 Pseudoxanthomonas mexicana Dipeptidyl aminopeptidase 4 Proteins 0.000 description 1
- 102000012479 Serine Proteases Human genes 0.000 description 1
- 108010022999 Serine Proteases Proteins 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- 206010047700 Vomiting Diseases 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- 239000002250 absorbent Substances 0.000 description 1
- 230000002745 absorbent Effects 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 150000001279 adipic acids Chemical class 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 235000010419 agar Nutrition 0.000 description 1
- 235000004279 alanine Nutrition 0.000 description 1
- 125000003295 alanine group Chemical group N[C@@H](C)C(=O)* 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- ZSBOMTDTBDDKMP-OAHLLOKOSA-N alogliptin Chemical compound C=1C=CC=C(C#N)C=1CN1C(=O)N(C)C(=O)C=C1N1CCC[C@@H](N)C1 ZSBOMTDTBDDKMP-OAHLLOKOSA-N 0.000 description 1
- 229960001667 alogliptin Drugs 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- SNAAJJQQZSMGQD-UHFFFAOYSA-N aluminum magnesium Chemical compound [Mg].[Al] SNAAJJQQZSMGQD-UHFFFAOYSA-N 0.000 description 1
- 230000006538 anaerobic glycolysis Effects 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 238000013103 analytical ultracentrifugation Methods 0.000 description 1
- 230000003579 anti-obesity Effects 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000003125 aqueous solvent Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 229960003121 arginine Drugs 0.000 description 1
- 210000000227 basophil cell of anterior lobe of hypophysis Anatomy 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- JUHORIMYRDESRB-UHFFFAOYSA-N benzathine Chemical compound C=1C=CC=CC=1CNCCNCC1=CC=CC=C1 JUHORIMYRDESRB-UHFFFAOYSA-N 0.000 description 1
- MSWZFWKMSRAUBD-UHFFFAOYSA-N beta-D-galactosamine Natural products NC1C(O)OC(CO)C(O)C1O MSWZFWKMSRAUBD-UHFFFAOYSA-N 0.000 description 1
- 229960003237 betaine Drugs 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- FNEXNZUHBCBQTI-UHFFFAOYSA-N butyl 2-(2,4,5-trichlorophenoxy)acetate Chemical group CCCCOC(=O)COC1=CC(Cl)=C(Cl)C=C1Cl FNEXNZUHBCBQTI-UHFFFAOYSA-N 0.000 description 1
- 229960001948 caffeine Drugs 0.000 description 1
- VJEONQKOZGKCAK-UHFFFAOYSA-N caffeine Natural products CN1C(=O)N(C)C(=O)C2=C1C=CN2C VJEONQKOZGKCAK-UHFFFAOYSA-N 0.000 description 1
- FUFJGUQYACFECW-UHFFFAOYSA-L calcium hydrogenphosphate Chemical compound [Ca+2].OP([O-])([O-])=O FUFJGUQYACFECW-UHFFFAOYSA-L 0.000 description 1
- 159000000007 calcium salts Chemical class 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 229930003827 cannabinoid Natural products 0.000 description 1
- 239000003557 cannabinoid Substances 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 description 1
- 229960001231 choline Drugs 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 230000002860 competitive effect Effects 0.000 description 1
- 239000011365 complex material Substances 0.000 description 1
- 230000000536 complexating effect Effects 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 125000000753 cycloalkyl group Chemical group 0.000 description 1
- XCIXKGXIYUWCLL-UHFFFAOYSA-N cyclopentanol Chemical compound OC1CCCC1 XCIXKGXIYUWCLL-UHFFFAOYSA-N 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 238000010511 deprotection reaction Methods 0.000 description 1
- 238000001212 derivatisation Methods 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 235000019700 dicalcium phosphate Nutrition 0.000 description 1
- 230000029087 digestion Effects 0.000 description 1
- 102000038379 digestive enzymes Human genes 0.000 description 1
- 108091007734 digestive enzymes Proteins 0.000 description 1
- 238000007907 direct compression Methods 0.000 description 1
- 150000002016 disaccharides Chemical class 0.000 description 1
- 229940000406 drug candidate Drugs 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 230000004064 dysfunction Effects 0.000 description 1
- 210000003158 enteroendocrine cell Anatomy 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 201000010063 epididymitis Diseases 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 1
- 229940093471 ethyl oleate Drugs 0.000 description 1
- LIWAQLJGPBVORC-UHFFFAOYSA-N ethylmethylamine Chemical compound CCNC LIWAQLJGPBVORC-UHFFFAOYSA-N 0.000 description 1
- 239000003777 experimental drug Substances 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 230000037406 food intake Effects 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 235000019525 fullness Nutrition 0.000 description 1
- 235000011087 fumaric acid Nutrition 0.000 description 1
- 210000005095 gastrointestinal system Anatomy 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000007903 gelatin capsule Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- MASNOZXLGMXCHN-ZLPAWPGGSA-N glucagon Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(O)=O)C(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C1=CC=CC=C1 MASNOZXLGMXCHN-ZLPAWPGGSA-N 0.000 description 1
- 229960004666 glucagon Drugs 0.000 description 1
- 230000004110 gluconeogenesis Effects 0.000 description 1
- 229960002442 glucosamine Drugs 0.000 description 1
- 230000009229 glucose formation Effects 0.000 description 1
- 150000002304 glucoses Chemical class 0.000 description 1
- 229930182470 glycoside Natural products 0.000 description 1
- 150000002338 glycosides Chemical class 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 239000007902 hard capsule Substances 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 150000002391 heterocyclic compounds Chemical class 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- XGIHQYAWBCFNPY-AZOCGYLKSA-N hydrabamine Chemical compound C([C@@H]12)CC3=CC(C(C)C)=CC=C3[C@@]2(C)CCC[C@@]1(C)CNCCNC[C@@]1(C)[C@@H]2CCC3=CC(C(C)C)=CC=C3[C@@]2(C)CCC1 XGIHQYAWBCFNPY-AZOCGYLKSA-N 0.000 description 1
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 1
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 1
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 1
- 229940126904 hypoglycaemic agent Drugs 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 239000007972 injectable composition Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- 210000001596 intra-abdominal fat Anatomy 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 239000003456 ion exchange resin Substances 0.000 description 1
- 229920003303 ion-exchange polymer Polymers 0.000 description 1
- JJWLVOIRVHMVIS-UHFFFAOYSA-N isopropylamine Chemical compound CC(C)N JJWLVOIRVHMVIS-UHFFFAOYSA-N 0.000 description 1
- 239000007951 isotonicity adjuster Substances 0.000 description 1
- 229940090473 januvia Drugs 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 208000006443 lactic acidosis Diseases 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 238000012417 linear regression Methods 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 229940098895 maleic acid Drugs 0.000 description 1
- LBSANEJBGMCTBH-UHFFFAOYSA-N manganate Chemical compound [O-][Mn]([O-])(=O)=O LBSANEJBGMCTBH-UHFFFAOYSA-N 0.000 description 1
- WPBNNNQJVZRUHP-UHFFFAOYSA-L manganese(2+);methyl n-[[2-(methoxycarbonylcarbamothioylamino)phenyl]carbamothioyl]carbamate;n-[2-(sulfidocarbothioylamino)ethyl]carbamodithioate Chemical compound [Mn+2].[S-]C(=S)NCCNC([S-])=S.COC(=O)NC(=S)NC1=CC=CC=C1NC(=S)NC(=O)OC WPBNNNQJVZRUHP-UHFFFAOYSA-L 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 235000012054 meals Nutrition 0.000 description 1
- 238000002483 medication Methods 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- QARBMVPHQWIHKH-UHFFFAOYSA-N methanesulfonyl chloride Chemical compound CS(Cl)(=O)=O QARBMVPHQWIHKH-UHFFFAOYSA-N 0.000 description 1
- NDBQJIBNNUJNHA-AENDTGMFSA-N methyl (2r)-2-amino-3-hydroxypropanoate;hydrochloride Chemical compound Cl.COC(=O)[C@H](N)CO NDBQJIBNNUJNHA-AENDTGMFSA-N 0.000 description 1
- NDBQJIBNNUJNHA-DFWYDOINSA-N methyl (2s)-2-amino-3-hydroxypropanoate;hydrochloride Chemical compound Cl.COC(=O)[C@@H](N)CO NDBQJIBNNUJNHA-DFWYDOINSA-N 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 239000011259 mixed solution Substances 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- LSCYTCMNCWMCQE-UHFFFAOYSA-N n-methylpyridin-4-amine Chemical compound CNC1=CC=NC=C1 LSCYTCMNCWMCQE-UHFFFAOYSA-N 0.000 description 1
- 230000008693 nausea Effects 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 239000002547 new drug Substances 0.000 description 1
- 239000012457 nonaqueous media Substances 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 230000003204 osmotic effect Effects 0.000 description 1
- 239000006072 paste Substances 0.000 description 1
- 239000000813 peptide hormone Substances 0.000 description 1
- 230000003132 peptidolytic effect Effects 0.000 description 1
- 210000001428 peripheral nervous system Anatomy 0.000 description 1
- 210000002824 peroxisome Anatomy 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 150000004885 piperazines Chemical class 0.000 description 1
- 229920000768 polyamine Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- MFDFERRIHVXMIY-UHFFFAOYSA-N procaine Chemical compound CCN(CC)CCOC(=O)C1=CC=C(N)C=C1 MFDFERRIHVXMIY-UHFFFAOYSA-N 0.000 description 1
- 229960004919 procaine Drugs 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 230000003979 response to food Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 230000036186 satiety Effects 0.000 description 1
- 235000019627 satiety Nutrition 0.000 description 1
- 150000003335 secondary amines Chemical class 0.000 description 1
- 230000001235 sensitizing effect Effects 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 210000002027 skeletal muscle Anatomy 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- 239000012321 sodium triacetoxyborohydride Substances 0.000 description 1
- 239000007901 soft capsule Substances 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 230000000707 stereoselective effect Effects 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 235000011044 succinic acid Nutrition 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 229940066771 systemic antihistamines piperazine derivative Drugs 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- WMXCDAVJEZZYLT-UHFFFAOYSA-N tert-butylthiol Chemical compound CC(C)(C)S WMXCDAVJEZZYLT-UHFFFAOYSA-N 0.000 description 1
- 150000003512 tertiary amines Chemical class 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- RWRDLPDLKQPQOW-UHFFFAOYSA-N tetrahydropyrrole Substances C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 1
- 229960004559 theobromine Drugs 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 239000000196 tragacanth Substances 0.000 description 1
- 235000010487 tragacanth Nutrition 0.000 description 1
- 229940116362 tragacanth Drugs 0.000 description 1
- JLTRXTDYQLMHGR-UHFFFAOYSA-N trimethylaluminium Chemical compound C[Al](C)C JLTRXTDYQLMHGR-UHFFFAOYSA-N 0.000 description 1
- JBWKIWSBJXDJDT-UHFFFAOYSA-N triphenylmethyl chloride Chemical compound C=1C=CC=CC=1C(C=1C=CC=CC=1)(Cl)C1=CC=CC=C1 JBWKIWSBJXDJDT-UHFFFAOYSA-N 0.000 description 1
- YFTHZRPMJXBUME-UHFFFAOYSA-N tripropylamine Chemical compound CCCN(CCC)CCC YFTHZRPMJXBUME-UHFFFAOYSA-N 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 229960000281 trometamol Drugs 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 208000002670 vitamin B12 deficiency Diseases 0.000 description 1
- 230000008673 vomiting Effects 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 238000005303 weighing Methods 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4965—Non-condensed pyrazines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/02—Halogenated hydrocarbons
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/155—Amidines (), e.g. guanidine (H2N—C(=NH)—NH2), isourea (N=C(OH)—NH2), isothiourea (—N=C(SH)—NH2)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/4439—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. omeprazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/64—Sulfonylureas, e.g. glibenclamide, tolbutamide, chlorpropamide
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7028—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/02—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/141—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers
- A61K9/145—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers with organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2059—Starch, including chemically or physically modified derivatives; Amylose; Amylopectin; Dextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/582—Recycling of unreacted starting or intermediate materials
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Diabetes (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Obesity (AREA)
- Hematology (AREA)
- Molecular Biology (AREA)
- Dermatology (AREA)
- Inorganic Chemistry (AREA)
- Endocrinology (AREA)
- Emergency Medicine (AREA)
- Child & Adolescent Psychology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
composição farmacêutica para prevenção e tratamento de diabetes ou obesidade compreendendo um composto que inibe a atividade de dipeptidil peptidase-iv, e outros agentes antidiabéticos ou antiobesidade como ingredientes ativos. a presente invenção refere-se a uma composição farmacêutica para a prevenção e tratamento de diabetes ou obesidade compreendendo como ingredientes ativos um composto que inibe a atividade de dipeptidil peptidase-iv(dpp-iv), um sal farmaceuticamente aceitável do mesmo, um hidrato do mesmo, ou um solvato do mesmo, e um ou mais outros agentes antidiabéticos ou antiobesidade. a composição farmacêutica exibe excelente tolerância à glicose e pode ser útil na prevenção e tratamento de diabetes, obesidade, e similares por eficazmente inibir os níveis de glicose sanguínea e reduzir a massa de gordura.
Description
[001] A presente invenção refere-se a uma composição farmacêutica para a prevenção e tratamento de diabetes ou obesidade compreendendo como ingredientes ativos um composto que inibe a atividade de dipeptidil peptidase-IV (DPP-IV), um sal farmaceuticamente aceitável do mesmo, um hidrato do mesmo, ou um solvato do mesmo, e um ou mais outros agentes antidiabéticos ou antiobesidade.
[002] DipeptidiL peptidase-IV (Posteriormente, referida como DPP-IV) é uma enzima que é geralmente identificada como EC 3.4.14.5 por classificação de enzima, funcionalmente pertence à serina protease (Barrett A. J. et al, Arch. Biochem. Biophys., 1995, 247-250), e diva o dipeptideo de terminal N de peptídeos que começam com a sequência H-Xaa-Pro-Y (ou H-Xaa-Ala-Y em que Xaa representa qualquer aminoácido lipofilico, Pro representa prolina, e Ala representa alanina) (Heins J., et al., Biochim. et Biophys. Acta 1988, 161), e é também conhecida como DP-IV, DP-4, ou DAP-IV. A enzima é amplamente distribuída e encontrada em uma variedade de tecidos mamíferos tais como rim, fígado e intestino delgado (Hegen M. et al., J. Immunol., 1990, 2908-2914). DPP-IV foi primeiro identificada como uma proteína ligada à membrana. Mais recentemente, uma forma solúvel da mesma foi identificada (Duke-Cohan J. S. et al., J. Biol. Chem., 1995, 14107-14114). De acordo com os estudos e relatórios que foram recentemente publicados, foi revelado que uma tal forma solúvel de DPP-IV tem a mesma estrutura e função como uma forma ligada à membrana da enzima e é encontrada sem um certo domínio ligado à membrana no sangue (Christine D. et. al, Eur. J. Biochem.,2000, 5608-5613).
[003] Interesse inicial em DPP-IV tem focalizado sobre seu papel na ativação de linfócitos T. DPP-IV responsável pela ativação de linfó- citos T foi especificamente designada como CD26. Com o relatório mostrando que CD26 liga-se a ou interage com o vírus da imunodeficiência humana (HIV) (Guteil W. G. et al, Proc. Natl. Acad. Sei., 1994, 6594-6598), foi proposto que inibidores de DPP-IV podem ser úteis no tratamento de AIDS (Doreen M. A. et al., Bioorg. Med. Chem. Lett., 1996, 2745-2748).
[004] Além de um papel crucial participando no sistema imune, a função principal de DPP-IV origina-se de sua atividade peptidolítica como descrito acima. Atenção foi particularmente dada ao papel de DPP-IV quando é descoberto que a DPP-IV é uma enzima chave implicada na degradação de proteína 1 semelhante a glucagon (posteriormente, referida como "GLP-1") no intestino delgado (Mentlein R. et al., Eur. J. Biochem., 1993, 829-835). GLP-1 é um hormônio de peptídeo de 30 aminoácidos que é secretado por células L intestinais como uma resposta à ingestão de alimento do intestino delgado (Goke R. et. al, J. Biol. Chem., 1993, 19650-19655). Uma vez que este hormônio é conhecido ter efeitos potencializadores sobre a ação de insulina no controle de níveis de glicose sanguínea pós-prandiais (Hoist J. J. et al., Diabetes Care, 1996, 580-586), foi postulado que inibidores de DPP-IV podem também ser vantajosamente empregados no tratamento de diabetes tipo 2. Com base nesta suposição, uma forma precoce do inibidor de DPP-IV foi desenvolvida com alguns relatórios demonstrando a eficácia terapêutica de um medicamento em experimentos animais (Pauly R. P. et al., Metabolism, 1999, 385-389). Além disso, camundongos ou ratos deficientes de DPP-IV manteram a atividade de GLP- 1 e níveis de insulina elevados, resultando em níveis de glicose sanguínea diminuídos e uma tal mutação ou interrupção genética do gene de DPP-IV não exibiu nenhum efeito significante sobre a sobrevivência de animais individuais (Marguet D. et al., Proc. Natl. Acad. Sei., 2000, 6874-6879). Como uma consequência, foi proposto que DPP-IV é exequível como um agente terapêutico potente para o tratamento de diabetes tipo 2, o que resultou em pesquisa acelerada e desenvolvimento do inibidor de DPP-IV.
[005] Ligação de GLP-1 com um receptor em uma variedade de tecidos resulta em saciedade (sensação de plenitude), esvaziamento gástrico retardado, e desenvolvimento facilitado de células beta pan- creáticas. Portanto, experiências clínicas para o tratamento da diabetes tipo 2 como descrito acima estão gradualmente crescendo através da administração intravenosa de GLP-1 por si só (Verdich C. et al, J. Clin. Endocrinol. Metab., 2001, 4382-4389). Uma meia-vida in vivo de GLP-1 é meramente 2 min (Kieffer T. J., et al., Endocrinology, 1995, 3585-3596), desse modo uma tal meia-vida curta é um obstáculo principal ao uso direto de GLP-1 como um agente terapêutico. Desde então, numerosos grupos e instituições de pesquisa têm feito muitas experiências com respeito à derivatização de GLP-1, resultando em desenvolvimento e comercialização de um peptideo que é capaz de prolongar a meia-vida in vivo curta (Deacon C. F., Diabetes, 2004, 2181- 2189). Entretanto, um tal derivado de GLP-1 ainda sofre de uma limitação fundamental pelo fato de que ele é uma formulação injetável. Além disso, muito interesse foi cada vez mais focalizado no desenvolvimento de um inibidor de DPP-IV eficiente, devido ao fato de que o GLP-1 ativo (7-36) é degradado por DPP-IV e em seguida convertido em GLP-1 inativo (9-36) somente dentro de um curto período de tempo, por exemplo, 2 minutos.
[006] O início no desenvolvimento de inibidores de DPP-IV foi similar à tendência de desenvolvimento de outros inibidores. Isto é, a maioria dos resultados de pesquisa foi para os análogos de substrato. O representativo destes análogos de substrato é um dipeptídeo derivado que foi obtido como o produto da pesquisa anterior que foi realizada sobre o núcleo origem tendo uma estrutura similar àquele da Pro- lina (Pro), com base no fato de que DPP-IV exibe afinidade pronunciada para um peptídeo contendo um certo aminoácido Prolina (Chin- naswamy T. et al, J. Biol. Chem., 1990, 1476-1483). Exemplos típicos de estruturas similares à prolina incluem pirrolidida e tiazolidida, e derivados contendo estes compostos de origem de núcleo exibem atividade inibitória competitiva reversível para a enzima DPP-IV (Augus- tyns K J L., et al, Eur. J. Med. Chem., 1997, 301-309). Entre os produtos de tal pesquisa extensiva e desenvolvimento, existem experimentos de continuação sobre o mecanismo de ação e eficácia de certos compostos, especificamente Val-Pyr (Valina-Pirrolidida), Ile-Thia (Iso- leucina-Tiazolidida), e similares. Particularmente, muita atenção tem sido focada na Ile-Thia, por que a estrutura de Val-Pyr exibiu atividade inibitória relativamente pobre sobre DPP-IV (Hanne B. R., et al, Nat. Struct. Biol., 2003, 19-25), que como tal incitou pesquisa intensiva e estudo sobre derivados do composto de Ile-Thia.
[007] Além dos compostos derivados focados e obtidos pela pesquisa e estudo acima mencionados, um composto tendo atividade mais proeminente foi a série de tiazolidida de beta-aminoácido que Merck & Co. Inc. tentou desenvolver, entretanto, de acordo com os resultados de experimentos farmacodinâmicos e farmacocinéticos realizados em ratos, o composto obtido exibiu biodisponibilidade significan- temente baixa em conjunto com uma limitação evidente na inibição de atividade enzimática (Jinyou Xu, et al, Bioorg. Med. Chem. Lett., 2004, 4759-4762). Como uma consequência, outro desenvolvimento sobre compostos desta série foi descontinuado devido a profundas desvantagens.
[008] Durante a investigação acima mencionada, Merck noticiou que um beta-aminoácido, em adição a um núcleo origem de tiazolidi- da, é também um fator essencial tendo efeitos significantes sobre o inibidor de atividade de DPP-IVy. Esta descoberta foi aplicado ao método para substituição do núcleo origem de tiazolidida com um diferente composto de núcleo origem (Linda L. B., et al, Bioorg. Med. Chem. Lett., 2004, 4763-4766). Com tal pesquisa subsequente, uma variedade de derivados tendo substituição do núcleo origem de tiazolidida com um núcleo origem de piperazina foi sintetizada com teste de eficácia de fármaco e estudos farmacodinâmicos. Infelizmente, os deri- vadoss de piperazina de Merck ainda sofreram de biodisponibilidade significantemente pobre. De acordo com a otimização do composto para enfrentar tal desvantagem, sitagliptina, o produto MK-0431 (nome comercial: JANUVIA), foi desenvolvido com modificação de uma porção de piperazina para uma porção de triazolopiperazina. Este produto é atualmente comercialmente disponível sob nova aprovação de fármaco pelo US FDA em 2006. [Sitagliptina]
[009] Desse modo, os presentes inventores descobriram que quando uma substituição incluindo um heteroátomo é feita sobre uma porção de piperazinona, o composto desse modo modificado não somente tem excelente atividade inibidora de DPP-IVy, porém também é capaz de obter biodisponibilidade significantemente melhorada, em comparação com inibidores convencionais de DPP-IV, então bem- sucedido em síntese de um novo composto heterocíclico contendo um grupo beta-amino, e completou uma invenção de um composto repre- sentado pela seguinte fórmula 1. Com base nisto, seu pedido foi depositado como Pedido de Patente Coreano No. 2007-0038462. Fórmula 1
[0010] (Na fórmula 1, X é OR1, SR1, ou NR1R2, em que R1 e R2 são independentemente uma Ci~Cs alquila inferior, ou R1 e R2 de NR1R2 podem formar um anel de 5 membros a 7 membros contendo um elemento hetero de O.)
[0011] Além dos inibidores de DPP-IV que estão atualmente sob desenvolvimento ativo, agentes terapêuticos de diabetes ou obesidade que são clinicamente usados ou sob desenvolvimento incluem inibidores de a-glicosidase, Biguanidas, secretagogos de insulina, sensibili- zadores de insulina, antagonistas de receptor canabinoide do tipo 1, e similares.
[0012] Inibidores de a-glicosidase exibem a ação de retardo da absorção de carboidrato do intestino delgado e incluem acarbose, vo- glibose, emiglitato, miglitol, e similares. Exemplos de biguanidas incluem metformina, fenformina, ou buformina. Secretagogos de insulina podem ser divididos em espécies de sulfonilureia e não-sulfonilureia. Exemplos de espécies de sulfonilureia incluem glibenclamida (gliburi- da), glipizida, gliclazida, glimepirida, tolazamida, tolbutamida, aceto- examida, carbutamida, clorpropamida, glibornurida, gliquidona, glisen- tida, glisolamida, glisoxepida, gliclopiamida, glicilamida, glipentida, e similares. Exemplos de espécies de não-sulfonilureia incluem repagli- nida, nateglinida, e similares.
[0013] Metformina, uma representativa Biguanida, é um agente hipoglicêmico que regula altos níveis níveis de glicose sanguínea sem estimular a secreção de insulina do pâncreas, e é vantajoso pelo fato de que o fármaco pode ser aplicado a pacientes diabéticos obesos por que a metformina não está associada com o ganho de peso e aplicada também a pacientes que não são suscetíveis a fármacos de sulfonilu- reia devido a seu diferente mecanismo de ação. Embora a o mecanismo de ação de metform não seja claramente conhecido, o fármaco somente reduz níveis de glicose sanguínea de pacientes diabéticos, sem afetar os níveis de glicose sanguínea de indivíduos normais, e não tem qualquer ação de estimulação de células β no pâncreas para estimular a secreção de insulina em comparação com fármacos de sul- fonilureia. É conhecido que a metformina aumenta a ação de insulina em células periféricas, tais como fígado e músculos e diminui a produção de glicose do fígado, e foi reportado em alguns estudos que a metformina age em músculos esqueletais e aumenta o movimento de glicose através da membrana celular. Além disso, o fármaco é caracteri-zado por melhorar a dislipidemia para reduzir os níveis de colesterol LDL e triglicerídeo. Clinicamente, a metformina pode ser administrada em uma dose relativamente alta, até 200 mg por dia, e duas vezes ao dia, por exemplo, manhã e tarde. Quando a metformina é administrada em excesso de 2.000 mg, ela é administrada com refeição, três vezes ao dia, e a dose máxima por dia é de 2.500 mg.
[0014] Quando a metformina é aplicada a pacientess diabéticos com sobrepeso, ela é avaliada como um exelente agente terapêutico de diabetes. Entretanto, cuidado deve ser tomado por que seus efeitos colaterais adversos podem se acompanhados por distúrbios do sistema gastrointestinal, tais como diarreia, náuse, vômito, e similares, distúrbios do sistema sanguíneo, tais como deficiência de vitamin B12 e similares, acidose lática que é uma severa complicação metabólica que é rara, porém pode induzir a 50% de mortalidade por acúmulo in- terno de metformina, e similares.
[0015] Sensibilizadores de insulina são fármacos relativamente recentemente desenvolvidos, têm uma estrutura de tiazolidina-diona (TZD), e agem sobre receptores ativados por proliferador de pero- xisoma (PPARs). Exemplos de sensibilizadores de insulina incluem troglitazona, ciglitazona, rosiglitazona (AVNADIA), pioglitazona (AC- TOS), englitazona, e similares. Além deles, vários estudos estão em andamento.
[0016] Antagonistas de receptor-1 de canabinoite são fármacos- alvos relativamente recentemente desenvolvidos, inibem a atividade excessiva de endocanabinoide para regular o equilíbrio de peso e energia corporal, bem como o metabolismo de glicose e lipídeo, e agem sobre o receptor-1 de canabinoite (receptor CB1) presente nos sistemas nervosos central e periférico.
[0017] Exemplos de antagonistas de receptor canabinoide do tipo 1 incluem Rimonabanto (ACOMPLIA), Otenabante, Ibinabante, Suri- nabante, e similares. Além deles, vários estudos estão em andamento.
[0018] Entretanto, por que a diabetes ou obesidade é uma doença crônica, e suas condições são complicadas, existem muitos casos em que os sintomas da doença estão em progresso, acompanhados por várias complicações. Portanto, é necessário escolher uma medicação mais apropriada para as condições do paciente individual. Quando medicações individuais são administradas sozinhas, existem casos em que efeitos suficientes podem ser obtidos de acordo com seus sintomas. Além disso, existem muitos casos em que é difício na prática clínica escolher uma medicação devido a muitos problemas tais como aumento em dose ou ocorrência de efeitos colaterais adversos que resultam de administração prolongada. Desse modo, em vez de métodos para a administração de um único fármaco, vários métodos para administração de um ou mais fármacos com diferentes mecanismos em combinação foram recentemente sugeridos.
[0019] Em particular, estudos sobre literaturas de administração combinada de inibidores de DPP-IV e agentes terapêuticos de diabetes convencionais mostram que uma composição farmacêutica preparada por mistura de 3 ~ 20% (peso/peso) of sitagliptina, 25 ~ 94% (pe- so/peso) de metformina, 0,1 ~ 10% (peso/peso) de um lubrificante, e 0 ~ 35% (peso/peso) de um aglutinante é descrita. No caso de vidaglipti- na que é um composto comercialmente disponível como um nome comercial de Galvus de Novartis, pílulas combinadas de vildagliptina e metformina em relações de 50 ~ 98%, 60 ~ 98%, 70 ~ 98%, ou 80 ~ 98% são descritas na Publicação Internacional Gazette WO 07/078726, e pílulas combinadas de vidagliptina e pioglitazona, um agonista de PPAR, por método de compressão direta são descritos na Publicação Internacional Gazette WO 06/135693. Entretanto, estas literaturas descrevem relações de composição farmaceuticamente ideais em uma preparação incluindo um inibidor de DPP-IV e metformina ou um agonista de PPAR, em vez de efeitos sinergísticos dos dois fármacos.
[0020] Além disso, é descrito em JPET (2004), 310.614-619 que um inibidor de DPP-IV valina-pirrolidina (val-pyr), quando administrado a um animal em combinação com metformina, aumentou os níveis de proteína similar ao glucagon, diminuiu a ingestão de alimento e ganho de peso, e sinergisticamente melhorou a tolerância à glicose.
[0021] É descrito em Life Science (2007), 81, 72-79 que a administração combinada de vildagliptina e rosiglitazona realizou significante melhora em glicose de soro, triglicerídeo, e tolerância a glicoses, e efeitos colaterais adversos preexistentes, tais como edema de rosiglitazona e similares, foram aliviados por administração combinada de vildagliptina.
[0022] É identificado na Publicação Internacional Gazette WO 04/052362 que, como um resultado da tolerância à glicose, teste sobre vildagliptina e um fenofibrato micronizado agonista de PPAR, a área sob a curva (AUC) foi diminuída em 18% com administração única de vildagliptina e em 7% com administração única de fenofibrato, enquanto que a AUC foi diminuída em 33%, a sensibilidade à insulina foi melhorada, e o ganho de peso foi reduzido com uma administração combinada dos dois fármacos.
[0023] É mencionado em J. Pharmacol Sei. (2007), 104, 29-38 que níveis elevados pós-prandial de glicose sanguínea são eficazmente diminuídos com uma administração combinada de E3024 que é um inibidor de DPP-IV, voglibose que é um inibidor de a-glicosidase, e acarbose, e em JPET (2007), 320(2), 738-746 que quando E3024 é administrado em combinação com glibenclamida ou nateglinida, que é um tipo de secretagogo de insulina, os níveis de glicose elevados pós- prandiais são também eficazmente diminuídos.
[0024] É mencionado na Publicação de Patente Coreana N° 2003- 0019440 que, quando um composto descrito na Publicação Internacional Gazette WO 99/061431 é administrado em combinação com um agente terapêutico de diabetes convencional, a atividade de DPP-IV plasmático, a concentração de hemoglobina (HbA1C, %), e glicose plasmática são significantemente reduzidas.
[0025] É descrito na Publicação Internacional Gazette WO 07/074884 que, quando a alogliptina é administrada em combinação com voglibose, pioglitazona, e similares, os efeitos protetores do pâncreas são realçados.
[0026] É mencionado na Publicação Internacional Gazette WO 07/006769 que a vildagliptina e rimonabanto, que são antagonistas de receptor canabinoide do tipo 1, são administrados em combinação, os níveis de glicose sanguínea e lipídeo e peso são eficazmente melhorados, e descrito no WO 06/119260 que, quando sitagliptina e um an- tagonista de receptor canabinoide do tipo 1 são administrados em combinação, tolerância à glicose e resistência à insulina são melhorados.
[0027] Desse modo, os presentes inventores desenvolveram um composto de fórmula 1, que é um novo inibidor de DPP-IV, descobriram que quando o composto é administrado em combinação com um agente antidiabético ou antiobesidade, uma excelente tolerância à glicose é exibida, níveis de glicose sanguínea são eficazmente inibidos, e a massa gordurosa é reduzida, desse modo induzindo à conclusão da presente invenção.
[0028] Um objetivo da presente invenção é fornecer uma composição farmacêutica para a prevenção e tratamento de diabetes ou obesidade compreendendo como ingredientes ativos um composto que inibe a atividade de dipeptidil peptidase-IV e outros agentes antidiabé- ticos ou antiobesidade.
[0029] De acordo com a presente invenção, uma composição farmacêutica para a prevenção e tratamento de diabetes ou obesidade compreendendo como ingredientes ativos (1) um composto representado pela seguinte fórmula 1, um sal farmaceuticamente aceitável do mesmo, um hidrato do mesmo, ou um solvato do mesmo, e (2) um ou mais outros agentes antidiabéticos ou antiobesidade. Fórmula 1 (Na fórmula 1, X é como definido aqui).
[0030] De acordo com a presente invenção, uma composição farmacêutica compreendendo como ingredientes ativos um composto que é um tipo de um novo inibidor de DPP-IV e um ou mais outros agentes antidiabéticos ou antiobesidade pode ser útil na prevenção e tratamento de diabetes, obesidade, e similares por administração da composição para realçar os efeitos de tolerância à glicose, inibição de níveis de glicose sanguínea, e redução de efeitos de massa de gordu-ra, comparada a outros agentes antidiabéticos ou antiobesidade convencionais.
[0031] A figura 1 é um isobolograma mostrando efeitos antidiabéticos de composições mistas contendo um composto de fórmula 1 e me- tformina;
[0032] figura 2 é um gráfico mostrando a porcentagem de inibição dos componentes somente e uma composição mista de um composto de fórmula 1 e metformina em várias doses de administração de animal;
[0033] figura 3 é um gráfico mostrando a porcentagem de inibição em termos de melhora em tolerância à glicose de uma única dose de composto 1, metformina, e uma composição mista em várias relações de dose de administração de animal de 1:50 a 1:150 em camundongos obesos;
[0034] figura 4 é um gráfico mostrando a porcentagem de inibição em termos de glicose plasmática de um composto 1, metformina, e uma composição mista por administração em várias relações de dose de administração de animal de 1:50 a 1:150 durante duas semanas em camundongos obesos;
[0035] figura 5 é um gráfico mostrando a porcentagem de inibição em termos de glicose sanguínea de um composto 1, um agonista de PPARy, e uma composição mista por administração em várias relações de dose de administração de animal de 1:0,01 a 1:0,4 durante sete dias em camundongos diabéticos;
[0036] figura 6 é um gráfico mostrando a porcentagem de inibição em termos de glicose sanguínea de um composto 1, um agente de série de sulfonil ureia, e uma composição mista por administração em várias relações de dose de 1:0,2 a 1:3,2;
[0037] figura 7 é um gráfico mostrando a porcentagem de inibição em termos de melhora em tolerância à glicose de um composto 1, um inibidor de a-glicosidase, e uma composição mista por administração em várias relações de dose de 1:0,03 a 1:0,18; e
[0038] figura 8 é um gráfico mostrando a porcentagem de inibição em termos de melhora em tolerância à glicose de um composto 1, um antagonista de receptor canabinoide do tipo 1, uma composição mista por administração em várias relações de dose de 1:1 a 1:10.
[0039] Posteriormente, a presente invenção será descrita em detalhes.
[0040] A presente invenção fornece uma composição farmacêutica para a prevenção e tratamento de diabetes ou obesidade compreendendo como ingredientes ativos (1) um composto representado pela seguinte fórmula 1, um sal farmaceuticamente aceitável do mesmo, um hidrato do mesmo, ou um solvato do mesmo, e (2) um ou mais outros agentes antidiabéticos ou antiobesidade. Fórmula 1
[0041] Na formulai,
[0042] X é OR1, SR1, ou NR1R2,
[0043] em que R1 e R2 são independentemente uma Ci~Cs alquila inferior, ou R1 e R2 de NR1R2 podem formar um anel de 5 membros a 7 membros contendo um elemento hetero de O.
[0044] A Ci~C5 alquila inferior na fórmula 1 pode incluir uma Ci a Cs alquila e uma cicloalquila.
[0045] O composto representado pela fórmula 1 pode ter dois centros assimétricos, e desse modo pode ter centros assimétricos no carbono β e no carbono de posição 3 de piperazina. Portanto, o centro pode estar presente na forma de um único diastereômero, racemato, mistura racêmica ou mistura diastereoisomérica, todos dos quais podem ser incluídos no composto representado pela fórmula 1 de acordo com a presente invenção.
[0046] Além disso, o composto representado pela fórmula 1 da presente invenção pode estar parcialmente presente como um tautô- mero, e tautômeros individuais bem como misturas dos mesmos podem ser incluídas no composto da presente invenção.
[0047] O estereômero da presente invenção pode ser obtido por síntese estereoseletiva de acordo com um método convencional co nhecido na técnica, usando um material de partida oticamente puro ou um reagente conhecido.
[0048] Exemplos preferíveis do composto representado pela fórmula 1 da presente invenção são como segue. 1) (R)-4-[(R)-3-amino-4-(2,4,5-trifluorofeniQbutanoil]-3-(t- bu- toximetil)piperazin-2-ona; 2) (S)-4-[(R)-3-amino-4-(2,4,5-trifluorofenil)butanoil]-3-(t- bu- toximetil)piperazin-2-ona; 3) (R)-4-[(R)-3-amino-4-(2,4,5-trifluorofenil)butanoil]-3- (me- toximetil)piperazin-2-ona; 4) (R)-4-[(R)-3-amino-4-(2,4,5-trifluorofenil)butanoil]-3- (iso- propoximetil)piperazin-2-ona; 5) (R)-4-[(R)-3-amino-4-(2,4,5-trifluorofenil)butanoil]-3- (ci- clopentiloximetil)piperazin-2-ona; 6) (R)-4-[(R)-3-amino-4-(2,4,5-trifluorofenil)butanoil]-3- [(die- tilamino)metil]piperazin-2-ona; 7) (R)-4-[(R)-3-amino-4-(2,4,5-trifluorofenil)butanoil]-3- [(etilmetilamino)metil]piperazin-2-ona; 8) (R)-4-[(R)-3-amino-4-(2,4,5-trifluorofenil)butanoil]-3- (mor- folinometil)piperazin-2-ona; 9) (R)-4-[(R)-3-amino-4-(2,4,5-trifluorofenil)butanoil]-3-(t- bu- tiltiometil)piperazin-2-ona.
[0049] O sal farmaceuticamente aceitável do composto hetero contendo grupo beta-amino de fórmula 1 de acordo com a presente invenção pode ser preparado por qualquer método convencional para preparação de sais conhecidos na técnica.
[0050] Como usado aqui, o termo "sal farmaceuticamente aceitável" refere-se a um sal preparado de um ácido ou base não tóxico farmaceuticamente aceitável incluindo uma base inorgânica ou orgânica e um ácido inorgânico ou orgânico. Exemplos do sal derivado de uma base inorgânica incluem alumínio, amónio, cálcio, cobre, férrico, ferroso, lítio, magnésio, manganato, manganês, potássio, sódio, zinco, e similares. Particularmente preferidos são sais de amónio, cálcio, magnésio, potássio e sódio. Um sal sólido pode ter uma ou mais estruturas cristais, ou de outro modo pode ser na forma de um hidrato. Exemplos do sal derivado de uma base orgânica não tóxica farmaceuticamente aceitável incluem uma amina primária, secundária ou terciária, uma amina substituída tal como uma amina substituída de ocorrência natural, uma amina cíclica, ou uma resina de troca de íon básica tais como arginina, betaína, cafeína, colina, N,N'-dibenziletilenodiamina, dietila- mina, 2-dietilaminoetanol, 2-dimetilaminoetanol, etanolamina, etileno- diamina, N-etilmorfolina, N-etilpiperidina, glucamina, glucosamina, histidina, hidrabamina, isopropilamina, lisina, metilglucamina, morfolina, piperazina, piperidina, resina de poliamina, procaína, purina, teobromo, trietilamina, trimetilamina, tripropilamina, trometamina, e similares.
[0051] Quando o composto da presente invenção for básico, um sal do mesmo pode ser preparado de ácidos não tóxicos farmaceuticamente aceitáveis incluindo ácidos inorgânicos e orgânicos. Exemplos do ácido incluem ácido acético, ácido benzenossulfônico, ácido benzoico, ácido canforsulfônico, ácido cítrico, ácido etanossulfônico, ácido fumárico, ácido glucônico, ácido glutâmico, ácido bromídrico, ácido clorídrico, ácido isetiônico, ácido lático, ácido maleico, ácido má- lico, ácido mandélico, ácido metanossulfônico, ácido múcico, ácido nítrico, ácido pamoico, ácido pantotênico, ácido fosfórico, ácido succíni- co, ácido sulfúrico, ácido tartárico, ácido p-tolueno sulfônico, ácido adípico, e similares. Preferivelmente, o sal farmaceuticamente aceitável pode ser ácidos acético, cítrico, clorídrico, málico, fosfórico, succí- nico, tartárico e adípico. Mais preferivelmente, o sal farmaceuticamente aceitável pode ser ácido tartárico.
[0052] Como usado aqui, o composto de fórmula 1 designado é pretendido abranger um sal farmaceuticamente aceitável do mesmo.
[0053] Um hidrato de um composto de fórmula 1 da presente invenção ou um sal farmaceuticamente aceitável do mesmo é pretendido abranger uma quantidade estequiométrica ou não estequiométrica de água ligada a ele por forças intermoleculares não covalentes. O hidrato pode conter 1 ou mais equivalente de água, tipicamente 1 a 5 equivalentes de água. O hidrato pode ser preparado por cristalização do composto de fórmula 1 da presente invenção ou um sal farmaceuti- camente aceitável do mesmo em água ou solvente contendo água.
[0054] Um solvato de um composto de fórmula 1 da presente invenção ou um sal farmaceuticamente aceitável do mesmo é pretendido abranger uma quantidade estequiométrica ou não estequiométrica de um solvente ligado a ele por forças intermoleculares não covalentes. Solventes preferidos são voláteis, não tóxicos, e adequados para administração a humanos. Por exemplo, menção pode ser feita a etanol, metanol, propanol, cloreto de metileno, e similares.
[0055] Um composto de fórmula 1 da presente invenção pode ser facilmente obtido como descrito em Pedido de Patente da Coreia n°. 2007-0038462. Especificamente, (R)-(3-t-butoximetil)piperazin-2-ona sintetizado de 1) ácido (3R)-t-butoxicarbonilamino-4-(2,4,5- trifluorofenil)butanoico e metil éster de D-serina como materiais de partida podem ser sintetizados em um intermediário (R)-4[(R)-2-(t- butoximetil)-3-oxopiperazin-1-il]-4-oxo-1-(2,4,5-trifluorofenil)-butan-2- ilcarbamato de t-butila por reação de peptidização padrão (etapa 1), e em seguida submetidos à desproteção (etapa 2), seguido por neutralização para obter um composto na forma de fórmula 1.
[0056] O composto de fórmula 1 é um tipo de inibidor de DPP-IV, exibe excelente atividade inibitória sobre DPP-IV e biodisponibilidade, e pode ser útil na prevenção e tratamento de doenças tais como diabetes, obesidade, e similares, causadas por DPP-IV.
[0057] Um agente antidiabético ou antiobesidade que é misturado com um composto representado pela fórmula 1 na presente invenção para fornecer uma composição para prevenção e tratamento de diabetes ou obesidade pode ser preferivelmente selecionado do grupo con- sistindo em inibidor de α-glicosidase, Biguanida, secretagogo de insulina, sensibilizador de insulina, e antagonista de receptor canabinoide do tipo 1. Entretanto, não é limitado a estes.
[0058] A Biguanida da presente invenção refere-se a um fármaco incluindo uma estrutura de biguanida e tendo efeitos, tais como efeitos promotores de glicólise anaeróbica, realce de efeitos de insulina periférica, supressão de absorção de glicose do trato intestinal, e supressão de gliconeogênese do fígado. A Biguanida pode ser selecionada do grupo consistindo em metformina, buformina, e fenformina, porém não é limitada a estas.
[0059] O sensibilizador de insulina da presente invenção refere-se a um fármaco que melhora a disfunção da ação de insulina para diminuir os níveis de glicose sanguínea, comumente tem uma estrutura de tiazolidinadiona (TZD), e age sobre os receptores ativados por prolife- rador de peroxissoma (PRARs). O sensibilizador de insulina pode ser selecionado do grupo consistindo em troglitazona, ciglitazona, rosigli- tazona (AVNADIA), pioglitazona (ACTOS), e englitazona, porém não é limitado a estes.
[0060] O secretagogo de insulina da presente invenção refere-se a um fármaco que promove a secreção de insulina de células beta do pâncreas, e pode ser um fármaco tendo uma estrutura de sulfonil ureia ou não sulfonilureia. Preferivelmente, o secretagogo de insulina pode ser um fármaco tendo uma estrutura de sulfonil ureia, selecionado do grupo consistindo em glibenclamida (gliburida), glipizida, gliclazida, glimepirida, tolazamida, tolbutamida, acetoexamida, carbutamida, clor- propamida, glibornurida, gliquidona, glisentida, glisolamida, glisoxepi- da, gliclopiamida, glicilamida, e glipentida, ou um fármaco tendo uma estrutura não sulfonilureia, tal como repaglinida ou nateglinida, porém não é limitado a estes.
[0061] O inibidor de a-glicosidase da presente invenção refere-se a um fármaco que competitivamente inibe a a-glicosidase que é um tipo de enzima digestiva no intestino para suprimir a digestão e absorção de amido, dissacarídeos, e similares. O inibidor de a-glicosidase pode ser selecionado do grupo consistindo em acarbose, voglibose, emiglitato, e miglitol, porém não é limitado a estes.
[0062] O antagonista de receptor canabinoide do tipo 1 da presente invenção refere-se a um fármaco que inibe a atividade excessiva de endocanabinoide para regular o equilíbrio de peso corporal e energia bem como o metabolismo de glicose e lipídeo. O antagonista de receptor canabinoide do tipo 1 pode ser selecionado do grupo consistindo em rimonabanto (ACOMPLIA), Otenabante, Ibinabante, e Surinabante, porém não é limitado a estes.
[0063] A dose ou dosagem de uma composição farmacêutica de acordo com a presente invenção varia dependendo de um peso corporal do paciente, idade, sexo, condições de saúde, dieta, tempo de administração, método de administração, taxa de evacuação, a severidade de uma doença, e similares. A unidade de dosagem geral é calculada com base na quantidade de ingrediente ativo que pode ser fornecida a um indivíduo humano de 70 kg em uma única dose para julgar se uma dose terapeuticamente eficaz é atingida. Entretanto, será apreciado que a dose terapeuticamente eficaz precisa dos ingredientes ativos variará dependendo da quantidade relativa de cada componente ativo sendo usado, do fármaco particular sendo usado e das relações sinergísticas mencionadas acima.
[0064] O composto de fórmula 1 pode ser preferivelmente incluído na composição farmacêutica em uma faixa de cerca de 0,1 a cerca de 1.500 mg. Entretanto, a faixa pode aumentar ou diminuir, dependendo do sintoma.
[0065] Além disso, uma dose recomendada bem conhecida é adequada como uma dose clínica diária de outros agentes antidiabéticos ou antiobesidade incluídos em uma composição farmacêutica da presente invenção. Por exemplo, uma dose de cerca de 500 mg a cerca de 2000 mg é geralmente conhecida como uma dose clínica diária de metformina.
[0066] Uma relação de mistura de um composto representado pela fórmula 1 incluído em uma composição farmacêutica da presente invenção e outros agentes antidiabéticos ou antiobesidade pode ser selecionada na faixa de 1:16,7 a 1:450 com base em uma dose a ser administrada. Doses terapeuticamente eficazes ideais para serem administradas podem ser facilmente determinadas por aqueles versados na técnica e variarão com a quantidade de ingredientes ativos usada em uma relação sinergística com base em uma fração de seus respectivos valores de ED30, a intensidade da preparação, 0 modo de administração e 0 avanço da condição ou distúrbio a ser tratado. Além disso, fatores associados com 0 indivíduo particular a ser tratado, incluindo idade do indivíduo, peso corporal, dieta e tempo de administração, resultarão na necessidade de ajuste da dose para um nível terapeuticamente eficaz apropriado.
[0067] A composição farmacêutica da presente invenção pode ser administrada dentro da faixa de uma relação sinergística com base em uma fração de seus respectivos valores de ED30. O valor de ED30 refe- re-se a uma dose de uma composição farmacêutica, na qual 30% da porcentagem de inibição são exibidos. A porcentagem de inibição pode ser obtida calculando-se uma área sob a curva de um grupo experimental, exceto para uma área sob a curva de um grupo em que glicose não foi administrada, na curva de mudança de glicose sanguínea, comparando 0 valor com aquele de um grupo controle em que glicose foi administrada, e calculando a relação de inibição. Em geral, é sugerido que uma dose eficaz é definida como uma dose para suprimir a AUC em 30% ou mais em experimentos de camundongo (W02006/076231 A2).
[0068] Na composição farmacêutica da presente invenção, o composto de fórmula 1 e Biguanida podem ser incluídos na faixa de relação de 9:1 a 1:3 com base em uma fração de seus respectivos valores de ED30, e mais preferivelmente na relação de 1:1.
[0069] Na composição farmacêutica da presente invenção, quando a relação de mistura do composto de fórmula 1 e Biguanida é 1:16,7 ou menos, ou 1:450 ou mais com base na relação de peso, eficácia pobre ou efeitos colaterais adversos podem ocorrer. Ao contrário, na faixa de 1:16,7 a 1:450, efeitos sinergísticos de melhora em tolerância à glicose podem ocorrer. Portanto, os dois agentes podem ser preferivelmente incluídos na faixa de 1:16,7 a 1:450 com base na relação de peso. Entretanto, a relação não é limitada a estas.
[0070] Na composição farmacêutica da presente invenção, quando a relação de mistura do composto representado pela fórmula 1 e um sensibilizador de insulina é 1:0,01 ou menos, ou 1:0,4 ou mais com base na relação de peso, eficácia pobre ou efeitos colaterais adversos podem ocorrer porque este é um valor divergindo de uma dose clínica diária do sensibilizador de insulina. Ao contrário, na faixa de 1:0,01 a 1:0,4, efeitos sinergísticos de melhora em eficácia podem ocorrer. Por-tanto, a relação de mistura do composto 1 e 0 sensibilizador de insulina pode ser preferivelmente na faixa de 1:0,01 a 1:0,4 com base na relação de peso. Entretanto, a relação não é limitada a estas e pode ser ajustada dependendo dos sintomas.
[0071] Na composição farmacêutica da presente invenção, quando a relação de mistura do composto de fórmula 1 e um secretagogo de insulina é 1:0,2 ou menos, ou 1:3,2 ou mais com base na relação de peso, a dose pode exceder uma dose clínica diária do secretagogo de insulina ou eficácia pobre pode ocorrer. Ao contrário, efeitos sinergísticos de melhora em eficácia podem ocorrer na faixa de 1:0,2 a 1:3,2. Portanto, a relação de mistura do composto 1 e o secretagogo de insulina pode ser preferivelmente na faixa de 1:0,2 a 1:3,2. Entretanto, a relação não é limitada a estas.
[0072] Além disso, na composição farmacêutica da presente invenção, quando a relação de mistura do composto representado pela fórmula 1 e um inibidor de a-glicosidase é 1:0,03 ou menos, ou 1:0,18 ou mais com base na relação de peso, a dose pode exceder uma dose clínica diária do inibidor de a-glicosidase ou eficácia pobre pode ocorrer. Ao contrário, efeitos sinergísticos de melhora em eficácia podem ocorrer na faixa de 1:0,03 a 1:0,18. Portanto, é preferível ter a relação de mistura do composto 1 e o inibidor de a-glicosidase na faixa de 1:0,03 a 1:0,18. Entretanto, a relação não é limitada a estas.
[0073] Na composição farmacêutica da presente invenção, quando a relação de mistura do composto de fórmula 1 e um antagonista de receptor canabinoide do tipo 1 é 1:0,1 ou menos, ou 1:1 ou mais com base na relação de peso, a dose pode exceder uma dose clínica diária do antagonista de receptor canabinoide do tipo 1 ou eficácia pobre pode ocorrer. Portanto, é preferível ter a relação de mistura do composto 1 e o antagonista de receptor canabinoide do tipo 1 na faixa de 1:1 a 1:10. Entretanto, a relação não é limitada a estas.
[0074] Como usado aqui, o termo "administração" significa a introdução de um material predeterminasdo em pacientes usando um método adequado. A composição da presente invenção pode ser oralmente ou parenteralmente administrada por meio de qualquer das rotinas comuns, contanto que ela seja capaz de atingir o tecido desejado. Além disso, a composição pode ser administrada usando um certo aparato capaz de transportar substâncias ativas em células-alvos. É preferable oralmente administrar a composição farmacêutica da presente invenção, porém não é limitado a esta. A administração parenteral inclui injeções subcutâneas, intravenosas, intramusculares ou intra- torácicas, porém não está limitada a estas.
[0075] A composição farmacêutica da presente invenção pode ser formulada de várias formas orais ou parenterais de uma ampla faixa durante a administração clínica e pode ser administrada.
[0076] Exemplos da forma de dosagem para administração oral podem incluir comprimidos, pílulas, cápsulas duras/macias, soluções, suspensões, emulsões, xaropes, grânulos, elixires, e similares. Estas formulações farmacêuticas podem conter, além do ingrediente ativo, um ou mais diluentes ou excipientes conventionais, tais como cargas, extensores, agentes umectantes, disintegrantes, deslizantes, aglutinantes, tensoativos, e similares. Exemplos dos desintegrantes podem incluir ágar, amido, ácido algínico ou um sal de sódio do mesmo, fosfato de monoidrogênio de cálcio anidroso, e similares. Exemplos dos deslizantes podem incluir sílica, talco, ácido esteárico ou magnésio ou sal de cálcio do mesmo, polietileno glicol, e similares. Exemplos do aglutinante podem incluir silicato de alumínio de magnésio, pasta de amido, gelatina, tragacanto, metilcelulose, carboximetilcelulose sódica, polivinilpirrolidona, hidróxipropil celulose pouco substituída, e similares. Além disso, a formulação farmacêutica pode incluir diluentes, por exemplo, lactose, dextrose, sacarose, manitol, sorbitol, celulose, glicina, e similares. Se desejado, a formulação pode também conter con-vencionalmente misturas efervescentes, absorventes, colorantes, aro- matizantes, adoçantess e similares conhecidos.
[0077] Exemplos da forma de dosagem para administração parenteral podem incluir soluções aquosas esterilizadas, soluções não aquosas, suspensões, emulsões, agentes liofilizados, ou supositórios. Como solventes não aquosos ou agentes de suspensão, propileno glicol, polietileno glicol, óleos vegetais, tais como óleo de oliva, ésteres injetáveis, tais como oleato de etila, e similares podem ser usados. Como a base da preparação injetável, aditivos convencionais tais co- mo solubilizantes, agentes isotônicos, agentes de suspensão, agentes emulsificantes, estabilizantes e preservativos podem ser usados. A composição farmacêutica, de acordo com um exemplo da presente invenção, pode ser preparada como uma solução ou suspensão mistu- rando-se o composto de fórmula 1 ou um sal farmaceuticamente aceitável do mesmo e metformina com um estabilizante ou tampão em água, e pode ser preparado em uma forma de dosagem unitária (por exemplo, ampola ou frasconete). A composição pode ser esterilizada ou conter um adjuvante (por exemplo, um preservativo, um estabilizante, um agente umectante, ou um emulsificante, um sal para regulação osmótica, um agente de tamponamento, e similares). Além disso, a composição pode também conter outras substâncias terapeuticamente úteis. A composição pode ser preparada de uma maneira convencional por métodos de mistura, granulação ou revestimento.
[0078] Posteriormente, a presente invenção será descrita em maiores detalhes com referência aos seguintes Exemplos de Preparação, Exemplos, Exemplos Experimentais, e Exemplos de Preparação. Entretanto, os seguintes exemplos são fornecidos para propósitos ilustrativos somente, e o escopo da presente invenção não deve ser limitado a eles de qualquer maneira.
[0079] 200 g de cloridrato de metil éster de D-serina foram adicio nados a 1,8 L de clorofórmio, e a solução reacional foi resfriada para 0°C, a qual 448 ml_ de trietilamina foram em seguida lentamente adicionados. 358,4 g de cloreto de tritila foram lentamente adicionados à mistura reacional que foi em seguida agitada durante 1 hora. A mistura reacional foi aquecida para a temperatura ambiente, e 1 L de clorofórmio foi adicionado a ela, seguido por lavagem com 2,5 L de água. A camada orgânica foi secada sobre sulfato de magnésio e novamente resfriada para 0°C, a qual 484 ml_ de trietilamina e 15,7 g de 4- metilaminopiridina foram em seguida sequencialmente e lentamente adicionados. A mistura reacional foi agitada durante 5 min e 139 mL de cloreto de metano sulfonila foram lentamente adicionados a ela. A mistura reacional foi aquecida para a temperatura ambiente, agitada durante mais 4 horas e em seguida refluxada durante 12 horas. A mistura reacional foi resfriada para temperatura ambiente, e lavada com 4 L de água e em seguida 3 L de salmoura. A camada orgânica foi secada sobre sulfato de magnésio e concentrada até a secura sob pressão reduzida. 3 L de etanol foram adicionados ao resíduo resultante que foi em seguida agitado. Os sólidos resultantes foram filtrados para fornecer 329 g do composto do título.
[0080] 1H RMN (400 MHz, CDCh): 7,42-7,49 (m, 6H), 7,18-7,32 (m, 9H), 7,68 (s, 1H), 3,74 (s, 3H), 2,24 (m, 1H), 1,87 (m, 1H), 1,40 (m, 1H)
[0081] 328,4 g de 1 -tritilaziridina-2-carboxilato de (R)-metila foram dissolvidos em 1,4 L de clorofórmio e a solução reacional foi resfriada para 0°C, a qual 462 mL de ácido trifluoroacético foram em seguida lentamente adicionados. A mistura reacional foi agitada durante 1 hora, a qual 2 L de água foram em seguida adicionados, seguido por agitação durante 10 min e remoção da camada orgânica. A camada aquosa foi neutralizada com carbonato de hidrogênio de sódio e usada em reações subsequentes sem outra purificação.
[0082] 2 L de dietil éter e 120,5 g de carbonato de hidrogênio de sódio foram adicionados à camada aquosa, e a solução reacional foi resfriada para 0°C, a qual 165 ml_ de cloroformiato de benzila foram em seguida lentamente adicionados gota a gota. A mistura reacional foi agitada durante mais 2 horas e a camada aquosa foi removida. A camada orgânica foi secada sobre sulfato de magnésio, concentrada e secada sob pressão reduzida, e purificada por cromatografia de coluna, desse modo fornecendo 108,5 g do composto do título.
[0083] 1H RMN (400 MHz, DMSO) : 7,32-7,36 (m, 5H), 5,13 (s, 2H), 3,09 (dd, J=3,2, 5,4Hz, 1H), 2,58 (dd, J=1,2, 3,2Hz, 1H), 2,47 (dd, J=1,2, 5,4Hz, 1H),
[0084] 1,1 g de aziridina-1,2-dicarboxilato de (R)-1-benzil 2-metila foi dissolvido em 11 ml_ de clorofórmio, ao qual 18 mL de t-butanol foram em seguida adicionados. À mistura reacional foi lentamente adicionado gota a gota 1,2 mL de BF3OEt2, seguido por agitação durante 12 horas. A reação foi terminada com adição de 2 L de água à mistura reacional. Em seguida, a camada orgânica foi separada e secada sobre sulfato de magnésio, concentrada e secada sob pressão reduzida, e em seguida usada em reações subsequentes sem outra purificação.
[0085] O resíduo resultante foi dissolvido em 10 mL de metanol, ao qual 740 mg de paládio/carbono em 2 mL de acetato de etila foram em seguida adicionados, seguido por borbulhamento de hidrogênio durante 1 hora sob pressão atmosférica ambiente. A mistura reacional foi filtrada e secada sob pressão reduzida para fornecer 736 mg do composto do título.
[0086] 1H RMN (400 MHz, CD3OD) : 4,21 (m, 1H), 3,82 (s, 3H), 3,74-3,88 (m, 2H), 1,20 (s, 9H)
[0087] 736 mg de metil éster de (R)-2-amino-3-t-butoxipropano preparado na etapa 3 foram dissolvidos em 14 mL de diclorometano, ao qual 6335 mg de metanol de N-t-butoxicarbonil-2-aminoacetaldeído foram em seguida lentamente adicionados. A mistura reacional foi resfriada para 0°C, seguido por adição gradual de 1,2 mL de trietilamina e 1,78 g de triacetoxiboroidreto de sódio. A mistura reacional foi aquecida para a temperatura ambiente, seguido por agitação durante 12 horas. Uma solução de carbonato de hidrogênio de sódio saturada foi adicionada para terminar a reação, e a camada orgânica foi lavada com 10 mL de água e salmoura, concentrada e secada sob pressão reduzida. O resíduo resultante foi purificado por cromatografia de coluna, desse modo fornecendo 355 mg do composto do título.
[0088] 1H RMN (400 MHz, CDCI3): 5,10 (m, 1H), 3,71 (s, 3H), 3,56 (m, 2H), 3,40 (m, 1H), 3,15-3,28 (m, 2H), 2,81 (m, 1H), 2,67 (m, 1H), 1,42 (s, 9H), 1,13 (s, 9H)
[0089] 355 mg de metil éster de ácido (R)-3-t-butóxi-2-(2-(t- butoxicarbonilamino)etilamino)propiônico preparado na etapa 4 foram dissolvidos em 11 mL de tetra-hidrofurano, e a mistura reacional foi resfriada para 0°C, a qual 187 mg de carbonato de hidrogênio de sódio foram em seguida adicionados. 192 de benzilcloroformiato foram lentamente adicionados gota a gota a ela, e a mistura reacional foi aquecida para a temperatura ambiente. Após 12 horas, a mistura rea-cional foi secada sob pressão reduzida, seguido por adição de 10 mL de acetato de etila, e a camada orgânica foi lavada com 10 mL de água. A camada orgânica foi secada sobre sulfato de magnésio, secada sob pressão reduzida, e purificada por cromatografia de coluna, desse modo fornecendo 410 mg do composto do título.
[0090] 1H RMN (400 MHz, CDCh): 7,36-7,25 (m, 5H), 5,82-5,72 (m, 1H), 5,17-5,03 (m, 2H), 4,15 (m, 1H), 3,98 (m, 1H), 3,81 (m, 1H), 3,73 (s, 3H), 3,60 (m, 1H), 3,42-3,28 (m, 3H), 1,40 (s, 9H), 1,14 (s, 9H)
[0091] 410 mg de metil éster de ácido (R)-2-((benziloxicarbonil)(2- t-butoxicarbonilamino)etil)amino)-3-t-butoxipropiônico preparado na etapa 5 foram dissolvidos em 10 mL de metanol, e a mistura reacional foi resfriada para 0°C, a qual 4 mL de 2 N de ácido clorídrico/dietil éter foram em seguida lentamente adicionados, seguido por agitação durante 3 horas. A mistura reacional foi secada sob pressão reduzida e usada em reações subsequentes sem outra purificação.
[0092] O resíduo resultante foi dissolvido em 10 mL de diclorome- tano e a mistura reacional foi resfriada para 0°C, a qual 152 de trieti- lamina foram em seguida lentamente adicionados. 1,1 mL de trimetila- lumínio (2,0 M de solução em tolueno) foi lentamente adicionado a ela, e a mistura reacional foi aquecida para a temperatura ambiente e em seguida agitada durante 12 horas. A mistura reacional foi resfriada para 0°C e uma solução aquosa de cloreto de amónio saturada foi adicionada para terminar a reação. 10 mL de acetato de etila foram adicionados à mistura reacional que foi em seguida lavada com 10 mL de salmoura. A camada orgânica foi secada sobre sulfato de magnésio e secada sob pressão reduzida. O resíduo resultante foi purificado por cromatografia de coluna para fornecer 103 mg do composto do título.
[0093] 1H RMN (400 MHz, CDCh): 7,34-7,25 (m, 5H), 6,27 (m, 1H), 5,14 (m, 2H), 4,57 (m, 1H), 4,19 (m, 1H), 4,08 (m, 1H), 3,94 (m, 1H), 3,74 (m, 1H), 3,64 (m, 1H), 3,42 (m, 1H), 3,29 (m, 1H), 1,09 (s, 9H)
[0094] 103 mg de 2-(t-butoximetil)-3-oxopiperazina-1-carboxilato de (R)-benzila preparado na etapa 6 foram dissolvidos em 2 mL de metanol, ao qual 50 mg de paládio/carbono em 1 mL de acetato de etila foram em seguida adicionados, seguido por borbulhamento de hidrogênio durante 1 hora sob pressão atmosférica ambiente. A mistura reacional foi filtrada e secada sob pressão reduzida para fornecer 58 mg do composto do título.
[0095] 1H RMN (400 MHz, CDCh): 6,41 (brs, 1H), 3,76 (m, 3H), 3,63 (m, 1H), 3,52 (m, 1H), 3,42 (m, 1H), 3,28 (m, 1H), 3,16 (m, 1H), 2,95 (m, 1H), 2,45 (brs, 1H), 1,17 (s, 9H)
[0096] 104 mg de ácido (3R)-t-butoxicarbonilamino-4-(2,4,5- trifluorofenil)butanoico e 58 mg de (R)-(3-t-butoximetil)piperazin-2-ona foram adicionados a 4 mL de N,N-dimetilformamida, a qual 63 mg de 1-hidroxibenzotriazol (HOBT) e 217 /J2 de diisopropiletilamina foram em seguida adicionados. A mistura reacional foi resfriada para 0°C e 78 mg de 1-etil-3-(3-dimetilaminopropil)carbodiimida (EDC) foram adicionados a ela, seguido por agitação em temperatura ambiente durante 12 horas. A mistura reacional foi diluída com 10 mL de acetato de etila e lavada duas vezes com salmoura. A camada orgânica foi secada sobre sulfato de magnésio e concentrada. O resíduo resultante foi purificado por cromatografia de coluna para fornecer 97 mg do com-posto do título.
[0097] 1H RMN (400 MHz, CDCh): 7,03 (m, 1H), 6,88 (m, 1H), 5,97 (m, 1H), 5,48 (m, 1H), 4,16-4,07 (m, 1H), 4,02-3,91 (m, 1H), 3,74 (m, 2H), 3,37 (m, 2H), 3,24 (m, 1H), 2,92 (m, 2H), 2,80 (m, 1H), 2,59 (m, 2H), 1,34 (d, 9H), 1,13 (s, 9H)
[0098] 97 mg de (R)-4-[(R)-2-(t-butoximetil)-3-oxopiperazin-1-il]-4- oxo-1-(2,4,5-trifluorofenil)butan-2-ilcarbamato de t-butila preparado na etapa 8 foram dissolvidos em 3 mL de metanol, seguido por adição de 2 mL de 2 N de ácido clorídrico/dietil éter e agitação em temperatura ambiente durante 3 horas.
[0099] A mistura reacional foi concentrada e secada sob pressão reduzida, a qual 10 mL de solução aquosa de carbonato de hidrogênio de sódio a 5% foram adicionados e 10 mL de solução mista de diclo- rometano/2-propanol (4/1 (v/v)) para extração duas vezes, seguido por secagem da camada orgânica sob pressão reduzida para fornecer 55 mg do composto do título como um sólido.
[00100] 1H RMN (400 MHz, CD3OD): 7,27 (m, 1H), 7,14 (m, 1H), 4,56-4,39 (m, 1H), 3,96-3,81 (m, 3H), 3,70 (m, 1H), 3,46 (m, 1H), 3,43-3,32 (m, 1H), 2,83-2,65 (m, 3H), 2,58-2,40 (m, 2H), 1,16 (s, 3H), 1,11 (s, 6H)
[00101] Metanol foi usado em vez de t-butanol na etapa 3 do exemplo de preparação 1, e 0 composto do título foi em seguida sintetizado similarmente às etapas 4 até 9 do exemplo de preparação 1.
[00102] Isopropanol foi usado em vez de t-butanol na etapa 3 do exemplo de preparação 1, e 0 composto do título foi em seguida sintetizado similarmente às etapas 4 até 9 do exemplo de preparação 1.
[00103] Ciclopentanol foi usado em vez de t-butanol na etapa 3 do exemplo de preparação 1, e 0 composto do título foi em seguida sintetizado similarmente às etapas 4 até 9 do exemplo de preparação 1.
[00104] Dietilamina foi adicionada em vez de t-butanol e o refluxo foi realizado em vez de adição de BFsOEt2 na etapa 3 do exemplo de preparação 1, e o composto do título foi em seguida sintetizado similarmente às etapas 4 até 9 do exemplo de preparação 1.
[00105] Etilmetilamina foi adicionada em vez de t-butanol e o refluxo foi realizado em vez de adição de BFsOEt2 na etapa 3 do exemplo 1, e o composto do título foi em seguida sintetizado similarmente às etapas 4 até 9 do exemplo de preparação 1.
[00106] Morfolina foi adicionada em vez de t-butanol e o refluxo foi realizado em vez de adição de BFsOEt2 na etapa 3 do exemplo de preparação 1, e o composto do título foi em seguida sintetizado similarmente às etapas 4 até 9 do exemplo de preparação 1.
[00107] t-Butil tiol foi usado em vez de t-butanol na etapa 3 do exemplo de preparação 1, e o composto do título foi em seguida sintetizado similarmente às etapas 4 até 9 do exemplo de preparação 1.
[00108] Cloridrato de metil éster de L-serina foi usado em vez de cloridrato de metil éster de D-serina na etapa 1 do exemplo de preparação 8, e o composto do título foi em seguida sintetizado similarmente às etapas 2 até 9 do exemplo de preparação 8.
[00109] Exemplo Preparação de uma composição contendo um composto de fórmula 1 e um fármaco antidiabético ou antiobesidade
[00110] O composto preparado no exemplo de preparação 1 e metformina foram pesados, e metilcelulose a 0,5% foi usada para preparar 10 mL/kg de uma suspensão com cada composição (0,045 ~ 0,36 mg/kg do composto preparado no exemplo de preparação 1 : 0,75 ~ 6 mg/kg de metformina)/10 mL.
[00111] A preparação foi realizada similarmente ao método no exemplo 1-1 para ter cada composição (0,042 ~ 0,33 mg/kg do composto preparado no exemplo de preparação 1 : 1,25 ~ 10 mg/kg de metformina)/10 mL.
[00112] A preparação foi realizada similarmente ao método no exemplo 1-1 para ter cada composição (0,025 ~ 0,2 mg/kg do composto preparado no exemplo de preparação 1 : 3,25 ~ 30 mg/kg de metformina)/! 0 mL.
[00113] A preparação foi realizada similarmente ao método no exemplo 1-1 para ter cada composição (0,0125 ~ 0,1 mg/kg do composto preparado no exemplo de preparação 1 : 5,625 ~ 45 mg/kg de metformina)/10 mL.
[00114] O composto preparado no exemplo de preparação 1 e rosi- glitazona foram pesados, e metilcelulose a 0,5% foi usada para preparar 5 mL/kg de uma suspensão com cada composição (1 mg do composto preparado no exemplo de preparação 1 + 0,4 mg de rosiglitazo- na)/5 mL.
[00115] A preparação foi realizada similarmente ao método no exemplo 2-1 para ter cada composição (40 mg do composto preparado no exemplo de preparação 1 + 0,4 mg de rosiglitazona)/5 mL.
[00116] O composto preparado no exemplo de preparação 1 e gli- mepirida foram pesados, e metilcelulose a 0,5% foi usada para prepa- rar 10 mL/kg de uma suspensão com cada composição (0,1 mg do composto preparado no exemplo de preparação 1 + 0,02 mg de glime- pirida)/10 mL.
[00117] A preparação foi realizada similarmente ao método no exemplo 3-1 para ter cada composição (0,1 mg do composto preparado no exemplo de preparação 1 + 0,32 mg de rosiglitazona)/10 mL. Exemplo 4 Preparação de uma composição mista de um composto representado pela fórmula 1 e inibidor de a-glicosidase
[00118] O composto preparado no exemplo de preparação 1 e voglibose foram pesados, e metilcelulose a 0,5% foi usada para preparar 10 mL/kg de uma suspensão com cada composição (0,3 mg do composto preparado no exemplo de preparação 1 + 0,009 mg de voglibo- se)/10 mL.
[00119] A preparação foi realizada similarmente ao método no exemplo 4-1 para ter cada composição (0,3 mg do composto preparado no exemplo de preparação 1 + 0,054 mg de voglibose)/10 mL.
[00120] O composto preparado no exemplo de preparação 1 e rimonabanto foram pesados, e metilcelulose a 0,5% foi usada para preparar 5 mL/kg de uma suspensão com cada composição (0,3 mg do composto preparado no exemplo de preparação 1 + 3 mg de rimona- banto)/5 mL.
[00121] A preparação foi realizada similarmente ao método no exemplo 5-1 para ter cada composição (3 mg do composto preparado no exemplo de preparação 1 + 3 mg de rimonabanto)/5 mL.
[00122] A fim de examinar os efeitos sinergísticos de uma composição mista de um composto preparado no exemplo de preparação 1 da presente invenção e metformina por administração única, o seguinte experimento foi realizado nos materiais individuais e na composição mista.
[00123] Camundongos de laboratório (C57BL/6 camundongos) como sujeitos experimentais foram jejuados durante 16 a 17 horas antes dos experimentos. O sangue foi coletado de veias caudais de camundongos na manhã do dia do experimento e o nível de glicose sanguínea foi medido com um medidor de glicose sanguínea ACCU-CHEK ACTIVE (Roche Diagnostics). A composição farmacêutica da presente invenção foi fornecida oralmente 30 min antes da administração de glicose (-30 min), seguido por administração oral de uma solução de glicose (2 g/kg/10 mL) após 30 min (0 min). A coleta de sangue foi feita em pontos do tempo designados-exatamente antes da administração de fármaco, exatamente antes da administração de glicose, e 15, 30, 60 e 90 min após a administração de glicose.
[00124] Efeitos de administração única dos agentes individuais sobre a curva de mudança de glicose sanguínea em um teste de tolerância à glicose oral (OGTT) foram identificados por porcentagem de inibição (%) e ED30. Os valores de porcentagem de inibição para cada tratamento foram gerados a partir dos dados de área sob a curva (AUC) normalizados aos controles não desafiados com glicose por AUC de glicose sanguínea subtraída de controles não desafiados com glicose de grupos desafiados com glicose, e comparando 0 valor com aquele de um grupo controle em que glicose foi administrada. Em geral, é sugerido que uma dose eficaz seja definida como uma dose para suprimir a AUC em 30% ou mais em experimentos de camundongo (W02006/076231 A2). O valor de ED30 refere-se a uma dose na qual 30% da porcentagem de inibição são exibidos, e foi calculado usando- se uma análise de regressão linear no terceiro intervalo de dose no presente exemplo.
[00125] Como um resultado, foi identificado que a ED30 de um composto preparado no exemplo de preparação 1 da presente invenção foi 0,20 mg/kg e a ED30 de metformina foi 29,6 mg/kg (Tabela 1, Tabela 2). Tabela 1 Resultados de tolerância á glicose de um composto preparado no exemplo de preparação 1 Tabela 1 Tabela 2 Resultados de tolerância à glicose de metformina Tabela 2
[00126] Efeitos sinergísticos exequíveis de uma composição em cada relação fixa foram analisados por isobolograma (R. J. Tallarida et al., Life Sei. 1989, 45, 947). Este processo inclui a decisão de uma dose da mistura, na qual a porcentagem de inibição de 30% é exibida (EDaomix) no experimento de OGTT e a dose correspondente (EDsoadd) esperada sob uma aditividade simples. Quando o resultado de EDsomix < EDaoadd é estabelecido em uma certa relação fixa, a mistura tem efeitos sinergísticos. EDsoadd foi calculada de ED30 de cada fármaco. Na figura 1, frações dos valores de ED30 de cada material estão presentes em cada eixo da mesma. O valor de ED30 do composto preparado no exemplo de preparação 1 somente é 0,2 mg/kg e mostrado como valor 1 na figura 1, e 0 valor de ED30 de metformina somente é 30 mg/kg e mostrado como valor 1 na figura 1. Portanto, a linha combinando os valores de ED30 dos dois fármacos individuais indica uma aditividade simples (EDsoadd) calculada de efeitos de tolerância à glicose em dife- rentes relações. Portanto, os pontos designados como A, B, C, e D na figura 1 com respeito a cada mistura estudada indicam frações de valores de ED30 (EDsomic) determinados por experimentos reais realizados nas misturas do composto preparado no exemplo de preparação 1 e metformina em relações de 9:1, 5:1, 1:1, e 1:3. Os pontos A', B', C, e D' na figura 1 indicam frações de doses (EDsoadd) correspondendo às misturas do composto preparado no exemplo de preparação 1 e metformina em relações de 9:1, 5:1, 1:1, e 1:3 esperadas sob uma aditivi- dade simples.
[00127] As relações de doses realmente administradas a animais em cada fração foram calculadas multiplicando-se 0,2 mg/kg e 30 mg/kg que são valores de ED30 do composto preparado no exemplo de preparação 1 e metformina, respectivamente com uma relação desejada. As administrações foram realizadas nas faixas de: 0,045 ~ 0,36 mg/kg do composto preparado no exemplo de preparação 1 + 0,75 ~ 6 mg/kg de metformina em uma relação de 9:1, 0,042 ~ 0,33 mg/kg do composto preparado no exemplo de preparação 1 + 1,25 ~ 10 mg/kg de metformina em uma relação de 5:1,0,025 ~ 0,2 mg/kg do composto preparado no exemplo de preparação 1 + 3,25 ~ 30 mg/kg de metformina em uma relação de 1:1, 0,0125 ~ 0,2 mg/kg do composto preparado no exemplo de preparação 1 + 5,625 ~ 45 mg/kg de metformina em uma relação de 1:3. Quando isto é aplicado a um adulto sadio (cerca de 70 kg), a dose corresponde a 0,88 ~ 25,2 mg do composto preparado no exemplo de preparação 1 e 52,5 ~ 3150 mg de metformina, e inclui uma dose clínica diária de metformina, que é 500 ~ 2000 mg.
[00128] Como um resultado de experimentos, os valores de EDsomix/EDsoadd de misturas em relações de 9:1, 5:1, 1:1, e 1:3 são 0,817, 0,437, 0,359, e 0,443, valores calculados com base em frações de cada valor de ED30 do composto preparado no exemplo de preparação 1 e metformina (Tabela 3). A partir deste resultado, EDsomix foi calculada multiplicando-se a dose real de EDsoadd correspondendo a cada relação com EDsomix/EDsoadd, e foi identificado que efeitos de melhora em tolerância à glicose sinergística foram observados devido a EDsomix < EDsoadd em todas as relações. Em particular, efeitos de melhora de 2 vezes ou mais em tolerância à glicose (EDsoadd/EDsomix) foram observados em misturas em relações de 5:1, 1:1, e 1:3. As interações de relações corretas selecionadas com base em frações de valores de ED30 de cada material são mostradas na tabela 3 e no isobolo- grama da figura 1. Tabela 3 Efeitos sinerqísticos de uma composição mista de um composto preparado no exemplo de preparação 1 e metformina Tabela 3 () indica uma posição no isobolograma na figura 1.
[00129] Além disso, a figura 2 mostra que a composição mista exibiu efeitos de melhora significantes em tolerância à glicose, comparado à porcentagem de inibição de cada material administrado sozinho.
[00130] Como um resultado, quando a relação é convertida em uma relação de doses de um composto preparado no exemplo de preparação 1 e metformina realmente administrados a animais, efeitos de melhora em tolerância à glicose foram observados sobre a ampla faixa de dose de 1:16,7 a 1:450.
[00131] A fim de examinar os efeitos sinergísticos de um composto preparado no exemplo de preparação 1 da presente invenção e complexo de metformina por administração repetida, os efeitos da administração única a camundongos obesos sobre uma curva de mudança de glicose sanguínea de OGTT e de uma administração repetida de 2 semanas sobre a porcentagem de inibição de glicose sanguínea foram avaliados. Camundongos de obesidade induzida por dieta obtidos por suprimento de camundongos experimentais (C57BL/6 camundongos) com forragem de gordura elevada (60 kcal % de gordura, Research Diets, D12492) durante 5 meses foram usados como sujeitos experimentais. Metilcelulose a 0,5% (MC) foi usada para preparar uma suspensão do composto 1 preparado no exemplo de preparação 1 com uma composição de 0,1 mg/kg e 0,15 mg/kg. MC a 0,5% foi usada para preparar uma suspensão de metformina com uma composição de 7,5 mg/kg e 15 mg/kg. 6 mL/kg do complexo foram preparados em doses de (0,1 mg/kg de um composto preparado no exemplo de preparação 1+15 mg/kg de metformina)/5 mL e (0,15 mg/kg de um composto preparado no exemplo de preparação 1 + 7,5 mg/kg de metformina)/5 mL.
[00132] Camundongos obesos foram jejuados durante 16 a 17 horas antes dos experimentos, o sangue foi coletado de veias caudais de camundongos na manhã do dia do experimento e o nível de glicose sanguínea foi medido com um medidor de glicose sanguínea ACCU- CHEK ACTIVE (Roche Diagnostics). A composição mista da presente invenção foi fornecida oralmente 30 min antes da administração de glicose (-30 min), seguido por administração oral de uma solução de glicose (2 g/kg/10 mL) após 30 min (0 min). A coleta de sangue foi feita em pontos do tempo designados-exatamente antes da administração de fármaco, exatamente antes da administração de glicose, e 15, 30, 60 e 90 min após a administração de glicose. O valor de porcentagem de inibição foi calculado calculando-se uma área sob a curva de cada grupo e comparando o valor com aquele de um grupo controle em que glicose foi administrada.
[00133] A porcentagem de inibição pela administração única de cada fármaco administrado foi mostrada na seguinte tabela 4, tabela 5, e figura 3. Tabela 4 Porcentagem de inibição de um composto preparado no exemplo de preparação 1 e metformina Tabela 4 Tabela 5 Porcentagem de inibição de uma composição mista de um composto preparado no exemplo de preparação 1 e metformina Tabela 5
[00134] Para melhora na AUC de glicose sanguínea, porcentagens de inibição de 2% e 3% foram exibidas por um composto preparado no exemplo de preparação 1 em 0,1 mg/kg e 0,15 mg/kg, enquanto porcentagens de inibição de 7% e 11% foram exibidas por metformina em 7,5 mg/kg e 15 mg/kg. Ao contrário, AUCs de glicose sanguínea de complexos de um composto preparado no exemplo de preparação 1 em 0,1 mg/kg + metformina em 15 mg/kg e um composto preparado no exemplo de preparação 1 em 0,15 mg/kg + metformina em 7,5 mg/kg foram inibidas em 19% e 28%, respectivamente. Isto indica que os efeitos sinergísticos maiores do que a soma aritmética de administrações únicas de fármacos individuais foram observados (figura 3).
[00135] A porcentagem de inibição por administração repetida 2 semanas após a administração é mostrada na tabela 6, tabela 7, e figura 4. Tabela 6 Porcentagem de inibição por administração de um composto preparado no exemplo de preparação 1 e metformina Tabela 6 Tabela 7 Porcentagem de inibição de uma composição mista de um composto preparado no exemplo de preparação 1 e metformina Tabela 7
[00136] Glicose plasmática por administração de um composto preparado no exemplo de preparação 1 em 0,1 e 0,15 mg/kg foi melhorada em 2% e 15%, comparada a um grupo controle. Metformina em 7,5 e 15 mg/kg melhorou a glicose plasmática em 13% e 14%, comparada a um nível de um grupo controle. Ao contrário, complexos de um composto preparado no exemplo de preparação 1 em 0,1 mg/kg + metformina em 15 mg/kg ou um composto preparado no exemplo de preparação 1 em 0,15 mg/kg + metformina em 7,5 mg/kg melhoraram a glicose plasmática em 21% e 31%, respectivamente. Isto indica que efeitos sinergísticos maiores do que a soma aritmética de administrações únicas de fármacos individuais foram observados (figura 4).
[00137] Como um resultado, quando a relação é convertida em uma relação de doses de um composto preparado no exemplo de preparação 1 e metformina realmente administrados a animais durante uma administração repetida, efeitos de melhora em eficácias sinergísticas foram observados sobre a ampla faixa de dose de 1:50 a 1:150.
[00138] A fim de examinar os efeitos sinergísticos de um complexo por um composto preparado no exemplo de preparação 1 da presente invenção e um agonista de PPARy sensibilizador de insulina, a porcentagem de inibição de glicose sanguínea por administração repetida do complexo a camundongos db/db como camundongos diabéticos foi avaliada. Camundongos machos de oito semanas de idade (camundongos db/db) foram usados como sujeitos experimentais. Sabe-se que rosiglitazona é um fármaco de série de TZD que tem o mesmo núcleo origem como pioglitazona que é atualmente usada na prática clí-nica e regula a glicose sanguínea através do mesmo mecanismo, e a dose na presente avaliação foi selecionada como 0,4 mg/kg em retribuição por uma relação essencial de dose clínica com base em ED30 com respeito à redução de glicose sanguínea em um experimento de camundongo diabético. A dose de um composto preparado no exemplo de preparação 1 com respeito à rosiglitazona em uma dose fixa foi selecionada em 1 mg/kg e 40 mg/kg (relação de complexo 1:0,01 ~1:0,4) em retribuição por uma relação de complexo em uma dose clínica esperada. Uma vez que a relação de complexo de 1:0,01 ou menos a 1:0,4 ou mais é um valor divergindo de uma dose clínica diária de rosiglitazona e existe preocupação em torno da possibilidade de eficácia pobre ou efeitos colaterais adversos, a relação de complexo foi limitada a 1:0,01 ~1:0,4. Metilcelulose a 0,5% (MC) foi usada em cada concentração de fármaco para preparar suspensões. Cada composto foi pesado, e metilcelulose a 0,5% foi usada para preparar 5 mL/kg de suspensões com cada composição de (1 mg do composto preparado no exemplo de preparação 1 + 0,4 mg de rosiglitazona)/5 mL e (40 mg do composto preparado no exemplo de preparação 1 + 0,4 mg de rosiglitazona)/5 mL.
[00139] O fármaco foi oralmente fornecido a camundongos diabéti- cos e o sangue foi coletado de veias caudais dos camundongos após 1 hora da administração para medir a glicose sanguínea com um medidor de glicose sanguínea ACCU-CHEK ACTIVE (Roche Diagnostics). O valor de porcentagem de inibição com respeito à glicose sanguínea foi calculado por comparação com um grupo controle.
[00140] Resultados experimentais a cerca da porcentagem de inibição de glicose sanguínea em comparação com um grupo controle por administração do fármaco durante 7 dias são mostrados na seguinte tabela 8, tabela 9, e Figura 5. Tabela 8 Porcentagem de inibição durante administração de um composto preparado no exemplo de preparação 1 e rosiqlitazona Tabela 8 Tabela 9 Porcentagem de inibição durante administração de uma composição mista de um composto preparado no exemplo de preparação 1 e rosiqlitazona Tabela 9
[00141] As porcentagens de inibição de glicose sanguínea por administração de um composto preparado no exemplo de preparação 1 em 1 mg/kg e 40 mg/kg comparado a um grupo controle foram calculadas como 21% e 11%, respectivamente, e melhora de 10% foi feita por administração de um agonista de PPARy rosiglitazona em 0,4 mg/kg. Além disso, melhoras em complexos de um composto preparado no exemplo de preparação 1 em 1 mg/kg + rosiglitazona em 0,4 mg/kg ou um composto preparado no exemplo de preparação 1 em 40 mg/kg + rosiglitazona em 0,4 mg/kg foram calculadas como 49% e 79%, respectivamente. Isto indica que efeitos sinergísticos maiores do que a soma aritmética de administrações únicas de fármacos individuais foram observados (figura 5).
[00142] Como um resultado, quando a relação é convertida em uma relação de doses de um composto preparado no exemplo de preparação 1 e um agonista de PPARy rosiglitazona realmente administrados a camundongos diabéticos, efeitos de melhora em eficácias sinergísti- cas foram observados sobre a faixa de dose de 1:0,01 a 1:0,4.
[00143] A fim de examinar os efeitos sinergísticos de um complexo de um composto preparado no exemplo de preparação 1 da presente invenção e um fármaco de série de sulfonil ureia secretagogo de insulina, as porcentagens de inibição de curvas de mudança de glicose sanguínea de OGTT de administração única por materiais individuais e complexos foram avaliadas. Camundongos experimentais machos de 8 semanas de idade (C57BL/6 camundongos) foram usados e jejuados durante 16 a 17 horas antes dos experimentos. O sangue foi coletado de veias caudais de camundongos na manhã do dia do experimento e o nível de glicose sanguínea foi medido com um medidor de glicose sanguínea ACCU-CHEK ACTIVE (Roche Diagnostics). A composição mista da presente invenção foi fornecida oralmente 30 min antes da administração de glicose (-30 min), seguido por administração oral de uma solução de glicose (2 g/kg/10 mL) após 30 min (0 min). A coleta de sangue foi feita em pontos do tempo designados-exatamente antes da administração de fármaco, exatamente antes da administração de glicose, e 15, 30, 60 e 90 min após a administração de glicose. O valor de porcentagem de inibição foi calculado calculando-se uma área sob a curva de cada grupo, exceto para um grupo em que glicose não foi administrada, e comparando o valor com aquele de um grupo controle em que glicose foi administrada. A fim de avaliar os efeitos sinergísticos ou aditivos por complexo na presente avaliação, metilcelulose a 0,5% (MC) foi usada para preparar uma suspensão com a dose de um composto preparado no exemplo de preparação 1 em 0,1 mg/kg, e MC a 0,5% foi também usada para preparar uma suspensão com uma composição de um fármaco de série de sulfonil ureia secretagogo de insulina e glimepirida em 0,02 mg/kg e 0,32 mg/kg de modo que uma relação de complexo possa ser incluída em uma dose clínica esperada em um estado fixo de um composto preparado no exemplo de preparação 1. Glimepirida é um fármaco que promove a secreção de insulina do pâncreas com o mesmo mecanismo como glipizida, glibenclami- da, e similares. Um complexo do mesmo foi preparado em 10 mL por kg pesando-se compostos individuais e misturando os compostos com cada composição ((um composto preparado no exemplo de preparação 1 0,1 mg + glimepirida 0,02 mg)/10 mL e (um composto preparado no exemplo de preparação 1 0,1 mg + glimepirida 0,32 mg)/10 mL)). Quando a relação de mistura é 1:0,2 ou menos, ou 1:3,2 ou mais, eficácia pobre ou efeitos colaterais adversos podem ocorrer. Desse modo, a relação de mistura de um composto preparado no exemplo de preparação 1 e glimepirida foi fixada em 1:0,2~ 1:3,2.
[00144] Resultados experimentais da porcentagem de inibição de glicose sanguínea em comparação com um grupo controle em experimentos são mostrados na seguinte tabela 10, tabela 11, e figura 6. Tabela 10 Porcentagem de inibição por administração de um composto preparado no exemplo de preparação 1 e qlimepirida Tabela 10 Tabela 11 Porcentagem de inibição por administração de uma composição mista de um composto preparado no exemplo de preparação 1 e Qlimepirida Tabela 11
[00145] Como um resultado do experimento, 7,7% de porcentagem de inibição foram exibidos no caso de um composto 1 preparado no exemplo de preparação 1 em 0,1 mg/kg em comparação com um grupo controle. Quando glimepirida foi usada em 0,02 mg/kg e 0,32 mg/kg, a porcentagem de inibição de glicose sanguínea foi calculada em -3,69% e 10,9%, respectivamente, comparada a um grupo controle. Além disso, quando complexos de um composto preparado no exemplo de preparação 1 em 0,1 mg/kg + glimepirida em 0,02 mg/kg e um composto preparado no exemplo de preparação 1 em 0,1 mg/kg + glimepirida em 0,32 mg/kg foram usados, a porcentagem de inibição foi calculada como 20,2% e 48,7%, respectivamente. Isto indica que efeitos sinergísticos maiores do que a soma aritmética de administrações únicas de fármacos individuais foram observados (figura 6).
[00146] Em resumo, melhoras em efeitos sinergísticos foram observadas sobre a relação de dose de 1:0,2 a 1:3,2 de um composto preparado no exemplo de preparação 1 e glimepirida.
[00147] A fim de examinar os efeitos sinergísticos de um composto preparado no exemplo de preparação 1 da presente invenção e um fármaco de série de inibidor de a-glicosidase complexando-se fármacos, a porcentagem de inibição em uma curva de mudança de glicose sanguínea de teste de tolerância à sacarose oral de administração única por materiais individuais e um complexo dos mesmos foi avaliada. Camundongos experimentais machos de 8 semanas de idade (C57BL/6 camundongos) foram usados como sujeitos experimentais. Os camundongos foram jejuados durante 16 a 17 horas antes dos experimentos. O sangue foi coletado de veias caudais de camundongos na manhã do dia do experimento e o nível de glicose sanguínea foi medido com um medidor de glicose sanguínea ACCU-CHEK ACTIVE (Roche Diagnostics). A composição farmaceuticamente mista da presente invenção foi fornecida oralmente 30 min antes da administração de sacarose (-30 min), seguido por administração oral de uma solução de glicose (2 g/kg/10 mL) após 30 min (0 min). A coleta de sangue foi feita em pontos do tempo designados-exatamente antes da adminis- tração de fármaco, exatamente antes da administração de sacarose, e 15, 30, 60, 90, e 120 min após a administração de sacarose. O valor de porcentagem de inibição foi calculado calculando-se uma área sob a curva de cada grupo, exceto para um grupo em que sacarose não foi administrada, e comparando o valor com aquele de um grupo controle em que sacarose foi administrada. A fim de avaliar os efeitos sinergísticos ou aditivos por complexos na presente avaliação, metilcelulose a 0,5% (MC) foi usada para preparar uma suspensão com um composto preparado no exemplo de preparação 1 em uma dose de 0,3 mg/kg, e MC a 0,5% foi também usada para preparar uma suspensão com uma composição de um inibidor de a-glicosidase e voglibose em 0,009 mg/kg e 0,054 mg/kg (relação de complexo 1:0,03~1:0,18) de modo que uma relação de complexo possa ser incluída em uma dose clínica esperada em um estado onde uma dose de um composto preparado no exemplo de preparação 1 foi fixada. Voglibose é um fármaco com o mesmo mecanismo como acarbose, e fármacos individuais foram pesados para ter uma composição ((um composto preparado no exemplo de preparação 1 0,3 mg + voglibose 0,009 mg)/10 mL e (um composto preparado no exemplo de preparação 1 0,3 mg + voglibose 0,054 mg)/10 mL e preparar 10 mL por kg de uma suspensão. Quando a relação de mistura é 1:0,03 ou menos, ou 1:0,18 ou mais, eficácia pobre ou efeitos colaterais adversos podem ocorrer. Desse modo, a relação de mistura foi fixada em 1:0,03~1:0,18.
[00148] Resultados experimentais da porcentagem de inibição de glicose sanguínea em comparação com um grupo controle em experimentos são mostrados na tabela 12, tabela 13, e figura 7. Tabela 12 Porcentagem de inibição durante administração de um composto preparado no exemplo de preparação 1 e voglibose Tabela 12 Tabela 13 Porcentagem de inibição durante administração de uma composição mista de um composto preparado no exemplo de preparação 1 e voglibose Tabela 13
[00149] Como um resultado do experimento, 12% de porcentagem de inibição foram exibidos no caso de um composto 1 preparado no exemplo de preparação 1 em 0,3 mg/kg em comparação com um grupo controle. Quando voglibose foi usada em 0,009 mg/kg e 0,054 mg/kg, a porcentagem de inibição de glicose sanguínea foi calculada em 1% e 53%, respectivamente, comparada a um grupo controle. Além disso, quando complexos de um composto preparado no exemplo de preparação 1 em 0,3 mg/kg + voglibose em 0,009 mg/kg e um composto preparado no exemplo de preparação 1 em 0,3 mg/kg + voglibose em 0,054 mg/kg foram usados, a porcentagem de inibição foi calculada como 25% e 65,7%, respectivamente. Isto indica que efeitos sinergísticos ou aditivos maiores do que a soma aritmética de administrações únicas de fármacos individuais foram observados (figura 7).
[00150] Em resumo, melhoras em efeitos sinergísticos ou aditivos foram observadas sobre a ampla relação de dose de 1:0,03 a 1:0,18 de um composto preparado no exemplo de preparação 1 e voglibose.
[00151] A fim de examinar os efeitos sinergísticos por administração repetida de um composto preparado no exemplo de preparação 1 e antagonista de receptor canabinoide do tipo 1, efeitos de administração de 4 semanas a camundongos obesos sobre uma curva de mudança de glicose sanguínea de OGTT e sobre a massa de gordura foram avaliados. Camundongos de obesidade induzida por dieta obtidos por suprimento de camundongos experimentais (C57BL/6 camundongos) com forragem de gordura elevada (60 kcal % de gordura, Research Diets, D12492) durante 5 meses foram usados como sujeitos experimentais. Metilcelulose a 0,5% (MC) foi usada para preparar uma suspensão do composto 1 preparado no exemplo de preparação 1 com uma composição de 0,3 mg/kg que é suposta ser uma dose de eficácia efetiva mínima e 3 mg/kg. MC a 0,5% foi usada para preparar uma suspensão de rimonabanto, um antagonista de receptor canabinoide do tipo 1 com uma composição de 3 mg/kg. Rimonabanto tem a mesma estrutura de núcleo origem como um antagonista de receptor canabinoide do tipo 1, tais como Otenabante, Ibinabante, e Surinaban- te, e 5 mL/kg do complexo do mesmo foram preparados em doses de (0,3 mg de um composto preparado no exemplo de preparação 1 + 3 mg de rimonabanto)/5 mL e (3 mg de um composto preparado no exemplo de preparação 1 + 3 mg/kg de rimonabanto)/5 mL. Quando a relação de mistura é 1:0,1 ou menos, ou 1:1 ou mais, a dose pode exceder uma dose clínica diária de rimonabanto ou eficácia pobre pode ocorrer. Desse modo, a relação de mistura foi fixada em 1:1 ~1:10.
[00152] Camundongos obesos foram jejuados durante 16 a 17 horas antes dos experimentos, o sangue foi coletado de veias caudais de camundongos na manhã do dia do experimento e o nível de glicose sanguínea foi medido com um medidor de glicose sanguínea ACCU- CHEK ACTIVE (Roche Diagnostics). A composição farmaceuticamente mista da presente invenção foi fornecida oralmente 30 min antes da administração de glicose (-30 min), seguido por administração oral de uma solução de glicose (2 g/kg/10 mL) após 30 min (0 min). A coleta de sangue foi feita em pontos do tempo designados-exatamente antes da administração de fármaco, exatamente antes da administração de glicose, e 15, 30, 60, 90, e 120 min após a administração de glicose. O valor de porcentagem de inibição foi calculado calculando-se uma área sob a curva de cada grupo e comparando o valor com aquele de um grupo controle em que glicose foi administrada.
[00153] Resultados experimentais da porcentagem de inibição de glicose sanguínea em comparação com um grupo controle em experimentos são mostrados na tabela 14, tabela 15, e figura 8. Tabela 14 Porcentagem de inibição de um composto preparado no exemplo de preparação 1 e rimonabanto por administração Tabela 14 Tabela 15 Porcentagem de inibição de uma composição mista de um composto preparado no exemplo de preparação 1 e rimonabanto por administração Tabela 15
[00154] A AUC sanguínea por 0,3 mg/kg e 3 mg/kg de um composto preparado no exemplo de preparação 1 foi inibida em 18,2% e 35,3% comparada a um grupo controle. A AUC sanguínea por 3 mg/kg de rimonabanto foi inibida em 1,1%, comparada a um grupo controle. Ao contrário, a AUC sanguínea por 0,3 mg/kg de um composto preparado no exemplo de preparação 1 + 3 mg/kg de rimonabanto ou 3 mg/kg de um composto preparado no exemplo de preparação 1 + 3 mg/kg de rimonabanto foi inibida em 32,8% e 30,7%, respectivamente. Desse modo, os efeitos sinergísticos ou aditivos foram observados (figura 8).
[00155] Experimentos foram realizados no sujeito experimental e fármaco experimental da mesma maneira como no exemplo experimental 5-1, a massa de gordura foi calculada como uma soma de gordura epididimal e gordura retroperitoneal, e a massa de gordura 4 semanas após a administração foi medida.
[00156] Os resultados são mostrados nas seguintes tabelas 16 e 17. Tabela 16 Efeitos de um composto preparado no exemplo de preparação 1 e rimonabanto sobre a redução de massa de gordura Tabela 16 *P>0,05 vs. grupo controle HF-DIO Tabela 17 Efeitos de um composto preparado no exemplo de preparação 1 e rimonabanto sobre a redução de massa de gordura Tabela 17 *P>0,05 vs. grupo controle HF-DIO
[00157] Após 4 semanas de administração, a massa de gordura por administração de um composto preparado no exemplo de preparação 1 em 0,3 mg/kg ou 3 mg/kg foi reduzida em -1,65% e 8,71%, respectivamente, enquanto a massa de gordura por administração de um antagonista de receptor canabinoide do tipo 1 em 3 mg/kg foi reduzida em 41,5%. Além disso, a massa de gordura por administração de um composto preparado no exemplo de preparação 1 em 0,3 mg/kg + um antagonista de receptor canabinoide do tipo 1 em 3 mg/kg ou um composto preparado no exemplo de preparação 1 em 3 mg/kg + um antagonista de receptor canabinoide do tipo 1 em 3 mg/kg foi reduzida em 42,1% e 51,2%, respectivamente. Desse modo, efeitos aditivos foram observados.
[00158] Consequentemente, efeitos de eficácia sinergísticos ou aditivos de melhora de um composto preparado no exemplo de preparação 1 e um antagonista de receptor canabinoide do tipo 1 foram observados sobre camundongos obesos sobre a relação de dose de 1:1 a 1:10.
[00160] Os ingredientes acima são misturados e carregados em uma bolsa hermética para preparar uma formulação em pó.
[00162] sados de Estearato de magnésio Os ingredientes acima são misturados e em seguida pren- convencional para preparar uma formulação de comprimido.
[00164] Os ingredientes acima foram misturados, e em seguida selados em uma cápsula de gelatina de acordo com um método de preparação convencional para preparar uma formulação de cápsula.
[00166] Após dissolver o derivado de 7a-aminoesteroide de fórmula 1 em cloreto de sódio BP para injeção tendo um volume apropriado, o pH da solução formada foi ajustado para pH 3,5 com ácido clorídrico diluído BP. O volume da solução foi controlado com cloreto de sódio BP para injeção, e em seguida suficientemente misturado. Após carregar a solução em uma ampola tipo I de 5 ml feita de vidro transparente, a ampola foi selada fundindo-se a parte vazia superior da ampola, e esterilizada durante mais do que 15 minutos a 120°C em uma autoclave para preparar uma solução de injeção.
[00167] Embora as modalidades preferidas da presente invenção tenham sido descritas para propósitos ilustrativos, aqueles versados na técnica apreciarão que várias modificações, adições e substituições são possíveis, sem afastar-se do escopo e espírito da invenção como descrito nas reivindicações acompanhantes.
Claims (22)
1. Composição farmacêutica para a prevenção e tratamento de diabetes ou obesidade, caracterizada pelo fato de que compreende como ingredientes ativos: (1) um composto representado pela seguinte fórmula 1 ou um sal farmaceuticamente aceitável do mesmo, e (2) um ou mais outros agentes antidiabéticos ou antiobesidade, em que os outros agentes antidiabéticos ou antiobesidade são selecionados do grupo consistindo em Biguanidas, sensibilizadores de insulina, secretagogos de insulina, inibidores de a- glucosidase e antagonistas do receptor canabinoide do tipo 1,<Fórmula 1> (onde, X é OR1, SR1, ou NR1R2, em que R1 e R2 são independentemente uma Ci~Cs alquila inferior, ou R1 e R2 de NR1R2 podem formar um anel de 5 membros a 7 membros contendo um elemento hetero de O).
2. Composição de acordo com reivindicação 1, caracterizada pelo fato de que o composto representado pela fórmula 1 é selecionado do grupo consistindo em: 1) (R)-4-[(R)-3-amino-4-(2,4,5-trifluorofenil)butanoil]-3-(t- butoxi meti I) pi perazi n-2-ona; 2) (S)-4-[(R)-3-amino-4-(2,4,5-trifluorofenil)butanoil]-3-(t- butoxi meti I) pi perazi n-2-ona; 3) (R)-4-[(R)-3-amino-4-(2,4,5-trifluorofenil)butanoil]-3- (metoximetil)piperazin-2-ona; 4) (R)-4-[(R)-3-amino-4-(2,4,5-trifluorofenil)butanoil]-3- (isopropoximetil)piperazin-2-ona; 5) (R)-4-[(R)-3-amino-4-(2,4,5-trifluorofenil)butanoil]-3- (ciclopentiloximetil)piperazin-2-ona; 6) (R)-4-[(R)-3-amino-4-(2,4,5-trifluorofenil)butanoil]-3- [(dietilamino)metil]piperazin-2-ona; 7) (R)-4-[(R)-3-amino-4-(2,4,5-trifluorofenil)butanoil]-3- [(etilmetilamino)metil]piperazin-2-ona; 8) (R)-4-[(R)-3-amino-4-(2,4,5-trifluorofenil)butanoil]-3- (morfolinometil)piperazin-2-ona; e 9) (R)-4-[(R)-3-amino-4-(2,4,5-trifluorofenil)butanoil]-3-(t- butiltiometil)piperazin-2-ona.
3. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que o sal farmaceuticamente aceitável é selecionado do grupo consistindo em ácido acético, ácido benzenossulfônico, ácido benzoico, ácido canforsulfônico, ácido cítrico, ácido etanossulfônico, ácido fumárico, ácido glucônico, ácido glutâmico, ácido bromídrico, ácido clorídrico, ácido isetiônico, ácido láctico, ácido maleico, ácido málico, ácido mandélico, ácido metanossulfônico, ácido múcico, ácido nítrico, ácido pamoico, ácido pantotênico, ácido fosfórico, ácido succínico, ácido sulfúrico, ácido tartárico, ácido p-tolueno sulfônico, e ácido adípico.
4. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que o composto representado pela seguinte fórmula 1 ou o sal farmaceuticamente aceitável do mesmo é um inibidor de Dipeptidil Peptidase-IV (DPP-IV).
5. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que os outros agentes antidiabéticos ou antiobesidade são Biguanidas.
6. Composição de acordo com a reivindicação 5, caracterizada pelo fato de que a Biguanida é metformina, buformina ou fenformina.
7. Composição de acordo com a reivindicação 5, caracterizada pelo fato de que compreende 16,7 a 450 partes por peso da Biguanida com base em 1 parte por peso do composto 1 representado pela fórmula 1.
8. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que os outros agentes antidiabéticos ou antiobesidade são sensibilizadores de insulina.
9. Composição de acordo com a reivindicação 8, caracterizada pelo fato de que o sensibilizador de insulina tem uma estrutura de tiazolidin-diona (TZD).
10. Composição de acordo com a reivindicação 8, caracterizada pelo fato de que o sensibilizador de insulina é selecionado do grupo consistindo em troglitazona, ciglitazona, rosiglitazona, pioglitazona e englitazona.
11. Composição de acordo com a reivindicação 8, caracterizada pelo fato de que a composição farmacêutica compreende 0,01 a 0,4 partes por peso do sensibilizador de insulina com base em 1 parte por peso do composto representado pela fórmula 1.
12. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que os outros agentes antidiabéticos ou antiobesidade são secretagogos de insulina.
13. Composição de acordo com a reivindicação 12, caracterizada pelo fato de que o secretagogo de insulina é selecionado do grupo consistindo em glibenclamida (gliburida), glipizida, gliclazida, glimepirida, tolazamida, tolbutamida, acetoexamida, carbutamida, clorpropamida, glibornurida, gliquidona, glisentida, glisolamida, glisoxepida, gliclopiamida, glicilamida, glipentida, repaglinida e nateglinida.
14. Composição de acordo com a reivindicação 12, caracterizada pelo fato de que compreende 0,2 a 3,2 partes por peso do secretagogo de insulina com base em 1 parte por peso do composto representado pela fórmula 1.
15. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que os outros agentes antidiabéticos ou antiobesidade são inibidores de alfa-glicosidase.
16. Composição de acordo com a reivindicação 15, caracterizada pelo fato de que o inibidor de alfa-glicosidase é selecionado do grupo consistindo em acarbose, voglibose, emiglitato e miglitol.
17. Composição de acordo com a reivindicação 15, caracterizada pelo fato de que compreende 0,03 a 0,18 partes por peso do inibidor de alfa-glicosidase com base em 1 parte por peso do composto representado pela fórmula 1.
18. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que os outros agentes antidiabéticos ou antiobesidade são antagonistas do receptor canabinoide do tipo 1.
19. Composição de acordo com a reivindicação 18, caracterizada pelo fato de que o antagonista do receptor canabinoide do tipo 1 é selecionado do grupo consistindo em Rimonabanto, Otenabante, Ibinabante e Surinabante.
20. Composição de acordo com a reivindicação 18, caracterizada pelo fato de que compreende 1 a 10 partes por peso do antagonista do receptor canabinoide do tipo 1 com base em 1 parte por peso do composto representado pela fórmula 1.
21. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que o composto representado pela seguinte fórmula 1 ou o sal farmaceuticamente aceitável do mesmo e os outros agentes antidiabéticos ou antiobesidade são pré-misturados para formulação ou separadamente formulados.
22. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que a composição farmacêutica é formulada para ser oralmente administrada.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR10-2008-0101932 | 2008-10-17 | ||
| KR1020080101932A KR101054911B1 (ko) | 2008-10-17 | 2008-10-17 | 디펩티딜펩티다아제-ⅳ의 활성을 저해하는 화합물 및 다른 항당뇨 또는 항비만 약물을 유효성분으로 함유하는 당뇨 또는 비만의 예방 및 치료용 약학적 조성물 |
| PCT/KR2009/005970 WO2010044637A2 (ko) | 2008-10-17 | 2009-10-16 | 디펩티딜펩티다아제-ⅳ의 활성을 저해하는 화합물 및 다른 항당뇨 또는 항비만 약물을 유효성분으로 함유하는 당뇨 또는 비만의 예방 및 치료용 약학적 조성물 |
Publications (4)
| Publication Number | Publication Date |
|---|---|
| BRPI0920351A2 BRPI0920351A2 (pt) | 2016-03-08 |
| BRPI0920351A8 BRPI0920351A8 (pt) | 2016-10-04 |
| BRPI0920351B1 true BRPI0920351B1 (pt) | 2020-09-29 |
| BRPI0920351B8 BRPI0920351B8 (pt) | 2021-05-25 |
Family
ID=42107077
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0920351A BRPI0920351B8 (pt) | 2008-10-17 | 2009-10-16 | composição farmacêutica para prevenção e tratamento de diabetes ou obesidade |
Country Status (17)
| Country | Link |
|---|---|
| US (1) | US8440669B2 (pt) |
| EP (1) | EP2351567B1 (pt) |
| JP (1) | JP5364168B2 (pt) |
| KR (1) | KR101054911B1 (pt) |
| CN (1) | CN102256605B (pt) |
| AU (1) | AU2009304028B2 (pt) |
| BR (1) | BRPI0920351B8 (pt) |
| CA (1) | CA2740570C (pt) |
| ES (1) | ES2656812T3 (pt) |
| HU (1) | HUE036475T2 (pt) |
| IL (1) | IL212330A (pt) |
| MX (1) | MX2011004064A (pt) |
| NZ (1) | NZ592567A (pt) |
| PT (1) | PT2351567T (pt) |
| RU (1) | RU2466727C1 (pt) |
| TR (1) | TR201802120T4 (pt) |
| WO (1) | WO2010044637A2 (pt) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103848825B (zh) * | 2012-12-03 | 2017-01-25 | 中国药科大学 | 具有α‑葡萄糖苷酶抑制活性的锍糖类天然产物及其衍生物的制备方法及用途 |
| BR112015032410B8 (pt) * | 2013-06-26 | 2021-10-26 | Dong A St Co Ltd | Uso de uma composição farmacêutica compreendendo inibidores de dpp-iv no preparo de um medicamento para prevenção ou tratamento de doenças renais |
| CN103599540B (zh) * | 2013-11-15 | 2016-09-14 | 深圳奥萨医药有限公司 | 含有格列奈类药物和b族维生素的药物组合物及其用途 |
| CN115109161B (zh) * | 2022-06-28 | 2023-08-11 | 广东赛尔生物科技有限公司 | 含有间充质干细胞的减肥药物组合物 |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE19823831A1 (de) | 1998-05-28 | 1999-12-02 | Probiodrug Ges Fuer Arzneim | Neue pharmazeutische Verwendung von Isoleucyl Thiazolidid und seinen Salzen |
| GB0014969D0 (en) * | 2000-06-19 | 2000-08-09 | Smithkline Beecham Plc | Novel method of treatment |
| UA74912C2 (en) * | 2001-07-06 | 2006-02-15 | Merck & Co Inc | Beta-aminotetrahydroimidazo-(1,2-a)-pyrazines and tetratriazolo-(4,3-a)-pyrazines as inhibitors of dipeptylpeptidase for the treatment or prevention of diabetes |
| US7262207B2 (en) * | 2002-09-19 | 2007-08-28 | Abbott Laboratories | Pharmaceutical compositions as inhibitors of dipeptidyl peptidase-IV (DPP-IV) |
| KR20050067418A (ko) * | 2002-10-18 | 2005-07-01 | 머크 앤드 캄파니 인코포레이티드 | 당뇨병을 치료 또는 예방하기 위한 베타-아미노헤테로사이클릭 디펩티딜 펩티다제 억제제 |
| EP1572196B1 (en) | 2002-12-10 | 2008-08-13 | Novartis AG | Combination of a dpp-iv inhibitor and a ppar-alpha compound |
| US7205409B2 (en) * | 2003-09-04 | 2007-04-17 | Abbott Laboratories | Pharmaceutical compositions as inhibitors of dipeptidyl peptidase-IV (DPP-IV) |
| KR20070038462A (ko) | 2004-05-12 | 2007-04-10 | 퓨전원 인코포레이티드 | 향상된 접속 인식 시스템 |
| DOP2006000008A (es) | 2005-01-10 | 2006-08-31 | Arena Pharm Inc | Terapia combinada para el tratamiento de la diabetes y afecciones relacionadas y para el tratamiento de afecciones que mejoran mediante un incremento de la concentración sanguínea de glp-1 |
| WO2006119260A2 (en) | 2005-05-02 | 2006-11-09 | Merck & Co., Inc. | Combination of dipeptidyl peptidase-iv inhibitor and a cannabinoid cb1 receptor antagonist for the treatment of diabetes and obesity |
| GT200600218A (es) | 2005-06-10 | 2007-03-28 | Formulación y proceso de compresión directa | |
| JP2007024960A (ja) | 2005-07-12 | 2007-02-01 | Internatl Business Mach Corp <Ibm> | システム、プログラムおよび制御方法 |
| AU2006297444B2 (en) | 2005-09-29 | 2010-08-12 | Novartis Ag | Formulation comprising metformin and vildagli ptin |
| US8414921B2 (en) | 2005-12-16 | 2013-04-09 | Merck Sharp & Dohme Corp. | Pharmaceutical compositions of combinations of dipeptidyl peptidase-4 inhibitors with metformin |
| NZ569661A (en) | 2005-12-28 | 2011-06-30 | Takeda Pharmaceutical | Therapeutic agent for diabetes |
| JP2008031064A (ja) * | 2006-07-27 | 2008-02-14 | Astellas Pharma Inc | ジアシルピペラジン誘導体 |
| CN101663282B (zh) * | 2007-04-19 | 2012-02-15 | 东亚制药株式会社 | 包含β-氨基的DPP-Ⅳ抑制剂及其制备方法以及用于预防和治疗糖尿病或肥胖症的含有所述抑制剂的药物组合物 |
-
2008
- 2008-10-17 KR KR1020080101932A patent/KR101054911B1/ko active Active
-
2009
- 2009-10-16 NZ NZ592567A patent/NZ592567A/xx unknown
- 2009-10-16 WO PCT/KR2009/005970 patent/WO2010044637A2/ko not_active Ceased
- 2009-10-16 ES ES09820787.1T patent/ES2656812T3/es active Active
- 2009-10-16 EP EP09820787.1A patent/EP2351567B1/en active Active
- 2009-10-16 BR BRPI0920351A patent/BRPI0920351B8/pt active IP Right Grant
- 2009-10-16 TR TR2018/02120T patent/TR201802120T4/en unknown
- 2009-10-16 AU AU2009304028A patent/AU2009304028B2/en active Active
- 2009-10-16 HU HUE09820787A patent/HUE036475T2/hu unknown
- 2009-10-16 CA CA2740570A patent/CA2740570C/en active Active
- 2009-10-16 PT PT98207871T patent/PT2351567T/pt unknown
- 2009-10-16 RU RU2011119616/15A patent/RU2466727C1/ru active
- 2009-10-16 US US13/124,150 patent/US8440669B2/en active Active
- 2009-10-16 MX MX2011004064A patent/MX2011004064A/es active IP Right Grant
- 2009-10-16 JP JP2011532021A patent/JP5364168B2/ja active Active
- 2009-10-16 CN CN200980151387.8A patent/CN102256605B/zh active Active
-
2011
- 2011-04-14 IL IL212330A patent/IL212330A/en active IP Right Grant
Also Published As
| Publication number | Publication date |
|---|---|
| HK1160031A1 (en) | 2012-08-10 |
| EP2351567A4 (en) | 2013-12-04 |
| ES2656812T3 (es) | 2018-02-28 |
| EP2351567A2 (en) | 2011-08-03 |
| RU2466727C1 (ru) | 2012-11-20 |
| US8440669B2 (en) | 2013-05-14 |
| CN102256605B (zh) | 2014-05-07 |
| US20110201624A1 (en) | 2011-08-18 |
| KR101054911B1 (ko) | 2011-08-05 |
| BRPI0920351B8 (pt) | 2021-05-25 |
| AU2009304028A1 (en) | 2010-04-22 |
| PT2351567T (pt) | 2018-02-12 |
| CA2740570C (en) | 2015-02-03 |
| IL212330A0 (en) | 2011-06-30 |
| WO2010044637A2 (ko) | 2010-04-22 |
| NZ592567A (en) | 2012-08-31 |
| HUE036475T2 (hu) | 2018-07-30 |
| MX2011004064A (es) | 2011-05-10 |
| IL212330A (en) | 2015-11-30 |
| CA2740570A1 (en) | 2010-04-22 |
| WO2010044637A9 (ko) | 2010-10-07 |
| JP2012505876A (ja) | 2012-03-08 |
| AU2009304028B2 (en) | 2013-05-16 |
| EP2351567B1 (en) | 2017-11-22 |
| BRPI0920351A2 (pt) | 2016-03-08 |
| KR20100042786A (ko) | 2010-04-27 |
| CN102256605A (zh) | 2011-11-23 |
| BRPI0920351A8 (pt) | 2016-10-04 |
| WO2010044637A3 (ko) | 2010-08-19 |
| TR201802120T4 (en) | 2018-03-21 |
| JP5364168B2 (ja) | 2013-12-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| TW202202139A (zh) | 以2-〔(4-{6-〔(4-氰基-2-氟苄基)氧基〕吡啶-2-基}哌啶-1-基)甲基〕-1-〔(2s)-氧雜環丁烷-2-基甲基〕-1h-苯並咪唑-6-甲酸或其藥學上的鹽治療第2型糖尿病或肥胖症或體重過重 | |
| US20160051525A1 (en) | Combination therapy for proliferative disorders | |
| KR101860120B1 (ko) | 글루코키나아제 활성화제와 병용되는 메트포르민의 용도, 및 메트포르민과 글루코키나아제 활성화제를 포함하는 조성물 | |
| IL139862A (en) | History of thiazolidine or pyroladine as effects of dipheptidyl peptides IV and pharmaceutical preparations containing them | |
| BRPI0810246B1 (pt) | Inibidor da dpp-iv incluindo o grupo beta-amino.método de preparação do mesmo e composição famacêutica contendo o mesmo para prevenção e tratamento da dibetes ou obesidade | |
| EP4244221B1 (en) | Prodrug of pyrrolidone derivatives as glucokinase activator | |
| AU2014207748B2 (en) | Combinations of a GLP1R agonist and metformin and use thereof for the treatment of type 2 diabetes and other disorders | |
| BRPI0920351B1 (pt) | Composição farmacêutica para prevenção e tratamento de diabetes ou obesidade | |
| JP2014531469A (ja) | Kv1.3カリウムチャネルの薬理学的標的化による肥満症および肥満症関連障害の治療 | |
| KR20080091366A (ko) | 트리아진 유도체 및 인슐린 분비 자극제의 조합물 | |
| EP1752146A1 (en) | Therapeutic agent for diabetes | |
| WO2010050422A1 (ja) | 糖尿病治療剤 | |
| EP3833354B1 (en) | Tissue transglutaminase modulators for medicinal use | |
| JP2016034930A (ja) | 血糖値低減剤 | |
| JP2023505948A (ja) | 抗精神病薬誘発性体重増加のミリコリラントによる治療方法 | |
| HK1160031B (en) | Pharmaceutical composition for prevention and treatment of diabetes or obesity comprising a compound that inhibits activity of dipeptidyl peptidase-iv, and other antidiabetic or antiobesity agents as active ingredients | |
| JPWO2011002012A1 (ja) | Sglt1阻害薬とインスリン抵抗性改善薬を組み合わせてなる医薬 | |
| TW592702B (en) | Pharmaceutical composition for treating diabetes | |
| WO2012133693A1 (ja) | 糖尿病治療用の組合せ医薬 | |
| ERION | QUN DANG*, PAUL D. VAN POELJE AND | |
| AU2003262286A1 (en) | Novel Effectors of Dipeptidyl Peptidase IV |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B25D | Requested change of name of applicant approved |
Owner name: DONG-A SOCIO HOLDINGS CO., LTD. (KR) |
|
| B25A | Requested transfer of rights approved |
Owner name: DONG-A ST CO., LTD. (KR) |
|
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] | ||
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 10 (DEZ) ANOS CONTADOS A PARTIR DE 29/09/2020, OBSERVADAS AS CONDICOES LEGAIS. |
|
| B16C | Correction of notification of the grant [chapter 16.3 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 16/10/2009 OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF |