BRPI0920767B1 - tiazóis substituídos por heterociclila como agentes protetores de cultura, seus usos e seus processos de preparação, composições e seu processo de preparação, e método para combate a fungos nocivos fitopatogênicos - Google Patents
tiazóis substituídos por heterociclila como agentes protetores de cultura, seus usos e seus processos de preparação, composições e seu processo de preparação, e método para combate a fungos nocivos fitopatogênicos Download PDFInfo
- Publication number
- BRPI0920767B1 BRPI0920767B1 BRPI0920767A BRPI0920767A BRPI0920767B1 BR PI0920767 B1 BRPI0920767 B1 BR PI0920767B1 BR PI0920767 A BRPI0920767 A BR PI0920767A BR PI0920767 A BRPI0920767 A BR PI0920767A BR PI0920767 B1 BRPI0920767 B1 BR PI0920767B1
- Authority
- BR
- Brazil
- Prior art keywords
- formula
- compounds
- methyl
- solvent
- reaction
- Prior art date
Links
- 0 CC#Cc1c(*)[s]c(C(*2)C=CN2C=*)n1 Chemical compound CC#Cc1c(*)[s]c(C(*2)C=CN2C=*)n1 0.000 description 4
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/72—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms
- A01N43/74—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms five-membered rings with one nitrogen atom and either one oxygen atom or one sulfur atom in positions 1,3
- A01N43/78—1,3-Thiazoles; Hydrogenated 1,3-thiazoles
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/72—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms
- A01N43/80—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms five-membered rings with one nitrogen atom and either one oxygen atom or one sulfur atom in positions 1,2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Dentistry (AREA)
- Wood Science & Technology (AREA)
- Plant Pathology (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Agronomy & Crop Science (AREA)
- General Health & Medical Sciences (AREA)
- Pest Control & Pesticides (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- Plural Heterocyclic Compounds (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Description
(54) Título: TIAZÓIS SUBSTITUÍDOS POR HETEROCICLILA COMO AGENTES PROTETORES DE CULTURA, SEUS USOS E SEUS PROCESSOS DE PREPARAÇÃO, COMPOSIÇÕES E SEU PROCESSO DE PREPARAÇÃO, E MÉTODO PARA COMBATE A FUNGOS NOCIVOS FITOPATOGÊNICOS (51) Int.CI.: C07D 417/04; C07D 417/14; A01N 43/78 (30) Prioridade Unionista: 01/10/2008 EP 08165625.8 (73) Titular(es): BAYER INTELLECTUAL PROPERTY GMBH (72) Inventor(es): NICOLA RAHN; ULRIKE WACHENDORF-NEUMANN; PIERRE CRISTAU; STEFAN HERRMANN; TOMOKI TSUCHIYA; ARND VOERSTE; JÜRGEN BENTING; PIERRE WASNAIRE; SEBASTIAN HOFFMANN
1/159
Relatório Descritivo da Patente de Invenção para TIAZÓIS SUBSTITUÍDOS POR HETEROCICLILA COMO AGENTES PROTETORES DE CULTURA, SEUS USOS E SEUS PROCESSOS DE PREPARAÇÃO, COMPOSIÇÕES E SEU PROCESSO DE PREPARAÇÃO, E MÉTODO PARA COMBATE A FUNGOS NOCIVOS FITOPATOGÊNICOS.
[001] A presente invenção se refere a tiazóis substituídos por heterociclila e a seus sais de ação agroquímica, ao seu uso e a métodos e composições para o comabte de fungos nocivos fitopatogênicos em e/ou sobre plantas ou em e/ou sobre semente de plantas, a processos para preparação de tais composições e semente tratada e também ao seu uso para o combate a fungos nocivos fitopatogênicos na agricultura, horticultura e silvicultura, em cultivo animal, na proteção de materiais e no campo doméstico e de higiene. A presente invenção, além disso, se refere a um processo de preparação de tiazóis substituídos por heterociclila.
[002] Já é conhecido que certos tiazóis substituídos por heterociclila podem ser empregados como agentes de proteção de cultura fungicidas (vide documento de patente WO 07/014290, WO 08/013925, WO 08/013622, WO 08/091594, WO 08/091580, WO 09/055514). Porém, a ação fungicida desses compostos nem sempre é suficiente, particularmente em taxas de aplicação baixas.
[003] Como as demandas ecológicas e econômicas feitas para modernos agentes de proteção de cultura vem aumentando constantemente, por exemplo com respeito a espectro de atividade, toxicidade, seletividade, taxa de aplicação, formação de resíduos e produção favorável, e além disso podem ocorrer problemas por exemplo com resistência, existe uma constante necessidade em desenvolver novos agentes de proteção de cultura, particularmente de fungicidas que, pelo menos em algumas áreas, apresentam vantagens sobre os fungiciPetição 870180002928, de 12/01/2018, pág. 6/185
2/159 das conhecidos.
[004] Surpreendentemente, verificou-se recentemente que os tiazóis substituídos por heterociclila resolvem pelo menos alguns aspectos dos objetos mencionados e são adequados para o uso como agentes de proteção de cultura particularmente como fungicidas.
[005] Alguns tiazóis substituídos por heterociclila já são conhecidos como compostos de ação farmacêutica (vide, por exemplo, EP 1832586, WO 04/058750, WO 04/058751, WO 05/003128, WO 06/032322, WO 07/104558, WO 07/115805, WO 08/083238), mas não sua surpreendente ação fungicida.
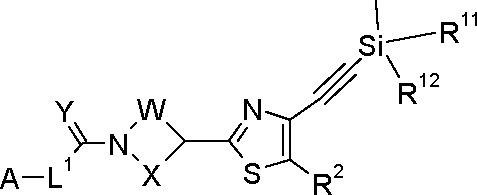
[006] A invenção prove compostos da Fórmula (I),
[007] Na qual os símbolos apresentam os seguintes significados: [008] A representa metila [009] ou [0010] A representa fenila não substituída ou substituída, [0011] sendo que os substituintes independentemente entre si são selecionados da lista abaixo [0012] ciano, nitro, halogênio, (A-Ce-alquila, CrCs-haloalquila, C3C6-cicloalquila, C3-C6-halocicloalquila, C4-C10-cicloalquilalquila, C4-C10alquilcicloalquila, C5-C10-alquilcicloalquilalquila, C2-C6-alquenila, C2-C6haloalquenila, C2-C6-alquinila, C2-C6-haloalquinila, trKCrC^alquiljsilila, benzila, fenila, hidroxila, Ci-C4-alcóxi, C1-C4-haloalcóxi, OCH2OCH3, SH, (A-CZ-alquiltio, CrCe-haloalquiltio, CHO, COOH, (C-|-C4alcóxi)carbonila, CONR6R7, CR6=NOR7, (C1-C4-alquil)carbonila, (C-|-C4haloalquil)carbonila, (Ci-C4-alquil) carbonilóxi, (C1-C4-alquil)carboniltio, C1-C4-alquilsulfinila, C1-C4-haloalquilsulfinila, C1-C4-alquilsulfonila, Cr
Petição 870180002928, de 12/01/2018, pág. 7/185
3/159
C4-haloalquilsulfonila, NR6R7, NR6COR7, SF5, SO2NR6R7, C2-C4alcoxialquila ou 1-metoxiciclopropila [0013] ou [0014] A é uma heteroarila de 5 a 6 membros não substituída ou substituída benzo-fundida, sendo que os substituintes independentemente entre si são selecionados da lista abaixo substituentes em carbono:
[0015] ciano, nitro, halogênio, C^Ce-alquila, CrCs-haloalquila, C3C6-cicloalquila, C3-C6-halocicloalquila C4-C10-cicloalquilalquila, C4-C10alquilcicloalquila, C5-C10-alquilcicloalquilalquila, C2-C6-alquenila, C2-C6haloalquenila, C2-C6-alquinila, C2-C6-haloalquinila, trKCrC^alquiQsilila, benzila, fenila, hidroxila, Ci-C4-alcóxi, CrC^haloalcóxi, OCH2OCH3, SH, CrC^alquiltio, CrCe-haloalquiltio, CHO, COOH, (Ci-C4alcóxi)carbonila, CONR6R7, CR6=NOR7, (CrC^alquiQcarbonila, (Ci-C4haloalquil)carbonila, (CrC^alquiQcarbonilóxi, (CrC^alquiQcarboniltio, CrC^alquilsulfinila, CrC^haloalquilsulfinila, CrC^alquilsulfonila, Ci-C4haloalquilsulfonila, NR6R7, NR6COR7, SF5, SO2NR6R7, C2-C4alcoxialquila ou 1-metoxiciclopropila substituente em nitrogênio:
[0016] hidroxila, NR6R7, C^Ce-alquila, CrCs-haloalquila, C3-C6cicloalquila, C3-C6-halocicloalquila, C4-C10-alquilcicloalquila, C2-C6alquenila, C2-C6-haloalquenila, C2-C6-alquinila, ou C2-C6-haloalquinila [0017] L1 representa (C(R1)2)n [0018] sendo que n = 0 a 3 [0019] R1 são idênticos ou diferentes independentemente entre si e representam hidrogênio, halogênio, C^C^alquila, CrC^haloalquila ou ciano, [0020] com a condição de que L1 pode conter no máximo dois R1 quie podem ser diferentes de hidrogênio [0021] Y representa enxofre ou oxigênio,
Petição 870180002928, de 12/01/2018, pág. 8/185
4/159 [0022] W representa uma cadeia de carbono Cr a C3- não substituída ou monossubstituída, sendo que o substituinte é selecionado do grupo consistindo em oxo, hidroxila, ciano e CrC4-alquila [0023] X representa uma cadeia de carbono Cr a C2- não substituída ou monossubstituída, sendo que o substituinte é selecionado do grupo consistindo em oxo, hidroxila, ciano e CrC4-alquila [0024] R2 representa hidrogênio, CrC2-alquila, CrC2-haloalquila ou halogênio [0025] L2 representa -C(R8)2-C(R8)2- ou -CR9=CR9- ou -C^C[0026] L3 representa uma ligação direta [0027] ou [0028] L3 representa uma cadeia de carbono Cr a C4- que pode conter até dois substituintes, sendo que os substituintes independnetemente entre são selecionados da lista abaixo:
[0029] halogênio, CrC2-alquila, CrC2-alcóxi, CrC2-haloalquila ou C3-C6-cicloalquila [0030] R3 representa metila, CrC2-haloalquila, -CH=CH2, -C^CH, ou C3-C10-cicloalquila não substituída ou monossubstituída, sendo que o substituinte é selecionado da lista abaixo:
[0031] ciano, halogênio, CrC6-alquila, CrC3-haloalquila, C3-C6cicloalquila, C2-C6-alquenila, C2-C6-haloalquenila, C2-C6-alquinila, C2C6-haloalquinila, tri(CrC2-alquil)silila, fenila, hidroxila, oxo, CrC6alcóxi, CrC6-haloalcóxi, C2-C6-alquenilóxi, C2-C6-alquinilóxi, CrC6alquiltio ou CrC6-haloalquiltio, [0032] ou [0033] R3 representa fenila não substituída ou substituída, [0034] sendo que os substituintes independentemente entre si são selecionados da lista abaixo:
[0035] ciano, nitro, halogênio, CrC6-alquila, CrC3-haloalquila, C3C6-cicloalquila, C3-C6-halocicloalquila, C4-C10-cicloalquilalquila, C4-C10Petição 870180002928, de 12/01/2018, pág. 9/185
5/159 halocicloalquilalquila, C4-C10-alquilcicloalquila, C5-C10alquilcicloalquilalquila, C4-C10-cicloalcoxialquila, C2-C6-alquenila, C2-C6haloalquenila, C3-C8-cicloalquenila, C3-C8-halocicloalquenila, C2-C6alquinila, C2-C6-haloalquinila, C2-C6-alcoxialquila, C2-C6haloalcoxialquila, C3-C8-alcoxialcoxialquila, tri(C1-C2-alquil)silila, benzila, fenila, hidroxila, CrCg-alcóxi, C2-C6-alcoxialcóxi, CrCg-haloalcóxi, C2-C6-alquenilóxi, C2-C6-haloalquenilóxi, C2-C6-alquinilóxi, C2-C6haloalquinilóxi, C3-C6-cicloalcóxi, C3-C6-cicloalquilóxi, C3-C6halocicloalcóxi, C4-C10-cicloalquilalquilóxi, NR6R7, SH, SF5, CrCgalquiltio, CrCg-haloalquiltio, C2-C6-alquilalquiltio, C3-C6-cicloalquiltio, CHO, COOH, (Ci-C6-alcóxi) carbonila, CONR6R7, CR6=NOR7, (Ci-C6alquil)carbonila, (CrCg-haloalquil) carbonila, (CrCg-alquiQcarbonilóxi, (CrCe-haloalquiQcarbonilóxi, (CrCg-alquiQcarboniltio, CrCgalquilsulfinila, CrCg-haloalquilsulfinila, CrCg-alquilsulfonila, CrCghaloalquilsulfonila, NR6COR7 ou SO2NR6R7 [0036] ou [0037] R3 representa naftila ou indenila saturada ou parcial ou totalmente insaturada [0038] que pode conter até dois substituintes, independentemente entre si são selecionados da lista abaixo:
[0039] ciano, halogênio, CrCg-alquila, CrCs-haloalquila, C3-C6cicloalquila, C2-C6-alquenila, C2-C6-haloalquenila, C2-C6-alquinila, C2C6-haloalquinila, tri(C1-C2-alquil)silila, fenila, hidroxila, CrCg-alcóxi, Cr C6-haloalcóxi, C2-C6-alquenilóxi, C2-C6-alquinilóxi, CrCg-alquiltio ou CrCg-haloalquiltio, [0040] ou [0041] R3 representa um radical heteroarila de 5 a 6 membros não substituída ou substituída, [0042] Sendo os substituintes independentemente entre si são selecionados da lista abaixo:
Petição 870180002928, de 12/01/2018, pág. 10/185
6/159 [0043] substituentes em carbono: ciano, nitro, halogênio, Ο-ι-Ο6alquila, CrCs-haloalquila, C3-C6-cicloalquila, C3-C6-halocicloalquila C4Cw-cicloalquilalquila, C4-C10-alquilcicloalquila, C5-C10alquilcicloalquilalquila, C2-C6-alquenila, C2-C6-haloalquenila, C2-C6alquinila, C2-C6-haloalquinila, tri(C1-C2-alquil)silila, benzila, fenila, hidroxila, Ci-C4-alcóxi, CrC^haloalcóxi, OCH2OCH3, SH, CrC^alquiltio, CrCe-haloalquiltio, COOH, (Ci-C4-alcóxi) carbonila, CONR6R7, (Ci-C4alquil)carbonila, (Ct-C^haloalquil) carbonila, (CrC^alquiQcarbonilóxi, (CrC^alquiQcarboniltio, CrC^alquilsulfinila, CrC^haloalquilsulfinila, CrC^alquilsulfonila, CrC^haloalquilsulfonila, NR6R7, NR6COR7, SF5, SO2NR6R7, C2-C4-alcoxialquila ou 1-metoxiciclopropila [0044] substituentes em nitrogênio: hidroxila, CrCe-alcila, 0^03haloalcila, C3-C6-cicloalcila, C3-C6-halocicloalcila, C4-C10-alcilcicloalcila, C2-C6-alquenila, C2-C6-haloalquenila, C2-C6-alcinila, C2-C6-haloalcinila ou fenila [0045] ou [0046] R3 representa heteroarila de 5 a 6 membros não substituída ou substituída benzo-fundida que pode conter até dois substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo:
[0047] substituentes em carbono: ciano, nitro, halogênio, Ο-ι-Ο6alquila, CrCs-haloalquila, C3-C6-cicloalquila, C3-C6-halocicloalquila C4C10-cicloalquilalquila, C4-C10-alquilcicloalquila, C5-C10alquilcicloalquilalquila, C2-C6-alquenila, C2-C6-haloalquenila, C2-C6alquinila, C2-C6-haloalquinila, tri(C1-C2-alquil)silila, benzila, fenila, hidroxila, Ci-C4-alcóxi, Ct-C^haloalcóxi, OCH2OCH3, SH, C^-C4alquiltio, CrCe-haloalquiltio, COOH, (Ci-C4-alcóxi) carbonila, CONR6R7, (CrC^alquiQcarbonila, (CrC^haloalquiQcarbonila, (Ci-C4alquil)carbonilóxi, (CrC^alquiQcarboniltio, C1-C4-alquilsulfinila, C^-C4haloalquilsulfinila, CrC^alquilsulfonila, CrC^haloalquilsulfonila,
Petição 870180002928, de 12/01/2018, pág. 11/185
7/159
NR6R7, NR6COR7, SF5, SO2NR6R7, C2-C4-alcoxialquila ou 1metoxiciclopropila [0048] substituentes em nitrogênio: CrCe-alquila, (Y-C3haloalquila, C3-C6-cicloalquila, C3-C6-halocicloalquila, C4-C10alquilcicloalquila, C2-C6-alquenila, C2-C6-haloalquenila, C2-C6-alquinila, C2-C6-haloalquinila ou fenila [0049] ou [0050] R3 é um radical heterociclila de 5 a 15 membros que é ligado através de um átomo de carbon e que pode conter até dois heteroátomos selecionados do grupo consistindo em nitrogênio, oxigênio e enxofre, sendo que 0 substituinte é selecionado da lista abaixo:
[0051] substituentes em carbono: ciano, halogênio, C^Ce-alquila, CrCjj-haloalquila, C3-C6-cicloalquila, C2-C6-alquenila, C2-C6haloalquenila, C2-C6-alquinila, C2-C6-haloalquinila, trKCrC^alquiQsilila, fenila, hidroxila, CrCe-alcóxi, CrCe-haloalcóxi, C2-C6-alquenilóxi, C2C6-alquinilóxi, CrCe-alquiltio ou CrCe-haloalquiltio [0052] substituentes em nitrogênio: CrCe-alquila, (Y-C3haloalquila, C3-C6-cicloalquila, C2-C6-alquenila, C2-C6-haloalquenila, C2-C6-alquinila, C2-C6-haloalquinila, trKCrC^alquiQsilila ou fenila [0053] R6, R7 independentemente entre si representam hidrogênio,
C1-C4-alquila, CrCjj-haloalquila, C3-C6-cicloalquila, [0054] R8 é idêntico ou diferente e independentemente entre si representa hidrogênio, halogênio, C1-C4-alquila, C1-C4-alcóxi, C3-C6cicloalquila ou CrCjj-haloalquila, [0055] R9 é idêntido ou diferente independentemente entre si e representa hidrogênio, C1-C4-alquila, ou C3-C6-cicloalquila, [0056] e também sais de ação agroquímica destes.
[0057] A invenção também prove 0 uso dos compostos da Fórmula (I) como fungicidas.
Petição 870180002928, de 12/01/2018, pág. 12/185
8/159 [0058] Tiazóis substituídos por heterociclila da Fórmula (I), de acordo com a invenção e também seus sais de ação agroquímica são altamente adequados para o combate de fungos nocivos fitopatogênicos. Os compostos de acordo com a invenção acima mencionados apresentam ação fungicida particularmente forte e podem ser usados tanto na proteção de cultura, no campo doméstico e de higiene e na proteção de materiais.
[0059] Os compostos da Fórmula (I) podem estar presentes tanto na forma pura como misturas de várias formas isoméricas, particularmente de estereoisômeros tais como E e Z, treo e eritro, e também isôimeros ópticos, tais como isômeros R e S ou atropisômeros, e, se apropriado, também de tautômeros. São reivindicados tanto isômeros E como isômeros Z, e o treo e eritro, e também os isômeros ópticos, misturas desses isômeros, e também as possíveis formas tautoméricas.
[0060] São preferidos compostos da Fórmula (I) na qual um ou mais dos símbolos apresentam um dos significados abaixo:
[0061] A representa metila [0062] ou [0063] A representa fenila que pode conter até dois substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo:
[0064] ciano, nitro, halogênio, CrC^alquila, CrCs-haloalquila, C3C6-cicloalquila, C2-C4-alquenila, C2-C4-alquinila, hidroxila, C1-C4-alcóxi, C1-C4-haloalcóxi, C^-C^-alquiltio, C1-C4-haloalquiltio, (C-|-C4alcóxi)carbonila, (Ct-C^-alquiljcarbonila, (C1-C4-haloalquil)carbonila, CrC^-alquilsulfinila, C1-C4-haloalquilsulfinila, CrC^-alquilsulfonila ou C1-C4-haloalquilsulfonila, [0065] ou [0066] A representa um radical heteroaromático selecionado do
Petição 870180002928, de 12/01/2018, pág. 13/185
9/159 grupo abaixo: furan-2-ila, furan-3-ila, tiofen-2-ila, tiofen-3-ila, isoxazol3-ila, isoxazol-4-ila, isoxazol-5-ila, 1 H-pirrol-1 -ila, 1 H-pirrol-2-ila, 1Hpirrol-3-ila, oxazol-2-ila, oxazol-4-ila, oxazol-5-ila, tiazol-2-ila, tiazol-4ila, tiazol-5-ila, isotiazol-3-ila, isotiazol-4-ila, isotiazol-5-ila, pirazol-1 -ila, pirazol-3-ila, pirazol-4-ila, imidazol-1-ila, imidazol-2-ila, imidazol-4-ila, 1,2,4-oxadiazol-3-ila, 1,2,4-oxadiazol-5-ila, 1,3,4-oxadiazol-2-ila, 1,2,4tiadiazol-3-ila, 1,2,4-tiadiazol-5-ila, 1,3,4-tiadiazol-2-ila, 1,2,3-triazol-1ila, 1,2,3-triazol-2-ila, 1,2,3-triazol-4-ila, 1,2,4-triazol-1-ila, 1,2,4-triazol3-ila, piridin-2-ila, piridin-3-ila, piridin-4-ila, piridazin-3-ila, piridazin-4-ila, pirimidin-2-ila, pirimidin-4-ila, pirimidin-5-ila, pirazin-2-ila, 1,3,5-triazin2-ila, 1,2,4-triazin-3-ila, 1 H-indol-1-ila, 1 H-indol-2-ila, 1 H-indol-3-ila, 1Hindol-4-ila, 1 H-indol-5-ila, 1 H-indol-6-ila, 1 H-indol-7-ila, 1Hbenzimidazol-1-ila, 1H-benzimidazol-2-ila, 1H-benzimidazol-4-ila, benzimidazol-5-ila, 1 H-indazol-1 -ila, 1H-indazol-3-ila, 1H-indazol-4-ila, 1Hindazol-5-ila, 1H-indazol-6-ila, 1H-indazol-7-ila, 2H-indazol-2-ila, 1benzofuran-2-ila, 1-benzofuran-3-ila, 1-benzofuran-4-ila, 1-benzofuran5-ila, 1-benzofuran-6-ila, 1-benzofuran-7-ila, 1-benzotiofen-2-ila, 1benzotiofen-3-ila, 1-benzotiofen-4-ila, 1-benzotiofen-5-ila, 1benzotiofen-6-ila, 1-benzotiofen-7-ila, 1,3-benzotiazol-2-ila, 1,3benzoxazol-2-ila, quinolin-2-ila, quinolin-3-ila, quinolin-4-ila, quinolin-5ila, quinolin-6-ila, quinolin-7-ila, quinolin-8-ila, isoquinolin-1 -ila, isoquinolin-3-ila, isoquinolin-4-ila, isoquinolin-5-ila, isoquinolin-6-ila, isoquinolin-7-ila ou isoquinolin-8-ila, [0067] que pode conter até dois substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo: [0068] substituentes em carbono: ciano, halogênio, C^C^alquila, CrCs-haloalquila, hidroxila, Ci-C4-alcóxi, CrC^haloalcóxi, Ci-C4alquiltio ou CrC^haloalquiltio, [0069] substituentes em nitrogênio: CrC^alquila, CrCshaloalquila, ciclopropila, C2-C4-alquenila ou C2-C4-alquinila,
Petição 870180002928, de 12/01/2018, pág. 14/185
10/159 [0070] L1 representa (C(R1)2)n [0071] sendo que n = 0 a 3 [0072] R1 é idêntico ou diferente e independentemente entre si representa hidrogênio, cloro, flúor, metila, CF3 ou ciano, [0073] com a condição de que L1 pode conter no máximo até dois R1 diferentes de hidrogênio, [0074] Y representa enxofre ou oxigênio, [0075] W representa uma cadeia de carbono Cr a C2- não substituída ou monossubstituída, sendo que o substituinte é selecionado do grupo consistindo em ciano e CrC2-alquila, [0076] X representa uma cadeia de carbono Cr a C2- não substituída ou monossubstituída, sendo que o substituinte é selecionado do grupo consistindo em ciano e CrC2-alquila, [0077] R2 representa hidrogênio, CrC2-alquila ou halogênio, [0078] L2 representa -C(R8)2-C(R8)2- ou -CR9=CR9- ou -C=C-, [0079] L3 representa uma ligação direta, [0080] ou [0081] L3 representa uma cadeia de carbono Cr a C4- que pode conter até dois substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo:
[0082] CrC2-alquila, CrC2-alcóxi, CrC2-haloalquila ou ciclopropila, [0083] R3 representa metila, CrC2-haloalquila, -CH=CH2, -C^CH, ou C3-C10-cicloalquila não substituída ou monossubstituída, sendo que o substituinte é selecionado da lista abaixo:
[0084] halogênio, CrC6-alquila, C3-C6-cicloalquila, C2-C6-alquenila,
C2-C6-alquinila, tri(CrC2-alquil)silila, fenila ou oxo, [0085] ou [0086] R3 representa fenila, que pode conter até três substituintes, sendo que os substituintes independentemente entre si são selecionaPetição 870180002928, de 12/01/2018, pág. 15/185
11/159 dos da lista abaixo;
[0087] ciano, nitro, halogênio, CrCe-alquila, CrCs-haloalquila, C3C6-cicloalquila, C3-C6-halocicloalquila, C2-C6-alquenila, C2-C6haloalquenila, C2-C6-alquinila, C2-C6-haloalquinila, tri(C1-C2-alquil)silila, fenila, hidroxila, CrCe-alcóxi, CrCe-haloalcóxi, C^-Cs-alquiltio ou Cr C6-haloalquiltio, [0088] ou [0089] R3 representa naftalen-1-ila, naftalen-2-ila, 1,2,3,4-tetrahidronaftalen-1-ila, 1,2,3,4-tetra-hidronaftalen-2-ila, 5,6,7,8-tetrahidronaftalen-1-ila, 5,6,7,8-tetra-hidronaftalen-2-ila, decalin-1-ila, decalin-2-ila, 1 H-inden-1-ila, 1H-inden-2-ila, 1H-inden-3-ila, 1H-inden-4-ila, 1H-inden-5-ila, 1H-inden-6-ila, 1H-inden-7-ila, 2,3-di-hidro-1H-inden-1ila, 2,3-di-hidro-1 H-inden-2-ila, 2,3-di-hidro-1 H-inden-4-ila ou 2,3-dihidro-1H-inden-5-ila, [0090] que pode conter até dois substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo: [0091] ciano, halogênio, CrCe-alquila, CrCs-haloalquila, C3-C6cicloalquila, fenila, hidroxila, CrCe-alcóxi, CrCs-haloalcóxi, C-|-C6alquiltio ou CrCs-haloalquiltio, [0092] ou [0093] R3 representa furan-2-ila, furan-3-ila, tiofen-2-ila, tiofen-3-ila, isoxazol-3-ila, isoxazol-4-ila, isoxazol-5-ila, 1 H-pirrol-1-ila, 1 H-pirrol-2ila, 1 H-pirrol-3-ila, oxazol-2-ila, oxazol-4-ila, oxazol-5-ila, tiazol-2-ila, tiazol-4-ila, tiazol-5-ila, isotiazol-3-ila, isotiazol-4-ila, isotiazol-5-ila, pirazol-1-ila, pirazol-3-ila, pirazol-4-ila, imidazol-1 -ila, imidazol-2-ila, imidazol-4-ila, 1,2,4-oxadiazol-3-ila, 1,2,4-oxadiazol-5-ila, 1,3,4-oxadiazol2-ila, 1,2,4-tiadiazol-3-ila, 1,2,4-tiadiazol-5-ila, 1,3,4-tiadiazol-2-ila,
1,2,3-triazol-1 -ila, 1,2,3-triazol-2-i la, 1,2,3-triazol-4-i la, 1,2,4-triazol-1 ila, 1,2,4-triazol-3-ila, piridin-2-ila, piridin-3-ila, piridin-4-ila, piridazin-3Petição 870180002928, de 12/01/2018, pág. 16/185
12/159 ila, piridazin-4-ila, pirimidin-2-ila, pirimidin-4-ila, pirimidin-5-ila, pirazin 2-ila, 1,3,5-triazin-2-ila ou 1,2,4-triazin-3-ila, [0094] que pode conter até dois substituintes, sendo que indepen dentemente entre si são selecionados da lista abaixo:
[0095] substituintes em carbono: ciano, halogênio, C^Ce-alquila CrCs-haloalquila, C3-C6-cicloalquila, fenila, hidroxila, Ci-C4-alkóxi, Cr C4-haloalcóxi, CrC^alquiltio ou CrC^haloalquiltio, [0096] substituintes em nitrogênio: C^Ce-alquila, CrCs-haloalquila
C3-C6-cicloalquila, C2-C6-alquenila, C2-C6-alquinila ou fenila, [0097] ou [0098] R3 representa 1 H-indol-1-ila, 1 H-indol-2-ila, 1 H-indol-3-ila 1 H-indol-4-ila, 1 H-indol-5-ila, 1 H-indol-6-ila, 1 H-indol-7-ila, 1H benzimidazol-1-ila, 1H-benzimidazol-2-ila, 1H-benzimidazol-4-ila, ben zimidazol-5-ila, 1 H-indazol-1-ila, 1H-indazol-3-ila, 1H-indazol-4-ila, 1H indazol-5-ila, 1H-indazol-6-ila, 1H-indazol-7-ila, 2H-indazol-2-ila, 1 benzofuran-2-ila, 1-benzofuran-3-ila, 1-benzofuran-4-ila, 1-benzofuran 5-ila, 1-benzofuran-6-ila, 1-benzofuran-7-ila, 1-benzotiofen-2-ila, 1 benzotiofen-3-ila, 1-benzotiofen-4-ila, 1-benzotiofen-5-ila, 1 benzotiofen-6-ila, 1-benzotiofen-7-ila, quinolin-2-ila, quinolin-3-ila, qui nolin-4-ila, quinolin-5-ila, quinolin-6-ila, quinolin-7-ila, quinolin-8-ila isoquinolin-1-ila, isoquinolin-3-ila, isoquinolin-4-ila, isoquinolin-5-ila isoquinolin-6-ila, isoquinolin-7-ila ou isoquinolin-8-ila, [0099] que pode conter até dois substituintes, sendo que os substi tuintes independentemente entre si são selecionados da lista abaixo: [00100] substituintes em carbono: ciano, halogênio, C^Ce-alquila CrCs-haloalquila, C3-C6-cicloalquila, fenila, hidroxila, Ci-C4-alcóxi, Cr C4-haloalcóxi, CrC^alquiltio ou CrC^haloalquiltio, [00101] substituintes em nitrogênio: C^Ce-alquila, CrCs-haloalquila C3-C6-cicloalquila, C2-C6-alquenila, C2-C6-alquinila ou fenila, [00102] ou
Petição 870180002928, de 12/01/2018, pág. 17/185
13/159 [00103] R3 representa um radical heterociclila de 5 a 6 membros não substituída ou monossubstituída que é ligado através de um átomo de carbono e que pode conter até dois outros heteroátomos selecionados do grupo consistindo em nitrogênio, oxigênio e enxofre, sendo que o substituinte é selecionado da lista abaixo:
[00104] substituintes em carbono: C^Ce-alquila, CrCs-haloalquila, C3-C6-cicloalquila, C2-C6-alquenila, C2-C6-alquinila, trKCrC^alquiQsilila ou fenila, [00105] substituintes em nitrogênio: C^Ce-alquila, C3-C6cicloalquila, C2-C6-alquenila, C2-C6-alquinila, trKCrC^alquiQsilila ou fenila, [00106] R8são idênticos ou diferentes e independentemente entre si representam hidrogênio, halogênio, CrC^alquila, Ci-C2-alcóxi, ciclopropila ou CrC^haloalquila, [00107] R9 são idênticos ou diferentes e independentemente entre si representam hidrogênio, CrC^alquila, ou ciclopropila [00108] e também ao sais destes de ação agroquímica.
[00109] São preferidos compostos da Fórmula (I) na qual um ou mais dos símbolos apresentam um dos significados abaixo:
[00110] A representa metila, [00111] ou [00112] A representa fenila, que pode conter até dois substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo:
[00113] ciano, nitro, halogênio, CrC^alquila, CrC^haloalquila, hidroxila, Ci-C2-alcóxi ou CrC^haloalcóxi, [00114] ou [00115] A representa um radical heteroaromático selecionado do grupo abaixo: furan-2-ila, furan-3-ila, tiofen-2-ila, tiofen-3-ila, oxazol-2ila, oxazol-4-ila, oxazol-5-ila, tiazol-2-ila, tiazol-4-ila, tiazol-5-ila; pirazolPetição 870180002928, de 12/01/2018, pág. 18/185
14/159
1-ila, pirazol-3-ila, pirazol-4-ila, imidazol-1-ila, imidazol-2-ila, imidazol4-ila, 1,2,4-triazol-1 -ila, piridin-2-ila, piridin-3-ila, piridin-4-ila, 1,2,4triazin-3-ila, 1H-benzimidazol-2-ila ou 1,3-benzotiazol-2-ila, [00116] que pode conter até dois substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo: [00117] substituintes em carbono: ciano, halogênio, C1-C2-alquila, C1-C2-haloalquila, hidroxila, C1-C2-alcóxi ou C1-C2-haloalcóxi, [00118] substituintes em nitrogênio: C1-C2-alquila ou C^-C2haloalquila, [00119] L1 representa (C(R1)2)n [00120] sendo que n = 0 a 3, [00121] R1 são idênticos ou diferentes e independentemente entre si representam hidrogênio ou metila, [00122] com a condição de que L1 pode conter no máximo dois substituintes metila, [00123] Y representa enxofre ou oxigênio, [00124] W representa -CH2CH2-, [00125] X representa -CH2CH2-, [00126] R2 representa hidrogênio, metila ou halogênio, [00127] L2 representa -C(R8)2-C(R8)2- ou -CR9=CR9- ou -C=C-, [00128] L3 representa uma ligação direta, [00129] ou [00130] L3 representa uma cadeia de carbono a C4- que pode conter até dois substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo:
[00131] metila, metóxi ou CF3 [00132] R3 representa metila, C1-C2-haloalquila, -CH=CH2, -C^CH, ou C3-C10-cicloalquila não substituído ou monossubstituído, sendo que o substituinte é selecionado da lista abaixo:
[00133] flúor, cloro, metila, etila, ciclopropila, ciclopentila ou cicloPetição 870180002928, de 12/01/2018, pág. 19/185
15/159 hexila, [00134] ou [00135] R3 representa fenila que contém até três substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo:
[00136] ciano, halogênio, C^Ce-alquila, CrCs-haloalquila, fenila, hidroxila, CrCe-alcóxi, CrCe-haloalcóxi, Cg-Cs-alquiltio ou C-|-C6haloalquiltio, [00137] ou [00138] R3 representa naftalen-1-ila, naftalen-2-ila, 1,2,3,4-tetrahidronaftalen-1-ila, 1,2,3,4-tetra-hidronaftalen-2-ila, 5,6,7,8-tetrahidronaftalen-1-ila, 5,6,7,8-tetra-hidronaftalen-2-ila, decalin-1-ila, decalin-2-ila, 1 H-inden-1-ila, 1H-inden-2-ila, 1H-inden-3-ila, 1H-inden-4-ila, 1H-inden-5-ila, 1H-inden-6-ila, 1H-inden-7-ila, 2,3-di-hidro-1H-inden-1ila, 2,3-di-hidro-1 H-inden-2-ila, 2,3-di-hidro-1 H-inden-4-ila ou 2,3-dihidro-1H-inden-5-ila, [00139] que pode conter até dois substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo: [00140] flúor, cloro, bromo, iodo, metila, etila, CF3, CHF2, ciclopropila, fenila, hidroxila, OMe, OEt, OCF3, OCHF2, OC2F5, SMe ou SCF3, [00141] ou [00142] R3 representa furan-2-ila, furan-3-ila, tiofen-2-ila, tiofen-3-ila, isoxazol-3-ila, isoxazol-4-ila, isoxazol-5-ila, 1 H-pirrol-1-ila, 1 H-pirrol-2ila, 1 H-pirrol-3-ila, oxazol-2-ila, oxazol-4-ila, oxazol-5-ila, tiazol-2-ila, tiazol-4-ila, tiazol-5-ila, isotiazol-3-ila, isotiazol-4-ila, isotiazol-5-ila, pirazol-1-ila, pirazol-3-ila, pirazol-4-ila, imidazol-1 -ila, imidazol-2-ila, imidazol-4-ila, 1,2,4-oxadiazol-3-ila, 1,2,4-oxadiazol-5-ila, 1,3,4-oxadiazol2-ila, 1,2,4-tiadiazol-3-ila, 1,2,4-tiadiazol-5-ila, 1,3,4-tiadiazol-2-ila,
1,2,3-triazol-1 -ila, 1,2,3-triazol-2-i la, 1,2,3-triazol-4-i la, 1,2,4-triazol-1 ila, 1,2,4-triazol-3-ila, piridin-2-ila, piridin-3-ila, piridin-4-ila, piridazin-3Petição 870180002928, de 12/01/2018, pág. 20/185
16/159 ila, piridazin-4-ila, pirimidin-2-ila, pirimidin-4-ila, pirimidin-5-ila, pirazin2-ila, 1,3,5-triazin-2-ila ou 1,2,4-triazin-3-ila, [00143] que pode ocnter até dois substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo: [00144] substituintes em carbono: ciano, flúor, cloro, bromo, iodo, metila, etila, 1-metiletil, 1,1-dimetiletil, CF3, CHF2, C2F5, CCI3, ciclopropila, fenila, hidroxila, OMe, OEt, O/soPr, OCF3, OCHF2, OC2F5, SMe ou SCF3, [00145] substituintes em nitrogênio: metila, etila, 1-metiletila, 1,1dimetiletila, ciclopropila ou fenila, [00146] ou [00147] R3 representa 1 H-indol-1-ila, 1 H-indol-2-ila, 1 H-indol-3-ila, 1 H-indol-4-ila, 1 H-indol-5-ila, 1 H-indol-6-ila, 1 H-indol-7-ila, 1Hbenzimidazol-1-ila, 1H-benzimidazol-2-ila, 1H-benzimidazol-4-ila, benzimidazol-5-ila, 1 H-indazol-1-ila, 1H-indazol-3-ila, 1H-indazol-4-ila, 1Hindazol-5-ila, 1H-indazol-6-ila, 1H-indazol-7-ila, 2H-indazol-2-ila, 1benzofuran-2-ila, 1-benzofuran-3-ila, 1-benzofuran-4-ila, 1-benzofuran5-ila, 1-benzofuran-6-ila, 1-benzofuran-7-ila, 1-benzotiofen-2-ila, 1benzotiofen-3-ila, 1-benzotiofen-4-ila, 1-benzotiofen-5-ila, 1benzotiofen-6-ila, 1-benzotiofen-7-ila, quinolin-2-ila, quinolin-3-ila, quinolin-4-ila, quinolin-5-ila, quinolin-6-ila, quinolin-7-ila, quinolin-8-ila, isoquinolin-1-ila, isoquinolin-3-ila, isoquinolin-4-ila, isoquinolin-5-ila, isoquinolin-6-ila, isoquinolin-7-ila ou isoquinolin-8-ila, [00148] que pode conter até dois substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo: [00149] substituintes em carbono: ciano, flúor, cloro, bromo, iodo, metila, etila, 1-metiletila, 1,1-dimetiletila, CF3, CHF2, C2F5, CCI3, ciclopropila, fenila, hidroxila, OMe, OEt, O/soPr, OCF3, OCHF2, OC2F5, SMe ou SCF3,
Petição 870180002928, de 12/01/2018, pág. 21/185
17/159 [00150] substituintes em nitrogênio: metila, etila, 1-metiletila, 1,1dimetiletila, ciclopropila ou fenila, [00151] ou [00152] R3 representa pirrolidin-2-ila não substituída ou monossubstituída, pirrolidin-3-ila, morfolin-3-ila, morfolin-2-ila, piperidin-2-ila, piperidin-3-ila ou piperazin-2-ila, sendo que o substituinte é selecionado da lista abaixo:
[00153] substituintes em carbono: metila, etila, CF3, ciclopropila ou fenila, [00154] substituintes em nitrogênio: metila, etila, ciclopropila ou fenila, [00155] R8são idênticos ou diferentes e independentemente entre si representam hidrogênio, metila, etila ou CF3, [00156] R9são idênticos iou diferentes e independentemente entre si representam hidrogênio, metila ou etila, [00157] e também os sais destes de ação agroquímica.
[00158] São muito particularmente preferidos compostos da Fórmula (I) na qual um ou mais dos símbolos apresentam um dos significados abaixo:
[00159] A representa metila, [00160] ou [00161] A representa fenila que pode conter até dois substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo:
[00162] ciano, flúor, cloro, bromo, iodo, metila, etila, CF3, CHF2, C2F5, CCI3, hidroxila, OMe, OCF3, OCHF2, OCH2CF3 ou OC2F5, [00163] ou [00164] A representa um radical heteroaromático selecionado do grupo abaixo: tiofen-3-ila, pirazol-1-ila, pirazol-4-ila, piridin-4-ila, 1Hbenzimidazol-2-ila ou 1,3-benzotiazol-2-ila,
Petição 870180002928, de 12/01/2018, pág. 22/185
18/159 [00165] Que pode conter até dois substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo: [00166] substituintes em carbono: ciano, flúor, cloro, bromo, iodo, metila, etila, CF3, CHF2, C2F5, CCI3 , hidroxila, OMe, OCF3, OCHF2, OCH2CF3 ou OC2F5, [00167] substituintes em nitrogênio: metila, etila ou CF3, [00168] L1 representa (C(R1)2)n [00169] sendo que n = 0 a 3, [00170] R1 sao idênticos ou diferentes e independentemente entre si representam hidrogênio ou metila, [00171] com a condição de que L1 possa conter no máximo um substituinte metila, [00172] Y representa enxofre ou oxigênio, [00173] W representa -CH2CH2-, [00174] X representa -CH2CH2-, [00175] R2 representa hidrogênio, metila, cloro ou bromo, [00176] L2 representa -C(R8)2-C(R8)2- ou -CR9=CR9- ou -C=C-, [00177] L3 representa uma ligação direta, [00178] ou [00179] L3 representa uma cadeia de carbono Cr a C4, [00180] R3 representa metil, CF3, -CH=CH2, -C^CH, ciclopropila, ciclobutila, ciclopentila, ciclo-hexila, ciclo-heptila ou ciclo-octila, [00181] ou [00182] R3 representa fenila que pode conter até dois substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo:
[00183] ciano, flúor, cloro, bromo, iodo, metila, etila, 1-metiletila, 1,1-dimetiletila, CF3, CHF2, C2F5, CCI3, fenila, hidroxila, OMe, OEt, O/soPr, OCF3, OCHF2, OC2F5, SMe ou SCF3, [00184] ou
Petição 870180002928, de 12/01/2018, pág. 23/185
19/159 [00185] R3 representa naftalen-1 -ila, naftalen-2-ila, 1,2,3,4-tetrahidronaftalen-1-ila, 1,2,3,4-tetra-hidronaftalen-2-ila, 5,6,7,8-tetrahidronaftalen-1-ila, 5,6,7,8-tetra-hidronaftalen-2-ila, decalin-1-ila, decalin-2-ila, 1 H-inden-1-ila, 1H-inden-2-ila, 1H-inden-3-ila, 1H-inden-4-ila, 1H-inden-5-ila, 1H-inden-6-ila, 1H-inden-7-ila, 2,3-di-hidro-1H-inden-1ila, 2,3-di-hidro-1 H-inden-2-ila, 2,3-di-hidro-1 H-inden-4-ila ou 2,3-dihidro-1H-inden-5-ila, [00186] ou [00187] R3 representa furan-2-ila, furan-3-ila, tiofen-2-ila, tiofen-3-ila, isoxazol-3-ila, isoxazol-4-ila, isoxazol-5-ila, 1 H-pirrol-1-ila, 1 H-pirrol-2ila, 1 H-pirrol-3-ila, oxazol-2-ila, oxazol-4-ila, oxazol-5-ila, tiazol-2-ila, tiazol-4-ila, tiazol-5-ila, isotiazol-3-ila, isotiazol-4-ila, isotiazol-5-ila, pirazol-1-ila, pirazol-3-ila, pirazol-4-ila, imidazol-1-ila, imidazol-2-ila, imidazol-4-ila, 1,2,4-oxadiazol-3-ila, 1,2,4-oxadiazol-5-ila, 1,3,4-oxadiazol2-ila, 1,2,4-tiadiazol-3-ila, 1,2,4-tiadiazol-5-ila, 1,3,4-tiadiazol-2-ila,
1,2,3-triazol-1 -ila, 1,2,3-triazol-2-i la, 1,2,3-triazol-4-i la, 1,2,4-triazol-1 ila, 1,2,4-triazol-3-ila, piridin-2-ila, piridin-3-ila, piridin-4-ila, piridazin-3ila, piridazin-4-ila, pirimidin-2-ila, pirimidin-4-ila, pirimidin-5-ila, pirazin2-ila, 1,3,5-triazin-2-ila ou 1,2,4-triazin-3-ila, [00188] ou [00189] R3 representa 1 H-indol-1-ila, 1 H-indol-2-ila, 1 H-indol-3-ila, 1 H-indol-4-ila, 1 H-indol-5-ila, 1 H-indol-6-ila, 1 H-indol-7-ila, 1Hbenzimidazol-1-ila, 1H-benzimidazol-2-ila, 1H-benzimidazol-4-ila, benzimidazol-5-ila, 1 H-indazol-1-ila, 1H-indazol-3-ila, 1H-indazol-4-ila, 1Hindazol-5-ila, 1H-indazol-6-ila, 1H-indazol-7-ila, 2H-indazol-2-ila, 1benzofuran-2-ila, 1-benzofuran-3-ila, 1-benzofuran-4-ila, 1-benzofuran5-ila, 1-benzofuran-6-ila, 1-benzofuran-7-ila, 1-benzotiofen-2-ila, 1benzotiofen-3-ila, 1-benzotiofen-4-ila, 1-benzotiofen-5-ila, 1benzotiofen-6-ila, 1-benzotiofen-7-ila, quinolin-2-ila, quinolin-3-ila, quinolin-4-ila, quinolin-5-ila, quinolin-6-ila, quinolin-7-ila, quinolin-8-ila,
Petição 870180002928, de 12/01/2018, pág. 24/185
20/159 isoquinolin-1 -ila, isoquinolin-3-ila, isoquinolin-4-ila, isoquinolin-5-ila, isoquinolin-6-ila, isoquinolin-7-ila ou isoquinolin-8-ila, [00190] ou [00191] R3 representa pirrolidin-2-ila, pirrolidin-3-ila, morfolin-3-ila, morfolin-2-ila, piperidin-2-ila, piperidin-3-ila ou piperazin-2-ila, [00192] R8são idênticos ou diferentes e independentemente entre si representam hidrogênio, metila ou etila, [00193] R9são idênticos ou diferentes e independentemente entre si representam hidrogênio, metila ou etila, [00194] e também os sais destes de ação agroquímica.
[00195] São extraordinariamente preferidos compostos da Fórmula (I) na qual um ou mais dos símbolos apresentam um dos significados abaixo:
[00196] A representa metila, 1,3-di-hidro-2H-indazol-2-ila, 3-clorofenila, 2,5-diclorofenila, 3-(trifluorometil)fenila, 3,4-dimetoxifenila, 2,5dibromofenila, 2-bromo-5-(trifluorometil)fenila, 5-bromo-2-metilfenila, 5iodo-2-metilfenila, 2,5-bis(trifluorometil)fenila, 2-cloro-5(trifIuorometil)fenila, 1 H-pirazol-1 -ila, 3-(trifIuorometiI)-1 H-pirazol-1 -ila, 3,5-dimetiI-1 H-pirazol-1 -ila, 5-metil-3-(trifluorometil)-1 H-pirazol-1 -ila, 4cloro-5-metil-3-(trifluorometil)-1 H-pirazol-1-ila, 3,5-bis(trifluorometil)-1 Hpirazol-1 -ila, 5-(difluorometil)-3-metil-1 H-pirazol-1 -ila, 3,5-dicloro-1 Hpirazol-1 -ila, 3,5-dibromo-1 H-pirazol-1 -ila, 5-cloro-1 -metil-1 H-pirazol-4ila, tiofen-3-ila, piridin-4-ila, 3-cloro-5-(trifluorometil) piridin-2-ila, 1Hbenzimidazol-2-ila ou 1,3-benzotiazol-2-ila, [00197] L1 é uma ligação direta, [00198] ou [00199] L1 representa -CH2-, -CH2CH2-, -CH2CH2CH2- ou -CHCH3-, [00200] Y representa enxofre ou oxigênio, [00201 ] W representa -CH2CH2-, [00202] X representa -CH2CH2-,
Petição 870180002928, de 12/01/2018, pág. 25/185
21/159 [00203] R2 representa hidrogênio, metila ou bromo, [00204] L2 representa -CH2CH2-, -CH2CHCH3-, -CH=CH- (Z), -CH=CH(E) ou -C=C-, [00205] L3 representa uma ligação direta, [00206] ou [00207] L3 representa -CH2-, -CH2C(CH3)2-, -CH2CHCH3-, [00208] R3 representa metil, -C=C2, -C^C, CF3 ciclo-hexila, fenil, 4clorofenila, 4-metoxifenila, 3-(trifluorometil)fenila, naftalen-1-ila, naftalen-2-ila ou piridin-3-ila, [00209] e também os sais destes de ação agroquímica.
[00210] São extraordinariamente preferidos compostos da Fórmula (I) na qual [00211] A representa pirazol-1 -ila ou pirazol-4-ila não substituída ou substituída, [00212] que pode conter até dois substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo: [00213] substituintes em carbono: ciano, flúor, cloro, bromo, iodo, metila, etila, CF3, CHF2, C2F5, CCI3 , hidroxila, OMe, OCF3, OCHF2, OCH2CF3, ou OC2F5 [00214] substituintes em nitrogênio: metila, etila ou CF3 [00215] e L1 representa -CH2-, [00216] sendo que os outros substituintes apresentam um ou mais dos significados acima mencionados, [00217] e os sais destes de ação agroquímica.
[00218] Além disso, são extraordinariamente preferidos compostos da fórmulaFórmula (I) na qual [00219] A representa fenila não substituída ou substituída, [00220] sendo que os substtuintes independnetemente entre si são selecionados da lista abaixo:
[00221] ciano, flúor, cloro, bromo, iodo, metila, etila, CF3, CHF2,
Petição 870180002928, de 12/01/2018, pág. 26/185
22/159
C2F5, CCI3, hidroxila, OMe, OCF3, OCHF2, OCH2CF3 ou OC2F5 [00222] e L1 representa -CH2-, [00223] sendo que os outros substituintes apresentam um ou mais dos significados acima mencionados, [00224] e os sais destes de ação agroquímica.
[00225] Além disso, são extraordinariamente preferidos compostos da Fórmula (I) na qual [00226] Y representa oxigênio, [00227] sendo que os outros substituintes apresentam um ou mais dos significados acima mencionados, [00228] e os sais destes de ação agroquímica.
[00229] Além disso, são extraordinariamente preferidos compostos da Fórmula (I) na qual um ou mais dos símbolos apresentam um dos significados abaixo:
[00230] W representa -CH2CH2[00231 ] X representa -CH2CH2[00232] sendo que os outros substituintes apresentam um ou mais dos signficados acima, [00233] e os sais destes de ação agroquímica.
[00234] Além disso, são extraordinariamente preferidos compostos da Fórmula (I) na qual [00235] R2 representa hidrogênio, halogênio ou metila, [00236] sendo que os outros subtituintes apresentam um ou mais dos significados acima mencionados, [00237] e os sais destes de ação agroquímica.
[00238] São extraordinariamente preferidos compostos da Fórmula (I) na qual [00239] L2 representa -CH2CH2-, [00240] sendo que os outros substituintes apresentam um ou mais dos significados acima mencionados,
Petição 870180002928, de 12/01/2018, pág. 27/185
23/159 [00241] e os sais destes de ação agroquímica.
[00242] São extraordinariamente preferidos compostos da Fórmula (I) na qual [00243] L2 representa -CH=CH- (Z), [00244] sendo que os outros substituintes apresentam um ou mais dos significados acima mencionados, [00245] e os sais destes de ação agroquímica.
[00246] Além disso, são extraordinariamente preferidos compostos da Fórmula (I) na qual [00247] L2 representa -CH=CH- (E), [00248] sendo que os outros substituintes apresentam um ou mais dos significados acima mencionados, [00249] e os sais destes de ação agroquímica.
[00250] Além disso, são extraordinariamente preferidos compostos da Fórmula (I) na qual [00251] L2 representa-C^C-, [00252] sendo que os outros substituintes apresentam um ou mais dos significados acima mencionados, [00253] e os sais destes de ação agroquímica.
[00254] Além disso, são extraordinariamente preferidos compostos da Fórmula (I) na qual [00255] L3 representa uma ligação direta, [00256] Sendo que os outros substituintes apresentam um ou mais dos significados acima mencionados, [00257] e os sais destes de ação agroquimica.
[00258] São extraordinariamente preferidos compostos da Fórmula (I) na qual [00259] L3 representa -CH2-, [00260] sendo que os outros substiuintesapresentam um ou mais dos significados acima mencionados,
Petição 870180002928, de 12/01/2018, pág. 28/185
24/159 [00261] e os sais destes de ação agroquímica.
[00262] Além disso, são extraordinariamente preferidos compostos da Fórmula (I) na qual [00263] R3 representa naftalen-1-ila ou naftalen-2-ila não substituído, [00264] sendo que os outros substituintes apresentam um ou mais dos significados acima mencionados, [00265] e os sais destes de ação agroquímica.
[00266] Além disso, são extraordinariamente preferidos compostos da Fórmula (I) na qual [00267] R3 representa fenila não substituído, [00268] sendo que os outros substituintes apresentam um ou mais dos significados acima mencionados, [00269] e os sais destes de ação agroquímica.
[00270] Além disso, são extraordinariamente preferidos compostos da Fórmula (I) na qual [00271] A representa 2,5-dimetilfenila, 2,3,6-trifluorofenila, 3,5bis(difIuorometiI)-1 H-pirazol-1 -ila, 3-(propan-2-ila)-5-(trifluorometil)-1 Hpirazol-1 -ila, 3-tert-butil-5-(pentafIuoroetiI)-1 H-pirazol-1 -ila, 3-tert-butil5-(trifIuorometiI)-1 H-pirazol-1 -ila, 5-etil-3-(trifIuorometiI)-1 H-pirazol-1 -ila, 5-tert-buti l-3-(pentaf I uoroeti I)-1 H-pirazol-1 -ila, 5-tert-buti I-3(trifluorometil)-l H-pirazol-1-ila, 2H-indazol-2-ila, 1,3-benzodioxol-5-ila ou 1H-benzimidazol-2-ila, [00272] sendo que os outros substituintes apresentam um ou mais dos significados acima mencionados, [00273] e os sais destes de ação agroquímica.
[00274] Além disso, são extraordinariamente preferidos compostos da Fórmula (I) na qual [00275] R3 representa 2,4-diclorofenila, 2,4-dimetoxifenila, 2,5dimetoxifenila, 2-metoxifenila, 2-metilfenila, 3,5-dimetilisoxazol-4-ila, 3Petição 870180002928, de 12/01/2018, pág. 29/185
25/159 metilpiridin-2-ila, quinolin-8-ila, morfolin-4-ila, naftaleno, tert-butila, trimetilsilila, 1,2,3,4-tetra-hidronaftalen-1-ila, ciclo-hexila, 2-bromofenila, 2-clorofenila, 2-cloro-6-fluorofenila, 2,6-difluorofenila, [00276] sendo que os outros substituintes apresentam um ou mais dos significados acima mencionados, [00277] e os sais destes de ação agroquímica.
[00278] As definições de radical acima indicadas podem ser combinadas com uma outra conforme desejado. Além disso, definições individuais não podem ser aplicadas.
[00279] Dependendo da natureza dos substituintes acima definidos, os compostos da Fórmula (I) apresentam propriedades acídicas ou básicas e podem formar sais, se apropriado inclusive sais internos, ou adutos com ácidos inorgânicos ou ácidos orgânicos ou com bases ou com íons de metal. Se os compostos da Fórmula (I) portarem amino, alquilamino ou outros grupos que induzem propriedades básicas, esses compostos poderão ser reagidos com ácidos para formar sais, ou eles são diretamente obtidos como sais na síntese. Se os compostos da Fórmula (I) portarem hidroxila, carboxila ou outros grupos que induzem propriedades acídicas, esses compostos poderão ser reagidos com bases para formar sais. Bases adequadas são por exemplo, hidróxidos, carbonatos, bicarbonatos dos metais alcalinos e metais terrosos alcalinos, particularmente aqueles de sódio, potássio, magnésio e cálcio além disso, amônia, aminas primárias, secundárias e terciárias que apresentam grupos (CrC^-alquila, mono-, di- e trialcanolaminas de (CrC^-alcanóis, colina e também clorocolina.
[00280] Os sais assim obtidos também apresentam propriedades fungicidas, herbicidas e inseticidas.
[00281] Exemplos de ácidos inorgânicos são ácidos hidroálicos, tais como fluoreto de hidrogênio, cloreto de hidrogênio, brometo de hidrogênio e iodeto de hidrogênio, ácido sulfúrico, ácido fosfórico e ácido
Petição 870180002928, de 12/01/2018, pág. 30/185
26/159 nítrico,e sais acídicos, tais como NaHSO4 e KHSO4. Ácidos orgânicos adequados são, por exemplo, ácido fórmico, ácido carbônico e ácidos alcanoicos, tais como ácido acético, ácido trifluoroacético, ácido tricloroacético e ácido propiônico, e também ácido glicólico, ácido tiociânico, ácido láctico, ácido succínico, ácido cítrico, ácido benzoico, ácido cinâmico, ácido oxálico, ácidos alquilsulfônicos (ácidos sulfônicos que apresentam radicais alquila ramificados de 1 a 20 átomos de carbono), ácidos arilsulfônicosou ácidos arildissulfônicos (radicais aromáticos, tais como fenila ou naftila, que portam um ou dois grupos sulfônicos), ácidos alquilfosfônicos (ácidos fosfônicos que apresentam cadeia linear ou radicais alquila ramificados de 1 a 20 átomos de carbono), ácidos arilfosfônicos ou ácidos arildifosfônicos (radicais aromáticos, tais como fenila e naftila, que portam um ou dois radicais ácido fosfônico), sendo que os radicais alquila e arila podem portar outros substituintes, por exemplo ácido p-toluenossulfônico, ácido salicílico, ácido paminossalicílico, ácido 2-fenoxibenzoico, ácido 2-acetoxibenzoico, etc. [00282] íons de metal adequado são particularmente os ions dos elementos do Segundo grupo principal, particularmente cálcio e magnésio, do terceiro e quarto grupo pincipal, particularmente alumínio, estanho e chumbo, e também do primeiro ao oitavo grupo de transição, particularmente cromo, manganês, ferro, cobalto, níquel, cobre, zinco e outros. São particularmente preferidos os ions de metal dos elementos do quarto período. Neste caso, os metais podem estar presentes em várias valências que eles podem assumir.
[00283] Grupos opcionalmente substituídos podem ser mono- ou polissubstituídos, sendo que no caso de polisubstituição os substituintes podem ser idênticos ou diferentes.
[00284] Nas definições dos símbolos indicadas na fórmula acima, foram usados termos coletivos que em geral são representativos dos seguintes substituintes:
Petição 870180002928, de 12/01/2018, pág. 31/185
27/159 [00285] halogênio: flúor, cloro, bromo e iodo;
[00286] alquila: radicais hidrocarboneto saturados, de cadeia inear ou ramificados que apresentam de 1 a 8 átomos de carbono, por exemplo (mas não limitado a isso) CrCe-alquila, tais como metila, etila, propila, 1-metiletila, butila, 1-metilpropila, 2-metilpropila, 1,1dimetiletila, pentila, 1-metilbutila, 2-metilbutila, 3-metilbutila, 2,2dimetilpropila, 1-etilpropila, hexila, 1,1-dimetilpropila, 1,2-dimetilpropila,
1- metilpentila, 2-metilpentila, 3-metilpentila, 4-metilpentila, 1,1dimetilbutila, 1,2-dimetilbutila, 1,3-dimetilbutila, 2,2-dimetilbutila, 2,3dimetilbutila, 3,3-dimetilbutila, 1-etilbutila, 2-etilbutila, 1,1,2-trimetilpropila, 1,2,2-trimetilpropila, 1-etil-1-metilpropila e 1-etil-2metilpropila;
[00287] alquenila: radicais hidrocarboneto insaturados, de cadeia linear ou ramificados que apresentam 2 a 8 átomos de carbono e uma ligação dupla em qualquer posição, por exemplo (mas não limitado a isso) C2-C6-alquenila, tais como etenila, 1-propenila, 2-propenila, 1metiletenila, 1-butenila, 2-butenila, 3-butenila, 1-metil-1-propenila, 2metil-1-propenila, 1-metil-2-propenila, 2-metil-2-propenila, 1-pentenila,
2- pentenila, 3-pentenila, 4-pentenila, 1 -metil-1 -butenila, 2-metil-1butenila, 3-metil-1 -butenila, 1-metil-2-butenila, 2-metil-2-butenila, 3metil-2-butenila, 1-metil-3-butenila, 2-metil-3-butenila, 3-metil-3butenila, 1,1 -dimetil-2-propenila, 1,2-dimetil-1 -propenila, 1,2-dimetil-2propenila, 1-etil-1-propenila, 1-etil-2-propenila, 1-hexenila, 2-hexenila,
3- hexenila, 4-hexenila, 5-hexenila, 1-metil-1-pentenila, 2-metil-1pentenila, 3-metil-1 -pentenila, 4-metil-1 -pentenila, 1-metil-2-pentenila, 2-metil-2-pentenila, 3-metil-2-pentenila, 4-metil-2-pentenila, 1-metil-3pentenila, 2-metil-3-pentenila, 3-metil-3-pentenila, 4-metil-3-pentenila, 1-metil-4-pentenila, 2-metil-4-pentenila, 3-metil-4-pentenila, 4-metil-4pentenila, 1,1 -d i meti l-2-buten i la, 1,1 -dimetil-3-butenila, 1,2-d i meti I-1 butenila, 1,2-dimetil-2-butenila, 1,2-dimetil-3-butenila, 1,3-dimetil-1 Petição 870180002928, de 12/01/2018, pág. 32/185
28/159 butenila, 1,3-dimetil-2-butenila, 1,3-dimetil-3-butenila, 2,2-dimetil-3butenila, 2,3-dimetil-1 -butenila, 2,3-dimetil-2-butenila, 2,3-dimetil-3butenila, 3,3-dimetil-1 -butenila, 3,3-dimetil-2-butenila, 1-etil-1-butenila, 1-etil-2-butenila, 1-etil-3-butenila, 2-etil-1-butenila, 2-etil-2-butenila, 2etil-3-butenila, 1,1,2-trimetil-2-propenila, 1-etil-1-metil-2-propenila, 1etil-2-metil-1 -propenila e 1 -etil-2-metil-2-propenila;
[00288] alquinila: grupos hidrocarboneto de cadeia linear ou ramificados que apresentam de 2 a 8 átomos de carbono e uma ligação tripla em qualquer posição, por exemplo (mas não limitado a isso) C2-C6alcinila, tais como etinila, 1-propinila, 2-propinila, 1-butinila, 2-butinila,
3-butinila, 1 -metil-2-propinila, 1-pentinila, 2-pentinila, 3-pentinila, 4pentinila, 1 -metil-2-butinila, 1 -metil-3-butinila, 2-metil-3-butinila, 3-metil1-butinila, 1,1 -dimetil-2-propinila, 1-etil-2-propinila, 1-hexinila, 2hexinila, 3-hexinila, 4-hexinila, 5-hexinila, 1 -metil-2-pentinila, 1-metil-3pentinila, 1 -metil-4-pentinila, 2-metil-3-pentinila, 2-metil-4-pentinila, 3metil-1-pentinila, 3-metil-4-pentinila, 4-metil-1 -pentinila, 4-metil-2pentinila, 1,1 -d i meti l-2-buti n i Ia, 1,1 -d i meti l-3-buti n i Ia, 1,2-d i meti I-3butinila, 2,2-dimetil-3-butinila, 3,3-dimetil-1 -butinila, 1-etil-2-butinila, 1etil-3-butinila, 2-etil-3-butinila e 1 -etil-1 -metil-2-propinila;
[00289] alcóxi: radicais alcóxi saturados, de cadeia linear ou ramificados que apresentam de 1 a 8 átomos de carbono, por exemplo (mas não limitado a isso) CrCe-alcóxi, tais como metóxi, etóxi, propóxi, 1metiletóxi, butóxi, 1-metiIpropóxi, 2-metilpropóxi, 1,1-dimetiletóxi, pentóxi, 1-metiIbutóxi, 2-metilbutóxi, 3-metilbutóxi, 2,2-dimetilpropóxi, 1etilpropóxi, hexóxi, 1,1-dimetilpropóxi, 1,2-dimetilpropóxi, 1 metilpentóxi, 2-metilpentóxi, 3-metilpentóxi, 4-metilpentóxi, 1,1dimetilbutóxi, 1,2-dimetilbutóxi, 1,3-dimetilbutóxi, 2,2-dimetilbutóxi, 2,3dimetilbutóxi, 3,3-dimetilbutóxi, 1-etilbutóxi, 2-etilbutóxi, 1,1,2trimetilpropóxi, 1,2,2-trimetilpropóxi, 1-etil-1-metilpropóxi e 1-etil-2-metilpropóxi;
Petição 870180002928, de 12/01/2018, pág. 33/185
29/159 [00290] alquiltio: radicais alquitio saturados, de cadeia linear ou ramificados que apresentam de 1 a 8 átomos de carbono, por exemplo (mas não limitado a isso) CrCe-alquiltio, tal como metiltio, etiltio, propiltio, 1-metiletiltio, butiltio, 1-metilpropiltio, 2-metilpropiltio, 1,1dimetiletiltio, pentiltio, 1-metilbutiltio, 2-metilbutiltio, 3-metilbutiltio, 2,2dimetilpropiltio, 1-etilpropiltio, hexiltio, 1,1-dimetilpropiltio, 1,2dimetilpropiltio, 1-metilpentiltio, 2-metilpentiltio, 3-metilpentiltio, 4metilpentiltio, 1,1-dimetilbutiltio, 1,2-dimetilbutiltio, 1,3-dimetilbutiltio,
2,2-dimetilbutiltio, 2,3-dimetilbutiltio, 3,3-dimetilbutiltio, 1-etilbutiltio, 2etilbutiltio, 1,1,2-trimetilpropiltio, 1,2,2-trimetilpropiltio, 1-etil-1 metilpropiltio e 1 -etil-2-metilpropiltio;
[00291] alcoxicarbonila: um grupo alcóxi que apresenta 1 a 6 átomos de carbono (conforme acima mencionado) que é ligado ao esqueleto via um grupo carbonila (-CO-);
[00292] alquilsulfinila: radicais alquilsulfinila saturados, de cadeia linear ou ramificados que apresentam de 1 a 8 átomos de carbono, por exemplo (mas não limitado a isso) CrCe-alquilsulfinila, tais como metilsulfinila, etilsulfinila, propilsulfinila, 1-metiletilsulfinila, butilsulfinila, 1metilpropilsulfinila, 2-metilpropilsulfinila, 1,1-dimetiletilsulfinila, pentilsulfinila, 1-metilbutilsulfinila, 2-metilbutilsulfinila, 3-metilbutilsulfinila, 2,2dimetilpropilsulfinila, 1-etilpropilsulfinila, hexilsulfinila, 1,1dimetilpropilsulfinila, 1,2-dimetilpropilsulfinila, 1-metilpentilsulfinila, 2metilpentilsulfinila, 3-metilpentilsulfinila, 4-metilpentilsulfinila, 1,1dimetilbutilsulfinila, 1,2-dimetilbutilsulfinila, 1,3-dimetilbutilsulfinila, 2,2dimetilbutilsulfinila, 2,3-dimetilbutilsulfinila, 3,3-dimetilbutilsulfinila, 1etilbutilsulfinila, 2-etilbutilsulfinila, 1,1,2-trimetilpropilsulfinila, 1,2,2trimetilpropilsulfinila, 1-etil-1-metilpropilsulfinila e 1-etil-2metilpropilsulfinila;
[00293] alquilsulfonila: radicasi alquilsulfonila saturados, de cadeia linear ou ramificados que apresentam de 1 a 8 átomos de carbono, por
Petição 870180002928, de 12/01/2018, pág. 34/185
30/159 exemplo (mas não limitado a isso) CrCe-alquilsulfonila, tais como metilsulfonila, etilsulfonila, propilsulfonila, 1-metiletilsulfonila, butilsulfonila, 1-metilpropilsulfonila, 2-metilpropilsulfonila, 1,1-dimetiletilsulfonila, pentilsulfonila, 1-metilbutilsulfonila, 2-metilbutilsulfonila, 3metilbutilsulfonila, 2,2-dimetilpropilsulfonila, 1-etilpropilsulfonila, hexiIsulfonila, 1,1-dimetilpropilsulfonila, 1,2-dimetilpropilsulfonila, 1metilpentilsulfonila, 2-metilpentilsulfonila, 3-metilpentilsulfonila, 4metilpentilsulfonila, 1,1-dimetilbutilsulfonila, 1,2-dimetilbutilsulfonila,
1,3-d imetil butilsulfoni la, 2,2-d imetil buti Isulfoni la, 2,3-d imetilbutilsulfonila, 3,3-dimetilbutilsulfonila, 1-etilbutilsulfonila, 2etilbutilsulfonila, 1,1,2-trimetilpropilsulfonila, 1,2,2-trimetilpropilsulfonila, 1 -etil-1 -metilpropilsulfonila e 1 -etil-2-metilpropilsulfonila;
[00294] cicloalquila: grupos hidrocarboneto monocíclicos, saturados que apresentam de 3 a 10 membros no anel de carbono, por exemplo (mas não limitado a isso) ciclopropila, ciclopentila e ciclohexila;
[00295] haloalquila: grupos alquila de cadeia linear ou ramificados que apresentam de 1 a 8 átomos de carbono (conforme mencionado acima), sendo que nesses grupos alguns ou todos os átomos de hidrogênio podem ser substituídos por átomos de halogênio conforme acima mencionado, por exemplo (mas não limitado a isso) CrCshaloalquila, tais como clorometila, bromometila, diclorometila, triclorometila, fluorometila, difluorometila, trifluorometila, clorofluorometila, diclorofluorometila, clorodifluorometila, 1-cloroetila, 1-bromoetila, 1fluoroetila, 2-fluoroetila, 2,2-difluoroetila, 2,2,2-trifluoroetila, 2-cloro-2fluoroetila, 2-cloro-2,2-difluoroetila, 2,2-dicloro-2-fluoroetila, 2,2,2tricloroetila, pentafluoroetila e 1,1,1-trifluoroprop-2-ila;
[00296] haloalcóxi: grupos alcóxi de cadeia linear ou ramificados que apresentam de 1 a 8 átomos de carbono (conforme acima mencionado), sendo que nesses grupos alguns ou todos os átomos de hiPetição 870180002928, de 12/01/2018, pág. 35/185
31/159 drogênio podm ser substituídos por átomos de halogênio conforme acima mencionado, por exemplo (mas não limitado a isso) CrCshaloalcóxi, tais como clorometóxi, bromometóxi, diclorometóxi, triclorometóxi, fluorometóxi, difluorometóxi, trifluorometóxi, clorofluorometóxi, diclorofluorometóxi, clorodifluorometóxi, 1-cloroetóxi, 1-bromoetóxi, 1-fluoroetóxi, 2-fluoroetóxi, 2,2-difluoroetóxi, 2,2,2-trifluoroetóxi, 2cloro-2-fluoroetóxi, 2-cloro-2,2-difluoroetóxi, 2,2-dicloro-2-fluoroetóxi, 2,2,2-tricloroetóxi, pentafluoroetóxi e 1,1,1-trifluoroprop-2-óxi;
[00297] haloalquiltio: grupos alquitio de cadeia linear ou ramificados que apresentam de 1 a 8 átomos de carbono (conforme acima definido), sendo que nesses grupos alguns ou todos os átomos de hidrogênio podem ser substituídos por átomos de halogênio conforme acima mencionado, por exemplo (mas não limutado a isso) CrCshaloalquiltio, tais como clorometiltio, bromometiltio, diclorometiltio, triclorometiltio, fluorometiltio, difluorometiltio, trifluorometiltio, clorofluorometiltio, diclorofluorometiltio, clorodifluorometiltio, 1-cloroetiltio, 1bromoetiltio, 1-fluoroetiltio, 2-fluoroetiltio, 2,2-difluoroetiltio, 2,2,2trifluoroetiltio, 2-cloro-2-fluoroetiltio, 2-cloro-2,2-difluoroetiltio, 2,2dicloro-2-fluoroetiltio, 2,2,2-tricloroetiltio, pentafluoroetiltio e 1,1,1trifluoroprop-2-iltio;
[00298] heteroarila: um sistema de anel monocíclico completamente insaturados de 5 ou 6 membros que contém um a quarto heteroátomos do grupo consistindo em oxigênio, nitrogênio e enxofre; se o anel contiver uma pluralidade de átomos de oxigênio, estes não serão diretamente adjacentes;
[00299] heteroarila de 5 membros que contêm um a quatro átomos de nitrogênio ou um a três átomos de nitrogênio e um átomo de enxofre ou oxigênio: grupos heteroarila de 5 membros que, adicionalmente ao átomos de carbono, podem conter um a quatro átomos de nitrogênio ou um a três átomos de nitrogênio e um átomo
Petição 870180002928, de 12/01/2018, pág. 36/185
32/159 de enxofre ou oxigênio como membros de anel, por exemplo (mas não limitado a isso) 2-furila, 3-furila, 2-tienila, 3-tienila, 2-pirrolila, 3-pirrolila,
3-isoxazolila, 4-isoxazolila, 5-isoxazolila, 3-isotiazolila, 4-isotiazolila, 5isotiazolila, 3-pirazolila, 4-pirazolila, 5-pirazolila, 2-oxazolila, 4oxazolila, 5- oxazolila, 2-tiazolila, 4-tiazolila, 5-tiazolila, 2-imidazolila, 4imidazolila, 1,2,4-oxadiazol-3-ila, 1,2,4-oxadiazol-5-ila, 1,2,4-tiadiazol3-ila, 1,2,4-tiadiazol-5-ila, 1,2,4-triazol-3-ila, 1,3,4-oxadiazol-2-ila, 1,3,4tiadiazol-2-ila e 1,3,4-triazol-2-ila;
[00300] heteroarila de 5 membros que são ligados via nitrogênio e contêm um a quarto átomos de nitrogênio, ou heteroarila de 5 membros benzo-fundidos que são ligados via nitrogênio e contêm um a três átomos de nitrogênio: grupos heteroarila de 5 membros, adicionalmente a átomos de carbono, podem conter um a quarto átomos de nitrogênio e um a três átomos de nitrogênio, respectivamente, como membros de anel e no qual dois membros de anel carbono adjacentes ou um nitrogênio e um membro de anel carbono adjacente podem ser ligados em ponte por um grupo buta-1,3-dien-1,4diila no qual um ou dois átomos de carbono podem ser substituídos por átomos de nitrogênio, sendo que esses anéis são ligados ao esqueleto via um dos membros de anel de nitrogênio, por exemplo, (mas não limitado a isso) 1-pirrolila, 1-pirazolila, 1,2,4-triazol-1-ila, 1-imidazolila, 1,2,3-triazol-1-ila, 1,3,4-triazol-1-ila;
[00301] heteroarila de 6 membros que contêm um a quarto átomos de nitrogênio: grupos heteroarila de 6 membros que, adicionalmente a átomos de carbono, podem conter um a três ou um a quatro átomos de nitrogênio como membros de anel, por exemplo, (mas não limitado a isso) 2-piridinila, 3-piridinila, 4-piridinila, 3-piridazinila, 4piridazinila, 2-pirimidinila, 4-pirimidinila, 5-pirimidinila, 2-pirazinila, 1,3,5-triazin-2-ila, 1,2,4-triazin-3-ila e 1,2,4,5-tetrazin-3-ila;
Petição 870180002928, de 12/01/2018, pág. 37/185
33/159 [00302] heteroarila de 5 membros benzo-fundidos que contêm um a três átomos de nitrogênio ou um átomo de nitrogênio e um átomo de oxigênio ou enxofre: por exemplo (mas não limitado a isso) 1 H-indol-1 -ila, 1 H-indol-2-ila, 1 H-indol-3-ila, 1 H-indol-4-ila, 1Hindol-5-ila, 1 H-indol-6-ila, 1 H-indol-7-ila, 1H-benzimidazol-1-ila, 1Hbenzimidazol-2-ila, 1H-benzimidazol-4-ila, benzimidazol-5-ila, 1Hindazol-1 -ila, 1H-indazol-3-ila, 1H-indazol-4-ila, 1H-indazol-5-ila, 1Hindazol-6-ila, 1H-indazol-7-ila, 2H-indazol-2-ila, 1-benzofuran-2-ila, 1benzofuran-3-ila, 1-benzofuran-4-ila, 1-benzofuran-5-ila, 1-benzofuran6-ila, 1-benzofuran-7-ila, 1-benzotiofen-2-ila, 1-benzotiofen-3-ila, 1benzotiofen-4-ila, 1-benzotiofen-5-ila, 1-benzotiofen-6-ila, 1-benzotiofen-7-ila, 1,3-benzotiazol-2-ila e 1,3-benzoxazol-2-ila, [00303] heteroarila de 6 membros benzo-fundidos que contêm um a três átomos de nitrogênio: por exemplo (mas não limitado a isso) quinolin-2-ila, quinolin-3-ila, quinolin-4-ila, quinolin-5-ila, quinolin6-ila, quinolin-7-ila, quinolin-8-ila, isoquinolin-1-ila, isoquinolin-3-ila, isoquinolin-4-ila, isoquinolin-5-ila, isoquinolin-6-ila, isoquinolin-7-ila, e isoquinolin-8-ila;
[00304] heterociclila: um heterociclo de três a quinze membros saturados ou parcilamente insaturados que contêm um a quatro heteroátomos do grupo consistindo em oxigênio, nitrogênio e enxofre: heterociclos mono-, bi- ou tricíclicos que contém, adicionalmente a membros de anel de carbono, um a três átomos de nitrogênio e/ou um átomo de oxigênio ou enxofre ou um ou dois átomos de oxigênio e/ou enxofre; se o anel contiver uma pluralidade de átomos de oxigênio, esses não serão diretamente adjacentes; tais como, por exemplo (mas não limitado a isso), oxiranila, aziridinila, 2-tetra-hidrofuranila, 3-tetrahidrofuranila, 2-tetra-hidrotienila, 3-tetra-hidrotienila, 2-pirrolidinila, 3pirrolidinila, 3-isoxazolidinila, 4-isoxazolidinila, 5-isoxazolidinila, 3isotiazolidinila, 4-isotiazolidinila, 5-isotiazolidinila, 3-pirazolidinila, 4Petição 870180002928, de 12/01/2018, pág. 38/185
34/159 pirazolidinila, 5-pirazolidinila, 2-oxazolidinila, 4-oxazolidinila, 5oxazolidinila, 2-tiazolidinila, 4-tiazolidinila, 5-tiazolidinila, 2imidazolidinila, 4-imidazolidinila, 1,2,4-oxadiazolidin-3-ila, 1,2,4oxadiazolidin-5-ila, 1,2,4-tiadiazol idin-3-ila, 1,2,4-tiadiazolid in-5-ila,
1.2.4- triazol idin-3-i la, 1,3,4-oxadiazolidin-2-ila, 1,3,4-tiadiazol idin-2-ila,
1.3.4- triazolidin-2-ila, 2,3-di-hidrofur-2-ila, 2,3-di-hidrofur-3-ila, 2,4-dihidrofur-2-ila, 2,4-di-hidrofur-3-ila, 2,3-di-hidrotien-2-ila, 2,3-di-hidrotien-3-ila, 2,4-di-hidrotien-2-ila, 2,4-di-hidrotien-3-ila, 2-pirrolin-2-ila, 2pirrolin-3-ila, 3-pirrolin-2-ila, 3-pirrolin-3-ila, 2-isoxazolin-3-ila, 3isoxazolin-3-ila, 4-isoxazolin-3-ila, 2-isoxazolin-4-ila, 3-isoxazolin-4-ila,
4-isoxazolin-4-ila, 2-isoxazolin-5-ila, 3-isoxazolin-5-ila, 4-isoxazolin-5ila, 2-isotiazolin-3-ila, 3-isotiazolin-3-ila, 4-isotiazolin-3-ila, 2-isotiazolin4- ila, 3-isotiazolin-4-ila, 4-isotiazolin-4-ila, 2-isotiazolin-5-ila, 3isotiazolin-5-ila, 4-isotiazolin-5-ila, 2,3-di-hidropirazol-1-ila, 2,3-dihidropirazol-2-ila, 2,3-di-hidropirazol-3-ila, 2,3-di-hidropirazol-4-ila, 2,3di-hidropirazol-5-ila, 3,4-di-hidropirazol-1 -ila, 3,4-di-hidropirazol-3-ila,
3.4- d i-h id ropi razol-4-i la, 3,4-d i-h id ropi razo l-5-i la, 4,5-di-hidroopirazol-1 ila, 4,5-di-hidropirazol-3-ila, 4,5-di-hidropirazol-4-ila, 4,5-di-hidropirazol5- ila, 2,3-di-hidrooxazol-2-ila, 2,3-di-hidrooxazol-3-ila, 2,3-di-hidrooxazol-4-ila, 2,3-di-hidrooxazol-5-ila, 3,4-di-hidrooxazol-2-ila, 3,4-dihidrooxazol-3-ila, 3,4-di-hidrooxazol-4-ila, 3,4-di-hidrooxazol-5-ila, 3,4di-hidrooxazol-2-ila, 3,4-di-hidrooxazol-3-ila, 3,4-di-hidrooxazol-4-ila, 2piperidinila, 3-piperidinila, 4-piperidinila, 1,3-dioxan-5-ila, 2-tetrahidropiranila, 4-tetra-hidropiranila, 2-tetra-hidrotienila, 3-hexahidropiridazinila, 4-hexa-hidropiridazinila, 2-hexa-hidropirimidinila, 4hexa-hidropirimidinila, 5-hexa-hidropirimidinila, 2-piperazinila, 1,3,5hexa-hidrotriazin-2-ila e 1,2,4-hexa-hidrotriazin-3-ila;
[00305] grupo de saída: grupo de saída SN1 ou SN2, por exemplo, halogênio (cloro, bromo, iodo), alquilsulfonatos (-OSO2-alquila, por
Petição 870180002928, de 12/01/2018, pág. 39/185
35/159 exemplo -OSO2CH3, -OSO2CF3) ou arilsulfonatos (-OSO2-arila, por exemplo -OSO2Ph, -OSO2PhMe).
[00306] Não estão incluídas combinações que contradizem leis naturais e que o versado na técnica por isso teria excluído com base em seu conhecimento especializado. Estão excluídos, por exemplo, estruturas de anel que apresentam três ou mais átomos de oxigênio adjacentes.
[00307] A presente invenção, além disso, se refere a um processo para a preparação dos tiazóis substituídos por heterociclila da Fórmula (I) de acordo com a invenção, compreendendo pelo menos uma das etapas (a) a (u) abaixo:
(a) A conversão de compostos da fórmula (VII) na presença de um composto organometálico R9-M e, se apropriado, na presença de um solvente, em compostos da fórmula (VIII), de acordo com o esquema de reação abaixo (esquema 1):
O OH
W N
PG-Nv >-(' |
X S (VII)
R
H R—M W FT
-- PG-Ns >-<z I
R solvente
X S (VIII) [00308] em que [00309] PG = fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecionados do grupo consistindo em metila, metóxi, nitro, dioxolano), acetila, C1-C4alcoxicarbonila e benziloxicarbonila, [00310] M = por exemplo, MgCI, MgBr, Mgl, Li, [00311 ] R9 = C1-C4-alquila ou C3-C6-cicloalquila, [00312] W, X, e R2 são conforme definido para Fórmula (I) acima.
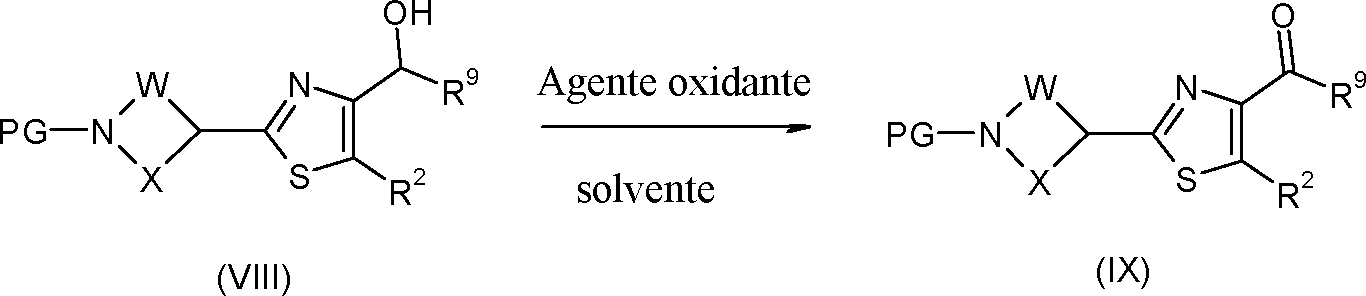
(b) A reação de alcoóis da fórmula (VIII) com um agente oxidante na presença de um solvente, para formar cetonas da fórmula (IX), de acordo com o esquema de reação abaixo (esquema 2):
Petição 870180002928, de 12/01/2018, pág. 40/185
36/159
[00313] em que [00314] PG = fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecionados do grupo consistindo em metila, metóxi, nitro, dioxolano), acetila e C1-C4alcoxicarbonila, [00315] R9 = CrC^alquila ou C3-C6-cicloalquila, [00316] W, X, e R2 são conforme definido para Fórmula (I) acima.
(c) a conversão de cetonas da fórmula (IX) na presença de uma base ou um ácido e, se apropriado, um solvente, em compostos da fórmula (IVb), de acordo com o esquema de reação abaixo (es-
base ou ácido, solvente
W
PG— X
N //
S'
Zl2-r3 (IVb) [00317] em que [00318] PG = fenilmetila não substituída ou substituída (sendo que os substituinmtes independentemente entre si são selecionados do grupo consistindo em metila, metóxi, nitro, dioxolano), acetila e Ci-C4alcoxicarbonila, [00319] L2=-CR9=CR9-, [00320] W, X, L3, R2, R3 e R9 são conforme definido para Fórmula (I) acima.
(d) A conversão de aldeídos da fórmula (VII) na presença de uma base ou um ácido e, se apropriado, um solvente, em compostos da fórmula (IVb), de acordo com o esquema de reação abaixo (esquema 4):
Petição 870180002928, de 12/01/2018, pág. 41/185
37/159
base ou ácido, solvente |_\ 3 3 l_—R3
PG—N XR2 (iVb) [00321] em que [00322] PG = fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecionados do grupo consistindo em metila, metóxi, nitro, dioxolano), acetila e C1-C4alcoxicarbonila, [00323] L2 = -CR9=CR9-, [00324] W, X, L3, R2, R3 e R9 são conforme definido para Fórmula (I) acima.
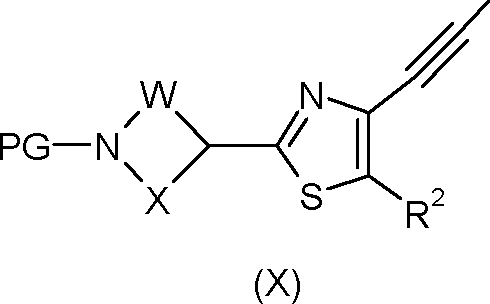
(e) A conversão de aldeídos da fórmula (VII) na presença de uma base e, se apropriado, um solvente, em alquinos da fórmula (X) de acordo com o esquema de reação abaixo (esquema 5):
[00325] em que [00326] PG = fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecionados do grupo consistindo em metila, metóxi, nitro, dioxolano), acetila e Ci-C4alcoxicarbonila, [00327] W, X e R2 são conforme definidio para Fórmula (I) acima.
(f) A reação de alquinos da fórmula (X) com um haleto
R3-L3- emu ma reação de acoplamento C-C opcionalmente catalisada na presença de uma base e, se apropriado, um solvente, para formar compostos da fórmula (IVc), de acordo com o esuema de reação abaixo(esquema 6):
Petição 870180002928, de 12/01/2018, pág. 42/185
38/159
| -H | R3-L3-Hal | ||
| PG—N | W X X S R2 | catalisador base solvente | 1 2 W N^/lZZr 3 PG_N z |
| (X) | (IVc) | ||
| [00328] | em que | ||
| [00329] | PG = fenilmetila não substituída ou substituída (sendo que |
os substituintes independentemente entre si são selecionados do grupo consistindo em metila, metóxi, nitro, dioxolano), acetila e C1-C4alcoxicarbonila, [00330] Hal = Cl, Brou I, [00331] L2=-ChC-, [00332] W, X, L3, R2 e R3 são conforme definido para Fórmula (I) acima.
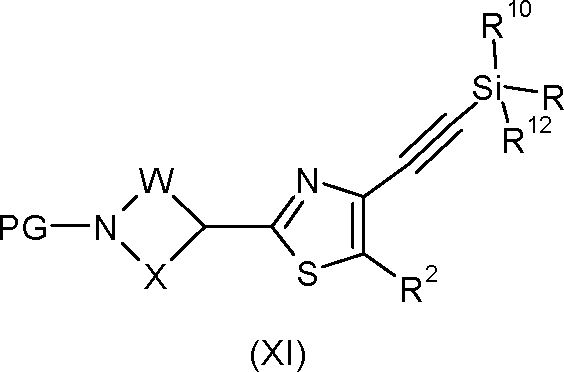
(g) A reação de alquinos da fórmula (X) com um cloreto de trialquilsilila (R10R11R12)SiCI ou triflato de trialquilsilila (R10R11R12)SiOSO2CF3 ou outros agentes de sililação conhecidos na presença de uma base e, se apropriado, um solvente, para formar compostos da fórmula (XI), de acordo com o esquema de reação abaixo (esquema 7):
base solvente (R10RnR12) SiCl
OU (R10R11R12)SiOSO2CF3
[00333] em que [00334] PG = fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecionados do grupo consistindo em metila, metóxi, nitro, dioxolano), acetila e Ci-C4alcoxicarbonila, [00335] R10, R11 e R12 = C1-C4 alquila ou fenila, [00336] W, X e R2 são conforme definido para Fórmula (I) acima.
(h) A reação de alquinos da fórmula (XI) com um composPetição 870180002928, de 12/01/2018, pág. 43/185
39/159 to R3-L3-Hal, se apropriado na presença de um catalisador, na presença de uma base e, se apropriado, um solvente, para formar compostos da fórmula (IVc), de acordo com o esquema de reação abaixo (esquema 8):
[00337] em que [00338] PG = fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si sao selecionados do grupo consisitndo em metila, metóxi, nitro, dioxolano), acetila e Ci-C4alcoxicarbonila, [00339] Hal = Cl, Brou I, [00340] R2 = hidrogênio, Ct^-alquila ou C1-C2-haloalquila, [00341] L2=-ChC-, [00342] R10, R11 e R12 = Ci-C4-alquila ou fenila, [00343] W, X, L3 e R3 são conforme definido para Fórmula (I) acima.
(i) A reação de tioamidas da fórmula (V) com compostos da fórmula (Via) ou (Vlb) na presença de uma base e, se apropriado, na presença de um solvente, para formar compostos da fórmula (IVa) ou (IVb), de acordo com o esquema de reação abaixo (esquema 9):
(V) (Via), (Vlb) (IVa), (IVb) [00344] em que [00345] PG = fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecionados do grupo consistindo em metila, metóxi, nitro, dioxolano), acetila, Ci-C4alcoxicarbonila e benziloxicarbonila, [00346] Hal = Cl, Brou I,
Petição 870180002928, de 12/01/2018, pág. 44/185
40/159 [00347] L2 = -C(R3)2-C(R3)2- para compostos da fórmula (IVa) e (Via), [00348] L2 = -CR9=CR9- para compostos da fórmula (IVb) e (Vlb), [00349] W, X, L3, R2, R3, R8 e R9 são conforme definido para Fórmula (I) acima.
(j) A conversão de compostos da fórmula (IVb) ou (IVc) na presença de hidrogênio, um catalisador e, se apropriado, um solvente, em compostos da fórmula (IVa), de acordo com o esquema de reação abaixo, (esquema 10):
h2
(IVb), (IVc) (IVa) [00350] em que [00351] PG = acetila ou (A-C^alcoxicarbonila, [00352] L2 = -C(R8)2-C(R8)2- para compostos da fórmula (IVa), [00353] L2 = -CR9=CR9- para compostos da fórmula (IVb), [00354] L2 = -C=C- para composto da fórmula (IVc), [00355] W, X, L3, R2, R3, R3 e R9 são conforme definido para Fórmula (I) acima.
(k) A conversão de compostos da fórmula (IV), se apropriada na presença de um solvente e, se apropriado na presença de um ácido ou, se apropriado, na presença de uma base ou, se apropriado, na presença de uma fonte de hidrogênio, em compostos da fórmula (II), de acordo com o esquema de reação abaixo (esquema 11):
se apropriado na base ou se apropriado no ácido ou se apropriado H2
(li) solvente (iv) [00356] em que [00357] PG = acetila, (A-C^alcoxicarbonila ou benziloxicarbonila,
Petição 870180002928, de 12/01/2018, pág. 45/185
41/159 [00358] W, X, L2, L3, R2, e R3são conforme definido para Fórmula (I) acima.
(I) A conversão de compostos da fórmula (lia’) na presença de um agente halogenante, se apropriado na presença de um ácido e um solvente, em compostos da fórmula (Ila), de acordo com o esquema de reação abaixo (esquema 12):
w HN\
I L^l_3_p3 Agente halogenante solvente se apropriado no ácido ou na base
L-R3 [00359] [00360] [00361] [00362] [00363] em que
L2 = -C(R8)2-C(R8)2R2 = I, Br ou Cl para compostos da fórmula (Ila),
R2 = hidrogênio para compostos da fórmula (lia’),
W, X, L3, R3 e R8 são conforme definido para fórmulaFórmula (I) acima.
(m) A reação de compostos da fórmula (III) com compostos da fórmulafórmula (II), se apropriado na presença de um agente de acoplamento, uma base e um solvente, para formar compostos da Fórmula (I), de acordo com o esquema de reação abaixo (esquema
13):
w HN\ z
Y' |_\ 3 3 ^L-R solvente se apropriado na base, se apropriado de um agente de acoplamento
Y. w
Ar3
A— L (II) (III) (I) [00364] em que [00365] B = OH, cloro, bromo ou iodo, [00366] Y = oxigênio, [00367] A, W, X, L1, L2, L3, R2, e R3 são conforme definido para
Fórmula (I) acima.
(η) A conversão de compostos da Fórmula (I) na presença
Petição 870180002928, de 12/01/2018, pág. 46/185
42/159 de um agente sulfurizante e, se apropriado, na presença de um solvente, em compostos da Fórmula (I), de acordo com o esquema de reação abaixo (esquema 14):
Y. W I
Vr3 agente sulfurizante
A—L solvente
Y. W khI ,— L X S^x„2 [00368] [00369] (l)
Y = o em que A, W, X, L1
Y =s (l)
L2, L3, R2, e R3 são conforme definido para
Fórmula (I) acima.
(o) A conversão de aldeídos da fórmula (XII) na presença de uma base e, se apropriado, um solvente, em alquinos da fórmula (XIII), de acordo com o esquema de reação abaixo (esquema 17):
[00370] em que [00371] A, W, X, Y, L1 e R2 são conforme definido para Fórmula (I) acima.
(p) A reação de alquinos da fórmula (XIII) com um cloreto de trialquilsilila (R10R11R12)SiCI ou triflato de trialquilsilila (R10R11R12)SiOSO2CF3 ou outros agentes sililantes conhecidos na presença de uma base e, se apropriado, um solvente, para formar compostos da fórmula (XIV), de acorod com o esquema de reação abaixo (esquema 18):
[00372] em que [00373] R10,R11eR12 (R10RnR12) SiCl
OU (R10R11R12)SiOSO2CF3 base solvente
A-L
C1-C4 alquila ou fenila,
Petição 870180002928, de 12/01/2018, pág. 47/185
43/159 [00374] A, W, X, Υ, L1 e R2 são conforme definidos para Fórmula (I) acima.
(q) A reação de alquinos da fórmula (XIII) com um haleto R3-L3- emu ma reação de acoplamento C-C opcionalmente catalisada na presença de uma base e, se apropriado, um solvente para formar compostos da fórmula (lc), de acordo com o esquema de reação abaixo (esquema 19):
[00375] em que [00376] Hal = Cl, Brou I, [00377] L2=-ChC-, [00378] A, W, X, Y, L1 L3, R2 e R3 são conforme definidos para Fórmula (I) acima.
(r) A reação de alquinos da fórmula (XIV) com um composto R3-L3-Hal, se apropriado na presença de um catalisador, na presença de uma base e, se apropriado, um solvente, para formar compostos da fórmula (lc), de acordo com o esquema de reação abaixo (esquema 20):
R3-L3-Hal catalisador base solvente
W
-NZ 1 \
A-L1 X (lc)
V-r3 [00379] em que [00380] Hal = Cl, Brou I, [00381] L2=-ChC-, [00382] R10, R11 e R12 = Ci-C4-alquila ou fenila,
Petição 870180002928, de 12/01/2018, pág. 48/185
44/159 [00383] A, W, X, Y, L1 L3, R2 e R3 são conforme definido para Fórmula (I) acima.
(s) A conversão de aldeídos da fórmula (XII) na presença de uma base ou um ácido e, sew apropriado, um solvente, em compostos da fórmula (lb), de acordo com o esquema de reação abaixo (esquema 21):
y
A-L1
(lb)
Y-R3 em que
L2=-CR9=CR9-, [00384] [00385] [00386]
A, W, X, Y, L1 L3, R2, R3 e R9 são conforme definido para
Fórmula (I) acima.
(t) A conversão de compostos da fórmula (lc) na presença de hidrogênio, um catalisador e, se apropriado, um solvente, em compostos da fórmula (lb), de acordo com o esquema de reação abaixo (esquema 22):
h2
[00387] em que [00388] L2 = -CR9=CR9- para compostos da fórmula (lb), [00389] L2 = -C=C- para compostos da fórmula (lc), [00390] A, W, X, Y, L1 L3, R2, R3 e R9 são conforme definido para a Fórmula (I) acima.
(u) A conversão de compostos da fórmula (lb) ou (lc) na presença de hidrogênio, um catalisador e, se apropriado, um solvente em compostos da fórmula (la), de acordeo com o esquema de reação abaixo (esquema 23):
Petição 870180002928, de 12/01/2018, pág. 49/185
45/159
Η.
A-L
l:
catalisador solvente
R'
Y
A-L
l:
R' (lc) (lb) [00391] em que [00392] L2 = -C(R3)2-C(R3)2- para compostos da fórmula (la), [00393] L2 = -CR9=CR9- para compostos da fórmula (lb), [00394] L2 = -C=C- para compostos da fórmula (lc), [00395] A, W, X, Y, L1 L3, R2, R3, R8 e R9 são conforme definido para Fórmula (I) acima.
[00396] Um sumário geral das trajetórias de síntese é mostrado nos esquemas 15 e 24.
[00397] Um composto da fórmula geral (V) é reagido com um composto da fórmula (Via) ou (Vlb) para formar um composto cíclico da fórmula (IVa) ou (IVb) (esquema 9). Outra opção de compostos de preparação da fórmula (IV) é iniciar com compostos da fórmula (VII). Esses podem ser submetidos a uma reação com um substrato da fórmula geral R9-M (esquema 1). Um álcoolálcool secundário da fórmula (VIII) é formado, sendo em seguida oxidizado, formando um composto da fórmula (IX) (esquema 2). Um composto da fórmula (VII) ou (IX) é submetido a uma olefinação para preparar um composto da fórmula (IVb) (esquema 3 e esquema 4). Outra possível rota de preparação de compostos da fórmula (IV) também inicia com um composto da fórmula (VII). Um composto da fórmula (VII) é alquinilatado para preparar um alquino terminal da fórmula geral (X) (esquema 5). Uma reação de acoplamento C-C metal-catalisadcatalisado de transição de um composto da fórmula (X) com um haleto da fórmula R3-L3-Hal forma um composto da fórmula (IVc) (esquema 6). Um composto da fórmula (X) também pode ser provido com um grupo silila, que resulta em um composto da fórmula (XI) (esquema 7). Este é então submetido a uma
Petição 870180002928, de 12/01/2018, pág. 50/185
46/159 reação de acoplamento metal-catalisada de transição, nomeadamente com um substrato da fórmula geral R3-L3-Hal, para preparar um composto da fórmula (IVc) (esquema 8). Sob utilização de hidrogênio, as ligações duplas e triplas de um compost da fórmula (IVb) e (IVc) podem ser hidrogenadas para formar um composto da fórmula (IVa) (esquema 10). O grupo protetor de um composto da fórmula (IV), que é identificada por PG, é então removido, formando um composto da fórmula (II) ou o sal correspondente (esquema 11). Um composto da fórmula (lia’) pode ser halogenado para formar um composto da fórmula (Ila) (esquema 12). Um composto da fórmula (II) ou um sal correspondente é acoplado com um substrato da fórmula (III), que permite a preparação de um composto da Fórmula (I) (esquema13). Um composto da Fórmula (I) é tratado com um agente sulfurizante para gerar um composto da Fórmula (I) (esquema 14).
Esquema 15
PG-N oi
V w s PG-N >—C
X N
3
L-R yv VV xh? T
A-L X 'Mr3 (R10RnR12) SiCl (R10R11R12)SiOSO2CF3 base solvente (I)
S (XI) (V)
R3-L3-Hal
C-C-acoplamento
R3-L3-Hal (Via), (Vlb) ciclização
W w J
-L X S^| (I) sulfurização
N^x^l-R3
Vb
A-L1 (Hl)
W N . pg-n' >—<' I
X S' (X)
C-C-aco- a W N^X^L plamento PG“Nx 2-Ç ||
V
L-, Ir3 (IVa) (IVb) (IVc) desproteção
W
-► h-n; >—c solvente R (Ila), (llb), (llc) ,N^/L'L-R3 alquinilado (IVc)(IVb)“(IVa)
-(IVa) halogenação (Ila') (Ila) olefinação olefinação
OH w N^X^H r—M W N^X^R'
PG-Nx >-<z T -► PG-Ν' >-<' T
X S^R2 χ solvente | oxidação
W N . pg-n; >—<z I (VII) (VIII) (IX) [00398] Outra possível via de preparação de compostos da Fórmula (I) inicia com um composto da fórmula (XII) (esquema 24). Um comPetição 870180002928, de 12/01/2018, pág. 51/185
47/159 posto da fórmula (XII) é alquinilado para preparar um alquino terminal da fórmula geral (XIII) (esquema 17). Uma reação de acoplamento C-C metal-catalisada de transição de um composto da fórmula (XIII) com um haleto da fórmula R3-L3-Hal resulta em um composto da fórmula (lc) (esquema 19). Um composto da fórmula (XIII) também pode ser provido com um grupo silila, que resulta em um composto da fórmula (XIV) (esquema 18). Este é então submetido a uma reação de acoplamento metal-catalisada de transição, nomeadamente com um substrato da fórmula geral R3-L3-Hal, para preparar um composto da fórmula (lc) (esquema 20). Um composto da fórmula (XII) é submetido a uma olefinação para preparar um composto da fórmula (lb) (esquema 21). Sob utilização de hidrogênio, a ligação tripla de um composto da fórmula (lc) pode ser hidrogenada, para formar um composto da fórmula (lb) (esquema 22). Utilizando-se hidrogênio, as ligações duplas e triplas de um composto da fórmula (lb) e (lc) podem ser hidrogenadas para formar um composto da fórmula (la) (esquema 23).
Esquema 24
R3-L3-Hal
C-C-acoplamento (xiv) (R10RnR12) SiCl
OU (R10R11R12)SiOSO2CF3 base solvente
(lb)
R3-L3-Hal C-Cacoplamento
L~R (lc) (lc) -► (la) (lc) -► (lb) (lb) -► (la) [00399] Uma via de preparação do intermediário (VIII) do composto (VII) é conhecida no esquema 1.
Petição 870180002928, de 12/01/2018, pág. 52/185
48/159 [00400] Materiais de partida da fórmula (VIII) são preparados a partir do aldeído (VII) mediante adição de um reagente organometálico R9-M (por exemplo M = Mg, Li). Os alcoóis (VIII) são preferivelmente preparados mediante adição de um reagente Grignard R9-MgX (X = Cl, Br, ou I) a compostos (VII) em tetra-hidrofurano sob -78Ό, sob uma atmosfera inerte (vide, por exemplo, WO 07/039177).
[00401] O aldeído (VII) encontra-se comercialmente disposnível (por exemplo Maybridge) ou pode ser preparado a partir de precursores comercialmente disponíveis de acordo com procedimentos descritos na literatura. O aldeído (VII) é preparado, por exemplo, a partir da metila correspondente ou etil éster (XV) mediante redução com hidreto de alumínio e lítio em tetra-hidrofurano sob 0Ό, seguido de uma oxidação do álcool correspondente com reagente Dess-Martin sob temperatura ambiente em diclorometano (vide, por exemplo, WO 07/147336 e WO 07/039177 para a redução com hidreto de alumínio e lítio e J. Am. Chem. Soc. 1978, 100, 300-301; 1979, 101, 5294-5299; 1991, 113, 7277-7287 para a oxidação usando reagente Dess-Martin).
Figura 1
(XV) [00402] em que [00403] R = H ou grupos protetores amina ácido-lábeis, tais como, por exemplo, t-butoxicarbonila (tBoc) ou benziloxicarbonila (Cbz) ou um grupo protetor benzila, tais como, por exemplo, benzila (Bn).
[00404] W e X são conforme definido para Fórmula (I) acima.
[00405] Metil ou etil ésteres (XV) são conhecidos e podem ser preparados a partir de precursores comercialmente disponíveis de acordo com métodos descritos na literatura, por exemplo a partir de nitrilas da fórmula (XVI), ácidos carboxílicos da fórmula (XVII), cloretos de carboPetição 870180002928, de 12/01/2018, pág. 53/185
49/159 nila da fórmula (XVIII), amidas da fórmula (XIX) ou tioamidas da fórmula (V) (Figura 2). Um método preferido é a síntese de tiazóis de Hantzsch. Partindo de (V) e etil ou metal halpiruvato comercialmente disponível em etanol ou em /V,/V-dimetilformamida na presença de, por exemplo, trietilamina sob temperatura ambiente (por exemplo, vide o documento WO 07/014290 e as referências aqui citadas).
Figura 2 w
R—N\ z o
/
Cl (XVI)
W R_N\ / (XVII)
(XVIII) (xix) (V) [00406] em que [00407] R = H ou grupos protetores amina ácido-lábeis, tais como, por exemplo, t-butoxicarbonila (tBoc) ou benziloxicarbonila (Cbz) ou um grupo protetor benzila, tais como, por exemplo, benzila (Bn).
[00408] W e X são conforme definido para a Fórmula (I) acima. [00409] Uma via de preparação de intermediário (IX) a partir do composto (VIII) é mostrada no esquema 2.
[00410] Compostos da fórmula (IX) são preparados por oxidação do álcool (VIII). Existem numerosos métodos para preparação de cetonas a partir de alcoóis secundários na literatura (vide Oxidation of Alcohols to Aldehydes e Ketones, Gabriel Tojo, Marcos Fernández , Springer Berlin, 2006, 1-97, e a literatura aqui citada). A oxidação é preferivelmente executada sob condições de Swern ou mediante o uso de periodinano Dess-Marti (vide, por exemplo, J. Am. Chem. Soc. 1978, 100, 300301). Solventes adequados são todos os solventes que por sua vez não são oxidados pelo agente oxidante tais como, por exemplo, diclorometano, clorofórmio ou acetonitrila, se apropriado na presença de um auxiliar de reação, por exemplo, um ácido (por exemplo ácido sulPetição 870180002928, de 12/01/2018, pág. 54/185
50/159 fúrico ou ácido clorídrico) ou senão uma base (por exemplo, trietilamina ou piridina).
[00411] Uma via de obtenção de intermediário (IX) a partir do composto (VIII) é, por exemplo, utilizando periodinano Dess-Martin (15% em diclorometano, comercialmente disponível, por exemplo, de Acros). [00412] São adequados para uso como solventes todos os solventes usuais que são inertes sob as condiçoes de reação, tais como, por exemplo, éteres cíclicos e acíclicos (por exemplo, dietil éter, tetrahidrofurano, dioxano), hidrocarbonetos aromáticos (por exemplo, benzeno, tolueno, xileno), hidrocarbonetos halogenados (por exemplo, diclorometano, clorofórmio, tetracloreto de carbono), hidrocarbonetos aromáticos halogenados (por exemplo, clorobenzeno, diclorobenzeno), nitrilas (por exemplo, acetonitrila), ésteres carboxílicos (por exemplo, acetato de etila), amidas (por exemplo, Ν,Ν-dimetilformamida, N,Ndimetilacetamida), sulfóxido de dimetila, 1,3-dimetil-2-imidazolinona e água, e a reação pode ser realizada em misturas de dois ou mais desses solventes.
[00413] Os materiais de partida são empregados em quantidades equimolares; porém, o agente oxidante pode, se necessário, também ser usado em excesso. A reação é usualmente realizada sob temperaturas de 0Ό - 100Ό e preferivelmente sob temperat ura ambiente, porém também pode ser feita na temperatura de refluxo da mistura de reação. O período de reação varia em função da escala da reaçÃO e da temperatura de reação, mas em geral situa-se entre alguns minutos e 48 horas.
[00414] Após a reação ter terminado, o composto (IX) é removido da mistura de reação utilizando-se uma das técnicas de separação usuais. Se necessário, os compostos são purificados por recristalização, destilação e cromatografia, ou eles podem, se necessário, também ser usados para a próxima etapa sem purificação prévia.
Petição 870180002928, de 12/01/2018, pág. 55/185
51/159 [00415] Uma via de preparação do intermediário (IVb) a partir do composto (IX) ou (VII) é mostrada nos esquemas 3 e 4.
[00416] Cetonas da fórmula (IX) ou aldeídos da fórmula (VII) são convertidos em (Z)- ou (E)-(IVb), por exemplo, por uma olefinação de Wittig ou Horner-Wadsworth-Emmons (vide, por exemplo, Chem. Rev. 1989, 89, 863-927 e as referências aqui citadas) ou, por exemplo, através de uma olefinação Julia (vide, por exemplo, Tetrahedron Lett., 1973, 14, 4833-4836) ou, por exemplo, por uma olefinação de Peterson (vide, por exemplo, J. Org. Chem. 1968, 33, 780). Preferivelmente, a olefinação é realizada sob condições de Wittig ou HornerWadsworth-Emmons.
[00417] Os reagentes, tais como sais de fosfônio e reagentes de fosfonato, estão tanto comercialmente disponíveis como podem ser obtidos da maneira descrita na literatura (vide, pore exemplo, The Chemistry of Organophosphorus Compounds; John Wiley & Sons, 1994, Vol 3, 45-184, e na literatura aqui citada).
[00418] São adequados para o uso como solventes, todos os solvents usuais que são inertes sob as condições de reação, tais como por exemplo, éteres cíclicos e acíclicos (por exemplo dietil éter, tetrahidrofurano, dioxano), hidrocarbonetos aromáticos (por exemplo, benzeno, tolueno, xileno), hidrocarbonetos halogenados (por exemplo, diclorometano, clorofórmio, tetracloreto de carbono), hidrocarbonetos aromáticos halogenados (por exemplo clorobenzeno, diclorobenzeno), e a reação pode ser realizada em misturas de dois ou mais desses solventes. Os solventes preferidos são tetra-hidrofurano e tolueno. [00419] São adequados para o uso como bases as bases usualmente empregadas nas reações de olefinação acima, por exemplo, NaH, tBuOK, nBuLi, (vide, por exemplo, Rev. 1989, 89, 863-927 e as referênciasaqui citadas). Ácidos adequados são aqueles que sçao
Petição 870180002928, de 12/01/2018, pág. 56/185
52/159 usualmente empregados em reações de olefinação, tais como por exemplo,, ácidos sulfônicos ou ácido sulfúrico.
[00420] Os materiais de partida são empregados em quantidades equimolares; porém, os sais de fosfônio ou fosfonatos podem, se necessário, também ser usados em excesso. A reação é usualmente realizada sob temperaturas de 0Ό - 100Ό e preferível mente sob 0Ό 25Ό, mas ela também pode ser realizada sob a tempe ratura de refluxo da mistura de reação. O period de reação varia em função da escala e da temperatura de reação, mas em geral situa-se entre alguns minutes e 48 horas.
[00421] Após a reação ter terminado, compostos (IVb) são removidos da mistura de reação utilizando-se as técnicas de separação usuais. Se necessário, os compostos são purificados por recristalização, destilação ou cromatografia, ou eles podem, se necessário, também ser usados para a p'roxima etapa sem purificação prévia.
[00422] Uma via de preparação do intermediário (X) a partir do composto (VII) é mostrada no esquema 5.
[00423] Ela é conhecida da literatura em que alquinilações de aldeídos podem ser feitas por uma reação de Corey-Fuchs (Tetrahedron Lett. 1972, 36, 3769-3772) ou por uma homologação de SeyferthGilbert (vide, por exemplo, J. Org. Chem., 1996, 61, 2540-2541). Alternativamente, o alquino (X) também pode ser preparado a partir do aldeído (VII) utilizando-se o reagente de Bestmann-Ohira analogamente aos procedimentos da literatura (vide, por exemplo, Synthesis 2004, 1, 59-62).
[00424] São adequados para o uso como solventes todos os solventes usuais que são inertes sob as condições de reação, tais como, por exemplo, éteres cíclicos e acíclicos (por exemplo, dietil éter, tetrahidrofurano, dioxano),hidrocarbonetos aromáticos (por exemplo, benzeno, tolueno, xileno), hidrocarbonetos halogenados (por exemplo, diPetição 870180002928, de 12/01/2018, pág. 57/185
53/159 clorometano, clorofórmio, tetracloreto de carbono) e hidrocarbonetos aromáticos halogenados (por exemplo, clorobenzeno, diclorobenzeno), e a reação pode ser feita em misturas de dois ou mais desses solventes. Os solventes preferidos são tetra-hidrofurano e tolueno.
[00425] Todas as bases conhecidas podem ser usadas na reação; porém, é preferido o uso de óxidos de metal alcalino e de metal alcalino-terroso, hidróxidos e carbonatos. Pelo menos, um equivalente da base deve ser adicionado ao reagente de Bestmann-Ohira e, se necessário, a base pode ser usada em excesso.
[00426] Os materiais de partida são empregados em quantidades equimolares; porém, o reagente de Bestmann-Ohira pode, se necessário, também ser usado em excesso. A reação é usualmente realizada sob temperaturas de 0Ό - 60Ό e preferivelmente so b 0Ό - 40Ό, mas também pode ser feita na temperatura de refluxo da mistura de reação. O period de reação varia em função da escala e da temperatura de reação, mas em geral situa-se entre alguns minutos e 48 horas. [00427] Após a reação ter terminado, os compostos (Vlc) são removidos da mistura de reação utilizando-se uma das técnicas de separação costumeira. Se necessário, os compostos são purificados por recristalização, destilação ou cromatografia, ou eles podem, se apropriado, também ser usados para a próxima etapa sem purificação prévia.
[00428] Analogamente ao método acima descrito, os compostos (XIII) podem ser sintetizados a partir dos compostos correspondentes (XII) conforme mostrado no esquema 17. O aldeído (XII) pode ser preparado de acordo com os procedimentos conhecidos na literatura (por exemplo, vide os documentos WO 08/013925, WO 08/013622 e as referências aqui citadas).
[00429] Uma via de preparação do intermediário (IVc) do composto (X) é mostrada no esquema 6.
Petição 870180002928, de 12/01/2018, pág. 58/185
54/159 [00430] Um composto da fórmula geral (IVc) pode ser obtido a partir do alquino da fórmula geral (X) por acoplamento transversal paládiocatalisado analogamente a procedimentos descritos na literatura (vide, por exemplo, J. Am. Chem. Soc. 2003, 125, 13642-13643, Synlett. 2006, 18, 2941-2946), nomeadamente utilizando um haleto da fórmula R3-L3-Hal, sendo que o haleto primário é reagido na presença de um catalisador tais como, por exemplo, [(n-alil)PdCI]2, Pd(OAc)2, PdCI2(CH3CN)2, Pd(PPh3)4 ou PdCI2(PPh3)2 e, se necessário, na presença de outros co-catalisadores, tais como, por exemplo, Cul, Cs2CO3 e cloreto de 1,3-bis(1-adamantil)imidazólio, por exemplo, em uma mistura de solvente de DMF e dietil éter sob 0-80Ό.
[00431] Haletos da fórmula R3-L3-Hal são comercialmente disponíveis ou podem ser obtidos por métodos conhecidos na literatura. [00432] Alternativamente, o alquino terminal também pode ser provido de um grupo protetor, tais como por exemplo, por reação com cloreto de benzila na presença de um catalisador de paládio (II), tais como, por exemplo, Pd(OAc)2 ou PdCI2(CH3CN)2, e carbonato de césioe também 2-diciclo-hexilfosfino-2’,4’,6’-triisopropilbifenila, em tetrahidrofurano ou acetonitrila sob 0-80Ό.
[00433] Após a reação ter terminado, os compostos (IVc) são removidos a partir da mistura de reação utilizando-se uma das técnicas de separação costumeiras. Se necessário, os compostos são purificados por recristalização, destilação ou cromatografia, ou eles podem, se necessário, ser usados para a próxima etapa sem purificação prévia. [00434] Analogamente ao método descrito acima, os compostos (lc) podem ser sintetizados a partir de compostos correspondentes (XIII) conforme mostrado no esquema 19.
[00435] Uma via de preparação do intermediário (XI) a partir do composto (X) é mostrada no esquema 7.
Petição 870180002928, de 12/01/2018, pág. 59/185
55/159 [00436] Para formar uma ligação direta entre a ligação tripla (L2 é C=C~) e R3, pode ser necessário sililatar o alquino terminal antes da reação de acoplamento paládio-catalisada. Sililações de alquinos terminais são realizadas utilizando-se um dos métodos mostrados para sililação de alquinos terminais, tais como, por exemplo, mediante adição de uma base (tais como, por exemplo, hexametildissilazida de lítio) sob -78°C em um solvente aprótico polar ao alq uino terminal e mediante captura do intermediário resultante utilizando-se, por exemplo, um haleto de silila (CHEMBIOCHEM, 2001, 1, 69-75) ou triflato de silila.
[00437] São adequados para uso como solventes todos solventes costumeiros que são inertes sob as condições de reação, tais como, por exemplo, éteres cíclicos e acíclicos (por exemplo, dietil éter, tetrahidrofurano, dioxano), hidrocarbonetos aromáticos (por exemplo benzeno, tolueno, xileno), hidrocarbonetos halogenados (por exemplo diclorometano, clorofórmio, tetracloreto de carbono) e hidrocarbonetos aromáticos halogenados (por exemplo clorobenzeno, diclorobenzeno). A reação também pode ser feita em misturas de dois ou mais desses solventes. Os solventes preferidos são tetra-hidrofurano e tolueno. [00438] Todas as bases conhecidas podem ser empregadas; porém, é preferido o uso de hexametildisilazida de lítio, hexametildisilazida de sódio, hexametildisilazida de potássio e di-isopropilamida de lítio para a reação. Pelo menos, um equivalente da base deve ser adicionado ao alquino da fórmula geral (X), e se necessário pode ser usado em excesso.
[00439] Pelo menos um equivalente de cloreto de silila ou triflato de silila pode ser usado como fonte do grupo silila na reação.
[00440] A reação é usualmente realizada sob temperaturas de 78Ό - 100Ό e preferivelmente sob -20Ό - 40Ό, ma s também pode ser feita na temperatura de refluxo da mistura de reação. O período de
Petição 870180002928, de 12/01/2018, pág. 60/185
56/159 reação varia em função da escala da reação e da temperatura de reaçao, mas em geral situa-se em alguns minutes e 48 horas.
[00441] Após a reação ter sido terminada, os compostos (XI) são removidos da mistura de reação utilizando-se uma das técnicas de separação costumeria. Se necessário, os compostos são purificados por recristalização, destilação e cromatografia, ou eles podem, se necessário, também ser usados para a próxima etapa sem purificação prévia.
[00442] Analogamente ao método acima descrito, os compostos (XIV) podem ser sintetizados a partir de compostos correspondentes (XIII) conforme mostrado no esquema 18.
[00443] Uma via de preparação do intermediário (IVc) a partir do composto (IX) é mostrada no esquema 8.
[00444] Um composto da fórmula geral (IVc) pode ser preparado a partir de um alquino da fórmula geral (XI) por reações de acoplamento paládio-catalisadas, tais como por exemplo a reação de Sonogashira (J. Med. Chem. 2006, 49, 1080-1110), sendo que o haleto apresenta a fórmula geral haleto R3-L3- na qual L3 é uma ligação direta.
[00445] Adequados para o uso como solventes são todos os solventes usuais que são inertes sob as condições de reação, tais como, por exemplo, éteres cíclicos e acíclicos (por exemplo, dietil éter, tetrahidrofurano, dioxano), hidrocarbonetos aromáticos (por exemplo, benzeno, tolueno, xileno), hidrocarbonetos halogenados (por exemplo, diclorometano, clorofórmio, tetracloreto de carbono), ésteres carboxílicos (por exemplo, acetato de etila), amidas (por exemplo, N,Ndimetilformamida, Ν,Ν-dimetilacetamida), sulfóxido de dimetila e 1,3dimetil-2-imidazolinona, e a reação pode ser realizada em misturas desses solventes. O solvente preferido é /V,/V-dimetilformamida.
[00446] A reação poderia ser feita na presença dos seguintes aditivos: trietilamina (pelo menos um equivalente baseado no composto
Petição 870180002928, de 12/01/2018, pág. 61/185
57/159 (XI)), cobre (I) iodo (pelo menos 0,1 equivalente com base no composto (XI)) e uma fonte de fluoreto tais como, por exemplo, fluoreto de tetra-n-butilamônio (pelo menos 1 equivalente baseado no composto (XI) ou um ligeiro excesso).
[00447] Um grande número dos catalisadores de paládio (0) comercialmente disponíveis são adequados para o uso na reação; porém, é preferido o uso de tetracistrifenilfosfinapaládio (Aldrich) na reação. A quantidade de catlisador usada é pelo menos 1% em relação a um excesso baseado no material de partida (XI).
[00448] A reação é usualmente realizada sob temperaturas sob temperaturas de 25Ό - 120Ό e preferivelmente sob 70Ό - 90Ό, mas também pode ser feita na temperatura de refluxo da mistura de reação. O periodo de reação varia em função da escala da reação e da temperature de reação, mas em geral situa-se entre alguns minutes e 48 horas.
[00449] Após a reação ter terminado, os compostos (IVc) são removidos da mistura de reação utilizando-se uma das técnicas de separação usuais. Se necessário, os compostos são purificados por recristalização, destilação e cromatografia, ou eles podem, se necessário, também ser usados para a próxima etapa sem purificação prévia. [00450] Analogamente ao método acima descrito, os compostos (lc) podem ser sintetizados a partir de compostos correspondentes (XIV) conforme mostrado no esquema 20.
[00451] Uma via de sintetização de compostos da fórmula (IVa) ou (IVb) é mostrada no esquema 9.
[00452] Tiocarboxamidas (V) encontram-se tanto comercialmente disponíveis como podem ser obtidos através de métodos conhecidos a partir da literatura, por exemplo, por sulfurização da carboxamida comercialmente disponível correspondente utilizando-se, por exemplo, reagente de Lawesson (Org Synth.\/o\. 7, 1990, 372) sob temperatura
Petição 870180002928, de 12/01/2018, pág. 62/185
58/159 ambiente em uma mistura de clorofórmio /dimetoxietano (1/2.5). Neste caso, PG representa um grupo protetor conforme definido no esquema 2.
[00453] α-Halocetonas (Via) e (Vlb) encontram-se tanto comercialmente disponíveis como podem ser obtidos através de métodos conhecidos a partir da literatura (por exemplo vide Molecules, 2003, 8, 793-865). Alternativamente, enolatos ou sililenol éteres preparados a partir de (Xlla) ou (Xllb) cpodem ser reagidos com uma fonte de halogênio para formar α-halocetonas (Via) ou (Vlb), (J. Med. Chem. 2006, 49, 7877-7886; J. Med. Chem. 2006, 49, 1080-1110; Org. Synth. Vol. 6, 1988, 175; Org. Synth. Vol. 53, 1973, 111). (esquema 16)
Esquema 16
Hal + solvente base
Hal (Xlla), (Xllb) (Via), (Vlb) [00454] No esquema 16, [00455] Hal = Cl, Br ou I, [00456] L2 = -C(R8)2-C(R8)2- para compostos da fórmula (Via) e (Xlla), [00457] L2 = -CR9=CR9- para compostos da fórmula (Vlb) e (Xllb), [00458] L3, R2, R3, R3 e R9 são conforme definido para Fórmula (I) acima.
[00459] Os tiazóis (IVa) ou (IVb) podem ser obtidos através da síntese de tiazóis de Hantzscha partir de tiocarboxamidas (V) e ahalocetonas (Via) ou (Vlb) (vide, por exemplo, Comprehensive Heterocyclic Chemistry, Pergamon Press, 1984; Vol 6, páginas 235-363, Comprehensive Heterocyclic Chemistry II, Pergamon Press, 1996; Vol 3, páginas 373-474 e as referências citadas aqui, e o documento WO 07/014290).
Petição 870180002928, de 12/01/2018, pág. 63/185
59/159 [00460] São adequados para o uso como solventes todos os solvents usuais que são inertes sob as condições de reação, tais como, por exemplo alcoóis ( por exemplo, metanol, etanol, propanol), éteres cíclicos e acíclicos (por exemplo, dietil éter, tetra-hidrofurano, dioxano), hidrocarbonetos aromáticos (por exemplo, benzeno, tolueno, xileno), hidrocarbonetos halogenados (por exemplo, diclorometano, clorofórmio, tetracloreto de carbono), hidrocarbonetos aromáticos halogenados (por exemplo clorobenzeno, diclorobenzeno), nitrilas (por exemplo, acetonitrila), ésteres carboxílicos (por exemplo, acetato de etila), amidas (por exemplo, N,N-dimetilformamida, Ν,Ν-dimeilacetamida), sulfóxido de dimetila, 1,3-dimetil-2-imidazolinona, água e ácido acético, ou a reação pode ser feita em misturas de um ou mais desses solventes. Os solventes preferidos são /V,/V-dimetilformamida e etanol.
[00461] Se necessário, é usada uma base auxiliar tal como por exemplo, trietilamina.
[00462] Os materiais de partida são empregados em quantidades equimolares. Porém, (V) ou (VI) podem respectivamente também ser usados em excesso. A reação é usualmente realizada sib temperaturas de 0Ό - 100Ό e preferivelmente sob temperatur a ambiente, mas ele também pode ser feita na temperatura de refluxo da mistura de reação. O period de reação varia em função da escala da reação e da temperatura de reação, mas em geral situa-se entre alguns minutes e 48 horas.
[00463] Se necessário, os compostos são purificados por recristalização ou cromatografia, ou eles podem, se necessário, também ser usados na próxima etapa sem previa purificação.
[00464] Uma via de preparação do intermediário (IVa) a partir do composto (IVb) ou (IVc) é mostrada no esquema 10.
[00465] Uma ligação tripla ou uma ligação dupla é convertida por hidrogenação utilizando-se um catalisador adequado em uma ligação
Petição 870180002928, de 12/01/2018, pág. 64/185
60/159 simples. Um catalisador para a reação no esquema 10 é selecionado dos catalisadores de hidrogenação conhecios da literatura (Reductions in Organic Chemistry”, Milos Hudlicky, John Wiley & Sons, 1984), tais como por exemplo, paládio em carbono ativado ou catalisador de Pearlmans (Pd(OH)2 em carbono ativado). Utilizando-se um catalisador, é possível preparar um composto da fórmula (IVa) a partir de um composto da fórmula (IVb) ou (IVc).
[00466] São adequados para o uso como solventes todos os solvents usuais que são inertes sob as condições de reaçao, tais como por exemplo, alcoóis (por exemplo, metanol, etanol, propanol), éteres cíclicos e acíclicos (por exemplo, dietil éter, tetra-hidrofurano, dioxano, dimetoxietano), hidrocarbonetos aromáticos (por exemplo, benzeno, tolueno, xileno), hidrocarbonetos halogenados (por exemplo, diclorometano, clorofórmio, tetracloreto de carbono), hidrocarbonetos aromáticos halogenados (por exemplo, clorobenzeno, diclorobenzeno), nitrilas (por exemplo, acetonitrila), ésteres carboxílicos (por exemplo, acetato de etila), amidas (por exemplo, N,N-dimetilformamida, N,Ndimetilacetamida), sulfóxido de dimetila, 1,3-dimetil-2-imidazolinona, água e ácido acético ou a reação pode ser feita em misturas de dois ou mais desses solventes. Os solventes preferidos são /V,/V-dimetilformamida e etanol.
[00467] A quantidade de catalisador usada é 0,1-90 moles porcento com base no material de partida; é preferido o uso de 1-30 moles porcento % do catalisador com base no material de partida. A reação pode ser realizada sob pressão superatmosférica (1-1000 bar) ou, preferivelmente, sob pressão atmosférica. A reação é usualmente realizada sob temperaturas de 0Ό - 150Ό e preferivelmente s ob temperatura ambiente, mas também pode ser feita na temperatura de refluxo da mistura de reação. O periodo de reação varia em função da escala da
Petição 870180002928, de 12/01/2018, pág. 65/185
61/159 reação e da temperatura de reação, mas em geral situa-se entre em alguns minutos e 48 horas.
[00468] Após a reação ter terminado, os compostos (IVa) são removidos da mistura de reação utilizando-se uma das técnicas de separação usuais. Se necessário, os compostos são purificados por recristalização, destilação ou cromatografia, ou eles podem, se apropriado, também ser usados para a próxima etapa sem prurificação prévia. [00469] Uma via de preparação do intermediário (II) a partir de compostos correspondentes (IV) é mostrada no esquema 11.
[00470] Um composto da fórmula geral (IV) é convertido em um composto correspondente da fórmula geral (II) através de métodos adequados, descritos na literatura, para remoção de grupos protetores (Protective Groups in Organic Synthesis', Third Edition; Theodora W. Greene, Peter G. M. Wuts; 494-653, e na literatura aqui citada).
[00471] Grupos protetores t-Butoxicarbonila e benziloxicarbonila podem ser removidos em um meio acídico (por exemplo, utilizando-se ácido clorídrico ou ácido trifluoroacético). Grupos protetores acetila podem ser removidos sob condições básicas (utilizando, por exemplo, carbonato de potássio ou carbonato de césio). Grupos protetores benzílicos podem ser removidos hidrogenoliticamente utilizando-se hidrogênio na presença de um catalisador (por exemplo, paládio ou carbono ativado).
[00472] São adequados para o uso como solventes todos os solventes usuais que são inertes sob as condições de reação, tais como por exemplo alcoóis (por exemplo, metanol, etanol, propanol), éteres cíclicos e acíclicos (por exemplo, dietil éter, tetra-hidrofurano, dioxano), hidrocarbonetos aromáticos (por exemplo, benzeno, tolueno, xileno), hidrocarbonetos halogenados (por exemplo, diclorometano, clorofórmio, tetracloreto de carbono), hidrocarbonetos halogenados aromáticos (por exemplo clorobenzeno, diclorobenzeno), nitrilas (por exemplo,
Petição 870180002928, de 12/01/2018, pág. 66/185
62/159 acetonitrila), ésteres carboxílicos (por exemplo, acetato de etila), amidas (por exemplo, Ν,Ν-dimetilformamida, Ν,Ν-dimetilacetamida), sulfóxido de dimetila, 1,3-dimetil-2-imidazolinona, água e ácido acético, ou a reação pode ser feita em misturas de dois ou mais desses solventes. [00473] Ácidos que podem ser usados para esta reação de desproteção de grupos t-butoxicarbonila e benziloxicarbonila são, por exemplo, ácido trifluoroacético, ácido clorídrico ou outros ácidos, conforme descrito na literatura (por exemplo, Protective Groups in Organic Synthesis', Third Edition; Theodora W. Greene, Peter G. M. Wuts; pp. 494-653).
[00474] A reação é usualmente feita sob temperaturas de 0Ό 150Ό e preferivelmente sob temperature ambiente, mas ela também pode ser feita na temperatura de refluxo da mistura de reação. O period de reação varia em função da escala da reação e da temperature de reação, mas em geral situa-se entre meia hora e 72 horas.
[00475] Após a reação ter terminado, os compostos (II) são removidos da mistura de reação utilizando-se uma das técnicas usuais de separação. Se necessário, os compostos são purificados por recristalização, destilação ou cromatografia, ou eles podem, se apropriado, também ser usados para a etapa seguinte sem prévia purificação. Além disso, é possível isolar o composto da fórmula geral (II) como um sal, por exemplo, como um sal de ácido clorídrico ou ácido trifluoroacético.
[00476] Uma via de preparação do intermediário (Ila) a partir do composto (lia’) é mostrada no esquema 12.
[00477] Um composto da fórmula geral (Ila) na qual R2 = Cl, Br e I é obtido por halogenação a partir de um composto da fórmula geral (lia’) em que R2 = H, vide, por exemplo, Org. Lett., 2005, 7(2), 299301; Angew. Chem., Int. Ed., 2004, 43(34), 4471-4475; Eur. J. Org. Chem., 2002, (13), 2126-2135.
Petição 870180002928, de 12/01/2018, pág. 67/185
63/159 [00478] São adequados para o uso como solventes todos os solvents usuais que são inertes sob as condições de reação, tais como, por exemplo, alcoóis (por exemplo, metanol, etanol, propanol), éteres cíclicos e acíclicos (por exemplo, dietil éter, tetra-hidrofurano, dioxano), hidrocarbonetos aromáticos (por exemplo, benzeno, tolueno, xileno), hidrocarbonetos halogenados (por exemplo, diclorometano, clorofórmio, tetracloreto de carbono), hidrocarbonetos aromáticos halogenados (por exemplo, clorobenzeno, diclorobenzeno), ésteres carboxílicos (por exemplo acetato de etila), amidas (por exemplo, Λ/,Λ/dimetilformamida, /V,/V-dimetilacetamida), sulfóxido de dimetila, 1,3dimetil-2-imidazolinona, água e ácido cético, ou a reação pode ser feita em misturas de dois ou mais desses soloventes.
[00479] São adequados para o uso como fonte de halogênio, por exemplo, /V-bromossuccinimida, /V-clorossuccinimida, /Viodossuccinimida, tribrometo de piridínio, bromo, iodo ou cloro.
[00480] Se apropriado, uma base, tais como por exemplo, di-isopropilamida de lítio ou butillítio, pode ser usada para litiar a posição 5 dos tiazóis antes da adição da fonte de halogênio eletrofílica.
[00481] A reação pode, se necessário, ser realizada utilizando-se um ácido, tais como por exemplo, ácido acético, ácido sulfúrico, ácido bromídrico ou ácido clorídrico.
[00482] Os materiais de partida e o agente de halogenação são empregados em quantidades equimolares. O agente halogenante também pode ser usado em excesso. A reação é usualmente realizada sob temperaturas de 0Ό - 60Ό e preferivelmente so b 0Ό - 30Ό, mas ela também pode ser feita na temperatura de refluxo da mistura de reação. O periodo de reação varia em função da escala da reação e da temperatura de reação, mas em geral situa-se entre alguns minutos e 48 horas.
Petição 870180002928, de 12/01/2018, pág. 68/185
64/159 [00483] Após a reação ter terminado, os compostos (II) são removidos da mistura de reação utilizando-se uma das técnicas usuais de separação. Se necessário, os compostos são purificados por recristalização, destilação e cromatografia, ou eles podem, se apropriado, também ser usados para a próxima etapa sem prévia purificação.
[00484] Uma via de preparação da Fórmula (I) na qual Y = oxigênio a partir de compostos correspondentes (II) é mostrada no esquema 13. [00485] Haletos de ácido (III) (B = halogênio) ou os ácidos carboxílicos correspondentes (III) (B = OH) encontram-se comercialmente disponíveis ou podem ser preparados por processos descritos na literatura. Além disso, o substrato da fórmula geral (III) em que B = Cl pode ser preparado a partir do ácido correspondente (B = OH) por clorinação utilizando-se processos conhecidos da literatura (por exemplo, 7etrahedron 2005, 61, 10827-10852, e da literatura aqui citada).
[00486] Um composto da fórmula geral (I) em que Y = O pode ser sintetizado através de uma reação de acoplamento de um composto da fórmula geral correspondente (II) com um substrato da fórmula geral (III) em que B = Cl, se necessário, na presença de um varredor de ácido / uma base.
[00487] São adequados para o uso como solventes todos os solvents usuais que são inertes sob as condições de reação, tais como, por exemplo, alcoóis (por exemplo, metanol, etanol, propanol), éteres cíclicos ou acíclicos (por exemplo, dietil éter, tetra-hidrofurano, dioxano), hidrocarbonetos aromáticos (por exemplo, benzeno, tolueno, xileno), hidrocarbonetos halogenados (por exemplo, diclorometano, clorofórmio, tetracloreto de carbono), hidrocarbonetos aromáticos halogenados (por exemplo, clorobenzeno, diclorobenzeno) e nitrilas (por exemploacetonitrila), ou a reação pode ser feita em misturas de dois ou mais desses solventes. Os solventes preferidos são are tetrahidrofurano e diclorometano.
Petição 870180002928, de 12/01/2018, pág. 69/185
65/159 [00488] Pelo menos um equivalente de um varredor de ácido / uma base (por exemplo, base de Hünig, trietilamina ou varredores de ácido polimérico comercialomente disponíveis) é empregado com base no material de partida da fórmula geral (II). Se o material de partida for um sal, pelo menos dois equivalentes do varredor de ácido serão necessários.
[00489] A reação é usualmente realizada sob temperaturas de OO 100Ό e preferivelmente sob 20Ό - 30Ό, mas ela ta mbém pode ser feita na temperatura de refluxo da mistura de reação. O período de reação varia em função da escala da reação e da temperatura de reação, mas em geral situa-se entre alguns minutos e 48 horas.
[00490] Após a reação ter terminado, os compostos (I) são removidos da mistura de reação utilizando-se uma das técnicas de separação convencionais. Se necessário, os compostos são purificados por recristalização, destilação e cromatografia, ou eles podem, se apropriado, também ser usados para a etapa seguinte sem prévia purificação. [00491] Alternativamente, um compost da Fórmula (I) em que Y = O ctambém pode ser sintetizado a partir do composto correspondente da fórmula geral (II) utilizando-se um substrato da fórmula geral (III) em que B = OH na presença de um agente de acoplamento, analogamente aos procedimentos na literatura (por exemplo Tetrahedron 2005, 61, 10827-10852, e as referências aqui citadas).
[00492] São adequados como agentes de acoplamento por exemplo, agentes de acoplamento de peptídeo (por exemplo, 1-etil-3-(30dimetilamino) carbodiimida misturada com 4-dimetilaminopiridina, 1etil-3-(30-dimetilamino)carbodiimida misturada com hidroxibenzotriazol, hexafluorofosfato de bromotri(pirrolidino)fosfônio, 2-(1H-7azabenzotriazol-1-il)-1,1,3,3-tetrametilurônio hexafluoro-fosfato metanamínio, etc.)
Petição 870180002928, de 12/01/2018, pág. 70/185
66/159 [00493] Se necessário, uma base, tal como por exemplo, trietilamina ou base de Hünig, pode ser empregada na reação.
[00494] São adequados para o uso como solventes todos os solventes usuais que são inertes sob as condições de reação, tais como, por exemplo, alcoóis (por exemplo, metanol, etanol, propanol), éteres cíclicos e acíclicos (por exemplo, dietil éter, tetra-hidrofurano, dioxano), hidrocarbonetos aromáticos (por exemplo, benzeno, tolueno, xileno), hidrocarbonetos halogenados (por exemplo, diclorometano, clorofórmio, tetracloreto de carbono), hidrocarbonetos aromáticos halogenados (por exemplo, clorobenzeno, diclorobenzeno), nitrilas (por exemplo acetonitrila) e amidas (por exemplo, Ν,Ν-dimetilformamida, N,Ndimetilacetamida), ou a reação pode ser realizada em misturas de dois ou mais desses solventes. Os solventes preferidos são Λ/,Λ/dimetilformamida e diclorometano.
[00495] A reação é usualmente feita sob temperaturas de 0Ό 100Ό e preferivelmente sob 0Ό - 30Ό, mas ela tam bém pode ser feita na temperatura de refluxo da mistura de reação. O periodo de reação varia em função da escala da reação e da temperatura de reação, mas em geral situa-se entre alguns minutes e 48 horas.
[00496] Após a reação ter terminado, os compostos (I) são removidos da mistura de reação utilizando-se uma das técnicas de seperação convencionais. Se necessário, os compostos são purificados por recristalização, destilação ou cromatografia, ou eles podem, se necessário, também ser usados para a próxima etapa sem prévia purificação. [00497] Uma via de preparação de compostos da Fórmula (I) na qual Y = enxofre, a partir de compostos correspondentes (I) em que Y é oxigênio é mostrada no esquema 14.
[00498] São adequados para o uso como solventes todos os solventes convencionais, que são inertes sob as condições de reação tais como por exemplo alcoóis (por exemplo, metanol, etanol, propanol),
Petição 870180002928, de 12/01/2018, pág. 71/185
67/159 éteres cíclicos e acíclicos (por exemplo, dietil éter, tetra-hidrofurano, dioxano), hidrocarbonetos aromáticos (por exemplo, benzeno, tolueno, xileno), hidrocarbonetos halogenados (por exemplo, diclorometano, clorofórmio, tetracloreto de carbono), hidrocarbonetos aromáticos halogenados (por exemplo, clorobenzeno, diclorobenzeno), nitrilas (por exemplo, acetonitrila), ésteres carboxílicos (por exemplo acetato de etila) e amidas (por exemplo Ν,Ν-dimetilformamida, N,Ndimetilacetamida), ou a reação pode ser realizada em misturas de dois ou mais desses solventes. Os solventes preferidos são clorofórmio e 1,2-dimetoxietano.
[00499] Agentes sulfurizantes adequados são, por exemplo, reagente de Lawesson (s. Tetrahedron 1986, 42, 6555-6564, Tetrahedron Lett. 1993, 46, 7459-7462) e pentassulfeto de fósforo. O material de partida e o agente sulfurizante são empregados em quantidades equimolares; porém, o agente sulfurizante pode, se necessário, também ser empregado em excesso.
[00500] A reação é usualmente realizada sob temperaturas de 0Ό 150Ό e preferivelmente sob 0Ό - 100Ό, mas ela ta mbém pode ser feita na temperatura de refluxo da mistura de reação. O period de reação varia em função da escala da reação e da temperatura de reação, mas em geral situa-se entre aluns minutos e 48 horas.
[00501] Após a reação ter terminado, os compostos (I) são removidos da mistura de reação utilizando-se uma das técnicas de separação convencionais. Se necessário, os compostos são purificados por recristalização, destilação e cromatografia.
[00502] Novos são compostos da fórmula (IX) na qual o
X (ix)
Petição 870180002928, de 12/01/2018, pág. 72/185
68/159 [00503] os símbolos apresentam os significados abaixo [00504] PG representa fenimetila não substituida ou substituída (sendo que os substituintes independentemente entre si são selecionados do grupo consistindo emem metila, metóxi, nitro, dioxolano), acetila, Ct-C^alcoxicarbonila ou benziloxicarbonila, [00505] R9= CrC^alquila, C3-C6-cicloalquila, [00506] W, X e R2 apresentam os significados gerais indicados acima, preferidos, particularmente preferidos ou muito particularmente preferidos.
[00507] Novos são compostos da fórmula (X) na qual
H
[00508] Os símbolos apresentam os significados abaixo:
[00509] PG representa fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecionados a partir do grupo consistindo em metila, metóxi, nitro, dioxolano), acetila, Ct-C^alcoxicarbonila ou benziloxicarbonila, [00510] W, X e R2 apresentam os significados gerais, acima indicados, preferidos, particularmente preferidos ou muito particularmente preferidos.
[00511] Novos são compostos da fórmula (XI) na qual
[00512] os símbolos apresentam os significados abaixo [00513] PG representa fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecionados do grupo consistindo em metila, metóxi, nitro, dioxolano), acetila, CrC^alcoxicarbonila ou benziloxicarbonila,
Petição 870180002928, de 12/01/2018, pág. 73/185
69/159 [00514] R10, R11 e R12 = Ci-C4-alquila ou fenila, [00515] W, X e R2 apresentam os significados gerais, acima indicados, preferidos, particularmente preferidos ou muito particularmente preferidos.
[00516] Novos são compostos da fórmula (IV) na qual
(IV) [00517] os símbolos apresentam os significados abaixo [00518] PG representa fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecionados do grupo consistindo em metila, metóxi, nitro, dioxolano), acetila, CrC^alcoxicarbonila ou benziloxicarbonila, [00519] W, X, L2, L3, R2, R3, R8 e R9 apresentam os significados gerais, acima indicados, preferidos, particularmente preferidos ou muito particularmente preferidos.
[00520] Novos são compostos da fórmula (llb) e (Ilc) na qual
(llb), (llc) [00521] os símbolos apresentam os significados abaixo [00522] L2 representa -CR9=CR9- para compostos da fórmula (llb) [00523] L2 representa -C=C- para compostos da fórmula (llc) [00524] W, X, L3, R2 R3, e R9 apresentam os significados gerais, acioma indicados preferidos, particularmente preferidos ou muito particularmente preferidos.
[00525] Novos são compostos da fórmula (XIII) na qual
Petição 870180002928, de 12/01/2018, pág. 74/185
70/159 [00526] os símbolos apresentam significados abaixo [00527] A, W, X, Y e R2 apresentam os significados gerais, acima indicados, preferidos, particularmente preferidos ou muito particularmente preferidos.
[00528] Novos são compostos da fórmula (XIV) na qual
(XIV) [00529] os símbolos apresentam os significados abaixo [00530] R10, R11 e R12 representam CrC^alquila ou fenila, [00531] A, W, X, Y, L1 e R2 apresentam os significados gerais, acima indicados, preferidos, particularmente preferidos ou muito particularmente preferidos.
[00532] Os processos, de acordo com a invenção para preparação dos compostos da Fórmula (I) são preferivelmente realizados utilizando-se um ou mais auxiliares de reação.
[00533] Auxiliares de reação adequados são, se apropriado, as bases orgânicas ou inorgânicas convencionais ou aceitadores de ácido. Esses acetados de metal alcalino ou de metal alcalinoterroso, amidas, carbonatos, bicarbonatos, hidretos, hidróxidos ou alcóxidos, tais como por exemplo, acetato de sódio, acetato de potássio ou acetato de cálcio, amida de lítio, amida de sódio, amida de potássio ou amida de cálcio, carbonato de sódio, carbonato de potássio ou carbonato de cálcio, hidreto de lítio, hidreto de sódio, hidreto de potássio ou hidreto de cálcio, hidróxido de lítio, hidróxido de sódio, hidróxido de potássio ou hidróxido de cálcio, metóxido de sódio, etóxido, n- ou isopropóxido, n-, iso-, s- ou t-butóxido, ou metóxido de potássio, etóxido, n- ou isopropóxido, n-, iso-, s- ou t-butóxido, além disso também compostos de nitrogênio orgânicos básicos, tais como, por exemplo, trimetilamina, trietilamina, tripropilamina, tributilamina, etildi-isopropilamina, N,NPetição 870180002928, de 12/01/2018, pág. 75/185
71/159 dimetilciclo-hexilamina, diciclo-hexilamina, etildiciclo-hexilamina, N,Ndimetilanilina, Ν,Ν-dimetilbenzilamina, piridina, 2-metil-, 3-metil-, 4metil-, 2,4-dimetil-, 2,6-dimetil-, 3,4-dimetil- e 3,5-dimetilpiridina, 5-etil2-metilpiridina, 4-dimetilaminopiridina, N-metilpiperidina, 1,4diazabiciclo[2.2.2]-octano (DABCO), 1,5-diazabiciclo[4.3.0]-non-5-eno (DBN), ou 1,8-diazabiciclo[5.4.0]-undec-7-eno (DBU).
[00534] Os processos de acordo com a invenção são preferivelmente realizados utilizando-se um ou mais diluentes. Diluentes adequados são virtualmente todos os solventes orgânicos inertes. Esses incluem preferivelmente hidrocarbonetos opcionalmente halogenados, alifáticos e aromáticos tais como pentano, hexano, heptano, ciclo-hexano, éter de petróleo, benzina, ligroína, benzeno, tolueno, xileno,cloreto de metileno, cloreto de etileno, clorofórmio, tetracloreto de carbono, clorobenzeno e o-diclorobenzeno, eteres, tais como dietil éter e dibutil éter, dimetil éter glicol e dimetil éter diglicol, tetra-hidrofurano e dioxano, cetonas, tais como acetona, metil etil cetona, metil isopropil cetona ou metil isobutil cetona, ésteres, tais como acetato de metila ou acetato de etila, nitrilas, tais como por exemplo, acetonitrila ou propionitrila, amidas, tais como por exemplo, dimetilformamida, dimetilacetamida e Nmetilpirrolidona, e também sulfóxido de dimetila, tetrametileno sulfona e triamida hexametilfosfórica e DMPU.
[00535] Nos processos de acordo com a invenção, as temperaturas de reação podem variar dentro de uma faixa relativamente extensa. Em geral, os processos são realizados sob temperaturas entre OO e 250Ό, preferivelmente sob temperaturas entre 10Ό e 185Ό.
[00536] Os processos de acordo com a invenção são em geral sob pressão atmosférica. Porém, também é possível operar sob pressão elevada ou reduzida.
[00537] Para realizar os processos de acordo com a invenção, os materiais de partida necessários respectivamente são em geral emPetição 870180002928, de 12/01/2018, pág. 76/185
72/159 pregados em quantidades aproximadamente equimolares. Porém, também é possível usar um excess relativamento amplo de respectivamente um dos componentes usados. A preparação nos processos de acordo com a invenção é respectivamente feita através de métodos convencionais (cf. os exemplos de preparação).
[00538] Além disso, a invenção prove o uso não-medicinal dos tiazóis substituídos por heterociclila de acordo com a invenção para o combate de microorgnismos indesejados.
[00539] A invenção, além disso, se refere a uma composição para o combate de micro-organismos indesejados que compreende pelo menos um tiazol substituído por heterociclila de acordo com a presente invenção.
[00540] Além disso, a invenção se refere a um método para o combate de micro-organismos indesejados, caracterizado pelo fato de os tiazóis substituídos por heterociclila de acordo com a invenção serem aplicados aos micro-organismos e/ou ao seu habitat.
[00541] Além disso, a invenção se refere a uma semente tratada com pelo menos um tiazol substituído por heterociclila de acordo com a invenção.
[00542] Umúltimo objeto da presente invenção se refere a um método para proteção de semente contra micro-organismos indesejados utilizando-se semente tratada com pelo menos um tiazol substituído por heterociclila de acordo com a presente invenção.
[00543] Os compostos de acordo com a invenção apresentam forte ação microbicida e podem ser usados para o combate de microorganismos indesejados, tais como fungos e bactérias, em proteção de cultura e na proteção de materiais.
[00544] Os tiazóis substituídos por heterociclila da Fórmula (I) de acordo com a invenção apresentam propriedades fungicidas muito boas e podem ser usados na proteção de cultura, por exemplo, para o
Petição 870180002928, de 12/01/2018, pág. 77/185
73/159 combate de plasmodioforomicetos, Oomicetos, quitridiomicetos, zigomicetos, ascomicetos, basidiomicetos e deuteromicetos.
[00545] Na cultura de proteção, bactericidas podem ser usados para o combate, por exemplo, de Pseudomonadaceae, Rhizobiaceae, Enterobacteriaceae, Corynebacteriaceae e Streptomycetaceae.
[00546] As composições fungicidas, de acordo com a invenção, podem ser usadas para o controle curativo ou protetor de fungos fitopatogênicos. Correspondentemente, a invenção também se refere a métodos curativos e protetores para o combate de fungos fitopatogênicos utilizando-se os compostos ativos ou composições de acordo com a invenção, que são aplicados à semente, à planta ou partes de planta, a fruto ou ao solo no qual as plantas crescem.
[00547] As composições, de acordo com a invenção para o combate de fungos fitopatogênicos na proteção de cultura compreendem uma quantidade eficaz, mas não fitotóxica dos compostos ativos de acordo com a invenção. Quantidade eficaz, mas não fitotóxica significa uma quantidade da composição de acordo com a invenção que é suficiente para combater as doenças fúngicas da planta de maneira satisfatória ou para erradicar a doença fúngica completamente, e que, ao mesmo tempo, não causa quaisquer sintomas significativos de fitotoxicidade. Em geral, esta taxa de aplicação pode variar dentro de uma faixa relativamente ampla. Isso depende de uma pluralidade de fatores, por exemplo, do fungo a ser combatido, da planta, das condições climáticas e das substâncias das composições de acordo com a invenção.
[00548] Todas as plantas e partes de plantas podem ser tratadas de acordo com a invenção. Entende-se por plantas neste caso todas as plantas e populações de plantas, tais como plantas selvagens desejadas ou indesejadas ou plantas de cultivo (incluindo plantas de cultura de ocorrência natural). Plantas de cultivo podem ser plantas que poPetição 870180002928, de 12/01/2018, pág. 78/185
74/159 dem ser obtidas por melhoramento genético convencional e métodos de otimização ou por métodos de engenharia biotecnológica ou genética ou combinações desses métodos, incluindo as plantas transgênicas e incluindo cultivares de plantas que podem ou não ser protegidas por certificados de reprodutores de plantas. Entende-se por partes de plantas todas as partes e órgãos das plantas aéreos e subterrâneos, tais como broto, folha, flor e raiz, podendo ser mencionados como exemplos folhas, hastes, caules, troncos, flores, polpas de fruta, frutas e sementes e também raízes, tubérculos e rizomas. Partes de plantas também incluem material cultivado e material vegetativo e generativo, por exemplo, sementeiras, tubérculos, rizomas, entalhos e sementes. [00549] As plantas a seguir podem ser mencionadas como plantas que podem ser tratadas de acordo com a invenção: algodão, linho, videiras, fruto, vegetais, tais como Rosaceae sp. (por exemplo, fruto pomáceo, tais como maças e pêras, mas também fruto de caroço, tais como abacates, cerejas, amêndoas e pêssegos e bagas tais como morangas), Ribesioidae sp., Juglandaceae sp., Betulaceae sp., Anacardiaceae sp., Fagaceae sp., Moraceae sp., Oleaceae sp., Actinidaceae sp., Lauraceae sp., Musaceae sp. (por exemplo, bananeiras e plantações), Rubiaceae sp. (por exemplo, café), Theaceae sp., Sterculiceae sp., Rutaceae sp. (por exemplo, limões, laranjas e toranjas), Solanaceae sp. (por exemplo, tomates), Liliaceae sp., Asteraceae sp. (por exemplo, alface), Umbelliferae sp., Cruciferae sp., Chenopodiaceae sp., Cucurbitaceae sp. (por exemplo, peinos), Alliaceae sp. ( por exemplo alho-prró, cebolas), Papilionaceae sp. (por exemplo, ervilhas): plantas de cultura maior, tais como Gramineae sp. (por exemplo, milho, relva, cereais tais como trigo, centeio, arroz, cevada, aveias, painço e triticale), Asteraceae sp. (por exemplo, girassóis), Brassicaceae sp. (por exemplo, repolho branco, repolho roxo, brócolis, couve-flor, couve-de-bruxelas, acelga, couve-rábano, rabanete,e também e também
Petição 870180002928, de 12/01/2018, pág. 79/185
75/159 colza oleaginosa, mustarda, rábano-picante e agrião), Fabacae sp. (por exemplo, feijões, amendoins), Papilionaceae sp. (por exemplo, feijão de soja), Solanaceae sp. (por exemplo, batatas), Chenopodiaceae sp. (por exemplo, beterraba sacarina, beterraba de forragem, acelga, raiz de beterraba); plantas de cultura e plantas ornamentais de jardim e floresta; e também respectivamente variedades geneticamente modificadas dessas plantas. Preferivelmente, plantas de cereal são tratadas de acordo com a invenção.
[00550] Alguns patógenosde doenças fúngicas que podem ser tratados de acordo com a invenção podem ser mencionados a título de exemplo, porém não em caráter restritivo:
[00551] Doenças causadas por patógenos de mofo pulvurulento, tais como por exemplo, espécies de Blumeria, como por exemplo, Blumeria graminis; espécies de Podosphaera, como por exemplo, Podosphaera leucotricha; espécies de Sphaerotheca como por exemplo Sphaerotheca fuliginea; espécies de Uncinula como por exemplo Uncinula necator;
[00552] Doenças causadas por patógenos de de doença de ferrugem tais como por exemplo, espécies de Gymnosporangium como por exemplo Gymnosporangium sabinae; espécies de Hemileia como por exemplo Hemileia vastatrix; espécies de Phakopsora, como por exemplo Phakopsora pachyrhizi e Phakopsora meibomiae; espécies de Puccinia, como por exemplo, Puccinia recôndita, Puccinia graminis ou Puccinia striformis; espécies de Uromyces, como por exemplo, Uromyces appendiculatus;
[00553] Doenças causadas por patógenos do grupo das Oomicetos, tais como por exemplo, espécies de Albugo, como por exemplo Albugo cundida, espécies de Bremia, tais como por exemplo, Bremia lactucae; espécies de Peronospora, tais como por exemplo Peronospora pisi ou
P. brassicae; espécies de Phytophthora, tais como por exemplo,
Petição 870180002928, de 12/01/2018, pág. 80/185
76/159
Phytophthora infestans; espécies de Plasmopara como por exemplo, Plasmopara viticola; espécies de Pseudoperonospora, como por exemplo, Pseudoperonospora humuli ou Pseudoperonospora cubensis; espécies de Pythium, como por exemplo, Pythium ultimum;
[00554] Doenças de manchas foliares causadas por exemplo, pelas species de Alternaria, como por exemplo, Alternaria solani; espécies de Cercospora, como por exemplo Cercospora beticola; espécie Cladiosporium como por exemplo, Cladiosporium cucumerinum; espécies de Cochliobolus, como por exemplo, Cochliobolus sativus (forma conidia: Drechslera, Sin: Helminthosporium) ou Cochliobolw miyabeanus; espécies de Colletotrichum como por exemplo, Colletotrichum lindemuthanium; espécies de Cycloconium, como por exemplo, Cycloconium oleaginum; espécies de Diaporthe, como por exemplo Diaporthe citri; espécies de Elsinoe, como por exemplo, Elsinoe fawcettii; espécies de Gloeosporium, como por exemplo, Gloeosporium laeticolor; espécies de Glomerella, como por exemplo, Glomerella cingulata; espécies de Guignardia, como por exemplo, Guignardia bidwelli; espécies de Leptosphaeria, como por exemplo, Leptosphaeria maculans; espécies de Magnaporthe, como por exemplo, Magnaporthe grisea; espécies de Microdochium, como por exemplo, Microdochium nivale; espécies de Mycosphaerella, como por exemplo, Mycosphaerella graminicola, Mycosphaerella arachidicola ou Mycosphaerella fijiensis; espécies de Phaeosphaeria, como por exemplo Phaeosphaeria nodorum; espécies de Pyrenophora, como por exemplo Pyrenophora teres ou Pyrenophora tritici repentis; espécies de Ramularia, como por exemplo, Ramularia collo-cygni ou Ramulania areola; espécies de Rhynchosporium, como por exemplo, Rhynchosporium secalis; espécies de Septoria, como por exemplo Septoria apii ou Septoria lycopersici; espécies de Stagonospora, como por exemplo, Stagonospora nodorum;
Petição 870180002928, de 12/01/2018, pág. 81/185
77/159 espécies de Typhula, como por exemplo Typhula incarnata; espécies de Venturia, como por exemplo Venturia inaequalis;
[00555] Doenças de raiz e de caule causadas, por exemplo, por species de Corticium, como por exemplo, Corticium graminearum; espécies de Fusarium, como por exemplo, Fusarium oxysporum; espécies de Gaeumannomyces, como por exemplo, Gaeumannomyces graminis; espécies de Plasmodiophora, como por exemplo, Plasmodiophora brassicae; espécies de Rhizoctonia, como por exemplo Rhizoctonia solani; espécies de Sarocladium, como por exemplo, Sarocladium oryzae; espécies de Sclerotium, como por exemplo Sclerotium oryzae; espécies de Tapesia, como por exemplo Tapesia acuformis; espécies de Thielaviopsis, como por exemplo Thielaviopsis basicola; [00556] Doenças de panículas (incluindo espigas) causadas, por exemplo, por espécies Alternaria, como por exemplo, Alternaria spp.; espécies de Aspergillus, como por exemplo, Aspergillus flavus; espécies de Cladosporium, como por exemplo, Cladosporium cladosporioides; espécies de Claviceps, como por exemplo, Claviceps purpurea; espécies de Fusarium, como por exemplo, Fusarium culmorum; espécies de Gibberella, como por exemplo Gibberella zeae; espécies de Monographella, como por exemplo Monographella nivalis; espécies de Stagonospora, como por exemplo, Stagonospora nodorum;
[00557] Doenças causadas por fungos de fuligem, como por exemplo, espécies de Sphacelotheca, como por exemplo, Sphacelotheca reiliana; espécies de Tilletia, como por exemplo, Tilletia caries ou Tilletia controversa; espécies de Urocystis, como por exemplo, Urocystis occulta; espécies de Ustilago, como por exemplo, Ustilago nuda; [00558] Podridão de fruto causada, por exemplo, por espécies de Aspergillus, como por exemplo, Aspergillus flavus; espécies de Botrytis, tais como por exemplo, Botrytis cinerea; espécies de Penicillium, tais como por exemplo Penicillium expansum ou Penicillium purpuroPetição 870180002928, de 12/01/2018, pág. 82/185
78/159 genum; espécies de Rhizopus, tais como por exemplo, Rhizopus stolonifer; espécies de Sclerotinia, tais como por exemplo Sclerotinia sclerotiorum; espécies de Verticilium, como por exemplo Verticilium alboatrum;
[00559] Podridão de semente e de solo e doenças de murcha e também doenças de sementeira, causadas por exemplo, por species de Alternaria, como por exemplo, Alternaria brassicicola; espécies de Aphanomyces, como por exemplo, Aphanomyces euteiches; espécies de Ascochyta, como por exemplo Ascochyta lentis; espécies de Aspergillus, como por exemplo Aspergillus flavus; espécies de Cladosporium, como por exemplo Cladosporium herbarum; espécies de Cochliobolus, como por exemplo, Cochliobolus sativus (conidia form: Drechslera, Bipolaris sin: Helminthosporium); espécies de Colletotrichum, como por exemplo, Colletotrichum coccodes; espécies de Fusarium, como por exemplo, Fusarium culmorum; espécies de Gibberella, como por exemplo, Gibberella zeae; espécies de Macrophomina, como por exemplo, Macrophomina phaseolina; espécies de Microdochium, como por exemplo, Microdochium nivale; espécies de Monographella, como por exemplo, Monographella nivalis; espécies de Penicillium, como por exemplo, Penicillium expansum; espécies de Phoma, como por exemplo, Phoma lingam; espécies de Phomopsis, como por exemplo, Phomopsis sojae; espécies de Phytophthora, como por exemplo, Phytophthora cactorum; espécies de Pyrenophora, como por exemplo, Pyrenophora graminea; espécies de Pyricularia, como por exemplo, Pyricularia oryzae; espécies de Pythium, como por exemplo, Pythium ultimum; espécies de Rhizoctonia, como por exemplo, Rhizoctonia solani; espécies de Rhizopus, como por exemplo, Rhizopus oryzae; espécies de Sclerotium, como por exemplo, Sclerotium rolfsii; espécies de Septoria, como por exemplo, Septoria nodorum; espécies de
Petição 870180002928, de 12/01/2018, pág. 83/185
79/159
Typhula, como por exemplo, Typhula incarnata; espécies de Verticillium, como por exemplo Verticillium dahliae;
[00560] Doenças cancerosas, biles e vassouras de bruxa, por exemplo, por espécies de Nectria, como por exemplo, Nectria galligena;
[00561] Murchas causadas por exemplo, por espécies de Monilinia, como por exemplo, Monilinia laxa;
[00562] Deformações de folhas, flores e frutos causadas, por exemplo, por espécies de Exobasidium, como por exemplo Exobasidium vexams; espécies de Taphrina, como por exemplo, Taphrina deformans;
[00563] Doenças degenerativas de plantas de algodão causadas, por exemplo, por espécies Esca, como por exemplo, Phaeomoniella chlamydospora, Phaeoacremonium aleophilum ou Fomitiporia mediterrânea; espécies Ganoderma, como por exemplo, Ganoderma boninense;
[00564] Doenças de flores e sementes, por exemplo, por espécies Botrytis, como por exemplo, Botrytis cinerea;
[00565] Doenças de tubérculos de planta causadas, por exemplo, por espécies Rhizoctonia, como por exemplo, Rhizoctonia solani; espécies de Helminthosporium, como por exemplo Helminthosporium solani;
[00566] Doenças causadas por patógenos bacterianos, como por exemplo, espécies de Xanthomonas, como por exemplo, Xanthomonas campestris pv. oryzae; espécies de Pseudomonas, como por exemplo Pseudomonas syringae pv. lachrymans; espécies de Erwinia, como por exemplo, Erwinia amylovora.
[00567] Preferivelmente, podem ser combatidas as seguintes doenças de feijões de soja:
[00568] Doenças fúngicas de folhas, colmos, vagens e sementes
Petição 870180002928, de 12/01/2018, pág. 84/185
80/159 causadas por, por exemplo, por mancha de alternaria (Alternaria spec. atrans tenuissima), antracnose (Colletotrichum gloeosporoides dematium var. truncatum), mancha marrom (Septoria glycines), mancha folear por cercospora e pragas (Cercospora kikuchii), praga de folha por choanephora (Choanephora infundibulifera trispora (Syn.)), mancha folear por dactuliophora (Dactuliophora glycines), mofo penujento (Peronospora manshurica), praga por drechslera (Drechslera glycini), mancha folear por fungo (Cercospora sojina), mancha folear por leptosphaerulina (Leptosphaerulina trifolii), mancha folear por (Phyllosticta sojaecola), praga de vagem e caule (Phomopsis sojae), mofo pulvurulento (Microsphaera diffusa), mancha folear por pyrenochaeta (Pyrenochaeta glycines), rhizoctonia aerial, praga de folhagem, e mela de miniestacas (Rhizoctonia solani), ferrugem (Phakopsora pachyrhizi Phakopsora meibomiae), crosta (Sphaceloma glycines), praga folear por stemphylium (Stemphylium botryosum), mancha alvo (Corynespora cassiicola).
[00569] Doenças fúngicas de raízes e na base do caule causadas, por exemplo, por podridão negra (Calonectria crotalariae), podridão cinzenta de caule (Macrophomina phaseolina), praga por fusarium ou murcha, podridão de raiz, e podridão de vagem e colo (Fusarium oxysporum, Fusarium orthoceras, Fusarium semitectum, Fusarium equiseti), podridão de raiz por mycoleptodiscus (Mycoleptodiscus terrestris), neocosmospora (Neocosmospora vasinfecta), queima de vagem e caule (Diaporthe phaseolorum), cancro no caule (Diaporthe phaseolorum var. caulivora), podridão por phytophthora (Phytophthora megasperma), podridão parda de haste (Phialophora gregata), podridão por pythium (Pythium aphanidermatum, Pythium irregulare, Pythium debaryanum, Pythium myriotylum, Pythium ultimum), podridão de raiz por rhizoctonia, decomposição de caule, e tombamento(Rhizoctonia solani), decomposição de caule por sclerotinia (ScleroPetição 870180002928, de 12/01/2018, pág. 85/185
81/159 tinia sclerotiorum), murcha do Sul por sclerotinia (Sclerotinia rolfsii), podridão de raiz por thielaviopsis (Thielaviopsis basicola).
[00570] As substâncias ativas de acordo com a invenção também mostram uma ação revitalizante intensa em plantas. Correspondentemente, elas são adeauadas para mobilização das defesas internas da plantar contra o ataque por micro-organismos indesejados.
[00571] No presente contexto, entende-se por substâncias revitalizantes de planta (indutora de resistência) substâncias que são capazes de estimular o sistema de defesa d eplantas de forma que, quando as plantas tratadas são em seguida inoculadas com micro-organismos indesejados, elas exibem resistência substancial em relação a esses micro-organismos.
[00572] No presente caso, entende-se por micro-organismos indesejados fungos fitopatogênicos e bactérias. As substâncias, de acordo com a invenção, pode assim ser utilizada para proteger plantas contra o ataque dos patógenos nocivos mencionados durante um certo período de tempo, após o tratamento. O período de tempo dentro do qual essa proteção é conferida, se estende em geral de 1 a 10 dias, preferivelmente de 1 a 7 dias, após o tratamento das plantas com as substâncias ativas.
[00573] O fato de as substâncias ativas serem bem toleradas por plantas nas concentrações necessárias para combater as doenças de planta, torna possível o tratamento de partes áreas de plantas, de material de propagação e semente, assim como do solo.
[00574] Neste contexto, os compostos ativos de acordo com a invenção podem ser empregados particularmente com êxito para o combate de doenças na viticultura e no cultivo de fruto, batatas e vegetais, tais como por exemplo, particularmente contra fungos de mofo pulvurulento, Oomicetos, tais como, por exemplo, espécies de Phytophthora, Plasmopara, Pseudoperonospora e Pythium.
Petição 870180002928, de 12/01/2018, pág. 86/185
82/159 [00575] Os compostos ativos, de acordo com a invenção também são adequados para aumentar o rendimento. Além disso, eles exibem um baixo grau de toxicidade e são muito bem tolerados por plantas. [00576] Se apropriado, os compostos de acordo com a invenção podem, em certas concentrações ou taxas de aplicação, também ser usados como herbicidas, agentes protetores, reguladores do crescimento ou agentes para melhorar as propriedades de plantas, ou como microbicidas, por exemplo, como fungicidas, antimicóticos, bactericidas, viricidas (incluindo agentes contra viroides) ou como agentes contra MLO (organismos tipo Micoplasma) e RLO (organismos tipo Rickettsia). Se apropriado, eles podem também ser empregados como inseticidas. Se apropriado, eles podem ser também empregados como intermediários ou precursores para a síntese de outros compostos ativos.
[00577] Os compostos ativos de acordo com a invenção, em combinação com boa tolerância de planta e toxicidade favorável em relação a animais de sangue quente e sendo tolerados muito bem pelo meio ambiente, são adequados para proteger plantas e órgãos de plantas, para aumentar aumentar rendimentos de colheita e para melhorar a qualidade de material colhido na agricultura, na horticultura, na pecuária,em florestas, em jardins e em instalações recreativas , na proteção de produtos armazenados e de materiais, e no setor de higiene. Eles são preferivelmente empregados como agentes de proteção de cultura. Eles são normalmente ativos contra esécias sensíveis e resistentes e contra todos os estágios ou alguns estágios de desenvolvimento.
[00578] O tratamento de acordo com a invenção das plantase partes de plantas com os compostos ativos ou composições é realizado diretamente ou pela ação de seu meio, habitat ou espaço de armazenamento utilizando-se métodos convencionais, por exemplo, por imerPetição 870180002928, de 12/01/2018, pág. 87/185
83/159 são, atomização, irrigação, evaporação, pulverização, nebulização, semeadura, formação de espuma, aplicação de camada, dispersão, irrigação (rega), irrigação por gotejamento e, no caso de material de propagação, particularmente no caso de sementes, além disso, como um pó para tratamento de semente a seco, uma solução para o tratamento de semente úmido, um pó hidrossolúvel para tratamento de argamassa, por encrustação, por revestimento com uma ou mais camadas de revestimento etc. Além disso, também é possível aplicar os compostos ativos através do método de volume ultra baixo ou injetar a preparação de composto ativo ou o composto ativo propriamente dito no solo.
[00579] Na proteção de materiais, as composições ou compostos ativos de acordo com a invenção podem também ser empregados para proteger materiais industriais contra o ataque e destruição por micro-organismos indesejados, tais como, por exemplo, fungos.
[00580] No presente contexto, entende-se por materiais industriais materiais não-ativas que foram feitas para serem aplicadas em tecnologia. Por exemplo, materiais industriais que devem ser protegidos por compostos ativos de acordo com a invenção a partir da modificação microbiana ou destruição podem ser colas, pegas, papéis e papelões, materiais têxteis, couro, madeiramentos, tintas e artigos plásticos, lubrificantes frios e outros materiais que podem ser atacados por microorganismos. Partes de plantas de produção, por exemplo, circuitos de água-refrigeração que podem ser adversamente atacados pela multiplicação de micro-organismos também podem ser mencionados entre os materiais a serem protegidos. Materiais industriais que podem ser mencionados preferivelmente para fins da presente invenção são colas, pegas, papéis e papelões, couro, toras de madeira, tintas, lubrificantes frios e fluidos de transferência de calor, especialmente preferivelmente toras de madeira. As composições ou compostos ativos de
Petição 870180002928, de 12/01/2018, pág. 88/185
84/159 acordo com a invenção podem evitar efeitos desvantajosos tais como apodrecimento, decomposição, descoloração, desbotamento ou a formação de mofo.
[00581] O método, de acordo com a invenção, para o combate de fungos indesejados, também pode ser empregado para proteger mercadorias de estoque. Neste caso, entendem-se mercadorias de estoque substâncias naturais de origem animal ou vegetal ou produtos de processo destes de origem natural, para os quais é desejada proteção a longo prazo. Mercadorias de estoque de origem vegetal tais como por exemplo, plantas ou partes de planta, como caules, folhas, tubérculos, sementes, frutos, grãos, podem ser protegidos logo após serem colhidos ou após processamento por (pré)secagem, umedecimento, trituração, moagem, prensagem ou torrefação. Mercadorias de estoque também incluem toras de madeira, tanto não processadas, tais como tora de madeira de construção, e pólos de eletricidade e barreiras, como na forma de produtos acabados, tais como moveis. Mercadorias de estoque de origem animal são, por exemplo, peles de animal, couros, pelicas e cabelos. Os compostos ativos de acordo com a invenção podem evitar efeitos desvantajosos tais como apodrecimento, desintegração, descoloração, desbotamento ou a formação de mofo.
[00582] Micro-organismos que podem degrader ou alterar os materiais industriais que podemos mencionar são por exemplo bacteriaa, fungos, leveduras, algas e organismos viscosos. Os compostos ativos de acordo com a invenção agem preferivelmente contra fungos, particularmente, bolores, fungos de desbotamento de madeira e de destruição de madeira (Basidiomicetos) e contra organismos viscosos e algas. Micro-organismos dos gêneros a seguir que pode-se mencionar como exemplos são: Alternaria, tais como Alternaria tenuis; Aspergillus, tais como Aspergillus niger; Chaetomium, tais como ChaetoPetição 870180002928, de 12/01/2018, pág. 89/185
85/159 mium globosum; Coniophora, tais como Coniophora puetana; Lentinus, tais como Lentinus tigrinus; Penicillium, tais como Penicillium glaucum; Polyporus, tais como Polyporus versicolor; Aureobasidium, tais como Aureobasidium pullulans; Sclerophoma, tais como Sclerophoma pityophila; Trichoderma, tais como Trichoderma viride; Escherichia, tais como Escherichia coli; Pseudomonas, tais como Pseudomonas aeruginosa; Staphylococcus, tais como Staphylococcus aureus.
[00583] A presente invenção se refere também a uma composição para o combate de micro-organismos indesejados compreendendo pelo menos um dos tiazóis substituídos por heterociclila de acordo com a invenção. Eles são preferivelmente composições fungicidas compreendendo substâncias auxiliares, solventes, portadores, tensoativos ou extensores adequados para o uso na agricultura.
[00584] De acordo com a invenção, um portador é uma substância natura ou sintética, orgânica ou inorgânica à qual os compsotos ativos são misturados para uma melhor aplicabilidade, particularmente para aplicação em plantas ou partes de planta ou semente. O portador, que pode ser sólido ou líquido, em geral é inerte e pode ser adequado para o uso na agricultura.
[00585] Portadores sólidos adequados são: por exemplo, sais de amônio e minerais naturais moidos tais como caolinas, argilas, talco, giz, quartzo, atapulgita, montmorilonita ou minerais terrosos diatomáceos, e minerais sintéticos moidos, tais como silica finamente dividida, alumina e silicatos; portadores sólidos adequados para grânulos são: por exemplo, pedras naturais fracionadas trituradas, tais como calcita, mármore, pedra-pomes, sepiolita e dolomita, e também grânulos sintéticos de farinhas inorgânicas ou orgânicas, e grânulos de material orgânico, tais como serragem, cascas de coco, sabugos de grãos e talos de tabaco; emulsificantes adequados e/ou agentes espumantes são: por exemplo emulsificantes não iônicos e aniônicos, tais como ésteres
Petição 870180002928, de 12/01/2018, pág. 90/185
86/159 de ácido graxo de polioxietileno, éteres de álcool graxo de polioxietileno, por exemplo, éteres alquilaril poliglicol , alquilsulfonatos, sulfatos de alquila, arilsulfonatos e também hidrosilatos de proteína; dispersantes adequados são substâncias não iônicas/ou iônicas, por exemplo, das classes do álcool/éteres POE e/ou POP, ácido e/ou ésteres POP/POE, alquilarila e/ou éteres POP/POE, gordura e/ou adutos POP/POE, derivados de POE e/ou POP poliol, POE e/ou POP/sorbitano ou adutos de açúcar, sulfatos de alquila ou arila, sulfonatos e fosfatos, ou os aductos de éter de PO correspondentes. Além disso, oligo- ou polímeros, por exemplo, aqueles derivados de monomeros vinílicos, de ácido acrílico, de EO e/ou PO isoladamente ou em combinação com, por exemplo, (poli)alcoóis ou (poli)aminas. Também é possível empregar lignina e seus derivados de ácido sulfônico, celuloses não modificadas ou modificadas, ácidos sulfônicos aromáticos e/ou alifáticos e seus aductos com formaldeído.
[00586] Os compostos ativos podem ser convertidos em formulações convencionais tais como solouções, emulsões, pós molháveis, suspensões a base de água-em-óleo, pós, pastas, grânulos solúveis, grânulos para disseminação, concentrados suspensão-emulsão, materiais naturais impregnados com composto ativo, materiais sintéticos impregnados com composto ativo, fertilizantes e também microencapsulamentos em substâncias poliméricas.
[00587] Os compostos ativos podem ser usados como na forma de suas formulações ou nas formas de uso preparadas a partir deles, tais como soluções prontas-para-uso, emulsões, suspensões a base de água-e-óleo, pós, pós molháveis, pastas, pós solúveis, grânulos solúveis para disseminação, concntrados suspensão-emulsão, materiais naturais impregnados com composto ativo, materiais sintéticos impregnados com composto ativo, fertilizantes e também microencapsulações em substância polimérica. A aplicação é feita de forma convenPetição 870180002928, de 12/01/2018, pág. 91/185
87/159 cional, por exemplo, por despejo, aplicação de spray, atomização, disseminação, pulverização, formação de espuma, aplicação de camada etc. Além disso, é possível aplicar os compostos ativos pelo método de volume-ultrabaixo ou injetar a preparação de compsotos ativos ou o composto ativo propriamente dito no solo. Também é possível, tartar a semente das plantas.
[00588] As formulações mencionadas podem ser preparadas da forma conhecida pela mistura dos compostos ativos com pelo menos um extensor convencional, solvente ou diluente, emulsificante, dispersante e/ou ligante ou fixativo, agente umectante, repelente de água, se necessário, secativos e estabilisadores UV e se necessário colorantes e pigmentos, antiespumantes, conservantes, espessantes secundários, colas, giberelinas e outros auxiliares de processamento.
[00589] As composições, de acordo com a invenção, incluem não somente formulações que já estão prontas para uso e podem ser aplicadas às plantas ou semente utilizando-se um equipamento adequado, mas também concentrados comerciais, que precisam ser diluídos com água antes do uso.
[00590] Os compostos ativos, de acordo com a invenção, podem estar presentes como tais ou em suas formulações (comerciais) e também nas formas de uso preparadas a partir dessas formulações como uma mistura com outros compostos ativos (conhecidos) tais como inseticidas, atrativos, estelizantes, bactericidas, acaricidas, nematicidas, fungicidas, reguladores do crescimento, herbicidas, fertilizantes, agentes protetores e/ou semioquímicos.
[00591] São adequados para o uso como auxiliares substâncias que são adequadas para proporcionar às composições propriamente ditas e/ou às preparações a partir destas (por exemplo, licores em spray, revestimentos de semente) propriedades particulares tais como propriedades técnicas e/ou também propriedades biológicas particulaPetição 870180002928, de 12/01/2018, pág. 92/185
88/159 res. Auxiliares tipicamente adequados são: extensores, solventes e portadores.
[00592] Extensores adequados são, por exemplo, água, líquidos químicos orgânicos polares a apoiares, por exemplo, a partir das classes dos hidrocarbonetos aromáticos e não-aromáticos (tais como parafinas, alquilbenzenos, alquilnaftalenos, clorobenzenos), os alcoóis e polióis (que, se necessário, podem também ser substituídos, eterificados e/ou esterificados), as cetonas (tais como acetona, ciclohexanona), ésteres (incluindo gorduras e óleos) e (poli)éteres, as aminas não substituídas e substituídas, amidas, lactamas (tais como Nalquilpirrolidonas) e lactonas, as sulfonas e sulfóxidos (tais como sulfóxido de dimetila).
[00593] Extensores gasosos liquefeitos ou portadores são líquidos que são gasosos em temperatura ambiente e sob pressão atmosférica, por exemplo, propelantes em aerossol, tais como hidrocarbonetos halogenados, e também butano, propano, nitrogênio e dióxido de carbono.
[00594] Agentes promotores de pega, tais como carboximetilcelulose e polímeros sintéticos e naturais na forma de pós, grânulos e látices, tais como goma arábica, álcool polivinílico, acetato polivinílico, ou ainda fosfolipídeos naturais, tais como cefalinas e lecitinas e fosfolipídeos sintéticos podem ser usados nas formulações. Outros possíveis aditivos são óleos minerais e vegetais.
[00595] Se o extensor usado for água, também é possível usar, por exemplo, solventes orgânicos como solventes auxiliares. Solventes líquidos adequados são essencialmente: compostos aromáticos, tais como xileno, tolueno ou alquilnaftalenos, compostos aromáticos clorinados ou hidrocarbonetos alifáticos clorinados, tais como clorobenzenos, cloroetilenos ou cloreto de metileno, hidrocarbonetos alifáticos, tais como ciclo-hexano ou parafinas, por exemplo, frações de óleo miPetição 870180002928, de 12/01/2018, pág. 93/185
89/159 neral, alcoóis, tais como butanol ou glicol, e também éteres e ésteres destes, cetonas, tais como acetona, metil etil cetona, metil isobutil cetona ou ciclo-hexanona, solventes fortemente polares, tais como dimetilformamida e sulfóxido de dimetila, e também água.
[00596] As composições de acordo com a invenção podem compreender adicionalmente outros componentes, tais como, por exemplo, tensoativos. Tensoativos adequados são emulsificantes e/ou formadores de espuma, dispersantes ou agentes umectantes que apresentam propriedades iônicas e não iônicas, ou misturas desses tensoativos. Exemplos destes são sais de ácido poliacrílico, sais de ácido lignosulfônico, sais de ácido fenolsulfônico ou ácido naftalenossulfônico, policondensados de óxido de etileno com alcoóis graxos ou com ácidos graxos ou com aminas graxas, fenóis substituídos (preferivelmente alquilfenóis ou arilfenóis), sais de ésteres sulfossuccínicos, derivados de taurino (preferivelmente tauratos de alquila), ésteres fosfóricos de alcopois polietoxilados ou fenóis, ésteres graxos de polióis, e derivados dos compostos contendo sulfatos, sulfonatos e fosfatos, por exemplo, éteres alquilaril poliglicol, alquilsulfonatos, sulfatos de alquila, arilsulfonatos, hidrolisados de proteína, ácidos gastos de lignosulfito e metilcelulose. A presença de um surfactante é necessária se um dos compostos ativos e/ou um dos portadores inertes for insolúvel em água e a aplicação for feita em água. A proporção de tensoativos situa-se entre 5 e 40 porcento em peso das composições de acordo com a invenção. [00597] É possível usar colorantes tais como pigmentos inorgânicos, por exemplo, óxido de ferro, óxido de titânio, azul da Prússia e Prussian e corantes orgânicos, tais como corantes à base de alizarina, azo corantes e corantes à base de ftalocianina metálica, e nutrientestraço tais como sais de ferro, manganês, boro, cobre, cobalto, molibdênio e zinco.
Petição 870180002928, de 12/01/2018, pág. 94/185
90/159 [00598] Outros possíveis aditivos são perfumes, oleos minerais ou vegetais, se apropriado ceras e nutrients modificados (incluindo traços de nutrientes), tais como sais de ferro, manganês, boro, cobre, cobalto, molibdênio e zinco.
[00599] Estabilizantes tais como estabilizantes de baixatemperatura, conservantes, antioxidantes, estabilizantes de luz ou outros agentes que melhorem a estabilidade química e/ou física também podem estar presentes.
[00600] Se necessário, também é possível para outros componentes adicionais estarem presentes, por exemplo, coloides protetores, ligantes, colas, espessantes, agentes tixotrópicos, agentes promotores de penetração, estabilizantes, sequestrantes, formadores complexos. Em geral, os compostos ativos podem ser combinados com qualquer aditivo sólido ou líquido costumeiramente usado para fins de formulação.
[00601] As formulações em geral compreendem entre 0,05 e 99% em peso, 0,01 e 98% em peso, preferivelmente entre 0,1 e 95% em peso, particularmente preferivelmente entre 0,5 e 90% em peso, de composto ativo, muito particularmente preferivelmente entre 10 e 70 porcento em peso.
[00602] As formulações acima descritas podem ser empregadas em um método de acordo com a invenção para o combate de microorganismos indesejados em que os tiazóis substituídos por heterociclila de acordo com a invenção são aplicados aos micro-organismos e/ou ao seu habitat.
[00603] Os compostos ativos de acordo com a invenção, tais como em suas formulações, também podem ser usados em uma mistura com fungicidas conhecidos, bactericidas, acaricidas, nematicidas ou inseticidas, por exemplo, para disseminar o espectro de atividade ou evitar o desenvolvimento de resistência.
Petição 870180002928, de 12/01/2018, pág. 95/185
91/159 [00604] Pares de mistura adequados são, por exemplo, fungicidas conhecidos, inseticidas, acaricidas, nematicidas ou ainda bactericidas (vide também Manual Pesticida, 13a ed.).
[00605] Uma mistura com outros compostos ativos conhecidos, tais como herbicidas, ou com fertilizantes e reguladores de crescimento, agentes protetores e/ou semioquímicos também é possível.
[00606] A aplicação é feita de forma adaptada às formas de uso. [00607] Além disso, a invenção compreende um método para tratamento de semente.
[00608] Um outro aspecto da presente invenção se refere particularmente a semente tratada com pelo menos um dos tiazóis substituídos por heterociclila de acordo com a invenção. A semente de acordo com a invenção é usada em métodos para proteger semente contra fungos nocivos fitopatogênicos. Nesses métodos, é usada semente tratada com pelo menos um composto ativo de acordo com a invenção.
[00609] As composições e compostos ativos de acordo com a invenção também são adequados para tratamento de semente. Uma grande parte dos danos a plantas de cultura que é causado por organismos nocivos ocorre quando a semente é atacada durante a armazenagem ou após a semente ser introduzida no solo, e também durante e após a germinação da planta. Esta fase é particularmente crítica já que as raízes e brotos da planta em crescimento são particularmente sensíveis e mesmo um dano menor pode levar à morte de toda a planta. Portanto proteger a semente e a planta em germinação pelo uso e composições adequadas é muito importante.
[00610] O combate de fungos nocivos fitopatogênicos pelo tratamento da semente de plantas já há muito tempo, é objeto de melhoramentos contínuos. Porém, no tratamento de semente, vários problemas são encontrados, que nem sempre podem ser resolvidos de
Petição 870180002928, de 12/01/2018, pág. 96/185
92/159 forma satisfatória. Assim, é desejável desenvolver métodos para proteger a semente e a planta em germinação que dispensam a aplicação adicional de agentes protetores de cultura após semeadura ou após a emergência das plantas ou em que aplicações adicionais são pelo menos significativamente reduzidas. Além disso, é desejável otimizar a quantidade de composto ativo empregado de tal forma a prover máxima proteção para a semente e para a planta em germinação contra o ataque de fungos fitopatogênicos, mas sem danificar a própria planta através do composto ativo empregado. Particularmente, métodos para o tratamento de semente devem levar particularmente em consideração as propriedades fúngicas intrínsecas de plantas transgênicas a fim de obter uma proteção ideal da semente e da planta em germinação com um mínimo de agentes protetores a serem empregados.
[00611] A presente invenção, portanto, também se refere a um método para a proteção de semente e planta em germinação contra o ataque de pestes animais e/ou fungos nocivos fitopatogênicos, através do tratamento da semente com uma composição de acordo com a invenção. A invenção se refere igualmente ao uso das composições de acordo com a invenção para o tratamento de semente para proteger a semente e a planta em germinação contra fungos fitopatogênicos. Além disso, a invenção se refere à semente que foi tratada com uma composição de acordo com a invenção de forma a proporcionar proteção contra fungos fitopatogênicos.
[00612] Pestes animais e/ou fungos nocivos fitopatogênicos que danificam a planta após a emergência são a princípio combatidos pelo tratamento do solo e as partes aéreas das plantas com agentes protetores de cultura. Devido a preocupações com um possível impacto dos agents protetores de cultura sobre o meio ambiente e a saúde humana e animal, são feitos esforços para reduzir a quantidade de compostos ativos aplicados.
Petição 870180002928, de 12/01/2018, pág. 97/185
93/159 [00613] Uma das vantagens da presente invenção é que as propriedades sistêmicas particulars das composições de acordo com a invenção significa que o tratamento da semente com essas composições não apenas protege a própria semente, mas também as plantas resultantes após a emergência, contra pestes animais e/ou fungos nocivos fitopatogênicos. Desse modo, o tratamento imediato da cultura no momento da semeadura ou pouco depois pode ser dispensado. [00614] Deve-se também considerar vantajoso o fato de as composições e compostos ativos de acordo com a invenção poderem ser usados particularmente também para semente transgênica, sendo que o crescimento da planta pode expressar uma proteína que age contra pestes. Através do tratamento de tal semente com as composições e compostos ativos de acordo com a invenção, é possível controlar certas pestes mesmo pela expressão de, por xemplo, proteína inseticida. Surpreendentemente, um outro efeito sinergístico pode ser aqui observado, que ainda mlehora a eficácia da proteção contra o ataque por pestes.
[00615] As composições de acordo com a invenção são adequadas para proteger a semente de qualquer variedade de planta que seja empregada na agricultura, na estufa de plantas, em plorestas ou na horticultura. Particularmente, isso assume a forma de semente de cereais (tais como trigo, cevada, centeio, painço e aveias), milho amarelo, algodão, feijão de soja, arroz, batata, girassol, feijão, café, beterraba (por exemplo, beterraba sacarina e beterraba de forragem), amendoins, vegetais(tais como tomates, pepinos, cebolas e alfaces), relvas e plantas ornamentais. O tratamento de semente de cereais (tais como trigo, cevada, centeio e aveias) milho amarelo e arroz é particularmente importante.
[00616] Conforme também abaixo descrito, o tratamento de semente transgênica com as composições ou compostos ativos de acordo
Petição 870180002928, de 12/01/2018, pág. 98/185
94/159 com a invenção também é particularmente importante. Isso implica em semente de plantas que compreende pelo menos um gene heterogêneo que gorverna a expressão de um polipeptídeo ou proteína com propriedades inseticidas. O gene heterogêneo em semente tansgênica pode ser derivado, por exemplo, de micro-organismos das espécies Bacillus, Rhizobium, Pseudomonas, Serratia, Trichoderma, Clavibacter, Glomus ou Gliocladium. O gene heterogêneo se origina preferivelmente de Bacillus sp., o produto gênico que apresenta atividade contra a broca do milho e/ou Diabrotica virgifera Le Conte. É particularmente preferido um gene heterólogo derivado de Bacillus thuringiensis.
[00617] No contexto da presente invenção, a composição de acordo com a invenção é aplicada à semente tanto isoladamente como em uma formulação adequada. Preferivelmente, a semente é tratada em um estado suficiente para evitar danos durante tratamento. Em geral, a semente pode ser tratada em qualquer momento entre o cultivo e semeadura. A semente usada normalmente é separada da planta e livre de sabugos, cascas, talos, peles, pelos a póla de fruto. Assim, por exemplo, é possível usar semente que tenha sido cultivada, limpa e secada até um teor de mistura abaixo de 15% em peso. Alternativamente, também é possível usar semente que, após secagem, tenha sido tratada com água e em seguida secada novamente.
[00618] Ao tratar a semente, é precido observar atentamente para que a quantidade da composição de acordo com a invenção aplicada à semente e/ou a quantidade de outros aditivos seja selecionada de tal forma que a germinação da semente não seja adversamente afetada, ou que a planta resultante não seja danificada. Deve-se tomar cuidado principalmente no caso de compostos ativos que podem apresentar efeitos fitotóxicos a certas taxas de aplicação.
Petição 870180002928, de 12/01/2018, pág. 99/185
95/159 [00619] As composições, de acordo com a invenção, podem ser aplicadas diretamente, isto é, sem compreender outros components e sem ter sido diluída. Em geral, é preferido aplicar a composição na semente na forma de uma formulação adequada. Formulações adequadas é métodos para o tratamento de semente são conhecidos pelo versado na técnica e são descritos, por exemplo, nos documentos a seguir: US 4,272,417 A, US 4,245,432 A, US 4,808,430 A, US 5,876,739 A, US 2003/0176428 A1, WO 2002/ 080675 A1, WO 2002/028186 A2.
[00620] O composto ativo que pode ser usado de acordo com a invenção pode ser convertido em formulações de revestimento de semente convencionais, tais como soluções, emulsões, suspensões, pós, espumas, pastas ou outros materiais de revestimento para semente, e também formulações ULV.
[00621] Essas formulações são preparadas de forma convencional mediante mistura dos compostos ativos ou combinações de compost ativo com aditivos convencionais, tais como, por exemplo, extensores convencionais, e também solventes ou diluentes, colorantes, agentes umectantes, dispersantes, emulsificantes, antiespumaentes, conservantes, espessantes secundários, adesivos, giberelinas e também água.
[00622] Colorantes adequados podem estar presentes nas formulações de revestimento de semente que podem ser usadas de acordo com a invenção incluem todos os colorantes normais para tais finalidades. Neste caso, podem ser empregados pigmentos pouco solúveis em água como corantes que são solúveis em água. Exemplos que podemos citar incluem os corantes conhecidos sob os nomes de rodamina B, C.l. Pigment Red 112, e C.l. Solvent Red 1.
[00623] Agentes umectantes adequados que podem estar presentes nas formulações de revestimento de semente incluem todas as
Petição 870180002928, de 12/01/2018, pág. 100/185
96/159 substâncias que promovem umidade e são aplicadas normalmente na formulação de compostos agroquímicos ativos. São preferivelmente usados alquilnaftaleno-sulfonatos, tais como di-isopropil- ou diisobutilnaftaleno-sulfonatos.
[00624] Dispersantes adequados e/ou emulsificantes que podem estar presents nas formulações de revestimento de semente que podem ser usados de acordo com a invenção incluem todos os dispersantes não iônicos, aniônicos, e catiônicos, que são usualmente usados na formulação de compostos agroquímicos ativos. Preferivelmente, é possível usar dispersantes não iônicos ou aniônicos ou misturas de dispersantes não iônicos ou aniônicos. Particularmente, dispersantes não iônicos adequados são polímeros em bloco de óxido de etileno - óxido de propileno, éteres alquilfenol poliglicol, e éteres tristirilfenol poliglicol, e seus derivados fosfatados ou sulfatados. Particularmente, dispersantes aniônicos adequados são are lignosulfonatos, sais poliacrílicos, e condensados de arilsulfonato-formaldeído.
[00625] Antiespumaentes adequados que podem estar presentes nas formulações de revestimento de semente que podem ser usados de acordo com a invenção incluem todas as substâncias inibidoras que estão usualmente na formulação de compostos agroquímicos ativos. Preferivelmente é possível usar antiespumantes de silicone e estearato de magnésio.
[00626] Conservantes adequados podem estar presentes nas formulações de revestimento de semente que podem ser usados de acordo com a invenção incluem todas as substâncias que podem ser usadas para tais finalidades em composições agroquímicas. A título de exemplo, podem-se citar diclofeno e hemiformal de álcool benzílico. [00627] Espessantes secundários adequados que podem estar presentes nas formulações de revestimento de semente que podem ser usados de acordo com a invenção incluem todas as substâncias que
Petição 870180002928, de 12/01/2018, pág. 101/185
97/159 podem ser usadas para tais finalidades em composições agroquímicas. São preferivelmente adequados derivados de celulose, derivados de ácido acrílico, xantana, argilas modificadas, e sílica finamente dividida.
[00628] Adesivos adequados que podem estar presentes nas formulações de revestimento de semente que podem ser usados de acordo com a invenção incluem todos os ligantes usuais que podem ser usados no revestimento de semente. Podem-se citar preferivelmente polivinilpirrolidona, acetato polivinílico, álcool polivinílico e tilose. [00629] Giberelinas adequadas que podem estar presentes nas formulações de revestimento de semente que podem ser usadas de acordo com a invenção são preferivelmente a giberelinas A1, A3 (= ácido giberelínico), A4 e A7; é particularmente preferivelmente usado ácido giberelínico. As giberelinas são conhecidas (cf. R. Wegler „Chemie der Pflanzenschutz- e Schàdlingsbekàmpfungsmittel, Vol. 2, Springer Verlag, 1970, pp. 401-412).
[00630] As formulações de revestimento de semente que podem ser usadas de acordo com a invenção podem ser usadas diretamente ou após prévia diluição com água para tratar a semente de qualquer outra ampla variedade de tipos. Por exemplo, os concentrados ou as preparações possíveis destes mediante diluição com água podem ser usados para revestir cereais, tais como, trigo, cevada, centeio, aveia, e triticale, e também a semente de milho amarelo, arroz, colza oleaginosa, ervilhas, feijão branco, algodão, girassol e beterrabas, ou ainda semente vegetal de qualquer outra grande variedade de tipos. As formulações de revestimento de semente que podem ser usadas de acordo com a invenção ou suas preparações diluídas também podem ser usadas para revestir semente de plantas transgênicas. Neste contexto, efeitos sinergísticos adicionais também podem surgir em interação com as substâncias formadas por expressão.
Petição 870180002928, de 12/01/2018, pág. 102/185
98/159 [00631] Equipamento misturador adequado para tratamento de semente com as formulações de revestimento de semente, que podem ser usadas de acordo com a invenção ou as preparações preparadas a partir delas mediante adição de água, inclui todo o equipamento misturador que pode usualmente ser usado para revestimento. O procedimento específico adotado durante o revestimento inclui introdução da semente em um misturador, adição da quantidade particularmente desejada de formulação de revestimento de semente, seja como tal ou após prévia diluição com água, e realização da mistura até a formulação ser uniformemente distribuída na semente. Opcionalmente, pode seguir uma operação de secagem.
[00632] A taxa de aplicação das formulações de revestimento de semente que podem ser usadas de acordo com a invenção pode variar dentro de uma faixa relativamente ampla. Depende do respectivo teor dos compostos ativos nas formulações e na semente. Em geral, as taxas de aplicação de combinação de composto ativo situam-se entre 0,001 e 50 g por quilograma de semente, preferivelmente entre 0,01 e 15 g por quilograma de semente.
[00633] Além disso, os compostos da Fórmula (I), de aordo com a invenção também apresentam uma atividade antimicótica muito boa. Eles apresentam um espectro de atividade animicótica bastante extenso particularmente contra dermatófitos e leveduras, mofos e fungos difásicos (por exemplo, contra espécies de Candida como Candida albicans, Candida glabrata) e Epidermophyton floccosum, espécies de Aspergillus tais como Aspergillus niger e Aspergillus fumigatus, espécies de Trichophyton tais como Trichophyton mentagrophytes, espécies de Microsporon tais como Microsporon canis e audouinii. A relação desses fungos não representa em hipótese alguma uma restrição do espectro micótico que pode ser abrangido, mas somente a título de ilustração.
Petição 870180002928, de 12/01/2018, pág. 103/185
99/159 [00634] Correspondentemente, os compostos ativos da Fórmula (I), de acordo com a invenção podem ser usados em aplicações médicas e não médicas.
[00635] Os compostos ativos podem ser aplicados como tais, na forma de suas formulações ou nas formas de uso preparadas a partir destes, tais como soluções prontas-para-o-uso, suspensões, pós moIháveis, pastas, pós solúveis, pós e grânulos. A aplicação é feita de forma convencional, por exemplo, por rega, atomização, borrifação, disseminação, pulverização, formação de espuma, aplicação de camada etc. Também é possível aplicar os compostos ativos pelo método de volume ultrabaixo ou para injetar a preparação de composto ativo ou o composto propriamente dito no solo. Também é possível tartar a semente das plantas.
[00636] Ao utilizar os compostos ativos de acordo com a invenção como fungicidas, as taxas de aplicação podem variar dentro de uma faixa relativamente ampla, em função do tipo de aplicação. A taxa de aplicação dos compostos ativos de acordo com a invenção é •no tratamento de partes de plantas, por exemplo folhas: de 0,1 a 10 000 g/ha, preferivelmente de 10 a 1000 g/ha, particularmente preferivelmente de 50 a 300 g/ha (se a aplicação for feita por rega ou imersão, é possível também redizar a taxa de aplicação ainda mais, particularmente quando são usados substratos inertes tais como lã de pedra ou perlita);
•no tratamento de semente: de 2 a 200 g por 100 kg de semente, preferivelmente de 3 a 150 g por 100 kg de semente, particularmente preferivelmente de 2,5 a 25 g por 100 kg de semente, muito particularmente preferivelmente de 2,5 a 12,5 g por 100 kg de semente;
•no tratamento de solo: de 0,1 a 10 000 g/ha, preferivelmente de 1 a 5000 g/ha.
Petição 870180002928, de 12/01/2018, pág. 104/185
100/159 [00637] Essas taxas de aplicação são mencionadas apenas a título de exemplo e não possuem caráter restritivo em relação ao propósito da invenção.
[00638] No setor veterinário e na manutenção de animais, os compostos ativos de acordo com a invenção são aplicados de forma conhecida mediante administração enteral na forma de, por exemplo, comprimidos, cápsulas, bebidas, doses de remédio, grânulos, pastas, pílulas volumosas, método de feed-through, supositórios, por administração parenteral, tais como, por exemplo, por injeções (intramuscular, subcutânea, intravenosa, intraperitoneal e similar), implantes, por aplicação nasal, por aplicação dérmica na forma de, por exemplo, banho ou imersão, pulverização, despejamento e nebulização, lavagem, polvilhamento, e com auxílio de composto ativo que compreende artigos conformados tais como colares, tags de orelha, fitas de braço, prendedores, dispositivos marcadores e similares.
[00639] Quando usados para gado, aves domésticas e similares, os compostos ativos da Fórmula (I) podem ser aplicados como formulações (por exemplo, pós, emulsões, soluções escoáveis) que compreendem os compostos ativos em uma quantidade de 1 a 80% em peso, seja diretamente ou após 100- 10 000-vezes diluídos, ou ainda como banho químico.
[00640] Se necessário, as composições prontas-para-uso podem compreender também inseticidas e, se apropriado, um ou mais outros fungicidas.
[00641] Com relação a possíveis pares de mistura adicionais, é feita referência aos inseticidas e fungicidas acima citados.
[00642] Os compostos de acordo com a invenção também podem ser usados para proteger objetos que entram em contato com água salgada ou água salobre, tais como cascos, telas, redes, edificações, ancoradouros e sistemas de sinalização, contra colonização.
Petição 870180002928, de 12/01/2018, pág. 105/185
101/159 [00643] Os compostos de acordo com a invenção, inidivualmente ou em combinação com outros compostos ativos, podem, além disso, ser empregaos como agentes anticontaminantes.
[00644] O método de tratamento de acordo com a invenção pode ser usado para tartar organismos geneticamente modificados (GMOs), por exemplo, plantas ou sementes. Plantas geneticamente modificadas (ou plantas transgênicas) são plantas nas quais um gene heterólogo havia sido estavelmente integrado no genoma. A expressão gene heterólogo significa essencialmente um gene que é provido ou construído fora da planta e quando introduzido no genoma nuclear, cloroplástico ou mitocondrial resulta na planta transformada nova ou agronomicamente melhorada ou outras propriedades pela expressão de uma proteína ou polipeptídeo de interesse ou por infrarregulação ou silenciamento de outro(s) gene(s) que estã/estão presentes na planta (utilizando por exemplo, tecnologia antissenso, tecnologia de cossupressão ou tecnologia de interferência RNA (RNAi). Um gene heterólogo que fica localizado no genoma é também chamado de transgene. Um transgene que é definido por sua localização particular no genoma da planta é chamado de evento de transformação ou transgênico. [00645] Dependendo das espécies de planta ou cultivares de planta e condições de crescimento (solos, clima, período de vegetação, dieta), o tratamento de acordo com a invenção também pode resultar em efeitos superaditivos (sinergísticos). Assim são possíveis, por exemplo, taxas de aplicação reduzidas e/ou aumento na atividade de substâncias e composições que podem ser usadas, de acordo com a invenção, melhor crescimento da planta, tolerância aumentada a temperaturas elevadas e baixas, aumento de tolerância à estiagem ou teor de água ou de sal no solo, desempenho maior de florescência, colheita mais fácil, maturação acelerada, aumento dos produtos de colheita, melhor qualidade e/ou um valor nutricional mais elevado dos produtos
Petição 870180002928, de 12/01/2018, pág. 106/185
102/159 de colheita, melhor estabilidade de estocagem e/ou processabilidade dos produtos colhidos, que ultrapassam os efeitos que atualmente eram de ser esperar.
[00646] A certas taxas de aplicação, as combinações de substâncias ativas de acordo com a invenção também podem apresentar um efeito de fortalecimento em plantas. Correspondentemente, elas são adequadas para mobilizar o sistema de defesa da planta contra o ataque de fungos fitopatogênicos indesejados e/ou micro-organismos e/ou vírus. Desse modo, se necessário, pode ser uma das razões para a atividade intensificada das combinações de acordo com a invenção, por exemplo, contra fungos. Substâncias (resistência-indutoras) de fortalecimento de plantas devem ser entendidas, no presente contexto, como aquelas substâncias ou combinações de substâncias que são capazes de estimular o sistema de defesa de plantas de tal modo que quando em seguida inoculadas com fungos fitopatogênicos indesejados e/ou micro-organismos e/ou vírus, as plantas tratadas apresentam um grau de resistência significativo em relação a esses fugos fitopatogênicos indesejados e/ou micro-organismos e/ou vírus. No presente caso, fungos fitopatogênicos indesejados, e/ou micro-organismos e/ou vírus devem ser entendidos como fungos fitopatogênicos, bactérias e vírus. Desse modo, a substância de acordo com a invenção pode ser empregada para proteger plantas contra o ataque por patógenos acima mencionados dentro de um determinado período de tempo após o tratamento. O período de tempo dentro do qual a proteção é eficaz, se estende em geral de 1 a 10 dias, preferivelmente de 1 a 7 dias, após o tratamento das plantas com as substâncias ativas.
[00647] Plantas e cultivares de planta que são preferivelmente tratados de acordo com a invenção incluem todas as plantas que apresentam material genético que confere características vantajosas espePetição 870180002928, de 12/01/2018, pág. 107/185
103/159 cífics, úteis a estas plantas (sejam obtidas por melhoramento genético e/ou meios biotecnológicos).
[00648] Plantas e cultivares de planta que também são preferivelmente tratados de acordo com a invenção são resistentes contra um ou mais estresses bióticos, ou seja, as ditas plantas mostram uma defesa melhor contra pestes animais e microbianas, tais como contra nemátodos, insetos, ácaros, fungos fitopatogênicos, bactérias, vírus e/ou viroides.
[00649] Plantas e cultivares de planta que também podem ser tratados de acordo com a invenção são aquelas plantas que são resistentes a um ou mais estresses abióticos. Condições de estresse abiótico podem incluir, por exemplo, seca, exposição a temperaturas baixas, exposição ao calor, estresse osmótico, inundação, salinidade do solo aumentada, exposição mineral aumentada, exposição ao ozônio, exposição à iluminação, disponibilidade limitada de nutrientes de nitrogênio, disponibilidade limitada de nutrientes fósforo, evitar sombra. [00650] Plantas e cultivares de planta que também podem ser tratados de acordo com a invenção, são aquelas plantas caracterizadas por características de rendimento otimizado. Rendimento aumentado nas ditas plantas pode ser o resultado de, por exemplo, fisiologia, crescimento e desenvolvimento de planta melhorados, tais como eficiência no uso de água, eficiência em retenção de água, uso de nitrogênio melhorado, assimilação de carbono intensificada, fotosíntese melhorada, eficiência em germinação aumentada e maturação acelerada. Além disso, o redimento pode ser afetado pela arquitetura da planta melhorada (sob condições de estresse e não estresse), incluindo florescimento prematuro, controle de florescimento para produção de semente híbrida, vigor de semeadura, tamanho da planta, número internodal e distância internodal, crescimento de raiz, tamanho da semente, tamanho do fruto, tamanho da vagem, número de vagem ou
Petição 870180002928, de 12/01/2018, pág. 108/185
104/159 espiga, número de sementes por vagem ou espiga, massa de semente, carga de semente aumentada, dispersai de semente reduzido, dehicência reduzida em vaso e resistência ao acamamento. Outras características de rendimento incluem composição da semente, tais como teor de carbohidrato, conteúdo de proteína, teor e composição de óleo, valor nutricional, redução em compostos antinutricionais, processabilidade melhorada e melhor estabilidade a armazenagem.
[00651] Plantas que podem ser tratadas de acordo com a invenção são plantas híbridas que já expressam as características de heterosis ou vigor híbrido que resulta em geral em rendimento mais elevado, maior vigor, saúde e resistência em relação a fatores de estresse biótico e abiótico. Tais plantas são tipicamente produzidas por cruzamento em linhagem-mãe macho-estéril inata (linhagem mãe fêmea) com outra linhagem mãe macho-estéril inata (linhagem mãe macho). Semente híbrida é tipicamente colhida das plantas macho-estéril e vendidas a agricultores. Plantas macho-estéril algumas vezes (por exemplo, em milho) podem ser produzidas por despendoamento (ou seja, a remoção mecânica dos orgãos reprodutivos masculinos ou flores macho), porém, mais tipicamente, macho-esterilidade é o resultado de determinantes genéticos no genoma da planta. Neste caso, e especialmente quando a semente é o produto desejado que deve ser colhido das plantas híbridas, é tipicamente útil assegurar que macho-fertilidade em plantas híbridas que contêm os determinantes genéticos responsáveis por macho-esterilidade é totalmente restaurada. Pode-se assegurar que os genitores masculinos apresentam genes restauradores de fertilidade apropriados que são capazes de restaurar a macho-fertilidade em plantas híbridas que contêm os determinantes genéticos responsáveis por macho esterilidade. Determinantes genéticos para machoesterilidade podem estar localizados no citoplasma. Exemplos de macho-esterilidade citoplásmica (CMS) foram por exemplo descritos em
Petição 870180002928, de 12/01/2018, pág. 109/185
105/159 espécies Brassica. Porém, determinantes genéticos para machoesterilidade podem também estar localizados no genoma nuclear. Plantas macho-estéreis tambpem podem ser obtidas por métodos de biotecnologia, tais como engenharia genética. Um meio particularmente útil de obtenção de plantas macho-estéreis é descrito na publicação WO 89/10396 na qual, por exemplo, uma ribonuclease, tais como barnase, é seletivamente expressada nas células do tapete nos estames. A fertilidade pode ser restaurada pela expressão nas células de tapete de um inibidor de ribonuclease, tais como barstar.
[00652] Plantas ou cultivares de planta (obtidos por métodos biotecnológicos de planta tais como engenharia genética) que podem ser tratados de acordo com a invenção, são plantas herbicida-tolerantes, ou seja, plantas feitas tolerantes em relação a um ou mais determinados herbicidas. Tais plantas podem ser obtidas seja por transformação genética, ou por seleção de plantas contendo uma mutação que proporciona tal tolerância a herbicida.
[00653] Plantas herbicida-tolerantes são, por exemplo, plantas glifosato-tolerantes, ou seja, plantas feitas tolerantes em relação a glifosato herbicida ou a seus sais. Por exemplo, plantas glifosato-tolerantes podem ser obtidas pela transformação da planta com um gene que codifica a sintase da enzima 5-enolpiruvilchiquimato-3-fosfato (EPSPS). Exemplos de tais genes EPSPS são o gene AroA (mutante CT7) da bactéria Salmonella typhimurium, os genes que codificam a EPSPS de petúnia, um EPSPS de tomate) ou um EPSPS de eleusina. Também pode ser um mutante de EPSPS. Plantas glifosato-tolerantes também são obtidas pela expressão de um gene que codifica uma enzima glifosato oxidorreductase. Plantas glifosato-tolerantes também podem ser obtidas pela expressão de um gene que codifica uma enzima glifosato acetil transferase. Plantas glifosato-tolerantes também
Petição 870180002928, de 12/01/2018, pág. 110/185
106/159 podem ser obtidas contendo mutações que ocorrem naturalmente dos genesacima referidos.
[00654] Outras plantas herbicida-resistentes são, por exemplo, plantas que são feitas tolerantes em relação a herbicidas que inibem a enzima glutamina sintase, tais como bialafos, fosfinotricina ou glufosinato. Tais plantas podem ser obtidas pela expressão de uma enzima que desentoxica o herbicida ou um mutante da enzima glutamina sintase que é resistente à inibição. Uma enzima de ação desintoxicante eficaz desse tipo é uma enzima que codifica uma fosfinotricina acetiltransferase (tais como a proteína bar ou pat da espécie Streptomyces). Plantas que expressam uma fosfinotricina acetiltransferase exógena são, por exemplo, conforme acima descritas.
[00655] Outras plantas herbicida-tolerantes também são plantas que são feitas tolerantes em relação a herbicidas que inibem a enzima hidroxifenilpiruvatodioxigenase (HPPD). Hidroxifenilpiruvatodioxigenases são enzimas que catalisam a reação na qual parahidroxifenilpiruvato (HPP) é transformado em homogentisato. Plantas tolerantes a inibidores de HPPD podem ser transformadas com um gene que codifica uma enzima HPPD resistente que ocorre naturalmente ou um gene que codifica um mutante da enzima HPPD. Tolerância a inibidores de HPPD também pode ser obtida pela transformação de plantas com genes que codificam determinadas enzimas que capacitam a formação de homogentisato apesar da inibição da enzima HPPD nativa através do inibidor de HPPD. Tolerância de plantas a inibidores de HPPD também pode ser melhorada pela transformação de plantas com um gene que codifica uma enzima prefenato dehidrogenase além de um gene que codifica uma enzima HPPD-tolerante. [00656] Outras plantas herbicida-resistentes são plantas que são feitas tolerantes em relação a inibidores de acetolactato sintase (ALS). Inibidores de ALS conhecidos incluem, por exemplo, sulfonilureia, imiPetição 870180002928, de 12/01/2018, pág. 111/185
107/159 dazolinona, triazolopirimidinas, pirimidinilóxi(tio)benzoatos e/ou herbicidas sulfonilaminocarboniltriazolinona. Mutações diferentes na enzima ALS (também conhecida como acetohidroxiácido sintase, AHAS) são conhecidas para conferir tolerância a diferentes herbicidas e grupos de herbicidas. A produção de plantas sulfonilureia-tolerantes e plantas imidazoli na-tolerantes foi descrita na publicação internacional W0 1996/033270. Outras plantas sulfonilureia- e imidazolinonatolerantes também foram descritas, por exemplo, no documento WO 2007/024782.
[00657] Outras plantas tolerantes à imidazolinona e/ou sulfonilureia podem ser obtidas pela mutagenese induzida, seleção em culturas celulares na presença de herbicida ou indução de mutação.
[00658] Plantas ou cultivares de planta (obtidos por métodos biotecnológicos tais como engenharia genética) que podem também ser tratados de acordo com a inveção são plantas inseto-resistentes, ou seja, plantas feitas resistentes ao ataque por certos insetos-alvo. Tais plantas podem ser obtidas pela transformação genética ou pela seleção de plantas que contêm uma mutação que confere tal resistência a insetos.
[00659] No presente contexto, o termo planta transgênica insetoresistente inclui qualquer planta contendo pelo menos um transgene compreendendo uma sequência de codificação que codifica:
1)uma proteína cristal inseticida de Bacillus thuringiensis ou uma porção inseticida desta, tais como, as proteínas cristais inseticidas relacionadas por Crickmore et al., Microbiology e Molecular Biology Reviews (1998), 62, 807-813, atualizada por Crickmore et al. (2005) at the Bacillus thuringiensis toxin nomenclature, online em: http://www.lifesci.sussex.ac. uk/Home/Neil_Crickmore/Bt/), ou porções inseticidas destas, p.ex. proteínas da proteína Cry classes CrylAb, CrylAc, Cry1F, Cry2Ab, Cry3Ae ou Cry3Bb ou porções inseticidas
Petição 870180002928, de 12/01/2018, pág. 112/185
108/159 destas ou
2) uma proteína cristal Bacillus thuringiensis ou uma porção desta que é inseticida na presença de uma segunda proteína cristal de Bacillus thuringiensis ou uma porção desta, tais como a toxina binária feita das proteínas cristais Cy34 e Cy35 (Moellenbeck et al., Nat. Biotechnol. (2001), 19, 668-72; Schnepf et al., Applied Environm. Microb. (2006), 71, 1765-1774); ou
3) uma proteína inseticida híbrida compreendendo partes de duas proteínas cristais inseticidas diferentes de Bacillus thuringiensis, tais como um híbrido das protéinas de 1) acima ou um híbrido das protéinas de 2) acima, p.ex. a proteína Cry1A.1O5 produzida pelo milho MON98034 (WO 2007/027777); ou
4) uma proteína de qualquer uma da 1) a 3) acima em que alguns, particularmente de 1 a 10, aminoácidos foram substituídos por outro aminoácido para obter uma atividade inseticida maior em relação a espécies de inseto alvo, e/ou para ampliar a faixa de espécies de inseto alvo afetadas, e/ou por causa alterações introduzidas na codificaçãodo DNA durante a clonagem ou transformação, tais como a protéina Cry3Bb1 em eventos do milho MON863 ou MON88017, ou a proteína Cry3A em evento de milho MIR 604;
5) uma proteína inseticida secretada de Bacillus thuringiensis ou Bacillus cereus, ou uma porção inseticida desta, tais como as proteínas inseticidas vegetativas (VIP) relacionadas em http://www.lifesci.sussex.ac. uk/Home/Neil_Crickmore/Bt/vip.html, p.ex., proteínas da classe VIP3Aa; ou
6) uma protein secretada de Bacillus thuringiensis ou Bacillus cereus que é inseticida na presença de uma segunda proteína secretada de Bacillus thuringiensis ou B. cereus, tais como a toxina binária feita das proteínas VIP1A e VIP2A (WO 1994/21795);
7) uma proteína inseticida híbrida, compreendendo partes
Petição 870180002928, de 12/01/2018, pág. 113/185
109/159 de diferentes proteínas secretadas de Bacillus thuringiensis ou Bacillus cereus, tais como um híbrido das proteínas em 1) acima ou um híbrido das proteínas em 2) acima; ou
8)uma proteína de qualquer uma de 1) a 3) acima sendo que alguns, particularmente de 1 a 10, aminoácidos são substituídos por outro aminoácido para obter uma atividade inseticida maior em relação a espécies de inseto alvo afetadas, e/oupor causa de alterações introduzidas na codificação de DNA durante a clonagem ou transformação (enquanto a codificação de uma proteína inseticida permanece), tais como a protéina VIP3Aa em evento de algodão COT 102. [00660] Naturalmente, uma planta transgênica inseto-resistente, conforme aqui utilizada, também inclui qualquer planta compreendendo uma combinação de genes que codificam as proteínas de qualquer uma das classes acima de 1 a 8. Em uma forma de concretização, uma planta inseto-resistente contém mais do que um transgene que codifica uma proteína de qualquer uma das classes acima de 1 a 8, para ampliar a faixa de espécies de inseto alvo afetadas ou para retardar o desenvolvimento de resistência a inseto em relação a plantas pela utilização de diferentes proteínas inseticidas à mesma espécie de inseto alvo, porém que apresentam um modo diferente de ação, tais como ligação a diferentes sítios de ligação de receptor no inseto. [00661] Plantas ou cultivares de planta (obtidos por métodos biotecnológicos tais como engenharia genética) que podem ser tratados de acordo com a invenção são tolerantes ao estresse abiótico. Tais plantas podem ser obtidas pela transformação genética, ou pela seleção de plantas contendo uma mutação que confere tal resistência a inseto. Plantas tolerantes ao estresse particularmente úteis incluem:
a.plantas que contêm um transgene capaz de reduzir a expressão e/ou a atividade da do gene poli(ADP-ribose)polimerase (PARP) nas células de planta ou plantas;
Petição 870180002928, de 12/01/2018, pág. 114/185
110/159
b. plantas que contêm um transgene que melhora a tolerância ao estresse capaz de reduzir a expressão e/ou atividade dos genes PARG codificadores das plantas ou células de planta;
c. plantas que contêm um transgene que melhora a tolerância ao estresse, os quais codificam uma enzima planta-funcional davia de biossíntese de salvamento de nicotinamida adenina dinucleotídeo, incluindo nicotinamidase, nicotinato fosforibosiltransferase, mononucleotídeo adeniltransferase de ácido nicotínico, nicotinamida adenina dinucleotídeo sintetase ou nicotinamida fosforibosiltransferase.
[00662] Plantas ou cultivares de planta (obtidos por métodos biotecnológicos de plantas tais como, engenharia genetica) que podem ser também tratados de acordo com a invenção, mostram qualidade, estabilidade a armazenagem e/ou quantidade alterada do produto colhido e/ou propriedades alteradas de ingredientes específicos do produto colhido tais como:
1) plantas transgênicas que sintetizam um amido modificado, que é alterado quanto às suas características físico-químicas, particularmente o conteúdo de amilase ou a razão amilase /amilopectina, o grau de ramificação, o comprimento médio de cadeia, a distribuição de cadeia lateral, o comportamento de viscosidade, a resistência à gelificação, o tamanho do grão de amido e/ou a morfologia do grão de amido, em comparação ao amido sintetizado em células ou plantas do tipo selvagem, de forma que esse amido modificado seja mais adequados para aplicações especiais.
2) plantas transgênicas que sintetizam polímeros de carboidrato não-amido com propriedades alteradas em comparação com plantas do tipo selvagem sem modificação genética. Exemplos são plantas que produzem polifrutose, especialmente da inulina e tipo levan, plantas que produzem alfa-1,4-glucanos, plantas que produzem alfa-1,6 ramificado afa-1,4-glucanos, e plantas que produzem alternan.
Petição 870180002928, de 12/01/2018, pág. 115/185
111/159
3) plantas transgênicas que produzem hialuronan.
[00663] Plantas ou cultivares de planta (obtidos por métodos biotecnológicos de plantas, tais como engenharia genética) que podem ser também tratados de acordo com a invenção, são plantas, tais como plantas de algodão, com características de fibra alteradas. Tais plantas podem ser obtidas por transformação genética, ou por seleção de plantas contendo uma mutaçao que confere tais características de fibra alteradas e incluem:
a) plantas, tais como plantas de algodão, contendo uma forma alterada de genes de celulose sintase,
b) plantas, tais como plantas de algodão, contendo uma forma alterada de ácidos nucléicos homólogos rsw2 ou rsw3;
c) plantas, tais como plantas de algodão, com expressão aumentada de sacarose fosfato sintase;
d) plantas, tais como plantas de algosão, com expressão aumentada de sacarose sintase;
e) plantas, tais como plantas de algodão, sendo que o momento da passagem plasmodesmatal na base da célula de fibra é alterado, por exemplo, através da infra-regulação de 3-1,3-glucanase fibra-seletiva;
f) plantas, tais como plantas de algosão, contendo fibras com reatividade alterada, por exemplo, através da expressão do gene da N-acetilglucosamina transferase incluindo genes nodC e quitina sintase.
[00664] Plantas ou cultivares de planta (obtidos por métodos biotecnológicos de planta, tais como engenharia genética) que também podem ser tratados de acordo com a invenção, são plantas, tais como colza de semente oleaginosa ou plantas Brassica associadas, com características da composição de óleo alteradas. Tais plantas podem ser obtidas por transformação genética ou por seleção de plantas contenPetição 870180002928, de 12/01/2018, pág. 116/185
112/159 do uma mutação que confere tais características de óleo alteradas e incluem:
a) plantas, tais como plantas de colza de semente oleaginosa, que produzem óleo com alto teor de ácido oleico;
b) plantas tais como plantas de colza de semente oleaginosa, que produzem óleo com baixo teor de ácido linolênico;
c) plantas tais como plantas de colza de semente oleaginosa, que produzem óleo com baixo nível de ácidos graxos.
[00665] Plantas transgênicas particularmente úteis que podem ser tratadas de acordo com a invenção, são plantas que compreendem um ou mais genes que codificam uma ou mais toxinas são as plantas transgênicas vendidas sob os seguintes nomes comerciais: YIELD GARD® (por exemplo, milho, algodão, feijão de soja), KnockOut® (por exemplo, milho), BiteGard® (por exemplo, milho), BT-Xtra® (por exemplo, milho), StarLink® (por exemplo, milho), Bollgard® (algodão), Nucotn® (algodão), Nucotn 33B® (algodão), NatureGard® (por exemplo, milho), Protecta® e NewLeaf® (batata). Exemplos de plantas herbicidatolerantes que podem ser mencionadas são variedades de milho, variedades de algodão variedades de feijão de soja vendidas sobos seguintes nomes comerciais: Roundup Ready® (tolerância a gliosato, por exemplo, milho, algodão, feijão de soja), Liberti Link® (tolerância a fosfinotricina, por exemplo, bagaço de semente oleaginosa), IMI® (tolerância a imidazolinonas) e SCS® (tolerância a sulfonilureias, por exemplo, milho). Plantas herbicida-resistentes (plantas cultivadas de maneira convencional quanto a tolerância herbicida) que podemos citar também, incluem as variedades vendidas sob o nome comercial Clearfield® (por exemplo, milho).
[00666] Plantas transgênicas particularmente úteis quepodem ser tratadas de acordo com a invenção, são plantas contendo eventos de transformação, ouuma combinação de eventos de transformação, rePetição 870180002928, de 12/01/2018, pág. 117/185
113/159 lacionados, por exemplo, nos bancos de dados das agências regulatórias regionais (vide, por exemplo http://gmoinfo.jrc.it/gmp_browse.aspx e http://www.agbios.com/ dbase.php).
[00667] De acordo com a invenção, as plantas relacionadas podem ser tratadas vantajosamente com os compostos da fórmula geral (I) ou as misturas de composto ativo de acordo com a invenção. As faixas preferidas acima indicadas para os compostos ativos e misturas também se aplicam ao tratamento dessas plantas. É particualrmente preferido o tratamento das plantas com compostos e misturas indicados no presente texto.
[00668] As composições ou compostos ativos de acordo com a invenção também podem ser usados para proteger plantas por um determinado período após o tratamento contra o ataque por patógenos referidos. O período pelo qual é provida proteção geralmente se estende por 1 a 28 dias, preferivelmente por 1 a 14 dias, particularmante preferivelmente por 1 a 10 dias, muito particularmente preferivelmente por 1 a 7 dias, após o tratamento das plantas com os compostos ativos, ou por até 200 dias após o tratamento de semente.
[00669] Preparação e uso dos compostos ativos da Fórmula (I) de acordo com a invenção aparecem indicados nos exemplos abaixo. Porém, a invenção não se limita a esses exemplos.
[00670] Observações gerais: Desde que não conste anotação contrária, todas as etapas de purificação cromatográfica e de separação foram realizadas em sílica-gel utilizando-se um gradiente de solvente de 0:100 acetato de etila /ciclo-hexano a 100:0 acetato de etila /ciclo-hexano.
Preparação de materiais de partida da fórmula (IX):
4-(4-acetil-1,3-tiazol-2-il)piperidina-1-carboxilato de terc-butila (IX1)
Petição 870180002928, de 12/01/2018, pág. 118/185
114/159 [00671] Sob temperatura ambiente, 1,1,1-triacetóxi-1,1-di-hidro-1,2benziodoxol-3(1H)-ona (solução a 15% em diclorometano, 28 g) são adicionados em gotas a uma solução de 4-[4-(1-hidroxietil)-1,3-tiazol2-il] piperidina-1-carboxilato de terc-butila (VIII-1, 2.06 g) em diclorometano (40 ml). A mistura de reação foi agitada sob temperatura ambiente durante a noite, 5 g de sílica-gel foram em seguida adicionados e o solvente removido sob pressão reduzida. O resíduo foi purificado por cromatografia. Isso resultou em 4-(4-acetil-1,3-tiazol-2-il)piperidina1-carboxilato de terc-butila (1,65 g).
[00672] 1H RMN (DMSO-d6): δ 8,34 (s, 1H), 4,00 (d, 2H), 3,26 (m, 1H), 2,93 (td, 2H), 2,54 (s, 3H), 2,09-2,03 (m, 2H), 1,60 (qd, 2H), 1,41 (s, 9H) [00673] MS (ESI): 255 (M-C(CH3)3+H)
Preparação de materiais de partida das fórmulas (IVa), (IVb) e ílVçl:
4-[4-(2-fen i leti I )-1,3-tiazol-2-i I] pi perid i na-1 -carboxilato de tercbutila (IV-1) [00674] Sob 0Ό, uma solução de 4-carbamotioilpiper idina-1carboxilato de terc-butila (1,95 g) é adicionada em gotas a uma solução de 1-bromo-4-fenilbutan-2-ona (2,00 g) em etanol (20 ml). Sob argônio, a mistura de reação é agitada sob temperatura ambiente durante a noite. Trietilamina (1,7 ml) é adicionada, e a mistura é diluída com acetato de etila e lavada com solução de cloreto de sódio concentrada. A fase aquosa foi removida e extraída com acetato de etila. As fases orgânicas combinadas foram secadas sobre sulfato de sódio e concentradas sob pressão reduzida, que resulta em uma mistura de 4-[4-(2feniletil)-1,3-tiazol-2-il]piperidina-1-carboxilato de terc-butila e 4-[4hidróxi-4-(2-feniletil)-4,5-di-hidro-1,3-tiazol-2-il]piperidina-1-carboxilato de terc-butila. Os dois compostos foram separados por cromatografia. Isso resultou em 4-[4-(2-feniletil)-1,3-tiazol-2-il]piperidina-1-carboxilato
Petição 870180002928, de 12/01/2018, pág. 119/185
115/159 de terc-butila (800 mg) e fer-butil 4-[4-hidróxi-4-(2-feniletil)-4,5-di-hidro1,3-tiazol-2-il]piperidina-1 -carboxilato (640 mg). Ambos os compostos podem ser usados para o processo 1.2 já que o ultimi composto é, sob condições de reação, convertido no formador.
[00675] 1H RMN (DMSO-d6): δ 7,28-7.25 (m, 2H), 7,22-7,22 (m, 2H), 7,20-7,18 (m, 1H), 7,13 (s, 1H), 4,00 (bs, 2H), 3,35 (s, 2H), 3,16 (m, 1H), 2,95 (s, 4H), 2,00 (d, 2H), 1,52 (qd, 2H), 1,41 (s, 9H) ppm [00676] MS (ESI): 373 ([M+H]+)
4-{4-[(E)-2-(naftalen-1 -i l)eten i I]-1,3-tiazol -2-i l}pi perid i na-1 carboxilato de ferc-butila (IV-2) [00677] Sob argônio, dietil 1-naftilmetilfosfonato (1.88 g) é dissolvido em tetra-hidrofurano (20 ml) e resfriado a 0Ό. 757 mg de tercbutóxido de potássio foram adicionados, e por conseguinte a cor da solução muda para vermelho-escuro. Após mais 10 minutos de agitação, 4-(4-formil-1,3-tiazol-2-il)piperidina-1-carboxilato de ferc-butila (1.00 g) foi adicionado. A mistura foi agitada sob 0Ό por 30 minutos e em seguida aquecida sob temperatura ambiente. Após mais 20 minutos, foi adicionada solução de cloreto de amônio conc. A fase aquosa foi separada e extraída com acetato de etila. As fases orgânicas combinadas foram secadas sobre sulfato de sódio e concentradas, e o resíduo purificado por cromatografia. Isso resultou em fer-butil 4-{4-[(E)2-(naftalen-1 -il)etenil]-1,3-tiazol-2-i l}pi perid i na-1 -carboxilato (1,16 g) como o isômero E.
[00678] 1H RMN (DMSO-d6): δ 8,23 (d, 1H), 8,14 (d, 1H), 7.94 (d, 1H), 7.87 (d, 1H), 7.83 (d, 1H), 7.62 (s, 1H), 7.62-7.51 (m, 3H), 7.26 (d, 1H), 4.04 (d, 2H), 3.27 (m, 1H), 2.94 (t, 2H), 2.15-2.05 (m, 2H), 1.66 (qd, 2H), 1.42 (s, 9H) ppm [00679] MS (ESI): 421 ([M+H]+)
4-{4-[(Z)-2-(naftalen-1 -i l)eten i I]-1,3-tiazol -2-i l}pi perid i na-1 -carboxilato de terc-butila (IV-3)
Petição 870180002928, de 12/01/2018, pág. 120/185
116/159 [00680] Sob argônio, cloreto de (l-naftilmetil)trifenilfosfônio (2,96 g) foi dissolvido em 20 ml de tetra-hidrofurano e resfriado a 0Ό, e terbutóxido de potássio(757 mg) adicionado, e por conseguinte a cor da solução muda para vermehlo-escura. Após 10 minutos de agitação, é adicionado 4-(4-formil-1,3-tiazol-2-il)piperidina-1-carboxilato de tercbutila (1.00 g). A mistura é agitada sob 0Ό por ma is 30 minutos e em seguida lentamente aquecida sob temperatura ambiente. Após mais 20 minutos, é adicionada solução de cloreto de amônio, e separada a fase aquosa. Após extração da fase aquosa com acetato de etila, as fases orgânicas combinadas são secadas sobre sulfato de sódio e concentradas sob pressão reduzida. Após purificação por cromatografia, obtém-se 4-{4-[(Z)-2-(naftalen-1-il)etenil]-1,3-tiazol-2-il} piperidina1-carboxilato de ferc-butila (1,2 g, isômero Z).
[00681] 1H RMN (DMSO-d6): δ 7,92 (t, 2H), 7,87-7,80 (m, 1H), 7,507,48 (m, 4H), 7,10 (d, 1H), 6,91 (d, 1H), 6,86 (s, 1H), 3,75 (d, 2H), 2.98 (m, 1H), 2,80 (t, 2H), 1,80-1,70 (m, 2H), 1,40 (s, 9H), 1,30 (qd, 2H) PPm [00682] MS (ESI): 421 ([M+H]+)
4-{4-[(1Z)-4-fenilpent-1 -en-1 -il]-1,3-tiazol -2-i l}pi perid i na-1 -carboxilato de ferc-butila (IV-4) [00683] 4-(4-formil-1,3-tiazol-2-il)piperidina-1-carboxilato de tercbutila (1,00 g) foi reagida com iodeto de trifenil(3-fenilbutil)fosfônio (3,53 g) e purificado conforme descrito em IV-3. Obteve-se 4-{4-[(1Z)4-fenilpent-1 -en-1 -il]-1,3-tiazol-2-il}piperidina-1 -carboxilato de tercbutila (1,23 g) na forma do isômero Z.
[00684] 1H RMN (DMSO-d6): δ 7,30 (s, 1H), 7,26-7,22 (m, 4H), 7,15 (m, 1H), 6,33 (s, 1H), 5,59 (m, 1H), 3,98 (d, 2H), 3,19 (m, 1H), 3,002,83 (m, 5H), 2,06-1,97 (m, 2H), 1,60 (qd, 2H), 1,41 (s, 9H), 1,24 (d, 3H)ppm [00685] MS (ESI): 413 ([M+H]+)
Petição 870180002928, de 12/01/2018, pág. 121/185
117/159 fer-buti I 4-[4-(3-fenilprop-1 -in-1 -i I)-1,3-tiazol -2-i I] pi perid i na-1 carboxilato (IV-5) [00686] Sob argônio, são adicionados cloreto de benzila (134 mg), bis(acetonitril)dicloropaládio(ll) (5.5 mg), 2-diciclo-hexilfosfino-2’,4’,6’triisopropilbifenila (30 mg) e carbonato de césio (363 mg) a uma solução desgaseificada de 4-(4-etinil-1,3-tiazol-2-il)piperidina-1-carboxilato de ferc-butila (X-1, 310 mg) em tetra-hidrofurano (4 ml). A mistura é em seguida aquecida a 65Ό. Após resfriamento em seguida, o catalisador é removido por filtração sobre Celite e o filtrado foi concentrado sob pressão reduzida. Após purificação por cromatografia, obteve-se 4-[4-(3-fenilprop-1 -in-1 -il)-1,3-tiazol-2-il]piperidina-1-carboxilato de tercbutila (329 mg).
[00687] 1H RMN (CD3CN): δ 7,40-7,20 (m, 6H), 4,10-4,05 (m, 2H), 3,83 (s, 2H), 3,15 (m, 1H), 2,94-2,35 (m, 2H), 2,08-2,00 (m, 2H), 1,63 (qd,2H), 1,43 (s, 9H) ppm [00688] MS (ESI): 383 ([M+H]+)
4-[4-(naftalen-1 -i leti n i I )-1,3-tiazol -2-i I] pi perid i na-1 -carboxilato de ferc-butila (IV-6) [00689] Tetracis(trifenilfosfina)paládio (0) (95 mg), cobre(l) iodo (31 mg) e trietilamina (200 mg) foram adicionados a uma solução de 4-{4[(trimetilsilil)etinil]-1,3-tiazol-2-il}piperidina-1-carboxilato de ferc-butila (XI-1, 600 mg) e 1-bromonaftaleno (375 mg) em Ν,Ν-dimetilformamida desgaseificada. Após aquecimento a 85Ό, fluoreto de tetra-nbutilamônio (1M in THF, 1.81 ml) é adicionado em gotas. A mistura de reação é em seguida diluída com água e extraído acetato de etila. Os extratos orgânicos foram secados sobre sulfato de sódio e concentrados sob pressão reduzida. Após purificação por cromatografia, obtevese 4-[4-(naftalen-1 -iletinil)-1,3-tiazol-2-il]piperidina-1-carboxilato de ferc-butila (576 mg).
Petição 870180002928, de 12/01/2018, pág. 122/185
118/159 [00690] 1H RMN (CD3CN): δ 8,38 (d, 1H), 7,95 (d, 2H), 7,79 (d, 1H), 7,70 (s, 1H), 7,67-7,50 (m, 3H), 4,12 (d, 2H), 3,24 (m, 1H), 2,94 (t, 2H), 2,15-2,08 (m, 2H), 1,72 (qd, 2H), 1,45 (s, 9H) ppm [00691 ] MS (ESI): 419 ([M+H]+)
4-[4-( pi rid i n -3-i leti n i l)-1,3-tiazol -2-i I] pi pe rid i na-1 -carboxilato de ferc-butila (IV-7) [00692] 4-{4-[(tri meti Isi I i l)eti n i I]-1,3-tiazol-2-i l}pi perid i na-1 -carboxilato de ferc-butila (XI-1, 610 mg) foi reagido analogamente ao exemplo IV6 com 3-bromopiridina (291 mg). Obteve-se 4-[4-(piridin-3-iletinil)-1,3tiazol-2-il]piperidina-1-carboxilato de ferc-butila (469 mg).
[00693] 1H RMN (CD3CN): δ 8,74 (d, 1H), 8,55 (dd, 1H), 7,87 (s, 1H), 7,63 (m, 1H), 7,35 (dd, 1H), 4,10 (d, 2H), 3,20 (m, 2H), 2,93 (t, 2H), 2,13-2,05 (m, 2H), 1,69 (qd, 2H), 1,44 (s, 9H) ppm [00694] MS (ESI): 270 ([M+2H-C=OOC(CH3) 3]+)
4-{4-[2-(naftalen-1 -iI)etiI]-1,3-tiazol-2-il}piperidina-1 -carboxilato de ferc-butila (IV-8) [00695] 4-{4-[(Z)-2-(naftalen-1 -il)etenil]-1,3-tiazol-2-i l}pi perid i na-1 carboxilato de ferc-butila (IV-3, 1.5 g) é dissolvido em 90 ml de metanol e, sob 30Ό, hidrogenado sob uma pressão de hidrogênio de 1 mPa (10 bar) utilizando-se 10% Pd/C como catalisador. Remoção do catalisador por filtração e remoção do solvente sob pressão reduzida obteve-se 4-{4-[2-(naftalen-1 -il)etil]-1,3-tiazol-2-i l}pi perid i na-1 carboxilato de ferc-butila (1.48 g) como um óleo descolorido.
[00696] 1H RMN (DMSO-d6): δ 8,08 (d, 1H), 7,88 (d, 1H), 7,74 (d, 1H), 7,55-7,45 (m, 2H), 7,42-7,32 (m, 2H), 7.10 (s, 1H), 4,00 (d, 2H), 3,43 (t, 2H), 3,32-3,06 (m, 3H), 2,92 (t, 2H), 2,04-1,98 (m, 2H), 1,58 (qd, 2H), 1,42 (s, 9H) ppm [00697] MS (ESI): 423 ([M+H]+)
Preparação de materiais de partida da fórmula (X):
4-(4-etinil-1,3-tiazol-2-il)piperidina-1-carboxilato de terc-butila (X-1)
Petição 870180002928, de 12/01/2018, pág. 123/185
119/159 [00698] Sob argônio, 4-(4-formil-1,3-tiazol-2-il)piperidina-1carboxilato de ferc-butila (600 mg) é dissolvido em metanol, e adicionados carbonato de potássio (839 mg) e 1-diazo-2-oxopropilfosfonato dimetila (786 mg). A mistura é agitada sob temperatura ambiente por 3 horas. Após preparação aquosa, a mistura é extraída com acetato de etila e os extratos são secados com sulfato de sódio e concentrada sob pressão reduzida. O resídio é purificado por cromatografia. Obteve-se 4-(4-etinil-1,3-tiazol-2-il)piperidina-1-carboxilato de ferc-butila (493 mg).
[00699] 1H RMN (CD3CN): δ 7,51 (s, 1H), 4,07 (d, 2H), 3,36 (s, 1H), 3,16 (m, 1H), 2,90 (t, 2H), 2,10-2,00 (m, 2H), 1,65 (qd, 2H), 1,43 (s, 9H)ppm [00700] MS (ESI): 237 ([M+2H-C(CH3) 3]+)
Preparação de materiais de partida da fórmula (XI):
4-{4-[(tri meti Is i li I )eti n il]-1,3-tiazol-2-il}pi perid i na-1 -carboxilato de ferc-butila (XI-1) [00701] Sob argônio, 4-(4-etinil-1,3-tiazol-2-il)piperidina-1-carboxilato de ferc-butila (X-1, 940 mg) é dissolvido em tetra-hidrofurano sob -78Ό, e hexametildissilazano de lítio (1M em hexan o, 4,82 ml) é adicionado em gotas. Após 30 minutos, é adicionado em gotas cloreto de trimetilsilila (699 mg), e resfriado removido. A mistura é agitada durante a noite, e em seguida adicionado cloreto de amônio saturado e a mistura extraída com acetato de etila. Os extratos orgânicos foram secados sobre sulfato de sódio e concentrados sob pressão reduzida. O resíduo foi purificado por cromatografia. Obteve-se 4-{4[(trimetilsilil)etinil]-1,3-tiazol-2-il} piperidina-1-carboxilato de ferc-butila (1,28 g).
[00702] 1H RMN (CD3CN): δ 7,42 (s, 1H), 4,05-3,97 (m, 2H), 3,09 (m, 1H), 2,83 (t, 2H), 2,05-1,90 (m, 2H), 1,59 (qd, 2H), 1,37 (s, 9H), 0,17 (s, 9H) ppm
Petição 870180002928, de 12/01/2018, pág. 124/185
120/159 [00703] MS (ESI): 309 ([M+2H-C(CH3) 3]+)
Preparação de materiais de partida da fórmula fila), (llb) e (llc):
Cloridrato (11-1) de 4-[4-(2-feniletil)-1,3-tiazol-2-il]piperidina [00704] Sob OO, uma solução molar 2 de cloreto de hidrogênio em dietil éter é adicionada em gotas a uma solução de 4-[4-(2-feniletil)1.3- tiazol-2-il]piperidin-1-carboxilato de ferc-butila (IV-1, 640 mg). A mistura de reação é agitada sob 0Ό e em seguida le ntamente aquecida sob temperatura ambiente. A mistura é agitada durante a noite, e o solvente e cloreto de hidrogênio em excesso são então removidos. Obteve-se hidrocloreto de 4-[4-(2-feniletil)-1,3-tiazol-2-il]piperidina (590 mg).
[00705] 1H RMN (DMSO-d6): δ 7,25-7,23 (m, 2H), 7,19-7,16 (m, 3H), 7,11 (s, 1H), 3,40-3,30 (m, 5H), 2,98 (s, 4H), 2,21-2,14 (m, 2H), 1,951,87 (m, 2H) ppm [00706] MS (ESI): 273 ([M-CI]+)
Cloridrato de 4-{4-[2-(Naftalen-1-il)etil]-1,3-tiazol·2-il}piperidina (II2) [00707] Sob argônio e sob 0Ό, uma solução de cloreto de hidrogênio em dietil éter (2 M, 25 ml) é adicionada a 4-{4-[2-(naftalen-1 -il)etil]1.3- tiazol-2-il}piperidina-1 -carboxilato de ferc-butila (IV-2, 1.40 g). A mistura é agitada sob 0Ό e então lentamente aquecí da sob temperatura ambiente. A mistura é agitada durante a noite, e o ácido em excesso e solvente são removidos sob pressão reduzida. Obteve-se cloridrato de 4-{4-[2-(naftalen-1 -il)etil]-1,3-tiazol-2-il}piperidina (1.28 g). [00708] 1H RMN (DMSO-d6): δα 9,18 (bs, 1H), 8,93 (bs, 1H), 8,08 (d, 1H), 7,89 (d, 1H), 7,75 (d, 1H), 7,56-7,45 (m, 2H), 7,73-7,32 (m, 2H), 7,16 (s, 1H), 3,45 (d, 1H), 3,43 (d, 1H), 3,38-3,28 (m, 2H), 3,152.95 (m, 4H), 2,25-2,17 (m, 2H), 2,00 (qd, 2H) ppm [00709] MS (ESI): 323 ([M-CI]+)
4-[5-Bromo-4-(2-feniletil)-1,3-tiazol-2-iI]piperidina (11-3)
Petição 870180002928, de 12/01/2018, pág. 125/185
121/159 [00710] Sob 0Ό, é adicionado bromo (123 mg) em gotas a uma solução de cloridrato de 4-[4-(2-feniletil)-1,3-tiazol-2-il]piperidina (11-1, 200 mg) em ácido acético (2 ml). A mistura é agitada durante 30 minutos, e depois é adicionada solução de bicarbonato de sódio saturada. A fase aquosa é separada e extraída com acetato de etila. As fases orgânicas combinadas são secadas sobre carboanto de sódio anidro, concentradas sob pressão reduzida e purificadas por cromatografia. Obteve-se 4-[5-bromo-4-(2-feniletil)-1,3-tiazol-2-il]piperidina (127 mg). [00711] logP (pH2.3): 1.72 [00712] MS (ESI): 351,353 ([M+1 ]+)
Preparação de compostos da fórmula (la)
MÉTODO A:
2-[5-metil-3-(trifluorometil)-1 H-pirazol-1 -II]-1 -{4-[4-(2-fen i leti l)-1,3tiazol-2-iI]piperidin-1 -iljetanona (I-53) [00713] Sob 0Ό, cloreto de oxalila (134 mg) e uma gota de N,Ndimetilformamida são adicionados à solução de ácido [5-metil-3(trifluorometil)-l H-pirazol-1 -il]acético (185 mg) em diclorometano. A mistura de reação é agitada sob temperatura ambiente por 3 horas. O solvente e reagente em excesso são removidos sob pressão reduzida. O resíduo sólido é então onze vezes dissolvido em diclorometano e, sob 0Ό, adicionado em gotas a uma solução de clori drato de 4-[4-(2feniletil)-1,3-tiazol-2-il]piperidina (11-1, 250 mg) e trietilamina (410 mg) em diclorometano. Uma solução de cloreto de amônio concentrada é em seguida adicionada à solução de reação, e a fase aquosa removida e extraída com acetato de etilae. As fases orgânicas combinadas são secadas sobre sulfato de sódio e concentradas. Obteve-se 2-[5metil-3-(trifluorometil)-1 H-pirazol-1 -il]-1 -{4-[4-(2-fen i leti I)-1,3-tiazol-2il]piperidin-1 -iljetanona (122 mg).
[00714] 1H RMN (DMSO-d6): δ 7,28-7,26 (m, 2H), 7,22-7,21 (m, 2H), 7,19-7,15 (m, 2H), 6,51 (s, 1H), 5,33 (d, 1H), 5,25 (d, 1H), 4,36 (d, 1H),
Petição 870180002928, de 12/01/2018, pág. 126/185
122/159
3,95 (d, 1H), 3,35-3,20 (m, 2H), 2,96 (s, 4H), 2,82 (t, 1H), 2,21 (s, 3H), 2,09 (d, 1H), 2,07 (d, 1H), 1,78 (m, 1H), 1,53 (m, 1H) ppm [00715] MS (ESI): 463 (]M+H]+)
-{4-[4-(2-feniletil)-1,3-tiazol-2-iI]piperidin-1 -il}pentan-1 -ona (I-58) [00716] Cloreto de pentanoíla (133 mg) é adicionado a uma solução de cloridrato de 4-[4-(2-feniletil)-1,3-tiazol-2-il]piperidina (11-1,309 mg) e trietilamina (0,7 ml) em diclorometano (3 ml). A mistura é agitada durante a noite, e é adicionada emn seguida água. A fase aquosa é separada e extraída com acetato de etila, e as fases orgânicas combinadas em seguida secadas com sulfato de sódio e concentradas. O resíduo é purificado. Obteve-se 1-{4-[4-(2-feniletil)-1,3-tiazol-2-il]piperidin1- il}pentan-1-ona (179 mg).
[00717] 1H RMN (DMSO-d6): δ 7,27-7,21 (m, 2H), 7,20-7,14 (m, 3H), 7,05 (s, 1H), 4,37 (bs, 1H), 3,95 (bs, 1H), 3,26-3,18 (m, 2H), 2,96 (s, 4H), 2,80 (bs, 1H), 2,33 (t, 2H), 2,04 (d, 2H), 1,55 (bs, 2H), 1,50 (tt, 2H), 1,33 (tq,2H), 0,90 (t, 3H) ppm [00718] MS (ESI): 357 ([M+H]+)
2- [5-metil-3-(trifluorometil)-1 H-pirazol-1 -i I]-1 -(4-{4-[2-(naftalen-1 il)etil]-1,3-tiazol-2-il}piperidin-1 -il)etanona (1-81) [00719] Cloreto de oxalila (183 mg) e uma gota de N,N-dimetilformamida são adicionados a uma solução de ácido [5-metil-3(trifluorometil)-l H-pirazol-1 -il]acético (100 mg) em diclorometano (5 ml). A mistura de reação é agitada sob temperatura ambiente durante a noite. Após a remoção dos solventes sob pressão reduzida, o resíduo é então dissolvido em diclorometano (5 ml) e uma solução de cloridrato de 4-{4-[2-(naftalen-1-il)etil]-1,3-tiazol-2-il}piperidina (II-2, 172 mg) e base Hünig (186 mg) em diclorometano (5 ml) é adicionada em gotas sob 0Ό. Após a adição de solução de cloreto de amônio concentrada, a fase aquosa é separada e extraída com acetato de etila. As fases orgânicas combinadas são secadas sobre sulfato de sódio e
Petição 870180002928, de 12/01/2018, pág. 127/185
123/159 concentradas sob pressão reduzida. O resíduo é purificado por cromatografia. Obteve-se 2-[5-metil-3-(trifluorometil)-1 H-pirazol-1 -il]-1 -(4-{4[2-(naftalen-1-il) etil]-1,3-tiazol-2-il}piperidin-1 -il)etanona (150 mg). [00720] 1H RMN (DMSO-d6): δ 8,09 (d, 1H), 7,90 (d, 1H), 7,75 (d,
1H), 7,56-7,46 (m, 2H), 7,42-7,33 (m, 2H), 7,12 (s, 1H), 6,45 (s, 1H),
5.22 (bs, 2H), 4,31 (bs, 1H), 3,98 (bs, 1H), 3,44 (t, 2H), 3,35-3,26 (m,
2H), 3,15-3,05 (m, 2H), 2,90 (bs, 1H), 2,23 (s, 3H), 2,15-2,05 (m, 2H),
1,75 (bs, 1H), 1,62 (bs, 1H) ppm [00721] MS (ESI): 513 ([M+H]+)
2-[5-metil-3-(trifluorometil)-1 H-pirazol-1 -II]-1 -{4-[4-(4-fenilpentil)1,3-tiazol-2-iI]piperidin-1 -iljetanona (I-80) [00722] 4-{4-[(1 Z)-4-fenilpent-1 -en-1 -il]-1,3-tiazol-2-i l}pi perid i na-1 carboxilato de ferc-butila (IV-4, 1,00 g) é dissolvido em metanol e, sob 40Ό, hidrogenado sob uma pressão H2 de 1 mPa (10 bar) na presença de Pd/C (10%) por 5 horas. Após filtração e remoção do solvente sob pressão reduzida obteve-se 4-[4-(4-fenilpentil)-1,3-tiazol-2il]piperidina-1-carboxilato de ferc-butila (1,00 g) como um óleo incolor. Esse é desprotegido analogamente ao exemplo II-2. Obtevem-se 850 mg de cloridrato de 4-[4-(4-fenilpentil)-1,3-tiazol-2-il]piperidina. 169 mg são em seguida reagidos analogamente ao exemplo 1-81 com ácido [5metil-3-(trifluorometil)-1 H-pirazol-1 -il]acético (100 mg). Após purificação por cromatografia, obteve-se 2-[5-metil-3-(trifluorometil)-1Hpirazol-1 -il]-1 -{4-[4-(4-feni I pentiI)-1,3-tiazol-2-iI]pi peridin-1 -il} etanona (180 mg) como um óleo incolor.
[00723] 1H RMN (DMSO-d6): δ 07,28-7,23 (m, 2H), 7,19-7,14 (m, 3H), 7,02 (s, 1H), 6,44 (s, 1H), 5,20 (bs, 2H), 4,30 (bs, 1H), 3,95 (bs, 1H), 3,30-3,20 (m, 2H), 2,87 (bs, 1H), 2,72 (m, 1H), 2,67-2,62 (m, 2H),
2.22 (s, 3H), 2,07-2,02 (m, 2H), 1,72 (bs, 1H), 1,63-1,47 (m, 5H), 1,19 (d, 3H) ppm [00724] MS (ESI): 505 ([M+H]+)
Petição 870180002928, de 12/01/2018, pág. 128/185
124/159
-{4-[5-bromo-4-(2-feniletil)-1,3-tiazol-2-i I] pi perid i n-1 -i l}-2-[5-m eti I3-(trifluorometil)-1 H-pirazol-1 -il]etanona (I-78) [00725] 4-[5-bromo-4-(2-feniletil)-1,3-tiazol-2-il]piperidina (II-3, 127 mg) é reagida analogamente ao exemplo 1-81 com ácido [5-metil-3(trifluorometil)-l H-pirazol-1-il]acético (118 mg). Após purificação por cromatografia, obteve-se 1-{4-[5-bromo-4-(2-feniletil)-1,3-tiazol-2i I] pi perid i n-1 -i l}-2-[5-meti l-3-(trif I uorometi I)-1 H-pirazol-1 -il]etanona (52 mg).
[00726] 1H RMN (DMSO-d6): δ 7,27-7,22 (m, 2H), 7,18-7,13 (m, 3H), 6,45 (s, 1H), 5,22 (bs, 2H), 4,38 (bs, 1H), 3,95 (bs, 1H), 3,33-3,20 (m, 2H), 2,94 (s, 4H), 2,93 (bs, 1H), 2,22 (s, 3H), 2,09-2,02 (m, 2H), 1,801,50 (m, 2H) ppm [00727] MS (ESI): 541 ([M+H]+)
MÉTODO B:
-{4-[4-(2-fen i leti l)-1,3-tiazol -2-i I] pi perid i n-1 -i l}-2-(tiofen-3-i I) etanona (I-63) [00728] Ácido tiofen-3-ilacético (156 mg) e base Hünig (323 mg) são dissolvidos em diclorometano (10 ml) e agitados por 30 minutos. Cloridrato de 4-[4-(2-feniletil)-1,3-tiazol-2-il]piperidina (11-1, 309 mg), preparado de acordo com o processo 1.2, é adicionado, e a mistura é agitada por mais 5 minutos antes de ser adicionado hexafluorofosfato de bromo-tris-pirrolidino-fosfônio (599 mg). A mistura de reação é agitada sob temperatura ambiente durante a noite. Após a remoção do solvente sob pressão reduzida, o resíduo é purificado por cromatografia. Obteve-se 1-{4-[4-(2-feniletil)-1,3-tiazol-2-il] piperidin-1 -il}-2-(tiofen-3il)etanona (99 mg).
[00729] 1H RMN (DMSO-d6): δ 7,44-7,43 (m, 1H), 7,28-7,12 (m, 6H), 7.05 (s, 1H), 6,99 (d, 1H), 4,38 (bs, 1H), 3,99 (bs, 1H), 3,72 (s, 2H), 3,22-3,15 (m, 2H), 2,96 (s, 4H), 2,81 (bs, 1H), 2,00 (d, 2H), 1,52 (m, 2H)ppm
Petição 870180002928, de 12/01/2018, pág. 129/185
125/159 [00730] MS (ESI): 397 ([M+H]+)
2-[2-cloro-5-(trifluorometil)fenil]-1-{4-[4-(2-feniletil)-1,3-tiazol-2il]piperidin-1 -iljetanona (I-67) [00731] Cloridrato de 4-[4-(2-feniletil)-1,3-tiazol-2-il]piperidina (11-1, 309 mg) é reagido analogamente ao exemplo I-63 com ácido [2-cloro5-(trifluorometil)fenil]acético (262 mg). Após purificação por cromatografia, obteve-se 2-[2-cloro-5-(trif I uorometi l)fen i I]-1 -{4-[4-(2-fen i leti I)1,3-tiazol-2-il]piperidin-1 -il} etanona (210 mg).
[00732] 1H RMN (DMSO-d6): δ 7,71-7,58 (m, 3H), 7,27-7,12 (m, 5H), 7,07 (s, 1H), 4,37 (bs, 1H), 4,05 (bs, 1H), 3,97 (s, 2H), 3,35-3,23 (m, 2H), 2,97 (s, 4H), 2,88 (bs, 1H), 2,07 (d, 2H), 1,65 (bs, 2H) ppm [00733] MS (ESI): 439 ([M+H]+)
2-(5-cloro-1 -metil-1 H-pirazol-4-il)-1 -{4-[4-(2-fen i leti l)-1,3-tiazol-2il]piperidin-1-iljetanona (I-65) [00734] Cloridrato de 4-[4-(2-feniletil)-1,3-tiazol-2-il]piperidina (11-1, 280 mg) é reagido analogamente ao exemplo I-63 com ácido (5-cloro1- metil-1 H-pirazol-4-il)acético (174 mg). Após purificação por cromatografia, obteve-se 2-(5-cloro-1-metil-1 H-pirazol-4-il)-1-{4-[4-(2-feniletil)1,3-tiazol-2-il]piperidin-1 -iljetanona (89 mg).
[00735] 1H RMN (DMSO-d6): δ 7,40 (s, 1H), 7,26-7,15 (m, 5H), 7,06 (s, 1H), 4,35 (bs, 1H), 4,05 (bs, 1H), 3,76 (s, 3H), 3,49 (s, 2H), 3,303,19 (m, 2H), 2,99 (s, 4H), 2,82 (bs, 1H), 2,08-2,00 (m, 2H), 1,58 (bs, 2H)ppm [00736] MS (ESI): 429 ([M+H]+)
2- [4-cloro-5-metil-3-(trifluorometil)-1 H-pirazol-1 -il]-1 -{4-[4-(2feniletiI)-1,3-tiazol-2-iI]piperidin-1 -il}propan-1 -ona (I-64) [00737] Cloridrato de 4-[4-(2-feniletil)-1,3-tiazol-2-il]piperidina (11-1, 309 mg) é reagido analogamente ao exemplo I-63 com ácido 2-[4cloro-5-metil-3-(trifluorometil)-1 H-pirazol-1-il]propanoico (282 mg). Após purificação por cromatografia, obteve-se 2-[4-cloro-5-metil-3Petição 870180002928, de 12/01/2018, pág. 130/185
126/159 (trifl uorometi I)-1 H-pirazol-1 -il]-1 -{4-[4-(2-feniletil)-1,3-tiazol-2il]piperidin-1 -il}propan-1 -ona (165 mg).
[00738] 1H RMN (DMSO-d6): δ 7,26-7,21 (m, 2H), 7,20-7,13 (m, 3H), 7,06 (s, 1H), 5,70 (m, 1H), 4,30 (bs, 1H), 4,00 (bs, 1H), 3,30-3,19 (m, 2H), 2,96 (s, 5H), 2,26 (d, 3H), 2,08-1,96 (m, 2H), 1,64-1,54 (m, 5H) PPm [00739] MS (ESI): 511 ([M+H]+) [2,5-Bis(trifluorometil)fenil]{4-[4-(2-feniletil)-1,3-tiazol-2il]piperidin-1 -il} metanona (1-61) [00740] Cloridrato de 4-[4-(2-feniletil)-1,3-tiazol-2-il]piperidina (11-1, 309 mg) é reagido analogamente ao exemplo I-63 com cloreto de 2,5bis (trifluorometil)benzenocarbonila (304 mg). Após purificação por cromatografia, obteve-se [2,5-bis(trifluorometil)fenil]{4-[4-(2-feniletil)1,3-tiazol-2-il]piperidin-1 -iljmetanona (282 mg).
[00741] 1H RMN (DMSO-d6): δ 8,07-7,90 (m, 3H), 7,26-7,21 (m, 2H), 7.,20-7,14 (m, 3H), 7,08 (s, 1H), 4,50 (d, 1H), 3,35-3,23 (m, 4H), 2,97 (s, 4H), 2,22-2,10 (m, 1H), 2,00-1,87 (m, 2H), 1,87-1,45 (m, 2H) ppm [00742] MS (ESI): 513 ([M+H]+)
3-(3,4-dimetoxifenil)-1 -{4-[4-(2-f en I leti l)-1,3-tiazol -2-i I] pi perid i n-1 il}propan-1-ona (I-66) [00743] Cloridrato de 4-[4-(2-feniletil)-1,3-tiazol-2-il]piperidina (11-1, 309 mg) é reagido analogamente ao exemplo I-63 com ácido 3-(3,4dimetoxifenil)propanoico (231 mg). Após purificação por cromatografia, obteve-se 3-(3,4-dimetoxifenil)-1-{4-[4-(2-feniletil)-1,3-tiazol-2il]piperidin-1 -il}propan-1 -ona (139 mg).
[00744] 1H RMN (DMSO-d6): δ 7,26-7,21 (m, 2H), 7,20-7,12 (m, 3H), 7,05 (s, 1H), 6,85-6,80 (m, 3H), 6,75-6,71 (dd, 1H), 3,93 (bs, 1H), 3,74 (s, 3H), 3,69 (s, 3H), 3,20 (m, 1H), 2,96 (s, 4H), 2,80-2,74 (m, 2H), 2,65-2,55 (bs, 2H), 2,04-1,97 (m, 2H), 1,58-1,42 (m, 2H), 1,28 (t, 2H) PPm
Petição 870180002928, de 12/01/2018, pág. 131/185
127/159 [00745] MS (ESI): 465 ([M+H]+)
2-( 1,3-Benzotiazol-2-il)-1 -{4-[4-(2-fen i leti l)-1,3-tiazol-2-i I] pi perid i n-1 iljetanona (1-71) [00746] Cloridrato de 4-[4-(2-feniletil)-1,3-tiazol-2-il]piperidina (11-1, 308 mg) é reagido analogamente ao exemplo I-63 com ácido 1,3benzotiazol-2-ilacético (252 mg). Após purificação por cromatografia, obteve-se 2-(1,3-benzotiazol-2-il)-1-{4-[4-(2-feniletil)-1,3-tiazol-2il]piperidin-1 -iljetanona (109 mg).
[00747] 1H RMN (DMSO-d6): δ 8,03 (d, 1H), 7,93 (d, 1H), 7,47 (t, 1H), 7,40 (t, 1H), 7,25-7,16 (m, 5H), 7,06 (s, 1H), 4,40 (bs, 1H), 4,34 (s, 2H), 4,09 (bs, 1H), 3,40-3,15 (m, 3H), 2,96 (s, 4H), 2,08-2,02 (m, 2H), 1,65 (bs, 2H) ppm [00748] MS (ESI): 448 ([M+H]+)
2-(2H-indazol-2-il)-1 -{4-[4-(2-fen i leti I )-1,3-tiazol-2-i I] pi perid i n-1 iljetanona (I-70) [00749] Cloridrato de 4-[4-(2-feniletil)-1,3-tiazol-2-il]piperidina (11-1, 309 mg), preparado de acordo com o processo 1.2, é reagido analogamente ao exemplo I-63 com ácido 2H-indazol-2-ilacético (194 mg). Após purificação por cromatografia, obteve-se 2-(2H-indazol-2-il)-1-{4[4-(2-feniletil)-1,3-tiazol-2-il]piperidin-1 -iljetanona (67 mg).
[00750] 1H RMN (CD3CN): δ 8,10 (s, 1H), 7,71 (d, 1H), 7,60 (d, 1H), 7,29-7,15 (m, 6H), 7,07 (dd, 1H), 6,87 (s, 1H), 5,45 (d, 1H), 5,36 (d, 1H), 4,48 (d, 1H), 4,00 (d, 1H), 3,35-3,23 (m, 2H), 3,00 (s, 4H), 2,86 (t, 1H), 2,18-2,06 (m, 2H), 1,80 (qd, 1H), 1,66 (qd, 1H) ppm [00751] MS (ESI): 431 ([M+H]+)
MÉTODO C:
2-[5-metil-3-(trifluorometil)-1 H-pirazol-1 -i I]-1 -(4-{4-[2-(naftalen-1 il)etil]-1,3-tiazol-2-ilJpiperidin-1-iljetanona (1-81) [00752] 2-[5-meti l-3-(trif I uorometi I)-1 H-pirazol-1 -il]-1 -{4-[4-(naftalen1-iletinil)-1,3-tiazol-2-il]piperidin-1 -iljetanona (i-50, 157 mg) é dissolvido
Petição 870180002928, de 12/01/2018, pág. 132/185
128/159 em metanol (1,5 ml) e, sob 60Ό, reagido com formiato de amônio (195 mg) e 20% Pd(OH)2/C (4 mg) como catalisador. O catalisador é removido por filtração e o solvente removido sob pressão reduzida, resultantdo em 2-[5-metil-3-(trifluorometil)-1 H-pirazol-1 -il]-1 -(4-{4-[2(naftalen-1-il)etil]-1,3-tiazol-2-il} piperidin-1-il)etanona (86 mg) como um óleo incolor.
[00753] O produto foi caracterizado como o composto descrito anteriormente.
Preparação de compostos da fórmula (lb)
2-[5-metil-3-(trifluorometil)-1 H-pirazol-1 -i I]-1 -(4-{4-[(E)-2-(naftalen1- il) etenil]-1,3-tiazol-2-il}piperidin-1-il)etanona (I-27) [00754] 4-{4-[(E)-2-(naftalen-1 -il)etenil]-1,3-tiazol-2-i l}pi perid i na-1 carboxilato de terc-butila (IV-2, 171 mg) é desprotegido analogamente ao exemplo II-2 e em seguida reagido analogamente ao exemplo 1-81 com ácido [5-metil-3-(trifluorometil)-1 H-pirazol-1 -iljacético (100 mg). Após purificação por cromatografia, obteve-se 2-[5-metil-3(trif I uorometi I)-1 H-pirazol-1 -il]-1 -(4-{4-[(E)-2-(naftalen-1 -il)etenil]-1,3tiazol-2-il}piperidin-1-il)etanona (180 mg).
[00755] 1H RMN (DMSO-d6): δ 8,23 (d, 1H), 8,16 (d, 1H), 7,95 (d, 1H), 7,88 (d, 1H), 7,83 (d, 1H), 7,64 (s, 1H), 7,63-7,51 (m, 3H), 7,27 (d, 1H), 6,46 (s, 1H), 5,24 (bs, 2H), 4,38 (bs, 1H), 4,03 (bs, 1H), 3,40 (m, 1H), 3,32 (bs, 1H), 2,94 (bs, 1H), 2,24 (s, 3H), 2,23-2,12 (m, 2H), 1,85 (bs, 1H), 1,70 (bs, 1H) ppm [00756] MS (ESI): 511 ([M+H]+)
2- [5-metil-3-(trifluorometil)-1 H-pirazol-1 -i I]-1 -(4-{4-[(Z)-2-(naftalen1-il) etenil]-1,3-tiazol-2-il}piperidin-1-il)etanona (I-2) [00757] 4-{4-[(Z)-2-(naftalen-1 -il)etenil]-1,3-tiazol-2-i l}pi perid i na-1 carboxilato de terc-butila (IV-3, 171 mg) é desprotegido analogamente ao exemplo II-2 e em seguida reagido analogamente ao exemplo 1-81 com ácido [5-metil-3-(trifluorometil)-1 H-pirazol-1-iljacético (100 mg).
Petição 870180002928, de 12/01/2018, pág. 133/185
129/159
Após purificação por cromatografia, obteve-se 2-[5-metil-3(trif I uorometi I)-1 H-pirazol-1 -il]-1 -(4-{4-[(E)-2-(naftalen-1 -il)etenil]-1,3tiazol-2-il}piperidin-1-il)etanona (200 mg).
[00758] 1H RMN (DMSO-d6): δ 7,95-7,92 (m, 2H), 7,87-7,84 (m, 1H), 7,52-7,43 (m, 4H), 7,11 (d, 1H), 6,93 (d, 1H), 6,88 (s, 1H), 6,45 (s, 1H), 5,14 (s, 2H), 4,05 (bs, 1H), 3,74 (bs, 1H), 3,20-3,05 (m, 2H), 2,88 (bs, 1H), 2,24 (s, 3H), 1,90-1,78 (bs, 2H), 1,50 (bs, 1H), 1,35 (bs, 1H) ppm [00759] MS (ESI): 511 ([M+H]+)
2-[5-metil-3-(trifluorometil)-1 H-pirazol-1-il]-1-(4-{4-[(1Z)-4-fenilpent1 -en-1 -il]-1,3-tiazol-2-il}piperidin-1 -il)etanona (I-3) [00760] 4-{4-[(1 Z)-4-fenilpent-1 -en-1 -il]-1,3-tiazol-2-i l}pi perid i na-1 carboxilato de terc-butila (IV-4, 168 mg) é desprotegido analogamente ao exemplo II-2 e em seguida reagido analogamente ao exemplo 1-81 com ácido [5-metil-3-(trifluorometil)-1 H-pirazol-1 -il]acético (100 mg). Obteve-se 2-[5-metil-3-(trifluorometil)-1 H-pirazol-1 -il]-1 -(4-{4-[(1 Z)-4fenilpent-1-en-1-il]-1,3-tiazol-2-il} piperidin-1-il)etanona (200 mg). [00761] 1H RMN (DMSO-d6): δ 7,32 (s, 1H), 7,29-7,22 (m, 4H), 7,15 (m, 1H), 6,44 (s, 1H), 6,35 (d, 1H), 5,60 (m, 1H), 5,20 (bs, 2H), 4,30 (bs, 1H), 3,98 (bs, 1H), 3,38-3,25 (m, 2H), 3,05-2,84 (m, 4H), 2,22 (s, 3H), 2,17-2,05 (m, 2H), 1,85-1,56 (m, 2H), 1,26 (d, 3H) ppm [00762] MS (ESI): 503 ([M+H]+)
2-[5-metil-3-(trifluorometil)-1 H-pirazol-1 -II]-1 -(4-{4-[(Z)-2-(2naftiI)vinil]-1,3-tiazol-2-il}piperidin-1 -il)etanona (I-20) [00763] Cloreto de (2-naftilmetil)(trifenil)fosfônio (454 mg) é dissolvido em 5 ml de tetra-hidrofurano e resfriado sob 0Ό sob argônio, e adicionado terc-butóxido de potássio (125 mg), e portanto a cor da solução muda para vermelho escuro. Após 10 minutos de agitação, é adicionado 2-(1-{[5-metil-3-(trifluorometil)-1 H-pirazol-1 il]acetil}piperidin-4-il)-1,3-tiazol-4-carbaldeído (200 mg). A mistura é agitada sob 0Ό por mais 30 minutos e em seguida le ntamente aquePetição 870180002928, de 12/01/2018, pág. 134/185
130/159 cida sob temperatura ambiente. Após mais 20 minutos, é adicionada solução de cloreto de amônio saturada, e a fase aquosa é separada. Após extração da fase aquosa com acetato de etila, as fases orgânicas combinadas são secas sobre sulfato de sódio e concentradas sob pressão reduzida. Após purificação por cromatografia, obteve-se 2-[5metil-3-(trifluorometil)-1 H-pirazol-1 -il]-1 -(4-{4-[(Z)-2-(2-nafti I) vi n i I]-1,3tiazol-2-il} piperidin-1-il)etanona (260 mg).
[00764] MS (ESI): 511 ([M+H]+)
2-[5-metil-3-(trifluorometil)-1 H-pirazol-1 -i I]-1 -(4-{4-[(E)-2feniletenil]-1,3-tiazol-2-il}piperidin-1 -il)etanotiona (I-93) [00765] Anidrido etoxifenilditiofosfônico (62 mg) foi adicionado a uma solução de 2-[5-metil-3-(trifluorometil)-1 H-pirazol-1-il]-1-(4-{4-[(E)2-feniletenil]-1,3-tiazol-2-il}piperidin-1-il)etanona (141 mg) em clorofórmio (1 ml) e 1,2-dimetoxietano (2 ml). A mistura de reação é agitada sob temperatura ambiente por 24 horas e sob 40Ό po r 3 horas. Após remoção do solvente sob pressão reduzida, o resíudio é purificado por cromatografia. Obteve-se 2-[5-metil-3-(trifluorometil)-1 H-pirazol-1 -il]-1 (4-{4-[(E)-2-feniletenil]-1,3-tiazol-2-il} piperidin-1-il)etanotiona (45 mg) como óleo incolor.
[00766] 1H RMN (CD3CN): δ 7,55 (d, 2H), 7,43 (d, 1H), 7,37 (t, 2H), 7,30-7,28 (m, 2H), 7,18 (d, 1H), 6,39 (s, 1H), 5,41 (d, 1H), 5,26 (s, 2H), 4,42 (d, 1H), 3,54 (t, 1H), 3,45 (m, 1H), 3,38 (t, 1H), 2,31 (s, 3H), 2,302,23 (m, 2H), 1,95-1,80 (m, 2H) ppm [00767] MS (ESI): 477 ([M+H]+)
Preparação de compostos da fórmula (lc)
2-[5-metil-3-(trifluorometil)-1 H-pirazol-1 -i I]-1 -{4-[4-(naftalen-1 i leti n i I )-1,3-tiazol -2-i I] pi perid i n-1 -iljetanona (I-50) [00768] 4-[4-(naftalen-1 -i leti n i I)-1,3-tiazol-2-i I] pi perid i na-1 -carboxilato de terc-butila (IV-6, 200 mg) é desprotegido analogamente ao exemplo II-2 e em seguida reagido analogamente ao exemplo 1-81
Petição 870180002928, de 12/01/2018, pág. 135/185
131/159 com ácido [5-metil-3-(trifluorometil)-1H-pirazol-1-il]acético (117 mg). Após purificação por cromatografia, obteve-se 2-[5-metil-3(trif I uorometi I)-1 H-pirazol-1 -il]-1 -{4-[4-(naftalen-1 -i leti n i I)-1,3-tiazol-2il]piperidin-1 -iljetanona (112 mg).
[00769] 1H RMN (CD3CN): δ 8,39 (d, 1H), 7,96 (d, 2H), 7,80 (d, 1H), 7,72 (s, 1H), 7,67-7,50 (m, 3H), 6,37 (s, 1H), 5,05 (s, 2H), 4,45 (bs, 1H), 3,98 (bs, 1H), 3,40-3,20 (m, 2H), 2,93 (bs, 1H), 2,25 (s, 3H), 2,252,15 (m, 2H), 1,90-1,75 (m, 2H) ppm [00770] MS (ESI): 509 ([M+H]+)
2-[5-metil-3-(trifluorometil)-1 H-pirazol-1 -i I]-1 -{4-[4-(pi rid i n-3iletinil)-1,3-tiazol-2-il]piperidin-1 -iIJetanona (1-51) [00771] 4-[4-(piridin-3-iletinil)-1,3-tiazol-2-il]piperidina-1-carboxilato de terc-butila (IV-7, 469 mg) é desprotegido analogamente ao exemplo II-2 resultando em cloridrato de 3-{[2-(piperidin-4-il)-1,3-tiazol-4il]etinil}piridina (407 mg). Este é imediatamente reagido sob temperatura ambiente com ácido [5-metil-3-(trifluorometil)-1 H-pirazol-1 -iljacético (277 mg) na presença de 4-dimetilaminopiridina (16 mg) e 1 -etil-3-(3’dimetilaminopropil)carbodi-imida (268 mg) em diclorometano (5 ml). Agitação sob temperatura ambiente durante a noite, concentração e purificação por cromatografia resulta em 2-[5-metil-3-(trifluorometil)1 H-pirazol-1 -il]-1 -{4-[4-(pi rid i η-3-i leti n i I)-1,3-tiazol-2-i I] pi perid i n-1 iljetanona (65 mg).
[00772] 1H RMN (CD3CN): δ 8,74 (dd, 1H), 8,59 (dd, 1H), 7,99 (s, 1H), 7,96 (m, 1H), 7,45 (dd, 1H), 6,45 (s, 1H), 5,22 (bs, 2H), 4,35 (bs, 1H), 4,00 (bs, 1H), 3,40-3,20 (m, 3H), 2,22 (s, 3H), 2,17-2,10 (m, 2H), 1,90-1,55 (m, 2H) ppm [00773] MS (ESI): 460 ([M+H]+)
2-[5-metil-3-(trifluorometil)-1 H-pirazol-1 -i I]-1 -{4-[4-(3-fenilprop-1 -in1 -il)-1,3-tiazol -2-i I] pi perid i n-1 -iljetanona (I-52)
Petição 870180002928, de 12/01/2018, pág. 136/185
132/159 [00774] 4-[4-(3-fenilprop-1 -in-1 -il)-1,3-tiazol-2-i I] pi perid i na-1 -carboxilato de terc-butila (IV-5, 320 mg) é em seguida desprotegido analogamente ao exemplo II-2 e depois reagido analogamente ao exemplo
1- 81 com ácido [5-metil-3-(trifluorometil)-1H-pirazol-1-il]acético (174 mg). Após purificação por cromatografia, obteve-se 2-[5-metil-3(trif I uorometi I)-1 H-pirazol-1 -il]-1 -{4-[4-(3-fenilprop-1 -in-1 -il)-1,3-tiazol-2il]piperidin-1 -iljetanona (33 mg).
[00775] 1H RMN (CD3CN): δ 7,46 (s, 1H), 7,42-7,34 (m, 4H), 7,307,25 (m, 1H), 6,39 (s, 1H), 5,09 (d, 1H), 5,02 (d, 1H), 4,45 (d, 1H), 3,91 (d, 1H), 3,84 (s, 2H), 3,25 (m, 2H), 2,82 (t, 1H), 2,23 (s, 3H), 2,18-2,05 (m, 2H), 1,82 (qd, 1H), 1,66 (qd, 1H) ppm [00776] MS (ESI): 473 ([M+H]+)
-[4-(4-eti n i 1-1,3-tiazol-2-i I) pi peri d i n-1 -il]-2-[5-metil-3(trifluorometil)-lH-pirazol-1 -il]etanona (I-86) [00777] Sob argônio, 2-(1-{[5-metil-3-(trifluorometil)-1 H-pirazol-1iljacetil} piperidin-4-il)-1,3-tiazol-4-carbaldeído (200 mg) é dissolvido em metanol (5 ml) e carbonato de potássio (215 mg) e diazo-2oxopropilfosfonato de dimetila (199 mg) são adicionados. A mistura é agitada sob 40Ό. Após preparação aquosa, a mistura é extraída com acetato de etila e os extratos são secos com sulfato de sódio e concentrados sob pressão reduzida. O resíduo é purificado por cromatografia. Obteve-se 1-[4-(4-etinil-1,3-tiazol-2-il) piperidin-1 -il]-2-[5-metil-3(trifluorometil)-l H-pirazol-1 -il]etanona (67 mg).
[00778] 1H RMN (DMSO-d6): δ 7,86 (s, 1H), 6,44 (s, 1H), 5,20 (bs, 2H), 4,31 (bs, 1H), 4,08 (s, 1H), 3,98 (bs, 1H), 3,31 (m, 1H), 3,28 (bs, 1H), 2,88 (bs, 1H), 2,22 (s, 3H), 2,13-2,05 (m, 2H), 1,78 (bs, 1H), 1,61 (bs, 1H) ppm [00779] MS (ESI): 383 ([M+H]+)
2- [5-metil-3-(trifluorometil)-1 H-pirazol-1 -II]-1 -(4-{4[(trimetiIsiIiI)etiniI]-1,3-tiazol-2-iI}piperidin-1 -il)etanona (I-98)
Petição 870180002928, de 12/01/2018, pág. 137/185
133/159 [00780] Sob argônio, 1-[4-(4-etinil-1,3-tiazol-2-il)piperidin-1-il]-2-[5metil-3-(trifluorometil)-1 H-pirazol-1-iljetanona (I-86, 525 mg) é, sob 78Ό, dissolvido em tetra-hidrofurano (10 ml), e hexametildissilazano de lítio (1M em hexano, 1.40 ml) é adicionado em gotas. Após 10 minutos, cloreto de trimetilsilila (179 mg) é adicionado em gotas. Após 30 minutos de agitação, é adicionada solução de cloreto de amônio saturada e a mistura é extraída com acetato de etila. Os extratos orgânicos são secos sobre sulfato de sódio e concentrados sob pressão reduzida. O resíduo é purificado por cromatografia. Obteve-se 2-[5-metil-3(trifl uorometi I)-1 H-pirazol-1 -il]-1 -(4-{4-[(tri meti Isi I i l)etin i I]-1,3-tiazol-2il}piperidin-1-il)etanona (540 mg).
[00781] 1H RMN (DMSO-d6): δ 7,70 (s, 1H), 6,27 (s, 1H), 5,08 (d, 1H), 5,01 (d, 1H), 4,12 (bd, 1H), 3,76 (bd, 1H), 3,05 (t, 1H), 2,59 (t, 1H), 1,97 (s, 3H), 1,88-1,77 (m, 2H), 1,56 (tdd, 1H), 1,30 (tdd, 1H), 0,00 (s, 9H) ppm [00782] MS (ESI): 455 ([M+1 ]+)
-(4-{4-[(4-metoxifen i I )eti n i I]-1,3-tiazol-2-i l}pi perid i n-1 -il)-2-[5-metil3-(trifluorometil)-1 H-pirazol-1 -il]etanona (1-100) [00783] Tetraquis(trifenilfosfina)paládio (0) (25 mg), cobre(l) iodo (8 mg) e trietilamina (53 mg) são adicionados a uma solução de 2-[5metil-3-(trifluorometil)-1 H-pirazol-1 -il]-1 -(4-{4-[(tri meti Isi I i l)eti n i I]-1,3tiazol-2-il} piperidin-1-il)etanona (I-98, 200 mg) e 1-bromo-4metoxibenzeno (91 mg) em Ν,Ν-dimetilformamida desgaseificada (2 ml). Após aquecimento a 85Ό, fluoreto de tetra-n-b utilamônio (1M in THF, 0,48 ml) é adicionado em gotas. A mistura de reação foi então diluída com água e extraída com acetato de etila. Os extratos orgânicos são secos sobre sulfato de sódio e concentrados sob pressão reduzida. Após purificação por cromatografia, obteve-se 1-(4-{4-[(4metoxifenil)etinil]-1,3-tiazol-2-il}piperidin-1 -il)-2-[5-metil-3-(trifluorometil)-1 H-pirazol-1 -iljetanona (84 mg).
Petição 870180002928, de 12/01/2018, pág. 138/185
134/159 [00784] 1H RMN (DMSO-d6): δ 7,84 (s, 1H), 7,49 (d, 2H), 6,98 (d, 2H), 6,45 (s, 1H), 5,22 (bs, 2H), 4,33 (bs, 1H), 3,98 (bs, 1H), 3,80 (s, 3H), 3,34 (m, 1H), 3,28 (bs, 1H), 2,89 (bs, 1H), 2,22 (s, 3H), 2,15-2,09 (m, 2H), 1,80 (bs, 1H), 1,63 (bs, 1H) ppm [00785] MS (ESI): 489 ([M+H]+)
-(4-{4-[(2-metoxifenil)etinil]-1,3-tiazol-2-i l}pi perid i n-1 -il)-2-[5-metil3-(trifluorometil)-1 H-pirazol-1 -il]etanona (1-103) [00786] Tetraquis(trifenilfosfina)paládio (0) (25 mg), cobre(l) iodo (7 mg) e trietilamina (48 mg) são adicionados a uma solução de 1-[4-(4etinil-1,3-tiazol-2-iI)pi peridin-1 -il]-2-[5-metil-3-(trifIuorometi I)-1 H-pirazol1-il]etanona (I-86, 150 mg) e 1-iodo-2-metoxibenzeno (101 mg) Ν,Νdimetilformamida desgaseificada (1.5 ml). Após 2 horas de agitação sob 85Ό, a mistura de reação é então diluída com água e extraída com acetato de etila. Os extratos orgânicos são secos sobre sulfato de sódio e concentrados sob pressão reduzida. Após purificação por cromatografia, obteve-se 1-(4-{4-[(2-metoxifenil)etinil]-1,3-tiazol-2il}piperidin-1 -il)-2-[5-metil-3-(trifluorometiI)-1 H-pirazol-1 -il]etanona (100 mg).
[00787] 1H RMN (DMSO-d6): δ 7,86 (s, 1H), 7,47 (dd, 1H), 7,40 (td, 1H), 7,09 (d, 1H), 6,98 (td, 1H), 6,45 (s, 1H), 5,23 (bs, 2H), 4,33 (bs, 1H), 3,98 (bs, 1H), 3,86 (s, 3H), 3,35 (m, 1H), 3,29 (bs, 1H), 2,89 (bs, 1H), 2,23 (s, 3H), 2,15-2,08 (m, 2H), 1,80 (bs, 1H), 1,63 (bs, 1H) ppm [00788] MS (ESI): 489 ([M+H]+)
Exemplos [00789] Os compostos da fórmula I relacionados na tabela 1 abaixo podem ser obtidos analogamente aos métodos acima indicados.
\\
VW <>
X //
-v n-yl4?-r3 [00790] em que
Petição 870180002928, de 12/01/2018, pág. 139/185
135/159
TABELA I
| Q. cn _o | 3,91LDJ | _ | 00 | _ | Q CO LO | [ali-V V | a CM | Q CM O | Q O) CO | Q co | ||||
| Ό or | fenila | naftalen-1-ila | fenila | ciclo-hexila | ciclo-hexila | ciclo-hexila | fenila | fenila | 4-clorofenila | 4-clorofenila | 4-clorofenila | 4-metoxifenila | 4-metoxifenila | 4-metoxifenila |
| Ό _l | ligação | ligação | CO I o I o CM I o | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação |
| _l | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) |
| or | I | I | I | I | I | I | I | I | I | I | I | I | I | I |
| X | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o |
| § | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o |
| > | o | o | o | o | o | o | o | o | o | o | o | o | o | o |
| Lj | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o |
| < | 5-meti l-3-(trifl uorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 3-(trifluorometil)-1 H-pirazol1-ila | 4-cloro-5-metil-3-(trifluorometil)-1 H-pirazol-1-ila | 3-(trifluorometil)-1 H-pirazol1-ila | 4-cloro-5-metil-3-(trifluorometil)-1 H-pirazol-1-ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 3-(trifluorometil)-1 H-pirazol1-ila | 4-cloro-5-metil-3-(trifluorometil)-1 H-pirazol-1 -ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 3-(trifl uorometil)-1 H-pirazol1-ila | 4-cloro-5-metil-3-(trifluorometil)-1 H-pirazol-1 -ila |
| X LU | CM | co | LO | CO | Γγ | 00 | σ> | O | - | CM | CO |
Petição 870180002928, de 12/01/2018, pág. 140/185
136/159
Tabela I Continuação
| Q. cn _o | 4,51LDJ | a CO | Q CO O LO | Q Tb co | [aiLLl | 4,61LDJ | Q Tb co | Q CO o LO | íall-V V | Q CD O co | rqi£9'fr | |||
| Ό tr | 3-(trifluorometila)- fenila | 3-(trifluorometila)- fenila | 3-(trifluorometila)- fenila | naftalen-1-ila | naftalen-1-ila | naftalen-2-ila | naftalen-2-ila | naftalen-2-ila | fenila | fenila | fenila | fenila | naftalen-1-ila | CO LL O |
| Ό _l | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | CM I o | CM I o | CM I o | ligação | ligação | CM I O |
| _l | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (Z) | CH=CH (E) | CH=CH (E) | CH=CH (E) |
| tr | I | I | I | I | I | I | I | I | I | I | I | I | I | I |
| X | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o |
| § | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o |
| > | o | o | o | o | o | o | o | o | o | o | o | o | o | o |
| Lj | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o |
| < | 5-meti l-3-(trifl uorometil)-1 Hpirazol-1-ila | 3-(trifluorometil)-1 H-pirazol- 1-ila | 4-cloro-5-metil-3- (trifl uorometi l)-1 H-pirazol-1- ila | 3-(trifluorometil)-1 H-pirazol- 1-ila | 4-cloro-5-metil-3- (trifl uorometi l)-1 H-pirazol-1- ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 3-(trifluorometil)-1 H-pirazol- 1-ila | 4-cloro-5-metil-3- (trifl uorometi l)-1 H-pirazol-1- ila | 5-meti l-3-(trifl uorometil)-1 Hpirazol-1-ila | 3-(trifluorometil)-1 H-pirazol1-ila | 4-cloro-5-metil-3- (trifl uorometi l)-1 H-pirazol-1- ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifl uorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifl uorometil)-1 Hpirazol-1-ila |
| X LU | LO | CO | 00 | O | O CM | CM | CM CM | CO CM | 3- CM | LO CM | CO CM | h- CM | 00 CM |
Petição 870180002928, de 12/01/2018, pág. 141/185
137/159
Tabela I Continuação
| Q. cn _o | íqlZ£'e | Q O) 00 | CD Tb | |||||||||||||||||||
| Ό or | terc-butila | _ro Έ φ -1—< Φ | _çp Έ M—· Φ | ciclo-hexila | morfolin-4-ila | piridin-3-ila | _çp Έ φ M— | ω c Φ M— | ω c Φ M— | ω c Φ M— | ω c Φ M— | ω c Φ M— | ω c Φ M— | ω c Φ M— | naftalen-1-ila | naftalen-1-ila | naftalen-1 -ila | naftalen-1-ila | naftalen-1-ila | naftalen-1-ila | naftalen-1-ila | naftalen-1-ila |
| Ό _l | CM I o | CM I O | CM I O | CM I o | CM I o | O O ω σ) | O O ω σ) | O O ω cn | O O ω cn | O O ω σ) | O O ω cn | O O ω cn | O O ω cn | O O ω cn | O O ω σ) | O O ω σ) | O O ω σ) | O O ω cn | O O ω cn | O O ω σ) | O O ω σ) | O O ω σ) |
| _l | CH=CH (E) | CH=CH (E) | CH=CH (E) | CH=CH (E) | CH=CH (E) | CH=CH (E) | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM T O CM T o | ο III Ο |
| or | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I | T | Τ |
| X | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM T o CM T o | CM Τ ο CM Τ ο |
| § | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM T o CM T o | CM Τ ο CM Τ ο |
| > | o | o | o | o | o | o | o | o | o | o | o | o | o | o | o | o | o | o | o | o | o | ο |
| Lj | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM T o | CM T o | CM Τ ο |
| < | 5-meti l-3-(trifl uorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 5-(difluorometil)-3-metil-1 Hpirazol-1-ila | 3,5-dicloro-1 H-pirazol-1-ila | 3,5-dibromo-1 H-pirazol-1-ila | 2-bromo-5- (trifluorometil)fenila | 5-bromo-2-metilfenila | 2,5-diclorofenila | 2,5-dibromofenila | 5-iodo-2-metilfenila | 3,5-bis(trifluorometil)-1 H-pirazol-1-ila | 5-(difluorometil)-3-metil-1 Hpirazol-1-ila | 3,5-dicloro-1 H-pirazol-1-ila | 3,5-dibromo-1 H-pirazol-1-ila | 2-cloro-5-(trifluorometil)fenila | 2-bromo-5-(trifluorometil) fenila | 5-bromo-2-metilfenila | 5-meti l-3-(trifluorometil)-1 Ηpirazol-1-ila |
| X LU | O c\l | O co | co | CM CO | CO co | 3- co | LO CO | CD CO | h- co | 00 co | O co | O | CM | CO | LD | CD | h- | 00 | O | Ο ίθ |
Petição 870180002928, de 12/01/2018, pág. 142/185
138/159
Tabela I Continuação
| Q. 03 _o | Q CO CD CN | Q CO 00 co | rô1 03 ri- co | (? CO 00 CN | Q ri- lO co | Q CD CN | Q | Q cb ri- co | rdSfrT | Q co | Q ri- CD_ | θ’ cb CN | Q ri- co | [aZ9T | Q CO 03 cm | Q cb co | Q cb ri- | θ’ cb 03 co | Q CD IO cm | 1 1 | Q CO CD co |
| Ό or | _ro cò c Jo õ_ | ω Έ φ M— | ω Έ φ M— | ω Έ φ M— | ω Έ φ M— | ω c Φ M— | ω c Φ M— | ω c Φ M— | ω c Φ M— | ω Έ φ M— | ω c Φ M— | ω c Φ M— | ω c Φ M— | ω c Φ M— | ω Έ φ M— | ω c Φ M— | ω c Φ M— | ω c Φ M— | ω c φ M— | ω c Φ M— | ω c Φ M— |
| Ό _l | o o ω 03 | CM I O | O O ω 03 | O O ω 03 | O O ω 03 | O O ω 03 | O O ω 03 | O O ω 03 | O O ω 03 | O O ω 03 | O O ω 03 | O O ω 03 | O O ω 03 | O O ω 03 | O O ω 03 | O O ω 03 | O í(D 0 ω 03 | O O ω 03 | O í(D 0 ω 03 | O í(D 0 ω 03 | O O ω 03 |
| _l | o III O | o III O | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM T O CM T o | CM T O CM T o | CM T O CM T o | CM T O CM T 0 | CM T O CM T O | CM T O CM T O | CM T O CM T O | CM T O CM T O | CM T O CM T O | CM T O CM T O |
| or | I | I | I | I | I | I | I | I | I | I | T | T | T | T | T | T | T | T | T | T | T |
| X | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM T 0 CM T 0 | CM T 0 CM T 0 | CM T 0 CM T 0 | CM T 0 CM T 0 | CM T 0 CM T 0 | CM T 0 CM T 0 | CM T 0 CM T 0 |
| § | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM T 0 CM T O | CM T 0 CM T O | CM T 0 CM T O | CM T 0 CM T O | CM T 0 CM T O | CM T 0 CM T O | CM T 0 CM T O |
| > | o | o | o | o | o | o | o | o | o | o | o | o | o | o | 0 | O | O | O | O | O | O |
| Lj | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o CM I o CM I o | CM I o | CM I o | o c o JD | o c o JD | CM T o | CO T o T o | CM T 0 | CM T O CM T O | CM T O | CO T 0 T 0 | CM T O | CM T O | CM T O |
| < | T φ E o o =3 ^3 (D CO / +3 Õ Φ N E 2 LO Q. | T φ E o o =3 ^3 (D CO / +3 Õ Φ N E 2 LO Q. | T φ E o o =3 ^3 (D CO / +3 Õ Φ N E 2 IO q. | _ro õ N ro õ. T φ E o ιό co | õ N 2 õ_ T φ E o o =3 M— CO | _ro Έ φ M— φ E o o =3 -1—< cò | _ro Έ φ M— O o o cò | CO O | T φ E o o =s ω M— ~ -1—< ~ õ -9 N lo 2 co Q. | ò o 1 = M—' y— <? o = N -S £ E 4 LO I 2 7 ° 5Ξ O <D 4 E | _ro Έ φ M— E o o o -1—< 'ω la iò cm | _ro Έ φ M— E o o o -1—< cò | _ro cò c Φ M— O M—· | ò o 1 = M—* y— <7 o = N -55 £ E ? LO I 2 7 ° 5Ξ O <D 4 E | 4 õ N 2 õ_ T φ E ò _o V ω lo — | _ro Έ φ M— X 0 φ E 0 4 co | _ro Έ φ M— E 0 0 0 M— -1—< IO ò 0 0 CM | õ N 2 õ_ T φ E 0 0 0 M— h CÒ | _ro õ N 2 õ. T | _ro CN õ N ω o c T CM | _ro CN õ N .2 M—· O N C Φ JD cò |
| X LU | LO | CM IO | co IO | 3- IO | IO IO | CD IO | ri- IO | 00 IO | 03 IO | O CD | CD | CM CD | CO CD | 3- CD | 10 CD | CD CD | ri- CO | 00 CD | 03 CD | O ri- | ri- |
Petição 870180002928, de 12/01/2018, pág. 143/185
139/159
Tabela I Continuação
| Ω cn _o | Ω Ib r- CO | Ib 00 co | Ω CÓ h- co | θ’ CO LO co | 4,71LDJ | σ> C0 co | θ’ Α r- | θ’ Α C0 | θ’ CÓ 00 co | Ω^ o co | CÓ 00 co | Ω1 A LO CN | |||||||||
| Ό tr | _ro Έ φ M— | I | _φ c Φ φ Φϊ φ c | _φ Έ φ Μ— | _φ C φ φ φί φ C | _Φ C Φ Φ Φί Φ c | _φ Έ φ Μ— | _Φ C Φ Φ Φί Φ C | _φ Έ φ Μ— | _φ C φ φ φί φ C | _Φ C0 C Α Ω_ | _φ Έ φ Μ— | _φ Έ φ M— | _φ Έ Φ M— | T | _Φ C Φ Φ ΦΪ Φ c | _φ c φ φ Φϊ φ c | _φ c Φ Φ ΦΪ Φ c | _Φ Έ φ M— | _φ c Φ Φ ΦΪ Φ c | _φ c Φ Φ ΦΪ Φ c |
| Ό _l | O »Φ O φ σ) | o »Φ O φ σ) | ο »Φ Ο φ σ) | Ο ίφ Ο φ σ) | ο ίφ ο φ | ο ίφ ο φ σ) | Ο »Φ ο φ | ο ίφ ο φ σ) | CO Τ ο τ ο CM 5 | ο ίφ ο φ σ) | Ο »Φ Ο Φ σ) | CO Τ ο τ ο CM τ ο | O »Φ o φ O) | CO T o T o CM 5 | o ίφ o Φ O) | o ίφ o Φ O) | o ίφ o Φ O) | o ίφ o Φ O) | O »Φ O Φ O) | o ίφ o Φ O) | o ίφ o Φ O) |
| _l | CM I o CM I o | CM I O | ο III Ο | CM Τ Ο CM Τ ο | Ν Τ Ο II Τ ο | LLJ Τ Ο II Τ ο | CM Τ Ο CM Τ ο | CM Τ Ο CM Τ ο | CM Τ ο CM Τ ο | CM Τ Ο CM Τ ο | CM Τ Ο CM Τ ο | CM τ ο CM Τ ο | LLJ T O II T o | ω T o II T o | o III O | CM T O CM T o | CM T O CM T o | CM T O CM T o | CM T O CM T o | CM T O CM T o | CM T O CM T o |
| tr | I | _φ '5. o _Ω_ φ E CN | Τ | τ | τ | τ | ώ | τ | τ | τ | τ | τ | T | T | T | T | T | T | T | T | T |
| X | CM I o CM I o | CM I O CM I o | CM Τ ο CM Τ ο | CM Τ ο CM Τ ο | CM τ ο CM τ ο | CM τ ο CM τ ο | CM Τ Ο CM Τ ο | CM Τ ο CM Τ ο | CM τ ο CM Τ ο | CM Τ ο CM Τ ο | CM Τ ο CM Τ ο | CM τ ο CM Τ ο | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM T o CM T o |
| § | CM I o CM I o | CM I o CM I o | CM Τ ο CM Τ ο | CM Τ ο CM Τ ο | CM Τ ο CM Τ ο | CM Τ ο CM Τ ο | CM Τ ο CM Τ ο | CM Τ ο CM Τ ο | CM Τ ο CM Τ ο | CM Τ ο CM Τ ο | CM Τ ο CM Τ ο | CM Τ ο CM Τ ο | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM T o CM T o |
| > | o | o | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο | o | o | o | o | o | o | o | o | ω |
| Lj | CM I o | CM I o | CM Τ ο | CM Τ ο | CM Τ ο | CM Τ ο | CM Τ ο | CM Τ ο | CM Τ ο | CM Τ ο | CM Τ ο | CM Τ ο | CM T o | CM T o | CM T o | CM T o | CM T o | CM T o | CM T o | CM T o | CM T o |
| < | _φ CN õ N φ Ό E N C Φ _Ω T | T φ E o o =3 ^3 (D CO A +3 Õ Φ N E 2 LO Ω. | _φ Õ Ν φ Ω Τ φ Ε b LO co | _φ Α C Α Ω | _φ Õ Ν Φ Ω. Τ φ Ε b LO co | _φ Õ Ν Φ ω Τ φ Ε b ιό co | τ φ Ε ο ο Ω _^3 Φ CO Α +3 Õ Φ Ν Ε 2 LO Ω. | _φ Õ Ν Φ ω Τ φ Ε b ιό co | τ φ Ε ο ο Ω _^3 Φ CO Α +3 Õ Φ Ν Ε 2 LO Ω. | τ φ Ε ο ο Ω _^3 Φ CO Α +3 Õ Φ Ν Ε 2 LO Ω. | τ φ Ε ο ο Ω Φ C0 Α += Õ Φ Ν Ε 2 LD Ω. | _φ Õ Ν Φ Ω. Τ φ Ε b ib co | _φ õ N Φ 'ω T φ E b LO co | _φ õ N Φ Ω. T φ E b LO co | T φ E o o Ω ^3 Φ CO A += õ Φ N E 2 LO Ω. | _φ Έ φ M— O o o b LO CN | _φ Έ φ M— O E o JD b LO CN | _φ Έ φ M— E CN Ò Ό O LO | Ω. φ E o o Ω M— -1—< LO 2 c\i ° £= 2 =5 CO IZ | Ω. φ E o o Ω M— -1—< lo 15 2 c\i ° £= 2 =5 CO ’iZ | T φ E o o Ω ^3 Φ CO A += õ Φ N E £5 LO Ω. |
| X LU | CN Γγ | CO Γγ | Γγ | ΙΟ Γγ | CD Γγ | r- Γγ | 00 Γγ | σ> Γγ | Ο 00 | 00 | CN 00 | co 00 | 00 | LO 00 | CD 00 | h- 00 | 00 00 | O 00 | O Cp | Cp | CN Cp |
Petição 870180002928, de 12/01/2018, pág. 144/185
140/159
Tabela I Continuação
| Q. cn _o | θ’ Tb co | Ω CO | θ’ Το ΙΟ co | Ω^ fi- | Ω1 00 C4 | Ω1 CM 00 CO | α σ> fi- CO | Ω1 CM | Ω1 fi- co | Ω1 fi- co co | Ω1 fi- co co | Ω1 CM fi- | Ω1 Το CO co | Ω^ ο | Ω1 Το ο | Ω1 Το C\[ | |
| Ό or | _ro Έ φ M— | φ Ε ο ο =3 ω è'E γΛ φ CO μ— | _φ Έ φ Μ— | φ Ε ο ο =3 ω è'E γΛ φ CO μ— | _φ C φ φ Φϊ φ C | _φ Τϋ ω _φ φ Ε -I—< | _Φ Έ φ Μ— | _φ Έ φ Μ— X ο φ Ε 4 | _Φ Έ φ Μ— Ο Ο ο CN | _φ Έ φ Μ— Ο Ο ο 4 | _φ Έ φ Μ— X ο φ Ε CN | _φ Έ φ Μ— X ο φ Ε το 4 <?\ί | _Φ Έ φ Μ— Ο Ο ο το 4 C\í | _φ Έ φ Μ— X ο φ Ε το ιό C4 | _φ C φ φ φϊ φ C | _φ C φ φ φί φ C | _φ C φ φ φί φ C |
| Ό _l | O »Φ O ω σ) | Ο »Φ Ο Φ σ> | Ο »Φ ο φ σι | Ο »Φ Ο Φ σ> | ο ίφ ο φ σι | ο »φ ο φ σ> | Ο »Φ Ο φ σ> | ο »φ ο φ σ> | Ο »Φ Ο Φ σ> | ο ίφ ο φ σ> | Ο »Φ Ο Φ σ> | ο »φ ο φ σ> | ο »φ ο φ σ> | Ο ίφ ο φ σ> | ο ίφ ο φ σι | ο ίφ ο φ σ> | ο ίφ ο φ σ> |
| _l | lu τ ο II Τ ο | ω τ ο II Τ ο | CI τ ο CI τ ο | ω τ ο II Τ ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | CI τ ο CI τ ο | CM Τ ο CM Τ ο | CM Τ ο CM Τ ο |
| or | τ | τ | τ | τ | Τ | Τ | Τ | Τ | Τ | Τ | Τ | Τ | Τ | Τ | τ | τ | τ |
| X | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CM τ ο CM Τ ο | CM τ ο CM Τ ο |
| § | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CI τ ο CI τ ο | CM Τ ο CM Τ ο | CM Τ ο CM Τ ο |
| > | ω | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο |
| Lj | CI τ ο | CI τ ο | CI τ ο | CI τ ο | CI τ ο | CI τ ο | CI τ ο | CI τ ο | CI τ ο | CI τ ο | CI τ ο | CI τ ο | CI τ ο | CI τ ο | CI τ ο | CM Τ ο | CM Τ ο |
| < | τ φ Ε ο ο =3 ^3 Φ CO /- +3 Õ Φ Ν Ε 2 ιό ο. | τ φ Ε ο ο =3 ^3 Φ CO /- +3 Õ Φ Ν Ε 2 ιό ο. | _φ ΙΟ Õ X ο TD Ο Ν C φ _Ω cò | _φ Õ Ν Φ Ω_ Τ φ Ε TD ιό co | _φ Έ φ Μ— Ο ο =3 Μ— +ρ» CO co C4 | τ φ Ε ο ο =3 ^3 Φ cò /- +3 Õ Φ Ν Ε 2 ιό ο. | τ φ Ε ο ο =3 ^3 Φ cò /- +3 Õ Φ Ν Ε 2 ιό ο. | τ φ Ε ο ο =3 ^3 Φ cò /- +3 Õ Φ Ν Ε 2 ιό ο. | τ φ Ε ο ο =3 ^3 Φ cò /- +3 Õ Φ Ν Ε 2 ιό ο. | τ φ Ε ο ο =3 ^3 Φ cò /- +3 Õ Φ Ν Ε 2 ιό ο. | τ φ Ε ο ο =3 ^3 Φ C0 /- += Õ Φ Ν Ε 2 ιό ο. | τ φ Ε ο ο =3 ^3 Φ C0 /- += Õ Φ Ν Ε 2 ιό ο. | τ φ Ε ο ο =3 Φ C0 /- += Õ Φ Ν Ε 2 ιό ο. | τ φ Ε ο ο =3 Φ C0 /- += Õ Φ Ν Ε 2 ιό ο. | _φ Õ Ν Φ '0. Τ Φ ΤΟ ιό co | τ φ Ε ο ο ί*ϊ~ φ Ί—< 1 ύ — Ν φ 2 ιό Õ. | τ φ Ε ο ο ZS ω q_ Τ3 τ- ~ ο -9 Ν ιο 2 co ’ο. |
| X LU | CO σ> | φ σ> | LO σ> | CO σ> | fi- co | 00 σ> | σ> | ο ο | ο | CM Ο | C0 ο | ”3- ο | LO ο | CO ο | fi- co | 00 ο | σ> ο |
Petição 870180002928, de 12/01/2018, pág. 145/185
141/159
Tabela I Continuação
| Q. cn _o | Ω O CO LO | õj LO | Ω 00 fr- io | õj LO LO | Ω CÓ ο Ιθ | θ’ CM | Ω 00 | õj | Ω 00 Ιθ | õj lo | α σ> LO LO | Ω σ> 00 | θ’ σ> σ> | õj h- h- h- | θ’ -Q CM hLO lo lo | θ’ 00 o co | θ’ -Q O 00 T- O |
| Ό or | _ro £Z Φ ω Φϊ ω c | _φ £Ζ φ φ φί φ C | _φ C φ φ φί φ C | _φ c φ φ φί φ C | _φ C φ φ φί φ C | _Φ C Φ Φ Φί Φ C | _φ c Φ Φ φί Φ c | _Φ C Φ Φ Φί Φ C | _φ C φ φ φί φ C | _φ c φ φ φί φ C | _φ C φ φ Φί φ C | _φ C φ φ Φί φ C | _φ C φ φ Φί φ C | _φ Έ Φ M— o o o 4 cm | _φ c Φ Φ ΦΪ Φ C | T | _Φ Έ φ M— _φ Ε CM |
| Ό _l | ο »Φ Ο ω σ) | ο ίφ ο φ σ) | ο ίφ ο φ σ) | ο ίφ ο φ σ> | ο ίφ ο φ σ> | ο ίφ ο φ σι | o ίφ o Φ O) | ο ίφ ο φ σ> | ο ίφ ο φ σ> | ο ίφ ο φ σ> | ο ίφ ο φ σ> | ο ίφ ο φ σ> | ο ίφ ο φ σ> | o ίφ o Φ O) | O ίφ o Φ O) | o ίφ o Φ O) | Ο »Φ Ο Φ Ο) |
| _l | Cl I ο Cl I ο | CI I ο CI I ο | CI I ο CI I ο | CI I ο CI I ο | ο III Ο | ο III Ο | o III O | ο III Ο | ο III Ο | ο III Ο | ο III Ο | CM I Ο CM I ο | ο III Ο | CM T O CM T o | o III O | o III O | CM I Ο CM I ο |
| or | I | I | I | I | I | I | I | I | I | I | I | I | I | T | T | T | I |
| X | CI I ο CI I ο | CI I ο CI I ο | CI I ο CI I ο | CI I ο CI I ο | CI I ο CI I ο | CI I ο CI I ο | CM I o CM I o | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM I ο CM I ο |
| § | CI I ο CI I ο | CI I ο CI I ο | CI I ο CI I ο | CI I ο CI I ο | CI I ο CI I ο | CI I ο CI I ο | CM I o CM I o | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM T o CM T o | CM T o CM T o | CM T o CM T o | CM I ο CM I ο |
| > | ο | ο | ο | ο | ο | ο | o | ο | ο | ο | ο | ο | ο | o | o | o | ο |
| Lj | CI I ο | CI I ο | CI I ο | CI I ο | CI I ο | CI I ο | CM I o | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM T o | CM T o | CM T o | CM I ο |
| < | φ Ε ο ο =3 Μ— Φ^-Ε ιο ηÕ ZS Ν _Ω Φ t '5. Φ 1 Ύ I CO Τ- | φ Ε ο ο =3 Μ— co ηÕ ZS Ν _Ω Φ t Ξ Φ 1 Ύ I ΙΟ Τ- | φ Ο Ο =3 Μ— Φ -1—< C Φ ΖΤΧ Q_ _Φ ιο ηÕ ZS Ν _Ω Φ i δ- Ύ I CO Τ- | φ Ο Ο =3 Μ— Φ -1—< C Φ ΖΤΧ Q_ _Φ CO η- Õ ZS Ν _Ω Φ i δ- Ύ I ΙΟ Τ- | τ φ Ε ο ο ο φ Μ— ~ Ί—< ~ õ -9 Ν ΙΟ Ε co Ω. | _φ Õ Ν Φ Ω. Τ Φ ιό co | T φ E o o ί*ϊ~ Φ Ί—< 1 1 ύ = Ν Φ Ε LO Ω. | τ φ Ε ο ο ZS ω Μ— Τ3 τ- ~ õ -9 Ν ιο Ε co Ω. | φ Ε ο ο =3 Μ— Φ^ ιο ηÕ ZS Ν ^2 Φ t Ξ Φ 1 Ύ I CO Τ- | φ Ε ο ο Μ— co ηÕ ZS Ν ^2 Φ i δ- Ύ I LO Τ- | φ Ο Ο =3 Μ— Φ -1—< C Φ ΖΤΧ Q_ _Φ C0 η- Õ ZS Ν ^2 Φ i δ- Ύ I LO Τ- | Ò ο -Ε · ·-{ lo V χ-U ο Φ Ν = Φ Έ. φ ± ο_^ Ο X-U cò Ε | Ò ο -Ε · ·-{ lo V χ-U ο Φ Ν = Φ Ξ φ ± ο_^ ο cò Ε | T φ E o o =3 ^3 Φ co / += Õ Φ N Ε E lÒ q. | _φ Έ φ M— O E o JD lÒ cm | _φ Έ φ M— O o o lÒ cm | τ φ Ε ο ο =3 Φ C0 / += Õ Φ Ν Ε Ε ιό ο. |
| X LU | ο | - | CM | C0 | LO | CO | υ- | 00 | σ> | ο CM | CM | CM CM | co CM | CM | LO CM | CO CM |
Petição 870180002928, de 12/01/2018, pág. 146/185
142/159
Tabela I Continuação
| Q. cn _o | O O CO CO | 5,01LDJ | Q Tb o | Q CD h- LO | |||||||||||
| Ό az | 2-bromofenila | 2,6-difluorofenila | quinolin-8-ila | 3-metilapiridin-2-ila | 3,5-dimetilaisoxazol- 4-ila | ciclo-hexila | 1,2,3,4-tetra-hidro- naftalen-1-ila | 2-metilafenila | 2-bromofenila | 2,6-difluorofenila | quinolin-8-ila | 3-metilapiridin-2-ila | 3,5-dimetilaisoxazol- 4-ila | ciclo-hexila | 1,2,3,4-tetra-hidro- naftalen-1-ila |
| Ό _l | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) |
| _l | CM I o CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o |
| az | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I |
| X | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o |
| § | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o |
| > | o | o | o | o | o | o | o | o | o | o | o | o | o | o | o |
| Lj | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o |
| < | 5-meti l-3-(trifl uorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifluorometil)-1 Hpirazol-1-ila | 3,5-bis(trifl uorometil )-1 Hpirazol-1-ila | 3,5-bis(trifl uorometil )-1 Hpirazol-1-ila | 3,5-bis(trifl uorometil )-1 Hpirazol-1-ila | 3,5-bis(trifl uorometil )-1 Hpirazol-1-ila | 3,5-bis(trifl uorometil )-1 Hpirazol-1-ila | 3,5-bis(trifl uorometil )-1 Hpirazol-1-ila | 3,5-bis(trifl uorometil )-1 Hpirazol-1-ila | 3,5-bis(trifl uorometil )-1 Hpirazol-1-ila |
| X LU | h- CM | 00 CM | O CM | O co | CO | CM CO | CO co | co | LO CO | CD CO | h- co | 00 co | O co | O 3- | 5 |
Petição 870180002928, de 12/01/2018, pág. 147/185
143/159
Tabela I Continuação
| Q. cn _o | Q h- 00 | Q 00 h- | θ’ h- hh- CD | θ’ Tb oo LD ”3- | ||||||||||||||||
| Ό or | 2-metilafenila | 2-bromofenila | 2,6-difluorofenila | quinolin-8-ila | 3-metilapiridin-2-ila | 3,5-dimetilaisoxazol-4-ila | ciclo-hexila | 1,2,3,4-tetra-hidro-naftalen- 1-ila | _ro Έ φ M— _ÇD φ E CN | 2-bromofenila | 2,6-difluorofenila | quinolin-8-ila | 3-metilapiridin-2-ila | 3,5-dimetilaisoxazol-4-ila | ciclo-hexila | 1,2,3,4-tetra-hidro-naftalen- 1-ila | 2-metilafenila | _çp Έ φ M— O E o _Q CN | 2,6-difluorofenila | quinolin-8-ila |
| Ό _l | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) | O O ω cn | O O ω cn | O O ω cn | O O ω cn | O O ω cn | O O ω cn | O O ω cn | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) | O O ω σ) |
| _l | CM I o CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | CM T O CM T o | CM T O CM T o |
| or | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I | T | T |
| X | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM T o CM T o | CM T o CM T o |
| § | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM T o CM T o | CM T o CM T o |
| > | o | o | o | o | o | o | o | o | o | o | o | o | o | o | o | o | o | o | o | o |
| Lj | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM T o | CM T o |
| < | 3,5-bis(difl uorometil )-1 Hpirazol-1-ila | 3,5-bis(difl uorometil )-1 Hpirazol-1-ila | 3,5-bis(difl uorometil )-1 Hpirazol-1-ila | 3,5-bis(difl uorometil )-1 Hpirazol-1-ila | 3,5-bis(difl uorometil )-1 Hpirazol-1-ila | 3,5-bis(difl uorometil )-1 Hpirazol-1-ila | 3,5-bis(difl uorometil )-1 Hpirazol-1-ila | 3,5-bis(difl uorometil )-1 Hpirazol-1-ila | 2,5-diclorofenila | 2,5-diclorofenila | 2,5-diclorofenila | 2,5-diclorofenila | 2,5-diclorofenila | 2,5-diclorofenila | 2,5-diclorofenila | 2,5-diclorofenila | 2,5-dimetilfenila | 2,5-dimetilfenila | 2,5-dimetilfenila | 2,5-dimetilfenila |
| X LU | CM 3- | CO 3- | 3- | LO 3- | CD 3- | h- 3- | 00 3- | O 3- | O LD | LD | CM LD | CO LD | LD | LD LD | CD LD | h- LD | 00 LD | O LD | O CD | δ |
Petição 870180002928, de 12/01/2018, pág. 148/185
144/159
Tabela I Continuação
| Q. o _o | Ω CO CN 4 | ΦΞ1 σ> CO 4 4 | ΦΞ1 Ο τΟ CN co 4 | ΦΞ1 σ> rο ο 4“ ld | ΦΞ1 CN Ο Ο τ- 4 4 | Ω CÓ ο 4 | θ’ Ο Ο 4 | θ’ 00 00 4 | |||||||||
| Ό or | _ro CN c õ. _ro φ E cò | O N (D X o ω E Υ ω LD ~ CO 4 | _φ X Φ _£= ò o Ό | Ò Ό lc (D — Ί—' Jφ V Ύ c 3- φ co ω ri Is T- C | _φ Έ φ M— _φ φ Ε CN | _φ Έ φ Μ— Ο Ε ο CN | _Φ Έ φ Μ— Ο Ο =3 ώ CN | _Φ 00 C Õ C 4 σ- | _φ CN C Ja Ω_ _φ φ Ε cò | Ο Ν Φ X Ο ω φ Ε ? φ LO ~ co 4 | _φ X φ Ò ο Ό | Ò TD lc Λ Φ Φ — Ί—' _1- φ V Ύ c 3- φ co Φ rils Τ- C | _φ Έ φ Μ— _φ Ε CN | _φ Έ φ Μ— Ο Ε ο CN | _φ Έ φ Μ— Ο ο =3 CD CN | _Φ 00 C Õ C 4 σ- | _Φ CN c Ja Ω_ _φ φ Ε cò |
| Ό _l | o »Φ O ω o | O »Φ O ω σ) | o »Φ o ω o | O »Φ O ω σ) | O »Φ O ω σ) | Ο »Φ Ο Φ σ> | ο ίφ ο φ ο | ο »φ ο φ ο | ο ίφ ο φ ο | ο ίφ ο φ ο | ο »φ ο φ ο | Ο »Φ Ο Φ ο | Ο »Φ Ο Φ ο | Ο »Φ Ο Φ ο | Ο »Φ Ο Φ ο | ο »φ ο φ ο | ο ίφ ο φ ο |
| _l | CM I o CM I o | CM I O CM I o | CM I O CM I o | CM I O CM I o | φ Ό ω ΰ -2 ω Êri ω I 2 Ο Φ 4 Ε I <ο Ο .<£ | φ Ό ω ΰ -2 ω Êri ω I 2 Ο Φ 4 Ε I <ο Ο .<£ | φ Ό ω ϋ .2 ω Êri ω I 2 Ο Φ 4 Ε I <ο Ο .<£ | φ Ό ω ΰ .2 ω Êri ω I 2 Ο Φ 4 Ε I <ο Ο .<£ | φ Ό ω ΰ .2 ω - Êri ω I 2 Ο Φ 4 Ε I <ο Ο .<£ | φ Ό ω ΰ .2 ω - Êri ω I 2 Ο Φ 4 Ε I <ο Ο .<£ | φ Ό ω ΰ .2 ω - Êri ω I 2 Ο Φ 4 Ε I <ο Ο | φ Ό ω ΰ .2 ω - Êri ω I 2 Ο Φ 4 Ε I <ο Ο .<£ | φ Ό ω ΰ .2 ω - Êri ω I 2 Ο Φ 4 Ε I <ο Ο .<£ | φ Ό ω ΰ .2 ω - Êri ω I 2 Ο Φ 4 Ε I <ο Ο .<£ | φ Ό ω ΰ .2 ω - Êri ω I 2 Ο Φ 4 Ε I <ο Ο .<£ | φ Ό ω ΰ .2 ω - Êri ω I 2 Ο Φ 4 Ε I <ο Ο .<£ | φ Ό ω SÜ .2 ω Êri ω I 2 Ο Φ 4 Ε I <ο Ο .<£ |
| or | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I |
| X | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο |
| § | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο |
| > | o | o | o | o | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο |
| Lj | CM I o | CM I o | CM I o | CM I o | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο |
| < | _φ Έ φ M— E LO CN | _φ Έ φ M— E LO CN | _φ Έ φ M— E LO CN | _φ Έ φ M— E LO CN | τ φ Ε ο ο =3 Φ CO 4 +3 Õ Φ Ν Ε 2 LO Ο. | τ φ Ε ο ο =3 Φ CO 4 +3 Õ Φ Ν Ε 2 LO Ο. | τ φ Ε ο ο =3 Φ CO 4 +3 Õ Φ Ν Ε 2 LO Ο. | τ φ Ε ο ο =3 Φ C0 4 +3 Õ Φ Ν Ε 2 LO Ο. | τ φ Ε ο ο =3 Φ C0 4 += Õ Φ Ν Ε 2 LD Ο. | τ φ Ε ο ο =3 Φ C0 4 += Õ Φ Ν Ε 2 LD Ο. | τ φ Ε ο ο =3 Φ C0 4 += Õ Φ Ν Ε 2 LD Ο. | τ φ Ε ο ο =3 Φ C0 4 += Õ Φ Ν Ε 2 LD Ο. | τ φ Ε ο ο φ Μ— ~ Ί—< Τ“ ~ ο -9 Ν LD 2 co ’ο. | τ φ Ε ο ο φ Μ— ~ Ί—< Τ“ ~ ο -9 Ν LD 2 co ’ο. | τ φ Ε ο ο φ Μ— ~ Ί—< Τ“ ~ ο -9 Ν LD 2 co ’ο. | τ φ Ε ο ο φ Μ— ~ Ί—< Τ“ ~ ο -9 Ν LD 2 co ’ο. | τ φ Ε ο ο φ Μ— ~ Ί—< Τ“ ~ ο -9 Ν LD 2 co ’ο. |
| X LU | CN CD | CO CD | CD | LD CD | CD CD | h- CD | 00 CD | σ> CD | Ο h- | h- | CN h- | C0 h- | ”3- h- | LD h- | CD h- | h- h- | 00 h- |
Petição 870180002928, de 12/01/2018, pág. 149/185
145/159
Tabela I Continuação
| Q. cn _o | ΦΞ1 σ> οο LO co LO LO | ΦΞ1 O 00 CO h- LO LO | ΦΞ1 lo σ> C\[ CN | ΦΞ1 ”3- LO h- O CO ’ςΤ | ΦΞ1 σ> lo h- 00 | ΦΞ1 τ- h00 O | ||||||||||
| Ό OL | 3,5-dimetilaisoxazol- 4-ila | ciclo-hexila | 1,2,3,4-tetra-hidronaftalen-1-ila | 2-metilafenila | 2-bromofenila | 2,6-difluorofenila | quinolin-8-ila | 3-metilapiridin-2-ila | 3,5-dimetilaisoxazol- 4-ila | ciclo-hexila | 1,2,3,4-tetra-hidro- naftalen-1-ila | 2-metilafenila | 2-bromofenila | 2,6-difluorofenila | quinolin-8-ila | 3-metilapiridin-2-ila |
| Ό _l | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação |
| _l | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) |
| N OL | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I |
| X | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o |
| § | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o |
| > | o | o | o | o | o | o | o | o | o | o | o | o | o | o | o | o |
| Lj | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o |
| < | 3,5-bis(trifl uorometil )-1 Hpirazol-1-ila | 3,5-bis(trifl uorometil )-1 Hpirazol-1-ila | 3,5-bis(trifl uorometil )-1 Hpirazol-1-ila | 3,5-bis(difl uorometil )-1 Hpirazol-1-ila | 3,5-bis(difl uorometil )-1 Hpirazol-1-ila | 3,5-bis(difl uorometil )-1 Hpirazol-1-ila | 3,5-bis(difl uorometil )-1 Hpirazol-1-ila | 3,5-bis(difl uorometil )-1 Hpirazol-1-ila | 3,5-bis(difl uorometil )-1 Hpirazol-1-ila | 3,5-bis(difl uorometil )-1 Hpirazol-1-ila | 3,5-bis(difl uorometil )-1 Hpirazol-1-ila | 2,5-diclorofenila | 2,5-diclorofenila | 2,5-diclorofenila | 2,5-diclorofenila | 2,5-diclorofenila |
| X LU | 1-179 | O 00 | 00 | 1-182 | 1-183 | co | 1-185 | 1-186 | 1-187 | 00 00 | 1-189 | 1-190 | 1-191 | 1-192 | 1-193 | 1-194 |
Petição 870180002928, de 12/01/2018, pág. 150/185
146/159
Tabela I Continuação
| Q. cn _o | Ο -Q LO LO | Ο -Q O) CD | Ο -Q CD CO 00 00 co~ co~ | ||||||||||||
| Ό az | 3,5-dimetilaisoxazol- 4-ila | ciclo-hexila | 1,2,3,4-tetrahidronaftalen-1 -ila | 2-metilafenila | 2-bromofenila | 2,6-difluorofenila | quinolin-8-ila | 3-metilapiridin-2-ila | 3,5-dimetilaisoxazol- 4-ila | ciclo-hexila | 1,2,3,4-tetra-hidro- naftalen-1-ila | 2-metilafenila | 2-bromofenila | 2,6-difluorofenila | quinolin-8-ila |
| Ό _l | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação | ligação |
| _l | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | CH=CH mistura de isômeros (Z) e (E)) | O III O | O III O | O III O | O III O |
| az | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I |
| X | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o |
| § | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o | CM I o CM I o |
| > | o | o | o | o | o | o | o | o | o | o | o | o | o | o | o |
| Lj | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o | CM I o |
| < | 2,5-diclorofenila | 2,5-diclorofenila | 2,5-diclorofenila | 2,5-dimetilfenila | 2,5-dimetilfenila | 2,5-dimetilfenila | 2,5-dimetilfenila | 2,5-dimetilfenila | 2,5-dimetilfenila | 2,5-dimetilfenila | 2,5-dimetilfenila | 5-meti l-3-(trifl uorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifl uorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifl uorometil)-1 Hpirazol-1-ila | 5-meti l-3-(trifl uorometil)-1 Hpirazol-1-ila |
| X LU | LO O | CD O | h- σ> | 00 o | O o | O o CM | O CM | CM O CM | CO o CM | A- o CM | LO O CM | CD O CM | h- o CM | 00 o CM | O o CM |
Petição 870180002928, de 12/01/2018, pág. 151/185
147/159
Tabela I Continuação
| Q. cn _o | Ο -Q Tb CM O hcm cm | Ω CO h- | Ω^ h- | Ω^ | Ω1 h- C0 co | θ’ -Ω cm σ> ο σ> co | 3ο ο | CO£m h- hco co | θ’ -Ω TÒ οο 00 CD cm cm | Ω1 σ> ο co | Ω^ σ> | Ω^ σ> | Ω1 CM LO | |||||
| Ό or | _φ CM c b õ_ _ro φ E cò | _Φ Õ Ν Φ X ο ω φ Ε b LO CO | _Φ Έ φ Μ— _φ Ε CM | _φ Έ φ Μ— ο Ε ο CM | _φ Έ φ Μ— Ο Ο =3 b ώ cm | _Φ 00 C Õ C b σ- | _φ CM C b Ω_ _φ φ Ε cò | _Φ Õ Ν Φ X ο ω φ Ε b LO co | _φ Έ φ Μ— _φ Ε CM | _φ Έ φ Μ— Ο Ε ο CM | _φ Έ φ Μ— ο ο =3 b ώ cm | _Φ 00 C Õ C b σ- | _φ CM c Ja Ω_ _φ φ Ε cò | _φ Õ Ν φ X ο ω φ Ε b LO co | _φ Έ φ Μ— _φ Ε CM | _φ Έ φ Μ— Ο Ε ο CM | _Φ Έ φ M— O O =3 b ώ cm | _Φ oò c õ c b CJ |
| Ό _l | o »Φ O ω cn | Ο »Φ Ο φ cn | Ο »Φ Ο Φ cn | Ο »Φ Ο Φ cn | ο »φ ο φ cn | ο »φ ο φ cn | ο ίφ ο φ cn | ο ίφ ο φ cn | Ο »Φ Ο Φ cn | Ο »Φ Ο Φ σ> | ο »φ ο φ σ> | ο »φ ο φ | ο ίφ ο φ | ο ίφ ο φ | Ο »Φ Ο Φ | Ο »Φ Ο Φ cn | o »φ o φ cn | o ίφ o Φ cn |
| _l | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | ο III Ο | o III O | o III O |
| or | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I | I | T | T |
| X | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM T o CM T o | CM T o CM T o |
| § | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM T o CM T o | CM T o CM T o |
| > | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο | ο | o | o |
| Lj | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM T o | CM T o |
| < | τ φ Ε ο ο =3 Φ CO / +3 Õ Φ Ν Ε 2 LD Q. | τ φ Ε ο ο =3 Φ CO / +3 Õ Φ Ν Ε 2 LO Q. | τ φ Ε ο ο =5 φ Μ— ~ Ί—< ~ õ -9 Ν ΙΟ Ε co ο. | τ φ Ε ο ο =5 φ Μ— ~ Ί—< ~ õ -9 Ν ΙΟ Ε co ο. | τ φ Ε ο ο =5 φ Μ— ~ Ί—< ~ õ -9 Ν ΙΟ Ε CO Ω. | τ φ Ε ο ο =5 φ Μ— ~ Ί—< ~ õ -9 Ν ΙΟ Ε CO Ω. | τ φ Ε ο ο Ω φ Μ— ~ Ί—< ~ õ -9 Ν ΙΟ Ε co Ω. | τ φ Ε ο ο Ω φ Μ— ~ Ί—< ~ õ -9 Ν ΙΟ Ε co Ω. | τ φ Ε ο ο ZS ω q_ Τ3 τ- ~ ο -9 Ν LO Ε co Q. | τ φ Ε ο ο ZS ω q_ Τ3 τ- ~ ο -9 Ν LO Ε co Q. | τ φ Ε ο ο ZS ω q_ Τ3 τ- ~ ο -9 Ν LO Ε co Q. | τ φ Ε ο ο ZS ω q_ Τ3 τ- ~ ο -9 Ν LO Ε co Q. | τ φ Ε ο ο ZS ω q_ Τ3 τ- ~ ο -9 Ν LO Ε co Q. | τ φ Ε ο ο ZS ω q_ Τ3 τ- ~ ο -9 Ν LO Ε co Q. | _φ Έ φ Μ— Ο ο ο b LO cm | _φ Έ φ Μ— Ο ο ο b LO cm | _φ Έ φ M— O o o b LO cm | _φ Έ φ M— O o o b LO cm |
| X LU | ο CM | CM | CM CM | CO CM | CM | LO CM | CD CM | h- CM | 00 CM | σ> CM | Ο CM CM | CM CM | CM CM CM | C0 CM CM | CM CM | LO CM CM | CD CM CM | h- CM CM |
Petição 870180002928, de 12/01/2018, pág. 152/185
148/159
Tabela I Continuação
| Q. σι _o | ο -O Tb lo LO co co co | Ω Tb 00 co | Ω Tb ri- 00 ri- | Ω ri- ri- cò | θ’ Tb co CD co | θ’ ri- co co ri- co | Ω1 Tb cm | Ω1 Το 00 Το ο | α_ LO σ> cmJJ Ή co σ> cm | Ω1 Tb cm | Ω1 CD Ο LO Φ LO 00 | Ω1 Το C0 φ ο ο | Ω1 00 3- | ||
| Ό CL | _ro CM c Ja ã_ _ro φ E cò | õ N ω X o ω Tp φ E ? ω LO ~ co 4 | _çp Έ φ M— _çp φ Ε CM | _çp Έ φ Μ— Ο Ε ο _Ω CM | _φ Έ φ M— O o σ σ ώ cm | _φ oò c õ c ’σ σ | _φ CM c Ja õ. _φ φ Ε cò | 4 õ N Φ X o ω Jçp E σ LQ zr, - Φ co — | _φ CM c Ja ã_ _φ φ Ε cò | _φ Έ φ Μ— _φ φ Ε CM | I | I | _φ Έ φ Μ— ο ο σ Μ— ώ ό ο ο CM | _φ Έ φ Μ— ο ο σ Μ— ώ ό ο ο CM | _φ Έ φ Μ— Ο ο σ Μ— ώ ό ο ο CM |
| Ό _l | o »Φ O ω O) | o »Φ O ω O) | Ο »φ ο ω σι | Ο »Φ Ο Φ σι | o »φ o φ σι | ο »φ ο φ σι | ο ίφ ο φ σι | o »φ o φ σ) | ο ίφ ο φ σ) | ο ίφ ο φ σι | ο ίφ ο φ σι | ο ίφ ο φ σ) | ο ίφ ο φ σ) | ο ίφ ο φ σ) | ο ίφ ο φ σ) |
| _l | o III O | o III O | ο III Ο | ο III Ο | o III O | ο III Ο | ο III Ο | o III O | Ν I Ο II I ο | Ν I Ο II I ο | ο III Ο | ο III Ο | φ Ό LU φ - φ « Ν Ε ω ι 2 Ο φ 4 Ε I ·Ο Ο | φ Ό LU φ - φ « Ν ι 2 Ο φ 4 Ε I ·Ο Ο | φ Ό LU φ - φ « Ν Ε ω ι 2 Ο φ 4 Ε I ·Ο Ο |
| N CL | I | I | I | I | I | I | I | T | I | I | I | I | I | I | I |
| X | CM I o CM I o | CM I o CM I o | CM I ο CM I ο | CM I ο CM I ο | CM I o CM I o | CM I ο CM I ο | CM I ο CM I ο | CM T o CM T o | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο |
| § | CM I o CM I o | CM I o CM I o | CM I ο CM I ο | CM I ο CM I ο | CM I o CM I o | CM I ο CM I ο | CM I ο CM I ο | CM T o CM T o | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο | CM I ο CM I ο |
| > | o | o | ο | ο | o | ο | ο | o | ο | ο | ο | ο | ο | ο | ο |
| Lj | CM I o | CM I o | CM I ο | CM I ο | CM I o | CM I ο | CM I ο | CM T o | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο | CM I ο |
| < | _φ Έ φ M— O o o σ LO CM~ | _çp Έ φ M— O o o σ LO cm | _φ Έ φ Μ— Ε σ ιό cm | _φ Έ φ Μ— Ε σ ιό cm | _φ Έ φ M— E σ ιό cm | _φ Έ φ Μ— Ε σ ιό cm | _φ Έ φ Μ— Ε σ ιό cm | _φ Έ φ M— E σ ιό cm | τ φ Ε ο ο φ Μ— ~ -1—< ~ ο -9 Ν lo Ε co ’ο. | Έ φ Μ— Ε σ ιό cm | _φ Έ φ Μ— Ε σ ιό cm | τ φ Ε ο ο σ φ q_ σ τ- ~ ο -9 Ν lo Ε co ο. | τ φ Ε ο ο φ Μ— ~ -1—< ~ ο -9 Ν lo Ε co ’ο. | τ φ Ε ο ο σ φ q_ σ τ- ~ ο -9 Ν lo Ε co ο. | τ φ Ε ο ο σ Φ C0 4 += Õ Φ Ν Ε Ε ιό ο. |
| X LU | 00 CM CM | o CM CM | ο C0 CM | co CM | cm co CM | co co CM | C0 CM | LO co CM | CO C0 CM | ri- CO CM | 00 co CM | σ> C0 CM | ο 3- CM | 4 CM | CM 3- CM |
M— s_
CD
O ro
E o
ΙΟ
O _i
Q_
I
ΙΟ
Q.
<
>
O
X (D c
<
cõ σ5 rO
LU
LU >
(D s_
T3
E o
o
Ό
ΙΟ o
<D
Ό «
O
Ό c
(D
H—· <15
Ό
E
ΙΟ
M—
CL
CD
O «
(D
ΙΟ >
«
O o
« o
=3 cr
O
O
O
X 'ro .Ω «
o
T3
O
O
E «
o (D «
O
Ό
C
N «
ΙΟ >
(D
ΙΟ «
M— (D
T3 «
C _g o
E (D
C (D
Q.
E (D «
(D
O
O
-t—» < (D T3 05 g '=3 cr «
O
M—
O g
Ό '05 x?
ox
O <D
T3 «
<D >
-O
E «
(D «
M— «
<D «
O
Ό
C
N
CO Csi
I Q.
E =3 05
O g
O
X 'ro
M—
C
Η—* <D
O >05
O g
E
ΙΟ
H—» (D
T3 e acetonitrila; gradiente linear a partir 10% acetonitrila a 95% acetonitrila.
[b] A determinação LC-MS na faixa acídica foi feita com pH 2,7 utilizando-se as fases móveis de 0,1% ácido fórmico
Petição 870180002928, de 12/01/2018, pág. 153/185
149/159 aquoso e acetonitrila (contém 0,1% de ácido fórmico); gradiente linear de 10% acetonitrila a 95% acetonitrila [c] A determinação LC-MS na faixa neutral foi feita com pH 7,8 utilizando-se as fases móveis 0,001 de solução de bi05
C
O (D
O χΡ cr
LO
CD
C
O
H—' (D
O χΡ cr
O (D
T3 s_ <D
C (D c
<d
T3 s_
CD
Ò3
C
O
H—' (D
O <D s_ ro o
o c
<o
E <D
T3
O
C
O _Q s_
O o
_Q s_
O (D
T3 «
O '05 CO
CO
E 05 c (D « (D ιΩ.
<D =3 σ «
T3 05 .2 05
E
ΙΟ >05
C «
C
O
CN £Z
O <D «
O
T3 c
N
H—* <D
O i05
O
O
CD bO
O (D «
O
T3
C
N
O >05
O c
(D (D
ΙΟ
T3 «
O
T3
O
ΙΟ
Q.
«
O
T3 «
>
CL
CD
O «
(D >
«
O
T3
O
105
O
C (D (D «
O
Ό (D
ΧΣ
C
O o
CL
CD
O «
(D >
E o
« >
« (D
O =3 «
«
C
O c
O «
=3
T3 (D s_ c
(D s_ <D
C
O
105
O ro o
Q.
ΙΟ «
O (D «
O
T3
C
N «
o o
M— '05 s_
CD
O
E o
ιΟ «
C «
O
T3
O
E x
'05
E ω
>
o c
« o
T3 c
(D (D
T3
E
T3 _Q
E ro x
E «
(D >
«
O
CN
CD bO
O
É c
o o
Ν’
E c
o o
CN <D
T3 >
=) «
O s_ o
(D
Q.
« (D
Petição 870180002928, de 12/01/2018, pág. 154/185
150/159
Dados RMN de exemplos selecionados
| Ex | Dados RMN |
| 1-1 | 1HRMN δ = 7,46 (m, 2H), 7,31-7,18 (m, 4H), 6,62 (d, 1H), 6,57 (d, 1H), 6,44 (s, 1H), 5,19 (bs, 2H), 4,20 (bs, 1H), 3,90 (bs, 1H), 3,26 (m, 2H), 2,90 (m, 1H), 2,21 (s, 3H), 2,05(m, 2H), 1,80-1,50 (m, 2H) ppm |
| I-2 | 1HRMN δ = 7,95-7,92 (m, 2H), 7,87-7,84 (m, 1H), 7,52-7,43 (m, 4H), 7,11 (d, 1H), 6,93 (d, 1H), 6,88 (s, 1H), 6,45 (s, 1H), 5,14 (s, 2H), 4,05 (bs, 1H), 3,74 (bs, 1H), 3,20-3,05 (m, 2H), 2,88 (bs, 1H), 2,24 (s, 3H), 1,901,78 (bs, 2H), 1,50 (bs, 1H), 1,35 (bs, 1H) ppm |
| I-3 | 1HRMN δ = 7,32 (s, 1H), 7,29-7,22 (m, 4H), 7,15 (m, 1H), 6,44 (s, 1H), 6,35 (d, 1H), 5,60 (m, 1H), 5,20 (bs, 2H), 4,30 (bs, 1H), 3,98 (bs, 1H), 3,38-3,25 (m, 2H), 3,05-2,84 (m, 4H), 2,22 (s, 3H), 2,17-2,05 (m, 2H), 1,85-1,56 (m, 2H), 1,26 (d, 3H) ppm |
| I-26 | 1HRMN δ = 7,56 (d, 2H), 7,50 (s, 1H), 7,39-7,34 (m, 3H), 7,28-7,18 (m, 2H), 6,45 (s, 1H), 5,23 (bs, 2H), 4,37 (bs, 1H), 4,01 (bs, 1H), 3,35 (m, 1H), 3,32 (bs, 1H), 2,90 (bs, 1H), 2,23 (s, 3H), 2,18-2,10 (m, 2H), 1,80 (bs, 1H), 1,63 (bs, 1H) ppm |
| I-27 | 1HRMN δ = 8,23 (d, 1H), 8,16 (d, 1H), 7,95 (d, 1H), 7,88 (d, 1H), 7,83 (d, 1H), 7,64 (s, 1H), 7,63-7,51 (m, 3H), 7,27 (d, 1H), 6,46 (s, 1H), 5,24 (bs, 2H), 4,38 (bs, 1H), 4,03 (bs, 1H), 3,40 (m, 1H), 3,32 (bs, 1H), 2,94 (bs, 1H), 2,24 (s, 3H), 2,23-2,12 (m, 2H), 1,85 (bs, 1H), 1,70 (bs, 1H) ppm |
| I-50 | 1HRMN (CD3CN) δ = 8,39 (d, 1H), 7,96 (d, 2H), 7,80 (d, 1H), 7,72 (s, 1H), 7,67-7,50 (m, 3H), 6,37 (s, 1H), 5,05 (s, 2H), 4,45 (bs, 1H), 3,98 (bs, 1H), 3,40-3,20 (m, 2H), 2,93 (bs, 1H), 2,25 (s, 3H), 2,25-2,15 (m, 2H), 1,901,75 (m, 2H) ppm |
| 1-51 | 1HRMN (CD3CN) δ = 8,74 (dd, 1H), 8,59 (dd, 1H), 7,99 (s, 1H), 7,96 (m, 1H), 7,45 (dd, 1H), 6,45 (s, 1H), 5,22 (bs, 2H), 4,35 (bs, 1H), 4,00 (bs, 1H), 3,40-3,20 (m, 3H), 2,22 (s, 3H), 2,17-2,10 (m, 2H), 1,90-1,55 (m, 2H) PPm |
| I-52 | 1HRMN (CD3CN) δ = 7,46 (s, 1H), 7,42-7,34 (m, 4H), 7,30-7,25 (m, 1H), 6,39 (s, 1H), 5,09 (d, 1H), 5,02 (d, 1H), 4,45 (d, 1H), 3,91 (d, 1H), 3,84 (s, 2H), 3,25 (m, 2H), 2,82 (t, 1H), 2,23 (s, 3H), 2,18-2,05 (m, 2H), 1,82 (qd, 1H), 1,66 (qd, 1H) ppm |
| I-53 | 1HRMN δ = 7,28-7,26 (m, 2H), 7,22-7,21 (m, 2H), 7,19-7,15 (m, 2H), 6,51 (s, 1H), 5,33 (d, 1H), 5,25 (d, 1H), 4,36 (d, 1H), 3,95 (d, 1H), 3,35-3,20 (m, 2H), 2,96 (s, 4H), 2,82 (t, 1H), 2,21 (s, 3H), 2,09 (d, 1H), 2,07 (d, 1H), 1,78 (m, 1H), 1,53 (m, 1H) ppm |
| I-54 | 1HRMN δ = 7,26-7,13 (m, 5H), 7,06 (s, 1H), 5,77 (s, 1H), 4,91 (bs, 2H), 4,28 (m, 1H), 4,03 (m, 1H), 3,25 (m, 1H), 3,16 (m, 1H), 2,97 (m, 4H), 2,85 (m, 1H), 2,11 (s, 3H), 2,10-1,97 (m+s, 5H), 1,61 (m, 2H) ppm |
| I-55 | 1HRMN δ = 7,85 (d, 1H), 7,26-7,13 (m, 5H), 7,06 (s, 1H), 6,66 (d, 1H), 5,27 (bs, 2H), 4,30 (bs, 1H), 3,95 (bs, 1H), 3,26 (m, 1H), 3,20-2,80 (m+s, 6H), 2,07 (m, 2H), 1,80-1,50 (m, 2H) ppm |
| I-57 | 1HRMN δ= 7,34-7,12 (m, 9H), 7,04 (s, 1H), 4,38 (bs, 1H), 4,00 (bs, 1H), 3,75 (s, 2H), 3,27-2,98 (m, 2H), 2,96 (m, 4H), 2,80 (bs, 1H), 2,02 (m, 2H), 1,51 (m, 2H) ppm |
| I-58 | 1HRMN δ= 7,27-7,21 (m, 2H), 7,20-7,14 (m, 3H), 7,05 (s, 1H), 4,37 (bs, 1H), 3,95 (bs, 1H), 3,26-3,18 (m, 2H), 2,96 (s, 4H), 2,80 (bs, 1H), 2,33 (t, 2H), 2,04 (d, 2H), 1,55 (bs, 2H), 1,50 (tt, 2H), 1,33 (tq, 2H), 0,90 (t, 3H) PPm |
Petição 870180002928, de 12/01/2018, pág. 155/185
151/159
| Ex | Dados RMN |
| 1-59 | 1HRMN δ = 7,47 (s, 1H), 7,26-7,13 (m, 5H), 7,07 (s, 1H), 5,46 (m, 2H), 4,27 (bs, 1H), 3,93 (bs, 1H), 3,30 (m, 1H), 3,20-2,85 (m+s, 6H), 2,05 (m, 2H), 1,79 (bs, 1H), 1,57 (bs, 1H) ppm |
| 1-60 | 1HRMN δ = 7,26-7,13 (m, 5H), 7,07 (s, 1H), 5,29 (bs, 2H), 4,30 (bs, 1H), 3,92 (bs, 1H), 3,28 (m, 1H), 3,20 (m, 1H), 3,00-2,80 (m, 5H), 2,20 (s, 3H), 2,07 (m, 2H), 1,80 (bs, 1H), 1,60 (bs, 1H) ppm |
| 1-61 | 1HRMN δ = 8,07-7,90 (m, 3H), 7,26-7,21 (m, 2H), 7,20-7,14 (m, 3H), 7,08 (s, 1H), 4,50 (d, 1H), 3,35-3,23 (m, 4H), 2,97 (s, 4H), 2,22-2,10 (m, 1H), 2,00-1,87 (m, 2H), 1,87-1,45 (m, 2H) ppm |
| I-63 | 1HRMN δ = 7,44-7,43 (m, 1H), 7,28-7,12 (m, 6H), 7,05 (s, 1H), 6,99 (d, 1H), 4,38 (bs, 1H), 3,99 (bs, 1H), 3,72 (s, 2H), 3,22-3,15 (m, 2H), 2,96 (s, 4H), 2,81 (bs, 1H), 2,00 (d, 2H), 1,52 (m, 2H) ppm |
| I-64 | 1HRMN δ = 7,26-7,21 (m, 2H), 7,20-7,13 (m, 3H), 7,06 (s, 1H), 5,70 (m, 1H), 4,30 (bs, 1H), 4,00 (bs, 1H), 3,30-3,19 (m, 2H), 2,96 (s, 5H), 2,26 (d, 3H), 2,08-1,96 (m, 2H), 1,64-1,54 (m, 5H) ppm |
| I-65 | 1HRMN δ = 7,40 (s, 1H), 7,26-7,15 (m, 5H), 7,06 (s, 1H), 4,35 (bs, 1H), 4,05 (bs, 1H), 3,76 (s, 3H), 3,49 (s, 2H), 3,30-3,19 (m, 2H), 2,99 (s, 4H), 2,82 (bs, 1H), 2,08-2,00 (m, 2H), 1,58 (bs, 2H) ppm |
| I-66 | 1HRMN δ = 7,26-7,21 (m, 2H), 7,20-7,12 (m, 3H), 7,05 (s, 1H), 6,85-6,80 (m, 3H), 6,75-6,71 (dd, 1H), 3,93 (bs, 1H), 3,74 (s, 3H), 3,69 (s, 3H), 3,20 (m, 1H), 2,96 (s, 4H), 2,80-2,74 (m, 2H), 2,65-2,55 (bs, 2H), 2,04-1,97 (m, 2H), 1,58-1,42 (m, 2H), 1,28 (t, 2H) ppm |
| I-67 | 1HRMN δ = 7,71-7,58 (m, 3H), 7,27-7,12 (m, 5H), 7,07 (s, 1H), 4,37 (bs, 1H), 4,05 (bs, 1H), 3,97 (s, 2H), 3,35-3,23 (m, 2H), 2,97 (s, 4H), 2,88 (bs, 1H), 2,07 (d, 2H), 1,65 (bs, 2H) ppm |
| I-68 | 1HRMN δ = 7,99 (d, 1H), 7,26-7,12 (m, 5H), 7,05 (s, 1H), 6,69 (d, 1H), 5,74 (q, 1H), 4,40-3,95 (m, 2H), 3,24 (m, 1H), 3,20-2,75 (m+s, 6H), 2,05 (m, 2H), 1,30-1,70 (m+d, 5H) ppm |
| I-70 | 1HRMN (CD3CN) δ = 8,10 (s, 1H), 7,71 (d, 1H), 7,60 (d, 1H), 7,29-7,15 (m, 6H), 7,07 (dd, 1H), 6,87 (s, 1H), 5,45 (d, 1H), 5,36 (d, 1H), 4,48 (d, 1H), 4,00 (d, 1H), 3,35-3,23 (m, 2H), 3,00 (s, 4H), 2,86 (t, 1H), 2,18-2,06 (m, 2H), 1,80 (qd, 1H), 1,66 (qd, 1H) ppm |
| 1-71 | 1HRMN δ = 8,03 (d, 1H), 7,93 (d, 1H), 7,47 (t, 1H), 7,40 (t, 1H), 7,25-7,16 (m, 5H), 7,06 (s, 1H), 4,40 (bs, 1H), 4,34 (s, 2H), 4,09 (bs, 1H), 3,40-3,15 (m, 3H), 2,96 (s, 4H), 2,08-2,02 (m, 2H), 1,65 (bs, 2H) ppm |
| I-74 | 1HRMN δ = 8,31 (d, 1H), 8,02 (d, 2H), 7,82 (d, 1H), 7,69 (t, 1H), 7,63 7,51 (m, 3H), 5,79 (s, 1H), 4,95 (s, 2H), 3,41 - 3,32 (m, 2H), 2,19 - 2,09 (m, 3H), 2,12 (s, 3H), 2,07 (s, 3H), 1,81 -1,53 (m, 4H) ppm |
| I-76 | 1HRMN δ = 8,21 (d, 1H), 8,13 (d, 1H), 7,95 (d, 1H), 7,89 (d, 1H), 7,84 (d, 1H), 7,62 - 7,51 (m, 4H), 7,28 (d, 1H), 5,79 (s, 1H), 4,92 (s, 1H), 3,42 3,31 (m, 2H), 2,21 - 2,09 (m, 3H), 2,12 (s, 3H), 2,07 (s, 3H), 1,85 - 1,59 (m, 4H) ppm |
| I-77 | 1HRMNô = 7,29 (dd, 2H), 7,85 (dd, 1H), 7,55 - 7,41 (m, 4H), 7,11 (d, 1H), 6,90 (t, 2H), 5,79 (s, 1H), 4,86 (s, 2H), 3,10 (m, 1H), 2,51 (m, 2H), 2,11 (s, 3H), 2,06 (s, 3H), 2,88 - 2,72 (m, 2H), 1,49 -1,31 (m, 4H) ppm |
| I-78 | 1HRMN δ = 7,27-7,22 (m, 2H), 7,18-7,13 (m, 3H), 6,45 (s, 1H), 5,22 (bs, 2H), 4,38 (bs, 1H), 3,95 (bs, 1H), 3,33-3,20 (m, 2H), 2,94 (s, 4H), 2,93 (bs, 1H), 2,22 (s, 3H), 2,09-2,02 (m, 2H), 1,80-1,50 (m, 2H) ppm |
Petição 870180002928, de 12/01/2018, pág. 156/185
152/159
| Ex | Dados RMN |
| 1-79 | 1HRMN δ = 8,09 (d, 1H), 7,89 (d, 1H), 7,76 (d, 1H), 7,56 - 7,43 (m, 2H), 7,41 - 7,32 (m, 2H), 7,11 (s, 1H), 5,78 (s, 1H), 4,92 (s, 2H), 3,47 - 3,41 (m, 4H), 3,46 - 3,22 (m, 3H), 2,12 (s, 3H), 2,09 - 2,02 (m, 2H), 2,06 (s, 3H), 1,77- 1,49 (m, 4H) ppm |
| 1-80 | 1HRMN δ = 7,28-7,23 (m, 2H), 7,19-7,14 (m, 3H), 7,02 (s, 1H), 6,44 (s, 1H), 5,20 (bs, 2H), 4,30 (bs, 1H), 3,95 (bs, 1H), 3,30-3,20 (m, 2H), 2,87 (bs, 1H), 2,72 (m, 1H), 2,67-2,62 (m, 2H), 2,22 (s, 3H), 2,07-2,02 (m, 2H), 1,72 (bs, 1H), 1,63-1,47 (m, 5H), 1,19 (d, 3H) ppm |
| 1-81 | 1HRMN δ = 8,09 (d, 1H), 7,90 (d, 1H), 7,75 (d, 1H), 7,56-7,46 (m, 2H), 7,42-7,33 (m, 2H), 7,12 (s, 1H), 6,45 (s, 1H), 5,22 (bs, 2H), 4,31 (bs, 1H), 3,98 (bs, 1H), 3,44 (t, 2H), 3,35-3,26 (m, 2H), 3,15-3,05 (m, 2H), 2,90 (bs, 1H), 2,23 (s, 3H), 2,15-2,05 (m, 2H), 1,75 (bs, 1H), 1,62 (bs, 1H) ppm |
| I-83 | 1HRMN δ = 7,32-7,21 (m, 2H), 7,19-7,11 (m, 4H), 7,02 (s, 1H), 5,75 (s, 1H), 4,87 (s, 1H), 3,26 - 3,12 (m, 2H), 2,72 - 2,68 (m, 2H), 2,67 - 2,59 (m, 4H), 2,11 (s, 3H), 2,05 (s, 3H), 2,02 - 1,91 (m, 4H), 1,61 - 1,42 (m, 4H), 1,19 (d, 3H) ppm |
| I-84 | 1HRMN δ= 7,56 (d, 2H), 7,50 (s, 1H), 7,37 (d, 2H), 7,34 (s, 1H), 7,30 7,16 (m, 2H), 5,79 (s, 1H), 4,93 (s, 2H), 3,41 - 3,26 (m, 2H), 2,93 - 2,76 (m, 1H), 2,12 (s, 3H), 2,04 (s, 3H), 2,11 - 2,03 (m, 2H), 1,78 - 1,54 (m, 4H) ppm |
| I-85 | 1HRMN δ= 7,31 - 7,21 (m, 5H), 7,19 - 7,12 (m, 1H), 6,33 (d, 1H), 5,79 (s, 1H), 5,62 - 5,52 (m, 1H), 4,92 (s, 2H), 4,38 - 4,12 (m, 1H), 4,12 - 3,92 (m, 1H), 3,33 - 3,22 (m, 2H), 2,96 - 2,81 (m, 4H), 2,10 (s, 3H), 2,03 (s, 3H), 1,72 - 1,53 (m, 4H), 1,21 (d, 3H) ppm |
| I-86 | 1HRMN δ= 7,86 (s, 1H), 6,44 (s, 1H), 5,20 (bs, 2H), 4,31 (bs, 1H), 4,08 (s, 1H), 3,98 (bs, 1H), 3,31 (m, 1H), 3,28 (bs, 1H), 2,88 (bs, 1H), 2,22 (s, 3H), 2,13-2,05 (m, 2H), 1,78 (bs, 1H), 1,61 (bs, 1H) ppm |
| I-93 | 1HRMN (CD3CN) δ= 7,55 (d, 2H), 7,43 (d, 1H), 7,37 (t, 2H), 7,30-7,28 (m, 2H), 7,18 (d, 1H), 6,39 (s, 1H), 5,41 (d, 1H), 5,26 (s, 2H), 4,42 (d, 1H), 3,54 (t, 1H), 3,45 (m, 1H), 3,38 (t, 1H), 2,31 (s, 3H), 2,30-2,23 (m, 2H), 1,95-1,80 (m, 2H) ppm |
| I-94 | 1HRMN δ= 7,91 (s, 1H), 7,72 (d, 1H), 7,61 - 7,49 (m, 2H), 7,47 (s, 1H), 6,65 (s, 1H), 6,44 (s, 1H), 5,12 (s, 1H), 3,29 - 3,18 (m, 2H), 2,89 - 2,74 (m, 1H), 2,23 - 2,17 (m, 2H), 2,20 (s, 3H), 2,01 (d, 2H), 1,72 - 1,61 (m, 2H), 1,61 - 1,49 (m, 2H) ppm |
| I-96 | 1HRMN δ= 7,92 (s, 1H), 7,72 (d, 1H), 7,61 - 7,51 (m, 2H), 7,45 (s, 1H), 6,64 (s, 1H), 5,78 (s, 1H), 4,85 (s, 1H), 3,28 - 3,12 (m, 2H), 3,11 - 3,05 (m, 1H), 2,12 - 2,09 (m, 2H), 2,10 (s, 3H), 2,05 (s, 3H), 1,98 (d, 2H), 1,63 - 1,48 (m, 4H) ppm |
| I-97 | 1HRMN δ= 8,34 (d, 1H), 8,08 (s, 1H), 8,01 (d, 2H), 7,83 (dd, 1H), 7,68 (m, 1H), 7,62 (m, 1H), 7,57 (dd, 1H), 7,37 (m, 1H), 7,07 (m, 1H), 4,37 (bs, 1H), 4,15 (bs, 1H), 3,86 (bs, 2H), 3,40 (m, 1H), 3,34 (bs, 1H), 2,88 (bs, 1H), 2,16 (bs, 2H), 1,78 (bs, 1H), 1,64 (bs, 1H) ppm |
| I-98 | 1HRMN δ= 7,70 (s, 1H), 6,27 (s, 1H), 5,08 (d, 1H), 5,01 (d, 1H), 4,12 (bd, 1H), 3,76 (bd, 1H), 3,05 (t, 1H), 2,59 (t, 1H), 1,97 (s, 3H), 1,88-1,77 (m, 2H), 1,56 (tdd, 1H), 1,30 (tdd, 1H), 0,00 (s, 9H) ppm |
| I-99 | 1HRMN δ= 7,92 (s, 1H), 7,57-7,54 (m, 2H), 7,45-7,41 (m, 3H), 6,45 (s, 1H), 5,23 (bs, 2H), 4,33 (bs, 1H), 3,98 (bs, 1H), 3,36 (m, 1H), 3,28 (bs, 1H), 2,89 (bs, 1H), 2,23 (s, 3H), 2,16-2,08 (m, 2H), 1,80 (bs, 1H), 1,63 (bs, 1H) ppm |
Petição 870180002928, de 12/01/2018, pág. 157/185
153/159
| Ex | Dados RMN |
| 1-100 | 1HRMN δ= 7,84 (s, 1H), 7,49 (d, 2H), 6,98 (d, 2H), 6,45 (s, 1H), 5,22 (bs, 2H), 4,33 (bs, 1H), 3,98 (bs, 1H), 3,80 (s, 3H), 3,34 (m, 1H), 3,28 (bs, 1H), 2,89 (bs, 1H), 2,22 (s, 3H), 2,15-2,09 (m, 2H), 1,80 (bs, 1H), 1,63 (bs, 1H) ppm |
| 1-101 | 1HRMN δ= 7,99 (s, 1H), 7,67 (dd, 1H), 7,56 (dd, 1H), 7,45 (td, 1H), 7,39 (td, 1H), 6,45 (s, 1H), 5,23 (bs, 2H), 4,33 (bs, 1H), 3,98 (bs, 1H), 3,37 (m, 1H), 3,28 (bs, 1H), 2,89 (bs, 1H), 2,23 (s, 3H), 2,15-2,09 (m, 2H), 1,80 (bs, 1H), 1,63 (bs, 1H) ppm |
| 1-102 | 1HRMN δ= 7,95 (s, 1H), 7,60-7,55 (m, 2H), 7,52-7,46 (m, 2H), 6,45 (s, 1H), 5,22 (bs, 2H), 4,33 (bs, 1H), 3,98 (bs, 1H), 3,35 (m, 1H), 3,28 (bs, 1H), 2,89 (bs, 1H), 2,22 (s, 3H), 2,15-2,08 (m, 2H), 1,80 (bs, 1H), 1,63 (bs, 1H) ppm |
| 1-103 | 1HRMN δ= 7,86 (s, 1H), 7,47 (dd, 1H), 7,40 (td, 1H), 7,09 (d, 1H), 6,98 (td, 1H), 6,45 (s, 1H), 5,23 (bs, 2H), 4,33 (bs, 1H), 3,98 (bs, 1H), 3,86 (s, 3H), 3,35 (m, 1H), 3,29 (bs, 1H), 2,89 (bs, 1H), 2,23 (s, 3H), 2,15-2,08 (m, 2H), 1,80 (bs, 1H), 1,63 (bs, 1H) ppm |
| 1-104 | 1HRMN δ= 7,81 (s, 1H), 7,38 (d, 1H), 6,63 (d, 1H), 6,56 (dd, 1H), 6,45 (s, 1H), 5,22 (bs, 2H), 4,33 (bs, 1H), 3,98 (bs, 1H), 3,85 (s, 3H), 3,81 (s, 3H), 3,34 (m, 1H), 3,29 (bs, 1H), 2,89 (bs, 1H), 2,22 (s, 3H), 2,15-2,07 (m, 2H), 1,80 (bs, 1H), 1,64 (bs, 1H) ppm |
| 1-105 | 1HRMN (CD3CN) δ= 7,67 (s, 1H), 7,58 (d, 1H), 7,57 (d, 1H), 7,38 (dd, 1H), 6,37 (s, 1H), 5,04 (bs, 2H), 4,46 (bs, 1H), 3,95 (bs, 1H), 3,33 (m, 1H), 3,29 (bs, 1H), 2,90 (bs, 1H), 2,24 (s, 3H), 2,20-2,13 (m, 2H), 1,901,66 (m, 2H) ppm |
| 1-106 | 1HRMN δ= 7,87 (s, 1H), 7,04-6,95 (m, 3H), 6,45 (s, 1H), 5,22 (bs, 2H), 4,33 (bs, 1H), 3,98 (bs, 1H), 3,81 (s, 3H), 3,74 (s, 3H), 3,34 (m, 1H), 3,29 (bs, 1H), 2,89 (bs, 1H), 2,23 (s, 3H), 2,15-2,08 (m, 2H), 1,80 (bs, 1H), 1,63 (bs, 1H) ppm |
| 1-123 | 1HRMN (CD3CN) δ= 7,44 (d, 1H), 7,22 (dd, 1H), 7,18 (d, 1H), 6,88 (s, 1H), 6,40 (s, 1H), 5,11 (d, 1H), 5,04 (d, 1H), 4,45 (bd, 1H), 3,91 (bd, 1H), 3,27 (m, 1H), 3,09 (t, 2H), 3,00 (t, 2H), 2,84 (td, 1H), 2,23 (s, 3H), 2,15 (bd, 1H), 2,10 (bd, 1H), 1,81 (tdd, 1H), 1,63 (tdd, 1H) ppm |
| 1-124 | 1HRMN (CD3CN) δ= 8,40 (d, 1H), 7,98 (d, 2H), 7,82 (dd, 1H), 7,76 (s, 1H), 7,68 (m, 1H), 7,62 (m, 1H), 7,56-7,45 (m, 3H), 7,33 (dd, 1H), 4,45 (bd, 1H), 4,06 (bd, 1H), 3,88 (d, 1H), 3,81 (d, 1H), 3,36 (m, 1H), 3,30 (t, 1H), 2,84 (t, 1H), 2,25-2,10 (m, 2H), 1,84 (m, 1H), 1,70 (m, 1H) ppm |
| 1-125 | 1HRMN δ= 7,93 (s, 1H), 7,46-7,40 (m, 2H), 7,36 (d, 1H), 4,45-4,35 (m, 1H), 4,23 (s, 1H), 4,11-4,02 (m, 1H), 3,87 (d, 2H), 2,88-2,72 (m, 1H), 2,15-2,00 (m, 2H), 1,79-1,66 (m, 1H), 1,60-1,46 (m, 1H) |
| 1-126 | 1HRMN (CD3CN) δ= 7,16-7,05 (m, 4H), 6,87 (s, 1H), 6,39 (s, 1H), 5,11 (d, 1H), 5,03 (d, 1H), 4,46 (d, 1H), 3,91 (d, 1H), 3,32-3,23 (m, 2H), 3,01-2,93 (m, 4H), 2,84 (t, 1H), 2,27 (s, 3H), 2,23 (s, 3H), 2,18-2,07 (m, 2H), 1,82 (tdd, 1H), 1,65 (tdd, 1H) |
| 1-128 | 1HRMN (CD3CN) □= 7,28-7,19 (m, 1H), 6,96-6,88 (m, 3H), 6,39 (s, 1H), 5,10 (d, 1H), 5,03 (d, 1H), 4,43 (d, 1H), 3,90 (d, 1H), 3,32-3,19 (m, 2H), 3,07-2,94 (m, 4H), 2,88 (td, 1H), 2,23 (s, 3H), 2,16-2,03 (m, 2H), 1,79 (tdd, 1H), 1,62 (tdd, 1H) |
| 1-132 | 1HRMN δ= 7,12 (s, 1H), 6,49 (s, 1H), 5,31 (d, 1H), 5,22 (d, 1H), 4,35 (d, 1H), 3,95 (d, 1H), 3,45-3,20 (m, 2H), 2,82 (dd, 1H), 2,67 (dd, 2H), 2,21 (s, 3H), 2,06 (dd, 2H), 1,80-1,49 (m, 8H), 1,30-1,09 (m, 5H), 0,98-0,85 (m, 2H) ppm |
Petição 870180002928, de 12/01/2018, pág. 158/185
154/159
| Ex | Dados RMN |
| 1-133 | 1HRMN (CD3CN) δ= 7,16-7,12 (m, 1H), 7,11-7,02 (m, 3H), 6,93 (s, 1H), 6,38 (s, 1H), 5,08 (d, 1H), 5,01 (d, 1H), 4,45 (bd, 1H), 3,99 (bd, 1H), 3,283,18 (m, 2H), 2,86-2,65 (m, 5H), 2,21 (s, 3H), 2,17-2,03 (m, 3H), 1,941,57 (m, 8H) ppm |
| 1-134 | 1HRMN (CD3CN) δ= 7,17 (s, 1H), 7,14-7,07 (m, 4H), 6,88 (s, 1H), 5,35 (d, 1H), 5,28 (d, 1H), 4,43 (d, 1H), 3,86 (d, 1H), 3,31-3,24 (m, 2H), 3,00-2,95 (m, 4H), 2,86 (ddd, 1H), 2,27 (s, 3H), 2,16 (d, 1H), 2,10 (d, 1H), 1,82 (tdd, 1H), 1,65 (tdd, 1H) ppm |
| 1-136 | 1HRMN (CD3CN) δ= 7,21 (m, 1H), 7,17 (s, 1H), 6,94-6,86 (m, 3H), 5,34 (d, 1H), 5,28 (d, 1H), 4,39 (d, 1H), 3,84 (d, 1H), 3,30-3,22 (m, 2H), 3,02 (t, 2H), 2,97 (t, 2H), 2,87 (ddd, 1H), 2,13 (d, 1H), 2,06 (d, 1H), 1,79 (tdd, 1H), 1,61 (tdd, 1H) ppm |
| 1-138 | 1HRMN (CD3CN) δ= 8,32 (d, 1H), 7,44 (d, 1H), 7,17 (s, 1H), 7,06 (dd, 1H), 6,89 (s, 1H), 5,34 (d, 1H), 5,28 (d, 1H), 4,42 (d, 1H), 3,85 (d, 1H), 3,30-3,23 (m, 2H), 3,12 (s, 4H), 2,86 (ddd, 1H), 2,23 (s, 3H), 2,15 (d, 1H), 2,09 (d, 1H), 1,80 (tdd, 1H), 1,62 (tdd, 1H) ppm |
| 1-140 | 1HRMN (CD3CN) δ= 7,17 (s, 1H), 6,90 (s, 1H), 5,35 (d, 1H), 5,27 (d, 1H), 4,42 (d, 1H), 3,86 (d, 1H), 3,32-3,21 (m, 2H), 2,86 (ddd, 1H), 2,75-2,67 (m, 2H), 2,20-2,04 (m, 2H), 1,85-1,50 (m, 9H), 1,42-1,12 (m, 4H), 1,000,88 (m, 2H) ppm |
| 1-148 | 1HRMN δ= 7,18 (t, 1H), 7,13 (t, 1H), 7,03 (t, 1H), 6,91 (s, 1H), 5,43 (d, 1H), 5,35 (s, 1H), 4,32 (d, 1H), 3,94 (d, 1H), 3,30-3,21 (m, 2H), 2,82 (dd, 1H), 2,67 (dd, 2H), 2,10-2,00 (m, 2H), 1,83-1,48 (m, 8H), 1,35-1,10 (m, 5H), 0,95-0,85 (m, 2H) ppm |
| 1-149 | 1HRMN (CD3CN) δ = 7,17-7,10 (m, 1H), 7,11-7,03 (m, 3H), 6,95 (s, 1H), 6,89 (t, 1H), 6,82 (s, 1H), 6,78 (t, 1H), 5,23 (d, 1H), 5,17 (d, 1H), 4,44 (bd, 1H), 3,88 (bd, 1H), 3,30-3,21 (m, 2H), 2,98-2,67 (m, 5H), 2,15-2,03 (m, 3H), 1,94-1,58 (m, 8H) ppm |
| 1-158 | 1HRMN δ= 7,18-7,05 (m, 5H), 7,03 (d, 1H), 6,93 (d, 1H), 6,90 (s, 1H), 4,47 (d, 1H), 3,94 (d, 1H), 3,70 (d, 1H), 3,62 (d, 1H), 3,35-3,22 (m, 2H), 2,95-2,85 (m, 4H), 2,78 (t, 1H), 2,25 (s, 3H), 2,23 (s, 3H), 2,15 (s, 3H), 2,10-1,94 (m, 2H), 1,61-1,45 (m, 2H) |
| 1-160 | 1HRMN (CD3CN) δ= 7,28-7,17 (m, 1H), 7,05 (d, 1H), 6,96 (d, 1H), 6,956,85 (m, 4H), 4,52 (d, 1H), 3,93 (d, 1H), 3,68 (d, 1H), 3,62 (d, 1H), 3,263,11 (m, 2H), 3,06-2,92 (m, 4H), 2,79 (td, 1H), 2,26 (s, 3H), 2,18 (s, 3H), 2,09-1,97 (m, 2H), 1,60 (qd, 2H) |
| 1-166 | 1HRMN δ= 7,65-7.54 (m, 2H), 7,25-7,10 (m, 4H), 6,88 e 6,74 (s, 1H), 6,50 (s, 1H), 5,37-5,18 (m, 2H), 4,40 e 4,20 (d, 1H), 4,00 e 3,85 (d, 1H), 3,423,18 (m, 2H), 2,85 (dd, 1H), 2,38 e 2,20 (s, 3H), 2,22 e 2,20 (s, 3H), 2,192,10 e 2,05-1,93 (m, 2H), 1,83 e 1,67 (tdd, 1H), 1,59 e 1,48 (tdd, 1H) ppm |
| 1-167 | 1HRMN δ= 7,86 (dd, 1H), 7,67-7,62 (m, 2H), 7,56 (dd, 1H), 7,43 (dd, 1H), 7,27 (d, 1H), 7,23 (dd, 1H), 6,50 (s, 1H), 5,34 (d, 1H), 5,24 (d, 1H), 4,40 (d, 1H), 3,99 (d, 1H), 3,45-3,20 (m, 2H), 2,83 (dd, 1H), 2,20 (s, 3H), 2,182,08 (m, 2H), 1,82 (tdd, 1H), 1,58 (tdd, 1H) ppm |
| 1-172 | 1HRMN δ= 7,37 e 7,30 (s, 1H), 6,49 (s, 1H), 6,44 e 5,49 (dd, 1H), 6,35 e 6,24 (d, 1H), 5,35-5,18 (m, 2H), 4,37 e 4,29 (d, 1H), 3,95 (bs, 1H), 3,353,13 (m, 3H), 2,93 e 2,82 (dd, 1H), 2,21 (s, 3H), 2,18-2,02 (m, 2H), 1,851,48 (m, 6H), 1,35-1,05 (m, 6H) ppm |
Petição 870180002928, de 12/01/2018, pág. 159/185
155/159
| Ex | Dados RMN |
| 1-173 | 1HRMN δ= 7,51 e 7,34 (s, 1H), 7,13-7,04 (m, 4H), 6,54 e 5,67 (dd, 1H), 6,48 e 6,47 (s, 1H), 6,45 e 6,38 (d, 1H), 5,30 e 5,29 (d, 1H), 5,21 e 5,19 (d, 1H), 4,94 e 3,62 (m, 1H), 4,32 e 4,29 (d, 1H), 3,94 (m, 1H), 3,36-3,20 (m, 2H), 2,92-2,73 (m, 3H), 2,20 e 2,18 (s, 3H), 2,16-1,63 (m, 7H), 1,58 (m, 1H) ppm |
| 1-174 | 1HRMN δ= 7,65-7,55 (m, 3H), 7,24-7,17 (m, 4H), 7,15 e 7,11 (s, 1H), 6,89 e 6,72 (s, 1H), 5,65-5,46 (m, 2H), 4,37 e 4,16 (d, 1H), 3,98 e 3,82 (d, 1H), 3,43-3,19 (m, 2H), 2,87 (dd, 1H), 2,38 e 2,20 (s, 3H), 2,18-2,10 e 2,051,92 (m, 2H), 1,82 e 1,66 (tdd, 1H), 1,58 e 1,43 (tdd, 1H) ppm |
| 1-175 | 1HRMN δ= 7,84 (dd, 1H), 7,67-7,56 (m, 4H), 7,41 (t, 1H), 7,27 (d, 1H), 7,23 (td, 1H), 5,62 (d, 1H), 5,50 (d, 1H), 4,37 (d, 1H), 3,98 (d, 1H), 3,453,15 (m, 2H), 2,87 (dd, 1H), 2,18-2,09 (m, 2H), 1,82 (tdd, 1H), 1,56 (tdd, 1H) ppm |
| 1-180 | 1HRMN (CD3CN) δ= 7,17 (s, 1H), 7,13 e 7,02 (s, 1H), 6,49 e 5,55 (dd, 1H), 6,37 e 6,23 (d, 1H), 5,34 (d, 1H), 5,31 (d, 1H), 4,43 e 4,37 (d, 1H), 3,86 (d, 1H), 3,37-3,18 (m, 3H), 2,96 e 2,87 (ddd, 1H), 2,22-2,07 (m, 2H), 1,95-1,52 (m, 6H), 1,42-1,08 (m, 6H) ppm |
| 1-181 | 1HRMN (CD3CN) δ= 7,25-7,03 (m, 6H), 6,58 e 5,71 (dd, 1H), 6,46 e 6,39 (d, 1H), 5,35-5,23 (m, 2H), 4,98 e 4,67 (m, 1H), 4,42 e 4,34 (d, 1H), 3,84 e 3,63 (m, 1H), 3,34-3,23 (m, 2H), 2,96-2,65 (m, 3H), 2,20-2,04 (m, 2H), 2,00-1,58 (m, 6H) ppm |
| 1-182 | 1HRMN δ= 7,65-7,57 (m, 2H), 7,33-6,70 (m, 8H), 5,43-5,33 (m, 2H), 4,38 e 4,17 (bd, 1H), 3,99 e 3,84 (bd, 1H), 3,43-3,18 (m, 2H), 2,85 (t, 1H), 2,38 e 2,20 (s, 3H), 2,17-1,90 (m, 2H), 1,88-1,42 (m, 2H) ppm |
| 1-183 | 1HRMN δ= 7,86 (ddd, 1H), 7,68-7,62 (m, 2H), 7,55 (dd, 1H), 7,45-7,38 (m, 1H), 7,27 (d, 1H), 7,23 (dd, 1H), 7,18 (t, 1H), 7,03 (t, 1H), 6,90 (s, 1H), 5,50-5,32 (m, 2H), 4,38 e 4,12 (d, 1H), 3,99 e 3,80 (d, 1H), 3,45-3,15 (m, 2H), 2,86 (dd, 1H), 2,18-2,08 (m, 2H), 1,95 e 1,83 (tdd, 1H), 1,59 e 1,43 (tdd, 1H) ppm |
| 1-188 | 1HRMN δ= 7,37 e 7,30 (s, 1H), 7,18 e 7,16 (t, 1H), 7,03 e 7,02 (t, 1H), 6,90 (s, 1H), 6,44 e 5,49 (dd, 1H), 6,35 e 6,24 (d, 1H), 5,45-5,30 (m, 2H), 4,35 e 4,28 (d, 1H), 3,94 (d, 1H), 3,40-3,15 (m, 3H), 2,93 e 2,82 (dd, 1H), 2,20-2,02 (m, 2H), 1,85-1,48 (m, 6H), 1,37-1,05 (m, 6H) ppm |
| 1-189 | 1HRMN δ= 7,52 e 7,38 (s, 1H), 7,17 e 7,15 (t, 1H), 7,13-7,03 (m, 4H), 7,03 e 7,02 (t, 1H), 6,90 (s, 1H), 6,54 e 5,67 (dd, 1H), 6,45 e 6,38 (d, 1H), 5,45-5,32 (m, 2H), 4,95 e 3,63 (dd, 1H), 4,33 e 4,28 (d, 1H), 3,96-3,90 (m, 1H), 3,40-3,20 (m, 2H), 2,85 e 2,80 (dd, 1H), 2,82-2,70 (m, 2H), 2,161,68 (m, 6H), 1,60-1,49 (m, 2H) ppm |
| I-206 | 1HRMN (CD3CN) δ= 7,62 (s, 1H), 7,50 (d, 1H), 7,33-7,26 (m, 2H), 7,257,17 (m, 1H), 6,39 (s, 1H), 5,10 (d, 1H), 5,03 (d, 1H), 4,48 (d, 1H), 3,92 (d, 1H), 3,36-3,21 (m, 2H), td (2,84, 1H), 2,48 (s, 3H), 2,22 (s, 3H), 2,202,09 (m, 2H), 1,85 (tdd,1 H), 1,68 (tdd, 1H) |
| I-207 | 1HRMN δ= 8,05 (s, 1H), 7,76 (dd, 1H), 7,68 (dd, 1H), 7,46 (td, 1H), 7,38 (td, 1H), 6,49 (s, 1H), 5,32 (d, 1H), 5,23 (d, 1H), 4,37 (d, 1H), 3,98 (d, 1H), 3,43-3,20 (m, 2H), 2,84 (t, 1H), 2,20 (s, 3H), 2,09 (t, 2H), 1,82 (tdd, 1H), 1,58 (tdd, 1H) |
| I-208 | 1HRMN δ= 8,14 (s, 1H), 7,62-7,51 (m, 1H), 7,28 (d, 1H), 7,26 (d, 1H), 6,49 (s, 1H), 5,32 (d, 1H), 5,23 (d, 1H), 4,37 (d, 1H), 3,97 (d, 1H), 3,443,20 (m, 2H), 2,85 (t, 1H), 2,21 (s, 3H), 2,12 (t, 2H), 1,89-1,76 (m, 1H), 1,65-1,50 (m, 1H) |
Petição 870180002928, de 12/01/2018, pág. 160/185
156/159
| Ex | Dados RMN |
| 1-210 | 1HRMN δ= 8,44 (d, 1H), 8,12 (s, 1H), 7,75 (d, 1H), 7,35 (dd, 1H), 6,49 (s, 1H), 5,32 (d, 1H), 5,23 (d, 1H), 4,37 (d, 1H), 3,98 (d, 1H), 3,44-3,21 (m, 2H), 2,85 (t, 1H), 2,46 (s, 3H), 2,21 (s, 3H), 2,08-1,96 (m, 2H), 1,88-1,65 (m, 1H), 1,65-1,51 (m, 1H) |
| 1-212 | 1HRMN δ= 7,98 (s, 1H), 7,58 (s, 1H), 7,51 (d, 1H), 7,33 (m, 2H), 7,24 (m, 1H), 5,60 (d, 1H), 5,50 (d, 1H), 4,34 (m, 1H), 3,96 (m, 1H), 3,40-3,25 (m, 2H), 2,86 (m, 1H), 2,45 (s, 3H), 2,09 (m, 2H), 1,80 (m, 1H), 1,55 (m, 1H) PPm |
| 1-213 | 1HRMN δ= 8,05 (s, 1H), 7,76 (dd, 1H), 7,68 (dd, 1H), 7,58 (s, 1H), 7,45 (td, 1H), 7,36 (td, 1H), 5,60 (d, 1H), 5,50 (d, 1H), 4,34 (m, 1H), 3,95 (m, 1H), 3,25-3,39 (m, 2H), 2,86 (m, 1H), 2,10 (m, 2H), 1,80 (m, 1H), 1,55 (m, 1H) ppm |
| 1-214 | 1HRMN δ= 8,14 (s, 1H), 7,60-7,52 (m, 2H), 7,31-7,25 (m, 2H), 5,59 (d, 1H), 5,50 (d, 1H), 4,33 (m, 1H), 3,96 (m, 1H), 3,49-3,15 (m, 2H), 2,86 (m, 1H), 2,11 (m, 2H), 1,80 (m, 1H), 1,54 (m, 1H) ppm |
| 1-216 | 1HRMN δ= 8,44 (dd, 1H), 8,12 (s, 1H), 7,75 (d, 1H), 7,58 (s, 1H), 7,34 (dd, 1H), 5,60 (d, 1H), 5,50 (d, 1H), 4,34 (m, 1H), 3,97 (m, 1H), 3,42-3,26 (m, 2H), 2,87 (m, 1H), 2,46 (s, 3H), 2,12 (m, 2H), 1,81 (m, 1H), 1,56 (m, 1H) ppm |
| 1-218 | 1HRMN δ= 7,98 (s, 1H), 7,60-7,50 (m, 1H), 7,36-7,30 (m, 2H), 7,30-7,21 (m, 1H), 7,18 (t, 1H), 7,02 (t, 1H), 6,90 (s, 1H), 5,43 (d, 2H), 4,41-4,32 (m, 1H), 4,02-3,91 (m, 1H), 2,90-2,80 (m, 1H), 2,46 (s, 3H), 2,19-2,05 (m, 2H), 1,90-1,73 (m, 1H), 1,65-1,52 (m, 1H) |
| 1-219 | 1HRMN δ= 8,05 (s, 1H), 7,76 (d, 1H), 7,69 (d, 1H), 7,46 (t, 1H), 7,39 (t, 1H), 7,18 (t, 1H), 7,02 (t, 1H), 6,90 (s, 1H), 5,39 (d, 2H), 4,40-4,29 (m, 1H), 4,01-3,91 (m, 1H), 2,92-2,81 (m, 1H), 2,19-2,06 (m, 2H), 1,89-1,74 (m, 1H), 1,65-1,50 (m, 1H) |
| I-220 | 1HRMN δ= 8,14 (s, 1H), 7,65-7,52 (m, 1H), 7,30-7,21 (m, 2H), 7,18 (t, 1H), 7,02 (t, 1H), 6,90 (s, 1H), 5,39 (d, 2H), 4,40-4,29 (m, 1H), 4,02-3,91 (m, 1H), 2,90-2,77 (m, 1H), 2,18-2,02 (m, 2H), 1,90-1,76 (m, 1H), 1,681,51 (m, 1H) |
| I-222 | 1HRMN δ= 8,45 (bs, 1H), 8,12 (s, 1H), 7,75 (d, 1H), 7,38-7,33 (m, 1H), 7,18 (t, 1H), 7,02 (t, 1H), 6,90 (s, 1H), 5,39 (d, 2H), 4,39-4,31 (m, 1H), 4,01-3,92 (m, 1H), 3,00-2,78 (m, 1H), 2,46 (s, 3H), 2,18-2,03 (m, 2H), 1,89-1,76 (m, 1H), 1,65-1,52 (m, 1H) |
| I-223 | 1HRMN δ= 8,02 (s, 1H), 7,15 (t, 1H), 7,02 (t, 1H), 6,90 (s, 1H), 5,38 (d, 2H), 4,39-4,30 (m, 1H), 4,04-3,91 (m, 1H), 2,87-2,79 (m, 1H), 2,28 (s, 3H), 2,16-2,04 (m, 2H), 1,90-1,73 (m, 1H), 1,62-1,49 (m, 1H) |
| I-224 | 1HRMN δ= 7,98 (s, 1H), 7,50 (d, 1H), 7,47-7,42 (m, 2H), 7,39-7,32 (m, 3H), 7,27-7,20 (m, 1H), 4,46-4,38 (m, 1H), 4,12-4,04 (m, 1H), 3,88 (d, 2H), 2,85-2,76 (m, 1H), 2,46 (s, 3H), 2,17-2,05 (m, 2H), 1,79-1,67 (m, 1H), 1,62-1,48 (m, 1H) |
| I-225 | 1HRMN δ= 8,05 (s, 1H), 7,76 (d, 1H), 7,68 (d, 1H), 7,50-7,44 (m, 3H), 7,41-7,30 (m, 2H), 4,46-4,36 (m, 1H), 4,11-4,02 (m, 1H), 3,87 (d, 2H), 2,86-2,74 (m, 1H), 2,17-2,05 (m, 2H), 1,80-1,68 (m, 1H), 1,64-1,50 (m, 1H) |
| I-226 | 1HRMN δ= 8,13 (s, 1H), 7,65-7,52 (m, 2H), 7,49-7,43 (m, 2H), 7,35 (d, 1H), 7,25 (t, 1H), 4,46-4,37 (m, 1H), 4,13-4,04 (m, 1H), 3,88 (d, 2H), 2,86-2,75 (m, 1H), 2,18-2,04 (m, 2H), 1,80-1,69 (m, 1H), 1,62-1,50 (m, 1H) |
Petição 870180002928, de 12/01/2018, pág. 161/185
157/159
| Ex | Dados RMN |
| 1-228 | 1HRMN δ= 8,46 (bs, 1H), 8,12 (s, 1H), 7,76 (d, 1H), 7,68-7,52 (m, 1H), 7,48-7,42 (m, 2H), 7,39-7,32 (m, 1H), 4,46-4,39 (m, 1H), 4,13-4,04 (m, 1H), 3,87 (d, 2H), 2,88-2,75 (m, 1H), 2,47 (s, 3H), 2,18-2,05 (m, 2H), 1,81-1,69 (m, 1H), 1,62-1,50 (m, 1H) |
| 1-229 | 1HRMN δ= 8,01 (s, 1H), 7,47-7,41 (m, 2H), 7,34 (d, 1H), 4,44-4,35 (m, 1H), 4,12-4,04 (m, 1H), 3,87 (d, 2H), 2,86-2,75 (m, 1H), 2,28 (s, 3H), 2,17-2,04 (m, 2H), 1,80-1,68 (m, 1H), 1,61-1,50 (m, 1H) |
| 1-230 | 1HRMN δ= 7,97 (s, 1H), 7,51 (d, 1H), 7,34 (d, 2H), 7,28-7,20 (m, 1H), 7,03 (d, 1H), 6,93 (d, 1H), 6,90 (s, 1H), 4,48 (d, 1H), 3,97 (d, 1H), 3,69 (d, 1H), 3,64 (d, 1H), 3,40-3,25 (m, 1H), 3,20 (t, 1H), 2,78 (t, 1H), 2,45 (s, 3H), 2,24 (s, 3H), 2,15 (s, 3H), 2,02 (t, 2H), 1,65-1,47 (m, 2H) |
| 1-231 | 1HRMN δ= 8,03 (s, 1H), 7,76 (dd, 1H), 7,68 (dd, 1H), 7,45 (td, 1H), 7,38 (td, 1H), 7,03 (d, 1H), 6,93 (d, 1H), 6,88 (s, 1H), 4,48 (d, 1H), 3,98 (d, 1H), 3,70 (d, 1H), 3,64 (d, 1H), 3,40-3,26 (m, 1H), 3,20 (t, 1H), 2,79 (t, 1H), 2,23 (s, 3H), 2,15 (s, 3H), 2,03 (t, 2H), 1,68-1,47 (m, 2H) |
| I-232 | 1HRMN δ= 8,12 (s, 1H), 7,62-7,51 (m, 1H), 7,27 (t, 2H), 7,03 (d, 1H), 6,93 (d, 1H), 6,90 (s, 1H), 4,53-4,45 (m, 1H), 4,01-3,93 (m, 1H), 3,69 (d, 1H), 3,63 (d, 1H), 3,40-3,15 'm, 2H), 2,78 (t, 1H), 2,23 (s, 3H), 2,15 (s, 3H), 2,14-2,00 (m, 2H), 1,68-1,48 (m, 2H) |
| I-235 | 1HRMN δ= 8,00 (s, 1H), 7,03 (d, 1H), 6,93 (d, 1H), 6,89 (s, 1H), 4,48 (d, 1H), 3,96 (d, 1H), 3,68 (d, 1H), 3,63 (d, 1H), 3,40-3,15 (m, 2H), 2,77 (t, 1H), 2,28 (s, 3H), 2,23 (s, 3H), 2,15 (s, 3H), 2,04 (t, 2H), 1,65-1,48 (m, 2H) |
| I-236 | 1HRMN δ= 8,40 (dd, 1H), 7,74-7,56 (m, 5H), 7,17 (dd, 1H), 5,62 (d, 1H), 5,50 (d, 1H), 4,37 (m, 1H), 3,97 (m, 1H), 3,50-3,20 (m, 2H), 2,87 (m, 1H), 2,40 (s, 3H), 2,12 (m, 2H), 1,85 (m, 1H), 1,57 (m, 1H) ppm |
| I-237 | 1HRMN δ= 7,68-7,50 (m, 3H), 7,25-7,15 (m, 3H), 7,11 (d, 1H), 7,03 (d, 1H), 6,93 (d, 1H), 6,90 (s, 1H), 4,51 (d, 1H), 3,97 (d, 1H), 3,71 (d, 1H), 3,63 (d, 1H), 3,40-3,15 (m, 2H), 2,79 (t, 1H), 2,38 (s, 3H), 2,24 (s, 3H), 2,14 (s, 3H), 2,12-2,00 (m, 2H), 1,65-1,48 (m, 2H) |
| I-238 | 1HRMN δ= 7,92 (s, 1H), 7,02 (d, 1H), 6,93 (d, 1H), 6,89 (s, 1H), 4,46 (d, 1H), 4,22 (s, 1H), 3,95 (d, 1H), 3,68 (d, 1H), 3,62 (d, 1H), 3,34-3,23 (m, 1H), 3,18 (t, 1H), 2,77 (t, 1H), 2,23 (s, 3H), 2,14 (s, 3H), 2,02 (t, 2H), 1,63-1,44 (m, 2H) |
| I-239 | 1HRMN δ= 7,93 (s, 1H), 7,17 (t, 1H), 7,02 (t, 1H), 6,90 (s, 1H), 5,38 (d, 2H), 4,37-4,30 (m, 1H), 4,23 (s, 1H), 4,01-3,89 (m, 1H), 2,89-2,77 (m, 1H), 2,15-2,00 (m, 2H), 1,84-1,70 (m, 1H), 1,61-1,49 (m, 1H) |
| I-240 | 1HRMN δ= 7,73 (s, 1H), 7,59 (s, 1H), 7,54 (d, 1H), 7,42-7,27 (m, 4H), 5,63 (d, 1H), 5,50 (d, 1H), 4,37 (d, 1H), 3,98 (d, 1H), 3,45-3,20 (m, 2H), 2,87 (dd, 1H), 2,18-2,08 (m, 2H), 1,83 (tdd, 1H), 1,58 (tdd, 1H) ppm |
| 1-241 | 1HRMN δ= 7,73 (s, 1H), 7,54 (d, 1H), 7,42-7,27 (m, 4H), 7,19 (t, 1H), 7,03 (t, 1H), 6,91 (s, 1H), 5,45 (d, 1H), 5,36 (d, 1H), 4,38 (d, 1H), 4,01 (d, 1H), 3,45-3,22 (m, 2H), 2,86 (dd, 1H), 2,20-2,09 (m, 2H), 1,83 (tdd, 1H), 1,60 (tdd, 1H) ppm |
| I-242 | 1HRMN δ= 7,92 (d, 1H), 7,73 (s, 1H), 7,58-7,53 (dd, 1H), 7,45-7,28 (m, 3H), 6,50 (s, 1H), 5,34 (d, 1H), 5,23 (d, 1H), 4,40 (d, 1H), 3,99 (d, 1H), 3,43-3,20 (m, 2H), 2,85 (dd, 1H), 2,21 (s, 3H), 2,18-2,09 (m, 2H), 1,84 (tdd, 1H), 1,59 (tdd, 1H) ppm |
Petição 870180002928, de 12/01/2018, pág. 162/185
158/159 [00793] As alterações químicas RMN foram medidas em ppm at 400 MHz, desde que não conste outra indicação, no solvente DMSOd6 utilizando-se tetrametilsilano como padrão interno.
[00794] As abreviações a seguir descrevem divisão de sinal:
[00795] b = amplo, s = simples, d = duplo, t = triplo, q = quádruplo, m = múltiplo
Exemplos de aplicação
Exemplo A
Teste de Phytophthora (tomate) / atividade protetora
Solvente: 49 partes em peso de Ν,Ν-dimetilformamida
Emulsificante: 1 parte em peso de éter alquilaril poliglicol [00796] Para produzir a preparação adequada de composto ativo, 1 parte em peso de compost ativo é misturada com as quantidades indicadas de solvente e emulsificante e o concentrado é diluído com água até a concentração desejada.
[00797] Para o teste de atividade protetora, plantas de tomate jovens são espalhadas com a preparação de composto ativo na taxa de aplicação indicada. 1 dia após o tratamento, as plantas são inoculadas com uma suspensão de esporos de Phytophthora infestans e então mantidas sob 100% de umidade relativa do ar e 22°C por 24 horas. As plantas foram então colocadas em uma câmara climatizada a aproximadamente 96% de umidade relativa atmosférica e a uma temperatura de aproximadamente 20Ό.
[00798] Foi feita avaliação 7 dias após a inoculação. 0% significa uma eficácia que coresponde àquela do controle, enquanto uma eficácia de 100% significa que não foi observada infecção.
[00799] Neste teste, os compostos de acordo com a invenção 1-1, I2, I-3, I-9, 1-15, I-26, I-27, I-35, I-43, I-50, 1-51, I-52, I-53, I-59, I-74, I77, I-79, I-80, 1-81, I-83, I-93, I-96, I-98, I-99, 1-100, 1-101, 1-102, 1-103, 1-104, 1-105, 1-107, 1-108, 1-109, 1-114, 1-115, 1-116, 1-117, 1-121, 1-122 e
Petição 870180002928, de 12/01/2018, pág. 163/185
159/159
1-123 mostram a uma concentração de composto ativo de 500 ppm, uma eficácia de 70% ou mais.
Exemplo B
Teste de Plasmopara (videira) / atividade protetora
Solventes: 24,5 partes em peso de acetona
24,5 partes em peso de dimetilacetamida
Emulsificante:1 parte em pesode éter alquilaril poliglicol [00800] Para produzir a preparação adequada de composto ativo, 1 parte em peso de compost ativo é misturada com as quantidades indicadas de solvente e emulsificante e o concentrado é diluído com água até a concentração desejada.
[00801] Para o teste de atividade protetora, plantas de tomate jovens são espalhadas com a preparação de composto ativo na taxa de aplicação indicada. Após o revestimento por atomização ter seco, as plantas foram inoculadas com uma suspensão de esporos aquosa de Plasmopara viticola e em seguida mantidas em uma cabine de inoculação a aproximadamente 20Ό e 100% de umidade relativa do ar por 1 ia. As plantas foram então colocadas emu ma estufa a aproximadamente 21Ό e uma umidade atmosférica de aproximadam ente 90% por 4 dias. As plantas foram então umedecidas e colocadas em uma cabine de incubação por 1 dia.
[00802] A avaliação foi feita 6 dias após a inoculação. 0% significa uma eficácia que coresponde àquela do controle, enquanto uma eficácia de 100% significa que não foi observada infecção.
[00803] Neste teste, os compostos de acordo com a invenção 1-1, I9, I-35, I-43, i-50, 1-51, I-53, I-59, I-74, i-80, 1-81, I-93, I-96, I-98, I-99, I100, 1-101, 1-102, 1-103, 1-104, 1-105, 1-108, 1-109, 1-114, 1-115, 1-116 e 1-117 mostram, a uma concentração de composto ativo de 100 ppm, uma eficácia de 70% ou mais.
Petição 870180002928, de 12/01/2018, pág. 164/185
1/14
Claims (14)
- REIVINDICAÇÕES1. Composto, caracterizado pelo fato de que apresenta a Fórmula (I), na qual os símbolos apresentam os seguintes significados:A representa fenila, que pode conter até dois constituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo:ciano, flúor, cloro, bromo, iodo, metila, etila, CF3, CHF2, C2F5, CCI3, hidroxila, OMe, OCF3, OCHF2, OCH2CF3 ou OC2F5, ouA representa um radical heteroaromático selecionado do grupo abaixo: tiofen-3-ila, pirazol-1 -ila, pirazol-4-ila, piridin-4-ila, 1Hbenzimidazol-2-ila ou 1,3-benzotiazol-2-ila, que pode conter até dois substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo:substituintes em carbono: ciano, flúor, cloro, bromo, iodo, metila, etila, CF3, CHF2, C2F5, CCI3 , hidroxila, OMe, OCF3, OCHF2, OCH2CF3 ou OC2F5, substituintes em nitrogênio: metila, etila ou CF3L1 representa (C(R1)2)n sendo que n = 0 to 3,R1 é idêntico ou diferente e independnetemente entre si representa hidrogênio ou metila, com a condição de que L1 pode conter no máximo um substituinte metila,Y representa enxofre ou oxigênio,W representa -CH2CH2-,Petição 870180002928, de 12/01/2018, pág. 165/185
- 2/14X representa -CH2CH2-,R2 representa hidrogênio, metila, cloro ou bromo,L2 representa -C(R8)2-C(R8)2- ou -CR9=CR9- ou -C^C-,L3 representa uma ligação direta, ouL3 representa uma cadeia de carbono Cr a C4-,R3 representa ciclopropila, ciclobutila, ciclopentila, ciclohexila, ciclo-heptila ou ciclo-octila, ouR3 representa fenila que pode conter até dois substituintes, sendo que os substituintes independentemente entre si são selecionados da lista abaixo:ciano, flúor, cloro, bromo, iodine, metila, etila, 1-metiletila, 1,1-dimetiletila, CF3, CHF2, C2F5, CCI3, fenila, hidroxila, OMe, OEt, O/soPr, OCF3, OCHF2, OC2F5, SMe ou SCF3, ouR3 representa naftalen-1-ila, naftalen-2-ila, 1,2,3,4-tetrahidronaftalen-1-ila, 1,2,3,4-tetra-hidronaftalen-2-ila, 5,6,7,8-tetrahidronaftalen-1-ila, 5,6,7,8-tetra-hidronaftalen-2-ila, decalin-1-ila, decalin-2-ila, 1 H-inden-1-ila, 1H-inden-2-ila, 1H-inden-3-ila, 1H-inden-4-ila, 1H-inden-5-ila, 1H-inden-6-ila, 1H-inden-7-ila, 2,3-di-hidro-1H-inden-1ila, 2,3-di-hidro-1 H-inden-2-ila, 2,3-di-hidro-1 H-inden-4-ila ou 2,3-dihidro-1H-inden-5-ila, ouR3 representa furan-2-ila, furan-3-ila, tiofen-2-ila, tiofen-3-ila, isoxazol-3-ila, isoxazol-4-ila, isoxazol-5-ila, 1 H-pirrol-1-ila, 1 H-pirrol-2ila, 1 H-pirrol-3-ila, oxazol-2-ila, oxazol-4-ila, oxazol-5-ila, tiazol-2-ila, tiazol-4-ila, tiazol-5-ila, isotiazol-3-ila, isotiazol-4-ila, isotiazol-5-ila, pirazol-1-ila, pirazol-3-ila, pirazol-4-ila, imidazol-1 -ila, imidazol-2-ila, imidazol-4-ila, 1,2,4-oxadiazol-3-ila, 1,2,4-oxadiazol-5-ila, 1,3,4-oxadiazolPetição 870180002928, de 12/01/2018, pág. 166/185
- 3/142-ila, 1,2,4-tiadiazol-3-ila, 1,2,4-tiadiazol-5-ila, 1,3,4-tiadiazol-2-ila, 1,2,3-triazol-1 -ila, 1,2,3-triazol-2-i la, 1,2,3-triazol-4-i la, 1,2,4-triazol-1 ila, 1,2,4-triazol-3-ila, piridin-2-ila, piridin-3-ila, piridin-4-ila, piridazin-3ila, piridazin-4-ila, pirimidin-2-ila, pirimidin-4-ila, pirimidin-5-ila, pirazin2-ila, 1,3,5-triazin-2-ila ou 1,2,4-triazin-3-ila, ouR3 representa 1 H-indol-1 -ila, 1 H-indol-2-ila, 1 H-indol-3-ila, 1 H-indol-4-ila, 1 H-indol-5-ila, 1 H-indol-6-ila, 1 H-indol-7-ila, 1Hbenzimidazol-1-ila, 1H-benzimidazol-2-ila, 1H-benzimidazol-4-ila, benzimidazol-5-ila, 1 H-indazol-1 -ila, 1H-indazol-3-ila, 1H-indazol-4-ila, 1Hindazol-5-ila, 1H-indazol-6-ila, 1H-indazol-7-ila, 2H-indazol-2-ila, 1benzofuran-2-ila, 1-benzofuran-3-ila, 1-benzofuran-4-ila, 1-benzofuran5-ila, 1-benzofuran-6-ila, 1-benzofuran-7-ila, 1-benzotiofen-2-ila, 1benzotiofen-3-ila, 1-benzotiofen-4-ila, 1-benzotiofen-5-ila, 1benzotiofen-6-ila, 1-benzotiofen-7-ila, quinolin-2-ila, quinolin-3-ila, quinolin-4-ila, quinolin-5-ila, quinolin-6-ila, quinolin-7-ila, quinolin-8-ila, isoquinolin-1 -ila, isoquinolin-3-ila, isoquinolin-4-ila, isoquinolin-5-ila, isoquinolin-6-ila, isoquinolin-7-ila ou isoquinolin-8-ila, ouR3 representa pirrolidin-2-ila, pirrolidin-3-ila, morfolin-3-ila, morfolin-2-ila, piperidin-2-ila, piperidin-3-ila ou piperazin-2-ila,R3é idêntico ou diferente e independentemente entre si representa hidrogênio, metila ou etila,R9é idêntico ou diferente e independentemente entre si representa hidrogênio, metila ou etila, e também os sais de ação agroquímica destes.2. Método para combate a fungos nocivos fitopatogênicos, caracterizado pelo fato de que compostos da Fórmula (I), como definido na reivindicação 1, são aplicados aos fungos nocivos fitopatogênicos e/ou ao seu habitat, excluído tratamento em humanos e/ou aniPetição 870180002928, de 12/01/2018, pág. 167/185
- 4/14 mais.3. Composições para combate a fungos nocivos fitopatogênicos, caracterizadas pelo fato de que compreendem um composto, como definido na reivindicação 1, além do extensores e/ou tensoativos.4. Uso de tiazóis substituídos por heterociclila da Fórmula (I), como definidos na reivindicação 1, caracterizado pelo fato de que é para o combate de fungos nocivos fitopatogênicos, excluído tratamento em humanos e/ou animais.
- 5. Processo para preparação de composições para o combate de fungos nocivos fitopatogênicos, caracterizado pelo fato de tiazóis substituídos por heterociclila da Fórmula (I), como definidos na reivindicação 1, são misturados com extensores e/ou tensoativos.
- 6. Processo para preparação dos compostos da Fórmula (I), como definidos na reivindicação 1, caracterizado pelo fato de que compreende pelo menos uma das etapas (a) a (n) abaixo:(a)a conversão de compostos da fórmula (VII), na presença de um composto organometálico R9-M, e, se necessário, na presença de um solvente, em compostos da fórmula (VIII), de acordo com o esquema de reação abaixo (esquema 1):H R—M solvente na qualPG = fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecionados do grupo consistindo em metila, metóxi, nitro, dioxolano), acetila, C1-C4alcoxicarbonila e benziloxicarbonila,M = por exemplo, MgCI, MgBr, Mgl, Li,R9= CrC^alquila ou C3-C6-cicloalquila,Petição 870180002928, de 12/01/2018, pág. 168/1855/14W, X, e R2 são conforme definido na Fórmula (I) na reivindicação 1;(b)a reação de alcoóis da fórmula (VIII) com um agente oxidante na presença de um solvente, para formar cetonas da fórmula (IX), de acordo com o esquema de reação abaixo (esquema 2):na qualPG = fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecionados do grupo consistindo em metila, metóxi, nitro, dioxolano), acetila e C1-C4alcoxicarbonila,R9= CrC^alquila ou C3-C6-cicloalquila,W, X, e R2 são conforme definido para Fórmula (I) na reivindicação 1;(c)a conversão de cetonas da fórmula (IX) na presença de uma base ou um ácido e, se apropriado, um solvente, em compostos da fórmula (IVb), de acordo com o esquema de reação abaixo(esquema 3):nas quaisPG = fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecionados do grupo consistindo em metila, metóxi, nitro, dioxolano), acetila e Ci-C4alcoxicarbonila,L2=-CR9=CR9-,Petição 870180002928, de 12/01/2018, pág. 169/1856/14W, X, L3, R2, R3 e R9 são conforme definidos para Fórmula (I) na reivindicação 1;(d)a conversão de aldeídos da fórmula (VII) na presença de uma base ou um ácido e, se necessário, um solvente, em, compostos da fórmula (IVb), de acordo com o esquema de reação abaixo (esquema 4):nas quaisPG = fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecinados do grupo consistindo em metila, metóxi, nitro, dioxolano), acetila e C1-C4alcoxicarbonila,L2=-CR9=CR9-,W, X, L3, R2, R3 e R9 são conforme definidos para Fórmula (I) na reivindicação 1;(e)a conversão de aldeídos da fórmula (VII) na presença de uma base e, se necessário, um solvente, em alquinos da fórmula (X) de acordo com o esquema de reação abaixo (esquema 5):nas quaisPG = fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecionados do grupo consistindo em metila, metóxi, nitro, dioxolano), acetila e C1-C4alcoxicarbonila, lulexW, X e R2 são conforme definido para Fórmula (I) na reivinPetição 870180002928, de 12/01/2018, pág. 170/185
- 7/14 d i cação 1;(f)a reação de alquinos da fórmula (X) com um R3-L3-haleto em uma reação de acoplamento C-C opcionalmente catalisada na presença de uma base e, se necessário, um solvente, para formar compostos da fórmula (IVc), de acordo com o esquema de reação abaixo (esquema 6):nas quaisPG = fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecionados do grupo consisitndo em metila, metóxi, nitro, dioxolano), acetila e C1-C4alcoxicarbonila,Hal = Cl, Br ou I,L2=-CeC-,W, X, L3, R2 e R3 são conforme definidos para Fórmula (I) na reivindicação 1;(g)a reação de alquinos da fórmula (X) com um cloreto de trialquilsilila (R10R11R12)SiCI ou triflato de trialquilsilila (R10R11R12)SiOSO2CF3 ou outros agentes conhecidos de sililação na presença de uma base, se necessário, um solvente, para formar compostos da fórmula (XI), de acordo com Oe squema de reação abaixo (esquema 7):nas quais (R10R11R12)SiCI ou (R10R11R12)SiOSO2CF3 base ~~ solventPetição 870180002928, de 12/01/2018, pág. 171/185
- 8/14PG = fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecionados do grupo consisitndo em metila, metóxi, nitro, dioxolano), acetila e C^-C4alcoxicarbonila,R10, R11 e R12 = Ci-C4 alquila ou fenila,W, X e R2 são conforme definidos para Fórmula (I) na reivindicação 1;(h)a reação de alquinos da fórmula (XI) com um composto R3-L3-Hal, se necessário na presença de um catalisador, na presença de uma base e, se necessário, um solvente para formar compostos da fórmula (IVc), de acordo com o esquema de reação abaixo (esquema 8):nas quaisPG = fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecionados do grupo consistindo em metila, metóxi, nitro, dioxolano), acetila e C^-C4alcoxicarbonila,Hal = Cl, Br ou I,R2 = hidrogênio, Ct-C^alquila ou C1-C2-haloalquila,L2=-CeC-,R10, R11 e R12 = CrC^alquila ou fenila,W, X, L3 e R3 conforme definido para Fórmula (I) na reivindicação 1;(i)a reação de tioamidas da fórmula (V) com compostos da fórmula (Via) ou (VIb) na presença de uma base e,se apropriado, na presença de um solvente, para formar compostos da fórmula (IVa) ouPetição 870180002928, de 12/01/2018, pág. 172/185
- 9/14 (IVb), de acordo com o esquema de reação abaixo (esquema 9):zvvPG—NZ x(V) (Via), (VIb) (IVa), (IVb) nas quaisPG = fenilmetila não substituída ou substituída (sendo que os substituintes independentemente entre si são selecionados do grupo consisitndo em metila, metóxi, nitro, dioxolano), acetila, C1-C4alcoxicarbonila e benziloxicarbonila,Hal = Cl, Brou I,L2 = -C(R8)2-C(R8)2- para compostos da fórmula (IVa) e (Via),L2= -CR9=CR9- para compostos da fórmula (IVb) e (VIb),W, X, L3, R2, R3, R8 e R9 são conforme definido para Fórmula (I) na reivindicação 1;(j)a conversão de compostos da fórmula (IVb) ou (IVc) na presença de hidrogênio, um catalisador e, se apropriado, um solvente, em compostos da fórmula (IVa), de acordo com o esquema de reação abaixo, (esquema 10):(IVb), (IVc) (IVa) nas quaisPG = acetila ou CrC^alcoxicarbonila,L2 = -C(R8)2-C(R8)2- para compostos da fórmula (IVa),L2= -CR9=CR9- para compostos da fórmula (IVb),L2= -C=C- para compostos da fórmula (IVc),W, X, L3, R2, R3, R3 e R9 são definidos para Fórmula (I) na reivindicação 1;Petição 870180002928, de 12/01/2018, pág. 173/185
- 10/14 (k)a conversão de compostos da fórmula (IV), se apropriado na presença de um solvente e, se apropriado, na presença de um ácido ou, se apropriado, na presença de uma base ou, se apropriado, na presença de uma fonte de hidrogênio, em compostos da fórmula (II), de acordo com o esquema de reação abaixo (esquema 11):(iv) (ii) nas quaisPG = acetila, Ct-C^alcoxicarbonila ou benziloxicarbonila,W, X, L2, L3, R2, e R3 são conforme definido para Fórmula (I) na reivindicação 1;(l)conversão de compostos da fórmula (lia’) na presença de um agente de halogenação, se apropriado na presença de um ácido e um solvente, em compostos da fórmula (lia), de acordo com o esquema de reação abaixo (esquema 12):(lia) |_—p3 Agente de halogenação W solvente se apropriado ácido ou base nas quaisL2 = -C(R8)2-C(R8)2-,R2 = I, Br ou Cl para compostos da fórmula (lia),R2 = hidrogênio para compostos da fórmula (lia’),W, X, L3, R3 e R8 são conforme definido para Fórmula (I) na reivindicação 1;(m)a reação de compostos da fórmula (III) com compostos da fórmula (II), se apropriad na presença de um agente de acoplamento, uma base e um solvente, para formar compostos da Fórmula (I), de acordo com esquema de reação abaixo (esquema 13):Petição 870180002928, de 12/01/2018, pág. 174/185
- 11/14 wHN\ z x' , 2 kLLR3 S R2Solvente se apropriado base, se apropriado agente de acoplamentoVb a—A-L1 (I) (II) nas quaisB = OH, cloro, bromo ou iodo,Y = oxigênio,A, W, X, L1, L2, L3, R2, e R3 são conforme definido paraFórmula (I) na reivindicação 1;(n)a conversão de compostos da Fórmula (I) na presença de um agente de sulfurização e, se apropriado, na presença de um solvente, em compostos da Fórmula (I), de acordo com o esquema de reação abaixo (esquema 14):A—LY W —r3 Agente de sulfuração Y w N kkX, ......... ·. xzyX w N—R3X (I) γ = o S R2 solventeA—LY =S Xr2 (I) nas quaisA, W, X, L1, L2, L3, R2, e R3 são conforme definido paraFórmula (I) na reivindicação 1.7. Processo para preparação dos compostos da Fórmula (I), caracterizado pelo fato de que compreendendo pelo menos uma das etapas (o) a (u) abaixo:(o)a conversão da fórmula (XII) na presença de uma base e, se apropriado, um solvente, em alquinos da fórmula (XIII), de acordo com o esquema de reação abaixo (esquema 17):nas quaisPetição 870180002928, de 12/01/2018, pág. 175/185
- 12/14A, W, X, Y, L1 e R2 são conforme definido para Fórmula (I) na reivindicação 1;(p)a reação de alquinos da fórmula (XIII) com um cloreto de trialquilsilila (R10R11R12)SiCI ou triflato de trialquilsilila (R10R11R12)SiOSO2CF3 ou outros agentes de sililação conhecidos na presença de uma base e, se apropriado, um solvente, formando compostos da fórmula (XIV), de acordo com o esquema de reação abaixo (esquema 18):base solventeR10R11R12)SiCIOUR10R11R12)SiOSO2CF3 nas quaisR10, R11 e R12 = C-|-C4 alquila ou fenila,A, W, X, Y, L1 e R2 são conforme definido para Fórmula (I) na reivindicação 1;(q)a reação de alquinos da fórmula (XIII) com um R3-L3haleto emu ma reação de acoplamento C-C opcionalmente catalisada na presença de uma base e, se apropriado, a solvente, para formar compostos da fórmula (lc), de acordo com 0 esquema de reação abaixo (esquema 19):R3-L3-Hal catalisador base solventey.A-L 'Y-r3 (lc) nas quaisHal = Cl, Br ou I,L2=-CeC-,A, W, X, Y, L1 L3, R2 e R3 são definidos para a Fórmula (I) na reivindicação 1;Petição 870180002928, de 12/01/2018, pág. 176/185
- 13/14 (r)a reação de alquinos da fórmula (XIV) com um composto R3-L3-Hal, se apropriado na presença de um catalisador, na presença de uma base e, se necessário, um solvente, para formar compostos da fórmula (Ic), de acordo com o esquema de reação abaixo (esquema 20):R3-L3-Hal catalisador base solventeA-L' (Ic)Ά—R3 nas quaisHal = Cl, Br ou I,L2=-CeC-,R10, R11 e R12 = CrC^alquila ou fenila,A, W, X, Y, L1 L3, R2 e R3 são conforme definido para Fórmula (I) na reivindicação 1;(s)a conversão de aldeídos da fórmula (XII) na presença de uma base ou de um ácido e, se apropriado, um solvente, em compostos da fórmula (lb), de acordo com o esquema de reação abaixo (esquema 21):nas quaisL2=-CR9=CR9-,A, W, X, Y, L1 L3, R2, R3 e R9 são conforme definido para Fórmula (I) na reivindicação 1;(t)a conversão de compostos da fórmula (Ic) na preseça de hidrogênio, um catalisador e, se apropriado, um solvente, em compostos da fórmula (lb), de acordo com o esauema de reação abaixo (esquema 22):Petição 870180002928, de 12/01/2018, pág. 177/185
- 14/14A-L1W N\ x'N //S h2I 2 'L\ 3 3 catalisadorL R solventeR2 (lb) (lc) nas quaisL2= -CR9=CR9- para compostos da fórmula (lb),L2= -C=C- para compostos da fórmula (lc),A, W, X, Y, L1 L3, R2, R3 e R9 são conforme definidos paraFórmula (I) na reivindicação 1;(u)a conversão de compostos da fórmula (lb) ou (lc) na presença de hidrogênio, um catalisador e, se apropriado, um solvente, em compostos da fórmula (la), de acordo com o esquema de reação abaixo (esquema 23):Y, W N-^/1 hhXA-L1 X S-^X,Ύ-r3 catalisador solvente khXA-L1 X S-^\,Ύ- R3 (lc) -* (la) (lb) -* (la) nas quaisL2 = -C(R8)2-C(R8)2- para compostos da fórmula (la),L2= -CR9=CR9- para compostos da fórmula (lb),L2= -C=C- para compostos da fórmula (lc),A, W, X, Y, L1 L3, R2, R3, R8 e R9 são conforme definidos para Fórmula (I) na reivindicação 1.Petição 870180002928, de 12/01/2018, pág. 178/185
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP08165625 | 2008-10-01 | ||
| PCT/EP2009/006755 WO2010037479A1 (de) | 2008-10-01 | 2009-09-18 | Heterocyclyl substituierte thiazole als pflanzenschutzmittel |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| BRPI0920767A2 BRPI0920767A2 (pt) | 2015-08-18 |
| BRPI0920767A8 BRPI0920767A8 (pt) | 2016-05-24 |
| BRPI0920767B1 true BRPI0920767B1 (pt) | 2018-07-17 |
Family
ID=41279299
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0920767A BRPI0920767B1 (pt) | 2008-10-01 | 2009-09-18 | tiazóis substituídos por heterociclila como agentes protetores de cultura, seus usos e seus processos de preparação, composições e seu processo de preparação, e método para combate a fungos nocivos fitopatogênicos |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US7943774B2 (pt) |
| EP (1) | EP2334669B1 (pt) |
| JP (1) | JP5785495B2 (pt) |
| KR (1) | KR20110067052A (pt) |
| CN (1) | CN102216296B (pt) |
| AR (1) | AR073317A1 (pt) |
| BR (1) | BRPI0920767B1 (pt) |
| CO (1) | CO6361854A2 (pt) |
| MX (1) | MX2011003151A (pt) |
| WO (1) | WO2010037479A1 (pt) |
| ZA (1) | ZA201102506B (pt) |
Families Citing this family (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TWI428091B (zh) * | 2007-10-23 | 2014-03-01 | Du Pont | 殺真菌劑混合物 |
| AU2009322486A1 (en) * | 2008-12-02 | 2010-06-10 | E. I. Du Pont De Nemours And Company | Fungicidal heterocyclic compounds |
| CN101594336B (zh) | 2009-06-19 | 2012-12-19 | 中兴通讯股份有限公司 | 一种定位参考信号的发送方法 |
| WO2011051243A1 (en) * | 2009-10-29 | 2011-05-05 | Bayer Cropscience Ag | Active compound combinations |
| KR20120101019A (ko) | 2009-10-30 | 2012-09-12 | 바이엘 크롭사이언스 아게 | 헤테로아릴피페리딘 및 -피페라진 유도체 |
| MX2012007200A (es) | 2009-12-21 | 2012-07-10 | Bayer Cropscience Ag | Bis(difluorometil)pirazoles como fungicidas. |
| BR112012027762B1 (pt) | 2010-04-28 | 2018-06-05 | Bayer Intellectual Property Gmbh | Derivados de cetoheteroarilpiperidina e - piperazina como fungicidas |
| US8815775B2 (en) * | 2010-05-18 | 2014-08-26 | Bayer Cropscience Ag | Bis(difluoromethyl)pyrazoles as fungicides |
| EP2576539B1 (de) | 2010-05-27 | 2017-12-13 | Bayer CropScience AG | Pyridinylcarbonsäure derivate als fungizide |
| US20120122928A1 (en) | 2010-08-11 | 2012-05-17 | Bayer Cropscience Ag | Heteroarylpiperidine and -Piperazine Derivatives as Fungicides |
| US8759527B2 (en) | 2010-08-25 | 2014-06-24 | Bayer Cropscience Ag | Heteroarylpiperidine and -piperazine derivatives as fungicides |
| EP2423210A1 (de) | 2010-08-25 | 2012-02-29 | Bayer CropScience AG | Heteroarylpiperidin- und -piperazinderivate als Fungizide |
| EP2632922B1 (de) | 2010-10-27 | 2019-02-27 | Bayer CropScience Aktiengesellschaft | Heteroarylpiperidin und -piperazinderivate als fungizide |
| WO2012104273A1 (de) | 2011-02-01 | 2012-08-09 | Bayer Cropscience Ag | Heteroarylpiperidin und -piperazinderivate als fungizide |
| US10004232B2 (en) | 2011-09-15 | 2018-06-26 | Bayer Intellectual Property Gmbh | Piperidine pyrazoles as fungicides |
| DK2797899T3 (en) | 2011-12-27 | 2016-04-04 | Bayer Ip Gmbh | Heteroarylpiperidin and -piperazinderivater as fungicides |
| US9266876B2 (en) | 2012-02-02 | 2016-02-23 | Actelion Pharmaceuticals Ltd. | 4-(benzoimidazol-2-yl)-thiazole compounds and related aza derivatives |
| MX355542B (es) * | 2012-08-30 | 2018-04-20 | Bayer Cropscience Ag | Procedimiento de descarboxilacion de derivados de acido 3,5-bis(haloalquil)-pirazol-4-carboxilico. |
| EP2801575A1 (en) | 2013-05-07 | 2014-11-12 | Bayer CropScience AG | Heteroaryldihydropyridine derivatives as fungicides |
| WO2014206896A1 (en) | 2013-06-24 | 2014-12-31 | Bayer Cropscience Ag | Piperidinecarboxylic acid derivatives as fungicides |
| EA030067B1 (ru) | 2013-07-22 | 2018-06-29 | Идорсиа Фармасьютиклз Лтд | Производные 1-(пиперазин-1-ил)-2-([1,2,4]триазол-1-ил)этанона |
| US9924721B2 (en) | 2013-08-28 | 2018-03-27 | Bayer Cropscience Aktiengesellschaft | Malonic ester derivatives of heteroarylpiperidines and -piperazines as fungicides |
| PT3122746T (pt) | 2014-03-24 | 2018-07-27 | Bayer Cropscience Ag | Derivados de fenilpiperidinacarboxamida como fungicidas |
| AR099789A1 (es) | 2014-03-24 | 2016-08-17 | Actelion Pharmaceuticals Ltd | Derivados de 8-(piperazin-1-il)-1,2,3,4-tetrahidro-isoquinolina |
| WO2016024350A1 (ja) | 2014-08-13 | 2016-02-18 | 株式会社エス・ディー・エス バイオテック | 縮合11員環化合物及びそれらを含有する農園芸用殺菌剤 |
| WO2016094307A1 (en) | 2014-12-08 | 2016-06-16 | The Research Foundation For The State University Of New York | Anti-fungals targeting the synthesis of fungal shingolipids |
| AR103399A1 (es) | 2015-01-15 | 2017-05-10 | Actelion Pharmaceuticals Ltd | Derivados de (r)-2-metil-piperazina como moduladores del receptor cxcr3 |
| JP6337218B2 (ja) | 2015-01-15 | 2018-06-06 | イドーシア ファーマシューティカルズ リミテッドIdorsia Pharmaceuticals Ltd | Cxcr3受容体調節剤としてのヒドロキシアルキル−ピペラジン誘導体 |
| CN108602765B (zh) | 2016-02-08 | 2022-05-03 | 高文有限公司 | 1,2-苯二甲醇化合物的制造方法 |
| KR102605762B1 (ko) | 2016-02-08 | 2023-11-27 | 고완 크롭 프로텍션 리미티드 | 살균성 조성물 |
| WO2018232298A1 (en) | 2017-06-16 | 2018-12-20 | The Research Foundation For The State University Of New York | Anti-fungals compounds targeting the synthesis of fungal sphingolipids |
| CN108558857B (zh) * | 2018-05-07 | 2021-07-02 | 南开大学 | 一类噻唑哌啶呋喃酮衍生物及其制备方法和用途 |
Family Cites Families (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4272417A (en) * | 1979-05-22 | 1981-06-09 | Cargill, Incorporated | Stable protective seed coating |
| US4245432A (en) * | 1979-07-25 | 1981-01-20 | Eastman Kodak Company | Seed coatings |
| US4808430A (en) * | 1987-02-27 | 1989-02-28 | Yazaki Corporation | Method of applying gel coating to plant seeds |
| GB8810120D0 (en) * | 1988-04-28 | 1988-06-02 | Plant Genetic Systems Nv | Transgenic nuclear male sterile plants |
| CA2218526C (en) * | 1995-04-20 | 2012-06-12 | American Cyanamid Company | Structure-based designed herbicide resistant products |
| US5876739A (en) * | 1996-06-13 | 1999-03-02 | Novartis Ag | Insecticidal seed coating |
| US6503904B2 (en) * | 1998-11-16 | 2003-01-07 | Syngenta Crop Protection, Inc. | Pesticidal composition for seed treatment |
| US6660690B2 (en) * | 2000-10-06 | 2003-12-09 | Monsanto Technology, L.L.C. | Seed treatment with combinations of insecticides |
| US20020134012A1 (en) | 2001-03-21 | 2002-09-26 | Monsanto Technology, L.L.C. | Method of controlling the release of agricultural active ingredients from treated plant seeds |
| GB0230162D0 (en) * | 2002-12-24 | 2003-02-05 | Metris Therapeutics Ltd | Compounds useful in inhibiting angiogenesis |
| FR2856685B1 (fr) * | 2003-06-25 | 2005-09-23 | Merck Sante Sas | Derives de thiazolylpiperidine, leurs procedes de preparation et les compositions pharmaceutiques qui les contiennent |
| WO2006032322A1 (en) | 2004-09-20 | 2006-03-30 | 4Sc Ag | NOVEL HETEROCYCLIC NF-κB INHIBITORS |
| TW200738701A (en) * | 2005-07-26 | 2007-10-16 | Du Pont | Fungicidal carboxamides |
| MEP3508A (xx) * | 2005-08-24 | 2010-02-10 | Pioneer Hi Bred Int | Kompozicije koje obezbjeđuju otpornost na više hibricida i njihov postupak upotrebe |
| MX2008002802A (es) * | 2005-08-31 | 2008-04-07 | Monsanto Technology Llc | Secuencias nucleotidicas que codifican proteinas insecticidas. |
| JP2009509988A (ja) * | 2005-09-29 | 2009-03-12 | サノフィ−アベンティス | フェニル−及びピリジニル−1,2,4−オキサジアゾロン誘導体、その製造方法、及び医薬品としてのその使用 |
| EP1832586A1 (en) | 2006-03-10 | 2007-09-12 | Oridis Biomed Forschungs- und Entwicklungs GmbH | Thiazole-piperidine derivatives in treatment of diseases of liver and the pancreas |
| EP1834954A1 (en) | 2006-03-15 | 2007-09-19 | 4Sc Ag | Thiazoles as NF-kB Inhibitors (proteasome inhibitors) |
| WO2007115805A2 (en) | 2006-04-05 | 2007-10-18 | European Molecular Biology Laboratory (Embl) | Aurora kinase inhibitors |
| KR101130380B1 (ko) | 2006-06-13 | 2012-04-23 | 상하이 인스티튜트 오브 마테리아 메디카 차이니즈 아카데미 오브 싸이언시즈 | 헤테로시클릭 비뉴클레오시드 화합물, 그의 제조방법, 약학적 조성물 및 항바이러스성 약제로서의 용도 |
| WO2008013622A2 (en) * | 2006-07-27 | 2008-01-31 | E. I. Du Pont De Nemours And Company | Fungicidal azocyclic amides |
| US7638541B2 (en) * | 2006-12-28 | 2009-12-29 | Metabolex Inc. | 5-ethyl-2-{4-[4-(4-tetrazol-1-yl-phenoxymethyl)-thiazol-2-yl]-piperidin-1-yl}-pyrimidine |
| WO2008091594A2 (en) | 2007-01-24 | 2008-07-31 | E. I. Du Pont De Nemours And Company | Fungicidal mixtures |
| JP5337711B2 (ja) * | 2007-01-25 | 2013-11-06 | イー・アイ・デュポン・ドウ・ヌムール・アンド・カンパニー | 殺菌性アミド |
| TWI428091B (zh) | 2007-10-23 | 2014-03-01 | Du Pont | 殺真菌劑混合物 |
-
2009
- 2009-09-18 EP EP09778607.3A patent/EP2334669B1/de not_active Not-in-force
- 2009-09-18 BR BRPI0920767A patent/BRPI0920767B1/pt not_active IP Right Cessation
- 2009-09-18 JP JP2011529464A patent/JP5785495B2/ja not_active Expired - Fee Related
- 2009-09-18 WO PCT/EP2009/006755 patent/WO2010037479A1/de not_active Ceased
- 2009-09-18 KR KR1020117009858A patent/KR20110067052A/ko not_active Withdrawn
- 2009-09-18 CN CN200980139002.6A patent/CN102216296B/zh not_active Expired - Fee Related
- 2009-09-18 MX MX2011003151A patent/MX2011003151A/es active IP Right Grant
- 2009-09-25 AR ARP090103699A patent/AR073317A1/es not_active Application Discontinuation
- 2009-09-29 US US12/568,961 patent/US7943774B2/en not_active Expired - Fee Related
-
2011
- 2011-03-25 CO CO11036972A patent/CO6361854A2/es active IP Right Grant
- 2011-04-05 ZA ZA2011/02506A patent/ZA201102506B/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| BRPI0920767A2 (pt) | 2015-08-18 |
| JP2012504561A (ja) | 2012-02-23 |
| EP2334669A1 (de) | 2011-06-22 |
| WO2010037479A1 (de) | 2010-04-08 |
| US20100137245A1 (en) | 2010-06-03 |
| MX2011003151A (es) | 2011-04-27 |
| ZA201102506B (en) | 2012-06-27 |
| JP5785495B2 (ja) | 2015-09-30 |
| AR073317A1 (es) | 2010-10-28 |
| KR20110067052A (ko) | 2011-06-20 |
| CO6361854A2 (es) | 2012-01-20 |
| CN102216296A (zh) | 2011-10-12 |
| BRPI0920767A8 (pt) | 2016-05-24 |
| CN102216296B (zh) | 2015-03-18 |
| EP2334669B1 (de) | 2015-12-23 |
| US7943774B2 (en) | 2011-05-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BRPI0920767B1 (pt) | tiazóis substituídos por heterociclila como agentes protetores de cultura, seus usos e seus processos de preparação, composições e seu processo de preparação, e método para combate a fungos nocivos fitopatogênicos | |
| KR101797060B1 (ko) | 살진균제로서의 헤테로아릴피페리딘 및 -피페라진 유도체 | |
| KR101797074B1 (ko) | 살진균제로서의 헤테로아릴 피페리딘 및 헤테로아릴 피페라진 유도체 | |
| KR101807640B1 (ko) | 살진균제로서의 헤테로아릴피페리딘 및 -피페라진 유도체 | |
| ES2661849T3 (es) | Piperidinpirazoles como fungicidas | |
| ES2613066T3 (es) | Derivados de cetoheteroarilpiperidina y -piperazina como fungicidas | |
| JP6345844B2 (ja) | 殺菌剤としてのヘテロアリールピペリジン誘導体及びヘテロアリールピペラジン誘導体 | |
| KR20100135952A (ko) | 식물 보호제로서의 티아졸-4-카복실산 에스테르 및 티오에스테르 | |
| KR20120102135A (ko) | 살진균제로 사용되는 비스(디플루오로메틸)피라졸 | |
| KR20120050434A (ko) | 살진균제로서의 티아졸릴피페리딘 유도체 | |
| CN102292334A (zh) | 噻唑基肟醚和腙植物保护剂 | |
| BR112013019667B1 (pt) | Compostos derivados de heteroaril-piperidina e -piperazina, seus usos, composição, processos de produção de compostos e de composições, método para o controle de fungos fitopatogênicos prejudiciais | |
| ES2729753T3 (es) | Derivados de heteroarilpiperidina y piperazina como fungicidas | |
| AU2015205864B2 (en) | Heteroarylpiperidine and -piperazine derivatives as fungicides | |
| BR122018001911B1 (pt) | compostos derivados de heteroaril-piperidina e -piperazina, composição os compreendendo, método para o controle de fungos fitopatogênicos nocivos, processo para a produção de composições e utilização dos compostos |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B25A | Requested transfer of rights approved |
Owner name: BAYER INTELLECTUAL PROPERTY GMBH (DE) |
|
| B07A | Application suspended after technical examination (opinion) [chapter 7.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] | ||
| B21F | Lapse acc. art. 78, item iv - on non-payment of the annual fees in time |
Free format text: REFERENTE A 13A ANUIDADE. |
|
| B24J | Lapse because of non-payment of annual fees (definitively: art 78 iv lpi, resolution 113/2013 art. 12) |
Free format text: EM VIRTUDE DA EXTINCAO PUBLICADA NA RPI 2688 DE 12-07-2022 E CONSIDERANDO AUSENCIA DE MANIFESTACAO DENTRO DOS PRAZOS LEGAIS, INFORMO QUE CABE SER MANTIDA A EXTINCAO DA PATENTE E SEUS CERTIFICADOS, CONFORME O DISPOSTO NO ARTIGO 12, DA RESOLUCAO 113/2013. |