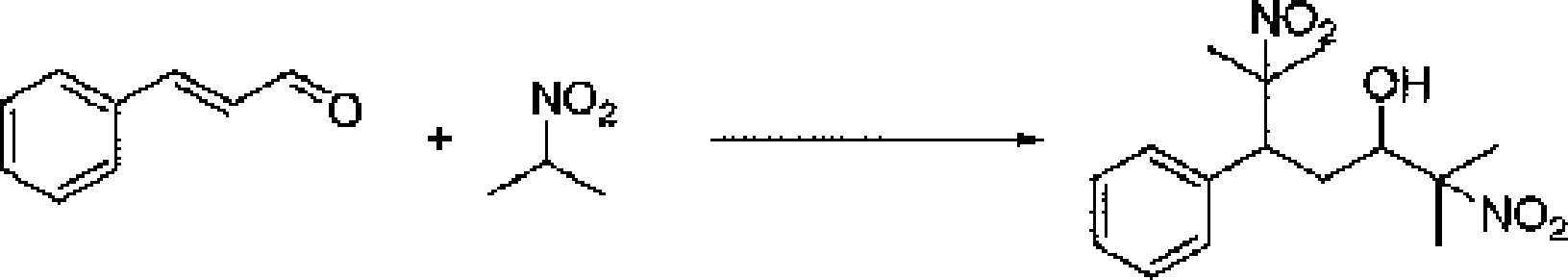“FORMULAÇÃO DE REVESTIMENTO AQUOSA”
Campo da Invenção [0001] A presente invenção diz respeito a uma nova classe de compostos, isto é, diamino álcoois, um processo para produzir os mesmos, e seus usos como dispersantes em formulações de revestimento.
Fundamentos da Invenção [0002] Os compostos de amina simples são conhecidos por fornecer propriedades neuralizantes, dispersantes e endurecedoras quando adicionados a revestimentos, pastas minerais e formulação epóxi. Os métodos para a fabricação de composto de amina simples são bem documentados e conhecidos na técnica e quando o objetivo é preparar aminas primárias, as vias preferidas frequentemente envolvem compostos de nitroálcool intermediários. Por várias razões, deve ser vantajoso ter compostos com mais do que um grupo amino e teor de composto orgânico volátil (“VOC”).
[0003] Os compostos orgânicos voláteis são compostos químicos orgânicos que têm pressões de vapor altas o bastante sob condições normais (isto é, 1 atmosfera e 25°C) para vaporizar significantemente e entrar na atmosfera. Estes incluem uma variedade de produtos químicos, muitos dos quais têm efeitos de saúde adversos e são emitidos por uma ampla variedade de produtos que incluem mas não são limitados a: tintas e vernizes, retiradores de tinta, suprimentos de limpeza, pesticidas, materiais de construção e mobílias, equipamento de escritório tais como copiadoras e impressoras, fluidos de correção e papel copiador sem carbono, materiais gráficos e craft incluindo colas e adesivos, marcadores permanentes, e soluções fotográficas. A minimização de teor de VOC tornou-se foco de atenção pública bem como regulação do governo.
[0004] Os processos para a fabricação dos compostos de nitroálcool intermediários, são conhecidos e tipicamente envolvem a reação de nitroaldol (Reação de Henry) entre nitroalcanos e aldeídos. Existe referência ocasional à preparação de dinitro álcoois que envolve uma adição de Michael tandem e Reação de Henry de um nitroalcano com um aldeído α,β-insaturado. Por exemplo, ver
Petição 870190029238, de 27/03/2019, pág. 9/29
2/21 “Secondary dinitro alcohols,” Smith, Curtis W. (Shell Development Co.) 1949 e Patente U. S. N° 2,475,996, que descreve a fabricação do nitro álcool 2,5,6-trimetil-
2,6-dinitro-3-heptanol. Este nitro álcool também é preparado como um intermediário para a fabricação de um inibidor de vasopeptidase, como debatido em Efficient Asymmetric Synthesis of the Vasopeptidase Inhibitor BMS-189921 de Janak Singh et al., Org. Lett. (2003), 5, 17, 3155-3158. Além disso, a fabricação do composto de nitro álcool 2,6-dinitro-5-fenil-heptan-3-ol foi descrito em David St. Clair Black et. al. Australian Journal of Chemistry, 1976, 29(11), 2511. Também é bem estabelecido, compostos de nitro álcool podem ser facilmente convertidos aos compostos de aminoálcool pela hidrogenação com o hidrogênio em um catalisador adequado, por exemplo níquel de Raney ou um catalisador com base em platina ou paládio (Pt ou Pd na forma elementar ou como óxidos, com ou sem suportes, por exemplo, carbono). Aqueles habilitados na técnica também estão cientes que outros agentes redutores que reduzirão nitroalcanos a aminas primárias incluem combinações de metal/ácido, por exemplo, ferro/ácido acético e hidretos de alumínio. Os agentes redutores preferidos incluem gás hidrogênio em combinação com qualquer um dos catalisadores: níquel de Raney, platina ou paládio.
[0005] Os compostos de diaminoálcool e seus usos, por outro lado, são representados de maneira não corrente na técnica anterior.
[0006] Os amino álcoois tais como 2-amino-2-metil-1-propanol (“AMP”) são usados em formulações de tinta com base aquosa com aminas neutralizadoras que co-dispersam eficazmente os pigmentos. Em muitas regiões fabricantes de tintas estão encarando regulamentações adicionais para reduzir o teor de VOC de suas formulações e a preferência do consumidor é conduzida no desenvolvimento de formulações de tinta com baixo odor. As aminas neutralizadoras, tais como AMP são 100 % voláteis de acordo com um Método de Teste EPA modificado 24 e, quando usado em uma formulação de tinta de VOC baixo, o odor da amina de AMP torna-se mais perceptível. Duas opções como neutralizadores que são, por definição, não contribuidores de VOC são amônia e bases inorgânicas, tais como KOH. Amônia, enquanto um neutralizador eficiente, tem um odor muito forte e é, portanto,
Petição 870190029238, de 27/03/2019, pág. 10/29
3/21 inadequado para o uso em formulações de tinta de odor baixo. O uso de bases inorgânicas, tais como KOH, produzem revestimento com fricção deficiente e resistência a desfiguração. Adicionalmente, nem a amônia e nem as bases inorgânicas têm a capacidade de auxiliar na dispersão de pigmentos na formulação. [0007] Existe uma necessidade quanto a amino álcoois neutralizadores eficientes orgânicos que são co-dispersantes eficazes com nenhum VOC ou baixo e têm nenhum odor de amina ou muito baixo. Os novos compostos de diaminoálcool descritos acima e ainda em detalhes a seguir, são aminas multifuncionais de odor baixo excelentes com o benefício de não ter nenhum VOC ou baixo como medido por um método similar ao Método de Teste EPA 24 que é o método requerido para medir o VOC de uma formulação de tinta acabada. Um benefício adicional destes produtos é que se projetando este pode-se apenas conter grupos funcionais de amina primária que não podem gerar compostos N-nitrosos tóxicos. Sumário da Invenção [0008]
A presente invenção fornece um composto de diamino álcool tendo a fórmula:
[0009] em que R é independentemente hidrogênio, alquila, arila ou -CH2OH; R1 é independentemente hidrogênio, alquila ou -CH2OH; alternativamente, R e R1 podem ser ligados juntos para formar um cicloalquila; R2 é independentemente hidrogênio, metila, alquila, fenila ou fenila substituída; R3 é independentemente hidrogênio, alquila, fenila ou fenila substituída ou -CH2OH; R4 é independentemente hidrogênio, alquila ou -CH2OH e alternativamente, R3 e R4 podem ser ligados juntos para formar um cicloalquila.
[0010] A presente invenção também fornece um processo para a produção do dito composto de diaminoálcool, que compreende reagir (1) um nitroalcano primário ou secundário e (2) um aldeído α,β-insaturado para formar um dinitro álcool e então
Petição 870190029238, de 27/03/2019, pág. 11/29
4/21 ainda reduzir o nitro álcool ao diamino álcool correspondente sob condições de hidrogenação e na presença de um catalisador. A reação é realizada sob condições em que a adição de Michael do nitroalcano ocorre mais rapidamente do que a Reação de Henry, permitindo que as reações sequenciais para produzir um dinitroálcool. O (1) nitroalcano e o (2) aldeído são fornecidos em uma razão molar de 2:1 durante a primeira etapa de reação que produz o dinitro álcool. O nitroalcano primário ou secundário pode ser um nitroalcano C1-C. O aldeído α,β-insaturado pode ser selecionado do grupo que consiste de: acroleína, crotonaldeído e cinamaldeído. [0011] Quando o produto desejado é um composto de diamino poli-álcool, o (1) nitroalcano é um nitroalcano primário e o processo para a produção do composto de diamino poli-álcool compreende adicionalmente, após reagir o (1) nitroalcano primário e (2) aldeído α,β-insaturado, mas antes de reduzir o nitro álcool resultante, ainda reage o nitro álcool resultante com (3) um aldeído, tal como formaldeído, para formar um composto de dinitro poli-álcool, que, então, ainda é reduzido sob condições de hidrogenação e na presença de um catalisador.
[0012] A presente invenção ainda fornece uma formulação de revestimento aquosa com o composto de diamino álcool. Mais particularmente, a formulação de revestimento aquosa compreende: (a) 25 a 99 % em peso de um carreador aquoso que compreende água e pelo menos uma resina; (b) até 20 % em peso de um pigmento e (c) 0,01 a 5 % em peso do dito composto de diaminoálcool, em que todas as porcentagens em peso são fundamentadas no peso total da formulação de revestimento aquosa. A resina é um polímero que compreende unidades derivadas de pelo menos um monômero selecionado do grupo que consiste de: acrilatos de alquila, metacrilatos de alquila, estireno-butadieno, ésteres vinílicos de um ácido alifático, ésteres de ácido acrílico, ésteres de ácido metacrílico de um álcool e hidrocarbonetos mono e di-etilenicamente insaturados. O pigmento pode ser um ou mais de: dióxido de titânio e outros pigmentos de titânio, chumbo branco, óxido de zinco, sulfeto de zinco, sulfato de bário, carbonato de cálcio, litopona, sílica, talco, mica, argilas, óxido de ferro, negro de fumo, sulfeto de cádmio, vermelho toluidina, laranja cromo, amarelo cromo, verde cromo.
Petição 870190029238, de 27/03/2019, pág. 12/29
5/21
Breve Descrição dos Desenhos [0013] Um entendimento mais completo da presente invenção será conseguido por referência à figura anexa que fornece gráficos de barra comparando-se as características de formulações de revestimento preparadas com um diamino álcool da presente invenção e com vários compostos amina comercialmente disponíveis. Descrição Detalhada da Invenção [0014] Uma classe nova e útil de composto amino, isto é, diamino álcoois, foi descoberta, juntos com os processos para a sua fabricação. Estes compostos são produzidos por Reação de Michael e de Reação tandem de nitroalcano com um ou mais aldeídos α,β-insaturado aldeídos e, opcionalmente, pós-reagido com um aldeído tal como formaldeído. Como um resultado, os compostos de diaminoálcool produzidos têm grupos amina primários, preferivelmente ligados aos átomos de carbono terciários, com teor baixo dos compostos orgânicos voláteis (VOCs). Estes podem ser representados pela seguinte fórmula:

[0015] em que R é independentemente hidrogênio, alquila, arila ou -CH2OH; R1 é independentemente hidrogênio, alquila ou -CH2OH; alternativamente, R e R1 podem ser ligados juntos para formar um cicloalquila; R2 é independentemente hidrogênio, metila, alquila, fenila ou fenila substituída; R3 é independentemente hidrogênio, alquila, fenila ou fenila substituída ou -CH2OH; R4 é independentemente hidrogênio, alquila ou -CH2OH e alternativamente, R3 e R4 podem ser ligados juntos para formar um cicloalquila, [0016] A categoria precedente de diamino álcoois inclui vários graus de poliálcoois (“polióis”) bem como diamino mono-álcoois simples. Os diamino monoálcoois mais simples devem ter a seguinte fórmula:
Petição 870190029238, de 27/03/2019, pág. 13/29
6/21
R3
R h2n nh2
OH [0017] em que R é independentemente hidrogênio, alquila, fenila ou fenila substituída; Ri é independentemente hidrogênio ou alquila; alternativamente, R e Ri podem ser ligados juntos para formar um cicloalquila; R2 é independentemente hidrogênio, alquila ou fenila ou fenila substituído; R3 é independentemente hidrogênio, alquila ou arila; R4 é independentemente hidrogênio ou alquila e alternativamente, R3 e R4 podem ser ligados juntos para formar um cicloalquila.
[0018] Os diamino mono-álcoois da presente invenção podem ser produzidos pela reação de um nitroalcano e um aldeído α,β-insaturado que produz um composto de dinitro álcool intermediário. Esta reação é tipicamente operada em temperaturas entre 0°C e 100°C sob pressão atmosférica, por exemplo, sem limitação entre 0°C e 50°C. Os requerentes observaram surpreendente e convenientemente que esta reação precede sequencialmente com a adição de Michael de nitroalcano à olefina que ocorre primeiro, seguido pela reação de aldol (Henry) em que o segundo nitroalcano é adicionado ao aldeído, para produzir uma espécie simples de intermediário de dinitro mono-álcool.
[0019] O nitroalcano pode ser um nitroalcano primário ou secundário tendo a fórmula:
NO2 [0020] em que R é hidrogênio, R1 é hidrogênio, alquila, fenila ou fenila substituída ou em que R é alquila, fenila ou fenila substituído, e R1 é alquila ou R e R1 podem ser ligados juntos para formar um cicloalquila. Por exemplo, sem limitação, nitrometano, nitroetano, 2-nitropropano, nitrocicloexano etc. são todos nitroalcanos adequados para o uso como materiais de partida para preparar os
Petição 870190029238, de 27/03/2019, pág. 14/29
7/21 compostos de diaminoálcool de acordo com a presente invenção. Mais particularmente, o nitroalcano primário ou secundário pode ser um nitroalcano CiC20, um nitroalcano C1-C10 ou ainda um nitroalcano C2-C6.
[0021] Os aldeídos α,β-insaturados adequados têm a seguinte fórmula:
H
[0022] em que R é hidrogênio, metila (alquila), fenila ou fenila substituída. Os aldeídos insaturados incluem, mas não são limitados a, acroleína, crotonaldeído, cinamaldeído, derivados de cinamaldeído substituído no anel aromático, etc.
[0023] A reação de Michael-Henry sequencial precedente entre o nitroalcano e aldeído insaturado ocorre na presença de um catalisador adequado que inclui, mas não limitado a, bases orgânicas, tais como 1,8-Diazabiciclo[5.4.0]undec-7-eno (“DBU”), 2-dimetilamino-2-metil-1-propanol (“DMAMP”), trimetilamina (TMA), dimetilisopropilamina (DMIPA), Ν,Ν,Ν',Ν'-tetrametilguanidina (TMG), base de Verkade, etc. Alternativamente, as bases inorgânicas, tais como carbonato de potássio, e hidróxido de sódio também podem ser usados como catalisadores para a reação de Michael-Henry sequencial descrita acima.
[0024] Os materiais de partida são fornecidos em uma razão molar de nitroalcano a aldeído de tipicamente 2:1. A reação pode ser realizada com ou sem um solvente, de acordo com a preferência do prático. Os solventes adequados incluem mas não são limitados a tetra-hidrofurano, 2-metiltetra-hidrofurano, dioxano. [0025] Quando o produto desejado é um composto de diamino poli-álcool, o (1) nitroalcano é um nitroalcano primário e o processo para a produção do composto de diamino poli-álcool compreende adicionalmente, após reagir o (1) nitroalcano primário e (2) aldeído α,β-insaturado, mas antes de reduzir o nitro álcool resultante, ainda reage o nitro álcool resultante com (3) um aldeído, tal como formaldeído, para formar um composto de dinitro poli-álcool, que, então, ainda é reduzido sob condições de hidrogenação e na presença de um catalisador.
[0026] Mais particularmente, a produção de compostos de diamino poli-álcool
Petição 870190029238, de 27/03/2019, pág. 15/29
8/21 (poliol) procede como segue: (A) reagir (1) um nitroalcano primário e (2) um aldeído α,β-insaturado aldeído para formar um dinitroálcool; (B) ainda reage o dinitroálcool com (3) um aldeído, tal como formaldeído, para formar um produto dinitro poli-álcool (por exemplo, um dinitro-diálcool ou dinitro-triálcool) e (C) então, ainda reduzir o produto de dinitro poli-álcool ao produto de diamino poli-álcool correspondente sob condições de hidrogenação, na presença de um catalisador. A reação é realizada sob condições em que a adição de Michael do nitroalcano ocorre mais rapidamente do que a Reação de Henry (isto é, temperaturas entre 0°C e 100°C sob pressão atmosférica, por exemplo, sem limitação, entre 0°C e 50°C), permitindo que as reações sequenciais produzam o dinitro poli-álcool. O (1) nitroalcano e o (2) aldeído são fornecidos em uma razão molar de 2:1 durante a primeira etapa de reação que produz o dinitro álcool. O nitroalcano primário pode ser um nitroalcano C1-C20 primário, por exemplo, sem limitação, um nitroalcano C1-C10 primário. O aldeído α,βinsaturado pode ser selecionado do grupo que consiste de: acroleína, crotonaldeído, cinamaldeído e derivados de cinamaldeído substituído no anel aromático.
[0027] A reação subsequente do dinitro álcool com um segundo aldeído, tal como formaldeído, ocorre após a finalização da reação para formar o nitro álcool foi confirmada (por exemplo, tal como por métodos analíticos conhecido por pessoas de habilidade comum na técnica que inclui, mas não limitado a, cromatografia gasosa cromatografia líquida de alto desempenho). A razão do formaldeído ao dinitro álcool é tipicamente 2:1 para esta etapa de reação sequencial. Novamente, esta reação pode ser realizada com ou sem o solvente, de acordo com a preferência do prático, tal como, sem limitação, tetra-hidrofurano, 2-metiltetra-hidrofurano, dioxano.
[0028] O composto de dinitro álcool intermediário produzido pela reação de Michael-Henry sequencial descrita acima tem a seguinte fórmula:
Petição 870190029238, de 27/03/2019, pág. 16/29
9/21 [0029] em que R é independentemente hidrogênio, alquila, arila ou -CH2OH; R1 é independentemente hidrogênio, alquila ou -CH2OH; alternativamente, R e R1 podem ser ligados juntos para formar um cicloalquila; R2 é independentemente hidrogênio, metila, alquila, fenila ou fenila substituída; R3 é independentemente hidrogênio, alquila, fenila ou fenila substituída ou -CH2OH; R4 é independentemente hidrogênio, alquila ou -CH2OH e alternativamente, R3 e R4 podem ser ligados juntos para formar um cicloalquila.
[0030] Em uma forma de realização particular, o nitroalcano é 2-nitropropano e o aldeído α,β-insaturado é crotonaldeído ou cinamaldeído, que deve produzir um composto de dinitro mono-álcool.
[0031] O intermediário de dinitro álcool, mono- ou poli-álcool, ainda é então reduzido sob condições de hidrogenação na presença de um catalisador adequado para produzir o diamino álcool desejado que compreende dois grupos amino, cada um dos quais é ligado a um átomo de carbono terciário. Os catalisadores de desidrogenação adequados incluem, sem limitação, níquel de Raney, ou um catalisador com base em platina ou paládio, (por exemplo, platina ou paládio na forma elementar ou como óxidos, com ou sem suportes, por exemplo, carbono). Outros agentes de redução adequados incluem, sem limitação, combinações de metal/ácido, por exemplo, ferro/ácido acético e hidretos de alumínio. Um exemplo de um sistema de catalisador de hidrogenação adequado para o uso de acordo com a presente invenção é gás hidrogênio em combinação com qualquer um de níquel de Raney, platina ou paládio.
[0032] A hidrogenação de dinitro álcool para produzir o diaminoálcool pode ser realizada em pressões entre 100 e 1000 libras por polegada quadrada (“psi”) (6,89 e 68,95 bar) e temperaturas entre 30°C e 100°C. Um solvente pode ser usado, tal como, sem limitação, tetra-hidrofurano ou metanol.
[0033] Os compostos de diaminoálcool resultantes fornecem características melhoradas quando usados como um dispersante em formulações de revestimento tal como, sem limitação, tintas e películas com base aquosa. As formulações de revestimento aquosas em que os compostos de diaminoálcool da presente invenção
Petição 870190029238, de 27/03/2019, pág. 17/29
10/21 são usados, em vez das aminas previamente conhecidas, tais como AMP, têm teor baixo de VOC e odor baixo enquanto ainda resulta e dispersão boa dos pigmentos na formulação.
[0034] Por exemplo, em uma forma de realização, uma formulação de revestimento aquosa de acordo com a presente invenção, pode compreender (a) até 99 % em peso de um carreador aquoso que compreende água e pelo menos uma resina; (b) até 20 % em peso de um pigmento e (c) 0,01 a 5 % em peso de um dispersante que compreende um composto de diamino álcool tendo a fórmula:
[0035] em que R é independentemente hidrogênio, alquila, arila, ou -CH2OH; R1 é independentemente hidrogênio, alquila, ou -CH2OH; alternativamente, Re Ri pode ser ligado junto para formar um cicloalquila; R2 é independentemente hidrogênio, metila, alquila, fenila ou fenila substituída; R3 é independentemente hidrogênio, alquila, fenila ou fenila substituída, ou -CH2OH; R4é independentemente hidrogênio, alquila, ou -CH2OH e alternativamente, R3 e R4 pode ser ligado junto para formar um cicloalquila; em que todas as porcentagens em peso são fundamentadas no peso total da formulação de revestimento aquosa.
[0036] Muitos tipos de resinas são conhecidos e usados no carreador aquoso das formulações de revestimento aquosas. Particularmente comum são aqueles com base em um látex de polímero de acrilato, em que o polímero de acrilato é um éster de alquila inferior, tal como a metila, etila ou éster de butila, dos ácidos acrílicos e metacrílicos e copolímeros de tais ésteres com outros monômeros co-polimerizáveis etilinicamente insaturados que são conhecidos na técnica a ser adequado na preparação de látexes de polímero acrílicos, também podem ser utilizados. Os comonômeros adequados incluem acetato de vinila, que podem ser usados como um co-monômero com, por exemplo, acrilato de butila em uma razão de 70/30 ou menor
Petição 870190029238, de 27/03/2019, pág. 18/29
11/21 do acetato de vinila ao acrilato de butila. As resinas acrílicas do acrilato e tipo de metacrilato são bem conhecidos por sua estabilidade nas tintas domésticas.
[0037] Outras resinas conhecidas e usadas nas formulações de revestimento aquosas incluem, sem limitação, homopolímeros e copolímeros de: (1) ésteres de vinila de um ácido alifático, tal como acetato de vinila, (2) ésteres do ácido acrílico e ésteres do ácido metacrílico de um álcool, tal como acrilato de metila, acrilato de etila, acrilato de butila, acrilato de 2-etilexila, metacrilato de metila, metacrilato de etila e metacrilato de butila e (3) mono- e di-hidrocarbonetos etilenicamente insaturados, tal como etileno, isobutileno, estireno e dienos alifáticos, tal como butadieno, isopreno e cloropreno.
[0038] É também bem conhecido para o uso de poli(acetato de vinila) e copolímeros de acetato de vinila com um ou mais dos seguintes monômeros; cloreto de vinila, cloreto de vinilideno, estireno, viniltolueno, acrilonitrila, metacrilonitrila, um ou dois ésteres do ácido metacrílico e acrílico mencionados acima. Similarmente, os copolímeros de um ou mais dos ésteres do ácido acrílico e metacrílico mencionados acima com um ou mais dos seguintes monômeros: acetato de vinila, cloreto de vinila, cloreto de vinilideno, estireno, viniltolueno, acrilonitrila e metacrilonitrila também são mais ou menos convencionalmente utilizados nas formulações de revestimento aquosas. Os homopolímeros de etileno, isobutileno e estireno e copolímeros de um ou mais destes hidrocarbonetos com um ou mais ésteres, nitrilas ou amidas do ácido acrílico ou do ácido metacrílico ou com ésteres de vinila, tal como acetato de vinila e cloreto de vinila, ou com cloreto de vinilideno também são usados. Os polímeros de dieno são geralmente usados nas formulações de revestimento aquosas na forma de copolímeros com um ou mais seguintes monômeros: estireno, viniltolueno, acrilonitrila, metacrilonitrila, ésteres do ácido acrílico ou metacrilonitrila e ésteres do ácido metacrílico.
[0039] Os pigmentos não são particularmente limitados e muitos são bem conhecidos e usados pelas pessoas de habilidade comum na técnica relevante. Alguns dos pigmentos típicos incluem, sem limitação, dióxido de titânio e outros pigmentos de titânio, chumbo branco, óxido de zinco, sulfeto de zinco, sulfato de
Petição 870190029238, de 27/03/2019, pág. 19/29
12/21 bário, carbonato de cálcio, litopona, sílica, talco, mica, argila, óxido de ferro, negro de fumo, sulfeto de cádmio, toluidina vermelha, cromo laranja, cromo amarelo e cromo verde. Particularmente os pigmentos adequados incluem, sem limitação, como dióxido de titânio (por exemplo, TIPURE® R942 comercialmente disponível de DuPont, localizado em Wilmington, Delaware, USA) e carbonato de cálcio triturado (por exemplo, OMYACARB® UF comercialmente disponível de Omya, Inc., localizado em Cincinnati, Ohio, USA).
[0040] A formulação de revestimento aquosa da presente invenção também pode incluir vários outros tipos de aditivos, auxiliares e agentes, por exemplo, um auxiliar de coalescência, um auxiliar espessante, um auxiliar de dispersão, um ligante, um modificador de reologia, um agente de reticulação, um agente umectante, um desespumante e um biocida.
[0041] Os agentes de reticulação adequados também pode ser incluídos e são bem conhecidos na técnica, tal como, por exemplo, triacrilato de trimetilolpropano.
[0042] Os ligantes adequados incluem, sem limitação, UCARTM Látex 379 e 6030, ambos comercialmente disponível de Arkema Chemicals, localizados em Philadelphia, Pensilvânia, USA.
[0043] Os espessantes adequados e modificadores de reologia incluem, sem limitação, hidroxietilcelulose (por exemplo, CELLOSIZETM HEC comercialmente disponível de The Dow Chemical Company, localizado em Midland, Michigan, USA) e agente espessante associativo não iônico de solvente livre/HEUR uretano de óxido de polietileno hidrofobicamente modificado (ACRYSOLTM RM-5000 comercialmente disponível de Dow Advanced Materials, localizado em Philadelphia, Pensilvânia, USA).
[0044] Os desespumantes tal como, sem limitação, DREW PLUS Y-381 comercialmente disponível de Ashland, localizado em Covington, Kentucky, USA, também são adequados para o uso com a presente invenção.
[0045] Como descrito no detalhe adicional anteriormente mencionado, o desempenho dos compostos de diaminoálcool da presente invenção são testados como neutralizantes, agentes de co-dispersão e relativos comparados aos
Petição 870190029238, de 27/03/2019, pág. 20/29
13/21 neutralizadores comerciais na formulação de semi-brilho de látex com base aquosa. Os neutralizadores comparativos incluem 2-metil-2-aminopropanol (AMP), 2-etil-2amino-l,3-propanodiol (AEPD) e N-butildietanolamina (NBDA).
EXEMPLOS
Exemplo 1 [0046] Síntese de 2,5,6-trimetil-2,6-dinitroeptan-3-ol (intermediário de dinitro álcool)
[0047] Um frasco de fundo redondo de 3 bocas equipado com uma barra de agitação, termoligação, funil de gotejamento coberto com entrada de nitrogênio e o condensador foi carregado com 2-nitropropano (“2-NP”) (50 g, 0,56 mois, 5,0 equivalentes) e quantidade catalítica de DBU. A solução amarela foi misturada sob nitrogênio por cerca de trinta minutos. Para esta mistura foi adicionado crotonaldeído (7,9 g, 9,2 mL, 0,112 mois, 1,0 equivalente) às gotas em um período de vinte minutos. A adição de crotonaldeído foi feito em três condições diferentes, como seguem e todos destes produziram os mesmos resultados.
[0048] Condições:
A: Adição às gotas de crotonaldeído quando a mistura 2-NP/DBU está a 30°C e aquecido em temperatura ambiente.
B: Adição às gotas de crotonaldeído quando a mistura 2-NP/DBU está a 20°C e aquecido em temperatura ambiente.
C: Adição às gotas de crotonaldeído quando a mistura 2-NP/DBU está a temperatura ambiente [0049] Em cada caso, após adição completa, a reação foi agitada por aproximadamente 5 a 6 horas em temperatura ambiente. Durante este período, sólido branco retirado da solução. Neste ponto, análise GC mostrou a ausência de qualquer crotonaldeído na mistura de reação. Após deixar a mistura de reação agitar durante a noite em temperatura ambiente e sob nitrogênio, o sólido branco foi
Petição 870190029238, de 27/03/2019, pág. 21/29
14/21 isolado pela filtração à vácuo e o sólido foi lavado em toda parte com água. O sólido foi secado em ar, seguido pela secagem à vácuo, a 45°C. O rendimento total do álcool nitro desejado foi 72 % (27,8 g). O teste de ressonância magnética nuclear (“RMN”) e cromatografia líquida (LC) mostrou que o produto foi > 99 % puro. 1H RMN (CDCIs): δ 0,82-1,56 (m, 18H), 4,02-4,07 (m, 1H), 13C RMN (CDCIs): a 14,1, 20,7, 22,5, 23,1, 23,6, 33,5, 37,9, 73,1, 91,8 e 92,1 ppm. A reação também foi realizada com razão molar menor do aldeído insaturado ao nitroalcano. Os resultados similares foram obtidos ao exemplo acima, quando uma razão de aldeído insaturado ao nitroalcano foi 1:2.9.
[0050] Síntese de 2,6-diamino-2,5,6-trimetileptan-3-ol (diaminoálcool)
[0051] 25 g do álcool nitro acima foi dissolvido em 200 ml_ de metanol e hidrogenado sob autoclave a 60°C usando 14,2 g de RaNi 3111 como um catalisador e na pressão 600 psi. Após o trabalho que inclui a filtração do catalisador e remoção de metanol, aproximadamente 11 g (59 % de rendimento) do líquido incolor/verde claro viscoso inferior foi obtido. RMN e análise de espectroscopia de massa da cromatografia de gás (“GC-MS”) confirmou a presença do álcool amino desejado. A espectrometria de massa de ionização química CI-MS mostrou [M+H] = 189 e GC mostrou que a pureza do material a ser 94 %. O ponto de ebulição do material foi aproximadamente 110°C a 120°C a 0,5 a 1.5 torr. O pKa das aminas foi 10,12. 1H RMN (CDCIs): 5 0,48-1,22 (m, 18H), 2,84-2,89 (m, 1H), 13CRMN (CDCIs): 5 16,8, 25,2, 27,9, 30,8, 34,7, 42,2, 51,8, 52,8 e 77,3 ppm.
[0052] O produto do diaminoálcool deste exemplo 1 é rotulado “CROT-AMPNH2” nas figuras anexas.
Exemplo 2 [0053] Síntese de 6-metil-3,7-dinitrononan-4-ol (intermediário de dinitro álcool)
Petição 870190029238, de 27/03/2019, pág. 22/29
15/21

Η [0054] Um frasco de fundo redondo de 3 bocas equipado com uma barra de agitação, termoligação, funil de gotejamento coberto com entrada de nitrogênio e o condensador foi carregado com 2-Nitropropano (50 g, 0,56 rnols, 5,0 equivalentes) e quantidade catalítica de DBU. A solução amarela profunda foi misturada sob nitrogênio por cerca de trinta minutos. Para esta mistura foi adicionado crotonaldeído (7,9 g, 9,2 mL, 0,112 rnols, 1,0 equivalente) às gotas em um período de vinte minutos. A adição de crotonaldeído neste caso foi feito em temperatura ambiente e durante a adição, exotermia de cerca de 12°C a 15°C foi observado. Após adição completa, a reação foi agitada em temperatura ambiente por 6 horas. Neste ponto, análise GC mostrou a ausência de crotonaldeído a partir da mistura. A reação foi deixada agitar em temperatura ambiente durante a noite e análise de cromatografia líquida de alto desempenho (HPLC) mostrou a presença de apenas dois picos que correspondem ao 1-NP no qual está em excesso e o produto desejado (aduto 1 CA + 2NP). O excesso 1-NP foi removido pela destilação à vácuo e o líquido viscoso laranja resultante foi submetido a hidrogenação. Este material foi de cerca de 37,2 g de peso total entretanto ainda tem algum 1-NP remanescente.
[0055] Síntese de 3,7-diamino-6-metilnonan-4-ol (intermediário de diaminoálcool)
[0056] 37,2 g do álcool nitro acima foi dissolvido em 50 mL de metanol e hidrogenado sob hidrogênio na autoclave a 60°C, usando 14,3 g RaNi 3111 como um catalisador e na pressão 600 psi. Após o trabalho que inclui a filtração do catalisador e remoção de metanol, aproximadamente 18 g (64 % de rendimento) do líquido amarelo viscoso inferior foi obtido. Análise GC-MS confirmou a presença do álcool amino desejado. CI-MS mostrou [M+H] = 189 e GC mostrou que a pureza do material a ser 50 %. Os restantes foram os materiais de ebulição inferiores. O pKa
Petição 870190029238, de 27/03/2019, pág. 23/29
16/21 das aminas foi 9,85.
Exemplo 3 [0057] Síntese de 2,6-dimetil-2,6-dinitro-5-fenileptan-3-ol (intermediário de dinitro álcool)
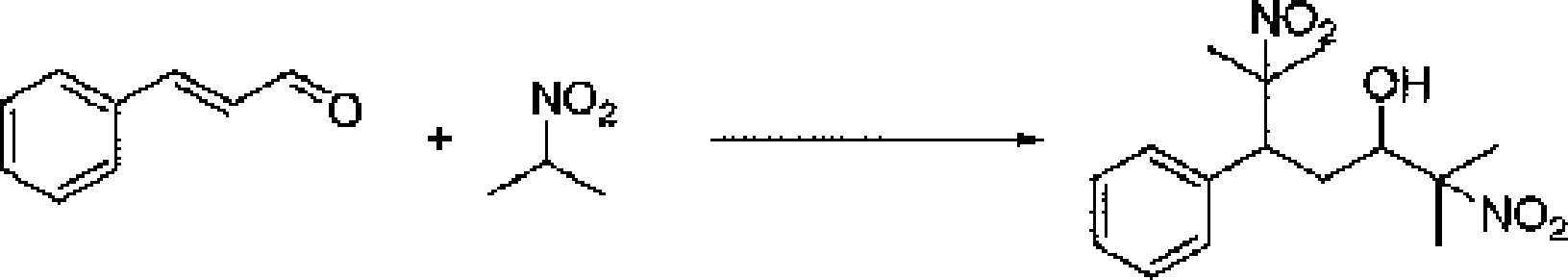
[0058] Um frasco de fundo redondo de 3 bocas equipado com uma barra de agitação, termoligação, funil de gotejamento coberto com entrada de nitrogênio e o condensador foi carregado com 2-Nitropropano (101,1 g, 1,14 mols, 6,0 equivalentes) e quantidade catalítica de DBU. A solução amarela foi misturada sob nitrogênio por cerca de vinte minutos. Para esta mistura foi adicionado transcinamaldeído (25,0 g, 0,19 mols, 1,0 equivalente) às gotas em um período de vinte minutos. Durante a adição de trans-cinamaldeído a nitro parafina, um exotermia de aproximadamente 22°C foi observado. Após adição completa, a mistura de reação foi aquecida a 50°C por 4 horas. Após o período de aquecimento, a mistura foi deixada esfriar levemente em temperatura ambiente. Quando a temperatura de mistura de reação atingiu 36,8°C, a sólido amarelo claro retirado da solução. O sólido foi filtrado através de um funil Buchner e lavado em toda parte com pentano e éter. O pó branco foi deixado secar sob vácuo por 1 hora. O rendimento total do álcool nitro desejado foi 62 % (36 g). RMN mostrou que o produto foi >99 % puro. 1H
RMN (CDCIs): δ 1,45-2,27 (m, 15H), 3,52-3,54 (m, 1H), 3,67-3,74 (m, 1H), 7,17-7,34 (m, 5H), 13C RMN (CDCIs): 8 20,8, 22,4, 23,2, 25,8, 31,3, 50,3, 72,9, 91,5, 91,6, 128,1, 128,7, 129,4, 136,6 ppm.
[0059] Síntese de 2,6-diamino-2,6-dimetil-5-fenileptan-3-ol (diaminoálcool)
Petição 870190029238, de 27/03/2019, pág. 24/29
17/21 [0060] 50 g do álcool nitro acima foi dissolvido em 300 mL de metanol e hidrogenado na autoclave a 60°C usando 24,3 g de RaNi 3111 como um catalisador e na pressão 600 psi. Após o trabalho que inclui a filtração do catalisador e remoção de metanol, aproximadamente 40 g (68 % de rendimento) do líquido incolor/amarelo claro viscoso alto foi obtido. RMN e Análise GC-MS confirmou a presença do álcool amino desejado. Cl-MS mostrou [M+H] = 251 e GC mostrou que a pureza do material a ser 78 % reto a partir da autoclave. O restante do material visto ser monoaduto obtido da reversão da reação de Henry. A mistura foi purificada pela destilação à vácuo aproximadamente 96,2 % de pureza do material desejado foi obtido. O ponto de ebulição do material foi aproximadamente 145°C a 155°C a 0,9 a 1,1 torr. O pKa das aminas foi 9,65. O VOC do material, como determinado pelo método EPA modificado 24, é 4,4 %. 1H RMN (CDCb): δ 0,91-0,99 (m, 12H), 1,671,81 (m, 3H), 2,71-2,76 (m, 2H), 7,08-7,23 (m, 5H), 13C RMN (CDCb): a 24,6, 27,9, 28,3, 29,8, 31,6, 51,8, 52,6, 54,2, 75,9, 126,3, 127,8, 129,4, 142,0 ppm.
[0061] O produto do diaminoálcool deste exemplo 3 é rotulado “CINNAM-AMPNH2” nas figuras anexas.
[0062] Os compostos de diaminoálcool preparados nos Exemplos 1 e 3 são comparados com os compostos amino comercialmente disponíveis que são correntemente usados nas formulações de revestimento aquosas para a dispersão de pigmentos. A seguinte lista fornece os rótulo e fontes dos compostos amino comercialmente disponíveis e conhecidos usados para a comparação:
[0063] AMP 95 = composto amina (2-amino-2-metil-1-propanol), disponível de ANGUS Chemical Company, um subsidiário totalmente pertencente à Dow Chemical Company of Midland, Michigan, USA, que é útil como um dispersante nas formulações de revestimento.
[0064] N-Butil-dietanolamina (NBDA) = Também denominado Vantex® T um composto amina disponível de Taminco of Ghent, Bélgica (e Atlanta, Geórgia, USA), advertido como útil como um dispersante tendo teor VOC baixo e odor baixo para as formulações de revestimentos.
[0065] AEPD VOX 1000 = composto amina, disponível de ANGUS Chemical
Petição 870190029238, de 27/03/2019, pág. 25/29
18/21
Company, um subsidiário totalmente pertencente à Dow Chemical Company of Midland, Michigan, USA, que é útil como um dispersante nas formulações de revestimento com teor e odor VOC reduzido.
[0066] Os gráficos de barra da Figura 1 mostrou como o teor VOC e pKa de cada um dos compostos de diaminoálcool do Exemplo 1 (CBOT-AMP-NH2) e Exemplo 3 (CINNAM-AMP-NP2) comparado com aqueles das aminas comerciais.
Exemplo 4
Formulação de Revestimento [0067] O 2,6-diamino-2,5,6-trimetileptan-3-ol (CROT-AMP-NH2) preparado nos Exemplo 1 foi testado como uma amina de co-dispersão, neutralizante e comparada com relação a AMP, AEPD (VOX 1000) e N-butil-dietanolamina (Vantex T) em uma formulação de revestimento de semi-brilho de látex com base aquosa. A receita para a formulação de revestimento (tinta) (usando AMP como o dispersante) é fornecido na tabela abaixo. Outras aminas (Vantex T, VOV 1000 e o diaminoálcool do Exemplo 1) foram usados nas quantidades equimolares com relação ao peso molecular.
[0068] ANGUS - Base pastel de semi-brilho interior (com substituição de tensoativo aniônico)
|
TRITURAÇÃO |
mfr/ fornecedor |
s,q, |
Peso |
Peso g/6,25 mL |
|
Água |
|
1,00 |
140,00 |
1,049 |
|
Espessante HEC Cellulosize QP
300 |
Dow |
1,41 |
140,00 |
1,049 |
|
Água |
|
1,00 |
10,00 |
0,075 |
|
agitado 10 minutos em velocidade alta então adicionado o seguinte em velocidade baixa |
|
|
|
|
|
Dispersante Tamol 1124 |
Rohm & Haas |
1,19 |
5,00 |
0,037 |
|
Tensoativo não iônico Triton CF-10 |
Dow |
1,08 |
2,00 |
0,015 |
|
Tensoativo aniônico Triton GRPG70 |
Dow |
1,11 |
0,43 |
0,003 |
|
Desespumante Drew Plus Y-381 |
Ashland / Drew I |
0,87 |
1,00 |
0,007 |
|
Etileno glicol |
Dow |
1,12 |
30,00 |
0,225 |
|
AMP-95 |
Dow |
0,94 |
2,00 |
0,015 |
|
Carbonato de cálcio Omyacarb UF |
Omya |
2,72 |
25,00 |
0,187 |
Petição 870190029238, de 27/03/2019, pág. 26/29
19/21
|
Água |
|
1,00 |
20,00 |
0,150 |
|
Trituração subtotal |
|
|
240,43 |
1,801 |
|
Disperso em velocidade alta por 15 minutos, trituração checada então adicionado o seguinte em velocidade baixa |
|
|
|
|
|
ENFRAQUECIMENTO |
|
|
|
|
|
UCAR Latex 379, Acrílico de vinila |
Dow |
1,09 |
375,00 |
2,809 |
|
UCAR Latex 6030, Acrílico |
Dow |
1,06 |
47,00 |
0,352 |
|
Coalescente butil carbitol |
Dow |
0,95 |
6,00 |
0,045 |
|
Archer RC Coalescente reativo |
ADM (Archer Dai |
0,92 |
12,00 |
0,090 |
|
Desespumante Drew Plus Y-381 |
Ashland / Drew |
0,87 |
1,50 |
0,011 |
|
TiPure R942 Pasta de dióxido de titânio (76,5 % de sólidos) |
DuPont |
2,33 |
250,00 |
1,873 |
|
Modificador de reologia ACRYSOL RM-5000 |
Rohm & Haas |
1,04 |
30,00 |
0,225 |
|
Água |
|
1,00 |
64,58 |
0,484 |
|
disperso em velocidade alta por 10 minutos |
|
|
|
|
|
Desespumante Drew Plus Y-381 |
Ashland / Drew |
0,87 |
1,50 |
0,011 |
|
Agitado em velocidade baixa por 10 minutos |
|
|
|
|
|
Fórmula total |
|
|
1028,00 |
7,700 |
|
pH > 9.0 |
|
|
|
|
|
Viscosidade: 86 - 92 KU |
|
|
|
|
|
Fórmula total |
|
|
1728,44 |
|
[0069] O diaminoálcool do Exemplo 1, (2,6-diamino-2,5,6-trimetileptan-3-ol / CROTAMP-NP2), tem cerca da metade do teor de VOC de AMP e realiza igualmente ou levemente melhor em mais testes. O CROT-AMP-NH2 é também comparável no desempenho das formulações de revestimento de aditivos de aminas comercialmente disponíveis AEPD VOX 1000 e VANTEX T e também tem odor baixo. Os gráficos de barra da Figura 2 fornecem as comparações de várias características relevantes das formulações de revestimento preparadas e avaliadas com cada um dos compostos de amina.
[0070] O pH, tamanho de partícula, opacidade de película, brilho e VOC das formulações contendo os vários compostos testados são determinados como seguem:
Petição 870190029238, de 27/03/2019, pág. 27/29
20/21 [0071] Propriedades ópticas de revestimento (opacidade e brilho). A opacidade, brilho a 20, 60 e 85° e cor das películas secadas é medida usando um robô espessante/brilho/cor automática com base em um módulo Symyx XCM. A cor é medida usando uma esfera de integração Ocean Optics ISP-REF com uma abertura de amostragem 0,4” conectado por um cabo de fibra ótica a um espectrômetro Ocean Optics USB 4000.
[0072] As medições são realizadas com iluminação D65. Este mecanismo é localizado no braço direito de um robô Symyx Core Module que capacita o colorímetro a ser movido na amostra nas localizações múltiplas. Para este estudo das medições são feitos em três áreas separadas tanto nas partes brancas quanto nas pretas de cada papel Lenota. O brilho é medido usando um metro BYK microTri-gloss. Este instrumento é associado ao braço direito do robô Symyx Core Module, junto com uma garra de placa usada para mover as amostras a partir do hotel da amostra BenchCel à cobertura do módulo. O brilho é medido em três marcas diferentes no revestimento tanto nas partes brancas quanto pretas do papel Lenota.
[0073] Análise do tamanho de partícula. A distribuição do tamanho de partícula na formulação é medida usando um analisador de tamanho de partícula Beckman Coulter LS-230 usando um acessório de Micro-Volume. Uma gota da formulação é adicionada a aproximadamente 20 mL da água desionizada e bem agitada. Esta solução é então adicionada às gotas ao acessório de micro-volume por pipeta até a leitura de absorbância ser pelo menos 8 %. A amostra é continuamente agitada durante a medição. Os tamanhos de partícula de 0,04 a 2000 mícrons podem ser detectados. A distribuição do tamanho de partícula de uma talha padrão com os 35 mícrons de tamanho de partícula nominal é medido ser 36 ± 15 mícrons.
[0074] Medições de pH. A formulação de pH é medida usando um metro Fisher Scientific Accumet 15 pH, equipado com um eletrodo de pH de combinação ThermoElectron Orion 9203BN. Os tampões de pH comerciais são usados para calibrar o equipamento antes de cada uso. Os valores relacionados são a média de três leituras separadas em cada formulação, a sonda é limpa com água DI entre
Petição 870190029238, de 27/03/2019, pág. 28/29
21/21 cada medição.
[0075] Teor orgânico volátil (VOC). VOC é medido seguindo o método EPA 24 modificado. O VOC foi medido para apenas a amina limpa e não o sistema totalmente formulado. As aminas são pesadas em um cadinho e mantidas em um forno por 1 hora a 105 a 110°C. A perda de peso percentual é relacionada como o VOC, corrigida para o teor de água em uma amostra que pode ser medida pela titulação Karl Fisher.