BRPI1006729B1 - Creme medicinal de ácido fusídico preparado utilizando fusidato de sódio e incorporando um biopolímero e seu processo de preparação - Google Patents
Creme medicinal de ácido fusídico preparado utilizando fusidato de sódio e incorporando um biopolímero e seu processo de preparação Download PDFInfo
- Publication number
- BRPI1006729B1 BRPI1006729B1 BRPI1006729-9A BRPI1006729A BRPI1006729B1 BR PI1006729 B1 BRPI1006729 B1 BR PI1006729B1 BR PI1006729 A BRPI1006729 A BR PI1006729A BR PI1006729 B1 BRPI1006729 B1 BR PI1006729B1
- Authority
- BR
- Brazil
- Prior art keywords
- cream
- group
- amount
- combination
- mixture
- Prior art date
Links
- 229960004675 fusidic acid Drugs 0.000 title claims abstract description 211
- IECPWNUMDGFDKC-MZJAQBGESA-N fusidic acid Chemical compound O[C@@H]([C@@H]12)C[C@H]3\C(=C(/CCC=C(C)C)C(O)=O)[C@@H](OC(C)=O)C[C@]3(C)[C@@]2(C)CC[C@@H]2[C@]1(C)CC[C@@H](O)[C@H]2C IECPWNUMDGFDKC-MZJAQBGESA-N 0.000 title claims abstract description 209
- IECPWNUMDGFDKC-UHFFFAOYSA-N Fusicsaeure Natural products C12C(O)CC3C(=C(CCC=C(C)C)C(O)=O)C(OC(C)=O)CC3(C)C1(C)CCC1C2(C)CCC(O)C1C IECPWNUMDGFDKC-UHFFFAOYSA-N 0.000 title claims abstract description 110
- 229920001222 biopolymer Polymers 0.000 title claims abstract description 33
- 238000002360 preparation method Methods 0.000 title abstract description 7
- 239000006071 cream Substances 0.000 claims abstract description 170
- 239000000203 mixture Substances 0.000 claims abstract description 108
- 239000008186 active pharmaceutical agent Substances 0.000 claims abstract description 84
- 229920001661 Chitosan Polymers 0.000 claims abstract description 78
- 238000000034 method Methods 0.000 claims abstract description 50
- 238000011282 treatment Methods 0.000 claims abstract description 42
- 230000008569 process Effects 0.000 claims abstract description 39
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims abstract description 37
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims abstract description 36
- 239000011261 inert gas Substances 0.000 claims abstract description 32
- 238000011065 in-situ storage Methods 0.000 claims abstract description 22
- 229910052757 nitrogen Inorganic materials 0.000 claims abstract description 18
- 238000004519 manufacturing process Methods 0.000 claims abstract description 16
- 239000002994 raw material Substances 0.000 claims abstract description 13
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims abstract description 10
- 239000001301 oxygen Substances 0.000 claims abstract description 10
- 229910052760 oxygen Inorganic materials 0.000 claims abstract description 10
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 claims description 51
- 238000002156 mixing Methods 0.000 claims description 34
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 claims description 30
- 239000002253 acid Substances 0.000 claims description 29
- 230000000699 topical effect Effects 0.000 claims description 27
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 claims description 20
- 239000012071 phase Substances 0.000 claims description 18
- 208000035143 Bacterial infection Diseases 0.000 claims description 17
- 208000022362 bacterial infectious disease Diseases 0.000 claims description 17
- 238000001816 cooling Methods 0.000 claims description 16
- 239000000463 material Substances 0.000 claims description 16
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 claims description 15
- 239000004310 lactic acid Substances 0.000 claims description 15
- 235000014655 lactic acid Nutrition 0.000 claims description 15
- 229910017604 nitric acid Inorganic materials 0.000 claims description 15
- 229920000642 polymer Polymers 0.000 claims description 15
- 239000008213 purified water Substances 0.000 claims description 15
- SVTBMSDMJJWYQN-UHFFFAOYSA-N 2-methylpentane-2,4-diol Chemical compound CC(O)CC(C)(C)O SVTBMSDMJJWYQN-UHFFFAOYSA-N 0.000 claims description 14
- 239000008346 aqueous phase Substances 0.000 claims description 14
- 239000006184 cosolvent Substances 0.000 claims description 14
- 239000003995 emulsifying agent Substances 0.000 claims description 14
- CFKMVGJGLGKFKI-UHFFFAOYSA-N 4-chloro-m-cresol Chemical compound CC1=CC(O)=CC=C1Cl CFKMVGJGLGKFKI-UHFFFAOYSA-N 0.000 claims description 12
- BNIILDVGGAEEIG-UHFFFAOYSA-L disodium hydrogen phosphate Chemical compound [Na+].[Na+].OP([O-])([O-])=O BNIILDVGGAEEIG-UHFFFAOYSA-L 0.000 claims description 12
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 claims description 12
- 229910052753 mercury Inorganic materials 0.000 claims description 12
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 claims description 12
- 239000003755 preservative agent Substances 0.000 claims description 12
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 claims description 12
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 claims description 11
- 239000003963 antioxidant agent Substances 0.000 claims description 11
- 239000006172 buffering agent Substances 0.000 claims description 11
- 239000002738 chelating agent Substances 0.000 claims description 11
- 239000003906 humectant Substances 0.000 claims description 11
- 235000011149 sulphuric acid Nutrition 0.000 claims description 11
- 238000012546 transfer Methods 0.000 claims description 11
- 230000029663 wound healing Effects 0.000 claims description 11
- 239000005711 Benzoic acid Substances 0.000 claims description 10
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 claims description 10
- 150000007513 acids Chemical class 0.000 claims description 10
- 235000010233 benzoic acid Nutrition 0.000 claims description 10
- 229940082500 cetostearyl alcohol Drugs 0.000 claims description 10
- -1 liquid paraffin Substances 0.000 claims description 10
- GLDOVTGHNKAZLK-UHFFFAOYSA-N octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCO GLDOVTGHNKAZLK-UHFFFAOYSA-N 0.000 claims description 10
- 239000000244 polyoxyethylene sorbitan monooleate Substances 0.000 claims description 10
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 claims description 10
- 229940068968 polysorbate 80 Drugs 0.000 claims description 10
- 229920000053 polysorbate 80 Polymers 0.000 claims description 10
- 230000002335 preservative effect Effects 0.000 claims description 10
- OULAJFUGPPVRBK-UHFFFAOYSA-N tetratriacontyl alcohol Natural products CCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCO OULAJFUGPPVRBK-UHFFFAOYSA-N 0.000 claims description 10
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 claims description 9
- 230000003078 antioxidant effect Effects 0.000 claims description 9
- 239000000839 emulsion Substances 0.000 claims description 9
- 239000007787 solid Substances 0.000 claims description 9
- 238000003860 storage Methods 0.000 claims description 9
- 239000004322 Butylated hydroxytoluene Substances 0.000 claims description 7
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 claims description 7
- 229920002565 Polyethylene Glycol 400 Polymers 0.000 claims description 7
- 238000013019 agitation Methods 0.000 claims description 7
- 235000010354 butylated hydroxytoluene Nutrition 0.000 claims description 7
- 229940095259 butylated hydroxytoluene Drugs 0.000 claims description 7
- 229940051250 hexylene glycol Drugs 0.000 claims description 7
- 238000000265 homogenisation Methods 0.000 claims description 7
- 239000012188 paraffin wax Substances 0.000 claims description 7
- 229940068918 polyethylene glycol 400 Drugs 0.000 claims description 7
- 229960004063 propylene glycol Drugs 0.000 claims description 7
- IQXJCCZJOIKIAD-UHFFFAOYSA-N 1-(2-methoxyethoxy)hexadecane Chemical compound CCCCCCCCCCCCCCCCOCCOC IQXJCCZJOIKIAD-UHFFFAOYSA-N 0.000 claims description 6
- CHHHXKFHOYLYRE-UHFFFAOYSA-M 2,4-Hexadienoic acid, potassium salt (1:1), (2E,4E)- Chemical compound [K+].CC=CC=CC([O-])=O CHHHXKFHOYLYRE-UHFFFAOYSA-M 0.000 claims description 6
- 239000004255 Butylated hydroxyanisole Substances 0.000 claims description 6
- 239000003109 Disodium ethylene diamine tetraacetate Substances 0.000 claims description 6
- ZGTMUACCHSMWAC-UHFFFAOYSA-L EDTA disodium salt (anhydrous) Chemical compound [Na+].[Na+].OC(=O)CN(CC([O-])=O)CCN(CC(O)=O)CC([O-])=O ZGTMUACCHSMWAC-UHFFFAOYSA-L 0.000 claims description 6
- NWGKJDSIEKMTRX-AAZCQSIUSA-N Sorbitan monooleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O NWGKJDSIEKMTRX-AAZCQSIUSA-N 0.000 claims description 6
- 229960004365 benzoic acid Drugs 0.000 claims description 6
- 235000019282 butylated hydroxyanisole Nutrition 0.000 claims description 6
- CZBZUDVBLSSABA-UHFFFAOYSA-N butylated hydroxyanisole Chemical compound COC1=CC=C(O)C(C(C)(C)C)=C1.COC1=CC=C(O)C=C1C(C)(C)C CZBZUDVBLSSABA-UHFFFAOYSA-N 0.000 claims description 6
- 229940043253 butylated hydroxyanisole Drugs 0.000 claims description 6
- 229950009789 cetomacrogol 1000 Drugs 0.000 claims description 6
- 229960002242 chlorocresol Drugs 0.000 claims description 6
- 235000019301 disodium ethylene diamine tetraacetate Nutrition 0.000 claims description 6
- 229910000397 disodium phosphate Inorganic materials 0.000 claims description 6
- 235000019800 disodium phosphate Nutrition 0.000 claims description 6
- 229940057995 liquid paraffin Drugs 0.000 claims description 6
- 235000010270 methyl p-hydroxybenzoate Nutrition 0.000 claims description 6
- 239000004292 methyl p-hydroxybenzoate Substances 0.000 claims description 6
- 229960002216 methylparaben Drugs 0.000 claims description 6
- 235000010241 potassium sorbate Nutrition 0.000 claims description 6
- 239000004302 potassium sorbate Substances 0.000 claims description 6
- 229940069338 potassium sorbate Drugs 0.000 claims description 6
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 claims description 6
- 239000004405 propyl p-hydroxybenzoate Substances 0.000 claims description 6
- 229960003415 propylparaben Drugs 0.000 claims description 6
- 239000003871 white petrolatum Substances 0.000 claims description 6
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 claims description 5
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 claims description 5
- 229910052799 carbon Inorganic materials 0.000 claims description 5
- 235000011187 glycerol Nutrition 0.000 claims description 5
- 239000000600 sorbitol Substances 0.000 claims description 5
- GNFTZDOKVXKIBK-UHFFFAOYSA-N 3-(2-methoxyethoxy)benzohydrazide Chemical compound COCCOC1=CC=CC(C(=O)NN)=C1 GNFTZDOKVXKIBK-UHFFFAOYSA-N 0.000 claims description 4
- 238000010438 heat treatment Methods 0.000 claims description 4
- 239000005457 ice water Substances 0.000 claims description 4
- 239000002736 nonionic surfactant Substances 0.000 claims description 4
- 239000001993 wax Substances 0.000 claims description 4
- FGUUSXIOTUKUDN-IBGZPJMESA-N C1(=CC=CC=C1)N1C2=C(NC([C@H](C1)NC=1OC(=NN=1)C1=CC=CC=C1)=O)C=CC=C2 Chemical compound C1(=CC=CC=C1)N1C2=C(NC([C@H](C1)NC=1OC(=NN=1)C1=CC=CC=C1)=O)C=CC=C2 FGUUSXIOTUKUDN-IBGZPJMESA-N 0.000 claims description 2
- 238000003756 stirring Methods 0.000 claims 2
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 claims 1
- 229960004217 benzyl alcohol Drugs 0.000 claims 1
- 230000001580 bacterial effect Effects 0.000 abstract description 20
- 208000015181 infectious disease Diseases 0.000 abstract description 16
- 206010052428 Wound Diseases 0.000 abstract description 15
- 208000027418 Wounds and injury Diseases 0.000 abstract description 15
- 206010040872 skin infection Diseases 0.000 abstract description 13
- 239000002245 particle Substances 0.000 abstract description 10
- 208000003251 Pruritus Diseases 0.000 abstract description 5
- 206010072170 Skin wound Diseases 0.000 abstract description 5
- 230000003716 rejuvenation Effects 0.000 abstract description 4
- 230000000172 allergic effect Effects 0.000 abstract 1
- 208000010668 atopic eczema Diseases 0.000 abstract 1
- 239000000047 product Substances 0.000 description 52
- 238000009472 formulation Methods 0.000 description 31
- 239000000546 pharmaceutical excipient Substances 0.000 description 25
- 230000000844 anti-bacterial effect Effects 0.000 description 20
- 238000012360 testing method Methods 0.000 description 19
- 239000002674 ointment Substances 0.000 description 16
- 239000004480 active ingredient Substances 0.000 description 15
- 230000001225 therapeutic effect Effects 0.000 description 15
- 208000017520 skin disease Diseases 0.000 description 14
- 230000023555 blood coagulation Effects 0.000 description 12
- 230000035876 healing Effects 0.000 description 12
- 238000004458 analytical method Methods 0.000 description 11
- 239000003242 anti bacterial agent Substances 0.000 description 10
- 239000011159 matrix material Substances 0.000 description 10
- 230000008901 benefit Effects 0.000 description 9
- 239000004094 surface-active agent Substances 0.000 description 9
- 238000002560 therapeutic procedure Methods 0.000 description 9
- 239000003246 corticosteroid Substances 0.000 description 8
- 230000000694 effects Effects 0.000 description 8
- 241000894006 Bacteria Species 0.000 description 7
- 206010012438 Dermatitis atopic Diseases 0.000 description 7
- 241001465754 Metazoa Species 0.000 description 7
- 201000008937 atopic dermatitis Diseases 0.000 description 7
- 230000000740 bleeding effect Effects 0.000 description 7
- 230000001010 compromised effect Effects 0.000 description 7
- 239000003814 drug Substances 0.000 description 7
- 229940079593 drug Drugs 0.000 description 7
- 239000002904 solvent Substances 0.000 description 7
- 239000000126 substance Substances 0.000 description 7
- 206010012442 Dermatitis contact Diseases 0.000 description 6
- 229940088710 antibiotic agent Drugs 0.000 description 6
- 230000003115 biocidal effect Effects 0.000 description 6
- 125000002091 cationic group Chemical group 0.000 description 6
- 208000028659 discharge Diseases 0.000 description 6
- 238000002474 experimental method Methods 0.000 description 6
- 238000004128 high performance liquid chromatography Methods 0.000 description 6
- 238000010348 incorporation Methods 0.000 description 6
- 230000003993 interaction Effects 0.000 description 6
- 230000010388 wound contraction Effects 0.000 description 6
- 229920002125 Sokalan® Polymers 0.000 description 5
- 238000013459 approach Methods 0.000 description 5
- 230000015556 catabolic process Effects 0.000 description 5
- 239000003795 chemical substances by application Substances 0.000 description 5
- 150000001875 compounds Chemical class 0.000 description 5
- 238000006731 degradation reaction Methods 0.000 description 5
- 238000000691 measurement method Methods 0.000 description 5
- 238000010525 oxidative degradation reaction Methods 0.000 description 5
- 150000003431 steroids Chemical class 0.000 description 5
- 208000003322 Coinfection Diseases 0.000 description 4
- 201000004624 Dermatitis Diseases 0.000 description 4
- 206010061218 Inflammation Diseases 0.000 description 4
- 241000191967 Staphylococcus aureus Species 0.000 description 4
- 125000000129 anionic group Chemical group 0.000 description 4
- 229940121375 antifungal agent Drugs 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 229960001334 corticosteroids Drugs 0.000 description 4
- 239000006185 dispersion Substances 0.000 description 4
- 230000004054 inflammatory process Effects 0.000 description 4
- 230000007803 itching Effects 0.000 description 4
- 230000000813 microbial effect Effects 0.000 description 4
- 229960002744 mometasone furoate Drugs 0.000 description 4
- WOFMFGQZHJDGCX-ZULDAHANSA-N mometasone furoate Chemical compound O([C@]1([C@@]2(C)C[C@H](O)[C@]3(Cl)[C@@]4(C)C=CC(=O)C=C4CC[C@H]3[C@@H]2C[C@H]1C)C(=O)CCl)C(=O)C1=CC=CO1 WOFMFGQZHJDGCX-ZULDAHANSA-N 0.000 description 4
- 239000003883 ointment base Substances 0.000 description 4
- 230000008929 regeneration Effects 0.000 description 4
- 238000011069 regeneration method Methods 0.000 description 4
- 239000012049 topical pharmaceutical composition Substances 0.000 description 4
- 239000003981 vehicle Substances 0.000 description 4
- 229920001285 xanthan gum Polymers 0.000 description 4
- 239000000230 xanthan gum Substances 0.000 description 4
- 235000010493 xanthan gum Nutrition 0.000 description 4
- 229940082509 xanthan gum Drugs 0.000 description 4
- NIXOWILDQLNWCW-UHFFFAOYSA-N Acrylic acid Chemical compound OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 3
- 241000233866 Fungi Species 0.000 description 3
- 201000004681 Psoriasis Diseases 0.000 description 3
- 230000002378 acidificating effect Effects 0.000 description 3
- 208000002029 allergic contact dermatitis Diseases 0.000 description 3
- 230000000845 anti-microbial effect Effects 0.000 description 3
- 239000003429 antifungal agent Substances 0.000 description 3
- 230000000975 bioactive effect Effects 0.000 description 3
- 229960001631 carbomer Drugs 0.000 description 3
- 210000004027 cell Anatomy 0.000 description 3
- 238000002648 combination therapy Methods 0.000 description 3
- 230000000295 complement effect Effects 0.000 description 3
- 208000010247 contact dermatitis Diseases 0.000 description 3
- 201000010099 disease Diseases 0.000 description 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 3
- 239000012467 final product Substances 0.000 description 3
- 230000006872 improvement Effects 0.000 description 3
- 238000000338 in vitro Methods 0.000 description 3
- 230000002757 inflammatory effect Effects 0.000 description 3
- 230000005764 inhibitory process Effects 0.000 description 3
- 244000005700 microbiome Species 0.000 description 3
- 230000007935 neutral effect Effects 0.000 description 3
- 238000004806 packaging method and process Methods 0.000 description 3
- 230000035515 penetration Effects 0.000 description 3
- 230000035699 permeability Effects 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 230000002829 reductive effect Effects 0.000 description 3
- 210000003705 ribosome Anatomy 0.000 description 3
- 238000004448 titration Methods 0.000 description 3
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- 241000238557 Decapoda Species 0.000 description 2
- 206010014199 Eczema infected Diseases 0.000 description 2
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 2
- 229920000084 Gum arabic Polymers 0.000 description 2
- 241000978776 Senegalia senegal Species 0.000 description 2
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 2
- 239000000205 acacia gum Substances 0.000 description 2
- 235000010489 acacia gum Nutrition 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 229910052782 aluminium Inorganic materials 0.000 description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 2
- 150000001413 amino acids Chemical class 0.000 description 2
- 230000003110 anti-inflammatory effect Effects 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- 210000002421 cell wall Anatomy 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- MYSWGUAQZAJSOK-UHFFFAOYSA-N ciprofloxacin Chemical compound C12=CC(N3CCNCC3)=C(F)C=C2C(=O)C(C(=O)O)=CN1C1CC1 MYSWGUAQZAJSOK-UHFFFAOYSA-N 0.000 description 2
- 238000004090 dissolution Methods 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 238000009510 drug design Methods 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 230000008030 elimination Effects 0.000 description 2
- 238000003379 elimination reaction Methods 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- 239000010419 fine particle Substances 0.000 description 2
- 230000002538 fungal effect Effects 0.000 description 2
- 229940115747 halobetasol Drugs 0.000 description 2
- 239000008309 hydrophilic cream Substances 0.000 description 2
- 230000001965 increasing effect Effects 0.000 description 2
- 230000002458 infectious effect Effects 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 230000002452 interceptive effect Effects 0.000 description 2
- 239000006210 lotion Substances 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 229960001664 mometasone Drugs 0.000 description 2
- QLIIKPVHVRXHRI-CXSFZGCWSA-N mometasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(Cl)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CCl)(O)[C@@]1(C)C[C@@H]2O QLIIKPVHVRXHRI-CXSFZGCWSA-N 0.000 description 2
- 230000003647 oxidation Effects 0.000 description 2
- 238000007254 oxidation reaction Methods 0.000 description 2
- 238000003921 particle size analysis Methods 0.000 description 2
- 244000052769 pathogen Species 0.000 description 2
- 239000008194 pharmaceutical composition Substances 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 239000002244 precipitate Substances 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 238000001243 protein synthesis Methods 0.000 description 2
- 238000010926 purge Methods 0.000 description 2
- 230000005808 skin problem Effects 0.000 description 2
- 238000012496 stress study Methods 0.000 description 2
- 230000009885 systemic effect Effects 0.000 description 2
- 239000006208 topical dosage form Substances 0.000 description 2
- 230000014616 translation Effects 0.000 description 2
- LEHFPXVYPMWYQD-XHIJKXOTSA-N ulobetasol Chemical compound C1([C@@H](F)C2)=CC(=O)C=C[C@]1(C)[C@]1(F)[C@@H]2[C@@H]2C[C@H](C)[C@@](C(=O)CCl)(O)[C@@]2(C)C[C@@H]1O LEHFPXVYPMWYQD-XHIJKXOTSA-N 0.000 description 2
- 239000000080 wetting agent Substances 0.000 description 2
- CPKVUHPKYQGHMW-UHFFFAOYSA-N 1-ethenylpyrrolidin-2-one;molecular iodine Chemical compound II.C=CN1CCCC1=O CPKVUHPKYQGHMW-UHFFFAOYSA-N 0.000 description 1
- HIQIXEFWDLTDED-UHFFFAOYSA-N 4-hydroxy-1-piperidin-4-ylpyrrolidin-2-one Chemical compound O=C1CC(O)CN1C1CCNCC1 HIQIXEFWDLTDED-UHFFFAOYSA-N 0.000 description 1
- 206010060968 Arthritis infective Diseases 0.000 description 1
- 108010077805 Bacterial Proteins Proteins 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- 241000238366 Cephalopoda Species 0.000 description 1
- 241000028872 Cylindrospermum minutissimum Species 0.000 description 1
- 230000006820 DNA synthesis Effects 0.000 description 1
- 206010048768 Dermatosis Diseases 0.000 description 1
- 206010056340 Diabetic ulcer Diseases 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 208000035874 Excoriation Diseases 0.000 description 1
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 1
- 229930182566 Gentamicin Natural products 0.000 description 1
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 206010021531 Impetigo Diseases 0.000 description 1
- 208000002260 Keloid Diseases 0.000 description 1
- RJQXTJLFIWVMTO-TYNCELHUSA-N Methicillin Chemical compound COC1=CC=CC(OC)=C1C(=O)N[C@@H]1C(=O)N2[C@@H](C(O)=O)C(C)(C)S[C@@H]21 RJQXTJLFIWVMTO-TYNCELHUSA-N 0.000 description 1
- 239000004909 Moisturizer Substances 0.000 description 1
- OVRNDRQMDRJTHS-UHFFFAOYSA-N N-acelyl-D-glucosamine Natural products CC(=O)NC1C(O)OC(CO)C(O)C1O OVRNDRQMDRJTHS-UHFFFAOYSA-N 0.000 description 1
- OVRNDRQMDRJTHS-FMDGEEDCSA-N N-acetyl-beta-D-glucosamine Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O OVRNDRQMDRJTHS-FMDGEEDCSA-N 0.000 description 1
- 206010031252 Osteomyelitis Diseases 0.000 description 1
- 229920000153 Povidone-iodine Polymers 0.000 description 1
- 230000006819 RNA synthesis Effects 0.000 description 1
- URWAJWIAIPFPJE-UHFFFAOYSA-N Rickamicin Natural products O1CC(O)(C)C(NC)C(O)C1OC1C(O)C(OC2C(CC=C(CN)O2)N)C(N)CC1N URWAJWIAIPFPJE-UHFFFAOYSA-N 0.000 description 1
- 208000032023 Signs and Symptoms Diseases 0.000 description 1
- 241000191963 Staphylococcus epidermidis Species 0.000 description 1
- 241000194017 Streptococcus Species 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 208000007536 Thrombosis Diseases 0.000 description 1
- 208000000558 Varicose Ulcer Diseases 0.000 description 1
- YTAHJIFKAKIKAV-XNMGPUDCSA-N [(1R)-3-morpholin-4-yl-1-phenylpropyl] N-[(3S)-2-oxo-5-phenyl-1,3-dihydro-1,4-benzodiazepin-3-yl]carbamate Chemical compound O=C1[C@H](N=C(C2=C(N1)C=CC=C2)C1=CC=CC=C1)NC(O[C@H](CCN1CCOCC1)C1=CC=CC=C1)=O YTAHJIFKAKIKAV-XNMGPUDCSA-N 0.000 description 1
- 238000005299 abrasion Methods 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 239000013566 allergen Substances 0.000 description 1
- 230000002009 allergenic effect Effects 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 239000012871 anti-fungal composition Substances 0.000 description 1
- 230000000843 anti-fungal effect Effects 0.000 description 1
- 229940030225 antihemorrhagics Drugs 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 230000003385 bacteriostatic effect Effects 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 235000013871 bee wax Nutrition 0.000 description 1
- 239000012166 beeswax Substances 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 239000000227 bioadhesive Substances 0.000 description 1
- 239000012620 biological material Substances 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 230000001914 calming effect Effects 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 229910002092 carbon dioxide Inorganic materials 0.000 description 1
- 229960003405 ciprofloxacin Drugs 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 230000035602 clotting Effects 0.000 description 1
- 229940000425 combination drug Drugs 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 239000002537 cosmetic Substances 0.000 description 1
- 238000005520 cutting process Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 238000002651 drug therapy Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 208000004000 erythrasma Diseases 0.000 description 1
- PGBHMTALBVVCIT-VCIWKGPPSA-N framycetin Chemical compound N[C@@H]1[C@@H](O)[C@H](O)[C@H](CN)O[C@@H]1O[C@H]1[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](N)C[C@@H](N)[C@@H]2O)O[C@@H]2[C@@H]([C@@H](O)[C@H](O)[C@@H](CN)O2)N)O[C@@H]1CO PGBHMTALBVVCIT-VCIWKGPPSA-N 0.000 description 1
- 239000003349 gelling agent Substances 0.000 description 1
- 229960002518 gentamicin Drugs 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- 244000144993 groups of animals Species 0.000 description 1
- 229910001385 heavy metal Inorganic materials 0.000 description 1
- 239000001307 helium Substances 0.000 description 1
- 229910052734 helium Inorganic materials 0.000 description 1
- SWQJXJOGLNCZEY-UHFFFAOYSA-N helium atom Chemical compound [He] SWQJXJOGLNCZEY-UHFFFAOYSA-N 0.000 description 1
- 239000002874 hemostatic agent Substances 0.000 description 1
- 238000003898 horticulture Methods 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 239000002054 inoculum Substances 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 230000001788 irregular Effects 0.000 description 1
- 229940074928 isopropyl myristate Drugs 0.000 description 1
- 210000001117 keloid Anatomy 0.000 description 1
- 230000002147 killing effect Effects 0.000 description 1
- 235000019388 lanolin Nutrition 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 239000008308 lipophilic cream Substances 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 230000007721 medicinal effect Effects 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 229960003085 meticillin Drugs 0.000 description 1
- 244000000010 microbial pathogen Species 0.000 description 1
- 239000003607 modifier Substances 0.000 description 1
- 230000001333 moisturizer Effects 0.000 description 1
- 230000003232 mucoadhesive effect Effects 0.000 description 1
- 210000004400 mucous membrane Anatomy 0.000 description 1
- DDHVILIIHBIMQU-YJGQQKNPSA-L mupirocin calcium hydrate Chemical compound O.O.[Ca+2].C[C@H](O)[C@H](C)[C@@H]1O[C@H]1C[C@@H]1[C@@H](O)[C@@H](O)[C@H](C\C(C)=C\C(=O)OCCCCCCCCC([O-])=O)OC1.C[C@H](O)[C@H](C)[C@@H]1O[C@H]1C[C@@H]1[C@@H](O)[C@@H](O)[C@H](C\C(C)=C\C(=O)OCCCCCCCCC([O-])=O)OC1 DDHVILIIHBIMQU-YJGQQKNPSA-L 0.000 description 1
- 229950006780 n-acetylglucosamine Drugs 0.000 description 1
- 229940053050 neomycin sulfate Drugs 0.000 description 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 1
- 231100000344 non-irritating Toxicity 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 238000006213 oxygenation reaction Methods 0.000 description 1
- 230000037368 penetrate the skin Effects 0.000 description 1
- 235000019271 petrolatum Nutrition 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 230000004260 plant-type cell wall biogenesis Effects 0.000 description 1
- 231100000614 poison Toxicity 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 229960001621 povidone-iodine Drugs 0.000 description 1
- 239000000955 prescription drug Substances 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 230000001172 regenerating effect Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 229960003600 silver sulfadiazine Drugs 0.000 description 1
- UEJSSZHHYBHCEL-UHFFFAOYSA-N silver(1+) sulfadiazinate Chemical compound [Ag+].C1=CC(N)=CC=C1S(=O)(=O)[N-]C1=NC=CC=N1 UEJSSZHHYBHCEL-UHFFFAOYSA-N 0.000 description 1
- 238000009097 single-agent therapy Methods 0.000 description 1
- URWAJWIAIPFPJE-YFMIWBNJSA-N sisomycin Chemical compound O1C[C@@](O)(C)[C@H](NC)[C@@H](O)[C@H]1O[C@@H]1[C@@H](O)[C@H](O[C@@H]2[C@@H](CC=C(CN)O2)N)[C@@H](N)C[C@H]1N URWAJWIAIPFPJE-YFMIWBNJSA-N 0.000 description 1
- 230000037380 skin damage Effects 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- APSBXTVYXVQYAB-UHFFFAOYSA-M sodium docusate Chemical compound [Na+].CCCCC(CC)COC(=O)CC(S([O-])(=O)=O)C(=O)OCC(CC)CCCC APSBXTVYXVQYAB-UHFFFAOYSA-M 0.000 description 1
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 1
- 159000000000 sodium salts Chemical group 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 239000007916 tablet composition Substances 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 239000003440 toxic substance Substances 0.000 description 1
- 208000012313 wound discharge Diseases 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/06—Ointments; Bases therefor; Other semi-solid forms, e.g. creams, sticks, gels
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/575—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of three or more carbon atoms, e.g. cholane, cholestane, ergosterol, sitosterol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0014—Skin, i.e. galenical aspects of topical compositions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Life Sciences & Earth Sciences (AREA)
- Epidemiology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Dermatology (AREA)
- Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
creme medicinal de ácido fusídico preparado utilizando fusidato de sódio e incorporando um biopolímero e seu processo de preparação. a presente invenção se refere a uma composição medicinal para o tratamento de infecções bacterianas da pele feridas relacionadas, e também outras feridas de pele incluindo aquelas causadas por queimaduras. o creme também causa rejuvenescimento da pele através do processo de epitelização. o creme compreende um biopolímero na forma de quitosana, b) um ingrediente ativo farmacêutico (api) na forma de ácido fusídico, c) uma base creme e d) água. a invenção também divulga um processo para preparar o creme medicinal na qual o ácido fusídico que é formado in situ a partir de fusidato de sódio como matéria-prima , convertendo-o em ácido fusídico sob ambiente livre de oxigênio criado usando gás inerte, preferivelmente nitrogênio. o creme produzido pelo processo da presente invenção tem uma maior estabilidade de vida de prateleira e tamanho das partículas menores do api do que os cremes convencionais que contêm ácido fusídico e descobriu-se ser surpreendentemente superior para o uso contra infecções de pele com alergia e prurido, e ferimentos em pele humana do que cremes alternativos atualmente disponíveis.
Description
A presente invenção refere-se ao tratamento de infecções dermatológicas bacterianas primárias e secundárias e feridas incluindo queimaduras. Em particular, refere-se a um creme incorporando ácido fusídico e um biopolímero na forma de quitosana e o processo de preparação do mesmo e sua utilização no tratamento dessas infecções e feridas. Além disso, o ácido fusídico no dito creme que foi gerado in situ usando fusidato de sódio como princípio ativo farmacêutico (API) de partida.
Inúmeros tratamentos, tópico e sistêmico, estão disponíveis para infecção dermatológica primária e secundária causada por organismos Gram-positivos sensíveis como Staphylococcus aureus, Streptococcus spp, etc. Composições de tratamento de infecção bacteriana tópica e sistêmica tipicamente empregam pelo menos um princípio ativo farmacêutico (API) em combinação com um componente base. Na forma de creme, os API’s tipicamente compreendem um antibiótico/antibactericida, tal como, ácido fusídico e similares.
Em cremes de ácido fusídico comercialmente disponíveis, o ácido fusídico na forma de pó fino é utilizado como fonte de API. O menor tamanho de partícula aumenta o seu contato com a pele por prover uma ampla superfície de contato específica e penetração, e proporciona uma suave sensação na aplicação à pele. No entanto, uma grave deficiência para o tamanho de partículas finas do ácido fusídico é que apresenta uma grande área de superfície para o contato e reação com moléculas de oxigênio durante fabricação, manipulação e processamento do creme. Isto apresenta sérias implicações a sua estabilidade química e resulta em rápida redução na potência do API (ácido fusídico) na formulação final do creme.
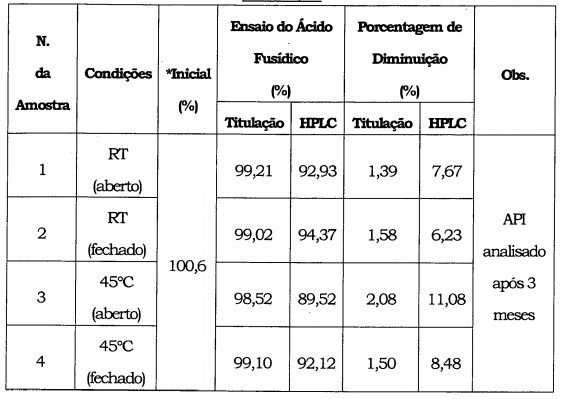
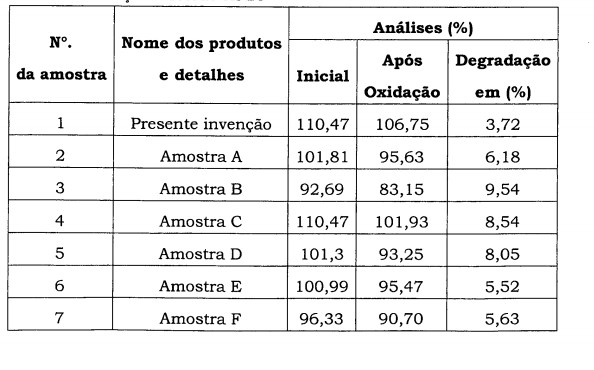
A degradação devido à oxigenação é a principal causa da instabilidade dos cremes de ácido fusídico atualmente disponíveis. A tabela 1 mostra que a degradação nas amostras de API (ácido fusídico) expostas ao oxigênio varia entre 7,7% e 11% para condições variando de temperatura ambiente a 45°C quando analisados num período de exposição de três meses nas condições acima.
Sabe-se que quanto maior o tempo de exposição do ácido fusídico como matéria-prima do API ao oxigênio, maiores as limitações de estabilizar o ácido fusídico em uma formulação. No entanto, não há dados publicados sobre a estabilidade do ácido fusídico durante um período de tempo.
Como uma alternativa para o ácido fusídico, o fusidato de sódio é conhecido por estar sendo utilizado para fazer medicamentos dermacêuticos para aplicação tópica. No entanto, estes estão na forma de pomada ao invés de creme. Os inconvenientes das pomadas sobre os cremes são bem conhecidos e é geralmente preferido o uso de creme ao invés de pomadas para aplicação tópica.
Vários aspectos do ácido fusídico como um API são conhecidos: • Ser termolábil; • Estar disponível em formulações de creme; • Poder ser obtido a partir do fusidato de sódio por dissolução do último em uma fase aquosa e adicionando ácido à solução, pelo qual o ácido fusídico precipita. No entanto, o ácido fusídico é difícil de processar na forma de creme, primeiro devido ao seu tamanho de partículas grossas e irregulares e, segundo recuperar o ácido fusídico de um bolo úmido envolve secagem e posterior manipulação o qual deteriora o ácido fusídico devido à exposição ao oxigênio. • A estabilidade do API em um creme de ácido fusídico é incerta devido à natureza termolábil do ácido fusídico.
A estabilização de medicamentos contendo ácido fusídico versusoxidação envolve observar uma série de rigorosos procedimentos de precaução durante fabricação e armazenamento. Estes incluem: • substituir o oxigênio em recipientes farmacêuticos com gases inertes, tais como, nitrogênio, dióxido de carbono, hélio e similares. • evitar o contato do medicamento com íons de metal pesado os quais catalisam a oxidação, • armazenar o API em temperaturas reduzidas por toda sua vida de prateleira antes do processamento.
Na pratica isso significa controles mais restritos durante produção bem como o armazenamento de tal API (armazenando-o normalmente de 2°C a 8°C em recipientes hermeticamente fechados em toda a sua vida de prateleira).
Há, portanto a necessidade de fornecer um processo de obtenção de um creme de ácido fusídico em que o ácido fusídico apresentará maior estabilidade que a estabilidade do cremes convencionais de ácido fusídico, particularmente, no momento da fabricação do creme, e que sustentará sua estabilidade em um nível aceitável durante toda a sua vida de prateleira.
Em seguida, vamos olhar para os tipos de doenças dermatológicas e os métodos de tratamento disponíveis para eles. Doenças de pele podem ser amplamente classificadas como aqueles decorrentes de formas de bactérias ou fungos. Composições antifúngieas ou antibacterianas são tradicionalmente aplicadas como loções, cremes ou pomadas. Além disso, em muitos casos, é difícil de saber se a condição da pele é devido a um agente bacteriano ou fungo.
Uma abordagem para o tratamento de doenças dermatológicas é através da eliminação por tentativa e erro. Composições antibacterianas ou antifúngicas são aplicadas, por sua vez e a resposta monitorada e o tratamento modificado. A grande desvantagem desta abordagem é que o tratamento deve ser aplicado várias vezes ao dia durante o período de tratamento. Isso é muito inconveniente e também não é rentável para a maioria da população humana, particularmente nas nações subdesenvolvidas.
Existem vários tratamentos disponíveis para tratar doenças de pele causadas por bactérias ou fungos. Tipicamente, tais composições usam esteróides, agentes antibacterianos ou antifúngicos, (ou uma combinação de dose fixa destes) e concentram-se nesses ingredientes farmaceuticamente ativos. A composição de tais formulações é a base para aprimorar seu perfil químico/ físico/bioliberação.
Várias doenças de pele causada pela inflamação bacteriana e ataques bacterianos levam ao prurido e coceiras subsequentes, que, entre outras causas, pode levar a graves e complicadas infecções secundárias. Os tratamentos convencionais disponíveis não incidem sobre a cicatrização da pele ou rejuvenescimento, normalmente estes dois aspectos são deixados para a cura natural.
A palavra cura relacionada às condições da pele comprometida (cortes, feridas, infecções, inflamações, escoriações, etc.) não são apenas sobre a prevenção, controle, eliminação da causa, como bactérias ou fungos, mas também para restaurar a pele ao seu estado de pré-infecção.
As abordagens atuais de tratamento da pele podem ser classificadas em duas etapas, a. cura; b. restauração da pele ao estado da pré-doença. A parte da cura inclui a eliminação, na medida do possível, da raiz da causa da doença. Este pode ser a eliminação de bactérias ou fungos que causam a infecção através de um tratamento adequado de agentes antibacterianos ou antifúngicos ou redução da inflamação através de tratamento com esteróides. Embora este tratamento esteja em andamento, a condição permanente comprometida da pele continua a ser suscetíveis a infecções secundárias que podem ser de natureza muito grave. No caso da pele arranhada ou ferida, é importante para a coagulação sanguínea ocorrer rapidamente, reduzir as chances de infecções secundárias. O foco desses tratamentos, que são administrados através de cremes, loções, pomadas é sobre a ação de ingredientes farmacêuticos ativos. Bases de creme ou bases de pomada são apenas vistos como veículos para a administração de API’s para os locais da doença.
No entanto, o aspecto de restauração da pele de volta ao seu estado de pré-doença é quase que completamente deixado para a natureza. Portanto, uma desvantagem principal das abordagens do tratamento dermatológico existente é que eles mantêm o risco de infecções secundárias devido ao lento processo de coagulação sanguínea e cura da ferida.
Além disso, a partir do estudo de várias faltas de aspectos do estado da técnica dos produtos dermatológicos de prescrição existentes utilizados para o tratamento tópico de doenças de pele. Isto é manifestado pelo fato de que a matriz da base do creme ou da base da pomada tem sido negligenciada por quaisquer potenciais benefícios terapêuticos. Em particular, nenhum das composições do estado da arte sugere: - Formulações dermatológicas tópicas podem proporcionar a cura ou regeneração da pele além da atividade dos principais API’s de tal forma que o efeito terapêutico dos principais API’s seja reforçado. - A adição de polímeros biologicamente ativos (os chamados biopolímeros) é um processo complexo em que a estabilidade das formulações pode ser comprometida se o biopolímero correto ou excipientes da formulação interagindo naturalmente ou parâmetros do processo não forem bem estudadas e otimizadas para melhorar e complementar os resultados da terapia na fase de concepção do medicamento em si. - Incorporação de um polímero excipiente funcionalmente bioativo na matriz creme, mantendo a estabilidade funcional do API em um formato de dose única do creme dermacêutico envolve a resolução de problemas específicos para a estabilidade física da matriz creme.
Um olhar sobre algumas das patentes existentes ilustra os pontos acima. O ácido fusídico tem sido utilizado na forma de creme. A publicação internacional WO 2009/063493 revela uma terapia de combinação de um antibiótico tópico e um esteróide tópico para o tratamento de dermatoses inflamatórias associadas com infecções bacterianas secundárias. Em particular, refere-se a composições farmacêuticas tópicas compreendendo uma combinação de ácido fusídico e corticosteróides, como o furoato de mometasona útil no tratamento de eczema infectado, tais como dermatites secundárias infectadas, incluindo dermatite secundária de contato infectada, psoríase, dermatite de contacto alérgica e dermatite atópica com infecções bacterianas secundárias da pele. Em particular, a publicação reivindica composições farmacêuticas tópicas compreendendo uma combinação de ácido fusídico e corticosteróides como o furoato de mometasona útil na prevenção de infecção em casos de dermatite, especialmente dermatites atópicas que sofrem de dermatite atópica que estão em risco de contrair a infecção bacteriana secundária.
As reivindicações do pedido produzem inventividade na afirmação de que o estado da técnica não revela composição que compreende uma combinação de ácido fusídico com corticosteróides, especialmente, mometasona ou halobetasol. Os inventores da [publicação internacional WO 2009/063493 surpreendentemente descobriram que a ação antibiótica do ácido fusídico e o efeito antiinílamatório do corticosteróide, como mometasona onde ambos desempenham um papel importante na redução de S. aureuse melhoram os sintomas do paciente e os sinais de infecções inflamatórias da pele. Os inventores do WO 2009/063493 também, surpreendentemente descobriram que a ação antibiótica de ácido fusídico e o efeito antiinílamatório do corticosteróide, como halobetasol, onde ambos desempenham papéis importantes na prevenção de infecções bacterianas secundárias em pacientes com dermatoses não- infecciosas e em tratamento de dermatoses infecciosa responsivas aos esteróides, dermatose secundária infectadas, incluindo dermatite secundária de contato infectada, dermatite de contacto alérgica, dermatite atópica, psoríase e outras dermatoses responsivas aos corticosteróides (CRD) com infecções bacterianas secundárias da pele.
A invenção divulgada na publicação internacional WO 2009/063493 refere-se a uma terapia de combinação de um antibiótico tópico e um esteróide tópico para o tratamento de dermatoses inflamatórias associadas com infecções bacterianas secundárias. Em particular, a presente invenção refere-se a composições farmacêuticas tópicas compreendendo uma combinação de ácido fusídico e corticosteróide, tal como, o furoato de mometasona útil no tratamento de eczema infectado como dermatite secundária infectada, incluindo dermatite secundária de contato, infectada, psoríase, dermatite de contacto alérgica e dermatite atópica com infecções bacterianas secundárias da pele. Em particular, a presente invenção também se refere a composições farmacêuticas tópicas compreendendo uma combinação de ácido fusídico e corticosteróide, tal como, o furoato de mometasona útil na prevenção de infecção nos casos de dermatite, especialmente dermatites atópicas que sofrem de dermatite atópica que estão em risco de contrair a infecção bacteriana secundária.
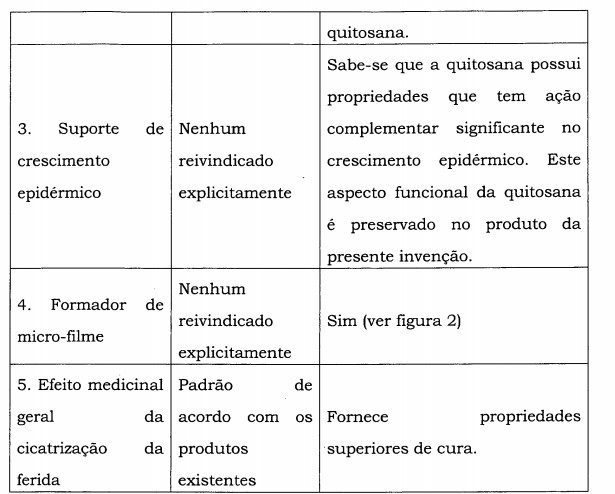
É evidente a partir do exemplo acima e outras fontes semelhantes que o estado da técnica não ensina ou sugere: - Uso da matriz da base do creme como um elemento funcional do creme ao invés de um mero carreador para os API’s principais. - Usar um conhecido biopolímero como excipiente funcional junto com o agente bacteriano fusidato de sódio. - Fornecer efeitos de cura muito superior como a formação do microfilme, coagulação sanguínea, suportar o crescimento epidérmico, imobilização eletrostática microbiana em vigor simultaneamente, em vez de uma após a outra, como seria o caso na terapia de droga única convencional. - Melhorar de forma geral as propriedades medicinais do creme, complementando o API utilizado na matriz do creme.
Há, portanto, a necessidade de um tratamento tópico de dose única do API que será provido em uma base de creme, que base de creme forneça um valor terapêutico complementar ao proporcionado pelos API’s principais e sirva a uma melhor proposta de ser um mero carreador ou mecanismo de liberação.
Portanto, é um objeto da presente invenção fornecer um processo de preparação de um creme medicinal que contenha ácido fusídico como API ativo, mas que apresente uma maior estabilidade do API do que o ácido fusídico fabricado utilizando outros meios, ao longo de sua vida de prateleira, usando uma base de creme funcional que contenha quitosana que proporcionará um tratamento eficaz contra infecções bacterianas e também auxiliar ativamente pele rejuvenescer.
Outro objeto da presente invenção é fornecer um creme medicinal que seja eficaz no tratamento de feridas, incluindo queimaduras.
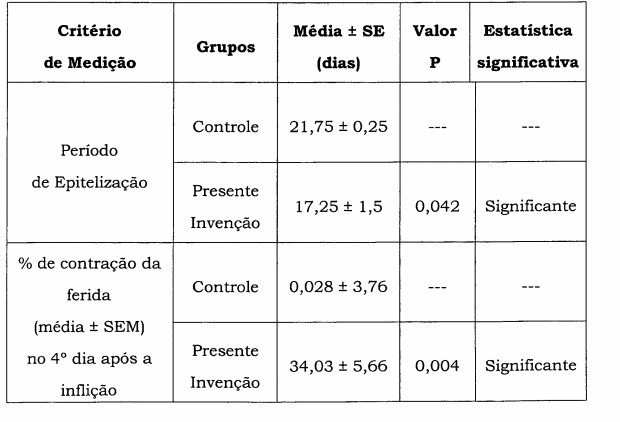
Ainda, objetos da presente invenção fornecem formulações de prescrição medicinal para tratamento tópico da pele que: - Possam proporcionar a cicatrização da pele ou regeneração além da atividade do fusidato de sódio de tal forma que o efeito terapêutico do API principal é reforçado.
Contenham polímeros biologicamente ativos (os chamados biopolímeros), sem comprometer a estabilidade das formulações que possam ser comprometidas se o biopolímero correto não for selecionado. - Incorporem um polímero excipiente funcionalmente bioativo na matriz do creme, mantendo a estabilidade funcional do API em um formato dose única.
A figura 1 mostra a natureza não-homogénea dos cremes contendo quitosana com excipientes não-compatíveis, como carbômero.
A figura 2 demonstra a formação de filme usando quitosana.
A presente invenção é direcionada a uma composição medicinal para o tratamento de infecções bacterianas da pele e feridas relacionadas, e também feridas na pele, incluindo aquelas causadas por queimaduras. O creme também provoca o rejuvenescimento da pele através de um processo de epitelização. O creme é composto por: a) um biopolímero na forma de quitosana; b) um ingrediente farmacêutico ativo (API), na forma de ácido fusídico que foi gerado in situa partir de fusidato de sódio; c) uma base de creme contendo tensoativos primários e secundários, materiais cerosos, co-solventes, ácidos, conservantes, agentes tamponantes, antioxidantes, agentes quelantes e umectantes; d) água.
Os ingredientes ativos, ou seja, a quitosana e um agente antibacteriano são incorporados na base creme para o uso no tratamento de infecções bacterianas da pele com alergia e prurido, e feridas na pele humana envolvendo o contato da pele humana com a composição acima identificada.
A invenção também divulga um processo de preparação do creme medicinal contendo ácido fusídico que é formado in situa partir de fusidato de sódio como matéria-prima de partida, onde o fusidato de sódio é convertido em ácido fusídico em ambiente livre de oxigênio criado usando gás inerte, de preferência, nitrogênio e quitosana. O creme produzido pelo processo da presente invenção tem uma maior estabilidade de vida de prateleira e tamanho de partícula mais finas do API do que os cremes convencionais que contêm ácido fusídico. O creme produzido pelo processo da presente invenção contém ácido fusídico como a API que foi formado in situa partir do fusidato de sódio, em uma base de creme compreendendo um conservante, um ácido, um co- solvente, um tensoativo e um material ceroso, juntamente com água, de preferência água purificada.
O creme produzido pelo processo da presente invenção opcionalmente contém um ingrediente selecionado de um grupo que compreende um agente de tamponamento, um antioxidante, um agente quelante, e um umectante, ou qualquer combinação destes.
Discutimos anteriormente os aspectos conhecidos das preparações tópicas contendo ácido fusídico e fusidato de sódio como API’s. É evidente a partir do estado da técnica de que: - Cremes contendo ácido fusídico que é preparado usando fusidato de sódio como API de partida não estão disponíveis.
Não há dados publicados sobre a estabilidade do fusidato de sódio como API. O fusidato de sódio não é considerado inerentemente mais estável como API do que o ácido fusídico. - Cremes contendo quitosana e ácido fusídico que foi criado in situ a partir do fusidato de sódio não estão disponíveis comercialmente.
Em face disto, foi surpreendentemente descoberto que o fusidato de sódio como API é significativamente mais estável do que o ácido fusídico e que o ácido fusídico se deteriora mais rapidamente do que fusidato de sódio.
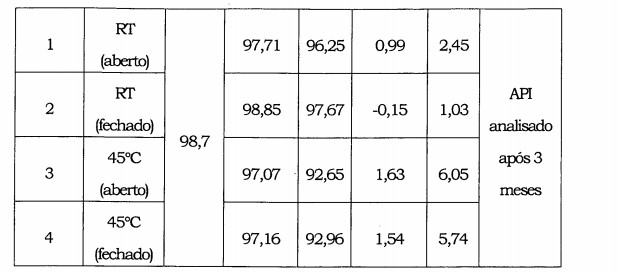
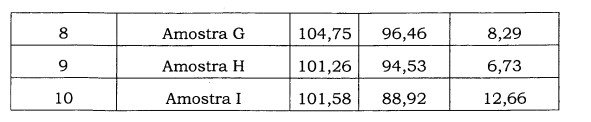
Não há dados publicados sobre a estabilidade do fusidato de sódio como API. O Depositante realizou experimentos com fusidato de sódio para avaliar a sua estabilidade. Eles podem ser vistos na tabela 2 que a degradação do fusidato de sódio em uma faixa de temperatura da temperatura ambiente a 45°C variaram entre 2,45% e 6%.
As tabelas 1 e 2 também mostram a comparação entre a estabilidade do ácido fusídico e fusidato de sódio como API’s. O estudo foi efetuado através de um método de HPLC in-house desenvolvido pelo Depositante, cujo acredita ser um método indicador de estabilidade real ao contrário do método de titulação sugerido na Farmacopéia Britânica (FB). Isso ocorre porque o método FB não diferencia entre o API intacto e sob a forma degradada. ANÁLISES DE ESTABILIDADE DO ÁCIDO FUSÍDICO: TABELA 1: RESULTADOS DE 3 MESES DE ANÁLISE DO ÁCIDO FUSÍDICO(API) ANTERIOR POR MÉTODO DE HPLC INDICADOR DE ESTABILIDADE E MÉTODO DE TITULAÇÃO
Nome da amostra: Ácido fusídico (Farmacopeia Britânica - (FB)). Embalagem: Placa de PetriAberta e Fechada. ANALISES DE ESTABILIDADE DO FUSIDATO DE SÓDIO: TABELA 2: RESULTADOS DE 3 MESES DE ANÁLISE DO FUSIDATO DE SÓDIO (API) POR MÉTODO DE HPLC INDICADOR DE ESTABILIDADE E MÉTODO DE TITULAÇÃO
Nome da amostra: Fusidato de Sódio (Farmacopéia Britânica - (FB)). Embalagem: Placa de PetriAberta e Fechada.
Em ambos os estudos o *Inicial denota os resultados das amostras testadas no momento do recebimento do API pelo fornecedor.
Pode ser observado nas tabelas 1 e 2 que: • No caso do ácido fusídico, há cerca de 7,7% de perda em 3 meses em temperatura ambiente (condição aberta) e cerca de 11% de perda em 3 meses a 45°C (condição aberta). • No caso do fusidato de sódio, há cerca de 2,5% de perda em 3 meses em temperatura ambiente (condição aberta) e cerca de 6% de perda em 3 meses a 45°C (condição aberta).
Assim os dados mostram que o fusidato de sódio como um API é mais estável que o ácido fusídico.
A Depositante explorou a possibilidade de elaborar um creme (ao invés de uma pomada) contendo quitosana e fusidato de sódio (ao invés de ácido fusídico) como matéria-prima. Embora o fusidato de sódio tenha sido usado em aplicações dermacêuticas, não foi possível elaborar cremes que usem fusidato de sódio. Isto por causa da inerente alcalinidade do fusidato de sódio (pH 7,5 a 9), que significa não pode ser usado na forma de creme, portanto todos os produtos fabricados usando fusidato de sódio como matéria-prima são pomadas. Um creme dermacêutico que usa fusidato de sódio exploraria o beneficio do fato que o fusidato de sódio é mais estável que o ácido fusídico e também forneceria uma formulação creme da qual é superior em sua qualidade de aplicação do que uma pomada. Assim, preencheria uma necessidade existente para um creme que teria melhor estabilidade do que os cremes atualmente disponíveis contendo ácido fusídico.
A requerente, portanto, descobriu surpreendentemente que, a fim de alcançar maior estabilidade do API em um creme dermacêutico, o fusidato de sódio ao invés de ácido fusídico pode ser usado como matéria-prima do API durante a fabricação dos cremes. Usando fusidato de sódio como matéria-prima elimina a desvantagem associada com a fabricação e armazenamento dos cremes de ácido fusídico existentes.
A requerente também descobriu que o creme de ácido fusídico preparado usando fusidato de sódio como matéria-prima do API mostra boa estabilidade química, eficácia e sensibilidade microbiana.
A Depositante descreve um processo para a fabricação de um creme contendo ácido fusídico (o API) que foi preparado usando fusidato de sódio como matéria-prima do API, em que o ácido fusídico forma in situsob ambiente totalmente livre de oxigênio criado utilizando um gás inerte, preferencialmente, nitrogênio por lenta adição de um ácido, em uma forma molecular de dispersão (devido à presença de um co-solvente) na fase intermediária, e em que o ácido fusídico regenera como uma dispersão extremamente fina quando adicionado a uma base creme final, resultando assim em um ácido fusídico disperso finamente e homogeneamente no creme final. Todas essas operações são realizadas em um ambiente livre do oxigênio atmosférico criado utilizando gás inerte, preferencialmente, nitrogênio. O creme feito usando o processo da presente invenção contém ácido fusídico como o ingrediente ativo (API) que foi formado in situa partir de fusidato de sódio, em uma base creme compreendendo um agente de tamponamento, um conservante, um ácido, um co-solvente, um tensoativo e um material ceroso junto com água, preferencialmente, água purificada.
O fusidato de sódio que pode ser empregado no processo da presente invenção como matéria-prima do API é bem conhecido no estado da técnica para o tratamento de infecções bacterianas primárias e secundárias.
O composto ativo fusidato de sódio requer um componente base para ser usado na composição farmacêutica que use o composto, desde que o composto não possa, entre si, ser depositado diretamente sobre a pele humana devido sua dureza.
O componente base usualmente contém um biopolímero, tensoativos primários e secundários, material ceroso, co-solventes, ácidos, conservantes, água purificada e similares.
A base creme do creme preparado utilizando o processo da presente invenção, opcionalmente, inclui um ingrediente selecionado de um grupo composto por um antioxidante, um agente quelante e um umectante ou qualquer combinação dos mesmos.
A presente invenção provê um processo para a fabricação de um novo creme que foi produzido usando fusidato de sódio como matéria-prima, e na qual o creme contém ácido fusídico de alta eficácia terapêutica e de estabilidade química que é geralmente superior aos cremes comercialmente disponíveis contendo ácido fusídico.
O creme de ácido fusídico elaborado pelo processo da presente invenção foi produzido em um ambiente totalmente livre de oxigênio sob purga com gás inerte e aplicação de vácuo o gás inerte sendo preferencialmente, nitrogênio. Sob estas condições, o fusidato de sódio é convertido in situem ácido fusídico. O creme da presente invenção é usado em tratamento de infecções bacterianas dermatológicas.
A partir do estudo do estado da técnica várias faltas de aspectos de formulações de tratamento tópico existentes no campo de medicamentos de prescrição são evidentes. O estado da técnica não ensina ou sugere que: - Formulações dermatológicas tópicas podem proporcionar a cura ou regeneração da pele além da atividade dos principais API’s de tal forma que o efeito terapêutico dos principais API’s seja reforçado. - A adição de polímeros biologicamente ativos (os chamados biopolímeros) é um processo complexo em que a estabilidade das formulações pode ser comprometida se o biopolímero correto não for selecionado. - Incorporação de um polímero excipiente funcionalmente bioativo na matriz creme, mantendo a estabilidade funcional do API em um formato de dose única do creme dermacêutico envolve a resolução de problemas específicos para a estabilidade física da matriz creme.
Exemplos de agentes antibacteriano tópico adequados, que podem ser usados, incluem, porém não se limitam ao sulfato de neomicina, fusidato de sódio, mupirocina de cálcio, gentamicina, sulfadiazina de prata, ciprofloxacina, sulfato de framicetina, quinidoclor, iodopovidona, sisomicina, nitro furai e seus similares.
Exemplos de biopolímeros adequados, que podem ser utilizados, incluem, mas não se limitam a quitosana e similares.
A quitosana é um polissacarídeo linear composto por ligações β-(l-4)-D-glucosamina (unidade desacetilada) e N-acetil-D- glucosamina (unidade acetilada). A quitosana é conhecida por ter um número de usos comerciais na agricultura e horticultura, tratamento de água, indústria química, farmacêutica e biomédica.
Suas conhecidas propriedades incluem acelerar a coagulação sanguínea. No entanto, não é conhecido por técnicos no assunto que o comportamento da quitosana com um ingrediente ativo farmacêutico, como um agente antibacteriano ou antifúngico precisa ser tratado com precaução.
Ela é conhecida por ter propriedades de formação de filme, mucoadesiva e aumento de viscosidade e tem sido utilizada como aglutinante e um agente desintegrante em formulações de comprimidos.
A quitosana geralmente absorve a umidade da atmosfera/ ambiente e a quantidade absorvida depende do teor de umidade inicial, temperatura e a umidade relativa do ambiente.
É considerada como um material não-tóxico e não-irritante. É biocompatível com a pele saudável e infectada e tem demonstrado ser biodegradável, uma vez que é derivado de camarões, lulas e caranguejos.
A quitosana, devido à sua propriedade física única acelera a cura de feridas e cicatrização. É positivamente carregada e solúvel em solução ácida a neutra. A quitosana é bioadesiva e se liga prontamente a superfícies carregadas negativamente, tais como as membranas das mucosas. A quitosana aumenta o transporte de drogas polares através das superfícies epiteliais. As propriedades da quitosana permitem a ela coagular o sangue rapidamente, e recentemente ganhou a aprovação nos EUA para uso em bandagens e outros agentes hemostáticos.
A quitosana é não-alergênica e tem propriedades naturais antibacterianas, adicionalmente, reforçando seu uso. Como um biomaterial formador de micro-filme, a quitosana auxilia na redução da extensão da ferida, controla a permeabilidade ao oxigênio no local, absorve as descargas da ferida e degrada através das enzimas do tecido que são extremamente necessárias para a cura em um ritmo mais rápido. Também reduz a prurido, proporcionando um efeito calmante. Ela também atua como um hidratante. Também é útil no tratamento de cortes de rotina e pequena feridas, queimaduras, quelóides, úlceras diabéticas e úlceras venosas. A quitosana utilizada na presente invenção mostra-se em vários pesos moleculares variando de 1 kdal a 5.000 kdal.
A quitosana é discutida no fórum da Farmacopéia Americana (USP) em relação à sua categoria de excipiente funcional. Uma vez que a quitosana é basicamente um polímero, ela está disponível em vários graus, dependendo do peso molecular. Os vários graus de quitosana incluem quitosana de cadeia longa, quitosana de cadeia média e quitosana de cadeia curta. Os graus de cadeia longa, média e de curta correspondem diretamente ao peso molecular da quitosana.
Geralmente, o grau de cadeia longa tem um peso molecular na faixa de 500.000 a 5.000.000 Da, o grau de cadeia média tem um peso molecular na faixa de 1.000.000 a 2.000.000 Da e o grau de cadeia curta tem um peso molecular na faixa de 50.000 a 1.000.000 Da.
O peso molecular da quitosana desempenha um papel importante na formulação. Quitosana de maior peso molecular fornece uma maior viscosidade ao sistema e quitosana de baixo peso molecular transmite uma menor viscosidade ao sistema.
No entanto, a quitosana de grau de cadeia média proporcionou um ótimo nível de viscosidade para a formulação. Uma vez que a forma de dosagem é um creme, níveis adequados de viscosidade são necessários para atingir um bom espalhabilidade sobre a pele.
Os inventores decidiram pela quitosana de grau de cadeia média para a presente invenção, uma vez que transmitiu as propriedades reológicas necessárias ao creme, sem comprometer a atividade terapêutica dos ativos, por exemplo, fusidato de sódio como princípio ativo e quitosana. A concentração de quitosana de grau de cadeia média foi cuidadosamente alcançada com base em vários testes in house e estudos de pré-clínicos de animais para eficácia.
Os antibacterianos tópicos são pretendidos para serem utilizados na pele para infecções bacterianas causadas por Staphylococcus aureus, Staphylococcus epidermidis, Staphylococcus aureusresistentes à meticilina (MRSA), etc.
Os antibactericidas atuam pela inibição da síntese da parede celular através da combinação com os ribossomos bacterianos e interferindo com a combinação de mRNA ribossomo.
Em outra hipótese acredita-se que antibacterianos induzem os ribossomos produzirem cadeias peptídicas com aminoácidos errados, que destroem a célula bacteriana.
Fusidato de sódio pertence ao grupo de medicamentos conhecidos como antibióticos.
Ele é usado para tratar infecções bacterianas, como infecções das articulações e ossos, matando ou impedindo o crescimento das bactérias responsáveis.
A fórmula molecular do fusidato de sódio é C31H47. O nome químico é ácido de sal de sódio 3, 11,16 β-Trihidroxi 29-nor-8, 9 β, 13, 14 β-dammara-17 (20) [10,21-cis], 24-dien-21-óico 16-acetato. É um pó branco cristalino solúvel em uma parte da água a 20°C.
O fusidato de sódio inibe a síntese protéica bacteriana através da interferência com a transferência de aminoácidos de aminoacil-sRNA à proteína nos ribossomos. O fusidato de sódio pode ser bacteriostático ou bactericida, dependendo do tamanho do inóculo.
Embora as células bacterianas parem de se dividir por volta de 2 minutos após o contato com o antibiótico in vitro,a síntese de DNA e RNA continua por 45 minutos e 1 a 2 horas, respectivamente. O fusidato de sódio é praticamente inativo contra bactérias gram- negativas. Acredita-se que as diferenças de atividade contra organismos gram-negativos e gram-positivos sejam devido a uma diferença na permeabilidade da parede celular.
Células de mamíferos são muito menos susceptíveis à inibição da síntese de proteínas por fusidato de sódio do que as células bacterianas sensíveis. Acredita-se que essas diferenças sejam devido, principalmente, a uma diferença na permeabilidade da parede celular. Indicações: O fusidato de sódio é indicado para o tratamento de infecções de pele primárias e secundárias causadas por cepas sensíveis de S. aureus,espécies de Streptococcuse C. minutissimum. As infecções cutâneas primárias que podem ser esperadas para responder ao tratamento com fusidato sódio tópico incluem: impetigo contagioso, eritrasma e infecções secundárias de pele, como feridas infectadas e queimaduras infectadas.
A maioria dos produtos tópicos é formulada como cremes ou pomadas. Um creme é uma preparação tópica utilizada para aplicação na pele. Cremes são emulsões semi-sólidas, que são misturas de óleo e água, em que API’s (ingredientes ativos farmacêuticos) são incorporados. Eles são divididos em dois tipos: cremes óleo-em-água (O/A) que se compõem de pequenas gotas de óleo dispersas em uma fase aquosa contínua, e cremes água-em-óleo (A/O) compostos por pequenas gotículas de água dispersas em uma fase oleosa contínua. Os cremes óleo-em-água são de fácil utilização e, portanto, cosmeticamente aceitáveis, eles são menos gordurosos e facilmente lavados com água. Uma pomada é uma preparação viscosa semi-sólida contendo API’s, que são usadas topicamente sobre uma variedade de superfícies do corpo. O veículo de uma pomada é conhecido como base de pomada. A escolha de uma base depende da indicação clínica da pomada, e os diferentes tipos de bases pomada normalmente utilizados são: - Bases de hidrocarbonetos, por exemplo, parafina sólida, vaselina; - Bases de absorção, por exemplo, gordura de lã, cera de abelhas;
Ambas as bases acima são oleosas e gordurosas na natureza e isso leva a efeitos indesejáveis, como dificuldade na aplicação e remoção da pele. Além disso, isto também leva ao manchamento das roupas. A maioria dos produtos tópicos está disponível como formulação de creme, por causa de seu apelo cosmético.
A escala ácida do pH é de 1 a 7, e a escala básica do pH é de 7 a 14. O valor do pH das peles humanas está entre 4,5 e 6. O pH da pele de um bebê recém-nascido está mais perto do neutro (pH 7), mas rapidamente se transforma em ácida. A natureza desenvolveu isto provavelmente para proteger a pele das crianças pequenas, já que a acidez elimina as bactérias. Com as pessoas ficando mais velhas, a pele se torna mais e mais neutra, e não elimina tantas bactérias como antes. É por isso que a pele fica fraca e começa a ter problemas. O valor de pH vai para além de 6, quando uma pessoa tem realmente um problema de pele ou doenças de pele. Isso mostra que é necessário escolher apresentações tópicas que tenham um valor de pH próximo ao da pele de um jovem adulto.
Um leve deslocamento para o pH alcalino forneceria um ambiente melhor para os microorganismos se desenvolverem. A maioria dos produtos tópicos está disponível como creme. Os compostos ativos em formulações de creme estão disponíveis no estado ionizado, enquanto que, no caso de pomadas estas estão presentes em estado não-ionizado. Geralmente, as formulações de creme são a primeira escolha dos formuladores em desenho e desenvolvimento de formas farmacêuticas tópicas, como as formulações creme são cosmeticamente elegantes, e também como o composto ativo está disponível no estado ionizado, e a droga pode penetrar na camada de pele de forma rápida o que torna a formulação totalmente adequada ao paciente.
O pH do creme de quitosana com agente antibacteriano - fusidato de sódio da presente invenção é de cerca de 3 a 6. Por outro lado, pomadas que estão comercialmente disponíveis são gordurosas e não cosmeticamente elegantes. Além disso, como o composto ativo em uma pomada está na forma não-ionizada, a penetração na pele é lenta.
É essencial que o ingrediente ativo penetre na pele para a eficácia biodérmica ideal. O tamanho de partícula do ingrediente ativo desempenha um papel importante aqui. É necessário que o ingrediente ativo esteja disponível em estado coloidal ou molecular disperso para que o produto encontre-se na forma altamente eficaz. Também, este deverá ser alcançado em ambiente de pH seguro compatível com a pele (4,0 a 6,0). Para conseguir tudo isso, é essencial escolher veículos apropriados ou co-solventes para a dissolução ou dispersão da droga. O produto da presente invenção é altamente eficaz devido à atividade antibacteriana e de cicatrização da ferida dos ingredientes ativos, que estão disponíveis na forma coloidal de tamanho ultra-micro, o que aumenta a penetração cutânea.
Inúmeros tratamentos tópicos são empregados atualmente para o tratamento de infecções bacterianas. No entanto não existe uma terapia de dose-única eficaz para proteger a pele, controlando o sangramento superficial, feridas e queimaduras. Para atender essa necessidade e proporcionar uma terapia segura e acessível para o segmento da população dispersa em todos os países/ comunidades, uma terapia com combinação única de quitosana, um biopolímero com propriedades de rejuvenescimento da pele com antibacterianos é proposto como um novo creme.
O fusidato de sódio tópico tem grande eficácia em infecções bacterianas primárias e secundárias da pele de etiologia variada, devido a suas propriedades antibacterianas. A desvantagem da mono terapia com qualquer antibactericida tópico foi o início relativamente lento do efeito.
Através do emprego de fusidato de sódio e quitosana em uma formulação, as propriedades de ambos, antibactericida e a quitosana, são otimizados. Como a quitosana é material formador de filme, biocompatível e antialérgico ela auxilia a proteger a pele, agindo como uma barreira. Além disso, ela controla o sangramento superficial causado pelo arranhão e também interrompe a mobilidade dos patógenos, devido à sua carga catiônica.
As propriedades dos aspectos regenerativos da pele do fusidato de sódio e da quitosana são bem exploradas na presente invenção e o benefício máximo terapêutico é repassado para o paciente, com isso ajuda na cicatrização mais rápida. Isso garante que o paciente se beneficie no tratamento de feridas da pele e queimaduras com infecções bacterianas.
A inclusão da quitosana na formulação cuida de muitos atributos, que são considerados essenciais no tratamento de doenças da pele. A combinação da quitosana com fusidato de sódio é única e inovadora, uma vez que esta não está disponível comercialmente no mundo.
O conceito da combinação é justificado, considerando as propriedades físicas, químicas e terapêuticas da quitosana usada em combinação com ácido fusídico preparado in situa partir de fusidato de sódio.
Outro aspecto inventivo da presente invenção é que a adição de um excipiente funcional na base de creme não é um processo direto de mera adição. O inventor descobriu que a compatibilidade do excipiente funcional, tais como, a quitosana com outros agentes no creme é de fundamental importância. Isto porque a incompatibilidade iria comprometer a estabilidade do produto final. Como exemplos, os inventores descobriram que os excipientes conhecidos como goma xantana e carbômero que foram diversas vezes usados como agentes de estabilização, não podem ser utilizados em combinação com biopolímeros funcionais, tais como, a quitosana.
Os excipientes para formas farmacêuticas tópicas incluem polímeros, surfactantes, materiais cerosos, emulsificantes, etc. Os polímeros são usados como agentes gelificantes, agentes de suspensão, geradores de viscosidade, modificadores de liberação, diluentes, etc. Os surfactantes são utilizados como agentes umectantes, emulsificantes, agentes de solubilização intensificadores de liberação, etc.
Geralmente polímeros e surfactantes podem ou não possuir carga iônica. Eles podem ser de natureza aniônica, catiônica ou não- iônica. Se os excipientes aniônicos são incluídos na formulação eles interagem com excipientes catiônicos da formulação e produzem produtos que não são homogéneos, não esteticamente atraente e dão origem a produtos indesejados, possíveis alérgenos, impurezas, substâncias tóxicas, etc., devido à incompatibilidade.
Uma vez que a dose é para o tratamento de pacientes doentes, essas incompatibilidades nos produtos não podem ser aceitas e estas adicionam mais complicações para os pacientes.
Os inventores cuidadosamente selecionaram os excipientes que incluíram os polímeros e surfactantes para o desenvolvimento de uma formulação. Um estudo completo foi realizado após a triagem dos excipientes em curta lista. As possíveis interações entre os excipientes foram focalizadas e experimentos detalhados foram realizados. Para citar alguns exemplos sobre a interação aniônico- catiônica na forma de dosagem de creme os inventores propuseram algumas formulações de fusidato de sódio (ver tabelas 3 a 7), contendo goma xantana e quitosana, polímero de ácido acrílico e quitosana, lauril sulfato de sódio e quitosana, docusato de sódio e quitosana e goma arábica e quitosana. Os resultados indicam claramente a ocorrência de interações que foram muito visíveis e observando-se grumos em todo o sistema. O produto final também não estava esteticamente atraente, sem homogeneidade. A figura 1 anexa mostra claramente a interação entre a quitosana e excipientes aniônicos inadequados. Com base nas observações e no completo conhecimento sobre os excipientes, os inventores chegaram a uma fórmula robusta, sem qualquer possibilidade de interação. TABELA 3 CREME DE ÁCIDO FUSÍDICO INCORPORANDO QUITOSANA E GOMA XANTANA
TABELA 4 CREME DE ÁCIDO FUSÍDICO INCORPORANDO QUITOSANA E POLÍMERO DE ÁCIDO ACRÍLICO
TABELA 5 CREME DE ÁCIDO FUSÍDICO INCORPORANDO QUITOSANA E LAURIL SULFATO DE SÓDIO TABELA6 CREME DE ÁCIDO FUSÍDICO INCORPORANDO QUITOSANA E DOCUSATO DE SÓDIO TABELA 7 CREME DE ÁCIDO FUSÍDICO INCORPORANDO QUITOSANA E GOMA ARÁBICA
Os produtos acima (tabelas 3 a 7) são exemplos de produtos que não formam cremes homogêneos, e produzem cremes não- homogêneos do tipo ilustrado na figura 1. Ainda, as proporções estabelecidas nestes exemplos são as únicas que um técnico no assunto 5 pode usar com base no conhecimento disponível atualmente. Somente após de completos e extensos ensaios e erros foi possível chegar a certos tipos e proporções de excipientes.
Como já discutido anteriormente em uma terapia, o ácido fusídico proporciona alívio contra infecções bacterianas. No entanto, os 10 aspectos, tais como, a proteção da pele, o sangramento no local, a mobilidade de patógenos de um local para outro, etc., não são abordados até agora em uma terapia de dose-única que inclui ácido fusídico gerado in situa partir de fusidato de sódio.
Esta invenção presente com a sua aplicação de dose-única 15 preenche esta lacuna através da incorporação de quitosana e atesta os benefícios exigidos de proteção da pele (por meio da propriedade formação de filme), parando o sangramento (por meio de propriedade de coagulação do sangue) e imobilização de microrganismos patogênicos (devido sua propriedade eletrostática catiônica).
A adição do valor terapêutico pela incorporação de um excipiente funcional na forma de uma quitosana, que é um biopolímero na matriz do creme é um subconjunto integrado dos seguintes atributos funcionais do biopolímero: - formulação de um micro-filme na superfície da pele; - coagulação sanguínea acelerada, em comparação com cremes que não contenham biopolímeros formadores de filme; - imobilização eletrostática de microrganismos da superfície devido à carga catiônica do biopolímero; - melhora significativa da epitelização da pele ou regeneração que é de particular auxílio no dano da pele causado por infecções severas bem como feridas e queimaduras.
Os esforços inventivos envolvidos no desenvolvimento da tecnologia de base coberta pela incorporação de um biopolímero funcional em produtos de prescrição dermacêutica são: - na identificação do valor complementar terapêutico que tal incorporação oferece; - na identificação de assuntos relacionadas com a estabilidade físico- química do produto resultante da incorporação do biopolímero; - fornecer um formato de dose-única em que a infecção bacteriana tenha sido identificada.
A importância de um tratamento de dose-única, particularmente, nos países subdesenvolvidos não pode ser subestimada. Na ausência do acesso a um médico clínico-geral na maior parte do sul da Ásia ou da África e, muito menos um especialista dermatológico, uma formulação de dose-única aumenta drasticamente as chances de eliminar a raiz do problema de pele e ao mesmo tempo permitindo que a pele se regenere.
Durante as condições dermatológicas, terapias atualmente disponíveis não abordam as questões como proteger a pele, deter o sangramento, etc. A formulação única e inovadora da presente invenção trata das doenças da pele, tratando-as juntamente com o controle do sangramento superficial no local. É bem compreendido que, se o sangramento superficial for deixado sem tratamento, ele irá levar a infecções microbianas secundárias. A presente invenção vantajosamente proporciona uma solução para esta necessidade não atendida.
Além disso, com as pressões crescentes sobre os sistemas de apoio médico e à escassez ao atendente/ alto custo do mesmo, há uma necessidade emergente em todo o mundo para abordar as seguintes questões em tais casos: - Espera demasiada dos pacientes para o tratamento; - Longa permanência quando chegam ao hospital; - Ter que voltar mais vezes do que eles precisam
Reduzir o período de permanência é um problema fundamental a ser abordado na maioria dos casos. A presente invenção com a sua terapia de dose-única reduz o tempo total de tratamento de uma doença de pele significativamente grave.
Estes são fornecidos na forma de diferentes incorporações que descrevem o produto da presente invenção e seu processo de fabricação.
Um creme medicinal para o tratamento tópico de infecções bacterianas na pele, e para a cura de feridas relacionadas, em que o dito creme compreende um agente antibacteriano, fusidato de sódio e um biopolímero fornecido em uma base creme, dita base creme compreendendo pelo menos um de cada conservante, tensoativos primário e secundário, um material ceroso, um co-solvente, um ácido e água, de preferência água purificada.
Um creme medicinal como divulgado na incorporação preferida n°. 1, em que o dito creme ainda compreende qualquer de um grupo composto por um agente de tamponamento, um antioxidante, um agente quelante, um umectante, ou qualquer combinação destes.
Um novo creme dermacêutico como divulgado na incorporação preferida n°. 1 e na realização 1, onde: - o dito ácido fusídico está presente em uma quantidade entre cerca de 0,1% p/p a cerca de 25% p/p, preferencialmente entre 0,5% p/p a cerca de 5% p/p, e mais preferivelmente cerca de 2,0% (p/p), e em que a quantidade do dito fusidato de sódio utilizado para formar in situ o dito ácido fusídico está na faixa entre cerca de 0,1% (p/p) a cerca de 25% (p/p), preferencialmente a partir de 0,5% (p/p) a cerca de 5% (p/p) e mais preferivelmente cerca de 2,08% (p/p); e - o dito biopolímero está na forma de quitosana, adicionado em uma quantidade entre cerca de 0,01% e cerca de 1%, em peso, de preferência de cerca de 0,01% p/p de cerca de 0,5% p/p e mais preferencialmente, cerca de 0,25% p/p, - os ditos emulsificantes primários e secundários são selecionados a partir de um grupo composto por álcool cetoestearílico, Cetomacrogol- 1000, polissorbato-80, Span-80 e seus similares e adicionados em uma quantidade de cerca de 1% (p/p) a 20% (p/p); - os ditos materiais cerosos são selecionados a partir de um grupo composto por vaselina branca, parafina líquida, parafina sólida e similares, ou qualquer combinação destes, e adicionados em quantidades de cerca de 5% (p/p) a 30% (p/p); - o dito o co-solvente é selecionado a partir de um grupo composto por propilenoglicol, hexilenoglicol, polietilenoglicol-400, miristato de isopropila e similares, ou qualquer combinação dos mesmos, e adicionados em uma quantidade de cerca de 5% (p/p) a 50% (p/p); - o dito o ácido é selecionado a partir de um grupo composto por HC1, H2SO4, HNO3, ácido lático e similares, ou qualquer combinação dos mesmos, e adicionado em uma quantidade de cerca de 0,005% (p/p) a 0,5% (p/p); - o dito conservante é selecionado a partir de um grupo composto por metilparabeno, propilparabeno, clorocresol, sorbato de potássio, ácido benzóico e similares, ou qualquer combinação dos mesmos, e adicionado em uma quantidade de cerca de 0,05% (p/p) a 0,5% (p/p); - a dita a água é adicionada em quantidade na faixa de 20% (p/p) a 75% (p/p), de preferência de 30% (p/p) a 50% (p/p), mais preferencialmente de 35% (p/p) a 45% (p/p), de preferência água purificada.
Um novo creme medicinal como divulgado na incorporação preferida n°. 1, e na realização n°. 2, compreendendo ainda um agente tamponante que é selecionado a partir de um grupo composto por hidrogênio ortofosfato dissódico, hidrogênio ortofosfato de sódio e similares, ou qualquer combinação dos mesmos, e adicionado em um montante de cerca de 0,001% (p/p) a 1,00% (p/p).
Um novo creme medicinal como revelado na incorporação preferida n°. 1 e nas realizações n°, 2 e n°. 3, ainda compreendendo um antioxidante que é selecionado de um grupo compreendendo hidroxianisol butilado, hidroxitolueno butilado e similares, ou qualquer combinação destes e adicionado em quantidades de cerca de 0,001% (P/P) a 1% (p/p).
Um novo creme medicinal como revelado na incorporação preferida n°. 1 e nas realizações n°. 2 a n°. 4, compreendendo ainda um agente quelante que é selecionado a partir de um grupo composto por EDTA dissódico e similares, ou qualquer combinação destes, e adicionado em um montante de cerca de 0,05% (p/p) a 1% (p/p).
Um novo creme medicinal como revelado na incorporação preferida n°. 1 e nas realizações n°. 2 a n°. 5, compreendendo ainda um umectante que é selecionado a partir de um grupo composto por glicerina, sorbitol, propilenoglicol e similares, ou qualquer combinação dos mesmos, e adicionado em uma quantidade de cerca de 5% (p/p) para 50% (p/p).
Em uma incorporação preferida da presente invenção um processo de fabricação de um creme dermacêutico contendo ácido fusídico, dito processo compreendendo a etapa de utilização de fusidato de sódio como API de partida e convertendo-o in situem ácido fusídico sob ambiente livre de oxigênio em uma base creme.
Em uma realização da presente invenção do processo de fabricação da composição é divulgada, onde a etapa de conversão do fusidato de sódio in situem ácido fusídico na incorporação preferida n. 2 compreende as etapas de: a. aquecer a água purificada na faixa de 20% (p/p) a 75% (p/p), preferencialmente, 30% (p/p) a 50% (p/p), mais preferivelmente de 35% (p/p) a 45% (p/p) em um recipiente da fase aquosa em 70°C a 80°C, b. adicionar ao dito recipiente da fase aquosa um conservante selecionado a partir de um grupo composto por metilparabeno, propilparabeno, clorocresol, sorbato de potássio, ácido benzóico e similares, individualmente ou qualquer combinação dos mesmos, em uma quantidade de cerca de 0,05% (p/p) a 0,5% (p/p), de preferência 0,3% (p/p), mais preferencialmente, de 0,2% (p/p) de preferência ácido benzóico, c. misturar a mistura usando um agitador de 10 a 50 RPM, enquanto mantém a temperatura da mistura em 70°C a 80°C, d. adicionar material ceroso selecionado de um grupo composto por vaselina branca, parafina líquida, parafina sólida e similares, individualmente ou qualquer combinação dos mesmos, em uma quantidade de cerca de 5% (p/p) a 20% (p/p), de preferência, 15% (p/p), mais preferencialmente, 12,5% (p/p), a um recipiente de fase oleosa e fundir a dita cera por aquecimento em 70°C a 80°C, e. adicionar ao dito recipiente da fase oleosa um emulsificante primário, preferencialmente na forma de um surfactante não-iônico selecionado de um grupo composto por álcool cetoestearílico, Cetomacrogol-1000, individualmente ou qualquer combinação dos mesmos, preferencialmente, álcool cetoestearílico em uma quantidade entre 1% (p/p) a 15% (p/p), de preferência, 15% (p/p), mais preferivelmente, 12,5% (p/p), e opcionalmente, um emulsificante secundário selecionado de um grupo composto por polissorbato-80, Span-80 e similares, preferencialmente, polissorbato-80 em uma quantidade entre 1% (P/P) a 5% (p/p), mais preferivelmente, 2% (p/p) e misturar a mistura completamente, preferencialmente, usando um agitador a 10 a 50 RPM, enquanto mantém a temperatura da mistura em 70°C a 80°C, f. transferir sob vácuo em uma faixa de -1000 a - 300 de mm de mercúrio e em 70°C a 80°C o conteúdo dos recipientes da fase aquosa e da fase oleosa a um recipiente de mistura e misturar a mistura completamente, preferencialmente, usando um agitador de 10 a 50 RPM para formar uma emulsão, g. resfriar a dita emulsão para 45°C, de preferência pela circulação de água gelada, preferivelmente, em 8°C a 15°C a partir de uma torre de resfriamento na camisa do recipiente de mistura, h. em um recipiente do API adicionar um co-solvente selecionado a partir de um grupo composto por propilenoglicol, hexilenoglicol, polietilenoglicol-400 e similares, individualmente ou qualquer combinação dos mesmos, em uma quantidade entre 5% (p/p) a 40% (p/p), preferivelmente, 30% (p/p), mais preferencialmente, 25% (p/p), de preferência propilenoglicol, submetendo os conteúdos do dito recipiente do API a descarga de gás inerte, dito gás inerte sendo, preferencialmente, nitrogênio, e adicionar fusidato de sódio a mistura, dito fusidato de sódio adicionado em uma quantidade entre 0,1% (p/p) a cerca de 25% (p/p), de preferência, de cerca 0,5% (p/p) a cerca de 5% (p/p), mais preferencialmente, de cerca de 2,08% (p/p), e dissolvendo o dito fusidato de sódio na mistura, i. ajustar o pH da mistura no recipiente do API, da etapa h, para abaixo de 2 pela adição de ácido, selecionado a partir de um grupo composto por ácidos, tais como, HC1, H2SO4, HNO3, ácido lático e similares, individualmente ou qualquer combinação dos mesmos, de preferência, ácido nítrico em uma quantidade entre cerca de 0,005% (p/p) a 0,5% (p/p), mais preferencialmente, 0,3% (p/p), mais preferivelmente, 0,25% (P/P), j. transferir o conteúdo do dito recipiente do API, da etapa i, para o recipiente de mistura da etapa g com agitação contínua de 10 a 50 RPM e homogeneização da mistura a 1.000 a 3.000 RPM sob uma descarga de gás inerte e sob vácuo de -1.000 para -300 mm de mercúrio, dito gás inerte sendo preferencialmente nitrogênio, k. em um recipiente separado adicionar um ácido selecionado de um grupo composto por ácidos, tais como, HC1, H2SO4, HNO3, ácido lático e similares, individualmente ou qualquer combinação dos mesmos, de preferência, ácido láctico em uma quantidade entre cerca de 0,005% (p/p) a 0,5% (p/p), mais preferencialmente, 0,3% (p/p), mais preferivelmente, 0,1% (p/p), e água purificada a partir de cerca de 0,1% (p/p) a 10% (p/p), preferencialmente 8% (p/p), mais preferivelmente 5% (p/p) para formar uma mistura e dissolver o dito polímero, quitosana em uma quantidade entre cerca de 0,01% a cerca de 1% em peso, de preferência, a partir de cerca de 0,01% (p/p) a cerca de 0,5% p/p e mais preferencialmente cerca de 0,25% p/p, l. transferir o conteúdo da mistura do biopolímero da etapa k para o recipiente de mistura da etapa g com agitação contínua de 10 a 50 RPM e homogeneização da mistura a 1.000 a 3.000 RPM sob uma descarga de gás inerte e sob vácuo de -1.000 a -300 mm de mercúrio, dito gás inerte sendo preferencialmente nitrogênio, m. resfriamento do conteúdo do recipiente de mistura a 30°C a 37°C usando circulação de água gelada a partir de uma torre de resfriamento de 8°C a 15°C em uma camisa do recipiente de mistura, n. desligar o agitador e homogeneizador e remover a mistura do recipiente de mistura da etapa m para um recipiente de armazenamento.
Em uma realização da presente invenção, o co-solvente da etapa h da realização n. 7 acima também serve como um umectante. No entanto, em uma outra realização da invenção, um umectante adicional pode ser adicionado, selecionado de um grupo composto por glicerina, sorbitol, propilenoglicol e similares, individualmente ou qualquer combinação dos mesmos, para formar um de cerca de 5% (p/p) a 40% (p/p), de preferência de 30% (p/p), mais preferencialmente 25% (p/p).
Em uma outra realização da presente invenção o processo descrito na realização n. 8 incorpora ainda a adição de um agente quelante selecionado a partir de um grupo composto por EDTA dissódico e similares, individualmente ou qualquer combinação dos mesmos, para formar um de cerca de 0,01% (p/p) para 1% (p/p), de preferência de 0,5% (p/p), de preferência mais de 0,1% (p/p).
Ainda, em outra realização da presente invenção o processo descrito nas realizações n. 8 e n. 9 ainda incorporam um agente tamponante selecionado a partir de um grupo composto por hidrogênio ortofosfato dissódico, hidrogênio ortofosfato de sódio e similares, a partir de cerca de 0,001% (p/p) a 1,00% (p/p), de preferência, 0,05% (p/p), mais preferencialmente 0,5% (p/p).
Ainda, em uma realização da presente invenção o processo descrito nas realizações n. 8 a n. 10 incorpora ainda um antioxidante selecionado a partir de um grupo compreendendo hidroxianisol butilado, hidroxitolueno butilado e similares a partir de cerca de 0,001% (p/p) a 5% (p/p), de preferência, 0,1% (p/p), preferivelmente 0,01% (p/p).
Ainda, outro processo de fabricação da composição de acordo com as realizações preferidas é divulgado, o dito processo compreende as etapas de: a. aquecer a água purificada na faixa de 20% (p/p) a 75% (p/p), preferencialmente, 30% (p/p) a 50% (p/p), mais preferivelmente de 35% (p/p) a 45% (p/p) em um recipiente da fase aquosa em 70°C a 80°C, b. adicionar ao dito recipiente da fase aquosa um conservante selecionado a partir de um grupo composto por metilparabeno, propilparabeno, clorocresol, sorbato de potássio, ácido benzóico e similares, individualmente ou qualquer combinação dos mesmos, em uma quantidade de cerca de 0,05% (p/p) a 0,5% (p/p), de preferência 0,3% (p/p), mais preferencialmente, de 0,2% (p/p) de preferência ácido benzóico, c. adicionar ao dito recipiente de fase aquosa da etapa b, um agente quelante selecionado a partir de um grupo composto por EDTA dissódico e similares, individualmente ou qualquer combinação dos mesmos, em uma quantidade entre 0,01% (p/p) para 1% (p/p), de preferência de 0,5% (p/p), de preferência mais de 0,1% (p/p). d. adicionar ao dito recipiente de fase aquosa da etapa c, um agente tamponante selecionado a partir de um grupo composto por hidrogênio ortofosfato dissódico, hidrogênio ortofosfato de sódio e similares, em uma quantidade entre 0,001% (p/p) a 1,00% (p/p), de preferência, 0,05% (p/p), mais preferencialmente 0,5% (p/p). e. misturar a mistura da etapa d utilizando um agitador a 10 a 50 RPM enquanto mantém a temperatura da mistura em 70°C a 80°C. f. adicionar material ceroso selecionado de um grupo composto por vaselina branca, parafina líquida, parafina sólida e similares, individualmente ou qualquer combinação dos mesmos, em uma quantidade de cerca de 5% (p/p) a 20% (p/p), de preferência, 15% (p/p), mais preferencialmente, 12,5% (p/p), a um recipiente de fase oleosa e fundir a dita cera por aquecimento em 70°C a 80°C, g. adicionar ao dito recipiente da fase oleosa da etapa f, um emulsificante primário, preferencialmente na forma de um surfactante não-iônico selecionado de um grupo composto por álcool cetoestearílico, Cetomacrogol-1000, individualmente ou qualquer combinação dos mesmos, preferencialmente, álcool cetoestearílico em uma quantidade entre 1% (p/p) a 15% (p/p), de preferência, 15% (p/p), mais preferivelmente, 12,5% (p/p), e opcionalmente, um emulsificante secundário selecionado de um grupo composto por polissorbato-80, Span-80 e similares, preferencialmente, polissorbato-80 em uma quantidade entre 1% (p/p) a 5% (p/p), mais preferivelmente, 2% (p/p) e misturar a mistura completamente, preferencialmente, usando um agitador a 10 a 50 RPM, enquanto mantém a temperatura da mistura em 75°C ± 5°C, h. transferir sob vácuo em uma faixa de -1000 a - 300 de mm de mercúrio e em 75°C ± 5°C o conteúdo dos recipientes da fase aquosa e da fase oleosa a um recipiente de mistura e misturar a mistura completamente, preferencialmente, usando um agitador de 10 a 50 RPM para formar uma emulsão, i. resfriar a dita emulsão para 45°C, de preferência pela circulação de água gelada, preferivelmente, em 8°C a 15°C a partir de uma torre de resfriamento na camisa do recipiente de mistura, j. em um recipiente do API adicionar um co-solvente selecionado a partir de um grupo composto por propilenoglicol, hexilenoglicol, polietilenoglicol-400 e similares, individualmente ou qualquer combinação dos mesmos, em uma quantidade entre 5% (p/p) a 40% (p/p)> preferivelmente, 30% (p/p), mais preferencialmente, 25% (p/p), de preferência propilenoglicol e dissolvendo um antioxidante selecionado a partir de um grupo compreendendo hidroxianisol butilado, hidroxitolueno butilado e similares, individualmente ou em qualquer combinação dos mesmos, em uma quantidade entre 0,001% (p/p) a 5% (p/p), de preferência, 0,1% (p/p), preferivelmente 0,01% (p/p), preferencialmente hidroxitolueno butilado em dito glicol por mistura contínua, k. submetendo os conteúdos do dito recipiente do API a descarga de gás inerte, dito gás inerte sendo, preferencialmente, nitrogênio, e adicionar fusidato de sódio a mistura, o dito fusidato de sódio sendo adicionado em uma quantidade entre 0,1% (p/p) a cerca de 25% (p/p), de preferência, de cerca 0,5% (p/p) a cerca de 5% (p/p), mais preferencialmente, de cerca de 2,08% (p/p), e dissolvendo o dito fusidato de sódio na mistura, l. ajustar o pH da mistura no recipiente do API, da etapa k, para abaixo de 2 pela adição de ácido, selecionado a partir de um grupo composto por ácidos, tais como, HC1, H2SO4, HNO3, ácido lático e similares, individualmente ou qualquer combinação dos mesmos, de preferência, ácido nítrico em uma quantidade entre 0,005% (p/p) a 0,5% (p/p), mais preferencialmente, 0,3% (p/p), mais preferivelmente, 0,25% (p/p), m. transferir o conteúdo do dito recipiente do API, da etapa 1, para o recipiente de mistura da etapa i com agitação contínua de 10 a 50 RPM e homogeneização da mistura a 1.000 a 3.000 RPM sob uma descarga de gás inerte e sob vácuo de -1.000 para -300 mm de mercúrio, dito gás inerte sendo preferencialmente nitrogênio, n. em um recipiente separado adicionar um ácido selecionado de um grupo composto por ácidos, tais como, HC1, H2SO4, HNO3, ácido lático e similares, individualmente ou qualquer combinação dos mesmos, de preferência, ácido láctico para formar um a partir de cerca de 0,005% (p/p) a 0,5% (p/p), mais preferencialmente, 0,3% (p/p), mais preferivelmente, 0,1% (p/p), e água purificada a partir de cerca de 0,1% (p/p) a 10% (p/p), preferencialmente 8% (p/p), mais preferivelmente 5% (p/p) para formar uma mistura e dissolver o dito polímero, quitosana em uma quantidade entre cerca de 0,01% a cerca de 1% em peso, de preferência, a partir de cerca de 0,01% (p/p) a cerca de 0,5% p/p e mais preferencialmente cerca de 0,25% p/p, o. transferir o conteúdo da mistura do biopolímero da etapa n para o recipiente de mistura da etapa i com agitação contínua de 10 a 50 RPM e homogeneização da mistura a 1.000 a 3.000 RPM sob uma descarga de gás inerte e sob vácuo de -1.000 a -300 mm de mercúrio, dito gás inerte sendo preferencialmente nitrogênio, p. resfriamento do conteúdo do recipiente de mistura da etapa o para 30°C a 37°C usando circulação de água gelada a partir de uma torre de resfriamento de 8°C a 15°C em uma camisa do recipiente de mistura, q. desligar o agitador e homogeneizador e remover a mistura do recipiente de mistura da etapa n para um recipiente de armazenamento.
O co-solvente da etapa j serve também como um umectante. No entanto, em uma realização da invenção, um umectante adicional pode ser adicionado, selecionado de um grupo composto por glicerina, sorbitol, propilenoglicol e similares, individualmente ou qualquer combinação dos mesmos, para formar um de cerca de 5% (p/p) a 40% (p/p), de preferência de 30% (p/p), mais preferencialmente de 25% (P/P).
O creme obtido utilizando o processo da presente invenção é homogêneo e branco ao esbranquiçado em cor e viscoso em consistência. O pH do produto preparado utilizando o processo da presente invenção é de cerca de 3 a 6. Por outro lado, pomadas de fusidato de sódio que estão comercialmente disponíveis são gordurosas e não cosmeticamente elegantes.
É essencial que o ingrediente ativo penetre a pele para a eficácia biodérmica ideal. O tamanho de partícula do ingrediente ativo 5 desempenha um papel importante aqui. É necessário que o ingrediente ativo esteja disponível em uma forma dispersa finamente para que o produto seja eficaz. Também, este deverá ser alcançado em ambiente de pH seguro compatível com a pele (4,0 a 6,0). Para conseguir tudo isso, é essencial escolher veículos apropriados ou co-solventes para a 10 dissolução ou dispersão da droga.
A análise granulométrica foi realizada no creme preparado usando o processo da presente invenção e em algumas amostras do produtos comercialmente disponíveis (amostras A, C, D, F, G e K). Os tamanhos de partículas máximo e mínimo, o tamanho de partícula 15 médio, desvio padrão e o coeficiente de variação foram avaliados. TABELA 8 ANÁLISE DE TAMANHO DE PARTÍCULAS
Os resultados das análises de distribuição do tamanho de
partícula indicam, na tabela 8, claramente a presença de ácido fusídico de tamanho de partícula fino no produto da presente invenção, o tamanho que é vantajosamente mais reduzido do que os produtos convencionais. Isto é atribuído ao fato de que o produto instantâneo é elaborado usando fusidato de sódio através da conversão in situ de fusidato de sódio ao ácido fusídico em uma forma dispersa finamente. Todos os parâmetros medidos são melhores do que os encontrados para os cremes comercialmente disponíveis contendo ácido fusídico. Essa é outra vantagem clara do produto divulgado aqui sobre os produtos disponíveis no mercado.
O produto da presente invenção é eficaz devido ao pronunciada atividade antibacteriana do ácido fusídico regenerado que está disponível em tamanho de partícula reduzido do que em produtos convencionais, e em uma forma finamente dispersada.
A Depositante selecionou diferentes co-solventes, tais como, propilenoglicol, hexilenoglicol, polietilenoglicol-400 e similares, e fusidato de sódio dissolvido em um dos co-solventes acima variando de cerca de 5% (p/p) a 40% (p/p) sob purga de gás inerte e sob vácuo, e convertido em ácido fusídico in situpor adição de um ácido, tal como, HC1, H2SO4, HNO3, ácido láctico e similares de cerca de 0,005% (p/p) para cerca de 0,5% (p/p) sob agitação e obtido o ácido fusídico na forma mais estabilizado e em solução, o que torna nosso produto final em uma base creme que penetra facilmente a pele e altamente eficaz, e também altamente dermo-compatível por ter um pH de cerca de 3,0 a cerca de 6,0.
A estabilidade do produto é confirmada pelos estudos de estabilidade realizados por 6 meses conforme diretrizes ICH e uma comparação dos estudos de estresse feitos para produtos “in-housé’ com aquelas amostras de produtos comparáveis comercialmente disponíveis.
Experimentos da estabilidade do API foram realizados (ver tabelas 10 a 15) utilizando o produto da presente invenção e produtos disponíveis no mercado atualmente. Os testes foram realizados para observar (ou medir como apropriado) a aparência física do produto, o valor de pH e ensaio do API por um período de tempo. Os testes também foram realizados para avaliar a estabilidade submetendo o produto a estudos de estresse, tais como, teste de autoclave e teste de degradação oxidativa. Adicionalmente, Estudos de inibição da zona antimicrobiana in vitro,tais como estudos de coagulação sanguínea e cicatrização de feridas de queimaduras foram também realizados por um período de tempo. Cada grama do produto da presente invenção usado para os testes contém fusidato de sódio como princípio ativo em uma quantidade necessária para produzir ácido fusídico 2% (p/p) no produto acabado.
O produto usado para os testes de estudos de estabilidade, autoclave e degradação oxidativa apresentou aproximadamente 10% extra do API (excesso). O produto da presente invenção utilizado para os estudos continha creme de ácido fusídico preparado usando fusidato de sódio como matéria-prima. O produto foi embalado em bisnaga de alumínio e cada grama do produto contendo 20,8 mg de fusidato de sódio (em conformidade com a (FB)), que é equivalente a 20 mg de ácido fusídico (conforme (FB)). Os detalhes da análise dos produtos comparáveis disponíveis no mercado (cremes de ácido fusídico) são fornecidos nas tabelas 14 e 15 conforme o caso.
É evidente a partir de tabelas de 10 a 12 que em todos os aspectos, o valor de pH, a aparência física e estabilidade, o produto da presente invenção é muito bom.
A tabela 13 fornece dados de referência para as amostras A- 5 I, que foram tomadas a partir de cremes disponíveis no mercado de ácido fusídico e utilizados para análise.
A presente invenção será ainda elucidada com referência ao exemplo seguinte contendo a composição e os dados dos estudos de estabilidade, que não tem, no entanto, a intenção de limitar a invenção 10 de qualquer maneira.
A composição do creme final é mostrada na tabela 9 abaixo. EXEMPLO: TABELA 9 - CREME DE ÁCIDO FUSÍDICO (EQUIVALENTE A FUSIDATO DE SÓDIO 2,08% P/P) + QUITOSANA 0,25% (P/P)
Composição: Cada grama contém: fusidato de sódio (FB) equivalente ao ácido fusídico (FB) 2% TABELA 10: TESTE DE DESCRIÇÃO, N°. DO LOTE SCC-41 Parâmetro Medido: Aparência física Melhor valor do parâmetro medido: Creme homogêneo do branco ao viscoso esbranquiçado; Método de Medição: Observação a olho nu. TABELA 11: TESTE DO PH, N°. DO LOTE SCC-41
Parâmetro Medido: pH; Limites do parâmetro medido: 3-6 Método de Medição: Medidor de pH Digital TABELA 12: TESTE DE ENSAIO (%), N°. DO LOTE SCC-41
Parâmetro Medido: Ensaio (%); Limites do parâmetro medido: 90-110 Método de Medição: Método HPLC
TABELA 13 TABELA 14: TESTE DA ANÁLISE DE AUTOCLAVE (%) Parâmetro Medido: Ensaio (%); Limites do parâmetro medido: 90-110% Método de Medição: Método HPLC
TABELA 15: TESTE DA ANÁLISE DE DEGRADAÇÃO OXIDATIVA (%)
A inferência da tabela 14: Os resultados do ensaio da
Análise de Autoclave (121°C aplicado por 15 minutos) indicam que as amostras comercialmente disponíveis de creme de ácido fusídico (amostras nos. 2 a 10) mostram maior diminuição percentual no conteúdo do ingrediente ativo (API) do que para o produto da presente invenção (amostra n°. 1).
A inferência da tabela 15: Os resultados acima do ensaio da Análise de Degradação Oxidativa (30% de uma solução de peróxido de hidrogênio ao longo de um período de 12 horas) indicam que várias amostras comerciais do creme de ácido fusídico (amostras nos. 2 a 10) mostram uma degradação significante do API (indicado pela diminuição da porcentagem no conteúdo do API) do que para o produto da presente invenção (amostra n°. 1).
A partir dos dados acima, é evidente que o produto da presente invenção é bastante estável em condições ambientes e também a temperatura elevada e condições de umidade de armazenamento. Também os estudos de autoclave e estudos de degradação oxidativa confirmam ainda mais a estabilidade do produto. Esta é uma grande vantagem sobre os cremes de ácido fusídico atualmente disponíveis. A estabilidade do produto é ainda apurado pela previsão de vida de prateleira da formulação utilizando o gráfico de Arrhenius da degradação empregando o software Nova-LIMS.
A atividade microbiana/antibactericida do produto é confirmado pelos estudos de inibição da zona antimicrobiana in vitro para o produto contra Staphylococcus aureus.Os detalhes dos estudos são detalhados abaixo na tabela 16. TABELA 16
A partir dos dados acima, é evidente que o produto tem atividade antimicrobiana/ antibacteriana adequada para o tratamento de infecções bacterianas primárias e secundárias.
Uma comparação da tabela 9 com as tabelas 3 a 7 ilustrarão a diferença nos produtos que seria baseado nos desenhos de drogas convencionais e a abordagem inovadora adotada na presente invenção.
O creme é aplicado após a limpeza completa e secagem da área afetada. O creme deve ser aplicado suficientemente para cobrir a pele afetada e a área circundante. O creme deve ser aplicado de 2 a 4 vezes ao dia, dependendo das condições da pele pelo período completo de tratamento, mesmo que os sintomas tenham melhorado.
Experimentos foram realizados com o creme em laboratório, bem como utilizando modelos de animais adequados infligidos com ferimentos por excisão. Quatro aspectos foram testados - contração da ferida, epitelização, o tempo de coagulação do sangue e a formação de filme. Estes aspectos, juntos, sugerem que os microrganismos foram imobilizados, dessa forma levando a cura eficaz das feridas. A. CONTRAÇÃO DA FERIDA: A atividade de cura da excisão do creme da presente invenção foi determinada através de testes em animais. Uma excisão de 2,5 cm de diâmetro foi infligida cortando-se toda a espessura da pele. O total de contração da ferida observado ao longo de um período indicou que o creme da presente invenção proporciona melhoria significativa da contração da ferida do que a alcançada pela aplicação de um creme convencional. B. PERÍODO DE EPITELIZAÇÃO; A epitelização da ferida ocorreu em um menor número de dias utilizando o creme da presente invenção em relação aos dias esperados para epitelização usando creme convencional. Portanto, um benefício do creme da presente invenção é que ele facilita a rápida epitelização da pele do que através do uso de cremes convencionais. C. COAGULAÇÃO SANGUÍNEA:
O tempo de coagulação do sangue foi observado em ambos os grupos de animais, grupo controle sem tratamento e o grupo de teste dos animais tratados com o produto da presente invenção. A diminuição estatisticamente significativa no tempo de coagulação do sangue nos animais do grupo tratado foi observada quando comparada com a dos animais do grupo controle. A redução percentual média de a 45% foi observada para o tempo de coagulação do sangue usando o produto da presente invenção.
É evidente a partir figura 1 que a quitosana não perde sua 5 propriedade de formação de filme na presença dos excipientes utilizados nas preparações de creme na presente invenção.
É evidente que as propriedades da quitosana, quando utilizada em formulações contendo os excipientes utilizados na atual 10 invenção não estão comprometidas. Isto foi conseguido através de uma cuidadosa seleção dos excipientes. Por exemplo, nossos experimentos mostram que excipientes amplamente utilizados, tais como, goma xantana ou carbômero precipitam em combinação com quitosana, devido às interações catiônicas e aniônicas.
O impacto terapêutico, como observado a partir da experimentação animal, da adição de quitosana ao fusidato de sódio é mostrado na tabela a seguir, considerando diferentes aspectos da cura terapêutica de uma condição de pele comprometida: TABELA 17
TABELA 18: PROPRIEDADES DE CURA DA FERIDA DA PRESENTE INVENÇÃO
Estudos da cura de feridas foram realizados em animais e usando o creme da presente invenção. Os resultados foram incorporados na tabela 18.
É evidente que a capacidade de formar filme da quitosana 5 incorporada no creme permite um melhor acesso do agente antibacteriano, fusidato de sódio, a área infectada e resulta em um melhor funcionamento desse API.
A eficácia terapêutica do creme aplicado topicamente da presente invenção é devido à atividade antibacteriana acentuada do 10 fusidato de sódio contra os organismos responsáveis pelas infecções de pele, a capacidade única dos ativos de penetrar na pele intacta e cicatrização de feridas e propriedades suavizantes da quitosana.
É evidente a partir da tabela 18 que a habilidade do creme da presente invenção um nível estatisticamente significante da epitelização bem como contração da ferida é surpreendente maior que as terapias disponíveis atualmente.
É evidente a partir da discussão anterior que a presente invenção oferece as seguintes vantagens e aspectos exclusivos face às composições dermacêuticas disponíveis atualmente para infecções bacterianas e cura de feridas da pele: 1. O creme da presente invenção incorpora um biopolímero compatível com a pele na forma de quitosana proporcionando melhor resultados terapêuticos. Isto é evidente a partir do tempo de coagulação sanguínea reduzido, aumento do efeito epitelial, alívio mais rápido da infecção, inflamação e contração da ferida. 2. O creme da presente invenção incorpora um biopolímero, sem comprometer a estabilidade da matriz do creme e sem prejudicar o funcionamento dos conhecidos ingredientes farmacêuticos ativos. Isto foi conseguido através de uma cuidadosa seleção dos excipientes funcionais para contornar os aspectos indesejáveis da estabilidade físico-química/ compatibilidade e bioliberação. 3. O creme da presente invenção provê um sistema integrado de dose única ou uma terapia de dose-única até então indisponíveis em formulações de prescrição dermacêutica. 4. O novo creme da presente invenção é adequadamente estável/ eficaz em condições ambiente e não necessita de controle de temperatura especial durante o transporte/ armazenamento - por conseguinte, conquistando um longo caminho para atingir estes objetivos sociais.
De acordo com uma outra realização da presente invenção, também se fornece um processo para o tratamento de infecções bacterianas da pele e cura de feridas envolvendo o contato com a pele humana com a composição acima divulgada.
Embora a descrição acima contenha certa especificidade, estes não devem ser interpretados como limitação do escopo da 5 invenção, mas sim como uma exemplificação das incorporações preferidas dos mesmos. Deve ser percebido que as realizações e as variações são possíveis com base na descrição dada acima, sem se afastar do espírito e escopo da invenção. Assim, o escopo da invenção deve ser determinado não pelas incorporações ilustradas, mas pelas 10 reivindicações anexadas e seus equivalentes legal.
Claims (14)
1) CREME MEDICINAL para tratamento tópico de infecções bacterianas e para a cura de feridas, dito creme compreendendo ácido fusídico e um biopolímero, preferencialmente quitosana, caracterizado por dito ácido fusídico ser preparado in situ sob ambiente livre de oxigênio utilizando fusidato de sódio, em que o dito creme compreende ácido fusídico preparado in situ pela conversão do fusidato de sódio e um biopolímero fornecido em uma base creme, dita base creme compreendendo pelo menos um de cada emulsificante primário e secundário, um material ceroso, um co-solvente, um ácido e água.
2) CREME MEDICINAL, de acordo com a reivindicação 1, caracterizado por dita base creme compreender um conservante, um ácido, um co-solvente, um emulsificante e um material ceroso junto com água, preferencialmente água purificada.
3) CREME MEDICINAL, de acordo com a reivindicação 1, caracterizado por: - dito ácido fusídico estar presente em uma quantidade de cerca de 0,1% (p/p) a cerca de 25% (p/p), de preferência, de cerca de 0,5% (p/p) a cerca de 5% (p/p) e mais preferencialmente cerca de 2,00% (p/p), e em que a quantidade do dito fusidato de sódio usado para formar in situ o dito ácido fusídico está na faixa de cerca de 0,1 % (p/p) a cerca de 25% (p/p), preferivelmente de cerca de 0,5% (p/p) a cerca de 5,0% (p/p) e mais preferencialmente cerca de 2,08% (p/p), e - dito biopolímero ser na forma de quitosana, adicionado em uma quantidade entre cerca de 0,01% (p/p) e cerca de 1% (p/p), de preferência de cerca de 0,01% (p/p) a cerca de 0,5% (p/p) e mais preferencialmente, cerca de 0,25% (p/p), - ditos emulsificantes primários e secundários serem selecionados a partir de um grupo composto por álcool cetoestearílico, Cetomacrogol-1000, polissorbato-80, Span-80 e seus similares e adicionados em uma quantidade de cerca de 1% (p/p) a 20% (p/p); - ditos materiais cerosos serem selecionados a partir de um grupo composto por vaselina branca, parafina líquida, parafina sólida e similares, ou combinação dos mesmos, e adicionados em quantidades de cerca de 5% (p/p) a 30% (p/p); - dito co-solvente ser selecionado a partir de um grupo composto por propilenoglicol, hexilenoglicol, polietilenoglicol-400 e similares, ou combinação dos mesmos, e adicionados em uma quantidade de cerca de 5% (p/p) a 50% (p/p); - dito o ácido ser selecionado a partir de um grupo composto por HCl, H2SO4, HNO3, ácido lático e similares, ou combinação dos mesmos, e adicionado em uma quantidade de cerca de 0,005% (p/p) a 0,5% (p/p); - dito conservante ser selecionado a partir de um grupo composto por metilparabeno, propilparabeno, clorocresol, sorbato de potássio, ácido benzóico e similares, ou combinação dos mesmos, e adicionado em uma quantidade de cerca de 0,05% (p/p) a 0,5% (p/p); - dita água ser adicionada em quantidade na faixa de 20% (p/p) a 75% (p/p), de preferência de 30% (p/p) a 50% (p/p), mais preferencialmente de 35% (p/p) a 45% (p/p), de preferência água purificada.
4) CREME MEDICINAL, de acordo com as reivindicações 1 e 3, caracterizado por compreender ainda um agente tamponante selecionado de um grupo composto por hidrogênio ortofosfato dissódico, hidrogênio ortofosfato de sódio e similares, ou combinação dos mesmos, e adicionado em um montante de cerca de 0,001% (p/p) a 1,00% (p/p).
5) CREME MEDICINAL, de acordo com as reivindicações 1, 3 e 4, caracterizado por compreender ainda um antioxidante selecionado de um grupo compreendendo hidroxianisol butilado, hidroxitolueno butilado e similares, ou combinação destes e adicionado em quantidades de cerca de 0,001% (p/p) a 1% (p/p).
6) CREME MEDICINAL, de acordo com as reivindicações 1 e 3 a 5, caracterizado pelo por compreender ainda um agente quelante selecionado a partir de um grupo composto por EDTA dissódico e similares, ou combinação destes, e adicionado em um montante de cerca de 0,05% (p/p) a 1% (p/p).
7) CREME MEDICINAL, de acordo com as reivindicações 1 e 3 a 6, caracterizado por compreender ainda um umectante selecionado a partir de um grupo composto por glicerina, sorbitol, propilenoglicol e similares, ou combinação dos mesmos, e adicionado em uma quantidade de cerca de 5% (p/p) para 50% (p/p).
8) PROCESSO DE FABRICAÇÃO DE UM CREME DE ÁCIDO FUSÍDICO CONTENDO QUITOSANA, dito processo caracterizado por compreender a etapa de utilização do fusidato de sódio como matéria-prima do ingrediente farmacêutico ativo e convertendo o dito fusidato de sódio in situ em ácido fusídico sob ambiente livre de oxigênio em uma base creme.
9) PROCESSO, de acordo com a reivindicação 8, caracterizado pelo fato da etapa de utilização de fusidato de sódio como ingrediente farmacêutico ativo e conversão do fusidato de sódio in situ em ácido fusídico em ambiente livre de oxigênio em uma base creme compreender as etapas de: a. aquecer a água purificada na faixa de 20% (p/p) a 75% (p/p), preferencialmente, 30% (p/p) a 50% (p/p), mais preferivelmente de 35% (p/p) a 45% (p/p) em um recipiente da fase aquosa em 70°C a 80°C, b. adicionar ao dito recipiente da fase aquosa um conservante selecionado a partir de um grupo composto por metilparabeno, propilparabeno, clorocresol, sorbato de potássio, ácido benzóico e similares, individualmente ou combinação dos mesmos, em uma quantidade de cerca de 0,05% (p/p) a 0,5% (p/p), de preferência 0,3% (p/p), mais preferencialmente, de 0,2% (p/p) de preferência ácido benzóico, c. misturar a mistura usando um agitador de 10 a 50 RPM, enquanto mantém a temperatura da mistura em 70°C a 80°C, d. adicionar materiais cerosos selecionados de um grupo composto por vaselina branca, parafina líquida, parafina sólida e similares, individualmente ou combinação dos mesmos, em uma quantidade de cerca de 5% (p/p) a 20% (p/p), de preferência, 15% (p/p), mais preferencialmente, 12,5% (p/p), a um recipiente de fase oleosa e fundir a dita cera por aquecimento em 70°C a 80°C, e. adicionar ao dito recipiente da fase oleosa um emulsificante primário, preferencialmente na forma de um surfactante não-iônico selecionado de um grupo composto por álcool cetoestearílico, Cetomacrogol-1000, individualmente ou combinação dos mesmos, preferencialmente, álcool cetoestearílico em uma quantidade entre 1% (p/p) a 15% (p/p), de preferência, 15% (p/p), mais preferivelmente, 12,5% (p/p), e opcionalmente, um emulsificante secundário selecionado de um grupo composto por polissorbato- 80, Span-80 e similares, preferencialmente, polissorbato-80 em uma quantidade entre 1% (p/p) a 5% (p/p), mais preferivelmente, 2% (p/p) e misturar a mistura completamente, preferencialmente, usando um agitador a 10 a 50 RPM, enquanto mantém a temperatura da mistura em 70°C a 80°C, f. transferir sob vácuo em uma faixa de -1000 a -300 de mm de mercúrio e em 70°C a 80°C o conteúdo dos recipientes da fase aquosa e da fase oleosa a um recipiente de mistura e misturar a mistura completamente, preferencialmente, usando um agitador de 10 a 50 RPM para formar uma emulsão, g. resfriar a dita emulsão para 45°C, de preferência pela circulação de água gelada, preferivelmente, em 8°C a 15°C a partir de uma torre de resfriamento na camisa do recipiente de mistura, h. em um recipiente do API adicionar um co-solvente selecionado a partir de um grupo composto por propilenoglicol, hexilenoglicol, polietilenoglicol-400 e similares, individualmente ou combinação dos mesmos, em uma quantidade entre 5% (p/p) a 40% (p/p), preferivelmente, 30% (p/p), mais preferencialmente, 25% (p/p), de preferência propilenoglicol, submetendo os conteúdos do dito recipiente do API a descarga de gás inerte, dito gás inerte sendo, preferencialmente, nitrogênio, e adicionar fusidato de sódio a mistura, dito fusidato de sódio adicionado em uma quantidade entre 0,1% (p/p) a cerca de 25% (p/p), de preferência, de cerca 0,5% (p/p) a cerca de 5% (p/p), mais preferencialmente, de cerca de 2,08% (p/p), e dissolvendo o dito fusidato de sódio na mistura, i. ajustar o pH da mistura no recipiente do API, da etapa h, para abaixo de 2 pela adição de ácido, selecionado a partir de um grupo composto por ácidos, tais como, HCl, H2SO4, HNO3, ácido lático e similares, individualmente ou combinação dos mesmos, de preferência, ácido nítrico em uma quantidade entre cerca de 0,005% (p/p) a 0,5% (p/p) mais preferencialmente, 0,3% (p/p), mais preferivelmente, 0,25% (p/p), j. transferir o conteúdo do dito recipiente do API, da etapa i, para o recipiente de mistura da etapa g com agitação continua de 10 a 50 RPM e homogeneização da mistura a 1.000 a 3.000 RPM sob uma descarga de gás inerte e sob vácuo de -1.000 para -300 mm de mercúrio, dito gás inerte sendo preferencialmente nitrogênio, k. em um recipiente separado adicionar um ácido selecionado de um grupo composto por ácidos, tais como, HCl, H2SO4, HNO3, ácido lático e similares, individualmente ou combinação dos mesmos, de preferência, ácido láctico em uma quantidade entre cerca de 0,005% (p/p) a 0,5% (p/p), mais preferencialmente, 0,3% (p/p), mais preferivelmente, 0,1% (p/p), e água purificada a partir de cerca de 0,1% (p/p) a 10% (p/p), preferencialmente 8% (p/p), mais preferivelmente 5% (p/p) para formar uma mistura e dissolver o dito polímero, quitosana em uma quantidade entre cerca de 0,01% (p/p) a cerca de 1% em peso, de preferência, a partir de cerca de 0,01% (p/p) a cerca de 0,5% (p/p) e mais preferencialmente cerca de 0,25% (p/p), l. transferir o conteúdo da mistura do biopolímero da etapa k para o recipiente de mistura da etapa g com agitação contínua de 10 a 50 RPM e homogeneização da mistura a 1.000 a 3.000 RPM sob uma descarga de gás inerte e sob vácuo de -1.000 a -300 mm de mercúrio, dito gás inerte sendo preferencialmente nitrogênio, m. resfriamento do conteúdo do recipiente de mistura a 30°C a 37°C usando circulação de água gelada a partir de uma torre de resfriamento de 8°C a 15°C em uma camisa do recipiente de mistura, n. desligar o agitador e homogeneizador e remover a mistura do recipiente de mistura da etapa m para um recipiente de armazenamento.
10) PROCESSO, de acordo com a reivindicação 9, caracterizado por dito umectante ser adicionado ao recipiente de mistura da etapa a, na reivindicação 9, dito umectante sendo selecionado a partir de um grupo composto por glicerina, sorbitol, propilenoglicol, e similares, individualmente ou combinação dos mesmos, de cerca de 5% (p/p) a 40% (p/p), de preferência 30% (p/p), mais preferencialmente 25% (p/p).
11) PROCESSO, de acordo com as reivindicações 9 e 10, caracterizado pelo fato de um agente quelante ser adicionado à etapa a, da reivindicação 9, dito agente quelante sendo selecionado a partir de um grupo composto por EDTA dissódico e similares, individualmente ou combinação dos mesmos, de cerca de 0,01% (p/p) a 1% (p/p), de preferência 0,5% (p/p), mais preferencialmente 0,1% (p/p).
12) PROCESSO, de acordo com as reivindicações 9, 10 e 11, caracterizado pelo fato do agente tamponante ser adicionado a etapa a da reivindicação 9, dito agente tamponante ser selecionado a partir de um grupo composto por hidrogênio ortofosfato dissódico, hidrogênio ortofosfato de sódio e similares de cerca de 0,001% (p/p) a 1,00% (p/p), de preferência 0,05% (p/p), mais preferencialmente 0,5% (p/p).
13) PROCESSO, de acordo com as reivindicações 9 a 12, caracterizado pelo fato de ainda compreender a adição de antioxidantes a etapa h, da reivindicação 9, dito antioxidante sendo selecionado a partir de um grupo composto por hidroxianisol butilado, hidroxitolueno butilado e similares de cerca de 0,001% (p/p) a 5% (p/p), de preferência 0,1% (p/p), mais preferencialmente 0,01% (p/p).
14) PROCESSO, de acordo com a reivindicação 8, caracterizado pelo fato da etapa de utilização de fusidato de sódio como ingrediente farmacêutico ativo e convertendo o dito fusidato de sódio in situ em ácido fusídico em ambiente livre de oxigênio em uma base creme compreender as etapas de: a. aquecer a água purificada na faixa de 20% (p/p) a 75% (p/p), preferencialmente, 30% (p/p) a 50% (p/p), mais preferivelmente de 35% (p/p) a 45% (p/p) em um recipiente da fase aquosa em 70°C a 80°C, b. adicionar ao dito recipiente da fase aquosa um conservante selecionado a partir de um grupo composto por metilparabeno, propilparabeno, clorocresol, sorbato de potássio, ácido benzóico e similares, individualmente ou combinação dos mesmos, em uma quantidade de cerca de 0,05% (p/p) a 0,5% (p/p), de preferência 0,3% (p/p), mais preferencialmente, de 0,2% (p/p) de preferência ácido benzóico, c. adicionar ao dito recipiente de fase aquosa da etapa b, um agente quelante selecionado a partir de um grupo composto por EDTA dissódico e similares, individualmente ou combinação dos mesmos, em uma quantidade entre 0,01% (p/p) para 1% (p/p), de preferência de 0,5% (p/ p), de preferência mais de 0,1% (p/p), d. adicionar ao dito recipiente de fase aquosa da etapa c, um agente tamponante selecionado a partir de um grupo composto por hidrogênio ortofosfato dissódico, hidrogênio ortofosfato de sódio e similares, em uma quantidade entre 0,001% (p/p) a 1,00% (p/p), de preferência, 0,05% (p/p), mais preferencialmente 0,5% (p/p), e. misturar a mistura da etapa d utilizando um agitador a 10 a 50 RPM enquanto mantém a temperatura da mistura em 70°C a 80°C, f. adicionar materiais cerosos selecionados de um grupo composto por vaselina branca, parafina líquida, parafina sólida e similares, individualmente ou combinação dos mesmos, em uma quantidade de cerca de 5% (p/p) a 20% (p/p), de preferência, 15% (p/p), mais preferencialmente, 12,5% (p/p), a um recipiente de fase oleosa e fundir a dita cera por aquecimento em 70°C a 80°C, g. adicionar ao dito recipiente da fase oleosa da etapa f, um emulsificante primário, preferencialmente na forma de um surfactante não-iônico selecionado de um grupo composto por álcool cetoestearílico, Cetomacrogol- 1000, individualmente ou combinação dos mesmos, preferencialmente, álcool cetoestearílico em uma quantidade entre 1% (p/p) a 15% (p/p), de preferência, 15% (p/p), mais preferivelmente, 12,5% (p/p), e opcionalmente, um emulsificante secundário selecionado de um grupo composto por polissorbato- 80, Span-80 e similares, preferencialmente, polissorbato-80 em uma quantidade entre 1% (p/p) a 5% (p/p), mais preferivelmente, 2% (p/p) e misturar a mistura completamente, preferencialmente, usando um agitador a 10 a 50 RPM, enquanto mantém a temperatura da mistura em 75°C ± 5°C, h. transferir sob vácuo em uma faixa de -1000 a -300 de mm de mercúrio e em 75°C ± 5°C o conteúdo dos recipientes da fase aquosa e da fase oleosa a um recipiente de mistura e misturar a mistura completamente, preferencialmente, usando um agitador de 10 a 50 RPM para formar uma emulsão, i. resfriar a dita emulsão para 45°C, de preferência pela circulação de água gelada, preferivelmente, em 8°C a 15°C a partir de uma torre de resfriamento na camisa do recipiente de mistura, j. em um recipiente do API adicionar um co-solvente selecionado a partir de um grupo composto por propilenoglicol, hexilenoglicol, polietilenoglicol-400 e similares, individualmente ou combinação dos mesmos, em uma quantidade entre 5% (p/p) a 40% (p/p), preferivelmente, 30% (p/p), mais preferencialmente, 25% (p/p), de preferência propilenoglicol e dissolvendo um antioxidante selecionado a partir de um grupo compreendendo hidroxianisol butilado, hidroxitolueno butilado e similares, individualmente ou em combinação dos mesmos, em uma quantidade entre 0,001% (p/p) a 5% (p/p), de preferência, 0,1% (p/p), preferivelmente 0,01% (p/p), preferencialmente hidroxitolueno butilado em dito propilenoglicol por mistura continua, k. submetendo os conteúdos do dito recipiente do API a descarga de gás inerte, dito gás inerte sendo, preferencialmente, nitrogênio, adicionando fusidato de sódio em uma quantidade entre 0,1% (p/p) a cerca de 25% (p/p), de preferência, de cerca 0,5% (p/p) a cerca de 5°% (p/p), mais preferencialmente, de cerca de 2,08% (p/p), e dissolvendo o dito fusidato de sódio na mistura, l. ajustar o pH da mistura no recipiente do API, da etapa k, para abaixo de 2 pela adição de ácido, selecionado a partir de um grupo composto por ácidos, tais como, HCl, H2SO4, HNO3, ácido lático e similares, individualmente ou combinação dos mesmos, de preferência, ácido nítrico em uma quantidade entre 0,005% (p/p) a 0,5% (p/p), mais preferencialmente, 0,3% (p/p), mais preferivelmente, 0,25% (p/p), m. transferindo o conteúdo do dito recipiente do API, da etapa l, para o recipiente de mistura da etapa i com agitação contínua de 10 a 50 RPM e homogeneização da mistura a 1.000 a 3.000 RPM sob uma descarga de gás inerte e sob vácuo de -1.000 para -300 mm de mercúrio, dito gás inerte sendo preferencialmente nitrogênio, n. em um recipiente separado adicionar um ácido selecionado de um grupo composto por ácidos, tais como, HCl, H2SO4, HNO3, ácido lático e similares, individualmente ou combinação dos mesmos, de preferência, ácido láctico para formar um a partir de cerca de 0,005% (p/p) a 0,5% (p/p), mais preferencialmente, 0,3% (p/p), mais preferivelmente, 0,1% (p/p), e água purificada a partir de cerca de 0,1% (p/p) a 10% (p/p), preferencialmente 8% (p/p), mais preferivelmente 5% (p/p) para formar uma mistura e dissolver o dito polímero, quitosana em uma quantidade entre cerca de 0,01% a cerca de 1% em peso, de preferência, a partir de cerca de 0,01% (p/p) a cerca de 0,5% (p/p) e mais preferencialmente cerca de 0,25% (p/p), o. transferindo o conteúdo da mistura do biopolímero da etapa n para o recipiente de mistura da etapa i com agitação contínua de 10 a 50 RPM e homogeneização da mistura a 1.000 a 3.000 RPM sob uma descarga de gás inerte e sob vácuo de -1.000 a -300 mm de mercúrio, dito gás inerte sendo preferencialmente nitrogênio, p. resfriamento do conteúdo do recipiente de mistura da etapa o para 30°C a 37°C usando circulação de água gelada a partir de uma torre de resfriamento de 8°C a 15°C em uma camisa do recipiente de mistura, q. desligar o agitador e homogeneizador e remover a mistura do recipiente de mistura da etapa n para um recipiente de armazenamento.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IN960/MUM/2009 | 2009-04-13 | ||
| IN960MU2009 | 2009-04-13 | ||
| PCT/IB2010/051552 WO2010119385A1 (en) | 2009-04-13 | 2010-04-12 | A medicinal fusidic acid cream made using sodium fusidate and incorporating a biopolymer and a process to make it |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI1006729A2 BRPI1006729A2 (pt) | 2020-10-06 |
| BRPI1006729B1 true BRPI1006729B1 (pt) | 2021-10-05 |
Family
ID=42558569
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI1006729-9A BRPI1006729B1 (pt) | 2009-04-13 | 2010-04-12 | Creme medicinal de ácido fusídico preparado utilizando fusidato de sódio e incorporando um biopolímero e seu processo de preparação |
Country Status (19)
| Country | Link |
|---|---|
| US (1) | US8895542B2 (pt) |
| EP (1) | EP2419087B1 (pt) |
| JP (1) | JP5205549B2 (pt) |
| KR (1) | KR101642537B1 (pt) |
| CN (1) | CN102159191B (pt) |
| BR (1) | BRPI1006729B1 (pt) |
| CA (1) | CA2795611C (pt) |
| CY (1) | CY1113885T1 (pt) |
| DK (1) | DK2419087T3 (pt) |
| ES (1) | ES2404156T3 (pt) |
| HR (1) | HRP20130149T1 (pt) |
| IL (1) | IL215641A (pt) |
| MX (1) | MX2011010784A (pt) |
| PL (1) | PL2419087T3 (pt) |
| PT (1) | PT2419087E (pt) |
| RU (1) | RU2537023C2 (pt) |
| SI (1) | SI2419087T1 (pt) |
| SM (1) | SMT201300059B (pt) |
| WO (1) | WO2010119385A1 (pt) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101457789B1 (ko) * | 2013-02-13 | 2014-11-03 | 동아제약 주식회사 | 상처 치료용 필름형성 약제학적 조성물 및 그의 제조방법 |
| SG11201507141SA (en) * | 2013-03-15 | 2015-10-29 | Techulon Inc | Antisense molecules for treatment of staphylococcus aureus infection |
| WO2017091167A1 (en) | 2015-11-28 | 2017-06-01 | Pharmacti̇ve İlaç San. Ve Ti̇c. A.Ş. | Topical pharmaceutical composition comprising fusidic acid, isoconazole, dexpanthenol and hydrocortisone |
| FI3638251T3 (fi) | 2017-06-12 | 2024-04-29 | Lakewood Amedex Inc | Bisfosfosiinin geeliformulaatioita ja niiden käyttötapoja |
| CN107224426A (zh) * | 2017-07-08 | 2017-10-03 | 天津双硕医药科技有限公司 | 一种含有夫西地酸的外用乳膏组合物 |
| CN111012747B (zh) * | 2018-10-10 | 2022-11-25 | 四川海思科制药有限公司 | 一种注射用夫西地酸钠药物组合物及其制备方法 |
| CN114432250B (zh) * | 2022-02-22 | 2022-10-04 | 深圳市泰力生物医药有限公司 | 一种非晶态夫西地酸的稳定方法 |
| WO2025099639A1 (en) * | 2023-11-08 | 2025-05-15 | Sulur Vishagan Vanangamudi | Compositions and methods for treating skin disorders |
Family Cites Families (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB8500310D0 (en) * | 1985-01-07 | 1985-02-13 | Leo Pharm Prod Ltd | Pharmaceutical preparation |
| SU1380751A2 (ru) * | 1986-03-12 | 1988-03-15 | Всесоюзный научно-исследовательский институт антибиотиков | Средство дл лечени гнойно-воспалительных заболеваний кожи и м гких тканей |
| DK603988D0 (da) * | 1988-10-28 | 1988-10-28 | Klaus Bendtzen | Farmaceutisk praeparat |
| TW460296B (en) * | 1994-09-01 | 2001-10-21 | Janssen Pharmaceutica Nv | Topical ketoconazole emulsion compositions without sodium sulfite |
| BR9815016A (pt) * | 1997-11-25 | 2000-10-03 | Yamanouchi Europ Bv | Utilização de uma mistura de um diol e um ácido alfa-hidroxi para o tratamento de doenças hiperceratóticas da pele |
| US20070265352A1 (en) * | 2002-02-19 | 2007-11-15 | Joachim Roeding | Synergistic mixtures of at least one 1,2 alkanediol such as 1,2-hexanediol and 1,2-octanediol with a further compound having antimicrobial properties |
| ES2204331B1 (es) * | 2002-10-09 | 2005-03-01 | Ercros Industrial, S.A. | Procedimiento para la obtencion de acido fusidico a partir de un caldo de fermentacion. |
| US20080206161A1 (en) * | 2002-10-25 | 2008-08-28 | Dov Tamarkin | Quiescent foamable compositions, steroids, kits and uses thereof |
| RU2240781C1 (ru) * | 2003-06-05 | 2004-11-27 | Уральский научно-исследовательский институт дерматовенерологии и иммунопатологии | Способ лечения воспалительных процессов вульвы и влагалища |
| US20080275078A1 (en) * | 2004-03-16 | 2008-11-06 | Glaxo Group Limited | Pyrazolo[3,4-B] Pyridine Compounds and Their Use as Pde4 Inhibitors |
| ZA200805981B (en) * | 2006-02-02 | 2009-11-25 | Leo Pharma As | A topical composition comprising an antibacterial substance |
| US9132071B2 (en) | 2006-07-28 | 2015-09-15 | Santen Sas | Compositions containing quaternary ammonium compounds |
| US20080182819A1 (en) * | 2007-01-29 | 2008-07-31 | Act Iii Licensing, Llc | Chitosan compositions and methods for using chitosan compositions in the treatment of health disorders |
| US20110257144A1 (en) * | 2008-12-19 | 2011-10-20 | Apex Laboratories Private Limited | Novel dermaceutical cream made using sodium fusidate |
| WO2010095091A1 (en) * | 2009-02-18 | 2010-08-26 | Sulur Subramaniam Vanangamudi | A process to make fusidic acid cream |
-
2010
- 2010-04-12 BR BRPI1006729-9A patent/BRPI1006729B1/pt active IP Right Grant
- 2010-04-12 ES ES10718707T patent/ES2404156T3/es active Active
- 2010-04-12 JP JP2012505268A patent/JP5205549B2/ja active Active
- 2010-04-12 CA CA2795611A patent/CA2795611C/en active Active
- 2010-04-12 PL PL10718707T patent/PL2419087T3/pl unknown
- 2010-04-12 PT PT107187072T patent/PT2419087E/pt unknown
- 2010-04-12 US US13/263,846 patent/US8895542B2/en active Active
- 2010-04-12 MX MX2011010784A patent/MX2011010784A/es active IP Right Grant
- 2010-04-12 DK DK10718707.2T patent/DK2419087T3/da active
- 2010-04-12 RU RU2011146230/15A patent/RU2537023C2/ru active
- 2010-04-12 KR KR1020117026914A patent/KR101642537B1/ko active Active
- 2010-04-12 HR HRP20130149AT patent/HRP20130149T1/hr unknown
- 2010-04-12 CN CN201080002688.7A patent/CN102159191B/zh active Active
- 2010-04-12 WO PCT/IB2010/051552 patent/WO2010119385A1/en not_active Ceased
- 2010-04-12 EP EP10718707A patent/EP2419087B1/en active Active
- 2010-04-12 SI SI201030186T patent/SI2419087T1/sl unknown
-
2011
- 2011-10-09 IL IL215641A patent/IL215641A/en active IP Right Grant
-
2013
- 2013-03-27 CY CY20131100257T patent/CY1113885T1/el unknown
- 2013-06-05 SM SM201300059T patent/SMT201300059B/xx unknown
Also Published As
| Publication number | Publication date |
|---|---|
| SI2419087T1 (sl) | 2013-06-28 |
| RU2011146230A (ru) | 2013-05-20 |
| US20120040946A1 (en) | 2012-02-16 |
| BRPI1006729A2 (pt) | 2020-10-06 |
| KR20120023653A (ko) | 2012-03-13 |
| CA2795611A1 (en) | 2010-10-21 |
| RU2537023C2 (ru) | 2014-12-27 |
| DK2419087T3 (da) | 2013-05-06 |
| CN102159191B (zh) | 2014-04-02 |
| EP2419087A1 (en) | 2012-02-22 |
| MX2011010784A (es) | 2012-01-12 |
| PL2419087T3 (pl) | 2013-06-28 |
| HRP20130149T1 (hr) | 2013-03-31 |
| CY1113885T1 (el) | 2016-07-27 |
| JP2012523451A (ja) | 2012-10-04 |
| IL215641A0 (en) | 2012-01-31 |
| SMT201300059B (it) | 2013-07-09 |
| ES2404156T3 (es) | 2013-05-24 |
| PT2419087E (pt) | 2013-04-26 |
| WO2010119385A1 (en) | 2010-10-21 |
| KR101642537B1 (ko) | 2016-07-25 |
| JP5205549B2 (ja) | 2013-06-05 |
| CN102159191A (zh) | 2011-08-17 |
| CA2795611C (en) | 2016-09-20 |
| EP2419087B1 (en) | 2013-01-23 |
| US8895542B2 (en) | 2014-11-25 |
| IL215641A (en) | 2014-09-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BRPI1006729B1 (pt) | Creme medicinal de ácido fusídico preparado utilizando fusidato de sódio e incorporando um biopolímero e seu processo de preparação | |
| US20120022019A1 (en) | Medicinal Steroids Cream And A Process To Make It | |
| EP2410975A1 (en) | A medicinal antibacterial cream and a process to make it | |
| WO2010109423A1 (en) | A medicinal antifungal and steroids cream comprising chitosan and a process to make it | |
| WO2010109418A1 (en) | A medicinal antifungal cream and a process to make it | |
| US20120108539A1 (en) | Medicinal Anti Acne Cream And A Process To Make It | |
| WO2011101831A2 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating a biopolymer, a corticosteroid - clobetasone butyrate, and an antifungal agent -terbinafine hydrochloride and a process to make it | |
| WO2012017383A1 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating biopolymer, beclomethasone dipropionate, terbinafine hydrochloride and a process to make it | |
| WO2011101825A1 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating a biopolymer, clotrimazole and clobetasone, and a process to make it | |
| WO2012017381A1 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating, biopolymer, beclomethasone dipropionate, clotrimazole and a process to make it | |
| WO2010122494A1 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating a biopolymer and mometasone, and a process to make it | |
| WO2012017372A1 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating, biopolymer, clobetasol propionate, miconazole nitrate and a process to make it | |
| WO2011101824A1 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating a biopolymer, miconazole, dexamethasone, and a process to make it | |
| WO2012049545A1 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating a biopolymer and a process to make it | |
| WO2012023079A1 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating a biopolymer, fluticasone propionate, oxiconazole nitrate and a process to make it | |
| WO2010122492A1 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating a biopolymer and a corticosteroid, and a process to make it | |
| WO2011101829A2 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating a biopolymer, a corticosteroid - betamethasone dipropionate and an antifungal agent - miconazole nitrate, and a process to make it | |
| WO2012017371A1 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating a biopolymer, clobetasole propionate, terbinafine hydrochloride and a process to make it | |
| WO2012023081A1 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating a biopolymer, a corticosteroid - hydrocortisone acetate, and an antifungal agent - oxiconazole nitrate, and a process to make it | |
| WO2011101822A2 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating a biopolymer, and a corticosteroid - dexamethasone acetate, and a process to make it | |
| WO2011101830A1 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating a biopolymer and clobetasone, and a process to make it | |
| WO2012017368A1 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating a biopolymer, beclomethasone dipropionate and a process to make it | |
| WO2012023078A1 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating a biopolymer, a corticosteroid - dexamethasone acetate, and an antifungal agent - oxiconazole nitrate, and a process to make it | |
| WO2011101827A2 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating a biopolymer, a corticosteroid - clobetasone butyrate, and an antifungal agent - miconazole nitrate, and a process to make it | |
| WO2012017369A1 (en) | A medicinal fusidic acid cream made using sodium fusidate and incorporating biopolymer, betamethasone dipropionate, clotrimazole and a process to make it |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] |
Free format text: DE ACORDO COM O ARTIGO 229-C DA LEI NO 10196/2001, QUE MODIFICOU A LEI NO 9279/96, A CONCESSAO DA PATENTE ESTA CONDICIONADA A ANUENCIA PREVIA DA ANVISA. CONSIDERANDO A APROVACAO DOS TERMOS DO PARECER NO 337/PGF/EA/2010, BEM COMO A PORTARIA INTERMINISTERIAL NO 1065 DE 24/05/2012, ENCAMINHA-SE O PRESENTE PEDIDO PARA AS PROVIDENCIAS CABIVEIS. |
|
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] | ||
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 12/04/2010, OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF, QUE DETERMINA A ALTERACAO DO PRAZO DE CONCESSAO. |