CN103804330A - ent-半日花烷二萜衍生物的制备及抗肿瘤用途 - Google Patents
ent-半日花烷二萜衍生物的制备及抗肿瘤用途 Download PDFInfo
- Publication number
- CN103804330A CN103804330A CN201410062373.1A CN201410062373A CN103804330A CN 103804330 A CN103804330 A CN 103804330A CN 201410062373 A CN201410062373 A CN 201410062373A CN 103804330 A CN103804330 A CN 103804330A
- Authority
- CN
- China
- Prior art keywords
- add
- compound
- dichloromethane
- ether
- reaction
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 0 C[C@@](C*)(C(C[C@]1*)[C@@](C)(CC2)[C@@](CC(*)c3c[o]cc3*)C1=*)C2I* Chemical compound C[C@@](C*)(C(C[C@]1*)[C@@](C)(CC2)[C@@](CC(*)c3c[o]cc3*)C1=*)C2I* 0.000 description 6
- PNHRUERWJDCVHB-MLYOOKFZSA-N CC(C)([C@@H](CC1)[C@@](C)(CC2)[C@H](CCc3c[o]cc3)C1=C)[C@@H]2O Chemical compound CC(C)([C@@H](CC1)[C@@](C)(CC2)[C@H](CCc3c[o]cc3)C1=C)[C@@H]2O PNHRUERWJDCVHB-MLYOOKFZSA-N 0.000 description 2
- OORLEQZMJDOXFM-LRZBKABASA-N CC(C)(C(CC1)[C@@](C)(CC2)[C@H](/C=C/c3c[o]cc3)C1=O)[C@@H]2[O]1CC1 Chemical compound CC(C)(C(CC1)[C@@](C)(CC2)[C@H](/C=C/c3c[o]cc3)C1=O)[C@@H]2[O]1CC1 OORLEQZMJDOXFM-LRZBKABASA-N 0.000 description 1
- HEFYOZYTPGNWHA-DBRAHOGNSA-N CC(C)(C(CC1)[C@@](C)(CC2)[C@H](CCc3c[o]cc3)C1=O)[C@@H]2O Chemical compound CC(C)(C(CC1)[C@@](C)(CC2)[C@H](CCc3c[o]cc3)C1=O)[C@@H]2O HEFYOZYTPGNWHA-DBRAHOGNSA-N 0.000 description 1
- CJYNCAQERTWOLE-VDNWCZEISA-N CC(C)(OC)O[C@H](CC1)C(C)(C)[C@@H](CC2)[C@]1(C)[C@H](C/C=C(\[C@@H](CO1)O)/C1=O)C2=C Chemical compound CC(C)(OC)O[C@H](CC1)C(C)(C)[C@@H](CC2)[C@]1(C)[C@H](C/C=C(\[C@@H](CO1)O)/C1=O)C2=C CJYNCAQERTWOLE-VDNWCZEISA-N 0.000 description 1
- DTNJUDZVPUVJNG-WGJUQESYSA-N CC(C)(OC)O[C@H](CC1)C(C)(C)[C@@H]2[C@]1(C)[C@H](CC(C1=CCOC1=O)O)C(C)(C)CC2 Chemical compound CC(C)(OC)O[C@H](CC1)C(C)(C)[C@@H]2[C@]1(C)[C@H](CC(C1=CCOC1=O)O)C(C)(C)CC2 DTNJUDZVPUVJNG-WGJUQESYSA-N 0.000 description 1
- PGBUZEKTPZZKEW-IKVWTGGYSA-N CC(C)([C@@H](CC1)[C@@](C)(CC2)[C@H](CCC3=C(C)COC3=O)C1=C)[C@@H]2O Chemical compound CC(C)([C@@H](CC1)[C@@](C)(CC2)[C@H](CCC3=C(C)COC3=O)C1=C)[C@@H]2O PGBUZEKTPZZKEW-IKVWTGGYSA-N 0.000 description 1
- CZRLVKFAVVHBPQ-XCJLJZCSSA-N CC(C)([C@@H](CC1)[C@@](C)(CC2)[C@H](CCc3c[o]cc3C)C1=C)[C@@H]2O Chemical compound CC(C)([C@@H](CC1)[C@@](C)(CC2)[C@H](CCc3c[o]cc3C)C1=C)[C@@H]2O CZRLVKFAVVHBPQ-XCJLJZCSSA-N 0.000 description 1
- YMOMDYDVIFSKKY-QSVCCXCDSA-N CC(CC1)[C@@H](CCC2=CCOC2=O)[C@](C)(CC2)[C@H]1[C@](C)(CO)[C@@H]2O Chemical compound CC(CC1)[C@@H](CCC2=CCOC2=O)[C@](C)(CC2)[C@H]1[C@](C)(CO)[C@@H]2O YMOMDYDVIFSKKY-QSVCCXCDSA-N 0.000 description 1
- PHVZOPDJIPCCQH-FUMNGEBKSA-N C[C@@]12[IH]CC[C@@](C)([C@H](CCc3c[o]cc3C)C(CC3)=C)[C@@]13[N]#C2 Chemical compound C[C@@]12[IH]CC[C@@](C)([C@H](CCc3c[o]cc3C)C(CC3)=C)[C@@]13[N]#C2 PHVZOPDJIPCCQH-FUMNGEBKSA-N 0.000 description 1
- CVPSZXYGEAKQEZ-IPFAQRCESA-N C[C@](CO)(C(CC1)[C@@](C)(CC2)[C@H](CCc3c[o]cc3)C1=O)[C@@H]2O Chemical compound C[C@](CO)(C(CC1)[C@@](C)(CC2)[C@H](CCc3c[o]cc3)C1=O)[C@@H]2O CVPSZXYGEAKQEZ-IPFAQRCESA-N 0.000 description 1
- ONTLIQFLLKJXBH-PHTMUNBKSA-N C[C@](COC(c(cc1)ccc1[N+]([O-])=O)=O)(C(CC1)[C@@](C)(CC2)[C@H](CCc3c[o]cc3)C1=C)C2OC(c(cc1)ccc1[N+]([O-])=O)=O Chemical compound C[C@](COC(c(cc1)ccc1[N+]([O-])=O)=O)(C(CC1)[C@@](C)(CC2)[C@H](CCc3c[o]cc3)C1=C)C2OC(c(cc1)ccc1[N+]([O-])=O)=O ONTLIQFLLKJXBH-PHTMUNBKSA-N 0.000 description 1
- SLSBMDHBSDCMPH-GFOJFJKKSA-N C[C@]1(C(CC2)=O)C#[N][C@]1(CC1)[C@]2(C)[C@H](CCc2c[o]cc2C)C1=C Chemical compound C[C@]1(C(CC2)=O)C#[N][C@]1(CC1)[C@]2(C)[C@H](CCc2c[o]cc2C)C1=C SLSBMDHBSDCMPH-GFOJFJKKSA-N 0.000 description 1
- NUZDMMPRDHJFHY-ANULTFPQSA-N C[C@]1(CCC2)C=N[C@]1(CC1)[C@]2(C)[C@H](CCc2c[o]cc2C)C1=C Chemical compound C[C@]1(CCC2)C=N[C@]1(CC1)[C@]2(C)[C@H](CCc2c[o]cc2C)C1=C NUZDMMPRDHJFHY-ANULTFPQSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/02—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings
- C07D307/34—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D307/38—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D307/40—Radicals substituted by oxygen atoms
- C07D307/42—Singly bound oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/02—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings
- C07D307/34—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D307/38—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D307/40—Radicals substituted by oxygen atoms
- C07D307/46—Doubly bound oxygen atoms, or two oxygen atoms singly bound to the same carbon atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/02—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings
- C07D307/34—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D307/38—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D307/52—Radicals substituted by nitrogen atoms not forming part of a nitro radical
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
Abstract
本发明涉及由穿心莲内酯合成一类新型ent-半日花烷二萜衍生物的合成方法、及抗肿瘤的细胞毒活性。化合物用通式I表示,其中R1、R2、R3、R4、R5、R6的定义见说明书。本发明公开了这类化合物的制备方法、初步的抗肿瘤活性,以及1H-NMR、MS、IR等结构鉴定的物理数据。
Description
技术领域
本发明涉及由穿心莲内酯合成一类新型ent-半日花烷二萜衍生物的合成方法及抗肿瘤用途。
背景技术
对于药物化学的科研领域中,源于天然产物的化合物由于结构的多样性及其独特的生物活性,至今仍然是药物先导化合物的重要来源。穿心莲内酯(Andrographolide)系爵床科植物穿心莲(Andrographis paniculata)的主要二萜类内酯成分之一,为一类以十氢化萘为母核的ent-半日花烷二萜,在我国有着广泛的应用,具有清热解毒、凉血消肿等功效,被称为“万苦之王”。现代药理学研究揭示了穿心莲内酯为多靶点作用的物质,穿心莲内酯及其衍生物具有一系列生物活性,如消炎抗菌、抗病毒、抗肿瘤、抗糖尿病、保肝、抗饲育等。穿心莲内酯作为一类天然产物,它的骨架还有很大的改造空间,近年来报道了很多以穿心莲内酯为原料进行的结构改造或半合成,有些具有很强的生物活性,因此,以穿心莲内酯为母体的结构改造是获得活性更强的先导物的重要途径。
近年来对于穿心莲内酯及其衍生物的抗肿瘤活性研究有很多报道,穿心莲内酯能够抑制多种癌细胞,如结肠癌细胞、肝癌细胞、前列腺癌细胞、乳腺癌细胞、胶质母细胞瘤、非小细胞性肺癌细胞、淋巴癌细胞、鳞状细胞癌、胰腺癌细胞。穿心莲针对乳腺MCF-7/ADR癌细胞、人类星形胶质细胞瘤细胞U251、结肠癌细胞SW620、肺癌细胞H522、卵巢癌细胞株SK OV3、前列腺癌细胞DU145、肾癌细胞A498的半数抑制抑制量(GI50)分别达到15μm、3μm、10μm、17μm、15μm、20μm、30μm,是一个比较优良的先导化合物。(Nanduri,S.;Nyavanandi,V.K.;Thunuguntla,S.S.;Kasu,S.;Pallerla,M.K.;Ram,P.S.;Rajagopal,S.;Kumar,R.A.;Ramanujam,R.;Babu,J.M.;Vyas,K.;Devi,A.S.;Reddy,G.O.;Akella,V.,Synthesis and structure-activity relationships of andrographolide analogues as novel cytotoxic agents.Bioorganic & medicinal chemistry letters2004,14(18),4711-7.)
穿心莲内酯作为一个多靶点的抗癌物质,近年来有多篇文献报道了其抗癌机制。在肝癌细胞系中(Huh-7、QGY-7703、Bel-7402),穿心莲内酯不会产生凋亡效果,而是通过干扰细 胞线粒体膜电位和活性氧的种类而启动的自吞噬体的细胞死亡,亲环蛋白(cyclophilin D)在这个过程中起到重要的作用。(Chen,W.;Feng,L.;Nie,H.;Zheng,X.,Andrographolide induces autophagic cell death in human liver cancer cells through cyclophilin D-mediated mitochondrial permeability transition pore.Carcinogenesis2012,33(11),2190-8.)
穿心莲内酯对于人类癌细胞的细胞周期的作用,发现针对于肝癌细胞(HepG2),穿心莲内酯能够阻滞细胞G2周期,阻碍有丝分裂的进入和完成,可能的原因是干扰了有丝分裂的纺锤体,对于HepG2细胞与Hela细胞,穿心莲内酯能够诱导DNA损伤,而且血红素加氧酶1和热休克蛋白70的出现,提示了穿心莲内酯可能通过氧化压力的抗癌机制。(Cheung,M.T.;Ramalingam,R.;Lau,K.K.;Chiang,W.L.;Chiu,S.K.,Cell type-dependent effects of andrographolide on human cancer cell lines.Life sciences2012,91(15-16),751-760.)Yanchun Li等人提出穿心莲内酯阻滞人类胶质母细胞瘤G2/M细胞周期,可能是通过抑制PI3K/Akt途径进行的。(Li,Y.;Zhang,P.;Qiu,F.;Chen,L.;Miao,C.;Li,J.;Xiao,W.;Ma,E.,Inactivation of PI3K/Akt signaling mediates proliferation inhibition and G2/M phase arrest induced by andrographolide in human glioblastoma cells.Life sciences2012,90(25-26),962-7.)
穿心莲内酯对于人类非小细胞型肺癌细胞(A549)的抑制机制,发现穿心莲内酯可能调节TGFβ1/PHD/HIF-1α通路,即在穿心莲的作用下,通过泛素依赖型的降解,HIF-1α的细胞蛋白水平降低,与此同时伴随着HIF-1α羟基化酶与脯氨酰羟基化酶(PHD2)表达增多,而HIF-1α的失活又导致了血管内皮生长因子(VEGF)水平的降低。(Lin,H.H.;Tsai,C.W.;Chou,F.P.;Wang,C.J.;Hsuan,S.W.;Wang,C.K.;Chen,J.H.,Andrographolide down-regulates hypoxia-inducible factor-1alpha in human non-small cell lung cancer A549cells.Toxicology and applied pharmacology2011,250(3),336-45.)
穿心莲内酯对于大鼠肝癌细胞(SMMC-7721)的抑制作用,发现穿心莲内酯能够激活线粒体凋亡途径,通过诱导p53基因的表达,Bax构型改变,从而激活线粒体凋亡途径,进一步活化caspase-3,8,9,从而造成凋亡发生。(Yang,L.;Wu,D.;Luo,K.;Wu,S.;Wu,P.,Andrographolide enhances 5-fluorouracil-induced apoptosis via caspase-8-dependent mitochondrial pathway involving p53 participation in hepatocellular carcinoma(SMMC-7721)cells.Cancer Letters2009,276(2),180-188.)
穿心莲对于JAK-STAT3通路有抑制作用,通过对于两面神经激酶(JAK)1/2的抑制和与STAT3、gp130的接触,从而穿心莲内酯能够抑制STAT3的磷酸化和IL-6诱导的STAT3磷酸化,以及随后的癌细胞中的核易位,包括bcl-xL与Mcl-1。(Zhou,J.;Ong,C.N.;Hur,G.M.;Shen,H.M.,Inhibition of the JAK-STAT3 pathway by andrographolide enhances chemosensitivity of cancer cells to doxorubicin.Biochemical pharmacology2010,79(9),1242-50.)
穿心莲内酯针对非小细胞型肺癌细胞A549的转移和入侵的抑制作用,提出了穿心莲内酯能够下调PI3K/Akt信号途径,从而抑制活化蛋白-1(AP-1)与DNA结合的活性,从而下调MMP-7的活性,mRNA水平和蛋白水平,从而对于肿瘤细胞的转移和入侵造成抑制。(Lee,Y.C.;Lin,H.H.;Hsu,C.H.;Wang,C.J.;Chiang,T.A.;Chen,J.H.,Inhibitory effects of andrographolide on migration and invasion in human non-small cell lung cancer A549 cells via down-regulation of PI3K/Akt signaling pathway.European journal of pharmacology2010,632(1-3),23-32.)
发明内容
本发明以天然产物穿心莲内酯为起始原料,通过一系列化学反应合成出一类新型ent-半日花烷二萜衍生物,并测试其化合物的药理活性,证明此类化合物具有较强的抗肿瘤活性。
本发明的目的是公开新型ent-半日花烷二萜衍生物的结构。
本发明的另一目的是提供上述化合物的抗肿瘤的生物活性。
本发明的提供的化合物结构类型通式I如下:
通式I结构中,
R1、R2、R6的结构可以表示为:H、OH、OR7、OCOR7、OCOR7R8、NR7R8、F、Cl、Br、I;其中,R7、R8表示氢、取代或非取代的直链、支链或环状的烃基、苯基、苄基, 其中m=1~8,呋喃或吡喃型五、六元糖基或取代糖基,或2~5个以1,2-、1,4-、1,6-方式连接的葡萄糖基或取代葡萄糖基;上述直链、支链或环状的烃基可进一步表述为:(1)C1~C10烷基;(2)C3~C6环烷基;(3)C3~C10烯基;(4)C3~C10炔基;
R1的结构还可以表示为:=O、=N-OH;
R3的结构表示为:H、OH;
R4的结构表示为:O、CH2;
R5的结构表示为:H、CH3。
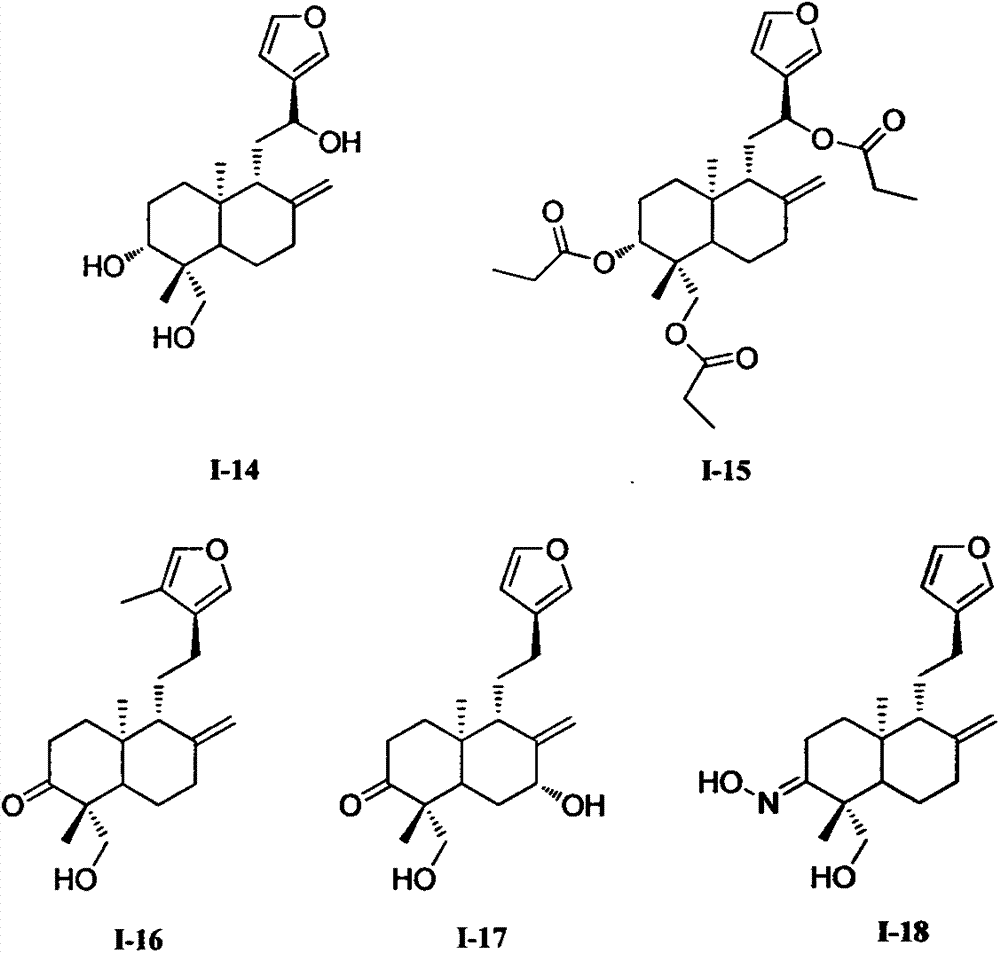
其中部分典型化合物(I-1,I-2,I-3,I-4,I-5,I-6,I-7,I-8,I-9,I-10,I-11,I-12,I-13,I-14,I-15,I-16,I-17,I-18)的结构式为:
典型化合物合成路线列举
I-1,I-2,I-11合成途径:
a)acetic anhydride,DCM,ZnCl2,reflux;b)KBH4,MeOH,rt;c)5%KHCO3,MeOH,reflux;d)DIBALH,THF,-80℃;
e)propionic anhydride,DMAP,DCM,rt;f)SeO2,t-BuOOH,DCM,rt;
I-1,I-2,I-11的合成:
1.
穿心莲内酯投入反应瓶中,加入有机溶剂溶解,再加入催化剂和乙酰化试剂,搅拌加热回流2-50h后,停止反应,反应液冷却至室温,二氯甲烷萃取,分别用饱和碳酸氢钠溶液和饱和食盐水洗涤三次,无水硫酸钠干燥,蒸干得化合物2。其中,有机溶剂为二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、甲醚、乙醚、丙醚、异丙醚、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮、吡啶、吡咯、吗啉、喹啉、1,4-二氧六环、二硫化碳、苯、甲苯、二甲苯中的一种;催化剂为氯化锌、三乙胺、4-二甲氨基吡啶中的一种;乙酰化试剂为乙酰氯、醋酸、乙酸酐中的一种。
2.
化合物2投入反应瓶中,加入有机溶剂溶解,缓慢加入还原试剂,室温反应2-10h后处理,反应液中加入稀盐酸搅拌15-40min后,蒸去溶剂得白色固体化合物3。其中,有机溶剂为甲醇、乙醇、丙醇、异丙醇、正丁醇、乙二醇、1,2-丙二醇、1,3-丙二醇、1,2-丁二醇、1,3-丁二醇、1,4-丁二醇,苄醇中的一种;还原试剂为硼氢化钾、硼氢化钠、氢化铝锂中的一种。
3.
化合物3投入反应瓶,加入有机溶剂溶解,加入脱保护基试剂水溶液,加热回流反应2-50h后,冷却至室温,乙酸乙酯萃取,分别用碳酸钾水溶液和饱和食盐水洗涤三次,无水硫酸钠干燥,经过柱纯化得化合物4。其中,有机溶剂为甲醇、乙醇、丙醇、异丙醇、正丁醇、乙二醇、1,2-丙二醇、1,3-丙二醇、1,2-丁二醇、1,3-丁二醇、1,4-丁二醇、苄醇中的一种;脱保护基试剂为碳酸氢钾、碳酸氢钠中的一种。
4.
化合物4投入反应瓶,加入有机溶剂溶解,密封,氮气保护,液氮低温-78℃恒温状态下,缓慢滴加还原剂,保持低温反应2-10h,等到温度恢复到零度以上后,加入淬灭剂淬灭反应,再搅拌1-10h,加入大量水搅拌,乙酸乙酯萃取,饱和碳酸氢钠和饱和食盐水分别萃取三次,无水硫酸钠干燥,过柱纯化得化合物I-1。其中,有机溶剂为乙醚、四氢呋喃、2-甲基四氢呋喃、3-甲基呋喃、2,5-二甲基呋喃、2-甲基四氢呋喃、四氢吡喃、二氢吡喃、乙腈、二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、乙醚、1,4-二氧六环、苯、甲苯、二甲苯、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮中的一种;还原剂为二异丁基氢化铝;淬灭剂为5~20%稀盐酸或5~20%稀硫酸。
5.
化合物I-1投入反应瓶,加入有机溶剂溶解,加入酰化催化剂,加入酰基化试剂,常温反应2-50h,反应液中加入水,二氯甲烷萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得化合物I-2。其中,有机溶剂为二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、甲醚、乙醚、丙醚、异丙醚、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮、吡啶、吡咯、吗啉、喹啉、1,4-二氧六环、二硫化碳、苯、甲苯、二甲苯中的一种;酰化催化剂为4-二甲氨基吡啶,二环己基碳二亚胺,1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐,苯并三氮唑-1-基氧基三(二甲基氨基)磷鎓六氟磷酸盐中的一种;酰基化试剂为丙酸酐,丙酸,丙酰氯中的一种。
6.
化合物I-2投入反应瓶,加入有机溶剂,加入二氧化硒与叔丁基过氧化氢,反应2-50h,反应液中加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,饱和食盐水干燥,过柱纯化得I-11。其中,有机溶剂为二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、甲醚、乙醚、丙醚、异丙醚、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮、吡啶、吡咯、吗啉、喹啉、1,4-二氧六环、二硫化碳、苯、甲苯、二甲苯中的一种。
I-3的合成途径:
a)propionic anhydride,DMAP,DCM,rt.
I-3的合成:
化合物I-1投入反应瓶,加入有机溶剂,加入酰化催化剂,加入酰基化试剂,常温反应2-50h,反应液中加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得I-3。其中,有机溶剂为二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、甲醚、乙醚、丙醚、异丙醚、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮、吡啶、吡咯、吗啉、喹啉、1,4-二氧六环、二硫化碳、苯、甲苯、二甲苯中的一种;酰化催化剂为4-二甲氨基吡啶,二环己基碳二亚胺,1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐,苯并三氮唑-1-基氧基三(二甲基氨基)磷鎓六氟磷酸盐中的一种;酰基化试剂为二氯乙酸、二氯乙酸酐中的一种。
I-4的合成途径:
a)phenoxyacetic acid,EDCI,DMAP,DCM,rt
I-4的合成:
化合物I-1投入反应瓶,加入有机溶剂,加入1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐,加入4-二甲氨基吡啶,加入苯氧乙酸,常温反应2-50h,反应液中加入大量水,二氯甲烷萃 取,饱和食盐水洗涤三次,饱和食盐水干燥,过柱纯化得I-4。其中,有机溶剂为二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、甲醚、乙醚、丙醚、异丙醚、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮、吡啶、吡咯、吗啉、喹啉、1,4-二氧六环、二硫化碳、苯、甲苯、二甲苯中的一种。
I-5的合成途径:
a)4-nitrobenzoic acid,EDCI,DMAP,DCM,rt
I-5的合成:
化合物I-1投入反应瓶,加入有机溶剂,加入1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐,加入4-二甲氨基吡啶,加入对硝基苯甲酸,常温反应2-50h,反应液中加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得I-5。其中,有机溶剂为二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、甲醚、乙醚、丙醚、异丙醚、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮、吡啶、吡咯、吗啉、喹啉、1,4-二氧六环、二硫化碳、苯、甲苯、二甲苯中的一种。
I-6的合成途径:
a)4-nitrobenzoic acid,EDCI,DMAP,DCM,rt
I-6的合成:
化合物I-1投入反应瓶,加入有机溶剂,加入1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐,加入4-二甲氨基吡啶,加入对硝基苯甲酸,常温反应2-50h,反应液中加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得I-6。其中,有机溶剂为二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、甲醚、乙醚、丙醚、异丙醚、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮、吡啶、吡咯、吗啉、喹啉、1,4-二氧六环、二硫化碳、苯、甲苯、二甲苯中的一种。
I-7的合成途径:
a)4-methoxybenzoic acid,EDCI,DMAP,DCM,rt
I-7的合成:
化合物I-1投入反应瓶,加入有机溶剂,加入1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐,加入4-二甲氨基吡啶,加入对甲氧基苯甲酸,常温反应2-50h,反应液中加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得I-7。其中,有机溶剂为二氯 甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、甲醚、乙醚、丙醚、异丙醚、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮、吡啶、吡咯、吗啉、喹啉、1,4-二氧六环、二硫化碳、苯、甲苯、二甲苯中的一种。
I-8的合成途径:
a)acetic anhydride,DMAP,DCM,rt;b)KMnO4,TBAB,magnesium sulfatev heptahydrate,benzene,water,60℃;
c)NaOH,CH3OH.rt.
I-8的合成:
1.
化合物I-1投入反应瓶,加入有机溶剂溶解,加入酰化催化剂,加入酰基化试剂,常温反应2-50h,反应液中加入水,二氯甲烷萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得化合物5。其中,有机溶剂为二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、甲醚、乙醚、丙醚、异丙醚、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮、吡啶、吡咯、吗啉、喹啉、1,4-二氧六环、二硫化碳、苯、甲苯、二甲苯中的一种;酰化催化剂为4-二甲氨基吡啶,二环己基碳二亚胺,1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐,苯并三氮唑-1-基氧基三(二甲基氨基)磷鎓六氟磷酸盐中的一种;酰基化试剂为乙酸酐、乙酸、乙酰氯中的一种。
2.
化合物5投入反应瓶,加入四丁基溴化铵,用苯溶解,加入用水溶解的七水硫酸镁,加入用水溶解的高锰酸钾,控制温度在50-60℃,反应2-50h,反应液中加入水,二氯甲烷萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得化合物6。
3.
化合物6投入反应瓶,有机溶剂溶解,加入碱,搅拌1-10h,加入大量饱和碳酸氢钠水溶液,二氯甲烷萃取,饱和碳酸氢钠水溶液和饱和食盐水各洗涤三遍,无水硫酸钠干燥,过柱纯化得II-8。其中有机溶剂为甲醇或乙醇其中一种;碱为5~20%氢氧化钾溶液、5~20%氢氧化钠溶液、5~20%碳酸钾溶液、5~20%碳酸氢钾溶液、5~20%碳酸钠溶液、5~20%碳酸氢钠溶液、吡啶、三乙胺、N,N-二甲基氨基吡啶、脂肪胺和芳香胺中的一种。
I-10,I-9的合成途径:
a)SeO2,t-BuOOH,DCM,rt;b)NaOH,CH3OH.rt.
I-10的合成:
化合物5投入反应瓶,加入有机溶剂,加入二氧化硒与叔丁基过氧化氢,反应2-50h,反应液中加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得I-10。其中,有机溶剂为二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、甲醚、乙醚、丙醚、异丙醚、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮、吡啶、吡咯、吗啉、喹啉、1,4-二氧六环、二硫化碳、苯、甲苯、二甲苯中的一种;酰化催化剂为4-二甲氨基吡啶、二环己基碳二亚胺、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐、苯并三氮唑-1-基氧基三(二甲基氨基)磷鎓六氟磷酸盐中的一种;酰基化试剂为丙酸酐、丙酸、丙酰氯中的一种。
I-9的合成:
化合物I-10投入反应瓶,有机溶剂溶解,加入碱,搅拌1-10h,加入大量饱和碳酸氢钠水溶液,二氯甲烷萃取,饱和碳酸氢钠水溶液和饱和食盐水各洗涤三遍,无水硫酸钠干燥,过柱纯化得I-9。其中有机溶剂为甲醇或乙醇其中一种;碱为5~20%氢氧化钾溶液、5~20%氢氧化钠溶液、5~20%碳酸钾溶液、5~20%碳酸氢钾溶液、5~20%碳酸钠溶液,、5~20%碳酸氢钠溶液、吡啶、三乙胺、N,N-二甲基氨基吡啶、脂肪胺和芳香胺中的一种。
I-12,I-13的合成途径:
a)diazomethane,diethylether,rt;b)DMF,reflux;c)5%KHCO3,MeOH,reflux;d)DIBALH,THF,-80℃;e)Ac2O,DMAP,DCM,rt;
f)SeO2,t-BuOOH,DCM,rt;g)NaOH,CH3OH.rt.
I-12,I-13的合成:
1.
化合物3投入反应瓶,乙醚溶解,加入重氮甲烷乙醚溶液,密封,常温搅拌1day-30day,过滤,过柱纯化得化合物7。
2.
化合物7投入反应瓶,N,N-二甲基甲酰胺溶解,加热回流,搅拌1-50h小时,冷却至室温,加入大量水,乙酸乙酯萃取,饱和食盐水洗涤三遍,无水硫酸钠干燥,浓缩得化合物8。
3.
化合物8投入反应瓶,加入有机溶剂溶解,加入脱保护基试剂水溶液,加热回流反应2-50h后,冷却至室温,乙酸乙酯萃取,分别用碳酸钾水溶液和饱和食盐水洗涤三次,无水硫酸钠干燥,经过柱纯化得化合物9。其中,有机溶剂为甲醇、乙醇、丙醇、异丙醇、正丁醇、乙二醇、1,2-丙二醇、1,3-丙二醇、1,2-丁二醇、1,3-丁二醇、1,4-丁二醇,苄醇中的一种;脱保护基试剂为碳酸氢钾、碳酸氢钠中的一种。
4.
化合物9投入反应瓶,加入有机溶剂溶解,密封,氮气保护,液氮低温-78℃恒温状态下,缓慢滴加还原剂,保持低温反应2-10h,等到温度恢复到零度以上后,加入淬灭剂淬灭反应,再搅拌1-10h,加入大量水搅拌,乙酸乙酯萃取,饱和碳酸氢钠和饱和食盐水分别萃取三次,无水硫酸钠干燥,过柱纯化的化合物I-12。其中,有机溶剂为乙醚、四氢呋喃、2-甲基四氢呋喃、3-甲基呋喃、2,5-二甲基呋喃、2-甲基四氢呋喃、四氢吡喃、二氢吡喃、乙腈、二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、乙醚、1,4-二氧六环、苯、甲苯、二甲苯、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮中的一种;还原剂为二异丁基氢化铝;淬灭剂为5~20%稀盐酸或5~20%稀硫酸。
5.
化合物I-12投入反应瓶,加入有机溶剂溶解,加入酰化催化剂,加入酰基化试剂,常温反应2-50h,反应液中加入水,二氯甲烷萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得化合物10。其中,有机溶剂为二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、甲醚、乙醚、丙醚、异丙醚、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮、吡啶、吡咯、吗啉、喹啉、1,4-二氧六环、二硫化碳、苯、甲苯、二甲苯中的一种;酰化催化剂为4-二甲氨基吡啶、二环己基碳二亚胺、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐、苯并三氮唑-1-基氧基三(二甲基氨基)磷鎓六氟磷酸盐中的一种;酰基化试剂为乙酸酐、乙酸、乙酰氯中的一种。
6.
化合物10投入反应瓶,加入有机溶剂,加入二氧化硒与叔丁基过氧化氢,反应2-50h,反应液中加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,饱和食盐水干燥,过柱纯化得11。其中,有机溶剂为二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、甲醚、乙醚、丙醚、异丙醚、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮、吡啶、吡咯、吗啉、喹啉、1,4-二氧六环、二硫化碳、苯、甲苯、二甲苯中的一种。
7.
化合物11投入反应瓶,有机溶剂溶解,加入碱,搅拌1-10h,加入大量饱和碳酸氢钠水溶液,二氯甲烷萃取,饱和碳酸氢钠水溶液和饱和食盐水各洗涤三遍,无水硫酸钠干燥,过柱纯化得I-13。其中有机溶剂为甲醇或乙醇其中一种;碱为5~20%氢氧化钾溶液、5~20%氢氧化钠溶液、5~20%碳酸钾溶液、5~20%碳酸氢钾溶液、5~20%碳酸钠溶液、5~20%碳酸氢钠溶液、吡啶、三乙胺、N,N-二甲基氨基吡啶、脂肪胺和芳香胺中的一种。
I-14,I-15的合成途径:
a)2,2-dimethoxypropane,p-toluenesulfonic acid,tolune∶DMSO=7∶1,reflux;b)PDC,DCM,rt;c)AcOH∶H2O=3∶1,rt;
d)DIBALH,THF,-80℃;e)propionic anhydride,DMAP,DCM,rt.
I-14,I-15的合成:
1.
将穿心莲内酯投入反应瓶,甲苯跟二甲亚砜溶解,加入对甲苯磺酸催化,加入2,2-二甲氧基丙烷,加热回流,反应液加热回流反应1.5-12h,冷却至室温,加入乙酸乙酯稀释,加入大量水,乙酸乙酯萃取三遍,再分别用水和饱和食盐水洗涤三次,无水硫酸钠干燥,浓缩得化合物12。
2.
将化合物12投入反应瓶,有机溶剂溶解,加入重铬酸吡啶嗡盐,搅拌2-50h,浓缩,加入大量乙酸乙酯,过滤,过柱纯化得化合物13。其中,有机溶剂为二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、甲醚、乙醚、丙醚、异丙醚、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮、吡啶、吡咯、吗啉、喹啉、1,4-二氧六环、二硫化碳、苯、甲苯、二甲苯中的-种。
3.
将化合物13投入反应瓶,加入醋酸水溶液搅拌,搅拌1-10h,在反应液中加入大量的饱和碳酸氢钠水溶液,乙酸乙酯萃取三遍,再分别用饱和碳酸氢钠水溶液和饱和食盐水萃取三遍,无水硫酸钠干燥,过柱纯化得化合物14。
4.
化合物14投入反应瓶,加入有机溶剂溶解,密封,氮气保护,液氮低温-78℃恒温状态下,缓慢滴加还原剂,保持低温反应2-10h,等到温度恢复到0℃以上后,缓慢滴加醋酸水溶液,再搅拌1-10h,加入大量水搅拌,乙酸乙酯萃取,饱和碳酸氢钠和饱和食盐水分别萃取三次,无水硫酸钠干燥,过柱纯化得化合物I-14。其中,有机溶剂为乙醚、四氢呋喃、2-甲基四氢呋喃、3-甲基呋喃、2,5-二甲基呋喃、2-甲基四氢呋喃、四氢吡喃、二氢吡喃、乙腈、二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、乙醚、1,4-二氧六环、苯、甲苯、二甲苯、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮中的一种。
5.
化合物I-14投入反应瓶,加入有机溶剂溶解,加入酰化催化剂,加入酰基化试剂,常温反应2-50h,反应液中加入水,二氯甲烷萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得化合物I-15。其中,有机溶剂为二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、甲醚、乙醚、丙醚、异丙醚、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮、吡啶、吡咯、吗啉、喹啉、1,4-二氧六环、二硫化碳、苯、甲苯、二甲苯中的一种;酰化催化剂为4-二甲氨基吡啶、二环己基碳二亚胺、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐、苯并三氮唑-1-基氧基三(二甲基氨基)磷鎓六氟磷酸盐中的一种;酰基化试剂为丙酸酐、丙酸、丙酰氯中的 一种。
1-16的合成途径:
a)TrCl,DIPEA,DCM,rt;b)PDC,DMF,50℃;c)p-toluenesulfonic acid,MeOH,rt.
I-16的合成:
1.
将化合物I-12投入反应瓶中,二氯甲烷溶解,加入三苯基氯甲烷,室温下搅拌2-50h,加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得化合物15。
2.
将化合物15投入反应瓶中,二甲亚砜溶解,加入重铬酸吡啶嗡盐,室温下搅拌2-50h,反应液中加入大量水,乙酸乙酯萃取三遍,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得16。
3.
将化合物16投入反应瓶中,甲醇溶解,加入对甲苯磺酸,室温下搅拌1-10h,加入大量水和饱和碳酸氢钠水溶液,乙酸乙酯萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得I-16。
I-17,I-18的合成途径:
a)TrCl,DIPEA,DCM,rt;b)PDC,DMF,50℃;(c)p-toluenesulfonic acid,MeOH,rt;(d)SeO2,t-BuOOH,DCM,rt;
(e)NH2OH-HCl,Pyridine,40℃.
I-17,I-18的合成:
1.
将化合物I-1投入反应瓶中,二氯甲烷溶解,加入三苯基氯甲烷,室温下搅拌2-50h,加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得化合物17。
2.
将化合物17投入反应瓶中,二甲亚砜溶解,加入重铬酸吡啶嗡盐,室温下搅拌2-50h,反应液中加入大量水,乙酸乙酯萃取三遍,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得化合物18。
3.
将化合物18投入反应瓶中,甲醇溶解,加入对甲苯磺酸,室温下搅拌1-10h,加入大量水和饱和碳酸氢钠水溶液,乙酸乙酯萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得化合物19。
4.
化合物19投入反应瓶,加入有机溶剂,加入二氧化硒与叔丁基过氧化氢,反应2-50h,反应液中加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,饱和食盐水干燥,过柱纯化得化合物I-17。其中,有机溶剂为二氯甲烷、氯仿、四氯化碳、1,2-二氯乙烷、1,1-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、1,2-二氯丙烷、1,3-二氯丙烷、1,2,3-三氯丙烷、四氢呋喃、甲醚、乙醚、丙醚、异丙醚、苯甲醚、苯乙醚、环氧乙烷、二苯醚、丙酮、丁酮、甲基丙酮、2-戊酮、3-戊酮、2-己酮、3-己酮、吡啶、吡咯、吗啉、喹啉、1,4-二氧六环、二硫化碳、苯、甲苯、二甲苯中的一种。
5.
化合物19投入反应瓶,吡啶溶解,加入盐酸羟胺,室温下搅拌1-10h,用稀盐酸中和,乙酸乙酯萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得化合物I-18。
化合物的药理测试结果
1.测试细胞株
人尿路上皮癌细胞株(NTUB1),人乳腺癌细胞株(MCF-7),人乳腺癌细胞株(MDA-MB-231),抗顺铂的人尿路上皮癌细胞株(NP14)。
2.实验原理
MTT法是利用活细胞线粒体中存在与NADP相关的脱氢酶能使外源性的MTT还原成难溶性的蓝紫色结晶物(Formazan)并沉积在细胞中,而死细胞无此功能,再用二甲基亚砜(DMSO) 或三联液(10%SDS-5%异丁醇-0.01mol/L HCL)溶解细胞中的紫色结晶物,用酶联免疫检测仪在570nm波长处测定其OD值间接反应其活细胞量。本法是目前抗肿瘤药物体外研究、尤其是大规模筛选最常用的方法。
3.实验方法及要点
将处于细胞对数生长期的要进行实验的肿瘤细胞按一定的细胞量接种于96孔培养板内,培养24h后加入所筛样品(悬浮细胞接板后可直接加),细胞在37℃5%CO2条件下继续培养48小时后,加入MTT继续培养4小时,用DMSO溶解在酶标仪下进行检测。
4.样品编号
5.样品作用时间:48小时
6.药理测试过程
体外培养人尿路上皮癌细胞株(NTUB1),人乳腺癌细胞株(MCF-7),人乳腺癌细胞柱(MDA-MB-231),抗顺铂的人尿路上皮癌细胞株(NP14)。细胞生长至数周后,用胰酶消化细胞,1000rpm离心5分钟,弃上层清夜,用适量培养基悬浮,调整细胞浓度至4.5×104/ml.将细胞悬液接种到96孔细胞培养板中,每孔100μl,放置细胞培养箱(37℃,5%)中培养24小时后,各用药组分分别加入细胞培养基稀释的I-1,I-2,I-3,I-4,I-5,I-6,I-7,I-8,I-9,I-10,I-11,I-12,I-13,I-14,I-15,I-16,I-17,I-18100μl,得到个不同浓度的化合物组分,阴性对照组0.5%DMSO,各组均设3个复孔。培养箱中培养48小时后,每孔加入5mg/mlde MTT20μl,在温度为37℃的条件下放置4个小时。每孔加入200μl DMSO,37℃的条件下摇床震摇20分钟,在ELISA酶标仪上比色对照组和各加样组的OD值,测定波长为570nm,参考波长为450nm。计算各加药浓度处理的药物对细胞的抑制率,据细胞抑制曲线计算药物的半抑制浓度IC50值(μM)。
7.药理测试结果
NA:没有活性。
具体实施方式
以下结合具体事例说明本发明的典型化合物。
实例1:I-1、I-2、I-11、I-3、I-4、I-5、I-6和I-7合成
1.穿心莲内酯(3.0g,8.6mmol)投入反应瓶中,加入60.0mL二氯甲烷溶解,再加入氯化锌(3.6g,26.5mmol)和15.0mL乙酸酐,磁力搅拌,加热回流2h后,停止反应,反应液冷却至室温,加水,CH2Cl2萃取三次,合并有机相,分别用饱和碳酸氢钠溶液和饱和食盐水洗涤两次,无水硫酸钠干燥,蒸干得4.0g白色固体化合物2,收率为97.6%。mp:122℃;IR(KBr v cm-1):2944,2855,1735,1675,1640,1437,1372,1274,1235,1189,1104,1074,1025,980,900,764,749,609;1H NMR(300MHz,CDCl3, δ,ppm):6.99-7.04(t,1H),5.92-5.94(s,1H),4.92(s,1H),4.58-4.65(dd,1H),4.53-4.55(m,1H),4.35-4.39(d,1H),4.24-4.28(dd,1H),4.12-4.16(d,1H),2.40-2.47(m,3H),2.13(s,3H),2.06(s,6H),1.56(s,4H),1.05(s,3H),0.77(s,3H);ESI-MS:494[M+NH4]+.
2.化合物2(4.0g,8.4mmol)投入反应瓶中,加入60.0mL甲醇溶解,缓慢加入过量的硼氢化钾(1.4g,25.9mmol),室温反应2h后处理,反应液中加入稀盐酸搅拌15min后,蒸去溶剂得3.4g白的固体化合物3,收率为96.4%。mp:107-110℃;IR(KBr v cm-1):2943,2867,1735,1640,1448,1375,1254,1136,1077,1033,903,833,765,744;1H NMR(300MHz,CDCl3,δ,ppm):7.1(s,1H),4.9(s,1H),4.78(s,2H),4.57-4.63(m,2H),4.34-4.38(d,1H),4.07-4.11(d,1H),2.41-2.45(m,2H),2.04(s,6H),0.99(s,3H)0.72(s,3H);ESI-MS:436[M+NH4]+.
3.化合物3(6g,14.34mmol)投入反应瓶中,加入80mL甲醇,加入5%碳酸氢钾水溶液270mL,加热至回流,搅拌10h,冷却至室温,浓缩除去部分甲醇,乙酸乙酯萃取反应液,饱和食盐水洗涤,无水硫酸钠干燥,柱层析得到3.9g白色固体化合物4,收率为81.4%。m.p:176-177℃.IR(KBr,v):3285,3074,2966,2929,1753,1652,1632,1439,1381,1350cm-1;1HNMR(CDCl3,ppm):7.13(s,1H),4.88(s,1H),4.79(s,2H),4.59(s,1H),4.17(d,1H,J=10.9Hz),3.69(br,2H),3.44(s,1H,J=7.4Hz),3.29(d,1H,J=10.9Hz),2.48-2.39(m,2H),2.13-1.79(m,6H),1.58(s,3H),1.33-1.16(m,7H),0.63(s,3H);ESI-MS:m/z333.2[M-H]-.
4.化合物4(3.5g,10.46mmol)投入反应瓶,加入100mL四氢呋喃,密封反应瓶,氮气保护,液氮降温至-78℃后,向反应液中缓慢滴加二异丁基氢化铝(20.9ml of solution1.5M in toluene,31.38mmol),滴加完后保持低温搅拌3h,等温度上升到零度后,缓慢滴加10%硫酸30mL,搅拌1h,反应液中加入大量水,乙酸乙酯萃取,饱和碳酸氢钠水溶液和饱和食盐水各洗涤三次,无水硫酸钠干燥,经柱层析得2.7g白色固体化合物I-1,收率为81.8%。m.p.124-127℃.IR(KBr,v):3245,3079,2758,2937,2867,1639,1443,1384,1255,1166,1040,1023,895,872,782cm-1;1H NMR(CDCl3,ppm):7.35(s,1H),7.17(s,1H),6.25(s,1H),4.88(s,1H),4.58(s,1H),4.18(d,1H,J=11.2Hz),3.48-3.43(m,1H),3.31(d,1H,J=11.1Hz),2.69-2.49(m,3H),2.43-1.64(m,7H),1.59(s,3H),1.33-0.85(m,8H),0.63(s,3H);ESI-MS:m/z353.4[M+Cl]-.
5.将化合物I-1(0.200g,0.63mmol)投入反应瓶中,加入5mL二氯甲烷溶解,加入0.23ml(2.52mmol)丙酸酐,加入催化量的4-二甲氨基吡啶,搅拌5h,反应液中加入水,二氯甲烷萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,柱层析得0.265g无色液体I-2,产率为98.1%。IR(KBr,v):2929,2852,1734,1644,1591,1463,1385,1348,1262,1238,1193,1129, 1083,1019,967,889,873,804,698,600,455cm-1;1H NMR(CDCl3,ppm):7.35(s,1H),7.18(s,1H),6.24(s,1H),4.89(s,1H),4.60(s,1H),4.58-4.55(m,1H),4.38(d,1H,J=11.7Hz),4.09(d,1H,J=11.7Hz),2.52-2.27(m,7H),1.91-1.47(m,11H),1.15-1.10(m,6H),0.98(s,3H),0.70(s,3H);ESI-MS:m/z453.3[M+Na]+.
6.化合物I-2(0.120g,0.279mmol)投入反应瓶,加入5mL,加入二氧化硒(26mg,0.234mmol)与叔丁基过氧化氢(≥65%,0.1ml),反应12h,反应液中加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,饱和食盐水干燥,柱层析得0.902g无色液体I-11,产率72.5%。IR(KBr,v):2941,2360,1733,1463,1275,1261,1195,1019,764,750cm-1;1H NMR(CDCl3,ppm):7.36(s,1H),7.20(s,1H),6.25(s,1H),5.11(s,1H),4.73(s,1H),4.65-4.61(m,1H),4.40(s,1H),4.32(d,1H,J=11.7Hz),4.16(d,1H,J=11.7Hz),2.52-2.29(m,7H),2.01-1.43(m,9H),1.15-1.10(m,6H),0.98(s,3H),0.70(s,3H);ESI-MS:m/z469.2[M+Na]+.
7.化合物I-1(50mg,0.157mmol)投入反应瓶,加入二氯甲烷5mL,加入二氯乙酸(0.06mL,0.628mmol),加入催化量的4-二甲氨基吡啶,加入1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(145mg,0.756mmol),常温反应10h,反应液中加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,饱和食盐水干燥,柱层析得82.8mg无色液体化合物I-3,产率为97.3%。IR(KBr,v):2925,2851,2360,1759,1591,1463,1385,1276,1261,1238,1169,1127,1018,873,814,764,750,699,600,511,404cm-1;1H NMR(CDCl3,ppm):7.35(s,1H),7.18(s,1H),6.24(s,1H),5.96(d,2H,J=6.12Hz),4.89(s,1H),4.72-4.67(m,1H),4.60(s,1H),4.53(d,1H,J=11.7Hz),4.32(d,1H,J=11.7Hz),2.59-2.23(m,3H),1.97-1.32(m,13H),1.11(s,3H),0.70(s,3H);ESI-MS:m/z565.1[M+Na]+.
8.化合物I-1(50mg,0.157mmol)投入反应瓶,加入二氯甲烷5mL,加入苯氧乙酸(95.5mg,0.628mmol),加入催化量的4-二甲氨基吡啶,加入1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(145mg,0.756mmol),常温反应10h,反应液中加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,饱和食盐水干燥,柱层析得23mg无色液体化合物I-4,产率为32.3%。IR(KBr,v):2928,2851,2349,1754,1590,1495,1463,1385,1275,1261,1238,1196,1019,873,801,764,750,697,600,509cm-1;1HNMR(CDCl3,ppm):7.35(s,1H),7.28(d,2H,J=8.79Hz),7.18(s,1H),6.99(t,1H,J=7.26Hz),6.89(d,2H,J=7.92Hz),6.24(s,1H),4.89(s,1H),4.62(s,2H),,4.59(s,1H),4.49(d,1H,J=11.6Hz),4.18(d,1H,J=11.6Hz),3.28(m,1H),2.42-2.25(m,3H),1.91-1.36(m,11H),1.12(s,3H),0.0.66(s,3H);ESI-MS:m/z475.2.[M+Na]+.
9.化合物I-1(50mg,0.157mmol)投入反应瓶,加入二氯甲烷5mL,加入对硝基苯甲酸(105mg, 0.628mmol),加入催化量的4-二甲氨基吡啶,加入1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(145mg,0.756mmol),常温反应10h,反应液中加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,饱和食盐水干燥,柱层析得34mg无色液体化合物I-5,产率为35.2%。IR(KBr,v):2922,2851,2360,1721,1591,1528,1463,1276,1262,1102,1017,764,750cm-1;1H NMR(CDCl3,ppm):8.23-8.07(m,8H),7.35(s,1H),7.18(s,1H),6.24(s,1H),4.95(s,1H),4.88(d,1H,J=11.6Hz),4.65(s,1H),4.50(d,1H,J=11.6Hz),3.99(m,1H),2.65-2.25(m,3H),1.91-1.36(m,11H),1.22(s,3H),0.73(s,3H);ESI-MS:m/z639.2.[M+Na]+.
10.化合物I-1(50mg,0.157mmol)投入反应瓶,加入二氯甲烷5mL,加入对硝基苯甲酸(105mg,0.628mmol),加入催化量的4-二甲氨基吡啶,加入1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(145mg,0.756mmol),常温反应10h,反应液中加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,饱和食盐水干燥,柱层析得17mg白色固体化合物I-6,产率为23.4%。m.p.250-254℃.IR(KBr,v):3132,1720,1655,1530,1273,1122,722,545cm-1;1HNMR(CDCl3,ppm):8.28(d,2H,J=8.79Hz),8.16(d,2H,J=8.79Hz),7.36(s,1H),7.19(s,1H),6.26(s,1H),4.91(s,1H),4.68(d,1H,J=11.7Hz),4.65(s,1H),4.35(d,1H,J=11.7Hz),3.39(m,1H),2.60-2.22(m,3H),2.01-1.49(m,10H),1.26(s,3H),0.73(s,3H);ESI-MS:m/z490.2[M+Na]+.
11.化合物I-1(50mg,0.157mmol)投入反应瓶,加入二氯甲烷5mL,加入对甲氧苯基(96mg,0.628mmol),加入催化量的4-二甲氨基吡啶,加入1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(145mg,0.756mmol),常温反应10h,反应液中加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,饱和食盐水干燥,柱层析得23.8mg白色固体化合物I-7,产率为33.6%。m.p.218-221℃.IR(KBr,v):3185,3110,2365,1789,1686,1605,1578,1544,1512,1400,1306,1263,1169,1106,1027,1002,845,773,696,616,548,505cm-1;1HNMR(CDCl3,ppm):7.95(d,2H,J=8.73Hz),7.35(s,1H),7.20(s,1H),6.91(d,2H,J=8.88Hz),6.26(s,1H),4.90(s,1H),4.60(s,1H),4.56(d,1H,J=11.7Hz),4.28(d,1H,J=11.7Hz),3.85(s,3H),3.38-3.32(m,1H),2.47-2.27(m,3H),1.96-1.49(m,11H),1.29(s,3H),0.73(s,3H);ESI-MS:m/z475.2[M+Na]+.
实例2:I-8的合成
1.化合物I-1(2.5g,7.85mmol)投入反应瓶,加入50mL二氯甲烷溶解,加入催化量的4-二甲氨基吡啶,加入乙酸酐(4.4ml,23.55mmol),常温反应5h,反应液中加入水,二氯甲烷萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得3.1g无色液体化合物5,产率98.1%。IR(KBr,v):2948,2853,1736,1644,1445,1374,1239,1027,988,874,780cm-1;1H NMR(CDCl3,ppm):7.35(s,1H),7.18(s,1H),6.24(s,1H),4.89(s,1H),4.60(s,1H),4.58-4.55(m,1H),4.38(d,1H,J=11.7Hz),4.09(d,1H,J=11.7Hz),2.58-2.22(m,3H),2.05(s,6H),1.96-1.22(m,11H),1.01(s,3H),0.72(s,3H);ESI-MS:m/z425.2[M+Na]+.
2.化合物5(570mg,1.42mmol)投入反应瓶,加入催化量的四丁基溴化铵,用10mL苯溶解,加入用20mL水溶解的七水硫酸镁(75mg,0.304mmol),加入用水溶解的高锰酸钾(1.35g,8.52mmol),控制温度在50-60℃,反应12h,反应液中加入水,二氯甲烷萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,柱层析得120mg无色液体化合物6,产率21%。IR(KBr,v):2948,2853,1736,1644,1445,1374,1239,1027,988,874,780cm-1;1H NMR(CDCl3,ppm):7.35(s,1H),7.18(s,1H),6.24(s,1H),4.58-4.55(m,1H),4.38(d,1H,J=11.7Hz),4.09(d,1H,J=11.7Hz),2.58-2.22(m,3H),2.05(s,6H),1.96-1.22(m,11H),1.01(s,3H),0.72(s,3H);ESI-MS:m/z427.2[M+Na]+.
3.化合物6(18mg,0.044mmol)投入反应瓶,2mL甲醇溶解,加入5%强氧化钾0.3mL,搅拌2h,加入大量饱和碳酸氢钠水溶液,二氯甲烷萃取,饱和碳酸氢钠水溶液和饱和食盐水各洗涤三遍,无水硫酸钠干燥,柱层析得12mg无色液体化合物I-8,产率84.2%。IR(KBr,v):3385,2925,2360,2342,1653,1591,1463,1386,1303,1261,1238,1112,1071,1018,697,669cm-1;1H NMR(CDCl3,ppm):7.35(s,1H),7.17(s,1H),6.25(s,1H),4.18(d,1H,J=11.2Hz),3.54-3.49(m,1H),3.31(d,1H,J=11.1Hz),2.69-2.49(m,4H),2.35-1.63(m,7H),1.30(s,3H),0.99-0.78(m,3H),0.68(s,3H);
ESI-MS:m/z319.2[M-H]-.
实例3:I-10和I-9合成
1.化合物5(1.92g,4.78mmol)投入反应瓶,加入50mL二氯甲烷,加入二氧化硒(0.32g,2.87mmol)与叔丁基过氧化氢(≥65%,1.4ml),反应12h,反应液中加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,饱和食盐水干燥,柱层析得1.45g无色液体化合物I-10,产率72.5%。IR(KBr,v):3444,2949,2873,1735,1643,1454,1375,1256,1036,901,873,764,749cm-1;1H NMR(CDCl3,ppm):7.33(s,1H),7.17(s,1H),6.23(s,1H),5.09(s,1H),4.71(s,1H),4.62-4.57(m,1H),4.38-4.32(m,2H),4.11-4.07(d,1H,J=11.8Hz),2.53-2.17(m,3H),2.02(s,6H),1.84-1.23(m,10H),0.99(s,3H),0.69(s,3H);ESI-MS:m/z441.2[M+Na]+.
2.化合物I-10(1.45g,3.46mmol)投入反应瓶,加入50ml甲醇,加入5%氢氧化钾16mL,搅拌3h,加入大量碳酸氢钠饱和溶液中和,乙酸乙酯萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,柱层析得1.14g无色液体化合物I-9,产率为98.5%。IR(KBr,v):3385,3074,2949, 2932,2876,1643,1501,1466,1444,1383,1167,1063,1036,1025,973,901,873,770cm-1;1HNMR(CDCl3,ppm):7.35(s,1H),7.19(s,1H),6.25(s,1H),5.09(s,1H),4.71(s,1H),4.39-4.37(m,1H),4.18(d,1H,J=11.1Hz),3.52-3.47(m,1H),3.28(d,1H,J=11.1Hz),2.57-1.47(m,12H),1.23(s,3H),0.62(s,3H);ESI-MS:m/z333.1[M-H]-.
实例4:I-12和I-13合成
1.化合物3(5g,11.95mmol)投入反应瓶,加入100mL乙醚,加入重氮甲烷乙醚溶液200mL,密封,常温搅拌7day,过滤,乙醚洗涤,得4g白色固体化合物7,产率72.7%。m.p.130-133℃.IR(KBr,v):2956,2842,1763,1728,1646,1451,1431,1376,1248,1176,1133,1074,1028,1011,988,904cm-1;1H NMR(CDCl3,ppm):4.90(d,1H,J=7.6Hz),4.85-4.79(m,2H),4.60-4.58(br,2H),4.48(t,1H,J=9.2Hz),4.35(d,1H,J=11.8Hz),4.08(d,1H,J=11.8Hz),3.83-3.78(m,1H),2.43-2.39(m,1H),2.04(s,6H),1.96-1.22(m,13H),1.01(s,3H),0.68(s,3H);ESI-MS:rn/z478.2[M+NH4]+.
2.化合物7(4g,8.68mmol)投入反应瓶,50mLN,N-二甲基甲酰胺溶解,加热回流,搅拌5h,冷却至室温,加入大量水,乙酸乙酯萃取,饱和食盐水洗涤三遍,无水硫酸钠干燥,柱层析得3.7g白色固体化合物8,产率为98.7%。m.p.116-124℃.IR(KBr,v):3452,2956,2931,2853,1755,1739,1725,1676,1645,1441,1397,1378,1254,1239,1085,1063,1038,982,906cm-1;1H NMR(CDCl3,ppm):4.93(s,1H),4.72(s,1H),4.63(s,2H),4.61-4.56(m,1H),4.36(d,1H,J=11.7Hz),4.09(d,1H,J=11.8Hz),2.46-2.07(m,2H),2.03(s,6H),1.99(s,3H),1.96-1.22(m,10H),1.01(s,3H),0.69(s,3H);ESI-MS:m/z431.2[M+H]-.
3.白色固体化合物9(合成方法与化合物4相同),产率87.3%。IR(KBr,v):3262,2939,2849,1743,1677,1643,1441,1388,1325,1157,1087,1065,1039,904,782,597cm-1;1H NMR(CDCl3,ppm):4.91(s,1H),4.67(s,1H),4.63(s,2H),4.16(d,1H,J=11.2Hz),3.44(t,1H,J=8.1Hz),3.28(d,1H,J=11.1Hz),3.16(s,2H),2.44-2.04(m,3H),1.98(s,3H),1.93-1.24(m,9H),1.22(s,3H),1.18-1.01(m,2H),0.61(s,3H);ESI-MS:m/z697.2[2M+H]+.
4.白色固体化合物I-12(合成方法同化合物I-1),产率80.9%。m.p.130-134℃.IR(KBr,v):3363,3068,2966,2944,2862,2839,1641,1543,1460,1424,1387,1305,1285,1201,1143,1077,1037,1019,887,874,799,765,750cm-1;1H NMR(CDCl3,ppm):7.14(s,1H),7.12(s,1H),4.88(s,1H),4.59(s,1H),4.17(d,1H,J=11.1Hz),3.47-3.42(m,1H),3.31(d,1H,J=11.1Hz),2.67(br,2H),2.53-1.99(m,4H),1.94(s,3H),1.90-1.25(m,8H),1.23(s,3H),1.19-1.08(m,2H),0.64(s,3H);ESI-MS:m/z332.1[M-H]-.
5.无色液体化合物10(合成方法同化合物5),产率为99.8%。IR(KBr,v):2947,2853,1737,1637,1450,1374,1240,1134,1044,889,874,792,751cm-1;1H NMR(CDCl3,ppm):7.14(s,1H),7.12(s,1H),4.89(s,1H),4.62(s,1H),4.59-4.55(m,1H),4.37(d,1H,3=11.8Hz),4.09(d,1H,J=11.7Hz),2.49-2.10(m,3H),2.03(s,6H),1.93(s,3H),1.90-1.18(m,11H),1.01(s,3H),0.70(s,3H);ESI-MS:m/z417.2[M+H]-.
6.无色液体化合物11(合成方法同化合物I-10),产率为72.5%。IR(KBr,v):3485,3079,2948,2876,1732,1650,1452,1375,1247,1162,1131,1078,1037,947,906,835,736,701cm-1;1HNMR(CDCl3,ppm):7.15(s,1H),5,13(s,1H),4.80(s,2H),4.77(s,1H),4.65-4.59(m,1H),4.39-4.34(m,2H),4.10(d,1H,J=11.7Hz),2.45-2.17(m,3H),2.04(s,6H),1.98-1.24(m,11H),1.02(s,3H),0.71(s,3H);ESI-MS:m/z457.1[M+Na]+.
7.白色固体化合物I-13(合成方法同化合物I-9),产率为91.6%。m.p.96-100℃.IR(KBr,v):3250,3073,2943,2871,1745,1666,1648,1443,1384,1359,1336,1211,1155,1075,1055,1029,946,918,854cm-1;1H NMR(DMSO-d6,ppm):7.45(s,1H),4.95(s,1H),4.81(s,2H),4.62-4.60(m,2H),4.20-4.08(m,2H),3.85-3.80(m,1H),3.24-3.18(m,3H),2.30-1.98(m,4H),1.76-1.46(m,6H),1.15-1.09(m,2H),1.03(s,3H),0.57(s,3H);ESI-MS:m/z349.1[M-H]-.
实例5:I-14、I-15的合成
1.将穿心莲内酯(20g,57mmol)投入反应瓶,加入甲苯跟二甲亚砜的混合溶液(240mL,7∶3),加入催化量的对甲苯磺酸,加入2,2-二甲氧基丙烷(21.3mL,171mmol),加热回流,反应液加热回流反应3h,冷却至室温,加入乙酸乙酯稀释,加入大量水,乙酸乙酯萃取三遍,再分别用水和饱和食盐水洗涤三次,无水硫酸钠干燥,浓缩后乙醚洗涤数遍得21.2g白色固体化合物12,产率95%。m.p.191-192℃;IR(KBr)3482,2939,1746,1223,1066,901,860cm-1;1H NMR(CDCl3,ppm):6.97(1H,td,J=6.9,1.4Hz,H-12),5.05(1H,d,J=5.7Hz,H-14),4.91(1H,s,H-17a),4.62(1H,s,H-17b),4.46(1H,dd,J=10.4,5.9Hz,H-15a),4.27(1H,dd,J=10.4,1.9Hz,H-15b),3.97(1H,d,J=11.6Hz,H-19a),3.52(1H,s,H-3),3.18(1H,d,J=11.6Hz,H-19b),2.57(2H,t,J=6.8Hz,H-11),1.42(3H,s,CH3),1.37(3H,s,CH3),1.20(3H,s,H-18),0.97(3H,s,H-20);EIMS m/z:390[M+].
2.将化合物12(9.1g,23.3mmol)投入反应瓶,150mL二氯甲烷溶解,加入重铬酸吡啶嗡盐(17.6g,28mmol),搅拌5h,浓缩,加入大量乙酸乙酯,反复过滤,滤液浓缩,柱层析得7.28g白色固体化合物13,产率80%。1H NMR(CDCl3,ppm):7.29(s,1H),4.91(s,1H),4.83(s,1H), 4.75(s,1H),4.55-4.50(m,1H),3.94(d,1H,J=11.7Hz),3.48-3.43(m,1H),3.14(d,1H,J=11.7Hz),2.76(s,1H),2.43-2.16(m,2H),2.05-1.59(m,8H),1.40(s,3H),1.35(s,3H),1.30-1.21(m,2H),1.18(s,3H),0.89(s,3H);ESI-MS:m/z413.2[M+Na]+.
3.将化合物13(5g,12.8mmol)投入反应瓶,加入醋酸水溶液(50ml,7∶3)搅拌,搅拌3h,在反应液中加入大量的饱和碳酸氢钠水溶液,乙酸乙酯萃取三遍,再分别用饱和碳酸氢钠水溶液和饱和食盐水萃取三遍,无水硫酸钠干燥,过柱纯化得4g白色固体化合物14,产率90%。mp:136-140℃;IR(Neat):3351,2937,1746,1448,1034cm-1;1H NMR(CDCl3,ppm):δ7.28(1H,brd,J=1.0Hz,H-14),4.91(1H,brs,H-17b),4.83(2H,brs,H-15),4.73(1H,brs,H-17a),4.52(1H,brt,J07.0Hz,H-12),4.15(1H,d,J=11.0Hz,H-19b),3.45(1H,dd,J=10.0,6.0Hz,H-3),3.29(1H,d,J=11.0Hz,H-19a),2.66(1H,brs,OH),2.42(1H,ddd,J=14.0,3.5,2.5Hz,H-7b),2.03(1H,ddd,J=14.0,9.0,1.5Hz),1.97-1.75(6H,m),1.56(1H,d,J011.0Hz),1.34-1.05(3H,m),1.22(3H,s,H-18),0.63(3H,s,H-20);ESI-MS:m/z487.2856[M+Na]+.
4.化合物14(2.8g,7.99mmol)投入反应瓶,加入100mL四氢呋喃,密封反应瓶,氮气保护,液氮降温至-78℃后,向反应液中缓慢滴加二异丁基氢化铝(16ml of solution 1.5M in toluene,23.97mmol),滴加完后保持低温搅拌3h,等温度上升到零度后,缓慢滴加醋酸水溶液(7∶3)20mL,搅拌1h,反应液中加入大量水,乙酸乙酯萃取,饱和碳酸氢钠水溶液和饱和食盐水各洗涤三次,无水硫酸钠干燥,经柱层析得0.8g白色固体化合物I-14,收率为30%。m.p.>300℃.IR(KBr,v):3630,3131,2926,2853,2361,1647,1400,1082,860,785,549cm-1;1H NMR(CDCl3,ppm):7.41(s,1H),7.34(s,1H),6.41(s,1H),4.90(s,1H),4.75(s,1H),4.71(m,1H),4.18(d,1H,J=11.2Hz),3.48-3.43(m,1H),3.31(d,1H,J=11.1Hz),2.49-2.04(m,3H),2.00-1.73(m,9H),1.20(s,3H),0.65(s,3H);ESI-MS:m/z357.1[M+Na]+.
5.无色液体化合物I-15(合成方法同I-2),产率77.1%。IR(KBr,v):2925,2852,2360,2341,1733,1591,1463,1385,1275,1261,1075,1261,1075,1018,764,750,699cm-1;1H NMR(CDCl3,ppm):7.41(s,1H),7.34(s,1H),6.41(s,1H),4.90(s,1H),4.75(s,1H),4.71(m,1H),4.18(d,1H,J=11.2Hz),3.48-3.43(m,1H),3.31(d,1H,J=11.1Hz),2.49-2.04(m,9H),2.00-1.73(m,9H),1.22(s,9H),1.20(s,3H),0.65(s,3H);ESI-MS:m/z525.3[M+Na]+.
实例6:I-17、I-16、I-18的合成
1.将化合物I-1(2.5g,7.85mmol)投入反应瓶中,加入50mL二氯甲烷,加入三苯基氯甲烷(2.6g,9.42mmol),加入0.82mLN,N-二异丙基乙胺,搅拌18h,加入大量水,二氯甲烷萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,柱层析得3.5g无色液体化合物17,产率80.5%。IR(KBr,v):3440,3056,3031,2932,2851,1643,1597,1491,1448,1384,1221,1153,1081,1045,1026,909,873,767,733,704cm-1;1H NMR(CDCl3,ppm):7.29-7.00(m,17H),6.06(s,1H),4.63(s,1H),4.34(s,1H),3.97-3.94(t,1H),3.21(d,1H,J=9.33Hz),3.06(br,1H),2.98(d,1H,J=9.27Hz),2.34-1.44(m,6H),1.39(s,3H),1.35-1.13(m,4H),1.01-0.80(m,4H),0.77-0.70(m,3H);ESI-MS:m/z583.2[M+Na]+.
2.将化合物17(3.5g,6.24mmol)投入反应瓶中,加入30mL二甲亚砜,加入重铬酸吡啶嗡盐(3.5g,9.36mmol),常温搅拌18h,反应液中加入大量水,乙酸乙酯萃取三遍,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得2.3g无色液体化合物18,产率65.5%。IR(KBr,v):3500,2930,2850,1731,1644,1595,1490,1448,1384,1275,11261,1048,1027,893,873,764,749,706cm-1;1HNMR(CDCl3,ppm):7.38-7.13(m,17H),6.18(s,1H),4.82(s,1H),4.54(s,1H),3.45(d,1H,J=8.97Hz),3.08(d,1H,J=8.97Hz),2.51-1.54(m,12H),1.37(s,3H),1.34-1.15(m,2H),0.41(s,3H);ESI-MS:m/z581.2[M+Na]+.
3.将化合物18(2g,3.58mmol)投入反应瓶中,加入30mL甲醇溶解,加入对甲苯磺酸,室温搅拌3h,加入大量水和饱和碳酸氢钠水溶液,乙酸乙酯萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,过柱纯化得1.1g无色液体化合物19,产率93.5%。IR(KBr,v):3417,2948,2856,1705,1643,1500,1450,1384,1168,1025,892,873,776cm-1;1H NMR(CDCl3,ppm):7.26(s,1H),7.19(s,1H),6.25(s,1H),4.94(s,1H),4.65(s,1H),3.92(d,1H,J=11.2Hz),3.44(s,1H,J=11.2Hz),2.59-1.91(m,6H),1.84-1.39(s,8H),1.24(s,3H),0.79(s,3H);ESI-MS:m/z317.1[M+H]+.
4.无色液体化合物I-17(合成方法同I-11),产率61.4%。IR(KBr,v):3362,2952,2858,1703,1643,1448,1385,1274,1261,1166,1063,1025,921,899,873,764,749cm-1;1H NMR(CDCl3,ppm):7.35(s,1H),7.19(s,1H),6.24(s,1H),4.91(s,1H),4.62(s,1H),4.35(br,2H),3.82(d,1H,J=10.9Hz),3.38(d,1H,J=10.9Hz),2.97-2.22(m,5H),2.09-1.38(m,9H),1.33(s,3H),0.35(s,3H); ESI-MS:m/z333.2[M+H]+355.2[M+Na]+.
5.化合物19(200mg,0.63mmol)投入反应瓶,加入8mL吡啶,加入盐酸羟胺(52mg,0.76mmol),室温搅拌3h,加入20mL10%盐酸,乙酸乙酯萃取,饱和食盐水洗涤三次,无水硫酸钠干燥,柱层析得191mg无色液体化合物I-18,产率91.5%。IR(KBr,v):3344,2948,2853,1704,1644,1446,1384,1275,1260,1025,945,873,764,749cm-1;1H NMR(CDCl3,ppm):7.36(s,1H),7.21(s,1H),6.26(s,1H),5.15(s,1H),4.77(s,1H),4.42(s,1H),4.12(d,1H,J=7.5Hz),3.45(d,1H,J=11.2Hz),2.60-1.89(m,10H),1.84-1.61(m,4H),1.23(s,3H),0.77(s,3H);ESI-MS:m/z332.2[M+Na]+.
6.无色液体化合物15(制备方法同化合物17),产率81.5%.IR(KBr,v):3506,2931,2867,1738,1643,1597,1490,1448,1384,1275,1260,1139,1081,1047,896,764,749,706cm-1;1H NMR(CDCl3,ppm):7.32-6.94(m,17H),4.64(s,1H),4.36(s,1H),3.98(t,1H,J=8.4Hz),3.21(d,1H,J=9.3Hz),3.08(br,1H),2.99(d,1H,J=9.3Hz),2.32-1.97(m,3H),1.76(s,3H),1.66-1.51(m,3H),1.41(s,3H),1.38-0.87(m,8H),0.85-0.74(m,3H)592.2;ESI-MS:m/z592.2[M+Na]+.
7.无色液体化合物16(制备方法同化合物18,产率64.5%.IR(KBr,v):3058,2948,2854,1713,1643,1596,1490,1448,1384,1275,1261,1221,1067,1047,898,872,764,749,706cm-1;1H NMR(CDCl3,ppm):7.35-7.06(m,17H),4.82(s,1H),4.55(s,1H),3.45(d,1H,J=8.9Hz),3.08(d,1H,J=8.9Hz),2.47-2.04(m,5H),1.88(s,3H),1.84-1.41(m,6H),1.38(s,3H),1.34-0.79(m,3H),0.41(s,3H);ESI-MS:m/z595.0[M+Na]+.
8.无色液体化合物I-16(制备方法同化合物19),产率94.5%.IR(KBr,v):3417,2926,2852,1709,1644,1454,1384,1275,1260,1046,891,873,764,750cm-1;1H NMR(CDCl3,ppm):7.14(d,2H,J=5.7Hz),4.94(s,1H),4.66(s,1H),3.92(d,1H,J=11.6Hz),3.44(d,1H,J=11.1Hz),2.56-1.97(m,7H),1.94(s,3H),1.84-1.35(m,8H),1.22(s,3H),0.78(s,3H);ESI-MS:m/z331.2[M+H]+。
Claims (2)
1.具有下列结构通式为I的ent-半日花烷二萜衍生物及其药学上可接受的盐:
其中:
R1、R2、R6的结构可以表示为:H、OH、OR7、OCOR7、OCOR7R8、NR7R8、F、Cl、Br、I;其中,R7、R8表示氢、取代或非取代的直链、支链或环状的烃基、苯基、苄基, 其中m=1~8,呋喃或吡喃型五、六元糖基或取代糖基,或2~5个以1,2-、1,4-、1,6-方式连接的葡萄糖基或取代葡萄糖基;上述直链、支链或环状的烃基可进一步表述为:(1)C1~C10烷基;(2)C3~C6环烷基;(3)C3~C10烯基;(4)C3~C10炔基;
R1的结构还可以表示为:=O、=N-OH;
R3的结构表示为:H、OH;
R4的结构表示为:O、CH2;
R5的结构表示为:H、CH3。
2.具有通式为I结构的化合物作为治疗癌症的药物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201410062373.1A CN103804330A (zh) | 2014-02-25 | 2014-02-25 | ent-半日花烷二萜衍生物的制备及抗肿瘤用途 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201410062373.1A CN103804330A (zh) | 2014-02-25 | 2014-02-25 | ent-半日花烷二萜衍生物的制备及抗肿瘤用途 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN103804330A true CN103804330A (zh) | 2014-05-21 |
Family
ID=50701767
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201410062373.1A Pending CN103804330A (zh) | 2014-02-25 | 2014-02-25 | ent-半日花烷二萜衍生物的制备及抗肿瘤用途 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN103804330A (zh) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN104398502A (zh) * | 2014-11-24 | 2015-03-11 | 西宁意格知识产权咨询服务有限公司 | 半日花烷型二萜Leoleorin H在制备抗肿瘤药物中的应用 |
| CN105198893A (zh) * | 2015-10-09 | 2015-12-30 | 杭州启澄科技有限公司 | 一种用于治疗胃癌的二萜化合物 |
| CN106565641A (zh) * | 2016-11-14 | 2017-04-19 | 中国科学院昆明植物研究所 | 呋喃半日花烷二萜衍生物及其药物组合物和其在制药中的应用 |
| CN106831667A (zh) * | 2017-01-11 | 2017-06-13 | 中国科学院昆明植物研究所 | 8‐epi‐Hypophyllin E及其衍生物和其药物组合物与其在制药中的应用 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1326343A (zh) * | 1998-11-19 | 2001-12-12 | 白奥诺里卡股份公司 | 降促乳素药物 |
-
2014
- 2014-02-25 CN CN201410062373.1A patent/CN103804330A/zh active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1326343A (zh) * | 1998-11-19 | 2001-12-12 | 白奥诺里卡股份公司 | 降促乳素药物 |
Non-Patent Citations (1)
| Title |
|---|
| AKITA,H., ET AL.: "Alternative syntheses of versatile chiral intermediate for drimane sesquiterpenes and labdane diterpenes using (R,R)-cycloheptane-1,2-diol as a chiral auxiliary", 《TETRAHEDRON: ASYMMETRY》, vol. 15, 31 December 2004 (2004-12-31), pages 725 - 732, XP004488811, DOI: 10.1016/j.tetasy.2003.12.040 * |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN104398502A (zh) * | 2014-11-24 | 2015-03-11 | 西宁意格知识产权咨询服务有限公司 | 半日花烷型二萜Leoleorin H在制备抗肿瘤药物中的应用 |
| CN105198893A (zh) * | 2015-10-09 | 2015-12-30 | 杭州启澄科技有限公司 | 一种用于治疗胃癌的二萜化合物 |
| CN106565641A (zh) * | 2016-11-14 | 2017-04-19 | 中国科学院昆明植物研究所 | 呋喃半日花烷二萜衍生物及其药物组合物和其在制药中的应用 |
| CN106565641B (zh) * | 2016-11-14 | 2019-04-02 | 中国科学院昆明植物研究所 | 呋喃半日花烷二萜衍生物及其药物组合物和其在制药中的应用 |
| CN106831667A (zh) * | 2017-01-11 | 2017-06-13 | 中国科学院昆明植物研究所 | 8‐epi‐Hypophyllin E及其衍生物和其药物组合物与其在制药中的应用 |
| CN106831667B (zh) * | 2017-01-11 | 2019-04-26 | 中国科学院昆明植物研究所 | 8‐epi‐Hypophyllin E及其衍生物和其药物组合物与其在制药中的应用 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Srinivas et al. | Ruthenium catalyzed synthesis of 2, 3-unsaturated C-glycosides from glycals | |
| Lin et al. | Cembrane diterpenoids from the Taiwanese soft coral Sinularia flexibilis | |
| CN105073710B (zh) | 新异羟肟酸衍生物或其盐 | |
| CN103804330A (zh) | ent-半日花烷二萜衍生物的制备及抗肿瘤用途 | |
| Srikanth et al. | Synthesis of dihydrosterculic acid-based monoglucosyl diacylglycerol and its analogues and their biological evaluation | |
| Ji et al. | Highly oxygenated triterpenoids from the marine red alga Laurencia mariannensis (Rhodomelaceae) | |
| Popsavin et al. | 2-Substituted thiazole-4-carboxamide derivatives as tiazofurin mimics: Synthesis and in vitro antitumour activity | |
| Tamburrini et al. | Facile access to pseudo-thio-1, 2-dimannoside, a new glycomimetic DC-SIGN antagonist | |
| Jana et al. | C-Triazolyl β-d-furanosides as LpxC inhibitors: stereoselective synthesis and biological evaluation | |
| CN106496183A (zh) | 咖啡酸酯连接的大环内酯衍生物及其制备方法 | |
| CN105111272A (zh) | 3-单糖醛酸氧苷齐墩果烷型和乌苏烷型三萜皂苷衍生物及其制备方法和应用 | |
| Sun et al. | Synthesis of glycoglycerolipid of 1, 2-dipalmitoyl-3-(N-palmitoyl-6′-amino-6′-deoxy-α-d-glucosyl)-sn-glycerol and its analogues, inhibitors of human Myt1-kinase | |
| Slättegård et al. | Synthesis of fused bicyclic thioglycosides of N-acylated glucosamine as analogues of mycothiol | |
| Li et al. | Synthesis and Anti‐tumor Evaluation of Novel C‐37 Modified Derivatives of Gambogic Acid | |
| Kavitha et al. | Scalable synthesis of the unusual amino acid segment (ADMOA unit) of marine anti-inflammatory peptide: solomonamide A | |
| CN105461681A (zh) | 具有抗肿瘤活性的krn7000类似物及合成方法 | |
| CN103275169A (zh) | 呋甾皂苷及其合成方法 | |
| Kitamura et al. | Preparation of L-vancosamine-related glycosyl donors | |
| Cai et al. | Synthesis of aminodisaccharide–nucleoside conjugates for RNA binding | |
| Yashunsky et al. | Synthesis and biological evaluation of cyanogenic glycosides | |
| Bauer et al. | Impact of stereochemistry on the biological activity of novel oleandomycin derivatives | |
| Sharma et al. | Synthesis of new chiral 18-crown-6 ethers from D-xylose | |
| KR101975916B1 (ko) | 삼환계 유사체, 이의 제조방법과 용도 | |
| Aoyagi et al. | Synthesis of 1-O-monoacyl or 12-O-monoacyl, 1-, 12-O-diacyl-, and 11, 12-dehydrated excisanin A 7, 14-acetonides and their cytotoxic activity | |
| Airoldi et al. | Synthesis of 3-Deoxy-d-threo pentofuranose 5-Phosphate, a Substrate of Arabinose 5-Phosphate Isomerase |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20140521 |