CN112624924A - Ca基固体碱非均相催化剂在制备碳酸二甲酯中的应用 - Google Patents
Ca基固体碱非均相催化剂在制备碳酸二甲酯中的应用 Download PDFInfo
- Publication number
- CN112624924A CN112624924A CN202011536779.0A CN202011536779A CN112624924A CN 112624924 A CN112624924 A CN 112624924A CN 202011536779 A CN202011536779 A CN 202011536779A CN 112624924 A CN112624924 A CN 112624924A
- Authority
- CN
- China
- Prior art keywords
- catalyst
- application according
- carbonate
- dimethyl carbonate
- salt
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C68/00—Preparation of esters of carbonic or haloformic acids
- C07C68/06—Preparation of esters of carbonic or haloformic acids from organic carbonates
- C07C68/065—Preparation of esters of carbonic or haloformic acids from organic carbonates from alkylene carbonates
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/002—Mixed oxides other than spinels, e.g. perovskite
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/70—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper
- B01J23/76—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36
- B01J23/78—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36 with alkali- or alkaline earth metals
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/02—Impregnation, coating or precipitation
- B01J37/03—Precipitation; Co-precipitation
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/02—Impregnation, coating or precipitation
- B01J37/03—Precipitation; Co-precipitation
- B01J37/036—Precipitation; Co-precipitation to form a gel or a cogel
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/08—Heat treatment
- B01J37/082—Decomposition and pyrolysis
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Physics & Mathematics (AREA)
- Thermal Sciences (AREA)
- Dispersion Chemistry (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
本发明提供了一种Ca基固体碱非均相催化剂在制备碳酸二甲酯中的应用,所述Ca基固体碱非均相催化剂为Ca3Co4O9催化剂,用于环状碳酸酯与甲醇酯交换制备碳酸二甲酯反应中。本发明的Ca基固体碱非均相催化剂Ca3Co4O9具有耐高温、抗氧化、热稳定性好和化学稳定性高等优点,能够有效抑制Ca活性组分的流失,并且在常压、低温反应条件下实现较高的碳酸二甲酯收率,除此之外,该催化剂制备方法简单,重复使用性能稳定,易于工业化放大。
Description
技术领域
本发明涉及催化剂领域,具体涉及一种Ca基固体碱非均相催化剂在制备碳酸二甲酯中的应用。
背景技术
碳酸二甲酯(简称DMC)是一种新型的、低污染、环境友好型基础化工原料,应用范围广、市场容量大、绿色低毒、附加值高。可有效促进绿色溶剂、非光气聚碳、非光气聚氨酯、新能源锂电、绿色药物合成等行业的发展。近年来,美国提出用DMC逐步替代MTBE作为汽油添加剂,提高辛烷值,更引起了世界各国学者对DMC的关注。
目前国内酯交换法生产DMC的工艺大多以甲醇钠或甲醇钾为催化剂,如专利CN101774888A和CN1569807A均以甲醇和碳酸丙烯酯为原料,使用甲醇钠作为均相催化剂,获得较高收率的DMC产品。然而,均相催化剂甲醇钠或甲醇钾对水敏感,并且反应之后甲醇钠变成氢氧化钠,不能循环使用。为从产物中分离出氢氧化钠,目前在含有氢氧化钠的混合产物中通入CO2和水使氢氧化钠转化成碳酸钠结晶予以除去,分离路线增长、加之大量甲醇钠的使用导致DMC的生产成本增加。
为克服现有均相催化剂分离、回收困难的问题,非均相固体碱催化剂受到了广大科研工作者和企业的青睐。对此,Amberlyst 39 Wet离子交换树脂催化剂(AppliedCatalysis B: Environmental: 2012, 125: 486-491);MgO-CeO2复合金属氧化物催化剂(Catalysis Letters: 2007, 118: 30-35);Na/ZrO2负载型催化剂(Microporous andMesoporous Materials: 2007, 102: 304-309)等非均相催化剂虽然能够取得较好的碳酸二甲酯收率,但是反应温度较高,普遍都在130~170 ℃之间,并且负载型碱金属催化剂或者离子交换树脂催化剂仍存在活性组分流失的难题。为此,具有低温、高活性的Ca基金属氧化物催化剂一度成为热点。专利CN105879892B采用类水滑石结构固定活性组分Ca的策略,合成的Ca-Al-O-X(X=CO3 2-、NO3 -、F-、Cl-或Br-)催化剂,在常压、反应温度30-70 ℃、反应时间0.5-2 h的条件下,DMC收率30.7~58.4%。虽然该催化剂能在低温下合成DMC,但是经过5次重复使用,碳酸二甲酯收率从55.7%下降到47.2%,催化剂活性组分Ca仍然存在流失现象,并且该催化剂制备过程复杂、类水滑石结构的准确控制比较困难。
总体来说,现有非均相固体碱催化剂一般需要较高的反应温度,高温又容易导致副产物的生成,同时高温还容易使得多元醇聚合。因此,如何设计和调整催化剂结构,获得具有低温、高活性的新型Ca基固体碱催化剂显得尤为紧迫。
发明内容
本发明提出了一种Ca基固体碱非均相催化剂在制备碳酸二甲酯中的应用,借助钴钙复合金属氧化物特殊的失配层钴酸盐结构Ca3Co4O9,旨在高效固定活性组分Ca,从而提供一种用于甲醇酯交换制备DMC的低温、高活性、绿色环保的高性能非均相固体碱催化剂。
实现本发明的技术方案是:
Ca基固体碱非均相催化剂在制备碳酸二甲酯中的应用,所述Ca基固体碱非均相催化剂为Ca3Co4O9催化剂,用于环状碳酸酯与甲醇酯交换制备碳酸二甲酯反应中。
将甲醇与环状碳酸酯混合,加入Ca3Co4O9催化剂,在10~70 ℃温度下反应10~120min,反应压力为常压。
优选地,环状碳酸酯可以是碳酸乙烯酯或者碳酸丙烯酯。
所述甲醇与环状碳酸酯的摩尔比为(2~12):1混合,催化剂用量为环状碳酸酯质量的0.5~2.5wt%。
所述Ca3Co4O9催化剂通过溶胶凝胶法、共沉淀法或者直接焙烧法制备得到。
所述溶胶凝胶法具体如下:
(1)将Ca盐、Co盐、柠檬酸和去离子水共同转移至三口烧瓶中,80 ℃在磁力搅拌下回流6 h,然后升温至105 ℃,并加入乙二醇分散剂,继续回流搅拌6 h,得到凝胶;
(2)将步骤(1)得到的凝胶置于鼓风干燥箱中干燥,研磨成细粉后在马弗炉中煅烧,得Ca3Co4O9催化剂。
所述步骤(1)中柠檬酸与Ca和Co的总摩尔比为(1~1.5):1,去离子水和柠檬酸的摩尔比为(30~50):1,分散剂乙二醇与柠檬酸的质量比为(0.3~1):1。
所述共沉淀法具体如下:
(1)将Ca盐、Co盐溶解于去离子水中,并在40℃磁力搅拌使其充分混合,得到混合溶液A;
(2)将氢氧化钠和碳酸钠溶解于去离子水中形成沉淀剂B;
(3)搅拌过程中保持pH=8~10将沉淀剂B滴加入混合溶液A,滴加完成后40℃静置2~6 h,过滤、洗涤后于鼓风干燥箱中干燥,最后在马弗炉中煅烧,得到Ca3Co4O9催化剂。
所述步骤(1)中混合溶液A的浓度为0.2~2 mol/L;步骤(2)中氢氧化钠和碳酸钠的摩尔比为1:1。
所述直接焙烧法步骤如下:将Ca盐、Co盐前驱体机械研磨使其均匀混合,然后于干燥箱中100~120 ℃干燥4~12 h,最后在马弗炉中煅烧,得到Ca3Co4O9催化剂。
所述Ca与Co的摩尔比为3:4,马弗炉中煅烧温度为600~1000 ℃,煅烧4h,升温速率2~10 ℃/min。
本发明的有益效果是:本发明的Ca基固体碱非均相催化剂Ca3Co4O9具有耐高温、抗氧化、热稳定性好和化学稳定性高等优点,能够有效抑制Ca活性组分的流失,并且在常压、低温反应条件下实现较高的碳酸二甲酯收率,除此之外,该催化剂制备方法简单,重复使用性能稳定,易于工业化放大。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
图1为失配层钴酸盐结构Ca3Co4O9催化剂扫描电子显微镜(SEM)图谱。
图2为失配层钴酸盐结构Ca3Co4O9催化剂高倍透射电镜(HR-TEM)图谱。
具体实施方式
下面将结合本发明实施例,对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有付出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1
采用溶胶凝胶法制备催化剂,称取10.12g的Ca(NO3)2·4H2O、16.63g的Co (NO3)2·6H2O盐,柠檬酸19.21g,去离子水54mL,共同转移至250mL三口烧瓶中,80 ℃在磁力搅拌下回流6 h,然后升温至105 ℃,并加入分散剂乙二醇5.76g,继续回流搅拌6 h。然后将形成的凝胶置于鼓风干燥箱中110 ℃干燥12 h,研磨成细粉后在马弗炉中800 ℃煅烧4 h,升温速率2 ℃ /min,由此获得Ca3Co4O9催化剂。
取催化剂0.20g加入釜式反应器中,加入6.40g甲醇和2.55g碳酸丙烯酯原料,60℃搅拌下反应2h,待产物冷却后用气相色谱进行分析,碳酸丙烯酯转化率为57.5%,碳酸二甲酯收率为53.9%。
实施例2
采用溶胶凝胶法制备催化剂,称取10.12g的Ca(NO3)2·4H2O、16.63g的Co (NO3)2·6H2O盐,柠檬酸28.82g,去离子水90mL,共同转移至250mL三口烧瓶中,80 ℃在磁力搅拌下回流6 h,然后升温至105 ℃,并加入分散剂乙二醇8.64g,继续回流搅拌6 h。然后将形成的凝胶置于鼓风干燥箱中110 ℃干燥12 h,研磨成细粉后在马弗炉中800 ℃煅烧4 h,升温速率2 ℃ /min,由此获得Ca3Co4O9催化剂。
取催化剂0.20g加入釜式反应器中,加入6.40g甲醇和2.55g碳酸丙烯酯原料,60℃搅拌下反应2h,待产物冷却后用气相色谱进行分析,碳酸丙烯酯转化率为55.5%,碳酸二甲酯收率为52.7%。
实施例3
采用溶胶凝胶法制备催化剂,称取10.12g的Ca(NO3)2·4H2O、16.63g的Co (NO3)2·6H2O盐,柠檬酸24.01g,去离子水90mL,共同转移至250mL三口烧瓶中,80 ℃在磁力搅拌下回流6 h,然后升温至105 ℃,并加入分散剂乙二醇9.0g,继续回流搅拌6 h。然后将形成的凝胶置于鼓风干燥箱中110 ℃干燥12 h,研磨成细粉后在马弗炉中800 ℃煅烧4 h,升温速率2 ℃ /min,由此获得Ca3Co4O9催化剂。
取催化剂0.20g加入釜式反应器中,加入6.40g甲醇和2.55g碳酸丙烯酯原料,60℃搅拌下反应2h,待产物冷却后用气相色谱进行分析,碳酸丙烯酯转化率为71.2%,碳酸二甲酯收率为70.3%。
实施例4
催化剂制备方法和评价条件与实施例3存在如下区别:催化剂评价在30 ℃搅拌下反应2h,碳酸丙烯酯转化率为70.2%,碳酸二甲酯收率为69.5%。
实施例5
催化剂制备方法和评价条件与实施例3存在如下区别:催化剂评价在60 ℃搅拌下反应10min,碳酸丙烯酯转化率为20.5%,碳酸二甲酯收率为18.4%。
实施例6
催化剂制备方法和评价条件与实施例3存在如下区别:催化剂评价在10 ℃搅拌下反应2h,碳酸丙烯酯转化率为25.4%,碳酸二甲酯收率为24.8%。
实施例7
催化剂制备方法和评价条件与实施例3存在如下区别:加入6.40g甲醇和1.7g碳酸丙烯酯原料,碳酸丙烯酯转化率为69.8%,碳酸二甲酯收率为68.7%。
实施例8
催化剂制备方法和评价条件与实施例3存在如下区别:加入6.40g甲醇和10.20g碳酸丙烯酯原料,碳酸丙烯酯转化率为49.4%,碳酸二甲酯收率为48.2%。
实施例9
采用共沉淀法制备催化剂,称取9.38g的CaCl2·6H2O、13.59g的C℃l2·6H2O盐溶解于100 ml去离子水中,并在40 ℃磁力搅拌使其充分混合形成混合溶液A。然后5.6g的氢氧化钠和14.84g的碳酸钠,溶解于50 ml去离子水中形成沉淀剂B;在搅拌过程中保持pH=9将B溶液滴加入溶液A,滴加完成后40 ℃静置4 h,过滤、洗涤后于鼓风干燥箱120 ℃干燥12h,最后在马弗炉中800 ℃煅烧4 h,升温速率2 ℃ /min。即得Ca3Co4O9催化剂。
取催化剂0.20g加入釜式反应器中,加入6.40g甲醇和2.55g碳酸丙烯酯原料,60℃搅拌下反应2h,待产物冷却后用气相色谱进行分析,碳酸丙烯酯转化率为67.2%,碳酸二甲酯收率为65.4%。
实施例10
采用直接焙烧法制备催化剂,称取7.55g的Ca(CH3COO)2、14.23g的Co(CH3COO)2·4H2O盐前驱体机械研磨使其均匀混合。然后直接于干燥箱中110 ℃干燥12 h,然后在马弗炉中800 ℃煅烧4 h,升温速率2 ℃/min,即得Ca3Co4O9催化剂。
取催化剂0.20g加入釜式反应器中,加入6.40g甲醇和2.55g碳酸丙烯酯原料,60℃搅拌下反应2h,待产物冷却后用气相色谱进行分析,碳酸丙烯酯转化率为58.8%,碳酸二甲酯收率为56.7%。
实施例11
催化剂制备方法和评价条件与实施例10存在如下区别:在马弗炉中600 ℃煅烧4h,碳酸丙烯酯转化率为55.1%,碳酸二甲酯收率为54.0%。
实施例12
催化剂制备方法和评价条件与实施例10存在如下区别:在马弗炉中1000 ℃煅烧4h,碳酸丙烯酯转化率为51.5%,碳酸二甲酯收率为50.4%。
实施例13
催化剂制备方法和评价条件与实施例10存在如下区别:催化剂评价在10 ℃搅拌下反应2h,碳酸丙烯酯转化率为21.2%,碳酸二甲酯收率为20.1%。
实施例14
催化剂制备方法和评价条件与实施例10存在如下区别:加入6.40g甲醇和2.20g碳酸乙烯酯原料,碳酸乙烯酯转化率为61.5%,碳酸二甲酯收率为59.8%。
实施例15
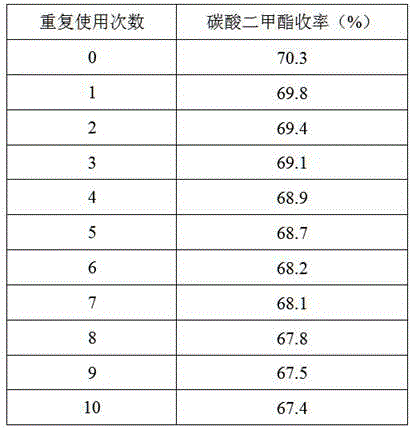
将实施例3中使用后的催化剂离心分离后重新加入进行上述反应,反应条件不变,如此重复10次,实验结果如下:
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
Claims (10)
1.Ca基固体碱非均相催化剂在制备碳酸二甲酯中的应用,其特征在于:所述Ca基固体碱非均相催化剂为Ca3Co4O9催化剂,用于环状碳酸酯与甲醇酯交换制备碳酸二甲酯反应中。
2.根据权利要求1所述的应用,其特征在于:将甲醇与环状碳酸酯混合,加入Ca3Co4O9催化剂,在10~70 ℃温度下反应10~120 min,反应压力为常压。
3.根据权利要求2所述的应用,其特征在于:所述甲醇与环状碳酸酯的摩尔比为(2~12):1混合,催化剂用量为环状碳酸酯质量的0.5~2.5wt%。
4.根据权利要求1-3任一项所述的应用,其特征在于:所述Ca3Co4O9催化剂通过溶胶凝胶法、共沉淀法或者直接焙烧法制备得到。
5.根据权利要求4所述的应用,其特征在于,所述溶胶凝胶法具体如下:
(1)将Ca盐、Co盐、柠檬酸和去离子水共同转移至三口烧瓶中,80 ℃在磁力搅拌下回流6 h,然后升温至105 ℃,并加入乙二醇分散剂,继续回流搅拌6 h,得到凝胶;
(2)将步骤(1)得到的凝胶置于鼓风干燥箱中干燥,研磨成细粉后在马弗炉中煅烧,得Ca3Co4O9催化剂。
6.根据权利要求5所述的应用,其特征在于:所述步骤(1)中柠檬酸与Ca和Co的总摩尔比为(1~1.5):1,去离子水和柠檬酸的摩尔比为(30~50):1,分散剂乙二醇与柠檬酸的质量比为(0.3~1):1。
7.根据权利要求4所述的应用,其特征在于,所述共沉淀法具体如下:
(1)将Ca盐、Co盐溶解于去离子水中,并在40℃磁力搅拌使其充分混合,得到混合溶液A;
(2)将氢氧化钠和碳酸钠溶解于去离子水中形成沉淀剂B;
(3)搅拌过程中保持pH=8~10将沉淀剂B滴加入混合溶液A,滴加完成后40℃静置2~6 h,过滤、洗涤后于鼓风干燥箱中干燥,最后在马弗炉中煅烧,得到Ca3Co4O9催化剂。
8.根据权利要求7所述的的应用,其特征在于:所述步骤(1)中混合溶液A的浓度为0.2~2 mol/L;步骤(2)中氢氧化钠和碳酸钠的摩尔比为1:1。
9.根据权利要求4所述的应用,其特征在于,所述直接焙烧法步骤如下:将Ca盐、Co盐前驱体机械研磨使其均匀混合,然后于干燥箱中100~120 ℃干燥4~12 h,最后在马弗炉中煅烧,得到Ca3Co4O9催化剂。
10.根据权利要求5-9任一项所述的应用,其特征在于:所述Ca与Co的摩尔比为3:4,马弗炉中煅烧温度为600~1000 ℃,煅烧4h,升温速率2~10 ℃/min。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202011536779.0A CN112624924B (zh) | 2020-12-23 | 2020-12-23 | Ca基固体碱非均相催化剂在制备碳酸二甲酯中的应用 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202011536779.0A CN112624924B (zh) | 2020-12-23 | 2020-12-23 | Ca基固体碱非均相催化剂在制备碳酸二甲酯中的应用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN112624924A true CN112624924A (zh) | 2021-04-09 |
| CN112624924B CN112624924B (zh) | 2022-01-21 |
Family
ID=75321477
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202011536779.0A Active CN112624924B (zh) | 2020-12-23 | 2020-12-23 | Ca基固体碱非均相催化剂在制备碳酸二甲酯中的应用 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN112624924B (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN113429291A (zh) * | 2021-06-29 | 2021-09-24 | 山东海科创新研究院有限公司 | 非均相催化剂CaO/Al2O3@XaSiOb在合成碳酸二甲酯过程中的应用 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0478073A2 (en) * | 1990-09-20 | 1992-04-01 | Union Carbide Chemicals And Plastics Company, Inc. | Processes for the preparation of carboxylated compounds |
| CN1389430A (zh) * | 2002-06-21 | 2003-01-08 | 清华大学 | 一种钴酸钙基氧化物热电材料及其制备方法 |
| CN105879892A (zh) * | 2016-05-27 | 2016-08-24 | 中国科学院山西煤炭化学研究所 | 酯交换法合成碳酸二甲酯的固体碱催化剂及制法和应用 |
| US20180319734A1 (en) * | 2015-03-23 | 2018-11-08 | Council Of Scientific & Industrial Research | A process for the synthesis of dialkyl carbonates |
-
2020
- 2020-12-23 CN CN202011536779.0A patent/CN112624924B/zh active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0478073A2 (en) * | 1990-09-20 | 1992-04-01 | Union Carbide Chemicals And Plastics Company, Inc. | Processes for the preparation of carboxylated compounds |
| CN1389430A (zh) * | 2002-06-21 | 2003-01-08 | 清华大学 | 一种钴酸钙基氧化物热电材料及其制备方法 |
| US20180319734A1 (en) * | 2015-03-23 | 2018-11-08 | Council Of Scientific & Industrial Research | A process for the synthesis of dialkyl carbonates |
| CN105879892A (zh) * | 2016-05-27 | 2016-08-24 | 中国科学院山西煤炭化学研究所 | 酯交换法合成碳酸二甲酯的固体碱催化剂及制法和应用 |
Non-Patent Citations (5)
| Title |
|---|
| 《化工百科全书》编辑委员会: "《化工百科全书 第16卷 天然药物-无机过氧化物和过氧化和物 tian-wu》", 31 December 1997, 化学工业出版社 * |
| CHEE SHAN LIM ET AL.: "Alternating Misfit Layered Transition/Alkaline Earth Metal Chalcogenide Ca3Co4O9 as a New Class of Chalcogenide Materials for Hydrogen Evolution", 《CHEMISTRY OF MATERIALS》 * |
| SHAOJIE FENG ET AL.: "Effect of the preparation method on the catalytic performance of Ca3Co4O9 for methane oxidation", 《J SOL-GEL SCI TECHNOL》 * |
| YUNHUI LIAO ET AL.: "Solid base catalysts derived from Ca-Al-X (X = F-, Cl- and Br-) layered double hydroxides for methanolysis of propylene carbonate", 《RSC ADV.》 * |
| 张龙等: "《绿色化学(第二版)》", 31 August 2014, 华中科技大学出版社 * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN113429291A (zh) * | 2021-06-29 | 2021-09-24 | 山东海科创新研究院有限公司 | 非均相催化剂CaO/Al2O3@XaSiOb在合成碳酸二甲酯过程中的应用 |
| CN113429291B (zh) * | 2021-06-29 | 2022-06-24 | 山东海科创新研究院有限公司 | 非均相催化剂CaO/Al2O3@XaSiOb在合成碳酸二甲酯过程中的应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN112624924B (zh) | 2022-01-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN102544475B (zh) | 富锂锰酸锂固溶体正极材料的制备方法 | |
| CN112563484A (zh) | 一种钠离子电池正极材料及其制备方法、钠离子电池 | |
| WO2016180288A1 (zh) | 制备具有铝元素梯度分布的镍钴铝前驱材料和正极材料的方法 | |
| CN104425815B (zh) | 高密度球形镍钴铝酸锂材料及其前驱体的制备方法 | |
| CN109768272A (zh) | 一种富锂三元正极材料及其绿色制备方法 | |
| CN116764665B (zh) | 一种复合氮掺杂碳催化剂及其制备方法和应用 | |
| CN116713009B (zh) | 一种ZnCdS/NiO复合光催化剂的制备方法及其应用 | |
| CN106128801A (zh) | 一种超级电容器NiCo2O4基复合材料的制备方法 | |
| CN116135308B (zh) | 一种钴掺杂锰基型催化剂及其制备和应用 | |
| CN112624924B (zh) | Ca基固体碱非均相催化剂在制备碳酸二甲酯中的应用 | |
| CN116885129A (zh) | 双改性钠离子电池正极材料、其制备方法和应用 | |
| CN103296269A (zh) | 一种绿色可控的镍钴锰酸锂的制备工艺方法 | |
| CN106748782B (zh) | 一种镁铝镧复合氧化物催化合成碳酸甲乙酯的方法 | |
| CN118847219B (zh) | 一种多功能化MOFs材料的制备方法及其催化应用 | |
| CN114804213A (zh) | 一种化学链重整耦合水分解制氢超轻介孔载氧体制备方法 | |
| CN113398912A (zh) | 一种用于氨基甲酸甲酯醇解合成碳酸二甲酯的催化剂 | |
| CN113244940A (zh) | 用于合成碳酸二甲酯的固体碱催化剂及其制备方法和碳酸二甲酯的制备方法 | |
| CN117000266B (zh) | 一种空心多孔棒状Mn3O4-Co纳米材料的制备方法及其应用 | |
| CN115646497B (zh) | 一种生物柴油磁性双组分钙基固体碱催化剂及其制备方法和应用 | |
| CN114478250B (zh) | 一种碳酸甲乙酯联产碳酸二乙酯的制备方法 | |
| CN102259909B (zh) | 一种用于固体推进剂的碳酸铅燃烧催化剂的制备方法 | |
| CN101973537A (zh) | 一种过渡金属磷化物的制备方法 | |
| CN108620080A (zh) | 一种稀土元素掺杂的钙基磁性固体碱催化剂及其制备方法 | |
| CN101916852B (zh) | 一种负衰减系数锂离子电池正极材料钒酸锂的制备方法 | |
| CN110165175A (zh) | 一种高镍三元正极材料及其制备方法和应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |