-
TECHNISCHES GEBIET
-
Die
vorliegende Patentanmeldung betrifft im Allgemeinen Brennstoffzellen
und insbesondere ein Verfahren zum Beschichten einer Oberfläche einer
Brennstoffzellenplatte.
-
HINTERGRUND
-
Eine
bipolare Platte ist ein Bauteil in einer PEM(Protonenelektrolytmembran)-Brennstoffzelle.
Die bipolare Platte macht ungefähr
80% des Gesamtgewichts der Brennstoffzelle aus und macht ungefähr 45% der Stapelkosten
aus. Die bipolare Platte ist im Allgemeinen so ausgestaltet, dass
diese Reaktanden gleichmäßig über die
aktiven Gebiete verteilt, dass diese Hitze von den aktiven Gebieten
entfernt, dass diese Strom von einer Zelle zu einer anderen trägt, und,
dass diese eine Leckage von Reaktanden und Kühlmittel verhindert.
-
ZUSAMMENFASSUNG
-
Es
wird hier ein Verfahren zum Beschichten einer Oberfläche einer
Brennstoffzellenplatte offenbart. Das Verfahren umfasst das Ausbilden
einer Sol-Gel-Mischung durch Mischen einer schwachen Säure und
einer Zusammensetzung, welche wenigstens zwei Metalloxidvorläufer enthält. Einer
der Metalloxidvorläufer
ist so ausgestaltet, dass dieser durch eine schwache Säure hydrolysiert
wird, um mit einem anderen der Metalloxidvorläufer mit wenigstens einer organischen
funktionellen Gruppe, welche nicht durch die schwache Säure hydrolysiert
wird, ein vermischtes Metalloxid-Netzwerk auszubilden. Das Verfahren
umfasst des Weiteren das Aufbringen der Sol-Gel-Mischung auf die
Oberfläche
der Brennstoffzellenplatte, das Kondensieren der Sol-Gel-Mischung
durch Aussetzen derselben gegenüber
Luft bei wenigstens einer vorbestimmten Temperatur für eine vorbestimmte
Zeitdauer und das Eintauchen der Sol-Gel-Mischung in Wasser bei
einer vorbestimmten Temperatur für
eine vorbestimmte Zeit, um einen porösen, hydrophilen und leitfähigen Film
auf der Oberfläche der
Brennstoffzellenplatte auszubilden, wodurch die schwache Säure verursacht,
dass der eine der Metalloxidvorläufer
hydrolysiert wird und das vermischte Metalloxid-Netzwerk ausbildet.
-
KURZE BESCHREIBUNG DER ZEICHNUNGEN
-
Merkmale
und Vorteile der vorliegenden Erfindung werden durch Bezugnahme
auf die nachfolgende detaillierte Beschreibung und die Zeichnungen
offensichtlich werden, in denen gleiche Bezugszeichen ähnlichen,
aber möglicherweise
nicht identischen Bauteilen entsprechen. Zum Zwecke der Kürze können Bezugszeichen
oder Merkmale mit einer zuvor beschriebenen Funktion in Verbindung
mit anderen Zeichnungen, in denen diese auftauchen, beschrieben
werden oder nicht beschrieben werden.
-
Die 1 ist
eine schematische Querschnittsansicht einer Ausführungsform einer PEM-Brennstoffzelle.
-
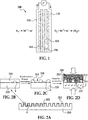
Die 2A bis 2D sind
schematische Diagramme, welche zusammen eine Ausführungsform
einer beschichteten bipolaren Platte (2A) zeigen
und Explosionsansichten eines Verfahrens zum Herstellen und Stapeln
derselben (2B bis 2D) zeigen.
-
Die 3 ist
ein Flussdiagramm, welches eine Ausführungsform eines Verfahrens
zum Ausbilden eines Ausführungsbeispiels
des Beschichtens auf einer Brennstoffzellenplatte zeigt.
-
Die 4A und 4B zeigen
zusammen vier Fotografien, welche Vergleichsergebnisse aus einer Beschichtungsgleichmäßigkeitsuntersuchung
und einer Wasserhydrophilizitätsuntersuchung
zeigen, wobei die 4A die Ergebnisse der TiO2, Ti/Si (1:4) und SiO2 enthaltenden
Beschichtungen zeigt, und, wobei die 4B die
Ergebnisse einer Ti/Si (1:2) enthaltenden Beschichtung zeigt.
-
Die 5 ist
eine Darstellung, welche die Verringerung in der Veränderung
des normalisierten Kontaktwiderstands (%) unter zunehmendem Druck
(psi) gemäß einer
Ausführungsform
der hier offenbarten Beschichtung zeigt, wobei BA die Ergebnisse
vor der Aktivierung zeigt und AA die Ergebnisse nach der Aktivierung
zeigt.
-
DETAILLIERTE BESCHREIBUNG
-
Ausführungsformen
der hier offenbarten Beschichtung der bipolaren Metallplatte sind
leitend und weisen ebenfalls vorteilhafterweise eine sehr stabile
Hydrophilizität
auf. Als solche verbessert die hier offenbarte Beschichtung auch
das Wassermanagement für
herkömmliche
PEM-Brennstoffzellensysteme zusätzlich
zu den herkömmlichen
Funktionen von bipolaren Platten, wie beispielsweise die gleichmäßige Verteilung
von Reaktanden über
die aktiven Gebiete, das Entfernen von Hitze aus den aktiven Gebieten,
das Tragen von Strom von Zelle zu Zelle und das Verhindern von Leckage
von Reaktanden und Kühlmittel.
Dies verbessert wiederum die Leistungsfähigkeit und die Langlebigkeit
der Brennstoffzelle, in welche diese eingebaut ist.
-
Es
wird erachtet, dass die hier offenbarte Beschichtung wenigstens
einen bemerkenswerten Vorteil aufweist, nämlich aufgrund von verbesserter
chemischer Robustheit eine robuste Hydrophilizität in einer Brennstoffzellenumgebung.
Die verbesserte chemische Robustheit ist wenigstens teilweise auf
die gemischte Oxidzusammensetzung sowie auf das Verfahren zum Herstellen
der Beschichtung zurückzuführen. Wie
zuvor erwähnt,
trägt die
Hydrophilizität
zu dem Wassermanagement in dem PEM-Brennstoffzellensystem bei. Beispielsweise
liefert die Beschichtung einen bestimmten Grad an relativer Feuchtigkeit
in der Brennstoffzelle, welche die Protonenleitfähigkeit unter verschiedenen
Brennstoffzellenbedingungen verbessert. Die Beschichtung liefert
ebenfalls Pfade zur schnellen Entfernung von Wasser, um dadurch
ein Fluten bei niedrigen Stromdichtebedingungen zu verringern oder
zu verhindern. Ferner verhindert die Leitfähigkeit der Beschichtung einen
möglichen
Abfall in der Zellspannung, welche andernfalls resultieren kann,
wenn eine Beschichtungsschicht auf der bipolaren Platte vorliegt.
-
Bezug
nehmend nunmehr auf die 1 ist eine typische PEM-Brennstoffzelle 100 dargestellt.
Die Brennstoffzelle 100 umfasst eine Anodenelektrodenschicht 112,
eine Protonenaustauschmembran 116 und eine Kathodenelektrodenschicht 114,
welche allesamt zwischen zwei bipolaren Platten 110 angeordnet
sind.
-
In
der hier offenbarten Brennstoffzelle 100 ist auf den bipolaren
Platten 110 eine Beschichtung (in der 1 nicht
gezeigt) vorgesehen. Diese Beschichtung ist eine gemischte Oxidschicht,
welche durch einen Cogelsynthesansatz erzeugt wird, bei welchem
eine schwache Säure
zur Hydrolyse der Alkoxidvorläufer
eingesetzt wird. Dies erlaubt die Ausbildung eines gemischten Oxid-Netzwerks
bei niedriger Temperatur in situ auf der Oberfläche der bipolaren Metallplatten 110.
Wie zuvor erwähnt
und wie nachfolgend weiter erörtert,
verschafft dieses gemischte Oxidnetzwerk der Brennstoffzelle 100 Hydrophilizität und Stabilität.
-
In
einer Ausführungsform
ist die Beschichtung aus einer Mischung aus Titanoxid und aus Siliziumdioxid
hergestellt, was, verglichen mit Siliziumdioxid alleine, eine stabile
Hydrophilizität
in einer Brennstoffzellenumgebung liefert. In einer anderen Ausführungsform
sind in einigen der Metallalkoxidvorläufer spezielle funktionelle
Gruppen enthalten und es wird erachtet, dass diese funktionellen
Gruppen zu einer verbesserten Partikelhaftung der Beschichtung auf
der Oberfläche
der bipolaren Metallplatten 110 beiträgt. Ferner werden Elektronen
leitende Pfade erzeugt, und zwar durch eine dünne Beschichtungsschicht und
einen Aktivierungsprozess, welcher zu einer Morphologie führt, welche
es erlaubt, dass die Gasdiffusionsmedien in die bipolaren Platten 110 eindringen
können
und diese kontaktieren.
-
Die 2A bis 2D und 3 illustrieren
eine Ausführungsform
des Verfahrens zum Ausbilden der Beschichtung. Wie in der 3 dargestellt,
umfasst das Verfahren im Allgemeinen, wie an dem Bezugszeichen 300 gezeigt,
das Ausbilden einer Sol-Gel-Mischung durch Vermischen einer schwachen
Säure und einer
Zusammensetzung, welche wenigstens zwei Metalloxidvorläufer enthält, wobei
einer der Metalloxidvorläufer
so ausgestaltet ist, dass dieser durch die schwache Säure hydrolysiert
wird, um mit einem anderen der Metalloxidvorläufer mit wenigstens einer organischen
funktionellen Gruppe, welche durch die schwache Säure nicht
hydrolysiert wird (oder nicht hydrolysiert werden kann), ein gemischtes
Metalloxid-Netzwerk auszubilden. Das Verfahren umfasst dann, wie
bei dem Bezugszeichen 302 gezeigt, das Aufbringen der Sol-Gel-Mischung auf
die Oberfläche
der bipolaren Platte der Brennstoffzelle und dann, wie bei dem Bezugszeichen 304 gezeigt, das
Kondensieren der Sol-Gel-Mischung durch Aussetzen der aufgebrachten
Mischung gegenüber
Luft bei einer oder mehreren vorbestimmten Temperaturen für eine vorbestimmte
Zeit. Die kondensierte Sol-Gel-Mischung wird dann, wie bei dem Bezugszeichen 306 gezeigt,
bei einer vorbestimmten Temperatur für eine vorbestimmte Zeit in
Wasser eingetaucht, um auf der Oberfläche der bipolaren Platte der
Brennstoffzelle einen porösen,
hydrophilen und leitfähigen
Film auszubilden. Vor, während
oder nach dem Eintauchschritt und wie zuvor erwähnt verursacht die schwache
Säure,
dass der eine Metalloxidvorläufer
hydrolysiert wird und mit dem anderen Metalloxidvorläufer das
gemischte Metalloxid-Netzwerk ausbildet.
-
Die 2A bis 2C illustrieren
das in der 3 gezeigte Verfahren und es
wird eine zusätzliche Beschreibung
unter Bezugnahme auf diese Figuren dargestellt. Die 2A zeigt
eine bipolare Platte 210 für eine PEM-Brennstoffzelle
(beispielsweise in der 1 als 100 gezeigt),
welche mit einer Ausführungsform
der hier offenbarten leitfähigen,
hydrophilen Schicht/Beschichtung 212 beschichtet ist. Während die
Beschichtung 212 entlang der Oberfläche S der bipolaren Platte 210 als
im Wesentlichen kontinuierlich gezeigt ist, ist es zu verstehen,
dass die Beschichtung 212 porös ist und folglich bei bestimmten
Gebieten Teile der leitfähigen
bipolaren Plattenoberfläche
S (oder einer darauf aufgebrachten leitfähigen Beschichtung (nicht gezeigt))
freiliegt. Insbesondere werden während
der Kondensation/dem Wasserbehandlungsverfahren (nachfolgend weiter
beschrieben) auf der Oberfläche
S (wie in der 2C dargestellt) kleine poröse Partikel 212 gebildet,
welche die Beschichtung 212 ausbilden, und die Poren oder
Räume zwischen
den porösen
Partikeln 212 liefern während
des Zusammenbaus des Stapels eine Kontaktfläche für die Ausbildung von Elektronen
leitenden Pfaden (wie in der 2D gezeigt).
Während
die Beschichtung 212 auf der Oberfläche S einheitlich ausgebildet sein
kann, umfasst solch eine Beschichtung 212 Poren/Räume darin.
-
Es
wird erachtet, dass die Beschichtungsschicht 212 kostengünstige Materialien
und einen kostengünstigen
Ansatz zum Verbessern des Wassermanagements unter PEM-Brennstoffzellenbedingungen
liefert. Die zur Ausbildung der Beschichtung 212 eingesetzten
Materialien umfassen, sind aber nicht beschränkt auf eine schwache Säure und
auf zwei Metalloxidvorläufer,
welche zusammen eine Sol-Gel-Mischung ausbilden. Die schwache Säure wird
aus den nachfolgenden Säuren
ausgewählt:
Sulfonsäure,
Essigsäure,
Phosphorsäure,
Zitronensäure,
Borsäure
oder andere organische Säuren
(beispielsweise Phenylsulfonsäure
(PSA)) und Mischungen hiervon. Die Metalloxidvorläufer werden
aus den Vorläufern
der nachfolgenden Metalloxide ausgewählt: Siliziumdioxid, Titandioxid,
Zinndioxid, Tantaloxid, Hafniumdioxid, Zirkoniumdioxid, Niobdioxid,
Molybdänoxid,
Iridiumoxid, Rutheniumoxid, Aluminiumoxid oder deren Mischungen.
Spezifische, nicht beschränkende
Beispiele für
geeignete Metalloxidvorläufer
schließen
N-Triethoxysilylpropylharnstoff (TEOSPU) als ein Vorläufer für Siliziumdioxid
sowie Titantetraisopropanoxid (TTIP) als ein Vorläufer für Titandioxid
ein.
-
Die
Menge der Vorläufer
und der Säure,
welche eingesetzt werden, können
abhängig
von den Syntheseprozessbedingungen, den eingesetzten Materialien
etc. variieren. Theoretisch und in einer Ausführungsform werden dieselben
Mole der sauren funktionellen Gruppe und der alkoxidfunktionellen
Gruppe eingesetzt, um ein perfektes (oder so perfektes wie möglich) Metalloxid-Netzwerk
auszubilden. Allerdings kann in vielen Fällen die Menge von Säure leicht
höher als
ihre theoretische Zahl sein.
-
Wenigstens
einer der Metalloxidvorläufer
in der Sol-Gel-Mischung ist so ausgestaltet, dass dieser während des
Verfahrens durch die schwache Säure
hydrolysiert wird. Die schwache Säure initiiert vorteilhafterweise
die Ausbildung des gemischten Metalloxid-Netzwerks und trägt dazu
bei. Es ist zu verstehen, dass die sauren funktionellen Gruppen
chemisch nicht an die Oberfläche
des Metalloxidvorläufers
oder des resultierenden gemischten Metalloxid-Netzwerks anhaftet.
Vielmehr werden die sauren funktionellen Gruppen während des
Wasserbehandlungsverfahrens ausgewaschen. Es wird erachtet, dass
das resultierende poröse
gemischte Metalloxid-Netzwerk die Hydrophilizität, die Haftung, die Stabilität und die
Dispergierbarkeit der Komponenten der Sol-Gel-Beschichtung 212 erhöht.
-
In
einer Ausführungsform
umfasst der andere der Metalloxidvorläufer eine organische funktionelle Gruppe.
Es wird erachtet, dass solche funktionelle Gruppe(n) eine bessere
Haftung für
die Beschichtungsschicht 212 erzeugen. Nicht beschränkende Beispiele
für solche
organische funktionelle Gruppen schließen Amide, Epoxide, Acrylate
und Acrylharnstoffe (wie beispielsweise in einer nicht beschränkenden
Ausführungsform
Propylharnstoff) ein. Es sollte verstanden werden, dass diese organischen
funktionellen Gruppen so ausgewählt
werden, dass diese während
des Sol-Gel-Verfahrens
nicht hydrolysieren und auch nicht hydrolysieren können.
-
In
einem nicht beschränkenden
Beispiel wird die Sol-Gel-Mischung durch Vermischen einer vorbestimmten
Menge von Essigsäure
und von N-Triethoxysilylpropylharnstoff in Methanol, um dadurch
eine Lösung zu
erzeugen, und durch Zugabe einer vorbestimmten Menge von Titantetraisopropanoxid
zu der Lösung,
um dadurch ein Titandioxid-Siliziumdioxid-Sol-Gel auszubilden, erzeugt.
-
Unter
Bezugnahme nunmehr auf die 2B umfasst
das relativ kostengünstige
und einfache Beschichtungsverfahren, welches hier offenbart wird,
einen Aufbringschritt, bei dem die Sol-Gel-Mischung auf die bipolare
Platte 210 aufgebracht wird, um eine poröse Dünnfilm-Cogel-Beschichtung 214 auszubilden.
Die Dünnfilm-Cogel-Beschichtung 214 wird
so aufgebracht, dass diese eine Dicke im Nanomaßstab oder im Mikromaßstab aufweist.
Ferner kann die Dicke basierend auf den Leistungsanforderungen der
Brennstoffzelle 100 variiert werden. Es kann jede geeignete
Abscheidetechnik eingesetzt werden, um die Beschichtung auszubilden,
und in einem nicht beschränkenden
Beispiel ist die Technik eine Eintauchtechnik.
-
Nach
dem Aufbringschritt erfolgt die Kondensation der Dünnfilm-Cogel-Beschichtung 214.
Die Kondensation wird über
die Aussetzung der Beschichtung 214 gegenüber Luft
bei Umgebungstemperatur (beispielsweise in einem Bereich zwischen
ungefähr
20°C und
ungefähr
30°C) für eine vorbestimmte
Zeit erreicht. Die Zeit der Kondensation wird zumindest abhängig von
den Metalloxidvorläufern,
welche eingesetzt werden, variieren. In einem nicht beschränkenden
Beispiel beträgt
die Zeit weniger als oder gleich 2 Stunden. Das Kondensationsverfahren
kann gefolgt werden durch Aussetzen der Beschichtung 214 gegenüber Luft
für eine
vorbestimmte Zeit bei einer erhöhten
Temperatur (d. h. bei jeder Temperatur, welche höher ist als Umgebungstemperatur),
welche in einem nicht beschränkenden
Beispiel ungefähr
100°C beträgt. Wiederum
wird die Aussetzungszeit gegenüber
der erhöhten
Temperatur von den eingesetzten Materialien abhängen.
-
Nachdem
der Kondensationsschritt abgeschlossen ist, wird die Dünnfilm-Cogel-Beschichtung 214 für eine vorbestimmte
Zeit in Wasser eingetaucht. Während
dieses Schritts kann das Wasser auf eine Temperatur von ungefähr 80°C erhitzt
werden. Im Allgemeinen liegt die Wassertemperatur in einem Bereich
zwischen ungefähr
50°C und
ungefähr
100°C. Diese
Heißwasserbehandlung
aktiviert die Sol-Gel-Mischung und erzeugt die poröse, hydrophile,
gemischte Metalloxid-Sol-Gel-Beschichtung 212. Das Erzeugen
der porösen
Beschichtung 212 setzt ebenfalls die leitfähige Oberfläche S der
bipolaren Platte 210 frei. Die Beschichtung 212 nach der
Kondensation und der Wasserbehandlung ist schematisch in der 2C gezeigt.
-
Um
Hydrophilizität
zu erzeugen, wird die Dünnfilm-Cogel-Beschichtung 214 (2B)
durch das Sol-Gel-Verfahren und das Nassaktivierungsverfahren behandelt,
welche sowohl die zuvor beschriebene Kondensationsbehandlung als
auch die Wasserbehandlung einschließen. In einigen Fällen kann
es wünschenswert
sein, dass die Beschichtungsschicht 212 nicht bei einer
hohen Temperatur kalziniert wird, welche oftmals in herkömmlichen
Ansätzen
für poröse Materialien
eingesetzt wird. Es ist herausgefunden worden, dass das Nassaktivierungsverfahren
ohne Kalzination bei der Herstellung von porösen Filmen 212 mit
guter Stabilität hilft.
-
In
einigen Ausführungsformen
kann vor der Aktivierung der Sol-Gel-Mischung (d. h. vor dem Eintauchen
derselben in Wasser) die Brennstoffzellenplatte 212 mit
der Beschichtung 214 weiter getrocknet werden. Der zusätzliche
Schritt des Trocknens wird in einem Beispiel durch Aussetzen der
beschichteten Brennstoffzellenplatte 210, 214 gegenüber Umgebungsluft
für eine
vorbestimmte Zeitspanne und dann durch Aussetzen der beschichteten
Brennstoffzellenplatte 210, 214 gegenüber einer
Temperatur, welche höher
als die Umgebungsluft ist, für
eine andere vorbestimmte Zeitspanne erreicht. In einer Ausführungsform
liegt die höhere
Temperatur zwischen ungefähr
80°C und
ungefähr
200°C und
die Umgebungstemperatur ist niedriger als 80°C.
-
Während dem
Zusammenbau des PEM-Brennstoffzellenstapels wird normalerweise Druck
auf die Beschichtung 212 auf der bipolaren Platte 210 aufgebracht,
um eine bessere Leitfähigkeit
zwischen dem Kohlenstoffdiffusionspapier 218 und den bipolaren
Platten 210 zu erreichen (siehe 2D). Im
Hinblick auf die Brennstoffzelle 100 der 1 werden
in jeder der Anodenschicht 112 und der Kathodenschicht 114 Kohlenstoffdiffusionspapiere 218 (in
der 1 nicht dargestellt) eingesetzt und diese kontaktieren
jeweils die bipolaren Platten 110, 210, welche
benachbart zu der Anodenschicht 112 und der Kathodenschicht 114 sind.
Wiederum auf die 2C und 2D zusammen
Bezug nehmend, kann durch diese Maßnahme die Gasdiffusionsschicht (beispielsweise
das Kohlenstoffdiffusionspapier 218) durch den Hohlraum 220 in
die gemischten Metalloxid-Sol-Gel-Beschichtung 212 eindringen
und in direkten Kontakt mit der Oberfläche S der bipolaren Platten 210 kommen,
um so elektronische Pfade 222 dahin und davon weg zu liefern.
Die Leitfähigkeit
wird durch die operative Verbindung zwischen dem Kohlenstoffdiffusionspapier 218 und
der Oberfläche
S der bipolaren Platten 210 erzeugt.
-
Die
elektronisch leitfähigen
Pfade 222, welche nach dem Nassaktivierungsverfahren und
während dem
Stapelzusammenbauverfahren erzeugt werden, reduzieren oder eliminieren
eine Erhöhung
des Kontaktwiderstandes, welcher durch die Metalloxidbeschichtungsschicht 212 verursacht
wird. Wenn die bipolare Platte 210 mit SiO2 oder
mit anderen Metalloxiden beschichtet wird, besteht eine dahingehende
Tendenz, dass die Grenzfläche
nicht leitend wird. Allerdings verbessert die hier beschriebene
Beschichtung 212 die Grenzflächenleitfähigkeit beträchtlich.
Daher ermöglichen
die hier offenbarten Ausführungsformen
das Aufbringen einer sehr hydrophilen Beschichtung 212 auf
die hydrophobe Oberfläche
der bipolaren Metallplatten 210, während eine gewünschte Leitfähigkeit
der bipolaren Platten 210 aufrechterhalten wird.
-
Vor
dem Beschichtungsverfahren, welches in den 2B bis 2D dargestellt
ist, kann die Oberfläche
S der bipolaren Metallplatte 210 in einigen Fällen vorbehandelt
werden. In einer Ausführungsform
wird die Vorbehandlung durch Oberflächenätzen mit Säure, wie beispielsweise mit
H2SO4 erreicht,
um eine raue und saubere Oberfläche
zu erzeugen. Bei dieser Ausführungsform
wird die Platte 210 in eine Lösung der Säure bei Raumtemperatur oder
bei einer erhöhten
Temperatur für
eine geeignete Zeit eingetaucht, um die gewünschte Oberflächenbehandlung
zu erreichen. Die vorbehandelte Oberfläche wird dann mit Wasser gespült, bevor
die Sol-Gel-Mischung darauf aufgebracht wird.
-
In
einer anderen Ausführungsform
kann die Vorbehandlung der Oberfläche S der metallischen bipolaren
Platte 210 vor dem Beschichten der Oberfläche S mit
der Sol-Gel-Mischung durch teilweises oder vollständiges Beschichten
der Oberfläche
S mit einem anderen, leitfähigeren
Metall, wie beispielsweise mit Pt, Cu etc., erreicht werden. Es
kann ein Elektroplattierverfahren eingesetzt werden, um diese leitfähige Metallbeschichtung
aufzubringen. Das Elektroplattierverfahren nutzt elektrischen Strom,
um die Kationen eines gewünschten Materials,
typischerweise Metall, aus einer Lösung zu reduzieren, und, um
einen leitfähiges
Gegenstand (beispielsweise die Oberfläche S) mit einer dünnen Schicht
des anderen Materials (in diesem Beispiel ein leitfähigeres
Metall als das Metall der bipolaren Platte 210) zu beschichten.
Insbesondere werden eine Anode, welche durch ein elektrisch leitendes
Metall gebildet wird, wie beispielsweise Pt, Cu etc., sowie eine
Kathode, welche durch die bipolare Platte 210 gebildet
wird, zusammen mit einer äußeren Versorgung
für direkten
Strom verbunden, während
sowohl die Anode als auch die Kathode in eine Elektrolytlösung eingetaucht
sind. Die Anode wird mit dem positiven Ende der Versorgung verbunden
und die Kathode wird mit dem negativen Ende verbunden. Wenn die
externe Stromversorgung angeschaltet ist, wird das Metall an der
Anode von dem Valenzzustand null oxidiert, um Kationen mit einer
positiven Ladung zu bilden. Diese Kationen verbinden sich mit den Anionen
in der Elektrolytlösung.
Die Kationen werden dann an der Kathode (d. h. der Oberfläche S der
Platte 210) reduziert, um eine weitere zusätzliche
leitfähige
Schicht in dem metallischen Valenzzustand null abzuscheiden.
-
Als
ein nicht beschränkendes
Beispiel für
dieses Vorbehandlungsverfahren wird das Kupfer, wenn das Plattierungsmetall
Kupfer ist, in einer sauren Lösung
an der Anode durch Verlieren von zwei Elektronen zu Cu2+ oxidiert.
Das Cu2+-Anion verbindet sich mit dem Anion
SO4
2- in der Lösung, um
Kupfersulfat zu bilden. An der Kathode wird das Cu2+ durch
Aufnahme von zwei Elektronen zu metallischem Kupfer reduziert. Das
Ergebnis ist der wirksame Transfer von Kupfer von der Anodenquelle,
um eine Metallplattierungsschicht auszubilden, welche die Oberfläche S der
bipolaren Platte 210 beschichtet.
-
Um
Ausführungsform(en)
der vorliegenden Erfindung weiter zu illustrieren, werden nachfolgend
verschiedene Beispiele wiedergegeben. Es ist zu verstehen, dass
diese lediglich für
illustrative Zwecke wiedergegeben werden und nicht dazu gedacht
sind, den Schutzbereich der offenbarten Ausführungsform(en) zu beschränken.
-
BEISPIELE
-
Beispiel 1
-
Gemäß der nachfolgenden
Beschreibung wurde auf einem 304 SS- (eine Art von standardisiertem rostfreiem
Stahl) Formling eine TiO2-SiO2-Beschichtung (Ti/Si
= 1:2) gebildet und aufgebracht.
-
Es
wurden 2,4 g TEOSPU (N-Triethoxysilylpropylharnstoff in 50% Methanol
(United Chemical Tech. Inc.)) und 5,0 g Essigsäure (99,8% Reagenz Plus, Aldrich)
zusammen unter Rühren
für 10
Min. bei Raumtemperatur zugegeben. In die zuvor genannte Lösung wurde
unter kontinuierlichem Rühren
für 30
Min. bei Raumtemperatur 4,4 g TTIP (Titantetraisopropanoxid, 97%,
Aldrich) zugegeben. Die erhaltene Lösung betrug ungefähr 11,8
g TiO2-SiO2-Sol-Gel.
Das Sol-Gel wurde nach Stunden bei Raumtemperatur kondensiert.
-
Ein
blanker 304 SS-Formling wurde in die Sol-Gel-Mischung eingetaucht,
bevor diese kondensierte. Der beschichtete Formling wurde dann bei
Raumtemperatur für
2 Stunden in Luft getrocknet. Dann wurde der beschichtete Formling
bei 100°C
in Luft über
Nacht getrocknet. Schließlich
wurde der getrocknete Formling in Wasser platziert und bei 80°C für wenigstens
4 Stunden gehalten.
-
Beispiel 2 (Vergleichsbeispiel)
-
Auf
einem 304 SS-Formling wurde gemäß der nachfolgenden
Beschreibung eine TiO2-Beschichtung gebildet
und aufgebracht.
-
Es
wurden 7,1 g TTIP (Titantetraisopropanoxid, 97%, Aldrich) und 6,0
g Essigsäure
(99,8% Reagenz Plus, Aldrich) zusammen unter Rühren für 30 Min. bei Raumtemperatur
zugegeben. Die erhaltene Lösung
betrug ungefähr
11,8 g TiO2-Sol-Gel. Das Sol-Gel könnte nach
Stunden bei Raumtemperatur kondensiert werden.
-
Dann
wurde ein blanker 304 SS-Formling in das Sol-Gel eingetaucht, bevor
dieses kondensierte. Der kondensierte Formling wurde dann bei Raumtemperatur
für 2 Stunden
in Luft getrocknet. Dann wurde der getrocknete Formling bei 100°C in Luft über Nacht
getrocknet. Schließlich
wurde der getrocknete Formling in Wasser platziert und bei 80°C für wenigstens
4 Stunden gehalten.
-
Beispiel 3 (Vergleichsbeispiel)
-
Gemäß der nachfolgenden
Beschreibung wurde eine SiO2-Beschichtung
auf einen 304 SS-Formling gebildet und aufgebracht.
-
Es
wurden 7,4 g TEOSPU (N-Triethoxysilylpropylharnstoff in 50% Methanol
(United Chemical Tech. Inc.)) und 4,5 g Essigsäure (99,8% Reagenz Plus, Aldrich)
zusammen unter Rühren
für 30
Min. bei Raumtemperatur zugegeben.
-
Dann
wurde ein blanker 304 SS-Formling in das Sol-Gel eingetaucht, bevor
dieses kondensierte. Der beschichtete Formling wurde dann bei Raumtemperatur
für 2 Stunden
in Luft getrocknet. Dann wurde der beschichtete Formling bei 100°C in Luft über Nacht
getrocknet.
-
Schließlich wurde
der getrocknete Formling in Wasser platziert und bei 80°C für wenigstens
4 Stunden gehalten.
-
Beispiel 4
-
Auf
Basis der in dem Beispiel 1 und in den Vergleichsbeispielen 2 und
3 beschriebenen Verfahren wurden Formlinge hergestellt. Insbesondere
wurden verschiedene Formlinge mit den nachfolgenden Mol-Verhältnissen
von Ti/Si hergestellt: 1:1, 1:2, 1:4, 1:8, 1:0 und 0:1. Die erhaltenen
Hydrophilizitätsdaten
basierten auf dem Durchmesser eines 10 μl Wassertropfens. Ein Tropfen
ist dann hydrophil, wenn sich der Tropfen auf der gesamten Oberfläche des
Formlings (1 Quadratinch) ausbreitet. Es wurden ebenfalls Leitfähigkeitsdaten
auf Basis des Kontaktwiderstandes, welcher unter einer fixen Stromdichte
unter verschiedenen Drücken
gemessen wurde, erhalten.
-
Nachdem
alle der beschichteten Formlinge (ausgenommen Ti/Si = 1:8) bei 100°C über Nacht
getrocknet wurden, waren alle die TiO2 enthaltenden
Beschichtungen hydrophil. Die SiO2-Beschichtung
(Ti/Si = 0:1) ist, nachdem diese getrocknet ist, hydrophob. Es wurde
beobachtet, dass die SiO2-Lösung nicht kondensiert werden
konnte, was zeigt, dass die Essigsäure den SiO2-Vorläufer, TEOSPU,
nicht hydrolysieren konnte. Andererseits wurden offensichtlich alle
der TiO2-SiO2-Sol-Gele
aufgrund der Gegenwart des Titanvorläufers (TTIP) durch Essigsäure hydrolysiert.
-
Die
Tabelle 1 fasst die Erkenntnisse von den zuvor beschriebenen Proben,
welche sowohl TiO
2 als auch SiO
2 enthalten,
zusammen. Tabelle 1: Zusammenfassung der TiO
2-SiO
2 beschichteten
304 SS-Formlinge
| Formling | Ti/Si
(Mol) | Hydrophil
nach dem Trocknen? | Hydrophil
nach der Wasserbehandlung? | Leitfähig? |
| 1 | 1:1 | Ja | Ja | Ja |
| 2 | 1:2 | Ja | Ja | Ja |
| 3 | 1:4 | Ja | Ja | Ja |
| 4 | 1:8 | Nein | Ja | Ja |
| 5 | 1:0 | Ja | Ja | N/A |
| 6 | 0:1 | Nein | Nein | N/A |
-
Die
Beschichtungen auf den Formlingen wurden gemäß dem Verfahren des Trocknens
bei 100°C über Nacht
in Luft getrocknet. Die Beschichtungen auf den Formlingen wurden
gemäß dem Verfahren
des Platzierens derselben in Wasser bei 80°C über Nacht, nachdem diese getrocknet
waren, mit Wasser behandelt. Die Leitfähigkeit konnte für die 1:0-
und für
die 0:1 Ti/Si-Formlinge nicht gemessen werden, und zwar aufgrund
von Rissen und von Aggregation.
-
In
den wie zuvor beschrieben hergestellten Formlingen wurde die Beschichtungsgleichmäßigkeit
und die Wasserhydrophilizität
untersucht. Wie in den 4A und 4B dargestellt,
weisen gemischten TiO2-SiO2-Beschichtungen eine
bessere Qualität
und eine bessere Gleichmäßigkeit
auf (siehe 4(A) Ti/Si (1:4)). Im Vergleich
dazu mangelt es den Beschichtungen in Formlingen mit einem von,
aber nicht mit beiden von TiO2 oder SiO2, wie in der 4A gezeigt,
an einigen von für
diese gewünschten
Qualitäten.
Nachdem die TiO2-Beschichtung über Nacht
bei 100°C
getrocknet worden war, zeigte die Beschichtung eine schlechtere Haftung
und tendierte dazu, von der Oberfläche des Formlings abzublättern, wie
dies in der 4A dargestellt ist. In dem Fall
der SiO2-Beschichtung
zeigte die Beschichtung nach dem Trocknen der Beschichtung über Nacht
bei 100°C
eine bessere Haftung, diese war jedoch nicht gleichmäßig, wie
dies in der 4A ebenfalls dargestellt ist.
In der 4B ist eine Ti/Si-(1:2)-Beschichtung
gezeigt, auf welcher ein Hydrophilizitätstest durchgeführt wurde.
Dieser Test wurde durch Platzieren eines Wassertropfens von 10 μl auf der
getrockneten Beschichtung mit einem Ti/Si-Verhältnis von 1:2 durchgeführt. Die 4B zeigt,
dass die Beschichtungsschicht eine höhere Hydrophilizität aufwies,
weil sich der Wassertropfen gleichmäßig über die gesamte Oberfläche der
Beschichtung ausbreitete, was eine Eigenschaft ist, welche Hydrophilizität anzeigt.
-
Beispiel 5
-
Im
Hinblick auf den Formling TiO2-SiO2 (T/Si = 1:2), wie zuvor beschrieben, wurde
der beschichtete Formling zunächst
(d. h. vor dessen Aktivierung, BA) getrocknet und dieser wurde dann
(d. h. nach der Aktivierung, AA) mit Wasser behandelt. In der 5 sind
Vergleichsdaten gezeigt, welche sich auf den Prozentsatz der Veränderung
des Kontaktwiderstands für
die BA-Probe und die AA-Probe beziehen. Die Daten wurden für den Formling
bei 100 psi durch Vergleichen des AA-Widerstands mit dem BA-Widerstand erhalten.
Die Ergebnisse zeigen den Unterschied in dem Kontaktwiderstand bei
einer Erhöhung
des Drucks. Der Widerstand wurde klar drastisch reduziert, nachdem
die Probe in Wasser behandelt worden ist.
-
Als
ein Teil des Experiments wurde die Leitfähigkeit des gemischten Metalloxids
untersucht, wobei die beschichteten Formlinge zwischen zwei Kohlenstoffpapieren
platziert worden waren. Es wurde herausgefunden, dass das gemischte
Metalloxid nicht leitfähig
war. Dies zeigt, dass die Leitfähigkeit
durch die Verbindung des Kohlenstoffpapiers und die blanke Oberfläche des
Formlings, wie zuvor beschrieben, erzeugt wird.
-
Während verschiedene
Ausführungsformen
im Detail beschrieben worden sind, wird es für einen Fachmann offensichtlich
sein, dass die offenbarten Ausführungsformen
modifiziert werden können.
Damit ist die vorstehende Beschreibung als exemplarisch und nicht
als beschränkend
anzusehen.