ES2706185T3 - Pirimidinil y 1,3,5-triazinil bencimidazoles y sus usos en la terapia contra el cáncer - Google Patents
Pirimidinil y 1,3,5-triazinil bencimidazoles y sus usos en la terapia contra el cáncer Download PDFInfo
- Publication number
- ES2706185T3 ES2706185T3 ES14168117T ES14168117T ES2706185T3 ES 2706185 T3 ES2706185 T3 ES 2706185T3 ES 14168117 T ES14168117 T ES 14168117T ES 14168117 T ES14168117 T ES 14168117T ES 2706185 T3 ES2706185 T3 ES 2706185T3
- Authority
- ES
- Spain
- Prior art keywords
- fluoromethyl
- triazn
- amine
- amino
- morpholinyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 CC(C=I)=C*=C(*)N Chemical compound CC(C=I)=C*=C(*)N 0.000 description 4
- OQJVXNHMUWQQEW-UHFFFAOYSA-N C1NC=CNC1 Chemical compound C1NC=CNC1 OQJVXNHMUWQQEW-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
Description
DESCRIPCIÓN
Pirimidinil y 1,3,5-triazinil bencimidazoles y sus usos en la terapia contra el cáncer
Campo
Se proporcionan en este documento pirimidinil y 1,3,5-triazinil bencimidazoles, y sus composiciones farmacéuticas, preparación, y dichos agentes o fármacos para su uso en un método de terapia oncológica, ya sea solo o en combinación con radiación y/u otros fármacos anticancerígenos.
Antecedentes de la invención
Las fosfoinositida-3-quinasas (PI3K) son un grupo de quinasas de lípidos, que fosforilan el 3-hidroxilo de los fosfoinositidos. Se clasifican en, al menos, tres clases (clases I, II y III) y desempeñan un papel importante en la señalización celular (Stephens et al., Curr. Opin. Pharmacol. 2005, 5, 357). Las enzimas de clase I se clasifican además en las clases Ia y Ib en función de su mecanismo de activación; la clase IA PI3K son estructuras heterodiméricas que consisten en una subunidad catalítica (p110a, p110p o p1105) en complejo con una subunidad regulatoria P85, mientras que la clase-Ib PI3K (p110Y) es estructuralmente similar pero carece de la subunidad reguladora P85 y, en su lugar, se activa por las subunidades del pY de las G-proteínas heterotriméricas (Walker et al., Mol. Cell. 2000, 6 , 909). La secuencia de proteínas humanas de la isoforma p110a se describe en Volina et al., Genomics 1994, 24, 472; y Stirdivant et al., Bioorg. Med. Chem. 1997, 5, 65.
Las PI3K desempeñan una variedad de funciones en la fisiología normal de los tejidos (Foukas & Shepherd, Biochem. Soc. Trans. 2004, 32, 330; Shepherd, Acta Physiol. Scand. 2005, 183, 3), con p110aquetienen una función específica en el crecimiento del cáncer, p110p en la formación de trombos mediada por la integrina anp3 (Jackson et al., Nat. Med. 2005, 11, 507) y p110Y en la inflamación, artritis reumatoide (Camps et al., Nat. Med. 2005, 11, 936) y otros estados de inflamación crónica (Barber et al., Nat. Med. 2005, 11, 933). Las enzimas PI3K producen fosfoinositida 3, 4,5-trifosfato (PIP3) del difosfato correspondiente (PIP2), reclutando así AKT (proteína quinasa B) a través de su dominio de homología Pleckstrin (PH) a la membrana plasmática. Una vez unido, AKT es fosforilado y activado por otras quinasas unidas a membrana y es central a una cascada de eventos que conducen a la inhibición de la apoptosis (Berrie, Exp. Opin. Invest. Drugs2001, 10, 1085).
La isoforma p110a se amplifica selectivamente y se activa en una serie de tipos de cáncer (Stephens et al., Curr. Opin. Pharmacol. 2005, 5, 357; Stauffer et al., Curr. Med. Chem.-Anti-Cancer Agents 2005, 5, 449). Además, hay una alta frecuencia de mutaciones no aleatorias en sitios específicos, principalmente en el dominio C2 y o el bucle de activación, de la quinasa en varias líneas celulares de cáncer humano, incluyendo el colon, el cerebro, la mama y el estómago (Samuels et al., Science 2004, 304, 554). Esto da como resultado una enzima activa constitutivamente (Ikenoue et al., Cancer Res. 2005, 65, 4562; Kang et al., Proc. Natl. Acad. Sci. USA 2005, 102, 802), haciendo de p110a uno de los oncogenes más altamente mutados que se encuentran en los tumores humanos. Los estudios estructurales han demostrado que muchas de las mutaciones aparecen en los residuos que se encuentran en las interfaces entre p110 a y p85a o entre el dominio de la quinasa de p110a y otros dominios dentro de la subunidad catalítica (Miled et al., Science 2007, 317, 239; Huang et al., Science 2007, 318, 1744).
Mientras que las isoenzimas PI3K desempeñan importantes funciones en muchos procesos celulares, los estudios experimentales publicados en ratones con xenoinjertos de tumores humanos demuestran que el inhibidor de la pan-PI3K LY294002 es bien tolerado, reduce la señalización a través de la vía PI3K, causa la reducción del volumen tumoral, y es más activo en las líneas celulares que sobreexpresan las formas mutantes de p110 a que las células de control parental (Semba et al., Clin. Cancer Res. 2002, 8, 1957; Hu et al., Cancer Res. 2002, 62, 1087 ).
Por lo tanto, PI3K, especialmente la isoforma p110a, es una diana interesante para la intervención farmacológica. Se han identificado varias clases de compuestos como inhibidores reversibles; por ejemplo, LY 294002 (no selectivo) (Walker et al., Mol .Cell. 2000, 6 , 909), PI103 (a-ligeramente selectivo) (Knight et al., Cell 2006, 125, 733; Hayakawa et al., Bioorg. Med. Chem. Lett. 2007, 17, 2438; Raynaud et al., Cancer Res. 2007, 67, 5840), ZSTK474 (no selectivo) (Yaguchi et al., J. Natl. Cancer Inst. 2006, 98, 545; Kong et al., Cancer Sci. 2007, 98, 1639), TGX221 (p-selectivo) (jackson et al., Nat. Med. 2005, 11, 507), oxazinas (Y-selectivas) (Lanni et al., Bioorg. Med. Chem. Lett. 2007, 17, 756), IC87114 (8-selectiva) (Sadhu et al., documento WO 2001/81346; Billottet et al., Oncogene 2006, 25, 6648), AS605240 (Y-selectivo) (Camps et al., Nat. Med. 2005, 11, 936), las imidazo[1,2-a]piridinas (a-selectivas) (Hayakawa et al., Bioorg. Med. Chem. 2007, 15, 403; Hayakawa et al., Bioorg. Med. Chem. 2007, 15, 5837), y la imidazo[4,5-c]quinolina NVP-BEZ235 (Garcia-Echeverria, et al., WO 2006/122806).
El documento WO2008/032086 describe un derivado de pirimidina que tiene la fórmula I:
para la prevención y el tratamiento de tumores.
A pesar de los avances en el desarrollo de inhibidores PI3K, hay una necesidad de inhibidores PI3K para el tratamiento del cáncer.
RESUMEN DE LA DESCRIPCIÓN
En este documento se incluye un compuesto de la fórmula I, IA o IB:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato; donde:
cada R1 es independientemente hidrógeno, alquilo C 1-6 , -S-alquilo C1-6 , -S(O)-alquilo C1-6 , o -SO2-alquilo C1-6
cada R2 y R3 es, independientemente, (a) hidrógeno, ciano, halo o nitro; (b) alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, cicloalquilo C3 -7 , arilo C6 -14 , aralquilo C7 -15 , heteroarilo o heterociclilo; o (c) -C(O)R1 a , -C(O)OR1b , -C(O)NR1bR1 c , -C(NRa)NR1bR1 c , -OR1 a , -OC(O)R1 a , -OC(O)OR1a , -OC(O)NR1b R1 c , -OC(=NR1a)NR1bR1 c , -OS(O)R1 a , -OS(O)2 R1a , -OS(O)NR1bR1 c , -OS(O)2NR1bR1 c , -NR1bR1 c , -NR1aC(O)R1d , -NR1aC(O)OR1d , -NR1aC(O)NR1b R1 c , -NR1aC(=NR1d)NR1b R1 c , -NR1aS(O)R1d , -NR1aS(O)2 R1d , -NR1aS(O)NR1bR1 c , -NR1aS(O)2NR1bR1 c , -SR1a , -S(O)R1a , -S(O)2 R1a , -S(O)NR1bR1 c , o-S(O)2 NR1bR1 c ;
cada R4 y R5 es independientemente hidrógeno o alquilo C1.6 o R 4 y R 5 unidos para formar un enlace, alquileno C1-6, heteroalquileno C1-6 , alquenileno C2-6, o heteroalquenileno C2-6;
cada R6 es independiente arilo C6-14, aralquilo C7-15, heteroarilo, o heteroaril-alquilo C1-6;
cada U es independientemente un enlace, -C(O)-, -C(O)O-, -C(O)NR1a-, -O-, -OC(O)O-, -OC(O)NR1a-, -NR1a-, -NR1aC(O)NR1d-, -NR1aS(O)-, -NR1aS(O)2-, -NR1aS(O)NR1d-, -NR1aS(O)2 NR1d-, -S-, -S(O)-, o -S(O)2-;
cada X, Y y Z es N; Y
cada A, B, D, y E es independientemente un enlace, C, O, N, S, NR9CR9 o CR9 R10, donde cada R9 y R10 es independientemente hidrógeno, halo, alquilo C 1-6 , alquenilo C2-6, o alquinilo C2-6 ; donde los enlaces entre A, B, D y E pueden ser saturados o insaturados; con la condición de que no más de uno de A, B, D y E son un enlace;
cada R1 a , R1b , R1c y R1d es, independientemente, (i) hidrógeno; o (ii) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo;
en donde cada alquilo, alquileno, heteroalquileno, alquenilo, alquenileno, heteroalquenileno, alquinilo, cicloalquilo, arilo, aralquilo, heteroarilo, y heterociclilo en R1, R2, R3, R4, R5, R6, R9, R10, R1a, R1b, R1c o R1d se sustituye opcionalmente por uno o más, en una realización, uno, dos, tres o cuatro grupos, cada uno seleccionado
independientemente de (a) ciano, halo y nitro; (b) alquilo C i -6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6- i 4, aralquilo C7-15, heteroarilo, y heterociclilo, cada uno de los cuales está además opcionalmente sustituido por uno o más, en una realización, uno, dos, tres o cuatro, sustituyentes Q; y (c) -C(O)Ra , -C (o)oR a , -C(O)NRbRc , -C(NRa)NRbRc , -ORa , -OC(O)Ra , -OC(O)ORa , -OC(O)NRbRc , -OC(=NRa)NRbRc , -OS(O)Ra , -OS(O)2Ra , -OS(O)NRbRc , -OS(O)2NRbRc , -NRbRc , -NRaC(O)Rd, -NRaC(O)Od, -NRaC(O)NRbRc , -NRaC(=NRd)NRbRc , -NRaS(O)Rd, -NRaS(O)NRbRc , -SRa , -S(O)Ra , y-S(O)NRbRc , donde cada Ra , Rb, Rc y Rd es, independientemente, (i) hidrógeno; (ii) alquilo C1-6, alquenilo C2-6 , alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo, o heterociclilo, cada uno opcionalmente sustituido por uno o más, en una realización, uno, dos, tres, o cuatro, sustituyentes Q; o (iii) Rb y Rc , junto con el átomo N al que se unen, forman heterociclilo, opcionalmente sustituidos por uno o más, en una realización, uno, dos, tres o cuatro, sustituyentes Q;
donde cada Q se selecciona independientemente del grupo consistente en (a) ciano, halo y nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo, y heterociclilo; y (c) -C(O)Re , -C(O)ORe , -C(O)NRfRg, -C(NRe)NRfRg, -ORe , -OC(O)Re, -OC(O)ORe , -OC(O)NRfRg, -OC(=NRe)NRfRg, -OS(O)Re, -OS(O)2Re , -OS(O)NRfRg, -OS(O)2 NRfRg, -NRfRg , -NReC(O)Rh, -NReC(O)ORh, -NReC(O)NRfRg , -NReC(=NRh)NRfRg, -NReS(O)Rh, -NReS(O)NRfRg , -SRe , -S(O)Re, y -S(O)NRfRg, donde cada Re, Rf, Rg y Rh es, independientemente, (i) hidrógeno; (ii) alquilo C1 -6 , alquenilo C2-6 , alquinilo C2-6, cicloalquilo C3 -7 , arilo C6 -14 , aralquilo C7 -15 , heteroarilo o heterociclilo; o (iii) Rf y Rg, junto con el átomo N al que se unen, forman heterociclilo.
También se proporciona en este documento un compuesto de la fórmula I:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato; donde:
R1 es hidrógeno, alquilo C1-6, -S-alquilo C1-6, -S(O)-alquilo C1-6, o -SO2-alquilo C1-6
R2 y R3 son cada uno, independientemente, (a) hidrógeno, ciano, halo, o nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo; o (c) -C(O)R1a, -C(O)OR1b, -C(O)NR1bR1c, -C(NRa)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c, o-S(O)2NR1bR1c;
R4 y R5 son cada uno, independientemente, hidrógeno o alquilo C1-6;
R6 es arilo C6-14, aralquilo C7-15, heteroarilo, o heteroaril-alquilo C1-6;
U es un enlace, -C(O)-, -C(O)O-, -C(O)NR1a-, -O-, -OC(O)O-, -OC(O)NR1a-, -NR1a-, -NR1aC(O)NR1d-, -NR1aS(O)-, -NR1aS(O)2-, -NR1aS(O)NR1d-, -NR1aS(O)2NR1d-, -S-, -S(O)-, o -S(O)2-;
X, Y y Z son N; y
cada R1 a , R1b , R1c y R1d es, independientemente, (i) hidrógeno; o (ii) alquilo C 1 -6 , alquenilo C2-6, alquinilo C2-6, cicloalquilo C3 -7 , arilo C6 -14 , aralquilo C7 -15 , heteroarilo o heterociclilo;
donde cada alquilo, alquenilo, alquinilo, cicloalquilo, arilo, aralquilo, heteroarilo, y heterociclilo se substituyen opcionalmente por uno o más grupos, cada uno seleccionado independientemente de (a) ciano, halo, y nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo, y heterociclilo, cada uno sustituido opcionalmente con uno o más, en una realización, uno, dos, tres, o cuatro, sustituyentes Q; y (c) -C(O)Ra , C(O)ORa , -C(O)NRbRc , -C(NRa)NRbRc, -Oa, -OC(O)Ra , -OC(O)ORa , -OC(O)NRbRc , -OC(=NRa)NRbRc, -OS(O)Ra , -OS(O)2Ra , -OS(O)NRbRc , -OS(O)2NRbRc, -NRbRc, -NRaC(O)Rd, -NRaC(O)Od, -NRaC(O)NRbRc, -NRaC(=NRd)NRbRc, -NRaS(O)Rd, -NRaS(O)NRbRc , -sR a , -S(O)Ra, y -S(O)NRbRc, donde cada Ra , Rb, Rc y Rd es, independientemente, (i) hidrógeno; (ii) alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, cicloalquilo C3.7 , arilo C6 -14, aralquilo C7 -15 , heteroarilo, o heterociclilo, cada uno opcionalmente sustituido por uno o más, en una realización, uno, dos, tres, o cuatro, sustituyentes Q; o (iii) Rb y Rc, junto con el átomo N al que se unen, forman heterociclilo, opcionalmente sustituidos por uno o más, en una realización, uno, dos, tres o cuatro, sustituyentes Q;
donde cada Q se selecciona independientemente del grupo consistente en (a) ciano, halo y nitro; (b) alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, cicloalquilo C3 -7 , arilo C6 -14 , aralquilo C7 -15 , heteroarilo, y heterociclilo; y (c) -C(O)Re , -C(O)ORe , -C(O)NRfRg, -C(NRe)NRfRg, -ORe , -OC(O)Re, -OC(O)ORe , -OC(O)NRfRg, -OC(=NRe)NRfRg, -OS(O)Re, -OS(O)2Re , -OS(O)NRfRg, -OS(O)2NRfRg, -NRfRg, -NReC(O)Rh, -NReC(O)ORh, -NReC(O)NRfRg, -NReC(=NRh)NRfRg, -NReS(O)Rh, -NReS(O)NRfRg, -SRe, -S(O)Re, y -S(O)NRfRg, donde cada Re, Rf, Rg y Rh es, independientemente, (i) hidrógeno; (ii) alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, cicloalquilo C3 -7 , arilo C6 -14, aralquilo C7 -15 heterociclilo; o (iii) Rf y Rg, junto con el átomo N al que se unen, forman heterociclilo.
A continuación se proporcionan composiciones farmacéuticas que comprenden un compuesto descrito en este documento, es decir, un compuesto de fórmula I, IA o IB, incluyendo un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereómeros; o su sal farmacéutica aceptable, solvato o hidrato; en combinación con uno o más vehículos farmacéuticos aceptables.
Adicionalmente se proporcionan en este documento compuestos para el uso en un método para tratar, prevenir, o aliviar uno o más síntomas de un trastorno, enfermedad o afección mediada por PI3K en un sujeto, que comprende administrar al sujeto una cantidad terapéuticamente efectiva de un compuesto descrito en este documento; es decir, un compuesto de fórmula I, IA o IB, un enantiómero, una mezcla de enantiómeros, una mezcla de dos o más diastereómeros; o sus sales farmacéuticas aceptables, solvatos, o hidratos.
Los compuestos proporcionados en este documento se pueden utilizar en un método para modular la actividad PI3K, que comprende poner en contacto un PI3K con una cantidad terapéuticamente efectiva de un compuesto descrito en este documento, por ejemplo, un compuesto de fórmula I, IA o IB, incluyendo un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereómeros; o sus sales farmacéuticas aceptables, solvatos, o hidratos.
DESCRIPCIÓN DETALLADA
Para facilitar la comprensión de la descripción que se expone en este documento, se definen a continuación una serie de términos.
Por lo general, la nomenclatura utilizada en el presente documento y los procedimientos de laboratorio en química orgánica, química medicinal y farmacología descritos en este documento son muy conocidos y comúnmente empleados en la técnica. A menos que se defina lo contrario, todos los términos técnicos y científicos utilizados en este documento generalmente tienen el mismo significado que se entiende comúnmente por cualquier experto ordinario al que pertenece esta descripción.
El término "sujeto" se refiere a un animal, incluyendo, entre otros, un primate (por ejemplo humano), vaca, cerdo, oveja, cabra, caballo, perro, gato, conejo, rata o ratón. Los términos "sujeto" y "paciente" se utilizan indistintamente en este documento en referencia, por ejemplo, a un sujeto mamífero, como un sujeto humano; en una realización, un ser humano.
Las expresiones "tratar", "que trata" y "tratamiento" están destinados a incluir aliviar o eliminar un trastorno, enfermedad o afección, o uno o más de los síntomas asociados con el trastorno, enfermedad o afección; o aliviar o erradicar la(s) causa(s) del propio desorden, enfermedad o condición.
Las expresiones "prevenir", "que previene" y "prevención" están destinados a incluir un método para retrasar y/o excluir la aparición de un trastorno, enfermedad o afección, y/o sus síntomas acompañantes; salvo que el sujeto adquiera el trastorno, enfermedad o condición; o reducir el riesgo de que un sujeto adquiera un trastorno, enfermedad o afección.
La expresión "cantidad terapéuticamente efectiva" pretende incluir la cantidad de un compuesto que, cuando se administra, es suficiente para prevenir el desarrollo de uno o más de los síntomas del trastorno, enfermedad o afección que se está tratando o aliviarlo, en cierta medida. La expresión "cantidad terapéuticamente efectiva" también se refiere a la cantidad de un compuesto suficiente para provocar la respuesta biológica o médica de una molécula biológica
(por ejemplo una proteína, enzima, ARN o ADN), célula, tejido, sistema, animal o humano, que está siendo buscada por los investigadores, veterinarios, médicos o personal clínico.
La expresión "vehículo farmacéuticamente aceptable", "excipiente farmacéuticamente aceptable", "vehículo fisiológicamente aceptable" o "excipiente fisiológicamente aceptable" se refiere a un material, composición o vehículo farmacéuticamente aceptable como un relleno líquido o sólido, diluyente, disolvente o material encapsulante. En una realización, cada componente es "farmacéuticamente aceptable" en el sentido de ser compatible con los otros
ingredientes de una formulación farmacéutica, y adecuado para su uso en contacto con el tejido o el órgano de seres humanos y de animales sin excesiva toxicidad, irritación, respuesta alérgica, inmunogenicidad u otros problemas o complicaciones, en consonancia con una relación beneficio/riesgo razonable. Ver Remington: The Science and Practice of Pharmacy, 21a edición, Lippincott Williams & Wilkins: Filadelfia, PA, 2005; Handbook of Pharmaceutical Excipients, 5a edición, Rowe et al., eds., The Pharmaceutical Press and the American Pharmaceutical Association: 2005; y Handbook of Pharmaceutical Additives, 3a edición, Ash and Ash eds., Editorial Gower: 2007; Pharmaceutical Preformulation and Formulation, 2a edición, Gibson Ed., CRC Press LLC: Boca Raton, FL, 2009.
La expresión "alrededor de" o "aproximadamente" significa un error aceptable para un valor particular determinado por cualquier experto ordinario, que depende en parte de cómo se mide o se determina el valor. En ciertas realizaciones, la expresión "alrededor de" o "aproximadamente" significa dentro de 1, 2, 3 ó 4 desviaciones estándar. En ciertas realizaciones, el término "aproximadamente" o "aproximado" significa dentro del 50%, 20%, 15%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1%, 0,5%, o 0,05% de un valor o intervalo determinado.
Las expresiones "ingrediente activo" y "sustancia activa" se refieren a un compuesto, que se administra, solo o en combinación con uno o más excipientes farmacéuticos aceptables, a un sujeto para tratar, prevenir o aliviar uno o más síntomas de un afección, trastorno o enfermedad. Como se utiliza en este documento, "ingrediente activo" y "sustancia activa" puede ser un isómero ópticamente activo de un compuesto descrito en este documento.
Las expresiones "fármaco", "agente terapéutico" y "agente quimioterapéutico" se refieren a un compuesto, o a sus composiciones farmacéuticas, que se administra a un sujeto para tratar, prevenir o aliviar uno o más síntomas de una afección, trastorno o enfermedad.
El término "PI3K" se refiere a una fosfoinositida 3-quinasa o su mutante, que es capaz de fosforilar el anillo de inositol de PI en la posición D-3. La expresión "mutante PI3K" pretende incluir proteínas sustancialmente homólogas a un PI3K nativo; es decir, proteínas que tienen una o más deleciones, inserciones o sustituciones de aminoácidos naturales o no naturales (por ejemplo, derivados, homólogos y fragmentos de PI3K), en comparación con la secuencia de aminoácidos de un PI3K natural. La secuencia de aminoácidos de un mutante PI3K es, al menos, aproximadamente 80% idéntico, al menos aproximadamente 90% idéntico, o al menos aproximadamente 95% idéntico a un PI3K natural. Los ejemplos de PI3K incluyen, entre otros, p110a, p110p, p1108, p110Y, PI3K-C2a, PI3K-C2p, PI3K-C2y, Vps34, mToR, ATM, ATR, y DNA-PK. Ver Fry, Biochem. Biophys. Acta 1994, 1226, 237-268; Vanhaesebroeck y Waterfield, Exp. Cell. Res. 1999, 253, 239-254; y Fry, Breast Cancer Res. 2001,3, 304-312. Las PI3K se clasifican en al menos tres clases. La clase I incluye p110a, p110p, p1105 y p110Y. La clase II incluye PI3K-C2a, PI3K-C2p y PI3K-C2y. La clase III incluye Vps34. La clase IV incluye mTOR, ATM, ATR y DNA-PK. En ciertas realizaciones, el PI3K es una quinasa de clase I. En ciertas realizaciones, el PI3K es p110a, p110p, p1105, o p110Y. En ciertas realizaciones, el PI3K es un mutante de una quinasa de la clase I. En ciertas realizaciones, el PI3K es un mutante p110a. Los ejemplos de mutantes p110a incluyen, entre otros, R38H, G106V, K111N, K227E, N345K, C420R, P539R, E542K, E545A, E545G, E545K, Q546K, Q546P, E453Q, H710P, I800L, T1025S, M1043I, M1043V, H1047L, H1047R y H1047Y (Ikenoue et al., Cancer Res. 2005, 65, 4562-4567; Gymnopoulos et al., Proc. Natl. Acad. Sci., 2007, 104, 5569-5574). En ciertas realizaciones, el PI3K es una quinasa de clase II. En ciertas realizaciones, el PI3K es PI3K-C2a, PI3K-C2p, o PI3K-C2y. En ciertas realizaciones, el PI3K es una quinasa de clase III. En ciertas realizaciones, el PI3K es Vps34. En ciertas realizaciones, el PI3K es una quinasa de clase IV. En ciertas realizaciones, el PI3K es mTOR, ATM, ATR, o DNA-PK.
Las expresiones "trastorno o enfermedad mediada por PI3K" y "una afección, trastorno o enfermedad mediada por PI3K" se refieren a una afección, trastorno o enfermedad caracterizada, por ejemplo, por una actividad PI3K menor o mayor que lo normal. La actividad funcional de PI3K inadecuada puede surgir como resultado de la expresión PI3K en las células que normalmente no expresan PI3K, aumento de la expresión de PI3K o grado de activación intracelular; o disminución de la expresión PI3K. Una afección, trastorno o enfermedad mediada por PI3K puede estar mediada total o parcialmente por una actividad PI3K inadecuada. En particular, una condición, trastorno o enfermedad mediada por PI3K es aquella en la que la modulación de una actividad enzimática PI3K produce algún efecto sobre la afección o trastorno subyacente; por ejemplo, un inhibidor de PI3K da como resultado una mejoría en, al menos, algunos de los pacientes tratados.
El término "alquilo" se refiere a un radical hidrocarburo monovalente saturado, lineal o ramificado. Como se utiliza en este documento, el término "alquilo" abarca tanto alquilo lineal como ramificado, a menos que se especifique lo contrario. Por ejemplo, alquilo C1-6 se refiere a un radical hidrocarburo monovalente, saturado, lineal de 1 a 6 átomos de carbono o de un radical hidrocarburo monovalente, saturado, ramificado de 3 a 6 átomos de carbono. En ciertas realizaciones, el alquilo es un radical hidrocarburo monovalente, saturado, lineal que tiene de 1 a 20 (C1-20), de 1 a 15 (C1 - 15 ), de 1 a 10 (C1 -10 ), o de 1 a 6 (C1 -6 ) átomos de carbono, o radicales de hidrocarburo monovalentes, saturados y ramificados de 3 a 20 (C3-20), de 3 a 15 (C3 -15 ), de 3 a 10 (C3 -10 ), o de 3 a 6 (C3-6) átomos de carbono. Como se usa en este documento, los grupos alquilo lineales C1-6 y ramificados C3-6 también se denominan "alquilos inferiores". Ejemplos de grupos alquilos incluyen, entre otros, metilo, etilo, propilo (incluyendo todas las formas isoméricas, p. ej., n-propilo y 2-propil), butilo (incluyendo todas las formas isoméricas, por ejemplo, n-butilo, 2-metilpropilo (isobutil), 1-metilpropilo (sec-butil) y 1,1 -dimetiletilo (f-butil)), pentilo (incluyendo todas las formas isoméricas, por ejemplo, npropilo, 2-metilbutilo (isopropil), y 2,2-dimetilpropilo (neopentil)), hexilo (incluyendo todas las formas isoméricas, nhexilo, 2-metilpentilo (isohexil), 3-metilpentilo, 2,3-dimetilbutilo y 2,2-dimetilbutilo (neohexil)), heptilo (incluyendo todas las formas isoméricas, por ejemplo, n-heptilo, 2-metilhexilo, 3-metilhexilo, 2,2-dimetilpentilo, 2,3-dimetilpentilo, 2,4-dimetilpentilo, 3-etilpentilo, y 2,2,3-trimetilbutil), octilo (incluyendo todas las formas isoméricas, p. ej., n-octilo, 2-metilheptilo, 3-metilheptilo, 2,5-dimetilhexilo, y 2,2,4-trimetilpentilo (isooctil)), nonilo (incluyendo todas las formas isoméricas, por ejemplo, n-nonil), decilo (incluyendo todas las formas isoméricas, p. ej., n-decil), undecilo (incluyendo todas las formas isoméricas, p. ej., n-undecil), dodecilo (incluyendo todas las formas isoméricas, p. ej., n-dodecil), tridecilo (incluyendo todas las formas isoméricas, p. ej., n-tridecil), tetradecilo (incluyendo todas las formas isoméricas, p. ej., n-tetradecil), pentadecilo (incluyendo todas las formas isoméricas, por ejemplo, n-pentadecil), hexadecilo (incluyendo todas las formas isoméricas, p. ej., n-hexadecilo (palmitil)), heptadecilo (incluyendo todas las formas isoméricas, p. ej., n-heptadecil), octadecilo (incluyendo todas las formas isoméricas, por ejemplo, n-octadecilo (estearil)), nonadecilo (incluyendo todas las formas isoméricas, por ejemplo, n-nonadecil), e icosilo (incluyendo todas las formas isoméricas, p. ej., n-icosil).
El término "alquileno" se refiere a un radical hidrocarburo divalente, saturado, lineal o ramificado, donde el alquileno puede sustituirse opcionalmente como se describe en este documento. Por ejemplo, alquileno C1-6 se refiere a un radical divalente, saturado, lineal de hidrocarburo de 1 a 6 átomos de carbono o un radical divalente, saturado, ramificado de hidrocarburo de 3 a 6 átomos de carbono. En ciertas realizaciones, el alquileno es un radical hidrocarburo divalente, saturado, lineal que tiene de 1 a 20 (C1 -20 ), de 1 a 15 (C1 - 15 ), de 1 a 10 (C1 -10 ), o de 1 a 6 (C1 -6 ) átomos de carbono, o radicales de hidrocarburos divalentes, saturados, ramificados de 3 a 20 (C3-20), de 3 a 15 (C3 -15 ), de 3 a 10 (C3 -10 ), o de 3 a 6 (C3-6) átomos de carbono. Como se usa en este documento, los grupos alquileno lineal C1-6 y ramificado C3-6 también se denominan "alquileno inferior". Ejemplos de grupos de alquileno incluyen, entre otros, metileno, etileno, propileno (incluyendo todas las formas isoméricas), n-propileno, isopropileno, butileno (incluyendo todas las formas isoméricas), n-butileno, isobutileno, f-butileno, pentileno (incluyendo todas las formas isoméricas), y hexileno (incluyendo todas las formas isoméricas).
El término "heteroalquileno" se refiere a un radical hidrocarburo divalente, saturado, lineal o ramificado que contiene uno o más heteroátomos seleccionados independientemente de O, S y N en la cadena de hidrocarburos. Por ejemplo, el heteroalquileno C1-6 se refiere a un radical divalente, saturado, lineal de hidrocarburo de 1 a 6 átomos de carbono o a un radical divalente, saturado, ramificado de hidrocarburo de 3 a 6 átomos de carbono. En ciertas realizaciones, el heteroalquileno es un radical hidrocarburo divalente, saturado, lineal que tiene de 1 a 20 (C1 -20 ), de 1 a 15 (C1 - 15 ), de 1 a 10 (C1 -10 ), o de 1 a 6 (C1 -6 ) átomos de carbono, o radicales de hidrocarburos divalentes, saturados, ramificados de 3 a 20 (C3-20), de 3 a 15 (C3 -15 ), de 3 a 10 (C3 -10 ), o de 3 a 6 (C3-6) átomos de carbono. Como se usa en este documento, los grupos heteroalquileno lineales C1-6 y ramificados C3-6 también se denominan "heteroalquileno inferior". Los ejemplos de grupos heteroalquileno incluyen, entre otros, -CH2O-, -CH2OCH2-, -CH2CH2O-, -CH2 NH-, -CH2 NHCH2-, -CH2CH2 NH-, -CH2S-, -CH2SCH2-, y-CH2CH2S-. En ciertas realizaciones, el heteroalquileno puede también ser substituido, opcionalmente, según lo descrito en este documento.
El término "alquenilo" se refiere a un radical hidrocarburo monovalente, lineal o ramificado, que contiene un doble enlace. El término "alquenilo" también abarca a los radicales que tiene configuraciones cis y trans o, alternativamente, configuraciones "Z" y "E", según lo apreciado por los expertos ordinarios en la técnica. Como se utiliza en este documento, el término "alquenilo" abarca tanto alquenilo lineal como ramificado, a menos que se especifique lo contrario. Por ejemplo, alquenilo C2-6 se refiere a un radical hidrocarburo monovalente, lineal no saturado de 2 a 6 átomos de carbono o un radical hidrocarburo monovalente, no saturado, ramificado de 3 a 6 átomos de carbono. En ciertas realizaciones, el alquenilo es un radical monovalente, lineal de hidrocarburo de 2 a 20 (C2-20), de 2 a 15 (C2 -15 ), de 2 a 10 (C2 -10 ), o de 2 a 6 (C2-6) átomos de carbono, o un radical hidrocarburo monovalente, ramificado de 3 a 20 (C3-20), de 3 a 15 (C3 -15 ), de 3 a 10 (C3 -10 ), o de 3 a 6 (C3-6) átomos de carbono. Los ejemplos de los grupos alquenilo incluyen, entre otros, etenilo, propen-1-ilo, propen-2-ilo, alilo, butenilo, y 4-metilbutenilo.
El término "alquenileno" se refiere a un radical hidrocarburo divalente, lineal o ramificado, que contiene un doble enlace. El término "alquenileno" abarca a los radicales con configuración cis o trans o sus mezclas o, alternativamente, una configuración "Z" o "E" o sus mezclas, según lo apreciado por los expertos ordinarios en la técnica. Por ejemplo, alquenileno C2-6 se refiere a un radical hidrocarburo divalente, no saturado, lineal de 2 a 6 átomos de carbono o un radical hidrocarburo divalente, no saturado, ramificado de 3 a 6 átomos de carbono. En ciertas realizaciones, el alquenileno es un radical divalente de hidrocarburo lineal de 2 a 20 (C2-20), de 2 a 15 (C2 -15 ), de 2 a 10 (C2 -10 ), o de 2 a 6 (C2-6) átomos de carbono, o un radical hidrocarburo divalente ramificado de 3 a 20 (C3-20), de 3 a 15 (C3 -15 ), de 3 a 10 (C3 -10 ), o de 3 a 6 (C3-6) átomos de carbono. Los ejemplos de los grupos alquenileno incluyen, entre otros, el etenileno, alileno, propenileno, butenileno, y 4-metilbutenileno.
El término "heteroalquenileno" se refiere a un radical hidrocarburo divalente, lineal o ramificado, que contiene un doble enlace carbono-carbono, y que contiene uno o más heteroátomos cada uno independientemente seleccionado de O, S, y N en la cadena de hidrocarburos. El término "heteroalquenileno" abarca a los radicales con configuración cis o trans o sus mezclas o, alternativamente, una configuración "Z" o "E" o sus mezclas, según lo apreciado por los expertos ordinarios en la técnica. Por ejemplo, heteroalquenileno C2-6 se refiere a un radical hidrocarburo divalente, no saturado, lineal de 2 a 6 átomos de carbono o un radical hidrocarburo divalente, no saturado, ramificado de 3 a 6 átomos de carbono. En ciertas realizaciones, el heteroalquenileno es un radical divalente, lineal de hidrocarburo de 2 a 20 (C2-20), de 2 a 15 (C2 -15 ), de 2 a 10 (C2 -10 ), o de 2 a 6 (C2-6) átomos de carbono, o un radical hidrocarburo divalente
ramificado de 3 a 20 (C3-20), de 3 a 15 (C3 -15 ), de 3 a 10 (C3 -10 ), o de 3 a 6 (C3-6) átomos de carbono. Los ejemplos de grupos del heteroalquenileno incluyen, entre otros, -CH=Ch O-, -CH=CHOCH2-, -CH=CHCH2O-, -CH=CHS-, -CH=CHSCH2-, -CH=CHCH2S-, o -CH=CHCH2NH-.
El término "alquinilo" se refiere a un radical hidrocarburo monovalente, lineal o ramificado, que contiene un triple enlace. El término "alquinilo" también abarca el alquinilo lineal y ramificado, a menos que esté especificado de otra manera. En ciertas realizaciones, el alquinilo es un radical monovalente, lineal de hidrocarburo de 2 a 20 (C2-20), de 2 a 15 (C2 -15 ), de 2 a 10 (C2 -10 ), o de 2 a 6 (C2-6) átomos de carbono, o un radical hidrocarburo monovalente, ramificado de 3 a 20 (C3-20), de 3 a 15 (C3 -15 ), de 3 a 10 (C3 -10 ), o de 3 a 6 (C3-6) átomos de carbono. Los ejemplos de grupos alquinilo incluyen, entre otros, etinilo (-C=H) y propargilo (-CH2CECH). Por ejemplo, alquinilo C2-6 se refiere a un radical monovalente, lineal no saturado de hidrocarburo de 2 a 6 átomos de carbono o un radical hidrocarburo no saturado monovalente, ramificado de 3 a 6 átomos de carbono.
El término "cicloalquilo" se refiere a un radical hidrocarburo, monovalente, saturado, cíclico. En ciertas realizaciones, el cicloalquilo tiene de 3 a 20 (C3-20), de 3 a 15 (C3 -15 ), de 3 a 10 (C3 -10 ), o de 3 a 7 (C3-7) átomos de carbono. Los ejemplos de grupos cicloalquilo incluyen, entre otros, ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo, cicloheptilo, y decalinilo.
El término "arilo" se refiere a un grupo aromático monocíclico y/o grupo aromático monovalente multicíclico que contiene al menos un anillo aromático de hidrocarburos. En ciertas realizaciones, el arilo tiene de 6 a 20 (C6-20), de 6 a 15 (C6 -15), o de 6 a 10 (C6 -10) átomos de anillo. Los ejemplos de grupos arilo incluyen, entre otros, fenilo, naftilo, fluorenilo, azulenilo, antrilo, fenantrilo, pirenilo, bifenilo, y terfenilo. Arilo también se refiere a los anillos de carbono bicíclicos o tricíclicos, donde uno de los anillos es aromático y cuyos otros pueden ser saturados, parcialmente insaturados, o aromáticos, por ejemplo, dihidronaftilo, indenilo, indanilo, o tetrahidronaftilo (tetralinil).
El término "aralquilo" o "aril-alquilo" se refiere a un grupo alquilo monovalente sustituido por arilo.
El término "heteroarilo" se refiere a un grupo aromático monocíclico y/o grupo aromático multicíclico que contienen al menos un anillo aromático, donde al menos un anillo aromático contiene uno o más heteroátomos seleccionados independientemente de O, S y N. Cada anillo de un grupo heteroarilo puede contener uno o dos átomos de O, uno o dos átomos de S, y/o de uno a cuatro átomos de N, siempre que el número total de heteroátomos en cada anillo sea cuatro o menos y cada anillo contiene al menos un átomo de carbono. En ciertas realizaciones, el heteroarilo tiene de 5 a 20, de 5 a 15, o de 5 a 10 átomos de anillo. Ejemplos de grupos heteroarilo monocíclicos incluyen, entre otros, furanilo, imidazolilo, isotiazolilo, isoxazolilo, oxadiazolilo, oxadiazolilo, oxazolilo, pirazinilo, pirazolilo, piridazinilo, piridilo, pirimidinilo, pirrolilo, tiadiazolilo, tiazolilo, tienilo, tetrazolilo, triazinilo y triazolilo. Ejemplos de grupos heteroarilo bicíclicos incluyen, entre otros, benzofuranilo, bencimidazolilo, benzoisoxazolilo, benzopiranilo, benzotiadiazolilo, benzotiazolilo, benzotienilo, benzotiofenilo, benzotriazolilo, benzoxazolilo, furopiridilo, imidazopiridinilo, imidazotiazolilo, indolizinilo, indolilo, indazolilo, isobenzofuranilo, isobenzotienilo, isoindolilo, isoquinolinilo, isotiazolilo, naftiridinilo, oxazolopiridinilo, ftalazinilo, pteridinilo, purinilo, piridopiridilo, pirrolopiridilo, quinolinilo, quinoxalinilo, quinazolinilo, tiadiazolopirimidilo, y tienopiridilo. Los ejemplos de grupos heteroarilo tricíclicos incluyen, entre otros, acridinilo, bencindolilo, carbazolilo, dibenzofuranilo, perimidinilo, fenantrolinilo, fenantridinilo, fenarsazinilo, fenazinilo, fenotiazinilo, fenoxazinilo, y xantenilo.
El término "heterociclilo" o "heterocíclico" se refiere a un sistema monocíclico de anillo no aromático y/o sistema de anillo multicíclico que contiene al menos un anillo no aromático, en el que uno o más de los átomos de anillo no aromáticos son heteroátomos seleccionados independientemente de O, S, o N; y los átomos de anillo restantes son átomos de carbono. En ciertas realizaciones, el grupo heterociclilo o heterocíclico tiene de 3 a 20, de 3 a 15, de 3 a 10, de 3 a 8, de 4 a 7, o de 5 a 6 átomos de anillo. En ciertas realizaciones, el heterociclilo es un sistema de anillo monocíclico, bicíclico, tricíclico o tetracíclico, que puede incluir un sistema de anillo fusionado o puenteado, y en el que los átomos de nitrógeno o azufre pueden ser opcionalmente oxidados, los átomos de nitrógeno pueden ser opcionalmente cuaternizados, y algunos anillos pueden estar, parcialmente o completamente, saturados, o ser aromáticos. El heterociclilo se puede unir a la estructura principal en cualquier heteroátomo o átomo de carbono que resulte en la creación de un compuesto estable. Los ejemplos de tales radicales heterocíclicos incluyen, entre otros, azepinilo, benzodioxanilo, benzodioxolilo, benzofuranonilo, benzopiranonilo, benzopiranilo, benzotetrahidrofuranilo, benzotetrahidrotienilo, benzotiopiranilo, benzoxazinilo, p-carbolinilo, cromanilo, cromonilo, cinnolinilo, coumarinilo, decahidroisoquinolinilo, dihidrobencisotiazinilo, dihidrobencisoxazinilo, dihidrofurilo, dihidroisoindolilo, dihidropiranilo, dihidropirazolilo, dihidropirazinilo, dihidropiridinilo, dihidropirimidinilo, dihidropirrolilo, dioxolanilo, 1,4-ditianilo, furanonilo, imidazolidinilo, imidazolinilo, indolinilo, isobenzotetrahidrofuranilo, isobenzotetrahidrotienilo, isocromanilo, isocoumarinilo, isoindolinilo, isotiazolidinilo, isoxazolidinilo, morfolinilo, octahidroindolilo, octahidroisoindolilo, oxazolidinonilo, oxazolidinilo, oxiranilo, piperazinilo, piperidinilo, 4-piperidonilo, pirazolidinilo, pirazolinilo, pirrolidinilo, pirrolinilo, quinuclidinilo, tetrahidrofurilo, tetrahidroisoquinolinilo, tetrahidropiranilo, tetrahidrotienilo, tiamorfolinilo, tiazolidinilo, tetrahidroquinolinilo, y 1,3,5-tritianilo.
El término "halógeno", "haluro" o "halo" se refiere a flúor, cloro, bromo y/o yodo.
En una realización, cada Q se selecciona independientemente del grupo que consiste en (a) ciano, halo, y nitro; y (b) alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6 -14 , aralquilo C7 -15 , heteroarilo, y heterociclilo; y (c) C(O)Re , -C(O)ORe, -C(O)NRfRg, -C(NRe)NRfRg, -ORe, -OC(O)Re , -OC(O)ORe, -OC(O)NRfRg, -OC(=NRe)NRfRg, -OS(O)Re , -OS(O)2 Re , -OS(O)NRfRg , -OS(O)2 NRfRg , -NRfRg , -NReC(O)Rh, -NReC(O)ORh, -NReC(O)NRfRg , -NReC(=NRh)NRfRg , -NReS(O)Rh, -NReS(O)2 Rh, -NReS(O)NRfRg, -NReS(O)2 NRfRg, -SRe, -S(O)Re , -S(O)2 Re , -S(O)NRfRg, y-S(O)2 NRfRg; donde cada Re , Rf, Rg y Rh es, independientemente, (i) hidrógeno; (ii) alquilo C i -6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo; o (iii) Rf y Rg , junto con el N átomo al cual se unen, forman heteroarilo o heterociclilo.
En ciertas realizaciones, "ópticamente activo" y "enantioméricamente activo" se refieren a una colección de moléculas, que tiene un exceso enantiomérico de no menos de aproximadamente 50%, no menos de aproximadamente el 70%, no menos de aproximadamente 80%, no menos de aproximadamente 90%, no menos de aproximadamente 91%, no menos de aproximadamente 92%, no menos de aproximadamente 93%, no menos de aproximadamente 94%, no menos de aproximadamente 95%, no menos de aproximadamente 96%, no menos de aproximadamente 97%, no menos de aproximadamente 98%, no menos de aproximadamente 99%, no menos de aproximadamente 99,5%, o no menos de aproximadamente 99,8%. En ciertas realizaciones, el compuesto comprende aproximadamente 95% o más del enantiómero deseado y aproximadamente el 5% o menos del enantiómero menos preferido basado en el peso total del racemato en cuestión.
En la descripción de un compuesto ópticamente activo, los prefijos R y S se utilizan para denotar la configuración absoluta de la molécula sobre su(s) centro(s) quiral(es). Los (+) y (-) se utilizan para denotar la rotación óptica del compuesto, es decir, la dirección en la que un plano de luz polarizada es desplazado por el compuesto ópticamente activo. El prefijo (-) indica que el compuesto es levorotatorio, es decir, el compuesto desvía el plano de la luz polarizada a la izquierda o en sentido antihorario. El prefijo (+) indica que el compuesto es dextrorotatorio, es decir, el compuesto desplaza el plano de la luz polarizada a la derecha o en sentido horario. Sin embargo, el signo de rotación óptica, (+) y (-), no está relacionado con la configuración absoluta de la molécula, R y S.
El término "solvato" se refiere a un compuesto provisto en el presente o a una sal del mismo, que incluye además una cantidad estequiométrica o no estequiométrica de disolvente unida por fuerzas intermoleculares no covalentes. Cuando el disolvente es agua, el solvato es un hidrato.
La frase "un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato" tiene el mismo significado que la frase "un solo enantiómero, una mezcla de enantiómeros, o una mezcla de diastereoisómeros del compuesto referenciado en él; o una sal, solvato, o hidrato farmacéuticamente aceptable del compuesto referido en éste, o un enantiómero, una mezcla de enantiómeros, o una mezcla de diastereoisómeros del compuesto referido en éste". Compuestos
En una realización, en este documento se incluye un compuesto de la fórmula I, IA o IB:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato; donde:
cada R1 es independientemente hidrógeno, alquilo C i -6, -S-alquilo C i -6, -S(O)-alquilo C i -6, o -SO2-alquilo C i -6;
cada R2 y R3 son, independientemente, (a) hidrógeno, ciano, halo o nitro; (b) alquilo C 1-6 , alquenilo C2-6, alquinilo C2-6, cicloalquilo C3 -7 , arilo C6 -14 , aralquilo C7 -15 , heteroarilo o heterociclilo; o (c) -C(O)R1a , -C(O)OR1b , -C(O)NR1bR1 c , -C(NRa)NR1b R1 c , -OR 1a , -OC(O)R1 a , -OC(O)OR1 a , -OC(O)NR1bR1 c , -OC(=NR1a)NR1b R1 c , -OS(O)R1a , -OS(O)2 R1a , -OS(O)NR1b R1 c , -OS(O)2NR1b R1 c , -NR1b R1 c , -NR1aC(O)R1d , -NR1aC(O)OR1d , -NR1aC(O)NR1bR1 c , -NR1aC(=NR1d)NR1b R1 c , -NR1aS(O)R1d , -NR1aS(O)2 R1d , -NR1aS(O)NR1bR1 c , -NR1aS(O)2NR1bR1 c , -SR1a , -S(O)R1a , -S(O)2 R1a , -S(O)NR1bR1 c , o-S(O)2 NR1b R1 c ;
cada R4 y R5 es independientemente hidrógeno o alquilo C 1-6 o R4 y R5 se unen para formar un enlace, alquileno C 1 -6 , heteroalquileno C1 -6 , alquenileno C2-6 , o heteroalquenileno C2-6;
cada R6 es independientemente arilo C6-14, aralquilo C7-15, heteroarilo, o heteroaril-alquilo C1-6;
cada U es independientemente un enlace, -C(O)-, -C(O)O-, -C(O)NR1a-, -O-, -OC(O)O-, -OC(O)NR1a-, -NR1a-, -NR1aC(O)NR1d-, -NR1aS(O)-, -NR1aS(O)2-, -NR1a S(O)NR1d-, -NR1aS(O)2 NR1d-, -S-, -S(O)-, o -S(O)2-;
cada X, Y y Z es N; y
cada A, B, D, y E es independientemente un enlace C, O, N, S, NR9CR9 o CR9 R10, donde cada R9 y R10 es independientemente hidrógeno, halo, alquilo C1-6, alquenilo C2-6, o alquinilo C2-6; donde los enlaces entre A, B, D y E pueden ser saturados o insaturados; con la condición de que no más de uno de A, B, D y E sean un enlace;
cada R1 a , R1b , R1c y R1d es, independientemente, (i) hidrógeno; o (ii) alquilo C 1 -6 , alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6 -14 , aralquilo C7 -15 , heteroarilo o heterociclilo;
en donde cada alquilo, alquileno, heteroalquileno, alquenilo, alquenileno, heteroalquenileno, alquinilo, cicloalquilo, arilo, aralquilo, heteroarilo, y heterociclilo en R1, R2 , R3, R4 , R5 , R6, R9 , R10, R1 a , R1b , R1c o R1d se sustituye opcionalmente por uno o más, en una realización, uno, dos, tres o cuatro grupos, cada uno seleccionado independientemente de (a) ciano, halo y nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo, y heterociclilo, cada uno de los cuales se sustituye opcionalmente con uno o más, en una realización, uno, dos, tres, o cuatro sustituyentes Q; y (c) -C(O)Ra , -C(O)ORa , -C(O)NRbRc , -C(NRa)NRbRc , -ORa , -OC(O)Ra , -OC(O)ORa , -OC(O)NRbRc , -OC(=NRa)NRbRc , -OS(O)Ra , -OS(O)2 Ra , -OS(O)NRbRc , -OS(O)2 NRbRc , -NRbRc , -NRaC(O)Rd, -NRaC(O)ORd, -NRaC(O)NRbRc , -NRaC(=NRd)NRbRc , -NRaS(O)Rd, -NRaS(O)NRbRc , -SRa , -S(O)Ra , y-S(O)NRbRc , donde cada Ra , Rb, Rc y Rd es, independientemente, (i) hidrógeno; (ii) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo, o heterociclilo, cada uno opcionalmente sustituido por uno o más, en una realización, uno, dos, tres, o cuatro, sustituyentes Q; o (iii) Rb y Rc , junto con el átomo N al que se unen, forman heterociclilo, opcionalmente sustituidos por uno o más, en una realización, uno, dos, tres, o cuatro, sustituyentes Q;
donde cada Q se selecciona independientemente del grupo consistente en (a) ciano, halo y nitro; (b) alquilo C 1 -6 , alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo, y heterociclilo; y (c) -C(O)Re , -C(O)ORe , -C(O)NRfRg, -C(NRe)NRfRg, -ORe , -OC(O)Re, -OC(O)ORe , -OC(O)NRfRg , -OC(=NRe)NRfRg, -OS(O)Re, -OS(O)2 Re , -OS(O)NRfRg, -OS(O)2 NRfRg, -NRfRg, -NReC(O)Rh, -NReC(O)ORh, -NReC(O)NRfRg , -NReC(=NRh)NRfRg, -NReS(O)Rh, -NReS(O)NRfRg , -SRe, -S(O)Re, y -S(O)NRfRg, donde cada Re, Rf, Rg y Rh es, independientemente, (i)
hidrógeno; (ii) alquilo C i-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-i4, aralquilo C7-i5, heteroarilo o heterociclilo; o (iii) Rf y Rg, junto con el átomo N al que se unen, forman heterociclilo.
En otra realización, en este documento se incluye un compuesto de la fórmula I:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato; donde:
R1 es hidrógeno, alquilo C1-6, -S-alquilo C1-6, -S(O)-alquilo C1.6 , o -SO2-alquilo C1-6;
R2 y R3 son cada uno, independientemente, (a) hidrógeno, ciano, halo, o nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo; o (c) -C(O)R1 a , -C(O)OR1b , -C(O)NR1bR1 c , -C(NRa)NR1bR1 c , -OR1 a , -OC(O)R1 a , -OC(O)OR1a , -OC(O)NR1b R1 c , -OC(=NR1a)NR1bR1 c , -OS(O)R1 a , -OS(O)2 R1a , -OS(O)NR1bR1 c , -OS(O)2NR1bR1 c , -NR1bR1 c , -NR1aC(O)R1d , -NR1aC(O)OR1d , -NR1aC(O)NR1b R1 c , -NR1aC(=NR1d)NR1b R1 c , -NR1aS(O)R1d , -NR1aS(O)2 R1d , -NR1aS(O)NR1bR1 c , -NR1aS(O)2NR1bR1 c , -SR1a , -S(O)R1a , -S(O)2 R1a , -S(O)NR1bR1 c , o-S(O)2 NR1bR1 c ;
R4 y R5 son cada uno, independientemente, hidrógeno o alquilo C1-6;
R6 es arilo C6-14, aralquilo C7-15, heteroarilo, o heteroaril-alquilo C1-6;
U es un enlace, -C(O)-, -C(O)O-, -C(O)NR1a-, -O-, -OC(O)O-, -OC(O)NR1a-, -NR1a-, -NR1aC(O)NR1d-, -NR1aS(O)-, -NR1aS(O)2-, -NR1aS(O)NR1d-, -NR1aS(O)2 NR1d-, -S-, -S(O)-, o -S(O)2-;
X, Y y Z son N; y
cada R1 a , R1b , R1c y R1d es, independientemente, (i) hidrógeno; o (ii) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo;
donde cada alquilo, alquenilo, alquinilo, cicloalquilo, arilo, aralquilo, heteroarilo, y heterociclilo se substituyen opcionalmente por uno o más grupos, cada uno seleccionado independientemente de (a) ciano, halo, y nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo, y heterociclilo, cada uno sustituido opcionalmente con uno o más, en una realización, uno, dos, tres, o cuatro, sustituyentes Q; y (c) -C(O)Ra , -C(O)ORa , -C(O)NRbRc , -C(NRa)NRbRc , -ORa , -OC(O)Ra , -OC(O)ORa , -OC(O)NRbRc , -OC(=NRa)NRbRc , -OS(O)Ra , -OS(O)2Ra , -OS(O)NRbRc , -OS(O)2NRbRc , -NRbRc , -NRaC(O)Rd , -NRaC(O)Od, -NRaC(O)NRbRc , -NRaC(=NRd)NRbRc , -NRas(o )R d, -NRaS(O)NRbRc , -SRa , -S(O)Ra , y -S(O)NRbRc , donde cada Ra , Rb, Rc y Rd es, independientemente, (i) hidrógeno; (ii) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo, o heterociclilo, cada uno opcionalmente sustituido por uno o más, en una realización, uno, dos, tres, o cuatro, sustituyentes Q; o (iii) Rb y Rc , junto con el átomo N al que se unen, forman heterociclilo, opcionalmente sustituidos por uno o más, en una realización, uno, dos, tres o cuatro, sustituyentes Q;
donde cada Q se selecciona independientemente del grupo consistente en (a) ciano, halo y nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo, y heterociclilo; y (c) -C(O)Re , -C(O)ORe , -C(O)NRfRg, -C(NRe)NRfRg, -ORe , -OC(O)Re, -OC(O)ORe , -OC(O)NRfRg, -OC(=NRe)NRfRg, -OS(O)Re, -OS(O)2Re , -OS(O)NRfRg, -OS(O)2 NRfRg, -NRfRg , -NReC(O)Rh, -NReC(O)ORh, -NReC(O)NRfRg , -NReC(=NRh)NRfRg, -NRes(o )R h, -NReS(O)NRfRg , -SRe , -S(O)Re, y -S(O)NRfRg, donde cada Re, Rf, Rg y Rh es, independientemente, (i) hidrógeno; (ii) alquilo C1 -6 , alquenilo C2-6 , alquinilo C2-6, cicloalquilo C3 -7 , arilo C6 -14 , aralquilo C7 -15 , heteroarilo o heterociclilo; o (iii) Rf y Rg, junto con el átomo N al que se unen, forman heterociclilo.
En otra realización más, se proporciona en este documento un compuesto de fórmula I, donde R1, R2, R3, R4, R5, R6, U, X, Y, y Z son cada uno como se define en este documento, con la condición de que cuando R6 es arilo C6-14 o heteroarilo, entonces U no es un enlace.
En otra realización más, se proporciona en este documento un compuesto de fórmula I, donde R1, R2, R3, R4, R5, R6, U, X, Y, y Z son cada uno como se define en este documento, con la condición de que cuando R2, R3, R4 y R5 son hidrógeno, U es un enlace, R6 no es fenilo sustituido.
En otra realización más, se proporciona en este documento un compuesto de fórmula I, donde R1, R2, R3, R4, R5, R6, U, X, Y, y Z son cada uno como se define en este documento, con la condición de que cuando R2, R3, R4 y R5 son hidrógeno, U es un enlace, R6 no es 3-piridinilo o 4-piridinilo sustituido.
En otra realización más, se proporciona en este documento un compuesto de fórmula I, donde R1, R2, R3, R4, R5, R6, U, X, Y y Z son cada uno como se define en este documento, con la condición de que cuando R2, R3, R4 y R5 son hidrógeno, U es un enlace, R6 no es 5-piridinilo sustituido.
En otra realización más, se proporciona en este documento un compuesto de fórmula I, donde R1, R2, R3, R4, R5, R6, U, X, Y, y Z son cada uno como se define en este documento, con la condición de que cuando R2, R4 y R5 son hidrógeno, U es un enlace, R6 no es 4-indolilo no sustituido.
En otra realización más, se proporciona en este documento un compuesto de fórmula I, donde R1, R2, R3, R4, R5, R6, U, X, Y, y Z son cada uno como se define en este documento, con la condición de que cuando R2, R4 y R5 son hidrógeno, U es un enlace, R6 no es fenilo, 3-piridinilo, 4-piridinilo, 5-pirimidinilo, o 4-indolilo.
En otra realización más, se proporciona en este documento un compuesto de fórmula I, donde R1, R2, R3, R4, R5, R6, U, X, Y, y Z son cada uno como se define en este documento, con la condición de que cuando R2, R4y R5 son hidrógeno, U es un enlace, R6 no es fenilo, piridinilo, pirimidinilo, o indolilo.
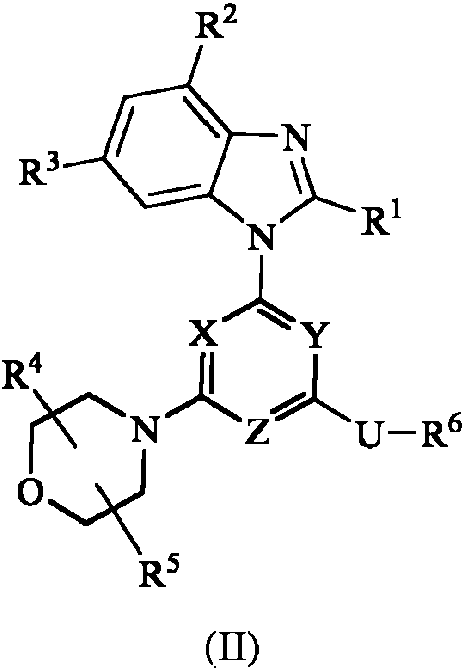
En otra realización, se incluye en este documento un compuesto de fórmula II:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato; donde R1, R2, R3, R4, R5, R6, U, X, Y y Z son cada uno como se definen en este documento.
En otra realización más, se proporciona en este documento un compuesto de fórmula II, en el que R1, R2, R3, R4, R5, R6, U, X, Y, y Z son cada uno como se define en este documento, con la condición de que cuando R6 es arilo C6-14 o heteroarilo, entonces U no es un enlace.
En otra realización más, se proporciona en este documento un compuesto de fórmula II, donde R1, R2, R3, R4, R5, R6, U, X, Y, y Z son cada uno como se define en este documento, con la condición de que cuando R2, R3, R4 y R5 son hidrógeno, U es un enlace, R6 no es fenilo sustituido.
En otra realización más, se proporciona en este documento un compuesto de fórmula II, donde R1, R2, R3, R4, R5, R6, U, X, Y, y Z son cada uno como se define en este documento, con la condición de que cuando R2, R3, R4 y R5 son hidrógeno, U es un enlace, R6 no es 3-piridinilo o 4-piridinilo sustituido.
En otra realización más, se proporciona en este documento un compuesto de fórmula II, donde R1, R2, R3, R4, R5, R6, U, X, Y, y Z son cada uno como se define en este documento, con la condición de que cuando R2, R3, R4 y R5 son hidrógeno, U es un enlace, R6 no es 5-piridinilo sustituido.
En otra realización más, se proporciona en este documento un compuesto de fórmula II, donde R1, R2, R3, R4, R5, R6, U, X, Y, y Z son cada uno como se define en este documento, con la condición de que cuando R2, R4 y R5 son hidrógeno, U es un enlace, R6 no es 4-indolilo no sustituido.
En otra realización más, se proporciona en este documento un compuesto de fórmula II, donde R1, R2, R3, R4, R5, R6, U, X, Y, y Z son cada uno como se define en este documento, con la condición de que cuando R2, R4 y R5 son hidrógeno, U es un enlace, R6 no es fenilo, 3-piridinilo, 4-piridinilo, 5-pirimidinilo, o 4-indolilo.
En otra realización más, se proporciona en este documento un compuesto de fórmula II, donde R1, R2, R3, R4, R5, R6, U, X, Y, y Z son cada uno como se define en este documento, con la condición de que cuando R2, R4 y R5 son hidrógeno, U es un enlace, R6 no es fenilo, piridinilo, pirimidinilo, o indolilo.
En otra realización más, se proporciona en este documento un compuesto de fórmula III:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato; donde:
R1, R2, R3, R4 , R5 , X, Y y Z son cada uno como se define en este documento;
U es-C(O)-, -C(O)O-, -C(O)NR1a-, -O-, -OC(O)O-, -OC(O)NR1a-, -NR1a-, -NR1aC(O)NR1d-, -NR1aS(O)-, -NR1aS(O)2-, -NR1aS(O)NR1d-, -NR1aS(O)2 NR1d-, -S-, -S(O)-, o -S(O)2-; y
R8 es (a) hidrógeno, ciano, halo o nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7 -15 , heteroarilo o heterociclilo; cada uno de ellos se sustituye opcionalmente por uno o más sustituyentes según se describe en este documento; o (c) -C(O)R1a , -C(O)OR1b , -C(O)NR1bR1 c , -C(NRa)NR1bR1c , -OR1a , -OC(O)R1a , -OC(O)OR1a , -OC(O)NR1bR1 c , -OC(=NR1a)NR1bR1 c , -OS(O)R1 a , -OS(O)2R1a , -OS(O)NR1bR1 c , -OS(O)2NR1b R1 c , -NR1bR1 c , -NR1aC(O)R1d , -NR1a C(O)OR1d , -NR1aC(O)NR1bR1 c , -NR1aC(=NR1d)NR1bR1 c , -NR1aS(O)R1d , -NR1aS(O)2R1d , -NR1aS(O)NR1bR1 c , -NR1aS(O)2 NR1b R1 c , -SR1 a , -S(O)R1a , -S(O)2 R1 a , -S(O)NR1bR1 c , o -S(O)2 NR1bR1 c ; donde R1 a , R1b , R1 c y R1d son cada uno como se definen en este documento.
En otra realización, en este documento se encuentra un compuesto de fórmula IV:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato; donde:
R1, R2, R3, R4 , R5 , R8, X, Y y Z son cada uno como se definen en este documento;
U es un enlace, -C(O)-, -C(O)O-, -C(O)NR1a-, -O-, -OC(O)O-, -OC(O)NR1a-, -NR1a-, -NR1aC(O)NR1d-, -NR1a S(O)-, -NR1aS(O)2-, -NR1aS(O)NR1d-, -NR1aS(O)2 NR1d-, -S-, -S(O)-, o -S(O)2-;
RAy RB son cada uno, independientemente, (a) hidrógeno, ciano, halo, o nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo; cada uno opcionalmente sustituido por uno o más sustituyentes según se describe en este documento; y
m es un número entero de 1,2 ó 3.
En otra realización, se proporciona en este documento un compuesto de fórmula V:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato; donde:
R1, R2, R3, R4 , R5 , U, X, Y y Z son cada uno como se definen en este documento;
A2 , A3 , y A4 son cada uno, independientemente, N o CR8; con la condición de que no más de uno de A2 , A3 , y A4 es N;
RA y RB son cada uno, independientemente, (a) hidrógeno, ciano, halo, o nitro; (b) alquilo C1-6 , alquenilo C2-6 , alquinilo C2-6, cicloalquilo C3 -7 , arilo C6 -14 , aralquilo C7 -15 , heteroarilo o heterociclilo; cada uno opcionalmente sustituido por uno o más sustituyentes según se describe en este documento;
p es un número entero de 0, 1, 2 ó 3; y
cada R8 es, independientemente, (a) hidrógeno, ciano, halo o nitro; (b) alquilo C 1 -6 , alquenilo C2-6, alquinilo C2-6, cicloalquilo C3 -7 , arilo C6 -14 , aralquilo C7 -15 , heteroarilo o heterociclilo; cada uno opcionalmente sustituido por uno o más sustituyentes según se describe en este documento; o (c) -C(O)R1 a , -C(O)OR1b , -C(O)NR1bR1 c , -C(NRa)NR1bR1 c , -OR1 a , -OC(O)R1a , -OC(O)OR1 a , -OC(O)NR1bR1 c , -OC(=NR1a)NR1b R1 c , -OS(O)R1 a , -OS(O)2R1a , -OS(O)NR1b R1 c , -OS(O)2NR1bR1 c , -NR1b R1c , -NR1aC(O)R1d , -NR1aC(O)OR1d , -NR1aC(O)NR1bR1 c , -NR1aC(=NR1d)NR1bR1 c , -NR1aS(O)R1d , -NR1aS(O)2 R1d , -NR1aS(O)NR1b R1 c , -NR1aS(O)2 NR1bR1 c , -SR 1a , -S(O)R1a , -S(O)2 R1 a , -S(O)NR1bR1 c , o -S(O)2 NR1b R1 c ; donde cada R1 a , R1b , R1c y R1d se define en este documento.
En otra realización, a continuación se incluye un compuesto de fórmula V o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato; donde:
R1, R2, R3, R4 , R5 , R8, RA , RB , U, X, Y, y Z, y p son cada uno como se define en este documento; y
A2 , A3, y A4 son cada uno, independientemente, C, N, o CR8; con la condición de que no más de uno de A2 , A3 , y A4 es N.
En una realización, se proporciona en este documento un compuesto de fórmula V, donde R1, R2, R3, R4, R5, R8, RA, RB A2, A3, A4, U, X, y, Z y p son como se define en este documento, con la condición de que A2 y A4 son CR8, y p es 0, entonces U no es un enlace.
En ciertas realizaciones, A2 es C. En ciertas realizaciones, A2 es N. En ciertas realizaciones, A2 es CR8, donde R8 es como se define en este documento. En ciertas realizaciones, A2 es CH. En ciertas realizaciones, A3 es C. En ciertas realizaciones, A3 es N. En ciertas realizaciones, A3 es CR8, donde R8 es como se define en este documento. En ciertas realizaciones, A3 es CH. En ciertas realizaciones, A4 es C. En ciertas realizaciones, A4 es N. En ciertas realizaciones, A4 es CR8, donde R8 es como se define en este documento. En ciertas realizaciones, A4 es CH.
En ciertas realizaciones, A2, A3 y A4 son independientemente CR8, donde R8 es como se define en este documento. En ciertas realizaciones, A2, A3, y A4 son CH. En ciertas realizaciones, A2 es N, y A3 y A4 son independientemente CR8, donde R8 es como se define en este documento. En ciertas realizaciones, A2 y A4 son independientemente CR8, y A3 es N, donde R8 es como se define en este documento. En ciertas realizaciones, A2 y A3 son independientemente Cr8, y A4 es N, donde R8 es como se define en este documento.
En otra realización más, se proporciona en este documento un compuesto de la fórmula VI:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato; donde:
R1, R2, R3, R4 , R5 , U, X, Y y Z son cada uno como se definen en este documento; y
R8 es (a) hidrógeno, ciano, halo o nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo; cada uno opcionalmente sustituido por uno o más sustituyentes según se describe en este documento; o (c) -C(O)R1a , -C(O)OR1b , -C(O)NR1b R1 c , -C(NRa)NR1b R1 c , -OR1 a , -OC(O)R1a , -OC(O)OR1a , -OC(O)NR1bR1 c , -OC(=NR1a)NR1b R1 c , -OS(O)R1 a , -OS(O)2R1 a , -OS(O)NR1b R1 c , -OS(O)2NR1bR1 c , -NR1bR1 c , -NR1aC(O)R1d , -NR1aC(O)OR1d , -NR1aC(O)NR1bR1 c , -NR1aC(=NR1d)NR1bR1 c , -NR1aS(O)R1d , -NR1aS(O)2 R1d , -NR1aS(O)NR1bR1 c , -NR1aS(O)2 NR1bR1 c , -SR1a , -S(O)R1a , -S(O)2 R1a , -S(O)NR1b R1 c , o -S(O)2 NR1bR1 c ; donde cada R1 a , R1b , R1c y R1d son como se define en este documento.
En una realización, R8 en la fórmula VI es hidrógeno.
En otra realización, se proporciona en este documento un compuesto de la fórmula VI, donde R1, R2, R3, R4, R5, R8, U, X, Y, y Z son cada uno como se define en este documento, con la condición de que cuando R2, R3 , R4 y R5 son hidrógeno, U es un enlace; R8 es hidrógeno.
En otra realización más, se proporciona en este documento un compuesto de la fórmula VI, donde R1, R2 , R3, R4 , R5 , R8 , U, X, Y, y Z son cada uno como se define en este documento, con la condición de que U no es un enlace.
En otra realización más, se proporciona en este documento un compuesto de la fórmula VII:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato; donde:
R1, R2, R3 , R4 , R5 , U, X, Y y Z son cada uno como se definen en este documento;
E2 , E3 y E4 son cada uno, independientemente, CR8, N o NR8 , O, o S;
RA y RB son cada uno, independientemente, (a) hidrógeno, ciano, halo, o nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo; cada uno opcionalmente sustituido por uno o más sustituyentes según se describe en este documento;
p es un número entero de 0, 1,2 ó 3; y
cada R8 es, independientemente, (a) hidrógeno, ciano, halo o nitro; (b) alquilo C 1 -6 , alquenilo C2-6, alquinilo C2-6, cicloalquilo C3 -7 , arilo C6 -14, aralquilo C7 -15 , heteroarilo o heterociclilo; cada uno opcionalmente sustituido por uno o más sustituyentes según se describe en este documento; o (c) -C(O)R1 a , -C(O)OR1b , -C(O)NR1b R1 c , -C(NRa)NR1b R1 c , -OR1a , -OC(O)R1a , -OC(O)OR1 a , -OC(O)NR1b R1 c , -OC(=NR1a)NR 1bR1 c , -OS(O)R1 a , -OS(O)2 R1 a , -OS(O)NR1b R1 c , -OS(O)2 NR1bR1 c , -NR1bR1c , -NR1aC(O)R1d , -NR1aC(O)OR1d , -NR1aC(O)NR1b R1 c , -NR1aC(=NR1d)NR1b R1 c , -NR1aS(O)R1d, -NR1aS(O)2 R1d , -NR1aS(O)NR1bR1 c , -NR1aS(O)2 NR1b R1 c , -SR1a , -S(O)R1a , -S(O)2 R1 a , -S(O)NR1b R1 c , o -S(O)2 NR1b R1 c ; donde cada R1 a , R1b , R1c y R1d es como se define en este documento.
En otra realización más, se proporciona en este documento un compuesto de fórmula VII o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato; donde R1, R2 , R3 , R4 , R5, R8, RA , RB , U, X, Y, Z y p son como se definen en este documento; y E2, E3 y E4 son cada uno, independientemente, C, N, O, S, CR8, o NR8.
En ciertas realizaciones, E2, E3 y E4 son CR8, donde R8 es como se define en este documento. En ciertas realizaciones, E2 y E4 son CR8y E3 es NR8 , O, o S, donde R8 es como se define en este documento. En ciertas realizaciones, E2 y E3 son N, y E4 es CR8. En ciertas realizaciones, E2 , E3 y E4 son N.
En otra realización, en este documento se incluye un compuesto de la fórmula IA o IB:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato, o hidrato; donde R1, R2, R3, R4, R5, R6, A, B, D, E, y U son cada uno como se define en este documento.
En otra realización, el compuesto de fórmula Ib tiene la estructura de fórmula VIII:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato;
donde R1, R2, R3, R4, R5, R6, A, B, D, y U son cada uno según lo definido en este documento, y el enlace entre D y B es un enlace simple o doble. En una realización, A es N. En otra realización, A y D son N. En otra realización más, A y D son N, B es CR9, y el enlace entre B y D es un doble enlace, donde R9 es como se define en este documento. En otra realización más, A y D son N, B es CH, y el enlace entre B y D es un enlace doble. En otra realización más, A, B y D son N, y el enlace entre B y D es un enlace doble. En otra realización más, A es N, B y D son cada uno, independientemente, CR9, y el enlace entre B y D es un doble enlace, donde R9 es como se define en este documento. En otra realización más, A es N, B y D son cada CH, y el enlace entre B y D es un enlace doble. En otra realización más, A es N, B y D son cada uno, independientemente, CHR9, y el enlace entre B y D es un enlace sencillo, donde R9 es como se define en este documento. En otra realización más, A es N, B y D son cada uno CH2, y el enlace entre B y D es un enlace sencillo.
En aún otra realización, el compuesto de fórmula Ib tiene la estructura de fórmula IX:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato, o hidrato;
donde R1, R2, R3, R4, R5, R6, A, B, D, y U es cada uno según lo definido en este documento, y el enlace entre D y B es un enlace simple o doble. En una realización, A es N. En otra realización, A y D son N. En otra realización más, A y D son N, B es Cr9, y el enlace entre B y D es un doble enlace, donde R9 es como se define en este documento. En
otra realización más, A y D son N, B es CH, y el enlace entre B y D es un enlace doble. En otra realización más, A, B y D son N, y el enlace entre B y D es un enlace doble. En otra realización más, A es N, B y D son cada uno, independientemente, CR9, y el enlace entre B y D es un doble enlace, donde R9 es como se define en este documento. En otra realización más, A es N, B y D son cada uno CH, y el enlace entre B y D es un enlace doble. En otra realización más, A es N, B y D son cada uno, independientemente, CHR9, y el enlace entre B y D es un enlace sencillo, donde R9 es como se define en este documento. En otra realización más, A es N, B y D son cada CH2, y el enlace entre B y D es un enlace sencillo.
Los grupos, R1, R2, R3, R4, R5, R6, R8, RA, RB, A, B, D, E, U, X, Y, Z, m y p en las fórmulas proporcionadas en este documento, por ejemplo, las fórmulas I, IA, IB, Ia, Ib, II, III, IV, V, VI, VII, VIII y IX, se definen además en las realizaciones descritas en este documento.
En ciertas realizaciones, R1 es hidrógeno, alquilo C1-6, -S-alquilo C1-6, -S(O)-alquilo C1-6, o -SO2-alquilo C1-6; donde cada alquilo se sustituye opcionalmente por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R1 es hidrógeno, alquilo C1-6, o -SO2-alquilo C1-6. En ciertas realizaciones, R1 es hidrógeno. En ciertas realizaciones, R1 es alquilo C1-6, opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R1 es alquilo C1-6, sustituido por uno o más, en una realización, de uno a tres, halo. En ciertas realizaciones, R1 es alquilo C1-6, sustituido por de uno a tres, en una realización, uno, dos, o tres, grupos fluoro. En ciertas realizaciones, R1 es metilo, fluorometilo, difluorometilo o trifluorometilo. En ciertas realizaciones, R1 es difluorometilo. En ciertas realizaciones, R1 es-S- alquilo C1-6, opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R1 es metanosulfanilo (-SCH3). En ciertas realizaciones, R1 es -S(O)-alquilo C1-6, opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R1 es metanosulfinilo (-SOCH3). En ciertas realizaciones, R1 es -SO2-alquilo C1-6, opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R1 es metanosulfonilo (-SO2CH3).
En ciertas realizaciones, R2 es (a) hidrógeno, ciano, halo o nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo, o heterociclilo, cada uno opcionalmente sustituido con uno o más sustituyentes según lo descrito en este documento; o (c) -C(O)R1a, -C(O)OR1b, -C(O)NR1bR1c, -C(NRa)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c, o -S(O)2NR1bR1c, donde cada R1a, R1b, R1c y R1d son como se describe en este documento. En ciertas realizaciones, R2 es hidrógeno. En ciertas realizaciones, R2 es ciano, halo o nitro. En ciertas realizaciones, R2 es alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquil C7-15, heteroarilo, o heterociclilo, cada uno opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R2 es -C(O)R1a, -C(O)OR1b, -C(O)NR1bR1c, o -C(NRa)NR1bR1c, donde R1a, R1b, y R1c son como se definen en este documento. En ciertas realizaciones, R2 es -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c o -OS(O)2NR1bR1c, donde R1a, R1b y R1c son como se definen en este documento. En ciertas realizaciones, R2 es -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, o -NR1aS(O)2NR1bR1c, donde R1a, R1b, R1c y R1d son como se definen en este documento. En ciertas realizaciones, R2 es -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c, o -S(O)2NR1bR1c; donde R1a, R1b y R1c son como se definen en este documento. En ciertas realizaciones, R2 es -OR1a, donde R1a es metilo, etilo o propilo (p. ej., n-propilo, isopropilo, o 2-isopropil), cada uno opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R2 es metoxi, etoxi, propoxi, o isopropoxi. En ciertas realizaciones, R2 es metoxi.
En ciertas realizaciones, R3 es (a) hidrógeno, ciano, halo o nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo, o heterociclilo, cada uno opcionalmente sustituido con uno o más sustituyentes según lo descrito en este documento; o (c) -C(O)R1a, -C(O)OR1b, -C(O)NR1bR1c, -C(NRa)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c, o -S(O)2NR1bR1c, donde cada R1a, R1b, R1c y R1d son como se describe en este documento. En ciertas realizaciones, R3 es hidrógeno. En ciertas realizaciones, R3 es ciano, halo o nitro. En ciertas realizaciones, R3 es alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo, o heterociclilo, cada uno opcionalmente sustituido con uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R3 es -C(O)R1a, -C(O)OR1b, -C(O)NR1bR1c, o -C(NRa)NR1bR1c, donde R1a, R1b y R1c son como se define en este documento. En ciertas realizaciones, R3 es -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c o -OS(O)2NR1bR1c, donde R1a, R1b y R1c son como se define en este documento. En ciertas realizaciones, R3 es -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, o -NR1aS(O)2NR1bR1c, donde R1a, R1b, R1c y R1d son como se define en este documento. En ciertas realizaciones, R3 es amino. En ciertas realizaciones, R3 es -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c, o -S(O)2NR1bR1c; donde R1a, R1b y R1c son como se define en este documento. En ciertas realizaciones, R3 es -OR1a, donde R1a es metilo, etilo o propilo (p. ej., n-propilo, isopropilo o 2-isopropil), cada uno de los cuales se sustituye opcionalmente por
uno o más sustituyentes según se describe en este documento. En ciertas realizaciones, R3 es metoxi, etoxi, propoxi, o isopropoxi.
En ciertas realizaciones, R4 es hidrógeno o alquilo C1-6 , opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R4 es hidrógeno. En ciertas realizaciones, R4 es alquilo C1 -6 , opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R4 es hidrógeno, metilo, etilo o propilo (p. ej., n-propilo, isopropilo o 2-isopropil), cada uno de los cuales se sustituye opcionalmente por uno o más sustituyentes según se describe en este documento. En ciertas realizaciones, R4 es metilo, etilo, n-propilo, o isopropilo.
En ciertas realizaciones, R5 es hidrógeno o alquilo C1-6 , opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R5 es hidrógeno. En ciertas realizaciones, R5 es alquilo C1 -6 , opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R5 es hidrógeno, metilo, etilo o propilo (p. ej., n-propilo, isopropilo o 2-isopropil), cada uno de los cuales se sustituye opcionalmente por uno o más sustituyentes según se describe en este documento. En ciertas realizaciones, R5 es metilo, etilo, n-propilo, o isopropilo.
En ciertas realizaciones, R4 y R5 son ambos hidrógeno.
En ciertas realizaciones, R4 y R5 se unen para formar un enlace. En ciertas realizaciones, R4 y R5 se unen para formar alquileno C1 -6 , opcionalmente sustituido por uno o más sustituyentes. En ciertas realizaciones, R4 y R5 se unen para formar metileno, etileno o propileno, cada uno de los cuales se sustituye opcionalmente por uno o más sustituyentes.
En ciertas realizaciones, R6 es arilo C6 -14 , aralquilo C7 -15 , heteroarilo, o heteroaril-alquilo C1 -6 , cada uno sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R6 es arilo C6 -14, opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R6 es fenilo, opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R6 es fenilo, opcionalmente sustituido por uno o más sustituyentes Q, cada uno independientemente seleccionado del grupo consistente en halo, ciano, nitro, amino, y metoxi. En ciertas realizaciones, R6 es fenilo, aminofenilo, nitrofenilo o metoxifenilo. En ciertas realizaciones, R6 es fenilo, 3-aminofenilo, 3-nitrofenilo, o 3-metoxifenilo.
En ciertas realizaciones, R6 es aralquilo C7 -15 , opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R6 es -(CRARB)m-arilo C6 -14 , en donde RA y RB son independientemente (a) hidrógeno, ciano, halo o nitro; (b) alquilo C1-6 , alquenilo C2-6, alquinilo C2-6, cicloalquilo C3 -7 , arilo C6 -14 , aralquilo C7-15 , heteroarilo o heterociclilo; y m es un número entero de 1, 2 ó 3; y donde cada alquilo, alquenilo, alquinilo, cicloalquilo, arilo, aralquilo, heteroarilo, y heterociclilo se substituyen opcionalmente con uno o más sustituyentes según lo descrito en este documento. En ciertas realizaciones, R6 es -(CH2 )m-arilo C6 -14 , donde m es un número entero de 1, 2, o 3, y el arilo se sustituye opcionalmente por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R6 es bencilo, opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R6 es bencilo. En ciertas realizaciones, R6 es fenil-etilo, opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R6 es bencilo o 2-feniletilo.
En ciertas realizaciones, R6 es heteroarilo, opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R6 es pirazolilo, imidazolilo, tiazolilo, 1,2,3-triazolilo, tetrazolilo, piridinilo, piridazinilo, pirimidinilo, pirazinilo, o quinolinilo, cada uno sustituido opcionalmente con uno o más sustituyentes descritos en este documento. En ciertas realizaciones, cada sustituyente es independientemente -L-(CRC RD)n-RE , donde RC y RD son como se definen en este documento; RE es hidrógeno, -NRFRG , o heterociclilo; L es un enlace, -O , o -N(RH)-; RF , RG y RH son cada uno, independientemente, hidrógeno o alquilo C1-6 y n es un número entero de 0, 1, 2 ó 3; y donde cada alquilo y heterociclilo está independiente y opcionalmente sustituido con uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, RC es hidrógeno. En ciertas realizaciones, RD es hidrógeno. En ciertas realizaciones, RC y RD son hidrógeno. En ciertas realizaciones, RC es hidrógeno, metilamino, dimetilamino, pirrolidinilo, piperidinilo, o morfolinilo, en donde pirrolidinilo, piperidinilo, y morfolinilo están, independientemente, sustituidos opcionalmente con metilo. En ciertas realizaciones, L es un enlace, -O-, -NH-, o -N (CH3)-.
En ciertas realizaciones, cada sustituyente en R6 se selecciona independientemente del grupo que consiste en amino, fluoro, cloro, metilo, (dimetilamino)metilo, (dimetilamino)etilo, (dimetilamino)propilo, morfolinilmetilo, (morfolinil)etilo, (morfolinil)propilo, metoxi, (dimetilamino)etoxi, (dimetilamino)propoxi, (morfolinil)etoxi, (morfolinil)propoxi, (metilpiperidinil)oxi, (metil-pirrolidinil)oxi, metilamino, dimetilamino, (dimetilamino)etilamino, (dimetilaminoetil)(metil)amino, (dimetilamino)propilamino, ((dimetilamino)propil)(metil)amino, (morfolinil)etilamino, ((morfolinil)etil)(metil)amino, (morfolinil)propilamino, ((morfolinil)propil)(metil)amino, metil-piperidinilamino, (metil-piperidinil)(metil)amino, metilpiperazinilo, o (dimetilamino)-piperidinilo. En ciertas realizaciones, cada sustituyente en R6 se selecciona independientemente del grupo que consiste en amino, fluoro, cloro, metilo, (dimetilamino)metilo, 2-(dimetilamino)etilo, 3-(dimetilamino)propil, 4-morfolinilmetilo, 2-(4-morfolinil)etilo, 3-(4-morfolinil)propilo, metoxi, 2-(dimetilamino)etoxi, 3-(dimetilamino)propoxi, 2-(4-morfolinil)etoxi, 3-(4-morfolinil)propoxi, (1-metil-4-piperidinil)oxi, (1-metil-3-pirrolidinil)oxi, metilamino, dimetilamino, 2-(dimetilamino)etilamino, (2-dimetilaminoetil)-(metil)amino, 3-(dimetilamino)propilamino, (3
(dimetilamino)propil)(metil)amino, 2-(4-morfolinil)etilamino, (2-(4-morfolinil)etil)(metil)amino, 3-(4-morfolinil)-propilamino, (3-(4-morfolinil)propil)(metil)amino, 1-metil-4-piperidinilamino, (1-metil-4-piperidinil)(metil)amino, 4-metil-1- piperazinilo, y 4-(dimetilamino)-1-piperidinilo.
En ciertas realizaciones, R6 es pirazolilo, metil-pirazolilo, [2-(dimetilamino)etil]-pirazolilo, [3-(dimetilamino)propil]-pirazolilo, [2-(4-morfolinil)etil]-pirazolilo, o [3-(4-morfolinil)propil]-pirazolilo. En ciertas realizaciones, R6 es pirazol-1-ilo, 1H-pirazol-4-ilo, 1-metil-1H-pirazol-3-ilo, 1-metil-1H-pirazol-4-ilo, 1 -metil-1 H-pirazol-5-ilo, 1-[2-(dimetilamino)etil]-1H-pirazol-4-ilo, 1-[3-(dimetilamino)propil]-1H-pirazol-4-ilo, 1 -[2-(4-morfolinil)etil]-1 H-pirazol-4-ilo, o 1-[3-(4-morfolinil)propil]-1 H-pirazol-4-ilo.
En ciertas realizaciones, R6 es imidazolilo o metil-imidazolilo. En ciertas realizaciones, R6 es imidazol-1-ilo o 1-metil-1H-imidazol-5-ilo.
En ciertas realizaciones, R6 es tiazolilo, [(dimetilamino)metil]-tiazolilo, o (4-morfolinilmetil)-tiazolilo. En ciertas realizaciones, R6es 1,3-tiazol-5-ilo, 2-[(dimetilamino)metil]-1,3-tiazol-5-ilo, o 2-(4-morfolinilmetil)-1,3-tiazol-5-ilo.
En ciertas realizaciones, R6 es triazolilo o metil-1,2,3-triazolilo. En ciertas realizaciones, R6 es 1-metil-1H-1,2,3-triazol-4- ilo, 1 -metil-1 H-1,2,3-triazol-5-ilo, o 2-metil-2H-1,2,3-triazol-4-ilo.
En ciertas realizaciones, R6 es tetrazolilo o metil-tetrazolilo. En ciertas realizaciones, R6 es 1-metil-1H-tetrazol-5-ilo o 2- metil-2H-tetrazol-5-ilo.
En ciertas realizaciones, R6 es pirazinilo, aminopirazinilo, o metoxipirazinilo. En ciertas realizaciones, R6 es 2-pirazinilo, 5- amino-2-pirazinilo, 6-amino-2-pirazinilo, o 6-metoxi-2-pirazinilo.
En ciertas realizaciones, R6 es piridazinilo o metoxipiridazinilo. En ciertas realizaciones, R6 es piridazin-3-ilo, piridazin-4- ilo, o 6-metoxipiridazin-3-ilo.
En ciertas realizaciones, R6 es piridinilo, fluoropiridinilo, cloropiridinilo, amino-piridinilo, metilamino-piridinilo, dimetilamino-piridinilo, [2-(dimetilamino)etilamino]-piridinilo, [(2-dimetilaminoetil)(metil)amino]-piridinilo, [3-(dimetilamino)propilamino]-piridinilo, [(3-(dimetilamino)propil)(metil)amino]-piridinilo, [2-(4-morfolinil)etilamino]-piridinilo, [(2-(4-morfolinil)etil)-(metil)amino]-piridinilo, [3-(4-morfolinil)propilamino]-piridinilo, [(3-(4-morfolinil)propil)(metil)amino]-piridinilo, (4-metil-1-piperazinil)-piridinilo, [4-(dimetilamino)-1-piperidinil]-piridinilo, [1-metil-4-piperidinilamino]-piridinilo, [(1-metil-4-piperidinil)(metil)amino]-piridinilo, metoxi-piridinilo, [2-(dimetilamino)etoxi]-piridinilo, [3-(dimetilamino)propoxi]-piridinilo, [2-(4-morfolinil)etoxi]-piridinilo, [3-(4-morfolinil)propoxi]-piridinilo, [(1-metil-4-piperidinil)oxi]-piridinilo, [(1-metil-3-pirrolidinil)oxi]-piridinilo, [2-(dimetilamino)etil]-piridinilo, y [2-(4-morfolinil)etil]-piridinilo. En ciertas realizaciones, R6 es piridinilo.
En ciertas realizaciones, R6 es piridin-2-ilo, piridin-3-ilo, piridin-4-ilo, 2-fluoropiridin-5-ilo, 2-cloropiridin-5-ilo, 2-amino-5- piridinilo, 2-metilamino-3-piridinilo, 2-dimetilamino-5-piridinilo, 2-[2-(dimetilamino)etilamino]-5-piridinilo, 2-[(2-dimetilaminoetil)(metil)amino]-3-piridinilo, 2-[3-(dimetilamino)propilamino]-5-piridinilo, 2-[(3-(dimetilamino)propil)(metil)amino]-5-piridinilo, 2-[2-(4-morfolinil)etilamino]-3-piridinilo, 2-[(2-(4-morfolinil)etil)(metil)amino]-3-piridinilo, 2-[3-(4-morfolinil)propilamino]-3-piridinilo, 2-[(3-(4-morfolinil)propil)(metil)amino]-3-piridinilo, 6-(4-metil-1-piperazinil)-3-piridinilo, 6-[4-(dimetilamino)-1-piperidinil]-3-piridinilo, 2-[1-metil-4-piperidinilaminol-5-piridinilo, 2-[(1-metil-4-piperidinil)(metil)amino]-5-piridinilo, 2-metoxi-4-piridinilo, 4-metoxi-3-piridinilo, 5-metoxi-3-piridinilo, 6-metoxi-3-piridinilo, 2-[2-(dimetilamino)etoxi]-4-piridinilo, 5-(2-(dimetilamino)etoxi)-2-piridinilo, 6-[2-(dimetilamino)etoxi]-3-piridinilo, 2-[3-(dimetilamino)propoxi]-4-piridinilo, 2-[3-(dimetilamino)propoxi]-5-piridinilo, 5-[3-(dimetilamino)propoxi]-3-piridinilo, 6-[3-(dimetilamino)propoxi]-3-piridinilo, 2-[2-(4-morfolinil)etoxi]-4-piridinilo, 5-[2-(4-morfolinil)etoxi]-3-piridinilo, 6-[2-(4-morfolinil)etoxi]-3-piridinilo, 2-[3-(4-morfolinil)propoxi]-4-piridinilo, 5-[3-(4-morfolinil)propoxi]-3-piridinilo, 6-[3-(4-morfolinil)propoxi]-3-piridinilo, 6-[(1-metil-4-piperidinil)oxi]-3-piridinilo, 6-[(1-metil-3-pirrolidinil)oxi]-3-piridinilo, 2-[2-(dimetilamino)etil]-3-piridinilo, y 2-[2-(4-morfolinil)etil]-3-piridinilo. En ciertas realizaciones, R6 es 3-piridinilo.
En ciertas realizaciones, R6 es pirimidinilo, cloro-pirimidinilo, metoxi-pirimidinilo, [2-(dimetilamino)etil]-pirimidinilo, [2-(4-morfolinil)etil]-pirimidinilo, [2-(dimetilamino)etoxi]-pirimidinilo, [3-(dimetilamino)propoxi]-pirimidinilo, [2-(4-morfolinil)etoxi]-pirimidinilo, [3-(4-morfolinil)propoxi]-pirimidinilo, amino-pirimidinilo, [2-(dimetilamino)etilamino]-pirimidinilo, [(2-(dimetilamino)etil)(metil)amino]-pirimidinilo, [3-(dimetilamino)propilamino]-pirimidinilo, [(3-(dimetilamino)propil)(metil)amino]-pirimidinilo, [2-(4-morfolinil)etilamino]-pirimidinilo, [(2-(4-morfolinil)etil)(metil)amino]-pirimidinilo, [3-(4-morfolinil)propilamino]-pirimidinilo, [(3-(4-morfolinil)propil)(metil)amino]-pirimidinilo, (4-metil-1-piperazinil)-pirimidinilo, [4-(dimetilamino)-1-piperidinil]-pirimidinilo, (1-metil-4-piperazinilamino)-pirimidinilo, [(1-metil-4-piperazinil)(metil)amino]-pirimidinilo, [(1-metil-4-piperidinil)oxi]-pirimidinilo, o [(1-metil-3-pirrolidinil)oxi]-pirimidinilo.
En ciertas realizaciones, R6 es pirimidin-2-ilo, pirimidin-4-ilo, pirimidin-5-ilo, 2-cloro-5-pirimidinilo, 2-metoxi-5-pirimidinilo, 6-metoxi-4-pirimidinilo, 2-[2-(dimetilamino)etil]-5-pirimidinilo, 2-[2-(4-morfolinil)etil]-5-pirimidinilo, 2-[2-(dimetilamino)etoxi]-5-pirimidinilo, 2-[3-(dimetilamino)propoxi]-5-pirimidinilo, 2-[2-(4-morfolinil)etoxi]-5-pirimidinilo, 2-[3-(4-morfolinil)propoxi]-5-pirimidinilo, 2-amino-5-pirimidinilo, 2-[2-(dimetilamino)etilamino]-5-pirimidinilo, 2-[(2-(dimetilamino)etil)(metil)amino]-5-pirimidinilo, 2-[3-(dimetilamino)propilamino]-5-pirimidinilo, 2-[(3(dimetilamino)propil)(metil)amino]-5-pirimidinilo, 2-[2-(4-morfolinil)etilamino]-5-pirimidinilo, 2-[(2-(4-morfolinil)etil)(metil)amino]-5-pirimidinilo, 2-[3-(4-morfolinil)propilamino]-5-pirimidinilo, 2-[(3-(4-morfolinil)propil)(metil)amino]-5-pirimidinilo, 2-(4-metil-1-piperazinil)-5-pirimidinilo, 2-[4-(dimetilamino)-1-piperidinil]-5-pirimidinilo, 2-(1-metil-4-piperazinilamino)-5-pirimidinilo, 2-[(1-metil-4-piperazinil)(metil)amino]-5-pirimidinilo, 2-[(1-metil-4-piperidinil)oxi]-5-pirimidinilo, o 2-[(1-metil-3-pirrolidinil)oxi]-5-pirimidinilo.
En ciertas realizaciones, R6 es heteroalquilquinolinilo. En ciertas realizaciones, R6 es quinolin-2-ilo, quinolin-3-ilo, quinolin-4-ilo, quinolin-5-ilo, quinolin-6-ilo, quinolin-7-ilo, o quinolin-8-ilo.
En ciertas realizaciones, R6 es heteroaril-alquilo C1.6 , opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R6 es heteroaril-(CR6aR6b)p-, donde R6a y R6b se definen en este documento; p es un número entero de 1,2 ó 3; y el heteroarilo se sustituye opcionalmente por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R6 es heteroaril-(CH2)p-, donde p es un número entero de 1, 2 ó 3; y el heteroarilo se sustituye opcionalmente por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, R6 es imidazoliletilo, piridinilmetilo, o piridiniletilo. En ciertas realizaciones, R6 es 2-piridinilmetilo, 3-piridinilmetilo, 4-piridinilmetilo, 2-(1H-imidazol-4-il)etilo, 2-(2-piridinil)etilo, 2-(3-piridinil)etilo, o 2-(4-piridinil)etilo.
En ciertas realizaciones, cada R8 es, independientemente, (a) hidrógeno, ciano, halo o nitro; (b) alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, cicloalquilo C3 -7 , arilo C6 -14 , aralquilo C7 -15 , heteroarilo o heterociclilo; o (c) -C(O)R1 a , -C(O)OR1b , -C(O)NR1b R1 c , -C(NRa )NR1bR1c , -OR1 a , -OC(O)R1 a , -OC(O)OR1 a , -OC(O)NR1b R1 c , -OC(=NR1 a )NR1bR1 c , -OS(O)R1 a , -OS(O)2R1 a , -OS(O)NR1bR1 c , -OS(O)2NR1bR1 c , -NR1bR1 c , -NR1 a C(O)R1d , -NR1 a C(O)OR1d , -NR1 a C(O)NR1bR1 c , -NR1 a C(=NR1d )NR1bR1 c , -NR1 a S(O)R1d , -NR1 a S(O)2R1d , -NR1aS(O)NR1bR1 c , -NR1aS(O)2NR1bR1 c , -SR1 a , -S(O)R1 a , -S(O)2 R1 a , -S(O)NR1bR1 c , o -S(O)2 NR1bR1 c ; donde cada R1 a , R1b , R1c y R1d es como se define en este documento. En ciertas realizaciones, R8 es hidrógeno. En ciertas realizaciones, cada R8 es independientemente -L-(CRC RD)n-RE , donde RC y RD son como se definen en este documento; RE es hidrógeno, -NRFRG , o heterociclilo; L es un enlace, -O , o -N(RH)-; RF , RG y RH son cada uno, independientemente, hidrógeno o alquilo C1-6 y n es un número entero de 0, 1, 2 ó 3; y donde cada alquilo y heterociclilo está, independiente y opcionalmente, sustituido con uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, RC es hidrógeno. En ciertas realizaciones, RD es hidrógeno. En ciertas realizaciones, RC y RD son hidrógeno. En ciertas realizaciones, RE es hidrógeno, metilamino, dimetilamino, pirrolidinilo, piperidinilo, o morfolinilo, en donde pirrolidinilo, piperidinilo, y morfolinilo están, independiente y opcionalmente, sustituidos con metilo. En ciertas realizaciones, L es un enlace, -O-, -NH-, o -N(CH3)-
En ciertas realizaciones, cada R8 se selecciona independientemente del grupo que consiste en amino, fluoro, cloro, metilo, (dimetilamino)metilo, (dimetilamino)etilo, (dimetilamino)propilo, morfolinilmetilo, (morfolinil)etilo, (morfolinil)propilo, metoxi, (dimetilamino)etoxi, (dimetilamino)propoxi, (morfolinil)etoxi, (morfolinil)propoxi, (metilpiperidinil)oxi, (metil-pirrolidinil)oxi, metilamino, dimetilamino, (dimetilamino)etilamino, (dimetilaminoetil)(metil)amino, (dimetilamino)propilamino, ((dimetilamino)propil)(metil)amino, (morfolinil)etilamino, ((morfolinil)etil)(metil)amino, (morfolinil)propilamino, ((morfolinil)propil)(metil)amino, metil-piperidinilamino, (metil-piperidinil)(metil)amino, metilpiperazinilo, o (dimetilamino)-piperidinilo.
En ciertas realizaciones, cada R8 se selecciona independientemente del grupo que consiste en amino, fluoro, cloro, metilo, (dimetilamino)metilo, 2-(dimetilamino)etilo, 3-(dimetilamino)propil, 4-morfolinilmetilo, 2-(4-morfolinil)etilo, 3-(4-morfolinil)propilo, metoxi, 2-(dimetilamino)etoxi, 3-(dimetilamino)propoxi, 2-(4-morfolinil)etoxi, 3-(4-morfolinil)propoxi, (1-metil-4-piperidinil)oxi, (1-metil-3-pirrolidinil)oxi, metilamino, dimetilamino, 2-(dimetilamino)etilamino, (2-dimetilaminoetil)(metil)amino, 3-(dimetilamino)propilo, (3-(dimetilamino)propil)(metil)amino, 2-(4-morfolinil)etilamino, (2-(4-morfolinil)etil)(metil)amino, 3-(4-morfolinil)propilamino, (3-(4-morfolinil)propil)(metil)amino, 1-metil-4-piperidinilamino, (1-metil-4-piperidinil)(metil)amino, 4-metil-1 -piperazinilo, o 4-(dimetilamino)-1 -piperidinilo.
En ciertas realizaciones, RA es hidrógeno. En ciertas realizaciones, RB es hidrógeno. En ciertas realizaciones, RA y RB son hidrógeno.
En ciertas realizaciones, A es independientemente un enlace. En ciertas realizaciones, A es independientemente un átomo de nitrógeno, oxígeno, o azufre. En ciertas realizaciones, A es N. En ciertas realizaciones, A es independientemente CR9 o CHR9, donde R9 es como se define en este documento. En ciertas realizaciones, A es independientemente CR9 , donde R9 es hidrógeno, halo o alquilo C1-6.
En ciertas realizaciones, B es independientemente un enlace. En ciertas realizaciones, B es independientemente un átomo de nitrógeno, oxígeno, o azufre. En ciertas realizaciones, B es N. En ciertas realizaciones, B es independientemente CR9 o CHR9, donde R9 es como se define en este documento. En ciertas realizaciones, B es independientemente CR9, donde R9 es hidrógeno, halo o alquilo C1 -6. En ciertas realizaciones, B es CH. En ciertas realizaciones, B es CH2.
En ciertas realizaciones, D es independientemente un enlace. En ciertas realizaciones, D es independientemente un átomo de nitrógeno, oxígeno, o azufre. En ciertas realizaciones, D es N. En ciertas realizaciones, D es independientemente CR9 o CHR9 , donde R9 es como se define en este documento. En ciertas realizaciones, D es
independientemente CR9, donde R9 es hidrógeno, halo o alquilo C1 -6. En ciertas realizaciones, D es CH. En ciertas realizaciones, D es CH2.
En ciertas realizaciones, E es independientemente un enlace. En ciertas realizaciones, E es independientemente un átomo de nitrógeno, oxígeno, o azufre. En ciertas realizaciones, E es N. En ciertas realizaciones, E es independientemente CR9 o CHR9, donde R9 es como se define en este documento. En ciertas realizaciones, E es independientemente CR9, donde R9 es hidrógeno, halo o alquilo C1 -6. En ciertas realizaciones, E es CH. En ciertas realizaciones, E es CH2.
En ciertas realizaciones, U es un enlace, -C(O)-, -C(O)O-, -C(O)NR1a -, -O-, -OC(O)O-, -OC(O)NR1a-, -NR1a-, -NR1 a C(O)NR1d-, -NR1 a S(O)-, -NR1 a S(O)2-, -NR1 a S(O)NR1d-, -NR1 a S(O)2 NR1d-, -S-, -S(O)-, o -S(O)2-, donde R1a y R1d son como se definen en este documento. En ciertas realizaciones, U es un enlace. En ciertas realizaciones, U no es un enlace. En ciertas realizaciones, U es -C(O)-, -C(O)O-, o-C(O)NR1a-; donde R1a es como se define en este documento. En ciertas realizaciones, U es -O-, -OC(O)O-, o -OC(O)NR1a -, donde R1a es como se define en este documento. En ciertas realizaciones, U es -NR1a-, -NR1 a C(O)NR1d-, -NR1 a S(O)-, -NR1 a S(O)2-, -NR1 a S(O)NR1d-, o -NR1 a S(O)2 NR1d-; donde R1a y R1d son como se definen en este documento. En ciertas realizaciones, U es -NR1a-, donde R1a es hidrógeno o alquilo C1-6 , opcionalmente sustituido por uno o más sustituyentes como se describe en este documento. En ciertas realizaciones, U es -NH- o -N(CH3 )-. En ciertas realizaciones, U es -NH-. En ciertas realizaciones, U es -S-, -S(O)-, o -S(O)2-.
En ciertas realizaciones, m es un número entero de 1, 2 ó 3. En ciertas realizaciones, m es 0. En ciertas realizaciones, m es 1. En ciertas realizaciones, m es 2. En ciertas realizaciones, m es 3.
En ciertas realizaciones, p es un número entero de 0, 1,2 ó 3. En ciertas realizaciones, p es 0. En ciertas realizaciones, p es 1. En ciertas realizaciones, p es 2. En ciertas realizaciones, p es 3.
En una realización, se proporciona en este documento un compuesto seleccionado de:
4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-W-(3-piridinil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-A/-(3-piridinil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-A/-metil-6-(4-morfolinil)-W-(3-piridinil)-1,3,5-tnazin-2-amina;
4-[2-(metilsulfanil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-W-(3-piridinil)-1,3,5-triazin-2-amina;
4-[2-(metilsulfonil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-W-(3-piridinil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-W-fenil-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazol-1-il]-W-metil-6-(4-morfolinil)-W-fenil-1,3,5-triazin-2-amina;
W-bencil-4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-amina;
W-bencil-4-[2-(difluorometil)-1H-bencimidazol-1-il]-W-metil-6-(4-morfolinil)-1,3,5-triazin-2-amina;
2-(difluorometil)-1-[4-(4-morfolinil)-6-fenoxi-1,3,5-triazin-2-il]-1H-bencimidazol;
2-(difluorometil)-1-[4-(4-morfolinil)-6-(fenilsulfanil)-1,3,5-triazin-2-il]-1H-bencimidazol;
2-(difluorometil)-1-[4-(4-morfolinil)-6-(fenilsulfonil)-1,3,5-triazin-2-il]-1H-bencimidazol;
W-(2-cloro-5-pirimidinil)-4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-1H-bencimidazol-1-il]-W-metil-6-(4-morfolinil)-W-(5-pirimidinil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-A/-metil-6-(4-morfolinil)-W-(5-pinmidinil)-1,3,5-triazin-2-amina; 2-(difluorometil)-1-[4-(4-morfolinil)-6-(3-piridinil)-1,3,5-triazin-2-il]-1H-bencimidazol;
2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(3-piridinil)-1,3,5-triazin-2-il]-1H-bencimidazol;
2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(1H-pirazol-4-il)-1,3,5-triazin-2-il]-1H-bencimidazol;
W-[3-({5-[2-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-4-pirimidinil]-2-piridinil}oxi)propil]-W,W-dimetilamina; 2-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-4,5'-bipirimidina;
2-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-4,5 '-bipirimidina;
2-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡n¡l)-2'-metox¡-4,5'-b¡p¡r¡m¡d¡na;
2-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfol¡n¡l)-4,5'-b¡p¡r¡m¡d¡na-2'-am¡na;
2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(1H-p¡razoM-¡l)-1,3,5-tr¡az¡n-2-¡l]-1H-benc¡m¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(1H-p¡razoM-¡l)-1,3,5-tr¡az¡n-2-¡l]-1H-benc¡m¡dazol-6-¡lam¡na;
2-(d¡fluoromet¡l)-4-metoxM-[4-(1-met¡MH-p¡razol-3-¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-1H-benc¡m¡dazol-6-¡lam¡na; 2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(1H-p¡razol-4-¡l)-1,3,5-tr¡az¡n-2-¡l]-1H-benc¡m¡dazol-6-¡lam¡na;
2-(d¡fluoromet¡l)-1-[4-(1H-¡m¡dazoM-¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-¡l]-4-metox¡-1H-benc¡m¡dazol; y
2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(3-p¡r¡d¡ml)-2-p¡r¡m¡d¡ml]-1H-benc¡m¡dazol-6-¡lam¡na;
y sus enant¡ómeros, mezclas de enant¡ómeros, o mezclas de dos o más d¡astereómeros; y sus sales farmacéut¡cas aceptables, solvatos e h¡dratos.
En otra real¡zac¡ón más, en este documento se ¡ncluye un compuesto selecc¡onado de:
W-[4-[6-am¡no-2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-A/-(3-p¡r¡d¡ml)amma; W5-[4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[3-(d¡met¡lam¡no)prop¡l]-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[3-(d¡met¡lam¡no)prop¡l]-W2-met¡l-2,5-p¡r¡d¡nd¡am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-(6-metox¡-3-p¡r¡d¡n¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{6-[3-(d¡met¡lam¡no)propox¡]-3-p¡r¡d¡ml}-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-W-(5-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-W-(3-p¡r¡daz¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-(1-met¡MH-¡m¡dazol-5-¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-(1-met¡MH-p¡razol-5-¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
2-(d¡fluoromet¡l)-1-[4-(1H-¡m¡dazoM-¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-¡l]-4-metox¡-1H-benc¡m¡dazol-6-am¡na;
2-(d¡fluoromet¡l)-4-metoxM-[4-(1-met¡MH-p¡razol-4-¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-1H-benc¡m¡dazol;
W-(2-{4-[4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-1H-p¡razoM-¡l}et¡l)-W,W-d¡met¡lam¡na;
W-(3-{4-[4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-1H-p¡razoM-¡l}prop¡l)-W,W-d¡met¡lam¡na; y
2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(3-p¡r¡d¡ml)-1,3,5-tr¡az¡n-2-¡l]-1H-benc¡m¡dazol-6-¡lam¡na;
y sus enant¡ómeros, mezclas de enant¡ómeros, o mezclas de dos o más d¡astereómeros; y sus sales farmacéut¡cas aceptables, solvatos y h¡dratos.
En otra real¡zac¡ón más, se proporc¡ona en este documento un compuesto selecc¡onado de:
2-(d¡fluoromet¡l)-1-[4-(4-morfol¡ml)-6-(3-p¡r¡d¡n¡l)-2-p¡r¡m¡d¡n¡l]-1H-benc¡m¡dazol;
2-(d¡fluoromet¡l)-4-metox¡-1-[4-(4-morfol¡n¡l)-6-(3-p¡r¡d¡n¡l)-2-p¡r¡m¡d¡n¡l]-1H-benc¡m¡dazol;
2-(d¡fluoromet¡l)-1-[6-(4-morfol¡ml)-2-(3-p¡r¡d¡n¡l)-4-p¡r¡m¡d¡n¡l]-1H-benc¡m¡dazol;
2-(d¡fluoromet¡l)-4-metox¡-1-[6-(4-morfol¡n¡l)-2-(3-p¡r¡d¡n¡l)-4-p¡r¡m¡d¡n¡l]-1H-benc¡m¡dazol;
2-(d¡fluoromet¡l)-1-[2-(4-morfol¡ml)-6-(3-p¡r¡d¡n¡l)-4-p¡r¡m¡d¡ml]-1H-benc¡m¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[2-(4-morfol¡ml)-6-(3-p¡r¡d¡ml)-4-p¡r¡m¡d¡ml]-1H-bendm¡dazol;
4-[4-metox¡-2-(met¡lsulfon¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-N-(3-p¡r¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-(2-p¡r¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-(2-p¡r¡d¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-(4-p¡r¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-(4-p¡r¡d¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-(4-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-(4-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-(5-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
2-(d¡fluoromet¡l)-1-[4-(4-morfol¡ml)-6-(3-p¡r¡d¡mlox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(3-p¡r¡d¡mlox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-1-[4-(4-morfol¡ml)-6-(5-p¡r¡m¡d¡mlox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(5-p¡r¡m¡d¡mlox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-(1-met¡l-1H-p¡razol-4-¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-N-(1-met¡MH-p¡razol-4-¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-(2-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-(2-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-W-(3-p¡r¡d¡n¡lmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-(3-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-(4-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-(4-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-met¡l-6-(4-morfol¡ml)-W-(2-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-met¡l-6-(4-morfolm¡l)-W-(2-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-met¡l-6-(4-morfol¡ml)-W-(3-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-met¡l-6-(4-morfolm¡l)-W-(3-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-met¡l-6-(4-morfol¡ml)-W-(4-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-met¡l-6-(4-morfolm¡l)-W-(4-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na; 2-(d¡fluoromet¡l)-1-[4-(4-morfol¡ml)-6-(2-p¡r¡d¡mlmetox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(2-p¡r¡d¡mlmetox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-1-[4-(4-morfol¡ml)-6-(3-p¡r¡d¡mlmetox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(3-p¡r¡d¡mlmetox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-1-[4-(4-morfol¡ml)-6-(4-p¡r¡d¡mlmetox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(4-p¡r¡d¡mlmetox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-[2-(2-p¡r¡d¡n¡l)et¡l]-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-[2-(2-p¡r¡d¡n¡l)et¡l]-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-[2-(3-p¡r¡d¡n¡l)et¡l]-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-[2-(3-p¡r¡d¡n¡l)et¡l]-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-[2-(4-p¡r¡d¡n¡l)et¡l]-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-N-[2-(4-p¡r¡d¡n¡l)et¡l]-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-[2-(1H-¡m¡dazol-4-¡l)et¡l]-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-N-[2-(1H-¡m¡dazol-4-¡l)et¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; W-[4-[6-am¡no-2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-A/-(3-p¡r¡d¡n¡l)am¡na;
W-[4-[2-(d¡fluoromet¡l)-6-(met¡lam¡no)-1H-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-¡l]-W-(3-p¡r¡dm¡l)am¡na; W-[4-[2-(d¡fluoromet¡l)-4-metox¡-6-(met¡lam¡no)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-A/-(3-p¡r¡d¡n¡l)am¡na;
W-[4-[2-(d¡fluoromet¡l)-6-(d¡met¡lam¡no)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W-(3-p¡r¡d¡n¡l)am¡na; W-[4-[2-(d¡fluoromet¡l)-6-(d¡met¡lam¡no)-4-metox¡-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-A/-(3-p¡r¡d¡n¡l)am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-(6-metox¡-3-p¡r¡d¡n¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-(2-metox¡-4-p¡r¡d¡n¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-(2-metox¡-4-p¡r¡d¡n¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-(2-metox¡-5-p¡r¡m¡d¡n¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-(2-metox¡-5-p¡r¡m¡d¡ml)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-{6-[2-(d¡met¡lam¡no)etox¡]-3-p¡r¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-{6-[2-(d¡met¡lam¡no)etox¡]-3-p¡r¡d¡ml}-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-{6-[2-(4-morfolm¡l)etox¡]-3-p¡r¡d¡ml}-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-{6-[2-(4-morfol¡ml)etox¡]-3-p¡r¡d¡ml}-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-{6-[3-(d¡met¡lam¡no)propox¡]-3-p¡r¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-{6-[3-(4-morfolm¡l)propox¡]-3-p¡r¡d¡ml}-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-{6-[3-(4-morfol¡ml)propox¡]-3-p¡r¡d¡ml}-1,3,5-tr¡az¡n-2-am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-met¡l-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-met¡l-2,5-p¡r¡d¡nd¡am¡na; W5-[4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2,W2-d¡met¡l-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazol-1-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2,W2-d¡met¡l-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(d¡met¡lam¡no)et¡l]-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(d¡met¡lam¡no)et¡l]-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(4-morfolm¡l)et¡l]-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-[2-(4-morfolinil)etil]-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-[2-(dimetilamino)etil]-W2-metil-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-[2-(dimetilamino)etil]-Wemetil-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-[2-(4-morfolinil)etil]-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-[2-(4-morfolinil)etil]-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-[3-(dimetilamino)propil]-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-[3-(dimetilamino)propil]-W2-metil-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-[3-(4-morfolinil)propil]-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-[3-(4-morfolinil)propil]-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-[3-(4-morfolinil)propil]-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-[3-(4-morfolinil)propil]-2,5-piridindiamina;
4-[2-(difluorometil)-1H-bencimidazoM-il]-W-{6-[2-(dimetilamino)etil]-3-piridiml}-6-(4-morfolmil)-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-{6-[2-(dimetilamino)etil]-3-piridiml}-6-(4-morfolmil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazoM-il]-6-(4-morfolmil)-W-{6-[2-(4-morfolmil)etil]-3-piridiml}-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-6-(4-morfoliml)-A/-{6-[2-(4-morfoliml)etil]-3-piridiml}-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazoM-il]-W-{2-[2-(dimetilamino)etil]-5-pirimidiml}-6-(4-morfoliml)-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-{2-[2-(dimetilamino)etil]-5-pirimidiml}-6-(4-morfolmil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-W-{2-[2-(4-morfolinil)etil]-5-pirimidinil}-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-6-(4-morfoliml)-A/-{2-[2-(4-morfoliml)etil]-5-pirimidiml}-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazol-1-il]-W-{5-[2-(dimetilamino)etoxi]-3-piridinil}-6-(4-morfolinil)-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-{5-[2-(dimetilamino)etoxi]-3-piridiml}-6-(4-morfoliml)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-6-(4-morfoliml)-A/-{5-[2-(4-morfoliml)etoxi]-3-piridiml}-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazoM-il]-6-(4-morfolmil)-W-{5-[2-(4-morfolmil)etoxil-3-piridiml}-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-1H-bencimidazol-1-il]-W-{5-[3-(dimetilamino)propoxi]-3-piridinil}-6-(4-morfolinil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-{5-[3-(dimetilamino)propoxi]-3-piridiml}-6-(4-morfoliml)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-W-{5-[3-(4-morfolinil)propoxi]-3-piridinil}-1,3,5-triazin-2-amina;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-{5-[3-(4-morfol¡ml)propox¡]-3-p¡r¡d¡ml}-1,3,5-triazin-2-amina;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-{2-[2-(d¡met¡lam¡no)etox¡]-4-p¡r¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{2-[2-(d¡met¡lam¡no)etox¡]-4-p¡r¡d¡ml}-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-W-{2-[2-(4-morfolm¡l)etox¡]-4-p¡r¡d¡ml}-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-{2-[2-(4-morfol¡ml)etox¡]-4-p¡r¡d¡ml}-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-{2-[3-(d¡met¡lam¡no)propox¡]-4-p¡r¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{2-[3-(d¡met¡lam¡no)propox¡]-4-p¡r¡d¡ml}-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-W-{2-[3-(4-morfolm¡l)propox¡]-4-p¡r¡d¡ml}-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-{2-[3-(4-morfol¡ml)propox¡]-4-p¡r¡d¡ml}-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-{2-[2-(d¡met¡lam¡no)etox¡]-5-p¡r¡m¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazoM-¡l]-A/-{2-[2-(d¡met¡lam¡no)etox¡]-5-p¡r¡m¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-{2-[3-(d¡met¡lam¡no)propox¡]-5-p¡r¡m¡d¡ml}-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{2-[3-(d¡met¡lam¡no)propox¡]-5-p¡r¡m¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-W-{2-[2-(4-morfolm¡l)etox¡]-5-p¡r¡m¡d¡ml}-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-{2-[2-(4-morfol¡ml)etox¡]-5-p¡r¡m¡d¡ml}-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-W-{2-[3-(4-morfolm¡l)propox¡]-5-p¡r¡m¡d¡ml}-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-{2-[3-(4-morfol¡ml)propox¡]-5-p¡r¡m¡d¡ml}-1,3,5-tr¡az¡n-2-am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(d¡met¡lam¡no)et¡l]-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(d¡met¡lam¡no)et¡l]-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(d¡met¡lam¡no)et¡l]-W2-met¡l-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(d¡met¡lam¡no)et¡l]-W2-met¡l-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[3-(d¡met¡lam¡no)prop¡l]-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[3-(d¡met¡lam¡no)prop¡l]-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[3-(d¡met¡lam¡no)prop¡l]-W2-met¡l-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[3-(d¡met¡lam¡no)prop¡l]-W2-met¡l-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-[2-(4-morfolinil)etil]-2,5-pirimidindiamina;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-[2-(4-morfolinil)etil]-2,5-pirimidindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-[2-(4-morfolinil)etil]-2,5-pirimidindiamina;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-[2-(4-morfolinil)etil]-2,5-pirimidindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-[3-(4-morfolinil)propil]-2,5-pirimidindiamina;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-[3-(4-morfolinil)propil]-2,5-pirimidindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-[3-(4-morfolinil)propil]-2,5-pirimidindiamina;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-[3-(4-morfolinil)propil]-2,5-pirimidindiamina;
4-[2-(difluorometil)-1H-bencimidazoM-il]-W-[6-(4-metiM-piperaziml)-3-piridiml]-6-(4-morfolmil)-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-[6-(4-metiM-piperazinil)-3-piridiml]-6-(4-morfolmil)-1,3,4-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazoM-il]-W-[2-(4-metiM-piperaziml)-5-pirimidiml]-6-(4-morfoliml)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-[2-(4-metiM-piperazinil)-5-pirimidiml]-6-(4-morfolmil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazoM-il]-W-{6-[4-(dimetilamino)-1-piperidiml]-3-piridiml}-6-(4-morfolmil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-{6-[4-(dimetilamino)-1-piperidiml]-3-piridiml}-6-(4-morfoliml)-1.3.5- triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazol-1-il]-W-{2-[4-(dimetilamino)-1-piperidinil]-5-pirimidinil}-6-(4-morfolinil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-{2-[4-(dimetilamino)-1-piperidiml]-5-pirimidiml}-6-(4-morfolmil)-1.3.5- triazin-2-amina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-(1-metil-4-piperidinil)-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-(1-metil-4-piperidinil)-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-(1-metil-4-piperidinil)-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-(1-metil-4-piperidinil)-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-(1-metil-4-piperidinil)-2,5-pirimidindiamina;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-(1-metil-4-piperidinil)-2,5-pirimidindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-(1-metil-4-piperidinil)-2,5-pirimidindiamina;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-(1-metil-4-piperidinil)-2,5-pirimidindiamina;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-N-{6-[(1-met¡l-4-p¡per¡d¡ml)ox¡]-3-p¡r¡d¡ml}-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-amina;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{6-[(1-met¡l-4-p¡per¡d¡ml)ox¡]-3-p¡r¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-{2-[(1-met¡l-4-p¡per¡d¡ml)ox¡]-5-p¡r¡m¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{2-[(1-met¡l-4-p¡per¡d¡ml)ox¡]-5-p¡r¡m¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-{6-[(1-met¡l-3-p¡rrol¡d¡n¡l)ox¡]-3-p¡r¡d¡ml}-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazoM-¡l]-A/-{6-[(1-met¡l-3-p¡rrol¡d¡ml)ox¡]-3-p¡r¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-{2-[(1-met¡l-3-p¡rrol¡d¡n¡l)ox¡]-5-p¡r¡m¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{2-[(1-met¡l-3-p¡rrol¡d¡ml)ox¡]-5-p¡r¡m¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-{1-[2-(d¡met¡lam¡no)et¡l]-1H-p¡razol-4-yl}-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{1-[2-(d¡met¡lam¡no)et¡l]-1H-p¡razol-4-¡l}-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-W-{1-[2-(4-morfol¡n¡l)et¡l]-1H-p¡razol-4-¡l}-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-{1-[2-(4-morfol¡ml)et¡l]-1H-p¡razol-4-¡l}-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-W-{1-[3-(d¡met¡lam¡no)prop¡l]-1H-p¡razol-4-¡l}-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{1-[3-(d¡met¡lam¡no)prop¡l]-1H-p¡razol-4-¡l}-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-W-{1-[3-(4-morfol¡n¡l)prop¡l]-1H-p¡razol-4-¡l}-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-{1-[3-(4-morfol¡ml)prop¡l]-1H-p¡razol-4-¡l}-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-W-(1,3-t¡azol-5-¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-(1,3-t¡azol-5-¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-W-{2-[(d¡met¡lam¡no)met¡l]-1,3-t¡azol-5-¡l}-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{2-[(d¡met¡lam¡no)met¡l]-1,3-t¡azol-5-¡l}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-W-[2-(4-morfol¡n¡lmet¡l)-1,3-t¡azol-5-¡l]-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-[2-(4-morfol¡mlmet¡l)-1,3-t¡azol-5-¡l]-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-(1-met¡MH-¡m¡dazol-5-¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-W-(1-met¡l-1H-1,2,3-tr¡azol-5-¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-(1-met¡MH-1,2,3-tr¡azol-5-¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-(2-met¡l-2H-1,2,3-tr¡azol-4-¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-(2-met¡l-2H-1,2,3-tr¡azol-4-¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-(1-met¡MH-1,2,3-tr¡azol-4-¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-(1-met¡MH-1,2,3-tr¡azol-4-¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-(2-met¡l-2H-tetrazol-5-¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-(2-met¡l-2H-tetrazol-5-¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-(1-met¡MH-tetrazol-5-¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4- [2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-(1-met¡MH-tetrazol-5-¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na; 2-(d¡fluoromet¡l)-1-[4-(4-morfol¡ml)-6-(4-p¡r¡d¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(4-p¡r¡d¡ml)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-1-[4-(4-morfol¡ml)-6-(5-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(5-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-1-[4-(2-metox¡-5-p¡r¡m¡d¡n¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(2-metox¡-5-p¡r¡m¡d¡n¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-1-[4-(6-metox¡-3-p¡r¡d¡n¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(6-metox¡-3-p¡r¡d¡ml)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-1-[4-(5-metox¡-3-p¡r¡d¡n¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(5-metox¡-3-p¡r¡d¡ml)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-1-[4-(2-metox¡-4-p¡r¡d¡n¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(2-metox¡-4-p¡r¡d¡ml)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-1-[4-(1-met¡MH-p¡razol-4-¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metox¡-1-[4-(1-met¡MH-p¡razol-4-¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-1-[4-(4-morfol¡ml)-6-(1,3-t¡azol-5-¡l)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(1,3-t¡azol-5-¡l)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
W5-[4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-2,5-p¡r¡m¡dmd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-2,5-p¡r¡m¡d¡nd¡am¡na;
5- [4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-2-p¡r¡d¡nam¡na;
5-[4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-¡l]-2-p¡r¡d¡nam¡na;
5-[4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-2-p¡r¡m¡dmam¡na;
5-[4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-¡l]-2-p¡r¡m¡dmam¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-(2-p¡raz¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-(2-p¡raz¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
W2-[4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-2,5-p¡raz¡nd¡am¡na;
W2-[4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazol-1-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-2,5-p¡raz¡nd¡am¡na;
W2-[4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-2, 6-p¡raz¡nd¡am¡na;
W2-[4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazol-1-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-2,6-p¡raz¡nd¡am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-(6-metox¡-2-p¡raz¡n¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-(6-metox¡-2-p¡raz¡ml)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na; 6-[4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-2-p¡raz¡nam¡na;
6-[4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-2-p¡razmam¡na;
2-(d¡fluoromet¡l)-1-[4-(6-metox¡-2-p¡raz¡n¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-1H-benc¡m¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(6-metox¡-2-p¡raz¡n¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-1H-benc¡m¡dazol; y
W-[4-[6-am¡no-2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-A/-(3-p¡r¡d¡ml)amma; y sus enant¡ómeros, mezclas de enant¡ómeros, o mezclas de dos o más d¡astereómeros; y sus sales farmacéut¡cas aceptables, solvatos y h¡dratos.
En otra real¡zac¡ón más, se proporc¡ona en este documento un compuesto selecc¡onado de:
W-[4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-3-qu¡nol¡nam¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-W-(2-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-W-(4-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-W-(5-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-(4-metox¡-3-p¡r¡d¡n¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-(6-fluoro-3-p¡r¡d¡n¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
W-(6-cloro-3-p¡r¡dm¡l)-4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-(2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l)-A/-(6-metox¡p¡r¡m¡d¡n-4-¡l)-6-morfol¡no-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-(3-p¡r¡daz¡n¡l)-1,3,5-tr¡az¡n-2-am¡na; y
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-(6-metox¡-3-p¡r¡daz¡n¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na; y sus enant¡ómeros, mezclas de enant¡ómeros, o mezclas de dos o más d¡astereómeros; y sus sales farmacéut¡cas aceptables, solvatos y h¡dratos.
En otra real¡zac¡ón más, se proporc¡ona en este documento un compuesto selecc¡onado de:
4-(4-(2-(d¡fluoromet¡l)-4-metoxMH-benzo[d]¡m¡dazoM-¡l)-7-(p¡r¡d¡n-3-¡l)-6,7-d¡h¡dro-5H-p¡rrolo[2,3-d]p¡r¡m¡d¡n-2-¡l)morfol¡na;
4-(4-(2-(d¡fluoromet¡l)-4-metox¡-1H-benzo[d]¡m¡dazol-1-¡l)-7-(p¡r¡d¡n-3-¡l)-7H-p¡rrolo [2,3-d]p¡r¡m¡d¡n-2-¡l)morfol¡na; 4-(6-(2-(d¡fluoromet¡l)-4-metox¡-1H-benzo[d]¡m¡dazol-1-¡l)-9-(p¡r¡d¡n-3-¡l)-9H-pur¡n-2-¡l)morfol¡na;
4-(7-(2-(d¡fluoromet¡l)-4-metox¡-1H-benzo[d]¡m¡dazol-1-¡l)-3-(p¡r¡d¡n-3-¡l)-3H-[1,2,3]tr¡azolo[4,5-d]p¡r¡m¡d¡n-5-¡l)morfol¡na;
4-(2-(2-(d¡fluoromet¡l)-4-metox¡-1H-benzo[d]¡m¡dazol-1-¡l)-9-(p¡r¡d¡n-3-¡l)-9H-pur¡n-6-¡l)morfol¡na;
4-(5-(2-(d¡fluoromet¡l)-4-metox¡-1H-benzo[d]¡m¡dazol-1-¡l)-3-(p¡r¡d¡n-3-¡l)-3H-[1,2,3]tr¡azolo[4,5-d]p¡r¡m¡d¡n-7-¡l)morfol¡na;
2-[2-(d¡fluoromet¡l)-4-metox¡-1H-benzo[d]¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-9-(3-p¡r¡d¡n¡l)-9H-pur¡na;
2-[2-(d¡fluoromet¡l)-4-metox¡-1H-benzo[d]¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-9-(5-p¡r¡m¡d¡n¡l)-9H-pur¡na;
6-[2-(d¡fluoromet¡l)-4-metox¡-1H-benzo[d]¡m¡dazol-1-¡l]-2-(4-morfol¡n¡l)-9-(3-p¡r¡d¡n¡l)-9H-pur¡na; y
6-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-2-(4-morfol¡n¡l)-9-(5-p¡r¡m¡d¡n¡l)-9H-pur¡na;
y sus enant¡ómeros, mezclas de enant¡ómeros, o mezclas de dos o más d¡astereómeros; y sus sales farmacéut¡cas aceptables, solvatos y h¡dratos.
Se pretende que los compuestos proporcionados en este documento abarquen a todos los estereoisómeros posibles, a menos que sea especificada alguna estereoquímica particular. Cuando el compuesto proporcionado en este documento contiene un grupo alquenilo o alquenileno, el compuesto puede existir como una o mezcla de isómeros geométricos cis/trans (o Z/E). Si los isómeros estructurales fueran interconvertibles, el compuesto podría existir como un solo tautómero o una mezcla de tautómeros. Esto puede tomar la forma de tautomerismo del protón en el compuesto que contiene, por ejemplo, un grupo imino, cetona u oxima; o el llamado tautomerismo de valencia en el compuesto que contiene una fracción aromática. De ello se desprende que un solo compuesto puede exhibir más de un tipo de isomerismo.
Los compuestos proporcionados en este documento pueden ser enantioméricamente puros, tales como un solo enantiómero o un solo diastereómero, o ser mezclas estereoisoméricas, tales como una mezcla de enantiómeros, por ejemplo, una mezcla racémica de dos enantiómeros; o una mezcla de dos o más diastereómeros. Como tal, cualquier experto en la técnica reconocerá que la administración de un compuesto en su forma (R) es equivalente, para compuestos que sufren de epimerización in vivo, a la administración del compuesto en su forma (S). Las técnicas convencionales para la preparación/aislamiento de enantiómeros individuales incluyen la síntesis de un precursor ópticamente puro adecuado, la síntesis asimétrica a partir de los materiales de partida aquirales, o la resolución de una mezcla enantiomérica, por ejemplo, cromatografía quiral, recristalización, resolución, formación de la sal diastereomérica, o derivatización en aductores diastereoméricos seguido por su separación.
Si el compuesto proporcionado en este documento contiene una fracción ácida o básica, también se puede proporcionar como una sal farmacéutica aceptable (Ver Berge et al., J. Pharm. Sci. 1977, 66, 1-19; y "Handbook of Pharmaceutical Salts, Properties, and Use", Stahl y Wermuth, Ed.; Wiley-VCH y VHCA, Zurich, 2002).
Los ácidos apropiados para su uso en la preparación de las sales farmacéuticamente aceptables incluyen, entre otros, ácido acético, ácido 2,2-dicloroacético, aminoácidos acilados, ácido adípico, ácido algínico, ácido ascórbico, ácido L-aspartico, ácido bencenosulfónico, ácido benzoico, ácido 4-acetamidobenzoico, ácido bórico, (+)-ácido alcanfórico, ácido alcanforsulfónico, (+)-(1S)-ácido alcanfor-10-sulfónico, ácido cáprico, ácido caproico, ácido caprílico, ácido cinámico, ácido cítrico, ácido ciclámico, ácido ciclohexanosulfámico, ácido dodecilsulfúrico, ácido etano-1,2-disulfónico, ácido etanosulfónico, ácido 2-hidroxi-etanosulfónico, ácido fórmico, ácido fumarico, ácido galactarico, ácido gentísico, ácido glucoheptónico, ácido D-glucónico, ácido D-glucurónico, ácido L-glutámico, ácido a-oxoglutárico, ácido glicólico, ácido hipúrico, ácido bromhídrico, ácido clorhídrico, ácido yodhídrico, (+)-ácido l-láctico, (±)-ácido DL-láctico, ácido lactobiónico, ácido laúrico, ácido maleico, (-)-ácido L-málico, ácido malónico, (±)-ácido DL-mandélico, ácido metansulfónico, ácido naftaleno-2-sulfónico, ácido naftaleno-1,5-disulfónico, ácido 1-hidroxi-2-naftoico, ácido nicotínico, ácido nítrico, ácido oleico, ácido orótico, ácido oxálico, ácido palmítico, ácido pamoico, ácido perclórico, ácido fosfórico, ácido L-piroglutámico, ácido sacárico, ácido salicílico, ácido 4-amino-salicílico, ácido sebácico, ácido esteárico, ácido succínico, ácido sulfúrico, ácido tánico, (+)-ácido L-tartárico, ácido tiociánico, ácido p-toluenosulfónico, ácido undecilénico y ácido valérico.
Bases apropiadas para su uso en la preparación de sales farmacéuticas aceptables, incluyendo, entre otras, bases inorgánicas, tales como hidróxido de magnesio, hidróxido de calcio, hidróxido de potasio, hidróxido de zinc o hidróxido de sodio; y bases orgánicas, como las aminas primarias, secundarias, terciarias y cuaternarias, alifáticas y aromáticas, incluyendo L-arginina, benetamina, benzatina, colina, deanol, dietanolamina, dietilamina, dimetilamina, dipropilamina, diisopropilamina, 2-(dietilamino)-etanol, etanolamina, etilamina, etilendiamamina, isopropilamina, N-metil-glucamina, hidrabamina, 1H-imidazol, L-lisina, morfolina, 4-(2-hidroxietil)-morfolina, metilamina, piperidina, piperazina, propilamina, pirrolidina, 1-(2-hidroxietil)-pirrolidina, piridina, quinuclidina, quinolina, isoquinolina, aminas secundarias, trietanolamina, trimetilamina, trietilamina, N-metil-D-glucamina, 2-amino-2-(hidroximetil)-1,3-propanodiol y trometamina.
En ciertas realizaciones, los compuestos proporcionados en este documento son las sales farmacológicamente aceptables de los compuestos con uno o más de los ácidos clorhídrico, sulfúrico, fosfórico, acético, cítrico, oxálico, malónico, salicílico, málico, fumarico, sucinto, ascórbico, maleico, metanosulfónico e isetónico; o con uno o más de carbonato de potasio, hidróxido de sodio o potasio, amoníaco, trietilamina y trietanolamina.
Métodos de síntesis
El compuesto proporcionado en este documento puede ser preparado, aislado u obtenido por cualquier método conocido por cualquier experto en la técnica, y los siguientes ejemplos son sólo representativos y no excluyen otros procedimientos relacionados.
Por ejemplo, los compuestos de la fórmula I se pueden preparar via sustitución aromática de un halo-1,3,5-triazina o halo-pirimidina, por ejemplo, cloro-1,3,5-triazina 1, con Hu R6 (Método A), como se ilustra en el esquema 1, donde U es N, O o S.
Los compuestos de la fórmula I donde U es un enlace sencillo se pueden preparar por medio de la sustitución de un grupo halo de un halo-1,3,5-triazina o halopirimidina con un grupo R6, por ejemplo, a través del acoplamiento de Suzuki mediante el uso de un ácido borónico o éster de boronato de R6 bajo condiciones de reacción catalizadas por paladio (método B), como se ilustra en el esquema 2, donde R es hidrógeno o alquilo.
La halo-1,3,5-triazina o halo-pirimidina utilizada en los métodos A y B también puede ser preparada, aisladas, u obtenida por cualquier método conocido por cualquier experto en la técnica. Por ejemplo, la halo-1,3,5-triazina se puede preparar a través de reacciones de sustitución aromática de clorotriazina con dos aminas diferentes, compuestos 2 y 4, como se muestra en el esquema 3.
Esquema 2
Los compuestos de la fórmula I también se pueden preparar mediante la combinación de una unidad de bencimidazol con una unidad de pirimidinilo o 1,3,5-triazinilo que contenga un enlace U-R6 preformado (método C), como se ilustra en el esquema 4.
El bencimidazol 4 utilizado en los esquemas 3 y 4 también puede ser preparado, aislado u obtenido por cualquier método conocido por cualquier experto en la técnica. Por ejemplo, el bencimidazol 4 puede ser como se muestra en el esquema 5.
Los compuestos de la fórmula I pueden prepararse mediante la modificación de los compuestos existentes de la fórmula I (método D), como se ilustra en el esquema 6, donde R1A, R2A, R3A, R4A, R5A, R6Ay UA se definen igual que R1, R2, R3, R4, R5 R6y U, respectivamente, pero al menos uno de R1A, R2A, R3A, R4A, R5A, R6A o UA es diferente de R1, R2, R3, R4, R5, R6o U.
Los compuestos de la fórmula I, IA o IB también se pueden preparar como se muestra en el Esquema 7.
Composiciones farmacéuticas
En una realización, se proporciona en este documento una composición farmacéutica que comprende un compuesto de fórmula I, IAo IB según se define en este documento, y un excipiente, adyuvante, vehículo, tampón o estabilizador farmacéuticos aceptables.
En una realización, el excipiente, coadyuvante, vehículo, tampón o estabilizador farmacéuticos aceptables no es tóxico y no interfiere con la eficacia del ingrediente activo. La naturaleza precisa del vehículo u otro material dependerá de la vía de administración, que puede ser oral o por inyección, como la inyección cutánea, subcutánea o intravenosa. En otra realización, se proporcionan composiciones farmacéuticas en una forma de dosificación para la administración parenteral, y uno o más excipientes o vehículos farmacéuticos aceptables. Cuando se puedan formular composiciones farmacéuticas para la inyección intravenosa, cutánea o subcutánea, el ingrediente estará en la forma de una solución acuosa aceptable parenteral, sin pirógenos y con un pH, isotonicidad y estabilidad adecuadas. Los expertos en la técnica pueden preparar soluciones adecuadas utilizando, por ejemplo, vehículos isotónicos, tales como inyección de cloruro de sodio, inyección de Ringer o inyección de Ringer lactato. Pueden incluirse, según sea necesario, conservantes, estabilizadores, tampones, antioxidantes y/u otros aditivos.
En una realización, se proporcionan composiciones farmacéuticas en una forma de dosificación para la administración oral, que comprenden el compuesto proporcionado en este documento, y uno o más excipientes o vehículos farmacéuticos aceptables. Las composiciones farmacéuticas proporcionadas en este documento que se formulan para la administración oral pueden estar en forma de tableta, cápsula, polvos o líquida. Un comprimido puede abarcar un vehículo sólido o un coadyuvante. Las composiciones farmacéuticas líquidas generalmente comprenden un vehículo líquido como agua, vaselina, aceites animales o vegetales, o aceite mineral o aceite sintético. Se puede incluir solución
salina fisiológica, dextrosa u otra solución de sacáridos, o glicoles como etilenglicol, propilenglicol o polietilenglicol. Una cápsula puede abarcar un vehículo sólido como la gelatina.
En otra realización más, se proporcionan composiciones farmacéuticas en una forma de dosificación para la administración tópica, que comprenden el compuesto proporcionado en este documento, y uno o más excipientes o vehículos farmacéuticos aceptables.
Las composiciones farmacéuticas también se pueden formular como formas de dosificación de liberación modificada, incluyendo las formas de administración retardada, extendida, prolongada, sostenida, pulsátil, controlada, acelerada y rápida, dirigida, de liberación programada y de retención gástrica. Estas formas de administración se pueden preparar de acuerdo a los métodos y técnicas convencionales conocidos por los expertos en la técnica (Ver, The Science and Practice of Pharmacy, supra; Modified-Release Drug Delivery Technology, 2a edición, Rathbone et al., eds., Marcel Dekker, Inc.: Nueva York, NY, 2008).
Las composiciones farmacéuticas proporcionadas en este documento se pueden proporcionar en una forma de administración unitaria o forma de administración múltiple. Una forma de administración unitaria, como se usa en este documento, se refiere a una unidad físicamente discreta adecuada para la administración a un sujeto humano y animal, y envasada individualmente como se conoce en la técnica. Cada dosis unitaria contiene una cantidad predeterminada de ingrediente(s) activo(s) suficiente para producir el efecto terapéutico deseado, en asociación con los vehículos farmacéuticos o excipientes requeridos. Los ejemplos de formas de administración unitaria incluyen las ampollas, jeringuillas y tabletas y las cápsulas individualmente envasadas. Una forma de administración unitaria se puede administrar en fracciones o múltiplos de éstas. Una forma de administración múltiple es una pluralidad de formas idénticas de administración unitaria envasadas en un solo envase que se administrará en una forma de administración unitaria segregada. Los ejemplos de formas de administración múltiple incluyen los viales, botellas de tabletas o cápsulas, o botellas de pintas o de galones.
Las composiciones farmacéuticas proporcionadas en este documento se pueden administrar a la vez, o varias veces a intervalos de tiempo. Se entiende que la dosis exacta y la duración del tratamiento pueden variar con la edad, el peso, y la condición del paciente que está siendo tratado, y se pueden determinar empíricamente usando conocidos protocolos de prueba o mediante extrapolación a partir de datos de prueba o diagnósticos in vivo o in vitro. Se entiende además que para cualquier individuo particular, los regímenes de dosificación específicos deben ajustarse con el tiempo según la necesidad individual y el criterio profesional de la persona que administra o supervisa la administración de las formulaciones.
En otra realización, las composiciones farmacéuticas proporcionadas en este documento comprenden además uno o más agentes quimioterapéuticos según se definen en este documento.
En otra realización más, se proporciona en este documento el uso de un compuesto de fórmula I, IA, o IB en la fabricación de un medicamento para el tratamiento del cáncer. En ciertas realizaciones, el medicamento está en la forma de una tableta, cápsula, polvos o líquidos. En ciertas realizaciones, el medicamento se formula según lo descrito en este documento.
A. Administración oral
Las composiciones farmacéuticas proporcionadas en este documento para la administración oral se pueden proporcionar en formas sólidas, semisólidas, o líquidas de dosificación para la administración oral. Como se usa en este documento, la administración oral también incluye la administración bucal, lingual y sublingual. Las formas de dosificación orales adecuadas incluyen, entre otras, tabletas, tabletas de disolución rápida, masticables, cápsulas, píldoras, tiras, tabletas para disolver en la boca, pastillas, sobres, peletes, chicles, polvos a granel, polvos o gránulos efervescentes o no efervescentes, aerosoles orales, soluciones, emulsiones, suspensiones, obleas, pulverizaciones, elixires y jarabes. Además del ingrediente o los ingredientes activos, las composiciones farmacéuticas pueden contener uno o más vehículos o excipientes farmacéuticos aceptables, incluyendo, entre otros, aglutinantes, rellenos, diluyentes, desintegrantes, agentes humectantes, lubricantes, agentes deslizantes, colorantes, inhibidores de la migración de colorantes, edulcorantes, agentes aromatizantes, agentes emulsionantes, agentes de suspensión y dispersión, conservantes, disolventes, líquidos no acuosos, ácidos orgánicos y fuentes de dióxido de carbono.
Los aglutinantes o granuladores imparten cohesión a las tabletas para asegurar que el comprimido permanezca intacto después de la compresión. Los aglutinantes o granuladores adecuados incluyen, entre otros, almidones, como el almidón de maíz, la fécula de patata y el almidón pregelatinizado (p. ej., STARCh 1500); gelatina, azúcares, como la sacarosa, la glucosa, la dextrosa, la melaza y la lactosa; gomas naturales y sintéticas, tales como acacia, ácido alginico, alginatos, extracto de musgo irlandés, chicle de Panwar, goma de Ghatti, mucílago de las cáscaras de Isabgol, carboximetilcelulosa, metilcelulosa, polivinilpirrolidona (PVP), Veegum, arabogalactan del alerce, tragacanto pulverizado, y goma guar; celulósicas, como etilcelulosa, acetato de celulosa, carboximetilcelulosa cálcica, carboximetilcelulosa de sodio, metilcelulosa, hidroxietilcelulosa (HEC), hidroxipropilcelulosa (HPC), hidroxipropil metilcelulosa (HPMC); celulosas microcristalinas, como AVICEL-PH-101, AVICEL-PH-103, AVICEL RC-581, AVICEL-PH-105 (FMC Corp., Marcus Hook, PA); y sus mezclas. Los rellenos apropiados incluyen, entre otros, talco, carbonato de calcio, celulosa microcristalina, celulosa en polvo, dextratos, caolín, manitol, ácido silícico, sorbitol, almidón, almidón
pre-gelatinizado y sus mezclas. La cantidad de un aglutinante o relleno en las composiciones farmacéuticas proporcionadas en este documento varía según el tipo de formulación, y es fácilmente discernible para los expertos ordinarios en la técnica. El aglutinante o relleno puede estar presente de aproximadamente 50 a aproximadamente 99% en peso en las composiciones farmacéuticas proporcionadas en este documento.
Los diluyentes apropiados incluyen, entre otros, fosfato dicálcico, sulfato de calcio, lactosa, sorbitol, sacarosa, inositol, celulosa, caolín, manitol, cloruro sódico, almidón seco y azúcar en polvo. Ciertos diluyentes, como manitol, lactosa, sorbitol, sacarosa e inositol, cuando están presentes en suficiente cantidad, puede impartir propiedades a algunas tabletas comprimidas para permitir la desintegración en la boca masticando. Estas tabletas comprimidas se pueden utilizar como comprimidos masticables. La cantidad de un diluyente en las composiciones farmacéuticas proporcionadas en este documento varía según el tipo de formulación, y es fácilmente discernible para los expertos ordinarios en la técnica.
Los desintegrantes apropiados incluyen, entre otros, agar; bentonita, celulósicas, como metilcelulosa y carboximetilcelulosa; productos de madera; esponja natural; resinas de intercambio catiónico; ácido alginico; gomas, como goma guary Veegum HV; pulpa de cítricos; celulosas reticulantes, como croscarmelosa; polímeros reticulantes, como la crospoviona; almidones reticulantes; carbonato cálcico; celulosa microcristalina, como el glicolato sódico de almidón; polacrilina potásico; almidones, como almidón de maíz, fécula de patata, almidón de tapioca y almidón pregelatinizado; arcillas; lodos y sus mezclas. La cantidad de un agente desintegrante en las composiciones farmacéuticas proporcionada en este documento varía según el tipo de formulación, y es fácilmente discernible para los expertos ordinarios en la técnica. La cantidad de un agente desintegrante en las composiciones farmacéuticas proporcionada en este documento varía según el tipo de formulación, y es fácilmente discernible para los expertos ordinarios en la técnica. Las composiciones farmacéuticas proporcionadas en este documento pueden contener de aproximadamente 0,5 a aproximadamente 15% o de aproximadamente 1 a aproximadamente 5% en peso de un agente desintegrante.
Los lubricantes adecuados incluyen, entre otros, estearato de calcio; estearato de magnesio; aceite mineral; aceite mineral ligero; glicerina; sorbitol; manitol; glicoles, como el behenato de glicerol y el polietilenglicol (PEG); ácido esteárico; lauril sulfato de sodio; talco; aceite vegetal hidrogenado, incluyendo el aceite de cacahuete, el aceite de semilla de algodón, el aceite de girasol, el aceite de sésamo, el aceite de oliva, el aceite de maíz y el aceite de soja; estearato de zinc; oleato de etilo; laureato de etilo; agar; almidón; licopodio; geles de sílice o sílice, como AEROSIL® 200 (W.R. Grace Co., Baltimore, MD) y CAB-O-SIL® (Cabot Co. de Boston, MA); y sus mezclas. Las composiciones farmacéuticas proporcionadas en este documento pueden contener de aproximadamente 0,1 a aproximadamente 5% en peso de un lubricante.
Los agentes deslizantes adecuados incluyen, entre otros, dióxido de silicio coloidal, CAB-O-SIL® (Cabot Co. de Boston, MA), y talco sin amianto. Los agentes colorantes apropiados incluyen, entre otros, cualquiera de los colorantes FD&C aprobados, certificados, solubles en agua, y colorantes FD&C insolubles en agua suspendidos en hidrato de alúmina, y pigmentos lake y mezclas de los mismos. Un pigmento lake es la combinación por adsorción de un colorante soluble en agua a un óxido hidruro de un metal pesado, dando como resultado una forma insoluble del tinte. Los agentes aromatizantes adecuados incluyen, entre otros, aromatizantes naturales extraídos de plantas, como frutas, y mezclas sintéticas de compuestos que producen una agradable sensación gustativa, como la hierbabuena y el salicilato de metilo. Los agentes edulcorantes apropiados incluyen, entre otros, sacarosa, lactosa, manitol, jarabes, glicerina y edulcorantes artificiales, como la sacarina y el aspartamo. Los agentes emulsionantes apropiados incluyen, entre otros, gelatina, acacia, tragacanto, bentonita y tensioactivos, tales como el monooleato del sorbitán del polioxietileno (Tween ® 20), polioxietileno sorbitán monooleato 80 (Tween® 80), y oleato de trietanolamina. Los agentes de suspensión y de dispersión adecuados incluyen, entre otros, carboximetilcelulosa de sodio, pectina, tragacanto, Veegum, acacia, carbometilcelulosa de sodio, hidroxipropil-metilcelulosa, y polivinilpirrolidona. Los conservantes adecuados incluyen, entre otros, glicerina, metil y propilparabeno, ácido benzoico, benzoato de sodio y alcohol. Los agentes humectantes adecuados incluyen, entre otros, monoestearato de propilenglicol, monooleato de sorbitán, monolaurato de dietilenglicol, y éter de polioxietileno lauril. Los disolventes apropiados incluyen, entre otros, glicerina, sorbitol, alcohol etílico, yjarabe. Los líquidos no acuosos adecuados utilizados en emulsiones incluyen, entre otros, aceite mineral y aceite de semilla de algodón. Los ácidos orgánicos adecuados incluyen, entre otros, ácido cítrico y tartárico. Las fuentes apropiadas de dióxido de carbono incluyen, entre otras, bicarbonato sódico y carbonato sódico.
Debe entenderse que muchos vehículos y excipientes pueden ofrecer varias funciones, incluso dentro de la misma formulación.
Las composiciones farmacéuticas proporcionadas en este documento para la administración oral se pueden proporcionar como tabletas comprimidas, triturados de tabletas, pastillas masticables, tabletas de disolución rápida, tabletas comprimidas múltiples, o tabletas de capas entéricas, revestidas de azúcar, o comprimidos recubiertos con películas. Los comprimidos entéricos recubiertos son comprimidos recubiertos con sustancias que resisten la acción del ácido estomacal pero que se disuelven o se desintegran en el intestino, protegiendo así los ingredientes activos del ambiente ácido del estómago. Los recubrimientos entéricos incluyen, entre otros, ácidos grasos, grasas, salicilato de fenilo, ceras, goma laca, goma laca amoniada y acetato ftalatos de celulosa. Las tabletas recubiertas de azúcar
son tabletas comprimidas rodeadas por un recubrimiento de azúcar, que puede ser beneficioso para encubrir sabores u olores objetables y para proteger las tabletas de la oxidación. Las tabletas recubiertas con película son tabletas comprimidas que están cubiertas con una capa delgada o una película de un material soluble en agua. Los recubrimientos de película incluyen, entre otros, hidroxietilcelulosa, carboxilmetilcelulosa de sodio, polietilenglicol 4000, y el acetato ftalato de celulosa. El recubrimiento de película imparte las mismas características generales que el recubrimiento de azúcar. Las tabletas comprimidas múltiples son tabletas comprimidas hechas por más de un ciclo de compresión, incluyendo tabletas en capas, y comprimidos recubiertos a presión o recubiertos con recubrimiento en seco.
Las formas de dosificación de tabletas pueden prepararse a partir del ingrediente activo en forma de polvos, cristalinas o granulares, solas o en combinación con uno o más vehículos o excipientes descritos en este documento, incluyendo aglutinantes, desintegrantes, polímeros de liberación controlada, lubricantes, diluyentes y/o colorantes. Los agentes aromatizantes y edulcorantes son especialmente útiles en la formación de tabletas y pastillas masticables.
Las composiciones farmacéuticas proporcionadas en este documento para la administración oral pueden proporcionarse como cápsulas blandas o duras, que se pueden hacer de gelatina, metilcelulosa, almidón o alginato de calcio. La cápsula de gelatina dura, también conocida como cápsula de relleno seco (DFC), consta de dos secciones, una recubriendo la otra, lo que encierra completamente el ingrediente activo. La cápsula elástica blanda (SEC) es una carcasa blanda y globular, como una carcasa de gelatina, que es plastificada por la adición de glicerina, sorbitol, o un poliol similar. Las carcasas de gelatina blanda pueden contener un conservante para prevenir el crecimiento de microorganismos. Los conservantes apropiados son los que se describen en este documento, incluyendo metil-y propil-parabenos, y ácido sórbico. Las formas de dosificación líquidas, semisólidas y sólidas proporcionadas en este documento pueden ser encapsuladas en una cápsula. Las formas de dosificación líquidas y semisólidas adecuadas incluyen soluciones y suspensiones en carbonato de propileno, aceites vegetales o triglicéridos. Las cápsulas que contienen estas soluciones se pueden preparar como se describe en U.S. Pat. Nos.
4.328.245; 4.409.239; y 4.410.545. Las cápsulas también pueden estar recubiertas como es conocido por los expertos en la técnica con el fin de modificar o mantener la disolución del ingrediente activo.
Las composiciones farmacéuticas proporcionadas en este documento para la administración oral se pueden proporcionar en formas de administración líquidas y semisólidas, incluyendo emulsiones, soluciones, suspensiones, elixires y jarabes. Una emulsión es un sistema de dos fases, en el cual un líquido se dispersa en forma de pequeños glóbulos a través de otro líquido, que puede ser aceite-en-agua o agua-en-aceite. Las emulsiones pueden incluir un líquido o disolvente, agente emulsionante y conservante no acuoso farmacéuticamente aceptable. Las suspensiones pueden incluir un agente de suspensión y un conservante farmacéuticamente aceptable. Las soluciones alcohólicas acuosas pueden incluir un acetal farmacéuticamente aceptable, tal como un acetal de di(alquilo inferior) de un aldehído de alquilo inferior, por ejemplo, acetaldehído dietílico de acetal; y un disolvente miscible en agua que tiene uno o más grupos hidroxilo, tales como propilenglicol y etanol. Los elixires son soluciones claras, endulzadas e hidroalcohólicas. Los jarabes son soluciones acuosas concentradas de un azúcar, por ejemplo, sacarosa, y también pueden contener un conservante. Para una forma de dosificación líquida, por ejemplo, una solución en un polietilenglicol puede diluirse con una cantidad suficiente de un vehículo líquido farmacéuticamente aceptable, por ejemplo, agua, que se mide adecuadamente para la administración.
Otras formas útiles de dosificación líquida y semisólida incluyen, entre otras, las que contienen el ingrediente o los ingredientes activos proporcionados en este documento, y un mono o polialquilenglicol dialquilado, incluyendo, 1,2-dimetoximetano, diglima, triglima, tetraglima, polietilenglicol-350-dimetil éter, polietilenglicol-550-dimetil éter, polietilenglicol-750-dimetil éter, en donde 350, 550, y 750 se refieren al peso molecular promedio aproximado del polietilenglicol. Estas formulaciones pueden abarcar aún más uno o más antioxidantes, tales como hidroxitolueno butilado (BHT), hidroxianisol butilado (BHA), galato de propilo, vitamina E, hidroquinona, hidroxicoumarinas, etanolamina, lecitina, cefalina, ácido ascórbico, ácido málico, sorbitol, ácido fosfórico, bisulfito, metabisulfito de sodio, ácido tiodipropiónico y sus ésteres, y ditiocarbamatos.
Las composiciones farmacéuticas proporcionadas en este documento para la administración oral se pueden también proporcionar en las formas de liposomas, micelas, microesferas o nanosistemas. Las formas de dosificación micelar se pueden preparar como se describe en U.S. Pat. No. 6.350.458.
Las composiciones farmacéuticas proporcionadas en este documento para la administración oral se pueden proporcionar como gránulos y polvos no efervescentes o efervescentes, para ser reconstituidos en una forma de administración líquida. Los vehículos y excipientes farmacéuticos aceptables utilizados en los gránulos o polvos no efervescentes pueden incluir diluyentes, edulcorantes y agentes humectantes. Los vehículos y excipientes farmacéuticos aceptables utilizados en los gránulos efervescentes o polvos pueden incluir ácidos orgánicos y una fuente de dióxido de carbono.
Los agentes colorantes y aromatizantes se pueden utilizar en todas las formas de dosificación anteriores.
Las composiciones farmacéuticas proporcionadas en el presente documento para la administración oral pueden formularse como formas de dosificación de liberación inmediata o modificada, incluyendo formas de liberación retardada, sostenida, pulsada, controlada, dirigida y programada.
B. Administración parenteral
Las composiciones farmacéuticas proporcionadas en este documento pueden administrarse por vía parenteral por inyección, infusión o implantación, para la administración local o sistémica. La administración parenteral, tal como se utiliza en este documento, incluye la administración endovenosa, intraarterial, intraperitoneal, intratecal, intraventricular, intrauretral, intrasternal, intracraneal, intramuscular, intrasinovial, intravesical y subcutánea.
Las composiciones farmacéuticas proporcionadas en el presente documento para la administración parenteral se pueden formularen cualquier forma de dosificación que sea adecuada para la administración parenteral, incluyendo soluciones, suspensiones, emulsiones, micelas, liposomas, microesferas, nanosistemas y formas sólidas adecuadas para soluciones o suspensiones en líquido antes de la inyección. Tales formas de dosificación se pueden preparar de acuerdo a los métodos convencionales conocidos por los expertos en la técnica de la ciencia farmacéutica (Ver, Remington: The Science and Practice of Pharmacy, supra).
Las composiciones farmacéuticas destinadas a la administración parenteral pueden incluir uno o más vehículos y excipientes farmacéuticos aceptables, incluyendo, entre otros, vehículos acuosos, vehículos miscibles en agua, vehículos no acuosos, agentes antimicrobianos o conservantes contra el crecimiento de microorganismos, estabilizadores, potenciadores de la solubilidad, agentes isotónicos, agentes tamponanes, antioxidantes, anestésicos locales, agentes de suspensión y dispersión, agentes humectantes o emulsionantes, agentes complejantes, agentes secuestrantes o quelantes, crioprotectores, lioprotectores, agentes espesantes, agentes de ajuste del pH y gases inertes.
Los vehículos acuosos adecuados incluyen, entre otros, agua, solución salina, solución salina fisiológica o solución salina tamponada con fosfato (PBS), inyección de cloruro sódico, inyección de Ringers, inyección isotónica de dextrosa, inyección de agua estéril, dextrosa e inyección de Ringers lactato. Los vehículos no acuosos adecuados incluyen, entre otros, aceites fijos de origen vegetal, aceite de ricino, aceite de maíz, aceite de semilla de algodón, aceite de oliva, aceite de cacahuete, aceite de menta, aceite de cártamo, aceite de sésamo, aceite de soja, aceites vegetales hidrogenados, aceite de soja hidrogenado y triglicéridos de cadena media de aceite de coco y aceite de semilla de palma. Los vehículos miscibles en agua adecuados incluyen, entre otros, etanol, 1,3-butanodiol, polietilenglicol líquido (por ejemplo, polietilenglicol 300 y polietilenglicol 400), propilenglicol, glicerina, A/-metil-2-pirrolidona, W,W-dimetilacetamida y dimetil sulfóxido.
Los agentes antimicrobianos o conservantes adecuados incluyen, entre otros, fenoles, cresoles, mercuriales, alcohol bencílico, clorobutanol, p-hidroxibenzoatos de metilo y propilo, timerosal, cloruro de benzalconio (por ejemplo, cloruro de benzetonio), metil- y propil-parabenos y ácido sórbico. Los agentes isotónicos adecuados incluyen, entre otros, cloruro de sodio, glicerina, y dextrosa. Los agentes tamponantes apropiados incluyen, entre otros, fosfato y citrato. Los antioxidantes apropiados son los que se describen en este documento, incluyendo bisulfito y metabisulfito de sodio. Los anestésicos locales apropiados incluyen, entre otros, clorhidrato de procaína. Los agentes de suspensión y de dispersión adecuados son aquellos según lo descrito en este documento, incluyendo carboximetilceluosa de sodio, hidroxipropil metilcelulosa y polivinilpirrolidona. Los agentes emulsionantes adecuados son aquellos descritos en este documento, incluyendo polioxietileno sorbitán monolaurato, polioxietileno sorbitán monooleato 80 y oleato de trietanolamina. Los agentes secuestrantes o quelantes adecuados incluyen, entre otros, EDTA. Los agentes de ajuste del pH apropiados incluyen, entre otros, hidróxido de sodio, ácido clorhídrico, ácido cítrico y ácido láctico. Los agentes complejantes apropiados incluyen, entre otros, ciclodextrinas, incluyendo a-ciclodextrinas, p-ciclodextrinas, hidroxipropil-p-ciclodextrinas, sulfobutiléter-p-ciclodextrinas, y sulfobutiléter 7-p-ciclodextrinas (CAPTlSOL®, CyDex, Lenexa, KS).
Cuando las composiciones farmacéuticas proporcionadas en este documento se formulan para la administración de dosificación múltiple, las formulaciones parenterales de dosificación múltiple deben contener a un agente antimicrobiano en las concentraciones bacteriostáticas o fungistáticas. Todas las formulaciones parenterales deben ser estériles, como se conocen y se usan en la técnica.
En una realización, se proporcionan composiciones farmacéuticas para la administración parenteral como soluciones estériles listas para usar. En otra realización, las composiciones farmacéuticas se suministran como productos solubles en seco estériles, incluyendo polvos liofilizados y tabletas hipodérmicas, para ser reconstituidos con un vehículo antes de su uso. En otra realización más, se proporcionan composiciones farmacéuticas como suspensiones estériles listas para usar. En otra realización más, las composiciones farmacéuticas se suministran como productos insolubles secos estériles para ser reconstituidos con un vehículo antes de su uso. En aún otra realización, se proporcionan composiciones farmacéuticas como emulsiones estériles listas para usar.
Las composiciones farmacéuticas proporcionadas en este documento para la administración parenteral pueden formularse como formas de dosificación de liberación inmediata o modificada, incluyendo formas de liberación retardada, sostenida, pulsada, controlada, dirigida y programada.
Las composiciones farmacéuticas proporcionadas en este documento para la administración parenteral se pueden formular como una suspensión, sólido, semisólido, o líquido tixotrópico, para la administración como depósito implantado. En una realización, las composiciones farmacéuticas proporcionadas en este documento se dispersan en
una matriz interna sólida, que está rodeada por una membrana polimérica externa que es insoluble en fluidos corporales pero permite que el ingrediente activo en las composiciones farmacéuticas se difunda a través.
Las matrices internas adecuadas incluyen, entre otras, polimetilmetacrilato, polibutil-metacrilato, cloruro de polivinilo plastificado o no plastificado, nylon plastificado, tereftalato de polietileno plastificado, caucho natural, poliisopreno, poliisobutileno, polibutadieno, polietileno, copolímeros de etileno-acetato de vinilo, cauchos de silicona, polidimetilsiloxanos, copolímeros de carbonato de silicona, polímeros hidrófilos, como hidrogeles de ésteres de ácido acrílico y metacrílico, colágeno, alcohol de polivinilo reticulado y acetato de polivinilo parcialmente reticulado e hidrolizado.
Las membranas poliméricas externas adecuadas incluyen, entre otras, polietileno, polipropileno, copolímeros del etileno/propileno, copolímeros de etileno/acrilato de etilo, copolímeros de etileno/acetato de vinilo, cauchos de silicona, siloxanes del polidimetilo, caucho de neopreno, polietileno clorado, poli(cloruro de vinilo), copolímeros de cloruro de vinil con acetato de vinilo, cloruro de vinilideno, etileno y propileno, ionómero de tereftalato de polietileno, cauchos de epiclorohidrina de caucho butílico, copolímero de etileno/alcohol de vinilo, terpolímero etileno/acetato de vinilo/alcohol de vinilo y copolímero de etileno/viniloxietanol.
C. Administración tópica
Las composiciones farmacéuticas proporcionadas en este documento se pueden administrar tópicamente a la piel, los orificios o la mucosa. La administración tópica, como se usa en este documento, incluye la administración (intra)dérmica, conjuntival, intracorneal, intraocular, oftálmica, auricular, transdérmica, nasal, vaginal, uretral, respiratoria y rectal.
Las composiciones farmacéuticas proporcionadas en este documento se pueden formular en cualquier forma de dosificación que sean adecuadas para la administración tópica para el efecto local o sistémico, incluyendo emulsiones, soluciones, suspensiones, cremas, geles, hidrogeles, ungüentos, polvos de desempolvamiento, apósitos, elixires, lociones, suspensiones, tinturas, pastas, espumas, películas, aerosoles, irrigaciones, aerosoles, supositorios, vendajes y parches dérmicos. La formulación tópica de las composiciones farmacéuticas en este documento provistas también puede comprender liposomas, micelas, microesferas, nanosistemas y sus mezclas.
Los vehículos y excipientes farmacéuticos aceptables adecuados para su uso en las formulaciones tópicas que se proporcionan en este documento incluyen, entre otros, vehículos acuosos, vehículos miscibles en agua, vehículos no acuosos, agentes antimicrobianos o conservantes contra el crecimiento de microorganismos, estabilizantes, potenciadores de la solubilidad, agentes isotónicos, agentes tamponantes, antioxidantes, anestésicos locales, agentes de suspensión y dispersión, agentes humectantes o emulsionantes, agentes complejantes, agentes secuestrantes o quelantes, potenciadores de penetración, crioprotectores, lioprotectores, agentes espesantes y gases inertes.
Las composiciones farmacéuticas también pueden administrarse por vía tópica mediante electroporación, iontoforesis, fonoforesis, sonoforesis o inyección con microagujas o sin aguja, como POWDERJECT™ (Chiron Corp., Emeryville, CA) y BIOJECT™ (Bioject Medical Technologies Inc., Tualatin, OR).
Las composiciones farmacéuticas proporcionadas en este documento se pueden proporcionar en las formas de ungüentos, de cremas, y de geles. Los vehículos apropiados de los ungüentos incluyen los vehículos oleaginosos o de hidrocarburos, incluyendo la manteca de cerdo, la manteca de cerdo benzoinada, el aceite de semilla de algodón, y otros aceites, vaselina blanca; vehículos emulsionables o de absorción, como la vaselina hidrófila, el sulfato de hidrostearina y la lanolina anhidra; vehículos eliminadores de agua, tales como pomadas hidrófilas; vehículos de ungüentos solubles en agua, incluyendo polietilenglicoles de diversos pesos moleculares; vehículos de emulsión, ya sea emulsiones de agua en aceite (W/O) o emulsiones de aceite en agua (O/W), incluyendo alcohol cetílico, monoestearato de glicerilo, lanolina y ácido esteárico (Ver, Remington: The Science and Practice of Pharmacy, supra). Estos vehículos son emolientes pero generalmente requieren la adición de antioxidantes y conservantes.
La base de la crema adecuada puede ser aceite-en-agua o agua-en-aceite. Los vehículos de cremas adecuados pueden ser lavables en agua, y contener una fase de aceite, un emulsionante y una fase acuosa. La fase de aceite también se llama fase "interna", que se compone generalmente de vaselina y de un alcohol graso tal como alcohol cetílico o estearílico. La fase acuosa generalmente, aunque no necesariamente, supera a la fase aceitosa en volumen, y contiene generalmente un humectante. El emulsionante en una formulación de crema puede ser un tensioactivo no iónico, aniónico, catiónico o anfoterico.
Los geles son sistemas tipo suspensión semisólidos. Los geles monofásicos contienen macromoléculas orgánicas distribuidas sustancialmente uniformemente en todo el vehículo líquido. Los agentes gelificantes apropiados incluyen, entre otros, los polímeros ácidos acrílico reticulados, tales como carbómeros, carboxipolialquilenos, y CARBOPOl®; polímeros hidrófilos, tales como óxidos de polietileno, copolímeros de polioxietileno-polioxipropileno y poli(alcohol vinílico); polímeros celulósicos, tales como hidroxipropilcelulosa, hidroxietilcelulosa, hidroxipropilmetilcelulosa, hidroxipropil metilcelulosa ftalato y metilcelulosa; gomas, como goma de tragacanto y xantano; alginato de sodio; y gelatina. Con el fin de preparar un gel uniforme, se pueden añadir agentes dispersantes como el alcohol o la glicerina, o el agente gelificante puede dispersarse mediante trituración, mezclado mecánicamente y/o por agitación.
Las composiciones farmacéuticas proporcionadas en este documento se pueden administrar por vía rectal, uretralmente, vaginalmente, o perivaginalmente en las formas de supositorios, pesarios, bougies, cataplasmas, pasturas, polvos, apósitos, cremas, yesos, anticonceptivos, ungüentos, soluciones, emulsiones, suspensiones, tampones, geles, espumas, aerosoles o enemas. Estas formas de dosificación se pueden fabricar usando procesos convencionales como se describe en Remington: The Science and Practice of Pharmacy, supra.
Los supositorios rectales, uretrales y vaginales son cuerpos sólidos para su inserción en los orificios corporales, que son sólidos a temperaturas ordinarias, pero que se derriten o suavizan a temperatura corporal para liberar el ingrediente o los ingrediente activos dentro de los orificios. Los vehículos farmacéuticos aceptables utilizados en los supositorios rectales y vaginales incluyen bases o vehículos, tales como agentes de endurecimiento, que tienen un punto de fusión próximo a la temperatura del cuerpo, cuando están formulados con las composiciones farmacéuticas proporcionadas en el presente documento; y agentes antioxidantes, como se describen en este documento, incluyendo bisulfito y metabisulfito de sodio. Los vehículos apropiados incluyen, entre otros, manteca de cacao (aceite de Theobroma), glicerina-gelatina, carbowax (polioxietilenglicol), Spermaceti, parafina, cera blanca y amarilla, y las mezclas apropiadas de mono-, di- y tri-glicéridos de ácidos grasos, e hidrogeles, tales como poli(alcohol vinílico), metacrilato de hidroxietilo y ácido poliacrílico. También se pueden utilizar combinaciones de distintos vehículos. Los supositorios rectales y vaginales se pueden preparar comprimiendo o moldeando. El peso típico de un supositorio rectal y vaginal es de aproximadamente 2 a 3 g.
Las composiciones farmacéuticas provistas en este documento pueden ser administradas oftálmicamente en las formas de soluciones, suspensiones, ungüentos, emulsiones, soluciones formadoras de gel, polvos para soluciones, geles, plaquitas oculares e implantes.
Las composiciones farmacéuticas proporcionadas en este documento se pueden administrar intranasalmente o por inhalación al tracto respiratorio. Las composiciones farmacéuticas se pueden proporcionar en forma de un aerosol o solución para su administración usando un recipiente presurizado, bomba, aerosol, atomizador, tal como un atomizador usando electrohidrodinámica para producir una niebla fina o nebulizador, solo o en combinación con un propulsor adecuado, como 1,1,1,2-tetrafluoroetano o 1,1,1,2,3,3,3-heptafluoropropano. Las composiciones farmacéuticas también se pueden proporcionar como un polvo seco para insuflación, solo o en combinación con un vehículo inerte como lactosa o fosfolípidos; y gotas nasales. Para el uso intranasal, el polvo puede comprender un agente bioadhesivo, incluyendo el quitosano o la ciclodextrina.
Las soluciones o suspensiones para su uso en recipientes presurizados, bombas, pulverizadores, atomizadores o nebulizadores pueden formularse para contener etanol, etanol acuoso o un agente alternativo adecuado para dispersar, solubilizar o extender la liberación del ingrediente activo proporcionada en el presente documento; un propulsor como disolvente; y/o un tensioactivo, como el trioleato de sorbitán, el ácido oleico o un ácido oligoláctico.
Las composiciones farmacéuticas proporcionadas en este documento pueden ser micronizadas a un tamaño adecuado para su administración por inhalación, por ejemplo aproximadamente 50 micrómetros o menos, o aproximadamente 10 micrómetros o menos. Las partículas de tales tamaños se pueden preparar usando un método de trituración conocido por los expertos en la técnica, tales como el fresado de chorro en espiral, el fresado de chorro en lecho fluido, el procesamiento de fluidos supercríticos para formar nanopartículas, la homogeneización a alta presión o el secado por pulverización.
Pueden formularse cápsulas, ampollas y cartuchos para su uso en un inhalador o insuflador para que contengan una mezcla en polvo de las composiciones farmacéuticas proporcionadas en el presente documento; una base en polvo adecuada, como lactosa o almidón; y un modificador del rendimiento, como /-leucina, manitol o estearato de magnesio. La lactosa puede ser anhidra o estar en forma de monohidrato. Otros excipientes o vehículos apropiados incluyen, entre otros, dextrano, glucosa, maltosa, sorbitol, xilitol, fructosa, sacarosa y trehalosa. Las composiciones farmacéuticas proporcionadas en el presente documento para la administración inhalada/intranasal pueden abarcar además un aromatizante adecuado, como el mentol y el levomentol; y/o edulcorantes, como la sacarina y la sacarina sódica.
Las composiciones farmacéuticas proporcionadas en este documento para la administración tópica se pueden formular para ser de liberación inmediata o liberación modificada, incluyendo la liberación retardada, sostenida, pulsada, controlada, dirigida y programada.
D. Liberación modificada
Las composiciones farmacéuticas proporcionadas en este documento se pueden formular como una forma de dosificación de liberación modificada. Como se utiliza en este documento, la expresión "liberación modificada" se refiere a una forma de dosificación en la que la velocidad o el lugar de liberación del ingrediente o los ingredientes activos son diferentes de los de una forma de dosificación inmediata, cuando se administran por la misma ruta. Las formas de dosificación de liberación modificada incluyen, entre otras, formas de administración retrasada, extendida, prolongada, sostenida, pulsátil, controlada, acelerada y rápida, dirigida, de liberación programada y de retención gástrica. Las composiciones farmacéuticas en las formas de administración de liberación modificada se pueden preparar utilizando una variedad de dispositivos de liberación modificada y métodos conocidos por los expertos en la
técnica, incluyendo, entre otros, dispositivos de liberación controlada por matriz, dispositivos de liberación controlada osmótica, dispositivos de liberación controlada multiparticulada, resinas de intercambio iónico, recubrimientos entónicos, recubrimientos multicapa, microesferas, liposomas y sus combinaciones. La velocidad de liberación del ingrediente o los ingredientes activos también puede modificarse variando los tamaños de partícula y el polimorfismo del ingrediente o los ingredientes activos.
Los ejemplos de liberación modificada incluyen, entre otros, los descritos en U.S. Pat. Nos.: 3.845.770; 3.916.899; 3.536.809; 3.598.123; 4.008.719; 5.674.533; 5.059.595; 5.591.767; 5.120.548; 5.073.543; 5.639.476; 5.354.556; 5.639.480; 5.733.566; 5.739.108; 5.891.474; 5.922.356; 5.972.891; 5.980.945; 5.993.855; 6.045.830; 6.087.324; 6.113.943; 6.197.350; 6.248.363; 6.264.970; 6.267.981; 6.376.461; 6.419.961; 6.589.548; 6.613.358; y 6.699.500.
1. Dispositivos de liberación controlada por matriz
Las composiciones farmacéuticas proporcionadas en este documento en una forma de administración de liberación modificada se pueden fabricar usando un dispositivo de liberación controlada por matriz conocido por los expertos en la técnica (Ver Takada et al. en "Encyclopedia of Controlled Drug Delivery", Vol. 2, Matiowitz Ed., Wiley, 1999).
En ciertas realizaciones, las composiciones farmacéuticas proporcionadas en este documento en una forma de administración de liberación modificada se formula usando un dispositivo de matriz erosionable, que consiste en polímeros que se hinchan en agua, erosionables o solubles, incluyendo, entre otros, polímeros sintéticos y polímeros y derivados naturales, como polisacáridos y proteínas.
Los materiales útiles para formar una matriz erosionable incluyen, entre otros, quitina, quitosano, dextrano y el pululano; goma agar, goma arábiga, goma Karaya, goma de garrofín, goma de tragacanto, carragenina, goma ghatti, goma guar, goma xantano y escleroglucano; almidones, como la dextrina y la maltodextrina; coloides hidrófilos, como la pectina; fosfatidas, como la lecitina; alginatos; alginato de propilenglicol; gelatina; colágeno; celulósicos, tales como la etil-celulosa (EC), metiletil-celulosa (MEC), carboximetil-celulosa (CMC), CMEC, celulosa hidroxietílica (HEC), hidroxipropil-celulosa (HPC), acetato de celulosa (CA), propionato de celulosa (CP), butirato de celulosa (CB), acetato butirato de celulosa (Ca B), CAP, CAT, hidroxipropilmetilcelulosa (HPMC), HPMCP, HPMCAS, acetato trimelitato de hidroxipropilmetilcelulosa (HPMCAT), y etilhidroxietilcelulosa (EHEC); polivinilpirrolidona; poli(alcohol vinílico); poli(acetato de vinilo); ésteres de ácidos grasos de glicerol; poliacrilamida; ácido poliacrílico; copolímeros de ácido etacrílico o ácido metacrílico (EUDRAGIT®, Rohm America, Inc., Piscataway, NJ); poli(2-hidroxietil-metacrilato); polilactidas; copolímeros de ácido L-glutamico y etil-L-glutamato; copolímeros de ácidos lácticos degradables-ácido glicólico; ácido poli-D-(-)-3-hidroxibutírico; y otros derivados del ácido acrílico, como los homopolímeros y los copolímeros de butilmetacrilato, metacrilato de metilo, metacrilato de etilo, etilacrilato, (2-dimetilaminoetil)metacrilato, y cloruro de (trimetilaminoetil)metacrilato.
En ciertas realizaciones, las composiciones farmacéuticas proporcionadas en este documento se formulan con un dispositivo de matriz no erosionable. El ingrediente o los ingredientes activos se disuelven o se dispersan en una matriz inerte y se liberan principalmente por difusión a través de la matriz inerte una vez administrado. Los materiales adecuados para su uso como dispositivo de matriz no erosionable incluyen, entre otros, plásticos insolubles, como polietileno, polipropileno, poliisopreno, poliisobutileno, polibutadieno, polimetilmetacrilato, polibutilmetacrilato, polietileno clorado, poli(cloruro de vinilo), copolímeros de metilacrilato-metil metacrilato, copolímeros de etileno-vinil acetato, copolímeros de etileno/propileno, copolímeros de etileno/etilacrilato, copolímeros de cloruro de vinilo con acetato de vinilo, cloruro de vinilideno, etileno y propileno, ionómero poli(tereftalato de etileno), cauchos butílicos, cauchos de epiclorohidrina, copolímero de etileno/alcohol de vinilo, terpolímero de etileno/acetato de vinilo/alcohol de vinilo, copolímero de etileno/viniloxietanol, poli(cloruro de vinilo), nylon plastificado, tereftalato de polietileno plastificado, caucho natural, cauchos de silicona, polidimetilsiloxanos y copolímeros de carbonato de silicona; polímeros hidrófilos, como la celulosa etílica, el acetato de celulosa, la crospovidona y el acetato de polivinilo parcialmente hidrolizado reticulado; y compuestos grasos, como la cera de carnauba, cera microcristalina y los triglicéridos.
En un sistema de liberación controlado por matriz, la cinética de liberación deseada puede ser controlada, por ejemplo, vía el tipo de polímero empleado, la viscosidad del polímero, los tamaños de partícula del polímero y/o el ingrediente o los ingredientes activos, la relación entre los ingredientes activos versus el polímero, y otros excipientes o vehículos en las composiciones.
Las composiciones farmacéuticas proporcionadas en este documento en una forma de administración de liberación modificada se pueden preparar por métodos conocidos por los expertos en la técnica, incluyendo la compresión directa, la granulación en seco o húmedo seguida por la compresión, y la granulación en fundido seguido por la compresión.
2. Dispositivos de liberación controlada osmótica
Las composiciones farmacéuticas proporcionadas en este documento en una forma de administración de liberación modificada se pueden fabricar usando un dispositivo de liberación controlado osmótico, incluyendo, entre otros, sistema de una cámara, sistema de dos cámaras, tecnología asimétrica de membrana (AMT) y sistemas de extrusión
de núcleos (ECS). En general, estos dispositivos tienen al menos dos componentes: (a) un núcleo que contiene un ingrediente activo; y (b) una membrana semipermeable con al menos una entrada de administración, que encapsula el núcleo. La membrana semipermeable controla la afluencia de agua al núcleo desde un ambiente acuoso de uso para causar la liberación del fármaco por extrusión a través de la entrada o entradas de administración.
Además del ingrediente o los ingredientes activos, el núcleo del dispositivo osmótico incluye opcionalmente un agente osmótico, que crea una fuerza motriz para el transporte de agua desde el medio ambiente de uso en el núcleo del dispositivo. Una clase de agente osmótico es un polímero hidrófilo hinchable en agua, que también se denomina "osmopolímero" e "hidrogel". Los polímeros hidrófilos adecuados hinchables en agua como agentes osmóticos incluyen, entre otros, los polímeros hidrófilos de vinilo y de acrílico, polisacáridos tales como alginato de calcio, óxido de polietileno (PEO), polietilenglicol (PEG), polipropilenglicol ( PPG), poli(2-hidroxietil metacrilato), poli(ácido acrílico), poli(ácido metacrílico), polivinilpirrolidona (PVP), PVP reticulado, poli(alcohol vinílico) (PVA), copolímeros PVA/PVP, copolímeros PVA/PVP con monómeros hidrófobos como el metacrilato de metilo y el acetato de vinilo, poliuretanos hidrófilos que contienen grandes bloques PEO, croscarmelosa de sodio, carragenina, hidroxietilcelulosa (HEC), hidroxipropilcelulosa (HPC), hidroxipropilmetilcelulosa (HPMC), carboximetilcelulosa (CMC) y carboxietilcelulosa (CEC), alginato sódico, policarbofilión, gelatina, goma xantano y glicolato sódico de almidón.
La otra clase de agentes osmóticos son los osmógenos, que son capaces de empapar con agua para producir un gradiente osmótico de la presión a través de la barrera del recubrimiento circundante. Los osmógenos apropiados incluyen, entre otros, sales inorgánicas, tales como sulfato de magnesio, cloruro de magnesio, cloruro de calcio, cloruro de sodio, cloruro de litio, sulfato de potasio, fosfatos de potasio, carbonato de sodio, sulfito de sodio, sulfato de litio, cloruro de potasio y sulfato sódico; azúcares, tales como dextrosa, fructosa, glucosa, inositol, lactosa, maltosa, manitol, raffinosa, sorbitol, sacarosa, trehalosa, y xilitol; ácidos orgánicos, como ácido ascórbico, ácido benzoico, ácido fumarico, ácido cítrico, ácido maleico, ácido sebácico, ácido sórbico, ácido adípico, ácido edético, ácido glutámico, ácido p-toluenosulfónico, ácido succínico, y ácido tartárico; urea y sus mezclas.
Pueden emplearse agentes osmóticos de diferentes velocidades de disolución para influir en la rapidez con que el ingrediente o los ingredientes activos se suministran inicialmente a partir de la forma de administración. Por ejemplo, se pueden utilizar azúcares amorfos, como MANNOGEM™ EZ (SPI Pharma, Lewes, DE) para proporcionar una administración más rápida durante el primer par de horas para producir rápidamente el efecto terapéutico deseado, y de forma gradual y continua liberar la cantidad restante para mantener el nivel deseado de efecto terapéutico o profiláctico durante un largo período de tiempo. En este caso, el ingrediente o los ingredientes activos se liberan a tal velocidad para sustituir la cantidad del ingrediente activo metabolizado y excretado.
El núcleo también puede incluir una amplia variedad de otros excipientes y vehículos como se describe en este documento para mejorar el rendimiento de la forma de administración o para promover la estabilidad o el procesamiento.
Los materiales útiles en la formación de la membrana semipermeable incluyen varios grados de acrílicos, vinilos, éteres, poliamidas, poliésteres, y derivados celulósico que son permeables al agua e insolubles en agua a pH fisiológicamente relevante, o son susceptibles de volverse insolubles en agua por alteración química, tal como reticulación. Ejemplos de polímeros adecuados útiles para la formación del recubrimiento, incluyen acetato de celulosa plastificado, no plastificado y reforzado (CA), diacetato de celulosa, triacetato de celulosa, propionato de CA, nitrato de celulosa, acetato butirato de celulosa (CAB), CA carbamato de etilo, CAP, CA metil carbamato, CA succinato, acetato trimelitato de celulosa (CAT), CA dimetilaminoacetato, CA carbonato de etilo, CA cloroacetato, CA oxalato de etilo, CA sulfonato de metilo, CA sulfonato de butilo, CA p-tolueno sulfonato, agar acetato, amilosa triacetato, beta glucano acetato, beta glucano triacetato, acetaldehído dimetil acetato, triacetato de goma de garrofín, etilenovinilacetato hidroxilado, EC, PEG, PPG, copolímeros PEG/PPG, PVP, HEC, HPC, CMC, CMEC, HPMC, HPMCP, HPMCAS, HPMCAT, poli(ácidos y ésteres acrílicos) y poli-(ácidos y ésteres metacrílicos) y sus copolímeros, almidón, dextrano, dextrina, quitosán, colágeno, gelatina, polialquenos, poliéteres, polisulfonas, polietersulfonas, poliestirenos, poli(haluros de vinilo), poli(ésteres de vinilo) y ceras naturales y ceras sintéticas.
La membrana semipermeable puede también ser una membrana microporosa hidrófoba, en donde los poros se llenan substancialmente de un gas y no son humedecidos por el medio acuoso pero son permeables al vapor de agua, según lo descrito en U.S. Pat. No. 5.798.119. Tal membrana hidrófoba, pero permeable al vapor de agua, se compone típicamente de polímeros hidrófobos tales como polialquenos, polietileno, polipropileno, politetrafluoroetileno, derivados del ácido poliacrílico, poliéteres, polisulfonas, polietersulfonas, poliestirenos, poli(haluros de vinilo), poli(fluoruro de vinillideno), poli(ésteres y éteres de vinilo), ceras naturales y ceras sintéticas.
La entrada o entradas de administración de la membrana semipermeable se pueden formar después del recubrimiento mediante perforación mecánica o láser. Las entradas de administración también se pueden formar in situ por erosión de un tapón de material soluble en agua o por ruptura de una parte más delgada de la membrana por una hendidura del núcleo. Además, se pueden formar entradas de administración durante el proceso de recubrimiento, como en el caso de recubrimientos de membrana asimétrica del tipo descrito en U.S. Pat. Nos. 5.612.059 y 5.698.220.
La cantidad total del ingrediente o los ingredientes activos liberados y la velocidad de liberación puede sustancialmente ser modulada vía el grosor y la porosidad de la membrana semipermeable, la composición del núcleo y el número, tamaño y posición de las entradas de administración.
Las composiciones farmacéuticas en una forma de administración de liberación controlada osmótica pueden abarcar adicionalmente excipientes convencionales adicionales o vehículos como se describe en este documento para promover el rendimiento o el procesamiento de la formulación.
Se pueden preparar formas de administración de liberación controlada osmótica de acuerdo con métodos y técnicas convencionales conocidos por los expertos en la técnica (Ver, Remington: The Science and Practice of Pharmacy, supra; Santus y Baker, J. Controlled Release 1995, 35, 1-21; Verma et al., Drug Development and Industrial Pharmacy 2000, 26, 695-708; Verma et al., J. Controlled Release 2002, 79, 7-27).
En ciertas realizaciones, las composiciones farmacéuticas proporcionadas en este documento se formulan como una forma de administración de liberación controlada AMT, que incluye una membrana osmótica asimétrica que cubre un núcleo que comprende el ingrediente o los ingredientes activos y otros excipientes o vehículos farmacéuticos aceptables. Ver U.S. Pat. No. 5.612.059 y WO 2002/17918. Las formas de administración de liberación controlada AMT se pueden preparar de acuerdo con los métodos y técnicas convencionales conocidos por los expertos en la técnica, incluyendo la compresión directa, granulación en seco, granulación en húmedo, y un método de recubrimiento por inmersión.
En ciertas realizaciones, las composiciones farmacéuticas proporcionadas en este documento se formulan como una forma de administración de liberación controlada ESC, que comprende una membrana osmótica que recubre un núcleo que comprende el ingrediente o los ingredientes activos, una hidroxiletil celulosa y otros excipientes o vehículos farmacéuticos aceptables.
3. Dispositivos de liberación controlada multiparticulados
Las composiciones farmacéuticas proporcionadas en este documento en una forma de administración de liberación modificada se pueden fabricar como un dispositivo de liberación controlada multiparticulado, que comprende una multiplicidad de partículas, gránulos, o peletes, extendiéndose desde aproximadamente 10 pm a aproximadamente 3 milímetros, de aproximadamente 50 pm a aproximadamente 2,5 mm, o de aproximadamente 100 pm a aproximadamente 1 mm de diámetro. Tales multiparticulados se pueden hacer por los procesos conocidos por los expertos en la técnica, incluyendo granulación en húmedo y seco, extrusión/esferonización, compactación por rodillos, solidificación en fundido y por recubrimiento por pulverización de núcleos de semillas. Ver, por ejemplo, Multiparticulate Oral Drug Delivery; Marcel Dekker: 1994; and Pharmaceutical Pelletization Technology; Marcel Dekker: 1989.
Pueden mezclarse otros excipientes o vehículos, como se describen en este documento, con las composiciones farmacéuticas para ayudar en el procesamiento y la formación de las multiparticulas. Las partículas resultantes pueden por sí mismas constituir el dispositivo multiparticulado o pueden ser revestidas por los diversos materiales formadores de películas, tales como polímeros entéricos, hinchables en agua y polímeros solubles en agua. Los multiparticulados pueden ser procesados como cápsulas o tabletas.
4. Administración dirigida
Las composiciones farmacéuticas provistas en este documento también pueden formularse para ser dirigidas a un tejido particular, receptor, u otra área del cuerpo del sujeto que se tratará, incluyendo los sistemas de administración basados en anticuerpos, eritrocitos y liposomas. Los ejemplos incluyen, entre otros, los descritos en U.S. Pat. Nos.
6.316.652; 6.274.552; 6.271.359; 6.253.872; 6.139.865; 6.131.570; 6.120.751; 6.071.495; 6.060.082; 6.048.736; 6.039.975; 6.004.534; 5.985.307; 5.972.366; 5.900.252; 5.840.674; 5.759.542; y 5.709.874.
Métodos de uso
En una realización, se proporcionan los compuestos de la invención para su uso en un método de tratamiento, prevención o mejoramiento de uno o más síntomas de un trastorno, enfermedad o condición, definidos en las reivindicaciones, asociados con la actividad PI3K en un sujeto, que comprende administrar al sujeto una cantidad terapéuticamente efectiva del compuesto proporcionado en este documento; por ejemplo, un compuesto de fórmula I, IA o IB, incluido un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereoisómeros de los mismos; o sus sales farmacéuticas aceptables, solvatos, o hidratos.
En otras realizaciones, se proporcionan los compuestos de la invención para su uso en un método de tratamiento, prevención o mejoramiento de uno o más síntomas de un trastorno, enfermedad o condición, como se define en las reivindicaciones, sensible a la modulación de la actividad PI3K en un sujeto, que comprende la administración al sujeto de una cantidad terapéuticamente efectiva del compuesto proporcionado en el presente documento; por ejemplo, el compuesto de fórmula I, IA o IB, incluyendo un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereoisómeros de los mismos; o sus sales farmacéuticas aceptables, solvatos, o hidratos.
En otra realización más, se proporcionan los compuestos de la invención para su uso en un método de tratamiento, prevención, o alivio de uno o más síntomas de un trastorno, enfermedad o condición, como se define en las reivindicaciones, mediada por una enzima PI3K en un sujeto, que comprende la administración al sujeto de una cantidad terapéuticamente efectiva del compuesto proporcionado en el presente documento; por ejemplo, el compuesto de fórmula I, IA o IB, incluyendo un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereómeros del mismo; o sus sales farmacéuticas aceptables, solvatos, o hidratos.
En otra realización más, se proporcionan los compuestos de la invención para su uso en un método de tratamiento, prevención o mejoramiento de uno o más síntomas de cáncer en un sujeto, que comprende la administración al sujeto de una cantidad terapéuticamente efectiva del compuesto proporcionado en este documento; por ejemplo, el compuesto de fórmula I, IA o IB, incluyendo un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereoisómeros de los mismos; o sus sales farmacéuticas aceptables, solvatos, o hidratos.
También se describen en este documento los usos del compuesto proporcionado en este documento; por ejemplo, un compuesto de fórmula I, IA o IB, incluido un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereoisómeros de los mismos; o sus sales farmacéuticas aceptables, solvatos, o hidratos, en la fabricación de un medicamento para el tratamiento del cáncer.
En ciertas realizaciones, el compuesto se dirige selectivamente a la subunidad p110a de PI3K. En ciertas realizaciones, el compuesto inhibe selectivamente el PI3K vía su interacción con su subunidad p110a. En ciertas realizaciones, el compuesto alquila de forma selectiva la subunidad p110a de PI3K.
En ciertas realizaciones, el PI3K es un PI3K natural. En ciertas realizaciones, el PI3K es un PI3K mutante.
En ciertas realizaciones, el PI3K es una quinasa de clase I. En ciertas realizaciones, el PI3K es p110a, p110p, p1105, o p110Y. En ciertas realizaciones, el PI3K es una quinasa de clase I natural. En ciertas realizaciones, el PI3K es un mutante de una quinasa de clase I.
En ciertas realizaciones, el PI3K es p110a. En ciertas realizaciones, el PI3K es un p110a natural. En ciertas realizaciones, el PI3K es un p110a mutante. En ciertas realizaciones, el p110a mutante es R38H, G106V, K111N, K227E, N345K, C420R, P539R, E542K, E545A, E545G, E545K, Q546K, Q546P, E453Q, H710P, I800L, T1025S, M1043I, M1043V, H1047L, H1047R, o H1047Y. En ciertas realizaciones, el mutante p110a es R38H, K111N, N345K, C420R, P539R, E542K, E545A, E545G, E545K, Q546K, Q546P, I800L, T1025S, M1043I, H1047L, H1047R, o H1047Y. En ciertas realizaciones, el mutante p110a es C420R, E542K, E545A, E545K, Q546K, I800L, M1043I, H1047L, o H1047Y.
En ciertas realizaciones, el PI3K es una quinasa de clase IV. En ciertas realizaciones, el PI3K es una quinasa de clase IV natural. En ciertas realizaciones, el PI3K es un mutante de una quinasa de clase IV. En ciertas realizaciones, el PI3K es mTOR, ATM, ATR, o DNA-PK. En ciertas realizaciones, el PI3K es mTOR.
En una realización, el sujeto es un mamífero. En otra realización más, el sujeto es un ser humano. En otra realización más, el sujeto es un primate distinto de un ser humano, un animal de granja como el ganado, un animal usado para deportes o una mascota como un caballo, un perro o un gato.
En ciertas realizaciones, el compuesto proporcionado en este documento; por ejemplo, el compuesto de fórmula I, IA o IB, incluyendo un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereoisómeros de los mismos; o su sal farmacéutica aceptable, solvato o hidrato; tiene mejores propiedades farmacocinéticas (por ejemplo, solubilidad, biodisponibilidad, volumen de distribución, AUC, Cmáx, concentración en estado estacionario, porcentaje de unión a proteínas, ti/2, tasa de eliminación, aclaramiento, aclaramiento renal, aclaramiento metabólico, constante de la tasa de eliminación y/o toxicidad) en comparación con los inhibidores conocidos de PI3K.
En ciertas realizaciones, el compuesto proporcionado en este documento; por ejemplo, el compuesto de fórmula I, IA o IB, incluyendo un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereoisómeros de los mismos; o su sal farmacéutica aceptable, solvato o hidrato; tiene una vida media en un sujeto que va desde aproximadamente 10 min a aproximadamente 100 h, desde aproximadamente 20 min a aproximadamente 50 h, de aproximadamente 1 a aproximadamente 25 h, o de aproximadamente 2 a 10 h.
En ciertas realizaciones, el compuesto proporcionado en este documento; por ejemplo, el compuesto de fórmula I, IA 0 IB, incluyendo un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereoisómeros de los mismos; o su sal farmacéutica aceptable, solvato o hidrato; se administra diariamente en una dosis única o en dosis divididas para una dosis diaria total suficiente para lograr una concentración plasmática del compuesto en estado estacionario que oscila entre aproximadamente 0,001 y aproximadamente 100, de aproximadamente 0,01 a aproximadamente 10, de aproximadamente 0,1 a aproximadamente 5 , o de aproximadamente 0,1 a aproximadamente 1 |j M. Como se utiliza en este documento, la expresión "concentración plasmática en estado estacionario" es la concentración alcanzada después de un período de administración de un compuesto. Una vez que se alcanza el estado estacionario, hay picos y valles menores en la curva dependiente del tiempo de la concentración plasmática del compuesto administrado.
En ciertas realizaciones, el compuesto proporcionado en este documento; por ejemplo, el compuesto de la fórmula I, IA o IB, incluyendo un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereoisómeros de los mismos; o su sal farmacéutica aceptable, solvato o hidrato; se administra en una dosis única o dosis divididas para una dosis diaria total suficiente para lograr una CMax que va desde aproximadamente 0,1 a aproximadamente 100, de aproximadamente 0,2 a aproximadamente 50, de aproximadamente 0,5 a aproximadamente 25, o de aproximadamente 1 a aproximadamente 10 pM.
En ciertas realizaciones, el compuesto proporcionado en este documento; por ejemplo, el compuesto de fórmula I, IA o IB, incluyendo un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereoisómeros de los mismos; o su sal farmacéutica aceptable, solvato o hidrato; se administra en una dosis única o dosis divididas para una dosis diaria total suficiente para lograr una CMax que oscila entre aproximadamente 0,1 y aproximadamente 100, de aproximadamente 0,2 a aproximadamente 50, de aproximadamente 1 a aproximadamente 20, o de aproximadamente 1 a aproximadamente 10 pg/mL.
En ciertas realizaciones, el compuesto proporcionado en este documento; por ejemplo, el compuesto de fórmula I, IA o IB, incluyendo un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereoisómeros de los mismos; o su sal farmacéutica aceptable, solvato o hidrato; se administra en una dosis única o dosis divididas para una dosis diaria total suficiente para lograr una AUC que oscila entre 1 y aproximadamente 1.000, de aproximadamente 10 a aproximadamente 500, de aproximadamente 20 a aproximadamente 250, o de aproximadamente 50 a aproximadamente 100 pg*h/mL.
En ciertas realizaciones, el compuesto proporcionado en este documento; por ejemplo, el compuesto de fórmula I, IA o IB, incluyendo un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereoisómeros de los mismos; o su sal farmacéutica aceptable, solvato o hidrato; se administra en una dosis única o dosis divididas para una dosis diaria total suficiente para lograr una AUC que oscila entre aproximadamente 1 y aproximadamente 1.000, de aproximadamente 10 a aproximadamente 500, de aproximadamente 20 a aproximadamente 250, o de aproximadamente 50 a aproximadamente 100 pM*h.
Los trastornos, enfermedades o afecciones que se pueden tratar con el compuesto proporcionado en este documento incluyen, entre otros, (1) enfermedades inflamatorias o alérgicas, incluyendo anafilaxia sistémica y trastornos de hipersensibilidad, dermatitis atópica, urticaria, alergias a fármacos, alergias a la picadura de insectos, alergias alimentarias (incluyendo enfermedades celiacas y similares), y mastocitosis; (2) enfermedades inflamatorias del intestino, incluyendo la enfermedad de Crohn, colitis ulcerosa, ileitis, y enteritis; (3) vasculitis, y síndrome de Behcet; (4) psoriasis y dermatosis inflamatorias, incluyendo dermatitis, eczema, dermatitis atópica, dermatitis de contacto alérgica, urticaria, patologías cutáneas virales incluyendo las derivadas del virus del papiloma humano, infección por VIH o RLV, patologías bacterianas, fúngicas y otras patologías cutáneas parasitales, y lupus eritematoso cutáneo; (5) asma y enfermedades alérgicas respiratorias, incluyendo asma alérgica, asma inducida por el ejercicio, rinitis alérgica, otitis media, conjuntivitis alérgica, enfermedades pulmonares de hipersensibilidad y enfermedad pulmonar obstructiva crónica; (6) enfermedades autoinmunes, incluyendo artritis (incluyendo reumatoide y psoriática), lupus eritematoso sistémico, diabetes tipo I, miastenia gravis, esclerosis múltiple, enfermedad de Graves y glomerulonefritis; (7) rechazo del injerto (incluyendo rechazo de aloinjertos y enfermedad de injerto vs. huésped), por ejemplo rechazo de injerto de piel, rechazo de trasplante de órgano sólido, rechazo de trasplante de médula ósea; (8) fiebre; (9) trastornos cardiovasculares, incluyendo insuficiencia cardíaca aguda, hipotensión, hipertensión, angina de pecho, infarto de miocardio, cardiomiopatía, insuficiencia cardíaca congestiva, aterosclerosis, enfermedad de las arterias coronarias, restenosis y estenosis vascular; (10) trastornos cerebrovasculares, incluyendo lesión cerebral traumática, accidente cerebrovascular, lesión de reperfusión isquémica y aneurisma; (11) cánceres de mama, piel, próstata, cuello uterino, útero, ovario, testículos, vejiga, pulmón, hígado, laringe, cavidad bucal, colon y tracto gastrointestinal (por ejemplo, esófago, estómago, páncreas), cerebro, tiroides, sangre y sistema linfático; (12) fibrosis, enfermedad del tejido conjuntivo y sarcoidosis, (13) afecciones genitales y reproductivas, incluida la disfunción eréctil; (14) trastornos gastrointestinales, incluyendo gastritis, úlceras, náuseas, pancreatitis y vómitos; (15) trastornos neurológicos, incluyendo la enfermedad de Alzheimer; (16) trastornos del sueño, incluyendo insomnio, narcolepsia, síndrome de apnea del sueño, y síndrome de Pickwick; (17) dolor; (18) trastornos renales; (19) trastornos oculares, incluyendo glaucoma; y (20) enfermedades infecciosas, incluido el VIH.
En ciertas realizaciones, el cáncer tratable con los métodos proporcionados en este documento incluye, entre otros, (1) leucemias, incluyendo, entre otros, leucemia aguda, leucemia linfocítica aguda, leucemias mielocíticas agudas tales como leucemias mieloblástica, promielocítica, mielomonocítica, monocítica, eritroleucemia y síndrome mielodisplásico o un síntoma de los mismos (tales como anemia, trombocitopenia, neutropenia, bicitopenia o pancitopenia), anemia refractaria (RA), RA con sideroblastos anillados (RARS), RA con exceso de blastos (RAEB), RAEB en transformación (RAEB-T), preleucemia y leucemia mielomonocítica crónica (CMML), (2) leucemias crónicas, incluyendo, entre otros, leucemia mielocítica crónica (granulocítica), leucemia linfocítica crónica y leucemia de células pilosas; (3) policitemia Vera; (4) linfomas, incluyendo, entre otros, la enfermedad de Hodgkin y la enfermedad no de Hodgkin; (5) mielomas múltiples, incluyendo, entre otros, mieloma múltiple quiescente, mieloma no secretor, mieloma osteosclerótico, leucemia de células de plasma, plasmacitoma solitario y plasmacitoma extramedular; (6) macroglobulinemia de Waldenstrom; (7) gammopatía monoclonal de significación indeterminada; (8) gammopatía monoclonal benigna; (9) enfermedad de cadena pesada; (10) sarcomas de hueso y tejido conjuntivo, incluyendo, entre
otros, sarcoma óseo, osteosarcoma, condrosarcoma, sarcoma de Ewing, tumor maligno de células gigantes, fibrosarcoma de hueso, cordoma, sarcoma perióstico, sarcomas de tejido blando, angiosarcoma ( hemangiosarcoma), fibrosarcoma, sarcoma de Kaposi, leiomiosarcoma, liposarcoma, linfangiosarcoma, cánceres metastásicos, neurilemmoma, rabdomiosarcoma y sarcoma sinovial; (11) tumores cerebrales, incluyendo, entre otros, glioma, astrocitoma, glioma del tronco encefálico, ependimoma, oligodendroglioma, tumor no glial, neurinoma acústico, craneofaringioma, meduloblastoma, meningioma, pineocitoma, pineoblastoma y linfoma del cerebro primario (12) cáncer de mama, incluyendo, entre otros, adenocarcinoma, carcinoma lobular (células pequeñas), carcinoma intraductal, cáncer de mama medular, cáncer de mama mucinoso, cáncer de mama tubular, cáncer de mama papilar, cánceres primarios, enfermedad de Paget, y cáncer de mama inflamatorio; (13) cáncer suprarrenal, incluyendo, entre otros, feocromocitoma y carcinoma adrenocortical; (14) cáncer de tiroides, incluyendo, entre otros, cáncer de tiroides papilar o folicular, cáncer de tiroides medular, y cáncer de tiroides anaplástico; (15) cáncer pancreático, incluyendo, entre otros, insulinoma, gastrinoma, glucagonoma, vipoma, omatostatinoma, ytumorcarcinoide o de células del islote; (16) cáncer de la hipófisis, incluyendo, pero limitado a, enfermedad de Cushing, tumor secretor de prolactina, acromegalia, y diabetes insipius; (17) cáncer ocular, que incluye, entre otros, melanoma ocular, como el melanoma del iris, el melanoma coroides y el melanoma del cuerpo cilliario, y el retinoblastoma; (18) cáncer vaginal, incluyendo, entre otros, carcinoma de células escamosas, adenocarcinoma y melanoma; (19) cáncer vulvar, incluyendo, entre otros, carcinoma de células escamosas, melanoma, adenocarcinoma, carcinoma basocelular, sarcoma y enfermedad de Paget; (20) cánceres de cuello uterino, incluyendo, entre otros, carcinoma de células escamosas y adenocarcinoma; (21) cáncer uterino, incluyendo, entre otros, carcinoma endometrial y sarcoma uterino; (22) cáncer ovárico, incluyendo, entre otros, carcinoma epitelial ovárico, tumor de bajo potencial de malignidad, tumor de la célula de germen, y tumor estromal; (23) cáncer de esófago, incluyendo, entre otros, el cáncer escamoso, adenocarcinoma, carcinoma enquistado adenoideo, carcinoma mucoepidermoide, carcinoma adenoescamoso, sarcoma, melanoma, plasmacitoma, carcinoma verrucoso, y carcinoma de células en grano de avena (células pequeñas) (24) cáncer de estómago, incluyendo, entre otros, adenocarcinoma, linfoma maligno fúngico (polipoide), ulcerante, de propagación superficial, de propagación difusa, liposarcoma, fibrosarcoma, y carcinosarcoma; (25) cáncer de colon; (26) cáncer rectal; (27) cáncer de hígado, incluyendo, entre otros, carcinoma hepatocelular y hepatoblastoma (28) cáncer de la vesícula biliar, incluyendo, entre otros, adenocarcinoma; (29) colangiocarcinomas, incluyendo, entre otros, papilar, nodular y difuso; (30) cáncer de pulmón, incluyendo, entre otros, cáncer de pulmón de células no pequeñas, carcinoma de células escamosas (carcinoma epidermoide), adenocarcinoma, carcinoma de células grandes y cáncer de pulmón de células pequeñas; (31) cáncer testicular, incluyendo, entre otros, tumor germinal, seminoma, anaplásico, clásico (típico), espermatocítico, no seminoma, carcinoma embrionario, carcinoma de teratoma, y coriocarcinoma (tumor del saco de yema de huevo); (32) cáncer de próstata, incluyendo, entre otros, adenocarcinoma, leiomiosarcoma, y rabdomiosarcoma; (33) cáncer renal; (34) cáncer bucal, incluyendo, entre otros, carcinoma de células escamosas; (35) cáncer basal; (36) cáncer de la glándula salival, incluyendo, entre otros, adenocarcinoma, carcinoma mucoepidermoide, y carcinoma adenoidenquistado; (37) cáncer de faringe, incluyendo, entre otros, cáncer de células escamosas y verrucoso; (38) cáncer de piel, incluyendo, entre otros, carcinoma de células basales, carcinoma de células escamosas y melanoma, melanoma superficial diseminante, melanoma nodular, melanoma maligno lentigo y melanoma lentiginoso acral; (39) cáncer de riñón, incluyendo, entre otros, cáncer de células renales, adenocarcinoma, hipernefroma, fibrosarcoma y cáncer de células transitorias (pelvis renal y/o uréter); (40) tumor de Wilms; (41) cáncer de vejiga, incluyendo, entre otros, carcinoma de células transicionales, cáncer de células escamosas, adenocarcinoma y carcinosarcoma; y otros cánceres, incluyendo, entre otros, mixosarcoma, sarcoma osteogénico, endotelosarcoma, linfangio-endotelosarcoma, mesotelioma, sinovioma, hemangioblastoma, carcinoma epitelial, cistadenocarcinoma, carcinoma broncogénico, carcinoma de glándula sebácea, carcinoma papilar y adenocarcinomas papilares (Ver Fishman et al., 1985, Medicine, 2a ed., J.B. Lippincott Co., Philadelphia y Murphy et al., 1997, Informed Decisions: The Complete Book of Cancer Diagnosis, Treatment, and Recovery, Viking Penguin, Penguin Books U.S.A., Inc., Estados Unidos de América).
Dependiendo del trastorno, enfermedad o condición a tratar, y la condición del sujeto, los compuestos o las composiciones farmacéuticas proporcionadas en este documento se pueden administrar por vía oral, parenteral (p. ej., intramuscular, intraperitoneal, intravenosa, ICV, inyección o infusión intracisternal, inyección subcutánea o implante), vías de administración por inhalación, nasal, vaginal, rectal, sublingual o tópica (por ejemplo, transdérmica 0 local) y pueden formularse, solos o juntos, en una unidad dosificadora adecuada con excipientes, vehículos, adyuvantes y vehículos adecuados para cada vía de administración. También se proporciona la administración de los compuestos o composiciones farmacéuticas proporcionadas en este documento en una formulación de depósito, en la que el ingrediente activo se libera durante un período de tiempo predefinido.
En el tratamiento, la prevención o el mejoramiento de uno o más síntomas de los trastornos, enfermedades o afecciones descritas en este documento, un nivel de administración adecuado generalmente oscila entre aproximadamente 0,001 y 100 mg por kg de peso corporal por día (mg/kg por día), de aproximadamente 0,01 a aproximadamente 75 mg/kg por día, de aproximadamente 0,1 a aproximadamente 50 mg/kg por día, de aproximadamente 0,5 a aproximadamente 25 mg/kg por día, o de aproximadamente 1 a aproximadamente 20 mg/kg por día, que se puede administrar en dosis únicas o múltiples. Dentro de este intervalo, la administración puede oscilar entre aproximadamente 0,005 y aproximadamente 0,05, de aproximadamente 0,05 a aproximadamente 0,5, de aproximadamente 0,5 a aproximadamente 5,0, de aproximadamente 1 a aproximadamente 15, de aproximadamente 1 a aproximadamente 20, o de aproximadamente 1 a aproximadamente 50 mg/kg por día.
Para la administración oral, las composiciones farmacéuticas proporcionadas en este documento se pueden formular en forma de tabletas que contienen de aproximadamente 1,0 a aproximadamente 1.000 mg del ingrediente activo, en una realización, aproximadamente 1, aproximadamente 5, aproximadamente 10, aproximadamente 15, aproximadamente 20, aproximadamente 25, aproximadamente 50 , aproximadamente 75, aproximadamente 100, aproximadamente 150, aproximadamente 200, aproximadamente 250, aproximadamente 300, aproximadamente 400, aproximadamente 500, aproximadamente 600, aproximadamente 750, aproximadamente 800, aproximadamente 900, y aproximadamente 1.000 mg del ingrediente activo para el ajuste sintomático de la administración al paciente que se tratará. Las composiciones farmacéuticas se pueden administrar en un régimen de 1 a 4 veces al día, incluyendo una vez, dos, tres veces, y cuatro veces al día.
Se entenderá, sin embargo, que el nivel de dosis específico y la frecuencia de administración para cualquier paciente en particular puedes ser variados y dependerá de una variedad de factores incluyendo la actividad del compuesto específico empleado, la estabilidad metabólica y el tiempo de acción de ese compuesto, la edad, el peso corporal, la salud general, el sexo, la dieta, el modo y el tiempo de administración, la tasa de excreción, la combinación de fármacos, la gravedad de la afección en particular y el huésped sometido al tratamiento.
También se describen en este documento métodos de modulación de la actividad PI3K, que comprenden poner en contacto una enzima PIK3 con el compuesto proporcionado en este documento; por ejemplo, el compuesto de fórmula I, IA o IB, incluyendo un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereoisómeros de los mismos; o sus sales farmacéuticas aceptables, solvatos, o hidratos. En una realización, la enzima PIK3 está dentro de una célula.
En ciertas realizaciones, el PI3K es un PI3K natural. En ciertas realizaciones, el PI3K es un PI3K mutante.
En ciertas realizaciones, el PI3K es una quinasa de clase I. En ciertas realizaciones, el PI3K es p110a, p110p, p1105, o p110Y. En ciertas realizaciones, el PI3K es una quinasa de clase I natural. En ciertas realizaciones, el PI3K es una quinasa de clase I mutante.
En ciertas realizaciones, el PI3K es p110a. En ciertas realizaciones, el PI3K es un p110a natural. En ciertas realizaciones, el PI3K es un p110a mutante. En ciertas realizaciones, el p110a mutante es R38H, G106V, K111N, K227E, N345K, C420R, P539R, E542K, E545A, E545G, E545K, Q546K, Q546P, E453Q, H710P, I800L, T1025S, M1043I, M1043V, H1047L, H1047R, o H1047Y. En ciertas realizaciones, el p110a mutante es R38H, K111N, N345K, C420R, P539R, E542K, E545A, E545G, E545K, Q546K, Q546P, I800L, T1025S, M1043I, H1047L, H1047R, o H1047Y. En ciertas realizaciones, el p110a mutante es C420R, E542K, E545A, E545K, Q546K, I800L, M1043I, H1047L, o H1047Y.
En ciertas realizaciones, el PI3K es una quinasa de clase IV. En ciertas realizaciones, el PI3K es una quinasa de clase IV natural. En ciertas realizaciones, el PI3K es una quinasa de clase IV mutante. En ciertas realizaciones, el PI3K es mTOR, ATM, ATR, o DNA-PK. En ciertas realizaciones, el PI3K es mTOR.
En ciertas realizaciones, los compuestos proporcionados en este documento, p. ej., un compuesto de fórmula I, IA, o IB, incluyendo un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereoisómeros de los mismos; o su sal farmacéutica aceptable, solvato, o hidrato, muestra actividad inhibitoria contra un PI3Ky su mutante.
En ciertas realizaciones, los compuestos proporcionados en este documento, p. ej., un compuesto de fórmula I, IA, o IB, incluyendo un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereoisómeros de los mismos; o sus sales farmacéuticas aceptables, solvatos, o hidratos, muestran actividad inhibitoria contra un PI3K natural. En ciertas realizaciones, el PI3K es p110a. En ciertas realizaciones, el PI3Kes mTOR.
En ciertas realizaciones, los compuestos proporcionados en este documento, p. ej., un compuesto de fórmula I, IA, o IB, incluyendo un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereoisómeros de los mismos; o una sal farmacéuticamente aceptable, solvato, o hidrato de los mismos, muestran actividad inhibitoria contra un PI3K mutante. En ciertas realizaciones, el mutante PI3K es un PI3K mutante. En ciertas realizaciones, el PI3K mutante es un p110a mutante. En ciertas realizaciones, el p110a mutante es C420R, E542K, E545A, E545K, Q546K, I800L, M1043I, H1047L, o H1047Y.
Los compuestos proporcionados en este documento, por ejemplo un compuesto de fórmula I, IA o IB, incluyendo un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más diastereoisómeros de los mismos; o una sal farmacéutica aceptable, soluble o hidratado de los mismos, también puede combinarse o utilizarse en combinación con otros agentes o terapias útiles en el tratamiento, la prevención o la mejora de uno o más síntomas de los trastornos, enfermedades o condiciones para que los compuestos proporcionados en este documento sean útiles, incluyendo asma, rinitis alérgica, eczema, psoriasis, dermatitis atópica, fiebre, sepsis, lupus eritematoso sistémico, diabetes, artritis reumatoide, esclerosis múltiple, aterosclerosis, rechazo de trasplante, enfermedad inflamatoria intestinal, cáncer, enfermedades infecciosas y las patologías indicadas en este documento.
Otros agentes terapéuticos adecuados también pueden incluir, entre otros, (1) agentes alfa-adrenérgicos; (2) agentes antiarrítmicos; (3) agentes antiateroscleróticos, como los inhibidores de la ACAT; (4) antibióticos, como antraciclinas,
bleomicinas, mitomicina, dactinomicina y plicamicina; (5) agentes anticancerígenos y agentes citotóxicos, por ejemplo agentes alquilantes, tales como mostazas de nitrógeno, alquil-sulfonatos, nitrosoureas, etileniminas y triazenos; (6) anticoagulantes, como acenocoumarol, argatroban, bivalirudina, lepirudina, fondaparinux, heparina, fenindiona, warfarina y ximelagatrán; (7) agentes antidiabéticos, como biguanidas (por ejemplo, metformina), inhibidores de la glucosidasa (por ejemplo, acarbosa), insulinas, meglitinidas (por ejemplo, repaglinida), sulfonilureas (por ejemplo, glimepirida, gliburida y glipizida), tiozolidinedionas (por ejemplo, troglitazona, rosiglitazona y pioglitazona) y agonistas PPAR-gamma; (8) agentes antifúngicos, como amorolfina, anfotericina B, anidulafungina, bifonazol, butenafina, butoconazol, caspofungina, ciclopirox, clotrimazol, econazol, fenticonazol, filipin, fluconazol, isoconazol, itraconazol, ketoconazol, micafungina, miconazol, naftifina, natamicina, nistatina, oxiconazol, ravuconazol, posaconazol, rimocidina, sertaconazol, sulconazol, terbinafina, terconazol, tioconazol y voriconazol; (9) antiinflammatorios, por ejemplo agentes antiinflamatorios no esteroideos, tales como aceclofenac, acemetacina, amoxiprina, aspirina, azapropazona, benorilato, bromfenac, carprofen, celecoxib, salicilato de magnesio de colina, diclofenac, diflunisal, etodolac, etoricoxib, faislamina, fenbufen, fenoprofen, flurbiprofeno, ibuprofeno, indometacina, ketoprofeno, ketorolac, lornoxicam, loxoprofeno, lumiracoxib, ácido meclofenámico, ácido mefenámico, meloxicam, metamizol, salicilato de metilo, salicilato de magnesio, nabumetona, naproxeno, nimesulida, oxifenbutazona, parecoxib, fenilbutazona, piroxicam, salicilato del salicilo, sulindac, sulfinpirazona, suprofen, tenoxicam, ácido tiaprofénico, y tolmetin; (10) antimetabolitos, como antagonistas de folatos, análogos de purina y análogos de pirimidina; (11) agentes antiplaquetarios, como bloqueadores de GPIIb/IIIa (por ejemplo, abciximab, eptifibatida y tirofiban), antagonistas de P2Y (AC) (por ejemplo, clopidogrel, ticlopidina y CS-747), cilostazol, dipiridamol y aspirina; (12) antiproliferativos, como metotrexato, FK506 (tacrolimus) y micofenolato mofetilo; (13) anticuerpos anti-TNF o receptor soluble de TNF, tales como etanercept, rapamicina y leflunimida; (14) inhibidores del aP2; (15) agentes beta-adrenérgicos, como carvedilol y metoprolol; (16) secuestrantes de ácido biliar, como questran; (17) bloqueadores de los canales de calcio, como el besilato de amlodipino; (18) agentes quimioterapéuticos; (19) inhibidores de la ciclooxigenasa-2 (COX-2), como celecoxib y rofecoxib; (20) ciclosporinas; (21) fármacos citotóxicos, como azatioprina y ciclofosfamida; (22) diuréticos, como clorotiazida, hidroclorotiazida, flumetiazoida, hidroflumetiazida, bendroflumetiazida, metilclorotiacida, triclorometiazoida, poliotiazida, benzotiazida, ácido etacrínico, ticrinafen, clortalidona, furosenida, muzolimina, bumetanida, triamtereno, amilorida y espironolactona; (23) inhibidores de la enzima convertidora de endotelina (ECE), como el fosforamidon; (24) enzimas, como L-asparaginasa; (25) inhibidores del factor VIIa e inhibidores del factor Xa; (26) inhibidores de la farnesilo-proteína transferasa; (27) fibratos; (28) inhibidores del factor de crecimiento, tales como moduladores de la actividad de PDGF; (29) secretagogos de la hormona del crecimiento; (30) inhibidores de HMG CoA reductasa, tales como pravastatina, lovastatina, atorvastatina, simvastatina, NK-104 (a.k.a. itavastatina, nisvastatina, o nisbastatina), y ZD-4522 (también conocido como rosuvastatina, atavastatina, o visastatina); inhibidores de la endopeptidasa neutra (NEP); (31) agentes hormonales, como los glucocorticoides (por ejemplo, cortisona), estrógenos/antiestrógenos, andrógenos/antiandrógenos, progestinas y antagonistas de la hormona liberadora de hormonas luteinizantes y acetato de octreotida; (32) inmunosupresores; (33) antagonistas del receptor de mineralocorticoides, como espironolactona y eplerenona; (34) agentes disruptores de microtúbulo, como ecteinascidinas; (35) agentes estabilizadores de microtúbulos, como pacitaxel, docetaxel y epotilones A-F; (36) inhibidores de MTP; (37) niacina; (38) inhibidores de la fosfodiesterasa, como los inhibidores de la PDE III (por ejemplo, cilostazol) e inhibidores de la PDE V (por ejemplo, sildenafilo, tadalafil y vardenafil); (39) productos derivados de plantas, como alcaloides de la vinca, epipodofilotoxinas y taxanos; (40) antagonistas del factor activador plaquetario (PAF); (41) complejos de coordinación de platino, como cisplatino, satraplatina y carboplatino; (42) activantes del canal de potasio; (43) inhibidores de la prenilo-proteína transferasa; (44) inhibidores de la proteína tirosina cinasa; (45) inhibidores de renina (46) inhibidores de la escualeno sintetasa; (47) esteroides, tales como aldosterona, beclometasona, betametasona, acetato de desoxicorticosterona, fludrocortisona, hidrocortisona (cortisol), prednisolona, prednisona, metilprednisolona, dexametasona y triamcinolona; (48) inhibidores de la TNF-alfa, tales como tenidap; (49) inhibidores de la trombina, como hirudina; (50) agentes trombolíticos, como anistreplasa, reteplasa, tenecteplasa, activador plasminógeno tisular (TPA), TPA recombinante, estreptoquinasa, uroquinasa, prouroquinasa y complejo activador de estreptoquinasa plasminógena anisoilada (APSAC); (51) antagonistas del receptor de tromboxano, como ifetroban; (52) inhibidores de la topoisomerasa; (53) inhibidores de la vasopeptidasa (inhibidores duales de la NEP-ECA), como omapatrilat y gemopatrilato; y (54) otros agentes misceláneos, tales como, hidroxiurea, procarbazina, mitotana, hexametilmelamina y compuestos de oro.
En ciertas realizaciones, las otras terapias que se pueden utilizar conjuntamente con los compuestos proporcionados en este documento incluyen, entre otros, cirugía, terapia endocrina, modificadores de la respuesta biológica (por ejemplo, interferones, interleucinas y factor de necrosis tumoral (TNF)), hipertermia y crioterapia, y agentes para atenuar cualquier efecto adverso (por ejemplo, antieméticos).
En ciertas realizaciones, los otros agentes terapéuticos que se pueden utilizar conjuntamente con los compuestos proporcionados en este documento incluyen, entre otros, fármacos alquilantes (mecloretamina, clorambucil, ciclofosfamida, melfalan, e ifosfamida), antimetabolitos (citarabina (también conocida como citosina arabinósido o Ara-C), HDAC (dosis alta de citarabina) y metotrexato), antagonistas de purina y antagonistas de pirimidina (6-mercaptopurina, 5-fluorouracilo, citarbina y gemcitabina), venenos del huso (vinblastina, vincristina y vinorelbina), podofilotoxinas (etopósido, irinotecán y topotecán), antibióticos (daunorubicina, doxorubicina, bleomicina y mitomicina), nitrosoureas (carmustina y lomustina), enzimas (asparaginasa) y hormonas (tamoxifeno, leuprolida, flutamida y megestrol), imatinib, adriamicina, dexametasona y ciclofosfamida. Para una discusión más comprensiva
de terapias actualizadas del cáncer; ver http://www.nci.nih.gov/, una lista de los fármacos oncológicos aprobados por la FDAen http://www.fda.gov/cder/cancer/druglistframe.htm, y el manual Merck, decimoséptima ed. 1999.
En otra realización, el método descrito en este documento comprende administrar un compuesto de fórmula I, IA o IB, junto con administrar uno o más agentes quimioterapéuticos y/o terapias seleccionadas de: agentes alquilantes (por ejemplo cisplatina, carboplatino); antimetabolitos (por ejemplo, metotrexato y 5-FU); antibióticos antitumorales (por ejemplo, adriamimicina y bleomicina); alcaloides vegetales antitumorales (por ejemplo, taxol y etopósido); hormonas antitumorales (por ejemplo, dexametasona y tamoxifeno); agentes inmunológicos antitumorales (por ejemplo, interferón a, p y y); radioterapia; y cirugía. En ciertas realizaciones, los uno o más agentes quimioterapéuticos y/o terapias se administran al sujeto antes, durante o después de la administración del compuesto de la fórmula I, IA o IB tal como se define en el presente documento.
Estos otros agentes, o fármacos, pueden ser administrados, por una ruta y en una cantidad comúnmente utilizada para ello, simultáneamente o secuencialmente, con los compuestos proporcionados en el presente documento, por ejemplo un compuesto de fórmula I, IA o IB, incluyendo un solo enantiómero, una mezcla de enantiómeros, o una mezcla de diastereoisómeros de los mismos; o una sal farmacéutica aceptable, o solvato de la misma. Cuando el compuesto proporcionado en este documento se utiliza simultáneamente con uno o más otros fármacos, una composición farmacéutica que contenga tales otros fármacos, además del compuesto proporcionado en este documento puede ser utilizado, pero no es necesario. En consecuencia, las composiciones farmacéuticas en este documento proporcionadas en este documento incluyen aquellas que también contienen uno o más ingredientes activos o agentes terapéuticos, además del compuesto proporcionado en este documento.
La relación en peso del compuesto proporcionado en el presente documento respecto al segundo ingrediente activo puede variarse, y dependerá de la dosis efectiva de cada ingrediente. Por lo general, se utilizará una dosis efectiva de cada uno. Así, por ejemplo, cuando el compuesto proporcionado en este documento se combina con un NSAID, la relación en peso del compuesto frente al NSAID puede variar entre aproximadamente 1000:1 a aproximadamente 1:1000, o aproximadamente 200:1 a aproximadamente 1:200. Combinaciones del compuesto proporcionado en este documento y otros ingredientes activos generalmente también estarán dentro del intervalo antes mencionado, pero en cada caso, se debe utilizar una dosis efectiva de cada ingrediente activo.
Los compuestos proporcionados en este documento también se pueden proporcionar como un artículo de fabricación utilizando materiales de envasado bien conocidos por los expertos en la técnica. Véase, p. ej., U.S. Pat. Nos.
5.323.907; 5.052.558; y 5.033.252. Ejemplos de materiales de envasado farmacéutico incluyen, entre otros, blísters, botellas, tubos, inhaladores, bombas, bolsas, viales, recipientes, jeringas, y cualquier material de envasado adecuado para una formulación seleccionada y el modo previsto de administración y tratamiento.
En este documento se proporcionan también kits que, cuando son utilizados por el médico, pueden simplificar la administración de cantidades apropiadas de ingredientes activos a un sujeto. En ciertas realizaciones, el kit proporcionado en este documento incluye un recipiente y una forma de administración del compuesto proporcionado en este documento, incluyendo un solo enantiómero o una mezcla de diastereoisómeros de los mismos; o una sal farmacéutica aceptable, o solvato de los mismos.
En ciertas realizaciones, el kit incluye un recipiente que comprende una forma de administración del compuesto proporcionado en este documento, incluyendo un solo enantiómero o una mezcla de diastereómeros de los mismos; o una sal farmacéutica aceptable, o solvato de los mismos, en un recipiente que comprende uno o más otros agentes terapéuticos descritos en este documento.
Los kits proporcionados en este documento pueden incluir además dispositivos que se utilizan para administrar los ingredientes activos. Algunos ejemplos de estos dispositivos incluyen, entre otros, jeringas, bolsas de goteo de inyectores sin aguja, parches e inhaladores. Los kits proporcionados en este documento también pueden incluir conservantes para la administración de los ingredientes activos.
Los kits proporcionados en este documento pueden incluir también vehículos farmacéuticos aceptables que se pueden utilizar para administrar uno o más ingredientes activos. Por ejemplo, si se proporciona un ingrediente activo en una forma sólida que se debe reconstituir para la administración parenteral, el kit puede incluir un recipiente sellado de un vehículo adecuado en el cual el ingrediente activo puede disolverse para formar una solución estéril sin partículas que sea adecuada para la administración parenteral. Los ejemplos de vehículos farmacéuticos aceptables incluyen, entre otros: vehículos acuosos, incluyendo, entre otros, agua para la inyección USP, inyección de cloruro de sodio, inyección de Ringer, inyección de dextrosa, inyección de dextrosa y cloruro de sodio e inyección de Ringer lactato; vehículos miscibles con agua, incluidos, entre otros, alcohol etílico, polietilenglicol y polipropilenglicol; y vehículos no acuosos, incluyendo, entre otros, aceite de maíz, aceite de semilla de algodón, aceite de cacahuete, aceite de sésamo, oleato de etilo, miristato de isopropilo y benzoato de bencilo.
La descripción se entenderá aún más mediante los siguientes ejemplos no limitantes.
Ejemplos
Como se utiliza en este documento, los símbolos y convenciones utilizados en estos procesos, esquemas y ejemplos, independientemente de si está específicamente definida una abreviatura particular, son consistentes con las utilizadas en la literatura científica contemporánea, por ejemplo, la Journal of the American Chemical Society o la Journal of Biological Chemistry. Concretamente, entre otras, se pueden utilizar las siguientes abreviaturas en los ejemplos y a lo largo de la memoria descriptiva: g (gramos); mg (miligramos); mL (mililitros); ^L (microlitros); M (molar); mM (milimolar); ^M (micromolar); eq. (equivalente); Hz (Hertz); MHz (megahercios); mmol (milimoles); h (horas); min (minutos); mp (punto de fusión); HRMS (espectrometría de masas de alta resolución); fA b (bombardeo por átomos rápidos); aq. (acuoso); DMF (dimetiformamida); DMSO (dimetilsulfóxido); DMSO-CÍ6 (dimetilsulfóxido deuterado); EtOH (etanol); EtOAc (acetato de etilo); /-Pr2O (éter diisopropilo); MeOH (metanol); THF (tetrahidrofurano); DIPeA (N,N-diisopropiletilamina); DMAP (dimetilaminopiridina); HOAc (ácido acético); LdA (diisopropilamina de litio); TFA (ácido trifluoroacético); e Dc I (1-etil-3-(3'-dimetilamino-propil)carbodiimida); cDl, (N,N-carbonildiimidazol); TBDMSCl (tercbutilclorodimetilsilano); TBAF (fluoruro de tetra-n-butilamonio); Me (metilo); Et (etilo); PdCh(dppf), ((1,1'-bis (difenilfosfino)ferroceno)dicloropaladio (II)); NAHMDS [hexametildisilazano de sodio o bis(trimetilsilil)amida de sodio)]; y EDTA (ácido etilendiamaminatetraacético).
Para todos los siguientes ejemplos, pueden ser utilizados métodos de trabajo estándar y de purificación conocidos por los expertos en la técnica. A menos que se indique lo contrario, todas las temperaturas se expresan en °C (grados centigrados). Todas las reacciones realizadas a temperatura ambiente a menos que se indique lo contrario. Las metodologías sintéticas ilustradas en este documento están destinadas a ejemplificar la química aplicable mediante el uso de ejemplos específicos y no son indicativos del alcance de la descripción.
Información general experimental.
Se llevaron a cabo análisis elementales (análisis de la combustión) en el laboratorio Microquímico de la Universidad de Otago, Dunedin, Nueva Zelanda. Los puntos de fusión se determinaron en un aparato electrotérmico 9100 de punto de fusión. Los espectros RMN se obtuvieron en un Espectrómetro Bruker Avance-400 a 400 MHz para 1H y 100 MHz para espectros 13C, referenciados a TMS (Si(CH3)4). Los espectros de masas se determinaron en un espectrómetro de masas VG-70SE utilizando un potencial ionizador de 70 eV a una resolución nominal de 1.000. Se obtuvieron espectros de alta resolución con resoluciones nominales de 3.000, 5.000, o 10.000 según proceda. Todos los espectros del MS fueron obtenidos como impacto del electrón (EI) usando el perfluoroqueroseno (PFK) como referencia a menos que se indique de otra manera. La cromatografía en columna se realizó en gel de sílice (Merck 230-400 malla), a menos que se indique lo contrario.
Ejemplo 1
Síntesis de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(3-piridinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
Se añadió 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1H-bencimidazol (publicación de solicitud de patente de EE.UU. 2007/244110) (0,183 g, 0,5 mmol) a una mezcla de 3-aminopiridina (0,20 g, 2 mmol) y LDA (1,0 mL, 2 M en THF, 2 mmol) en 10 mL de THF a temperatura ambiente. Después de 5 min, la mezcla fue neutralizada con HOAc, diluida con agua, extraída con EtOAc, y secada (Na2SO4). La cromatografía en alúmina eluyendo con CH2Cl2/EtOAc (4:1) dio un sólido, que fue recristalizado a partir de /-Pr2O para dar 92 mg (43% de rendimiento) de (4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(3-piridinil)-1,3,5-triazin-2-amina: mp (/-Pr2O) 228-230°C; 1H RMN (CDCh) 58,86 (ancho, 1H), 8,42 (d, J=2,0 Hz, 1H), 8,38 (d, J= 6,2 Hz, 1H), 7,98 (d, J=8,2 Hz, 1H), 7,89 (dd, J=6,2, 2,9 Hz, 1H), 7,58 (t ancho, Jhf=53,8 Hz, 1H), 7,42 (m, 2H), 7,34 (dd, J=8,3, 4,7 Hz, 1H), 7,28 (m, intercambiable con D2O, 1H), 3,93 (m, 4H), 3,82 (m, 4H); Anal. Calc. para C20H18F2N8O: C, 56,6; H, 4,3; N, 26,4; Encontrado: C, 56,5; H, 4,4; N, 26,1%.
Ejemplo 2
Síntesis de 4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-f3-piridinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
Se hidrogenó 2-amino-3-metoxinitrobenceno (15,10 g, 0,09 mol) en paladio sobre carbono en metanol, y la solución se filtró a través de celite en una solución de HCl metanólico. El disolvente se eliminó bajo vacío y la sal de clorhidrato resultante se combinó con ácido difluoroacético (19,2 g, 0,18 mol) y 4 M de HCl (100 mL). La mezcla se calentó bajo reflujo durante 3 horas, se diluyó con agua, se decolorizó con carbón vegetal, y se filtró a través de celite. La neutralización con amoníaco acuoso dio 2-difluorometil-4-metoxi-1H-bencimidazol (15,2 g, 84%) como un sólido: 1H RMN (CDCl3) (mezcla tautomérica) 59,95-9,70 (m, intercambiable con D2O, 1H), 7,44 (d ancho, J=7,9 Hz, 0,4H), 7,31 7,24 (m, 1H), 7,12 (d ancho, J=8,0 Hz, 0,5 H), 6,89 (t, Jhf=53,8 Hz, 1H), 6,82-6,74 (m, 1H), 4,03 y 3,98 (2s, 3H).
Una mezcla de 3,96 g (20 mmol) del bencimidazol antedicho, 4,70 g (20 mmol) de 2,4-dicloro-6-(4-morfolinil)-1,3,5-triazina, y 22 g (80 mmol) de pulverizado K2CO3 en 150 mL de DMF a temperatura ambiente se agitó rápidamente durante 3 horas y luego se diluyó con agua. El precipitado resultante fue recogido, lavado con agua, y luego con etanol frío, y secado para dar 6,82 g (86%) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-4-metoxi-1H-bencimidazol: mp (CHCls/EtOH) 263-266°C; 1H RMN (CDCls) 57,99 (d, J=8,4 Hz, 1H), 7,48 (t, Jhf=53,4 Hz, 1H), 7,40 (t, J=8,3 Hz, 1H), 6,86 (d, J=8,1 Hz, 1H), 4,05 (s, 3H), 3,96 (m, 4H), 3,82 (m, 4H); Anal. Calc. para C16H15C F 2N6O2: C, 48,4; H, 3,8; N, 21,2; Encontrado: C, 48,3; H, 3,8; N, 21,1%.
A una solución de 3-aminopiridina (1,88 g, 20 mmol) en 100 mL de THF se añadió LDA (10 mL, 2 M en THF; 20 mmol) y a la suspensión resultante se añadieron 1,99 g (5 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-4-metoxi-1H-bencimidazol a temperatura ambiente. Después de 5 min., la reacción se neutralizó con ácido acético y se diluyó con agua. Después de que el pH se hizo ligeramente alcalino con NH3ac., se recolectó el precipitado, se lavó con agua caliente y se secó. La recristalización a partir de EtOH (utilizando CH2Cl2 para ayudar a la solubilidad inicial) dio 1,65 g (73% de rendimiento) de 4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(3-piridinil)-1,3,5-triazin-2-amina: mp 221-223°C; 1H RMN (CDCl3) 58,86 (ancho, 1H), 8,42 (d, J=2,0 Hz, 1H), 7,99 (d, J=7,8 Hz, 1H), 7,92 (d, J= 8,1 Hz, 1H), 7,48 (t ancho, Jhf=53,6 Hz, 1H), 7,35-7,31 (m, 2H), 7,22 (m, intercambiable con D2O, 1H), 6,82 (d, J=8,0 Hz, 1H), 4,04 (s, 3H), 3,92 (m, 4H), 3,81 (m, 4H); Anal. Calc. para C21H20F2N8O2: C, 55,5; H, 4,4; N, 24,7; Encontrado: C, 55,5; H, 4,4; N, 24,4%.
Una suspensión de 4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(3-piridinil)-1,3,5-triazin-2-amina en MeOH fue tratada con un exceso leve de ácido metansulfónico, para dar una solución clara. La adición de EtOAc dio un precipitado, que fue recogido por la filtración y el lavado con EtOAc. La recristalización con MeOH/EtOAc dio 4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(3-piridinil)-1,3,5-triazin-2-amina metanosulfonato: mp 279-282°C; 1H RMN (cf6DMSO 5 10,63 (s, intercambiable con D2O, 1H), 9,19 (s, 1H), 8,55 (d, J=5,5 Hz, 1H), 8,53 (m, 1H), 8,08 (m, 1 H), 7,90 (dd, J=8,5, 5,4 Hz, 1H), 7,82 (t ancho, Jhf=53,0 Hz, 1H), 7,43 (t, J=8,2 Hz, 1H), 6,98 (d, J=7,8 Hz, 1H), 4,56 (m ancho, intercambiable con D2O, 1H), 3,99 (s, 3H), 3,86 (m, 4H), 3,75 (m, 4H); Anal. Calc. para C22H24F2N8O5S: C, 48,0; H, 4,4; N, 20,4; Encontrado: C, 47,8; H, 4,4; N, 20,2%.
Ejemplo 3
Síntesis de 4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-N-metil-6-(4-morfolinil)-N-(3-piridinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método D.
Una solución de 4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benám¡dazoM-¡l]-6-(4-morfol¡ml)-N-(3-p¡rid¡ml)-1,3,5-triaz¡n-2-am¡na (0,544 g, 1 mmol) en 15 ml de DMF fue tratado con de NaH y entonces fue agregado un exceso leve de yodometano. Después de 10 m¡n, la reacc¡ón se neutral¡zó con ác¡do acét¡co y se d¡luyó con agua. Después de que el pH se h¡zo l¡geramente alcal¡no con NH3ac., el prec¡p¡tado fue recog¡do y secado. La cromatografía en alúm¡na eluyendo con CH2Cl2/EtOAc (9:1) d¡o 0,26 g (53% de rend¡m¡ento) de 4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-N-metil-6-(4-morfolinil)-N-(3-piridinil)-1,3,5-triazin-2-amina: mp (MeOH) 200-201°C; 1H RMN (DMSO-de) 58,67 (d, J=2,2 Hz, 1H), 8,55 (d, J=4,1 Hz, 1H), 7,89 (ddd, J=8,1,2,6, 1,5 Hz, 1H), 7,70-7,29 (m, 3H), 6,90 (d, J=8,0 Hz, 1H), 3,94 (s, 3H), 3,84 3.61 (m, 8H), 3,55 (s, 3H); Anal. Calc. para C22H22F2N8O2: C, 56,4; H, 4,7; N, 23,9; Encontrado: C, 56,5; H, 4,75; N, 24,5%.
Ejemplo 4
Síntes¡s de 4-[2-(met¡lsulfan¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-N-(3-p¡r¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na
El compuesto fue s¡ntet¡zado según el método A.
Una mezcla de 2-(met¡lsulfan¡l)-1H-benc¡m¡dazol (1,64 g, 10 mmol), 2,4-d¡cloro-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡na (2,35 g, 10 mmol) y K2CO3 en polvo (11 g, 80 mmol) en DMF (50 mL) se ag¡tó a temperatura amb¡ente durante 1 hora. La mezcla se d¡luyó con agua y el prec¡p¡tado resultante fue recolectado, lavado con agua y luego etanol, y secado para dar 3,56 g (98% de rend¡m¡ento) de 1-[4-cloro-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-2-(met¡lsulfan¡l)-1H-benc¡m¡dazol: mp (CHCl3/EtOH) 260-261°C; 1H RMN (CDCl3) 58,42 (dd ancho, J=7,0, 1,9 Hz, 1H), 7,65 (dd ancho, J=6,8, 1,9 Hz, 1H), 7,30 (m, 2H), 4,06 (m, 2H), 3,95 (m, 2H), 3,84 (m, 2H), 3,80 (m, 2H), 2,74 (s, 3H); Anal. Calc. para C15H15ClN6OS: C, 49,65; H, 4,2; N, 23,2; Encontrado: C, 49,8; H, 4,1; N, 23,1%.
Una soluc¡ón de 3-am¡nop¡r¡d¡na (2 g, 21 mmol) en 100 mL de THF fue tratada con 10,6 mL (21 mmol) LDA 2 M en THF para dar una suspens¡ón que fue tratada con 1,81 g (5 mmol) de 1 -[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(met¡lsulfan¡l)-1H-benc¡m¡dazol a temperatura amb¡ente. Después de 5 m¡n, la mezcla se neutral¡zó con HOAc y se d¡luyó con agua para dar 1,65 g (78%) de 4-[2-(met¡lsulfan¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-N-(3-p¡r¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na: mp (CHCls/EtOH) 240-241°C; 1H RMN (CDCl3) 58,85 (s ancho, 1H), 8,39 (d, J=4,0 Hz, 1H), 8,34 (d, J=7,5 Hz, 1H), 8,02 (d, J=7,3 Hz, 1H), 7,66 (dd, J=7,9, 0,5 Hz, 1H), 7,32 (dd, J=8,5, 4,9 Hz, 1H), 7,28 (dt, J=7,3, 1,1 Hz, 1H), 7,22 (t, J=7,4 Hz, 1H), 7,15 (s ancho, ¡ntercamb¡able con D2O, 1H), 4,05 (m, 2H), 3,90 (m, 2H), 3,81 (m, 4H), 2,73 (s, 3H); Anal. Calc. para C20H20N8OS: C, 57,1; H, 4,8; N, 26,65; Encontrado: C, 57,0; H, 4,9; N, 27,0%.
Ejemplo 5
Síntes¡s de 4-[2-(met¡lsulfon¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-N-(3-p¡r¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na
El compuesto fue s¡ntet¡zado según el método D.
Una soluc¡ón de 0,421 g (1 mmol) de 4-[2-(met¡lsulfan¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-N-(3-p¡r¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na (a part¡r del ejemplo 4) en 130 mL de acetona y 20 mL de HOAc fueron tratados con 1 g de KMnO4 en
10 mL de agua a temperatura ambiente. Después de 30 minutos, la reacción fue decoloreada con una solución de Na2SO3 ac. y la acetona se eliminó al vacío. El residuo se diluyó con agua y el pH se ajustó al neutro para dar un precipitado que se disolvió en CHCl3y se secó. La cromatografía en alúmina, eluyendo con CHCl3/EtOAc (9:1) dio 140 mg (31%) de 4-[2-(metilsulfonil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(3-piridinil)-1,3,5-triazin-2-amina: mp (MeOH) 208-211°C; 1H RMN (CDCl3) 58,88 (s ancho, 1H), 8,38 (dd, J=4,7, 1,4 Hz, 1H), 8,26 (d, J=7,9 Hz, 1H), 8,00 (d, J=7,8 Hz, 1H), 7,77 (dd, J=7,3, 1,2 Hz, 1H), 7,46-7,38 (m, 3H; 2H después de intercambio con D2O), 7,31 (dd, J=8,3, 4,7 Hz, 1H), 4,08 (m, 2H), 3,83 (m, 2H), 3,76 (m, 4H), 3,62 (s, 3H); Anal. Calc. para C20H20NsO3S 0,5 H2O: C, 52,0; H, 4,6; N, 24,3; Encontrado: C, 51,8; H, 4,6; N, 24,3%.
Ejemplo 6
Síntesis de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-fenil-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
Una mezcla de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1H-bencimidazol (92 mg, 0,25 mmol) y anilina (58 mg, 0,625 mmol) en dioxano (5 mL) se calentó bajo reflujo durante 1 hora y se enfrió. La dilución con agua dio un precipitado blanco, que fue recristalizado con MeOH para dar 52 mg (49% de rendimiento) de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-fenil-1,3,5-triazin-2-amina: mp 171-174°C; 1H RMN (CDCl3) 5 8,40 (m, 1H), 7,89 (m, 1H), 7,58 (t, Jhf=54,7 Hz, 1H), 7,55 (d, J=7,5 Hz, 1H), 7,43-7,38 (m, 4H), 7,20 (t, J=7,3 Hz, 1H), 7,09 (ancho, intercambiable con D2O, 1H), 3,93 (m, 4H), 3,81 (m, 4H); Anal. Calc. para C21H19F2N7O: C, 59,6; H, 4,5; N, 23,2; Encontrado: C, 59,6; H, 4,5; N, 23,3%.
Ejemplo 7
Síntesis de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-N-metil-6-(4-morfolinil)-N-fenil-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
Una mezcla de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1H-bencimidazol (92 mg, 0,25 mmol) y la N-metilanilina (67 mg, 0,625 mmol) en dioxano (5 mL) se calentaron bajo reflujo durante 1 hora y se enfrió. La dilución con agua dio un precipitado, que fue recogido y secado. La cromatografía en SiO2 eluyendo con CH2Cl2 dio 70 mg (64% de rendimiento) de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-N-metil-6-(4-morfolinil)-N-fenil-1,3,5-triazin-2-amina: mp (hexanos) 160-162°C; 1H RMN (CDCl3) 58,04 (m, 1H), 7,82 (d, J=7,8 Hz, 1H), 7,49 (t, J=7,6 Hz, 2H), 7,45 7,06 (m, 7H), 3,91 (m, 4H), 3,81 (m, 4H), 3,56 (s, 3H); Anal. Calc. para C22H21F2N7O: C, 60,4; H, 4,8; N, 22,4; Encontrado: C, 60,2; H, 5,0; N, 22,5%.
Ejemplo 8
Síntesis de N-bencil-4-[2-(difluorometil)-1 H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
Una mezcla de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1H-bencimidazol (92 mg, 0,25 mmol) y bencilamina (67 mg, 0,625 mmol) en dioxano (5 mL) se calentó al reflujo durante 5 min y se enfrió. La mezcla se diluyó con agua para dar un precipitado blanco, que fue recristalizado con EtOH para dar 73 mg (67% de rendimiento) de N-bencil-4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-amina: mp 185-188°C; 1H RMN (CDCl3) (rotámeros) 58,41 y 8,28 (2d, J=7,4 y 7,7 Hz, 1H), 7,89 (m, 1H), 7,64 y 7,50 (2t, Jhf=53,8 y 53,7 Hz, 1H), 7,43-7,29 (m, 7H), 5,62 (m, intercambiable con D2O, 1H), 4,72 y 4,68 (2d, J=6,0 y 5,9 Hz, 2H), 3,89 (m, 4H), 3,78 (m, 4H); Anal. Calc. para C22H21F2N7O: C, 60,4; H, 4,8; N, 22,4; Encontrado: C, 60,6; H, 4,8; N, 22,7%.
Ejemplo 9
Síntesis de N-bencil-4-[2-(difluorometil)-1 H-bencimidazol-1-il]-N-metil-6-(4-morfolinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
Una mezcla de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1H-bencimidazol (92 mg, 0,25 mmol) y N-metilbenzilamina (76 mg, 0,625 mmol) en dioxano (5 mL) se calentó a reflujo durante 5 min y se enfrió. La mezcla se diluyó con agua para dar un precipitado blanco, que fue recristalizado con EtOH para dar N-bencil-4-[2-(difluorometil)-1H-bencimidazol-1-il]-N-metil-6-(4-morfolinil)-1,3,5-triazin-2-amina: mp 147-150°C; 1H RMN (CDCl3) (rotámeros) 5 8,45 y 8,22 (2d, J=7,6 y 7,9 Hz, 1H), 7,90 y 7,85 (2d, J=8,3 y 7,7 Hz, 1H), 7,68 y 7,44 (2t, Jhf=53,7 y 53,6 Hz, 1H), 7,43-7,25 (m, 7H), 4,92 y 4,90 (2s, 2H), 3,95-3,73 (m, 8H), 3,22 y 3,20 (2s, 3H); Anal. Calc. para C23H23F2N7O: C, 61,2; H, 5,1; N, 21,7; Encontrado: C, 61,45; H, 5,2; N, 21,95%.
Ejemplo 10
Síntesis de 2-(difluorometil)-1-[4-(4-morfolinil)-6-fenoxi-1,3,5-triazin-2-il]-1 H-bencimidazol;
El compuesto fue sintetizado según el método A.
Se combinaron fenol (200 mg, 21 mmol) y NaOH (85 mg, 21 mmol) en agua para dar una solución clara, que luego se evaporó hasta secarse. Se agregaron 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1 H-bencimidazol (184 mg, 0,5 mmol) y tris[2-(2-metoxietoxi)etil]amina (TDA-1; 16 mg, 0,05 mmol) y la mezcla se calentó bajo reflujo en dioxano (10 mL) durante 2 h. Después de enfriarse, la mezcla se diluyó con agua para dar un sólido blanco, que fue recogido y recristalizado con MeOH para dar 93 mg (44% de rendimiento) de 2-(difluorometil)-1-[4-(4-morfolinil)-6-fenoxi-1,3,5-triazin-2-il]-1 H-bencimidazol: mp 228-231°C; 1H RMN (CDCls) 58,06 (d, J=8,2 Hz, 1H), 7,84 (d, J=7,8 Hz, 1H), 7,49 (t ancho, J=7,9 Hz, 2H), 7,36 (t ancho, J=7,5 Hz, 2H), 7,30 (dt, J=7,6, 1,1 Hz, 1H), 7,22 (m, 2H), 7,11 (t, Jhf=53,6 Hz, 1H), 3,99-3,93 (m, 4H), 3,86-3,79 (m, 4H); Anal. Calc. para C21H18F2N6O2: C, 59,4; H, 4,3; N, 19,8; Encontrado: C, 59,65; H, 4,2; N, 19,9%.
Ejemplo 11
Síntesis de 2-(difluorometil)-1-[4-(4-morfolinil)-6-(fenilsulfanil)-1,3,5-triazin-2-il]-1 H-bencimidazol
El compuesto fue sintetizado según el método A.
Se combinaron tiofenol (230 mg, 2,1 mmol) y NaOH (85 mg, 2,1 mmol) en agua para dar una solución clara, que luego se evaporó hasta secarse. Se agregaron 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1 H-bencimidazol (184 mg, 0,5 mmol) y tris[2-(2-metoxietoxi)etil]amina (TDA-1; 16 mg, 0,05 mmol) y la mezcla se calentó bajo reflujo en dioxano (10 mL) durante 2 h. Después de enfriar, la mezcla se diluyó con agua para dar un sólido, que fue recristalizado con EtoH para dar 167 mg (76% de rendimiento) de 2-(difluorometil)-1-[4-(4-morfolinil)-6-(fenilsulfanil)-1,3,5-triazin-2-il]-1 H-bencimidazol: mp 245-248°C; 1H RMN (CDCls) 5 7,83 (t, J=8,6 Hz, 2H), 7,67 (dd, J=8,1, 1,3 Hz, 2H), 7,58 (t ancho, J=7,4 Hz, 1H), 7,52 (t ancho, J=7,3 Hz, 2H), 7,34 (dt, J=7,9, 1,2 Hz, 1H), 7,25 (dd, J=7,8, 1,2 Hz, 1H), 6,91 (t, Jhf=53,5 Hz, 1H), 3,89 (m, 4H), 3,82-3,77 (m, 4H); Anal. Calc. para C21H18F2N6OS: C, 57,3; H, 4,1; N, 19,1; Encontrado: C, 57,2; H, 4,1; N, 19,2%.
Ejemplo 12
Síntesis de 2-(difluorometil)-1-[4-(4-morfolinil)-6-(fenilsulfonil)-1,3,5-triazin-2-il]-1 H-bencimidazol
El compuesto fue sintetizado según el método D.
Una solución de 0,1 g (0,23 mmol) de (2-(difluorometil)-1-[4-(4-morfolinil)-6-(fenilsulfanil)-1,3,5-triazin-2-il]-1H-bencimidazol (del ejemplo 11) en 10 mL de acetona y 10 mL de HoAc fue tratada con porciones de KMnO4 ac. al 4% hasta que el color se mantuvo. La mezcla fue entonces decoloreada con una solución de Na2SO3 ac., neutralizada con NH3 ac. y extraída con CH2Cl2. La cromatografía en sílice eluyendo con CH2Cl2/EtOAc (9:1) dio 26 mg (24% de rendimiento) de 2-(difluorometil)-1-[4-(4-morfolinil)-6-(fenilsulfonil)-1,3,5-triazin-2-il]-1 H-bencimidazol: mp (EtOH) 237-239°C; 1H RMN (CDCh) 58,13 (dd, J=8,4, 1,2 Hz, 2H), 7,99 (d, J=7,7 Hz, 1H), 7,86 (d, J=7,5 Hz, 1H), 7,80 (dt, J=7,5, 1,8 Hz, 1H), 7,67 (t, J=7,8 Hz, 2H), 7,41 (dt, J=7,8, 1,3 Hz, 1H), 7,35 (dt, J=7,8, 1,3 Hz, 1H), 7,13 (t, Jhf=53,3 Hz, 1H),
4,04 (m, 2H), 3,98 (m, 2 H), 3,84 (m, 4H); Anal. Calc. para C21H18F2N6O3S: C, 53,4; H, 3,8; N, 17,8; Encontrado: C, 53,4; H, 3,8; N, 18,0%.
Ejemplo 13
Síntesis de 4-[2-(difluorometil)-1 H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-N-(2-p¡r¡d¡n¡lmet¡l)-1,3,5-tr¡az¡n-2-am¡na
El compuesto fue s¡ntet¡zado según el método A.
Una mezcla ag¡tada de 1-[4-cloro-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-2-(d¡fluoromet¡l)-1H-benc¡m¡dazol (0,183 g, 0,5 mmol) y 2-am¡nomet¡lp¡r¡d¡na (0,135 g, 1,25 mmol) en 10 mL de d¡oxano se calentó suavemente hasta que se obtuvo una soluc¡ón clara. Después de enfriarse, la mezcla fue d¡lu¡da con agua para dar un sól¡do ace¡toso, que fue recr¡stal¡zado con MeOH acuoso para dar 0,11 g (50% de rend¡m¡ento) de 4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-N-(2-p¡r¡d¡n¡lmet¡l)-1,3,5-tr¡az¡n-2-am¡na: mp 192-193°C; 1H RMN (Cd CI3) (rotámeros) 58,65 (d, J=1,8 Hz, 1H), 8,57 (dd, J=4,7, 1,0 Hz, 1H), 8,40 y 8,25 (2d, J=7,5 y 5,5 Hz, 1H), 7,88 (m, 1H), 7,70 (d, J=7,7 Hz, 1H), 7,62 (t, Jhf=54,5 Hz, 1H), 7,43-7,37 (m, 2H), 7,30 (ddd, J=7,9, 4,8, 0,7 Hz, 1H), 5,75 y 5,64 (2 m, ¡ntercamb¡able con D2O, 1H), 4,76 y 4,69 (2 d, J=5,7 y 5,8 Hz, 2H), 3,87 (m, 4H), 3,78 (m, 4H); Anal. Calc. para C21H20F2N8O: C, 57,5; H, 4,6; N, 25,6; Encontrado: C, 57,5; H, 4,5; N, 25,6%.
Ejemplo 14
Síntes¡s de 4-[2-(d¡fluoromet¡l)-1 H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-N-(3-p¡r¡d¡n¡lmet¡l)-1,3,5-tr¡az¡n-2-am¡na
El compuesto fue s¡ntet¡zado según el método A.
Una mezcla ag¡tada de 1-[4-cloro-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-2-(d¡fluoromet¡l)-1H-benc¡m¡dazol (0,183 g, 0,5 mmol) y 3-am¡nomet¡lp¡r¡d¡na (0,135 g, 1,25 mmol) en 10 mL de d¡oxano se calentó bajo reflujo suave durante 5 m¡n. Después de enfriar, la mezcla se d¡luyó con agua para dar un sól¡do ace¡toso, que fue recr¡stal¡zado con MeOH para dar 0,13 g (59% de rend¡m¡ento) de 4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-N-(3-p¡r¡d¡n¡lmet¡l)-1,3,5-tr¡az¡n-2-am¡na: mp 160-161°C; 1H RMN (CDCI3) (rotámeros) 58,61 (d, J=4,4 Hz, 1H), 8,42 y 8,32 (2d, J=7,6 y 8,4 Hz, 1H), 7,89-7,87 (m, 1H), 7,70 (dt, J=7,7, 1,65 Hz, 1H), 7,65 y 7,59 (2t, Jhf=53,7 y 53,5 Hz, 1H), 7,43-7,37 (m, 2H), 7,34 (t ancho, J=8,7 Hz, 1H), 7,24 (t ancho, J=6,2 Hz, 1H), 6,55 y 6,41 (2 m, ¡ntercamb¡able con D2O, 1H), 4,82 y 4,78 (2 d, J=5,3 y 5,1 Hz, 2H), 3,88 (m, 4H), 3,78 (m, 4H); Anal. Calc. para C21H20F2N8O: C, 57,5; H, 4,6; N, 25,6; Encontrado: C, 57,7; H, 4,5; N, 25,7%.
Ejemplo 15
Síntes¡s de 4-[2-(d¡fluoromet¡l)-1 H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-N-(4-p¡r¡d¡n¡lmet¡l)-1,3,5-tr¡az¡n-2-am¡na
El compuesto fue sintetizado según el método A.
Una mezcla agitada de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1H-bencimidazol (0,183 g, 0,5 mmol) y 4-aminometilpiridina (0,135 g, 1,25 mmol) en 10 mL de dioxano se calentó bajo reflujo suave durante 5 min, antes de enfriarse y diluirse con agua. La mezcla se extrajo con CH2Cl2 y la capa orgánica se secó con Na2SO4. La cromatografía en alúmina, eluyendo con CH2Ch/EtOAc (9:1), seguida de cromatografía en sílice, eluyendo con CH2Cl2/EtOAc (3:2) dio 56 mg (26% de rendimiento) de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(4-piridinilmetil)-1,3,5-triazin-2-amina: mp 188-190°C; 1H Rm N (Cd CI3) (rotámeros) 58,60 (s ancho, 2H), 8,42 y 8,13 (2d, J=7,4 y 8,0 Hz, 1H), 7,88 (m, 1H), 7,64 (t, Jhf=53,6 Hz, 1H), 7,44-7,25 (m, 4H), 5,78 y 5,71 (2 m, intercambiable con D2O, 1H), 4,74 y 4,70 (2 d, J=6,0 y 6,0 Hz, 2H), 3,92-3,69 (m, 8H).
Ejemplo 16
Síntesis de 4-[2-(difluorometil)-1 H-bencimidazol-1-il]-6-(4-morfolinil)-N-(2-piridinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
Se agregaron a 0,224 g (2,38 mmol) de 2-aminopiridina en THF (3 mL) 2,5 mL de bis(trimetilsilil)amida de litio (solución 1 M en THF) y la mezcla se agitó durante 10 min. Una solución de 0,204 g (0,56 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1H-bencimidazol se añadió en THF (4 mL) y la mezcla se agitó durante 1 hora. La mezcla resultante fue neutralizada con ácido acético, diluida con agua y extraída con EtOAc. La capa orgánica fue lavada con agua y NH3 acuoso y secada. Después de la extracción del disolvente, el residuo fue purificado por cromatografía en alúmina, eluyendo con CH2Cl2/EtOAc (1:5) para dar un polvo anaranjado. La recristalización con EtOH/CH2Cl2 dio 31,5 mg (13% de rendimiento) de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(2-piridinil)-1,3,5-triazin-2-amina: mp 230-232°C; 1H RMN (CDCl3) 58,41-8,37 (m, 2H), 8,20 (d, J=8,4 Hz, 1H), 8,12 (s ancho, 1H), 7,91-7,89 (m, 1H), 7,75 (td, J=7,5, 1,8 Hz, 1H), 7,60 (t, Jh f =53,5 Hz, 1H), 7,45-7,39 (m, 2H), 7,05 (ddd, J=7,3, 4,9, 0,9 Hz, 1H), 3,96-3,94 (m, 4H), 3,85-3,82 (m, 4H); HRMS (FAB+) MNa+ Calc. para C20H1sF2NsNaO: m/z 447,1466; Encontrado: m/z 447,1464.
Ejemplo 17
Síntesis de 4-[2-(difluorometil)-1 H-bencimidazol-1-il]-6-(4-morfolinil)-N-(4-piridinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
Una mezcla de 0,048 g (0,51 mmol) de 4-aminopiridina y 0,095 g (0,26 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1H-bencimidazol en DMSO (1,5 mL) se calentó a 120°C durante 1 hora. La mezcla de reacción se enfrió a temperatura ambiente y se añadió agua. El sólido fue recogido por filtración y lavado con agua para dar 0 ,022 g (20 % de rendimiento) de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(4-piridinil)-1,3,5-triazin-2-amina: mp (MeOH) 222-224°C; 1H RMN (DMSO-de) 5 10,30 (s ancho, 1H), 8,59-8,46 (m, 3H), 7,91-7,86 (m, 4H), 7,55-7,44 (m, 2H), 3,88 (s ancho, 4H), 3,77-3,76 (m, 4H); HRMS (FAB+) MNa+ Calc. para C20H1sF2NsNaO: m/z 447,1466; Encontrado: m/z 447,1464; HRMS (FAB+) MH+ Calc. para C20H19F2N8NO: m/z 425,1644; Encontrado: m/z 425,1629.
Ejemplo 18
Síntesis de N-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-3-quinolinamina
El compuesto fue sintetizado según el método A.
A una solución de 0,323 g (2,24 mmol) de 3-aminoquinolina en THF (5 mL) a 0°C se añadieron 1,6 mL de NaHMDS (solución 2 M en THF), y la mezcla se agitó durante 15 min. Una solución de 0,280 g (0,77 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1H-bencimidazol se añadió en THF (4 mL) y la mezcla resultante se agitó durante 1 hora a TA. La mezcla resultante fue neutralizada con ácido acético, diluida con agua, y extraída con EtOAc. La capa orgánica fue lavada secuencialmente con agua y NHsac., secada y concentrada. La cromatografía en alúmina, eluyendo primero con hexanos/EtOAc (1:1), y luego cH 2Cl2-EtOAc (1:3) dio un polvo rosado. La recristalización con etanol dio 0,167 g (46% de rendimiento) de N-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-3-quinolinamina: mp 270-273°C; 1H RMN (CDCls) 59,08 (s ancho, 1H), 8,48-8,43 (m, 2H), 8,12 (d, J=8,4 Hz, 1H),
Ejemplo 19
Síntesis de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(2-pirimidinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
A una solución de 0,214 g (2,25 mmol) de 2-aminopirimidina en THF (4 mL) a 0 °C se añadieron 1,25 mL de NaHMDS (solución 2 M en THF) y la mezcla se agitó durante 20 min. Una solución de 0,275 g (0,75 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1H-bencimidazol se añadió en THF (4 mL), y la mezcla resultante se agitó durante 1 hora a TA. Después de la neutralización con ácido acético, la mezcla se diluyó con agua y se extrajo con EtOAc. La capa orgánica fue lavada secuencialmente con agua y NH3 ac., secada y concentrada. La cromatografía en alúmina, eluyendo primero con hexanos/EtOAc (4:1), luego con CH2Cl2/EtOAc (1:3) dio un polvo anaranjado. La recristalización con etanol dio 0,098 g (31% de rendimiento) de 4-[2-(difluorometil)-1 H-bencimidazol-1 H-bencimidazol-1-il]-6-(4-morfolinil)-N-(2-pirimidinil)-1,3,5-triazin-2-amina: mp 261-263°C; 1H RMN (CDCls) 58,69-8,67 (m, 3H), 8,34 (t, Jh f = 53,3 Hz, 1H), 8,07 (s ancho, 1H), 7,91 (dd, J = 7,9, 0,9 Hz, 1H), 7,49-7,40 (m, 2H), 7,05 (t, J=4,8 Hz, 1H), 3,96 (m, 4H), 3,83 (m, 4H); Anal. Calc. para C19H17F2N9O: C, 53,65; H, 4,0; N, 29,6; Encontrado: C, 53,6; H, 4,1; N, 29,4%. Ejemplo 20
Síntesis de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(4-pirimidinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
A una solución de 0,214 g (2,25 mmol) de 4-aminopirimidina en THF (4,5 mL) a 0°C se añadió 1,25 mL de NaHMDS (solución 2 M en THF), y la mezcla se agitó durante 20 min. Una solución de 0,282 g (0,77 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1H-bencimidazol se añadió en THF (6 mL) y la mezcla resultante se agitó durante 1 hora a TA. Después de la neutralización con ácido acético, la mezcla se diluyó con agua y se extrajo con EtOAc. La capa orgánica fue lavada secuencialmente con agua y NH3 ac., secada y concentrada. La cromatografía en alúmina, eluyendo con CH2Ch/EtOAc (1:3) dio un polvo blanco. La recristalización con etanol dio 0,020 g (6% de rendimiento) de 4-[2-(difluorometil)-1 H-bencimidazol-1-il]-6-(4-morfolinil)-N-(4-pirimidinil)-1,3,5-triazin-2-amina: mp 233-235°C; 1H RMN (CDCls) 58,92 (d, J=1,4 Hz, 1H), 8,67 (d, J=5,8 Hz, 1H), 8,39 (dd, J=6,8, 1,7 Hz, 1H), 8,22 (dd, J=5,8, 1,3 Hz, 1H), 8,01 (s, 1H), 7,92 (dd, J=6,8, 1,7 Hz, 1H), 7,56 (t, Jh f =53,5 Hz, 1H), 7,49-7,43 (m, 2H), 3,98-3,96 (m, 4H), 3,86-3,85 (m, 4H); Anal. Calc. para C19H17F2N9O: C, 53,65; H, 4,1; N, 29,6; Encontrado: C, 53,35; H, 4,2; N, 29,4%.
Ejemplo 21
Síntesis de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(5-pirimidinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
A una solución de 0,186 g (1,96 mmol) de 5-aminopirimidina en THF (4 mL) a 0°C se añadió 1,1 mL de NaHMDS (solución 2 M en THF), y la mezcla se agitó durante 15 min. Una solución de 0,238 g (0,65 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1H-bencimidazol se añadió en THF (5 mL) y la mezcla resultante se agitó durante 1 hora a TA. Después de la neutralización con ácido acético, la mezcla se diluyó con agua y se extrajo con EtOAc. La capa orgánica fue lavada secuencialmente con agua y NH3 ac., secada y concentrada. La cromatografía en alúmina, eluyendo primero con CH2Cl2/EtOAc (1:9) y luego con CH2Cl2/EtOAc (1:3) a CH2Cl2/EtOAc (7:3) dio un polvo blanquecino. La recristalización con etanol dio 0,123 g (47% de rendimiento) de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(5-pirimidinil)-1,3,5-triazin-2-amina: mp 290-292°C; 1H RMN (Cd CI3) 5 9,07 (s, 2H), 9,02 (s, 1H), 8,37 (d, J=7,2 Hz, 1H), 7,89 (dd, J=7,7, 1,5 Hz, 1H), 7,57 (t, Jh f =53,7 Hz, 1H), 7,47-7,40 (m, 2H), 7,11 (s, 1H), 3,95-3,92 (m, 4H), 3,83 (s ancho, 4H); Anal. Calc. para C19H17F2N9O: C, 53,65; H, 4,1; N, 29,6; Encontrado: C, 53,4; H, 4,2; N, 29,4%.
Ejemplo 22
Síntesis de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(2-pirazinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
A una solución de 0,219 g (2,30 mmol) de aminopirazina en THF (5 mL) a 0°C se añadió 1,3 mL de NaHMDS (solución 2 M en THF), y la mezcla se agitó durante 15 min. Una solución de 0,238 g (0,65 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1H-bencimidazol se añadió en THF (6 mL), y la mezcla resultante se agitó durante 1 hora a TA. Después de la neutralización con ácido acético, la mezcla se diluyó con agua y se extrajo con EtOAc. La capa orgánica fue lavada secuencialmente con agua y NH3 ac., secada y concentrada. La cromatografía en alúmina, eluyendo primero con hexanos/EtOAc (1:1) y luego con CH2Cl2/EtOAc (1:4) a CH2Cl2/EtOAc (1:1) dio un polvo blanco. La recristalización con etanol/CH2Cl2 dio 0,170 g (54% de rendimiento) de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(2-pirazinil)-1,3,5-triazin-2-amina: mp 271-274°C; 1H RMN (CDCl3) 59,59 (s, 1H), 8,42-8,33 (m, 3H), 7,92 (d, J=7,4 Hz, 1H), 7,81 (s, 1H), 7,60 (t, Jh f =53,5 Hz, 1H), 7,48-7,41 (m, 2H), 3,98 (d, J=4,2 Hz, 4H), 3,85 (d, J=4,2 Hz, 4H); Anal. Calc. para C19H17F2N9O: C, 53,65; H, 4,1; N, 29,6; Encontrado: C, 53,9; H, 3,8; N, 29,7%.
Ejemplo 23
Síntesis de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(3-piridazinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
Una mezcla de 0,063 g (0,486 mmol) de 6-cloro-3-piridazinamina (J. Med. Chem. 2006, 49, 4409-4424), 0,022 g (0,55 mmol) de NaOH y 0,045 g de 10% de Pd/C en etanol (15 mL) se agitaron bajo una atmósfera de hidrógeno durante 18 horas. Después de la filtración a través del celite, el disolvente fue concentrado para dar 0,046 g (rendimiento del 99,5%) de 3-aminopiridazina: 1H RMN (DMSO-d6) 58,39 (dd, J=4,4, 1,2 Hz 1H), 7,21 (dd, J=8,8, 4,4 Hz, 1H), 6,74 (dd, J=9,2, 1,6 Hz, 1H), 6,26 (s ancho, 2H).
A una solución de 0,159 g (1,67 mmol) de 3-aminopiridazina en THF (3 mL) a 0°C se añadieron 0,93 mL de NaHMDS (solución 2 M en THF), y la mezcla se agitó durante 15 min. Una solución de 0,317 g (0,84 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1H-bencimidazol se añadió en THF (6 mL) y la mezcla resultante se agitó durante 1 hora a TA. Después de la neutralización con ácido acético, la mezcla se diluyó con agua y se extrajo con EtOAc. La capa orgánica fue lavada secuencialmente con agua y NH3 ac., secada y concentrada. La cromatografía en alúmina, eluyendo primero con Hexano-EtOAc (8:2) luego con CH2Cl2/EtOAc (2:1) a CH2Cl2/EtOAc (1:1) dio un polvo blanco. La recristalización con etanol/CH2Cl2 dio 0,065 g (18% de rendimiento) de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(3-piridazinil)-1,3,5-triazin-2-amina: mp271-273°C; 1H RMN (DMSO-CÍ6) 511,16 (s ancho, 1H), 8,98 (dd, J=4,7, 1,4 Hz, 1H), 8,67 (d, J=8,0 Hz, 1H), 8,61 (d, J=8,4 Hz, 1H), 8,08 (t, Jh f =52,8 Hz, 1H), 7,86 (dd, J=7,7, 0,7 Hz, 1H), 7,73 (dd, J=9,1, 4,7 Hz, 1H), 7,53-7,43 (m, 2H), 3,86 (s, 4H), 3,75 (s, 4H); Anal. Calc. para C19H17F2N9O: C, 53,65; H, 4,1; N, 29,6; Encontrado: C, 53,7; H, 4,2; N, 29,5%.
Ejemplo 24
Síntesis de 2-(difluorometil)-1-[4-(4-morfolinil)-6-(3-piridiniloxi)-1,3,5-triazin-2-il]-1H-bencimidazol
El compuesto fue sintetizado según el método A.
Una mezcla de 0,301 g (3,16 mmol) de 3-hidroxipiridina y 0,132 g (3,30 mmol) de NaOH fue agitada en agua hasta que una solución clara fue obtenida. El agua se retiró y el residuo se combinó con una mezcla de 0,301 g (3,16 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1H-bencimidazol y 0,02 g (0,06 mmol) de tris[2-(2-metoxietoxi)etil]amina (TDA-1) en dioxano (12 mL). La mezcla resultante se calentó bajo reflujo durante 2 h antes de ser enfriado, y se diluyó con agua. El precipitado resultante fue recogido por filtración, y recristalizado con metanol para dar 0,160 g (50% rendimiento) de 2-(difluorometil)-1-[4-(4-morfolinil)-6-(3-piridiniloxi)-1,3,5-triazin-2-il]-1H-bencimidazol: mp 229-231°C; 1H RMN (CDCls) 58,63-8,60 (m, 2H), 8,12 (dd, J=7,1, 1,4 Hz, 1H), 7,87 (dd, J=7,1, 1,4 Hz, 1H), 7,59 (ddd, J=8,3, 2,7, 1,4 Hz, 1H), 7,45 (ddd, J=8,2, 4,6, 0,3 Hz, 1H), 7,41-7,34 (m, 2H), 7,25 (t, Jh f =53,6 Hz, 1H), 3,99-3,96 (m, 2H), 3,89-3,83 (m, 4H), 3,79-3,77 (m, 2H); Anal. Calc. para C20H17F2N7O20,7 H2O: C, 54,8; H, 4,2; N, 22,4. Encontrado: C, 54,5; H, 4,0; N, 22,0%.
Ejemplo 25
Síntesis de 4-[2-(difluorometil)-1 H-bencimidazol-1-il]-N-(1 -metil-1 H-pirazol-4-il)-6-(4-morfolinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
Una mezcla de 0,996 g (8,82 mmol) de 4-nitropirazol (J. Med. Chem. 2005, 48, 5780-5793) y 1,33 g (10,6 mmol) de dimetil-sulfato en 10 mL de NaOH 1 M se calentó a 35°C durante 48 horas. La mezcla de reacción se enfrió a RT y el precipitado se filtró, se lavó con agua y se secó para dar 0,561 g (50% de rendimiento) de 1-metil-4-nitro-1H-pirazol 1H RMN (DMSO-CÍ6) 58,83 (s, 1H), 8,22 (s, 1H), 3,91 (s, 3H).
Una mezcla de 0,144 g (1,14 mmol) de 1-metil-4-nitro-1H-pirazol, 0,017 g (0,07 mmol) de óxido de platino y acetato de etilo (5 mL) en etanol (15 mL) se agitó bajo 202650 Pa (2 atmósferas) de hidrógeno durante 14 horas. El catalizador fue eliminado por filtración a través de una almohadilla del Celitey el disolvente fue eliminado para dar 0,080 mg (73% de producción) de 4-amino-1-metil-1H-pirazol como un residuo púrpura, que fue utilizado en el paso siguiente sin más purificación: 1H RMN (DMSO-cfe) 56,98 (s, 1H), 6,88 (s, 1H), 3,76 (s ancho, 2H), 3,65 (s, 3H).
Una mezcla de 0,405 g (4,27 mmol) de 4-amino-1-metilpirazol y 0,695 g (1,90 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1H-bencimidazol en DMSO (5 mL) se calentó a 125°C durante 15 min. La mezcla de reacción se enfrió a temperatura ambiente y se añadió agua. El sólido fue recogido por filtración, lavado con agua, y secado. La cromatografía en alúmina, eluyendo con hexanos/EtOAc (1:1) dio un polvo marrón. La recristalización con etanol/CH2Cl2 dio 0,145 g (18% de rendimiento) de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-N-(1-metil-1H-pirazol-4-il)-6-(4-morfolinil)-1,3,5-triazin-2-amina: mp 225-226°C; 1H RMN (DMSO-^) (rotámeros) 510,00 (s, 1H), 9,73 (s, 0,2H), 8,60 (d, J=8,0 Hz, 1H), 8,29 (d, J=7,6 Hz, 0,2 H), 7,92 (t, Jh f =52,8 Hz, 1H), 7,86-7,80 (m, 2,6H), 7,68 (t, Jh f =52,6 Hz, 0,2 H), 7,59 (s, 1H), 7,52-7,42 (m, 2,9H), 3,85-3,82 (m, 8,4H), 3,75-3,73 (m, 4,8 H); Anal. Calc. para ^ ^ ^ ^ 0 - 0 , 0 6 EtOAc-0,24 H2O: C, 52,9; H, 4,6; N, 28,8; Encontrado: C, 52,9; H, 4,5; N, 28,6%.
Ejemplo 26
Síntesis de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-N-(4-metoxi-3-piridinil)-6-(4-morfolinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
Una mezcla de 0,475 g (3,08 mmol) de 4-metoxi-3-nitropiridina (Org. Process Res. Dev. 2004, 8, 903-908) y 0,301 g (2,84 mmol) de paladio al 10% en carbono en etanol (30 mL) se agitó bajo una atmósfera de hidrógeno durante 48 h. El catalizador fue eliminado por filtración a través de una almohadilla de Celite, y el disolvente fue eliminado para dar 0,380 mg (99%) de 3-amino-4-metoxipiridina como polvo rosado, que fue utilizado en el paso siguiente sin más purificación: 1H RMN (DMSO-^) 58,09 (dd, J=6,4, 1,2 Hz, 1H), 7,93 (d, J=1,2 Hz, 1H), 7,36 (d, J=6,4 Hz, 1H), 6,01 (s ancho, 2H), 4,06 (s, 3H).
A una solución de 0,134 g (1,08 mmol) de 3-amino-4-metoxipiridina en THF (3 ml) se añadió 0,5 ml de butil-litio (solución 2,5 M en hexanos), y la mezcla se agitó durante 15 min. Una solución de 0,133 g (0,36 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1H-bencimidazol se añadió en THF (6 mL) y la mezcla resultante se agitó durante 1 hora. Después de la neutralización con ácido acético, la mezcla se diluyó con agua y se extrajo con EtOAc. La capa orgánica fue lavada secuencialmente con agua y NH3 ac., secada y concentrada. La cromatografía en alúmina, eluyendo primero con hexanos/EtOAc (1:1) y luego con CH2Cl2/Et0Ac (2:3) dio un polvo blanco. La recristalización con etanol/CH2Cl2 dio 0,078 g (48% de rendimiento) de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-N-(4metoxi-3-piridinil)-6-(4-morfolinil)-1,3,5-triazin-2-amina: mp 161-163°C; 1H RMN (DMSO-cf6) 6 9,43 (s ancho, 1H), 8,61 8,37 (m, 3H), 7,83-7,81 (m, 2H), 7,41 (s ancho, 2H), 7,20 (d, J=5,6 Hz, 1H), 3,89 (s, 3H), 3,81 (s, 4H), 3,71 (s, 4H); Anal. Calc. para C21H20F2N8O2 : C, 55,5; H, 4,4; N, 24,7; Encontrado: C, 55,5; H, 4,4; N, 24,5%.
Ejemplo 27
Síntesis de 4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-N-(4-metox¡-3-p¡r¡d¡n¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-amina
El compuesto fue s¡ntet¡zado según el método A.
A una soluc¡ón de 0,121 g (0,98 mmol) de 3-am¡no-4-metox¡p¡r¡d¡na en THF (3 ml) se añad¡eron 0,44 ml de but¡l-l¡t¡o (soluc¡ón 2,5 M en hexanos), y la mezcla se ag¡tó durante 15 m¡n. Una soluc¡ón de 0,128 g (0,32 mmol) de 1-[4-cloro-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol se añad¡ó en THF (6 mL) y la mezcla resultante se ag¡tó durante 1 hora. Después de la neutral¡zac¡ón con ác¡do acét¡co, la mezcla se d¡luyó con agua y se extrajo con EtOAc. La capa orgán¡ca fue lavada secuenc¡almente con agua y NH3 ac., secada y concentrada. La cromatografía en alúm¡na, eluyendo pr¡mero con hexanos/EtOAc (8:2) y luego con CH2Ch/EtOAc (2:1) a CH2Cl2/EtOAc (1:1) d¡o un polvo amar¡llo. La recr¡stal¡zac¡ón con etanol/cH2Cl2 d¡o 0,065 g (42% de rend¡m¡ento) de 4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-N-(4-metox¡-3-p¡r¡d¡n¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na: mp 239-241°C; 1H RMN (CDCls) 69,43 (s ancho, 1H), 8,31 (d, J=5,6 Hz, 1H), 7,96 (d, J=8,2 Hz, 1H), 7,54 (t, Jhf=53,4 Hz, 1H), 7,39-7,35 (m, 2H), 6,89 (d, J=5,6 Hz, 1H), 6,83 (d, J=8,2 Hz, 1H), 4,05 (s, 3H), 4,00 (s, 3H), 3,94 (s, 4H), 3,82-3,80 (m, 4H); Anal. Calc. para C22H22F2N8O3: C, 54,5; H, 4,6; N, 23,1; Encontrado: C, 54,4; H, 4,5; N, 22,9%.
Ejemplo 28
Síntes¡s de 4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-N-(6-metox¡-3-p¡r¡d¡n¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na
El compuesto fue s¡ntet¡zado según el método A.
A una soluc¡ón de 0,310 g (2,50 mmol) de 5-am¡no-2-metox¡p¡r¡d¡na en THF (3 mL) a 0°C se añad¡eron 1,35 mL de d¡¡soprop¡lam¡da de l¡t¡o (soluc¡ón 2 M en benceno/heptanos/THF), y la mezcla se ag¡tó durante 20 m¡n. Una soluc¡ón de 0,240 g (0,61 mmol) de 1-[4-cloro-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol se añad¡ó en THF (5 mL), y la mezcla resultante se ag¡tó durante 1 hora a Ta . Después de la neutral¡zac¡ón con ác¡do acét¡co, la mezcla se d¡luyó con agua y se extrajo con EtOAc. La capa orgán¡ca fue lavada secuenc¡almente con agua y NH3 ac., secada y concentrada. La cromatografía en alúm¡na, eluyendo primero con hexanos/EtOAc (1:1) y luego con CH2Cl2/EtOAc (1:3) d¡o un polvo roj¡zo. La recr¡stal¡zac¡ón con etanol/CH2Cl2 d¡o 0,010 g (4% de rend¡m¡ento) de 4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-N-(6-metox¡-3-p¡r¡d¡n¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na: mp
201-202°C; 1H RMN (CDCI3) 58,33 (s ancho, 1H), 7,93 (s ancho, 1H), 7,79 (dd, J=8 ,8 , 2,7 Hz, 1H), 7,32-7,31 (m, 2H), 6,88-6,79 (m, 3H), 4,04 (s, 3H), 3,97 (s, 3H), 3,90 (s, 4H), 3,79 (s, 4H); Anal. Calc. para C22H22F2N8O3: C, 54,5; H, 4,6; N, 23,1; Encontrado: C, 54,6; H, 4,5; N, 22,9%.
Ejemplo 29
Síntesis de 4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-N-(6-fluoro-3-p¡r¡d¡n¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-amina
El compuesto fue s¡ntet¡zado según el método A.
A 0,240 g (2,14 mmol) de 5-am¡no-2-fluorop¡r¡d¡na en THF (5 mL) se añad¡ó 0,94 mL de n-but¡l¡t¡o (soluc¡ón 2,5 M en hexanos), y la mezcla se ag¡tó durante 10 m¡n. Una soluc¡ón de 0,283 g (0,71 mmol) de 1-[4-cloro-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol se agregó (Ejemplo 2) en THF (5 mL). La mezcla resultante se ag¡tó a temperatura amb¡ente durante 1 hora. Después de la neutral¡zac¡ón con ác¡do acét¡co, la mezcla se d¡luyó con agua y se extrajo con EtOAc. La capa orgán¡ca fue lavada suces¡vamente con agua y NH3 acuoso y secado. La el¡m¡nac¡ón del d¡solvente segu¡do de la cromatografía en alúm¡na eluyendo pr¡mero con hexanos/EtOAc (1:1) y luego CH2Ch/EtOAc (1:3) d¡o un polvo marrón. La recr¡stal¡zac¡ón con etanol/CH2Cl2 d¡o 0,135 g (40% de rend¡m¡ento) de 4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-N-(6-fluoro-3-p¡r¡d¡n¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na: mp261-263°C; 1H RMN (CDCl3) 58,44 (s ancho, 1H), 8,03-8,01 (m, 1H), 7,90 (s ancho, 1H), 7,61-7,31 (m, 2H), 7,07 (s ancho, 1H), 6,99 (dd, J=8,3, 3,4 Hz, 1H), 6,83 (d, J=8,0 Hz, 1H), 4,05 (s, 3H), 3,93-3,88 (m, 4H), 3,80 (s, 4H); Anal. Calc. para C21H19F3N8O2: C 53,4; H 4,05; N 23,7; Encontrado: C, 53,5; H, 4,0; N, 23,8%.
Ejemplo 30
Síntes¡s de N-(6-cloro-3-p¡r¡d¡n¡l)-4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na
El compuesto fue s¡ntet¡zado según el método A.
A 0,246 g (1,92 mmol) de 5-am¡no-2-clorop¡r¡d¡na en THF (4 mL) se añad¡eron 0,85 mL de n-but¡l-l¡t¡o (soluc¡ón 2,5 M en hexanos), y la mezcla se ag¡tó durante 10 m¡n. Una soluc¡ón de 0,260 g (0,66 mmol) de 1-[4-cloro-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol se agregó (ejemplo 2) en THF (5 mL). La mezcla resultante se ag¡tó a temperatura amb¡ente durante 1 hora. Después de la neutral¡zac¡ón con ác¡do acét¡co, la mezcla se d¡luyó con agua y se extrajo con EtOAc. La capa orgán¡ca fue lavada suces¡vamente con agua y NH3 acuoso y secada. La el¡m¡nac¡ón del d¡solvente y la cromatografía del res¡duo en alúm¡na eluyendo pr¡mero con hexanos/EtOAc (1:1) y luego con CH2Cl2-EtOAc (1:5) d¡o un polvo marrón. La recr¡stal¡zac¡ón con etanol/CH2Cl2 d¡o 0,016 g (5% de rend¡m¡ento) de N-(6-cloro-3-p¡r¡d¡n¡l)-4-[2-(d¡fluoromet¡l)-4-metox¡-1 H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n2-amina: mp 260-262°C; 1H RMN (CDCI3) 5 8,69 (s, 1H), 7,95-7,90 (m, 2H), 7,48 (t, Jhf=53,5 Hz, 1H), 7,37-7,33 (m, 2H), 7,11 (s, 1H), 6,83 (d, J=8,0 Hz, 1H), 4,05 (s, 3H), 3,94-3,87 (m, 4H), 3,81 (m, 4H); Anal. Calc. para C21H19CIF2N8O2: C, 51,6; H 3,9; N 22,9; Cl, 7,25; Encontrado: C, 52,1; H, 3,9; N, 22,5; Cl, 7,1%.
Ejemplo 31
Síntesis de 4-[2-(d¡fluoromet¡l)-4-metox¡-1 H-benc¡m¡dazol-1 -¡l]-6-(4-morfol¡n¡l)-N-(5-p¡rim¡d¡n¡l)-1,3,5-triaz¡n-2-am¡na
El compuesto fue s¡ntet¡zado según el método A.
A 0,207 g (2,18 mmol) de 5-am¡nop¡r¡m¡d¡na en THF (4 mL) se añad¡eron 0,96 mL de n-but¡l-l¡t¡o (soluc¡ón 2,5 M en hexanos) y la mezcla se ag¡tó durante 10 m¡n. Una soluc¡ón de 0,260 g (0,66 mmol) de 1-[4-cloro-6-(4-morfol¡n¡l)-1,3,5-triaz¡n-2-¡l]-2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol se agregó (ejemplo 2) en THF (5 mL). La mezcla resultante se ag¡tó a temperatura amb¡ente durante 1 hora. Después de la neutral¡zac¡ón con ác¡do acét¡co, la mezcla se d¡luyó con agua y se extrajo con EtOAc. La capa orgán¡ca fue lavada suces¡vamente con agua y NH3 acuoso y secada. La el¡m¡nac¡ón del d¡solvente, segu¡do por cromatografía en síl¡ce eluyendo con hexanos/EtOAc (1:1) d¡o un polvo amar¡llo. La recr¡stal¡zac¡ón con etanol/CH2Cl2 d¡o 0,068 g (20% de rend¡m¡ento) de 4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-N-(5-p¡rim¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na: mp 293-295°C; 1H RMN (CdC|3) 5 9,07 (s, 2H), 9,01 (s, 1H), 7,92 (d, J=8,4 Hz, 1H), 7,48 (t, Jh f =53,2 Hz, 1H), 7,37 (t, J=8,2 Hz, 1H), 7,14 (s, 1H), 6,84 (d, J=8,0 Hz, 1H), 4,05 (s, 3H), 3,95-3,90 (m, 4H), 3,82-3,81 (m, 4H); Anal. Calc. para C20H19F2N9O2: C 52,75; H 4,2; N 27,7; Encontrado: C, 52,9; H, 4,2; N, 27,7%.
Ejemplo 32
Síntes¡s de 4-(2-(d¡fluoromet¡l)-4-metox¡-1 H-benc¡m¡dazol-1 -¡l)-N-(6-metox¡p¡rim¡d¡n-4-¡l)-6-morfol¡no-1,3,5-tr¡az¡n-2-am¡na
El compuesto fue s¡ntet¡zado según el método A.
A 0,282 g (2,25 mmol) de 4-am¡no-6-metox¡p¡r¡m¡d¡na en THF (4 mL) fueron agregados 1,30 mL de NaHMDS (soluc¡ón 2 M en THF) y la mezcla fue ag¡tada durante 10 m¡nutos. Una soluc¡ón de 0,297 g (0,75 mmol) de 1-[4-cloro-6-(4-morfol¡n¡l)-1,3,5-triaz¡n-2-¡l]-2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol se agregó (ejemplo 2) en THF (5 mL). La mezcla resultante se ag¡tó a temperatura amb¡ente durante 1 hora. Después de la neutral¡zac¡ón con ác¡do acét¡co, la mezcla se d¡luyó con agua y se extrajo con EtOAc. La capa orgán¡ca fue lavada suces¡vamente con agua y NH3 acuoso y secada. La el¡m¡nac¡ón del d¡solvente, segu¡da de la cromatografía en síl¡ce eluyendo con CH2Cl2/EtOAc (1:1) d¡o un polvo blanco. La recr¡stal¡zac¡ón con etanol/CH2Cl2 d¡o 0,103 g (30% de rend¡m¡ento) de 4-(2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l)-N-(6-metox¡p¡r¡m¡d¡n-4-¡l)-6-morfol¡no-1,3,5-tr¡az¡n-2-am¡na: mp 256-259°C; 1H RMN (CDCl3) 5 8,52 (s, 1H), 7,96-7,94 (m, 2H), 7,59 (s, 1H), 7,49 (t, Jh f =53,5 Hz, 1H), 7,36 (d, J=8,4 Hz, 1H), 6,84 (d, J=8,1 Hz, 1H),
4,06 (s, 3H), 4,00 (s, 3H), 3,99-3,96 (m, 4H), 3,84 (s, 4H); HRMS (FAB MH+) Calc. para C21H22F2N9O3 : m/z 486,1808; Encontrado: m/z 486,1808,
Ejemplo 33
Síntesis de 4-[2-(difluorometil)-4-metoxi-1 H-bencimidazol-1 -il]-6-(4-morfolinil)-N-(3-piridazinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
A 0,215 g (2,26 mmol) de 3-aminopiridazina (ejemplo 23) en THF (4 mL) se añadieron 1,30 mL de NaHMDS (solución 2 M en THF), y la mezcla se agitó durante 10 min. Una solución de 0,297 g (0,75 mmol) de 1-[4-cloro-6-(4-morfolinil)-I , 3,5-triazin-2-il]-2-(difluorometil)-4-metoxi-1H-bencimidazol se agregó (ejemplo 2) en THF (5 mL). La mezcla resultante se agitó a temperatura ambiente durante 1 hora. Después de la neutralización con ácido acético, la mezcla se diluyó con agua y se extrajo con EtOAc. La capa orgánica fue lavada sucesivamente con agua y NH3 acuoso y secada. La eliminación del disolvente, seguida de la cromatografía en sílice eluyendo con CH2Cl2/EtOAc (1:1) dio un polvo blanco. La recristalización con etanol/CH2Cl2 dio 0,103 g (30% de rendimiento) de 4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(3-piridazinil)-1,3,5-triazin-2-amina: mp 261-263°C; 1H RMN (d Ms O-cÍ6) 5 I I , 13 (s, 1H), 8,97 (dd, J=4,7, 1,4 Hz, 1H), 8,38 (d, J=8,4 Hz, 1H), 8,20 (d, J=8,4 Hz, 1H), 8,05 (t, Jh f =52,9 Hz, 1H), 7,73 (dd, J=9,1, 4,7 Hz, 1H), 7,41 (t, J=8,3 Hz, 1H), 6,97 (d, J=7,8 Hz, 1H), 3,98 (s, 3H), 3,85 (s, 4H), 3,75 (s, 4H); Anal. Calc. para C20H19F2N9O2: C 52,75; H 4,2; N 27,7; Encontrado: C, 52,7; H, 4,25; N, 27,7%.
Ejemplo 34
Síntesis de 4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-N-(6-metoxi-3-piridazinil)-6-(4-morfolinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
A 0,216 g (1,73 mmol) de 6-metoxi-3-piridazinamina (J. Med. Chem. 2006, 49, 4409-4424) en THF (3 mL) se añadieron 0,97 mL de NaHMDS (solución 2 M en THF), y la mezcla se agitó durante 10 min. Una solución de 0,233 g (0,59 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-4-metoxi-1H-bencimidazol se añadió (ejemplo 2) y se agitó la mezcla resultante durante 10 min. La mezcla resultante fue neutralizada con ácido acético, diluida con agua, y extraída con EtOAc. La capa orgánica fue lavada sucesivamente con agua y NH3 acuoso, secada y concentrada. La recristalización con etanol/CH2Cl2 dio 0,086 g (rendimiento del 30%) de 4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-N-(6-metoxi-3-piridazinil)-6-(4-morfolinil)-1,3,5-triazin-2-amina: mp 256-259°C; 1H RMN (DMSO-d6) 5 10,85 (s, 1H), 8,24 (d, J=9,2 Hz, 1H), 8,15 (d, J=7,7 Hz, 1H), 7,99 (t, Jh f =52,6 Hz, 1H), 7,40 (t, J=8,2 Hz, 1H), 7,29 (d, J=9,5 Hz, 1H), 6,96 (d, J=8,0 Hz, 1H), 4,00 (s, 3H), 3,97 (s, 3H), 3,84-3,79 (m, 4H) y 3,72 (s, 4H); Anal. Calc. para C21H21F2N9O3 0,5 H2O: C, 51,1; H, 4,5; N, 25,5; Encontrado: C, 51,4; H, 4,6; N, 25,0%.
Ejemplo 35
Síntesis de 4-[2-(difluorometil)-1 H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-N-(5-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na
El compuesto fue s¡ntet¡zado según el método A.
A 0,186 g (1,96 mmol) de 5-am¡nop¡r¡m¡d¡na en THF (4 mL) se añad¡eron 1,1 mL de NaHMDS (soluc¡ón 2 M en THF) a 0°C y la mezcla se ag¡tó durante 15 m¡n. Una soluc¡ón de 0,238 g (0,65 mmol) de 1-[4-cloro-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-2-(d¡fluoromet¡l)-1H-benc¡m¡dazol se añad¡ó en THF (5 mL) y la mezcla resultante se ag¡tó durante 1 hora a temperatura amb¡ente. La mezcla resultante fue neutral¡zada con ác¡do acét¡co, d¡lu¡da con agua, y extraída con EtOAc. La capa orgán¡ca fue lavada con agua, y NH3 ac. y secada. La el¡m¡nac¡ón del d¡solvente, segu¡do de la cromatografía en alúm¡na, eluyendo con CH2Ch/EtOAc (1:9), luego CH2Ch/EtOAc (1:3), d¡o un polvo blanquec¡no. La recr¡stal¡zac¡ón con etanol d¡o 0,123 g (47% de rend¡m¡ento) de 4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-N-(5-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na: mp 290-292°C; 1H RMN (CDCl3) 59,07 (s, 2H), 9,02 (s, 1H), 8,37 (d, J=7,2 Hz, 1H), 7,89 (dd, J=7,7, 1,5 Hz, 1H), 7,57 (t, Jh f =53,7 Hz, 1H), 7,47-7,40 (m, 2H), 7,11 (s, 1H), 3,95-3,92 (m, 4H), 3,83 (s ancho, 4H); Anal. Calc. para C19H17F2N9O: C, 53,65; H, 4,0; N, 29,6; Encontrado: C, 53,4; H, 4,2; N, 29,4%. A 99 mg (0,23 mmol) del compuesto anterior en CH2Cl2 (3 mL) se añad¡eron 16 ^L (0,25 mmol) de ác¡do metanosulfón¡co en MeOH (0,5 mL). La mezcla se ag¡tó durante 5 m¡n y se concentró en vacío para dar un polvo blanco. La recr¡stal¡zac¡ón con MeOH/EtOAc d¡o 85 mg (71%) de 4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-N-(5-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na metanosulfonato: mp 163-166°C; 1H RMN (DMSO-cfe) 5 10,32 (s, 1 H), 9,13 (s, 2H), 8,92 (s, 1H), 8,56 (s ancho, 1H), 8,13-7,77 (m, 2H), 7,53-7,43 (m, 2H), 3,85 (s, 4H), 3,76-3,69 (m, 4H), 2,35 (s, 3H); Anal. Calc. para C2üH21F2N9O4S 0,31 H2O: C, 45,6; H, 4,1; N, 23,9; Encontrado: C, 45,2; H, 4,35; N, 23,8%.
Ejemplo 36
Síntes¡s de 4-[2-(d¡fluoromet¡l)-4-metox¡-1 H-benc¡m¡dazol-1 -¡l]-6-(4-morfol¡n¡l)-N-f4-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na
El compuesto fue s¡ntet¡zado según el método A.
A 0,225 g (2,37 mmol) de 4-am¡nop¡r¡m¡d¡na en THF (3 mL) se añad¡eron 1,30 mL de NaHMDS (soluc¡ón 2 M en THF) y la mezcla se ag¡tó durante 10 m¡n. Una soluc¡ón de 0,320 g (0,81 mmol) de 1-[4-cloro-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol se añad¡ó en THF (5 mL) y la mezcla resultante se ag¡tó durante 1 hora. La mezcla de reacc¡ón fue neutral¡zada con ác¡do acét¡co, d¡lu¡da con agua y extraída con EtOAc. La capa orgán¡ca fue lavada con agua, y NH3 ac. y secada. La el¡m¡nac¡ón del d¡solvente, segu¡do de la cromatografía en síl¡ce, eluyendo primero con hexanos-EtOAc (1:1), luego CH2Ch/EtOAc (1:1) a CH2Ch/EtOAc (1:3) d¡o un polvo blanco. La recr¡stal¡zac¡ón con EtOH/CH2Cl2 d¡o 0,058 g (16% de rend¡m¡ento) de 4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-N-(4-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na: mp 234-236°C; 1H RMN (CDCl3) 5 8,91 (d, J=1,0 Hz, 1H), 8,65 (d, J=5,8 Hz, 1H), 8,23 (dd, J=5,8, 1,3 Hz, 1H), 7,99 (s, 1H), 7,93 (dd, J=8,3, 0,5 Hz, 1H), 7,47 (t, Jh f =53,4 Hz, 1H), 7,38 (t, J=8,2 Hz, 1H), 6,85 (d, J=7,8 Hz, 1H), 4,06 (s, 3H), 3,97-3,96 (m, 4H), 3,86-3,84 (m, 4H); Anal. Calc. para C20H19F2N9O2-0,31 H2O: C 52,1; H 4,3; N 27,3; Encontrado: C, 51,7; H, 4,15; N, 27,3%.
Ejemplo 37
Síntesis de W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-2,5-piridindiamina
El compuesto fue sintetizado según el método A.
A 0,652 g (4,69 mmol) de 2-amino-5-nitropiridina en THF (5 mL) se añadieron 3,5 mL de NaHMDS (solución 2M en THF) a 0°C. Después de 20 min, se añadió una solución de 1,085 g (4,97 mmol) de dicarbonato de tere-butilo en THF (6 mL) y la mezcla se calentó lentamente a temperatura ambiente durante la noche. Se añadió agua y se extrajo la mezcla con EtOAc (x4). La capa orgánica fue lavada con salmuera, se secó (Na2SO4) y concentró. La cromatografía en sílice con hexanos-EtOAc (7:3), dio 0,695 g (62% de rendimiento) de tere-butil-5-n¡trop¡r¡dina-2-¡lcarbamato como un polvo naranja: 1H RMN (CDCls) 59,19 (dd, J=2,8, 0,5 Hz, 1H), 8,93 (s ancho, 1H), 8,46 (ddd, J=9,4, 2,8, 0,5 Hz, 1H), 8,20 (dd, J=9,5, 0,5 Hz, 1H), 1,59 (s, 9H); LCMS (APCI-) m/z: 238 (MH+, 100%).
A 0,314 g (1,31 mmol) del compuesto nitro anterior en THF-MeOH (16 mL, 1:1) se añadieron 0,460 g de 10% Pd/C y la mezcla se agitó bajo hidrógeno (135456 Pa (40 pulg/Hg)) durante 4 horas. La mezcla de reacción se filtró a través de celite, se lavó con MeOH y se concentró para dar 0,277 g (99% de rendimiento) de 5-aminopiridin-2-il-carbamato de tere-butilo como un polvo blanco: 1H RMN (DMSO-d6) 59,00 (s ancho, 1H), 7,62 (dd, J=2,7, 0,4 Hz, 1H), 7,39 (d, J=8,7 Hz, 1H), 6,94 (dd, J=8,7, 2,8 Hz, 1H), 4,92 (s, 2H), 1,44 (s, 9H).
A 0,277 g (1,33 mmol) del compuesto amino anterior en THF (3 mL) se añadieron 0,61 mL de n-butil-litio (solución 2,5 M en hexanos) y la mezcla se agitó durante 10 min. Una solución de 0,176 g (0,44 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-4-metoxi-1H-bencimidazol se añadió en THF (5 mL) y la mezcla resultante se agitó durante 1 hora a temperatura ambiente. La mezcla de reacción fue neutralizada con ácido acético, diluida con agua, y extraída con EtOAc. La capa orgánica fue lavada con agua y NH3 ac., secada y concentrada. La cromatografía en sílice eluyendo con hexanos-EtOAc (7:3), luego con CH2Cl2-EtOAc (3:1), dio 0,033 g (13% de rendimiento) de 5-{[4-[2-(difluorometil)-4-metoxi-1 H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]amino}-2-piridinilcarbamato de terebutilo: 1H RMN (DMSO-CÍ6) 510,02 (s, 1H), 9,66 (s, 1H), 8,54 (s, 1H), 8,17-7,80 (m, 4H), 7,39 (d, J=8,7 Hz, 1H), 6,97 6,93 (m, 1H), 3,98 (s, 3H), 3,82 (s, 4H), 3,74-3,72 (m, 4H), 1,48 (s, 9H).
A 0,033 g (0,06 mmol) del carbamato anterior en CH2Cl2 (3 mL) se añadieron 0,1 mL (1,30 mmol) de ácido trifluoroacético, y la mezcla se agitó durante 5 horas. La mezcla de reacción se diluyó con CH2Cl2 y NH4OH ac., y la capa orgánica fue lavada con salmuera, secada (Na2SO4) y concentrada. El residuo fue recristalizado con EtOH/CH2Cl2 para dar 0,0133 g (49% de rendimiento) de N5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-2,5-piridindiamina, como un polvo marrón: mp267-270°C; 1H RMN (DMSO-cf6) 59,67-9,49 (m, 1H), 8,18-7,27 (m, 5H), 6,96 (d, J=7,6 Hz, 1H), 6,48 (d, J=8,4 Hz, 1H), 5,87-5,75 (m, 2H), 3,98 (s, 3H), 3,81 (s, 4H), 3,71 (s, 4H); HRMS (ESI) M H+ Calc. para C21H22F2N9O2: m/z 470,1859; Encontrado: m/z 470,1867.
Ejemplo 38
Síntesis de W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-N2-metil-2,5-piridindiamina
El compuesto fue sintetizado según el método A.
A 0,652 g (4,69 mmol) de 2-amino-5-nitropiridina en THF (5 mL) se añadieron 3,5 mL de NaHMDS (solución 2M en THF) a 0°C. Después de 20 min, se añadió una solución de 1,085 g (4,97 mmol) de dicarbonato de tere-butilo en THF (6 mL), y la mezcla se calentó lentamente a temperatura ambiente durante la noche. Se añadió agua y se extrajo la mezcla con EtOAc (x4). Las capas orgánicas combinadas se lavaron con salmuera, secaron (Na2SO4) y concentraron. La purificación por cromatografía de columna Flash sobre sílice, eluyendo con hexanos -EtoAc (7:3), dio 0,695 g (62% de rendimiento) de 5-nitro-2-piridinilcarbamato de tere-butilo como un polvo anaranjado: 1H RMN (CDCl3) 59,19 (dd, J=2,8, 0,5 Hz, 1H), 8,93 (s ancho, 1H), 8,46 (ddd, J=9,4, 2,8, 0,5 Hz, 1H), 8,20 (dd, J=9,5, 0,5 Hz, 1H), 1,59 (s, 9H); LCMS (APCI-) m/z: 238 (MH+, 100%).
A 0,378 g (1,58 mmol) del compuesto nitro anterior en DMF (6 mL) a 0°C se añadieron 0,067 g (2,80 mmol) de hidruro sódico. Después de 20 minutos, se añadieron 0,12 mL (1,93 mmol) de yoduro de metilo, y la mezcla se agitó durante 2 horas. Se añadió agua y se extrajo la mezcla con EtOAc (x 4). La capa orgánica combinada fue lavada sucesivamente con HCl 1M, Sat. solución NaHCO3, y salmuera, secada (Na2SO4), y concentrada, para dar 0,40 g (99% de rendimiento) de metil-(5-nitro-2-piridinil)carbamato de tere-butilo: 1H RMN (c DCI3) 59,19 (d, J=2,7 Hz, 1H), 8,36 (dd, J=9,4, 2,7 Hz, 1H), 8,14 (dd, J=9,4, 0,3 Hz, 1H), 3,50 (s, 3H), 1,57 (s, 9H); LCMS (APCI-) m/z: 253 (MH+, 100%).
A 0,40 g (1,58 mmol) del compuesto nitro anterior en MeOH (25 mL) se añadieron 0,4 g de 10% Pd/C y la mezcla se agitó bajo hidrógeno (135456 Pa (40 pulg/Hg)) durante 4 horas. Después de la filtración a través del celite la mezcla de la reacción fue concentrada, para dar 0,36 g (97% de rendimiento) de 5-amino-2-piridin-2-il(metil)carbamato de tere-butilo, como un aceite amarillo: 1H RMN (DMSO-^) 57,70 (dd, J=2,9, 0,5 Hz, 1H), 7,07 (d, J=8,6 Hz, 1H), 6,93 (dd, J=8,6, 2,9 Hz, 1H), 3,12 (s, 3H), 1,39 (s, 9H).
A 0,356 g (1,53 mmol) de la amina anterior en THF (3 mL) se añadieron 0,70 mL de n-butil-litio (solución 2,5 M en hexanos) y la mezcla se agitó durante 10 min. Una solución de 0,21 g (0,52 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-4-metoxi-1H-bencimidazol se añadió en THF (5 mL), y la mezcla resultante se agitó durante 1 hora. La mezcla de reacción fue neutralizada con ácido acético, diluida con agua, y extraída con EtOAc. La capa orgánica fue lavada con agua y NH3 ac. y secada. El disolvente fue retirado bajo vacío, y la mezcla de producto fue purificada por cromatografía de columna Flash, eluyendo con CH2Cl2/EtOAc (3:1), para dar 0,075 g (13% de rendimiento) de 5-{[4-[2-(difluorometil)-4-metoxi-1 H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]amino}-2-piridinil(metil)carbamato de tere-butilo, como un polvo amarillo: 1H RMN (d Ms O-cí6) 510,11 (s, 1h), 8,68-7,41 (m, 5H), 7,61 (d, J=9,0 Hz, 1H), 6,97 (d, J=8,1 Hz, 1H), 3,98 (s, 3H), 3,83 (s, 4H), 3,74-3,73 (m, 4H), 3,29 (s, 3H), 1,47 (s, 9H); LCMS (APCI+) MLZ: 585 (MH+, 100%).
A 0,0750 g (0,13 mmol) del carbamato anterior en CH2Cl2 (3 mL) se añadieron 0,1 mL (1,30 mmol) de ácido trifluoroacético y la mezcla se agitó durante 5 horas. Después de la dilución con CH2Cl2, la mezcla fue tratada con H2O y NH3 ac., y la capa orgánica fue lavada con salmuera, secada (Na2SO4) y concentrada. El residuo fue recristalizado con EtOH/CH2Cl2 para dar 0,0472 g (75% de rendimiento) de N5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-N2-metil-2,5-piridindiamina: mp 218-221°C; 1H RMN (CDCl3) 58,31-7,73 (m, 2H), 7,62 (dd, J=8,8, 2,6 Hz, 1H), 7,56-7,31 (m, 2H), 6,82-6,80 (m, 2H), 6,46 (d, J=8,8 Hz, 1H), 4,76 (s ancho, 1H), 4,04 (s, 3H), 3,89 (s, 4H), 3,79 (s, 4H), 2,96 (s, 3H); HRMS (ESI) M H+ Calc. para C22H24F2N9O2: m/z 484,2016; Encontrado: m/z 484,2023.
Ejemplo 39
Síntesis de ^ 5-[4-[2-(difluorometil)-4-metoxi-1 H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-N2,W2-dimetil-2,5-piridindiamina
El compuesto fue sintetizado según el método A.
A 0,314 g (1,99 mmol) de 2-cloro-5-nitropiridina en MeOH (1 mL) se añadieron 5 mL de dimetilamina (solución 2M en MeOH) a 0°C y la mezcla se calentó a temperatura ambiente. La mezcla de reacción se concentró y se extrajo con EtOAc. La capa orgánica fue lavada sucesivamente con solución sat. NaHCO3 y salmuera, secada (Na2SO4), y concentrada para dar 0,313 g (94% de rendimiento) de 2-dimetilamino-5-nitropiridina como un polvo naranja: 1H Rm N (CDCl3) 59,06 (d, J=2,7 Hz, 1H), 8,20 (dd, J=9,5, 2,7 Hz, 1H), 6,46 (dd, J=9,5, 0,4 Hz, 1H), 3,23 (s, 6H); LCMS (APCI+) m/z: 168 (MH+, 100%).
Una mezcla de 0,312 g (1,87 mmol) del compuesto nitro anteriory 0,205 g de 10% Pd/C en metanol (40 mL) se agitó bajo hidrógeno (84659,7 Pa (25 pulgadas/Hg) durante 5 horas. La mezcla de reacción se filtró a través de celite, y el disolvente se concentró, para dar 0,236 g (92% de rendimiento) de ^ 2,^ 2-dimetil-2,5-piridindiamina: 1H RMN (CDCl3) 5 7,78 (d, J=2,9 Hz, 1H), 6,98 (dd, J=8,8, 2,9 Hz, 1H), 6,45 (dd, J=8,8, 0,5 Hz, 1H), 2,99 (s, 6H); LCMS (APCI+) m/z: 138 (MH+, 100%).
A 0,236 g (1,72 mmol) de la diamina anterior en THF (3,5 mL) se añadió 0,79 mL de n-butil-litio (solución 2,5 M en hexanos) y la mezcla se agitó durante 10 min. Una solución de 0,231 g (0,58 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-4-metoxi-1H-bencimidazol se añadió en THF (5 mL) y la mezcla resultante se agitó durante 1 hora. La mezcla de reacción fue neutralizada con ácido acético, diluida con agua y extraída con EtOAc. La capa orgánica fue lavada con agua y NH3 ac., secada y concentrada. La cromatografía en sílice eluyendo primero con hexanos-EtOAc (1:1), luego CH2Cl2-EtOAc (1:1) dio un polvo marrón palo. La recristalización con etanol/CH2Cl2 dio 0,144 g (50% de rendimiento) de N5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-^2,N2-dimetil-2,5-piridindiamina: mp 136-137°C; 1H RMN (CDCl3) 58,35-7,83 (m, 2H), 7,63 (dd, J=9,0, 2,5 Hz, 1H), 7,57-7,29 (m, 1H), 6,81-6,80 (m, 2H), 6,57 (d, J=9,0 Hz, 1H), 4,04 (s, 3H), 3,89 (s, ancho, 4H), 3,79 (s, 4H), 3,13 (s, 6H); Anal. Calc. para C23H25F2NgO2- 0,16 EtOH: C, 55,5; H, 5,2; N, 25,0; Encontrado: C, 55,3; H, 5,2; N, 24,6%.
Ejemplo 40
Síntesis de 4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-N-(2-metoxi-5-pirimidinil)-6-(4-morfolinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
A una solución de metóxido de sodio (0,090 g de sodio) en MeOH (12 ml) se añadieron 0,486 g (3,03 mmol) de 2-cloro-5-nitropirimidina, y la mezcla fue calentada bajo reflujo durante 1 hora. Después del enfriamiento, la mezcla se concentró in vacuo, fue extraída con EtOAc, y se lavó con agua. La capa acuosa se extrajo con CHCl3 y las capas orgánicas combinadas se secaron (Na2SO4), y concentraron, para dar 0,347 g (75% de rendimiento) de 2-metox¡-5-nitropirimidina como un polvo amarillo: 1H RMN (CDCl3) 59,31 (s, 2H), 4,17 (s, 3H); LCMS (APCI+) m/z: 156 (MH+, 100%).
A 0,342 g (2,20 mmol) del compuesto nitro anterior en MeOH (20 mL) se añadieron 0,30 g de 10% Pd/C y la mezcla se agitó bajo hidrógeno (84659 Pa (25 pulgadas/Hg)) durante 18 horas. La mezcla de reacción fue filtrada a través
celite, y concentrada para dar 0,274 g (rendimiento del 100%) de 5-amino-2-metoxipirimidina como aceite incoloro: 1H RMN (DMSO-CÍ6) 58,05 (s, 2H), 3,94 (s, 3H); LCMS (APCI+) m/z: 126 (MH+, 100%).
A 0,274 g (2,19 mmol) del compuesto amino anterior en THF (3 mL) se añadieron 1,25 mL de NaHMDS (solución 2 M en THF) y la mezcla se agitó durante 10 min. Una solución de 0,31 g (0,78 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-4-metoxi-1H-bencimidazol se añadió en THF (5 mL) y se agitó la mezcla resultante durante 90 min. La mezcla de reacción fue neutralizada con ácido acético, diluida con agua, y extraída con EtOAc. La capa orgánica fue lavada con agua y NH3 ac., secada y concentrada. La recristalización con EtOH/CH2Cl2 dio 0,098 g (rendimiento del 26%) de 4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-N-(2-metoxi-5-pirimidinil)-6-(4-morfolinil)-1,3,5-triazin-2-amina: mp 255-258°C; 1H RMN (DMSO-^) 5 10,07 (s, 1H), 8,88-8,74 (m, 2H), 8,15-7,42 (m, 3H), 6,97 (d, J=8,0 Hz, 1H), 3,98 (s, 3H), 3,93 (s, 3H), 3,82-3,72 (m, 8H); Anal. Calc. para C21H21F2N9O3: C, 52,0; H 4,4; N 26,0; Encontrado: C, 52,1; H, 4,5; N, 26,0%.
Ejemplo 41
Síntesis de N-(2-cloro-5-pirimidinil)-4-[2-(difluorometil)-4-metoxi-1 H-bencimidazol-1 -il]-6-(4-morfolinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método A.
Una suspensión de 3,5 g (63 mmol) de polvo de hierro en 10 mL de 1,5% AcOH ac. y 35 mL de EtOH al 65% se calentó a 80°C, y 1,005 g (6,28 mmol) de 2-cloro-5-nitropirimidina fue agregada. La mezcla de reacción se calentó a 90°C durante 1 hora. Después de enfriarse a la temperatura ambiente, la mezcla de la reacción fue neutralizada con NH3 ac., filtrada a través de celite, y concentrada in vacuo. El residuo se extrajo con EtOAc (x 4), y la capa orgánica se lavó con salmuera, se secó (Na2SO4) y concentró. La cromatografía en sílice, eluyendo con hexanos/EtOAc (6:4), dio 0,49 g (60% de rendimiento) de 5-amino-2-cloropirimidina como un polvo amarillo: 1H RMN (DMSO-cf6) 58,03 (s, 2H); LCMS (APCI+) m/z: 130 (MH+, 100%).
Una mezcla de 0,28 g (0,71 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-4-metoxi-1H-bencimidazol, 0,076 g (0,56 mmol) de la amina anterior, 0,026 g (0,04 mmol) de BINAP, 0,01 g (0,04 mmol) de Pd(OAc)2y 0,266 g (0,82 mmol) de Cs2CO3 en 1,4-dioxano (4 mL) se calentó a 100°C durante 3 horas bajo nitrógeno. La mezcla se enfrió a temperatura ambiente, se añadió una solución NaHCO3 sat., y la mezcla resultante se extrajo con EtOAc (x4). La capa orgánica fue lavada con salmuera, secada (Na2SO4) y concentrada. Cromatografía en sílice, eluyendo con CH2Cl2/EtOAc (6 :1 ), dio 0 ,10 g (36% de rendimiento) de N-(2-cloro-5-pirimidinil)-4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-amina, como polvo blanco: mp 295°C (Decomp.); 1H RMN (DMSO-CÍ6) 510,43 (s, 1H), 9,08 (s, 2H), 8,09-7,69 (m, 2H), 7,42 (t, J=8,0 Hz, 1H), 6,98 (d, J=7,6 Hz, 1H), 3,98 (s, 3H), 3,83 (s, 4H), 3,75-3,73 (m, 4H); Anal. Calc. para C20H1sClF2NgO2: C, 49,0; H, 3,7; N, 25,7; Encontrado: C, 49,2; H, 3,9; N 25,45%.
Ejemplo 42
Síntesis de N5-[4-[2-(difluorometil)-4-metoxi-1 H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-N2-[2-(dimetilamino)etil]-N2-metil-2,5-pirimidindiamina
El compuesto fue sintetizado según el método D.
A 0,101 g (0,21 mmol) de N-(2-cloro-5-p¡r¡m¡d¡n¡l)-4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na (ejemplo 41) en EtOH (5 mL) se añad¡eron 0,28 mL (2,14 mmol) de N,N,N'-tr¡met¡let¡lend¡am¡na, y la mezcla fue calentada a 120°C en un tubo sellado durante 1,5 h. La concentrac¡ón del d¡solvente, segu¡da de cromatografía en síl¡ce, eluyendo primero con CH2Ch/EtOAc (1:3), y luego con CH2Cl2/MeOH/NH3 (95:5:0,1), d¡o N5-[4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-N2-[2-(d¡met¡lam¡no)et¡l]-N2-met¡l-2,5-p¡r¡m¡d¡nd¡am¡na como un ace¡te pardusco, que sol¡d¡f¡có en vacío: mp 96-98°C; 1H RMN (CDCh) 58,47 (s, 1 H), 8,36 (s, 1H), 8,05-7,31 (m, 3H), 7,00-6,61 (m, 2H), 4,04 (s, 3H), 3,90-3,79 (m, 10H), 3,22 (s, 3H), 2,97-2,89 (m, 2H), 2,33 (s, 6 H); HRMS (ESI) M H+ Calc. para C25H32F2N11O2: m/z 556,2703; Encontrado: m/z 556,2694.
Ejemplo 43
Síntes¡s de N5-[4-[2-(d¡fluoromet¡l)-4-metox¡-1 H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-N2-[3-(d¡met¡lam¡no)prop¡l]-N2-met¡l-2,5-p¡r¡m¡d¡nd¡am¡na
El compuesto fue s¡ntet¡zado según el método D.
A 0,095 g (0,19 mmol) de N-(2-cloro-5-p¡r¡m¡d¡n¡l)-4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na (ejemplo 41) en EtOH (5 mL) se añad¡eron 0,28 mL (1,91 mmol) de N,N,N'-tr¡met¡l-1,3-propanod¡am¡na, y la mezcla se calentó a 120 °C en un tubo sellado durante 2 horas. La concentrac¡ón del d¡solvente, segu¡da de cromatografía en síl¡ce, eluyendo primero con CH2Cl2/EtOAc (1:3) y luego con CH2Cl2/MeOH/NH3 (95:5:0,1), d¡o N5-[4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-N2-[3-(d¡met¡lam¡no)prop¡l]-N2-met¡l-2,5-p¡r¡m¡d¡nd¡am¡na como un ace¡te amar¡llo, que sol¡d¡f¡có en vacío: mp 97-99°C; 1H RMN (CDCl3) 58,63-8,35 (m, 2H), 7,99-7,21 (m, 3H), 6,81-6,59 (m, 2H), 4,04 (s, 3H), 3,90 (s, 4H), 3,79 (s, 4H), 3,70 (t, J=7,2 Hz, 2H), 3,20 (s, 3H), 2,35 (t, J=7,2 Hz, 2H), 2,56 (s, 6 H), 1,87-1,80 (m, 2H); HRMS (ESI) M H+ Calc. para C26H34F2Nh O2: m/z 570,2860; Encontrado: m/z 570,2857.
Ejemplo 44
Síntes¡s de 4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-N-met¡l-6-(4-morfol¡n¡l)-N-(5-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na
El compuesto fue sintetizado según el método D.
A una solución de 99 mg (0,23 mmol) de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(5-pirimidinil)-1,3,5-triazin-2-amina (ejemplo 22) en DMF (2 ml) se agregó NaH (95%, 7,9 mg, 0,31 mmol), y después de 10 m¡n se añad¡ó yodometano (15 pl, 0,24 mmol), y la mezcla resultante se agitó durante 2 horas. Se añadió agua y se extrajo la mezcla con EtoAc (x 4). La capa orgánica fue lavada con salmuera, secada (Na2SO4) y concentrada. La cromatografía en sílice, eluyendo primero con CH2Cl2/EtOAc (1:1) y luego con CH2Cl2/EtOAc(1:2), dio un polvo blanco (0,082 g), que fue recristalizado con CH2Cl2 para dar 0,073 g (72% de rendimiento) de 4-[2-(difluorometil)-1H-bencimidazol-1-il]-N-metil-6-(4-morfolinil)-N-(5-pirimidinil)-1,3,5-triazin-2-amina: mp 202-205°C; 1H RMN (DMSO-da) 5 9,14 (s, 1H), 8,83 (s, 2H), 8,18 (s ancho, 1H), 7,89-7,87 (m, 1H), 7,41-7,37 (m, 3H), 3,91 (s, ancho, 2H), 3,80-3,75 (m, 6 H), 3,66 (s, 3H); Anal. Calc. para C20H19F2N9O: C, 54,7; H, 4,4; N, 28,6; Encontrado: C, 54,7; H, 4,4; N, 29,1%. Ejemplo 45
Síntesis de 4-[2-(difluorometil)-4-metoxi-1 H-bencimidazol-1-il]-N-metil-6-(4-morfolinil)-N-(5-pirimidinil)-1,3,5-triazin-2-amina
El compuesto fue sintetizado según el método D.
A una solución de 0,1033 g (0,23 mmol) de 4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(5-pirimidinil)-1,3,5-triazin-2-amina (ejemplo 32) en d Mf (2 ml) se añadió NaH (95%, 8,7 mg, 0,34 mmol), y después de 10 min se añadió yodometano (15 pl, 0,24 mmol), y la mezcla resultante se agitó durante 2 horas. Se añadió agua y se extrajo la mezcla con EtOAc (x 4). La capa orgánica fue lavada con salmuera, secada (Na2SO4) y concentrada. La cromatografía en sílice, eluyendo con CH2Cl2/EtOAc (1:1), dio un polvo blanco que fue recristalizado con CH2Cl2 para dar 0,061 g (56% de rendimiento) de 4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-N-metil-6-(4-morfolinil)-N-(5-pirimidinil)-1,3,5-triazin-2-amina: mp 214-217°C; 1H RMN (DMSO-d6) 59,13 (s, 1H), 8,98 (s, 2H), 7,66-7,28 (m, 3H), 6,93 (d, J=8,0 Hz, 1H), 3,98 (s, 3H), 3,82-3,70 (m, 8 H), 3,59 (s, 3H); HRMS (ESI) M H+ Calc. para C21H22F2N9O2: m/z 470,1859; Encontrado: m/z 470,1852.
Ejemplo 46
Síntesis de 2-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(3-piridinil)-4-pirimidinamina (no reivindicado)
El compuesto fue sintetizado según el método A.
Se añadió 1-(4,6-dicloro-2-pirimidinil)-2-(difluorometil)-1 H-bencimidazol (Publ. Internacional No. WO 2002/088112 (0,315 g, 1 mmol) a una mezcla de 3-aminopiridina (0,28 g, 3 mmol) y LDA (1,5 mL, 2 M en THF, 3 mmol) en 10 mL de THF a temperatura ambiente. Después de 10 min, la mezcla fue neutralizada con HOAc, diluida con agua, extraída con EtOAc, y secada (Na2SO4). La cromatografía en sílice, eluyendo con CH2Cl2/EtOAc (3:2) dio un sólido, que fue recristalizado con /-Pr2O para dar 0,252 g (67% de rendimiento) de 6-cloro-2-[2-(difluorometil)-1H-bencimidazol-1-il]-N-(3-piridinil)-4-pirimidinamina: mp (/-Pr2O) 233-236°C; 1H RMN (DMSO-^) 5 10,42 (ancho, 1H), 8,72 (d, J= 2,3 Hz, 1H), 8,43 (dd, J=4,7, 1,4 Hz, 1H), 8,26 (m, 1H), 8,01 (ddd, J=8,3, 2,5, 1,5 Hz, 1H), 7,86 (m, 1 H), 7,62 (t, Jhf=52,9 Hz, 1H), 7,48-7,42 (m, 3H), 6,86 (s, 1H); Anal. Calc. para C ^ H n C ^ ^ : C, 54,8; H, 3,0; N, 22,55; Encontrado: C, 54,75; H, 3,0; N, 22,7%.
El compuesto antedicho fue sometido a reflujo con morfolina en THF para dar 280 mg (98% de rendimiento) de 2-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-N-(3-piridinil)-4-pirimidinamina: mp (/-Pr2O) 192-194°C; 1H r Mn (DMSO-CÍ6) 59,63 (ancho, 1H), 8,69 (d, J=2,4 Hz, 1H), 8,27 (dd, J=4,7, 1,4 Hz, 1H), 8,23 (td, J=4,7, 2,8 Hz, 1H), 7,98 (ddd, J=8,3, 2,6, 1,5 Hz, 1H), 7,83 (td, J=6,4, 2,8 Hz, 1H), 7,70 (t, Jhf=52,7 Hz, 1H), 7,42-7,39 (m, 2H), 7,36 (dd, J=8,6, 4,8 Hz, 1H), 6,00 (s, 1H), 3,74 (m, 4H), 3,59 (m, 4H).
Ejemplo 47
Síntesis de 2-(difluorometil)-1-[4-(4-morfolinil)-6-(3-piridinil)-1,3,5-triazin-2-il]-1 H-bencimidazol;
El compuesto fue sintetizado según el método B.
Una mezcla de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-1 H-bencimidazol (0,183 g, 0,5 mmol), ácido 3-piridilborónico (92 mg, 0,75 mmol), PdCl2(dppf) (28 mg), y Na2CO3 ac. (2M, 4 mL) en dioxano (20 mL) se calentó bajo reflujo bajo nitrógeno durante 1 hora. Después de enfriarse, la mezcla se diluyó con agua, se extrajo con CH2Cl2 y se secó. La cromatografía en alúmina, eluyendo con CH2Cl2, dio 0,13 g (rendimiento del 64%) de 2-(difluorometil)-1 -[4-(4-morfolinil)-6-(3-piridinil)-1,3,5-triazin-2-il]-1 H-bencimidazol: mp (MeOH) 199-201°C; 1H RMN (DMSO-de) 59,59 (d, J=1,6 Hz, 1H), 8,85 (dd, J=4,8, 1,7 Hz, 1H), 8,75 (td, J=8,0, 1,9 Hz, 1H), 8,50 (d, J=8,2 Hz, 1H), 7,90 (d, J=7,9 Hz, 1H), 7,86 (t, Jhf=52,6 Hz, 1H), 7,65 (ddd, J=8,0, 4,8, 0,7 Hz, 1H), 7,59 (dt, J=7,8, 1,1 Hz, 1H), 7,49 (dt, J=7,6, 1,1 Hz, 1H), 4,09 (m, 2H), 3,94 (m, 2H), 3,79 (m, 4 H); Anal. Calc. para C20H17F2N7O: C, 58,7; H, 4,2; N, 23,95; Encontrado: C, 58,45; H, 4,1; N, 24,2%.
Ejemplo 48
Síntesis de 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(3-piridinil)-1,3,5-triazin-2-il]-1 H-bencimidazol
El compuesto fue sintetizado según el método B.
Reacción de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-4-metoxi-1 H-bencimidazol (ejemplo 2) y ácido 3-piridinilborónico, como en el ejemplo 47, dio 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(3-piridinil)-1,3,5-triazin-2-il]-1 H-bencimidazol en 61% de rendimiento: mp (C^Ch/MeOH) 208-210°C; 1H RMN (DMSO-cfe) 59,59 (dd, J=2,2, 0,7 Hz, 1H), 8,85 (dd, J=4,8, 1,7 Hz, 1H), 8,75 (dt, J=8,0, 1,9 Hz, 1H), 8,35 (dd, J=8,4, 0,4 Hz, 1H), 7,83 (t, Jh f =52,6 Hz, 1H), 7,66 (ddd, J=8,0, 4,8, 0,8 Hz, 1H), 7,50 (t, J=8,3 Hz, 1H), 7,02 (d, J=7,8 Hz, 1H), 4,09 (t, J=7,8 Hz, 2H), 4,00 (s, 3H), 3,94 (m, 2H), 3,78 (m, 4H); Anal. Calc. para C21H^F2N7O4-0,3H2O: C, 56,7; H, 4,4; N, 22,0; Encontrado: C, 56,6; H, 4,0; N, 22,1%.
Ejemplo 49
Síntesis de 5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-piridinamina
El compuesto fue sintetizado según el método B.
Una mezcla de 0,30 g (0,75 mmol) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-4-metoxi-1H-bencimidazol, 0,21 g (0,95 mmol) de 5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-2-piridinamina, y 0,057 g (0,08 mmol) de PdCl2(dppf) en una mezcla de 1,4-dioxano (30 mL) y solución Na2CO32M (6 mL) se calentó a 100°C durante 5 horas bajo nitrógeno. Después del enfriamiento, la mezcla se concentró, se diluyó con agua y se extrajo con EtOAc (x 4). La capa orgánica fue lavada con salmuera, secada (Na2SO4) y concentrada. La cromatografía en sílice, eluyendo primero con CH2Cl2-EtOAc (3:1) y luego con CH2Cl2-EtOAc (1:3), dio un polvo blanquecino, que fue recristalizado con CH2Cl2 para dar 0,144 g (43% de rendimiento) de 5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-piridinamina: mp259-261°C; 1H RMN (DMSO-d6) 59,04 (d, J=2,2 Hz, 1H), 8,32 (dd, J=8,8, 2,4 Hz, 1H), 8,04 (d, J=8,3 Hz, 1H), 7,79 (t, Jh f =52,8 Hz, 1H), 7,47 (t, J=8,2 Hz, 1H), 6,99 (d, J=7,9 Hz, 1H), 6,85 (s, 2H), 6,57 (d, J=8,8 Hz, 1H), 4,04-4,00 (m, 5H), 3,89 (s ancho, 2H), 3,76 (s, 4H); Anal. Calc. para C21H20F2NsO2-0,49H2O: C, 54,45; H, 4,6; N, 24,2; Encontrado: C, 54,8; H, 4,2; N, 24,2%.
Ejemplo 50
Síntesis de 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(1H-pirazol-4-il)-1,3,5-triazin-2-il]-1 H-bencimidazol
El compuesto fue sintetizado según el método B.
La reacción de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-4-metoxi-1 H-bencimidazol con 4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-pirazol-1-carboxilato de tere-butilo (documento WO 2006/021881) por un procedimiento similar al ejemplo 47 dio una mezcla de 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(1H-pirazol-4-il)-1,3,5-triazin-2-il]-1 H-bencimidazol y 4-[4-[2-(difluorometil)-4-metoxi-1 H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-1H-pirazol-1-carboxilato de tere-butilo. El tratamiento de la mezcla con TFA en CH2Cl2, como para los ejemplos anteriores, dio 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(1H-pirazol-4-il)-1,3,5-triazin-2-il]-1 H-bencimidazol en 55% de rendimiento: mp (CH2Ch/MeOH) 289-291°C; 1H RMN (DMSO-d6) 513,46 (s, 1H), □ □ 8,60 (d, J=1,4 Hz, 1H), 8,24 (d, J=1,5 Hz, 1H), 8,07 (d, J=8,0 Hz, 1H), 7,84 (t, Jh f =52,8 Hz, 1H), 7,46 (t, J=8,2 Hz, 1H), 6,99 (d, J=7,9 Hz, 1H), 4,01 (ancho, 2H), 3,99 (s, 3H), 3,88 (ancho, 2H), 3,76 (ancho, 4H); Anal. Calc. para C19H18F2N8O2: C, 53,3; H, 4,2; N, 26,2; Encontrado: C, 53,1; H, 4,3; N, 26,0%.
Ejemplo 51
Síntesis de 2-(difluorometil)-1-[4-(4-morfolinil)-6-(3-piridinil)-2-pirimidinil]-1 H-bencimidazol;
El compuesto fue sintetizado según el método B.
Usando un procedimiento similar al ejemplo 47, la reacción de 1-[4-cloro-6-(4-morfolinil)-2-pirimidinil]-2-(difluorometil)-1 H-bencimidazol (Publ. internacional no. WO 2008/032028) y ácido 3-piridinilborónico dio 2-(difluorometil)-1-[4-(4-morfolinil)-6-(3-piridinil)-2-pirimidinil]-1 H-bencimidazol en 77% de rendimiento: mp (CH2Ch/hexanos) 172-179°C; 1H RMN (DMSO-CÍ6) 59,44 (d, J=2,2 Hz, 1H), 8,75 (dd, J=4,8, 1,5 Hz, 1H), 8,61 y 8,59 (2m, 1H), 8,39 (d, J=8,20 Hz, 1H), 7,88 (d, J= 8,0 Hz, 1H), 7,82 (t, Jh f =52,8 Hz, 1H), 7,62 (dd, J=8,0, 4,8 Hz, 1H), 7,55-7,51 (m, 2H), 7,46-7,42 (m, 1H), 3,88-3,84 (m, 4H), 3,79-3,77 (m, 4H); Anal. Calc. para C21H18F2^O-1,9 H2O: C, 49,1; H, 4,8; N, 15,6; Encontrado: C, 49,0; H, 4,4; N, 15,0%
Ejemplo 52
Síntesis de 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(3-piridinil)-2-pirimidinil]-1 H-bencimidazol
El compuesto fue sintetizado según el método B.
La reacción de 1-(4,6-dicloro-2-pirimidinil)-2-(difluorometil)-4-metoxi-1H-bencimidazol; (Publ. internacional no. WO 2005/095389) (50 mg, 0,145 mmol) con diez veces de exceso de morfolínea en THF a temperatura ambiente dio 51 mg (89% rendimiento) de 1-[4-cloro-6-(4-morfolinil)-2-pirimidinil]-2-(difluorometil)-4-metoxi-1H-bencimidazol: mp (CH2Cl2/MeOH) 261-263°C; 1H RMN (CDCls) 57,90 (dd, J=8,4, 0,7 Hz, 1H), 7,47 (t, Jh f =53,6 Hz, 1H), 7,37 (t, J=8,2 Hz, 1H), 6,82 (d, J=7,7 Hz, 1H), 6,47 (s, 1H), 4,07 (s, 3H), 3,84 (m, 4H), 3,73 (m, 4H); Anal. Calc. para C17H16C F 2N5O2: C, 51,6; H, 4,1; N, 17,7; Encontrado: C, 51,7; H, 4,1; N, 17,9%.
La reacción del compuesto antedicho de cloro con el ácido 3-piridinilborónico, como en el ejemplo 47, dio 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(3-piridinil)-2-pirimidinil]-1H-bencimidazol en un 85% de rendimiento: mp (CH2Cl2/hexanos) 208-210°C; 1H RMN □ (DMSO-^) 59,43 (dd, J=2,3, 0,7 Hz, 1H), 8,75 (dd, J=4,8, 1,6 Hz, 1H), 8,68 8,61 y 8,59-8,58 (2m, 1H), 7,93 (dd, J=8,3, 0,5 Hz, 1H), 7,77 (t, Jh f =53,4 Hz, 1H), 7,64-7,60 (m, 1H), 7,54 (s, 1H), 7,43 (t, J=8,2 Hz, 1H), 7,00 (d, J=7,7 Hz, 1H), 4,00 (s, 3H), 3,87-3,80 (m, 4H), 3,79-3,76 (m, 4H); Anal. Calc. para C22H20F2N6O2: C, 60,3; H, 4,6; N, 19,2; Encontrado: C, 60,1; H, 4,4; N, 19,0%.
Ejemplo 53
Síntesis de 2-(difluorometil)-1-[4-(6-metoxi-3-piridinil)-6-(4-morfolinil)-1,3,5-triazin-2-il]-1H-bencimidazol
El compuesto fue sintetizado según el método B.
La reacción del ácido 6-metoxi-3-piridinilborónico y 1-[4-cloro-6-(4-morfolinil)-2-pirimidinil]-2-(difluorometil)-1H-bencimidazol (Publ. internacional no. Wo 2008/032028), como en el ejemplo 47, dio 2-(difluorometil)-1-[4-(6-metoxi-3-piridinil)-6-(4-morfolinil)-1,3,5-triazin-2-il]-1H-bencimidazol en un 81% de rendimiento: mp (CH2Cl2/hexanos) 224-226°C; 1H RMN (DMSO-^) 59,09 (dd, J=2,1,0,5 Hz, 1H), 8,54 (dd, J= 8,8, 2,5 Hz, 1H), 8,37 (d, J=8,2 Hz, 1H), 7,87 (d, J=7,9 Hz, 1H), 7,80 (t, Jh f =52,8 Hz, 1H), 7,53 (td, J=7,7, 1,1 Hz, 1H), 7,45 (d, J=8,2 Hz, 1H), 7,42 (s ancho, 1H), 7,02 (d, J=8,7, 0,4 Hz, 1H), 3,96 (s, 3H), 3,86-3,83 (m, 4H), 3,79-3,76 (m, 4H); Anal. Calc. para C22H20F2N6O2: C, 60,3; H, 4,6; N, 19,2; Encontrado: C, 60,4; H, 4,7; N, 19,5%.
Ejemplo 54
Síntesis de N-[3-({5-[2-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-4-pirimidinil]-2-piridinil}oxi)propil]-N,N-dimetilamina
El compuesto fue sintetizado según el método B.
De forma semejante, la reacción de 1-[4-cloro-6-(4-morfolinil)-2-pirimidinil]-2-(difluorometil)-1H-bencimidazol y N,N-dimetil-3-{[5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-2-piridinil]oxi}-1-propanamina, como en el ejemplo 47, dio N-[3-({5-[2-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-4-pirimidinil]-2-piridinil}oxi)-N,N-dimetilamina en un 33% de rendimiento: mp (C^Ch/hexanos) 140-141°C; 1H RMN (DMSO-d6) 59,07 (d, J=2,2 Hz, 1H), 8,53 (dd, J=8 ,8 , 2,5 Hz, 1H), 8,37 (d, J=8,2 Hz, 1H), 7,87 (d, J=7,9 Hz, 1H), 7,80 (t, Jh f =52,8 Hz, 1H), 7,52 (dt, J=7,8, 1,0 Hz, 1H), 7,50 (dd J=8,1, 1,0 Hz, 1H), 7,42 (s, 1H), 7,00 (d, J=8,7 Hz, 1H), 4,39 (t, J=6,6 Hz, 2H), 3,85-3,84 (m, 4H), 3,78-3,76 (m, 4H), 2,39 (t, J=7,1 Hz, 2H), 2,17 (s, 6 H), 1,89 (quinteto, 2H); Anal. Calc. para C26H29F2N7O: C, 61,3; H, 5,7; N, 19,2; Encontrado: C, 61,0; H, 5,5; N, 19,1%.
Ejemplo 55
Síntesis de 2-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-4,5'-bipirimidina
El compuesto fue sintetizado según el método B.
Una mezcla de 1-[4-cloro-6-(4-morfolinil)-2-pirimidinil]-2-(difluorometil)-1H-bencimidazol (200 mg, 0,547 mmol), ácido pirimidin-5-borónico (203 mg, 1,64 mmol), PdCl2(dppf) (45 mg, 0,0551 mmol) y K2CO3 ac. (2M, 4 ml) en 1,4-dioxano (20 ml) fue sometido a reflujo bajo nitrógeno durante 2,5 h. Se añadió más ácido pirimidin-5-borónico (203 mg, 1,64 mmol) y PdCl2(dppf) (23 mg, 0,0282 mmol), y la mezcla se sometió a reflujo durante 16,5 horas más bajo nitrógeno. La mezcla se enfrió a temperatura ambiente, se diluyó con H2O, se extrajo con CH2Cl2 (4 x), y los extractos orgánicos combinados se secaron (Na2SO4) y los disolventes se retiraron bajo vacío. La cromatografía en sílice, eluyendo con CH2Cl2/MeOH (de 100:0 a 97:3), seguida de la recristalización con CH2Cl2/MeOH//-Pr2O dio 2-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-4,5'-bipirimidina (177 mg, 79%): mp 209-211°C; 1H RMN (CDCls) 59,37 (s, 2H), 9,37 (s, 1H), 8,37 (m, 1H), 7,93 (m, 1H), 7,59 (t, Jh f =53,7 Hz, 1H), 7,49-7,41 (m, 2H), 6,86 (s, 1H), 3,91 (m, 4H), 3,85 (m, 4H); Anal. Calc. para C20H17F2N7O: C, 58,7; H, 4,2; N, 23,95; Encontrado: C, 58,4; H, 3,9; N, 23,9%.
Ejemplo 56
Síntesis de 2-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-4,5'-bipirimidina
El compuesto fue sintetizado según el método B.
De forma semejante al ejemplo 55, fue sometida a reflujo una mezcla de 1-[4-cloro-6-(4-morfolinil)-2-pirimidinil]-2-(difluorometil)-4-metoxi-1H-bencimidazol (106 mg, 0,268 mmol), ácido pirimidin-5-borónico (188 mg, 1,52 mmol), PdCl2(dppf) (40 mg, 0,05 mmol) y K2CO3 ac. (2M, 4 ml) en 1,4-dioxano (20 ml) bajo nitrógeno durante 24 h. Después de enfriar a temperatura ambiente, la mezcla se diluyó con H2O, y se extrajo con CH2Cl2 (4 x). Los extractos orgánicos combinados se secaron (Na2SO4) y los disolventes se eliminaron al vacío. La cromatografía en sílice, eluyendo con CH2Cl2/MeOH (de 100:0 a 97:3), seguida de la recristalización con CH2Cl2/MeOH/hexanos dio 2-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-4,5'-bipirimidina (89 mg, 75%): mp 222-224°C; 1H Rm N (Cd CI3) 59,38 (s, 2H), 9,36 (s, 1H), 7,92 (dd, J=8,4, 0,6 Hz, 1H), 7,49 (t, J=53,6 Hz, 1H), 7,38 (t, J=8,2 Hz, 1H), 6,86 (s, 1H), 6,84 (d, J=7,7 Hz, 1H), 4,07 (s, 3H), 3,89 (m, 4H), 3,85 (m, 4H); Anal. Calc. para C ^ H ^ N ^ ^ ^ MeOH: C, 57,0; H, 4,5; N, 21,9; Encontrado: C, 56,95; H, 4,45; N, 22,0%.
Ejemplo 57
Síntesis de 2-[2-(difluorometil)-4-metoxi-1 H-bencimidazol-1 -il]-6-(4-morfolinil)-2'-metoxi-4,5'-bipirimidina
El compuesto fue sintetizado según el método B.
De forma semejante al ejemplo 56, una mezcla de 1-[4-cloro-6-(4-morfolinil)-2-pirimidinil]-2-(difluorometil)-4-metoxi-1H-bencimidazol (148 mg, 0,374 mmol), ácido 2-metoxi-5-pirimidinilborónico (211 mg, 1,52 mmol), PdCl2(dppf) (40 mg, 0,05 mmol) y K2CO3 ac. (2M, 4 ml) en 1,4-dioxano (20 ml) se sometió a reflujo bajo nitrógeno durante 24 h. Después de enfriar a temperatura ambiente, la mezcla se diluyó con H2O, y se extrajo con CH2Cl2 (4 x). Los extractos orgánicos combinados se secaron (Na2SO4) y los disolventes se retiraron bajo vacío. La cromatografía en sílice, eluyendo con CH2Cl2/MeOH (de 100:0 a 98:2), seguida de la recristalización con CH2Cl2/MeOH//-Pr2O dio 2-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-2'-metoxi-4,5'-bipirimidina (61 mg, 35%): mp 238-241°C; 1H RMN (CDCI3) 59,18 (s, 2H), 7,91 (d, J=8,1 Hz, 1H), 7,49 (t, Jh f =53,6 Hz, 1H), 7,37 (t, J=8,2 Hz, 1H), 6,83 (d, J=7,9 Hz, 1H), 6,77 (s, 1H), 4,13 (s, 3H), 4,07 (s, 3H), 3,88 (dd, J=5,6, 3,7 Hz, 4H), 3,82 (m, 4H); Anal. Calc. para C22H21F2N7O3: C, 56,3; H, 4,5; N, 20,9; Encontrado: C, 56,1; H, 4,3; N, 20,6%.
Ejemplo 58
Síntesis de 2-[2-(difluorometil)-1 H-bencimidazol-1-il]-6-(4-morfolinil)-4,5'-bipirimidina-2'-amina
El compuesto fue sintetizado según el método B.
Similar al ejemplo 57, una mezcla de 1-[4-cloro-6-(4-morfolinil)-2-pirimidinil]-2-(difluorometil)-1H-bencimidazol (200 mg, 0,547 mmol), 5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-2-pirimidinilamina (302 mg, 1,38 mmol), PdCl2(dppf) (45 mg, 0,0551 mmol) y K2CO3 ac. (2M, 4 ml) en 1,4-dioxano (20 ml) fue sometida a reflujo bajo nitrógeno durante 24 hrs. La mezcla se enfrió a temperatura ambiente, se diluyó con H2O, se extrajo con CH2CI2 (4 x), y los extractos orgánicos combinados se secaron (Na2SO4) y los disolventes se eliminaron al vacío. La cromatografía en alúmina, eluyendo con CH2Cl2/EtOAc (de 100:0 a 80:20) a CH2Cl2/MeOH (de 100:0 a 98,5:1.5), seguida de la recristalización con CH2Cl2/MeOH//-Pr2O dio 2-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-4,5'-bipirimidin-2'-amina (157 mg,
66% de rendimiento): mp 281-285°C; 1H RMN (DMSO-de) 5 9,09 (s, 2H), 8,35 (d, J=8,2 Hz, 1H), 7,86 (d, J=8,0 Hz, 1H), 7,79 (t, J hf =52,8 Hz, 1H), 7,52 (t, J=7,5 Hz, 1H), 7,43 (t, J=7,3 Hz, 1H), 7,32 (s, 1H), 7,24 (s, 2H), 3,82 (m, 4H), 3,77 (m, 4H).
Ejemplo 59
Síntesis de 2-[2-(difluorometil)-4-metoxi-1 H-bencimidazol-1 -il]-6-(4-morfolinil)-9-(3-piridinil)-9H-purina
El compuesto fue sintetizado por una modificación del método C.
Una mezcla de 4 (2,6-dicloro-5-nitro-4-pirimidinil)morfolina (Publ. de solicitud de patente de EE.UU. no. 2009/0181963) (1,89 g, 3,6 mmol) y 3-aminopiridina (0,68 g, 7,2 mmol) en THF a -70°C fue tratada con 7,2 mL de LiHMDS (solución 1m en THF, 2 eq.) y la mezcla se agitó a esa temperatura durante 1,5 h, y luego se permitió que se calentara a temperatura ambiente. El disolvente fue retirado y el producto crudo se extrajo con HCl 0,5 M. Después de la filtración, la solución acuosa se hizo básica con Na2CO3sat. para dar un precipitado, que fue recogido por filtración, y secado, para dar 1,12 g (52% de rendimiento) de 2-cloro-6-(4-morfolinil)-5-nitro-N-(3-piridinil)-4-pirimidinamina: mp (MeOH ac.) > 310°C; 1H RMN (CDCls) 510,19 (s ancho, 1H), 8,74 (d, J=2,5 Hz, 1H), 8,45 (dd, J=4,8, 1,4 Hz, 1H), 8,12 (ddd, J=8,3, 2,6, 1,5 Hz, 1H), 7,35 (dd, J=8,4, 4,8 Hz, 1H), 3,81 (m, 4H), 3,61 (m, 4H).
Una mezcla de 0,23 g del compuesto nitro antedicho (0,68 mmol), 0,147 g (0,74 mmol) de 2-difluorometil-4-metoxi-1H-bencimidazol (ejemplo 2) y 0,38 g (2,75 mmol) de K2CO3 en polvo en 4 mL de DMSO se calentó a 120°C durante 4 horas. La mezcla de reacción se diluyó con agua, y se extrajo con EtOAc (x 4). Las capas orgánicas combinadas se lavaron con salmuera, se secaron y concentraron. El residuo fue purificado por cromatografía en sílice, eluyendo primero con hexanos/EtOAc (1:1), y luego con CH2Ch/EtOAc (2:1), para dar 0,253 g (75% de rendimiento) de 2-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-5-nitro-H-(3-piridinil)-4-pirimidinamina como un polvo amarillo: 1H RMN (CDCl3) 510,26 (s, 1H), 8,72 (d, J=2,4 Hz, 1H), 8,60 (dd, J=4,8, 1,4 Hz, 1H), 7,95 (ddd, J=8,3, 2,4, 1,6 Hz, 1H), 7,45 (dd, J=8,3, 0,6 Hz, 1H), 7,40 (dd, J=8,3, 4,8 Hz, 1H), 7,18 (t, J=8,3 Hz, 1H), 7,11 (t, Jhf=53,5 Hz, 1H), 6,78 (d, J=7,8 Hz, 1H), 4,03 (s, 3H), 3,88 (t, J=4,5 Hz, 4H), 3,70 (t, J=4,5 Hz, 4H).
A 0,253 g (0,51 mmol) del compuesto nitro anterior en MeOH (30 mL) se añadió 0,15 g de Pt al 5% en carbón activado, y la mezcla se agitó bajo hidrógeno a 101,6 Kpa (30 pulgadas/Hg) durante 1,5 h. La mezcla de la reacción fue filtrada a través de celite, y concentrada para dar 0,203 g de 2-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-M4-(3-piridinil)-4,5-pirimidindiamina crudo: 1H RMN (Dm So -cí6) 58,81 (s, 1H), 8,75 (d, J=2,4 Hz, 1H), 8,27 (dd, J=4,7, 1,5 Hz, 1H), 8,02 (ddd, J= 8,3, 2,4, 1,5 Hz, 1H), 7,64 (dd, J=8,3, 0,6 Hz, 1H), 7,56 (t, Jhf=53,1 Hz, 1H), 7,34 (ddd, J=8,3, 4,7, 0,5 Hz, 1H), 7,25 (t, J=8,3 Hz, 1H), 6,87 (d, J=7,7 Hz, 1H), 4,79 (s, 2H), 3,96 (s, 3H), 3,82 (t, J=4,5 Hz, 4H), 3,24 (t, J=4,5 Hz, 4H).
Una mezcla de 0,155 g (0,33 mmol) de la diamina anterior, ortoformiato de trimetilo (2,5 mL, 22,8 mmol), y monohidrato de p-toluenosulfonato (0,05 g, 0,26 mmol) se calentó a 95°C durante 4 horas. La mezcla de reacción se enfrió a temperatura ambiente, se concentró, y el producto fue recristalizado con CH2Cl2 para dar 0,113 g (54% sobre 2 pasos) de 2-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-9-(3-piridinil)-9H-purina como un polvo blanquecino: mp 229-231°C; 1H RMN (CDCl3) 58,97 (d, J=2,4 Hz, 1H), 8,76 (dd, J=4,8, 1,5 Hz, 1H), 8,19 (ddd, J=8,2, 2,4, 1,5 Hz, 1H), 8,09 (s, 1H), 7,77 (dd, J= 8,3, 0,6 Hz, 1H), 7,57 (ddd, J=8,3, 4,8, 0,7 Hz, 1H), 7,41 (t, Jhf=53,8 Hz, 1H), 7,32 (t, J=8,2 Hz, 1H), 6,80 (d, J=7,7 Hz, 1H), 4,44 (s, ancho, 4H), 4,05 (s, 3H), 3,91 (t, J=4,8 Hz, 4H).
Ejemplo 60
Síntesis de 2-[2-(difluorometil)-4-metoxi-1 H-bencimidazol-1 -il]-6-(4-morfolinil)-9-(5-pirimidinil)-9H-purina;
El compuesto fue sintetizado por una modificación del método C.
A 0,482 g (5,06 mmol) de 5-aminopirimidina en THF (10 mL) se añadieron 2,90 mL de NaHMDS (solución 2 M en THF) a 0°C, y la mezcla se agitó durante 10 min. Se añadió una solución de 0,5924 g (2,12 mmol) de 4-(2,6-dicloro-5-nitro-4-pirimidinil)morfolina (publicación de solicitud de patente de EE.UU. no. 2009/0181963) en THF (5 mL), y la mezcla resultante se agitó durante 15 min. La mezcla de reacción fue neutralizada con ácido acético, diluida con agua, y extraída con EtOAc. La capa orgánica fue lavada con agua y NH3 ac., secada y concentrada. La cromatografía en sílice, eluyendo con hexanos/EtOAc (8:2), dio 0,465 g (65% de rendimiento) de 2-cloro-6-(4-morfolinil)-5-nitro-N-(5-pirimidinil)-4-pirimidinamina como un polvo blanco: 1H r Mn (DMSO-cfe) 510,34 (s, 1H), 8,98 (s, 1H), 8,92 (s, 2H), 3,70 (t, J=4,8 Hz, 4H), 3,50 (t, J=4,8 Hz, 4H).
Una mezcla de 0,465 g (1,38 mmol) del compuesto nitro anterior, 0,368 g (1,86 mmol) de 2-difluorometil-4-metoxi-1H-bencimidazol (ejemplo 2) y 0,762 g (5,52 mmol) de K2CO3 en polvo en 5 mL de DMSO se calentó a 120°C durante 8 horas. La mezcla de reacción se diluyó con agua, y se extrajo con EtOAc (x 4). La capa orgánica fue lavada con salmuera, secada y concentrada. La cromatografía en sílice, eluyendo primero con hexanos/EtOAc (7:3) y luego con CH2Cl2/EtOAc (1:2), dio 0,592 g (rendimiento del 86%) de 2-[2-(difluorometil)-7-metoxi-2,3-dihidro-1H-bencimidazol-1-il]-6-(4-morfolinil)-5-nitro-N-(5-pirimidinil)-4-pirimidinamina, como un polvo amarillo: 1H RMN (CDCl3) 5 10,26 (s, 1H), 9,16 (s, 1H), 8,98 (s, 2H), 7,38 (dd, J=8,4, 0,6 Hz, 1H), 7,20 (t, J=8,4 Hz, 1H), 7,12 (t, Jh f =53,5 Hz, 1H), 6,78 (d, J=7,8 Hz, 1H), 4,01 (s, 3H), 3,87 (t, J=4,8 Hz, 4H), 3,70 (t, J=4,8 Hz, 4H).
A 0,162 g (0,33 mmol) del compuesto nitro anterior en THF (40 mL) se añadieron 0,2 g de Ptal 5% en carbón activado, y la mezcla se agitó bajo hidrógeno (135456 Pa (40 pulg/Hg)) durante 17 horas. La mezcla de reacción se filtró a través de celite, y se concentró para dar 0,155 g de la 2-[2-(difluorometil)-7-metoxi-2,3-dihidro-1H-bencimidazol-1-il]-6-(4-morfolinil)-N4-(5-pirimidinil)-4,5-pirimidindiamina cruda: 1H RMN (c Dc I3) 5 8,97-8,92 (m, 3H), 7,76 (s, 1H), 7,67 (d, J=8,3 Hz, 1H), 7,43 (t, Jh f =53,8 Hz, 1H), 7,28-7,26 (m, 1H), 6,97 (s, 2H), 6,76 (d, J=7,9 Hz, 1H), 3,97 (s, 3H), 3,88 (t, J=4,6 Hz, 4H), 3,36 (t, J=4,6 Hz, 4H).
Una mezcla de la diamina cruda antedicha (0,155 g, 0,33 mmol), ortoformiato de trimetilo (2,5 ml, 22,8 mmol), y ptoluenesulfonato monohidrato (0,05 g, 0,26 mmol) se calentó a 95°C durante 3 horas. La mezcla de reacción se enfrió y concentró, y el residuo fue purificado por cromatografía en sílice, eluyendo con CH2Cl2/EtOAc (1:3) para dar 0,115 g (73% sobre 2 pasos) de 2-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-9-(5-pirimidinil)-9H-purina como un polvo amarillo: mp 248-251°C; 1H RMN (CDCI3) 59,34 (s, 1H), 9,23 (s, 2H), 8,09 (s, 1H), 7,73 (dd, J=8,4, 0,6 Hz, 1H), 7,41 (t, Jh f =53,5 Hz, 1H), 7,34 (t, J=8,2 Hz, 1H), 6,80 (d, J=7,7 Hz, 1H), 4,43 (s ancho, 4H), 4,05 (s, 3H), 3,91 (t, J=4,8 Hz, 4H); Anal. Calc. para C22H19F2N9O2, 0,09 EtOAc: C, 55,1; H, 4,1; N, 25,9; Encontrado: C, 55,05; H, 4,00; N, 25,5%.
Ejemplo 62
Síntesis de 6-[2-(difluorometil)-4-metoxi-1 H-bencimidazol-1 -il]-2-(4-morfolinil)-9-(3-piridinil)-9H-purina;
Se añadió NaH (148 mg, 6,17 mmol) a una solución de 2-difluorometil-4-metoxi-1H-bencimidazol (ejemplo 2) (638 mg, 3,22 mmol) en DMF (10 mL) a 0°C, y la mezcla se calentó a temperatura ambiente y se agitó durante 45 min. Se
añadió 2,6-dicloro-9-tetrahidro-2H-piran-2-il-9H-purina (800 mg, 2,93 mmol) después y se agitó la mezcla resultante a temperatura ambiente durante 5 días, se inactivó con H2O, y se extrajo con EtOAc (2 x). Los extractos orgánicos combinados se lavaron con H2O (3 x), se secaron (Na2SO4) y el disolvente se retiró bajo vacío. La cromatografía en sílice, eluyendo con hexanos/EtOAc (de 100:0 a 60:40) dio 2-cloro-6-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-9-tetrahidro-2H-piran-2-il-9H-purina (645 mg, 51%): 1H RMN (CDCls) 58,38 (s, 1H), 7,52 (t, Jhf=54,2 Hz, 1H), 7,37 7,31 (m, 2H), 6,84 (m, 1H), 5,86 (dd, J=10,7, 2,5 Hz, 1H), 4,23 (ddd, J=10,0, 3,8, 1,8 Hz, 1H), 4,07 (s, 3H), 3,83 (dt, J=11,7, 2,8 Hz, 1H), 2,26 (m, 1H), 2,14 (m, 1H), 2,03 (m, 1H), 1,91-1,69 (m, 3H).
Se calentó una mezcla del compuesto cloro (629 mg, 1,45 mmol) y morfolina (0,65 mL, 7,43 mmol) en EtOH absoluto (30 mL) a 70°C durante 17 horas. El disolvente fue retirado bajo vacío y el residuo diluido con H2O. El precipitado resultante fue filtrado, lavado con H2O y MeOH ac., y secado para dar 6-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-2-(4-morfolinil)-9-tetrahidro-2H-piran-2-il-9H-purina (633 mg, 90%) que se utilizó en el siguiente paso sin purificación: 1H RMN (CDCls) 58,01 (s, 1H), 7,30 (t, Jhf=53,7 Hz, 1H), 7,32-7,23 (m, 2H), 6,80 (dd, J=7,8, 0,7 Hz, 1H), 5,67 (dd, J=10,0, 2,6 Hz, 1H), 4,19 (m, 1H), 4,06 (s, 3H), 3,88 (m, 4H), 3,83-3,75 (m, 5H), 2,17-2,05 (m, 3H), 1,88-1,67 (m, 3H).
Una mezcla del compuesto del piranilo antedicho (625 mg, 1,29 mmol) en EtOAc (50 ml) saturado con ácido clorhídrico fue agitado a 0°C durante 30 minutos, calentado a temperatura ambiente y agitado durante 24 horas. El sólido fue filtrado, lavado con H2O, y secado para dar 6-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-2-(4-morfolinil)-9H-purina (435 mg, 84%) que se utilizó en el siguiente paso sin purificación: 1H RMN (DMSO-CÍ6) 5 13,21 (s ancho, 1H), 8,30 (s, 1H), 7,51 (t, Jhf=52,7 Hz, 1H), 7,33 (t, J=8,1 Hz, 1H), 7,27 (d, J=8,1 Hz, 1H), 6,94 (d, J=7,4 Hz, 1H), 4,01 (s, 3H), 3,74-3,71 (m, 8H).
Se añadió trans-N,N'-dimetilciclohexano-1,2-diamina (0,04 mL, 0,254 mmol) en DMF (6 mL) a una mezcla de la purina anterior (155 mg, 0,386 mmol), 3-yodopiridina (158 mg, 0,748 mmol), Cul (37 mg, 0,194 mmol) y Cs2CO3 (264 mg, 0,811 mmol) bajo nitrógeno. Después de calentar la mezcla a 95-100°C durante 21 horas, fueron agregados Cul adicional (37 mg, 0,194 mmol) y trans-N,N'-dimetilciclohexano-1,2-diamina (0,04 mL, 0,254 mmol) y la mezcla fue calentada a 105-110°C durante 2 días bajo nitrógeno. En este momento, se añadieron más 3-yodopiridina (80 mg, 0,390 mmol), Cul (37 mg, 0,194 mmol), y trans-N,N'-dimetilciclohexano-1,2-diamina (0,03 mL, 0,190 mmol) y se calentó la mezcla de reacción durante 24 horas adicionales bajo nitrógeno. La mezcla se enfrió a temperatura ambiente, se diluyó con CH2Cl2 y se filtró a través de celite. Los disolventes fueron retirados. La cromatografía en sílice, eluyendo con CH2Cl2/MeOH (de 100:0 a 98:2), seguido por cromatografía en sílice eluyendo con hexanos/EtOAc (de 67:33 a 20:80) dio 6-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-2-(4-morfolinil)-9-(3-piridinil)-9H-purina (62 mg, 34%): mp 206-209°C; 1H RMN (CDCh) 59,12 (d, J=2,4 Hz, 1H), 8,74 (dd, J=4,8, 1,4 Hz, 1H), 8,14-8,11 (m, 2H), 7,57 (ddd, J=8,3, 4,8, 0,7 Hz, 1H), 7,33 (t, Jhf=53,7 Hz, 1H), 7,37-7,28 (m, 2H), 6,83 (dd, J=7,8, 0,8 Hz, 1H), 4,08 (s, 3H), 3,89 (m, 4H), 3,79 (m, 4H).
Ejemplo 63
Síntesis de 6-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-2-(4-morfolinil)-9-(5-pirimidinil)-9H-purina;
El compuesto fue sintetizado por una modificación del método C.
Se añadió trans-N,N '-dimetilciclohexano-1,2-diamina (0,071 mL, 0,450 mmol) en DMF (5 mL) a una mezcla de 6-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-2-(4-morfolinil)-9H-purina (180 mg, 0,448 mmol), 5-bromopirimidina (356 mg, 2,24 mmol), Cul (85 mg, 0,448 mmol) y Cs2CO3 (321 mg, 0,986 mmol) bajo nitrógeno, y la mezcla se calentó a 100-105°C durante 3 días. La mezcla se enfrió a temperatura ambiente, se diluyó con CH2Cl2y se filtró a través de celite. El tapón de celite se lavó con CH2Cl2 y CH2Cl2/MeOH (9:1) antes de retirar los disolventes al vacío. La cromatografía en sílice, eluyendo con hexanos/EtOAc (de 70:30 a 20:80), seguida de la recristalización con EtOAc/hexanos dio 6-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-2-(4-morfolinil)-9-(5-pirimidinil)-9H-purina; (113 mg, 53%): mp (EtOAc/hexanos) 238-240°C; 1H RMN (CDCh) 59,47 (s, 2H), 9,30 (s, 1H), 8,89 (s, 1H), 7,53 (t, Jhf=52,6 Hz, 1H), 7,37 (t, J=8,1 Hz, 1H), 7,29 (dd, J=8,4, 0,7 Hz, 1H), 6,97 (d, J=7,5 Hz, 1H), 4,02 (s, 3H), 3,80 (m, 4H), 3,72 (m, 4H); Anal. Calc. para C22H19F2N9O2: C, 55,1; H, 4,0; N, 26,3; Encontrado: C, 55,3; H, 4,1; N, 26,5.
Ejemplo 64
Síntesis de 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(1H-pirazol-1-il)-1,3,5-triazin-2-il]-1H-bencimidazol
El compuesto fue sintetizado según el método A.
Una mezcla de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-4-metoxi-1H-bencimidazol (ejemplo 2) (0,49 mg, 1,22 mmol), 1H-pirazol (1,0 g, 14,7 mmol) y DIp Ea (3 mL) se calentó a 120°C durante 40 min, se enfrió a 2o°C y se diluyó con agua (50 mL). El precipitado resultante fue recogido por filtración, lavado con agua y secado. La cromatografía en sílice, eluyendo con CH2Cl2/EtOAc (4:1), dio 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(1H-pirazol-1-il)-1,3,5-triazin-2-il]-1 H-bencimidazol (428 mg, 82%): mp (CH2Cl2/hexanos) 274-277°C; 1H RMN (DMSO-da) 58,79 (dd, J=2,8, 0,5 Hz, 1H), 8,14 (dd, J=8,3, 0,5 Hz, 1H), 8,01 (d, J=0,8 Hz, 1H), 7,88 (t, Jh f =52,8 Hz, 1H), 7,49 (t, J=8,2 Hz, 1H), 7,02 (d, J=7,8 Hz, 1H), 6,70 (dd, J=2,8, 1,5 Hz, 1H), 4,01 (m, 2H), 4,00 (s, 3H), 3,93 (m, 2H), 3,80-3,75 (m, 4H); Anal. Calc. para C19H18F2N8O2: C, 53,3; H, 4,2; N, 26,2; Encontrado: C, 53,1; H, 4,1; N, 25,9%.
Ejemplo 65
Síntesis de 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(1H-pirazol-1-il)-1,3,5-triazin-2-il]-1H-bencimidazol-6-ilamina
El compuesto fue sintetizado según el método A.
Una mezcla de 2,3-diamino-5-nitroanisol (Horner et al., Annalen 1953, 579, 212) (1,10 g, 6 mmol) y ácido difluoroacético (2,31 g, 24 mmol) en ácido polifosfórico (PPA) (50 g) se calentó a 130°C en un baño de aceite durante 1 hora. La solución caliente fue vertida en agua y el pH fue ajustado a pH neutro con enfriamiento para dar 2-(difluorometil)-4-metoxi-6-nitro-1H-bencimidazol (1,33 g, 91%): mp (EtOH/H2O) 192-194°C; 1H RMN (DMSO-de) 5 14,18 (ancho, intercambiable con D2O, 1H), 8,18 (ancho, 1H), 7,65 (dd, J=1,4 Hz, 1H), 7,30 (t, Jhf=52,9 Hz, 1H), 4,07 (s, 3H); Anal. Calc. para C9H7F2N3O3: C, 44,45; H, 2,9; N, 17,3; Encontrado: C, 44,75; H, 3,0; N, 17,3%.
Una solución de 2-(difluorometil)-4-metoxi-6-nitro-1H-bencimidazol (1,22 g, 5 mmol) en MeOH (50 mL) se hidrogenó con Pd sobre C al 10% (50 mg). Después la filtración para quitar el catalizador Pd/C, la solución fue evaporada hasta secarse. El residuo se combinó con dicarbonato de di-ferc-butilo (3,2 g, 15 mmol) en dioxano (20 mL), y la mezcla se calentó bajo reflujo durante 5 horas. El disolvente fue retirado bajo vacío y el residuo se disolvió en MeOH (30 mL) conteniendo NaOH acuoso (2 M, 12,5 mL, 5 equiv.). La mezcla se agitó a temperatura ambiente durante 1 hora, se neutralizó con HOAc, y se evaporó hasta secarse. El residuo se extrajo con EtOAc, se lavó con solución de NaHCO3, y se secó sobre Na2SO4. La cromatografía en sílice, eluyendo con CH2Ch/EtOAc (9:1), dio 1,54 g (98% de rendimiento) de 2-(difluorometil)-4-metoxi-1H-bencimidazol-6-il-carbamato de ferc-butilo: mp (/-Pr2O) 189-191°C; 1H RMN (DMSO-d6) 513,0 (ancho, intercambiable con D2O, 1H), 9,31 (s ancho, intercambiable con D2O, 1 H), 7,42 (s ancho, 1H), 7,15 (t, Jh f =53,4 Hz, 1H), 6,90 (ancho, 1H), 3,90 (s, 3H), 1,49 (s, 9H); Anal. Calc. para C14H17F2N3O3: C, 53,7; H, 5,5; N, 13,4; Encontrado: C, 53,9; H, 5,6; N, 13,4%.
Una mezcla del bencimidazol antedicho (0,47 g, 1,5 mmol), 2,4-dicloro-6-(4-morfolinil)-1,3,5-triazina (0,35 g, 1,5 mmol), y K2CO3 pulverizado (0,83 g, 6 mmol) en DMF (10 mL) se agitó a temperatura ambiente durante 30 min. La mezcla de
reacción se diluyó con agua. El precipitado resultante fue recogido, lavado con agua y luego MeOH, y secado para dar 0,45 g (59% de rendimiento) de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-4-metoxi-1H-bencimidazol-6-il-carbamato de tere-butilo: mp (CH2Ch/MeOH) > 300°C; 1H RMN (CDCls) 5 8,45 (d, J=0,6 Hz, 1H), 7,57 (t, Jhf=53,6 Hz, 1H), 6,67 (ancho, intercambiable con D2O, 1H), 6,63 (d, J=0,9 Hz, 1H), 4,11 (m, 2H), 4,02 (s, 3H), 3,97 (m, 2H), 3,88 (m, 2H), 3,82 (m, 2H), 1,52 (s, 9H); Anal. Calc. para C21H24C F 2N7O4: C, 49,3; H, 4,7; N, 19,15; Encontrado: C, 49,4; H, 4,8; N, 19,2%.
La reacción del compuesto cloro anterior con 1H-pirazol, como en el ejemplo 64, dio 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(1H-pirazol-1-il)-1,3,5-triazin-2-il]-1H-bencimidazol-6-ilcarbamato de tere-butilo en un 85% de rendimiento: mp (CH2Cl2/hexanos) 252-254°C; 1H RMN (DMSO-d6) 59,62 (s, 1H), 8,84 (d, J=2,3 Hz, 1H), 8,71 (s ancho, 1H), 7,98 (d, J=1,0 Hz, 1H), 7,93 (t, Jhf=53,2 Hz, 1H), 6,93 (d, J=1,7 Hz, 1H), 6,68 (dd, J=2,8, 1,5 Hz, 1H), 4,08 (m, 2H), 4,01 (m, 2H), 3,93 (s, 3H), 3,81-3,76 (m, 4H), 1,52 (s, 9H); Anal. Calc. para C24H27F2N9O4: C, 53,0; H, 5,0; N, 23,2; Encontrado: C, 53,2; H, 5,2; N, 23,0%.
A una solución del carbamato anterior (284 mg, 0,52 mmol) en CH2Cl2 (5 mL) se añadió TFA (5 mL). La mezcla de la reacción fue agitada a 20°C durante 30 horas, basificada con NH3 ac. y el CH2Cl2 fue retirado bajo vacío. El precipitado resultante fue recogido por filtración, lavado con agua y secado. La recristalización con CH2Ch/MeOH dio 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(1H-pirazol-1-il)-1,3,5-triazin-2-il]-1H-bencimidazol-6-ilamina en 91% de rendimiento.
Sal de metanosulfonato: mp (MeOH/EtOAc) > 300°C; 1H RMN (DMSO-^) 58,79 (dd, J=2,2, 0,5 Hz, 1H), 7,99 (dd, J=1,4, 0,5 Hz, 1H), 7,87 (t, Jhf=53,0 Hz, 1H), 7,71 (s, 1H), 6,71 (dd, J=2,8, 1,6 Hz, 1H), 6,90 (s ancho, 1H), 4,01 (m, 2H), 3,92 (s, 3H), 3,94 (m, 2H), 3,80-3,75 (m, 4H), 2,33 (s, 6H); Anal. Calc. para C20H23F2NgO6S 0,75 H2O: C, 43,4; H, 4,5; N, 22,8; Encontrado: C, 43,3; H, 4,1; N, 22,8%.
Ejemplo 66
Síntesis de 2-(difluorometil)-4-metoxi-1-[4-(1-metil-1H-pirazol-3-il)-6-(4-morfolinil)-1,3,5-triazin-2-il]-1H-bencimidazol-6-ilamina
El compuesto fue sintetizado según el método B.
Una mezcla de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-4-metoxi-1H-bencimidazol-6-il-carbamato de tere-butilo (ejemplo 65) (313 mg, 0,61 mmol), ácido 1-metil-1H-pirazol-4-ilborónico (155 mg, 1 ,22 mmol) y K2CO32 M ac. (4,1 mL) en 1,4-dioxano (20 mL) se desgasificó con N2 durante 30 min y luego Pd(dppf)Cl2 (30 mg), y la mezcla se desgasificó durante otros 10 minutos. La mezcla de reacción se calentó bajo reflujo durante 1 hora, se enfrió a 20°C, se diluyó con agua y se extrajo con CH2Cl2 (20 mL * 3). Los extractos CH2Cl2 combinados se secaron (Na2SO4) y los disolventes fueron retirados para dar un producto crudo que fue purificado por cromatografía en sílice, eluyendo con CH2Cl2/EtOAc (4:1) para dar2-(difluorometil)-4-metoxi-1-[4-(1-metil-1H-pirazol-3-il)-6-(4-morfolinil)-1,3,5-triazin-2-il]-1 H-bencimidazol-6-ilcarbamato de tere-butilo (233 mg, 69% de rendimiento): mp (CH2Cl2/hexanos) 224-227°C; 1H RMN (DMSO-CÍ6) 59,60 (s, 1H), 8,75 (s, 1H), 8,64 (s, 1H), 8,28 (m, 1H), 7,82 (t, Jh f =53,1 Hz, 1H), 6,92 (d, J=1,7 Hz, 1H), 3,99-3,96 (m, 4H), 3,96 (s, 3H), 3,92 (s, 3H), 3,76 (m, 4H), 1,53 (s, 9H); Anal. Calc. para C25H29F2N9O4.0,25 H2O: C, 53,4; H, 5,3; N, 22,4; Encontrado: C, 53,3; H, 5,3; N, 22,3%.
La desprotección del carbamato anterior con TFA/CH2Cl2 como en el ejemplo 65 dio 2-(difluorometil)-4-metoxi-1-[4-(1-metil-1H-pirazol-3-il)-6-(4-morfolinil)-1,3,5-triazin-2-il]-1H-bencimidazol-6-ilamina al 96% de rendimiento.
Sal de metanosulfonato: mp (MeOH/EtOAc) > 300°C; 1H RMN (DMSO-^) 58,59 (s, 1H), 8,27 (s ancho, 1H), 7,78 (t, Jh f =52,9 Hz, 1H), 7,79 (s ancho, 1H), 6,70 (s, 1H), 3,97 (ancho, 2H), 3,97 (s, 3H), 3,96 (s, 3H), 3,86 (ancho, 2H), 3,75 (ancho, 4H), 2,33 (s, 3H); Anal. Calc. para C21H25F2N9O5S: C, 45,6; H, 4,55; N, 22,8; Encontrado: C, 45,8; H, 4,55; N, 22,9%.
Ejemplo 67
Síntesis de 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(1 H-pirazol-4-il)-1,3,5-triazin-2-il]-1 H-bencimidazol-6-ilamina
El compuesto fue sintetizado según el método B.
De forma semejante al ejemplo 50, la reacción de 2-(difluorometil)-4-metoxi-1-[4-(4-morfofinil)-6-(1H-pirazol-1-il)-1,3,5-triazin-2-il]-1H-bencimidazol-6-ilcarbamato de tere-butilo con 4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-pirazol-1-carboxilato de tere-butilo (documento WO 2006/021881) dio una mezcla de 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(1H-pirazol-4-il)-1,3,5-triazin-2-il]-1H-bencimidazol-6-ilcarbamato de tere-butilo y 4-[4-[6-[(terebutoxicarbonil)amino]-2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-1H-pirazol-1-carboxilato de tere-butilo. La desprotección de la mezcla con C ^C h/TFA durante 20 h a 20°C dio 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(1H-pirazol-3-il)-1,3,5-triazin-2-il]-1H-bencimidazol-6-ilamina, que fue tratada con ácido metansulfónico en MeOH, para dar la sal de metanosulfonato en un rendimiento total del 50%: mp (MEOH/EtOAc) > 300°C; 1H RMN (DMSO-^) 58,48 (s, 2H), 7,88 (s ancho, 1H), 7,79 (t, Jh f =52,9 Hz, 1H), 6,76 (d ancho, J=1,3 Hz, 1H), 4,01 (m, 2H), 3,99 (s, 3H), 3,87 (m, 2H), 3,76 (m, 4H), 2,34 (s, 3H); Anal. Calc. para C20H23F2N9O5S: C, 44,5; H, 4,3; N, 23,4; Encontrado: C, 44,5: H, 4,5; N, 23,1%.
Ejemplo 68
Síntesis de 2-(difluorometil)-1-[4-(1 H-imidazol-1-il)-6-(4-morfolinil)-1,3,5-triazin-2-il]-4-metoxi-1 H-bencimidazol
El compuesto fue sintetizado según el método A.
De forma semejante al ejemplo 64, la reacción de 1-[4-cloro-6-(4-morfolinil)-1,3,5-triazin-2-il]-2-(difluorometil)-4-metoxi-1 H-bencimidazol e imidazol a 120°C durante 1h dio 2-(difluorometil)-1 -[4-(1 H-imidazol-1 -il)-6-(4-morfolinil)-1,3,5-triazin-2-il]-4-metoxi-1 H-bencimidazol en un 71% de rendimiento: mp (CH2Cl2/hexanos) 272-275°C; 1H RMN (Dm SO-efe) 58,74 (s, 1H), 8,04 (t, J=1,4 Hz, 1H), 8,00 (d, J=7,8 Hz, 1H), 7,78 (t, Jh f =52,5 Hz, 1H), 7,50 (t, J=8,3 Hz, 1H), 7,22 (dd, J=1,5, 0,8 Hz, 1H), 7,02 (d, J=7,8 Hz, 1H), 4,03 (m, 2H), 4,00 (s, 3H), 3,94 (m, 2H), 3,80-3,75 (m, 4H); Anal. Calc. para C19H18F2N8O2: C, 53,3; H, 4,2: N, 26,2; Encontrado: C, 53,6; H, 4,3; N, 26,7%.
Ejemplo 69
Síntesis de 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(3-piridinil)-2-pirimidinil]-1H-bencimidazol-6-ilamina
El compuesto fue sintetizado según el método B.
Una mezcla de 2-(difluorometil)-4-metoxi-1H-bencimidazol-6-ilcarbamato de tere-butilo (ejemplo 65) (3,13 g, 10 mmol), 4-(2,6-dicloro-4-pirimidinil)morfolina (2,64 g, 11 mmol), y K2CO3 en polvo (5 g, 40 mmol) en 30 mL de DMF se calentó a 100°C durante 8 horas. La mezcla se enfrió y se diluyó con agua para dar un precipitado que fue recogido y secado. La cromatografía en sílice eluyendo con CH2Ch/EtOAc (19:1) dio 1-[4-cloro-6-(4-morfolinil)-2-pirimidinil]-2-(difluorometil)-4-metoxi-1H-bencimidazol-6-ilcarbamato de tere-butilo (2,49 g, 44% de rendimiento): mp (/-Pr2O) 233 236 °C; 1H RMN (CDCls) 58,30 (s, 1H), 7,57 (t, Jh f =53,8 Hz, 1H), 6,64 (m, 1H), 6,63 (d, J=1,8 Hz, 1H), 6,43 (s, 1H), 4,01 (s, 3H), 3,88-3,85 (m, 4H), 3,82-3,77 (m, 4H), 1,52 (s, 9H); Anal. Calc. para C22H25C F 2N6O4: C, 51,7; H, 4,9; N, 16,45; Encontrado: C, 52,0; H, 4,9; N, 16,6%.
La reacción del compuesto antedicho de cloro (0,41 g, 0,8 mmol) con ácido 3-piridinilborónico (0,15 g, 12 mmol) como en el ejemplo 47, seguido por la cromatografía en alúmina eluyendo con CH2Ch/EtOAc (4:1), dio 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(3-piridinil)-2-pirimidinil]-1H-bencimidazol-6-ilcarbamato de tere-butilo (0 ,22 g, 50% de rendimiento): 1H RMN □ (DMSO-^) 59,53 (s, 1H), 9,45 (d, J=1,7 Hz, 1H), 8,74 (dd, J=4,7, 1,6 Hz, 1H), 8,66 (dt, J=8,3, 1,9 Hz, 1H), 8,54 (s ancho, 1H), 7,75 (t, Jh f =53,1 Hz, 1H), 7,58 (ddd, J=8,0, 4,8, 0,5 Hz, 1H), 7,51 (s, 1H), 6,91 (d, J= 1,7 Hz, 1H), 3,93 (s, 3H), 3,92-3,88 (m, 4H), 3,81-3,78 (m, 4H), 1,51 (s, 9H).
La reacción del carbamato anterior con TFA (5 mL) en CH2Cl2 (10 mL) durante 12 horas dio 2-(difluorometil)-4-metoxi-1-[4-(4-morfolinil)-6-(3-piridinil)-2-pirimidinil]-1H-bencimidazol-6-ilamina con un 94% de rendimiento: 1H RMN □ (DMSO-CÍ6) 59,42 (d, J=2,3 Hz, 1H), 8,74 (dd, J=4,8, 1,6 Hz, 1H), 8,58 (dt, J=8,1, 2,0 Hz, 1H), 7,64 (t, Jh f =53,6 Hz, 1H), 7,60 (ddd, J=8,0, 4,8, 0,7 Hz, 1H), 7,48 (s, 1H), 7,05 (d, J=1,7 Hz, 1H), 6,28 (d, J= 1,7 Hz, 1H), 5,40 (m, 2H), 3,89 (s, 3H), 3,86-3,83 (m, 4H), 3,79-3,77 (m, 4H).
Sal de dimetanosulfonato: mp (MeOH/EtOAc) 246°C; Anal. Calc. para C24H29F2N7O8S2: C, 44,65; H, 4,5; N, 15,2; Encontrado: C, 44,6; H, 4,6; N, 15,1%.
Ejemplo 70
Actividad biológica
A. inhibición de la enzima aislada
Los compuestos fueron evaluados por su capacidad para inhibir las enzimas de la clase I PI 3-Quinasa p1105/p85, p110a/p85, y p110p/p85. Mezclas de reacción que comprendían 0,1 ^g de una enzima recombinante, 10 ^g de L-afosfatidilinositol, y 2X tampón lipídico de quinasa (Tris-HCl 40 mM, pH 7,4, NaCl 200 mM, EDTA 1 mM), que contenía tanto DMSO como un control o el compuesto de prueba en DMSO (la concentración de DMSO final es del 1%), se activaron mediante la adición de una mezcla ATP (MgCl2 5 mM, ATP 100 ^M y 0,1 ^L [y33P] ATP). Las reacciones fueron incubadas a temperatura ambiente durante 1 hora, y luego se detuvieron por la adición de HCl 1M. Los lípidos se extrajeron con un procedimiento de dos pasos. En primer lugar, se añadieron 200 |jL de cloroformo/metanol (1:1), las reacciones bifásicas se mezclaron y centrifugaron brevemente, y la fase inorgánica fue retirada y desechada. A continuación se añadieron 80 ^L de metanol:HCl (1:1) y se siguió el mismo procedimiento. La fase orgánica (70 ^L) se transfirió después a un tubo limpio de 1,6 mL y las reacciones se secaron con un Speedvac, sin calentamiento, durante 30 min. Las reacciones se detectaron en placas TLC (Merck Ltd) y se desarrollaron durante 1 hora en propanolácido acético 1:2 M (13:7). Las placas TLC se secaron entonces a temperatura ambiente y se cuantificaron utilizando un fosforimager (StormImager, Amersham). Se utilizaron nueve concentraciones de compuesto para cada compuesto de prueba para determinar su valor IC50. Cada experimento se realizó dos veces y el valor IC50 promedio se utiliza en este documento. Los resultados se resumen en la tabla 1.
B. Inhibición del crecimiento celular.
Los compuestos fueron evaluados frente a dos líneas de células humanas de paso temprano NZB5y NZOV9 (Marshall et al., Oncol. Res. 2004, 14, 297). Las células se cultivaron en su medio ITS (insulina, transferrina, selenita suplementada con medio esencial a-modificado mínimo, y 5% de suero bovino fetal) y se cultivaron en placas de cultivo de tejido de 96 pocillos bajo una atmósfera de O2 al 5%, CO2 al 5% y N2 al 90%, Los pocillos individuales contenían 500-1000 células (dependiendo de la tasa de crecimiento) en un volumen de 150 ^L. Los compuestos se
añadieron en etapas de concentración de 10 veces a un máximo de 20 pM y las placas fueron incubadas durante cinco días, con 3H-timidina añadido en las últimas 6 horas. Las células fueron recogidas y la radiactividad incorporada fue medida. Se analizaron muestras duplicadas para cada dosis de compuesto con varias muestras de control. Los datos fueron ajustados por un método de mínimos cuadrados a una exponencial de la forma y=yo ae-bx, donde y es la radiactividad (corregida para el fondo y normalizada al 100% del control), x es la dosis de radiación, y yo, a y b son variables, y el valor IC50 definido como la concentración de compuesto reduciendo niveles de 3H-timidina en un 50%. Los resultados se resumen en la tabla 1.
TABLA 1. Actividad biológica
Los ejemplos expuestos anteriormente se proporcionan para dar a los expertos ordinarios en la técnica una descripción completa y descripción de cómo hacer y utilizar las realizaciones reivindicadas y no pretenden limitar el alcance de lo que se describe en este documento. Las modificaciones que son obvias para las personas expertas en la técnica están destinadas a integrarse dentro del alcance de las siguientes reivindicaciones.
Claims (15)
1. Un compuesto de fórmula I, IA o IB:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato;
donde:
cada R1 es independientemente hidrógeno, alquilo C i-6, -S-alquilo C i-6, -S(O)-alquilo C i-6, o -SO2-alquilo C i-6 cada R2 y R3 es, independientemente, (a) hidrógeno, ciano, halo o nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo; o
(c) -C(O)R1a, -C(O)OR1b, -C(O)NR1bR1c, -C(NRa)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c, o-S(O)2NR1bR1c;
cada R4 y R5 es independientemente hidrógeno o alquilo C1-6 o R4 y R5 unidos para formar un enlace, alquileno C1-6, heteroalquileno C1-6, alquenileno C2-6, o heteroalquenileno C2-6;
cada R6 es independiente aralquilo C7-15, arilo C6-14, heteroarilo, o heteroaril-alquilo C1-6;
cada U es independientemente -NR1a-, -C(O)-, -C(O)O-, -C(O)NR1a-, -O-, -OC(O)O-, -OC(O)NR1a-, -NR1aC(O)NR1d-, -NR1aS(O)-, -NR1aS(O)2-, -NR1aS(O)NR1d-, -NR1aS(O)2NR1d-, -S-, -S(O)-, o -S(O)2-;
cada X, Y y Z es N;
cada A, B, D, y E es independientemente un enlace, C, O, N, S, NR9, CR9 o CR9R10, donde cada R9 y R10 es independientemente hidrógeno, halo, alquilo C1-6 , alquenilo C2-6 , o alquinilo C2-6 ; donde los enlaces entre A, B, D y E pueden ser saturados o insaturados; con la condición de que no más de uno de A, B, D y E son un enlace;
cada R1a, R1b, R1c y R1d es, independientemente, (i) hidrógeno; o (ii) alquilo C i-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo;
en donde cada alquilo, alquileno, heteroalquileno, alquenilo, alquenileno, heteroalquenileno, alquinilo, cicloalquilo, arilo, aralquilo, heteroarilo, y heterociclilo en R1, R2, R3, R4, R5, R6, R9, R10, R1a, R1b, R1c o R1d se sustituye opcionalmente por uno o más grupos, cada uno seleccionado independientemente de (a) ciano, halo y nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo, y heterociclilo, cada uno de los cuales está además opcionalmente sustituido por uno o más sustituyentes Q; y (c) -C(O)Ra, -C(O)ORa, -C(O)NRbRc, -C(NRa)NRbRc, -ORa, -OC(O)Ra, -OC(O)ORa, -OC(O)NRbRc, -OC(=NRa)NRbRc, -OS(O)Ra, -OS(O)2Ra, -OS(O)NRbRc, -OS(O)2NRbRc, -NRbRc, -NRaC(O)Rd, -NRaC(O)Od, -NRaC(O)NRbRc, -NRaC(=NRd)NRbRc, -NRaS(O)Rd, -NRaS(O)NRbRc, -SRa, -S(O)Ra, y -S(O)NRbRc, donde cada Ra, Rb, Rc y Rd es, independientemente, (i) hidrógeno; (ii) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo, o heterociclilo, cada uno opcionalmente sustituido por uno o más sustituyentes Q; o (iii) Rb y Rc, junto con el átomo N al que se unen, forman heterociclilo, opcionalmente sustituidos por uno o más sustituyentes Q;
donde cada Q se selecciona independientemente del grupo consistente en (a) ciano, halo y nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo, y heterociclilo; y (c) -C(O)Re, -C(O)ORe, -C(O)NRfRg, -C(NRe)NRfRg, -ORe, -OC(O)Re, -OC(O)ORe, -OC(O)NRfRg, -OC(=NRe)NRfRg, -OS(O)Re, -OS(O)2Re, -OS(O)NRfRg, -OS(O)2NRfRg, -NRfRg, -NReC(O)Rh, -NReC(O)ORh, -NReC(O)NRfRg, -NReC(=NRh)NRfRg, -NReS(O)Rh, -NReS(O)NRfRg, -SRe, -S(O)Re, y -S(O)NRfRg, donde cada Re, Rf, Rg y Rh es, independientemente, (i) hidrógeno; (ii) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo; o (iii) Rf y Rg, junto con el átomo N al que se unen, forman heterociclilo.
2. El compuesto de la reivindicación 1,
con la estructura de fórmula II, la o Ib:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato; o
con la estructura de fórmula VIII:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o una sal, solvato, o hidrato farmacéuticamente aceptable, de la misma; o
con la estructura de fórmula IX:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o sus sales farmacéuticas aceptables, solvatos, o hidratos.
3. El compuesto de la reivindicación 1 ó 2,
donde A es N; y/o
donde B es N, o B es CH o CH2; y/o
donde D es N, o D es CH o CH2,
4. El compuesto de cualquiera de las reivindicaciones 1 a 3,
donde R6 es arilo C6-i4, opcionalmente sustituido por uno o más sustituyentes; o
donde R6 es fenilo, opcionalmente sustituido por uno o más sustituyentes, cada uno seleccionado independientemente del grupo consistente en halo, ciano, nitro, amino, hidroxilo y metoxi; o
donde R6 es fenilo, aminofenilo, nitrofenilo o metoxifenilo; o
donde R6 es aralquilo C7-15, opcionalmente sustituido por uno o más sustituyentes; o
donde R6 es -(CRARB)m-arilo C6-14, y RA y RB son independientemente (a) hidrógeno, ciano, halo o nitro; o (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo; y m es un número entero de 1, 2 ó 3; donde cada alquilo, alquenilo, alquinilo, cicloalquilo, arilo, aralquilo, heteroarilo, y heterociclilo se substituyen opcionalmente con uno o más substituents; o
donde R6 es bencilo, opcionalmente sustituido por uno o más sustituyentes; o
donde R6 es bencilo o fenil-etilo, cada uno opcionalmente sustituido por uno o más sustituyentes.
5. El compuesto de cualquiera de las reivindicaciones 1 a 3,
donde R6 es heteroarilo, opcionalmente sustituido por uno o más sustituyentes; o
donde R6 es pirazolilo, Imidazolilo, tiazolilo, 1,2,3-triazolilo, tetrazolilo, piridinilo, piridazinilo, pirimidinilo, pirazinilo, o quinolinilo, cada uno sustituido opcionalmente con uno o más sustituyentes; preferiblemente en donde R6 es piridinilo; más preferiblemente donde R6 es 3-piridinilo;
opcionalmente, donde cada sustituyente es independientemente -L-(CRCRD)n-RE, donde RC y RD son cada uno, independientemente, (a) hidrógeno, ciano, halo, o nitro; o (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo; cada uno sustituido opcionalmente por uno o más sustituyentes Q; RE es hidrógeno, -NRFRG, o heterociclilo; L es un enlace, -O-, o -N(RH)-; RF, -RG y RH son cada uno, independientemente, hidrógeno o alquilo C1-6; y n es un número entero de 0, 1,2 ó 3; donde cada alquilo y heterociclilo es independientemente, opcionalmente sustituido por uno o más sustituyentes;
en donde L es preferiblemente un enlace, -O-, -NH-, o
-N(CH3)-; donde RC y RD son preferentemente hidrógeno; donde RE es preferiblemente hidrógeno, metilamino, dimetilamino, pirrolidinilo, piperidinilo, o morfolinilo, en donde el pirrolidinilo, el piperidinilo, y el morfolinilo están, independiente y opcionalmente, sustituidos con metilo; o
opcionalmente, donde cada sustituyente se selecciona independientemente del grupo que consiste en amino, fluoro, cloro, metilo, (dimetilamino)metilo, (dimetilamino)etilo, (dimetilamino)propilo, morfolinilmetilo, (morfolinil)etilo, (morfolinil)propilo, metoxi, (dimetilamino)etoxi, (dimetilamino)propoxi, (morfolinil)etoxi, (morfolinil)propoxi, (metilpiperidinil)oxi, (metil-pirrolidinil)-oxi, metilamino, dimetilamino, (dimetilamino)etilamino, (dimetilaminoetil)-(metil)amino, (dimetilamino)propilamino, ((dimetilamino)propil)(metil)amino, (morfolinil)etilamino, ((morfolinil)etil)(metil)amino, (morfolinil)propilamino, ((morfolinil)propil)(metil)amino, metil-piperidinilamino, (metil-piperidinil)-(metil)amino, metilpiperazinilo, y (dimetilamino)-piperidinilo.
6. El compuesto de la reivindicación 1,
con la estructura de fórmula III:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato;
donde:
U es -C(O)-, -C(O)O-, -C(O)NR1a-, -O-, -OC(O)O-, -OC(O)NR1a-, -NR1a-, -NR1aC(O)NR1d-, -NR1aS(O)-, -NR1aS(O)2-, -NR1aS(O)NR1d-, -NR1aS(O)2NR1d-, -S-, -S(O)-, o -S(O)2-; y
R8 es (a) hidrógeno, ciano, halo o nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo; cada uno sustituido opcionalmente por uno o más sustituyentes; o (c)-C(O)R1a, -C(O)OR1b, -C(O)NR1bR1c, -C(NRa)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a,
-OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c, o -S(O)2NR1bR1c; preferiblemente en donde R8 es hidrógeno, hidroxilo o metoxi; o
con la estructura de la fórmula IV:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato o hidrato;
donde:
R8 es (a) hidrógeno, ciano, halo o nitro; (b) alquilo C i-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-i4, aralquilo C7-15, heteroarilo o heterociclilo; cada uno sustituido opcionalmente por uno o más sustituyentes; o (c) -C(O)R1a, -C(O)OR1b, -C(O)NR1bR1c, -C(NRa)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a,
-OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c, o -S(O)2NR1bR1c;
RA y RB son cada uno, independientemente, (a) hidrógeno, ciano, halo, o nitro; o (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo; cada uno sustituido opcionalmente por uno o más sustituyentes; y
m es un número entero de 1,2 ó 3; o
con la estructura de fórmula V:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o su sal farmacéutica aceptable, solvato, o hidrato;
donde:
A2, A3, y A4 son cada uno, independientemente, C, N, o CR8; con la condición de que no más de uno de A2, A3, y A4 es N; preferiblemente en donde A2, A3, y A4 son independientemente CR8; o A2 es N, y A3y A4 son independientemente CR8; o A2 y A4 son independientemente CR8, y A3 es N; o A2 y A3 son independientemente CR8, y A4 es N;
RA y RB son cada uno, independientemente, (a) hidrógeno, ciano, halo, o nitro; o (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo; cada uno sustituido opcionalmente por uno o más sustituyentes;
cada R8 es, independientemente, (a) hidrógeno, ciano, halo o nitro; (b) alquilo Ci-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo; cada uno sustituido opcionalmente por uno o más sustituyentes; o (c) -C(O)R1a, -C(O)OR1b, -C(O)NR1bR1c,
-C(NRa)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c, o -S(O)2NR1bR1c; y
p es un número entero de 0, 1,2 ó 3; o
con la estructura de fórmula VI:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o sus sales farmacéuticas aceptables, solvatos, o hidratos, donde R8 es como se define para la fórmula V; o
con la estructura de fórmula VII:
o un enantiómero, una mezcla de enantiómeros, o una mezcla de dos o más de sus diastereoisómeros; o una sal, solvato, o hidrato farmacéutica aceptable, de la misma;
donde:
E2, E3 y E4 son cada uno, independientemente, C, N, O, S, CR8, o NR8; preferiblemente en donde E2, E3y E4 son CR8; o E2 y E4 son CR8y E3 es NR8, O , o S ; o E 2y E3 son N, y E4 es CR8; o E2, E3 y E4 son N.
RA y RB son cada uno, independientemente, (a) hidrógeno, ciano, halo, o nitro; o (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo; cada uno sustituido opcionalmente por uno o más sustituyentes;
cada R8 es, independientemente, (a) hidrógeno, ciano, halo o nitro; (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo; cada uno sustituido opcionalmente por uno o más sustituyentes; o (c) -C(O)R1a, -C(O)OR1b, -C(O)NR1bR1c,
-C(NRa)NR1bR1c, -OR1a, -OC(O)R1a, -OC(O)OR1a, -OC(O)NR1bR1c, -OC(=NR1a)NR1bR1c, -OS(O)R1a, -OS(O)2R1a, -OS(O)NR1bR1c, -OS(O)2NR1bR1c, -NR1bR1c, -NR1aC(O)R1d, -NR1aC(O)OR1d, -NR1aC(O)NR1bR1c, -NR1aC(=NR1d)NR1bR1c, -NR1aS(O)R1d, -NR1aS(O)2R1d, -NR1aS(O)NR1bR1c, -NR1aS(O)2NR1bR1c, -SR1a, -S(O)R1a, -S(O)2R1a, -S(O)NR1bR1c, o -S(O)2NR1bR1c; y
p es un número entero de 0, 1,2 ó 3,
7. El compuesto de la reivindicación 6,
donde R8 es hidrógeno; o
donde R8 es -L-(CRCRD)n-RE, donde RC y RD son cada uno, independientemente, (a) hidrógeno, ciano, halo, o nitro; o (b) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3.7, arilo C6-14, aralquilo C7-15, heteroarilo o heterociclilo; cada uno sustituido opcionalmente por uno o más sustituyentes Q; RE es hidrógeno, -NRFRG, o heterociclilo; L es un enlace, -O-, o -N(RH)-; RF, RGy RH son cada uno, independientemente, hidrógeno o alquilo C1-6; y n es un número entero de 0, 1, 2 ó 3; donde cada alquilo y heterociclilo es independientemente opcionalmente sustituido por uno o más sustituyentes; donde L es preferiblemente un enlace, -O-, -NH-, o -N(CH3)-; donde RC y RD son preferentemente hidrógeno; RE es preferiblemente hidrógeno, metilamino, dimetilamino, pirrolidinilo, piperidinilo, o morfolinilo, en donde el pirrolidinilo, el piperidinilo, y el morfolinilo están, independiente y opcionalmente, sustituidos con metilo; o donde R8 se selecciona independientemente del grupo que consiste en amino, fluoro, cloro, metilo, (dimetilamino)metilo, (dimetilamino)etilo, (dimetilamino)propilo, morfolinilmetilo, (morfolinil)etilo, (morfolinil)propilo, metoxi, (dimetilamino)etoxi, (dimetilamino)propoxi, (morfolinil)etoxi, (morfolinil)propoxi, (metil-piperidinil)oxi, (metilpirrolidinil)oxi, metilamino, dimetilamino, (dimetilamino)etilamino, (dimetilaminoetil)(metil)amino, (dimetilamino)propilamino, ((dimetilamino)propil)(metil)amino, (morfolinil)etilamino, ((morfolinil)etil)(metil)amino, (morfolinil)propilamino, ((morfolinil)propil)(metil)amino, metil-piperidinilamino, (metil-piperidinil)(metil)amino, metilpiperazinilo, y (dimetilamino)-piperidinilo; y
donde RA y RB son hidrógeno.
8. El compuesto de cualquiera de las reivindicaciones 1 a 7,
donde R1 es alquilo C1-6, -S-alquilo C1-6, o -SO2-alquilo C1-6, donde cada alquilo es independientemente opcionalmente sustituido por de uno a tres halo; preferiblemente en donde R1 es metilo, fluorometilo, difluorometilo, trifluorometilo, metanosulfanilo, o metanosulfonilo, o R1 es difluorometilo, o R1 es metanosulfanilo, o R1 es metanosulfonilo; y/o donde R2 es hidrógeno, alquilo C1-6, o -O-alquilo C1-6, donde cada alquilo se sustituye opcionalmente por uno o más sustituyentes; preferiblemente en donde R2 es hidrógeno, o R2 es metoxi; y/o
donde R3 es hidrógeno, amino, o alquilo C1-6, opcionalmente sustituido por uno o más sustituyentes; preferiblemente en donde R3 es hidrógeno o R3 es amino.
9. El compuesto de cualquiera de las reivindicaciones 1 a 8,
donde R4 es hidrógeno o alquilo C1-6, opcionalmente sustituido por uno o más sustituyentes; preferiblemente en donde R4 es hidrógeno; y/o
donde R5 es hidrógeno o alquilo C1-6, opcionalmente sustituido por uno o más sustituyentes; preferiblemente en donde R5 es hidrógeno; o
donde R4 y R5 están unidos para formar un enlace o alquileno C1-6; preferiblemente en donde R4 y R5 se unen para formar un enlace, metileno o etileno.
10. El compuesto de cualquiera de las reivindicaciones 1 a 9,
donde U es -O-, -NR1a-, -S-, -S(O)-, o -S(O)2-, donde R1a es alquilo C1-6, opcionalmente sustituido por uno o más sustituyentes; preferiblemente donde U es -O-, -NH-, -NCH3-, -S-,
-S(O)-, o -S(O)2-; preferiblemente en donde U es -NH-.
11. El compuesto de la reivindicación 1,
seleccionado del grupo que consiste en:
4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-W-(3-piridinil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-A/-('3-piridinil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-A/-metil-6-(4-morfolinil)-W-(3-piridinil)-1,3,5-triazin-2-amina;
4-[2-(met¡lsulfan¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-(3-p¡r¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(met¡lsulfon¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-(3-p¡r¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-femM,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-met¡l-6-(4-morfol¡ml)-W-femM,3,5-tr¡az¡n-2-am¡na;
W-bendl-4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
W-bendl-4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-met¡l-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
2-(d¡fluoromet¡l)-1-[4-(4-morfol¡ml)-6-fenox¡-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-1-[4-(4-morfol¡ml)-6-(femlsulfaml)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-1-[4-(4-morfol¡ml)-6-(femlsulfoml)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
W-(2-doro-5-p¡r¡m¡d¡n¡l)-4-[2-(d¡fluoromet¡l)-4-metox¡-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-met¡l-6-(4-morfol¡ml)-W-(5-p¡r¡m¡d¡ml)-1,3,5-tr¡az¡n-2-am¡na; y
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-met¡l-6-(4-morfolm¡l)-W-(5-p¡r¡m¡d¡ml)-1,3,5-tr¡az¡n-2-am¡na; y enant¡ómeros, mezclas de enant¡ómeros, o mezclas de dos o más d¡astereómeros de los m¡smos; y las sales farmacéuticas aceptables, solvatos, e h¡dratos de la m¡sma; o
selecc¡onado del grupo que cons¡ste en:
W-[4-[6-am¡no-2-(d¡fluorometil)-4-metoxMH-bendm¡dazol-1-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-A/-(3-p¡r¡d¡ml)amma; W5-[4-[2-(d¡fluorometil)-4-metoxMH-bendm¡dazol-1-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluorometil)-4-metoxMH-bendm¡dazol-1-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[3-(d¡metilam¡no)prop¡l]-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluorometil)-4-metoxMH-bendm¡dazol-1-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[3-(d¡metilam¡no)prop¡l]-W2-met¡l-2,5-p¡r¡d¡nd¡am¡na;
4-[2-(d¡fluorometil)-4-metox¡-1H-bendm¡dazoM-¡l]-A/-(6-metox¡-3-p¡r¡d¡n¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluorometil)-4-metoxMH-bendm¡dazoM-¡l]-A/-{6-[3-(d¡metilam¡no)propox¡]-3-p¡r¡d¡ml}-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluorometil)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-(5-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluorometil)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-(3-p¡r¡daz¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluorometil)-1H-bendm¡dazoM-¡l]-W-(1-metiMH-¡m¡dazol-5-¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; y 4-[2-(d¡fluorometil)-1H-bendm¡dazoM-¡l]-W-('1-metiMH-p¡razol-5-¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
o enant¡ómeros, mezclas de enant¡ómeros, o mezclas de dos o más d¡astereómeros de los m¡smos; o sales farmacéut¡cas aceptables, solvatos e h¡dratos de los m¡smos; o
selecc¡onados del grupo que cons¡ste en:
4-[4-metox¡-2-(met¡lsulfon¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-W-(3-p¡r¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-W-(2-p¡r¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluorometil)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-(2-p¡r¡d¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-W-(4-p¡r¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-(4-p¡r¡d¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-W-(4-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluorometil)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-(4-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-('5-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
2-(d¡fluoromet¡l)-1-[4-(4-morfol¡ml)-6-(3-p¡r¡d¡mlox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(3-p¡r¡d¡mlox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-1-[4-(4-morfol¡ml)-6-(5-p¡r¡m¡d¡mlox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(5-p¡r¡m¡d¡mlox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-(1-met¡l-1H-p¡razol-4-¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-(1-met¡MH-p¡razol-4-¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-(2-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-(2-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-(3-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-(3-p¡nd¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-(4-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-(4-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-met¡l-6-(4-morfol¡ml)-W-(2-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-met¡l-6-(4-morfolm¡l)-W-(2-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-met¡l-6-(4-morfol¡ml)-W-(3-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-met¡l-6-(4-morfolm¡l)-W-(3-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-met¡l-6-(4-morfol¡ml)-W-(4-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-met¡l-6-(4-morfolm¡l)-W-(4-p¡r¡d¡mlmet¡l)-1,3,5-tr¡az¡n-2-am¡na; 2-(d¡fluoromet¡l)-1-[4-(4-morfol¡ml)-6-(2-p¡r¡d¡mlmetox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(2-p¡r¡d¡mlmetox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-1-[4-(4-morfol¡ml)-6-(3-p¡r¡d¡mlmetox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(3-p¡r¡d¡mlmetox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-1-[4-(4-morfol¡ml)-6-(4-p¡r¡d¡mlmetox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
2-(d¡fluoromet¡l)-4-metoxM-[4-(4-morfol¡ml)-6-(4-p¡r¡d¡mlmetox¡)-1,3,5-tr¡az¡n-2-¡l]-1H-bendm¡dazol;
4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-[2-(2-p¡r¡d¡n¡l)et¡l]-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-[2-(2-p¡r¡d¡n¡l)et¡l]-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-[2-(3-p¡r¡d¡n¡l)et¡l]-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-[2-(3-p¡r¡d¡n¡l)et¡l]-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-W-[2-(4-p¡r¡d¡n¡l)et¡l]-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-A/-[2-(4-p¡r¡d¡n¡l)et¡l]-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-W-[2-(1H-¡m¡dazol-4-¡l)et¡l]-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-bendm¡dazoM-¡l]-A/-[2-(1H-¡m¡dazol-4-¡l)et¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; W-[4-[6-am¡no-2-(d¡fluoromet¡l)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-A/-(3-p¡r¡d¡n¡l)am¡na;
W-[4-[2-(d¡fluoromet¡l)-6-(met¡lam¡no)-1H-bendm¡dazoM-¡l]-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-¡l]-W-(3-p¡r¡dm¡l)am¡na; W-[4-[2-(d¡fluoromet¡l)-4-metox¡-6-(met¡lam¡no)-1H-bendm¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-A/-(3-p¡r¡d¡n¡l)am¡na;
W-[4-[2-(d¡fluoromet¡l)-6-(d¡met¡lam¡no)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-triaz¡n-2-¡l]-W-(3-p¡r¡d¡n¡l)am¡na; W-[4-[2-(d¡fluoromet¡l)-6-(d¡met¡lam¡no)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-A/-(3-p¡r¡d¡n¡l)am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-(6-metox¡-3-p¡r¡d¡n¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-(2-metox¡-4-p¡r¡d¡n¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-(2-metox¡-4-p¡r¡d¡n¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-(2-metox¡-5-p¡r¡m¡d¡n¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-(2-metox¡-5-p¡rim¡d¡ml)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-{6-[2-(d¡met¡lam¡no)etox¡]-3-p¡r¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{6-[2-(d¡met¡lam¡no)etox¡]-3-p¡nd¡ml}-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-W-{6-[2-(4-morfolm¡l)etox¡]-3-p¡r¡d¡ml}-1,3,5-tnaz¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-{6-[2-(4-morfol¡ml)etox¡]-3-p¡r¡d¡ml}-1,3,5-tnaz¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-{6-[3-(d¡met¡lam¡no)propox¡]-3-p¡r¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tnaz¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-W-{6-[3-(4-morfolm¡l)propox¡]-3-p¡r¡d¡ml}-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-{6-[3-(4-morfol¡ml)propox¡]-3-p¡nd¡ml}-1,3,5-tr¡az¡n-2-am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-met¡l-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-met¡l-2,5-p¡r¡d¡nd¡am¡na; W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2,W2-d¡met¡l-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2,W2-d¡met¡l-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(d¡met¡lam¡no)et¡l]-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(d¡met¡lam¡no)et¡l]-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(4-morfol¡n¡l)et¡l]-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(4-morfol¡n¡l)et¡l]-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(d¡met¡lam¡no)et¡l]-W2-met¡l-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(d¡met¡lam¡no)et¡l]-Aiemet¡l-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2met¡l-W2-[2-(4-morfol¡n¡l)et¡l]-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2'met¡l-W2-[2-(4-morfol¡n¡l)et¡l]-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[3-(d¡met¡lam¡no)prop¡l]-2,5-p¡r¡d¡nd¡am¡na;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-[3-(dimetilamino)propil]-W2-metil-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-[3-(4-morfolinil)propil]-2,5-piridindiamina;
W2-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-[3-(4-morfolinil)propil]-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-[3-(4-morfolinil)propil]-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-[3-(4-morfolinil)propil]-2,5-piridindiamina;
4-[2-(difluorometil)-1H-bencimidazoM-il]-W-{6-[2-(dimetilamino)etil]-3-piridiml}-6-(4-morfolmil)-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-{6-[2-(dimetilamino)etil]-3-piridiml}-6-(4-morfolmil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazoM-il]-6-(4-morfolmil)-W-{6-[2-(4-morfolmil)etil]-3-piridiml}-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-6-(4-morfoliml)-A/-{6-[2-(4-morfoliml)etil]-3-piridiml}-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazoM-il]-W-{2-[2-(dimetilamino)etil]-5-pirimidiml}-6-(4-morfoliml)-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-{2-[2-(dimetilamino)etil]-5-pirimidiml}-6-(4-morfolmil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-W-{2-[2-(4-morfolinil)etil]-5-pirimidinil}-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-6-(4-morfoliml)-A/-{2-[2-(4-morfoliml)etil]-5-pirimidiml}-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazol-1-il]-W-{5-[2-(dimetilamino)etoxi]-3-piridinil}-6-(4-morfolinil)-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-{5-[2-(dimetilamino)etoxi]-3-piridiml}-6-(4-morfoliml)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-6-(4-morfoliml)-A/-{5-[2-(4-morfoliml)etoxi]-3-piridiml}-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-W-{5-[2-(4-morfolinil)etoxi]-3-piridinil}-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-1H-bencimidazol-1-il]-W-{5-[3-(dimetilamino)propoxi]-3-piridinil}-6-(4-morfolinil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-{5-[3-(dimetilamino)propoxi]-3-piridiml}-6-(4-morfoliml)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-W-{5-[3-(4-morfolinil)propoxi]-3-piridinil)-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-6-(4-morfoliml)-A/-{5-[3-(4-morfoliml)propoxi]-3-piridiml}-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazol-1-il]-W-{2-[2-(dimetilamino)etoxi]-4-piridinil}-6-(4-morfolinil)-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-{2-[2-(dimetilamino)etoxi]-4-piridiml)-6-(4-morfoliml)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-W-{2-[2-(4-morfolinil)etoxi]-4-piridinil}-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-6-(4-morfoliml)-A/-{2-[2-(4-morfoliml)etoxi]-4-piridiml}-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazol-1-il]-W-{2-[3-(dimetilamino)propoxi]-4-piridinil}-6-(4-morfolinil)-1,3,5-triazin-2-amina;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{2-[3-(d¡met¡lam¡no)propox¡]-4-p¡r¡d¡ml}-6-(4-morfol¡ml)-1,3,5-triazin-2-amina;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-W-{2-[3-(4-morfolm¡l)propox¡]-4-p¡r¡d¡ml}-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-{2-[3-(4-morfol¡ml)propox¡]-4-p¡nd¡ml}-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-{2-[2-(d¡met¡lam¡no)etox¡]-5-p¡r¡m¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{2-[2-(d¡met¡lam¡no)etox¡]-5-p¡r¡m¡d¡n¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-{2-[3-(d¡met¡lam¡no)propox¡]-5-p¡nm¡d¡ml}-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{2-[3-(d¡met¡lam¡no)propox¡]-5-p¡r¡m¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-W-{2-[2-(4-morfolm¡l)etox¡]-5-p¡r¡m¡d¡ml}-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-{2-[2-(4-morfol¡ml)etox¡]-5-p¡r¡m¡d¡ml}-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-W-{2-[3-(4-morfolm¡l)propox¡]-5-p¡r¡m¡d¡ml}-1,3,5-tnaz¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-{2-[3-(4-morfol¡ml)propox¡]-5-p¡nm¡d¡ml}-1,3,5-tr¡az¡n-2-am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(d¡met¡lam¡no)et¡l]-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(d¡met¡lam¡no)et¡l]-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(d¡met¡lam¡no)et¡l]-W2-met¡l-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(d¡met¡lam¡no)et¡l]-Wemet¡l-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[3-(d¡met¡lam¡no)prop¡l]-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[3-(d¡met¡lam¡no)prop¡l]-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[3-(d¡met¡lam¡no)prop¡l]-W2-met¡l-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[3-(d¡met¡lam¡no)prop¡l]-W2-met¡l-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(4-morfol¡n¡l)et¡l]-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[2-(4-morfol¡ml)et¡l]-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-met¡l-W2-[2-(4-morfol¡n¡l)et¡l]-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-met¡l-W2-[2-(4-morfol¡n¡l)et¡l]-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-¡l]-W2-[3-(4-morfolm¡l)prop¡l]-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-[3-(4-morfolinil)propil]-2,5-pirimidindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-[3-(4-morfolinil)propil]-2,5-pirimidindiamina;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-[3-(4-morfolinil)propil]-2,5-pirimidindiamina;
4-[2-(difluorometil)-1H-bencimidazoM-il]-W-[6-(4-metiM-piperaziml)-3-piridiml]-6-(4-morfolmil)-1,3,5-triazin-2-amina; 4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-[6-(4-metiM-piperazinil)-3-piridiml]-6-(4-morfolmil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazoM-il]-W-[2-(4-metiM-piperaziml)-5-pirimidiml]-6-(4-morfoliml)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-[2-(4-metiM-piperazinil)-5-pirimidiml]-6-(4-morfolmil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazoM-il]-W-{6-[4-(dimetilamino)-1-piperidiml]-3-piridiml}-6-(4-morfolmil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-{6-[4-(dimetilamino)-1-piperidiml]-3-piridiml}-6-(4-morfoliml)-1.3.5- triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazol-1-il]-W-{2-[4-(dimetilamino)-1-piperidinil]-5-pirimidinil}-6-(4-morfolinil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-{2-[4-(dimetilamino)-1-piperidiml]-5-pirimidiml}-6-(4-morfolmil)-1.3.5- triazin-2-amina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-(1-metil-4-piperidinil)-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-(1-metil-4-piperidinil)-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-(1-metil-4-piperidinil)-2,5-piridindiamina;
W-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-(1-metil-4-piperidinil)-2,5-piridindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-(1-metil-4-piperidinil)-2,5-pirimidindiamina;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-(1-metil-4-piperidinil)-2,5-pirimidindiamina;
W5-[4-[2-(difluorometil)-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2metil-W2-(1-metil-4-piperidinil)-2,5-pirimidindiamina;
W5-[4-[2-(difluorometil)-4-metoxi-1H-bencimidazol-1-il]-6-(4-morfolinil)-1,3,5-triazin-2-il]-W2-metil-W2-(1-metil-4-piperidinil)-2,5-pirimidindiamina;
4-[2-(difluorometil)-1H-bencimidazol-1-il]-W-{6-[(1-metil-4-piperidinil)oxi]-3-piridinil}-6-(4-morfolinil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-{6-[(1-metil-4-piperidiml)oxi]-3-piridiml}-6-(4-morfolmil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazol-1-il]-W-{2-[(1-metil-4-piperidinil)oxi]-5-pirimidinil}-6-(4-morfolinil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-4-metoxMH-bencimidazoM-il]-A/-{2-[(1-metil-4-piperidiml)oxi]-5-pirimidiml}-6-(4-morfolmil)-1,3,5-triazin-2-amina;
4-[2-(difluorometil)-1H-bencimidazol-1-il]-W-{6-[(1-metil-3-pirrolidinil)oxi]-3-piridinil}-6-(4-morfolinil)-1,3,5-triazin-2-amina;
4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazoM-¡l]-A/-{6-[(1-met¡l-3-p¡rrol¡d¡ml)ox¡]-3-p¡r¡d¡ml}-6-(4-morfolm¡l)-1,3,5-triazin-2-amina;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-{2-[(1-met¡l-3-p¡rrol¡d¡n¡l)ox¡]-5-p¡r¡m¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{2-[(1-met¡l-3-p¡rrol¡d¡ml)ox¡]-5-p¡r¡m¡d¡ml}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-{1-[2-(d¡met¡lam¡no)et¡l]-1H-p¡razol-4-¡l}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{1-[2-(d¡met¡lam¡no)et¡l]-1H-p¡razol-4-¡l}-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-6-(4-morfolm¡l)-W-{1-[2-(4-morfolm¡l)et¡l]-1H-p¡razol-4-¡l}-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-{1-[2-(4-morfol¡ml)et¡l]-1H-p¡razol-4-¡l}-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-{1-[3-(d¡met¡lam¡no)prop¡l]-1H-p¡razol-4-¡l}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{1-[3-(d¡met¡lam¡no)prop¡l]-1H-p¡razol-4-¡l}-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-W-{1-[3-(4-morfol¡n¡l)prop¡l]-1H-p¡razol-4-¡l}-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/{1-[3-(4-morfolm¡l)prop¡l]-1H-p¡razol-4-¡l}-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-W-('1,3-t¡azol-5-¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-('1,3-t¡azol-5-¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-{2-[(d¡met¡lam¡no)met¡l]-1,3-t¡azol-5-¡l}-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-{2-[(d¡met¡lam¡no)met¡l]-1,3-t¡azol-5-¡l}-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-W-[2-(4-morfol¡n¡lmet¡l)-1,3-t¡azol-5-¡l]-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-6-(4-morfol¡ml)-A/-[2-(4-morfol¡mlmet¡l)-1,3-t¡azol-5-¡l]-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-(1-met¡l-1H-¡m¡dazol-5-¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazoM-¡l]-W-(1-met¡MH-1,2,3-tr¡azol-5-¡l)-6-(4-morfolm¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-(1-met¡MH-1,2,3-tr¡azol-5-¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-W-(2-met¡l-2H-1,2,3-tr¡azol-4-¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-(2-met¡l-2H-1,2,3-tr¡azol-4-¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-W-(1-met¡l-1H-1,2,3-tr¡azol-4-¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-(1-met¡MH-1,2,3-tr¡azol-4-¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-W-(2-met¡l-2H-tetrazol-5-¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metoxMH-benc¡m¡dazoM-¡l]-A/-(2-met¡l-2H-tetrazol-5-¡l)-6-(4-morfol¡ml)-1,3,5-tr¡az¡n-2-am¡na; 4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-W-(1-met¡l-1H-tetrazol-5-¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-A/-(1-met¡l-1H-tetrazol-5-¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na; W5-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-2,5-p¡r¡m¡d¡nd¡am¡na;
W5-[4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-2,5-p¡r¡m¡d¡nd¡am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-W-(2-p¡raz¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-A/-(2-p¡raz¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
W2-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-2,5-p¡raz¡nd¡am¡na;
W2-[4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-2,5-p¡raz¡nd¡am¡na;
W2-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-2,6-p¡raz¡nd¡am¡na;
W2-[4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-2,6-p¡raz¡nd¡am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-W-(6-metox¡-2-p¡raz¡n¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-A/-(6-metox¡-2-p¡raz¡n¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na; y W[4-[6-am¡no-2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-W-(3-p¡r¡d¡n¡l)am¡na; y enant¡ómeros, mezclas de enant¡ómeros, o mezclas de dos o más d¡astereómeros de los m¡smos; y las sales farmacéuticas aceptables, solvatos, e h¡dratos de la m¡sma; o
selecc¡onados del grupo que cons¡ste en:
W-[4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-¡l]-3-qu¡nol¡nam¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-W-(2-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-W-(4-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-W-(5-p¡r¡m¡d¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-1H-benc¡m¡dazol-1-¡l]-W-(4-metox¡-3-p¡r¡d¡n¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-A/-(6-fluoro-3-p¡r¡d¡n¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
W-(6-cloro-3-p¡r¡d¡n¡l)-4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na;
4-(2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l)-A/-(6-metox¡p¡r¡m¡d¡n-4-¡l)-6-morfol¡no-1,3,5-tr¡az¡n-2-am¡na;
4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-6-(4-morfol¡n¡l)-N-(3-p¡r¡daz¡n¡l)-1,3,5-tr¡az¡n-2-am¡na; y
4-[2-(d¡fluoromet¡l)-4-metox¡-1H-benc¡m¡dazol-1-¡l]-N-(6-metox¡-3-p¡r¡daz¡n¡l)-6-(4-morfol¡n¡l)-1,3,5-tr¡az¡n-2-am¡na; o enant¡ómeros, mezclas de enant¡ómeros, o mezclas de dos o más d¡astereómeros de los m¡smos; o sales farmacéut¡cas aceptables, solvatos, o h¡dratos de los m¡smos.
12. Una compos¡c¡ón farmacéut¡ca que comprende un compuesto de cualqu¡era de las re¡v¡nd¡cac¡ones 1 a 11, o un enant¡ómero, una mezcla de enant¡ómeros, o una mezcla de dos o más de sus d¡astereo¡sómeros; o una sal, solvato, o h¡drato farmacéut¡camente aceptables de los m¡smos.
13. La compos¡c¡ón farmacéut¡ca de la re¡v¡nd¡cac¡ón 12,
en el que la compos¡c¡ón comprende además un segundo agente terapéut¡co; y/o
en el que la compos¡c¡ón está formulada para la adm¡n¡strac¡ón de dos¡s ún¡cas; y/o
en el que la compos¡c¡ón se formula como una forma de adm¡n¡strac¡ón oral, parenteral, o ¡ntravenosa, opc¡onalmente donde la forma de adm¡n¡strac¡ón oral es una tableta o cápsula.
14. El compuesto de cualqu¡era de las re¡v¡nd¡cac¡ones 1 a 11 o la compos¡c¡ón farmacéut¡ca de la re¡v¡nd¡cac¡ón 12 ó 13 para su uso en un método de tratam¡ento, prevenc¡ón o mejoram¡ento de una enfermedad selecc¡onada del grupo cons¡stente en: enfermedades ¡nflamator¡as o alérg¡cas; enfermedades ¡nflamator¡as ¡ntest¡nales; vascul¡t¡s, y síndrome de Behcet; psor¡as¡s y dermatos¡s ¡nflamator¡a; asma y enfermedades alérg¡cas resp¡rator¡as; enfermedades auto¡nmunes; rechazo de ¡njerto; f¡ebre; trastornos card¡ovasculares; trastornos cerebrovasculares; cáncer, en part¡cular cánceres de mama, p¡el, próstata, cuello uter¡no, útero, ovar¡o, testículos, vej¡ga, pulmón, hígado, lar¡nge,
cavidad bucal, colon y tracto gastrointestinal, cerebro, tiroides, sangre y sistema linfático; fibrosis, enfermedad del tejido conjuntivo, sarcoidosis; afecciones genitales y reproductivas; trastornos gastrointestinales; trastornos neurológicos; trastornos del sueño; dolor; trastornos renales; trastornos oculares; y enfermedades infecciosas.
15. El compuesto o la composición farmacéutica para su uso de acuerdo con la reivindicación 14, en el que el compuesto o la composición farmacéutica se utiliza en un método de tratamiento, prevención o mejoramiento del cáncer, donde el cáncer es preferiblemente seleccionado del grupo que consiste en leucemias, policitemia vera, linfomas, mieloma múltiple, macroglobulinernia de Waldenstrom, gammopatía monoclonal de significación indeterminada, gammopatía monoclonal benigna, enfermedad de cadena pesada, sarcomas del hueso y del tejido conectivo, tumores del cerebro, cáncer de mama, cáncer suprarrenal, cáncer de tiroides, cáncer de páncreas, cáncer de la hipófisis, cáncer de ojos, cáncer vaginal, incluyendo, cáncer vulvar, cáncer de cuello uterino, cáncer de ovario, cáncer de esófago, cáncer de estómago, cáncer de colon; cáncer rectal; cáncer de hígado, cáncer de la vesícula biliar, colangiocarcinomas, cáncer de pulmón, cáncer testicular, cáncer de próstata, cáncer penal, cáncer bucal, cáncer de glándulas salivales, cáncer de faringe, cáncer de piel, cáncer de riñón, tumor de Wilms y cáncer de vejiga.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US22368409P | 2009-07-07 | 2009-07-07 | |
| US24744809P | 2009-09-30 | 2009-09-30 | |
| US31819510P | 2010-03-26 | 2010-03-26 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2706185T3 true ES2706185T3 (es) | 2019-03-27 |
Family
ID=42791020
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES14168117T Active ES2706185T3 (es) | 2009-07-07 | 2010-07-06 | Pirimidinil y 1,3,5-triazinil bencimidazoles y sus usos en la terapia contra el cáncer |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US8486939B2 (es) |
| EP (3) | EP2451802A1 (es) |
| AR (1) | AR080945A1 (es) |
| CA (2) | CA2987503C (es) |
| DK (1) | DK3072890T3 (es) |
| ES (1) | ES2706185T3 (es) |
| TW (1) | TW201105662A (es) |
| WO (1) | WO2011005119A1 (es) |
Families Citing this family (51)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US12110555B2 (en) | 2004-12-08 | 2024-10-08 | Cedars-Sinai Medical Center | Diagnosis and treatment of inflammatory bowel disease |
| US11268149B2 (en) | 2004-12-08 | 2022-03-08 | Cedars-Sinai Medical Center | Diagnosis and treatment of inflammatory bowel disease |
| JP2011512963A (ja) * | 2008-02-29 | 2011-04-28 | ザ リージェンツ オブ ザ ユニバーシティ オブ ミシガン | 組織における変化を撮像するためのシステムおよび方法 |
| JP5555378B2 (ja) * | 2010-07-14 | 2014-07-23 | エフ.ホフマン−ラ ロシュ アーゲー | Pi3kp110デルタに選択的なプリン化合物とその使用の方法 |
| WO2012044641A1 (en) * | 2010-09-29 | 2012-04-05 | Pathway Therapeutics Inc. | 1,3,5-triazinyl benzimidazole sulfonamides and their use in cancer therapy |
| JP2014509648A (ja) * | 2011-03-28 | 2014-04-21 | メイ プハルマ,インコーポレーテッド | (α−置換シクロアルキルアミノ及びヘテロシクリルアミノ)ピリミジニル及び1,3,5−トリアジニルベンズイミダゾール、その医薬組成物、並びに増殖性疾患の治療におけるそれらの使用 |
| ES2608967T3 (es) * | 2011-03-28 | 2017-04-17 | Mei Pharma, Inc. | (Aralquilamino sustituido en alfa y heteroarilalquilamino)pirimidinil y 1,3,5-triazinil benzimidazoles, composiciones farmacéuticas que los contienen, y estos compuestos para usar en el tratamiento de enfermedades proliferativas |
| WO2012135166A1 (en) * | 2011-03-28 | 2012-10-04 | Pathway Therapeutics Inc. | (fused ring arylamino and heterocyclylamino) pyrimidynyl and 1,3,5-triazinyl benzimidazoles, pharmaceutical compositions thereof, and their use in treating proliferative diseases |
| WO2013003826A1 (en) | 2011-06-29 | 2013-01-03 | The Regents Of The University Of Michigan | Analysis of temporal changes in registered tomographic images |
| KR20140069235A (ko) | 2011-09-27 | 2014-06-09 | 노파르티스 아게 | 돌연변이체 idh의 억제제로서의 3-피리미딘-4-일-옥사졸리딘-2-온 |
| UY34632A (es) | 2012-02-24 | 2013-05-31 | Novartis Ag | Compuestos de oxazolidin- 2- ona y usos de los mismos |
| US9851426B2 (en) | 2012-05-04 | 2017-12-26 | The Regents Of The University Of Michigan | Error analysis and correction of MRI ADC measurements for gradient nonlinearity |
| WO2014016849A2 (en) | 2012-07-23 | 2014-01-30 | Sphaera Pharma Pvt. Ltd. | Novel triazine compounds |
| WO2014055647A1 (en) * | 2012-10-03 | 2014-04-10 | Mei Pharma, Inc. | (sulfinyl and sulfonyl benzimidazolyl) pyrimidines and triazines, pharmaceutical compositions thereof, and their use for treating proliferative diseases |
| US9737521B2 (en) | 2012-11-08 | 2017-08-22 | Rhizen Pharmaceuticals Sa | Pharmaceutical compositions containing a PDE4 inhibitor and a PI3 delta or dual PI3 delta-gamma kinase inhibitor |
| US9296733B2 (en) | 2012-11-12 | 2016-03-29 | Novartis Ag | Oxazolidin-2-one-pyrimidine derivative and use thereof for the treatment of conditions, diseases and disorders dependent upon PI3 kinases |
| KR20220143164A (ko) | 2012-11-21 | 2022-10-24 | 피티씨 테라퓨틱스, 인크. | 치환된 리버스 피리미딘 bmi-1 저해제 |
| EP2968345B1 (en) | 2013-03-13 | 2017-12-13 | The Regents of The University of Michigan | Dual mek/pi3k inhibitors and their application in the treatment of cancer diseases |
| EP2970240B1 (en) | 2013-03-14 | 2018-01-10 | Novartis AG | 3-pyrimidin-4-yl-oxazolidin-2-ones as inhibitors of mutant idh |
| WO2014160521A1 (en) | 2013-03-15 | 2014-10-02 | Blueprint Medicines Corporation | Piperazine derivatives and their use as kit modulators |
| US9212180B2 (en) | 2013-06-12 | 2015-12-15 | The Regents Of The University Of Michigan | Menin-MLL inhibitors and methods of use thereof |
| WO2014200479A1 (en) * | 2013-06-12 | 2014-12-18 | The Regents Of The University Of Michigan | Menin-mll inhibitors and methods of use thereof |
| TWI666208B (zh) * | 2013-08-02 | 2019-07-21 | 美商阿吉斯藥品有限公司 | 治療活性化合物及其使用方法(三) |
| AR093580A1 (es) | 2013-08-30 | 2015-06-10 | Ptc Therapeutics Inc | Inhibidores bmi-1 de pirimidina sustituidos |
| US9334263B2 (en) | 2013-10-17 | 2016-05-10 | Blueprint Medicines Corporation | Compositions useful for treating disorders related to kit |
| MX365614B (es) | 2013-10-17 | 2019-06-07 | Blueprint Medicines Corp | Composiciones utiles para tratar trastornos relacionados con kit. |
| WO2015076800A1 (en) | 2013-11-21 | 2015-05-28 | Ptc Therapeutics, Inc. | Substituted pyridine and pyrazine bmi-1 inhibitors |
| WO2016022569A1 (en) | 2014-08-04 | 2016-02-11 | Blueprint Medicines Corporation | Compositions useful for treating disorders related to kit |
| WO2017019442A1 (en) | 2015-07-24 | 2017-02-02 | Blueprint Medicines Corporation | Compounds useful for treating disorders related to kit and pdgfr |
| US10650512B2 (en) | 2016-06-14 | 2020-05-12 | The Regents Of The University Of Michigan | Systems and methods for topographical characterization of medical image data |
| ES3002745T3 (en) | 2016-07-06 | 2025-03-07 | Univ Michigan Regents | Multifunctional inhibitors of mek/pi3k and mtor/mek/pi3k biological pathways and therapeutic methods using the same |
| US11040979B2 (en) | 2017-03-31 | 2021-06-22 | Blueprint Medicines Corporation | Substituted pyrrolo[1,2-b]pyridazines for treating disorders related to KIT and PDGFR |
| US11304953B2 (en) * | 2017-05-23 | 2022-04-19 | Mei Pharma, Inc. | Combination therapy |
| CN107266422A (zh) * | 2017-06-12 | 2017-10-20 | 西安交通大学 | 2‑(5‑嘧啶基)‑4‑吗啉基‑6‑取代均三嗪类化合物及其盐、制备方法和应用 |
| AU2018316175B2 (en) | 2017-08-11 | 2023-02-23 | The Regents Of The University Of Michigan | Inhibitors of MEK/PI3K, JAK/MEK, JAK/PI3K/mTOR and MEK/PI3K3k/mTOR biological pathways and methods for improving lymphatic uptake, bioavailability, and solubility of therapeutic compounds |
| KR20200041358A (ko) | 2017-08-14 | 2020-04-21 | 메이 파마, 아이엔씨. | 병용 요법 |
| KR20190043437A (ko) | 2017-10-18 | 2019-04-26 | 씨제이헬스케어 주식회사 | 단백질 키나제 억제제로서의 헤테로고리 화합물 |
| WO2019121872A1 (en) | 2017-12-20 | 2019-06-27 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods for the diagnosis and treatment of liver cancer |
| ES2962715T3 (es) | 2018-04-30 | 2024-03-20 | Cedars Sinai Medical Center | Métodos y sistemas para selección y tratamiento de pacientes con enfermedades inflamatorias |
| CR20210281A (es) | 2018-10-30 | 2021-10-25 | Repare Therapeutics Inc | Compuestos, composiciones farmacéuticas y métodos de preparación de compuestos y de uso como inhibidores de la cinasa atr |
| KR102195348B1 (ko) * | 2018-11-15 | 2020-12-24 | 에이치케이이노엔 주식회사 | 단백질 키나제 억제제로서의 신규 화합물 및 이를 포함하는 약제학적 조성물 |
| US10829493B2 (en) | 2019-04-12 | 2020-11-10 | Blueprint Medicines Corporation | Compositions and methods for treating KIT- and PDGFRA-mediated diseases |
| WO2020210669A1 (en) | 2019-04-12 | 2020-10-15 | Blueprint Medicines Corporation | Crystalline forms of (s)-1-(4-fluorophenyl)-1-(2-(4-(6-(1-methyl-1h-pyrazol-4-yl)pyrrolo[2,1-f][1,2,4]triazin-4-yl)piperazinyl)-pyrimidin-5-yl)ethan-1-amine and methods of making |
| CN118619944A (zh) * | 2019-06-06 | 2024-09-10 | 北京泰德制药股份有限公司 | 作为atr激酶抑制剂的2,4,6-三取代的嘧啶化合物 |
| CN113993870B (zh) * | 2019-08-09 | 2023-06-13 | 四川科伦博泰生物医药股份有限公司 | 含有并环基团的咪唑并嘧啶类化合物、其制备方法及用途 |
| JP7508593B2 (ja) * | 2020-05-20 | 2024-07-01 | 北京泰徳製薬股▲フン▼有限公司 | Atrキナーゼ阻害剤としての2,4,6-トリ置換ピリミジン化合物 |
| WO2022159981A1 (en) * | 2021-01-25 | 2022-07-28 | Athos Therapeutics, Inc. | Triazine compounds and methods of making and using the same |
| WO2022203399A1 (ko) * | 2021-03-26 | 2022-09-29 | 주식회사 스탠다임 | 아데노신 a2a 수용체 길항제 및 이의 용도 |
| CN117751127A (zh) * | 2021-08-20 | 2024-03-22 | 南京大美生物制药有限公司 | 一种五元含氮杂环并杂芳基类衍生物及其用途 |
| PL247180B1 (pl) * | 2023-06-29 | 2025-05-26 | Politechnika Krakowska Im Tadeusza Kosciuszki | Nowa pochodna 1,3,5-triazyny i jej zastosowanie |
| PL247231B1 (pl) * | 2023-06-29 | 2025-06-02 | Politechnika Krakowska Im Tadeusza Kosciuszki | Nowa pochodna 1,3,5-triazyny i jej zastosowanie |
Family Cites Families (107)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3536809A (en) | 1969-02-17 | 1970-10-27 | Alza Corp | Medication method |
| US3598123A (en) | 1969-04-01 | 1971-08-10 | Alza Corp | Bandage for administering drugs |
| US3845770A (en) | 1972-06-05 | 1974-11-05 | Alza Corp | Osmatic dispensing device for releasing beneficial agent |
| US3916899A (en) | 1973-04-25 | 1975-11-04 | Alza Corp | Osmotic dispensing device with maximum and minimum sizes for the passageway |
| US4008719A (en) | 1976-02-02 | 1977-02-22 | Alza Corporation | Osmotic system having laminar arrangement for programming delivery of active agent |
| US4328245A (en) | 1981-02-13 | 1982-05-04 | Syntex (U.S.A.) Inc. | Carbonate diester solutions of PGE-type compounds |
| US4410545A (en) | 1981-02-13 | 1983-10-18 | Syntex (U.S.A.) Inc. | Carbonate diester solutions of PGE-type compounds |
| US4409239A (en) | 1982-01-21 | 1983-10-11 | Syntex (U.S.A.) Inc. | Propylene glycol diester solutions of PGE-type compounds |
| HU196714B (en) | 1984-10-04 | 1989-01-30 | Monsanto Co | Process for producing non-aqueous composition comprising somatotropin |
| IE58110B1 (en) | 1984-10-30 | 1993-07-14 | Elan Corp Plc | Controlled release powder and process for its preparation |
| US5052558A (en) | 1987-12-23 | 1991-10-01 | Entravision, Inc. | Packaged pharmaceutical product |
| US5033252A (en) | 1987-12-23 | 1991-07-23 | Entravision, Inc. | Method of packaging and sterilizing a pharmaceutical product |
| US5073543A (en) | 1988-07-21 | 1991-12-17 | G. D. Searle & Co. | Controlled release formulations of trophic factors in ganglioside-lipsome vehicle |
| US5612059A (en) | 1988-08-30 | 1997-03-18 | Pfizer Inc. | Use of asymmetric membranes in delivery devices |
| IT1229203B (it) | 1989-03-22 | 1991-07-25 | Bioresearch Spa | Impiego di acido 5 metiltetraidrofolico, di acido 5 formiltetraidrofolico e dei loro sali farmaceuticamente accettabili per la preparazione di composizioni farmaceutiche in forma a rilascio controllato attive nella terapia dei disturbi mentali organici e composizioni farmaceutiche relative. |
| PH30995A (en) | 1989-07-07 | 1997-12-23 | Novartis Inc | Sustained release formulations of water soluble peptides. |
| US5120548A (en) | 1989-11-07 | 1992-06-09 | Merck & Co., Inc. | Swelling modulated polymeric drug delivery device |
| US5585112A (en) | 1989-12-22 | 1996-12-17 | Imarx Pharmaceutical Corp. | Method of preparing gas and gaseous precursor-filled microspheres |
| IT1246382B (it) | 1990-04-17 | 1994-11-18 | Eurand Int | Metodo per la cessione mirata e controllata di farmaci nell'intestino e particolarmente nel colon |
| US5733566A (en) | 1990-05-15 | 1998-03-31 | Alkermes Controlled Therapeutics Inc. Ii | Controlled release of antiparasitic agents in animals |
| US5543390A (en) | 1990-11-01 | 1996-08-06 | State Of Oregon, Acting By And Through The Oregon State Board Of Higher Education, Acting For And On Behalf Of The Oregon Health Sciences University | Covalent microparticle-drug conjugates for biological targeting |
| US5580578A (en) | 1992-01-27 | 1996-12-03 | Euro-Celtique, S.A. | Controlled release formulations coated with aqueous dispersions of acrylic polymers |
| US5323907A (en) | 1992-06-23 | 1994-06-28 | Multi-Comp, Inc. | Child resistant package assembly for dispensing pharmaceutical medications |
| TW333456B (en) | 1992-12-07 | 1998-06-11 | Takeda Pharm Ind Co Ltd | A pharmaceutical composition of sustained-release preparation the invention relates to a pharmaceutical composition of sustained-release preparation which comprises a physiologically active peptide. |
| US5591767A (en) | 1993-01-25 | 1997-01-07 | Pharmetrix Corporation | Liquid reservoir transdermal patch for the administration of ketorolac |
| US6274552B1 (en) | 1993-03-18 | 2001-08-14 | Cytimmune Sciences, Inc. | Composition and method for delivery of biologically-active factors |
| US5523092A (en) | 1993-04-14 | 1996-06-04 | Emory University | Device for local drug delivery and methods for using the same |
| US5985307A (en) | 1993-04-14 | 1999-11-16 | Emory University | Device and method for non-occlusive localized drug delivery |
| US6087324A (en) | 1993-06-24 | 2000-07-11 | Takeda Chemical Industries, Ltd. | Sustained-release preparation |
| US6004534A (en) | 1993-07-23 | 1999-12-21 | Massachusetts Institute Of Technology | Targeted polymerized liposomes for improved drug delivery |
| IT1270594B (it) | 1994-07-07 | 1997-05-07 | Recordati Chem Pharm | Composizione farmaceutica a rilascio controllato di moguisteina in sospensione liquida |
| US5759542A (en) | 1994-08-05 | 1998-06-02 | New England Deaconess Hospital Corporation | Compositions and methods for the delivery of drugs by platelets for the treatment of cardiovascular and other diseases |
| EP0711804A3 (de) | 1994-11-14 | 1999-09-22 | Ciba SC Holding AG | Kryptolichtschutzmittel |
| US5660854A (en) | 1994-11-28 | 1997-08-26 | Haynes; Duncan H | Drug releasing surgical implant or dressing material |
| US6316652B1 (en) | 1995-06-06 | 2001-11-13 | Kosta Steliou | Drug mitochondrial targeting agents |
| US5798119A (en) | 1995-06-13 | 1998-08-25 | S. C. Johnson & Son, Inc. | Osmotic-delivery devices having vapor-permeable coatings |
| AU6242096A (en) | 1995-06-27 | 1997-01-30 | Takeda Chemical Industries Ltd. | Method of producing sustained-release preparation |
| JP3512911B2 (ja) | 1995-07-11 | 2004-03-31 | 富士写真フイルム株式会社 | 紫外線吸収剤前駆体化合物、それを含有する感光性樹脂組成物及び画像形成方法 |
| TW448055B (en) | 1995-09-04 | 2001-08-01 | Takeda Chemical Industries Ltd | Method of production of sustained-release preparation |
| JP2909418B2 (ja) | 1995-09-18 | 1999-06-23 | 株式会社資生堂 | 薬物の遅延放出型マイクロスフイア |
| US6039975A (en) | 1995-10-17 | 2000-03-21 | Hoffman-La Roche Inc. | Colon targeted delivery system |
| US5980945A (en) | 1996-01-16 | 1999-11-09 | Societe De Conseils De Recherches Et D'applications Scientifique S.A. | Sustained release drug formulations |
| TW345603B (en) | 1996-05-29 | 1998-11-21 | Gmundner Fertigteile Gmbh | A noise control device for tracks |
| US6264970B1 (en) | 1996-06-26 | 2001-07-24 | Takeda Chemical Industries, Ltd. | Sustained-release preparation |
| US6419961B1 (en) | 1996-08-29 | 2002-07-16 | Takeda Chemical Industries, Ltd. | Sustained release microcapsules of a bioactive substance and a biodegradable polymer |
| HUP0000116A3 (en) | 1996-10-01 | 2000-08-28 | Stanford Res Inst Int | Taste-masked microcapsule compositions and methods of manufacture |
| CA2217134A1 (en) | 1996-10-09 | 1998-04-09 | Sumitomo Pharmaceuticals Co., Ltd. | Sustained release formulation |
| DE69730093T2 (de) | 1996-10-31 | 2006-07-20 | Takeda Pharmaceutical Co. Ltd. | Zubereitung mit verzögerter Freisetzung |
| US6131570A (en) | 1998-06-30 | 2000-10-17 | Aradigm Corporation | Temperature controlling device for aerosol drug delivery |
| WO1998027980A2 (en) | 1996-12-20 | 1998-07-02 | Takeda Chemical Industries, Ltd. | Method of producing a sustained-release preparation |
| US5891474A (en) | 1997-01-29 | 1999-04-06 | Poli Industria Chimica, S.P.A. | Time-specific controlled release dosage formulations and method of preparing same |
| US6120751A (en) | 1997-03-21 | 2000-09-19 | Imarx Pharmaceutical Corp. | Charged lipids and uses for the same |
| US6060082A (en) | 1997-04-18 | 2000-05-09 | Massachusetts Institute Of Technology | Polymerized liposomes targeted to M cells and useful for oral or mucosal drug delivery |
| KR100563514B1 (ko) * | 1997-07-24 | 2006-03-27 | 젠야쿠코교가부시키가이샤 | 헤테로고리 화합물 및 이를 유효성분으로 하는 항종양제 |
| JPH11174638A (ja) | 1997-12-08 | 1999-07-02 | Konica Corp | ハロゲン化銀カラー写真感光材料 |
| US6350458B1 (en) | 1998-02-10 | 2002-02-26 | Generex Pharmaceuticals Incorporated | Mixed micellar drug deliver system and method of preparation |
| US6613358B2 (en) | 1998-03-18 | 2003-09-02 | Theodore W. Randolph | Sustained-release composition including amorphous polymer |
| US6048736A (en) | 1998-04-29 | 2000-04-11 | Kosak; Kenneth M. | Cyclodextrin polymers for carrying and releasing drugs |
| KR19990085365A (ko) | 1998-05-16 | 1999-12-06 | 허영섭 | 지속적으로 약물 조절방출이 가능한 생분해성 고분자 미립구 및그 제조방법 |
| US6248363B1 (en) | 1999-11-23 | 2001-06-19 | Lipocine, Inc. | Solid carriers for improved delivery of active ingredients in pharmaceutical compositions |
| US6271359B1 (en) | 1999-04-14 | 2001-08-07 | Musc Foundation For Research Development | Tissue-specific and pathogen-specific toxic agents and ribozymes |
| ES2788383T3 (es) | 2000-04-25 | 2020-10-21 | Icos Corp | Inhibidores de delta fosfatidilo-inositol 3-quinasa humana |
| AP2001002264A0 (en) | 2000-08-30 | 2001-09-30 | Pfizer Prod Inc | Sustained release formulations for growth hormone secretagogues. |
| EP1389617B1 (en) | 2001-04-27 | 2007-01-03 | Zenyaku Kogyo Kabushiki Kaisha | Heterocyclic compound and antitumor agent containing the same as active ingredient |
| KR101046015B1 (ko) | 2002-10-25 | 2011-07-01 | 젠야쿠코교가부시키가이샤 | 헤테로고리 화합물 및 이것을 유효성분으로 하는 항종양제 |
| US7423148B2 (en) | 2002-11-21 | 2008-09-09 | Chiron Corporation | Small molecule PI 3-kinase inhibitors and methods of their use |
| WO2005028467A1 (en) | 2003-09-15 | 2005-03-31 | Anadys Pharmaceuticals, Inc. | Antibacterial 3,5-diaminopiperidine-substitute aromatic and heteroaromatic compounds |
| CA2561406C (en) | 2004-03-31 | 2012-07-03 | Zenyaku Kogyo Kabushiki Kaisha | Heterocyclic compound and anti-malignant-tumor agent comprising the same as effective component |
| ME01309B (me) | 2004-08-26 | 2013-12-20 | Pfizer | Pirazolom supstituirani heteroarilni spojevi kao inhibitori proteinskih kinaza |
| TWI381841B (zh) | 2005-03-11 | 2013-01-11 | Zenyaku Kogyo Kk | An immunosuppressive agent and an antitumor agent containing a heterocyclic compound as an active ingredient |
| GB0510390D0 (en) | 2005-05-20 | 2005-06-29 | Novartis Ag | Organic compounds |
| GB0525080D0 (en) | 2005-12-09 | 2006-01-18 | Astrazeneca Ab | Pyrimidine derivatives |
| GB0525081D0 (en) | 2005-12-09 | 2006-01-18 | Astrazeneca Ab | Pyrimidine derivatives |
| JO2660B1 (en) | 2006-01-20 | 2012-06-17 | نوفارتيس ايه جي | Pi-3 inhibitors and methods of use |
| US20070244110A1 (en) | 2006-04-14 | 2007-10-18 | Zenyaku Kogyo Kabushiki Kaisha | Treatment of prostate cancer, melanoma or hepatic cancer |
| TWI498332B (zh) * | 2006-04-26 | 2015-09-01 | Hoffmann La Roche | 作為pi3k抑制劑之嘧啶衍生物及相關製備方法、醫藥組合物、用途、套組及產物 |
| CN101511840A (zh) | 2006-04-26 | 2009-08-19 | 吉宁特有限公司 | 磷酸肌醇3-激酶抑制剂化合物及其使用方法 |
| DK2050749T3 (en) | 2006-08-08 | 2018-01-08 | Chugai Pharmaceutical Co Ltd | PYRIMIDINE DERIVATIVES AS PI3K INHIBITOR AND USE THEREOF |
| JP2010503651A (ja) * | 2006-09-14 | 2010-02-04 | アストラゼネカ アクチボラグ | 増殖性障害の治療用のPI3K及びmTOR阻害剤としての2−ベンゾイミダゾリル−6−モルホリノ−フェニルピリミジン誘導体 |
| WO2008032091A1 (en) | 2006-09-14 | 2008-03-20 | Astrazeneca Ab | 4-benzimidaz0lyl-6-m0rph0lin0-2-piperidin-4-ylpyrimidine derivatives as pi3k and mtor inhibitors for the treatment of proliferative disorders |
| EP2069330A1 (en) | 2006-09-14 | 2009-06-17 | AstraZeneca AB | 2 -benzimidazolyl- 6 -morpholino-4- (azetidine, pyrrolidine, piperidine or azepine) pyrimidine derivatives as pi3k and mtor inhibitors for the treatment of proliferative disorders |
| WO2008032041A1 (en) | 2006-09-14 | 2008-03-20 | Astrazeneca Ab | Pyrimidine derivatives having inhibitory activity against pi3k enzymes |
| WO2008032027A1 (en) * | 2006-09-14 | 2008-03-20 | Astrazeneca Ab | Pyrimidine derivatives |
| WO2008032033A1 (en) | 2006-09-14 | 2008-03-20 | Astrazeneca Ab | 4-benzimidazolyl-2-morpholino-6-piperazinylpyrimidine derivatives as pi3k and mtor inhibitors for the treatment of proliferative disorders |
| WO2008032089A1 (en) | 2006-09-14 | 2008-03-20 | Astrazeneca Ab | 4-benzimidaz0lyl-2-m0rph0lin0-6-piperidin-4-ylpyrimidine derivatives as pi3k and mtor inhibitors for the treatment of proliferative disorders |
| CN101595103A (zh) | 2006-09-14 | 2009-12-02 | 阿斯利康(瑞典)有限公司 | 嘧啶衍生物 |
| WO2008032077A1 (en) * | 2006-09-14 | 2008-03-20 | Astrazeneca Ab | Pyrimidine derivatives |
| WO2008032060A1 (en) | 2006-09-14 | 2008-03-20 | Astrazeneca Ab | 4-benzimidaz0lyl-6-m0rph0lin0-2-piperazinylpyrimidine derivatives as p13k and mtor inhibitors for the treatment of proliferative disorders |
| WO2008032036A1 (en) | 2006-09-14 | 2008-03-20 | Astrazeneca Ab | 6-benzimidaz0lyl-2-m0rph0lin0-4- (azetidine, pyrrolidine, piperidine or azepine) pyrimidine derivatives as pi3k and mtor inhibitors for the treatment of proliferative disorders |
| WO2008032072A1 (en) | 2006-09-14 | 2008-03-20 | Astrazeneca Ab | 2-benzimidaz0lyl-6-m0rph0lin0-4-piperidin-4-ylpyrimidine derivatives as pi3k and mtor inhibitors for the treatment of proliferative disorders |
| WO2008098058A1 (en) | 2007-02-06 | 2008-08-14 | Novartis Ag | Pi 3-kinase inhibitors and methods of their use |
| US20080234262A1 (en) | 2007-03-21 | 2008-09-25 | Wyeth | Pyrazolopyrimidine analogs and their use as mtor kinase and pi3 kinase inhibitors |
| US20080233127A1 (en) | 2007-03-21 | 2008-09-25 | Wyeth | Imidazolopyrimidine analogs and their use as pi3 kinase and mtor inhibitors |
| BRPI0817503B8 (pt) | 2007-10-05 | 2021-05-25 | Sstarbio Pte Ltd | derivados de purina substituídos por pirimidina, composição farmacêutica compreendendo ditos compostos e uso dos mesmos para a prevenção ou tratamento de uma condição proliferativa |
| EP2209785A1 (en) | 2007-10-05 | 2010-07-28 | S*BIO Pte Ltd | 2-morpholinylpurines as inhibitors of pi3k |
| TWI482768B (zh) | 2007-11-22 | 2015-05-01 | Zenyaku Kogyo Kk | 雜環化合物之非晶質體、含有其之固體分散體、藥劑及其製法 |
| WO2009091788A1 (en) | 2008-01-15 | 2009-07-23 | Wyeth | 3h-[1,2,3]triazolo[4,5-d]pyrimidine compounds, their use as mtor kinase and pi3 kinase inhibitors, and their syntheses |
| WO2009093981A1 (en) | 2008-01-23 | 2009-07-30 | S Bio Pte Ltd | Triazine compounds as kinase inhibitors |
| US20090192176A1 (en) | 2008-01-30 | 2009-07-30 | Wyeth | 1H-PYRAZOLO[3,4-D]PYRIMIDINE, PURINE, 7H-PURIN-8(9H)-ONE, 3H-[1,2,3]TRIAZOLO[4,5-D]PYRIMIDINE, AND THIENO[3,2-D]PYRIMIDINE COMPOUNDS, THEIR USE AS mTOR KINASE AND PI3 KINASE INHIBITORS, AND THEIR SYNTHESES |
| TW200938201A (en) | 2008-02-07 | 2009-09-16 | Chugai Pharmaceutical Co Ltd | Pyrrolopyrimidine derivative as PI3K inhibitor and use thereof |
| EP2276750A2 (en) | 2008-03-27 | 2011-01-26 | Auckland Uniservices Limited | Substituted pyrimidines and triazines and their use in cancer therapy |
| AP2775A (en) | 2008-05-23 | 2013-09-30 | Wyeth Llc | Triazine compounds as P13 kinase and MTOR inhibitors |
| EP2310391A1 (en) | 2008-06-27 | 2011-04-20 | S*BIO Pte Ltd | Pyrazine substituted purines |
| JP2011527342A (ja) | 2008-07-07 | 2011-10-27 | エックスカバリー ホールディング カンパニー エルエルシー | Pi3kアイソフォーム選択的阻害剤 |
| GB2465405A (en) | 2008-11-10 | 2010-05-19 | Univ Basel | Triazine, pyrimidine and pyridine analogues and their use in therapy |
| US20120165309A1 (en) | 2009-02-12 | 2012-06-28 | Astellas Pharma Inc. | Hetero ring derivative |
| SG174527A1 (en) * | 2009-03-27 | 2011-11-28 | Pathway Therapeutics Inc | Pyrimidinyl and 1,3,5-triazinyl benzimidazole sulfonamides and their use in cancer therapy |
-
2010
- 2010-07-06 US US12/831,128 patent/US8486939B2/en active Active
- 2010-07-06 EP EP10742315A patent/EP2451802A1/en not_active Withdrawn
- 2010-07-06 DK DK14168117.1T patent/DK3072890T3/en active
- 2010-07-06 CA CA2987503A patent/CA2987503C/en active Active
- 2010-07-06 EP EP12182995A patent/EP2532659A1/en not_active Withdrawn
- 2010-07-06 EP EP14168117.1A patent/EP3072890B1/en active Active
- 2010-07-06 TW TW099122213A patent/TW201105662A/zh unknown
- 2010-07-06 CA CA2767008A patent/CA2767008C/en active Active
- 2010-07-06 WO PCT/NZ2010/000139 patent/WO2011005119A1/en not_active Ceased
- 2010-07-06 ES ES14168117T patent/ES2706185T3/es active Active
- 2010-07-06 AR ARP100102428A patent/AR080945A1/es not_active Application Discontinuation
Also Published As
| Publication number | Publication date |
|---|---|
| CA2987503C (en) | 2019-02-26 |
| EP2451802A1 (en) | 2012-05-16 |
| WO2011005119A1 (en) | 2011-01-13 |
| US8486939B2 (en) | 2013-07-16 |
| DK3072890T3 (en) | 2019-02-11 |
| CA2767008C (en) | 2018-01-30 |
| AR080945A1 (es) | 2012-05-23 |
| EP3072890B1 (en) | 2018-10-17 |
| CA2767008A1 (en) | 2011-01-13 |
| TW201105662A (en) | 2011-02-16 |
| CA2987503A1 (en) | 2011-01-13 |
| US20110009405A1 (en) | 2011-01-13 |
| EP2532659A1 (en) | 2012-12-12 |
| EP3072890A1 (en) | 2016-09-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2706185T3 (es) | Pirimidinil y 1,3,5-triazinil bencimidazoles y sus usos en la terapia contra el cáncer | |
| JP5766177B2 (ja) | ピリミジニル及び1,3,5−トリアジニルベンゾイミダゾールスルホンアミド及びガンの療法におけるその使用 | |
| US12059422B2 (en) | (Alpha-substituted aralkylamino and heteroarylalkylamino) pyrimidinyl and 1,3,5-triazinyl benzimidazoles, pharmaceutical compositions thereof, and their use in treating proliferative diseases | |
| US11427565B2 (en) | Benzimidazoles for use in the treatment of cancer and inflammatory diseases | |
| ES2891734T3 (es) | Derivados de bencimidazol como inhibidores de tirosina quinasa ERBB para el tratamiento del cáncer | |
| US20110053907A1 (en) | Substituted pyrimidines and triazines and their use in cancer therapy | |
| HK1228387B (en) | Pyrimidinyl and 1,3,5-triazinyl benzimidazoles and their use in cancer therapy | |
| HK1228387A1 (en) | Pyrimidinyl and 1,3,5-triazinyl benzimidazoles and their use in cancer therapy |