ES2727344T3 - Proceso para la producción de 1-(5,5-dimetilciclohex-1-en-1-il)etanona y 1-(5,5-dimetilciclohex-6-en-1-il)etanona - Google Patents
Proceso para la producción de 1-(5,5-dimetilciclohex-1-en-1-il)etanona y 1-(5,5-dimetilciclohex-6-en-1-il)etanona Download PDFInfo
- Publication number
- ES2727344T3 ES2727344T3 ES15712621T ES15712621T ES2727344T3 ES 2727344 T3 ES2727344 T3 ES 2727344T3 ES 15712621 T ES15712621 T ES 15712621T ES 15712621 T ES15712621 T ES 15712621T ES 2727344 T3 ES2727344 T3 ES 2727344T3
- Authority
- ES
- Spain
- Prior art keywords
- formula
- group
- complex
- iii
- anion
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000000034 method Methods 0.000 title claims abstract description 48
- 238000004519 manufacturing process Methods 0.000 title claims abstract description 10
- JIYZCVGAWRMUDR-UHFFFAOYSA-N 1-(3,3-dimethylcyclohexen-1-yl)ethanone Chemical compound CC(=O)C1=CC(C)(C)CCC1 JIYZCVGAWRMUDR-UHFFFAOYSA-N 0.000 title description 4
- NZMDEABOJIQLEP-UHFFFAOYSA-N 1-(5,5-dimethylcyclohexen-1-yl)ethanone Chemical compound CC(=O)C1=CCCC(C)(C)C1 NZMDEABOJIQLEP-UHFFFAOYSA-N 0.000 title description 4
- 150000001875 compounds Chemical class 0.000 claims abstract description 30
- 150000001450 anions Chemical class 0.000 claims abstract description 20
- -1 tetra(3,5-bis(trifluoromethyl)phenyl)- borate Chemical compound 0.000 claims abstract description 12
- 239000013110 organic ligand Substances 0.000 claims abstract description 8
- 150000003871 sulfonates Chemical class 0.000 claims abstract description 6
- 229910001914 chlorine tetroxide Inorganic materials 0.000 claims abstract description 4
- VLTRZXGMWDSKGL-UHFFFAOYSA-M perchlorate Chemical compound [O-]Cl(=O)(=O)=O VLTRZXGMWDSKGL-UHFFFAOYSA-M 0.000 claims abstract description 4
- 125000004209 (C1-C8) alkyl group Chemical group 0.000 claims abstract description 3
- 125000005843 halogen group Chemical group 0.000 claims abstract description 3
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims abstract description 3
- 125000001424 substituent group Chemical group 0.000 claims abstract description 3
- 238000006243 chemical reaction Methods 0.000 claims description 13
- 239000003054 catalyst Substances 0.000 claims description 11
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 9
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 claims description 9
- BTANRVKWQNVYAZ-UHFFFAOYSA-N butan-2-ol Chemical compound CCC(C)O BTANRVKWQNVYAZ-UHFFFAOYSA-N 0.000 claims description 9
- 239000002904 solvent Substances 0.000 claims description 9
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 claims description 8
- 230000017105 transposition Effects 0.000 claims description 8
- HFKJQIJFRMRSKM-UHFFFAOYSA-N [3,5-bis(trifluoromethyl)phenoxy]boronic acid Chemical compound OB(O)OC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 HFKJQIJFRMRSKM-UHFFFAOYSA-N 0.000 claims description 4
- 239000000203 mixture Substances 0.000 claims description 3
- 239000000758 substrate Substances 0.000 claims description 3
- 238000006462 rearrangement reaction Methods 0.000 abstract 2
- 239000010931 gold Substances 0.000 description 14
- 239000011541 reaction mixture Substances 0.000 description 6
- 150000003839 salts Chemical class 0.000 description 5
- HIHHHOINJQWJTO-UHFFFAOYSA-N 1-ethynyl-3,3-dimethylcyclohexan-1-ol Chemical group CC1(C)CCCC(O)(C#C)C1 HIHHHOINJQWJTO-UHFFFAOYSA-N 0.000 description 3
- 238000011065 in-situ storage Methods 0.000 description 3
- 239000003446 ligand Substances 0.000 description 3
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 3
- 239000007858 starting material Substances 0.000 description 3
- ITMCEJHCFYSIIV-UHFFFAOYSA-M triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-M 0.000 description 3
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 235000019253 formic acid Nutrition 0.000 description 2
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- UCCVJKNWIINNSP-UHFFFAOYSA-M 1,1'-biphenyl chlorogold dicyclohexylphosphane Chemical compound Cl[Au].c1ccc(cc1)-c1ccccc1.C1CCC(CC1)PC1CCCCC1 UCCVJKNWIINNSP-UHFFFAOYSA-M 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- 239000007848 Bronsted acid Substances 0.000 description 1
- PGLJGGZEXXANSZ-POHAHGRESA-N CCC(C)(CCC1)C/C1=C\C=O Chemical compound CCC(C)(CCC1)C/C1=C\C=O PGLJGGZEXXANSZ-POHAHGRESA-N 0.000 description 1
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 230000002860 competitive effect Effects 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 239000003205 fragrance Substances 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 239000013067 intermediate product Substances 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 238000007086 side reaction Methods 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000004332 silver Substances 0.000 description 1
- QRUBYZBWAOOHSV-UHFFFAOYSA-M silver trifluoromethanesulfonate Chemical compound [Ag+].[O-]S(=O)(=O)C(F)(F)F QRUBYZBWAOOHSV-UHFFFAOYSA-M 0.000 description 1
- GGCZERPQGJTIQP-UHFFFAOYSA-N sodium;9,10-dioxoanthracene-2-sulfonic acid Chemical compound [Na+].C1=CC=C2C(=O)C3=CC(S(=O)(=O)O)=CC=C3C(=O)C2=C1 GGCZERPQGJTIQP-UHFFFAOYSA-N 0.000 description 1
- 239000011877 solvent mixture Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C45/00—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds
- C07C45/51—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by pyrolysis, rearrangement or decomposition
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C45/00—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds
- C07C45/51—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by pyrolysis, rearrangement or decomposition
- C07C45/511—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by pyrolysis, rearrangement or decomposition involving transformation of singly bound oxygen functional groups to >C = O groups
- C07C45/512—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by pyrolysis, rearrangement or decomposition involving transformation of singly bound oxygen functional groups to >C = O groups the singly bound functional group being a free hydroxyl group
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/24—Phosphines, i.e. phosphorus bonded to only carbon atoms, or to both carbon and hydrogen atoms, including e.g. sp2-hybridised phosphorus compounds such as phosphabenzene, phosphole or anionic phospholide ligands
- B01J31/2404—Cyclic ligands, including e.g. non-condensed polycyclic ligands, the phosphine-P atom being a ring member or a substituent on the ring
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/10—Complexes comprising metals of Group I (IA or IB) as the central metal
- B01J2531/18—Gold
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
- Catalysts (AREA)
Abstract
Un proceso para la producción de compuestos de la fórmula (I)**Fórmula** por una reacción de transposición del compuesto de la fórmula (II)**Fórmula** en el que la reacción de transposición se cataliza por al menos un complejo de Au (I), en el que se usa al menos un complejo de Au (I) del siguiente compuesto de la fórmula (III)**Fórmula** Y-Au (I)-Z (III) en la que Z es un anión, que se selecciona del grupo que consiste en [BX4]-, [PX6]-, [SbF6]-, [ClO4]-, CF3COO-10 , sulfonatos, tetra(3,5-bis(trifluorometil)fenil)-borato (BArF -), tetrafenilborato, y el anión de la fórmula (IV)**Fórmula** en la que Q representa un fenilo o un alquilo C1-8 que preferentemente se sustituye por al menos un sustituyente elegido del grupo que consiste en F, Cl, NO2 y X es un átomo de halógeno, especialmente F y Cl, y Y es un ligando orgánico, en el que el ligando orgánico Y del complejo de Au (I) de la fórmula (III) se selecciona del grupo que consiste en**Fórmula**
Description
DESCRIPCIÓN
Proceso para la producción de 1-(5,5-dimetilciclohex-1-en-1-il)etanona y 1-(5,5-dimetilciclohex-6-en-1-il)etanona La presente invención se refiere a un método mejorado de producción de 1-(5,5-dimetilciclohex-1-en-1-il)etanona y 1 -(5,5-dimetilciclohex-6-en-1 -il)etanona.
La 1-(5,5-dimetilciclohex-1-en-1-il)etanona (compuesto de la fórmula (I')) y 1-(5,5-dimetilciclohex-6-en-1-il)etanona (compuesto de la fórmula (I"))
son productos intermedios versátiles e importantes para la síntesis de diversos compuestos de fragancia conocidos. En el contexto de la presente solicitud de patente, los compuestos de la fórmula (I') y de la fórmula (I") se resumen por la siguiente fórmula (I)
Los compuestos de la fórmula (I) (que significa ya sea el compuesto de la fórmula (I') o el compuesto de la fórmula (I") como tales, además de cualquier mezcla de estos dos compuestos) se pueden usar para producir, por ejemplo, los siguientes compuestos de las fórmulas (Ia) a (Ig):
Se conocen bien del estado de la técnica todas estas reacciones para obtener los compuestos de la fórmula (la) a (Ig) a partir del compuesto de la fórmula (I).
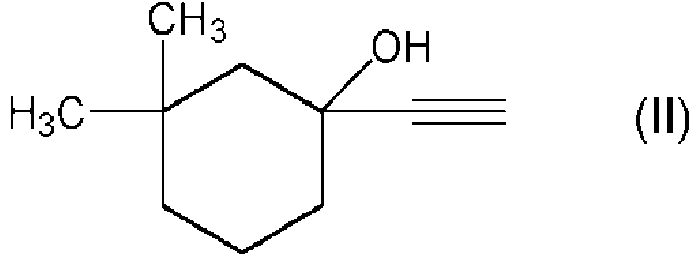
Los compuestos de la fórmula (I) se producen normalmente usando ácido fórmico (HCOOH) como catalizador en la transposición de compuestos que tienen la fórmula (II)
Esta reacción se describe, por ejemplo, en el documento de patente US4147672.
El uso de P2O5 como catalizador también se conoce del documento de patente WO2004050602 y P. Kraft et al. en European Journal of Organic Chemistry, 2004, 2, 354-365.
El método de producción usando ácidos fuertes de Bronsted en condiciones de reacción corrosivas provoca algunos problemas.
Por ejemplo, es necesario usar equipo caro resistente a los ácidos para la producción. Además, la manipulación de los compuestos corrosivos no es fácil para el equipo de producción.
Debido a la importancia de los compuestos de la fórmula (I), siempre existe una necesidad de descubrir un método mejorado para la producción de los compuestos de la fórmula (I). Sorprendentemente, se descubrió que es posible producir los compuestos de la fórmula (I) por una transposición de Rupe-Kambli catalizada con oro.
Por tanto, la presente invención se refiere a un proceso (A) para la producción de los compuestos de la fórmula (I)
por una reacción de transposición del compuesto de la fórmula (II)
en la que la reacción de transposición se cataliza en presencia de al menos un complejo de Au (I) como se define más adelante.
Un problema adicional, que ocurre cuando se sintetizan los compuestos de la fórmula (I), es que existen reacciones competitivas que ocurren, tales como la transposición de Meyer Schuster:
Usando el catalizador de oro se suprime (más o menos) la reacción secundaria anteriormente mencionada (que no conduce a los compuestos de la fórmula (I)), que significa que son excelentes el rendimiento y la conversión del nuevo proceso según la presente invención.
Los complejos de Au (I) usados como catalizadores para el proceso según la presente invención son de la siguiente fórmula (III):
Y-Au (I)-Z (III),
en la que
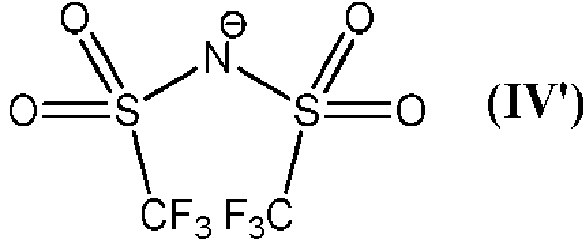
Z es un anión, que se selecciona del grupo que consiste en [BX4]', [PX6]", [SbF6]", [ClO4]', CF3COO', sulfonatos, tetra(3,5-bis(trifluorometil)fenil)borato (BArF-), tetrafenilborato, y el anión de la fórmula (IV);
en la que Q representa un fenilo o un alquilo C1-8 que se sustituye preferentemente por al menos un sustituyente elegido del grupo que consiste en F, Cl, nO2 y
X es un átomo de halógeno, especialmente F y Cl, y
Y es un ligando orgánico,
en la que Y es un ligando orgánico seleccionado del grupo que consiste en los siguientes ligandos (Y1) a (Y10):
Preferentemente, Z es un anión seleccionado del grupo que consiste en los siguientes aniones [BF4]", [PFs]-, [SbFs]-, [CD4]", CF3COO', sulfonatos (tales como triflato CF3SO3"), tetra(3,5-bis(trifluorometil)fenil)borato (BArF-), tetrafenilborato, y el anión de la fórmula (IV')
Por tanto, la presente invención también se refiere al proceso (B), que es el proceso (A), en el que el anión Z se selecciona del grupo que consiste en los siguientes aniones [BF4]-, [PF6]-, [SbFs]-, [ClO4]-, CF3COO-, sulfonatos (tales como triflato CF3SO3- ), tetra(3,5-bis(trifluorometil)fenil)borato (BArF-), tetrafenilborato, y el anión de la fórmula (IV')
El catalizador (el complejo de Au (I)) se puede añadir a la mezcla de reacción en la forma, que se define por la fórmula (I), pero también es posible que el complejo de Au (I) se forme in situ en la mezcla de reacción (antes de añadir el material de partida o después de añadir el material de partida).
Por ejemplo, es posible añadir el ligando orgánico en forma de una sal (tal como, por ejemplo, un cloruro: Y-Au (I)CI) y el anión en forma de una sal metálica (tal como, por ejemplo, una sal de plata Ag (I)Z). Entonces se forma in situ el complejo de Au (I) y la sal metálica resultante (por ejemplo, AgCI) no interfiere negativamente.
Por tanto, la presente invención se refiere a un proceso (C), que es el proceso (A) o (B), en el que el complejo de Au (I) se añade a la mezcla de reacción como tal.
Además, la presente invención se refiere a un proceso (D), que es el proceso (A), (B) o (C), en el que el complejo de Au (I) se forma in situ en la mezcla de reacción.
Los complejos de Au (I) preferidos de la fórmula (III) son los siguientes.
en las que Cy es ciclohexilo, iPr es isopropilo y Tf es triflato.
Por tanto, proceso preferido se refiere a un proceso como se ha descrito anteriormente en el que se usa al menos un complejo de la fórmula (III'), (III") y/o (III'").
El proceso según la presente invención se lleva a cabo normalmente en un disolvente (o una mezcla de disolventes). Los disolventes adecuados son hidrocarburos alifáticos, alcoholes. Los disolventes preferidos son alcoholes, tales como metanol, etanol, 2-butanol y terc-butanol.
Por tanto, la presente invención también se refiere a un proceso (E), que es el proceso (A), (B), (C) o (D), en el que el proceso se lleva a cabo en un disolvente o una mezcla de disolventes.
Además, la presente invención se refiere a un proceso (E'), que es el proceso (E), en el que el disolvente se elige del grupo que consiste en metanol, etanol, 2-butanol y terc-butanol.
El proceso según la presente invención se lleva a cabo normalmente a temperatura elevada, normalmente 30 °C -120 °C. Una temperatura de reacción preferida es entre 40 °C y 110 °C, más preferida entre 50 °C y 100 °C.
Por tanto, la presente invención también se refiere a un proceso (F), que es el proceso (A), (B), (C), (D) o (E), en el que el proceso se lleva a cabo a temperatura elevada.
Por tanto, la presente invención también se refiere a un proceso (F'), que es el proceso (F), en el que el proceso se lleva a cabo a una temperatura desde 30 °C hasta 120 °C.
Por tanto, la presente invención también se refiere a un proceso (F"), que es el proceso (F), en el que el proceso se lleva a cabo a una temperatura desde 40 °C hasta 110 °C.
Por tanto, la presente invención también se refiere a un proceso (F'"), que es el proceso (F), en el que el proceso se lleva a cabo a una temperatura desde 50 °C hasta 100 °C.
Normalmente, el complejo de Au (I) está presente en una cantidad, en la que la relación entre el sustrato (compuesto de la fórmula (II)) y el catalizador relación es 2 : 1 a 10000 : 1, se prefiere 10 : 1 a 3000 : 1.
Por tanto, la presente invención también se refiere a un proceso (I), que es el proceso (A), (B), (C), (D), (E), (E'), (F'), (F") o (F"'), en el que la relación entre sustrato (compuesto de la fórmula (II)) y el catalizador es 2 : 1 a 10000 : 1, preferentemente l0 : 1 a 3000 : 1.
El tiempo de reacción del proceso (para obtener el producto deseado en cantidad razonable) según la presente invención es normalmente 60 minutos a 300 minutos.
Como se ha establecido anteriormente, los compuestos de la fórmula (I) se pueden usar como material de partida para la síntesis de otros compuestos orgánicos (especialmente aquellos de las fórmulas (Ia) - (Ig)).
Los siguientes ejemplos sirven para ilustrar la invención. Si no se establece de otro modo, la temperatura se da en grado Celsius y todas las partes están relacionadas con el peso.
Ejemplos
Ejemplo 1: Transposición de 1 -etinil-3,3-dimetilciclohexanol
Se disolvieron 118,8 mg (0,2 mmoles, 0,1 equiv.) de cloruro de diciclohexilfosfina bifenil oro (I) y 56,88 mg (0,2 mmoles, 0,1 equiv.) de triflato de plata bajo argón a 23 °C en 5,0 ml de terc-butanol en una botella con diafragma. Se añadieron 362,6 gl (90 %, 2 mmoles, 1 equiv.) de 1-etinil-3,3-dimetilciclohexanol (90 %, 2 mmoles, 1 equiv.). La mezcla de reacción se agitó durante 105 min a 80 °C. Después, la mezcla de reacción se enfrió hasta 23 °C. Se tomó una muestra y se analizó por CG y RMN.
La conversión de esta reacción fue 98,9 %. Se obtuvieron los productos de las fórmulas (I" y I") con un rendimiento de 89,6 % en peso.
Es posible separar los dos isómeros, si se desea.
Ejemplos 2 - 6
Se llevaron a cabo los siguientes ejemplos en la misma condición de reacción que en el Ejemplo 1.
Los ligandos se definen como antes y los ligandos se añaden en la forma de cloruro y los aniones en forma de la sal de Ag (I).
Ejemplos comparativos (Ejemplos 7 - 11)
Se repitió la misma reacción que se describe en el Ejemplo 1, pero se usaron catalizadores de Au, que no se encuentran bajo el alcance de las reivindicaciones.
El Ejemplo 7 y 8 se llevan a cabo sin ligandos orgánicos. Se usó AuCI en combinación con la sal de plata
El Ejemplo 9, 10 y 11 y 8 se llevan a cabo con catalizadores donde se adsorbe Au (0) sobre un soporte.
Por tanto, se puede observar que es esencial la elección del catalizador adecuado (reivindicado).
Claims (7)
1. Un proceso para la producción de compuestos de la fórmula (I)
por una reacción de transposición del compuesto de la fórmula (II)
en el que la reacción de transposición se cataliza por al menos un complejo de Au (I), en el que se usa al menos un complejo de Au (I) del siguiente compuesto de la fórmula (III)
Y-Au (I)-Z (III)
en la que
Z es un anión, que se selecciona del grupo que consiste en [BX4]-, [PX6]-, [SbF6]-, [CD4]-, CF3COO-, sulfonatos, tetra(3,5-bis(trifluorometil)fenil)-borato (BArF-), tetrafenilborato, y el anión de la fórmula (IV)
en la que Q representa un fenilo o un alquilo C1-8 que preferentemente se sustituye por al menos un sustituyente elegido del grupo que consiste en F, Cl, nO2 y
X es un átomo de halógeno, especialmente F y Cl, y
Y es un ligando orgánico,
2. Proceso según la reivindicación 1, en el que el anión Z del complejo de Au (I) de la fórmula (III) se selecciona del grupo que consiste en los siguientes aniones [BF4]-, [PF6]-, [SbF6]-, [ClO4]-, CF3COO-, sulfonatos, tetra(3,5-bis(trifluorometil)fenil)borato (BArF-), tetrafenilborato, y el anión de la fórmula (IV')
3. Proceso según cualquiera de las reivindicaciones precedentes, en el que el proceso se lleva a cabo en un disolvente o una mezcla de disolventes.
4. Proceso según la reivindicación 3, en el que el disolvente se elige del grupo que consiste en metanol, etanol, 2-butanol y terc-butanol.
5. Proceso según cualquiera de las reivindicaciones precedentes, en el que el proceso se lleva a cabo a temperatura elevada.
6. Proceso según la reivindicación 5, en el que el proceso se lleva a cabo a una temperatura desde 30 °C hasta 1202C.
7. Proceso según cualquiera de las reivindicaciones precedentes, en el que la relación entre el sustrato de la fórmula (II) y el catalizador es 2 : 1 a 10000 : 1, preferentemente 10 : 1 a 3000 : 1.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP14162237 | 2014-03-28 | ||
| PCT/EP2015/056595 WO2015144832A1 (en) | 2014-03-28 | 2015-03-26 | Process of production of 1-(5,5-dimethylcyclohex-1-en-1-yl)ethanone and 1-(5,5-dimethylcyclohex-6-en-1-yl)ethanone |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2727344T3 true ES2727344T3 (es) | 2019-10-15 |
Family
ID=50389908
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES15712621T Active ES2727344T3 (es) | 2014-03-28 | 2015-03-26 | Proceso para la producción de 1-(5,5-dimetilciclohex-1-en-1-il)etanona y 1-(5,5-dimetilciclohex-6-en-1-il)etanona |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US10005710B2 (es) |
| EP (1) | EP3122713B1 (es) |
| JP (1) | JP6535915B2 (es) |
| CN (1) | CN106132916B (es) |
| ES (1) | ES2727344T3 (es) |
| WO (1) | WO2015144832A1 (es) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB201602644D0 (en) * | 2016-02-15 | 2016-03-30 | Givaudan Sa | Process |
| JP7044720B2 (ja) | 2016-06-22 | 2022-03-30 | フイルメニツヒ ソシエテ アノニム | 力強いウッディでパウダリーな匂い物質 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CH586551A5 (es) * | 1974-01-29 | 1977-04-15 | Firmenich & Cie | |
| CH603071A5 (en) * | 1975-01-31 | 1978-08-15 | Firmenich & Cie | Di:methyl-cyclohexene-alkenone cpds. |
| GB0227807D0 (en) | 2002-11-29 | 2003-01-08 | Givaudan Sa | Improvements in or relating ot organic compounds |
| BRPI0812460B1 (pt) * | 2007-06-11 | 2017-12-19 | Givaudan Sa | "organic compounds". |
| US8674143B2 (en) | 2008-10-15 | 2014-03-18 | Dsm Ip Assets, B.V. | Synthesis of green ketone intermediate |
| EP2213644A1 (en) | 2009-01-28 | 2010-08-04 | Hexion Specialty Chemicals Research Belgium S.A. | Process for the preparation of an allyl alkyl ether by catalyic allylation |
| CN102397794B (zh) | 2010-09-17 | 2013-09-11 | 中国科学院大连化学物理研究所 | 一种络合催化剂体系及其在分解环烷基过氧化氢中的应用 |
-
2015
- 2015-03-26 US US15/129,948 patent/US10005710B2/en active Active
- 2015-03-26 CN CN201580017335.7A patent/CN106132916B/zh active Active
- 2015-03-26 JP JP2016559583A patent/JP6535915B2/ja active Active
- 2015-03-26 WO PCT/EP2015/056595 patent/WO2015144832A1/en not_active Ceased
- 2015-03-26 ES ES15712621T patent/ES2727344T3/es active Active
- 2015-03-26 EP EP15712621.0A patent/EP3122713B1/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US20170217864A1 (en) | 2017-08-03 |
| EP3122713A1 (en) | 2017-02-01 |
| JP6535915B2 (ja) | 2019-07-03 |
| EP3122713B1 (en) | 2019-04-24 |
| CN106132916A (zh) | 2016-11-16 |
| CN106132916B (zh) | 2018-09-21 |
| JP2017514794A (ja) | 2017-06-08 |
| WO2015144832A1 (en) | 2015-10-01 |
| US10005710B2 (en) | 2018-06-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5006059B2 (ja) | キラルなイリジウムアクア錯体およびそれを用いた光学活性ヒドロキシ化合物の製造方法 | |
| ES2727344T3 (es) | Proceso para la producción de 1-(5,5-dimetilciclohex-1-en-1-il)etanona y 1-(5,5-dimetilciclohex-6-en-1-il)etanona | |
| Grassi et al. | Copper-free asymmetric allylic alkylation of trisubstituted cyclic allyl bromides using Grignard reagents. | |
| EP3099657B1 (en) | Process of production of 2,5-dimethylphenol | |
| Dijk et al. | On the role of DNA in DNA-based catalytic enantioselective conjugate addition reactions | |
| Goodrich et al. | Using chiral ionic liquid additives to enhance asymmetric induction in a Diels–Alder reaction | |
| Chapman et al. | Solid-state structure, solution-state behaviour and catalytic activity of electronically divergent C, N-chelating palladium–N-heterocyclic carbene complexes | |
| EP3099658B1 (en) | Process of production of 2,3,6-trimethylphenol | |
| CN105585584A (zh) | 氮杂环卡宾铜配合物的合成方法 | |
| JP2022516764A (ja) | マンガン触媒およびケトンの水素化におけるその使用 | |
| ES2718506T3 (es) | Hidrogenación por transferencia selectiva de citral o etil citral | |
| Chen et al. | Synthesis of allene ferrocenes through CuI-mediated Crabbé homologation reaction | |
| Söhner et al. | Halogen-free water-stable aluminates as replacement for persistent fluorinated weakly-coordinating anions | |
| JP2010037332A (ja) | キラルなイリジウムアクア錯体およびそれを用いた光学活性ヒドロキシ化合物の製造方法 | |
| CN105037319B (zh) | 金催化的分子内重氮偶联选择性生成反式大环烯烃的方法 | |
| WO2008135386A1 (fr) | Ligands chiraux de type carbenes n-heterocycliques pour la catalyse asymetrique | |
| JP2016505632A (ja) | 4−メチルペント−3−エン−1−オール誘導体の製造方法 | |
| JPWO2019069828A1 (ja) | 光学活性な2,3−ビスホスフィノピラジン誘導体、その製造方法、遷移金属錯体及び有機ホウ素化合物の製造方法 | |
| KR101631141B1 (ko) | 프롤린 유도체 및 이소티오우로늄 염을 포함하는 촉매 조성물 및 이의 제조 방법 | |
| CN102532200B (zh) | 一种n,n-配位二聚铑(ii)配合物及其制备方法和应用 | |
| ES2373291B2 (es) | Procedimiento para la oxidación catalítica de benceno a fenol. | |
| KR101059454B1 (ko) | N-함유 헤테로폴리시클릭 화합물의 신규 제조 방법 | |
| JP2018162218A (ja) | 新規な環状尿素誘導体−三臭化水素酸塩 | |
| Korenaga et al. | Synthesis of novel oxazaborolidines B-C6F5 and their effectiveness as asymmetric catalysts | |
| Zhang et al. | Chiral palladacycle promoted asymmetric synthesis of functionalized bis-phosphine monoxide ligand |