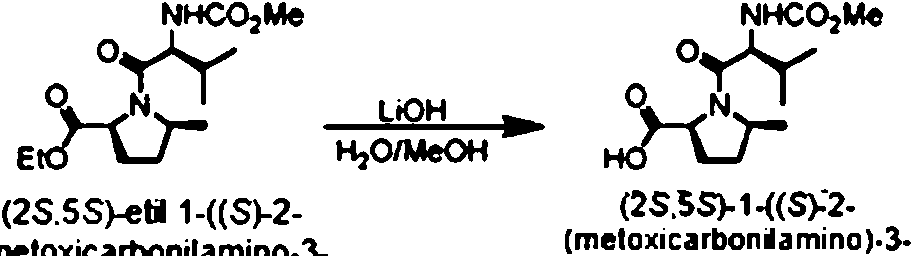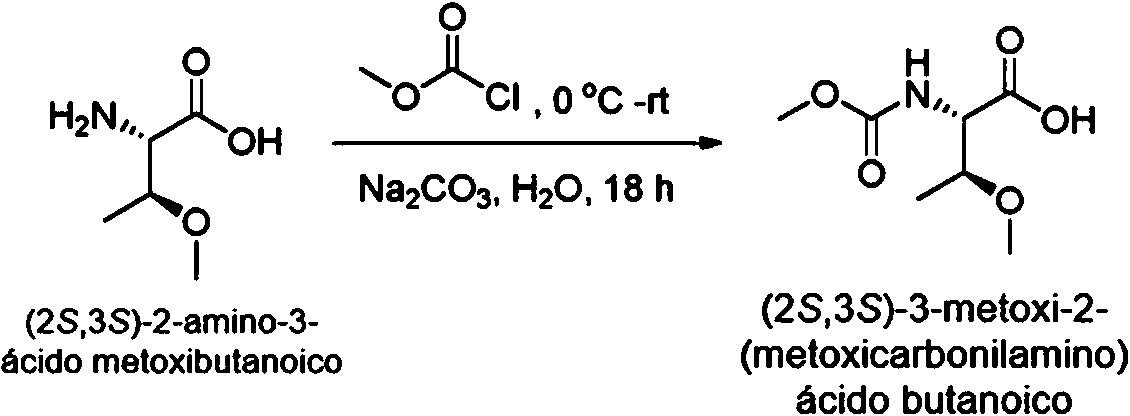ES2738012T3 - Derivados de 9-(1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-D]imidazol y su utilización como inhibidores de HCV NS5A - Google Patents
Derivados de 9-(1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-D]imidazol y su utilización como inhibidores de HCV NS5A Download PDFInfo
- Publication number
- ES2738012T3 ES2738012T3 ES17160683T ES17160683T ES2738012T3 ES 2738012 T3 ES2738012 T3 ES 2738012T3 ES 17160683 T ES17160683 T ES 17160683T ES 17160683 T ES17160683 T ES 17160683T ES 2738012 T3 ES2738012 T3 ES 2738012T3
- Authority
- ES
- Spain
- Prior art keywords
- methyl
- imidazol
- methylpyrrolidin
- naphtho
- methoxycarbonylamino
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 CC(C)C(C1C(C)CCCC1C)=*C Chemical compound CC(C)C(C1C(C)CCCC1C)=*C 0.000 description 5
- JSTLHMXBODWVPO-JLHFDRMNSA-N CCCC(N([C@@H](C)CC1)[C@@H]1c1ncc(-c(cc2COc3c4)ccc2-c3cc(cc2)c4c3c2nc([C@H](CC[C@@H]2/C=[O]/C)N2C(CCC)=O)[nH]3)[nH]1)=O Chemical compound CCCC(N([C@@H](C)CC1)[C@@H]1c1ncc(-c(cc2COc3c4)ccc2-c3cc(cc2)c4c3c2nc([C@H](CC[C@@H]2/C=[O]/C)N2C(CCC)=O)[nH]3)[nH]1)=O JSTLHMXBODWVPO-JLHFDRMNSA-N 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4188—1,3-Diazoles condensed with other heterocyclic ring systems, e.g. biotin, sorbinil
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
- A61K31/7056—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing five-membered rings with nitrogen as a ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
- A61K31/706—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom
- A61K31/7064—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines
- A61K31/7068—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines having oxo groups directly attached to the pyrimidine ring, e.g. cytidine, cytidylic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
- A61K31/706—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom
- A61K31/7064—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines
- A61K31/7068—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines having oxo groups directly attached to the pyrimidine ring, e.g. cytidine, cytidylic acid
- A61K31/7072—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines having oxo groups directly attached to the pyrimidine ring, e.g. cytidine, cytidylic acid having two oxo groups directly attached to the pyrimidine ring, e.g. uridine, uridylic acid, thymidine, zidovudine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/21—Interferons [IFN]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/04—Ortho-condensed systems
- C07D491/044—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring
- C07D491/052—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring the oxygen-containing ring being six-membered
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Virology (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Gastroenterology & Hepatology (AREA)
- Zoology (AREA)
- Immunology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
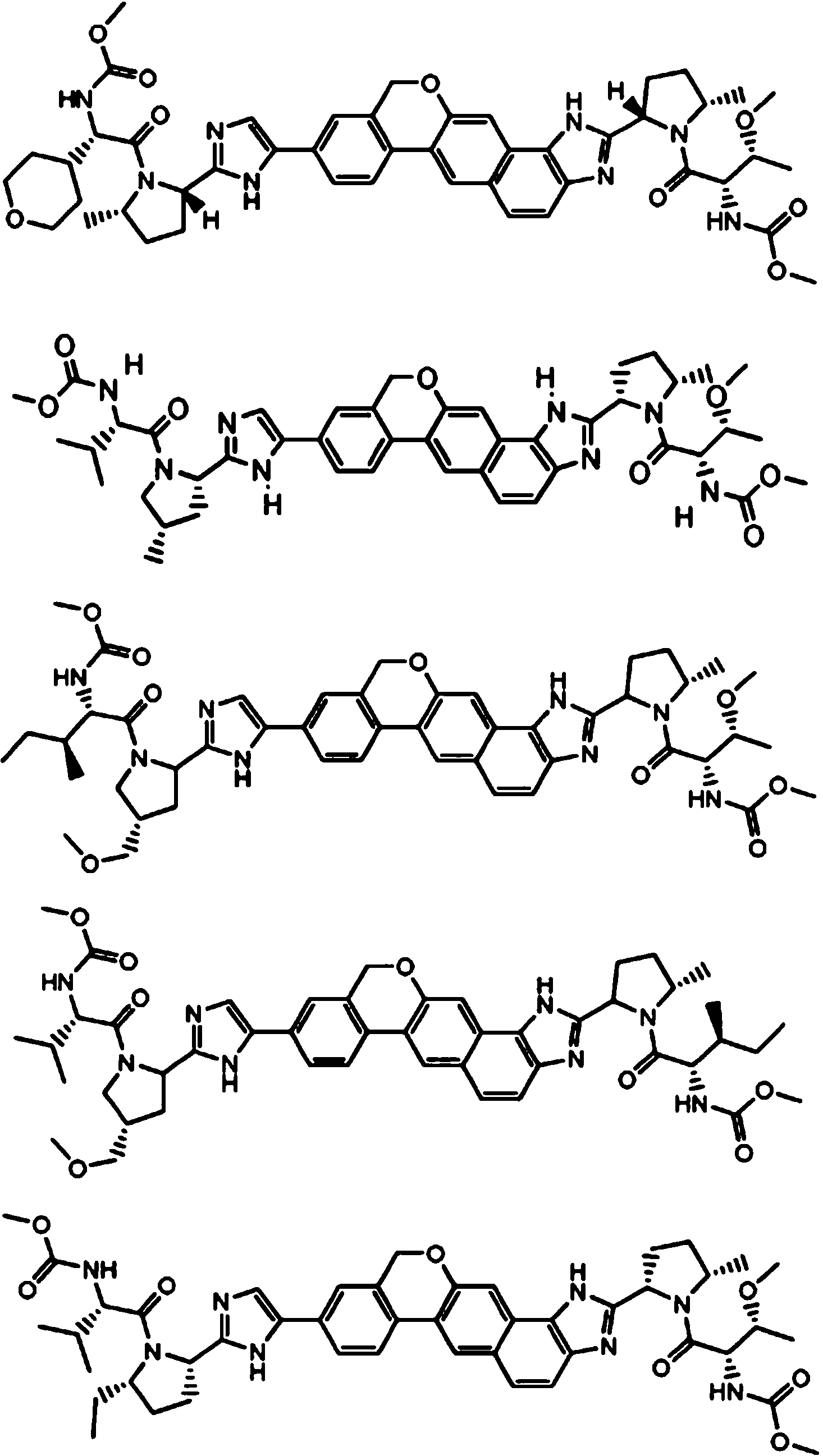
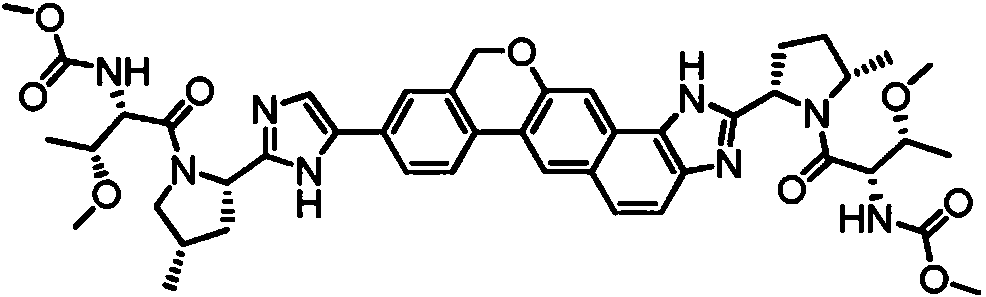
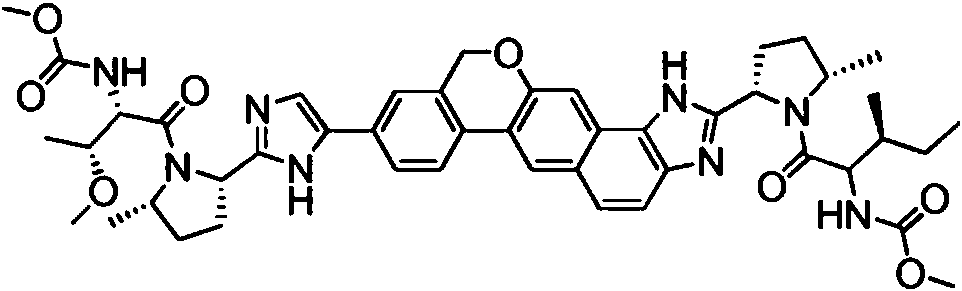
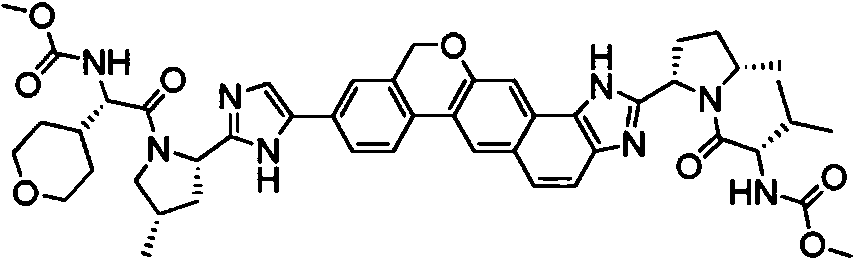
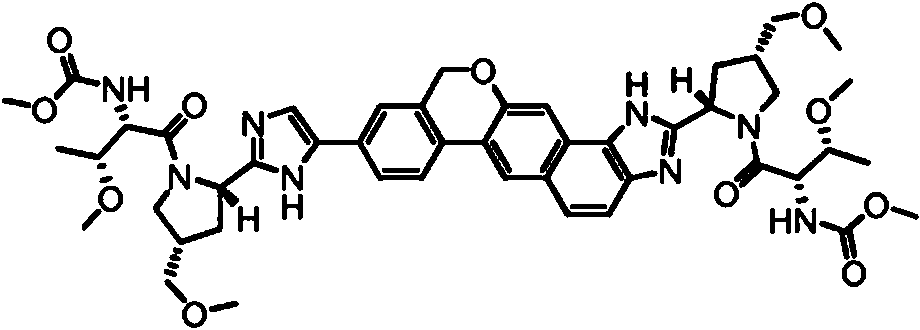
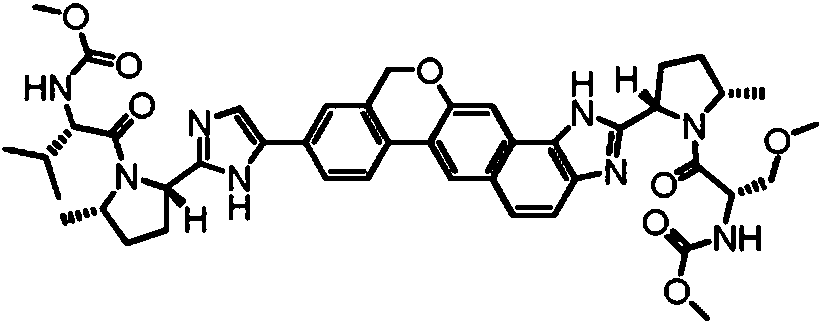
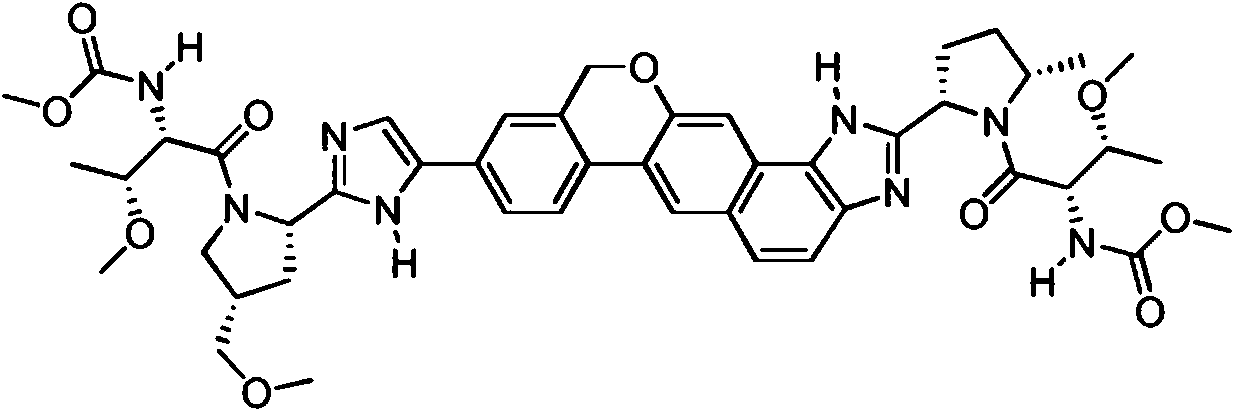
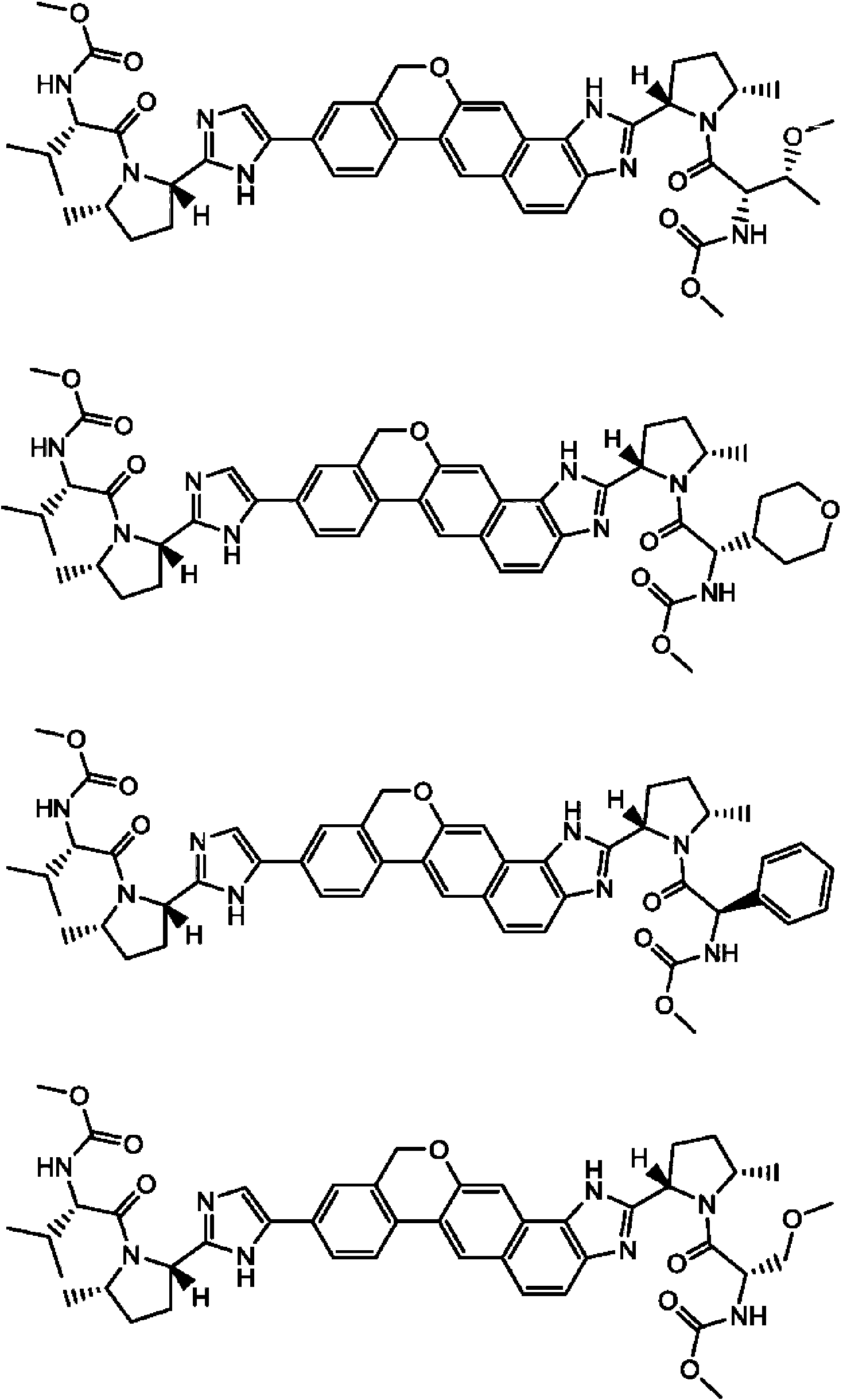
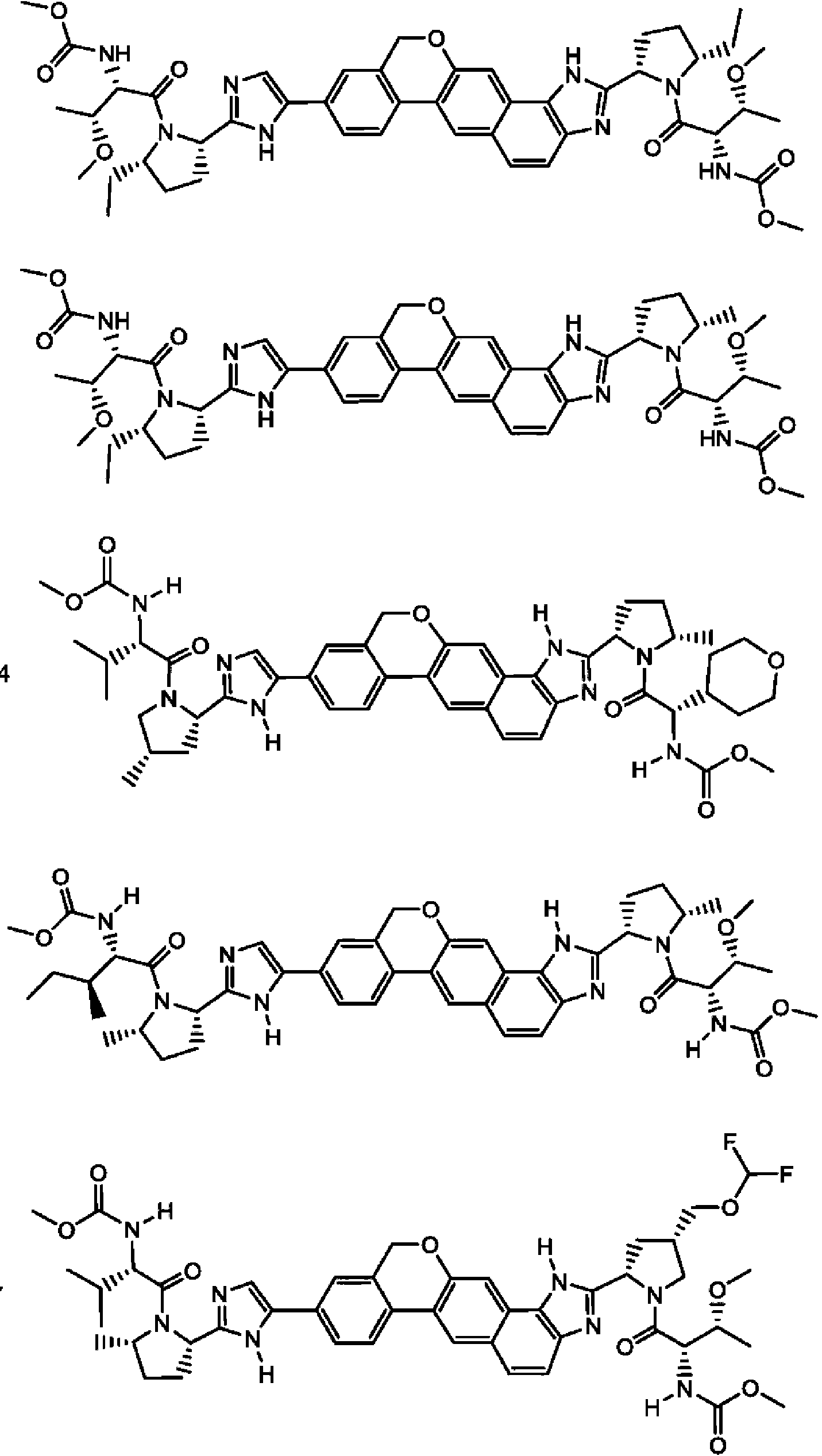
Un compuesto seleccionado de:**Fórmula** o una sal farmacéuticamente aceptable del mismo.
Description
DESCRIPCIÓN
Derivados de 9-(1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-D]imidazol y su utilización como inhibidores de HCV NS5A
ANTECEDENTES
[0001] La hepatitis C se reconoce como una enfermedad viral crónica del hígado que se caracteriza por una enfermedad hepática. Aunque los fármacos dirigidos al hígado se usan ampliamente y han demostrado efectividad, la toxicidad y otros efectos secundarios han limitado su utilidad. Los inhibidores del virus de la hepatitis C (HCV) son útiles para limitar el establecimiento y la progresión de la infección por e1HCV, así como en los ensayos de diagnóstico para el HCV.
[0002] Existe la necesidad de nuevos agentes terapéuticos contra el HCV. En particular, existe la necesidad de agentes terapéuticos contra el HCV que tengan una amplia actividad contra los genotipos de1HCV (por ejemplo, los genotipos 1a, 1b, 2a, 3a, 4a). También existe una necesidad particular de agentes que sean menos susceptibles a la resistencia viral. Se han descrito mutaciones de resistencia a los inhibidores para e1HCV NS5A para los genotipos 1a y 1b en Antimicrobial Agents and Chemotherapy, septiembre de 2010, volumen 54, p. 3641-3650,
RESUMEN
[0003] En una realización, la invención proporciona un compuesto seleccionado de:
o una sal farmacéuticamente aceptable del mismo.
[0004] La presente descripción también proporciona una composición farmacéutica que comprende un compuesto de la invención o una de sus sales farmacéuticamente aceptables y al menos un vehículo farmacéuticamente aceptable.
[0005] La presente divulgación también proporciona una composición farmacéutica para uso en el tratamiento de la hepatitis C (HCV). En una realización, la composición comprende al menos un agente terapéutico adicional para tratar el HCV. En una realización, el agente terapéutico se selecciona de ribavirina, un inhibidor de la proteasa NS3, un inhibidor de nucleósidos o nucleótidos de la polimerasa NS5B del HCV, un inhibidor de la alfa-glucosidasa 1, un hepatoprotector, un inhibidor no nucleósido del polímero del HCV, o combinaciones de los mismos. En una realización, la composición comprende además un nucleósido o inhibidor de nucleótidos de la polimerasa NS5B de1HCV. En una realización, el inhibidor de nucleósidos o nucleótidos de la polimerasa NS5B de1HCV se selecciona entre ribavirina, viramidina, levovirina, un L-nucleósido o isatoribina.
[0006] En una realización, se proporciona una composición farmacéutica que comprende un compuesto como se describe en el presente documento y al menos un inhibidor de nucleósidos o nucleótidos de NS5B polimerasa de HCV, y al menos un vehículo farmacéuticamente aceptable. En una realización, la composición comprende además un interferón, un interferón pegilado, ribavirina o combinaciones de los mismos. En una realización, el nucleósido o inhibidor de nucleótidos de la polimerasa NS5B del HCV es sofosbuvir. En una realización, se proporciona una composición farmacéutica que comprende un compuesto como se describe en el presente documento y al menos un inhibidor de la proteasa NS3, y al menos un vehículo farmacéuticamente aceptable. En una realización, la composición comprende además sofosbuvir.
[0007] La presente divulgación también proporciona una composición farmacéutica que comprende además un interferón o un interferón pegilado.
[0008] La presente divulgación también proporciona una composición farmacéutica que comprende además un análogo de nucleósido.
[0009] La presente divulgación también proporciona una composición farmacéutica en la que dicho análogo de nucleósido es seleccionado de ribavirina, viramidina, levovirina, un L-nucleósido e isatoribina y dicho interferón es ainterferón o pegilado a-interferón.
[0010] En otro aspecto, la descripción proporciona un compuesto de la invención, o una sal farmacéuticamente aceptable del mismo, para uso en el tratamiento profiláctico o terapéutico de la hepatitis C o un trastorno asociado con la hepatitis C.
DESCRIPCIÓN DETALLADA
[0011] Ahora se hará referencia en detalle a ciertas realizaciones de la divulgación, cuyos ejemplos se ilustran en las estructuras y fórmulas que se acompañan. Aunque la divulgación se describirá junto con las realizaciones enumeradas, se entenderá que no pretenden limitar la divulgación a esas realizaciones.
[0012] "Alquilo" es un hidrocarburo C1-C18 que contiene átomos de carbono normales, secundarios, terciarios o cíclicos. Los ejemplos son metilo (Me, -CH3), etilo (Et, -CH2CH3), 1 -propilo (n-Pr, n-propilo, -CH2CH2CH3), 2-propilo (i-Pr, i-propilo, -CH(CH3)2), 1- butil (n-Bu, n-butil, -CH2CH2CH2CH3), 2-metil-1-propilo (i-Bu, i-butil, -CH2CH(CH3)2), 2-butilo (s-Bu, s-butil, -CH(CH3)CH2CH3), 2-metil-2-propil (t-Bu, t-butil, -C(Ch 3)3), 1-pentil (n-pentilo, -CH2CH2CH2CH2CH3), 2-pentil (-CH(CH3)CH2CH2CH3), 3-pentil (-CH(CH2CH3)2), 2-metil-2-butilo (-C(CH3)2CH2CH3), 3-metil-2-butilo (-CH(CH3)CH(CH3)2), 3-metil-1-butilo (-CH2CH2CH(CH3)2), 2-metil-1-butilo (-CH2CH(CH3)CH2CH3), 1-hexil (-CH2CH2CH2CH2CH3), 2-hexil (-CH(CH3)CH2CH2CH2CH3), 3-hexil (-CH(CH2CH3)(CH2CH2CH3)), 2-metil-2-pentil (-C(CH3)2CH2CH2CH3), 3-metil-2-pentilo (-CH(CH3)CH(CH3)CH2CH3), 4-metil-2-pentil (-CH(CH3)CH2CH(CH3)2), 3
metil-3-pentil (-C(CHa)(CH2CHa)2), 2-metil-3-pentil (-CH(CH2CH3)CH(CH3)2), 2,3-dimetil-2-butilo (-C(CH3)2CH(CH3)2), 3,3-dimetil-2-butilo (-CH(CH3)C(CH3)3, y ciclopropilmetilo
[0013] "Arilo" significa un radical hidrocarbonado aromático monovalente de 6-20 átomos de carbono derivado de la eliminación de un átomo de hidrógeno de un solo átomo de carbono de un sistema de anillo aromático parental. Los grupos arilo típicos incluyen, pero no se limitan a, radicales derivados de benceno, benceno sustituido, naftaleno, antraceno, bifenilo y similares.
[0014] El término "amino", como se usa en el presente documento, se refiere a -NH2,
[0015] El término "quiral" se refiere a moléculas que tienen la propiedad de no superponibilidad de la pareja de imagen especular, mientras que el término "aquiral" se refiere a las moléculas que son superponibles en su compañero de imagen espejo.
[0016] El término "estereoisómeros" se refiere a compuestos que tienen una constitución química idéntica, pero difieren con respecto a la disposición de los átomos o grupos en el espacio.
[0017] "Diastereómero" se refiere a un estereoisómero con dos o más centros de quiralidad y cuyas moléculas no son imágenes especulares entre sí. Los diastereómeros tienen diferentes propiedades físicas, por ejemplo, puntos de fusión, puntos de ebullición, propiedades espectrales y reactividades. Las mezclas de diastereómeros se pueden separar en procedimientos analíticos de alta resolución, como por ejemplo, electroforesis y cromatografía.
[0018] Los "enantiómeros" se refieren a dos estereoisómeros de un compuesto que son imágenes especulares no superponibles entre sí.
[0019] El término "tratamiento" o "tratar", en la medida en que se relaciona con una enfermedad o afección incluye prevenir la aparición de la enfermedad o afección, inhibir la enfermedad o afección, eliminar la enfermedad o afección, y/o aliviar uno o más síntomas de la enfermedad o condición.
[0020] Las definiciones y convenciones estereoquímicas utilizadas en el presente documento generalmente siguen a SP Parker, DE., Dic. McGraw-Hill de Chemical Terms (1984) McGraw-Hill Book Company, Nueva York; y Eliel, E. y Wilen, S., StereoChemistry of Organic Compounds (1994) John Wiley & Sons, Inc., Nueva York. Muchos compuestos orgánicos existen en formas ópticamente activas, es decir, tienen la capacidad de rotar el plano de la luz polarizada en el plano. Al describir un compuesto ópticamente activo, los prefijos (D y L) o (R y S) se utilizan para denotar la configuración absoluta de la molécula sobre su(s) centro(s) quiral(s). Los prefijos d y 1 o (+) y (-) se emplean para designar el signo de rotación de la luz polarizada en el plano por el compuesto, con (-) o 1 lo que significa que el compuesto es levorotatorio. Un compuesto con el prefijo (+) o d es dextrorotatorio. Para una estructura química dada, estos estereoisómeros son idénticos, excepto que son imágenes especulares entre sí. Un estereoisómero específico también puede denominarse un enantiómero, y una mezcla de tales isómeros a menudo se denomina una mezcla enantiomérica. Una mezcla 50:50 de enantiómeros se denomina una mezcla racémica o un racemato, que puede ocurrir donde no ha habido estereoselección o estereoespecificidad en una reacción o proceso químico. Los términos "mezcla racémica" y "racemato" se refieren a una mezcla equimolar de dos especies enantioméricas, sin actividad óptica. La descripción incluye todos los estereoisómeros de los compuestos descritos en el presente documento.
Profármacos
[0021] El término "profármaco", como se usa en el presente documento, se refiere a cualquier compuesto que cuando se administra a un sistema biológico genera un compuesto de la divulgación que inhibe la actividad de1HCV ("el compuesto inhibidor activo"). El compuesto se puede formar a partir del profármaco como resultado de: (i) reacciones químicas espontáneas, (ii) reacciones químicas catalizadas por enzimas, (iii) fotólisis y/o (iv) reacciones químicas metabólicas).
[0022] El "resto profármaco" se refiere a un grupo funcional lábil que se separa del compuesto inhibidor activo durante el metabolismo, sistémicamente, dentro de una célula, por hidrólisis, escisión enzimática o por algún otro proceso (Bundgaard, Hans, "Diseño y aplicación de Prodrugs "en A Textbook of Drug Design and Development (1991), P. Krogsgaard-Larsen y H. Bundgaard, Eds. Harwood Academic Publishers, pp. 113-191). Las enzimas que son capaces de un mecanismo de activación enzimática con los compuestos profármacos de la divulgación incluyen, pero no se limitan a, amidasas, esterasas, enzimas microbianas, fosfolipasas, colinesterasas y fosfasas. Los restos profármacos pueden servir para mejorar la solubilidad, la absorción y la lipofilicidad para optimizar la administración de fármacos, la biodisponibilidad y la eficacia. Un resto profármaco puede incluir un metabolito activo o un fármaco en sí mismo.
[0023] Los ejemplos de restos de profármacos incluyen los ésteres de aciloximetilo sensibles a la hidrólisis o lábiles -CH2OC(=O)R99 y carbonatos de aciloximetilo -CH2OC(=O)OR99 donde R99 es C1-C6 alquilo, C1-C6 alquilo sustituido, C6-C20 arilo o C6-C20 arilo sustituido. El éster de aciloxialquilo se usó primero como una estrategia de profármaco para los ácidos carboxílicos y luego se aplicó a los fosfatos y fosfonatos de Farquhar et al. (1983) J. Pharm. Sci. 72: 324; también las patentes de EE.UU. Nos 4816570, 4968788, 5663159 y 5792756, Posteriormente, se usó el éster de aciloxialquilo para administrar ácidos fosfónicos a través de las membranas celulares y para mejorar la biodisponibilidad oral. Una variante cercana del éster aciloxialquílico, el éster alcoxicarbonilxialquílico (carbonato), también puede mejorar la biodisponibilidad oral como un resto profármaco en los compuestos de las combinaciones de la divulgación. Un ejemplo de éster de aciloximetilo es pivaloiloximetoxi, (POM)-CH2OC(=O)C(CH3)3 , Un resto de profármaco de carbonato de aciloximetilo ejemplar es pivaloiloximetilcarbonato (POC)-CH2OC(=O)OC(CH3)3 ,
Grupos protectores
[0024] En el contexto de la presente divulgación, los grupos protectores incluyen restos de profármacos y grupos protectores químicos.
[0025] El "grupo protector" se refiere a un resto de un compuesto que enmascara o altera las propiedades de un grupo funcional o las propiedades del compuesto en su totalidad. Los grupos de protección química y las estrategias para la protección/desprotección son bien conocidos en la técnica. Véase, por ejemplo, Protective Groups in Organic Chemistry, Theodora W. Greene, John Wiley & Sons, Inc., Nueva York, 1991, Los grupos protectores a menudo se utilizan para enmascarar la reactividad de ciertos grupos funcionales, para ayudar en la eficiencia de las reacciones químicas deseadas., por ejemplo, hacer y romper enlaces químicos de una manera ordenada y planificada. La protección de los grupos funcionales de un compuesto altera otras propiedades físicas además de la reactividad del grupo funcional protegido, como, por ejemplo, la polaridad, lipofilicidad (hidrofobicidad) y otras propiedades que pueden medirse con herramientas analíticas comunes. Los intermedios protegidos químicamente pueden ser biológicamente activos o inactivos.
[0026] Los compuestos protegidos también pueden presentar propiedades alteradas y, en algunos casos, optimizadas in vitro e in vivo, como, por ejemplo, el paso a través de membranas celulares y la resistencia a la degradación o el secuestro enzimático. En esta función, los compuestos protegidos con los efectos terapéuticos previstos pueden denominarse profármacos. Otra función de un grupo protector es convertir el fármaco parental en un profármaco, por lo que el fármaco parental se libera tras la conversión del profármaco in vivo. Debido a que los profármacos activos pueden absorberse más efectivamente que el fármaco parental, los profármacos pueden poseer una mayor potencia in vivo que el fármaco parental. Los grupos protectores se eliminan ya sea in vitro, en el caso de intermediarios químicos, o in vivo, en el caso de profármacos. Con productos químicos intermedios, no es particularmente importante que los productos resultantes después de la desprotección, por ejemplo, los alcoholes, sean fisiológicamente aceptables, aunque en general es más deseable si los productos son farmacológicamente inocuos.
[0027] Los grupos protectores están disponibles, se conocen y se usan comúnmente, y se usan opcionalmente para prevenir reacciones secundarias con el grupo protegido durante procedimientos sintéticos, es decir, rutas o métodos para preparar los compuestos de la divulgación. En su mayor parte, la decisión sobre qué grupos proteger, cuándo hacerlo y la naturaleza del grupo químico de protección "PG" dependerá de la química de la reacción que se va a proteger (por ejemplo, ácido, básico, oxidativo), condiciones reductivas u otras) y la dirección prevista de la síntesis. Los PG no necesitan ser, y generalmente no lo son, lo mismo si el compuesto está sustituido con múltiples PG. En general, se utilizará PG para proteger grupos funcionales tales como, por ejemplo, grupos carboxilo, hidroxilo, tio o amino y, por lo tanto, para prevenir reacciones secundarias o para facilitar la eficacia sintética. El orden de desprotección para producir grupos desprotegidos libres depende de la dirección prevista de la síntesis y de las condiciones de reacción que se van a encontrar, y puede ocurrir en cualquier orden según lo determinado por el experto.
[0028] Pueden protegerse diversos grupos funcionales de los compuestos de la divulgación. Por ejemplo, los grupos protectores para grupos -OH (ya sean hidroxilo, ácido carboxílico, ácido fosfónico u otras funciones) incluyen "grupos formadores de éter o éster". Los grupos formadores de éter o éster son capaces de funcionar como grupos protectores químicos en los esquemas sintéticos expuestos en este documento. Sin embargo, algunos grupos protectores de hidroxilo y tio no son grupos formadores de éter ni éster, como entenderán los expertos en la técnica, y se incluyen con amidas, que se describen a continuación.
[0029] Se describe un gran número de grupos protectores de hidroxilo y grupos formadores de amida y las correspondientes reacciones de escisión química en Grupos Protectores en Síntesis Orgánica, Theodora W. Greene (John Wiley & Sons, Inc., Nueva York, 1991, ISBN 0 -471-62301-6) ("Greene"). Véase también Kocienski, Philip J.; Grupos protectores (Georg Thieme Verlag Stuttgart, Nueva York, 1994). En particular, Capítulo 1, Grupos de protección: descripción general, páginas 1-20, CapítulO2, Grupos de protección de hidroxilo, páginas 21-94, Capítulo 3, Grupos de protección contra Diol, páginas 95-117, Capítulo 4, Grupos de protección de carboxilo, páginas 118-154, Capítulo 5, Grupos protectores de carbonil, páginas 155-184, Para los grupos protectores para ácido carboxílico, ácido fosfónico, fosfonato, ácido sulfónico y otros grupos protectores para ácidos, consulte Greene como se describe a
continuación.
Estereoisómeros
[0030] Los compuestos de la divulgación pueden tener centros quirales, por ejemplo, átomos de carbono o fósforo quirales. Los compuestos de la divulgación incluyen así todos los estereoisómeros, incluidos los enantiómeros, diastereómeros y atropisómeros. Además, los compuestos de la divulgación incluyen isómeros ópticos enriquecidos o resueltos en cualquiera o todos los átomos quirales asimétricos. En otras palabras, los centros quirales que se desprenden de las representaciones se proporcionan como mezclas no racémicas o racémicas. Las mezclas racémicas y diastereoméricas, así como los isómeros ópticos individuales aislados o sintetizados, sustancialmente libres de sus socios enantioméricos o diastereoméricos, están todos dentro del alcance de la divulgación. Las mezclas racémicas se separan en sus isómeros individuales, sustancialmente ópticamente puros, mediante técnicas bien conocidas como, por ejemplo, la separación de sales diastereoméricas formadas con adyuvantes ópticamente activos, por ejemplo, ácidos o bases seguidas por la conversión de nuevo a las sustancias ópticamente activas. En la mayoría de los casos, el isómero óptico deseado se sintetiza por medio de reacciones estereoespecíficas, comenzando con el estereoisómero apropiado del material de partida deseado o a través de reacciones enantioselectivas.
[0031] Los compuestos de la divulgación también pueden existir como isómeros tautoméricos en ciertos casos. Aunque solo se puede representar un tautómero, todas estas formas se contemplan dentro del alcance de la divulgación. Por ejemplo, los tautómeros de ene-amina pueden existir para los sistemas de purina, pirimidina, imidazol, guanidina, amidina y tetrazol, y todas sus posibles formas tautoméricas están dentro del alcance de la divulgación.
Sales e Hidratos
[0032] Los ejemplos de sales fisiológica o farmacéuticamente aceptables de los compuestos de la divulgación incluyen sales derivadas de una base apropiada, tal como, por ejemplo, un metal alcalino (por ejemplo, sodio), un metal alcalinotérreo (por ejemplo, magnesio), amonio y NX4+ (en donde X es C1-C4 alquilo). Las sales fisiológicamente aceptables de un átomo de hidrógeno o un grupo amino incluyen sales de ácidos carboxílicos orgánicos tales como, por ejemplo, ácidos acético, benzoico, láctico, fumárico, tartárico, maleico, malónico, málico, isetiónico, lactobiónico y succínico; ácidos sulfónicos orgánicos, tales como, por ejemplo, ácidos metanosulfónico, etanosulfónico, bencenosulfónico y p-toluenosulfónico; y ácidos inorgánicos, tales como, por ejemplo, ácidos clorhídrico, sulfúrico, fosfórico y sulfámico. Las sales fisiológicamente aceptables de un compuesto de un grupo hidroxi incluyen el anión de dicho compuesto en combinación con un catión adecuado tal como, por ejemplo, Na+ y NX4+ (en donde X se selecciona independientemente de H o un grupo C1-C4 alquilo).
[0033] Para uso terapéutico, las sales de los ingredientes activos de los compuestos de la divulgación serán típicamente fisiológicamente aceptables, es decir, serán sales derivadas de un ácido o base fisiológicamente aceptable. Sin embargo, las sales de ácidos o bases que no son fisiológicamente aceptables también pueden ser útiles, por ejemplo, en la preparación o purificación de un compuesto fisiológicamente aceptable. Todas las sales, ya sean derivadas o no de un ácido o base fisiológicamente aceptable, están dentro del alcance de la presente divulgación.
[0034] Las sales metálicas típicamente se preparan haciendo reaccionar el hidróxido metálico con un compuesto de esta descripción. Ejemplos de sales metálicas que se preparan de esta manera son sales que contienen Li+ , Na+ y K+. Una sal metálica menos soluble puede precipitarse a partir de la solución de una sal más soluble mediante la adición del compuesto metálico adecuado.
[0035] Además, las sales pueden formarse a partir de la adición de ácidos de ciertos ácidos orgánicos e inorgánicos, por ejemplo, HCl, HBr, H2SO4, H3PO4 o ácidos orgánicos sulfónicos, a centros básicos, típicamente aminas, o a grupos ácidos. Finalmente, debe entenderse que las composiciones de la presente invención comprenden compuestos de la divulgación en su forma no ionizada, así como zwitteriónica, y combinaciones con cantidades estequiométricas de agua como en hidratos.
[0036] También se incluyen dentro del alcance de esta descripción las sales de los compuestos parentales con uno o más aminoácidos. Cualquiera de los aminoácidos naturales o no naturales es adecuado, especialmente los aminoácidos naturales que se encuentran como componentes de proteínas, aunque el aminoácido típicamente es uno que lleva una cadena lateral con un grupo básico o ácido, por ejemplo, lisina, arginina o ácido glutámico o un grupo neutro tal como, por ejemplo, glicina, serina, treonina, alanina, isoleucina o leucina.
Métodos de inhibición del HCV
[0037] En este documento se describen métodos para inhibir la actividad de1HCV que comprenden el paso de tratar una muestra sospechosa de contener HCV con un compuesto o composición de la divulgación.
[0038] El paso de tratamiento comprende agregar el compuesto de la divulgación a la muestra o comprende agregar un precursor de la composición a la muestra. El paso de adición comprende cualquier método de administración como
se describe anteriormente.
[0039] Si se desea, la actividad del HCV después de la aplicación del compuesto puede observarse mediante cualquier método, incluidos los métodos directos e indirectos para detectar la actividad de1HCV. Se contemplan todos los métodos cuantitativos, cualitativos y semicuantitativos para determinar la actividad de1HCV. Típicamente, uno de los métodos de selección descritos anteriormente se aplica, sin embargo, cualquier otro método tal como, por ejemplo, la observación de las propiedades fisiológicas de un organismo vivo también son aplicables.
[0040] Muchos organismos contienen HCV. Los compuestos de esta descripción son útiles en el tratamiento o la profilaxis de afecciones asociadas con la activación del HCV en animales o en el hombre.
[0041] Sin embargo, en la selección de compuestos capaces de inhibir la actividad de1HCV, se debe tener en cuenta que los resultados de los ensayos enzimáticos no siempre se correlacionan con los ensayos de cultivos celulares. Por lo tanto, un ensayo basado en células típicamente debería ser la herramienta de selección primaria.
Formulaciones farmacéuticas
[0042] Los compuestos de esta descripción se formulan con vehículos y excipientes convencionales, que se seleccionarán de acuerdo con la práctica habitual. Las tabletas contendrán excipientes, deslizantes, rellenos, aglutinantes y similares. Las formulaciones acuosas se preparan en forma estéril y, cuando están destinadas a ser administradas por una administración diferente a la oral, generalmente serán isotónicas. Todas las formulaciones contendrán opcionalmente excipientes tales como, por ejemplo, los expuestos en e1Handbook of Pharmaceutical Excipients (1986). Los excipientes incluyen ácido ascórbico y otros antioxidantes, agentes quelantes tales como, por ejemplo, EDTA, carbohidratos tales como, por ejemplo, dextrina, hidroxialquilcelulosa, hidroxialquilmetilcelulosa, ácido esteárico y similares. El pH de las formulaciones varía de aproximadamente 3 a aproximadamente 11, pero generalmente es de aproximadamente 7 a 10, Normalmente, el compuesto se administrará en una dosis de 0,01 miligramos a 2 gramos. En una realización, la dosis será de aproximadamente 10 miligramos a 450 miligramos. Se contempla que el compuesto se puede administrar una, dos o tres veces al día.
[0043] En algunas realizaciones, el compuesto se administra durante aproximadamente 12 semanas o menos. En realizaciones adicionales, el compuesto se administra durante aproximadamente 12 semanas o menos, aproximadamente 8 semanas o menos, aproximadamente 8 semanas o menos, aproximadamente 6 semanas o menos, o aproximadamente 4 semanas o menos. El compuesto se puede administrar una vez al día, dos veces al día, una vez cada dos días, dos veces a la semana, tres veces a la semana, cuatro veces a la semana o cinco veces a la semana.
[0044] En realizaciones adicionales, se logra una respuesta virológica sostenida en aproximadamente 12 semanas, en aproximadamente 8 semanas, en aproximadamente 6 semanas, o en aproximadamente 4 semanas, o aproximadamente en 4 meses, o aproximadamente en 5 meses, o aproximadamente en 6 semanas. meses, o alrededor de 1 año, o alrededor de 2 años.
[0045] Si bien es posible que los ingredientes activos se administren solos, puede ser preferible presentarlos como formulaciones farmacéuticas. Las formulaciones, tanto para uso veterinario como para uso humano, de la divulgación comprenden al menos un ingrediente activo, como se definió anteriormente, junto con uno o más vehículos aceptables y, por lo tanto, otros ingredientes terapéuticos. El (los) portador(es) debe(n) ser "aceptable(s)" en el sentido de ser compatible(s) con los otros ingredientes de la formulación y fisiológicamente inocuo(s) para el receptor de la misma.
[0046] Las formulaciones incluyen aquellas adecuadas para las rutas de administración anteriores. Las formulaciones pueden presentarse convenientemente en forma de dosis unitaria y pueden prepararse por cualquiera de los métodos bien conocidos en la técnica de la farmacia. Las técnicas y formulaciones generalmente se encuentran en Remington's Pharmaceutical Sciences (Mack Publishing CO, Easton, PA). Tales métodos incluyen el paso de asociar el ingrediente activo con el vehículo que constituye uno o más ingredientes accesorios. En general, las formulaciones se preparan asociando de manera uniforme e íntima el ingrediente activo con portadores líquidos o portadores sólidos finamente divididos o ambos, y luego, si es necesario, dando forma al producto.
[0047] Las formulaciones de la presente divulgación adecuadas para administración oral pueden presentarse como unidades discretas tales como, por ejemplo, cápsulas, sellos o comprimidos que contienen cada uno una cantidad predeterminada del ingrediente activo; como un polvo o gránulos; como una solución o una suspensión en un líquido acuoso o no acuoso; o como una emulsión líquida de aceite en agua o una emulsión líquida de agua en aceite. El ingrediente activo también puede administrarse como un bolo, electuario o pasta.
[0048] Una tableta se fabrica por compresión o moldeo, opcionalmente con uno o más ingredientes accesorios. Los comprimidos comprimidos pueden prepararse comprimiendo en una máquina adecuada el ingrediente activo en una forma de flujo libre como, por ejemplo, un polvo o gránulos, opcionalmente mezclados con un aglutinante, lubricante, diluyente inerte, conservante, agente de superficie activa o dispersante. Las tabletas moldeadas pueden fabricarse moldeando en una máquina adecuada una mezcla del ingrediente activo en polvo humedecido con un diluyente líquido
inerte. Los comprimidos pueden opcionalmente recubrirse o marcarse y opcionalmente se formulan para proporcionar una liberación lenta o controlada del ingrediente activo de los mismos.
[0049] Para la administración al ojo u otros tejidos externos, por ejemplo, la boca y la piel, las formulaciones se aplican preferiblemente como una pomada o crema tópica que contiene el (los) ingrediente(s) activo(s) en una cantidad de, por ejemplo, 0,075 a 20% p/w (incluyendo ingrediente(s) activo(s) en un rango entre 0,1% y 20% en incrementos de 0,1% p/p tal como, por ejemplo, 0,6% p/p, 0,7% p/p, etc.), preferiblemente 0,2 a 15% p/p, y lo más preferiblemente 0,5 a 10% p/p. Cuando se formulan en una pomada, los ingredientes activos pueden emplearse con una base de pomada parafínica o miscible en agua. Alternativamente, los ingredientes activos pueden formularse en una crema con una base de crema de aceite en agua.
[0050] Si se desea, la fase acuosa de la base de crema puede incluir, por ejemplo, al menos el 30% p/p de un alcohol polihídrico, es decir, un alcohol que tiene dos o más grupos hidroxilo tales como, por ejemplo, propilenglicol, butano.
1,3-diol, manitol, sorbitol, glicerol y polietilenglicol (incluyendo PEG 400) y mezclas de los mismos. Las formulaciones tópicas pueden incluir deseablemente un compuesto que mejore la absorción o penetración del ingrediente activo a través de la piel u otras áreas afectadas. Los ejemplos de dichos potenciadores de la penetración dérmica incluyen dimetilsulfóxido y análogos relacionados.
[0051] La fase oleosa de las emulsiones de esta descripción puede estar constituida por ingredientes conocidos de una manera conocida. Aunque la fase puede comprender simplemente un emulsionante (también conocido como un agente emulgente), deseablemente comprende una mezcla de al menos un emulsionante con una grasa o un aceite o con una grasa y un aceite. Preferiblemente, se incluye un emulsionante hidrófilo junto con un emulsionante lipófilo que actúa como un estabilizante. También se prefiere incluir tanto un aceite como una grasa. Juntos, el (los) emulsionante(s) con o sin estabilizador(es) forman la llamada cera emulsionante, y la cera junto con el aceite y la grasa forman la llamada base de ungüento emulsionante que forma la fase oleosa dispersa de las formulaciones de crema.
[0052] Los emulgentes y estabilizantes de emulsión adecuados para uso en la formulación de la divulgación incluyen Tween® 60, Span® 80, alcohol cetoestearílico, alcohol bencílico, alcohol miristílico, monoestearato de glicerilo y laurilsulfato de sodio.
[0053] La elección de aceites o grasas adecuados para la formulación se basa en lograr las propiedades cosméticas deseadas. La crema debe ser preferiblemente un producto no graso, que no manche y lavable con una consistencia adecuada para evitar fugas de los tubos u otros recipientes. Éster alquílico mono o dibásico de cadena lineal o ramificada como, por ejemplo, di-isoadipato, estearato de isocetilo, diéster de propilenglicol de ácidos grasos de coco, miristato de isopropilo, oleato de decilo, palmitato de isopropilo, estearato de butil, estearato de 2-etilhexilo o a Se puede usar una mezcla de ésteres de cadena ramificada conocida como Crodamol CAP, los tres últimos son ésteres preferidos. Estos pueden usarse solos o en combinación dependiendo de las propiedades requeridas. Alternativamente, se utilizan lípidos de alto punto de fusión como, por ejemplo, parafina blanda blanca y/o parafina líquida u otros aceites minerales.
[0054] Las formulaciones farmacéuticas de acuerdo con la presente divulgación comprenden uno o más compuestos de la divulgación junto con uno o más vehículos o excipientes farmacéuticamente aceptables y opcionalmente otros agentes terapéuticos. Las formulaciones farmacéuticas que contienen el ingrediente activo pueden estar en cualquier forma adecuada para el método de administración deseado. Cuando se usan para uso oral, por ejemplo, pueden prepararse tabletas, trociscos, pastillas, suspensiones acuosas o de aceite, polvos o gránulos dispersables, emulsiones, cápsulas duras o blandas, jarabes o elixires. Las composiciones destinadas a uso oral pueden prepararse de acuerdo con cualquier método conocido en la técnica para la fabricación de composiciones farmacéuticas y tales composiciones pueden contener uno o más agentes que incluyen agentes edulcorantes, agentes aromatizantes, agentes colorantes y agentes conservantes, con el fin de proporcionar un sabor agradable. preparación. Las tabletas que contienen el ingrediente activo en mezcla con un excipiente farmacéuticamente aceptable no tóxico que son adecuados para la fabricación de tabletas son aceptables. Estos excipientes pueden ser, por ejemplo, diluyentes inertes, tales como, por ejemplo, carbonato de calcio o sodio, lactosa, lactosa monohidrato, croscarmelosa de sodio, povidona, calcio o fosfato de sodio; agentes de granulación y desintegración, tales como, por ejemplo, almidón de maíz o ácido algínico; agentes aglutinantes, tales como, por ejemplo, celulosa, celulosa microcristalina, almidón, gelatina o acacia; y agentes lubricantes, tales como, por ejemplo, estearato de magnesio, ácido esteárico o talco. Los comprimidos pueden no estar recubiertos o pueden recubrirse mediante técnicas conocidas, incluida la microencapsulación para retrasar la desintegración y la adsorción en el tracto gastrointestinal y, por lo tanto, proporcionar una acción sostenida durante un período más largo. Por ejemplo, puede emplearse un material de retardo temporal tal como, por ejemplo, monoestearato de glicerilo o diestearato de glicerilo solo o con una cera.
[0055] Las formulaciones para uso oral también pueden presentarse como cápsulas de gelatina dura en las que el ingrediente activo se mezcla con un diluyente sólido inerte, por ejemplo, fosfato de calcio o caolín, o como cápsulas de gelatina blanda en las que el ingrediente activo se mezcla con agua o un aceite. medio, tal como, por ejemplo, aceite de cacahuete, parafina líquida o aceite de oliva.
[0056] Las suspensiones acuosas de la divulgación contienen los materiales activos en mezcla con excipientes adecuados para la fabricación de suspensiones acuosas. Dichos excipientes incluyen un agente de suspensión, tal como, por ejemplo, carboximetilcelulosa de sodio, metilcelulosa, hidroxipropilmetilcelulosa, alginato de sodio, polivinilpirrolidona, goma de mascar y goma de acacia, y agentes dispersantes o humectantes como, por ejemplo, un fosfátido de origen natural (eg, lecithin), a condensation product of an alquilene oxide with a fatty acid (eg, polioxietilene stearate), a condensation product of etilene oxide with a long chain aliphatic alcohol (eg, heptadecaetileneoxicetanol), a condensation product of etilene oxide with a partial ester derived from a fatty acid and a hexitol anhydride (eg, polioxietilene sORbitan monooleate). La suspensión acuosa también puede contener uno o más conservantes tales como, por ejemplo, p-hidroxibenzoato de etilo o n-propilo, uno o más agentes colorantes, uno o más agentes saborizantes y uno o más agentes edulcorantes, tales como, por ejemplo, sacarosa o sacarina.
[0057] Las suspensiones de aceite pueden formularse suspendiendo el ingrediente activo en un aceite vegetal, tal como, por ejemplo, aceite de cacahuete, aceite de oliva, aceite de sésamo o aceite de coco, o en un aceite mineral como, por ejemplo, parafina líquida. Las suspensiones orales pueden contener un agente espesante, como, por ejemplo, cera de abeja, parafina dura o alcohol cetílico. Agentes edulcorantes, tales como, por ejemplo, los expuestos anteriormente, y agentes aromatizantes pueden agregarse para proporcionar una preparación oral sabrosa. Estas composiciones pueden conservarse mediante la adición de un antioxidante tal como, por ejemplo, ácido ascórbico.
[0058] Los polvos y gránulos dispersables de la divulgación adecuados para la preparación de una suspensión acuosa mediante la adición de agua proporcionan el ingrediente activo en mezcla con un agente dispersante o humectante, un agente de suspensión y uno o más conservantes. Los agentes dispersantes o humectantes adecuados y los agentes de suspensión se ejemplifican por los descritos anteriormente. También pueden estar presentes excipientes adicionales, por ejemplo, agentes edulcorantes, saborizantes y colorantes.
[0059] Las composiciones farmacéuticas de la divulgación también pueden estar en forma de emulsiones de aceite en agua. La fase oleosa puede ser un aceite vegetal, tal como, por ejemplo, aceite de oliva o aceite de cacahuete, un aceite mineral, tal como, por ejemplo, parafina líquida, o una mezcla de estos. Los agentes emulsionantes adecuados incluyen gomas naturales, tales como, por ejemplo, goma arábiga y goma tragacanto, fosfátidos naturales, tales como, por ejemplo, lecitina de soja, ésteres o ésteres parciales derivados de ácidos grasos y anhídridos de hexitol, tales como ejemplo, monooleato de sorbitán y productos de condensación de estos ésteres parciales con óxido de etileno, tales como, por ejemplo, monooleato de polioxietileno sorbitán. La emulsión también puede contener agentes edulcorantes y aromatizantes. Los jarabes y elixires se pueden formular con agentes edulcorantes, como, por ejemplo, glicerol, sorbitol o sacarosa. Tales formulaciones también pueden contener un demulcente, un conservante, un saborizante o un agente colorante.
[0060] Las composiciones farmacéuticas de la divulgación pueden estar en forma de una preparación inyectable estéril, tal como, por ejemplo, una suspensión acuosa u oleaginosa inyectable estéril. Esta suspensión puede formularse de acuerdo con la técnica conocida usando aquellos agentes dispersantes o humectantes adecuados y agentes de suspensión que se han mencionado anteriormente. La preparación inyectable estéril también puede ser una solución o suspensión inyectable estéril en un diluyente o disolvente no tóxico parenteralmente aceptable, como, por ejemplo, una solución en 1,3-butanodiol o preparada como un polvo liofilizado. Entre los vehículos y disolventes aceptables que pueden emplearse están el agua, la solución de Ringer y la solución isotónica de cloruro de sodio. Además, los aceites fijos estériles pueden emplearse convencionalmente como un disolvente o medio de suspensión. Para este propósito, se puede emplear cualquier aceite fijo insípido, incluyendo mono o diglicéridos sintéticos. Además, ácidos grasos tales como, por ejemplo, ácido oleico se pueden usar igualmente en la preparación de inyectables.
[0061] La cantidad de ingrediente activo que se puede combinar con el material portador para producir una forma de dosis única variará dependiendo del huésped tratado y del modo particular de administración. Por ejemplo, una formulación de liberación prolongada destinada a la administración oral a humanos puede contener aproximadamente de 1 a 1000 mg de material activo compuesto con una cantidad adecuada y conveniente de material portador que puede variar de aproximadamente 5 a aproximadamente 95% del total de composiciones (peso:peso). La composición farmacéutica puede prepararse para proporcionar cantidades fácilmente medibles para administración. Por ejemplo, una solución acuosa destinada a infusión intravenosa puede contener de aproximadamente 3 a 500 |jg del ingrediente activo por mililitro de solución para que pueda producirse la infusión de un volumen adecuado a una velocidad de aproximadamente 30 ml/h.
[0062] Las formulaciones adecuadas para la administración en el ojo incluyen gotas oculares en las que el ingrediente activo se disuelve o suspende en un vehículo adecuado, especialmente un disolvente acuoso para el ingrediente activo. El ingrediente activo está presente preferiblemente en tales formulaciones en una concentración de 0,5 a 20%, ventajosamente de 0,5 a 10%, particularmente alrededor de 1,5% p/p.
[0063] Las formulaciones adecuadas para la administración tópica en la boca incluyen pastillas que comprenden el ingrediente activo en una base con sabor, usualmente sacarosa y goma arábiga o tragacanto; pastillas que comprenden el ingrediente activo en una base inerte tal como, por ejemplo, gelatina y glicerina, o sacarosa y acacia; y enjuagues bucales que comprenden el ingrediente activo en un vehículo líquido adecuado.
[0064] Las formulaciones para administración rectal pueden presentarse como un supositorio con una base adecuada que comprende, por ejemplo, manteca de cacao o un salicilato.
[0065] Las formulaciones adecuadas para administración intrapulmonar o nasal tienen un tamaño de partícula, por ejemplo, en el intervalo de 0,1 a 500 micras (incluidos los tamaños de partícula en un intervalo de 0,1 a 500 micras en incrementos de micras tales como, por ejemplo, 0,5, 1, 30). micras, 35 micras, etc.), que se administra por inhalación rápida a través del pasaje nasal o por inhalación por la boca para llegar a los sacos alveolares. Las formulaciones adecuadas incluyen soluciones acuosas u oleosas del ingrediente activo. Las formulaciones adecuadas para la administración de aerosol o polvo seco pueden prepararse de acuerdo con métodos convencionales y pueden administrarse con otros agentes terapéuticos tales como, por ejemplo, los compuestos utilizados hasta ahora en el tratamiento o la profilaxis de afecciones asociadas con la actividad del HCV.
[0066] Las formulaciones adecuadas para administración vaginal se pueden presentar como pesarios, tampones, cremas, geles, pastas, espumas o formulaciones en aerosol que contienen además del ingrediente activo, los vehículos que se conocen en la técnica como apropiados.
[0067] Las formulaciones adecuadas para administración parenteral incluyen soluciones de inyección estériles acuosas y no acuosas que pueden contener antioxidantes, tampones, bacteriostáticos y solutos que hacen que la formulación sea isotónica con la sangre del receptor deseado; y suspensiones estériles acuosas y no acuosas que pueden incluir agentes de suspensión y agentes espesantes.
[0068] Las formulaciones se presentan en contenedores de dosis unitarias o de dosis múltiples, por ejemplo, ampollas y viales sellados, y pueden almacenarse en un estado liofilizado (liofilizado) que requiere solo la adición del vehículo líquido estéril, por ejemplo, agua. Para inyección, inmediatamente antes de su uso. Las soluciones y suspensiones para inyección extemporáneas se preparan a partir de polvos, gránulos y comprimidos estériles del tipo descrito anteriormente. Las formulaciones de dosificación unitaria preferidas son aquellas que contienen una dosis diaria o una dosis parcial diaria, según se cita aquí anteriormente, o una fracción apropiada de la misma, del ingrediente activo.
[0069] Debe entenderse que además de los ingredientes particularmente mencionados anteriormente, las formulaciones de esta divulgación pueden incluir otros agentes convencionales en la técnica teniendo en cuenta el tipo de formulación en cuestión, por ejemplo, los adecuados para la administración oral pueden incluir agentes aromatizantes.
[0070] La descripción proporciona además composiciones veterinarias que comprenden al menos un ingrediente activo como se define anteriormente junto con un vehículo veterinario.
[0071] Los portadores veterinarios son materiales útiles para el fin de administrar la composición y pueden ser materiales sólidos, líquidos o gaseosos que, de otro modo, son inertes o aceptables en la técnica veterinaria y son compatibles con el ingrediente activo. Estas composiciones veterinarias se pueden administrar por vía oral, parenteral o por cualquier otra vía deseada.
[0072] Los compuestos de la divulgación también pueden formularse para proporcionar una liberación controlada del ingrediente activo para permitir una dosificación menos frecuente o para mejorar el perfil farmacocinético o de toxicidad del ingrediente activo. Por consiguiente, la divulgación también proporciona composiciones que comprenden uno o más compuestos de la divulgación formulada para liberación sostenida o controlada.
[0073] La dosis efectiva de ingrediente activo depende al menos de la naturaleza de la condición tratada, la toxicidad, si el compuesto se usa profilácticamente (dosis más bajas), el método de administración y la formulación farmacéutica, y estará determinado por el clínico utilizando estudios de dosis convencionales.
Vías de administración
[0074] Se pueden administrar uno o más compuestos de la divulgación (en este documento denominados ingredientes activos) por cualquier vía apropiada para la afección que se va a tratar. Las vías adecuadas incluyen vía oral, rectal, nasal, tópica (incluyendo bucal y sublingual), vaginal y parenteral (incluyendo subcutánea, intramuscular, intravenosa, intradérmica, intratecal y epidural), y similares. Se apreciará que la vía preferida puede variar, por ejemplo, con la condición del destinatario. Una ventaja de los compuestos de esta descripción es que están biodisponibles por vía oral y pueden dosificarse por vía oral.
Terapia de combinación de HCV
[0075] En otra realización, los ejemplos no limitantes de combinaciones adecuadas incluyen combinaciones de uno o más compuestos de la invención con uno o más interferones, ribavirina o sus análogos, inhibidores de la proteasa NS3 del HCV, inhibidores de la alfa-glucosidasa 1, hepatoprotectores, nucleósidos o inhibidores de nucleótidos de la polimerasa NS5B del HCV, inhibidores no nucleósicos de la polimerasa NS5B de1HCV, inhibidores de la NS5A del HCV, agonistas de TLR-7, inhibidores de la ciclofilina, inhibidores IRES de1HCV, potenciadores farmacocinéticos y
otros fármacos o agentes terapéuticos para tratar el HCV.
[0076] Más específicamente, uno o más compuestos de la invención se pueden combinar con uno o más compuestos seleccionados del grupo que consiste en
1) interferones, por ejemplo, rIFN-alfa 2b pegilado (PEG-Intron®), rIFN-alfa 2a pegilado (Pegasys®), rIFN-alfa 2b (Intron® A), rIFN-alfa 2a (Roferon®-A), interferón alfa (m Or -22, OPC-18, Alfaferone®, Alfanative®, Multiferon®, subalin), interferon alfacon-1 (Infergen®), interferon alfa-n1 (Wellferon), interferon alfa-n3 (Alferon®), interferon- beta (Avonex®, DL-8234), interferón-omega (omega DUROS®, Biomed® 510), albinterferón alfa-2b (Albuferon®), IFN alfa-2b XL, BLX-883 (Locteron®), DA-3021, interferón alfa-2b glicosilado (AVI-005), PEG-Infergen, interferón lambda-1 PEGilado (IL-29 PEGilado) y belerofon®;
2) ribavirina y sus análogos, por ejemplo, ribavirina (Rebetol®, Copegus®) y taribavirina (Viramidine®);
3) inhibidores de la proteasa NS3 del HCV, por ejemplo, boceprevir (SCH-503034, SCH-7), telaprevir (VX-950), TMC435350, BI-1335, BI-1230, MK-7009, VBY-376, VX-500, GS -9256, GS-9451, BMS-605339, PHX-1766, AS-101, YH-5258, YH5530, YH5531, ABT-450, ACH-1625, ITMN-191, AT26893, MK5172, MK6325 y MK2748;
4) inhibidores de alfa-glucosidasa 1, por ejemplo, celgosivir (MX-3253), Miglitol y UT-231B;
5) hepatoprotectores, por ejemplo, emericasan (IDN-6556), ME-3738, GS-9450 (LB-84451), silibilin y MitoQ;
6) inhibidores nucleosídicos o nucleotídicos de la polimerasa NS5B de1HCV, por ejemplo, R1626, R7128 (R4048), IDX184, IDX-102, BCX-4678, valopicitabina (NM-283), MK-0608, sofosbuvir (GS-7977 (anteriormente PSI- 7977)), VLX-135 (anteriormente ALS-2200) e INX-189 (ahora BMS986094);
7) inhibidores no nucleosídicos de la polimerasa NS5B del HCV, por ejemplo, PF-868554, VCH-759, VCH-916, JTK-652, MK-3281, GS-9190, VBY-708, VCH-222, A848837, ANA-598, GL60667, GL59728, A-63890, A-48773, A-48547. BC-2329, VCH-796 (nesbuvir), GSK625433, BILN-1941, XTL-2125, ABT-072, ABT-333, GS-9669, PSI-7792, y GS-9190;
8) inhibidores de NS5A de HCV, por ejemplo, AZD-2836 (A-831), BMS-790052, ACH-3102, ACH-2928, MK8325, MK4882, MK8742, PSI-461, IDX719, GS-5885 y A-689;
9) agonistas de TLR-7, por ejemplo, imiquimod, 852A, GS-9524, ANA-773, ANA-975 (isatoribina), AZD-8848 (DSP-3025) y SM-360320;
10) inhibidores de ciclofilina, por ejemplo, DEBIO-025, SCY-635 y NIM811;
11) Inhibidores IRES del HCV, por ejemplo, MCI-067;
12) potenciadores farmacocinéticos, por ejemplo, BAS-100, SPI-452, PF-4194477, TMC-41629, GS-9350 (cobicistat), GS-9585 y roxitromicina; y
13) otros medicamentos para el tratamiento del HCV, por ejemplo, timosina alfa 1 (Zadaxin), nitazoxanida (Alinea, NTZ), BIVN-401 (virostat), PYN-17 (altirex), KPE02003002, actilon (CPG-10101), GS-9525, KRN-7000, civacir, GI-5005, XTL-6865, BIT225, PTX-111, ITX2865, TT-033i, ANA 971, NOV-205, tarvacin, EHC-18, VGX-410C, EMZ-702, AVI 4065, BMS-650032, BMS-791325, Bavituximab, MDX-1106 (ONO-4538), Oglufanide, y VX-497 (merimepodib).
[0077] En otra realización más, la presente solicitud describe composiciones farmacéuticas que comprenden un compuesto como se describe en el presente documento, o una sal farmacéuticamente aceptable de los mismos, en combinación con al menos un agente terapéutico y un portador o excipiente farmacéuticamente aceptable.
[0078] En otra realización, se proporciona una composición farmacéutica que comprende un compuesto de la invención y sofosbuvir y/o GS-5885 y opcionalmente un interferón o ribavirina.
[0079] En otra realización, se proporciona una composición farmacéutica que comprende un compuesto de la invención y un inhibidor de nucleósidos o nucleótidos de la polimerasa NS5B de1HCV y opcionalmente un interferón o ribavirina.
[0080] Se contempla que los agentes terapéuticos adicionales se administrarán de una manera que es conocida en la técnica y la dosis puede ser seleccionada por alguien experto en la materia. Por ejemplo, pueden administrarse agentes terapéuticos adicionales en una dosis de aproximadamente 0,01 miligramos a aproximadamente 2 gramos por día.
Metabolitos de los compuestos
[0081] Los productos metabólicos in vivo de los compuestos pueden resultar, por ejemplo, de la oxidación, reducción, hidrólisis, amidación, esterificación y similares del compuesto administrado, principalmente debido a procesos enzimáticos. Tales productos típicamente se identifican mediante la preparación de un compuesto radiomarcado (p.ej., C14 o H3) de la divulgación, administrándolo por vía parenteral en una dosis detectable (p.ej., Mayor que aproximadamente 0,5 mg/kg) a un animal como, por ejemplo, rata, ratón, cobaya, mono o al hombre, lo que permite un tiempo suficiente para que se produzca el metabolismo (por lo general, alrededor de 30 segundos a 30 horas) y el aislamiento de sus productos de conversión de la orina, sangre u otras muestras biológicas. Estos productos se aíslan fácilmente ya que están marcados (otros se aíslan mediante el uso de anticuerpos capaces de unirse a epítopos que sobreviven en el metabolito). Las estructuras de los metabolitos se determinan de manera convencional, por ejemplo, mediante análisis de MS o RMN. En general, el análisis de los metabolitos se realiza de la misma manera que los estudios de metabolismo de fármacos convencionales bien conocidos por los expertos en la técnica. Los productos de conversión, siempre que no se encuentren de otra manera in vivo, son útiles en ensayos de diagnóstico para la dosificación terapéutica de los compuestos de la divulgación incluso si no poseen actividad inhibidora de HCV por sí mismos.
[0082] Se conocen métodos para determinar la estabilidad de compuestos en secreciones gastrointestinales por sustitución.
Métodos ejemplares para hacer los compuestos
[0083] Las composiciones se preparan mediante cualquiera de las técnicas aplicables de síntesis orgánica. Muchas de estas técnicas son bien conocidas en la técnica. Sin embargo, muchas de las técnicas conocidas se elaboran en el Compendio de métodos orgánicos sintéticos (John Wiley & Sons, Nueva York), vol. 1, Ian T. Harrison y Shuyen Harrison, 1971; Vol. 2, Ian T. Harrison y Shuyen Harrison, 1974; Vol. 3, Louis S. Hegedus y Leroy Wade, 1977; Vol. 4, Leroy G. Wade, Jr., 1980; Vol. 5, Leroy G. Wade, Jr., 1984; y vol. 6, Michael B. Smith; así como March, J., Advanced Organic Chemistry, tercera edición, (John Wiley & Sons, Nueva York, 1985), Comprehensive Organic Synthesis. Selectividad, estrategia y eficiencia en la química orgánica moderna. En 9 volúmenes, Barry M. Trost, editor en jefe (Pergamon Press, Nueva York, 1993 impresión). Otros métodos adecuados para preparar compuestos de la divulgación se describen en la publicación de solicitud de patente internacional número WO 2006/020276,
[0084] En los esquemas y ejemplos a continuación se proporcionan varios métodos ejemplares para la preparación de las composiciones de la divulgación. Estos métodos pretenden ilustrar la naturaleza de tales preparaciones y no pretenden limitar el alcance de los métodos aplicables.
[0085] En general, las condiciones de reacción tales como, por ejemplo, la temperatura, el tiempo de reacción, los disolventes, los procedimientos de elaboración y similares, serán las comunes en la técnica para que se lleve a cabo la reacción particular. El material de referencia citado, junto con el material citado en el mismo, contiene descripciones detalladas de tales condiciones. Normalmente, las temperaturas serán de -100°C a 200°C, los solventes serán apróticos o próticos, y los tiempos de reacción serán de 10 segundos a 10 días. La preparación generalmente consiste en apagar los reactivos sin reaccionar seguidos de la partición entre un sistema de capa orgánica/agua (extracción) y separar la capa que contiene el producto.
[0086] Las reacciones de oxidación y reducción se llevan a cabo típicamente a temperaturas cercanas a la temperatura ambiente (aproximadamente 20°C), aunque para reducciones de hidruros metálicos frecuentemente la temperatura se reduce de 0°C a -100°C, los disolventes son típicamente apróticos para reducciones y pueden ser próticos o apróticos para oxidaciones. Los tiempos de reacción se ajustan para lograr las conversiones deseadas.
[0087] Las reacciones de condensación se llevan a cabo típicamente a temperaturas cercanas a la temperatura ambiente, aunque para condensaciones controladas cinéticamente no equilibradas también son comunes las temperaturas reducidas (0°C a -100°C). Los solventes pueden ser próticos (comunes en reacciones de equilibrio) o apróticos (comunes en reacciones controladas cinéticamente).
[0088] Las técnicas sintéticas estándar tales como, por ejemplo, la eliminación azeotrópica de los subproductos de la reacción y el uso de condiciones de reacción anhidras (por ejemplo, ambientes de gas inerte) son comunes en la técnica y se aplicarán cuando sea aplicable.
[0089] Los términos "tratado", "tratamiento", "tratar" y similares, cuando se usan en relación con una operación química sintética, significan contacto, mezcla, reacción, permitiendo reaccionar, ponerse en contacto y otros términos comunes. en la técnica para indicar que una o más entidades químicas se tratan de tal manera que se conviertan en una o más entidades químicas. Esto significa que "tratar el compuesto uno con el compuesto dos" es sinónimo de "permitir que el compuesto uno reaccione con el compuesto dos", "poner en contacto el compuesto uno con el compuesto dos", "reaccionar el compuesto uno con el compuesto dos”, y otras expresiones comunes en la técnica de síntesis orgánica para indicar razonablemente que el compuesto uno fue "tratado", "reaccionó", "se le permitió reaccionar”, etc., con el
compuesto 2, Por ejemplo, tratar indica la manera razonable y habitual en que los químicos orgánicos pueden reaccionar. A menos que se indique lo contrario, se refiere a concentraciones normales (0,01M a 10M, típicamente 0,1M a 1M), temperaturas (-100°C a 250°C, típicamente -78°C a 150°C, más típicamente -78°C a 100°C, aún más típicamente de 0°C a 100°C), recipientes de reacción (típicamente vidrio, plástico, metal), solventes, presiones, atmósferas (típicamente aire para reacciones insensibles al oxígeno y al agua o nitrógeno o argón para oxígeno) o sensibles al agua), etc.. El conocimiento de reacciones similares conocidas en la técnica de la síntesis orgánica se utiliza para seleccionar las condiciones y el aparato para "tratar" en un proceso dado. En particular, un experto en la materia en la técnica de la síntesis orgánica selecciona condiciones y aparatos razonablemente Se espera que lleve a cabo con éxito las reacciones químicas de los procesos descritos en base al conocimiento en la técnica.
[0090] Las modificaciones de cada uno de los esquemas ejemplares y en los Ejemplos (en adelante, "esquemas ejemplares") conducen a varios análogos de los materiales ejemplares específicos producidos. Las citas citadas anteriormente que describen métodos adecuados de síntesis orgánica son aplicables a tales modificaciones.
[0091] En cada uno de los esquemas ejemplares, puede ser ventajoso separar los productos de reacción entre sí y/o de los materiales de partida. Los productos deseados de cada paso o serie de pasos se separan y/o purifican (en lo sucesivo, se separan) hasta el grado deseado de homogeneidad mediante las técnicas comunes en la técnica. Típicamente, tales separaciones implican extracción multifase, cristalización de un disolvente o mezcla de disolventes, destilación, sublimación o cromatografía. La cromatografía puede involucrar cualquier número de métodos que incluyen, por ejemplo: fase inversa y fase normal; exclusión de tamaño; intercambio iónico; métodos y aparatos de cromatografía líquida de alta, media y baja presión; analítica a pequeña escala; simulación de lecho móvil (SMB) y cromatografía preparativa de capa fina o gruesa, así como técnicas de cromatografía flash y de capa fina a pequeña escala.
[0092] Otra clase de métodos de separación implica el tratamiento de una mezcla con un reactivo seleccionado para unirse a un producto deseado que se puede separar de otro modo, material de partida sin reaccionar, reacción por producto, o similares. Tales reactivos incluyen adsorbentes o absorbentes tales como, por ejemplo, carbón activado, tamices moleculares, medios de intercambio iónico, o similares. Alternativamente, los reactivos pueden ser ácidos en el caso de un material básico, bases en el caso de un material ácido, reactivos de unión tales como, por ejemplo, anticuerpos, proteínas de unión, quelantes selectivos tales como, por ejemplo, éteres de corona, líquido/reactivos de extracción de iones líquidos (LIX) o similares.
[0093] La selección de los métodos apropiados de separación depende de la naturaleza de los materiales involucrados. Por ejemplo, punto de ebullición y peso molecular en destilación y sublimación, presencia o ausencia de grupos funcionales polares en cromatografía, estabilidad de materiales en medios ácidos y básicos en extracción multifase, y similares. Un experto en la materia aplicará las técnicas más probables para lograr la separación deseada.
[0094] Se puede obtener un solo estereoisómero, por ejemplo, un enantiómero, sustancialmente libre de su estereoisómero por resolución de la mezcla racémica usando un método tal como, por ejemplo, formación de diastereómeros usando agentes de resolución ópticamente activos (estereoquímica de compuestos de carbono, 1962) por EL Eliel, McGraw Hill; Lochmuller, CH, (1975) J. Cromatogr., 113, 3) 283-302). Las mezclas racémicas de compuestos quirales de la divulgación se pueden separar y aislar por cualquier método adecuado, que incluye: (1) formación de sales iónicas, diastereoméricas con compuestos quirales y separación por cristalización fraccionada u otros métodos, (2) formación de compuestos diastereoméricos con quirales reactivos de derivación, separación de los diastereómeros y conversión a los estereoisómeros puros, y (3) separación de los estereoisómeros sustancialmente puros o enriquecidos directamente en condiciones quirales.
[0095] En el método (1), las sales diastereoméricas se pueden formar por reacción de bases quirales enantioméricamente puras como, por ejemplo, brucina, quinina, efedrina, estricnina, a-metil-p-feniletilamina (anfetamina) y similares con compuestos asimétricos que tienen funcionalidad ácida, como, por ejemplo, ácido carboxílico y ácido sulfónico. Las sales diatereoméricas se pueden inducir a separar por cristalización fraccionada o cromatografía iónica. Para la separación de los isómeros ópticos de los compuestos amino, la adición de ácidos carboxílicos o sulfónicos quirales, tales como, por ejemplo, ácido canforsulfónico, ácido tartárico, ácido mandélico o ácido láctico puede dar como resultado la formación de sales diastereoméricas.
[0096] Alternativamente, por el método (2), el sustrato a resolver se hace reaccionar con un enantiómero de un compuesto quiral para formar un par diastereomérico (Eliel, E. y Wilen, S. (1994) Estereoquímica de compuestos orgánicos, John Wiley & Sons, Inc., p. 322). Los compuestos diastereoméricos pueden formarse haciendo reaccionar compuestos asimétricos con reactivos de derivación quiral enantioméricamente puros, tales como, por ejemplo, derivados de mentilo, seguidos de la separación de los diastereoisómeros y la hidrólisis para producir el sustrato libre, enantioméricamente enriquecido. Un método para determinar la pureza óptica implica hacer ésteres quirales, como, por ejemplo, un éster de mentilo, por ejemplo, (-) cloroformiato de mentilo en presencia de una base, o éster de Mosher, a-metoxi-a-(trifluorometil)fenil acetato (Jacob III. (1982) J. Org. Chem. 47: 4165), de la mezcla racémica, y analizando el espectro de RMN para la presencia de los dos diastereoisómeros atropisoméricos. Los diastereómeros estables de los compuestos atropisoméricos se pueden separar y aislar mediante cromatografía de fase normal e inversa siguiendo los métodos para la separación de naftil-isoquinolinas atropisoméricas (Hoye, T., WO 96/15111). Por el método (3),
una mezcla racémica de dos enantiómeros se puede separar por cromatografía usando una fase estacionaria quiral (Chiral Liquid Cromatography (1989)WJ Lough, DE. Chapman y Hall, Nueva York; Okamoto, (1990) J. de Cromatogr.
513: 375-378). Los enantiómeros enriquecidos o purificados se pueden distinguir por métodos utilizados para distinguir otras moléculas quirales con átomos de carbono asimétricos, como, por ejemplo, la rotación óptica y el dicroísmo circular.
Esquemas y ejemplos
[0097] Los aspectos generales de estos métodos ejemplares se describen a continuación y en los Ejemplos. Cada uno de los productos de los siguientes procesos se separa, se aísla y/o se purifica opcionalmente antes de su uso en procesos posteriores.
[0098] En el siguiente ejemplo, se proporcionan varios métodos ejemplares para la preparación de compuestos de la divulgación, por ejemplo, en los siguientes ejemplos. Estos métodos pretenden ilustrar la naturaleza de tales preparaciones y no pretenden limitar el alcance de los métodos aplicables. Ciertos compuestos de la divulgación se pueden usar como intermedios para la preparación de otros compuestos de la divulgación. En los métodos ejemplares descritos aquí, el fragmento E-V- también puede escribirse como R9-. PG representa un grupo protector común para el grupo funcional dado que se adjunta. La instalación y eliminación del grupo protector se puede lograr utilizando técnicas estándar, como, por ejemplo, las descritas en Wuts, PGM, Greene, T. Protective Groups in Organic Synthesis, 4a DE.; John Wiley & Sons, Inc.: Hoboken, Nueva Jersey, 2007.
Esquema 1. Síntesis representativa de E-V-C(=O)-P-W-P-C(=O)-V-E
[0099] El esquema 1 muestra una síntesis general de una molécula E-V-C(=O)-P-W-P-C(=O)-V-E de la invención en la que, con fines ilustrativos, E es metoxicarbonilamino. El tratamiento de 1a o 1c con uno o dos equivalentes respectivamente de cloroformiato de metilo en condiciones básicas (por ejemplo, hidróxido de sodio) proporciona la molécula 1b o 1d.
Esquema 2. Síntesis representativa de E-V-C(=O)-P-W-P-C(=O)-V-E
[0100] El esquema 2 muestra una síntesis general de una molécula E-V -E de la invención en la que, con fines ilustrativos, P es pirrolidina. El acoplamiento de la amin realiza utilizando un reactivo de acoplamiento peptídico (por ejemplo, HATu ) para proporciona amina 2d se acopla con dos equivalentes de 2b en condiciones similares para proporcionar 2
Esquema 6. Síntesis representativa de R1-V-C(=O)-P-R2
[0101] El Esquema 6 muestra una síntesis general de un intermedio R1-VC(=O)-P-R2 en donde, para fines ilustrativos, P es pirrolidina, R1 es un grupo genérico que se representa como -E o un grupo protector de amino y R2 es un grupo genérico que se representa como -W-P-C(=O)-V-E, -W-P-C(=O)-V-NH-PG, -W-P-NH-PG, o -W-NH-PG. El acoplamiento de la amina 6a (o 6d, 6h, 6k) con el ácido 6b o 6e se realiza utilizando un reactivo de acoplamiento peptídico (por ejemplo, HATU) para proporcionar 6c (o 6f, 6g, 6i, 6j, 6l, 6m) respectivamente.
Esquema 7. Síntesis representativa de E-V-C(=O)-R1
[0102] El Esquema 7 muestra una síntesis general de un intermedio E-V-C(=O)-R1 en el que, para fines ilustrativos, E es metoxicarbonilamino y R1 es un grupo genérico que se representa como -P-W-P-C(=O)-V-NH-PG, -P-W-P-PG, -P-W-PG, -P-PG, o -O-PG. El tratamiento de 7a (o 7c, 7e, 7g, 7i) con cloroformiato de metilo en condiciones básicas (por ejemplo, hidróxido de sodio) proporciona la molécula 7b (o 7d, 7f, 7h, 7j).
Esquema 9. Síntesis representativa de R1-P-R2
[0103] El esquema 9 muestra una síntesis general de un intermedio de R1-P-R2 en el que, con fines ilustrativos, R1 es -C(=O)-V-E o un grupo protector y R2 es un benzamidazol sustituido. La formación del bencimidazol se logra acoplando el ácido 9b o 9e con una arilamina 9a, utilizando un reactivo de acoplamiento peptídico tal como HATU, para proporcionar 9c o 9d. La ciclación de la amida en presencia de un ácido (como el ácido acético) produce la molécula que contiene bencimidazol 9d o 9g.
[0104] La formación de múltiples bencimidazoles se realiza de la misma manera, comenzando con una bis-diamina para proporcionar el correspondiente bis-benzamidazol.
Esquema 20. Síntesis representativa de R1-P-W-P-R2
[0105] El esquema 20 muestra una síntesis general de un intermedio de R1-P-W-P-R2 de la invención en el que, con fines ilustrativos, R1 y R2 son grupos protectores independientes y W es una unidad de dos anillos aromáticos construida a través de una ciclación mediada por un metal de transición. La alquilación de fenol 20b con un bromuro de alquilo, tal como 20a, proporciona el éter 20c. La ciclación de los anillos aromáticos en presencia de un catalizador de paladio proporciona el compuesto 20d. El tratamiento de 20d con CuBR2 proporciona la a-halocetona 20e, que proporciona 20f con la adición de un ácido en condiciones básicas (por ejemplo, Et3N). La reacción de 20f con una amina o sal de amina (por ejemplo, acetato de amonio) produce la molécula que contiene imidazol 20g. La oxidación de 20g, 20i o 20l se puede lograr calentando en presencia de MnO2 para proporcionar 20h, 20j o 20m, respectivamente. La conversión de 20g o 20h con un catalizador de paladio, como Pd2dba3 y X-Phos, y una fuente de boro tal como bis(piinasa) diboron, proporciona el éster borónico 20i o 20j. El éster borónico se acopla con una pareja
de acoplamiento apropiado (por ejemplo, 20k) usando un catalizador de paladio, como Pd(PPh3)4 o PdCh(dppf), para proporcionar 20l o 20m. Para cada reacción de acoplamiento cruzado mediada por metal de transición, las funciones del nucleófilo y el electrófilo pueden invertirse para proporcionar el mismo producto de acoplamiento. Otros acoplamientos cruzados mediados por metales de transición que permiten la construcción de W, pero que emplean parejas y reactivos de acoplamiento alternativos, incluyen, entre otros, los acoplamientos Negishi, Kumada, Stille y Ullman. Para la preparación de dos anillos aromáticos alternativos que contienen grupos W, este esquema general puede aplicarse a través de la elección apropiada de los reactivos de partida.
Esquema 21. Síntesis representativa de R1-P-W-P-R2
[0106] El esquema 21 muestra una síntesis general de un intermedio R1-P-W-P-R2 de la invención en el que, con fines ilustrativos, R1 y R2 son grupos protectores independientes y W es una unidad de dos anillos aromáticos construida a través de una ciclación mediada por metales de transición. El tratamiento de 20d con un reactivo de vinilo activado (por ejemplo, viniltrifluoroborato de potasio) en presencia de un catalizador de paladio (por ejemplo, acetato de paladio y S-Phos) proporciona el compuesto de vinilo 21a. La conversión a a-halo cetona correspondiente se puede realizar mediante bromación con N-bromosuccinimida, seguida de oxidación con MnO2, El desplazamiento de a-halo cetona se produce mediante la adición de un ácido en condiciones básicas (por ejemplo, Et3N). La bromación de 21d continúa con el tratamiento con tribromuro de piridinio, y se sigue la adición de un segundo ácido en condiciones básicas para proporcionar el diéster 21e. La reacción de 21e con una amina o sal de amina (por ejemplo, acetato de amonio) produce la molécula que contiene imidazol 21f. La oxidación de 21f se puede lograr en presencia de MnO2 para proporcionar 21g.
Esquema 22. Síntesis representativa de E-V-C(=O)-P-W-P-R
[0107] El esquema 22 muestra una síntesis general de un intermedio de E-V-C(=O)-P-W-PR de la invención en el que, con fines ilustrativos, R es un grupo protector y W es una unidad de anillo aromático dos. El desplazamiento de la ahalo cetona 21b se produce mediante la adición de un ácido en condiciones básicas (por ejemplo, Et3N). La bromación de 22b se produce tras el tratamiento con tribromuro de piridinio, y se sigue la adición de un segundo ácido en condiciones básicas para proporcionar el diéster 22c. La reacción de 22c con una amina o sal de amina (por ejemplo, acetato de amonio) produce la molécula que contiene imidazol 22d. La oxidación de 22d se puede lograr en presencia de MnO2 para proporcionar 22e.
Esquema 23. Síntesis representativa de R-P-W-P-C(=O)-V-E
[0108] El esquema 23 muestra una síntesis general de un intermedio E-V-C(=O)-P-W-P-R de la invención en el que, con fines ilustrativos, R es un grupo protector y W es una unidad de anillo aromático dos. El desplazamiento de la ahalo cetona 21d se realiza mediante la adición de un ácido en condiciones básicas (por ejemplo, Et3N). La reacción de 23a con una amina o sal de amina (por ejemplo, acetato de amonio) produce la molécula que contiene imidazol 23b. La oxidación de 23b se puede lograr en presencia de MnO2 para proporcionar 23c.
Esquema 25. Síntesis representativa de E-V-C(=O)-P-W-P-C(=O)-V-E
[0109] El esquema 25 muestra una síntesis general de una molécula E-V-C(=O)-P-W-P-C(=O)-V-E de la invención en la que, con fines ilustrativos, E es etilcarbonilamino. El tratamiento de 25a o 25c con uno o dos equivalentes respectivamente de cloruro de propionilo en condiciones básicas (por ejemplo, hidróxido de sodio) proporciona la molécula 25b o 25d.
Esquema 26. Síntesis representativa de E-V-C(=O)-P-R y R1-P-R
[0110] El esquema 26 muestra una síntesis general de una E-V-C(=O)-P-R y una molécula R1-P-R de la invención en la que, con fines ilustrativos, R es un haloimidazol. El tratamiento del aldehído 26a con glioxal, en presencia de hidróxido de amonio, proporciona el imidazol 26b. El tratamiento con N-bromosuccinamida o yodo proporciona el haloimidazol correspondiente 26c y 26d, respectivamente. La separación del compuesto bis-halogenado correspondiente puede realizarse mediante cromatografía de HPLC preparativa. La conversión del bis-haloimidazol en el mono-haloimidazol también se puede llevar a cabo calentando en presencia de sulfito de sodio. Se puede lograr una funcionalización adicional del grupo P tras la eliminación del grupo protector y el acoplamiento con un ácido apropiado (E-V-C(=O)-OH).
Esquema 27. Síntesis representativa de R1-P-W-P-R2
[0111] El esquema 27 muestra una síntesis general alternativa de un intermedio R1-P-W-P-R2 de la invención en el que, para fines ilustrativos, R1 y R2 son grupos protectores independientes y W es una unidad de dos anillos aromáticos construida a través de una ciclación mediada por un metal de transición. La bromación de 21b con un agente de bromación (es decir, tribromuro de piridinio) proporciona el dibromuro 27a. El desplazamiento del bromuro primario luego procede mediante la adición de un ácido en condiciones básicas (por ejemplo, K2CO3) para proporcionar 21d. La conversión a 21f o 21g se puede lograr siguiendo los métodos descritos en el Esquema 21.
Esquema 28. Síntesis representativa de E-V-C(=O)-P-W-P-R
[0112] El esquema 28 muestra una síntesis general alternativa de un intermedio E-V-C(=O)-P-W-P-R de la invención en el que, con fines ilustrativos, R es un grupo protector y W es una unidad de anillo aromático dos. La bromación de 21b con un agente de bromación (es decir, tribromuro de piridinio) proporciona el dibromuro 27a. El desplazamiento del bromuro primario luego procede mediante la adición de un ácido en condiciones básicas (por ejemplo, K2CO3) para proporcionar 22d. La conversión a 22d o 22e se puede lograr siguiendo los métodos descritos en el Esquema 22.
Realización específica
[0113] En una realización, se proporciona un compuesto de la fórmula:
o una sal farmacéuticamente aceptable del mismo.
[0114] La divulgación se ilustrará ahora mediante los siguientes ejemplos no limitativos. Las siguientes abreviaturas se utilizan a lo largo de la especificación, incluidos los ejemplos.
_______________________
Ejemplos
Ejemplo BN (Referencia)
[0115]
(2S,5S)-cta 5- (Sy2- metiipirrobdina-2- (metoxicarbonilamino)
cartooxilato-TFA -3-ácido metilbutanoico
metilbu!anoil)-5- metilbutanoil)-S-meUpirrolidina-2-carboxilato mebipirroMina-2-ácido carboxílico
[0116] (2S,5S)-Etilo 1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-carboxilato: (2S,5S)-Etilo 5-metNpirroNdina-2-carboxNato-TFA (10,0 g, 39,3 mmol), (S)-2-(metoxicarbonNamino)-3-áddo metilbutanoico (6,88 g, 39,3 mmol) y HATU (14,9 g, 39,3 mmol) se combinaron en DMF (100 mL) y se añadió DIPEA (15,0 mL, 86,5 mmol). Después de agitarse durante 1 h a TA, la mezcla de reacción se diluyó con EtOAc. La fase orgánica se lavó sucesivamente con HCl al 10%, NaHCO3 acuoso saturado y salmuera, luego se secó sobre MgSO4, se filtró y se concentró a presión reducida para proporcionar (2S,5S)-etilo 1-((S)-2-(metoxicarbonilamino))-3-metilbutanoil)-5-metilpirrolidina-2-carboxilato. El material bruto se continuó sin purificación adicional.
[0117] (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirirolidina-2-ácido carboxílico: (2S,5S)-Etilo 1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-carboxilato (39,3 mmol, suponiendo conversión completa de la transformación previa) se suspendió en MeOH (200 ml) y se añadió LiOH acuoso (1,0 M, 100 ml, 100 mmol). La mezcla de reacción se agitó o/n, luego se concentró a presión reducida para eliminar la mayor parte del MeOH. La solución acuosa se lavó 2x con DCM antes de acidificarse a pH ~ 1-2 con HCl al 10%. La fase acuosa ácida se extrajo luego 5x con EtOAc. Los extractos de EtOAc combinados se secaron sobre MgSO4, se filtraron y se concentraron a presión reducida para producir (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoil)-5-metilpirrolidina-2-ácido carboxílico (6,89 g, 56% en 2 pasos).
Ejemplo DU (Referencia)
[0118]
[0119] 9-bromo-3-(2-bromoacetil)-10,11-dihidro-5H-dibenzo[c,g]cromen-8(9H)-ona: A 3-(2-bromo-1-hidroxietilo)-10,11-dihidro-5H-dibenzo[c,g]cromen-8(9H)-ona (20,3g, 54,4 mmol) en DCM (365 mL) se añadió MeOH (22 mL) y tribromuro de piridinio (18,24 g, 57,0 mmol). Después de 2 h, se añadió agua (100 ml) y, después de agitarse brevemente, se dividieron las capas y se recogió la capa orgánica inferior. La capa orgánica se lavó luego con 1 M HCl (100 ml) y la capa orgánica inferior que contenía 9-bromo-3-(2-bromo-1-hidroxietil)-10,11-dihidro-5H-dibenzo[c,g]cromeno-8(9H)-ona fue recogida. 1H RMN a 400 MHz (CDCls) 7,75 (d, J = 8,1 Hz, 1H), 7,68 (s, 1H), 7,61 (s, 1H), 7,42 (d, J = 7,5 Hz, 1H), 7,24 (s, 1H), 5,13 (s, 2H), 4,99-4,96 (m, 1H), 4,73 (dd, J = 4,1,4,1 Hz, 1H), 3,69-3,66 (m, 1H), 3,58-3,53 (m, 1H), 3,35-3,27 (m, 1H), 2,96-2,90 (m, 1H), 2,58-2,44 (m, 2H), no se observa C-OH.
[0120] A 9-bromo-3-(2-bromo-1-hidroxietil)-10,11-dihidro-5H-dibenzo[c,g]cromen-8(9H)-ona (aprox. 54,4 mmol) en DCM (365 ml) se añadió bicarbonato de sodio (5,45 g), bromuro de sodio (6,14 g), TEMPO (16,55 mg) y agua (60 ml). La solución se enfrió entre 0-5°C y se añadió un 6% de blanqueador (91,5 ml). Después de 1 h, se añadió alcohol isopropílico (20 ml) y la mezcla de reacción se calentó a temperatura ambiente. La agitación se detuvo, las capas se separaron y la capa orgánica inferior se recogió y se concentró, eliminando aproximadamente 345 g de disolvente. La suspensión se filtró y la torta se lavó con 50 mL de agua y luego con 50 mL de DCM (previamente enfriado a 5°C). Los sólidos se recogieron y se secaron al vacío para obtener 9-bromo-3-(2-bromoacetil)-10,11-dihidro-5H-dibenzo[c,g]cromen 8 (9H)-ona (18,6 g, 76%). rendimiento). 400 MHz 1H RMN (CDCla) 88,03-8,01 (m, 1H), 7,85 (d, J = 8,2 Hz, 1H), 7,82 (s, 1H), 7,71 (s, 1H), 7,67 (s, 1H), 5,19 (s, 2H), 4,74 (dd, J = 4,1,4,1 Hz, 1H), 4,45 (s, 2H), 3,37 3,29 (m, 1H), 2,99-2,92 (m, 1H), 2,59-2,46 (m, 2H); 100 MHz 13C RMN (CDCls) 8 190,4, 189,6, 154,2, 136,6, 134,1, 133,9, 132,9, 131,8, 129,3, 127,2, 125,6, 124,2, 123,3, 117,0, 68,1,49,9, 31,8, 30,4, 25,5.
Ejemplo DX
[0121]
K0CO3
9-bromo-3-(2-bromoacetilo)-10,11 -dihidro-5H- (2S,5S)-1-(terc-butoxicarbnilo)-dibenzo[c,g]cromen-8(9H)-ona 5-metilpirrolidina-2-ácido carboxilico
(2S,5S)-2-(2-(9-bromo-8-oxo-8,9,10,11 -tetrahidro-5/-/- (2S,5S)-1-((S)-2-(metoxicarbomlamino)-3 Dibenzo[c,g]cromen-3-il)-2-oxoetilo) 1-tere-butilo 5 metilbutanoil)-5-metilpirrolidina-2
Metilpirrolidina-1,2-dicarboxilato acido carboxilico
(2S,5S)-1-tercbutilo 2-(2-(9-((2S,5S)-1-((S)-2
metoxicarbonilamino)-3-metilbutanoil)-5-metilpirrolidina-2
carboniloxi)-8-oxo-8,9,10,11-tetrahidro-5H-dibenzo[c,sí]cromen-3-il)-2-oxoetilo) 5-metilpirrolidina-1,2-dicarboxilato
Tere-butilo (2S,4S)-2-[5-[5-(2S,4S)-1 -[N-metoxícarbonilo)-
[4’,3’:6,7]naftol[1,2-d]imidazol-9-il)-1 H-imidazol-2-il]-5-metilpirrolidina-1-carboxilato
Metilo {(2S)-1-[(2S,4S)-2-(5-{2-[(2S,5S)-1-{(2Sl3R)-3-metoxi-2-[(metoxicarbonilo)amino]butanoil}-5-metilpirrolidina-2-il]-1,11-Dihidroisocromeno[4’,3':6,7]naftol[1,2-d]imidazol-9-il}-1 H-lmidazol-2-il)-5-metilpirrolidina-1-il]-3-metil-1-oxobutan-2-¡l}carbamato
[0122] (2S,5S)-2-(2-(9-bromo-8-oxo-8,9,10,11-tetrahidro-5H-dibenzo[c,g]cromen-3-il)-2-oxoetil) 1-íerc-butilo 5-metilpirrolidina-1,2-dicarboxilato: 9-bromo-3-(2-bromoacetil)-10,11-dihidro-5H-dibenzo[c,g]cromen-8(9H)-ona (1,43 g, 3,17 mmol) se trató con una solución de (2S,5S)-1-(terc-butoxicarbonil)-5-metil-pirrolidina-2-ácido carboxílico (800
mg, 3,49 mmol) en diclorometano (14 ml) y K2CO3 (658 mg, 1,18 mmol). La mezcla de reacción agitada se agitó a temperatura ambiente y se diluyó con C ^ C h y se extrajo 3X. La fase orgánica se lavó con salmuera, luego se secó sobre MgSO4 , se filtró y se concentró a presión reducida para proporcionar ((2S,5S)-2-(2-(9-bromo 8-oxo-8,9,10,11-tetrahidro-5H-dibenzo[c,g]cromen-3-il)-2-oxoetil) 1 -terc-butilo 5-metilpirrolidina-1,2-dicarboxilato (1,61 g, 84%).
[0122] (2S,5S)-1 -terc-butilo 2-(2-(9-((2S,5S)-1-((S)-2-(metoxicarbomlammo)-3-metNbutanoNo)-5-metMpirroNdma-2-carbomlxi)-8-oxo-8,9,10,11-tetrahidro-5H-dibenzo[c,g]cromen-3-M)-2-oxoetN) 5-metilpirrolidina-1, 2-dicarboxilato: ((2S,5S)-2-(2-(9-bromo-8-oxo-8,9,10,11-tetrahidro-5H-dibenzo[c,g]cromen-3-il)-2- oxo-til) 1 -terc-butilo 5-metilpirrolidina-1,2-dicarboxilato (1,59 g, 2,66 mmol) se trató con una solución de (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoil)-5-metilpirrolidina-2-ácido carboxílico (1,14 g, 3,99 mmol) en THF (16 ml) y CS2CO3 (692 mg, 2,12 mmol). La mezcla de reacción agitada se calentó a 50°C. durante 16 h, luego se enfrió a temperatura ambiente y se diluyó con CH2Cl2 y se extrajo 3X. La fase orgánica se lavó con salmuera, luego se secó sobre MgSO4, se filtró y se concentró a presión reducida. El residuo crudo se purificó por cromatografía de columna de sílice (20% EtOAc/hexanos) para proporcionar (2S,5S)-1-terc-butilo 2-(2-(9-((2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoil)-5-metilpirrolidina-2-carbonilxi)-8-oxo-8,9,10,11-tetrahidro-5H-dibenzo[c,g]cromen-3-il)-2-oxoetilo) 5-metilpirrolidina-1,2-dicarboxilato (1,26 g, 59%).
[0124] Terc-butilo (2S,4S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonM)-L-vamo]-5-metNpirroNdm-2-M}-1A5,11-tetrahidroisocromeno[4\3':6,7]nafto[1,2-d]imidazol-9-M)-1H-imidazol-2-M]-5-metMpirroMdma-1-carboxMato: (2S,5S)-1-terc-butilo 2-(2-(9-((2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-carbonilxi)-8-oxo-8,9,10,11-tetrahidro-5H-dibenzo[c,g]cromen-3-il)-2-oxoetil) 5-metilpirrolidina-1,2-dicarboxilato (1,2 g, 1,49 mmol), hexametildisilazano (2,5 ml, 11,9 mmol) y ácido propiónico (3,3 ml, 44,8 mmol) se suspendieron en PhMe (12 ml). La mezcla de reacción agitada se calentó a 9o°C durante 20 h, luego se enfrió a temperatura ambiente y se diluyó con EtOAc. La fase orgánica se lavó con 98:2 de agua/NH4OH, luego se secó sobre MgSO4 , se filtró y se concentró a presión reducida. El residuo crudo se purificó mediante cromatografía en columna de sílice (0% a 30% de MeOH/EtOAc) para proporcionar ferc-butilo (2S,4S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-L-valilo]-5-metilpirrolidin-2-il}-1,4,5,11-tetrahidroiso-cromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidina-1-carboxilato (474 mg, 41%).
[0125] Terc-butilo (2S,4S)-2-[5-(2-{(2S,4S)-1-[N-(metoxicarbonM)-L-vamo]-5-metMp irroMdm-2-No}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidina-1-carboxilato:
(2S,4S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-L-valilo]-5-metilpirrolidin-2-il}-1,4,5,11-tetrahidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidina-1-carboxilato (474 mg, 0,70 mmol) se suspendieron en d Cm (5 ml) y se añadió MnO2 activado (2,1 g, 21,7 mmol) en una sola porción. Después de agitarse durante 15 h, la mezcla se filtró sobre celite. La torta del filtro se lavó con abundante cH 2Cl2 y EtOAc y el filtrado se concentró a presión reducida para proporcionar terc-butilo (2S,4S)-2-[5-(2-{(2S,4S)-1-[N-(metoxicarbonil)-L-valilo]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidina-1carboxilato (432 mg, 81%) que se llevó al siguiente paso sin purificación adicional.
[0126] Metilo {(2S)-1-[(2S,4S)-2-(5-£2-[(2S,5S)-1-{(2S,3R)-3-metoxi-2-[(metoxicarboml)ammo]butanoMo}-5-metilpirrolodin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-5-metilpirrolidin-1-il]-3-metil-1-oxobutan-2-il}carbamato: Terc-butilo (2S,4S)-2-[5-(2-{(2S,4S)-1-[N-(metoxicarbonil)-L-valilo]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafta[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidina-1-carboxilato (216 mg, 0,28 mmol) se disolvió en EtOH (3 ml) y se añadió HCl (1 ml). La mezcla de reacción se agitó durante 1 hora a 60°C y luego se concentró a presión reducida. El residuo crudo se trató con (2S,3R)-3- metoxi-2-(metoxicarbonilamino)ácido butanoico (71 mg, 0,38 mmol), HATU (126 mg, 0,33 mmol) y DMF (3 ml), luego DIPEA (0,15). Se añadió gota a gota mL, 0,86 mmol). Después de 2 h, la mezcla se diluyó con MeOH al 10%/EtOAc y se lavó sucesivamente con NaHCO3 acuoso saturado y salmuera. Los extractos orgánicos se secaron sobre MgSO4 , se filtraron y se concentraron a presión reducida. El residuo crudo se purificó por HPLC de fase inversa (Gemini, 15 a 43% de ACN/H2O 0,1% de TFA). para proporcionar metilo {(2S)-1-[(2S,4S)-2-(5-{2-[(2S,5S)-1-{(2S,3R)-3-metoxi-2-[(metoxicarbonil)amino]butanoilo}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-5-metilpirrolidin-1-il]-3-metil-1-oxobutan-2-il}carbamato (96,7 mg, 41%). 1H RMN (400 MHz, dmso) 88,64 (s, 1H), 7,74 (m, Hz, 8H), 5,27 (s, 2H), 5,15 (s, 1H), 4,98 (s, 1H), 4,70 (s, 2H), 4,20 - 3,22 (m, 10H), 3,17 (s, 3H), 2,22 (m, 5H), 1,84 (m, 2H), 1,47 (m, 6H), 1,31 - 0,97 (m, 3H), 0,92 (d, 3H), 0,83 (d, 3H), 0,72 (d, 3H). MS (ESI) mlz 835,76 [M+H]+.
Ejemplo DY
[0127]
Metilo [(2S,3R)-3-metoxi-1-[(2S-5S)-2-[9-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metilo-L-treonilo]-5-metilpirrolidin-2-il}-lH-imidazol-5-il)-1,11-hidroisocromeno [4',3':6,7]nafto[1,2-díimidazol-2-il]-4-metilpirrolidin-1-il}-1-oxobutano-2-il]carbamato
[0128] [(2S,3R)-3-metoxM-£(2S,5S)-2-[9-(2-£(2S,5S)-1-[N-(metoxicarboml)-O-de metilo metil-L-treonil]-5-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-4-metilpirrolidin-1-il}-1-oxobutan-2-il]carbamato se sintetizó de manera similar al Ejemplo DX sustituyendo (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,4S)-1-(tercbutoxicarbonil)-4-metilpirrolidina-2-ácido carboxílico. 1H RMN (400 MHz, dmso) 8 8,70 (s, 1H), 8,31 - 7,45 (m, 8H), 7,05 (s, 1H), 5,29 (s, 2H), 5,22 - 5,14 (m, 1H), 5,03- 4,92 (m, 1H), 4,68 - 4,60 (m, 1H), 4,21 (d, 4H), 3,75 - 3,06 (m, 14H), 2,36 -2,02 (m, 2H), 1,94 - 1,75 (m, 2H), 1,45 (s, 3H), 1,26 -1,18 (m, 2H), 1,14 (s, 3H), 1,05 (s, 2H), 0,95 (d, 6H). MS (ESI) mlz 851,79 [M+H]+.
Ejemplo DZ
[0129]
Metilo [(2S,3R)-3-metoxi-1-[(2S-5S)-2-[9-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metilo-L-treonilo]-4-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-hidroisocromeno [4',3':6,7]nafto[1,2-díimidazol-2-il]-5-metilpirrolidin-1-il}-1-oxobutano-2-il]carbamato
[0130] [(2S,3R)-3-metoxM-£(2S,5S)-2-[9-(2-{(2S,5S)-HN-(metoxicarboml)-O-metil-L-treomlH-metilpirrolidm-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-2-il]-5-metilpirrolidin-1-il}-1-oxobutan-2-il]carbamato se sintetizó de manera similar al Ejemplo DX sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidin-2-ácido carboxílico con (2S,4S)-1-(terc-butoxicarbonil)-4-metilpirrolidina-2-ácido carboxílico y (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-(tercbutoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico. 1H RMN (400 MHz, dmso) 8 8,62 (s, 1H), 8,34 - 7,47 (m, 8H), 7,10 (s, 1H), 5,26 (s, 2H), 5,18 - 5,00 (m, 2H), 4,79 - 4,66 (m, 2H), 4,54 - 4,40 (m, 1H), 4,31 - 4,01 (m, 2H), 3,43 (m, 10H), 3,15 (s, 3H), 2,43-2,23 (m, 4H), 2,18 -2,01 (m, 2H), 1,82 (s, 2H), 1,50 (s, 3H), 1,28 -1,17 (m, 1H), 1,02 (d, 4H), 0,95 (d, 6H). MS (ESI) m/z 851,82 [M+H]+.
Ejemplo EA
[0131]
Metilo(1-[(2S,5S)-2-[9-(2-{(2S,5S)-1-[(2S)-2-[(metoxicarbonil
)amino]-2-(tetrahidro-2H-piran-4-il)acetil]-5-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]
Nafto[1,2-d]imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il)carbamato
[0132] metilo (1-{(2S,5S)-2-[9-(2-£(2S,5S)-H(2S)-2-[(metoxicarboml)ammo]-2-(tetrahidro-2H-piran-4-il)acetil]-5-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il)carbamato se sintetizó de una manera similar a la del ejemplo DX que
sustituye (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (S)-2-(metoxicarbonNamino)-2-(tetrahidro-2H-piran-4-il)ácido acético. 1H RMN (400 MHz, dmso) 88,66 (s, 1H), 8,18 (s, 1H), 8,04 - 7,50 (m, 8H), 5,27 (s, 2H), 5,15 (s, 1H), 4,99 (s, 1H), 4,66 (m, 2H), 4,24 -3,43 (m, 9H), 3,15 (s, 2H), 2,35 (s, 3H), 2,15 (s, 3H), 1,98 - 1,97 (m, 1H), 1,83 (s, 3H), 1,57 (s, 1H), 1,47 (m, 6H), 1,20 (s, 4H), 0,90 (s, 2H), 0,83 (d, 3H), 0,72 (d, 3H). MS (ESI) m/z 861,82 [M+H]+.
Ejemplo EB
[0133]
Metilo [(1S)-2-[(2S,5S)-2-{2-[[(2S,5S)-1-{[(metoxicarbonil)
amino](tetrahidro-2H-piran-4-il)acetil}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno [4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-5-metilpirrolidin-1-il]-2-oxo-1 -(tetrahidro-2H-piran-4-il)etil]carbamato
[0134] metilo [[1S)-2-[(2S,5S)-2-(5-{2-[(2S,5S)-1-£[(metoxicarboml)ammo] (tetrahidro-2H-piran-4)metil -il)acetil>-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-9-il}-1H-imidazol 2-il)-5-metilpirrolidin-1-il]-2-oxo-1-(tetrahidro-2H-piran-4-il)etilo]carbamato. Se sintetizó de manera similar al Ejemplo DX sustituyendo el (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metil butanoilo)-5-metilpirrolidina-2-ácido carboxílico con (2S,4S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico y sustituyendo el (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (S)-2-(metoxicarbonilamino)-2-(tetrahidro-2H-piran-4-il)ácido acético. 1H RMN (400 MHz, dmso) 88,67 (s, 1H), 8,19 (d, J = 8,1 Hz, 1H), 8,07 - 7,50 (m, 8H), 5,27 (s, 2H), 5,19 - 5,08 (m, 1H), 4,98 (m, 1H), 4,66 (m, 2H), 4,03 (m, 2H), 3,75 (m, 4H), 3,56 - 3,39 (m, 6H), 3,26 - 2,95 (m, 4H), 2,22 (m, 6H), 1,83 (s, 3H), 1,58 (d, 2H), 1,47 (m, 6H), 1,21 (m, 8H). MS (ESI) m/z 903,60 [M+H]+.
Ejemplo EC
[0135]
Metilo {(2S,3S)-1-[(2S,5S)-2-(9-{2-[(2S,5S)-1-{(2S,3S)-2-[(metoxicarbonil)amino]-3-metilpentanil}-5-metilpirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto
[1,2]-d]imidazol-2-il)-5-metilpirrolodin-1-il]-3-metil-1-oxopentan-2-il}carbamato
[0136] Metilo {(2S,3S)-1-[(2S,5S)-2-(9-{2-[(2S,5S)-1-{(2S,3S)-2-[(metoxicarbonil)amino]-3-metilpentanil}-5-metilpirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2]-d]im idazol-2-il)-5-metilpirrolodin-1-il]-3-metil-1-oxopentan-2-il}carbamato se sintetizó de manera similar a un ejemplo DX que sustituye ((2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,4S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico y sustituyendo (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (2S,3S)-2-(metoxicarbonilamino)-3-ácido metilpentanoico. 1H RMN (400 MHz, dmso) 88,68 (s, 1H), 8,18 (d, J = 8,3 Hz, 1H), 8,02 (m, 1H), 7,94 - 7,80 (m, 3H), 7,73 (s, 1H), 7,63 (m, 1H), 7,51 (m, 2H), 5,67 (d, J = 10,9 Hz, 1H), 5,25 (d, J = 6,5 Hz, 2H), 5,18 -5,09 (m, 1H), 5,03-4,91 (m, 1H), 4,72 -4,56 (m, 2H), 4,23-4,03 (m, 1H), 3,97 (m, 2H), 3,48 (t, 5H), 3,38 (s, 1H), 2,33 (s, 2H), 2,26-2,02 (m, 3H), 2,08 (m, 2H), 1,81 (m, 1H), 1,64 (s, 2H), 1,45 (m, 7H), 1,17 (d, 1H), 1,04 (m, 2H), 0,75 (m, 7H), 0,63 (d, 5H). MS (ESI) m/z 847,78 [M+H]+.
Ejemplo DE
[0137]
metNo{(2S,3S)-1-[(2S,4S)-2-(9-{2-[(2S,5S)-1-{(2S,3R)-3-metoxi-2-[(metoxicarbonN)amino]butanoNo}-5-metNpirroNdin-2-N]-1H-imidazol-5-il}-1,11-dihidroisochromeno[4',3':6,7]nafto[1,2-d]
imidazol-2-il)-4-(metoximetil) pirrolidin-1 -il]-3-metil-1 -oxopentan-2-il}carbamato
[0138] Metilo {(2S,3S)-H(2S,4S)-2-(9-£2-[(2S,5S)-1-{(2S,3R)-3-metoxi-2-[(metoxicarboml)ammo]butanoMo}-5-metilpirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisochromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-4-(metoximetil) pirrolidin-1-il]-3-metil-1-oxopentan-2-il}carbamato se sintetizó de una manera similar a la del Ejemplo DX sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-((2S,3R)-3-metoxi-2-(metoxicarbonilamino)butanoilo)-5-metilpirrolidina2-ácido carboxílico; (2S,5S)-1-((S)-2-(metoxicarbonil amino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,4S)-1-(terc-butoxicarbonil)-4-(metoximetil)pirrolidin-2-ácido carboxílico y (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (2S,3S)-2-(metoxicarbonil amino)-3-ácido metilpentanoico. 1H RMN (400 MHz, dmso) 88,70 (s, 1H), 8,16 (s, 1H), 7,87 (s, 4H), 7,74 (d, 1H), 7,65 (d, 1H), 7,57 (d, 1H), 7,28 (d, 1H), 5,29 (s, 2H), 5,24 - 5,16 (m, 1H), 4,97 (d, 1H), 4,63 (s, 1H), 4,27 - 4,02 (m, 2H), 3,60 - 3,37 (m, 14H), 2,68 (m, 1H), 2,51 (m, 1H), 2,32 (m, 3H), 2,18 - 1,91 (m, 3H), 1,82 (s, 1H), 1,63 (s, 1H), 1,45 (d, 3H), 1,24 (m, 2H), 0,99 (d, 5H), 0,79 - 0,64 (m, 7H). MS (ESI) m/z 879,85 [M+H]+.
Ejemplo EE
metNo{(3S)-1-[(2S,5S)-2-(5-{2-[(2S,4S)-1-[N-(metoxicarbonN)-O-metil-D-alonononilo]-4-(metoximetil)pirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-N}-1H-imidazol-2-il)-5-metilpirrolidin-1-il]-3-metil-1 -oxopentan-2-il}carbamato
[0139] metilo{(3S)-1-[(2S,5S)-2-(5-{2-[(2S,4S)-1-[N-(metoxicarbonM)-O-metN-D-alotreonMo]-4-(metoximetN)pirroNdm-2-M]-1,11-dihidroisocromeno[4\3':6,7]nafto[1,2-d]imidazol-9-M}-1H-imidazol-2-M)-5-metilpirrolidin-1-il]-3-metil-1-oxopentan-2-il}carbamato se sintetizó de manera similar al Ejemplo DX sustituyendo (2S,5S)-1-(terc-butoxicarbonil))-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-((2S,3S)-2-(metoxicarbonilamino)-3-metilpentanoil)-5-metilpirrolidina-2-ácido carboxílico y (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,4S)-1-(terc-butoxicarbonil)-4-(metoxi metil)pirrolidina-2-ácido carboxílico.
1H RMN (400 MHz, dmso) 88,73 (s, 1H), 8,20 (d, 1H), 8,04 (s, 1H), 7,90 (m, 3H), 7,77 (s, 1H), 7,68 (d, 1H), 7,55 (d, 1H), 7,07 (d, 1H), 5,35 - 5,15 (m, 3H), 5,06 - 4,94 (m, 1H), 4,64 (s, 1H), 4,33- 4,25 (m, 1H), 4,19 (s, 1H), 4,08 (s, 1H), 3,98 (t, 1H), 3,62 (t, 1H), 3,54 -3,41 (m, 8H), 3,27 (s, 3H), 3,11 (s, 3H), 2,69 (s, 1H), 2,59-2,49 (m, 1H), 2,48 -2,41 (m, 2H), 2,28 (m, 2H), 2,18 -1,94 (m, 2H), 1,82 (m, 1H), 1,67 (m, 1H), 1,44 (d, 3H), 1,15 -1,01 (m, 1H), 0,98 (d, 3H), 0,79 (m, 4H), 0,65 (d, 3H). MS (ESI) m/z 879,90 [M+H]+.
Ejemplo EF
[0140]
metNo[(1S)-2-[(2S,4S)-2-(9-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbonN) amino]-3-metMbutanoil}-5-metMpirrolidin-2-il]-1H-imidazol-5-il}-1,11 dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-N)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-(tetrahidro-2H-piran-4-il)
etilo]carbamato
[0141] metMo[(1S)-2-[(2S,4S)-2-(9-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbonM)ammo]-3-metMbutanoM}-5-metilpirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-2-il)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-(tetrahidro-2H-piran-4-il)etilo]carbamato se sintetizó de una manera similar a la del Ejemplo DX que sustituye (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoil)-5-metilpirrolidina-2-ácido carboxílico; (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,4S)-1-(terc-butoxicarbonil)-4-(metoximetil)pirrolidina-2-ácido carboxílico y (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (S)-2-(metoxicarbonilamino)-2-(tetra-hidro-2H-piran-4-il)ácido acético. 1H RMN (400 MHz, dmso) 8 8,66 (s, 1H), 8,15 (m, 1H), 7,97 (s, 1H), 7,78 (m, 4H), 7,59 (d, 1H), 7,49 (d, 2H), 7,27 (d, 1H), 5,30 - 5,10 (m, 3H), 5,01 - 4,89 (m, 1H), 4,59 (s, 1H), 4,13 (m, 3H), 3,92 -2,95 (m, 9H), 2,65 (s, 2H), 2,52 -2,37 (m, 2H), 2,18 (m, 4H), 1,98 - 1,69 (m, 4H), 1,40 (d, 5H), 1,22 (m, 5H), 0,84 (m, 5H), 0,68 (d, 3H). MS (ESI) m/z 891,65 [M+H]+.
Ejemplo EG
[0142]
[0143] metilo{2-[(2S,5S)-2-(9-{2-[(2S,5S)-1-{(2S,3R)-3-metoxi-2-[(metoxicarbonil)amino]butanoilo}-5-metilpirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-2-il)-5-metilpirrolidin-1-il]-2-oxo-1-(tetrahidro-2H-piran-4-il)etilo}carbamato se sintetizó de una manera similar a la del Ejemplo DX sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-((2S,3R)-3-metoxi-2-(metoxicarbonilamino)butanoílo)-5-metilpirrolidina-2-ácido carboxílico; (2S,5S)-1-((S)-2-(metoxicarbonil amino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-(terc-butoxi carbonil)-5-metil-pirrolidina-2-ácido carboxílico y (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (S)-2-(metoxicarbonilamino)-2-(tetrahidro-2H-pirano-4-il)ácido acético. 1H RMN (400 MHz, dmso) 88,60 (s, 1H), 8,13 (s, 1H), 7,94 (s, 1H), 7,76 (m, 4H), 7,54 (m, 3H), 5,23 (s, 2H), 5,11 (t, 1H), 4,95 (s, 1H), 4,63 (m, 2H), 4,42 -4,16 -3,95 (m, 2H), 3,86 -3,30 (m, 8H), 3,26 -2,89 (m, 5H), 2,21 (m, 5H), 1,80 (s, 3H), 1,54 (m, 2H), 1,44 (m, 6H), 1,16 (m, 5H), 1,02 (d, 1H), 0,88 (d, 3H). MS (ESI) mlz 877,77 [M+H]+.
Ejemplo EH
[0144]
metilo{(3S)-1-[(2S,5S)-2-(9-{2-[(2S,5S)-1-{(2S,3R)-3-metoxi-2-[(metoxicarbonil)amino]butanoilo}-5-metilpirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-il]-3-metil-1-oxopentan-2-il}carbamato
[0145] metMo{(3S)-1-[(2S,5S)-2-(9-[2-[(2S,5S)-1-{(2S,3R)-3-metoxi-2-[(metoxicarbonM)ammo]butanoMo}-5-metilpirrolidin-2-il]-lH-im idazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-2-il)-5-metilpirrolidin-1-il]-3-metil-1-oxopentan-2-il}carbamato se sintetizó de manera similar a la del Ejemplo DX sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-((2S,3R)-3-metoxi-2-(metoxicarbonilamino)butanoilo)-5-metilpirrolidina-2-ácido carboxílico; (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico y (2S,3R)-3-metoxi-2-(metoxicarbonilaminoácido butanoico con (2S,3S)-2-(metoxi carbonilamino)-3ácido metilpentanoico. 1H RMN (400 MHz, dmso) 88,63 (s, 1H), 8,21 - 7,49 (m, 8H), 5,26 (s, 2H), 5,13 (m, 1H), 4,98 (s, 1H), 4,68 (m, 2H), 4,14 (s, 1H), 4,02 (m, 1H), 3,34 (m, 9H), 2,36 (m, 2H), 2,11 (m, 4H), 1,84 (m, 2H), 1,70 - 1,60 (m 1H), 1,47 (m, 6H), 1,13 (m, 4H), 0,92 (d, 3H), 0,84 (m, 2H), 0,74 (m, 3H), 0,66 (d, 3H). MS (ESI) m/z 849,74 [M+H]+.
Ejemplo EI
[0146]
[0147] metilo[(1S)-2-[(2S,4S)-2-(9-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbonil)amino]-3-metilbutanoil}-5-metilpirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-2-il)-4-metilpirrolidin-1-il]-2-oxo-1-(tetrahidro2H-piran-4-il)etilo]carbamato se sintetizó de una manera similar a la del Ejemplo DX sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-((2S,3R)-3-metoxi-2-(metoxicarbonilamino)butanoilo)-5-metilpirrenidina-2-ácido carboxílico; (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metil butanoilo)-5-metilpirrolidina-2-ácido carboxílico con (2S,4S)-1-(terc-butoxi carbonil)-4-metilpirrolidina-2-ácido carboxílico y (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butaico con (S)-2-(metoxicarbonilamino)-2-(tetrahidro-2H)pirano-4-il)ácido acético. 1H RMN (400 MHz, dmso) 88,73 (s, 1H), 8,21 (m, 1H), 8,06 (s, 1H), 7,98 - 7,84 (m, 3H), 7,73 (m, 2H), 7,52 (d, 1H), 7,27 (d, 1H), 5,31 (s, 2H), 5,24 - 5,14 (m, 1H), 5,05 -4,96 (m, 1H), 4,62 (s, 1H), 4,29 - 3,48 (m, 10H), 3,26 - 3,03 (m, 4H), 2,65 - 2,52 (m, 2H), 2,41 - 2,03 (m, 4H), 1,97 -1,75 (m, 4H), 1,44 (d, 3H), 1,32 (s, 2H) 1,20 (m, 2H), 1,09 (d, 3H), 0,87 (m, 4H), 0,72 (d, 3H). MS (ESI) m/z 861,75 [M+H]+.
Ejemplo EJ
[0148]
metilo[(2S)-1-{(2S,5S)-2-[9-(2-{(2S,4S)-1-[(2S)-2-[(metoxicarbonil) amino]-2-(tetrahidro-2H-piran-4-il)acetil]-4-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato
[0149] metilo[(2S)-1-{(2S,5S)-2-[9-(2-{(2S,4S)-1-[(2S)-2-[(metoxicarbonil)amino]-2-(tetrahidro-2H-piran-4
il)acetil]-4-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato se sintetizó de una manera similar a la del Ejemplo DX que sustituye (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-(terc-butoxicarbonil)-4-metilpirrolidina-2-ácido carboxílico y (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (S)-2-(metoxicarbonilamino)-2-(tetrahidro-2H-piran-4-il)ácido acético. 1H RMN (400 MHz, dmso) 88,68 (s, 1H), 8,18 (d, 1H), 8,09 -7,96 (m, 1H), 7,83 (m, 2H), 7,73-7,43 (m, 2H), 7,27 (d, 1H), 5,24 (d, 2H), 5,13 (m, 1H), 5,01 (m, 1H), 4,72 -4,59 (m, 1H), 4,21 - 4,03 (m, 4H), 3,91 (m, 1H), 3,74 (s, 2H), 3,55 - 3,31 (m, 8H), 3,25 - 3,03 (m, 3H), 2,51 - 2,25 (m, 4H), 2,12 (m, 1H), 1,79 (m, 3H), 1,47 (d, 3H), 1,34 - 1,12 (m, 3H), 1,12 - 0,93 (m, 4H), 0,86 (s, 1H), 0,79 (d, 3H), 0,69 (d, 3H). MS (ESI) m/z 861,79 [M+H]+.
Ejemplo EK
[0150]
metilo[(2S,3R)-1-{(2S,5S)-2-[5-(2-{(2S,5S)-5-etilo-1-[N-(metoxicarbonil)-O-metil-L-treonil]pirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidin-1-il}-3-metoxi-1-oxobutan-2-il]carbamato
[0151] metilo[(2S,3R)-1-{(2S,5S)-2-[5-(2-{(2S,5S)-5-etilo-1-[N-(metoxicarbonil)-O-metil-L-treonil]pirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidin-1-il}-3-metoxi-1-oxobutan-2-il]carbamato se sintetizó de manera similar al Ejemplo DX sustituyendo (2s ,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-(terc-butoxicarbonil)-5-etilpirrolidina-2-ácido carboxílico . 1H RMN (400 MHz, dmso) 88,66 (s, 1H), 8,19 (d, 1H), 8,00 (d, 1H), 7,81 (m, 3H), 7,59 (m, 2H), 5,27 (s, 2H), 5,20 - 5,08 (m, 1H), 5,05 - 4,94 (m, 1H), 4,63 (s, 1H), 4,53 (s, 1H), 4,42 (s, 1H), 4,24 - 3,98 (m, 4H), 3,61 -3,36 (m, 5H), 3,28 -3,12 (m, 6H), 2,43-2,08 (m, 6H), 1,92 (m, 4H), 1,45 (d, 3H), 1,05 (m, 12H), 0,71 (s, 1H). MS (ESI) m/z 865,74 [M+H]+.
Ejemplo EL
[0152]
metilo [(2S,3R)-3-metoxi-1-{(2S,5S)-2-[5-(2-{(2S,4S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-4-metilpirrolidin-2-il}-1,11dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidin-1-il}-1-oxo butan-2-il]carbamato
[0153] metilo [(2S,3R)-3-metoxi-1-[(2S,5S)-2-[5-(2-{(2S,4S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-4-m etilpirrolidin-2-il}-1,1ldihidroisocrom eno[4',3':6,7]nafto[l,2-d]im idazol-9-il)-1H-im idazol-2-il]-5-m etilpirrolidin-1-il}-1-oxo butan-2-il]carbamato se sintetizó de manera similar al Ejemplo DX sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-(terc-butoxicarbonil)-5-etilpirrolidina-2-ácido carboxílico y (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-(terc-butoxicarbonil)-5-etilpirrolidina-2-ácido carboxílico. 1H RMN (400 MHz, dmso) 88,66 (s, 1H), 8,19 (d, 1H), 7,99 (d, 1H), 7,93- 7,57 (m, 6H), 5,27 (s, 2H), 5,14 (m, 1H), 5,02 - 4,93 (m, 1H), 4,56 - 4,26 (m, 2H), 4,22 - 4,08 (m, 2H), 3,77 - 3,08 (m, 16H), 2,39 - 2,08 (m, 4H), 1,91 (m, 6H), 1,16 - 1,03 (m, 2H), 1,01 - 0,83 (m, 10H), 0,79 - 0,64 (m, 3H). MS (ESI) m/z 879,87 [M+H]+.
Ejemplo EM
metNo[[2S,3R)-1-{(2S,5S)-2-etNo-5-[5-(2S,5S)-1-[N-(metoxicarbonN)-O-metil-L-treonil]-5-metMpirrolidin-2-il}-1,11 dihidroisocromeno[4',3':6,7] nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]pirrolidin-1-il}-3-metoxi-1-oxo
butan-2-il]carbamato
[0155] metilo[[2S,3R)-1-{(2S,5S)-2-etilo-5-[5-(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[l,2-d]im idazol-9-il)-1H-imidazol-2-il]pirrolidin-1-il}-3-metoxi-1-oxobutan-2-il]carbamato se sintetizó de manera similar al Ejemplo DX sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico (2S,5S)-1-(terc-butoxicarbonil)-5-etilpirrolidina-2-ácido carboxílico, y (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metil butanoilo)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-(tercbutoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico. 1H RMN (400 MHz, dmso) 88,66 (s, 1H), 8,19 (d, 1H), 8,06 - 7,68 (m, 5H), 7,59 (m, 2H), 5,27 (s, 2H), 5,19 - 5,08 (m, 1H), 5,03- 4,94 (m, 1H), 4,71 (s, 1H), 4,47 (s, 1H), 4,31 (s, 1H), 4,23-4,05 (m, 3H), 3,87 -3,09 (m, 16H), 2,34 (s, 3H), 2,15 (s, 3H), 1,98 (s, 2H), 1,85 (s, 3H), 1,50 (d, 2H), 1,25 (s, 1H), 1,08 (d, 2H), 0,94 (m, 6H), 0,75 (s, 1H). MS (ESI) mlz 865,85 [M+H]+.
Ejemplo EN
[0156]
[0157] MetMo[(1S)-2-[(2S,5S)-2-(9-{2-[(2S,5S)-5-etMo-1-{(2S)-2[(metoxicarboml)ammo]-3-metilbutanoil}pirrolidin-2-il]-1H-im idazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metMpirroNdm-1-M]-2-oxo-1(tetrahidro-2H-piran-4-N)etMo]carbamato se sintetizó de una manera similar a la del Ejemplo DX sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-(tercbutoxicarbonil)-5-etilpirrolidina-2-ácido carboxílico (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metil butanoilo)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-((S)-2-(metoxicarbonNamino)-2-(tetrahidro-2H-pirano-4-N)acetN)-5-metilpirrolidina-2-ácido carboxílico y (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butaico con (S)-2-(metoxicarbonilamino)-3-metilo ácido butanoico. 1H RMN (400 Mh z , dmso) 88,63 (s, 1H), 8,22 - 8,11 (m, 1H), 7,68 (m, 8H), 5,26 (s, 2H), 5,13 (s, 1H), 4,99 (s, 1H), 4,77 -4,64 (m, 1H), 4,38 -4,25 (m, 1H), 4,03 (s, 1H), 3,85 (d, 2H), 3,60 - 2,92 (m, 9H), 2,63 (s, 1H), 2,29 (s, 4H), 1,90 (m, 6H), 1,58 (s, 1H), 1,49 (d, 4H), 1,15 (s, 4H), 0,95 (d, 4H), 0,84 (d, 4H), 0,71 (d, 4H). MS (ESI) m/z 875,67 [M+H]+.
Ejemplo EO
[0158]
[0159] metilo [(1S)-2-[(2S,5S)-2-etilo-5-(9-{2-[(2S,5S)-1-{(2S)-2[(metoxicarbonM)ammo]-3-metMbutanoM}-5-metilpirrolidin-2-il]-1H-im idazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-2-il)pirrolidin-1-il]-2-oxo-1-(tetrahidro-2H-piran-4-il)etilo]carbamato se sintetizó de una manera similar a la del Ejemplo DX sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-((2S,3R)-3-metoxi-2
(metoxicarbonilamino)butanoilo)-5-metilo ácido pirrolidina-2 carboxílico; (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-(terc-butoxicarbonil)-5-etilpirrolidina-2-ácido carboxílico y (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (S)-2-(metoxicarbonilamino)-2-(tetrahidro-2H-piran-4-ilo))ácido acético. 1H RMN (400 MHz, dmso) 88,66 (s, 1H), 8,20 (d, 1H), 8,02 (d, 1H), 7,81 (m, 3H), 7,58 (m, 3H), 5,27 (d, 2H), 5,15 (s, 1H), 5,04 -4,93 (m, 1H), 4,62 (s, 1H), 4,39 (s, 1H), 4,03 (s, 2H), 3,94 -3,34 (m, 9H), 3,26 -2,96 (m, 4H), 2,43-2,06 (m, 4H), 2,00 (s, 2H), 1,84 (s, 4H), 1,59 (d, 1H), 1,44 (d, 3H), 1,28 (d, 4H), 0,97 (m, 2H), 0,84 (d, 4H), 0,69 (m, 4H). MS (ESI) m/z 875,74 [M+H]+.
Ejemplo EP
[0160]
metilo {(2S,3R)-1-[(2S,5S)-2-etilo-5-(9-{2-[(2S,5S)-1-{(2SH(metoxicarbonil)amino
]-3-metilbutanoil}-5-metilpirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroiso cromeno[4',3':6,7]nafto[1,2]-d]imidazol-2-il)pirrolidin-1-il]-3-metoxi-1-oxobutan
-2-il}carbamato
[0161] metilo {(2S,3R)-H(2S,5S)-2-etMo-5-(9-£2-[(2S,5S)-1-{(2SH(metoxicarboml)ammo]-3-metNbutanoM}-5-metMpirroMdm-2-M]-1H-imidazol-5-M}-1,11-dihidroisocromeno[4\3':6,7]nafto[1,2]-d]imidazol-2-M)pirroMdm-1-M]-3-metoxM-oxobutan-2-N}carbamato. se sintetizó de manera similar al Ejemplo DX, sustituyendo (2S,5S)-1-(tercbutoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-((2S,3R)-3-metoxi-2-(metoxicarbonilamino)butanoilo)-5-metilpirrolidina-2-ácido carboxílico y (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-(terc-butoxicarbonil)-5-etilpirrolidina-2-ácido carboxílico. 1H RMN (400 MHz, dmso) 88,69 (s, 1H), 8,21 (d, 1H), 8,07 (s, 1H), 8,01 - 7,48 (m, 6H), 5,28 (s, 2H), 5,14 (m, 1H), 5,06 -4,94 (m, 1H), 4,70 -4,35 (m, 2H), 4 ,23-3,82 (m, 3H), 3,52 (m, 6H), 3,41 (s, 3H), 3,25 (s, 1H), 3,15 (s, 2H), 2,42 - 2,06 (m, 4H), 1,90 (m, 4H), 1,44 (d, 3H), 1,08 (d, 1H), 1,02 - 0,76 (m, 10H), 0,71 (d), 4H). MS (ESI) m/z 849,79 [M+H]+.
Ejemplo EQ
[0162]
metilo{(2S,3R)-1-[(2S,5S)-2-(9-{2-[(2S,5S)-5-etilo-1-{(2S)-2-[(metoxi carbonil)amino]-3-metilbutanoil}pirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metil
pirrolidin-1-il]-3-metoxi-1 -oxobutan-2-il}carbamato
[0163] metilo{(2S,3R)-1-[(2S,5S)-2-(9-{2-[(2S,5S)-5-etilo-1-{(2S)-2-[(metoxicarbonil)amino]-3-metilbutanoil}pirrolidin-2-il]-1H-im idazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-il]-3-metoxi-1-oxobutan-2-il}carbamato se sintetizó de manera similar al Ejemplo DX, sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-5-etilo-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoil)pirrolidina-2-ácido carboxílico y (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico. 1H RMN (400 MHz, dmso) 88,68 (s, 1H), 8,19 (m, 1H), 8,05 (s, 1H), 8,00 -7,70 (m, 4H), 7,60 (m, 2H), 5,28 (s, 2H), 5,19 - 5,08 (m, 1H), 5,05 - 4,94 (m, 1H), 4,71 (s, 1H), 4,29 (s, 1H), 4,22 - 4,06 (m, 2H), 3,94 - 3,82 (m, 3H), 3,75 - 3,19 (m, 9H), 3,14 (s, 2H), 2,36 (m, 2H), 2,14 (m, 2H), 1,87 (m, 3H), 1,50 (d, 3H), 1,25 (d, 1H), 1,15-1,01 (m, 1H), 1,01 - 0,76 (m, 10H), 0,71 (d, 3H). MS (ESI) m/z 849,83 [M+H]+.
Ejemplo ER
[0164]
metilo {(2S)-1-[(2S,4S)-2-(9-{2-[(2S,5S)-5-etNo-1-1(2S)-2-[(metoxi carbonil)amino]-3-metilbutanoil}pirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-N)-4-(metoximetil)pirrolidin-1-il]-3-metil-1-oxobutan-2-il}carbamato
[0165] metilo {(2S)-1-[(2S,4S)-2-(9-{2-[(2S,5S)-5-etMo-1-1(2S)-2-[(metoxicarbonN)ammo]-3-metilbutanoil}pirrolidin-2-il]-1H-im idazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-3-metil-1-oxobutan-2-il}carbamato. Se sintetizó de manera similar al Ejemplo DX, sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-5-etilo-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)pirrolidina-2-ácido carboxílico; (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,4S)-1-(terc-butoxicarbonN)-4-(metoximetN)pirroNdine-2-ácido carboxílico y (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (S)-2-(metoxicarbonilamino)-3-ácido metilbutanoico. 1H RMN (400 MHz, dmso) 88,72 (s, 1H), 8,25 - 8,11 (m, 1H), 8,07 - 7,84 (m, 3H), 7,67 (m, 3H), 7,26 (d, 1H), 5,30 (s, 2H), 5,25 -5,15 (m, 1H), 5,06 -4,91 (m, 1H), 4,36 -4,00 (m, 3H), 3,94 -3,81 (m, 2H), 3,65 -3,35 (m, 10H), 3,27 (s, 3H), 2,69 (s, 2H), 2,51 (m, 1H), 2,33 (s, 1H), 2,19 (s, 2H), 2,05 - 1,63 (m, 7H), 0,99 - 0,63 (m, 12H). MS (ESI) m/z 863,88 [M+H]+.
Ejemplo ES
[0166]
metNo{(2R,3R)-1-[(2S,4S)-2-(9-{2-[(2S,5S)-5-etNo-1-{(2S)-2-[(metoxi carbonN)aminoj-3-metNbutanoN}pirroNdin-2-N]-1H-imidazol-5-N}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-N)-4-(metoximetil)pirrolidin-1-il]-3-metoxi-1-oxobutan-2-il}carbamato
[0167] metilo{(2R,3R)-1-[(2S,4S)-2-(9-{2-[(2S,5S)-5-etilo-1-{(2S)-2-[(metoxicarbonil)amino]-3-metilbutanoil}pirrolidin-2-il]-1H-im idazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-3-metoxi-1-oxobutan-2-il}carbamato. Se sintetizó de manera similar al Ejemplo DX, sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-5-etilo-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)pirrolidina-2-ácido carboxílico; (2S,5S)-1-((S)-2-(metoxicarboninilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,4S)-1-(terc-butoxicarbonil)-4-(metoxi metil)pirrolidin a-2-ácido carboxílico. 1H RMN (400 MHz, dmso) 88,71 (s, 1H), 8,19 (m, 1H), 7,94 (m, 3H), 7,76 (m, 1H), 7,65 (d, 1H), 7,57 (d, 1H), 7,12 (d, 1H), 5,29 (s, 1H), 5,25 - 5,16 (m, 1H), 5,06 - 4,93 (m, 1H), 4,37 - 4,10 (m, 3H), 3,95 - 3,82 (m, 2H), 3,51 (m, 8H), 3,25 (m, 3H), 3,11 (s, 3H), 2,60 (m, 3H), 2,25 (m, 3H), 2,06 - 1,65 (m, 6H), 1,11 - 0,77 (m, 8H), 0,71 (d, 3H). MS (ESI) m/z 879,81 [M+H]+.
Ejemplo ET
[0168]
(2S,5S)-1-((2S,3S)-2-(metoxicarbonilamino)-3-metilpentanoíl)-5 metilpirrolidina-2-ácido carboxílico
[01699] (2S,5S)-1-((2S,3S)-2-(metoxicarbonilamino)-3-metilpentanoíl)-5 metilpirrolidina-2-ácido carboxílico. Se sintetizó de manera similar al Ejemplo BN, sustituyendo el (S)-2-(metoxicarbonilamino)-3-ácido metilbutanoico con (2S,3S)-2-(metoxicarbonilamino)-3-ácido metilpentanoico MS (ESI) mlz 301,19 [M+H]+.
Ejemplo EU
[0170]
(2S,5S)-1-((S)-2-(metoxicarbonilamino)-2-(tetrahidro-2H-piran-4-il)acetil)-5-metilpirrolidina-2-ácido carboxílico
[0171] (2S,5S)-1-((S)-2-(metoxicarbonilamino)-2-(tetrahidro-2H-piran-4-il)acetil)-5-metilpirrolidina-2-ácido carboxílico. Se sintetizó de manera similar al Ejemplo BN, sustituyendo el (S)-2-(metoxicarbonilamino)-3-ácido metilbutanoico con (S)-2-(metoxicarbonilamino)-2-(tetrahidro-2H-piran-4-il)ácido acético. MS (ESI) m/z 329,36 [M+H]+. Ejemplo EV
[0172]
(2S,5S)-1-((2S,3R)-3-metoxi-2-(metoxi
carbonilamino)butanoilo)-5-metilpirrolidina-2-ácido carboxílico
[0173] (2S,5S)-1-((2S,3R)-3-metoxi-2-(metoxicarbonilamino)butanoilo)-5-metilpirrolidina-2-ácido carboxílico. Se sintetizó de manera similar al Ejemplo BN, sustituyendo el (S)-2-(metoxicarbonilamino)-3-ácido metilbutanoico con (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico. m S (ESI) m/z 303,19 [M+H]+.
Ejemplo EW
[0174]
(2S,5S)-5-etilo-1-((S)-2-(metoxicarbonil
amino)-3-metilbutanoílo)pirrolidina-2-ácido carboxílico
[0175] (2S,5S)-5-etilo-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)pirrolidina-2-ácido carboxílico. Se sintetizó de manera similar al Ejemplo BN, sustituyendo (2S,5S)-etilo-5-metilpirrolidina-2-carboxilato-TFA con (2S,5S)-metil-5-etilpirrolidina-2-carboxilato-HCl. MS (ESI) m/z 301,15 [M+H]+.
Ejemplo EX
[0176]
metilo {(2S,3R)-3-metoxi-1-[(2S,4S)-2-(9-{2-[(2S,4S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-4-(metoximetil)pirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-1-oxobutan-2-il}carbamato
[0177] metilo {(2S,3R)-3-metoxM-[(2S,4S)-2-(9-£2-[(2S,4S)-HN-(metoxicarboml)-O-metil-L-treomlH-(metoximetil)pirrolidm-2-M]-1H-imidazol-5-M}-1,11-dihidroisocromeno[4\3':6,7]nafto[1,2-d]imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-1-oxobutan-2-il}carbamato se sintetizó de manera similar a un Ejemplo DX que sustituye (2S,5s)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico y (2S,5S)-1-(2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,4S)-1-(terc-butoxicarbonil)-4-(metoximetil)pirrolidina-2-ácido carboxílico. (0,083 g) LCMS-ESI+: calculado para C47H58N8O11: 910,42; observado [M+1]+: 911,78,1H RMN (400 MHz, cdaod) 88,63 (s, 1H), 8,19 (d, 1H), 8,00 (d, 1H), 7,91 (d, 2H), 7,83 (d, 1H), 7,68 (s, 1H), 7,63 (d, 1H), 5,45 - 5,37 (m, 1H), 5,32 (s, 2H), 5,30 -5,24 (m, 1H), 4,55 -4,44 (m, 2H), 4,37 -4,23 (m, 3H), 3,78 -3,65 (m, 10H), 3,65 -3,54 (m, 5H), 3,41 (s, 7H), 3,28 (s, 3H), 2,90 -2,59 (m, 6H), 2,12 (dq, 3H), 1,12 (q, 6H).
Ejemplo EY
[0178]
metilo {(1R)-2-[(2S,4S)-2-(5-{2-[(2S,4S)-1-{(2R)-2-[(metoxicarbonil)amino]-2-fenilacetil}-4-(metoximetil)pirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato
[0179] metilo {(1R)-2-[(2S,4S)-2-(5-£2-[(2S,4S)-1-{(2R)-2-[(metoxicarboml)ammo]-2-femlacetil}-4-(metoximetil)pirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-9-il}-1H-imidazol-2-il)-4
(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato se sintetizó de manera similar a metilo {(2S,3R)-3-metoxi-1-[(2S,4S)-2-(9-{2-[(2S,4S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-4-(metoximetil)pirrolidina-2-il]-1H-imidazol-5-il}-1,1l-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-1-oxobutan-2-il}carbamato, sustituyendo el (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (R)-2-(metoxicarbonilamino)-2-ácido fenilacético y sustituyendo HATU con COMU. (0,068 g) LCMS-ESI+: calculado para C53H54N8O9: 946,40; observado [M+1]+: 947,83, 1H RMN (400 MHz, acetona) 88,21 (s, 1H), 7,95 (s, 1H), 7,88 - 7,71 (m, 3H), 7,59 (d, 3H), 7,51 (d, 2H), 7,48 -7,32 (m, 7H), 7,27 -7,18 (m, 1H), 5,74 (t, 1H), 5,63 (dd, 2H), 5,52 (t, 1H), 5,11 (s, 3H), 3,98 -3,87 (m, 2H), 3,83 (d, 2H), 3,78 (s, 3H), 3,60 (s, 3H), 3,51 - 3,37 (m, 4H), 3,25 (d, 3H), 3,19 (s, 3H), 2,86 - 2,75 (m, 1H), 2,73- 2,54 (m, 4H), 2,25 (dd, 1H), 2,18 - 2,10 (m, 1H).
Ejemplo EZ
[0180]
metilo [[2S,3R)-3-metoxi-1-{(2S,4S)-2-[9-(2-{(2S,4S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-4-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-4-metilpirrolidin-1-il}-1-oxobutan-2-il]carbamato
[0181] metilo [[2S,3R)-3-metoxi-1-[(2S,4S)-2-[9-(2-{(2S,4S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-4-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-4-metilpirrolidin-1-il}-1-oxobutan-2-il]carbamato se sintetizó de manera similar al Ejemplo DX sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico y (2S,5S)-1-(2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,4S)-1-(terc-butoxicarbonil)-4-metilpirrolidina-2-ácido carboxílico. (0,068 g) LCMS-ESI+: calculado para C45H54N8O9: 850,40; observado [M+1]+: 851,78,1H RMN (400 MHz, cdaod) 88,65 (s, 1H), 8,20 (d, 1H), 8,04 (d, 1H), 7,93 (s, 1H), 7,90 (s, 1H), 7,87 - 7,81 (m, 1H), 7,69 (s, 1H), 7,64 (d, 1H), 5,39 (q, 1H), 5,33 (s, 2H), 5,25 (q, 1H), 4,51 (dd, 2H), 4,43- 4,23 (m, 3H), 3,73- 3,62 (m, 8H), 3,57 - 3,46 (m, 2H), 3,45 - 3,35 (m, 2H), 3,27 (s, 3H), 2,83-2,63 (m, 3H), 2,61 -2,47 (m, 2H), 1,93 (dq, 3H), 1,26 (dd, 6H), 1,22 -1,14 (m, 2H), 1,11 (t, 6H).
Ejemplo FA
[0182]
metilo [(2S)-1-{(2S,5S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato
[0183] metilo [(2S)-1-{(2S,5S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato se sintetizó de manera similar a la del Ejemplo DX sustituyendo (2S,5S)-1-(tercbutoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metil-butanoilo)-5-metilpirrolidina-2-ácido carboxílico, y sustituyendo (2S,5S)-1-(2-(metoxicarbonilamino)-3-metilbutanoil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico. (0,102g) LCMS-ESI+: calculado para C4hH54N8O8: 834,41; observado [M+1]+: 835,77, 1H RMN (400 MHz, cdaod) 88,68 - 8,61 (m, 1H), 8,25 - 8,17 (m, 1H), 8,09 - 7,97 (m, 2H), 7,96 - 7,91 (m, 1H), 7,88 - 7,82 (m, 1H), 7,73- 7,63 (m, 2H), 6,10 -6,01 (m, 1H), 5,75 - 5,66 (m, 1H), 5,33 (d, 3H), 5,22 - 5,11 (m, 1H), 4,84 -4,75 (m, 2H), 4,68 -4,58 (m, 1H), 4,42 (d,
1H), 4,35 -4,25 (m, 1H), 4,18 -4,07 (m, 1H), 3,76 (d, 2H), 3,67 (d, 4H), 3,62 -3,55 (m, 1H), 3,40 (s, 1H), 3,28 (s, 2H), 2,67 -2,46 (m, 3H), 2,44 -2,26 (m, 4H), 2,10 -1,90 (m, 3H), 1,61 (d, 2H), 1,56 (d, 3H), 1,34 - 1,22 (m, 4H), 1,14 -1,06 (m, 2H), 1,03 (d, 1H), 0,98 (d, 2H), 0,87 (d, 3H).
Ejemplo FB
[0184]
metilo {(1R)-2-[(2S,5S)-2-(9-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbonil)amino]-3-metilbutanoil}-5-metilpirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-il]-2-oxo-1-feniletil}carbamato
[0185] metilo {(1R)-2-[(2S,5S)-2-(9-{2-[(2S,5S)-H(2S)-2-[(metoxicarboml)ammo]-3-metMbutanoM}-5-metMpirroNdm-2-M]-1H-imidazol-5-M}-1,11-dihidroisocromeno[4\3':6,7]nafto[1,2-d]imidazol-2-N)-5-metilpirrolidin-1-il]-2-oxo-1-feniletil}carbamato se sintetizó de manera similar al metilo [(2S)-1-{(2S,5S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato por sustituyendo (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (R)-2-(metoxicarbonilamino)-2-ácido fenilacético, y sustituyendo HATU con COMU. (0,033 g) LCMS-ESI+: calculado para C48H52N8O7: 852,40; observado [M+1]+: 853,77,1H RMN (400 MHz, cdaod) 88,67 (s, 1H), 8,27 - 8,17 (m, 1H), 8,14 - 8,03 (m, 2H), 8,02 - 7,96 (m, 1H), 7,93 (s, 1H), 7,89 - 7,78 (m, 1H), 7,72 - 7,65 (m, 2H), 7,57 - 7,51 (m, 2H), 7,51 - 7,42 (m, 2H), 5,62 (s, 1H), 5,50 (t, 1H), 5,33 (s, 2H), 5,22 - 5,13 (m, 1H), 4,84 -4,78 (m, 1H), 4,35 -4,24 (m, 1H), 4,21 -4,07 (m, 1H), 3,82 -3,72 (m, 3H)), 3,67 (s, 3H), 2,75 -2,49 (m, 3H), 2,47 - 2,25 (m, 4H), 2,10 - 1,95 (m, 3H), 1,92 - 1,83 (m, 1H), 1,59 (dd, 6H)), 1,33- 1,27 (m, 1H), 1,06 (dd, 2H), 0,99 (d, 2H), 0,88 (d, 3H).
Ejemplo FC
[0186]
dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-il]-2-oxo-1-(tetrahidro-2H-piran-4-il)etilo]carbamato
[0187] metilo [(1S)-2-[(2S,5S)-2-(9-{2-[(2S,5S)-H(2S)-2-[(metoxicarboml)ammo]-3-metMbutanoM}-5-metilpirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-2-il)-5-metilpirrolidin-1-il]-2-oxo-1-(tetrahidro-2H-piran-4-il)etilo]carbamato se sintetizó de manera similar a la del metilo [(2S)-1-{(2S,5S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metilpirrolidin-2-il}-1,11-dihidroquiocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidin-1-il}-3-metilo-1-oxobutan-2-il]carbamato sustituyendo el (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (S)-2-(metoxicarbonilamino)-2-(tetrahidro-2H)-piran-4-il)ácido acético. (0,116 g) LCMS-ESI+: calculado para C47H56N8O8: 860,42; observado [M+1]+: 861,42, 1H RMN (400 MHz, cdaod) 88,65 (s, 1H), 8,27 - 8,17 (m, 1H), 8,08 - 7,97 (m, 1H), 7,93 (s, 1H), 7,88 - 7,83 (m, 1H), 7,73- 7,62 (m, 2H), 5,41 - 5,26 (m, 3H), 5,21 - 5,12 (m, 1H), 4,85 - 4,76 (m, 1H), 4,39 - 4,21 (m, 2H), 4,12 (d, 1H)), 4,04 - 3,90 (m, 2H), 3,87 - 3,81 (m, 1H), 3,76 (d, 2H), 3,67 (d, 4H), 3,50 - 3,38 (m, 1H), 3,25 -3,10 (m, 2H), 2,68 - 2,21 (m, 7H), 2,12 - 1,87 (m, 4H), 1,85 - 1,70 (m, 1H), 1,64 (d, 2H), 1,56 (d, 3H), 1,51 - 1,33 (m, 2H), 1,32 - 1,25 (m, 2H), 1,25 -1,18 (m, 1H), 1,06 (dd, 2H), 0,99 (d, 2H), 0,88 (d, 2H).
Ejemplo FD
[0188]
(S)-2-amino-3- (S)-3-metoxi-2-Hidrocloruro de ácido (metoxicarbonilamino)
metoxipropanoico ácido metoxipropanoico
[0189] (S)-3-metoxi-2-(metoxicarbonilamino)ácido propanoico. A una solución de clorhidrato de (S)-2-amino-3-ácido metoxipropenico (2,5 g, 16,17 mmol) en THF (40 ml) se añadió NaOH acuoso (6M, 6,47 ml, 38,82 mmol) y cloroformiato de metilo (1,50 ml), 19,41mmol). La solución se agitó durante 18 h. Se añadió lentamente HCl acuoso (1 M, 40 ml). La solución se extrajo con acetato de etilo (3 veces) y las capas orgánicas combinadas se secaron sobre sulfato de sodio y se concentraron para proporcionar (S)-3-metoxi-2-(metoxicarbonilamino)ácido propanoico (1,60 g, 56%). 1H RMN (400 MHz, CDCl3) 85,61 (d, 1H), 4,52 (d, 1H), 3,88 (d, 1H), 3,72 (s, 3H), 3,65 (dd, 1H), 3,43- 3,35 (s, 3H).
Ejemplo FE
[0190]
metilo [(2S)-1-{(2S,5S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-serilo]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato
[0191] metilo [(2S)-1-{(2S,5S)-2-[5-(2-£(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-serilo]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato se sintetizó de manera similar a la del metilo [(2S)-1-{(2S,5S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato sustituyendo el (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (S)-3-metoxi-2-(metoxicarbonilamino)ácido propanoico. (0,059 g) LCMS-ESI+: calculado para C44H52N8O8: 820,39; observado [M+1]+: 821,76, 1H RMN (400 MHz, cd3od) 88,66 - 8,57 (m, 1H), 8,24 - 8,14 (m, 2H), 8,06 - 7,94 (m, 2H), 7,93- 7,88 (m, 1H), 7,85 - 7,80 (m, 1H), 7,79 - 7,74 (m, 1H), 7,69 - 7,60 (m, 2H), 6,01 - 5,59 (m, 2H), 5,38 - 5,24 (m, 3H), 5,21 - 5,07 (m, 1H), 4,82 - 4,63 (m, 3H), 4,34 - 4,21 (m, 1H), 4,09 (d, 1H), 3,81 (s, 2H), 3,72 (s, 1H), 3,62 - 3,44 (m, 2H), 3,37 (s, 1H), 3,31 (s, 1H), 2,86 - 2,74 (m, 1H), 2,69 - 2,45 (m, 3H), 2,42 - 2,24 (m, 4H), 2,07 - 1,88 (m, 3H), 1,55 (dd, 5H), 1,27 (d, 2H), 1,05 (dd, 2H), 0,96 (d, 2H), 0,85 (d, 3H).
Ejemplo FF
[0192]
(2S,3R)-3-ferc-butoxi-2
(2S,3R)-2-amino-3-terc (metoxicarbomlamino)
acido butoxibutanoico acido butanoico
[0193] (2S,3R)-3-terc-butoxi-2-(metoxicarbonilamino)ácido butanoico se sintetizó de manera similar a la del (S)-3-metoxi-2-(metoxicarbonilamino)ácido propanoico que sustituye (S)-2-amino-3-hidrocloruro de ácido metoxipropanoico con (2S,3R)-2-amino-3-terc-ácido butbutanoico. (1,33g, 99%) 1H RMN (400 MHz, cdcl3) 85,65 (s, 1H), 4,41 -4,25 (m, 2H), 3,71 (s, 3H), 1,29 (d, 9H), 1,16 (d, 3H).
Ejemplo FG
[0194]
metilo {(2S,3R)-3-terc-butoxi-1-[(2S,5S)-2-(9-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbonN)amino]-3-metNbutanoN}-5-metilpirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4’,3':6,7]nafto[1,2-d]imidazol-2-il)-5-metMpirrolidin-1-il]-1-oxobutan-2-il}carbamato
[0195] metilo {(2S,3R)-3-terc-butoxM-[(2S,5S)-2-(9-[2-[(2S,5S)-1-[(2S)-2-[(metoxicarboml)ammo]-3-metilbutanoil}-5-metilpirrolidm-2-il]-1H-im idazol-5-il}-1,11-dihidroisocromeno[4\3':6,7]nafto[1,2-d]im idazol-2-il)-5-metilpirrolidin-1-il]-1-oxobutan-2-il}carbamato se sintetizó de manera similar al metilo [(2S)-1-{(2S,5S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato que sustituye al (2S,3R)-3-metoxi-2-(metoxicarbonNamino)ácido butanoico con (2S,3R)-3-terc-butoxi-2-(metoxicarbonilamino)ácido butanoico. (0,133 g) LCMS-ESI+: calculado para C48H60N8O8: 876,45; observado [M+1]+: 877,73, 1H RMN (400 MHz, cd3od) 8 8,62 (d, 1H), 8,24 -8,13 (m, 1H), 8,07 -7,76 (m, 4H), 7,73- 7,59 (m, 2H), 5,32 (d, 2H), 5,20 -5,11 (m, 1H), 4,82 -4,75 (m, 2H), 4,70 - 4,62 (m, 1H), 4,47 - 4,22 (m, 3H), 4,19 - 3,98 (m, 2H), 3,94 - 3,85 (m), 1H), 3,80 - 3,61 (m, 6H), 2,85 -2,46 (m, 4H), 2,43- 2,25 (m, 4H), 2,11 - 1,91 (m, 3H), 1,64 (d, 2H), 1,56 (d), 3H), 1,31 (dd, 2H), 1,25 - 1,17 (m, 6H), 1,14 -1,07 (m, 2H), 1,04 (s, 4H), 0,98 (d, 2H), 0,88 (d, 2H).
Ejemplo FH
[0196]
[0197] (2S,3R)-3-hidroxi-2-(metoxicarbonilamino)ácido butanoico se sintetizó de manera similar (S)-3-metoxi-2-(metoxicarbonilamino)ácido propanoico que sustituye al ácido (S)-2-amino-3-hidrocloruro de ácido metoxipropanoico con (2S,3R)-2-amino-3-terc-ácido butoxibutanoico. (0,59 g, 39%) 1H RMN (400 MHz, cdcla) 85,95 (d, 1H), 4,52 -4,29 (m, 2H), 4,08 (d, 1H), 3,75 (d, 4H), 1,57 (t, 3H).
Ejemplo FI
[0198]
metilo {(2S,3R)-3-hidroxi-1-[(2S,5S)-2-(9-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbonil)amino]-3-metilbutanoil}-5-metilpirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-il]-1-oxobutan-2-il}carbamato
[0199] metilo {(2S,3R)-3-hidroxi-1-[(2S,5S)-2-(9-[2-[(2S,5S)-1-{(2S)-2-[(metoxicarbonil)amino]-3-metilbutanoil}-5-metilpirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-2-il)-5
metilpirrolidin-1-il]-1-oxobutan-2-il}carbamato se sintetizó de manera similar a la del metilo [(2S)-1-{(2S,5S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metilpirrolidin-2-il}-1,11-dihidroiso-cromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato que sustituye el (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (2S,3R)-3-hidroxi-2-(metoxicarbonilamino)ácido butanoico. (0,013 g) LCMS-ESI+: calculado para C44H52N8O8: 820,39; observado [M+1]+: 821,73, 1H RMN (400 MHz, cdaod) 88,63 (s, 1H), 8,19 (d, 1H), 8,09 -7,76 (m, 4H), 7,71 -7,62 (m, 2H), 5,47 -5,26 (m, 3H), 5,20 -5,12 (m, 1H), 4,83-4,71 (m, 3H), 4,58 - 4,40 (m, 2H), 4,32 (s, 1H), 4,19 - 3,97 (m, 3H), 3,80 - 3,64 (m, 6H)), 2,71 - 2,44 (m, 4H), 2,41 - 2,27 (m, 3H), 2,08 - 1,92 (m, 3H), 1,67 - 1,47 (m, 5H), 1,33- 1,24 (m, 3H), 1,17 (d, 2H), 1,05 (dd, 2H), 0,98 (d, 2H), 0,87 (d, 2H).
Ejemplo FJ
[0200]
[0201] A una solución del compuesto 1 (7 g, 0,053 mol) en agua (260 ml) se le añadió Na2CO3 (11,2 g, 0,106 mol) en porciones, y la mezcla resultante se enfrió a 0°C. Luego se añadió cloroformiato de metilo (5,5 g, 0,058 mol) gota a gota durante 5 minutos. La reacción se dejó agitar a temperatura ambiente durante 18 horas. La TLC mostró que la reacción se había completado. A continuación, la mezcla se repartió entre 1 N HCl y EtOAc, se separó. La capa orgánica se recogió y la capa acuosa se extrajo adicionalmente con EtOAc adicional. Las capas orgánicas combinadas se lavaron con salmuera, se secaron sobre sulfato de magnesio, se concentraron, se purificaron por cromatografía (PE/EA = 5/1 a 1/1) para dar G-01431-1 (5,6 g, 55%) como un aceite amarillo puro. 1HRMN: (400 M CD3) 88,88 (br, 1H), 5,51-5,49 (m, 1H), 4,56-4,53 (m, 1H), 3,73 (s, 3H), 3,73 (br, 1H), 3,41 (s, 3H), 1,29 (d, 3H).
Ejemplo FK
[0202]
metilo [(2S)-1-{(2S,5S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-alotreonilo]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato
[0203] metilo [(2S)-1-£(2S,5S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-alotreonilo]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato se sintetizó de manera similar a la del metilo [(2S)-1-{(2S,5S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato sustituyendo el (2s,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (2S,3S)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico. (0,150 g) LCMS-ESI+: calculado para C45H54N8O8: 834,41; observado [M+1]+: 835,76,1H RMN (400 MHz, cdaod) 88,61 (s, 1H), 8,23 (s, 1H), 8,18 (d, 1H), 8,07 - 7,87 (m, 3H), 7,83 (d, 1H), 7,77 (s, 1H), 7,66 (t, 2H), 6,00 (d, 1H), 5,74 - 5,65 (m, 1H), 5,30 (d, 2H), 5,21 -5,11 (m, 1H), 4,82 -4,75 (m, 1H), 4,36 (t, 1H), 4,32 -4,25 (m, 1H), 4,11 (d, 1H), 3,85 (s, 2H), 3,73 (s, 1H), 3,66 (d, 3H), 3,63-3,56 (m, 1H), 3,51 -3,41 (m, 1H), 3,36 (s, 2H), 3,09 (s, 1H), 2,86 -2,77 (m, 1H), 2,71 -2,58 (m, 1H), 2,57 - 2,47 (m, 1H), 2,44 - 2,21 (m, 4H), 2,09 - 1,91 (m, 3H), 1,63 (d, 2H), 1,55 (d, 3H), 1,27 (t, 4H), 1,20 (d, 1H), 1,04 (dd, 2H), 0,97 (d, 2H), 0,87 (d, 2H).
Ejemplo FL
[0204]
butoxicarbonilamino)-3- (2S,3K)-metilo 2-(ferchidroxibutanoato butoxicarbonilarruno)-3-(difluorometoxi)butanoato
(difluorometoxi)-2- (difluorometoxi)-2-(metoxicarbomlamino) (metoxicarbomlamino)
butanoato acido butanoico
[0205] 2-íerc-butoxicarbomlammo-3-difluorometoxi-éster metílico del ácido butírico: A una mezcla de 2-tercbutoxi-carbonilamino-3-hidroxi-éster metílico de ácido butírico (630 mg, 2,70 mmol) y cobre (I) yoduro (105 mg, 0,55 mmol) en acetonitrilo a 45°C se añadió una solución de 2-(fluorosulfonil)ácido difluoroacético (0,560 ml, 5,42 mmol) en acetonitrilo (2 ml) mediante una bomba de jeringa durante 45 minutos. La reacción se agitó entonces a 45°C durante 30 minutos. Se añadió otra solución de 2-(fluorosulfonil)ácido difluoroacético (0,560 ml, 5,42 mmol) en acetonitrilo (2 ml) mediante una bomba de jeringa durante 45 minutos a 45°C. La reacción se agitó durante 30 minutos a 45°C después de que se completó la adición de la segunda bomba de jeringa. Se añadió agua cuidadosamente para apagar la reacción, y la mezcla se diluyó con acetato de etilo. La capa orgánica se separó, se lavó con agua y salmuera, se secó (MgSO4) y se concentró. El material bruto se purificó por cromatografía flash (acetato de etilo al 10%/hexanos) para producir el 2-terc-butoxicarbon¡lam¡no-3-d¡fluorometoxi-éster metílico de ácido butírico (276 mg, 36%). 1H-RMN: 400 MHz, (CDCIs) □ : 6,16 (t, JHF = 74,0 Hz, 1H), 5,23-5,16 (br, 1H), 4,86-4,80 (m, 1H), 4,40 (br d, J = 9,8 Hz, 1H), 3,76 (s, 3H), 1,46 (br s, 9H), 1,36 (d, J = 6,4 Hz, 3H) ppm.
[0206] (2S,3R)-metil-3-(difluorometoxi)-2-(metoxicarbonilamino)butanoato: En una solución de 2-tercbutoxicarbonilamino-3-difluorometoxi-éster metílico del ácido butírico (3 g, 10,6 mmol)) en metanol (40 ml) se añadió solución concentrada de HCl (10 ml) y la reacción se agitó a 50°C durante 1 hora. La reacción se concentró en un evaporador rotatorio y el residuo resultante se basificó con una solución saturada de NaHCO3, La capa acuosa se extrajo dos veces con acetato de etilo. La capa orgánica se separó, se lavó con salmuera, se secó (MgSO4) y se concentró. A una solución del material crudo en diclorometano (50 ml) se le añadió diisopropiletilamina (4,2 ml, 24,2 mmol), seguido de cloroformiato de metilo (0,95 ml, 12,3 mmol). La reacción se agitó a temperatura ambiente durante 2 horas, se detuvo mediante la adición cuidadosa de una solución saturada de NH4Cl y se diluyó con acetato de etilo. La capa orgánica se separó, se lavó con agua y salmuera, se secó (MgSO4) y se concentró. El material bruto se purificó por cromatografía flash para producir (2S,3R)-metil-3-(difluorometoxi)-2-(metoxicarbonilamino)butanoato (1,2 g, 47%).
[0207] (2S,3R)-3-(difluorometoxi)-2-(metoxicarbonilamino)ácido butanoico: En una solución de (2S,3R)-metil-3-(difluorometoxi)-2-(metoxicarbonilamino)butanoato (265 mg), 1,1 mmol) en dicloroetano (10 ml) se añadió hidróxido de trimetilestaño (1 g, 5,5 mmol) y la mezcla resultante se calentó a 80°C durante 1 hora. La reacción se enfrió a temperatura ambiente, se diluyó con acetato de etilo, se lavó dos veces con una solución acuosa al 5% de HCl y salmuera, se secó (MgSO4) y se concentró. El material bruto resultante (209 mg, 84%) se usó sin purificación adicional.
Ejemplo FM
[0208]
metilo {(2S)-1-[(2S,5S)-2-(5-{2-[(2S,5S)-1-{(2S,3R)-3-(difluorometoxi)-2-[(metoxicarbonil)amino]butanoilo-5-metilpirrolidin-2-il]-1,11 -dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-5-metMpirrolidin-1 -il]-3-metil-1 -oxobutan-2-il}carbamato
[0209] metilo {(2S)-H(2S,5S)-2-(5-{2-[(2S,5S)-1-£(2S,3R)-3-(difluorometoxi)-2-[(metoxicarbonil)amino]butanoilo-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-9-il}-1H-imidazol-2-il)-5-metilpirrolidin-1-il]-3-metil-1-oxobutan-2-il}carbamato se sintetizó de manera similar a la del Metilo [(2S)-1-{(2S,5S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato que sustituye al ácido (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (2S,3R)-3-(difluorometoxi)-2-(metoxicarbonilamino)ácido butanoico. (0,092 g) LCMS-ESI+: calculado para C45H52F2N8O8: 870,39; observado [M+1]+: 871,78, 1H RMN (400 MHz, cdaod) 88,64 (s, 1H), 8,18 (d, 1H), 8,12 - 7,96 (m, 2H), 7,92 (s, 1H), 7,87 -7,77 (m, 1H), 7,71 -7,61 (m, 2H), 6,31 (t, 2H), 5,92 -5,70 (m, 1H), 5,38 -5,26 (m, 3H), 5,22 -5,11 (m, 1H), 4,83 4,75 (m, 1H), 4,73- 4,64 (m, 1H), 4,62 - 4,52 (m, 1H), 4,50 - 4,40 (m, 1H), 4,29 (s, 1H), 4,13 (d, 1H), 3,78 - 3,62 (m, 5H), 3,40 (s, 1H), 2,72 -2,58 (m, 2H), 2,56 -2,44 (m, 2H), 2,42 -2,24 (m, 3H), 2,12 - 1,90 (m, 3H), 1,76 (d, 1H), 1,62 (d, 2H), 1,55 (d, 2H), 1,40 (d, 1H), 1,35 (d, 1H), 1,29 (d, 1H), 1,25 (d, 2H), 1,07 (d, 1H), 1,02 (d, 1H), 0,98 (d, 2H), 0,87 (d, 2H).
Ejemplo FN
[0210]
metilo [(2S)-1-{(2S,4S)-2-[5-(2-{(2S,5S)-1-[(2S)-2-[(metoxicarboml)amino]-2-(tetrahidro-2H-piran-4-il)acetN]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-4-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato
[0211] metilo [(2S)-1-£(2S,4S)-2-[5-(2-{(2S,5S)-1-[(2S)-2-[(metoxicarboml)ammo]-2-(tetrahidro-2H-piran-4-il)acetil]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-4-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato se sintetizó de una manera similar a la de los ejemplos de sustitución de DX (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con ácido (2S,4S)-1-(tercbutoxicarbonil)-4-metilpirrolidina-2-ácido carboxílico, y sustitución (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoilo)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-((S)-2-(metoxicarbonilamino)-2-(tetrahidro-2H-piran-4-il)acetil)-5-metilpirrolidina-2-ácido carboxílico, y sustituyendo el (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (S)-2-(metoxicarbonilamino)-3-ácido metilbutanoico. (0,022 g) LCMS-ESI+: calculado para C47H56N8O8: 860,42; observado [M+1]+: 861,91, 1H RMN (400 MHz, cdaod) 88,62 (s, 1H), 8,27 - 8,13 (m, 1H), 7,92 (s, 2H), 7,85 -7,77 (m, 1H), 7,73-7,60 (m, 2H), 5,37 -5,13 (m, 4H), 4,43-4,12 (m, 4H), 4,04 -3,78 (m, 3H), 3,76 -3,60 (m, 5H), 3,50 - 3,37 (m, 2H), 3,20 - 3,09 (m, 1H), 2,92 - 2,20 (m, 9H), 2,14 -1,75 (m, 6H), 1,63 (d, 3H), 1,24 (d, 5H), 0,89 (dd, 6H).
Ejemplo FO
[0212]
[[2S,3R)-1-{(2S,4S)-4-[(difluorometoxi)metil]-2-[9-(2-{(2S,5S)-1-[N-(metoxicarbonil)-L-valilo]-5-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]pirrolidin-1-il}-3-metoxi-1-oxobutan-2-il]carbamato
[0213] [[2S,3R)-1-{(2S,4S)-4-[(difluorometoxi)metil]-2-[9-(2-{(2S,5S)-1-[N-(metoxicarbonil)-L-valilo]-5-metMpirrolidm-2-M}-1H-imidazol-5-M)-1,11-dihidroisocromeno[4\3':6,7]nafto[1,2-d]imidazol-2-il]pirrolidm-1-il}-3-metoxi-1-oxobutan-2-il]carbamato se sintetizó de una manera similar a la del Ejemplo DX sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico, y su sustitución (2S,5S)-1-((S)-2-(metoxicarboninilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,4S)-1-(terc-butoxicarbonil)-4-((difluorometoxi)metil)pirrolidina-2-ácido carboxílico. (0,079 g) LCMS-ESI+: calculado para C46H54F2N8O9: 900,40; observado [M+1]+: 901,78, 1H RMN (400 MHz, cdaod) 88,61 (s, 1H), 8,17 (d, 1H), 8,06 - 7,95 (m, 2H), 7,89 (d, 1H), 7.84 - 7,75 (m, 1H), 7,71 - 7,57 (m, 2H), 6,47 (t, 2H), 5,50 - 5,39 (m, 1H), 5,30 (s, 2H), 5,22 - 5,12 (m, 1H), 4,83- 4,75 (m, 1H), 4,52 (d, 1H), 4,42 - 4,24 (m, 2H), 4,19 - 4,03 (m, 3H), 3,86 - 3,72 (m, 2H), 3,68 (s, 4H), 3,28 (s, 2H), 2,98 -2.85 (m, 2H), 2,82 - 2,72 (m, 1H), 2,71 - 2,65 (m, 1H), 2,59 - 2,48 (m, 1H), 2,44 - 2,14 (m, 4H), 2,08 - 1,94 (m, 2H), 1,56 (d, 2H), 1,30 (d, 1H), 1,12 (d, 2H), 1,06 (dd, 2H), 0,99 (d, 2H), 0,89 (d, 2H).
Ejemplo FP
[0214]
metilo [[2S)-1-{(2S,4S)-2-[9-(2-{(2S,5S)-1-[(2S)-2-[(metoxicarbonil)amino]-2-(tetrahidro-2H-piran-4-il)acetil]-5-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-4-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato
[0215] metilo [[2S)-1-£(2S,4S)-2-[9-(2-{(2S,5S)-H(2S)-2-[(metoxicarboml)ammo]-2-(tetrahidro-2H-piran-4-il)acetil]-5-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,l1-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-2-il]-4-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato se sintetizó de una manera similar a la del ejemplo DX que sustituye (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-((S)-2-(metoxicarbonilamino)-2-(tetrahidro-2H-pirano-4-il)acetil)-5-metilpirrolidina-2-ácido carboxílico, y sustituyendo a (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,4S)-1-(tercbutoxicarbonil)-4-metilpirrolidina-2-ácido carboxílico, y sustituyendo (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (S)-2-(metoxicarbonilamino)-3-ácido metilbutanoico. (0,005 g) LCMS-ESI+: calculado para C47H56N8O8: 860,42; observado [M+1]+: 861,90, 1H RMN (400 MHz, cdaod) 88,62 (s, 1H), 8,18 (d, 1H), 8,06 - 7,93 (m, 1H), 7,90 -7,73 (m, 3H), 7,68 - 7,58 (m, 2H), 5,40 - 5,26 (m, 2H), 5,18 - 5,09 (m, 1H), 4,44 - 4,33 (m, 1H), 4,31 - 4,15 (m, 3H), 4,04 - 3,83 (m, 3H), 3,79 - 3,60 (m, 6H), 3,56 - 3,42 (m, 2H), 2,80 - 2,45 (m, 5H), 2,42 - 2,19 (m, 3H), 2,08 - 1,86 (m, 4H), 1,74 (d, 2H), 1,55 (d), 3H), 1,48 - 1,33 (m, 3H), 1,30 -1,17 (m, 4H), 1,05 - 0,75 (m, 7H).
Ejemplo FQ
[0216]
metilo [[1S)-2-[(2S,5S)-2-(5-{2-[(2S,5S)-1-{(2S,3S)-2-[(metoxicarbonil)amino]-3-metilpentanoil}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-5-metilpirrolidin-1-il]-2-oxo-1-(tetrahidro-2H-piran-4-il)etilo]carbamato
[0217] metilo [[1S)-2-[(2S,5S)-2-(5-{2-[(2S,5S)-H(2S,3S)-2-[(metoxicarbonM)ammo]-3-metMpentanoM}-5-metMpirroNdm-2-M]-1,11-dihidroisocromeno[4\3':6,7]nafto[1,2-d]imidazol-9-M}-1H-imidazol-2-M)-5-metilpirrolidin-1-il]-2-oxo-1-(tetrahidro-2H-piran-4-il)etilo]carbamato se sintetizó de una manera similar a la del Ejemplo DX sustituyendo (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-((2S,3S)-2-(metoxicarbonilamino)-3-metilpentanoíl)-5-metilpirrolidina-2-ácido carboxílico, y sustituyendo (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (S)-2-(metoxicarbonilamino)-2-(tetahahidro-2H)-piran-4-il)ácido acético. (0,094 g) LCMS-ESI+: calculado para C48H58N8O8: 874,44; observado [M+1]+: 875,81, 1H RMN (400 MHz, cdaod) 88,39 (t, 1H), 8,21 - 7,24 (m, 8H), 5,71 - 5,33 (m, 2H), 5,30 - 5,01 (m, 3H), 4,85 -4,70 (m, 2H), 4,45 -4,13 (m, 3H), 4,06 -3,71 (m, 4H), 3,67 (s, 4H), 3,51 -3,38 (m, 1H), 3,26 -3,18 (m, 1H), 3,08 -2,94 (m, 1H), 2,91 - 2,55 (m, 2H), 2,53- 2,07 (m, 5H), 2,05 - 1,88 (m, 2H), 1,87 - 1,66 (m, 3H), 1,56 (dd, 5H), 1,43- 1,22 (m, 3H), 1,19 -1,08 (m, 2H), 1,06 - 0,92 (m, 3H), 0,90 - 0,72 (m, 3H).
Ejemplo FR
[0218]
metilo [[1S)-2-[(2S,5S)-2-(5-{2-[(2S,5S)-1-{(2S,3R)-3-metoxi-2-[(metoxicarbonil)amino]butanoilo}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-5-metilpirrolidin-1-il]-2-oxo-1-(tetrahidro-2H-piran-4-il)etilo]carbamato
[0219] metilo [[1S)-2-[(2S,5S)-2-(5-£2-[(2S,5S)-1-{(2S,3R)-3-metoxi-2-[(metoxicarbonM)ammo]butanoMo}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-9-il}-1H-imidazol-2-il)-5-metilpirrolidin-1-il]-2-oxo-1-(tetrahidro-2H-piran-4-il)etilo]carbamato se sintetizó de una manera similar a la del Ejemplo DX sustituyendo (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-((2S,3R)-3-metoxi-2-(ácido metoxicarbonilamino)butanoilo)-5-metilpirrolidina-2-ácido carboxílico, y sustituyendo el (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (S)-2-(metoxicarbonilamino)-2-(tetrahidro-2H)-piran-4-il)ácido acético. (0,089 g) LCMS-ESI+: calculado para C47H56N8O9: 876,42; observado [M+1]+: 877,81, 1H RMN (400 MHz, cdaod) 88,52 - 8,28 (m, 1H), 8,21 - 7,82 (m, 3H), 7,81 - 7,28 (m, 6H), 5,88 - 5,67 (m, 1H), 5,51 - 5,02 (m, 4H), 4,82 - 4,71 (m, 1H), 4,69 - 4,58 (m, 1H), 4,55 - 4,33 (m, 2H), 4,31 -4,13 (m, 2H), 4,04 -3,77 (m, 4H), 3,75 -3,54 (m, 5H), 3,40 (s, 2H), 3,28 -3,21 (m, 1H), 2,98 -2,67 (m, 2H), 2,64 -2,44 (m, 2H), 2,40 - 2,09 (m, 4H), 2,06 - 1,87 (m, 2H), 1,84 - 1,70 (m, 1H), 1,56 (dd, 5H), 1,43- 1,00 (m, 8H).
Ejemplo FS
[0220]
metilo {(2S,3S)-1-[(2S,5S)-2-(9-{2-[(2S,4S)-1-{(2S)-2-[(metoxicarbonN)amino]]-3-metNbutanoN}-4-(metoximetil)pirrolidin-2-il]-1H-imidazoI-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metiIpirroIidin-1-iI]-3-metiI-1-oxopentan-2-iI}carbamato
[0221] metilo {(2S,3S)-H(2S,5S)-2-(9-£2-[(2S,4S)-H(2S)-2-[(metoxicarboml)ammo]]-3-metilbutanoil}-4-(metoximetil)pirrolidm-2-M]-1H-imidazol-5-M}-1,11-dihidroisocromeno[4\3':6,7]nafto[1,2-d]imidazol-2-M)-5-metilpirrolidin-1-il]-3-metil-1-oxopentan-2-il}carbamato se sintetizó de manera similar a un Ejemplo DX sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,4S)-1-(terc-butoxicarbonil)-4-(metoximetil)pirrolidina-2-ácido carboxílico, y sustituyendo (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-((2S,3S)-2-(metoxicarbonNamino)-3-metN-pentanoil)-5-metilpirrolidina-2-ácido carboxílico, y sustituyendo el (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico por (S)-2-(metoxicarbonilamino)-3-ácido metilbutanoico. (0,119 g) LCMS-ESI+: calculado para C47H58N8O8: 862,44; observado [M+1]+: 863,87, 1H RMN (400 MHz, cdaod) 88,60 (s, 1H), 8,31 -8,13 (m, 2H), 8,00 (d, 1H), 7,90 (d, 2H), 7,83- 7,78 (m, 1H), 7,70 -7,60 (m, 2H), 5,38 -5,15 (m, 4H), 4,41 -4,15 (m, 4H), 3,78 (s, 1H), 3,72 -3,48 (m, 7H), 3,41 (s, 3H), 2,92 -2,72 (m, 2H), 2,69 -2,55 (m, 2H), 2,52 -2,29 (m, 3H), 2,13-1,96 (m, 3H), 1,91 -1,69 (m, 2H), 1,64 (d, 3H), 1,32 - 1,13 (m, 3H), 1,07 - 0,75 (m, 12H).
Ejemplo FT
[0222]
metilo {(2S,3S)-1-[(2S,4S)-2-(5-{2-[(2S,5S)-1-{(2S,3R)-3-metoxi-2-[(metoxicarbonil)amino]butanoilo}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-3-metil-1 -oxopentan-2-il}carbamato
[0223] metilo {(2S,3S)-1-[(2S,4S)-2-(5-£2-[(2S,5S)-1-{(2S,3R)-3-metoxi-2-[(metoxicarboml)ammo]butanoNo}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-9-il}-1H-imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-3-metil-1-oxopentan-2-il}carbamato se sintetizó de una manera similar a la del Ejemplo DX sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,4S)-1-(tercbutoxicarbonil)-4-(metoximetil)pirrolidina-2-ácido carboxílico, y sustituyendo a (2S,5S))-1-((S)-2-(metoxicarboninilamino)-3-metilbutanoílo)-5-metilpirrolidina-2-ácido carboxílico con (2S,5S)-1-((2S,3R)-3-metoxi-Ácido 2-(metoxicarbonilamino)butanoilo)-5-metilpirrolidina-2-ácido carboxílico, y sustituyendo el (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (2S,3S)-2-(metoxicarbonilamino)-3-ácido metilpentanoico. (0,118 g) LCMS-ESI+: calculado para C47H58N8O9: 878,43; observado [M+1]+: 879,86, 1H RMN (400 MHz, cdaod) 88,52 (s, 1H), 8,23 8,07 (m, 1H), 7,99 - 7,72 (m, 2H), 7,68 - 7,55 (m, 1H), 5,30 - 5,24 (m, 1H)), 4,81 (s, 8H), 4,61 - 4,18 (m, 3H), 4,14 -4,00 (m, 6H), 3,95 -3,76 (m, 1H), 3,72 -3,47 (m, 3H), 3,37 (d, 1H)), 3,33 (s, 3H), 3,29 (s, 2H), 3,26 (s, 1H), 2,86 -2,68 (m, 1H), 2,66 -2,54 (m, 1H), 2,50 -2,27 (m, 2H), 2,11 -2,03 (m, 1H), 1,99 (s, 9H), 1,80 - 1,69 (m, 1H), 1,57 (d, 1H), 1,49 - 1,33 (m, 1H), 1,21 (t, 10H), 1,16 -1,02 (m, 2H), 0,92 -0,78 (m, 2H).
Ejemplo FV
[0224]
metilo {(2S,3S)-1-[(2S,5S)-2-(9-{2-[(2S,4S)-1-{(2S)-2-[(metoxicarbonil)amino]-3-metilbutanoil}-4-(metoximetil)pirrolidin-2-il]-1H-imidazol-5-il}-1,1l-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-il]-3-metil-1-oxobutan-2-il}carbamato
metilo {(1R)-2-[(2S,4S)-2-(4-bromo-5-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbonil)amino]-3-metilbutanoil}-5-metilpirrolidin-2-il]-1,l1-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato
metilo {(1R)-2-[(2S,4S)-2-(4-ciclopropil-5-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbonil)amino]-3-metilbutanoil}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato
[0225] metilo {(1R)-2-[(2S,4S)-2-(4-bromo-5-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarboml)ammo]-3-metMbutanoM}-5-metMpirroNdm-2-M]-1,11-dihidroisocromeno[4\3':6,7]nafto[1,2-d]imidazol-9-M}-1H-imidazol-2-M)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato. A una solución de metilo {(2S,3S)-1-[(2S,5S)-2-(9-{2-[(2S,4S)-1-{(2S)-2-[(metoxicarbonil)amino]-3-metilbutanoil}-4-(metoximetil)pirrolidin-2-il]-lH-imidazol-5-il}-1,l1-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-il]-3-metil-1-oxobutan-2-il}carbamato (0,06 g, 0,07 mmol) en AcOH (1,0 mL) se añadió bromo (0,004 mL), 0,08 mmol) en AcOH (0,4 ml). La solución se agitó a temperatura ambiente durante 1 h y se concentró al vacío. El aceite crudo se purificó por HPLC de fase inversa (Gemini, 10 ^ 65% de MeCN/H2O (0,1% de TFA)). Las fracciones deseadas se combinaron, se basificaron con bicarbonato de sodio acuoso y se extrajeron con CH2Cl2, Las capas orgánicas combinadas se secaron sobre Na2SO4 y concentrado al vacío para proporcionar metilo {(1R)-2-[(2S,4S)-2-(4-bromo-5-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbonil)amino]-3-metilbutanoil}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato(0,04 g, 54%). LCMS-ESI+: calculado para C46H55BrNsO8: 926,33 (M ); Encontrado: 927,17 (M H+).
[0226] metNo{(1R)-2-[(2S,4S)-2-(4-cidopropN-5-£2-[(2S,5S)-1-{(2S)-2-[(metoxicarboml)ammo]-3-metNbutanoN}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-9-il}-1H-imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato. A una solución de metilo {(1R)-2-[(2S,4S)-2-(4-bromo-5-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbonil))amino]-3-metilbutanoil}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato (0,04 g, 0,036 mmol) en tolueno (0,75 ml) se añadió c-ácido propilborónico (0,006 g, 0,08 mmol), acetato de paladio (0,005 g, 0,007 mmol), tetrafluoroborato de triciclohexilfosfina (0,005 g, 0,014 mmol) y fosfato de potasio (acuoso, 2 M, 0,075 ml, 0,15 mmol). La solución se desgasificó con argón durante 5 minutos y se calentó a 100°C (baño de aceite externo) durante 20 h. La solución se enfrió a temperatura ambiente, se diluyó con CH2O 2 y se
lavó con agua. La capa acuosa se extrajo de nuevo con CH2Cl2/MeOH (2x). Las capas orgánicas combinadas se secaron sobre Na2SO4 y se concentraron al vacío. El aceite crudo se purificó por HPLC de fase inversa (Gemini, 10 ^ 50% de MeCN/H2O (0,1% de TFA)). Las fracciones deseadas se combinaron y se concentraron a presión reducida para eliminar los compuestos orgánicos volátiles. La adición de bicarbonato de sodio acuoso con agitación dio como resultado la precipitación de un sólido blanco. El precipitado se filtró a través de un filtro de membrana y se lavó con agua. El secado a presión reducida proporcionó metilo {(1R)-2-[(2S,4S)-2-(4-ciclopropil-5-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbonil)amino]-3-metilbutanoil-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato(0,01 g, 42%). LCMS-ESI+: calculado para C49H60N8O8: 888,45 (M ); Encontrado: 889,86 (M H+). 1H RMN (400 MHz, cdaod) 8 (mezcla de rotómeros) 8,38 (d, 1H), 8,01 (d, 1H), 7,85 (d, 2H), 7,73- 7,60 (m, 2H), 7,53- 7,42 (m, 1H), 5,33- 5,16 (m, 3H), 4,38 - 4,27 (m, 1H), 4,26 -4,14 (m, 2H), 4,14 - 4,00 (m, 2H), 3,69 (s, 3H), 3,63 (s, 3H), 3,60 - 3,51 (m, 2H), 3,38 (s, 3H), 2,85 - 2,65 (m, 2H), 2,65 - 2,47 (m, 2H), 2,37 - 2,16 (m, 2H), 2,16 - 1,91 (m, 5H), 1,48 (d, 3H), 1,18 (d, 2H), 1,09 - 0,94 (m, 5H), 0,91 (d, 3H), 0,89 - 0,84 (m, 2H), 0,82 (d, 3H), 0,65 (s, 1H).
Ejemplo FW
[0227]
[0228] metilo{(2S,3R)-3-metoxi-1-[(2S,4S)-2-(9-£2-[(2S,4S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-4-(metoximetN)pirroNdm-2-M]-1H-imidazol-5-M}-1,11-dihidroisocromeno[4\3':6,7]nafto[1,2-d]imidazol-2-M)-4-metilpirrolidin-1-il]-1-oxobutan-2-il}carbamato. Siguiendo el Ejemplo DX, sustituyendo (2S,5S)-1-(tercbutoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,4S)-1-(terc-butoxicarbonil)-4-(metoximetil)pirrolidina-2-ácido carboxílico, (1R, 3S)-2-(2-(metoxicarbonilamino)-3-metilbutanoílo)-3-ácido metilciclopentanocarboxílico con (2S,4S)-1-(terc-butoxicarbonil)-4-metilpirrolidina-2-ácido carboxílico, y usando 2 equivalentes de (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico, proporcionó metilo {(2S,3R)-3-metoxi-1-[(2S,4S)-2-(9-{2-[(2S,4S)-1-[N-(metoxicarbonil)-0-metil-L-treonil]-4-(metoximetil)pirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-4-metilpirrolidin-1-il]-1-oxobutan-2-il}carbamato (0,08 g). LCMS-ESI+: calculado para C46H56N8O10: 880,41 (M ); Encontrado: 882,11 (M H+). 1H RMN (400 MHz, cdaod) 8 (mezcla de rotómeros) 8,21 (d, 1H), 7,91 -7,72 (m, 2H), 7,70 -7,33 (m, 4H), 7,33-7,11 (m, 2H), 5,24 -5,13 (m, 1H), 5,13-4,91 (m, 3H), 4,45 - 4,29 (m, 2H), 4,26 - 3,97 (m, 3H), 3,57 (s, 6H), 3,50 - 3,37 (m, 3H), 3,28 (s, 3H), 3,19 - 3,10 (m, 7H), 2,62 -2,45 (m, 2H), 2,45 -2,30 (m, 2H), 2,09 - 1,74 (m, 4H), 1,14 (d, 3H), 1,11 -0,97 (m, 6H).
Ejemplo FX
[0229]
metilo {(2S,3R)-3-metoxi-1-[(2S,5S)-2-(9-{2-[(2S,4S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-4-(metoximetil)pirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-il]-1-oxobutan-2-il}carbamato
[0230] metilo {(2S,3R)-3-metoxi-1-[(2S,5S)-2-(9-£2-[(2S,4S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-4-(metoximetil)pirrolidin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-2-il)-5-metilpirrolidin-1-il]-1-oxobutan-2-il}carbamato. Siguiendo el Ejemplo DX, sustituyendo (2S,5S)-1-(tercbutoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico con (2S,4S)-1-(terc-butoxicarbonil)-4-(metoximetil)pirrolidin-2-ácido carboxílico, (1 R, 3S)-2-(2-(metoxicarbonilamino)-3-metilbutanoílo)-3-ácido metilciclopentanocarboxílico con
(2S,4S)-1-(terc-butoxicarbonil)-5-metilpirrolidina-2-ácido carboxílico, y usando 2 equivalentes de (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico, proporcionó metilo {(2S,3R)-3-metoxi-1-[(2S,5S)-2-(9-{2-[(2S,4S)-1-[N-(metoxicarboml)-O-metil-L-treoml]-4-(metoximetil)pirroNdin-2-il]-1H-imidazol-5-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-il]-1-oxobutan-2-il}carbamato (0,14 g). LCMS-ESI+: calculado para C46H56N8O10: 880,41 (M ); encontrado: 881,85 (M H+). 1H RMN (400 MHz, cdaod) 8 (mezcla de rotómeros) 8,40 - 8,22 (m, 2H), 8,07 - 7,84 (m, 2H), 7,83 - 7,25 (m, 6H), 5,75 (s, 1H), 5,29 - 5,07 (m, 4H), 4,42 (d, 2H), 4,32 -4,12 (m, 2H), 3,86 (s, 1H), 3,75 -3,44 (m, 9H), 3,41 -3,32 (m, 4H), 3,26 -3,19 (m, 4H), 2,72 -2,35 (m, 4H), 2,35 - 1,87 (m, 5H), 1,55 (d, 3H), 1,23 (s, 2H), 1,13 (d, 5H).
Ejemplo FY
[0231]
metilo {(1 R)-2-[(2S,4S)-2-(4-cloro-5-{2-[(2S,5S)-1 -{(2S)-2-[(metoxícarbonil)amino]-3-metilbutanoil}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno^’.S’ie.ZJnaftoIl^-dlimidazol-Q-ilJ-IH-imidaz ol-2-il)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato
[0232] terc-butilo (2S,4S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-L-valilo]-5-metilpirrolidin-2-il}-1,11-dihidrodroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-9-il)-1H-4-cloroimidazol-2-il]-4-(metoximetil)pirrolidin-1-carboxilato. A una solución de terc-butilo (2S,4S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-L-valilo]-5-metilpirrolidin-2 il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-4-(metoximetil)pirrolidina-1-carboxilato
(0,1 g, 0,12 mmol) en DMF (1 ml) se añadió N-clorosuccinimida (0,02 g, 0,16 mmol). La solución resultante se agitó a temperatura ambiente durante 1 h, y luego se calentó a 45°C durante 4 h. La solución se purificó por HPLC de fase inversa (Gemini, 10 ^ 68% de MeCN/H2O (0,1% de TFA)). Las fracciones deseadas se diluyeron con EtOAc y se lavaron con una mezcla 1:1 de bicarbonato de sodio acuoso y salmuera. Las capas acuosas se volvieron a extraer con EtOAc (2x). Las capas orgánicas combinadas se secaron sobre Na2SO4 y se concentraron al vacío para proporcionar terc-butilo (2S,4S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-L-valilo]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-4-cloroimidazol-2-il]-4-(metoximetil)pirrolidina-1-carboxilato (0,09 g, 87%). LCMS-ESI+: calculado para C44H52ClNyO7: 825,36 (M ); Encontrado: 827,13 (M+H+).
[0233] metilo {(1R)-2-[(2S,4S)-2-(4-doro-5-{2-[(2S,5S)-H(2S)-2-[(metoxicarboml)ammo]-3-metMbutanoM}-5-metMpirroNdm-2-M]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-M}-1H-imidazol-2-M)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato. A una solución de terc-butilo (2S,4S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-L-valilo]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-4-cloroimidazol-2-il]-4-(metoximetilo) 1-carboxilato de pirrolidina (0,09 g, 0,11 mmol) en una mezcla de CH2Cl2 (1,5 ml) y metanol (0,25 ml) se añadió HCl (en dioxanos, 4M, 0,8 ml, 3,20 mmol). La solución resultante se agitó a 40°C durante 1 h, y se concentró al vacío. El sólido resultante se suspendió en CH2Ch (1,5 ml) y se añadieron (R)-2-(metoxicarbonilamino)-2-ácido fenilacético (0,04 g, 0,17 mmol) y diisopropiletilamina (0,07 ml, 0,40 mmol). La reacción se enfrió a -40°C (baño de MeCN/CO2) y se añadió COMU (0,07 g, 0,18 mmol). La solución resultante se dejó calentar a temperatura ambiente durante 30 minutos y se agitó a temperatura ambiente durante 1,5 horas. La reacción se diluyó con CH2Cl2 y se lavó con bicarbonato de sodio acuoso. La capa acuosa se extrajo de nuevo con CH2Cl2 , y las capas orgánicas combinadas se secaron (Na2SO4) y se concentraron. El aceite crudo se purificó por HPLC de fase inversa (Gemini, 10 ^ 58% de MeCN/H2O (0,1% de TFA)). Las fracciones deseadas se diluyeron con EtOAc y se lavaron con salmuera. La capa acuosa se extrajo de nuevo con EtOAc (2x). Las capas orgánicas combinadas se secaron sobre Na2SO4 y se concentraron al vacío. El material resultante se liofilizó de MeCN y agua para proporcionar metilo {(1R)-2-[(2S,4S)-2-(4-cloro-5-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbonil)amino]-3-metilbutanoil}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato (0,09 g, 90%). LCMS-ESI+: calculado para C49Hs3ClN2Oa: 916,37 (M ); Encontrado: 918,28 (M+H+).
1H RMN (400 MHz, cdaod) 8 (mezcla de rotómeros) 8,43 (s, 1H), 8,18 - 7,94 (m, 2H), 7,90 - 7,78 (m, 1H), 7,77 - 7,55 (m, 3H), 7,53- 7,29 (m, 4H), 7,13- 6,95 (m, 1H), 5,49 - 5,30 (m, 2H), 5,31 - 5,13 (m, 2H), 5,12 - 5,00 (m, 1H), 4,40 -4,08 (m, 3H)), 3,89 (s, 1H), 3,72 - 3,61 (m, 3H), 3,58 (s, 2H), 3,26 (s, 3H), 2,57 (s, 2H), 2,50 - 2,00 (m, 7H), 2,00 -1,84 (m, 3H), 1,56 (d, 3H), 1,10 (d, 2H), 1,07 - 0,73 (m, 7H).
Ejemplo FZ
[0234]
[0235] terc-butilo (2S,4S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-L-valilo]-5-metilpirrolidin-2-il}-1,11-dihidrodroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-9-il)-1H-4-bromoimidazol-2-il]-4-(metoximetil)pirrolidin-1-carboxilato. A una solución de terc-butilo (2S,4S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-L-valiloí-5-metilpirrolidin-2 il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-4-(metoximetil)pirrolidin-1-carboxilato-N-bromosuccinimida (0,3 g, 0,38 mmol) se añadió en DMF (3,8 ml) a 0°C (0,067 g, 0,38 mmol). La solución resultante se agitó a 0°C durante 1 h. La solución se purificó por HPLC de fase inversa (Gemini, 10 ^ 65% de MeCN/H2O (0,1% de TFA)). Las fracciones deseadas se diluyeron con EtOAc y se lavaron con una mezcla 1:1 de bicarbonato de sodio acuoso y salmuera. Las capas acuosas se volvieron a extraer con EtOAc (2x). Las capas orgánicas combinadas se secaron sobre Na2SO4 y se concentraron al vacío para proporcionar terc-butilo (2S,4S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarboninilo)-L-valilo]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-4-bromoimida dazol-2-il]-4-(metoximetil)pirrolidina-1-carboxilato (0,33 g, 99%). LCMS-ESI+: calculado para C44H52BrNyOy: 869,31 (M+); Encontrado: 871,61 (M+H+).
[236] terc-butilo (2S,4S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-L-valilo]-5-metilpirrolidin-2-il}-1,11-dihidrobromoceno[4\3':6,7]nafto[1,2-d]imidazol-9-M)-1H-4-ciclopropiUmidazol-2-M]-4-(metoximetMo))pirroNdma-1-carboxilato. A una solución de terc-butilo (2S,4S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-L-valilo]-5-metil-pirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-4-bromoimidazol-2-il]-4-(metoximetil)pirrolidina-1-carboxilato (0,20 g, 0,23 mmol) en tolueno (2,5 ml). Se añadió ácido ciclopropilborónico (0,04 g, 0,47 mmol), Pd(OAc)2 (0,03 g, 0,05 mmol), triciclohexilfosfina triclorato de boro (0,04 g), 0,12 mmol) y fosfato de potasio (acuoso, 2M, 0,40 ml, 0,80 mmol). La suspensión se desgasificó con argón durante 5 minutos y se calentó a 100°C (baño de aceite
externo) durante 20 horas. La reacción se enfrió a temperatura ambiente, se diluyó con EtOAc y se filtró a través de celite. El filtrado se concentró y se purificó por cromatografía en columna (SiO2 , MeOH/EtOAc del 0 al 30%) para proporcionar terc-butilo (2S,4S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-L-valilo]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-4-ciclopropil-imidazol-2-il]-4-(metoximetil)pirrolidina-1-carboxilato (0,13 g, 67%). LCMS-ESI+ : calculado para C47H57N7O7: 831,43 (M ); Encontrado: 832,62 (M+H+ ).
[0237] metilo {(1R)-2-[(2S,4S)-2-(4-cidopropN-5-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarboml))ammo]-3-metilbutanoN}-5-metMpirroNdm-2-N]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-M}-1H-imidazol-2-M)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato. A una solución de terc-butilo (2S,4S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-L-valilo]-5-metilpirrolidin-2-il}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-4-ciclopropil-imidazol-2-il]-4-(metoximetil)pirrolidina-1-carboxilato (0,13 g, 0,15 mmol) en una mezcla de CH2Cl2 (3,0 ml) y metanol (0,25 ml) se le añadió HCl (en dioxanos, 4M, 1,1 ml, 4,40 mmol). La solución resultante se agitó a 40°C durante 1 h, y se concentró al vacío. El sólido resultante se suspendió en CH2Ch (3,0 ml) y se añadieron ácido (R)-2-(metoxicarbonilamino)-2-fenilacético (0,05 g, 0,23 mmol) y diisopropiletilamina (0,1 ml, 0,57 mmol). La reacción se enfrió a -40°C (baño de MeCN/CO2) y se añadió COMU (0,11 g, 0,25 mmol). La solución resultante se dejó calentar a temperatura ambiente durante 30 minutos y se agitó a temperatura ambiente durante 1,5 horas. La reacción se diluyó con CH2Cl2 y se lavó con bicarbonato de sodio acuoso. La capa acuosa se extrajo de nuevo con CH2Cl2, y las capas orgánicas combinadas se secaron (Na2SO4) y se concentraron. El aceite crudo se purificó por HPLC de fase inversa (Gemini, 10 ^ 58% de MeCN/H2O (0,1% de TFA)). Las fracciones deseadas se combinaron con MeOH y se concentraron para eliminar los volátiles. La solución resultante se basificó con bicarbonato de sodio acuoso (sat.). La suspensión resultante se agitó a temperatura ambiente durante 30 minutos, se filtró (filtro de membrana de nailon (0,45 um)) y se lavó con agua. El sólido se secó al vacío para proporcionar metilo {(1R)-2-[(2S,4S)-2-(4-ciclopropil-5-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbonil)amino]-3-metilbutanoil}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato (0,05 g, 38%). LCMS-ESI+ : calculado para C52H58N8O8 : 922,44 (M ); Encontrado: 923,69 (M+H+ ).
1H RMN (400 MHz, cdaod) 8 (Mezcla de rotómeros) 8,28 (s, 2H), 7,93 (s, 2H), 7,74 - 7,52 (m, 3H), 7,52 - 7,32 (m, 3H), 7,27 - 7,07 (m, 4H), 5,48 - 5,38 (m, 2H), 4,10 - 3,98 (m, 2H), 3,67 - 3,48 (m, 4H), 3,42 - 3,34 (m, 6H), 3,06 (s, 3H), 2,43 2,16 (m, 4H), 2,16 -1,61 (m, 8H), 1,55 - 1,32 (m, 3H), 1,02 -0,50 (m, 11H).
Ejemplo GA
[0238]
metil [(2S)-1-1(2S,4S)-2-[9-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonilo]-5-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-4-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato
[0239] metil [(2S)-1-1(2S,4S)-2-[9-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonilo]-5-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-4-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato. Siguiendo el Ejemplo DX, sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidin-2-ácido carboxílico con (2S,5S)-1-((2S,3R)-3-metoxi-2-(metoxicarbonilamino)butanoilo)-5-metil-pirrolidin-2-ácido carboxílico, (1R, 3S)-2-(2-(metoxicarbonilamino)-3-metilbutanoílo)-3-ácido metilciclopenacárico con (2S,4S)-1-(tercbutoxicarbonil)-4-metilpirrolidin-2-ácido carboxílico y el (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (S)-2-(metoxicarbonilamino)-3-ácido metilbutanoico proporcionaron metilo [(2S)-1-{(2S,4S)-2-[9-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-4-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato (0,12 g). LCMS-ESI+: calculado para C45H54N8O8: 834,41 (M ); Encontrado: 835,47 (M+H+). 1H RMN (400 MHz, cdaod) 8 (mezcla de rotómeros) 8,29 (s, 2H), 8,02 - 7,71 (m, 3H), 7,71 - 7,20 (m, 5H), 5,52 (s, 1H), 5,31 - 4,98 (m, 4H), 4,74 - 4,62 (m, 1H), 4,56 - 4,04 (m, 5H), 3,74 (s, 1H), 3,65 (s, 2H), 3,63 (s, 2H), 3,59 - 3,44 (m, 2H), 3,35 (s, 2H), 2,65 - 2,28 (m, 4H), 2,27 - 1,82 (m, 5H), 1,53 1,44 (m, 2H), 1,26 (s, 1H), 1,21 (d, 3H), 1,18 -1,06 (m, 3H), 1,03-0,77 (m, 6H).
Ejemplo GB
[0240]
terc-butilo (2S,4S)-2-(9-{2-[(2S,4S)-1-(terc-butoxicarbonil)-4-metilpirirolidin-2-il]-1H-imidazol-5-il}-1,4,5,11-tetrahidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-carboxilato
terc-butilo (2S,4S)-2-(9-{2-[(2S,4S)-1-(terc-butoxicarbonil)-4-metilpirrolidin-2-il]-1H-4-cloroimidazol-5-il}-1,4,5,11-tetrahidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1 -carboxilato
metilo [(2S,3R)-1-{(2S,5S)-2-[9-(4-cloro-2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metilpirrolidin-2-il}-1H-Imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-il}-3-metoxi-1-oxobutan-2-il]carboxilato
[0241] terc-butilo (2S,4S)-2-(9-{2-[(2S,4S)-1-(terc-butoxicarboml)-4-metNpiriroNdm-2-M]-1H-imidazol-5-M}-1.4.5.11- tetrahidroisocromeno[4\3':6,7]nafto[1,2-d]imidazol-2-N)-5-metMpirroMdm-1-carboxNato. Siguiendo el Ejemplo DX, sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidin-2-ácido carboxílico y (1R, 3S)-2-(2-(metoxicarbonilamino)-3-metilbutanoilo)-3-ácido metilciclopentanocarboxílico con (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidin-2-ácido carboxílico, y omitiendo el paso final, proporcionó terc-butilo (2S,4S)-2-(9-{2-[(2S,4S)-1-(tercbutoxicarbonil)-4-metilpirrolidin-2-il]-1H-imidazol-5-il}-1,4,5,11-tetrahidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-carboxilato (0,83 g). LCMS-ESI+: calculado para C41H48N6O5: 704,37 (M+); Encontrado: 705,52 (M+H+).
[0242] terc-butilo (2S,4S)-2-(9-{2-[(2S,4S)-1-(terc-butoxicarbonM)-4-metMpirroNdm-2-M]-1H-4-doroimidazol-5-M}-1.4.5.11- tetrahidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-2-il)-5-metilpirrolidin-1-carboxilato. A una solución de terc-butilo (2S,4S)-2-(9-{2-[(2S,4S)-1-(terc-butoxicarbonM)-4-metMpirroNdm-2-M]-1H-imidazol-5-il}-1,4,5,11-tetrahidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-carboxilato (0,15 g, Se añadieron 0,21 mmol) en DMF (2,2 ml) N-clorosuccinimida (0,04 g, 0,28 mmol). La solución resultante se calentó a 45°C durante 3 h. La solución se enfrió a temperatura ambiente, se diluyó con EtOAc y se lavó con LiCl acuoso (5%, 2x). Las capas acuosas se volvieron a extraer con EtOAc. Las capas orgánicas combinadas se secaron sobre (Na2SO4) y se concentraron al vacío. El aceite crudo se purificó por cromatografía en columna (SO 2, 50 al 100% de EtOAc (5% de MeOH)/Hexanos) para proporcionar terc-butilo (2S,4S)-2-(9-{2-[(2S,4S)-1-(terc-butoxicarbonil)-4-metilpirrolidin-2-il]-1H-4-cloroimidazol-5-il}-1,4,5,11-tetrahidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-carboxilato (0,13 g, 86%). LCMS-ESI+: calculado para C41H47ClNaO5: 738,33 (M+); Encontrado: 739,84 (M+H+).
[0243] metilo[(2S,3R)-1-{(2S,5S)-2-[9-(4-cloro-2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-5-metilpirrolidin-1-il}-3-metoxi-1-oxobutan-2-il]carbamato. A una solución de terc-butilo (2S,4S)-2-(9-{2-[(2S,4S)-1-(terc-butoxicarbonil)-4-metilpirrolidin-2-il]-1H-4-cloroimidazol-5-il}-1,4,5,11-tetrahidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-carboxilato (0,14 g, 0,19 mmol) en una mezcla de CH2Cl2 (2,0 ml) y metanol (0,5 ml) se le añadió HCl (en dioxanos, 4M, 1,3 ml, 5,20 mmol). La solución resultante se agitó a 40°C durante 1 h, y se concentró al vacío. El sólido resultante se suspendió en CH2O 2 (2,0 ml) y (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico (0,04 g, 0,23 mmol), HATU (0,08 g, 0,22 mmol) y diisopropilo. Se añadieron etilamina (0,1 ml, 0,57 mmol). La solución resultante se agitó a temperatura ambiente durante 2 h. La reacción se diluyó con DMF y se concentró. El aceite crudo se purificó por HPLC de fase inversa (Gemini, 10 ^ 60% de MeCN/H2O (0,1% de TFA)). Las fracciones deseadas se combinaron con MeOH y se concentraron para eliminar los volátiles. La solución resultante se basificó con bicarbonato de sodio acuoso (sat.). La suspensión espesa resultante se agitó a
temperatura ambiente durante 30 min, se filtró (filtro de membrana de nailon (0,45um)) y se lavó con agua. El sólido se secó al vacío para proporcionar Metilo [(2S,3R)-1-{(2S,5S)-2-[9-(4-cloro-2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metil-pirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3’:6,7]na1:to[1,2-d]imidazol-2-il]-5-metilpirrolidin-1-il}-3-metoxi-1-oxobutan-2-il]carbamato (0,05 g, 62%). LCMS-Es I+: calculado para C45H53ClN8Og: 884,36 (M+); Encontrado: 886,33 (M+H+). 1H RMN (400 MHz, cd3od) 8 (mezcla de rotómeros) 8,35 (s, 1H), 8,10 - 7,87 (m, 2H), 7,88 - 7,82 (m, 1H), 7,77 - 7,57 (m, 2H), 7,57 - 7,45 (m, 1H), 5,77 - 5,63 (m, 1H), 5,51 - 5,42 (m, 1H), 5,24 -5,06 (m, 2H), 4,98 - 4,86 (m, 1H), 4,70 - 4,51 (m, 2H), 4,43 (d, 1H), 4,24 (d, 1H), 4,21 - 4,06 (m, 2H), 3,81 (s, 1H), 3,63 (s, 2H), 3,58 (s, 2H), 3,57 (s, 2H), 3,48 (s, 2H), 3,32 - 3,27 (m, 3H), 2,90 - 2,77 (m, 1H), 2,60 (s, 2H), 2,27 (d, 6H), 1,84 (s, 1H), 1,48 (d, 2H), 1,42 (d, 2H), 1,29 - 0,89 (m, J = 31,3, 29,3, 19,7 Hz, 9H).
Ejemplo GC
[0244]
terc-butilo (2S,4S)-2-(9-{2-[(2S,4S)-1-(terc-butoxicarbonil)-4-metilpirirolidin-2-il]-1H-4-ciclopropil-imidazol-5-il}-1,4,5,11-tetrahidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-carboxilato
metilo[(2S,3R)-1-{(2S,5S)-2-[9-(4-ciclopropil-2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-5-metilpirrolidin-1-il}-3-metoxi-1-oxobutan-2-il]carbamato
[0245] terc-butilo (2S,4S)-2-(9-{2-[(2S,4S)-1-(terc-butoxicarbonM)-4-metNpiNroMdm-2-M]-1H-4-cid opropN-imidazol-5-M}-1,4,5,11-tetrahidroisocromeno[4\3':6,7]nafto[1,2-d]imidazol-2-M)-5-metNpirroMdm-1-carboxNato. Siguiendo el Ejemplo FZ, sustituyendo terc-butilo (2S,4S)-2-[5-(2-{(2S,5S)-1-[N-(metoxicarbonil)-L-valilo]-5-metilpirrolidin-2-ilo}-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il)-1H-imidazol-2-il]-4-(metoximetil)pirrolidin-1-carboxilato con terc-butilo (2S,4S)-2-(9-{2-[(2S,4S)-1-(terc-butoxicarbonil)-4-metilpirrolidin-2-il]-1H-imidazol 5-il}-1,4,5,11-tetrahidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-carboxilato, proporcionado terc-butilo (2S,4S)-2-(9-{2-[(2S,4s)-1-(terc-butoxicarbonil)-4-metilpirrolidin-2-il]-1H-4-ciclopropilimidazol 5-il}-1,4,5,11-tetrahidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-carboxilato de 0,27 g). LCMS-ESI+: calculado para C44H52N6O5: 744,40 (M+); Encontrado: 745,46 (M+H+).
[0246] metilo[(2S,3R)-1-{(2S,5S)-2-[9-(4-cidopropil-2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-5-metilpirrolidin-1-il}-3-metoxi-1-oxobutan-2-il]carbamato. A una solución de terc-butilo (2S,4S)-2-(9-{2-[(2S,4S)-1-(terc-butoxicarbonil)-4-metilpirrolidin-2-il]-1H-4-cloroimidazol-5-il}-1,4,5,11-tetrahidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-carboxilato (0,27 g, 0,36 mmol) en una mezcla de CH2Ch (3,5 mL) y metanol (0,5 mL) se le añadió HCl (en dioxanos, 4M, 2,7 mL, 10,80 mmol). La solución resultante se agitó a 40°C durante 1 h, y se concentró al vacío. El sólido resultante se suspendió en CH2O 2 (2,0 ml) y (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico (0,17 g, 0,91 mmol), HATU (0,35 g, 0,91 mmol) y diisopropilo. Se añadieron etilamina (0,5 ml, 2,86 mmol). La solución resultante se agitó a temperatura ambiente durante 2 h. La reacción se diluyó con DMF y se concentró. El aceite crudo se purificó por HPLC de fase inversa (Gemini, 10 ^ 45% MeCN/H2O (0,1% TFA)). Las fracciones deseadas se diluyeron con EtOAc y se lavaron con salmuera. La capa acuosa se extrajo de nuevo con EtOAc (2x). Las capas orgánicas combinadas se secaron sobre Na2SO4 y se concentraron al vacío. El material resultante se liofilizó de MeCN y agua para proporcionar Metilo [(2S,3R)-1-{(2S,5S)-2-[9-(4-ciclopropil-2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-5-metilpirrolidin-1-il}-3-metoxi-1-oxobutan-2-il]carbamato (0,16 g, 48%). LCMS-ESI+: calculado para C48H58N8O9: 890,43 (M+); Encontrado: 891,88 (M+H+). 1H RMN (400 MHz, cdaod) 8 (mezcla de rotómeros) 8,41 (s, 1H), 8,13- 7,93 (m, 2H), 7,91 - 7,79 (m, 1H), 7,78 - 7,40 (m, 3H), 5,85 - 5,68 (m, 1H), 5,46 (d, 1H), 5,33-5,14 (m, 3H), 5,09 -4,92 (m, 1H), 4,78 -4,59 (m, 1H), 4,44 -4,32 (m, 2H), 4,31 -4,11 (m, 2H), 3,88 (s, 1H), 3,74 - 3,48 (m, 6H), 3,41 - 3,32 (m, 3H), 2,75 - 2,39 (m, 3H), 2,38 - 1,79 (m, 7H)), 1,55 (d, 2H), 1,47 (d, 2H), 1,33- 1,03 (m, 9H), 0,98 (s, 3H), 0,81 (s, 2H), 0,66 (s, 1H).
Ejemplo GD
[0247]
metilo [(2S,3R)-3-metoxi-1-{(2S,5S)-2-[9-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metilpirrolidin-2-il}-4-metil-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-5-metilpirrolidin-1-il}-1-oxobutan-2-il]carbamato
[0248] metilo [(2S,3R)-3-metoxi-1-£(2S,5S)-2-[9-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metMpirroNdm-2-M}-4-metiMH-imidazol-5-M)-1,11-dihidroisocromeno[4\3':6,7]nafto[1,2-d]imidazol-2-M]-5-metilpirrolidin-1-il}-1-oxobutan-2-il]carbamato. A continuación del Ejemplo GC, sustituyendo ácido metilborónico por ácido ciclopropilborónico, se proporcionó metilo [(2S,3R)-3-metoxi-1-{(2S,5S)-2-[9-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-treonil]-5-metMpirrolidin-2-il}-4-metil-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-5-metilpirrolidin-1-il}-1-oxobutan-2-il]carbamato (0,08 g). LCMS-ESI+: calculado para C46H56N8O9: 864,42 (M+); Encontrado: 865,91 (M+H+). 1H RMN (400 MHz, cdaod) 8 (mezcla de rotómeros) 8,40 (s, 1H), 8,14 -7,85 (m, 2H), 7,78 - 7,34 (m, 4H), 5,78 (s, 1H), 5,47 (s, 1H), 5,30 -5,13 (m, 3H), 5,11 -4,96 (m, 1H), 4,79 -4,58 (m, 2H), 4,48 -4,30 (m, 2H), 4,30 -4,13 (m, 2H), 3,88 (s, 1H), 3,73-3,50 (m, 6H), 3,42 -3,32 (m, 4H), 2,57 -2,03 (m, 9H), 2,03- 1,76 (m, 2H), 1,55 (d, 3H), 1,47 (d, 2H), 1,39-0,99 (m, 10H).
Ejemplo GE
[0249]
metilo [(2S,3S)-3-metoxi-1-{(2S,5S)-2-[9-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-alotreonil]-5-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-5-metilpirrolidin-1-il}-1-oxobutan-2-il]carbamato
[0250] metilo [(2S,3S)-3-metoxi-1-{(2S,5S)-2-[9-(2-{(2S,5S)-1-[N-(metoxicarbonil)-O-metil-L-alotreonil]-5-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-5-metilpirrolidin-1-il}-1-oxobutan-2-il]carbamato. Siguiendo el Ejemplo DX, sustituyendo (2S,5s)-1-(terc-butoxicarbonil)-5-metilpirrolidin-2-ácido carboxílico y (1R, 3S)-2-(2-(metoxicarbonilamino)-3-metilbutanoilo)-3-ácido metilciclopentanocarboxílico con (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidin-2-ácido carboxílico, y sustituyendo (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con 2 equivalentes de (2S,3S)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico, proporcionó metilo [(2S,3S)-3-metoxi-1-{(2S,5S)-2-[9-(2-{(2S,5S)-1-[N-(metoxicarbononil)-O-metil-L-alotreonil]-5-metilpirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-5-metilpirrolidin-1-il}-1-oxobutan-2-ilo]carbamato (0,27 g). LCMS-ESI+: calculado para C45H54N8O9: 850,40 (M+); Encontrado: 851,80 (M+H+). 1H RMN (400 MHz, cdaod) 8 (mezcla de rotómeros) 8,43- 8,29 (m, 1H), 8,12 - 7,90 (m, 2H), 7,87 - 7,61 (m, 3H), 7,61 - 7,32 (m, 3H), 5,74 (d, 1H), 5,54 (d, 1H), 5,24 -5,09 (m, 2H), 4,76 -4,60 (m, 1H), 4,46 -4,30 (m, 2H), 4,31 -4,12 (m, 2H), 3,89 (s, 2H), 3,80 -3,60 (m, 4H), 3,60 - 3,44 (m, 2H), 3,34 (s, 2H), 3,32 (s, 2H), 2,97 - 2,63 (m, 2H), 2,62 - 2,35 (m, 2H), 2,35 - 1,78 (m, 6H), 1,65 - 1,52 (m, 2H), 1,50 (d, 1H), 1,42 (d, 1H), 1,35 - 1,04 (m, 10H).
Ejemplo GF
[0251]
Metilo {(2S,3S)-1-[(2S,5S)-2-(5-{2-[(2S,5S)-1-{(2S,3R)-3-metoxi-2-[(metoxicarbonil)amino]butanoilo}-5-metilpirrolidin-2-il]-1,11 -dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-5-metilpirrolidin-1 -il]-3-metil-1-oxopentan-2-il}carbamato
[0252] Metilo {(2S,3S)-H(2S,5S)-2-(5-£2-[(2S,5S)-H(2S,3R)-3-metoxi-2-[(metoxicarboml)ammo]butanoilo}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-9-il}-1H-imidazol-2-il)-5-metilpirrolidin-1-il]-3-metil-1-oxopentan-2-il}carbamato. Siguiendo el Ejemplo DX, sustituyendo (2S,5S)-1-(tercbutoxicarbonil)-5-metilpirrolidin-2-ácido carboxílico con (2S,5S)-1-((2S,3S)-2-(metoxicarbonNamino)-3-metNpentanoíl)-5-metilpirrolidin-2-ácido carboxílico y (1R, 3S)-2-(2-(metoxicarbonilamino)-3-metilbutanoílo)-3-ácido metilciclopentanocarboxílico con (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidin-2-ácido carboxílico, proporcionó metilo {(2S,3S)-1-[(2S,5S)-2-(5-{2-[(2S,5S)-1-{(2S,3R)-3-metoxi-2-[(metoxicarbonil)amino]butanoilo}-5-metilpirrolidin-2-il]-1,11 -dihidroisocromeno[4',3’:6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-5-metilpirrolidin-1 -il]-3-metil-1 -oxopentan-2-il}carbamato (0,14 g). LCMS-ESI+: calculado para C46H56N8O8: 848,42 (M+); Encontrado: 849,80 (M+H+).
1H RMN (400 MHz, cdaod) 8 (mezcla de rotómeros) 8,43 - 8,14 (m, J = 14,6 Hz, 2H), 8,09 - 7,75 (m, 3H), 7,75 - 7,24 (m, 5H), 5,80 - 5,64 (m, 1H), 5,38 - 4,95 (m, 4H), 4,80 - 4,67 (m, 1H), 4,31 - 4,09 (m, J = 20,2, 7,7 Hz, 2H), 3,85 (s, 1H), 3,72 - 3,54 (m, J = 20,5 Hz, 4H), 3,37 (s, 2H), 2,94 - 2,64 (m, J = 51,0 Hz, 2H), 2,63- 2,37 (m, J = 35,2 Hz, 2H), 2,37 - 2,01 (m, 4H), 2,00 - 1,83 (m, 1H), 1,83- 1,69 (m, 1H), 1,67 - 1,51 (m, J = 6,6 Hz, 3H), 1,47 (d, J = 6,6 Hz, 2H), 1,35 - 1,00 (m, 7H), 1,00 - 0,69 (m, 7H).
Ejemplo GH
[0253]
metilo {(2S)-1-[(2S,4S)-2-(5-{2-[(2S,5S)-1-{(2S,3R)-3-metoxi-2-[(metoxicarbonil)amino]butanoilo}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-4-metilpirrolidin-1-il]-3-metil-1-oxobutan-2-il}carbamato
[0254] metilo {(2S)-1-[(2S,4S)-2-(5-£2-[(2S,5S)-1-{(2S,3R)-3-metoxi-2-[(metoxicarboml)ammo]butanoMo}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]im idazol-9-il}-1H-imidazol-2-il)-4-metilpirrolidin-1-il]-3-metil-1-oxobutan-2-il}carbamato. Siguiendo el Ejemplo DX, sustituyendo (2S,5S)-1-(tercbutoxicarbonil)-5-metilpirrolidin-2-ácido carboxílico con (2S,4S)-1-(terc-butoxicarbonil)-4-metilpirrolidin-2-ácido carboxílico, (1R, 3S)-2-(2-(metoxicarbonilamino)-3-metilbutanoílo)-3-ácido metilciclopentanocarboxílico con (2S,5S)-1-((2S,3R)-3-metoxi-2-(metoxicarbonilamino)butanoilo)-5-metilpirrolidin-2-ácido carboxílico, y (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (S)-2-(metoxicarbonilamino)-3-ácido metilbutanoico, me proporcionó metilo {(2S)-1-[(2S,4S)-2-(5-{2-[(2S,5S)-1-{(2S,3R)-3-metoxi-2-[(metoxicarbonil)amino]butanoilo}-5-metilpirrolidin-2-il]-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-4-metilpirrolidin-1-il]-3-metil-1-oxobutan-2-il}carbamato (0,16 g). LCMS-ESI+: calculado para C45H54N8O8: 834,41 (M+); encontrado: 835,86 (M+H+). 1H RMN (400 MHz, cdaod) 8 (mezcla de rotómeros) 8,23 -8,09 (m, 1H), 7,94 -7,68 (m, 3H), 7,67 -7,13 (m, 6H), 5,70 -5,56 (m, 1H), 5,23-5,13 (m, 1H), 5,12 -4,91 (m, 4H), 4,25 -4,08 (m, 3H), 3,76 (s, 2H), 3,66 -3,52 (m, 5H), 3,39 -3,25 (m, 3H)), 3,18 (s, 1H), 2,45 - 2,07 (m, 4H), 2,03- 1,73 (m, 3H), 1,47 (d, 2H), 1,25 - 0,98 (m, 8H), 0,94 - 0,81 (m, 4H)), 0,79 (d, 3H).
Ejemplo GI
[0255]
metilo [[2S)-1-{(2S,4S)-2-[9-(2-{(2S,5S)-1-[(2S)-2-[(metoxicarbonil)amino]-2-(tetrahidro-2H-piran-4-il)acetil]-4-(metoximetil)pirrolidin-2-il}-lH-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato
[0256] metilo [[2S)-1-{(2S,4S)-2-[9-(2-{(2S,5S)-1-[(2S)-2-[(metoxicarbonil)amino]-2-(tetrahidro-2H-piran-4-il)acetil]-4-(metoximetil)pirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato. Siguiendo el Ejemplo DX, sustituyendo (2S,5S)-1-(terc-butoxicarbonil)-5-metilpirrolidin-2-ácido carboxílico con (2S,4S)-1-(terc-butoxicarbonil)-4-(metoximetilo)pirrolidin-2-ácido carboxílico, (1R, 3S)-2-(2-(metoxicarbonilamino)-3-metilbutanoílo)-3-ácido metilciclopentanocarboxílico con (2S,5S)-1-((S)-2-(metoxicarbonilamino)-3-metilbutanoílo)-5-metilpirrolidin-2-ácido carboxílico, y (2S,3R)-3-metoxi-2-(metoxicarbonilamino)ácido butanoico con (S)-2-(metoxicarbonilamino)-2-(tetrahidro-2H-piran-4-il)ácido acético, siempre que el metilo [(2S)-1-{(2S,4S)-2-[9-(2-{(2S,5S)-1-[(2S)-2-[(metoxicarbonil)amino]-2-(tetrahidro-2H-piran-4-il)acetil]-4-(metoximetil)pirrolidin-2-il}-1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il]-5-metilpirrolidin-1-il}-3-metil-1-oxobutan-2-il]carbamato (0,06 g). LCMS-ESI+: calculado para C48H58N8O9: 890,43 (M+); Encontrado: 891,81 (M+H+). 1H RMN (400 MHz, cdaod) 8 (mezcla de rotómeros) 8,50 (s, 1H), 8,17 -8,01 (m, 2H), 7,88 (t, 1H), 7,83- 7,74 (m, 2H), 7,74 - 7,63 (m, 1H), 7,62 - 7,48 (m, 2H), 5,72 (d, 1H), 5,26 - 5,08 (m, 4H), 4,33- 4,12 (m, 3H), 4,05 (d, 1H), 3,90 - 3,76 (m, 2H), 3,67 (d, 1H), 3,58 (s, 2H), 3,56 (s, 2H), 3,54 - 3,39 (m, 3H), 3,29 (s, 3H), 2,75 -2,60 (m, 2H), 2,60 - 2,17 (m, 5H), 2,06 - 1,76 (m, 5H), 1,53 (d, 2H), 1,48 - 1,17 (m, 5H), 1,15 (d, 1H), 0,98 (dd, 2H), 0,86 (d, 2H), 0,77 (d, 2H).
Ejemplo GK
[0257]
metilo {(1R)-2-[(2S,4S)-2-(5-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbonil)amino]-3-metilbutanoil}-5-metilpirrolidin-2-il]-11-oxo-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato
Metilo {(1R)-2-[(2S,4S)-2-(5-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbononilo)amino]-3-metilbutanoil}-5-metilpirrolidin-2-il]-11-oxo-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato
[0258] metilo {(1R)-2-[(2S,4S)-2-(5-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbonil)amino]-3-metilbutanoil}-5-metilpirrolidin-2-il]-11 -oxo-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato. A una solución de metilo {(2S)-1-[(2S,5S)-2-(9-{2-[(2S,4S)-1-{(2R)-2-[(metoxicarbonil)amino]-2-fenilacetil}-4-(metoximetil)pirrolidin-2-il]-1H-imidazol-5-il}-1,1-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-2-il)-5-metilpirrolidin-1-il]-3-metil-1-oxobutan-2-il}carbamato (0,19 g, 0,22 mmol) en CH2O 2 (3 mL) se añadió clorhidrato de piridinio (0,48 g, 2,21 mmol). La suspensión resultante se agitó a temperatura ambiente durante 5 días. La reacción se diluyó con MeOH y se filtró. El filtrado se diluyó con CH2O 2 y se lavó con agua y bicarbonato de sodio acuoso (saturado). Las capas acuosas se volvieron a extraer con CH2O 2,
Las capas orgánicas combinadas se secaron sobre Na2SO4 y se concentraron al vacío. El aceite crudo se purificó por HPLC de fase inversa (Gemini, 10 ^ 55% MeCN/H2O (0,1% TFA)). Las fracciones deseadas se combinaron y se concentraron a presión reducida para eliminar los compuestos orgánicos volátiles. La adición de bicarbonato de sodio acuoso con agitación dio como resultado la precipitación de un sólido blanco. El precipitado se filtró a través de un filtro de membrana y se lavó con agua. El secado a presión reducida proporcionó metilo {(1R)-2-[(2S,4S)-2-(5-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbononilo)amino]-3-metilbutanoil}-5-metilpirrolidin-2-il]-11-oxo-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletil}carbamato (0,08 g, 39%). LCMS-ESI+ : calculado para C49H52N8O9 : 896,39 (M+ ); Encontrado: 897,72 (M+H+).
ENSAYOS BIOLOGICOS
[0259] Efecto de las proteínas séricas sobre la potencia del replicón: Los ensayos de replicón se realizan en medio de cultivo celular normal (DMEM+10% FBS) suplementado con concentraciones fisiológicas de albúmina sérica humana (40 mg/ml) o glicoproteína de a-ácido (1 pm/ml). Las CE50 en presencia de proteínas séricas humanas se comparan con las CE50 en medio normal para determinar el cambio de potencia en la potencia.
[0260] Citotoxicidad de células MT-4: Las células MT4 se tratan con diluciones en serie de compuestos durante un período de cinco días. La viabilidad celular se mide al final del período de tratamiento utilizando el ensayo Promega CellTiter-Glo y se realiza una regresión no lineal para calcular la CC50.
[0261] Concentración del compuesto asociada con células a CE50: Los cultivos Huh-luc se incuban con compuesto en concentraciones iguales a CE50. En múltiples puntos de tiempo (0 - 72 horas), las células se lavan 2X con medio frío y se extraen con acetonitrilo al 85%; También se extraerá una muestra de los medios en cada punto temporal. Los extractos de células y medios se analizan por LC/MS/MS para determinar la concentración molar de compuestos en cada fracción. Los compuestos representativos de la divulgación han mostrado actividad.
[0262] Solubilidad y estabilidad: La solubilidad se determina tomando una alícuota de solución madre de DMSO 10 mM y preparando el compuesto a una concentración final de 100 mM en las soluciones de medios de prueba (PBS, pH 7,4 y 0,1 N HCl, pH 1,5) con una concentración total de DMSO del 1%. Las soluciones de los medios de prueba se incuban a temperatura ambiente con agitación durante 1 hora. Las soluciones se centrifugarán y los sobrenadantes recuperados se analizarán en HPLC/UV. La solubilidad se calculará comparando la cantidad de compuesto detectado en la solución de prueba definida en comparación con la cantidad detectada en DMSO a la misma concentración. También se determinará la estabilidad de los compuestos después de una incubación de 1 hora con PBS a 37°C.
[0263] Estabilidad en hepatocitos humanos, perros y ratas crioconservados: Cada compuesto se incuba durante hasta 1 hora en suspensiones de hepatocitos (100 pl, 80,000°células por pocillo) a 37°C. Los hepatocitos crioconservados se reconstituyen en el medio de incubación sin suero. La suspensión se transfiere a placas de 96 pocillos (50 pl/pocillo). Los compuestos se diluyen a 2 pM en medio de incubación y luego se agregan a suspensiones de hepatocitos para comenzar la incubación. Las muestras se toman a los 0, 10, 30 y 60 minutos después del inicio de la incubación y la reacción se detendrá con una mezcla que consiste en 0,3% de ácido fórmico en 90% de acetonitrilo/10% de agua. La concentración del compuesto en cada muestra se analiza utilizando LC/MS/MS. La vida media de desaparición del compuesto en la suspensión de hepatocitos se determina ajustando los datos de tiempo de concentración con una ecuación exponencial monofásica. Los datos también se ampliarán para representar el aclaramiento hepático intrínseco y/o el aclaramiento hepático total.
[0264] Estabilidad en la fracción hepática S9 de humanos, perros y ratas: Cada compuesto se incuba durante hasta 1 hora en suspensión S9 (500 pl, 3 mg de proteína/ml) a 37°C (n = 3). Los compuestos se añaden a la suspensión S9 para comenzar la incubación. Las muestras se toman a los 0, 10, 30 y 60 minutos después del inicio de la incubación. La concentración del compuesto en cada muestra se analiza utilizando LC/MS/MS. La vida media de desaparición del compuesto en suspensión S9 se determina ajustando los datos de concentración-tiempo con una ecuación exponencial monofásica.
[0265] Permeabilidad de Caco-2: Los compuestos se analizan a través de un servicio contratado (Absorption Systems, Exton, PA). Los compuestos se proporcionan al contratista de manera ciega. Se medirán tanto la permeabilidad directa (A a B) como la inversa (B a A). Las monocapas de Caco-2 se cultivan hasta confluencia en membranas de policarbonato microporosas, recubiertas de colágeno, en placas Costar TRANSWELL® de 12 pocillos. Los compuestos se dosifican en el lado apical para la permeabilidad hacia adelante (A a B), y se dosifican en el lado basolateral para la permeabilidad inversa (B a A). Las células se incuban a 37°C con 5% de CO2 en una incubadora humidificada. Al comienzo de la incubación y en 1 hora y 2 horas después de la incubación, se toma una parte alícuota de 200 pl de la cámara receptora y se reemplaza con tampón de ensayo nuevo. La concentración del compuesto en cada muestra se determina con LC/MS/MS. Se calcula la permeabilidad aparente, Papp.
[0266] Unión a proteínas plasmáticas: La unión a proteínas plasmáticas se mide mediante diálisis en equilibrio. Cada compuesto se inyecta en plasma en blanco a una concentración final de 2 pM. El plasma enriquecido y el tampón de fosfato se colocan en lados opuestos de las células de diálisis ensambladas, que luego se rotarán lentamente en un baño de agua a 37°C. Al final de la incubación, se determina la concentración del compuesto en plasma y tampón
fosfato. El porcentaje no consolidado se calcula utilizando la siguiente ecuación:
% No enlazado = 100 • ------ -—
Iq o J
[0267] Donde Cf y Cb son concentraciones libres y unidas determinadas como el tampón de posdiálisis y las concentraciones de plasma, respectivamente.
[0268] Perfil de CYP450: Cada compuesto se incuba con cada una de 5 enzimas CYP450 humanas recombinantes, incluidas CYP1A2, CYP2C9, CYP3A4, CYP2D6 y CYP2C19 en presencia y ausencia de NADPH. Se tomarán muestras en serie de la mezcla de incubación al comienzo de la incubación y a los 5, 15, 30, 45 y 60 minutos después del inicio de la incubación. La concentración del compuesto en la mezcla de incubación se determina por LC/MS/MS. El porcentaje del compuesto restante después de la incubación en cada punto de tiempo se calcula comparando con el muestreo al inicio de la incubación.
[0269] Estabilidad en plasma de rata, perro, mono y humano: Los compuestos se incubarán hasta 2 horas en plasma (rata, perro, mono o humano) a 37°C. Los compuestos se agregan al plasma en concentraciones finales de 1 y 10 |jg/ml. Las alícuotas se toman a los 0, 5, 15, 3o, 60 y 120 minutos después de agregar el compuesto. La concentración de compuestos y metabolitos principales en cada punto de tiempo se mide por LC/MS/MS.
[0270] Evaluación de la actividad anti-HCV basada en células: La potencia antiviral (CE50) se determinó utilizando un ensayo de reportero de replicón de HCV basado en luciferasa de Renilla (RLuc). Para realizar el ensayo para el genotipo 1 y 2a JFH-1, células de replicón RLuc de HCV 1a estables (que albergan un replicón H77 de genotipo dicistrónico 1a que codifica un informador RLuc), células de replicón RLuc de HCV 1b estables (que albergan un genón dicistrónico 1b Con1 que codifica un reportero RLuc), o células de replicón Rluc HCV 2a JFH-1 estables (que albergan un genotipo dicistrónico 2a JFH-1 replicón que codifica un reportero RLuc; con L31 presente en NS5A) se dispensaron en placas de 384 pocillos para CE50 ensayos. Para realizar el ensayo del genotipo 2a (con M31 presente en NS5A) o 2b, el genotipo quimérico NS5A2a JFH-1 replica que codifica un reportero RLuc-Neo y el genotipo 2a J6 cepa NS5A o el genotipo 2b MD2b-1 gen NS5A (ambos con M31 presente) respectivamente, fueron o bien transfectados transitoriamente (t) en células Huh-Lunet o se establecieron como réplica estable de células. Cualquiera de las células se dispensó en placas de 384 pocillos para los ensayos de CE50, Para realizar el ensayo para los genotipos 3 y 4, los replicones del genotipo 1b Con1 quimérico NS5A que codifican un reportero Pi-RLuc y el gen NS5A de la cepa NS5A del genotipo S52 o genotipo 4a ED4 respectivamente, fueron transfectados transitoriamente (t) en Huh-Lunet Células, que posteriormente se dispensaron en placas de 384 pocillos. Los compuestos se disolvieron en DMSO a una concentración de 10 mM y se diluyeron en DMSO manualmente o usando un instrumento de pipeteo automático. Los compuestos diluidos en 3 veces en serie se mezclaron manualmente con medios de cultivo celular y se agregaron a las células sembradas o se agregaron directamente a las células usando un instrumento automatizado. El DMSO se usó como control negativo (solvente, sin inhibición) y el inhibidor de la proteasa ITMN-191 se incluyó a una concentración >100 x CE50 como control positivo. 72 horas más tarde, las células se lisaron y la actividad de luciferasa de Renilla se cuantificó según lo recomendado por el fabricante (Promega-Madison, WI). Se realizó una regresión no lineal para calcular los valores de CE50,
[0271] Para determinar la potencia antiviral (CE50) frente a mutantes de resistencia, mutaciones de resistencia, incluyendo M28T, Q30R, Q30H, Q30E, L31M, Y93C, Y93H y Y93N en el genotipo 1a NS5A, Y93H y L31V/Y93H en el genotipo 1b NS5A, y Y93H para en el genotipo 3a NS5A, se introdujeron individualmente en los replicones 1a Pi-Rluc o 1b Pi-Rluc por mutagénesis dirigida al sitio. El ARN de replicón de cada mutante resistente se transfectó transitoriamente en células 51 curadas derivadas de Huh-7 y se determinó la potencia antiviral en estas células transfectadas como se describe anteriormente.
[0272] Estudios farmacocinéticos de dosis única IV y PO en ratas SD: la farmacocinética de compuestos seleccionados se caracterizó en ratas Sprague-Dawley (SD) macho (250-300 g). En este estudio, dos grupos de ratas SD de raza pura (N = 3 por grupo, en ayunas durante la noche) recibieron el compuesto seleccionado como una infusión intravenosa (IV) (1 mg/kg durante 30 minutos) a través de la vena yugular o gavage oral (2 mg/kg). El vehículo de dosificación intravenosa (IV) fue 5% de etanol, 35% de polietilenglicol 400 (PEG 400) y 60% de agua, pH2,0, El vehículo de dosificación oral fue 5% de etanol, 55% de PEG 400 y 40% de tampón citrato pH2,2,
[0273] Se recogieron muestras de sangre en serie (aproximadamente 0,3 ml cada una) de la vena yugular u otra vena adecuada en puntos de tiempo especificados. Para el grupo de infusión IV, las muestras de sangre se tomaron antes de la dosis y a 0,25, 0,48, 0,58, 0,75, 1,5, 3, 6, 8, 12 y 24 horas después del inicio de la infusión. Para el grupo oral, las muestras de sangre se tomaron antes de la dosis y a 0,25, 0,50, 1, 2, 4, 6, 8, 12 y 24 horas después de la dosificación. Las muestras de sangre se recogieron en tubos Vacutainer™ que contenían EDTA-K3 como anticoagulante y se centrifugaron a aproximadamente 4°C para obtener plasma. Las muestras de plasma se almacenaron a -20°C hasta su análisis por LC/MS/MS.
[0274] Se desarrolló un método bioanalítico que utiliza cromatografía líquida de alto rendimiento acoplada a
espectrometría de masas en tándem (LC/MS/MS) para el análisis del compuesto seleccionado en plasma de rata. La detección se realizó utilizando un monitoreo de reacción seleccionado (SRM); Los iones que representan la especie precursora (M+H)+ se seleccionaron en el cuadrupolo 1 (Q1) y colisionaron con el gas argón en la célula de colisión (Q2) para generar un ión producto específico, que posteriormente se monitorizó mediante el cuadrupolo 3 (Q3). La curva estándar y las muestras de control de calidad se prepararon en plasma de rata macho y se procesaron de la misma manera que las muestras de prueba para generar datos cuantitativos.
[0275] Los parámetros farmacocinéticos se generaron usando análisis farmacocinéticos no compartimentales (Phoenix WinNonlin, versión 6,3). A los valores que se encuentran por debajo del límite inferior de cuantificación (LLOQ) se les asignó un valor de cero si estaban predose y se consideraron como perdidos posteriormente. El área bajo la curva (AUC) se calculó utilizando la regla trapezoidal lineal. La biodisponibilidad oral (% F) se determinó por comparación del área bajo la curva (AUC) del compuesto y/o un metabolito generado en plasma después de la administración oral con el generado después de la administración intravenosa.
Tabla 1A
(continuado)
(continuado)
Tabla 1B
(continuado)
Claims (9)
3. El compuesto o sal farmacéuticamente aceptable de la reivindicación 1, para uso en el tratamiento profiláctico o terapéutico de la hepatitis C.
4. El compuesto de la reivindicación 2, para uso en el tratamiento profiláctico o terapéutico de la hepatitis C.
5. Una composición farmacéutica que comprende el compuesto o sal farmacéuticamente aceptable de la reivindicación 1, y al menos un vehículo farmacéuticamente aceptable.
6. Una composición farmacéutica que comprende el compuesto de la reivindicación 2, y al menos un vehículo farmacéuticamente aceptable.
7. La composición farmacéutica de la reivindicación 5 o la reivindicación 6, formulada para administración oral.
8. La composición farmacéutica de la reivindicación 5 o la reivindicación 6, formulada en forma de comprimido.
9. La composición farmacéutica de la reivindicación 5 o la reivindicación 6 para uso en el tratamiento profiláctico o terapéutico de la hepatitis C.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201261647966P | 2012-05-16 | 2012-05-16 | |
| US13/831,116 US20130309196A1 (en) | 2012-05-16 | 2013-03-14 | Antiviral compounds |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2738012T3 true ES2738012T3 (es) | 2020-01-17 |
Family
ID=49581469
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES17160683T Active ES2738012T3 (es) | 2012-05-16 | 2013-05-15 | Derivados de 9-(1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-D]imidazol y su utilización como inhibidores de HCV NS5A |
| ES13726936.1T Active ES2628350T3 (es) | 2012-05-16 | 2013-05-15 | Compuestos antivíricos inhibidores de NS5A de HCV |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES13726936.1T Active ES2628350T3 (es) | 2012-05-16 | 2013-05-15 | Compuestos antivíricos inhibidores de NS5A de HCV |
Country Status (19)
| Country | Link |
|---|---|
| US (5) | US20130309196A1 (es) |
| EP (2) | EP2850085B1 (es) |
| JP (2) | JP6209209B2 (es) |
| KR (2) | KR20200017557A (es) |
| CN (3) | CN104487442B (es) |
| AU (3) | AU2013262874B2 (es) |
| BR (1) | BR112014028221B1 (es) |
| CA (1) | CA2873485C (es) |
| EA (2) | EA034749B1 (es) |
| ES (2) | ES2738012T3 (es) |
| HK (1) | HK1245262B (es) |
| IL (1) | IL235645A0 (es) |
| IN (1) | IN2014MN02459A (es) |
| MX (1) | MX362060B (es) |
| PL (2) | PL3239153T3 (es) |
| PT (2) | PT2850085T (es) |
| SG (2) | SG10201703451RA (es) |
| SI (2) | SI3239153T1 (es) |
| WO (1) | WO2013173488A1 (es) |
Families Citing this family (27)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2345657A1 (en) | 2003-05-30 | 2011-07-20 | Pharmasset, Inc. | Modified fluorinated nucleoside analogues |
| SI2640719T1 (sl) | 2010-11-17 | 2017-07-31 | Gilead Pharmasset Llc | Antivirusne spojine |
| JP6082749B2 (ja) | 2011-11-16 | 2017-02-15 | ギリアド ファーマセット エルエルシー | 抗ウイルス化合物としての縮合イミダゾリルイミダゾール |
| US20130309196A1 (en) | 2012-05-16 | 2013-11-21 | Gilead Sciences, Inc. | Antiviral compounds |
| US9233974B2 (en) * | 2012-12-21 | 2016-01-12 | Gilead Sciences, Inc. | Antiviral compounds |
| EA201690473A1 (ru) | 2013-08-27 | 2017-03-31 | ГАЙЛИД ФАРМАССЕТ ЭлЭлСи | Комбинированный состав двух противовирусных соединений |
| US20150064252A1 (en) * | 2013-08-27 | 2015-03-05 | Gilead Pharmasset Llc | Solid dispersion formulation of an antiviral compound |
| TW202014413A (zh) * | 2014-06-11 | 2020-04-16 | 美商基利法瑪席特有限責任公司 | 製備抗病毒化合物之方法 |
| TWI721947B (zh) * | 2014-06-11 | 2021-03-21 | 美商基利法瑪席特有限責任公司 | 抗病毒化合物的固態形式 |
| US10112962B2 (en) | 2014-07-02 | 2018-10-30 | Xavier University | Boron-based prodrug strategy for increased bioavailability and lower-dosage requirements for drug molecules containing at least one phenol (or aromatic hydroxyl) group |
| DK3236972T3 (en) | 2014-12-26 | 2021-10-04 | Univ Emory | Antivirale N4-hydroxycytidin-derivativer |
| JP6904970B2 (ja) | 2016-03-07 | 2021-07-21 | エナンタ ファーマシューティカルズ インコーポレイテッド | B型肝炎抗ウイルス剤 |
| WO2017191546A1 (en) * | 2016-05-05 | 2017-11-09 | Laurus Labs Private Ltd. | Process for the preparation of intermediates useful in the preparation of hepatitis c virus (hcv) inhibitors |
| CN109414508A (zh) | 2016-05-27 | 2019-03-01 | 吉利德科学公司 | 使用ns5a、ns5b或ns3抑制剂治疗乙型肝炎病毒感染的方法 |
| CN108368123B (zh) * | 2016-07-08 | 2021-02-19 | 深圳市塔吉瑞生物医药有限公司 | 一种取代的咪唑基化合物及其药物组合物 |
| CN106220639A (zh) * | 2016-07-22 | 2016-12-14 | 上海众强药业有限公司 | 一种维帕他韦中间体新晶型 |
| CN107759577B (zh) * | 2016-11-30 | 2020-03-27 | 上海博志研新药物技术有限公司 | Gs5816中间体、制备方法及应用 |
| US10952978B2 (en) | 2017-08-28 | 2021-03-23 | Enanta Pharmaceuticals, Inc. | Hepatitis B antiviral agents |
| CN107501280A (zh) * | 2017-09-05 | 2017-12-22 | 安徽华昌高科药业有限公司 | 一种维帕他韦的合成方法 |
| JP6804790B1 (ja) | 2017-12-07 | 2020-12-23 | エモリー ユニバーシティー | N4−ヒドロキシシチジンおよび誘導体ならびにそれらに関連する抗ウイルス用途 |
| US11198693B2 (en) | 2018-11-21 | 2021-12-14 | Enanta Pharmaceuticals, Inc. | Functionalized heterocycles as antiviral agents |
| CN111018870B (zh) * | 2019-11-29 | 2021-07-23 | 南京正济医药研究有限公司 | 一种维帕他韦中间体的制备方法 |
| WO2021188414A1 (en) | 2020-03-16 | 2021-09-23 | Enanta Pharmaceuticals, Inc. | Functionalized heterocyclic compounds as antiviral agents |
| WO2022040058A1 (en) * | 2020-08-18 | 2022-02-24 | Merck Sharp & Dohme Corp. | Cyclopentapyrrole orexin receptor agonists |
| US12274700B1 (en) | 2020-10-30 | 2025-04-15 | Accencio LLC | Methods of treating symptoms of coronavirus infection with RNA polymerase inhibitors |
| CA3220903A1 (en) * | 2021-05-21 | 2022-11-24 | Gilead Sciences, Inc. | Pentacyclic derivatives as zika virus inhibitors |
| CA3219397A1 (en) | 2021-05-21 | 2022-11-24 | Gilead Sciences, Inc. | Tetracyclic compounds for the treatment of zika virus infection |
Family Cites Families (41)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4816570A (en) | 1982-11-30 | 1989-03-28 | The Board Of Regents Of The University Of Texas System | Biologically reversible phosphate and phosphonate protective groups |
| US4968788A (en) | 1986-04-04 | 1990-11-06 | Board Of Regents, The University Of Texas System | Biologically reversible phosphate and phosphonate protective gruops |
| EP0481214B1 (en) | 1990-09-14 | 1998-06-24 | Institute Of Organic Chemistry And Biochemistry Of The Academy Of Sciences Of The Czech Republic | Prodrugs of phosphonates |
| US5543523A (en) | 1994-11-15 | 1996-08-06 | Regents Of The University Of Minnesota | Method and intermediates for the synthesis of korupensamines |
| CA2448737C (en) | 2001-07-20 | 2010-06-01 | Boehringer Ingelheim (Canada) Ltd. | Viral polymerase inhibitors |
| KR101164070B1 (ko) * | 2003-05-09 | 2012-07-12 | 베링거 인겔하임 인터내셔날 게엠베하 | C형 간염 바이러스 ns5b 폴리머라제 억제제 결합 포켓 |
| US7157492B2 (en) | 2004-02-26 | 2007-01-02 | Wyeth | Dibenzo chromene derivatives and their use as ERβ selective ligands |
| RS51974B (sr) | 2004-07-16 | 2012-02-29 | Gilead Sciences Inc. | Antivirusna jedinjenja |
| US7759495B2 (en) | 2006-08-11 | 2010-07-20 | Bristol-Myers Squibb Company | Hepatitis C virus inhibitors |
| US8329159B2 (en) | 2006-08-11 | 2012-12-11 | Bristol-Myers Squibb Company | Hepatitis C virus inhibitors |
| US7659270B2 (en) | 2006-08-11 | 2010-02-09 | Bristol-Myers Squibb Company | Hepatitis C virus inhibitors |
| US7741347B2 (en) * | 2007-05-17 | 2010-06-22 | Bristol-Myers Squibb Company | Hepatitis C virus inhibitors |
| ATE551337T1 (de) | 2008-02-12 | 2012-04-15 | Bristol Myers Squibb Co | Inhibitoren des hepatitis-c-virus |
| US8147818B2 (en) * | 2008-02-13 | 2012-04-03 | Bristol-Myers Squibb Company | Hepatitis C virus inhibitors |
| HRP20120706T1 (hr) | 2008-02-13 | 2012-09-30 | Bristol-Myers Squibb Company | Imidazolil bifenil imidazoli kao inhibitori virusa hepatitisa c |
| US8729077B2 (en) | 2008-11-28 | 2014-05-20 | Glaxosmithkline Llc | Anti-viral compounds, compositions, and methods of use |
| WO2010065668A1 (en) | 2008-12-03 | 2010-06-10 | Presidio Pharmaceuticals, Inc. | Inhibitors of hcv ns5a |
| WO2010096777A1 (en) * | 2009-02-23 | 2010-08-26 | Presidio Pharmaceuticals, Inc. | Inhibitors of hcv ns5a |
| KR101411889B1 (ko) | 2009-02-27 | 2014-06-27 | 이난타 파마슈티칼스, 인코포레이티드 | C형 간염 바이러스 억제제 |
| SG174883A1 (en) | 2009-03-27 | 2011-11-28 | Presidio Pharmaceuticals Inc | Fused ring inhibitors of hepatitis c |
| WO2010132538A1 (en) | 2009-05-12 | 2010-11-18 | Schering Corporation | Fused tricyclic aryl compounds useful for the treatment of viral diseases |
| PT3309157T (pt) * | 2009-05-13 | 2019-12-02 | Gilead Pharmasset Llc | Compostos antivirais |
| TWI598358B (zh) | 2009-05-20 | 2017-09-11 | 基利法瑪席特有限責任公司 | 核苷磷醯胺 |
| US8138215B2 (en) | 2009-05-29 | 2012-03-20 | Bristol-Myers Squibb Company | Hepatitis C virus inhibitors |
| EA201290089A1 (ru) | 2009-09-04 | 2012-09-28 | ГЛАКСОСМИТКЛАЙН ЭлЭлСи | Химические соединения |
| WO2011031904A1 (en) | 2009-09-11 | 2011-03-17 | Enanta Pharmaceuticals, Inc | Hepatitis c virus inhibitors |
| JP2013512246A (ja) | 2009-11-25 | 2013-04-11 | メルク・シャープ・アンド・ドーム・コーポレーション | ウイルス疾患治療に有用な縮合型三環式化合物およびその誘導体 |
| US8476225B2 (en) | 2009-12-04 | 2013-07-02 | Gilead Sciences, Inc. | Antiviral compounds |
| US8377980B2 (en) | 2009-12-16 | 2013-02-19 | Bristol-Myers Squibb Company | Hepatitis C virus inhibitors |
| US20130156731A1 (en) | 2009-12-22 | 2013-06-20 | Kevin X. Chen | Fused tricyclic compounds and methods of use thereof for the treatment of viral diseas |
| EA201290882A1 (ru) | 2010-03-09 | 2013-04-30 | Мерк Шарп Энд Домэ Корп. | Конденсированные трициклические силильные соединения и способы их применения для лечения вирусных заболеваний |
| US20110312996A1 (en) | 2010-05-17 | 2011-12-22 | Intermune, Inc. | Novel inhibitors of hepatitis c virus replication |
| WO2011150243A1 (en) * | 2010-05-28 | 2011-12-01 | Presidio Pharmaceuticals, Inc. | Inhibitors of hcv ns5a |
| BR112013004520A2 (pt) | 2010-08-26 | 2016-06-07 | Univ Emory | inibidores potentes e seletivos do virus da hepatite c |
| WO2012050918A2 (en) * | 2010-09-29 | 2012-04-19 | Presidio Pharmaceutical, Inc. | Tricyclic fused ring inhibitors of hepatitis c |
| WO2012048421A1 (en) | 2010-10-14 | 2012-04-19 | Boehringer Ingelheim International Gmbh | Hepatitis c inhibitor compounds |
| SI2640719T1 (sl) * | 2010-11-17 | 2017-07-31 | Gilead Pharmasset Llc | Antivirusne spojine |
| WO2012087976A2 (en) | 2010-12-21 | 2012-06-28 | Intermune, Inc. | Novel inhibitors of hepatitis c virus replication |
| JP6082749B2 (ja) * | 2011-11-16 | 2017-02-15 | ギリアド ファーマセット エルエルシー | 抗ウイルス化合物としての縮合イミダゾリルイミダゾール |
| US20130309196A1 (en) | 2012-05-16 | 2013-11-21 | Gilead Sciences, Inc. | Antiviral compounds |
| US9233974B2 (en) | 2012-12-21 | 2016-01-12 | Gilead Sciences, Inc. | Antiviral compounds |
-
2013
- 2013-03-14 US US13/831,116 patent/US20130309196A1/en not_active Abandoned
- 2013-05-15 PT PT137269361T patent/PT2850085T/pt unknown
- 2013-05-15 EA EA201790963A patent/EA034749B1/ru unknown
- 2013-05-15 ES ES17160683T patent/ES2738012T3/es active Active
- 2013-05-15 KR KR1020207003891A patent/KR20200017557A/ko not_active Ceased
- 2013-05-15 PT PT17160683T patent/PT3239153T/pt unknown
- 2013-05-15 BR BR112014028221-8A patent/BR112014028221B1/pt active IP Right Grant
- 2013-05-15 SG SG10201703451RA patent/SG10201703451RA/en unknown
- 2013-05-15 WO PCT/US2013/041201 patent/WO2013173488A1/en not_active Ceased
- 2013-05-15 KR KR1020147034784A patent/KR102078233B1/ko active Active
- 2013-05-15 CA CA2873485A patent/CA2873485C/en active Active
- 2013-05-15 JP JP2015512796A patent/JP6209209B2/ja active Active
- 2013-05-15 SG SG11201407533SA patent/SG11201407533SA/en unknown
- 2013-05-15 SI SI201331447T patent/SI3239153T1/sl unknown
- 2013-05-15 EP EP13726936.1A patent/EP2850085B1/en active Active
- 2013-05-15 AU AU2013262874A patent/AU2013262874B2/en active Active
- 2013-05-15 IN IN2459MUN2014 patent/IN2014MN02459A/en unknown
- 2013-05-15 PL PL17160683T patent/PL3239153T3/pl unknown
- 2013-05-15 CN CN201380029171.0A patent/CN104487442B/zh active Active
- 2013-05-15 EA EA201492002A patent/EA028026B1/ru unknown
- 2013-05-15 EP EP17160683.3A patent/EP3239153B1/en active Active
- 2013-05-15 PL PL13726936T patent/PL2850085T3/pl unknown
- 2013-05-15 ES ES13726936.1T patent/ES2628350T3/es active Active
- 2013-05-15 SI SI201330651T patent/SI2850085T1/sl unknown
- 2013-05-15 CN CN201811468769.0A patent/CN109970749A/zh active Pending
- 2013-05-15 MX MX2014013660A patent/MX362060B/es active IP Right Grant
- 2013-05-15 CN CN201610856469.4A patent/CN106432254B/zh not_active Expired - Fee Related
-
2014
- 2014-06-26 US US14/316,573 patent/US20140316144A1/en not_active Abandoned
- 2014-11-11 IL IL235645A patent/IL235645A0/en active IP Right Grant
-
2015
- 2015-10-28 US US14/925,203 patent/US9682989B2/en active Active
-
2017
- 2017-05-09 US US15/590,846 patent/US20170342085A1/en not_active Abandoned
- 2017-06-26 JP JP2017124206A patent/JP6408656B2/ja active Active
- 2017-10-20 AU AU2017248566A patent/AU2017248566A1/en not_active Abandoned
-
2018
- 2018-04-10 HK HK18104656.7A patent/HK1245262B/en unknown
- 2018-12-04 US US16/209,860 patent/US10800789B2/en active Active
-
2019
- 2019-06-24 AU AU2019204423A patent/AU2019204423A1/en not_active Abandoned
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2738012T3 (es) | Derivados de 9-(1H-imidazol-5-il)-1,11-dihidroisocromeno[4',3':6,7]nafto[1,2-D]imidazol y su utilización como inhibidores de HCV NS5A | |
| EP2935279B1 (en) | Antiviral compounds | |
| ES2544107T3 (es) | Imidazolilimidazoles condensados como compuestos antivirales | |
| US9079887B2 (en) | Antiviral compounds | |
| HK1245262A1 (en) | 9-(1h-imidazol-5-yl)-1,11-dihydroisochromeno[4',3':6,7]naphtho[1,2-d]imidazole derivatives and their use as inhibitors of hcv ns5a | |
| AU2015274863B2 (en) | Antiviral compounds | |
| HK40002411B (en) | Condensed imidazolylimidazoles as antiviral compounds | |
| HK40002411A (en) | Condensed imidazolylimidazoles as antiviral compounds | |
| HK1216177B (en) | Antiviral compounds | |
| HK1205126B (en) | Antiviral compounds inhibitors of hcv ns5b | |
| HK1242304A1 (en) | Antiviral compounds |