ES2742829T3 - Solución de monóxido de carbono para el tratamiento de una enfermedad, incluida anemia de células falciformes - Google Patents
Solución de monóxido de carbono para el tratamiento de una enfermedad, incluida anemia de células falciformes Download PDFInfo
- Publication number
- ES2742829T3 ES2742829T3 ES12734547T ES12734547T ES2742829T3 ES 2742829 T3 ES2742829 T3 ES 2742829T3 ES 12734547 T ES12734547 T ES 12734547T ES 12734547 T ES12734547 T ES 12734547T ES 2742829 T3 ES2742829 T3 ES 2742829T3
- Authority
- ES
- Spain
- Prior art keywords
- disease
- liquid composition
- carbon monoxide
- amount
- dissolved
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/42—Proteins; Polypeptides; Degradation products thereof; Derivatives thereof, e.g. albumin, gelatin or zein
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/44—Oils, fats or waxes according to two or more groups of A61K47/02-A61K47/42; Natural or modified natural oils, fats or waxes, e.g. castor oil, polyethoxylated castor oil, montan wax, lignite, shellac, rosin, beeswax or lanolin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/46—Ingredients of undetermined constitution or reaction products thereof, e.g. skin, bone, milk, cotton fibre, eggshell, oxgall or plant extracts
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0087—Galenical forms not covered by A61K9/02 - A61K9/7023
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0087—Galenical forms not covered by A61K9/02 - A61K9/7023
- A61K9/0095—Drinks; Beverages; Syrups; Compositions for reconstitution thereof, e.g. powders or tablets to be dispersed in a glass of water; Veterinary drenches
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/06—Antianaemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/02—Non-specific cardiovascular stimulants, e.g. drugs for syncope, antihypotensives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01F—MIXING, e.g. DISSOLVING, EMULSIFYING OR DISPERSING
- B01F23/00—Mixing according to the phases to be mixed, e.g. dispersing or emulsifying
- B01F23/40—Mixing liquids with liquids; Emulsifying
- B01F23/45—Mixing liquids with liquids; Emulsifying using flow mixing
- B01F23/454—Mixing liquids with liquids; Emulsifying using flow mixing by injecting a mixture of liquid and gas
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/107—Emulsions ; Emulsion preconcentrates; Micelles
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Inorganic Chemistry (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Botany (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Pain & Pain Management (AREA)
- Rheumatology (AREA)
- Gastroenterology & Hepatology (AREA)
- Oncology (AREA)
- Vascular Medicine (AREA)
- Communicable Diseases (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicinal Preparation (AREA)
Abstract
Una composición líquida que comprende burbujas gaseosas disueltas o gaseosas atrapadas de monóxido de carbono (CO) en una cantidad de 30 mg/l o más para su uso en el tratamiento de un sujeto que padece o corre el riesgo de desarrollar una enfermedad tratable con CO; comprendiendo el uso administrar la composición líquida al sujeto por medio del tracto gastrointestinal (GI), donde la cantidad de CO es una cantidad suficiente para reducir o eliminar al menos un síntoma clínico de la enfermedad, prevenir el desarrollo o la recidiva de la enfermedad, limitar las morbilidades de la enfermedad, o curar la enfermedad, donde la enfermedad es una enfermedad hematológica.
Description
DESCRIPCIÓN
Solución de monóxido de carbono para el tratamiento de una enfermedad, incluida anemia de células falciformes ANTECEDENTES DE LA INVENCIÓN
Cualquier referencia en la descripción a un tratamiento o a un método de tratamiento se refiere a las composiciones para su uso en un método de tratamiento.
Campo de la invención
La presente invención se refiere a los campos de composiciones terapéuticas y médicas. Más específicamente, la invención se refiere a métodos de tratamiento para enfermedades hematológicas que pueden tratarse con niveles terapéuticos de monóxido de carbono, incluida anemia de células falciformes, y a formulaciones y vehículos de administración que son útiles para realizar los métodos.
Descripción de la técnica relacionada
En la actualidad, los métodos y dispositivos para el tratamiento de las crisis de células falciformes (denominadas en el presente documento “SCC”) y su prevención no son adecuados para controlar la enfermedad. Los Centros para el Control y la Prevención de Enfermedades de EE.UU. han estimado que entre 70.000 y 100.000 pacientes padecen la anemia de células falciformes (denominada en el presente documento “SCD”) en e E.UU., y la esperanza de vida de estas personas afectadas es de solo aproximadamente 40 años. Cuando un paciente ingresa en el hospital, el tratamiento se basa en los síntomas, principalmente a través de analgésicos análogos a la morfina, reemplazo de líquidos, transfusiones y otras medidas de apoyo. Actualmente, el único método consistente y fiable del tratamiento de SCC es a través de la transfusión de sangre. Sin embargo, este método de tratamiento es costoso e incómodo, y puede ser peligroso. Se ha encontrado que el uso de hidroxiurea para prevenir crisis tiene una eficacia marginal y tiene efectos secundarios, y la respuesta por paciente es muy variable. También es posible curar la SCD a través del trasplante de médula ósea, pero este procedimiento rara vez se usa debido a su peligro inherente, su alto coste y las comorbilidades del tratamiento necesario.
Se sabe que el monóxido de carbono (CO) es tóxico a altas concentraciones, lo que interfiere con la capacidad de los glóbulos rojos para transportar oxígeno. Se ha informado que las saturaciones de hemoglobina (denominadas en el presente documento “Hb”) de más del 67 % probablemente producen la muerte inducida por CO a menos que se proporcione tratamiento. Además, se informa que las saturaciones de Hb superiores al 30 % provocan pérdida de conciencia, entre otras morbilidades graves, y pueden provocar la muerte si se mantienen a largo plazo. Además, se informa que las saturaciones de Hb entre el 16 % y el 20 % provocan dolor de cabeza y anomalías en la respuesta visual evocada (Stewart RD. The effect of carbon monoxide on humans. Annu Rev Pharmacol 15: 409-423, 1975). Como tal, se debe tener extrema precaución en situaciones en las que el CO está presente.
Sin embargo, es posible que el CO pueda tener efectos positivos en la SCD y en otras enfermedades y trastornos. Por ejemplo, se ha informado que el CO prolonga la vida útil de los glóbulos rojos en pacientes con s Cd . (Beutler, E., 1975, “The effect of carbon monoxide on red cell life span in sickle cell disease.” Blood 46(2): 253-9.) También se ha planteado la hipótesis de que el CO podría desempeñar un papel en la prevención formación de células falciformes al evitar la polimerización de la hemoglobina (Sirs, J.A., 1963, “The use of carbon monoxide to prevent sickle cell formation”, Lancet 1, 7288: 971-2). Además, se ha informado que el CO podría tener un efecto preventivo sobre la aparición de síntomas clínicos de SCD. (Yallop, D., E. R. Duncan, et al., 2007, “The associations between air quality and the number of hospital admissions for acute pain and sickle-cell disease in an urban environment.” Br J Haematol 136(6): 844-8.) El estudio de Yallop documenta que hay una disminución en los ingresos hospitalarios de pacientes con SCC en días con mayor contenido de CO en el aire respirado.
Investigaciones recientes también han encontrado que el CO puede tener beneficios para la salud más extendidos en múltiples enfermedades y sistemas de órganos, incluidos el cardiovascular, renal, hepático, pulmonar e intestino (Inge Bauer y Benedikt HJ Pannen, “Bench-to-bedside review: Carbon monoxide - from mitochondrial poisoning to therapeutic use”, Critical Care 2009, 13:220). Otras investigaciones apuntan a efectos positivos en enfermedades inflamatorias y cardiovasculares (Foresti R, Bani-Hani MG, Motterlini R., “Use of carbon monoxide as a therapeutic agent: promises and challenges”, Intensive Care Med. 2008 Apr;34(4):649-58. Epub 20 de febrero de 2008).
En vista de los efectos beneficiosos propuestos del CO sobre ciertas enfermedades y trastornos, se han realizado una serie de esfuerzos utilizando diferentes mecanismos de administración para emplear el CO como tratamiento
para la enfermedad. Estos incluyen: administración de gas CO a través de administración pulmonar (Motterlini, R., Otterbein L., “The therapeutic potential of carbon monoxide”, Nat Rev Drug Discov. 2010 Sep;9(9):728-43); la administración de CO unido a un metal no ferroso en una molécula pequeña a través de infusión intravenosa, inyección intraperitoneal o ingestión oral (Motterlini, R., Otterbein L., “The therapeutic potential of carbon monoxide”, Nat Rev Drug Discov. 2010 Sep;9(9):728-43); y la administración de CO unido a un tetrámero de hemoglobina humana o bovina químicamente modificado mediante infusión intravenosa (Vandegriff, K. D., M. A. Young, et al. (2008). “CO-MP4, a polyethylene glycol-conjugated haemoglobin derivative and carbon monoxide carrier that reduces myocardial infarct size in rats”. Br J Pharmacol 154(8): 1649-61; publicación de solicitud de patente de Estados Unidos número 20100311657 Abuchowski, Abraham et al. “h Em OGLOBIN COMPOSITIONS” 9 de diciembre de 2010; y publicación de solicitud de patente de Estados Unidos número 20090082257Winslow, Robert M. “MalPEG-Hb conjugate- containing compositions for delivering carbon monoxide (CO) to cells” 26 de marzo de 2009). Sin embargo, estos esfuerzos se enfrentan una serie de problemas y deficiencias importantes.
Con respecto a la administración de gas CO por inhalación, existen varios problemas que han impedido su uso clínico. Una de las principales razones de la falta de uso clínico se refiere a la importancia de la dosificación en la administración de CO. La dosis eficaz de CO está relativamente cerca de su dosis tóxica. Esto dificulta la administración pulmonar dadas las diferencias en la función pulmonar en diversas enfermedades, incluida la SCD. Una segunda complicación es que el CO se excreta a través de los pulmones. Como tal, la administración pulmonar de CO requiere la absorción y excreción a través del mismo órgano, lo que complica significativamente la farmacocinética y las determinaciones de seguridad. Otro desafío con la administración pulmonar es que la administración pulmonar es incómoda para los pacientes debido a la incomodidad de utilizar un aparato de respiración y la restricción de la movilidad del paciente dada la necesidad de estar cerca del aparato de respiración durante los periodos de dosificación. Este es un asunto potencialmente significativo, ya que las molestias para los pacientes están altamente correlacionadas con la falta de cumplimiento del paciente. Además, la toxicidad inherente del CO y sus propiedades inodoras e incoloras hacen que el uso de la administración pulmonar sea un desafío. El almacenamiento de la cantidad de CO que se necesitaría para tratar a un paciente a largo plazo podría, en el caso del hogar, poner en peligro al paciente y a otros miembros de la familia y, en el caso del hospital, requeriría precauciones de seguridad nuevas y costosas tales como monitorización y ventilación antes de su uso, e incluso con dichas salvaguardas podrían poner en peligro al personal del hospital.
La utilización de portadores a base de metales de transición de molécula pequeña de CO (denominados en el presente documento moléculas liberadoras de monóxido de carbono o “CORM”) también presenta desafíos importantes para la administración clínica de CO. Al vincular el monóxido de carbono a un metal de transición, la toxicidad del metal de transición se añade al CO de toxicidad inherente. Esta toxicidad del metal de transición puede limitar la dosis aceptable y, para ciertos metales, impide su uso en seres humanos por completo. El rutenio y el molibdeno son dos de los metales de transición más utilizados en la formación de CORM, y estos metales se han clasificado como metales de gran preocupación para la seguridad por la Agencia Europea de Medicamentos (EMEA COMMITTEE FOR MEDICINAL PRODUCTS FOR HUMAN USE (CHMP), “GUIDELINE ON THE SPECIFICATION LIMITS FOR RESIDUES OF METAL CATALYSTS OR METAL REAGENTS”, Londres, 21 de febrero de 2008, Doc. Ref. EMEA/CHMP/SWP/4446/2000). Esta toxicidad de alto potencial de CORM debido a los portadores de metales de transición impide el uso de CORM en ciertas indicaciones debido a una dosificación potencialmente limitada por toxicidad y también a través de una relación riesgo:beneficio más difícil debido al riesgo añadido del metal de transición. Los pacientes particularmente inestables, incluidos los pacientes con SCD, pueden estar particularmente en riesgo. Además, la toxicidad de los portadores de metales de transición presenta una barrera significativa para el uso recurrente de CORM en indicaciones crónicas. Dado que la SCD es una afección hereditaria de por vida, es poco probable que el uso a largo plazo de los CORM como terapia para la prevención del SCC sea seguro, ya que los portadores de metales de transición se acumularán con el tiempo, lo que agrava la toxicidad potencial. En resumen, el uso de compuestos de metales de transición como portadores de CO tiene serios inconvenientes en comparación con los enfoques menos tóxicos.
El uso de tetrámeros de hemoglobina modificados químicamente como portadores de CO (CO-Hb acelular) también presenta problemas relacionados con la toxicidad. Se ha demostrado que ciertos eventos de seguridad significativos están asociados con el uso clínico de transportadores de oxígeno basados en tetrámero de hemoglobina, incluidos el infarto de miocardio y la muerte, entre otros (Natanson C, et. al. “Cell-free hemoglobin-based blood substitutes and risk of myocardial infarction and death: a meta-analysis”, JAMA. 21 de mayo de 2008;299(19):2304-12). La toxicidad potencial de CO-Hb acelular debido al uso de hemoglobina acelular como portador de CO impide el uso de CO-Hb en ciertas indicaciones debido a una dosificación potencialmente limitada por toxicidad y también a través de una relación riesgo:beneficio más difícil debido al riesgo adicional del tetrámero de hemoglobina. Los pacientes particularmente inestables, incluidos los pacientes con SCD, pueden estar particularmente en riesgo. Además, la toxicidad de la Hb acelular, además de la posible carga de hierro problemática, presenta una barrera significativa
para el uso recurrente de CO-Hb en indicaciones crónicas, incluso para su uso en la prevención de SCC.
Además, desde hace tiempo se sabe que el CO, como la mayoría de los gases, es soluble a bajos niveles a presión ambiente en soluciones acuosas. Las soluciones se han preparado previamente en laboratorios académicos para demostrar este hecho. Además, las soluciones acuosas se prepararon previamente a presión ambiente y entre 4 °C y 21 °C, y se usaron ex vivo en estudios no humanos para determinar si la administración de CO por dichas soluciones podría mejorar los resultados en el trasplante de tejidos de intestino, hígado y pulmón (Nakao A et. al. “Ex vivo application of carbon monoxide in University of Wisconsin solution to prevent intestinal cold ischemia/reperfusion injury”, Am J Transplant. 2006; 6(10):2243-2255; Ikeda, A et. al. “Liver graft exposure to carbon monoxide during cold storage protects sinusoidal endothelial cells and emeliorates reperfusion injury in rats”, Liver Transpl. noviembre de 2009; 15(11): 1458-1468; Nakao A et. al. “Ex vivo carbon monoxide prevents cytochrome P450 degradation and ischemia/reperfusion injury of kidney grafts”, Kidney International. 2008; 74:989-991). Un estudio también analizó el uso de tal solución preparada a temperatura y presión ambiente e inyectada por vía intraperitoneal (denominada en el presente documento “IP”) para investigar si tal solución podría mejorar el íleo postoperatorio en ratones (Atsunori N, et. al., “A Single Intraperitoneal Dose of Carbon Monoxide-Saturated Ringer's Lactate Solution Ameliorates Postoperative Ileus in Mice”, JPET 319:1265-1275, 2006). Sin embargo, el uso de esta solución fue muy limitado. Primero, al preparar la solución a temperatura y presión ambiente, la cantidad de CO disuelto fue muy baja. Esta metodología de preparación fue necesaria en este caso porque inyectar una solución fría podría ser dañino si se inyecta directamente en el peritoneo y, además, a medida que el líquido se calienta, el CO burbujearía de la solución al peritoneo, lo que probablemente causaría complicaciones potencialmente graves. Además, aunque la administración de IP se usa en investigaciones no humanas, rara vez se usa en el tratamiento de enfermedades humanas por razones tanto de seguridad como de conveniencia. Primero, el potencial de infección en la inyección IP es significativo, lo que crea un riesgo adicional para esta ruta de administración. Además, los inconvenientes para los pacientes debido a la administración IP pueden corresponder a una falta de cumplimiento del paciente o del médico. Además, para permitir la infusión IP en el hogar, se tendría que colocar un acceso permanente al espacio peritoneal en el paciente, similar al utilizado en la diálisis IP. Esto añadiría inconvenientes significativos y también posibles morbilidades, tal como el riesgo de infección, en comparación con una ruta de administración diferente de IP. Además, la ruta de administración IP se basa en la provisión de una pequeña cantidad de CO localmente, usando la administración directa al tracto gastrointestinal, lo que es inherentemente limitante con respecto al tratamiento de la enfermedad.
En resumen, hasta la fecha, no ha habido un método ampliamente adecuado, conveniente y seguro para administrar CO en cantidades que sean terapéuticas para tratar enfermedades y trastornos, evitando al mismo tiempo la toxicidad y proporcionando el nivel de conveniencia necesario para aquellos que lo necesiten.
RESUMEN DE LA INVENCIÓN
La presente invención proporciona una composición líquida que comprende burbujas gaseosas disueltas o gaseosas atrapadas de monóxido de carbono (CO) en una cantidad de 30 mg/l o más para su uso en el tratamiento de un sujeto que padece o corre el riesgo de desarrollar una enfermedad tratable con CO; comprendiendo el uso administrar la composición líquida al sujeto por medio del tracto gastrointestinal (GI), donde la cantidad de CO es una cantidad suficiente para reducir o eliminar al menos un síntoma clínico de la enfermedad, prevenir el desarrollo o la recidiva de la enfermedad, limitar las morbilidades de la enfermedad, o curar la enfermedad, donde la enfermedad es una enfermedad hematológica. El método de la invención administra de forma segura CO al paciente afectado, y proporciona una solución a una antigua necesidad en la técnica de un método de tratamiento seguro y un vehículo de administración para CO. Como se usa en el presente documento, al término “líquido” se le da su más amplio significado razonable, y por lo tanto, incluye tanto líquidos newtonianos como líquidos no newtonianos. Por lo tanto, incluye composiciones en las que el componente principal, en peso, es un líquido. Por lo tanto, el término incluye pastas, geles y emulsiones. Asimismo, incluye espumas en las que quedan atrapadas burbujas de CO. Para facilitar la referencia, dentro de la presente descripción, se hace referencia a “líquidos” en los que el CO está “disuelto”. Sin embargo, debe entenderse que dichas referencias no se limitan a líquidos newtonianos en los que el CO está en solución, sino a todos los líquidos, pastas, geles, emulsiones, espumas, etc. en los que el CO gaseoso se disuelve, se atrapa, etc. Se cree que este es el primer informe de administración in vivo de un líquido que contiene CO a través del tracto GI con fines terapéuticos o profilácticos. La invención permite la administración de cantidades establecidas (es decir, es decir, predeterminadas) de CO a un paciente sistémicamente para tratar la enfermedad. El líquido que contiene CO, en realizaciones ejemplares, se administra por vía oral.
En un primer aspecto, la invención proporciona una composición líquida que contiene CO disuelto en una cantidad suficiente para la administración del CO a un paciente (usado en el presente documento de manera intercambiable con “sujeto” y “persona que lo necesita”), donde la administración al paciente da como resultado un tratamiento
eficaz en una enfermedad o trastorno que es tratable con CO. A diferencia de las composiciones líquidas que contienen CO conocidas en la técnica, la composición líquida según la presente invención tiene una concentración de CO que es suficientemente alta con respecto a una cantidad eficaz de CO que puede administrarse al paciente en un volumen conveniente de líquido. Es decir, las composiciones líquidas que contienen CO conocidas en la técnica, tales como las conocidas para investigar el efecto del CO sobre tejidos alterados quirúrgicamente, tienen concentraciones relativamente bajas de CO y no son adecuadas para la administración in vivo de CO para tratar enfermedades y trastornos. En contraste, la composición líquida de la presente invención comprende una concentración relativamente alta de CO, y puede usarse para la administración in vivo de cantidades eficaces para el tratamiento de CO a los pacientes. Aunque no está tan limitada, en general, la composición de la presente invención comprende una composición a base de agua en la que se disuelve el CO. Preferiblemente, el CO está en forma gaseosa en solución, y no forma un complejo con un metal o una o más moléculas o complejos de Hb. En realizaciones ejemplares, la composición líquida es una bebida, tal como una proporcionada en un recipiente sellable.
En otro aspecto, la presente invención proporciona un método para tratar a un paciente que padece, o corre el riesgo de desarrollar, una enfermedad o trastorno que puede tratarse o prevenirse mediante la administración de una cantidad eficaz de CO. En general, el método comprende administrar a un paciente una composición líquida que contiene CO disuelto en una cantidad suficiente para la administración del CO al paciente, donde administrar la composición da como resultado un tratamiento eficaz en una enfermedad o trastorno que es tratable con CO. A diferencia de los intentos anteriores de administrar CO a través de la inhalación directa de CO gaseoso en los pulmones, la presente invención utiliza una composición líquida que se administra a través del tracto GI para administrar CO gaseoso in vivo al paciente. En realizaciones ejemplares, la composición líquida se administra por vía oral bebiendo la composición. El método de la invención se puede poner en práctica para tratar una enfermedad o trastorno crónico, es decir, la etapa de administración se puede repetir varias veces durante un periodo de tiempo relativamente largo (por ejemplo, años), o durante un periodo de tiempo relativamente corto (por ejemplo, unos días, una semana, o la duración de un episodio agudo de una enfermedad o trastorno). El método se puede poner en práctica como un método terapéutico para tratar una enfermedad o trastorno activo. Como alternativa, el método se puede poner en práctica para prevenir el desarrollo de una enfermedad o trastorno. El método se puede poner en práctica además para reducir la probabilidad de desarrollar una enfermedad o trastorno o para reducir la frecuencia y/o gravedad de los síntomas clínicos de una enfermedad o trastorno y/o sus consecuencias sobre la función orgánica y del cuerpo.
En otro aspecto más de la invención, se proporcionan métodos para elaborar una composición líquida que contiene CO disuelto en una cantidad eficaz para el tratamiento. En general, el método comprende disolver CO en un líquido en condiciones que permiten que cantidades relativamente altas de CO se disuelvan en el líquido. Las condiciones adecuadas para composiciones acuosas incluyen presión relativamente alta, temperatura relativamente baja, o una combinación de ambas. Las condiciones adecuadas para las composiciones basadas en lípidos/aceites pueden no requerir una presión relativamente alta o una temperatura relativamente baja. En realizaciones preferidas, el método comprende además dispensar el líquido en un recipiente, antes, durante o después de disolver el CO en el líquido. Preferiblemente, el recipiente se sella tras disolver el CO en el líquido. Preferiblemente, el espacio superior del recipiente comprende Co . En realizaciones ejemplares, la composición líquida es una bebida, tal como una proporcionada en un recipiente sellable. En realizaciones ejemplares, la composición líquida comprende una composición a base de agua en la que se disuelve el CO. En otras realizaciones ejemplares, la composición líquida comprende una espuma a base de aceite o grasa en la que quedan atrapadas burbujas de CO. Preferiblemente, el método proporciona una composición líquida en la que el CO está en forma gaseosa en solución o atrapada en burbujas en una espuma, y no forma un complejo con un metal o una o más moléculas o complejos de Hb.
Un aspecto general adicional de la invención se refiere a un método para determinar la dosificación apropiada de la composición líquida que se proporciona. El método generalmente comprende el uso de uno o más de los siguientes para determinar un régimen de dosificación apropiado: función pulmonar, hemoglobina del paciente y mediciones de glóbulos rojos, volumen de sangre del paciente y la concentración de CO en el líquido. Las técnicas para realizar dichos ensayos se conocen en la técnica y se pueden poner en práctica sin demasiada o excesiva experimentación. El método se puede poner en práctica regularmente para monitorizar y, si es necesario, ajustar el régimen de dosificación. En realizaciones, el método es un método para determinar la dosificación apropiada del líquido, donde el método comprende ajustar hacia arriba la dosificación del líquido para determinar el tratamiento óptimo. El método puede incluir la medición de uno o más de los siguientes: exhalación de CO, función pulmonar, hemoglobina de CO y farmacocinética.
DESCRIPCIÓN DETALLADA DE REALIZACIONES EJEMPLARES
A menos que se defina lo contrario, todos los términos técnicos y científicos utilizados en el presente documento tienen el mismo significado que el entendido comúnmente por un experto en la técnica a la que pertenece el término.
Como se usa en el presente documento y en las reivindicaciones adjuntas, las formas singulares “un”, “una” y “el/la” incluyen referentes plurales a menos que el contexto indique claramente lo contrario. Por lo tanto, por ejemplo, la referencia a “una proteína” incluye una pluralidad de dichas proteínas (incluidas múltiples copias de la misma proteína y múltiples proteínas diferentes) y la referencia a “el paciente” incluye una referencia a uno o más pacientes, etc. Además, el uso de términos que pueden describirse usando términos equivalentes incluye el uso de estos términos equivalentes. Por lo tanto, por ejemplo, el uso del término “sujeto” debe entenderse que incluye los términos “animal”, “ser humano” y otros términos usados en la técnica para indicar que está sujeto a un tratamiento médico. Como otro ejemplo, debe entenderse que el uso del término “enfermedad” incluye el término “trastorno” (y viceversa) y todos los demás términos utilizados en la técnica para indicar una afección médica anormal o aberrante.
La presente invención proporciona una composición líquida que contiene CO disuelto en una cantidad suficiente para la administración del CO a un paciente, donde la administración al paciente da como resultado un tratamiento eficaz para una enfermedad o trastorno que es tratable con CO. Debido, al menos en parte, al método de elaboración de la composición (como se describe en el presente documento), la composición líquida de la presente invención tiene una concentración de CO gaseoso que no puede lograrse usando técnicas conocidas en la técnica para crear composiciones que contienen CO gaseoso. Más específicamente, la composición de la presente invención tiene una concentración de CO disuelto de al menos 30 miligramos por litro (mg/l). El límite superior del
CO disuelto está dictado solo por la física y la química.
En realizaciones ejemplares relacionadas con composiciones acuosas, la concentración de CO disuelto generalmente no excederá de 400 mg/l. Por ejemplo, una concentración eficaz para la dosificación conveniente de
CO para tratar SCC y SCD está entre aproximadamente 100 mg/l y 400 mg/l, aunque las concentraciones entre aproximadamente 50 mg/l y aproximadamente 100 mg/l también son adecuadas para pacientes susceptibles a la ingesta de volúmenes relativamente grandes de líquido durante los periodos de tratamiento. Asimismo, las concentraciones en el extremo inferior de estos rangos pueden ser adecuadas para pacientes con SCC o SCD, que típicamente tienen niveles de Hb relativamente bajos y, por lo tanto, no requieren una dosis tan alta de CO como los pacientes que tienen niveles más normales de Hb. Aunque el experto en la técnica entenderá de inmediato que todos los valores particulares dentro del rango de aproximadamente 30 mg/l y aproximadamente 400 mg/l están específicamente contemplados por esta aplicación, los siguientes valores de concentración, y los diversos rangos definidos por la recopilación de valores específicos, proporcionan puntos de referencia convenientes para que el profesional desarrolle composiciones según la presente invención: 30 mg/l, 35 mg/l, 40 mg/l, 45 mg/l, 50 mg/l,
55 mg/l, 57 mg/l, 60 mg/l 65 mg/l, 70 mg/l, 75 mg/l, 78 mg/l, 80 mg/l, 85 mg/l, 90 mg/l, 95 mg/l, 100 mg/l, 105 mg/l,
110 mg/l, 115 mg/l, 120 mg/l, 125 mg/l, 130 mg/l, 135 mg/l, 140 mg/l, 145 mg/l, 150 mg/l, 155 mg/l, 160 mg/l,
165 mg/l, 170 mg/l, 175 mg/l, 180 mg/l, 190 mg/l, 200 mg/l, 210 mg/l, 225 mg/l, 250 mg/l, 275 mg/l, 300 mg/l,
325 mg/l, 350 mg/l, y 375 mg/l. Las composiciones acuosas según la presente invención pueden comprender cualquier valor de concentración específica entre 30 mg/l y 400 mg/l, pueden comprender cualquier rango de concentración específica entre 30 mg/l y 400 mg/l, o pueden contener una concentración de CO disuelto de al menos cualquiera de los valores de concentración entre 30 mg/l y 400 mg/l.
En realizaciones ejemplares relacionadas con composiciones a base de lípidos/aceites/grasas, la concentración de
CO disuelto generalmente no excederá de 4.400 mg/l. Por ejemplo, una concentración eficaz para la dosificación conveniente de CO para tratar SCC y SCD es entre aproximadamente 500 mg/l y 4.400 mg/l, tal como entre aproximadamente 500 mg/l y 4.000 mg/l, aunque las concentraciones entre aproximadamente 75 mg/l y aproximadamente 500 mg/l también son adecuadas para pacientes susceptibles a la ingesta de volúmenes relativamente grandes de dichos líquidos durante los periodos de tratamiento. Asimismo, las concentraciones en el extremo inferior de estos rangos pueden ser adecuadas para pacientes con SCC o SCD, que típicamente tiene niveles de Hb relativamente bajos y, por lo tanto, no requieren una dosis tan alta de CO como los pacientes que tienen niveles más normales de Hb. Aunque el experto en la técnica entenderá de inmediato que todos los valores particulares dentro del rango de aproximadamente 30 mg/l y aproximadamente 4.400 mg/l están específicamente contemplados por esta aplicación, los siguientes valores de concentración, y los diversos rangos definidos por la recopilación de valores específicos, proporcionan puntos de referencia convenientes para que el profesional desarrolle composiciones según la presente invención: 75 mg/l, 100 mg/l, 125 mg/l, 150 mg/l, 175 mg/l, 200 mg/l,
225 mg/l, 250 mg/l, 275 mg/l, 300 mg/l, 325 mg/l, 350 mg/l, 375 mg/l, 400 mg/l, 425 mg/l, 450 mg/l, 475 mg/l,
500 mg/l, 525 mg/l, 550 mg/l, 575 mg/l, 600 mg/l, 625 mg/l, 650 mg/l, 675 mg/l, 700 mg/l, 725 mg/l, 750 mg/l,
775 mg/l, 800 mg/l, 825 mg/l, 850 mg/l, 875 mg/l, 900 mg/l, 925 mg/l, 950 mg/l, 975 mg/l, 1000 mg/l, 1025 mg/l,
1050 mg/l, 1075 mg/l, 1100 mg/l, 1125 mg/l, 1150 mg/l, 1175 mg/l, 1200 mg/l, 1225 mg/l, 1250 mg/l, 1275 mg/l,
1300 mg/l, 1325 mg/l, 1350 mg/l, 1375 mg/l, 1400 mg/l, 1425 mg/l, 1450 mg/l, 1475 mg/l, 1500 mg/l, 1525 mg/l, 1550 mg/l, 1575 mg/l, 1600 mg/l, 1625 mg/l, 1650 mg/l, 1675 mg/l, 1700 mg/l, 1725 mg/l, 1750 mg/l, 1775 mg/l, 1800 mg/l, 1825 mg/, 1850 mg/l, 1875 mg/l, 1900 mg/l, 1925 mg/l, 1950 mg/l, 1975 mg/l, 2000 mg/l, 2050 mg/l, 2100 mg/l, 2150 mg/l, 2200 mg/l, 2250 mg/l, 2300 mg/l, 2350 mg/l, 2400 mg/l, 2450 mg/l, 2500 mg/l, 2550 mg/l, 2600 mg/l, 2650 mg/l, 2700 mg/l, 2750 mg/l, 2800 mg/l, 2850 mg/l, 2900 mg/l, 2950 mg/l, 3000 mg/l, 3100 mg/l, 3200 mg/l, 3300 mg/l, 3400 mg/l, 3500 mg/l, 3600 mg/l, 3700 mg/l, 3800 mg/l, 3900 mg/l, 4000 mg/l, 4100 mg/l, 4200 mg/l, 4300 mg/l, y 4400 mg/l. Las composiciones de lípidos/aceites/grasas según la presente invención pueden comprender cualquier valor de concentración específica entre 30 mg/l y 4400 mg/l, pueden comprender cualquier rango de concentración específica entre 30 mg/l y 4400 mg/l, o pueden contener una concentración de CO disuelto de al menos cualquiera de los valores de concentración entre 30 mg/l y 4400 mg/l.
La composición líquida de la presente invención no está particularmente limitada en sus componentes, aunque las realizaciones ejemplares descritas en el presente documento han demostrado ser superiores en la cantidad de CO que se puede disolver. Aunque no está tan limitado en todas las realizaciones, en realizaciones ejemplares, la composición líquida de la invención es una composición a base de agua. Debe entenderse que el término “composición a base de agua” incluye todas las composiciones que comprenden agua como disolvente, incluyendo, pero sin limitación: composiciones en las que el agua es el único disolvente; mezclas de agua y aceite (por ejemplo, emulsiones de agua en aceite y aceite en agua); soluciones acuosas, suspensiones, coloides y dispersiones; mezclas de agua y alcohol; y combinaciones de estos.
Se ha encontrado inesperadamente que las composiciones acuosas que comprenden uno o más componentes “complejos” proporcionan una capacidad superior de disolución de CO. Los componentes “complejos”, como se usan en el presente documento, son sustancias que son de naturaleza polimérica, de naturaleza biológica, tal como las derivadas de ácidos grasos, o que de otra manera comprenden al menos un sitio de interacción de unión para CO. Las interacciones pueden ser físicas (por ejemplo, hidrófobas, Van der Waals), o químicas (por ejemplo, iónicas o covalentes). Los ejemplos de componentes complejos incluyen, pero sin limitación: proteínas, polipéptidos y péptidos; polisacáridos; lípidos, grasas y aceites; y alcoholes que tienen dos o más átomos de carbono. En algunas realizaciones, los lípidos, proteínas o ambos están presentes en las composiciones. En estas realizaciones, es preferible que la cantidad combinada de proteínas y lípidos sea superior al 5 % (p/v), e incluso tan alta como del 40 % de lípidos y proteínas, o superior. En algunas formulaciones, la composición comprende más del 5 % de lípidos y más del 5 % de proteínas.
Las estructuras químicas precisas de los componentes complejos no están particularmente limitadas. En su lugar, es suficiente con que los componentes complejos funcionen para ayudar a aumentar la solubilidad del CO en la composición. Sin embargo, para ayudar al profesional en la selección de componentes complejos apropiados, la siguiente es una lista no limitante de tipos de componentes complejos: proteínas y grasas/aceites/lípidos/triglicéridos de origen animal, tales como los de la leche; proteínas y grasas/aceites/lípidos/triglicéridos de origen vegetal; mono, di y polisacáridos; vitaminas; edulcorantes naturales y artificiales; y saporíferos naturales y artificiales. Cualquiera y todas las diversas moléculas que están incluidas dentro de estos grupos se incluyen como parte de la presente invención. Los expertos en la técnica reconocerán inmediatamente dichas moléculas sin la necesidad de una lista exhaustiva en el presente documento.
En las realizaciones, la composición líquida de la invención adopta la forma de una bebida para consumo oral. Ejemplos no limitativos de bebidas según la invención son: agua embotellada, tal como agua con sabor a frutas o bayas; complementos dietéticos/nutricionales, tales como los formulados para bebés y niños pequeños (por ejemplo, fórmulas para bebés, tales como Similac® (Abbott, Abbott Park, IL) y Enfamil® (Mead Johnson & Company, Glenview, IL)) o adultos (por ejemplo, Ensure® (Abbott, Abbott Park, IL), y Peptamen® y Nutren® (Nestle, Vevey, Suiza)); lácteos líquidos o productos a base de lácteos, tales como leche, crema, yogur o batidos; soja líquida o productos a base de soja, tales como leche de soja o yogur de soja; arroz líquido o productos a base de arroz, tales como bebidas de arroz; bebidas deportivas o complementos dietéticos, tales como bebidas a base de proteína de suero y Gatorade® (Pepsico, Purchase, NY); bebidas a base de café, tales como las complementadas con productos lácteos; y refrescos con o sin azúcar. Como se describe con más detalle a continuación, ciertas composiciones líquidas de la invención están sobresaturadas con CO a temperatura ambiente y presión atmosférica. Como tal, ciertas bebidas pueden ser efervescentes como resultado de la liberación de una porción del CO sobresaturado. Esta propiedad efervescente puede mejorar la experiencia del paciente al ingerir la bebida, y puede mejorar el cumplimiento de un régimen de dosificación.
En las realizaciones, la composición líquida de la invención adopta la forma de un producto alimenticio a base de espuma o gel. Por ejemplo, en algunas realizaciones, la composición líquida se proporciona en forma de gel, tal como gelatina o budín, tales como los disponibles comercialmente con la marca Jell-O® (KraftFoods, Inc., Glenview,
IL). Una vez más, en algunas realizaciones, la composición líquida se proporciona en forma de espuma, tales como las disponibles comercialmente con la marca Coolwhip® (KraftFoods, Inc., Glenview, IL) y la marca ReddiWip® (ConAgra Foods, Inc., Omaha, NE).
Una bebida o producto alimenticio según la invención puede proporcionarse en un recipiente. En realizaciones preferidas, el recipiente es un recipiente sellable del tipo ampliamente utilizado para proporcionar bebidas comerciales y productos alimenticios al público. Los ejemplos no limitativos de recipientes sellables para contener la bebida y/o producto alimenticio son: botellas de plástico con tapones a rosca; latas de aluminio con tapas abre fácil; botellas de vidrio con tapas a rosca; y botellas de vidrio con tapones de aluminio selladas a presión o tapas hechas de otros metales flexibles. Por comodidad en la administración de una cantidad eficaz de CO a un sujeto que lo necesita, en realizaciones preferidas, la cantidad de bebida o producto alimenticio en un solo recipiente es un volumen adecuado de bebida o producto alimenticio para suministrar una dosis única de CO (por ejemplo, 5 ml, 10 ml, 30 ml, 50 ml, 75 ml, 100 ml, 150 ml, 177 ml, 180 ml, 237 ml., 300 ml, 355 ml, 500 ml, un litro). Como tal, se reconoce que las composiciones líquidas de la invención pueden proporcionarse de tal manera que una dosificación diaria para el tratamiento de una enfermedad o trastorno (por ejemplo, un síntoma de los mismos) se proporcione convenientemente en volúmenes de aproximadamente 3 litros o menos, tal como 2,5 litros, 2 litros, 1,8 litros, 1,5 litros, 1 litro, 330 ml, 300 ml, 180 ml, 30 ml o menos. Sin embargo, debe entenderse que, en situaciones donde la bebida o el producto alimenticio se suministra en un recipiente resellable (por ejemplo, una botella con un tapón a rosca), la cantidad de bebida o producto alimenticio en el recipiente puede representan más de una dosis de CO.
Por lo tanto, la invención proporciona productos para poner en práctica el método de la invención (analizado en detalle a continuación). Los productos pueden estar en forma de productos más fáciles de administrar, tales como soluciones o alimentos enlatados o embotellados. La tecnología es simple de aplicar, es poco probable que se asocie con efectos secundarios significativos, y es aceptable para la población afectada, lo que da como resultado una utilización fiable del método de tratamiento.
En resumen, en diversas realizaciones ejemplares, la presente invención proporciona una composición líquida que comprende monóxido de carbono gaseoso (CO) disuelto en una cantidad de 30 mg/l a 4400 mg/l en la composición líquida. En realizaciones, la composición comprende CO gaseoso disuelto en una cantidad de 50 mg/l a 400 mg/l, de 75 mg/l a 750 mg/l, y de 550 mg/l a 4400 mg/l. En general, el CO disuelto está presente en una cantidad suficiente para prevenir o tratar al menos un síntoma clínico de una enfermedad o trastorno afectado por CO. A continuación se analizan diversas enfermedades y trastornos que se pueden tratar con la composición. En realizaciones, además del CO gaseoso disuelto, la composición comprende además al menos uno de: proteínas, lípidos, grasas, triglicéridos, carbohidratos complejos, azúcar, sustituto de azúcar, zumo de frutas, carbohidratos, celulosa, fibra, ácido cítrico, saporíferos artificiales, saporíferos naturales, goma, pectina, ácido ascórbico, conservante, saponina, aceite, emulsión de aceite, tampón de pH y una sal. Para la porción líquida de la composición, en realizaciones ejemplares, se usan agua, etanol, o ambos. En las realizaciones, la composición líquida es aquella en la que la cantidad de CO disuelto es mayor que la que se produce a temperatura y presión ambiente y a un pH de 7,0 y/o un pH de 7,0, presión atmosférica y 21 °C. Por ejemplo, el CO disuelto puede ser dos o más veces la cantidad disuelta a temperatura y presión ambiente y a un pH de 7,0 y/o un pH de 7,0, presión atmosférica y 21 °C.
Como se menciona anteriormente, la composición líquida puede comprender CO gaseoso disuelto o CO gaseoso atrapado en burbujas, en una cantidad de al menos 0,03 gramos de gas por kilogramo de agua u otro líquido (es decir, al menos 30 mg/l). En realizaciones, la cantidad de CO disuelto o atrapado es mayor de 0,04 gramos de gas por kilogramo de agua u otro líquido. En las realizaciones, la cantidad de CO disuelto es igual o mayor que la cantidad que se produce a dos atmósferas de presión a 10 °C y a un pH de 7,0. En ciertas realizaciones, la composición líquida es una en la que el CO disuelto o atrapado puede administrarse por vía oral, o de otro modo a través del tracto gastrointestinal, y que no contiene componentes potencialmente tóxicos distintos de CO.
La composición líquida de la invención permite tratar a un paciente que padece una enfermedad o trastorno, que es susceptible de tratamiento con CO. Por lo tanto, un aspecto de la presente invención es un método para tratar a un paciente que padece, o en riesgo de desarrollar, una enfermedad o trastorno y/o que padece las consecuencias de la enfermedad o trastorno en la función de los órganos que pueden tratarse o prevenirse mediante la administración de una cantidad eficaz de CO. Pensado de otra manera, el método puede considerarse un método para tratar una enfermedad o trastorno que puede tratarse o prevenirse mediante la administración de una cantidad eficaz de CO. En términos generales, el método comprende administrar a un paciente una composición líquida que comprende una cantidad terapéuticamente eficaz o profilácticamente eficaz de CO gaseoso disuelto, donde la administración de la composición da como resultado un tratamiento eficaz para una enfermedad o trastorno que es tratable con CO. La administración puede realizarse por cualquier técnica adecuada conocida en el arte. Sin embargo, se ha determinado que la administración a través del tracto gastrointestinal es superior a otras vías de administración. La
administración a través del tracto GI se realiza preferiblemente a través de la ingestión oral (por ejemplo, bebiendo). Sin embargo, la invención contempla la administración a través de otros puntos en el tracto GI, tal como por medio de un enema o por medio de administración directa al intestino delgado o grueso.
Muchas enfermedades y trastornos que pueden tratarse con CO son de naturaleza crónica. Como tal, el tratamiento a largo plazo a menudo es necesario. La presente invención es particularmente adecuada para el tratamiento de dichas enfermedades y trastornos crónicos porque permite la administración a largo plazo de cantidades predefinidas y reguladas con precisión de CO gaseoso a un paciente. A diferencia de la administración de CO aéreo a los pulmones por inhalación, la presente invención, mediante la administración de CO gaseoso disuelto en un líquido al tracto GI, administra CO a través de un órgano distinto de los pulmones. Si bien es probable que se necesiten ajustes en el régimen de dosificación durante un largo curso de tratamiento, la evitación de los pulmones como el sitio de administración evita un factor de complicación para una dosificación precisa y exacta, lo que es una consideración importante en vista de la pequeña diferencia en la concentración de Co entre niveles terapéuticos y niveles tóxicos. Lo mismo puede decirse de la administración por infusión IV, aunque la ingestión oral es mucho más conveniente y rentable.
La presente invención también es adecuada para el tratamiento de episodios agudos de enfermedades y trastornos que pueden tratarse con CO. La administración de una composición según la invención al tracto GI o al torrente sanguíneo permite una dosificación rápida de CO un paciente. Los niveles sistémicos terapéuticos de CO se pueden alcanzar rápidamente, lo que permite la reducción de los síntomas clínicos de una enfermedad o trastorno. Entre los beneficios proporcionados por la invención está la limitación de la extensión del tejido dañado y, por lo tanto, la extensión del dolor asociado con la SCC. Más específicamente, al aumentar rápidamente el contenido de CO de la sangre, el daño causado durante la SCC puede limitarse al sitio del dolor original, reduciendo así la propagación del daño y el dolor. Además, debido a que un paciente que experimenta una SCC habrá sido diagnosticado con SCD (excepto, potencialmente, para el primer episodio de SCC), se puede determinar fácilmente la cantidad apropiada de CO a administrar, lo que permite una administración precisa y exacta de una cantidad eficaz, pero no tóxica, de CO para el paciente.
El método de tratamiento según la invención es un método que trata a pacientes que padecen enfermedades y trastornos que pueden tratarse con CO. Debido a que se conoce el agente bioactivo eficaz y se conoce su papel en el tratamiento de la enfermedad o trastorno, el método según la invención se puede poner en práctica tanto terapéuticamente para tratar una enfermedad o trastorno, como profilácticamente para prevenir o retrasar la aparición de los síntomas clínicos de una enfermedad o trastorno. Es decir, debido a que el Co es el agente activo que reduce y, por último, elimina los síntomas clínicos de una enfermedad o trastorno abarcado por la presente invención, también es el agente activo que previene o retrasa la aparición de un síntoma clínico de una enfermedad o trastorno abarcado por la presente invención. Por ejemplo, en el caso de SCD, el tratamiento profiláctico con CO puede reducir o eliminar la formación de glóbulos rojos falciformes, previniendo o retrasando así la aparición de SCC y mitigando las complicaciones de SCC. Por supuesto, los expertos en la materia entenderán que el término “prevenir” no implica la prevención absoluta de ningún desarrollo y progresión de una enfermedad o trastorno, sino que en su lugar indica el bloqueo, al menos en cierta medida, del desarrollo o progresión natural de la enfermedad o trastorno.
El método de la invención comprende administrar una composición líquida que contiene CO a un paciente que lo necesite. Aunque la invención contempla realizar la etapa de administración una sola vez, la etapa de administrar puede repetirse cualquier número de veces. De hecho, en realizaciones preferidas, la etapa de administración se repite un número suficiente de veces para lograr una concentración de carbonmonoxi-hemoglobina (en lo sucesivo en el presente documento denominada “CO-Hb”) adecuada para la enfermedad o trastorno que se está tratando. Por ejemplo, para el tratamiento de SCD, es deseable una concentración promedio de CO-Hb de entre el 3 % y el 15 %, más preferiblemente entre el 3 % y el 12 %, mucho más preferiblemente entre el 3 % y el 9 %, tal como aproximadamente del 3 % al 6 %. Se sabe que la semivida de la fase alfa de CO en el torrente sanguíneo humano es de aproximadamente 4 - 6 horas. Por lo tanto, se puede lograr una concentración promedio de CO-Hb en el torrente sanguíneo, por ejemplo, a través de un régimen de dosificación de cuatro o menos dosis al día, preferiblemente con una separación igual, tal como cuatro dosis al día (es decir, cada seis horas), tres dosis al día (es decir, una dosis cada ocho horas), dos dosis al día (es decir, cada doce horas), o una dosis al día. Debido a la concentración relativamente alta de CO que se puede lograr en una composición líquida según la presente invención, se pueden administrar volúmenes relativamente pequeños de composición líquida por dosis o al día, tales como: 2 litros al día, 1,5 litros al día, 1 litro al día, 0,7 litros al día, 0,5 litros al día, 0,25 litros al día, y 0,1 litros al día, y otras cantidades descritas en el presente documento. La dosificación de pequeños volúmenes mejora el cumplimiento del paciente y proporciona un resultado general superior para el paciente. Dado que no se conocen efectos perjudiciales para la exposición a largo plazo al CO a estos niveles, la administración diaria se puede realizar
de forma indefinida. Los expertos en la técnica reconocerán que este concepto es igualmente aplicable a otras enfermedades y trastornos tratables con CO, y que el nivel promedio de CO-Hb adecuado para el tratamiento de estas enfermedades y trastornos puede ser diferente, pero puede determinarse fácilmente.
La presente invención se basa, al menos en parte, en el entendimiento de que la dosificación con CO debe estar bien controlada debido al hecho de que el nivel tóxico de CO está cerca del nivel terapéutico. Más específicamente, generalmente se reconoce que los niveles de CO en el torrente sanguíneo que dan como resultado hasta aproximadamente un 15 % de CO-Hb muestran eficacia para reducir la SCC sin efectos secundarios o toxicidad perjudiciales significativos. Sin embargo, también se reconoce generalmente que, a niveles de CO-Hb entre aproximadamente el 16 % y el 20 %, se observa cierta toxicidad, y que a niveles de CO-Hb superiores al 20 %, se observan habitualmente toxicidad y efectos secundarios. La presente invención tiene en cuenta la proximidad de niveles de dosis eficaces sin efectos secundarios o toxicidad sustanciales adversos y niveles de dosis que dan como resultado toxicidad y efectos secundarios. La presente invención proporciona productos y métodos de tratamiento que de manera conveniente, precisa y reproducible, logran una dosificación eficaz de CO a los pacientes evitando niveles tóxicos y/o efectos secundarios.
Entre las enfermedades hematológicas que pueden tratarse según la presente invención están aquellas que implican hemoglobina anormal, tales como SCD, enfermedad de hemoglobina C, enfermedad de hemoglobina SC y betatalasemia de hemoglobina S.
Con respecto a SCD, la presente invención proporciona una nueva forma de tratar la enfermedad, incluyendo la prevención y el tratamiento de SCC usando CO gaseoso. En el tratamiento de SCC, el CO se administra a un sujeto que lo necesite (es decir, paciente) en una cantidad que afecta al menos a un síntoma clínico de SCC. En realizaciones preferidas, el método de tratamiento reduce o elimina al menos un síntoma clínico de SCC, pero en una cantidad que no induce niveles inaceptables de toxicidad o efectos secundarios adversos. En la prevención de SCC, el CO se administra a un sujeto que lo necesita (es decir, el paciente) de forma regular en una cantidad que afecta el número de SCC experimentado por el sujeto que lo necesita. En realizaciones preferidas, el método de prevención reduce el número o la gravedad de SCC experimentado por el sujeto que lo necesita. En realizaciones preferidas, la administración es a través de la ingestión oral del líquido. Aunque el CO es tóxico en altas concentraciones, no es tóxico en las concentraciones relativamente bajas útiles según la presente invención. Además, debido a que el CO se une a la hemoglobina S (“Hb-S”) con una afinidad mucho más alta que el oxígeno, y debido a que la Hb debe estar en una configuración no unida a gases a polimerizar (lo que da como resultado el desarrollo de células falciformes), pueden usarse dosis relativamente bajas de CO para prevenir y tratar SCD y SCC. El método también puede comprender administrar CO a un sujeto de forma regular en una cantidad que sea suficiente para reducir el número de SCC experimentado por el paciente y/o reducir el daño orgánico resultante causado por la formación de células falciformes. Los órganos afectados incluyen, pero sin limitación, pulmones, cerebro, corazón, riñones, hueso, bazo, hígado, glándulas endocrinas y órganos sexuales masculinos. El impacto de la formación de células falciformes en el tiempo extiende el grado de daño a los órganos. En realizaciones, el método se repite regularmente para proporcionar un régimen de tratamiento crónico.
Aunque existen varias formas de administrar el CO para tratar SCD y SCC, la más conveniente es mediante la administración de un líquido infundido con CO. El CO absorbido a través del sistema GI se une rápidamente a la Hb, proporcionando así un tratamiento eficaz y rápido.
El tratamiento de SCC según los métodos de la invención puede tener los siguientes efectos para uso agudo: puede acortar las crisis y aliviar la gravedad de las crisis. El tratamiento del SCC según los métodos de la invención puede tener los siguientes efectos para uso crónico: puede disminuir la frecuencia de las crisis, puede disminuir la gravedad de las crisis, puede disminuir la extensión, la progresión y la frecuencia del daño orgánico, y puede prevenir directamente las crisis.
La administración de CO a un paciente a través de la administración de líquido se logra más convenientemente usando recipientes generalmente disponibles, tal como una lata de metal o una botella de vidrio o plástico. El líquido y el tipo de recipiente no están particularmente limitados, con la excepción de que el líquido debe permitir que se disuelvan los niveles adecuados de CO, mientras que el recipiente debe estar fabricado de material que sea suficientemente impermeable al CO y suficientemente resistente a la presión. Por supuesto, el profesional necesitará ajustar la composición del líquido en algunas situaciones para optimizar la disolución de CO en el líquido y, por lo tanto, la absorción en el cuerpo del paciente. Por ejemplo, la salinidad, el pH, el contenido de azúcar, la cantidad de compuestos orgánicos (por ejemplo, alcohol), el contenido de proteínas, el contenido de lípidos, etc., se pueden variar para optimizar el sabor, la consistencia, etc. de la composición, y la cantidad de CO que se disuelve en el líquido y también para optimizar la absorción de CO una vez que se administra al paciente. Además, la presión, la
temperatura y los componentes en la composición durante la disolución de CO pueden variarse para optimizar la cantidad de CO que se disuelve en el líquido. Asimismo, se pueden usar soluciones no acuosas de diversos constituyentes, así como composiciones acuosas o no acuosas que incluyen constituyentes no disueltos.
Entre los muchos recipientes que se pueden usar, se pueden mencionar: botellas de vidrio, botellas de plástico; y latas de aluminio, y recipientes fabricados a partir de combinaciones de vidrio, plástico, aluminio y otros metales. El CO tiene una serie de propiedades médicas y ha demostrado ser prometedor en el tratamiento de una diversidad de enfermedades. El desafío principal al usar el CO como agente terapéutico dada su toxicidad potencial es administrar una cantidad pequeña pero suficiente de CO para tratar la enfermedad sin causar daño. Hasta ahora, no ha sido posible hacer esto.
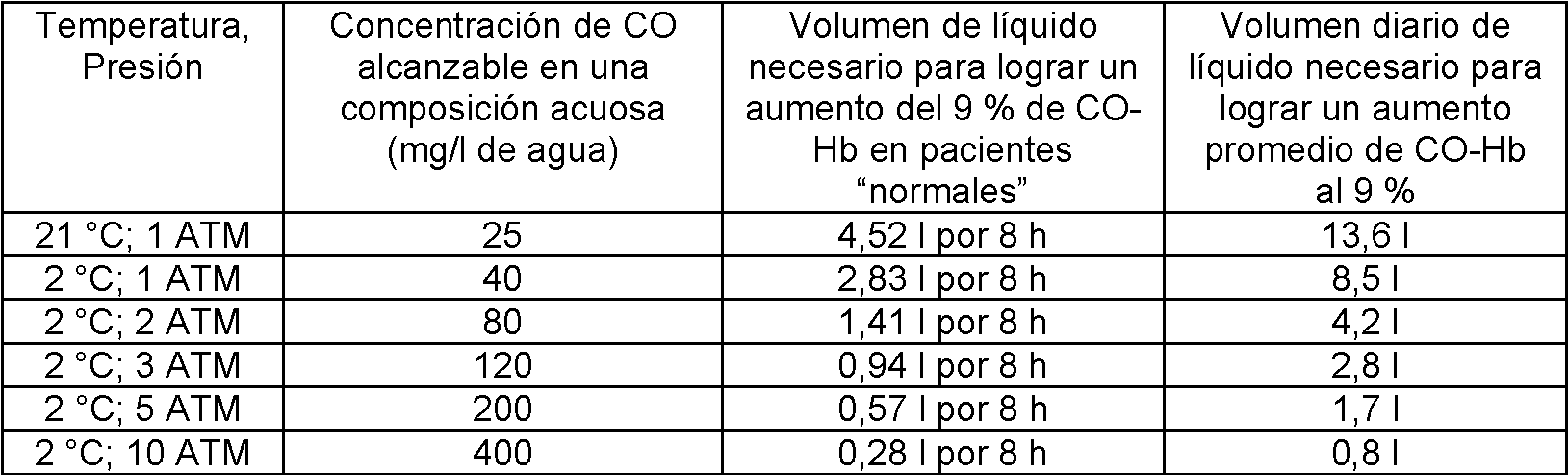
Hay una serie de limitaciones significativas para usar la administración de CO disuelto en líquido y usado a través del tracto GI con fines terapéuticos o profilácticos. Estas limitaciones se han superado en la presente invención. La barrera principal hasta la fecha ha sido la administración de cantidades suficientes de CO. La solubilidad del CO en soluciones acuosas es baja a temperatura ambiente y presión atmosférica normal (ATM). Por lo tanto, utilizando enfoques previamente propuestos en la técnica, que se basan en disolver CO en una composición acuosa a temperatura ambiente y a presión atmosférica, el volumen de líquido necesario para administrar una dosis terapéutica de CO es logísticamente prohibitivo. Sin embargo, usando la presente invención, se pueden lograr niveles terapéuticamente útiles de CO. La tabla 1 proporciona un resumen de los volúmenes necesarios para lograr una dosis terapéutica que proporciona un aumento promedio del 9 % de CO-Hb, que proporciona un nivel promedio de CO-Hb en la sangre de aproximadamente el 7 % en promedio sin aumentar por encima del 15 % en ningún momento dado. Los valores se presentan para pacientes con SCD. La tabla 2 proporciona un resumen similar de los volúmenes necesarios para tratar pacientes con niveles normales de Hb y función pulmonar normal.
Tabla 1:
Tabla 2:
Las tablas 1 y 2 demuestran que, a presión ambiente, incluso a baja temperatura, no es posible alcanzar una concentración de CO en solución que permita una dosis terapéutica de CO utilizando un volumen de solución acuosa que razonablemente puede tomarse por vía oral por un paciente en un periodo de 24 horas.
Con el fin de lograr una mayor concentración de CO que permita un volumen de solución acuosa que se pueda tomar razonablemente por vía oral en un periodo de 24 horas, en la presente invención se han realizado una serie de mejoras en los intentos anteriores en la técnica.
Primero, en la presente invención, en particular en lo que se refiere a realizaciones donde están implicadas
composiciones acuosas, el CO se disuelve en un líquido acuoso a una presión superior a la presión ambiente. El uso de presión para disolver el CO aumenta la concentración alcanzable de CO en solución. Las tablas 1 y 2 demuestran el aumento significativo de las concentraciones de CO que se pueden lograr a presión y la correspondiente disminución sustancial de la cantidad necesaria de solución acuosa necesaria para proporcionar una dosis eficaz de CO. Un experto en la técnica reconocerá de inmediato que la disminución de la temperatura por debajo de 2 °C y el aumento de la presión por encima de 10 ATM puede lograr una concentración aún mayor de CO disuelto en la solución acuosa, y que los valores presentados en la tabla 1 son solo para fines de demostración. Aunque elevar la presión por encima de 10 ATM puede no ser comercialmente factible, es tecnológicamente factible en este momento.
Las tablas 1 y 2 demuestran que bajo una presión mayor que la ambiente y a baja temperatura, es posible lograr una concentración de CO en solución que permita una dosis terapéutica de CO en un volumen de solución acuosa que puede tomarse razonablemente por vía oral por un paciente en un periodo de 24 horas. Los volúmenes necesarios a administrar al día están dentro de las cantidades tomadas diariamente por muchas personas. Por lo tanto, el cumplimiento por parte de los pacientes debería mejorarse enormemente en comparación con cualquier intento de tratamiento con líquidos que contienen CO conocidos en la técnica.
En segundo lugar, el uso de una formulación para el GI (por ejemplo, una formulación para administración oral) supera el desafío de usar una composición acuosa con infusión de CO como agente terapéutico. Una formulación acuosa oral o para el GI permite el uso de una solución con CO disuelto a una presión superior a la ambiente y a baja temperatura, lo que permite una dosis terapéutica de CO. Cuando el CO se disuelve en una solución a una presión mayor que la ambiente, y la solución se traslada a un entorno de presión ambiente tras la administración de la solución, el gas CO saldrá por burbujeo de la solución (de forma similar a las soluciones líquidas que contienen CO2 disuelto). Las burbujas de gas representan un peligro sustancial para un paciente en muchos mecanismos de administración, tal como IP y administración intravenosa, entre otros. Sin embargo, el burbujeo de gas CO fuera de la solución en el estómago o el intestino no representa un riesgo de seguridad sustancial. Por lo tanto, el uso de una ruta de administración que permita el burbujeo de CO fuera de la solución permite el uso de esta invención en indicaciones terapéuticas que requieren una alta concentración de CO. Además, la disolución de CO en solución a temperaturas cercanas o inferiores a 0 °C aumenta la saturación de CO de la solución, en comparación con la disolución de CO a temperatura ambiente. La administración de una solución muy fría presenta incomodidad y peligro para un paciente en muchos mecanismos de administración, tales como IP y administración intravenosa, entre otros. Sin embargo, el uso de un líquido frío en el estómago o el intestino no representa un riesgo de seguridad sustancial o una molestia sustancial. Por lo tanto, el uso de una ruta de suministro que permite la administración de una solución fría permite el uso de esta invención en indicaciones terapéuticas que requieren una alta concentración de CO. Además, aunque la presente invención contempla disolver el Co en un líquido a temperaturas relativamente bajas, el CO no necesita administrarse a un paciente por medio de un líquido frío. Por ejemplo, una composición líquida que contiene CO puede prepararse en un recipiente sellable. Una vez sellado, no es necesario mantener el recipiente a temperatura fría para que el CO permanezca en solución. Aunque se escapará una mayor cantidad de CO de la solución si el recipiente se abre a temperaturas más altas que a temperaturas más bajas, la ingestión (u otra administración) del líquido al paciente en un periodo de tiempo relativamente corto después de la apertura del recipiente minimizará la pérdida de CO del líquido.
En tercer lugar, la presente invención reconoce que las composiciones líquidas complejas son superiores al agua o composiciones acuosas relativamente simples para la administración terapéutica de Co . Intentos anteriores para administrar CO a las células utilizaron CO disuelto en agua o en soluciones acuosas de agua y sales. Según las realizaciones preferidas de la presente invención, la composición líquida para la administración de CO es una composición acuosa que contiene una o más moléculas relativamente complejas, tales como proteínas, lípidos, aceites, alcoholes y/o carbohidratos. Se ha encontrado que la presencia de estas moléculas complejas permite una mayor solubilidad de CO en comparación con las composiciones que carecen de ellas. Como tal, la inclusión de estas moléculas complejas supera el desafío de usar CO como agente terapéutico. Las realizaciones preferidas de la invención incluyen, por lo tanto, la administración de composiciones acuosas complejas que comprenden concentraciones terapéuticas de CO mezcladas con uno o más lípidos, proteínas u otras sustancias que ayudan a aumentar la concentración de CO en la composición acuosa.
Cuarto, otra característica de la presente invención que supera un desafío con el uso de CO como un producto terapéutico es el uso en pacientes con bajas concentraciones de Hb, incluidos aquellos pacientes con SCD. Como se menciona anteriormente, la cantidad de líquido que se puede administrar a un paciente es un factor limitante dada la relativamente baja solubilidad del CO en líquidos. Sin embargo, debido a que la cantidad de Hb es menor en ciertas poblaciones de pacientes, tales como aquellos con SCD, los niveles de dosificación terapéutica de CO también son más bajos en dichos pacientes. La alta concentración de CO posible en líquidos según la presente
invención permite una mayor facilidad de uso, un mejor cumplimiento del paciente, y una mejora general en el efecto terapéutico, en comparación con otros tratamientos propuestos en la técnica.
Como se analiza anteriormente, la invención proporciona un método para tratar a un paciente que padece una enfermedad o trastorno, o en riesgo de desarrollar una enfermedad o trastorno, que puede tratarse o prevenirse mediante la administración de CO. Por lo tanto, la invención proporciona el uso de una composición líquida que comprende una cantidad terapéuticamente eficaz de CO en el tratamiento de una enfermedad o trastorno, o la prevención de una enfermedad o trastorno, que puede tratarse o prevenirse mediante la administración de CO. La invención proporciona además el uso de una composición líquida que comprende una cantidad terapéuticamente eficaz de Co en la preparación de una composición medicinal para el tratamiento o prevención de una enfermedad o trastorno que puede tratarse con CO.
En otro aspecto general más de la invención, se proporcionan métodos para elaborar una composición líquida que contiene CO disuelto en una cantidad eficaz para el tratamiento. Los intentos anteriores en la técnica para crear una composición líquida que contenga CO gaseoso disuelto implicaron disolver CO en un líquido acuoso a temperatura ambiente y presión atmosférica, dando como resultado una composición que no es adecuada para su uso como agente terapéutico o profiláctico in vivo debido al bajo contenido de CO en el líquido. La presente invención, por el contrario, logra un agente terapéutico y profilácticamente eficaz a través del uso de un método de preparación que incluye el uso de alta presión, temperatura fría o una combinación de ambos. Preferiblemente, el método también incluye el uso de una composición líquida que incluye uno o más componentes complejos, que ayudan a aumentar la concentración de CO disuelto en la composición.
El método para elaborar una composición líquida que contiene CO típicamente comprende someter una composición líquida a una presión alta mientras se expone la composición a CO gaseoso durante un periodo de tiempo suficiente para lograr una concentración de CO adecuada en la composición líquida para proporcionar una composición terapéuticamente eficaz y/o profilácticamente eficaz. Sin embargo, debe observarse que, en ciertas realizaciones en las que las composiciones comprenden lípidos, grasas o aceites, la introducción de niveles terapéuticos de CO podría no requerir el uso de una presión superior a la atmosférica. En realizaciones preferidas, la etapa de exponer comprende infundir CO en la composición líquida por burbujeo a través de una cánula, aireador u otro dispositivo o método equivalente. En algunas realizaciones, la composición líquida se somete a mezcla o agitación durante el proceso de exposición al CO para facilitar la disolución del CO en la composición líquida.
Aunque no es necesario, en realizaciones relacionadas con la producción comercial de la composición líquida, se prefiere que la composición líquida que contiene CO se selle en un recipiente impermeable al CO para evitar la pérdida de CO disuelto con el tiempo. Por consiguiente, en las realizaciones, el método para elaborar una composición líquida que contiene CO comprende dispensar la composición líquida en un recipiente impermeable al CO sellable y sellar el recipiente después de que se haya disuelto una cantidad apropiada de CO en la composición líquida. La dispensación del líquido se puede realizar antes, durante o después de disolver el CO en la composición líquida. Típicamente, el sellado se realizará bajo gas CO y en condiciones superiores a las atmosféricas para minimizar la pérdida de CO disuelto durante el proceso de sellado. Como tal, es preferible que el recipiente y el mecanismo de sellado (por ejemplo, tapa, tapón) sean resistentes a las presiones usadas durante la disolución de CO en la composición (por ejemplo, de aproximadamente 1,1 ATM a aproximadamente 8 ATM o más). Como se analiza anteriormente, se conoce cualquier cantidad de recipientes sellables y tapas en la técnica de embotellado y envasado de líquidos, y cualquiera de estos puede usarse dentro del contexto de la presente invención.
El método de elaborar una composición líquida que contiene CO se basa en el uso de una presión superior a la atmosférica (es decir, presión “alta”) para aumentar la cantidad de CO disuelto en la composición líquida. Según la invención, se utilizan al menos 1,1 atmósferas (ATM) de presión en el proceso de introducción de CO en la composición líquida. Preferiblemente, cuando se usa alta presión, se usan al menos 1,2 ATM. En ciertas realizaciones ejemplares, se usan 2 ATM, 3 ATM o 5 ATM durante la introducción de CO en la composición líquida. La invención contempla que las presiones superiores a 5 ATM también son adecuadas, tales como 6 ATM, 7 a Tm , 8 ATM y 10 ATM o más. Según el análisis relativo a los rangos establecidos anteriormente, el experto en la técnica reconocerá que todos los valores específicos, y todos los rangos posibles, que están dentro de las condiciones atmosféricas analizadas en el presente documento, se contemplan como parte de la invención, y que no hay necesidad de mencionar específicamente todos y cada uno de los valores y rangos posibles para que el experto en la técnica reconozca que todos estos valores y rangos están previstos como parte de la invención. Además, debe entenderse que las variaciones en la fuente de CO, el equipo utilizado para introducir el CO en la composición líquida, la presión del CO que se utiliza (es decir, el volumen suministrado por unidad de tiempo), y las presiones atmosféricas utilizadas afectarán a la cantidad de tiempo requerido para lograr una concentración adecuada de CO en la composición. Los expertos en la materia pueden identificar fácilmente los parámetros correctos para lograr una
composición que contiene CO utilizando solo procedimientos estándar y directos conocidos en la técnica, sin demasiada o excesiva experimentación.
El método para elaborar una composición líquida que contiene CO comprende preferiblemente someter la composición a una temperatura baja durante la etapa de exponer el líquido al CO. Se ha encontrado que bajar la temperatura de la temperatura ambiente (aproximadamente 21 °C) a aproximadamente 2 °C aumenta la cantidad de
CO que se disuelve en la composición líquida. Según la invención, una temperatura baja es una temperatura igual o inferior a 4 °C, preferiblemente igual o inferior a 2 °C, tal como 1 °C, 0 °C, -1 °C, -2 °C, -3 °C, -4 °C, -5 °C, -6 °C, -10 °C, -12 °C, -14 °C, -16 °C, -18 °C, -20 °C, o inferior. En realizaciones en las que la composición se expone a una temperatura baja, se prefiere que la composición líquida que contiene CO se selle para evitar la pérdida de CO disuelto con el tiempo. Por consiguiente, en las realizaciones, el método para elaborar una composición líquida que contiene CO comprende dispensar la composición líquida en un recipiente sellable y sellar el recipiente después de que se haya disuelto una cantidad apropiada de CO en la composición líquida. La dispensación del líquido se puede realizar antes, durante o después de disolver el CO en la composición líquida. Típicamente, el sellado se realizará a baja temperatura para minimizar la pérdida de CO disuelto durante el proceso de sellado. Como se analiza anteriormente, se conoce cualquier cantidad de recipientes sellables y tapas en la técnica de embotellado y envasado de líquidos, y cualquiera de estos puede usarse dentro del contexto de la presente invención. En aras de claridad, en realizaciones en las que se usan tanto alta presión como baja temperatura, se prefiere que el sellado se realice tanto a alta presión como a baja temperatura, aunque no es necesario usar la misma presión y temperatura utilizadas para disolver el CO en el líquido. Además, debe entenderse que, una vez que el líquido que contiene CO se sella en un recipiente con gas Co , no es necesario mantener el recipiente sellado a alta presión y baja temperatura, ya que el recipiente sellado no permitirá que el CO disuelto escape de la solución.
La presente invención identifica tres parámetros importantes para lograr una composición líquida que tenga una cantidad terapéutica y/o profilácticamente eficaz de CO gaseoso disuelto: introducción de CO gaseoso a alta presión; introducción de CO gaseoso a baja temperatura; y la presencia de sustancias complejas en la composición líquida. Sin embargo, debe entenderse que otros parámetros pueden ajustarse para mejorar o alterar de otro modo la concentración de CO en solución, o simplemente para alterar el sabor y la consistencia general. Estos parámetros se pueden ajustar por varias razones, incluyendo, pero sin limitación: alterar el sabor del líquido; alterar la dulzura, acidez o sabor del líquido; alterar el pH del líquido; alterar la salinidad del líquido; y alterar la consistencia del líquido.
Se ha encontrado que las alteraciones en muchos parámetros no afectan significativamente a la capacidad de carga global de CO de una composición líquida, con las principales excepciones de la alteración de la presión, la temperatura, y la presencia de componentes complejos, como se describe anteriormente. Por ejemplo, las pruebas muestran que, para una combinación dada de presión, temperatura y componentes complejos, las variaciones en el pH, concentraciones de azúcar simples y concentraciones de sal tienen poco efecto sobre los niveles de CO disuelto.
EJEMPLOS
Ejemplo 1: Formulaciones ejemplares
La presente invención proporciona un avance sobre la técnica anterior al proporcionar una composición líquida que comprende cantidades terapéutica y/o profilácticamente eficaces de CO gaseoso disuelto en formas de dosificación.
Las formulaciones se basan en tres criterios principales: el nivel de presión en fase gaseosa durante la disolución de
CO en la composición líquida; la temperatura durante la disolución de CO en la composición líquida; y la presencia de componentes complejos en la composición líquida. Las tablas 3-5 muestran datos que indican el papel de las proteínas, grasas y otros componentes complejos en el aumento de la concentración de CO disuelto en composiciones líquidas según la presente invención.
Con referencia a la tabla 3, se puede ver que el CO se puede disolver en composiciones líquidas que comprenden grasas y proteínas (Ensure® (Abbott, Abbott Park, IL), 10 %-50 % en agua) y nata estándar de leche de vaca (50 % de nata en agua, v/v) a concentraciones superiores a las que se pueden lograr solo en agua, del orden de al menos
28 mg/l. Si bien se pueden lograr concentraciones mejoradas de CO disuelto a 1 ATM y 21 °C utilizando bajos niveles de proteínas y grasas (por ejemplo, Ensure® al 10 %), la cantidad de CO disuelto se puede aumentar al aumentar las cantidades de proteínas y grasas, y aumentando la presión de la fase gaseosa aplicada durante el proceso de disolución.
Tabla 3: Concentraciones de CO con diversas soluciones que contienen proteínas y grasa ____________________ (~1 atmósfera de presión; Soluciones en agua)______________ _____
| Solución | Temperatura | Concentración de CO (mg/l) | N |
Al observar ahora la tabla 4, se puede ver que la cantidad de presión proporcionada durante el proceso de disolución de CO en una composición líquida que contiene agua es un factor importante para lograr una composición con niveles terapéuticos de CO. Más específicamente, la tabla 4 muestra que, para un porcentaje dado de Ensure® o nata estándar, el aumento de la presión durante la disolución de CO da como resultado un aumento significativo en la cantidad de CO infundido en la composición.
Tabla 4: Concentraciones de CO con soluciones que contienen proteína y grasa a diversas presiones Soluciones en a ua
La tabla 5 muestra una comparación de las cantidades de composición líquida necesarias para proporcionar una dosis terapéutica de CO a sujetos sin SCD (denominados pacientes “normales”) usando composiciones acuosas y composiciones que comprenden proteínas y grasas (es decir, una composición de nata al 50 %). Como se puede ver en la tabla, el volumen de composición que se necesita administrar es la mitad o menos para las composiciones líquidas que comprenden proteínas y grasas en comparación con las composiciones acuosas simples.
Tabla 5: Volúmenes necesarios para conseguir una dosis terapéutica de CO en pacientes normales
-
Como se puede ver en las tablas 3-5, las composiciones que contienen niveles terapéutica y profilácticamente eficaces de CO se pueden producir según la presente invención. Además, los métodos según la invención, y las composiciones preparadas usando los métodos, son superiores en la captura de CO en solución mediante el uso de presiones superiores a 1 ATM, temperaturas inferiores a 21 °C, y composiciones que comprenden sustancias complejas, tales como proteínas y/o grasas.
Ejemplo 2: Eficacia in vivo de composiciones de la invención
Se ha establecido la capacidad de las composiciones según la presente invención para administrar niveles terapéuticos de CO al torrente sanguíneo de seres humanos y ratas, como se informa en este Ejemplo. Más específicamente, se preparó una formulación acuosa disolviendo CO en agua a aproximadamente 2 °C y aproximadamente 1,2 ATM, dando como resultado una composición que contiene una concentración de CO de 0,05 g/l. El voluntario normal tomó aproximadamente 350 ml del agua infundida con CO dos veces por vía oral a un intervalo de 1,5 horas, con los siguientes resultados (tabla 6). Estos resultados se alinean con los resultados estequiométricos esperados dentro de las bandas de error esperadas y la pérdida de CO con el tiempo:
Tabla 6: n n r i n -H n n r n n rm l l ificación
Este experimento muestra no solo que los niveles terapéuticamente eficaces de CO pueden infundirse en composiciones líquidas según la invención, sino que dichas composiciones pueden ingerirse por vía oral y pueden administrar dosis terapéuticas de CO al torrente sanguíneo, según lo ensayado por concentraciones de CO-Hb. Para mostrar adicionalmente la eficacia de la presente invención en la creación de composiciones líquidas terapéuticamente eficaces para la administración de CO, se preparó una composición líquida que comprendía proteínas y grasas según el proceso de la invención, y se probó su actividad de administración de CO en ratas. Más específicamente, se preparó una formulación de nata al 50 % en agua y se introdujo CO a aproximadamente 2 °C y aproximadamente 1,2 ATM, dando como resultado una composición que tiene una concentración de 0,075 g/l (75 mg/l). Tres (3) ml de la formulación se administró a ratas por medio de sonda, y los niveles de CO-Hb resultantes se ensayaron y se compararon con un control negativo que recibió un líquido que no contenía CO a través de sonda. Más específicamente, las ratas de laboratorio con un peso de 250-300 gramos se trataron mediante sonda con: 1) sin sonda (control negativo); 2) 3 ml de agua infundida con CO dos veces en los tiempos 0 y 1 hora; y 3) 3 ml de nata al 50 % infundida con CO dos veces en los tiempos 0 y aproximadamente 1,25 horas. El muestreo de sangre se realizó aproximadamente 1,5 horas después de la segunda sonda para cada rata.
Los resultados de las pruebas se presentan en la tabla 7. Los resultados muestran que el CO puede administrarse al torrente sanguíneo de la rata en una cantidad que es eficaz para tratar enfermedades y trastornos asociados con resultados eficaces de CO a través de una ruta oral usando composiciones según a la presente invención. Se obtuvieron resultados similares a los presentados en la tabla 7 con una composición que comprendía Ensure® al 40 % preparada y administrada de la misma manera que la nata al 50 %.
T abla 7: Administración de cantidades tera éuticamente eficaces de CO in vivo
Por lo tanto, el presente Ejemplo muestra que las composiciones según la presente invención pueden usarse con éxito preclínicamente in vivo para administrar cantidades terapéuticamente eficaces de CO a la sangre de los sujetos.
REFERENCIAS
Aroutiounian, S et al., “Evidence for carbon monoxide binding to sickle cell polymers during melting.” Biophysical Chemistry 91 (2001) 167-181.
Akamatsu, Y., M. Haga, et al. (2004). “Heme oxygenase-1-derived carbon monoxide protects hearts from transplant associated ischemia reperfusion injury.” Faseb J 18(6): 771-2.
Bauer, Inge et al., “Bench-to-bedside review: Carbon monoxide - from mitochondrial poisoning to therapeutic use.” Critical Care 2009, 13:220
Beckman J, Belcher, JD, et al. “ Inhaled carbon monoxide reduces leukocytosis in a murine model of sickle cell disease.” Am J Physiol Heart Circ Physiol 297: H1243-H1253, 2009.
Beutler E. The effect of carbon monoxide on red cell life span in sickle cell disease. Blood 46: 253-259, 1975.
Bunn, H. F. (1997). “Pathogenesis and treatment of sickle cell disease.” N Engl J Med 337(11): 762-9.
Clark, J. E., P. Naughton, et al. (2003). “Cardioprotective actions by a water-soluble carbón monoxide-releasing molecule.” Circ Res 93(2): e2-8.
EMA COMMITTEE FOR MEDICINAL PRODUCTS FOR HUMAN USE (CHMP), “GUIDELINE ON THE SPECIFICATION LIMITS FOR RESIDUES OF METAL CATALYSTS OR METAL REAGENTS”, London, 21 February 2008, Doc. Ref. EMEA/CHMP/SWP/4446/2000
Foresti R et al., “Use of carbon monoxide as a therapeutic agent: promises and challenges”, Intensive Care Med.
2008 Apr;34(4):649-58. Epub 2008 Feb20
Guo, Y., A. B. Stein, et al. (2004). “Administration of a CO-releasing molecule at the time of reperfusion reduces infarct size in vivo.” Am J Physiol Heart Circ Physiol 286(5): H1649-53.
Hampson NB, Hauff NM: Carboxyhemoglobin levels in carbon monoxide poisoning: do they correlate with the clinical picture? Am J Emerg Med 2008, 26:665-669.
Ikeda, A et. al. “Liver graft exposure to carbon monoxide during cold storage protects sinusoidal endothelial cells and emeliorates reperfusion injury in rats”, Liver Transpl. 2009 November; 15(11): 1458-1468.
Kaczorowski DJ, Zuckerbraun BS. Carbon monoxide: medicinal chemistry and biological effects. Curr Med Chem 14: 2720-2725, 2007.
Kohmoto, J., A. Nakao, et al. (2007). “Carbon monoxide protects rat lung transplants from ischemia-reperfusion injury via a mechanism involving p38 MAPK pathway.” Am J Transplant 7(10): 2279-90.
Motterlini, R., Otterbein L., “The therapeutic potential of carbon monoxide”, Nat Rev Drug Discov. 2010 Sep;9(9):728-43
Nakao, A., J. S. Neto, et al. (2005). “Protection against ischemia/reperfusion injury in cardiac and renal transplantation with carbon monoxide, biliverdin and both.” Am J Transplant 5(2): 282-91.
Nakao A et. al. “Ex vivo application of carbon monoxide in University of Wisconsin solution to prevent intestinal cold ischemia/reperfusion injury. Am J Transplant. 2006; 6(10):2243-2255.
Nakao, A., et. al., “A Single Intraperitoneal Dose of Carbon Monoxide-Saturated Ringer's Lactate Solution Ameliorates Postoperative Ileus in Mice”, JPET 319:1265-1275, 2006
Nakao A et. al. “Ex vivo carbon monoxide prevents cytochrome P450 degradation and ischemia/reperfusion injury of kidney grafts”. Kidney International. 2008; 74:989-991
Natanson C, et. al. “Cell-free hemoglobin-based blood substitutes and risk of myocardial infarction and death: a metaanalysis”, JAMA. 2008 May 21;299(19):2304-12
Neto, J. S., Nakao, A. et al. (2004). “Protection of transplant-induced renal ischemia-reperfusion injury with carbon monoxide.” Am J Physiol Renal Physiol 287(5): F979-89.
Piantadosi CA: Biological chemistry of carbon monoxide. Antioxid Redox Signal 2002, 4:259-270.
Platt OS, Brambilla DJ, Rosse WF, et al. Mortality in sickle cell disease. Life expectancy and risk factors for early death. N Engl J Med. 1994;330(23):1639-1644.
Platt OS, Thorington BD, Brambilla DJ, et al. Pain in sickle cell disease. Rates and risk factors. N Engl J Med.
1991;325(1):11-16.
Rodkey FL, O'Neal JD, Collison HA, Uddin DE: Relative affinity of hemoglobin S and hemoglobin A for carbon monoxide and oxygen. Clin Chem 1974, 20:83-84.
Sirs, J. A. (1963). “The use of carbon monoxide to prevent sickle-cell formation.” Lancet 1(7288): 971-2.
Stein, A. B., Y. Guo, et al. (2005). “Administration of a CO-releasing molecule induces late preconditioning against myocardial infarction.” J Mol Cell Cardiol 38(1): 127-34.
Stewart RD. The effect of carbon monoxide on humans. Annu Rev Pharmacol 15: 409-423, 1975.
Stewart RD, Peterson JE, Baretta ED, Bachand RT, Hosko MJ, Herrmann AA: Experimental human exposure to carbon monoxide. Arch Environ Health 1970, 21:154-164.
Stuart, M. J. and R. L. Nagel (2004). “Sickle-cell disease.” Lancet 364(9442): 1343-60.
Stupfel M, Bouley G: Physiological and biochemical effects on rats and mice exposed to small concentrations of carbon monoxide for long periods. Ann N Y Acad Sci 1970, 174:342-368.
United States Patent Application 20100311657 Abuchowski; Abraham et al. “HEMOGLOBIN COMPOSITIONS” December 9, 2010
United States Patent Application 20090082257 Winslow; Robert M. “MalPEG-Hb conjugate-containing compositions for delivering carbon monoxide (CO) to cells” March 26, 2009
Van Meter KW: Carbon monoxide poisoning. In Emergency Medicine. Edited by Tintinalli JE, Kelen GD, Stapczynski JS. New York: McGraw Hill: New York; 2003:1238-1242.
Vandegriff, K. D., M. A. Young, et al. (2008). “CO-MP4, a polyethylene glycol-conjugated haemoglobin derivative and carbon monoxide carrier that reduces myocardial infarct size in rats.” Br J Pharmacol 154(8): 1649-61.
Weaver LK. Clinical Practice. Carbon monoxide poisoning. N Engl J Med 360: 1217-1225, 2009
Wu L, Wang R. Carbon monoxide: endogenous production, physiological functions, and pharmacological applications. Pharmacol Rev 57: 585-630, 2005.
Yallop, D., E. R. Duncan, et al. (2007). “The associations between air quality and the number of hospital admissions for acute pain and sickle-cell disease in an urban environment.” Br J Haematol 136(6): 844-8.
Zuckerbraun, B. S., C. A. McCIoskey, et al. (2005). “Carbón monoxide prevents múltiple organ injury in a model of hemorrhagic shock and resuscitation.” Shock 23(6): 527-32.
Claims (10)
1. Una composición líquida que comprende burbujas gaseosas disueltas o gaseosas atrapadas de monóxido de carbono (CO) en una cantidad de 30 mg/l o más para su uso en el tratamiento de un sujeto que padece o corre el riesgo de desarrollar una enfermedad tratable con CO; comprendiendo el uso administrar la composición líquida al sujeto por medio del tracto gastrointestinal (GI), donde la cantidad de CO es una cantidad suficiente para reducir o eliminar al menos un síntoma clínico de la enfermedad, prevenir el desarrollo o la recidiva de la enfermedad, limitar las morbilidades de la enfermedad, o curar la enfermedad, donde la enfermedad es una enfermedad hematológica.
2. Una composición líquida que comprende burbujas gaseosas disueltas o gaseosas atrapadas de monóxido de carbono (CO) en una cantidad de 30 mg/l o más para su uso según la reivindicación 1, donde la enfermedad hematológica es causada por una hemoglobina anormal.
3. Una composición líquida que comprende burbujas gaseosas disueltas o gaseosas atrapadas de monóxido de carbono (CO) en una cantidad de 30 mg/l o más para su uso según la reivindicación 2, donde la enfermedad es anemia de células falciformes, enfermedad de hemoglobina C, enfermedad de hemoglobina SC o beta-talasemia de hemoglobina S.
4. Una composición líquida que comprende burbujas gaseosas disueltas o gaseosas atrapadas de monóxido de carbono (CO) en una cantidad de 30 mg/l o más para su uso según cualquiera de las reivindicaciones 1-3, que comprende además al menos uno de: proteínas, lípidos, grasas, triglicéridos, carbohidratos complejos, azúcar, sustituto de azúcar artificial, zumo de frutas, carbohidratos, celulosa, fibra, ácido cítrico, saporíferos artificiales, saporíferos naturales, goma, pectina, ácido ascórbico, conservante, saponina, aceite, emulsión de aceite, y una sal.
5. Una composición líquida que comprende burbujas gaseosas disueltas o gaseosas atrapadas de monóxido de carbono (CO) en una cantidad de 30 mg/l o más para su uso según cualquiera de las reivindicaciones 1-4, donde el líquido comprende agua, etanol, o ambos.
6. Una composición líquida que comprende burbujas gaseosas disueltas o gaseosas atrapadas de monóxido de carbono (CO) en una cantidad de 30 mg/l o más para su uso según cualquiera de las reivindicaciones 1-5, donde la administración es por ingestión oral.
7. Una composición líquida que comprende burbujas gaseosas disueltas o gaseosas atrapadas de monóxido de carbono (CO) en una cantidad de 30 mg/l o más para su uso según cualquiera de las reivindicaciones 1-6, donde el volumen de la composición líquida administrada al día es de 2 litros o menos.
8. Una composición líquida que comprende burbujas gaseosas disueltas o gaseosas atrapadas de monóxido de carbono (CO) en una cantidad de 30 mg/l o más para su uso según cualquiera de las reivindicaciones 1-6, donde el volumen de la composición líquida administrada al día es de 1 litro o menos.
9. Una composición líquida que comprende burbujas gaseosas disueltas o gaseosas atrapadas de monóxido de carbono (CO) en una cantidad de 75 mg/l a 4000 mg/l para su uso según cualquiera de las reivindicaciones 1-8.
10. Una composición líquida que comprende burbujas gaseosas disueltas o gaseosas atrapadas de monóxido de carbono (CO) en una cantidad de 50 mg/l a 400 mg/l para su uso según cualquiera de las reivindicaciones 1-8.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201161432843P | 2011-01-14 | 2011-01-14 | |
| US201161434639P | 2011-01-20 | 2011-01-20 | |
| PCT/US2012/020710 WO2012096912A1 (en) | 2011-01-14 | 2012-01-10 | Solution of carbon monoxide for treatment of disease, including sickle cell disease |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2742829T3 true ES2742829T3 (es) | 2020-02-17 |
Family
ID=46507397
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES12734547T Active ES2742829T3 (es) | 2011-01-14 | 2012-01-10 | Solución de monóxido de carbono para el tratamiento de una enfermedad, incluida anemia de células falciformes |
Country Status (8)
| Country | Link |
|---|---|
| US (3) | US9980981B2 (es) |
| EP (2) | EP3583851A1 (es) |
| JP (1) | JP6118731B2 (es) |
| CN (2) | CN103491783A (es) |
| BR (1) | BR112013017933B1 (es) |
| CA (1) | CA2824056C (es) |
| ES (1) | ES2742829T3 (es) |
| WO (1) | WO2012096912A1 (es) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2742829T3 (es) | 2011-01-14 | 2020-02-17 | Los Angeles Childrens Hospital | Solución de monóxido de carbono para el tratamiento de una enfermedad, incluida anemia de células falciformes |
| CN107625954A (zh) * | 2016-07-19 | 2018-01-26 | 上海本素医药科技有限公司 | 含一氧化碳的血红蛋白制剂及其在抗炎症中的应用 |
| EP3804731A4 (en) * | 2018-06-08 | 2022-04-06 | Sumitomo Seika Chemicals Co., Ltd. | COMPOSITION FOR SKIN WOUNDS |
| WO2019235165A1 (ja) * | 2018-06-08 | 2019-12-12 | 住友精化株式会社 | 炎症性消化器官疾患用組成物 |
| US12370210B2 (en) | 2019-06-06 | 2025-07-29 | The General Hospital Corporation | Carbon monoxide as a treatment for neurodegenerative disease |
| WO2022055991A1 (en) * | 2020-09-08 | 2022-03-17 | The Brigham And Women's Hospital, Inc. | Therapeutic carbon monoxide formulations |
| CN119403560A (zh) * | 2022-06-23 | 2025-02-07 | 学校法人爱知医科大学 | 抑制腹膜劣化组合物、抑制腹膜劣化组合物试剂盒、腹膜透析液及腹膜透析液试剂盒 |
| CN119855493A (zh) | 2022-09-09 | 2025-04-18 | 巴伐利亚州尤利乌斯-马克西米利安-维尔茨堡大学 | 贮存器、一氧化碳释放装置、治疗系统、活细胞处理装置、治疗哺乳动物的方法以及一氧化碳 |
Family Cites Families (26)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5261875A (en) | 1991-02-14 | 1993-11-16 | Wayne State University | Method and apparatus for injection of gas hydrates |
| US5407426A (en) | 1991-02-14 | 1995-04-18 | Wayne State University | Method and apparatus for delivering oxygen into blood |
| US5086620A (en) | 1991-02-14 | 1992-02-11 | Wayne State University | Method of microencapsulation of hyperbaric gas |
| US6344489B1 (en) * | 1991-02-14 | 2002-02-05 | Wayne State University | Stabilized gas-enriched and gas-supersaturated liquids |
| US5569180A (en) | 1991-02-14 | 1996-10-29 | Wayne State University | Method for delivering a gas-supersaturated fluid to a gas-depleted site and use thereof |
| US8128963B2 (en) * | 1996-09-27 | 2012-03-06 | The Trustees Of Columbia University In The City Of New York | Methods for treating ischemic disorders using carbon monoxide |
| US5834519A (en) * | 1996-10-11 | 1998-11-10 | Wayne State University | Stabilized gas-supersaturated emulsions and suspensions |
| US7678390B2 (en) * | 1999-04-01 | 2010-03-16 | Yale University | Carbon monoxide as a biomarker and therapeutic agent |
| CA2451266A1 (en) * | 2001-06-21 | 2003-01-03 | Beth Israel Deaconess Medical Center Inc. | Carbon monoxide improves outcomes in tissue and organ transplants and suppresses apoptosis |
| CA2475209A1 (en) * | 2002-02-04 | 2003-08-14 | Alfama - Investigacao E Desenvolvimento De Produtos Farmaceuticos Lda. | Use of co-releasing compounds for the manufacture of a medicament for the treatment of inflammatory diseases |
| US7364757B2 (en) * | 2002-02-13 | 2008-04-29 | University Of Pittsburgh Of The Commonwealth System Of Higher Education | Methods of treating vascular disease |
| US7981448B2 (en) * | 2002-04-15 | 2011-07-19 | University Of Pittsburgh | Methods of treating necrotizing enterocolitis |
| ES2546280T3 (es) * | 2002-04-15 | 2015-09-22 | University Of Pittsburgh - Of The Commonwealth System Of Higher Education | Monóxido de carbono para su uso en un método para tratar íleo |
| MXPA04011113A (es) * | 2002-05-09 | 2005-02-14 | Univ Johns Hopkins | Monoxido de carbono en la forma de biomarcador y agente terapeutico. |
| EA200401622A1 (ru) * | 2002-06-05 | 2005-06-30 | Йейл Юниверсити | Способы лечения ангиогенеза, роста опухолей и метастазов |
| DE10230165A1 (de) * | 2002-07-04 | 2004-01-15 | Ino Therapeutics Gmbh | Verfahren und Vorrichtung zur Administration von Kohlenmonoxid |
| WO2004043341A2 (en) * | 2002-11-07 | 2004-05-27 | University Of Pittsburgh Of The Commonwealth System Of Higher Education | Treatment for hemorrhagic shock |
| US20080124436A1 (en) * | 2004-03-05 | 2008-05-29 | Eldon Roth | Method and apparatus for treating meat products with a treatment liquid containing carbon monoxide |
| CA2600927C (en) | 2005-03-07 | 2017-04-18 | Sangart, Inc. | Compositions and methods for delivering carbon monoxide (co) and nitric oxide (no) to tissue using heme proteins as carriers |
| US7976743B2 (en) * | 2006-10-16 | 2011-07-12 | Northwestern University | Gas-containing liposomes |
| JP2008179569A (ja) * | 2007-01-25 | 2008-08-07 | Tomohisa Takagi | 薬剤及び薬剤の適用方法 |
| WO2009120707A1 (en) * | 2008-03-24 | 2009-10-01 | Altus Pharmaceuticals Inc. | Uricase compositions and methods of use |
| CN101590228A (zh) * | 2008-05-26 | 2009-12-02 | 江苏大学附属医院 | 一氧化碳释放分子在制备早期治疗脓毒症药物中的应用 |
| DK2440239T3 (en) | 2009-06-09 | 2017-10-16 | Prolong Pharmaceuticals Llc | HEMOGLOBIN FORMATIONS |
| US8500104B2 (en) * | 2010-06-07 | 2013-08-06 | James Richard Spears | Pressurized liquid stream with dissolved gas |
| ES2742829T3 (es) | 2011-01-14 | 2020-02-17 | Los Angeles Childrens Hospital | Solución de monóxido de carbono para el tratamiento de una enfermedad, incluida anemia de células falciformes |
-
2012
- 2012-01-10 ES ES12734547T patent/ES2742829T3/es active Active
- 2012-01-10 CN CN201280007431.XA patent/CN103491783A/zh active Pending
- 2012-01-10 CN CN201910226268.XA patent/CN109925318A/zh active Pending
- 2012-01-10 US US13/979,510 patent/US9980981B2/en active Active
- 2012-01-10 JP JP2013549484A patent/JP6118731B2/ja active Active
- 2012-01-10 EP EP19173168.6A patent/EP3583851A1/en not_active Withdrawn
- 2012-01-10 BR BR112013017933-3A patent/BR112013017933B1/pt active IP Right Grant
- 2012-01-10 EP EP12734547.8A patent/EP2663193B1/en active Active
- 2012-01-10 CA CA2824056A patent/CA2824056C/en active Active
- 2012-01-10 WO PCT/US2012/020710 patent/WO2012096912A1/en not_active Ceased
-
2018
- 2018-04-26 US US15/963,446 patent/US10716806B2/en active Active
-
2020
- 2020-06-11 US US16/899,449 patent/US20200297757A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| BR112013017933A2 (pt) | 2016-07-12 |
| JP6118731B2 (ja) | 2017-04-19 |
| CA2824056C (en) | 2019-01-08 |
| JP2014508135A (ja) | 2014-04-03 |
| US10716806B2 (en) | 2020-07-21 |
| EP3583851A1 (en) | 2019-12-25 |
| US20200297757A1 (en) | 2020-09-24 |
| CN103491783A (zh) | 2014-01-01 |
| EP2663193A1 (en) | 2013-11-20 |
| US9980981B2 (en) | 2018-05-29 |
| CA2824056A1 (en) | 2012-07-19 |
| EP2663193A4 (en) | 2015-06-10 |
| WO2012096912A1 (en) | 2012-07-19 |
| BR112013017933B1 (pt) | 2021-02-23 |
| CN109925318A (zh) | 2019-06-25 |
| US20180303872A1 (en) | 2018-10-25 |
| US20130309279A1 (en) | 2013-11-21 |
| EP2663193B1 (en) | 2019-05-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2742829T3 (es) | Solución de monóxido de carbono para el tratamiento de una enfermedad, incluida anemia de células falciformes | |
| JP4585765B2 (ja) | 壊死性腸炎の治療方法 | |
| WO1995028906A1 (en) | Transfusion container, transfusion preparation, and comprehensive vitamin-containing high-calorie transfusion preparation | |
| ES2634142T3 (es) | Composición de nutrición parenteral que contiene hierro | |
| JP5939550B2 (ja) | 酸化型アルブミン低下剤 | |
| Zheng et al. | Acute effects of peritoneal dialysis solutions on appetite in non-uremic rats | |
| CN106031710A (zh) | 一种富马酸氟呐普拉赞的注射剂及其制备方法 | |
| WO2023137178A1 (en) | Combinations of vitamin d3, niacinamide and lipoic acid for use in the maintenance of healthy blood glucose levels | |
| CN109069532A (zh) | 含铬组合物用于改善健康和健身 | |
| US20080051373A1 (en) | Parenteral preparations of GI-safer phospholipid-associated anti-inflammatories and methods of preparation and use | |
| BRPI0915744A2 (pt) | composição nutriente, forma bde dosagem e método de uso da mesma | |
| WO2015107241A1 (es) | Formulación de sales de rehidratación liposomal | |
| JPH03284620A (ja) | 腸管洗浄用組成物 | |
| JP4011594B2 (ja) | 安定性及び生物学的利用率が高められた複合体及びその製造方法 | |
| JP5823131B2 (ja) | 防風通聖散含有組成物 | |
| JPH04198126A (ja) | 腸管洗浄用液剤 | |
| EP2068833B1 (en) | Parenteral preparations of gi-safer phospholipid-associated anti-inflammatories and methods of preparation and use | |
| JPH08709A (ja) | 輸液入り容器、輸液製剤及びビタミン配合総合高カロリー輸液製剤 | |
| BR112020004453B1 (pt) | Composição para suplementação de cálcio | |
| Rajendran et al. | Study on the effective supplementation of Aloe vera gel antacid to peptic ulcer patients | |
| WO2023033750A1 (en) | Preservative free liquid formulation of lipozomal iron | |
| EP4629847A1 (en) | Compositions for pre-surgical nutritional supplements | |
| ES2943432A2 (es) | Composiciones que contienen una sal mineral para uso oral | |
| BR102021017964A2 (pt) | Solubilização de ativos farmacêuticos utilizando plasmas eutéticos | |
| Papadopoulos | Osmolality of electrolyte infusions. |