ES2760264T3 - Compuestos herbicidas de piridazinona - Google Patents
Compuestos herbicidas de piridazinona Download PDFInfo
- Publication number
- ES2760264T3 ES2760264T3 ES15739220T ES15739220T ES2760264T3 ES 2760264 T3 ES2760264 T3 ES 2760264T3 ES 15739220 T ES15739220 T ES 15739220T ES 15739220 T ES15739220 T ES 15739220T ES 2760264 T3 ES2760264 T3 ES 2760264T3
- Authority
- ES
- Spain
- Prior art keywords
- alkyl
- alkoxy
- compound
- halogen
- haloalkyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 CC1(*)C=C(CO/C2=C/*(*)/C=C/C(*)/C=C2\C(C(N(*)N=C2*)=O)=C2O)C=CC=C1 Chemical compound CC1(*)C=C(CO/C2=C/*(*)/C=C/C(*)/C=C2\C(C(N(*)N=C2*)=O)=C2O)C=CC=C1 0.000 description 1
- CTFVYMARONBICU-ZVHZXABRSA-N CCOC(/C(/C)=N/N(C)C(Cc(c(Cl)ccc1Cl)c1OCc1ccccc1)=O)=O Chemical compound CCOC(/C(/C)=N/N(C)C(Cc(c(Cl)ccc1Cl)c1OCc1ccccc1)=O)=O CTFVYMARONBICU-ZVHZXABRSA-N 0.000 description 1
- UEMDTQCVOKUEAI-UHFFFAOYSA-N OC(Cc(c(Cl)ccc1Cl)c1OCc1ccccc1)=O Chemical compound OC(Cc(c(Cl)ccc1Cl)c1OCc1ccccc1)=O UEMDTQCVOKUEAI-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D237/00—Heterocyclic compounds containing 1,2-diazine or hydrogenated 1,2-diazine rings
- C07D237/02—Heterocyclic compounds containing 1,2-diazine or hydrogenated 1,2-diazine rings not condensed with other rings
- C07D237/06—Heterocyclic compounds containing 1,2-diazine or hydrogenated 1,2-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members
- C07D237/10—Heterocyclic compounds containing 1,2-diazine or hydrogenated 1,2-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D237/14—Oxygen atoms
- C07D237/16—Two oxygen atoms
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/48—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with two nitrogen atoms as the only ring hetero atoms
- A01N43/58—1,2-Diazines; Hydrogenated 1,2-diazines
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Dentistry (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Plant Pathology (AREA)
- General Health & Medical Sciences (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- Pest Control & Pesticides (AREA)
- Agronomy & Crop Science (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
Un compuesto de fórmula (I)**Fórmula** (I), o una sal o N-óxido del mismo, R1 se selecciona del grupo que consiste en alquilo C1-C4, cicloalquilo C3-C6, alcoxi C3-C6, alcoxi C1-C2-alquilo C1-C2, alquenilo C2-C4, haloalquilo C1-C4, cianoalquilo C1-C4, haloalquenilo C2-C4, alquinilo C2-C4 y haloalquinilo C2-C4; R2 se selecciona del grupo que consiste en hidrógeno, halógeno, ciano, alquilo C1-C6, haloalquilo C1-C6, haloalcoxi C1-C6, haloalcoxi C1-C3-alquilo C1-C3-, alcoxi C1-C6, alcoxi C1-C3-alquilo C1-C3, alcoxi C1-C3-alcoxi C1-C3-alquilo C1- C3-, cicloalquilo C3-C6, alquenilo C2-C6, haloalquenilo C2-C6, alquinilo C2-C6, hidroxialquilo C1-C6-, alquilcarbonilo C1- C6-, alquil C1-C6-S(O)m-, amino, alquilamino C1-C6, dialquilamino C1-C6, -C(alquil C1-C3)=N-O-alquilo C1-C3 y haloalquinilo C2-C6; G es hidrógeno o C(O)R3; X e Y cada uno es independientemente hidrógeno, alquilo C1-C3, alcoxi C1-C3, haloalquilo C1-C3, haloalcoxi C1-C3 o halógeno; Z es alquilo C1-C3, alcoxi C1-C3, haloalquilo C1-C3, haloalcoxi C1-C3 o halógeno; m es un número entero de 0, 1 o 2; n es un número entero de 0, 1, 2, 3, 4 o 5; R3 se selecciona del grupo que consiste en alquilo C1-C6, alcoxi C1-C6, alquenilo C1-C6, alquinilo C1-C6, alquil C1-C6- S-, -NR4R5 y fenilo opcionalmente sustituido con uno o más R6; R4 y R5 se seleccionan independientemente del grupo que consiste en alquilo C1-C6 y alcoxi C1-C6, o R4 y R5 juntos pueden formar un anillo de morfolinilo; y, R6 se selecciona del grupo que consiste en halógeno, ciano, nitro, alquilo C1-C3, haloalquilo C1-C3, alcoxi C1-C3 y haloalcoxi C1-C3.
Description
DESCRIPCIÓN
Compuestos herbicidas
La presente invención se refiere a derivados de fenil-piridazina-diona benciloxi-sustituidos y fenil-piridazinona benciloxi-sustituidos herbicidas de fórmula (I), así como a procesos e intermedios usados para la preparación de dichos derivados. La invención se refiere además a composiciones herbicidas que comprenden dichos derivados, así como al uso de dichos compuestos y composiciones en el control del crecimiento de plantas indeseables; en particular el uso en el control de malas hierbas, tales como malas hierbas dicotiledóneas latifolias, en cultivos de plantas útiles.
Las piridazinonas herbicidas se conocen del documento WO 2009/086041 y el documento WO 2014/119770. Además, las piridazinonas heterociclil-sustituidas de 5/6 miembros herbicidas se conocen del documento WO 2011/045271. Mientras que el documento WO 2013/160126 describe derivados de indolil-piridazinona, que muestran actividad herbicida. El documento WO 2009/035150 y el documento WO 2010/104217 describe herbicidas de fenil-piridazinona 2-alquil C1-C6- o 2-alcoxi C1-C6-sustituida. El documento WO 2014/119770 describe fenil-piridazinonas sustituidas herbicidas, en las que el grupo fenilo comprende un arilo condensado mono- o bicíclico unido a éter en la posición para.
La presente invención se basa en el hallazgo de que los derivados de fenil-piridazina-diona benciloxi-sustituidos y fenil-piridazinona benciloxi-susituidos de fórmula (I) muestran actividad herbicida sorprendentemente buena.
Por tanto, en un primer aspecto se proporciona un compuesto de fórmula (I)
haloalquilo C1-C4, cianoalquilo C1-C4, haloalquenilo C2-C4, alquinilo C2-C4 y haloalquinilo C2-C4; R2 se selecciona del grupo que consiste en hidrógeno, halógeno, ciano, alquilo C1-C6, haloalquilo C1-C6, haloalcoxi C1-C6, haloalcoxi C1-C3-alquilo C1-C3-, alcoxi C1-C6, alcoxi C1-C3-alquilo C1-C3, alcoxi C1-C3-alcoxi C1-C3-alquilo C1-C3-, cicloalquilo C3-C6, alquenilo C2-C6, haloalquenilo C2-C6, alquinilo C2-C6, hidroxialquilo C1-C6-, alquil C1-C6carbonilo-, -S(O)malquilo C1-C6, amino, alquilamino C1-C6, dialquilamino C1-C6, -C(alquil C1-C3)=N-O-alquilo C1-C3 y haloalquinilo C2-C6; G es hidrógeno o C(O)R3; X e Y son cada uno independientemente hidrógeno, alquilo C1-C3, alcoxi C1-C3, haloalquilo C1-C3, haloalcoxi C1-C3 o halógeno; Z es alquilo C1-C3, alcoxi C1-C3, haloalquilo C1-C3, haloalcoxi C1-C3 o halógeno; m es un número entero de 0, 1 o 2; n es un número entero de 0, 1, 2, 3, 4 o 5; R3 se selecciona del grupo que consiste en alquilo C1-C6, alquenilo C1-C6, alquinilo C1-C6, alquinil C1-C6-S-, -NR4R5 y fenilo opcionalmente sustituido con uno o más R6; R4 y R5 se seleccionan independientemente del grupo que consiste en alquilo C1-C6 y alcoxi C1-C6, o R4 y R5 juntos pueden formar un anillo de morfolinilo; y R6 se selecciona del grupo que consiste en halógeno, ciano, nitro, alquilo C1-C3, haloalquilo C1-C3, alcoxi C1-C3 y haloalcoxi C1-C3.
Los compuestos de fórmula (I) pueden contener centros asimétricos y pueden estar presentes como un enantiómero individual, pares de enantiómeros en cualquier proporción o, cuando hay más de un centro asimétrico presente, contienen diaestereoisómeros en todos los cocientes posibles. Habitualmente, uno de los enantiómeros tiene una actividad biológica potenciada en comparación con las otras posibilidades.
Asimismo, cuando hay alquenos disustituidos, estos pueden estar presentes en forma E o Z o como mezclas de ambas en cualquier proporción.
Además, los compuestos de fórmula (I) pueden estar en equilibrio con formas tautoméricas alternativas. Por ejemplo, un compuesto de fórmula (I-i), es decir, un compuesto de fórmula (I) en la que R2 es hidrógeno y G es hidrógeno, puede dibujarse en al menos tres formas tautoméricas:
Se apreciará que todas las formas tautoméricas (tautómeros individuales o mezclas de los mismos), mezclas racémicas e isómeros individuales están incluidos dentro del alcance de la presente invención.
Cada resto alquilo, en solitario o como parte de un grupo más grande (tal como alcoxi, alquiltio, alcoxicarbonilo, alquilcarbonilo, alquilaminocarbonilo o dialquilaminocarbonilo, etc.), puede ser de cadena lineal o ramificado. Típicamente, el alquilo es, por ejemplo, metilo, etilo, n-propilo, isopropilo, n-butilo, sec-butilo, isobutilo, ferc-butilo, npentilo, neopentilo o n-hexilo. Los grupos alquilo en general son grupos alquilo C1-C6 (excepto cuando ya se han definido en sentido más estricto), pero son preferibleme
nte grupos alquilo C1-C4 o alquilo C1-C3 y, más preferiblemente, son grupos alquilo C1-C2 (tal como metilo).
Los restos alquenilo y alquinilo pueden estar en forma de cadenas lineales o ramificadas, y los restos alquenilo, cuando sea apropiado, pueden estar en la configuración (E) o (Z). Los restos alquenilo o alquinilo son típicamente alquenilo C2-C4 o alquinilo C2-C4, más específicamente vinilo, alilo, etinilo, propargilo o prop-1-inilo. Los restos alquenilo y alquinilo pueden contener uno o más dobles y/o triples enlaces en cualquier combinación; pero preferiblemente contienen solamente un doble enlace (para alquenilo) o solamente un triple enlace (para alquinilo).
Preferiblemente, el término cicloalquilo se refiere a ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo.
En el contexto de la presente memoria descriptiva, el término "arilo" preferiblemente significa fenilo. El término "heteroarilo", como se usa en este documento, significa un sistema de anillo aromático que contiene al menos un heteroátomo en el anillo y consiste en un anillo individual. Preferiblemente, los anillos individuales contendrán 1,2 o 3 heteroátomos en el anillo, seleccionados independientemente de nitrógeno, oxígeno y azufre. Típicamente, "heteroarilo" es furilo, tienilo, pirrolilo, pirazolilo, imidazolilo, 1,2,3-triazolilo, 1,2,4-triazolilo, oxazolilo, isoxazolilo, tiazolilo, isotiazolilo, 1,2,4-oxadiazolilo, 1,3,4-oxadiazolilo, 1,2,5-oxadiazolilo, 1,2,3-tiadiazolilo, 1,2,4-tiadiazolilo, 1,3,4-tiadiazolilo, 1,2,5-tiadiazolilo, piridilo, pirimidinilo, piridazinilo, pirazinilo, 1,2,3-triazinilo, 1,2,4-triazinilo o 1,3,5-triazinilo.
Los grupos heterociclilo y anillos heterocíclicos (en solitario o como parte de un grupo más grande, tal como heterociclilalquilo-) son sistemas de anillo que contienen al menos un heteroátomo y pueden estar en forma mono- o bicíclica. Preferiblemente, los grupos heterociclilo contendrán hasta dos heteroátomos que se elegirán preferiblemente de nitrógeno, oxígeno y azufre. Ejemplos de grupos heterocíclicos incluyen oxetanilo, tietanilo, azetidinilo y 7-oxabiciclo[2.2.1]hept-2-ilo. Los grupos heterociclilo que contienen un solo átomo de oxígeno como heteroátomo son los más preferidos. Los grupos heterociclilo son preferiblemente anillos de 3 a 8 miembros, más preferiblemente de 3 a 6 miembros.
Halógeno (o halo) abarca flúor, cloro, bromo o yodo. Lo mismo se aplica correspondientemente a halógeno en el contexto de otras definiciones, tales como haloalquilo o halofenilo.
Los grupos haloalquilo que tienen una longitud de cadena de 1 a 6 átomos de carbono son, por ejemplo, fluorometilo, difluorometilo, trifluorometilo, clorometilo, diclorometilo, triclorometilo, 2,2,2-trifluoroetilo, 2-fluoroetilo, 2-cloroetilo, pentafluoroetilo, 1,1 -difluoro-2,2,2-tricloroetilo, 2,2,3,3-tetrafluoroetilo y 2,2,2-tricloroetilo, heptafluoro-n-propilo y perfluoro-n-hexilo.
Los grupos alcoxi tienen preferiblemente una longitud de cadena de 1 a 6 átomos de carbono. Alcoxi es, por ejemplo, metoxi, etoxi, propoxi, isopropoxi, n-butoxi, isobutoxi, sec-butoxi o ferc-butoxi o un isómero de pentiloxi o hexiloxi, preferiblemente metoxi y etoxi. Debe apreciarse que dos sustituyentes alcoxi pueden estar presentes en el mismo átomo de carbono.
Haloalcoxi es, por ejemplo, fluorometoxi, difluorometoxi, trifluorometoxi, 2,2,2-trifluoroetoxi, 1,1,2,2-tetrafluoroetoxi, 2-fluoroetoxi, 2-cloroetoxi, 2,2-difluoroetoxi o 2,2,2-tricloroetoxi, preferiblemente difluorometoxi, 2-cloroetoxi o trifluorometoxi.
Alquil C1-C6-S- (alquiltio) es, por ejemplo, metiltio, etiltio, propiltio, isopropiltio, n-butiltio, isobutiltio, sec-butiltio o ferc-butiltio, preferiblemente metiltio o etiltio.
Alquil Ci-C6-S(O)- (alquilsulfinilo) es, por ejemplo, metilsulfinilo, etilsulfinilo, propilsulfinilo, isopropiisulfinilo, n-butilsulfinilo, isobutilsulfinilo, sec-butilsulfinilo o ferc-butilsulfinilo, preferiblemente metilsulfinilo o etilsulfinilo.
Alquil Ci-C6-S(O)2- (alquilsulfonilo) es, por ejemplo, metilsulfonilo, etilsulfonilo, propilsulfonilo, isopropilsulfonilo, nbutilsulfonilo, isobutilsulfonilo, sec-butilsulfonilo o ferc-butilsulfonilo, preferiblemente metilsulfonilo o etilsulfonilo.
El grupo Q
(Q) se denomina en este documento como el resto de piridazina-diona/piridazinona, en el que B indica el punto de adhesión del resto de la molécula (es decir, al resto de benzoiloxi-fenilo opcionalmente sustituido).
La presente invención también incluye sales agronómicamente aceptables que los compuestos de fórmula (I) pueden formar con aminas (por ejemplo, amoniaco, dimetilamina y trietilamina), bases de metales alcalinos y metales alcalinotérreos o bases de amonio cuaternario. Entre los hidróxidos, óxidos, alcóxidos, hidrogenocarbonatos y carbonatos de metales alcalinos y metales alcalinotérreos usados como formadores de sales, cabe destacar los hidróxidos, alcóxidos, óxidos y carbonatos de litio, sodio, potasio, magnesio y calcio, pero especialmente los de sodio, magnesio y calcio. También puede usarse la sal de trimetilsulfonio correspondiente. Los compuestos de fórmula (I) de acuerdo con la invención también incluyen hidratos que pueden formarse durante la formación de sales.
Valores preferidos de R1, R2, R3, R4, R5, R6, G, X, Y, Z, m y n son como se exponen a continuación, y un compuesto de fórmula (I) de acuerdo con la invención puede comprender cualquier combinación de dichos valores. Los expertos en la materia apreciarán que los valores para cualquier conjunto especificado de realizaciones pueden combinarse con valores para cualquier otro conjunto de realizaciones donde dichas combinaciones no son mutuamente excluyentes.
Preferiblemente, R1 se selecciona del grupo que consiste en metilo, etilo, propilo (en particular n- o c-propilo), propargilo o haloalquilo C1. Más preferiblemente, R1 es metilo, etilo, ciclopropilo, propargilo o fluoroalquilo C1. Más preferiblemente aún, R1 es metilo, etilo, ciclopropilo o propargilo.
Preferiblemente, R2 se selecciona del grupo que consiste en hidrógeno, alquilo C1-C6, haloalquilo C1-C6, alcoxi C1-C6, alcoxi C1-C3-alquilo C1-C3, cicloalquilo C3-C6, alquenilo C2-C6, haloalquenilo C2-C6, alquinilo C2-C6 y haloalquinilo C2-C6. Más preferiblemente, R2 se selecciona del grupo que consiste en metilo, etilo, ciclopropilo, trifluorometilo y metoximetilo, más preferiblemente aún, ciclopropilo, trifluorometilo o metilo, mucho más preferiblemente ciclopropilo o metilo. En un conjunto de realizaciones de la presente invención, R2 es hidrógeno. En un conjunto adicional de realizaciones, R2 es ciclopropilo, en un tercer conjunto de realizaciones, R2 es metilo y en un cuarto conjunto de realizaciones, R2 es trifluorometilo.
Como se describe en este documento, G puede ser hidrógeno o -C(O)-R3, y R3 se selecciona del grupo que consiste en alquilo C1-C6, alquenilo C2-C6, alquinilo C2-C6, alquil C1-C6-S-, alcoxi C1-C6, -NR4R5 y fenilo opcionalmente sustituido con uno o más R6. Como se define en este documento, R4 y R5 se seleccionan independientemente del grupo que consiste en alquilo C1-C6, alcoxi C1-C6-; o juntos pueden formar un anillo de morfolinilo. Preferiblemente, R4 y R5 cada uno se selecciona independientemente del grupo que consiste en metilo, etilo, propilo, metoxi, etoxi y propoxi. R6 se selecciona del grupo que consiste en halógeno, ciano, nitro, alquilo C1-C3, haloalquilo C1-C3, alcoxi C1-C3 y haloalcoxi C1-C3.
Preferiblemente, R3 es alquilo C1-C4, alquenilo C2-C3, alquinilo C2-C3, -alcoxi C1-C3 o -NR4R5, en el que R4 y R5 juntos forman un anillo de morfolinilo. Más preferiblemente, R3 es isopropilo, f-butilo, metilo, etilo, propargilo y metoxi.
En un conjunto de realizaciones, G es hidrógeno o -C(O)-R3, en el que R3 es alquilo C1-C4, alquenilo C2-C3, alquinilo C2-C3 o -alcoxi C1-C3. En un conjunto adicional de realizaciones, G es hidrógeno o -C(O)-R3, en el que R3 es isopropilo, f-butilo, metilo, etilo, propargilo o metoxi. Sin embargo, es particularmente preferido que G sea hidrógeno.
X es preferiblemente hidrógeno, halógeno o haloalquilo C1, más preferiblemente, hidrógeno, flúor, cloro, bromo o fluoroalquilo C1 y más preferiblemente aún, hidrógeno, flúor, cloro o trifluorometilo. En un conjunto de realizaciones, se prefiere que X esté orfo con respecto al resto piridazinona/piridazina-diona (grupo Q). Es particularmente preferido que X sea flúor, cloro o haloalquilo C1 (en particular, fluoroalquilo C1) y esté orfo con respecto al resto piridazinona/piridazina-diona (grupo Q).
Y es preferiblemente hidrógeno, alquilo C1-C3, haloalquilo C1-C3 o halógeno. Más preferiblemente, Y es hidrógeno, cloro, flúor o bromo.
En un conjunto de realizaciones, se prefiere que Y esté orto con respecto al resto benciloxi. En un conjunto adicional de realizaciones, Y está para con respecto al resto piridazinona/piridazina-diona (grupo Q).
Es particularmente preferido que Y esté orto con respecto al resto benciloxi y sea halógeno, en particular cloro o flúor; más preferiblemente cloro.
Como se describe en este documento, Z puede ser alquilo C1-C3, alcoxi C1-C3, haloalquilo C1-C3, haloalcoxi C1-C3 o halógeno y n es un número entero de 0, 1, 2, 3, 4 o 5. Por consiguiente, el resto bencilo de fórmula (I) puede representarse de la siguiente manera, en la que p indica el punto de adhesión al resto de la molécula mediante el enlace éter:
Preferiblemente, cada radical Z se selecciona independientemente de halógeno (en particular cloro), metilo, metoxi y trifluorometilo. Más preferiblemente, cada radical Z es independientemente halógeno (en particular cloro) o metoxi. Se prefiere que n sea 0, 1 o 2. Cuando n es 1, se prefiere que Z esté para con respecto al conector metoxi (es decir, Z está en la posición Z3). Cuando n es 2, se prefiere que un sustituyente esté para y el otro esté meta con respecto al conector metoxi (es decir, un radical Z estará en posición Z2 o Z4, y el otro radical Z estará en posición Z3).
En un conjunto particularmente preferido de realizaciones, n es 0 (es decir, las posiciones Z1, Z2, Z3, Z4 y Z5 tienen todas hidrógeno).
En un conjunto particularmente preferido adicional de realizaciones, n es 2 y cada Z es independientemente halógeno, preferiblemente cada Z es cloro.
En un conjunto particularmente preferido adicional de realizaciones, n es 1, Z está para con respecto al conector metoxi y es metoxi (es decir, Z3 es metoxi, Z1, Z2, Z4 y Z5 tienen todos hidrógeno).
La tabla 1 a continuación proporciona 87 ejemplos específicos de compuestos de fórmula (I) de la invención.
TABLA 1 Compuestos herbicidas de la presente invención.
En la estructura anterior, el sistema de numeración usado para Indicar la posición de X e Y se muestra con fines de claridad únicamente.
Los compuestos de la presente invención pueden prepararse de acuerdo con los siguientes esquemas, en que los sustituyentes R1, R2, R3, R4, R5, R6, G, X, Y, Z, m y n tienen (salvo que se indique otra cosa de forma explícita) las definiciones descritas anteriormente en este documento.
Determinados compuestos (1) de la presente invención pueden prepararse a partir de compuestos de fórmula (2) como se muestra en el esquema de reacción 1.
Esquema de reacción 1
Los compuestos de fórmula (1) pueden prepararse por tratamiento de compuestos de éster (2) con 1,8-diazabiciclo[5.4.0]undec-7-eno (DBU) en disolvente acetonitrilo, a una temperatura entre 100 y 150 °C. Puede usarse calentamiento por microondas o calentamiento convencional.
Los compuestos de fórmula (2) pueden prepararse a partir de compuestos de fórmulas (3) y (4) como se muestra en el esquema de reacción 2.
Esquema de reacción 2
Los compuestos de fórmula (2) pueden prepararse por /V-acilación de hidrazonas (4) con el derivado de cloruro de acilo de compuestos (3), en presencia de una base adecuada y disolvente, a una temperatura entre 0 y 25 °C. El cloruro de acilo se preforma por tratamiento de ácidos (3) con cloruro de oxalilo en un disolvente adecuado, opcionalmente con inclusión de W,W-dimetilformamida como catalizador, a una temperatura entre 0 y 50 °C. Ejemplos de bases adecuadas son trietilamina o diisopropiletilamina. Ejemplos de disolventes adecuados son diclorometano y cloroformo.
Los compuestos de fórmula (4) pueden prepararse por condensación de a-ceto ésteres con hidrazinas como se muestra en el esquema de reacción 3.
.
Esquema de reacción 4
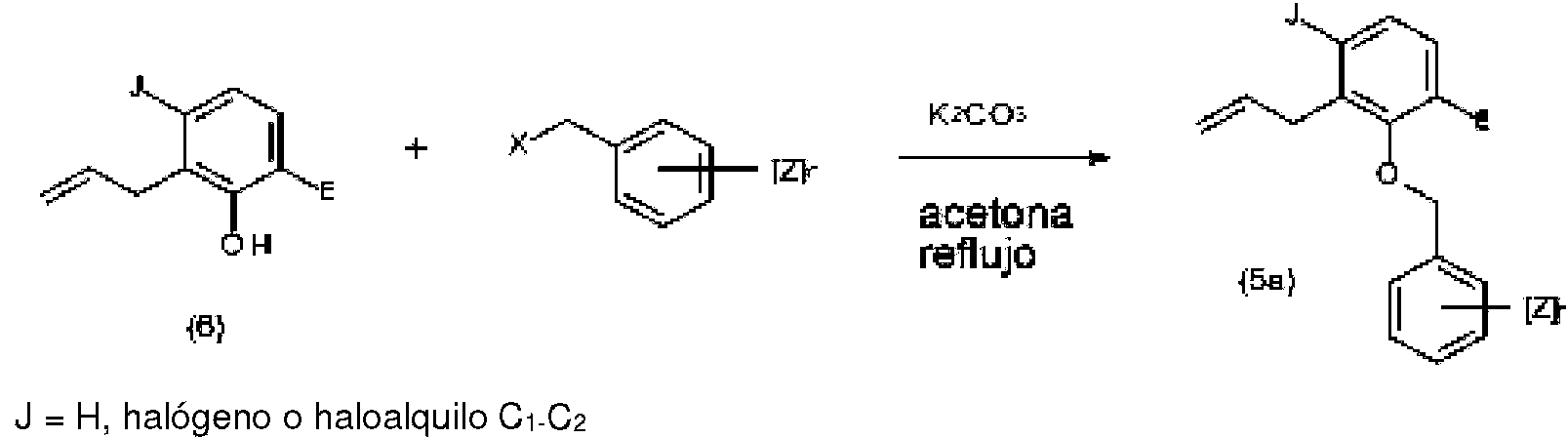
Determinados compuestos de olefina (5), específicamente el subconjunto (5a), pueden prepararse por O-alquilación de 2-alil-fenoles (6) con un compuesto de haluro de bencilo, como se muestra en el esquema de reacción 5.
Esquema de reacción 5
E = halógeno
X = halógeno
Con referencia al esquema de reacción 5, muchos haluros de bencilo están disponibles en el mercado. Un ejemplo es bromuro de bencilo. Los 2 -alil-fenoles (6) pueden prepararse como se muestra en el esquema de reacción 6.
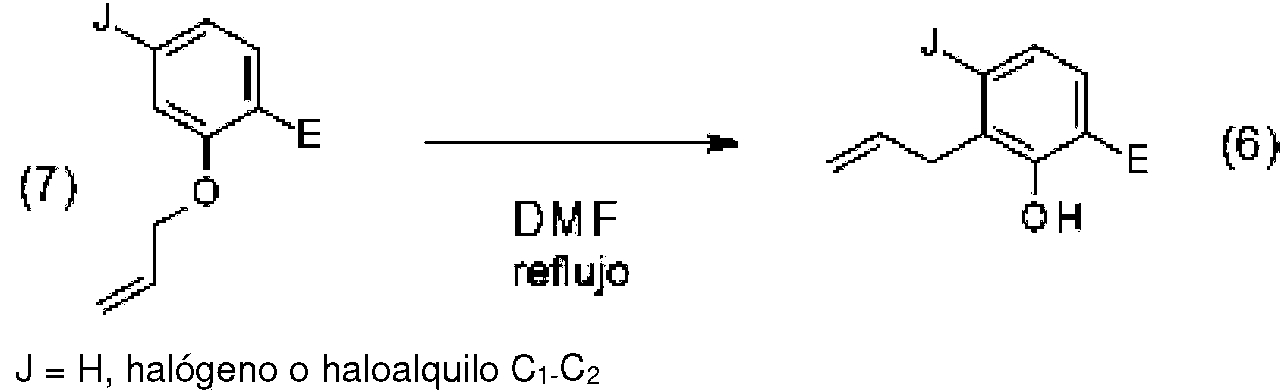
Esquema de reacción 6
E = halógeno
Con referencia al esquema de reacción 6 , un ejemplo de compuestos (7) es 2-aliloxi-1,4-dicloro-benceno, preparado de acuerdo con J. Chem. Soc., Perkin Trans.2 , 2001,1824. Otros compuestos (7) pueden sintetizarse de forma similar, de acuerdo con el esquema de reacción 7.
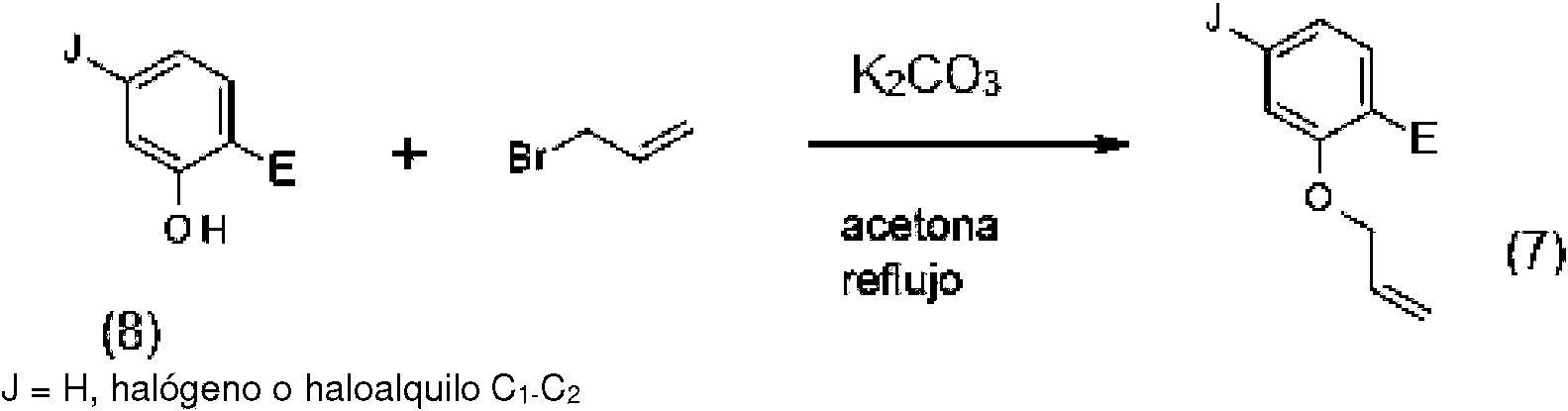
Esquema de reacción 7
E = halógeno
Con referencia al esquema de reacción 7, muchos compuestos de fenol (8) están disponibles en el mercado. Ejemplos incluyen 2,5-diclorofenol y 2-cloro-5-fluorofenol.
Los compuestos de fórmula (I) de acuerdo con la invención pueden usarse como herbicidas por sí mismos, pero generalmente se formulan en composiciones herbicidas usando adyuvantes de formulación, tales como vehículos, disolventes y agentes tensioactivos (AT). Por tanto, la presente invención proporciona además una composición herbicida que comprende un compuesto herbicida de acuerdo con una cualquiera de las reivindicaciones previas y un adyuvante de formulación agronómicamente aceptable. La composición puede estar en forma de concentrados que se diluyen antes de usarlos, aunque también se pueden preparar composiciones listas para usar. La dilución final se suele hacer con agua, pero se puede hacer, en lugar de con agua, o además de con esta, con, por ejemplo, fertilizantes líquidos, micronutrientes, organismos biológicos, aceite o disolventes.
Las composiciones herbicidas generalmente comprenden de un 0,1 a un 99 % en peso, especialmente de un 0,1 a un 95 % en peso, de compuestos de fórmula I, y de un 1 a un 99,9 % en peso de un adyuvante de formulación que incluye preferiblemente de un 0 a un 25 % en peso de una sustancia tensioactiva.
Las composiciones se pueden elegir entre varios tipos de formulaciones, muchas de las cuales se describen en el Manual Sobre el Desarrollo y el Uso de las Especificaciones para Productos para la Protección de Plantas de la FAO, 5.a edición, 1999. Estas incluyen polvos espolvoreables (PE), polvos solubles (PS), gránulos solubles en agua (GS),
gránulos dispersables en agua (GD), polvos humectables (PH), gránulos (GR) (de liberación lenta o rápida), concentrados solubles (SL), líquidos miscibles en aceite (LAc), líquidos de volumen ultrabajo (LU), concentrados emulsionables (CE), concentrados dispersables (CD), emulsiones (tanto de aceite en agua (EAg) como de agua en aceite (EAc)), microemulsiones (ME), concentrados en suspensión (CS), aerosoles, suspensiones de cápsulas (SC) y formulaciones para el tratamiento de semillas. El tipo de formulación elegido en cualquier caso dependerá del objetivo específico previsto y de las propiedades físicas, químicas y biológicas del compuesto de fórmula (I).
Los polvos espolvoreables (PE) se pueden preparar mezclando un compuesto de fórmula (I) con uno o más diluyentes sólidos (por ejemplo, arcillas naturales, caolín, pirofilita, bentonita, alúmina, montmorillonita, diatomita, carbonato de calcio, tierras diatomeas, fosfatos de calcio, carbonatos de calcio y magnesio, azufre, cal, harinas, talco y otros vehículos sólidos orgánicos e inorgánicos) y moliendo mecánicamente la mezcla hasta un polvo fino.
Los polvos solubles (PS) se pueden preparar mezclando un compuesto de fórmula (I) con una o más sales inorgánicas solubles en agua (tales como bicarbonato de sodio, carbonato de sodio o sulfato de magnesio) o uno o más sólidos orgánicos solubles en agua (tales como polisacáridos) y, opcionalmente, uno o más agentes humectantes, uno o más agentes dispersantes o una mezcla de dichos agentes para mejorar la dispersibilidad/solubilidad en agua. A continuación, la mezcla se muele hasta obtener un polvo fino. También se pueden granular composiciones similares para formar gránulos solubles en agua (GS).
Los polvos humectables (PH) se pueden preparar mezclando el compuesto de fórmula (I) con uno o más diluyentes o vehículos sólidos, uno o más agentes humectantes y, preferiblemente, uno o más agentes dispersantes y, opcionalmente, uno o más agentes de suspensión para facilitar la dispersión en líquidos. A continuación, la mezcla se muele hasta obtener un polvo fino. También se pueden granular composiciones similares para formar gránulos dispersables en agua (GD).
Los gránulos (GR) se pueden formar granulando una mezcla de un compuesto de fórmula (I) y uno o más diluyentes o vehículos sólidos en polvo, o a partir de gránulos sin tratar preformados por absorción de un compuesto de fórmula (I) (o una solución del mismo, en un agente adecuado) en un material granular poroso (tal como piedra pómez, arcillas de atapulgita, tierra de batán, diatomita, tierras diatomeas o mazorcas de maíz molidas) o adsorbiendo el compuesto de fórmula (I) (o una solución del mismo, en un agente adecuado) sobre un material central duro (tal como arenas, silicatos, carbonatos minerales, sulfatos o fosfatos) y secando si fuera necesario. Los agentes que se usan habitualmente para facilitar la absorción o adsorción incluyen disolventes (tales como alcoholes, éteres, cetonas, ésteres y disolventes del petróleo aromáticos y alifáticos) y agentes aglutinantes (tales como poli(acetatos de vinilo), poli(alcoholes vinílicos), dextrinas, azúcares y aceites vegetales). También se pueden incluir uno o más aditivos diferentes en los gránulos (por ejemplo, un agente emulsionante, agente humectante o agente dispersante).
Los concentrados dispersables (CD) se pueden preparar disolviendo un compuesto de fórmula (I) en agua o un disolvente orgánico tal como una cetona, alcohol o éter glicólico. Estas soluciones pueden contener un agente tensioactivo (por ejemplo, para mejorar la dilución en agua o evitar la cristalización en un depósito de pulverización).
Los concentrados emulsionables (CE) o las emulsiones de aceite en agua (EAg) se pueden preparar disolviendo un compuesto de fórmula (I) en un disolvente orgánico (que contenga opcionalmente uno o más agentes humectantes, uno o más agentes emulsionantes o una mezcla de dichos agentes). Disolventes orgánicos adecuados para su uso en CE incluyen hidrocarburos aromáticos (tales como alquilbencenos o alquilnaftalenos, por ejemplo, SOLVESSO 100, SOLVESSO 150 y SOLVESSO 200; SOLVESSO es una marca comercial registrada), cetonas (tales como ciclohexanona o metilciclohexanona) y alcoholes (tales como alcohol bencílico, alcohol furfurílico o butanol), N-alquilpirrolidonas (tales como N-metilpirrolidona o N-octilpirrolidona), dimetilamidas de ácidos grasos (tales como dimetilamida de un ácido graso C8-C10) e hidrocarburos clorados. Un producto de tipo CE puede emulsionar espontáneamente al añadir agua, para producir una emulsión con una estabilidad suficiente para permitir la aplicación por pulverización con un equipo adecuado.
La preparación de una EAg implica obtener un compuesto de fórmula (I), ya sea como un líquido (si no es un líquido a temperatura ambiente, se puede fundir a una temperatura razonable, normalmente inferior a 70 °C) o en solución (disolviéndolo en un disolvente adecuado), y a continuación emulsionar el líquido o la solución resultante en agua que contenga uno o más AT, con un cizallamiento elevado, para producir una emulsión. Disolventes adecuados para su uso en EAg incluyen aceites vegetales, hidrocarburos clorados (tales como clorobencenos), disolventes aromáticos (tales como alquilbencenos o alquilnaftalenos) y otros disolventes orgánicos adecuados que presenten una solubilidad baja en agua.
Las microemulsiones (ME) se pueden preparar mezclando agua con una mezcla de uno o más disolventes con uno o más AT, para producir de forma espontánea una formulación líquida isotrópica termodinámicamente estable. Hay un compuesto de fórmula (I) presente inicialmente en el agua o en la mezcla de disolventes/AT. Los disolventes adecuados para emplear en las ME incluyen los descritos previamente en este documento para su uso en CE o en EAg. Una ME puede ser un sistema de aceite en agua o de agua en aceite (se puede determinar qué sistema está presente mediante medidas de conductividad) y puede ser adecuada para mezclar plaguicidas solubles en agua y
solubles en aceite en la misma formulación. Una ME es adecuada para diluirla en agua, en cuyo caso se puede mantener como una microemulsión o puede formar una emulsión de aceite en agua convencional.
Los concentrados en suspensión (CS) pueden comprender suspensiones acuosas o no acuosas de partículas sólidas insolubles finamente divididas de un compuesto de fórmula (I). Los CS se pueden preparar moliendo el compuesto de fórmula (I) sólido con un molino de bolas o de microesferas en un medio adecuado, opcionalmente con uno o más agentes dispersantes, para producir una suspensión de partículas finas del compuesto. Se pueden incluir uno o más agentes humectantes en la composición y se puede incluir un agente de suspensión para reducir la velocidad a la que sedimentan las partículas. Como alternativa, un compuesto de fórmula (I) puede molerse en seco y añadirse a agua, que contenga agentes descritos anteriormente en este documento, para producir el producto final deseado.
Las formulaciones en aerosol comprenden un compuesto de fórmula (I) y un propulsor adecuado (por ejemplo, nbutano). Un compuesto de fórmula (I) también puede disolverse o dispersarse en un medio adecuado (por ejemplo, agua o un líquido miscible en agua, tal como n-propanol) para proporción
ar composiciones para su uso en bombas de pulverización no presurizadas, accionadas manualmente.
Las suspensiones de cápsulas (SC) se pueden preparar de una manera similar a la preparación de formulaciones de EAg, pero con una fase de polimerización adicional de modo que se obtenga una dispersión acuosa de gotas de aceite, en que cada gota de aceite está encapsulada por una envoltura polimérica y contiene un compuesto de fórmula (I) y, opcionalmente, un vehículo o diluyente para el mismo. La envoltura polimérica se puede producir mediante una reacción de policondensación interfacial o mediante un procedimiento de coacervación. Las composiciones pueden proporcionar una liberación controlada del compuesto de fórmula (I) y se pueden utilizar para el tratamiento de semillas. Un compuesto de fórmula (I) también puede formularse en una matriz polimérica biodegradable para proporcionar una liberación lenta y controlada del compuesto.
La composición puede incluir uno o más aditivos para mejorar el rendimiento biológico de la composición, por ejemplo, mejorando la humectación, retención o distribución en superficies; la resistencia a la lluvia en superficies tratadas; o la captación o movilidad de un compuesto de fórmula (I). Dichos aditivos incluyen agentes tensioactivos (AT), aditivos de pulverización de base oleosa, por ejemplo, determinados aceites de vaselina o aceites vegetales naturales (tales como aceite de soja y de semilla de colza) y mezclas de estos con otros adyuvantes biopotenciadores (ingredientes que pueden ayudar o modificar la acción de un compuesto de fórmula (I)).
Los agentes humectantes, agentes dispersantes y agentes emulsionantes pueden ser AT de tipo catiónico, aniónico, anfótero o no iónico.
AT de tipo catiónico adecuados incluyen compuestos de amonio cuaternario (por ejemplo, bromuro de cetiltrimetilamonio), imidazolinas y sales de aminas.
AT aniónicos adecuados incluyen sales de metales alcalinos de ácidos grasos, sales de monoésteres alifáticos de ácido sulfúrico (por ejemplo, laurilsulfato de sodio), sales de compuestos aromáticos sulfonados (por ejemplo, dodecilbencenosulfonato de sodio, dodecilbencenosulfonato de calcio, butilnaftalensulfonato y mezclas de di/'sopropily tri/'sopropil-naftalensulfonatos de sodio), sulfatos de éter, sulfatos de éter alcohólicos (por ejemplo, laureth-3-sulfato de sodio), carboxilatos de éter (por ejemplo laureth-3-carboxilato de sodio), ésteres de fosfato (productos de la reacción entre uno o más alcoholes grasos y ácido fosfórico (predominantemente monoésteres) o pentóxido de fósforo (predominantemente diésteres), por ejemplo, la reacción entre alcohol laurílico y ácido tetrafosfórico; adicionalmente, estos productos pueden estar etoxilados), sulfosuccinamatos, sulfonatos, tauratos y lignosulfonatos de parafina u olefina.
AT de tipo anfótero adecuados incluyen betaínas, propionatos y glicinatos.
AT de tipo no iónico adecuados incluyen productos de condensación de óxidos de alquileno, tales como óxido de etileno, óxido de propileno, óxido de butileno o mezclas de los mismos, con alcoholes grasos (tales como alcohol oleílico o alcohol cetílico) o con alquilfenoles (tales como octilfenol, nonilfenol u octilcresol); ésteres parciales derivados de ácidos grasos de cadena larga o anhídridos de hexitol; productos de condensación de dichos ésteres parciales con óxido de etileno; polímeros de bloque (que comprenden óxido de etileno y óxido de propileno); alcanolamidas; ésteres simples (por ejemplo, ésteres polietilenglicólicos de ácidos grasos); óxidos de aminas (por ejemplo, óxido de laurildimetilamina); y lecitinas.
Agentes de suspensión adecuados incluyen coloides hidrófilos (tales como polisacáridos, polivinilpirrolidona o carboximetilcelulosa de sodio) y arcillas esponjosas (tales como bentonita o atapulgita).
La composición de la presente puede comprender además al menos un plaguicida adicional. Por ejemplo, los compuestos de acuerdo con la invención también se pueden usar en combinación con otros herbicidas o reguladores del crecimiento de las plantas. En una realización preferida, el plaguicida adicional es un herbicida y/o un protector para herbicidas. Ejemplos de dichas mezclas son (en que 'I' representa un compuesto de fórmula (I)). I acetoclor, I acifluorfén, I acifluorfén-sodio, I aclonifén, I acroleína, I alaclor, I aloxidim, I ametrina, I amicarbazona, I amidosulfurón, I aminopiralid, I amitrol, I anilofós, I asulam, I atrazina, I azafenidina, I azimsulfurón, I
+ BCPC, I beflubutamida, I benazolina, I bencarbazona, I benfluralina, I benfuresato, I bensulfurón, I bensulfurón-metilo, I bensulida, I bentazona, I benzfendizona, I benzobiciclón, I benzofenap, I biciclopirona, I bifenox, I bilanafós, I bispiribac, I bispiribac-sodio, I bórax, I bromacilo, I bromobutida, I bromoxinilo, I butaclor, I butamifós, I butralina, I butroxidim, I butilato, I ácido cacodílico, I clorato de calcio, I cafenstrol, I carbetamida, I carfentrazona, I carfentrazona-etilo, I clorflurenol, I clorflurenol-metilo, I cloridazón, I clorimurón, I clorimurón-etilo, I ácido cloroacético, I clorotolurón, I clorprofam, I clorsulfurón, I clortal, I clortal-dimetilo, I cinidón-etilo, I cinmetilina, I cinosulfurón, I cisanilida, I cletodim, I clodinafop, I clodinafoppropargilo, I clomazona, I clomeprop, I clopiralid, I cloransulam, I cloransulam-metilo, I cianazina, I cicloato, I ciclosulfamurón, I cicloxidim, I cihalofop, I cihalofop-butilo, I 2,4-D, I daimurón, I dalapón, I dazomet, I 2,4-DB, I I desmedifam, I dicamba, I diclobenilo, I diclorprop, I diclorprop-P, I diclofop, I diclofopmetilo, I diclosulam, I difenzoquat, I metilsulfato de difenzoquat, I diflufenicán, I diflufenzopir, I dimefurón, I dimepiperato, I dimetaclor, I dimetametrina, I dimetenamida, I dimetenamida-P, I dimetipina, I ácido dimetilarsínico, I dinitramina, I dinoterb, I difenamida, I dipropetrina, I diquat, I dibromuro de diquat, I ditiopir, I diurón, I endotal, I EPTC, I esprocarb, I etalfluralina, I etametsulfurón, I etametsulfurón-metilo, I etefón, I etofumesato, I etoxifeno, I etoxisulfurón, I etobenzanida, I fenoxaprop-P, I fenoxaprop-P-etilo, I fentrazamida, I sulfato ferroso, I flamprop-M, I flazasulfurón, I florasulam, I fluazifop, I fluazifop-butilo, I fluazifop-P, I fluazifop-P-butilo, I fluazolato, I flucarbazona, I flucarbazona-sodio, I flucetosulfurón, I flucloralina, I flufenacet, I flufenpir, I flufenpir-etilo, I flumetralina, I flumetsulam, I flumiclorac, I flumicloracpentilo, I flumioxazina, I flumipropina, I fluometurón, I fluoroglicofeno, I fluoroglicofeno-etilo, I fluoxaprop, I flupoxam, I flupropacilo, I flupropanato, I flupirsulfurón, I flupirsulfurón-metil-sodio, I flurenol, I fluridona, I flurocloridona, I fluroxipir, I flurtamona, I flutiacet, I flutiacet-metilo, I fomesafeno, I foramsulfurón, I fosamina, I glufosinato, I glufosinato-amonio, I glifosato, I halauxifeno, I halosulfurón, I halosulfurón-metilo, I haloxifop, I haloxifop-P, I hexazinona, I imazametabenz, I imazametabenz-metilo, I imazamox, I imazapic, I imazapir, I imazaquina, I imazetapir, I imazosulfurón, I indanofano, I indaziflam, I yodometano, I yodosulfurón, I yodosulfurón-metil-sodio, I ioxinilo, I isoproturón, I isourón, I isoxabeno, I isoxaclortol, I isoxaflutol, I isoxapirifop, I karbutilato, I lactofeno, I lenacilo, I linurón, I mecoprop, I mecoprop-P, I mefenacet, I mefluidida, I mesosulfurón, I mesosulfurón-metilo, I mesotriona, I metam, I metamifop, I metamitrón, I metazaclor, I metabenztiazurón, I metazol, I ácido metilarsónico, I metildimrón, I isotiocianato de metilo, I metolaclor, I S-metolaclor, I metosulam, I metoxurón, I metribuzina, I metsulfurón, I metsulfurón-metilo, I molinato, I monolinurón, I naproanilida, I napropamida, I naptalam, I neburón, I nicosulfurón, I glifosato de n-metilo, I ácido nonanoico, I norflurazón, I ácido oleico (ácidos grasos), I orbencarb, I ortosulfamurón, I orizalina, I oxadiargilo, I oxadiazona, I oxasulfurón, I oxaziclomefona, I oxifluorfeno, I paraquat, I dicloruro de paraquat, I pebulato, I pendimetalina, I penoxsulam, I pentaclorofenol, I pentanoclor, I pentoxazona, I petoxamida, I fenmedifam, I picloram, I picolinafeno, I pinoxadeno, I piperofós, I pretilaclor, I primisulfurón, I primisulfurón-metilo, I prodiamina, I profoxidim, I prohexadionacalcio, I prometón, I prometrina, I propaclor, I propanilo, I propaquizafop, I propazina, I profam, I propisoclor, I propoxicarbazona, I propoxicarbazona-sodio, I propizamida, I prosulfocarb, I prosulfurón, I piraclonilo, I piraflufeno, I piraflufeno-etilo, I pirasulfotol, I pirazolinato, I pirazosulfurón, I pirazosulfurónetilo, I pirazoxifeno, I piribenzoxim, I piributicarb, I piridafol, I piridato, I piriftalida, I piriminobac, I piriminobac-metilo, I pirimisulfano, I piritiobac, I piritiobac-sodio, I piroxasulfona, I piroxsulam, I quinclorac, I quinmerac, I quinoclamina, I quizalofop, I quizalofop-P, I rimsulfurón, I saflufenacilo, I setoxidim, I sidurón, I simazina, I simetrina, I clorato de sodio, I sulcotriona, I sulfentrazona, I sulfometurón, I sulfometurón-metilo, I sulfosato, I sulfosulfurón, I ácido sulfúrico, I tebutiurón, I tefuriltriona, I tembotriona, I tepraloxidim, I terbacilo, I terbumetona, I terbutilazina, I terbutrina, I tenilclor, I tiazopir, I tifensulfurón, I tiencarbazona, I tifensulfurón-metilo, I tiobencarb, I topramezona, I tralkoxidim, I tri-alato, I triasulfurón, I triaziflam, I tribenurón, I tribenurón-metilo, I triclopir, I trietazina, I trifloxisulfurón, I trifloxisulfurón-sodio, I trifluralina, I triflusulfurón, I triflusulfurón-metilo, I trihidroxitriazina, I trinexapac-etilo, I tritosulfurón, I éster etílico del ácido [3-[2-cloro-4-fluoro-5-(1 -metil-6-trifluorometil-2,4-dioxo-1,2,3,4-tetrahidropirimidin-3-il)fenoxi]-2-piridiloxijacético) (n.° de reg. CAS 353292-31-6). Los compuestos de la presente invención también se pueden combinar con compuestos herbicidas divulgados en los documentos WO 06/024820 y/o WO 07/096576.
Los compañeros de mezcla del compuesto de fórmula (I) también pueden estar en forma de ésteres o sales, como se menciona, por ejemplo, en The Pesticide Manual, decimocuarta edición, Consejo Británico para la Protección de Cultivos, 2006.
El compuesto de fórmula (I) también puede usarse en mezclas con otros agentes agroquímicos tales como fungicidas, nematicidas o insecticidas, cuyos ejemplos se proporcionan en The Pesticide Manual.
El cociente de mezcla del compuesto de fórmula (I) respecto al compañero de mezcla es preferiblemente de 1: 100 a 1000 :1.
Las mezclas pueden usarse ventajosamente en las formulaciones mencionadas anteriormente (en cuyo caso el "ingrediente activo" se refiere a la mezcla respectiva de compuesto de fórmula I con el compañero de mezcla).
Los compuestos de fórmula (I) de acuerdo con la invención también pueden usarse en combinación con uno o más protectores. Asimismo, también pueden usarse mezclas de un compuesto de fórmula I de acuerdo con la invención
con uno o más herbicidas adicionales en combinación con uno o más protectores. Los protectores pueden ser AD 67 (MON 4660), benoxacor, cloquintocet-mexilo, ciprosulfamida (n.° de reg. CAS 221667-31-8), diclormida, fenclorazoletilo, fenclorim, fluxofenim, furilazol y el isómero R correspondiente, isoxadifeno-etilo, mefenpir-dietilo, oxabetrinilo, N-isopropil-4-(2-metoxibenzoilsulfamoil)benzamida (n.° de reg. CAS 221668-34-4). Otras posibilidades incluyen compuestos protectores divulgados, por ejemplo, en el documento EP0365484, por ejemplo, N-(2-metoxibenzoil)-4-[(metilaminocarbonil)amino]bencenosulfonamida. Particularmente se prefieren mezclas de un compuesto de fórmula I con ciprosulfamida, isoxadifeno-etilo, cloquintocet-mexilo y/o N-(2-metoxibenzoil)-4-[(metilaminocarbonil)amino]bencenosulfonamida.
Los protectores del compuesto de fórmula I también pueden estar en forma de ásteres o sales, como se menciona, por ejemplo, en The Pesticide Manual, 14.a edición (BCPC), 2006. La referencia a cloquintocet-mexilo también se aplica a una sal de litio, sodio, potasio, calcio, magnesio, aluminio, hierro, amonio, amonio cuaternario, sulfonio o fosfonio del mismo, como se describe en el documento WO 02/34048, y la referencia a fenclorazol-etilo también se aplica a fenclorazol, etc.
Preferiblemente, el cociente de mezcla del compuesto de fórmula (I) respecto al protector es de 100:1 a 1:10, especialmente de 20:1 a 1 :1.
Las mezclas pueden usarse ventajosamente en las formulaciones mencionadas anteriormente (en cuyo caso el "ingrediente activo" se refiere a la mezcla respectiva del compuesto de fórmula I con el protector).
La presente invención proporciona además un método para controlar selectivamente malas hierbas en un emplazamiento que comprende plantas de cultivo y malas hierbas, en el que el método comprende aplicar al emplazamiento una cantidad de una composición de acuerdo con la presente invención que controle las malas hierbas. "Controlar" significa eliminar, reducir o ralentizar el crecimiento, o prevenir o reducir la germinación. Generalmente, las plantas que se tienen que controlar son plantas no deseadas (malas hierbas). "Emplazamiento" significa el área en la que las plantas están creciendo o crecerán.
Las tasas de aplicación de los compuestos de fórmula (I) pueden variar dentro de límites amplios y dependen de la naturaleza del suelo, el método de aplicación (antes o después de la germinación; riego superficial de las semillas; aplicación al surco de las semillas; aplicación a tierra no labrada, etc.), la planta de cultivo, la mala hierba o malas hierbas a controlar, las condiciones climáticas predominantes y otros factores regidos por el método de aplicación, el momento de la aplicación y el cultivo diana. Los compuestos de fórmula I de acuerdo con la invención se aplican generalmente a una tasa de 10 a 2000 g/ha, especialmente de 50 a 1000 g/ha.
La aplicación se realiza generalmente pulverizando la composición, normalmente mediante un pulverizador montado en un tractor para áreas grandes, pero también se pueden utilizar otros métodos tales como espolvoreo (para polvos), goteo o empapado.
Las plantas útiles en las que puede usarse la composición de acuerdo con la invención incluyen cultivos tales como cereales, por ejemplo, cebada y trigo, algodón, colza oleaginosa, girasol, maíz, arroz, soja, remolacha azucarera, caña de azúcar y pasto.
Las plantas de cultivo también pueden incluir árboles, tales como árboles frutales, palmeras, cocoteros u otros frutos secos. También se incluyen vides tales como uvas, arbustos frutales, plantas frutales y hortalizas.
Debe entenderse que los cultivos también incluyen aquellos cultivos que se han modificado para que sean tolerantes a herbicidas o clases de herbicidas (por ejemplo, inhibidores de ALS, GS, EPSPS, PPO, ACCasa y HPPD) mediante métodos convencionales de cultivo selectivo o por ingeniería genética. Un ejemplo de un cultivo que se ha modificado para que sea tolerante a imidazolinonas, por ejemplo, imazamox, mediante métodos convencionales de cultivo selectivo es la colza de verano (canola) Clearfield®. Ejemplos de cultivos que se han modificado para que sean tolerantes a los herbicidas mediante métodos de ingeniería genética incluyen, por ejemplo, variedades de maíz resistentes al glifosato y al glufosinato disponibles en el mercado con los nombres comerciales RoundupReady® y LibertyLink®. En un aspecto particularmente preferido, la planta de cultivo se ha genomanipulado para que sobreexprese la homogentisato solanesiltransferasa como se muestra en, por ejemplo, el documento WO 2010/029311.
También debe entenderse que los cultivos son aquellos que se han modificado para que sean resistentes a insectos nocivos mediante métodos de ingeniería genética, por ejemplo, el maíz Bt (resistente al barrenador del maíz europeo), algodón Bt (resistente al gorgojo del algodón) y también patatas Bt (resistentes al escarabajo de Colorado). Ejemplos de maíz Bt son los híbridos de maíz Bt 176 de NK® (Syngenta Seeds). La toxina Bt es una proteína producida de manera natural por la bacteria del suelo Bacillus thuringiensis. Ejemplos de toxinas, o plantas transgénicas que pueden sintetizar dichas toxinas, se describen en los documentos EP-A-451 878, EP-A-374753, WO 93/07278, WO 95/34656, WO 03/052073 y EP-A-427529. Ejemplos de plantas transgénicas que comprenden uno o más genes que codifican una resistencia a insecticidas y expresan una o más toxinas son KnockOut® (maíz), Yield Gard® (maíz), NuCOTIN33B® (algodón), Bollgard® (algodón), NewLeaf® (patatas), NatureGard® y Protexcta®. Los cultivos de plantas o sus materiales de semillas pueden ser tanto resistentes a los herbicidas como, al mismo tiempo, resistentes
a la alimentación por insectos (eventos transgénicos "apilados"). Por ejemplo, las semillas pueden tener la capacidad de expresar una proteína Cry3 insecticida y a la vez ser tolerantes a glifosato.
También debe entenderse que los cultivos incluyen aquellos que se obtienen mediante métodos convencionales de cultivo selectivo o ingeniería genética y que contienen los denominados rasgos productivos (por ejemplo, estabilidad mejorada en almacenamiento, mayor valor nutritivo y mejor sabor).
Otras plantas útiles incluyen pasto, por ejemplo, en campos de golf, praderas, parques y arcenes, o que se cultivan comercialmente para obtener césped, y plantas ornamentales tales como flores o arbustos.
Las composiciones se pueden emplear para controlar plantas no deseadas (colectivamente, "malas hierbas"). Las malas hierbas a controlar incluyen tanto especies monocotiledóneas, por ejemplo Agrostis, Alopecurus, Avena, Brachiaria, Bromus, Cenchrus, Cyperus, Digitaria, Echinochloa, Eleusine, Lolium, Monochoria, Rottboellia, Sagittaria, Scirpus, Setaria y Sorghum, como especies dicotiledóneas, por ejemplo Abutilon, Amaranthus, Ambrosia, Chenopodium, Chrysanthemum, Conyza, Galium, Ipomoea, Nasturtium, Sida, Sinapis, Solanum, Stellaria, Veronica, Viola y Xanthium. Las malas hierbas también pueden incluir plantas que se pueden considerar plantas de cultivo, pero que crecen fuera de un área de cultivo ("escapes") o que crecen a partir de semillas abandonadas de una plantación previa de un cultivo diferente ("voluntarios"). Dichos voluntarios o escapes pueden ser tolerantes a otros herbicidas determinados.
Diversos aspectos y realizaciones de la presente invención se ilustrarán ahora en mayor detalle a modo de ejemplo.
EJEMPLOS DE PREPARACIÓN
Ejemplo 1 Preparación de 4-(2-benc¡lox¡-3,6-d¡chloro-fen¡l)-2,6-dimet¡l-p¡r¡daz¡na-3,5-d¡ona
1.1 2-Al¡l-3,6-d¡cloro-fenol
Una mezcla de 2-aliloxi-1,4-dicloro-benceno (1,0 g, 4,9 mmol, 1,0 equiv.) y DMF (0,1 ml) se calentó a una temperatura externa de 220 °C durante 1 hora. La mezcla se dejó enfriar hasta temperatura ambiente y se concentró al vacío para proporcionar 2-alil-3,6-dicloro-fenol como un aceite pardo (0,99 g, 99 %).
1.2 2-Al¡l-3-benc¡lox¡-1,4-d¡cloro-benceno
Se añadió bromuro de bencilo (3,2 ml, 27 mmol, 1,1 equiv.) a una suspensión de 2-alil-3,6-dicloro-fenol (5,0 g, 25 mmol, 1.0 equiv.) y carbonato de potasio (3,7 g, 27 mmol, 1,1 equiv.) en acetona (49 ml) y la mezcla se calentó a reflujo durante 6 horas. La mezcla se dejó enfriar hasta temperatura ambiente y se filtró. El filtrado se concentró al vacío y el producto en bruto se purificó por cromatografía en columna ultrarrápida para proporcionar 2-alil-3-benciloxi-1,4-dicloro-benceno (4,031 g, 56 %) como un aceite incoloro.
7,24 (1H,
1.3 Ácido 2-(2-benciloxi-3,6-dicloro-fenil)acético
Una solución de 2-alil-3-benciloxi-1,4-dicloro-benceno (38,1 g, 130 mmol, 1,00 equiv.) en diclorometano (650 ml) en un matraz de 3 bocas se enfrió hasta -78 °C. Una boca lateral se conectó a un frasco de Dreshel que contenía una solución acuosa de KI (100 ml, 15 % p/p). Se burbujeó ozono a través de la solución hasta que el 2-alil-3-benciloxi-1,4-dicloro-benceno se había consumido completamente (4 horas). Se burbujeó aire a través de la solución durante 10 minutos para eliminar el exceso de ozono. El burbujeo del gas a través de la solución se detuvo y se añadió sulfuro de dimetilo (95,4 ml, 1300 mmol, 10,0 equiv.). La mezcla se dejó calentar hasta temperatura ambiente y se agitó durante 12 horas. La mezcla se lavó con salmuera (2 x 200 ml) y los extractos orgánicos se pasaron a través de una frita hidrófoba. La mezcla se concentró al vacío para proporcionar un aceite amarillo (43 g). El residuo se disolvió en una mezcla de ferc-butanol (260 ml) y agua (130 ml), después se enfrió hasta 0 °C. Se añadió 2-metilbut-2-eno (135 ml, 1300 mmol, 10,0 equiv.), dihidrogenofosfato de sodio (62,4 g, 520 mmol, 4,00 equiv.) y clorito de sodio (44,1 g, 390 mmol, 3,00 equiv.). La mezcla se agitó durante 2 horas, después se diluyó con salmuera (300 ml) y ácido clorhídrico 2,0 M (300 ml). La mezcla se extrajo con EtOAc (3 x 200 ml). Los extractos orgánicos combinados se lavaron con una solución saturada acuosa de metabisulfito de sodio (200 ml), después se pasó a través de una frita hidrófoba y se concentró al vacío para proporcionar un sólido amarillo pálido (41,4 g). El residuo se suspendió en H2O (200 ml) y se añadió una solución acuosa de NaOH (30 ml, 2,0 M) produciendo una solución transparente. La mezcla se lavó con Et2O (100 ml) y la capa acuosa se acidificó mediante la adición de HCl concentrado (20 ml) provocando la formación de un precipitado. La mezcla se filtró y el filtrado se secó al vacío para proporcionar ácido 2-(2-benciloxi-3,6-dicloro-fenil)acético (29,2 g, 72 %) como un sólido blanco.
1.4 (2E/Z)-2-(Metilhidrazono)propanoato de etilo
Un matraz de 500 ml de 3 bocas equipado con una barra agitadora, embudo de adición y termómetro se colocó en atmósfera de N2. Se cargó cloroformo (60 ml), 2-oxopropanoato de etilo (12,9 g, 111 mmol) y sulfato de magnesio (13,3 g, 111 mmol) al recipiente con agitación. La suspensión resultante se enfrió hasta 0 °C (baño de hielo). El embudo de adición entonces se cargó con cloroformo (20 ml) y metilhidrazina (5,00 g, 109 mmol). La solución de metilhidrazina entonces se añadió gota a gota a la mezcla de reacción agitada, estableciendo la tasa de adición para mantener la temperatura < 10 °C. Después de completarse la adición, la reacción se calentó hasta temperatura ambiente y después se agitó durante 16 h más.
La reacción se filtró, lavando con cloroformo. El filtrado se concentró a presión reducida para dar la hidrazona deseada etil-2-(metilhidrazono)propanoato (15,1 g, 105 mmol, 96,5 % de rendimiento), un aceite amarillo, como una mezcla de isómeros E/Z.
1H RMN datos para el isómero principal: (400 MHz, CDCI3): 5h: 5,58 (1H, s a), 4,30 (2H, c), 3,24 (3H, s), 1,92 (3H, s), 1,34 (3H, t).
1.5 2-[[2-(2-Benciloxi-3,6-dicloro-fenil)acetil]-metil-hidrazono]propanoato de etilo
Se disolvió ácido 2-(2-benciloxi-3,6-dicloro-fenil)acético (1,32 mmol, 0,41 g) en diclorometano (10 ml) en N2 con agitación. Se añadió cloruro de oxalilo (3,95 mmol, 0,50 g, 0,34 ml). Después de 2 min, se añadió gota a gota N,N-dimetilformamida (0,13 mmol, 0,01 ml). Se observó efervescencia. Después de 1 h de agitación a temperatura ambiente, el análisis por CL/EM de una alícuota inactivada en MeOH mostró conversión completa del material de partida ácido en el éster metílico (que evidencia la formación de cloruro de acilo).
La mezcla de reacción se concentró al vacío para proporcionar una goma naranja.
El cloruro de ácido en bruto entonces se volvió a disolver en diclorometano (10 ml) en atmósfera de N2 y se enfrió hasta 0 °C. Se añadió 2-(metilhidrazono)propanoato de etilo (1,34 mmol, 0,194 g) con agitación. Se añadió gota a gota trietilamina (2,64 mmol, 0,37 ml) en diclorometano (0,5 ml) durante 10 min. La mezcla de reacción se agitó a 0 °C durante 15 min más, antes de calentarla hasta temperatura ambiente y se continuó durante 4 h más.
El disolvente se evaporó al vacío y el residuo volvió a disolverse en acetato de etilo (30 ml). Los extractos orgánicos se lavaron con solución diluida ac. de HCl (2 x 10 ml), solución saturada ac. de NaHCOa (2 x 10 ml) y salmuera (2 x 10 ml), antes de pasarlos a través de un cartucho separador de fases y se concentraron al vacío.
La cromatografía en columna ultrarrápida (sílice, eluyente de gradiente de un 0-5 % de acetato de etilo en hexano) produjo el producto deseado 2-[[2-(2-benciloxi-3,6-dicloro-fenil)acetil]-metil-hidrazono]propanoato de etilo (0,21 g, 36,5 %) como una goma amarilla.
1.6 4-(2-Benciloxi-3,6-dicloro-fenil)-2,6-dimetil-piridazina-3,5-diona
Un vial de microondas se cargó con 2-[[2-(2-benciloxi-3,6-dicloro-fenil)acetil]-metil-hidrazono]propanoato de etilo (0,46 mmol, 0,20 g), acetonitrilo (4 ml) y 1,8-diazabiciclo[5.4.0]undec-7-eno (0,98 mmol, 0,15 g, 0,15 ml). La mezcla se calentó con radiación microondas a 125 °C durante 50 min antes de que el análisis de CL/EM mostrara reacción completa. La mezcla de reacción se diluyó con acetato de etilo (20 ml) y agua (10 ml) y se acidificó hasta pH 4-5 con ácido clorhídrico diluido. Los extractos orgánicos se separaron y se lavaron adicionalmente con solución saturada acuosa de cloruro de amonio (2 x 10 ml), después salmuera (10 ml). Los extractos orgánicos entonces se pasaron a través de un cartucho separador de fases y se concentraron al vacío para producir una goma amarilla en bruto. La cromatografía en columna ultrarrápida (sílice, eluyente de gradiente de un 0-25 % de acetato de etilo en hexano) produjo el producto deseado 4-(2-benciloxi-3,6-dicloro-fenil)-2,6-dimetil-piridazina-3,5-diona (0,11 g, 61 %) como una goma amarilla pálida.
2,22 (3H, s), 3,66 (3H, s), 4,70 (1H, d), 5,08 (1H,
EJEMPLOS BIOLÓGICOS
B1 Eficacia tras la germinación
Se siembran semillas de una diversidad de especies de ensayo en suelo convencional en macetas: - Solanum nigrum (SOLNI), Amaranthus retoflexus (AMARE), Setaria faberi (s Et FA), Alopecurus myosuroides (ALOMY), Echinochloa crus-galli (ECHCG), Ipomoea hederacea (IPOHE), Lolium perenne (LOLPE). Después de 8 días de cultivo (después de la germinación) en condiciones controladas en un invernadero (a 24/16 °C, día/noche; 14 horas de luz; 65 % de humedad), las plantas se pulverizan con una solución acuosa de pulverización derivada de la formulación del ingrediente activo técnico en solución de acetona/agua (50:50) que contiene Tween 20 (monolaurato de polioxietelilensorbitán, n.° de reg. CAS 9005-64-5) al 0,5 %. Los compuestos se aplican a 1000 g/ha. Las plantas de ensayo entonces se cultivan en un invernadero en condiciones controladas en un invernadero (a 24/16 °C, día/noche; 14 horas de luz; 65 % de humedad) y se riegan dos veces al día. Después de 13 días, la prueba se evalúa con el fin de determinar el porcentaje de daños provocados en la planta. Las actividades biológicas se evalúan en una escala de cinco puntos (5 = 80-100 %, 4 = 60-79 %, 3 = 40-59 %, 2 = 20-39 %, 1 = 0-19 %). Un valor en blanco en la tabla es indicativo de que el compuesto no se ensayó en esa especie.
Tabla 2 Control de especies de malas hierbas mediante compuestos de fórmula (I) después de aplicación tras la _______ germinación a una tasa de 1000 g/ha_______________________________________________________
Compuesto LOLPE SOLNI AMARE SETFA ALOMY ECHCG IPOHE
1.001 5 5 5 4 5 5
1.002 1 5 4 1 1 1
1.003 5 5 4 3 5 5
1.004 5 5 5 5 5 5
1.005 5 5 5 5 5 5
1.006 2 5 5 3 3 5
1.007 4 5 5 5 5 5
1.009 5 5 5 5 5 5
1.010 4 5 5 3 4 5
1.012 5 5 5 5 5 5
1.014 3 5 4 5 4 5
1.016 4 5 5 5 5 5
1.037 5 5 5 4 5 5
1.041 4 5 5 5 5 5
1.044 5 5 5 5 5 5
1.067 5 5 2 5 5 5
1.068 2 5 3 4 4 4
1.069 3 5 3 5 5 5
1.070 5 5 5 5 5 5
1.071 3 5 3 5 4 5
1.072 2 5 2 5 4 5
1.073 3 5 3 5 5 5
1.074 5 5 5 5 5 5
1.075 4 5 4 5 5 5
1.076 4 5 2 5 5 5
1.077 5 5 5 5 5 5
1.078 1 5 3 3 2 4
1.079 1 5 1 1 1 5
1.080 2 5 2 1 1 5
Compuesto LOLPE SOLNI AMARE SETFA ALOMY ECHCG IPOHE 1.081 2 5 3 4 2 4 1.082 1 5 1 2 1 3 1.083 2 5 1 3 1 5 1.084 4 5 3 2 1 5 1.085 5 5 5 3 4 5 1.086 4 5 3 4 2 5 1.087 5 5 5 5 5 5
Claims (18)
1. Un compuesto de fórmula (I)
(I), o una sal o N-óxido del mismo,
R1 se selecciona del grupo que consiste en alquilo C1-C4, cicloalquilo C3-C6, alcoxi C3-C6, alcoxi C1-C2-alquilo C1-C2, alquenilo C2-C4, haloalquilo C1-C4, cianoalquilo C1-C4, haloalquenilo C2-C4, alquinilo C2-C4 y haloalquinilo C2-C4; R2 se selecciona del grupo que consiste en hidrógeno, halógeno, ciano, alquilo C1-C6, haloalquilo C1-C6, haloalcoxi C1-C6, haloalcoxi C1-C3-alquilo C1-C3-, alcoxi C1-C6, alcoxi C1-C3-alquilo C1-C3, alcoxi C1-C3-alcoxi C1-C3-alquilo C1-C3-, cicloalquilo C3-C6, alquenilo C2-C6, haloalquenilo C2-C6, alquinilo C2-C6, hidroxialquilo C1-C6-, alquilcarbonilo C1-C6-, alquil C1-C6-S(O)m-, amino, alquilamino C1-C6, dialquilamino C1-C6, -C(alquil C1-C3)=N-O-alquilo C1-C3 y haloalquinilo C2-C6;
G es hidrógeno o C(O)R3;
X e Y cada uno es independientemente hidrógeno, alquilo C1-C3, alcoxi C1-C3, haloalquilo C1-C3, haloalcoxi C1-C3 o halógeno;
Z es alquilo C1-C3, alcoxi C1-C3, haloalquilo C1-C3, haloalcoxi C1-C3 o halógeno;
m es un número entero de 0, 1 o 2;
n es un número entero de 0, 1, 2, 3, 4 o 5;
R3 se selecciona del grupo que consiste en alquilo C1-C6, alcoxi C1-C6, alquenilo C1-C6, alquinilo C1-C6, alquil C1-C6-S-, -NR4R5 y fenilo opcionalmente sustituido con uno o más R6;
R4 y R5 se seleccionan independientemente del grupo que consiste en alquilo C1-C6 y alcoxi C1-C6, o R4 y R5 juntos pueden formar un anillo de morfolinilo; y,
R6 se selecciona del grupo que consiste en halógeno, ciano, nitro, alquilo C1-C3, haloalquilo C1-C3, alcoxi C1-C3 y haloalcoxi C1-C3.
2. El compuesto de acuerdo con la reivindicación 1, en el que G es hidrógeno o C(O)R3 en el que R3 es isopropil, f-butilo, metilo, etilo, propargilo, metoxi, etoxi o ferc-butoxi.
3. El compuesto de la reivindicación 2, en el que G es hidrógeno o R3 es isopropilo.
4. El compuesto de una cualquiera de las reivindicaciones precedentes, en el que X es hidrógeno, halógeno o haloalquilo C1.
5. El compuesto de una cualquiera de las reivindicaciones precedentes, en el que Y es hidrógeno, alquilo C1-C3, haloalquilo C1-C3 o halógeno.
6. El compuesto de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que X está orto con respecto al resto piridazinona/piridazina-diona.
7. El compuesto de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que Y está orto con respecto al resto benciloxi.
8. El compuesto de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que R1 es metilo, etilo, n-propilo, ciclopropilo, propargilo o haloalquilo C1.
9. El compuesto de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que R2 se selecciona del grupo que consiste en hidrógeno, alquilo C1-C6, haloalquilo C1-C6, alcoxi C1-C6, alcoxi C1-C3-alquilo C1-C3, cicloalquilo C3-C6, alquenilo C2-C6, haloalquenilo C2-C6, alquinilo C2-C6 y haloalquinilo C2-C6.
10. El compuesto de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que R2 se selecciona del grupo que consiste en metilo, etilo, ciclopropilo, trifluorometilo y metoximetilo.
11. El compuesto de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que R2 es ciclopropilo o metilo.
12. El compuesto de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que n es 0, 1 o 2.
13. El compuesto de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que cada Z se selecciona independientemente de halógeno, metilo, metoxi y trifluorometilo.
14. Una composición herbicida que comprende un compuesto herbicida de acuerdo con una cualquiera de las reivindicaciones 1-13 y un adyuvante de formulación agronómicamente aceptable.
15. Una composición herbicida de acuerdo con la reivindicación 14, que comprende, además, al menos un plaguicida adicional.
16. Una composición herbicida de acuerdo con la reivindicación 15, en la que el plaguicida adicional es un herbicida o un protector para herbicidas.
17. Un método de control del crecimiento de plantas indeseadas, que comprende aplicar un compuesto de fórmula (I) como se define en una cualquiera de las reivindicaciones 1 a 13, o una composición herbicida de acuerdo con una cualquiera de las reivindicaciones 14 a 16, a las plantas indeseadas o al emplazamiento de las mismas.
18. Uso de un compuesto de fórmula (I) como se define en una cualquiera de las reivindicaciones 1 a 13 como herbicida.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB1412735.1A GB201412735D0 (en) | 2014-07-17 | 2014-07-17 | Herbicidal compounds |
| PCT/EP2015/065827 WO2016008816A1 (en) | 2014-07-17 | 2015-07-10 | Herbicidal pyridazinone derivatives |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2760264T3 true ES2760264T3 (es) | 2020-05-13 |
Family
ID=51494757
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES15739220T Active ES2760264T3 (es) | 2014-07-17 | 2015-07-10 | Compuestos herbicidas de piridazinona |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US9944608B2 (es) |
| EP (1) | EP3169668B1 (es) |
| JP (1) | JP6524207B2 (es) |
| KR (1) | KR102459331B1 (es) |
| CN (1) | CN106536486B (es) |
| AR (1) | AR101201A1 (es) |
| BR (1) | BR112017000541B8 (es) |
| ES (1) | ES2760264T3 (es) |
| GB (1) | GB201412735D0 (es) |
| WO (1) | WO2016008816A1 (es) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB201507464D0 (en) * | 2015-04-30 | 2015-06-17 | Syngenta Participations Ag | Herbicidal compounds |
| GB2546336A (en) * | 2016-01-18 | 2017-07-19 | Syngenta Participations Ag | Intermediate compounds |
| GB201800305D0 (en) * | 2018-01-09 | 2018-02-21 | Syngenta Participations Ag | Herbicidal compounds |
| GB201800894D0 (en) * | 2018-01-19 | 2018-03-07 | Syngenta Participations Ag | Improvements in or relating to organic compounds |
| MX2021003530A (es) * | 2018-09-27 | 2021-05-27 | Fmc Corp | Herbicidas de piridazinona e intermediarios de piridazinona usados para preparar un herbicida. |
| JP7063231B2 (ja) * | 2018-10-26 | 2022-05-09 | 住友化学株式会社 | ジピリダジニルエーテル化合物及びその用途 |
| GB201819747D0 (en) | 2018-12-04 | 2019-01-16 | Syngenta Participations Ag | Herbicidal compositions |
| GB201910291D0 (en) | 2019-07-18 | 2019-09-04 | Syngenta Crop Protection Ag | Herbicidal compounds |
| GB201910290D0 (en) | 2019-07-18 | 2019-09-04 | Syngenta Crop Protection Ag | Herbicidal compounds |
| GB202012651D0 (en) | 2020-08-13 | 2020-09-30 | Syngenta Crop Protection Ag | Herbicidal compositions |
| GB202116307D0 (en) | 2021-11-12 | 2021-12-29 | Syngenta Crop Protection Ag | Herbicide resistance |
| IL315190A (en) * | 2022-03-30 | 2024-10-01 | Ishihara Sangyo Kaisha | A pyridazinone compound or a salt thereof and a pesticide containing them |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH09208565A (ja) * | 1996-02-07 | 1997-08-12 | Sumitomo Chem Co Ltd | テトラゾリノン誘導体、その用途およびその製造中間体 |
| ZA200807796B (en) * | 2006-03-17 | 2009-12-30 | Sumitomo Chemical Co | Pyridazinone compound and use thereof as herbicides |
| TWI375669B (en) * | 2006-03-17 | 2012-11-01 | Sumitomo Chemical Co | Pyridazinone compound and use thereof |
| CL2008002703A1 (es) * | 2007-09-14 | 2009-11-20 | Sumitomo Chemical Co | Compuestos derivados de 1,4-dihidro-2h-piridazin-3-ona; composicion herbicida que comprende a dichos compuestos; metodo de control de malezas; uso de dichos compuestos para el control de malezas; y compuestos intermediarios. |
| CL2008003785A1 (es) * | 2007-12-21 | 2009-10-09 | Du Pont | Compuestos derivados de piridazina; composiciones herbicidas que comprenden a dichos compuestos; y método para controlar el crecimiento de la vegetación indeseada. |
| EP2204366A1 (de) | 2008-12-19 | 2010-07-07 | Bayer CropScience AG | Herbizid und insektizid wirksame phenylsubstituierte Pyridazinone |
| JP2010235603A (ja) * | 2009-03-13 | 2010-10-21 | Sumitomo Chemical Co Ltd | ピリダジノン化合物及びその用途 |
| WO2010113986A1 (ja) * | 2009-03-30 | 2010-10-07 | 住友化学株式会社 | ピリダジノン化合物の有害節足動物防除用途 |
| WO2011035878A1 (de) * | 2009-09-25 | 2011-03-31 | Bayer Cropscience Ag | Herbizid wirksame phenylsubstituierte pyridazinone |
| GB201117019D0 (en) * | 2011-10-04 | 2011-11-16 | Syngenta Ltd | Herbicidal compounds |
| WO2011161035A1 (de) * | 2010-06-22 | 2011-12-29 | Bayer Cropscience Ag | 3-aryl-4-(2-thienylmethylen)-isoxazol-5(4h)-one als fungizide |
| JP5842594B2 (ja) * | 2010-12-27 | 2016-01-13 | 住友化学株式会社 | ピリダジノン化合物、それを含有する除草剤及び有害節足動物防除剤 |
| WO2014119770A1 (ja) | 2013-01-30 | 2014-08-07 | 住友化学株式会社 | ピリダジノン化合物及びそれを含有する除草剤 |
-
2014
- 2014-07-17 GB GBGB1412735.1A patent/GB201412735D0/en not_active Ceased
-
2015
- 2015-07-10 CN CN201580038716.3A patent/CN106536486B/zh active Active
- 2015-07-10 BR BR112017000541A patent/BR112017000541B8/pt active IP Right Grant
- 2015-07-10 ES ES15739220T patent/ES2760264T3/es active Active
- 2015-07-10 KR KR1020177002447A patent/KR102459331B1/ko active Active
- 2015-07-10 JP JP2017502578A patent/JP6524207B2/ja active Active
- 2015-07-10 EP EP15739220.0A patent/EP3169668B1/en active Active
- 2015-07-10 WO PCT/EP2015/065827 patent/WO2016008816A1/en not_active Ceased
- 2015-07-10 US US15/325,816 patent/US9944608B2/en active Active
- 2015-07-14 AR ARP150102237A patent/AR101201A1/es active IP Right Grant
Also Published As
| Publication number | Publication date |
|---|---|
| KR102459331B1 (ko) | 2022-10-25 |
| EP3169668A1 (en) | 2017-05-24 |
| GB201412735D0 (en) | 2014-09-03 |
| AR101201A1 (es) | 2016-11-30 |
| US9944608B2 (en) | 2018-04-17 |
| CN106536486B (zh) | 2019-11-01 |
| JP2017522318A (ja) | 2017-08-10 |
| WO2016008816A1 (en) | 2016-01-21 |
| BR112017000541A2 (pt) | 2018-06-26 |
| US20170166535A1 (en) | 2017-06-15 |
| KR20170029528A (ko) | 2017-03-15 |
| EP3169668B1 (en) | 2019-09-04 |
| BR112017000541B1 (pt) | 2020-06-02 |
| BR112017000541B8 (pt) | 2020-06-23 |
| JP6524207B2 (ja) | 2019-06-05 |
| CN106536486A (zh) | 2017-03-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2760264T3 (es) | Compuestos herbicidas de piridazinona | |
| ES2659553T3 (es) | Compuestos herbicidas | |
| ES2577381T3 (es) | Compuestos herbicidas de piridacinona | |
| ES2575396T3 (es) | Compuestos herbicidas | |
| ES2836423T3 (es) | Compuestos herbicidas | |
| ES2897918T3 (es) | Herbicidas | |
| ES2534218T3 (es) | Compuestos herbicidas | |
| ES2715452T3 (es) | Quinolinas herbicidas | |
| ES2921649T3 (es) | Herbicidas | |
| ES2976054T3 (es) | Compuestos herbicidas | |
| BR112014023417B1 (pt) | Composto herbicida, seu uso, composição herbicida e método de controle de ervas daninhas | |
| JP2018503682A (ja) | 除草剤としてのチアゾロピリジノン | |
| EP3063147B1 (en) | Herbicidal 3-(2-benzyloxyphenyl)-2,4-dihydroxy-1,8-naphthyridine derivatives | |
| ES3038377T3 (en) | N-(tetrazol-5-yl)-benzamide compounds useful as herbicides | |
| ES2670695T3 (es) | Compuestos herbicidas | |
| ES3032457T3 (en) | 2-phenoxy-pyrimidine derivatives as herbicidal compounds | |
| ES2715759T3 (es) | Derivados de triazolotriazinona con actividad como herbicidas | |
| ES2904913T3 (es) | Derivados de piridil-/pirimidil-pirimidina activos como herbicidas | |
| ES2904789T3 (es) | Derivados de pirazin-4-carbamato en calidad de herbicidas | |
| ES2750074T3 (es) | Compuestos herbicidas | |
| ES3031051T3 (en) | Herbicidal tetrazole compounds | |
| ES3027366T3 (en) | Herbicidal compounds | |
| ES2741798T3 (es) | Piridazinonas en calidad de compuestos herbicidas | |
| ES2903441T3 (es) | Derivados de pirimidin-4-carbamato o urea en calidad de herbicidas | |
| ES2939686T3 (es) | Derivados de pirazina-4-carbamato o -urea como herbicidas |