ES2765409T3 - Composiciones mejoradas de especies de bacterias ácido lácticas hetero- y homofermentadoras para la conservación del ensilaje de doble función - Google Patents
Composiciones mejoradas de especies de bacterias ácido lácticas hetero- y homofermentadoras para la conservación del ensilaje de doble función Download PDFInfo
- Publication number
- ES2765409T3 ES2765409T3 ES15767097T ES15767097T ES2765409T3 ES 2765409 T3 ES2765409 T3 ES 2765409T3 ES 15767097 T ES15767097 T ES 15767097T ES 15767097 T ES15767097 T ES 15767097T ES 2765409 T3 ES2765409 T3 ES 2765409T3
- Authority
- ES
- Spain
- Prior art keywords
- silage
- composition
- lactic acid
- lactobacillus
- inoculated
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 title claims abstract description 164
- 239000004460 silage Substances 0.000 title claims abstract description 125
- 239000004310 lactic acid Substances 0.000 title claims abstract description 82
- 235000014655 lactic acid Nutrition 0.000 title claims abstract description 82
- 241000894006 Bacteria Species 0.000 title claims abstract description 45
- 239000000203 mixture Substances 0.000 title description 172
- 239000002054 inoculum Substances 0.000 claims abstract description 53
- 241000186679 Lactobacillus buchneri Species 0.000 claims abstract description 42
- 241000194036 Lactococcus Species 0.000 claims abstract description 17
- 241000194033 Enterococcus Species 0.000 claims abstract description 16
- 240000001929 Lactobacillus brevis Species 0.000 claims abstract description 10
- 241000186840 Lactobacillus fermentum Species 0.000 claims abstract description 10
- 229940012969 lactobacillus fermentum Drugs 0.000 claims abstract description 10
- 241000186604 Lactobacillus reuteri Species 0.000 claims abstract description 9
- 229940001882 lactobacillus reuteri Drugs 0.000 claims abstract description 8
- 238000000034 method Methods 0.000 claims description 21
- 239000000463 material Substances 0.000 claims description 20
- 238000004519 manufacturing process Methods 0.000 claims description 19
- 235000013957 Lactobacillus brevis Nutrition 0.000 claims description 5
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 72
- 240000008042 Zea mays Species 0.000 description 64
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 63
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 51
- 235000005822 corn Nutrition 0.000 description 51
- 241000894007 species Species 0.000 description 35
- 238000000855 fermentation Methods 0.000 description 33
- 230000001580 bacterial effect Effects 0.000 description 28
- 230000004151 fermentation Effects 0.000 description 25
- 235000011054 acetic acid Nutrition 0.000 description 24
- 239000004459 forage Substances 0.000 description 24
- 239000000047 product Substances 0.000 description 19
- 238000002474 experimental method Methods 0.000 description 17
- 239000007789 gas Substances 0.000 description 17
- 238000011081 inoculation Methods 0.000 description 16
- 244000025254 Cannabis sativa Species 0.000 description 15
- 241000196324 Embryophyta Species 0.000 description 14
- 238000000354 decomposition reaction Methods 0.000 description 14
- 240000006024 Lactobacillus plantarum Species 0.000 description 13
- 235000016383 Zea mays subsp huehuetenangensis Nutrition 0.000 description 12
- 235000009973 maize Nutrition 0.000 description 12
- 238000011282 treatment Methods 0.000 description 12
- 244000057717 Streptococcus lactis Species 0.000 description 11
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 11
- 241000194031 Enterococcus faecium Species 0.000 description 10
- 241000219793 Trifolium Species 0.000 description 9
- 230000000694 effects Effects 0.000 description 9
- 150000007524 organic acids Chemical class 0.000 description 9
- 244000005700 microbiome Species 0.000 description 8
- 108010053775 Nisin Proteins 0.000 description 7
- NVNLLIYOARQCIX-MSHCCFNRSA-N Nisin Chemical compound N1C(=O)[C@@H](CC(C)C)NC(=O)C(=C)NC(=O)[C@@H]([C@H](C)CC)NC(=O)[C@@H](NC(=O)C(=C/C)/NC(=O)[C@H](N)[C@H](C)CC)CSC[C@@H]1C(=O)N[C@@H]1C(=O)N2CCC[C@@H]2C(=O)NCC(=O)N[C@@H](C(=O)N[C@H](CCCCN)C(=O)N[C@@H]2C(NCC(=O)N[C@H](C)C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCSC)C(=O)NCC(=O)N[C@H](CS[C@@H]2C)C(=O)N[C@H](CC(N)=O)C(=O)N[C@H](CCSC)C(=O)N[C@H](CCCCN)C(=O)N[C@@H]2C(N[C@H](C)C(=O)N[C@@H]3C(=O)N[C@@H](C(N[C@H](CC=4NC=NC=4)C(=O)N[C@H](CS[C@@H]3C)C(=O)N[C@H](CO)C(=O)N[C@H]([C@H](C)CC)C(=O)N[C@H](CC=3NC=NC=3)C(=O)N[C@H](C(C)C)C(=O)NC(=C)C(=O)N[C@H](CCCCN)C(O)=O)=O)CS[C@@H]2C)=O)=O)CS[C@@H]1C NVNLLIYOARQCIX-MSHCCFNRSA-N 0.000 description 7
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 7
- 239000011521 glass Substances 0.000 description 7
- 239000004309 nisin Substances 0.000 description 7
- 235000010297 nisin Nutrition 0.000 description 7
- 238000004458 analytical method Methods 0.000 description 6
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 6
- 235000015097 nutrients Nutrition 0.000 description 6
- 238000012360 testing method Methods 0.000 description 6
- 241000273930 Brevoortia tyrannus Species 0.000 description 5
- 241000186660 Lactobacillus Species 0.000 description 5
- 238000011534 incubation Methods 0.000 description 5
- 229940039696 lactobacillus Drugs 0.000 description 5
- 230000000813 microbial effect Effects 0.000 description 5
- 235000005985 organic acids Nutrition 0.000 description 5
- 239000004033 plastic Substances 0.000 description 5
- 229920003023 plastic Polymers 0.000 description 5
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 4
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 4
- 241001112696 Clostridia Species 0.000 description 4
- SRBFZHDQGSBBOR-IOVATXLUSA-N D-xylopyranose Chemical compound O[C@@H]1COC(O)[C@H](O)[C@H]1O SRBFZHDQGSBBOR-IOVATXLUSA-N 0.000 description 4
- 241000234642 Festuca Species 0.000 description 4
- 235000013965 Lactobacillus plantarum Nutrition 0.000 description 4
- 235000015724 Trifolium pratense Nutrition 0.000 description 4
- PYMYPHUHKUWMLA-UHFFFAOYSA-N arabinose Natural products OCC(O)C(O)C(O)C=O PYMYPHUHKUWMLA-UHFFFAOYSA-N 0.000 description 4
- 150000001720 carbohydrates Chemical class 0.000 description 4
- 235000014633 carbohydrates Nutrition 0.000 description 4
- 239000008367 deionised water Substances 0.000 description 4
- 229910021641 deionized water Inorganic materials 0.000 description 4
- 238000003306 harvesting Methods 0.000 description 4
- 229940072205 lactobacillus plantarum Drugs 0.000 description 4
- 235000013526 red clover Nutrition 0.000 description 4
- KDYFGRWQOYBRFD-UHFFFAOYSA-N succinic acid Chemical compound OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 4
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 3
- 241000588921 Enterobacteriaceae Species 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- 241001147746 Lactobacillus delbrueckii subsp. lactis Species 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 235000014897 Streptococcus lactis Nutrition 0.000 description 3
- 230000006866 deterioration Effects 0.000 description 3
- 235000019253 formic acid Nutrition 0.000 description 3
- 238000011068 loading method Methods 0.000 description 3
- 230000020477 pH reduction Effects 0.000 description 3
- 239000013641 positive control Substances 0.000 description 3
- 238000004321 preservation Methods 0.000 description 3
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 3
- 239000004299 sodium benzoate Substances 0.000 description 3
- 235000010234 sodium benzoate Nutrition 0.000 description 3
- 239000000243 solution Substances 0.000 description 3
- 239000008399 tap water Substances 0.000 description 3
- 235000020679 tap water Nutrition 0.000 description 3
- 230000004580 weight loss Effects 0.000 description 3
- OSNSWKAZFASRNG-WNFIKIDCSA-N (2s,3r,4s,5s,6r)-6-(hydroxymethyl)oxane-2,3,4,5-tetrol;hydrate Chemical compound O.OC[C@H]1O[C@H](O)[C@H](O)[C@@H](O)[C@@H]1O OSNSWKAZFASRNG-WNFIKIDCSA-N 0.000 description 2
- HNSDLXPSAYFUHK-UHFFFAOYSA-N 1,4-bis(2-ethylhexyl) sulfosuccinate Chemical compound CCCCC(CC)COC(=O)CC(S(O)(=O)=O)C(=O)OCC(CC)CCCC HNSDLXPSAYFUHK-UHFFFAOYSA-N 0.000 description 2
- IGIDLTISMCAULB-UHFFFAOYSA-N 3-methylvaleric acid Chemical compound CCC(C)CC(O)=O IGIDLTISMCAULB-UHFFFAOYSA-N 0.000 description 2
- 229920001817 Agar Polymers 0.000 description 2
- 108010062877 Bacteriocins Proteins 0.000 description 2
- YASYEJJMZJALEJ-UHFFFAOYSA-N Citric acid monohydrate Chemical compound O.OC(=O)CC(O)(C(O)=O)CC(O)=O YASYEJJMZJALEJ-UHFFFAOYSA-N 0.000 description 2
- LKDRXBCSQODPBY-VRPWFDPXSA-N D-fructopyranose Chemical compound OCC1(O)OC[C@@H](O)[C@@H](O)[C@@H]1O LKDRXBCSQODPBY-VRPWFDPXSA-N 0.000 description 2
- 241000588724 Escherichia coli Species 0.000 description 2
- 244000068988 Glycine max Species 0.000 description 2
- 235000010469 Glycine max Nutrition 0.000 description 2
- 241000588748 Klebsiella Species 0.000 description 2
- 241000186869 Lactobacillus salivarius Species 0.000 description 2
- 241000192132 Leuconostoc Species 0.000 description 2
- 239000012901 Milli-Q water Substances 0.000 description 2
- 241000192001 Pediococcus Species 0.000 description 2
- 239000001888 Peptone Substances 0.000 description 2
- 108010080698 Peptones Proteins 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- 241000282849 Ruminantia Species 0.000 description 2
- 241000607142 Salmonella Species 0.000 description 2
- 229920002472 Starch Polymers 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 239000008272 agar Substances 0.000 description 2
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 2
- SRBFZHDQGSBBOR-KLVWXMOXSA-N beta-L-arabinopyranose Chemical compound O[C@H]1CO[C@H](O)[C@H](O)[C@H]1O SRBFZHDQGSBBOR-KLVWXMOXSA-N 0.000 description 2
- 229940041514 candida albicans extract Drugs 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 229910002092 carbon dioxide Inorganic materials 0.000 description 2
- 229960002303 citric acid monohydrate Drugs 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- 239000012153 distilled water Substances 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- 235000019441 ethanol Nutrition 0.000 description 2
- 229960002737 fructose Drugs 0.000 description 2
- 230000014509 gene expression Effects 0.000 description 2
- 150000002402 hexoses Chemical class 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 229940116298 l- malic acid Drugs 0.000 description 2
- 235000011090 malic acid Nutrition 0.000 description 2
- JSPANIZMKMFECH-UHFFFAOYSA-L manganese(II) sulfate dihydrate Chemical compound O.O.[Mn+2].[O-]S([O-])(=O)=O JSPANIZMKMFECH-UHFFFAOYSA-L 0.000 description 2
- 230000002906 microbiologic effect Effects 0.000 description 2
- 230000003278 mimic effect Effects 0.000 description 2
- 235000016709 nutrition Nutrition 0.000 description 2
- 235000019319 peptone Nutrition 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- 230000008092 positive effect Effects 0.000 description 2
- VWDWKYIASSYTQR-UHFFFAOYSA-N sodium nitrate Chemical compound [Na+].[O-][N+]([O-])=O VWDWKYIASSYTQR-UHFFFAOYSA-N 0.000 description 2
- 239000007921 spray Substances 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 239000008107 starch Substances 0.000 description 2
- 239000001384 succinic acid Substances 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 239000003039 volatile agent Substances 0.000 description 2
- 239000012138 yeast extract Substances 0.000 description 2
- NFBQIWJDUKFHJP-SQOUGZDYSA-N (2r,3s,4r,5r)-3,4,5,6-tetrahydroxy-2-phosphonooxyhexanoic acid Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](C(O)=O)OP(O)(O)=O NFBQIWJDUKFHJP-SQOUGZDYSA-N 0.000 description 1
- 241000193155 Clostridium botulinum Species 0.000 description 1
- 241000193171 Clostridium butyricum Species 0.000 description 1
- 241000193468 Clostridium perfringens Species 0.000 description 1
- 241000193470 Clostridium sporogenes Species 0.000 description 1
- 241000193452 Clostridium tyrobutyricum Species 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 240000001046 Lactobacillus acidophilus Species 0.000 description 1
- 235000013956 Lactobacillus acidophilus Nutrition 0.000 description 1
- 244000199866 Lactobacillus casei Species 0.000 description 1
- 235000013958 Lactobacillus casei Nutrition 0.000 description 1
- 241001134659 Lactobacillus curvatus Species 0.000 description 1
- 241000186673 Lactobacillus delbrueckii Species 0.000 description 1
- 240000002605 Lactobacillus helveticus Species 0.000 description 1
- 235000013967 Lactobacillus helveticus Nutrition 0.000 description 1
- 241000186612 Lactobacillus sakei Species 0.000 description 1
- 240000003483 Leersia hexandra Species 0.000 description 1
- 240000004658 Medicago sativa Species 0.000 description 1
- 235000010624 Medicago sativa Nutrition 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 241000202223 Oenococcus Species 0.000 description 1
- 239000004695 Polyether sulfone Substances 0.000 description 1
- 241000607768 Shigella Species 0.000 description 1
- 241000194017 Streptococcus Species 0.000 description 1
- 241000607479 Yersinia pestis Species 0.000 description 1
- 235000007244 Zea mays Nutrition 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- XKMRRTOUMJRJIA-UHFFFAOYSA-N ammonia nh3 Chemical compound N.N XKMRRTOUMJRJIA-UHFFFAOYSA-N 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 229940077731 carbohydrate nutrients Drugs 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 235000013339 cereals Nutrition 0.000 description 1
- 239000013066 combination product Substances 0.000 description 1
- 229940127555 combination product Drugs 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 238000004821 distillation Methods 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 235000021107 fermented food Nutrition 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 238000007710 freezing Methods 0.000 description 1
- 230000008014 freezing Effects 0.000 description 1
- 238000004817 gas chromatography Methods 0.000 description 1
- 238000001030 gas--liquid chromatography Methods 0.000 description 1
- 229960001031 glucose Drugs 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 125000002791 glucosyl group Chemical group C1([C@H](O)[C@@H](O)[C@H](O)[C@H](O1)CO)* 0.000 description 1
- 230000034659 glycolysis Effects 0.000 description 1
- 239000004312 hexamethylene tetramine Substances 0.000 description 1
- 235000010299 hexamethylene tetramine Nutrition 0.000 description 1
- VKYKSIONXSXAKP-UHFFFAOYSA-N hexamethylenetetramine Chemical compound C1N(C2)CN3CN1CN2C3 VKYKSIONXSXAKP-UHFFFAOYSA-N 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 238000009533 lab test Methods 0.000 description 1
- 229940039695 lactobacillus acidophilus Drugs 0.000 description 1
- 229940017800 lactobacillus casei Drugs 0.000 description 1
- 229940054346 lactobacillus helveticus Drugs 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 230000002879 macerating effect Effects 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 244000000010 microbial pathogen Species 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- LWGJTAZLEJHCPA-UHFFFAOYSA-N n-(2-chloroethyl)-n-nitrosomorpholine-4-carboxamide Chemical compound ClCCN(N=O)C(=O)N1CCOCC1 LWGJTAZLEJHCPA-UHFFFAOYSA-N 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 150000002823 nitrates Chemical class 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 150000002972 pentoses Chemical class 0.000 description 1
- 229920006393 polyether sulfone Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 230000005070 ripening Effects 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 239000004317 sodium nitrate Substances 0.000 description 1
- 235000010344 sodium nitrate Nutrition 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 238000005507 spraying Methods 0.000 description 1
- 239000012086 standard solution Substances 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 230000009897 systematic effect Effects 0.000 description 1
- 235000019640 taste Nutrition 0.000 description 1
- 238000005303 weighing Methods 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23K—FODDER
- A23K30/00—Processes specially adapted for preservation of materials in order to produce animal feeding-stuffs
- A23K30/10—Processes specially adapted for preservation of materials in order to produce animal feeding-stuffs of green fodder
- A23K30/15—Processes specially adapted for preservation of materials in order to produce animal feeding-stuffs of green fodder using chemicals or microorganisms for ensilaging
- A23K30/18—Processes specially adapted for preservation of materials in order to produce animal feeding-stuffs of green fodder using chemicals or microorganisms for ensilaging using microorganisms or enzymes
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23K—FODDER
- A23K10/00—Animal feeding-stuffs
- A23K10/10—Animal feeding-stuffs obtained by microbiological or biochemical processes
- A23K10/16—Addition of microorganisms or extracts thereof, e.g. single-cell proteins, to feeding-stuff compositions
- A23K10/18—Addition of microorganisms or extracts thereof, e.g. single-cell proteins, to feeding-stuff compositions of live microorganisms
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2400/00—Lactic or propionic acid bacteria
- A23V2400/11—Lactobacillus
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2400/00—Lactic or propionic acid bacteria
- A23V2400/11—Lactobacillus
- A23V2400/157—Lactis
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Microbiology (AREA)
- Polymers & Plastics (AREA)
- Engineering & Computer Science (AREA)
- Food Science & Technology (AREA)
- Animal Husbandry (AREA)
- Zoology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Molecular Biology (AREA)
- Physiology (AREA)
- Fodder In General (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
Un inóculo de ensilaje que, como componentes activos, solo comprende (a) bacterias ácido lácticas heterofermentadoras obligatorias de al menos una de las especies Lactobacillus brevis, Lactobacillus buchneri, Lactobacillus fermentum, y Lactobacillus reuteri; y (b) bacterias ácido lácticas homofermentadoras de al menos una de las especies Enterococcus y Lactococcus que no reducen el crecimiento de (a) y que reducen el pH con rapidez sin producir una cantidad excesiva de ácido láctico.
Description
DESCRIPCIÓN
Composiciones mejoradas de especies de bacterias ácido lácticas hetera- y homofermentadoras para la conservación del ensilaje de doble función
Campo de la invención
La presente invención proporciona un inóculo de ensilaje que, como componentes activos, solo comprende (a) bacterias ácido lácticas heterofermentadoras obligatorias de al menos una de las especies Lactobacillus brevis, Lactobacillus buchneri, Lactobacillus fermentum, y Lactobacillus reuteri, y (b) bacterias ácido lácticas homofermentadoras de al menos una de las especies Enterococcus y Lactococcus que no reducen el crecimiento de (a) y que reducen el pH con rapidez sin producir una cantidad excesiva de ácido láctico. Las composiciones son útiles para producir un producto de pienso fermentado, tal como ensilaje. Por tanto, la invención también proporciona métodos para producir un producto alimentario fermentado, y dicho método comprende inocular un material vegetal con el inóculo de ensilaje descrito en la presente. En algunas realizaciones, el material vegetal inoculado es adecuado para su uso después de un periodo corto de incubación, tal como un periodo de incubación de 2, 3, 4, 5, 6, 7 u 8 días.
Antecedentes de la invención
El ensilaje es un producto vegetal fermentado que puede usarse para alimentar a rumiantes. El ensilaje puede prepararse a partir de diversos materiales vegetales que se conservan bajo condiciones anaerobias para estimular la fermentación anaerobia. Pueden añadirse inóculos bacterianos para estimular el proceso de fermentación y/o para mejorar el producto de ensilaje. El ensilaje se conserva estableciendo unas condiciones anaerobias y mediante la reducción rápida del pH asociada con la producción de ácidos orgánicos por las bacterias nativas o bacterias ácido lácticas inoculadas. El pH bajo inhibe el crecimiento de muchas cepas de descomposición que, de otro modo, podrían provocar la pérdida de una gran cantidad de nutrientes.
Cuando el ensilaje se expone al aire, tal como cuando el búnker, el silo, la pila o la paca de ensilaje se abre para acceder al ensilaje para su uso, las condiciones aerobias pueden provocar el crecimiento de cualquier cepa de descomposición aerobia presente en el ensilaje. El crecimiento de cepas de descomposición aerobias provoca un aumento de la temperatura y una elevada pérdida de nutrientes.
Así, la descomposición al inicio del proceso de fermentación y la descomposición aerobia cuando se extrae el ensilaje para el uso representan fuentes de pérdidas económicas significativas para los agricultores.
La primera generación de inóculos de ensilaje bacterianos incluye especies bacterias homofermentadoras obligatorias (por ejemplo, L. acidophilius, L. salivarius) y heterofermentadoras facultativas (por ejemplo, L. plantarum) dirigidas a reducir el pH con rapidez para evitar el crecimiento de cepas de descomposición que aparecen de modo natural en el material vegetal, tales como las Enterobacteraceae Gram-negativas (por ejemplo, Salmonella, Escherichia coli, Yersinia pestis, Klebsiella, Shigella) o Clostridia Gram-positivas (C. tyrobutyricum, C. perfringens, C. botulinum, C. sporogenes, C. butyricum). La prevención de las cepas de descomposición mediante la reducción rápida del pH reduce la pérdida de nutrientes y, a menudo, mejora en algún grado la estabilidad aerobia (Jatkauskas et al. (2013), Jatkauskas y Vrotniakiene (2013)).
La segunda generación de inóculos de ensilaje bacterianos se centra en L. buchneri, una especie heterofermentadora obligatoria, que se descubrió que tenía una actuación mejor con respecto a evitar la descomposición aerobia realizada por las cepas de descomposición aerobias en el momento de usar el ensilaje, cuando el búnker/pial de ensilaje se expone al aire. Sin embargo, un inconveniente de utilizar L. buchneri como inóculo de ensilaje bacteriano consiste en que tiene una fase de retraso más larga comparada con otras especies y que, en la etapa temprana de la fermentación, su producción de ácido acético y ácido láctico no disminuye con rapidez el pH cuando se compara con especies homofermentadoras obligatorias o heterofermentadoras facultativas. La figura 1 de Jatkauskas y Vrotniakiene (2013) muestra que L. buchneri por sí solo (P0) es mejor comparado con los otros productos ensayados con respecto a la estabilidad aerobia, es decir, el tiempo que tardan las cepas de descomposición aerobias en calentar un búnker de ensilaje cuando se reexpone al aire. El segundo mejor producto para mantener baja la temperatura durante muchas horas fue un producto de combinación de heterofermentador obligatorio/heterofermentador facultativo/homofermentador que contenía L. buchneri, L. plantarum, E. faecium (P1), y los siguientes mejores productos eran productos puramente de heterofermentador facultativo/homofermentador que contenían L. plantarum, E. faecium, L. lactis con benzoato de sodio (P2a) o sin benzoato de sodio (P2b), un producto de heterofermentador facultativo/homofermentador que contenía L. plantarum, E. faecium, L. lactis (P3), y un producto de heterofermentador facultativo que contenía dos cepas de L. plantarum (P4) (el ensilaje que no se inoculó presentó la estabilidad aerobia más baja).
Por tanto, siguen siendo necesarias composiciones mejores de inóculos de ensilaje bacterianos.
Sumario de la invención
Se proporcionan composiciones de inóculos bacterianos mejoradas útiles, por ejemplo, para la producción y la conservación del ensilaje. También se proporcionan métodos que comprenden inocular un material vegetal con los inóculos de ensilaje descritos en la presente.
La presente invención proporciona un inóculo de ensilaje que, como componentes activos, solo comprende (a) bacterias ácido lácticas heterofermentadoras obligatorias de al menos una de las especies Lactobacillus brevis, Lactobacillus buchneri, Lactobacillus fermentum, y Lactobacillus reuteri , y (b) bacterias homofermentadoras de al menos una de las especies Enterococcus y Lactococcus que no reducen el crecimiento de (a) y que reducen el pH con rapidez sin producir una cantidad excesiva de ácido láctico. En algunas realizaciones, las bacterias ácido lácticas heterofermentadoras obligatorias son de la cepa Lactobacillus buchneri depositada como DSM 22501. En algunas realizaciones, al menos una de las especies bacterianas homofermentadoras es un Enterococcus, por ejemplo, un Enterococcus faecium. En algunas realizaciones, al menos una de las especies bacterianas homofermentadoras es un Lactococcus, tal como un Lactococcus lactis, tal como la cepa depositada como DSM 11037. En realizaciones específicas, los inóculos de ensilaje consisten fundamentalmente en un Lactobacillus buchneri y un Lactococcus.
En algunas realizaciones, se proporcionan métodos para producir un producto de pienso fermentado, y dicho método comprende inocular un material vegetal con un inóculo de ensilaje como se describe en la presente. En algunas realizaciones, el material vegetal se incuba con el inóculo de ensilaje durante un periodo de hasta 2 días, o hasta 4 días, o hasta 7 días, o hasta 8 días, o hasta 14 días, o hasta 28 días, o al menos 90 días.
Descripción detallada de la invención
Tal como se indicó anteriormente, la presente invención proporciona inóculos de ensilaje mejorados útiles, por ejemplo, para la producción y la conservación del ensilaje. En realizaciones específicas, el inóculo de ensilaje solo comprende, como componentes activos: (a) bacterias ácido lácticas heterofermentadoras obligatorias de al menos una de las especies Lactobacillus brevis, Lactobacillus buchneri, Lactobacillus fermentum, y Lactobacillus reuteri, y (b) bacterias ácido lácticas homofermentadoras de al menos una de las especies Enterococcus y Lactococcus que no reducen el crecimiento de (a) y que reducen el pH con rapidez sin producir una cantidad excesiva de ácido láctico. Las composiciones son útiles para producir un producto de pienso fermentado, tal como ensilaje. Por tanto, también se proporcionan métodos que comprenden inocular un material vegetal con el inóculo de ensilaje descrito en la presente. En algunas realizaciones, el material inoculado es adecuado para su uso después de un periodo corto de incubación.
Definiciones
Debe considerarse que el uso de los términos "un/una" y "el/la" y referentes similares en el contexto de la descripción de la invención (en especial en el contexto de las reivindicaciones que aparecen a continuación) abarca el singular y el plural, a menos que se indique lo contrario en la presente o que el contexto lo contradiga claramente. Los términos "comprende", "tiene", "incluye" y "contiene" deben considerarse términos abiertos (es decir, que significan "incluye, pero no se limita a") a menos que se indique lo contrario. La indicación de intervalos de valores en la presente solo pretende servir como un método abreviado de referirse individualmente a cada valor distinto que se encuentra dentro del intervalo, a menos que en la presente se indique lo contrario, y cada valor distinto se incorpora en la memoria descriptiva del mismo modo que si se mencionase individualmente en la presente. Todas las etapas de los métodos descritos en la presente pueden realizarse en cualquier orden adecuado, a menos que se indique lo contrario en la presente o que el contexto lo contradiga claramente. El uso de cualquiera y todos los ejemplos, o expresiones que indican ejemplos (por ejemplo, "tal como") proporcionadas en la presente solo pretende describir mejor la invención, y no plantea una limitación del alcance de la invención, a menos que se reivindique de otro modo. Ninguna de las expresiones de la memoria descriptiva debe interpretarse como que indique cualquier elemento no reivindicado como fundamental para la práctica de la invención.
Las bacterias ácido lácticas incluyen géneros tales como Lactococcus spp., Enterococcus spp., Oenococcus spp., Pediococcus spp., Streptococcus spp., Leuconostoc spp. y Lactobacillus spp. Pueden dividirse en tres subgrupos: heterofermentadoras obligatorias, heterofermentadoras facultativas y homofermentadoras. Las bacterias ácido lácticas del género Lactobacillus pueden ser heterofermentadoras facultativas u homofermentadoras, dependiendo de la especie (Vandamme et al., 1996).
Las bacterias ácido lácticas heterofermentadoras obligatorias fermentan las hexosas para producir ácido láctico, ácido acético y dióxido de carbono por medio de la vía de fosfo-gluconato. Los ejemplos de especies de bacterias ácido lácticas heterofermentadoras obligatorias son Leuconostoc y Lactobacillus, tales como Lactobacillus brevis, Lactobacillus buchneri, Lactobacillus fermentum, Lactobacillus reuteri.
Las bacterias ácido lácticas heterofermentadoras facultativas también pueden fermentar las pentosas para producir ácido láctico, ácido acético y ácido fórmico y etanol, cuando existe limitación de glucosa. Los ejemplos de bacterias ácido lácticas heterofermentadoras facultativas son Pediococcus spp., Lactobacillus casei, Lactobacillus curvatus, Lactobacillus plantarum, Lactobacillus sakei.
Las bacterias ácido lácticas homofermentadoras se definen como bacterias que degradan principalmente hexosas a través de la vía de Embden-Meyerhof para producir ácido láctico. Los ejemplos de bacterias ácido lácticas homofermentadoras son Lactococcus spp., Enterococcus spp. y Lactobacillus, tales como Lactobacillus acidophilus, Lactobacillus delbrueckii, Lactobacillus helveticus, Lactobacillus salivarius.
Muchos productos del mercado combinan cepas heterofermentadoras facultativas/homofermentadoras de alta producción de ácido láctico con L. buchneri. Sin embargo, los presentes inventores han descubierto que esta combinación de bacterias no logra la mejor estabilidad aerobia posible (es decir, no estimula el mantenimiento de la temperatura ambiente en el momento de usar el ensilaje). Aunque no se pretenda limitación alguna por la teoría, los inventores creen que esta combinación de bacterias reduce el crecimiento de L. buchneri y/o produce cantidades elevadas de ácido láctico que puede ser utilizado por las cepas de descomposición aerobias, con lo cual se inicia el deterioro del ensilaje tras su exposición al aire. Según algunas realizaciones, los inóculos descritos en la presente solucionan este problema combinando una especie heterofermentadora obligatoria (por ejemplo, L. buchneri) con especies bacterianas que reducen el pH con rapidez sin producir una cantidad excesiva de ácido láctico (por ejemplo, Lactococcus y Enterococcus). Estas especies homofermentadoras seleccionadas no contrarrestan el efecto positivo de las especies heterofermentadoras obligatorias, o al menos lo hacen en un grado mucho menor.
Por tanto, en algunas realizaciones, la presente invención proporciona un inóculo de ensilaje que, como componentes activos, solo comprende (a) bacterias ácido lácticas heterofermentadoras obligatorias de al menos una de las especies Lactobacillus brevis, Lactobacillus buchneri, Lactobacillus fermentum, y Lactobacillus reuteri, y (b) bacterias ácido lácticas homofermentadoras de al menos una de las especies Enterococcus y Lactococcus que no reducen el crecimiento de las bacterias ácido lácticas heterofermentadoras obligatorias y que reducen el pH con rapidez sin producir una cantidad excesiva de ácido láctico.
"Consiste fundamentalmente en" significa que el inóculo de ensilaje solo comprende las bacterias especificadas como componentes activos, y no comprende otro u otros componentes activos, tales como cualquier otra bacteria, enzima, ácido orgánico, benzoato de sodio, nitrato de sodio o hexamina. Un inóculo, tal como se describe en la presente, que consiste fundamentalmente en las bacterias especificadas no incluye Lactobacillus plantarum.
La expresión "al menos una" significa que la composición de inóculo puede comprender una, dos, tres o cuatro especies diferentes de bacterias ácido lácticas heterofermentadoras obligatorias, y una o dos especies bacterianas homofermentadoras diferentes.
Las bacterias ácido lácticas homofermentadoras de al menos una de las especies Enterococcus y Lactococcus no reducen el crecimiento de las bacterias ácido lácticas heterofermentadoras obligatorias. Esta propiedad puede ensayarse cultivando cepas las bacterianas homofermentadoras y cepas de bacterias ácido lácticas heterofermentadoras obligatorias durante la noche en medio de Mann-Rogosa-Sharpe (MRS) a 37°C, sembrando en estrías ambas cepas o especies bacterianas homofermentadoras y las cepas o especies de bacterias ácido lácticas heterofermentadoras obligatorias que se van a ensayar sobre la misma placa de agar MRS sustancialmente al mismo tiempo, y después incubando la placa de agar bajo condiciones anaerobias a 37°C durante la noche. Si el crecimiento de las bacterias ácido lácticas heterofermentadoras obligatorias es inhibido en al menos 5 mm, entonces la especie o cepa homofermentadora ensayada no tiene esta propiedad deseada. Si el inóculo de ensilaje incluye más de una especie o cepa de bacterias ácido lácticas heterofermentadoras obligatorias o más de una especie o cepa bacteriana homofermentadora, se ensayan todas las combinaciones pertinentes.
Mediante este tipo de ensayos, se ha descubierto que ciertas cepas productoras de nisina de la especie homofermentadora Lactobacillus lactis, tales como L. lactis NCIMB 30l17 y L. lactis ATCC 11454, inhiben a L. buchneri DSM 22501, mientras que L. lactis DSM 11037 y E. faecium DSM 16656, que son cepas que no producen nisina, no inhiben a L. buchneri DSM 22501.
Aunque no se pretenda limitación alguna por la teoría, estos resultados indican que solo las cepas homofermentadoras productoras de nisina de la especie Lactobacillus lactis inhiben la especie o cepa heterofermentadora obligatoria, y que las cepas o especies homofermentadoras que producen bacteriocina que no producen nisina no inhiben la especie o cepa heterofermentadora obligatoria. Por consiguiente, el requisito de que al menos una especie o cepa bacteriana homofermentadora no reduzca el crecimiento de al menos una especie de bacteria ácido láctica heterofermentadora obligatoria puede cumplirse si la especie o cepa bacteriana homofermentadora no produce nisina. Así, en realizaciones específicas, la especie o cepa homofermentadora es una especie o cepa homofermentadora que produce bacteriocina que no produce nisina, aunque una selección directa, tal como se bosquejó anteriormente, puede identificar otras cepas que muestren esta propiedad. La invención indica que el inóculo de ensilaje consiste fundamentalmente en al menos una especie de bacteria ácido láctica heterofermentadora obligatoria (o una de sus cepas) y al menos una especie bacteriana homofermentadora (o una de sus cepas) que (i) no produce nisina, y (ii) reduce el pH con rapidez sin producir una cantidad excesiva de ácido láctico.
En realizaciones específicas, la especie o cepa bacteriana homofermentadora reduce el pH con rapidez sin producir una cantidad excesiva de ácido láctico. Tal como se indicó anteriormente, una reducción rápida en el pH puede inhibir la descomposición en etapas tempranas de la producción de ensilaje, mediante la inhibición del crecimiento
de microorganismos de descomposición, tales como Clostridia, Enterobacteriaceae, levaduras y mohos. Los microorganismos de descomposición pueden conducir a la pérdida de nutrientes, el crecimiento de microorganismos patógenos, y sabores desagradables que hacen que el ensilaje sea menos agradable de comer para los animales, tales como rumiantes, a los cuales se le suministra como alimento.
Tal como se emplea en la presente, "una especie o cepa que reduce el pH con rapidez sin producir una cantidad excesiva de ácido láctico" se define como una especie o cepa que no produce más de 3 mg/ml de ácido láctico después de 24 horas de la inoculación en un baño de agua a 30°C de un tubo que contiene 150.000 CFU/ml de la cepa en 10 ml de medio de ensilaje estéril producido mezclando 5 g/l de extracto de levadura (Oxoid L21), 5 g/l de peptona de soja neutralizada (Oxoid LP0044C), 0,8 g/l de almidón soluble (Merck 1252), 0,08 g/l de sulfato de manganeso(II) dihidrato (Sigma M-1114), 0,037 g/l de ácido succínico (laboratorio de ensayo), 0,069 g/l de ácido cítrico monohidrato, y 0,14 ácido L-málico (Merck 244) en 900 ml de agua Milli Q hasta que se disuelven, ajustando el pH a 6,3, distribuyendo en botellas pequeñas y sometiendo a autoclave a 121°C durante 15 minutos, y después añadiendo 100 ml de disolución de azúcar filtrada estéril que contiene 56 g/l de D(-)-fructosa (Merck 4007), 32 g/l de D(+)-glucosa monohidrato (Merck 8342), 20 g/l de D(+)-xilosa (Merck 8689), 20 g/l de L(+)-arabinosa (Aldrich A9, 190-6), y 32 g/l de sacarosa (Merck 7651).
Según la presente invención, el inóculo de ensilaje incluye al menos una cepa de bacteria ácido láctica heterofermentadora obligatoria que es una especie de Lactobacillus seleccionada del grupo que consiste en Lactobacillus brevis, Lactobacillus buchneri, Lactobacillus fermentum, y Lactobacillus reuteri. En una realización específica, la cepa de bacteria ácido láctica heterofermentadora obligatoria es un Lactobacillus buchneri. Los ejemplos de Lactobacillus buchneri que se contemplan como útiles en la presente invención son L. buchneri KKP .907, L buchneri DSM 22963, L buchneri NCIMB 40788, L. buchneri NCIMB 30139, L. buchneri DSM 16774, L buchneri DSM 22963, L. buchneri DSM 12856. En realizaciones específicas, el Lactobacillus buchneri es la cepa de Lactobacillus buchneri depositada como DSM 22501.
En algunas realizaciones, el inóculo de ensilaje incluye al menos una especie o cepa bacteriana que reduce el pH con rapidez sin producir una cantidad excesiva de ácido láctico que es un Enterococcus, tal como un Enterococcus faecium. Los ejemplos de Enterococci que se contemplan como útiles en la presente invención son E. faecium NCIMB 10415, E. faecium CNCM I-3236, E faecium BIO 34 y E. faecium DSM 16573.
En otras realizaciones, el inóculo de ensilaje incluye al menos una especie o cepa bacteriana que reduce el pH con rapidez sin producir una cantidad excesiva de ácido láctico que es un Lactococcus, tal como un Lactococcus lactis. En realizaciones específicas, el Lactococcus lactis es la cepa depositada como DSM 11037.
Por tanto, en algunas realizaciones, el inóculo de ensilaje consiste fundamentalmente en una cepa de Lactobacillus buchneri y una cepa de Enterococcus que no reduce el crecimiento de la especie (o cepa) de bacteria ácido láctica heterofermentadora obligatoria y que reduce el pH con rapidez sin producir una cantidad excesiva de ácido láctico. En otras realizaciones, el inóculo de ensilaje consiste fundamentalmente en una cepa de Lactobacillus buchneri y una cepa de Lactococcus que no reduce el crecimiento de la especie (o cepa) de bacteria ácido láctica heterofermentadora obligatoria y que reduce el pH con rapidez sin producir una cantidad excesiva de ácido láctico. La presente invención también proporciona métodos para producir un producto de pienso fermentado, tal como un ensilaje, que comprende inocular un material vegetal con el inóculo de ensilaje bacteriano tal como se describe en la presente. Se ha descubierto, de modo sorprendente, que los inóculos de ensilaje descritos en la presente son capaces de proporcionar un efecto muy rápido, es decir, el material inoculado con un inóculo de ensilaje bacteriano, según se describe, puede resultar adecuado para su uso después de un periodo corto de incubación, tal como un periodo de incubación de tan solo 2, 3, 4, 5, 6, 7 u 8 días. Así, en algunas realizaciones, el método comprende incubar el material vegetal con un inóculo de ensilaje, según se describe en la presente, durante un periodo de hasta 2 días, o de hasta 4 días, antes de exponer el ensilaje al aire, tal como mediante la apertura del búnker de ensilaje. Sin embargo, el material vegetal también puede incubarse durante un periodo de tiempo más largo, tal como hasta 7 días, hasta 8 días, hasta 14 días, o hasta 28 días, o incluso durante más tiempo, tal como un periodo de al menos 60 días o al menos 90 días, siendo este último el periodo convencional para ensayar el efecto de los inóculos de ensilaje.
Tal como se indicó anteriormente, en realizaciones específicas, los inóculos de ensilaje bacterianos descritos en la presente pueden lograr una reducción rápida del pH al inicio del proceso de ensilaje, manteniendo al mismo tiempo una elevada estabilidad aerobia en el momento del uso del ensilaje, es decir, los inóculos de ensilaje bacterianos descritos en la presente pueden mostrar una fermentación inicial rápida que reduce la pérdida de materia seca ("dry matter", DM) y la descomposición en la fase temprana de la fermentación, y también pueden lograr una estabilidad aerobia que es igual o comparable a la inoculación con una cepa heterofermentadora obligatoria, tal como L. buchneri por sí sola. Así, los inóculos descritos en la presente logran una mejor estabilidad aerobia que los productos que contienen solo cepas homofermentadoras o/y heterofermentadoras facultativas, aunque su estabilidad aerobia puede no ser tan buena como la que se logra con el heterofermentador obligatorio L. buchneri por sí solo.
Cepas depositadas
Una cepa de Lactobacillus plantarum ha sido depositada en DSMZ (Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH, Inhoffenstrasse 7B, D-38124 Braunschweig) con el número de registro DSM 16568 con la fecha de depósito del 13 de julio de 2004, por Chr. Hansen A/S, Dinamarca. El depósito se ha realizado bajo las condiciones del Tratado de Budapest sobre el Reconocimiento Internacional del Depósito de Microorganismos para los fines del Procedimiento en Materia de Patentes.
Una cepa de Lactobacillus buchneri ha sido depositada en DSMZ (Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH, Inhoffenstrasse 7B, D-38124 Braunschweig) con el número de registro DSM 22501 con la fecha de depósito del 22 de abril de 2009, por Chr. Hansen A/S, Dinamarca. El depósito se ha realizado bajo las condiciones del Tratado de Budapest sobre el Reconocimiento Internacional del Depósito de Microorganismos para lo fines del Procedimiento en Materia de Patentes.
Una cepa de Enterococcus faecium ha sido depositada en DSMZ (Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH, Inhoffenstrasse 7B, D-38124 Braunschweig) con el número de registro DSM 22502 con la fecha de depósito del 22 de abril de 2009, por Chr. Hansen A/S, Dinamarca. El depósito se ha realizado bajo las condiciones del Tratado de Budapest sobre el Reconocimiento Internacional del Depósito de Microorganismos para lo fines del Procedimiento en Materia de Patentes.
Para los microorganismos depositados identificados anteriormente, se aplican las siguientes indicaciones adicionales: con respecto a las respectivas Oficinas de Patentes de los respectivos estados designados, los solicitantes piden solo se dé acceso a una muestra de los microorganismos depositados mencionados anteriormente a un experto indicado por el peticionario hasta la fecha en que se conceda la patente, o hasta la fecha en que la solicitud se rechace o retire o se estime que se va a retirar.
La cepa de Lactobacillus lactis DSM 11037 ha sido depositada en DSMZ (Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH, Inhoffenstrasse 7B, D-38124 Braunschweig) el 26 de junio de 1996 por Chr. Hansen A/S, Dinamarca, y se menciona en la patente concedida EP 928333.
A continuación se describen realizaciones de la presente invención, como ejemplos no limitantes.
Leyenda de las figuras
Figura 1a: Reducción de pH a lo largo de 48 h de un medio de ensilaje estéril inoculado con la composición 1 (A), la composición 2 (□), la composición 3 (o), la composición 4 (0) y la composición 5 (X). La inoculación inicial fue de 150.000 CFU/ml y la temperatura se mantuvo a 30°C, n = 1.
Figura 1b: Concentración de ácido láctico en mg/ml a lo largo de 48 h de un medio de ensilaje estéril inoculado con la composición 1 (A), la composición 2 (□), la composición 3 (o), la composición 4 (0) y la composición 5 (X). La inoculación inicial fue de 150.000 CFU/ml y la temperatura se mantuvo a 30°C, n = 1.
Figura 1c: Concentración de ácido acético en mg/ml a lo largo de 48 h de un medio de ensilaje estéril inoculado con la composición 1 (A), la composición 2 (□), la composición 3 (o), la composición 4 (0) y la composición 5 (X). La inoculación inicial fue de 150.000 CFU/ml y la temperatura se mantuvo a 30°C.
Figura 2: Reducción de pH a lo largo de 72 h de un medio de ensilaje estéril inoculado con la composición 2 (□), la composición 4 (0) y la composición 6 (i— i) La inoculación inicial fue de 150.000 CFU/ml y la temperatura se mantuvo a 30°C.
Figura 3: Proporción de ácido acético/ácido láctico de maíz recolectado en 2011 en Dinamarca (minisilo 1) y no inoculado (barras blancas), o inoculado con la composición 4 (barras grises) o la composición 7 (barras negras). Las bolsas de vacío del minisilo se conservaron a 25°C hasta su apertura después de 7, 28, 61 y 88 días.
Figura 4: Estabilidad aerobia de maíz recolectado en 2012 en Dinamarca (minisilo 2) y no inoculado (^ H ), o inoculado con la composición 4 (0) o la composición 5 (X). En el eje de abscisas se encuentra el tiempo (h) y en el eje de ordenadas la temperatura (°C). La línea negra discontinua muestra la temperatura ambiente, mientras que la línea gris discontinua es la temperatura ambiente 3°C.
Figura 5. El pH del minisilo con ensilaje de maíz recolectado en 2012 (minisilo 2) después de siete días de exposición aerobia que incluye PEE de cuatro observaciones. No se inoculó (barra blanca), o se inoculó con la composición 4 (barra gris) o la composición 5 (barra punteada).
Figura 6: Estabilidad aerobia de maíz recolectado en 2013 en Dinamarca (minisilo 3) y no inoculado (^ H ), o inoculado con la composición 2 (□) o la composición 4 (0). En el eje de abscisas se encuentra el tiempo (h) y en el eje de ordenadas la temperatura (°C). La línea negra discontinua muestra la temperatura ambiente, mientras que la línea gris discontinua es la temperatura ambiente 3°C.
Figura 7: Estabilidad aerobia de forraje de maíz rojo recolectado en 2013 (minisilo 4) y no inoculado (^ H ), o
inoculado con la composición 2 (□), la composición 4 (0) y la composición 7 (A). En el eje de abscisas se encuentra el tiempo (h) y en el eje de ordenadas la temperatura (°C). La línea negra discontinua muestra la temperatura ambiente, mientras que la línea gris discontinua es la temperatura ambiente 3°C.
Figura 8: Estabilidad aerobia de forraje de trébol rojo:heno de Timothy:festuca recolectado en 2013 (minisilo 5) y no inoculado (^ H ), o inoculado con la composición 2 (□), la composición 4 (0) y la composición 7 (A). En el eje de abscisas se encuentra el tiempo (h) y en el eje de ordenadas la temperatura (°C). La línea negra discontinua muestra la temperatura ambiente, mientras que la línea gris discontinua es la temperatura ambiente 3°C.
Figura 9a: Estabilidad aerobia (horas) en ensilaje de maíz (minisilo 6a) después de 7 y 14 días de fermentación, seguido de 7 días de exposición aerobia (7+7 y 14+7, respectivamente) y no inoculado (blanco), o inoculado con la composición 4 (gris) o la composición 7 (negro).
Figura 9b: Estabilidad aerobia (horas) en ensilaje de maíz (minisilo 6b) después de 2, 4, y 8 días de fermentación, seguido de 7 días de exposición aerobia (2+7, 4+7, y 8+7, respectivamente) y no inoculado (blanco), o inoculado con la composición 4 (gris).
Figura 10: Número de levaduras (cfu/g) en ensilaje de maíz (minisilo 6a) después de 2, 7 y 14 días de fermentación y no inoculado (blanco), o inoculado con la composición 4 (gris) o la composición 7 (negro).
Figura 11: Desarrollo del pH de ensilaje de maíz (minisilo 6a) después de 2, 7 y 14 días de fermentación y no inoculado (blanco), o inoculado con la composición 4 (gris) o la composición 7 (negro).
Figura 12: Producción de gas acumulada a lo largo de 162 horas de maíz de recolectado en 2014 (minisilo 7a) y no inoculado (cuadrados grises) o inoculado con la composición 4 (círculos negros). En el eje de abscisas se encuentra el tiempo (h) y en el eje de ordenadas aparece el volumen en ml/g de forraje fresco.
Figura 13: Diferencia en la producción de gas entre un control y maíz inoculado con la composición 4 (minisilo 7b). En el eje de abscisas se encuentra el tiempo (h) y en el eje de ordenadas aparece la diferencia en volumen en ml/g de forraje fresco.
Figura 14: Porcentaje de pérdida de peso de maíz envasado al vacío recolectado en 2014 después de 162 horas (minisilo 7b) y no inoculado (blanco) o inoculado con la composición 4 (gris) o la composición 7 (negro).
Figura 15: Diferencia en la emisión de gas en maíz envasado al vacío recolectado en 2014 después de 6 días de fermentación. Bolsas envasadas al vacío de forraje sin inoculación (lado izquierdo de la fotografía) o con inoculación de la composición 4 (150.000 CFU/g de maíz, lado derecho de la fotografía).
Ejemplos
Ejemplo 1: Cultivos discontinuos in vitro estériles
Se ensayaron cepas individuales de bacterias ácido lácticas homofermentadoras y heterofermentadoras y productos de combinación en dos configuraciones experimentales independientes usando un medio de ensilaje estéril que contenía diversas fuentes de carbohidratos para imitar la composición de carbohidratos del pasto. El pH y el contenido en ácidos orgánicos se midieron a lo largo del tiempo. El medio contenía 5 g/l de extracto de levadura (Oxoid L21), 5 g/l de peptona de soja neutralizada (Oxoid LP0044C), 0,8 g/l de almidón soluble (Merck 1252), 0,08 g/l de sulfato de manganeso(II) dihidrato (Sigma M-1114), 0,037 g/l de ácido succínico (laboratorio de ensayo), 0,069 g/l de ácido cítrico monohidrato, y 0,14 ácido L-málico (Merck 244) que se mezclaron en 900 ml de agua Milli Q hasta que se disolvieron. El pH se ajustó a 6,3 y se distribuyó en botellas pequeñas y se sometió a autoclave a 121°C durante 15 minutos. Después de someter a autoclave, se añadieron 100 ml de una disolución de azúcar filtrada estéril que contenía 56 g/l de D(-)-fructosa (Merck 4007), 32 g/l de D(+)-glucosa monohidrato (Merck 8342), 20 g/l de D(+)-xilosa (Merck 8689), 20 g/l de L(+)-arabinosa (Aldrich A9, 190-6) y 32 g/l de sacarosa (Merck 7651) para obtener el medio de ensilaje final. En ambos experimentos 1 y 2 se usó el medio de ensilaje estéril y se inoculó con las diversas composiciones de inóculos diferentes indicadas en la tabla 1.
Tabla 1 - Composiciones usadas en los dos estudios de cultivos discontinuos in vitro
Experimento 1
Se distribuyeron 10 ml del medio de ensilaje inoculado con las diversas composiciones de inóculos de la tabla 1 en cada uno de siete tubos estériles y se mantuvieron en un baño de agua a 30°C. Después de 0, 2, 4, 6, 7, 8, 9, 11, 14, 24 y 48 horas, se tomaron muestras para el análisis de los ácidos orgánicos volátiles ("volatile organic acid", VFA) y del ácido láctico y el pH. El pH se controló usando un pH-metro manual, mientras que los ácidos orgánicos volátiles se analizaron con una HPLC (Dionex).
Experimento 2
El experimento 2 fue similar al experimento 1 con respecto al medio de ensilaje estéril, el nivel de inoculación y la temperatura. Se usaron las composiciones 2, 4 y 6 como inóculos. Se usó un pH-metro automático, y el ácido acético, el ácido láctico y el ácido fórmico se midieron con una HPLC (Dionex) después de 72 h.
Resultados
Se proporcionan los resultados de los experimentos 1 y 2 que muestran los efectos de las diversas composiciones de inóculos sobre el pH y el contenido en ácidos orgánicos en las figuras 1a, b, c y la figura 2, así como en la tabla 2. La figura 1a muestra el cambio en el pH a lo largo del tiempo del experimento 1. La composición 2 reduce el pH muy lentamente. La composición 1 y la composición 3 reducen el pH con mucha más rapidez y, después de 14 horas, el pH se encontraba por debajo de 5,0, mientras que la composición 2 aún mantenía un pH por encima de 6,0. La composición 4 reduce el pH con la misma rapidez que la composición 3. La composición 5 produjo una curva de pH muy similar a la composición 1.
La figura 1b muestra la concentración de ácido láctico a lo largo del tiempo del experimento 1. Después de 24 horas, la composición 1 produjo mucho más ácido láctico, comparado con la composición 2, la composición 3 o la composición 4. Después de 48 horas, la concentración de ácido láctico de la composición 1 era mayor que 8 mg/ml, en oposición a 4 mg/ml o menor con la composición 2, la composición 3 o la composición 4. La composición 5 produjo una concentración de ácido láctico muy similar a la composición 1.
La figura 1c muestra la concentración de ácido acético a lo largo del tiempo del experimento 1. Después de 48 horas, la composición 2 presentaba una concentración de ácido acético mayor que 2 mg/ml, mientras que la composición 1 y la composición 3 produjo menos de 0,5 mg/ml de ácido acético. La composición 4 produjo 1 mg/ml de ácido acético después de 48 horas, mientras que la composición 5 produjo una concentración menor que 0,5 mg/ml.
La figura 2 muestra el cambio en el pH a lo largo del tiempo del experimento 2. De nuevo, la composición 2 reduce el pH muy lentamente. La composición 4 reduce el pH con mucha más rapidez y, después de 15 horas, el pH se encontraba por debajo de 4,5, mientras que la composición 6 aún mantenía un pH por encima de 6,0. La composición 6 produjo una disminución en el pH ligeramente más lenta comparado con la composición 4. Sin embargo, la reducción en el pH continúa con rapidez y el pH ya se encontraba por debajo de 4,0 después de 18 horas. Después de 72 horas, el pH de la composición 2 y de la composición 4 alcanzó 3,6 y 3,7, respectivamente, mientras que la composición 6 bajó tanto como 3,2.
Tabla 2 - Producción de ácidos orgánicos del medio de ensilaje estéril inoculado después de 72 horas (experimento 2)
La tabla 2 muestra que la producción de ácido acético se redujo mucho con la composición 6, que contiene L. buchneri DSM 22501 y L. plantarum DSM 16568, por contraste con la composición 4, que contiene L. buchneri DSM 22501 y L. lactis DSM 11037. La composición 6 también mostró una alta concentración de ácido láctico después de 72 horas. La composición 4 no solo presenta una concentración de ácido acético mucho mayor, comparado con la composición 6, sino que también presenta una concentración alta de ácido fórmico.
Ejemplo 2: Estabilidad aerobia en minisilos
Minosilos 1, 2 y 3 - Recolección de maíz en 2011, 2012 y 2013, Dinamarca
Se configuraron cinco experimentos de minisilos diferentes para ensayar diversas composiciones de inóculos de ensilaje. Tres experimentos se configuraron en Dinamarca con el maíz recolectado de tres granjas diferentes en 2011 (minisilo 1), 2012 (minisilo 2) y 2013 (minisilo 3), y dos experimentos se llevaron a cabo en Lituania en 2013 usando maíz y trébol rojo:heno de Timothy:césped de festuca (60:30:10) (minisilos 4 y 5). En la tabla 3 se lista un resumen de los inóculos usados y las tasas de aplicación.
Tabla 3 - Composiciones de cepas usadas en los estudios de minisilos
Para el minisilo 1, el maíz se recolectó en el sudoeste de Jutlandia. El tiempo de transporte hasta el laboratorio fue de 4 horas. Después, el maíz se conservó durante la noche en el exterior antes de congelarse a -20°C. En el momento de la inoculación, el maíz se descongeló durante 1-2 horas y después se mantuvo en una nevera a 4-5°C. Los inóculos se suspendieron en agua del grifo y se introdujeron en botellas de pulverización. La dosificación deseada para cada tratamiento fue de 150.000 CFU/g de maíz, y la cantidad necesaria para alcanzar la dosificación deseada del inóculo se calculó basándose en la potencia real de las composiciones. Se pesaron 1000 g de maíz en una bolsa de plástico poco a poco, para que el inóculo pudiera pulverizarse de modo homogéneo sobre el maíz. La bolsa después se agitó para asegurar una distribución igualitaria del inóculo en la bolsa. Los 1000 g de maíz inoculados después se distribuyeron en cinco bolsas Alubag a 200 g en cada una para cada momento del tiempo (7, 28, 61 y 88 días). Las bolsas Alubag envasadas al vacío se conservaron a 25°C.
Se abrieron cinco bolsas Alubag por tratamiento en los diferentes momentos del tiempo. Las muestras después se ensayaron para ácidos orgánicos pequeños.
Para el minisilo 2, se recogió maíz recién recolectado de una granja en Zelandia central, Dinamarca, y se transportó inmediatamente al laboratorio. Se ensayaron los cinco tratamientos diferentes listados en la tabla 3, así como un grupo control en la configuración de minisilo. Los inóculos se suspendieron en agua del grifo y se introdujeron en
botellas de pulverización. La dosificación deseada para cada tratamiento fue de 150.000 CFU/g de maíz, y la cantidad necesaria para alcanzar el inóculo deseado se calculó basándose en la potencia real de las composiciones. Se pesaron 1000 gramos de maíz en una bolsa de plástico poco a poco, para que el inóculo pudiera pulverizarse de modo homogéneo sobre el maíz. Después de agitar la bolsa para asegurarse de una mejor distribución del inóculo, la bolsa se envasó al vacío. Se prepararon cuatro bolsas de cada tratamiento y se conservaron a 25°C para su posterior análisis después de tres meses. Después de tres meses se configuró un estudio de estabilidad aerobia usando el ensilaje que se había conservado en bolsas de vacío. El ensilaje se distribuyó en recipientes (botellas de plástico abiertas en su parte superior y con un orificio en la parte inferior) con un detector de temperatura localizado en la parte intermedia, se colocaron en un nicho de poliestireno, se cubrieron con una placa de plástico grande y se conservaron a temperatura ambiente. Se controló la temperatura de cada muestra individual después de su exposición al aire a lo largo de un periodo de 7 días.
Para el minisilo 3, se recogió maíz recién recolectado de una granja del noreste de Zelandia. El procedimiento fue el mismo que el descrito para el minisilo 2, excepto que el estudio de estabilidad aerobia se realizó después de tan solo dos semanas.
Resultados de los minisilos 1, 2 y 3
En la figura 3 se muestran las proporciones de ácido acético a ácido láctico en el ensilaje del minisilo 1 a diferentes momentos. La proporción de ácido acético a ácido láctico es mayor en el control no inoculado comparado con la composición 7 después de siete días y después de 28 días. Sin embargo, después de 88 días, la composición 7 presenta una elevada proporción de ácido acético a ácido láctico comparado con el control. La composición 4 presenta una elevada proporción de ácido acético a ácido láctico desde el día siete, que aumenta a lo largo del tiempo. El pH promedio de todas las muestras fue menor que 4,0 en todos los momentos.
Los resultados del minisilo 2 se muestran en la figura 4. Puede observarse que la temperatura del ensilaje control no inoculado estaba a más de 3°C por encima de la temperatura ambiente después de 78 horas, mientras que con la composición 5 aumentó por encima de 3°C de la temperatura ambiente después de 96 horas. La composición 4 mantuvo el ensilaje de maíz estable durante las 162 horas de mediciones. Tal como se muestra en la figura 5, después de 162 horas, el pH del control se encontraba a un promedio de 6,74, mientras que el ensilaje tratado con la composición 5 presentaba un pH promedio de 5,67 y la composición 4 presentaba un pH promedio de 4,05.
Para el minisilo 3, el ensilaje envasado al vacío abierto después de la conservación que no se había inoculado resultó inestable después de 93 horas, mientras que el ensilaje inoculado con la composición 2 fue estable durante todo el periodo de 160 horas, y el ensilaje inoculado con la composición 4 fue estable durante 129 horas (figura 6). Minosilos 4 y 5 - Recolección de maíz y pasto/trébol en 2013, Lituania
Para el mini-silo 4, se recolectó maíz (Zea mays L.) en el estadio masoso de la maduración del grano. La concentración de materia seca (DM) del maíz era del 38,85 % y la concentración de carbohidratos hidrosolubles era del 2,54 %. El maíz se cortó mediante una cosechadora de forraje bajo condiciones de granja en trozos con una longitud de aproximadamente 2 cm.
Para el minisilo 5, se recolectó una mezcla de pasto y trébol que contenía 60% de trébol rojo, 30% de heno Timothy y 10% de césped de festuca y se secó hasta alcanzar 32,8 % de materia seca. Esta mezcla de forraje se denomina mezcla de pasto/trébol. El contenido en carbohidratos hidrosolubles era de 20,3 g/kg de DM (2,03 % de forraje fresco). La mezcla de pasto/trébol se cortó mediante una cosechadora de forraje bajo condiciones de granja en trozos con una longitud de 2-3 cm.
En el minisilo 4 y el minisilo 5, se tomaron cinco muestras representativas (>500 g cada una) para el análisis del valor nutricional de los forrajes y el tratamiento. Los forrajes se transportaron en una bolsa de polietileno hasta el laboratorio. Los experimentos en el laboratorio comenzaron dentro de 0,5 h desde la preparación de la cosecha. Se tomó una muestra representativa de 500 g de hierba marchita y cortada para los análisis del valor nutricional, capacidad tampón, nitratos y composición microbiana. Se usaron los mismos inóculos de ensilaje y procedimientos en los ensayos de maíz y de forraje de pasto/trébol.
El inóculo de ensilaje se suspendió en agua destilada inmediatamente antes de su aplicación hasta una dosis deseada como se describe en la tabla 3. Se realizaron cinco duplicados para cada tratamiento. Las tasas de aplicación de los productos se calcularon según la dosis indicada en la tabla 3 y la concentración bacteriana real de los productos. Se usó agua sin cloro en la dilución de los productos. Se empleó el mismo volumen de agua destilada en lugar de la suspensión en el tratamiento control (para la fermentación espontánea). Después de la inoculación, se rellenaron tarros de vidrio de 3 l con 1,80-1,84 kg de la cosecha fresca que es igual a 1 kg de DM por 5 litros de volumen. Los tarros se cerraron con tapas 15 min después de ser rellenados. La producción de gas durante la fermentación se liberó con un purgador de gas durante el experimento. Después de 90 días de conservación en los tarros de vidrio a una temperatura constante de 20°C, se realizaron los análisis químicos y microbianos.
Para medir la estabilidad aerobia de los ensilajes, se controló la temperatura dentro del ensilaje durante 10 días. Para ello, se insertaron cables de termopares en el punto intermedio de las muestras de ensilaje que se colocaron
en cajas de poliestireno abiertas. La parte superior e inferior de las cajas contenían un orificio de 2 cm de diámetro para permitir la entrada del aire y la salida del CO2. Se colocó un transductor en el centro de la masa del ensilaje a través de un orificio en la cubierta de la caja, que expone el ensilaje al aire. Estos ensilajes no se tocaron durante el periodo de registro de las temperaturas. Las cajas se mantuvieron a una temperatura ambiente constante (“ 20°C). La temperatura ambiente y la temperatura de cada ensilaje se registraron cada 6 h mediante un registrador de datos. La temperatura ambiente de la estancia se midió usando una caja control vacía. Se examinó la estabilidad aerobia de los ensilajes calculando las diferencias entre la temperatura del ensilaje y la temperatura ambiente de la estancia. El deterioro aerobio se indicó por medio de los días (u horas) hasta el inicio de un aumento sostenido en la temperatura de más de 3°C por encima de la temperatura ambiente.
Tabla 4 - Métodos analíticos
* Se recogieron cinco muestras de pasto inmediatamente después de pulverizar y en el momento de cargar los silos.
** Se tomaron muestras de los ensilajes de cada silo en cada variante (incluyendo el control) después de 90 días de conservación.
*** Si aparecen más de 1500 cfu/g de clostridios en el forraje fresco, se realizan análisis del ensilaje para determinar la presencia de clostridios
Se determinaron las concentraciones de VFA y ácido láctico y alcoholes inferiores mediante una cromatografía de gas-líquido de extractos de ensilaje acuosos obtenidos macerando 30 g de ensilaje fresco en 150 ml de agua desionizada durante 16 horas a 40°C en un recipiente sellado, seguido de una filtración preliminar a través de un papel de filtro de 3 pm. Se añadió agua desionizada (3 ml) de una disolución de patrón interno (0,5 g de ácido 3-metil-n-valérico en 1000 ml de ácido oxálico 0,15 mol l-1) a 1 ml del filtrado anterior, y la disolución se filtró a través de una membrana de poliétersulfona de 0,45 pm hacia un vial de muestras cromatográfico para el análisis. El cromatógrafo de gas-líquido GC-2010 SHIMADZU emplea una columna capilar de orificio ancho (Stabilwax®-DA 30 m, 0,53 mm, DI, 0,5 pm) según los métodos oficiales de analizador de cromatografía de gases y bioquímica. Se determinó el amoniaco-nitrógeno (NH3N) mediante destilación - AOAC 941.04.
Resultados de los minisilos 4 y 5
Los resultados del minisilo 4 de maíz se muestran en la figura 5. Los tres ensilajes de maíz inoculados tenían un pH significativamente menor (P>0,05) comparados con el control después de 3 días de fermentación anaerobia. La composición 4 y la composición 7 tienen una pérdida de DM significativamente menor (%/kg), una fracción de N-NH3 significativamente menor (P<0,05) (%/kg del N total) y una concentración de ácido láctico significativamente mayor (P<0,05) (%/kg de DM) comparadas con la composición 2 y el control. La inoculación del maíz con la composición 2 y la composición 4 produjo unas concentraciones significativamente mayores (P<0,05) de ácido acético (%/kg de DM) y ácido propiónico (%/kg de DM) comparadas con la composición 7 y el control. Todos los ensilajes de maíz inoculados tenían un recuento de levaduras y mohos menor (log CFU/g) comparados con el control.
Tal como puede observarse en la figura 7, la exposición aerobia de 10 días produjo un aumento de la temperatura mayor que 3°C por encima de la temperatura ambiente después de 66 horas para el ensilaje control no inoculado, mientras que la composición 7 aumentó a más de 3°C por encima de la temperatura ambiente después de 178 horas, que es un tiempo significativamente mayor (P<0,05) comparado con el control y un tiempo significativamente menor (P<0,05) comparado con las composiciones 2 y 4. Después de 240 horas de exposición aerobia, el pH del control era tan alto como 8,29, mientras que la composición 7 tenía un pH de 5,66, que es significativamente menor (P<0,05) comparado con el control.
Tabla 5 - Efecto de diversas composiciones sobre las variables de fermentación y la composición microbiana del maíz ensilado
Las diferentes letras en una fila muestran la diferencia estadísticamente significativa (P<0,05).
No se produjo efluyente en los silos tras su apertura.
| Materia seca corregida para los volátiles.
Los resultados del minisilo 5 cuando se emplea una mezcla de pasto/trébol se muestran en la tabla 6. Los tres ensilajes de pasto/trébol inoculados tienen un pH significativamente menor (P>0,05) comparados con el control después de 3 días de fermentación anaerobia. La composición 4 y la composición 7 presentan una pérdida de DM significativamente menor (P<0,05) (%/kg). Mientras que todos los ensilajes de pasto/trébol inoculados presentaban una fracción de N-NH3 significativamente menor (P<0,05) (%/kg del N total) comparados con el control, y una concentración de ácido láctico significativamente mayor (P<0,05) (%/kg de DM) que el control, la inoculación del maíz con la composición 4 produjo una concentración de ácido acético significativamente mayor (P<0,05) (%/kg de DM) comparada con la composición 7 y el control. Todos los ensilajes de pasto/trébol inoculados tenían un recuento de levaduras y mohos menor (log CFU/g) comparados con el control.
Tal como puede observarse en la figura 8, la exposición aerobia de 10 días produjo un aumento de la temperatura del ensilaje control no inoculado hasta más de 3°C por encima de la temperatura ambiente después de 91 horas, mientras que la composición 7 aumentó a más de 3°C por encima de la temperatura ambiente después de 169 horas. La composición 4 aumentó a más de 3°C después de 191 horas, y la composición 2 alcanzó el mismo incremento después de 214 horas. Después de 240 horas de exposición aerobia, el pH del control era tan alto como 7,93, mientras que el pH de la composición 7 era de 5,41, el pH de la composición 4 era de 5,35, y el pH de la composición 2 era el más bajo, de 4,93.
Tabla 6 - Efecto de diversas composiciones sobre las variables de fermentación y la composición microbiana de trébol rojo:heno Timothy:festuca ensilado
Las diferentes letras en una fila muestran la diferencia estadísticamente significativa (P<0,05).
No se produjo efluyente en los silos tras su apertura.
| Materia seca corregida para los volátiles.
Minosilo 6a - Recolección de maíz en 2014, EE. UU.
Para el minisilo 6a, el maíz se recolectó en Delaware, EE. UU., con aproximadamente 35% de contenido en DM en la planta completa. Las composiciones 4 y 7 se disolvieron en agua desionizada y se aplicaron a cinco pilas de 20 kg de forraje de maíz recién troceado por tratamiento para obtener duplicados verdaderos. El forraje de cada pila se ensiló en silos de cubeta de 7,6 l y se selló con tapas de plástico con juntas tóricas.
Se prepararon un total de 5 muestras en el día 0 (material fresco) y 5 cubetas por tratamiento para cada intervalo de fermentación (días 2, 7 y 14). Las cubetas se cargaron con aproximadamente 6 kg de forraje fresco para lograr una densidad de carga final de entre 0,208-0,266 kg de DM/l. Las cubetas se conservaron a 22 1°C y se abrieron después de 2, 7 y 14 días de ensilaje.
Para la determinación de la estabilidad aerobia, se introdujeron 2 kg de una muestra representativa de cada silo en una cubeta limpia (sin cargar) y se colocó un registrador de datos en el centro geométrico de la masa de forraje. Los registradores se ajustaron para que registraran la temperatura cada 10 minutos y se promediaron por hora. Las cubetas se cubrieron con estopilla por la parte superior para evitar un secado excesivo y se dejaron en incubación en una estancia a 22 1°C. La temperatura ambiente en la estancia se midió y se registró simultáneamente. La estabilidad aerobia se define como la cantidad de tiempo antes de que la masa de ensilaje aumente 3°C por encima de una línea de base estable tras la exposición al aire.
Resultados del minisilo 6a
Los resultados para el minisilo 6a se muestran en las figuras 10 y 11 y en la tabla 7a.
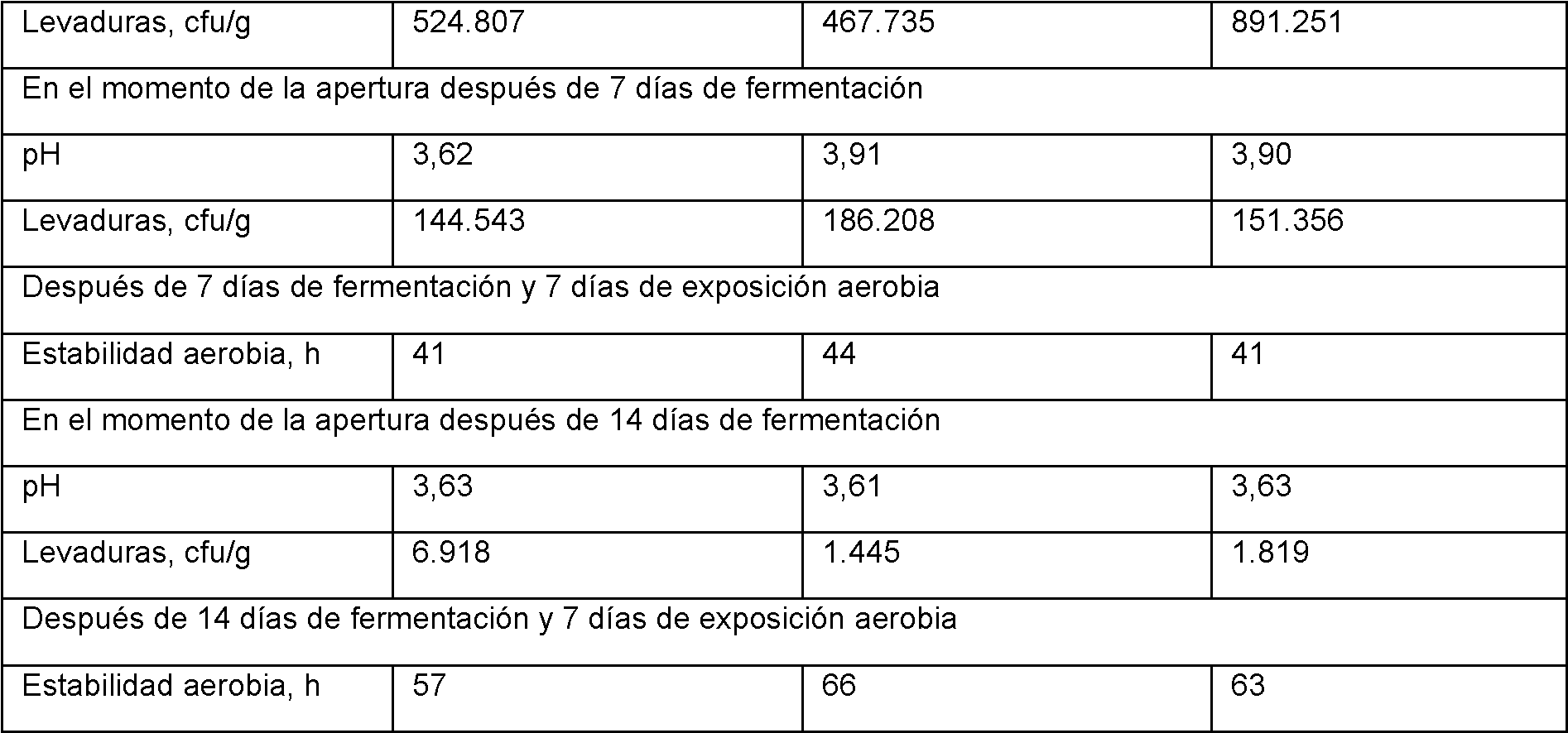
Tabla 7a - Efecto de diversas composiciones sobre el pH y el recuento de levaduras en el momento de la apertura después de diversos periodos de fermentación y sobre la estabilidad aerobia a lo largo de un periodo de 7 días de exposición aerobia
Minosilo 6b - Recolección de maíz en 2014, Lituania
Para el minisilo 6b, el maíz se recolectó en Lituania, con aproximadamente 35% de contenido en DM en la planta completa. La composición 4 se disolvió en agua desionizada y se aplicó a 150.000 cfu/g de forraje a una pila de forraje de maíz recién troceado para obtener duplicados verdaderos. El forraje de esta pila, así como una pila de control sin tratar, se ensiló en tarros de cristal de 3 l sellados con juntas tóricas.
Se prepararon un total de 5 muestras en el día 0 (material fresco) y 5 tarros de cristal por tratamiento para cada intervalo de fermentación (días 2, 4 y 8). Los tarros se cargaron con aproximadamente 1 kg de forraje fresco para lograr una densidad de carga final de entre 0,208-0,266 kg de DM/l. Los tarros de cristal se conservaron a (20 1°C) y se abrieron después de 2, 4 y 8 días de fermentación anaerobia.
Estabilidad aerobia:
Se determinó la estabilidad aerobia controlando el aumento de temperatura en los ensilajes conservados en tubos de PVC aislados (1300 ml) a 20 1°C de temperatura ambiente (temperatura ambiente de la estancia documentada durante el experimento) (figura 9a).
El deterioro aerobio se indicó por medio de las horas hasta que la temperatura del ensilaje alcanzó 3°C por encima de la temperatura ambiente (tabla 7b y figura 9b).
Resultados del minisilo 6b
Tabla 7b - Efecto de la composición 4 sobre la estabilidad aerobia
El aumento del tiempo de la fermentación anaerobia aumentó la estabilidad del ensilaje control y del ensilaje de maíz inoculado con la composición 4. Sin embargo, merece la pena advertir que la inoculación con la composición 4 fue capaz de mantener el ensilaje de maíz estable durante 18 horas más que el control después de tan solo dos días de fermentación anaerobia, y que la diferencia entre el control y la composición 4 sigue siendo considerable (10 y 29 horas, respectivamente) cuando se fermenta durante 4 días o 8 días antes de la exposición aerobia.
Minosilos 7a, 7b y 7c - Recolección de maíz en 2014, Dinamarca
Para el minisilo 7a, se recogió maíz recién recolectado (28,6% de DM) de una granja en el norte de Zelandia, Dinamarca, y se transportó inmediatamente al laboratorio. El maíz se usó para ensayar el efecto de la composición 4 frente al control empleando tarros de vidrio de 1,8 l con purgadores de liberación de gases automáticos (www.ANKOM.com). Los tarros de vidrio se rellenaron con un promedio de 746 g de maíz recién recolectado que se inoculó con 150.000 CFU/g de la composición 4 (n = 5) o se inoculó con la misma cantidad de agua del grifo (n = 5) como control. Los tarros se mantuvieron a una temperatura ambiente de aproximadamente 21°C. La producción de gas se midió en intervalos de 10 minutos automáticamente, y el gas también se liberó automáticamente cuando se alcanzaba 10,34 kPa (1,5 psi). El gas acumulado se convirtió en ml por g de forraje fresco (Volumen = P (presión en psi) x C (volumen del tarro)/promedio de presión atmosférica registrada de 0 a 162 horas x muestra total del pienso (peso fresco)). La producción de gas se midió durante 162 horas (figura 12), y la diferencia entre el control y el maíz tratado con la composición 4 se muestra en la figura 13.
Para el minisilo 7b, se usó 1 kg del mismo maíz que en el minisilo 7a el mismo día y se envasó al vacío retirando 90% del aire y se selló. Se usaron cinco bolsas por tratamiento sin inoculación (barra blanca), con la composición 4 (150.000 CFU/g de maíz, barra gris) o con la composición 7 (150.000 CFU/g de maíz, barra punteada). Después de 162 horas, las bolsas se abrieron, se liberó el gas y se midió la pérdida de peso (figura 14).
Para el minisilo c, se usó el mismo maíz que en el minisilo 7a después de conservarse en la nevera a -18°C. Tras esto, el forraje se descongeló, y se envasaron al vacío muestras de 1 kg retirando 90% del aire y se sellaron. Las bolsas envasadas al vacío de forraje sin inóculo o con la composición 4 (150.000 CFU/g de maíz) se dejaron en el exterior a temperatura ambiente para imitar las "condiciones verdaderas del exterior" y para averiguar la producción de gas después de 6 días de fermentación (figura 15).
Resultados de los minisilos 7a, 7b y 7c
Una producción muy temprana (primeras 48 horas) de gas en el ensilaje se asocia con microorganismos aerobios epifíticos de la familia Enterobacteriaceae (por ejemplo, E. coli, Salmonella, Klebsiella, etc.). La producción de gas está relacionada con la pérdida de nutrientes del ensilaje. La inoculación del maíz con la composición 4 dio como resultado una menor producción de gas, comparado con el maíz no inoculado (figura 12). La diferencia en la producción de gas aumentó desde 10 horas a 116 horas, cuando alcanzó un máximo con una diferencia de 0,17 ml de gas por g de maíz (figura 13).
En el maíz envasado al vacío, la pérdida de nutrientes puede evaluarse pesando las bolsas. La composición 4 tiene una pérdida de peso menor comparado con el control, pero también comparado con la composición 7 (figura 14). En condiciones reales, muchos agricultores indican que sus búnkeres de ensilaje tienden a "inflarse" después del sellado. Tal como se ilustra en la figura 15, la diferencia en la emisión de gas entre el maíz no inoculado (a la izquierda) e inoculado con la composición 4 (a la derecha) puede detectarse fácilmente de modo visual.
Análisis
Se sabe que el ácido acético producido por L. buchneri es un ácido importante para combatir el crecimiento de cepas de descomposición aerobias en el momento de usar el ensilaje, cuando el ensilaje se expone al oxígeno. Sin embargo, el crecimiento de L. buchneri tiene un tiempo de retraso largo, y la reducción en el pH por la utilización de L. buchneri es muy lenta. Para solucionarlo, se ha combinado L. buchneri con una especie bacteriana productora de una elevada cantidad de ácido láctico, tal como L. plantarum. Sin embargo, la combinación de cepas productoras de una elevada cantidad de ácido láctico puede contrarrestar la eficacia de L. buchneri sobre la estabilidad aerobia. Este fenómeno aparece en el minisilo 2, en el que la composición 5, que contiene 70% de L. buchneri DSM 22501 y 10% de L. plantarum DSM 16568, 20% de L. lactis Ds M 11037, produce un ensilaje mucho menos estable comparado con la composición 4, que contiene solo una cepa productora de una baja cantidad de ácido láctico (50% de L. lactis DSM 11037) combinada con L. buchneri DSM 22501 (50%) (figura 4).
La composición 4 logra un nivel de pH rápido y alto comparado con otras combinaciones con especies productoras de una elevada cantidad de ácido láctico. Aunque no se pretenda limitación alguna por la teoría, se cree que, en la composición 4, L. buchneri DSM 22501 sigue siendo capaz de crecer y/o ser metabólicamente activo, tal como indica el elevado nivel de ácido acético (figura 1c). La elevada proporción de ácido acético/ácido láctico de la composición 4 también puede observarse en el minisilo 1 (figura 3). Además, la elevada proporción de ácido acético/ácido láctico en una etapa temprana de la fermentación anaerobia aparentemente tiene un efecto positivo sobre la estabilidad aerobia en el minisilo 3, que se abrió después de tan solo un periodo corto (2 semanas) de fermentación anaerobia.
Estos resultados también demuestran que la pérdida de DM, un importante parámetro de la calidad del forraje, fue tan baja para la composición 4 como para los productos que contienen cepas productoras de una elevada cantidad de ácido láctico (véanse el minisilo 4 y el minisilo 5), mientras que la composición 4 también logró una elevada producción de ácido acético. El elevado nivel de ácido acético produce un ensilaje muy estable (figuras 4, 5, 6 y 7) que, en los tres casos con los minisilos (ejemplo 2), fue superior comparado con las otras composiciones con L. buchneri DSM 22501 (composiciones 5 y 7), en las que se incluyó L. plantarum DSM 16568, una cepa productora de una elevada cantidad de ácido láctico.
Tal como se muestra en la figura 9a, la composición 4 aumentó la estabilidad aerobia comparada con el control no tratado tras un corto periodo de fermentación de 7 días o 14 días. Además, y de modo muy sorprendente, la composición 4 también mostró una estabilidad aerobia mejor que la del control positivo (composición 7) en ambos momentos.
Tal como se ilustra en la figura 9b, la composición 4 aumentó la estabilidad aerobia comparada con el control no tratado después de 8 días de fermentación, seguidos de 7 días de exposición aerobia. Además, y de modo muy sorprendente, la composición 4 aumentó la estabilidad aerobia comparada con el control no tratado incluso tras un periodo de fermentación muy corto de tan solo 2 días o 4 días.
Tal como se ilustra en la figura 10, se observó un patrón de reducción en los recuentos de levaduras en general reconocido como función de un mayor tiempo de fermentación. Sin embargo, de modo sorprendente, la reducción en los recuentos de levaduras fue mayor usando la composición 4, frente al control negativo y positivo (composición 7) después de 2 y de 14 días de fermentación.
De modo sorprendente, tal como se ilustra en la figura 11, el nivel de pH cuando se emplea la composición 4 se redujo al mismo nivel que el control positivo (composición 7), a pesar de la falta de Lactobacillus plantarum en la composición 4.
Por tanto, estos experimentos demuestran que el inóculo de ensilaje que consiste fundamentalmente en la cepa heterofermentadora facultativa L. buchneri y solo cepas homofermentadoras logra una buena calidad del forraje con una mejor estabilidad aerobia incluso en ensilajes abiertos después de tan solo un corto periodo de fermentación anaerobia.
Referencias
Jatkauskas, J. y V. Vrotniakiene, "Evaluation of fermentation parameters, microbiological composition and aerobic stability of grass and whole crop maize silages treated with microbial inoculants", Zemdirbyste-Agriculture., 2013, vol.
100, n.° 2, págs. 143-150.
Jatkauskas, J. et al. (2013), The effects of three silage inoculants on aerobic stability in grass, clover-grass, lucerne and maize silages, Agricultural and Food Science, 2013, 22, 137-144,
Vandamme, B. et al., Polyphasic Taxonomy, a Consensus Approach to Bacterial Systematics, Microbiological Reviews, 1996, vol. 60, n.° 2, 407-438.
Claims (12)
1. - Un inóculo de ensilaje que, como componentes activos, solo comprende
(a) bacterias ácido lácticas heterofermentadoras obligatorias de al menos una de las especies Lactobacillus brevis, Lactobacillus buchneri, Lactobacillus fermentum, y Lactobacillus reuteri;
y
(b) bacterias ácido lácticas homofermentadoras de al menos una de las especies Enterococcus y Lactococcus que no reducen el crecimiento de (a) y que reducen el pH con rapidez sin producir una cantidad excesiva de ácido láctico.
2. - El inóculo de ensilaje según la reivindicación 1, que consiste fundamentalmente en un Lactobacillus brevis y un Enterococcus.
3. - El inóculo de ensilaje según la reivindicación 1, que consiste fundamentalmente en un Lactobacillus brevis y un Lactococcus.
4. - El inóculo de ensilaje según la reivindicación 1, que consiste fundamentalmente en un Lactobacillus fermentum y un Enterococcus.
5. - El inóculo de ensilaje según la reivindicación 1, que consiste fundamentalmente en un Lactobacillus fermentum y un Lactococcus.
6. - El inóculo de ensilaje según la reivindicación 1, que consiste fundamentalmente en un Lactobacillus reuteri y un Enterococcus.
7. - El inóculo de ensilaje según la reivindicación 1, que consiste fundamentalmente en un Lactobacillus reuteri y un Lactococcus.
8. - Un método para producir un producto de pienso fermentado, comprendiendo dicho método inocular un material vegetal con el inóculo de ensilaje según una cualquiera de las reivindicaciones 1 a 7.
9. - Un método según la reivindicación 8, en el que el material vegetal se inocula con el inóculo de ensilaje y se incuba durante un periodo de hasta 7 días.
10. - Un método según la reivindicación 8, en el que el material vegetal se inocula con el inóculo de ensilaje y se incuba durante un periodo de hasta 14 días.
11. - Un método según la reivindicación 8, en el que el material vegetal se inocula con el inóculo de ensilaje y se incuba durante un periodo de hasta 28 días.
12. - Un método según la reivindicación 8, en el que el material vegetal se inocula con el inóculo de ensilaje y se incuba durante un periodo de hasta 90 días.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP14182628.9A EP2989899B1 (en) | 2014-08-28 | 2014-08-28 | Compositions of hetero- and homofermentative lactic acid bacterial species for dual purpose silage preservation |
| EP14188993 | 2014-10-15 | ||
| DKPA201400652 | 2014-11-10 | ||
| US201562156999P | 2015-05-05 | 2015-05-05 | |
| PCT/EP2015/069627 WO2016030456A1 (en) | 2014-08-28 | 2015-08-27 | Improved compositions of hetero- and homofermentative lactic acid bacterial species for dual purpose silage preservation |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2765409T3 true ES2765409T3 (es) | 2020-06-09 |
Family
ID=55398785
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES15767097T Active ES2765409T3 (es) | 2014-08-28 | 2015-08-27 | Composiciones mejoradas de especies de bacterias ácido lácticas hetero- y homofermentadoras para la conservación del ensilaje de doble función |
Country Status (18)
| Country | Link |
|---|---|
| US (2) | US11160294B2 (es) |
| EP (1) | EP3185696B1 (es) |
| CN (2) | CN112753866A (es) |
| BR (1) | BR112017003137B1 (es) |
| CA (1) | CA2957854C (es) |
| CY (1) | CY1122461T1 (es) |
| DK (1) | DK3185696T3 (es) |
| EA (1) | EA035954B1 (es) |
| ES (1) | ES2765409T3 (es) |
| HR (1) | HRP20200038T1 (es) |
| HU (1) | HUE047956T2 (es) |
| LT (1) | LT3185696T (es) |
| PL (1) | PL3185696T3 (es) |
| PT (1) | PT3185696T (es) |
| RS (1) | RS59813B1 (es) |
| SI (1) | SI3185696T1 (es) |
| SM (1) | SMT202000007T1 (es) |
| WO (1) | WO2016030456A1 (es) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6807160B2 (ja) * | 2016-03-15 | 2021-01-06 | 雪印種苗株式会社 | サイレージ調製用乳酸菌及びサイレージ調製用添加剤 |
| CN106635911A (zh) * | 2016-12-29 | 2017-05-10 | 中粮生物科技(北京)有限公司 | 一种复合菌种发酵剂及青贮饲料的制备方法 |
| CN109306327A (zh) * | 2017-07-27 | 2019-02-05 | 内蒙古蒙正牧康实业有限公司 | 玉米粒鲜贮发酵菌剂及鲜贮发酵工艺 |
| CN109430540A (zh) * | 2018-10-30 | 2019-03-08 | 齐鲁工业大学 | 一种藜麦青贮饲料的制备方法 |
| CN110150488A (zh) * | 2019-05-30 | 2019-08-23 | 中科元生生物技术(天津)有限公司 | 一种猪用饲料添加剂及其制备方法和应用 |
| KR20230044134A (ko) * | 2020-07-26 | 2023-04-03 | 로커스 아이피 컴퍼니 엘엘씨 | 신규 사일리지 첨가제 조성물 |
| CN112553103B (zh) * | 2020-10-10 | 2022-09-20 | 重庆市畜牧科学院 | 牛鞭草青贮乳酸菌添加剂及其制备方法 |
| CN114908018B (zh) * | 2022-05-31 | 2023-03-10 | 四川农业大学 | 一种短乳杆菌及其在青贮中的应用 |
| CN116024122B (zh) * | 2022-09-16 | 2024-08-09 | 兰州大学 | 一种罗伊氏乳杆菌在制备青贮饲料中的应用 |
| CN118813470A (zh) * | 2024-07-31 | 2024-10-22 | 中国科学院微生物研究所 | 一株抑制苜蓿青贮梭菌发酵的乳酸乳球菌及其应用 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| NZ250858A (en) | 1993-12-27 | 1995-08-28 | Hayashibara Biochem Lab | Alkali-treated bagasse, its fermentation and use as animal feed |
| TW323222B (es) | 1993-12-27 | 1997-12-21 | Hayashibara Biochem Lab | |
| DE19917715A1 (de) | 1999-04-09 | 2000-10-19 | Danisco A S Kopenhagen Koebenh | Neuartige Schutzkulturen und deren Verwendung bei der Konservierung von Lebensmitteln |
| JP2001299230A (ja) | 2000-04-27 | 2001-10-30 | Korin Korea Co Ltd | 飼料添加物およびその製造方法 |
| US6403084B1 (en) | 2000-11-03 | 2002-06-11 | Pioneer Hi-Bred International, Inc. | Mixed cultures for improved fermentation and aerobic stability of silage |
| EP1931763A1 (en) | 2005-09-12 | 2008-06-18 | Vrije Universiteit Brussel | Starter cultures and fermentation method |
| US20080138461A1 (en) * | 2006-12-11 | 2008-06-12 | Pioneer Hi-Bred International, Inc. | Lactobacillus buchneri strain LN1297 and its use to improve aerobic stability of silage |
| US20090028992A1 (en) | 2006-12-11 | 2009-01-29 | Pioneer Hi-Bred International, Inc. | Lactobacillus buchneri strain LN1286 and its use to improve aerobic stability of silage |
| EP2312955B1 (de) | 2008-07-21 | 2015-10-28 | Erber Aktiengesellschaft | Verfahren zur behandlung von futtersilage für wiederkäuer sowie futtersilagezusatz |
| EP2245944A1 (fr) | 2009-04-30 | 2010-11-03 | Danisco A/S | Procédé pour améliorer la digestibilité et l'assimilabilité des céréales et/ou des fibres chez un animal herbivore monogastrique |
| EP2228067B1 (de) | 2010-02-22 | 2013-12-11 | LR Health & Beauty Systems GmbH | Probiotische Zusammensetzung und deren Verwendung |
| WO2014170233A2 (en) * | 2013-04-18 | 2014-10-23 | Chr. Hansen A/S | Method for improving milk quality in milk-producing animals |
-
2015
- 2015-08-27 ES ES15767097T patent/ES2765409T3/es active Active
- 2015-08-27 CA CA2957854A patent/CA2957854C/en active Active
- 2015-08-27 SI SI201531062T patent/SI3185696T1/sl unknown
- 2015-08-27 LT LTEP15767097.7T patent/LT3185696T/lt unknown
- 2015-08-27 RS RS20200008A patent/RS59813B1/sr unknown
- 2015-08-27 CN CN202110238815.3A patent/CN112753866A/zh active Pending
- 2015-08-27 EA EA201790311A patent/EA035954B1/ru not_active IP Right Cessation
- 2015-08-27 SM SM20200007T patent/SMT202000007T1/it unknown
- 2015-08-27 HR HRP20200038TT patent/HRP20200038T1/hr unknown
- 2015-08-27 PL PL15767097T patent/PL3185696T3/pl unknown
- 2015-08-27 CN CN201580047684.3A patent/CN107223017B/zh active Active
- 2015-08-27 DK DK15767097.7T patent/DK3185696T3/da active
- 2015-08-27 WO PCT/EP2015/069627 patent/WO2016030456A1/en not_active Ceased
- 2015-08-27 BR BR112017003137-0A patent/BR112017003137B1/pt active IP Right Grant
- 2015-08-27 HU HUE15767097A patent/HUE047956T2/hu unknown
- 2015-08-27 US US14/838,024 patent/US11160294B2/en active Active
- 2015-08-27 EP EP15767097.7A patent/EP3185696B1/en active Active
- 2015-08-27 PT PT157670977T patent/PT3185696T/pt unknown
-
2020
- 2020-01-08 CY CY20201100010T patent/CY1122461T1/el unknown
-
2021
- 2021-10-27 US US17/512,592 patent/US20220117268A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| CN112753866A (zh) | 2021-05-07 |
| CN107223017B (zh) | 2021-03-19 |
| EA201790311A1 (ru) | 2017-08-31 |
| EA035954B1 (ru) | 2020-09-04 |
| EP3185696A1 (en) | 2017-07-05 |
| BR112017003137B1 (pt) | 2023-01-17 |
| PL3185696T3 (pl) | 2020-05-18 |
| US11160294B2 (en) | 2021-11-02 |
| CY1122461T1 (el) | 2021-01-27 |
| BR112017003137A8 (pt) | 2022-07-19 |
| HRP20200038T1 (hr) | 2020-04-03 |
| SI3185696T1 (sl) | 2020-03-31 |
| CA2957854C (en) | 2021-06-08 |
| EP3185696B1 (en) | 2019-10-23 |
| CN107223017A (zh) | 2017-09-29 |
| CA2957854A1 (en) | 2016-03-03 |
| US20220117268A1 (en) | 2022-04-21 |
| BR112017003137A2 (pt) | 2017-11-28 |
| HUE047956T2 (hu) | 2020-05-28 |
| LT3185696T (lt) | 2020-01-27 |
| SMT202000007T1 (it) | 2020-03-13 |
| RS59813B1 (sr) | 2020-02-28 |
| WO2016030456A1 (en) | 2016-03-03 |
| PT3185696T (pt) | 2020-01-21 |
| US20160058034A1 (en) | 2016-03-03 |
| DK3185696T3 (da) | 2020-01-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2765409T3 (es) | Composiciones mejoradas de especies de bacterias ácido lácticas hetero- y homofermentadoras para la conservación del ensilaje de doble función | |
| ES2911175T3 (es) | Bacterias ácido lácticas para la preparación de ensilaje y aditivo para la preparación de ensilaje | |
| CA2436823C (en) | Mixed cultures for improved fermentation and aerobic stability of silage | |
| ES2771857T3 (es) | Cepas de Lactobacillus de acción rápida y su uso para mejorar la estabilidad aeróbica del ensilado | |
| DK2727994T3 (en) | New lactic acid bacteria and process for preparing silage or fermented feed using it | |
| US20080138461A1 (en) | Lactobacillus buchneri strain LN1297 and its use to improve aerobic stability of silage | |
| AU2002239449A1 (en) | Mixed cultures for improved fermentation and aerobic stability of silage | |
| US20080138463A1 (en) | Lactobacillus buchneri strain LN5689 and its use to improve aerobic stability of silage | |
| US20090028991A1 (en) | Lactobacillus buchneri strain LN1284 and its use to improve aerobic stability of silage | |
| US20090028993A1 (en) | Lactobacillus buchneri strain LN1326 and its use to improve aerobic stability of silage | |
| US20090028992A1 (en) | Lactobacillus buchneri strain LN1286 and its use to improve aerobic stability of silage | |
| CN113273639A (zh) | 一种含益生菌的保鲜昆虫的制备方法 | |
| LT6271B (lt) | Augalinės kilmės fermentuoti pašarai | |
| EP0071858A1 (en) | Silage preservation with propionic acid producing microorganisms | |
| US20240075080A1 (en) | Use of lactic acid bacteria to inhibit methanogen growth or reduce methane emissions | |
| ES2596445T3 (es) | Composiciones de especies bacterianas de ácido láctico hetero y homofermentativas para la conservación del ensiladocon doble fin | |
| Steidlová et al. | The effects of using lactic acid bacteria inoculants in maize silage on the formation of biogenic amines | |
| HK1222095B (en) | Compositions of hetero- and homofermentative lactic acid bacterial species for dual purpose silage preservation | |
| JP2006042647A (ja) | 新規乳酸菌株および当該菌株によるサイレージ好気的変敗の抑制法 | |
| Adesoji et al. | Physicochemical Screening of Lactobatillus plantarum and its Effects on the Fermentation of Panicum maximum Grass for Silage Production | |
| BR112020007863A2 (pt) | método de produção de materiais vegetais ensilados usando megasphaera elsdenii | |
| ASHBELL et al. | The effect of addition of lactic acid bacteria inoculum to wheat and corn silages in Israel |