ES2773601T3 - Sistemas de fijación de carbono mejorados en plantas y algas - Google Patents
Sistemas de fijación de carbono mejorados en plantas y algas Download PDFInfo
- Publication number
- ES2773601T3 ES2773601T3 ES15745345T ES15745345T ES2773601T3 ES 2773601 T3 ES2773601 T3 ES 2773601T3 ES 15745345 T ES15745345 T ES 15745345T ES 15745345 T ES15745345 T ES 15745345T ES 2773601 T3 ES2773601 T3 ES 2773601T3
- Authority
- ES
- Spain
- Prior art keywords
- protein
- plant
- hla3
- transgenic
- pgr5
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/82—Vectors or expression systems specially adapted for eukaryotic hosts for plant cells, e.g. plant artificial chromosomes (PACs)
- C12N15/8241—Phenotypically and genetically modified plants via recombinant DNA technology
- C12N15/8261—Phenotypically and genetically modified plants via recombinant DNA technology with agronomic (input) traits, e.g. crop yield
- C12N15/8262—Phenotypically and genetically modified plants via recombinant DNA technology with agronomic (input) traits, e.g. crop yield involving plant development
- C12N15/8269—Photosynthesis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/415—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from plants
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N1/00—Microorganisms; Compositions thereof; Processes of propagating, maintaining or preserving microorganisms or compositions thereof; Processes of preparing or isolating a composition containing a microorganism; Culture media therefor
- C12N1/12—Unicellular algae; Culture media therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/82—Vectors or expression systems specially adapted for eukaryotic hosts for plant cells, e.g. plant artificial chromosomes (PACs)
- C12N15/8241—Phenotypically and genetically modified plants via recombinant DNA technology
- C12N15/8261—Phenotypically and genetically modified plants via recombinant DNA technology with agronomic (input) traits, e.g. crop yield
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P1/00—Preparation of compounds or compositions, not provided for in groups C12P3/00 - C12P39/00, by using microorganisms or enzymes
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A40/00—Adaptation technologies in agriculture, forestry, livestock or agroalimentary production
- Y02A40/10—Adaptation technologies in agriculture, forestry, livestock or agroalimentary production in agriculture
- Y02A40/146—Genetically Modified [GMO] plants, e.g. transgenic plants
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Genetics & Genomics (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Biotechnology (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Microbiology (AREA)
- Biophysics (AREA)
- Cell Biology (AREA)
- Physics & Mathematics (AREA)
- Plant Pathology (AREA)
- Botany (AREA)
- Medicinal Chemistry (AREA)
- Physiology (AREA)
- Gastroenterology & Hepatology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Mycology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Tropical Medicine & Parasitology (AREA)
- Virology (AREA)
- Breeding Of Plants And Reproduction By Means Of Culturing (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Nutrition Science (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Saccharide Compounds (AREA)
- Fats And Perfumes (AREA)
Abstract
Una planta C3 transgénica, que comprende dentro de su genoma, y que expresa o sobreexpresa, una combinación de secuencias de nucleótidos heterólogas que codifican: un transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática; y una proteína moduladora de la transferencia de electrones cíclica en la que la proteína moduladora de la transferencia de electrones cíclica se selecciona del grupo que consiste en una proteína PGRL1, una proteína PGR5, una proteína FNR1, una proteína FNR2, una proteína Fdl, o cualquier combinación de las mismas, y en la que el transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática es una proteína HLA3.
Description
DESCRIPCIÓN
Sistemas de fijación de carbono mejorados en plantas y algas
Referencia cruzada a solicitudes relacionadas
La presente solicitud reclama la prioridad y el beneficio de la presentación de la Solicitud de patente provisional de Estados Unidos núm. 62/027,354, titulada "Carbon Fixation Systems in Plants and Algae", presentada el 22 de julio de 2014.
Declaración sobre investigación patrocinada federalmente
La presente invención se realizó con el apoyo del gobierno bajo las subvenciones núm. DOE-CECO Prime núm.: DEAR0000202, Sub núm.: 21018-N; DOE-CABS Prime núm: DE-SC0001295, Sub núm: 21017-NM NSF EF-1219603, NSF núm: 1219603. El Gobierno de Estados Unidos tiene ciertos derechos en la invención.
Listado de secuencias
La solicitud presente contiene una lista de secuencias que se envió electrónicamente en formato ASCII. Dicha copia ASCII, creada el 20 de julio de 2015, se llama 072215_NMC0001-101-US_Sequence_Listing_ST25.txt y tiene un tamaño de 284 bytes.
Incorporación por referencia de material presentado en un disco compacto
No aplicable.
Material sujeto a derechos de autor
No aplicable.
Antecedentes
Un factor importante que limita la eficiencia fotosintética es la inhibición competitiva de la fijación del CO2 por oxígeno, debido a la falta de especificidad de la enzima RuBisCO. La incorporación de oxígeno por RuBisCO es la primera etapa dedicada en la fotorrespiración, una vía que respira CO2, y agrava la ineficiencia fotosintética. En general, la fotorrespiración reduce la productividad fotosintética hasta en un 50 % [1]. Hasta la fecha, los intentos de modificar genéticamente una actividad oxigenasa reducida en RuBisCO no tuvieron éxito.
Significativamente, las cianobacterias, microalgas eucariotas, y plantas C4 desarrollaron mecanismos para reducir la fotorrespiración al concentrar CO2 cerca de RuBisCO, que inhibe competitivamente la actividad oxigenasa y conduce a aumentos sustanciales en el rendimiento y la eficiencia del uso del agua por unidad de carbono fijada. Sin embargo, los sistemas de concentración de carbono (CCM) no están operativos en la gran mayoría de las especies de plantas (es decir, plantas C3).
Los intentos de reconstituir CCM funcionales en plantas C3 se intentaron previamente por los solicitantes y por otros, principalmente con enfoque en la modificación genética de vías que participan directamente en facilitar el transporte de CO2 a cloroplastos de las hojas. Téngase en cuenta, por ejemplo, la Publicación internacional del PCT núm. WO 2012/125737; Sage and Sage (2009) Plant and Cell Physiol. 50(4):756-772; Zhu y otros (2010) J Interg. Plant Biol.
52(8):762-770; Furbank y otros (2009) Funct. Plant Biol. 36(11):845-856; Weber y von Caemmerer (2010) Curr. Opin. Plant Biol.; Price (2013) J. Exp. Bot. 64(3):753-68; y Publicación de solicitud de patente de Estados Unidos núm.
2013/0007916 A1.
Sin embargo, la producción de ATP y NADPH a través de las etapas de recolección de luz y transferencia de electrones deben coordinarse con las etapas de asimilación de carbono y de requerimiento de energía adicionales que incluyen sistemas CCM para prevenir la fotoinhibición y mejorar el crecimiento. Adicionalmente, el flujo asimilatorio y las tasas de almacenamiento pueden limitar la fijación de carbono debido a la inhibición por retroalimentación cuando la demanda del sumidero no coincide con la capacidad de la fuente [2].
Así, existe una necesidad crítica de mejorar la productividad de la planta a través de enfoques de ingeniería de sistemas integrados que equilibren las interacciones fuente/sumidero con la producción reductora y de energía para desarrollar CCM artificiales, que requieran energía que puedan imitar efectivamente a los que se encuentran en la naturaleza. Breve sumario de la invención
En consecuencia, en respuesta a esta necesidad, la presente divulgación proporciona procedimientos para elevar la actividad de transferencia electrónica de electrones, mejorar la concentración de carbono, y mejorar la fijación de
carbono en C3, y producir biomasa u otros productos a partir de C3, seleccionados entre, por ejemplo, almidones, aceites, ácidos grasos, lípidos, celulosa u otros carbohidratos, alcoholes, azúcares, nutracéuticos, productos farmacéuticos, compuestos saborizantes y fragancias, y ácidos orgánicos, así como plantas transgénicas producidas por los mismos. Estos procedimientos y plantas transgénicas abarcan la expresión, o sobreexpresión, de varias combinaciones de genes que mejoran los sistemas de concentración de carbono en las plantas, tales como proteínas de transporte de bicarbonato, anhidrasa carbónica, bomba de protones impulsada por luz, reguladores del flujo de electrones cíclicos, etc. Así, entre sus diversas realizaciones, la presente divulgación proporciona las siguientes:
Una primera realización de la presente invención proporciona una planta transgénica, que comprende dentro de su genoma, y que expresa o sobreexpresa, una combinación de secuencias de nucleótidos heterólogas que codifican un transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática y una proteína moduladora de la transferencia de electrones cíclica. La proteína moduladora de la transferencia de electrones cíclica puede seleccionarse de una proteína PGRL1 (por ejemplo, SEQ ID NO:3), una proteína PGR5 (por ejemplo, SEQ ID NO:1), una proteína FNR1 de hoja (por ejemplo, s Eq ID NO:96), una proteína FNR2 de hoja (por ejemplo, SEQ ID NO:97), una proteína Fd1 (por ejemplo, SEQ ID NO:95), o cualquier combinación de las mismas y, por ejemplo, el transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática puede ser una proteína HLA3 (por ejemplo, SEQ ID NO:77). La planta transgénica descrita puede comprender, además, dentro de su genoma, y expresar o sobreexpresar la secuencia de nucleótidos heteróloga que codifica una proteína transportadora de aniones bicarbonato localizada en la envoltura del cloroplasto. La planta transgénica descrita en la presente memoria puede comprender, además, dentro de su genoma, y expresar o sobreexpresar la secuencia de nucleótidos heteróloga que codifica una proteína anhidrasa carbónica. En una realización preferente, la proteína moduladora de la transferencia de electrones cíclica es una proteína PGR5, en otra realización preferente la proteína moduladora de la transferencia de electrones cíclica es proteína Fd1, aun en otra realización preferente, en otra realización preferente más la proteína moduladora de la transferencia de electrones cíclica es FNR1 de hoja, en una realización preferente adicional la proteína moduladora de la transferencia de electrones cíclica es PGRL1. En una realización preferente las secuencias de nucleótidos heterólogas de la planta transgénica codifican i) una proteína PGR5, y una proteína HLA3; o ii) una proteína PGR5, una proteína HLA3 y una proteína PGRL1 o una proteína PGR5, una proteína HLA3, y una proteína LCIA o una proteína PGR5, una proteína HLA3, una proteína PGRL1, una proteína LCIA, y una proteína BCA o HCA2. En otra realización preferente las secuencias de nucléotidos heterólogas de la planta transgénica de la que codifican una proteína PGR5, una proteína HLA3, una proteína LCIA y un BCA u opcionalmente una proteína HCA2. La planta transgénica como se describe en la que la proteína PGR5 tiene una secuencia de aminoácidos al menos 80 % idéntica a SEQ ID NO:1; la proteína HLA3 tiene una secuencia de aminoácidos al menos 80 % idéntica a la SEQ ID NO:77; la proteína PGRL1 tiene una secuencia de aminoácidos al menos 80 % idéntica a la SEQ ID NO:3; la proteína LCIA tiene una secuencia de aminoácidos al menos 80 % idéntica a la SEQ ID NO:18; y/o la proteína BCA tiene una secuencia de aminoácidos al menos 80 % idéntica a la SEQ ID NO:21. Alternativamente, la identidad de secuencia/similitud de secuencia es aproximadamente del 75 %, 85 %, 90 %, 91 %, 92 %, 93 %, 94 %, 95 %, 96 %, 97 %, 98 %, 99 %, 100 % para aquellas específicamente divulgadas que incluyen, por ejemplo, proteínas sin una secuencia de péptido de tránsito y la proteína funcional.
Una segunda realización proporciona una planta transgénica, que comprende dentro de su genoma, y que expresa o sobreexpresa, una combinación de secuencias de nucleótidos heterólogas que codifican: Se proporciona proteína LCIA y proteína BCA o proteína HCA. En una realización preferente las secuencias de nucleótidos heterólogas codifican plantas transgénicas en las que la proteína LCIA tiene una secuencia de aminoácidos al menos 80 % idéntica a la SEQ ID NO:18; y/o la proteína BCA tiene una secuencia de aminoácidos al menos 80 % idéntica a SEQ ID NO:21 y la proteína hCa tiene una secuencia de aminoácidos al menos 80 % idéntica a SEQ ID NO:19. Alternativamente, la identidad de secuencia/similitud de secuencia es aproximadamente del 75 %, 85 %, 90 %, 91 %, 92 %, 93 %, 94 %, 95 %, 96 %, 97 %, 98 %, 99 %, 100 % para aquellas específicamente divulgadas que incluyen, por ejemplo, proteínas sin una secuencia de péptido de tránsito y la proteína funcional.
Una tercera realización proporciona una planta transgénica, que comprende dentro de su genoma, y que expresa o sobreexpresa, una combinación de secuencias de nucleótidos heterólogas que codifican un transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática (por ejemplo, SEQ ID NO:77), un transportador de aniones bicarbonato localizado en la envoltura del cloroplasto (por ejemplo, SEQ ID NO:18), una anhidrasa carbónica, una proteína proteorodopsina dirigida a las membranas de los tilacoides (por ejemplo, SEQ ID NO:98) y una proteína p caroteno monooxigenasa (por ejemplo, SEQ ID NO:100). En otra realización preferente la proteorodopsina comprende un péptido de tránsito de cloroplasto seleccionado entre un dominio de transmembrana de parada de transferencia de psbX fusionado a su extremo C, un péptido de tránsito de DNAJ, un péptido de tránsito de CAB, un péptido de tránsito de PGR5, y un péptido de tránsito de psaD. En otra realización preferente la p-caroteno monooxigenasa se expresa bajo el control de un promotor seleccionado entre un promotor génico inducible por etanol y un promotor específico de hoja/tejido verde seleccionado entre CAB y rbcS. La proteorodopsina puede comprender una sustitución de aminoácidos seleccionada entre L219E/T206S, M79T, y M79Y, y combinaciones de las mismas.
La anhidrasa carbónica de la primera, segunda, o tercera realización puede ser una proteína BCA u opcionalmente una HCA2. El transportador de aniones bicarbonato localizado en la envoltura del cloroplasto de la primera, segunda y tercera realización puede ser una proteína LCIA. El transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática de la primera y tercera realizaciones puede ser HLA3.
Una cuarta realización proporciona un procedimiento para hacer una planta transgénica o de una primera realización en la que dicho procedimiento comprende expresar, o sobreexpresar, en una planta C3, una combinación de secuencias de nucleótidos heterólogas que codifican un transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática y una proteína moduladora de la transferencia de electrones cíclica. La proteína moduladora de la transferencia de electrones cíclica puede seleccionarse de una proteína PGRL1, una proteína PGR5, una proteína FNR1, una proteína FNR2 (isótopos en forma de hoja), una proteína Fd1, o cualquier combinación de las mismas y en la que el transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática es una proteína HLA3. Las secuencias de nucleótidos heterólogas de la cuarta realización codifican, además, una proteína transportadora de aniones bicarbonato localizada en la envoltura del cloroplasto, por ejemplo, la proteína transportadora de anión bicarbonato es LCIA. Adicionalmente, las secuencias de nucleótidos heterólogas codifican una proteína de anhidrasa carbónica, por ejemplo, una proteína BCA u opcionalmente una proteína HCA2. En una realización preferente, la proteína moduladora de la transferencia de electrones cíclica es una proteína PGR5 y opcionalmente una proteína PGRL1 y/o una combinación de las mismas.
Una quinta realización proporciona un procedimiento para hacer una planta transgénica como se describe en una segunda realización, en la que dicho procedimiento comprende expresar, o sobreexpresar, en una planta C3, una combinación de secuencias de nucleótidos heterólogas que codifican una proteína LCIA y una proteína BCA u opcionalmente un proteína HCA.
Una sexta realización proporciona un procedimiento para hacer una planta transgénica de una tercera realización en la que dicho procedimiento comprende expresar, o sobreexpresar, en una planta C3, una combinación de secuencias de nucleótidos heterólogas que codifican un transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática, un transportador de aniones bicarbonato, una anhidrasa carbónica, una proteína proteorodopsina dirigida a las membranas de los tilacoides, y una proteína p-caroteno monooxigenasa. En una realización preferente la proteorodopsina comprende un péptido de tránsito de cloroplasto seleccionado entre un dominio de transmembrana de parada de transferencia de psbX fusionado a su extremo C, un péptido de tránsito de DNAJ, un péptido de tránsito de CAB, un péptido de tránsito de PGR5, y un péptido de tránsito de psaD. En otra realización preferente la p-caroteno monooxigenasa se expresa bajo el control de un promotor seleccionado entre un promotor génico inducible por etanol y un promotor específico de hoja/tejido verde seleccionado entre CAB y rbcS. En una realización preferente la proteorodopsina comprende una sustitución de aminoácidos seleccionada entre L219E/T206S, M79T, y M79Y, y combinaciones de las mismas. En otra realización preferente el transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática es HLA3.
La planta transgénica de una realización divulgada en la presente memoria puede ser una planta C3 tal como una planta oleaginosa transgénica o una planta de cultivo alimentario transgénica que puede incluir los géneros Brassica (por ejemplo, colza/canola (Brassica napus; Brassica carinata; Brassica nigra; Brassica olerácea), Camelina, Miscanthus, y Jatropha; Jojoba (Simmondsia chinensis), coco; algodón; maní; arroz; cártamo, sésamo; soja; mostaza que no sea Arabidopsis; trigo; lino (linaza); girasol; aceituna; maíz; palma; almendra de palma; caña de azúcar; ricino; zacate; Borago officinalis; Echium plantagineum; Cuphea hookeriana; Cuphea pulcherrima; Cuphea lanceolata; Ricinus communis; Coriandrum sativum; Crepis alpina; Vernonia galamensis; Momordica charantia; y Crambe abyssinica, trigo, arroz, maíz (maíz), cebada, avena, sorgo, centeno, y mijo; maní, garbanzos, lentejas, frijoles, soya, habas; papas, batatas, y yuca; soja, maíz, canola, maní, palma, coco, cártamo, algodón, girasol, lino, oliva, y cártamo; caña de azúcar y remolacha azucarera; plátanos, naranjas, manzanas, peras, fruta del pan, piñas, y cerezas; tomates, lechugas, zanahorias, melones, fresas, espárragos, brócoli, guisantes, col rizada, anacardos, maní, nueces, pistachos, almendras; forraje y césped; alfalfa, trébol; café, cacao, nuez de cola, amapola; vainilla, salvia, tomillo, anís, azafrán, mentol, menta, hierbabuena y cilantro y, preferentemente, trigo, arroz y canola. El transgénico de una realización divulgada en la presente memoria puede seleccionarse de entre una especie de Chlorella, una especie de Nanocloropsis, y una especie de Chlamydomonas. Las secuencias de nucleótidos heterólogas que se describen en una realización pueden optimizarse con codones para la expresión en dicha planta transgénica. Un aspecto de la presente invención proporciona una planta transgénica como se describe en una realización que exhibe una fijación de CO2 mejorada en comparación con una planta de control por lo demás idéntica cultivada en las mismas condiciones, por ejemplo, en la que la fijación de CO2 se mejora en el intervalo de aproximadamente 10 % a aproximadamente 50 % en comparación con el de una planta de control por lo demás idéntica cultivada en las mismas condiciones.
Una cuarta realización proporciona una parte de dicha planta transgénica de cualquier realización descrita en la presente memoria. Por ejemplo, la parte de dicha planta transgénica puede seleccionarse entre un protoplasto, una célula, un tejido, un órgano, un corte, un explante, un tejido reproductivo, un tejido vegetativo, biomasa, una inflorescencia, una flor, un sépalo, un pétalo, un pistilo, un estigma, un estilo, un ovario, un óvulo, un embrión, un receptáculo, una semilla, una fruta, un estambre, un filamento, una antera, un gametofito masculino o femenino, un grano de polen, un meristemo, una yema terminal, una yema axilar, una hoja, un tallo, una raíz, una raíz tuberosa, un rizoma, un tubérculo, un estolón, un cormo, un bulbo, un brote lateral, una célula de dicha planta en cultivo, un tejido de dicha planta en cultivo, un órgano de dicha planta en cultivo, un callo, materiales de propagación, germoplasma, esquejes, divisiones, y propagaciones.
Una quinta realización proporciona una progenie o derivado de dicha planta transgénica de cualquier realización descrita en la presente memoria. Por ejemplo, la progenie o derivados pueden seleccionarse entre clones, híbridos, muestras, semillas, y material recolectado de los mismos y pueden producirse sexualmente o asexualmente.
Otra realización de la presente invención proporciona un procedimiento para elevar la actividad de CET en una planta C3, en el que dicho procedimiento comprende expresar o sobreexpresar, en una planta C3, una combinación de secuencias de nucleótidos heterólogas que codifican un transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática y proteína moduladora de la transferencia de electrones cíclica.
Aún otra realización proporciona un procedimiento para mejorar la fijación de carbono en una planta C3, en el que dicho procedimiento comprende expresar, o sobreexpresar, en una planta C3, una combinación de secuencias de nucleótidos heterólogas que codifican un transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática y una proteína moduladora de la transferencia de electrones cíclica.
Aun otro procedimiento proporciona un procedimiento para producir biomasa u otros productos a partir de una planta C3, en el que dichos productos se seleccionan entre almidones, aceites, ácidos grasos, triacilgliceroles, lípidos, celulosa u otros carbohidratos, alcoholes, azúcares, nutracéuticos, productos farmacéuticos, compuestos saborizantes y fragancias, y ácidos orgánicos en el que dicho procedimiento comprende expresar, o sobreexpresar, en una planta C3, una combinación de secuencias de nucleótidos heterólogas que codifican un transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática y una proteína moduladora de la transferencia de electrones cíclica. Este procedimiento comprende, además, cultivar dicha planta y cosechar dicha biomasa o recuperar dicho producto de dicha planta. Otro aspecto de la presente invención proporciona biomasa u otro producto producido a partir de una planta seleccionada entre almidones, aceites, ácidos grasos, lípidos, celulosa u otros carbohidratos, alcoholes, azúcares, nutracéuticos, productos farmacéuticos, compuestos saborizantes y fragancias, y ácidos orgánicos, hecho por un procedimiento de uno cualquiera de los procedimientos para hacer una realización de plantas transgénicas en la presente memoria.
Otra realización proporciona un procedimiento para elevar la actividad de transferencia de electrones cíclica (CET) en una planta C3, en el que dicho procedimiento comprende expresar o sobreexpresar, en una planta C3, una combinación de secuencias de nucleótidos heterólogas que codifican un transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática, un transportador de aniones bicarbonato, una anhidrasa carbónica, una proteína proteorodopsina dirigida a las membranas de los tilacoides; y una proteína p caroteno monooxigenasa.
Otra realización proporciona un procedimiento para mejorar la fijación de carbono en una planta C3, en el que dicho procedimiento comprende expresar, o sobreexpresar, en una planta C3, una combinación de secuencias de nucleótidos heterólogas que codifican un transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática, un transportador de aniones bicarbonato, una anhidrasa carbónica, una proteína proteorodopsina dirigida a las membranas de los tilacoides; y una proteína p caroteno monooxigenasa.
Otra realización proporciona un procedimiento para producir biomasa u otros productos a partir de una planta C3, en el que dichos productos se seleccionan entre almidones, aceites, ácidos grasos, triacilgliceroles, lípidos, celulosa u otros carbohidratos, alcoholes, azúcares, nutracéuticos, productos farmacéuticos, compuestos saborizantes y fragancias, y ácidos orgánicos en los que dicho procedimiento comprende expresar, o sobreexpresar, en una planta C3, una combinación de secuencias de nucleótidos heterólogas que codifican un transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática, un transportador de aniones bicarbonato, una anhidrasa carbónica, una proteína proteorodopsina dirigida a las membranas de los tilacoides; y una proteína p caroteno monooxigenasa. El procedimiento comprende, además, cultivar dicha planta y recolectar dicha biomasa o recuperar dicho producto de dicha planta.
Otra realización proporciona el uso de una construcción que comprende uno o más ácidos nucleicos que codifican una proteína PGR5, y una proteína HLA3;
una proteína PGR5, una proteína HLA3 y una proteína PGRL1;
una proteína PGR5, una proteína HLA3, y una proteína LCIA;
una proteína PGR5, una proteína HLA3, una proteína LCIA y una proteína BCA o HCA2;
una proteína PGR5, una proteína HLA3, una proteína PGRL1 y una proteína LCIA;
una proteína PGR5, una proteína HLA3, una proteína PGRL1, una proteína LCIA, y una proteína BCA o HCA2; una proteína PGR5, una proteína HLA3, y una proteína BCA o HCA2; o
una proteína PGR5, una proteína HLA3, una proteína PGRL1, y una proteína BCA o HCA2
para
i) hacer una planta transgénica de una primera realización;
ii) elevar la actividad de CET en una planta C3;
iii) mejorar la fijación de carbono en una planta C3; o
iv) producir biomasa u otros productos a partir de una planta C3, en la que dichos productos se seleccionan entre almidones, aceites, ácidos grasos, triacilgliceroles, lípidos, celulosa u otros carbohidratos, alcoholes, azúcares, nutracéuticos, productos farmacéuticos, compuestos saborizantes y fragancias, y ácidos orgánicos.
Otra realización proporciona el uso de una construcción que comprende uno o más ácidos nucleicos que codifican a) una proteína LCIA y una proteína BCA o HCA2;
Para
i) hacer una planta transgénica de una segunda realización;
ii) elevar la actividad de CET en una planta C3;
iii) mejorar la fijación de carbono en una planta C3; o
iv) producir biomasa u otros productos a partir de una planta C3, en la que dichos productos se seleccionan entre almidones, aceites, ácidos grasos, triacilgliceroles, lípidos, celulosa u otros carbohidratos, alcoholes, azúcares, nutracéuticos, productos farmacéuticos, compuestos saborizantes y fragancias, y ácidos orgánicos.
Un aspecto de la presente invención proporciona una planta transgénica, que comprende dentro de su genoma, y que expresa o sobreexpresa, una combinación de secuencias de nucleótidos heterólogas que codifican:
1.
i) una proteína PGRL1, una proteína PGR5, y una proteína HLA3; o
ii) una proteína PGRL1, una proteína PGR5, una proteína HLA3, una proteína LCIA, y una proteína BCA o HCA2; o
iii) una proteína Fd1, una proteína HLA3, una proteína LCIA, y una proteína BCA o HCA2; o
iv) una proteína FNR1 de hoja, una proteína HLA3, una proteína LCIA, y una proteína BCA o HCA2; o v) una proteína proteorodopsina dirigida a las membranas de los tilacoides, una proteína HLA3, una proteína LCIA, una proteína BCA o HCA2, y una p-caroteno monooxigenasa.
2. La planta transgénica de 1, en la que dicha proteorodopsina comprende un péptido de tránsito de cloroplasto seleccionado entre un dominio de transmembrana de parada de transferencia de psbX fusionado a su extremo C, un péptido de tránsito de DNAJ, un péptido de tránsito de CAB, un péptido de tránsito de PGR5, y un péptido de tránsito de psaD.
3. La planta transgénica de 1 o 2, en la que dicha p-caroteno monooxigenasa se expresa bajo el control de un promotor seleccionado entre un promotor génico inducible por etanol y un promotor específico de hoja/tejido verde seleccionado entre CAB y rbcS.
4. La planta transgénica de uno cualquiera de 1-3, en la que dicha proteorodopsina comprende una sustitución de aminoácidos seleccionada entre L219E/T206S, M79T, y M79Y, y combinaciones de las mismas.
5. La planta transgénica de uno cualquiera de 1-4, que es una planta C3.
6. La planta transgénica de uno cualquiera de 1-5, que es una planta de semillas oleaginosas transgénicas o una planta de cultivo alimentario transgénica.
7. La planta oleaginosa transgénica de 6, que se selecciona entre las plantas de los géneros Brassica (por ejemplo, colza/canola (Brassica napus; Brassica carinata; Brassica nigra; Brassica olerácea), Camelina, Miscanthus, y Jatropha; Jojoba (Simmondsia chinensis), coco; algodón; maní; arroz; cártamo sésamo; soja; mostaza que no sea Arabidopsis; trigo; lino (linaza); girasol; aceituna; maíz; palma; almendra de palma; caña de azúcar; ricino; zacate; Borago officinalis; Echium plantagineum; Cuphea hookeriana; Cuphea pulcherrima; Cuphea lanceolata; Ricinus communis; Coriandrum sativum; Crepis alpina; Vernonia galamensis; Momordica charantia; y Crambe abyssinica. 8. El alga transgénica de uno cualquiera de 1-5, que se selecciona entre Chlorella sp., Nanocloropsis sp., y Chlamydomonas sp.
9. La planta transgénica de uno cualquiera de 1-8, en la que dichas secuencias de nucleótidos heterólogas se optimizan con codones para la expresión en dicha planta transgénica.
10. La planta transgénica de uno cualquiera de 1-9, que exhibe fijación de CO2 mejorada en comparación con una planta de control por lo demás idéntica cultivada en las mismas condiciones.
11. La planta transgénica de 10, en la que la fijación de CO2 se mejora en el intervalo de aproximadamente 10 % a aproximadamente 50 % en comparación con el de una planta de control por lo demás idéntica cultivada en las mismas condiciones.
12. Una parte de dicha planta transgénica de uno cualquiera de 1-11.
13. La parte de dicha planta transgénica de 12, que se selecciona entre un protoplasto, una célula, un tejido, un órgano, un corte, un explante, un tejido reproductivo, un tejido vegetativo, biomasa, una inflorescencia, una flor, un sépalo, un pétalo, un pistilo, un estigma, un estilo, un ovario, un óvulo, un embrión, un receptáculo, una semilla, una fruta, un estambre, un filamento, una antera, un gametofito masculino o femenino, un grano de polen, un meristemo, una yema terminal, una yema axilar, una hoja, un tallo, una raíz, una raíz tuberosa, un rizoma, un tubérculo, un estolón, un cormo, un bulbo, un brote lateral, una célula de dicha planta en cultivo, un tejido de dicha planta en cultivo, un órgano de dicha planta en cultivo, un callo, materiales de propagación, germoplasma, esquejes, divisiones, y propagaciones.
14. Progenie o derivados de dicha planta transgénica de uno cualquiera de 1-11.
15. La progenie o derivados de 14, que se seleccionan entre clones, híbridos, muestras, semillas, y material recolectado de los mismos.
16. La progenie de 14 o 15, que se produce sexualmente.
17. La progenie de 14 o 15, que se produce asexualmente.
Otro aspecto de la presente invención proporciona un procedimiento seleccionado entre:
18.
i) hacer una planta transgénica de uno cualquiera de 1-11;
ii) elevar la actividad de CET en una planta C3;
iii) mejorar la fijación de carbono en una planta C3; y
iv) producir biomasa u otros productos a partir de una planta C3, en la que dichos productos se seleccionan entre almidones, aceites, ácidos grasos, triacilgliceroles, lípidos, celulosa u otros carbohidratos, alcoholes, azúcares, nutracéuticos, productos farmacéuticos, compuestos saborizantes y fragancias, y ácidos orgánicos, en donde dicho procedimiento comprende expresar, o sobreexpresar, en una planta C3, una combinación de secuencias de nucleótidos heterólogas que codifican:
a) una proteína PGRL1, una proteína PGR5, y una proteína HLA3; o
b) una proteína PGRL1, una proteína PGR5, una proteína HLA3, una proteína LCIA, y una proteína BCA o HCA2; o
c) una proteína Fd1, una proteína HLA3, una proteína LCIA, y una proteína BCA o HCA2; o
d) una proteína FNR1 de hoja, una proteína HLA3, una proteína LCIA, y una proteína BCA o HCA2; o e) una proteína proteorodopsina dirigida a las membranas de los tilacoides, una proteína HLA3, una proteína LCIA, una proteína BCA o HCA2 y una p-caroteno monooxigenasa.
19. El procedimiento de 18, en el que la etapa iv) comprende, además, cultivar dicha planta y recolectar dicha biomasa o recuperar dicho producto de dicha planta.
20. El procedimiento de 18 o 19, en el que dicha proteorodopsina comprende un péptido de tránsito de cloroplasto seleccionado entre un dominio de transmembrana de parada de transferencia de psbX fusionado a su extremo C, un péptido de tránsito de DNAJ, un péptido de tránsito de CAB, un péptido de tránsito de PGR5, y un péptido de tránsito de psaD.
21. El procedimiento de uno cualquiera de 18-20, en el que dicha p-caroteno monooxigenasa se expresa bajo el control de un promotor seleccionado entre un promotor génico inducible por etanol y un promotor específico de hoja/tejido verde seleccionado entre CAB y rbcS.
22. El procedimiento de uno cualquiera de 18-21, en el que dicha proteorodopsina comprende una sustitución de aminoácidos seleccionada entre L219E/T206S, M79T y M79Y, y combinaciones de las mismas.
23. El procedimiento de uno cualquiera de las reivindicaciones 18-22, en el que dicha planta transgénica es una planta C3.
24. El procedimiento de uno cualquiera de 18-23, en el que dicha planta transgénica es una planta oleaginosa transgénica o una planta de cultivo alimentario transgénica.
25. El procedimiento de 24, en el que dicha planta de semillas oleaginosas transgénicas se selecciona de entre las plantas de los géneros Brassica (por ejemplo, colza/canola (Brassica napus; Brassica carinata; Brassica nigra; Brassica oleracea), Camelina, Miscanthus, y Jatropha; Jojoba (Simmondsia chinensis), coco; algodón; maní; arroz; cártamo; sésamo; soja; mostaza que no sea Arabidopsis; trigo; lino (linaza); girasol; aceituna; maíz; palma; almendra de palma; caña de azúcar; ricino; zacate; Borago officinalis; Echium plantagineum; Cuphea hookeriana; Cuphea pulcherrima; Cuphea lanceolata; Ricinus communis; Coriandrum sativum; Crepis alpina; Vernonia galamensis; Momordica charantia; y Crambe abyssinica.
26. El procedimiento de uno cualquiera de 18-23, en el que dicho se selecciona de entre Chlorella sp., Nanocloropsis sp., y Chlamydomonas sp.
27. El procedimiento de uno cualquiera de 18-26, en el que dichas secuencias de nucleótidos heterólogas se optimizan con codones para la expresión en dicha planta transgénica.
28. El procedimiento de uno cualquiera de 18-27, en el que dicha planta transgénica exhibe una fijación de CO2 mejorada en comparación con una planta de control por lo demás idéntica cultivada en las mismas condiciones. 29. El procedimiento de 28, en el que la fijación de CO2 se mejora en el intervalo de aproximadamente 10 % a aproximadamente 50 % en comparación con el de una planta de control por lo demás idéntica cultivada en las mismas condiciones.
Otro aspecto de la presente invención proporciona una planta transgénica hecha por el procedimiento de uno cualquiera de 18-29.
Aun otro aspecto de la presente invención proporciona una biomasa u otro producto de una planta, seleccionado entre almidones, aceites, ácidos grasos, lípidos, celulosa u otros carbohidratos, alcoholes, azúcares, nutracéuticos, productos farmacéuticos, compuestos saborizantes y fragancias, y ácidos orgánicos, hechos por el procedimiento de uno cualquiera de 18-29.
En adición a las diversas realizaciones enumeradas anteriormente, en los ejemplos a continuación, y en las reivindicaciones, la presente divulgación abarca de manera diversa las combinaciones de proteínas de CCM actualmente divulgadas y reivindicadas en combinaciones adicionales con los genes y proteínas que se centran en vías modificadas genéticamente que están directamente involucradas en facilitar el transporte de CO2 a cloroplastos de hojas, divulgados y reivindicados en la solicitud anterior de los inventores Publicación internacional del PCT núm. WO 2012/125737. La presente divulgación abarca cualquier combinación de genes divulgados en la presente memoria con
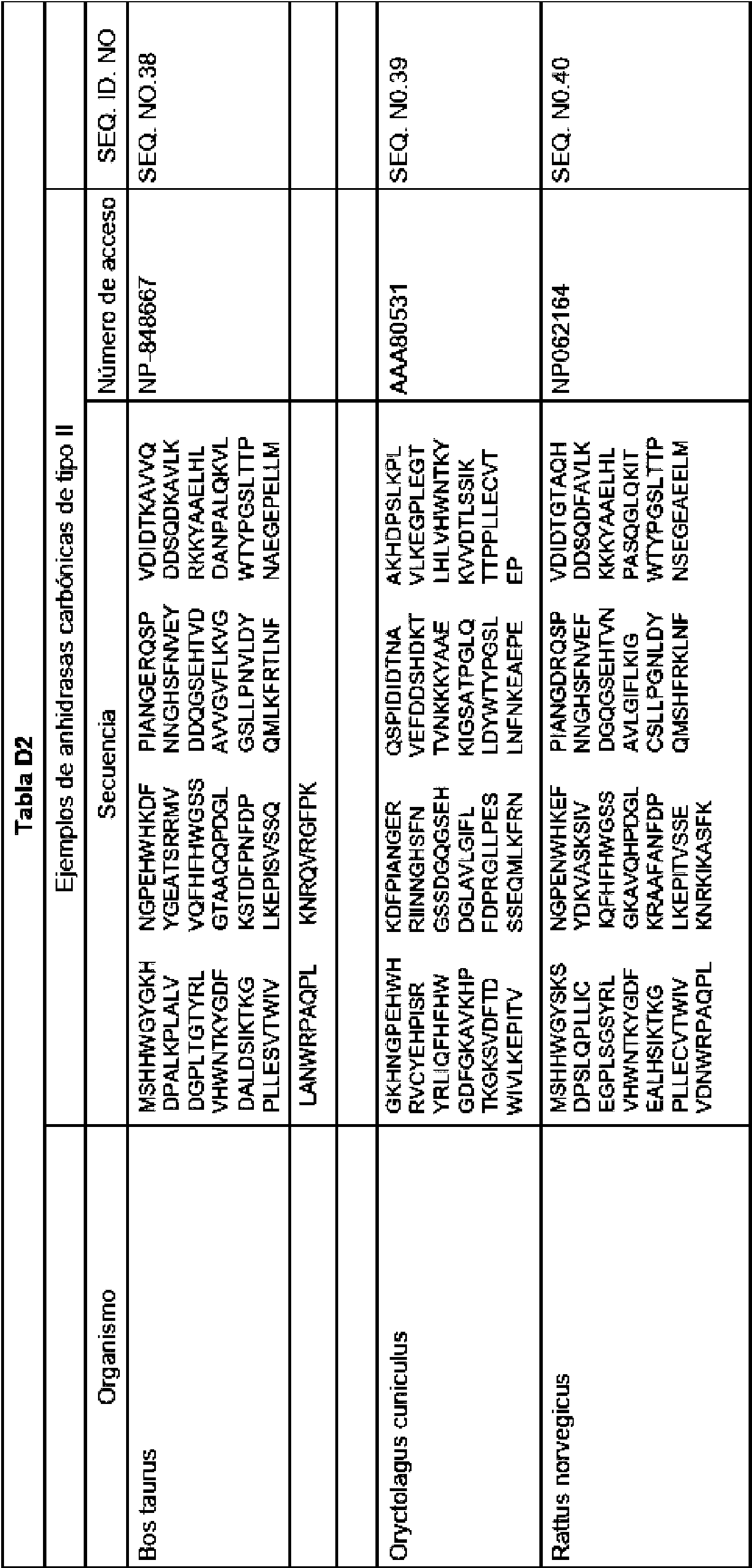
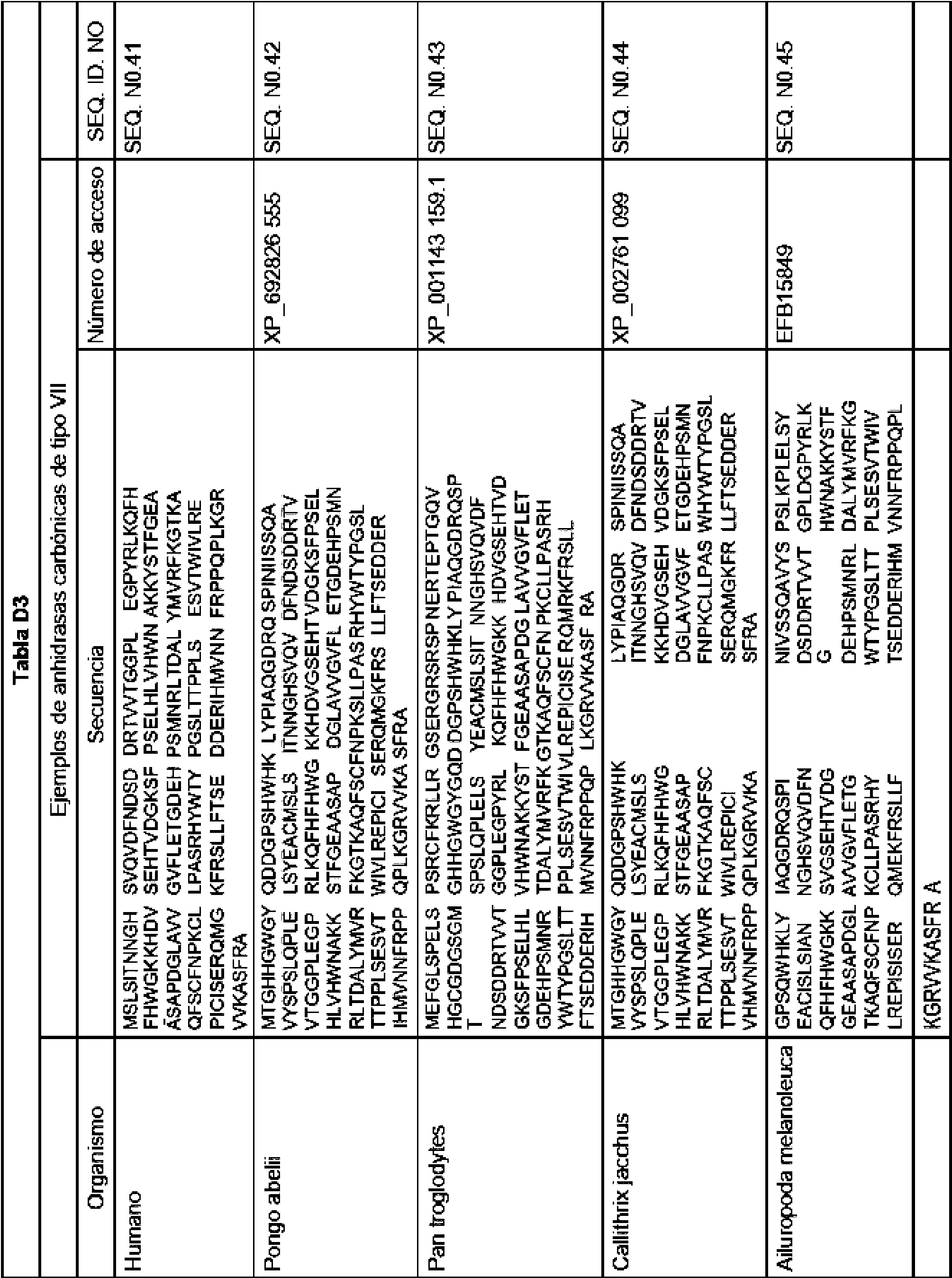
cualquier combinación de genes divulgados en el documento núm. WO 2012/125737 y en las Tablas D1-D9 para mejorar los sistemas de concentración de carbono (CCM) en plantas.
La Tabla D1 representa diferentes clases de a-CA encontradas en mamíferos.
La Tabla D2-D4 representa especies representativas, números de acceso al Gene bank y secuencias de aminoácidos para diversas especies de genes CA adecuados.
La Tabla D5 representa la secuencia de ADN optimizada con codones para la expresión en cloroplastos en Chlamydomonas reinhardtii. En la Tabla D5, las secuencias subrayadas representan sitios de restricción, y las bases cambiadas para optimizar la expresión de cloroplastos se enumeran en minúsculas. La Tabla D6 proporciona un desglose del número y tipo de cada codón optimizado.
Las especies representativas y los números de acceso al Gene bank para varias especies de transportadores de bicarbonato se enumeran a continuación en las Tablas D8-D9.
El ámbito adicional de la aplicabilidad de las realizaciones divulgadas actualmente se hará evidente a partir de la descripción detallada y los dibujos proporcionados a continuación. Sin embargo, debe entenderse que la descripción detallada y los ejemplos específicos, si bien indican las realizaciones preferentes de la presente divulgación, se proporcionan solamente a modo de ilustración, ya que varios cambios y modificaciones dentro del espíritu y ámbito de la invención serán evidentes para los expertos en la técnica a partir de la descripción detallada.
Breve descripción del listado de secuencias
La divulgación puede entenderse más completamente a partir de la siguiente descripción detallada y de la Lista de secuencias adjunta, que forman parte de la presente solicitud.
Las descripciones de las secuencias resumen la Lista de secuencias adjunta a la presente. La Lista de secuencias contiene símbolos estándar y el formato usado para los datos de secuencia de nucleótidos y aminoácidos cumple con las reglas establecidas en 37 C.F.R. § 1.822.
Breve descripción de los dibujos
Los aspectos anteriores y otros aspectos, características y ventajas de la presente divulgación se entenderán mejor a partir de las siguientes descripciones detalladas tomadas junto con las dibujos adjuntos, todas las cuales se proporcionan a modo de ilustración únicamente y no son limitativos de las realizaciones actualmente divulgadas, en las cuales:
Figura 1. Modelo de CCM de Chlamydomonas que muestra la localización de transportadores de carbono inorgánico (HLA3, LCIA) y anhidrasa carbónica (CAH: CAH1, CAH3, y CAH6) [5]), y Rubisco. LCIB es una proteína esencial para CCM en Chlamydomonas. Su función exacta se desconoce.
Figura 2. (A) Fenotipos de crecimiento de Arabidopsis transgénica HLA3 (T3) y WT inicialmente cultivadas en medios MS (más nitrato, NO3- ). (B) medios MS (más amonio (NH/) y sacarosa) o en suelo (solo amonio). X indica que las plantas que murieron. Los números se refieren a líneas de plantas.
Figura 3. (A) Fenotipos de crecimiento de Arabidopsis transgénica HCA-II (T1) y WT 4 semanas después de la germinación. (B) Fenotipo de crecimiento de Arabidopsis WT (Col-0, izquierda) y el transgénico de BCA (T3) (derecha). Figura 4. Tasa de asimilación fotosintética de CO2 en tres líneas transgénicas (P1, P5, P6) de Arabidopsis que expresan BCA (anhidrasa carbónica bacteriana) medida con un analizador de gases LICOR 6400. Estas líneas mostraron un aumento de ~ 30 % en su eficiencia fotosintética en comparación con Arabidopsis WT (Col.-0). Figura 5. (A) Fenotipos de crecimiento de plantas de Arabidopsis transgénicas de LCIA (T1) y WT cuatro semanas después de la germinación. (B) Camelina WT de cuatro semanas (4 plantas izquierda) y transgénica independiente (derecha 4 plantas) que expresan LCIA. (C) Tasas fotosintéticas dependientes de CO2 de Camelina WT y transgénica de LCIA.
Figura 6. Fenotipo de transgénicos de HLA3 cultivados en nitrato. Carga de energía y potencial reductor de Arabidopsis transgénica de HLA3 y WT. Niveles de adenilato, cofactores de nucleótidos, y fosfato inorgánico medidos como nmol/gFW para plantas cultivadas en nitrato. Los valores son promedios ± SE.
Figura 7. Radiación fotosintéticamente activa en proteorodopsina en relación con la clorofila de origen vegetal [49]. Figura 8. Plásmido pB110-CAB-PGR5-NOS (Ejemplo 1).
Figura 9. Plásmido pB110-HLA3-pgr5-dsred (Ejemplo 1).
Figura 10. Plásmido pBI 121-CAB1-Tp-NgCAf2-dsred (Ejemplo 1).
La Figura 11 ilustra las curvas de respuesta a la luz de las líneas Camelina BCA.
La Figura 12 ilustra la expresión de LCIA en Camelina vs WT.
Descripción detallada de varias realizaciones
La siguiente descripción detallada se proporciona para ayudar a los expertos en la técnica a practicar las diversas realizaciones de la presente divulgación descritas en la presente memoria, que incluyen todos los procedimientos, usos,
composiciones, etc., descritos en la presente memoria. Aun así, la siguiente descripción detallada no debe interpretarse como una limitación indebida de la presente divulgación, ya que los expertos en la técnica pueden realizar modificaciones y variaciones en las realizaciones discutidas en la presente memoria sin apartarse del espíritu o ámbito de los presentes descubrimientos.
La presente divulgación se explica con mayor detalle a continuación. La presente divulgación no pretende ser un catálogo detallado de todas las diferentes formas en que pueden implementarse realizaciones de la presente divulgación, o todas las características que pueden adicionarse a las realizaciones instantáneas. Por ejemplo, las características ilustradas con respecto a una realización pueden incorporarse en otras realizaciones, y las características ilustradas con respecto a una realización particular pueden eliminarse de esa realización. En adición, numerosas variaciones y adiciones a las diversas realizaciones sugeridas en la presente memoria serán evidentes para los expertos en la técnica a la luz de la divulgación instantánea, cuyas variaciones y adiciones no se apartan del ámbito de la divulgación instantánea. Por lo tanto, la siguiente especificación pretende ilustrar algunas realizaciones particulares de la divulgación, y no especificar exhaustivamente todas las permutaciones, combinaciones y variaciones de las mismas.
Cualquier característica o combinación de las características descritas en la presente memoria se incluyen dentro del ámbito de la presente divulgación siempre que las características incluidas en cualquier combinación no sean mutuamente incompatibles como resultará evidente a partir del contexto, esta especificación, y el conocimiento del experto en la técnica. Las ventajas y aspectos adicionales de la presente divulgación son evidentes en la descripción detallada y las reivindicaciones siguientes.
Definiciones
Las siguientes definiciones se proporcionan para ayudar al lector a comprender los diversos aspectos de la presente divulgación. A menos que se defina de cualquier otra manera, todos los términos técnicos y científicos usados en la presente memoria tienen el mismo significado que el comprendido comúnmente por el experto en la técnica a la que pertenece la presente divulgación.
Como se usa en la presente memoria y en las reivindicaciones adjuntas, las formas singulares "un", "una", y "el/la" incluyen referentes plurales a menos que el contexto lo indique claramente en contra. Así, por ejemplo, la referencia a "una planta" incluye una pluralidad de tales plantas, la referencia a "una célula" incluye una referencia a una o más células y equivalentes de las mismas conocidos por los expertos en la técnica, etcétera. Similarmente, la palabra "o" pretende incluir "y" a menos que el contexto lo indique claramente de cualquier otra forma. Por lo tanto "que comprende A o B" significa que incluye A, o B, o A y B. Además, el uso del término "que incluye", así como otras formas relacionadas, tales como "incluye" e "incluido", no es limitativo.
El término "aproximadamente" como se usa en la presente memoria es una palabra flexible con un significado similar a "aproximadamente" o "casi". El término "aproximadamente" indica que no se reclama exactitud, sino más bien una variación contemplada. Así, como se usa en la presente memoria, el término "aproximadamente" significa dentro de 1 o 2 desviaciones estándar del valor específicamente referido, o ± un intervalo de hasta 20 %, hasta 15 %, hasta 10 %, hasta 5 %, o hasta 4 %, 3 %, 2 %, o 1 % en comparación con el valor específicamente referido.
El término "que comprende" como se usa en una reivindicación en la presente memoria es abierto, y significa que la reivindicación debe tener todas las características específicamente mencionadas allí, pero que no hay impedimento para que características adicionales que no se mencionan también estén presentes. El término "que comprende" deja abierta la reivindicación para la inclusión de ingredientes no especificados incluso en grandes cantidades. El término "que consiste esencialmente en" en una reivindicación significa que la invención necesariamente incluye los ingredientes enumerados, y está abierta a ingredientes no listados que no afectan materialmente a las propiedades básicas y novedosas de la invención. Una reivindicación "que consiste esencialmente en" ocupa un término medio entre las reivindicaciones cerradas que se escriben en un formato cerrado "que consiste en" y las reivindicaciones completamente abiertas que se redactan en un formato "que comprende". Estos términos pueden usarse indistintamente en la presente memoria si, y cuando, esto puede ser necesario. Además, el uso del término "que incluye", así como otras formas relacionadas, tales como "incluyen" e "incluido", no es limitativo.
"BCA" se refiere a la anhidrasa carbónica bacteriana.
"CCM" y similares se refieren a sistemas de concentración de carbono.
"CET" se refiere a la transferencia de electrones cíclica.
"LET" se refiere a la transferencia lineal de electrones.
"WT" se refiere a tipo salvaje.
La "proteína moduladora de transferencia de electrones cíclica" se refiere a cualquier proteína natural o sintética que mejora la separación de carga a través de la membrana del tilacoide, lo que resulta en una fotofosforilación mejorada con la producción de energía química. Ejemplos de tales moduladores son las reductasas PGR5 y PRGL1, sin embargo las proteínas mejoradas en la cadena de transporte de electrones tales como los citocromos, ATPasas, ferredoxina-NADP reductasa, NAD(P)H-plastoquinona reductasa, y lo similar también son proteínas moduladoras de CET.
A menos que se indique en contra, las secuencias de ácido nucleico en el texto de la presente especificación se dan, cuando se leen de izquierda a derecha, en la dirección 5' a 3'. Las secuencias de ácido nucleico pueden proporcionarse como ADN o como ARN, como se especifica; la divulgación de una define necesariamente a la otra, como es conocido por un experto en la técnica y se entiende que se incluyen en realizaciones en las que sería apropiado. Los nucleótidos pueden referirse por sus códigos de una letra comúnmente aceptados. A menos que se indique en contra, las secuencias de aminoácidos se escriben de izquierda a derecha en orientación de amino a carboxilo, respectivamente. Los aminoácidos pueden referirse en la presente memoria ya sea por los símbolos de tres letras comúnmente conocidos o por los símbolos de una letra recomendados por la IUPAC-IUM Biochemical Nomenclature Commission. Debe entenderse, además, que todos los tamaños de bases o tamaños de aminoácidos, y todos los valores de peso molecular o masa molecular, dados para ácidos nucleicos o polipéptidos son aproximados, y se proporcionan con fines descriptivos y no deben ser excesivamente limitativos.
Con respecto a los intervalos divulgados, los puntos finales de todos los intervalos dirigidos al mismo componente o propiedad son inclusivos y combinables independientemente (por ejemplo, intervalos de hasta aproximadamente 25 % en peso, o, más específicamente, aproximadamente de 5 % en peso a aproximadamente 20 % en peso," incluye los puntos finales y todos los valores intermedios de los intervalos de "aproximadamente 5 % en peso a aproximadamente 25 % en peso," etc.). Los intervalos numéricos referidos con la especificación son inclusivos de los números que definen el intervalo e incluyen cada número entero dentro del intervalo definido.
Como se usa en la presente memoria, "alterar el nivel de producción" o "alterar el nivel de expresión" significa cambiar, ya sea por aumento o disminución, el nivel de producción o expresión de una secuencia de ácido nucleico o una secuencia de aminoácidos (por ejemplo, un polipéptido, un ARNsi, un ARNmi, un ARNm, un gen), en comparación con un nivel de control de producción o expresión.
"Sustituciones de aminoácidos conservadoras": Es bien conocido que ciertos aminoácidos pueden sustituirse por otros aminoácidos en una estructura de proteína sin una pérdida apreciable de actividad bioquímica o biológica. Dado que la capacidad de interacción y la naturaleza de una proteína es lo que define la actividad biológica funcional de esa proteína, pueden hacerse ciertas sustituciones de la secuencia de aminoácidos en una secuencia proteica y, por supuesto, en su secuencia codificante de ADN, y no obstante obtener una proteína con propiedades similares. Así, pueden realizarse varios cambios en las secuencias de aminoácidos divulgadas en la presente memoria, o en las secuencias de ADN correspondientes que codifican estas secuencias de aminoácidos, sin pérdida apreciable de su utilidad o actividad biológica.
Las proteínas y péptidos biológicamente funcionalmente equivalentes a las proteínas y péptidos divulgados en la presente memoria incluyen secuencias de aminoácidos que contienen cambios conservadores de aminoácidos en la secuencia de aminoácidos fundamental. En tales secuencias de aminoácidos, uno o más aminoácidos en la secuencia fundamental pueden sustituirse, por ejemplo, con otro(s) aminoácido(s), cuya(s) carga(s) y polaridad(es) sea(n) similar(es) a la del aminoácido nativo, es decir, una sustitución de aminoácidos conservadora, lo que resulta en un cambio silencioso.
Cabe señalar que hay varios sistemas de clasificación diferentes en la técnica que se desarrollaron para describir la intercambiabilidad de aminoácidos entre sí dentro de péptidos, polipéptidos, y proteínas. La siguiente discusión es meramente ilustrativa de algunos de estos sistemas, y la presente divulgación abarca cualquiera de los cambios de aminoácidos "conservadores" que serían evidentes para un experto en la técnica de la química de péptidos, polipéptidos, y proteínas de cualquiera de estos diferentes sistemas.
Como se divulga en la Patente de Estados Unidos núm. 5,599,686, ciertos aminoácidos en un péptido, polipéptido, o proteína biológicamente activos pueden reemplazarse por otros aminoácidos homólogos, isostéricos, y/o isoelectrónicos, en los que la actividad biológica de la molécula original se conserva en el péptido, polipéptido, o proteína modificado. La siguiente lista de reemplazos de aminoácidos pretende ser ilustrativa y no limitativa:
En otro sistema, los sustitutos de un aminoácido dentro de una secuencia fundamental pueden seleccionarse de otros miembros de la clase a la que pertenece el aminoácido natural. Los aminoácidos pueden dividirse en los siguientes cuatro grupos: (1) aminoácidos ácidos; (2) aminoácidos básicos; (3) aminoácidos polares neutros; y (4) aminoácidos no polares neutros. Los aminoácidos representativos dentro de estos diversos grupos incluyen, pero no se limitan a: (1) aminoácidos ácidos (cargados negativamente) tales como ácido aspártico y ácido glutámico; (2) aminoácidos básicos (cargados positivamente) tales como arginina, histidina, y lisina; (3) aminoácidos polares neutros tales como glicina, serina, treonina, cisteína, cistina, tirosina, asparagina y glutamina; (4) aminoácidos neutros no polares (hidrófobos) tales como alanina, leucina, isoleucina, valina, prolina, fenilalanina, triptófano, y metionina.
Los cambios conservadores de aminoácidos dentro de una secuencia fundamental de péptidos, polipéptidos, o proteínas pueden realizarse mediante la sustitución de un aminoácido dentro de uno de estos grupos con otro aminoácido dentro del mismo grupo.
Algunos de los otros sistemas para clasificar la intercambiabilidad conservadora de aminoácidos en péptidos, polipéptidos, y proteínas aplicables a las secuencias de la presente divulgación incluyen, por ejemplo, los siguientes:
Definir funcionalmente las propiedades comunes entre aminoácidos individuales mediante el análisis de las frecuencias normalizadas de los cambios de aminoácidos entre las proteínas correspondientes de organismos homólogos (Schulz, GE y RH Schirmer (1979) Principles of Protein Structure (Springer Advanced Texts in Chemistry), Springer-Verlag). De acuerdo con tales análisis, pueden definirse grupos de aminoácidos donde los aminoácidos dentro de un grupo se intercambian, preferentemente, entre sí y por lo tanto se parecen más en su impacto en la estructura proteica general;
Hacer cambios de aminoácidos basados en el índice hidropático de aminoácidos como se describe por Kyte y Doolittle (1982) J. Mol. Biol. 157(1):105-32. Ciertos aminoácidos pueden sustituirse por otros aminoácidos que tienen un índice o puntaje hidropático similar y aún resultan en una proteína con actividad biológica similar, es decir, todavía se obtiene una proteína biológica funcionalmente equivalente. Al realizar tales cambios, se prefiere la sustitución de aminoácidos cuyos índices hidropáticos están dentro de 2, aquellos que están dentro de 1 se prefieren particularmente, y aquellos dentro de 0,5 se prefieren particularmente aún más;
Sustitución de aminoácidos similares sobre la base de la hidrofilicidad. La patente de Estados Unidos núm.
4,554,101 establece que la mayor hidrofilicidad media local de una proteína, según se rige por la hidrofilicidad de sus aminoácidos adyacentes, se correlaciona con una propiedad biológica de la proteína. Como se detalla en esta patente, los siguientes valores de hidrofilicidad se asignaron a residuos de aminoácidos: arginina (+3,0); lisina (+3,0); aspartato (+ 3,0 0,1); glutamato (+ 3,0 0,1); serina (+0,3); asparagina (+0,2); glutamina (+0,2); glicina (0); treonina (-0,4); prolina (-0,5 0.1); alanina (-0,5); histidina (-0,5); cisteína (-1,0); metionina (-1,3); valina (-1,5); leucina (-1,8); isoleucina (-1,8); tirosina (-2,3); fenilalanina (-2,5); triptófano (-3,4).Betts y Russell ((2003), "Amino Acid Properties and Consequences of Substitutions", Bioinformatics for Geneticists, Michael R. Barnes e Ian C. Gray,
Eds., John Wiley & Sons, Ltd, capítulo 14, pág. 289-316) revisan la naturaleza de las mutaciones y las propiedades de los aminoácidos en una variedad de contextos proteicos diferentes con el propósito de ayudar a anticipar e interpretar el efecto que un cambio particular de aminoácidos tendrá en la estructura y función de la proteína. Los autores señalan que las características de las proteínas relevantes para considerar las mutaciones de aminoácidos incluyen entornos celulares, estructura tridimensional, y evolución, así como las clasificaciones de aminoácidos basadas en principios evolutivos, químicos, y estructurales, y la función de los aminoácidos de diferentes clases en la estructura y función de proteínas en diferentes contextos. Los autores señalan que la clasificación de aminoácidos en categorías como las que se muestran en la Figura 14.3 de su revisión, que implica propiedades fisicoquímicas comunes, tamaño, afinidad por el agua (polar y no polar; carga negativa o positiva), aromaticidad y alifaticidad, capacidad de enlace de hidrógeno, propensión a regiones que giran bruscamente, etc., deja en claro que la dependencia de clasificaciones simples puede ser peligrosa, y sugiere que aminoácidos alternativos podrían modificarse en una proteína en cada posición. Los criterios para interpretar cómo una mutación particular podría afectar la estructura y función de la proteína se resumen en la sección 14.7 de la presente revisión, e incluyen primero preguntar sobre la proteína, y después sobre la sustitución de aminoácidos particular contemplada.
Los equivalentes funcionales biológicamente/enzimáticamente de las proteínas y péptidos divulgados en la presente memoria pueden tener 10 o menos cambios conservadores de aminoácidos, con mayor preferencia siete o menos cambios conservadores de aminoácidos, y con la máxima preferencia cinco o menos cambios conservadores de aminoácidos, es decir, 10, 9, 8, 7, 6, 5, 4, 3, 2 o 1 cambios conservadores de aminoácidos. La secuencia de nucleótidos codificante (por ejemplo, gen, ADN plasmídico, ADNc, ADN optimizado con codones u otro ADN sintético) tendrá así las sustituciones de bases correspondientes, lo que le permitirá codificar la forma equivalente biológicamente funcionalmente de la proteína o péptido. Debido a la degeneración del código genético, es decir, la existencia de más de un codón para la mayoría de los aminoácidos que se producen naturalmente en las proteínas, otras secuencias de ADN (y ARN) que contienen esencialmente la misma información genética que estos ácidos nucleicos, y que codifican la misma secuencia de aminoácidos que la codificada por estos ácidos nucleicos, puede usarse en los procedimientos divulgados en la presente memoria. Este principio se aplica también a cualquiera de las otras secuencias de nucleótidos divulgadas en la presente memoria.
"Control" o "nivel de control" significa el nivel de una molécula, tal como un polipéptido o ácido nucleico, que normalmente se encuentra en la naturaleza bajo una determinada condición y/o en un entorno genético específico. En ciertas realizaciones, puede medirse el nivel de control de una molécula en una célula o muestra que se sometió, directa o indirectamente, a un tratamiento. Un nivel de control se conoce, además, como tipo salvaje o nivel basal. Los expertos en la técnica entienden estos términos. Una planta de control, es decir, una planta que no contiene un ADN recombinante que confiera (por ejemplo) un rasgo mejorado en una planta transgénica, se usa como línea de base para la comparación para identificar un rasgo mejorado en la planta transgénica. Una planta de control adecuada puede ser una planta no transgénica de la línea parental usada para generar una planta transgénica. En algunos casos una planta de control puede ser una línea de planta transgénica que comprende un vector o gen marcador vacío, pero no contiene el ADN recombinante, o no contiene todos los ADN recombinantes, en la planta de prueba.
Los términos "potenciar", "potenciando", "aumentar" o "aumentado" se refieren a un aumento estadísticamente significativo. Para evitar dudas, estos términos generalmente se refieren a aproximadamente un aumento del 5 % en un parámetro o valor dado, aproximadamente un aumento del 10 %, aproximadamente un aumento del 15 %, aproximadamente un aumento del 20 %, aproximadamente un aumento del 25 %, aproximadamente un aumento del 30 %, aproximadamente un aumento de 35 %, aproximadamente un aumento del 40 %, aproximadamente un aumento del 45 %, aproximadamente un aumento del 50 %, aproximadamente un aumento del 55 %, aproximadamente un aumento del 60 %, aproximadamente un aumento del 65 %, aproximadamente un aumento del 70 %, aproximadamente un aumento del 75 %, aproximadamente un aumento del 80 %, aproximadamente un aumento del 85 %, aproximadamente un aumento del 90 %, aproximadamente un aumento del 95 %, aproximadamente un aumento del 100 %, o más sobre el valor de control. Estos términos abarcan, además, intervalos que consisten en cualquier valor indicado más bajo a cualquier valor indicado más alto, por ejemplo "de aproximadamente 5 % a aproximadamente 50 %", etc.
"Expresión" o "expresando" se refiere a la producción de un producto funcional, tal como, la generación de un transcripto de ARN a partir de una construcción introducida, una secuencia de ADN endógeno, o una secuencia de ADN heterólogo incorporada de forma estable. Una secuencia codificante de nucleótidos puede comprender una secuencia intermedia (por ejemplo, intrones) o puede carecer de tales secuencias intermedias no traducidas (por ejemplo, como en el ADNc). Los genes expresados incluyen los que se transcriben en ARNm y luego se traducen en proteínas y los que se transcriben en ARN pero no se traducen (por ejemplo, ARNip, ARN de transferencia y ARN ribosómico). El término puede referirse, además, a un polipéptido producido a partir de un ARNm generado a partir de cualquiera de los precursores de ADN anteriores. Así, la expresión de un fragmento de ácido nucleico, tal como un gen o una región promotora de un gen, puede referirse a la transcripción del fragmento de ácido nucleico (por ejemplo, la transcripción que produce ARNm u otro ARN funcional) y/o la traducción de ARN a un proteína precursora o madura (polipéptido), o ambas.
Un "casete de expresión" se refiere a una construcción de ácido nucleico, que cuando se introduce en una célula huésped, da como resultado la transcripción y/o traducción de un ARN o polipéptido, respectivamente.
El término "genoma", tal como se aplica a las células de una planta, abarca no solo el ADN cromosómico que se encuentra dentro del núcleo, sino también el ADN de los orgánulos que se encuentra dentro de los componentes subcelulares (por ejemplo, mitocondrial, de plastidios) de la célula. Como se usa en la presente memoria, el término "genoma" se refiere al genoma nuclear a menos que se indique en contra. Sin embargo, la expresión en un genoma de plastidio, por ejemplo, un genoma de cloroplasto, o el direccionamiento a un genoma de plastidiotal como un cloroplasto mediante el uso de una secuencia de direccionamiento de plastidio, también se abarca por la presente divulgación.
El término "heterólogo" se refiere a un fragmento de ácido nucleico o proteína que es extraño a su entorno. En el contexto de un fragmento de ácido nucleico, esto se logra típicamente mediante la introducción de tal fragmento, derivado de una fuente, en un huésped diferente. Los fragmentos de ácido nucleico heterólogo, como las secuencias de codificación que se insertaron en un organismo huésped, normalmente no se encuentran en el complemento genético del organismo huésped. Como se usa en la presente memoria, el término "heterólogo" se refiere, además, a un fragmento de ácido nucleico derivado del mismo organismo, pero que se encuentra en una ubicación diferente, por ejemplo, no nativa, dentro del genoma de este organismo. Así, el organismo puede tener más del número habitual de copias de tal fragmento ubicado en su posición normal dentro del genoma y en adición, en el caso de las células vegetales, dentro de diferentes genomas dentro de una célula, por ejemplo, en el genoma nuclear y también dentro de un genoma de plastidio o mitocondrial. Un fragmento de ácido nucleico que es heterólogo con respecto a un organismo en el que se insertó o se transfirió a veces se denomina "transgen."
Una secuencia de nucleótidos que codifica la proteína péptido de tránsito de CAB o una proteína PGRL1 "heteróloga", etc., puede ser una o más copias adicionales de una secuencia de nucleótidos que codifica la proteína péptido de tránsito de CAB o proteína PGRL1 endógena, o una secuencia de nucleótidos de otra planta u otra fuente. PGRL1 es una posible ferredoxina-plastoquinona reductasa implicada en el flujo de electrones cíclicos fotosintético. Además, estas pueden ser secuencias de nucleótidos genómicas o no genómicas. Las secuencias de nucleótidos no genómicas que codifican tales proteínas y péptidos incluyen, a modo de ejemplos no limitativos, ARNm; ADN producido sintéticamente que incluye, por ejemplo, ADNc y secuencias optimizadas con codones para una expresión eficiente en diferentes plantas transgénicas que reflejan el patrón de uso de codones en tales plantas; secuencias de nucleótidos que codifican las mismas proteínas o péptidos, pero que se degeneran de acuerdo con la degeneración del código genético; que contienen sustituciones conservadoras de aminoácidos que no afectan negativamente a su actividad, etc., como conocen los expertos en la técnica.
El término "homología" describe una comparación matemáticamente basada en similitudes de secuencia que se usa para identificar genes o proteínas con funciones o motivos similares. Las secuencias de ácido nucleico y proteína de la presente invención pueden usarse como una "secuencia de consulta" para realizar una búsqueda en bases de datos públicas para, por ejemplo, identificar a otros miembros de la familia, secuencias relacionadas, u homólogos. El término "homólogo" se refiere a la relación entre dos secuencias de ácido nucleico y/o proteína que poseen un "origen evolutivo común", incluidos los ácidos nucleicos y/o proteínas de superfamilias (por ejemplo, la superfamilia de inmunoglobulinas) en la misma especie de animal, así como ácidos nucleicos homólogos y/o proteínas de diferentes especies de animales (por ejemplo, polipéptido de cadena ligera de miosina, etc.; véase Reeck y otros, (1987) Cell, 50:667). Tales proteínas (y sus ácidos nucleicos codificadores) pueden tener homología de secuencia, como se refleja por la similitud de secuencia, ya sea en términos de porcentaje de identidad o por la presencia de residuos o motivos específicos y posiciones conservadas. Los procedimientos divulgados en la presente memoria contemplan el uso de las secuencias nucleicas y de proteínas descritas actualmente, así como las secuencias que tienen identidad y/o similitud de secuencia, y una función similar.
Célula huésped" significa una célula que contiene un vector y admite la replicación y/o expresión del vector. Las células huésped pueden ser células procariotas tales como E. coli, o células eucariotas tales como células de levadura, insecto, anfibio, o mamífero. Alternativamente, las células huésped son células vegetales de monocotiledóneas o dicotiledóneas.
El término "introducido" significa proporcionar un ácido nucleico (por ejemplo, una construcción de expresión) o proteína en una célula. "Introducido" incluye referencia a la incorporación de un ácido nucleico en una célula eucariota o procariota donde el ácido nucleico puede incorporarse en el genoma de la célula, e incluye referencia a la provisión transitoria de un ácido nucleico o proteína a la célula. "Introducido" incluye referencias a procedimientos de transformación estables o transitorios, así como al cruce sexual. Así, "introducido" en el contexto de insertar un fragmento de ácido nucleico (por ejemplo, una construcción de ADN recombinante/construcción de expresión) en una célula, puede significar "transfección" o "transformación" o "transducción", e incluye referencias a la incorporación de un fragmento de ácido nucleico en una célula eucariota o procariota donde el fragmento de ácido nucleico puede incorporarse al genoma de la célula (por ejemplo, cromosoma, plásmido, plastidio, o ADN mitocondrial), convertirse en un replicón autónomo, o expresarse de manera transitoria (por ejemplo, ARNm transfectado).
El término "aislado" se refiere a un material tal como una molécula de ácido nucleico, polipéptido, o molécula pequeña, que se separó del entorno del que se obtuvo. Puede significar, además, alterado del estado natural. Por ejemplo, un polinucleótido o un polipéptido presente de forma natural en un animal vivo no está "aislado", pero el mismo polinucleótido o polipéptido separado de los materiales coexistentes de su estado natural está "aislado", según el término que se emplea en la presente memoria. Así, un polipéptido o polinucleótido producido y/o contenido dentro de una célula huésped recombinante se considera aislado. Se entiende, además, como "polipéptidos aislados" o
"moléculas de ácido nucleico aisladas", etc., a los polipéptidos o moléculas de ácido nucleico que se purificaron, parcial o sustancialmente, de una célula huésped recombinante o de una fuente nativa.
Como se usa en la presente memoria, "ácido nucleico" o "secuencia de nucleótidos" significa un polinucleótido (u oligonucleótido), que incluye polímeros mono o bicatenarios de bases de desoxirribonucleótidos o ribonucleótidos y, a menos que se indique en contra, abarca análogos de nucleótidos sintéticos y de origen natural que tienen la naturaleza esencial de nucleótidos naturales porque hibridan con ácidos nucleicos monocatenarios complementarios de manera similar a los nucleótidos naturales. Los ácidos nucleicos pueden incluir, además, fragmentos y secuencias de nucleótidos modificadas. Los ácidos nucleicos divulgados en la presente memoria pueden ser de origen natural, por ejemplo, ácidos nucleicos genómicos, o ácidos nucleicos aislados, purificados, no genómicos, que incluyen secuencias de ácido nucleico producidas sintéticamente, tales como las producidas por síntesis de oligonucleótidos químicos en fase sólida, síntesis enzimática, o por procedimientos de recombinación, que incluyen, por ejemplo, ADNc, secuencias optimizadas con codones para una expresión eficiente en diferentes plantas transgénicas que reflejan el patrón de uso de codones en tales plantas, secuencias de nucleótidos que difieren de las secuencias de nucleótidos divulgadas en la presente memoria debido a la degeneración del código genético pero que aún codifican las proteínas de interés divulgadas en la presente memoria, secuencias de nucleótidos que codifican las proteínas descritas actualmente que comprenden sustituciones de aminoácidos conservadoras (o no conservadoras) que no afectan negativamente a su actividad normal, secuencias de nucleótidos amplificadas por PCR, y otras formas no genómicas de secuencias de nucleótidos familiares para los expertos en la técnica.
Las secuencias de nucleótidos que codifican proteínas y las secuencias de nucleótidos promotoras usadas para conducir su expresión, divulgadas en la presente memoria pueden ser secuencias de nucleótidos genómicas o no genómicas. Las secuencias y los promotores que codifican secuencias nucleotídicas no genómicas codificantes de proteínas incluyen, por ejemplo, ARNm natural, ARNm producido sintéticamente, ADN natural, o ADN producido sintéticamente. Las secuencias de nucleótidos sintéticas pueden producirse por medios bien conocidos en la técnica, que incluyen síntesis química o enzimática de oligonucleótidos, e incluyen, por ejemplo, ADNc, secuencias optimizadas con codones para una expresión eficiente en diferentes plantas transgénicas que reflejan el patrón de uso de codones en tales organismos, variantes que contienen sustituciones de aminoácidos conservadoras (o no conservadoras) que no afectan negativamente a su actividad normal, secuencias de nucleótidos amplificadas por PCR, etc.
"Una proteína PGRL1", "una proteína PGR5", "una proteína HLA3", "un péptido de tránsito de CAB", "un péptido de tránsito de PGR5", o cualquier otra proteína o péptido actualmente ampliamente divulgado y utilizado en cualquiera de los procedimientos de CCM y plantas descritas en la presente memoria se refieren a una proteína o péptido que exhibe actividad enzimática/funcional similar o idéntica a la actividad enzimática/funcional de la proteína o péptido específicamente nombrado. Las actividades enzimáticas/funcionales de las proteínas y péptidos divulgadas en la presente memoria se describen a continuación. La actividad enzimática/funcional "similar" de una proteína o péptido puede estar en el intervalo de aproximadamente 75 % a aproximadamente 125 % o más de la actividad enzimática/funcional de la proteína o péptido específicamente nombrado cuando iguales cantidades de tanto proteínas como péptidos se ensayan, prueban, o expresan como se describe a continuación en condiciones idénticas y, por lo tanto, pueden sustituirse satisfactoriamente por las proteínas o péptidos específicamente nombrados en los presentes procedimientos mejorados de CCM y plantas transgénicas.
"Construcción de ácido nucleico" o "construcción" se refiere a un polinucleótido aislado que puede introducirse en una célula huésped. Esta construcción puede comprender cualquier combinación de desoxirribonucleótidos, ribonucleótidos, y/o nucleótidos modificados. Esta construcción puede comprender un casete de expresión que puede introducirse y expresarse en una célula huésped.
"Vinculado operativamente" se refiere a una disposición funcional de elementos. Una primera secuencia de ácido nucleico se une operativamente con una segunda secuencia de ácido nucleico cuando la primera secuencia de ácido nucleico se coloca en una relación funcional con la segunda secuencia de ácido nucleico. Por ejemplo, un promotor se une operativamente a una secuencia codificante si el promotor efectúa la transcripción o expresión de la secuencia codificante. Los elementos de control no necesitan ser contiguos a la secuencia codificante, siempre que funcionen para dirigir la expresión de la misma. Así, por ejemplo, las secuencias transcritas aún no traducidas que intervienen pueden estar presentes entre un promotor y la secuencia codificante y el promotor todavía puede considerarse "unido operativamente" a la secuencia codificante.
Los términos "planta" o "plantas" que pueden usarse en los presentes procedimientos incluyen ampliamente las clases de plantas superiores e inferiores susceptibles de técnicas de transformación, incluidas las angiospermas (plantas monocotiledóneas y dicotiledóneas), gimnospermas, helechos, etc. El término "planta" incluye, además, plantas que se modificaron por reproducción, mutagénesis, o ingeniería genética (plantas transgénicas y no transgénicas). Este incluye plantas de una variedad de niveles de ploidía, que incluyen aneuploide, poliploide, diploide, haploide, y hemicigoto. La planta puede estar en cualquier forma, incluidos cultivos en suspensión, embriones, regiones meristemáticas, tejido calloso, gametofitos, esporofitos, polen, microsporas, plantas enteras, estructuras/órganos vegetativos de brotes (por ejemplo, hojas, tallos y tubérculos), raíces, flores y estructuras/órganos florales, semillas (que incluyen embriones, endospermo y revestimiento de semillas) y frutos, tejidos vegetales (por ejemplo, tejidos vasculares, tejidos del suelo, y lo similar) y células, y la progenie de los mismos.
Las realizaciones de la presente divulgación incluyen, además, partes de plantas, que pueden seleccionarse entre un protoplasto, una célula, un tejido, un órgano, un corte, un explante, un tejido reproductivo, un tejido vegetativo, biomasa, una inflorescencia, una flor, un sépalo, un pétalo, un pistilo, un estigma, un estilo, un ovario, un óvulo, un embrión, un receptáculo, una semilla, una fruta, un estambre, un filamento, una antera, un gametofito masculino o femenino, un grano de polen, un meristemo, una yema terminal, una yema axilar, una hoja, un tallo, una raíz, una raíz tuberosa, un rizoma, un tubérculo, un estolón, un cormo, un bulbo, un brote lateral, una célula de dicha planta en cultivo, un tejido de dicha planta en cultivo, un órgano de dicha planta en cultivo, un callo, materiales de propagación, germoplasma, esquejes, divisiones, y propagaciones.
Otras realizaciones incluyen la progenie o derivados de plantas transgénicas divulgadas en la presente memoria seleccionadas, por ejemplo, entre clones, híbridos, muestras, semillas, y material recolectado. La progenie puede producirse asexualmente o sexualmente por procedimientos bien conocidos en la técnica.
Plantas C3 útiles
Las plantas a las que pueden aplicarse ventajosamente los procedimientos divulgados en la presente memoria incluyen plantas C3, que incluyen plantas de "cultivo alimentario" y "semillas oleaginosas".
Plantas de cultivo alimentario
El término "planta de cultivo alimentario" se refiere a plantas que son directamente comestibles o que producen productos comestibles, y que se usan habitualmente para alimentar a los seres humanos, ya sea directa o indirectamente a través de animales. Los ejemplos no limitativos de tales plantas incluyen:
1. Cultivos de cereales: trigo, arroz, maíz (maíz), cebada, avena, sorgo, centeno, y mijo;
2. Cultivos proteicos: maní, garbanzos, lentejas, frijoles, soja, habas;
3. Raíces y tubérculos: papas, batatas, y yuca;
4. Cultivos oleaginosos: soja, maíz, canola, maní, palma, coco, cártamo, algodón, girasol, lino, oliva, y cártamo; 5. Cultivos de azúcar: caña de azúcar y remolacha azucarera;
6. Cultivos frutales: plátanos, naranjas, manzanas, peras, fruta del pan, piñas, y cerezas;
7. Cultivos de hortalizas y tubérculos: tomates, lechugas, zanahorias, melones, espárragos, etc.
8. Nueces: anacardos, maní, nueces, pistachos, almendras;
9. Forraje y césped;
10. Legumbres forrajeras: alfalfa, trébol;
11. Cultivos de fármacos: café, cacao, nuez de cola, amapola;
12. Cultivos de especias y saborizantes: vainilla, salvia, tomillo, anís, azafrán, mentol, menta, menta verde, cilantro. En ciertas realizaciones de la presente divulgación, las plantas de cultivos alimentarios son soja, canola, tomate, patata, yuca, trigo, arroz, avena, lechuga, brócoli, remolacha, remolacha azucarera, frijoles, guisantes, col rizada, fresa, y maní. "Plantas de semillas oleaginosas", "Plantas de cultivos oleaginosos", "Cultivos de biocombustibles", "Cultivos energéticos"
Los términos "planta oleaginosa" o "planta de cultivo oleaginoso", y lo similar, a los que también pueden aplicarse los presentes procedimientos y composiciones, se refieren a plantas que producen semillas o frutos con un contenido de aceite en el intervalo de aproximadamente 1 a 2 %, por ejemplo, trigo, hasta aproximadamente 20 %, por ejemplo, soja, hasta más del 40 %, por ejemplo, girasoles y colza (canola). Estos incluyen cultivos oleaginosos mayores y menores, así como especies de plantas silvestres que se usan, o se investigan y/o desarrollan, como fuentes de biocombustibles debido a su importante producción y acumulación de aceite.
Las plantas ejemplares de semillas oleaginosas o cultivos oleaginosos útiles para practicar los procedimientos divulgados en la presente memoria incluyen, pero no se limitan a, plantas del género Brassica (por ejemplo, colza/canola (Brassica napus; Brassica carinata; Brassica nigra; Brassica oleracea), Camelina, Miscanthus, y Jatropha; Jojoba (Simmondsia chinensis), coco; algodón; maní; arroz; cártamo; sésamo; soja; mostaza; trigo; lino (linaza); girasol; aceituna; maíz; palma; almendra de palma; caña de azúcar; ricino; hierba de ricino; Borago officinalis; Echium plantagineum; Cuphea hookeriana; Cuphea pulcherrima; Cuphea lanceolata; Ricinus communis; Coriandrum sativum; Crepis alpina; Vernonia galamensis; Momordica charantia; y Crambe abyssinica.
Un ejemplo no limitativo de un tubérculo que acumula cantidades significativas de lípidos de reserva es el tubérculo de Cyperus esculentus (chufa o nueces del tigre), que se propuso como un cultivo oleaginoso para la producción de biocombustibles. En el caso de la chufa, el uso de un promotor constitutivo o específico del tubérculo sería útil en los procedimientos divulgados en la presente memoria.
Las plantas ejemplares de cultivos alimentarios incluyen trigo, arroz, maíz (maíz), cebada, avena, sorgo, centeno, y mijo; maní, garbanzos, lentejas, frijoles, soya, habas; papas, batatas y yuca; soja, maíz, canola, maní, palma, coco, cártamo, algodón, girasol, lino, oliva y cártamo; caña de azúcar y remolacha azucarera; plátanos, naranjas, manzanas, peras,
fruta del pan, piñas, y cerezas; tomates, lechugas, zanahorias, melones, fresas, espárragos, brócoli, guisantes, col rizada, anacardos, maní, nueces, pistachos, almendras; forraje y césped; alfalfa, trébol; café, cacao, nuez de cola, amapola; vainilla, salvia, tomillo, anís, azafrán, mentol, menta, hierbabuena y cilantro y, preferentemente, trigo, arroz y canola.
Los términos "péptido", "polipéptido", y "proteína" se usan para referirse a polímeros de residuos de aminoácidos. Estos términos se pretende específicamente que cubran biomoléculas de origen natural, así como aquellas que se producen de forma recombinante o sintética, por ejemplo, mediante síntesis en fase sólida.
El término "promotor" o "elemento regulador" se refiere a una región o secuencia de ácido nucleico ubicada corriente arriba o corriente abajo del inicio de la transcripción e implicada en el reconocimiento y unión de la ARN polimerasa y/u otras proteínas para iniciar la transcripción del ARN. Los promotores no necesitan ser de origen vegetal. Por ejemplo, los promotores derivados de virus vegetales, tales como el promotor CaMV35S, o de otros organismos, pueden usarse en variaciones de las realizaciones discutidas en la presente memoria. Los promotores útiles en los presentes procedimientos incluyen, por ejemplo, promotores constitutivos, fuertes, débiles, específicos de tejido, específicos de tipo celular, específicos de semilla, inducibles, reprimibles, y regulados por el desarrollo.
Una persona experta apreciará que una secuencia promotora puede modificarse para proporcionar un intervalo de niveles de expresión de una molécula de ácido nucleico heterólogo unida operativamente. Puede utilizarse menos que la región promotora completa y puede retenerse la capacidad de conducir la expresión. Sin embargo, se reconoce que los niveles de expresión de ARNm pueden disminuirse con deleciones de porciones de la secuencia promotora. Así, el promotor puede modificarse para ser un promotor débil o fuerte. Un promotor se clasifica como fuerte o débil de acuerdo con su afinidad por la ARN polimerasa (y/o el factor sigma); esto se relaciona con qué tan cercana la secuencia promotora se parece a la secuencia de consenso ideal para la polimerasa. Generalmente, por "promotor débil" se entiende un promotor que impulsa la expresión de una secuencia codificante a un nivel bajo. Por "nivel bajo" se entiende niveles de aproximadamente 1/10.000 transcripciones a aproximadamente 1/100.000 transcripciones a aproximadamente 1/500.000 transcripciones. Por el contrario, un promotor fuerte impulsa la expresión de una secuencia codificante a un nivel alto, o de aproximadamente 1/10 transcripciones a aproximadamente 1/100 transcripciones a aproximadamente 1/1.000 transcripciones. El promotor de elección se elimina, preferentemente, de su fuente mediante enzimas de restricción, pero alternativamente puede amplificarse por PCR mediante el uso de cebadores que llevan sitios de restricción terminales apropiados. Debe entenderse que los grupos de promotores anteriores no son limitativos, y que un experto en la técnica podría emplear otros promotores que no se mencionan explícitamente en la presente memoria.
El término "purificado" se refiere a material como un ácido nucleico, una proteína, o una molécula pequeña, que está sustancialmente o esencialmente libre de componentes que normalmente acompañan o interactúan con el material como se encuentra en su entorno natural, y/o que opcionalmente puede comprender material no encontrado dentro del entorno natural del material purificado. Esto último puede ocurrir cuando el material de interés se expresa o sintetiza en un entorno no nativo. Los ácidos nucleicos y las proteínas que se aislaron incluyen ácidos nucleicos y proteínas purificadas por procedimientos de purificación estándar. El término abarca, además, ácidos nucleicos y proteínas preparados por expresión recombinante en una célula huésped, así como ácidos nucleicos sintetizados químicamente. "Recombinante" se refiere a una secuencia de nucleótidos, péptido, polipéptido, o proteína, cuya expresión se modifica o manipula genéticamente mediante el uso de la metodología recombinante estándar. Este término se aplica tanto a los procedimientos como a los productos resultantes. Como se usa en la presente memoria, una "construcción recombinante", "construcción de expresión", "construcción quimérica", "construcción" y "casete de expresión recombinante" se usan indistintamente en la presente memoria.
Como se usa en la presente memoria, la frase "identidad de secuencia" o "similitud de secuencia" es la similitud entre dos (o más) secuencias de ácido nucleico, o dos (o más) secuencias de aminoácidos. La identidad de secuencia se mide con frecuencia como el porcentaje de residuos idénticos de nucleótidos o aminoácidos en las posiciones correspondientes en dos o más secuencias cuando las secuencias se alinean para maximizar la coincidencia de secuencias, es decir, se tienen en cuenta los espacios e inserciones.
Un experto en la técnica apreciará que los intervalos de identidad de secuencia se proporcionan solo a modo de guía. Sin embargo, es completamente posible que las secuencias de ácido nucleico que no muestran un alto grado de identidad de secuencia puedan codificar secuencias de aminoácidos que tienen una actividad funcional similar. Se entiende que pueden hacerse cambios en la secuencia de ácido nucleico mediante el uso de la degeneración del código genético para producir múltiples moléculas de ácido nucleico que codifican sustancialmente la misma proteína. Instrumentos para hacer este ajuste son bien conocidos por los expertos en la técnica. Cuando se usa el porcentaje de identidad de secuencia en referencia a secuencias de aminoácidos, se reconoce que las posiciones de los residuos que no son idénticas a menudo difieren por sustituciones conservadoras de aminoácidos, donde los residuos de aminoácidos se sustituyen por otros residuos de aminoácidos con propiedades químicas similares (por ejemplo, carga o hidrofobicidad) y por lo tanto no cambian las propiedades funcionales de la molécula. Cuando las secuencias difieren en las sustituciones conservadoras, el porcentaje de identidad de secuencia se puede ajustar hacia arriba para corregir la naturaleza conservadora de la sustitución. Las secuencias que difieren en tales sustituciones conservadoras se dice que
tienen "similitud de secuencia" o "similitud". Instrumentos para hacer este ajuste son bien conocidos por los expertos en la técnica. Típicamente esto implica calificar una sustitución conservativa como una parcial en lugar de una no coincidencia total, de ese modo aumenta el porcentaje de identidad de secuencia.
El “porcentaje de identidad de secuencia” se determina por la comparación de dos secuencias óptimamente alineadas sobre una ventana de comparación, en la que la porción de la secuencia de polinucleótidos en la ventana de comparación puede comprender adiciones o deleciones (es decir, interrupciones) en comparación con la secuencia de referencia (que no comprende adiciones o deleciones) para la alineación óptima de las dos secuencias. El porcentaje se calcula determinando el número de posiciones en las que la base de ácido nucleico o el residuo de aminoácido idéntico ocurre en ambas secuencias para producir el número de posiciones coincidentes, dividiendo el número de posiciones coincidentes por el número total de posiciones en la ventana de comparación y multiplicando el resultado por 100 para obtener el porcentaje de identidad de secuencia.
La identidad o similitud de secuencia pueden calcularse fácilmente mediante los procedimientos conocidos, que incluyen pero no se limitan a los descritos en: Computational Molecular Biology, Lesk, A. M., ed., Oxford University Press, New York, 1988; Biocomputing: Informatics and Genome Projects, Smith, D. W., ed., Academic Press, New York, 1993; Computer Analysis of Sequence Data, Part I, Griffin, A. M., y Griffin, H. G., eds., Humana Press, New Jersey, 1994; Sequence Analysis in Molecular Biology, von Heinje, G., Academic Press, 1987; y Sequence Analysis Primer, Gribskov, M. y Devereux, J., eds., M Stockton Press, New York, 1991; y Carillo, H., y Lipman, D., SIAM J. Applied Math., 48: 1073 (1988). Los procedimientos para determinar la identidad se diseñan para dar la mayor coincidencia entre las secuencias probadas. Además, los métodos para determinar la identidad se codifican en programas informáticos disponibles al público. La alineación óptima de secuencias para la comparación puede realizarse, por ejemplo, mediante el algoritmo de homología local de Smith y Waterman, mediante los algoritmos de alineación de homología, mediante la búsqueda del procedimiento de similitud o mediante implementaciones computarizadas de estos algoritmos (GAP, BESTFIT, PASTA, y TFASTA en el Paquete GCG Wisconsin, disponible de Accelrys, Inc., San Diego, California, Estados Unidos de América), o mediante inspección visual. Véase en general, (Altschul, SF y otros, J. Mol. Biol. 215: 403-410 (1990) y Altschul y otros Nucl. Acids Res. 25: 3389-3402 (1997)).
Un ejemplo de un algoritmo que es adecuado para determinar el porcentaje de identidad de secuencia y la similitud de secuencia es el algoritmo BLAST, que se describe en (Altschul, S., y otros, NCBI NLM NIH Bethesda, Md. 20894; Y Altschul, S., y otros, J. Mol. Biol. 215: 403-410 (1990). El software para realizar el análisis de BLAST está públicamente disponible a través del Centro Nacional de Información de Biotecnología. Este algoritmo implica primero identificar los pares de secuencia con puntuación alta (HSP) mediante la identificación de palabras cortas de longitud W en la secuencia de consulta, que coincide o satisface algunas puntuaciones T umbrales de valor positivo cuando se alinean con una palabra de la misma longitud en una secuencia de la base de datos. T se refiere como el umbral de puntuación de la palabra vecina. Estos aciertos de palabras vecinas iniciales actúan como semillas para iniciar las búsquedas para encontrar HSP más largos que los contengan. Las coincidencias de palabras se extienden entonces en ambas direcciones a lo largo de cada secuencia, hasta alcanzar un punto en el cual la puntuación de alineamiento acumulado no aumente más. Los registros acumulativos se calculan por medio del uso de, para secuencias de nucleótidos, los parámetros M (puntuación de recompensa para un par de residuos coincidentes; siempre > 0) y N (puntuación de penalización para residuos no coincidentes; siempre < 0). Para las secuencias de aminoácidos, se usa una matriz de puntuación para calcular el registro acumulativo. Las extensiones de los aciertos de palabras en cada dirección se detienen cuando: la puntuación de alineamiento acumulativa disminuye en una cantidad X desde su máximo valor alcanzado; la puntuación acumulativa va a cero o por debajo de cero debido a la acumulación de uno o más alineamientos de residuos con puntuación negativa; o se alcanza el extremo de cualquiera de las secuencias. Los parámetros W, T y X del algoritmo BLAST determinan la sensibilidad y la velocidad del alineamiento. El programa BLASTN (para las secuencias de nucleótidos) usa por defecto una longitud de palabra (W) de 11, una expectativa (E) de 10, un valor de corte de 100, M = 5, N = -4, y una comparación de ambas cadenas. Para las secuencias de aminoácidos, el programa BLASTP usa por defecto una longitud de palabra (W) de 3, una expectativa (E) de 10, y la matriz de puntuación BLOSUM62 (véase Henikoff & Henikoff(1989) Proc. Natl. Acad. Sci. USA 89:10915).
En adición a calcular el porcentaje de identidad de secuencia, el algoritmo BLAST realiza, además, un análisis estadístico de la similitud entre dos secuencias (véase, por ejemplo, Karlin y Altschul, Proc. Nat'l. Acad. Sci. USA 90: 5873-5877 (1993)). Una medida de similitud proporcionada por el algoritmo BLAST es la probabilidad de suma más pequeña (P (N)), que proporciona una indicación de la probabilidad a la cual se producirá una coincidencia entre dos secuencias de nucleótidos o aminoácidos al azar. Las búsquedas por BLAST asumen que las proteínas pueden modelarse como secuencias aleatorias. Sin embargo, muchas proteínas reales comprenden regiones de secuencias no aleatorias que pueden ser tractos homopoliméricos, repeticiones de período corto, o regiones enriquecidas en uno o más aminoácidos. Tales regiones de baja complejidad pueden estar alineadas entre proteínas no relacionadas a pesar de que otras regiones de la proteína sean completamente diferentes. Un número de programas de filtro de baja complejidad se pueden emplear para reducir tales alineaciones de baja complejidad. Por ejemplo, pueden emplearse los filtros de baja complejidad SEG (Wooten y Federhen, Comput. Chern., 17: 149-163 (1993)) y Xn U (Claverie y Estados, Comput. Chern., 17: 191-201 (1993)) solos o en combinación.
Las construcciones y procedimientos divulgados en la presente memoria abarcan secuencias de ácido nucleico y proteínas que tienen identidad de secuencia/similitud de secuencia de al menos aproximadamente 75 %, 80 %, 85 %,
90 %, 91 %, 92 %, 93 %, 94 %, 95 %, 96 %, 97 %, 98 %, 99 %, 100 % respecto a aquellos específicamente y/o secuencias que tienen la misma o similar función, por ejemplo, si una proteína o ácido nucleico se identifica con un péptido de tránsito y el péptido de tránsito se escinde y deja la secuencia de proteína sin el péptido de tránsito entonces la identidad de secuencia/similitud de secuencia se compara con la proteína con y/o sin el péptido de tránsito.
Un organismo "transgénico", tal como una planta transgénica, es un organismo huésped que se modificó genéticamente de manera estable o transitoria para contener uno o más fragmentos de ácido nucleico heterólogo, incluidas secuencias de codificación de nucleótidos, casetes de expresión, vectores, etc. La introducción de ácidos nucleicos heterólogos en una célula huésped para crear una célula transgénica no está limitada a ningún modo particular de administración e incluye, por ejemplo, microinyección, inmersión floral, adsorción, electroporación, infiltración al vacío, bombardeo con pistola de partículas, transformación mediada por bigotes, administración mediada por liposomas, transferencia mediada por Agrobacterium, el uso de vectores virales y retrovirales, etc., como es bien conocido por los expertos en la técnica. Las técnicas convencionales de biología molecular, tecnología de ADN recombinante, microbiología y química útiles en la práctica de los procedimientos de la presente divulgación se describen, por ejemplo, en Green y Sambrook (2012) Molecular Cloning: A Laboratory Manual, Fourth Edition, Cold Spring Harbor Laboratory Press; Ausubel y otros (2003 y suplementos periódicos) Current Protocols in Molecular Biology, John Wiley & Sons, New York, N.Y.; Amberg y otros (2005) Methods in Yeast Genetics: A Cold Spring Harbor Laboratory Course Manual, edición 2005, Cold Spring Harbor Laboratory Press; Roe y otros (1996) DNA Isolation and Sequencing: Essential Techniques, John Wiley & Sons; J. M. Polak y James O'D. McGee (1990) In Situ Hybridization: Principles and Practice; Oxford University Press; M. J. Gait (Editor) (1984) Oligonucleotide Synthesis: A Practical Approach, IRL Press; D. M. J. Lilley y J. E. Dahlberg (1992) Methods in Enzymology: DNA Structure Part A: Synthesis and Physical Analysis of DNA, Academic Press; y Lab Ref: A Handbook of Recipes, Reagents, and Other Reference Tools for Use at the Bench, editado por Jane Roskams y Linda Rodgers (2002) Cold Spring Harbor Laboratory Press; Burgess y Deutscher (2009) Guide to Protein Purification, segunda edición (Methods in Enzymology, vol. 463), Academic Press. Note, además, las Patentes de Estados Unidos núm. 8,178,339; 8,119,365; 8,043,842; 8,039,243; 7,303,906; 6,989,265; US20120219994A1; y EP1483367B1. El contenido completo de cada uno de estos textos y documentos de patente es incorporado por referencia en la presente memoria.
Resultados preliminares: Plantas transgénicas que expresan genes de CCM de algas
Previamente, se propuso la reconstitución de un CCM inorgánico funcional en plantas C3 para suprimir la fotorrespiración y mejorar la fotosíntesis. En el documento núm. WO 2012/125737, se planteó la hipótesis de que la expresión de un mínimo de tres proteínas de CCM de algas sería suficiente para elevar las concentraciones de CO2 interno de los plástidios lo suficientemente altas como para suprimir la fotorrespiración. Estos tres genes de CCM de algas incluyeron el transportador de bicarbonato dependiente de ATP localizado en la membrana de Chlamydomonas, HLA3; el transportador de aniones bicarbonato localizado en la envoltura del cloroplasto, LCIA; y una anhidrasa carbónica localizada en el estroma del cloroplasto (HCA-II) para acelerar la conversión de bicarbonato en CO2. Se demostró individualmente que estos genes son importantes para el CCM en estudios previos ([3-5]). Para probar esta hipótesis, generamos múltiples plantas de Arabidopsis y Camelina transgénicas independientes que expresan cada gen de CCM como una construcción de un solo gen, así como una construcción de 3 genes apilados. La expresión de cada gen se controló por el promotor del gen Cab1 regulado por la luz [6].
Los resultados de los análisis fenotípicos de las plantas de Arabidopsis y Camelina transformadas con las construcciones del gen de CCM único fueron los siguientes:
Los transgénicos de Arabidopsis HLA3 variaron en sus fenotipos, pero generalmente tuvieron fenotipos de crecimiento reducidos en relación con las plantas de tipo silvestre (WT) (Figura 6). Cuando se usó el mismo plásmido para transformar Camelina, no se recuperaron semillas viables de ningún evento de transformación después de múltiples intentos, lo que indica que la expresión de HLA3 probablemente fue tóxica para Camelina.
Con respecto a los transgénicos de anhidrasa carbónica (CA), expresamos una anhidrasa carbónica humana-2 (HCA2 (SEQ ID NO:17)) o una anhidrasa carbónica bacteriana de Neisseria gonorrhoeae (BCA SEQ ID NO4)) en el estroma del cloroplasto [7]. Elegimos estas CA porque cada una tiene un número de rotación (Kcat = 106 seg-1) que es aproximadamente 10 veces más rápido que las CA de plantas/algas. Tanto en Arabidopsis como en Camelina, observamos fenotipos que eran similares a WT (HCA2) o sustancialmente mayores ( BCA) que las plantas WT (Figura 3B).
Las plantas transgénicas de Arabidopsis que expresan el gen LCIA sufrieron un deterioro sustancial en el crecimiento (Figura 5A). En contraste, los transgénicos de LCIA de Camelina crecieron mejor que WT, tuvieron tasas fotosintéticas hasta un 25 % más altas a concentraciones de CO2 ambientes, y redujo los puntos de compensación de CO2 (Figura 5B).
El hecho de que la expresión de genes de CCM individuales perjudicara el crecimiento en plantas C3 sugirió que es posible que se deban expresar o silenciar rasgos adicionales para lograr un rendimiento fotosintético óptimo.
Para determinar si podríamos reconstituir un complejo de CCM completamente funcional en plantas C3, transformamos Arabidopsis y Camelina con una construcción de c Cm de tres genes en la que la expresión de los genes HLA3, CA, y LCIA se condujo por el promotor Cab1 específico de tejido verde. Tanto en Arabidopsis como en Camelina hubo un deterioro sustancial en el crecimiento o las plantas no sobrevivieron (resultados no mostrados).
Así, la coexpresión del gen HLA3 con cualquier otro gen de CCM perjudicó el crecimiento incluso en plantas en las que la expresión de los otros genes de CCM, por ejemplo, LCIA en Camelina, o BCA en Arabidopsis, aumentó el crecimiento. Estos resultados indicaron que la expresión de HLA3 era problemática.
Dado que la proteína HLA3 cataliza el transporte activo de bicarbonato y es la primera etapa dedicada en el CCM modificado genéticamente, volvimos a centrar nuestros esfuerzos en tratar de determinar por qué la expresión de HLA3 era tóxica para las plantas y cómo mitigar sus efectos. Consideramos dos posibles hipótesis para la toxicidad de HLA3: 1) la expresión del transportador ABC HLA3 aumenta la demanda de ATP (1 ATP/CO2) para la fotosíntesis en un 25 % y reduce los niveles de ATP citoplasmático [3-5,8] y 2) los niveles elevados de bicarbonato en las plantas transgénicas HLA3 impactan negativamente los niveles de pH citoplasmático. Con respecto a la última hipótesis, es notable que a diferencia de las cianobacterias, las plantas tienen una actividad de CA citoplasmática robusta, lo que mitiga los efectos de los niveles elevados de bicarbonato en el pH citoplasmático.
La función de la demanda de ATP y la actividad de transferencia de electrones cíclica en los CCM
En contraste con las algas cultivadas en aire (4 ATP/2 NADPH/CO2) y plantas C4 (5 ATP/2 NADPH/CO2) que tienen demandas de ATP para la fotosíntesis aumentadas, las plantas C3 (3 ATP/2 NADPH/CO2) tienen una capacidad limitada para generar ATP adicional por cada electrón transferido [8-10]. El aumento de la demanda de ATP en un 25 % por carbono fijado en plantas transgénicas HLA3, por lo tanto, podría agotar los niveles de ATP citoplasmático, así como alterar el estado redox de la célula [8,10]. Un mecanismo para aumentar la síntesis de ATP para cada electrón transferido por la luz es la actividad de transferencia de electrones cíclica (CET). La CET impulsada por la luz es catalizada por la separación de carga mediada por el fotosistema I (PSI) que conduce a la reducción de ferredoxina (fd) y la proteína PGR5. La proteína PGR5 reduce y protona la plastoquinona (PQ). PQH2 se oxida después por el complejo citocromo b6f (Cyt b6f). Los protones liberados por la oxidación de PQH2 conducen la síntesis de a Tp . El ciclo de transferencia de electrones se completa con la reducción de plastocianina (PC) por Cyt b6f, que a su vez es oxidada por el donante primario de PSI P700+. Significativamente, los estudios moleculares demostraron que los genes que codifican proteínas funcionales en CET se sobreexpresan sustancialmente (4-10X) en plantas C4 y algas cultivadas en el aire en relación con especies C3 o algas cultivadas en alto contenido de CO2 relacionadas [9,11-17]. Estos genes de CET incluyen: los genes de regulación de gradiente de protones PGR5 y PGRL1, y ciertos miembros de las familias de genes Fd y ferredoxina NADP reductasa (FNR) [8-15]: Núm. de acceso: PGR5: NM_126585; PGRL1: NM_179091; Fd: AtFd1: At1g10960; AtFd2: At1g60950; FNR: LFNR1: At5g66190; LFRN2: At1g20020) [15]. La secuencia para la proteína PRG5 con la secuencia de aminoácidos del péptido de tránsito subrayada se proporciona como MAAASISAIG CNQTLIGTSF YGGWGSSISG EDYQTMLSKT VAPPQQARVS RKAIRAVPMMKNVNEGKGLF APLVVVTRNL VGKKRFNQLR GKAIALHSQV ITEFCKSIGA DAKQRQGLIRAKKNGERLG FL (SEQ ID NO:1). El péptido de tránsito se escinde para producir la proteína PGR5 funcional.
Para probar la hipótesis de que el agotamiento de ATP en los transgénicos de HLA3 resultó en un deterioro del crecimiento, comparamos los fenotipos de WT y de los transgénicos de HLA3 cultivados en nitrato que requerirían un transporte de electrones más lineal (LET) para facilitar la reducción del nitrato. Significativamente, el ATP adicional producido por LET no se requiere para la conversión de nitrato en amonio y por lo tanto se espera que aumenten los niveles totales de ATP. En contraste, las plantas cultivadas con amonio no requieren LET adicional. Finalmente, también cultivamos transgénicos en amonio con sacarosa que presumiblemente proporcionaría ATP adicional a través de la respiración [15,17]. Presumimos que el crecimiento en nitrato o amonio con sacarosa proporcionaría ATP adicional que potencialmente podría impulsar la actividad de HLA3.
Como se muestra en la Figura 2B, ninguno de los transgénicos de Arabidopsis de HLA3 (4 líneas independientes) creció en presencia de amonio, pero todas las líneas HLA3 se rescataron cuando se cultivaron en amonio con sacarosa. Además, las plantas cultivadas con amonio más sacarosa fueron fenotípicamente similares a WT (Figura 2B). En contraste, todas las plantas HLA3 cultivadas con nitrato sobrevivieron, pero algunas líneas (# 9, # 20) tenían fenotipos de crecimiento sustancialmente deteriorados. Se observaron resultados idénticos para la germinación y el crecimiento de semillas WT y transgénicas de HLA3 en placas de agar con medios MS mediante el uso de nitrato (sobrevivieron los transgénicos de HLA3) o amonio (murieron los transgénicos de HLA3) como la única fuente de nitrógeno (resultados no mostrados). En base a estas observaciones, proponemos que el aumento de la síntesis de ATP asociado con el metabolismo de LET y/o sacarosa impulsado por nitrato reduce el agotamiento de los niveles de ATP citoplasmático en los transgénicos de HLA3 y los rescata.
Esta interpretación se corroboró por análisis comparativos de metabolitos del estado de carga de energía de la hoja (EC) (ATP), niveles de fosfato inorgánico, y potencial reductor de la hoja (RP) de Arabidopsis WT y transgénica de HLA3 cultivada en nitrato. Como se muestra en la Figura 6, los transgénicos de HLA3 cultivados en nitrato tenían relaciones reducidas de CE y RP en relación con WT. La carga de energía se define como
([ATP]+1/2[ADP])/([ATP]+[ADP]+[AMP]). El potencial de reducción es una medida de la capacidad del sistema para ganar o perder electrones.
Significativamente, los niveles de fosfato inorgánico fueron dos veces mayores en la línea HLA3 # 20, mientras que el nivel de NADH fue dos veces menor que en WT.
Estos resultados son consistentes con la hipótesis de que la expresión de HLA3 aumenta la demanda de ATP en las plantas. Este aumento de la demanda de a Tp en los transgénicos de HLA3 puede satisfacerse en parte a través de la oxidación de NAD(P)H a través de la derivación redox de malato/oxaloacetato entre las mitocondrias y los cloroplastos [16].
El fenotipo LCIA depende de las especies de plantas
Como se indicó anteriormente, la expresión de LCIA en Arabidopsis transgénica dio como resultado plantas con fenotipos de crecimiento severamente deprimidos (Figura 5A). Por el contrario, la Camelina transgénica que expresa LCIA tuvo tasas de crecimiento aumentadas así como tasas fotosintéticas dependientes de CO2 mayores en relación con WT (Figura 5B). Proponemos que la fuerza del sumidero de carbono sustancialmente mayor de Camelina en relación con Arabidopsis explica el fenotipo de crecimiento mejorado observado en plantas LCIA de Camelina. En apoyo de esta hipótesis, observamos que los transgénicos de LCIA de Camelina tenían mayores tasas de fotosíntesis dependientes de CO2 y puntos de compensación de CO2 más bajos (40 vs. 53 ppm de CO2) que las plantas WT indicativo de la absorción de carbono inorgánico facilitado por LCIA (Figura 5C).
Descripción general: Mejora de la fijación de carbono fotosintético al aumentar la producción de ATP y limitar la difusión de CO2 fuera de líneas artificiales de CCM; Estrategias para facilitar la síntesis de ATP y CET en plantas C3
Los intentos anteriores para subvertir las limitaciones de la fotosíntesis se centraron en la modificación genética del rendimiento y la especificidad de RuBisCO [35] mediante la introducción de formas modificadas genéticamente y no nativas de la enzima [36], a través de alteraciones en la capacidad regenerativa del ciclo de Calvin [37,38] o mediante la modificación genética de derivaciones fotorrespiratorias [39]. Estos estudios produjeron resultados mixtos, lo que aboga así por un enfoque más integral a nivel de sistemas para mejorar y/o redirigir el flujo de carbono fotosintético.
Como lo demuestra nuestro trabajo previo descrito anteriormente, postulamos que tanto las etapas de asimilación de carbono como la generación basada en luz de ATP y NAPDH deben considerarse para desarrollar un CCM competente con una capacidad fotosintética significativamente mejorada. Para demostrar la prueba de concepto, se generará una línea de Arabidopsis que contiene un CCM funcional que incluye mecanismos para ajustar los niveles de ATP para satisfacer la demanda del transportador.
Mejora de la síntesis de ATP y CET para soportar la absorción de bicarbonato dependiente de HLA3
Para explotar la expresión de un CCM de algas en plantas C3 se requiere que cumplamos con las demandas de energía adicionales requeridas para transportar activamente carbono inorgánico. Como se discutió anteriormente en la sección titulada "La función de la demanda de ATP y la actividad de transferencia de electrones cíclica en CCM", las algas y plantas C4 tienen una actividad de CET robusta y sobreexpresan una variedad de genes implicados en CET [13,16,40 45] en comparación a plantas C3.
Se identifican varias estrategias en los siguientes ejemplos, para aumentar la síntesis de ATP para soportar el transporte de bicarbonato dependiente de HLA3. Varias de estas estrategias se centran en elevar la actividad de CET en plantas C3. Otro enfoque implica la expresión de una bomba de protones bacteriana impulsada por fotones verde en los tilacoides para complementar la síntesis de ATP impulsada por protones. Cada enfoque se diseña para complementar las líneas CCM existentes en Arabidopsis, Camelina, y papa que creamos, y se evalúan en función de los niveles medidos de adenilato, la producción de biomasa vegetal, y las mediciones fotosintéticas de asimilación de carbono. Los materiales y procedimientos empleados en los ejemplos a continuación son solo para fines ilustrativos y no pretenden limitar la práctica de las presentes realizaciones a los mismos. Cualquier material y procedimiento similar o equivalente a los descritos en la presente memoria, como sería evidente para un experto en la técnica, puede usarse en la prueba o práctica de las realizaciones presentes, es decir, los materiales, procedimientos y ejemplos son solo ilustrativos y no pretenden ser limitativos.
Ejemplo 1: Mejora de CET basada en la sobreexpresión de las proteínas reguladoras del gradiente de protones PGR5 y PGRL1 en plantas C3
La mejora de CET se basa en la sobreexpresión de las proteínas reguladoras del gradiente de protones PGR5 y/o PGRL1 que previamente se demostró que son importantes para CET [37].
Recientemente se demostró que la proteína PGRL1 tiene actividad ferredoxina-plastoquinona reductasa (FQR), sensible a la antimicina A (AA) [46]. En Chlamydomonas, PGRL1 es parte del supercomplejo Cytb6f/PSI que media CET. Significativamente, PGRL1 forma homodímeros así como heterodímeros con PGR5 a través de residuos de cisteína
activa redox. En condiciones de mucha luz, la tiorredoxina reduce los dímeros PGRL1 presentes en las pilas de grana, lo que aumenta la abundancia de monómeros PGRL1 y mejora CET [47]. Los estudios de mutaciones demostraron que la proteína PGR5 es necesaria para la oxidación de Fd y la reducción de PGRL1, pero no para la reducción de PQ. En adición, se demostró que los heterodímeros PGRL1/PGR5 son más activos en CET que los monómeros PGRL1. En las plantas C4 los niveles de expresión de PGR5 y PGRL1 son elevados (4X) en relación con las plantas C3 [9]. Similarmente, la expresión de PGR5 se regula positivamente en Chlamydomonas cultivadas en aire (actividad de HLA3 y CCM activa) en relación con células crecidas con CO2 alto (bajo CCM) [16,43]. Significativamente, la sobreexpresión de PGRL1 y PGR5 demostró, además, que aumenta CET sensible a AA en Arabidopsis transgénica [48]. Una realización de la presente invención proporciona una sobreexpresión del gen PGRL1 (SEQ ID NO:106) y el gen PGR5 con secuencia dirigida al cloroplasto (s Eq ID NO:2) con el gen de HLA3 (SEQ ID NO:12) o con el gen HLA3 (SEQ ID NO:12) y el gen LCIA (SEQ ID NO:16) y los codones del gen BCA optimizados para la expresión en Arabidopsis (SEQ ID NO:4) para producir tasas fotosintéticas sustancialmente aumentadas, particularmente en plantas con mayor potencia de sumidero (Camelina y papa, por ejemplo). La coexpresión del gen PGR5 (SEQ ID NO:2) junto con el gen HLA3 (SEQ ID NO:12) en Camelina rescató el gen HLA3 y ya no era letal. Estos resultados indican que el gen PGR5 permite la producción de suficiente ATP para satisfacer las demandas del producto del gen HLA3.
HLA3 (SEQ ID NO:12) y PGR5 (SEQ ID NO:2) se introducen como una construcción doble en Arabidopsis o Camelina, mediante transformación de plásmido Ti mediada por Agrobacterium mediante el uso de, por ejemplo, el plásmido pB110-HLA3-pgr5-dsred (Figura 9). Como la proteína PGR5 (SEQ ID NO:1) se dirige naturalmente a las membranas de los tilacoides, no se introducen secuencias de direccionamiento adicionales. Similarmente, dado que la proteína HLA3 (SEQ ID NO:77) se dirige naturalmente a la envoltura de cloroplasto, no se adicionan secuencias de direccionamiento adicionales. Se optimizan los codones de HLA3 para la expresión en plantas.
En una realización, la expresión de cada proteína se conduce por el promotor de CAB1 específico de hoja sensible a la luz (SEQ ID NO:7) y el terminador Nos (SEQ ID NO:9) (Figura 9).
El gen BCA (AAW89307; SEQ ID NO:4), bajo el control del promotor de CAB1, se introduce en Arabidopsis mediante la transformación del plásmido de Ti mediada por Agrobacterium mediante el procedimiento de inmersión floral mediante el uso de la construcción que se muestra en la Figura 10.
Como marcador visual, el plásmido incluye, además, un gen para la expresión de la proteína DsRed fluorescente bajo el control del promotor de CVMV y el terminador Nos (Figura 10).
Las plantas se transforman por el procedimiento de infiltración al vacío (Lu y Kang (febrero de 2008) Plant Cell Rep. 27 (2): 273-8), y se analizarán los parámetros de rendimiento de biomasa (incluido el peso de la planta, la altura, la ramificación y el rendimiento de semillas) y la eficiencia fotosintética medida como absorción de CO2 con la ayuda de un analizador de intercambio de gases LiCor 6400.
El gen PGRL1 de Arabidopsis (NM_179091 SEQ ID NO:3) se subclonará en un plásmido binario basado en pCambia1301 bajo el control del promotor de CAB1 (SEQ ID No :7) y el terminador Nos (SEQ ID NO:9). El plásmido portará, además, un gen para el marcador de selección de higromicina. La transformación mediada por Agrobacterium se lleva a cabo mediante el procedimiento estándar de inmersión floral seguido de la germinación de semillas en higromicina para seleccionar los transformantes. La expresión de PRGL1 se confirmará mediante RT-PCR, y las líneas de plantas transgénicas resultantes se cruzarán con plantas HLA3/PGR5 y se analizarán el rendimiento de biomasa y la tasa de fotosíntesis (fijación de CO2).
Ejemplo 2: Determinación de si la sobreexpresión del gen Fd1 puede soportar la CCM de algas y aumentar las tasas fotosintéticas
Recientemente se demostró que miembros específicos de la familia de genes de ferredoxina (Fd) facilitan la CET. La sobreexpresión de ferredoxina 1 de guisante (Fd1) mejoró la CET a expensas de la LET en el tabaco [16,40].
Por lo tanto, otra realización de la presente invención proporciona una mayor producción de ATP y titula la expresión del gen Fd1 de guisante en las tres plantas C3 modelo con y sin coexpresión de los genes de CCM para determinar si la sobreexpresión de Fd1 puede soportar los CCM de algas y el aumento de las tasas de fotosíntesis. Los resultados anteriores demostraron que la sobreexpresión de Fd1 deterioraba ligeramente la transferencia lineal de electrones (LET), lo que resulta en un fenotipo atrofiado [40]. Sin embargo, esperamos que la demanda adicional de ATP en los transgénicos de HLA3 mitigue estos efectos.
El gen Fd1 (At1g10960) se introducirá mediante la transformación del plásmido Ti mediado por Agrobacterium. El gen Fd1 se subclonará en plásmido binario basado en pCambia1301 bajo el control del promotor de CAB1 (SEQ ID NO:7) y el terminador Nos (SEQ ID NO:9). El plásmido portará, además, un gen para la selección de higromicina como marcador. La transformación mediada por Agrobacterium se lleva a cabo mediante el procedimiento de inmersión floral estándar, seguido de la germinación de semillas en higromicina para seleccionar los transformantes. La expresión de FD1 (SEQ ID NO:93) se confirmará mediante QPCR en tiempo real, y las líneas de plantas resultantes que exhiban
diferentes niveles de expresión de FD1 se cruzarán con plantas que expresan CCM y se analizará el rendimiento de biomasa y la tasa de fotosíntesis con la ayuda de un analizador de intercambio de gas CO2 LiCor 6400.
Ejemplo 3: Sobreexpresión de miembros de la familia de genes de ferredoxina NADP reductasa (FNR) únicos asociados con CET
Otra realización adicional se basa en la sobreexpresión de miembros de la familia de genes de ferredoxina NADP reductasa (FNR) únicos asociados con CET. FNR de hoja (LFNR) cataliza la reducción de Fd y está implicado tanto en LET como en CET [15]. Recientemente se demostró que hay tres miembros de la familia de genes LFNR expresados en hojas de maíz: Números de acceso BAA88236 (LFNR1), BAA88237 (LFNR2), y ACF85815 (LFNR3).
Se mostró que LFNR-1 se localiza en las membranas de los tilacoides y se asocia con los complejos Cytb6f. LFNR2 estaba presente en los tilacoides y el estroma asociados con los complejos Cytb6f. LFNR3 era soluble y no se asociaba con los complejos Cytb6f.
Significativamente, cuando las plantas se cultivaron con nitrato en lugar de amonio, la expresión de LFNR1 y LFNR2 fue elevada, pero no la de LFNR3. En contraste, los estudios que usan mutantes bloqueados de LFNR1 de Arabidopsis demostraron que la evolución de oxígeno dependiente de PGA (que requiere ATP adicional) se ve más negativamente afectada que la evolución de oxígeno dependiente de nitrato (sin demanda adicional de ATP), lo que sugiere que LFNR1 puede desempeñar una función en la regulación de CET [15]. Sin embargo, esta interpretación es equívoca.
Para determinar si la actividad de CET y la absorción de carbono inorgánico mediada por HLA3 pueden alterarse mediante la expresión diferencial de LFNR1, tanto sobreexpresaremos (promotor CAB1 (SEQ ID NO:7)) como subexpresamos (LFNR1 RNAi) LFNR1 en Arabidopsis transgénica para determinar el impacto de la expresión alterada de LFNR1 en la actividad funcional de CCM.
Para la sobreexpresión del LFNR1, el gen (At5g66190) se introducirá mediante la transformación del plásmido Ti mediado por Agrobacterium mediante inmersión floral. El gen LFNR1 se subclonará en un plásmido binario basado en pCambia1301 bajo el control del promotor de CAB1 (SEQ ID NO:7) y el terminador Nos (SEQ ID NO:9). El plásmido portará, además, un gen para la selección de higromicina como marcador. La expresión de LFNR1 se confirmará mediante QPCR en tiempo real, las líneas de plantas resultantes se cruzarán con plantas que expresan CCM, y se examinará el rendimiento de biomasa y la tasa de fotosíntesis con la ayuda de un analizador de intercambio de gas CO2 LiCor 6400.
Para la regulación negativa de los niveles de LFNR1, una construcción de RNAi que contiene una secuencia parcial de LFNR1 (At5g66190 o BAA88236) y una secuencia complementaria inversa de LFNR1 se subclonará en un plásmido binario basado en pCambia1301 bajo el control del promotor de CAB1 (SEC ID NO:7) y el terminador Nos (SEQ ID NO:9). El plásmido portará, además, un gen para la selección de higromicina como marcador. El nivel reducido de expresión de LFNR1 se confirmará por QPCR en tiempo real.
Las líneas resultantes se cruzarán con líneas que expresan CCM para generar mutantes dobles. Esos mutantes se examinarán para determinar los parámetros de rendimiento de biomasa (incluido el peso de la planta, la altura, la ramificación y el rendimiento de semillas) y la eficiencia fotosintética medida como absorción de CO2 con la ayuda de un analizador de intercambio de gases LiCor 6400.
Ejemplo 4: Transporte de protones vectorales facilitado mediante el uso de Proteorodopsina (PR)
En otra realización adicional, se emplearán fotones verdes, no absorbidos por la clorofila, para impulsar el transporte de protones a través de los tilacoides mediante la expresión de PR modificado [49]) para mejorar la síntesis de ATP (Figura 7).
PR es una proteína de siete hélices que se expande por la transmembrana similar a la bacteriorrodopsina que contiene retinal en su sitio activo. La isomerización cis-trans impulsada por la luz verde del retinal impulsa la transferencia de protones vectorales a través de la membrana [50-55]. Significativamente, se demostró que una PR funcional podría expresarse en un mutante de E. coli con insuficiencia respiratoria cuando se complementa con retinal totalmente trans exógeno [56]. Más recientemente, se demostró que la producción de hidrógeno aumenta casi dos veces en E. coli que expresa Pr cuando las células se exponen a intensidades de luz crecientes (70 a 130 j E), lo que indica que PR puede absorber la luz de manera eficiente incluso a bajas intensidades [57]. Hasta donde sabemos, no se informó de la complementación con retinal de otras rodopsinas. Significativamente, los mutantes respiratorios de E. coli que expresan PR generaron suficiente fuerza motriz de protones para soportar los niveles de síntesis de ATP, lo que condujo a una mayor viabilidad y movilidad celular cuando los transgénicos se expusieron a la luz solar como la única fuente de energía.
Estos resultados sugieren que dirigir PR a la membrana de los tilacoides mediante el uso de secuencias de direccionamiento apropiadas (por ejemplo, secuencias señal complejas de recolección de luz, N-terminal, con codificación nuclear) y la suplementación con retinal exógeno o retinal derivado de la escisión de p-caroteno) podría
conducir a una síntesis adicional de ATP. Una preocupación es que la sección transversal óptica del retinal es pequeña y la recolección de luz por PR no se complementa con complejos de antenas. Esta restricción puede superarse en parte mediante la sobreexpresión de PR en los tilacoides. En cualquier caso, el gradiente de protones adicional necesario para soportar la actividad de HLA3 es sustancialmente menor que el requerido para soportar la fijación de CO2 general. Los mejores niveles de expresión de PR alcanzables se determinarán empíricamente mediante el uso de diferentes promotores de genes, por ejemplo, psaD (SEQ ID NO:10), rbcs (SEQ ID nO:11) y cab1 (SEQ ID NO:7), para impulsar su expresión.
Generación de PR mejorada y su reconstitución funcional en cloroplastos
PR (AF279106), por ejemplo (SEQ ID NO:98), se introducirá en Arabidopsis, Camelina, y papa mediante la transformación del plásmido Ti y se dirigirá a la membrana de los tilacoides mediante el uso del péptido de tránsito de DNAJ (At5g21430, SEQ ID NO:22) o el dominio de transmembrana de parada de transferencia de psbX (At2g06520 SEQ ID NO:23) fusionado al extremo C de PR [58], o péptidos de tránsito de proteínas de cloroplasto codificadas nucleares como CAB (SEQ ID NO:13), PGR5 (s Eq ID NO:14) y psaD (SEQ ID No :15). La reconstitución con retinal exógeno se llevará a cabo de manera similar a las estrategias descritas para E. coli, excepto que el retinal se pintará en la superficie de la hoja [56] para demostrar la prueba de concepto. A la reconstitución con retinal le seguirá la supervisión de la absorción de las membranas de los tilacoides a 540 nm [59].
Si el retinal aplicado de manera exógena no se incorpora a PR, expresaremos bajos niveles de una p-caroteno monooxigenasa optimizada con codones de planta, por ejemplo (SEQ ID NO:100) en plástidos para escindir una pequeña fracción de p-caroteno para generar el retinal. Los ejemplos no limitativos de p-caroteno monooxigenasas que pueden usarse incluyen, por ejemplo, enzimas de ratón, humana, pez cebra y rata (Núm. De acceso AW044715, AK001592, AJ290390, y NM_053648, respectivamente). Alternativamente, si los niveles de p-caroteno se reducen severamente, expresaremos transitoriamente la p-caroteno monooxigenasa bajo el control de un promotor inducible transiente tal como un promotor de genes inducible por etanol. Este está disponible como un fragmento EcoRI/Pstl de Syngenta-Construct: pJL67- 5S::AlcR/AlcA::GUS en pMLBART (Weigel World, Max Planck Institute for Developmental Biology, Tubinga, Alemania) por períodos de tiempo suficientes para saturar completamente PR [60,61]. El funcionamiento de un fotociclo de retinal funcional en PR se confirmará mediante espectroscopía de absorción transiente [62]. Alternativamente, pueden usarse promotores tales como los promotores específicos de hoja/tejido verde tales como los promotores de CAB (At3g54890 SeQ ID NO:7) y rbcS (At5g38420 SEQ ID NO:11), por ejemplo, véase SEQ ID NO:5 para la proteína BCA con un péptido de tránsito de rbc-1a. Como bien sabrá la persona experta, pueden usarse varios promotores para promover la transcripción del ácido nucleico de la invención, es decir, el ácido nucleico que cuando se transcribe produce una molécula de ARN que modula la expresión y/o actividad de una proteína de acuerdo con la invención. Tales promotores incluyen, por ejemplo, promotores constitutivos, promotores inducibles (por ejemplo, promotores inducibles por la luz, promotores inducibles por estrés, promotores inducibles por sequía, promotores inducibles por hormonas, promotores inducibles por químicos, etc.), promotores específicos de tejido, promotores regulados por el desarrollo y lo similar.
Así, un promotor expresable de la planta puede ser un promotor constitutivo, es decir, un promotor capaz de dirigir altos niveles de expresión en la mayoría de los tipos de células (de manera independiente espacio-temporal). Los ejemplos de promotores constitutivos que pueden expresarse en plantas incluyen promotores de origen bacteriano, como los promotores de octopina sintasa (OCS) y nopalina sintasa (NOS) de Agrobacterium, pero también promotores de origen viral, tales como el del transcrito 35S del virus del mosaico de la coliflor (CaMV) (Hapster y otros, 1988, Mol. Gen. Genet. 212: 182-190) o genes de ARN 19S (Odell y otros, 1985, Nature. 6;313(60o5):8l0-2; Patente de Estados Unidos núm. 5,352,605; WO 84/02913; Benfey y otros, 1989, EMBO J. 8:2195-2202), el promotor 2x35S mejorado (Kay y otros, 1987, Science 236:1299-1302; Datla y otros (1993), Plant Sci 94:139-149) promotores del virus del mosaico de la vena de la yuca (CsVMV; WO 97/48819, US 7,053,205), 2xCsVMV (WO2004/053135) el promotor de circovirus (AU 689311), el promotor del badnavirus baciliforme de la caña de azúcar (ScBV) (Samac y otros, 2004, Transgenic Res. 13(4):349-61), el promotor del virus del mosaico de la escrofularia (FmV) (Sanger y otros, 1990, Plant Mol Biol. 14(3):433-43), el promotor del virus del trébol subterráneo núm. 4 o núm. 7 (WO 96/06932) y el promotor 35S mejorado como se describe en los documentos núm. US 5,164,316, US 5,196,525, US 5,322,938, US 5,359,142 y US 5,424,200. Entre los promotores de origen vegetal, se mencionarán los promotores del promotor del gen de la histona H4 de Arabidopsis thaliana (Chabouté y otros, 1987), los promotores de ubiquitina (Holtorf y otros, 1995, Plant Mol. Biol. 29:637-649, US 5.510.474) de maíz, arroz y caña de azúcar, el promotor de la actina 1 del arroz (Act-1, 5,641,876), los promotores de histonas como se describe en el documento núm. EP 0507698 A1, el promotor de la alcohol deshidrogenasa de maíz 1 (Adh-1) (de http://www.patentlens.net/daisy/promoters/242.html)).
Puede usarse una variedad de promotores de genes de plantas que regulan la expresión de genes en respuesta a señales ambientales, hormonales, químicas, de desarrollo y de manera activa en los tejidos para la expresión de una secuencia en plantas. La elección de un promotor se basa en gran medida en el fenotipo de interés y se determina por factores tales como el tejido (por ejemplo, semilla, fruto, raíz, polen, tejido vascular, flor, carpelo, etc.), inducibilidad (por ejemplo, en respuesta al calor, frío, sequía, luz, etc.), tiempo, etapa de desarrollo y lo similar.
Los promotores que pueden usarse para practicar esta invención incluyen aquellos que son específicos de tejido verde, como el promotor de la proteína 2 del complejo de recolección de luz (Sakamoto y otros Plant Cell Physiology, 1991,
32(3):385-393) o el promotor de la fructosa-1, 6-bisfosfatasa citosólica del arroz (Si y otros Acta Botánica Sínica 45: 3(2003): 359-364). Las realizaciones alternativas incluyen promotores inducibles por luz tales como promotores de la subunidad pequeña de la ribulosa-biscarboxilasa/oxigenasa (Rubisco) de la planta (documentos núm. US 4,962,028; WO99/25842) de zea mays y girasol. Puede usarse, además, el promotor de la subunidad pequeña del Crisantemo, combinado o no combinado con el uso del terminador respectivo (Outchkourov y otros, Planta, 216: 1003-1012, 2003).
Los promotores adicionales que pueden usarse para practicar esta invención son aquellos que provocan la expresión en respuesta al estrés, como los promotores RD29 que se activan en respuesta a la sequía, baja temperatura, estrés salino, o exposición a ABA (Yamaguchi-Shinozaki y otros, 2004, Plant Cell, vol. 6, 251-264; WO12/101118), pero también promotores inducidos en respuesta al calor (por ejemplo, véase Ainley y otros (1993) Planta Mol. Biol. 22: 13 23), luz (por ejemplo, el promotor de rbcS-3A de guisante, Kuhlemeier y otros (1989) Plant Cell 1: 471-478, y el promotor de rbcS de maíz, Schaffher y Sheen (1991) Plant Cell 3: 997-1012); heriente (por ejemplo, wunl, Siebertz y otros (1989) Plant Cell 1: 961-968); patógenos (tales como el promotor PR-I descrito en Buchel y otros (1999) Planta Mol. Biol. 40: 387-396, y el promotor de PDF 1.2 descrito en Manners y otros (1998) Planta Mol. Biol. 38: 1071-1080) y productos tales químicos como el metil jasmonato o el ácido salicílico (por ejemplo, véase Gatz (1997) Annu. Rev. Plant Physiol. Plant Mol. Biol. 48: 89-108). En adición, el momento de la expresión puede controlarse mediante el uso de promotores como los que actúan en la senescencia (por ejemplo, véase Gan y Amasino (1995) Science 270: 1986-1988); o desarrollo tardío de semillas (por ejemplo, véase Odell y otros (1994) Plant Physiol. 106: 447-458).
Puede hacerse uso, además, de promotores inducibles por sal, tales como el promotor de NHX1 inducible por sal de la variedad local de arroz Pokkali (PKN) (Jahan y otros, 6th International Rice Genetics symposium, 2009, resumen de póster P4-37), el promotor inducible por sal de la H+-pirofosfatasa vacuolar de Thellungiella halophila (TsVP1) (Sun y otros, BMC Plant Biology 2010, 10:90), el promotor inducible por sal del gen de Citrus sinensis que codifica la isoforma gpx1 de fosfolípido hidroperóxido (Avsian-Kretchmer y otros, Plant Physiology julio de 2004 vol. 135, p1685-1696).
En realizaciones en variante, se usan promotores específicos de tejido y/o etapa de desarrollo específica, por ejemplo, un promotor que puede promover la transcripción solo dentro de un cierto marco de tiempo de la etapa de desarrollo dentro de ese tejido. Véase, por ejemplo, Blazquez (1998) Plant Cell 10:791-800, que caracteriza el promotor del gen LEAFY de Arabidopsis. Véase, además, Cardon (1997) Plant J 12:367-77, que describe el factor de transcripción SPL3, que reconoce un motivo de secuencia conservada en la región promotora del gen de identidad de meristemo floral de A. thaliana API; y Mandel (1995) Plant Molecular Biology, vol. 29, págs. 995-1004, que describe el promotor de meristemos eIF4. Pueden usarse promotores específicos de tejido que están activos durante todo el ciclo de vida de un tejido particular. Otros promotores que pueden usarse para expresar los ácidos nucleicos de la invención incluyen,; un promotor específico de la hoja (véase, por ejemplo, Busk (1997) Plant J. 11:1285 1295, que describe un promotor específico de hoja en maíz); un promotor de tomate activo durante la maduración de la fruta, la senescencia y la abscisión de las hojas, un promotor preferencial de células protectoras, por ejemplo, como se describe en el documento núm. PCT/EP12/065608 y, en menor medida, pueden usarse de flores (véase, por ejemplo, Blume (1997) Plant J.
12:731 746); el gen Blec4 del guisante, que es activo en el tejido epidérmico de los ápices de los brotes vegetativos y florales de la alfalfa transgénica lo que lo convierte en un instrumento útil para dirigir la expresión de genes extraños a la capa epidérmica de brotes o fibras que crecen activamente; el gen BELI específico del óvulo (véase, por ejemplo, Reiser (1995) Cell 83: 735-742, GenBank núm. U39944); y/o, el promotor en Klee, Patente de Estados Unidos núm. 5,589,583, que describe una región promotora de planta es capaz de conferir altos niveles de transcripción en tejido meristemático y/o células que se dividen rápidamente. Otros promotores específicos de tejido que pueden usarse según la invención incluyen, promotores activos en tejido vascular (por ejemplo, véase Ringli y Keller (1998) Plant Mol. Biol. 37: 977-988), carpelos (por ejemplo, véase Ohl y otros (1990) Plant Cell 2. En realizaciones en variante, los promotores de plantas que son inducibles tras la exposición a hormonas de plantas, tales como las auxinas, se usan para expresar los ácidos nucleicos usados para practicar la invención. Por ejemplo, la invención puede usar el fragmento promotor El de elementos de respuesta a auxina (AuxRE) en la soja {Glycine max L.) (Liu (1997) Plant Physiol. 115: 397-407); el promotor de Arabidopsis GST6 sensible a auxina (también sensible al ácido salicílico y al peróxido de hidrógeno) (Chen (1996) Plant J. 10: 955-966); el promotor de parC inducible por auxina del tabaco (Sakai (1996) 37:906-913); un elemento de respuesta de biotina de planta (Streit (1997) Mol. Plant Microbe Interact. 10:933-937); y, el promotor sensible al ácido abscísico de la hormona del estrés (ABA) (Sheen (1996) Science 274:1900-1902). Otros promotores inducibles por hormonas que pueden usarse incluyen promotores inducibles por auxina (como el descrito en van der Kop y otros (1999) Planta Mol. Biol. 39: 979-990 o Baumann y otros, (1999) Plant Cell 11: 323-334), promotor inducible por citoquinina (por ejemplo, véase Guevara-García (1998) Planta Mol. Biol. 38: 743-753), promotores sensibles a la giberelina (por ejemplo, véase Shi y otros (1998) Planta Mol. Biol. 38: 1053-1060, Willmott y otros (1998) Plant Molec. Biol. 38: 817-825) y lo similar.
En realizaciones en variante, los ácidos nucleicos usados para practicar la invención pueden unirse operativamente, además, a promotores de plantas que son inducibles tras la exposición a reactivos químicos que pueden aplicarse a la planta, tales como herbicidas o antibióticos. Por ejemplo, puede usarse el promotor de maíz ln2-2, activado por protectores herbicidas de bencenosulfonamida (De Veylder (1997) Plant Cell Physiol. 38:568-577); la aplicación de diferentes protectores de herbicidas induce distintos patrones de expresión génica, incluida la expresión en la raíz, los hidatodos, y el meristemo apical del brote. La secuencia codificante puede estar bajo el control de, por ejemplo, un promotor inducible por tetraciclina, por ejemplo, como se describe con plantas de tabaco transgénicas que contienen el gen de la arginina descarboxilasa de Avena sativa L. (avena) (Masgrau (1997) Plant J. 11: 465-473); o un elemento
sensible al ácido salicílico (Stange (1997) Plant J. 11: 1315-1324). Mediante el uso de promotores inducidos químicamente (por ejemplo, por hormonas o pesticidas), es decir, promotor que responde a un químico que puede aplicarse a la planta transgénica en el campo, la expresión de un polipéptido de la invención puede inducirse en una etapa particular de desarrollo de la planta. Puede hacerse uso, además, del sistema de expresión inducible por estrógenos como se describe en la Patente de Estados Unidos núm. 6,784,340 y Zuo y otros (2000, Plant J. 24: 265 273) para impulsar la expresión de los ácidos nucleicos usados para practicar la invención.
En realizaciones en variante, puede usarse un promotor cuyo intervalo de huéspedes se limita a especies de plantas objetivo, tales como maíz, arroz, cebada, trigo, papa u otros cultivos, inducibles en cualquier etapa de desarrollo del cultivo.
En realizaciones en variante, un promotor de planta específico de tejido puede impulsar la expresión de secuencias unidas operativamente en tejidos distintos del tejido objetivo. En realizaciones en variante, se usa un promotor específico de tejido que impulsa la expresión, preferentemente, en el tipo de tejido o célula objetivo, pero que puede conducir, además, a cierta expresión en otros tejidos.
De acuerdo con la invención, puede hacerse uso, además, en combinación con el promotor, de otras secuencias reguladoras, que se encuentran entre el promotor y la secuencia codificante, tales como activadores de la transcripción ("potenciadores"), por ejemplo, el activador de la traducción del virus del mosaico del tabaco (TMV) descrito en la solicitud núm. WO 87/07644, o del virus del grabado del tabaco (TEV) descrito por Carrington y Freed 1990, J. Virol. 64: 1590-1597, por ejemplo.
Otras secuencias reguladoras que potencian la expresión del ácido nucleico de la invención también pueden ubicarse dentro del gen quimérico. Un ejemplo de tales secuencias reguladoras son los intrones. Los intrones son secuencias intermedias presentes en el pre ARNm pero ausentes en el ARN maduro después de la escisión por un mecanismo de corte y empalme preciso. La capacidad de los intrones naturales para mejorar la expresión génica, un proceso denominado mejora mediada por intrones (IME), se conoce en varios organismos, incluidos mamíferos, insectos, nematodos y plantas (documento núm. WO 07/098042, p11 -12). La IME generalmente se describe como un mecanismo postranscripcional que conduce a una mayor expresión génica por la estabilización de la transcripción. Se requiere que el intrón se coloque entre el promotor y la secuencia codificante en la orientación normal. Sin embargo, se describió, además, que algunos intrones afectan la traducción, funcionan como promotores o como potenciadores transcripcionales independientes de posición y orientación (Chaubet-Gigot y otros, 2001, Plant Mol Biol. 45(1):17-30, p27-28).
Los ejemplos de genes que contienen tales intrones incluyen los intrones 5' del gen de actina 1 del arroz (véase US5641876), el gen de la actina 2 del arroz, el gen de sacarosa sintasa de maíz (Clancy y Hannah, 2002, Plant Physiol.
130(2):918-29), los genes de la alcohol deshidrogenasa-1 de maíz (Adh-1) y Bronce-1 (Callis y otros 1987 Genes Dev. 1 (10):1183-200; Mascarenhas y otros 1990, Plant Mol Biol. 15(6):913-20), el gen de la proteína de choque térmico 70 de maíz (véase US5593874), el gen encogido 1 de maíz, el gen sensible a la luz 1 de Solanum tuberosum y el gen de la proteína de choque térmico 70 de Petunia hybrida (véase US 5659122), el gen de reemplazo de la histona H3 de la alfalfa (Keleman y otros 2002 Transgenic Res. 11(1):69-72) y el gen de reemplazo de la histona H3 (tipo histona H3.3) de Arabidopsis thaliana (Chaubet-Gigot y otros, 2001, Plant Mol Biol. 45(1):17-30).
Otras secuencias reguladoras adecuadas incluyen UTR 5'. Como se usa en la presente memoria, un UTR 5', también denominado secuencia líder, es una región particular de un ARN mensajero (ARNm) ubicado entre el sitio de inicio de la transcripción y el codón de inicio de la región codificante. Está implicada en la estabilidad del ARNm y la eficiencia de la traducción. Por ejemplo, el líder 5' no traducido de un gen de la proteína de unión a clorofila a/b de petunia corriente abajo del sitio de inicio de la transcripción 35S puede utilizarse para aumentar los niveles de expresión del gen informador en estado estacionario (Harpster y otros, 1988, Mol Gen Genet. 212(1):182-90). El documento núm. WO95/006742 describe el uso de secuencias líderes 5' no traducidas derivadas de genes que codifican proteínas de choque térmi
El gen quimérico puede comprender, además, una región del extremo 3', es decir, una secuencia de terminación de la transcripción o de poliadenilación, operable en células de plantas. Como secuencia de terminación de la transcripción o de poliadenilación, puede hacerse uso de cualquier secuencia correspondiente de origen bacteriano, como, por ejemplo, el terminador nos de Agrobacterium tumefaciens, de origen viral, como, por ejemplo, el terminador CaMV 35S, o de origen vegetal, como como, por ejemplo, un terminador de histona como se describe en la solicitud de patente publicada EP 0633 317 A1. La región de poliadenilación puede derivarse del gen natural, de una variedad de otros genes de plantas, o del ADN-T. La secuencia del extremo 3' a adicionar puede derivarse, por ejemplo, de los genes de nopalina sintasa o octopina sintasa, o alternativamente de otro gen de plantas, o menos, preferentemente, de cualquier otro gen eucariótico.
La expresión y el direccionamiento de la proteorodopsina a las membranas de los tilacoides aprovecharán el espectro de la energía verde que es inaccesible para la clorofila. Se espera un aumento en la cantidad de ATP en condiciones de fotosíntesis, a partir del gradiente de protones generado tanto por los fotosistemas como por la bomba de proteorodopsina. En condiciones de inhibición de la transferencia de electrones a través de los fotosistemas,
deberíamos poder observar una tasa constante de síntesis de ATP muy por encima de la tasa basal a través de la actividad de la bomba de protones de proteorodopsina.
En condiciones normales de pH, los protones son bombeados al espacio periplásmico bacteriano por PR [50]. El ciclo del retinal fotoimpulsado comienza con la fotoisomerización de todo el retinal trans a retinal 13-cis. El cambio conformacional resultante equilibra el sistema para la transferencia de un protón desde la base de Schiff (SB; pKa ~ 11) al contraión, Asp 97 (pKa ~ 7,5). El protón se transfiere al lumen a través de un canal conductor de protones, y la SB se reprotona desde el citoplasma. El mecanismo de liberación de protones en PR no se entiende tan bien como en bacteriorodopsina (BR); sin embargo, se espera que los principales eventos del fotociclo sean similares a los de BR. Un desafío potencial para bombear protones por PR en las membranas tilacoides es la reversibilidad dependiente del gradiente de pH de la transferencia de protones por PR. A pHs periplásmicos, < 5,5, se invierte el flujo de protones en PR, lo que potencialmente agota el gradiente de protones y perjudica la síntesis de ATP. Así, al pH lumenal de los tilacoides (4,5), es posible la transducción inversa de protones a través de PR. Uno de los residuos críticos implicados en el flujo reversible de protones es Asp97, que actúa como el aceptor de protones del retinal. El pKa de Asp97 en PR es ~ 7,5, mientras que el pKa de su contraparte en BR es ~ 2,5. Debido al extremadamente bajo pKa del contraión, BR puede retener su actividad de bombeo directo a pH tan bajos como 3,5. La capacidad de PR para actuar como una bomba de protones en la membrana de los tilacoides implica mantener la eficiencia de bombeo en condiciones de pH bajo que prevalecen en el lumen. Proponemos que el bombeo vectoral de protones en el lumen de los tilacoides puede lograrse mediante la disminución del pKa de Asp97 y/o mediante la protección de la SB del pH del lumen mediante mutagénesis racional, específica del sitio. El ambiente electrostático alrededor de la SB en Pr es presumiblemente mantenido por los contraiones, Asp97, Asp227 (análogo a BR Asp212), Arg94 (análogo a BR Arg82) e His75. En BR, el bajo pKa de Asp85 se atribuye a sus fuertes interacciones de enlace de hidrógeno con Thr89 y Arg82 [53,54]. Dado que las interacciones que reducen el pKa de Asp97 promoverán la actividad de bombeo de protones a un pH externo bajo, se explorará la mutación de Met79 a un residuo que puede unirse al hidrógeno con His75 y Asp212, como Tyr o Thr. Estas mutaciones se proponen mediante la superposición de las estructuras de BR y PR y la identificación de residuos que están en condiciones de efectuar el comportamiento deseado. Finalmente, la capacidad de un PR modificado para funcionar como una bomba eficiente de H+ a pH ácido implicará, además, proteger la SB del entorno extracelular. Con este fin, se generará un mutante L219E/T206S, en el que E219 y S206 formarán una puerta Glu-Ser que regula la transferencia de protones vectoriales como ocurre en BR.
Para determinar si alguno de los transgenes altera la actividad de síntesis de ATP o CET, compararemos la cinética de reducción en la oscuridad del donante primario del fotosistema I, P700+ en plantas WT y transgénicas, con y sin dibromotiroquinona (DBMIB), un inhibidor de la CET mediada por Cytb6f. Se espera que la cinética de reducción P700+ en la oscuridad sea más rápida en plantas con CET más activa. En adición, evaluaremos la amplitud de la banda de termoluminiscencia After Glow (AG) (~40 °C) asociada con la actividad de CET [11,14,16,43,63]. Los tamaños de las piscinas de ATP también se evaluarán en plantas WT y transgénicas mediante espectroscopía de masas.
Con referencia ahora a la Figura 11, se produjeron líneas de Camelina transgénicas adicionales que expresaban el gen BCA (SEQ ID NO:4) en el estroma del cloroplasto. Estas líneas se produjeron mediante el uso de los procedimientos de transformación mediados por Agrobacterium como se describió anteriormente. Se evaluaron tres líneas para determinar su capacidad de acumular biomasa y proporcionar mejores tasas fotosintéticas. La Camelina tipo salvaje y las líneas mutantes de BCA no fueron significativamente diferentes a niveles de luz más bajos (0-400 umol/m2/s) en su capacidad de asimilar dióxido de carbono. Sin embargo, a medida que aumentaba la intensidad de la luz, los transformantes de BCA mostraron una acumulación de CO2 entre un 10 y un 30 % mayor a 2.000 pmoles/m2/s con respecto al tipo salvaje. La línea BCA 9.2 fue la más alta, mientras que las líneas BCA 4.1 y BCA 5.7 fueron aproximadamente un 10 % más altas que las de tipo salvaje. Esta capacidad mejorada para asimilar CO2 se reflejó en dos de las líneas (BCA-5.7 y BCA-9.2) en una mayor acumulación de biomasa, con estas líneas que tienen aproximadamente un 15 % más de acumulación de biomasa que el tipo salvaje. La línea BCA-4.1 no mostró una mejor acumulación de biomasa en comparación con el control.
Con referencia ahora a la Figura 12, la capacidad de la proteína transportadora de bicarbonato localizada en la envoltura del cloroplasto (LCIA) para transportar bicarbonato y mejorar la captura de carbono inorgánico por la Camelina transgénica se determinó mediante el seguimiento del procedimiento de Farquhar y colegas (1989). La Camelina transgénica de LCIA se produjo mediante el uso de la transformación mediada por Agrobacterium procesada descrita anteriormente. Se comparó una línea mutante que expresa LCIA (CAM-LCIA) con Camelina de tipo salvaje (Cam-WT) para la discriminación observada del isótopo estable 13C. Esta discriminación de isótopos de carbono se expresa como la diferencia entre 13C en el aire y en una planta que se expuso previamente a 13CO2, la discriminación de isótopos de carbono se simboliza por A y se expresa en partes por millón (ppm) y se describe por Farquhar y colegas (1989). En las líneas transgénicas de LCIA, la discriminación observada por la planta fue 20 % menor que la observada en el tipo salvaje. Esto indica que la inserción de LCIA proporciona a la planta la capacidad de acumular y retener mejor el carbono inorgánico respecto a la planta de tipo salvaje y muestra una disminución de la "pérdida" frente al tipo salvaje.
Referencia para la discriminación de 13C: Carbon isotope discrimination and photosynthesis,G.D. Farquhar, J. R. Ehlieringery K. T. Hubick. Annu. Rev. Plant Physiol. Plant Mol. Biol. 1989, 40, 503-537.
(continuación)
(continuación)
TABLA D10 Péptidos de tránsito
TABLA D11 Proteínas moduladoras de la transferencia de electrones cíclica
Una secuencia de ADN optimizada ejemplar para el transportador de bicarbonato localizado en la membrana plasmática se muestra en la SEQ ID NO. 91
atgctgcccg gcctgggcgt catcctgctg gtgctgccca tgcagtacta cttcggctac 60
aagatcgtgc agatcaagct gcagaacgcc aagcacgtcg ccctgcgctc cgccatcatg 120
caggaggtgc tgcccgccat caagctggtc aagtactacg cctgggagca gttctttgag 180
aaccagatca gcaaggtccg ccgcgaggag atccgcctca acttctggaa ctgcgtgatg 240
aaggtcatca acgtggcctg cgtgttctgc gtgccgccca tgaccgcctt cgtcatcttc 300
accacctacg agttccagcg cgcccgcctg gtgtccagcg tcgccttcac caccctgtcg 360
ctgttcaaca ttctgcgctt ccccctggtc gtgctgccca aggccctgcg tgccgtgtcc 420
gaggccaacg cgtctctcca gcgcctggag gcctacctgc tggaggaggt gccctcgggc 480
actgccgccg tcaagacccc caagaacgct ccccccggcg ccgtcatcga gaacggtgtg 540
ttccaccacc cctccaaccc caactggcac ctgcacgtgc ccaagttcga ggtcaagccc 600
ggccaggtcg ttgctgtggt gggccgcatc gccgccggca agtcgtccct ggtgcaggcc 660
atcctcggca acatggtcaa ggagcacggc agcttcaacg tgggcggccg catctcctac 720
gtgccgcaga acccctggct gcagaacctg tccctgcgtg acaacgtgct gtttggcgag 780
cagttcgatg agaacaagta caccgacgtc atcgagtcct gcgccctgac cctggacctg 840
cagatcctgt ccaacggtga ccagtccaag gccggcatcc gcggtgtcaa cttctccggt 900
ggccagcgcc agcgcgtgaa cctggcccgc tgcgcctacg ccgacgccga cctggtgctg 960
ctcgacaacg ccctgtccgc cgtggaccac cacaccgccc accacatctt cgacaagtgc 1020
atcaagggcc tgttctccga caaggccgtg gtgctggtca cccaccagat cgagttcatg 1080
ccccgctgcg acaacgtggc catcatggac gagggccgct gcctgtactt cggcaagtgg 1140
aacgaggagg cccagcacct gctcggcaag ctgctgccca tcacccacct gctgcacgcc 1200
gccggctccc aggaggctcc ccccgccccc aagaagaagg ccgaggacaa ggccggcccc 1260 cagaagtcgc agtcgctgca gctgaccctg gcccccacct ccatcggcaa gcccaccgag 1320
aagcccaagg acgtccagaa gctgactgcc taccaggccg ccctcatcta cacctggtac 1380
ggcaacctgt tcctggttgg cgtgtgcttc ttcttcttcc tggcggctca gtgctctcgc 1440
cagatctccg atttctgggt gcgctggtgg gtgaacgacg agtacaagaa gttccccgtg 1500
aagggcgagc aggactcggc cgccaccacc ttctactgcc tcatctacct gctgctggtg 1560
ggcctgttct acatcttcat gatcttccgc ggcgccactt tcctgtggtg ggtgctcaag 1620
tcctcggaga ccatccgcag gaaggccctg cacaacgtcc tcaacgcgcc catgggcttc 1680
ttcctggtca cgccggtcgg cgacctgctg ctcaacttca ccaaggacca ggacattatg 1740
gatgagaacc tgcccgatgc cgttcacttc atgggcatct acggcctgat tctgctggcg 1800
accaccatca ccgtgtccgt caccatcaac ttcttcgccg ccttcaccgg cgcgctgatc 1860
atcatgaccc tcatcatgct ctccatctac ctgcccgccg ccactgccct gaagaaggcg 1920
cgcgccgtgt ctggcggcat gctggtcggc ctggttgccg aggttctgga gggccttggc 1980
gtggttcagg ccttcaacaa gcaggagtac ttcattgagg aggccgcccg ccgcaccaac 2040
atcaccaact ccgccgtctt caacgccgag gcgctgaacc tgtggctggc tttctggtgc 2100
gacttcatcg gcgcctgcct ggtgggcgtg gtgtccgcct tcgccgtggg catggccaag 2160
gacctgggcg gcgcgaccgt cggcctggcc ttctccaaca tcattcagat gcttgtgttc 2220
tacacctggg tggtccgctt catctccgag tccatctccc tcttcaactc cgtcgagggc 2280
atggcctacc tcgccgacta cgtgccccac gatggtgtct tctatgacca gcgccagaag 2340
gacggcgtcg ccaagcaaat cgtcctgccc gacggcaaca tcgtgcccgc cgcctccaag 2400
gtccaggtcg tggttgacga cgccgccctc gcccgctggc ctgccaccgg caacatccgc 2460
ttcgaggacg tgtggatgca gtaccgcctg gacgctcctt gggctctgaa gggcgtcacc 2520
ttcaagatca acgacggcga gaaggtcggc gccgtgggcc gcaccggctc cggcaagtcc 2580 accacgctgc tggcgctgta ccgcatgttc gagctgggca agggccgcat cctggtcgac 2640
ggcgtggaca tcgccaccct gtcgctcaag cgcctgcgca ccggcctgtc catcattccc 2700
caggagcccg tcatgttcac cggcaccgtg cgctccaacc tggacccctt cggcgagttc 2760
aaggacgatg ccattctgtg ggaggtgctg aagaaggtcg gcctcgagga ccaggcgcag 2820 cacgccggcg gcctggacgg ccaggtcgat ggcaccggcg gcaaggcctg gtctctgggc 2880 cagatgcagc tggtgtgcct ggctcgcgcc gccctgcgcg ccgtgcccat cctgtgcctg 2940
gacgaggcta ccgccgccat ggacccgcac actgaggcca tcgtgcagca gaccatcaag 3000 aaggtgttcg acgaccgcac caccatcacc attgcccacc gcctggacac catcatcgag 3060 tccgacaaga tcatcgtgat ggagcagggc tcgctgatgg agtacgagtc gccctcgaag 3120 ctgctcgcca accgcgactc catgttctcc aagctggtcg acaagaccgg ccccgccgcc 3180 gccgctgcgc tgcgcaagat ggccgaggac ttctggtcca ctcgctccgc gcagggccgc 3240 aaccagtaa (SEQ ID NO: 91)
Una secuencia de ADN optimizada ejemplar para el transportador de bicarbonato localizado en la envoltura del cloroplasto se muestra en la SEQ ID NO: 92
atgcagacca ctatgactcg cccttgcctt gcccagcccg tgctgcgatc tcgtgtgctc 60
cggtcgccta tgcgggtggt tgcagcgagc gctcctaccg cggtgacgac agtcgtgacc 120 tcgaatggaa atggcaacgg tcatttccaa gctgctacta cgcccgtgcc ccctactccc 180 gctcccgtcg ctgtttccgc gcctgtgcgc gctgtgtcgg tgctgactcc tcctcaagtg 240
tatgagaacg ccattaatgt tggcgcctac aaggccgggc taacgcctct ggcaacgttt 300 gtccagggca tccaagccgg tgcctacatt gcgttcggcg ccttcctcgc catctccgtg 360
ggaggcaaca tccccggcgt cgccgccgcc aaccccggcc tggccaagct gctatttgct 420 ctggtgttcc ccgtgggtct gtccatggtg accaactgcg gcgccgagct gttcacgggc 480 aacaccatga tgctcacatg cgcgctcatc gagaagaagg ccacttgggg gcagcttctg 540 aagaactgga gcgtgtccta cttcggcaac ttcgtgggct ccatcgccat ggtcgccgcc 600 gtggtggcca ccggctgcct gaccaccaac accctgcctg tgcagatggc caccctcaag 660 gccaacctgg gcttcaccga ggtgctgtcg cgctccatcc tgtgcaactg gctggtgtgc 720 tgcgccgtgt ggtccgcctc cgccgccacc tcgctgcccg gccgcatcct ggcgctgtgg 780 ccctgcatca ccgccttcgt ggccatcggc ctggagcact ccgtcgccaa catgttcgtg 840 attcctctgg gcatgatgct gggcgctgag gtcacgtgga gccagttctt tttcaacaac 900
ctgatccccg tcaccctggg caacaccatt gctggcgttc tcatgatggc catcgcctac 960
tccatctcgt tcggctccct cggcaagtcc gccaagcccg ccaccgcg 1008
(SEQ ID NO: 92)
Los expertos en la técnica reconocerán, o podrán determinar con el uso de no más que la experimentación habitual, muchos equivalentes a las realizaciones específicas de la divulgación descrita en la presente memoria. Por ejemplo, una planta transgénica de una realización divulgada en la presente memoria que comprende, además, dentro de su genoma, y que expresa o sobreexpresa, una combinación de secuencias de nucleótidos heterólogas que codifican adicionalmente una Rubisco (por ejemplo, SEQ ID NO:107). Además, una secuencia de aminoácidos de péptido de tránsito en la porción amino terminal de una secuencia de proteína identificada en la presente memoria puede escindirse y dejar solo la secuencia de proteína. El porcentaje de homología se aplica a la secuencia de proteínas sin la secuencia de péptido de tránsito también. Se pretende que esos equivalentes se abarquen en el alcance de las siguientes reivindicaciones.
Referencias mencionadas
1. Hausler RE, Hirsch HJ, Kreuzaler F, Peterhansel C (2002) Overexpression of C(4)-cycle enzymes in transgenic C(3) plants: a biotechnological approach to improve C(3)-photosynthesis. J Exp Bot 53: 591-607.
2. Goldschmidt EE, Huber SC (1992) Regulation of photosynthesis by end-product accumulation in leaves of plants storing starch, sucrose, and hexose sugars. Plant Physiol 99: 1443-1448.
3. Duanmu D, Miller Ar , Horken KM, Weeks DP, Spalding MH (2009) Knockdown of limiting-CO2-induced gene HLA3 decreases HCO3- transport and photosynthetic Ci affinity in Chlamydomonas reinhardtii. Proc Natl Acad Sci U S A 106: 5990-5995.
4. Moroney JV, Jungnick N, Dimario RJ, Longstreth DJ (2013) Photorespiration and carbon concentrating mechanisms: two adaptations to high O2, low CO2 conditions. Photosynth Res 117: 121-131.
5. Wang Y, Duanmu D, Spalding MH (2011) Carbon dioxide concentrating mechanism in Chlamydomonas reinhardtii: inorganic carbon transport and CO2 recapture. Photosynth Res 109: 115-122.
6. Perrine Z, Negi S, Sayre R (2012) Optimization of photosynthetic light energy utilization by microalgae. Algal Research 1: 134-142.
7. Elleby B, Chirica LC, Tu C, Zeppezauer M, Lindskog S (2003) Characterization of carbonic anhydrase from Neisseria gonorrhoeae. Eur J Biochem 286: 1613-1619.
8. Subramanian S, Barry AN, Pieris S, Sayre RT (2013) Comparative energetics and kinetics of autotrophic lipid and starch metabolism in chlorophytic microalgae: implications for biomass and biofuel production. Biotechnol Biofuels 6: 150.
9. Nakamura N, Iwano M, Havaux M, Yokota A, Munekage YN (2013) Promotion of cyclic electron transport around photosystem I during the evolution of NADP-malic enzyme-type C4 photosynthesis in the genus Flaveria. New Phytol 199: 832-842.
10. Kramer DM, Evans JR (2011) The importance of energy balance in improving photosynthetic productivity. Plant Physiol 155: 70-78.
11. Alric J (2010) Cyclic electron flow around photosystem I in unicellular green algae. Photosynth Res 106: 47-56.
12. Amunts A, Drory O, Nelson N (2007) The structure of a plant photosystem I supercomplex at 3.4 A resolution. Nature 447: 58-63.
13. Breyton C, Nandha B, Johnson GN, Joliot P, Finazzi G (2006) Redox modulation of cyclic electron flow around photosystem I in C3 plants. Biochemistry 45: 13465-13475.
14. Cardol P, Forti G, Finazzi G (2011) Regulation of electron transport in microalgae. Biochim Biophys Acta 1807: 912-918.
15. Hanke GT, Okutani S, Satomi Y, Takao T, Suzuki A, y otros (2005) Multiple iso-proteins of FNR in Arabidopsis: evidence for different contributions to chloroplast function and nitrogen assimilation. Plant Cell Environ 28: 1146 1157.
16. Johnson GN (2011) Physiology of PSI cyclic electron transport in higher plants. Biochim Biophys Acta 1807: 384 389.
17. Okutani S, Hanke GT, Satomi Y, Takao T, Kurisu G, y otros (2005) Three maize leaf ferredoxin:NADPH oxidoreductases vary in subchloroplast location, expression, and interaction with ferredoxin. Plant Physiol 139: 1451 1459.
18. Slewinski TL, Braun DM (2010) Current perspectives on the regulation of whole-plant carbohydrate partitioning. Plant Science 178: 341-349.
19. Arrivault S, Guenther M, Ivakov A, Feil R, Vosloh D, y otros (2009) Use of reverse-phase liquid chromatography, linked to tandem mass spectrometry, to profile the Calvin cycle and other metabolic intermediates in Arabidopsis rosettes at different carbon dioxide concentrations. Plant Journal 59: 824-839.
20. Huege J, Sulpice R, Gibon Y, Lisec J, Koehl K, y otros (2007) GC-EI-TOF-MS analysis of in vivo carbonpartitioning into soluble metabolite pools of higher plants by monitoring isotope dilution after (CO2)-C-13 labelling. Phytochemistry 68: 2258-2272.
21. Romisch-Margl W, Schramek N, Radykewicz T, Ettenhuber C, Eylert E, y otros (2007) (CO2)-C-13 as a universal metabolic tracer in isotopologue perturbation experiments. Phytochemistry 68: 2273-2289.
22. Sekiyama Y, Kikuchi J (2007) Towards dynamic metabolic network measurements by multidimensional NMR-based fluxomics. Phytochemistry 68: 2320-2329.
23. Szecowka M, Heise R, Tohge T, Nunes-Nesi A, Vosloh D, y otros (2013) Metabolic fluxes in an illuminated Arabidopsis rosette. Plant Cell 25: 694-714.
24. Ma F, Jazmin LJ, Young JD, Allen DK (Submitted) Isotopically nonstationary 13C flux analysis of Arabidopsis thaliana leaf metabolism at varying light intensities. Proc Natl Acad Sci USA.
25. Shastri AA, Morgan JA (2007) A transient isotopic labeling methodology for 13C metabolic flux analysis of photoautotrophic microorganisms. Phytochemistry 68: 2302-2312.
26. Young Jd , Shastri AA, Stephanopoulos G, Morgan JA (2011) Mapping photoautotrophic metabolism with isotopically nonstationary (13)C flux analysis. Metab Eng 13: 656-665.
27. Young JD (Submitted) INCA: A computational platform for isotopically nonstationary metabolic flux analysis. Bioinformatics.
28. Young JD, Walther JL, Antoniewicz MR, Yoo H, Stephanopoulos G (2008) An elementary metabolite unit (EMU) based method of isotopically nonstationary flux analysis. Biotechnol Bioeng 99: 686-699.
29. Masclaux-Daubresse C, Chardon F (2011) Exploring nitrogen remobilization for seed filling using natural variation in Arabidopsis thaliana. J Exp Bot 62: 2131-2142.
30. Hay RKM, Gilbert RA (2001) Variation in the harvest index of tropical maize: Evaluation of recent evidence from Mexico and Malawi. Annals of Applied Biology 138: 103-109.
31. Russell WA (1985) Evaluation for plant, ear and grain traits of maize cultivars representing seven years of breeding. Maydica 30: 85-96.
32. Sinclair TR (1998) Historical changes in harvest index and crop nitrogen accumulation. Crop Science 38: 638 643.
33. Victorio RG, Moreno U, Black Jr CC (1986) Growth, partitioning, and harvest index of tuber-bearing Solanum genotypes grown in two contrasting Peruvian environments. Plant Physiology 82: 103-108.
34. Vos J (1997) The nitrogen response of potato (Solanum tuberosum L.) in the field: Nitrogen uptake and yield, harvest index and nitrogen concentration. Potato Research 40: 237-248.
35. Parry MA, Andralojc PJ, Scales JC, Salvucci ME, Carmo-Silva AE, y otros (2013) Rubisco activity and regulation as targets for crop improvement. J Exp Bot 64: 717-730.
36. Sage RF (2002) Variation in the k(cat) of Rubisco in C(3) and C(4) plants and some implications for photosynthetic performance at high and low temperature. J Exp Bot 53: 609-620.
37. Henkes S, Sonnewald U, Badur R, Flachmann R, Stitt M (2001) A small decrease of plastid transketolase activity in antisense tobacco transformants has dramatic effects on photosynthesis and phenylpropanoid metabolism. Plant Cell 13: 535-551.
38. Miyagawa Y, Tamoi M, Shigeoka S (2001) Overexpression of a cyanobacterial fructose-1,6-/sedoheptulose-1,7-bisphosphatase in tobacco enhances photosynthesis and growth. Nature Biotechnology 19: 965-969.
39. Peterhansel C, Blume C, Offermann S (2013) Photorespiratory bypasses: how can they work? J Exp Bot 64: 709 715.
40. Blanco NE, Ceccoli RD, Via MV, Voss I, Segretin ME, y otros (2013) Expression of the minor isoform pea ferredoxin in tobacco alters photosynthetic electron partitioning and enhances cyclic electron flow. Plant Physiol 161: 866-879.
41. Busch KB, Deckers-Hebestreit G, Hanke GT, Mulkidjanian AY (2012) Dynamics of bioenergetic microcompartments. Biol Chem 394: 163-188.
42. Minagawa J (2011) State transitions--the molecular remodeling of photosynthetic supercomplexes that controls energy flow in the chloroplast. Biochim Biophys Acta 1807: 897-905.
43. Peltier G, Tolleter D, Billon E, Cournac L (2010) Auxiliary electron transport pathways in chloroplasts of microalgae. Photosynth Res 106: 19-31.
44. Peng L, Shikanai T (2011) Supercomplex formation with photosystem I is required for the stabilization of the chloroplast NADH dehydrogenase-like complex in Arabidopsis. Plant Physiol 155: 1629-1639.
45. Takahashi H, Clowez S, Wollman FA, Vallon O, Rappaport F (2013) Cyclic electron flow is redox-controlled but independent of state transition. Nat Commun 4: 1954.
46. Hertle AP, Blunder T, Wunder T, Pesaresi P, Pribil M, y otros (2013) PGRL1 is the elusive ferredoxinplastoquinone reductase in photosynthetic cyclic electron flow. Mol Cell 49: 511-523.
47. DalCorso G, Pesaresi P, Masiero S, Aseeva E, Schunemann D, y otros (2008) A complex containing PGRL1 and PGR5 is involved in the switch between linear and cyclic electron flow in Arabidopsis. Cell 132: 273-285.
48. Shikanai T (2014) Central role of cyclic electron transport around photosystem I in the regulation of photosynthesis. Current Opinion in Biotechnology 26: 25-30.
49. Walter JM, Greenfield D, Liphardt J (2010) Potential of light-harvesting proton pumps for bioenergy applications. Curr Opin Biotechnol 21: 265-270.
50. Dioumaev AK, Brown LS, Shih J, Spudich EN, Spudich JL, y otros (2002) Proton transfers in the photochemical reaction cycle of proteorhodopsin. Biochemistry 41: 5348-5358.
51. Friedrich T, Geibel S, Kalmbach R, Chizhov I, Ataka K, y otros (2002) Proteorhodopsin is a light-driven proton pump with variable vectoriality. J Mol Biol 321: 821-838.
52. Govindjee R, Ebrey TG, Crofts AR (1980) The quantum efficiency of proton pumping by the purple membrane of Halobacterium halobium. Biophys J 30: 231-242.
53. Govindjee R, Imasheva ES, Misra S, Balashov SP, Ebrey TG, y otros (1997) Mutation of a surface residue, lysine-129, reverses the order of proton release and uptake in bacteriorhodopsin; guanidine hydrochloride restores it. Biophys J 72: 886-898.
54. Govindjee R, Misra S, Balashov SP, Ebrey TG, Crouch RK, y otros (1996) Arginine-82 regulates the pKa of the group responsible for the light-driven proton release in bacteriorhodopsin. Biophys J 71: 1011-1023.
55. Lakatos M, Lanyi JK, Szakacs J, Varo G (2003) The photochemical reaction cycle of proteorhodopsin at low pH. Biophys J 84: 3252-3256.
56. Walter JM, Greenfield D, Bustamante C, Liphardt J (2007) Light-powering Escherichia coli with proteorhodopsin. Proc Natl Acad Sci U S A 104: 2408-2412.
57. Kim JY, Jo BH, Jo Y, Cha HJ (2012) Improved production of biohydrogen in light-powered Escherichia coli by coexpression of proteorhodopsin and heterologous hydrogenase. Microb Cell Fact 11: 2.
58. Froehlich JE, Keegstra K (2011) The role of the transmembrane domain in determining the targeting of membrane proteins to either the inner envelope or thylakoid membrane. Plant J 68: 844-856.
59. Beja O, Aravind L, Koonin EV, Suzuki MT, Hadd A, y otros (2000) Bacterial rhodopsin: evidence for a new type of phototrophy in the sea. Science 289: 1902-1906.
60. Lindqvist A, Andersson S (2002) Biochemical properties of purified recombinant human beta-carotene 15,15'-monooxygenase. J Biol Chem 277: 23942-23948.
61. Roslan HA, Salter MG, Wood CD, White MR, Croft KP, y otros (2001) Characterization of the ethanol-inducible alc gene-expression system in Arabidopsis thaliana. Plant J 28: 225-235.
62. Cao Y, Brown LS, Sasaki J, Maeda A, Needleman R, y otros (1995) Relationship of proton release at the extracellular surface to deprotonation of the schiff base in the bacteriorhodopsin photocycle. Biophys J 68: 1518 1530.
63. Joliot P, Johnson GN (2011) Regulation of cyclic and linear electron flow in higher plants. Proc Natl Acad Sci U S A 108: 13317-13322.
64. Fabre N, Reiter IM, Becuwe-Linka N, Genty B, Rumeau D (2007) Characterization and expression analysis of genes encoding alpha and beta carbonic anhydrases in Arabidopsis. Plant Cell Environ 30: 617-629.
65. Bihmidine S, Hunter CT, 3rd, Johns CE, Koch KE, Braun DM (2013) Regulation of assimilate import into sink organs: update on molecular drivers of sink strength. Front Plant Sci 4: 177.
66. Ihemere U, Arias-Garzon D, Lawrence S, Sayre R (2006) Genetic modification of cassava for enhanced starch production. Plant Biotechnol J 4: 453-465.
67. Wunsche JN, Greer DH, Laing WA, Palmer JW (2005) Physiological and biochemical leaf and tree responses to crop load in apple. Tree Physiol 25: 1253-1263.
68. Paul MJ, Foyer CH (2001) Sink regulation of photosynthesis. J Exp Bot 52: 1383-1400.
69. Sonnewald U, Lerchi J, Zrenner R, Frommer W (1994) Manipulation of sink-source relations in transgenic plants. Plant Cell Environ 17: 649-658.
70. Sonnewald U, Willmitzer L (1992) Molecular approaches to sink-source interactions. Plant Physiol 99: 1267-1270.
71. Willson WJ (1972) Control of crop processes In: Rees AR, Cockshull KE, Hand DW, Hurd RG, editores. Crop Processes in Controlled Environments: London Academic Press. pp. 7-30.
72. Jonik C, Sonnewald U, Hajirezaei MR, Flugge UI, Ludewig F (2012) Simultaneous boosting of source and sink capacities doubles tuber starch yield of potato plants. Plant Biotechnol J 10: 1088-1098.
73. Sweetlove LJ, Hill SA (2000) Source metabolism dominates the control of source to sink carbon flux in tuberizing potato plants throughout the diurnal cycle and under a range of environmental conditions. Plant, Cell and Environment 23: 523-529.
74. Allen DK, Goldford J, Gierse J, Mandy D, Diepenbrock C, y otros (2013) (submitted) Quantification of peptide m/z distributions form 13C-labeled cultures with high resolution mass spectrometry. Analytical Chemistry.
75. Choi J, Antoniewicz MR (2011) Tandem mass spectrometry: a novel approach for metabolic flux analysis. Metab Eng 13: 225-233.
76. Allen DK, Libourel IGL, Shachar-Hill Y (2009) Metabolic flux analysis in plants: Coping with complexity. Plant, Cell and Environment 32: 1241-1257.
77. Allen DK, Laclair RW, Ohlrogge JB, Shachar-Hill Y (2012) Isotope labelling of Rubisco subunits provides in vivo information on subcellular biosynthesis and exchange of amino acids between compartments. Plant, Cell and Environment 35: 1232-1244.
78. Allen DK, Shachar-Hill Y, Ohlrogge JB (2007) Compartment-specific labeling information in 13C metabolic flux analysis of plants. Phytochemistry 68: 2197-2210.
Claims (15)
1. Una planta C3 transgénica, que comprende dentro de su genoma, y que expresa o sobreexpresa, una combinación de secuencias de nucleótidos heterólogas que codifican:
un transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática; y una proteína moduladora de la transferencia de electrones cíclica en la que la proteína moduladora de la transferencia de electrones cíclica se selecciona del grupo que consiste en una proteína PGRL1, una proteína PGR5, una proteína FNR1, una proteína FNR2, una proteína Fdl, o cualquier combinación de las mismas, y en la que el transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática es una proteína HLA3.
2. La planta C3 transgénica de la reivindicación 1 que comprende, además, dentro de su genoma, y que expresa o sobreexpresa, una proteína transportadora de aniones bicarbonato transgénica localizada en la envoltura de cloroplasto.
3. La planta C3 transgénica de la reivindicación 2 en la que el transportador de aniones bicarbonato transgénico localizado en la envoltura del cloroplasto es una proteína LCIA.
4. La planta C3 transgénica de la reivindicación 3 que comprende, además, dentro de su genoma, y que expresa o sobreexpresa, una proteína anhidrasa carbónica transgénica.
5. La planta C3 transgénica de la reivindicación 4 en la que la anhidrasa carbónica transgénica es la proteína BCA.
6. La planta C3 transgénica de la reivindicación 1 en la que las secuencias de nucleótidos heterólogas codifican
i) la proteína PGR5, y la proteína HLA3; o
ii) la proteína PGR5, la proteína HLA3 y la proteína PGRL1.
7. La planta C3 transgénica de la reivindicación 3 en la que las secuencias de nucleótidos heterólogas codifican la proteína PGR5, la proteína HLA3, y la proteína LCIA.
8. La planta C3 transgénica de la reivindicación 5 en la que las secuencias de nucleótidos heterólogas codifican la proteína PGR5, la proteína HLA3, la proteína PGRL1, la proteína LCIA, y la proteína BCA.
9. La planta C3 transgénica de la reivindicación 5 en la que las secuencias de nucleótidos heterólogas codifican la proteína PGR5, la proteína HLA3, la proteína LCIA y la proteína BCA.
10. La planta transgénica C3 de la reivindicación 5 en la que las secuencias de nucleótidos heterólogas codifican la proteína PGR5, la proteína HLA3, la proteína LCIA y la proteína BCA, en la que
a) la proteína PGR5 tiene una secuencia de aminoácidos al menos 80 % idéntica a la SEQ ID NO:1;
b) la proteína HLA3 tiene una secuencia de aminoácidos al menos 80 % idéntica a la SEQ ID NO:77;
d) la proteína LCIA tiene una secuencia de aminoácidos al menos 80 % idéntica a la SEQ ID NO: 18; y/o e) la proteína BCA tiene una secuencia de aminoácidos al menos 80 % idéntica a la SEQ ID NO:21.
11. La planta C3 transgénica de cualquiera de las reivindicaciones 6-9, en la que
a) la proteína PGR5 tiene una secuencia de aminoácidos al menos 80 % idéntica a la SEQ ID NO:1;
b) la proteína HLA3 tiene una secuencia de aminoácidos al menos 80 % idéntica a la SEQ ID NO:77;
c) la proteína PGRL1 tiene una secuencia de aminoácidos al menos 80 % idéntica a la SEQ ID NO:3;
d) la proteína LCIA tiene una secuencia de aminoácidos al menos 80 % idéntica a la SEQ ID NO:18; y/o e) la proteína BCA tiene una secuencia de aminoácidos al menos 80 % idéntica a la SEQ ID NO:21.
12. Una parte celular de dicha planta C3 transgénica de la reivindicación 1 que comprende dentro de su genoma, y que expresa o sobreexpresa una combinación de secuencias de nucleótidos heterólogas que codifican: un transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática y una proteína moduladora de la transferencia de electrones cíclica.
13. Un procedimiento para elevar la actividad de CET o para mejorar la fijación de carbono o para producir biomasa u otros productos en una planta C3, en el que dicho procedimiento comprende expresar o sobreexpresar, en una planta C3, una combinación de secuencias de nucleótidos heterólogas que codifican:
un transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática; y una proteína moduladora de la transferencia de electrones cíclica, en la que la proteína moduladora de la transferencia de electrones cíclica se selecciona del grupo que consiste en una proteína PGRL1, una proteína PGR5, una proteína FNR1, una proteína FNR2, una proteína Fdl, o cualquier combinación de las mismas, y en la que el transportador de aniones bicarbonato dependiente de ATP localizado en la membrana plasmática es una proteína HLA3.
14. El procedimiento de la reivindicación 13 de producción de biomasa u otros productos que comprende, además, cultivar dicha planta C3 y recolectar dicha biomasa o recuperar dicho producto de dicha planta C3.
15. Uso de una construcción que comprende uno o más ácidos nucleicos que codifican
a) una proteína PGR5, y una proteína HLA3;
b) una proteína PGR5, una proteína HLA3 y una proteína PGRL1;
c) una proteína PGR5, una proteína HLA3, y una proteína LCIA;
d) una proteína PGR5, una proteína HLA3, una proteína LCIA y una proteína BCA u opcionalmente una proteína HCA2;
e) una proteína PGR5, una proteína HLA3, una proteína PGRL1 y una proteína LCIA;
f) una proteína PGR5, una proteína HLA3, una proteína PGRL1, una proteína LCIA, y una proteína BCA u opcionalmente una proteína HCA2;
g) una proteína PGR5, una proteína HLA3, y una proteína BCA; o
h) una proteína PGR5, una proteína HLA3, una proteína PGRL1, y una proteína BCA para
i) hacer una planta C3 transgénica de cualquiera de las reivindicaciones 1-10,
ii) elevar la actividad de CET en una planta C3;
iii) mejorar la fijación de carbono en una planta C3; o
iv) producir biomasa u otros productos a partir de una planta C3, en la que dichos productos se seleccionan del grupo que consiste en almidones, aceites, ácidos grasos, triacilgliceroles, lípidos, celulosa u otros carbohidratos, alcoholes, azúcares, nutracéuticos, productos farmacéuticos, compuestos saborizantes y fragancias, y ácidos orgánicos.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201462027354P | 2014-07-22 | 2014-07-22 | |
| PCT/US2015/041617 WO2016014720A2 (en) | 2014-07-22 | 2015-07-22 | Improved carbon fixation systems in plants and algae |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2773601T3 true ES2773601T3 (es) | 2020-07-13 |
Family
ID=53773567
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES15745345T Active ES2773601T3 (es) | 2014-07-22 | 2015-07-22 | Sistemas de fijación de carbono mejorados en plantas y algas |
Country Status (6)
| Country | Link |
|---|---|
| US (4) | US10233458B2 (es) |
| EP (1) | EP3172327B1 (es) |
| AU (2) | AU2015292616B2 (es) |
| CA (1) | CA2957921A1 (es) |
| ES (1) | ES2773601T3 (es) |
| WO (1) | WO2016014720A2 (es) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2773601T3 (es) * | 2014-07-22 | 2020-07-13 | Nmc Inc | Sistemas de fijación de carbono mejorados en plantas y algas |
| EP3029060A1 (en) * | 2014-12-01 | 2016-06-08 | Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. | Genetically modified higher plants with increased photosynthesis and/or biomass production, methods and uses thereof |
| WO2017136668A1 (en) * | 2016-02-04 | 2017-08-10 | Yield10 Bioscience, Inc. | Transgenic land plants comprising a putative bicarbonate transporter protein of an edible eukaryotic algae |
| KR102567405B1 (ko) * | 2016-06-20 | 2023-08-17 | 보드 오브 슈퍼바이저스 오브 루이지애나 스테이트 유니버시티 앤드 애그리컬추얼 앤드 메카니컬 컬리지 | 녹조류 비카르보네이트 수송체 및 그의 용도 |
| CA3054060C (en) * | 2017-02-22 | 2023-09-26 | Yield10 Bioscience, Inc. | Transgenic land plants comprising enhanced levels of mitochondrial transporter protein |
| WO2019191488A1 (en) * | 2018-03-28 | 2019-10-03 | New Mexico Consortium | Enhancing photosynthetic rates, abiotic stress tolerance and biomass yield by expressing c4 plant ferredoxins in c3 plants |
| JP7693534B2 (ja) * | 2018-07-13 | 2025-06-17 | ボード オブ スーパーバイザーズ オブ ルイジアナ ステイト ユニバーシティ アンド アグリカルチュラル アンド メカニカル カレッジ | 緑藻類ベストロフィン重炭酸塩トランスポーター |
| CN111321156B (zh) * | 2018-12-14 | 2021-05-25 | 华中农业大学 | OsLUT1基因在调控水稻光保护中的应用 |
| US12553040B2 (en) | 2020-08-12 | 2026-02-17 | Korea University Research And Business Foundation | Carbonic anhydrase complex and method for bioimmobilizing carbon dioxide and enhancing lipid production thereby |
| CN116751813B (zh) * | 2023-06-01 | 2025-03-25 | 浙江大学 | 碳酸酐酶基因βCA2在提高番茄果实产量和调控番茄开花时间中的应用 |
| WO2025183903A2 (en) * | 2024-02-12 | 2025-09-04 | The Regents Of The University Of California | A photosynthetic system for catalyzing carbon dioxide mineralization |
| CN119623843B (zh) * | 2024-11-25 | 2025-07-18 | 生态环境部南京环境科学研究所 | 一种生态系统碳汇统一监管方法及装置 |
Family Cites Families (37)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4554101A (en) | 1981-01-09 | 1985-11-19 | New York Blood Center, Inc. | Identification and preparation of epitopes on antigens and allergens on the basis of hydrophilicity |
| US5352605A (en) | 1983-01-17 | 1994-10-04 | Monsanto Company | Chimeric genes for transforming plant cells using viral promoters |
| DE3484215D1 (de) | 1983-01-17 | 1991-04-11 | Monsanto Co | Chimaerische gene geeignet zur expression in pflanzenzellen. |
| GB8613481D0 (en) | 1986-06-04 | 1986-07-09 | Diatech Ltd | Translation of mrna |
| US4962028A (en) | 1986-07-09 | 1990-10-09 | Dna Plant Technology Corporation | Plant promotors |
| US5164316A (en) | 1987-01-13 | 1992-11-17 | The University Of British Columbia | DNA construct for enhancing the efficiency of transcription |
| US5322938A (en) | 1987-01-13 | 1994-06-21 | Monsanto Company | DNA sequence for enhancing the efficiency of transcription |
| US5196525A (en) | 1987-01-13 | 1993-03-23 | University Of British Columbia | DNA construct for enhancing the efficiency of transcription |
| US5359142A (en) | 1987-01-13 | 1994-10-25 | Monsanto Company | Method for enhanced expression of a protein |
| CA1339684C (en) | 1988-05-17 | 1998-02-24 | Peter H. Quail | Plant ubquitin promoter system |
| US5641876A (en) | 1990-01-05 | 1997-06-24 | Cornell Research Foundation, Inc. | Rice actin gene and promoter |
| US5589583A (en) | 1990-01-11 | 1996-12-31 | Monsanto Company | Plant promoter |
| FR2673642B1 (fr) | 1991-03-05 | 1994-08-12 | Rhone Poulenc Agrochimie | Gene chimere comprenant un promoteur capable de conferer a une plante une tolerance accrue au glyphosate. |
| US5593874A (en) | 1992-03-19 | 1997-01-14 | Monsanto Company | Enhanced expression in plants |
| FR2706909B1 (es) | 1993-06-25 | 1995-09-29 | Rhone Poulenc Agrochimie | |
| US5362865A (en) | 1993-09-02 | 1994-11-08 | Monsanto Company | Enhanced expression in plants using non-translated leader sequences |
| US5599686A (en) | 1994-06-28 | 1997-02-04 | Merck & Co., Inc. | Peptides |
| AU689311B2 (en) | 1994-08-30 | 1998-03-26 | Commonwealth Scientific And Industrial Research Organisation | Plant transcription regulators from circovirus |
| MX9701601A (es) | 1994-08-30 | 1998-04-30 | Commw Scient Ind Res Org | Reguladores de transcripcion de plantas a partir de circovirus. |
| CA2258565C (en) | 1996-06-20 | 2011-11-22 | The Scripps Research Institute | Cassava vein mosaic virus promoters and uses thereof |
| FR2771104B1 (fr) | 1997-11-17 | 2000-12-08 | Rhone Poulenc Agrochimie | Gene chimere ayant un promoteur lumiere dependant conferant la tolerance aux inhibiteurs del'hppd |
| US6784340B1 (en) | 1998-01-28 | 2004-08-31 | The Rockefeller University | Chemical inducible promoter used to obtain transgenic plants with a silent marker |
| US8039243B2 (en) | 2002-01-23 | 2011-10-18 | Wisconsin Alumni Research Foundation | Insertion sequence-free bacteria |
| US8765408B2 (en) | 2002-01-23 | 2014-07-01 | Wisconsin Alumni Research Foundation | Prophage element-free bacteria |
| US6989265B2 (en) | 2002-01-23 | 2006-01-24 | Wisconsin Alumni Research Foundation | Bacteria with reduced genome |
| US8119365B2 (en) | 2002-01-23 | 2012-02-21 | Wisconsin Alumni Research Foundation | Insertion sequence-free bacteria |
| US7303906B2 (en) | 2002-09-06 | 2007-12-04 | Wisconsin Alumni Research Foundation | Competent bacteria |
| FR2848571A1 (fr) | 2002-12-12 | 2004-06-18 | Bayer Cropscience Sa | Cassette d'expression codant pour une hydroxy-phenyl pyruvate dioxygenase et plantes contenant un tel gene tolerantes aux herbicides |
| US20090241208A1 (en) * | 2005-10-12 | 2009-09-24 | Ceres, Inc. | Nucleotide sequences and polypeptides encoded thereby useful for modifying plant characteristics in response to cold |
| EP2543726B1 (en) | 2005-08-20 | 2018-10-03 | Scarab Genomics, LLC | Reduced genome E. coli |
| EP2843053A1 (en) | 2006-02-17 | 2015-03-04 | Monsanto Technology LLC | Chimeric regulatory sequences comprising introns for plant gene expression |
| US20110256605A1 (en) * | 2010-03-12 | 2011-10-20 | The Regents Of The University Of California, A California Corporation | Cells with non-natural physiologies derived by expressing light-powered proton pumps in one or more membranes |
| WO2012101118A1 (en) | 2011-01-24 | 2012-08-02 | Bayer Cropscience N.V. | Use of the rd29 promoter or fragments thereof for stress-inducible expression of transgenes in cotton |
| WO2012125737A2 (en) * | 2011-03-14 | 2012-09-20 | Donald Danforth Plant Science Center | Methods for increasing carbon fixation |
| US20130007916A1 (en) | 2011-07-01 | 2013-01-03 | Iowa State University Research Foundation, Inc. | Modulation of low carbon dioxide inducible proteins (lci) for increased biomass production and photosynthesis |
| ES2773601T3 (es) | 2014-07-22 | 2020-07-13 | Nmc Inc | Sistemas de fijación de carbono mejorados en plantas y algas |
| JP2019523783A (ja) | 2016-06-16 | 2019-08-29 | オンコセレクト セラピューティクス,エルエルシー | がんの治療に有用なポルフィリン化合物及び組成物 |
-
2015
- 2015-07-22 ES ES15745345T patent/ES2773601T3/es active Active
- 2015-07-22 AU AU2015292616A patent/AU2015292616B2/en not_active Ceased
- 2015-07-22 EP EP15745345.7A patent/EP3172327B1/en active Active
- 2015-07-22 WO PCT/US2015/041617 patent/WO2016014720A2/en not_active Ceased
- 2015-07-22 CA CA2957921A patent/CA2957921A1/en active Pending
-
2017
- 2017-01-20 US US15/411,854 patent/US10233458B2/en active Active
-
2019
- 2019-03-19 US US16/358,331 patent/US10696977B2/en active Active
-
2020
- 2020-06-30 US US16/917,028 patent/US11001853B2/en active Active
-
2021
- 2021-05-11 US US17/317,362 patent/US11459578B2/en active Active
- 2021-12-02 AU AU2021277727A patent/AU2021277727A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| CA2957921A1 (en) | 2016-01-28 |
| US11459578B2 (en) | 2022-10-04 |
| WO2016014720A2 (en) | 2016-01-28 |
| US11001853B2 (en) | 2021-05-11 |
| US20170211086A1 (en) | 2017-07-27 |
| EP3172327A2 (en) | 2017-05-31 |
| US20190203222A1 (en) | 2019-07-04 |
| EP3172327B1 (en) | 2019-11-27 |
| US20220042031A1 (en) | 2022-02-10 |
| WO2016014720A3 (en) | 2016-02-18 |
| AU2021277727A1 (en) | 2021-12-23 |
| US20200347397A1 (en) | 2020-11-05 |
| AU2015292616A1 (en) | 2017-03-02 |
| US10233458B2 (en) | 2019-03-19 |
| AU2015292616B2 (en) | 2021-09-02 |
| US10696977B2 (en) | 2020-06-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2773601T3 (es) | Sistemas de fijación de carbono mejorados en plantas y algas | |
| US20110302673A1 (en) | Transgenic Plants with Increased Yield | |
| US20120042418A1 (en) | Engineering NF-YB Transcription Factors for Enhanced Drought Resistance and Increased Yield in Transgenic Plants | |
| US20230066837A1 (en) | Enhancing Photosynthesis | |
| US20220204982A1 (en) | Transgenic plants with engineered redox sensitive modulation of photosynthetic antenna complex pigments and methods for making the same | |
| US10465202B2 (en) | Abiotic stress resistance | |
| US20160138038A1 (en) | Methods and Compositions for Improvement in Seed Yield | |
| CN110475471A (zh) | 展现增加的产量和干旱耐受的转基因玉米植物 | |
| US20210024948A1 (en) | Enhancement of photosynthetic rates, abiotic stress tolerance and biomass yield through expressiopn of a c4 plant ferredoxin in c3 photosynthetic plants | |
| Haag | Protecting The Electron Transport Chain In Sports turf | |
| Msanne | Abiotic Stress Responses in Photosynthetic Organisms | |
| Mubarakshina | Carbonic Anhydrases in Photosynthesizing Cells of C3 Higher Plants | |
| AU2013203387A1 (en) | Engineering NF-YB transcription factors for enhanced drought resistance and increased yield in transgenic plants |