ES2800983T3 - Materiales y métodos para conjugar un derivado de ácido graso soluble en agua con una proteína - Google Patents
Materiales y métodos para conjugar un derivado de ácido graso soluble en agua con una proteína Download PDFInfo
- Publication number
- ES2800983T3 ES2800983T3 ES11806103T ES11806103T ES2800983T3 ES 2800983 T3 ES2800983 T3 ES 2800983T3 ES 11806103 T ES11806103 T ES 11806103T ES 11806103 T ES11806103 T ES 11806103T ES 2800983 T3 ES2800983 T3 ES 2800983T3
- Authority
- ES
- Spain
- Prior art keywords
- growth factor
- fatty acid
- factor
- protein
- group
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 108090000623 proteins and genes Proteins 0.000 title claims abstract description 304
- 102000004169 proteins and genes Human genes 0.000 title claims abstract description 304
- 239000000194 fatty acid Substances 0.000 title claims abstract description 199
- 235000014113 dietary fatty acids Nutrition 0.000 title claims abstract description 189
- 229930195729 fatty acid Natural products 0.000 title claims abstract description 189
- 150000004665 fatty acids Chemical class 0.000 title claims abstract description 161
- 238000000034 method Methods 0.000 title claims description 69
- 230000001268 conjugating effect Effects 0.000 title description 8
- 239000000463 material Substances 0.000 title description 7
- 230000001225 therapeutic effect Effects 0.000 claims abstract description 130
- -1 fatty acid ester Chemical class 0.000 claims abstract description 103
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims abstract description 66
- 150000001720 carbohydrates Chemical class 0.000 claims abstract description 37
- 150000002923 oximes Chemical class 0.000 claims abstract description 22
- 125000003172 aldehyde group Chemical group 0.000 claims abstract description 16
- 230000000921 morphogenic effect Effects 0.000 claims description 72
- 210000000988 bone and bone Anatomy 0.000 claims description 71
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 59
- 102000004196 processed proteins & peptides Human genes 0.000 claims description 56
- 229920001184 polypeptide Polymers 0.000 claims description 54
- 125000005647 linker group Chemical group 0.000 claims description 53
- 108010054218 Factor VIII Proteins 0.000 claims description 46
- 102000001690 Factor VIII Human genes 0.000 claims description 45
- 108010009583 Transforming Growth Factors Proteins 0.000 claims description 43
- 102000009618 Transforming Growth Factors Human genes 0.000 claims description 43
- 102100022641 Coagulation factor IX Human genes 0.000 claims description 42
- 108010076282 Factor IX Proteins 0.000 claims description 40
- 229960000301 factor viii Drugs 0.000 claims description 40
- 238000005859 coupling reaction Methods 0.000 claims description 38
- 108010047303 von Willebrand Factor Proteins 0.000 claims description 37
- 229960004222 factor ix Drugs 0.000 claims description 36
- 102100036537 von Willebrand factor Human genes 0.000 claims description 36
- 229960001134 von willebrand factor Drugs 0.000 claims description 36
- 108010054265 Factor VIIa Proteins 0.000 claims description 35
- 229920001223 polyethylene glycol Polymers 0.000 claims description 35
- 239000002202 Polyethylene glycol Substances 0.000 claims description 34
- 230000008878 coupling Effects 0.000 claims description 34
- 238000010168 coupling process Methods 0.000 claims description 34
- 229940012414 factor viia Drugs 0.000 claims description 33
- JJYPMNFTHPTTDI-UHFFFAOYSA-N 3-methylaniline Chemical compound CC1=CC=CC(N)=C1 JJYPMNFTHPTTDI-UHFFFAOYSA-N 0.000 claims description 32
- 229920003169 water-soluble polymer Polymers 0.000 claims description 31
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 claims description 27
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 claims description 27
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 25
- 108010014173 Factor X Proteins 0.000 claims description 23
- 239000003153 chemical reaction reagent Substances 0.000 claims description 23
- 230000012010 growth Effects 0.000 claims description 23
- 102000005962 receptors Human genes 0.000 claims description 23
- 108020003175 receptors Proteins 0.000 claims description 23
- 239000002253 acid Substances 0.000 claims description 22
- 150000004702 methyl esters Chemical group 0.000 claims description 20
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 claims description 19
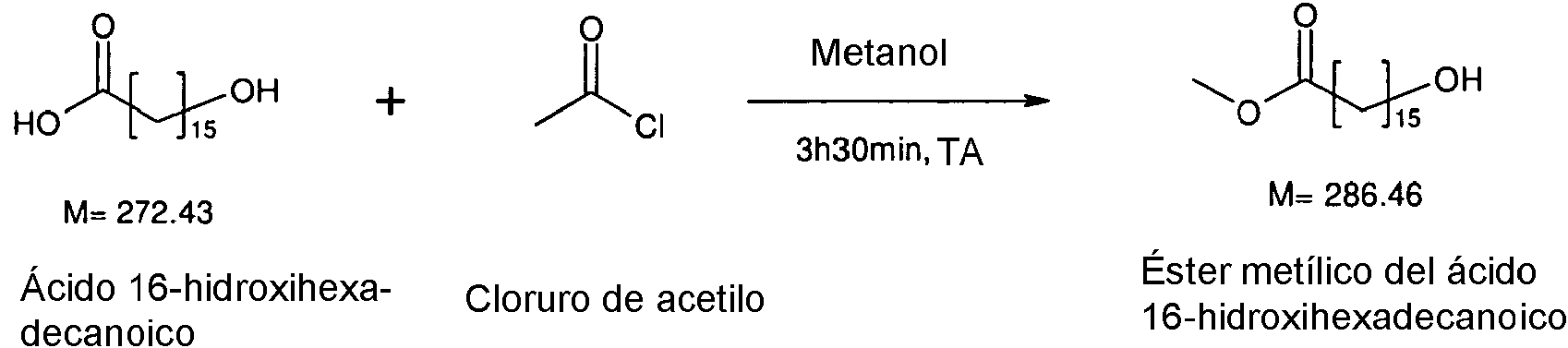
- UGAGPNKCDRTDHP-UHFFFAOYSA-N 16-hydroxyhexadecanoic acid Chemical compound OCCCCCCCCCCCCCCCC(O)=O UGAGPNKCDRTDHP-UHFFFAOYSA-N 0.000 claims description 18
- 108010080865 Factor XII Proteins 0.000 claims description 17
- 102000000429 Factor XII Human genes 0.000 claims description 17
- 239000000872 buffer Substances 0.000 claims description 17
- 230000021615 conjugation Effects 0.000 claims description 17
- 239000012011 nucleophilic catalyst Substances 0.000 claims description 17
- 108010014172 Factor V Proteins 0.000 claims description 16
- 102000008100 Human Serum Albumin Human genes 0.000 claims description 16
- 108091006905 Human Serum Albumin Proteins 0.000 claims description 16
- 235000014633 carbohydrates Nutrition 0.000 claims description 16
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 claims description 16
- AOTMRIXFFOGWDT-UHFFFAOYSA-N omega-hydroxyhexadecanoic acid methyl ester Natural products COC(=O)CCCCCCCCCCCCCCCO AOTMRIXFFOGWDT-UHFFFAOYSA-N 0.000 claims description 16
- 108010074864 Factor XI Proteins 0.000 claims description 15
- 108090000190 Thrombin Proteins 0.000 claims description 15
- 238000007254 oxidation reaction Methods 0.000 claims description 15
- 229960004072 thrombin Drugs 0.000 claims description 15
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 14
- 239000003795 chemical substances by application Substances 0.000 claims description 14
- 239000003102 growth factor Substances 0.000 claims description 14
- 230000003647 oxidation Effects 0.000 claims description 14
- JQWHASGSAFIOCM-UHFFFAOYSA-M sodium periodate Chemical compound [Na+].[O-]I(=O)(=O)=O JQWHASGSAFIOCM-UHFFFAOYSA-M 0.000 claims description 14
- 102000004127 Cytokines Human genes 0.000 claims description 13
- 108090000695 Cytokines Proteins 0.000 claims description 13
- 241000872931 Myoporum sandwicense Species 0.000 claims description 13
- 102000010780 Platelet-Derived Growth Factor Human genes 0.000 claims description 13
- 108010038512 Platelet-Derived Growth Factor Proteins 0.000 claims description 13
- 108010000499 Thromboplastin Proteins 0.000 claims description 13
- 102000002262 Thromboplastin Human genes 0.000 claims description 13
- 102000036693 Thrombopoietin Human genes 0.000 claims description 12
- 108010041111 Thrombopoietin Proteins 0.000 claims description 12
- 229920001612 Hydroxyethyl starch Polymers 0.000 claims description 11
- 108090001007 Interleukin-8 Proteins 0.000 claims description 11
- 102000004890 Interleukin-8 Human genes 0.000 claims description 11
- 230000015572 biosynthetic process Effects 0.000 claims description 11
- 239000012634 fragment Substances 0.000 claims description 11
- 229940050526 hydroxyethylstarch Drugs 0.000 claims description 11
- 150000004671 saturated fatty acids Chemical class 0.000 claims description 11
- 108010017080 Granulocyte Colony-Stimulating Factor Proteins 0.000 claims description 10
- 102000004269 Granulocyte Colony-Stimulating Factor Human genes 0.000 claims description 10
- 108010046938 Macrophage Colony-Stimulating Factor Proteins 0.000 claims description 10
- 102000007651 Macrophage Colony-Stimulating Factor Human genes 0.000 claims description 10
- 229920002472 Starch Polymers 0.000 claims description 10
- NKLCNNUWBJBICK-UHFFFAOYSA-N dess–martin periodinane Chemical compound C1=CC=C2I(OC(=O)C)(OC(C)=O)(OC(C)=O)OC(=O)C2=C1 NKLCNNUWBJBICK-UHFFFAOYSA-N 0.000 claims description 10
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 10
- 229920000233 poly(alkylene oxides) Polymers 0.000 claims description 10
- 229920001515 polyalkylene glycol Polymers 0.000 claims description 10
- 229920001451 polypropylene glycol Polymers 0.000 claims description 10
- 235000019698 starch Nutrition 0.000 claims description 10
- 239000008107 starch Substances 0.000 claims description 10
- 102000004877 Insulin Human genes 0.000 claims description 9
- 108090001061 Insulin Proteins 0.000 claims description 9
- 238000000338 in vitro Methods 0.000 claims description 9
- 238000001727 in vivo Methods 0.000 claims description 9
- 102000009027 Albumins Human genes 0.000 claims description 8
- 108010088751 Albumins Proteins 0.000 claims description 8
- 102000018233 Fibroblast Growth Factor Human genes 0.000 claims description 8
- 108050007372 Fibroblast Growth Factor Proteins 0.000 claims description 8
- 102000003956 Fibroblast growth factor 8 Human genes 0.000 claims description 8
- 108090000368 Fibroblast growth factor 8 Proteins 0.000 claims description 8
- 102000006992 Interferon-alpha Human genes 0.000 claims description 8
- 108010047761 Interferon-alpha Proteins 0.000 claims description 8
- 102100030703 Interleukin-22 Human genes 0.000 claims description 8
- 108090000630 Oncostatin M Proteins 0.000 claims description 8
- 102000004140 Oncostatin M Human genes 0.000 claims description 8
- 108010022233 Plasminogen Activator Inhibitor 1 Proteins 0.000 claims description 8
- 102100039418 Plasminogen activator inhibitor 1 Human genes 0.000 claims description 8
- 102000017975 Protein C Human genes 0.000 claims description 8
- 101800004937 Protein C Proteins 0.000 claims description 8
- 229940096437 Protein S Drugs 0.000 claims description 8
- 108010066124 Protein S Proteins 0.000 claims description 8
- 102000029301 Protein S Human genes 0.000 claims description 8
- 101800001700 Saposin-D Proteins 0.000 claims description 8
- 102100031294 Thymic stromal lymphopoietin Human genes 0.000 claims description 8
- 230000003213 activating effect Effects 0.000 claims description 8
- 229940125396 insulin Drugs 0.000 claims description 8
- 239000007800 oxidant agent Substances 0.000 claims description 8
- 229920002451 polyvinyl alcohol Polymers 0.000 claims description 8
- 229960000856 protein c Drugs 0.000 claims description 8
- LEHBURLTIWGHEM-UHFFFAOYSA-N pyridinium chlorochromate Chemical compound [O-][Cr](Cl)(=O)=O.C1=CC=[NH+]C=C1 LEHBURLTIWGHEM-UHFFFAOYSA-N 0.000 claims description 8
- 108010029307 thymic stromal lymphopoietin Proteins 0.000 claims description 8
- 235000021122 unsaturated fatty acids Nutrition 0.000 claims description 8
- 150000004670 unsaturated fatty acids Chemical class 0.000 claims description 8
- 229920002307 Dextran Polymers 0.000 claims description 7
- 102100035194 Placenta growth factor Human genes 0.000 claims description 7
- 108010073929 Vascular Endothelial Growth Factor A Proteins 0.000 claims description 7
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 claims description 7
- WETWJCDKMRHUPV-UHFFFAOYSA-N acetyl chloride Chemical compound CC(Cl)=O WETWJCDKMRHUPV-UHFFFAOYSA-N 0.000 claims description 7
- 239000012346 acetyl chloride Substances 0.000 claims description 7
- 150000002148 esters Chemical class 0.000 claims description 7
- HVBSAKJJOYLTQU-UHFFFAOYSA-N 4-aminobenzenesulfonic acid Chemical compound NC1=CC=C(S(O)(=O)=O)C=C1 HVBSAKJJOYLTQU-UHFFFAOYSA-N 0.000 claims description 6
- ALYNCZNDIQEVRV-UHFFFAOYSA-N 4-aminobenzoic acid Chemical compound NC1=CC=C(C(O)=O)C=C1 ALYNCZNDIQEVRV-UHFFFAOYSA-N 0.000 claims description 6
- 102400001368 Epidermal growth factor Human genes 0.000 claims description 6
- 101800003838 Epidermal growth factor Proteins 0.000 claims description 6
- 108090000386 Fibroblast Growth Factor 1 Proteins 0.000 claims description 6
- 102000003972 Fibroblast growth factor 7 Human genes 0.000 claims description 6
- 108090000385 Fibroblast growth factor 7 Proteins 0.000 claims description 6
- 102000004216 Glial cell line-derived neurotrophic factor receptors Human genes 0.000 claims description 6
- 108090000722 Glial cell line-derived neurotrophic factor receptors Proteins 0.000 claims description 6
- 101000911390 Homo sapiens Coagulation factor VIII Proteins 0.000 claims description 6
- 101000595923 Homo sapiens Placenta growth factor Proteins 0.000 claims description 6
- 108091008606 PDGF receptors Proteins 0.000 claims description 6
- 102000011653 Platelet-Derived Growth Factor Receptors Human genes 0.000 claims description 6
- 102000003990 Urokinase-type plasminogen activator Human genes 0.000 claims description 6
- 108090000435 Urokinase-type plasminogen activator Proteins 0.000 claims description 6
- RWZYAGGXGHYGMB-UHFFFAOYSA-N anthranilic acid Chemical compound NC1=CC=CC=C1C(O)=O RWZYAGGXGHYGMB-UHFFFAOYSA-N 0.000 claims description 6
- SQVRNKJHWKZAKO-UHFFFAOYSA-N beta-N-Acetyl-D-neuraminic acid Natural products CC(=O)NC1C(O)CC(O)(C(O)=O)OC1C(O)C(O)CO SQVRNKJHWKZAKO-UHFFFAOYSA-N 0.000 claims description 6
- 229940116977 epidermal growth factor Drugs 0.000 claims description 6
- 229940126864 fibroblast growth factor Drugs 0.000 claims description 6
- 150000004676 glycans Chemical class 0.000 claims description 6
- 125000004170 methylsulfonyl group Chemical group [H]C([H])([H])S(*)(=O)=O 0.000 claims description 6
- RNVCVTLRINQCPJ-UHFFFAOYSA-N o-toluidine Chemical compound CC1=CC=CC=C1N RNVCVTLRINQCPJ-UHFFFAOYSA-N 0.000 claims description 6
- RZXMPPFPUUCRFN-UHFFFAOYSA-N p-toluidine Chemical compound CC1=CC=C(N)C=C1 RZXMPPFPUUCRFN-UHFFFAOYSA-N 0.000 claims description 6
- 229920001282 polysaccharide Polymers 0.000 claims description 6
- 239000005017 polysaccharide Substances 0.000 claims description 6
- VBEQCZHXXJYVRD-GACYYNSASA-N uroanthelone Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CS)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)C(C)C)[C@@H](C)O)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CCSC)NC(=O)[C@H](CS)NC(=O)[C@@H](NC(=O)CNC(=O)CNC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CS)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CS)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O)C(C)C)[C@@H](C)CC)C1=CC=C(O)C=C1 VBEQCZHXXJYVRD-GACYYNSASA-N 0.000 claims description 6
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 claims description 5
- SQDAZGGFXASXDW-UHFFFAOYSA-N 5-bromo-2-(trifluoromethoxy)pyridine Chemical compound FC(F)(F)OC1=CC=C(Br)C=N1 SQDAZGGFXASXDW-UHFFFAOYSA-N 0.000 claims description 5
- 102100022987 Angiogenin Human genes 0.000 claims description 5
- 229920001661 Chitosan Polymers 0.000 claims description 5
- 229920001287 Chondroitin sulfate Polymers 0.000 claims description 5
- 102000016911 Deoxyribonucleases Human genes 0.000 claims description 5
- 108010053770 Deoxyribonucleases Proteins 0.000 claims description 5
- 229920000045 Dermatan sulfate Polymers 0.000 claims description 5
- 102000003745 Hepatocyte Growth Factor Human genes 0.000 claims description 5
- 108090000100 Hepatocyte Growth Factor Proteins 0.000 claims description 5
- 108090000723 Insulin-Like Growth Factor I Proteins 0.000 claims description 5
- 102000014150 Interferons Human genes 0.000 claims description 5
- 108010050904 Interferons Proteins 0.000 claims description 5
- 239000012359 Methanesulfonyl chloride Substances 0.000 claims description 5
- 102000007339 Nerve Growth Factor Receptors Human genes 0.000 claims description 5
- 108010032605 Nerve Growth Factor Receptors Proteins 0.000 claims description 5
- 239000004373 Pullulan Substances 0.000 claims description 5
- 229920001218 Pullulan Polymers 0.000 claims description 5
- 239000005482 chemotactic factor Substances 0.000 claims description 5
- 229940059329 chondroitin sulfate Drugs 0.000 claims description 5
- 229940051593 dermatan sulfate Drugs 0.000 claims description 5
- 229960002086 dextran Drugs 0.000 claims description 5
- 229920002674 hyaluronan Polymers 0.000 claims description 5
- 229960003160 hyaluronic acid Drugs 0.000 claims description 5
- 125000002768 hydroxyalkyl group Chemical group 0.000 claims description 5
- 208000032839 leukemia Diseases 0.000 claims description 5
- QARBMVPHQWIHKH-UHFFFAOYSA-N methanesulfonyl chloride Chemical compound CS(Cl)(=O)=O QARBMVPHQWIHKH-UHFFFAOYSA-N 0.000 claims description 5
- 210000000440 neutrophil Anatomy 0.000 claims description 5
- 230000001590 oxidative effect Effects 0.000 claims description 5
- 229920002627 poly(phosphazenes) Polymers 0.000 claims description 5
- 229920005646 polycarboxylate Polymers 0.000 claims description 5
- 229920000036 polyvinylpyrrolidone Polymers 0.000 claims description 5
- 239000001267 polyvinylpyrrolidone Substances 0.000 claims description 5
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 claims description 5
- 235000019423 pullulan Nutrition 0.000 claims description 5
- SQVRNKJHWKZAKO-OQPLDHBCSA-N sialic acid Chemical compound CC(=O)N[C@@H]1[C@@H](O)C[C@@](O)(C(O)=O)OC1[C@H](O)[C@H](O)CO SQVRNKJHWKZAKO-OQPLDHBCSA-N 0.000 claims description 5
- 229940032147 starch Drugs 0.000 claims description 5
- 210000000130 stem cell Anatomy 0.000 claims description 5
- 229960005356 urokinase Drugs 0.000 claims description 5
- ZIIUUSVHCHPIQD-UHFFFAOYSA-N 2,4,6-trimethyl-N-[3-(trifluoromethyl)phenyl]benzenesulfonamide Chemical compound CC1=CC(C)=CC(C)=C1S(=O)(=O)NC1=CC=CC(C(F)(F)F)=C1 ZIIUUSVHCHPIQD-UHFFFAOYSA-N 0.000 claims description 4
- YYROPELSRYBVMQ-UHFFFAOYSA-N 4-toluenesulfonyl chloride Chemical compound CC1=CC=C(S(Cl)(=O)=O)C=C1 YYROPELSRYBVMQ-UHFFFAOYSA-N 0.000 claims description 4
- 108010059616 Activins Proteins 0.000 claims description 4
- 108010081589 Becaplermin Proteins 0.000 claims description 4
- 102000004219 Brain-derived neurotrophic factor Human genes 0.000 claims description 4
- 108090000715 Brain-derived neurotrophic factor Proteins 0.000 claims description 4
- 108010008951 Chemokine CXCL12 Proteins 0.000 claims description 4
- 102000011022 Chorionic Gonadotropin Human genes 0.000 claims description 4
- 108010062540 Chorionic Gonadotropin Proteins 0.000 claims description 4
- 108010005939 Ciliary Neurotrophic Factor Proteins 0.000 claims description 4
- 102100031614 Ciliary neurotrophic factor Human genes 0.000 claims description 4
- 102100026735 Coagulation factor VIII Human genes 0.000 claims description 4
- 102400000686 Endothelin-1 Human genes 0.000 claims description 4
- 101800004490 Endothelin-1 Proteins 0.000 claims description 4
- 102100030323 Epigen Human genes 0.000 claims description 4
- 108010016906 Epigen Proteins 0.000 claims description 4
- 101800000155 Epiregulin Proteins 0.000 claims description 4
- 108010003471 Fetal Proteins Proteins 0.000 claims description 4
- 102000004641 Fetal Proteins Human genes 0.000 claims description 4
- 102100031706 Fibroblast growth factor 1 Human genes 0.000 claims description 4
- 102000004864 Fibroblast growth factor 10 Human genes 0.000 claims description 4
- 108090001047 Fibroblast growth factor 10 Proteins 0.000 claims description 4
- 102000014252 Fibroblast growth factor 11 Human genes 0.000 claims description 4
- 108050003237 Fibroblast growth factor 11 Proteins 0.000 claims description 4
- 102000014250 Fibroblast growth factor 12 Human genes 0.000 claims description 4
- 108050003239 Fibroblast growth factor 12 Proteins 0.000 claims description 4
- 102000012565 Fibroblast growth factor 17 Human genes 0.000 claims description 4
- 108050002074 Fibroblast growth factor 17 Proteins 0.000 claims description 4
- 102100031734 Fibroblast growth factor 19 Human genes 0.000 claims description 4
- 101710153349 Fibroblast growth factor 19 Proteins 0.000 claims description 4
- 102000003973 Fibroblast growth factor 21 Human genes 0.000 claims description 4
- 108090000376 Fibroblast growth factor 21 Proteins 0.000 claims description 4
- 102000003969 Fibroblast growth factor 4 Human genes 0.000 claims description 4
- 108090000381 Fibroblast growth factor 4 Proteins 0.000 claims description 4
- 102000003967 Fibroblast growth factor 5 Human genes 0.000 claims description 4
- 108090000380 Fibroblast growth factor 5 Proteins 0.000 claims description 4
- 102000003968 Fibroblast growth factor 6 Human genes 0.000 claims description 4
- 108090000382 Fibroblast growth factor 6 Proteins 0.000 claims description 4
- 102000003957 Fibroblast growth factor 9 Human genes 0.000 claims description 4
- 108090000367 Fibroblast growth factor 9 Proteins 0.000 claims description 4
- 102000012673 Follicle Stimulating Hormone Human genes 0.000 claims description 4
- 108010079345 Follicle Stimulating Hormone Proteins 0.000 claims description 4
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 claims description 4
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 claims description 4
- 101000998139 Homo sapiens Interleukin-32 Proteins 0.000 claims description 4
- 102100026818 Inhibin beta E chain Human genes 0.000 claims description 4
- 102100020881 Interleukin-1 alpha Human genes 0.000 claims description 4
- 102000003777 Interleukin-1 beta Human genes 0.000 claims description 4
- 108090000193 Interleukin-1 beta Proteins 0.000 claims description 4
- 108090000174 Interleukin-10 Proteins 0.000 claims description 4
- 102000003814 Interleukin-10 Human genes 0.000 claims description 4
- 108010065805 Interleukin-12 Proteins 0.000 claims description 4
- 108090000176 Interleukin-13 Proteins 0.000 claims description 4
- 102000003812 Interleukin-15 Human genes 0.000 claims description 4
- 108090000172 Interleukin-15 Proteins 0.000 claims description 4
- 101800003050 Interleukin-16 Proteins 0.000 claims description 4
- 102000013691 Interleukin-17 Human genes 0.000 claims description 4
- 108050003558 Interleukin-17 Proteins 0.000 claims description 4
- 108090000171 Interleukin-18 Proteins 0.000 claims description 4
- 108050009288 Interleukin-19 Proteins 0.000 claims description 4
- 108010082786 Interleukin-1alpha Proteins 0.000 claims description 4
- 108010065637 Interleukin-23 Proteins 0.000 claims description 4
- 108010002386 Interleukin-3 Proteins 0.000 claims description 4
- 101710181613 Interleukin-31 Proteins 0.000 claims description 4
- 108010067003 Interleukin-33 Proteins 0.000 claims description 4
- 108090000978 Interleukin-4 Proteins 0.000 claims description 4
- 102000004388 Interleukin-4 Human genes 0.000 claims description 4
- 108010002616 Interleukin-5 Proteins 0.000 claims description 4
- 108090001005 Interleukin-6 Proteins 0.000 claims description 4
- 102000004889 Interleukin-6 Human genes 0.000 claims description 4
- 108010002586 Interleukin-7 Proteins 0.000 claims description 4
- 108010002335 Interleukin-9 Proteins 0.000 claims description 4
- 108090001090 Lectins Proteins 0.000 claims description 4
- 102000004856 Lectins Human genes 0.000 claims description 4
- 108090001030 Lipoproteins Proteins 0.000 claims description 4
- 102000004895 Lipoproteins Human genes 0.000 claims description 4
- 102000009151 Luteinizing Hormone Human genes 0.000 claims description 4
- 108010073521 Luteinizing Hormone Proteins 0.000 claims description 4
- 102000004230 Neurotrophin 3 Human genes 0.000 claims description 4
- 108090000742 Neurotrophin 3 Proteins 0.000 claims description 4
- 102000003683 Neurotrophin-4 Human genes 0.000 claims description 4
- 108090000099 Neurotrophin-4 Proteins 0.000 claims description 4
- 108091005804 Peptidases Proteins 0.000 claims description 4
- 102000015439 Phospholipases Human genes 0.000 claims description 4
- 108010064785 Phospholipases Proteins 0.000 claims description 4
- 102000003946 Prolactin Human genes 0.000 claims description 4
- 108010057464 Prolactin Proteins 0.000 claims description 4
- 108010089836 Proto-Oncogene Proteins c-met Proteins 0.000 claims description 4
- 102000008022 Proto-Oncogene Proteins c-met Human genes 0.000 claims description 4
- 108010039491 Ricin Proteins 0.000 claims description 4
- 102000004584 Somatomedin Receptors Human genes 0.000 claims description 4
- 108010017622 Somatomedin Receptors Proteins 0.000 claims description 4
- 102100021669 Stromal cell-derived factor 1 Human genes 0.000 claims description 4
- 108010061174 Thyrotropin Proteins 0.000 claims description 4
- 102000011923 Thyrotropin Human genes 0.000 claims description 4
- 102000003978 Tissue Plasminogen Activator Human genes 0.000 claims description 4
- 108090000373 Tissue Plasminogen Activator Proteins 0.000 claims description 4
- 102000004338 Transferrin Human genes 0.000 claims description 4
- 108090000901 Transferrin Proteins 0.000 claims description 4
- 108060008682 Tumor Necrosis Factor Proteins 0.000 claims description 4
- 102100040247 Tumor necrosis factor Human genes 0.000 claims description 4
- 239000000488 activin Substances 0.000 claims description 4
- 108010023082 activin A Proteins 0.000 claims description 4
- 108010023079 activin B Proteins 0.000 claims description 4
- 229960002964 adalimumab Drugs 0.000 claims description 4
- 125000002344 aminooxy group Chemical group [H]N([H])O[*] 0.000 claims description 4
- 108010072788 angiogenin Proteins 0.000 claims description 4
- 229940077737 brain-derived neurotrophic factor Drugs 0.000 claims description 4
- 229940045110 chitosan Drugs 0.000 claims description 4
- 229940015047 chorionic gonadotropin Drugs 0.000 claims description 4
- 210000002919 epithelial cell Anatomy 0.000 claims description 4
- 229940011871 estrogen Drugs 0.000 claims description 4
- 239000000262 estrogen Substances 0.000 claims description 4
- 108060002885 fetuin Proteins 0.000 claims description 4
- 102000013361 fetuin Human genes 0.000 claims description 4
- 229940098448 fibroblast growth factor 7 Drugs 0.000 claims description 4
- 229940028334 follicle stimulating hormone Drugs 0.000 claims description 4
- 235000019410 glycyrrhizin Nutrition 0.000 claims description 4
- 229940048921 humira Drugs 0.000 claims description 4
- 238000011534 incubation Methods 0.000 claims description 4
- 102000006495 integrins Human genes 0.000 claims description 4
- 108010044426 integrins Proteins 0.000 claims description 4
- 229940079322 interferon Drugs 0.000 claims description 4
- 102000004114 interleukin 20 Human genes 0.000 claims description 4
- 108090000681 interleukin 20 Proteins 0.000 claims description 4
- 108010074108 interleukin-21 Proteins 0.000 claims description 4
- 108010074109 interleukin-22 Proteins 0.000 claims description 4
- 108090000237 interleukin-24 Proteins 0.000 claims description 4
- 239000002523 lectin Substances 0.000 claims description 4
- 229940040129 luteinizing hormone Drugs 0.000 claims description 4
- 229940032018 neurotrophin 3 Drugs 0.000 claims description 4
- 229940097998 neurotrophin 4 Drugs 0.000 claims description 4
- CTSLXHKWHWQRSH-UHFFFAOYSA-N oxalyl chloride Chemical compound ClC(=O)C(Cl)=O CTSLXHKWHWQRSH-UHFFFAOYSA-N 0.000 claims description 4
- 108010000685 platelet-derived growth factor AB Proteins 0.000 claims description 4
- 229920000765 poly(2-oxazolines) Polymers 0.000 claims description 4
- 229940097325 prolactin Drugs 0.000 claims description 4
- 229960000187 tissue plasminogen activator Drugs 0.000 claims description 4
- 239000012581 transferrin Substances 0.000 claims description 4
- CPEMIWRXQWEEGD-UHFFFAOYSA-N 16-[2-[2-[2-(2-aminooxyethoxy)ethoxy]ethoxy]ethoxyimino]hexadecanoic acid Chemical compound NOCCOCCOCCOCCON=CCCCCCCCCCCCCCCC(O)=O CPEMIWRXQWEEGD-UHFFFAOYSA-N 0.000 claims description 3
- PXBFMLJZNCDSMP-UHFFFAOYSA-N 2-Aminobenzamide Chemical compound NC(=O)C1=CC=CC=C1N PXBFMLJZNCDSMP-UHFFFAOYSA-N 0.000 claims description 3
- XFDUHJPVQKIXHO-UHFFFAOYSA-N 3-aminobenzoic acid Chemical compound NC1=CC=CC(C(O)=O)=C1 XFDUHJPVQKIXHO-UHFFFAOYSA-N 0.000 claims description 3
- 108010000063 Ciliary Neurotrophic Factor Receptor Proteins 0.000 claims description 3
- 102000016989 Ciliary Neurotrophic Factor Receptor Human genes 0.000 claims description 3
- 102000003974 Fibroblast growth factor 2 Human genes 0.000 claims description 3
- 108090000379 Fibroblast growth factor 2 Proteins 0.000 claims description 3
- 102000012558 Fibroblast growth factor 20 Human genes 0.000 claims description 3
- 108050002085 Fibroblast growth factor 20 Proteins 0.000 claims description 3
- 102100031000 Hepatoma-derived growth factor Human genes 0.000 claims description 3
- 102100037850 Interferon gamma Human genes 0.000 claims description 3
- 108010074328 Interferon-gamma Proteins 0.000 claims description 3
- 108010092277 Leptin Proteins 0.000 claims description 3
- 102000016267 Leptin Human genes 0.000 claims description 3
- AFBPFSWMIHJQDM-UHFFFAOYSA-N N-methyl-N-phenylamine Natural products CNC1=CC=CC=C1 AFBPFSWMIHJQDM-UHFFFAOYSA-N 0.000 claims description 3
- 108010025020 Nerve Growth Factor Proteins 0.000 claims description 3
- 102000015336 Nerve Growth Factor Human genes 0.000 claims description 3
- 239000004372 Polyvinyl alcohol Substances 0.000 claims description 3
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 claims description 3
- 102000016971 Proto-Oncogene Proteins c-kit Human genes 0.000 claims description 3
- 108010014608 Proto-Oncogene Proteins c-kit Proteins 0.000 claims description 3
- 101500026849 Rattus norvegicus C3a anaphylatoxin Proteins 0.000 claims description 3
- 102100031372 Thymidine phosphorylase Human genes 0.000 claims description 3
- 108700023160 Thymidine phosphorylases Proteins 0.000 claims description 3
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 claims description 3
- 108010031318 Vitronectin Proteins 0.000 claims description 3
- 102100035140 Vitronectin Human genes 0.000 claims description 3
- 229940050528 albumin Drugs 0.000 claims description 3
- 229960004050 aminobenzoic acid Drugs 0.000 claims description 3
- 125000004494 ethyl ester group Chemical group 0.000 claims description 3
- 102000003684 fibroblast growth factor 13 Human genes 0.000 claims description 3
- 108090000047 fibroblast growth factor 13 Proteins 0.000 claims description 3
- 230000010005 growth-factor like effect Effects 0.000 claims description 3
- 108010052188 hepatoma-derived growth factor Proteins 0.000 claims description 3
- 230000002401 inhibitory effect Effects 0.000 claims description 3
- 102000028416 insulin-like growth factor binding Human genes 0.000 claims description 3
- 108091022911 insulin-like growth factor binding Proteins 0.000 claims description 3
- NRYBAZVQPHGZNS-ZSOCWYAHSA-N leptin Chemical compound O=C([C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](N)CC(C)C)CCSC)N1CCC[C@H]1C(=O)NCC(=O)N[C@@H](CS)C(O)=O NRYBAZVQPHGZNS-ZSOCWYAHSA-N 0.000 claims description 3
- 229940039781 leptin Drugs 0.000 claims description 3
- UIYHCSCDARAPMG-UHFFFAOYSA-N methyl 16-[2-[2-[2-(2-aminooxyethoxy)ethoxy]ethoxy]ethoxyamino]hexadecanoate Chemical compound COC(=O)CCCCCCCCCCCCCCCNOCCOCCOCCOCCON UIYHCSCDARAPMG-UHFFFAOYSA-N 0.000 claims description 3
- VMPITZXILSNTON-UHFFFAOYSA-N o-anisidine Chemical compound COC1=CC=CC=C1N VMPITZXILSNTON-UHFFFAOYSA-N 0.000 claims description 3
- BHAAPTBBJKJZER-UHFFFAOYSA-N p-anisidine Chemical compound COC1=CC=C(N)C=C1 BHAAPTBBJKJZER-UHFFFAOYSA-N 0.000 claims description 3
- 239000011591 potassium Substances 0.000 claims description 3
- 229910052700 potassium Inorganic materials 0.000 claims description 3
- 159000000000 sodium salts Chemical class 0.000 claims description 3
- 229950000244 sulfanilic acid Drugs 0.000 claims description 3
- JXRGUPLJCCDGKG-UHFFFAOYSA-N 4-nitrobenzenesulfonyl chloride Chemical compound [O-][N+](=O)C1=CC=C(S(Cl)(=O)=O)C=C1 JXRGUPLJCCDGKG-UHFFFAOYSA-N 0.000 claims description 2
- 108090000669 Annexin A4 Proteins 0.000 claims description 2
- 102100034612 Annexin A4 Human genes 0.000 claims description 2
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 claims description 2
- 239000012027 Collins reagent Substances 0.000 claims description 2
- YXHKONLOYHBTNS-UHFFFAOYSA-N Diazomethane Chemical compound C=[N+]=[N-] YXHKONLOYHBTNS-UHFFFAOYSA-N 0.000 claims description 2
- 102000003971 Fibroblast Growth Factor 1 Human genes 0.000 claims description 2
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 claims description 2
- 239000004365 Protease Substances 0.000 claims description 2
- 229910052804 chromium Inorganic materials 0.000 claims description 2
- 239000011651 chromium Substances 0.000 claims description 2
- 229920000669 heparin Polymers 0.000 claims description 2
- 229960002897 heparin Drugs 0.000 claims description 2
- RCBVKBFIWMOMHF-UHFFFAOYSA-L hydroxy-(hydroxy(dioxo)chromio)oxy-dioxochromium;pyridine Chemical compound C1=CC=NC=C1.C1=CC=NC=C1.O[Cr](=O)(=O)O[Cr](O)(=O)=O RCBVKBFIWMOMHF-UHFFFAOYSA-L 0.000 claims description 2
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 claims description 2
- 210000002510 keratinocyte Anatomy 0.000 claims description 2
- NCBZRJODKRCREW-UHFFFAOYSA-N m-anisidine Chemical compound COC1=CC=CC(N)=C1 NCBZRJODKRCREW-UHFFFAOYSA-N 0.000 claims description 2
- 210000004498 neuroglial cell Anatomy 0.000 claims description 2
- NPRDHMWYZHSAHR-UHFFFAOYSA-N pyridine;trioxochromium Chemical compound O=[Cr](=O)=O.C1=CC=NC=C1.C1=CC=NC=C1 NPRDHMWYZHSAHR-UHFFFAOYSA-N 0.000 claims description 2
- OSBSFAARYOCBHB-UHFFFAOYSA-N tetrapropylammonium Chemical compound CCC[N+](CCC)(CCC)CCC OSBSFAARYOCBHB-UHFFFAOYSA-N 0.000 claims description 2
- 102100020880 Kit ligand Human genes 0.000 claims 2
- 101710177504 Kit ligand Proteins 0.000 claims 2
- 102100039037 Vascular endothelial growth factor A Human genes 0.000 claims 2
- ORILYTVJVMAKLC-UHFFFAOYSA-N Adamantane Natural products C1C(C2)CC3CC1CC2C3 ORILYTVJVMAKLC-UHFFFAOYSA-N 0.000 claims 1
- 102100034613 Annexin A2 Human genes 0.000 claims 1
- 108090000668 Annexin A2 Proteins 0.000 claims 1
- 102100034278 Annexin A6 Human genes 0.000 claims 1
- 108090000656 Annexin A6 Proteins 0.000 claims 1
- 101100452593 Caenorhabditis elegans ina-1 gene Proteins 0.000 claims 1
- 102400001329 Epiregulin Human genes 0.000 claims 1
- 102100037852 Insulin-like growth factor I Human genes 0.000 claims 1
- 108700021154 Metallothionein 3 Proteins 0.000 claims 1
- 102100028708 Metallothionein-3 Human genes 0.000 claims 1
- 102000013566 Plasminogen Human genes 0.000 claims 1
- 108010051456 Plasminogen Proteins 0.000 claims 1
- 102100040990 Platelet-derived growth factor subunit B Human genes 0.000 claims 1
- 101710103494 Platelet-derived growth factor subunit B Proteins 0.000 claims 1
- 102100037486 Reverse transcriptase/ribonuclease H Human genes 0.000 claims 1
- 206010054094 Tumour necrosis Diseases 0.000 claims 1
- AVJBPWGFOQAPRH-FWMKGIEWSA-L dermatan sulfate Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@H](OS([O-])(=O)=O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O)[C@H](C([O-])=O)O1 AVJBPWGFOQAPRH-FWMKGIEWSA-L 0.000 claims 1
- JEHCHYAKAXDFKV-UHFFFAOYSA-J lead tetraacetate Chemical compound CC(=O)O[Pb](OC(C)=O)(OC(C)=O)OC(C)=O JEHCHYAKAXDFKV-UHFFFAOYSA-J 0.000 claims 1
- 235000018102 proteins Nutrition 0.000 description 268
- 239000000243 solution Substances 0.000 description 37
- 239000000203 mixture Substances 0.000 description 35
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 34
- 238000006243 chemical reaction Methods 0.000 description 28
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 27
- 238000002360 preparation method Methods 0.000 description 23
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 21
- 230000023555 blood coagulation Effects 0.000 description 21
- 108010023321 Factor VII Proteins 0.000 description 20
- 102100023804 Coagulation factor VII Human genes 0.000 description 19
- 229940053200 antiepileptics fatty acid derivative Drugs 0.000 description 19
- 229940012413 factor vii Drugs 0.000 description 18
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 17
- 239000011780 sodium chloride Substances 0.000 description 17
- 125000003277 amino group Chemical group 0.000 description 14
- 239000000047 product Substances 0.000 description 14
- 239000011541 reaction mixture Substances 0.000 description 14
- 210000002381 plasma Anatomy 0.000 description 13
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 12
- 125000003275 alpha amino acid group Chemical group 0.000 description 11
- 229940024606 amino acid Drugs 0.000 description 11
- 239000003814 drug Substances 0.000 description 11
- 102000003886 Glycoproteins Human genes 0.000 description 10
- 108090000288 Glycoproteins Proteins 0.000 description 10
- 150000001413 amino acids Chemical class 0.000 description 10
- 238000006467 substitution reaction Methods 0.000 description 10
- 102000014914 Carrier Proteins Human genes 0.000 description 9
- 239000007864 aqueous solution Substances 0.000 description 9
- 108091008324 binding proteins Proteins 0.000 description 9
- 238000003786 synthesis reaction Methods 0.000 description 9
- NQTADLQHYWFPDB-UHFFFAOYSA-N N-Hydroxysuccinimide Chemical group ON1C(=O)CCC1=O NQTADLQHYWFPDB-UHFFFAOYSA-N 0.000 description 8
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 8
- 230000004913 activation Effects 0.000 description 8
- 229940079593 drug Drugs 0.000 description 8
- 230000000694 effects Effects 0.000 description 8
- 229920000642 polymer Polymers 0.000 description 8
- 108091033319 polynucleotide Proteins 0.000 description 8
- 102000040430 polynucleotide Human genes 0.000 description 8
- 239000002157 polynucleotide Substances 0.000 description 8
- 125000003396 thiol group Chemical group [H]S* 0.000 description 8
- 235000013878 L-cysteine Nutrition 0.000 description 7
- 239000004201 L-cysteine Substances 0.000 description 7
- 241000124008 Mammalia Species 0.000 description 7
- 230000004071 biological effect Effects 0.000 description 7
- 150000001875 compounds Chemical class 0.000 description 7
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 7
- 125000000524 functional group Chemical group 0.000 description 7
- 239000013598 vector Substances 0.000 description 7
- LAJAPQAOBXMVOH-UHFFFAOYSA-N 16-[2-[2-[2-(2-aminooxyethoxy)ethoxy]ethoxy]ethoxyamino]hexadecanoic acid Chemical compound NOCCOCCOCCOCCONCCCCCCCCCCCCCCCC(=O)O LAJAPQAOBXMVOH-UHFFFAOYSA-N 0.000 description 6
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 6
- 108010008165 Etanercept Proteins 0.000 description 6
- 206010065042 Immune reconstitution inflammatory syndrome Diseases 0.000 description 6
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 6
- 210000004027 cell Anatomy 0.000 description 6
- 230000007812 deficiency Effects 0.000 description 6
- 230000014509 gene expression Effects 0.000 description 6
- IPCSVZSSVZVIGE-UHFFFAOYSA-N hexadecanoic acid Chemical compound CCCCCCCCCCCCCCCC(O)=O IPCSVZSSVZVIGE-UHFFFAOYSA-N 0.000 description 6
- 150000007523 nucleic acids Chemical class 0.000 description 6
- 150000003904 phospholipids Chemical class 0.000 description 6
- OXCMYAYHXIHQOA-UHFFFAOYSA-N potassium;[2-butyl-5-chloro-3-[[4-[2-(1,2,4-triaza-3-azanidacyclopenta-1,4-dien-5-yl)phenyl]phenyl]methyl]imidazol-4-yl]methanol Chemical compound [K+].CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C2=N[N-]N=N2)C=C1 OXCMYAYHXIHQOA-UHFFFAOYSA-N 0.000 description 6
- 239000000523 sample Substances 0.000 description 6
- 239000000741 silica gel Substances 0.000 description 6
- 229910002027 silica gel Inorganic materials 0.000 description 6
- 102000043853 ADAMTS13 Human genes 0.000 description 5
- 108091005670 ADAMTS13 Proteins 0.000 description 5
- 102000015081 Blood Coagulation Factors Human genes 0.000 description 5
- 108010039209 Blood Coagulation Factors Proteins 0.000 description 5
- 0 CC=CC(NC(*)O)=CC#C Chemical compound CC=CC(NC(*)O)=CC#C 0.000 description 5
- 108010092408 Eosinophil Peroxidase Proteins 0.000 description 5
- 102100031939 Erythropoietin Human genes 0.000 description 5
- 108010048049 Factor IXa Proteins 0.000 description 5
- 102000012479 Serine Proteases Human genes 0.000 description 5
- 108010022999 Serine Proteases Proteins 0.000 description 5
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 5
- 229930003448 Vitamin K Natural products 0.000 description 5
- 102000015395 alpha 1-Antitrypsin Human genes 0.000 description 5
- 108010050122 alpha 1-Antitrypsin Proteins 0.000 description 5
- 238000005571 anion exchange chromatography Methods 0.000 description 5
- 238000013459 approach Methods 0.000 description 5
- 239000003114 blood coagulation factor Substances 0.000 description 5
- 230000003197 catalytic effect Effects 0.000 description 5
- 229940105778 coagulation factor viii Drugs 0.000 description 5
- 239000012043 crude product Substances 0.000 description 5
- 238000012217 deletion Methods 0.000 description 5
- 230000037430 deletion Effects 0.000 description 5
- 201000010099 disease Diseases 0.000 description 5
- 210000002950 fibroblast Anatomy 0.000 description 5
- 230000013595 glycosylation Effects 0.000 description 5
- 238000006206 glycosylation reaction Methods 0.000 description 5
- 208000031169 hemorrhagic disease Diseases 0.000 description 5
- 230000002163 immunogen Effects 0.000 description 5
- 238000003780 insertion Methods 0.000 description 5
- 230000037431 insertion Effects 0.000 description 5
- 238000001990 intravenous administration Methods 0.000 description 5
- 239000012528 membrane Substances 0.000 description 5
- 108020004707 nucleic acids Proteins 0.000 description 5
- 102000039446 nucleic acids Human genes 0.000 description 5
- 239000008194 pharmaceutical composition Substances 0.000 description 5
- SHUZOJHMOBOZST-UHFFFAOYSA-N phylloquinone Natural products CC(C)CCCCC(C)CCC(C)CCCC(=CCC1=C(C)C(=O)c2ccccc2C1=O)C SHUZOJHMOBOZST-UHFFFAOYSA-N 0.000 description 5
- 239000007858 starting material Substances 0.000 description 5
- 239000000126 substance Substances 0.000 description 5
- 235000019168 vitamin K Nutrition 0.000 description 5
- 239000011712 vitamin K Substances 0.000 description 5
- 150000003721 vitamin K derivatives Chemical class 0.000 description 5
- 229940046010 vitamin k Drugs 0.000 description 5
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 4
- 238000002965 ELISA Methods 0.000 description 4
- 102000004190 Enzymes Human genes 0.000 description 4
- 108090000790 Enzymes Proteins 0.000 description 4
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 4
- 108010074860 Factor Xa Proteins 0.000 description 4
- 208000009292 Hemophilia A Diseases 0.000 description 4
- 108010002350 Interleukin-2 Proteins 0.000 description 4
- 102000000588 Interleukin-2 Human genes 0.000 description 4
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 4
- 150000001299 aldehydes Chemical class 0.000 description 4
- AVJBPWGFOQAPRH-FWMKGIEWSA-N alpha-L-IdopA-(1->3)-beta-D-GalpNAc4S Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@H](OS(O)(=O)=O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O)[C@H](C(O)=O)O1 AVJBPWGFOQAPRH-FWMKGIEWSA-N 0.000 description 4
- 125000000539 amino acid group Chemical group 0.000 description 4
- 239000012298 atmosphere Substances 0.000 description 4
- 239000001110 calcium chloride Substances 0.000 description 4
- 229910001628 calcium chloride Inorganic materials 0.000 description 4
- 229910052799 carbon Inorganic materials 0.000 description 4
- 239000003054 catalyst Substances 0.000 description 4
- 238000004587 chromatography analysis Methods 0.000 description 4
- 238000003776 cleavage reaction Methods 0.000 description 4
- 230000015271 coagulation Effects 0.000 description 4
- 238000005345 coagulation Methods 0.000 description 4
- 230000003247 decreasing effect Effects 0.000 description 4
- 238000010586 diagram Methods 0.000 description 4
- POULHZVOKOAJMA-UHFFFAOYSA-N dodecanoic acid Chemical compound CCCCCCCCCCCC(O)=O POULHZVOKOAJMA-UHFFFAOYSA-N 0.000 description 4
- 210000002889 endothelial cell Anatomy 0.000 description 4
- 229940088598 enzyme Drugs 0.000 description 4
- UHBYWPGGCSDKFX-VKHMYHEASA-N gamma-carboxy-L-glutamic acid Chemical group OC(=O)[C@@H](N)CC(C(O)=O)C(O)=O UHBYWPGGCSDKFX-VKHMYHEASA-N 0.000 description 4
- 208000009429 hemophilia B Diseases 0.000 description 4
- 238000009396 hybridization Methods 0.000 description 4
- VKOBVWXKNCXXDE-UHFFFAOYSA-N icosanoic acid Chemical compound CCCCCCCCCCCCCCCCCCCC(O)=O VKOBVWXKNCXXDE-UHFFFAOYSA-N 0.000 description 4
- 239000007924 injection Substances 0.000 description 4
- 238000002347 injection Methods 0.000 description 4
- 150000002632 lipids Chemical class 0.000 description 4
- 125000003588 lysine group Chemical group [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 4
- 239000002773 nucleotide Substances 0.000 description 4
- 125000003729 nucleotide group Chemical group 0.000 description 4
- 238000000746 purification Methods 0.000 description 4
- 230000007017 scission Effects 0.000 description 4
- 239000007787 solid Substances 0.000 description 4
- 238000002560 therapeutic procedure Methods 0.000 description 4
- 208000012137 von Willebrand disease (hereditary or acquired) Diseases 0.000 description 4
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 3
- BHPQYMZQTOCNFJ-UHFFFAOYSA-N Calcium cation Chemical compound [Ca+2] BHPQYMZQTOCNFJ-UHFFFAOYSA-N 0.000 description 3
- 102100028892 Cardiotrophin-1 Human genes 0.000 description 3
- 108020004414 DNA Proteins 0.000 description 3
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 3
- 102000010911 Enzyme Precursors Human genes 0.000 description 3
- 108010062466 Enzyme Precursors Proteins 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical group OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- 201000003542 Factor VIII deficiency Diseases 0.000 description 3
- 108010080805 Factor XIa Proteins 0.000 description 3
- 238000005642 Gabriel synthesis reaction Methods 0.000 description 3
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 3
- 108060003951 Immunoglobulin Proteins 0.000 description 3
- 108010089308 Insulin Detemir Proteins 0.000 description 3
- 102000004218 Insulin-Like Growth Factor I Human genes 0.000 description 3
- 102100026720 Interferon beta Human genes 0.000 description 3
- 108090000467 Interferon-beta Proteins 0.000 description 3
- 108090000177 Interleukin-11 Proteins 0.000 description 3
- 102000003815 Interleukin-11 Human genes 0.000 description 3
- 102000000646 Interleukin-3 Human genes 0.000 description 3
- 102000000743 Interleukin-5 Human genes 0.000 description 3
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 3
- 102000004058 Leukemia inhibitory factor Human genes 0.000 description 3
- 108090000581 Leukemia inhibitory factor Proteins 0.000 description 3
- 235000021314 Palmitic acid Nutrition 0.000 description 3
- 102000035195 Peptidases Human genes 0.000 description 3
- 102100025498 Proepiregulin Human genes 0.000 description 3
- 108020004511 Recombinant DNA Proteins 0.000 description 3
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 3
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical class [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 208000027276 Von Willebrand disease Diseases 0.000 description 3
- 150000001412 amines Chemical class 0.000 description 3
- 150000001448 anilines Chemical class 0.000 description 3
- 239000011575 calcium Substances 0.000 description 3
- 229910052791 calcium Inorganic materials 0.000 description 3
- 229910001424 calcium ion Inorganic materials 0.000 description 3
- 108010041776 cardiotrophin 1 Proteins 0.000 description 3
- 238000004440 column chromatography Methods 0.000 description 3
- 239000002299 complementary DNA Substances 0.000 description 3
- 230000007547 defect Effects 0.000 description 3
- 229960001251 denosumab Drugs 0.000 description 3
- 230000001419 dependent effect Effects 0.000 description 3
- 238000001514 detection method Methods 0.000 description 3
- 238000011026 diafiltration Methods 0.000 description 3
- 150000002009 diols Chemical group 0.000 description 3
- 239000003937 drug carrier Substances 0.000 description 3
- 238000001035 drying Methods 0.000 description 3
- 229940073621 enbrel Drugs 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 229960000403 etanercept Drugs 0.000 description 3
- 108020001507 fusion proteins Proteins 0.000 description 3
- 102000037865 fusion proteins Human genes 0.000 description 3
- 238000001879 gelation Methods 0.000 description 3
- 238000006698 hydrazinolysis reaction Methods 0.000 description 3
- 102000018358 immunoglobulin Human genes 0.000 description 3
- 238000007918 intramuscular administration Methods 0.000 description 3
- 230000006623 intrinsic pathway Effects 0.000 description 3
- UGOZVNFCFYTPAZ-IOXYNQHNSA-N levemir Chemical group CCCCCCCCCCCCCC(=O)NCCCC[C@@H](C(O)=O)NC(=O)[C@@H]1CCCN1C(=O)[C@H]([C@@H](C)O)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)CNC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@H]1NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=2C=CC(O)=CC=2)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=2N=CNC=2)NC(=O)[C@H](CO)NC(=O)CNC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=2N=CNC=2)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@@H](NC(=O)[C@@H](N)CC=2C=CC=CC=2)C(C)C)CSSC[C@@H]2NC(=O)[C@@H](NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@@H](NC(=O)CN)[C@@H](C)CC)C(C)C)CSSC[C@H](NC(=O)[C@H]([C@@H](C)CC)NC(=O)[C@H](CO)NC(=O)[C@H]([C@@H](C)O)NC2=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC=2C=CC(O)=CC=2)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=2C=CC(O)=CC=2)C(=O)N[C@@H](CSSC1)C(=O)N[C@@H](CC(N)=O)C(O)=O)CC1=CC=C(O)C=C1 UGOZVNFCFYTPAZ-IOXYNQHNSA-N 0.000 description 3
- 210000004962 mammalian cell Anatomy 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- ZUSSTQCWRDLYJA-UMRXKNAASA-N n-hydroxy-5-norbornene-2,3-dicarboxylic acid imide Chemical compound C([C@@H]1C=C2)[C@@H]2[C@@H]2[C@H]1C(=O)N(O)C2=O ZUSSTQCWRDLYJA-UMRXKNAASA-N 0.000 description 3
- 239000012074 organic phase Substances 0.000 description 3
- 238000006053 organic reaction Methods 0.000 description 3
- 230000037361 pathway Effects 0.000 description 3
- 230000006320 pegylation Effects 0.000 description 3
- KHIWWQKSHDUIBK-UHFFFAOYSA-N periodic acid Chemical compound OI(=O)(=O)=O KHIWWQKSHDUIBK-UHFFFAOYSA-N 0.000 description 3
- NMHMNPHRMNGLLB-UHFFFAOYSA-N phloretic acid Chemical compound OC(=O)CCC1=CC=C(O)C=C1 NMHMNPHRMNGLLB-UHFFFAOYSA-N 0.000 description 3
- 230000036470 plasma concentration Effects 0.000 description 3
- 239000002243 precursor Substances 0.000 description 3
- 150000003141 primary amines Chemical class 0.000 description 3
- 230000009465 prokaryotic expression Effects 0.000 description 3
- 229940092597 prolia Drugs 0.000 description 3
- 239000011535 reaction buffer Substances 0.000 description 3
- 230000002829 reductive effect Effects 0.000 description 3
- 238000011160 research Methods 0.000 description 3
- 229910052938 sodium sulfate Inorganic materials 0.000 description 3
- 235000011152 sodium sulphate Nutrition 0.000 description 3
- 238000007614 solvation Methods 0.000 description 3
- 239000011877 solvent mixture Substances 0.000 description 3
- 230000002792 vascular Effects 0.000 description 3
- 208000017129 von Willebrand disease 2 Diseases 0.000 description 3
- YWWVWXASSLXJHU-AATRIKPKSA-N (9E)-tetradecenoic acid Chemical compound CCCC\C=C\CCCCCCCC(O)=O YWWVWXASSLXJHU-AATRIKPKSA-N 0.000 description 2
- 125000003088 (fluoren-9-ylmethoxy)carbonyl group Chemical group 0.000 description 2
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 2
- VVQWXWRLWZLELC-UHFFFAOYSA-N 16-oxo-octadecanoic acid Chemical compound CCC(=O)CCCCCCCCCCCCCCC(O)=O VVQWXWRLWZLELC-UHFFFAOYSA-N 0.000 description 2
- 102000029750 ADAMTS Human genes 0.000 description 2
- 108091022879 ADAMTS Proteins 0.000 description 2
- 208000035657 Abasia Diseases 0.000 description 2
- 108700028369 Alleles Proteins 0.000 description 2
- 102000007644 Colony-Stimulating Factors Human genes 0.000 description 2
- 108010071942 Colony-Stimulating Factors Proteins 0.000 description 2
- IMROMDMJAWUWLK-UHFFFAOYSA-N Ethenol Chemical compound OC=C IMROMDMJAWUWLK-UHFFFAOYSA-N 0.000 description 2
- 108010000196 Factor XIIIa Proteins 0.000 description 2
- 108010071241 Factor XIIa Proteins 0.000 description 2
- 108010073385 Fibrin Proteins 0.000 description 2
- 102000009123 Fibrin Human genes 0.000 description 2
- BWGVNKXGVNDBDI-UHFFFAOYSA-N Fibrin monomer Chemical compound CNC(=O)CNC(=O)CN BWGVNKXGVNDBDI-UHFFFAOYSA-N 0.000 description 2
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- 101000871708 Homo sapiens Proheparin-binding EGF-like growth factor Proteins 0.000 description 2
- 108090001117 Insulin-Like Growth Factor II Proteins 0.000 description 2
- 102100025947 Insulin-like growth factor II Human genes 0.000 description 2
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 2
- 101710167887 Major outer membrane protein P.IA Proteins 0.000 description 2
- 101710167885 Major outer membrane protein P.IB Proteins 0.000 description 2
- 238000006751 Mitsunobu reaction Methods 0.000 description 2
- TUNFSRHWOTWDNC-UHFFFAOYSA-N Myristic acid Natural products CCCCCCCCCCCCCC(O)=O TUNFSRHWOTWDNC-UHFFFAOYSA-N 0.000 description 2
- 229910019142 PO4 Inorganic materials 0.000 description 2
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 2
- 101000882917 Penaeus paulensis Hemolymph clottable protein Proteins 0.000 description 2
- 102000003992 Peroxidases Human genes 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- 102100033762 Proheparin-binding EGF-like growth factor Human genes 0.000 description 2
- 108010076504 Protein Sorting Signals Proteins 0.000 description 2
- 239000012564 Q sepharose fast flow resin Substances 0.000 description 2
- 239000012614 Q-Sepharose Substances 0.000 description 2
- PXIPVTKHYLBLMZ-UHFFFAOYSA-N Sodium azide Chemical compound [Na+].[N-]=[N+]=[N-] PXIPVTKHYLBLMZ-UHFFFAOYSA-N 0.000 description 2
- 235000021355 Stearic acid Nutrition 0.000 description 2
- 102100033732 Tumor necrosis factor receptor superfamily member 1A Human genes 0.000 description 2
- 101710187743 Tumor necrosis factor receptor superfamily member 1A Proteins 0.000 description 2
- 101710187830 Tumor necrosis factor receptor superfamily member 1B Proteins 0.000 description 2
- 102100033733 Tumor necrosis factor receptor superfamily member 1B Human genes 0.000 description 2
- 208000010287 Type 3 von Willebrand Disease Diseases 0.000 description 2
- 102000004504 Urokinase Plasminogen Activator Receptors Human genes 0.000 description 2
- 108010042352 Urokinase Plasminogen Activator Receptors Proteins 0.000 description 2
- 230000002776 aggregation Effects 0.000 description 2
- 238000004220 aggregation Methods 0.000 description 2
- 239000000427 antigen Substances 0.000 description 2
- 108091007433 antigens Proteins 0.000 description 2
- 102000036639 antigens Human genes 0.000 description 2
- YZXBAPSDXZZRGB-DOFZRALJSA-N arachidonic acid Chemical compound CCCCC\C=C/C\C=C/C\C=C/C\C=C/CCCC(O)=O YZXBAPSDXZZRGB-DOFZRALJSA-N 0.000 description 2
- DCXYFEDJOCDNAF-UHFFFAOYSA-M asparaginate Chemical compound [O-]C(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-M 0.000 description 2
- 150000001540 azides Chemical class 0.000 description 2
- 230000001580 bacterial effect Effects 0.000 description 2
- 239000002585 base Substances 0.000 description 2
- VYLDEYYOISNGST-UHFFFAOYSA-N bissulfosuccinimidyl suberate Chemical compound O=C1C(S(=O)(=O)O)CC(=O)N1OC(=O)CCCCCCC(=O)ON1C(=O)C(S(O)(=O)=O)CC1=O VYLDEYYOISNGST-UHFFFAOYSA-N 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 229940019700 blood coagulation factors Drugs 0.000 description 2
- 239000012267 brine Substances 0.000 description 2
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 2
- 238000012512 characterization method Methods 0.000 description 2
- 238000007385 chemical modification Methods 0.000 description 2
- 229940105774 coagulation factor ix Drugs 0.000 description 2
- 229940047120 colony stimulating factors Drugs 0.000 description 2
- 239000012141 concentrate Substances 0.000 description 2
- 239000003431 cross linking reagent Substances 0.000 description 2
- 238000010612 desalination reaction Methods 0.000 description 2
- 239000012538 diafiltration buffer Substances 0.000 description 2
- 208000035475 disorder Diseases 0.000 description 2
- 210000003527 eukaryotic cell Anatomy 0.000 description 2
- 239000013604 expression vector Substances 0.000 description 2
- 229950003499 fibrin Drugs 0.000 description 2
- 239000007850 fluorescent dye Substances 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 230000023597 hemostasis Effects 0.000 description 2
- 229940088597 hormone Drugs 0.000 description 2
- 229940072221 immunoglobulins Drugs 0.000 description 2
- 238000000099 in vitro assay Methods 0.000 description 2
- 239000003112 inhibitor Substances 0.000 description 2
- 229960003948 insulin detemir Drugs 0.000 description 2
- 102000002467 interleukin receptors Human genes 0.000 description 2
- 108010093036 interleukin receptors Proteins 0.000 description 2
- 238000005342 ion exchange Methods 0.000 description 2
- 229960000310 isoleucine Drugs 0.000 description 2
- ACKFDYCQCBEDNU-UHFFFAOYSA-J lead(2+);tetraacetate Chemical compound [Pb+2].CC([O-])=O.CC([O-])=O.CC([O-])=O.CC([O-])=O ACKFDYCQCBEDNU-UHFFFAOYSA-J 0.000 description 2
- 125000005439 maleimidyl group Chemical group C1(C=CC(N1*)=O)=O 0.000 description 2
- 238000004949 mass spectrometry Methods 0.000 description 2
- XHBGHEJULUAFGB-UHFFFAOYSA-N methyl 16-aminohexadecanoate Chemical compound COC(=O)CCCCCCCCCCCCCCCN XHBGHEJULUAFGB-UHFFFAOYSA-N 0.000 description 2
- GMQGZTCXTJPUFT-UHFFFAOYSA-N methyl 16-azidohexadecanoate Chemical compound COC(=O)CCCCCCCCCCCCCCCN=[N+]=[N-] GMQGZTCXTJPUFT-UHFFFAOYSA-N 0.000 description 2
- ZYTQDEJMRYPSHE-UHFFFAOYSA-N methyl 16-bromohexadecanoate Chemical compound COC(=O)CCCCCCCCCCCCCCCBr ZYTQDEJMRYPSHE-UHFFFAOYSA-N 0.000 description 2
- YPUALSULGZTUCP-UHFFFAOYSA-N methyl 16-methylsulfonylhexadecanoate Chemical group COC(=O)CCCCCCCCCCCCCCCS(C)(=O)=O YPUALSULGZTUCP-UHFFFAOYSA-N 0.000 description 2
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 2
- 102000035118 modified proteins Human genes 0.000 description 2
- 108091005573 modified proteins Proteins 0.000 description 2
- 239000000178 monomer Substances 0.000 description 2
- 230000035772 mutation Effects 0.000 description 2
- WQEPLUUGTLDZJY-UHFFFAOYSA-N n-Pentadecanoic acid Natural products CCCCCCCCCCCCCCC(O)=O WQEPLUUGTLDZJY-UHFFFAOYSA-N 0.000 description 2
- 210000005036 nerve Anatomy 0.000 description 2
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 2
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 2
- SECPZKHBENQXJG-FPLPWBNLSA-N palmitoleic acid Chemical compound CCCCCC\C=C/CCCCCCCC(O)=O SECPZKHBENQXJG-FPLPWBNLSA-N 0.000 description 2
- 108040007629 peroxidase activity proteins Proteins 0.000 description 2
- 230000003285 pharmacodynamic effect Effects 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 2
- 239000010452 phosphate Substances 0.000 description 2
- 230000017854 proteolysis Effects 0.000 description 2
- 230000002797 proteolythic effect Effects 0.000 description 2
- 229940024999 proteolytic enzymes for treatment of wounds and ulcers Drugs 0.000 description 2
- 108010013773 recombinant FVIIa Proteins 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 238000006722 reduction reaction Methods 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- 239000004627 regenerated cellulose Substances 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- IFZDQOGVPCSJPN-UHFFFAOYSA-M sodium;16-[2-[2-[2-(2-aminooxyethoxy)ethoxy]ethoxy]ethoxyimino]hexadecanoate Chemical compound [Na+].NOCCOCCOCCOCCON=CCCCCCCCCCCCCCCC([O-])=O IFZDQOGVPCSJPN-UHFFFAOYSA-M 0.000 description 2
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 125000006850 spacer group Chemical group 0.000 description 2
- 230000004936 stimulating effect Effects 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 2
- 208000015316 von Willebrand disease 3 Diseases 0.000 description 2
- 239000011534 wash buffer Substances 0.000 description 2
- PGOHTUIFYSHAQG-LJSDBVFPSA-N (2S)-6-amino-2-[[(2S)-5-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-4-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-5-amino-2-[[(2S)-5-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S,3R)-2-[[(2S)-5-amino-2-[[(2S)-2-[[(2S)-2-[[(2S,3R)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-5-amino-2-[[(2S)-1-[(2S,3R)-2-[[(2S)-2-[[(2S)-2-[[(2R)-2-[[(2S)-2-[[(2S)-2-[[2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-1-[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-amino-4-methylsulfanylbutanoyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-5-carbamimidamidopentanoyl]amino]propanoyl]pyrrolidine-2-carbonyl]amino]-3-methylbutanoyl]amino]-4-methylpentanoyl]amino]-4-methylpentanoyl]amino]acetyl]amino]-3-hydroxypropanoyl]amino]-4-methylpentanoyl]amino]-3-sulfanylpropanoyl]amino]-4-methylsulfanylbutanoyl]amino]-5-carbamimidamidopentanoyl]amino]-3-hydroxybutanoyl]pyrrolidine-2-carbonyl]amino]-5-oxopentanoyl]amino]-3-hydroxypropanoyl]amino]-3-hydroxypropanoyl]amino]-3-(1H-imidazol-5-yl)propanoyl]amino]-4-methylpentanoyl]amino]-3-hydroxybutanoyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-5-carbamimidamidopentanoyl]amino]-5-oxopentanoyl]amino]-3-hydroxybutanoyl]amino]-3-hydroxypropanoyl]amino]-3-carboxypropanoyl]amino]-3-hydroxypropanoyl]amino]-5-oxopentanoyl]amino]-5-oxopentanoyl]amino]-3-phenylpropanoyl]amino]-5-carbamimidamidopentanoyl]amino]-3-methylbutanoyl]amino]-4-methylpentanoyl]amino]-4-oxobutanoyl]amino]-5-carbamimidamidopentanoyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-4-carboxybutanoyl]amino]-5-oxopentanoyl]amino]hexanoic acid Chemical compound CSCC[C@H](N)C(=O)N[C@@H](Cc1c[nH]c2ccccc12)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N1CCC[C@H]1C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1CCC[C@H]1C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@@H](Cc1cnc[nH]1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](Cc1c[nH]c2ccccc12)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](Cc1ccccc1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](Cc1c[nH]c2ccccc12)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCCN)C(O)=O PGOHTUIFYSHAQG-LJSDBVFPSA-N 0.000 description 1
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- CSSMBUJNSXLHTR-UHFFFAOYSA-N 1,1-dichloro-2-[2-[2-[2-[2-(2-hydroxyethoxy)ethoxy]ethoxy]ethoxy]ethoxy]ethanol Chemical compound OCCOCCOCCOCCOCCOCC(O)(Cl)Cl CSSMBUJNSXLHTR-UHFFFAOYSA-N 0.000 description 1
- ZCFRYTWBXNQVOW-UHFFFAOYSA-N 1-(2-chloroethoxy)-2-[2-(2-chloroethoxy)ethoxy]ethane Chemical compound ClCCOCCOCCOCCCl ZCFRYTWBXNQVOW-UHFFFAOYSA-N 0.000 description 1
- ZHXUIGXEKZZCLT-UHFFFAOYSA-N 1-(4-aminooxybutyl)pyrrole-2,5-dione Chemical compound NOCCCCN1C(=O)C=CC1=O ZHXUIGXEKZZCLT-UHFFFAOYSA-N 0.000 description 1
- PFNCOYVEMJYEED-UHFFFAOYSA-N 16-bromohexadecanoic acid Chemical compound OC(=O)CCCCCCCCCCCCCCCBr PFNCOYVEMJYEED-UHFFFAOYSA-N 0.000 description 1
- IZAIPALZJVSRHT-UHFFFAOYSA-N 16-hydroxy stearic acid Chemical compound CCC(O)CCCCCCCCCCCCCCC(O)=O IZAIPALZJVSRHT-UHFFFAOYSA-N 0.000 description 1
- LMMHKCWKJBVEOX-UHFFFAOYSA-N 16-hydroxyhexadecanoic acid;16-oxohexadecanoic acid Chemical compound OCCCCCCCCCCCCCCCC(O)=O.OC(=O)CCCCCCCCCCCCCCC=O LMMHKCWKJBVEOX-UHFFFAOYSA-N 0.000 description 1
- BLSAPDZWVFWUTL-UHFFFAOYSA-N 2,5-dioxopyrrolidine-3-sulfonic acid Chemical compound OS(=O)(=O)C1CC(=O)NC1=O BLSAPDZWVFWUTL-UHFFFAOYSA-N 0.000 description 1
- 150000003923 2,5-pyrrolediones Chemical class 0.000 description 1
- PWKSKIMOESPYIA-UHFFFAOYSA-N 2-acetamido-3-sulfanylpropanoic acid Chemical compound CC(=O)NC(CS)C(O)=O PWKSKIMOESPYIA-UHFFFAOYSA-N 0.000 description 1
- TWJNQYPJQDRXPH-UHFFFAOYSA-N 2-cyanobenzohydrazide Chemical compound NNC(=O)C1=CC=CC=C1C#N TWJNQYPJQDRXPH-UHFFFAOYSA-N 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- YRNWIFYIFSBPAU-UHFFFAOYSA-N 4-[4-(dimethylamino)phenyl]-n,n-dimethylaniline Chemical compound C1=CC(N(C)C)=CC=C1C1=CC=C(N(C)C)C=C1 YRNWIFYIFSBPAU-UHFFFAOYSA-N 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- YWWVWXASSLXJHU-UHFFFAOYSA-N 9E-tetradecenoic acid Natural products CCCCC=CCCCCCCCC(O)=O YWWVWXASSLXJHU-UHFFFAOYSA-N 0.000 description 1
- ZJVUHXLOALFWGB-UHFFFAOYSA-N 9H-fluoren-9-ylmethyl N-[2-[2-(hexadecanoylamino)oxyethoxy]ethoxy]carbamate Chemical compound C1=CC=C2C(COC(=O)NOCCOCCONC(=O)CCCCCCCCCCCCCCC)C3=CC=CC=C3C2=C1 ZJVUHXLOALFWGB-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 102400000069 Activation peptide Human genes 0.000 description 1
- 101800001401 Activation peptide Proteins 0.000 description 1
- 206010067484 Adverse reaction Diseases 0.000 description 1
- 102100036826 Aldehyde oxidase Human genes 0.000 description 1
- 102000009840 Angiopoietins Human genes 0.000 description 1
- 108010009906 Angiopoietins Proteins 0.000 description 1
- 208000032467 Aplastic anaemia Diseases 0.000 description 1
- 101100437118 Arabidopsis thaliana AUG1 gene Proteins 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 102000015790 Asparaginase Human genes 0.000 description 1
- 108010024976 Asparaginase Proteins 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- ZNSMNVMLTJELDZ-UHFFFAOYSA-N Bis(2-chloroethyl)ether Chemical compound ClCCOCCCl ZNSMNVMLTJELDZ-UHFFFAOYSA-N 0.000 description 1
- 102000004506 Blood Proteins Human genes 0.000 description 1
- 108010017384 Blood Proteins Proteins 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 101710161573 Cardiotrophin-2 Proteins 0.000 description 1
- 102100035882 Catalase Human genes 0.000 description 1
- 108010053835 Catalase Proteins 0.000 description 1
- 229930186147 Cephalosporin Natural products 0.000 description 1
- 229910052684 Cerium Inorganic materials 0.000 description 1
- 206010053567 Coagulopathies Diseases 0.000 description 1
- 206010010774 Constipation Diseases 0.000 description 1
- 241000699800 Cricetinae Species 0.000 description 1
- 241000702421 Dependoparvovirus Species 0.000 description 1
- 206010059866 Drug resistance Diseases 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 102000018386 EGF Family of Proteins Human genes 0.000 description 1
- 108010066486 EGF Family of Proteins Proteins 0.000 description 1
- 108010041308 Endothelial Growth Factors Proteins 0.000 description 1
- 239000004593 Epoxy Substances 0.000 description 1
- 241000283073 Equus caballus Species 0.000 description 1
- 102000003951 Erythropoietin Human genes 0.000 description 1
- 108090000394 Erythropoietin Proteins 0.000 description 1
- 241000588724 Escherichia coli Species 0.000 description 1
- 108010049003 Fibrinogen Proteins 0.000 description 1
- 102000008946 Fibrinogen Human genes 0.000 description 1
- 102000012570 Fibroblast growth factor 16 Human genes 0.000 description 1
- 108050002072 Fibroblast growth factor 16 Proteins 0.000 description 1
- 101150094690 GAL1 gene Proteins 0.000 description 1
- 102000002464 Galactosidases Human genes 0.000 description 1
- 108010093031 Galactosidases Proteins 0.000 description 1
- 102100028501 Galanin peptides Human genes 0.000 description 1
- 102000034615 Glial cell line-derived neurotrophic factor Human genes 0.000 description 1
- 108091010837 Glial cell line-derived neurotrophic factor Proteins 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 102000009465 Growth Factor Receptors Human genes 0.000 description 1
- 108010009202 Growth Factor Receptors Proteins 0.000 description 1
- 208000031220 Hemophilia Diseases 0.000 description 1
- 208000005176 Hepatitis C Diseases 0.000 description 1
- 208000028782 Hereditary disease Diseases 0.000 description 1
- 241000238631 Hexapoda Species 0.000 description 1
- 108010000487 High-Molecular-Weight Kininogen Proteins 0.000 description 1
- 101000928314 Homo sapiens Aldehyde oxidase Proteins 0.000 description 1
- 101100121078 Homo sapiens GAL gene Proteins 0.000 description 1
- AVXURJPOCDRRFD-UHFFFAOYSA-N Hydroxylamine Chemical compound ON AVXURJPOCDRRFD-UHFFFAOYSA-N 0.000 description 1
- 108010024118 Hypothalamic Hormones Proteins 0.000 description 1
- 102000015611 Hypothalamic Hormones Human genes 0.000 description 1
- 102100026120 IgG receptor FcRn large subunit p51 Human genes 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 102100035792 Kininogen-1 Human genes 0.000 description 1
- 239000005639 Lauric acid Substances 0.000 description 1
- 102100021747 Leukemia inhibitory factor receptor Human genes 0.000 description 1
- OYHQOLUKZRVURQ-HZJYTTRNSA-N Linoleic acid Chemical compound CCCCC\C=C/C\C=C/CCCCCCCC(O)=O OYHQOLUKZRVURQ-HZJYTTRNSA-N 0.000 description 1
- 101710141347 Major envelope glycoprotein Proteins 0.000 description 1
- PEEHTFAAVSWFBL-UHFFFAOYSA-N Maleimide Chemical compound O=C1NC(=O)C=C1 PEEHTFAAVSWFBL-UHFFFAOYSA-N 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 235000021360 Myristic acid Nutrition 0.000 description 1
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 1
- AMBGUKPYXBQXRD-UHFFFAOYSA-N N-[2-(2-aminooxyethoxy)ethoxy]hexadecanamide Chemical compound CCCCCCCCCCCCCCCC(=O)NOCCOCCON AMBGUKPYXBQXRD-UHFFFAOYSA-N 0.000 description 1
- SQVRNKJHWKZAKO-PFQGKNLYSA-N N-acetyl-beta-neuraminic acid Chemical compound CC(=O)N[C@@H]1[C@@H](O)C[C@@](O)(C(O)=O)O[C@H]1[C@H](O)[C@H](O)CO SQVRNKJHWKZAKO-PFQGKNLYSA-N 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 108091005461 Nucleic proteins Proteins 0.000 description 1
- 108010064527 OSM-LIF Receptors Proteins 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- 235000021319 Palmitoleic acid Nutrition 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- 108010082093 Placenta Growth Factor Proteins 0.000 description 1
- 108010064851 Plant Proteins Proteins 0.000 description 1
- 108090000113 Plasma Kallikrein Proteins 0.000 description 1
- 206010035226 Plasma cell myeloma Diseases 0.000 description 1
- 102100037596 Platelet-derived growth factor subunit A Human genes 0.000 description 1
- 101710103506 Platelet-derived growth factor subunit A Proteins 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 102000029797 Prion Human genes 0.000 description 1
- 108091000054 Prion Proteins 0.000 description 1
- 102000014961 Protein Precursors Human genes 0.000 description 1
- 108010078762 Protein Precursors Proteins 0.000 description 1
- 108010001267 Protein Subunits Proteins 0.000 description 1
- 102000002067 Protein Subunits Human genes 0.000 description 1
- 108010094028 Prothrombin Proteins 0.000 description 1
- 102100027378 Prothrombin Human genes 0.000 description 1
- 241000125945 Protoparvovirus Species 0.000 description 1
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 1
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- 239000002262 Schiff base Substances 0.000 description 1
- 150000004753 Schiff bases Chemical class 0.000 description 1
- 229920002684 Sepharose Polymers 0.000 description 1
- 206010040047 Sepsis Diseases 0.000 description 1
- 208000026552 Severe hemophilia A Diseases 0.000 description 1
- 102000013275 Somatomedins Human genes 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 241000282898 Sus scrofa Species 0.000 description 1
- 238000006859 Swern oxidation reaction Methods 0.000 description 1
- 101150109894 TGFA gene Proteins 0.000 description 1
- 108700019146 Transgenes Proteins 0.000 description 1
- 108060008683 Tumor Necrosis Factor Receptor Proteins 0.000 description 1
- 208000009694 Type 2 von Willebrand Disease Diseases 0.000 description 1
- 241000700618 Vaccinia virus Species 0.000 description 1
- 108010004977 Vasopressins Proteins 0.000 description 1
- 102000002852 Vasopressins Human genes 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- 102000004210 Vitamin K Epoxide Reductases Human genes 0.000 description 1
- 108090000779 Vitamin K Epoxide Reductases Proteins 0.000 description 1
- 102100038182 Vitamin K-dependent gamma-carboxylase Human genes 0.000 description 1
- 210000001766 X chromosome Anatomy 0.000 description 1
- FRYDSOYOHWGSMD-UHFFFAOYSA-N [C].O Chemical compound [C].O FRYDSOYOHWGSMD-UHFFFAOYSA-N 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- LVAMVZXECCXUGI-UHFFFAOYSA-N acetic acid;thallium Chemical compound [Tl].CC(O)=O LVAMVZXECCXUGI-UHFFFAOYSA-N 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 230000006838 adverse reaction Effects 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 239000012670 alkaline solution Substances 0.000 description 1
- 125000005262 alkoxyamine group Chemical group 0.000 description 1
- 230000000172 allergic effect Effects 0.000 description 1
- 102000005840 alpha-Galactosidase Human genes 0.000 description 1
- 108010030291 alpha-Galactosidase Proteins 0.000 description 1
- 125000003368 amide group Chemical group 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 238000007098 aminolysis reaction Methods 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 230000001494 anti-thymocyte effect Effects 0.000 description 1
- 239000003146 anticoagulant agent Substances 0.000 description 1
- 239000003429 antifungal agent Substances 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 229940114079 arachidonic acid Drugs 0.000 description 1
- 235000021342 arachidonic acid Nutrition 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 229960003272 asparaginase Drugs 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 208000010668 atopic eczema Diseases 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000001588 bifunctional effect Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 244000309464 bull Species 0.000 description 1
- 210000004899 c-terminal region Anatomy 0.000 description 1
- 230000021523 carboxylation Effects 0.000 description 1
- 238000006473 carboxylation reaction Methods 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 229940124587 cephalosporin Drugs 0.000 description 1
- 150000001780 cephalosporins Chemical class 0.000 description 1
- 229940106189 ceramide Drugs 0.000 description 1
- 150000001783 ceramides Chemical class 0.000 description 1
- GWXLDORMOJMVQZ-UHFFFAOYSA-N cerium Chemical compound [Ce] GWXLDORMOJMVQZ-UHFFFAOYSA-N 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 230000001886 ciliary effect Effects 0.000 description 1
- SECPZKHBENQXJG-UHFFFAOYSA-N cis-palmitoleic acid Natural products CCCCCCC=CCCCCCCCC(O)=O SECPZKHBENQXJG-UHFFFAOYSA-N 0.000 description 1
- 230000035602 clotting Effects 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- QAHREYKOYSIQPH-UHFFFAOYSA-L cobalt(II) acetate Chemical compound [Co+2].CC([O-])=O.CC([O-])=O QAHREYKOYSIQPH-UHFFFAOYSA-L 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 239000003246 corticosteroid Substances 0.000 description 1
- 229960001334 corticosteroids Drugs 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 230000002939 deleterious effect Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- SYZWSSNHPZXGML-UHFFFAOYSA-N dichloromethane;oxolane Chemical compound ClCCl.C1CCOC1 SYZWSSNHPZXGML-UHFFFAOYSA-N 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 239000000539 dimer Substances 0.000 description 1
- 208000037765 diseases and disorders Diseases 0.000 description 1
- 239000002612 dispersion medium Substances 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 230000004064 dysfunction Effects 0.000 description 1
- 238000004520 electroporation Methods 0.000 description 1
- 239000012149 elution buffer Substances 0.000 description 1
- 230000003511 endothelial effect Effects 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 230000007515 enzymatic degradation Effects 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 239000006167 equilibration buffer Substances 0.000 description 1
- 229940105423 erythropoietin Drugs 0.000 description 1
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 230000006624 extrinsic pathway Effects 0.000 description 1
- 235000019197 fats Nutrition 0.000 description 1
- 235000019387 fatty acid methyl ester Nutrition 0.000 description 1
- 108091005632 fatty acylated proteins Proteins 0.000 description 1
- 229940012952 fibrinogen Drugs 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- IRXSLJNXXZKURP-UHFFFAOYSA-N fluorenylmethyloxycarbonyl chloride Chemical compound C1=CC=C2C(COC(=O)Cl)C3=CC=CC=C3C2=C1 IRXSLJNXXZKURP-UHFFFAOYSA-N 0.000 description 1
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 230000005714 functional activity Effects 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 102000034238 globular proteins Human genes 0.000 description 1
- 108091005896 globular proteins Proteins 0.000 description 1
- 108010013113 glutamyl carboxylase Proteins 0.000 description 1
- 230000001279 glycosylating effect Effects 0.000 description 1
- 210000003714 granulocyte Anatomy 0.000 description 1
- 239000000122 growth hormone Substances 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 230000003394 haemopoietic effect Effects 0.000 description 1
- 238000003306 harvesting Methods 0.000 description 1
- 230000002008 hemorrhagic effect Effects 0.000 description 1
- 230000002439 hemostatic effect Effects 0.000 description 1
- 208000005252 hepatitis A Diseases 0.000 description 1
- 206010073071 hepatocellular carcinoma Diseases 0.000 description 1
- 229960002885 histidine Drugs 0.000 description 1
- 229920001519 homopolymer Polymers 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 102000057593 human F8 Human genes 0.000 description 1
- 229960000900 human factor viii Drugs 0.000 description 1
- 229940042795 hydrazides for tuberculosis treatment Drugs 0.000 description 1
- 150000007857 hydrazones Chemical class 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 150000002443 hydroxylamines Chemical class 0.000 description 1
- 208000006575 hypertriglyceridemia Diseases 0.000 description 1
- 150000002466 imines Chemical class 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 230000005847 immunogenicity Effects 0.000 description 1
- 238000002513 implantation Methods 0.000 description 1
- 230000001976 improved effect Effects 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 230000002779 inactivation Effects 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 230000002458 infectious effect Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 230000002608 insulinlike Effects 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 229940047124 interferons Drugs 0.000 description 1
- 238000007917 intracranial administration Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- 239000007951 isotonicity adjuster Substances 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 229940102988 levemir Drugs 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 235000020778 linoleic acid Nutrition 0.000 description 1
- OYHQOLUKZRVURQ-IXWMQOLASA-N linoleic acid Natural products CCCCC\C=C/C\C=C\CCCCCCCC(O)=O OYHQOLUKZRVURQ-IXWMQOLASA-N 0.000 description 1
- 239000007791 liquid phase Substances 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 150000004668 long chain fatty acids Chemical class 0.000 description 1
- 229920002521 macromolecule Polymers 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 229940071125 manganese acetate Drugs 0.000 description 1
- UOGMEBQRZBEZQT-UHFFFAOYSA-L manganese(2+);diacetate Chemical compound [Mn+2].CC([O-])=O.CC([O-])=O UOGMEBQRZBEZQT-UHFFFAOYSA-L 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 150000004667 medium chain fatty acids Chemical class 0.000 description 1
- 210000003593 megakaryocyte Anatomy 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- TWXDDNPPQUTEOV-FVGYRXGTSA-N methamphetamine hydrochloride Chemical compound Cl.CN[C@@H](C)CC1=CC=CC=C1 TWXDDNPPQUTEOV-FVGYRXGTSA-N 0.000 description 1
- 230000001035 methylating effect Effects 0.000 description 1
- 108091070501 miRNA Proteins 0.000 description 1
- 239000002679 microRNA Substances 0.000 description 1
- 238000000520 microinjection Methods 0.000 description 1
- 230000003278 mimic effect Effects 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 238000006011 modification reaction Methods 0.000 description 1
- 238000001823 molecular biology technique Methods 0.000 description 1
- 238000010369 molecular cloning Methods 0.000 description 1
- 201000000050 myeloid neoplasm Diseases 0.000 description 1
- SQDFHQJTAWCFIB-UHFFFAOYSA-N n-methylidenehydroxylamine Chemical compound ON=C SQDFHQJTAWCFIB-UHFFFAOYSA-N 0.000 description 1
- 108010068617 neonatal Fc receptor Proteins 0.000 description 1
- 229940053128 nerve growth factor Drugs 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 239000012038 nucleophile Substances 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 229940127216 oral anticoagulant drug Drugs 0.000 description 1
- 125000003544 oxime group Chemical group 0.000 description 1
- 150000002924 oxiranes Chemical group 0.000 description 1
- 229910052763 palladium Inorganic materials 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 150000002960 penicillins Chemical class 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 239000012071 phase Substances 0.000 description 1
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 230000004962 physiological condition Effects 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 235000021118 plant-derived protein Nutrition 0.000 description 1
- 239000013612 plasmid Substances 0.000 description 1
- 108010017843 platelet-derived growth factor A Proteins 0.000 description 1
- 102000054765 polymorphisms of proteins Human genes 0.000 description 1
- 230000006267 polysialylation Effects 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 230000035935 pregnancy Effects 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 230000003449 preventive effect Effects 0.000 description 1
- 238000009117 preventive therapy Methods 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 239000003805 procoagulant Substances 0.000 description 1
- 230000002947 procoagulating effect Effects 0.000 description 1
- 229940002612 prodrug Drugs 0.000 description 1
- 239000000651 prodrug Substances 0.000 description 1
- 210000001236 prokaryotic cell Anatomy 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 108020001580 protein domains Proteins 0.000 description 1
- 230000006916 protein interaction Effects 0.000 description 1
- 238000001742 protein purification Methods 0.000 description 1
- 238000009163 protein therapy Methods 0.000 description 1
- 230000006337 proteolytic cleavage Effects 0.000 description 1
- 229940039716 prothrombin Drugs 0.000 description 1
- 108010014806 prothrombinase complex Proteins 0.000 description 1
- 239000002510 pyrogen Substances 0.000 description 1
- 101150079601 recA gene Proteins 0.000 description 1
- 229960000160 recombinant therapeutic protein Drugs 0.000 description 1
- 238000006268 reductive amination reaction Methods 0.000 description 1
- 230000011514 reflex Effects 0.000 description 1
- 238000009256 replacement therapy Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 235000003441 saturated fatty acids Nutrition 0.000 description 1
- 150000003335 secondary amines Chemical class 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 150000004666 short chain fatty acids Chemical class 0.000 description 1
- 238000010898 silica gel chromatography Methods 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- AKHNMLFCWUSKQB-UHFFFAOYSA-L sodium thiosulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=S AKHNMLFCWUSKQB-UHFFFAOYSA-L 0.000 description 1
- 235000019345 sodium thiosulphate Nutrition 0.000 description 1
- MIDXXTLMKGZDPV-UHFFFAOYSA-M sodium;1-[6-(2,5-dioxopyrrol-1-yl)hexanoyloxy]-2,5-dioxopyrrolidine-3-sulfonate Chemical compound [Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)CCCCCN1C(=O)C=CC1=O MIDXXTLMKGZDPV-UHFFFAOYSA-M 0.000 description 1
- XZJPNVSXVXZDNF-UHFFFAOYSA-M sodium;16-oxohexadecanoate Chemical compound [Na+].[O-]C(=O)CCCCCCCCCCCCCCC=O XZJPNVSXVXZDNF-UHFFFAOYSA-M 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 125000000020 sulfo group Chemical group O=S(=O)([*])O[H] 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-N sulfuric acid Substances OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 229940126585 therapeutic drug Drugs 0.000 description 1
- 230000008467 tissue growth Effects 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- 238000001890 transfection Methods 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- 102000003390 tumor necrosis factor Human genes 0.000 description 1
- 102000003298 tumor necrosis factor receptor Human genes 0.000 description 1
- 241001529453 unidentified herpesvirus Species 0.000 description 1
- 241001430294 unidentified retrovirus Species 0.000 description 1
- 229960005486 vaccine Drugs 0.000 description 1
- 150000004669 very long chain fatty acids Chemical class 0.000 description 1
- 230000003612 virological effect Effects 0.000 description 1
- 208000020294 von Willebrand disease 1 Diseases 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000002699 waste material Substances 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/542—Carboxylic acids, e.g. a fatty acid or an amino acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
- A61K47/60—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes the organic macromolecular compound being a polyoxyalkylene oligomer, polymer or dendrimer, e.g. PEG, PPG, PEO or polyglycerol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/04—Antihaemorrhagics; Procoagulants; Haemostatic agents; Antifibrinolytic agents
Landscapes
- Health & Medical Sciences (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Epidemiology (AREA)
- Organic Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Hematology (AREA)
- Diabetes (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
- Peptides Or Proteins (AREA)
Abstract
Conjugado de un derivado de ácido graso soluble en agua y una proteína terapéutica, en el que el derivado de ácido graso soluble en agua comprende un ácido graso o éster de ácido graso unido a un ligador soluble en agua, y en el que el derivado de ácido graso soluble en agua se une de manera estable a la proteína terapéutica mediante una unión oxima formada entre un grupo aminooxilo en el ligador soluble en agua y un grupo aldehído de un hidrato de carbono oxidado en la proteína terapéutica.
Description
DESCRIPCIÓN
Materiales y métodos para conjugar un derivado de ácido graso soluble en agua con una proteína
Campo de la invención
La presente invención se refiere a materiales y métodos para conjugar un derivado de ácido graso soluble en agua con una proteína.
Antecedentes de la invención
Se han descrito una variedad moléculas y/o compuestos para conjugar con proteínas terapéuticas para aumentar la semivida de las proteínas terapéuticas conjugadas tras la administración a un paciente (Veronese FM y Mero A, BioDrugs 2008;22:315-29; Gregoriadis G et al., Int J Pharm 2005; 300:125-30; y Shechter Y et al.; International Journal of Peptide Research and Therapeutics 2007; vol. 13 :105-17).
Los ácidos grasos (FA, por sus siglas en inglés) pueden conjugarse con proteínas terapéuticas para formar derivados de acción más prolongada. Este principio para la prolongación de la semivida de proteínas o péptidos se basa en el hecho de que el FA puede unirse a albúmina sérica humana (HSA; también denominada sondas de unión a albúmina). La asociación de un FA con albúmina sérica humana en el torrente circulatorio puede conducir a una prolongación sustancial de la semivida de la proteína terapéutica ya que se reciclará junto con la albumina a través del receptor Fc neonatal. El FA y derivados del mismo (por ejemplo, ésteres metílicos correspondiente) ha mostrado propiedades de unión a albúmina similares (Spector AA, J Lipid Res 1975;16:165-79).
Un ejemplo destacado para este principio de acción prolongada es insulina detemir (Levemir®) de Novo Nordisk. En insulina detemir, el grupo carboxilo de un FA se acopla de manera covalente al grupo g-amino de un residuo de lisina de la proteína de insulina (véanse, por ejemplo, los documentos US 5.866.538; US 6.011.007; y US 6.869.930). Otros grupos de investigación han descrito enfoques similares (Shechter Y et al., Bioconj Chem 2005;16:913-20; y Sasson K et al., J Control Release 2010;142:214-20). Por ejemplo, estos grupos describen un sistema FMOC liberable que contiene un éster de NHS activo para acoplar a grupos amino de proteínas. Sin embargo, la diferencia es que en este concepto el FA se une a la proteína a través de un grupo funcional en posición o convirtiéndose así en grupo carboxilo en intacto. Por tanto, pueden prepararse profármacos de acción prolongada que se unen a albúmina sérica humana, pero se disocian a lo largo del tiempo a medida que el sistema FMOC experimenta baja hidrólisis en condiciones fisiológicas (Sasson K et al., J Control Release 2010;142:214-20).
Además de los ácidos grasos, la preparación de conjugados formando una unión covalente entre el polímero soluble en agua y la proteína terapéutica puede llevarse a cabo por una variedad de métodos químicos. La pegilación de fármacos polipeptídicos los protege en la circulación y mejora sus perfiles farmacodinámicos y farmacocinéticos (Harris y Chess, Nat Rev Drug Discov. 2003;2:214-21). El procedimiento de pegilación une unidades de repetición de etilenglicol (polietilenglicol (PEG)) a un fármaco polipeptídico. Las moléculas de PEG tienen un gran volumen hidrodinámico (5-10 veces el tamaño de las proteínas globulares), son muy solubles en agua e hidratadas, no tóxicas, no inmunógenas y se someten a aclaramiento rápidamente del cuerpo. La pegilación de moléculas puede conducir a resistencia aumentada de los fármacos a la degradación enzimática, semivida aumentada in vivo, frecuencia de dosificación reducida, inmunogenicidad disminuida, estabilidad física y térmica aumentada, solubilidad aumentada, estabilidad en fase líquida aumentada y agregación reducida. Los primeros fármacos pegilados se aprobaron por la FDA a principios de la década de 1990. Desde entonces, la FDA ha aprobado varios fármacos pegilados para administración oral, inyectable y tópica.
El poli(ácido siálico) (PSA, por sus siglas en inglés), también denominado ácido colomínico (CA, por sus siglas en inglés), es un polisacárido que se produce de manera natural. Es un homopolímero del ácido N-acetilneuramínico con una unión cetosídica a (2 ^8 ) contiene grupos diol vecinos como su extremo no reductor. Está cargado negativamente y es un constituyente natural del cuerpo humano. Puede producirse fácilmente a partir de bacterias en grandes cantidades y con características físicas predeterminadas (patente estadounidense n.° 5.846.951). Ya que el PSA producido de manera bacteriana es química e inmunológicamente idéntico al PSA producido en el cuerpo humando, el PSA bacteriano no es inmunógeno, incluso cuando se acopla a proteínas. A diferencia de algunos polímeros, el ácido PSA es biodegradable. El acoplamiento covalente del ácido colomínico a la catalasa y asparaginasa ha demostrado aumentar la estabilidad enzimática en presencia de enzimas proteolíticas o plasma sanguíneo. Estudios comparativos in vivo con asparaginasa polisialilada y no modificada revelaron que la polisialilación aumentó la semivida de la enzima (Fernandes y Gregoriadis, Int J Pharm. 2001;217:215-24).
El acoplamiento de derivados de PEG a péptidos o proteínas fue revisado por Roberts et al. (Adv Drug Deliv Rev 2002; 54: 459-76). Un enfoque para acoplar polímeros solubles en agua a proteínas terapéuticas es la conjugación de los polímeros a través de los restos de hidratos de carbono de la proteína. Los grupos hidroxilo (OH) vecinos de hidratos de carbono en las proteínas pueden oxidarse fácilmente con peryodato de sodio (NaIO4 ) para formar grupos aldehído activos (Rothfus y Smith, J Biol Chem 1963; 238: 1402-10; van Lenten y Ashwell, J Biol Chem 1971; 246: 1889-94) Posteriormente, el polímero puede acoplarse a los grupos aldehído del hidrato de carbono mediante el uso de reactivos
que contienen, por ejemplo, un grupo hidrazida activo (Wilchek M y Bayer EA, Methods Enzymol 1987; 138: 429-42). Una tecnología más reciente es el uso de reactivos que contienen grupos aminooxilo que reaccionan con aldehídos para formar uniones oxima (documentos WO 96/40662, WO2008/025856).
Ejemplos adicionales que describen la conjugación de un polímero soluble en agua con una proteína terapéutica se describen en el documento WO 06/071801 que enseña la oxidación de restos de hidratos de carbono en el factor de von Willebrand y el posterior acoplamiento al PEG usando química de hidrazida; la publicación de patente estadounidense n.° 2009/0076237 que enseña la oxidación de rFVIII y el posterior acoplamiento a PEG y otros polímeros solubles en agua (por ejemplo, PSA, HES, dextrano) usando química de hidrazida; el documento WO 2008/025856 que enseña la oxidación de diferentes factores de coagulación, por ejemplo, rFIX, FVIII y FVIIa y el acoplamiento posterior a, por ejemplo, PEG, usando química de aminooxilo formando una unión oxima; la patente estadounidense n.° 5.621.039 que enseña la oxidación de FIX y el posterior acoplamiento a PEG usando química de hidrazida.
El documento WO2005117984 A2 que se refiere a un compuesto de unión a albúmina que comprende un grupo espaciador, un grupo de unión en puente soluble en agua, una cadena de ácido graso y un grupo ácido, caracterizado porque el grupo ácido se une al extremo distal de la cadena de ácido graso; y el documento WO2006084319 A1 que se refiere a moléculas inmunógenas autoadyuvantes capaces de estimular una respuesta inmunitaria a los epítopos de un polipéptido independientemente del tipo de HLA de un sujeto.
A pesar de los materiales y métodos anteriores para la conjugación de proteínas, se desean nuevos materiales y métodos que, por ejemplo, permitan la manipulación y preparación de conjugados de proteínas estables. Aunque los ácidos grasos pueden proporcionar el beneficio de unirse a HSA, los ácidos grasos a menudo son difíciles de manipular en un entorno acuoso y pueden liberarse o eliminarse de su compañero de unión a proteínas a lo largo del tiempo.
Sumario de la invención
La presente invención proporciona materiales y métodos para conjugar polímeros y derivados de ácido graso solubles en agua con proteínas lo que mejora las propiedades farmacodinámicas y/o farmacocinéticas de la proteína mientras que minimiza los costes asociados con los diversos reactivos y los riesgos para la salud a los pacientes receptores cuando la reacción de conjugación está catalizada por un catalizador nucleófilo. La presente invención proporciona materiales y métodos para conjugar derivados de ácido graso solubles en agua con proteínas en una disolución acuosa, produciendo así conjugados de proteínas estables en la que los derivados de ácidos grasos no se liberan a lo largo del tiempo.
En una realización de la presente invención, se proporciona un conjugado de un derivado de ácido graso soluble en agua y una proteína terapéutica, en la que el derivado de ácido graso soluble en agua comprende un ácido graso o éster de ácido graso unido a un ligador soluble en agua, y en la que el derivado de ácido graso se une de manera estable a la proteína terapéutica por una unión oxima formada entre un grupo aminooxilo en el ligador soluble en agua y un grupo aldehído de un hidrato de carbono oxidado en la proteína terapéutica. En otra realización, el conjugado derivado de ácido graso-proteína terapéutica se une a albúmina sérica humana (HSA) in vitro o in vivo. En todavía otra realización, el conjugado derivado de ácido graso-proteína terapéutica tiene una semivida aumentada en relación con una proteína terapéutica nativa. En aún otra realización, un conjugado derivado de ácido graso-proteína terapéutica mencionado anteriormente comprende un ácido graso saturado o ácido graso insaturado. En una realización relacionada, el ácido graso es un ácido graso saturado. En aún otra realización, el ácido graso es un ácido graso de cadena ramificada.
Se contemplan diversas longitudes de ácidos grasos en el conjugado derivado de ácido graso-proteína terapéutica. En una realización, se proporciona un conjugado derivado de ácido graso-proteína terapéutica mencionado anteriormente en el que el ácido graso comprende una longitud de cadena entre C10 y C24, incluyendo ácidos grasos sintéticos con números impares de carbonos. En una realización, se proporciona un conjugado derivado de ácido graso-proteína terapéutica mencionado anteriormente en el que el ácido graso comprende una longitud de cadena seleccionada del grupo que consiste en: C10, C12, C14, C16, C18, C20, C20, C22 y C24. En otra realización, el ácido graso tiene una longitud de cadena seleccionada del grupo que consiste en C14, C16 y C18. En todavía otra, el ácido graso tiene una longitud de cadena seleccionada del grupo que consiste en C13, C15 y C17.
En todavía otra realización, se proporciona un conjugado derivado de ácido graso-proteína terapéutica mencionado anteriormente en el que el ácido graso se une al ligador soluble en agua en un grupo en el ácido graso seleccionado del grupo que consiste en: grupo carboxilo terminal y grupo o. En otra realización, el ácido graso se une al ligador soluble en agua en el grupo o En todavía otra realización, el grupo o se selecciona del grupo que consiste en: hidroxilo, amino, tio y carboxilo.
En una realización de la presente invención, se proporciona un conjugado derivado de ácido graso-proteína terapéutica mencionado anteriormente en el que el ácido graso es ácido 16-hidroxihexadecanoico.
En otra realización, se proporciona un conjugado derivado de ácido graso-proteína terapéutica en el que el éster de
ácido graso se selecciona del grupo que consiste en: éster metílico y éster etílico. En una realización, el éster de ácido graso es éster metílico del ácido 16-hidroxihexadecanoico.
Se contemplan diversos ligadores solubles en agua en la presente invención. En una realización, se proporciona un conjugado derivado de ácido graso-proteína terapéutica mencionado anteriormente en el que el ligador soluble en agua comprende un polímero soluble en agua y al menos un grupo funcional unido a la proteína terapéutica.
El grupo funcional es un grupo aminooxilo.
Se contemplan numerosos polímeros solubles en agua en la presente invención. En una realización, se proporciona un conjugado derivado de ácido graso-proteína terapéutica mencionado anteriormente en el que el polímero soluble en agua, que es parte integral del ligador, se selecciona del grupo que consiste en: polietilenglicol (PEG), PEG ramificado, poli(ácido siálico) (PSA), almidón de hidroxialquilo (HAS), almidón de hidroxietilo (HES), hidrato de carbono, polisacáridos, pululano, quitosano, ácido hialurónico, sulfato de condroitina, sulfato de dermatán, almidón, dextrano, carboximetildextrano, poli(óxido de alquileno) (PAO), polialquilenglicol (PAG), polipropilenglicol (PPG), polioxazolina, poliacriloilmorfolina, poli(alcohol vinílico) (PVA), policarboxilato, polivinilpirrolidona, polifosfaceno, polietileno-co-anhídrido de ácido maleico, poliestireno-co-anhídrido de ácido maleico y poli(1-hidroximetiletilenhidroximetilformal) (PHF). En todavía otra realización, el polímero soluble en agua es PEG. También se contemplan diversas longitudes de polímeros solubles en agua en el presente documento. En una realización, se proporciona un conjugado derivado de ácido graso-proteína terapéutica en el que el polímero soluble en agua comprende una longitud de cadena seleccionada del grupo que consiste en O3, O5, O7, O9, O11, O13 y O15.
En una realización, se proporciona un conjugado derivado de ácido graso-proteína terapéutica en el que el ligador soluble en agua se selecciona del grupo que consiste en:
3-oxapentano-1,5-dioxiamina
3,6,9-triaoxaundecano-1,11-dioxiamina;
3,6,9,12,15-pentaoxaheptadecano-1,17-dioxiamina;
3,6,9,12,15,18,21-heptaoxatricosano-1,23-dioxiamina
Se proporciona un conjugado derivado de ácido graso-proteína terapéutica en el que el derivado de ácido graso se une de manera estable a la proteína terapéutica por una unión oxima. La unión oxima se forma entre un grupo aminooxilo en el ligador soluble en agua y un grupo aldehído de un hidrato de carbono oxidado en la proteína terapéutica.
En una realización de la invención, se proporciona un conjugado derivado de ácido graso-proteína terapéutica en el que el derivado de ácido graso se selecciona del grupo que consiste en:
a) sal de sodio del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiimino)-hexadecanoico de la fórmula:
b) éster metílico del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiamino)-hexadecanoico,
Se contemplan diversas proteínas terapéuticas en la presente invención. En una realización, se proporciona un conjugado derivado de ácido graso-proteína terapéutica mencionado anteriormente en el que la proteína terapéutica se selecciona del grupo que consiste en: factor IX (FIX), factor VIII (FVIII), factor VIIa (FVIIa), factor de von Willebrand (VWF), factor V (FV), factor X (FX), factor XI (FXI), factor XII (FXII), trombina (FII), proteína C, proteína S, tPA, PAI-1, tromboplastina tisular (TF), proteasa ADAMTS 13, IL-1 alfa, IL-1 beta, IL-2, IL-3, IL-4, IL-5, IL-6, IL-11, factor estimulante de colonias 1 (c SF-1), M-CSF, SCF, GM-CSF, factor estimulante de colonias de granulocitos (G-CSF), EPO, interferón alfa (IFN-alfa), interferón de consenso, IFN-beta, IFN-gamma, IFN-omega, IL-7, IL-8, IL-9, IL-10, IL-12, IL-13, IL-14, IL-15, IL-16, IL-17, IL-18, IL-19, IL-20, IL-21, IL-22, IL-23, IL-24, IL-31, IL-32 alfa, IL-33, trombopoyetina (TPO), Ang-1, Ang-2, Ang-4, Ang-Y, polipéptido similar a angiopoyetina 1 (ANGPTL1), polipéptido similar a angiopoyetina 2 (ANGPTL2), polipéptido similar a angiopoyetina 3 (ANGPTL3), polipéptido similar a angiopoyetina 4 (ANGPTL4), polipéptido similar a angiopoyetina 5 (ANGPTL5), polipéptido similar a angiopoyetina 6 (ANGPTL6), polipéptido similar a angiopoyetina 7 (ANGPTL7), vitronectina, factor de crecimiento endotelial vascular (VEGF), angiogenina, activina A, activina B, activina C, proteína morfogénica ósea 1, proteína morfogénica ósea 2, proteína morfogénica ósea 3, proteína morfogénica ósea 4, proteína morfogénica ósea 5, proteína morfogénica ósea 6, proteína morfogénica ósea 7, proteína morfogénica ósea 8, proteína morfogénica ósea 9, proteína morfogénica ósea 10, proteína morfogénica ósea 11, proteína morfogénica ósea 12, proteína morfogénica ósea 13, proteína morfogénica ósea 14, proteína morfogénica ósea 15, receptor IA de proteínas morfogénicas óseas, receptor IB de proteínas morfogénicas óseas, receptor II de proteínas morfogénicas óseas, factor neurotrófico derivado del cerebro, cardiotrofina 1, factor neurotrófico ciliar, receptor del factor neurotrófico ciliar, cripto, críptico, factor quimiotáctico de neutrófilos inducido por citocinas 1, factor quimiotáctico de neutrófilos inducido por citocinas 2a, factor quimiotáctico de neutrófilos inducido por citocinas 2p, factor de crecimiento de células endoteliales p, endotelina 1, factor de crecimiento epidérmico, Epigen, epirregulina, factor quimiotáctico para neutrófilos derivado de células epiteliales, factor de crecimiento de fibroblastos 4, factor de crecimiento de fibroblastos 5, factor de crecimiento de fibroblastos 6, factor de crecimiento de fibroblastos 7, factor de crecimiento de fibroblastos 8, factor de crecimiento de fibroblastos 8b, factor de crecimiento de fibroblastos 8c, factor de crecimiento de fibroblastos 9, factor de crecimiento de fibroblastos 10, factor de crecimiento de fibroblastos 11, factor de crecimiento de fibroblastos 12, factor de crecimiento de fibroblastos 13, factor de crecimiento de fibroblastos 16, factor de crecimiento de fibroblastos 17, factor de crecimiento de fibroblastos 19, factor de crecimiento de fibroblastos 20, factor de crecimiento de fibroblastos 21, factor de crecimiento ácido de fibroblastos, factor de crecimiento básico de fibroblastos, receptor a1 del factor neurotrófico derivado de la línea celular glial, receptor a2 del factor neurotrófico derivado de la línea celular glial, proteína relacionada con el crecimiento, proteína relacionada con el crecimiento a, proteína relacionada con el crecimiento p, proteína relacionada con el crecimiento y, factor de crecimiento epidérmico de unión a heparina, factor de crecimiento de hepatocitos, receptor del factor de crecimiento de hepatocitos, factor de crecimiento derivado del hepatoma, factor de crecimiento similar a la insulina I, receptor del factor de crecimiento similar a la insulina, factor de crecimiento similar a la insulina II, proteína de unión al factor de crecimiento similar a la insulina, factor de crecimiento de queratinocitos, factor inhibidor de la leucemia, receptor a del factor inhibidor de la leucemia, factor de crecimiento nervioso receptor del factor de crecimiento nervioso, neuropoyetina, neurotrofina 3, neurotrofina 4, oncostatina M (OSM), factor de crecimiento placentario, factor de crecimiento placentario 2, factor de crecimiento de células endoteliales derivado de plaquetas, factor de crecimiento derivado de plaquetas, cadena A del factor de crecimiento derivado de plaquetas, factor de crecimiento derivado de plaquetas AA, factor de crecimiento derivado de plaquetas AB, cadena B del factor de crecimiento derivado de plaquetas, factor de crecimiento derivado de plaquetas BB, receptor a del factor de crecimiento derivado de plaquetas, receptor p del factor de crecimiento derivado de plaquetas, factor estimulante del crecimiento de células pre-B, factor de células madre (SCF), receptor del factor de células madre, TNF, TNF0, TNF1, TNF2, factor de crecimiento transformante a, factor de crecimiento transformante p, factor de crecimiento transformante p1, factor de crecimiento transformante p1.2, factor de crecimiento transformante p2, factor de crecimiento transformante p3, factor de crecimiento transformante p5, factor de crecimiento transformante latente p1, proteína I de unión al factor de crecimiento transformante p, proteína II de unión al factor de crecimiento transformante p, proteína III de unión al factor de crecimiento transformante p, linfopoyetina estromal tímica (TSLP), receptor de tipo I del factor de necrosis tumoral, receptor de tipo II del factor de necrosis tumoral, receptor del activador del plasminógeno de tipo urocinasa, proteína de activación de fosfolipasas (PUP), insulina, lectina, ricina, prolactina, gonadotropina coriónica, hormona foliculoestimulante, hormona estimulante del tiroides, activador tisular del plasminógeno, IgG, IgE, IgM, IgA e IgD, a-galactosidasa, p-galactosidasa, ADNasa, fetuína, hormona luteinizante, estrógeno, albúmina, lipoproteínas, fetoproteína, transferrina, trombopoyetina, urocinasa, integrina, trombina, leptina, Humira (adalimumab), Prolia (denosumab), Enbrel (etanercept), una proteína en la tabla 1, o un fragmento, derivado o variante biológicamente activo de la misma. En otra realización, la proteína terapéutica es FVIIa. En aún otra realización, la proteína terapéutica es FVIII. En todavía otra realización, la proteína terapéutica es FIX.
También se divulga un conjugado derivado de ácido graso-proteína terapéutica en el que el derivado de ácido graso se une de manera estable a la proteína terapéutica por un grupo maleimida en el ligador soluble en agua a un grupo sulfhidrilo libre en la proteína terapéutica. En todavía otra realización, el derivado de ácido graso se une de manera estable a la proteína terapéutica por un éster de N-hidroxisuccinimida en el ligador soluble en agua a un grupo amino
libre en la proteína terapéutica.
También se contemplan métodos de preparación de derivados de ácidos grasos en la presente invención. En una realización, se proporciona un método de preparación de un derivado de ácido graso descrito en el presente documento que comprende: a) oxidar un grupo ro-hidroxilo en un ácido graso para generar un grupo aldehído en el ácido graso; y b) acoplar un ligador soluble en agua que comprende un grupo aminooxilo activo al grupo aldehído para formar una unión oxima estable, en el que el derivado de ácido graso es soluble en agua. En una realización, se proporciona el método mencionado anteriormente en el que el grupo ro-hidroxilo se oxida por un reactivo de oxidación seleccionado del grupo que consiste en: reactivo de peryodinano de Dess Martin, reactivo Tempo, oxidación Swern con cloruro de oxalilo/DMSO, perrutenato de tetrapropilamonio (TPAP), reactivos de cromo VI tales como reactivo de Collins, clorocromato de piridinio (PCC) y dicromato de piridinio. En todavía otra realización, el reactivo de oxidación es peryodinano de Dess Martin.
En otra realización, se proporciona un método mencionado anteriormente en el que el ácido graso es un ácido graso saturado o ácido graso insaturado. En todavía otra realización, el ácido graso es un ácido graso saturado.
En aún otra realización de la invención, se proporciona un método mencionado anteriormente en el que el ácido graso es un ácido graso de cadena ramificada.
Según otra realización, también se proporciona un método mencionado anteriormente en el que el ácido graso comprende una longitud de cadena entre C10 y C24, incluyendo ácidos grasos sintéticos con números impares de carbonos. En una realización, se proporciona un derivado de ácido graso mencionado anteriormente en el que el ácido graso comprende una longitud de cadena seleccionada del grupo que consiste en: C10, C12, C14, C16, C18, C20, C20, C22 y C24. En otra realización, el ácido graso tiene una longitud de cadena seleccionada del grupo que consiste en C14, C16 y C18. En todavía otra, el ácido graso tiene una longitud de cadena seleccionada del grupo que consiste en C13, C15 yC17.
En todavía otra realización, se proporciona un método mencionado anteriormente en el que el ligador soluble en agua comprende un polímero soluble en agua y al menos un grupo aminooxilo.
Se contemplan numerosos polímeros solubles en agua en la presente invención para su uso en un método mencionado anteriormente. En una realización, se proporciona un método mencionado anteriormente en el que el polímero soluble en agua se selecciona del grupo que consiste en: polietilenglicol (PEG), PEG ramificado, poli(ácido siálico) (PSA), almidón de hidroxialquilo (HAS), almidón de hidroxietilo (HES), hidrato de carbono, polisacáridos, pululano, quitosano, ácido hialurónico, sulfato de condroitina, sulfato de dermatán, almidón, dextrano, carboximetildextrano, poli(óxido de alquileno) (PAO), polialquilenglicol (PAG), polipropilenglicol (PPG), polioxazolina, poliacriloilmorfolina, poli(alcohol vinílico) (PVA), policarboxilato, polivinilpirrolidona, polifosfaceno, polietileno-co-anhídrido de ácido maleico, poliestireno-co-anhídrido de ácido maleico y poli(1-hidroximetiletilenhidroximetilformal) (PHF). En una realización, el polímero soluble en agua es PEG.
También se contemplan diversas longitudes de polímeros solubles en agua. En una realización, se proporciona un método mencionado anteriormente en el que el polímero soluble en agua comprende una longitud de cadena seleccionada del grupo que consiste en O5, O7, O9, O11, O13 y O15.
En todavía otra realización, se proporciona un método mencionado anteriormente en el que el ligador soluble en agua se selecciona del grupo que consiste en:
a) 3-oxapentano-1,5-dioxiamina de fórmula:
b) 3,6,9-triaoxaundecano-1,11-dioxiamina de fórmula:
c) 3,6,9,12,15-pentaoxaheptadecano-1,17-dioxiamina de fórmula:
d) 3,6,9,12,15,18,21-heptaoxatricosano-1,23-dioxiamina de fórmula:
En aún otra realización, se proporciona un método mencionado anteriormente en el que el ligador soluble en agua es 3,6,9-triaoxaundecano-1,11-dioxiamina de fórmula:
En todavía otra realización, se proporciona un método mencionado anteriormente en el que el ligador soluble en agua es 3,6,9,12,15-pentaoxaheptadecano-1,17-dioxiamina de fórmula:
Se contemplan todavía otros métodos para elaborar los derivados de ácidos grasos en el presente documento. En una realización, se proporciona un método de preparación de un derivado de ácido graso mencionado anteriormente que comprende: a) esterificar un grupo carboxilo en un ácido graso para generar un éster en el ácido graso; b) activar un grupo ro-hidroxilo en un ácido graso mediante la introducción de un grupo mesilo en el ácido graso de la etapa a); y c) acoplar un ligador soluble en agua que comprende un grupo aminooxilo activo sustituyendo el grupo mesilo de la etapa b) formándose así un enlace oxiamina-metileno estable; en el que el derivado de ácido graso es soluble en agua.
En una realización, se proporciona lo mencionado anteriormente en el que el grupo carboxilo se esterifica por un agente de esterificación seleccionado del grupo que consiste en: cloruro de acetilo, metanol en presencia de ácido, etanol en presencia de ácido, diazometano y yoduro de metilo. En otra realización, el agente de esterificación es cloruro de acetilo.
En todavía otra realización, se proporciona lo mencionado anteriormente en el que el grupo ro-hidroxilo se activa por un agente de activación seleccionado del grupo que consiste en: cloruro de mesilo, cloruro de tosilo y cloruro de nosilo. En una realización, el agente de activación es cloruro de mesilo.
Se contemplan diversos ácidos grasos para su uso en el método mencionado anteriormente. En una realización, se proporciona lo mencionado anteriormente en el que el ácido graso es un ácido graso saturado o ácido graso insaturado. En otra realización, el ácido graso es un ácido graso saturado. En aún otra realización, el ácido graso es un ácido graso de cadena ramificada.
En todavía otra realización, se proporciona el método mencionado anteriormente en el que el ácido graso comprende una longitud de cadena entre C10 y C24, incluyendo ácidos grasos sintéticos con números impares de carbonos. En una realización, se proporciona un derivado de ácido graso mencionado anteriormente en el que el ácido graso comprende una longitud de cadena seleccionada del grupo que consiste en: C10, C12, C14, C16, C18, C20, C20, C22 y C24. En otra realización, el ácido graso tiene una longitud de cadena seleccionada del grupo que consiste en C14, C16 y C18. En todavía otra, el ácido graso tiene una longitud de cadena seleccionada del grupo que consiste en C13, C15 y C17.
También se contemplan diversos polímeros solubles en agua para su uso en el método mencionado anteriormente. En una realización, se proporciona el método mencionado anteriormente en el que el ligador soluble en agua comprende un polímero soluble en agua y al menos un grupo aminooxilo. En otra realización, el polímero soluble en agua se selecciona del grupo que consiste en: polietilenglicol (PEG), PEG ramificado, poli(ácido siálico) (PSA), almidón de hidroxialquilo (HAS), almidón de hidroxietilo (HES), hidrato de carbono, polisacáridos, pululano quitosano, ácido hialurónico, sulfato de condroitina, sulfato de dermatán, almidón, dextrano, carboximetildextrano, poli(óxido de alquileno) (PAO), polialquilenglicol (PAG), polipropilenglicol (PPG), polioxazolina, poliacriloilmorfolina, poli(alcohol vinílico) (PVA), policarboxilato, polivinilpirrolidona, polifosfaceno, polietileno-co-anhídrido de ácido maleico, poliestireno-co-anhídrido de ácido maleico, y poli(1-hidroximetiletilenhidroximetilformal) (PHF). En otra realización, el polímero soluble en agua es PEG.
En todavía otra realización de la invención, se proporciona un método mencionado anteriormente en el que el polímero soluble en agua comprende una longitud de cadena seleccionada del grupo que consiste en O3, O5, O7, O9, O11, O13 y O15. En otra realización, el ligador soluble en agua se selecciona del grupo que consiste en:
También se contemplan métodos de preparación de proteínas conjugadas en la presente invención. En una realización, se proporciona un método de preparación de una proteína terapéutica conjugada que comprende poner en contacto un resto de hidrato de carbono oxidado en la proteína terapéutica con un derivado de ácido graso mencionado anteriormente (o un polímero soluble en agua tal como se describe en el presente documento) en
condiciones que permitan la conjugación; el resto de hidrato de carbono oxidado por incubación con un tampón que comprende un agente oxidante seleccionado del grupo que consiste en peryodato de sodio (NaIO4), tetraacetato de plomo (Pb(OAc)4 ) y perrutenato de potasio (KRuO4 ); en el que se forma una unión oxima entre el resto de hidrato de carbono oxidado y el grupo aminooxilo activo en el derivado de ácido graso; y en el que la formación de unión oxima se cataliza por un catalizador nucleófilo seleccionado del grupo que consiste en ácido o-aminobenzoico, ácido m-aminobenzoico, ácido p-aminobenzoico, ácido sulfanílico, o-aminobenzamida, o-toluidina, m-toluidina, p-toluidina, o-anisidina, m-anisidina y p-anisidina.
En otra realización, se proporciona el método mencionado anteriormente en el que la proteína terapéutica se selecciona del grupo que consiste en: factor IX (FIX), factor VIII (FVIII), factor VIIa (FVIIa), factor de von Willebrand (VWF), factor V (FV), factor X (FX), factor XI (FXI), factor XII (FXII), trombina (FII), proteína C, proteína S, tPA, PAI-1, tromboplastina tisular(TF),proteasa ADAMTS 13, IL-1 alfa, IL-1 beta, IL-2, IL-3, IL-4, IL-5, IL-6, IL-11, factor estimulante de colonias 1 (CSF-1), M-CSF, SCF, GM-CSF, factor estimulante de colonias de granulocitos (G-CSF), EPO, interferón alfa (IFN-alfa), interferón de consenso, IFN-beta, IFN-gamma, IFN-omega, IL-7, IL-8, IL-9, IL-10, IL-12, IL-13, IL-14, IL-15, IL-16, IL-17, IL-18, IL-19, IL-20, IL-21, IL-22, IL-23, IL-24, IL-31, IL-32 alfa, IL-33, trombopoyetina (TPO), Ang-1, Ang-2, Ang-4, Ang-Y, polipéptido similar a angiopoyetina 1 (ANGPTL1), polipéptido similar a angiopoyetina 2 (ANGPTL2), polipéptido similar a angiopoyetina 3 (ANGPTL3), polipéptido similar a angiopoyetina 4 (ANGPTL4), polipéptido similar a angiopoyetina 5 (ANGPTL5), polipéptido similar a angiopoyetina 6 (ANGPTL6), polipéptido similar a angiopoyetina 7 (ANGPTl7), vitronectina, factor de crecimiento endotelial vascular (VEGF), angiogenina, activina A, activina B, activina C, proteína morfogénica ósea 1, proteína morfogénica ósea 2, proteína morfogénica ósea 3, proteína morfogénica ósea 4, proteína morfogénica ósea 5, proteína morfogénica ósea 6, proteína morfogénica ósea 7, proteína morfogénica ósea 8, proteína morfogénica ósea 9, proteína morfogénica ósea 10, proteína morfogénica ósea 11, proteína morfogénica ósea 12, proteína morfogénica ósea 13, proteína morfogénica ósea 14, proteína morfogénica ósea 15, receptor IA de proteínas morfogénicas óseas, receptor IB de proteínas morfogénicas óseas, receptor II de proteínas morfogénicas óseas, factor neurotrófico derivado del cerebro, cardiotrofina 1, factor neurotrófico ciliar, receptor del factor neurotrófico ciliar, cripto, críptico, factor quimiotáctico de neutrófilos inducido por citocinas 1, factor quimiotáctico de neutrófilos inducido por citocinas 2a, factor quimiotáctico de neutrófilos inducido por citocinas 2p, factor de crecimiento de células endoteliales p, endotelina 1, factor de crecimiento epidérmico, Epigen, epirregulina, factor quimiotáctico para neutrófilos derivado de células epiteliales, factor de crecimiento de fibroblastos 4, factor de crecimiento de fibroblastos 5, factor de crecimiento de fibroblastos 6, factor de crecimiento de fibroblastos 7, factor de crecimiento de fibroblastos 8, factor de crecimiento de fibroblastos 8b, factor de crecimiento de fibroblastos 8c, factor de crecimiento de fibroblastos 9, factor de crecimiento de fibroblastos 10, factor de crecimiento de fibroblastos 11, factor de crecimiento de fibroblastos 12, factor de crecimiento de fibroblastos 13, factor de crecimiento de fibroblastos 16, factor de crecimiento de fibroblastos 17, factor de crecimiento de fibroblastos 19, factor de crecimiento de fibroblastos 20, factor de crecimiento de fibroblastos 21, factor de crecimiento ácido de fibroblastos, factor de crecimiento básico de fibroblastos, receptor a1 del factor neurotrófico derivado de la línea celular glial, receptor a2 del factor neurotrófico derivado de la línea celular glial, proteína relacionada con el crecimiento, proteína relacionada con el crecimiento a, proteína relacionada con el crecimiento p, proteína relacionada con el crecimiento y, factor de crecimiento epidérmico de unión a heparina, factor de crecimiento de hepatocitos, receptor del factor de crecimiento de hepatocitos, factor de crecimiento derivado del hepatoma, factor de crecimiento similar a la insulina I, receptor del factor de crecimiento similar a la insulina, factor de crecimiento similar a la insulina II, proteína de unión al factor de crecimiento similar a la insulina, factor de crecimiento de queratinocitos, factor inhibidor de la leucemia, receptor a del factor inhibidor de la leucemia, factor de crecimiento nervioso, receptor del factor de crecimiento nervioso, neuropoyetina, neurotrofina 3, neurotrofina 4, oncostatina M (OSM), factor de crecimiento placentario, factor de crecimiento placentario 2, factor de crecimiento de células endoteliales derivado de plaquetas, factor de crecimiento derivado de plaquetas, cadena A del factor de crecimiento derivado de plaquetas, factor de crecimiento derivado de plaquetas a A, factor de crecimiento derivado de plaquetas AB, cadena B del factor de crecimiento derivado de plaquetas, factor de crecimiento derivado de plaquetas BB, receptor a del factor de crecimiento derivado de plaquetas, receptor p del factor de crecimiento derivado de plaquetas, factor estimulante del crecimiento de células pre-B, factor de células madre (SCF), receptor del factor de células madre, TNF, TNF0, TNF1, TNF2, factor de crecimiento transformante a, factor de crecimiento transformante p, factor de crecimiento transformante p1, factor de crecimiento transformante p1.2, factor de crecimiento transformante p2, factor de crecimiento transformante p3, factor de crecimiento transformante p5, factor de crecimiento transformante latente p1, proteína I de unión al factor de crecimiento transformante p, proteína II de unión al factor de crecimiento transformante p, proteína III de unión al factor de crecimiento transformante p, linfopoyetina estromal tímica (TSLP), receptor de tipo I del factor de necrosis tumoral, receptor de tipo II del factor de necrosis tumoral, receptor del activador del plasminógeno de tipo urocinasa, proteína de activación de fosfolipasas (PUP), insulina, lectina, ricina, prolactina, gonadotropina coriónica, hormona foliculoestimulante, hormona estimulante del tiroides, activador tisular del plasminógeno, IgG, IgE, IgM, IgA e IgD, agalactosidasa, p-galactosidasa, ADNasa, fetuína, hormona luteinizante, estrógeno, albúmina, lipoproteínas, fetoproteína, transferrina, trombopoyetina, urocinasa, integrina, trombina, leptina, Humira (adalimumab), Prolia (denosumab), Enbrel (etanercept), una proteína en la tabla 1, o un fragmento, derivado o variante biológicamente activo de la misma.
En otra realización, se proporciona el método mencionado anteriormente en el que la proteína terapéutica es FVIIa. En todavía aún otra realización, se proporciona el método mencionado anteriormente en el que la proteína terapéutica
es FVIII. En aún otra realización, se proporciona el método mencionado anteriormente en el que la proteína terapéutica es FIX.
En todavía otra realización, se proporciona el método mencionado anteriormente en el que el agente oxidante es peryodato de sodio (NaIO4). En otra realización, se proporciona el método mencionado anteriormente en el que el catalizador nucleófilo es m-toluidina.
En aún otra realización, se proporciona el método mencionado anteriormente que comprende además purificar la proteína terapéutica conjugada.
En todavía otra realización, se proporciona el método mencionado anteriormente en el que el derivado de ácido graso se prepara mediante un método tal como se describe en el presente documento.
Se contemplan todavía otros métodos de preparación de derivados de ácidos grasos en la presente divulgación. En una realización, se proporciona un método de preparación de un derivado de ácido graso mencionado anteriormente que comprende: a) esterificar un grupo carboxilo en un ácido graso para generar un éster en el ácido graso; y b) acoplar un ligador soluble en agua que comprende un grupo maleimida activo a un grupo sulfhidrilo (SH) libre, formándose así un enlace tioéter estable; en el que el derivado de ácido graso es soluble en agua.
En todavía otra realización de la presente divulgación, se proporciona un método de preparación de un derivado de ácido graso mencionado anteriormente que comprende: a) esterificar un grupo carboxilo en un ácido graso para generar éster de ácido graso; b) hacer reaccionar el ácido graso resultante de la etapa a) con un reactivo de azida produciendo así una azida de ácido graso correspondiente; c) hidrogenar la azida de ácido graso de la etapa b) para producir una amina de ácido graso correspondiente; y d) acoplar un ligador soluble en agua que comprende un grupo NHS activo a un grupo amina libre, formando así un enlace estable; en el que el derivado de ácido graso es soluble en agua.
Figuras
La figura 1 muestra la síntesis del ligador soluble en agua 3-oxapentano-1,5-dioxiamina.
Descripción detallada de la invención
Las propiedades farmacológicas e inmunológicas de las proteínas terapéuticas pueden mejorarse mediante modificación y conjugación química con compuestos poliméricos tales como ácidos grasos y derivados de ácidos grasos según la presente invención.
La adición de un derivado de ácido graso soluble en agua tal como se describe en el presente documento es un enfoque para mejorar las propiedades de proteínas terapéuticas tales como las proteínas de la coagulación sanguínea factor IX (FIX), factor VIII (FVIII), factor VIIa (FVIIa), factor de von Willebrand (VWF), factor V (FV), factor X (FX), factor XI (FXI), factor XII (FXII), trombina (FII), proteína C, proteína S, tPA, PAI-1, tromboplastina tisular (TF) o proteasa ADAMTS 13, así como otras proteínas conocidas o fragmentos biológicamente/terapéuticamente activos de las mismas.
Proteínas terapéuticas
En determinadas realizaciones de la invención, los polipéptidos y polinucleótidos mencionados anteriormente se ejemplifican por las siguientes proteínas terapéuticas: enzimas, antígenos, anticuerpos, receptores, proteínas de coagulación sanguínea, factores de crecimiento, hormonas y ligandos. En determinadas realizaciones, la proteína terapéutica es una proteína de coagulación sanguínea tal como factor IX (FIX), factor VIII (FVIII), factor VIIa (FVIIa), factor de von Willebrand (VWF), factor V (FV), factor X (FX), factor XI (FXI), factor XII (FXII), trombina (FII), proteína C, proteína S, tPA, PAI-1, tromboplastina tisular (TF) o proteasa ADAMTS 13.
En determinadas realizaciones, la proteína terapéutica es inmunoglobulinas, citocinas tales como IL-1 alfa, IL-1 beta, IL-2, IL-3, IL-4, IL-5, IL-6, IL-11, factor estimulante de colonias 1 (CSF-1), M-CSF, SCF, GM-CSF, factor estimulante de colonias de granulocitos (G-CSF), EPO, interferón alfa (IFN-alfa), interferón de consenso, IFN-beta, IFN-gamma, IFN-omega, IL-7, IL-8, IL-9, IL-10, IL-12, IL-13, IL-14, IL-15, IL-16, IL-17, IL-18, IL-19, IL-20, IL-21, IL-22, IL-23, IL-24, IL-31, IL-32 alfa, IL-33, trombopoyetina (TPO), angiopoyetinas, por ejemplo Ang-1, Ang-2, Ang-4, Ang-Y, los polipéptidos similares a angiopoyetinas humanos ANGPTL1 a 7, vitronectina, factor de crecimiento endotelial vascular (VEGF), angiogenina, activina A, activina B, activina C, proteína morfogénica ósea 1, proteína morfogénica ósea 2, proteína morfogénica ósea 3, proteína morfogénica ósea 4, proteína morfogénica ósea 5, proteína morfogénica ósea 6, proteína morfogénica ósea 7, proteína morfogénica ósea 8, proteína morfogénica ósea 9, proteína morfogénica ósea 10, proteína morfogénica ósea 11, proteína morfogénica ósea 12, proteína morfogénica ósea 13, proteína morfogénica ósea 14, proteína morfogénica ósea 15, receptor IA de proteínas morfogénicas óseas, receptor IB de proteínas morfogénicas óseas, receptor II de proteínas morfogénicas óseas, factor neurotrófico derivado del cerebro, cardiotrofina 1, factor neurotrófico ciliar, receptor del factor neurotrófico ciliar, cripto, críptico, factor quimiotáctico de
neutrófilos inducido por citocinas 1, factor quimiotáctico de neutrófilos inducido por citocinas 2a, factor quimiotáctico de neutrófilos inducido por citocinas 2p, factor de crecimiento de células endoteliales p, endotelina 1, factor de crecimiento epidérmico, Epigen, epirregulina, factor quimiotáctico de neutrófilos derivado de células epiteliales, factor de crecimiento de fibroblastos 4, factor de crecimiento de fibroblastos 5, factor de crecimiento de fibroblastos 6, factor de crecimiento de fibroblastos 7, factor de crecimiento de fibroblastos 8, factor de crecimiento de fibroblastos 8b, factor de crecimiento de fibroblastos 8c, factor de crecimiento de fibroblastos 9, factor de crecimiento de fibroblastos 10, factor de crecimiento de fibroblastos 11, factor de crecimiento de fibroblastos 12, factor de crecimiento de fibroblastos 13, factor de crecimiento de fibroblastos 16, factor de crecimiento de fibroblastos 17, factor de crecimiento de fibroblastos 19, factor de crecimiento de fibroblastos 20, factor de crecimiento de fibroblastos 21, factor de crecimiento ácido de fibroblastos, factor de crecimiento básico de fibroblastos, receptor a1 del factor neurotrófico derivado de la línea celular glial, receptor a2 del factor neurotrófico derivado de la línea celular glial, proteína relacionada con el crecimiento, proteína relacionada con el crecimiento a, proteína relacionada con el crecimiento p, proteína relacionada con el crecimiento y, factor de crecimiento epidérmico de unión a heparina, factor de crecimiento de hepatocitos, receptor del factor de crecimiento de hepatocitos, factor de crecimiento derivado del hepatoma, factor de crecimiento similar a la insulina I, receptor del factor de crecimiento similar a la insulina, factor de crecimiento similar a insulina II, proteína de unión al factor de crecimiento similar a la insulina, factor de crecimiento de queratinocitos, factor inhibidor de la leucemia, receptor a del factor inhibidor de la leucemia, factor de crecimiento nervioso, receptor del factor de crecimiento nervioso, neuropoyetina, neurotrofina 3, neurotrofina 4, oncostatina M (OSM), factor de crecimiento placentario, factor de crecimiento placentario 2, factor de crecimiento de células endoteliales derivado de plaquetas, factor de crecimiento derivado de plaquetas, cadena A del factor de crecimiento derivado de plaquetas, factor de crecimiento derivado de plaquetas AA, factor de crecimiento derivado de plaquetas AB, cadena B del factor de crecimiento derivado de plaquetas, factor de crecimiento derivado de plaquetas BB, receptor a del factor de crecimiento derivado de plaquetas, receptor p del factor de crecimiento derivado de plaquetas, factor estimulante del crecimiento de células pre-B, factor de células madre (SCF), receptor del factor de células madre, TNF, incluyendo TNF0, TNF1, TNF2, factor de crecimiento transformante a, factor de crecimiento transformante p, factor de crecimiento transformante p1, factor de crecimiento transformante p1.2, factor de crecimiento transformante p2, factor de crecimiento transformante p3, factor de crecimiento transformante p5, factor de crecimiento transformante latente p1, proteína I de unión al factor de crecimiento transformante p, proteína II de unión al factor de crecimiento transformante p, proteína III de unión al factor de crecimiento transformante p, linfopoyetina estromal tímica (TSLP), receptor de tipo I del factor de necrosis tumoral, receptor de tipo II del factor de necrosis tumoral, receptor del activador del plasminógeno de tipo urocinasa, factor de crecimiento endotelial vascular, y proteínas quiméricas y fragmentos biológica o inmunológicamente activos de las mismas.
En determinadas realizaciones, la proteína terapéutica es interferones alfa, beta y gamma, factores estimulantes de colonias incluyendo factores estimulante de colonias de granulocitos, factores de crecimiento de fibroblastos, factores de crecimiento derivados de plaquetas, proteína de activación de fosfolipasas (PUP), insulina, proteínas vegetales tales como lectinas y ricinas, factores de necrosis tumoral y alelos relacionados, formas solubles de receptores de los factores de necrosis tumoral, receptores de interleucinas y formas solubles de receptores de interleucinas, factores de crecimiento tales como factores de crecimiento tisular, tales como TGFa o TGFp y factores de crecimiento epidérmico, hormonas, somatomedinas, hormonas pigmentarias, factores de liberación hipotalámicos, hormonas antidiuréticas, prolactina, gonadotropina coriónica, hormona foliculoestimulante, hormona estimulante del tiroides, activador tisular del plasminógeno e inmunoglobulinas tales como IgG, IgE, IgM, IgA e IgD, una galactosidasa, a-galactosidasa, pgalactosidasa, ADNasa, fetuína, hormona luteinizante, estrógeno, corticosteroides, albúmina, lipoproteínas, fetoproteína, transferrina, trombopoyetina, urocinasa, ADNasa, integrinas, trombina, factores de crecimiento hematopoyéticos, leptina, glicosidasas, Humira (adalimumab), Prolia (denosumab), Enbrel (etanercept), y fragmentos de los mismos, o cualquier proteína de fusión que comprende cualquiera de las proteínas mencionadas anteriormente o fragmentos de las mismas. Además de las proteínas mencionadas anteriormente, la siguiente tabla 1 proporciona proteínas terapéuticas contempladas por la presente invención:
Las proteínas terapéuticas proporcionadas en el presente documento no deben considerarse exclusivas. Más bien, como es evidente a partir de la divulgación proporcionada en el presente documento, los métodos de la invención son aplicables a cualquier proteína en la que se desee la unión de un derivado de ácido graso soluble en agua según la invención. Por ejemplo, se describen proteínas terapéuticas en el documento US 2007/0026485.
Proteínas de la coagulación sanguínea
En un aspecto, el material de partida de la presente invención es una proteína de la coagulación sanguínea, que puede derivarse del plasma humano o producirse mediante técnicas de ingeniería recombinante, tal como se describe en las patentes: patente estadounidense n.° 4.757.006; patente estadounidense n.° 5.733.873; patente estadounidense n.° 5.198.349; patente estadounidense n.° 5.250.421; patente estadounidense n.° 5.919.766; y documento EP 306968.
Los polipéptidos terapéuticos tales como proteínas de la coagulación sanguínea incluyendo factor IX (FIX), factor VIII (FVIII), factor VIIa (FVIIa), factor de von Willebrand (VWF), factor V (FV), factor X (FX), factor XI (FXI), factor XII (FXII), trombina (FII), proteína C, proteína S, tPA, PAI-1, tromboplastina tisular (TF) y proteasa ADAMTS 13 se degradan rápidamente por enzimas proteolíticas y se neutralizan por anticuerpos. Esto reduce su semivida y tiempo de circulación, limitando así su eficacia terapéutica. Se necesitan dosis relativamente altas y una administración frecuente para alcanzar y mantener el efecto terapéutico o profiláctico deseado de estas proteínas de la coagulación. Como consecuencia, la regulación adecuada de la dosis es difícil de obtener y la necesidad de administraciones intravenosas frecuentes impone restricciones en la forma de vida del paciente.
Tal como se describe en el presente documento, las proteínas de la coagulación sanguínea incluyendo, pero sin limitarse a, factor IX (FIX), factor VIII (FVIII), factor VIIa (FVIIa), factor de von Willebrand (VWF), factor V (FV), factor X (FX), factor XI, factor XII (FXII), trombina (FII), proteína C, proteína S, tPA, PAI-1, tromboplastina tisular (TF) y proteasa ADAMTS 13 están contempladas por la invención. Tal como se usa en el presente documento, el término “proteína de coagulación sanguínea” se refiere a cualquier factor IX (FIX), factor VIII (FVIII), factor VIIa (FVIIa), factor de von Willebrand (VWF), factor FV (FV), factor X (FX), factor XII (Fx II), trombina (FII), proteína C, proteína S, tPA, PAI-1, tromboplastina tisular (TF) y proteasa ADAMTS 13 que presenta actividad biológica asociada con esa proteína de la coagulación sanguínea nativa particular.
La cascada de la coagulación sanguínea se divide en tres segmentos distintos: las rutas intrínseca, extrínseca y común (Schenone et al., Curr Opin Hematol. 2004; 11: 272-7). La cascada implica una serie de enzimas serina proteasa (zimógenos) y cofactores de proteínas. Cuando se requiere, un precursor de zimógeno inactivo se convierte en la forma activa, que en consecuencia convierte la siguiente enzima en la cascada.
La ruta intrínseca requiere los factores de coagulación VIII, IX, X, XI y XII. El inicio de la ruta intrínseca se produce cuando la precalicreína, el quininógeno de alto peso molecular, el factor XI (FXI) y el factor XII (FXII) se exponen a una superficie cargada negativamente. También se requieren iones de calcio y fosfolípidos secretados por las plaquetas.
La ruta extrínseca se inicia cuando se daña la luz vascular de los vasos sanguíneos. La glicoproteína tromboplastina tisular de membrana se expone y luego se une al factor circulante VII (FVII) y a pequeñas cantidades preexistentes de su forma activada FVIIa. Esta unión facilita la conversión completa de FVII a FVIIa y, posteriormente, en presencia de calcio y fosfolípidos, la conversión del factor IX (FIX) a factor IXa (FIXa) y factor X (FX) a factor Xa (FXa). La asociación de FVIIa con tromboplastina tisular mejora la actividad proteolítica al acercar los sitios de unión de FVII para el sustrato (FIX y FX) e inducir un cambio conformacional, que mejora la actividad enzimática de FVIIa.
La activación de FX es el punto común de las dos rutas. Junto con el fosfolípido y el calcio, los factores Va (FVa) y Xa convierten la protrombina en trombina (complejo de protrombinasa), que luego escinde el fibrinógeno para formar monómeros de fibrina. Los monómeros se polimerizan para formar hebras de fibrina. El factor XIIIa (FXIIIa) une de manera covalente estos hilos entre sí para formar una malla rígida.
La conversión de FVII en FVIIa también está catalizada por una serie de proteasas, incluyendo trombina, FIXa, FXa, factor XIa (FXIa) y factor XIIa (FXIIa). Para la inhibición de la fase temprana de la cascada, el inhibidor de la ruta de la tromboplastina tisular selecciona como diana el complejo de productos FVIIa/tromboplastina tisular/FXa.
Factor VIIa
El FVII (también conocido como factor estable o proconvertina) es una glicoproteína de serina proteasa dependiente de vitamina K con un papel fundamental en la hemostasia y la coagulación (Figenbrot, Curr Protein Pept Sci. 2002; 3: 287-99).
El FVII se sintetiza en el hígado y se secreta como una glicoproteína monocatenaria de 48 kD. FVII comparte con todas las glicoproteínas de serina proteasa dependientes de vitamina K una estructura de dominio de proteína similar que consiste en un dominio de ácido gamma-carboxiglutámico (Gla) amino-terminal con 9-12 residuos responsables
de la interacción de la proteína con las membranas lipídicas, un dominio carboxi-terminal de serina proteasa (dominio catalítico) y dos dominios similares al factor de crecimiento epidérmico que contienen un sitio de unión a iones de calcio que media la interacción con la tromboplastina tisular. La gamma-glutamil carboxilasa cataliza la carboxilación de residuos Gla en la porción amino-terminal de la molécula. La carboxilasa depende de una forma reducida de vitamina K para su acción, que se oxida a la forma de epóxido. La vitamina K epóxido reductasa es necesaria para convertir de nuevo la forma de epóxido de vitamina K en la forma reducida.
La mayor proporción de FVII circula en plasma en forma de zimógeno, y la activación de esta forma da como resultado la escisión del enlace peptídico entre la arginina 152 y la isoleucina 153. El FVIIa activado resultante consiste en una cadena ligera derivada de NH2 (20 kD) y una cadena pesada derivada de COOH terminal (30 kD) unida a través de un enlace disulfuro único (Cys 135 a Cys 262). La cadena ligera contiene el dominio Gla de unión a la membrana, mientras que la cadena pesada contiene el dominio catalítico.
La concentración plasmática de FVII determinada por factores genéticos y ambientales es de aproximadamente 0,5 mg/ml (Pinotti et al., Blood. 2000; 95: 3423-8). Los genotipos de FVII diferentes pueden dar lugar a diferencias de varias veces en los niveles medios de FVII. Los niveles plasmáticos de FVII son elevados durante el embarazo en mujeres sanas y también aumentan con la edad y son más altos en mujeres y en personas con hipertrigliceridemia. El FVII tiene la semivida más corta de todos los factores procoagulantes (3-6 h). La concentración plasmática media de FVIIa es de 3,6 ng/ml en individuos sanos y la semivida circulante de FVIIa es relativamente larga (2,5 h) en comparación con otros factores de coagulación.
La deficiencia hereditaria de FVII es un trastorno hemorrágico autosómico recesivo poco frecuente con una prevalencia estimada en 1 caso por 500.000 personas en la población general (Acharya et al., J Thromb Haemost. 2004; 2248 56). La deficiencia adquirida de FVII de los inhibidores también es muy rara. También se han notificado casos en los que la deficiencia se produce en asociación con fármacos tales como cefalosporinas, penicilinas y anticoagulantes orales. Además, se ha notificado que la deficiencia adquirida de FVII se produce espontáneamente o con otros estados, tales como mieloma, septicemia, anemia aplásica, con terapia con interleucina 2 y concentrado de inmunoglobulinas antitimocíticas.
Las secuencias de polinucleótidos y polipéptidos de referencia incluyen, por ejemplo, los números de registro de GenBank J02933 para la secuencia genómica, M13232 para el ADNc (Hagen et al. p Na S 1986; 83: 2412-6) y P08709 para la secuencia de polipéptidos. Se ha descrito una variedad de polimorfismos de FVII, por ejemplo, véase, Sabater-Lleal et al. (Hum Genet.2006; 118: 741-51).
Factor IX
FIX es una proteína plasmática dependiente de la vitamina K que participa en la ruta intrínseca de la coagulación sanguínea al convertir FX a su forma activa en presencia de iones de calcio, fosfolípidos y FVIIIa. La capacidad catalítica predominante de FIX es como una serina proteasa con especificidad para un enlace arginina-isoleucina particular en FX. La activación de FIX se produce por FXIa que provoca la escisión del péptido de activación de FIX para producir una molécula FIX activada que comprende dos cadenas mantenidas por uno o más enlaces disulfuro. Los defectos en FIX son la causa de la hemofilia B recesiva ligada al cromosoma X.
La hemofilia A y B son enfermedades hereditarias caracterizadas por deficiencias en los polipéptidos FVIII y FIX, respectivamente. La causa subyacente de las deficiencias es con frecuencia el resultado de mutaciones en los genes FVIII y FIX, que se encuentran en el cromosoma X. La terapia tradicional para las hemofilias a menudo implica la administración intravenosa de mezcla de plasmas o proteínas de coagulación semipurificadas de individuos normales. Estas preparaciones pueden estar contaminadas por agentes patógenos o virus, como priones infecciosos, VIH, parvovirus, hepatitis A y hepatitis C. Por tanto, existe la necesidad urgente de agentes terapéuticos que no requieran el uso de suero humano.
El nivel de la disminución en la actividad de FIX es directamente proporcional a la gravedad de la hemofilia B. El tratamiento actual de la hemofilia B consiste en el reemplazo de la proteína que falta por FIX recombinante o derivado del plasma (denominado tratamiento o terapia de sustitución o reemplazo de FIX).
Las secuencias de polinucleótidos y polipéptidos de FIX pueden encontrarse, por ejemplo, en el n.° de registro de UniProtKB/Swiss-Prot P00740, y en la patente estadounidense n.° 6.531.298.
Factor VIII
El factor VIII de la coagulación (FVIII) circula en plasma a una concentración muy baja y se une de forma no covalente al factor de von Willebrand (VWF). Durante la hemostasia, el FVIII se separa del v W f y actúa como cofactor para la activación de FX mediada por el factor IX activado (FIXa) mejorando la velocidad de activación en presencia de calcio y fosfolípidos o membranas celulares.
El FVIII se sintetiza como un precursor de cadena sencilla de aproximadamente 270-330 kD con la estructura de
dominio A1-A2-B-A3-C1-C2. Cuando se purifica a partir de plasma (por ejemplo, “derivado de plasma” o “plasmático”), el FVIII se compone de una cadena pesada (A1-A2-B) y una cadena ligera (A3-C1-C2). La masa molecular de la cadena ligera es de 80 kD, mientras que, debido a la proteólisis en el dominio B, la cadena pesada está en el intervalo de 90-220 kD.
El FVIII también se sintetiza como una proteína recombinante para uso terapéutico en trastornos hemorrágicos. Se han ideado diversos ensayos in vitro para determinar la eficacia potencial del FVIII recombinante (rFVIII) como medicamento terapéutico. Estos ensayos imitan los efectos in vivo del FVIII endógeno. El tratamiento con trombina in vitro del FVIII da como resultado un aumento rápido y la disminución posterior en su actividad procoagulante, tal como se mide mediante ensayos in vitro. Esta activación e inactivación coincide con proteólisis limitada específica tanto en las cadenas pesadas como en las ligeras, que alteran la disponibilidad de diferentes epítopos de unión en FVIII, por ejemplo, permitiendo que FVIII se disocie de VWF y se una a una superficie de fosfolípidos o alterando la capacidad de unión a determinados anticuerpos monoclonales.
La falta o disfunción del FVIII se asocia con el trastorno hemorrágico más frecuente, la hemofilia A. El tratamiento de elección para el tratamiento de la hemofilia A es la terapia de reemplazo con concentrados derivados de plasma o rFVIII. Los pacientes con hemofilia A grave con niveles de FVIII por debajo del 1%, reciben generalmente terapia profiláctica con el objetivo de mantener el FVIII por encima del 1% entre dosis. Teniendo en cuenta las semividas promedio de los diversos productos de FVIII en la circulación, este resultado puede lograrse habitualmente administrando FVIII de dos a tres veces por semana.
Las secuencias de polinucleótidos y polipéptidos de referencia incluyen, por ejemplo, UniProtKB/Swiss-Prot P00451 (FA8_HUMAN); Gitschier J et al., Characterization ofthe human factor VIII gene, Nature, 312(5992): 326-30 (1984); Vehar GH et al., Structure of human factor VIII, Nature, 312(5992):337-42 (1984); Thompson AR. Structure and Function ofthe factor VIII gene and protein, Semin Thromb Hemost, 2003:29;11-29 (2002).
Factor de von Willebrand
El factor de von Willebrand (VWF) es una glicoproteína que circula en plasma como una serie de multímeros que oscilan en tamaño desde aproximadamente 500 hasta 20.000 kD. Las formas multiméricas de VWF se componen de subunidades de polipéptidos de 250 kD unidas entre sí por enlaces disulfuro. El VWF media la adhesión plaquetaria inicial al subendotelio de la pared del vaso dañado. Solo los multímeros más grandes presentan actividad hemostática. Se supone que las células endoteliales secretan grandes formas poliméricas de VWF y las formas de VWF que tienen un bajo peso molecular (VWF de bajo peso molecular) surgen de la escisión proteolítica. Los multímeros que tienen grandes masas moleculares se almacenan en los cuerpos de Weibel-Pallade de células endoteliales y se liberan tras la estimulación.
El VWF se sintetiza por las células endoteliales y los megacariocitos como prepro-VWF que consiste en gran medida en dominios repetidos. Tras la escisión del péptido señal, el pro-VWF se dimeriza a través de enlaces disulfuro en su región C-terminal. Los dímeros sirven como protómeros para la multimerización, que se rige por uniones disulfuro entre los extremos terminales libres. El ensamblaje en multímeros es seguido por la eliminación proteolítica de la secuencia de propéptido (Leyte et al., Biochem. J. 274 (1991), 257-261).
El producto de traducción primario predicho a partir del ADNc clonado de VWF es un polipéptido precursor de 2813 residuos (prepro-VWF). El prepro-VWF consiste en un péptido señal de 22 aminoácidos y un propéptido de 741 aminoácidos, con el VWF maduro que comprende 2050 aminoácidos (Ruggeri Z.A., y Ware, J., FASEB J., 308-316 (1993).
Los defectos en el VWF son causales de la enfermedad de von Willebrand (VWD), que se caracteriza por un fenotipo hemorrágico más o menos pronunciado. La VWD tipo 3 es la forma más grave en la que falta completamente el VWF, y el VWD tipo 1 se refiere una pérdida cuantitativa de VWF y su fenotipo puede ser muy leve. La VWD tipo 2 se refiere a defectos cualitativos de VWF y puede ser tan grave como VWD tipo 3. La VWD tipo 2 tiene muchas subformas, algunas asociadas con la pérdida o la disminución de multímeros de alto peso molecular. La enfermedad de von Willebrand tipo 2a (VWD-2A) se caracteriza por una pérdida de multímeros intermedios y grandes. La VWD-2B se caracteriza por una pérdida de multímeros de mayor peso molecular. Otras enfermedades y trastornos relacionados con VWF son conocidos en la técnica.
Las secuencias de polinucleótidos y aminoácidos de prepro-VWF están disponibles en los n.os de registro de GenBank NM_000552 y NP_000543, respectivamente.
Otras proteínas de coagulación sanguínea según la presente invención se describen en la técnica, por ejemplo, Mann KG, Thromb Haemost, 1999;82:165-74.
A. Polipéptidos
En un aspecto, el material de partida de la presente invención es una proteína o polipéptido. Tal como se describe en
el presente documento, el término proteína terapéutica se refiere a cualquier molécula de proteína terapéutica que presenta actividad biológica que está asociada con la proteína terapéutica. En una realización de la invención, la molécula de proteína terapéutica es una proteína de longitud completa.
Las moléculas de proteínas terapéuticas contempladas incluyen proteínas de longitud completa, precursores de proteínas de longitud completa, subunidades biológicamente activas o fragmentos de proteínas de longitud completa, así como derivados y variantes biológicamente activos de cualquiera de estas formas de proteínas terapéuticas. Por tanto, las proteínas terapéuticas incluyen aquellas que (1) tienen una secuencia de aminoácidos que tiene una identidad de secuencia de aminoácidos de más de aproximadamente el 60%, aproximadamente el 65%, aproximadamente el 70%, aproximadamente el 75%, aproximadamente el 80%, aproximadamente el 85%, aproximadamente el 90%, aproximadamente el 91%, aproximadamente el 92%, aproximadamente el 93%, aproximadamente el 94%, aproximadamente el 95%, aproximadamente el 96%, aproximadamente el 97%, aproximadamente el 98% o aproximadamente el 99% o más, en una región de al menos aproximadamente 25, aproximadamente 50, aproximadamente 100, aproximadamente 200, aproximadamente 300, aproximadamente 400, o más aminoácidos, a un polipéptido codificado por un ácido nucleico al que se hace referencia o una secuencia de aminoácidos descrita en el presente documento; y/o (2) se unen específicamente a anticuerpos, por ejemplo, anticuerpos policlonales o monoclonales, generados contra un inmunógeno que comprende una secuencia de aminoácidos a la que se hace referencia tal como se describe en el presente documento, un fragmento inmunogénico del mismo y/o una variante modificada de manera conservadora del mismo.
Según la presente invención, el término “proteína terapéutica recombinante” incluye cualquier proteína terapéutica obtenida mediante tecnología de ADN recombinante. En determinadas realizaciones, el término abarca proteínas tal como se describe en el presente documento.
Tal como se usa en el presente documento, “proteína terapéutica endógena” incluye una proteína terapéutica que se origina del mamífero destinado a recibir tratamiento. El término también incluye proteína terapéutica transcrita desde un transgén o cualquier otro ADN foráneo presente en dicho mamífero. Tal como se usa en el presente documento, “proteína terapéutica exógena” incluye una proteína de la coagulación sanguínea que no se origina del mamífero destinado a recibir tratamiento.
Tal como se usa en el presente documento, “proteína de la coagulación sanguínea derivada de plasma” o “plasmático” incluye todas las formas de la proteína encontrada en la sangre obtenida de un mamífero que tiene la propiedad que participa en la ruta de coagulación.
Tal como se usa en el presente documento, “derivado biológicamente activo” o “variante biológicamente activa” incluye cualquier derivado o variante de una molécula que tenga sustancialmente las mismas propiedades funcionales y/o biológicas de dicha molécula, tales como propiedades de unión y/o la misma base estructural, tal como un esqueleto peptídico o una unidad polimérica básica.
Un “análogo”, “variante” o “derivado” es un compuesto sustancialmente similar en estructura y que tiene la misma actividad biológica, aunque en determinados casos en un grado diferente, con respecto a una molécula que se produce de manera natural. Por ejemplo, una variante de polipéptido se refiere a un polipéptido que comparte una estructura sustancialmente similar y que tiene la misma actividad biológica que un polipéptido de referencia. Las variantes o análogos difieren en la composición de sus secuencias de aminoácidos en comparación con el polipéptido natural del que se deriva el análogo, basándose en una o más mutaciones que implican (i) deleción de uno o más residuos de aminoácidos en uno o más extremos terminales del polipéptido y/o una o más regiones internas de la secuencia de polipéptido natural (por ejemplo, fragmentos), (ii) inserción o adición de uno o más aminoácidos en uno o más extremos terminales (normalmente una “adición” o “fusión” ) del polipéptido y/o una o más regiones internas (normalmente una “inserción”) de la secuencia de polipéptido que se produce de manera natural o (iii) sustitución de uno o más aminoácidos por otros aminoácidos en la secuencia de polipéptido que se produce de manera natural. A modo de ejemplo, un “derivado” se refiere a un polipéptido que comparte la misma estructura o sustancialmente similar a un polipéptido de referencia que se ha modificado, por ejemplo, químicamente.
En diversas realizaciones, los análogos, variantes o derivados están diseñados para permitir, por ejemplo, la conjugación de otra molécula con el análogo, variante o derivado de proteína, formando así una proteína conjugada según la presente invención.
Los polipéptidos de variantes o análogos incluyen variantes de inserción, en las que se añaden uno o más residuos de aminoácidos a una secuencia terapéutica de aminoácidos de la proteína de la invención. Las inserciones pueden ubicarse en cualquiera o ambos extremos terminales de la proteína, y/o pueden colocarse dentro de las regiones internas de la secuencia terapéutica de aminoácidos de la proteína. Las variantes de inserción, con residuos adicionales en cualquiera o ambos extremos terminales, incluyen, por ejemplo, proteínas de fusión y proteínas que incluyen etiquetas de aminoácidos u otros marcadores de aminoácidos. En un aspecto, la molécula de proteína de la coagulación sanguínea contiene opcionalmente un Met N-terminal, especialmente cuando la molécula se expresa de manera recombinante en una célula bacteriana tal como E. coli.
En las variantes de deleción, se retiran uno o más residuos de aminoácidos en un polipéptido proteico terapéutico tal como se describe en el presente documento. Las deleciones pueden efectuarse en uno o ambos extremos terminales del polipéptido proteico terapéutico, y/o con la retirada de uno o más residuos dentro de la secuencia de aminoácidos de la proteína terapéutica. Por tanto, las variantes de deleción incluyen fragmentos de una secuencia terapéutica de polipéptidos proteicos.
En las variantes de sustitución, uno o más residuos de aminoácidos de un polipéptido proteico terapéutico se retiran y se reemplazan con residuos alternativos. En un aspecto, las sustituciones son de naturaleza conservadora y las sustituciones conservadoras de este tipo se conocen bien en la técnica. Alternativamente, la invención abarca sustituciones que también son no conservadoras. Se describen sustituciones conservadoras a modo de ejemplo en Lehninger, [Biochemistry, 2a edición; Worth Publishers, Inc., Nueva York (1975), págs.71-77] y se exponen inmediatamente a continuación.
SUSTITUCIONES CONSERVADORAS
CARACTERÍSTICA DE LA AMINOÁCIDO
CADENA LATERAL
No polar (hidrófobo):
A. Alifático A L I V P
B. Aromático F W
C. Que contiene azufre M
D. Límite G
Polar sin carga:
A. Hidroxilo S T Y
B. Amidas N Q
C. Sulfhidrilo C
D. Límite G
Cargado positivamente (básico) K R H
Cargado negativamente (ácido) D E
Alternativamente, las sustituciones conservadoras ejemplares se exponen inmediatamente a continuación.
SUSTITUCIONES CONSERVADORAS II
RESIDUO ORIGINAL SUSTITUCION A MODO
DE EJEMPLO
Ala (A) Val, Leu, Ile
Arg (R) Lys, Gln, Asn
Asn(N) Gln, His, Lys, Arg
Asp(D) Glu
Cys (C) Ser
Gln (Q) Asn
Glu (E) Asp
His (H) Asn, Gln, Lys, Arg
Ile (I) Leu, Val, Met, Ala, Phe,
Leu (L) Ile, Val, Met, Ala, Phe
Lys (K) Arg, Gln, Asn
Met (M) Leu, Phe, Ile
Phe (F) Leu, Val, Ile, Ala
Pro (P) Gly
Ser (S) Thr
Thr (T) Ser
Trp (W) Tyr
Tyr (Y) Trp, Phe, Thr, Ser
Val (V) Ile, Leu, Met, Phe, Ala
B. Polinucleótidos
Los ácidos nucleicos que codifican para una proteína terapéutica de la invención incluyen, por ejemplo y sin limitación, genes, pre-ARNm, miARN, ADNc, variantes polimórficas, alelos, mutantes sintéticos y que se producen de manera natural.
Los polinucleótidos que codifican para una proteína terapéutica de la invención también incluyen, sin limitación, aquellos que (1) se hibridan específicamente en condiciones de hibridación estrictas con un ácido nucleico que codifica para una secuencia de aminoácidos a la que se hace referencia tal como se describe en el presente documento, y variantes modificadas de manera conservadora de la misma; (2) tienen una secuencia de ácido nucleico que tiene una identidad de secuencia de nucleótidos mayor de aproximadamente el 95%, aproximadamente el 96%, aproximadamente el 97%, aproximadamente el 98%, aproximadamente el 99% o más, en una región de al menos aproximadamente 25, aproximadamente 50, aproximadamente 100, aproximadamente 150, aproximadamente 200, aproximadamente 250, aproximadamente 500, aproximadamente 1000 o más nucleótidos (hasta la secuencia de longitud completa de 1218 nucleótidos de la proteína madura), con respecto a una secuencia de ácido nucleico a la que se hace referencia tal como se describe en el presente documento. Las condiciones a modo de ejemplo de “hibridación estricta” incluyen hibridación a 42°C en formamida al 50%, 5X SSC, Na^PO420 mM, pH 6,8; y lavado en 1X SSC a 55°C durante 30 minutos. Se entiende que la variación en estas condiciones a modo de ejemplo puede realizarse basándose en la longitud y el contenido de nucleótidos GC de las secuencias que van a hibridarse. Las fórmulas convencionales en la técnica son apropiadas para determinar las condiciones de hibridación apropiadas. Véase Sambrook et al., Molecular Cloning: A Laboratory Manual (segunda edición, Cold Spring Harbor Laboratory Press, 1989) §§ 9.47-9.51.
Una secuencia polinucleotídica o polipeptídica “que se produce de manera natural” es normalmente de un mamífero que incluye, pero no se limita a, primates, por ejemplo, humanos; roedor, por ejemplo, rata, ratón, hámster; vaca, cerdo, caballo, oveja o cualquier mamífero. Los ácidos nucleicos y las proteínas de la invención pueden ser moléculas recombinantes (por ejemplo, heterólogas y que codifican para la secuencia de tipo natural o una variante de la misma, o que no se produce de manera natural).
C. Producción de proteínas terapéuticas.
La producción de una proteína terapéutica incluye cualquier método conocido en la técnica para (i) la producción de ADN recombinante mediante ingeniería genética, (ii) la introducción de ADN recombinante en células procariotas o eucariotas, por ejemplo y sin limitación, transfección, electroporación o microinyección, (iii) el cultivo de dichas células transformadas, (iv) la expresión de la proteína terapéutica, por ejemplo, de manera constitutiva o tras la inducción y (v) el aislamiento de dicha proteína de la coagulación sanguínea, por ejemplo, del medio de cultivo o recogiendo las células transformadas, para obtener proteína terapéutica purificada.
En otros aspectos, la proteína terapéutica se produce por expresión en un sistema huésped procariota o eucariota adecuado caracterizado por producir una molécula de proteína de la coagulación sanguínea farmacológicamente aceptable. Ejemplos de células eucariotas son células de mamíferos tales como CHO, COS, HEK 293, BHK, SK-Hep y HepG2.
Se usa una amplia variedad de vectores para la preparación de la proteína terapéutica y se seleccionan de vectores de expresión eucariotas y procariotas. Los ejemplos de vectores para la expresión procariota incluyen plásmidos tales como, y sin limitación, pRSET, pET y pBAD, en los que los promotores usados en los vectores de expresión procariota incluyen uno o más de, y sin limitación, lac, trc, trp, recA o araBAD. Los ejemplos de vectores para la expresión eucariota incluyen: (i) para la expresión en levadura, vectores tales como, y sin limitación, pAO, pPIC, pYES o pMET, usando promotores tales como, y sin limitación, AOX1, GAP, GAL1 o AUG1 ; (ii) para la expresión en células de insecto, vectores tales como y sin limitación, pMT, pAc5, pIB, pMIB o pBAC, usando promotores tales como y sin limitación PH, p10, MT, Ac5, OpIE2, gp64 o polh, y (iii) para la expresión en células de mamíferos, vectores tales como y sin limitación pSVL, pCMV, pRc/RSv, pcDNA3 o pBPV, y vectores derivados de, en un aspecto, sistemas virales tales como y sin limitación virus vaccinia, virus adenoasociados, virus del herpes o retrovirus, usando promotores tales como y sin limitación CMV, SV40, EF-1, UbC, RSV, ADV, BPV y p-actina.
En diversas realizaciones de la invención, las proteínas terapéuticas se modifican conjugando derivados de ácidos grasos solubles en agua o ligadores solubles en agua con uno o más hidratos de carbono en la proteína terapéutica. Por tanto, en una realización, la proteína terapéutica es una glicoproteína y se purifica de una célula huésped que permite la glicosilación (es decir, la proteína se glicosila in vivo y posteriormente se purifica como una glicoproteína). En diversas realizaciones, la proteína terapéutica es o no es una glicoproteína y se glicosila in vitro después de la
purificación de una célula huésped. Los métodos de glicosilación in vitro se conocen bien en la técnica (véase, por ejemplo, Meynial-Salles I y Combes D, Journal of Biotechnology 1996, 46: 1-14;/ Solá RJ y Griebenow K, BioDrugs 2010, 24: 9-21). Por supuesto, un experto en la técnica podría (1) purificar la proteína terapéutica; (2) modificar la proteína terapéutica para permitir la glicosilación in vitro, opcionalmente específica de sitio (por ejemplo, deleciones/inserción/sustituciones de aminoácidos); y (3) glicosilar la proteína modificada in vitro según los procedimientos conocidos en la técnica.
D. Administración
En una realización de la presente divulgación, una proteína terapéutica conjugada de la presente invención puede administrarse mediante inyección, tal como inyección intravenosa, intramuscular o intraperitoneal.
Para administrar composiciones que comprenden una proteína terapéutica conjugada de la presente invención a humanos o animales de prueba, en un aspecto, las composiciones comprenden uno o más portadores farmacéuticamente aceptables. Los términos “farmacéuticamente” o “farmacológicamente aceptables” se refieren a entidades moleculares y composiciones que son estables, inhiben la degradación de proteínas tales como productos de agregación y escisión, y además no producen reacciones alérgicas u otras reacciones adversas cuando se administran usando vías bien conocidas en la técnica, tal como se describe a continuación. Los “portadores farmacéuticamente aceptables” incluyen cualquiera y todos los disolventes, medios de dispersión, recubrimientos, agentes antibacterianos y antifúngicos, agentes isotónicos y retardadores de la absorción clínicamente útiles y similares, incluyendo los agentes divulgados anteriormente.
Tal como se usa en el presente documento, “cantidad eficaz” incluye una dosis adecuada para tratar una enfermedad o trastorno o mejorar un síntoma de una enfermedad o trastorno. En una realización, “cantidad eficaz” incluye una dosis adecuada para tratar un mamífero que tiene un trastorno hemorrágico tal como se describe en el presente documento.
Las composiciones pueden administrarse por vía oral, tópica, transdérmica, parenteral, mediante aerosol por inhalación, por vía vaginal, rectal o por inyección intracraneal. El término parenteral tal como se usa en el presente documento incluye inyecciones subcutáneas, intravenosas, intramusculares, inyección intracisternal o técnicas de infusión. También se contempla la administración por inyección intravenosa, intradérmica, intramuscular, intramamaria, intraperitoneal, intratecal, retrobulbar, intrapulmonar o implantación quirúrgica en un sitio particular. Generalmente, las composiciones están esencialmente libres de pirógenos, así como otras impurezas que podrían ser perjudiciales para el receptor.
Las administraciones únicas o múltiples de las composiciones pueden llevarse a cabo con los niveles de dosis y el patrón seleccionados por el médico tratante. Para la prevención o el tratamiento de la enfermedad, la dosis adecuada dependerá del tipo de enfermedad que va a tratarse, tal como se describió anteriormente, la gravedad y el curso de la enfermedad, si el medicamento se administra con fines preventivos o terapéuticos, la terapia previa, la historia clínica del paciente y respuesta al fármaco, y la discreción del médico tratante.
La presente invención también se refiere a una composición farmacéutica que comprende una cantidad eficaz de una proteína terapéutica conjugada tal como se define en el presente documento. La composición farmacéutica puede comprender además un portador, diluyente, sal, tampón o excipiente farmacéuticamente aceptable. La composición farmacéutica puede usarse para tratar los trastornos hemorrágicos definidos anteriormente. La composición farmacéutica de la invención puede ser una disolución o un producto liofilizado. Las disoluciones de la composición farmacéutica pueden someterse a cualquier procedimiento de liofilización adecuado. Como aspecto adicional, la invención incluye kits que comprenden una composición de la invención envasada de una manera que facilita su uso para la administración a sujetos. En una realización, tal kit incluye un compuesto o composición descrita en el presente documento (por ejemplo, una composición que comprende una proteína terapéutica conjugada), envasada en un recipiente tal como una botella o recipiente sellado, con una etiqueta pegada al recipiente o incluida en el paquete que describe el uso del compuesto o composición en la práctica del método. En una realización, el kit contiene un primer recipiente que tiene una composición que comprende una proteína terapéutica conjugada y un segundo recipiente que tiene una disolución de reconstitución fisiológicamente aceptable para la composición en el primer recipiente. En un aspecto, el compuesto o composición se envasa en una forma de dosificación unitaria. El kit puede incluir además un dispositivo adecuado para administrar la composición según una vía específica de administración. Preferiblemente, el kit contiene una etiqueta que describe el uso de la composición de proteína o de péptido terapéutica.
ÁCIDOS GRASOS, DERIVADOS DE ÁCIDOS GRASOS Y CONJUGADOS DERIVADOS PROTEÍNAS Y ÁCIDOS GRASOS
En un aspecto, una molécula derivada de proteína terapéutica (una proteína terapéutica conjugada) proporcionada en el presente documento está unida a un derivado de ácido graso soluble en agua. Tal como se usa en la presente divulgación, un “derivado de ácido graso soluble en agua” comprende un ácido graso (es decir, un ácido carboxílico) conjugado con un ligador soluble en agua (por ejemplo, un ligador aminooxilo) tal como se describe en el presente documento. El derivado de ácido graso soluble en agua según la presente invención comprende un ácido graso o un
éster de ácido graso conjugado con un ligador aminooxilo. Tales derivados de ácidos grasos, según la invención, son estables (es decir, no se liberan de la proteína), solubles en agua y capaces de unirse a albúmina sérica humana.
Ácidos grasos
Los ácidos grasos (es decir, FA) incluyen, pero no se limitan a, ácidos grasos saturados, ácidos grasos insaturados, ácidos grasos de cadena ramificada (Mukheriji etal., Prog Lipid Res 2003; 42: 359-76) y derivados de los mismos que son capaces de unirse a albúmina sérica humana según la presente invención.
A modo de ejemplo, los ácidos grasos tienen la siguiente estructura general:
FA saturado: estructura general
Éster metílico de FA saturado: estructura general
Los ácidos grasos, según diversas realizaciones de la presente invención, también comprenden diversas estructuras alternativas (por ejemplo, ésteres metílicos o etílicos) u otras estructuras tales como las que contienen grupos terminales en posición o (por ejemplo, grupos hidroxilo, amino, tio y carboxilo).
En una realización, el ácido graso es un ácido graso que se produce de manera natural. En diversas realizaciones, el ácido graso es un ácido graso de cadena corta (por ejemplo, menos de seis carbonos), un ácido graso de cadena media (por ejemplo, 6-12 carbonos), ácidos grasos de cadena larga (por ejemplo, más de 12 carbonos), o un ácido graso de cadena muy larga (por ejemplo, más de 22 carbonos). En otra realización, el ácido graso tiene entre 4 y 28 carbonos. En una realización, el ácido graso está en la configuración cis. En todavía otra realización, el ácido graso está en la configuración trans.
En una realización, el ácido graso es un ácido graso saturado de 12 a 20 carbonos de longitud. Tales ácidos grasos se conocen en la técnica, por ejemplo, C12 (ácido dodecanoico, ácido láurico), C14 (ácido tetradecanoico, ácido mirístico), C16 (ácido hexadecanoico, ácido palmítico), C18 (ácido octadecanoico, ácido esteárico) y C20 (ácido eicosanoico, ácido araquídico). Ejemplos de ácidos grasos insaturados son ácido miristoleico (C14:1), ácido palmitoleico (C16:1), ácido oleico (C18:1), ácido linoleico (C18:2) y ácido araquidónico (C20:4). La mayoría de los ácidos grasos están disponibles comercialmente y pueden prepararse mediante diferentes métodos químicos (Recent Developments in the Synthesis of Fatty Acid Derivatives, editores: Knothe G y Derksen JTB, AOCS Press 1999, ISBN 1-893997-00-6.)
En diversas realizaciones de la presente invención, el ácido graso comprende 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48 ó 50 carbonos.
B. Derivados de ácidos grasos.
La presente invención proporciona la preparación de una nueva clase de derivados de ácidos grasos activados (derivados de FA) que pueden unirse a albúmina sérica humana. Los derivados de FA contienen un espaciador o ligador soluble en agua, que permite el manejo y la manipulación de derivados de FA en disolución acuosa (es decir, los derivados de ácidos grasos según la presente invención son solubles en agua, a diferencia de los ácidos grasos correspondientes de los que se derivan). Los derivados de FA contienen un grupo aminooxilo activo, que permite el acoplamiento del derivado de FA a un resto de hidrato de carbono oxidado (predominantemente N-glicanos) de proteínas terapéuticas para formar uniones oxima estables. Tal como se usa en el presente documento, una unión “estable” significa que se forma un enlace covalente que es “no liberable” o no hidrolizable.
La modificación química a través de hidratos de carbono podría ser la opción preferida para proteínas de la coagulación como FVIII, FIX y FVIIa para formar conjugados con alta actividad residual.
A modo de ejemplo, la siguiente estrategia representa una realización según la presente invención para preparar un derivado de FA soluble en agua que contiene un grupo aminooxilo activo.
Estrategia 1:
El grupo ro-hidroxilo de un derivado de FA (por ejemplo, ácido 16-hidroxihexadecanoico) se somete a oxidación con peryodinano de Dess Martin para generar un grupo aldehído. En la siguiente etapa, un ligador de diaminooxilo que contiene una cadena de PEG soluble en agua (por ejemplo, 3,6,9-triaoxaundecano-1,11-dioxiamina) se acopla a este grupo aldehído para formar una unión oxima estable. El siguiente esquema representa un ejemplo según la estrategia 1:
Etapa 1: se oxidó selectivamente ácido 16-hidroxiesteárico con reactivo de Dess-Martin para producir ácido 16-oxoestearico. El producto bruto se purificó por cromatografía usando gel de sílice como agente de separación.
DCM THF 0°C 16h
27042
acido 16-hidroxihexadecanoico acido 16-oxohexadecanoico
Etapa 2: se hizo reaccionar el resto 16-oxo de la sal de sodio del ácido 16-oxoestearico con 3,6,9-triaoxaundecano-1,11-dioxiamina. El producto bruto se purificó por cromatografía usando gel de sílice como agente de separación.
Alternativamente, otra realización, la siguiente estrategia se emplea para preparar derivados de FA solubles en agua que contienen un grupo aminooxilo activo.
Estrategia 2:
El grupo carboxilo de un ácido graso ra-hidroxilo (por ejemplo, ácido 16-hidroxihexadecanoico) se esterifica con cloruro de acetilo. El grupo o-hidroxilo de este derivado de éster metílico se activa con cloruro de mesilo para introducir un mejor grupo saliente. Luego, el grupo mesilo se hace reaccionar con un ligador de diaminooxilo que contiene una cadena de PEG soluble en agua (por ejemplo, 3,6,9-triaoxaundecano-1,11-dioxiamina) para formar un enlace aminooxilo-metileno estable. Opcionalmente, el éster metílico puede hidrolizarse en disolución alcalina para generar un grupo carboxilo libre. El siguiente esquema representa un ejemplo según la estrategia 2:
Etapa 1: el resto de ácido carboxílico del ácido 16-hidroxihexadecanoico se protegió formando el éster metílico usando cloruro de acetilo como reactivo de metilación.
Etapa 2: el resto 16-hidroxilo de éster metílico del ácido 16-hidroxihexadecanoico se activó sustituyendo el grupo hidroxilo con mesilo, que es el mejor grupo saliente.
Etapa 3: el resto 16-mesilo de éster metílico del ácido 16-metilsulfonilhexadecanoico se sustituyó por un resto aminooxilo de la 3,6,9-triaoxaundecano-1,11-dioxiamina bifuncional. El producto bruto se purifica por cromatografía usando gel de sílice como agente de separación.
Éster metílico del ácido Éster metílico del ácido 16-(2-(2-(2-(2-aminoetoxi)-etoxi)-16-metilsulfonilhexadecanoico etoxi)-extoxiamino)-hexadecanoico
Se divulgan estrategias adicionales en el presente documento, pero no forman parte de la presente invención.
Tal como se describe en el presente documento, se divulga el uso de otras químicas que incluyen, pero no se limitan a, hidrazidas para acoplamiento a grupos aldehído, ésteres de NHS para acoplamiento a grupos amino y maleimidas para acoplamiento a grupos SH libres de proteínas terapéuticas.
A modo de ejemplo, un éster metílico de ácido graso preparado tal como se describió anteriormente se hace reaccionar con un MAL-PEG-COOH disponible comercialmente (mal-PEG(12)-COOH/IRIS Biotech GmbH, Marktredwitz, Alemania) tal como se describe en el presente documento. A modo de otro ejemplo más, un éster de ácido graso con un grupo amino reactivo se hace reaccionar con un NHS-PEG-NHS disponible comercialmente (NHS-dPEG(4)-NHS/IRIS Biotech GmbH, Marktredwitz, Alemania) tal como se describe en el presente documento.
Los ligadores solubles en agua incluyen, pero no se limitan a, polímeros solubles en agua (por ejemplo, PEG). El ligador puede consistir en cualquier estructura química que contenga uno o más grupos funcionales, lo que aumenta su solubilidad en agua. Estos grupos funcionales podrían tener la capacidad de formar una carga negativa o positiva, haciendo que el ligador sea soluble en agua. En una realización, este grupo funcional incluye, pero no se limita a un grupo sulfo o carboxilo. Además, puede usarse cualquier grupo funcional polar, lo que hace que el ligador sea más soluble en agua. Ejemplos de esto son los grupos hidroxilo, amino, amido, maleimido, aminooxilo e hidrazida, así como los ésteres de N-hidroxisuccinimida (NHS) y los ésteres de sulfo NHS.
En diversas realizaciones, el polímero soluble en agua incluye, pero no se limita a, polietilenglicol (PEG), PEG ramificado, poli(ácido siálico) (PSA), almidón de hidroxialquilo (HAS), almidón de hidroxietilo (HES), hidrato de carbono, polisacáridos, pululano, quitosano, ácido hialurónico, sulfato de condroitina, sulfato de dermatán, almidón, dextrano, carboximetildextrano, poli(óxido de alquileno) (PAO), polialquilenglicol (PAG), polipropilenglicol (PPG), polioxazolina, poliacriloilmorfolina, poli(alcohol vinílico) (PVA), policarboxilato, polivinilpirrolidona, polifosfaceno, polietileno-co-anhídrido de ácido maleico, poliestireno-co-anhídrido de ácido maleico y poli(1-hidroximetiletilenhidroximetilformal) (PHF).
En una realización, el polímero soluble en agua es PEG. En diversas realizaciones de la invención, el polímero soluble en agua comprende una longitud de cadena de entre aproximadamente 3 y 25 oxígenos. Por ejemplo, el polímero soluble en agua comprende 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23 ó 25 oxígenos, en diversas realizaciones según la presente invención.
C. Conjugados de derivados de proteínas y ácidos grasos
La presente invención contempla sistemas ligadores de aminooxilo (es decir, en los que un derivado de ácido graso soluble en agua comprende un ligador aminooxilo). Por ejemplo, en una realización de la invención, la reacción de hidroxilamina o derivados de hidroxilamina con aldehídos (en un resto de hidrato de carbono tras la oxidación) para formar un grupo oxima se aplica a la preparación de conjugados de proteínas. Por ejemplo, una glicoproteína (una proteína terapéutica según la presente invención) se oxida en primer lugar con un agente oxidante tal como peryodato
de sodio (NaIO4 ) (Rothfus JA y Smith EL., J Biol Chem 1963, 238, 1402-10; y Van Lenten L y Ashwell G., J Biol Chem 1971,246, 1889-94). La oxidación de peryodato de glicoproteínas se basa en la reacción clásica de Malaprade descrita en 1928, la oxidación de dioles vecinales con peryodato para formar un grupo aldehído activo (Malaprade L., Analytical application, Bull Soc Chim France, 1928, 43, 683-96). Ejemplos adicionales para tal agente oxidante son el tetraacetato de plomo (Pb(OAc)4), acetato de manganeso (MnO(Ac)3), acetato de cobalto (Co(OAc)2), acetato de talio (TIOAc), sulfato de cerio (Ce(SO4)2 ) (documento US 4.367,309) o perrutenato de potasio (KRuO4) (Marko et al., J Am Chem Soc 1997,119, 12661-2). Por “agente oxidante” se entiende un compuesto oxidante suave que es capaz de oxidar dioles vecinales en hidratos de carbono, generando así grupos aldehídos activos en condiciones de reacción fisiológicas.
La segunda etapa es el acoplamiento del polímero (derivado de ácido graso) que contiene un grupo aminooxilo al resto de hidrato de carbono oxidado para formar una unión oxima. En una realización de la invención, esta etapa puede llevarse a cabo en presencia de cantidades catalíticas del catalizador nucleófilo anilina o derivados de anilina (Dirksen A y Dawson PE, Bioconjugate Chem. 2008; Zeng Y et al., Nature Methods 2009; 6: 207-9). La catálisis de anilina acelera drásticamente la ligación de oxima permitiendo el uso de concentraciones muy bajas de los reactivos. En otra realización de la invención, la unión oxima se estabiliza por reducción con NaCNBH3 para formar una unión alcoxiamina. A continuación, se describen catalizadores adicionales. En otra realización, esta etapa se lleva a cabo en presencia de m-toluidina.
En una realización de la invención, las etapas de reacción para conjugar un ligador soluble en agua (derivado de ácido graso) con una proteína se llevan a cabo por separado y secuencialmente (es decir, materiales de partida (proteína terapéutica, ligador soluble en agua, etc.), reactivos (agentes oxidantes, anilina, etc.) y productos de reacción (hidrato de carbono oxidado en una proteína terapéutica, ligador de aminooxilo activado soluble en agua, etc.) se separan entre las etapas de reacción individuales). En otra realización, los materiales de partida y los reactivos necesarios para completar una reacción de conjugación según la presente invención se llevan a cabo en un único recipiente. En una realización, la proteína nativa se mezcla con el reactivo de aminooxilo-polímero. Posteriormente, se añade el reactivo oxidante y se realiza la reacción de conjugación.
Puede encontrarse información adicional sobre la tecnología de aminooxilo en las siguientes referencias: documento EP 1681303A1 (eritropoyetina HASilada); documento WO 2005/014024 (conjugados de un polímero y una proteína ligada por un grupo de unión de oxima); documento WO96/40662 (compuestos ligadores que contienen aminooxilo y su aplicación en conjugados); documento WO 2008/025856 (proteínas modificadas); Peri F et al., Tetrahedron 1998, 54, 12269-78; Kubler-Kielb J y Pozsgay V., J Org Chem 2005, 70, 6887-90; Lees A et al., Vaccine 2006, 24 (6), 716 29; y Heredia KL et al., Macromolecules 2007, 40 (14), 4772-9.
En determinados aspectos de la presente divulgación, las proteínas terapéuticas se conjugan con derivados de ácidos grasos solubles en agua por cualquiera de una variedad de métodos químicos (Roberts JM et al., Advan Drug Delivery Rev 2002; 54: 459-76). Por ejemplo, en una realización de la divulgación, una proteína terapéutica se modifica mediante la conjugación de derivados de ácidos grasos con grupos amino libres de la proteína usando ésteres de N-hidroxisuccinimida (NHS). En otra realización, el derivado de ácido graso soluble en agua se acopla a grupos SH libres usando química de maleimida. En una realización de la invención, el derivado de ácido graso soluble en agua se acopla mediante el uso de química aminooxilo a los restos de hidrato de carbono de la proteína terapéutica después de la oxidación previa.
En una realización de la divulgación, una proteína terapéutica se modifica a través de residuos de lisina mediante el uso de derivados de ácidos grasos solubles en agua que contienen un éster de N-hidroxisuccinimida (NHS) activo. Este derivado reacciona con los residuos de lisina de la proteína terapéutica en condiciones suaves formando un enlace amida estable.
En otra realización de la divulgación, la unión a través de un enlace peptídico entre un grupo carboxilo en uno de los derivados de proteína o ácido graso y un grupo amina de la proteína o derivado de ácido graso, o una unión éster entre un grupo carboxilo de la proteína o se contempla un derivado de ácido graso y un grupo hidroxilo de la proteína terapéutica o derivado de ácido graso. Otra unión por la que la proteína terapéutica se une de manera covalente al derivado de ácido graso es a través de una base de Schiff, por ejemplo, entre un grupo amino libre en la proteína que reacciona con un grupo aldehído formado en un extremo terminal de un ácido graso. La base de Schiff generada se estabiliza en un aspecto mediante reducción específica con NaCNBH3 para formar una amina secundaria. Un enfoque alternativo es la generación de grupos amino libres terminales en el derivado de ácido graso por aminación reductora con NH4Cl después de la oxidación previa. Pueden usarse reactivos bifuncionales para ligar dos grupos amino o dos grupos hidroxilo. Por ejemplo, un derivado de ácido graso que contiene un grupo amino se acopla a grupos amino de la proteína con reactivos como BS3 (bis(sulfosuccinimidil)suberato/Pierce, Rockford, IL). Además, se usan reactivos de reticulación heterobifuncionales como sulfo-EMCS (éster de N-g-maleimidocaproiloxi)sulfosuccinimida/Pierce), por ejemplo, para ligar grupos amina y tiol.
En otro enfoque divulgado en el presente documento, se prepara un derivado de ácido graso con un grupo hidrazida activo y se acopla al resto de hidrato de carbono de la proteína después de la oxidación previa y la generación de funciones aldehído.
Tal como se describió anteriormente, un grupo amina libre de la proteína terapéutica reacciona con el grupo 1-carboxilo de un derivado de ácido graso para formar un enlace peptidilo o se forma una unión éster entre el grupo ácido 1-carboxílico y un hidroxilo u otro grupo activo adecuado en una proteína
En diversas realizaciones, la proteína terapéutica se liga a o se asocia con el derivado de ácido graso en cantidades estequiométricas (por ejemplo, 1:1, 1:2, 1:3, 1:4, 1:5, 1:6, 1:7, 1:7, 1:8, 1:9 o 1:10, etc.). En diversas realizaciones, 1
6, 7-12 o 13-20 derivados de ácidos grasos se ligan a la proteína. En todavía otras realizaciones, 1, 2, 3, 4, 5, 6, 7, 8,
9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 o más derivados de ácidos grasos se ligan a la proteína.
En diversas realizaciones, la proteína terapéutica se modifica para introducir sitios de glicosilación (es decir, sitios distintos de los sitios de glicosilación nativos). Tal modificación puede lograrse usando técnicas convencionales de biología molecular conocidas en la técnica. Además, la proteína terapéutica, antes de la conjugación con un ligador soluble en agua a través de uno o más restos de hidrato de carbono, puede glicosilarse in vivo o in vitro. Estos sitios glicosilados pueden servir como dianas para la conjugación de las proteínas con ligadores solubles en agua (solicitud de patente estadounidense n.° 20090028822, solicitud de patente estadounidense n.° 2009/0093399, solicitud de patente estadounidense n.° 2009/0081188, solicitud de patente estadounidense n.° 2007/0254836, solicitud de patente estadounidense n.° 2006/0111279 y DeFrees S. et al., Glycobiology, 2006, 16, 9, 833-43).
En una realización, la proteína conjugada conserva la actividad funcional completa de los productos de proteínas terapéuticas nativas y proporciona una semivida prolongada in vivo, en comparación con los productos de proteínas
, el 42, el 43 , el 61, el 62 , el 80, el 81 , el 99, el 10 el 120, el 130, el 140 o el 150 por ciento (%) de actividad biológica en relación con la proteína nativa.
En un aspecto relacionado, las actividades biológicas de la proteína conjugada y la proteína de la coagulación sanguínea nativa se determinan por las razones de actividad cromogénica con respecto al valor de antígeno del factor de la coagulación sanguínea (factor de la coagulación sanguínea:Chr: factor de la coagulación sanguínea:Ag).
En todavía otra realización más de la invención, la semivida de la proteína conjugada se disminuye o aumenta 0,5,
0,6, 0,7, 0,8, 0,9, 1,0, 1,1, 1,2, 1,3, 1,4, 1,5, 2, 3, 4, 5, 6, 7, 8, 9 ó 10 veces en relación con la semivida in vivo de la proteína terapéutica nativa.
CATALIZADORES NUCLEÓFILOS
Tal como se describe en el presente documento, la anilina puede catalizar la conjugación de derivados de ácidos grasos solubles en agua con proteínas terapéuticas. La anilina cataliza fuertemente las reacciones acuosas de aldehídos y cetonas con aminas para formar iminas estables tales como hidrazonas y oximas. El siguiente diagrama compara una reacción de ligación de oxima catalizada por anilina frente a no catalizada (adaptada de Kohler JJ, ChemBioChem 2009; 10: 2147-50).
Sin embargo, considerando los numerosos riesgos para la salud asociados con la anilina, son deseables catalizadores alternativos. La presente invención proporciona derivados de anilina como catalizadores alternativos de ligación de oxima. Tales derivados de anilina incluyen, pero no se limitan a, ácido o-aminobenzoico, ácido m-aminobenzoico, ácido p-aminobenzoico, ácido sulfanílico, o-aminobenzamida, o-toluidina, m-toluidina, p-toluidina, o-anisidina, manisidina y p-anisidina. El siguiente diagrama compara una reacción de ligación de oxima catalizada por m-toluidina frente a no catalizada (documento PCT/US2011/45873):
En una realización de la invención, se usa m-toluidina (también conocida como meta-toluidina, m-metilanilina, 3-metilanilina o 3-amino-1-metilbenceno) para catalizar las reacciones de conjugación descritas en el presente documento. La m-toluidina y anilina tienen propiedades físicas similares y esencialmente el mismo valor de pKa (mtoluidina: pKa 4,73, anilina: pKa 4,63).
Los catalizadores nucleófilos de la invención son útiles para la ligación de oxima (usando unión aminooxilo). En diversas realizaciones de la invención, el catalizador nucleófilo se proporciona en la reacción de conjugación a una concentración de 0,1, 0,2, 0,3, 0,5, 0,5, 0,6, 0,7, 0,8, 0,9, 1,0, 1,5, 2,0, 2,5, 3,0, 3,5, 4,0, 4,5, 5,0, 5,5, 6,0, 6,5, 7,0, 7,5, 8,0, 8,5, 9,0, 9,5, 10,0, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30 , 35, 40, 45 ó 50 mM. En una realización, el catalizador nucleófilo se proporciona entre 1 y 10 mM. En diversas realizaciones de la invención, el intervalo de pH de la reacción de conjugación está entre 4,0 y 7,0, entre 4,5 y 7,0, entre 5,0 y 6,5, entre 5,0 y 6,5. En diversas realizaciones, el pH de la reacción de conjugación es pH 4,5, 5,0, 5,5, 6,0, 6,5, 7,0 y 7,5. En una realización, el pH está entre 5,5 y 6,5.
PURIFICACIÓN DE PROTEÍNAS CONJUGADAS
En diversas realizaciones, se desea la purificación de una proteína que se ha incubado con un agente oxidante y/o una proteína terapéutica que se ha conjugado con un derivado de ácido graso soluble en agua según la invención. Se conocen numerosas técnicas de purificación en la técnica e incluyen, sin limitación, métodos cromatográficos, métodos de filtración y métodos de precipitación (véase, por ejemplo, Guide to Protein Purification, Meth. Enzymology vol 463 (editado por Burgess RR y Deutscher MP), 2a edición, Academic Press 2009).
Los siguientes ejemplos ilustran realizaciones específicas de la invención.
Ejemplos
Ejemplo 1
Preparación del ligador homobifuncional NH2 ÍOCH2CH2 I2ONH2
El ligador homobifuncional NH2[OCH2CH2]2ONH2
Se sintetizó 3-oxapentano-1,5-dioxiamina que contenía dos grupos aminooxilo activos según Boturyn et al.
(Tetrahedron 1997; 53: 5485-92) en una reacción orgánica de dos etapas que emplea una síntesis de Gabriel modificada de aminas primarias (figura 1). En la primera etapa, se hizo reaccionar una molécula de 2,2-diclorodietil éter con dos moléculas de endo-N-hidroxi-5-norborneno-2,3-dicarboximida en DMF. Se preparó el producto homobifuncional deseado a partir del producto intermedio resultante por hidrazinolisis en etanol.
Ejemplo 2
Preparación del ligador homobifuncional NH2ÍOCH2CH216ONH2
El ligador homobifuncional NH2 [OCH2 CH2]6ONH2
Se sintetizó 3,6,9,12,15-pentaoxa-heptadecano-1,17-dioxiamina que contenía dos grupos aminooxilo activos según Boturyn et al. (Tetrahedron 1997; 53: 5485-92) en una reacción orgánica de dos etapas que emplea una síntesis de Gabriel modificada de aminas primarias. En la primera etapa, se hizo reaccionar una molécula de dicloruro de hexaetilenglicol con dos moléculas de endo-N-hidroxi-5-norborneno-2,3-dicarboximida en DMF. Se preparó el producto homobifuncional deseado a partir del producto intermedio resultante por hidrazinolisis en etanol.
Ejemplo 3
Preparación del ligador homobifuncional NHyfOCHyCHyUONH?
Se sintetizó el ligador homobifuncional NH2 [OCH2CH2]4ONH2 (3,6,9-triaoxaundecano-1,11-dioxiamina) que contenía dos grupos aminooxilo activos según Boturyn et al. (Tetrahedron 1997; 53: 5485-92) en una reacción orgánica de dos etapas que emplea una síntesis de Gabriel modificada de aminas primarias: En la primera etapa, se hizo reaccionar una molécula de bis-(2-(2-cloroetoxi)-etil)-éter con dos moléculas de endo-N-hidroxi-5-norborneno-2,3-dicarboximida en DMF. Se preparó el producto homobifuncional final a partir del producto intermedio resultante por hidrazinolisis en etanol.
Ejemplo 4
Preparación de sal de sodio del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiimino)-hexadecanoico
Se sintetizó el ligador de ácido graso-aminooxilo sal de sodio del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiimino)-hexadecanoico según Halligan y Nair (Arkivoc 2006 (ii) 101-106) y Hubbs y Heathcock (J Am Chem Soc, 2003; 125: 12836-43) en una reacción de dos etapas.
Producto intermedio 1: sal de sodio del ácido 16-oxohexadecanoico
A una disolución enfriada (0°C) de ácido 16-hidroxihexadecanoico (800 mg, 2,9 mmol) en diclorometano (10 ml) y tetrahidrofurano (20 ml) se le añadió peryodinano de Dess-Martin (1636 mg, 3,7 mmol) a 0°C. Se agitó la mezcla durante 3,5 horas a 0°C y 2,5 horas a temperatura ambiente bajo una atmósfera de Ar. Se añadió luego una disolución al 15% de tiosulfato de sodio en disolución saturada de bicarbonato de sodio, se agitó la mezcla a temperatura ambiente durante 1,5 horas. Se extrajo el producto intermedio 1 con dietil éter, después de secar sobre sulfato de sodio, se evaporó la fase orgánica hasta sequedad y se purificó por cromatografía en columna usando gel de sílice como agente de separación y una mezcla de disolventes de tolueno/acetato de etilo. Rendimiento: 34% (sólido blanco). Producto: sal de sodio del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiimino)-hexadecanoico
o
A una disolución de 3,6,9-triaoxaundecano-1,11-dioxiamina (146 mg, 0,65 mmol) en tetrahidrofurano anhidro (3 ml), se le añadió el producto intermedio 1 (19,1 mg, 0,07 mmol). Se agitó la mezcla durante 1,5 horas a temperatura ambiente bajo una atmósfera de Ar. Se evaporó luego la mezcla hasta sequedad y se purificó por cromatografía en columna usando gel de sílice como agente de separación y una mezcla de disolventes de diclorometano/metanol/base de Huenig. Rendimiento: 71% (sólido blanco).
Espectrometría de masas (ESI): m/z = 477,3529 para [M 2H]+
Ejemplo 5
Preparación de éster metílico del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiamino)-hexadecanoico Se sintetizó el ligador de éster metílico de ácidos grasos-aminooxilo éster metílico del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiamino)-hexadecanoico según Hang et al. (J Am Chem Soc 2007; 129: 2744-5) en una reacción de tres etapas.
Producto intermedio 1: éster metílico del ácido 16-hidroxihexadecanoico
A una disolución enfriada (0°C) de ácido 16-hidroxihexadecanoico (3000 mg, 10,79 mmol) en metanol anhidro (27 ml), se le añadió cloruro de acetilo (3,837 ml, 53,96 mmol) gota a gota a 0°C en el plazo de 2 minutos, se agitó luego la mezcla a temperatura ambiente durante 3,5 horas bajo una atmósfera de Ar. Posteriormente, se evaporó la mezcla hasta sequedad, se disolvió el residuo en diclorometano (100 ml), se lavó con disolución saturada de bicarbonato de sodio (2x50 ml) y disolución de salmuera (1x50 ml). Después de secar sobre sulfato de sodio, se evaporó la fase orgánica recogida hasta sequedad y se secó a vacío a temperatura ambiente. Rendimiento: 92% (sólido blanco). Producto intermedio 2: éster metílico del ácido 16-metilsulfonilhexadecanoico
A una disolución enfriada (0°C) del producto intermedio 1 (2807 mg, 9,80 mmol) en diclorometano (40 ml) se le añadió trietilamina (1,502 ml, 10,78 mmol), luego se le añadió una disolución preenfriada (0°C) de cloruro de mesilo (0,834 ml, 10,78 mmol) en diclorometano (5 ml) gota a gota en el plazo de 10 minutos a 0°C. Se agitó la mezcla durante 30 minutos a 0°C y durante 2,75 horas a temperatura ambiente. Luego se diluyó la mezcla con diclorometano (150 ml), se lavó con agua (1x100 ml), disolución saturada de bicarbonato de sodio (2x100 ml) y disolución de salmuera (1x100 ml). Después de secar sobre sulfato de sodio, se evaporó la fase orgánica recogida hasta sequedad y se secó a vacío a temperatura ambiente. Rendimiento: 95% (sólido blanco amarillo pálido).
Producto: éster metílico del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiamino)-hexadecanoico
A una disolución de 3,6,9-triaoxaundecano-1,11-dioxiamina (517 mg, 2,30 mmol) en N,N-dimetilformamida anhidra (22 ml) se le añadió una disolución de producto intermedio 2 (70 mg, 0,19 mmol) en N,N-dimetilformamida anhidra (7 ml) gota a gota durante 1 hora a temperatura ambiente bajo una atmósfera de Ar; se agitó la mezcla durante 2 días a diferentes temperaturas (temperatura ambiente, 50°C, 80°C) para completar la reacción. Se evaporó luego la mezcla hasta sequedad, se purificó el producto bruto por cromatografía en columna usando gel de sílice como agente de separación y una mezcla de disolventes de diclorometano/metanol. Rendimiento: 31% (aceite blanco incoloro parcialmente solidificado).
Espectrometría de masas (ESI): m/z = 493,3824 para [M H]+
Ejemplo 6
Acoplamiento de éster metílico del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiamino)-hexa-decanoico al resto de hidrato de carbono del factor VIII de la coagulación
Se prepara FA-rFVIII usando un procedimiento de dos etapas. En la primera etapa, se oxida rFVIII con NaIO4 y se purifica por cromatografía de intercambio aniónico (AEC). Posteriormente, el rFVIII oxidado se modifica con el reactivo FA-aminooxilo.
Se oxida rFVIII (material de partida de 45 mg) con NaIO4 (concentración final 200 |iM). Después de un tiempo de incubación de 30 minutos (22°C), se detiene la reacción de oxidación añadiendo una disolución acuosa de L-cisteína 1 M (concentración final: 10 mM). Se purifica el rFVIII oxidado por cromatografía de intercambio aniónico en EMD TMAE(M). Luego, se añaden 25 |il de una disolución al 10% (p/v) de éster metílico del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiamino)-hexadecanoico (preparado según el ejemplo 3) en DMSO al eluato (concentración de proteína 2 mg/ml) y se realiza la reacción de acoplamiento durante 18 horas a 4°C. Luego, se purifica el conjugado FA-rFVIII adicionalmente por HIC en Phenyl Sepharose 4 FF. Finalmente, se concentra el eluato por UF/DF usando una membrana de 30 kD (MILLIPORE).
Ejemplo 7
Acoplamiento de éster metílico del ácido 16-(2-(2-(2-(2-am¡noox¡etox¡)-etox¡)-etoxi)-etox¡am¡no)-hexa-decano¡co al resto de hidrato de carbono del factor IX de la coagulación
Se disuelven 10 mg de rFIX en tampón de reacción (L-histidina 20 mM, CaCl25 mM, NaCl 150 mM, pH 6,0) para dar una concentración final de 2,5 mg/ml. A esta disolución, se le añadió una disolución acuosa de NaIO4 para obtener una concentración final de 100 |iM. Se incubó la mezcla de reacción durante 1 hora a 4°C con agitación suave en la oscuridad. Luego, se carga la mezcla en columnas de desalación PD-10 preequilibradas para retirar el exceso de NaIO4. A esta mezcla, se le añaden 8 |il de una disolución al 10% (p/v) de éster metílico del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiamino)-hexa-decanoico (preparado según el ejemplo 3) en DMSO y se lleva a cabo la reacción de acoplamiento a pH 6,0 durante 18 h a 4°C. Luego, se purifica adicionalmente el conjugado por IEX en Q-Sepharose FF. Finalmente, se concentra el eluato por UF/DF usando dispositivos Vivaspin.
Ejemplo 8
Acoplamiento de éster metílico del ácido 16-(2-(2-(2-(2-am¡noox¡etox¡)-etox¡)-etoxi)-etox¡am¡no)-hexa-decano¡co al resto de hidrato de carbono del factor VIIa de la coagulación
Se disuelven 10 mg de rFVIIa en tampón de reacción ((Hepes 50 mM, cloruro de sodio 150 mM, cloruro de calcio 5 mM, pH 6,0) para dar una concentración final de 2,0 mg/ml. A esta disolución se le añade una disolución acuosa de NaIO4 5 mM para obtener una concentración final de 50 |iM. Se incuba la mezcla de reacción durante 1 h a 4°C con agitación suave en la oscuridad. Luego, se carga la mezcla en columnas de desalación PD-10 preequilibradas para retirar el exceso de NaIO4. A esta mezcla, se le añaden 8 |il de una disolución al 10% (p/v) de éster metílico del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiamino)-hexa-decanoico (preparado según el ejemplo 3) en DMSO y se lleva a cabo la reacción de acoplamiento a pH 6,0 durante 18 h a 4°C. Luego, se purifica adicionalmente el conjugado por IEX en Q-Sepharose FF. Finalmente, se concentra el eluato por UF/DF usando dispositivos Vivaspin.
Ejemplo 9
Acoplamiento de éster metílico del ácido 16-(2-(2-(2-(2-am¡noox¡etox¡)-etox¡)-etoxi)-etox¡am¡no)-hexa-decano¡co al resto de hidrato de carbono del factor VIII de la coagulación
Se disuelven 10 mg de rFVIII en tampón Hepes (Hepes 50 mM, NaCl 150 mM, cloruro de calcio 5 mM, pH 6,0) para dar una concentración de proteína de 2 mg/ml. Luego, se añaden 10 |il de una disolución al 10% (p/v) de éster metílico del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiamino)-hexadecanoico (preparado según el ejemplo 3) en DMSO a la disolución de FVIII. Posteriormente, se prepara una disolución acuosa del catalizador nucleófilo m-toluidina (50 mM) y se añade a la mezcla en el plazo de 15 minutos para obtener una concentración final de 10 mM. Finalmente, se añade una disolución acuosa de peryodato de sodio 40 mM para dar una concentración de 400 |iM. Se incuba la mezcla de reacción durante 120 minutos en la oscuridad a una temperatura de 22°C con agitación suave. Luego, se detiene la reacción mediante la adición de una disolución acuosa de L-cisteína (1 M) para dar una concentración final de 10 mM en la mezcla de reacción e incubación durante 60 minutos. Posteriormente, se carga la mezcla de reacción en una columna IEX cargada con Q-Sepharose FF (1,6 x 8 cm). Se lava la columna con 20 volúmenes de tampón de equilibrio de columna (Hepes 20 mM, CaCl2 5 mM, pH 7,4) y se eluye el conjugado FA-rFVIII con tampón B (Hepes 20 mM, CaCl2 5 mM), NaCl 0,5 M, pH 7,4). Finalmente, se somete el producto a UF/DF con dispositivos Vivaspin usando tampón Hepes, 7,4 (Hepes 20 mM, NaCl 150 mM, CaCl25 mM, pH 7,4) como tampón de diafiltración.
Ejemplo 10
Acoplamiento de éster metílico del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiamino)-hexa-decanoico al resto de hidrato de carbono del factor IX de la coagulación
Se disuelven 7 mg de rFIX en tampón His (His 20 mM, NaCl 150 mM, CaCl25 mM, pH 6,0) para dar una concentración de proteína de 2 mg/ml. Luego se añaden 7 |il de una disolución al 10% (p/v) de éster metílico del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiamino)-hexa-decanoico (preparado según el ejemplo 3) en DMSO a la disolución de FIX. Luego se prepara una disolución acuosa del catalizador nucleófilo m-toluidina (50 mM) y se añade a la mezcla en el plazo de 15 minutos para obtener una concentración final de 10 mM. Finalmente, se añade una disolución acuosa de peryodato de sodio 40 mM para dar una concentración de 250 |iM. Se incuba la mezcla de reacción durante 120 minutos en la oscuridad a una temperatura de 22°C con agitación suave. Posteriormente, se extingue la reacción mediante la adición de L-cisteína (concentración final: 5 mM) durante 30 minutos a temperatura ambiente.
Se purifica el conjugado FA-rFIX por cromatografía de intercambio aniónico. Se diluye la mezcla de reacción con 10 ml de tampón A (Hepes 50 mM, CaCl2 5 mM, pH 7,5) y se carga en una columna HiTrap Q FF de 5 ml (GE Healthcare, Fairfield, CT) equilibrada con el tampón A. Se lava la columna con 5 VC usando el mismo tampón. Luego, se eluye la columna con tampón B (Hepes 50 mM, NaCl 1 M, CaCl25 mM pH 7,5). Se concentran las fracciones que contienen conjugado por u F/DF usando una membrana de 10 kD compuesta por celulosa regenerada. Se realiza la etapa de diafiltración final contra tampón Hepes 20 mM, pH 7,2 que contenía NaCl 150 mM y CaCl25 mM.
Ejemplo 11
Acoplamiento de éster metílico del ácido 16-(2-(2-(2-(2-am¡noox¡etox¡)-etox¡)-etoxi)-etox¡am¡no)-hexa-decano¡co al resto de hidrato de carbono del factor VIIa de la coagulación
Se disuelven 10 mg de rFVIIa en tampón Hepes (Hepes 50 mM, cloruro de sodio 150 mM, cloruro de calcio 5 mM, pH 6,0). Luego, se añaden 10 |il de una disolución al 10% (p/v) de éster metílico del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiamino)-hexa-decanoico (preparado según el ejemplo 3) en DMSO a la disolución de FVIIa. Posteriormente, se prepara una disolución acuosa del catalizador nucleófilo m-toluidina (50 mM) y se añade a la mezcla en el plazo de 15 minutos para obtener una concentración final de 10 mM. Finalmente, se añade una disolución acuosa de peryodato de sodio 40 mM para dar una concentración de 250 |iM. Se incuba la mezcla de reacción durante 120 minutos en la oscuridad a una temperatura de 22°C con agitación suave. Posteriormente, se extingue la reacción mediante la adición de L-cisteína (concentración final: 5 mM) durante 30 minutos a temperatura ambiente. Se purifica el conjugado FA-rFVIIa por cromatografía de intercambio aniónico. Se diluye la mezcla de reacción con 10 ml de tampón A (Hepes 50 mM, pH 7,4) y se carga en una columna HiTrap Q f F de 5 ml (GE Healthcare, Fairfield, CT) equilibrada con el tampón A. Se lava la columna con 5 VC usando mismo tampón. Luego, se eluye la columna con tampón B (Hepes 50 mM, NaCl 1 M, CaCl25 mM pH 7,4). Se concentran las fracciones que contienen conjugado por UF/DF usando una membrana de 10 kD compuesta por celulosa regenerada. Se realiza la etapa de diafiltración final contra tampón Hepes 20 mM, pH 7,2 que contenía NaCl 150 mM y CaCl25 mM.
Ejemplo 12
Acoplamiento de un derivado de FA que contiene un grupo aminooxilo activo a un resto de hidrato de carbono oxidado en presencia de un catalizador nucleófilo
También se proporciona el acoplamiento de un derivado de FA que contiene un grupo aminooxilo activo a una proteína terapéutica oxidada (tal como las proteínas expuestas en la tabla 1 en el presente documento).
Para el acoplamiento de un derivado de FA que contiene un grupo aminooxilo, se oxidan en primer lugar los restos de hidrato de carbono (predominantemente N-glicanos) de una proteína terapéutica (por ejemplo, EPO, G-CSF o insulina; véase la tabla 1; concentración: 0,5-3 mg/ml) con NaIO4 (concentración: 200 |iM). Luego, se detiene la reacción mediante la adición de L-cisteína (concentración final: 5 mM) y se separan los reactivos por UF/DF. Después de la diafiltración, se añade el reactivo aminooxilo de FA (es decir, el derivado de FA) usando un exceso de 25 M y se realiza la reacción de acoplamiento a pH 6,0 durante 1 hora a temperatura ambiente con agitación suave en presencia del catalizador nucleófilo m-toluidina (concentración: 10 mM). Posteriormente, se carga la mezcla de reacción en una columna de intercambio iónico (IEX). Se lava la columna con> 5 VC de tampón de lavado y se eluye el conjugado con un gradiente lineal de NaCl. Finalmente, se someten las fracciones que contienen conjugado a u F/DF.
Ejemplo 13
Acoplamiento de un derivado de FA que contiene un grupo aminooxilo activo a un resto de hidrato de carbono oxidado en presencia de un catalizador nucleófilo
Para el acoplamiento de un derivado de FA que contiene un grupo aminooxilo con el resto de hidrato de carbono de una proteína terapéutica, se incuba la proteína (por ejemplo, EPO, G-CSF o insulina; véase la tabla 1; concentración: 0,5-3 mg/ml) a pH 6,0 con NaIO4 (concentración: 300 |iM) durante 1 hora a temperatura ambiente en presencia del
catalizador nucleófilo m-toluidina (concentración: 10 mM). Luego, se detiene la reacción mediante la adición de L-cisteína (concentración final: 5 mM) y se carga la mezcla de reacción en una columna de intercambio iónico (IEX). Se lava la columna con> 5 VC de tampón de lavado y se eluye el conjugado con un gradiente lineal de NaCl. Finalmente, se someten las fracciones que contienen conjugado a u F/DF.
Ejemplo 14
Acoplamiento de un derivado de FA que contiene un grupo aminooxilo activo con una proteína de la coagulación sanguínea oxidada en presencia de un catalizador nucleófilo
Puede llevarse a cabo el acoplamiento de un derivado de FA que contiene un grupo aminooxilo activo a una proteína de la coagulación sanguínea oxidada (tal como FIX, FVIII y FVIIa tal como se describe en los ejemplos anteriores) en presencia de un catalizador nucleófilo tal como m-toluidina en un intervalo de concentración de 2-20 mM.
Ejemplo 15
Preparación de un ligador de ácido graso de MAL soluble en agua
Se prepara un ligador de ácido graso que contiene una cadena de PEG soluble en agua en posición o y un grupo MAL activo en una síntesis de dos etapas:
Etapa 1: preparación de éster metílico del ácido 16-hidroxihexadecanoico:
O
- o ^ f4 r OH
Se esterifica ácido 16-hidroxihexadecanoico disponible comercialmente con cloruro de acetilo en metanol durante 5 h a temperatura ambiente según el ejemplo 3 para dar el éster metílico correspondiente (Hang et al., Chemical probes for the rapid detection of fatty-acylated proteins in mammalian cells, JACS 2007; 129: 2744-5).
Etapa 2: preparación del ligador de ácido graso de MAL:
Se hace reaccionar éster metílico del ácido 16-hidroxihexadecanoico con MAL-PEG-COOH disponible comercialmente (mal-Peg (12)-COOH/IRIS Biotech GmbH, Marktredwitz, Alemania) empleando una reacción de Mitsunobu en THF a temperatura ambiente durante la noche (Toyokuni et al., Synthesis of a New Heterobifunctional Linker, N-[4-(Aminooxy)butyl]-maleimide, for Facile Access to a Thiol-Reactive 18F-Labeling Agent, Bioconjugate Chem 2003; 14: 1253-9).
Ejemplo 16
Preparación de un ligador de ácido graso de NHS soluble en agua
Se prepara un ligador de ácido graso que contiene una cadena de PEG soluble en agua en posición o y un éster de NHS activo terminal mediante el uso de una síntesis de cuatro etapas:
Etapa 1: preparación de éster metílico del ácido 16-bromohexadecanoico
Se esterifica ácido 16-bromohexadecanoico disponible comercialmente con metanol y una cantidad catalítica de ácido sulfúrico concentrado durante la noche a temperatura de reflujo para dar el éster metílico correspondiente (Zinic et al., Positionally Isomeric Organic gelators: Structure-Gelation Study, Racemic versus Enantiomeric Gelators, and Solvation Effects, Chem Eur J 2010; 16: 3066-82).
Etapa 2: preparación de éster metílico del ácido 16-azidohexadecanoico
Se hace reaccionar éster metílico del ácido 16-bromohexadecanoico con azida de sodio en acetonitrilo durante cuatro días a temperatura de reflujo para dar la azida correspondiente (Zinic et al., Positionally Isomeric Organic Gelators: Structure-Gelation Study, Racemic versus Enantiomeric Gelators, and Solvation Effects, Chem. EUR. J. 2010; 16: 3066-82).
Etapa 3: preparación de éster metílico del ácido 16-aminohexadecanoico
Se hidrogena catalíticamente éster metílico del ácido 16-azidohexadecanoico con paladio/carbón activado en metanol a 3 bares durante tres horas para dar la amina correspondiente (Zinic et al., Positionally Isomeric Organic Gelators: Structure-Gelation Study, Racemic versus Enantiomeric Gelators, and Solvation Effects, Chem. EUR. J. 2010; 16: 3066-82).
Etapa 4: preparación del ligador de ácido graso de NHS
Se hace reaccionar éster metílico del ácido 16-aminohexadecanoico de NHS-PEG-NHS disponible comercialmente (NHS-dPEG (4)-NHS/IRIS Biotech GmbH, Marktredwitz, Alemania) en 1,4-dioxano a temperatura ambiente durante tres días para dar el ligador de ácido graso de NHS (Cline et al., The Aminolysis of N-Hydroxysuccinimide Esters. A Structure-Reactivity Study, JACS 1987; 109: 3087-91).
Ejemplo 17
Caracterización analítica de conjugados de proteínas FA
Las propiedades de unión a albúmina de las muestras de FA-rFVIII, rFIX o FVIIa preparadas según los ejemplos en el presente documento se verifican in vitro mediante el uso de sistemas de ensayo de inmunoabsorción ligado a enzimas (ELISA). Se recubre una placa de 96 pocillos con un anticuerpo policlonal dirigido contra la albúmina sérica humana (HSA). La siguiente etapa es el bloqueo de la placa de ELISA con un tampón de gelatina-PBS. Luego, se une HSA al anticuerpo seguido de la unión de la muestra de proteína FA, que se diluye a diferentes concentraciones. Finalmente, la muestra de proteína-HSA se detecta mediante un anticuerpo anti-VIII, anti-FIX o anti-FVIIa marcado con peroxidasa. La actividad peroxidasa se detecta usando tetrametilbencidina (TMB) como sustrato. La intensidad de color desarrollada se mide con un lector de ELISA a 450 nm. La unión de la muestra de proteína FA a HSA se evalúa trazando las diferentes concentraciones de muestra en el eje x y sus valores de absorbancia correspondientes en el eje y.
Ejemplo 18
Preparación de un ligador de ácido graso pegilado soluble en agua que contiene un grupo aminooxilo
Se prepara un ligador de ácido graso que contiene una cadena de PEG soluble en agua con un resto aminooxilo en posición ra conectada al grupo carboxilo de ácido graso en una síntesis de tres etapas usando 3-oxapentano-1,5-dioxiamina tal como se describe en el ejemplo 1.
Etapa 1: preparación de N-(9-fluorenilmetoxicarbonil)-3-oxapentano-1,5-dioxiamina
Se hizo reaccionar 3-oxapentano-1,5-dioxiamina con cloroformiato de 9-fluorenilmetilo en 1,4-dioxano a temperatura ambiental durante 1 hora. Se evaporó la disolución a presión reducida y se purificó el producto bruto empleando cromatografía en gel de sílice con diclorometano/metanol 20/1 (v/v) como la mezcla de disolventes para dar dioxiamina pura protegida con mono-FMOC (Boturyn et al., Synthesis of Fluorescent Probes for the Detection of Abasic Sites in DNA, Tetrahedron 1997; vol. 53, n.° 15, 5485-92).
Etapa 2: preparación de (2-(2-(N-(9-fluorenilmetoxicarbonil)aminooxi)etoxi)etoxi)amida de ácido hexadecanoico
Se hace reaccionar N-(9-fluorenilmetoxicarbonil)-3-oxapentano-1,5-dioxiamina con éster de N-hidroxisuccinimida de ácido palmítico disponible comercialmente en THF a temperatura ambiente durante la noche para dar el conjugado de ácido graso-aminooxilo protegido con mono-FMOC (Jong et al., Synthesis of ceramides using N-hydroxysuccinimide esters, Journal of Lipid Research 1972; Vol. 13, 819-22).
Etapa 3: preparación de (2-(2-aminooxietoxi)etoxi)amida de ácido hexadecanoico
Se hace reaccionar conjugado de ácido graso-aminooxilo protegido con mono-FMOC con piperidina en diclorometano a temperatura ambiental para dar el ligador de ácido graso-aminooxilo desprotegido como producto final (Boturyn et al., Synthesis of Fluorescent Probes for the Detection of Abasic Sites in DNA, Tetrahedron 1997; vol. 53, n.° 15, 5485 92).
Ejemplo 19 (ejemplo de referencia)
Acoplamiento de un ligador de ácido graso de MAL con A1PI
Se prepara un ligador de ácido graso que contenía un grupo MAL tal como se describe en el ejemplo 15 por reacción de éster metílico del ácido 16-hidroxihexadecanoico con Ma L-PEG-COOH disponible comercialmente (mal-Peg (12)-COOH/IRIS Biotech GmbH, Marktredwitz, Alemania) empleando una reacción de Mitsunobu. Se acopla este ligador al grupo SH libre de A1PI.
Se disuelven 10 mg de A1PI purificado (concentración: 1 mg/ml) en tampón de reacción (fosfato 20 mM, EDTA 5 mM, pH 7,0) y se añaden 10 | l de una disolución al 5% (p/v) del ligador de ácido graso de MAL en DMSO a la disolución de A1PI. Se realiza la reacción de modificación durante 2 horas a temperatura ambiente seguido de una etapa de enfriamiento usando L-cisteína (concentración final: 10 mM). Después de la adición de L-cisteína, se incuba la mezcla de reacción con agitación suave durante una hora adicional a la misma temperatura. Se diluye el A1PI modificado con tampón de equilibrio (fosfato 25 mM, pH 6,5) para corregir la conductividad de las disoluciones a <4,5 mS/cm y se carga en una columna HiTrap Q FF (GE-Healthcare) precargada con un volumen de columna (VC) de 5 ml. Luego se equilibra la columna con 10 VC de tampón de equilibrio (velocidad de flujo: 2 ml/min). Finalmente, se eluye el PEG-A1PI con un gradiente lineal con tampón de elución (Na2HPO425 mM, NaCl 1 M, pH 6,5).
Ejemplo 20 (ejemplo de referencia)
Acoplamiento de un ligador de ácido graso del NHS con factor de la coagulación VIII
Se prepara un ligador de ácido graso que contenía un grupo NHS tal como se describe en el ejemplo 16 por reacción de éster metílico del ácido 16-hidroxihexadecanoico de NHS-PEG-NHS disponible comercialmente (NHS-dPEG (4)-NHS (IRIS Biotech GmbH, Marktredwitz, Alemania). Se acopla este ligador a los grupos amino libres de residuos de lisina del factor VIII de la coagulación.
Se disuelven 10 mg de rFVIII en tampón Hepes (Hepes 50 mM, NaCl 150 mM, cloruro de calcio 5 mM, pH 6,0) para dar una concentración de proteína de 2 mg/ml. Luego se añaden 10 |il de una disolución al 10% (p/v) de ligador de ácido graso de NHS en d Ms O a la disolución de FVIII. Se incuba la mezcla de reacción durante 120 minutos en la oscuridad a una temperatura de 22°C con agitación suave. Luego, se detiene la reacción mediante la adición de una disolución acuosa de glicina (1 M) para dar una concentración final de 20 mM en la mezcla de reacción. Se incuba la mezcla durante 15 minutos a temperatura ambiente con agitación suave y posteriormente se carga en una columna IEX cargada con Q-Sepharose f F (1,6 x 8 cm). Se lava la columna con 20 volúmenes de tampón de equilibrio de columna (Hepes 20 mM, CaCh 5 mM, pH 7,4) y se eluye el conjugado FA-rFVIII con tampón B (Hepes 20 mM, CaCh 5 mM, NaCl 0,5 M, pH 7,4). Finalmente, se somete el producto a UF/DF con dispositivos Vivaspin usando tampón Hepes, 7,4 (Hepes 20 mM, NaCl 150 mM, CaCl25 mM, pH 7,4) como tampón de diafiltración.
Claims (18)
- REIVINDICACIONESi . Conjugado de un derivado de ácido graso soluble en agua y una proteína terapéutica, en el que el derivado de ácido graso soluble en agua comprende un ácido graso o éster de ácido graso unido a un ligador soluble en agua, y en el que el derivado de ácido graso soluble en agua se une de manera estable a la proteína terapéutica mediante una unión oxima formada entre un grupo aminooxilo en el ligador soluble en agua y un grupo aldehído de un hidrato de carbono oxidado en la proteína terapéutica.
- 2. Conjugado según la reivindicación 1, que une albúmina sérica humana (HSA) in vitro o in vivo, tiene semivida aumentada en relación con una proteína terapéutica nativa, y en el que el ácido graso es un ácido graso saturado o ácido graso insaturado.
- 3. Conjugado según la reivindicación 2, en el que el ácido graso es un ácido graso de cadena ramificada.
- 4. Conjugado según una cualquiera de las reivindicaciones 1-3, en el que el ácido graso comprende una longitud de cadena seleccionada del grupo que consiste en C10, C12, C14, C16, C18, C20, C22 y C24.
- 5. Conjugado según una cualquiera de las reivindicaciones 1-4, en el que el ácido graso se une al ligador soluble en agua a un grupo en el ácido graso seleccionado del grupo que consiste en: grupo carboxilo terminal y grupo o, en el que el grupo o se selecciona del grupo que consiste en: hidroxilo, amino, tio y carboxilo.
- 6. Conjugado según la reivindicación 1 o la reivindicación 2, en el que el ácido graso es ácido 16-hidroxihexadecanoico o el éster de ácido graso es éster metílico del ácido 16-hidroxihexadecanoico.
- 7. Conjugado según la reivindicación 1 o la reivindicación 2, en el que el éster de ácido graso es éster metílico o éster etílico.
- 8. Conjugado según una cualquiera de las reivindicaciones 1-7, en el que el ligador soluble en agua comprende un polímero soluble en agua y al menos un grupo aminooxilo unido a la proteína terapéutica.
- 9. Conjugado según la reivindicación 1 o la reivindicación 2, en el que el derivado de ácido graso soluble en agua esa) sal de sodio del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiimino)-hexadecanoico de fórmula:' ob) éster metílico del ácido 16-(2-(2-(2-(2-aminooxietoxi)-etoxi)-etoxi)-etoxiamino)-hexadecanoico,
- 10. Método de preparación de una proteína terapéutica conjugada que comprende poner en contacto un resto de hidrato de carbono oxidado en la proteína terapéutica con el derivado de ácido graso soluble en agua según la reivindicación 1, en condiciones que permitan la conjugación;dicho resto de hidrato de carbono oxidado mediante incubación con un tampón que comprende un agente oxidante seleccionado del grupo que consiste en peryodato de sodio (NaIO4), tetraacetato de plomo (Pb(OAc)4 ) y perrutenato de potasio (KRuO4 );en el que una unión oxima se forma entre el resto de hidrato de carbono oxidado y un grupo aminooxilo activo en el derivado de ácido graso;y en el que dicha formación de unión oxima se cataliza por un catalizador nucleófilo seleccionado del grupo que consiste en anilina, ácido o-aminobenzoico, ácido m-aminobenzoico, ácido p-aminobenzoico, ácido sulfanílico, o-aminobenzamida, o-toluidina, m-toluidina, p-toluidina, o-anisidina, m-anisidina y p-anisidina.
- 11. Método de preparación de una proteína terapéutica conjugada según la reivindicación 10, que comprende además un método de preparación del derivado de ácido graso soluble en agua según la reivindicación 1, que comprende:a) oxidar un grupo o-hidroxilo en un ácido graso para generar un grupo aldehído en el ácido graso; y b) acoplar un ligador soluble en agua que comprende un grupo aminooxilo activo al grupo aldehido para formar una unión oxima estable;en el que dicho derivado de ácido graso es soluble en agua; en el que el grupo o-hidroxilo se oxida por un reactivo de oxidación seleccionado del grupo que consiste en: reactivo de peryodinano de Dess Martin, reactivo Tempo, cloruro de oxalilo/DMSO, perrutenato de tetrapropilamonio (TPAP) y reactivos de cromo VI (reactivo de Collins, clorocromato de piridinio (PCC) y dicromato de piridinio); en el que el ácido graso es un ácido graso saturado o ácido graso insaturado.
- 12. Método de preparación de una proteína terapéutica conjugada según la reivindicación 10, que comprende además un método de preparación del derivado de ácido graso soluble en agua según la reivindicación 1, que comprende:a) esterificar un grupo carboxilo en un ácido graso para generar un éster en el ácido graso;b) activar un grupo o-hidroxilo en un ácido graso para generar un grupo mesilo en el ácido graso de la etapa a); yc) acoplar un ligador soluble en agua que comprende un grupo aminooxilo activo sustituyendo el grupo mesilo de la etapa b) formando así un enlace de oxiimina-metileno estable;en el que dicho derivado de ácido graso es soluble en agua; en el que el grupo carboxilo se esterifica por un agente de esterificación seleccionado del grupo que consiste en: cloruro de acetilo, metanol en presencia de ácido, etanol en presencia de ácido, diazometano y yoduro de metilo;en el que el grupo o-hidroxilo se activa por un agente de activación seleccionado del grupo que consiste en: cloruro de mesilo, cloruro de tosilo y cloruro de nosilo; y en el que el ácido graso es un ácido graso saturado o ácido graso insaturado.
- 13. Método según la reivindicación 11 o la reivindicación 12, en el que el ácido graso es un ácido graso de cadena ramificada.
- 14. Método según la reivindicación 11 o la reivindicación 12, en el que el ácido graso comprende una longitud de cadena seleccionada del grupo que consiste en C10, C12, C14, C16, C18, C20, C22 y C24, en el que opcionalmente el ácido graso es ácido 16-hidroxihexadecanoico.
- 15. Método según una cualquiera de las reivindicaciones 11 a 14, en el que el ligador soluble en agua comprende un polímero soluble en agua y al menos un grupo aminooxilo.
- 16. Conjugado según la reivindicación 8 o método según la reivindicación 15, en el que el polímero soluble en agua se selecciona del grupo que consiste en: polietilenglicol (PEG), PEG ramificado, poli(ácido siálico) (PSA), almidón de hidroxialquilo (HAS), almidón de hidroxietilo (HES), hidrato de carbono, polisacáridos, pululano, quitosano, ácido hialurónico, sulfato de condroitina, sulfato de dermatán, almidón, dextrano, carboximetildextrano, poli(óxido de alquileno) (PAO), polialquilenglicol (PAG), polipropilenglicol (PPG), polioxazolina, poliacriloilmorfolina, poli(alcohol vinílico) (PVA), policarboxilato, polivinilpirrolidona, polifosfaceno, polietileno-co-anhídrido de ácido maleico, poliestireno-co-anhídrido de ácido maleico, y poli(1-hidroximetiletilenhidroximetilformal) (PHF).
- 17. Conjugado o método según la reivindicación 16, en el que el polímero soluble en agua es PEG y comprende una longitud de cadena seleccionada del grupo que consiste en O3, O5, O7, O9, O11, O13 y O15.
- 18. Conjugado o método según la reivindicación 17, en el que el ligador soluble en agua se selecciona del grupo que consiste en:a) 3-oxapentano-1,5-dioxiamina de fórmula:b) 3,6,9-triaoxaundecano-1,11-dioxiamina de fórmula:c) 3,6,9,12,15-pentaoxaheptadecano-1,17-dioxiamina de fórmula:d) 3,6,9,12,15,18,21-heptaoxatricosano-1,23-dioxiamina de fórmula:Conjugado según cualquiera de las reivindicaciones 1-9 y 16-18 o método según cualquiera de las reivindicaciones 10 y 16-18, en el que la proteína terapéutica se selecciona del grupo que consiste en: factor IX (FIX), factor VIII (FVIII), factor VIIa (FVIIa), factor de von Willebrand (VWF), factor V (FV), factor X (FX), factor XI (FXI), factor XII (FXII), trombina (FII), proteína C, proteína S, tPA, PAI-1, tromboplastina tisular(TF), proteasa AdAm TS 13, IL-1 alfa, IL-1 beta, iL-2, IL-3, IL-4, IL-5, IL-6, IL-11, factor estimulante de colonias 1 (CSF-1), M-CSF, SCF, GM-CSF, factor estimulante de colonias de granulocitos (G-CSF), EPO, interferón alfa (IFN-alfa), interferón de consenso, IFN-beta, IFN-gamma, IFN-omega, IL-7, IL-8, IL-9, IL-10, IL-12, IL-13, IL-14, IL-15, IL-16, IL-17, IL-18, IL-19, IL-20, IL-21, IL-22, IL-23, IL-24, IL-31, IL-32 alfa, IL-33, trombopoyetina (TPO), Ang-1, Ang-2, Ang-4, Ang-Y, polipéptido similar a angiopoyetina 1 (ANGPTL1), polipéptido similar a angiopoyetina 2 (ANGPTL2), polipéptido similar a angiopoyetina 3 (ANGPTL3), polipéptido similar a angiopoyetina 4 (ANGPTL4), polipéptido similar a angiopoyetina 5 (ANGPTL5), polipéptido similar a angiopoyetina 6 (ANGPTL6), polipéptido similar a angiopoyetina 7 (ANGPTL7), vitronectina, factor de crecimiento endotelial vascular (VEGF), angiogenina, activina A, activina B, activina C, proteína morfogénica ósea 1, proteína morfogénica ósea 2, proteína morfogénica ósea 3, proteína morfogénica ósea 4, proteína morfogénica ósea 5, proteína morfogénica ósea 6, proteína morfogénica ósea 7, proteína morfogénica ósea 8, proteína morfogénica ósea 9, proteína morfogénica ósea 10, proteína morfogénica ósea 11, proteína morfogénica ósea 12, proteína morfogénica ósea 13, proteína morfogénica ósea 14, proteína morfogénica ósea 15, receptor IA de proteínas morfogénicas óseas, receptor IB de proteínas morfogénicas óseas, receptor II de proteínas morfogénicas óseas, factor neurotrófico derivado del cerebro, cardiotrofina 1, factor neurotrófico ciliar, receptor del factor neurotrófico ciliar, cripto, críptico, factor quimiotáctico de neutrófilos inducido por citocinas 1, factor quimiotáctico de neutrófilos inducido por citocinas 2a, factor quimiotáctico de neutrófilos inducido por citocinas 2p, factor de crecimiento de células endoteliales p, endotelina 1, factor de crecimiento epidérmico, Epigen, epirregulina, factor quimiotáctico para neutrófilos derivado de células epiteliales, factor de crecimiento de fibroblastos 4, factor de crecimiento de fibroblastos 5, factor de crecimiento de fibroblastos 6, factor de crecimiento de fibroblastos 7, factor de crecimiento de fibroblastos 8, factor de crecimiento de fibroblastos 8b, factor de crecimiento de fibroblastos 8c, factor de crecimiento de fibroblastos 9, factor de crecimiento de fibroblastos 10, factor de crecimiento de fibroblastos 11, factor de crecimiento de fibroblastos 12, factor de crecimiento de fibroblastos 13, factor de crecimiento de fibroblastos 16, factor de crecimiento de fibroblastos 17, factor de crecimiento de fibroblastos 19, factor de crecimiento de fibroblastos 20, factor de crecimiento de fibroblastos 21, factor de crecimiento ácido de fibroblastos, factor de crecimiento básico de fibroblastos, receptor a1 del factor neurotrófico derivado de la línea celular glial, receptor a2 del factor neurotrófico derivado de la línea celular glial, proteína relacionada con el crecimiento, proteína relacionada con el crecimiento a, proteína relacionada con el crecimiento p, proteína relacionada con el crecimiento y, factor de crecimiento epidérmico de unión a heparina, factor de crecimiento de hepatocitos, receptor del factor de crecimiento de hepatocitos, factor de crecimiento derivado del hepatoma, factor de crecimiento similar a la insulina I, receptor del factor de crecimiento similar a la insulina, factor de crecimiento similar a la insulina II, proteína de unión al factor de crecimiento similar a la insulina, factor de crecimiento de queratinocitos, factor inhibidor de la leucemia, receptor a del factor inhibidor de la leucemia, factor de crecimiento nervioso, receptor del factor de crecimiento nervioso, neuropoyetina, neurotrofina 3, neurotrofina 4, oncostatina M (OSM), factor de crecimiento placentario, factor de crecimiento placentario 2, factor de crecimiento de células endoteliales derivado de plaquetas, factor de crecimiento derivado de plaquetas, cadena A del factor de crecimiento derivado de plaquetas, factor de crecimiento derivado de plaquetas AA, factor de crecimiento derivado de plaquetas AB, cadena B del factor de crecimiento derivado de plaquetas, factor de crecimiento derivado de plaquetas BB, receptor a del factor de crecimiento derivado de plaquetas, receptor p del factor de crecimiento derivado de plaquetas, factor estimulante del crecimiento de células pre-B, factor de células madre (SCF), receptor del factor de células madre, TNF, TNF0, TNF1, TNF2, factor de crecimiento transformante a, factor de crecimiento transformante p, factor de crecimiento transformante p1, factor de crecimiento transformante p1.2, factor de crecimiento transformante p2, factor de crecimiento transformante p3, factor de crecimiento transformante p5, factor de crecimiento transformante latente p1, proteína I de unión al factor de crecimiento transformante p, proteína II de unión al factor de crecimiento transformante p, proteína III de unión al factor de crecimiento transformante p, linfopoyetina estromal tímica (TSLP), receptor de tipo I del factor de necrosis tumoral, receptor de tipo II del factor de necrosis tumoral, receptor activador del plasminógeno de tipo urocinasa, proteína de activación de fosfolipasas (PUP), insulina, lectina, ricina, prolactina, gonadotropina coriónica, hormona foliculoestimulante, hormona estimulante del tiroides, activador tisular del plasminógeno, IgG, IgE, IgM, IgA e IgD, agalactosidasa, p-galactosidasa, ADNasa, fetuína, hormona luteinizante, estrógeno, albúmina, lipoproteínas, fetoproteína, transferrina, trombopoyetina, urocinasa, integrina, trombina, leptina, Humira (adalimumab), Prolia (denosumab), Enbrel (etanercept), una proteína en la tabla 1, o un fragmento, derivado o variante biológicamente activo de la misma.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201061426356P | 2010-12-22 | 2010-12-22 | |
| PCT/US2011/065591 WO2012087838A1 (en) | 2010-12-22 | 2011-12-16 | Materials and methods for conjugating a water soluble fatty acid derivative to a protein |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2800983T3 true ES2800983T3 (es) | 2021-01-07 |
Family
ID=45464916
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES11806103T Active ES2800983T3 (es) | 2010-12-22 | 2011-12-16 | Materiales y métodos para conjugar un derivado de ácido graso soluble en agua con una proteína |
Country Status (20)
| Country | Link |
|---|---|
| US (1) | US8945897B2 (es) |
| EP (2) | EP2654794B8 (es) |
| JP (1) | JP6138052B2 (es) |
| KR (1) | KR102025442B1 (es) |
| CN (1) | CN103269723B (es) |
| AR (1) | AR084576A1 (es) |
| AU (2) | AU2011349574B9 (es) |
| BR (1) | BR112013015898A2 (es) |
| CA (1) | CA2822591C (es) |
| DK (1) | DK2654794T3 (es) |
| EA (1) | EA032056B1 (es) |
| ES (1) | ES2800983T3 (es) |
| HU (1) | HUE049352T2 (es) |
| MX (1) | MX345608B (es) |
| NZ (1) | NZ612320A (es) |
| PL (1) | PL2654794T3 (es) |
| PT (1) | PT2654794T (es) |
| SG (1) | SG191298A1 (es) |
| TW (1) | TWI546279B (es) |
| WO (1) | WO2012087838A1 (es) |
Families Citing this family (31)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2892908A4 (en) * | 2012-09-10 | 2016-05-11 | Univ Johns Hopkins | FESTPHASENGLYCAN AND GLYCOPEPTIDE ANALYSIS AND MICROFLUIDIC CHIP FOR GLYCOME EXTRACTION AND ANALYSIS AND METHOD FOR THEIR USE |
| CN103897031A (zh) * | 2012-12-25 | 2014-07-02 | 深圳先进技术研究院 | 化学修饰的胸腺五肽及其合成方法 |
| US20140243220A1 (en) * | 2013-02-25 | 2014-08-28 | J. Craig Venter Institute | Metaproteomic Method to Identify Secreted Pattern Recognition Molecules and Adhesive Antimicrobial Factors for Detection of Microbial Agents Eliciting Inflammation in the Human Host |
| EP2976365A1 (en) * | 2013-03-20 | 2016-01-27 | Fresenius Kabi Deutschland GmbH | Process for the preparation of thiol functionalized hydroxyalkyl starch derivatives |
| CN103636918B (zh) * | 2013-12-13 | 2015-11-04 | 东北农业大学 | 一种富含亚油酸的改性分离蛋白制备方法 |
| WO2015095553A1 (en) | 2013-12-20 | 2015-06-25 | Nephrogenesis, Llc | Methods and apparatus for kidney dialysis |
| EP2915569A1 (en) | 2014-03-03 | 2015-09-09 | Cytune Pharma | IL-15/IL-15Ralpha based conjugates purification method |
| CN107921103A (zh) * | 2015-08-12 | 2018-04-17 | 细胞机械股份有限公司 | 涉及长半衰期凝血复合物的方法和组合物 |
| CN106554425B (zh) * | 2015-09-18 | 2018-10-30 | 沈阳药科大学 | 一种聚唾液酸的脂质接枝衍生物及其应用 |
| KR20170065016A (ko) * | 2015-12-02 | 2017-06-12 | 한미약품 주식회사 | 지방산 유도체를 이용한 단백질 결합체 및 이의 제조방법 |
| CN108147990B (zh) * | 2016-12-02 | 2023-01-24 | 上海中医药大学 | 一种膜锚定元件及其应用 |
| CN110637027B (zh) | 2017-02-08 | 2024-08-30 | 百时美施贵宝公司 | 包含药代动力学增强子的修饰的松弛素多肽及其用途 |
| CN107141354A (zh) * | 2017-05-05 | 2017-09-08 | 李斯文 | 一种融合蛋白及光敏剂复合物及其制备方法和应用 |
| WO2019023295A1 (en) | 2017-07-27 | 2019-01-31 | Saint Louis University | Fatty acid modified human epidermal growth factor |
| JP6984923B2 (ja) * | 2017-09-19 | 2021-12-22 | イミュンワーク インク.Immunwork Inc. | アルブミンとの強化された結合親和性を有する医薬構築物 |
| US11845989B2 (en) | 2019-01-23 | 2023-12-19 | Regeneron Pharmaceuticals, Inc. | Treatment of ophthalmic conditions with angiopoietin-like 7 (ANGPTL7) inhibitors |
| JP2022523301A (ja) | 2019-01-23 | 2022-04-22 | リジェネロン・ファーマシューティカルズ・インコーポレイテッド | アンジオポエチン様7(angptl7)阻害剤による眼疾患の治療 |
| EP3819307A1 (en) * | 2019-11-07 | 2021-05-12 | CytoKi Pharma ApS | Therapeutic derivatives of interleukin-22 |
| TW202128961A (zh) | 2019-11-20 | 2021-08-01 | 美商安維塔生物科學股份有限公司 | 細胞激素融合蛋白及其醫藥組合物及治療應用 |
| US11897930B2 (en) | 2020-04-28 | 2024-02-13 | Anwita Biosciences, Inc. | Interleukin-2 polypeptides and fusion proteins thereof, and their pharmaceutical compositions and therapeutic applications |
| CN113967267B (zh) * | 2020-07-21 | 2022-10-25 | 四川大学 | 脂肪酸修饰的白蛋白的内质网靶向作用及其用途 |
| WO2022182768A1 (en) | 2021-02-26 | 2022-09-01 | Regeneron Pharmaceuticals, Inc. | Treatment of inflammation with glucocorticoids and angiopoietin-like 7 (angptl7) inhibitors |
| EP4089108A1 (en) * | 2021-05-11 | 2022-11-16 | CytoKi Pharma ApS | Therapeutic derivatives of interleukin-22 |
| EP4089107A1 (en) * | 2021-05-11 | 2022-11-16 | CytoKi Pharma ApS | Therapeutic derivatives of interleukin-22 |
| EP4337680A1 (en) * | 2021-05-11 | 2024-03-20 | Cytoki Pharma ApS | Therapeutic derivatives of interleukin-22 |
| CN114990175B (zh) * | 2021-10-22 | 2023-03-31 | 岩唐生物科技(杭州)有限责任公司 | 一种岩藻糖衍生物的合成方法 |
| EP4561630A1 (en) * | 2022-07-29 | 2025-06-04 | The Trustees of The University of Pennsylvania | Lymphatic targeted anti-coagulant for the prevention of lymphatic thrombosis |
| CN115894719B (zh) * | 2022-11-24 | 2023-10-20 | 武汉禾元生物科技股份有限公司 | 一种人血清白蛋白胰岛素偶联物及其制备方法 |
| WO2025133203A1 (en) * | 2023-12-22 | 2025-06-26 | Pam Theragnostics Gmbh | Compounds and methods for a long-lasting pam |
| CN118209737B (zh) * | 2024-05-22 | 2024-08-09 | 国科大杭州高等研究院 | 一种用于鉴定检测脂肪酸与蛋白质相互作用的方法 |
| CN120801727B (zh) * | 2025-09-15 | 2026-01-06 | 江西本草天工科技有限责任公司 | 系统性红斑狼疮的诊断标志物及其应用 |
Family Cites Families (148)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4179337A (en) | 1973-07-20 | 1979-12-18 | Davis Frank F | Non-immunogenic polypeptides |
| JPS54113492A (en) | 1978-02-24 | 1979-09-05 | Sanyo Chem Ind Ltd | Preparation of glucoprotein derivative |
| US4356170A (en) | 1981-05-27 | 1982-10-26 | Canadian Patents & Development Ltd. | Immunogenic polysaccharide-protein conjugates |
| US4757006A (en) | 1983-10-28 | 1988-07-12 | Genetics Institute, Inc. | Human factor VIII:C gene and recombinant methods for production |
| US4970300A (en) | 1985-02-01 | 1990-11-13 | New York University | Modified factor VIII |
| US5250421A (en) | 1986-01-03 | 1993-10-05 | Genetics Institute, Inc. | Method for producing factor VIII:C-type proteins |
| US5198349A (en) | 1986-01-03 | 1993-03-30 | Genetics Institute, Inc. | Method for producing factor VIII:C and analogs |
| JPH0387173A (ja) | 1987-09-10 | 1991-04-11 | Teijin Ltd | ヒト活性化天然型ファクター8cの製造方法及びそれに用いる形質転換体 |
| US5153265A (en) | 1988-01-20 | 1992-10-06 | Cetus Corporation | Conjugation of polymer to colony stimulating factor-1 |
| US4966999A (en) | 1988-06-07 | 1990-10-30 | Cytogen Corporation | Radiohalogenated compounds for site specific labeling |
| US5122614A (en) | 1989-04-19 | 1992-06-16 | Enzon, Inc. | Active carbonates of polyalkylene oxides for modification of polypeptides |
| SE465222C5 (sv) | 1989-12-15 | 1998-02-10 | Pharmacia & Upjohn Ab | Ett rekombinant, humant faktor VIII-derivat och förfarande för dess framställning |
| SE466754B (sv) | 1990-09-13 | 1992-03-30 | Berol Nobel Ab | Saett att kovalent binda biopolymerer till hydrofila ytor |
| US5492821A (en) | 1990-11-14 | 1996-02-20 | Cargill, Inc. | Stabilized polyacrylic saccharide protein conjugates |
| WO1992016555A1 (en) | 1991-03-18 | 1992-10-01 | Enzon, Inc. | Hydrazine containing conjugates of polypeptides and glycopolypeptides with polymers |
| US5846951A (en) | 1991-06-06 | 1998-12-08 | The School Of Pharmacy, University Of London | Pharmaceutical compositions |
| US6037452A (en) | 1992-04-10 | 2000-03-14 | Alpha Therapeutic Corporation | Poly(alkylene oxide)-Factor VIII or Factor IX conjugate |
| WO1994005332A2 (en) | 1992-09-01 | 1994-03-17 | Berlex Laboratories, Inc. | Glycolation of glycosylated macromolecules |
| DE69329795T2 (de) | 1992-10-02 | 2001-07-05 | Genetics Institute, Inc. | Zusammensetzung, welche den koagulationsfaktor viii beinhaltet; verfahren zu deren herstellung und die benutzung eines oberflächenaktiven stoffes als stabilisator |
| NZ250375A (en) | 1992-12-09 | 1995-07-26 | Ortho Pharma Corp | Peg hydrazone and peg oxime linkage forming reagents and protein derivatives |
| US5298643A (en) | 1992-12-22 | 1994-03-29 | Enzon, Inc. | Aryl imidate activated polyalkylene oxides |
| AU6029594A (en) | 1993-01-15 | 1994-08-15 | Enzon, Inc. | Factor viii - polymeric conjugates |
| US5621039A (en) | 1993-06-08 | 1997-04-15 | Hallahan; Terrence W. | Factor IX- polymeric conjugates |
| SE504074C2 (sv) | 1993-07-05 | 1996-11-04 | Pharmacia Ab | Proteinberedning för subkutan, intramuskulär eller intradermal administrering |
| US6011007A (en) | 1993-09-17 | 2000-01-04 | Novo Nordisk A/S | Acylated insulin |
| US6869930B1 (en) | 1993-09-17 | 2005-03-22 | Novo Nordisk A/S | Acylated insulin |
| CZ287945B6 (cs) | 1993-09-17 | 2001-03-14 | Novo Nordisk A/S | Inzulinový derivát a farmaceutický prostředek s jeho obsahem pro léčení diabetu |
| WO1996041813A2 (en) | 1994-11-09 | 1996-12-27 | Offord Robin E | Functionalized polymers for site-specific attachment |
| AU6255096A (en) | 1995-06-07 | 1996-12-30 | Mount Sinai School Of Medicine Of The City University Of New York, The | Pegylated modified proteins |
| WO1996040662A2 (en) | 1995-06-07 | 1996-12-19 | Cellpro, Incorporated | Aminooxy-containing linker compounds and their application in conjugates |
| SE9503380D0 (sv) | 1995-09-29 | 1995-09-29 | Pharmacia Ab | Protein derivatives |
| US5866538A (en) | 1996-06-20 | 1999-02-02 | Novo Nordisk A/S | Insulin preparations containing NaCl |
| EP0981548A4 (en) | 1997-04-30 | 2005-11-23 | Enzon Inc | GLYCOSYLATABLE SINGLE CHAIN ANTIGEN-BINDING PROTEINS, MANUFACTURE AND USE THEREOF |
| US6183738B1 (en) | 1997-05-12 | 2001-02-06 | Phoenix Pharamacologics, Inc. | Modified arginine deiminase |
| EP1717248A1 (en) | 1997-06-04 | 2006-11-02 | Oxford Biomedica (UK) Limited | Tumor targeted vector |
| WO1999003496A1 (en) | 1997-07-21 | 1999-01-28 | The University Of North Carolina At Chapel Hill | Factor ix antihemophilic factor with increased clotting activity |
| WO2001082943A2 (en) | 2000-05-03 | 2001-11-08 | Novo Nordisk A/S | Subcutaneous administration of coagulation factor vii |
| ES2252876T5 (es) | 1997-12-03 | 2014-04-03 | Roche Diagnostics Gmbh | Proceso para preparar polipéptidos con glicolización adecuada |
| US5985263A (en) | 1997-12-19 | 1999-11-16 | Enzon, Inc. | Substantially pure histidine-linked protein polymer conjugates |
| US6596398B1 (en) | 1998-08-21 | 2003-07-22 | Atofina Chemicals, Inc. | Solar control coated glass |
| US6552167B1 (en) | 1998-08-28 | 2003-04-22 | Gryphon Therapeutics, Inc. | Polyamide chains of precise length |
| DK1656952T3 (da) | 1998-10-16 | 2014-01-20 | Biogen Idec Inc | Polyalkylenglycolkonjugater af interferon beta-1A og anvendelser deraf |
| DE19852729A1 (de) | 1998-11-16 | 2000-05-18 | Werner Reutter | Rekombinante Glycoproteine, Verfahren zu ihrer Herstellung, sie enthaltende Arzneimittel und ihre Verwendung |
| EP2921180B1 (en) | 1999-02-22 | 2019-08-14 | University of Connecticut | Albumin-free factor VIII formulations |
| KR20020022691A (ko) * | 1999-06-08 | 2002-03-27 | 와이즈먼 앤드루 | 아미노옥시기를 포함하는 원자가 플랫폼 분자 |
| US6531122B1 (en) | 1999-08-27 | 2003-03-11 | Maxygen Aps | Interferon-β variants and conjugates |
| CN1309423C (zh) | 1999-11-12 | 2007-04-11 | 马克西根控股公司 | 干扰素γ偶联物 |
| US7074878B1 (en) | 1999-12-10 | 2006-07-11 | Harris J Milton | Hydrolytically degradable polymers and hydrogels made therefrom |
| US6413507B1 (en) | 1999-12-23 | 2002-07-02 | Shearwater Corporation | Hydrolytically degradable carbamate derivatives of poly (ethylene glycol) |
| DE60138364D1 (de) | 2000-02-11 | 2009-05-28 | Bayer Healthcare Llc | Gerinnungsfaktor vii oder viia konjugate |
| DE60143292D1 (de) | 2000-05-03 | 2010-12-02 | Novo Nordisk Healthcare Ag | Varianten des menschlichen Koagulationsfaktors VII |
| CN1434726A (zh) | 2000-06-08 | 2003-08-06 | 拉卓拉药物公司 | 包含高分子量聚环氧乙烷的多价平台分子 |
| US6423826B1 (en) | 2000-06-30 | 2002-07-23 | Regents Of The University Of Minnesota | High molecular weight derivatives of vitamin K-dependent polypeptides |
| US7118737B2 (en) | 2000-09-08 | 2006-10-10 | Amylin Pharmaceuticals, Inc. | Polymer-modified synthetic proteins |
| AU8755001A (en) | 2000-09-13 | 2002-03-26 | Novo Nordisk As | Human coagulation factor vii variants |
| EP1325127B1 (en) | 2000-10-02 | 2009-03-11 | Novo Nordisk Health Care AG | Method for the production of vitamin k-dependent proteins |
| GB0103877D0 (en) * | 2001-02-16 | 2001-04-04 | King S College London | Novel Drug Delivery system |
| MXPA03008590A (es) | 2001-03-22 | 2003-12-08 | Novo Nordisk Healthcare Ag | Derivados del factor vii de coagulacion. |
| US6913915B2 (en) | 2001-08-02 | 2005-07-05 | Phoenix Pharmacologics, Inc. | PEG-modified uricase |
| US6770625B2 (en) * | 2001-09-07 | 2004-08-03 | Nobex Corporation | Pharmaceutical compositions of calcitonin drug-oligomer conjugates and methods of treating diseases therewith |
| US7214660B2 (en) | 2001-10-10 | 2007-05-08 | Neose Technologies, Inc. | Erythropoietin: remodeling and glycoconjugation of erythropoietin |
| EP2042196B1 (en) | 2001-10-10 | 2016-07-13 | ratiopharm GmbH | Remodelling and glycoconjugation of Granulocyte Colony Stimulating Factor (G-CSF) |
| US7795210B2 (en) | 2001-10-10 | 2010-09-14 | Novo Nordisk A/S | Protein remodeling methods and proteins/peptides produced by the methods |
| US7265084B2 (en) | 2001-10-10 | 2007-09-04 | Neose Technologies, Inc. | Glycopegylation methods and proteins/peptides produced by the methods |
| AU2002352524B2 (en) | 2001-11-07 | 2007-10-04 | Nektar Therapeutics | Branched polymers and their conjugates |
| JP2005510229A (ja) | 2001-11-28 | 2005-04-21 | ネオーズ テクノロジーズ, インコーポレイテッド | アミダーゼを用いる糖タンパク質のリモデリング |
| JP2005535280A (ja) | 2001-11-28 | 2005-11-24 | ネオーズ テクノロジーズ, インコーポレイテッド | エンドグリカナーゼを用いる糖タンパク質のリモデリング |
| RU2362807C2 (ru) | 2002-06-21 | 2009-07-27 | Ново Нордиск Хелт Кэр Аг | Конъюгат полипептида фактора vii, способ его получения, его применение и содержащая его фармацевтическая композиция |
| US7087229B2 (en) | 2003-05-30 | 2006-08-08 | Enzon Pharmaceuticals, Inc. | Releasable polymeric conjugates based on aliphatic biodegradable linkers |
| US7122189B2 (en) | 2002-08-13 | 2006-10-17 | Enzon, Inc. | Releasable polymeric conjugates based on aliphatic biodegradable linkers |
| EP1400533A1 (en) | 2002-09-11 | 2004-03-24 | Fresenius Kabi Deutschland GmbH | HASylated polypeptides, especially HASylated erythropoietin |
| EP1681303B1 (en) | 2002-09-11 | 2013-09-04 | Fresenius Kabi Deutschland GmbH | HASylated polypeptides, especially HASylated erythropoietin |
| BR0314106A (pt) | 2002-09-11 | 2005-07-19 | Fresenius Kabi De Gmbh | Polipeptìdeos hasilados, especialmente eritropoietina hasilada |
| US20040062748A1 (en) | 2002-09-30 | 2004-04-01 | Mountain View Pharmaceuticals, Inc. | Polymer conjugates with decreased antigenicity, methods of preparation and uses thereof |
| WO2004060965A2 (en) | 2002-12-31 | 2004-07-22 | Nektar Therapeutics Al, Corporation | Hydrolytically stable maleimide-terminated polymers |
| EP1578841B2 (en) | 2002-12-31 | 2016-10-12 | Nektar Therapeutics AL, Corporation | Maleamic acid polymer derivatives and their bioconjugates |
| WO2004075923A2 (en) | 2003-02-26 | 2004-09-10 | Nektar Therapeutics Al, Corporation | Polymer-factor viii moiety conjugates |
| US7623892B2 (en) | 2003-04-02 | 2009-11-24 | Palm, Inc. | System and method for enabling a person to switch use of computing devices |
| CA2521784C (en) | 2003-04-08 | 2012-03-27 | Yeda Research And Development Co. Ltd. | Reversible pegylated drugs |
| EP2055189A1 (en) | 2003-04-09 | 2009-05-06 | Neose Technologies, Inc. | Glycopegylation methods and proteins/peptides produced by the methods |
| EP1653991A2 (en) | 2003-08-08 | 2006-05-10 | Fresenius Kabi Deutschland GmbH | Conjugates of a polymer and a protein linked by an oxime linking group |
| WO2005014655A2 (en) | 2003-08-08 | 2005-02-17 | Fresenius Kabi Deutschland Gmbh | Conjugates of hydroxyalkyl starch and a protein |
| CN1863549A (zh) * | 2003-08-08 | 2006-11-15 | 费森尤斯卡比德国有限公司 | 通过肟连接基团进行连接的聚合物和蛋白质的缀合物 |
| EP1654004A2 (en) | 2003-08-08 | 2006-05-10 | Novo Nordisk A/S | Synthesis and application of new structural well defined branched polymers as conjugating agents for peptides |
| WO2005016974A1 (en) | 2003-08-12 | 2005-02-24 | Lipoxen Technologies Limited | Sialic acid derivatives for protein derivatisation and conjugation |
| US8633157B2 (en) | 2003-11-24 | 2014-01-21 | Novo Nordisk A/S | Glycopegylated erythropoietin |
| AU2004296860B2 (en) | 2003-12-03 | 2010-04-22 | Novo Nordisk A/S | Glycopegylated factor IX |
| US20060040856A1 (en) | 2003-12-03 | 2006-02-23 | Neose Technologies, Inc. | Glycopegylated factor IX |
| KR101237884B1 (ko) | 2003-12-03 | 2013-02-27 | 바이오제너릭스 에이지 | 글리코 peg화 과립구 콜로니 자극인자 |
| US7338933B2 (en) | 2004-01-08 | 2008-03-04 | Neose Technologies, Inc. | O-linked glycosylation of peptides |
| WO2005092369A2 (en) | 2004-03-11 | 2005-10-06 | Fresenius Kabi Deutschland Gmbh | Conjugates of hydroxyethyl starch and erythropoietin |
| GB0412181D0 (en) * | 2004-06-01 | 2004-06-30 | Celltech R&D Ltd | Biological products |
| WO2006020372A2 (en) | 2004-07-23 | 2006-02-23 | Neose Technologies, Inc. | Enzymatic modification of glycopeptides |
| JP2008507990A (ja) | 2004-08-02 | 2008-03-21 | ノボ ノルディスク ヘルス ケア アクチェンゲゼルシャフト | Fviiの抱合体 |
| WO2006016168A2 (en) | 2004-08-12 | 2006-02-16 | Lipoxen Technologies Limited | Sialic acid derivatives |
| WO2006031811A2 (en) | 2004-09-10 | 2006-03-23 | Neose Technologies, Inc. | Glycopegylated interferon alpha |
| KR101468345B1 (ko) | 2004-11-12 | 2014-12-03 | 바이엘 헬스케어 엘엘씨 | Fviii의 부위 지향 변형 |
| EP1828224B1 (en) | 2004-12-22 | 2016-04-06 | Ambrx, Inc. | Compositions containing, methods involving, and uses of non-natural amino acids and polypeptides |
| CA2591852A1 (en) | 2004-12-27 | 2006-07-06 | Baxter International Inc. | Polymer-von willebrand factor-conjugates |
| JP2008526864A (ja) | 2005-01-06 | 2008-07-24 | ネオス テクノロジーズ インコーポレイテッド | 糖断片を用いる糖結合 |
| BRPI0607605A2 (pt) * | 2005-02-08 | 2009-09-15 | Queensland Inst Med Res | moléculas imunogênicas |
| EP1891231A4 (en) | 2005-05-25 | 2011-06-22 | Novo Nordisk As | GLYCOPEGYLATED FACTOR IX |
| BRPI0611872B8 (pt) | 2005-06-16 | 2021-05-25 | Nektar Therapeutics | reagente polimérico, conjugado, método para preparação de um conjugado e composição farmacêutica |
| EP1893632B1 (en) | 2005-06-17 | 2015-08-12 | Novo Nordisk Health Care AG | Selective reduction and derivatization of engineered factor vii proteins comprising at least one non-native cysteine |
| WO2007022784A2 (en) | 2005-08-26 | 2007-03-01 | Maxygen Holdings Ltd. | Liquid factor vii composition |
| CN101268098A (zh) * | 2005-08-30 | 2008-09-17 | 诺沃-诺迪斯克保健股份有限公司 | 聚乙二醇化生长激素的液体制剂 |
| BRPI0620316A2 (pt) | 2005-12-21 | 2011-11-08 | Wyeth Corp | formulações de proteìnas com viscosidades reduzida e seus usos |
| AU2007215566A1 (en) * | 2006-01-19 | 2007-08-23 | Ambrx, Inc. | Non-natural amino acid polypeptides having modulated immunogenicity |
| US7645860B2 (en) | 2006-03-31 | 2010-01-12 | Baxter Healthcare S.A. | Factor VIII polymer conjugates |
| CA2647314A1 (en) | 2006-03-31 | 2007-11-08 | Baxter International Inc. | Pegylated factor viii |
| EP2089052A4 (en) | 2006-05-24 | 2011-02-16 | Peg Biosciences | POLYETHYLENE GLYCOL-BASED LINK COMPOUNDS AND BIOLOGICALLY ACTIVE CONJUGATES BASED ON SAID COMPOUNDS |
| US7939632B2 (en) | 2006-06-14 | 2011-05-10 | Csl Behring Gmbh | Proteolytically cleavable fusion proteins with high molar specific activity |
| WO2008035373A2 (en) | 2006-07-13 | 2008-03-27 | Serum Institute Of India Ltd | Highly pure polysialic acid and process for preperation thereof |
| WO2008025856A2 (en) | 2006-09-01 | 2008-03-06 | Novo Nordisk Health Care Ag | Modified glycoproteins |
| US8969532B2 (en) | 2006-10-03 | 2015-03-03 | Novo Nordisk A/S | Methods for the purification of polypeptide conjugates comprising polyalkylene oxide using hydrophobic interaction chromatography |
| EP2094309A2 (en) * | 2006-11-17 | 2009-09-02 | Nya Hamlet Pharma AB | Alpha-lactalbumin composition |
| CA2670618C (en) | 2006-12-15 | 2016-10-04 | Baxter International Inc. | Factor viia- (poly) sialic acid conjugate having prolonged in vivo half-life |
| WO2008083346A1 (en) | 2006-12-28 | 2008-07-10 | Ambrx, Inc. | Phenazine and quinoxaline substituted amino acids and polypeptides |
| EP2099475B1 (en) | 2007-01-03 | 2016-08-24 | Novo Nordisk Health Care AG | Subcutaneous administration of coagulation factor viia-related polypeptides |
| WO2008119815A1 (en) | 2007-04-02 | 2008-10-09 | Novo Nordisk A/S | Subcutaneous administration of coagulation factor ix |
| JP5622569B2 (ja) | 2007-06-26 | 2014-11-12 | バクスター・インターナショナル・インコーポレイテッドBaxter International Incorp0Rated | 加水分解性ポリマーfmoc−リンカー |
| EP2173759A4 (en) | 2007-07-03 | 2014-01-29 | Childrens Hosp & Res Ct Oak | OLIGOSIAL INSERTS, PROCESS FOR THEIR PREPARATION AND ITS IMMUNOLOGICAL USE |
| KR20100090684A (ko) | 2007-10-09 | 2010-08-16 | 폴리테릭스 리미티드 | 신규한 접합 단백질 및 펩티드 |
| EP2070951A1 (en) | 2007-12-14 | 2009-06-17 | Fresenius Kabi Deutschland GmbH | Method for producing a hydroxyalkyl starch derivatives with two linkers |
| CA2711503A1 (en) | 2008-01-08 | 2009-07-16 | Biogenerix Ag | Glycoconjugation of polypeptides using oligosaccharyltransferases |
| KR101582841B1 (ko) | 2008-02-27 | 2016-01-11 | 노보 노르디스크 에이/에스 | 콘쥬게이트된 인자 viii 분자 |
| WO2009130602A2 (en) | 2008-04-24 | 2009-10-29 | Celtic Pharma Peg Ltd. | Factor ix conjugates with extended half-lives |
| WO2009141433A1 (en) | 2008-05-23 | 2009-11-26 | Novo Nordisk Health Care Ag | Low viscosity compositions comprising a pegylated gla-domain containing protein |
| CN102065899A (zh) | 2008-05-23 | 2011-05-18 | 诺沃-诺迪斯克保健股份有限公司 | 含有高浓度的芳香族防腐剂的peg-官能化的丝氨酸蛋白酶的制剂 |
| CA2726942A1 (en) | 2008-06-04 | 2009-12-10 | Bayer Healthcare Llc | Fviii muteins for treatment of von willebrand disease |
| EP2374481B1 (en) | 2008-07-21 | 2015-11-04 | Polytherics Limited | Novel reagents and method for conjugating biological molecules |
| CA2740793A1 (en) | 2008-11-03 | 2010-06-03 | Haiyan Jiang | Method for the treatment of hemophilia |
| WO2010083536A1 (en) | 2009-01-19 | 2010-07-22 | Bayer Healthcare Llc | Protein conjugate having an endopeptidase-cleavable bioprotective moiety |
| EP2398822B1 (en) | 2009-02-19 | 2013-01-02 | Novo Nordisk A/S | Modification of factor viii |
| US9005598B2 (en) | 2009-03-04 | 2015-04-14 | Polytherics Limited | Conjugated proteins and peptides |
| US20100330033A1 (en) | 2009-04-16 | 2010-12-30 | Nian Wu | Protein-carrier conjugates |
| EP2437786B1 (en) | 2009-06-01 | 2016-05-18 | Yeda Research and Development Co. Ltd. | Prodrugs containing albumin binding probe |
| EP2461821A4 (en) | 2009-07-31 | 2013-07-03 | Bayer Healthcare Llc | MODIFIED POLYPEPTIDES OF FACTOR IX AND USES THEREOF |
| DE102009028526A1 (de) | 2009-08-13 | 2011-02-24 | Leibniz-Institut Für Polymerforschung Dresden E.V. | Verfahren zur Modifikation und Funktionalisierung von Sacchariden |
| EP2480578A4 (en) | 2009-09-25 | 2013-04-17 | Vybion Inc | MODIFICATION OF POLYPEPTIDE |
| WO2011064247A1 (en) | 2009-11-24 | 2011-06-03 | Novo Nordisk Health Care Ag | Method of purifying pegylated proteins |
| US20130040888A1 (en) | 2010-02-16 | 2013-02-14 | Novo Nordisk A/S | Factor VIII Molecules With Reduced VWF Binding |
| JP5826772B2 (ja) * | 2010-02-16 | 2015-12-02 | ノヴォ ノルディスク アー/エス | コンジュゲートタンパク質 |
| GB201007357D0 (en) | 2010-04-30 | 2010-06-16 | Leverton Licence Holdings Ltd | Conjugated factor VIII |
| GB201007356D0 (en) | 2010-04-30 | 2010-06-16 | Leverton Licence Holdings Ltd | Conjugated factor VIIa |
| DK2598172T3 (da) | 2010-07-30 | 2019-07-01 | Baxalta GmbH | Nukleofile katalysatorer til oximforbindelse |
| WO2012068134A1 (en) | 2010-11-15 | 2012-05-24 | Biogen Idec Inc. | Enrichment and concentration of select product isoforms by overloaded bind and elute chromatography |
| CN103796670A (zh) | 2011-07-08 | 2014-05-14 | 比奥根艾迪克依蒙菲利亚公司 | 因子viii嵌合和杂合多肽及其使用方法 |
-
2011
- 2011-12-16 HU HUE11806103A patent/HUE049352T2/hu unknown
- 2011-12-16 DK DK11806103.5T patent/DK2654794T3/da active
- 2011-12-16 JP JP2013546263A patent/JP6138052B2/ja active Active
- 2011-12-16 AU AU2011349574A patent/AU2011349574B9/en active Active
- 2011-12-16 PT PT118061035T patent/PT2654794T/pt unknown
- 2011-12-16 WO PCT/US2011/065591 patent/WO2012087838A1/en not_active Ceased
- 2011-12-16 SG SG2013048194A patent/SG191298A1/en unknown
- 2011-12-16 KR KR1020137019066A patent/KR102025442B1/ko active Active
- 2011-12-16 NZ NZ612320A patent/NZ612320A/en unknown
- 2011-12-16 MX MX2013007369A patent/MX345608B/es active IP Right Grant
- 2011-12-16 EP EP11806103.5A patent/EP2654794B8/en active Active
- 2011-12-16 CN CN201180062472.4A patent/CN103269723B/zh active Active
- 2011-12-16 EA EA201390940A patent/EA032056B1/ru unknown
- 2011-12-16 US US13/329,002 patent/US8945897B2/en active Active
- 2011-12-16 EP EP19211476.7A patent/EP3673921A1/en not_active Withdrawn
- 2011-12-16 BR BR112013015898-0A patent/BR112013015898A2/pt not_active Application Discontinuation
- 2011-12-16 CA CA2822591A patent/CA2822591C/en active Active
- 2011-12-16 ES ES11806103T patent/ES2800983T3/es active Active
- 2011-12-16 PL PL11806103T patent/PL2654794T3/pl unknown
- 2011-12-21 TW TW100147675A patent/TWI546279B/zh active
- 2011-12-22 AR ARP110104911A patent/AR084576A1/es active IP Right Grant
-
2017
- 2017-06-14 AU AU2017204019A patent/AU2017204019A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| CA2822591C (en) | 2020-12-29 |
| EP2654794B8 (en) | 2020-04-22 |
| NZ612320A (en) | 2015-06-26 |
| EA201390940A1 (ru) | 2014-04-30 |
| CN103269723A (zh) | 2013-08-28 |
| CN103269723B (zh) | 2017-04-05 |
| EP2654794A1 (en) | 2013-10-30 |
| HUE049352T2 (hu) | 2020-09-28 |
| EP2654794B1 (en) | 2020-03-04 |
| EA032056B1 (ru) | 2019-04-30 |
| EP3673921A1 (en) | 2020-07-01 |
| KR102025442B1 (ko) | 2019-09-25 |
| US20120190096A1 (en) | 2012-07-26 |
| SG191298A1 (en) | 2013-07-31 |
| MX2013007369A (es) | 2013-09-26 |
| DK2654794T3 (da) | 2020-06-08 |
| MX345608B (es) | 2017-02-07 |
| AU2011349574B9 (en) | 2017-06-15 |
| PL2654794T3 (pl) | 2020-07-27 |
| PT2654794T (pt) | 2020-06-11 |
| AU2017204019A1 (en) | 2017-07-06 |
| JP2014501262A (ja) | 2014-01-20 |
| TW201305090A (zh) | 2013-02-01 |
| AR084576A1 (es) | 2013-05-29 |
| AU2011349574A1 (en) | 2013-07-11 |
| KR20130129254A (ko) | 2013-11-27 |
| TWI546279B (zh) | 2016-08-21 |
| AU2011349574B2 (en) | 2017-06-01 |
| BR112013015898A2 (pt) | 2018-06-26 |
| JP6138052B2 (ja) | 2017-05-31 |
| CA2822591A1 (en) | 2012-06-28 |
| US8945897B2 (en) | 2015-02-03 |
| WO2012087838A1 (en) | 2012-06-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2800983T3 (es) | Materiales y métodos para conjugar un derivado de ácido graso soluble en agua con una proteína | |
| JP7054407B2 (ja) | オキシム連結のための求核触媒 | |
| ES2597954T3 (es) | Conjugados de proteína de la coagulación sanguínea | |
| JP6560712B2 (ja) | オキシム連結のための求核触媒 |