ES2804545T3 - Nuevos moduladores de la actividad del receptor de 5-hidroxitriptamina 7 y su método de uso - Google Patents
Nuevos moduladores de la actividad del receptor de 5-hidroxitriptamina 7 y su método de uso Download PDFInfo
- Publication number
- ES2804545T3 ES2804545T3 ES14779591T ES14779591T ES2804545T3 ES 2804545 T3 ES2804545 T3 ES 2804545T3 ES 14779591 T ES14779591 T ES 14779591T ES 14779591 T ES14779591 T ES 14779591T ES 2804545 T3 ES2804545 T3 ES 2804545T3
- Authority
- ES
- Spain
- Prior art keywords
- ethyl
- piperazin
- diethyl
- dihydrofuran
- oxaspiro
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- NYBZSVLCAXABQM-UHFFFAOYSA-N CC(C)(C)c(cccc1)c1N1CCNCC1 Chemical compound CC(C)(C)c(cccc1)c1N1CCNCC1 NYBZSVLCAXABQM-UHFFFAOYSA-N 0.000 description 1
- 0 CCC(C(C)C(C)C**)[N+]([O-])=O Chemical compound CCC(C(C)C(C)C**)[N+]([O-])=O 0.000 description 1
- SWYCASSFUIEROZ-UHFFFAOYSA-N O=C1OC(CCN(CC2)CCN2c(cccc2)c2I)CC11CCCC1 Chemical compound O=C1OC(CCN(CC2)CCN2c(cccc2)c2I)CC11CCCC1 SWYCASSFUIEROZ-UHFFFAOYSA-N 0.000 description 1
- LWOHIFJITKACGQ-UHFFFAOYSA-N O=C1OC(CCN(CC2)CCN2c2ccccc2-c2ccccc2)CC11CCCC1 Chemical compound O=C1OC(CCN(CC2)CCN2c2ccccc2-c2ccccc2)CC11CCCC1 LWOHIFJITKACGQ-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/02—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings
- C07D307/26—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member
- C07D307/30—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D307/32—Oxygen atoms
- C07D307/33—Oxygen atoms in position 2, the oxygen atom being in its keto or unsubstituted enol form
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/94—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom spiro-condensed with carbocyclic rings or ring systems, e.g. griseofulvins
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/06—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Biomedical Technology (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Psychiatry (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Hospice & Palliative Care (AREA)
- Cardiology (AREA)
- Diabetes (AREA)
- Heart & Thoracic Surgery (AREA)
- Pain & Pain Management (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
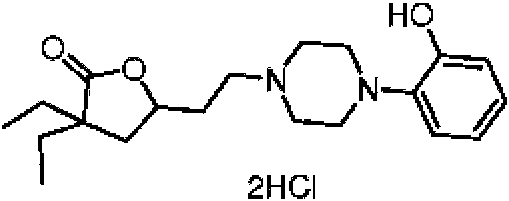
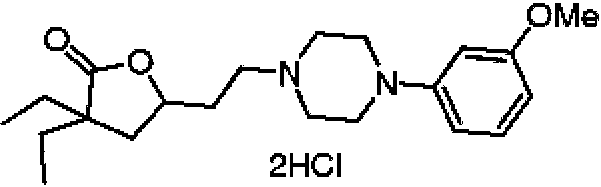
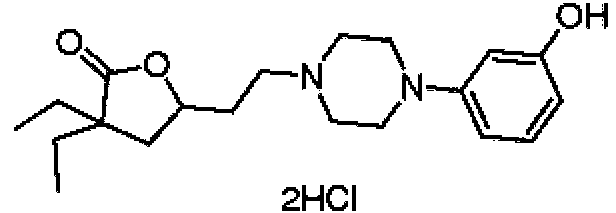
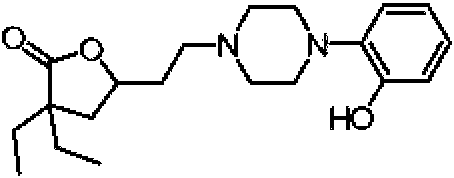
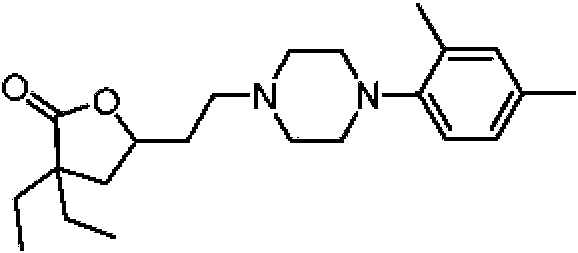
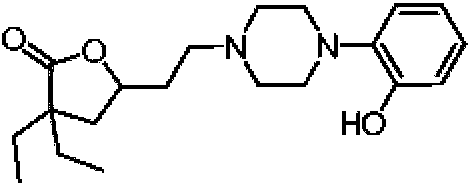
Compuesto seleccionado del grupo que consiste en: 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo; 3,3-dietil-5-(2-(4-(4-metoxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; 3,3-dietil-5-(2-(4-(4-hidroxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; 3,3-dietil-5-(2-(4-(4-nitrofenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; 3,3-dietil-5-(2-(4-(2-metoxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; 4-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo; 3,3-dietil-5-(2-(4-(2-hidroxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; 5-(2-(4-(4-aminofenil)piperazin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona; 3,3-dietil-5-(2-(4-(p-tolil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; 3,3-dietil-5-(2-(4-(3-metoxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; 3,3-dietil-5-(2-(4-(3-hidroxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; 5-(2-(4-(2,6-dimetilfenil)piperazin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona; 3,3-dietil-5-(2-(4-(o-tolil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; 3,3-dietil-5-(2-(4-(2-isopropilfenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; 5-(2-(4-(2,4-dimetilfenil)piperazin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona; 3-(2-(4-(2-isopropilfenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona; 3-(2-(4-(2-(tert-butil)fenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona; 3-(2-(4-(2,6-diisopropilfenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona; 3-(2-(4-(2-morfolinofenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona; 3-(2-(4-([1,1'-bifenil]-2-il)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona; 3-(2-(4-(2-(1H-pirrol-1-il)fenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona; 3-(2-(4-(2-yodofenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona; N-(2-(4-(2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil)piperazin-1-il)fenil)acetamida; 5-nitro-2-(4-(2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil)piperazin-1-il)benzonitrilo; y 3-(2-(4-(p-tolil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona; o una sal derivada farmacéuticamente aceptable.
Description
DESCRIPCIÓN
Nuevos moduladores de la actividad del receptor de 5-hidroxitriptamina 7 y su método de uso
[0001] Las formas de realización de la invención están dirigidas a nuevos compuestos útiles como moduladores de la actividad del receptor de 5-hidroxitriptamina 7 (5-HT7) y su uso.
[0002] La serotonina fue descubierta a finales de la década de los 40 y está presente en el sistema nervioso tanto periférico como central [Physiol. Res, 60 (2011) 15-25; Psychopharmacology 213 (2011) 167-169]. La serotonina o 5-hidroxitriptamina (5-HT) es un neurotransmisor monoamínico del grupo de las indolalquilaminas que actúa en las sinapsis de las células nerviosas. Se han identificado siete familias distintas de receptores de serotonina y se han clonado al menos 20 subpoblaciones basándose en la similitud de secuencia, el acoplamiento de la transducción de señales y las características farmacológicas. Las siete familias del receptor de 5-HT se denominan 5-HT1, 5-HT2, 5-HT3, 5-HT4, 5-HT5, 5-HT6 y 5 -HT7 y cada uno de estos receptores tiene a su vez subfamilias o subpoblaciones. Se ha estudiado el mecanismo de transducción de señales para las siete familias y se sabe que la activación de los receptores 5 -HT1 y 5 -HT5 causa una reducción en la cAMP intracelular, mientras que la activación de 5 -HT2, 5-HT3, 5-HT4, 5-HT6 y 5 -HT7 resulta en un aumento en el IP3 y el DAG intracelulares. Las vías de 5-HT en el cerebro están implicadas en trastornos del SNC. El neurotransmisor se une a su receptor acoplado a una proteína G y está implicado en una amplia variedad de acciones, incluidas la cognición, el humor, la ansiedad, la atención, el apetito, la función cardiovascular, la vasoconstricción y el sueño entre otros [ACS Medicinal Chemistry Letters 2 (2011) 929-932; Physiol. Res, 60 (2011) 15-25].
[0003] La presente invención se dirige también a composiciones que comprenden:
una cantidad eficaz de uno o más compuestos según la presente invención y un excipiente.
[0004] La presente invención también se refiere a aquellos nuevos compuestos y composiciones para usar en métodos para tratar o prevenir enfermedades que implican la desregulación de la actividad del receptor de 5-hidroxitriptamina 7, incluidos, trastorno del ritmo circadiano, depresión, esquizofrenia, inflamación neurogénica, hipertensión, enfermedades vasculares periféricas, migraña, dolor neuropático, dolor periférico, alodinia, trastorno de la termorregulación, trastorno del aprendizaje, trastorno de la memoria, trastorno de la señalización en el hipocampo, trastorno del sueño, trastorno de déficit de atención/hiperactividad, ansiedad, trastorno de personalidad elusiva, eyaculación prematura, trastorno alimentario, síndrome premenstrual, trastorno disfónico premenstrual, trastorno afectivo estacional y trastorno bipolar.
[0005] Estos y otros objetos, características y ventajas se harán evidentes para las personas expertas en la técnica a partir de una lectura de la siguiente descripción detallada y las reivindicaciones anexas. Todos los porcentajes, razones y proporciones están en la presente en peso, a menos que se especifique lo contrario. Todas las temperaturas están en grados Celsius (° C) a menos que se especifique lo contrario.
[0006] Existen pruebas que sugieren un papel para el receptor 5-HT7 en una serie de trastornos médicos. Es posible que los moduladores de la actividad del receptor 5-HT7 tengan un efecto beneficioso en pacientes que sufren estos trastornos. Los trastornos donde la desregulación del 5-HT7 juega un papel y para los que la modulación de la actividad del receptor 5-HT7 por un agente terapéutico puede ser un enfoque viable para el alivio terapéutico incluyen, pero de forma no limitativa, trastorno del ritmo circadiano, depresión, esquizofrenia, inflamación neurogénica, hipertensión, enfermedades vasculares periféricas, migraña (Vanhoenacker, P. et al. Trends in Pharmacological Sciences, 2000, 21,2, 70-77), dolor neuropático, dolor periférico, alodinia (EP1875899), trastorno de la termorregulación, trastorno del aprendizaje, trastorno de la memoria, trastorno de la señalización en el hipocampo, trastorno del sueño (WO20100197700) trastorno de déficit de atención/hiperactividad (TDAH) (WO20100069390), ansiedad, trastorno de personalidad elusiva, eyaculación prematura, trastorno alimentario, síndrome premenstrual, trastorno disfónico premenstrual, trastorno afectivo estacional y trastorno bipolar (WO20040229874).
[0007] Hay una necesidad largamente anhelada de nuevos moduladores del 5-HT7 que proporcionen alivio terapéutico de pacientes que sufren enfermedades asociadas a la desregulación de la actividad del receptor de 5-hidroxitriptamina 7. La invención aborda la necesidad de identificar nuevos moduladores del 5-HT7 capaces de tratar enfermedades asociadas a la desregulación de la actividad del receptor de 5-hidroxitriptamina 7. La presente invención aborda la necesidad de desarrollar nuevos agentes terapéuticos para el tratamiento y la prevención de trastorno del ritmo circadiano, depresión, esquizofrenia, inflamación neurogénica, hipertensión, enfermedades vasculares periféricas, migraña, dolor neuropático, dolor periférico, alodinia, trastorno de la termorregulación, trastorno del aprendizaje, trastorno de la memoria, trastorno de la señalización en el hipocampo, trastorno del sueño, trastorno de déficit de atención/hiperactividad, ansiedad, trastorno de personalidad elusiva, eyaculación prematura, trastorno alimentario, síndrome premenstrual, trastorno disfónico premenstrual, trastorno afectivo estacional y trastorno bipolar.
[0008] Los moduladores de la actividad del receptor de 5-hidroxitriptamina 7 de la presente invención son capaces de tratar y prevenir enfermedades asociadas a la desregulación de la actividad del receptor de 5-hidroxitriptamina 7, por ejemplo, trastorno del ritmo circadiano, depresión, esquizofrenia, inflamación neurogénica, hipertensión, enfermedades vasculares periféricas, migraña, dolor neuropático, dolor periférico, alodinia, trastorno de la termorregulación, trastorno del aprendizaje, trastorno de la memoria, trastorno de la señalización en el hipocampo, trastorno del sueño, trastorno de déficit de atención/hiperactividad, ansiedad, trastorno de personalidad elusiva, eyaculación prematura, trastorno alimentario, síndrome premenstrual, trastorno disfónico premenstrual, trastorno afectivo estacional y trastorno bipolar. Se ha descubierto que el receptor de 5-hidroxitriptamina 7 juega un papel en una serie de trastornos médicos y, por lo tanto, es posible que los moduladores de la actividad del receptor 5-HT7 tengan un efecto beneficioso en pacientes que sufren estos trastornos. Los trastornos donde la desregulación del 5-HT7 juega un papel y la modulación de la actividad del receptor 5-HT7 por un agente terapéutico puede ser un enfoque viable para el alivio terapéutico incluyen, pero de forma no limitativa, trastorno del ritmo circadiano, depresión, esquizofrenia, inflamación neurogénica, hipertensión, enfermedades vasculares periféricas, migraña (Vanhoenacker, P. et al. Trends in Pharmacological Sciences, 2000, 21, 2, 70-77), dolor neuropático, dolor periférico, alodinia (EP1875899), trastorno de la termorregulación, trastorno del aprendizaje, trastorno de la memoria, trastorno de la señalización en el hipocampo, trastorno del sueño (WO20100197700), trastorno de déficit de atención/hiperactividad (TDAH) (WO20100069390), ansiedad, trastorno de personalidad elusiva, eyaculación prematura, trastorno alimentario, síndrome premenstrual, trastorno disfónico premenstrual, trastorno afectivo estacional y trastorno bipolar (WO20040229874). Sin desear estar limitado por la teoría, se cree que los moduladores de la actividad receptora del receptor de 5-hidroxitriptamina 7 de la presente invención pueden mejorar, reducir, de otro modo causar el control de, enfermedades asociadas a la desregulación de la actividad del receptor de 5-hidroxitriptamina 7. Las enfermedades incluyen, pero de forma no limitativa, trastorno del ritmo circadiano, depresión, esquizofrenia, inflamación neurogénica, hipertensión, enfermedades vasculares periféricas, migraña, dolor neuropático, dolor periférico, alodinia, trastorno de la termorregulación, trastorno del aprendizaje, trastorno de la memoria, trastorno de la señalización en el hipocampo, trastorno del sueño, trastorno de déficit de atención/hiperactividad, ansiedad, trastorno de personalidad elusiva, eyaculación prematura, trastorno alimentario, síndrome premenstrual, trastorno disfónico premenstrual, trastorno afectivo estacional y trastorno bipolar.
[0009] En toda la descripción, cuando se describe que las composiciones tienen, incluyen o comprenden componentes específicos, o cuando se describe que los procesos tienen, incluyen o comprenden pasos del proceso específicos, se contempla que las composiciones de las presentes instrucciones consisten también esencialmente en, o consisten en, los componentes enumerados, y que los procesos de las presentes instrucciones consisten también esencialmente en, o consisten en, los pasos de procesamiento enumerados.
[0010] En la solicitud, cuando se dice que un elemento o componente está incluido en y/o se selecciona a partir de una lista de elementos o componentes enumerados, debe entenderse que el elemento o el componente puede ser cualquiera de los elementos o componentes enumerados y se puede seleccionar a partir de un grupo consistente en dos o más de los elementos o componentes enumerados.
[0011] El uso del singular en la presente incluye el plural (y viceversa) a menos que se indique específicamente lo contrario. Además, cuando el uso del término "aproximadamente" está antes de un valor cuantitativo, las presentes instrucciones incluyen también el propio valor cuantitativo específico, a menos que se indique específicamente lo contrario.
[0012] Se debe entender que el orden de los pasos o el orden para realizar ciertas acciones es irrelevante siempre y cuando las presente instrucciones permanezcan operables. Además, se pueden realizar dos o más pasos o acciones simultáneamente.
[0013] Como se utiliza en la presente, el término "halógeno" significará cloro, bromo, flúor y yodo.
[0014] Como se utiliza en la presente, a menos que se indique lo contrario, "alquilo" y/o "alifático", ya sea usado solo o como parte de un grupo sustituyente, se refiere a cadenas de carbono lineales y ramificadas con 1 a 20 átomos de carbono o cualquier número dentro de este rango, por ejemplo, de 1 a 6 átomos de carbono o de 1 a 4 átomos de carbono. Los números designados de átomos de carbono (por ejemplo, C1-6) se referirán independientemente al número de átomos de carbono en una fracción alquílica o a la parte alquílica de un sustituyente más grande que contiene alquilo. Los ejemplos no limitativos de grupos alquilo incluyen metilo, etilo, n-propilo, /sopropilo, n-butilo, sec-butilo, /sobutilo, ferf-butilo y similares. Los grupos alquilo pueden estar opcionalmente sustituidos. Los ejemplos no limitativos de grupos alquilo sustituidos incluyen hidroximetilo, clorometilo, trifluorometilo, aminometilo, 1 -cloroetilo, 2-hidroxietilo, 1,2-difluoroetilo, 3-carboxipropilo y similares. En grupos sustituyentes con múltiples grupos alquilo, tal como (C1-6alquil)2amino, los grupos alquilo pueden ser iguales o diferentes.
[0015] Como se utiliza en la presente, los términos grupos "alquenilo" y "alquinilo", ya sea usados solos o como parte de un grupo sustituyente, se refieren a cadenas de carbono lineales y ramificadas que tienen 2 o más átomos de carbono, preferiblemente de 2 a 20, donde una cadena de alquenilo tiene al menos un enlace doble en la cadena y una cadena de alquinilo tiene al menos un enlace triple en la cadena. Los grupos alquenilo y alquinilo pueden estar opcionalmente sustituidos. Los ejemplos no limitativos de grupos alquenilo incluyen etenilo, 3-propenilo, 1-propenilo (también 2-metiletenilo), isopropenilo (también 2-metileten-2-ilo), buten-4-ilo y similares. Los ejemplos no limitativos de grupos alquenilo sustituidos incluyen 2-cloroetenilo (también 2-clorovinilo), 4-hidroxibuten-1-ilo, 7-hidroxi-7-metiloct-4-en-2-ilo, 7-hidroxi-7-metiloct-3,5-dien-2-ilo y similares. Los ejemplos no limitativos de grupos de alquinilo incluyen etinilo, prop-2-inilo (también propargilo), propin-1-ilo y 2-metil-hex-4-in-1-ilo. Los ejemplos no limitativos de grupos alquinilo sustituidos incluyen 5-hidroxi-5-metilhex-3-inilo, 6-hidroxi-6-metilhept-3-in-2-ilo, 5-hidroxi-5-etilhept-3-inilo y similares.
[0016] Como se utiliza en la presente, "cicloalquilo", ya sea usado solo o como parte de otro grupo, se refiere a un anillo que contiene carbonos no aromáticos, incluidos grupos alquilo, alquenilo y alquinilo ciclados, por ejemplo, con de 3 a 14 átomos de carbono en el anillo, preferiblemente de 3 a 7 o de 3 a 6 átomos de carbono en el anillo o incluso de 3 a 4 átomos de carbono en el anillo, y que contienen opcionalmente uno o más (por ejemplo, 1, 2 o 3) enlaces dobles o triples. Los grupos cicloalquilo pueden ser monocíclicos (por ejemplo, ciclohexilo) o policíclicos (por ejemplo, que contienen sistemas de anillos fusionados, conectados y/o espiro), donde los átomos de carbono están situados en el interior o el exterior del sistema de anillos. Cualquier posición en el anillo adecuada del grupo cicloalquilo se puede enlazar de manera covalente a la estructura química definida. Los anillos cicloalquílicos pueden estar opcionalmente sustituidos. Los ejemplos no limitativos de grupos cicloalquilo incluyen: ciclopropilo, 2-metilciclopropilo, ciclopropenilo, ciclobutilo, 2,3-dihidroxiciclobutilo, ciclobutenilo, ciclopentilo, ciclopentenilo, ciclopentadienilo, ciclohexilo, ciclohexenilo, cicloheptilo, ciclooctanilo, decalinilo, 2,5-dimetilciclopentilo, 3,5-diclorociclohexilo, 4-hidroxiciclohexilo, 3,3,5-trimetilciclohex-1 -ilo, octahidropentalenilo, octahidro-1H-indenilo, 3a,4,5,6,7,7a-hexahidro-3H-inden-4-ilo, decahidroazulenilo; biciclo[6.2.0]decanilo, decahidronaftalenilo y dodecahidro-1H-fluorenilo. El término "cicloalquilo" incluye también anillos carbocíclicos que son anillos de hidrocarburos bicíclicos, los ejemplos no limitativos de los cuales incluyen, biciclo-[2.1.1]hexanilo, biciclo[2.2.1]heptanilo, biciclo[3.1.1]heptanilo, 1,3-dimetil[2.2.1]heptan-2-ilo, biciclo[2.2.2]octanilo y biciclo[3.3.3]undecanilo.
[0017] "Haloalquilo" pretende incluir grupos de hidrocarburos alifáticos saturados tanto de cadena lineal como ramificada con el número especificado de átomos de carbono, sustituidos con 1 o más halógenos. Los grupos haloalquilo incluyen grupos perhaloalquilo, donde se han reemplazado todos los hidrógenos de un grupo alquilo por halógenos (por ejemplo, -CF3, -CF2CF3). Los grupos haloalquilo pueden opcionalmente estar sustituidos con uno o más sustituyentes además de halógenos. Los ejemplos de grupos haloalquilo incluyen, pero de forma no limitativa, grupos fluorometilo, dicloroetilo, trifluorometilo, triclorometilo, pentafluoroetilo y pentacloroetilo.
[0018] El término "alcoxi" se refiere al grupo -O-alquilo, donde el grupo alquilo es tal como se ha definido anteriormente. Opcionalmente, los grupos alcoxi pueden estar sustituidos. El término alcoxi cíclico C3-C6 se refiere a un anillo que contiene de 3 a 6 átomos de carbono y al menos un átomo de oxígeno (por ejemplo, tetrahidrofurano, tetrahidro-2H-pirano). Opcionalmente, los grupos alcoxi cíclicos C3-C6 pueden estar sustituidos.
[0019] El término "haloalcoxi" se refiere al grupo O-haloalquilo, donde el grupo haloalquilo es tal como se ha definido anteriormente. Los ejemplos de grupos haloalcoxi incluyen, pero de forma no limitativa, fluorometoxi, difluorometoxi, trifluorometoxi y pentafluoroetoxilo.
[0020] El término "arilo", ya sea usado solo o como parte de otro grupo, se define en la presente como un anillo monocíclico insaturado y aromático de 6 miembros de carbono o a un anillo policíclico insaturado y aromático de 10 a 14 miembros de carbono. Los anillos arilo pueden ser, por ejemplo, un anillo fenilo o naftilo, cada uno sustituido opcionalmente con una o más fracciones capaces de reemplazar uno o más átomos de hidrógeno. Los ejemplos no limitativos de grupos arilo incluyen: fenilo, naftilen-1-ilo, naftilen-2-ilo, 4-fluorofenilo, 2-hidroxifenilo, 3-metilfenilo, 2-amino-4-fluorofenilo, 2-(A/,W-dietilamino)fenilo, 2-cianofenilo, 2,6-di-terf-butilfenilo, 3-metoxifenilo, 8-hidroxinaftilen-2-ilo 4,5-dimetoxinaftilen-1-ilo y 6-ciano-naftilen-1-ilo. Los grupos arilo incluyen también, por ejemplo, anillos fenilo o naftilo fusionados con uno o más anillos de carbono saturados o parcialmente saturados (por ejemplo, biciclo[4.2.0]octa-1,3,5-trienilo, indanilo), que pueden estar sustituidos en uno o más átomos de carbono de los anillos aromáticos y/o saturados o parcialmente saturados.
[0021] El término "arilalquilo" o "aralquilo" se refiere al grupo-alquil-arilo, donde los grupos alquilo y arilo son tal y como se define en la presente. Los grupos aralquilo de la presente invención están opcionalmente sustituidos. Los ejemplos de grupos de arilalquilo incluyen, por ejemplo, bencilo, 1 -feniletilo, 2-feniletilo, 3-fenilpropilo, 2-fenilpropilo, fluorenilmetilo y similares.
[0022] Los términos "heterocíclico" y/o "heterociclo" y/o "heterociclilo", ya sea usados solos o como parte de otro grupo, se definen en la presente como uno o más anillos con de 3 a 20 átomos, donde al menos un átomo en al menos un anillo es un heteroátomo seleccionado de nitrógeno (N), oxígeno (O) o azufre (S), y donde además el anillo que incluye el heteroátomo no es aromático. En grupos de heterociclos que incluyen 2 o más anillos fusionados, el anillo que no lleva heteroátomos puede ser arilo (por ejemplo, indolinilo, tetrahidroquinolinilo, cromanilo). Los grupos heterociclo ejemplares tienen de 3 a 14 átomos en el anillo de los cuales de 1 a 5 son heteroátomos seleccionados independientemente de nitrógeno (N), oxígeno (O) o azufre (S). Uno o más átomos N o S en un grupo heterociclo estar oxidado. Los grupos heterociclo pueden estar opcionalmente sustituidos.
[0023] Ejemplos de unidades heterocíclicas que tienen un único anillo incluyen: diazirinilo, aziridinilo, urazolilo, azetidinilo, pirazolidinilo, imidazolidinilo, oxazolidinilo, isoxazolinilo, isoxazolilo, tiazolidinilo, isotiazolilo, isotiazolinilo, oxatiazolidinonilo, oxazolidinonilo, hidantoinilo, tetrahidrofuranilo, pirrolidinilo, morfolinilo, piperazinilo, piperidinilo, dihidropiranilo, tetrahidropiranilo, piperidin-2-onilo (valerolactama), 2,3,4,5-tetrahidro-1H-azepin¡lo, 2,3-dihidro-1H-indol y 1,2,3,4-tetrahidro-quinolina. Los ejemplos no limitativos de unidades heterocíclicas que tienen 2 o más anillos incluyen: hexahidro-1H-pirrolizinilo, 3a,4,5,6,7,7a-hexahidro-1H-benzo[d]imidazolilo, 3a,4,5,6,7,7a-hexahidro-1H-indolilo, 1,2,3,4-tetrahidroquinolinilo, cromanilo, isocromanilo, indolinilo, isoindolinilo y decahidro-1H-cicloocta[b]pirrolilo.
[0024] El término "heteroarilo", ya sea usado solo o como parte de otro grupo, se define en la presente como uno o más anillos que tienen de 5 a 20 átomos, donde al menos un átomo en al menos un anillo es un heteroátomo elegido de nitrógeno (N), oxígeno (O) o azufre (S), y donde además al menos uno de los anillos que incluye un heteroátomo es aromático. En grupos heteroarilo que incluyen 2 o más anillos fusionados, el anillo que no lleva heteroátomos puede ser un carbociclo (por ejemplo, 6,7-dihidro-5H-ciclopentapirimidina) o un arilo (por ejemplo, benzofuranilo, benzotiofenilo, indolilo). Grupos heteroarilo ejemplares tienen de 5 a 14 átomos en el anillo y contienen de 1 a 5 heteroátomos en el anillo seleccionados independientemente de nitrógeno (N), oxígeno (O) o azufre (S). Uno o más átomos de N o S en un grupo heteroarilo puede estar oxidado. Los grupos heteroarilo pueden estar sustituidos. Los ejemplos no limitativos de anillos de heteroarilo que contienen un único anillo incluyen: 1,2,3,4-tetrazolilo, [1,2,3]triazolilo, [1,2,4]triazolilo, triazinilo, tiazolilo, 1H-imidazolilo, oxazolilo, furanilo, tiofenilo, pirimidinilo, 2-fenilpirimidinilo, piridinilo, 3-metilpiridinilo y 4-dimetilaminopiridinilo. Los ejemplos no limitativos de anillos de heteroarilo que contienen 2 o más anillos fusionados incluyen: benzofuranilo, benzotiofenilo, benzoxazolilo, benzotiazolilo, benzotriazolilo, cinnolinilo, naftiridinilo, fenantridinilo, 7H-purinilo, 9H-purinilo, 6-amino-9H-purinilo, 5H-pirrolo[3,2-d]pirimidinilo, 7H-pirrolo[2,3-d]pirimidinilo, pirido[2,3-d]pirimidinilo, 2-fenilbenzo[d]tiazolilo, 1H-indolilo, 4,5,6,7-tetrahidro-1 -W-indolilo, quinoxalinilo, 5-metilquinoxalinilo, quinazolinilo, quinolinilo, 8-hidroxiquinolinilo e isoquinolinilo.
[0025] Un ejemplo de un grupo heteroarilo como se ha descrito anteriormente es heteroarilo C1-C5, que tiene de 1 a 5 átomos de carbono en el anillo y al menos un átomo adicional en el anillo que es un heteroátomo (preferiblemente de 1 a 4 átomos adicionales en el anillo que son heteroátomos) seleccionados independientemente de nitrógeno (N), oxígeno (O) o azufre (S). Los ejemplos de heteroarilo C1-C5 incluyen, pero de forma no limitativa, triazinilo, tiazol-2-ilo, tiazol-4-ilo, imidazol-1-ilo, 1W-imidazol-2-ilo, 1W-imidazol-4-ilo, isoxazolin-5-ilo, furan-2-ilo, furan-3-ilo, tiofen-2-ilo, tiofen-4-ilo, pirimidin-2-ilo, pirimidin-4-ilo, pirimidin-5-ilo, piridin-2-ilo, piridin-3-ilo y piridin-4-ilo.
[0026] A menos que se indique lo contrario, cuando dos sustituyentes se toman en conjunto para formar un anillo con un número especificado de átomos en el anillo (por ejemplo, R2 y R3 junto con el nitrógeno (N) al que están unidos para formar un anillo con de 3 a 7 miembros del anillo), el anillo puede tener átomos de carbono y opcionalmente uno o más (por ejemplo, de 1 a 3) heteroátomos adicionales seleccionados independientemente de nitrógeno (N), oxígeno (O) o azufre (S). El anillo puede estar saturado o saturado parcialmente y puede estar opcionalmente sustituido.
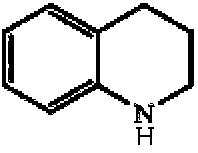
[0027] A efectos de la presente invención, se considerará que las unidades de anillos fusionados, así como los anillos espirocíclicos, los anillos bicíclicos y similares, que comprenden un único heteroátomo pertenecen a la familia cíclica correspondiente al heteroátomo que contiene el anillo. Por ejemplo, la 1,2,3,4-tetrahidroquinolina con la fórmula:
se considera, a efectos de la presente invención, una unidad heterocíclica. La 6,7-dihidro-5H-ciclopentapirimidina con la fórmula:
se considera, a efectos de la presente invención, una unidad de heteroarilo. Cuando una unidad de anillos fusionados contiene heteroátomos tanto en un anillo saturado como en uno de arilo, el anillo de arilo predominará y determinará el tipo de categoría a la que se asigna el anillo. Por ejemplo, 1,2,3,4-tetrahidro-[1,8]naftiridina con la fórmula:
se considera, a efectos de la presente invención, una unidad de heteroarilo.
[0028] Siempre que un término o cualquiera de sus raíces de prefijo aparecen en el nombre de un sustituyente, debe interpretarse que el nombre incluye aquellas limitaciones provistas en la presente. Por ejemplo, siempre que el término "alquilo" o "arilo" o cualquiera de sus raíces de prefijo aparecen en el nombre de un sustituyente (por ejemplo, arilalquilo, alquilamino), debe interpretarse que el nombre incluye aquellas limitaciones dadas anteriormente para "alquilo" y "arilo".
[0029] El término "sustituido/a/os/as" se usa en toda la descripción. El término "sustituido/a/os/as" se define en la presente como una fracción, ya sea acíclica o cíclica, que tiene uno o más átomos de hidrógeno reemplazados por un sustituyente o varios (por ejemplo, de 1 a 10) sustituyentes tal y como se define en la presente a continuación. Los sustituyentes son capaces de reemplazar uno o dos átomos de hidrógeno de una única fracción a la vez. Además, estos sustituyentes pueden reemplazar dos átomos de hidrógeno en dos carbonos adyacentes para formar dicho sustituyente, nueva fracción o unidad. Por ejemplo, una unidad sustituida que requiere una única sustitución de un átomo de hidrógeno incluye halógeno, hidroxilo y similares. Una sustitución de dos átomos de hidrógeno incluye carbonilo, oximino y similares. Una sustitución de dos átomos de hidrógeno de átomos de carbono adyacentes incluye epoxi y similares. El término "sustituido/a/os/as" se usa en toda la presente descripción para indicar que una fracción puede tener uno o más de los átomos de hidrógeno reemplazados por un sustituyente. Cuando una fracción se describe como "sustituida", cualquier número de los átomos de hidrógeno puede estar reemplazado. Por ejemplo, el difluorometilo es un alquilo C1 sustituido; el trifluorometilo es un alquilo C1 sustituido; el 4-hidroxifenilo es un anillo aromático sustituido; el (N,N-dimetil-5-amino)octanilo es un alquilo Cs sustituido; el 3-guanidinopropilo es un alquilo C3 sustituido; y el 2-carboxipiridinilo es un heteroarilo sustituido.
[0030] Los grupos variables definidos en la presente, por ejemplo, los grupos alquilo, alquenilo, alquinilo, cicloalquilo, alcoxi, ariloxi, arilo, heterociclo y heteroarilo definidos en la presente, ya sea usados solos o como parte de otro grupo, pueden estar opcionalmente sustituidos. Los grupos opcionalmente sustituidos se indicarán como tales.
[0031] En varios lugares en la presente descripción, los sustituyentes de los compuestos se describen en grupos o en rangos. Se pretende específicamente que la descripción incluya todas de cada una de las subcombinaciones individuales de los miembros de tales grupos y rangos. Por ejemplo, el término "alquilo C1-6" está destinado específicamente a describir individualmente alquilo C1, C2, C3, C4, C5, C6, C1-C6, C1-C5, C1-C4, C1-C3, C1-C2, C2-C6, C2-C5, C2-C4, C2-C3, C3-C6, C3-C5, C3-C4, C4-C6, C4-C5 y C5-C6.
[0032] A efectos de la presente invención los términos "compuesto", "análogo" y "composición de materia" representan igual de bien a los moduladores de la actividad del receptor de 5-hidroxitriptamina 7 descritos en la presente, incluidas todas las formas enantioméricas, formas diastereoméricas, sales y similares, y los términos "compuesto", "análogo" y "composición de materia" se usan de forma intercambiable en toda la presente descripción.
[0033] Los compuestos descritos en la presente pueden contener un átomo asimétrico (también denominado un centro quiral), y algunos de los compuestos pueden contener uno o más átomos o centros asimétricos, que pueden dar lugar así a isómeros ópticos (enantiómeros) y diastereómeros. Las presente instrucciones y compuestos descritos en la presente incluyen tales enantiómeros y diastereómeros, así como los estereoisómeros R y S racémicos y resueltos, enantioméricamente puros, así como otras mezclas de los estereoisómeros R y S y sales farmacéuticamente aceptables de los mismos. Los isómeros ópticos se pueden obtener en la forma pura por procedimientos estándar conocidos por las personas expertas en la técnica, que incluyen, pero de forma no limitativa, la formación de sales diastereoméricas, la resolución cinética y la síntesis asimétrica. Las presentes instrucciones abarcan también los isómeros cis y trans de compuestos que contienen fracciones de alquenilo (por
ejemplo, alquenos e iminas). También se entiende que las presentes instrucciones abarcan todos los posibles regioisómeros, y sus mezclas derivadas, que pueden obtenerse en la forma pura por procedimientos de separación estándar conocidos por las personas expertas en la técnica, e incluyen, pero de forma no limitativa, cromatografía en columna, cromatografía en capa fina y cromatografía en fase líquida de alta eficacia.
[0034] Las sales farmacéuticamente aceptables de los compuestos de las presentes instrucciones, que pueden tener una fracción ácida, se pueden formar usando bases orgánicas e inorgánicas. Se contemplan tanto sales mono como polianiónicas, dependiendo del número de hidrógenos ácidos disponibles para la desprotonación. Las sales adecuadas formadas con bases incluyen sales metálicas, tales como sales de metales alcalinos o de metales alcalinotérreos, por ejemplo sales de sodio, potasio o magnesio; sales de amoníaco y sales de amina orgánicas, tales como las formadas con morfolina, tiomorfolina, piperidina, pirrolidina, una mono-, di- o trialquilamina inferior (por ejemplo, etil-tert-butil-, dietil-, diisopropil-, trietil-, tributil- o dimetilpropilamina) o una mono-, di- o trihidroxialquilamina inferior (por ejemplo, mono-, di- o trietanolamina). Los ejemplos no limitativos específicos de bases inorgánicas incluyen NaHCO3, Na2CO3, KHCO3, K2CO3, Cs2CO3, LiOH, NaOH, KOH, NaH2PO4, Na2HPO4 y Na3PO4. También se pueden formar sales internas. De forma similar, cuando un compuesto descrito en la presente contiene una fracción básica, las sales se pueden formar usando ácidos orgánicos e inorgánicos. Por ejemplo, se pueden formar sales de los ácidos siguientes: acético, propiónico, láctico, bencenosulfónico, benzoico, canforsulfónico, cítrico, tartárico, succínico, dicloroacético, etenosulfónico, fórmico, fumárico, glucónico, glutámico, hipúrico, bromhídrico, clorhídrico, isetiónico, láctico, maleico, málico, malónico, mandélico, metanosulfónico, múcico, naftalenosulfónico, nítrico, oxálico, pamoico, pantoténico, fosfórico, ftálico, propiónico, succínico, sulfúrico, tartárico, toluenosulfónico y canforsulfónico, así como otros ácidos farmacéuticamente aceptables conocidos.
[0035] Cuando cualquier variable ocurre más de una vez en cualquier constituyente o en cualquier fórmula, su definición en cada aparición es independiente de su definición en cada una de las otras apariciones (por ejemplo, en N(R9)2, cada R9 puede ser igual o diferente al otro). Las combinaciones de sustituyentes y/o variables son permisibles solo si tales combinaciones resultan en compuestos estables.
[0036] Los términos "tratan" y "tratar" y "tratamiento" como se utilizan en la presente, se refieren a paliar, inhibir, mejorar y/o aliviar parcial o completamente una condición que se sospecha que sufre un paciente.
[0037] Como se utiliza en la presente, "terapéuticamente eficaz" y "dosis efectiva" se refieren a una sustancia o una cantidad que provoca una actividad o un efecto biológico deseable. Una cantidad de tal compuesto proporcionada al sujeto que resulta en una resolución completa de los síntomas de una enfermedad o trastorno, una reducción en la gravedad de los síntomas de la enfermedad o trastorno, o una ralentización de la progresión de una enfermedad o trastorno se considera una cantidad terapéuticamente eficaz.
[0038] Excepto cuando se indique, los términos "sujeto" o "paciente" se usan de forma intercambiable y se refieren a mamíferos tales como pacientes humanos y primates no humanos, así como animales experimentales tales como conejos, ratas y ratones, y otros animales. Por consiguiente, el término "sujeto" o "paciente" como se utiliza en la presente significa cualquier paciente o sujeto mamífero al que se le pueden administrar los compuestos de la invención. Para identificar pacientes sujetos para el tratamiento, se emplean métodos de cribado aceptados para determinar factores de riesgo asociados a una enfermedad o condición objetivo o sospechada o para determinar el estado de una enfermedad o condición existente en un sujeto. Estos métodos de cribado incluyen, por ejemplo, pruebas diagnósticas convencionales para determinar factores de riesgo que puedan estar asociados a la enfermedad o condición objetivo o sospechada. Estos y otros métodos de rutina permiten al clínico seleccionar pacientes que necesitan terapia usando los métodos y los compuestos de la presente invención.
Los moduladores de la actividad del receptor de 5-hidroxitriptamina 7
[0039] Los moduladores de la actividad del receptor de 5-hidroxitriptamina 7 de la presente invención incluyen todas las formas enantioméricas y diastereoméricas de los mismos y tienen la fórmula general
Incluidos hidratos, solvatos y sales farmacéuticamente aceptables de los mismos, donde:
A se selecciona de un grupo consistente en
R1a y R1b son un alquilo Ci-6 lineal;
R1a y R1b se toman junto con el átomo al que están unidos para formar un anillo con 5 átomos en el anillo; R2a y R2b son hidrógeno; R3 es un arilo sustituido; y n es 2;
[0040] La presente invención se refiere a compuestos que tienen la fórmula (II):
Incluidos hidratos, solvatos y sales farmacéuticamente aceptables de los mismos.
[0041] En algunas formas de realización, R1a es un alquilo C1-6 lineal.
[0042] En algunas formas de realización, R1b es un alquilo C1-6 lineal.
[0043] En algunas formas de realización, R1a y R1b se toman junto con el átomo al que están unidos para formar un anillo con 5 átomos en el anillo.
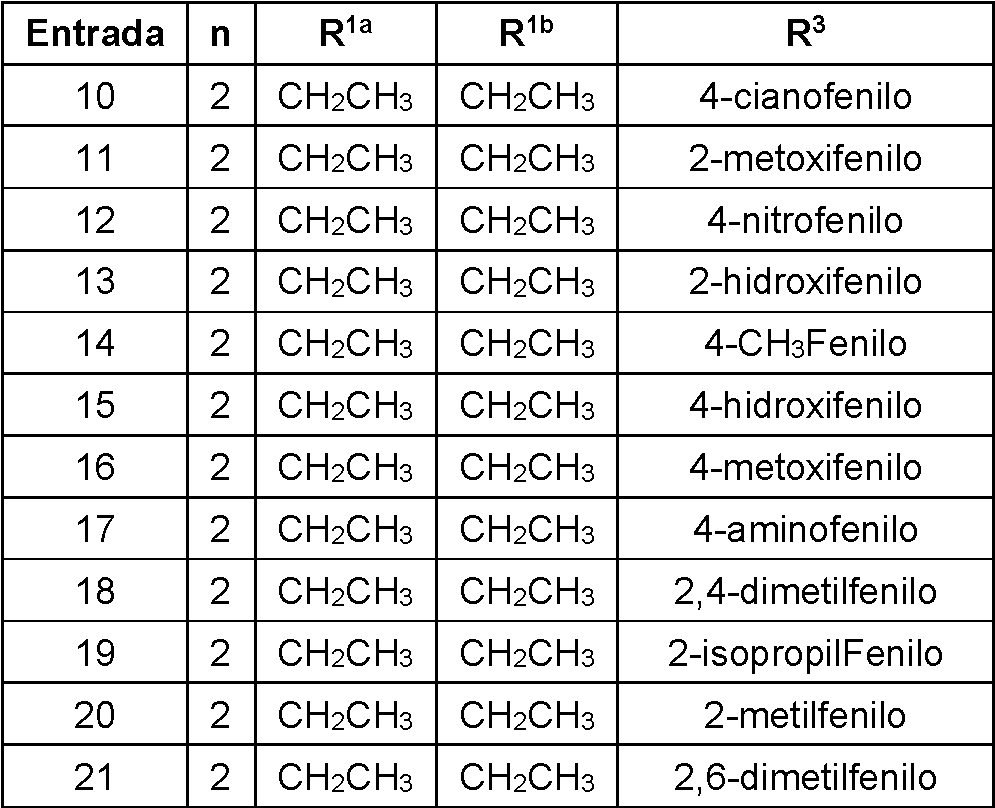
[0044] Las formas de realización inventivas son compuestos con la fórmula (II) o una forma salina farmacéuticamente aceptable de los mismos:
donde R1a, R1b, R3 y "n" se definen en la presente a continuación en la tabla 1.
Tabla 1.
[0045] A efectos de demostrar la manera en la que los compuestos de la presente invención se nombran y se denominan en la presente, el compuesto con la fórmula:
tiene el nombre químico 3,3-dietil-5-[2-(4-fenetil-piperazin-1 -M)-etil]-dihidro-fu ran-2-ona.
[0046] A efectos de la presente invención, un compuesto representado por la fórmula racémica, por ejemplo:
representará igual de bien a cualquiera de los dos enantiómeros con la fórmula:
o la fórmula:
o mezclas derivadas o, en el caso donde un segundo centro quiral esté presente, todos los diastereómeros.
PROCESO
[0047] La presente descripción divulga además un proceso para preparar los moduladores de la actividad del receptor de 5-hidroxitriptamina 7 de la presente invención.
[0048] Los compuestos de las presentes instrucciones se pueden preparar conforme a los procedimientos descritos en la presente, a partir de materiales de partida disponibles comercialmente, compuestos conocidos en la literatura o productos intermedios fácilmente preparados, empleando procedimientos y métodos sintéticos estándar conocidos por las personas expertas en la técnica. Los procedimientos y métodos sintéticos estándar para la preparación de moléculas orgánicas y transformaciones y manipulaciones de grupos funcionales se pueden obtener fácilmente de la literatura científica relevante o de libros de texto estándar en el campo. Se apreciará que, cuando se dan condiciones del proceso típicas o preferidas (es decir, temperaturas de reacción, tiempos, razones molares de reactivos, solventes, presiones, etc.), también pueden usarse otras condiciones del proceso a menos que se indique lo contrario. Las condiciones de reacción óptimas pueden variar con los reactivos o el solvente particulares usados, pero tales condiciones se pueden determinar por una persona experta en la técnica por procedimientos de optimización rutinarios. Aquellas personas expertas en la técnica de la síntesis orgánica reconocerán que la naturaleza y el orden de los pasos sintéticos presentados se pueden variar con el fin de optimizar la formación de los compuestos descritos en la presente.
[0049] Los procesos descritos en la presente se pueden monitorear según cualquier método adecuado conocido en la técnica. Por ejemplo, la formación de producto se puede monitorear por medios espectroscópicos, tales como espectroscopia de resonancia magnética nuclear (por ejemplo, 1H o 13C), espectroscopia infrarroja, espectrofotometría (por ejemplo, UV-visible), espectrometría de masas, o por cromatografía, tal como cromatografía en fase líquida de alta resolución (HPLC), cromatografía de gases (GC), cromatografía de permeación en gel (GPC) o cromatografía en capa fina (TLC).
[0050] La preparación de los compuestos pueden implicar la protección y la desprotección de varios grupos químicos. La necesidad de protección y desprotección y la selección de grupos protectores apropiados puede ser determinada fácilmente por una persona experta en la técnica. La química de grupos protectores se puede encontrar, por ejemplo, en Greene et al., Protective Groups in Organic Synthesis, 2a ed. (Wiley & Sons, 1991), toda la divulgación del cual se incorpora por referencia en la presente a todos los efectos.
[0051] Las reacciones o los procesos descritos en la presente se pueden realizar en solventes adecuados que pueden ser seleccionados fácilmente por una persona experta en la técnica de la síntesis orgánica. Típicamente, los solventes adecuados son sustancialmente no reactivos con los reactivos, los productos intermedios y/o los productos a las temperaturas a las cuales se realizan las reacciones, es decir, temperaturas que pueden variar desde la temperatura de congelación del solvente hasta la temperatura de ebullición del solvente. Una reacción dada se puede realizar en un solvente o una mezcla de más de un solvente. Dependiendo del paso de reacción particular, se pueden seleccionar solventes adecuados para un paso de reacción particular.
[0052] Los compuestos de estas instrucciones se pueden preparar por métodos conocidos en la técnica de la química orgánica. Los reactivos usados en la preparación de los compuestos de estas instrucciones pueden ser obtenidos comercialmente o se pueden preparar por procedimientos estándar descritos en la literatura. Por ejemplo, los compuestos de la presente invención se pueden preparar según el método ilustrado en los esquemas sintéticos generales:
ESQUEMAS SINTÉTICOS GENERALES PARA LA PREPARACIÓN DE COMPUESTOS.
[0053] Los reactivos usados en la preparación de los compuestos de esta invención pueden ser obtenidos comercialmente o se pueden preparar por procedimientos estándar descritos en la literatura. Conforme a esta invención, los compuestos en el género se pueden producir por uno de los siguientes esquemas de reacción.
[0054] Los compuestos de la divulgación se pueden preparar según el proceso descrito en el esquema 1-.
[0055] Un compuesto adecuadamente sustituido con la fórmula (1), un compuesto conocido o un compuesto preparado por métodos conocidos, se hace reaccionar con un compuesto con la fórmula (2), donde X es un grupo saliente tal como cloro, bromo, yodo, mesilato, tosilato y similares, en presencia de una base tal como diisopropilamida de litio, diisopropilamida de sodio, diisopropilamida de potasio, bis(trimetilsilil)amida de litio, bis(trimetilsilil)amida de sodio, bis(trimetilsilil)amida de potasio, hidruro sódico y similares en un solvente orgánico tal como tetrahidrofurano, 1,4-dioxano, 1,2-dimetoxietano, dimetilformamida, dimetilacetamida y similares, para proporcionar un compuesto con la fórmula (3 ). Un compuesto con la fórmula (3) se trata entonces con paraformaldehído en presencia de un ácido tal como ácido sulfúrico, ácido clorhídrico y similares, en presencia de ácido acético, y opcionalmente en un solvente orgánico tal como metanol, etanol, tetrahidrofurano, 1,4-dioxano, 1,2-dimetoxietano, dimetilformamida, dimetilacetamida y similares, opcionalmente con calentamiento, opcionalmente con irradiación de microondas para proporcionar un compuesto con la fórmula (4). Un compuesto con la fórmula (4) se trata entonces con una base tal como hidróxido sódico, hidróxido potásico, hidróxido de litio y similares, en un solvente tal como agua, metanol, etanol, isopropanol y similares, opcionalmente con calentamiento, y luego se trata con un ácido tal como ácido sulfúrico, ácido clorhídrico y similares, en un solvente tal como agua, metanol, etanol, isopropanol y similares, para proporcionar un compuesto con la fórmula (5). Un compuesto con la fórmula (5) se convierte entonces en un compuesto con la fórmula (6), donde LG es un mesilato, tosilato, nosilato y similares, usando métodos que son conocidos por una persona experta en la técnica. Así, un compuesto con la fórmula (5) se trata con un cloruro de sulfonilo tal como cloruro de metanosulfonilo, cloruro de toluenosulfonilo, cloruro de p-nitrofenilo sulfonilo y similares, en presencia de una base tal como trietilamina, diisopropilamina, piridina, 2,6-lutidina y similares, en un solvente orgánico tal como cloruro de metileno, dicloroetano, tetrahidrofurano, 1,4-dioxano, N,N-dimetilformamida, tetrahidrofurano, 1,4-dioxano y similares para proporcionar un compuesto con la fórmula (6). Un compuesto con la fórmula (6) se hace reaccionar con un compuesto con la fórmula (7), un compuesto conocido o un compuesto preparado por métodos conocidos, en un solvente orgánico tal como tetrahidrofurano, 1,4-dioxano, 1,2-dimetoxietano, dimetilformamida, dimetilacetamida y similares, opcionalmente en presencia de una base tal como trietilamina, diisopropiletilamina, piridina, 2,6-lutidina y similares, opcionalmente con calentamiento, opcionalmente con irradiación de microondas para proporcionar un compuesto con la fórmula (8).
[0056] Alternativamente, se pueden preparar compuestos con la fórmula (8) según el proceso descrito en el esquema 2:
[0057] Un compuesto adecuadamente sustituido con la fórmula (9), un compuesto conocido o un compuesto preparado por métodos conocidos, se hace reaccionar con un compuesto con la fórmula (2), donde X es un grupo saliente tal como cloro, bromo, yodo, mesilato, tosilato y similares, en presencia de una base tal como diisopropilamida de litio, diisopropilamida de sodio, diisopropilamida de potasio, bis(trimetilsilil)amida de litio, bis(trimetilsilil)amida de sodio, bis(trimetilsilil)amida de potasio, hidruro sódico, n-butil litio, sec-butil litio, tert-butil litio y similares en un solvente orgánico tal como tetrahidrofurano, 1,4-dioxano, 1,2-dimetoxietano, dimetilformamida, dimetilacetamida y similares, para proporcionar un compuesto con la fórmula (10). Un compuesto con la fórmula (10) se trata entonces con paraformaldehído en presencia de un ácido tal como ácido sulfúrico, ácido clorhídrico y similares, en presencia de ácido acético, y opcionalmente en un solvente orgánico tal como metanol, etanol, tetrahidrofurano, 1,4-dioxano, 1,2-dimetoxietano, dimetilformamida, dimetilacetamida y similares, opcionalmente con calentamiento, opcionalmente con irradiación de microondas para proporcionar un compuesto con la fórmula (4). Un compuesto con la fórmula (4) se trata entonces con una base tal como hidróxido sódico, hidróxido potásico, hidróxido de litio y similares, en un solvente tal como agua, metanol, etanol, isopropanol y similares, opcionalmente con calentamiento, y luego se trata con un ácido tal como ácido sulfúrico, ácido clorhídrico y similares, en un solvente tal como agua, metanol, etanol, isopropanol y similares, opcionalmente con calentamiento, para proporcionar un compuesto con la fórmula (5). Un compuesto con la fórmula (5) se convierte entonces en un compuesto con la fórmula (6), donde LG es un mesilato, tosilato, nosilato y similares, usando métodos que son conocidos por una persona experta en la técnica. Así, un compuesto con la fórmula (5) se trata con un cloruro de sulfonilo tal como cloruro de metanosulfonilo, cloruro de toluenosulfonilo, cloruro de p-nitrofenilo sulfonilo y
similares, en presencia de una base tal como trietilamina, diisopropilamina, piridina, 2,6-lutidina y similares, en un solvente orgánico tal como cloruro de metileno, dicloroetano, tetrahidrofurano, 1,4-dioxano, N,N-dimetilformamida, tetrahidrofurano, 1,4-dioxano y similares para proporcionar un compuesto con la fórmula (6). Un compuesto con la fórmula (6) se hace reaccionar con un compuesto con la fórmula (7), un compuesto conocido o un compuesto preparado por métodos conocidos, en un solvente orgánico tal como tetrahidrofurano, 1,4-dioxano, 1,2-dimetoxietano, dimetilformamida, dimetilacetamida y similares, opcionalmente en presencia de una base tal como trietilamina, diisopropiletilamina, piridina, 2,6-lutidina y similares, opcionalmente con calentamiento, opcionalmente con irradiación de microondas para proporcionar un compuesto con la fórmula (8).
[0058] Los compuestos con la fórmula (21) se pueden preparar según el proceso descrito en el esquema 3.
E m
[0059] Un compuesto adecuadamente sustituido con la fórmula (11), un compuesto conocido o un compuesto preparado por métodos conocidos, se hace reaccionar con un compuesto con la fórmula (12), en presencia de una sal de amonio tal como acetato amónico, formiato de amonio, sulfato amónico, cloruro amónico y similares, en presencia de un ácido tal como ácido fórmico, ácido acético, ácido clorhídrico, ácido sulfúrico y similares, en un solvente orgánico tal como tolueno, benceno, p-xileno, m-xileno, o-xileno, tetrahidrofurano, 1,4-dioxano, dimetilformamida y similares, opcionalmente con calentamiento, opcionalmente con irradiación de microondas para proporcionar un compuesto con la fórmula (13). Un compuesto con la fórmula (13) se hace reaccionar entonces con un compuesto con la fórmula (14), donde X es un halógeno, en presencia de un compuesto con la fórmula ZnX2, donde X es un halógeno, en un solvente orgánico tal como tetrahidrofurano, 1,4-dioxano, 1,2-dimetoxietano, dimetilformamida, dimetilacetamida y similares para proporcionar un compuesto con la fórmula (15). Un compuesto con la fórmula (15) se hace reaccionar entonces con una base tal como hidróxido potásico, hidróxido sódico, hidróxido de litio, carbonato potásico, carbonato de sodio, carbonato de litio y similares, en un solvente tal como metanol, etanol, isopropanol, etilenglicol, propilenglicol, agua y similares, opcionalmente con calentamiento para proporcionar un compuesto con la fórmula (16). Un compuesto con la fórmula (16) se hace reaccionar con paraformaldehído en presencia de un ácido tal como ácido sulfúrico, ácido clorhídrico y similares, en presencia de ácido acético, opcionalmente en presencia de un solvente tal como metanol, etanol, tetrahidrofurano, 1,4-dioxano, dimetilformamida y similares, opcionalmente con calentamiento para proporcionar un compuesto con la fórmula (17). Un compuesto con la fórmula (17) se trata entonces con una base tal como hidróxido sódico, hidróxido potásico, hidróxido de litio y similares, en un solvente tal como agua, metanol, etanol, isopropanol y similares, opcionalmente con calentamiento, y luego se trata con un ácido tal como ácido sulfúrico, ácido clorhídrico y similares, en un solvente tal como agua, metanol, etanol, isopropanol y similares, opcionalmente con calentamiento, para proporcionar un compuesto con la fórmula (18). Un compuesto con la fórmula (18) se convierte entonces en un compuesto con la fórmula (19), donde LG es un mesilato, tosilato, nosilato y similares, usando métodos que son conocidos por una persona experta en la técnica. Así, un compuesto con la fórmula (18) se trata con un cloruro de sulfonilo tal como cloruro de metanosulfonilo, cloruro de toluenosulfonilo, cloruro de p-nitrofenilo sulfonilo y similares, en presencia de una base tal como trietilamina, diisopropilamina, piridina, 2,6-lutidina y similares, en un solvente orgánico tal como cloruro de metileno, dicloroetano, tetrahidrofurano, 1,4-dioxano, N,N-dimetilformamida, tetrahidrofurano, 1,4-dioxano y similares para proporcionar un compuesto con la fórmula (19). Un compuesto con la fórmula (19) se hace reaccionar con un compuesto con la fórmula (20), un compuesto conocido o un compuesto preparado por métodos conocidos, en un solvente orgánico tal como tetrahidrofurano, 1,4-dioxano, 1,2-dimetoxietano, dimetilformamida, dimetilacetamida y similares, opcionalmente en presencia de una base tal como trietilamina, diisopropiletilamina, piridina, 2,6-lutidina y similares, opcionalmente con calentamiento, opcionalmente con irradiación de microondas para proporcionar un compuesto con la fórmula (21).
[0060] Los compuestos con la fórmula (26) se pueden preparar según el proceso descrito en el esquema 4.
[0061] Un compuesto con la fórmula (22) se hace reaccionar con una base tal como hidróxido sódico, hidróxido potásico, hidróxido de litio, carbonato de sodio, carbonato potásico, carbonato de litio y similares, en presencia de un solvente tal como metanol, etanol, isopropanol, agua y similares, opcionalmente con calentamiento, opcionalmente con irradiación de microondas para proporcionar un compuesto con la fórmula (23). Un compuesto con la fórmula (23) se hace reaccionar entonces con yodo en presencia de una base tal como bicarbonato sódico, bicarbonato de potasio, bicarbonato de litio, carbonato de sodio, carbonato potásico, bicarbonato de litio, hidróxido sódico, hidróxido potásico, hidróxido de litio y similares, en presencia de un solvente tal como tetrahidrofurano, etil éter, 1,4-dioxano y similares para proporcionar un compuesto con la fórmula (24). Un compuesto con la fórmula (24) se hace reaccionar con un compuesto con la fórmula (25), un compuesto conocido o un compuesto preparado por métodos conocidos, en un solvente orgánico tal como tetrahidrofurano, 1,4-dioxano, 1,2-dimetoxietano, dimetilformamida, dimetilacetamida y similares, opcionalmente en presencia de una base tal como trietilamina, diisopropiletilamina, piridina, 2,6-lutidina y similares, opcionalmente con calentamiento, opcionalmente con irradiación de microondas para proporcionar un compuesto con la fórmula (26).
[0062] Los compuestos con la fórmula (35) se pueden preparar según el proceso descrito en el esquema 5.
Esquema 5
[0063] Un compuesto con la fórmula (27) se hace reaccionar con cloruro de rutenio en presencia de peryodato de sodio en un solvente tal como acetonitrilo, metanol, etanol, isopropanol y similares, para proporcionar un compuesto con la fórmula (28). Un compuesto con la fórmula (28) se hace reaccionar con un compuesto con la fórmula (29), un compuesto conocido o un compuesto preparado por métodos conocidos, donde x es un halógeno, en presencia de un solvente tal como etil éter, tetrahidrofurano, 1,4-dioxano y similares para proporcionar un compuesto con la fórmula (30). Un compuesto con la fórmula (30) se hace reaccionar con cloruro de rutenio en presencia de peryodato de sodio en un solvente tal como acetonitrilo, metanol, etanol, isopropanol y similares, para proporcionar un compuesto con la fórmula (31). Un compuesto con la fórmula (31) se hace reaccionar con un agente reductor tal como borohidruro de litio, borohidruro de sodio, cianoborohidruro de sodio y similares, en un solvente tal como metanol, etanol, isopropanol, acetonitrilo y similares para proporcionar un compuesto con la fórmula (32). Un compuesto con la fórmula (32) se convierte entonces en un compuesto con la fórmula (33), donde LG es un mesilato, tosilato, nosilato y similares, usando métodos que son conocidos por una persona experta en la técnica. Así, un compuesto con la fórmula (32) se trata con un cloruro de sulfonilo tal como cloruro de metanosulfonilo, cloruro de toluenosulfonilo, cloruro de p-nitrofenilo sulfonilo y similares, en presencia de una base tal como trietilamina, diisopropilamina, piridina, 2,6-lutidina y similares, en un solvente orgánico tal como cloruro de metileno, dicloroetano, tetrahidrofurano, 1,4-dioxano, N,N-dimetilformamida, tetrahidrofurano, 1,4-dioxano y similares para proporcionar un compuesto con la fórmula (33). Un compuesto con la fórmula (33) se hace reaccionar con un compuesto con la fórmula (34), un compuesto conocido o un compuesto preparado por métodos conocidos, en un solvente orgánico tal como tetrahidrofurano, 1,4-dioxano, 1,2-dimetoxietano, dimetilformamida, dimetilacetamida y similares, opcionalmente en presencia de una base tal como trietilamina, diisopropiletilamina, piridina, 2,6-lutidina y similares, opcionalmente con calentamiento, opcionalmente con irradiación de microondas para proporcionar un compuesto con la fórmula (35).
[0064] Los compuestos con la fórmula (44) se pueden preparar según el proceso descrito en el esquema 6.
Esquema 6
[0065] Un compuesto con la fórmula (36) se hace reaccionar con cloruro de rutenio en presencia de peryodato de sodio en un solvente tal como acetonitrilo, metanol, etanol, isopropanol y similares, para proporcionar un compuesto con la fórmula (37). Un compuesto con la fórmula (37) se hace reaccionar con un compuesto con la fórmula (38), un compuesto conocido o un compuesto preparado por métodos conocidos, donde x es un halógeno, en presencia de un solvente tal como etil éter, tetrahidrofurano, 1,4-dioxano y similares para proporcionar un compuesto con la fórmula (39). Un compuesto con la fórmula (39) se hace reaccionar con cloruro de rutenio en presencia de peryodato de sodio en un solvente tal como acetonitrilo, metanol, etanol, isopropanol y similares, para proporcionar un compuesto con la fórmula (40). Un compuesto con la fórmula (40) se hace reaccionar con un agente reductor tal como borohidruro de litio, borohidruro de sodio, cianoborohidruro de sodio y similares, en un solvente tal como metanol, etanol, isopropanol, acetonitrilo y similares para proporcionar un compuesto con la fórmula (41). Un compuesto con la fórmula (41) se convierte entonces en un compuesto con la fórmula (42), donde LG es un mesilato, tosilato, nosilato y similares, usando métodos que son conocidos por una persona experta en la técnica. Así, un compuesto con la fórmula (41) se trata con un cloruro de sulfonilo tal como cloruro de metanosulfonilo, cloruro de toluenosulfonilo, cloruro de p-nitrofenilo sulfonilo y similares, en presencia de una base tal como trietilamina, diisopropilamina, piridina, 2,6-lutidina y similares, en un solvente orgánico tal como cloruro de metileno, dicloroetano, tetrahidrofurano, 1,4-dioxano, N,N-dimetilformamida, tetrahidrofurano, 1,4-dioxano y similares para proporcionar un compuesto con la fórmula (42). Un compuesto con la fórmula (42) se hace reaccionar con un compuesto con la fórmula (43), un compuesto conocido o un compuesto preparado por métodos conocidos, en un solvente orgánico tal como tetrahidrofurano, 1,4-dioxano, 1,2-dimetoxietano, dimetilformamida, dimetilacetamida y similares, opcionalmente en presencia de una base tal como trietilamina, diisopropiletilamina, piridina, 2,6-lutidina y similares, opcionalmente con calentamiento, opcionalmente con irradiación de microondas para proporcionar un compuesto con la fórmula (44).
[0066] Los compuestos con la fórmula (48) se pueden preparar según el proceso descrito en el esquema 7.
[0067] Se hace reaccionar dietanolamina con cloruro de 4-nitrobencenosulfonilo (NosCl) en presencia de una base tal como trietilamina, diisopropiletilamina, piridina, 2,6-lutidina y similares en un solvente tal como tetrahidrofurano, 1,4-dioxano, cloruro de metileno y similares para proporcionar un compuesto con la fórmula (45). Un compuesto con la fórmula (45) se hace reaccionar entonces con un compuesto con la fórmula (46), un compuesto conocido o uno preparado por métodos conocidos, en presencia de una base tal como trietilamina, diisopropiletilamina, piridina, 2,6-lutidina y similares, en un solvente tal como acetonitrilo, metanol, etanol, dimetilformamida, opcionalmente con calentamiento, opcionalmente con irradiación de microondas para proporcionar un compuesto con la fórmula (47). Un compuesto con la fórmula (47) se hace reaccionar con un tiofenol en presencia de una base tal como bicarbonato sódico, bicarbonato de potasio, bicarbonato de litio, carbonato de sodio, carbonato potásico, bicarbonato de litio, hidróxido sódico, hidróxido potásico, hidróxido de litio y similares, en presencia de un solvente tal como tetrahidrofurano, etil éter, 1,4-dioxano, acetonitrilo y similares, opcionalmente en presencia de dimetilsulfóxido, opcionalmente con calentamiento, opcionalmente con irradiación de microondas, para proporcionar un compuesto con la fórmula (48).
[0068] Los ejemplos proporcionados a continuación proporcionan métodos representativos para preparar compuestos ejemplares de la presente invención. El profesional experto sabrá cómo sustituir los reactivos apropiados, los materiales de partida y los métodos de purificación conocidos por las personas expertas en la técnica, para preparar los compuestos de la presente invención.
EJEMPLOS
[0069] La práctica de la invención se ilustra mediante los ejemplos siguientes. Los ejemplos provistos a continuación proporcionan métodos representativos para preparar compuestos ejemplares de la presente invención. El profesional experto sabrá cómo sustituir los reactivos apropiados, los materiales de partida y los métodos de purificación conocidos por las personas expertas en la técnica, para preparar los compuestos de la presente invención.
[0070] En los ejemplos que siguen, se obtuvieron espectros 1H-RMN en un Varian Mercury NMR de 300 MHz. Se determinaron los datos espectrales de pureza (%) y masa con un Waters Alliance 2695 HPLC/MS (Waters Symmetry C18, 4,6 x 75 mm, 3,5 um) con un detector de red de diodos 2996 de 210-400 nm.
[0071] Preparación de metil 2,2-dimetilpent-4-enoato: esta reacción fue realizada en material de vidrio secado en horno bajo una atmósfera de nitrógeno. A una solución bien agitada de diisopropilamida de litio recién preparada (1M, 1,10 equiv.) en 35 ml de tetrahidrofurano seco, se añadió éster metílico de ácido isobutírico (3,32 g, 32,6 mmol, 1,0 equiv.) gota a gota durante 0,5 horas a -78 °C. Se dejó la mezcla en agitación a esta temperatura durante 30 min seguido de la adición de bromuro de alilo (5,35 g, 44,0 mmol) y hexametilfosforamida (HMPA) (2,91 g, 16,3 mmol) gota a gota durante 0,5 h. La mezcla reactiva se agitó durante toda la noche a temperatura ambiente, se desactivó con HCl al 10% (mientras se enfría en un baño de hielo) hasta que se vuelve ácida (pH = 2). Se separó la capa orgánica y la capa acuosa se extrajo con hexanos (3 x 100 mL). El extracto se lavó con NaHCO3 al 10% (200 mL) y salmuera (200 mL). La solución se secó entonces sobre MgSO4, se concentró al vacío y se destiló para dar un producto puro. 1H RMN (400 MHz, CDCls) ó 5,73 (dd, J = 9,4, 17,7, 1H), 5,04 (dd, J = 1,9, 13,5, 2H), 4,12 (q, J = 7,1, 2H), 2,28 (d, J = 7,4, 2H), 1,25 (t, J = 7 ,1,3H), 1,17 (s, 6H); 13C RMN (101 MHz, CDCla) ó 177,42, 134,42, 117,88, 77,68, 77,36, 77,04, 60,35, 44,91, 42,25, 24,92, 14,35.
[0072] Los compuestos siguientes se pueden preparar por el procedimiento del metil 2,2-dimetilpent-4-enoato. El profesional experto sabrá cómo sustituir los reactivos apropiados, los materiales de partida y los métodos de purificación conocidos por las personas expertas en la técnica, para preparar los compuestos provistos en la presente.
[0073] Preparación de etil 2,2-dietilpent-4-enoato: el compuesto del título se preparó según el procedimiento para el metil 2,2-dimetilpent-4-enoato, excepto porque el éster etílico del ácido 2-etil-butírico se sustituyó por éster metílico de ácido isobutírico 1H RMN (300 MHz, CDCls) ó 5,68 (dd, J = 9,9, 17,2, 1H), 5,16 - 4,97 (m, 2H), 4,14 (q, J = 7,1, 2H), 2,33 (d, J = 7,4, 2H), 1,59 (dt, J = 6,5, 7,5, 5H), 1,26 (t, J = 7,1, 3H), 0,80 (t, J = 7,5, 6H).
[0074] Los compuestos siguientes se pueden preparar por el procedimiento del ácido 1-alilciclobutanocarboxílico.
El profesional experto sabrá cómo sustituir los reactivos apropiados, los materiales de partida y los métodos de purificación conocidos por las personas expertas en la técnica, para preparar los compuestos provistos en la presente.
[0075] Preparación del ácido 1-alilciclopentanocarboxílico: el compuesto del título se preparó según el procedimiento para el ácido 1-alilciclobutanocarboxílico, excepto porque el ácido carboxílico de ciclopentano se sustituyó por ácido ciclobutanocarboxílico: 1H RMN (400 MHz, CDCb) ó 5,77 (ddt, J = 7,2, 10,2, 17,4, 1H), 5,17 -4,94 (m, 2H), 2,38 (d, J = 7,2, 2H), 2,20 - 2,02 (m, 2H), 1,79 - 1,47 (m, 6H), 13C RMN (101 MHz, CDCb) ó 184,94, 134,96, 118,02, 53,75, 42,96, 35,89, 25,47. Rf, 0,50 (hexano: acetato de etilo 10:1); HRMS (CI): [M+H], calc. para C9H15O2, 155,1072; encontrado 155,1068.
[0076] Los compuestos siguientes se pueden preparar por el procedimiento de la 5-(2-hidroxietil)-3,3-dimetil-dihidrofuran-2-ona. El profesional experto sabrá cómo sustituir los reactivos apropiados, los materiales de partida y los métodos de purificación conocidos por las personas expertas en la técnica, para preparar los compuestos provistos en la presente.
[0077] Preparación de 3,3-dietil-5-(2-hidroxietil)dihidrofuran-2(3H)-ona: el compuesto del titulo se preparó según el procedimiento para la 5-(2-hidroxi-etil)-3,3-dimetil-dihidro-furan-2-ona, excepto porque el etil 2,2-dietilpent-4-enoato se sustituyó por metil 2,2-dimetilpent-4-enoato: 1H RMN (400 MHz, CDCb ) ó 4,62 (dtd, J = 5,3, 7,3, 9,5, 1H), 3,78 (t, J = 6,1, 2H), 3,20 (s, 1H), 2,19 (dd, J = 6,8, 13,1, 1H), 1,97 - 1,81 (m, 3H), 1,70 - 1,56 (m, 4H), 0,93 (dt, J = 7,5, 20,7, 6H); 13C RMN (101 MHz, CDCb ) ó 181,46, 75,10, 58,91, 48,77, 39,13, 37,76, 29,21, 28,30, 8,83, 8,73; Rf, 0,36 (hexano: acetato de etilo 5:2); Anal. calc. para C10H18O3: C, 64, 49; H, 9,74; encontrado: C, 64,20; H, 9,57.
[0078] Preparación de 3-(2-hidroxietil)-2-oxaspiro[4.4]nonan-1-ona: el compuesto del título se preparó según el procedimiento para la 5-(2-hidroxi-etil)-3,3-dimetil-dihidro-furan-2-ona, excepto porque el ácido 1-alilciclopentanocarboxílico se sustituyó por metil 2,2-dimetilpent-4-enoato: 1H RMN (400 MHz, CDCb ) ó 4,65 - 4,56 (m, 1H), 3,84 - 3,76 (m, 2H), 2,74 (s, 1H), 2,28 (dd, J = 5,8, 12,6, 1H), 2,20 - 2,10 (m, 1H), 2,00 - 1,56 (m, 10H); 13C RMN (101 MHz, CDCb ) ó 183,02, 75,77, 59,20, 50,35, 43,41, 38,41, 37,49, 36,93, 25,67, 25,58; Rf, 0,46 (hexano: acetato de etilo 1:2); HRMS (CI): [M+H], calc. para C10H17O3, 185,1178; encontrado 185,1171.
[0079] Los compuestos siguientes se pueden preparar por el procedimiento del 2-(4,4-dimetil-5-oxotetrahidrofuran-2-il)etil 4-metilbencenosulfonato. El profesional experto sabrá cómo sustituir los reactivos apropiados, los materiales de partida y los métodos de purificación conocidos por las personas expertas en la técnica, para preparar los compuestos provistos en la presente.
[0080] Preparación de 2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil 4-metilbencenosulfonato: el compuesto del título se preparó según el procedimiento para el 2-(4,4-dimetil-5-oxotetrahidrofuran-2-il)etil 4-metilbencenosulfonato, excepto porque la 3,3-dietil-5-(2-hidroxietil)dihidrofuran-2(3H)-ona se sustituyó por 5-(2-hidroxi-etil)-3,3-dimetildihidro-furan-2-ona: 1H RMN (300 MHz, CDCb) ó 7,79 (d, J = 8,3 Hz, 2H), 7,36 (d, J = 8,0 Hz, 2H), 4,55 - 4,33 (m, 1H), 4,14 (dd, J = 6,5, 13,3 Hz, 3H), 2,46 (s, 3H), 2,21 - 1,84 (m, 3H), 1,83 - 1,68 (m, 1H), 1,58 (t, J = 7,4 Hz, 4H), 0,89 (dt, J = 7,5, 18,0 Hz, 6H); 13C RMN (101 MHz, CDCb) ó 180,33, 145,30, 132,72, 130,15, 128,03, 77,68, 77,36, 77,04, 73,18, 66,95, 48,67, 37,53, 35,82, 29,14, 28,23, 21,76, 8,81, 8,74. Anal. calc. para C17H24O5S: C, 59,98; H, 7,11; encontrado: C, 60,27; H, 7,25.
[0081] Preparación de 2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil 4-metilbencenosulfonato: el compuesto del título se preparó según el procedimiento para el 2-(4,4-dimetil-5-oxotetrahidrofuran-2-il)etil 4-metilbencenosulfonato, excepto porque la 3-(2-hidroxietil)-2-oxaspiro[4.4]nonan-1-ona se sustituyó por 5-(2-hidroxi-etil)-3,3-dimetil-dihidrofuran-2-ona: 1H RMN (400 MHz, CDCb ) ó 7,79 (d, J = 8,3 Hz, 2H), 7,36 (d, J = 8,0 Hz, 2H), 4,51 - 4,35 (m, 1H), 4,25 - 4,06 (m, 2H), 2,45 (s, 3H), 2,28 - 2,08 (m, 2H), 2,08 - 1,91 (m, 2H), 1,87 - 1,52 (m, 9H); 13C RMN (101 MHz, CDCÍb) ó 181,90, 145,26, 132,76, 130,12, 128,07, 73,71, 66,85, 50,19, 43,07, 37,44, 36,81, 35,19, 25,61, 25,50, 21,79.
[0082] Preparación de ácido 2,2-dietilpent-4-enoico: se mezcla etil 2,2-dietilpent-4-enoato (0,2 g, 0,28 mmol) con NaOH (0,4 g, 10 mmol), MeOH (2,5 mL) y H2O (2,5 mL) en un vial de microondas. La mezcla se calienta entonces en un reactor de microondas a 160 °C durante 2 horas. La mezcla se acidificó luego con HCl al 10%, se lavó con éter (3 x 30 ml). La fase orgánica combinada se secó sobre MgSO4 y se concentró al vacío para dar un producto bruto que se usó en el siguiente paso sin más purificación.
[0083] Preparación de 3,3-dietil-5-(yodometil)dihidrofuran-2(3H)-ona: el ácido 2,2-dietilpent-4-enoico (1,77 g, 11,67 mmol) se agita con tetrahidrofurano (34 mL), éter (12 mL) y solución de NaHCO3 saturada (57 mL). La mezcla se protege de la luz solar. Se disolvió I2 en 12 mL de tetrahidrofurano y se añadió a la mezcla en una parte a 0 °C. Se dejó la mezcla en agitación durante toda la noche a temperatura ambiente. El tiosulfato de sodio saturado se añade a la mezcla para detener la reacción. La mezcla se extrajo con acetato de etilo (3 x 50 mL). La fase orgánica combinada se secó sobre MgSO4 y se concentró al vacío para dar un aceite bruto que fue purificado por cromatografía en columna rápida (gel de sílice; acetato de etilo-hexanos, 0% ~ 25%). 1H RMN (400 MHz, CDCb ) ó 4,42 (dtd, J = 9,0, 7,3, 4,6 Hz, 1H), 3,41 (dd, J = 10,2, 4,6 Hz, 1H), 3,23 (dd, J = 10,2, 7,5 Hz, 1H), 2,25 (dd, J = 13,3, 6,9 Hz, 1H), 1,86 (dd, J = 13,3, 9,1 Hz, 1H), 1,63 (m, 4H), 0,94 (dt, J = 10,4, 7,5 Hz, 6H), MS (LC/MS, M+H+):
283,0.
[0084] Los compuestos siguientes se pueden preparar por el procedimiento de la 3,3-dietil-5-(yodometil)dihidrofuran-2(3H)-ona. El profesional experto sabrá cómo sustituir los reactivos apropiados, los materiales de partida y los métodos de purificación conocidos por las personas expertas en la técnica, para preparar los compuestos provistos en la presente.
[0085] Preparación de 3-(yodometil)-2-oxaspiro[4.4]nonan-1-ona: el compuesto del título se preparó según el procedimiento para la 3,3-dietil-5-(yodometil)dihidrofuran-2(3H)-ona, excepto porque el ácido 1-alilciclopentanocarboxílico se sustituyó por ácido 2,2-dietilpent-4-enoico: 1H RMN (400 MHz, CDCb) ó 4,48 - 4,34 (m, 1H), 3,39 (dd, J = 10,2, 4,9 Hz, 1H), 3,23 (dd, J = 10,2, 7,5 Hz, 1H), 2,35 (dd, J = 12,9, 6,1 Hz, 1H), 2,20 - 2,04 (m, 1H), 1,93 - 1,54 (m, 8H); 13C RMN (101 MHz, CDCb ) ó 181,57, 75,96, 50,71,43,44, 37,84, 36,89, 25,45, 25,36, 7,02; MS (LC/MS, M+H+): 281,0.
[0086] Preparación de 3-hidroxi-2-oxaspiro[4.4]nonan-1-ona: a una mezcla agitada de ácido 1-alilciclopentanocarboxílico (10,93 g, 71 mmol, 1 equiv.), solución madre de RuCb (0,514 g, 0.035 M en agua, 0.035
equiv.) y CH3CN (500 mL), se añadió NalCM (30,8 g, 142 mmol, 2,04 equiv.) por partes durante un periodo de 30 min a temperatura ambiente. Se dejó la suspensión en agitación a temperatura ambiente durante otros 30 min. La reacción se desactivó con solución acuosa saturada de Na2S2O3 y las dos capas fueron separadas. La capa acuosa se extrajo con EtOAc (3 x 200 mL). La capa orgánica combinada se lavó con salmuera, se secó sobre MgSO4 anhidro, se filtró y se concentró. El residuo fue purificado por cromatografía rápida en columna (gel de sílice; acetato de etilo/hexanos, 10% ~ 50%) para dar el producto deseado. 1H RMN (400 MHz, CDCb ) ó 5,87 (s, 1H), 5,28 (s, 1H), 2,06 (dd, J = 35,1,28,9 Hz, 4H), 1,90 - 1,44 (m, 6H); 13C RMN (101 MHz, CDCb) ó 183,20, 49,58, 43,94, 38,28, 25,42.
[0087] Los compuestos siguientes se pueden preparar por el procedimiento de la 3-hidroxi-2-oxaspiro[4.4]nonan-1-ona. El profesional experto sabrá cómo sustituir los reactivos apropiados, los materiales de partida y los métodos de purificación conocidos por las personas expertas en la técnica, para preparar los compuestos provistos en la presente.
[0088] Preparación de 3-(but-3-en-1-il)-2-oxaspiro[4.4]nonan-1-ona: esta reacción fue realizada en material de vidrio secado en horno bajo una atmósfera de nitrógeno. A una solución bien agitada de reactivo de Grignard bromuro de but-1-eno magnesio (96 mmol, 1M, 3 equiv.) recién preparado en éter seco, se añadió 3-hidroxi-2-oxaspiro[4.4]nonan-1-ona (5,0 g, 32,0 mmol, 1,0 equiv.) gota a gota durante 0,5 horas a 0 °C. La mezcla reactiva se agitó durante toda la noche a temperatura ambiente, se desactivó con HCl al 10% (mientras se enfría en un baño de hielo) hasta que se vuelve ácida (pH = 2). La capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (3 x 200 mL). El extracto se lavó con NaHCO3 al 10% (100 mL) y salmuera (200 mL). La solución se secó entonces sobre MgSO4, se concentró al vacío y se purificó por cromatografía rápida en columna (gel de sílice; acetato de etilo/hexanos, 0% ~ 25%) para dar el producto deseado. 1H RMN (400 MHz, CDCb ) ó 5,79 (ddt, J = 16,9, 10,2, 6,7 Hz, 1H), 5,15 - 4,88 (m, 2H), 4,36 (ddt, J = 9,7, 7,9, 5,5 Hz, 1H), 2,18 (m, 4H), 1,93 - 1,46 (m, 10H); 13C RMN (101 MHz, CDCb) ó 182,55, 137,26, 115,62, 77,19, 50,28, 43,24, 37,51, 36,91, 34,83, 29,70, 25,56, 25,47.
[0089] Los compuestos siguientes se pueden preparar por el procedimiento de la 3-(but-3-en-1-il)-2-oxaspiro[4.4]nonan-1-ona. El profesional experto sabrá cómo sustituir los reactivos apropiados, los materiales de partida y los métodos de purificación conocidos por las personas expertas en la técnica, para preparar los compuestos provistos en la presente.
[0090] Preparación de 3-(1-oxo-2-oxaspiro[4.4]nonan-3-il)propil 4-metilbencenosulfonato: a una mezcla agitada de 3-(but-3-en-1-il)-2-oxaspiro[4.4]nonan-1-ona (0,194 g, 1 mmol, 1 equiv.), solución madre de RuCb (7,2 mg, 0,035 M en agua, 0,035 equiv.) y CH3CN (6 mL), se le añadió NaIO4 (434 mg, 2,04 mmol, 2,04 equiv.) por partes durante un periodo de 5 min a temperatura ambiente. Se dejó la suspensión en agitación a temperatura ambiente durante otros 30 min. La reacción se desactivó con solución acuosa saturada de Na2S2O3 y se separaron las dos capas. La capa acuosa se extrajo con EtOAc (3 x 20 mL). La capa orgánica combinada se lavó con salmuera, se secó sobre MgSO4 anhidro, se filtró y se concentró. El aldehído bruto se usó para el paso siguiente sin más purificación.
[0091] Esta reacción se realizó en material de vidrio secado en horno bajo una atmósfera de nitrógeno. A una solución bien agitada del aldehído bruto (0,196 g, 1 mmol, 1 equiv.) en metanol seco, se añadió a la mezcla NaBH4 (74 mg, 2,0 mmol, 2 equiv.) en una parte a 0 °C. La mezcla reactiva se agitó a temperatura ambiente durante otra 1 h, se desactivó con salmuera (mientras se enfría en un baño de hielo). La capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (3 x 20 mL). La fase orgánica combinada se secó entonces sobre MgSO4, se concentró al vacío. El alcohol bruto se usó para el paso siguiente sin más purificación.
[0092] A una solución agitada del alcohol bruto (0,396 g, 2 mmol, 1,0 equiv.) y Et3N (0,303 g, 3 mmol, 1,5 equiv.) en diclorometano seco, se añadió una solución de p-TosCl (0,475 g, 2,5 mmol, 1,25 equiv.) en diclorometano gota a gota a 0 °C. La mezcla resultante se agitó a 0 °C durante 1 hora y se dejó en agitación durante toda la noche a temperatura ambiente. Luego, la mezcla reactiva se diluyó con diclorometano (50 mL), se lavó con HCl al 10 %, salmuera, se secó sobre MgSO4 y se concentró al vacío para proporcionar un aceite amarillento. Este producto bruto fue purificado luego por cromatografía en columna rápida (gel de sílice; acetato de etilo/hexanos, 0% ~ 40%)
para proporcionar el tosilato deseado. 1H RMN ((400 MHz, CDCb) 57,82 - 7,71 (m, 2H), 7,35 (m, 2H), 4,37 - 4,23 (m, 1H), 4,06 (qdd, J = 10,0, 6,7, 5,2 Hz, 2H), 2,45 (s, 3H), 2,15 (m, 2H), 1,92 - 1,50 (m, 12H); 13C RMN (101 MHz, CDCb ) 5 182,29, 145,03, 133,05, 130,04, 128,00, 76,90, 69,91, 50,24, 43,20, 37,53, 36,92, 31,74, 25,59, 25,49, 25,37, 21,76.
[0093] Los compuestos siguientes se pueden preparar por el procedimiento del 3-(1-oxo-2-oxaspiro[4.4]nonan-3-il)propil 4-metilbencenosulfonato. El profesional experto sabrá cómo sustituir los reactivos apropiados, los materiales de partida y los métodos de purificación conocidos por las personas expertas en la técnica, para preparar los compuestos provistos en la presente.
[0094] Preparación de 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1 -il)benzonitrilo: se trató 2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil 4-metilbencenosulfonato (0,102 g, 0,3 mmol, 1,0 equiv.) con 2-piperazin-1-ilbenzonitrilo (168,3 mg, 0,9 mmol, 3,0 equiv.) en tetrahidrofurano seco y se sometió a reflujo durante 72 horas. El tetrahidrofurano se evaporó bajo presión reducida, el residuo se disolvió en diclorometano, se lavó con H2O, y salmuera, se secó luego sobre MgSO4 y se concentró al vacío para dar un producto bruto que fue purificado por cromatografía en columna rápida (gel de sílice; 2 % ~ 8 % MeOH en diclorometano) para proporcionar producto puro. El producto purificado se disolvió luego en éter y se trató con solución de HCl (2,0 M en éter dietílico) para proporcionar la sal de hidrocloruro que se recristalizó con isopropanol o una mezcla de MeOH/éter. 1H RMN (400 MHz, CDCb ) 57,62 - 7,42 (m, 2H), 7,01 (dd, J = 7,8, 5,0 Hz, 2H), 4,48 (dq, J = 9,2, 6,7 Hz, 1H), 3,35 - 3,17 (m, 4H), 2,81 - 2,51 (m, 6H), 2,14 (dd, J = 13,1, 6,8 Hz, 1H), 1,86 (m, 3H), 1,67 - 1,53 (m, 4H), 0,92 (dt, J = 20,1, 7,5 Hz, 6H); 13C RMN (101 MHz, CDCb ) 5180,82, 155,57, 134,43, 133,95, 122,03, 118,81, 118,50, 106,13, 75,50, 54,44, 53,22, 51,34, 48,71, 37,75, 33,60, 29,35, 28,39, 8,89, 8,81; MS (LC/MS, M+H+): 356,2.
[0095] Los compuestos siguientes se pueden preparar por el procedimiento del 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo. El profesional experto sabrá cómo sustituir los reactivos apropiados, los materiales de partida y los métodos de purificación conocidos por las personas expertas en la técnica, para preparar los compuestos provistos en la presente.
[0096] Preparación de la 3,3-dietil-5-(2-(4-(4-metoxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona: el compuesto del título se preparó según el procedimiento para el 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo, excepto porque la 1-(4-metoxi-fenil)-piperazina se sustituyó por 2-piperazin-1 -il-benzonitrilo: 1H RMN (400 MHz, CDCb ) 56,95 - 6,75 (m, 4H), 4,48 (ddd, J = 19,8, 8,4, 6,4 Hz, 1H), 3,76 (s, 3H), 3,14 - 2,99 (m, 4H), 2,67 - 2,46 (m, 6H), 2,15 - 2,07 (m, 1H), 1,92 - 1,79 (m, 3H), 1,62 (qd, J = 7,4, 4,7 Hz, 4H), 0,97 - 0,88 (m, 6H); 13C RMN (101 MHz, CDCb ) 5180,90, 153,93, 145,74, 118,29, 114,53, 75,71,55,67, 54,59, 53,51,50,69, 48,72, 37,81,33,91, 29,35, 28,41, 8,90, 8,82. MS (LC/MS, M+H+): 361,2.
[0097] Preparación de dihidrocloruro de 3,3-dietil-5-(2-(4-(4-hidroxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona: el compuesto del título se preparó según el procedimiento para el 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo, excepto porque el 4-piperazin-1 -il-fenol se sustituyó por 2-piperazin-1 -ilbenzonitrilo: 1H RMN (400 MHz, D2O) 57,16 (d, J = 9,0, 2H), 6,94 (d, J = 9,0, 2H), 4,71 (d, J = 10,6, 1H), 3,46 (ddd, J = 15,7, 16,9, 22,4, 10H), 2,36 (dd, J = 6,9, 13,5, 1H), 2,23 (dd, J = 9,2, 19,4, 2H), 2,01 (dd, J = 9,4, 13,5, 1H), 1,77 - 1,50 (m, 4H), 0,90 (dt, J = 7,5, 12,5, 6H); 13C RMN (101 MHz, D2O) 5 187,92, 155,62, 143,21, 123,52, 119,36, 79,53, 56,53, 54,17, 52,42, 52,07, 39,38, 32,83, 31,92, 30,68, 11,00, 10,87; MS (LC/MS, M+H+): 347,2. Anal. calc. para C20H32ChN2Oa: C, 57,28; H, 7,69; N, 6,68; encontrado: C, 57,53; H, 7,74; N, 6,62.
[0098] Preparación de hidrocloruro de 3,3-dietil-5-(2-(4-(4-nitrofenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona: el compuesto del título se preparó según el procedimiento para el 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo, excepto porque la 1-(4-nitro-fenil)-piperazina se sustituyó por 2-piperazin-1-ilbenzonitrilo: 1H RMN (400 MHz, MeOH) ó 8,15 (d, J = 9,3, 2H), 7,11 (d, J = 9,4, 2H), 4,59 (dd, J = 3,6, 6,5, 1H), 4,37 - 3,08 (m, 10H), 2,36 - 2,21 (m, 2H), 2,21 - 2,08 (m, 1H), 1,95 (dd, J = 9,4, 13,2, 1H), 1,75 - 1,52 (m, 4H), 0,94 (dt, J = 7,5, 13,2, 6H); 13C RMN (101 MHz, MeOH) ó 183,19, 156,05, 141,97, 127,53, 116,10, 77,01, 55,81, 53,54, 50,77, 50,50, 50,29, 50,07, 49,86, 49,65, 49,43, 49,22, 46,59, 39,19, 32,57, 30,89, 30,03, 9,85, 9,77; MS (LC/MS, M+H+): 376,2.
[0099] Preparación de dihidrocloruro de 3,3-dietil-5-(2-(4-(2-metoxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona: el compuesto del título se preparó según el procedimiento para el 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo, excepto porque la 1-(2-metoxi-fenil)-piperazina se sustituyó por 2-piperazin-1-ilbenzonitrilo: 1H RMN (400 MHz, D2O) ó 7,06 (ddd, J = 7,8, 7,2, 1,5 Hz, 2H), 6,96 (dd, J = 8,1, 1,3 Hz, 1H), 6,93 -6,82 (m, 1H), 4,50 (dt, J = 9,2, 7,5 Hz, 1H), 3,80 (s, 3H), 3,72 - 3,22 (m, 10H), 2,28 - 2,10 (m, 2H), 2,10 - 1,96 (m, 1H), 1,86 (dd, J = 13,3, 9,4 Hz, 1H), 1,68 - 1,42 (m, 4H), 1,00 - 0,75 (m, 6H); 13C RMN (101 MHz, D2O) ó 182,35, 153,90, 138,69, 126,90, 122,35, 120,49, 113,32, 76,15, 56,21, 54,97, 53,20, 49,93, 49,35, 38,35, 31,74, 30,05, 29,19, 9,00, 8,91; MS (LC/MS, M+H+): 361,2; Anal. calc. para C21Ha4Cl2N2Oa: C, 58,20; H, 7,91; N, 6,46; encontrado: C, 58,05; H, 7,95; N, 6,39.
[0100] Preparación de hidrocloruro de 4-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo: el compuesto del título se preparó según el procedimiento para el 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo, excepto porque el 4-piperazin-1 -il-benzonitrilo se sustituyó por 2-piperazin-1-ilbenzonitrilo: 1H RMN (400 MHz, MeOD) ó 7,69 - 7,54 (m, 2H), 7,23 - 7,02 (m, 2H), 4,59 (ddd, J = 15,8, 9,3, 3,7 Hz, 1H), 4,31 - 3,30 (m, 10H), 2,36 - 2,21 (m, 2H), 2,21 - 2,06 (m, 1H), 1,96 (dd, J = 13,3, 9,4 Hz, 1H), 1,65 (ddd, J = 17,4, 8,7, 6,2 Hz, 4H), 0,95 (dt, J = 13,3, 7,5 Hz, 6H); 13C RMN (101 MHz, MeOD) ó 182,32, 153,74, 134,73, 120,40, 116,55, 102,99, 76,15, 54,93, 52,76, 49,91, 45,91,38,33, 31,73, 30,04, 29,17, 9,00, 8,91; MS (LC/MS, M+H+): 356,2; Anal. calc. para C21H30ClNaO2: C, 64,35; H, 7,72; N, 10,72; encontrado: C, 64,46; H, 7,65; N, 10,65.
[0101] Preparación de dihidrocloruro de 3,3-dietil-5-(2-(4-(2-hidroxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona: el compuesto del título se preparó según el procedimiento para el 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo, excepto porque el 2-piperazin-1 -il-fenol se sustituyó por 2-piperazin-1 -ilbenzonitrilo: 1H RMN (400 MHz, D2O) ó 7,35 - 7,16 (m, 2H), 7,00 (m, 2H), 4,74 - 4,65 (m, 1H), 3,91 - 3,34 (m, 10H), 2,40 - 2,10 (m, 3H), 1,99 (dd, J = 13,5, 9,4 Hz, 1H), 1,72 - 1,48 (m, 4H), 0,87 (dt, J = 13,0, 7,5 Hz, 6H); 13C RMN (101 MHz, D2O) ó 185,26, 149,63, 133,87, 128,39, 121,34, 120,76, 116,89, 76,88, 53,96, 51,49, 49,77, 48,95, 36,75, 30,19, 29,27, 28,04, 8,37, 8,24; MS (LC/MS, M+H+): 347,2; Anal. calc. para C20H32ChN2O3: C, 57,28; H, 7,69; N, 6,68; encontrado: C, 57,37; H, 7,64; N, 6,59.
[0102] Preparación de dihidrocloruro de 5-(2-(4-(4-aminofenil)piperazin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona: el compuesto del título se preparó según el procedimiento para el 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo, excepto porque la 4-piperazin-1-il-fenilamina se sustituyó por 2-piperazin-1-ilbenzonitrilo: 1H RMN (400 MHz, MeOD) ó 7,31 (d, J = 9,0 Hz, 2H), 7,16 (d, J = 9,0 Hz, 2H), 4,58 (ddd, J = 15,9, 9,3, 3,8 Hz, 1H), 4,06 - 3,30 (m, 10H), 2,38 - 2,06 (m, 3H), 1,95 (dd, J = 13,3, 9,4 Hz, 1H), 1,78 - 1,50 (m, 4H), 0,94 (dt, J = 13,4, 7,5 Hz, 6H); 13C RMN (101 MHz, MeOD) ó 182,43, 151,41, 124,89, 124,66, 118,73, 76,22, 54,91, 53,06, 49,94, 47,42, 38,34, 31,72, 30,04, 29,17, 9,00, 8,92. MS (LC/MS, M+H+): 346,2.
[0103] Preparación de dihidrocloruro de 3,3-dietil-5-(2-(4-(p-tolil)piperazin-1 -il)etil)dihidrofuran-2(3H)-ona: el compuesto del título se preparó según el procedimiento para el 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo, excepto porque la 1-p-tolil-piperazina se sustituyó por 2-piperazin-1 -il-benzonitrilo:
1H RMN (400 MHz, MeOD) ó 7,25 - 7,13 (m, 4H), 4,62 - 4,45 (m, 1H), 4,05 - 3,28 (m, 10H), 2,30 - 2,01 (m, 6H), 1,88 (dd, J = 13,3, 9,4 Hz, 1H), 1,58 (m, 4H), 0,87 (dt, J = 13,7, 7,5 Hz, 6H); 13C RMN (101 MHz, MeOD) ó 182,36, 144,75, 136,86, 131,47, 119,95, 76,10, 54,89, 52,04, 50,53, 49,93, 38,31, 31,68, 30,03, 29,17, 20,76, 9,01, 8,92;
MS (LC/MS, M+H+): 345,2; Anal. calc. para C21Ha4ChN2O2: C, 60,43; H, 8,21; N, 6,71; encontrado: C, 60,33; H, 8,20; N, 6,61.
[0104] Preparación de dihidrocloruro de 3,3-dietil-5-(2-(4-(3-metoxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona: el compuesto del título se preparó según el procedimiento para el 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo, excepto porque la 1-(3-metoxi-fenil)-piperazina se sustituyó por 2-piperazin-1 -ilbenzonitrilo: 1H RMN (400 MHz, DMSO) ó 7,16 (t, J = 8,2 Hz, 1H), 6,65 - 6,35 (m, 3H), 4,54 (s, 1H), 3,82 (d, J = 8,9 Hz, 3H), 3,57 (s, 2H), 3,16 (dd, J = 27,5, 16,8 Hz, 6H), 2,28 - 2,04 (m, 3H), 1,82 (dd, J = 13,1, 9,4 Hz, 1H), 1,64 -1,44 (m, 4H), 0,85 (dt, J = 10,2, 7,5 Hz, 6H); 13C RMN (101 MHz, MeOD) ó 182,37, 162,23, 149,87, 131,32, 76,14, 55,89, 54,87, 52,48, 49,92, 38,31, 31,69, 30,03, 29,17, 9,01, 8,92. MS (LC/MS, M+H+): 361,2; Anal. calc. para C21Ha4Cl2N2Oa: C, 58,20; H, 7,91; N, 6,46; encontrado: C, 58,24; H, 7,93; N, 6,46.
[0105] Preparación de dihidrocloruro de 3,3-dietil-5-(2-(4-(3-hidroxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona: el compuesto del título se preparó según el procedimiento para el 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo, excepto porque el 3-piperazin-1-il-fenol se sustituyó por 2-piperazin-1-ilbenzonitrilo: 1H RMN (400 MHz, DMSO) ó 6,93 (t, J = 8,1, 1H), 6,33 (d, J = 8,2, 1H), 6,27 (s, 1H), 6,21 (d, J = 7,9, 1H), 4,43 (s, 10H), 3,64 (s, 2H), 3,47 (s, 2H), 3,12 (s, 2H), 3,00 (d, J = 9,1, 4H), 2,16 - 1,92 (m, 3H), 1,78 - 1,67 (m, 1H), 1,44 (dd, J = 7,4, 23,5, 4H), 0,75 (dt, J = 7,4, 10,3, 6H); 13C RMN (101 MHz, MeOD) ó 179,73, 158,25, 150,60, 129,75, 107,64, 107,07, 103,23, 74,26, 51,93, 50,56, 50,39, 45,47, 36,40, 29,62, 28,26, 27,58, 8,50, 8,45; MS (LC/MS, M+H+): 347,2; Anal. calc. para C20Ha2Cl2N2Oa: C, 57,28; H, 7,69; N, 6,68; encontrado: C, 57,33; H, 7,76;
N, 6,62.
[0106] Preparación de hidrocloruro de 5-(2-(4-(2,6-dimetilfenil)piperazin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona: el compuesto del título se preparó según el procedimiento para el 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo, excepto porque la 1-(2,6-dimetil-fenil)-piperazina se sustituyó por 2-piperazin-1-ilbenzonitrilo: 1H RMN (400 MHz, MeOH) ó 6,99 (s, 3H), 4,59 (ddd, J = 16,1, 9,4, 3,8 Hz, 1H), 3,99 - 3,32 (m, 8H), 3,27 - 2,98 (m, 2H), 2,39 - 2,05 (m, 9H), 1,96 (dd, J = 13,3, 9,4 Hz, 1H), 1,65 (m, 4H), 0,95 (dt, J = 14,7, 7,5 Hz, 6H); 13C RMN (101 MHz, MeOH) ó 182,40, 147,75, 127,37, 76,24, 55,23, 54,81, 54,72, 49,92, 48,11, 38,34, 31,75,
30,05, 29,18, 9,01, 8,92; MS (LC/MS, M+H+): 359,3; Anal. calc. para C22H35CIN2O2: C, 66,90; H, 8,93; N, 7,09; encontrado: C, 66,76, H, 8,89, N, 7,01.
[0107] Preparación de dihidrocloruro de 3,3-dietil-5-(2-(4-(o-tolil)piperazin-1 -il)etil)dihidrofuran-2(3H)-ona: el compuesto del título se preparó según el procedimiento para el 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1 -il)benzonitrilo, excepto porque la 1 -o-tolil-piperazina se sustituyó por 2-piperazin-1 -il-benzonitrilo: 1H RMN (400 MHz, MeOD) 67,21 - 6,90 (m, 4H), 4,62 - 4,45 (m, 1H), 3,65 (dd, J = 9,6, 5,4 Hz, 2H), 3,43 - 3,26 (m, 4H), 3,24 - 3,07 (m, 4H), 2,34 - 2,02 (m, 6H), 1,90 (dd, J = 13,3, 9,4 Hz, 1H), 1,60 (ddd, J = 17,2, 8,6, 6,4 Hz, 4H), 0,89 (dt, J = 14,0, 7,5 Hz, 6H); 13C RMN (101 MHz, MeOD) 6 182,40, 150,67, 134,07, 132,33, 127,96, 125,84, 120,39, 76,21, 54,96, 54,81, 53,99, 53,80, 50,26, 49,93, 38,33, 31,77, 30,05, 29,18, 17,84, 9,01, 8,92; MS (LC/MS, M+H+): 345,3.
[0108] Preparación de hidrocloruro de 3,3-dietil-5-(2-(4-(2-isopropilfenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona: el compuesto del título se preparó según el procedimiento para el 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo, excepto porque la 1-(2-isopropil-fenil)-piperazina se sustituyó por 2-piperazin-1 -ilbenzonitrilo: 1H RMN (400 MHz, DMSO) 67,30 (dd, J = 7,4, 1,6 Hz, 1H), 7,23 - 7,08 (m, 3H), 4,66 - 4,43 (m, 1H), 3,54 (t, J = 9,6 Hz, 2H), 3,41 (dd, J = 13,7, 6,8 Hz, 1H), 3,33 - 3,12 (m, 6H), 3,02 (d, J = 10,7 Hz, 2H), 2,31 - 2,03 (m, 3H), 1,83 (dd, J = 13,2, 9,3 Hz, 1H), 1,69 - 1,34 (m, 4H), 1,16 (d, J = 6,9 Hz, 6H), 0,85 (dt, J = 10,6, 7,5 Hz, 6H); 13C RMN (101 MHz, DMSO) 6 179,77, 148,90, 143,85, 126,51, 125,20, 120,36, 74,31, 52,05, 51,57, 51,43, 49,55, 47,87, 36,43, 29,72, 28,36, 27,66, 26,24, 23,99, 8,55, 8,51; MS (LC/MS, M+H+): 373,3.
[0109] Preparación de hidrocloruro de 5-(2-(4-(2,4-dimetilfenil)piperazin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona: el compuesto del título se preparó según el procedimiento para el 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo, excepto porque la 1-(2,4-dimetil-fenil)-piperazina se sustituyó por 2-piperazin-1 -ilbenzonitrilo: 1H RMN (400 MHz, DMSO) 67,11 - 6,75 (m, 3H), 4,55 (dt, J = 11,8, 8,4 Hz, 1H), 3,53 (m, 2H), 3,33 -3,02 (m, 8H), 2,31 - 2,07 (m, 9H), 1,83 (dd, J = 13,2, 9,3 Hz, 1H), 1,67 - 1,39 (m, 4H), 0,85 (dt, J = 10,6, 7,5 Hz, 6H); 13C RMN (101 MHz, DMSO) 6 179,75, 147,31, 132,64, 131,80, 131,62, 127,05, 118,82, 74,31, 52,11, 51,55, 51,38, 48,24, 47,85, 36,44, 29,71, 28,33, 27,64, 20,32, 17,27, 8,54, 8,49; MS (LC/MS, M+H+): 359,3.
[0110] Preparación de hidrocloruro de 3-(2-(4-(2-isopropilfenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona: el compuesto del título se preparó según el procedimiento para el 2-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo, excepto porque la 1-(2-isopropil-fenil)-piperazina se sustituyó por 2-piperazin-1 -ilbenzonitrilo, y el 2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil 4-metilbencenosulfonato se sustituyó por 2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil 4-metilbencenosulfonato: 1H RMN (400 MHz, D2O) 6 7,51-7,39 (m, 1h), 7,25 (m, 3H), 4,68 (m, 1H), 3,78 - 3,08 (m, 11H), 2,42 (dd, J = 12,8, 6,0 Hz, 1H), 2,22 (m, 2H), 2,09 - 1,93 (m, 2H), 1,90 - 1,60 (m, 7H), 1,20 (d, J = 6,9 Hz, 6H); 13C RMN (101 MHz, D2O) 6 189,43, 147,87, 130,06, 129,92, 129,00, 123,54, 79,88, 53,51, 52,89, 44,63, 40,17, 39,34, 32,14, 29,56, 28,12, 28,06, 26,11; MS (LC/MS, M+H+): 371,3.
[0111] Los compuestos siguientes se pueden preparar por el procedimiento de la 5-(2-(4-(1H-benzo[d]imidazol-2-il)piperidin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona. El profesional experto sabrá cómo sustituir los reactivos apropiados, los materiales de partida y los métodos de purificación conocidos por las personas expertas en la técnica, para preparar los compuestos provistos en la presente.
[0112] Preparación de 3-(2-(4-(2-(tert-butil)fenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona: el compuesto del título se preparó según el procedimiento para la 5-(2-(4-(1H-benzo[d]imidazol-2-il)piperidin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona, excepto porque la 1-(2-tert-butil-fenil)-piperazina se sustituyó por 2-piperazin-1-ilbenzonitrilo y el 2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil 4-metilbencenosulfonato se sustituyó por 2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil 4-metilbencenosulfonato: 1H RMN (400 MHz, CDCb ) 67,41-7,30 (m, 2H), 7,21 (m, 1H), 7,17 - 7,08 (m, 1H), 4,58 - 4,37 (m, 1H), 3,07 - 2,94 (m, 2H), 2,87 (m, 2H), 2,80 (m, 2H), 2,59 (m, 2H), 2,42 - 2,12 (m, 4H), 2,04 - 1,56 (m, 10H), 1,43 (s, 9H); 13C RMN (101 MHz, CDCb) 6182,54, 153,27, 147,62, 127,00, 126,92, 126,09, 125,75, 76,36, 54,86, 54,15, 54,06, 53,66, 50,26, 43,41, 37,58, 37,04, 35,67, 33,18, 30,95, 25,63, 25,55;
MS (LC/MS, M+H+): 385,1.
[0113] Preparación de 3-(2-(4-(2,6-diisopropilfenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona: el compuesto del título se preparó según el procedimiento para la 5-(2-(4-(1H-benzo[d]imidazol-2-il)piperidin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona, excepto porque la 1-(2,6-diisopropil-fenil)-piperazina se sustituyó por 2-piperazin-1-ilbenzonitrilo y el 2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil 4-metilbencenosulfonato se sustituyó por 2-(4,4-dietil-5-oxotetra hidrofu ran-2-il)etil 4-metilbencenosulfonato: 1H RMN (400 MHz, CDCb ) 67,17 (m, 1H), 7,12 - 7,05 (m, 2H), 4,49 (tt, J = 8,2, 5,6 Hz, 1H), 3,48 (dt, J = 13,8, 6,9 Hz, 2H), 3,22 - 3,07 (ancho, 4H), 2,58 (m, 6H), 2,32 - 2,11 (m, 2H), 2,01 - 1,58 (m, 10H), 1,19 (d, J = 6,9 Hz, 12H); 13C RMN (101 MHz, CDCb) 6 149,23, 126,71, 124,09, 76,42, 55,23, 54,64, 51,03, 50,26, 43,44, 37,61, 37,09, 33,18, 28,28, 25,64, 25,55, 24,44; MS (LC/MS, M+H+): 413,2.
[0114] Preparación de 3-(2-(4-(2-morfolinofenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona: el compuesto del título se preparó según el procedimiento para la 5-(2-(4-(1H-benzo[d]imidazol-2-il)piperidin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona, excepto porque la 4-(2-piperazin-1-il-fenil)-morfolina se sustituyó por 2-piperazin-1-ilbenzonitrilo y el 2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil 4-metilbencenosulfonato se sustituyó por 2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil 4-metilbencenosulfonato: 1H RMN (400 MHz, CDCb) 67,12-6,82 (m, 4H), 4,58 - 4,43 (m, 1H), 3,96 - 3,74 (m, 4H), 3,18 (ancho, 8H), 2,76 - 2,41 (m, 6H), 2,35 - 2,08 (m, 2H), 2,02 - 1,55 (m, 10H); 13C RMN (101 MHz, CDCb ) 6 182,46, 144,70, 144,54, 123,15, 123,05, 118,70, 118,30, 76,27, 67,70, 54,75, 54,10, 50,20, 50,02, 49,41,43,35, 37,52, 36,99, 33,15, 25,58, 25,49; MS (LC/MS, M+H+): 414,1.
[0115] Preparación de 3-(2-(4-([1,1'-bifenil]-2-il)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona: el compuesto del título se preparó según el procedimiento para la 5-(2-(4-(1H-benzo[d]imidazol-2-il)piperidin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona, excepto porque la 1-bifenil-2-il-piperazina se sustituyó por 2-piperazin-1-il-benzonitrilo y el 2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil 4-metilbencenosulfonato se sustituyó por 2-(4,4-dietil-5-oxotetra hidrofu ran-2-il)etil 4-metilbencenosulfonato: 1H RMN (400 MHz, CDCb ) 6 7,55 (dd, J = 5,1, 3,3 Hz, 2H),
7,31 (dd, J = 10,4, 4,7 Hz, 2H), 7,20 (m, 3H), 6,98 (m, 2H), 4,44 - 4,23 (m, 1H), 2,77 (ancho, 4H), 2,49 - 2,17 (m, 6H), 2,10 (d, J = 5,8 Hz, 2H), 1,86 - 1,42 (m, 10H); 13C RMN (101 MHz, CDCb) 6182,45, 150,24, 141,23, 135,03, 131,55, 128,93, 128,37, 128,26, 126,82, 122,72, 118,27, 76,26, 54,59, 53,43, 50,98, 50,18, 43,32, 37,51, 36,98, 33,08, 25,57, 25,49; MS (LC/MS, M+H+): 405,1.
[0116] Preparación de 3-(2-(4-(2-(1H-pirrol-1-il)fenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona: el compuesto del título se preparó según el procedimiento para la 5-(2-(4-(1H-benzo[d]imidazol-2-il)piperidin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona, excepto porque la 1-(2-pirrol-1-il-fenil)-piperazina se sustituyó por 2-piperazin-1-ilbenzonitrilo y el 2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil 4-metilbencenosulfonato se sustituyó por 2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil 4-metilbencenosulfonato: 1H RMN (400 MHz, CDCb) 67,23-7,06 (m, 2H), 7,05 - 6,89 (m, 4H), 6,20 (m, 2H), 4,45 - 4,26 (m, 1H), 2,64 (ancho, 4H), 2,51-2,28 (m, 6H), 2,19 - 1,95 (m, 2H), 1,91 - 1,45 (m, 10H); 13C RMN (101 MHz, CDCb ) 6182,47, 146,37, 133,69, 127,59, 126,62, 122,56, 121,25, 118,90, 109,06, 76,23, 54,55, 53,55, 50,19, 49,97, 43,33, 37,51, 36,98, 33,04, 25,58, 25,49; MS (LC/MS, M+H+): 394,1.
[0117] Preparación de 3-(2-(4-(2-yodofenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona: el compuesto del título se preparó según el procedimiento para la 5-(2-(4-(1H-benzo[d]imidazol-2-il)piperidin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona, excepto porque la 1-(2-yodo-fenil)-piperazina se sustituyó por 2-piperazin-1 -il-benzonitrilo y el 2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil 4-metilbencenosulfonato se sustituyó por 2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil 4-metilbencenosulfonato: 1H RMN (400 MHz, CDCb ) 67,84 (dd, J = 7,8, 1,4 Hz, 1H), 7,31 (td, J = 7,9, 1,5 Hz, 1H), 7,04 (dd, J = 8,0, 1,4 Hz, 1H), 6,79 (td, J = 7,7, 1,5 Hz, 1H), 4,59 - 4,39 (m, 1H), 3,02 (ancho, 4H), 2,79 - 2,47 (m, 6H), 2,31 - 2,09 (m, 2H), 2,00 - 1,54 (m, 10H); 13C RMN (101 MHz, CDCb ) 6182,51, 153,44, 140,20, 129,34, 125,59, 121,13, 98,29, 76,29, 54,63, 53,58, 52,34, 50,27, 43,43, 37,59, 37,05, 33,13, 25,64, 25,56; MS (LC/MS, M+H+): 455,0.
[0118] Preparación de N-(2-(4-(2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil)piperazin-1-il)fenil)acetamida: el compuesto del título se preparó según el procedimiento para la 5-(2-(4-(1H-benzo[d]imidazol-2-il)piperidin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona, excepto porque la N-(2-piperazin-1-il-fenil)-acetamida se sustituyó por 2-piperazin-1 -ilbenzonitrilo y el 2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil 4-metilbencenosulfonato se sustituyó por 2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil 4-metilbencenosulfonato: 1H RMN (400 MHz, CDCb) 68,45 (s, 1H), 8,33 (d, J = 8,0 Hz, 1H), 7,22 - 7,08 (m, 2H), 7,08 - 6,99 (m, 1H), 4,56 - 4,43 (m, 1H), 2,89 (ancho, 4H), 2,61 (m, 6H), 2,31 - 2,09 (m, 5H), 1,98 - 1,54 (m, 10H); 13C RMN (101 MHz, CDCb ) 6 182,47, 168,16, 140,92, 133,63, 125,67, 123,81, 120,55, 119,59, 76,13, 54,68, 54,21, 52,25, 50,26, 43,40, 37,59, 37,04, 33,21, 25,63, 25,54, 25,09; MS (LC/MS, M+H+): 386,1.
[0119] Preparación de 5-nitro-2-(4-(2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil)piperazin-1-il)benzonitrilo: el compuesto del título se preparó según el procedimiento para la 5-(2-(4-(1H-benzo[d]imidazol-2-il)piperidin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona, excepto porque el 5-nitro-2-piperazin-1-il-benzonitrilo se sustituyó por 2-piperazin-1-ilbenzonitrilo y el 2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil 4-metilbencenosulfonato se sustituyó por 2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil 4-metilbencenosulfonato: 1H RMN (400 MHz, CDCb ) 68,41 (d, J = 2,7 Hz, 1H), 8,25 (dd, J = 9,3, 2,7 Hz, 1H), 6,97 (d, J = 9,4 Hz, 1H), 4,48 (tt, J = 8,1, 5,7 Hz, 1H), 3,63 - 3,41 (m, 4H), 2,78 - 2,50 (m, 6H), 2,34 - 2,03 (m, 2H), 1,95 - 1,54 (m, 10H); 13C RMN (101 MHz, CDCb ) 6 182,31, 158,33, 139,60, 131,36, 129,00,
117,68, 117,01, 102,03, 75,83, 54,21, 52,75, 50,52, 50,14, 43,23, 37,46, 36,89, 32,90, 25,50, 25,41; MS (LC/MS, M+H+): 399,2.
[0120] Los compuestos siguientes se pueden preparar por el procedimiento del formiato de 1-(2-(4-(2-isopropilfenil)piperazin-1-il)etil)-2-oxaspiro[4.5]decan-3-ona. El profesional experto sabrá cómo sustituir los reactivos apropiados, los materiales de partida y los métodos de purificación conocidos por las personas expertas en la técnica, para preparar los compuestos provistos en la presente.
[0121] Preparación de formiato de 3-(2-(4-(p-tolil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona: el compuesto del título se preparó según el procedimiento para el formiato de 1 -(2-(4-(2-isopropilfenil)piperazin-1 -il)etil)-2-oxaspiro[4.5]decan-3-ona, excepto porque el 2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil 4-metilbencenosulfonato se sustituyó por 2-(3-oxo-2-oxaspiro[4.5]decan-1-il)etil 4-metilbencenosulfonato y la 1-p-tolil-piperazina se sustituyó por 1-(2-isopropil-fenil)-piperazina: 1H RMN (400 MHz, CDCla) 610,62 (ancho, 3H), 8,28 (s, 2H), 7,08 (m, 2H), 6,87 - 6,74 (m, 2H), 4,43 (tdd, J = 9,3, 5,8, 3,4 Hz, 1H), 3,42 - 3,29 (m, 4H), 3,29 - 3,13 (m, 5H), 3,11 - 3,01 (m, 1H), 2,30 - 2,01 (m, 7H), 1,89 - 1,52 (m, 8H); 13C RMN (101 MHz, CDCla) 6182,00, 166,29, 147,64, 131,31, 130,02, 117,45, 75,24, 54,21, 52,15, 50,06, 47,84, 42,92, 37,49, 36,82, 30,40, 25,58, 25,47, 20,58; MS (LC/MS, M+H+): 343,2.
[0122] Preparación de (((4-nitrofenil)sulfonil)azanediil)bis(etano-2,1-diil) bis(4-nitrobencenosulfonato): a una solución agitada de dietanolamina (130,31 mmol, 1 equiv.) y trietilamina (457,38 mmol, 3,5 equiv.) en THF anhidro (200 mL) a 0 °C bajo una atmósfera de nitrógeno, se añadió cloruro de 4-nitrobencenosulfonilo (430,02 mmol, 3,3 equiv.) poco a poco. Esta mezcla se agitó a 0 °C durante 1 h y luego durante toda la noche a temperatura ambiente. Al concluir este periodo, la mezcla reactiva se concentró a presión reducida. El residuo se disolvió en diclorometano (200 mL), se lavó con agua (25 mL), se secó (MgSCM), se filtró y se evaporó para proporcionar un sólido naranja. La recristalización de metanol-THF dio el compuesto del título como un cristal amarillento. 1H RMN (400 MHz, acetona) 68,55 (d, J = 9,0 Hz, 4H), 8,45 (d, J = 8,9 Hz, 2H), 8,25 (d, J = 9,0 Hz, 4H), 8,16 (d, J = 8,9 Hz, 2H), 4,38 (t, J = 5,6 Hz, 4H), 3,71 (t, J = 5,6 Hz, 4H).
[0123] Preparación de 1-(2-isopropilfenil)piperazina: las reacciones se realizaron en un sistema de reacción de microondas CEM accionado a 175 °C durante 1 h. Se mezclaron (((4-nitrofenil)sulfonil)azanodiil)bis(etano-2,1-diil) bis(4-nitrobencenosulfonato) (660 mg, 1,0 mmol), 2-isopropil-fenilamina (162 mg, 1,2 mmol), DIPeA (516 mg, 4,0 mmol) y CH3CN (3 mL) en un vial de reacción de microondas (10 mL) equipado con una tapa de vial no invasiva. Los viales de reacción con la mezcla se hicieron reaccionar en el microondas durante 1 h a 175°C. El perfil de temperatura-tiempo de reacción típico se muestra en el material de apoyo. Después de 1 h, el solvente se eliminó bajo presión reducida. El residuo se disolvió en diclorometano y se lavó con HCl (10%, 3 x 30 mL) y NaHCC3 saturado (40 mL). La fase orgánica se secó sobre MgSO4 y se concentró al vacío para proporcionar el producto bruto. Este producto bruto, 1-(2-isopropil-fenil)-4-(4-nitro-bencenosulfonil)-piperazina, se filtró a través de una almohadilla de sílice (hexanos/diclorometano 1:4, grosor de la almohadilla de sílice: 10 cm, diámetro: 4 cm) y se usó en reacciones posteriores sin más purificación.
[0124] Se añadió carbonato potásico (3,52 g, 25,47 mmol) a una mezcla de acetonitrilo y dimetilsulfóxido (c H3CN/DMSC 49:1) y se calentó a 50°C. Se añadió tiofenol (2,34 g, 21,23 mmol) gota a gota mediante una jeringa a la mezcla con agitación. Después de 30 min, se añadió una solución de 1-(2-isopropil-fenil)-4-(4-nitrobencenosulfonil)-piperazina (825 mg, 2,12 mmol) en CH3CN y DMSC (CH3CN/DMSC 49:1) gota a gota. La mezcla reactiva se agitó durante 3 horas, se desactivó con exceso de solución de NaCH (40%; también eliminó el desagradable olor del PhSH) y se concentró bajo presión reducida. El residuo se extrajo con diclorometano (5x30 mL) y la fase orgánica se secó sobre MgSO4 y se concentró al vacío para dar un aceite bruto. El aceite se purificó
por cromatografía de fase inversa (CH3CN en H2O, gradiente de 1%~100% con ácido fórmico al 0,1%) para proporcionar la sal de ácido fórmico de la piperazina deseada. La sal se disolvió en diclorometano, se lavó con solución de NaHCO3 saturada y se concentró al vacío la fase orgánica para proporcionar el producto. IR (KBr, cm-1): 3295, 2958, 2867, 2818, 1444, 1360, 1252, 1053, 932, 807, 762; 1H RMN (400 MHz, CDCb ) ó 7,23 - 7,14 (m, 1H), 7,13 - 6,97 (m, 3H), 3,43 (dt, J = 13,8, 6,9 Hz, 1H), 3,25 (s, 1H), 3,07 - 2,94 (m, 4H), 2,81 (m, 4H), 1,13 (d, J = 6,9 Hz, 6H); 13C RMN (101 MHz, CDCb ) ó 151,1, 144,9, 126,7, 126,6, 124,9, 120,1, 54,3, 46,6, 27,0, 24,3; MS (LC/MS, M+H+): 205,1.
[0125] Los compuestos siguientes se pueden preparar por el procedimiento de la 1-(2-isopropilfenil)piperazina. El profesional experto sabrá cómo sustituir los reactivos apropiados, los materiales de partida y los métodos de purificación conocidos por las personas expertas en la técnica, para preparar los compuestos provistos en la presente.
[0126] Preparación de 1-(2-tert-butilfenil)piperazina: el compuesto del título se preparó según el procedimiento para la 1-(2-isopropilfenil)piperazina, excepto porque la 2-tert-butil-fenilamina se sustituyó por 2-isopropil-fenilamina: IR (KBr, cm-1): 3330, 2952, 2824, 2715, 2474, 1452, 1216, 1136, 924, 764; 1H RMN (400 MHz, CDCla) ó 7,46 - 7,35 (m, 2H), 7,33 - 7,16 (m, 2H), 3,62 - 3,41 (m, 4H), 3,32 (t, J = 11,7 Hz, 2H), 3,01 (d, J = 12,6 Hz, 2H), 1,87 (s, 1H), 1,50 - 1,35 (s, 9H); 13C RMN (101 MHz, CDCb ) ó 151,5, 147,3, 127,7, 127,5, 127,3, 125,8, 51,0, 44,3, 35,7, 31,1. MS (LC/MS, M+H+): 219,1.
[0127] Preparación de 1-(2,6-diisopropilfenil)piperazina: el compuesto del título se preparó según el procedimiento para la 1-(2-isopropilfenil)piperazina, excepto porque la 2,6-diisopropil-fenilamina se sustituyó por 2-isopropilfenilamina: IR (KBr, cm-1): 3295, 2958, 1653, 1444, 1252, 1053, 932, 807, 762; 1H RMN (400 MHz, CDCb ) ó 7,10 (dd, J = 8,5, 6,7 Hz, 1H), 7,05 - 7,00 (m, 2H), 3,45 (dt, J = 13,8, 6,9 Hz, 2H), 3,04 (m, 4H), 2,97 - 2,87 (m, 4H), 2,03 (s, 1H), 1,13 (d, J = 6,9 Hz, 12H); 13C RMN (101 MHz, CDCb ) ó 149,4, 146,4, 126,9, 124,3, 52,3, 47,4, 28,5, 24,7. HRMS (CI): [M+H], calc. para C16H26N2, 247,2174; encontrado 247,2175.
[0128] Preparación de N-(2-(piperazin-1-il)fenil)acetamida: el compuesto del título se preparó según el procedimiento para la 1-(2-isopropilfenil)piperazina, excepto porque la N-(2-aminofenil)-acetamida se sustituyó por 2-isopropil-fenilamina: IR (KBr, cm'1): 3318, 2945, 2827, 1673, 1589, 1517, 1449, 1370, 1233, 761; 1H RMN (400 MHz, CDCb) ó 8,45 (s, 1H), 8,27 (d, J = 8,0 Hz, 1H), 7,13 - 7,03 (m, 2H), 6,98 (td, J = 7,6, 1,4 Hz, 1H), 3,00 (m, J = 12,5, 8,0 Hz, 4H), 2,83 - 2,71 (m, 4H), 2,14 (s, 3H), 1,99 (s, J = 10,8 Hz, 1H); 13C RMN (101 MHz, CDCb ) ó 168,4, 141,6, 133,8, 125,8, 124,1, 120,9, 119,7, 53,7, 47,2, 25,3. MS (LC/MS, M+H+): 220,1.
[0129] Preparación de 1-(bifenil-2-il)piperazina: el compuesto del título se preparó según el procedimiento para la 1-(2-isopropilfenil)piperazina, excepto porque la bifenil-2-ilamina se sustituyó por 2-isopropil-fenilamina: IR (KBr, cm-1): 3350, 3057, 2943, 2817, 1593, 1480, 1433, 1223, 770, 739, 699; 1H RMN (400 MHz, CDCb ) ó 7,55 (m, 2H), 7,38 - 7,25 (m, 2H), 7,25 - 7,14 (m, 3H), 7,05 - 6,90 (m, 2H), 2,73 (d, J = 7,4 Hz, 8H), 2,38 (s, 1H); 13C RMN (101
MHz, CDCI3) 8150,9, 141,4, 135,4, 131,8, 129,2, 128,6, 128,5, 127,1, 123,1, 118,7, 52,5, 46,2. MS (LC/MS, M+H+): 239,1.
[0130] Preparación de 1-(2-yodofeniI)piperazina: el compuesto del título se preparó según el procedimiento para la 1-(2-isopropiIfeniI)piperazina, excepto porque la 2-yodo-fenilamina se sustituyó por 2-isopropil-fenilamina: IR (KBr, cm-1): 3292, 3053, 2943, 2819, 1578, 1468, 1225, 1012, 760; 1H RMN (400 MHz, CDCb) 87,95 - 7,77 (m, 1H), 7,04 (dt, J = 7,4, 3,7 Hz, 1H), 6,80 (td, J = 7,8, 1,4 Hz, 1H), 3,20 - 2,88 (m, 8H), 1,25 (s, 1H); 13C RMN (101 MHz, CDCb ) 8 153,9, 140,4, 129,6, 125,9, 121,5, 98,7, 53,5, 46,3. MS (LC/MS, M+H+): 288,9.
[0131] Preparación de 1-(2-(1H-pirrol-1-il)fenil)piperazina: el compuesto del título se preparó según el procedimiento para la 1-(2-isopropilfenil)piperazina, excepto porque la 2-pirrol-1 -il-fenilamina se sustituyó por 2-isopropilfenilamina: IR (KBr, cm-1): 3309, 2943, 2822, 1598, 1503, 1449, 1319, 1235, 1069, 759, 727; 1H RMN (400 MHz, CDCb ) 87,24 - 7,07 (m, 2H), 7,03 - 6,88 (m, 4H), 6,20 (t, J = 2,2 Hz, 2H), 2,85 - 2,68 (m, 4H), 2,56 (m, 4H), 1,61 (s, 1H); 13C RMN (101 MHz, CDCb ) 8147,0, 133,9, 127,7, 126,7, 122,7, 121,4, 119,2, 109,2, 51,7, 46,5; MS (LC/MS, M+H+): 228,1.
[0132] Preparación de 4-(2-(piperazin-1-il)fenil)morfolina: el compuesto del título se preparó según el procedimiento para la 1-(2-isopropilfenil)piperazina, excepto porque la 2-morfolin-4-il-fenilamina se sustituyó por 2-isopropilfenilamina: IR (KBr, cm-1): 3313, 2950, 2817, 1591, 1493, 1446, 1227, 1117, 928, 764; 1H RMN (400 MHz, CDCb ) 8 6,91 (m, 2H), 6,88 - 6,78 (m, 2H), 3,83 - 3,68 (m, 4H), 3,07 (m, J = 21,5 Hz, 8H), 2,92 (t, J = 4,7 Hz, 4H), 1,80 (s, 1H); 13C RMN (101 MHz, CDCb ) 8 145,4, 144,8, 123,3, 123,2, 119,0, 118,4, 67,8, 51,2, 50,2, 47,0; HRMS (CI):
[M+H], calc. para C14H21N3O, 248,1762; encontrado, 248,1751.
FORMULACIONES
[0133] La presente invención también se refiere a composiciones o formulaciones farmacéuticas que comprenden los moduladores de la actividad del receptor de 5-hidroxitriptamina 7 según la presente invención. En general, las composiciones de la presente invención comprenden una cantidad eficaz de uno o más compuestos de la divulgación y sales derivadas según la presente invención que son eficaces para proporcionar la modulación de la actividad del receptor de 5-hidroxitriptamina 7; y uno o más excipientes.
[0134] A efectos de la presente invención, el término "excipiente" y "portador" se usan de forma intercambiable en toda la descripción de la presente invención y dichos términos se definen en la presente como, "ingredientes que se usan en la práctica de la formulación de una composición farmacéutica segura y eficaz".
[0135] El formulador entenderá que los excipientes se usan principalmente para servir para la administración de un producto farmacéutico seguro, estable y funcional, que no sirve solo como parte del vehículo general para la administración, sino también como un medio para conseguir una absorción eficaz por el receptor de la sustancia activa. Un excipiente puede tener un papel tan simple y directo como el de ser una carga inerte, o un excipiente como se utiliza en la presente puede ser parte de un sistema estabilizante del pH o un recubrimiento para asegurar la administración de los ingredientes de forma segura al estómago. El formulador puede aprovecharse también del hecho de que los compuestos de la presente invención tienen una potencia celular y propiedades farmacocinéticas mejoradas, así como una biodisponibilidad oral mejorada.
[0136] Las presentes instrucciones proporcionan también composiciones farmacéuticas que incluyen por lo menos un compuesto descrito en la presente y uno o más portadores, excipientes o diluyentes farmacéuticamente
aceptables. Ejemplos de tales portadores son bien conocidos por las personas expertas en la técnica y se pueden preparar conforme a procedimientos farmacéuticos aceptables, tales como, por ejemplo, aquellos descritos en Remington's Pharmaceutical Sciences, 17a edición, ed. Alfonoso R. Gennaro, Mack Publishing Company, Easton, PA (1985), toda la divulgación del cual se incorpora por referencia en la presente a todos los efectos. Como se utiliza en la presente, "farmacéuticamente aceptable" se refiere a una sustancia que es aceptable para usar en aplicaciones farmacéuticas desde una perspectiva toxicológica y no interactúa negativamente con la sustancia activa. Por consiguiente, portadores farmacéuticamente aceptables son aquellos que son compatibles con los otros ingredientes en la formulación y son biológicamente aceptables. También pueden incorporarse ingredientes activos complementarios en las composiciones farmacéuticas.
[0137] Los compuestos de las presentes instrucciones se pueden administrar por vía oral o por vía parenteral, solos o en combinación con portadores farmacéuticos convencionales. Los portadores sólidos aplicables pueden incluir una o más sustancias que pueden actuar también como agentes saborizantes, lubricantes, solubilizantes, agentes de suspensión, productos de relleno, deslizantes, auxiliares de compresión, ligantes o agentes de desintegración de comprimidos, o materiales de encapsulación. Los compuestos se pueden formular de manera convencional, por ejemplo, de una manera similar a la usada para los moduladores de la actividad del receptor 5-hidroxitriptamina 7 conocidos. Las formulaciones orales con un compuesto descrito en la presente pueden comprender cualquier forma oral usada de forma convencional, incluidas comprimidos, cápsulas, formas bucales, pastillas, grageas y líquidos, suspensiones o soluciones orales. En polvos, el portador puede ser un sólido finamente dividido, que es una mezcla con un compuesto finamente dividido. En comprimidos, un compuesto descrito en la presente se puede mezclar con un portador con las propiedades de compresión necesarias en proporciones adecuadas y compactarse en la forma y el tamaño deseados. Los polvos y los comprimidos pueden contener hasta un 99 % del compuesto.
[0138] Las cápsulas pueden contener mezclas de uno o más compuesto(s) descrito(s) en la presente con carga(s) inerte(s) y/o diluyente(s) tales como almidones farmacéuticamente aceptables (por ejemplo, almidón de maíz, patata o tapioca), azúcares, agentes edulcorantes artificiales, celulosas en polvo (por ejemplo, celulosas cristalinas y microcristalinas), harinas, gelatinas, gomas y similares.
[0139] Las formulaciones de comprimidos útiles se pueden preparar por métodos convencionales de compresión, granulación húmeda o granulación seca y utilizar diluyentes farmacéuticamente aceptables, agentes aglutinantes, lubricantes, desintegrantes, agentes modificadores de la superficie (incluidos surfactantes), agentes de suspensión o estabilizantes, incluidos, pero de forma no limitativa, estearato de magnesio, ácido esteárico, lauril sulfato de sodio, talco, azúcares, lactosa, dextrina, almidón, gelatina, celulosa, metilcelulosa, celulosa microcristalina, carboximetilcelulosa de sodio, carboximetilcelulosa de calcio, polivinilpirrolidina, ácido algínico, goma arábiga, goma xantana, citrato sódico, silicatos complejos, carbonato cálcico, glicina, sacarosa, sorbitol, fosfato dicálcico, sulfato de calcio, lactosa, caolín, manitol, cloruro sódico, ceras de baja fusión y resinas de intercambio iónico. Los agentes modificadores de la superficie incluyen agentes modificadores de la superficie no iónicos y aniónicos. Los ejemplos representativos de agentes modificadores de la superficie incluyen, pero de forma no limitativa, poloxámero 188, cloruro de benzalconio, estearato de calcio, alcohol cetoestearílico, cera emulsionante de cetomacrogol, ésteres de sorbitán, dióxido de silicio coloidal, fosfatos, dodecilsulfato de sodio, silicato de aluminio de magnesio y trietanolamina. Las formulaciones orales en la presente pueden utilizar formulaciones estándar de retardo o de liberación lenta para alterar la absorción del/de los compuesto(s). La formulación oral puede consistir también en la administración de un compuesto descrito en la presente en agua o zumo de frutas, con los solubilizantes o emulsionantes apropiados según sea necesario.
[0140] Los portadores líquidos se pueden usar en la preparación de soluciones, suspensiones, emulsiones, jarabes, elixires y para la administración por inhalación. Un compuesto de las presentes instrucciones se puede disolver o suspender en un portador líquido farmacéuticamente aceptable tal como agua, un solvente orgánico, o una mezcla de ambos, o unos aceites o grasas farmacéuticamente aceptables. El portador líquido puede contener otros aditivos farmacéuticos adecuados tales como solubilizantes, emulsionantes, tampones, conservantes, edulcorantes, agentes saborizantes, agentes de suspensión, agentes espesantes, colores, reguladores de la viscosidad, estabilizadores y osmorreguladores. Los ejemplos de portadores líquidos para la administración oral y parenteral incluyen, pero de forma no limitativa, agua (particularmente con aditivos como se describe en la presente, por ejemplo, derivados de celulosa tales como una solución de carboximetilcelulosa de sodio), alcoholes (incluidos alcoholes monohídricos y alcoholes polihídricos, por ejemplo, glicoles) y sus derivados, y aceites (por ejemplo, aceite de coco fraccionado y aceite de cacahuete). Para la administración parenteral, el portador puede ser un éster oleaginoso tal como oleato etílico y miristato de isopropilo. Se usan portadores líquidos estériles en las composiciones en forma líquida estéril para la administración parenteral. El portador líquido para las composiciones presurizadas puede ser hidrocarburo halogenado u otros propulsores farmacéuticamente aceptables.
[0141] Las composiciones farmacéuticas líquidas, que son soluciones o suspensiones estériles, se pueden utilizar mediante, por ejemplo, inyección intramuscular, intraperitoneal o subcutánea. Las soluciones estériles también se pueden administrar por vía intravenosa. Las composiciones para la administración oral pueden estar en forma o líquida o sólida.
[0142] Preferiblemente, la composición farmacéutica está en forma de dosificación unitaria, por ejemplo, como comprimidos, cápsulas, polvos, soluciones, suspensiones, emulsiones, gránulos o supositorios. En tal forma, la composición farmacéutica se puede subdividir en la(s) dosis(s) unitaria(s) con cantidades apropiadas del compuesto. Las formas de dosificación unitaria pueden ser composiciones envasadas, por ejemplo, polvos, viales, ampollas, jeringas precargadas o sobres que contienen líquidos envasados. Alternativamente, la forma de dosificación unitaria puede ser una cápsula o comprimido en sí misma, o puede ser el número apropiado de cualquiera de tales composiciones en forma de envase. Tal forma de dosificación unitaria puede contener de aproximadamente 1 mg/kg de compuesto a aproximadamente 500 mg/kg de compuesto y se puede dar en una dosis individual o en dos o más dosis. Tales dosis se pueden administrar de cualquier manera útil para dirigir el/los compuesto(s) al flujo sanguíneo del receptor, incluido por vía oral, mediante implantes, por vía parenteral (incluidas inyecciones intravenosas, intraperitoneales y subcutáneas), por vía rectal, por vía vaginal y por vía transdérmica.
[0143] Cuando se administra para el tratamiento o la inhibición de un estado de enfermedad o trastorno particular, se entiende que una dosificación eficaz puede variar dependiendo del compuesto particular utilizado, el modo de administración y la gravedad de la condición que se está tratando, así como los varios factores físicos relacionados con el individuo que se está tratando. En las aplicaciones terapéuticas, un compuesto de las presentes instrucciones puede proporcionarse a un paciente que ya sufre una enfermedad en una cantidad suficiente para curar o al menos mejorar parcialmente los síntomas de la enfermedad y sus complicaciones. Típicamente, la dosificación que se va a usar en el tratamiento de un individuo específico debe ser determinada subjetivamente por el médico responsable. Las variables implicadas incluyen la condición específica y su estado, así como el tamaño, la edad y el patrón de respuesta del paciente.
[0144] En algunos casos puede ser deseable administrar un compuesto directamente a las vías respiratorias del paciente, usando dispositivos tales como, inhaladores de dosis medidas, inhaladores accionados por la respiración, inhaladores de polvo seco multidosis, bombas, dispensadores de aerosol nebulizado accionados por compresión, dispensadores de aerosol y nebulizadores de aerosol. Para la administración por inhalación intranasal o intrabronquial, los compuestos de las presentes instrucciones se pueden formular en una composición líquida, una composición sólida o una composición de aerosol. La composición líquida puede incluir, a modo de ilustración, uno o más compuestos de las presentes instrucciones disueltos, parcialmente disueltos o suspendidos en uno o más solventes farmacéuticamente aceptables y se puede administrar mediante, por ejemplo, una bomba o un dispensador de aerosol nebulizado accionado por compresión. Los solventes pueden ser, por ejemplo, solución salina isotónica o agua bacteriostática. La composición sólida puede ser, a modo de ilustración, una preparación en polvo que incluye uno o más compuestos de las presentes instrucciones entremezclados con lactosa u otros polvos inertes que son aceptables para un uso intrabronquial, y se puede administrar mediante, por ejemplo, un dispensador de aerosol o un dispositivo que rompa o pinche una cápsula que encierra la composición sólida y suministra la composición sólida para su inhalación. La composición de aerosol puede incluir, a modo de ilustración, uno o más compuestos de las presentes instrucciones, propulsores, surfactantes y cosolventes, y se puede administrar mediante, por ejemplo, un dispositivo dosificado. Los propulsores pueden ser un clorofluorocarbono (CFC), un hidrofluoroalcano (HFA) u otros propulsores que sean fisiológica y medioambientalmente aceptables.
[0145] Los compuestos descritos en la presente se pueden administrar por vía parenteral o intraperitoneal. Se pueden preparar soluciones o suspensiones de estos compuestos o unas sales, hidratos o ésteres derivados farmacéuticamente aceptables en agua mezclados adecuadamente con un surfactante tal como hidroxipropilcelulosa. También pueden prepararse dispersiones en glicerol, polietilenglicoles líquidos y sus mezclas derivadas en aceites. Bajo condiciones ordinarias de almacenamiento y uso, estas preparaciones contienen típicamente un conservante para inhibir el crecimiento de microorganismos.
[0146] Las formas farmacéuticas adecuadas para su inyección pueden incluir soluciones o dispersiones acuosas estériles y polvos estériles para la preparación extemporánea de soluciones inyectables o dispersiones estériles. En algunas formas de realización, la forma puede ser estéril y su viscosidad permite que fluya a través de una jeringa. La forma es preferiblemente estable bajo las condiciones de producción y almacenamiento y se puede preservar contra la acción contaminante de microorganismos tales como bacterias y hongos. El portador puede ser un solvente o medio de dispersión que contiene, por ejemplo, agua, etanol, poliol (por ejemplo, glicerol, propilenglicol y polietilenglicol líquido), mezclas derivadas adecuadas y aceites vegetales.
[0147] Los compuestos descritos en la presente se pueden administrar por vía transdérmica, es decir, administrarse a través de la superficie del cuerpo y los revestimientos internos de conductos corporales, incluidos tejidos epiteliales y de las mucosas. Tal administración se puede llevar a cabo usando los compuestos de las presentes instrucciones, incluidas sales, hidratos o ésteres derivados farmacéuticamente aceptables, en lociones, cremas, espumas, parches, suspensiones, soluciones y supositorios (rectales y vaginales).
[0148] La administración transdérmica se puede conseguir a través del uso de un parche transdérmico que contiene un compuesto, tal como un compuesto descrito en la presente, y un portador que puede ser inerte al compuesto, puede ser no tóxico para la piel y puede permitir la administración del compuesto para la absorción sistémica en el
flujo sanguíneo a través de la piel. El portador puede tomar cualquier número de formas tales como cremas y pomadas, pastas, geles y dispositivos oclusivos. Las cremas y las pomadas pueden ser emulsiones viscosas líquidas o semisólidas del tipo de aceite en agua o de agua en aceite. También pueden ser adecuadas las pastas compuestas de polvos absorbentes dispersados en petróleo o petróleo hidrófilo con el compuesto. Se pueden usar una variedad de dispositivos oclusivos para liberar el compuesto en el flujo sanguíneo, tal como una membrana semipermeable que cubra un depósito que contiene el compuesto con o sin un portador, o una matriz que contenga el compuesto. Otros dispositivos oclusivos se conocen en la literatura.
[0149] Los compuestos descritos en la presente se pueden administrar por vía rectal o vaginal en forma de un supositorio convencional. Las formulaciones de supositorio se pueden hacer de materiales tradicionales, incluidos manteca de cacao, con o sin la adición de ceras para alterar el punto de fusión del supositorio, y glicerina. También pueden usarse bases de supositorio hidrosolubles, tales como polietilenglicoles de varios pesos moleculares.
[0150] Se pueden usar formulaciones o nanocápsulas lipídicas para introducir compuestos de las presentes instrucciones en células huésped in vitro o in vivo. Las formulaciones y las nanocápsulas lipídicas se pueden preparar por métodos conocidos en la técnica.
[0151] Para aumentar la eficacia de los compuestos de las presentes instrucciones, puede ser deseable combinar un compuesto con otros agentes eficaces en el tratamiento de la enfermedad objetivo. Por ejemplo, otros compuestos activos (es decir, otros agentes o ingredientes activos) eficaces para tratar la enfermedad objetivo se pueden administrar con compuestos de las presentes instrucciones. Los otros agentes se pueden administrar al mismo tiempo o en tiempos diferentes que los compuestos que se describen en la presente.
[0152] Los compuestos de las presentes instrucciones pueden ser útiles para el tratamiento o la inhibición de una condición patológica o trastorno en un mamífero, por ejemplo, un sujeto humano. Por consiguiente, las presentes instrucciones proporcionan métodos de tratamiento o inhibición de una condición patológica o trastorno al proporcionar a un mamífero un compuesto de las presentes instrucciones (incluida su sal farmacéuticamente aceptable) o una composición farmacéutica que incluye uno o más compuestos de las presentes instrucciones en combinación o asociación con portadores farmacéuticamente aceptables. Se pueden administrar compuestos de las presentes instrucciones solos o en combinación con otros compuestos terapéuticamente eficaces o terapias para el tratamiento o la inhibición de la condición patológica o trastorno.
[0153] Los ejemplos de composiciones según la presente invención incluyen de aproximadamente 0,001 mg a aproximadamente 1000 mg de uno o más compuestos de la divulgación según la presente invención y uno o más excipientes; de aproximadamente 0,01 mg a aproximadamente 100 mg de uno o más compuestos de la divulgación según la presente invención y uno o más excipientes; y de aproximadamente 0,1 mg a aproximadamente 10 mg de uno o más compuestos de la divulgación según la presente invención; y uno o más excipientes.
PROCEDIMIENTOS
[0154] Los procedimientos siguientes se pueden utilizar en la evaluación y la selección de compuestos como moduladores de la actividad del receptor de 5-hidroxitriptamina 7.
Estudios de unión de radiomarcadores para receptores de serotonina 5HT7, método 1:
[0155] Una solución del compuesto de la divulgación que se va a evaluar se prepara como una solución madre de 1 mg/ml en tampón de ensayo o DMSO según su solubilidad. Una solución madre similar del compuesto de referencia clorpromazina se prepara también como un control positivo. Se preparan once diluciones (concentración de ensayo 5x) del compuesto de la divulgación y clorpromazina en el tampón de ensayo por dilución en serie para producir concentraciones de ensayo finales correspondientes que varían de 10 pM a 10 pM.
[0156] Una concentración de solución madre de 5 nM de [3H]LSD (dietil amida de ácido lisérgico) se prepara en 50 mM de Tris-HCl, 10 mM de MgCb,1 mM de EDTA, pH 7,4 (tampón de ensayo). Se dispensan partes alícuotas (50 pl) de radioligando en los pocillos de una placa de 96 pocillos que contienen 100 pl de tampón de ensayo. Se añaden partes alícuotas de 50 pl por duplicado del compuesto de la prueba de la divulgación y diluciones en serie del compuesto de referencia de control positivo clorpromazina.
[0157] Se dispensan en cada pocillo fracciones de membrana de células que expresan receptores 5HT7 recombinantes (50 pL). Las membranas se obtienen a partir de líneas celulares transfectadas de forma estable que expresan receptores 5HT7 cultivadas en placas de 10 cm cosechando monocapas enjuagadas con PBS, resuspendiendo y lisando en 50 mM de Tris-HCl hipotónico frío, pH 7,4, centrifugando a 20.000 x g, decantando el sobrenadante y almacenándolas a -80 °C; las preparaciones de membrana se resuspenden en 3 ml de tampón de
ensayo frío y se homogeneizan mediante varios pasajes a través de una aguja de calibre 26 antes de usarlas en el ensayo.
[0158] Las reacciones de 250 pl se incuban a temperatura ambiente durante 1,5 horas, luego se cosechan por filtración rápida sobre alfombrillas filtrantes de 96 pocillos tratadas con polietilenimina al 0,3%, usando una cosechadora de 96 pocillos Filtermate. Se realizan cuatro lavados rápidos de 500 pl con tampón de ensayo frío para reducir la unión inespecífica. Las alfombrillas filtrantes se secan, luego se añade centelleante a los filtros y la radiactividad retenida en los filtros se cuenta en un contador de centelleo Microbeta.
[0159] Los datos brutos (dpm) que representan la unión de radioligando total (es decir, unión específica inespecífica) se representan en función del logaritmo de la concentración molar del competidor (es decir, compuesto de prueba o de referencia). La regresión no lineal de los datos brutos normalizados (es decir, el porcentaje de unión de radioligando en comparación con la observada en ausencia de compuesto de prueba o de referencia) se realiza en Prism 4.0 (GraphPad Software) usando el modelo logístico de tres parámetros incorporado que describe la unión competitiva de ligando a sitios marcados con radioligando:
y = inferior [(superior-inferior)/(1 10x-logIC5ü)]
donde inferior equivale a la unión de radioligando residual medida en presencia de 10 pM de compuesto de referencia (es decir, unión inespecífica) y superior equivale a la unión de radioligando total observada en ausencia de competidor. El log IC50 (es decir, el logaritmo de la concentración de ligando que reduce la unión de radioligando en un 50%) se estima así a partir de los datos y se usa para obtener la Ki aplicando la aproximación Cheng-Prusoff:
Ki = IC 50/1 + [ligando]/KD)
donde [ligando] equivale a la concentración de radioligando del ensayo y KD equivale a la constante de afinidad del radioligando por el receptor diana.
[0160] Los compuestos de la divulgación se criban también a una única concentración de 10 pM usando el mismo método descrito para los estudios de unión de radiomarcadores para receptores de serotonina 5HT7 para determinar el porcentaje de inhibición de la unión de [3H]LSD.
Estudios de unión de radiomarcadores para receptores de serotonina 5-HT7, método 2:
[0161] Una solución del compuesto de la divulgación que se va a evaluar se prepara como una solución madre de 1 mg/ml en tampón de ensayo o DMSO según su solubilidad. Una solución madre similar del compuesto de referencia clorpromazina se prepara también como un control positivo. Se preparan once diluciones (concentración de ensayo 5x) del compuesto de la divulgación y clorpromazina en el tampón de ensayo por dilución en serie para producir concentraciones de ensayo finales correspondientes que varían de 10 pM a 10 pM.
[0162] Una concentración de solución madre de 5 nM de [3H]-5-hidroxitriptamina ([3H]-5HT) se prepara en 50 mM de Tris-HCl, 10 mM de MgCl2,1 mM de EDTA, pH 7,4 (tampón de ensayo). Se dispensan partes alícuotas (50 pl) de radioligando en los pocillos de una placa de 96 pocillos que contienen 100 pl de tampón de ensayo. Se añaden partes alícuotas duplicadas de 50 pl del compuesto de la prueba de la divulgación y diluciones en serie del compuesto de referencia de control positivo clorpromazina.
[0163] Se dispensan en cada pocillo fracciones de membrana de células recombinantes que expresan receptores 5HT7 (50 pL). Las membranas se obtienen a partir de líneas celulares transfectadas de forma estable que expresan receptores 5HT7 cultivadas en placas de 10 cm cosechando monocapas enjuagadas con PBS, resuspendiendo y lisando en 50 mM de Tris-HCl hipotónico frío, pH 7,4, centrifugando a 20.000 x g, decantando el sobrenadante y almacenando a -80 °C; las preparaciones de membrana se resuspenden en 3 ml de tampón de ensayo frío y se homogeneizan mediante varios pasajes a través de una aguja de calibre 26 antes de usarlas en el ensayo.
[0164] Las reacciones de 250 pl se incuban a temperatura ambiente durante 1,5 horas, luego se cosechan por filtración rápida sobre alfombrillas filtrantes de 96 pocillos tratadas con polietilenimina al 0,3%, usando una cosechadora de 96 pocillos Filtermate. Se realizan cuatro lavados rápidos de 500 pl con tampón de ensayo frío para reducir la unión inespecífica. Las alfombrillas filtrantes se secan, luego se añade centelleante a los filtros y la radiactividad retenida en los filtros se cuenta en un contador de centelleo Microbeta.
[0165] Los datos brutos (dpm) que representan la unión de radioligando total (es decir, unión específica inespecífica) se representan en función del logaritmo de la concentración molar del competidor (es decir, compuesto
de prueba o de referencia). La regresión no lineal de los datos brutos normalizados (es decir, el porcentaje de unión de radioligando en comparación con la observada en ausencia de compuesto de prueba o de referencia) se realiza en Prism 4.0 (GraphPad Software) usando el modelo logístico de tres parámetros incorporado que describe la unión competitiva de ligando a sitios marcados con radioligando:
y = inferior [(superior-inferior)/(1 10x-logIC5o)]
donde inferior equivale a la unión de radioligando residual medida en presencia de 10 pM de compuesto de referencia (es decir, unión inespecífica) y superior equivale a la unión de radioligando total observada en ausencia de competidor. El log IC50 (es decir, el logaritmo de la concentración de ligando que reduce la unión de radioligando en un 50%) se estima así a partir de los datos y se usa para obtener la Ki aplicando la aproximación Cheng-Prusoff:
Ki = IC 50/1 + [ligando]/KD)
donde [ligando] equivale a la concentración de radioligando del ensayo y KD equivale a la constante de afinidad del radioligando por el receptor diana.
[0166] Los compuestos de la divulgación se criban también a una única concentración de 10 pM usando el mismo método descrito para los estudios de unión de radiomarcadores para receptores de serotonina 5 HT7 para determinar el porcentaje de inhibición de la unión de [3H]-5HT.
[0167] Los resultados de los compuestos representativos según la presente invención se enumeran en la tabla 18.
Tabla 18: resultados de los estudios de unión de radiomarcadores para receptores de serotonina 5 HT7 para compuestos ejemplares de la divulgación.
Ensayo de serotonina 5HT7 funcional, método 1:
[0168] Se siembran líneas celulares que expresan de forma estable receptores 5HT7 humanos en placas recubiertas con poli-L-lisina de 96 pocillos 48 horas antes del ensayo (40.000 células por pocillo) en medio Eagle modificado por Dulbecco (DMEM) que contiene un 5% de suero dializado. Veinte horas antes del ensayo, el medio se cambia a DMEM sin suero. El día del ensayo, el DMEM se lava y se sustituye con 30 pl de tampón de ensayo (tampón IX Krebs-Ringer bicarbonato glucosa, 0,75 mM de IBMX, pH 7,4). Se realiza una preincubación de 10 min en una incubadora a 37 grados centígrados humidificada. Luego, las células se estimulan mediante la adición de 30 pl de diluciones 2X de compuestos de la divulgación o clorpromazina (concentraciones finales que varían de 0,1 nM a 10 pM, cada concentración evaluada por triplicado). También se incluye un control positivo (100 pM de forskolina). Se deja que continúe la acumulación de cAMP durante 15 min, después de lo cual se elimina el tampón y las células se lisan con tampón de lisis celular (CatchPoint cAMP Assay Kit, Molecular Devices). A continuación, los lisados se transfieren a placas de 96 pocillos de fondo de cristal recubiertas con IgG anticonejo de cabra y se adsorben con anti-cAMP de conejo (Molecular Devices). Tras una incubación de 5 minutos, se añade conjugado de peroxidasa de rábano-cAMP (Molecular Devices) y se realiza una incubación de 2 horas a temperatura ambiente. Luego, después de tres lavados con tampón de lavado (Molecular Devices), se añade sustrato Stoplight Red (Molecular Devices), reconstituido en tampón de sustrato (Molecular Devices) con 1 mM de H2O2 recién añadido y, después de una incubación de 15 min a temperatura ambiente, se mide la fluorescencia (excitación 510-545 nm, emisión 565-625 nm). Para cada ensayo, se genera una curva de calibración de cAMP y se incluyen controles sin lisado y sin anticuerpo.
[0169] Para las pruebas de agonistas, se normalizan los datos brutos (fluorescencia máxima, unidades de fluorescencia) para cada concentración de los compuestos de la divulgación o clorpromazina respecto a la fluorescencia basal (estimulada por el vehículo) (proporcionados como factor de aumento sobre la basal) y se representan en función del logaritmo de la concentración molar del fármaco (es decir, compuesto de prueba o de referencia). La regresión no lineal de los datos normalizados se realiza en Prism 4.0 (GraphPad Software) usando el modelo logístico de tres parámetros incorporado (es decir, concentración-respuesta sigmoide) que describe la activación estimulada por agonistas de una población de receptores:
y = inferior [(superior-inferior)/(1 10x-logEC5ü)]
donde inferior equivale a la fluorescencia basal de mejor ajuste y superior equivale a la fluorescencia máxima de mejor ajuste estimulada por el compuesto de la divulgación o la clorpromazina. El log EC50 (es decir, el logaritmo de la concentración de fármaco que aumenta la fluorescencia en un 50% de la fluorescencia máxima observada
para el compuesto de la divulgación o la clorpromazina se estima así a partir de los datos, y se obtiene la EC50 (potencia del agonista). Para obtener una estimación de la eficacia relativa del compuesto de prueba (Emax rel.), su valor superior de mejor ajuste se compara con y se expresa como una razón de la de la clorpromazina (la Emax rel. del agonista de referencia es 1,00).
[0170] Para averiguar si los compuestos de la divulgación son antagonistas, se emplea un paradigma de adición doble. Primero, se añaden 30 pl de un compuesto de la divulgación (20 pM) (concentración final de 10 pM) y se realiza una incubación de 15 minutos. Luego, se añaden 30 pl de clorpromazina (3X; EC90) (la concentración final de agonista es EC30) y se deja que proceda la acumulación de cAMP durante 15 minutos. Las muestras se procesan entonces para las mediciones de cAMP como se ha detallado anteriormente. Las mediciones de acumulación de cAMP inducida por la clorpromazina se comparan con las señales provocadas por la clorpromazina tras la adición de vehículo en vez de compuesto de prueba y se expresan como una razón. Los 'candidatos potenciales' (compuestos que antagonizan los aumentos estimulados por la clorpromazina en la fluorescencia normalizada respecto a la línea base en al menos un 50%) se caracterizan entonces por un análisis de Schild modificado.
[0171] Para el análisis de Schild modificado, se genera una familia de isotermas de concentración de clorpromazinarespuesta en ausencia y en presencia de concentraciones graduadas de compuesto de prueba (añadido 15 min antes que el agonista de referencia). Teóricamente, los compuestos que son antagonistas competitivos causan un cambio dextral de isotermas de concentración de agonista-respuesta sin reducir la respuesta máxima al agonista (es decir, antagonismo superable). Sin embargo, a veces, los factores tales como el antagonismo no competitivo, el semiequilibrio y/o la reserva de receptores causan un antagonismo insuperable aparente. Para considerar tales desviaciones, aplicamos el método de Lew-Angus modificado para averiguar la potencia del antagonista (Christopoulos et al., 1999). Brevemente, las concentraciones equieficaces de agonista (concentraciones de agonista que provocan una respuesta igual al EC25% de la curva de control del agonista) se representan en función de la concentración del compuesto de la divulgación presente en los pocillos donde se midieron. La regresión no lineal de los datos normalizados respecto a la línea base se realiza en Prism 4.0 usando la ecuación siguiente:
pEC25% = -log ([B] 10-pK) - log c
donde EC25% equivale a la concentración de agonista que provoca una respuesta igual al 25% de la respuesta de la curva de control del agonista máxima y [B] equivale a la concentración del antagonista; K, c y s son parámetros de ajuste. El parámetro s es igual al factor de la pendiente de Schild. Si s no es significativamente diferente a la unidad, pK equivale a pKB; de lo contrario, se calcula pA2 (pA2 = pK/s). El parámetro c equivale a la razón EC25%/[B].
Ensayo de eficacia funcional para los receptores 5-HT7, método 2:
[0172] La eficacia funcional de los compuestos de la divulgación sobre los receptores de serotonina 5-HT7 se midió en un ensayo celular de complementación con fragmentos de enzima cAMP usando el ensayo de cAMP HitHunter (DiscoveRx). Las células que expresan de forma estable receptores 5HT7 humanos se sembraron en placas de 96 pocillos con 4000 células/pocillo, 16- 20 horas antes del ensayo en medio de cultivo (medio Ultraculture, 2 mM de GlutaMax y G418 1 mg/mL. Se prepararon diluciones en serie del agonista, 5-carboxamidotriptamina (5-CT), en un rango de concentración final de 10 pM a 10 nM. Se prepararon los compuestos de la divulgación en diluciones en serie de factor 3 para obtener un rango de concentración final de 10 pM a 0,1 nM. Se evalúan la actividad agonista en ausencia de 5-CT y la actividad antagonista en presencia de 5-CT de los compuestos de la divulgación. Para el ensayo de cAMP, se siguió el protocolo según las instrucciones proporcionadas por el proveedor. Brevemente, las células se incubaron con un compuesto de la divulgación durante 30 minutos a 37 °C antes de la adición de la concentración EC70 de 5-CT. Después de 30 minutos adicionales, se añadió anticuerpo cAMP/solución de lisis celular (20 pl/pocillo) y se incubó durante 60 minutos a temperatura ambiente. Se añadió reactivo cAMP XS EA (20 pl/pocillo) y se incubó durante 2 horas a temperatura ambiente. La luminiscencia se leyó en el lector de placas Envision Multilabel.
Claims (9)
1. Compuesto seleccionado del grupo que consiste en:
2- (4-(2-(4,4-d¡et¡l-5-oxotetrah¡drofuran-2-¡l)et¡l)p¡peraz¡n-1-¡l)benzon¡tr¡lo; 3.3- dietil-5-(2-(4-(4-metoxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; 3.3- d¡et¡l-5-(2-(4-(4-h¡drox¡fen¡l)p¡peraz¡n-1-¡l)et¡l)d¡h¡drofuran-2(3H)-ona; 3.3- dietil-5-(2-(4-(4-nitrofenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; 3.3- dietil-5-(2-(4-(2-metoxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; 4- (4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo; 3.3- dietil-5-(2-(4-(2-hidroxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; 5- (2-(4-(4-aminofenil)piperazin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona; 3.3- dietil-5-(2-(4-(p-tolil)piperazin-1 -il)etil)dihidrofuran-2(3H)-ona;
3.3- dietil-5-(2-(4-(3-metoxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; 3.3- d ietil-5-(2-(4-(3-hidroxifenil)piperazin-1 -il)etil)dihidrofu ran-2(3H)-ona; 5-(2-(4-(2,6-dimetilfenil)piperazin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona; 3.3- dietil-5-(2-(4-(o-tolil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
3.3- dietil-5-(2-(4-(2-isopropilfenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; 5-(2-(4-(2,4-dimetilfenil)piperazin-1 -il)etil)-3,3-dietildihidrofuran-2(3H)-ona; 3- (2-(4-(2-isopropilfenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona; 3-(2-(4-(2-(tert-butil)fenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona;
3-(2-(4-(2,6-diisopropilfenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona; 3-(2-(4-(2-morfolinofenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona;
3-(2-(4-([1,1'-bifenil]-2-il)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona;
3-(2-(4-(2-(1H-pirrol-1-il)fenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona; 3-(2-(4-(2-yodofenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona;
N-(2-(4-(2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil)piperazin-1-il)fenil)acetamida; 5-nitro-2-(4-(2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil)piperazin-1-il)benzonitrilo; y 3-(2-(4-(p-tolil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona;
o una sal derivada farmacéuticamente aceptable.
2. Compuesto según la reivindicación 1 seleccionado del grupo que consiste en:
3,3-dietil-5-(2-(4-(4-hidroxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
3,3-dietil-5-(2-(4-(4-nitrofenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
4-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo;
,3-dietil-5-(2-(4-(p-tolil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
,3-dietil-5-(2-(4-(2-hidroxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
,3-dietil-5-(2-(4-(3-metoxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
,3-dietil-5-(2-(4-(3-hidroxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
-(2-(4-(2,6-dimetilfenil)piperazin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona;
-(2-(4-(4-aminofenil)piperazin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona;
,3-dietil-5-(2-(4-(2-isopropilfenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
,3 -d ie t i l-5 -(2 -(4 -(o - to l i l)p ip e ra z in -1 - i l)e t i l) d ih id ro fu ra n -2 (3 H ) -o n a ;
5-(2-(4-(2,4-dimetilfenil)piperazin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona;
3-(2-(4-(2-isopropilfenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona;
3-(2-(4-(2-(tert-butil)fenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona;
3-(2-(4-(2-morfolinofenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona; y
3,3-dietil-5-(2-(4-(2-metoxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; o una sal derivada farmacéuticamente aceptable.
3. Composición farmacéutica que comprende una cantidad eficaz de al menos un compuesto según la reivindicación 1 o la reivindicación 2.
4. Composición farmacéutica según la reivindicación 3, que comprende además al menos un excipiente.
5. Composición farmacéutica según la reivindicación 3 o la reivindicación 4, donde el compuesto se selecciona del grupo que consiste en:
2 -(4 -(2 -(4 ,4 -d ie t i l- 5 -o x o te t ra h id ro fu ra n -2 - i l) e t i l)p ip e ra z in -1 - i l)b e n z o n it r i lo ;
3.3- dietil-5-(2-(4-(4-metoxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
3.3- dietil-5-(2-(4-(4-hidroxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
3.3- dietil-5-(2-(4-(4-nitrofenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
3.3- dietil-5-(2-(4-(2-metoxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
4-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo;
3.3- dietil-5-(2-(4-(2-hidroxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
5-(2-(4-(4-aminofenil)piperazin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona;
3.3- d ietil-5-(2-(4-(p-tolil)piperazin-1 -il)etil)dihidrofu ran-2(3H)-ona;
3.3- dietil-5-(2-(4-(3-metoxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
3,3-d ietil-5-(2-(4-(3-hidroxifenil)piperazin-1 -il)etil)dihidrofu ran-2(3H)-ona;
5-(2-(4-(2,6-dimetilfenil)piperazin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona;
3.3- dietil-5-(2-(4-(o-tolil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
3.3- dietil-5-(2-(4-(2-isopropilfenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
5-(2-(4-(2,4-dimetilfenil)piperazin-1 -il)etil)-3,3-dietildihidrofu ran-2(3H)-ona;
3-(2-(4-(2-isopropilfenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona;
3-(2-(4-(2-(tert-butil)fenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona;
3-(2-(4-(2,6-diisopropilfenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona;
3-(2-(4-(2-morfolinofenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona;
3-(2-(4-([1,1'-bifenil]-2-il)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona;
3-(2-(4-(2-(1H-pirrol-1-il)fenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona;
3-(2-(4-(2-yodofenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona;
N-(2-(4-(2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil)piperazin-1-il)fenil)acetamida;
5-nitro-2-(4-(2-(1-oxo-2-oxaspiro[4.4]nonan-3-il)etil)piperazin-1-il)benzonitrilo; y
3-(2-(4-(p-tolil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona;
o una sal derivada farmacéuticamente aceptable.
6. Composición farmacéutica según cualquiera de las reivindicaciones 3 a 5, donde el compuesto se selecciona del grupo que consiste en:
3,3-dietil-5-(2-(4-(4-hidroxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
3,3-dietil-5-(2-(4-(4-nitrofenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
4-(4-(2-(4,4-dietil-5-oxotetrahidrofuran-2-il)etil)piperazin-1-il)benzonitrilo;
3 ,3 -d ie t i l-5 -(2 -(4 -(p - to l i l)p ip e ra z in -1 - i l)e t i l) d ih id ro fu ra n -2 (3 H ) -o n a ;
,3-dietil-5-(2-(4-(2-hidroxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
,3-dietil-5-(2-(4-(3-metoxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
,3-dietil-5-(2-(4-(3-hidroxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
-(2-(4-(2,6-dimetilfenil)piperazin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona;
-(2-(4-(4-aminofenil)piperazin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona;
,3-dietil-5-(2-(4-(2-isopropilfenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona;
,3 -d ie t i l-5 -(2 -(4 -(o - to l i l)p ip e ra z in -1 - i l)e t i l) d ih id ro fu ra n -2 (3 H ) -o n a ;
5-(2-(4-(2,4-dimetilfenil)piperazin-1-il)etil)-3,3-dietildihidrofuran-2(3H)-ona;
3-(2-(4-(2-isopropilfenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona;
3-(2-(4-(2-(tert-butil)fenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona;
3-(2-(4-(2-morfolinofenil)piperazin-1-il)etil)-2-oxaspiro[4.4]nonan-1-ona; y
3,3-dietil-5-(2-(4-(2-metoxifenil)piperazin-1-il)etil)dihidrofuran-2(3H)-ona; o una sal derivada farmacéuticamente aceptable.
7. Compuesto según la reivindicación 1 o la reivindicación 2 o una composición farmacéutica según cualquiera de las reivindicaciones 3 a 6 para usar en un método de tratamiento de trastorno del ritmo circadiano, depresión, esquizofrenia, inflamación neurogénica, hipertensión, enfermedades vasculares periféricas, migraña, dolor neuropático, dolor periférico, alodinia, trastorno de la termorregulación, trastorno del aprendizaje, trastorno de la memoria, trastorno de la señalización en el hipocampo, trastorno del sueño, trastorno de déficit de atención/hiperactividad, ansiedad, trastorno de personalidad elusiva, eyaculación prematura, trastorno alimentario, síndrome premenstrual, trastorno disfónico premenstrual, trastorno afectivo estacional o trastorno bipolar.
8. Compuesto según la reivindicación 1 o la reivindicación 2 o una composición farmacéutica según cualquiera de las reivindicaciones 3 a 6 para el uso según la reivindicación 7 en un método de tratamiento de la depresión.
9. Compuesto según la reivindicación 1 o la reivindicación 2 o una composición farmacéutica según las reivindicaciones 3 a 6 para el uso según la reivindicación 7 en un método de tratamiento de la esquizofrenia.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361776117P | 2013-03-11 | 2013-03-11 | |
| PCT/US2014/023400 WO2014164756A1 (en) | 2013-03-11 | 2014-03-11 | Novel 5-hydroxytryptamine receptor 7 activity modulators and their method of use |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2804545T3 true ES2804545T3 (es) | 2021-02-08 |
Family
ID=51658965
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES14779591T Active ES2804545T3 (es) | 2013-03-11 | 2014-03-11 | Nuevos moduladores de la actividad del receptor de 5-hidroxitriptamina 7 y su método de uso |
Country Status (4)
| Country | Link |
|---|---|
| US (6) | US9802924B2 (es) |
| EP (2) | EP3738955A1 (es) |
| ES (1) | ES2804545T3 (es) |
| WO (1) | WO2014164756A1 (es) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3738955A1 (en) | 2013-03-11 | 2020-11-18 | Temple University Of The Commonwealth System Of Higher Education | Novel 5-hydroxytryptamine receptor 7 activity modulators and their method of use |
| US10544117B2 (en) * | 2014-09-10 | 2020-01-28 | Temple University—Of the Commonwealth System of Higher Education | 5-hydroxytryptamine receptor 7 activity modulators and their method of use |
| UA125631C2 (uk) * | 2016-11-15 | 2022-05-04 | Темпл Юніверсіті-Оф Дзе Коммонвелт Сістем Оф Хайєр Едьюкейшн | Нові модулятори 5-гідрокситриптамінового рецептора 7 і спосіб їх застосування |
| CN108299411B (zh) * | 2017-01-13 | 2021-02-05 | 中国人民解放军军事医学科学院毒物药物研究所 | 4,4-二苯基哌啶类化合物或其可药用盐、药物组合物及用途 |
| JP7365237B2 (ja) * | 2017-03-21 | 2023-10-19 | テンプル・ユニバーシティ-オブ・ザ・コモンウェルス・システム・オブ・ハイアー・エデュケイション | シグマ-2受容体の新規調節物質およびその使用方法 |
| MA49017A (fr) | 2017-03-21 | 2020-02-05 | Univ Temple | Modulateurs du récepteur 7 de la 5-hydroxytryptamine et utilisation de ces derniers en tant qu'agents thérapeutiques |
| WO2019217890A1 (en) * | 2018-05-11 | 2019-11-14 | Temple University-Of The Commonwealth System Of Higher Education | Novel functionalized lactams as modulators of the 5-hydroxytryptamine receptor 7 and their method of use |
| EP4058458A2 (en) * | 2019-11-13 | 2022-09-21 | Temple University - Of The Commonwealth System of Higher Education | Novel functionalized lactones as modulators of the 5-hydroxytryptamine receptor 7 and their method of use |
| EP4058455A1 (en) * | 2019-11-13 | 2022-09-21 | Temple University - Of The Commonwealth System of Higher Education | Novel functionalized lactams as modulators of the 5-hydroxytryptamine receptor 7 and their method of use |
Family Cites Families (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20040064499A1 (en) | 2002-09-26 | 2004-04-01 | Kasra Kasravi | Method and system for active knowledge management |
| BRPI0406704A (pt) | 2003-01-31 | 2005-12-20 | Pfizer Prod Inc | Antagonistas de 5ht~7~ e agonistas inversos |
| EP1875899A1 (en) | 2006-06-29 | 2008-01-09 | Laboratorios Del Dr. Esteve, S.A. | Use of 5HT7 receptor agonists for the treatment of pain |
| ATE548365T1 (de) | 2007-10-12 | 2012-03-15 | Lilly Co Eli | 5-ht7-rezeptorantagonisten |
| US7902091B2 (en) | 2008-08-13 | 2011-03-08 | Varian Semiconductor Equipment Associates, Inc. | Cleaving of substrates |
| EP2341912B1 (en) | 2008-09-05 | 2014-01-22 | Supernus Pharmaceuticals, Inc. | Method of treatment of attention deficit/hyperactivity disorder (adhd) |
| WO2010069390A1 (en) | 2008-12-19 | 2010-06-24 | Nokia Siemens Networks Oy | Method and device for data processing in an udwdm network and communication system comprising such device |
| WO2014085413A1 (en) | 2012-11-28 | 2014-06-05 | Temple University - Of The Commonwealth System Of Higher Education | Disubstituted oxazolidin-2-ones 5-hydroxytryptamine receptor 2b activity modulators |
| EP3738955A1 (en) * | 2013-03-11 | 2020-11-18 | Temple University Of The Commonwealth System Of Higher Education | Novel 5-hydroxytryptamine receptor 7 activity modulators and their method of use |
| US10544117B2 (en) | 2014-09-10 | 2020-01-28 | Temple University—Of the Commonwealth System of Higher Education | 5-hydroxytryptamine receptor 7 activity modulators and their method of use |
| WO2016183150A1 (en) | 2015-05-12 | 2016-11-17 | Temple University-Of The Commonwealth System Of Higher Education | Novel sigma-2 receptor binders and their method of use |
| UA125631C2 (uk) | 2016-11-15 | 2022-05-04 | Темпл Юніверсіті-Оф Дзе Коммонвелт Сістем Оф Хайєр Едьюкейшн | Нові модулятори 5-гідрокситриптамінового рецептора 7 і спосіб їх застосування |
| JP7365237B2 (ja) | 2017-03-21 | 2023-10-19 | テンプル・ユニバーシティ-オブ・ザ・コモンウェルス・システム・オブ・ハイアー・エデュケイション | シグマ-2受容体の新規調節物質およびその使用方法 |
| MA49017A (fr) | 2017-03-21 | 2020-02-05 | Univ Temple | Modulateurs du récepteur 7 de la 5-hydroxytryptamine et utilisation de ces derniers en tant qu'agents thérapeutiques |
| WO2019217890A1 (en) | 2018-05-11 | 2019-11-14 | Temple University-Of The Commonwealth System Of Higher Education | Novel functionalized lactams as modulators of the 5-hydroxytryptamine receptor 7 and their method of use |
-
2014
- 2014-03-11 EP EP20168684.7A patent/EP3738955A1/en active Pending
- 2014-03-11 ES ES14779591T patent/ES2804545T3/es active Active
- 2014-03-11 US US14/774,961 patent/US9802924B2/en active Active
- 2014-03-11 WO PCT/US2014/023400 patent/WO2014164756A1/en not_active Ceased
- 2014-03-11 EP EP14779591.8A patent/EP2970223B1/en active Active
-
2017
- 2017-09-27 US US15/716,752 patent/US10239868B2/en active Active
- 2017-09-27 US US15/716,773 patent/US10287274B2/en active Active
-
2019
- 2019-05-14 US US16/411,534 patent/US10676464B2/en active Active
-
2020
- 2020-04-28 US US16/861,075 patent/US11897870B2/en active Active
-
2023
- 2023-12-19 US US18/544,952 patent/US12503458B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US20180016262A1 (en) | 2018-01-18 |
| US11897870B2 (en) | 2024-02-13 |
| US20190367493A1 (en) | 2019-12-05 |
| US20200317648A1 (en) | 2020-10-08 |
| EP2970223A4 (en) | 2016-11-30 |
| US20240425487A1 (en) | 2024-12-26 |
| WO2014164756A1 (en) | 2014-10-09 |
| US10676464B2 (en) | 2020-06-09 |
| US9802924B2 (en) | 2017-10-31 |
| US20180016261A1 (en) | 2018-01-18 |
| EP3738955A1 (en) | 2020-11-18 |
| US10239868B2 (en) | 2019-03-26 |
| US20160016941A1 (en) | 2016-01-21 |
| EP2970223A1 (en) | 2016-01-20 |
| US12503458B2 (en) | 2025-12-23 |
| EP2970223B1 (en) | 2020-04-15 |
| US10287274B2 (en) | 2019-05-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2804545T3 (es) | Nuevos moduladores de la actividad del receptor de 5-hidroxitriptamina 7 y su método de uso | |
| US12338245B2 (en) | 5-hydroxytryptamine receptor 7 modulators and their use as therapeutic agents | |
| US12269809B2 (en) | 5-hydroxytryptamine receptor 7 activity modulators and their method of use | |
| ES3050660T3 (en) | 3-(2-(4-phenylpiperazin-1-yl)ethyl)-2-oxa-8-azaspiro[4.5]decan-1-one derivatives and related compounds as 5-hydroxytryptamine receptor 7 (5-ht7) modulators for treating e.g. inflammatory bowel disease, circadian rhythm disorder or depression | |
| EP3600290A1 (en) | Novel modulators of the sigma-2 receptor and their method of use | |
| WO2016183150A1 (en) | Novel sigma-2 receptor binders and their method of use | |
| WO2014085413A1 (en) | Disubstituted oxazolidin-2-ones 5-hydroxytryptamine receptor 2b activity modulators | |
| RU2676475C2 (ru) | Новые функционализированные 1,3-бензолдиолы и способ их применения для лечения печеночной энцефалопатии | |
| BR112019009908B1 (pt) | Novos moduladores do receptor 7 de 5-hidroxitriptamina e seu uso | |
| BR112016016138B1 (pt) | Novos 1,3-benzenodióis funcionalizados e método de uso dos mesmos para o tratamento da encefalopatia hepática | |
| EA039988B1 (ru) | Новые модуляторы 5-гидрокситриптаминового рецептора 7 и способ их применения |