ES2811127T3 - Composiciones para lograr niveles plasmáticos deseados del factor 2 de crecimiento glial - Google Patents
Composiciones para lograr niveles plasmáticos deseados del factor 2 de crecimiento glial Download PDFInfo
- Publication number
- ES2811127T3 ES2811127T3 ES16182139T ES16182139T ES2811127T3 ES 2811127 T3 ES2811127 T3 ES 2811127T3 ES 16182139 T ES16182139 T ES 16182139T ES 16182139 T ES16182139 T ES 16182139T ES 2811127 T3 ES2811127 T3 ES 2811127T3
- Authority
- ES
- Spain
- Prior art keywords
- ggf2
- myelination
- activation
- erk
- cell
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
- A61K38/1883—Neuregulins, e.g.. p185erbB2 ligands, glial growth factor, heregulin, ARIA, neu differentiation factor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
- A61K38/51—Lyases (4)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6872—Intracellular protein regulatory factors and their receptors, e.g. including ion channels
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6893—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids related to diseases not provided for elsewhere
- G01N33/6896—Neurological disorders, e.g. Alzheimer's disease
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/475—Assays involving growth factors
- G01N2333/4756—Neuregulins, i.e. p185erbB2 ligands, glial growth factor, heregulin, ARIA, neu differentiation factor
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/28—Neurological disorders
- G01N2800/285—Demyelinating diseases; Multipel sclerosis
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Biomedical Technology (AREA)
- Immunology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Molecular Biology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Epidemiology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Cell Biology (AREA)
- Gastroenterology & Hepatology (AREA)
- Zoology (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- Food Science & Technology (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Hospice & Palliative Care (AREA)
- Psychiatry (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Peptides Or Proteins (AREA)
Abstract
Factor de crecimiento glial 2 (GGF2) para su uso en la promocion de la remielinizacion celular en un paciente, donde el GGF2 se administra al paciente en una cantidad de 500 ng +/- 15% de GGF2 por kg de peso corporal.
Description
DESCRIPCIÓN
Composiciones para lograr niveles plasmáticos deseados del factor 2 de crecimiento glial
Campo de la invención
La presente invención se refiere a la administración del factor 2 de crecimiento glial (GGF2) a un paciente que lo necesite, para lograr niveles séricos de GGF2 dentro de una ventana terapéutica deseada, determinada en función de la enfermedad o del trastorno que afecta al paciente.
Antecedentes
Las Neuregulinas (NRG) y los receptores de NRG comprenden un sistema de tirosina quinasa de receptor de factor de crecimiento para la señalización de célula-célula que está involucrado en la organogénesis en nervios, músculos, epitelios y otros tejidos (Lemke, MoI. Cell. Neurosci. 7:247-262, 1996; Burden et al., Neuron 18: 847-855, 1997). La familia de NRG consta de tres genes que codifican numerosos ligandos que contienen un factor similar al factor de crecimiento epidérmico (EGF), inmunoglobulina (Ig) y otros dominios reconocibles. Numerosas isoformas secretadas y unidas a la membrana funcionan como ligandos en este sistema de señalización. Todos los receptores para NRG son miembros de la familia de receptores EGF (EGFR) e incluyen EGFR (o ErbB1), ErbB2, ErbB3 y ErbB4, también conocidos como HER1 a HER4, respectivamente, en humanos (Meyer et al., Development 124:3575-3586, 1997; Orr-Urtreger et al., Proc. Natl. Acad. Sci. USA 90: 1867-71, 1993; Marchionni et al., Nature 362: 312-8, 1993; Chen et al., J. Comp. Neurol 349:389-400, 1994; Corfas et al., Neuron 30-07-2020 13814:103 -115, 1995; Meyer et al., Proc. Natl. Acad. Sci. USA 91: 1064-1068, 1994; y Pinkas-Kramarski et al., Oncogene 15:2803-2815, 1997).
Los tres genes NRG, Nrg-1, Nrg-2 y Nrg-3, se asignan a loci cromosómicos distintos (Pinkas-Kramarski et al., Proc. Natl. Acad. Sci. Estados Unidos 91: 9387-91, 1994; Carraway et al., Nature 387:512-516, 1997; Chang et al., Nature 387:509-511, 1997; y Zhang et al., Proc. Natl. Acad. Sci. USA 94: 9562-9567, 1997), y codifican colectivamente un conjunto diverso de proteínas NRG. Los más estudiados hasta la fecha son los productos génicos de Nrg-1, que comprenden un grupo de aproximadamente 15 isoformas distintas relacionadas estructuralmente (Lemke, MoI. Cell. Neurosci. 7: 247-262, 1996 y Peles y Yarden, BioEssays 15:815-824, 1993). Las primeras isoformas identificadas de NRG-1 incluyeron el factor de diferenciación de Neu (Nd F; Peles et al., Cell 69, 205-216, 1992 y Wen et al., Cell 69, 559-572, 1992), Heregulin (HRG; Holmes et al., Science 256:1205-1210, 1992), inductor de actividad de receptor de acetilcolina (a RiA; Falls et al., Cell 72: 801-815, 1993), y los factores de crecimiento glial GGFl, GGF2 y GGF3 (Marchionni et al. al. Nature 362:312-8, 1993).
El gen Nrg-2 se identificó por clonación de homología (Chang et al., Nature 387: 509-512, 1997; Carraway et al., Nature 387: 512-516, 1997; y Higashiyama et al., J. Biochem. 122: 675- 680, 1997) y mediante enfoques genómicos (Busfield et al., MoI. Cell. Biol. 17:4007-4014, 1997). Los ADNc de NRG-2 también se conocen como activadores derivados de neural y timo de ErbB quinasas (NTAK; Genbank Accession No. AB005060), divergente de 57 Neuregulina (Don-1) y factor de crecimiento derivado del cerebelo (CDGF; solicitud PCT WO 97/09425). La evidencia experimental muestra que las células que expresan ErbB4 o la combinación ErbB2/ErbB4 pueden mostrar probablemente una respuesta particularmente robusta a NRG-2 (Pinkas-Kramarski et al., MoI. Cell. Biol. 18:6090-6101, 1998). También se sabe que el producto del gen Nrg-3 (Zhang et al., Supra) se une y activa los receptores ErbB4 (Hijazi et al., Int. J. Oncol. 13:1061-1067, 1998).
Un dominio similar a EGF está presente en el núcleo de todas las formas de NRGs, y es necesario para la unión y activación de los receptores ErbB. Las secuencias de aminoácidos deducidas de los dominios similares a EGF codificados en los tres genes son idénticas en aproximadamente 30-40% (comparaciones por pares). Además, parece haber al menos dos subformas de dominios similares a EGF en NRG-1 y NRG-2, que pueden conferir diferentes bioactividades y potencias específicas de tejido.
Las respuestas celulares a NRG están mediadas a través de las tirosinas quinasas de receptor NRG EGFR, ErbB2, ErbB3 y ErbB4 de la familia de receptores del factor de crecimiento epidérmico (Busfield et al., 1997, MoI Cell Biol.
17:4007-14; Carraway et al., 1997, Nature 387: 512-6; Chang et al., 1997, Nature 387: 509-12). La unión de alta afinidad de todos los NRG está mediada principalmente a través de ErbB3 o ErbB4 (Ferguson et al., 2000, EMBO J.
19: 4632-43). La unión de los ligandos NRG conduce a la dimerización con otras subunidades ErbB y a la transactivación por fosforilación en residuos de tirosina específicos (Honegger et al., 1990, MoI Cell Biol. 76 10:4035-44; Lemmon y Schlessinger, 1994, Trends Biochem Sci. 19:459-63; Heldin, 1995, Cell. 80:213-23; Hubbard et al., 1998, J Biol Chem. 273:11987-90). En determinados entornos experimentales, casi todas las combinaciones de receptores ErbB parecen ser capaces de formar dímeros en respuesta a la unión de las isoformas NRG-I. Sin embargo, ErbB2 parece ser una pareja de dimerización preferido que puede desempeñar un papel importante en la estabilización del complejo ligando-receptor.
Se ha demostrado que GGF2 promueve la proliferación, diferenciación y protección de las células de Schwann (Goodearl et al., 1993, J Biol Chem. 268:18095-102; Minghetti et al., 1996 J Neurosci Res. 43:684-93). La expresión de NRG-I, ErbB2 y ErbB4 también es necesaria para la trabeculación del miocardio ventricular durante el desarrollo del ratón (Meyer y Birchmeier 1995, Nature 378:386-90; Gassmann et al., 1995, Nature 378:390-4; Kramer et al., 1996, Proc Natl Acad Sci USA 93:4833-8). También se ha demostrado que GGF2 promueve la proliferación y protección de
las células de cardiomiocitos (Zhao et al., 1998, J Biol Chem 273:10261-10269). La neuroprotección mediada por GGF2 también se ha demostrado en modelos animales de accidente cerebrovascular, aunque los parámetros relacionados con la dosificación permanecen indefinidos.
La divulgación en el presente documento promueve el uso de GGF2 con respecto a aplicaciones terapéuticas al presentar una guía para los procedimientos de administración de GGF2 que optimizan el beneficio terapéutico, al tiempo que limitan los efectos adversos. En el presente documento se definen ventanas terapéuticas objetivo para los niveles de concentración sérica de GGF2 que se especifican con respecto a afecciones de enfermedad particulares.
El documento WO2004/110359 divulga composiciones capaces de usarse en el tratamiento de lesiones de la médula espinal y trastornos relacionados del sistema nervioso central (SNC). El documento WO94/04560 divulga un factor mitogénico de células de Schwann. Ogata et al 2004 24(30):6724-6732 revela información sobre la mielinización de células de Schwann. Maurel et al 2000 20(12):4635-4645 revela información sobre la regulación axonal de la proliferación y supervivencia de células de Schwann. Syed et al. 2010 30(17):6122-6131 revela información sobre neuregulina soluble.
Resumen
En un aspecto, la invención proporciona el factor 2 de crecimiento glial (GGF2) para su uso en la promoción de la remielinización celular en un paciente, en donde el GGF2 se administra al paciente en una cantidad de 500 ng /- 15% de GGF2 por kg de peso corporal.
En otro aspecto, la invención proporciona una composición farmacéutica que comprende el GGF2 para su uso de acuerdo con la invención y un inhibidor de la vía Mekl/Erk, en la que el inhibidor de la vía Mekl/Erk se selecciona del grupo que consiste en Arctigenin, PD 98059, SB202190, SB203580, SP600125, U0126, tipifarnib (Zarnestra®), sorafenib, ISIS 5132, CI-1040 y PD 0325901.
En otro aspecto, la invención proporciona GGF2 para su uso según la invención o la composición farmacéutica según la invención, en donde la célula es una célula de Schwann.
La divulgación en el presente documento se refiere a la administración de GGF2 a un paciente que lo necesite para alcanzar un nivel plasmático de GGF2 en suero dentro de una ventana terapéutica diana, determinada como efectiva en el tratamiento de una enfermedad o trastorno. De acuerdo con la divulgación, GGF2 puede administrarse en una composición farmacéutica.
De acuerdo con la descripción, se presenta un procedimiento para evitar la inhibición de la mielinización de células de Schwann después de la administración del factor 2 de crecimiento glial (GGF2) en un sujeto; dicho procedimiento comprende: proporcionar a un sujeto que necesita mielinización neuronal; proporcionar GGF2 en un vehículo farmacéuticamente aceptable; administrar el GGF2 al sujeto; y determinar que la cantidad de GGF2 es menor que la cantidad que inhibe la mielinización de las células de Schwann.
Otra divulgación se refiere a un procedimiento para promover la mielinización en un paciente afectado por una enfermedad o trastorno asociado con niveles reducidos de mielinización; el procedimiento comprende: seleccionar al paciente afectado por una enfermedad o trastorno asociado con niveles reducidos de mielinización; administrar el factor 2 de crecimiento glial (GGF2) al paciente en una cantidad de aproximadamente 500 ng de GGF2 por kg de peso corporal, por lo cual se promueve la mielinización.
Otra divulgación más se refiere a un procedimiento para promover la mielinización en un paciente afectado por una enfermedad o trastorno asociado con niveles reducidos de mielinización; el procedimiento comprende: seleccionar un paciente afectado por una enfermedad o trastorno asociado con niveles reducidos de mielinización; y administrar el factor 2 de crecimiento glial (GGF2) al paciente en una cantidad que alcance un nivel plasmático de aproximadamente 0.01 nM GGF2.
Una divulgación más se refiere a un procedimiento para ampliar el intervalo de dosis terapéuticas para GGF2 cuando se usa GGF2 para facilitar la mielinización; el procedimiento comprende:
seleccionar un sujeto con una enfermedad o trastorno asociado con niveles reducidos de mielinización;
administrar GGF2 y un inhibidor de la vía Mekl/Erk al paciente, y, por lo que la mielinización mediada por GGF2 se produce a dosis más altas de GGF2 de lo que ocurriría en ausencia de administración del inhibidor de la vía Mekl/Erk.
Otra divulgación se refiere a un procedimiento para determinar si una cantidad de GGF2 es una cantidad terapéuticamente efectiva para promover la mielinización; el procedimiento comprende: proporcionar a un sujeto que recibe terapia con GGF2; y medir los niveles de proteína c-Jun en el sujeto, por lo que un aumento en c-Jun en relación con los niveles basales de c-Jun indica que la cantidad de GGF2 está cerca de un umbral máximo de eficacia terapéutica para promover la mielinización.
En una realización particular de la invención, GGF2 se administra a un mamífero usando un régimen de dosificación dirigido a lograr una ventana terapéutica objetivo estrecha de las concentraciones plasmáticas de GGF2.
Como se indica aquí, se sabe que GGF2 puede promover la proliferación, diferenciación y protección de las células de Schwann. También se ha demostrado que g GF2 promueve la remielinización y reduce los síntomas en modelos animales de esclerosis múltiple, incluida la encefalomielitis autoinmune experimental. Sin embargo, en algunas circunstancias (por ejemplo, a altas concentraciones de GGF2), el GGF2 puede prevenir la mielinización de las neuronas co-cultivadas con las células de Schwann.
Los datos presentados en este documento demuestran que GGF2 es realmente capaz de promover la mielinización de los nervios periféricos, pero enseña que se requiere una dosificación precisa de GGF2 a un mamífero que lo necesite para lograr la mielinización de los nervios periféricos promovida, mediada por GGF2. Como se enseña aquí, GGF2 se administra para que esté dentro de una ventana terapéutica de las concentraciones plasmáticas de GGF2 para promover la mielinización. En ausencia de los resultados presentados aquí, no se aprecia la estrecha ventana terapéutica de las concentraciones plasmáticas de GGF2 requeridas para promover la mielinización en un mamífero que lo necesita.
Los datos presentados en este documento también demuestran que GGF2 es suficiente para promover la mielinización y rescatar el defecto de mielinización en axones deficientes en CRD-Nrg1. Sin embargo, a altas concentraciones, GGF2 inhibe la mielinización de una manera dependiente de Erk. Los resultados actuales demuestran que GGF2 es capaz de promover e inhibir la mielinización dependiendo de la concentración presentada a las células de Schwann.
Por consiguiente, la presente invención se refiere al sorprendente descubrimiento de que existe una correlación positiva hasta ahora no realizada entre la activación de la vía PI3-quinasa mediada por GGF2 y la promoción de la mielinización y existe una correlación negativa entre la activación de la vía Mekl/Erk mediada por GGF2 y la promoción de la mielinización. Enunciado de modo alternativo, los presentes inventores descubrieron que la administración de GGF2 puede ajustarse finamente para promover la mielinización mediante la evaluación de los niveles de activación de estas vías. De acuerdo con la presente divulgación, una ventana terapéutica objetivo para GGF2 con respecto a promover la mielinización en un sujeto es una cantidad de GGF2 que promueve la activación de la vía de PI3-quinasa (evaluada, por ejemplo, detectando Akt fosforilada) en ausencia de activación detectable de la vía de Mekl/Erk (evaluada, por ejemplo, mediante la detección de Erk fosforilada).
Las formulaciones y composiciones de la presente invención exhiben un perfil de liberación específico deseado que maximiza el efecto terapéutico mientras minimiza los efectos secundarios adversos. El perfil de liberación deseado puede describirse en términos de la concentración plasmática máxima del fármaco o agente activo (Cmax) y la concentración plasmática del fármaco o agente activo en un intervalo de dosificación específico (Ctau). Una relación de Cmax a Ctau. (Cmax. Ctau) puede calcularse a partir de la Cmax y Ctau observadas. Un intervalo de dosificación (tau) es el tiempo transcurrido desde la última administración del fármaco o agente activo. En la presente solicitud, el intervalo de dosificación (tau) puede ser, por ejemplo, doce (12) horas, en cuyo caso Ctau es la concentración del fármaco o agente activo a las doce (12) horas desde la última administración.
Además, las formulaciones y composiciones de la presente divulgación exhiben un perfil de liberación deseado que puede describirse en términos de la concentración plasmática máxima del fármaco o agente activo en estado estacionario (CmaxSS) y la concentración plasmática mínima del fármaco o agente activo en estado estacionario (CminSS). El estado estacionario se observa cuando la velocidad de administración (absorción) es igual a la velocidad de eliminación del fármaco o agente activo. Se puede calcular una relación de CmaxSS a CminSS (CmaxSS. CminSS) a partir de las CmaxSS y CminSS observadas. Además, las formulaciones y composiciones de la presente divulgación exhiben un perfil de liberación deseado que puede describirse en términos de la concentración plasmática máxima promedio del fármaco o agente activo en estado estacionario (CavSS).
En una forma de realización de la divulgación dirigida a un paciente que necesita remielinización, los niveles séricos máximos objetivo de GGF2 son aproximadamente 0.01 nM.
En una forma de realización de la divulgación dirigida a un paciente que necesita remielinización, los niveles séricos máximos objetivo de GGF2 están en o alrededor de cualquiera de los siguientes valores, o varían entre los siguientes valores desde aproximadamente 0.001 a 0.01 ng/ml; 0.01 a 0.1 ng/ml; 0.1 a 1.0 ng/ml; 1.0 a 10 ng/ml; 10 a 100 ng/ml; o 100 a 1000 ng/ml. En una realización particular, el nivel sérico máximo objetivo es aproximadamente 1.0 ng/ml.
En una forma de realización de la divulgación dirigida a un paciente que ha tenido un accidente cerebrovascular, los niveles séricos máximos objetivo de GGF2 están en o alrededor de cualquiera de los siguientes valores, o varían entre los siguientes valores de aproximadamente 0.00001 a 0.0001 ng/ml; 0.0001 a 0.001 ng/ml; 0.001 a 0.01 ng/ml; 0.001 a 0.01 ng/ml; 0.01 a 0.1 ng/ml; 0.1 a 1.0 ng/ml; 1.0 a 10 ng/ml; 10 a 100 ng/ml; 100 a 1000 ng/ml; 1000 a 10000 ng/ml; o 10000 a 100000 ng/ml. En una divulgación particular, el nivel sérico máximo objetivo es de aproximadamente 0.2 microgramos/ml.
En una forma de realización de la divulgación dirigida a un paciente que tiene neuropatía, los niveles séricos máximos objetivo de GGF2 están en o alrededor de cualquiera de los siguientes valores, o varían entre los siguientes valores de aproximadamente 0.001 a 0.01 ng/ml; 0.01 a 0.1 ng/ml; 0.1 a 1.0 ng/ml; 1.0 a 10 ng/ml; 10 a 100 ng/ml; o 100 a 1000 ng/ml. En una divulgación particular, el nivel sérico máximo objetivo es aproximadamente 6.25 ng/ml.
En una forma de realización de la divulgación dirigida a un paciente que tiene insuficiencia cardíaca, los niveles séricos máximos objetivo de GGF2 están en o alrededor de cualquiera de los siguientes valores, o varían entre los siguientes valores de aproximadamente 0.001 a 0.01 ng/ml; 0.01 a 0.1 ng/ml; 0.1 a 1.0 ng/ml; 1.0 a 10 ng/ml; 10 a 100 ng/ml; o 100 a 1000 ng/ml. En una divulgación particular, el nivel sérico máximo objetivo es de aproximadamente 6,8 microgramos/ml.
De acuerdo con la presente invención, las composiciones farmacéuticas que comprenden GGF2 para usar según la invención pueden administrarse a través de diferentes vías conocidas por los expertos en la técnica. Se puede emplear cualquier vía de administración apropiada, por ejemplo, intravenosa, parenteral, subcutánea, intramuscular, intracraneal, intraorbital, oftálmica, intraventricular, intracapsular, intraespinal, intracisternal, intraperitoneal, intranasal, aerosol, oral o tópica (por ejemplo, aplicando un parche adhesivo que lleva una formulación capaz de cruzar la dermis y entrar en el torrente sanguíneo). Se prevé que la administración oral incluya formas de dosificación oral de liberación sostenida que comprenden GGF2. Una composición farmacéutica de GGF2, como se describe en el presente documento, puede usarse para tratar individuos afectados con trastornos neurológicos en los que dicha composición farmacéutica maximiza el efecto terapéutico, mientras minimiza los efectos secundarios adversos.
En una primera forma de realización de la presente divulgación, GGF2 se administra a un mamífero afectado por un trastorno neurológico asociado con la desmielinización, en donde el GGF2 se administra en un régimen de dosificación para lograr y mantener una ventana terapéutica objetivo estrecha de las concentraciones plasmáticas de GGF2. Como se enseña en el presente documento, es necesaria una dosificación precisa de g GF2 para lograr los niveles plasmáticos de GGF2 en suero requeridos para la eficacia terapéutica con respecto a inducir mielinización en un sujeto que lo necesita. Los ejemplos de trastornos desmielinizantes para los cuales es necesaria una dosificación adecuada de GGF2 para lograr la eficacia terapéutica incluyen el síndrome de Guillain-Barré, polineuropatía desmielinizante inflamatoria crónica, desmielinización periférica debido a lesión traumática, esclerosis múltiple, neuritis óptica, desmielinización central debido a lesión traumática, transversal mielitis, leucoencefalopatía multifocal progresiva, enfermedad de Devic (neuromielitis óptica), encefalomielitis aguda diseminada, adrenoleucodistrofia y adrenoleucooneuropatía.
En una segunda forma de realización de la presente divulgación, GGF2 se administra a un mamífero afectado con un trastorno muscular cardíaco, tal como insuficiencia cardíaca congestiva, infarto de miocardio, lesión por reperfusión, cardiotoxicidad química, viral o idiopática, arritmias, en donde el GGF2 se administra en un régimen de dosificación para lograr una ventana terapéutica objetivo de las concentraciones plasmáticas de GGF2.
En una tercera forma de realización de la presente divulgación, GGF2 se administra a un mamífero que ha sufrido un accidente cerebrovascular, lesión de la médula espinal o lesión cerebral traumática, en donde el GGF2 se administra en un régimen de dosificación para lograr una ventana terapéutica objetivo de las concentraciones plasmáticas de GGF2.
Se apreciará que, para cualquiera de las aplicaciones detalladas en este documento, GGF2 puede administrarse en cualquier forma adecuada, o como un componente en una composición farmacéutica y por cualquier medio, todos los cuales se describen en este documento y/o se entienden en la técnica.
Por consiguiente, la presente invención está dirigida a la identificación de una ventana terapéutica objetivo con respecto a un nivel plasmático terapéuticamente efectivo de GGF2. La ventana terapéutica objetivo varía dependiendo de la enfermedad o trastorno que afecta al paciente y la actividad deseada conferida al lograr el nivel plasmático de GGF2 terapéuticamente efectivo apropiado.
Un procedimiento para seleccionar individuos basado en la presentación de síntomas también se incluye aquí. También se incluye un procedimiento para seleccionar individuos basado en la capacidad de respuesta para lograr el nivel plasmático de GGF2 terapéuticamente efectivo, como se indica para cada aplicación, también se incluye en este documento.
Además de los procedimientos de tratamiento establecidos anteriormente, la presente divulgación se extiende al uso de cualquiera de los compuestos divulgados aquí para la preparación de medicamentos o como medicamentos que pueden administrarse para tales tratamientos, así como a tales compuestos para tratamientos divulgados y especificados.
La presente divulgación también abarca una composición farmacéutica que comprende GGF2 o un dominio EGFL y un inhibidor de la vía Mekl/Erk y su uso en el tratamiento de un paciente afectado por una enfermedad o trastorno asociado con niveles reducidos de mielinización.
Breve descripción de los dibujos
La Figura 1A-C muestra (A) la activación de Akt y MAPK inducida por GGF2 en co-cultivos de neuronas DRG de células de Schwann. Los co-cultivos de células Schwann-DRG en condiciones mielinizantes se trataron con GGF (0.6 |jM) y 20 minutos después, se evaluaron los niveles de activación de Akt y MAPK mediante análisis de electrotransferencia Western. (B) Inhibición de la activación de MAPK inducida por GGF2 por U0125. Los cocultivos se pretrataron con dosis crecientes de U0125 durante 30 minutos y luego se estimularon con GGF2. Los cultivos de
control se dejaron sin tratar. La activación de MAPK se evaluó 20 minutos después. (C) La inhibición de la activación de MAPK inducida por GGF2 por U0125 (1 y 3 |j M) revierte el efecto inhibidor de GGF2 sobre la mielinización. Los cocultivos se trataron conjuntamente con g GF2 y U0125 (1 y 3 j M) en condiciones mielinizantes. Diez a doce días después, los cultivos se fijaron y se inmunotiñeron para MBP para evaluar el nivel de mielinización.
La Figura 2 muestra que GGF2 promueve la mielinización a bajas concentraciones. Los cocultivos se trataron con GGF2 a concentraciones que oscilaban entre 0.5 y 1000 pM (0.0005 a 1 nM) en condiciones mielinizantes. Diez a doce días después, la mielinización se evaluó mediante inmunotinción MBP. Más particularmente, las concentraciones de GGF2 de izquierda a derecha son las siguientes: NT, 0.5 pM, 1pM, 3 pM, 10 pM, 30 pM, 300 pM, 600 pM y 1,000 pM, respectivamente. Diez a doce días después, la mielinización se evaluó mediante inmunotinción MBP.
La Figura 3A-F muestra que un efecto inhibidor de GGF sobre la mielinización está mediado por la activación de Mekl/Erk. (A) Los cocultivos de células de Schwann DRG se trataron con GGF (0.01, 0.6 y 1 nM) y 45 minutos después se prepararon los lisados celulares y se determinaron los niveles de Erk activo (p-Erk) y Akt (p-Akt) por análisis de transferencia Western. A 1 nM (en recuadro), GGF indujo la activación de Erk y Akt. (B) Inhibición de la activación de Erk inducida por GGF en cocultivos. Los cocultivos de células Schwann-DRG se pretrataron con U0126 durante 30 minutos y luego se añadió GGF (0.6 nM) en presencia continua de U0126. Después de 45 minutos, se prepararon los lisados celulares y se determinó el nivel de p-Erk y p-Akt. El tratamiento con U0126 inhibió la activación de Erk tanto endógena como inducida por GGF sin afectar la activación de Akt. (C) Imágenes de segmentos de mielina MBP+ formados en cocultivos tratados con GGF o GGF+U0126 (1 nM). El tratamiento con UO 126 abolió el efecto inhibidor de GGF y la mielinización inducida. Los cultivos de control se mantuvieron sin ningún tratamiento (NT). Barra de escala: 100 jm . La cuantificación del resultado se muestra en (D). (E) La inhibición de la actividad de Erk endógena en cocultivos promueve la mielinización. Los cocultivos se trataron con una concentración creciente de U0126 (0.5, 1 y 3 nM) en condiciones mielinizantes y 11 días después se analizó la mielinización como anteriormente. Se observó un aumento significativo en la mielinización en cultivos tratados con U0126. Las barras de error indican ± SE (p <0.001). (F) La inhibición de la activación de Erk inducida por GGF se acompaña de una disminución en c-Jun y un aumento en la expresión de Krox20. Los cocultivos se mantuvieron en condiciones mielinizantes en presencia de GGF o GGF U0126 (0.5, 1 y 3 nM) durante 11 días y los lisados celulares se analizaron para determinar la expresión de MBP, c-Jun y Krox 20. El nivel de actina sirvió como control de carga. La expresión de c-Jun inducida por GGF se reguló a la baja con el tratamiento con U0126. El nivel de proteína Krox 20 pareció incrementado en cultivos tratados con U0126.
La Figura 4A-C muestra que GGF promueve la mielinización a baja concentración. (A) Las células de Schwann se trataron con concentraciones variables de GGF que variaban de 0.0003 a 10 nM) y 20 minutos después se prepararon los lisados celulares y se analizaron los niveles de activación de Erk y Akt mediante transferencia Western (arriba) y análisis densitométrico (abajo). Un aumento en la activación de Akt apareció en un rango de concentración más bajo (en recuadro) en comparación con la activación de Erk. (B) Los cocultivos se trataron con diferentes concentraciones de GGF (0.0005, 0.001,0.003, 0.01,0.03, 0.3, 0.6 e InM) durante 11 días en condiciones mielinizantes, luego se fijaron y se inmuno-tiñeron para MBP y DAPI. Las imágenes del control y los cultivos tratados con 0.01nM de GGF se muestran junto con la cuantificación del resultado (derecha). Se muestra un claro efecto bifásico de GGF que promueve la mielinización a bajas concentraciones (0.0005 a 0.01 nM) mientras inhibe el proceso a una concentración más alta (0.3 nM y superior). (C) La baja concentración de GGF (0.01 nM) aumentó significativamente la mielinización en las neuronas CRD-Nrg1+/' (p = 0.003). Las barras de error muestran ± SEM. Los datos fueron analizados por ANOVA unidireccional (*: p <0.001)
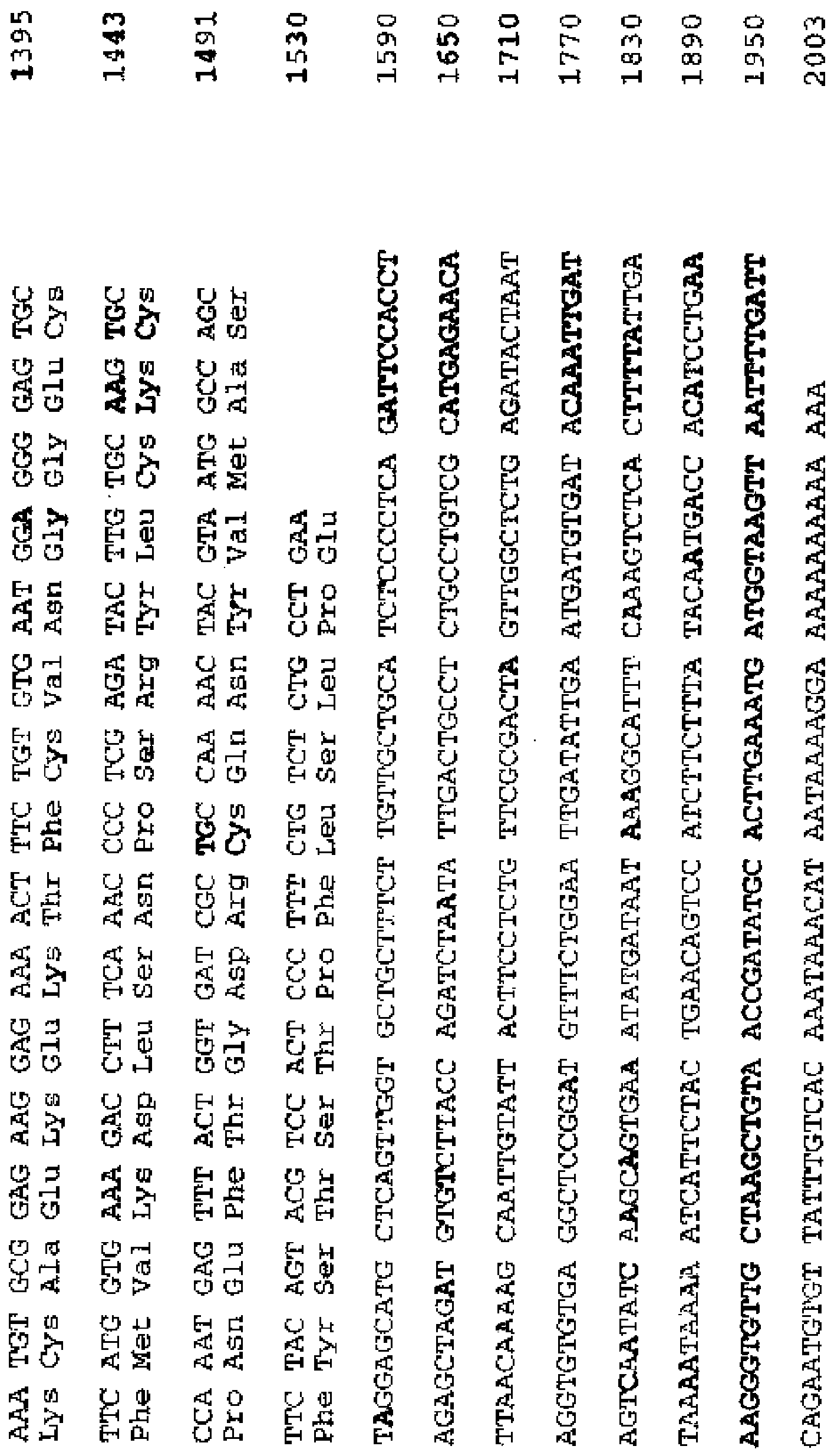
La Figura 5A-D muestra las secuencias de ácido nucleico y de aminoácidos de GGF2 de longitud completa.
Las figuras 6-11 muestran las secuencias de aminoácidos y ácidos nucleicos de los dominios 1-6 semejantes al factor de crecimiento epidérmico (EGFL).
La Figura 12 muestra una tabla relacionada con la nomenclatura de neuregulina.
Descripción detallada de la invención
Los datos presentados en el presente documento demostraron que, para promover la mielinización de los nervios periféricos, GGF2 debe administrarse a un mamífero utilizando un régimen de dosificación dirigido a lograr una ventana terapéutica de, por ejemplo, concentraciones plasmáticas de GGF2 o dosis de GGF2.
Definiciones
Los términos utilizados en este documento tienen significados reconocidos y conocidos por los expertos en la materia; sin embargo, por conveniencia e integridad, los términos particulares y sus significados se exponen a continuación
Como se usa en el presente documento "aproximadamente" significa un valor declarado más o menos otra cantidad; de esta manera se establece un intervalo de valores. En ciertas realizaciones preferidas, "aproximadamente" indica un intervalo relativo a un valor o cantidad base (o núcleo o referencia) más o menos hasta 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1%, .75%, .5%, .25% o .1%.
Por "dominio similar al factor de crecimiento epidérmico" o "dominio similar al EGF" se entiende un motivo de polipéptido codificado por el gen NRG-I, NRG-2 o NRG-3 que se une y activa ErbB2, ErbB3, ErbB4, o combinaciones del mismo, y tiene una similitud estructural con el dominio de unión al receptor de EGF como se describe en Holmes et al., Science 256: 1205-1210, 1992; Pat. estadounidense No. 5,530,109; Pat. estadounidense No. 5,716,930; U.S. Ser. No. 08/461.097; Hijazi et al., Int. J. Oncol. 13:1061-1067, 1998; Chang et al., Nature 387: 509-512, 1997; Carraway et al., Nature 351 387:512 -516, 1997; Higashiyama et al., J Biochem. 122: 675-680, 1997; y WO 97/09425). Véanse las Figuras 10-15 para las secuencias de aminoácidos y ácidos nucleicos de los dominios 1-6 semejantes al factor de crecimiento epidérmico (EGFL).
Por "neuregulina" o "NRG" se entiende un polipéptido que está codificado por un gen o ácido nucleico NRG-I, NRG-2 o NRG-3 (por ejemplo, un ADNc), y se une y activa receptores de ErbB2, ErbB3 o ErbB4, o combinaciones de los mismos.
Por "neuregulina-1", "NRG-1", "heregulina", "GGF2" o "ligando p185erbB2" se entiende un polipéptido que se une directamente a o transactiva el receptor ErbB2 y está codificado por el gen del ligando p185erbB2 descrito en la patente estadounidense No. 5,530,109; patente estadounidense No. 5,716,930; y patente estadounidense 7,037,888. Véanse las Figuras 9A-D para las secuencias de aminoácidos y ácido nucleico de GGF2 de longitud completa. Véase la Figura 12 para una tabla relacionada con la nomenclatura de neuregulina.
Los polipéptidos codificados por los genes NRG-1, NRG-2 y NRG-3 poseen dominios similares a EGF que les permiten unirse y activar los receptores ErbB. Holmes et al. (Science 256:1205-1210, 1992) han demostrado que el dominio similar a EGF solo es suficiente para unir y activar el receptor p185erbB2. En consecuencia, cualquier producto polipeptídico codificado por el gen NRG-1, NRG-2 o NRG-3, por ejemplo, un polipéptido que tiene un dominio similar a EGF codificado por un gen de neuregulina o ADNc (por ejemplo, un dominio similar a EGF, como se describe en la Patente de Estados Unidos No. 5.530.109, la Patente de Estados Unidos No. 5,716,930; la Patente de Estados Unidos 7,037,888, la Patente de Estados Unidos No. 7,135,456, y la Patente de Estados Unidos No. 7,319,019; o un dominio similar a EGF como se describe en el documento WO 97/09425) puede usarse en los procedimientos de la divulgación para lograr una ventana terapéutica en la que se logra un nivel plasmático eficaz de GGF2 en suero.
También se debe tener en cuenta que, como se usa en este documento y en las reivindicaciones adjuntas, las formas singulares "uno", "una" y "el" y "la" incluyen una referencia plural a menos que el contexto indique claramente lo contrario.
A menos que se defina lo contrario, todos los términos técnicos y científicos utilizados en este documento tienen los mismos significados que los entendidos comúnmente por un experto en la materia.
"Administración local" significa administración directa por una vía no sistémica en o cerca del sitio de aflicción o trastorno.
Los términos "paciente" y "sujeto" se usan aquí para referirse a todos los animales, incluidos los mamíferos. Los ejemplos de pacientes o sujetos incluyen humanos, vacas, perros, gatos, cabras, ovejas y cerdos.
El término "sales, ésteres, amidas y profármacos farmacéuticamente aceptables", como se usa en el presente documento, se refiere a aquellas sales de carboxilato, sales de adición de aminoácidos, ésteres, amidas y profármacos de los compuestos de la presente divulgación que dentro del alcance del buen juicio médico son adecuadas para su uso en contacto con los tejidos de pacientes sin toxicidad indebida, irritación, respuesta alérgica y similares, proporcionales a una relación beneficio/riesgo razonable, y eficaces para su uso previsto, así como las formas zwitteriónicas, cuando sea posible, de los compuestos de la divulgación.
El término "profármaco" se refiere a compuestos que se transforman rápidamente in vivo para producir los compuestos originales de la fórmula anterior, por ejemplo, por hidrólisis en sangre. Se proporciona una discusión exhaustiva en T. Higuchi y V. Stella, "Pro-drugs as Novel Delivery Systems", vol. 14 de la A.C.S. Symposium Series, y en Bioreversible Carriers in Drug Design, ed. Edward B. Roche, American Pharmaceutical Association y Pergamon Press, 1987.
El término "sales" se refiere a las sales de adición de ácido inorgánico y orgánico relativamente no tóxicas de los compuestos de la presente divulgación. Estas sales se pueden preparar in situ durante el aislamiento final y la purificación de los compuestos o haciendo reaccionar por separado el compuesto purificado en su forma de base libre con un ácido orgánico o inorgánico adecuado y aislando la sal así formada. Las sales representativas incluyen sales de bromhidrato, clorhidrato, sulfato, bisulfato, nitrato, acetato, oxalato, valerato, oleato, palmitato, estearato, laurato, borato, benzoato, lactato, fosfato, tosilato, citrato, maleato, fumarato, succinato, tartrato, mesilato de naftilato, glucoheptonato, lactobionato y laurilsulfonato, y similares. Estas pueden incluir cationes a base de metales alcalinos y alcalinotérreos, como sodio, litio, potasio, calcio, magnesio y similares, así como amonio no tóxico, tetrametilamonio, tetraetilamonio, metilamina, dimetilamina, trimetilamina, trietilamina, etilamina, y similares. (Véase, por ejemplo, S. M. Barge et al., "Pharmaceutical Salts", J. Pharm. Sci., 1977, 66: 1-19.
Una "cantidad terapéuticamente efectiva" es una cantidad suficiente para disminuir los síntomas asociados con una afección o enfermedad médica, para normalizar las funciones corporales en enfermedades o trastornos que dan lugar al deterioro de funciones corporales específicas, o para proporcionar una mejora en una o más de los parámetros
clínicamente medidos de una enfermedad. Preferiblemente, una mejora en los síntomas asociados con la enfermedad asociada con una enfermedad desmielinizante, por ejemplo, que incluye velocidad de marcha, tono muscular de las extremidades inferiores, fuerza muscular de las extremidades inferiores o espasticidad. En relación con la presente solicitud, una cantidad terapéuticamente efectiva es una cantidad suficiente para reducir el dolor o la espasticidad asociada con el trastorno neurológico que se está tratando, o una cantidad suficiente para mejorar la función sexual, vesical o intestinal en sujetos que tienen un trastorno neurológico que deteriora la conducción nerviosa; o que dificulta las funciones sexuales, vesicales o intestinales normales.
El "tratamiento" se refiere a la administración de medicamentos o la realización de procedimientos médicos con respecto a un paciente, para mejorar la condición clínica del paciente, lo que incluye una disminución de la duración de la enfermedad o la gravedad de la misma, o una mejora subjetiva en la calidad de vida del paciente o una supervivencia prolongada del paciente.
Como se usa en este documento, el término "ventana terapéutica objetivo" se refiere al intervalo de dosis o intervalo de concentración sérica que logra los resultados terapéuticos deseados. Con respecto al GGF2, en una divulgación particular, la ventana terapéutica objetivo se refiere a una cantidad de GGF2 suficiente para inducir la mielinización de células de Schwann en un sujeto; tal cantidad es menor que la cantidad suficiente para inhibir la mielinización en un sujeto. En un descubrimiento sorprendente, los presentes inventores identificaron la ventana terapéutica objetivo para g GF2 con respecto a su capacidad para promover la mielinización mediante la determinación de los niveles relativos de activación de activación de la vía de PI3-quinasa y la activación de la vía de Mekl/Erk. Más particularmente, los presentes inventores descubrieron la correlación positiva hasta ahora no realizada entre la activación de la vía PI3-quinasa mediada por GGF2 y la promoción de la mielinización y una correlación negativa entre la activación de la vía Mekl/Erk mediada por GGF2 y la promoción de la mielinización. Enunciado de modo alternativo, los presentes inventores descubrieron que la administración de GGF2 puede ajustarse finamente para promover la mielinización mediante la evaluación de los niveles de activación de estas vías. Una ventana terapéutica objetivo para GGF2 con respecto a promover la mielinización en un sujeto se define como una cantidad de g GF2 que promueve la activación de la vía de PI3-quinasa (evaluada, por ejemplo, mediante la detección de Akt fosforilada) en ausencia de activación detectable de la vía de Mekl/Erk (evaluada, por ejemplo, detectando Erk fosforilado). La detección de Akt fosforilada y Erk fosforilada se puede lograr utilizando ensayos estándar conocidos en la técnica, que incluyen ELISA, (inmuno) electrotransferencia Western, inmunocitoquímica, ensayo de quinasa in vitro, LC/MS (cromatografía líquida/espectrometría de masas), MaldiTOF MS (desorción/ionización láser asistida por matriz: espectrometría de masas de tiempo de vuelo) u otros sistemas de proteínas conocidos en el campo, como Luminex
Un experto en la materia apreciaría que otros marcadores intracelulares de la activación de la vía PI3-quinasa y la activación de la vía Mekl/Erk son conocidos y se usan de acuerdo con la presente divulgación. De acuerdo con la presente divulgación, se pueden usar otros indicadores de activación de la vía PI3-quinasa y activación de la vía Mekl/Erk para determinar la ventana terapéutica en la que GGF2 promueve la mielinización.
Además, los compuestos de la presente divulgación pueden existir en formas no solvatadas, así como solvatadas con disolventes farmacéuticamente aceptables tales como agua, etanol y similares. En general, las formas solvatadas se consideran equivalentes a las formas no solvatadas para los fines de la presente divulgación.
"Inhibidores de MAP quinasa"
Una lista no limitante de inhibidores de MAP quinasas que se pueden usar en la presente divulgación incluye: Arctigenina, que inhibe potentemente la actividad de MKK1 in vitro con un valor de IC50 de 1 nM y, por lo tanto, inhibe la fosforilación y activación de MAP quinasas ERK1/2, p38 quinasa y JNK y sus actividades en células Raw264.7 tratadas con l PS; PD 98059, que es un inhibidor potente, selectivo y permeable a las células de la MAP quinasa quinasa (también conocida como MAPK/ERK quinasa o MEK) que inhibe la fosforilación de MAP quinasa por MAP quinasa-quinasa, pero no inhibe la propia MAP quinasa. Los valores de IC50 para los efectos inducidos por PD 98059 están en el intervalo de 1-20 |jM para muchos ensayos; SB202190, que es un inhibidor altamente selectivo, potente y permeable a las células de p38 MAP quinasas que se une dentro del bolsillo ATP de la quinasa activa con un Kd de 38 nM medido en p38 humano recombinante e inhibe selectivamente las isoformas p38alfa y beta (valores IC50 son 50 y 100 nM para p38alpha/SAPK2alpha y p38beta2/SAPK2beta respectivamente); SB203580, que es un inhibidor altamente selectivo y permeable a las células de la proteína quinasa activada por mitógeno p38 con valores de IC50 de 50 y 500 nM para p38/SAPK2a y p38/SAPK2b respectivamente y también inhibe la proteína quinasa 1 dependiente de fosfoinositida (PDK1) a concentraciones 10 veces más altas (IC50-3-5 j M) (Muestra una selectividad de 100-500 veces sobre Lck, GSK3b y Akt/PKB); SL 327, que es un inhibidor selectivo de MEK1 y MEK2 con valores de IC50 de 180 y 220 nM, respectivamente. Bloquea la lTp del hipocampo in vitro y penetra en el cerebro in vivo, bloquea el condicionamiento al miedo y el aprendizaje en ratas y produce neuroprotección en ratones, después de la administración sistémica; SP600125, que es un inhibidor selectivo de la quinasa N-terminal c-Jun (JNK). Inhibe de forma competitiva y reversible JNK1, 2 y 3 (IC50 =40-90 nM) y se ha demostrado que tiene menos potencia inhibitoria en ERK2, p38b y un intervalo de otras quinasas y se sabe que es activo in vivo; y U0126, que es un inhibidor selectivo de las quinasas de proteínas quinasas activadas por mitógeno, MEK-1 y MEK-2, con una potencia 100 veces mayor que PD 98059 y es un inhibidor débil de PKC, Raf, ERK, JNK, MEKK, MKK-3, MKK-4/SEK, MKK-6, Abl, Cdk2 y Cdk4 e inhibe la transactivación de AP-1 en ensayos de reportero basados en células.
Otros inhibidores que se encuentran actualmente en el ensayo de fase de la FDA incluyen los inhibidores de farnesil transferasa (FTI). Zarnestra® (R115777, tipifarnib), por ejemplo, es la FTI que está más avanzada en su desarrollo. Una prueba de fase II de pacientes con cáncer de mama metastásico previamente tratado probó dos programas de dosificación diferentes: continua e intermitente. Las tasas de respuesta objetivas en los 2 grupos fueron del 10% y el 14%, con un 15% y un 9% adicionales que tenían enfermedad estable durante al menos 6 meses. Los principales efectos secundarios observados fueron la supresión de la médula ósea y la neuropatía, los cuales fueron menos en el grupo de dosificación intermitente que en el continuo. Se han realizado varios estudios de fase I de zarnestra y otras FTI en combinación con quimioterapia citotóxica y han demostrado la seguridad de estos regímenes combinados. Se están realizando ensayos de fase II en cáncer de mama, incluido uno que usa zarnestra en combinación con un inhibidor de aromatasa. La aprobación de la FDA para el uso de zarnestra en la leucemia mieloide aguda (LMA) está pendiente de datos de fase III, ya que el comité de la FDA votó en contra de la aprobación acelerada de zarnestra basada en datos de un ensayo de fase II de un solo brazo (grupo).
Con respecto a Zarnestra®, para los ensayos clínicos de fase I, Zarnestra® se administra a 400 mg administrados por vía oral dos veces al día durante dos semanas; Para los ensayos clínicos de fase II, Zarnestra® se administra a 300 mg administrados por vía oral dos veces al día durante los primeros 21 días de cada ciclo de 28 días; Para los ensayos clínicos de fase III, Zarnestra® se administra a 600 mg administrados por vía oral dos veces al día durante los primeros 21 días de cada ciclo de 28 días.
Los inhibidores de Raf comprenden otros tipos de inhibidores que se encuentran actualmente en ensayos de fase de la FDA. Sorafenib (BAY 43-9006), por ejemplo, es el primer compuesto que se dirige no solo a la vía de señalización Raf/MEK/Erk, sino también a las vías VEGFR y PDGFR. En marzo de 2004, la FDA le otorgó a sorafenib el estado Fast Track (vía rápida) para el cáncer metastásico de células renales. En abril de 2005, sorafenib fue aceptado en el Programa Piloto 1, que está diseñado para terapias a las que se les ha otorgado el estado Fast T rack de la FDA y que tienen el potencial de proporcionar un beneficio significativo sobre la terapia estándar existente. También hay varios estudios clínicos grandes, internacionales, de fase III, de múltiples instituciones, de sorafenib en curso en pacientes con cánceres primarios avanzados de riñón e hígado, así como melanoma metastásico.
Con respecto a Sorafenib, los ensayos clínicos de Fase I probaron dos niveles de dosis: Nivel de dosis 1: 200 mg de Sorafenib por vía oral dos veces al día durante un ciclo de 3 semanas o Nivel de dosis 2: 400 mg de Sorafenib por vía oral dos veces al día durante un ciclo de 3 semanas.
Recientemente se presentaron los resultados de un análisis provisional planificado de un ensayo en fase III en curso en pacientes con cáncer de riñón avanzado (Escudier et al. J Natl Cancer Inst. 2008100: 1454-63). Entre 769 pacientes analizados, la supervivencia libre de progresión (SLP) se duplicó a un valor medio de 24 semanas con sorafenib, en comparación con 12 semanas con placebo. Los beneficios del sorafenib se observaron en todos los subgrupos de pacientes, independientemente de la edad, la duración de la enfermedad o las terapias previas. El control de la enfermedad se logró en el 80% de los pacientes que recibieron sorafenib: el 78% tenía enfermedad estable (en comparación con el 55% en el brazo (grupo) de placebo) y el 2% tenía respuesta parcial (en comparación con ninguno en el grupo de placebo). La tasa libre de progresión de 12 semanas fue del 79% para sorafenib frente al 50% para placebo. Además, sorafenib fue muy bien tolerado en 768 pacientes, y los efectos secundarios más comunes fueron hipertensión, fatiga, diarrea y erupción cutánea, incluida una erupción en la mano y el pie (síndrome de manos y pies). Los ensayos de eficacia de fase II están estudiando sorafenib como un agente único en los cánceres avanzados de pulmón, mama y otros. Los ensayos clínicos de fase I/II están investigando sorafenib en combinación con una gama de quimioterapéuticos estándar y otros agentes anticancerosos.
ISIS 5132 es otro inhibidor de raf que ha mostrado una toxicidad aceptable en estudios de fase I. Los estudios de fase II ahora están en marcha en una variedad de tipos de cáncer.
Otros inhibidores que se encuentran actualmente en el ensayo de fase de la FDA incluyen los inhibidores de MEK. CI-1040, por ejemplo, es un inhibidor oral selectivo de moléculas pequeñas de MEK 1-2. Los estudios en animales y cultivos han demostrado la actividad de este agente en líneas celulares de cáncer de mama. Los estudios de fase I han encontrado efectos secundarios gastrointestinales y cutáneos leves. Desafortunadamente, un estudio de fase II en 67 pacientes con 4 tipos de tumores diferentes (cáncer colorrectal avanzado, NSCLC, cáncer de mama y pancreático) no encontró respuestas, aunque el tratamiento con CI-1040 fue bien tolerado.
PD 0325901, un inhibidor de MEK de segunda generación, recientemente ha pasado a desarrollo clínico y parece tener propiedades farmacológicas notablemente mejores en comparación con CI-1040, que los investigadores esperan que se traduzca en una mejor eficacia contra el cáncer. Ha mostrado alguna respuesta parcial en pacientes con melanoma.
Con respecto a PD 0325901, los ensayos clínicos de fase I y fase II probaron niveles de dosis múltiples. Administrado oralmente una o dos veces al día; varios programas de dosificación evaluados; programa de dosificación actual 5 días con el medicamento, 2 días sin medicamento durante 3 semanas en un ciclo de 28 días. Las dosis evaluadas variaron de 1 mg una vez al día a 30 mg dos veces al día. Los ensayos clínicos se interrumpieron prematuramente debido a problemas de seguridad, específicamente la toxicidad ocular y neurológica presentada en dosis de 10 mg dos veces al día y más altas.
Administración: Las neuregulinas y polipéptidos que contienen dominios similares a EGF codificados por genes de neuregulina pueden administrarse a pacientes o animales experimentales con un diluyente, vehículo o excipiente farmacéuticamente aceptable, en forma de dosificación unitaria. La práctica farmacéutica convencional puede emplearse para proporcionar formulaciones o composiciones adecuadas para administrar tales composiciones a pacientes o animales experimentales. Se puede emplear cualquier vía de administración apropiada, por ejemplo, intravenosa, parenteral, subcutánea, intramuscular, intracraneal, intraorbital, oftálmica, intraventricular, intracapsular, intraespinal, intracisternal, intraperitoneal, intranasal, aerosol, oral o tópica (por ejemplo, aplicando un parche adhesivo que lleva una formulación capaz de cruzar la dermis y entrar en el torrente sanguíneo). Las formulaciones terapéuticas pueden estar en forma de soluciones o suspensiones líquidas; para la administración oral, las formulaciones pueden estar en forma de tabletas o cápsulas; y para formulaciones intranasales, en forma de polvos, gotas nasales o aerosoles. Cualquiera de las formulaciones anteriores puede estar en una formulación de liberación sostenida.
Los procedimientos bien conocidos en la técnica para preparar formulaciones se encuentran, por ejemplo, en "Remington's Pharmaceutical Sciences". Las formulaciones para administración parenteral pueden contener, por ejemplo, excipientes, agua estéril o solución salina, polialquilenglicoles tales como polietilenglicol, aceites de origen vegetal o naftalenos hidrogenados. El polímero de lactida biodegradable, biocompatible y de liberación sostenida, el copolímero de lactida/glicólido o los copolímeros de polioxietileno-polioxipropileno pueden usarse para controlar la liberación de los compuestos. Otros sistemas de suministro parenteral útiles para administrar moléculas, divulgados en el presente documento, incluyen partículas de copolímero de etileno-acetato de vinilo, bombas osmóticas, sistemas de infusión implantables y liposomas. Las formulaciones para inhalación pueden contener excipientes, por ejemplo, lactosa, o pueden ser soluciones acuosas que contienen, por ejemplo, éter de polioxietilen-9-laurilo, glicocolato y desoxicolato, o pueden ser soluciones oleosas para administración en forma de gotas nasales, o como gel.
Por lo tanto, y como se indicó anteriormente, la presente divulgación incluye dentro de su alcance, y se extiende a, los procedimientos de tratamiento mencionados y al uso de tales compuestos para la preparación de medicamentos útiles para tales procedimientos.
Enfermedades desmielinizantes: las vainas de mielina cubren muchas fibras nerviosas en el sistema nervioso central y periférico. La presencia de vainas de mielina intactas acelera la transmisión axonal de los impulsos neurales. Los trastornos que afectan la mielina interrumpen la transmisión nerviosa y los síntomas de la enfermedad pueden reflejar déficits en cualquier parte del sistema nervioso.
La mielina formada por oligodendroglia en el sistema nervioso central (SNC) difiere química e inmunológicamente de la formada periféricamente por las células de Schwann. Por lo tanto, algunos trastornos de mielina (por ejemplo, síndrome de Guillain-Barré, polineuropatía desmielinizante inflamatoria crónica y otras polineuropatías de nervios periféricos) tienden a afectar principalmente a los nervios periféricos, mientras que otros trastornos de mielina afectan principalmente al SNC. Las áreas más comúnmente afectadas en el SNC son el cerebro, la médula espinal y los nervios ópticos.
La desmielinización suele ser secundaria a un trastorno infeccioso, isquémico, metabólico o hereditario. En los trastornos desmielinizantes primarios, aunque se desconoce la causa o causas, se sospecha un mecanismo autoinmune porque el trastorno a veces sigue a una infección viral o vacunación viral.
La desmielinización tiende a ser segmentaria o irregular, afectando múltiples áreas de forma simultánea o secuencial. Sin embargo, puede producirse remielinización con reparación, regeneración y recuperación completa de la función neural. Sin embargo, la pérdida extensa de mielina suele ir seguida de degeneración axonal y, a menudo, degeneración del cuerpo celular.
La esclerosis múltiple (EM) se caracteriza por parches diseminados de desmielinización en el cerebro y la médula espinal. Los síntomas comunes incluyen anomalías visuales y oculomotoras, parestesias, debilidad, espasticidad, disfunción urinaria y deterioro cognitivo leve. Típicamente, los déficits neurológicos son múltiples, con remisiones y exacerbaciones que producen discapacidad gradualmente. El diagnóstico es por antecedentes de remisiones y exacerbaciones más signos clínicos, resultados de pruebas, lesiones observadas en la resonancia magnética (MRI) u otros criterios (según los síntomas) para demostrar objetivamente >2 anormalidades neurológicas separadas. El tratamiento generalmente incluye corticosteroides para las exacerbaciones agudas, medicamentos inmunomoduladores para prevenir las exacerbaciones y medidas de apoyo.
En la EM, se producen áreas localizadas de desmielinización (placas), con destrucción de oligodendroglia, inflamación perivascular y cambios químicos en los constituyentes lipídicos y proteicos de la mielina en y alrededor de las placas. El daño axonal es posible, pero los cuerpos celulares y los axones tienden a estar relativamente bien conservados. La gliosis fibrosa se desarrolla en placas que se diseminan por todo el SNC, principalmente en la sustancia blanca, particularmente en las columnas laterales y posteriores (especialmente en las regiones cervicales), nervios ópticos y áreas periventriculares. Los tractos en el mesencéfalo, la protuberancia y el cerebelo también se ven afectados. La materia gris en el cerebro y la médula espinal puede verse afectada, pero en un grado mucho menor.
Enfermedad cardíaca
La enfermedad cardíaca es un término general para varias enfermedades diferentes que afectan el corazón. Es la principal causa de muerte en muchos países industrializados, incluido Estados Unidos. Las siguientes categorías generales de enfermedades del corazón se presentan a modo de introducción. Las cardiomiopatías extrínsecas son cardiomiopatías, en las que la patología primaria se encuentra fuera del miocardio. La mayoría de las cardiomiopatías son extrínsecas, porque la causa más común de cardiomiopatía es la isquemia. Las cardiomiopatías intrínsecas derivan de una debilidad en el músculo cardíaco que no se debe a una causa externa identificable. La enfermedad cardiovascular, por otro lado, se refiere a cualquier cantidad de enfermedades específicas que afectan el corazón mismo y/o el sistema de vasos sanguíneos, especialmente las venas y arterias que conducen hacia y desde el corazón. La investigación sobre el dimorfismo de la enfermedad sugiere que las mujeres que padecen enfermedades cardiovasculares generalmente sufren de formas que afectan los vasos sanguíneos, mientras que los hombres generalmente sufren de formas que afectan el músculo cardíaco mismo. Las causas conocidas o asociadas de enfermedad cardiovascular incluyen diabetes mellitus, hipertensión, hiperhomocisteinemia e hipercolesterolemia. La cardiopatía isquémica es otra categoría de enfermedad del corazón en sí, caracterizada por la reducción del suministro de sangre al órgano. La enfermedad cardíaca hipertensiva es un término utilizado para referirse a la enfermedad cardíaca causada por la presión arterial alta, especialmente la presión arterial alta localizada. La enfermedad cardíaca inflamatoria implica la inflamación del músculo cardíaco y/o el tejido que lo rodea. La enfermedad cardíaca valvular es cualquier proceso de enfermedad que involucra una o más válvulas del corazón. Las válvulas en el lado derecho del corazón son la válvula tricúspide y la válvula pulmonar y las válvulas en el lado izquierdo del corazón son la válvula mitral y la válvula aórtica.
La insuficiencia cardíaca congestiva, una de las principales causas de muerte en los países industrializados, es el resultado de una mayor carga de trabajo en el corazón y una disminución progresiva de su capacidad de bombeo. Puede ser el resultado de cualquier trastorno cardíaco estructural o funcional que afecte la capacidad del corazón para llenar o bombear una cantidad suficiente de sangre a través del cuerpo. Inicialmente, el aumento de la carga de trabajo que resulta de la presión arterial alta o la pérdida de tejido contráctil induce hipertrofia compensatoria de cardiomiocitos y engrosamiento de la pared ventricular izquierda, lo que mejora la contractilidad y mantiene la función cardíaca. Con el tiempo, sin embargo, la cámara ventricular izquierda se dilata, la función de la bomba sistólica se deteriora, los cardiomiocitos sufren la muerte celular apoptótica y la función miocárdica se deteriora progresivamente.
Los factores que subyacen tras la insuficiencia cardíaca congestiva incluyen presión arterial alta, cardiopatía isquémica, exposición a compuestos cardiotóxicos como los antibióticos de antraciclina y defectos genéticos conocidos por aumentar el riesgo de insuficiencia cardíaca.
Por "insuficiencia cardíaca congestiva" se entiende una función cardíaca deteriorada que hace que el corazón sea incapaz de mantener el gasto sanguíneo normal en reposo o con ejercicio, o de mantener un gasto cardíaco normal en el contexto de la presión de llenado cardíaco normal. Una fracción de eyección ventricular izquierda de aproximadamente 40% o menos es indicativa de insuficiencia cardíaca congestiva (a modo de comparación, una fracción de eyección de aproximadamente 60% es normal). Los pacientes con insuficiencia cardíaca congestiva muestran síntomas y signos clínicos bien conocidos, como taquipnea, derrames pleurales, fatiga en reposo o con ejercicio, disfunción contráctil y edema. La insuficiencia cardíaca congestiva se diagnostica fácilmente mediante procedimientos bien conocidos (ver, por ejemplo, "Recomendaciones de consenso para el tratamiento de la insuficiencia cardíaca crónica. "Am. J. Cardiol, 83(2A): lA-38-A, 1999).
La gravedad relativa y la progresión de la enfermedad se evalúan utilizando procedimientos bien conocidos, como el examen físico, la ecocardiografía, las imágenes de radionúclidos, la monitorización hemodinámica invasiva, la angiografía por resonancia magnética y la prueba de esfuerzo en cinta de correr junto con estudios de absorción de oxígeno.
Por "cardiopatía isquémica" se entiende cualquier trastorno resultante de un desequilibrio entre la necesidad miocárdica de oxígeno y la adecuación del suministro de oxígeno. La mayoría de los casos de cardiopatía isquémica resultan del estrechamiento de las arterias coronarias, como ocurre en la aterosclerosis u otros trastornos vasculares.
Por "infarto de miocardio" se entiende un proceso por el cual la enfermedad isquémica da como resultado que una región del miocardio sea reemplazada por tejido cicatricial.
Por "cardiotóxico" se entiende un compuesto que disminuye la función cardíaca al dirigir o dañar o matar indirectamente a los cardiomiocitos.
Por "hipertensión" se entiende la presión arterial que un profesional médico (por ejemplo, un médico o enfermero) considera que es más alta de lo normal e implica un mayor riesgo de desarrollar insuficiencia cardíaca congestiva.
Por "tratamiento" se entiende que la administración de una neuregulina o un polipéptido similar a la neuregulina retarda o inhibe la progresión de la insuficiencia cardíaca congestiva durante el tratamiento, en relación con la progresión de la enfermedad que ocurriría en ausencia de tratamiento, de una manera estadísticamente significativa. Se pueden utilizar indicios bien conocidos, como la fracción de eyección del ventrículo izquierdo, el rendimiento del ejercicio y otras pruebas clínicas, así como las tasas de supervivencia y hospitalización para evaluar la progresión de la enfermedad. Si un tratamiento ralentiza o inhibe la progresión de la enfermedad de una manera estadísticamente
significativa puede determinarse mediante procedimientos que son bien conocidos en la técnica (véase, por ejemplo, SOLVD Investigators, N. Engl. J. Med. 327: 685-691, 1992 y Cohn et al., N. Engl. J Med. 339:1810-1816, 1998).
Por "disminución de la progresión del adelgazamiento miocárdico" se entiende el mantenimiento de la hipertrofia de los cardiomiocitos ventriculares de modo que se mantenga o aumente el grosor de la pared ventricular.
Por "inhibe la apoptosis miocárdica" se entiende que el tratamiento con neuregulina inhibe la muerte de cardiomiocitos en al menos 10%, más preferiblemente en al menos 15%, aún más preferiblemente en al menos 25%, incluso más preferiblemente en al menos 50%, aún más preferiblemente en al menos un 75%, y lo más preferiblemente en al menos un 90%, en comparación con los cardiomiocitos no tratados.
Apoplejía
Apoplejía o accidente cerebrovascular (ACV) es un término utilizado para referirse a la pérdida de funciones cerebrales en rápido desarrollo debido a una alteración en los vasos sanguíneos que suministran sangre al cerebro. Una apoplejía ocurre cuando el suministro de sangre a una parte del cerebro se interrumpe repentinamente o cuando explota un vaso sanguíneo en el cerebro, derramando sangre en los espacios que rodean las células cerebrales. Las células cerebrales mueren cuando ya no reciben oxígeno y nutrientes de la sangre o hay un sangrado repentino dentro o alrededor del cerebro. Los síntomas de una apoplejía incluyen entumecimiento o debilidad repentinos, especialmente en un lado del cuerpo; confusión repentina o dificultad para hablar o entender el habla; dificultad repentina para ver en uno o ambos ojos; problemas repentinos al caminar, mareos o pérdida de equilibrio o coordinación; o dolor de cabeza intenso y repentino sin causa conocida. Hay dos formas de apoplejía: isquémico, que se debe al bloqueo de un vaso sanguíneo que irriga el cerebro (por ejemplo, causado por trombosis o embolia); y hemorrágico, que resulta del sangrado dentro o alrededor del cerebro.
Índice de ventana terapéutica
Para cada aplicación de enfermedad descrita en este documento, se establece una ventana terapéutica objetivo para los niveles plasmáticos de GGF2 en suero. De acuerdo con los resultados experimentales presentados aquí, cuando GGF2 se administra a un mamífero afectado por un trastorno neurológico asociado con la desmielinización, GGF2 debe administrarse en un régimen de dosificación para lograr y mantener una ventana terapéutica objetivo estrecha de las concentraciones plasmáticas de GGF2. Como se enseña en el presente documento, es necesaria una dosificación precisa de GGF2 para lograr los niveles plasmáticos de GGF2 en suero requeridos para la eficacia terapéutica con respecto a inducir mielinización en un sujeto que lo necesita.
En una forma de realización de la divulgación dirigida a factor 2 de crecimiento glial (GGF2) para usarse en la promoción de la remielinización en un paciente, en la cual el GGF2 se administra al paciente en una cantidad de 500 ng /- 15% de GGF2 por kg de peso corporal, el nivel plasmático de GGF2 en suero es de aproximadamente 0.01 nM.
Las composiciones de la presente divulgación pueden usarse en el tratamiento de una afección en un paciente que incluye establecer una concentración terapéuticamente efectiva de GGF2 en el paciente. Cuando sea deseable, las composiciones de la presente divulgación pueden formularse para evitar picos grandes en la liberación inicial de GGF2. Las composiciones de la presente divulgación, cuando se administran a un paciente que lo necesita, proporcionan el tratamiento de las enfermedades indicadas anteriormente. Preferiblemente, las composiciones se administran para lograr un nivel de GGF2 en plasma sanguíneo terapéuticamente eficaz que se mantiene en el paciente durante un período de al menos 6 horas, preferiblemente al menos 8 horas, y más preferiblemente al menos aproximadamente 10-12.
Ejemplos de referencia
Materiales y procedimientos
Anticuerpos
Para el análisis de inmunofluorescencia, se usó anticuerpo monoclonal (SM194) frente a la proteína básica de mielina (MBP) (monoclonales de Sternberger) a una dilución 1:500. Para el análisis de transferencia Western, se obtuvieron anticuerpos policlonales frente a erbB2 (p-Neu/Tyr 1248), erbB2 y erbB3 activos de Santa Cruz y se usaron a una dilución 1:1000. El anticuerpo monoclonal frente a Akt fosforilado y el anticuerpo policlonal frente a MAPK fosforilado se adquirieron en Cell Signaling y se usaron en diluciones de 1:1000 y 1:500, respectivamente. Los anticuerpos policlonales contra Akt y MAPK (Promega) se usaron en diluciones de 1:1000 y 1:5000, respectivamente.
Neuregulina-1 tipo II y tipo III
El factor de crecimiento glial humano recombinante II (rhGGF-II, Nrg1 tipo II) se obtuvo de Acorda Therapeutics, Inc. El factor derivado de neuronas sensoriales y motoras humanas recombinantes (rhSMDF, Nrg1 Tipo-Ill) se adquirió en R&D Systems. En el presente estudio, rhGGF-II y rhSMDF se denominan simplemente como GGF (o GGF2) y SMDF, respectivamente. El GGF era los residuos de aminoácidos 419 del extremo N que contenían el dominio EGF y el
dominio de tipo Ig. En consecuencia, GGF es una proteína soluble que carece de dominios transmembrana y citoplasmáticos.
Cultivo primario de células de Schwann de rata
Las células de Schwann se prepararon a partir de nervios ciáticos de ratas recién nacidas (1-2 días de edad) como se describió anteriormente (Brockes et al., Brain Res. 1979; 165:105-118). Para el cultivo de rutina, se cultivaron células de Schwann en medio Eagle modificado de Dulbecco (DMEM) con suero fetal bovino (FBS) al 10% suplementado con neuregulina-1 del dominio EGF (R&D Systems) (10 ng/ml) y forskolina (2 |jM). Las células entre el pasaje 2-4 se usaron en todos los experimentos descritos en el texto.
Co-cultivo de neuronas del ganglio de la raíz dorsal (ORG)-células de Schwann
Se prepararon DRG disociados a partir de embriones de rata del día 14.5 embrionario como se describió anteriormente (Eldridge et al., J Cell Biol. 1987; 105(2):1023-34) y se colocaron en placas sobre colágeno (colágeno de cola de rata tipo 1), cubreobjetos de vidrio recubiertos de 12 mm a una densidad de 1.25 DRG/cubreobjetos. Cinco a seis horas después, los cultivos se inundaron con medio neurobasal (Cellgro,) suplementado con B27 (GIBCO), glucosa al 20%, NGF (50 ng/ml) y 5-fluorodesoxiuridina (FUdR, 10 j M) y se mantuvieron en el medio durante 2-3 días adicionales para eliminar las células proliferativas no neuronales. Luego, los cultivos se cambiaron a medio fresco sin FUdR y se mantuvieron hasta que los axones DRG alcanzaron la periferia de los cubreobjetos. Después de que se establecieron las redes axonales, las células de Schwann se colocaron en placas sobre las neuronas a una densidad de 100.000 células/cubreobjetos. Cuatro a cinco días después, los cultivos se cambiaron a medio mielinizante: Medio esencial mínimo (MEM) suplementado con FBS inactivado por calor al 10%, glucosa al 20%, NGF (50 ng/ml) y ácido ascórbico (50 jg/ml). Diez a once días después, se evaluó la mielinización mediante inmunotinción para MBP.
Co-cultivo de neuronas del ganglio cervical superior (SCG)- células de Schwann
Se prepararon SCG disociados a partir de ratas de 1-2 días postnatales como se describió anteriormente y se colocaron en placas sobre cubreobjetos de vidrio recubiertos con colágeno de 12 mm a una densidad de 0.8 SCG/cubreobjetos. Al día siguiente, los cultivos se inundaron con medio neurobasal suplementado con B27 (GIBCO), glucosa al 20%, NGF (50 ng/ml) y 5-fluorodesoxiuridina (FUdR, 10 j M) y se mantuvieron en el medio durante 2-3 días adicionales con el fin de eliminar la proliferación de células no neuronales. Los cultivos se volvieron a cambiar a medio fresco sin FudR y se mantuvieron hasta que los axones se extendieron hacia la periferia de los cubreobjetos. Las células de Schwann se colocaron en placas sobre las neuronas y se mantuvieron en medio neurobasal con suplementos hasta que las células de Schwann poblaron los axones (aproximadamente 7-10 días). La mielinización se inició colocando los cultivos en medio mielinizante como se describe para el cocultivo de células DRG-Schwann. Cuarenta días después, la mielinización se evaluó mediante inmunotinción MBP.
Inmunoprecipitación y análisis por transferencia Western
Para preparar lisados celulares, se lavaron 90-95% de células Schwann de rata confluentes en placas de 60 mm o cocultivos dos veces en solución salina de pH regulado con fosfato (PBS) y luego se lisaron en 300 j l de regulador de pH de lisis helado (Tris HCl de 50 mM pH 7.4, NP-40 al 1%, desoxicolato de sodio al 0.25%, NaCl de 150 mM, EGTA de 1 mM, leupeptina de 10 jg/ml, aprotinina de 2 jg/ml, PMSF de 1 mM y ortovanadato de sodio de 0.5 mM). Los lisados se clarificaron por centrifugación durante 15 minutos a 14,000 rpm en frío y la concentración de proteínas de los sobrenadantes se determinó de acuerdo con las especificaciones del fabricante (Bio-Rad: Hercules, CA). Para el análisis de transferencia Western, se fraccionaron 50-70 jg de lisados de células de Schwann en geles de SDS-poliacrilamida al 10% y se transfirieron a membranas de PVDF. Después del bloqueo en leche al 5%, las membranas se incubaron con anticuerpos primarios apropiados preparados en solución de bloqueo. Después de incubar con anticuerpos secundarios conjugados con peroxidasa de rábano picante, las bandas de proteínas se visualizaron por quimioluminiscencia mejorada. Para la inmunoprecipitación, se incubaron 500 jg de lisados de células de Schwann con 0.6 jg de anticuerpo primario durante 3 horas a 4°C, luego se incubaron con 50 j l de perlas de Sepharose A durante 1 hora. Las perlas se lavaron 5 veces en el regulador de pH de lisis y las proteínas unidas a las perlas se fraccionaron en geles de SDS-poliacrilamida y se sometieron a análisis de transferencia Western.
Tinción por inmunofluorescencia para MBP
Los cultivos de células DRG-Schwann o SCG-Schwann se enjuagaron en solución salina con pH regulado con fosfato (PBS) y luego se fijaron en paraformaldehído al 4% durante 20 minutos. Después de lavar con PBS, las muestras se permeabilizaron en metanol helado durante 25 minutos y luego se incubaron en solución de bloqueo (5% de suero de cabra normal 0.3% de Triton X) durante 1 hora a temperatura ambiente. Esto fue seguido por incubación con anticuerpo primario preparado en solución de bloqueo durante la noche. Después de lavar con p Bs , las muestras se incubaron con anticuerpo secundario conjugado de cabra-anti-ratón Alexa-488 durante 45 minutos. Los núcleos de las células se visualizaron mediante tinción con DAPI.
PCR cuantitativa en tiempo real
Análisis estadístico
Se realizó ANOVA de una vía utilizando el software de programación SAS con un nivel de significancia del 95%.
Resultados
La función inhibitoria de GGF2 en la mielinización está mediada por la activación de MAPK. Un estudio anterior ha demostrado que Nrg1 tipo II (GGF2), cuando se agrega a los cocultivos de células neuronales de Schwann, inhibe la mielinización. También se ha informado que la activación de la vía Ras/Raf/MAPK inhibe la expresión génica asociada a la mielina en las células de Schwann, mientras que la activación de la vía PI3-quinasa promueve la mielinización, lo que lleva a la noción de que el estado de mielinización de la célula de Schwann está determinado por equilibrio entre las vías PI3-quinasa y Ras/Raf/MAPK (Ogata et al. J Neurosci 2004; 24:6724-32). Los presentes inventores predijeron que, si GGF2 actúa mediante la activación de MAPK para inhibir la mielinización, la inhibición de la activación de MAPK inducida por GGF2 revertiría el efecto inhibidor sobre la mielinización. Para evaluar la posibilidad de que el efecto inhibidor de GGF2 sobre la mielinización se deba a su capacidad para inducir una activación MAPK robusta en las células de Schwann, los presentes inventores utilizaron un sistema de cultivo de mielinización in vitro bien establecido en el que las células de Schwann se cultivan conjuntamente con neuronas del ganglio de la raíz dorsal (DRG) e inducidas a mielinizar los axones asociados mediante la adición de ácido ascórbico a los medios de cultivo. Primero, para determinar el efecto de GGF2 sobre la activación de MAPK en los cocultivos, se sembraron células primarias de Schwann en neuronas DRG y se les permitió propagar los axones. Una vez que los cultivos dejaron de proliferar, los cocultivos se estimularon con GGF2 a 0.6 nM. Veinte minutos después, se prepararon los lisados celulares y se determinó la activación de MAPK mediante análisis de transferencia Western. En los cocultivos de control, hubo un bajo nivel de MAPK activo. Como se muestra en la Figura 1, el tratamiento con GGF2 aumentó aún más el nivel de activación de MAPK. Para determinar si la activación de MAPK inducida por GGF2 podría bloquearse mediante el tratamiento con U0126, un inhibidor farmacológico de MAPK quinasa, se pretrataron los cocultivos con concentraciones crecientes (0.5, 1, 3 y 10 |jM) de U0126 durante 30 minutos antes de la estimulación con GGF2 y estas concentraciones se mantuvieron en el medio de cultivo. Los cultivos de control se trataron con el inhibidor en ausencia de tratamiento con GGF2. Tanto en cultivos de control como en cultivos experimentales, la inhibición de MAPK mediada por U0126 dependía de la concentración, como lo indica la disminución progresiva en los niveles de fosfo-MAPK. En cultivos tratados con GGF2 y U0126 a una concentración de 1 j M, el nivel de activación se redujo al nivel basal, mientras que a U0126 de 10 j M, la activación de MAPK en el cocultivo se abolió por completo. El U0126 no tuvo efecto sobre la activación de PI3quinasa inducida por GGF2.
Para evaluar el efecto de la inhibición de MAPK sobre la mielinización, los cocultivos se trataron con GGF2 en presencia o ausencia de U0126 al momento de iniciar la mielinización y se mantuvieron las mismas condiciones en la condición de mielinización descrita. Los cultivos de control no se trataron en la condición de mielinización descrita. Diez a once días después, los cultivos se fijaron y se inmunotiñeron para la proteína básica de mielina (MBP) para visualizar segmentos de mielina. En cultivos tratados con GGF2, hubo una marcada disminución en el número de segmentos de mielina como se mostró anteriormente, lo que reveló el efecto inhibidor de GGF2 sobre la mielinización. Sin embargo, en cultivos tratados conjuntamente con U0126, hubo un aumento de la mielinización dependiente de la dosis, lo que indica que el bloqueo de la activación de MAPK revirtió el efecto inhibidor de GGF2.
GGF2 promueve la mielinización a bajas concentraciones: aunque el nivel de activación de MAPK aumentó constantemente en las células de Schwann tratadas con concentraciones crecientes de GGF2, los presentes inventores observaron que a bajas concentraciones por debajo de 0.01 j M, mientras que el nivel de activación de Akt aumentó significativamente por encima del nivel basal, no hubo un nivel detectable de activación de MAPK. Si el estado de mielinización de una célula de Schwann está determinado por el equilibrio entre Akt y activación de MAPK, los presentes inventores buscaron evaluar si el aumento en la activación de Akt en ausencia de actividad de MAPK a estas concentraciones está correlacionado con un efecto positivo sobre la mielinización. Para investigar esta potencialidad, los cocultivos se trataron con GGF2 a concentraciones que oscilaban entre 0.0005 y 0.03 nM al momento de iniciar la mielinización. Los cultivos fueron luego fijados e inmunoteñidos para MBP. Como se predijo con base en los hallazgos instantáneos, hubo un aumento en el nivel de mielinización en cultivos tratados con dosis bajas de GGF2, que van desde 0.0005 a 0.01 nM, en comparación con los cultivos de control no tratados. Cuando se cuantificó, el resultado demostró que hubo un aumento dependiente de la dosis en el número de segmentos de mielina (Figura 2): un aumento de 1.9, 2.7 y 3.5 veces en la mielinización en relación con el nivel de control, a GGF2 de 0.0005, 0.001 y 0.01 nM, respectivamente. A 0.03 nM, hubo una disminución drástica en el nivel de mielinización a un nivel cercano o ligeramente por debajo de los cultivos de control. Los aumentos posteriores en la cantidad de GGF2 dieron como resultado una disminución adicional de la mielinización. La mielinización sensible al GGF2 se inhibió por completo a 0.6 nM de GGF2. Esta concentración correspondió a la aparición de MAPK activa en los cocultivos como se muestra en la Figura 1. Estos resultados sugieren que GGF2 desempeña dos funciones durante la mielinización: una que promueve y la otra que inhibe la mielinización, y las dos funciones opuestas están determinadas por la dosis de g GF2 presentada a las células de Schwann.
Las funciones opuestas de GGF2 están mediadas por la activación de Mek/Erk: para investigar más a fondo las funciones opuestas de GGF2, se realizaron experimentos adicionales. Estudios previos han implicado a Ras/Raf/Erk y PI-3 quinasa, respectivamente, como reguladores negativos y positivos de la mielinización, lo que sugiere que un equilibrio entre los dos está correlacionado con el estado de mielinización de las células de Schwann. Para delinear aún más los estados de activación de las vías inducidas por GGF2, los cocultivos se trataron con la proteína GGF2 soluble a 1 nM. Los presentes inventores determinaron que, a esta concentración, GGF2 inhibía efectivamente la
mielinización. Los lisados celulares se prepararon 30 minutos después del tratamiento con GGF2 y la presencia de las proteínas fosforiladas se determinó mediante análisis de transferencia Western (Figura 3A). A 1 nM (figura 3 A, carriles en caja) GGF2 aumentó la activación de Akt por encima del nivel basal. También se observó un aumento en la activación de Erk en cultivos tratados con GGF2 a esta concentración. Se demostró que concentraciones de GGF2 tan bajas como 0.6 nM eran suficientes para la activación de Erk en cultivos tratados con GGF2.
Para corroborar los resultados anteriores e investigar más a fondo el vínculo correlativo entre la activación de Erk y el efecto inhibidor de GGF sobre la mielinización, se realizaron experimentos adicionales. En consecuencia, los cocultivos se trataron con GGF2 junto con concentraciones crecientes de U0126, el inhibidor específico descrito anteriormente de la vía Mekl/Erk. El análisis de transferencia Western presentado en la figura 3B muestra que U0126 inhibió la activación de Erk inducida por GGF2 de una manera dependiente de la dosis, mientras que no tuvo ningún efecto sobre la activación de Akt. El bajo nivel de actividad Erk endógena que normalmente se observa en el sistema de cocultivo también disminuyó con el tratamiento farmacológico.
Los presentes inventores evaluaron adicionalmente el efecto de la inhibición de Mekl/Erk sobre la mielinización. Como se muestra en las Figuras 3C y 3D, la adición de GGF2 a alta concentración inhibió casi por completo la mielinización en los cocultivos. Sin embargo, en cultivos tratados conjuntamente con U0126, se revirtió el efecto inhibidor de GGF2, como lo indica el aumento dependiente de la dosis en el nivel de mielinización (figuras 3C y 3D). Este resultado proporciona evidencia directa de que el efecto inhibidor de GGF2 sobre la mielinización está mediado por la activación de Erk. Curiosamente, el tratamiento con U0126 en cocultivos en ausencia de GGF2 también dio lugar a un aumento en el nivel de mielinización (figura 3E), lo que indica que la actividad endógena Mekl/Erk funciona como un regulador negativo intrínseco de la mielinización.
El análisis de transferencia Western en lisados preparados a partir de los cocultivos también reveló que el tratamiento con GGF2 aumentó la expresión de la proteína c-Jun, un regulador negativo de la diferenciación y mielinización de las células de Schwann. La posterior inhibición de la actividad de Mekl/Erk inducida por GGF2 disminuyó los niveles de c-Jun, lo que, a su vez, estuvo acompañado por un aumento en la expresión de la proteína de mielina. A diferencia del efecto sobre c-Jun, el tratamiento con U0126 dio como resultado un aumento en la expresión de Krox20 en los cocultivos. Esto está de acuerdo con un informe reciente que sugiere una relación antagónica cruzada entre c-Jun y Krox20 en la regulación de la mielinización (Parkinson et al, 2008, Journal of Cell Biology 181:625-637).
GGF2 promueve la mielinización de las células de Schwann: para corroborar y ampliar los resultados presentados en este documento y evaluar aún más las funciones opuestas de GGF2, los presentes inventores evaluaron el efecto dependiente de la concentración de GGF2 en la activación de Ras/Raf/Erk y PI3-quinasa en células de Schwann. Las células se trataron con diversas concentraciones de GGF2 que variaban de 0.0003 a 10 nM y el nivel de activación de Erk y Akt se determinó mediante análisis de transferencia Western. Las imágenes y el aumento relativo en los niveles de activación se presentan en las figuras 4A y 4B. El nivel de Akt activo aumentó constantemente a partir de la dosis más baja probada, mientras que la activación de Erk requirió mayores concentraciones de GGF2. La activación diferencial de las dos vías a bajas concentraciones, como resultado, generó una ventana estrecha de dosis (0.003 a 0.01 nM, enmarcada en la Figura 4B) en la que Akt era la vía predominante activada en respuesta a GGF2. A continuación, se determinó el efecto de varias dosis de GGF2 sobre la mielinización en el sistema de cocultivo. En la ventana de baja concentración, GGF2 provocó un efecto promielinizante dependiente de la dosis: aumento de 1.5, 2.3, 2.2 y 2.8 veces en la mielinización en comparación con los cultivos de control a 0.0005, 0.001, 0.003 y 0.01 nM de GGF2, respectivamente (figura 4C). A medida que la concentración aumentó aún más, GGF2 comenzó a inhibir la mielinización, coincidiendo con la aparición de la activación de Erk. El efecto promielinizante de GGF2 también se demostró en cocultivos CRD-Nrg1+/- en los que dosis bajas de GGF2 rescataron el defecto de mielinización en los axones mutantes (figura 4D).
Nrg1 soluble puede promover e inhibir la mielinización: elección binaria determinada por la concentración: en el sistema nervioso periférico (SNP), GGF2 se ha considerado como una isoforma de Nrg1 asociada con la respuesta a la lesión de células de Schwann. La expresión ectópica in vivo de GGF-p3 en células de Schwann mielinizantes estimula la proliferación celular e induce la desmielinización (Huijbregts et al. J Neurosci 2003; 23:7269-80). Además, se ha demostrado que la adición de altas concentraciones de g GF2 (por ejemplo, las que superan el GGF20.25 nM) a los cocultivos de neuronas DRG de células de Schwann inhibe la mielinización (Zanazzi et al. J Cell Biol 2001; 152:1289-99). Por lo tanto, un resultado inesperado del presente estudio fue el descubrimiento de que, a baja concentración, GGF2 exhibe efectos promotores de la mielinización. Sin embargo, el efecto promielinizante se limitó a un intervalo de concentración bajo y un aumento en la concentración de GGF2 de este intervalo da como resultado la inhibición de la mielinización como se describió anteriormente. Este es un hallazgo intrigante ya que demuestra que el GGF2 soluble puede provocar dos funciones biológicas contrastantes en el mismo contexto celular únicamente en función de la cantidad presentada a la célula. También sugiere que los niveles de umbral de GGF2 determinan la función promielinizante e inhibidora durante la mielinización. Como se demostró por primera vez en el presente estudio, esto puede explicarse por la activación diferencial dependiente de la concentración de los efectores de señalización aguas abajo del receptor. Más específicamente, los datos actuales muestran que la función promielinizante del GGF2 se observa a concentraciones que activan preferentemente Akt, mientras que la transición al papel inhibidor a concentraciones más altas coincide con la aparición de la activación de Erk a pesar del aumento continuo en el nivel de Akt activo. Este resultado también respalda la noción anterior de que el equilibrio entre la activación de PI3-quinasa y Ras/Raf/Erk es crucial para determinar el estado de mielinización en las células de Schwann (Ogata et al. J Neurosci
2004; 24:6724-32). Sin embargo, los hallazgos actuales proporcionan evidencia directa de que la activación de la vía Ras/Raf/Erk funciona como un regulador negativo de la mielinización.
La función inhibitoria Nrg1 en la mielinización está mediada por la activación de Erk/Mekl: el papel inhibidor de la vía Ras/Raf/Erk en la mielinización ha sido sugerido previamente por estudios en los que la expresión de Mekl constitutivamente activo en las células de Schwann bloquea la expresión del gen de mielina inducida por forskolina, mientras que Ras dominante negativo bloquea la regulación negativa del gen de mielina inducida por Nrg1. Sin embargo, su efecto directo sobre la mielinización no se ha dilucidado antes de los presentes resultados. Como se demuestra en el presente documento, GGF2, cuando se usa por encima de una concentración umbral, inhibe la mielinización en los cocultivos. Los presentes inventores muestran aquí que la inhibición de la activación de Mek1/Erk1 restableció la mielinización en cocultivos tratados con GGF2, lo que demuestra que el papel inhibidor de GGF2 estaba mediado a través de su activación de Ras/Raf/Erk1. El mecanismo por el cual la activación de MekI/Erk inhibe la mielinización no está claro. Un posible mecanismo incluye la supresión de la expresión del gen de mielina como se describió anteriormente. En apoyo de esta sugerencia, los datos actuales revelaron que un aumento en la mielinización en cultivos tratados con U0126 estuvo acompañado por un aumento en la expresión de P0. También es posible que la vía Mekl/Erk pueda modular la expresión de los factores de transcripción implicados en la mielinización o la diferenciación de células de Schwann. Recientemente se ha demostrado que la expresión ectópica de c-Jun en las células de Schwann inhibe la mielinización, lo que sugiere que c-Jun funciona como un regulador negativo del programa de mielina. Los presentes hallazgos son consistentes con esta conclusión, ya que los presentes inventores determinaron que el tratamiento con GGF2 que inhibe la mielinización está acompañado por la inducción de c-Jun y, además, la inhibición de la actividad Mek1/Erk1 inducida por Nrg1 bloquea la expresión de c-Jun. Este resultado sugiere que la función inhibitoria de Mek1/Erk1 en la mielinización está en parte mediada por la inducción de c-Jun.
Otro hallazgo interesante del presente estudio es la presencia de una señal intrínseca dependiente de MekI/Erk en los cocultivos que sirve como regulador negativo de la mielinización. Esto se demostró en un experimento en el que el tratamiento de cocultivos mielinizantes normales con U0126 promovió la mielinización. La naturaleza de la señal que contribuye a la actividad Mek1/Erk1 durante la mielinización es actualmente desconocida, aunque es probable que sea de origen axonal, independiente del CRD-Nrg1 axonal. Los posibles candidatos son Ig-Nrg1 de tipo I y II que se expresan por las neuronas del PNS y luego se liberan de la membrana axonal por escisión proteolítica. Otro posible activador de Mek1/Erks es FGF-2, que se expresa en las neuronas del PNS y el receptor para el cual se expresa en las células de Schwann. El tratamiento con FGF-2 regula negativamente la expresión del gen de mielina e inhibe la mielinización in vitro. La pérdida de la expresión de FGF-2 da lugar a un aumento en el número de axones mielinizados durante la regeneración del nervio ciático. Las neuronas periféricas también expresan PDGF e IGF, con las correspondientes de tirosinas quinasas de receptor expresadas en las células de Schwann asociadas. Será de gran interés evaluar el papel regulador de estos factores de crecimiento durante la mielinización del SNP.
Uso terapéutico de GGF2: el trasplante experimental ha proporcionado una prueba abrumadora del potencial de reparar los nervios dañados mediante el trasplante de células gliales mielinizantes. Las células de Schwann son buenas candidatas para dicha terapia, ya que se expanden fácilmente en cultivo y ofrecen la posibilidad de un trasplante autólogo para promover la remielinización y restauración de la conducción nerviosa en las lesiones desmielinizadas no solo en el SNP sino también en el SNC. Sin embargo, la remielinización de las células de Schwann en los axones adultos en regeneración a menudo es incompleta, lo que da lugar a la formación de una vaina de mielina más delgada y un entrenudo más corto en comparación con los nervios normales. Por lo tanto, la presente demostración de la función promielinizante de GGF2 y la capacidad de evitar el obstáculo involuntario de la mielinización debido a los niveles de dosis de GGF2 es significativa ya que proporciona una estrategia terapéutica para el tratamiento de enfermedades desmielinizantes, así como para reconstruir la mielina después de una lesión nerviosa.
Listado de secuencias
<110> Kim, Haesun
Caggiano, Anthony
<120> PROCEDIMIENTO PARA LOGRAR NIVELES PLASMÁTICOS DESEADOS DE FACTOR DE CRECIMIENTO GLIAL 2
<130> 1094-1-038PCT
<140> PCT/US2009/001356
<141 > 2009-03-02
<150> 61/067,589
<151 > 2008-02-29
<160> 14
<170> FastSEQ for Windows Versión 4.0
<210> 1
<211> 2003
<212> ADN
<213> Homo sapiens
<400> 1
ggaattcctt tttttttttt tttttttctt rrtttttttt tgcccttata cctcttcgcc 60 tttctgtggt tccatccact tcttccccct cctcctccca taaacaactc tcctacccct 120 gcacccccaa taaataaata aaaggaggag ggcaaggggg gaggaggagg agtggtgctg 180 cgaggggaag gaaaagggag gcagcgcgag aagagccggg cagagtccga accgacagcc 240 agaagcccgc acgcacctcg caccatgaga tggcgacgcg ccccgcgccg ctccgggcgt 300 cccggccccc gggcccagcg ccccggctcc gccgcccgct cgtcgccgcc gctgccgctg 360 ctgccactac tgctgctgct ggggaccgcg gccctggcgc cgggggcggc ggccggcaac 420 gaggcggctc ccgcgggggc ctcggtgtgc tactcgtccc cgcccagcgt gggatcggtg 480 caggagctag ctcagcgcgc cgcggtggtc atcgagggaa aggtgcaccc gcagcggcgg 540 cagcaggggg cactcgacag gaaggcggcg gcggcggcgg gcgaggcagg ggcgtggggc 600 ggcgatcgcg agccgccagc cgcgggccca cgggcgctgg ggccgcccgc cgaggagccg 660 ctgctcgccg ccaacgggac cgtgccctct tggcccaccg ccccggtgcc cagcgccggc 720 gagcccgggg aggaggcgcc ctatctggtg aaggtgcacc aggtgtgggc ggtgaaagcc 780 gggggcttga agaaggactc gctgctcacc gtgcgcctgg ggacctgggg ccaccccgcc 840 ttcccctcct gcgggaggct caaggaggac agcaggtaca tcttcttcat ggagcccgac 900 gccaacagca ccagccgcgc gccggccgcc ttccgagcct ctttcccccc tctggagacg 960 ggccggaacc tcaagaagga ggtcagccgg gtgctgtgca agcggtgcgc cttgcctccc 1020 caattgaaag agatgaaaag ccaggaatcg gctgcaggtt ccaaactagt ccttcggtgt 1080 gaaaccagtt ctgaatactc ctctctcaga ttcaagtggt tcaagaatgg gaatgaattg 1140 aatcgaaaaa acaaaccaca aaatatcaag atacaaaaaa agccagggaa gtcagaactt 1200 cgcattaaca aagcatcact ggctgattct ggagagtata tgtgcaaagt gatcagcaaa 1260 ttaggaaatg acagtgcctc tgccaatatc accatcgtgg aatcaaacgc tacatctaca 1320 tccaccactg ggacaagcca tcttgtaaaa tgtgcggaga aggagaaaac tttctgtgtg 1380 aatggagggg agtgcttcat ggtgaaagac ctttcaaacc cctcgagata cttgtgcaag 1440 tgcccaaatg agtttactgg tgatcgctgc caaaactacg taatggccag cttctacagt 1500 acgtccactc cctttctgtc tctgcctgaa taggagcatg ctcagttggt gctgctttct 1560 tgttgctgca tctcccctca gattccacct agagctagat gtgtcttacc agatctaata 1620 ttgactgcct ctgcctgtcg catgagaaca ttaacaaaag caattgtatt acttcctctg 1680 ttcgcgacta gttggctctg agatactaat aggtgtgtga ggctccggat gtttctggaa 1740 ttgatattga atgatgtgat acaaattgat agtcaatatc aagcagtgaa atatgataat 1800 aaaggcattt caaagtctca cttttattga taaaataaaa atcattctac tgaacagtcc 1860 atcttcttta tacaatgacc acatcctgaa aagggtgttg ctaagctgta accgatatgc 1920 acttgaaatg atggtaagtt aattttgatt cagaatgtgt tatttgtcac aaataaacat 1980 aataaaagga aaaaaaaaaa aaa 2003
<210>2
<211> 422
<212> PRT
<213> Homo sapiens
<400> 2
Claims (3)
1. Factor de crecimiento glial 2 (GGF2) para su uso en la promoción de la remielinización celular en un paciente, donde el GGF2 se administra al paciente en una cantidad de 500 ng /- 15% de GGF2 por kg de peso corporal.
2. Una composición farmacéutica que comprende el GGF2 para usar de acuerdo con la reivindicación 1 y un inhibidor de la vía Mekl/Erk, donde el inhibidor de la vía Mekl/Erk se selecciona del grupo que consiste en Arctigenina, PD 98059, SB202190, SB203580, SP600125, U0126, tipifarnib (Zarnestra®), sorafenib, ISIS 5132, CI-1040 y PD 0325901.
3. El GGF2 para uso según la reivindicación 1 o la composición farmacéutica según la reivindicación 2, donde la célula es una célula de Schwann.
Figura 1
Figura 2
Sin tratamiento GGF (0.01 nM)
Figura 3
Figura 4
Eh G a u Eh tí Eh Ch
en u >u
01 u x: u ai
£ < £ 3 < < Eh h en
gE iH < o
o ü O < r3H Eh
h a O u
íes H Jtí a £
O > < < O o Eh CU < Eh
Figura 12
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US6758908P | 2008-02-29 | 2008-02-29 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2811127T3 true ES2811127T3 (es) | 2021-03-10 |
Family
ID=41016663
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES09715322.5T Active ES2613177T3 (es) | 2008-02-29 | 2009-03-02 | Método para conseguir niveles plasmáticos deseados de factor de crecimiento glial 2 |
| ES16182139T Active ES2811127T3 (es) | 2008-02-29 | 2009-03-02 | Composiciones para lograr niveles plasmáticos deseados del factor 2 de crecimiento glial |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES09715322.5T Active ES2613177T3 (es) | 2008-02-29 | 2009-03-02 | Método para conseguir niveles plasmáticos deseados de factor de crecimiento glial 2 |
Country Status (11)
| Country | Link |
|---|---|
| US (5) | US8410050B2 (es) |
| EP (3) | EP2262527B1 (es) |
| JP (2) | JP5697455B2 (es) |
| CN (2) | CN104645315A (es) |
| AU (1) | AU2009217606B2 (es) |
| BR (1) | BRPI0908271A2 (es) |
| CA (1) | CA2717193C (es) |
| ES (2) | ES2613177T3 (es) |
| PL (2) | PL2262527T3 (es) |
| RU (3) | RU2530650C2 (es) |
| WO (1) | WO2009108390A2 (es) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2262527B1 (en) | 2008-02-29 | 2016-08-03 | Acorda Therapeutics, Inc. | Compositions for achieving desired glial growth factor 2 plasma levels |
| DK2320933T3 (en) | 2008-07-17 | 2018-04-16 | Acorda Therapeutics Inc | THERAPEUTIC DOSAGE OF A NEUREGULIN OR A SUBSEQUENT THEREOF FOR TREATMENT OR PROPHYLAXY OF HEART FAILURE |
| CN102159237A (zh) | 2008-08-15 | 2011-08-17 | 阿索尔达治疗公司 | 在cns神经性损伤后非-急性期间处理的组合物及方法 |
| AU2010306777C1 (en) | 2009-10-14 | 2016-03-17 | Acorda Therapeutics, Inc. | Use of a neuregulin to treat peripheral nerve injury |
| RU2012157572A (ru) * | 2010-05-28 | 2014-07-10 | МЕН-ЭнЭрЖ СА | Изоформы нейрегулина, полипептиды нейрегулина и их применение |
| US20130143805A1 (en) * | 2010-08-13 | 2013-06-06 | Georgetown University | Ggf2 and methods of use |
| NZ700546A (en) * | 2012-03-30 | 2017-05-26 | Acorda Therapeutics Inc | Use of neuregulin to treat peripheral nerve injury |
| US11207354B2 (en) * | 2016-09-23 | 2021-12-28 | Osaka University | Schwann cell differentiation promoting agent and a peripheral nerve regeneration promoting agent |
| CN108653274B (zh) * | 2017-04-01 | 2022-09-16 | 鲁南制药集团股份有限公司 | 牛蒡子苷元在制备治疗骨髓损伤药物中的用途 |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5716930A (en) | 1991-04-10 | 1998-02-10 | Ludwig Institute For Cancer Research | Glial growth factors |
| US7319019B1 (en) | 1991-04-10 | 2008-01-15 | Acorda Therapeutics, Inc. | Glial mitogenic factors lacking an N-terminal signal sequence |
| US7135456B1 (en) | 1991-04-10 | 2006-11-14 | Acorda Therapeutics, Inc. | Glial mitogenic factors, their preparation and use |
| US5530109A (en) * | 1991-04-10 | 1996-06-25 | Ludwig Institute For Cancer Research | DNA encoding glial mitogenic factors |
| US7037888B1 (en) | 1992-04-03 | 2006-05-02 | Acorda Therapeutics, Inc. | Methods for treating muscle diseases and disorders |
| GB9217316D0 (en) * | 1992-08-14 | 1992-09-30 | Ludwig Inst Cancer Res | Schwann cell mitogenic factor,its preparation and use |
| US5912326A (en) | 1995-09-08 | 1999-06-15 | President And Fellows Of Harvard College | Cerebellum-derived growth factors |
| JP2003513995A (ja) * | 1999-11-19 | 2003-04-15 | アクスクシーマ ファルマシューティカルス アクチェンゲゼルシャフト | ヘリコバクターピロリにより誘発される胃腸疾患の阻害剤 |
| US20030232761A1 (en) | 2002-03-28 | 2003-12-18 | Hinke Simon A. | Novel analogues of glucose-dependent insulinotropic polypeptide |
| EP2354155B1 (en) | 2003-05-16 | 2017-05-03 | Acorda Therapeutics, Inc. | Fusion Proteins for Treatment of CNS |
| WO2005079458A2 (en) * | 2004-02-19 | 2005-09-01 | The Regents Of The University Of California | ENHANCEMENT OF Th2-DEPENDENT AND INFLAMMATORY RESPONSE |
| AU2006210537A1 (en) | 2005-02-02 | 2006-08-10 | Fox Chase Cencer Center | Amine derivative containing compositions and methods for the treatment of viral infections related to the etiology of cancer |
| WO2007028085A2 (en) | 2005-09-02 | 2007-03-08 | Morehouse School Of Medicine | Neuregulin for prevention and treatment of damage from acute assault on vascular and neuronal tissues |
| US20080003013A1 (en) * | 2006-06-30 | 2008-01-03 | Static Control Components, Inc. | Cartridge split rail clip |
| EP2262527B1 (en) | 2008-02-29 | 2016-08-03 | Acorda Therapeutics, Inc. | Compositions for achieving desired glial growth factor 2 plasma levels |
| MX2012011473A (es) | 2010-04-01 | 2012-11-16 | Procter & Gamble | Suavizante de telas. |
| US20130143805A1 (en) | 2010-08-13 | 2013-06-06 | Georgetown University | Ggf2 and methods of use |
-
2009
- 2009-03-02 EP EP09715322.5A patent/EP2262527B1/en active Active
- 2009-03-02 PL PL09715322T patent/PL2262527T3/pl unknown
- 2009-03-02 WO PCT/US2009/001356 patent/WO2009108390A2/en not_active Ceased
- 2009-03-02 CA CA2717193A patent/CA2717193C/en active Active
- 2009-03-02 ES ES09715322.5T patent/ES2613177T3/es active Active
- 2009-03-02 US US12/380,760 patent/US8410050B2/en not_active Expired - Fee Related
- 2009-03-02 JP JP2010548749A patent/JP5697455B2/ja not_active Expired - Fee Related
- 2009-03-02 RU RU2010139906/15A patent/RU2530650C2/ru active
- 2009-03-02 EP EP16182139.2A patent/EP3120863B1/en active Active
- 2009-03-02 EP EP20173000.9A patent/EP3750551A1/en not_active Withdrawn
- 2009-03-02 ES ES16182139T patent/ES2811127T3/es active Active
- 2009-03-02 BR BRPI0908271A patent/BRPI0908271A2/pt not_active IP Right Cessation
- 2009-03-02 CN CN201410709391.4A patent/CN104645315A/zh active Pending
- 2009-03-02 PL PL16182139.2T patent/PL3120863T3/pl unknown
- 2009-03-02 AU AU2009217606A patent/AU2009217606B2/en not_active Ceased
- 2009-03-02 CN CN200980114836.1A patent/CN102026651B/zh not_active Expired - Fee Related
-
2013
- 2013-03-29 US US13/853,386 patent/US9272015B2/en active Active
-
2014
- 2014-07-28 RU RU2014131265A patent/RU2687097C2/ru active
- 2014-10-17 JP JP2014212193A patent/JP5964920B2/ja not_active Expired - Fee Related
-
2016
- 2016-01-21 US US15/002,608 patent/US9744215B2/en not_active Expired - Fee Related
-
2017
- 2017-07-25 US US15/658,967 patent/US10675331B2/en active Active
-
2019
- 2019-04-09 RU RU2019110452A patent/RU2019110452A/ru unknown
-
2020
- 2020-05-18 US US16/876,702 patent/US20210060128A1/en not_active Abandoned
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2811127T3 (es) | Composiciones para lograr niveles plasmáticos deseados del factor 2 de crecimiento glial | |
| Jelkmann et al. | Beneficial and ominous aspects of the pleiotropic action of erythropoietin | |
| US11053321B2 (en) | ErbB2 signaling and nerve regeneration | |
| Syed et al. | Pituitary adenylate cyclase-activating polypeptide (PACAP) potently dilates middle meningeal arteries: implications for migraine | |
| Li et al. | Angiotensin AT2 receptor protects against cerebral ischemia‐induced neuronal injury | |
| Hata et al. | RGMa inhibition promotes axonal growth and recovery after spinal cord injury | |
| JP5905833B2 (ja) | 心筋虚血−再潅流障害の予防、処置または遅延のための、ニューレグリンを含む組成物およびその利用 | |
| Xie et al. | Intranasal administration of recombinant Netrin-1 attenuates neuronal apoptosis by activating DCC/APPL-1/AKT signaling pathway after subarachnoid hemorrhage in rats | |
| US20030113326A1 (en) | Reducing myelin-mediated inhibition of axon regeneration | |
| Yin et al. | DLK silencing attenuated neuron apoptosis through JIP3/MA2K7/JNK pathway in early brain injury after SAH in rats | |
| Joung et al. | Secretion of EGF-like domain of heregulinβ promotes axonal growth and functional recovery of injured sciatic nerve | |
| Deng et al. | α-amino-3-hydroxy-5-methyl-4-isoxazole propionate receptor subunit composition and cAMP-response element-binding protein regulate oligodendrocyte excitotoxicity | |
| AU2017203961B2 (en) | Method for achieving desired glial growth factor 2 plasma levels | |
| HK1152230B (en) | Compositions for achieving desired glial growth factor 2 plasma levels |