ES2828097T3 - Métodos para detectar dimetilarginina simétrica - Google Patents
Métodos para detectar dimetilarginina simétrica Download PDFInfo
- Publication number
- ES2828097T3 ES2828097T3 ES09790996T ES09790996T ES2828097T3 ES 2828097 T3 ES2828097 T3 ES 2828097T3 ES 09790996 T ES09790996 T ES 09790996T ES 09790996 T ES09790996 T ES 09790996T ES 2828097 T3 ES2828097 T3 ES 2828097T3
- Authority
- ES
- Spain
- Prior art keywords
- sdma
- antibody
- sample
- antibodies
- free
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 CCCC(NC)NCCCC(C(NCC(CC)CSC(CCC(*1)C1C*1C(C)([*+])CC)C1=O)=*)N Chemical compound CCCC(NC)NCCCC(C(NCC(CC)CSC(CCC(*1)C1C*1C(C)([*+])CC)C1=O)=*)N 0.000 description 2
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C279/00—Derivatives of guanidine, i.e. compounds containing the group, the singly-bound nitrogen atoms not being part of nitro or nitroso groups
- C07C279/04—Derivatives of guanidine, i.e. compounds containing the group, the singly-bound nitrogen atoms not being part of nitro or nitroso groups having nitrogen atoms of guanidine groups bound to acyclic carbon atoms of a carbon skeleton
- C07C279/12—Derivatives of guanidine, i.e. compounds containing the group, the singly-bound nitrogen atoms not being part of nitro or nitroso groups having nitrogen atoms of guanidine groups bound to acyclic carbon atoms of a carbon skeleton being further substituted by nitrogen atoms not being part of nitro or nitroso groups
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/44—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material not provided for elsewhere, e.g. haptens, metals, DNA, RNA, amino acids
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54366—Apparatus specially adapted for solid-phase testing
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6803—General methods of protein analysis not limited to specific proteins or families of proteins
- G01N33/6806—Determination of free amino acids
- G01N33/6812—Assays for specific amino acids
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Molecular Biology (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Biomedical Technology (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Food Science & Technology (AREA)
- Microbiology (AREA)
- Cell Biology (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Biotechnology (AREA)
- Biophysics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Genetics & Genomics (AREA)
- Bioinformatics & Computational Biology (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Peptides Or Proteins (AREA)
- Stereophonic System (AREA)
- Superheterodyne Receivers (AREA)
Abstract
Anticuerpo aislado específico para dimetilarginina simétrica libre (SDMA) en una muestra biológica, en el que la SDMA libre no forma parte de una cadena polipeptídica, en el que la SDMA libre es SDMA de fórmula, **(Ver fórmula)**
Description
DESCRIPCIÓN
Métodos para detectar dimetilarginina simétrica
Esta solicitud reivindica el beneficio de solicitud de patente provisional estadounidense con n.° de serie 61/086.870 presentada el 7 de agosto de 2008.
Antecedentes de la invención
Campo de la invención
La invención se refiere generalmente a la detección de dimetilarginina simétrica (SDMA). Más particularmente, la invención se refiere a análogos que pueden usarse para generar anticuerpos anti-SDMA, a los anticuerpos anti-SDMA generados usando los análogos de SDMA, y a usos para los anticuerpos anti-SDMA, incluyendo métodos y dispositivos de diagnóstico.
Técnica relacionada
Es importante poder medir la función renal de manera rápida y precisa. Por ejemplo, la dosificación de los fármacos debe adaptarse a los pacientes con insuficiencia renal. Por tanto, realizar una evaluación precisa de la función renal es un requisito en la medicina clínica. Sin embargo, el diagnóstico de insuficiencia renal se ve obstaculizado por la falta de marcadores fiables de la tasa de filtración glomerular (TFG) y/o pruebas de diagnóstico disponibles. Una medición de la TFG ampliamente usada es el aclaramiento de inulina, pero esta prueba es engorrosa y costosa, lo que reduce esencialmente su utilidad en la práctica clínica. Esto también es válido para las pruebas de aclaramiento de radioisótopos. Por tanto, en la práctica clínica, la creatinina sérica se usa normalmente para evaluar la función renal.
Sin embargo, una gran desventaja asociada con la medición de la creatinina sérica es que existe una considerable variabilidad interindividual asociada con la masa muscular, la ingesta de proteínas, la edad y el sexo. Además, incluso después de que se haya perdido una gran parte de la función renal del paciente, los niveles de creatinina sérica pueden permanecer en un intervalo normal, lo que significa que la creatinina sérica no es útil para la detección temprana de la insuficiencia renal. Además, aunque la aproximación de la TFG mediante el aclaramiento de creatinina puede ser más informativa que la creatinina sérica, la obtención de muestras de orina precisas y cronometradas en 24 horas requiere mucho trabajo y puede resultar difícil dependiendo de la población de pacientes que se va a someter a prueba, tal como lactantes, ancianos, personas con anomalías urológicas o animales. Por consiguiente, existe la necesidad de métodos y marcadores de diagnóstico alternativos para someter a prueba la función renal.
La dimetilarginina simétrica (SDMA) es el isómero estructural de la dimetilarginina asimétrica (ADMA) un inhibidor de la óxido nítrico sintetasa (NOS) endógena. Tanto ADMA como SDMA se derivan de la metilación intranuclear de residuos de L-arginina y se liberan en el citoplasma después de la proteólisis. La SDMA se produce por la proteína arginina metiltransferasa 5 (PRMT 5) y p Rm T 7. Las proteínas que portan metilargininas, tales como SDMA, monometilarginina y ADMA, desempeñan un papel en el procesamiento del ARN, el transporte de proteínas y la transducción de señales (Bedford y Richard, Mol. Cell, 2005, 29 de abril, 18 (3):263-72). La s DmA libre que resulta de la degradación de proteínas metiladas de este tipo se elimina principalmente por excreción renal, mientras que la ADMA se metaboliza en gran medida.
La ADMA se correlaciona fuertemente con factores de riesgo de enfermedad arterial coronaria (CAD) tal como hipertensión, hipercolesterolemia, hiperhomocisteinemia, resistencia a la insulina, edad y presión arterial media. La SDMA se correlaciona con parámetros de la función renal, tal como la tasa de filtración glomerular (TFG), el aclaramiento de inulina y el aclaramiento de creatinina. Sin embargo, la SDMA puede ser más que un indicador de la función renal. Por ejemplo, en animales, una dieta alta en grasas y colesterol aumenta los niveles séricos de SDMA sin afectar a la función renal, lo que indica que la SDMA también puede ser un factor de riesgo cardiovascular. Además, los anticuerpos anti-SDMA también pueden utilizarse como biomarcador para el lupus eritematoso sistémico (LES). Las proteínas D1 y D3 del complejo Sm, que se ha implicado que desempeñan un papel en la etiología del LES, contienen SDMA C-terminal. Kielstein, J.T. et al. en Nephrology dialysis transplantation, 2006, págs. 1-6 describen el papel de la SDMA como marcador de la función renal y su determinación mediante métodos GL-MS.
Por consiguiente, los inventores han identificado la necesidad en la técnica de un método simple, conveniente y rentable para identificar SDMA en muestras biológicas para evaluar, por ejemplo, la función renal, la función cardiovascular y el LES. Además, los inventores han identificado la necesidad de proporcionar anticuerpos anti-SDMA que sean específicos para SDMA, es decir, que discriminen entre moléculas que difieren sólo en el estado de metilación de los dos nitrógenos equivalentes en el grupo guanidino de SDMA, como arginina, monometilarginina y ADMA.
Breve sumario de la invención
En un aspecto, la invención proporciona nuevos anticuerpos anti-SDMA que pueden ser útiles en inmunoensayos de diagnóstico tal como se define adicionalmente en las reivindicaciones. Los anticuerpos pueden no tener ninguna o sustancialmente ninguna reactividad cruzada con arginina, monometilarginina y ADmA. En otro aspecto de referencia, los anticuerpos se preparan usando un inmunógeno tal como se describe en el presente documento. El inmunógeno incluye un análogo de SDMA conjugado con una proteína portadora. En otro aspecto, la memoria descriptiva se refiere al análogo de SDMA.
Los anticuerpos de la invención pueden usarse para detectar SDMA en muestra biológicas de un sujeto animal. En los diversos aspectos de la invención, se determina la presencia o cantidad de SDMA. La cantidad de SDMA en una muestra puede usarse para determinar la función renal y diagnosticar enfermedad renal en un animal.
En un aspecto de referencia adicional, pueden usarse análogos de SDMA para el diagnóstico de lupus eritematoso sistémico (LES) en un sujeto animal.
Características, ventajas y realizaciones adicionales de la invención pueden explicarse o resultar evidentes a partir de la consideración de la descripción detallada, dibujos y reivindicaciones a continuación. Además, debe entenderse que tanto el sumario anterior de la invención como la siguiente descripción detallada son a modo de ejemplo y pretenden proporcionar una explicación adicional sin limitar el alcance de la invención tal como se reivindica.
Breve descripción de los dibujos
Los dibujos adjuntos, que se incluyen para proporcionar una mayor comprensión de la invención, se incorporan en y constituyen una parte de esta memoria descriptiva, ilustran realizaciones de la invención, y junto con la descripción detallada sirven para explicar los principios de la invención. No se intentan mostrar los detalles estructurales de la invención con más detalle de lo que puede ser necesario para una comprensión fundamental de la invención y las diversas formas en las que se puede poner en práctica.
La figura 1 es un gráfico que compara los resultados del método de detección de SDMA según la invención con espectroscopía de masas.
La figura 2 es un gráfico de las concentraciones de SDMA medidas según el método de la invención en perros sanos y perros que tienen cáncer, enfermedad cardiaca o enfermedad cardiorrenal. La barra horizontal representa el valor de corte (determinado como concentración media de SDMA más 2 desviaciones estándar de una población de perros sanos).
La figura 3 es un gráfico de concentraciones de SDMA medidas según el método de la invención en gatos sanos y gatos que tienen enfermedad renal o cáncer. La barra horizontal representa el valor de corte (determinado como concentración media de SDMA más 2 desviaciones estándar de una población de gatos sanos).
La figura 4 es un gráfico de absorbancia a 280 nm frente al número de fracciones para elución de un conjugado SDMA-cistamida-proteína, en el que la proteína es KLH (♦ ) o BSA (■), a partir de una columna de filtración en gel Sephadex G-25M tal como se describe en los ejemplos.
Descripción detallada de la invención
En diversos aspectos, la invención proporciona un método para detectar SDMA en una muestra biológica de un animal tal como se define adicionalmente en las reivindicaciones. El método incluye detectarla presencia o cantidad de SDMA en la muestra usando un formato de inmunoensayo, tal como un inmunoensayo competitivo. El ensayo incluye el uso de anticuerpos contra SDMA que son específicos para SDMA y que tienen poca o ninguna reactividad cruzada con ADMA, L-arginina y N-metilarginina. El ensayo también usa análogos de s DmA que se conectan a marcadores y/o fases sólidas. La presencia o cantidad de SDMA en una muestra puede usarse para diagnosticar o predecir el estado patológico del animal, tal como enfermedad renal, enfermedad cardiovascular y LES.
Antes de describir la invención con más detalle, se definen varios términos:
Ac es anticuerpo.
ADMA es dimetilarginina asimétrica. La estructura de ADMA es:
BUN es nitrógeno ureico en sangre.
BSA es albúmina sérica bovina.
CMIA es inmunoensayo magnético quimioluminiscente.
DCM es diclorometano.
DIPEA es N,N-diisopropiletilamina.
DMF es dimetilformamida.
EIA es inmunoensayo de enzimas.
ELISA es ensayo de inmunoabsorción ligado a enzimas.
ESI-EM es espectrometría de masas de ionización por electropulverización.
FPIA es inmunoensayo de polarización fluorescente.
TFG es tasa de filtración glomerular.
HATU es metanamininio de hexafluorofosfato de (1H-7-azabenzotriazol-1-il)-1,1,3,3-tetrametiluranio. KLH es hemocianina de lapa californiana.
MEIA es inmunoensayo enzimático de micropartículas.
NOS es óxido nítrico sintasa.
PBS es solución salina tamponada con fosfato.
RIA es radioinmunoensayo.
SDMA es dimetilarginina simétrica. La estructura de SDMA es:
SDMA libre se refiere a SDMA que no forma parte de una cadena polipeptídica.
Uno o más residuos de aminoácido de SDMA pueden estar presentes en un polipéptido.
LES es lupus eritematoso sistémico.
TFA es ácido trifluoracético.
La estructura de arginina es:
N-MMA es N-monometilarginina, o simplemente N-metilarginina. La estructura de N-monometilarginina es:
El término “análogo”, tal como se usa en el presente documento, se refiere generalmente a un compuesto en el que uno o más átomos individuales han sido reemplazados con un/unos átomo(s) diferente(s) o con un/unos grupo(s) funcional(es) diferente(s). Por ejemplo, un análogo puede ser una forma modificada del analito que puede competir con el analito por un receptor, proporcionando la modificación un medio para unir el analito a otro resto, tal como un marcador o un soporte sólido. El análogo del analito puede unirse a un anticuerpo de una manera similar al analito.
El término “anticuerpo”, tal como se usa en el presente documento, se refiere generalmente a una glicoproteína producida por células de linfocitos B en respuesta a la exposición a un antígeno y se une específicamente a ese antígeno. El término “anticuerpo” se usa en su sentido más amplio y cubre específicamente anticuerpos monoclonales (incluyendo anticuerpos monoclonales de longitud completa), anticuerpos policlonales, anticuerpos multiespecíficos (por ejemplo, anticuerpos biespecíficos) y fragmentos de anticuerpos siempre que presenten la actividad biológica deseada.
Tal como se usa en el presente documento, un “anti-SDMA”, “porción de anticuerpo anti-SDMA” o “fragmento de anticuerpo anti-SDMA” y/o “variante de anticuerpo anti-SDMA” y similares incluyen cualquier proteína o péptido que contenga una molécula que comprenda al menos una porción de una molécula de inmunoglobulina, tal como, pero sin limitarse a, una región determinante de complementariedad (CDR) de una región constante de cadena pesada o cadena ligera, una región de entramado o cualquier porción de la misma.
El término “fragmento de anticuerpo” , tal como se usa en el presente documento, se refiere a una porción de un anticuerpo de longitud completa, generalmente el dominio variable o de unión a antígeno del mismo. Específicamente, por ejemplo, los fragmentos de anticuerpos pueden incluir fragmentos Fab, Fab’, F(ab’)2 y Fv; diacuerpos; anticuerpos lineales; moléculas de anticuerpo de cadena sencilla; y anticuerpos multiespecíficos de fragmentos de anticuerpos.
El término “antígeno”, tal como se usa en el presente documento, se refiere generalmente a una sustancia que es capaz, en condiciones apropiadas, de reaccionar con un anticuerpo específico para el antígeno.
El término “analito” , tal como se usa en el presente documento, se refiere generalmente a la sustancia o conjunto de sustancias en una muestra que se detectan y/o miden.
El término “muestra biológica”, tal como se usa en el presente documento, se refiere generalmente a una muestra de tejido o líquido de un ser humano o animal incluyendo, pero sin limitarse a, sangre completa, plasma, suero, líquido cefalorraquídeo, líquido linfático, líquido abdominal (ascitis), las secciones externas de piel, tractos respiratorio, intestinal y genitourinario, lágrimas, saliva, orina, glóbulos, tumores, órganos, tejido y muestra de constituyentes de cultivo celular in vitrn.
El término “reactividad cruzada” , tal como se usa en el presente documento, se refiere generalmente a la capacidad de un sitio de unión a antígeno individual de un anticuerpo para reaccionar con más de un determinante antigénico o la capacidad de una población de moléculas de anticuerpo para reaccionar con más de un antígeno. En general, las reacciones cruzadas surgen porque (i) el antígeno de reacción cruzada comparte un epítopo en común con el antígeno de inmunización o (ii) tiene un epítopo que es estructuralmente similar al del antígeno de inmunización (multiespecificidad).
El término “inmunoensayo” , tal como se usa en el presente documento, se refiere generalmente a una prueba que emplea complejos de anticuerpos y antígenos para generar una respuesta medible. Un “complejo anticuerpo:antígeno” puede usarse de manera intercambiable con el término “inmunocomplejo” . Los inmunoensayos incluyen, en general, inmunoensayos no competitivos, inmunoensayos competitivos, inmunoensayos homogéneos e inmunoensayos heterogéneos. En los “inmunoensayos competitivos”, el analito (o antígeno) no marcado en la muestra de prueba se mide por su capacidad para competir con el antígeno marcado en el inmunoensayo. El antígeno no marcado bloquea la capacidad del antígeno marcado para unirse porque el sitio de unión del anticuerpo ya está ocupado. En los “inmunoensayos competitivos” , la cantidad de antígeno presente en la muestra de prueba está inversamente relacionada con la cantidad de señal generada a partir del marcador. Por el contrario, en los “inmunoensayos no competitivos”, también conocidos como inmunoensayos de tipo “sándwich”, el analito se une entre dos reactivos de anticuerpos altamente específicos para formar un complejo y la cantidad de antígeno es directamente proporcional a la cantidad de señal asociada con el complejo. Los inmunoensayos que requieren la separación de los complejos anticuerpo:antígeno unidos se denominan generalmente “inmunoensayos heterogéneos” y los inmunoensayos que no requieren la separación de los complejos anticuerpo:antígeno se denominan generalmente “inmunoensayos
homogéneos”. Un experto en la técnica comprenderá fácilmente los diversos formatos de inmunoensayo.
El término “complejos inmunitarios”, tal como se usa en el presente documento, se refiere generalmente a los complejos formados por la unión de moléculas de antígeno y anticuerpo, con o sin fijación del complemento. Cuando se marca uno del anticuerpo o del antígeno, el marcador se asocia con el complejo inmunitario como resultado de la unión entre el antígeno y el anticuerpo. Por tanto, cuando se marca el anticuerpo, el marcador se asocia con el antígeno como resultado de la unión. De manera similar, cuando se marca el antígeno (por ejemplo, un análogo de analito que tiene un marcador), el marcador se asocia con el anticuerpo como resultado de la unión entre el antígeno y el anticuerpo.
El término “marcador”, tal como se usa en el presente documento, se refiere a un compuesto, composición o soporte sólido detectable, que puede conjugarse directa o indirectamente (por ejemplo, a través de medios covalentes o no covalentes, solos o encapsulados) con un anticuerpo, análogo de SDMA o antígeno de la invención. El marcador puede ser detectable por sí mismo (por ejemplo, marcadores de radioisótopos, tinte quimioluminiscente, marcadores electroquímicos, quelatos metálicos, partículas de látex o marcadores fluorescentes) o, en el caso de un marcador enzimático, puede catalizar la alteración química de un compuesto o composición de sustrato que es detectable (por ejemplo, enzimas tales como peroxidasa del rábano, fosfatasa alcalina y similares). El marcador empleado en la presente invención podría ser, pero no se limita a: fosfatasa alcalina; glucosa-6-fosfato deshidrogenasa (“G6PDH”); peroxidasa del rábano (HRP); agentes quimioluminiscentes tales como isoluminol, agentes fluorescentes tales como compuestos de fluoresceína y rodamina; ribozimas; y tintes. El marcador también puede ser una molécula de unión específica que en sí misma puede ser detectable (por ejemplo, biotina, avidina, estreptacidina, digioxigenina, maltosa, oligohistidina, 2,4-dinitrobenceno, fenilarsenato, ADNmc, ADNbc y similares). El marcador puede estar unido a otra molécula o soporte sólido y se elige por características específicas que permiten la detección de la molécula marcada. La utilización de un marcador produce una señal que puede detectarse mediante medios tales como la detección de radiación electromagnética o visualización directa, y que puede medirse opcionalmente.
El término “anticuerpo monoclonal”, tal como se usa en el presente documento, se refiere generalmente a un anticuerpo obtenido de una población de anticuerpos sustancialmente homogéneos, es decir, los anticuerpos individuales que componen la población son idénticos. Los anticuerpos monoclonales son muy específicos, dirigiéndose contra un único sitio antigénico. A diferencia de las preparaciones de anticuerpos policlonales, que típicamente incluyen diferentes anticuerpos dirigidos contra diferentes epítopos, cada anticuerpo monoclonal se dirige contra un solo epítopo en el antígeno. El modificador “monoclonal” se refiere simplemente al carácter del anticuerpo y no debe interpretarse que requiera la producción del anticuerpo por ningún método particular. Específicamente, por ejemplo, los anticuerpos monoclonales pueden prepararse mediante metodologías de hibridomas, o pueden prepararse mediante métodos de ADN recombinante, o pueden aislarse de bibliotecas de anticuerpos de fagos usando técnicas conocidas.
El término “polipéptido”, tal como se usa en el presente documento, se refiere generalmente a una molécula que tiene una secuencia de aminoácidos unidos por enlaces peptídicos. Este término incluye proteínas, proteínas de fusión, oligopéptidos, péptidos cíclicos y derivados polipeptídicos. Los anticuerpos y derivados de anticuerpos se comentaron anteriormente en una sección separada, pero los anticuerpos y derivados de anticuerpos, para los fines de la invención, se tratan como una subclase de los polipéptidos y derivados de polipéptidos.
El término “soporte sólido”, tal como se usa en el presente documento, se refiere a una matriz no acuosa a la que puede adherirse el anticuerpo o análogo de SDMA de la presente invención. Los ejemplos de soporte sólido incluyen soportes formados parcial o totalmente de vidrio (por ejemplo, vidrio de poro controlado), polímeros sintéticos y naturales, polisacáridos (por ejemplo, agarosa), poliacrilamidas, poliestireno, poli(alcoholes vinílicos) y siliconas, partículas magnéticas, partículas de látex, tiras cromatográficas, placas de poliestireno de microtitulación, o cualquier otra sustancia que permita lavar o separar antígenos y/o anticuerpos unidos de los materiales no unidos. En determinadas realizaciones, dependiendo de la aplicación, el soporte sólido puede ser el pocillo de una placa de ensayo o puede ser una columna de purificación (por ejemplo, una columna de cromatografía de afinidad).
“Receptor” se refiere a cualquier compuesto o composición capaz de reconocer una organización espacial y polar particular de una molécula, por ejemplo, un sitio epitópico o determinante. Los receptores ilustrativos incluyen anticuerpos, fragmentos Fab y similares.
“Especificidad de unión” o “unión específica” se refiere al reconocimiento sustancial de una primera molécula por una segunda molécula, por ejemplo, un polipéptido y un anticuerpo policlonal o monoclonal, o un fragmento de anticuerpo (por ejemplo, un fragmento Fv, Fv de cadena sencilla, Fab' o F(ab')2) específico para el polipéptido. Por ejemplo, “especificidad”, tal como se usa en el presente documento, se refiere generalmente a la capacidad de un sitio de combinación de anticuerpo individual para reaccionar con un sólo determinante antigénico o la capacidad de una población de moléculas de anticuerpo para reaccionar con un sólo antígeno. En general, existe un alto grado de especificidad en las reacciones antígeno-anticuerpo. Los anticuerpos pueden distinguir diferencias en (i) la estructura primaria de un antígeno, (ii) las formas isoméricas de un antígeno y (iii) la estructura secundaria y terciaria de un antígeno. Las reacciones anticuerpo-antígeno que presentan una alta especificidad presentan una baja reactividad cruzada.
“Unión sustancial” o “se une sustancialmente” se refiere a una cantidad de unión o reconocimiento específico entre moléculas en una mezcla de ensayo en condiciones de ensayo particulares. En su aspecto más amplio, la unión sustancial se refiere a la diferencia entre la incapacidad de una primera molécula de unirse a o reconocer una segunda molécula, y la capacidad de la primera molécula de unirse a o reconocer una tercera molécula, de manera que la diferencia es suficiente para permitir que se realice un ensayo significativo que distingue la unión específica en un conjunto particular de condiciones de ensayo, que incluye las concentraciones relativas de las moléculas y el tiempo y la temperatura de una incubación. En otro aspecto, una molécula es sustancialmente incapaz de unirse a o reconocer otra molécula en un sentido de reactividad cruzada cuando la primera molécula presenta una reactividad por una segunda molécula que es menos del 25%, menos del 10%, menos del 5% o menos del 1% de la reactividad presentada con respecto a una tercera molécula en un conjunto particular de condiciones de ensayo. La unión específica puede someterse a prueba usando varios métodos ampliamente conocidos, por ejemplo, un ensayo inmunohistoquímico, un ensayo de inmunoabsorción ligado a enzimas (ELISA), un radioinmunoensayo (RIA) o un ensayo de inmunotransferencia de tipo Western.
El término “sal”, tal como se usa en el presente documento, significa una sal formada entre un ácido y un grupo funcional básico de un compuesto. Las sales ilustrativas incluyen, pero no se limitan a, sales de sulfato, citrato, acetato, oxalato, cloruro, bromuro, yoduro, nitrato, bisulfato, fosfato, fosfato ácido, isonicotinato, lactato, salicilato, citrato ácido, tartrato, oleato, tanato, pantotenato, bitartrato, ascorbato, succinato, maleato, gentisinato, fumarato, gluconato, glucaronato, sacarato, formiato, benzoato, glutamato, metanosulfonato, etanosulfonato, bencenosulfonato, ptoluenosulfonato y pamoato (es decir, 1,1'-metilen-bis-(2-hidroxi-3-naftoato)). El término “sal” también se refiere a una sal formada entre un compuesto que tiene un grupo funcional ácido, tal como un grupo funcional ácido carboxílico, y una base orgánica o inorgánica. Las bases adecuadas incluyen, pero no se limitan a, hidróxidos de metales alcalinos tales como sodio, potasio y litio; hidróxidos de metales alcalinotérreos como calcio y magnesio; hidróxidos de otros metales, como aluminio y zinc; amoniaco y aminas orgánicas, tales como monoalquilaminas, dialquilaminas o trialquilaminas no sustituidas o sustituidas con hidroxilo; diciclohexilamina; tributilamina; piridina; N-metilo, N-etilamina; dietilamina; trietilamina; mono, bis o tris-(2-hidroxi-alquil inferior-aminas), como mono, bis o tris-(2-hidroxietil)amina, 2-hidroxi-terc-butilamina o tris-(hidroximetil)metilamina, N,N,-di-alquil inferior-N-(hidroxialquil inferior)-aminas, tales como N, N,-dimetil-N-(2-hidroxietil)amina o tri-(2-hidroxietil)amina ; N-metil-D-glucamina; y aminoácidos tales como arginina, lisina y similares.
Pasando ahora a los diversos aspectos de la invención, un aspecto de la invención se refiere a un método inmunológico, dispositivos y kits para detectar la presencia de una cantidad de SDMA libre en una muestra biológica. El método puede incluir controles, calibradores o patrones que comprenden uno o más análogos de SDMA. En particular, el método puede realizarse usando técnicas de inmunoensayo bien conocidas por los expertos en la técnica, incluyendo, pero sin limitarse a, el uso de microplacas y dispositivos de flujo lateral. Los sujetos animales de los que se obtienen muestras para detectar SDMA incluyen sujetos humanos y animales no humanos (por ejemplo, animales de compañía, ganado, etc.). La determinación de estados patológicos asociados con la presencia o cantidad de SDMA puede realizarse tanto para sujetos humanos como para no humanos.
El formato de ensayo en fase sólida es una técnica de ensayo de unión usada comúnmente. Existen varios dispositivos y procedimientos de ensayo en los que la presencia de un analito está indicada por la unión del analito a un conjugado y/o un miembro de unión complementario inmovilizado. En un aspecto particular, el miembro de unión inmovilizado (por ejemplo, anticuerpo anti-SDMA) está unido, o se une durante el ensayo, a una fase sólida tal como un pocillo de reacción, tira reactiva, tira de detección, almohadilla de flujo continuo, papel, matriz de fibra u otro material de fase sólida adecuado. La reacción de unión entre la SDMA libre en la muestra y el anticuerpo inmovilizado se determina añadiendo a la muestra una cantidad de un análogo de SDMA, que incluye SDMA conjugado con un marcador. Después de poner en contacto la mezcla de la muestra y el análogo de SDMA con la fase sólida, se incuban la mezcla y la fase sólida para permitir la unión entre el anticuerpo inmovilizado, la SDMA y el análogo de SDMA. Después de la incubación, los reactantes no unidos se eliminan de la fase sólida. Se mide la cantidad del marcador que se asocia con el anticuerpo mediante la unión del anticuerpo al análogo. La cantidad de marcador asociado con el anticuerpo es inversamente proporcional a la cantidad de SDMa libre en la muestra.
La inmovilización de uno o más anticuerpos contra SDMA en un dispositivo o soporte sólido se realiza de modo que no se eliminen los anticuerpos por procedimientos de lavado, muestra y/o diluyente. Pueden unirse uno o más anticuerpos a una superficie mediante adsorción física (es decir, sin el uso de grupos de unión químicos) o por enlace químico (es decir, con el uso de grupos de unión químicos). La unión química puede generar una unión más fuerte de anticuerpos sobre una superficie y proporcionar una orientación y conformación definidas de las moléculas unidas a la superficie.
En otro aspecto, los anticuerpos de SDMA producidos en una especie particular se unen a un soporte sólido mediante la interacción con un anticuerpo anti-especie que está unido al soporte. En un aspecto particular, los anticuerpos anti-SDMA se producen en conejos, y el soporte tiene, unido al mismo, anticuerpo anti-conejo que reconoce el anticuerpo anti-SDMA producido en conejos. En este aspecto, el anticuerpo puede estar en forma de antisuero obtenido de la especie. Los anticuerpos anti-SDMA pueden aplicarse a la fase sólida que tiene el anticuerpo anti-especie antes de añadir la muestra a la fase sólida, o los anticuerpos anti-SDMA pueden mezclarse con la muestra antes de añadir la
muestra a la fase sólida. En cualquier caso, los anticuerpos anti-SDMA se unen a la fase sólida mediante la unión al anticuerpo anti-especie en la fase sólida.
En otro aspecto, la invención incluye uno o más anticuerpos marcados que pueden mezclarse con una muestra de prueba antes de la aplicación de la mezcla a un soporte sólido. En este caso, puede unirse un análogo de SDMA al soporte sólido de modo que no se elimine el análogo por procedimientos de lavado, muestra y/o diluyente. Los anticuerpos marcados en la muestra se unen a SDMA en la muestra y, por tanto, no están disponibles para unirse con el análogo de SDMA en el soporte sólido. Después de la aplicación de la mezcla al soporte sólido y una incubación apropiada, la mezcla se elimina del soporte sólido por lavado. Los anticuerpos que no se han unido a la SDMA de la muestra se unirán al análogo de SDMA en el soporte sólido. La presencia o cantidad de SDMA en la muestra es inversamente proporcional a la cantidad de anticuerpo que se ha unido al análogo de SDMA. La señal asociada con el marcador en el anticuerpo puede medirse mediante el método apropiado.
La figura 1 muestra una comparación del método de detección de SDMA en sueros caninos combinados con adiciones conocidas de SDMA según la invención y la detección de SDMA usando espectroscopía de masas. Tal como se muestra, los valores de concentración de SDMA obtenidos a partir del método de la invención se correlacionan fuertemente con los obtenidos usando EM.
La detección de SDMA libre en una muestra biológica de un animal puede proporcionar una indicación de la función renal en el animal. Las enfermedades y trastornos renales (por ejemplo, disfunción renal, insuficiencia renal, enfermedad renal crónica, glomerulonefritis, nefropatía diabética, nefritis intersticial, enfermedad renal poliquística y enfermedad renal hipertensiva) tienden a disminuir la función renal general, incluyendo la TFG, y pueden diagnosticarse de varias formas, incluyendo el uso de los marcadores renales comunes creatinina y BUN. Comparando el nivel de SDMA, BUN y creatinina en animales sanos y enfermos, el nivel de SDMA en una muestra puede relacionarse con el estado patológico del animal. Por consiguiente, los animales “sanos” que muestran creatinina y BUN normales (intervalo de referencia) tendrán niveles de SDMA menores que los de los animales enfermos. En general, los animales que padecen un trastorno/enfermedad renal tendrán mayores niveles séricos de SDMA que los animales con función renal normal. En humanos sanos, los niveles plasmáticos de SDMA oscilan normalmente desde 0,3 hasta 0,7 pmol/l (J Am Soc Nephrol (2006) 17: 1128-1134; Eur J Clin Invest. Junio de 2007; 37 (5): 364-371. Nephrol Dial Transplant (2003) 18: 2542-2550; Nephrol Dial Transplant (2006) 21: 2446-2451; Kidney International, (2001) 59 (78): S14-S18).
De manera similar, el nivel de SDMA libre en una muestra biológica puede usarse como marcador de enfermedad cardiaca en el animal. El nivel de SDMA en la muestra puede compararse con los niveles de marcadores conocidos de enfermedad cardiaca para determinar un intervalo de punto de corte para el diagnóstico de enfermedad cardiaca (J Am Soc Nephrol (2006) 17: 1128-1134). Tal como se muestra en las figuras 2 y 3, se usó el método de la invención para determinar las concentraciones de SDMA en perros sanos (figura 2) y gatos sanos (figura 3), y en gatos y perros que padecen cáncer, enfermedades cardiacas y renales. Los animales que padecían enfermedad renal tenían mayores niveles de SDMA que los animales sanos.
La detección de los complejos anticuerpo:antígeno puede lograrse mediante una variedad de técnicas bien conocidas en la técnica, tales como, por ejemplo, turbidimetría, marcado enzimático, radiomarcado, luminiscencia o fluorescencia. Las metodologías de inmunoensayo son conocidas por los expertos en la técnica y se aprecia que incluyen, pero no se limitan a, radioinmunoensayo (RIA), inmunoensayos de enzimas (EIA), inmunoensayos de polarización fluorescente (FPIA), inmunoensayos enzimáticos de micropartículas (MEIA) e inmunoensayos magnéticos quimioluminiscentes (CMIA). En el RIA, un anticuerpo o antígeno se marca con radiactividad y se usa en un formato competitivo o no competitivo. En el EIA, un anticuerpo o antígeno se marca con una enzima que convierte un sustrato en un producto con una señal resultante que se mide, como un cambio de color. En el FPIA, un antígeno se marca con un marcador fluorescente y compite con el antígeno no marcado de la muestra. La cantidad de analito medida es inversamente proporcional a la cantidad de señal medida. En el MEIA, una micropartícula en fase sólida se recubre con anticuerpos contra un antígeno de interés y se usa para capturar el analito. El anticuerpo para la detección se marca con una enzima como en el método de EIA. La concentración de analito medida es proporcional a la cantidad de señal medida. En el CMIA, un marcador quimioluminiscente se conjuga con el anticuerpo o antígeno y produce luz cuando se combina con su sustrato. El CMIA puede configurarse en un formato competitivo o no competitivo y produce resultados que son inversa o directamente proporcionales a la cantidad de analito presente, respectivamente.
También es bien conocido el uso de tiras de detección impregnadas con reactivo en ensayos de unión específicos. En tales procedimientos, se aplica una muestra de prueba a una porción de la tira de detección y se deja que migre o se absorbe a través del material de la tira. Por tanto, el analito que va a detectarse o medirse se hace pasar a través o a lo largo del material, posiblemente con la ayuda de un disolvente de elución que puede ser la propia muestra de prueba o una disolución añadida por separado. El analito migra a una zona de captura o detección en la tira de detección, en la que se inmoviliza un miembro de unión complementario al analito. El grado en el que el analito se une a la zona de detección puede determinarse con la ayuda del conjugado que también puede incorporarse en la tira de detección o que puede aplicarse por separado. En una realización, un anticuerpo específico para SDMA se inmoviliza sobre un soporte sólido en una ubicación distinta. Después de la adición de la muestra, la detección de complejos SDMA-anticuerpo sobre el soporte sólido puede realizarse mediante cualquier medio conocido en la técnica. Por ejemplo, la
patente estadounidense n.° 5.726.010, describe un ejemplo de un dispositivo de flujo lateral, el dispositivo de inmunoensayo SNAP® (IDEXX Laboratories), útil en la presente invención.
Otras tecnologías de detección emplean partículas magnéticas o microperlas, por ejemplo, perlas de polímero impregnadas con óxido de hierro superparamagnético. Estas perlas se asocian, por ejemplo, con un componente de unión específico para el analito. Las perlas se unen a los analitos objetivo en la muestra que se está sometiendo a prueba y luego se aíslan o separan normalmente de la disolución de manera magnética. Una vez que se ha producido el aislamiento, pueden realizarse otras pruebas, incluyendo la observación de imágenes o marcadores particulares, ya sea directamente de manera óptica o por medio de una cámara.
En un aspecto adicional, la memoria descriptiva se refiere a análogos de SDMA y métodos para su producción y uso, particularmente análogos de SDMA que contienen tiol, que contienen hidroxilo, que contienen amino y que contienen carboxilato, en los que el grupo tiol, grupo hidroxilo, grupo amino o grupo carboxilato permite que la SDMA se una a otra molécula (diana de conjugación), como una proteína activada, para formar un conjugado de SDMA. Los análogos de SDMA permiten que la SDMA se una a una diana de conjugación tal como una proteína, polipéptido, marcador detectable, soporte sólido y similares para proporcionar el conjugado de SDMA. Los conjugados de SDMA pueden usarse para producir anticuerpos para su uso en inmunoensayos específicos para Sd Ma . Los anticuerpos de la invención tienen poca o ninguna reactividad cruzada con arginina, a DmA y/o monometilarginina. Los análogos de SDMA también pueden conjugarse con un marcador para su uso en inmunoensayos específicos para SDMA.
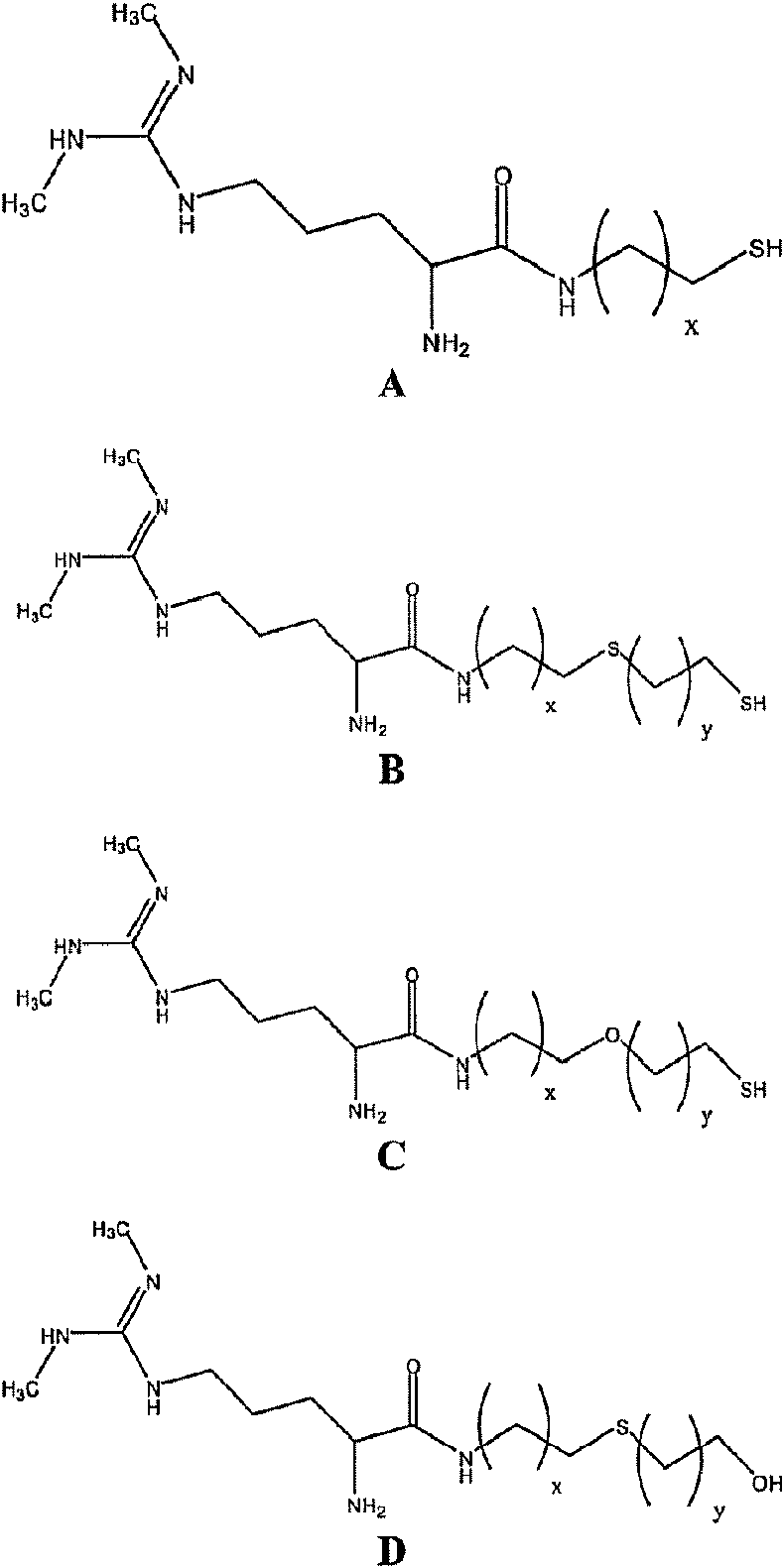
Los análogos de SDMA pueden tener las siguientes estructuras:
en las que x e y son números enteros que oscilan desde 1 hasta 5.
Según un aspecto, los análogos de SDMA tienen la siguiente fórmula general:
en la que Ri puede ser un grupo tiol (o tiol protegido), hidroxilo (o hidroxilo protegido), amino (o amino protegido), o un grupo carboxilato (incluyendo ácido carboxílico) o carboxilato protegido.
Los grupos protectores tiol, hidroxilo, amino y carboxilato adecuados son conocidos por los expertos en la técnica tal como los descritos, por ejemplo, en T.W. Greene, et al. Protective Groups in Organic Synthesis, 3a ed. (1999).
En un aspecto particular, la memoria descriptiva se refiere a un análogo de SDMA de fórmula (3):
o una sal del mismo. El compuesto de fórmula (3) proporciona un tiol disponible que puede reaccionar con una diana de conjugación que incluye un “sitio reactivo a tiol” apropiado, es decir, un sitio que reaccionará con un grupo tiol. Por ejemplo, maleimidas, haluros de alquilo y arilo, y alfa-haloacilos son sitios reactivos a tiol ilustrativo que puede reaccionar con tioles para formar tio-éteres. De manera similar, los disulfuros de piridilo pueden reaccionar con tioles para formar disulfuros mixtos.
En otra realización, Ri es X-R2 , en el que X es -S-, -O-, -N- o -COO- y R2 es un marcador que tiene un grupo reactivo tiol, hidroxilo, amino o carboxilato.
En una realización, R1 es X-R2, en el que X es -S-, -O-, -N- o -COO-y R2 es una proteína que se ha funcionalizado para incluir un grupo reactivo tiol, hidroxilo, amino o carboxilato.
En una realización, la SDMA se conjuga con una proteína portadora para formar un inmunógeno “portador de hapteno” que puede usarse para estimular una respuesta inmunitaria a un epítopo que incluye s Dm A. Las proteínas inmunogénicas a modo de ejemplo incluyen, pero no se limitan a, BSA, KLH y ovalbúmina. Protocolos para conjugar haptenos con proteínas inmunogénicas se conocen en la técnica (véase, por ejemplo, Antibodies: A Laboratory Manual, E. Harlow y D. Lane, eds., Cold Spring Harbor Laboratory (Cold Spring Harbor, NY, 1988) págs. 78-87). En una realización, el análogo de SDMA se conjuga con una proteína activada con maleimida, tal como, por ejemplo, proteína de lapa californiana (KLH) activada con maleimida o albúmina sérica bovina (BSA) activada con maleimida. En una realización, el compuesto de fórmula (3) se conjuga con una proteína activada con maleimida, tal como, por ejemplo, proteína de lapa californiana (KLH) activada con maleimida o albúmina sérica bovina (BSA) activada con maleimida.
Por tanto, en un aspecto específico, la memoria descriptiva se refiere a un conjugado de un compuesto de fórmula (3) y una proteína activada con maleimida que tiene la fórmula:
en la que m es un número entero.
Normalmente, m es mayor de 5. Sin embargo, el valor de m es variable. Por ejemplo, m es aproximadamente 15 grupos maleimida por proteína en BSA activada con maleimida disponible comercialmente de Sigma-Aldrich de St. Louis, MO; m es aproximadamente 80 grupos maleimida por proteína en KLH activada con maleimida disponible comercialmente de Sigma-Aldrich; m está en un intervalo de aproximadamente 15 a aproximadamente 25 grupos maleimida por proteína en BSA activada con maleimida disponible comercialmente de Thermo Scientific Pierce Protein Research Products de Rockford, IL; m es mayor de aproximadamente 400 grupos maleimida por proteína en KLH activada con maleimida disponible comercialmente de Thermo Scientific Pierce Protein Research Products; y m está en un intervalo de aproximadamente 150 a aproximadamente 300 grupos maleimida por proteína en KLH activada con maleimida disponible comercialmente de A. G. Scientific de San Diego, CA. En general, m está limitado por el número de grupos amina disponibles presentes en una proteína inmunogénica. El número de aminas disponibles puede aumentarse conjugando la proteína inmunogénica con poliaminas.
En una realización, PROTEÍNA es BSA y m es mayor de aproximadamente 5. En una realización, la PROTEÍNA es BSA y m es mayor de aproximadamente 10. En una realización, la PROTEÍNA es BSA y m es mayor de aproximadamente 25. En una realización, la PROTEÍNA es BSA y m es mayor de aproximadamente 50. En una realización, la PROTEÍNA es BSA y m es mayor de aproximadamente 75. En una realización, la PROTEÍNA es BSA y m está en un intervalo de aproximadamente 5 a aproximadamente 80. En una realización, la PROTEÍNA es BSA y m es mayor de aproximadamente 75. En una realización, la PROTEÍNA es BSA y m está en un intervalo de aproximadamente 10 a aproximadamente 80. En una realización, la PROTEÍNA es BSA y m es mayor de aproximadamente 75. En una realización, la PROTEÍNA es BSA y m está en un intervalo de aproximadamente 20 a aproximadamente 80. En una realización, la PROTEÍNA es BSA y m es mayor de aproximadamente 75. En una realización, la PROTEÍNA es BSA y m está en un intervalo de aproximadamente 30 a aproximadamente 80.
En una realización, la PROTEÍNA es KLH y m es mayor de aproximadamente 5. En una realización, la PROTEÍNA es KLH y m es mayor de aproximadamente 50. En una realización, la PROTEÍNA es KLH y m es mayor de aproximadamente 100. En una realización, la PROTEÍNA es KLH y m es mayor de aproximadamente 200. En una realización, la PROTEÍNA es KLH y m es mayor de aproximadamente 300. En una realización, la PROTEÍNA es KLH y m es mayor de aproximadamente 400. En una realización, la PROTEÍNA es KLH y m es mayor de aproximadamente 500. En una realización, la PROTEÍNA es KLH y m es mayor de aproximadamente 600. En una realización, la PROTEÍNA es KLH y m es mayor de aproximadamente 700. En una realización, la PROTEÍNA es KLH y m es mayor de aproximadamente 800. En una realización, la PROTEÍNA es KLH y m está en un intervalo de aproximadamente 5 a aproximadamente 800. En una realización, la PROTEÍNA es KLH y m en un intervalo de aproximadamente 5 a aproximadamente 600. En una realización, la PROTEÍNA es KLH y m en un intervalo de aproximadamente 5 a aproximadamente 400. En una realización, la PROTEÍNA es KLH y m en un intervalo de aproximadamente 5 a aproximadamente 200. En una realización, la PROTEÍNA es KLH y m en un intervalo de aproximadamente 5 a aproximadamente 100. En una realización, la PROTEÍNA es KLH y m en un intervalo de aproximadamente 100 a aproximadamente 200. En una realización, la PROTEÍNA es KLH y m oscila en un intervalo de 100 a aproximadamente 300. En una realización, la PROTEÍNA es KLH y m está en un intervalo de aproximadamente 100 a aproximadamente 400. En diversos aspectos, la PROTEÍNA es KLH y m está en un intervalo de aproximadamente 100 a aproximadamente 500, aproximadamente 100 a aproximadamente 600, aproximadamente 100 a aproximadamente 700, aproximadamente 100 a aproximadamente 800 o aproximadamente 100 a aproximadamente 1.000.
El conjugado de un compuesto de fórmula (3) y proteína activada con maleimida puede caracterizarse usando métodos bien conocidos por los expertos en la técnica (véase, por ejemplo, Sigma-Aldrich Technical Bulletin for Maleimide Activated BSA, K1H Conjugation Kit (n.° de catálogo MBK1)).
En una realización alternativa, el análogo de SDMA se une a un marcador detectable a través del grupo tiol, hidroxilo, amino o carboxilato. El marcador puede ser detectable por sí mismo (por ejemplo, marcadores de radioisótopos, tintes quimioluminiscentes, marcadores electroquímicos, quelatos metálicos, partículas de látex o marcadores fluorescentes) o, en el caso de un marcador enzimático, puede catalizar la alteración química de un compuesto o composición de sustrato que sea detectable (por ejemplo, enzimas tales como peroxidasa del rábano, fosfatasa alcalina y similares). El marcador puede ser una molécula de unión específica que en sí misma puede ser detectable (por ejemplo, biotina, avidina, estreptavidina, digioxigenina, maltosa, oligohistidina, 2,4-dinitrobenceno, fenilarsenato, ADNmc, ADNbc, etc.). La SDMA puede unirse a un marcador detectable usando métodos bien conocidos por los expertos en la técnica. Como un ejemplo ilustrativo, el análogo de SDMA puede unirse a peroxidasa activada con maleimida, de polvo liofilizado de rábano, más de aproximadamente 200 unidades/mg de proteína (disponible comercialmente en Sigma-Aldrich, St. Louis, MO (n.° de catálogo P1709) siguiendo las instrucciones en el manual del producto).
El análogo de fórmula (3) puede prepararse a partir de SDMA (disponible comercialmente de EMD Chemicals Inc. de Gibbstown, NJ) mediante el siguiente esquema de síntesis ilustrativo (1):
Esquema 1:
Los grupos amino primarios y secundarios de SDMA se protegen haciendo reaccionar SDMA con dicarbonato de diferc-butilo (Boc2O). La SDMA protegida con ferc-butoxicarbonilo (BOC) resultante ((Boc3)-SDMA, 1) se une entonces a una resina. Por ejemplo, la (Boc3)-SDMA (1) puede unirse a una resina de cisteamina-4-metoxitritilo (disponible comercialmente de EMD Chemicals, Inc. de Gibbstown, NJ) poniendo en contacto la (Boc3)-SDMA (1) con la resina en presencia de metanamininio de hexafluorofosfato 2-(1H-7-azabenzotriazol-1-il)-1,1,3,3-tetrametiluranio (HATU) y N,N-diisopropiletilamina (DIPEA) en dimetilformamida (DMF) para proporcionar (Boc3)-SDMA-cistamida unida a resina (2). Los grupos protectores BOC en la (Boc3)-SDMA-cistamida unida a resina (2) se eliminan y la SDMA-cistamida unida a resina resultante se escinde de la resina usando, por ejemplo, ácido trifluoroacético en diclorometano, para proporcionar SDMA-cistamida (3), que se convirtió en la sal de clorhidrato (4) mediante reacción con ácido clorhídrico.
Los análogos de fórmula A-D, descritos anteriormente, pueden elaborarse usando metodologías similares tal como se describe en el esquema 1.
Luego puede hacerse reaccionar la proteína activada con maleimida con SDMA-cistamida (3) para proporcionar un conjugado SDMA-cistamida-proteína tal como se describe a continuación en el esquema II:
Esquema II:
Conjugado
en el que n es un número entero que oscila desde 1 hasta 3 y m es un número entero tal como se definió anteriormente.
El conjugado resultante puede purificarse usando métodos conocidos por los expertos en la técnica incluyendo, pero no son limitarse a, cromatografía en columna, por ejemplo, usando cromatografía en columna de filtración en gel con Sephadex (por ejemplo, Sephadex G-25M) como soporte sólido (disponible comercialmente de Sigma-Aldrich).
Los conjugados de análogos A-D pueden elaborarse usando metodologías similares tal como se describe en el esquema 2.
El conjugado del análogo de fórmula A-D y KLH activada con maleimida o BSA activada con maleimida puede usarse como inmunógeno para generar anticuerpos que se unen sustancialmente a SDMA (es decir, anticuerpos anti-SDMA) y no muestran ninguna o sustancialmente ninguna reactividad cruzada con ADMA, L-arginina y/o N-metilarginina. El conjugado del análogo de fórmula (3) y KLH activada con maleimida o BSA activada con maleimida puede usarse como inmunógeno para generar anticuerpos que se unen sustancialmente a SDMA (es decir, anticuerpos anti-SDMA). Tales anticuerpos no muestran ninguna o sustancialmente ninguna reactividad cruzada con ADMA, L-arginina y/o N-metilarginina.
La invención también se refiere a anticuerpos anti-SDMA aislados, recombinantes, sintéticos y/o producidos in vivo.
La invención incluye, además, pero no se limita a, métodos para elaborar y usar tales anticuerpos, incluyendo composiciones, métodos y dispositivos de diagnóstico y terapéuticos. Los anticuerpos anti-SDMA útiles en los métodos y composiciones de la invención se caracterizan por una unión de alta afinidad a SDMA con poca o ninguna reactividad cruzada con ADMA, arginina y/o monometilarginina. Los anticuerpos anti-SDMA de la invención son útiles, por ejemplo, como marcador de diagnóstico de la función renal, como disfunción renal, insuficiencia renal, tasa de filtración glomerular (TFG), aclaramiento de inulina y aclaramiento de creatinina, y para trastornos/enfermedades renales, tales como enfermedad renal crónica, glomerulonefritis, nefropatía diabética, nefritis intersticial, enfermedad renal poliquística y enfermedad renal hipertensiva; así como otras enfermedades/trastornos, como LES, enfermedades cardiacas e insuficiencia hepática.
En una realización, los anticuerpos generados son capaces de detectar SDMA libre (es decir, SDMA que no forma parte de una cadena polipeptídica) y no muestran ninguna o sustancialmente ninguna reactividad cruzada con ADMA,
L-arginina y/o N-metilarginina. Tal como se muestra en los ejemplos, los anticuerpos de la invención muestran menos del 1% de reactividad cruzada con ADMA, L-arginina y/o N-metilarginina, basándose en concentraciones iguales de los antígenos. Como se entiende generalmente en la técnica, el impacto de la reactividad cruzada dependerá de la abundancia relativa del antígeno que reacciona de manera cruzada (por ejemplo, ADMA, L-arginina y/o N-metilarginina) en comparación con el antígeno de inmunización (SDMA) en una muestra de prueba. Por ejemplo, una reactividad cruzada tan alta como el 50% puede ser aceptable si la concentración del antígeno de inmunización es 100 veces mayor que la del antígeno de reacción cruzada. Por el contrario, una reactividad cruzada tan baja como el 1% puede ser problemática si la concentración del antígeno de reacción cruzada es 100 veces mayor que la del antígeno de inmunización. Por consiguiente, el impacto de la reactividad cruzada debe considerarse en el contexto de las abundancias relativas de cualquier antígeno que reaccione de manera cruzada y el antígeno de inmunización, en la muestra a analizar. En los diversos aspectos de la invención, la reactividad cruzada no afecta a la unión sustancial de SDMA o análogo de SDMA a un anticuerpo anti-SDMA.
Los métodos para elaborar los anticuerpos de la invención pueden incluir el uso de uno o más conjugados de SDMA como inmunógeno para estimular una respuesta inmunitaria. Los métodos incluyen administrar uno o más conjugados de SDMA a un animal usando un protocolo de inmunización adecuado y separar un anticuerpo apropiado del/delo líquido(s) corporal(es) del animal, tal como se describe, por ejemplo, en el ejemplo 3, citado a continuación. Alternativamente, los conjugados de SDMA de la invención pueden usarse en métodos de presentación en fagos para seleccionar fagos que exhiben en su superficie un anticuerpo apropiado, seguido por la separación de secuencias de ácido nucleico que codifican al menos una región de dominio variable de un anticuerpo apropiado. Los métodos de presentación en fagos son bien conocidos por los expertos en la técnica. (Véase, por ejemplo, Antibody Phage Display; Methods in Molecular Biology, vol. 178, O'Brien, Philippa M.; Aitken, Robert (Eds.) 2002). Los anticuerpos monoclonales contra SDMA pueden prepararse mediante métodos generalmente conocidos en la técnica.
Los análogos de SDMA de la invención pueden unirse a un marcador para proporcionar un conjugado detectable para su uso en ensayos de unión al receptor, tales como inmunoensayos para SDMA. De manera similar, los anticuerpos anti-SDMA pueden unirse a un marcador para proporcionar anticuerpos anti-SDMA detectables para su uso en ensayos de unión al receptor, tales como inmunoensayos para SDMA. Los análogos de SDMA y los anticuerpos anti-SDMA pueden unirse a un marcador usando métodos bien conocidos por los expertos en la técnica, por ejemplo, Immunochemical Protocols; Methods in Molecular Biology, vol. 295, editado por R. Burns (2005)). El conjugado de SDMA detectable o los anticuerpos anti-SDMA detectables pueden usarse en diversos formatos de ensayo homogéneos, de tipo sándwich, competitivos o no competitivos, para generar una señal que está relacionada con la presencia o cantidad de una SDMA en una muestra de prueba.
En una realización específica, las metodologías de inmunoensayo son inmunoensayos competitivos para la detección de anticuerpos anti-SDMA. El inmunoensayo competitivo puede llevarse a cabo de la siguiente manera ilustrativa. Una muestra, del líquido corporal de un animal, que contiene posiblemente anticuerpos anti-SDMA, se pone en contacto con un análogo de SDMA conjugado con un soporte sólido y con un anticuerpo anti-SDMA conjugado con un marcador detectable de la invención. Los anticuerpos anti-SDMA de interés, presentes en la muestra, compiten con el anticuerpo anti-SDMA conjugado con un marcador detectable por la unión con el análogo de SDMA conjugado con un soporte sólido. La cantidad del marcador asociado con el soporte sólido puede determinarse después de separar los anticuerpos no unidos y el soporte sólido. En una realización alternativa, el inmunoensayo competitivo se lleva a cabo de la siguiente manera ilustrativa. Una muestra, del líquido corporal de un animal, que contiene posiblemente anticuerpos anti-SDMA se pone en contacto con un análogo de SDMa unido a un marcador detectable y luego con un anticuerpo conjugado con un soporte sólido. Los anticuerpos anti-SDMA en la muestra compiten con los anticuerpos anti-SDMA en el soporte sólido por la unión con el conjugado de SDMA unido a un marcador detectable. En cualquier caso, la señal obtenida está inversamente relacionada con la cantidad de anticuerpo SDMA de interés presente en la muestra.
En una realización específica, los anticuerpos anti-SDMA de la invención pueden usarse para desarrollar un inmunoensayo competitivo para ayudar en el diagnóstico de LES en un paciente. En general, los pacientes que padecen LES producen de manera espontánea autoanticuerpos contra las proteínas específicas de LES, es decir, las proteínas Sm B/B', D1, D2, D3, E, F y G. D1 y D3 son los antígenos más comunes reconocidos por los autoanticuerpos anti-Sm, que son una población de autoanticuerpos que se encuentra exclusivamente en pacientes afectados por LES. La secuenciación de proteínas y la espectroscopía de masas han demostrado que todas las argininas en las repeticiones de dipéptidos arginina-glicina (RG) C-terminales de las proteínas Sm humanas D1 y D3 contienen SDMA. Por consiguiente, los anticuerpos anti-SDMA de la invención pueden reaccionar con la SDMA presente en las repeticiones de dipéptidos RG de D1 y D3.
En particular, el inmunoensayo para diagnosticar el LES puede llevarse a cabo de la siguiente manera. En una cámara de reacción, las proteínas D1 y D3 se inmovilizan sobre un soporte sólido usando métodos bien conocidos por los expertos habituales en la técnica. Se añade una alícuota de suero o plasma del paciente a la cámara de reacción. Si la muestra del paciente contiene autoanticuerpos anti-D1 y/o anti-D3, los autoanticuerpos anti-D1 y/o anti-D3 se unirán a los sitios de SDMA en las proteínas D1 y/o D3. Luego, se añaden a la cámara de reacción anticuerpos anti-SDMA de la invención conjugados con un marcador. Los anticuerpos anti-SDMA marcados sólo se unirán al sitio de SDMA en las proteínas D1 y/o D3 si los autoanticuerpos anti-D1 y/o anti-D3 no saturan todos los sitios de SDMA presentes
en la proteína D1 y/o D3. Por consiguiente, si los anticuerpos anti-SDMA marcados de la invención se unen a los sitios de SDMA en la proteína D1 y/o D3, los resultados son indicativos de la ausencia de autoanticuerpos anti-D1 y/o anti-D3 y pueden indicar que el paciente no padece LES. Sin embargo, a la inversa, si los anticuerpos anti-SDMA marcados de la invención no se unen a los sitios de SDMA en la proteína D1 y/o D3, esto es indicativo de la presencia de autoanticuerpos anti-D1 y/o D3, y que el paciente padece LES. Como es típico en los ensayos competitivos, la señal generada a partir del marcador conjugado en este ensayo será inversamente proporcional a la cantidad de autoanticuerpos anti-D1 y/o anti-D3 presentes en la muestra.
La invención proporciona además kits de diagnóstico que contienen reactivos para su uso en la detección de SDMA o anticuerpos anti-SDMA. Normalmente, tal kit contiene al menos un análogo de SDMA y/o al menos un reactivo que se une sustancialmente a SDMA, tal como un anticuerpo anti-SDMA de la invención. Los kits también incluyen normalmente indicaciones o instrucciones que describen cómo realizar los ensayos de diagnóstico descritos anteriormente y/o cómo interpretar los resultados obtenidos de ese modo. En algunos kits, los anticuerpos anti-SDMA se unen a un soporte sólido inmovilizado y/o el conjugado de SDMA es un análogo de SDMA inmovilizado sobre un soporte sólido. El anticuerpo anti-SDMA o el conjugado de SDMA pueden estar unidos o no a un marcador apropiado.
En un ejemplo particular, un kit de este tipo incluiría un dispositivo completo con reactivos de unión específicos (por ejemplo, un reactivo de unión específico marcado no inmovilizado y un reactivo de captura de analito inmovilizado) y reactivo de lavado, así como reactivo detector y reactivos de control positivo y negativo, si se desea o es apropiado. Además, pueden incluirse otros aditivos, tales como estabilizadores, tampones y similares. Las cantidades relativas de los diversos reactivos pueden variarse para proporcionar concentraciones en disolución de los reactivos que optimicen sustancialmente la sensibilidad del ensayo. Particularmente, los reactivos pueden proporcionarse como polvos secos, habitualmente liofilizados, que en disolución proporcionarán una disolución de reactivo que tiene las concentraciones apropiadas para combinar con una muestra.
El dispositivo también puede incluir un reactivo líquido que transporta material no unido (por ejemplo, muestra de líquido sin reaccionar y reactivos de unión específicos no unidos) lejos de la zona de reacción (fase sólida). Un reactivo líquido puede ser un reactivo de lavado y servir sólo para eliminar el material no unido de la zona de reacción, o puede incluir un reactivo detector y servir tanto para eliminar el material no unido como para facilitar la detección del analito. Por ejemplo, en el caso de un reactivo de unión específico conjugado con una enzima, el reactivo detector incluye un sustrato que produce una señal detectable tras la reacción con el conjugado enzima-anticuerpo en la zona reactiva. En el caso de un reactivo de unión específico marcado conjugado con una molécula radiactiva, fluorescente o absorbente de luz, el reactivo detector actúa simplemente como una disolución de lavado que facilita la detección de la formación de complejos en la zona reactiva eliminando por lavado el reactivo marcado no unido.
Pueden estar presentes dos o más reactivos líquidos en un dispositivo, por ejemplo, un dispositivo puede comprender un reactivo líquido que actúa como reactivo de lavado y un reactivo líquido que actúa como reactivo detector y facilita la detección del analito.
Un reactivo líquido puede incluir además una cantidad limitada de un “ inhibidor”, es decir, una sustancia que bloquea el desarrollo del producto final detectable. Una cantidad limitada es una cantidad de inhibidor suficiente para bloquear el desarrollo del producto final hasta que la mayor parte o todo el material no unido en exceso se transporta fuera de la segunda región, momento en el que se produce el producto final detectable.
Sin más elaboración, se cree que un experto en la técnica que use la descripción anterior puede utilizar la invención en la mayor medida posible. Otras características y ventajas de la invención resultarán evidentes a partir de los siguientes ejemplos. Lo siguiente se proporciona sólo con fines de ejemplificación y no pretende limitar el alcance de la invención descrita en términos generales anteriormente.
Ejemplos
Ejemplo 1: síntesis de la SDMA-cistamida (3) y sal de clorhidrato de SDMA-cistamida (4)
Se preparó SDMA-cistamida (3) según la vía de síntesis descrita en el esquema 1.
(BOC)3-SDMA (1): a una disolución de 4,36 g (20 mmol) dicarbonato de di-ferc-butilo (Boc2O) en 20 ml de dioxano se le añadió gota a gota 550 mg (2,0 mmol) de diclorhidrato de N,N-dimetilarginina (SDMA) (disponible comercialmente de EMD Chemicals Inc. de Gibbstown, NJ) disuelto en 10 ml de NaOH 5,0 N a lo largo de 30 minutos a temperatura ambiente con agitación. Se agitó la mezcla de reacción resultante durante la noche. Luego se añadieron 30 ml de diclorometano (DCM) y 30 ml de agua a la mezcla de reacción y se ajustó el pH a 6,5 con ácido acético (AcOH). Se separó la fase de DCM, se lavó con salmuera y se secó sobre Na2SO4 anhidro. Luego se retiró el DCM a presión reducida para proporciona un sólido. Se lavó el sólido resultante 2 veces con 10 ml de hexano. Luego se secó el sólido a vacío para proporcionar 800 mg de un sólido de color amarillo claro. Las reacciones posteriores no requieren purificación adicional. Se caracterizó el sólido mediante espectroscopía de masas. ESI-EM: 525,7 (M Na)+, 503,6 (M 1)+, 403,5 (M - Boc 1)+, 303,5 (M - 2Boc 1)+.
Resina de (Boc)3-SDMA-cistamina (2): a una mezcla de 600 mg (1,2 mmol) de (Boc)3-SDMA (1) y 627 mg (1,6 mmol) de metanaminio de hexafluorofosfato de 2-(1H-7-azabenzotriazol-1-il)-1,1,3,3-tetrametiluronio (HATU) en 15 ml de dimetilformamida (DMF) se le añadieron 420 |jl (2,4 mmol) de N,N-diisopropiletilamina (DIPEA). Luego se agitó la mezcla resultante durante 20 minutos bajo una atmósfera seca de N2. Por separado, se hinchó una resina de cistamina-4-metoxitritilo (1,0 g) (disponible comercialmente de EMD Chemicals, Inc. de Gibbstown, NJ) y se lavó usando DMF. Luego se añadió la resina hinchada a la mezcla de reacción y se agitó suavemente la mezcla de reacción bajo una atmósfera de N2 durante tres horas. Luego se recogió la resina mediante filtración y se lavó consecutivamente con 5 ml de DMF, 5 ml de metanol y 5 ml de DCM.
SDMA-cistamida (3): a la resina modificada se le añadieron 15 ml de ácido trifluoroacético al 90% (TFA), se agitó suavemente la mezcla resultante durante dos horas y se filtró. Se lavó la resina dos veces con 3 ml de TFA/DCM (1:1 (v/v)). Se combinaron el filtrado y los lavados y se añadieron a 200 ml de éter frío para proporcionar un precipitado. Se recogió el precipitado resultante mediante centrifugación y se secó a presión reducida para proporcionar 300 mg de SDMA-cistamida (3). Se caracterizó la SDMA-cistamida (3) mediante espectroscopia de masas. EIS-EM: 262,4 (M 1)+, 132,0 (M 2)+.
Sal de clorhidrato de SDMA-cistamida (4): se reconstituyó SDMA-cistamida 3 (300 mg) en 5 ml de HCl 1,0 N y se liofilizó la mezcla resultante para proporcionar un sólido de color amarillo claro como una espuma.
El mismo procedimiento general tal como se describió anteriormente puede usarse para preparar otros análogos de SDMA.
Ejemplo 2: conjugación de SDMA-cistamida (3) con proteína activada con maleimida
A. Procedimiento general para conjugar SDMA-cistamida (3) con KLH activada con maleimida:
1. Se abrió lentamente un vial de KLH activada con maleimida (disponible comercialmente de Sigma-Aldrich, St. Louis, MO (n.° de catálogo K0383)) para liberar el vacío.
2. Se reconstituyó el contenido del vial con 1 ml de agua para proporcionar una disolución 5 mg/ml de KLH activada con maleimida en tampón fosfato de sodio 20 mM con NaCl 230 mM, EDTA 2 mM y sacarosa 80 mM, pH 6,6.
3. Se preparó una disolución de tampón de conjugación de tampón fosfato de sodio 20 mM con EDTA 100 mM y sacarosa 80 mM, pH 6,6 reconstituyendo tampón de conjugación (disponible comercialmente de Sigma-Aldrich, St. Louis, m O (n.° de catálogo C3957)) con 10 ml de agua.
4. Se disolvieron aproximadamente 0,8 mg de hapteno (es decir, SDMA-cistamida (3)) en 0,5 ml de tampón de conjugación. Se retuvieron 50 ml de la disolución de péptidos resultante para la determinación de la eficiencia de acoplamiento (hap-total). Se almacenó la disolución de hapteno retenida a 2-8°C.
5. Se mezcló inmediatamente la disolución de hapteno de la etapa 4 con la disolución de KLH activada con maleimida de la etapa 2 en un vial de reacción equipado con una barra de agitación. Se desgasificó la mezcla resultante mientras se agitaba bajo una corriente suave de nitrógeno durante aproximadamente 1-2 minutos.
6. Se tapó el vial de reacción y se continuó la agitación a temperatura ambiente durante 2 horas o durante toda la noche a 2-8°C.
7. Se retuvieron 100 j l de la reacción de conjugación de la etapa 6 (hap-libre) para la determinación de la eficiencia de acoplamiento.
B: Procedimiento general para conjugar SDMA-cistamida (3) con BSA activada con maleimida:
1. Se abrió lentamente un vial de BSA activada con maleimida (disponible comercialmente de Sigma-Aldrich, St. Louis, MO (n.° de catálogo B7542)) para liberar el vacío.
2. Se reconstituyó el contenido del vial con 1 ml de agua para proporcionar una disolución 5 mg/ml de BSA activada con maleimida en tampón fosfato de sodio 20 mM con NaCl 230 mM, EDTA 2 mM y sacarosa 80 mM, pH 6,6.
3. Se disolvieron 5 mg de hapteno (es decir, SDMA-cistamida (3)) en 0,5 ml de tampón de conjugación (preparado tal como se describió anteriormente en la etapa A3). Se retuvieron 50 ml de la disolución de péptidos resultante para la determinación de eficiencia de acoplamiento (hap-total). Se almacenó la disolución de hapteno retenida a 2-8°C.
4. Se mezcló inmediatamente la disolución de hapteno de la etapa 3 con la disolución de BSA activada con
maleimida de la etapa 2 en un vial de reacción equipado con una barra de agitación. Se desgasificó la mezcla resultante mientras se agitaba bajo una corriente suave de nitrógeno durante aproximadamente 1-2 minutos.
5. Se tapó el vial de reacción y se continuó la agitación a temperatura ambiente durante 2 horas o durante toda la noche a 2-8°C.
6. Se retuvieron 100 j l de la reacción de conjugación de la etapa 5 (hap-libre) para la determinación de la eficiencia de acoplamiento.
C: Aislamiento de conjugados de KLH o BSA:
1. Se disolvió el contenido de un envase de solución salina tamponada con fosfato (PBS) (disponible comercialmente de Sigma-Aldrich, St. Louis, MO (n.° de catálogo P38l3)) en 1 litro de agua.
2. Se fijó una columna de filtración en gel Sephadex G-25M (disponible comercialmente de Sigma-Aldrich, St. Louis, MO (n.° de catálogo B4783)) sobre un vaso de precipitados.
3. Se retiró el tapón de la parte superior de la columna, se abrió mediante corte la punta inferior de la columna, y se dejó que fluyera a través el exceso de líquido. No se dejó que se secara la columna.
4. Se equilibró la columna con 30 ml de PBS.
5. Se aplicó la mezcla de reacción del ejemplo 2A o 2B a la columna.
6. Se eluyó la columna con PBS, usando un volumen total de aproximadamente 10 ml y se recogieron fracciones de aproximadamente 0,5-1,0 ml. Se monitorizó la presencia de proteína en las fracciones midiendo la absorbancia de cada fracción a 280 nm.
7. Se combinaron las fracciones que contenían proteína. La figura 1 proporciona una representación gráfica de un perfil de elución ilustrativo para las proteínas KLH (♦ ) y BSA (■). La figura 1 representa gráficamente la absorción frente al número de fracciones.
8. Se dividieron las fracciones que contenían proteína en pequeñas alícuotas que se almacenaron congeladas a -20°C.
D. Ensayo para determinar la eficiencia de acoplamiento:
1. Ensayo de patrón de cisteína - Para estimar la eficiencia de acoplamiento del análogo al péptido de cisteína, se preparó una curva patrón usando concentraciones conocidas de cisteína. El ensayo se basó en la reacción de 5,5'-ditiobis(2-ácido nitrobenzoico) (DTNB o reactivo de Ellman) que reacciona con grupos sulfhidrilo a pH 8,0 para producir un cromóforo con absorción máxima a 412 nm. Se siguió el siguiente procedimiento: a. Se preparó un tampón de DTNB disolviendo el contenido del vial del tampón de DTNB (disponible comercialmente de Sigma-Aldrich, St. Louis, MO (n.° de catálogo D4179) en 10 ml de agua. b. Luego se disolvió el reactivo de DTNB (disponible comercialmente de Sigma-Aldrich, St. Louis, MO (n.° de catálogo D8130)) en 5 ml del tampón de DTNB de la etapa a.
c. Inmediatamente antes de su uso, se preparó una disolución de cisteína disolviendo 32 mg de clorhidrato de L-cisteína monohidratado (disponible comercialmente de Sigma-Aldrich, St. Louis, MO (n.° de catálogo C7880)) en 1 ml de agua. Se diluye en serie la disolución resultante de clorhidrato de L-cisteína con agua para proporcionar disoluciones madre diluidas en el intervalo de 0,4-0,04 mg/ml. Se usaron inmediatamente las disoluciones madre diluidas.
d. A tubos de ensayo etiquetados se les añadieron 50 ml de las disoluciones madre diluidas. Se usó un tubo de ensayo que contenía 50 j l de agua como blanco.
e. A cada tubo de ensayo se le añadieron luego 0,1 ml de agua, 0,75 ml de tampón de DTNB, pH 8,0, e, inmediatamente, 0,1 ml de disolución de reactivo de DTNB (1 mg/ml) para proporcionar una disolución de ensayo de patrón de cisteína final con un volumen de 1 ml.
f. Se mezcló el contenido de cada tubo de ensayo.
g. Se determinó la absorbancia de cada disolución de ensayo de patrón de cisteína a 412 nm. Si la absorbancia estaba por encima de 1,4, se diluyeron las muestras y se repitió el ensayo.
h. Se representó gráficamente la absorbancia a 412 nm frente a la concentración de cisteína (mg/ml) para proporcionar una curva patrón. La parte lineal de la curva patrón, con concentraciones de cisteína que oscilan desde 2-20 pg/ml, se usó para determinar hap-total y hap-libre.
2. Ensayo de hapteno - Nota: si las muestras generaron valores mayores que el patrón de cisteína más alto en el ensayo de patrón de cisteína, se diluyeron las muestras y se repitió el ensayo.
a. A tubos de ensayo etiquetados de manera apropiada se les añadieron 50 pl de las siguientes disoluciones:
(i) tampón de DTNB (blanco)
(ii) Muestra de péptido diluida (hap-total, de la conjugación de KLH, de la etapa A4 del ejemplo 2)
(iii) Hapteno-KLH (hap-libre, de la conjugación de KLH de la etapa A7 del ejemplo 2) (iv) Muestra de péptido diluida (hap-total, de la conjugación de BSA de la etapa B3 del ejemplo 2)
(v) hap-BSA (hap-libre, de la conjugación de BSA, etapa B6 del ejemplo 2)
b. A cada tubo etiquetado de la etapa (a) se le añadieron 0,1 ml de agua, 0,75 ml de tampón de DTNB, pH 8,0, e, inmediatamente, 0,1 ml de disolución de reactivo de DTNB (1 mg/ml), para proporcionar una disolución de ensayo de hapteno final con un volumen de 1 ml.
c. Se mezcló el contenido de cada tubo.
d. Se determinó la absorbancia de la disolución en cada tubo etiquetado a 412 nm. Si la absorbancia estaba por encima de 1,4, se diluyen las muestras y se repite el ensayo.
e. Luego se determinó la concentración de hap-total a partir de la absorbancia medida usando la curva patrón obtenida tal como se describió anteriormente en la sección 1h. Se usaron la absorbancia medida para el tubo (ii) y el tubo (iv) para determinar el hap-total para KLH y BSA, respectivamente. Se usaron la absorbancia medida para el tubo (iii) y el tubo (v) para determinar el hap-libre para KLH y BSA, respectivamente. Luego se calculó la concentración de péptido en la disolución no diluida y la eficiencia de acoplamiento tal como se describe en los cálculos.
3. Cálculos
Para estimar las concentraciones de péptido y la eficiencia de acoplamiento, se preparó una curva patrón usando concentraciones conocidas de cisteína tal como se describió anteriormente (ensayo de patrón de cisteína). En este cálculo, un mol de cisteína es equivalente a un mol de hapteno que contiene sulfhidrilo.
Se usaron las siguientes fórmulas:
% de eficiencia de acoplamiento = {(Hap (conjugado) / Hap (total)} x 100 = [{Hap (total) - Hap (libre)} / Hap (total)] x 100
Hap (total) = Péptido (total) pmoles/ml
Hap (libre) = Péptido (libre) pmoles/ml
Hap (conjugado) = Hap (total) - Hap (libre)
(Véase, también, Sigma-Aldrich Technical Bulletin for Maleimide Activated BSA, KLH Conjugation Kit (n.° de catálogo MBK1)). Este mismo procedimiento general tal como se describe en los ejemplos 2A-D puede usarse para medir la eficiencia de la conjugación de otros análogos de SDMA con KLH y BSA.
Ejemplo 3: método para generar anticuerpos anti-SDMA
El protocolo de inmunización para generar los anticuerpos anti-SDMA de la invención se llevó a cabo de la siguiente manera:
Se inmunizaron seis conejos de raza californiana con un conjugado de SDMA de la invención. Se inmunizaron tres de los seis conejos con SDMA conjugada con BSA (conejos n.° 155, 156 y 157) y se inmunizaron los otros tres conejos
con SDMA conjugada con KLH (conejos n.° 152, 153 y 154) (preparado tal como se describe en el ejemplo 2). Para las inmunizaciones primarias, a cada conejo se le inyectaron 0,5 mg del conjugado de SDMA en 1 ml de solución salina tamponada con fosfato (PBS) mezclada con 1 ml de adyuvante completo de Freund. Cada conejo recibió 20-30 inyecciones intradérmicas en su lomo afeitado. Cada conejo recibió un refuerzo con 0,25 mg de inmunógeno en 1 ml de PBS mezclado con un volumen igual de adyuvante incompleto de Freund en las patas traseras. Se administraron las inyecciones de refuerzo cada mes tras la inyección primaria. Se extrajeron muestras de sangre de prueba de 5 ml de sangre de cada conejo 7-10 días tras cada refuerzo. Se extrajeron muestras de sangre de producción de 40 ml de cada conejo tras la tercera inyección de refuerzo, cuando el título de antisueros era mayor de aproximadamente 1:2000. El título de antisuero es la dilución de antisuero que genera la curva de calibración más inclinada para el ensayo.
Ejemplo 4: caracterización de anticuerpos anti-SDMA
Para evaluar la especificidad de los anticuerpos obtenidos mediante los procedimientos descritos en el ejemplo 3 anterior, se midió su reactividad frente a SDMA, ADMA, L-arginina y/o N-metilarginina en un ensayo de ELISA competitivo (tabla 1).
Se disolvieron cada uno de ADMA-2HCl, SDMA-2HCl, acetato de N-metilarginina (Sigma, n.° de cat. M7033) o L-arginina (Sigma, n.° de cat. A5006) en PBS para preparar disoluciones madre a 1 mg/ml. A partir de estas disoluciones madre, se prepararon disoluciones de trabajo a 100 pg/ml, 10 pg/m y 1 pg/m en PBS.
Se añadieron secuencialmente 50 pl del conjugado SDMA-HRP (tal como se describe en el ejemplo 5 a continuación), 50 pl de ADMA, SDMA, N-metilarginina o L-arginina (a concentraciones de desde 1-100 pg/ml tal como se describió anteriormente) y 50 pl de anticuerpo de conejo anti-SDMA en suero (título de 1:3000) a un pocillo individual en una placa de micropocillos de poliestireno de 96 pocillos, previamente recubierta con anticuerpo de oveja anti-IgG de conejo (disponible comercialmente de Beacon Analytical Systems Inc. de Portland, ME). Tras un periodo de incubación de 30 minutos a temperatura ambiente, se lavaron los pocillos 4 veces con PBST (solución salina tamponada con fosfato, Tween al 0,05%).
Posteriormente se añadieron 100 pl de 3,3',5,5'-tetrametilbencidina (disponible comercialmente de Promega Corporation de Madison, WI). Tras un periodo de incubación de 30 minutos a temperatura ambiente, se añadieron 100 pl de disolución de parada (HCl 1 N) y se midió la absorbancia a 450 nm usando un lector de placas BioTek ELX 808 (Winooski, VT). Se sometieron los datos a cuantificación usando el software Softmax (Molecular Devices, Sunnyvale, CA).
Se determinaron los valores de absorbancia obtenidos con 0 pg/ml, 1 pg/ml, 10 pg/ml y 100 pg/ml de ADMA, SDMA, N-metilarginina o L-arginina, respectivamente, y se representaron gráficamente. Se dividió la concentración de SDMA a la que el valor de absorbancia se redujo en un 50% (con respecto a la absorbancia máxima obtenida a 0 pg/ml de SDMA; es decir CI50) entre cada una de las concentraciones de ADMA, N-metilarginina o L-arginina, respectivamente, a las que el valor de absorbancia se redujo en un 50% (CI50). Se multiplicó el valor resultante por 100 para obtener el valor de “% de reactividad cruzada”. Cuando se observó una reducción de absorbancia de <50% a concentraciones de hasta, e incluyendo, 100 pg/ml, se indicó una reactividad cruzada de <1% (véase la tabla 1).
Tal como se muestra en la tabla 1, los 6 sueros anti-SDMA de conejo tenían reactividades cruzadas de <1% frente a ADMA, N-metilarginina o L-arginina, respectivamente.
Tabla 1
Conejo n.° 152 (1:5K)
CI50 % de reactividad cruzada
SDMA 1,10 ug/ml 100%
ADMA > 100 < 1%
L-Arginina > 100 < 1%
N-MMA > 100 < 1%
Conejo n.° 153 (1:2,5K)
CI50 % de reactividad cruzada
SDMA 0,65 ug/ml 100%
ADMA > 100 < 1%
L-Arginina > 100 < 1%
N-MMA > 100 < 1%
Conejo n.° 154 (1,25K)
CI50 % de reactividad cruzada
SDMA 0,49 ug/ml 100%
ADMA > 100 < 1%
L-Arginina > 100 < 1%
N-MMA > 100 < 1%
Conejo n.° 155 (1:3K)
CI50 % de reactividad cruzada
SDMA 0,73 ug/ml 100%
ADMA > 100 < 1%
L-Arginina > 100 < 1%
N-MMA 79 ug/ml < 1%
Conejo n.° 156 (1:20K)
CI50 % de reactividad cruzada
SDMA 1,3 ug/ml 100%
ADMA > 100 < 1%
L-Arginina > 100 < 1%
N-MMA > 100 < 1%
Conejo n.° 157 (1:15K)
CI50 % de reactividad cruzada
SDMA 1,6 ug/ml 100%
ADMA > 100 < 1%
L-Arginina > 100 < 1%
N-MMA > 100 < 1%
Un experimento similar al descrito en los ejemplos 1-4, pero en el que se usó ADMA en lugar de SDMA, también generó anticuerpos. Sin embargo, usar un conjugado de ADMA-proteína para generar anticuerpos produjo anticuerpos que no eran específicos para ADMA libre y no eran útiles en un ensayo para medir ADMA.
En otro experimento, usando sólo anticuerpo policlonal del conejo n.° 154, se determinó la especificidad del anticuerpo con mayor rigurosidad mediante el método descrito anteriormente. Estos datos muestran que la especificidad para el anticuerpo del conejo n.° 154 es incluso mayor que la mostrada en la tabla 1, anteriormente.
Especificidad (reactividad cruzada)
Conejo n.° 154
Ejemplo 5: inmunoensayo competitivo para detectar los niveles de SDMA in vivo
Clínicas/laboratorios veterinarios proporcionaron muestras de suero de animales que se sometieron a una exploración física de rutina y un panel químico de rutina.
Se preparó un conjugado de SDMA-HRP según el siguiente procedimiento:
1. Se reconstituyó polvo liofilizado de peroxidasa del rábano activada por maleimida, >200 unidades/mg de proteína (disponible comercialmente de Sigma-Aldrich, St. Louis, MO, n.° de producto P1709)) hasta 2 5 mg/ml en NaCl 0,15 M, fosfato de sodio 0,1 M, pH 7,0. Se desaireó el tampón y se purgó con nitrógeno o argón antes de su uso y el agua usada para preparar el tampón estaba libre de metales pesados traza y otros agentes oxidantes. Se realizó el acoplamiento en un vial ámbar para proteger la reacción frente a la luz.
2. Se disolvió análogo de SDMA (3) en el mismo tampón que el usado en la etapa 1 para proporcionar una disolución con una concentración de 2-5 mg/ml. Generalmente, se usaron 1-2-moles de peroxidasa por mol de compuesto de sulfhidrilo. El peso molecular de la peroxidasa es de aproximadamente 40.000.
3. Se combinó la disolución de la etapa 1 con la disolución de la etapa 2 y se agitó suavemente la disolución resultante durante 3 horas a temperatura ambiente. Luego se bloquearon los grupos maleimida no reaccionados añadiendo 2-mercaptoetanol 1 M (disponible comercialmente de Sigma-Aldrich, St. Louis, MO. (n.° de catálogo M 6250)) para proporcionar una concentración final de 0,0015 M de 2-mercaptoetanol y se agita la disolución resultante durante aproximadamente 15 minutos.
4. Luego se bloquearon los grupos sulfhidrilo no reaccionados añadiendo N-etilmaleimida 0,3 M (disponible comercialmente de Sigma-Aldrich, St. Louis, MO (n.° de catálogo D 8654)) a la disolución de la etapa 3 para proporcionar una concentración final de 0,003 M de N-etilmaleimida.
5. Luego se intercambió la disolución resultante del conjugado SDMA-HRP en PBS mediante cromatografía (usando el mismo procedimiento descrito anteriormente en el ejemplo para conjugar análogo de SDMA (3) con KLH y BSA activadas con maleimida) o diálisis en PBS (Spectra/Por3, MWCO 3500 Spectrum Labs, Rancho Dominguez, CA) según las instrucciones del fabricante. Luego se liofilizó la disolución resultante.
Véanse, también, Lin, F. T., et al., Biochemistry, 18(4), 690 (1979); Kitagawa, T., et al., Chem. Pharm. Bull., 29(4), 1131 (1981); Duncan, R. J. S., et al., Anal. Biochem., 132, 68 (1983); y Palmer, J. L., et al., J. Biol. Chem., 238(7), 2393 (1963).
Se añadieron secuencialmente 50 pl del conjugado de SDMA-HRP, 50 pl de muestra de suero (o calibrador, SDMA 2 HCl, disponible comercialmente de Calbiochem de San Diego, CA) y 50 pl de anticuerpo de conejo anti-SDMA en suero (título de 1:3000) a un pocillo individual en una placa de micropocillos de poliestireno de 96 pocillos, previamente recubierta con anticuerpo de oveja anti-IgG de conejo (disponible comercialmente de Beacon Analytical Systems Inc. de Portland, ME). Tras un periodo de incubación de 30 minutos a temperatura ambiente, se lavaron los pocillos 4 veces con PBST (solución salina tamponada con fosfato, Tween al 0,05%).
Posteriormente se añadieron 100 pl de 3,3',5,5'-tetrametilbencidina (disponible comercialmente de Promega Corporation de Madison, WI). Tras un periodo de incubación de 30 minutos a temperatura ambiente, se añadieron 100 pl de disolución de parada (HCl 1 N) y se midió la absorbancia a 450 nm usando un lector de placas BioTek ELX 808 (Winooski, VT). Se sometieron los datos a cuantificación usando el software Softmax (Molecular Devices, Sunnyvale, CA). Se generó una curva de calibración procesando una serie de patrones de SDMA (por ejemplo, 0, 0,05 pg/ml, 0,15 pg/ml, 0,45 pg/ml y 1,35 pg/ml). Se cuantificaron las muestras desconocidas usando la curva de calibración. Los resultados se resumen en la tabla 2.
Tabla 2
En la tabla 2, el estado “enfermedad renal” indica que la muestra extraída del animal mostraba valores de creatinina y nitrógeno ureico en sangre (BUN) por encima del intervalo de referencia normal y el estado “sano” indica que la muestra extraída del animal mostraba valores de creatinina y nitrógeno ureico en sangre (BUN) normales (intervalo de referencia). Para animales caninos, el límite superior del intervalo de referencia normal era de 27 mg/dl para BUN y de 1,8 mg/dl para creatinina. Para animales felinos, el límite superior del intervalo de referencia normal era de 34 mg/dl para BUN y de 2,3 mg/dl para creatinina.
Los resultados en la tabla 2 muestran que los niveles de SDMA eran elevados en perros y gatos con función renal afectada. Por tanto, puede usarse SDMA como marcador para diagnosticar enfermedad renal en animales.
Los ejemplos facilitados anteriormente son simplemente ilustrativos y no se pretende que sean una lista exhaustiva de todas las posibles realizaciones, aplicaciones o modificaciones de la invención. Por tanto, diversas modificaciones y variaciones de los métodos y sistemas de la invención descritos resultarán evidentes para los expertos en la técnica sin alejarse del alcance de la invención. Aunque la invención se ha descrito en relación con realizaciones específicas, debe entenderse que la invención tal como se reivindica no debe limitarse indebidamente a tales realizaciones específicas.
Se entiende que la invención no se limita a la metodología, protocolos y reactivos particulares, etc., descritos en el presente documento, ya que estos pueden variar como reconocerá el experto en la técnica. También debe entenderse que la terminología usada en el presente documento se usa con el fin de describir sólo realizaciones particulares, y no pretende limitar el alcance de la invención. También debe observarse que, tal como se usan en el presente documento y en las reivindicaciones adjuntas, las formas en singular “un/uno”, “una”, y “el/la” incluyen la referencia en plural a menos que el contexto indique claramente lo contrario. Por tanto, por ejemplo, una referencia a “un grupo de unión” es una referencia a uno o más grupos de unión y equivalentes de los mismos conocidos por los expertos en la técnica.
A menos que se defina lo contrario, todos los términos técnicos y científicos usados en el presente documento tienen los mismos significados que entiende habitualmente un experto habitual en la técnica a la que se refiere la invención. Las realizaciones de la invención y las diversas características y detalles ventajosos de las mismas se explican más completamente con referencia a las realizaciones no limitativas y/o se ilustran en los dibujos adjuntos y se detallan en la siguiente descripción. Debe observarse que las características ilustradas en los dibujos no están necesariamente dibujadas a escala, y pueden emplearse características de una realización con otras realizaciones tal como reconocerá el experto en la técnica, aunque no se mencione explícitamente en el presente documento.
Cualquier valor numérico mencionado en el presente documento incluye todos los valores desde el valor inferior hasta el valor superior en incrementos de una unidad siempre que haya una separación de al menos dos unidades entre cualquier valor inferior y cualquier valor superior. Como ejemplo, si se menciona que la concentración de un componente o el valor de una variable de procedimiento tal como, por ejemplo, tamaño, tamaño de ángulo, presión, tiempo y similares, es, por ejemplo, de desde 1 hasta 90, específicamente desde 20 hasta 80, más específicamente desde 30 hasta 70, se pretende que se indiquen expresamente valores tales como de 15 a 85, de 22 a 68, de 43 a 51, de 30 a 32, etc. en esta memoria descriptiva. Para valores que son inferiores a uno, se considera que una unidad es 0,0001, 0,001, 0,01 ó 0,1 según sea apropiado. Estos sólo son ejemplos de lo que se pretende específicamente y debe considerarse que todas las combinaciones posibles de valores numéricos entre el valor más bajo y el valor más alto indicados se mencionan expresamente en esta solicitud de una manera similar.
Se describen métodos, dispositivos y materiales particulares, aunque puede usarse cualquier método y material similares o equivalentes a los descritos en el presente documento en la práctica o pruebas de la invención.
Claims (6)
- 2. Anticuerpo según la reivindicación 1, en el que el anticuerpo tiene una reactividad de menos del 25%, en comparación con la reactividad para la SDMA, para uno o más compuestos seleccionados del grupo que consiste en dimetilarginina asimétrica (ADMA), L-arginina y N-metilarginina.
- 3. Anticuerpo según la reivindicación 1, en el que el anticuerpo no tiene reactividad cruzada con uno o más compuestos seleccionados del grupo que consiste en dimetilarginina asimétrica (ADMA), L-arginina y N-metilarginina.
- 4. Dispositivo para determinar la presencia de SDMA en una muestra que comprende un soporte sólido que tiene unido al mismo un anticuerpo anti-SDMA según una cualquiera de las reivindicaciones 1-3.
- 5. Método para detectar la presencia o cantidad de SDMA libre en una muestra biológica, comprendiendo el método:(a) poner en contacto la muestra con el anticuerpo anti-SDMA específico para SDMA libre según una cualquiera o más de las reivindicaciones 1 - 3 en una muestra biológica y una SDMA que comprende SDMA conjugada con un marcador, y(b) detectar la presencia o cantidad del marcador asociado con el anticuerpo, determinando así la presencia o cantidad de SDMA en la muestra, en el que la SDMA libre no forma parte de una cadena polipeptídica, en el que la SDMA libre es SDMA de la fórmula
- 6. Método para detectar la presencia o cantidad de SDMA libre en una muestra biológica, comprendiendo el método:(a) poner en contacto la muestra con el anticuerpo anti-SDMA específico para SDMA libre según una cualquiera o más de las reivindicaciones 1 - 3 en una muestra biológica y conjugada con un marcador y con un conjugado de SDMA que comprende SDMA conjugada con un soporte sólido;(b) detectar la presencia o cantidad del marcador asociado con el soporte sólido, determinando así la presencia o cantidad de SDMA en la muestra,en el que la SDMA libre no forma parte de una cadena polipeptídica, en el que la SDMA libre es SDMA de fórmulaMétodo según cualquiera de las reivindicaciones 5 ó 6, en el que el anticuerpo anti-SDMA tiene una reactividad de menos del 25%, en comparación con la reactividad para la SDMA, para un compuesto seleccionado del grupo que consiste en dimetilarginina asimétrica (ADMA), L-arginina y N-metilarginina. Método según cualquiera de las reivindicaciones 5 - 7, en el que el anticuerpo anti-SDMA no tiene reactividad cruzada con un compuesto seleccionado del grupo que consiste en dimetilarginina asimétrica (ADMA), L-arginina y N-metilarginina.Método para determinar la función renal en un sujeto animal que comprende:(a) realizar el método según una cualquiera de las reivindicaciones 5 - 8 para determinar la cantidad de SDMA libre en una muestra biológica obtenida del sujeto, y(b) determinar la función renal comparando la cantidad de SDMA en la muestra con uno o más patrones de SDMA que se correlacionan con la función renal en un animal.Método para diagnosticar una enfermedad renal en un sujeto que comprende:(a) determinar la cantidad de SDMA en una muestra biológica del sujeto según cualquiera de las reivindicaciones 5 - 8;(b) comparar la cantidad de SDMA en la muestra con la cantidad de SDMA en la muestra de un sujeto sano; (c) diagnosticar que el sujeto tiene una enfermedad renal cuando la cantidad de SDMA en la muestra del sujeto es mayor que la SDMA en la muestra del sujeto sano.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US8687008P | 2008-08-07 | 2008-08-07 | |
| PCT/US2009/052239 WO2010017089A1 (en) | 2008-08-07 | 2009-07-30 | Methods for detecting symmetrical demethylarginine |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2828097T3 true ES2828097T3 (es) | 2021-05-25 |
Family
ID=41016514
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES09790996T Active ES2828097T3 (es) | 2008-08-07 | 2009-07-30 | Métodos para detectar dimetilarginina simétrica |
Country Status (13)
| Country | Link |
|---|---|
| US (5) | US8481690B2 (es) |
| EP (2) | EP3808733A1 (es) |
| CY (1) | CY1123496T1 (es) |
| DK (1) | DK2313364T3 (es) |
| ES (1) | ES2828097T3 (es) |
| HR (1) | HRP20201734T1 (es) |
| HU (1) | HUE051130T2 (es) |
| LT (1) | LT2313364T (es) |
| PL (1) | PL2313364T3 (es) |
| PT (1) | PT2313364T (es) |
| SI (1) | SI2313364T1 (es) |
| SM (1) | SMT202000605T1 (es) |
| WO (1) | WO2010017089A1 (es) |
Families Citing this family (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3808733A1 (en) * | 2008-08-07 | 2021-04-21 | IDEXX Laboratories, Inc. | Methods for detecting symmetrical demethylarginine |
| US8956859B1 (en) | 2010-08-13 | 2015-02-17 | Aviex Technologies Llc | Compositions and methods for determining successful immunization by one or more vaccines |
| CN102628868B (zh) * | 2011-12-30 | 2014-09-17 | 北京九强生物技术股份有限公司 | 检测非对称二甲基精氨酸含量的胶乳增强免疫比浊法试剂盒 |
| AU2014315063B2 (en) * | 2013-09-05 | 2020-07-23 | Idexx Laboratories, Inc. | Methods for detecting renal disease |
| US10775365B2 (en) * | 2015-02-20 | 2020-09-15 | Idexx Laboratories, Inc. | Homogenous immunoassay with compensation for background signal |
| PL3289355T3 (pl) | 2015-04-30 | 2025-11-24 | Idexx Laboratories, Inc. | Sposoby wykrywania chorób nerek |
| CN109863503B (zh) * | 2016-09-02 | 2023-05-23 | 英维特公司 | 用于单分子定量的系统和方法 |
| CN110709705A (zh) | 2017-05-31 | 2020-01-17 | 马斯公司 | 诊断和治疗慢性肾脏病的方法 |
| EP3697499A4 (en) * | 2017-10-19 | 2021-07-21 | IDEXX Laboratories, Inc. | DETECTION OF SYMMETRICAL DIMETHYLARGININE |
| KR102818612B1 (ko) * | 2019-02-14 | 2025-06-11 | 주식회사 바이오노트 | 대칭적 디메틸아르기닌과 특이적으로 결합하는 항체 및 이의 용도 |
| WO2020184660A1 (ja) * | 2019-03-13 | 2020-09-17 | 味の素株式会社 | サルコペニアの評価方法、算出方法、評価装置、算出装置、評価プログラム、算出プログラム、記録媒体、評価システム、及び端末装置 |
| US10745492B1 (en) | 2019-04-03 | 2020-08-18 | Ark Diagnostics, Inc. | Antibodies to symmetrically dimethylated arginine analytes and use thereof |
| AU2020343654A1 (en) | 2019-09-05 | 2022-03-31 | The Regents Of The University Of California | Noninvasive method to quantify kidney function and functional decline |
| KR20230009394A (ko) | 2020-04-17 | 2023-01-17 | 아이덱스 래보러토리즈, 인코포레이티드 | 형광 소광 면역검정 |
| EP4263383A4 (en) | 2020-12-17 | 2024-10-23 | Nephrosant, Inc. | KITS FOR STABILIZATION OF URINE SAMPLES |
| AU2022229722A1 (en) * | 2021-03-02 | 2023-08-17 | Idexx Laboratories, Inc. | Biochemical probes attached to epoxy-based resins |
| WO2025070448A1 (ja) * | 2023-09-26 | 2025-04-03 | 富士フイルム株式会社 | 対称性ジメチルアルギニンを測定するためのキットおよび対称性ジメチルアルギニンの測定方法 |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0356160A3 (en) | 1988-08-24 | 1991-09-11 | The Board Of Trustees Of The Leland Stanford Junior University | Capillary device |
| US5726010A (en) | 1991-07-31 | 1998-03-10 | Idexx Laboratories, Inc. | Reversible flow chromatographic binding assay |
| AU7269098A (en) | 1997-05-01 | 1998-11-24 | Cooke Pharma, Inc. | Cardiovascular disease risk assessment |
| US6736957B1 (en) | 1997-10-16 | 2004-05-18 | Abbott Laboratories | Biosensor electrode mediators for regeneration of cofactors and process for using |
| US6358699B1 (en) | 1999-02-05 | 2002-03-19 | Cooke Pharma | Assay for asymmetrical NG, NG dimethyl-l-arginine |
| US6699673B2 (en) | 1999-12-22 | 2004-03-02 | The Research Foundation Of State University Of New York | Protein methylarginine-specific antibodies |
| WO2002004465A1 (en) | 2000-07-06 | 2002-01-17 | Fal Diagnostics | Methods and kits for the detection of arginine compounds |
| DE10040904A1 (de) | 2000-08-18 | 2002-02-28 | Boeger Rainer H | Verfahren und Mittel zum Nachweis einer Wahrscheinlichkeit zukünftigen Fortschreitens von Gefässerkrankungen |
| US7501053B2 (en) | 2002-10-23 | 2009-03-10 | Abbott Laboratories | Biosensor having improved hematocrit and oxygen biases |
| WO2004046314A2 (en) | 2002-11-15 | 2004-06-03 | The Board Of Trustees Of The Leland Stanford Junior University | Methods for detecting asymmetric dimethylarginine in a biological sample |
| ATE427497T1 (de) * | 2004-11-04 | 2009-04-15 | Germediq Forsch & Entw Ges Mbh | Methode zur bestimmung von arginin, methylierten argininen und deren derivate |
| US7879979B2 (en) | 2005-01-21 | 2011-02-01 | Alere International | Arginine analogs, and methods for their synthesis and use |
| DE102005060057A1 (de) | 2005-12-15 | 2007-06-28 | Kellner, Karl-Heinz, Dr. | Sandwich-Immunoassay für kleine Haptenmoleküle |
| JP2007176872A (ja) | 2005-12-28 | 2007-07-12 | Sentan Seimei Kagaku Kenkyusho:Kk | アシンメトリックジメチルアルギニンを認識する抗体及びその製造方法並びに翻訳後修飾アミノ酸含有タンパク質の検出方法 |
| EP1994184A2 (en) * | 2006-03-01 | 2008-11-26 | ARK Diagnostics, Inc. | Immunoassays, haptens, immunogens and antibodies for anti-hiv therapeutics |
| EP3808733A1 (en) * | 2008-08-07 | 2021-04-21 | IDEXX Laboratories, Inc. | Methods for detecting symmetrical demethylarginine |
| EP3697499A4 (en) * | 2017-10-19 | 2021-07-21 | IDEXX Laboratories, Inc. | DETECTION OF SYMMETRICAL DIMETHYLARGININE |
-
2009
- 2009-07-30 EP EP20193595.4A patent/EP3808733A1/en active Pending
- 2009-07-30 PL PL09790996T patent/PL2313364T3/pl unknown
- 2009-07-30 US US12/512,479 patent/US8481690B2/en active Active
- 2009-07-30 SM SM20200605T patent/SMT202000605T1/it unknown
- 2009-07-30 HU HUE09790996A patent/HUE051130T2/hu unknown
- 2009-07-30 EP EP09790996.4A patent/EP2313364B1/en not_active Revoked
- 2009-07-30 HR HRP20201734TT patent/HRP20201734T1/hr unknown
- 2009-07-30 LT LTEP09790996.4T patent/LT2313364T/lt unknown
- 2009-07-30 SI SI200932093T patent/SI2313364T1/sl unknown
- 2009-07-30 PT PT97909964T patent/PT2313364T/pt unknown
- 2009-07-30 WO PCT/US2009/052239 patent/WO2010017089A1/en not_active Ceased
- 2009-07-30 DK DK09790996.4T patent/DK2313364T3/da active
- 2009-07-30 ES ES09790996T patent/ES2828097T3/es active Active
-
2013
- 2013-06-14 US US13/918,531 patent/US9091684B2/en active Active
-
2014
- 2014-02-28 US US14/192,956 patent/US9970927B2/en active Active
-
2018
- 2018-05-11 US US15/977,284 patent/US20180335423A1/en not_active Abandoned
-
2020
- 2020-11-02 CY CY20201101033T patent/CY1123496T1/el unknown
-
2022
- 2022-03-28 US US17/705,924 patent/US20220221446A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| SI2313364T1 (sl) | 2021-01-29 |
| DK2313364T3 (da) | 2020-11-02 |
| US9091684B2 (en) | 2015-07-28 |
| US9970927B2 (en) | 2018-05-15 |
| US20100035274A1 (en) | 2010-02-11 |
| US20220221446A1 (en) | 2022-07-14 |
| HUE051130T2 (hu) | 2021-03-01 |
| WO2010017089A1 (en) | 2010-02-11 |
| LT2313364T (lt) | 2021-01-25 |
| US20180335423A1 (en) | 2018-11-22 |
| EP3808733A1 (en) | 2021-04-21 |
| SMT202000605T1 (it) | 2021-01-05 |
| EP2313364A1 (en) | 2011-04-27 |
| HRP20201734T1 (hr) | 2021-03-19 |
| EP2313364B1 (en) | 2020-09-02 |
| PT2313364T (pt) | 2020-11-10 |
| CY1123496T1 (el) | 2022-03-24 |
| US20130280740A1 (en) | 2013-10-24 |
| PL2313364T3 (pl) | 2021-03-08 |
| US8481690B2 (en) | 2013-07-09 |
| US20140242723A1 (en) | 2014-08-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20220221446A1 (en) | Methods for Detecting Symmetrical Dimethylarginine | |
| US20250271442A1 (en) | Methods for Detecting Renal Disease | |
| US20210239704A1 (en) | Analogs and conjugates of beta-aminoisobutyric acid (baib) | |
| BR112016004839B1 (pt) | Método para estimar a taxa de filtração glomerular (gfr) em uma amostra de um indivíduo animal, para diagnosticar uma doença renal ou uma disfunção renal em uma amostra de um indivíduo animal, para predizer a morte prematura ou determinar a mortalidade associada a uma doença renal em um indivíduo animal a partir de uma amostra do mesmo, dispositivo e kit | |
| HK40008342B (en) | Methods for detecting renal disease | |
| HK40008342A (en) | Methods for detecting renal disease | |
| HK1226979B (en) | Methods for detecting renal disease | |
| HK1226979A1 (en) | Methods for detecting renal disease |