ES2840253T3 - Combinaciones novedosas de un antagonista de H3 y un inhibidor de la recaptación de noradrenalina y usos terapéuticos de los mismos - Google Patents
Combinaciones novedosas de un antagonista de H3 y un inhibidor de la recaptación de noradrenalina y usos terapéuticos de los mismos Download PDFInfo
- Publication number
- ES2840253T3 ES2840253T3 ES18306017T ES18306017T ES2840253T3 ES 2840253 T3 ES2840253 T3 ES 2840253T3 ES 18306017 T ES18306017 T ES 18306017T ES 18306017 T ES18306017 T ES 18306017T ES 2840253 T3 ES2840253 T3 ES 2840253T3
- Authority
- ES
- Spain
- Prior art keywords
- combination
- disorder
- antagonist
- duloxetine
- disorders
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000002767 noradrenalin uptake inhibitor Substances 0.000 title claims abstract description 7
- 239000003395 histamine H3 receptor antagonist Substances 0.000 title claims description 12
- 229940127221 norepinephrine reuptake inhibitor Drugs 0.000 title abstract description 5
- 230000001225 therapeutic effect Effects 0.000 title description 4
- ZEUITGRIYCTCEM-KRWDZBQOSA-N (S)-duloxetine Chemical compound C1([C@@H](OC=2C3=CC=CC=C3C=CC=2)CCNC)=CC=CS1 ZEUITGRIYCTCEM-KRWDZBQOSA-N 0.000 claims abstract description 17
- 229960002866 duloxetine Drugs 0.000 claims abstract description 17
- 229940125425 inverse agonist Drugs 0.000 claims abstract description 9
- 239000000935 antidepressant agent Substances 0.000 claims abstract description 7
- 229940005513 antidepressants Drugs 0.000 claims abstract description 7
- 229960002430 atomoxetine Drugs 0.000 claims abstract description 7
- VHGCDTVCOLNTBX-QGZVFWFLSA-N atomoxetine Chemical compound O([C@H](CCNC)C=1C=CC=CC=1)C1=CC=CC=C1C VHGCDTVCOLNTBX-QGZVFWFLSA-N 0.000 claims abstract description 7
- 229960003770 reboxetine Drugs 0.000 claims abstract description 7
- CBQGYUDMJHNJBX-RTBURBONSA-N reboxetine Chemical compound CCOC1=CC=CC=C1O[C@H](C=1C=CC=CC=1)[C@@H]1OCCNC1 CBQGYUDMJHNJBX-RTBURBONSA-N 0.000 claims abstract description 7
- 230000001430 anti-depressive effect Effects 0.000 claims abstract description 6
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims abstract description 3
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims abstract description 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 29
- 150000001875 compounds Chemical class 0.000 claims description 22
- 208000035475 disorder Diseases 0.000 claims description 19
- SFLSHLFXELFNJZ-QMMMGPOBSA-N (-)-norepinephrine Chemical compound NC[C@H](O)C1=CC=C(O)C(O)=C1 SFLSHLFXELFNJZ-QMMMGPOBSA-N 0.000 claims description 12
- 229960002748 norepinephrine Drugs 0.000 claims description 12
- SFLSHLFXELFNJZ-UHFFFAOYSA-N norepinephrine Natural products NCC(O)C1=CC=C(O)C(O)=C1 SFLSHLFXELFNJZ-UHFFFAOYSA-N 0.000 claims description 12
- 208000007590 Disorders of Excessive Somnolence Diseases 0.000 claims description 8
- 206010041349 Somnolence Diseases 0.000 claims description 8
- 238000011282 treatment Methods 0.000 claims description 8
- 150000003839 salts Chemical class 0.000 claims description 6
- 230000001149 cognitive effect Effects 0.000 claims description 5
- 239000004615 ingredient Substances 0.000 claims description 5
- 208000006096 Attention Deficit Disorder with Hyperactivity Diseases 0.000 claims description 4
- 230000006735 deficit Effects 0.000 claims description 4
- 201000003631 narcolepsy Diseases 0.000 claims description 4
- 239000008194 pharmaceutical composition Substances 0.000 claims description 4
- 201000009032 substance abuse Diseases 0.000 claims description 4
- 231100000736 substance abuse Toxicity 0.000 claims description 4
- 208000011117 substance-related disease Diseases 0.000 claims description 4
- 208000001573 Cataplexy Diseases 0.000 claims description 3
- 230000002950 deficient Effects 0.000 claims description 3
- QCQCHGYLTSGIGX-GHXANHINSA-N 4-[[(3ar,5ar,5br,7ar,9s,11ar,11br,13as)-5a,5b,8,8,11a-pentamethyl-3a-[(5-methylpyridine-3-carbonyl)amino]-2-oxo-1-propan-2-yl-4,5,6,7,7a,9,10,11,11b,12,13,13a-dodecahydro-3h-cyclopenta[a]chrysen-9-yl]oxy]-2,2-dimethyl-4-oxobutanoic acid Chemical compound N([C@@]12CC[C@@]3(C)[C@]4(C)CC[C@H]5C(C)(C)[C@@H](OC(=O)CC(C)(C)C(O)=O)CC[C@]5(C)[C@H]4CC[C@@H]3C1=C(C(C2)=O)C(C)C)C(=O)C1=CN=CC(C)=C1 QCQCHGYLTSGIGX-GHXANHINSA-N 0.000 claims description 2
- 208000017164 Chronobiology disease Diseases 0.000 claims description 2
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 2
- 208000016588 Idiopathic hypersomnia Diseases 0.000 claims description 2
- 208000018737 Parkinson disease Diseases 0.000 claims description 2
- 201000010769 Prader-Willi syndrome Diseases 0.000 claims description 2
- 208000007271 Substance Withdrawal Syndrome Diseases 0.000 claims description 2
- 206010048010 Withdrawal syndrome Diseases 0.000 claims description 2
- 208000001797 obstructive sleep apnea Diseases 0.000 claims description 2
- 230000002265 prevention Effects 0.000 claims description 2
- 208000010877 cognitive disease Diseases 0.000 claims 2
- 208000036864 Attention deficit/hyperactivity disease Diseases 0.000 claims 1
- 208000015802 attention deficit-hyperactivity disease Diseases 0.000 claims 1
- 208000035231 inattentive type attention deficit hyperactivity disease Diseases 0.000 claims 1
- 239000005557 antagonist Substances 0.000 abstract description 4
- 206010062519 Poor quality sleep Diseases 0.000 description 15
- NNACHAUCXXVJSP-UHFFFAOYSA-N pitolisant Chemical compound C1=CC(Cl)=CC=C1CCCOCCCN1CCCCC1 NNACHAUCXXVJSP-UHFFFAOYSA-N 0.000 description 14
- 229940079593 drug Drugs 0.000 description 13
- 239000003814 drug Substances 0.000 description 13
- 239000000203 mixture Substances 0.000 description 13
- 229960003651 pitolisant Drugs 0.000 description 13
- 241000700159 Rattus Species 0.000 description 11
- 201000010099 disease Diseases 0.000 description 10
- 230000000694 effects Effects 0.000 description 10
- 230000036385 rapid eye movement (rem) sleep Effects 0.000 description 8
- 230000007958 sleep Effects 0.000 description 8
- 238000009472 formulation Methods 0.000 description 6
- 210000002442 prefrontal cortex Anatomy 0.000 description 6
- 238000000034 method Methods 0.000 description 5
- 239000000546 pharmaceutical excipient Substances 0.000 description 5
- 239000003981 vehicle Substances 0.000 description 4
- 210000001175 cerebrospinal fluid Anatomy 0.000 description 3
- 239000002552 dosage form Substances 0.000 description 3
- 238000001690 micro-dialysis Methods 0.000 description 3
- 230000002474 noradrenergic effect Effects 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 230000000699 topical effect Effects 0.000 description 3
- PNVNVHUZROJLTJ-UHFFFAOYSA-N venlafaxine Chemical compound C1=CC(OC)=CC=C1C(CN(C)C)C1(O)CCCCC1 PNVNVHUZROJLTJ-UHFFFAOYSA-N 0.000 description 3
- 229960004688 venlafaxine Drugs 0.000 description 3
- SJJCQDRGABAVBB-UHFFFAOYSA-N 1-hydroxy-2-naphthoic acid Chemical compound C1=CC=CC2=C(O)C(C(=O)O)=CC=C21 SJJCQDRGABAVBB-UHFFFAOYSA-N 0.000 description 2
- WXTMDXOMEHJXQO-UHFFFAOYSA-N 2,5-dihydroxybenzoic acid Chemical compound OC(=O)C1=CC(O)=CC=C1O WXTMDXOMEHJXQO-UHFFFAOYSA-N 0.000 description 2
- YFGHCGITMMYXAQ-UHFFFAOYSA-N 2-[(diphenylmethyl)sulfinyl]acetamide Chemical compound C=1C=CC=CC=1C(S(=O)CC(=O)N)C1=CC=CC=C1 YFGHCGITMMYXAQ-UHFFFAOYSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- NTYJJOPFIAHURM-UHFFFAOYSA-N Histamine Chemical compound NCCC1=CN=CN1 NTYJJOPFIAHURM-UHFFFAOYSA-N 0.000 description 2
- 229940115480 Histamine H3 receptor antagonist Drugs 0.000 description 2
- 229940122931 Histamine H3 receptor inverse agonist Drugs 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical class Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 2
- 241000700157 Rattus norvegicus Species 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 238000003745 diagnosis Methods 0.000 description 2
- -1 dihydrochloride Chemical compound 0.000 description 2
- 239000000890 drug combination Substances 0.000 description 2
- 238000003304 gavage Methods 0.000 description 2
- FUZZWVXGSFPDMH-UHFFFAOYSA-M hexanoate Chemical compound CCCCCC([O-])=O FUZZWVXGSFPDMH-UHFFFAOYSA-M 0.000 description 2
- 150000004677 hydrates Chemical class 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 229960001165 modafinil Drugs 0.000 description 2
- WWZKQHOCKIZLMA-UHFFFAOYSA-M octanoate Chemical compound CCCCCCCC([O-])=O WWZKQHOCKIZLMA-UHFFFAOYSA-M 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 239000012453 solvate Substances 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 230000005062 synaptic transmission Effects 0.000 description 2
- 230000002195 synergetic effect Effects 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- LSPHULWDVZXLIL-UHFFFAOYSA-N (+/-)-Camphoric acid Chemical compound CC1(C)C(C(O)=O)CCC1(C)C(O)=O LSPHULWDVZXLIL-UHFFFAOYSA-N 0.000 description 1
- LBLYYCQCTBFVLH-UHFFFAOYSA-M 2-methylbenzenesulfonate Chemical compound CC1=CC=CC=C1S([O-])(=O)=O LBLYYCQCTBFVLH-UHFFFAOYSA-M 0.000 description 1
- KPGXRSRHYNQIFN-UHFFFAOYSA-N 2-oxoglutaric acid Chemical compound OC(=O)CCC(=O)C(O)=O KPGXRSRHYNQIFN-UHFFFAOYSA-N 0.000 description 1
- ALKYHXVLJMQRLQ-UHFFFAOYSA-N 3-Hydroxy-2-naphthoate Chemical compound C1=CC=C2C=C(O)C(C(=O)O)=CC2=C1 ALKYHXVLJMQRLQ-UHFFFAOYSA-N 0.000 description 1
- ACQXFQGMLFJXEI-KRWDZBQOSA-N 4-[4-[3-[(3s)-3-methylpiperidin-1-yl]propoxy]phenyl]-1-oxidopyridin-1-ium Chemical compound C1[C@@H](C)CCCN1CCCOC1=CC=C(C=2C=C[N+]([O-])=CC=2)C=C1 ACQXFQGMLFJXEI-KRWDZBQOSA-N 0.000 description 1
- QCXJEYYXVJIFCE-UHFFFAOYSA-M 4-acetamidobenzoate Chemical compound CC(=O)NC1=CC=C(C([O-])=O)C=C1 QCXJEYYXVJIFCE-UHFFFAOYSA-M 0.000 description 1
- WUBBRNOQWQTFEX-UHFFFAOYSA-N 4-aminosalicylic acid Chemical compound NC1=CC=C(C(O)=O)C(O)=C1 WUBBRNOQWQTFEX-UHFFFAOYSA-N 0.000 description 1
- YCPXWRQRBFJBPZ-UHFFFAOYSA-N 5-sulfosalicylic acid Chemical compound OC(=O)C1=CC(S(O)(=O)=O)=CC=C1O YCPXWRQRBFJBPZ-UHFFFAOYSA-N 0.000 description 1
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- RGHNJXZEOKUKBD-SQOUGZDYSA-M D-gluconate Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C([O-])=O RGHNJXZEOKUKBD-SQOUGZDYSA-M 0.000 description 1
- AEMOLEFTQBMNLQ-AQKNRBDQSA-N D-glucopyranuronic acid Chemical compound OC1O[C@H](C(O)=O)[C@@H](O)[C@H](O)[C@H]1O AEMOLEFTQBMNLQ-AQKNRBDQSA-N 0.000 description 1
- HCYAFALTSJYZDH-UHFFFAOYSA-N Desimpramine Chemical compound C1CC2=CC=CC=C2N(CCCNC)C2=CC=CC=C21 HCYAFALTSJYZDH-UHFFFAOYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- BDAGIHXWWSANSR-UHFFFAOYSA-M Formate Chemical compound [O-]C=O BDAGIHXWWSANSR-UHFFFAOYSA-M 0.000 description 1
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- AEMRFAOFKBGASW-UHFFFAOYSA-M Glycolate Chemical compound OCC([O-])=O AEMRFAOFKBGASW-UHFFFAOYSA-M 0.000 description 1
- WTDRDQBEARUVNC-LURJTMIESA-N L-DOPA Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C(O)=C1 WTDRDQBEARUVNC-LURJTMIESA-N 0.000 description 1
- WTDRDQBEARUVNC-UHFFFAOYSA-N L-Dopa Natural products OC(=O)C(N)CC1=CC=C(O)C(O)=C1 WTDRDQBEARUVNC-UHFFFAOYSA-N 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-L Malonate Chemical compound [O-]C(=O)CC([O-])=O OFOBLEOULBTSOW-UHFFFAOYSA-L 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 1
- QIAFMBKCNZACKA-UHFFFAOYSA-N N-benzoylglycine Chemical compound OC(=O)CNC(=O)C1=CC=CC=C1 QIAFMBKCNZACKA-UHFFFAOYSA-N 0.000 description 1
- 229910002651 NO3 Inorganic materials 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- KYYIDSXMWOZKMP-UHFFFAOYSA-N O-desmethylvenlafaxine Chemical compound C1CCCCC1(O)C(CN(C)C)C1=CC=C(O)C=C1 KYYIDSXMWOZKMP-UHFFFAOYSA-N 0.000 description 1
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- BKRGVLQUQGGVSM-KBXCAEBGSA-N Revanil Chemical compound C1=CC(C=2[C@H](N(C)C[C@H](C=2)NC(=O)N(CC)CC)C2)=C3C2=CNC3=C1 BKRGVLQUQGGVSM-KBXCAEBGSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- ZMZDMBWJUHKJPS-UHFFFAOYSA-M Thiocyanate anion Chemical compound [S-]C#N ZMZDMBWJUHKJPS-UHFFFAOYSA-M 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- WNLRTRBMVRJNCN-UHFFFAOYSA-L adipate(2-) Chemical compound [O-]C(=O)CCCCC([O-])=O WNLRTRBMVRJNCN-UHFFFAOYSA-L 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000000556 agonist Substances 0.000 description 1
- 229940072056 alginate Drugs 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 230000000172 allergic effect Effects 0.000 description 1
- AWUCVROLDVIAJX-UHFFFAOYSA-N alpha-glycerophosphate Natural products OCC(O)COP(O)(O)=O AWUCVROLDVIAJX-UHFFFAOYSA-N 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 229940035678 anti-parkinson drug Drugs 0.000 description 1
- 229940124435 antinarcoleptic drug Drugs 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 229940072107 ascorbate Drugs 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 229940009098 aspartate Drugs 0.000 description 1
- 208000010668 atopic eczema Diseases 0.000 description 1
- 229940077388 benzenesulfonate Drugs 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-M benzenesulfonate Chemical compound [O-]S(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-M 0.000 description 1
- 229940050390 benzoate Drugs 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 229960002802 bromocriptine Drugs 0.000 description 1
- OZVBMTJYIDMWIL-AYFBDAFISA-N bromocriptine Chemical compound C1=CC(C=2[C@H](N(C)C[C@@H](C=2)C(=O)N[C@]2(C(=O)N3[C@H](C(N4CCC[C@H]4[C@]3(O)O2)=O)CC(C)C)C(C)C)C2)=C3C2=C(Br)NC3=C1 OZVBMTJYIDMWIL-AYFBDAFISA-N 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 229940114081 cinnamate Drugs 0.000 description 1
- 229940001468 citrate Drugs 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 230000001054 cortical effect Effects 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 230000001186 cumulative effect Effects 0.000 description 1
- 229940109275 cyclamate Drugs 0.000 description 1
- HCAJEUSONLESMK-UHFFFAOYSA-N cyclohexylsulfamic acid Chemical compound OS(=O)(=O)NC1CCCCC1 HCAJEUSONLESMK-UHFFFAOYSA-N 0.000 description 1
- GHVNFZFCNZKVNT-UHFFFAOYSA-M decanoate Chemical compound CCCCCCCCCC([O-])=O GHVNFZFCNZKVNT-UHFFFAOYSA-M 0.000 description 1
- 230000002939 deleterious effect Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 229960003914 desipramine Drugs 0.000 description 1
- 229960001623 desvenlafaxine Drugs 0.000 description 1
- 229940120124 dichloroacetate Drugs 0.000 description 1
- JXTHNDFMNIQAHM-UHFFFAOYSA-N dichloroacetic acid Chemical compound OC(=O)C(Cl)Cl JXTHNDFMNIQAHM-UHFFFAOYSA-N 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- POULHZVOKOAJMA-UHFFFAOYSA-M dodecanoate Chemical compound CCCCCCCCCCCC([O-])=O POULHZVOKOAJMA-UHFFFAOYSA-M 0.000 description 1
- MOTZDAYCYVMXPC-UHFFFAOYSA-N dodecyl hydrogen sulfate Chemical compound CCCCCCCCCCCCOS(O)(=O)=O MOTZDAYCYVMXPC-UHFFFAOYSA-N 0.000 description 1
- 229940043264 dodecyl sulfate Drugs 0.000 description 1
- 239000003937 drug carrier Substances 0.000 description 1
- 239000013583 drug formulation Substances 0.000 description 1
- 239000000428 dust Substances 0.000 description 1
- 238000000835 electrochemical detection Methods 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- AFAXGSQYZLGZPG-UHFFFAOYSA-L ethane-1,2-disulfonate Chemical compound [O-]S(=O)(=O)CCS([O-])(=O)=O AFAXGSQYZLGZPG-UHFFFAOYSA-L 0.000 description 1
- HHFAWKCIHAUFRX-UHFFFAOYSA-N ethoxide Chemical compound CC[O-] HHFAWKCIHAUFRX-UHFFFAOYSA-N 0.000 description 1
- 229940044170 formate Drugs 0.000 description 1
- 239000012458 free base Substances 0.000 description 1
- 229940050411 fumarate Drugs 0.000 description 1
- DSLZVSRJTYRBFB-DUHBMQHGSA-N galactaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)[C@@H](O)[C@H](O)C(O)=O DSLZVSRJTYRBFB-DUHBMQHGSA-N 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 229940114119 gentisate Drugs 0.000 description 1
- 229940050410 gluconate Drugs 0.000 description 1
- 229940097042 glucuronate Drugs 0.000 description 1
- 229930195712 glutamate Natural products 0.000 description 1
- JFCQEDHGNNZCLN-UHFFFAOYSA-N glutaric acid Chemical compound OC(=O)CCCC(O)=O JFCQEDHGNNZCLN-UHFFFAOYSA-N 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 230000003862 health status Effects 0.000 description 1
- IPCSVZSSVZVIGE-UHFFFAOYSA-M hexadecanoate Chemical compound CCCCCCCCCCCCCCCC([O-])=O IPCSVZSSVZVIGE-UHFFFAOYSA-M 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 229960001340 histamine Drugs 0.000 description 1
- 230000000742 histaminergic effect Effects 0.000 description 1
- ZMZDMBWJUHKJPS-UHFFFAOYSA-N hydrogen thiocyanate Natural products SC#N ZMZDMBWJUHKJPS-UHFFFAOYSA-N 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- SUMDYPCJJOFFON-UHFFFAOYSA-N isethionic acid Chemical compound OCCS(O)(=O)=O SUMDYPCJJOFFON-UHFFFAOYSA-N 0.000 description 1
- KQNPFQTWMSNSAP-UHFFFAOYSA-N isobutyric acid Chemical compound CC(C)C(O)=O KQNPFQTWMSNSAP-UHFFFAOYSA-N 0.000 description 1
- 229940001447 lactate Drugs 0.000 description 1
- 229940099584 lactobionate Drugs 0.000 description 1
- JYTUSYBCFIZPBE-AMTLMPIISA-N lactobionic acid Chemical compound OC(=O)[C@H](O)[C@@H](O)[C@@H]([C@H](O)CO)O[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1O JYTUSYBCFIZPBE-AMTLMPIISA-N 0.000 description 1
- 229940070765 laurate Drugs 0.000 description 1
- 229960004502 levodopa Drugs 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 229960003587 lisuride Drugs 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 229940049920 malate Drugs 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N malic acid Chemical compound OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 230000001730 monoaminergic effect Effects 0.000 description 1
- XTEGVFVZDVNBPF-UHFFFAOYSA-L naphthalene-1,5-disulfonate(2-) Chemical compound C1=CC=C2C(S(=O)(=O)[O-])=CC=CC2=C1S([O-])(=O)=O XTEGVFVZDVNBPF-UHFFFAOYSA-L 0.000 description 1
- KVBGVZZKJNLNJU-UHFFFAOYSA-N naphthalene-2-sulfonic acid Chemical compound C1=CC=CC2=CC(S(=O)(=O)O)=CC=C21 KVBGVZZKJNLNJU-UHFFFAOYSA-N 0.000 description 1
- 230000001537 neural effect Effects 0.000 description 1
- 230000000966 norepinephrine reuptake Effects 0.000 description 1
- 239000007764 o/w emulsion Substances 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 229940049964 oleate Drugs 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- PXQPEWDEAKTCGB-UHFFFAOYSA-N orotic acid Chemical compound OC(=O)C1=CC(=O)NC(=O)N1 PXQPEWDEAKTCGB-UHFFFAOYSA-N 0.000 description 1
- 230000000803 paradoxical effect Effects 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 238000011458 pharmacological treatment Methods 0.000 description 1
- 238000001050 pharmacotherapy Methods 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 229960001879 ropinirole Drugs 0.000 description 1
- UHSKFQJFRQCDBE-UHFFFAOYSA-N ropinirole Chemical compound CCCN(CCC)CCC1=CC=CC2=C1CC(=O)N2 UHSKFQJFRQCDBE-UHFFFAOYSA-N 0.000 description 1
- YGSDEFSMJLZEOE-UHFFFAOYSA-M salicylate Chemical compound OC1=CC=CC=C1C([O-])=O YGSDEFSMJLZEOE-UHFFFAOYSA-M 0.000 description 1
- 229960001860 salicylate Drugs 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 229940116351 sebacate Drugs 0.000 description 1
- CXMXRPHRNRROMY-UHFFFAOYSA-L sebacate(2-) Chemical compound [O-]C(=O)CCCCCCCCC([O-])=O CXMXRPHRNRROMY-UHFFFAOYSA-L 0.000 description 1
- AWUCVROLDVIAJX-GSVOUGTGSA-N sn-glycerol 3-phosphate Chemical compound OC[C@@H](O)COP(O)(O)=O AWUCVROLDVIAJX-GSVOUGTGSA-N 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 229940086735 succinate Drugs 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 1
- BDHFUVZGWQCTTF-UHFFFAOYSA-M sulfonate Chemical compound [O-]S(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-M 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 229940095064 tartrate Drugs 0.000 description 1
- WVSZBAHKLHXQFN-UHFFFAOYSA-N tetrahydrate;dihydrochloride Chemical compound O.O.O.O.Cl.Cl WVSZBAHKLHXQFN-UHFFFAOYSA-N 0.000 description 1
- 230000004797 therapeutic response Effects 0.000 description 1
- 230000008719 thickening Effects 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-M toluene-4-sulfonate Chemical compound CC1=CC=C(S([O-])(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-M 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- WBYWAXJHAXSJNI-VOTSOKGWSA-M trans-cinnamate Chemical compound [O-]C(=O)\C=C\C1=CC=CC=C1 WBYWAXJHAXSJNI-VOTSOKGWSA-M 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 239000007762 w/o emulsion Substances 0.000 description 1
- 230000002618 waking effect Effects 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4453—Non condensed piperidines, e.g. piperocaine only substituted in position 1, e.g. propipocaine, diperodon
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/135—Amines having aromatic rings, e.g. ketamine, nortriptyline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/135—Amines having aromatic rings, e.g. ketamine, nortriptyline
- A61K31/137—Arylalkylamines, e.g. amphetamine, epinephrine, salbutamol, ephedrine or methadone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/38—Heterocyclic compounds having sulfur as a ring hetero atom
- A61K31/381—Heterocyclic compounds having sulfur as a ring hetero atom having five-membered rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/4545—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a six-membered ring with nitrogen as a ring hetero atom, e.g. pipamperone, anabasine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/26—Psychostimulants, e.g. nicotine, cocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
- A61P25/32—Alcohol-abuse
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D295/00—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms
- C07D295/04—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms
- C07D295/08—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms substituted by singly bound oxygen or sulfur atoms
- C07D295/084—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms substituted by singly bound oxygen or sulfur atoms with the ring nitrogen atoms and the oxygen or sulfur atoms attached to the same carbon chain, which is not interrupted by carbocyclic rings
- C07D295/092—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms substituted by singly bound oxygen or sulfur atoms with the ring nitrogen atoms and the oxygen or sulfur atoms attached to the same carbon chain, which is not interrupted by carbocyclic rings with aromatic radicals attached to the chain
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Organic Chemistry (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Psychiatry (AREA)
- Addiction (AREA)
- Pain & Pain Management (AREA)
- Psychology (AREA)
- Emergency Medicine (AREA)
- Pulmonology (AREA)
- Hospice & Palliative Care (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Combinación de: - un antagonista o agonista inverso de H3 de fórmula: **(Ver fórmula)** donde en la fórmula (I): R1 es H o metilo, R2 es CI o **(Ver fórmula)** donde * representa la posición de fijación al anillo de fenilo, n es 0 o 1, y - un antidepresivo seleccionado de entre los inhibidores de la recaptación de noradrenalina seleccionados de entre duloxetina, reboxetina, atomoxetina.
Description
DESCRIPCIÓN
Combinaciones novedosas de un antagonista de H3 y un inhibidor de la recaptación de noradrenalina y usos terapéuticos de los mismos
[0001] La presente invención se refiere a combinaciones novedosas y sus usos para tratar trastornos de la vigilia en pacientes que padecen liberación deficiente de noradrenalina.
[0002] La vigilia se controla mediante varios sistemas neuronales monoaminérgicos en el cerebro, principalmente los sistemas histaminérgico y noradrenérgico, que están activos durante la vigilia y silentes durante el sueño. Por tanto, el aumento en la liberación de histamina o noradrenalina da como resultado la estimulación de la vigilia a expensas de los estados de sueño.
Se sabe que los antagonistas/agonistas inversos del receptor de histamina H3 (X. Ligneau y col. J. Pharmacol. Exp Ther. 2007, 320, 365, J.S. Lin y col. Neurobiology of Disease 2008, 30, 74, RX Guo y col. Brit. J. Pharmacol. 2009, 157, 104) modulan el ciclo de sueño/vigilia aumentando la vigilia.
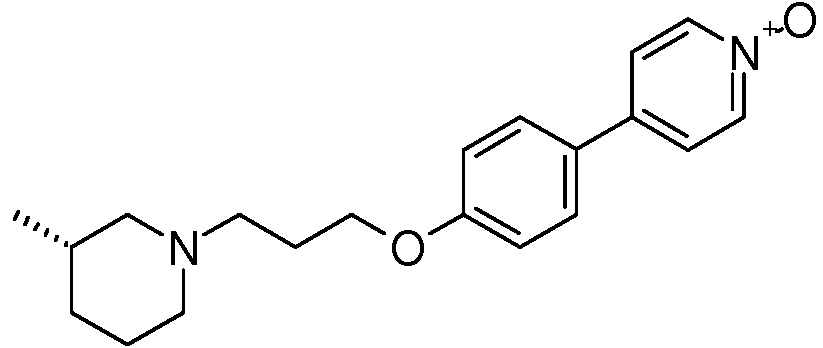
El documento WO 2006/117609 describe ligandos de H3 tales como 1-óxido de (3S)-4-{4-[3-(3-metilpiperidin-1-il)propoxi]fenil}piridina de fórmula:
denominado en esta memoria “compuesto (A)”, y sus sales, hidratos o sales hidratadas farmacéuticamente aceptables.
[0003] Pitolisant (Wakix®), es decir, la sal monoclorhidrato de 1-{3-[3-(4-clorofenil)propoxi]propil}piperidina ha sido uno de los primeros antagonistas/agonistas inversos de H3 en el mercado y actualmente está autorizada en Europa para el tratamiento de la narcolepsia, con o sin cataplejía.
El efecto de los antagonistas de H3 sobre la noradrenalina se ha descrito en AD Medhurst y col. (J. Pharmacol. Exp. Ther. 2007, 321, 1032-1045), G. Flik y col. (J. Mol. Neurosci. 2015, 56, 320-328) y J.S. Lin y col. (Neurobiology of Disease 2008, 30,74-83).
Los antidepresivos con propiedades inhibidoras de la recaptación de noradrenalina tales como duloxetina, reboxetina, atomoxetina, venlafaxina, etc. (C. Sánchez y col. Pharmacol. 2007, 86, 468) aumentan la vigilia a expensas del sueño profundo y/o el sueño MOR.
[0004] Kallweit y col. (EXPERT OPINION ON PHARMACOTHERAPY vol. 18, n.° 8, 2017, páginas 809-817) describen el tratamiento farmacológico de la narcolepsia con depresión y recomiendan, p. ej., venlafaxina.
Lin y col. (Neurobiology of Disease, vol. 30, n.° 1,2008, páginas 74-83) describen el uso de tiprolisant combinado con modafinilo.
[0005] Actualmente, se ha descubierto que la combinación de un antagonista de H3 con un antidepresivo seleccionado de entre los inhibidores de la recaptación de noradrenalina conduce inesperadamente a un aumento enorme de la vigilia tranquila y a la reducción del sueño MOR, efectos que están mejorados/reducidos, respectivamente, de una manera sinérgica supraaditiva en comparación con el efecto de cada compuesto administrado individualmente.
[0006] Por tanto, según un primer objetivo, la presente invención se refiere a una combinación de:
• un antagonista o agonista inverso de H3 de fórmula:
Donde en la fórmula (I):
R1 es H o metilo,
R2 es CI o
donde * representa la posición de fijación al anillo de fenilo,
n es 0 o 1,
y
• un antidepresivo seleccionado de entre los inhibidores de la recaptación de noradrenalina seleccionados de entre duloxetina, reboxetina, atomoxetina.
[0007] Según una realización, dicho antagonista/agonista inverso de H3 se selecciona de entre uno de los compuestos siguientes:
[0009] Más particularmente, dicho antagonista/agonista inverso de H3 es la sal clorhidrato de
[0010] Más particularmente, dicho antagonista/agonista inverso de H3 es la sal diclorhidrato tetrahidratada de
(denominada BP1.3656B en esta memoria).
[0011] Según una realización, los compuestos pueden estar en forma de su base libre o, alternativamente, en forma de sales farmacéuticamente aceptables tales como clorhidrato, oxalato, diclorhidrato, bromhidrato, dibromhidrato, naftaleno-1,5-disulfonato, sulfato, etano-1,2-disulfonato, ciclamato, toluenosulfonato, paratoluenosulfonato, tiocianato, nitrato, metanosulfonato, dodecilsulfato, naftaleno-2-sulfonato, bencenosulfonato, dicloroacetato, glicerofosfato, 2-hidroxietanosulfonato, aspartato, maleato, fosfato, etanosulfonato, canfor-10-sulfonato, glutamato, alginato, pamoato, 2-oxoglutarato, 1-hidroxi-2-naftoato, malonato, gentisato, salicilato, tartrato, fumarato, galactarato, citrato, glucuronato, lactobionato, 4-aminosalicilato, glicolato, sesquiglicolato, glucoheptonato, piroglutamato, mandelato, malato, hipurato, formiato, gluconato, lactato, oleato, ascorbato, benzoato, succinato, 4-acetamidobenzoato, glutarato, cinamato, adipato, sebacato, canforato, acetato, caproato, nicotinato, isobutirato,
propionato, caprato, caprilato, caproato, laurato, palmitato, estearato, undecen-10-oato, caprilato, orotato, carbonato, 5-sulfosalicilato, 1-hidroxi-2-naftoato, 3-hidroxi-2-naftoato; y/o solvatos tales como hidratos, etanolato, hemietanolato.
[0012] Por consiguiente, el término “compuesto”, como se emplea en esta memoria, se refiere a las sales farmacéuticamente aceptables de los mismos y/o los solvatos de estas, a menos que se especifique de otro modo.
[0013] Según una realización, el antidepresivo es duloxetina.
Según una realización, la combinación es la combinación de
[0014] Según otro objetivo, la presente invención también se refiere a una combinación según la invención, donde ambos ingredientes se administran simultáneamente, independientemente, o gradualmente a lo largo del tiempo.
Según otro objetivo, también se refiere a una composición farmacéutica que comprende la combinación de la invención, donde ambos ingredientes son adecuados para administración simultánea.
[0015] Según otro objetivo, la presente invención también se refiere a la combinación de la invención para uso en el tratamiento y/o la prevención de un trastorno seleccionado de entre somnolencia diurna excesiva, trastornos de abuso de sustancias tales como el alcohol, y/o con déficit de atención y cognitivo, en un paciente que padece liberación deficiente de noradrenalina.
La identificación de los sujetos con necesidad de tratamiento de las enfermedades y afecciones descritas en esta memoria está perfectamente comprendida en la capacidad de comprensión y los conocimientos de un experto en la materia. Un facultativo experto en la materia puede identificar fácilmente, mediante el uso de análisis clínicos, exploración física, pruebas genéticas y los antecedentes médicos/familiares, a los sujetos con necesidad de tal tratamiento.
[0016] Según una realización, dicho trastorno es somnolencia diurna excesiva y se presenta en un paciente que padece:
- narcolepsia, con o sin cataplejía,
- hipersomnia idiopática,
- trastornos de somnolencia diurna,
- apnea obstructiva del sueño,
-trastornos del ritmo circadiano de sueño-vigilia,
- enfermedad de Parkinson, o
- síndrome de Prader-Willi.
[0017] Según una realización alternativa, dicho trastorno es déficit de atención y cognitivo y se presenta en un paciente que padece trastorno por déficit de atención e hiperactividad (TDAH).
[0018] Según una realización alternativa adicional, dicho trastorno es somnolencia diurna excesiva, déficit de atención y cognitivo y se presenta en un paciente que padece depresión.
[0019] Según otra realización alternativa adicional, dicho trastorno se selecciona de entre síndromes de abstinencia del abuso de sustancias.
[0020] Cabe señalar que las realizaciones alternativas no son excluyentes entre sí y se pueden considerar adicionales.
[0021] Los niveles de administración reales de los compuestos se pueden variar para obtener una cantidad de principio activo que sea eficaz para obtener una respuesta terapéutica deseada para una composición y un método de administración particulares. Por lo tanto, el nivel de administración seleccionado depende del efecto terapéutico deseado, de la vía de administración, de la duración deseada del tratamiento, y de otros factores, p. ej., el estado del paciente.
Una cantidad terapéuticamente eficaz puede ser determinada fácilmente por el médico responsable del diagnóstico, como experto en la materia, mediante el uso de técnicas convencionales y observando los resultados obtenidos en circunstancias análogas. Al determinar la cantidad terapéuticamente eficaz, el médico responsable del diagnóstico
considera varios factores, que incluyen, pero no se limitan a: la especie del sujeto; su tamaño, edad y salud general; la enfermedad específica implicada; el grado de afectación o la gravedad de la enfermedad; la respuesta del sujeto individual; el compuesto particular administrado; el modo de administración; la biodisponibilidad característica de la preparación administrada; la pauta posológica seleccionada; el uso de medicación simultánea; y otras circunstancias relevantes.
La cantidad de los compuestos que es necesaria para conseguir el efecto biológico deseado variará en función de varios factores, que incluyen el tipo de formulación del fármaco que se va a administrar, el tipo de enfermedad, el estado de enfermedad del paciente y la vía de administración.
En términos generales, la dosis preferida de un fármaco que se va a administrar es probable que dependa de variables tales como el tipo y grado de progresión de la enfermedad o el trastorno, el estado de salud general del paciente particular, la eficacia biológica relativa del compuesto seleccionado y la formulación del excipiente del compuesto, y su vía de administración.
[0022] La dosis diaria del antagonista/agonista inverso de H3 (I) generalmente puede estar comprendida entrel |jg y 50 mg al día por paciente. A modo ilustrativo, las dosis preferidas para pitolisant son 5-40 mg/día, más preferentemente 10-30 mg/día, y para BP1.3656B 1-100 jg/día, preferentemente 5-30 jg/día.
[0023] La dosis diaria del antidepresivo generalmente puede estar comprendida entre 2 mg y 250 mg al día por paciente. Las dosis ilustradas se detallan a continuación:
desipramina: 10-300 mg/día, preferentemente 25-200 mg/día; duloxetina: 20-120 mg/día, preferentemente 30 60 mg/día; venlafaxina: 35-375 mg/día, preferentemente 35-225 mg/día; desvenlafaxina: 50-400 mg/día, preferentemente 50-100 mg/día; atomoxetina: 10-100 mg/día, preferentemente 10-60 mg/día; reboxetina: 2 12 mg/día, preferentemente 2-8 mg/día.
[0024] Según una realización adicional, el método de la invención también comprende la administración de uno o más principios activos adicionales, seleccionados de entre fármacos antiparkinsonianos, tales como levodopa, ropinirol, lisurida, bromocriptina, pramixepol, o seleccionados de entre fármacos antinarcolépticos o presuntamente antinarcolépticos de otra clase, entre otros, modafinilo.
[0025] Los compuestos se pueden formular en la misma o en distintas composiciones farmacéuticas mediante mezcla con uno o más excipientes farmacéuticamente aceptables.
Las composiciones se pueden administrar convenientemente en una forma farmacéutica unitaria y se pueden preparar mediante cualquiera de los métodos ampliamente conocidos en la técnica farmacéutica, por ejemplo, como se describe en Remington: The Science and Practice of Pharmacy, 20a ed.; Gennaro, A. R., Ed.; Lippincott Williams & Wilkins: Filadelfia, PA, 2000.
[0026] Los compuestos se pueden administrar mediante diversas vías de administración tales como la oral; parenteral, que incluye subcutánea, intramuscular, intravenosa; sublingual, tópica; local; endotraqueal; intranasal; transdérmica o rectal, combinando los principios activos con un excipiente o vehículo farmacéuticamente aceptable en una o dos composiciones farmacéuticas.
En particular, las composiciones adecuadas para administración parenteral son estériles e incluyen emulsiones, suspensiones, soluciones para inyección acuosas y no acuosas, que pueden contener agentes de suspensión y agentes espesantes y antioxidantes, tampones, bacteriostáticos y solutos que hacen la formulación isotónica, y tienen un pH debidamente ajustado, con la sangre del receptor previsto. Para la aplicación tópica, las composiciones de la invención se pueden usar como cremas, geles, pomadas o lociones.
[0027] Según la invención, se usa ventajosamente la administración oral del compuesto (I) o la composición en una formulación apropiada. Las formulaciones que son adecuadas para ser administradas por vía oral a un paciente incluyen unidades discretas tales como cápsulas, tales como de gelatina blanda o dura, comprimidos, que contienen cada uno una cantidad predeterminada del compuesto de fórmula (I). También incluyen polvo; gránulos; soluciones o suspensiones en un líquido acuoso o un líquido no acuoso, o emulsión de aceite en agua o emulsión de agua en aceite. Las formulaciones gastrorresistentes también se contemplan para las formulaciones orales, en particular para duloxetina.
[0028] “Farmacéuticamente” o “farmacéuticamente aceptable” se refiere a entidades moleculares y composiciones que no producen una reacción adversa, alérgica u otra reacción perjudicial cuando se administran a un animal, o un ser humano, según proceda. Como se emplea en esta memoria, “excipiente o vehículo farmacéuticamente aceptable” incluye en particular diluyentes, aditivos, excipientes o vehículos. El uso de tales ingredientes para sustancias farmacéuticamente activas es ampliamente conocido en la técnica.
[0029] En el contexto de la invención, el término “tratar” o “tratamiento”, como se emplea en esta memoria, significa revertir, aliviar, inhibir el progreso de, o prevenir el trastorno o la afección a la que se aplica tal término, o uno o más síntomas de tal trastorno o afección.
[0030] “Cantidad terapéuticamente eficaz” significa una cantidad de un compuesto/medicamento según la
presenta invención eficaz para producir el efecto terapéutico deseado.
[0031] Según la invención, el término “paciente” o “paciente con necesidad del mismo” está destinado a un mamífero humano o no humano afectado o que es probable que se vea afectado por los trastornos anteriores. Preferiblemente, el paciente es un ser humano.
[0032] Los compuestos se pueden administrar en formas farmacéuticas unitarias, donde el término “dosis unitaria” significa una dosis única que se puede administrar a un paciente, y que se puede manipular y envasar fácilmente, permaneciendo como una dosis unitaria física y químicamente estable que comprende el propio compuesto activo o como una o dos composiciones farmacéuticamente aceptables.
Las formas farmacéuticas unitarias apropiadas comprenden las formas orales; las formas sublinguales, bucales, endotraqueales, intraoculares, intranasales, por inhalación, las formas tópicas, transdérmicas, subcutáneas, intramusculares o intravenosas y rectales y los implantes.
FIGURAS:
[0033]
• La Figura 1 representa los cambios inducidos por los fármacos en el equilibrio sueño-vigilia a lo largo de 12 horas después de la administración en ratas (media ± EEM de 15 a 16 valores individuales) en la duración de la vigilia tranquila (Figura 1A) y la duración del sueño MOR (Figura 1B) después de la administración de pitolisant y duloxetina.
• La Figura 2 representa los cambios inducidos por los fármacos en el equilibrio sueño-vigilia a lo largo de 12 horas después de la administración en ratas (media ± EEM de 15 a 16 valores individuales) en la duración de la vigilia tranquila (Figura 2A) y la duración del sueño MOR (Figura 2B) después de la administración de compuesto BP1.3656B y duloxetina.
• La Figura 3 representa los cambios inducidos por los fármacos en el equilibrio sueño-vigilia a lo largo de 12 horas después de la administración en ratas (media ± EEM de 15 a 16 valores individuales) en la duración de la vigilia tranquila (Figura 3A) y la duración del sueño MOR (Figura 3B) después de la administración de pitolisant y reboxetina.
• La Figura 4 representa los cambios inducidos por los fármacos en el equilibrio sueño-vigilia a lo largo de 12 horas después de la administración en ratas (media ± EEM de 15 a 16 valores individuales) en la duración de la vigilia tranquila (Figura 4A) y la duración del sueño MOR (Figura 4B) después de la administración de pitolisant y atomoxetina.
• La Figura 5 representa el aumento inducido por los fármacos en la liberación de noradrenalina en la corteza prefrontal de ratas sobre la liberación basal (ABC a lo largo de 150 min después de la administración) después de la administración de pitolisant y duloxetina (media ± EEM de 6 a 9 valores individuales).
Ejemplos
Ejemplo 1: efecto sobre el ciclo sueño/vigilia
[0034] Los efectos sobre los parámetros de sueño/vigilia se investigaron en ratas Wistar macho. Brevemente, se implantaron estereotáxicamente electrodos corticales a las ratas para el registro del electroencefalograma (EEG) usando un sistema telemétrico (Data Sciences Int., Saint Paul, MN, EE. UU.) para la adquisición, la transferencia y el almacenamiento de la actividad motora y las señales del EEG. Las señales del e Eg se analizaron según un procedimiento adaptado a partir del algoritmo propuesto por R.P. Louis y col. (J. Neurosci. Methods, 2004, 133, 71 80) y el análisis de los estados de vigilancia según H. Kleinlogel (Neuropsychobiol. 1990-91,23, 197-204) después de una transformación de Fourier rápida de periodos de EEG de 8 segundos de duración. Esto permite la determinación para cada periodo de su etapa de vigilancia (es decir, vigilia activa, vigilia tranquila, sueños de ondas lentas ligeros o profundos y sueño MOR, también denominado sueño paradójico). Las ratas recibieron vehículo, fármaco o combinación de fármacos por vía oral (sonda) alrededor de 30 minutos antes del inicio de la fase diurna.
[0035] A continuación, se registraron de manera continua las señales del EEG y se integraron adicionalmente a lo largo de la fase diurna de 12 horas.
[0036] Los efectos sobre el sueño/vigilia en las ratas que recibieron fármacos solos o combinados se presentan en la Figura 1 (pitolisant/duloxetina), Figura 2 (BP1.3656B/duloxetina), Figura 3 (pitolisant/reboxetina) y Figure 4 (pitolisant/atomoxetina):
En el caso de la combinación pitolisant/duloxetina, se demostró que la combinación conduce a un aumento en la vigilia tranquila de 35% en comparación con un aumento acumulado de 19%. Además, cuando se combinan los dos compuestos, la reducción en el sueño MOR provocada por la duloxetina se potencia en comparación con el efecto de la duloxetina sola (-35 % frente a -23 %), mientras que el pitolisant por sí mismo, a lo largo de 12 horas, no tiene ningún efecto significativo.
Ejemplo 2: liberación de noradrenalina en la corteza prefrontal
[0037] Se sabe que tanto los antagonistas/agonistas inversos del receptor de histamina H3 (J.S. Lin y col.
Neurobiology of Disease 2008, 30, 74, G. Flik y col. J. Mol. Neurosci. 2015, 56, 320) como los inhibidores de la recaptación de noradrenalina (F.P. Bymastery col. Current Pharmaceutical Design, 2005, 11, 1475, F.P. Bymaster y col. Neuropsychopharmacol. 2002, 27, 699) mejoran la noradrenalina extracelular en la corteza prefrontal, lo que refleja una activación de la neurotransmisión noradrenérgica. Sin embargo, en ambos casos, la mejora es limitada.
[0038] Los efectos sobre la liberación de noradrenalina en la corteza prefrontal fueron investigados in vivo mediante microdiálisis en ratas Wistar macho en vigilia por AD Medhurst y col. (J. Pharmacol. Exp. Ther. 2007, 321, 1032-1045) y G. Flik y col. (J. Mol. Neurosci. 2015, 56, 320-328). Brevemente, se implantó una cánula guía a ratas anestesiadas para el muestreo en la corteza prefrontal. Después de al menos una semana de recuperación después de la cirugía, se introdujo la sonda de microdiálisis en la cánula guía y se perfundió de manera continua con líquido cefalorraquídeo (LCR) artificial. Las ratas se habituaron a la jaula de microdiálisis durante ~3 horas. A continuación, las ratas recibieron vehículo, fármaco o combinación de fármacos por vía oral (sonda). Las muestras de LCR recogidas cada 30 minutos se analizaron para determinar su contenido de noradrenalina mediante CLAR acoplada a una detección electroquímica. Los niveles de noradrenalina en las muestras se expresaron en porcentaje de la liberación basal de noradrenalina registrada a lo largo de 1,5 horas antes del tratamiento con vehículo o fármaco.
[0039] Inesperadamente, cuando se combinan los dos tipos de compuestos, la activación de la neurotransmisión noradrenérgica en la corteza prefrontal se mejora de una manera sinérgica, como muestran los datos siguientes y se ilustra en la Figura 5.
[0040] Por tanto, la asociación de las dos clases de compuestos puede permitir una reducción en la dosis de cada componente y, de ese modo, mejorar la tolerancia.
Claims (12)
1. Combinación de:
• un antagonista o agonista inverso de H3 de fórmula:
donde en la fórmula (I):
R1 es H o metilo,
R2 es CI o
donde * representa la posición de fijación al anillo de fenilo,
n es 0 o 1,
y
• un antidepresivo seleccionado de entre los inhibidores de la recaptación de noradrenalina seleccionados de entre duloxetina, reboxetina, atomoxetina.
3. Combinación según cualquiera de las reivindicaciones anteriores, donde dicho antagonista/agonista inverso de H3 es la sal clorhidrato de
6. Combinación según cualquiera de las reivindicaciones anteriores, donde ambos ingredientes son adecuados para administración simultánea, independiente o gradual a lo largo del tiempo.
7. Composición farmacéutica que comprende la combinación según cualquiera de las reivindicaciones anteriores, donde ambos ingredientes son adecuados para administración simultánea.
8. Combinación según cualquiera de las reivindicaciones 1 a 6 para uso en el tratamiento y/o la prevención de un trastorno seleccionado de entre somnolencia diurna excesiva, trastornos de abuso de sustancias, tales como el alcohol y/o con déficit de atención y cognitivo, en un paciente que padece liberación deficiente de noradrenalina.
9. Combinación para uso según la reivindicación 8, donde dicho trastorno es somnolencia diurna excesiva y se presenta en un paciente que padece:
- narcolepsia, con o sin cataplejía,
- hipersomnia idiopática,
- trastornos de somnolencia diurna,
- apnea obstructiva del sueño,
-trastornos del ritmo circadiano de sueño-vigilia,
- enfermedad de Parkinson, o
- síndrome de Prader-Willi.
10. Combinación para uso según la reivindicación 8, donde dicho trastorno es déficit de atención y cognitivo y se presenta en un paciente que padece trastorno por déficit de atención e hiperactividad (TDAH).
11. Combinación para uso según la reivindicación 8, donde dicho trastorno es somnolencia diurna excesiva, déficit de atención y cognitivo y se presenta en un paciente que padece depresión.
12. Combinación para uso según la reivindicación 8, donde dicho trastorno se selecciona de entre síndromes de abstinencia del abuso de sustancias.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP18306017.7A EP3598975B1 (en) | 2018-07-27 | 2018-07-27 | Novel combinations of a h3 antagonist and a noradrenaline reuptake inhibitor, and the therapeutical uses thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2840253T3 true ES2840253T3 (es) | 2021-07-06 |
Family
ID=63144936
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES18306017T Active ES2840253T3 (es) | 2018-07-27 | 2018-07-27 | Combinaciones novedosas de un antagonista de H3 y un inhibidor de la recaptación de noradrenalina y usos terapéuticos de los mismos |
Country Status (19)
| Country | Link |
|---|---|
| US (2) | US11229632B2 (es) |
| EP (1) | EP3598975B1 (es) |
| JP (1) | JP7509520B2 (es) |
| KR (1) | KR102841963B1 (es) |
| CN (1) | CN110772515A (es) |
| AU (1) | AU2019208166B2 (es) |
| BR (1) | BR102019015415A2 (es) |
| CA (1) | CA3050590A1 (es) |
| DK (1) | DK3598975T3 (es) |
| ES (1) | ES2840253T3 (es) |
| HU (1) | HUE052652T2 (es) |
| IL (1) | IL268208B (es) |
| MA (1) | MA46500B1 (es) |
| MX (1) | MX379400B (es) |
| PL (1) | PL3598975T3 (es) |
| PT (1) | PT3598975T (es) |
| TN (1) | TN2019000216A1 (es) |
| TW (2) | TWI887204B (es) |
| ZA (1) | ZA201904876B (es) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3378858A1 (en) * | 2017-03-21 | 2018-09-26 | Bioprojet | Tetrahydrate of h3 ligand, its process of preparation and pharmaceutical compositions comprising the same |
| JP7234955B2 (ja) | 2020-01-31 | 2023-03-08 | トヨタ自動車株式会社 | 車両 |
| WO2022159629A1 (en) * | 2021-01-20 | 2022-07-28 | Alto Neuroscience, Inc. | Combination drug strategy for the treatment of psychiatric and neurological disorders in which anhedonia or motivation- related dysfunction exists |
| US20240398777A1 (en) * | 2023-06-01 | 2024-12-05 | Harmony Biosciences, Llc | Method of treating symptoms of prader-willi syndrome |
| WO2025082974A1 (en) * | 2023-10-16 | 2025-04-24 | Bioprojet Pharma | New formulations of pitolisant and methods of use |
| WO2025162430A1 (zh) * | 2024-02-01 | 2025-08-07 | 重庆罗特司光电科技有限公司 | 一种药物联用及其在预防或治疗神经退行性疾病中的用途 |
| WO2025207664A1 (en) * | 2024-03-25 | 2025-10-02 | Axsome Therapeutics, Inc. | Use of reboxetine to treat narcolepsy |
| US12565478B1 (en) | 2025-01-21 | 2026-03-03 | Axsome Therapeutics, Inc. | (S)-2-((S)-(2-ethoxyphenoxy)(phenyl)methyl)-4-nitrosomorpholine |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0982300A3 (en) | 1998-07-29 | 2000-03-08 | Societe Civile Bioprojet | Non-imidazole alkylamines as histamine H3 - receptor ligands and their therapeutic applications |
| EP1717233A1 (en) | 2005-04-29 | 2006-11-02 | Bioprojet | Histamine H3-receptor ligands and their therapeutic application |
| EP1717235A3 (en) | 2005-04-29 | 2007-02-28 | Bioprojet | Phenoxypropylpiperidines and -pyrrolidines and their use as histamine H3-receptor ligands |
| EP1717234A1 (en) | 2005-04-29 | 2006-11-02 | Bioprojet | Phenoxypropylpiperidines and -pyrrolidines and their use as histamine H3-receptor ligands |
| EP3239138A1 (en) * | 2016-04-25 | 2017-11-01 | Sandoz Ag | Hydrogen fumarate salt of 1-[3-[3-(4-chlorophenyl)propoxy]propyl]piperidine |
| EP3378477A1 (en) | 2017-03-21 | 2018-09-26 | BIOPROJET Pharma | New therapeutical use of h3-ligands |
| EP3378858A1 (en) | 2017-03-21 | 2018-09-26 | Bioprojet | Tetrahydrate of h3 ligand, its process of preparation and pharmaceutical compositions comprising the same |
-
2018
- 2018-07-27 HU HUE18306017A patent/HUE052652T2/hu unknown
- 2018-07-27 PT PT183060177T patent/PT3598975T/pt unknown
- 2018-07-27 PL PL18306017T patent/PL3598975T3/pl unknown
- 2018-07-27 ES ES18306017T patent/ES2840253T3/es active Active
- 2018-07-27 EP EP18306017.7A patent/EP3598975B1/en active Active
- 2018-07-27 DK DK18306017.7T patent/DK3598975T3/da active
-
2019
- 2019-06-04 US US16/431,063 patent/US11229632B2/en active Active
- 2019-07-19 MX MX2019008637A patent/MX379400B/es unknown
- 2019-07-22 IL IL268208A patent/IL268208B/en unknown
- 2019-07-22 TN TNP/2019/000216A patent/TN2019000216A1/en unknown
- 2019-07-23 AU AU2019208166A patent/AU2019208166B2/en active Active
- 2019-07-24 CA CA3050590A patent/CA3050590A1/en active Pending
- 2019-07-25 TW TW108126312A patent/TWI887204B/zh active
- 2019-07-25 TW TW112133787A patent/TWI905542B/zh active
- 2019-07-25 ZA ZA2019/04876A patent/ZA201904876B/en unknown
- 2019-07-25 KR KR1020190090305A patent/KR102841963B1/ko active Active
- 2019-07-26 MA MA46500A patent/MA46500B1/fr unknown
- 2019-07-26 BR BR102019015415A patent/BR102019015415A2/pt unknown
- 2019-07-26 JP JP2019137983A patent/JP7509520B2/ja active Active
- 2019-07-26 CN CN201910681199.1A patent/CN110772515A/zh active Pending
-
2021
- 2021-11-26 US US17/456,617 patent/US12059416B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| AU2019208166B2 (en) | 2024-08-01 |
| IL268208B (en) | 2022-09-01 |
| TWI905542B (zh) | 2025-11-21 |
| MA46500A1 (fr) | 2021-01-29 |
| KR20200012781A (ko) | 2020-02-05 |
| JP7509520B2 (ja) | 2024-07-02 |
| BR102019015415A2 (pt) | 2020-01-28 |
| HUE052652T2 (hu) | 2021-05-28 |
| EP3598975B1 (en) | 2020-10-21 |
| CN110772515A (zh) | 2020-02-11 |
| DK3598975T3 (da) | 2020-11-02 |
| US20220079932A1 (en) | 2022-03-17 |
| TN2019000216A1 (en) | 2021-01-07 |
| RU2019123563A (ru) | 2021-01-26 |
| US11229632B2 (en) | 2022-01-25 |
| JP2020015724A (ja) | 2020-01-30 |
| EP3598975A1 (en) | 2020-01-29 |
| PL3598975T3 (pl) | 2021-04-19 |
| ZA201904876B (en) | 2020-05-27 |
| PT3598975T (pt) | 2020-12-21 |
| KR102841963B1 (ko) | 2025-08-04 |
| TWI887204B (zh) | 2025-06-21 |
| IL268208A (en) | 2019-11-28 |
| TW202007395A (zh) | 2020-02-16 |
| AU2019208166A1 (en) | 2020-02-13 |
| MX2019008637A (es) | 2020-01-28 |
| MX379400B (es) | 2025-03-11 |
| US20200030310A1 (en) | 2020-01-30 |
| US12059416B2 (en) | 2024-08-13 |
| CA3050590A1 (en) | 2020-01-27 |
| TW202404587A (zh) | 2024-02-01 |
| MA46500B1 (fr) | 2022-07-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2840253T3 (es) | Combinaciones novedosas de un antagonista de H3 y un inhibidor de la recaptación de noradrenalina y usos terapéuticos de los mismos | |
| US11590107B2 (en) | Methods for treating neurological disorders with α1A-AR partial agonists | |
| BRPI0613697A2 (pt) | tratamento de distúrbios de sono-vigìlia | |
| EP1682152A2 (en) | Compositions and methods for treatment of nervous system disorders | |
| Auffret et al. | Apomorphine pump in advanced Parkinson's disease: effects on motor and nonmotor symptoms with brain metabolism correlations | |
| ES2991605T3 (es) | Composiciones para el tratamiento de los trastornos relacionados con el estrés | |
| US10813901B2 (en) | Compositions and methods for treating autism | |
| ES2769607T3 (es) | Derivados de prolina sulfonamida como antagonistas del receptor de orexina | |
| CN116687906A (zh) | ANAVEX2-73的对映体及其在治疗阿尔海默氏病和其他由σ1受体调节的疾病中的用途 | |
| AU2020214641B2 (en) | Compositions and methods for treating anxiety-related disorders | |
| RU2809163C2 (ru) | Новые комбинации антагонистов н3-рецепторов и ингибиторов обратного захвата норадреналина и их терапевтическое применение | |
| US12150924B2 (en) | Compositions and methods for treating autism | |
| NZ755661A (en) | Novel combinations of a h3 antagonist and a noradrenaline reuptake inhibitor, and the therapeutical uses thereof | |
| HK40014956A (en) | Composition of h3 antagonist and noradrenaline reuptake inhibitor and application thereof | |
| KR20190138683A (ko) | 망막병증을 치료하기 위한 조성물 및 방법 | |
| US11974992B2 (en) | Use of serotonin 5-HT1A receptor agonists to treat diseases associated with sudden unexpected death in epilepsy | |
| WO2025193971A1 (en) | Methods of treating and reducing the likelihood of developing epilepsy | |
| WO2023144166A1 (en) | Use of serotonin 5-ht1a receptor agonists to treat diseases associated with sudden unexpected death in epilepsy | |
| EA046771B1 (ru) | Композиции и способы для лечения связанных с тревожностью нарушений | |
| BR112019026660A2 (pt) | tratamento para a enxaqueca | |
| BR112019026660B1 (pt) | Uso de acetil-leucina ou seu sal para preparação demedicamento para tratar ou prevenir enxaqueca ou sintomas associados |