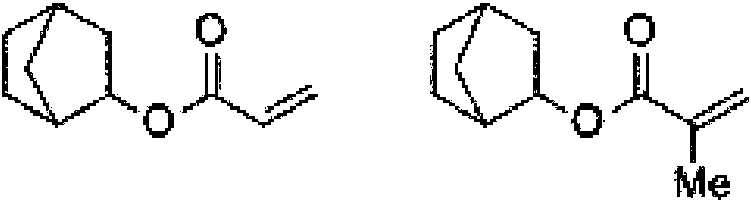ES2859667T3 - Procedimiento para la producción de ésteres de (met)acrilato de norbornilo - Google Patents
Procedimiento para la producción de ésteres de (met)acrilato de norbornilo Download PDFInfo
- Publication number
- ES2859667T3 ES2859667T3 ES18700600T ES18700600T ES2859667T3 ES 2859667 T3 ES2859667 T3 ES 2859667T3 ES 18700600 T ES18700600 T ES 18700600T ES 18700600 T ES18700600 T ES 18700600T ES 2859667 T3 ES2859667 T3 ES 2859667T3
- Authority
- ES
- Spain
- Prior art keywords
- meth
- norbornyl
- acrylic acid
- acrylate
- norbornene
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- SKKHNUKNMQLBTJ-UHFFFAOYSA-N 3-bicyclo[2.2.1]heptanyl 2-methylprop-2-enoate Chemical class C1CC2C(OC(=O)C(=C)C)CC1C2 SKKHNUKNMQLBTJ-UHFFFAOYSA-N 0.000 title claims abstract description 59
- 238000000034 method Methods 0.000 title claims abstract description 51
- 238000004519 manufacturing process Methods 0.000 title claims abstract description 13
- WTEOIRVLGSZEPR-UHFFFAOYSA-N boron trifluoride Chemical compound FB(F)F WTEOIRVLGSZEPR-UHFFFAOYSA-N 0.000 claims abstract description 90
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 claims abstract description 85
- JFNLZVQOOSMTJK-KNVOCYPGSA-N norbornene Chemical compound C1[C@@H]2CC[C@H]1C=C2 JFNLZVQOOSMTJK-KNVOCYPGSA-N 0.000 claims abstract description 64
- 229910015900 BF3 Inorganic materials 0.000 claims abstract description 46
- 239000011541 reaction mixture Substances 0.000 claims abstract description 34
- 239000003054 catalyst Substances 0.000 claims abstract description 6
- 239000000203 mixture Substances 0.000 claims description 70
- 239000003381 stabilizer Substances 0.000 claims description 54
- NWVVVBRKAWDGAB-UHFFFAOYSA-N p-methoxyphenol Chemical group COC1=CC=C(O)C=C1 NWVVVBRKAWDGAB-UHFFFAOYSA-N 0.000 claims description 40
- 239000003960 organic solvent Substances 0.000 claims description 30
- 238000004821 distillation Methods 0.000 claims description 22
- 238000000605 extraction Methods 0.000 claims description 22
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 14
- 239000001301 oxygen Substances 0.000 claims description 14
- 229910052760 oxygen Inorganic materials 0.000 claims description 14
- 150000001875 compounds Chemical class 0.000 claims description 12
- 150000002989 phenols Chemical class 0.000 claims description 6
- 125000000118 dimethyl group Chemical group [H]C([H])([H])* 0.000 claims description 4
- RTZKZFJDLAIYFH-UHFFFAOYSA-N ether Substances CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 claims description 4
- 125000004177 diethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 3
- 229950000688 phenothiazine Drugs 0.000 claims description 3
- 238000002955 isolation Methods 0.000 claims 2
- 230000009466 transformation Effects 0.000 claims 2
- 125000001033 ether group Chemical group 0.000 claims 1
- 125000001484 phenothiazinyl group Chemical group C1(=CC=CC=2SC3=CC=CC=C3NC12)* 0.000 claims 1
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 45
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 26
- 239000000243 solution Substances 0.000 description 23
- 239000012074 organic phase Substances 0.000 description 17
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 16
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 16
- 239000000047 product Substances 0.000 description 15
- 235000002639 sodium chloride Nutrition 0.000 description 15
- 235000011121 sodium hydroxide Nutrition 0.000 description 15
- NIXOWILDQLNWCW-UHFFFAOYSA-N 2-Propenoic acid Natural products OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 14
- 239000012071 phase Substances 0.000 description 14
- 239000007789 gas Substances 0.000 description 13
- DPDXVBIWZBJGSX-XUTVFYLZSA-N isoboonein Chemical compound C1C(=O)OC[C@@H]2[C@@H](C)[C@@H](O)C[C@@H]21 DPDXVBIWZBJGSX-XUTVFYLZSA-N 0.000 description 12
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 11
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 11
- 238000009835 boiling Methods 0.000 description 11
- 239000007788 liquid Substances 0.000 description 10
- 238000003756 stirring Methods 0.000 description 10
- 238000010438 heat treatment Methods 0.000 description 9
- KZMGYPLQYOPHEL-UHFFFAOYSA-N Boron trifluoride etherate Chemical compound FB(F)F.CCOCC KZMGYPLQYOPHEL-UHFFFAOYSA-N 0.000 description 8
- SKKHNUKNMQLBTJ-QIIDTADFSA-N [(1s,4r)-3-bicyclo[2.2.1]heptanyl] 2-methylprop-2-enoate Chemical compound C1C[C@H]2C(OC(=O)C(=C)C)C[C@@H]1C2 SKKHNUKNMQLBTJ-QIIDTADFSA-N 0.000 description 8
- 239000007864 aqueous solution Substances 0.000 description 8
- 238000005191 phase separation Methods 0.000 description 8
- 150000003839 salts Chemical class 0.000 description 8
- IQYMRQZTDOLQHC-ZQTLJVIJSA-N [(1R,4S)-2-bicyclo[2.2.1]heptanyl] prop-2-enoate Chemical group C1C[C@H]2C(OC(=O)C=C)C[C@@H]1C2 IQYMRQZTDOLQHC-ZQTLJVIJSA-N 0.000 description 7
- 238000000576 coating method Methods 0.000 description 7
- 238000010992 reflux Methods 0.000 description 7
- 239000011780 sodium chloride Substances 0.000 description 7
- QIGBRXMKCJKVMJ-UHFFFAOYSA-N Hydroquinone Chemical compound OC1=CC=C(O)C=C1 QIGBRXMKCJKVMJ-UHFFFAOYSA-N 0.000 description 6
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 6
- 238000005406 washing Methods 0.000 description 6
- 239000002253 acid Substances 0.000 description 5
- 238000000926 separation method Methods 0.000 description 5
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 4
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M Potassium chloride Chemical compound [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 description 4
- 239000006227 byproduct Substances 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 229920001577 copolymer Polymers 0.000 description 4
- 238000002474 experimental method Methods 0.000 description 4
- -1 for example Substances 0.000 description 4
- 230000036316 preload Effects 0.000 description 4
- 238000007639 printing Methods 0.000 description 4
- OPLCSTZDXXUYDU-UHFFFAOYSA-N 2,4-dimethyl-6-tert-butylphenol Chemical compound CC1=CC(C)=C(O)C(C(C)(C)C)=C1 OPLCSTZDXXUYDU-UHFFFAOYSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 238000001816 cooling Methods 0.000 description 3
- 238000004508 fractional distillation Methods 0.000 description 3
- 239000000976 ink Substances 0.000 description 3
- 150000002990 phenothiazines Chemical class 0.000 description 3
- 238000006116 polymerization reaction Methods 0.000 description 3
- 235000017557 sodium bicarbonate Nutrition 0.000 description 3
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- WJFKNYWRSNBZNX-UHFFFAOYSA-N 10H-phenothiazine Chemical compound C1=CC=C2NC3=CC=CC=C3SC2=C1 WJFKNYWRSNBZNX-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical compound [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 2
- LCGLNKUTAGEVQW-UHFFFAOYSA-N Dimethyl ether Chemical compound COC LCGLNKUTAGEVQW-UHFFFAOYSA-N 0.000 description 2
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 2
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 2
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- 239000003377 acid catalyst Substances 0.000 description 2
- 150000001252 acrylic acid derivatives Chemical class 0.000 description 2
- 150000005215 alkyl ethers Chemical class 0.000 description 2
- 235000019270 ammonium chloride Nutrition 0.000 description 2
- 239000000010 aprotic solvent Substances 0.000 description 2
- 229910052796 boron Inorganic materials 0.000 description 2
- YCIMNLLNPGFGHC-UHFFFAOYSA-N catechol Chemical compound OC1=CC=CC=C1O YCIMNLLNPGFGHC-UHFFFAOYSA-N 0.000 description 2
- 239000003086 colorant Substances 0.000 description 2
- 239000000470 constituent Substances 0.000 description 2
- 150000002170 ethers Chemical class 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 239000012467 final product Substances 0.000 description 2
- 238000004817 gas chromatography Methods 0.000 description 2
- 239000007791 liquid phase Substances 0.000 description 2
- 238000000622 liquid--liquid extraction Methods 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 239000003880 polar aprotic solvent Substances 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- 239000001103 potassium chloride Substances 0.000 description 2
- 235000011164 potassium chloride Nutrition 0.000 description 2
- WQGWDDDVZFFDIG-UHFFFAOYSA-N pyrogallol Chemical compound OC1=CC=CC(O)=C1O WQGWDDDVZFFDIG-UHFFFAOYSA-N 0.000 description 2
- GHMLBKRAJCXXBS-UHFFFAOYSA-N resorcinol Chemical compound OC1=CC=CC(O)=C1 GHMLBKRAJCXXBS-UHFFFAOYSA-N 0.000 description 2
- 238000000638 solvent extraction Methods 0.000 description 2
- 230000006641 stabilisation Effects 0.000 description 2
- 238000011105 stabilization Methods 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 238000005292 vacuum distillation Methods 0.000 description 2
- PJYUCLOYEILMHQ-UHFFFAOYSA-N 1,2-bis(1-phenylethyl)-10h-phenothiazine Chemical compound C=1C=C2SC3=CC=CC=C3NC2=C(C(C)C=2C=CC=CC=2)C=1C(C)C1=CC=CC=C1 PJYUCLOYEILMHQ-UHFFFAOYSA-N 0.000 description 1
- HECLRDQVFMWTQS-RGOKHQFPSA-N 1755-01-7 Chemical compound C1[C@H]2[C@@H]3CC=C[C@@H]3[C@@H]1C=C2 HECLRDQVFMWTQS-RGOKHQFPSA-N 0.000 description 1
- QTWJRLJHJPIABL-UHFFFAOYSA-N 2-methylphenol;3-methylphenol;4-methylphenol Chemical compound CC1=CC=C(O)C=C1.CC1=CC=CC(O)=C1.CC1=CC=CC=C1O QTWJRLJHJPIABL-UHFFFAOYSA-N 0.000 description 1
- STGFANHLXUILNY-UHFFFAOYSA-N 3,7-dioctyl-10h-phenothiazine Chemical compound C1=C(CCCCCCCC)C=C2SC3=CC(CCCCCCCC)=CC=C3NC2=C1 STGFANHLXUILNY-UHFFFAOYSA-N 0.000 description 1
- UZFMOKQJFYMBGY-UHFFFAOYSA-N 4-hydroxy-TEMPO Chemical group CC1(C)CC(O)CC(C)(C)N1[O] UZFMOKQJFYMBGY-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 description 1
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 239000002841 Lewis acid Substances 0.000 description 1
- 239000004820 Pressure-sensitive adhesive Substances 0.000 description 1
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 1
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical compound [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 1
- LVZGQWKTUCVPBQ-UHFFFAOYSA-N acetic acid;trifluoroborane Chemical class CC(O)=O.FB(F)F LVZGQWKTUCVPBQ-UHFFFAOYSA-N 0.000 description 1
- MEMUCXUKCBNISQ-UHFFFAOYSA-N acetonitrile;trifluoroborane Chemical class CC#N.FB(F)F MEMUCXUKCBNISQ-UHFFFAOYSA-N 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 125000000217 alkyl group Chemical group 0.000 description 1
- DIZPMCHEQGEION-UHFFFAOYSA-H aluminium sulfate (anhydrous) Chemical compound [Al+3].[Al+3].[O-]S([O-])(=O)=O.[O-]S([O-])(=O)=O.[O-]S([O-])(=O)=O DIZPMCHEQGEION-UHFFFAOYSA-H 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- BFNBIHQBYMNNAN-UHFFFAOYSA-N ammonium sulfate Chemical compound N.N.OS(O)(=O)=O BFNBIHQBYMNNAN-UHFFFAOYSA-N 0.000 description 1
- 229910052921 ammonium sulfate Inorganic materials 0.000 description 1
- 235000011130 ammonium sulphate Nutrition 0.000 description 1
- 235000013405 beer Nutrition 0.000 description 1
- 235000010354 butylated hydroxytoluene Nutrition 0.000 description 1
- AXCZMVOFGPJBDE-UHFFFAOYSA-L calcium dihydroxide Chemical compound [OH-].[OH-].[Ca+2] AXCZMVOFGPJBDE-UHFFFAOYSA-L 0.000 description 1
- 239000000920 calcium hydroxide Substances 0.000 description 1
- 229910001861 calcium hydroxide Inorganic materials 0.000 description 1
- 235000011116 calcium hydroxide Nutrition 0.000 description 1
- 235000013877 carbamide Nutrition 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 229960001701 chloroform Drugs 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 230000009918 complex formation Effects 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- KGGZTXSNARMULX-UHFFFAOYSA-L copper;dicarbamodithioate Chemical class [Cu+2].NC([S-])=S.NC([S-])=S KGGZTXSNARMULX-UHFFFAOYSA-L 0.000 description 1
- 238000005260 corrosion Methods 0.000 description 1
- 230000007797 corrosion Effects 0.000 description 1
- 229930003836 cresol Natural products 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 238000003795 desorption Methods 0.000 description 1
- CKJMHSMEPSUICM-UHFFFAOYSA-N di-tert-butyl nitroxide Chemical class CC(C)(C)N([O])C(C)(C)C CKJMHSMEPSUICM-UHFFFAOYSA-N 0.000 description 1
- ISRJTGUYHVPAOR-UHFFFAOYSA-N dihydrodicyclopentadienyl acrylate Chemical compound C1CC2C3C(OC(=O)C=C)C=CC3C1C2 ISRJTGUYHVPAOR-UHFFFAOYSA-N 0.000 description 1
- 238000006471 dimerization reaction Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 239000011552 falling film Substances 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 239000010408 film Substances 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 238000009413 insulation Methods 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 150000003951 lactams Chemical class 0.000 description 1
- 150000007517 lewis acids Chemical class 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 239000007769 metal material Substances 0.000 description 1
- 238000010327 methods by industry Methods 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 150000002825 nitriles Chemical class 0.000 description 1
- 150000002828 nitro derivatives Chemical class 0.000 description 1
- LYGJENNIWJXYER-UHFFFAOYSA-N nitromethane Chemical compound C[N+]([O-])=O LYGJENNIWJXYER-UHFFFAOYSA-N 0.000 description 1
- 150000002832 nitroso derivatives Chemical class 0.000 description 1
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 1
- CHNLPLHJUPMEOI-UHFFFAOYSA-N oxolane;trifluoroborane Chemical class FB(F)F.C1CCOC1 CHNLPLHJUPMEOI-UHFFFAOYSA-N 0.000 description 1
- 238000012856 packing Methods 0.000 description 1
- 239000003973 paint Substances 0.000 description 1
- 150000004986 phenylenediamines Chemical class 0.000 description 1
- 239000011736 potassium bicarbonate Substances 0.000 description 1
- 235000015497 potassium bicarbonate Nutrition 0.000 description 1
- 229910000028 potassium bicarbonate Inorganic materials 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- 235000011181 potassium carbonates Nutrition 0.000 description 1
- TYJJADVDDVDEDZ-UHFFFAOYSA-M potassium hydrogencarbonate Chemical compound [K+].OC([O-])=O TYJJADVDDVDEDZ-UHFFFAOYSA-M 0.000 description 1
- 235000011118 potassium hydroxide Nutrition 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 229940079877 pyrogallol Drugs 0.000 description 1
- 238000007650 screen-printing Methods 0.000 description 1
- 239000000565 sealant Substances 0.000 description 1
- 239000002453 shampoo Substances 0.000 description 1
- 229910052938 sodium sulfate Inorganic materials 0.000 description 1
- 235000011152 sodium sulphate Nutrition 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 150000003462 sulfoxides Chemical class 0.000 description 1
- 150000003860 tertiary carboxamides Chemical class 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 239000010409 thin film Substances 0.000 description 1
- 150000003585 thioureas Chemical class 0.000 description 1
- MVJKXJPDBTXECY-UHFFFAOYSA-N trifluoroborane;hydrate Chemical class O.FB(F)F MVJKXJPDBTXECY-UHFFFAOYSA-N 0.000 description 1
- 150000003672 ureas Chemical class 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C67/00—Preparation of carboxylic acid esters
- C07C67/48—Separation; Purification; Stabilisation; Use of additives
- C07C67/62—Use of additives, e.g. for stabilisation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C67/00—Preparation of carboxylic acid esters
- C07C67/04—Preparation of carboxylic acid esters by reacting carboxylic acids or symmetrical anhydrides onto unsaturated carbon-to-carbon bonds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C67/00—Preparation of carboxylic acid esters
- C07C67/04—Preparation of carboxylic acid esters by reacting carboxylic acids or symmetrical anhydrides onto unsaturated carbon-to-carbon bonds
- C07C67/05—Preparation of carboxylic acid esters by reacting carboxylic acids or symmetrical anhydrides onto unsaturated carbon-to-carbon bonds with oxidation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C67/00—Preparation of carboxylic acid esters
- C07C67/48—Separation; Purification; Stabilisation; Use of additives
- C07C67/52—Separation; Purification; Stabilisation; Use of additives by change in the physical state, e.g. crystallisation
- C07C67/54—Separation; Purification; Stabilisation; Use of additives by change in the physical state, e.g. crystallisation by distillation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C69/00—Esters of carboxylic acids; Esters of carbonic or haloformic acids
- C07C69/52—Esters of acyclic unsaturated carboxylic acids having the esterified carboxyl group bound to an acyclic carbon atom
- C07C69/533—Monocarboxylic acid esters having only one carbon-to-carbon double bond
- C07C69/54—Acrylic acid esters; Methacrylic acid esters
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2602/00—Systems containing two condensed rings
- C07C2602/36—Systems containing two condensed rings the rings having more than two atoms in common
- C07C2602/40—Systems containing two condensed rings the rings having more than two atoms in common the bicyclo ring system containing six carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2602/00—Systems containing two condensed rings
- C07C2602/36—Systems containing two condensed rings the rings having more than two atoms in common
- C07C2602/42—Systems containing two condensed rings the rings having more than two atoms in common the bicyclo ring system containing seven carbon atoms
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Crystallography & Structural Chemistry (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Catalysts (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Abstract
Procedimiento para la producción de (met)acrilato de norbornilo mediante reacción de norborneno con ácido (met)acrílico en presencia de trifluoruro de boro como catalizador, caracterizado porque a) se precarga trifluoruro de boro en ácido (met)acrílico, b) se calienta la carga previa a una temperatura de 75 a 110°C, c) se añade norborneno y d) se aísla el (met)acrilato de norbornilo obtenido de la mezcla de reacción.
Description
DESCRIPCIÓN
Procedimiento para la producción de ésteres de (met)acrilato de norbornilo
La presente invención se refiere a la producción de (met)acrilato de norbornilo. En el procedimiento conforme a la invención se transforman norborneno y ácido (met)acrílico en presencia de trifluoruro de boro.
El (met)acrilato de norbornilo se usa, por ejemplo, para producir copolímeros. Los copolímeros conteniendo (met)acrilato de norbornilo como comonómero en forma copolimerizada se utilizan, por ejemplo, como componente de composiciones curables. Las composiciones curables se utilizan en adhesivos, selladores, colores de impresión, tintas de impresión, así como en recubrimientos para electrónica, en recubrimientos en el campo de la industria automovilística y en general en el sector industrial.
Los procedimientos para la producción de (met)acrilato de norbornilo a partir de ácido (met)acrílico y norborneno son conocidos para el experto gracias al estado actual de la técnica. En general, la adición de ácido (met)acrílico a norborneno se lleva a cabo en presencia de un catalizador ácido. Como catalizadores ácidos sirven, por ejemplo, ácidos de Lewis como trifluoruro de boro o sus complejos.
En la Revista Rusa de Química Orgánica (Russian Journal of Organic Chemistry) (2010, Vol. 46, pág. 628-630) se describe la adición de ácido acrílico a norborneno en presencia de eterato dietílico de trifluoruro de boro. Según el ejemplo mostrado, se precargan norborneno, ácido acrílico y eterato dietílico de trifluoruro de boro y se calienta. El (met)acrilato de norbornilo se aísla a continuación de la mezcla de reacción mediante destilación fraccionada con un rendimiento del 80%.
La DE 1954548 A1 (BASF AG) revela un procedimiento para la producción de acrilato de dihidrodiciclopentadienilo agregando diciclopentadieno a una mezcla de ácido acrílico, hidroquinona y eterato dimetílico de trifluoruro de boro a una temperatura entre 70 y 80° C (Ejemplo 1). El producto se aísla lavándolo con agua.
El objeto era proporcionar un procedimiento mejorado para la producción de (met)acrilato de norbornilo. Mediante el procedimiento mejorado debería ser posible producir (met)acrilato de norbornilo con altos selectividad, rendimiento y pureza. Además, era deseable que el (met)acrilato de norbornilo pudiera aislarse a sólo bajo coste con altos pureza y rendimiento. Así es, por ejemplo, ventajoso que el (met)acrilato de norbornilo pueda aislarse de la mezcla de reacción sin destilación fraccionada con altos pureza y rendimiento.
El objeto se resuelve con un procedimiento para la producción de (met)acrilato de norbornilo mediante reacción de norborneno con ácido (met)acrílico en presencia de trifluoruro de boro como catalizador, caracterizado porque a) se precarga trifluoruro de boro en ácido (met)acrílico,
b) se calienta la carga previa a una temperatura de 75 a 110° C,
c) se añade norborneno
y
d) se aísla el (met)acrilato de norbornilo obtenido de la mezcla de reacción.
El objeto se resuelve también con un procedimiento para la producción de (met)acrilato de norbornilo mediante reacción de norborneno con ácido (met)acrílico en presencia de trifluoruro de boro como catalizador, caracterizado porque
a) se precarga trifluoruro de boro en un disolvente orgánico,
b) se calienta la carga previa a una temperatura de 75 a 110° C,
c) se añade una mezcla conteniendo norborneno y ácido (met)acrílico y
d) se aísla el (met)acrilato de norbornilo obtenido de la mezcla de reacción.
El (met)acrilato de norbornilo es acrilato de norbornilo o metacrilato de norbornilo.
El ácido (met)acrílico es ácido acrílico o ácido metacrílico. El ácido (met)acrílico usado en el procedimiento conforme a la invención es generalmente lo más puro posible. el ácido (met)acrílico lo más puro posible tiene una pureza de al menos un 95 por ciento en peso. Se prefiere que el ácido (met)acrílico usado en el procedimiento conforme a la invención tenga una pureza de al menos un 97 por ciento en peso y más preferentemente una pureza de al menos un 99 por ciento en peso.
En el procedimiento conforme a la invención se utiliza ácido (met)acrílico en una cantidad del 100 al 1000 por ciento molar, preferentemente del 105 al 750 por ciento molar y de manera especialmente preferente del 110 al 250 por ciento molar, relativo a la cantidad de norborneno.
Incluso cuando pueda usarse ácido (met)acrílico sin estabilizador en el procedimiento conforme a la invención, generalmente se prefiere que el ácido (met)acrílico empleado contenga un estabilizador o una mezcla de diferentes estabilizadores. Un estabilizador o una mezcla de diferentes estabilizadores sirve en general para inhibir la polimerización del ácido (met)acrílico o los correspondientes ésteres.
La cantidad de estabilizador contenida en el ácido (met)acrílico utilizado depende generalmente del tipo de estabilizador utilizado, o del tipo de estabilizadores utilizados, si se utiliza una mezcla de diferentes estabilizadores. Generalmente, la cantidad de estabilizador contenida en el ácido (met)acrílico usado es de 50 a 1000 ppm, preferentemente de 100 a 800 ppm y más preferentemente de 150 a 300 ppm.
Los estabilizadores que inhiben la polimerización del ácido (met)acrílico son conocidos por el experto o puede deducirlos de sus conocimientos especializados generales. Los estabilizadores conocidos son, por ejemplo, (met)acrilatos de cobre, ditiocarbamatos de cobre, fenotiazinas, compuestos fenólicos, N-oxilos, fenilendiaminas, compuestos nitrosos, ureas o tioureas. Estos estabilizadores se pueden usar individualmente o como cualquier mezcla. Los estabilizadores preferidos son fenotiazinas, compuestos fenólicos, N-oxilos o cualquier mezcla de estos. Las fenotiazinas pueden ser, por ejemplo, fenotiazina, bis-(a-metilbencil)fenotiazina, 3,7-dioctilfenotiazina, bis-(adimetilbencil)fenotiazina o cualquier mezcla de estas.
Los compuestos fenólicos pueden ser, por ejemplo, hidroquinona, éteres monometílicos de hidroquinona, como para-metoxifenol (MEHQ), pirogalol, catecol, resorcinol, fenol, cresol, 2,4-dimetil-6-terc-butilfenol, 2,6-di-terc-butilpara-cresol o cualquier mezcla de estos. Los compuestos fenólicos preferidos son para-metoxifenol (MEHQ), 2,4-dimetil-6-terc-butilfenol, 2,6-di-terc-butil-para-cresol o cualquier mezcla de estos. Se prefiere particularmente el parametoxifenol (MEHQ).
Los N-oxilos pueden ser, por ejemplo, nitróxido de di-terc-butilo, 2,2,6,6-tetrametil-4-hidroxipiperidil-1-oxilo, 2,2,6,6-tetrametilpiperidil-1-oxilo, 2,2,6,6-tetrametilpiperidinoxilo, 4-hidroxi-2,2,6,6-tetrametilpiperidinoxilo, fosfitos de 4,4',4"-tris-1 -(2,2,6,6-tetrametilpiperidinoxilo), o cualquier mezcla de estos.
Se prefiere especialmente que el ácido (met)acrílico utilizado en el procedimiento conforme a la invención esté estabilizado con para-metoxifenol (MEHQ). La cantidad de MEHQ en el ácido (met)acrílico usado en el procedimiento conforme a la invención es preferentemente de 150 a 300 ppm.
El norborneno se utiliza con la mayor pureza posible en el procedimiento conforme a la invención. En general, se usa norborneno con una pureza de al menos un 90 por ciento en peso. Se prefiere usar el norborneno con una pureza de al menos un 95 por ciento en peso y más preferentemente con una pureza de al menos el 97 por ciento en peso. La producción de norborneno con la pureza adecuada es conocida por el experto o puede deducirla de sus conocimientos especializados generales.
Según el procedimiento conforme a la invención, en el paso a) se precarga trifluoruro de boro en ácido (met)acrílico o en un disolvente orgánico. Generalmente, el ácido (met)acrílico o el disolvente orgánico está en fase líquida y el trifluoruro de boro se añade a la fase líquida existente. Se prefiere que el trifluoruro de boro se precargue en ácido (met)acrílico o en un disolvente orgánico a una temperatura de 15 a 50°C. Se prefiere además que el trifluoruro de boro se precargue en ácido (met)acrílico o en un disolvente orgánico a una temperatura de 20 a 35°C.
El trifluoruro de boro se precarga en ácido (met)acrílico o en un disolvente orgánico preferentemente en presencia de oxígeno. Así puede precargarse el trifluoruro de boro, por ejemplo, en presencia de un gas conteniendo oxígeno, como aire, aire pobre o aire seco, en ácido (met)acrílico o en un disolvente orgánico. En el contexto del procedimiento conforme a la invención, la presencia de oxígeno ha demostrado en general ser ventajosa, ya que de este modo se influye positivamente sobre la inhibición de la polimerización del ácido (met)acrílico utilizado y/o del (met)acrilato de norbornilo producido.
En general, el trifluoruro de boro se suministra en forma gaseosa o como complejo del ácido (met)acrílico precargado o del disolvente orgánico precargado. Si se suministra trifluoruro de boro gaseoso, es ventajoso que se introduzca trifluoruro de boro en el ácido (met)acrílico precargado o en el disolvente orgánico precargado. La introducción puede realizarse, por ejemplo, a través de uno o más tubos de inmersión o boquillas, resistentes a la corrosión por trifluoruro de boro. La introducción de trifluoruro de boro gaseoso en el ácido (met)acrílico precargado o en el disolvente orgánico precargado puede provocar la formación de complejos. Si se añade trifluoruro de boro como complejo al ácido (met)acrílico precargado o al disolvente orgánico precargado, puede producirse una recomplejación.
Los complejos de trifluoruro de boro son, por ejemplo, eteratos de trifluoruro de boro, complejos de trifluoruro de boro-acetonitrilo, hidratos de trifluoruro de boro, complejos de trifluoruro de boro-ácido carboxílico, como complejos de trifluoruro de boro-ácido acético o complejos de trifluoruro de boro-ácido (met)acrílico o cualquier mezcla de estos complejos. Se prefieren los eteratos de trifluoruro de boro. Los eteratos de trifluoruro de boro pueden ser, por ejemplo, eterato dimetílico de trifluoruro de boro, eterato dietílico de trifluoruro de boro, complejos de trifluoruro de boro-tetrahidrofurano o cualquier mezcla de estos. Entre los eteratos de trifluoruro de boro, se prefieren el eterato dimetílico de trifluoruro de boro y/o el eterato dietílico de trifluoruro de boro. Se prefiere especialmente el eterato dimetílico de trifluoruro de boro.
Si se alimenta trifluoruro de boro como complejo al ácido (met)acrílico o al disolvente orgánico precargado, el complejo puede estar disuelto en un disolvente. El disolvente suele ser el compuesto que se utilizó para formar el complejo.
En el procedimiento conforme a la invención, el trifluoruro de boro se utiliza en una cantidad del 0,1 al 5 por ciento molar, preferentemente en una cantidad del 0,2 al 2,5 por ciento molar y más preferentemente en una cantidad del 0,5 al 1,5 por ciento molar, relativo a la cantidad de norborneno. Así puede utilizarse trifluoruro de boro, por ejemplo, en una cantidad del 0,6, 0,7, 0,8, 0,9, 1,0, 1,1, 1,2, 1,3 ó 1,4 por ciento molar, relativo a la cantidad de norborneno. Como disolvente orgánico, en el que se precarga el trifluoruro de boro, sirven en principio todos los disolventes orgánicos que no entran en reacciones no deseadas con los materiales de partida, el catalizador y los productos ni conducen a la formación indeseada de subproductos. Es ventajoso que el punto de ebullición del disolvente orgánico esté por encima de 75°C a presión normal.
Como disolventes orgánicos, se pueden utilizar disolventes apróticos polares, disolventes apróticos apolares, ácido (met)acrílico, (met)acrilato de norbornilo o cualquier mezcla de estos. Los disolventes apróticos polares pueden ser, por ejemplo, nitrilos como acetonitrilo, nitrocompuestos como nitrometano, sulfóxidos como sulfóxido de dimetilo, lactamas como N-metil-2-pirrolidona, carboxamidas terciarias como dimetilformamida, cetonas, diclorometano, triclorometano o cualquier mezcla de estos. Los disolventes apróticos apolares pueden ser, por ejemplo, éteres como éteres de alquilo, tolueno o cualquier mezcla de estos. Los éteres de alquilo pueden ser, por ejemplo, éter dimetílico, éter dietílico, éter metil-terc-butílico, tetrahidrofurano, 1,4-dioxano o cualquier mezcla de estos. No se ha demostrado ventajoso el uso de norborneno como disolvente orgánico. Los disolventes orgánicos preferidos son: ácido (met)acrílico, (met)acrilato de norbornilo, éteres, donde se prefiere el 1,4-dioxano o cualquier mezcla de estos. También puede añadirse un estabilizador o una mezcla de diferentes estabilizadores al ácido (met)acrílico precargado o al disolvente orgánico precargado. Si también se añade un estabilizador o una mezcla de diferentes estabilizadores al ácido (met)acrílico precargado o al disolvente orgánico precargado, esto se hace generalmente antes de añadir trifluoruro de boro al ácido (met)acrílico precargado o al disolvente orgánico precargado.
La cantidad de estabilizador que se añade al ácido (met)acrílico precargado o al disolvente orgánico precargado depende del tipo de estabilizador o del tipo de mezcla de diferentes estabilizadores. En general, la cantidad de estabilizador que se añade adicionalmente es del 0,005 al 0,15 y preferentemente del 0,05 al 0,15 por ciento molar, referido a la cantidad de ácido (met)acrílico utilizado en el procedimiento conforme a la invención.
Como estabilizador se pueden utilizar los estabilizadores mencionados anteriormente. Generalmente es ventajoso utilizar el estabilizador o la mezcla de diferentes estabilizadores que ya están contenidos en el ácido (met)acrílico utilizado en el procedimiento conforme a la invención. Por consiguiente, se prefiere que se añada adicionalmente MEHQ al ácido (met)acrílico precargado o al disolvente orgánico precargado.
En configuraciones preferidas del procedimiento, el trifluoruro de boro se precarga en ácido (met)acrílico, (met)acrilato de norbornilo o en 1,4-dioxano. El trifluoruro de boro se precarga además en forma gaseosa o como complejo, preferentemente como eterato dimetílico o como eterato dietílico. La temperatura a la que se precarga el trifluoruro de boro en ácido (met)acrílico, (met)acrilato de norbornilo o en 1,4-dioxano es de 15 a 50°C. La temperatura puede valer, por ejemplo, 18, 20, 22, 24, 26, 28, 30, 32 ó 35°C. En otras configuraciones preferidas del procedimiento, el trifluoruro de boro se precarga en ácido (met)acrílico, (met)acrilato de norbornilo o en 1,4-dioxano. El trifluoruro de boro se precarga en forma gaseosa o como complejo, preferentemente como eterato dimetílico o como eterato dietílico, en una cantidad del 0,5 al 1,5 por ciento molar, relativo a la cantidad de norborneno. La temperatura a la que se precarga el trifluoruro de boro en el ácido (met)acrílico, el (met)acrilato de norbornilo o en el 1,4-dioxano es de 15 a 50°C. La temperatura puede valer, por ejemplo, 18, 20, 22, 24, 26, 28, 30, 32 ó 35°C.
Los procedimientos conformes a la invención se pueden llevar a cabo en reactores conocidos por el experto. Como reactores pueden utilizarse, por ejemplo, reactores de tanque agitado, reactores de bucle, reactores tubulares o cualquier combinación de estos. Los reactores suelen ser de material metálico, donde se prefiere el acero inoxidable.
Los reactores pueden ser reactores con calefacción de doble pared y/o serpentines de calefacción internos. Los reactores también pueden ser reactores con intercambiadores de calor externos y circulación natural o forzada (empleando una bomba). La mezcla en los reactores puede tener lugar mediante dispositivos de agitación y/o introduciendo un gas, preferentemente un gas conteniendo oxígeno.
Los procedimientos conformes a la invención se pueden llevar a cabo de forma continua o discontinua, donde se prefiere una ejecución discontinua. En general se prefieren los reactores que sirven para llevar a cabo la reacción de manera discontinua, por ejemplo, reactores de tanque agitado. Se pueden conectar varios reactores, preferentemente reactores de tanque agitado, en serie y/o en paralelo. Al seleccionar los reactores adecuados y su interconexión, el experto puede guiarse por sus conocimientos especializados generales y consideraciones prácticas.
En el paso b) del procedimiento conforme a la invención, se calienta la carga previa. La carga previa se calienta a una temperatura de 75 a 110°C, preferentemente de 80 a 105°C y más preferentemente a una temperatura de 85 a 100°C.
La carga previa generalmente se calienta en presencia de oxígeno. Así pueden alimentarse, por ejemplo, gases conteniendo oxígeno, como aire, aire pobre o aire seco, a la carga previa mientras se calienta. El gas conteniendo oxígeno que se alimenta a la carga previa durante el calentamiento generalmente se suministra al espacio de gas por encima de la carga previa. Sin embargo, el gas conteniendo oxígeno también se puede alimentar directamente a la carga previa, por ejemplo, a través de uno o más tubos de inmersión o boquillas a través de las cuales emana el gas conteniendo oxígeno.
En el paso c) del procedimiento conforme a la invención, se añade norborneno o una mezcla conteniendo norborneno y ácido (met)acrílico a la carga previa calentada. Si se agrega norborneno o una mezcla conteniendo norborneno y ácido (met)acrílico, la carga previa tiene una temperatura de 75 a 110°C, preferentemente de 80 a 105°C y más preferentemente una temperatura de 85 a 100°C.
El norborneno o una mezcla conteniendo norborneno y ácido (met)acrílico se puede agregar a la carga previa calentada una vez o gradualmente. La adición gradual se puede realizar de forma continua o discontinua. En general, el norborneno o una mezcla conteniendo norborneno y ácido (met)acrílico se añade continuamente a la carga previa calentada.
La velocidad de adición depende del calor generado por la reacción y debe elegirse además de forma que la temperatura de la carga previa no suba más de 20°C, preferentemente no más de 10°C y de manera especialmente preferente no más de 5°C.
Una adición continua de norborneno o de una mezcla conteniendo norborneno y ácido (met)acrílico puede realizarse mediante transportadores conocidos por el experto. Así puede realizarse una adición continua, por ejemplo, a través de un tornillo, una cinta transportadora, una bomba, un tambor transportador o cualquier combinación de estos. El norborneno se puede agregar a la carga previa calentada en forma sólida o líquida. El experto adapta naturalmente la selección de un medio de transporte adecuado a la naturaleza de la sustancia o mezcla de sustancias a transportar. Se prefiere añadir el norborneno a la carga previa calentada en forma líquida. El norborneno sólido se funde para este propósito. Una parte del calor necesario para esto se puede obtener, por ejemplo, integrando calor de la carga previa calentada, por ejemplo, a través del calor residual de la carga previa calentada. A continuación, el norborneno líquido se puede añadir a la carga previa calentada mediante líneas y/o medios de transporte calefactada/os.
Una mezcla conteniendo norborneno y ácido (met)acrílico se añade generalmente en forma líquida a la carga previa calentada. Para ello se puede disolver el norborneno en forma sólida o líquida en ácido (met)acrílico líquido. Además de norborneno y ácido (met)acrílico, la mezcla puede contener también un estabilizador o una mezcla de diferentes estabilizadores. Incluso cuando se use generalmente ácido (met)acrílico que ya contenga un estabilizador o una mezcla de diferentes estabilizadores, es ventajoso añadir además a la mezcla un estabilizador o una mezcla de diferentes estabilizadores. Si se añade adicionalmente un estabilizador o una mezcla de diferentes estabilizadores a la mezcla conteniendo norborneno y ácido (met)acrílico, resulta ventajoso utilizar un estabilizador o una mezcla de diferentes estabilizadores que ya estén contenidos en el ácido (met)acrílico.
La cantidad de estabilizador que se agrega adicionalmente a la mezcla conteniendo norborneno y ácido (met)acrílico depende del tipo de estabilizador o del tipo de mezcla de diferentes estabilizadores. Generalmente, la cantidad de estabilizador que se añade adicionalmente a la mezcla conteniendo norborneno y ácido (met)acrílico es del 0,005 al 0,15 y preferentemente del 0,05 al 0,15 por ciento molar, relativo a la cantidad de ácido (met)acrílico contenido en la mezcla.
Como estabilizador pueden usarse los estabilizadores mencionados anteriormente, donde se prefiere el MEHQ. La adición de norborneno o de una mezcla conteniendo norborneno y ácido (met)acrílico a la carga previa calentada se realiza favorablemente en presencia de oxígeno. Para ello, se puede alimentar un gas conteniendo oxígeno a la carga previa calentada, al espacio de gas encima de la carga previa calentada, a las líneas de alimentación y/o al flujo de alimentación de norborneno o de una mezcla conteniendo norborneno y ácido (met)acrílico. Si el gas conteniendo oxígeno se introduce en la carga previa calentada o en la corriente de alimentación de norborneno o de una mezcla conteniendo norborneno y ácido (met)acrílico, esto se puede hacer, por ejemplo, a través de uno o más tubos de inmersión o boquillas a través de lo/as cuales emana el gas conteniendo oxígeno.
Tras la reacción del componente deficitario, habitualmente norborneno, el (met)acrilato de norbornilo obtenido se aísla de la mezcla de reacción en la etapa d) del procedimiento conforme a la invención. La mezcla de reacción es la mezcla que se obtiene después de los pasos a) a c) del procedimiento conforme a la invención.
El (met)acrilato de norbornilo se puede aislar de la mezcla de reacción mediante extracción y/o separación destilativa (destilación) de los compuestos de bajo punto de ebullición.
Si el (met)acrilato de norbornilo se aísla por extracción, esto puede realizarse mediante uno o más pasos de extracción.
En general, para este fin se añade una disolución acuosa de una base a la mezcla de reacción y luego se separan las fases. La concentración de la disolución acuosa de base corresponde a las concentraciones habituales que se utilizan con fines de extracción y puede variar en un amplio intervalo. Un experto puede determinar concentraciones ventajosas mediante algunos experimentos de rutina, o puede deducirlas de sus conocimientos generales especializados o en base a consideraciones prácticas.
Una base es, por ejemplo, hidróxido sódico, hidróxido potásico, bicarbonato sódico, bicarbonato potásico, hidróxido cálcico, amoniaco, carbonato potásico o cualquier mezcla de estos. Se prefiere que la base sea hidróxido sódico. La disolución acuosa de una base puede contener adicionalmente una sal adicional. La sal adicional es, por ejemplo, cloruro sódico, cloruro potásico, cloruro amónico, sulfato amónico o cualquier mezcla de estos. Se prefiere que la sal adicional sea cloruro sódico. La cantidad de sal adicional corresponde a las concentraciones habituales que se pueden utilizar para fines de extracción. El experto puede determinar concentraciones ventajosas a través de algunos experimentos de rutina, o puede deducirlas de su conocimiento general especializado o en base a consideraciones prácticas.
La disolución acuosa de una base se añade de tal forma que la temperatura de la mezcla de reacción no suba más de 40°C y el pH sea de 10 a 14 tras la adición de la disolución acuosa de una base. El calor de neutralización se elimina en cada caso enfriando la mezcla de reacción, por ejemplo, mediante serpentines internos de enfriamiento o mediante enfriamiento de doble pared. En consecuencia, el recipiente, en el que se mezcla la mezcla de reacción con una disolución acuosa de una base, debe diseñarse correspondientemente.
Además, puede añadirse a la mezcla de reacción un disolvente orgánico poco hidrosoluble. Esto puede servir, por ejemplo, para controlar mejor la evolución de la temperatura al agregar una disolución acuosa de una base. Un disolvente orgánico, que sea poco hidrosoluble, tiene una solubilidad en agua de menos de 10 g/L de agua a 20°C, preferentemente de menos de 1 g/L de agua a 20°C.
La relación de concentraciones mezcla de reacción : disolución acuosa de una base puede variar en amplios intervalos. El experto puede determinar relaciones de concentraciones ventajosas mediante algunos experimentos de rutina, o puede deducirlas de su conocimiento general especializado o en base a consideraciones prácticas.
Para eliminar trazas de base y/o de sal de la mezcla de reacción tras la separación de fases, puede resultar ventajoso un lavado ulterior. Para ello se puede tratar la mezcla de reacción con un líquido de lavado. Un líquido de lavado es, por ejemplo, agua. Puede resultar ventajoso que el agua, como líquido de lavado, contenga una sal. Una sal es, por ejemplo, cloruro sódico, cloruro potásico, cloruro amónico, sulfato sódico, sulfato de aluminio o cualquier mezcla de estas. La cantidad de sal puede variar en un amplio rango. El experto puede determinar concentraciones ventajosas a través de algunos experimentos de rutina, o puede deducirlas de su conocimiento general especializado o en base a consideraciones prácticas.
En términos de ingeniería de procesos, para una extracción en el procedimiento conforme a la invención pueden usarse todos los procedimientos y aparatos de extracción y lavado conocidos per se, por ejemplo, los descritos en la Enciclopedia de Química Industrial de Ullman, 6a edición, versión electrónica de 1999, capítulo “extracción líquidolíquido - aparatos (Ullmann's Encyclopedia of Industrial Chemistry, 6th Ed., 1999 Electronic Release, Chapter "Liquid - Liquid Extraction - Aparatus"). Por ejemplo, estas pueden ser extracciones en una o varias etapas, preferentemente en una sola etapa, y extracciones en modo co-corriente o contracorriente. Los recipientes que sirven para la extracción son, por ejemplo, recipientes con agitación, columnas o aparatos mezcladores-decantadores.
La fase orgánica obtenida tras la extracción, que contiene (met)acrilato de norbornilo, se mezcla opcionalmente con un estabilizador o una mezcla de diferentes estabilizadores para establecer una concentración de estabilizador favorable. La concentración de estabilizador a establecer depende generalmente de la respectiva especificación del producto final y, para los (met)acrilatos de alquilo disponibles comercialmente, está en el rango de 15 a 200 ppm. Así puede resultar ventajoso establecer una concentración de estabilizador de 30, 50, 80, 100, 120, 150 ó 180 ppm. Como estabilizadores se utilizan generalmente compuestos fenólicos, como 2,6-di-terc-butil-4-metilfenol, 6-terc-butil-2,4-dimetilfenol, hidroquinona, éter monometílico de hidroquinona o cualquier mezcla de estos. Se prefiere el éter monometílico de hidroquinona (MEHQ).
Tras la extracción, la fase orgánica conteniendo (met)acrilato de norbornilo y opcionalmente un estabilizador o una mezcla de diferentes estabilizadores puede procesarse adicionalmente por métodos conocidos por el experto. para obtener (met)acrilato de norbornilo. Para ello, el (met)acrilato de norbornilo, eventualmente junto con el estabilizador o mezcla de diferentes estabilizadores, puede separarse de los demás constituyentes de la fase orgánica, por ejemplo, por destilación o desorción. Los componentes separados de la fase orgánica, preferentemente el disolvente orgánico, pueden reutilizarse, por ejemplo, en la extracción.
Si se aísla (met)acrilato de norbornilo separando los compuestos de bajo punto de ebullición por destilación, esto se puede hacer en uno o más pasos de destilación. En general, el ácido (met)acrílico sin reaccionar, opcionalmente el disolvente orgánico, el trifluoruro de boro y otros compuestos más volátiles se separan de la mezcla de reacción por destilación. El (met)acrilato de norbornilo permanece como fracción inferior. El procedimiento conforme a la invención minimiza la formación de subproductos de alto punto de ebullición, por ejemplo, subproductos que surgen de la dimerización del ácido (met)acrílico, de modo que se puede prescindir de la destilación fraccionada del (met)acrilato de norbornilo.
Dado que el propio (met)acrilato de norbornilo no tiene que aislarse por destilación y se obtiene como fracción de fondo con alta pureza, los compuestos de bajo punto de ebullición se pueden destilar en un aparato sencillo.
Para la separación por destilación de los compuestos de bajo punto de ebullición sirven generalmente todos los aparatos para la separación por destilación de mezclas de reacción conteniendo componentes líquidos. Los aparatos adecuados incluyen columnas de destilación, como columnas de bandeja, que pueden equiparse con bandejas de burbujas, placas de criba, bandejas de criba, lechos o materiales de relleno, o evaporadores de columna de banda giratoria, como evaporadores de película delgada, evaporadores de película descendente, evaporadores de circulación forzada, evaporadores Sambay, etc., y combinaciones de los mismos. Se pueden conectar uno o más pasos de destilación en serie. Los pasos de destilación se pueden realizar en el mismo o en diferentes aparatos.
Al seleccionar los rangos adecuados de temperatura y presión para la separación por destilación de los compuestos de bajo punto de ebullición, el experto en la técnica puede guiarse por las condiciones físicas de la tarea de separación (por ejemplo, curvas de presión de vapor), así como por sus conocimientos especializados generales y por consideraciones prácticas.
Es posible combinar extracción y destilación. Así, la mezcla de reacción puede, por ejemplo, someterse primero a una extracción y luego a una destilación, o viceversa. En el caso de una combinación de extracción y destilación, generalmente se prefiere someter primero la mezcla de reacción a una destilación para separar los compuestos de bajo punto de ebullición. La fracción de cola obtenida después de la separación de los compuestos de bajo punto de ebullición, conteniendo (met)acrilato de norbornilo, se puede procesar posteriormente por extracción.
El procedimiento conforme a la invención permite preparar (met)acrilato de norbornilo con alta pureza y alto rendimiento. Así puede aislarse (met)acrilato de norbornilo con una pureza de al menos el 99 por ciento en peso. El rendimiento de (met)acrilato de norbornilo es al menos del 90 por ciento.
Favorablemente, el propio (met)acrilato de norbornilo no tiene que someterse a ninguna purificación por destilación o rectificación para lograr la alta pureza. Como ya se ha dicho, el (met)acrilato de norbornilo se puede aislar con alta pureza mediante extracción y/o separación de los compuestos de bajo punto de ebullición por destilación. Esto tiene la ventaja adicional de que se puede producir y aislar (met)acrilato de norbornilo en aparatos relativamente simples. La carga térmica sobre el (met)acrilato de norbornilo durante el aislamiento también se reduce, por lo que se puede minimizar la formación de subproductos.
Para reducir el índice de color del (met)acrilato de norbornilo producido según el procedimiento conforme a la invención, puede resultar ventajoso destilar el (met)acrilato de norbornilo. Para ello, el (met)acrilato de norbornilo puede, por ejemplo, aislarse directamente de la mezcla de reacción por destilación. Si el (met)acrilato de norbornilo se aisló por extracción y/o separación de los compuestos de punto de ebullición más bajo por destilación, el (met)acrilato de norbornilo así obtenido también puede someterse a una destilación.
El (met)acrilato de norbornilo producido por el procedimiento conforme a la invención sirve, debido a su alta pureza, especialmente para la producción de homo- o copolímeros.
Los copolímeros, que contengan (met)acrilato de norbornilo en forma polimerizada, son adecuados como constituyentes de composiciones curables. Tales composiciones curables son adecuadas, por ejemplo, para su uso en adhesivos sensibles a la presión, colores de impresión, particularmente tintas de serigrafía, tintas de impresión y para pinturas, particularmente para imprimaciones, lacas de acabado, lacas de base o lacas transparentes. Dichas composiciones curables también son adecuadas para su uso en revestimientos para pantallas de LCD y LED, revestimientos para botellas de vidrio, especialmente botellas de cerveza, revestimientos para botellas de plástico, especialmente botellas de champú, revestimientos para papel térmico y revestimientos para películas reflectantes. A menos que se indique lo contrario, todas las descripciones relativas a ppm se refieren al peso total respectivo. A menos que se indique lo contrario, todas las descripciones relativas a porcentaje en peso (% en peso) se refieren al peso total respectivo.
La pureza del (met)acrilato de norbornilo se determinó mediante cromatografía de gases como se indica en la sección experimental.
Sección experimental:
La pureza se determinó mediante cromatografía de gases. Como disolvente para las muestras se utilizó diclorometano del Fab. Aldrich, pureza del 99,8%.
Como aparato se usó un cromatógrafo de gases de la empresa Hewlett Packard (7890B) con detector FID y columna de 50m CP-Sil 5 CB 50m * 0,25 mm * 0,25 mm de la empresa Agilent.
Como programa de temperatura se ajustó: inicio a 60°C, luego con 15°C/min a 280°C, 1 min a 280°C, tiempo total de ejecución 15,7 min.
[0072] El índice de color Hazen se midió con un dispositivo de medición del índice de color del Fab. Hach Lange (LICO 620) y se calculó según la DIN 5033 para iluminante estándar C y observador estándar de 2°.
Eductos utilizados:
Origen Pureza Estabilización ácido metacrílico, puro BASF >99.5% 200±20 ppm MEHQ ácido acrílico, puro BASF >99.5% 200±20 ppm MEHQ norborneno Aldrich >99%
BF3 eterato dimetílico Aldrich 59-61 % BF3
MEHQ Aldrich >99%
Dioxano Aldrich >99.5%
Origen Pureza Estabilización DCM BASF >98%
NaOH BerndKraft más puro posible
NaCl BerndKraft >99%
Ejemplo 1: acrilato de norbornilo con carga previa de acrilato de norbornilo:
En un matraz de fondo redondo de cuatro bocas de 250 ml con condensador de reflujo, agitador magnético, termómetro, embudo de goteo y entrada de aire se precargaron 5 ml de acrilato de norbornilo. Se añadieron 0,5 ml de eterato dimetílico de trifluoruro de boro. Se añadió gota a gota una disolución de 40 g de norborneno, 0,1 g de MEHQ y 61,5 g de ácido acrílico con introducción de aire (1 L/h), agitación (280 rpm) y calentamiento, de forma que la temperatura interna fuera de 90-92°C. La mezcla se agitó ulteriormente a temperatura durante 1 h. La mezcla de reacción enfriada a temperatura ambiente se mezcló con 300 mL de diclorometano y con 200 mL de una disolución al 12,5% de NaOH y se extrajo. Las fases se separaron, la fase orgánica se extrajo de nuevo con 100 mL de disolución al 12,5% de NaOH y se concentró tras la separación de fases. Se obtuvieron 71,6 g de producto (rendimiento del 94,5%) con una pureza del 99,5% en peso. El producto se estabilizó con 7 mg de MEHQ. El índice de color fue de 145 Hazen.
Ejemplo 2: acrilato de norbornilo con carga previa de dioxano:
En un matraz de fondo redondo de cuatro bocas de 250 mL con condensador de reflujo, agitador magnético, termómetro, embudo de goteo y entrada de aire se precargaron 5 mL de dioxano. Se añadieron 0,5 ml de eterato dimetílico de trifluoruro de boro. Se añadió gota a gota una disolución de 40 g de norborneno, 0,1 g de MEHQ y 61,5 g de ácido acrílico con introducción de aire (1 L/h) agitación (280 rpm) y calentamiento, de forma que la temperatura interna fuera de 90-92°C. La mezcla se agitó ulteriormente a temperatura durante 1 h. La mezcla de reacción enfriada a temperatura ambiente se mezcló con 300 mL de diclorometano y con 200 mL de una disolución al 12,5% de NaOH y se extrajo. Las fases se separaron, la fase orgánica se extrajo de nuevo con 100 mL de disolución al 12,5% de NaOH y se concentró después de la separación de fases. Se obtuvieron 65,5 g de producto (rendimiento del 92,8%) con una pureza del 99,5% en peso. El producto se estabilizó con 7 mg de MEHQ. El índice de color fue de 74 Hazen.
Ejemplo 3: metacrilato de norbornilo con carga previa de dioxano:
En un matraz de fondo redondo de cuatro bocas de 500 ml con condensador de reflujo, agitador magnético, termómetro, embudo de goteo y entrada de aire se precargaron 7,5 ml de dioxano. Se añadieron 0,9 ml de eterato dimetílico de trifluoruro de boro. Se añadió gota a gota una disolución de 75,1 g de norborneno, 0,22 g de MEHQ y 138 g de ácido metacrílico con introducción de aire (1 L/h), agitación (500 rpm) y calentamiento, de forma que la temperatura interna fuera de 90-95°C. La mezcla se agitó ulteriormente a temperatura durante 1 h. La mezcla de reacción enfriada a temperatura ambiente se mezcló con 200 mL de diclorometano y con 300 mL de una disolución al 12,5% de NaOH y se extrajo. Se separaron las fases, la fase orgánica se extrajo nuevamente con 100 mL de disolución al 12,5% de NaOH y, después de la separación de fases, se extrajo dos veces más, cada una con 100 mL de agua, se separaron las fases en cada caso y se concentró la fase orgánica. Se obtuvieron 136 g de producto (rendimiento del 94,7%) con una pureza del 99,7% en peso. El producto se estabilizó con 13,6 mg de MEHQ. El índice de color fue de 136 Hazen.
Ejemplo 4: metacrilato de norbornilo con carga previa de metacrilato de norbornilo
En un matraz de fondo redondo de cuatro bocas de 500 ml con condensador de reflujo, agitador magnético, termómetro, embudo de goteo y entrada de aire se precargaron 5 g de metacrilato de norbornilo. Se añadió 1 ml de eterato dimetílico de trifluoruro de boro. Se agregó gota a gota una disolución de 75,1 g de norborneno, 0,22 g de
MEHQ y 137,5 g de ácido metacrílico con introducción de aire (1 L/h), agitación (500 rpm) y calentamiento, de forma que la temperatura interna fuera de 95-97°C. La mezcla se agitó ulteriormente a temperatura durante 1 h. La mezcla de reacción enfriada a temperatura ambiente se mezcló con 200 mL de diclorometano y con 300 mL de una disolución al 12,5% de NaOH y se extrajo. Se separaron las fases, la fase orgánica se extrajo nuevamente con 100 mL de disolución al 12,5% de NaOH y, tras la separación de fases, se extrajo dos veces más, cada una con 100 mL de agua, las fases se separaron en cada caso y se concentró la fase orgánica. Se obtuvieron 145 g de producto (rendimiento del 97,6%) con una pureza del 99,9% en peso. El producto se estabilizó con 14,6 mg de MEHQ. El índice de color fue de 206 Hazen.
Ejemplo 5: metacrilato de norbornilo con una carga previa de ácido metacrílico:
En un matraz de fondo redondo de cuatro bocas de 2 L con accesorio estándar, agitador magnético, termómetro, embudo de goteo y entrada de aire Se precargaron 202 g de ácido metacrílico, 0,56 g de MEHQ y 2,5 mL de eterato dimetílico de trifluoruro de boro. La mezcla se calentó con agitación (500 rpm) e introducción de aire (1 L/h) y se añadió gota a gota una disolución de 275 g de norborneno y 100 g de ácido metacrílico, de forma que la temperatura interna fuera de 93-97°C. Tras concluir la adición, se continuó agitando durante 3,5 h más. El exceso de ácido se eliminó por destilación al vacío. La mezcla de reacción enfriada a temperatura ambiente se extrajo con NaOH al 30% (105 g) y las fases se separaron. A esto le siguieron dos extracciones y separaciones de fases adicionales con 250 mL de agua y 50 mL de solución salina/disolución de cloruro sódico saturada, así como 100 mL de agua y 150 mL de disolución de cloruro sódico saturada. La fase orgánica se mezcló con 50 mg de MEHQ, se concentró a 60°C hasta 5,5 mbar para eliminar las trazas de agua y opcionalmente de ácido metacrílico y luego se filtró. Se obtuvieron 493,4 g de producto (rendimiento del 93,7%) con una pureza del 99,4% en peso. El índice de color fue de 81 Hazen. Ejemplo 6: metacrilato de norbornilo con carga previa de ácido metacrílico:
En un matraz de fondo redondo de cuatro bocas de 500 ml con condensador de reflujo, agitador magnético, termómetro, embudo de goteo calefactable y entrada de aire se precargaron 54,9 g de ácido metacrílico, así como 26 mg de MEHQ. Se añadieron 0,65 ml de eterato dimetílico de trifluoruro de boro. Se añadió gota a gota norborneno fundido con introducción de aire (1 L/h), agitación (500 rpm) y calentamiento, de forma que la temperatura interna fuera de 85-105°C. La mezcla se agitó a 94°C durante 5,8 horas. La mezcla de reacción enfriada a temperatura ambiente se mezcló con 200 mL de diclorometano y con 20 g de disolución al 50% de NaOH y se extrajo. Las fases se separaron, la fase orgánica se extrajo dos veces más, cada una con 100 mL de disolución acuosa al 12,5% de cloruro sódico, las fases se separaron en cada caso y la fase orgánica se concentró a 60°C hasta 5,5 mbar para eliminar trazas de agua y, opcionalmente, de ácido metacrílico. Después de la filtración, se obtuvieron 92 g de producto (rendimiento del 96,1%) con una pureza del 99,6% en peso. El índice de color fue de 150 Hazen.
Ejemplo 7: metacrilato de norbornilo con carga previa de ácido metacrílico
En un matraz de fondo redondo de cuatro bocas de 2 L con un accesorio estándar, agitador magnético, termómetro, embudo de goteo y entrada de aire se precargaron 258 g de ácido metacrílico, 0,78 g de MEHQ, así como 2,5 ml de eterato dimetílico de trifluoruro de boro. La mezcla se calentó con agitación (500 rpm) e introducción de aire (1 L/h) y se añadió gota a gota una disolución de 275 g de norborneno y 245 g de ácido metacrílico, de forma que la temperatura interna fuera de 92-97°C. Una vez finalizada la adición, la mezcla se agitó ulteriormente durante otras 3 h. El exceso de ácido se eliminó parcialmente por destilación al vacío. La mezcla de reacción enfriada a temperatura ambiente se extrajo con NaOH al 30% (122 g) y se separaron las fases. Siguieron dos extracciones y separaciones de fases adicionales, con en cada caso 250 mL de agua y 50 mL de disolución de cloruro sódico saturada. La fase orgánica se concentró a 60°C hasta 5,5 mbar para eliminar trazas de agua y opcionalmente de ácido metacrílico y luego se filtró. Se obtuvieron 508,5 g de producto (rendimiento del 96,6%) con una pureza del 99,8% en peso. El producto final se estabilizó con 51 mg de MEHQ. El índice de color fue de 39 Hazen.
Ejemplo comparativo 1: acrilato de norbornilo con carga previa de norborneno:
En un matraz de fondo redondo de cuatro bocas de 250 mL con condensador de reflujo, agitador magnético, termómetro, embudo de goteo y entrada de aire, se precargaron y fundieron 40 g de norborneno. Se añadieron 0,1 g de MEHQ y 0,5 ml de eterato dimetílico de trifluoruro de boro. Se añadieron gota a gota 61,5 g de ácido acrílico a una temperatura interna de inicialmente 50°C. Una vez completado el goteo, la temperatura interna fue de 76°C. Se elevó la temperatura a 90°C y se agitó la mezcla ulteriormente durante 5 horas. La mezcla de reacción enfriada a temperatura ambiente se mezcló con 300 mL de diclorometano y con 250 mL de disolución al 8% de NaHCO3 y se extrajo. Se añadieron otros 30 g de NaHCO3. Las fases se separaron, la fase orgánica se extrajo nuevamente con 250 mL de disolución al 8% de NaHCO3 y se concentró tras la separación de fases. Se obtuvieron 55,3 g de producto con una pureza del 70,8% en peso.
Ejemplo 8: acrilato de norbornilo con carga previa de ácido acrílico:
En un matraz de fondo redondo de cuatro bocas de 500 ml con condensador de reflujo, agitador magnético, termómetro, embudo de goteo calefactable y entrada de aire se precargaron 76,5 g de ácido acrílico, así como 52 mg de MEHQ. Se añadieron 0,65 ml de eterato dimetílico de trifluoruro de boro. Se añadió gota a gota norborneno fundido con introducción de aire (1 L/h), agitación (500 rpm) y calentamiento, de forma que la temperatura interna fuera de 85-100°. La mezcla se agitó ulteriormente a 94°C durante 5,3 h. La mezcla de reacción enfriada a temperatura ambiente se mezcló con 20 g de una disolución al 50% de NaOH y se extrajo. Se separaron las fases, la fase orgánica se extrajo dos veces más con 100 mL de una disolución acuosa al 12,5% de cloruro sódico cada vez, se separaron las fases en cada caso y se concentró la fase orgánica a 60°C hasta 5,5 mbar para eliminar trazas de agua y opcionalmente de ácido acrílico. Después de la filtración, se obtuvieron 91 g de producto (rendimiento del 95,1%) con una pureza del 97% en peso. El índice de color fue de 34 Hazen.
Claims (14)
1. Procedimiento para la producción de (met)acrilato de norbornilo mediante reacción de norborneno con ácido (met)acrílico en presencia de trifluoruro de boro como catalizador, caracterizado porque
a) se precarga trifluoruro de boro en ácido (met)acrílico,
b) se calienta la carga previa a una temperatura de 75 a 110°C,
c) se añade norborneno
y
d) se aísla el (met)acrilato de norbornilo obtenido de la mezcla de reacción.
2. Procedimiento para la producción de (met)acrilato de norbornilo mediante reacción de norborneno con ácido (met)acrílico en presencia de trifluoruro de boro como catalizador, caracterizado porque
a) se precarga trifluoruro de boro en un disolvente orgánico,
b) se calienta la carga previa a una temperatura de 75 a 110°C,
c) se añade una mezcla conteniendo norborneno y ácido (met)acrílico
y
d) se aísla el (met)acrilato de norbornilo obtenido de la mezcla de reacción.
3. Procedimiento según la reivindicación 1 ó 2, caracterizado porque se emplea trifluoruro de boro en una cantidad del 0,1 al 5 por ciento molar, relativo a la cantidad de norborneno.
4. Procedimiento según una de las reivindicaciones 1 a 3, caracterizado porque se emplea trifluoruro de boro en una cantidad del 0,5 al 1,5 por ciento molar, relativo a la cantidad de norborneno.
5. Procedimiento según una de las reivindicaciones 1 a 4, caracterizado porque se emplea trifluoruro de boro como eterato dietílico, eterato dimetílico o cualquier mezcla de estos.
6. Procedimiento según una de las reivindicaciones 2 a 5, caracterizado porque el disolvente orgánico es éter, (met)acrilato de norbornilo, ácido (met)acrílico o cualquier mezcla de estos.
7. Procedimiento según la reivindicación 6, caracterizado porque el disolvente orgánico es ácido (met)acrílico.
8. Procedimiento según una de las reivindicaciones 1 a 7, caracterizado porque la transformación tiene lugar en presencia de un estabilizador y el estabilizador es fenotiazina, uno o varios compuestos fenólicos, uno o varios N-oxilos o cualquier mezcla estos.
9. Procedimiento según la reivindicación 8, caracterizado porque el estabilizador es para-metoxifenol (MEHQ).
10. Procedimiento según una de las reivindicaciones 1 a 9, caracterizado porque la transformación tiene lugar en presencia de oxígeno.
11. Procedimiento según una de las reivindicaciones 1 a 10, caracterizado porque se utiliza ácido (met)acrílico en una cantidad del 100 al 1000 por ciento molar, relativo a la cantidad de norborneno.
12. Procedimiento según una de las reivindicaciones 1 a 11, caracterizado porque el aislamiento del (met)acrilato de norbornilo de la mezcla de reacción comprende uno o varios pasos de extracción.
13. Procedimiento según una de las reivindicaciones 1 a 12, caracterizado porque el aislamiento del (met)acrilato de norbornilo de la mezcla de reacción comprende la separación de los compuestos más volátiles por destilación.
14. Procedimiento según la reivindicación 12 ó 13, caracterizado porque el (met)acrilato de norbornilo así aislado presenta una pureza de al menos un 99 por ciento en peso.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP17153566 | 2017-01-27 | ||
| PCT/EP2018/051381 WO2018138025A1 (de) | 2017-01-27 | 2018-01-22 | Verfahren zur herstellung von (meth)acrylsäurenorbornylestern |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2859667T3 true ES2859667T3 (es) | 2021-10-04 |
Family
ID=57909543
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES18700600T Active ES2859667T3 (es) | 2017-01-27 | 2018-01-22 | Procedimiento para la producción de ésteres de (met)acrilato de norbornilo |
Country Status (15)
| Country | Link |
|---|---|
| US (1) | US11028040B2 (es) |
| EP (1) | EP3573946B1 (es) |
| JP (1) | JP6768973B2 (es) |
| KR (1) | KR102112235B1 (es) |
| CN (1) | CN110198925B (es) |
| AU (1) | AU2018213816B2 (es) |
| BR (1) | BR112019015152B1 (es) |
| CA (1) | CA3050038C (es) |
| ES (1) | ES2859667T3 (es) |
| MX (1) | MX2019008908A (es) |
| MY (1) | MY197504A (es) |
| RU (1) | RU2730856C1 (es) |
| SG (1) | SG11201906488RA (es) |
| WO (1) | WO2018138025A1 (es) |
| ZA (1) | ZA201905540B (es) |
Family Cites Families (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE1954548C3 (de) * | 1969-10-30 | 1975-11-13 | Basf Ag, 6700 Ludwigshafen | Verfahren zur Herstellung von Dihydrodicyclopentadienylacrylat aus Dicyclopentadien und Acrylsäure in Gegenwart saurer Katalysatoren |
| US4319009A (en) * | 1978-01-03 | 1982-03-09 | The Dow Chemical Company | Cycloaliphatic acrylate compositions |
| JPH03148239A (ja) * | 1989-11-02 | 1991-06-25 | Mitsui Petrochem Ind Ltd | カルボン酸多環式アルキルエステルの製造方法 |
| JPH0413647A (ja) * | 1990-04-27 | 1992-01-17 | Tosoh Corp | 脂環式化合物の(メタ)アクリレートの製造方法 |
| JPH08134015A (ja) * | 1994-11-04 | 1996-05-28 | Idemitsu Petrochem Co Ltd | メチルノルボルネン(メタ)アクリレート及びその製造方法、並びに感光性樹脂組成物 |
| JP4163400B2 (ja) * | 2000-07-28 | 2008-10-08 | 三菱化学株式会社 | (メタ)アクリル酸エステルの製造方法 |
| JP2004210732A (ja) * | 2003-01-06 | 2004-07-29 | Fuji Photo Film Co Ltd | 不飽和モノカルボン酸エステルの製造方法、光学部材用重合性組成物および光学部材 |
| CN101010286A (zh) * | 2004-08-19 | 2007-08-01 | 三菱化学株式会社 | 2-甲基金刚烷-2-基(甲基)丙烯酸酯的制造方法以及2-甲基金刚烷-2-基(甲基)丙烯酸酯 |
| CN101348543B (zh) | 2008-07-28 | 2011-01-26 | 北京大学 | 一种单体组合物的制备方法 |
| CN102108051A (zh) * | 2010-12-03 | 2011-06-29 | 上海博康精细化工有限公司 | 冰片烯酯及其制备方法 |
| BR112017018072A2 (pt) | 2015-02-26 | 2018-04-10 | Basf Se | processo para preparação de di(met)acrilato de isossorbida através da transesterificação de (met)acrilato de alquila com isossorbida, e, uso de di(met)acrilato de isossorbida. |
| ES2745682T3 (es) | 2015-02-26 | 2020-03-03 | Basf Se | Procedimiento para la preparación de di(met)acrilato de etoxilato de isosorbida |
| MX2017011245A (es) | 2015-03-03 | 2017-11-01 | Basf Se | Metodo para producir una estructura tridimensional mediante el uso de dos materiales de soporte preliminares. |
| CA2977868A1 (en) | 2015-03-03 | 2016-09-09 | Basf Se | Method for producing a tridimensional structure by 3d printing |
| TWI695848B (zh) | 2015-03-03 | 2020-06-11 | 德商巴斯夫歐洲公司 | 銀奈米線與基於(甲基)丙烯酸酯之封端劑的合成 |
| WO2016165979A1 (de) | 2015-04-15 | 2016-10-20 | Basf Se | Dihydrooligocyclopentadienyl(meth)acrylate |
| CN107849224B (zh) | 2015-07-09 | 2021-06-08 | 巴斯夫欧洲公司 | 可固化组合物 |
| JP2018526487A (ja) | 2015-07-16 | 2018-09-13 | ビーエーエスエフ ソシエタス・ヨーロピアBasf Se | アルキル(メタ)アクリレートおよび特定の複素環式基を含む(メタ)アクリレートからのポリ(メタ)アクリレートを含むホットメルト接着剤 |
| EP3390338A1 (de) | 2015-12-15 | 2018-10-24 | Basf Se | Verfahren zur herstellung von hydroxybenzophenonpolyglykolether-(meth)acrylat |
| WO2018024563A1 (de) | 2016-08-05 | 2018-02-08 | Basf Se | Polyisobutengruppen tragende makromonomere und deren homo- oder copolymere |
-
2018
- 2018-01-22 SG SG11201906488RA patent/SG11201906488RA/en unknown
- 2018-01-22 CA CA3050038A patent/CA3050038C/en active Active
- 2018-01-22 EP EP18700600.2A patent/EP3573946B1/de active Active
- 2018-01-22 CN CN201880006924.9A patent/CN110198925B/zh active Active
- 2018-01-22 RU RU2019126822A patent/RU2730856C1/ru active
- 2018-01-22 JP JP2019540616A patent/JP6768973B2/ja active Active
- 2018-01-22 ES ES18700600T patent/ES2859667T3/es active Active
- 2018-01-22 WO PCT/EP2018/051381 patent/WO2018138025A1/de not_active Ceased
- 2018-01-22 MY MYPI2019004135A patent/MY197504A/en unknown
- 2018-01-22 US US16/480,703 patent/US11028040B2/en active Active
- 2018-01-22 MX MX2019008908A patent/MX2019008908A/es unknown
- 2018-01-22 KR KR1020197022049A patent/KR102112235B1/ko active Active
- 2018-01-22 BR BR112019015152-4A patent/BR112019015152B1/pt active IP Right Grant
- 2018-01-22 AU AU2018213816A patent/AU2018213816B2/en active Active
-
2019
- 2019-08-22 ZA ZA2019/05540A patent/ZA201905540B/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| ZA201905540B (en) | 2021-05-26 |
| MY197504A (en) | 2023-06-19 |
| EP3573946A1 (de) | 2019-12-04 |
| EP3573946B1 (de) | 2020-12-16 |
| CN110198925A (zh) | 2019-09-03 |
| SG11201906488RA (en) | 2019-08-27 |
| MX2019008908A (es) | 2019-09-13 |
| WO2018138025A1 (de) | 2018-08-02 |
| AU2018213816B2 (en) | 2020-01-02 |
| JP2020506185A (ja) | 2020-02-27 |
| JP6768973B2 (ja) | 2020-10-14 |
| CN110198925B (zh) | 2022-08-30 |
| BR112019015152A2 (pt) | 2020-03-24 |
| RU2730856C1 (ru) | 2020-08-26 |
| AU2018213816A1 (en) | 2019-08-22 |
| CA3050038A1 (en) | 2018-08-02 |
| US11028040B2 (en) | 2021-06-08 |
| US20200407309A1 (en) | 2020-12-31 |
| BR112019015152B1 (pt) | 2023-05-09 |
| CA3050038C (en) | 2020-06-09 |
| KR20190094473A (ko) | 2019-08-13 |
| KR102112235B1 (ko) | 2020-05-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2837539T3 (es) | Procedimiento para preparar (met)acrilatos de dimetilaminoalquilo | |
| KR102629665B1 (ko) | 알칸설폰산의 제조 방법 | |
| CN107848931B (zh) | 具有芴骨架的醇的晶体及其制造方法 | |
| ES2464442T3 (es) | Procedimiento para la preparación continua de alquilamino(met)acrilamidas | |
| JP2013533869A (ja) | ギ酸の製造方法 | |
| JP2015155481A (ja) | アルキル基中に少なくとも4個の炭素原子を有する(メタ)アクリル酸の3級アルキルエステルの製造法 | |
| ES2912349T3 (es) | Procedimiento para la preparación de metacrilato de carbonato de glicerol. | |
| ES2859667T3 (es) | Procedimiento para la producción de ésteres de (met)acrilato de norbornilo | |
| ES2912366T3 (es) | Procedimiento para la disolución continua de un sólido en un medio de reacción | |
| JP6762957B2 (ja) | 脂肪族カルボン酸のtert−ブチルエステルの製造 | |
| TW201139359A (en) | Process for inhibiting polymerization of (meth) acrylic acid and/or (meth) acrylic esters | |
| TWI764965B (zh) | 自丁基為正丁基或異丁基之粗丙烯酸丁酯藉由蒸餾分離出純丙烯酸丁酯之方法 | |
| JP2020502212A (ja) | 蒸留により対応する粗製アルキルアクリレートから純粋な2−エチルヘキシルアクリレートまたは純粋な2−プロピルヘプチルアクリレートを取得する方法 | |
| US9255069B2 (en) | Process for purifying N-alkylpyrrolidones | |
| TW201043598A (en) | Composition stabilized for a purification and process for purifying and for preparing hydroxyalkyl(meth)acrylates | |
| US20160090344A1 (en) | Method for dehydrating alpha-substituted carboxylic acids | |
| ES3052207T3 (en) | Method for the preparation of 2-octyl(meth)acrylate | |
| RU2778793C2 (ru) | Способ получения глицеринкарбонатметакрилата | |
| BR112020008603B1 (pt) | Processo para a preparação de metacrilato de carbonato de glicerol | |
| US20080011385A1 (en) | Method Of Storing (Meth)Acrylic Ester | |
| JP2020503309A (ja) | 蒸留により粗製tert−ブチル(メタ)アクリレートから純粋なtert−ブチル(メタ)アクリレートを取得する方法 | |
| JP2014076989A (ja) | グリシジルアクリレートの製造方法 | |
| CN104812731A (zh) | 生产甲酸的方法 |