ES2897467T3 - Método para producir ácido 5-hidroxipiperidin-2-carboxílico - Google Patents
Método para producir ácido 5-hidroxipiperidin-2-carboxílico Download PDFInfo
- Publication number
- ES2897467T3 ES2897467T3 ES18212248T ES18212248T ES2897467T3 ES 2897467 T3 ES2897467 T3 ES 2897467T3 ES 18212248 T ES18212248 T ES 18212248T ES 18212248 T ES18212248 T ES 18212248T ES 2897467 T3 ES2897467 T3 ES 2897467T3
- Authority
- ES
- Spain
- Prior art keywords
- group
- carbon atoms
- compound
- group containing
- formula
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 *[C@@](CCC1(*)*)CN1C(O)=C Chemical compound *[C@@](CCC1(*)*)CN1C(O)=C 0.000 description 12
- OXQMIXBVXHWDPX-UHFFFAOYSA-N CC(C)(C)N(C)C Chemical compound CC(C)(C)N(C)C OXQMIXBVXHWDPX-UHFFFAOYSA-N 0.000 description 1
- RKEYKDXXZCICFZ-WHFBIAKZSA-N O[C@@H](CC1)CN[C@@H]1C(O)=O Chemical compound O[C@@H](CC1)CN[C@@H]1C(O)=O RKEYKDXXZCICFZ-WHFBIAKZSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D211/00—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings
- C07D211/04—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D211/06—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members
- C07D211/36—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D211/60—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C233/00—Carboxylic acid amides
- C07C233/01—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms
- C07C233/45—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having the nitrogen atom of at least one of the carboxamide groups bound to a carbon atom of a hydrocarbon radical substituted by carboxyl groups
- C07C233/46—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having the nitrogen atom of at least one of the carboxamide groups bound to a carbon atom of a hydrocarbon radical substituted by carboxyl groups with the substituted hydrocarbon radical bound to the nitrogen atom of the carboxamide group by an acyclic carbon atom
- C07C233/47—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having the nitrogen atom of at least one of the carboxamide groups bound to a carbon atom of a hydrocarbon radical substituted by carboxyl groups with the substituted hydrocarbon radical bound to the nitrogen atom of the carboxamide group by an acyclic carbon atom having the carbon atom of the carboxamide group bound to a hydrogen atom or to a carbon atom of an acyclic saturated carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C309/00—Sulfonic acids; Halides, esters, or anhydrides thereof
- C07C309/63—Esters of sulfonic acids
- C07C309/64—Esters of sulfonic acids having sulfur atoms of esterified sulfo groups bound to acyclic carbon atoms
- C07C309/65—Esters of sulfonic acids having sulfur atoms of esterified sulfo groups bound to acyclic carbon atoms of a saturated carbon skeleton
- C07C309/66—Methanesulfonates
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D498/08—Bridged systems
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/55—Design of synthesis routes, e.g. reducing the use of auxiliary or protecting groups
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Hydrogenated Pyridines (AREA)
- Pyrane Compounds (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Un método para producir el compuesto representado por la fórmula (7) a continuación: **(Ver fórmula)** (en la que P representa un grupo protector, R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono), comprendiendo el método la etapa 1 de: proteger el grupo hidroxilo con un grupo protector en un compuesto representado por la fórmula (1) a continuación: **(Ver fórmula)** (en la que X representa Cl, Br o I, y R1 representa un átomo de hidrógeno o un grupo alquilo opcionalmente sustituido que contiene de 1 a 4 átomos de carbono) para sintetizar un compuesto representado por la fórmula (2) a continuación: **(Ver fórmula)** (en la que X representa Cl, Br o I, R1 representa un átomo de hidrógeno o un grupo alquilo opcionalmente sustituido que contiene de 1 a 4 átomos de carbono, y P representa un grupo protector) y después reducir el grupo éster en el compuesto (2) para sintetizar un compuesto representado por la fórmula (3) a continuación: **(Ver fórmula)** (en la que X representa Cl, Br o I, y P representa un grupo protector).
Description
DESCRIPCIÓN
Método para producir ácido 5-hidroxipiperidin-2-carboxílico
Campo técnico
La presente invención se refiere a un método para producir ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico y productos intermedios de síntesis del mismo. El ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico, que se produce mediante el método de la presente invención, es útil como producto intermedio de síntesis para un inhibidor de p-lactamasa y similares.
Técnica anterior
El ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico es un producto intermedio útil para la síntesis de un agente y similares que inhibe p-lactamasas en bacterias que muestran resistencia frente a la clase de antibióticos de plactama, siendo las p-lactamasas la causa principal de resistencia en las bacterias.
Se conoce un método de producción que usa ácido glutámico o ácido piroglutámico como materia prima de partida como método para producir ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico. Específicamente, el documento de patente 1 describe que se produce un compuesto de ácido 5-hidroxipiperidin-2-carboxílico protegido como producto intermedio de ácidos oxo-azacicloalquilcarboxílicos protegidos en N a partir de ácido piroglutámico como materia prima de partida mediante el procedimiento de homologación para aumentar los átomos de carbono y el procedimiento de ciclación.
Además, el documento no de patente 1 describe que se produce un compuesto de ácido 5-hidroxipiperidin-2-carboxílico protegido a partir de glutamina como materia prima de partida mediante el procedimiento de homologación para aumentar los átomos de carbono y el procedimiento de ciclación.
El documento no de patente 2 describe que se produce una mezcla de estereoisómeros de un compuesto de ácido 5-hidroxipiperidin-2-carboxílico protegido a partir de un compuesto de ácido glutámico protegido como materia prima de partida mediante el procedimiento de homologación para aumentar los átomos de carbono y el procedimiento de ciclación.
El documento no de patente 3 describe que se produce un compuesto de ácido 5-hidroxipiperidin-2-carboxílico protegido a partir de un compuesto de ácido piroglutámico protegido como materia prima de partida mediante el procedimiento de homologación para aumentar los átomos de carbono y el procedimiento de ciclación.
El documento de patente 2 describe que se produce un compuesto de ácido 5-hidroxipiperidin-2-carboxílico protegido a partir de un compuesto de ácido piroglutámico protegido como materia prima de partida mediante el procedimiento de homologación para aumentar los átomos de carbono y el procedimiento de ciclación en una etapa.
Documentos de la técnica anterior
[Bibliografía de patentes]
Documento de patente 1: documento WO2010/126820
Documento de patente 2: documento WO2006/125974
[Bibliografía no de patentes]
Documento no de patente 1: P. D. Bailey et al., Chem. Commun. 1996, 349.
Documento no de patente 2: P. D. Bailey et al., Tetrahedron Lett. 1988, 29, 2231.
Documento no de patente 3: M. A. Letavic et al., Bioorg. Med. Chem. Lett. 2002, 12, 1387.
Sumario de la invención
Problema técnico
El método descrito en el documento de patente 1 para producir ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico requiere usar un catalizador de iridio muy caro y, por tanto, no es adecuado para la producción industrial. El método de producción descrito en el documento no de patente 1 es difícil de emplear en la producción industrial porque el método también requiere usar un catalizador de rodio caro y, además, comprende la etapa de usar diazometano, que es difícil de usar en aplicaciones industriales.
El método de producción descrito en el documento no de patente 2 también es difícil de emplear en la producción industrial porque el método también comprende la etapa de usar diazometano, que es difícil de usar en aplicaciones
industriales, y además comprende un problema con respecto a un compuesto que puede obtenerse, en el que el compuesto se obtiene como una mezcla de estereoisómeros.
Los métodos de producción descritos en el documento no de patente 3 y el documento de patente 2 también son difíciles de emplear en la producción industrial porque los métodos comprenden la etapa de usar TMS diazometano, que es caro y difícil de usar en aplicaciones industriales. Además, el método de producción descrito en el documento de patente 2 requiere usar un catalizador de rodio caro. Cualquiera de los métodos de producción descritos en el documento no de patente 3 y el documento de patente 2 requiere realizar la reacción a una temperatura bastante baja y, por tanto, es difícil de emplear en la producción industrial.
A la vista de los problemas anteriormente mencionados, un objetivo de la presente invención es proporcionar un método para producir ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico y productos intermedios de síntesis del mismo incluyendo moléculas aquirales y quirales, estando el método disponible para su uso práctico en la producción industrial.
Solución al problema
Los inventores han estudiado intensamente para resolver los problemas anteriormente descritos y, en consecuencia, han encontrado que pueden sintetizarse eficazmente sustancias ópticamente activas de ácidos (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílicos usando productos intermedios de síntesis particulares y de ese modo han completado la presente invención.
Es decir, la presente invención es de la siguiente manera.
<1> Un método para producir el compuesto representado por la fórmula (7) a continuación:
(en la que P representa un grupo protector, R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono),
comprendiendo el método la etapa 1 de:
proteger el grupo hidroxilo con un grupo protector en un compuesto representado por la fórmula (1) a continuación:
OH
Xs^ X v v/COOR1
( 1 )
(en la que X representa Cl, Br o I, y R1 representa un átomo de hidrógeno o un grupo alquilo opcionalmente sustituido que contiene de 1 a 4 átomos de carbono)
para sintetizar un compuesto representado por la fórmula (2) a continuación:
( 2 )
(en la que X representa Cl, Br o I, R1 representa un átomo de hidrógeno o un grupo alquilo opcionalmente sustituido que contiene de 1 a 4 átomos de carbono, y P representa un grupo protector)
y después reducir el grupo éster en el compuesto (2) para sintetizar un compuesto representado por la fórmula (3) a continuación:
(en la que X representa Cl, Br o I, y P representa un grupo protector).
<2> El método para producir el compuesto (7) según el punto <1>, en el que el método comprende (i) la etapa 2 de: esterificar el grupo hidroxilo en el compuesto (3) con un grupo sulfonato para sintetizar un compuesto representado por la fórmula (4) a continuación:
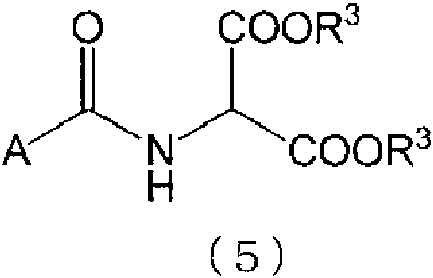
(en la que X representa Cl, Br o I, R2 representa un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquilo que contiene de 1 a 10 átomos de carbono o un grupo aralquilo que contiene de 7 a 20 átomos de carbono) y dejar reaccionar el compuesto (4) con un compuesto representado por la fórmula (5) a continuación:
(en la que R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono)
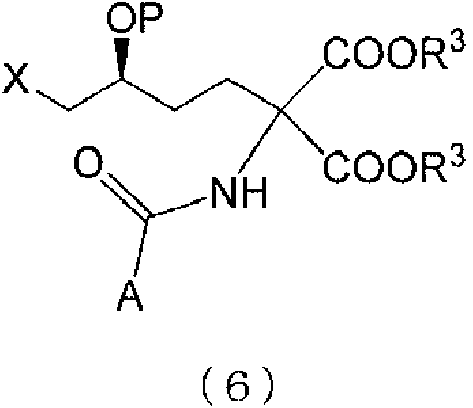
para sintetizar un compuesto representado por la fórmula (6) a continuación:
(en la que X representa Cl, Br o I, P representa un grupo protector, R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono);
y
(ii) la etapa 3 de:
ciclar el compuesto (6) para sintetizar el compuesto representado por la fórmula (7) a continuación:
(en la que P representa un grupo protector, R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).
<3> Un método para producir ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico representado por la fórmula (10) a continuación:
comprendiendo el método (i) la etapa 4 de:
retirar el grupo protector a partir del grupo hidroxilo en el compuesto representado por la fórmula (7) a continuación:
(en la que P representa un grupo protector, R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono)
para sintetizar el compuesto representado por la fórmula (8) a continuación:
(en la que R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono), en el que el compuesto (7) se sintetiza mediante el método según el punto <1> o <2>.
<4> El método para producir ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico según el punto <3>, comprendiendo el método además comprende (ii) la etapa 5 de:
(a) en el compuesto (8), hidrolizar los grupos éster, dejar reaccionar uno de los grupos carboxilo con el grupo
hidroxilo para permitir la lactonización, y descarboxilar adicionalmente el otro grupo carboxilo; o
(b) en el compuesto (8), hidrolizar los grupos éster, descarboxilar uno de los grupos carboxilo para formar una mezcla estereoisomérica de un ácido 2-monocarboxílico, y después isomerizar y lactonizar la mezcla estereoisomérica;
para sintetizar el compuesto representado por la fórmula (9) a continuación:
(en la que A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).
<5> El método para producir ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico según el punto <3> o <4>, que comprende además (iii) la etapa 6 de:
escindir el enlace amida en el compuesto (9) e hidrolizar la lactona en el compuesto (9) para sintetizar ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico.
<6> Un compuesto representado por la fórmula (7) a continuación:
(en la que P representa un grupo protector, R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).
<7> Un compuesto representado por la fórmula (6a) a continuación:
(en la que X representa Cl, Br o I, P' representa un grupo tetrahidropiranilo, grupo metoximetilo, grupo etoxietilo, grupo terc-butilo o grupo terc-butildimetilsililo, y R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).
Efecto ventajoso de la invención
La presente invención puede proporcionar ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico y un método de producción para el mismo excelente en cuanto a la seguridad y funcionamiento y disponible para su uso práctico en
la producción industrial. Además, la presente invención puede proporcionar productos intermedios de síntesis novedosos para la producción de ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico. El ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico, que se produce mediante el método de producción de la presente invención, está disponible como material de partida en la producción de un inhibidor de p-lactamasa y similares.
Breve descripción de los dibujos
La figura 1 muestra un aspecto del esquema para la síntesis de ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico. En el dibujo, X representa Cl, Br o I. P representa un grupo protector. A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono. R1 representa un átomo de hidrógeno o un grupo alquilo opcionalmente sustituido que contiene de 1 a 4 átomos de carbono. R2 representa un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquilo que contiene de 1 a 10 átomos de carbono o un grupo aralquilo que contiene de 7 a 20 átomos de carbono. R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono.
Descripción de las realizaciones
Ahora se describirá en detalle la presente invención.
En la presente memoria descriptiva, el “compuesto representado por la fórmula (1)” puede denominarse “compuesto (1)” y esto es válido para cualquier compuesto representado por otras fórmulas.
En la presente memoria descriptiva, Cl se refiere a un átomo de cloro, Br se refiere a un átomo de bromo, I se refiere a un átomo de yodo, y Et se refiere a un grupo etilo.
[1] Método de producción
La presente invención se refiere a la producción de sustancias ópticamente activas de ácidos (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílicos, que se producen usando un producto intermedio de síntesis particular representado por la fórmula (7) a continuación:
(en la que P representa un grupo protector, R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).
El compuesto (7) puede sintetizarse mediante el método que comprende la etapa 1 de:
proteger el grupo hidroxilo con un grupo protector en un compuesto representado por la fórmula (1) a continuación:
OH
Xs^ X v v/COOR1
( 1 )
(en la que X representa Cl, Br o I, y R1 representa un átomo de hidrógeno o un grupo alquilo opcionalmente sustituido que contiene de 1 a 4 átomos de carbono)
para sintetizar un compuesto representado por la fórmula (2) a continuación:
( 2 )
(en la que X representa Cl, Br o I, R1 representa un átomo de hidrógeno o un grupo alquilo opcionalmente sustituido
que contiene de 1 a 4 átomos de carbono, y P representa un grupo protector)
y después reducir el grupo éster en el compuesto (2) para sintetizar un compuesto representado por la fórmula (3) a continuación:
(en la que X representa Cl, Br o I, y P representa un grupo protector).
Productos intermedios adicionales en la producción de sustancias ópticamente activas de ácidos (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílicos están representados por los compuestos representados por la fórmula (8) a continuación:
(en la que R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono)
o la fórmula (9) a continuación:
(en la que A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, o un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono, un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).
El compuesto (8) puede sintetizarse mediante procedimientos habituales de química orgánica y preferiblemente se sintetiza mediante la etapa 4 a continuación.
La etapa 4 es un método para producir el compuesto representado por la fórmula (8) (compuesto (8)) a partir de un compuesto (7) como materia prima.
En la etapa 4, el grupo protector puede retirarse a partir del grupo hidroxilo en el compuesto representado por la fórmula (7) a continuación:
(en la que P representa un grupo protector, R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono)
para sintetizar el compuesto representado por la fórmula (8) a continuación:
(en la que R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).
Pueden emplearse condiciones habitualmente usadas en la desprotección de cada grupo de protección como condiciones para la desprotección. Normalmente, se usa un ácido o una combinación de un catalizador ácido y un alcohol.
Como ácido usado para la desprotección, normalmente se usa un ácido inorgánico tal como ácido clorhídrico, ácido sulfúrico, ácido fosfórico y similares, o u ácido orgánico tal como ácido metanosulfónico, ácido p-toluenosulfónico, ácido oxálico, ácido trifluoacético, ácido fórmico, ácido acético y similares y se usa preferiblemente ácido clorhídrico o ácido p-toluenosulfónico.
Como catalizador ácido, se usa normalmente un ácido inorgánico tal como ácido clorhídrico, ácido sulfúrico y similares, o un ácido orgánico tal como ácido metanosulfónico, ácido p-toluenosulfónico y similares y se usa preferiblemente ácido clorhídrico o ácido p-toluenosulfónico.
Como alcohol, se usa normalmente metanol, etanol, n-propanol, 2-propanol, n-butanol o similares y se usa preferiblemente metanol.
Por ejemplo, en casos en los que P en la fórmula (7) es un grupo tetrahidropiranilo o grupo etoxietilo, se aplica preferiblemente ácido clorhídrico como catalizador en disolvente de metanol y la desprotección puede lograrse fácilmente en este método.
De los compuestos representados por la fórmula (8), un compuesto representado por la fórmula (8a) a continuación:
(en la que Ac representa un grupo acetilo)
es cristalino y por tanto se aísla y se purifica fácilmente mediante cristalización tras la desprotección de modo que puede sintetizarse el compuesto (8a) de alta pureza. Dado que puede sintetizarse ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico de alta pureza realizando la síntesis usando el compuesto (8a) de alta pureza, el compuesto (8a) es particularmente preferible como producto intermedio de síntesis. Como disolvente de cristalización puede usarse, por ejemplo, tolueno o un disolvente mixto de tolueno y heptano.
Con respecto a esto, R3 y A en el compuesto (8) son sinónimos de R3 y A en el compuesto (5) descrito a continuación.
El compuesto (9) puede sintetizarse mediante procedimientos habituales de química orgánica y se sintetiza preferiblemente mediante la etapa 5 a continuación.
La etapa 5 es un método para producir el compuesto representado por la fórmula (9) (compuesto (9)) a partir del
compuesto (8) como materia prima. La siguiente etapa 5(a) o 5(b) es preferible como etapa 5.
En la etapa 5(a), en el compuesto (8), se hidrolizan los grupos éster, se deja reaccionar uno de los grupos carboxilo con el grupo hidroxilo para permitir la lactonización, y se descarboxila adicionalmente el otro grupo carboxilo para sintetizar el compuesto representado por la fórmula (9) a continuación:
(en la que A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, o un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono, un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).
En la etapa 5(a), en primer lugar se hidrolizan los grupos éster en el compuesto (8). Se usa una base en la hidrólisis de los grupos éster.
Se usa agua, metanol, etanol o similares como disolvente de reacción.
Como base, puede usarse hidróxido de sodio, hidróxido de potasio o similares y es preferible hidróxido de sodio entre otros.
La cantidad de la base que va a usarse es normalmente de 2 a 10 veces, preferiblemente de 2 a 5 veces, con respecto a la cantidad del compuesto (8) en una base molar.
La temperatura de reacción no está particularmente limitada, pero es normalmente de 0°C a 50°C y preferiblemente de 0°C a 10°C.
El tiempo de reacción no está particularmente limitado, pero es normalmente durante de 1 a 24 horas y preferiblemente durante de 5 a 10 horas.
A continuación, se deja reaccionar uno de los grupos carboxilo con el grupo hidroxilo para permitir la lactonización después de hidrolizarse los grupos éster en el compuesto (8) (degradación de éster).
Para realizar la reacción de descarboxilación tras la lactonización, en primer lugar se deja reaccionar el ácido dicarboxílico obtenido mediante la degradación de éster con un agente de deshidratación para inducir el grupo carboxilo en la posición cis con respecto al grupo hidroxilo en la posición 5 que va a lactonizarse.
Como agente de deshidratación, puede usarse un agente de deshidratación habitualmente usado tal como, por ejemplo, anhídrido acético, cloruro de acetilo o cloruro de tionilo.
El disolvente de reacción no está particularmente limitado siempre que no inhiba la reacción, pero se usa preferiblemente ácido acético o un disolvente mixto de ácido acético y tolueno.
La cantidad del agente de deshidratación que va a usarse es normalmente de 1a 20 veces, preferiblemente de 1 a 5 veces, con respecto a la cantidad del compuesto (8), en el que los grupos éster se han hidrolizado, en una base molar.
La temperatura de reacción no está particularmente limitada, pero es normalmente de 0°C a 80°C y preferiblemente de 30°C a 60°C.
El tiempo de reacción no está particularmente limitado, pero es normalmente de 1 a 12 horas y preferiblemente de 2 a 5 horas.
Después de lactonizarse uno de los grupos carboxilo, se descarboxila adicionalmente el otro grupo carboxilo.
Cuando el otro grupo carboxilo restante se descarboxila adicionalmente, se produce la protonación tras la descarboxilación de una manera estereoselectiva debido a la estructura estérica fijada por la lactonización y, por tanto, se obtiene el compuesto (9) en la estructura de 5-acil-2-oxa-5-azabiciclo[2.2.2]octan-3-ona que tiene un grupo hidroxilo y un grupo carboxilo en la posición cis.
La descarboxilación puede avanzar incluso calentando simplemente (calentamiento simple) pero la adición de una
base orgánica tal como trietilamina o piridina fomenta la reacción y permite que la reacción avance a una temperatura baja, de modo que es preferible.
La temperatura de reacción de la descarboxilación mediante calentamiento simple es normalmente de 100°C a 130°C, mientras que normalmente es de 60°C a 90°C en casos en los que se añade una base orgánica.
El disolvente de reacción no está particularmente limitado siempre que no inhiba la reacción, pero preferiblemente se usa ácido acético o un disolvente mixto de ácido acético y tolueno.
La cantidad de la base orgánica que va a usarse es normalmente de 0,1 a 2 veces, preferiblemente de 0,2 a 1 vez, con respecto a la cantidad del compuesto (8) lactonizado en una base molar.
El tiempo de reacción no está particularmente limitado, pero es normalmente de 1 a 12 horas y preferiblemente de 2 a 5 horas.
En la etapa 5(b), en el compuesto (8), se hidrolizan los grupos éster, se descarboxila uno de los grupos carboxilo para formar una mezcla estereoisomérica de un ácido 2-monocarboxílico y después se isomeriza la mezcla estereoisomérica y se lactoniza para sintetizar el compuesto representado por la fórmula (9) a continuación:
(en la que A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, o un grupo alquiloxilo que contiene de 1a 4 átomos de carbono, un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).
En la etapa 5(b), la hidrólisis de los grupos éster en el compuesto (8) puede realizarse en las mismas condiciones que las de la etapa 5(a).
Tras hidrolizar los grupos éster en el compuesto (8), se descarboxila uno de los grupos carboxilo para formar una mezcla estereoisomérica de un ácido 2-monocarboxílico.
En la etapa 5(b), dado que en primer lugar se realiza la descarboxilación, el ácido dicarboxílico obtenido mediante la degradación de éster se somete en primer lugar a la descarboxilación para formar una mezcla estereoisomérica de un ácido 2-monocarboxílico.
La descarboxilación puede avanzar incluso calentando simplemente (calentamiento simple) pero la adición de una base orgánica tal como trietilamina o piridina fomenta la reacción y permite que la reacción avance a una temperatura baja.
La temperatura de reacción de la descarboxilación mediante calentamiento simple es normalmente de 100°C a 130°C, mientras que es normalmente de 60°C a 90°C en casos en los que se añade una base orgánica.
El disolvente de reacción no está particularmente limitado siempre que no inhiba la reacción, pero preferiblemente se usa ácido acético o un disolvente mixto de ácido acético y metanol.
La cantidad de la base orgánica que va a usarse es normalmente de 0,1 a 2 veces, preferiblemente de 0,2 a 1 vez, con respecto a la cantidad del compuesto (8), en el que se han hidrolizado los grupos éster, en una base molar. El tiempo de reacción no está particularmente limitado, pero es normalmente de 1 a 12 horas y preferiblemente de 2 a 5 horas.
A continuación, se isomeriza la mezcla estereoisomérica y se lactoniza. Cuando se isomeriza y se lactoniza la mezcla estereoisomérica del ácido 2-monocarboxílico, se lactoniza inmediatamente un estereoisómero que tiene el grupo carboxilo en la posición 2 en la posición cis con respecto al grupo hidroxilo en la posición 5 con un agente de deshidratación y se isomeriza un estereoisómero que tiene el grupo carboxilo en la posición 2 en la posición trans con respecto al grupo hidroxilo en la posición 5 para dar el estereoisómero que tiene el grupo carboxilo en la posición 2 en la posición cis y después se lactoniza. Por consiguiente, en última instancia se obtiene el compuesto (9) en la estructura de 5-acil-2-oxa-5-azabiciclo[2.2.2]octan-3-ona que tiene un grupo hidroxilo y un grupo carboxilo en la posición cis a partir de todos los tipos de estereoisómeros del ácido 2-monocarboxílico. Los ejemplos de un agente usado en esta etapa para realizar la deshidratación y la isomerización al mismo tiempo (un agente de
deshidratación e isomerización/lactonización) incluyen anhídrido acético, una combinación de anhídrido acético y una amina, anhídrido trifluoroacético, una combinación de anhídrido trifluoroacético y una amina, una combinación de un éster de clorocarbonato y una amina y similares; y es preferible anhídrido acético o una combinación de anhídrido acético y una amina entre otros.
La cantidad del agente de deshidratación e isomerización/lactonización que va a usarse es normalmente de 1 a 20 veces, preferiblemente de 1 a 5 veces, con respecto a la cantidad de la mezcla estereoisomérica del ácido 2-monocarboxílico en una base molar.
En casos en los que se usa una combinación con una amina, se usa piridina, trietilamina o similares como amina, y es particularmente preferible trietilamina. La cantidad de la amina que va a usarse es normalmente de 0,1 a 3 veces, preferiblemente de 0,2 a 1 vez, con respecto a la cantidad de la mezcla estereoisomérica del ácido 2-monocarboxílico en una base molar.
La temperatura de reacción no está particularmente limitada, pero es normalmente de 20°C a 130°C y preferiblemente de 60°C a 90°C.
El tiempo de reacción no está particularmente limitado, pero es normalmente de 1 a 12 horas y preferiblemente de 2 a 5 horas.
En las etapas 5(a) y 5(b), también pueden realizarse los esquemas de síntesis sin aislamiento y purificación durante el transcurso de la síntesis a partir del ácido dicarboxílico derivado mediante la degradación de éster para dar el compuesto (9).
En ese caso, por ejemplo, el compuesto (9) puede sintetizarse disolviendo una sal de disodio del ácido dicarboxílico en ácido acético, añadiendo anhídrido acético para la formación de lactona intramolecular, después añadiendo trietilamina y calentando la mezcla para la descarboxilación.
Además, por ejemplo, el compuesto (9) también puede sintetizarse disolviendo una sal de disodio del ácido dicarboxílico en ácido acético, añadiendo trietilamina seguido por calentamiento para la descarboxilación para formar una mezcla estereoisomérica de un ácido 2-monocarboxílico, después añadiendo anhídrido acético y calentando la mezcla. En este caso, puede depositarse acetato de sodio como subproducto mediante adición de un mal disolvente tal como tolueno y después eliminarse mediante filtración.
En la etapa 5(a) o 5(b), en casos en los que A en el compuesto (9) que va a sintetizarse es grupo benciloxilo, el compuesto es cristalino y, por tanto, se aísla y se purifica mediante cristalización de modo que puede sintetizarse el compuesto (9) de alta pureza. Dado que puede sintetizarse ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico de alta pureza realizando la síntesis usando el compuesto (9) de alta pureza, el compuesto (9) es particularmente preferible como producto intermedio de síntesis. Como disolvente de cristalización puede usarse, por ejemplo, un disolvente mixto de tolueno y heptano.
Con respecto a esto, A en el compuesto (9) es sinónimo de A en el compuesto (5) descrito a continuación.
En este caso, el compuesto (7) como materia prima puede sintetizarse mediante procedimientos habituales de química orgánica y se sintetiza preferiblemente mediante las etapas (1) a (3) a continuación.
La etapa 1 es una etapa de producir un compuesto representado por la fórmula (3) (compuesto (3)) a partir de un compuesto representado por la fórmula (1) (compuesto (1)) como materia prima.
Se protege el grupo hidroxilo en un compuesto representado por la fórmula (1) a continuación:
(en la que X representa Cl, Br o I, y R1 representa un átomo de hidrógeno o un grupo alquilo opcionalmente sustituido que contiene de 1 a 4 átomos de carbono) con un grupo protector para sintetizar un compuesto representado por la fórmula (2) a continuación:
OP
x ^ A ^ . c o o r 1
( 2 )
(en la que X representa Cl, Br o I, R1 representa un átomo de hidrógeno o un grupo alquilo opcionalmente sustituido que contiene de 1 a 4 átomos de carbono, y P representa un grupo protector)
y después se reduce el grupo éster en el compuesto (2) para sintetizar un compuesto representado por la fórmula (3) a continuación:
(en la que X representa Cl, Br o I, y P representa un grupo protector).
El compuesto (1) es una materia prima de partida de la etapa 1.
X en la fórmula (1) representa Cl, Br o I, y X representa preferiblemente Cl. R1 representa un átomo de hidrógeno o un grupo alquilo opcionalmente sustituido que contiene de 1 a 4 átomos de carbono, y R1 representa preferiblemente un grupo alquilo opcionalmente sustituido que contiene de 1 a 4 átomos de carbono. Los ejemplos del grupo alquilo incluyen, por ejemplo, grupo metilo, grupo etilo, grupo n-propilo, grupo isopropilo, grupo n-butilo, grupo isobutilo, grupo sec-butilo, grupo terc-butilo y similares. Los ejemplos del sustituyente en el grupo alquilo incluyen átomos de halógeno, grupos alcoxilo y similares.
El compuesto (1) puede sintetizarse fácilmente según un método conocido, por ejemplo, un método descrito en Tetrahedron: Asymmetry, 12(12), 1713 (2001) y similares. Además, puede usarse un producto comercial como compuesto (1) representado por la fórmula (1), en la que X representa Cl o Br y R1 representa un grupo metilo o grupo etilo.
En primer lugar, se protege el grupo hidroxilo en el compuesto (1) con un grupo protector para sintetizar el compuesto (2).
Son preferibles grupos protectores de éter como grupo protector. El motivo para el uso de un grupo protector de éter es que los grupos protectores de éter son ventajosos en cuanto a la resistencia a las condiciones básicas en las etapas siguientes. Con respecto a esto, el átomo de oxígeno que se une al grupo protector P en el compuesto (2) se deriva a partir del grupo hidroxilo.
Los ejemplos del grupo protector incluyen grupo tetrahidropiranilo, grupo metoximetilo, grupo etoxietilo, grupo tercbutilo o grupo terc-butildimetilsililo. Esos grupos protectores pueden introducirse protegiendo un grupo hidroxilo mediante la reacción con una combinación de agentes de reacción, tales como una combinación de dihidropirano y un catalizador ácido, cloruro de metoximetilo y diisopropiletilamina, etil vinil éter y un catalizador ácido, isobutileno y un catalizador ácido, y cloruro de terc-butildimetilsililo e imidazol, respectivamente. Un grupo protector preferible es grupo tetrahidropiranilo, grupo metoximetilo, grupo etoxietilo, grupo terc-butilo o grupo terc-butildimetilsililo. Entre otros, es preferible el grupo tetrahidropiranilo como grupo protector porque tiene una alta seguridad.
En casos en los que se usa el grupo tetrahidropiranilo como grupo protector, por ejemplo, puede aplicarse dihidropirano y un catalizador ácido tal como ácido metanosulfónico, ácido p-toluenosulfónico o p-toluenosulfonato de piridinio al compuesto (1) en un disolvente de reacción para obtener el compuesto (2).
El disolvente de reacción no está particularmente limitado siempre que se permita que avance la reacción, pero puede usarse tolueno, heptano, diclorometano, acetato de etilo y similares. Además, puede dejarse avanzar la reacción incluso en ausencia de un disolvente.
La cantidad de dihidropirano que va a usarse es normalmente de 1 a 10 veces, preferiblemente de 1 a 1,5 veces, con respecto a la cantidad del compuesto (1) en una base molar.
La cantidad del catalizador ácido que va a usarse es normalmente de 0,001 a 0,1 veces, preferiblemente de 0,002 a 0,02 veces, con respecto a la cantidad del compuesto (1) en una base molar.
La temperatura de reacción no está particularmente limitada, pero es normalmente de 0°C a 80°C y preferiblemente de 20°C a 60°C.
El tiempo de reacción no está particularmente limitado, pero es normalmente de 0,5 a 10 horas y preferiblemente de 1 a 3 horas.
Además, X en el compuesto (2) representa Cl, Br o I, y X representa preferiblemente Cl.
En el compuesto (2), R1 representa un átomo de hidrógeno o un grupo alquilo opcionalmente sustituido que contiene de 1 a 4 átomos de carbono, y R1 representa preferiblemente un grupo alquilo opcionalmente sustituido que contiene de 1 a 4 átomos de carbono. Los ejemplos del grupo alquilo incluyen, por ejemplo, grupo metilo, grupo etilo, grupo npropilo, grupo isopropilo, grupo n-butilo, grupo isobutilo, grupo sec-butilo, grupo terc-butilo y similares. Los ejemplos del sustituyente en el grupo alquilo incluyen átomos de halógeno, grupos alcoxilo y similares.
En el compuesto (2), P representa un grupo protector, preferiblemente grupo tetrahidropiranilo, grupo metoximetilo, grupo etoxietilo, grupo terc-butilo o grupo terc-butildimetilsililo, y de manera particularmente preferible grupo tetrahidropiranilo.
A continuación, se reduce el grupo éster en el compuesto (2) para sintetizar el compuesto (3).
En la reducción del grupo éster en el compuesto (2) para dar alcohol, preferiblemente se usa un agente reductor de hidruro. Por ejemplo, puede usarse un agente reductor de hidruro de aluminio tal como hidruro de aluminio y litio, hidruro de diisobutil-aluminio o hidruro de sodio y bis(metoxietoxi)aluminio, o un agente reductor de hidruro de boro tal como borohidruro de sodio, borohidruro de litio, borohidruro de calcio o borano. Entre otros, se usa preferiblemente un agente reductor de hidruro de aluminio o borohidruro de litio debido a su alta actividad de reacción en la reducción de ésteres.
Por ejemplo, puede aplicarse un agente reductor de hidruro de aluminio al compuesto (2) en un disolvente de reacción para sintetizar el compuesto (3).
El disolvente de reacción no está particularmente limitado siempre que se permita que avance la reacción, pero puede usarse tetrahidrofurano, tolueno y similares. Además, puede dejarse avanzar la reacción incluso en ausencia de un disolvente.
La cantidad del agente reductor de hidruro que va a usarse, en cuanto al hidruro, es normalmente de 2 a 10 veces, preferiblemente de 2 a 3 veces, con respecto a la cantidad del compuesto (2) en una base molar.
La temperatura de reacción no está particularmente limitada, pero es normalmente de 0°C a 80°C y preferiblemente de 0°C a 20°C.
El tiempo de reacción no está particularmente limitado, pero es normalmente de 0,5 a 10 horas y preferiblemente de 1 a 3 horas.
Con respecto a esto, X y P en el compuesto (3) son sinónimos de X y P en el compuesto (2).
La etapa 2 es una etapa de producir un compuesto representado por la fórmula (6) (compuesto (6)) a partir del compuesto (3) como materia prima.
Se esterifica el grupo hidroxilo en el compuesto (3) con un grupo sulfonato para sintetizar un compuesto representado por la fórmula (4) a continuación:
(en la que X representa Cl, Br o I, R2 representa un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquilo que contiene de 1 a 10 átomos de carbono o un grupo aralquilo que contiene de 7 a 20 átomos de carbono) y después se deja reaccionar el compuesto (4) con un compuesto representado por la fórmula (5) a continuación:
(en la que R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono)
para sintetizar un compuesto representado por la fórmula (6) a continuación:
(en la que X representa Cl, Br o I, P representa un grupo protector, R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).
En primer lugar, se esterifica el grupo hidroxilo en el compuesto (3) con un grupo sulfonato para sintetizar el compuesto (4).
En la esterificación del grupo hidroxilo en el compuesto (3) con un grupo sulfonato, puede emplearse una combinación de un cloruro de alquilsulfonilo habitualmente usado y una base, o una combinación de un cloruro de arilsulfonilo habitualmente usado y una base. Por ejemplo, puede emplearse una combinación de cloruro de metanosulfonilo o cloruro de p-toluenosulfonilo y trietilamina.
Por ejemplo, pueden aplicarse un cloruro de alquilsulfonilo o cloruro de arilsulfonilo y una base al compuesto (3) en un disolvente de reacción para sintetizar el compuesto (4).
El disolvente de reacción no está particularmente limitado siempre que se permita que avance la reacción, pero puede usarse tolueno, cloruro de metileno, tetrahidrofurano, acetato de etilo y similares. Además, puede dejarse avanzar la reacción incluso en ausencia de un disolvente.
Además, puede usarse una base orgánica tal como piridina o trietilamina, o una base inorgánica tal como bicarbonato de sodio o hidróxido de sodio como base.
La cantidad del cloruro de alquilsulfonilo o cloruro de arilsulfonilo que va a usarse es normalmente de 1a 2 veces, preferiblemente de 1 a 1,2 veces, con respecto a la cantidad del compuesto (3) en una base molar.
La cantidad de la base que va a usarse es normalmente de 1 a 2 veces, preferiblemente de 1 a 1,5 veces, con respecto a la cantidad del compuesto (3) en una base molar.
La temperatura de reacción no está particularmente limitada, pero es normalmente de 0°C a 50°C y preferiblemente de 0°C a 20°C.
El tiempo de reacción no está particularmente limitado, pero es normalmente de 0,5 a 5 horas y preferiblemente de 1 a 2 horas.
Con respecto a esto, X y P en el compuesto (4) son sinónimos de X y P en el compuesto (2).
Además, en el compuesto (4), R2 representa un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquilo que contiene de 1 a 10 átomos de carbono o un grupo aralquilo que contiene de 7 a 20 átomos de carbono, representa preferiblemente un grupo arilo que contiene de 6 a 7 átomos de carbono, un grupo alquilo que contiene de 1 a 3 átomos de carbono o un grupo aralquilo que contiene de 7 a 11 átomos de carbono, y representa más preferiblemente un grupo metilo. Los ejemplos del grupo arilo incluyen, por ejemplo, grupo fenilo, grupo tolilo, grupo naftilo, grupo bifenilo y similares. Los ejemplos del grupo alquilo incluyen, por ejemplo, grupo metilo, grupo etilo, grupo n-propilo, grupo isopropilo, grupo n-butilo, grupo isobutilo, grupo sec-butilo, grupo terc-butilo, grupo pentilo, grupo hexilo, grupo heptilo, grupo octilo y similares. Los ejemplos del grupo aralquilo incluyen, por ejemplo, grupo bencilo, grupo fenetilo y similares.
A continuación, se deja reaccionar el compuesto (4) con compuesto (5) para sintetizar el compuesto (6).
En el compuesto (5), R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono y preferiblemente un grupo alquilo que contiene de 1 a 2 átomos de carbono. Los ejemplos del grupo alquilo incluyen, por ejemplo, grupo metilo, grupo etilo, grupo n-propilo, grupo isopropilo, grupo n-butilo, grupo isobutilo, grupo sec-butilo, grupo tercbutilo y similares.
Además, en el compuesto (5), A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono, representa preferiblemente un grupo arilo que contiene de 6 a 10 átomos de carbono, un grupo alquilo que contiene de 1 a 3 átomos de carbono, un grupo
alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 11 átomos de carbono, y representa más preferiblemente un grupo metilo. Los ejemplos del grupo arilo incluyen, por ejemplo, grupo fenilo, grupo naftilo, grupo bifenilo y similares. Los ejemplos del grupo alquilo incluyen, por ejemplo, grupo metilo, grupo etilo, grupo n-propilo, grupo isopropilo, grupo n-butilo, grupo isobutilo, grupo sec-butilo, grupo tercbutilo, grupo pentilo, grupo hexilo, grupo heptilo, grupo octilo y similares. Los ejemplos del grupo alquiloxilo incluyen grupo metiloxilo, grupo etiloxilo, grupo n-propiloxilo, grupo isopropiloxilo, grupo n-butiloxilo, grupo isobutiloxilo, grupo terc-butiloxilo y similares. Los ejemplos del grupo aralquiloxilo incluyen grupo benciloxilo, grupo fenetiloxilo y similares.
Puede usarse un producto comercial como compuesto (5). Un compuesto (5) puede estar disponible, por ejemplo, de TateyamaKasei Co., Ltd.
Cuando se realiza la reacción entre el compuesto (4) y el compuesto (5), se necesita una base para generar un anión en la posición a en el compuesto (5). Con este fin, la reacción se realiza preferiblemente en presencia, por ejemplo, de una base fuerte tal como hidruro de sodio, hexametildisilazano de sodio, hexametildisilazano de litio, diisopropilamida de litio, terc-butóxido de sodio, terc-butóxido de potasio, etóxido de sodio, metóxido de sodio, hidróxido de sodio o hidróxido de potasio; o una base débil tal como carbonato de cesio, carbonato de potasio o carbonato de sodio. La reacción se realiza preferiblemente en presencia de una base, tal como, entre otros, hidruro de sodio, terc-butóxido de sodio, terc-butóxido de potasio, etóxido de sodio, carbonato de cesio o carbonato de potasio.
La cantidad de la base que va a usarse es normalmente de no menos de 0,8 veces, preferiblemente de 0,8 a 1.2 veces en casos de una base fuerte y de 0,8 a 3 veces en casos de una base débil, con respecto a la cantidad del sustrato (compuesto (5)) en una base molar.
El disolvente de reacción no está particularmente limitado siempre que pueda disolver el sustrato, pero preferiblemente se usan disolventes polares apróticos tales como dimetilsulfóxido, N,N-dimetilformamida, N,N-dimetilacetamida, N-metilpirrolidona y similares; disolventes de alcohol tales como metanol, etanol, propanol, butanol y similares; disolventes de éter tales como tetrahidrofurano, dietil éter, metil terc-butil éter, metil ciclopropil éter y similares; y disolventes mixtos de los mismos con un disolvente de hidrocarburo tal como tolueno, hexano o heptano, o con un disolvente de halohidrocarburo tal como diclorometano, cloroformo o 1,2-dicloroetano. Incluso más preferiblemente, se usan dimetilsulfóxido, N,N-dimetilformamida, N-metilpirrolidona, tetrahidrofurano, disolventes mixtos de los mismos con tolueno, un disolvente mixto de etanol y tolueno.
La temperatura de reacción no está particularmente limitada, pero es normalmente de 0°C a 130°C y preferiblemente de 20°C a 80°C.
El tiempo de reacción no está particularmente limitado, pero es normalmente durante de 1 a 24 horas y preferiblemente de 1 a 5 horas.
En esta etapa, preferiblemente se añade una sal de yoduro con el fin de fomentar la reacción y aumentar la selectividad. Como ejemplos de la sal de yoduro, son preferibles sales de yoduro representadas por MI (M se refiere a un metal alcalino) y, entre otras, son preferibles sales de yoduro tales como yoduro de potasio, yoduro de sodio y similares.
La cantidad de estas sales que va a añadirse es de 0,02 a 1 vez, preferiblemente de 0,2 a 0,4 veces, con respecto a la cantidad del sustrato (compuesto (4)) en una base molar.
La cantidad del compuesto (5) que va a usarse para el compuesto (4) es de 1a 2 veces, preferiblemente de 1 a 1.2 veces, con respecto a la cantidad del compuesto (4) en una base molar.
Con respecto a esto, en el compuesto (6), X y P son sinónimos de X y P en el compuesto (2), y R3 y A son sinónimos de R3 y A en el compuesto (5).
La etapa 3 es una etapa de producir un compuesto representado por la fórmula (7) (compuesto (7)) a partir del compuesto (6) como materia prima.
Se cicla el compuesto (6) para sintetizar un compuesto representado por la fórmula (7) a continuación:
(en la que P representa un grupo protector, R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).
Se requiere una base en la etapa 3. Como base se usa, por ejemplo, una base fuerte tal como hidruro de sodio, hexametildisilazano de sodio, hexametildisilazano de litio, diisopropilamida de litio, terc-butóxido de sodio, tercbutóxido de potasio, etóxido de sodio, metóxido de sodio, hidróxido de sodio o hidróxido de potasio; o una base débil tal como carbonato de cesio, carbonato de potasio o carbonato de sodio, y se usa preferiblemente hidruro de sodio, terc-butóxido de sodio, terc-butóxido de potasio, carbonato de cesio o carbonato de potasio.
La cantidad de la base que va a usarse es normalmente de no menos de 1 vez, preferiblemente de 1 a 2 veces en casos de una base fuerte y de 1a 3 veces en casos de una base débil, con respecto a la cantidad del sustrato (compuesto (6)) en una base molar.
El disolvente de reacción no está particularmente limitado siempre que pueda disolver el sustrato (compuesto (6)), pero se usan preferiblemente disolventes polares apróticos tales como dimetilsulfóxido, N,N-dimetilformamida, N,N-dimetilacetamida, N-metilpirrolidona o similares; o disolventes de éter tales como tetrahidrofurano, dietil éter, metil terc-butil éter, metil ciclopropil éter y similares; y disolventes mixtos de los mismos con un disolvente de hidrocarburo tal como tolueno, hexano o heptano, o con un disolvente de halohidrocarburo tal como diclorometano, cloroformo o 1,2-dicloroetano, y se usan incluso más preferiblemente N,N-dimetilformamida, N-metilpirrolidona, tetrahidrofurano y disolventes mixtos de los mismos con tolueno.
La temperatura de reacción no está particularmente limitada, pero es normalmente de 0°C a 130°C, preferiblemente de 10°C a 50°C en casos de una base fuerte, y preferiblemente de 80°C a 130°C en casos de una base débil.
El tiempo de reacción no está particularmente limitado, pero es normalmente durante de 1 a 24 horas y preferiblemente de 1 a 6 horas.
Esta etapa se realiza preferiblemente en presencia de una sal de amonio cuaternario tal como bromuro de tetrabutilamonio y similares con el fin de fomentar la reacción y aumentar la selectividad. Las cantidades de estas sales que van a usarse son de 0,02 a 1 vez, preferiblemente de 0,2 a 0,4 veces, con respecto a la cantidad del sustrato (compuesto (6)) en una base molar.
Además, la etapa 2 y la etapa 3 también pueden realizarse en serie sin aislamiento y purificación del compuesto (6) durante el transcurso de la síntesis. En ese caso, la etapa 3 puede realizarse añadiendo una base a la mezcla de reacción después de haberse completado la reacción de la etapa 2.
Con respecto a esto, en el compuesto (7), P es sinónimo de P en el compuesto (2), y R3 y A son sinónimos de R3 y A en el compuesto (5).
En la presente invención, preferiblemente se sintetiza ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico con la siguiente etapa 6.
La etapa 6 es una etapa de producir un compuesto representado por la fórmula (10) (compuesto (10)) a partir del compuesto (9) como materia prima.
Se hidroliza la lactona en el compuesto (9) y se escinde el enlace amida en el compuesto (9) para sintetizar ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico representado por la fórmula (10) a continuación:
(1 O)
Puede dejarse que la hidrólisis de la lactona y la escisión del enlace amida en el compuesto (9) avancen al mismo tiempo.
Pueden emplearse condiciones habitualmente usadas en la escisión del enlace amida. Por ejemplo, en casos en los que A es un grupo alquilo o grupo arilo, la escisión puede lograrse fácilmente aplicando un ácido fuerte como catalizador, tal como ácido clorhídrico, ácido bromhídrico y similares, en un disolvente de reacción.
Como disolvente de reacción, se usan agua o disolventes acuosos tales como dioxano acuoso, dimetoxietano acuoso, acetona acuosa y similares.
La cantidad del ácido fuerte que va a usarse es normalmente de 1 a 10 veces, preferiblemente de 1 a 2 veces, con respecto a la cantidad del compuesto (9) en una base molar.
La temperatura de reacción no está particularmente limitada, pero es normalmente de 0°C a 100°C y preferiblemente de 80°C a 100°C.
El tiempo de reacción no está particularmente limitado, pero es normalmente de 1 a 12 horas y preferiblemente de 3 a 6 horas.
En la hidrólisis de la lactona, se usa un ácido o una base, por ejemplo, ácido clorhídrico o hidróxido de sodio, según un procedimiento de hidrólisis habitualmente empleado.
Como disolvente de reacción, se usan agua, metanol, etanol y similares.
La cantidad del ácido o la base que va a usarse es normalmente de 1 a 10 veces, preferiblemente de 1 a 2 veces, con respecto a la cantidad del compuesto (9) después de la escisión del enlace amida en una base molar.
La temperatura de reacción no está particularmente limitada, pero es normalmente de 0°C a 100°C y preferiblemente de 60°C a 100°C.
El tiempo de reacción no está particularmente limitado, pero es normalmente de 1 a 12 horas y preferiblemente de 8 a 12 horas.
En la etapa 6, en casos en los que el compuesto (9) es un compuesto representado por la fórmula (9a):
(en la que A' representa un grupo alquilo que contiene de 1 a 10 átomos de carbono o un grupo arilo que contiene de 6 a 12 átomos de carbono),
por ejemplo, la adición de ácido clorhídrico seguida por calentamiento permite realizar la hidrólisis de la lactona y el grupo acetilo al mismo tiempo.
En este caso, dado que el ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico resultante es un clorhidrato, la retirada de ácido clorhídrico y similares puede lograrse con resinas de intercambio iónico según un procedimiento habitualmente empleado para la purificación de aminoácidos. Además, se neutraliza el ácido clorhídrico usando hidróxido de litio o carbonato de litio para producir cloruro de litio o, alternativamente, usando trietilamina para producir clorhidrato de trietilamina. Después se concentra la mezcla de reacción y va seguido por la adición de un alcohol, acetona y similares, de modo que puede retirarse el cloruro de litio y el clorhidrato de trietilamina.
Con respecto a esto, en el compuesto (9a), A' representa un grupo alquilo que contiene de 1 a 10 átomos de carbono o un grupo arilo que contiene de 6 a 10 átomos de carbono, y representa preferiblemente un grupo alquilo que contiene de 1 a 3 átomos de carbono o un grupo arilo que contiene 6 átomos de carbono. Los ejemplos del grupo arilo incluyen, por ejemplo, grupo fenilo. Los ejemplos del grupo alquilo incluyen, por ejemplo, grupo metilo, grupo etilo, grupo n-propilo, grupo isopropilo, grupo n-butilo, grupo isobutilo, grupo sec-butilo, grupo terc-butilo, grupo pentilo, grupo hexilo, grupo heptilo, grupo octilo y similares.
Además, dado que el ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico es cristalino, puede purificarse realizando una recristalización. Como disolvente de recristalización puede usarse, por ejemplo, un sistema mixto de agua/etanol, un sistema mixto de metanol/acetona y similares.
En las etapas 1 a 5 de la presente invención, es preferible, en los compuestos (1) a (9), que X represente Cl, R1 y R3 representen un grupo etilo, R2 represente un grupo metilo o grupo p-tolilo, A represente un grupo metilo o grupo fenilo, y P represente un grupo tetrahidropiranilo o grupo metoximetilo, grupo etoxietilo, grupo terc-butildimetilsililo o grupo terc-butilo.
En la presente invención, se produce preferiblemente ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico mediante acoplar el éster de sulfonato de un 4-halo-hidroxibutanol protegido en 3 ópticamente activo (compuesto (4)), que se deriva de un éster de 4-halo-3-hidroxibutanoato ópticamente activo (compuesto (1)), con un diéster de acilaminomalonato (compuesto (5)) para obtener un diéster de 2-acilamino-2-[4-halo-hidroxibutilo protegido en 3]
malonato ópticamente activo (compuesto (6)); realizar la ciclación y desprotección en el mismo para obtener un diéster de 1-acil-5-hidroxipiperidin-2,2-dicarboxilato ópticamente activo (compuesto (8)); y después hidrolizar el éster, seguido por (a) formar una lactona a partir del grupo hidroxilo en la posición 5 y uno de los dicarboxilatos en la posición 2, y descarboxilar el carboxilato restante, o (b) descarboxilar para formar una mezcla estereoisomérica de un ácido 2-monocarboxílico, e isomerizar y lactonizar el ácido 2-monocarboxílico, para obtener 5-acil-2-oxa-5-azabiciclo[2.2.2]octan-3-ona (compuesto (9)); y finalmente realizar la desprotección e hidrólisis. Por consiguiente, pueden sintetizarse eficazmente las sustancias ópticamente activas.
[2] Compuestos
La presente invención hace uso de los compuestos indicados a continuación. Estos compuestos son útiles como productos intermedios de síntesis para un inhibidor de p-lactamasa y similares.
Estos compuestos que se usan en los métodos de la presente invención pueden sintetizarse mediante procedimientos habituales de química orgánica dado que esta memoria descriptiva ha indicado las estructuras de los mismos.
(A) Compuestos representados por la fórmula (2a) a continuación:
(en la que X representa Cl, Br o I, R1 representa un átomo de hidrógeno o un grupo alquilo opcionalmente sustituido que contiene de 1 a 4 átomos de carbono, P” representa un grupo tetrahidropiranilo o grupo etoxietilo).
X representa Cl, Br o I, y preferiblemente Cl.
R1 representa un átomo de hidrógeno o un grupo alquilo opcionalmente sustituido que contiene de 1 a 4 átomos de carbono, y preferiblemente un grupo alquilo opcionalmente sustituido que contiene de 1 a 4 átomos de carbono. Los ejemplos del grupo alquilo incluyen, por ejemplo, grupo metilo, grupo etilo, grupo n-propilo, grupo isopropilo, grupo nbutilo, grupo isobutilo, grupo sec-butilo, grupo terc-butilo y similares. Los ejemplos del sustituyente en el grupo alquilo incluyen átomos de halógeno, grupos alcoxilo y similares.
P” representa un grupo tetrahidropiranilo o grupo etoxietilo.
Entre los compuestos (2a), los compuestos representados por las siguientes fórmulas son de particular importancia:
(B) Compuestos representados por la fórmula (3a) a continuación:
(en la que X representa Cl, Br o I, y P' representa un grupo tetrahidropiranilo, grupo metoximetilo, grupo etoxietilo, grupo terc-butilo o grupo terc-butildimetilsililo).
P' representa un grupo tetrahidropiranilo, grupo metoximetilo, grupo etoxietilo, grupo terc-butilo o grupo tercbutildimetilsililo.
Con respecto a esto, en los compuestos (3a), X es sinónimo de X en el compuesto (2a).
Entre los compuestos (3a), los compuestos representados por las siguientes fórmulas son de particular importancia:
(en la que X representa Cl, Br o I, P' representa un grupo tetrahidropiranilo, grupo metoximetilo, grupo etoxietilo, grupo terc-butilo o grupo terc-butildimetilsililo, y R2 representa un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquilo que contiene de 1 a 10 átomos de carbono o un grupo aralquilo que contiene de 7 a 20 átomos de carbono).
R2 representa un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquilo que contiene de 1 a 10 átomos de carbono o un grupo aralquilo que contiene de 7 a 20 átomos de carbono, representa preferiblemente un grupo arilo que contiene de 6 a 7 átomos de carbono, un grupo alquilo que contiene de 1 a 3 átomos de carbono o un grupo aralquilo que contiene de 7 a 11 átomos de carbono, y representa más preferiblemente un grupo metilo. Los ejemplos del grupo arilo incluyen, por ejemplo, grupo fenilo, grupo tolilo, grupo naftilo, grupo bifenilo y similares. Los ejemplos del grupo alquilo incluyen, por ejemplo, grupo metilo, grupo etilo, grupo n-propilo, grupo isopropilo, grupo n-butilo, grupo isobutilo, grupo sec-butilo, grupo terc-butilo, grupo pentilo, grupo hexilo, grupo heptilo, grupo octilo y similares. Los ejemplos del grupo aralquilo incluyen, por ejemplo, grupo bencilo, grupo fenetilo y similares. Con respecto a esto, en los compuestos (4a), X es sinónimo de X en el compuesto (2a) y P' es sinónimo de P' en el compuesto (3a).
Entre los compuestos (4a), los compuestos representados por las siguientes fórmulas son de particular importancia:
La presente invención también se refiere a compuestos novedosos indicados a continuación.
(D) Compuestos novedosos representados por la fórmula (6a) a continuación:
(en la que X representa Cl, Br o I, P' representa un grupo tetrahidropiranilo, grupo metoximetilo, grupo etoxietilo, grupo terc-butilo o grupo terc-butildimetilsililo, y R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).
R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y preferiblemente un grupo alquilo que contiene de 1 a 2 átomos de carbono. Los ejemplos del grupo alquilo incluyen, por ejemplo, grupo metilo, grupo etilo, grupo n-propilo, grupo isopropilo, grupo n-butilo, grupo isobutilo, grupo sec-butilo, grupo terc-butilo y similares. A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que
contiene de 7 a 20 átomos de carbono, representa preferiblemente un grupo alquilo que contiene de 1 a 3 átomos de carbono, un grupo arilo que contiene de 6 a 10 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 11 átomos de carbono, y representa más preferiblemente un grupo metilo y grupo fenilo. Los ejemplos del grupo arilo incluyen, por ejemplo, grupo fenilo, grupo naftilo, grupo bifenilo y similares. Los ejemplos del grupo alquilo incluyen, por ejemplo, grupo metilo, grupo etilo, grupo n-propilo, grupo isopropilo, grupo n-butilo, grupo isobutilo, grupo sec-butilo, grupo terc-butilo, grupo pentilo, grupo hexilo, grupo heptilo, grupo octilo y similares. Los ejemplos del grupo alquiloxilo incluyen grupo metiloxilo, grupo etiloxilo, grupo n-propiloxilo, grupo isopropiloxilo, grupo n-butiloxilo, grupo isobutiloxilo, grupo tercbutiloxilo y similares. Los ejemplos del grupo aralquiloxilo incluyen grupo benciloxilo, grupo fenetiloxilo y similares. Con respecto a esto, en los compuestos (6a), X es sinónimo de X en el compuesto (2a) y P' es sinónimo de P' en el compuesto (3a).
Entre los compuestos (6a), los compuestos representados por las siguientes fórmulas son particularmente preferibles:
(en la que Ac representa un grupo acetilo y Bz representa un grupo benzoílo).
(E) Compuestos novedosos representados por la fórmula (7) a continuación:
(en la que P representa un grupo protector, R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).
P representa un grupo protector y representa preferiblemente un grupo tetrahidropiranilo, grupo metoximetilo, grupo etoxietilo, grupo terc-butilo o grupo terc-butildimetilsililo.
Con respecto a esto, en los compuestos (7), R3 y A son sinónimos de R3 y A en el compuesto (6a).
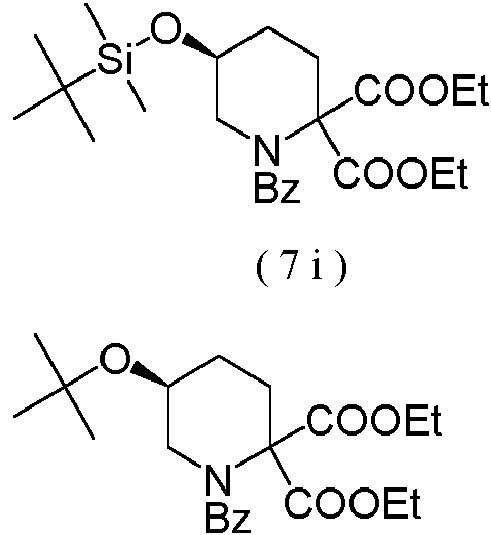
Entre los compuestos (7), los compuestos representados por las siguientes fórmulas son particularmente preferibles:
Ċ
(7j )
(en la que Ac representa un grupo acetilo y Bz representa un grupo benzoílo).
(F) En el método de la presente invención se usan compuestos representados por la fórmula (8) a continuación o sales de ácido dicarboxílico de los mismos:
(en la que R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).
Con respecto a esto, en los compuestos (8), R3 y A son sinónimos de R3 y A en el compuesto (6a).
Entre los compuestos (8), los compuestos representados por las siguientes fórmulas son de particular importancia:
(en la que Ac representa un grupo acetilo y Bz representa un grupo benzoílo).
Entre estos, el compuesto (8a) es preferible como producto intermedio de síntesis dado que es cristalino y, por tanto, puede aislarse y purificarse mediante cristalización.
(G) En el método de la presente invención se usan compuestos representados por la fórmula (9a) a continuación:
(en la que A' representa un grupo alquilo que contiene de 1 a 10 átomos de carbono o un grupo arilo que contiene de 6 a 12 átomos de carbono).
A' representa un grupo alquilo que contiene de 1 a 10 átomos de carbono o un grupo arilo que contiene de 6 a 12 átomos de carbono, y representa preferiblemente un grupo alquilo que contiene de 1 a 3 átomos de carbono o un grupo arilo que contiene 6 átomos de carbono. Los ejemplos del grupo alquilo incluyen, por ejemplo, grupo metilo, grupo etilo, grupo n-propilo, grupo isopropilo, grupo n-butilo, grupo isobutilo, grupo sec-butilo, grupo terc-butilo, grupo pentilo, grupo hexilo, grupo heptilo, grupo octilo y similares. Los ejemplos del grupo arilo incluyen grupo fenilo, grupo naftilo y similares.
Entre los compuestos (9a), los compuestos representados por las siguientes fórmulas son de particular importancia:
H f»!.. 0 ^ 0
\A
‘ N '""/iH
Bz
( 9 c )
(en la que Ac representa un grupo acetilo y Bz representa un grupo benzoílo).
(H) Un compuesto o una sal del mismo, el compuesto representado por la fórmula (11a) a continuación:
(en la que A' representa un grupo alquilo que contiene de 1 a 10 átomos de carbono o un grupo arilo que contiene de 6 a 12 átomos de carbono)
o la fórmula (11b) a continuación:
(en la que A' representa un grupo alquilo que contiene de 1 a 10 átomos de carbono o un grupo arilo que contiene de 6 a 12 átomos de carbono).
Con respecto a esto, en los compuestos (11a) y (11b), A es sinónimo de A en el compuesto (9a).
Entre los compuestos (11a) o (11b), los compuestos representados por las siguientes fórmulas son de particular importancia:
(11 f )
Ejemplos
Ahora se describirá la presente invención en más detalle a modo de ejemplos.
[Ejemplo 1] Producción de (3S)-4-cloro-3-(tetrahidropiran-2-iloxi)-butan-1-ol (un compuesto de la fórmula (3), en la que X = Cl, y P = grupo tetrahidropiranilo)
En un reactor de 50 ml, se colocaron 1,50 g (9 mmol) de éster de (3S)-4-cloro-3-hidroxibutanoato de etilo (un compuesto de la fórmula (1), en la que X = Cl, y R1 = grupo etilo), 1,51 g (18 mmol) de dihidropirano, 29 |il (0,45 mmol) de ácido metanosulfónico y 15 ml de tolueno y se agitó la mezcla durante 0,5 horas a temperatura ambiente, seguido por la adición de 250 |il (1,8 mmol) de trietilamina para detener la reacción. Se lavó esta mezcla con agua, se secó y después se concentró para obtener 3,14 g de un éster de (3S)-4-cloro-3-(tetrahidropiran-2-iloxi)-butanoato de etilo bruto aceitoso (un compuesto de la fórmula (2), en la que X = Cl, P = grupo tetrahidropiranilo, y R1 = grupo etilo).
1H-RMN (400 MHz, CDCla) 81,23 (3H, m), 1,44-1,85 (6H, m), 2,58-2,80 (2H, m), 3,47-3,95 (4H, m), 4,17 (2H, m), 4,20-4,37 (1H, m), 4,73-4,80 (1H, m).
A continuación, se disolvió el éster de (3S)-4-cloro-3-(tetrahidropiran-2-iloxi)-butanoato de etilo bruto obtenido (un compuesto de la fórmula (2), en la que X = Cl, P = grupo tetrahidropiranilo, y R1 = grupo etilo) en 15 ml de tetrahidrofurano anhidro (denominado a continuación en el presente documento “THF”) y se añadieron 0,34 g (9
mmol) de hidruro de aluminio y litio al mismo y se agitó la mezcla durante 2 horas a 5°C, seguido por la adición de 1 ml de acetato de etilo y después 1 ml de agua para degradar una cantidad en exceso del agente reductor y detener la reacción. Se filtró esta mezcla a través de Celite y se purificó mediante cromatografía en columna de gel de sílice para obtener 1,43 g de un aceite de (3S)-4-cloro-3-(tetrahidropiran-2-iloxi)-butan-1-ol (un compuesto de la fórmula (3), en la que X = Cl, y P = grupo tetrahidropiranilo) (el rendimiento total a lo largo de las dos etapas: 73 %).
1H-RMN (400 MHz, CDCls) 81,45-2,08 (8H, m), 3,35-4,13 (8H, m), 4,68-4,76 (1H, m).
[Ejemplo 2] Producción de éster de metanosulfonato de (3S)-4-cloro-3-(tetrahidropiran-2-iloxi)-butilo (un compuesto de la fórmula (4), en la que X = Cl, P = grupo tetrahidropiranilo, y R2 = grupo metilo)
En un reactor de 50 ml, se colocaron 1,43 g (6,8 mmol) del (3S)-4-cloro-3-(tetrahidropiran-2-iloxi)-butan-1-ol (un compuesto de la fórmula (3), en la que X = Cl, y P = grupo tetrahidropiranilo) obtenido en el ejemplo 1, 1,05 ml (7,5 mmol) de trietilamina y 14 ml de tolueno, y se añadieron 0,56 ml (7,18 mmol) de cloruro de metanosulfonilo al mismo a 5°C y se agitó la mezcla durante 1 hora a 5°C. Se lavó este líquido de reacción con agua, se secó y después se concentró para obtener 2,13 g de un éster de metanosulfonato de (3S)-4-cloro-3-(tetrahidropiran-2-iloxi)-butilo bruto aceitoso (un compuesto de la fórmula (4), en la que X = Cl, P = grupo tetrahidropiranilo, y R2 = grupo metilo) (rendimiento: 97 %).
1H-RMN (400 MHz, CDCla) 81,48-1,60 (4H, m), 1,72-1,85 (2H, m), 1,97-2,20 (2H, m), 3,02 (3H, s), 3,50-4,12 (5H, m), 4,30-4,45 (2H, m), 4,68 (1H, m).
[Ejemplo 3] Producción de éster de metanosulfonato de (3S)-4-cloro-3-(tetrahidropiran-2-iloxi)-butilo (un compuesto de la fórmula (4), en la que X = Cl, P = grupo tetrahidropiranilo, y R2 = grupo metilo)
En un reactor de 1 l, se colocaron 30 g (180,18 mmol) de éster de (3S)-4-cloro-3-hidroxibutanoato de etilo (un compuesto de la fórmula (1), en la que X = Cl, y R1 = grupo etilo), 18,16 g (216,22 mmol) de dihidropirano, 0,44 g (1,80 mmol) de p-toluenosulfonato de piridinio y 240 ml de tolueno y se agitó la mezcla durante 10 horas a 45°C para obtener una disolución de éster de (3S)-4-cloro-3-(tetrahidropiran-2-iloxi)-butanoato de etilo (un compuesto de la fórmula (2), en la que X = Cl, P = grupo tetrahidropiranilo, y R1 = grupo etilo) en tolueno.
Después, se añadieron 70 ml (252,25 mmol) de una disolución al 70 % de hidruro de sodio y bis(metoxietoxi)aluminio en tolueno a este líquido de reacción a de 5°C a 10°C y se agitó la mezcla durante 7 horas a de 5°C a 10°C. A este líquido de reacción, se le añadieron secuencialmente 22,7 ml de agua, 31,59 g de sulfato de magnesio y 22,7 ml de agua a de 5°C a 10°C y se agitó la mezcla durante 1 hora a de 5°C a 10°C y se dejó reposar durante la noche a 5°C, seguido por la filtración de sólidos. Después, se lavó el filtrado con salmuera saturada, se secó y posteriormente se concentró para obtener 247,39 g de (3S)-4-cloro-3-(tetrahidropiran-2-iloxi)-butan-1-ol (un compuesto de la fórmula (3), en la que X = Cl, y P = grupo tetrahidropiranilo) en disolución en tolueno (el rendimiento total a lo largo de las dos etapas: 91 %).
A continuación, a 237,3 g de esta disolución (que contenía 32,59 g (156,33 mmol) de (3S)-4-cloro-3-(tetrahidropiran-2-iloxi)-butan-1-ol (un compuesto de la fórmula (3), en la que X = Cl, y P = grupo tetrahidropiranilo)), se le añadieron 17,37 g (171,96 mmol) de trietilamina y después se añadieron 18,79 g (164,15 mmol) de cloruro de metanosulfonilo a la misma a de 5°C a 12°C y se agitó la mezcla durante 1 hora a de 5°C a 10°C. Se lavó este líquido de reacción con agua, se secó y después se concentró para obtener 51,72 g (contenido puro: 43,92 g) de éster de metanosulfonato de (3S)-4-cloro-3-(tetrahidropiran-2-iloxi)-butilo bruto (un compuesto de la fórmula (4), en la que X = Cl, P = grupo tetrahidropiranilo, y R2 = grupo metilo) (el rendimiento total a lo largo de las tres etapas: 89 %).
[Ejemplo 4-1] Producción de éster de metanosulfonato de (3S)-4-cloro-3-metoximetiloxi-butilo (un compuesto de la fórmula (4), en la que X = Cl, P = grupo metoximetilo, y R2 = grupo metilo)
En un reactor de 50 ml, se colocaron 1,50 g (9,01 mmol) de éster de (3S)-4-cloro-3-hidroxibutanoato de etilo (un compuesto de la fórmula (1), en la que X = Cl, y R1 = grupo etilo), 2,02 ml (11,71 mmol) de diisopropiletilamina y 15 ml de tolueno y se añadieron 1,18 g (11,71 mmol) de cloruro de metoximetilo al mismo a temperatura ambiente y se agitó la mezcla a temperatura ambiente. Tras completarse la reacción, se lavó el líquido de reacción con agua, se secó y después se concentró para obtener 2,54 g de éster de (3S)-4-cloro-3-metoximetiloxi-butanoato de etilo bruto (un compuesto de la fórmula (2), en la que X = Cl, P= grupo metoximetilo, y R1 = grupo etilo).
1H-RMN (400 MHz, CDCh) 81,26 (3H, t, J=7,6 Hz), 2,60-2,75 (2H, m), 3,38 (3H, s), 3,67 (2H, d, J=5,2 Hz), 4,15 (2H, q, J=7,3 Hz), 4,23 (1H, m), 4,71 (2H, dd, J=6,8, 22 Hz).
A continuación, se disolvieron 2,54 g de este éster de (3S)-4-cloro-3-metoximetiloxi-butanoato de etilo bruto (un compuesto de la fórmula (2), en la que X = Cl, P= grupo metoximetilo, y R1 = grupo etilo) en 14 ml de tolueno y después se añadieron 2,75 ml (9,91 mmol) de una disolución al 70 % de hidruro de sodio y bis(metoxietoxi)aluminio en tolueno al mismo a de 5°C a 10°C y se agitó la mezcla durante 1 hora a de 5°C a 10°C. A este líquido de reacción, se le añadieron secuencialmente 1,8 ml de agua, 0,56 g de sulfato de sodio y 0,68 g de sulfato de magnesio a de 5°C a 10°C, y se agitó la mezcla durante 1 hora a de 5°C a 10°C y se filtró para eliminar los sólidos. Después, se lavó el filtrado con salmuera saturada, se secó y posteriormente se concentró para obtener una
disolución de (3S)-4-doro-3-metoximetiloxi-butan-1-ol (un compuesto de la fórmula (3), en la que X = Cl, P = grupo metoximetilo) en tolueno.
1H-RMN (400 MHz, CDCls) 81,78-1,95 (2H, m), 3,43 (3H, s), 3,58-3,67 (2H, m), 3,98 (1H, m), 4,74 (2H, dd, J=7,2, 24 Hz).
A continuación, se añadieron 1,57 ml (11,29 mmol) de trietilamina a esta disolución y después se añadieron 0,83 ml (10,72 mmol) de cloruro de metanosulfonilo a la misma a de 5°C a 10°C y se agitó la mezcla durante 1 hora a de 5°C a 10°C. Se lavó este líquido de reacción con agua, se secó y después se concentró para obtener 1,39 g de éster de metanosulfonato de (3S)-4-cloro-3-metoximetiloxi-butilo (un compuesto de la fórmula (4), en la que X = Cl, P = grupo metoximetilo, y R2 = grupo metilo) (el rendimiento total a lo largo de las tres etapas: 62 %).
1H-RMN (400 MHz, CDCla) 81,98-2,15 (2H, m), 3,01 (3H, s), 3,40 (3H, s), 3,59-3,68 (2H, m), 3,92 (1H, m), 4,36 (1H, m), 4,71 (2H, dd, J=8,0, 13,6 Hz).
[Ejemplo 4-2] Producción de éster de metanosulfonato de (3S)-4-cloro-3-(1-etoxietiloxi)-butilo (un compuesto de la fórmula (4), en la que X = Cl, P = grupo etoxietilo, y R2 = grupo metilo)
En un reactor de 1 l, se colocaron 5,02 g (30,13 mmol) de éster de (3S)-4-cloro-3-hidroxibutanoato de etilo (un compuesto de la fórmula (1), en la que X = Cl, y R1 = grupo etilo), 2,39 g (33,14 mmol) de etil vinil éter, 0,08 g (0,30 mmol) de p-toluenosulfonato de piridinio y 25 ml de tolueno y se agitó la mezcla durante 3 horas a 40°C para obtener una disolución de éster de (3S)-4-cloro-3-(1-etoxietiloxi)-butanoato de etilo (un compuesto de la fórmula (2), en la que X=Cl, P=grupo etoxietilo, y R1 = grupo etilo) en tolueno.
1H-RMN (400 MHz, CDCh) 81,18-1,36 (9H, m), 2,58-2,77 (2H, m), 3,23-3,75 (4H, m), 4,10-4,35 (3H, m), 4,82 (1H, m).
Después, se añadieron 70 ml (252,25 mmol) de una disolución al 70 % de hidruro de sodio y bis(metoxietoxi)aluminio en tolueno a este líquido de reacción a de 5°C a 10°C y se agitó la mezcla durante 1 hora a de 5°C a 10°C. A este líquido de reacción, se le añadieron secuencialmente 3,25 ml de agua, 9,53 g de sulfato de magnesio y 3,25 ml de agua a de 5°C a 10°C, y se agitó la mezcla durante 4 horas a de 5°C a 10°C y se filtró para eliminar los sólidos. Después, se lavó el filtrado con salmuera saturada, se secó y posteriormente se concentró para obtener 5,81 g (contenido puro: 5,44 g) de (3S)-4-cloro-3-(1-etoxietiloxi)-butan-1-ol (un compuesto de la fórmula (3), en la que X = Cl, y P = grupo etoxietilo) en disolución en tolueno (el rendimiento total a lo largo de las dos etapas: 92 %).
1H-RMN (400 MHz, CDCh) 8 1,17-1,29 (3H, m), 1,30-1,37 (3H, m), 1,61-1,72 (0,6H, m), 1,80-2,00 (2H, m), 3,02 (0,4H, m), 3,50-3,90 (6H, m), 3,92-4,08 (1H, m), 4,79-4,86 (1H, m).
A continuación, a 4,44 g de esta disolución (que contenía 4,16 g (21,17 mmol) de (3S)-4-cloro-3-(1-etoxietiloxi)-butan-1-ol (un compuesto de la fórmula (3), en la que X = Cl, y P = grupo etoxietilo)), se le añadieron 20 ml de tolueno y 2,35 g (23,29 mmol) de trietilamina y después se añadieron 2,55 g (22,23 mmol) de cloruro de metanosulfonilo a la misma a de 5°C a 15°C y se agitó la mezcla durante 0,5 horas a de 5°C a 10°C. Se lavó este líquido de reacción con agua, se secó y después se concentró para obtener 10,83 g (contenido puro: 5,33 g) de éster de metanosulfonato de (3S)-4-cloro-3-(1-etoxietiloxi)-butilo bruto (un compuesto de la fórmula (4), en la que X = Cl, P = grupo etoxietilo, y R2 = grupo metilo) en disolución en tolueno (rendimiento: 92 %).
1H-RMN (400 MHz, CDCh) 81,20 (3H, t, J=5,9 Hz), 1,32 (3H, d, J=7,4 Hz), 1,92-2,19 (2H, m), 2,99 (3H, s), 3,43-3,71 (4H, m), 3,88 (0,5H, m), 4,02 (0,5H, m), 4,26-4,40 (2H, m), 4,78 (1H, m).
[Ejemplo 4-3] Producción de éster de metanosulfonato de (3S)-4-cloro-3-terc-butildimetilsililoxi-butilo (un compuesto de la fórmula (4), en la que X = Cl, P = grupo terc-butildimetilsililo, y R2 = grupo metilo)
En un reactor de 50 ml, se colocaron 5,00 g (30,01 mmol) de éster de (3S)-4-cloro-3-hidroxibutanoato de etilo (un compuesto de la fórmula (1), en la que X = Cl, y R1 = grupo etilo), 3,06 g (45,02 mmol) de imidazol y 25 ml de diclorometano y se añadieron 5,88 g (39,01 mmol) de cloruro de terc-butildimetilsililo y 1,18 g (11,71 mmol) de cloruro de metoximetilo al mismo sobre hielo y se agitó la mezcla a temperatura ambiente. Tras completarse la reacción, se lavó el líquido de reacción con agua y con disolución acuosa saturada de bicarbonato de sodio, se secó y se concentró para obtener 8,01 g de éster de (3S)-4-cloro-3-terc-butildimetilsililoxi-butanoato de etilo bruto (un compuesto de la fórmula (2), en la que X = Cl, P = grupo terc-butildimetilsililo, y R1 = grupo etilo) (rendimiento: 95 %).
1H-RMN (400 MHz, CDCh) 80,05 (3H, s), 0,11 (3H, s), 0,88 (9H, s), 1,26 (3H, t, J=7,4 Hz), 2,49-2,73 (2H, m), 3,52 (2H, s), 4,14 (2H, m), 4,31 (1H, m).
A continuación, se disolvieron 8,01 g de este éster de (3S)-4-cloro-3-terc-butildimetilsililoxi-butanoato de etilo bruto (un compuesto de la fórmula (2), en la que X=Cl, P=grupo terc-butildimetilsililo, y R1 = grupo etilo) en 25 ml de tolueno y se añadieron 9,5 ml (34,24 mmol) de una disolución al 70 % de hidruro de sodio y bis(metoxietoxi)aluminio en tolueno al mismo a de 5°C a 15°C y se agitó la mezcla durante 2,5 horas a de 5°C a 10°C. A este líquido de
reacción, se le añadieron secuencialmente 2,05 ml de ácido acético y 5,55 ml de agua a de 5°C a 10°C, y se agitó la mezcla durante 0,5 horas a temperatura ambiente y se filtró para eliminar los sólidos. Después, se lavó el filtrado con salmuera saturada, se secó y posteriormente se concentró para obtener 4,66 g (contenido puro: 4,28 g) de (3S)-4-cloro-3-terc-butildimetilsililoxi-butan-1-ol (un compuesto de la fórmula (3), en la que X = Cl, y P = grupo tercbutildimetilsililo) en disolución en tolueno (rendimiento: 63 %).
1H-RMN (400 MHz, CDCls) 80,14 (6H, s), 0,92 (9H, s), 1,80-2,01 (3H, m), 3,52 (2H, m), 3,81 (2H, m), 4,10 (1H, m).
A continuación, se añadieron 23 ml de tolueno y 2,17 ml (21,46 mmol) de trietilamina a esta disolución y después se añadieron 2,35 g (20,49 mmol) de cloruro de metanosulfonilo a la misma a de 5°C a 10°C y se agitó la mezcla durante 1 hora a de 5°C a 10°C. Se lavó este líquido de reacción con agua, se secó y después se concentró para obtener 6,09 g (contenido puro: 5,46 g) de éster de metanosulfonato de (3S)-4-cloro-3-terc-butildimetilsililoxi-butilo (un compuesto de la fórmula (4), en la que X = Cl, P = grupo terc-butildimetilsililo, y R2 = grupo metilo) en disolución en tolueno (rendimiento: 96 %).
1H-RMN (400 MHz, CDCla) 80,10 (6H, s), 0,89 (9H, s), 1,90-1,99 (1H, m), 2,06-2,17 (1H, m), 3,02 (3H, s), 3,47 (2H, m), 4,03 (1H, m), 4,28-4,40 (2H, m).
[Ejemplo 4-4] Producción de éster de metanosulfonato de (3S)-4-cloro-3-terc-butiloxi-butilo (un compuesto de la fórmula (4), en la que X = Cl, P = grupo terc-butilo, yR 2 = grupo metilo)
En un reactor de 100 ml, se colocaron 7,51 g (45,11 mmol) de éster de (3S)-4-cloro-3-hidroxibutanoato de etilo (un compuesto de la fórmula (1), en la que X = Cl, y R1 = grupo etilo) y 18 ml de n-hexano y se añadieron 0,47 g (4,51 mmol) de ácido sulfúrico concentrado y 6,17 g (110,07 mmol) de isobutileno al mismo sobre hielo y se agitó la mezcla durante 18 horas a 30-35°C. Después, se lavó el líquido de reacción con disolución acuosa saturada de bicarbonato de sodio, se secó, después se concentró y se purificó mediante cromatografía en gel de sílice para obtener 4,92 g de éster de (3S)-4-cloro-3-terc-butiloxi-butanoato de etilo (un compuesto de la fórmula (2), en la que X = Cl, P = grupo terc-butilo, y R1 = grupo etilo) (rendimiento: 49 %).
1H-RMN (400 MHz, CDCh) 81,20 (9H, s), 1,28 (3H, t, J=8 Hz), 2,51-2,76 (2H, m), 3,48-3,60 (2H, m), 4,15 (3H, m).
A continuación, se disolvieron 4,92 g (22,11 mmol) de este éster de (3S)-4-cloro-3-terc-butiloxi-butanoato de etilo bruto (un compuesto de la fórmula (2), en la que X = Cl, P = grupo terc-butilo, y R1 = grupo etilo) en 25 ml de tolueno y se añadieron 8 ml (28,74 mmol) de una disolución al 70 % de hidruro de sodio y bis(metoxietoxi)aluminio en tolueno al mismo a de 5°C a 15°C y se agitó la mezcla durante 2 horas a de 5°C a 10°C. A este líquido de reacción, se le añadieron secuencialmente 0,77 ml de etanol, 3,41 g de ácido cítrico y 20 ml de agua a de 5°C a 10°C y se agitó la mezcla durante 0,5 horas a de 5°C a 10°C y se lavó la fase orgánica separada con salmuera saturada, se secó, después se concentró y después se purificó mediante cromatografía en gel de sílice para obtener 3,29 g de (3S)-4-cloro-3-terc-butiloxi-butan-1-ol (un compuesto de la fórmula (3), en la que X = Cl y P = grupo terc-butilo) (rendimiento: 82 %).
1H-RMN (400 MHz, CDCh) 81,25 (9H, s), 1,80-1,88 (1H, m), 1,94-2,03 (1H, m), 2,58 (1H, m.a.), 3,44-3,56 (2H, m), 3,75 (1H, m), 3,83 (1H, m), 3,96 (1H, m).
A continuación, a 2,25 g (12,47 mmol) del (3S)-4-cloro-3-terc-butiloxi-butan-1-ol obtenido (un compuesto de la fórmula (3), en la que X = Cl y P = grupo terc-butilo), se le añadieron 23 ml de tolueno y 2,24 ml (16,21 mmol) de trietilamina y se añadieron 1,01 ml (13,09 mmol) de cloruro de metanosulfonilo al mismo a de 5°C a 10°C y se agitó la mezcla durante 2 horas a de 5°C a 10°C. Se lavó este líquido de reacción con agua, se secó y después se concentró para obtener 4,23 g (contenido puro: 3,19 g) de éster de metanosulfonato de (3S)-4-cloro-3-terc-butiloxibutilo (un compuesto de la fórmula (4), en la que X = Cl, P = grupo terc-butilo, y R2 = grupo metilo) en disolución en tolueno (rendimiento: 99 %).
1H-RMN (400 MHz, CDCh) 81,23 (9H, s), 1,88-1,96 (1H, m), 2,12-2,21 (1H, m), 3,02 (3H, s), 3,39-3,57 (2H, m), 3,86 (1H, m), 4,35 (2H, m).
[Ejemplo 4-5] Producción de éster de p-toluenosulfonato de (3S)-4-cloro-3-metoximetiloxi-butilo (un compuesto de la fórmula (4), en la que X = Cl, P = grupo metoximetilo, y R2 = grupo p-tolilo)
A 2,22 g (contenido puro: 2,00 g, 11,86 mmol) del (3S)-4-cloro-3-metoximetiloxi-butan-1-ol (un compuesto de la fórmula (3), en la que X = Cl, P = grupo metoximetilo) obtenido según el ejemplo 4, se le añadieron 9 ml de tolueno y 1,00 g (13,10 mmol) de piridina y se añadieron 2,40 g (12,50 mmol) de cloruro de p-toluenosulfonilo y 29 mg (0,24 mmol) de 4-dimetilaminopiridina a lo mismo a temperatura ambiente y se agitó la mezcla durante 16 horas a 40°C. Se lavó este líquido de reacción con agua, se secó, después se concentró y se purificó mediante cromatografía en gel de sílice para obtener 1,75 g de éster de p-toluenosulfonato de (3S)-4-cloro-3-metoximetiloxibutilo (un compuesto de la fórmula (4), en la que X = Cl, P = grupo metoximetilo, y R2 = grupo p-tolilo) (rendimiento: 46 %).
1H-RMN (400 MHz, CDCh) 81,88-2,03 (2H, m), 2,46 (3H, s), 3,35 (3H, s), 3,53-3,66 (2H, m), 3,87 (1H, m), 4,09-4,20
(4H, m), 4,61 (2H, m), 7,35 (2H, d, J=8,4 Hz), 7,79 (2H, d, J=8,4 Hz).
[Ejemplo 4-6] Producción de éster de p-toluenosulfonato de (3S)-4-cloro-3-(1-etoxietiloxi)-butilo (un compuesto de la fórmula (4), en la que X = Cl, P = grupo etoxietilo, yR 2 = grupo p-tolilo)
A 1,31 g (contenido puro: 6,23 mmol) del (3S)-4-doro-3-(1-etoxietiloxi)-butan-1-ol (un compuesto de la fórmula (3), en la que X = Cl, y P = grupo etoxietilo) obtenido según el ejemplo 4-2, se le añadieron 6,1 ml de tolueno, 0,69 g (6,85 mmol) de trietilamina, 1,19 g (6,23 mmol) de cloruro de p-toluenosulfonilo y 0,76 g (6,23 mmol) de 4-dimetilaminopiridina y se agitó la mezcla durante 33 horas a 40°C. Se lavó este líquido de reacción con agua, se secó, después se concentró y se purificó mediante cromatografía en gel de sílice para obtener 0,95 g (contenido puro: 0,44 g) de éster de p-toluenosulfonato de (3S)-4-cloro-3-(1-etoxietiloxi)-butilo (un compuesto de la fórmula (4), en la que X = Cl, P = grupo etoxietilo, y R2 = grupo p-tolilo) (rendimiento: 20 %).
1H-RMN (400 MHz, CDCla) 81,12-1,38 (6H, m), 1,80-2,10 (2H, m), 2,43 (3H, s), 3,40-3,85 (4H, m), 3,93-4,23 (3H, m), 4,80 (1H, m), 7,36 (2H, m), 7,80 (2H, m).
[Ejemplo 5] Producción de éster de (3S)-2-acetilamino-2-[4-cloro-3-(tetrahidropiran-2-iloxi)-butil]malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo metilo)
En un reactor de 20 ml, se colocaron 0,10 g (0,46 mmol) de éster de acetaminomalonato de dietilo (un compuesto de la fórmula (5), en la que R3 = grupo etilo y A = grupo metilo) y 1 ml de tolueno y se añadieron 180 |il (0,46 mmol) de etóxido de sodio al 20 % al mismo y se agitó la mezcla durante 1,5 horas a 25°C. A esta mezcla, se le añadieron 0,5 ml de la disolución en tolueno que contenía 0,15 g (contenido puro: 0,13 g, 0,46 mmol) del éster de metanosulfonato de (3S)-4-cloro-3-(tetrahidropiran-2-iloxi)-butilo bruto (un compuesto de la fórmula (4), en la que X = Cl, P = grupo tetrahidropiranilo, y R2 = grupo metilo) obtenido en el ejemplo 2, 0,08 g (0,46 mmol) de yoduro de potasio y 1 ml de etanol a 25°C y se calentó a reflujo durante la noche. Se añadió acetato de etilo a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó, después se concentró y se purificó mediante cromatografía en columna de gel de sílice para obtener 0,12 g de éster de (3S)-2-acetilamino-2-[4-cloro-3-(tetrahidropiran-2-iloxi)-butil]malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo metilo) (rendimiento: 63 %).
[Ejemplo 6] Producción de éster de (3S)-2-acetilamino-2-[4-cloro-3-(tetrahidropiran-2-iloxi)-butil]malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo metilo)
En un reactor de 50 ml, se colocaron 0,68 g (3,15 mmol) de éster de acetaminomalonato de dietilo (un compuesto de la fórmula (5), en la que R3 = grupo etilo y A = grupo metilo) y 3,4 ml de N,N-dimetilformamida y se añadieron 0,29 g (3,00 mmol) de terc-butóxido de sodio al mismo y se agitó la mezcla durante 1 hora a 30°C. A esta mezcla, se le añadieron 4 ml de la disolución en tolueno que contenía 1,01 g (contenido puro: 0,86 g, 3,00 mmol) del éster de metanosulfonato de (3S)-4-cloro-3-(tetrahidropiran-2-iloxi)-butilo bruto (un compuesto de la fórmula (4), en la que X = Cl, P = grupo tetrahidropiranilo, y R2 = grupo metilo) obtenido en el ejemplo 3 y 0,10 g (0,6 mmol) de yoduro de potasio a 30°C y se agitó la mezcla durante 7,5 horas a 60°C. Se lavó este líquido de reacción con agua, se secó y después se concentró para obtener 1,22 g (contenido puro: 1,01 g) de éster de (3S)-2-acetilamino-2-[4-cloro-3-(tetrahidropiran-2-iloxi)-butil]malonato de dietilo bruto (un compuesto de la fórmula (6), en la que X = Cl, P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo metilo) (rendimiento: 83 %).
1H-RMN (400 MHz, CDCla) 81,25 (6H, m), 1,15-1,83 (8H, m), 2,03 (3H, s), 2,30-2,50 (2H, m), 3,47-3,95 (5H, m), 4,20-4,30 (4H, m), 4,61 y 4,72 (1H, m), 6,80 (1H, s.a.).
[Ejemplo 7-1] Producción de éster de (3S)-2-acetilamino-2-(4-cloro-3-metoximetiloxi-butil)malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo metoximetilo, R3 = grupo etilo, y A = grupo metilo)
En un reactor de 30 ml, se colocaron 0,49 g (2,27 mmol) de éster de acetaminomalonato de dietilo (un compuesto de la fórmula (5), en la que R3 = grupo etilo y A = grupo metilo) y 2,5 ml de dimetilsulfóxido y se añadieron 0,23 g (2,38 mmol) de terc-butóxido de sodio al mismo y se agitó la mezcla durante 2 horas a 30°C. A esta mezcla, se le añadieron 2,5 ml de la disolución en tolueno que contenía 0,56 g (2,27 mmol) del éster de metanosulfonato de (3S)-4-cloro-3-metoximetiloxi-butilo bruto (un compuesto de la fórmula (4), en la que X = Cl, P = grupo metoximetilo, y R2 = grupo metilo) obtenido en el ejemplo 4 y 0,08 g (0,45 mmol) de yoduro de potasio a 30°C y se agitó la mezcla durante 5 horas a 80°C. Se extrajo una alícuota de 200 |il de este líquido de reacción y se añadió acetato de etilo a la misma y se lavó la mezcla resultante con agua, se secó y después se concentró para obtener 25 mg de éster de (3S)-2-acetilamino-2-(4-cloro-3-metoximetiloxi-butil)malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo metoximetilo, R3 = grupo etilo, y A = grupo metilo) (rendimiento: 94 %).1
1H-RMN (400 MHz, CDCh) 81,23 (6H, t, J=5,2 Hz), 1,33-1,50 (2H, m), 2,01 (3H, s), 2,30-2,46 (2H, m), 3,36 (3H, s), 3,55 (2H, d, J=5,2 Hz), 3,67 (1H, m), 4,21 (4H, q, J=7,3 Hz), 4,64 (2H, dd, J=7,2, 18 Hz), 6,77 (1H, s.a.).
[Ejemplo 7-2] Producción de éster de (3S)-2-acetilamino-2-(4-cloro-3-(1-etoxietiloxi)-butil)malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo etoxietilo, R3 = grupo etilo, y A = grupo metilo)
En un reactor de 50 ml, se colocaron 4,95 g (22,82 mmol) de éster de acetaminomalonato de dietilo (un compuesto de la fórmula (5), en la que R3 = grupo etilo y A = grupo metilo) y 22 ml de N,N-dimetilformamida y se añadieron 2,15 g (22,40 mmol) de terc-butóxido de sodio al mismo y se agitó la mezcla durante 1,5 horas a 40°C. A esta mezcla, se le añadieron 10,83 g (contenido puro: 5,33 g, 19,41 mmol) de la disolución en tolueno que contenía el éster de metanosulfonato de (3S)-4-cloro-3-(1-etoxietiloxi)-butilo bruto (un compuesto de la fórmula (4), en la que X = Cl, P = grupo etoxietilo, y R2 = grupo metilo) obtenido en el ejemplo 4-2, 4 ml de tolueno y 0,69 g (4,16 mmol) de yoduro de potasio a 40°C y se agitó la mezcla durante 2 horas a 80°C. Se añadió tolueno a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó y después se concentró para obtener 7,64 g (contenido puro: 7,14 g; rendimiento: 93 %) de éster de (3S)-2-acetilamino-2-(4-cloro-3-(1-etoxietiloxi)-butil)malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo etoxietilo, R3 = grupo etilo, y A = grupo metilo).
1H-RMN (400 MHz, CDCla) 81,15-1,32 (12H, m), 1,30-1,60 (2H, m), 2,03 (3H, s), 2,30-2,52 (2H, m), 3,47-3,83 (5H, m), 4,23 (4H, q, J=7,0 Hz), 4,73 y 4,81 (1H, m), 6,78 (1H, s.a.).
[Ejemplo 7-3] Producción de éster de (3S)-2-acetilamino-2-(4-cloro-3-terc-butildimetilsililoxi-butil)malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo terc-butildimetilsililo, R3 = grupo etilo, y A = grupo metilo)
En un reactor de 50 ml, se colocaron 1,15 g (5,29 mmol) de éster de acetaminomalonato de dietilo (un compuesto de la fórmula (5), en la que R3 = grupo etilo y A = grupo metilo) y 6,8 ml de N,N-dimetilformamida y se añadieron 0,50 g (5,19 mmol) de terc-butóxido de sodio al mismo y se agitó la mezcla durante 1 hora a 40°C. A esta mezcla, se le añadieron 1,70 g (contenido puro: 1,52 g, 4,81 mmol) de la disolución en tolueno que contenía el éster de metanosulfonato de (3S)-4-cloro-3-terc-butildimetilsililoxi-butilo bruto (un compuesto de la fórmula (4), en la que X = Cl, P = grupo terc-butildimetilsililo, y R2 = grupo metilo) obtenido en el ejemplo 4-3, 1 ml de tolueno y 0,16 g (0,96 mmol) de yoduro de potasio a 40°C y se agitó la mezcla durante 4 horas a 80°C. Se añadió tolueno a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó y después se concentró para obtener 2,10 g (contenido puro: 1,77 g; rendimiento: 84 %) de éster de (3S)-2-acetilamino-2-(4-cloro-3-tercbutildimetilsililoxi-butil)malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo tercbutildimetilsililo, R3 = grupo etilo, y A = grupo metilo).
1H-RMN (400 MHz, CDCla) 80,09 (6H, s), 0,90 (9H, s), 1,24 (6H, t, J=7,5 Hz), 1,29-1,55 (2H, m), 2,02 (3H, s), 2,30 2,50 (2H, m), 3,42 (2H, m), 3,83 (1H, m), 4,25 (4H, m), 6,75 (1H, s.a.).
[Ejemplo 7-4] Producción de éster de (3S)-2-acetilamino-2-(4-cloro-3-terc-butiloxibutil)malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo terc-butilo, R3 = grupo etilo, y A = grupo metilo)
En un reactor de 50 ml, se colocaron 0,87 g (4,00 mmol) de éster de acetaminomalonato de dietilo (un compuesto de la fórmula (5), en la que R3 = grupo etilo y A = grupo metilo) y 4,3 ml de N,N-dimetilformamida y se añadieron 0,38 g (3,92 mmol) de terc-butóxido de sodio al mismo y se agitó la mezcla durante 1 hora a 40°C. A esta mezcla, se le añadieron 1,25 g (contenido puro: 0,94 g, 3,64 mmol) de la disolución en tolueno que contenía el éster de metanosulfonato de (3S)-4-cloro-3-terc-butiloxi-butilo bruto (un compuesto de la fórmula (4), en la que X = Cl, P = grupo terc-butilo, y R2 = grupo metilo) obtenido en el ejemplo 4-4, 2 ml de tolueno y 0,12 g (0,73 mmol) de yoduro de potasio a 40°C y se agitó la mezcla durante 2 horas a 80°C. Se añadió tolueno a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó, después se concentró y se purificó mediante cromatografía en gel de sílice para obtener 1,06 g (contenido puro: 0,95 g; rendimiento: 69 %) de éster de (3S)-2-acetilamino-2-(4-cloro-3-terc-butiloxi-butil)malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo terc-butilo, R3 = grupo etilo, y A = grupo metilo).
1H-RMN (400 MHz, CDCh) 81,19 (9H, s), 1,25 (6H, t, J=7,2 Hz), 1,30-1,38 (1H, m), 1,49-1,59 (1H, m), 2,03 (3H, s), 2,30-2,47 (2H, m), 3,33-3,49 (2H, m), 3,65 (1H, m), 4,27 (4H, q, J=7,2 Hz), 6,78 (1H, s.a.).
[Ejemplo 7-5] Producción de éster de (3S)-2-acetilamino-2-(4-cloro-3-metoximetiloxi-butil)malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo metoximetilo, R3 = grupo etilo, y A = grupo metilo)
En un reactor de 50 ml, se colocaron 1,04 g (4,81 mmol) de éster de acetaminomalonato de dietilo (un compuesto de la fórmula (5), en la que R3 = grupo etilo y A = grupo metilo) y 5,4 ml de N,N-dimetilformamida y se añadieron 0,45 g (4,72 mmol) de terc-butóxido de sodio al mismo y se agitó la mezcla durante 1 hora a 40°C. A esta mezcla, se le añadieron 5,1 ml de la disolución en tolueno que contenía 1,80 g (contenido puro: 1,41 g, 4,37 mmol) del éster de ptoluenosulfonato de (3S)-4-cloro-3-metoximetiloxi-butilo bruto (un compuesto de la fórmula (4), en la que X = Cl, P = grupo metoximetilo, y R2 = grupo p-tolilo) obtenido en el ejemplo 4-5 y 0,15 g (0,87 mmol) de yoduro de potasio a 40°C y se agitó la mezcla durante 2 horas a 80°C. Se añadió tolueno a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó y después se concentró para obtener 2,08 g (contenido puro: 1,45 g; rendimiento: 90 %) de éster de (3S)-2-acetilamino-2-(4-cloro-3-metoximetiloxi-butil)malonato de dietilo (un
compuesto de la fórmula (6), en la que X = Cl, P = grupo metoximetilo, R3 = grupo etilo, y A = grupo metilo).
[Ejemplo 8-1] Producción de éster de (3S)-2-benzoilamino-2-[4-cloro-3-(tetrahidropiran-2-iloxi)-butil]malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo tetrahidropiranilo, y R3 = grupo etilo, y A = grupo fenilo)
En un reactor de 30 ml, se colocaron 0,38 g (1,37 mmol) de éster de benzoilaminomalonato de dietilo (un compuesto de la fórmula (5), en la que R3 = grupo etilo y A = grupo fenilo) y 1,9 ml de N,N-dimetilformamida y se añadieron 0,13 g (1,37 mmol) de terc-butóxido de sodio al mismo y se agitó la mezcla durante 1 hora a temperatura ambiente. A esta mezcla, se le añadieron 1,9 ml de la disolución en tolueno que contenía 0,51 g (contenido puro: 0,39 g, 1,37 mmol) del éster de metanosulfonato de (3S)-4-cloro-3-(tetrahidropiran-2-iloxi)-butilo bruto (un compuesto de la fórmula (4), en la que X = Cl, P = grupo tetrahidropiranilo, y R2 = grupo metilo) obtenido en el ejemplo 3 y 0,09 g (0,55 mmol) de yoduro de potasio a temperatura ambiente y se agitó la mezcla durante 1 hora a 80°C. Se extrajo un pequeño volumen de alícuota de este líquido de reacción y se añadió tolueno a la misma y se lavó la mezcla resultante con agua, se secó y después se concentró para obtener 27 mg de éster de (3S)-2-benzoilamino-2-[4-cloro-3-(tetrahidropiran-2-iloxi)-butil]malonato de dietilo bruto (un compuesto de la fórmula (6), en la que X = Cl, P = grupo tetrahidropiranilo, y R3 = grupo etilo, y A = grupo fenilo).
1H-RMN (400 MHz, CDCla) 81,20 (6H, m), 1,32-1,80 (8H, m), 1,97-2,20 (1H, m), 2,40-2,57 (1H, m), 3,16-3,92 (5H, m), 4,20 (4H, m), 4,52 y 4,65 (1H, m), 7,30 (3H, m), 7,80 (2H, m).
[Ejemplo 8-2] Producción de éster de (3S)-2-benzoilamino-2-[4-cloro-3-(metoximetiloxi-butil]malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo metoximetilo, R3 = grupo etilo, y A = grupo fenilo)
En un reactor de 50 ml, se colocaron 1,87 g (6,69 mmol) de éster de benzoilaminomalonato de dietilo (un compuesto de la fórmula (5), en la que R3 = grupo etilo y A = grupo fenilo) y 5,7 ml de N,N-dimetilformamida y se añadieron 0,63 g (6,57 mmol) de terc-butóxido de sodio al mismo y se agitó la mezcla durante 1 hora a 40°C. A esta mezcla, se le añadieron 6 ml de la disolución en tolueno que contenía 1,50 g (6,08 mmol) del éster de metanosulfonato de (3S)-4-cloro-3-(tetrahidropiran-2-iloxi)-butilo bruto (un compuesto de la fórmula (4), en la que X = Cl, P = grupo metoximetilo, y R2 = grupo metilo) obtenido en el ejemplo 3 y 0,20 g (1,22 mmol) de yoduro de potasio a 40°C y se agitó la mezcla durante 2 horas a 80°C. Se añadió tolueno a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó y después se concentró para obtener 2,83 g (contenido puro: 2,20 g; rendimiento: 84 %) de éster de (3S)-2-benzoilamino-2-[4-cloro-3-metoximetiloxi-butil]malonato de dietilo bruto (un compuesto de la fórmula (6), en la que X = Cl, P = grupo metoximetilo, R3 = grupo etilo, y A = grupo fenilo).
1H-RMN (400 MHz, CDCla) 81,26 (6H, t, J=7,5 Hz), 1,20-1,85 (8H, m), 2,45-2,65 (2H, m), 3,40-3,92 (5H, m), 4,29 (4H, m), 4,60 y 4,71 (1H, m), 7,42-7,55 (4H, m), 7,82 (2H, m).
[Ejemplo 8-3] Producción de éster de (3S)-2-benzoilamino-2-[4-cloro-3-(1-etoxietiloxi)-butil]malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo etoxietilo, R3 = grupo etilo, y A = grupo fenilo)
En un reactor de 30 ml, se colocaron 2,31 g (8,27 mmol) de éster de benzoilaminomalonato de dietilo (un compuesto de la fórmula (5), en la que R3 = grupo etilo y A = grupo fenilo) y 8 ml de N,N-dimetilformamida y se añadieron 0,78 g (8,12 mmol) de terc-butóxido de sodio al mismo y se agitó la mezcla durante 2 horas a 40°C. A esta mezcla, se le añadieron 4 ml de la disolución en tolueno que contenía 2,06 g (contenido puro: 1,99 g, 7,52 mmol) del éster de metanosulfonato de (3S)-4-cloro-3-(1-etoxietiloxi)-butilo bruto (un compuesto de la fórmula (4), en la que X = Cl, P = grupo etoxietilo, y R2 = grupo metilo) obtenido según el ejemplo 4-2 y 0,25 g (1,50 mmol) de yoduro de potasio a 40°C y se agitó la mezcla durante 4,5 horas a 80°C. Se añadió tolueno a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó, después se concentró y se purificó mediante cromatografía en gel de sílice para obtener 2,31 g de éster de (3S)-2-benzoilamino-2-[4-cloro-3-(1-etoxietiloxi)-butil]malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo etoxietilo, R3 = grupo etilo, y A = grupo fenilo) (rendimiento: 67 %).
1H-RMN (400 MHz, CDCh) 81,13-1,35 (12H, m), 1,40-1,63 (2H, m), 2,45-2,65 (2H, m), 3,43-3,83 (5H, m), 4,30 (4H, m), 4,72 y 4,80 (1H, m), 7,43-7,58 (4H, m), 7,83 (2H, m).
[Ejemplo 8-4] Producción de éster de (3S)-2-benzoilamino-2-[4-cloro-3-terc-butildimetilsililoxi-butil]malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo terc-butildimetilsililo, R3 = grupo etilo, y A = grupo fenilo)
En un reactor de 30 ml, se colocaron 1,48 g (5,29 mmol) de éster de benzoilaminomalonato de dietilo (un compuesto de la fórmula (5), en la que R3 = grupo etilo y A = grupo fenilo) y 6,8 ml de N,N-dimetilformamida y se añadieron 0,50 g (5,19 mmol) de terc-butóxido de sodio al mismo y se agitó la mezcla durante 1 hora a 40°C. A esta mezcla, se le añadieron 1 ml de la disolución en tolueno que contenía 1,70 g (contenido puro: 1,52 g, 4,81 mmol) del éster de metanosulfonato de (3S)-4-cloro-3-terc-butildimetilsililoxi-butilo bruto (un compuesto de la fórmula (4), en la que X = Cl, P = grupo terc-butildimetilsililo, y R2 = grupo metilo) obtenido en el ejemplo 4-3 y 0,16 g (0,96 mmol) de yoduro de
potasio a 40°C y se agitó la mezcla durante 4,5 horas a 80°C. Se añadió tolueno a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó y después se concentró para obtener 2,68 g de éster de (3S)-2-benzoilamino-2-[4-doro-3-terc-butildimetilsililoxi-butil]malonato de dietilo bruto (un compuesto de la fórmula (6), en la que X = Cl, P = grupo terc-butildimetilsililo, R3 = grupo etilo, y A = grupo fenilo) (contenido puro: 1,95 g; rendimiento: 81 %).
1H-RMN (400 MHz, CDCls) 80,10 (6H, s), 0,90 (9H, s), 1,30 (6H, t, J=8,3 Hz), 1,35-1,65 (2H, m), 2,48-2,65 (2H, m), 3,43 (2H, m), 3,85 (1H, m), 4,33 (4H, m), 7,45-7,60 (4H, m), 7,84 (2H, m).
[Ejemplo 8-5] Producción de éster de (3S)-2-benzoilamino-2-[4-cloro-3-terc-butiloxi-butil]malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo terc-butilo, R3 = grupo etilo, y A = grupo fenilo)
En un reactor de 50 ml, se colocaron 1,12 g (4,00 mmol) de éster de benzoilaminomalonato de dietilo (un compuesto de la fórmula (5), en la que R3 = grupo etilo y A = grupo fenilo) y 4,4 ml de N,N-dimetilformamida y se añadieron 0,38 g (3,92 mmol) de terc-butóxido de sodio al mismo y se agitó la mezcla durante 1 hora a 40°C. A esta mezcla, se le añadieron 2 ml de la disolución en tolueno que contenía 1,25 g (contenido puro: 0,94 g, 3,64 mmol) del éster 4-cloro-3-terc-butiloxi-butílico del ácido (3S)metanosulfónico bruto (un compuesto de la fórmula (4), en la que X = Cl, P = grupo terc-butilo, yR2= grupo metilo) obtenido en el ejemplo 4-4 y 0,12 g (0,73 mmol) de yoduro de potasio a 40°C y se agitó la mezcla durante 2 horas a 80°C. Se añadió tolueno a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó, después se concentró y se purificó mediante cromatografía en gel de sílice para obtener 1,24 g de éster de (3S)-2-benzoilamino-2-[4-cloro-3-terc-butiloxi-butil]malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo terc-butilo, R3 = grupo etilo, y A = grupo fenilo) (contenido puro: 1,10 g; rendimiento: 69 %).
1H-RMN (400 MHz, CDCla) 81,16 (9H, s), 1,25-1,29 (7H, m), 1,31-1,42 (1H, m), 2,48-2,57 (2H, m), 3,34-3,49 (2H, m), 3,65 (1H, m), 4,28 (4H, q, J=6,8 Hz), 7,44-7,53 (4H, m), 7,81 (2H, m).
[Ejemplo 9] Producción de éster de (5S)-1-acetil-5-(tetrahidropiran-2-iloxi)-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo metilo)
En un reactor de 100 ml, se colocaron 5,08 g (contenido puro: 4,35 g, 10,68 mmol) del éster de (3S)-2-acetilamino-2-[4-cloro-3-(tetrahidropiran-2-iloxi)-butil]malonato de dietilo bruto (un compuesto de la fórmula (6), en la que X = Cl, P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo metilo) obtenido en el ejemplo 5, 40 ml de dimetilformamida y 10,44 g (32,04 mmol) de carbonato de cesio y se agitó la mezcla durante 7 horas a 100°C. Se añadió tolueno a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó y después se concentró para obtener 4,18 g de éster de (5S)-1-acetil-5-(tetrahidropiran-2-iloxi)-piperidin-2,2-dicarboxilato de dietilo bruto (un compuesto de la fórmula (7), en la que P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo metilo) (rendimiento: 94 %).
1H-RMN (400 MHz, CDCla) 81,15-1,25 (6H, m), 1,32-1,95 (8H, m), 1,95-2,10 (1H, m), 2,10 (3H, s), 2,40-2,50 (1H, m), 3,02 y 3,22 (1H, m), 3,43 (1H, m), 3,55-3,70 (1H, m), 3,72-3,88 (2H, m), 4,10-4,25 (4H, m), 4,65 (1H, m).
[Ejemplo 10] Producción de éster de (5S)-1-acetil-5-(tetrahidropiran-2-iloxi)-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo metilo)
En un reactor de 100 ml, se colocaron 5,77 g (contenido puro: 4,95 g, 12,14 mmol) del éster de (3S)-2-acetilamino-2-[4-cloro-3-(tetrahidropiran-2-iloxi)-butil]malonato de dietilo bruto (un compuesto de la fórmula (6), en la que X = Cl, P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo metilo) obtenido en el ejemplo 5 y 58 ml de dimetilformamida y se colocaron 1,52 g (15,78 mmol) de terc-butóxido de sodio en el mismo en tres porciones a lo largo de 3 horas a 15°C y se agitó la mezcla durante 2 horas a 15°C. Se neutralizó una cantidad en exceso de la base añadiendo 0,22 ml de ácido acético a este líquido de reacción, se añadió tolueno al mismo y se lavó la mezcla resultante con agua, se secó y después se concentró para obtener 3,85 g (contenido puro: 2,77 g; rendimiento: 62 %) de éster de (5S)-1-acetil-5-(tetrahidropiran-2-iloxi)-piperidin-2,2-dicarboxilato de dietilo bruto (un compuesto de la fórmula (7), en la que P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo metilo).
[Ejemplo 11-1] Producción de éster de (5S)-1-acetil-5-(tetrahidropiran-2-iloxi)-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo metilo)
En un reactor de 10 ml, se colocaron 0,53 g (contenido puro: 0,5 g, 1,23 mmol) del éster de (3S)-2-acetilamino-2-[4-cloro-3-(tetrahidropiran-2-iloxi)-butil]malonato de dietilo bruto (un compuesto de la fórmula (6), en la que X = Cl, P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo metilo) obtenido en el ejemplo 5 y 2,7 ml de dimetilformamida y se colocaron carbonato de potasio (1,23 mmol) y bromuro de tetrabutilamonio (denominado a continuación en el presente documento “TBAB”) (1,227 mmol) en el mismo y se agitó la mezcla durante 15 horas a 100°C.
Se añadió tolueno a la mezcla y se lavó la mezcla resultante con salmuera, se secó y después se concentró para
obtener 0,61 g (contenido puro: 0,37 g; rendimiento: 80 %) de éster de (5S)-1-acetil-5-(tetrahidropiran-2-iloxi)-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo metilo).
[Ejemplo 11-2] Producción de éster de (5S)-1-acetil-5-metoximetiloxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo metoximetilo, R3 = grupo etilo, y A = grupo metilo)
En un reactor de 50 ml, se colocaron 1,41 g (contenido puro: 1,12 g, 3,04 mmol) del éster de (3S)-2-acetilamino-2-[4-cloro-3-metoximetiloxi-butil]malonato de dietilo bruto (un compuesto de la fórmula (6), en la que X = Cl, P = grupo metoximetilo, R3 = grupo etilo, y A = grupo metilo) obtenido según el ejemplo 7, 5,3 ml de dimetilformamida y 2,97 g (9,12 mmol) de carbonato de cesio y se agitó la mezcla durante 3 horas a 100°C. Se añadió tolueno a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó y después se concentró para obtener 0,95 g (contenido puro: 0,87 g; rendimiento: 87 %) de éster de (5S)-1-acetil-5-metoximetiloxi-piperidin-2,2-dicarboxilato de dietilo bruto (un compuesto de la fórmula (7), en la que P = grupo metoximetilo, R3 = grupo etilo, y A = grupo metilo).
1H-RMN (400 MHz, CDCh) 81,27-1,31 (6H, m), 1,50-1,59 (1H, m), 1,80-1,90 (1H, m), 2,08-2,17 (1H, m), 2,17 (3H, s), 2,48-2,55 (1H, m), 3,28-3,40 (1H, m), 3,40 (3H, s), 3,63 (1H, m), 3,76 (1H, m), 4,18-4,30 (4H, m), 4,71 (2H, m).
[Ejemplo 11-3] Producción de éster de (5S)-1-acetil-5-(1-etoxietiloxi)-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo etoxietilo, R3 = grupo etilo, y A = grupo metilo)
En un reactor de 100 ml, se colocaron 7,64 g (contenido puro: 7,14 g, 18,06 mmol) del éster de (3S)-2-acetilamino-2-[4-cloro-3-(1-etoxietiloxi)-butil]malonato de dietilo bruto (un compuesto de la fórmula (6), en la que X = Cl, P = grupo etoxietilo, R3 = grupo etilo, y A = grupo metilo) obtenido en el ejemplo 7-2 y 17,1 ml de dimetilformamida y se añadieron 853 mg (21,40 mmol) de hidruro de sodio al 60 % en porciones a lo largo de 5 horas a 40°C. A este líquido de reacción, se le añadieron 0,43 ml de ácido acético y tolueno y se lavó la mezcla resultante con agua y carbonato de potasio acuoso al 2 %, se secó y después se concentró para obtener 5,64 g (contenido puro: 5,31 g; rendimiento: 77 %) de éster de (5S)-1-acetil-5-(1-etoxietiloxi)-piperidin-2,2-dicarboxilato de dietilo bruto (un compuesto de la fórmula (7), en la que P = grupo etoxietilo, R3 = grupo etilo, y A = grupo metilo).
1H-RMN (400 MHz, CDCla) 81,20-1,35 (12H, m), 1,35-1,50 (1H, m), 1,90 (1H, m), 2,03-2,12 (1H, m), 2,14 (3H, s), 2,47-2,55 (1H, m), 3,02-3,15 y 3,44-3,86 (5H, m), 4,20-4,35 (4H, m), 4,81 (1H, m).
[Ejemplo 11-4] Producción de éster de (5S)-1-acetil-5-terc-butildimetilsililoxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo terc-butildimetilsililo, R3 = grupo etilo, y A = grupo metilo)
En un reactor de 50 ml, se colocaron 2,10 g (contenido puro: 1,77 g, 4,05 mmol) del éster de (3S)-2-acetilamino-2-[4-cloro-3-terc-butildimetilsililoxi-butil]malonato de dietilo bruto (un compuesto de la fórmula (6), en la que X = Cl, P = grupo terc-butildimetilsililo, R3 = grupo etilo, y A = grupo metilo) obtenido en el ejemplo 7-3, 8,4 ml de dimetilformamida y 3,96 g (12,15 mmol) de carbonato de cesio y se agitó la mezcla durante 3 horas a 100°C. Se añadió tolueno a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó, después se concentró y se purificó mediante cromatografía en gel de sílice para obtener 1,18 g (contenido puro: 1,13 g; rendimiento: 70 %) de éster de (5S)-1-acetil-5-terc-butildimetilsililoxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo terc-butildimetilsililo, R3 = grupo etilo, y A = grupo metilo).
1H-RMN (400 MHz, CDCla) 80,09 (3H, s), 0,10 (3H, s), 0,90 (9H, s), 1,25-1,30 (6H, m), 1,30-1,40 (1H, m), 1,75-1,85 (1H, m), 2,03-2,10 (1H, m), 2,15 (3H, s), 2,49-2,58 (1H, m), 3,02 (1H, dd, J=10,6, 12,1 Hz), 3,58 (1H, dd, J=3,0, 12,1 Hz), 3,83 (1H, m), 4,17-4,31 (4H, m).
[Ejemplo 11-5] Producción de éster de (5S)-1-acetil-5-terc-butiloxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo terc-butilo, R3 = grupo etilo, y A = grupo metilo)
En un reactor de 50 ml, se colocaron 1,06 g (contenido puro: 0,95 g, 2,50 mmol) del éster de (3S)-2-acetilamino-2-[4-cloro-3-terc-butiloxi-butil]malonato de dietilo bruto (un compuesto de la fórmula (6), en la que X = Cl, P = grupo tercbutilo, R3 = grupo etilo, y A = grupo metilo) obtenido en el ejemplo 7-4, 4 ml de dimetilformamida y 2,44 g (7,50 mmol) de carbonato de cesio y se agitó la mezcla durante 4 horas a 100°C. Se añadió tolueno a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó y después se concentró para obtener 0,73 g (contenido puro: 0,64 g; rendimiento: 75 %) de éster de (5S)-1-acetil-5-terc-butiloxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo terc-butilo, R3 = grupo etilo, y A = grupo metilo).
1H-RMN (400 MHz, CDCh) 81,22 (9H, s), 1,25-1,32 (6H, m), 1,35 (1H, m), 1,83-1,87 (1H, m), 2,00-2,07 (1H, m), 2,15 (3H, s), 2,50-2,56 (1H, m), 2,85-2,91 (1H, m), 3,63-3,66 (2H, m), 4,20-4,27 (4H, m).
[Ejemplo 11-6] Producción de éster de (5S)-1-benzoil-5-(tetrahidropiran-2-iloxi)-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo fenilo)
En un reactor de 50 ml, se colocaron 3,09 g (6,57 mmol) del éster de (3S)-2-benzoilamino-2-[4-cloro-3-(tetrahidropiran-2-iloxi)-butil]malonato de dietilo bruto (un compuesto de la fórmula (6), en la que X = Cl, P = grupo tetrahidropiranilo, y R3 = grupo etilo, y A = grupo fenilo) obtenido según el ejemplo 8, 12 ml de dimetilformamida y 6,42 g (19,71 mmol) de carbonato de cesio y se agitó la mezcla durante 4,5 horas a 100°C. Se añadió tolueno a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó, después se concentró y se purificó mediante cromatografía en gel de sílice para obtener 2,08 g (contenido puro: 1,88 g; rendimiento: 66 %) de éster de (5S)-1-benzoil-5-(tetrahidropiran-2-iloxi)-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo fenilo).
1H-RMN (400 MHz, CDCh) 81,23-1,35 (6H, m), 1,43-1,95 (8H, m), 2,20-2,31 (1H, m), 2,57-2,69 (1H, m), 3,22-3,89 (5H, m), 4,22-4,32 (4H, m), 4,50 y 4,69 (1H, m) 7,40 (3H, m), 7,53-7,61 (2H, m).
[Ejemplo 11-7] Producción de éster de (5S)-1-benzoil-5-metoximetiloxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo metoximetilo, R3 = grupo etilo, y A = grupo fenilo) En un reactor de 50 ml, se colocaron 1,42 g (contenido puro: 1,10 g, 2,56 mmol) del éster de (3S)-2-benzoilamino-2-[4-cloro-3-metoximetiloxi)-butil]malonato de dietilo bruto (un compuesto de la fórmula (6), en la que X = Cl, P = grupo metoximetilo, R3 = grupo etilo, y A = grupo fenilo) obtenido según el ejemplo 8-2, 5,2 ml de dimetilformamida y 2,50 g (7,68 mmol) de carbonato de cesio y se agitó la mezcla durante 3 horas a 100°C. Se añadió tolueno a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó y después se concentró para obtener 0,99 g (contenido puro: 0,93 g; rendimiento: 92 %) de éster de (5S)-1-benzoil-5-metoximetiloxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo metoximetilo, R3 = grupo etilo, y A = grupo fenilo).
1H-RMN (400 MHz, CDCla) 81,29-1,34 (6H, m), 1,58-1,68 (1H, m), 1,81-1,90 (1H, m), 2,21-2,30 (1H, m), 2,55-2,65 (1H, m), 3,20-3,30 (1H, m), 3,28 (3H, s), 3,40 (1H, m), 3,58 (1H, dd, J=3,2, 14,0 Hz), 3,75 (1H, m), 4,20-4,39 (4H, m), 4,54 y 4,63 (1H, d, J=7,2 Hz), 7,42 (3H, m), 7,55 (2H, m).
[Ejemplo 11-8] Producción de éster de (5S)-1-benzoil-5-(1-etoxietiloxi)-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo etoxietilo, R3 = grupo etilo, y A = grupo fenilo)
En un reactor de 50 ml, se colocaron 2,31 g (5,04 mmol) del éster de (3S)-2-benzoilamino-2-[4-cloro-3-(1-etoxietiloxi)-butil]malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo etoxietilo, R3 = grupo etilo, y A = grupo fenilo) obtenido en el ejemplo 8-3, 9,2 ml de dimetilformamida y 4,93 g (15,12 mmol) de carbonato de cesio y se agitó la mezcla durante 5 horas a 100°C. Se añadió tolueno a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó y después se concentró para obtener 0,92 g de éster de (5S)-1-benzoil-5-(1-etoxietiloxi)-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo etoxietilo, R3 = grupo etilo, y A = grupo fenilo) (rendimiento: 43 %).
1H-RMN (400 MHz, CDCla) 80,99-1,10 (3H, m), 1,17-1,35 (9H, m), 1,45-1,60 (1H, m), 1,83-1,92 (1H, m), 2,18-2,26 (1H, m), 2,57-2,65 (1H, m), 3,11 (1H, m), 4,20-4,33 (4H, m), 4,61 y 4,73 (1H, m), 7,40 (3H, m), 7,52 (2H, m).
[Ejemplo 11-9] Producción de éster de (5S)-1-benzoil-5-terc-butildimetilsililoxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo terc-butildimetilsililo, R3 = grupo etilo, y A = grupo fenilo)
En un reactor de 50 ml, se colocaron 2,68 g (contenido puro: 1,95 g, 3,91 mmol) del éster de (3S)-2-benzoilamino-2-[4-cloro-3-terc-butildimetilsililoxi-butil]malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo terc-butildimetilsililo, R3 = grupo etilo, y A = grupo fenilo) obtenido en el ejemplo 8-4, 10,7 ml de dimetilformamida, 3,82 g (11,73 mmol) de carbonato de cesio y se agitó la mezcla durante 3 horas a 100°C. Se añadió tolueno a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó, después se concentró y se purificó mediante cromatografía en gel de sílice para obtener 1,70 g (contenido puro: 1,45 g; rendimiento: 80 %) de éster de (5S)-1-benzoil-5-terc-butildimetilsililoxipiperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo terc-butildimetilsililo, R3 = grupo etilo, y A = grupo fenilo).
1H-RMN (400 MHz, CDCh) 80,02 (3H, s), 0,03 (3H, s), 0,90 (9H, s), 1,32 (6H, m), 1,50-1,59 (1H, m), 1,77-1,85 (1H, m), 2,20-2,30 (1H, m), 2,62-2,70 (1H, m), 3,16 (1H, dd, J=6,9, 12,0 Hz), 3,50 (1H, dd, J=1,7, 13,7 Hz), 3,83 (1H, m), 4,23-4,37 (4H, m), 4,65 (1H, m), 7,42 (3H, m), 7,58 (2H, m).
[Ejemplo 11-10] Producción de éster de (5S)-1-benzoil-5-terc-butiloxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo terc-butilo, R3 = grupo etilo, y A = grupo fenilo)
En un reactor de 50 ml, se colocaron 1,24 g (contenido puro: 1,10 g, 2,50 mmol) del éster de (3S)-2-benzoilamino-2-[4-cloro-3-terc-butiloxi-butil]malonato de dietilo (un compuesto de la fórmula (6), en la que X = Cl, P = grupo tercbutilo, R3 = grupo etilo, y A = grupo fenilo) obtenido en el ejemplo 8-5, 5 ml de dimetilformamida y 2,44 g (7,50 mmol) de carbonato de cesio y se agitó la mezcla durante 4 horas a 100°C. Se añadió tolueno a este líquido de reacción y se lavó el líquido de reacción resultante con agua, se secó y después se concentró para obtener 1,06 g (contenido puro: 0,84 g; rendimiento: 83 %) de éster de (5S)-1-benzoil-5-terc-butiloxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (7), en la que P = grupo terc-butilo, R3 = grupo etilo, y A = grupo fenilo).
1H-RMN (400 MHz, CDCI3) 81,11 (9H, s), 1,28-1,33 (6H, m), 1,42 (1H, m), 1,80-1,86 (1H, m), 2,17-2,24 (1H, m), 2,60-2,66 (1H, m), 2,94-2,99 (1H, m), 3,56-3,63 (2H, m), 4,26-4,31 (4H, m), 7,38-7,43 (3H, m), 7,54 (2H, m).
[Ejemplo 12-1] Producción de éster de (5S)-1-acetil-5-hidroxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo metilo)
En un reactor de 100 ml, se colocaron 4,18 g (10,68 mmol) del éster de (5S)-1-acetil-5-(tetrahidropiran-2-iloxi)-piperidin-2,2-dicarboxilato de dietilo bruto (un compuesto de la fórmula (7), en la que P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo metilo) obtenido en el ejemplo 10, 20 ml de metanol y 19 |il de ácido clorhídrico concentrado y se agitó la mezcla durante 4 horas a temperatura ambiente. Se detuvo la reacción añadiendo 45 |il de trietilamina a este líquido de reacción y se concentró metanol a vacío para obtener 3,7 g de una sustancia aceitosa. A continuación, se disolvió esta sustancia aceitosa en 20 ml de tolueno, se añadieron 10 ml de n-heptano a la misma a temperatura ambiente para la cristalización y se añadieron otros 10 ml de n-heptano a la misma para permitir avanzar la cristalización envejeciendo a temperatura ambiente y después se filtraron los cristales, se lavaron con nheptano y se secaron para obtener 2,30 g de éster de (5S)-1-acetil-5-hidroxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo metilo) (rendimiento: 75 %).
1H-RMN (400 MHz, CDCla) 81,20-1,30 (6H, m), 1,40-1,52 (1H, m), 1,80-1,90 (1H, m), 2,09-2,15 (1H, m), 2,15 (3H, s), 2,40-2,50 (1H, m), 3,23 (1H, dd, J=7,6, 14,4 Hz), 3,57 (1H, dd, J=4,8, 12,8 Hz), 3,92 (1H, m), 4,17-4,32 (4H, m).
[Ejemplo 12-2] Producción de éster de (5S)-1-acetil-5-hidroxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo metilo)
En un reactor de 50 ml, se colocaron 1,45 g (contenido puro: 1,28 g, 3,57 mmol) del éster de (5S)-1-acetil-5-(1-etoxietiloxi)-piperidin-2,2-dicarboxilato de dietilo bruto (un compuesto de la fórmula (7), en la que P = grupo etoxietilo, R3 = grupo etilo, y A = grupo metilo) obtenido en el ejemplo 11-3, 7,25 ml de metanol y 10 |il de ácido clorhídrico concentrado y se agitó la mezcla durante 4 horas a temperatura ambiente. Se concentró este líquido de reacción a vacío y se purificó mediante cromatografía en gel de sílice para obtener 0,79 g de éster de (5S)-1-acetil-5-hidroxipiperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo metilo) (rendimiento: 77 %).
[Ejemplo 12-3] Producción de éster de (5S)-1-acetil-5-hidroxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo metilo)
En un reactor de 10 ml, se colocaron 355 mg (contenido puro: 342 mg, 0,85 mmol) del éster de (5S)-1-acetil-5-tercbutildimetilsililoxi-piperidin-2,2-dicarboxilato de dietilo bruto (un compuesto de la fórmula (7), en la que P = grupo terc-butildimetilsililo, R3 = grupo etilo, y A = grupo metilo) obtenido en el ejemplo 11-4, 2 ml de metanol y 20 |il de ácido clorhídrico al 20 % y se agitó la mezcla durante 28,5 horas a temperatura ambiente. Se concentró este líquido de reacción a vacío y se purificó mediante cromatografía en gel de sílice para obtener 171 mg de éster de (5S)-1-acetil-5-hidroxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo metilo) (rendimiento: 70 %).
[Ejemplo 12-4] Producción de éster de (5S)-1-acetil-5-hidroxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo metilo)
En un reactor de 10 ml, se colocaron 0,30 mg (contenido puro: 0,26 g, 0,77 mmol) del éster de (5S)-1-acetil-5-tercbutiloxi-piperidin-2,2-dicarboxilato de dietilo bruto (un compuesto de la fórmula (7), en la que P = grupo terc-butilo, R3 = grupo etilo, y A = grupo metilo) obtenido en el ejemplo 11-5, 1 ml de tolueno y 0,5 ml de ácido trifluoacético y se agitó la mezcla durante 48,5 horas a temperatura ambiente. A este líquido de reacción, se le añadió 1 ml de trietilamina y se purificó el líquido de reacción resultante mediante cromatografía en gel de sílice para obtener 0,14 g de éster de (5S)-1-acetil-5-hidroxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo metilo) (rendimiento: 64 %).
[Ejemplo 12-5] Producción de éster de (5S)-1-benzoil-5-hidroxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo fenilo)
En un reactor de 50 ml, se colocaron 2,08 g (contenido puro: 1,88 g, 4,33 mmol) del éster de (5S)-1-benzoil-5-(tetrahidropiran-2-iloxi)-piperidin-2,2-dicarboxilato de dietilo bruto (un compuesto de la fórmula (7), en la que P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo fenilo) obtenido en el ejemplo 11-6, 10 ml de metanol y 20 |il de ácido clorhídrico concentrado y se agitó la mezcla durante 6 horas a temperatura ambiente. Se detuvo la reacción añadiendo 100 |il de trietilamina a este líquido de reacción y se concentró metanol a vacío y se purificó la mezcla resultante mediante cromatografía en gel de sílice para obtener 1,59 g (contenido puro: 1,46 g; rendimiento: 97 %) de éster de (5S)-1-benzoil-5-hidroxipiperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo fenilo).1
1H-RMN (400 MHz, CDCla) 81,29-1,35 (6H, m), 1,50-1,65 (1H, m), 1,82-1,90 (1H, m), 2,05 (1H, s.a.), 2,25-2,33 (1H, m), 2,56-2,62 (1H, m), 3,30 (1H, dd, J=6,8, 13,6 Hz), 3,50 (1H, dd, J=3,2, 14,0 Hz), 3,89 (1H, m), 4,21-4,38 (4H, m),
7,42 (3H, m), 7,52 (2H, m).
[Ejemplo 12-6] Producción de éster de (5S)-1-benzoil-5-hidroxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo fenilo)
En un reactor de 50 ml, se colocaron 0,38 g (contenido puro: 0,36 g, 0,92 mmol) del éster de (5S)-1-benzoil-5-metoximetiloxi-piperidin-2,2-dicarboxilato de dietilo bruto (un compuesto de la fórmula (7), en la que P = grupo metoximetilo, R3 = grupo etilo, y A = grupo fenilo) obtenido en el ejemplo 11-7, 5 ml de metanol y 50 |il de ácido clorhídrico concentrado y se agitó la mezcla durante 4,5 horas a 70°C. Se concentró este líquido de reacción a vacío para obtener 0,30 g (contenido puro: 0,29 g; rendimiento: 91 %) de éster de (5S)-1-benzoil-5-hidroxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo fenilo).
[Ejemplo 12-7] Producción de éster de (5S)-1-benzoil-5-hidroxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo fenilo)
En un reactor de 50 ml, se colocaron 0,86 g (2,03 mmol) del éster de (5S)-1-benzoil-5-(1-etoxietiloxi)-piperidin-2,2-dicarboxilato de dietilo bruto (un compuesto de la fórmula (7), en la que P = grupo etoxietilo, R3 = grupo etilo, y A = grupo fenilo) obtenido en el ejemplo 11-8, 4 ml de metanol y 10 |il de ácido clorhídrico concentrado y se agitó la mezcla durante 4 horas a temperatura ambiente. Se detuvo la reacción añadiendo 100 |il de trietilamina a este líquido de reacción y se concentró metanol a vacío y se purificó la mezcla resultante mediante cromatografía en gel de sílice para obtener 0,68 g (contenido puro: 0,60 g; rendimiento: 85 %) de éster de (5S)-1-benzoil-5-hidroxipiperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo fenilo).
[Ejemplo 12-8] Producción de éster de (5S)-1-benzoil-5-hidroxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo fenilo)
En un reactor de 50 ml, se colocaron 383 mg (contenido puro: 327 mg, 0,71 mmol) del éster de (5S)1-benzoil-5-tercbutildimetilsililoxi-piperidin-2,2-dicarboxilato de dietilo bruto (un compuesto de la fórmula (7), en la que P = grupo terc-butildimetilsililo, R3 = grupo etilo, y A = grupo fenilo) obtenido en el ejemplo 11-9, 2 ml de metanol y 50 |il de ácido clorhídrico al 20 % y se agitó la mezcla durante 28,5 horas a temperatura ambiente. Después, se concentró metanol a vacío y se purificó la mezcla resultante mediante cromatografía en gel de sílice para obtener 269 mg (contenido puro: 226 mg; rendimiento: 91 %) de éster de (5S)-1-benzoil-5-hidroxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo fenilo).
[Ejemplo 12-9] Producción de éster de (5S)-1-benzoil-5-hidroxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo fenilo)
En un reactor de 50 ml, se colocaron 0,29 g (contenido puro: 0,23 g, 0,57 mmol) del éster de (5S)-1-benzoil-5-tercbutiloxi-piperidin-2,2-dicarboxilato de dietilo bruto (un compuesto de la fórmula (7), en la que P = grupo terc-butilo, R3 = grupo etilo, y A = grupo fenilo) obtenido en el ejemplo 11-10, 1 ml de tolueno y 0,5 ml de ácido trifluoacético y se agitó la mezcla durante 48,5 horas a temperatura ambiente. Después, se añadió acetato de etilo al mismo y se lavó la mezcla resultante con disolución acuosa saturada de bicarbonato de sodio, se concentró y se purificó mediante cromatografía en gel de sílice para obtener 0,03 g de éster de (5S)-1-benzoil-5-hidroxi-piperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo fenilo) (rendimiento: 15 %).
[Ejemplo 13] Producción de (2S,5S)-5-acetil-2-oxa-5-azabiciclo[2.2.2]octan-3-ona (un compuesto de la fórmula (9), en la que A = grupo metilo)
En un reactor de 200 ml, se colocaron 8,7 g (23,45 mmol) del éster de (5S)-1-acetil-5-(tetrahidropiran-2-iloxi)-piperidin-2,2-dicarboxilato de dietilo bruto (un compuesto de la fórmula (7), en la que P = grupo tetrahidropiranilo, R3 = grupo etilo, y A = grupo metilo) obtenido en el ejemplo 10, 44 ml de metanol, 43,5 ml de tolueno y 0,24 g de ácido clorhídrico al 35 % y se agitó la mezcla durante 3 horas a temperatura ambiente para obtener una disolución de éster de (5S)-1-acetil-5-hidroxipiperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo metilo) en metanol y tolueno. A este líquido de reacción, se le añadieron 3,75 g de hidróxido de sodio y se agitó la mezcla durante 3 horas y se evaporó metanol a vacío para obtener una disolución en tolueno. A continuación, se añadieron 21,1 g de ácido acético y 12,0 g de anhídrido acético a esta disolución y se agitó la mezcla durante 1 hora a 50°C, se añadieron adicionalmente 0,47 g de trietilamina a la misma y se calentó la mezcla hasta 70°C y se agitó durante 5 horas. Se enfrió este líquido de reacción hasta 30°C y se añadieron 15 ml de tolueno al mismo para la deposición y se retiró el acetato de sodio depositado mediante filtración y se concentró el filtrado para obtener 2,83 g de (2S,5S)-5-acetil-2-oxa-5-azabiciclo[2.2.2]octan-3-ona (un compuesto de la fórmula (9), en la que A = grupo metilo) (rendimiento: 96 %).
1H-RMN (400 MHz, CDCla) 81,78-2,23 (4H, m), 2,06 y 2,12 (3H, s), 3,55 (1H, t, J=12,4 Hz), 3,65-3,77 (1H, m), 4,38 y 5,19 (1H, m), 4,83-4,90 (1H, m).
[Ejemplo 14-1] Producción de (2S,5S)-5-acetil-2-oxa-5-azabiciclo[2.2.2]octan-3-ona (un compuesto de la fórmula (9), en la que A = grupo metilo)
En un reactor de 500 ml, se colocaron 38,1 g (132,8 mmol) del éster de (5S)-1-acetil-5-hidroxipiperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo metilo) obtenido en el ejemplo 12, 190 ml de metanol y 21,2 g de hidróxido de sodio y se agitó la mezcla durante 3 horas a 50°C para obtener una disolución de sal de disodio de ácido (5S)-1-acetil-5-hidroxipiperidin-2,2-dicarboxílico (compuesto (8) (un compuesto con R3 = Na y A = grupo metilo) en metanol. A este líquido de reacción, se le añadieron 119,5 g de ácido acético y 1,3 g de trietilamina y se agitó la mezcla durante 1 hora a 95°C para obtener una mezcla de diastereómeros de ácido (5S)-1-acetil-5-hidroxipiperidin-2-carboxílico (compuestos (11c, 11d)) en una disolución mixta de ácido acético y metanol.
Ácido (2R,5S)-1-acetil-5-hidroxipiperidin-2-carboxílico
1H-RMN (400 MHz, D2O) 81,50-1,70 (2H, m), 1,85-2,10 (2H, m) 2,03 y 2,10 (3H, s), 2,81 (0,3H, d, J=8,9 Hz), 3,35 (0,7H, d, J=8,9 Hz), 3,75 (0,7H, d, J=8,9 Hz), 3,98 (1H, m), 4,26 (0,3H, d, J=8,9 Hz), 4,66 (0,3H, m), 5,08 (0,7H, m) Ácido (2S,5S)-1-acetil-5-hidroxipiperidin-2-carboxílico
1H-RMN (400 MHz, D2O) 81,23-1,36 (1H, m), 1,59-1,81 (1H, m), 1,98 (1H, m), 2,10 y 2,19 (3H, s), 2,24-2,36 (1H, m), 2,54 (0,4H, t, J=12,6 Hz), 3,03 (0,6H, dd, J=10,7 y 13,3 Hz), 3,55-3,65 (0,6H, m), 3,67-3,76 (0,8H, m), 3,92 (0,6H, dd, J=5,3 y 13,3 Hz), 4,44 (0,6H, m), 4,47 (0,4H, m), 4,94 (0,6H, m)
A continuación, se evaporó metanol a vacío a partir de la disolución y se añadieron 108 g de anhídrido acético a la misma y se agitó la mezcla durante 3 horas a 100°C. Se enfrió este líquido de reacción hasta 30°C y se añadieron 190 ml de tolueno al mismo. Se retiró el acetato de sodio depositado mediante filtración y se concentró el filtrado para obtener 2,83 g de (2S,5S)-5-acetil-2-oxa-5-azabiciclo[2.2.2]octan-3-ona en bruto (un compuesto de la fórmula (9), en la que A = grupo metilo) (rendimiento: 72 %).
[Ejemplo 14-2] Producción de (2S,5S)-5-benzoil-2-oxa-5-azabiciclo[2.2.2]octan-3-ona (un compuesto de la fórmula (9), en la que A = grupo fenilo)
En un reactor de 30 ml, se colocaron 1,29 g (3,68 mmol) del éster de (5S)1-benzoil-5-hidroxipiperidin-2,2-dicarboxilato de dietilo (un compuesto de la fórmula (8), en la que R3 = grupo etilo y A = grupo fenilo) obtenido según el ejemplo 12-5, 6,5 ml de metanol y 0,29 g (7,36 mmol) de hidróxido de sodio y se calentó la mezcla a reflujo durante 2 horas y se calentó adicionalmente durante 14,5 horas tras la adición de 0,15 g (3,68 mmol) de hidróxido de sodio. Después, se ajustó la mezcla sobre hielo a pH 1 con disolución acuosa de ácido sulfúrico y se retiró la sal inorgánica producida mediante filtración. Se ajustó la mezcla a pH 2 mediante adición de acetato de sodio y posteriormente se concentraron metanol y agua para obtener una mezcla de diastereómeros de ácido (5S)-1-benzoil-5-hidroxipiperidin-2-carboxílico (compuestos (11e, 11f)) en un sólido blanco.
Ácido (2R,5S)-1-benzoil-5-hidroxipiperidin-2-carboxílico
1H-RMN (400 MHz, D2O) 81,33-1,85 (2H, m), 2,20 (2H, m), 3,12 (0,5H, d, J=15,0 Hz), 3,40 (0,5H, m), 3,50-3,90 (1H, m), 4,09 (0,5H, s.a.), 4,47 (0,5H, m), 4,60 (0,5H, d, J=15,0 Hz), 5,46 (0,5H, m), 7,40-7,50 (5H, m).
Ácido (2S,5S)-1-benzoil-5-hidroxipiperidin-2-carboxílico
1H-RMN (400 MHz, D2O) 81,33-1,46 (1H, m), 1,65 (0,4H, m), 1,81 (0,6H, m), 2,02 (1H, m), 2,30 (0,4H, m), 2,43 (0,6H, m), 2,72 (0,4H, t, J=12,0 Hz), 3,03 (0,6H, t, J=12,0 Hz), 3,58 (0,6H, m), 3,65 (0,4H, m), 3,80 (0,6H, m), 4,40 (0,4H, m), 4,65 (0,4H, m), 5,40 (0,6H, m), 7,40 (5H, m).
A continuación, se añadieron 1,32 ml (22,08 mmol) de ácido acético, 5,2 ml de tolueno, 0,04 g (0,37 mmol) de trietilamina y 0,57 g (6,38 mmol) de anhídrido acético al sólido blanco y se agitó la mezcla durante 2,5 horas a 90°C. Se concentró este líquido de reacción y se añadió tolueno al mismo. Se retiró el acetato de sodio depositado mediante filtración y se concentró el filtrado y se purificó mediante cromatografía en gel de sílice para obtener 0,76 g (contenido puro: 0,65 g; rendimiento: 76 %) de (2S,5S)-5-benzoil-2-oxa-5-azabiciclo[2.2.2]octan-3-ona (un compuesto de la fórmula (9), en la que A = grupo fenilo).1
1H-RMN (400 MHz, CDCla) 81,88-2,30 (4H, m), 3,70 (1H, m), 3,90 (1H, m), 4,45 y 4,79 (1H, s.a.), 4,98 y 5,27 (1H, s.a.), 7,45 (5H, m).
[Ejemplo 15] Producción de ácido (2S,5S)-5-hidroxipiperidin-2-carboxílico (compuesto (10))
En un reactor de 200 ml, se colocaron 6,36 g (37,59 mmol) de la (2S,5S)-5-acetil-2-oxa-5-azabiciclo[2.2.2]octan-3-ona en bruto (un compuesto de la fórmula (9), en la que A = grupo metilo) obtenida en el ejemplo 13 y 93,98 ml (187,97 mmol) de ácido clorhídrico 2 mol/l y se agitó la mezcla durante 3 horas a 90°C. Se concentró este líquido de reacción y después se disolvió de nuevo en agua (42,9 ml) y se dejó adsorber sobre una resina de intercambio catiónico fuertemente ácida (88,69 ml). Se lavó la resina con agua y después se realizó la elución con agua amoniacal y se concentró la fracción eluída para obtener ácido (2S,5S)-5-hidroxi-piperidin-2-carboxílico bruto (compuesto (10)).
Se disolvió el ácido (2S,5S)-5-hidroxi-piperidin-2-carboxílico bruto obtenido (compuesto (10)) en agua (10 ml) y se añadieron 0,26 g de carbón activado al mismo y se agitó la mezcla durante 2 horas a 40°C. Se filtró el líquido de reacción y después se concentró y se añadió etanol al residuo para obtener cristales brutos y se recristalizaron adicionalmente los cristales obtenidos con agua/etanol/acetona para obtener 1,61 g de ácido (2S,5S)-5-hidroxipiperidin-2-carboxílico (compuesto (10)) (pureza: 96 %; rendimiento: 28 %).
1H-RMN (400 MHz, CD3OD) 81,73-1,90 (2H, m), 2,03-2,10 (2H, m), 3,09 (1H, dd, J=2,4, 12,8 Hz), 3,17-3,23 (1H, m), 3,45 (1H, m), 4,02 (1H, m).
[Ejemplo 16-1] Producción de ácido (2S,5S)-5-hidroxipiperidin-2-carboxílico (compuesto (10))
En un reactor de 1000 ml, se colocaron 18 g de una disolución acuosa de ácido acético que contenía 11,31 g (66,90 mmol) de la (2S,5S)-5-acetil-2-oxa-5-azabiciclo[2.2.2]octan-3-ona en bruto (en la fórmula (9), A = grupo metilo) preparada según el ejemplo 13 y 121 ml de ácido clorhídrico 2 mol/l y se agitó la mezcla durante 3 horas a 90°C. A este líquido de reacción, se le añadieron 1,2 g de carbón activado y se agitó la mezcla durante 1 hora a 45°C y después se filtró el carbón activado y se concentró el filtrado para obtener 20,5 g de un residuo. Después, se disolvió este residuo en 50 ml de agua y se añadieron 175 ml de resina DIAION®SAT10L (tipo de anión acetato) al mismo y se agitó la mezcla durante 30 minutos a temperatura ambiente y después se filtró y se concentró el filtrado para obtener 16,5 g de un residuo. Después, se añadieron 2,1 ml de agua y 70 ml de etanol a este residuo para su cristalización a 60°C y se filtraron los cristales a temperatura ambiente y se secaron para obtener 8,0 g de cristales brutos de ácido (2S,5S)-5-hidroxi-piperidin-2-carboxílico (compuesto (10)) (pureza: 93 %; rendimiento: 77 %).
[Ejemplo 16-2] Producción de clorhidrato de ácido (2S,5S)-5-hidroxipiperidin-2-carboxílico (un clorhidrato del compuesto (10))
En un reactor de 10 ml, se colocaron 0,43 g (contenido puro: 0,36 g, 1,58 mmol) de la (2S,5S)-5-benzoil-2-oxa-5-azabiciclo[2.2.2]octan-3-ona (en la fórmula (9), A = grupo fenilo) obtenida en el ejemplo 14-2, 1,5 ml de agua y 0,50 g de ácido clorhídrico al 35 % y se agitó la mezcla durante 15 horas a 100°C. Se retiró el ácido benzoico depositado mediante filtración y se sometieron 11,38 g del filtrado obtenido a la cuantificación mediante HPLC. Por consiguiente, se indicó que el filtrado contenía 1,50 mmol de clorhidrato de ácido (2S,5S)-5-hidroxipiperidin-2-carboxílico (rendimiento: 95 %).
Claims (7)
- REIVINDICACIONESi. Un método para producir el compuesto representado por la fórmula (7) a continuación:(en la que P representa un grupo protector, R3 representa un grupo alquilo que contiene de 1a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono),comprendiendo el método la etapa 1 de:proteger el grupo hidroxilo con un grupo protector en un compuesto representado por la fórmula (1) a continuación:OHXs^ X v v/COOR1( 1 )(en la que X representa Cl, Br o I, y R1 representa un átomo de hidrógeno o un grupo alquilo opcionalmente sustituido que contiene de 1 a 4 átomos de carbono)para sintetizar un compuesto representado por la fórmula (2) a continuación:( 2 )(en la que X representa Cl, Br o I, R1 representa un átomo de hidrógeno o un grupo alquilo opcionalmente sustituido que contiene de 1 a 4 átomos de carbono, y P representa un grupo protector)y después reducir el grupo éster en el compuesto (2) para sintetizar un compuesto representado por la fórmula (3) a continuación:(en la que X representa Cl, Br o I, y P representa un grupo protector).
- 2. El método para producir el compuesto (7) según la reivindicación 1, en el que el método comprende (i) la etapa 2 de:esterificar el grupo hidroxilo en el compuesto (3) con un grupo sulfonato para sintetizar un compuesto representado por la fórmula (4) a continuación:R2 representa un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquilo que contiene de 1 a 10 átomos de carbono o un grupo aralquilo que contiene de 7 a 20 átomos de carbono)y dejar reaccionar el compuesto (4) con un compuesto representado por la fórmula (5) a continuación:(en la que R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono)para sintetizar un compuesto representado por la fórmula (6) a continuación:(en la que X representa Cl, Br o I, P representa un grupo protector, R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono);y(ii) la etapa 3 de:ciclar el compuesto (6) para sintetizar el compuesto representado por la fórmula (7) a continuación:(en la que P representa un grupo protector, R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).Un método para producir ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico representado por la fórmula (10) a continuación:comprendiendo el método (i) la etapa 4 de:retirar el grupo protector a partir del grupo hidroxilo en un compuesto representado por la fórmula (7) a continuación:(en la que P representa un grupo protector, R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono)para sintetizar un compuesto representado por la fórmula (8) a continuación:
- (en la que R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono, o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono),en el que el compuesto (7) se sintetiza mediante el método según la reivindicación 1 o 2.
- 4. El método para producir ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico según la reivindicación 3, comprendiendo el método además (ii) la etapa 5 de:(a) en el compuesto (8), hidrolizar los grupos éster, dejar reaccionar uno de los grupos carboxilo con el grupo hidroxilo para permitir la lactonización, y descarboxilar adicionalmente el otro grupo carboxilo; o (b) en el compuesto (8), hidrolizar los grupos éster, descarboxilar uno de los grupos carboxilo para formar una mezcla estereoisomérica de un ácido 2-monocarboxílico y después isomerizar y lactonizar la mezcla estereoisomérica;para sintetizar un compuesto representado por la fórmula (9) a continuación:(en la que A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).
- 5. El método para producir ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico según la reivindicación 3 o 4, que comprende además (iii) la etapa 6 de:escindir el enlace amida en el compuesto (9) e hidrolizar la lactona en el compuesto (9) para sintetizar ácido (2S,5S)/(2R,5R)-5-hidroxipiperidin-2-carboxílico.
- 6. Un compuesto representado por la fórmula (7) a continuación:(en la que P representa un grupo protector, R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).
- 7. Un compuesto representado por la fórmula (6a) a continuación:(en la que X representa Cl, Br, o I, P' representa un grupo tetrahidropiranilo, grupo metoximetilo, grupo etoxietilo, grupo terc-butilo o grupo terc-butildimetilsililo, y R3 representa un grupo alquilo que contiene de 1 a 4 átomos de carbono, y A representa un grupo alquilo que contiene de 1 a 10 átomos de carbono, un grupo arilo que contiene de 6 a 12 átomos de carbono, un grupo alquiloxilo que contiene de 1 a 4 átomos de carbono o un grupo aralquiloxilo que contiene de 7 a 20 átomos de carbono).
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013272766 | 2013-12-27 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2897467T3 true ES2897467T3 (es) | 2022-03-01 |
Family
ID=53478965
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES18212248T Active ES2897467T3 (es) | 2013-12-27 | 2014-12-26 | Método para producir ácido 5-hidroxipiperidin-2-carboxílico |
| ES14873766T Active ES2762581T3 (es) | 2013-12-27 | 2014-12-26 | Método para producir ácido 5-hidroxipiperidina-2-carboxílico |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES14873766T Active ES2762581T3 (es) | 2013-12-27 | 2014-12-26 | Método para producir ácido 5-hidroxipiperidina-2-carboxílico |
Country Status (6)
| Country | Link |
|---|---|
| US (4) | US9790181B2 (es) |
| EP (3) | EP3486232B1 (es) |
| JP (2) | JP6687238B2 (es) |
| CN (4) | CN111499562B (es) |
| ES (2) | ES2897467T3 (es) |
| WO (1) | WO2015099126A1 (es) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN108752253B (zh) * | 2018-06-27 | 2020-11-24 | 深圳市茵诺圣生物科技有限公司 | 一种多元氮杂环状非天然手性氨基酸及其合成方法 |
| CN108659004B (zh) * | 2018-07-12 | 2020-11-10 | 福安药业集团重庆博圣制药有限公司 | 奥拉西坦异构体的制备方法 |
| US11897844B2 (en) * | 2018-09-21 | 2024-02-13 | Api Corporation | Method for producing amino acid derivatives |
| JP2020164488A (ja) * | 2019-03-29 | 2020-10-08 | 日本マイクロバイオファーマ株式会社 | シス−5−ヒドロキシ−2−ピペリジンカルボン酸の結晶及びその製造方法 |
| CN110577490B (zh) * | 2019-08-28 | 2020-09-22 | 山东安信制药有限公司 | 阿维巴坦中间体(2s,5s)-n-保护基-5-羟基-2-甲酸哌啶的合成方法 |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5164372A (en) * | 1989-04-28 | 1992-11-17 | Fujisawa Pharmaceutical Company, Ltd. | Peptide compounds having substance p antagonism, processes for preparation thereof and pharmaceutical composition comprising the same |
| US6399600B1 (en) * | 1997-06-23 | 2002-06-04 | Simon Fraser University | Oxazinones having antibacterial activity |
| AU2001288819A1 (en) * | 2000-09-11 | 2002-03-26 | Genentech, Inc. | Amidine inhibitors of serine proteases |
| US7605286B2 (en) * | 2003-08-06 | 2009-10-20 | Sumitomo Chemical Company, Limited | Hydroxy-protecting reagent and method of protecting hydroxy with the same |
| KR20080016577A (ko) * | 2005-05-24 | 2008-02-21 | 아스트라제네카 아베 | 항균 활성을 갖는 아미노피페리딘 퀴놀린 및 이들의아자이소스테릭 유사체 |
| KR100915551B1 (ko) * | 2007-07-18 | 2009-09-10 | 주식회사 알에스텍 | 3-히드록시 피롤리딘 및 이의 유도체의 효율적 제조방법 |
| WO2010126820A2 (en) | 2009-04-30 | 2010-11-04 | Merck Sharp & Dohme Corp. | Preparation of alkyl esters of n-protected oxo-azacycloalkylcarboxylic acids |
| BR112012015721A2 (pt) * | 2009-12-30 | 2017-09-26 | Avila Therapeutics Inc | modificação covalente de proteínas dirigida por ligante |
| CN102477019A (zh) * | 2010-11-26 | 2012-05-30 | 苏州凯达生物医药技术有限公司 | 制备s-3-羟基四氢呋喃的新方法 |
| HUE042605T2 (hu) * | 2012-05-08 | 2019-07-29 | Codexis Inc | Biokatalizátorok és kémiai vegyületek hidroxilálására szolgáló eljárások |
| SG10201705091YA (en) * | 2012-12-20 | 2017-07-28 | Api Corp | METHOD FOR PRODUCING cis-5-HYDROXY-2-PIPERIDINECARBOXYLIC ACID DERIVATIVE, AND METHOD FOR PURIFYING cis-5-HYDROXY-2-PIPERIDINECARBOXYLIC ACID |
-
2014
- 2014-12-26 CN CN202010330453.6A patent/CN111499562B/zh active Active
- 2014-12-26 WO PCT/JP2014/084518 patent/WO2015099126A1/ja not_active Ceased
- 2014-12-26 ES ES18212248T patent/ES2897467T3/es active Active
- 2014-12-26 EP EP18212248.1A patent/EP3486232B1/en active Active
- 2014-12-26 EP EP21184133.3A patent/EP3915975B1/en active Active
- 2014-12-26 US US15/108,141 patent/US9790181B2/en active Active
- 2014-12-26 JP JP2015555046A patent/JP6687238B2/ja active Active
- 2014-12-26 EP EP14873766.1A patent/EP3091002B1/en active Active
- 2014-12-26 CN CN201710817190.XA patent/CN107573277B/zh active Active
- 2014-12-26 ES ES14873766T patent/ES2762581T3/es active Active
- 2014-12-26 CN CN201480071310.0A patent/CN105899487B/zh active Active
- 2014-12-26 CN CN202311723462.1A patent/CN117886738A/zh active Pending
-
2017
- 2017-09-15 US US15/705,349 patent/US9988351B2/en active Active
-
2018
- 2018-04-27 US US15/965,289 patent/US10703719B2/en active Active
- 2018-04-27 US US15/965,316 patent/US10370330B2/en active Active
-
2020
- 2020-02-13 JP JP2020022050A patent/JP6947862B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US10703719B2 (en) | 2020-07-07 |
| US10370330B2 (en) | 2019-08-06 |
| CN111499562A (zh) | 2020-08-07 |
| CN105899487B (zh) | 2018-10-19 |
| CN105899487A (zh) | 2016-08-24 |
| EP3091002A1 (en) | 2016-11-09 |
| US9988351B2 (en) | 2018-06-05 |
| US9790181B2 (en) | 2017-10-17 |
| CN117886738A (zh) | 2024-04-16 |
| CN107573277A (zh) | 2018-01-12 |
| EP3915975C0 (en) | 2024-12-18 |
| CN107573277B (zh) | 2020-10-16 |
| WO2015099126A1 (ja) | 2015-07-02 |
| JP6687238B2 (ja) | 2020-04-22 |
| JP2020097613A (ja) | 2020-06-25 |
| US20180002286A1 (en) | 2018-01-04 |
| EP3915975B1 (en) | 2024-12-18 |
| EP3486232A1 (en) | 2019-05-22 |
| JP6947862B2 (ja) | 2021-10-13 |
| EP3486232B1 (en) | 2021-09-01 |
| JPWO2015099126A1 (ja) | 2017-03-23 |
| US20180244619A1 (en) | 2018-08-30 |
| CN111499562B (zh) | 2023-12-26 |
| ES2762581T3 (es) | 2020-05-25 |
| EP3091002B1 (en) | 2019-10-09 |
| EP3915975A1 (en) | 2021-12-01 |
| US20180244620A1 (en) | 2018-08-30 |
| US20160318867A1 (en) | 2016-11-03 |
| EP3091002A4 (en) | 2017-11-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6947862B2 (ja) | 5−ヒドロキシピペリジン−2−カルボン酸の製造方法 | |
| US20220169630A1 (en) | Chemical process for preparing phenylpiperidinyl indole derivatives | |
| WO2024216008A1 (en) | Synthesis of ras inhibitors | |
| EP2368870A1 (en) | Process for producing optically active carboxylic acid | |
| ES2343212T3 (es) | Procedimiento para preparar remifentanilo, intermedios del mismo, uso de dichos intermedios y procedimientos para su preparacion. | |
| WO2012165023A1 (ja) | 光学活性α-置換プロリン類の製造方法 | |
| KR102255357B1 (ko) | 2-아미노-1,3-프로판디올 화합물 및 이의 염의 제조방법 | |
| HU198452B (en) | Process for production of derivatives of oktahydroindole | |
| CN102417463B (zh) | 阿维莫泮的制备方法 | |
| Shirode et al. | Synthesis of (3S, 4R)-4-benzylamino-3-methoxypiperidine, an important intermediate for (3S, 4R)-Cisapride | |
| JP2012532145A (ja) | トランス−4−アミノシクロペンタ−2−エン−1−カルボン酸誘導体の製造 | |
| US6806384B2 (en) | Production method of β-amino-α-hydroxycarboxylic acid | |
| JP2008510761A (ja) | ジアリールシクロアルキル誘導体の製造方法 | |
| KR100858842B1 (ko) | 키랄아민을 이용한 광학활성 옥소라이보스유도체의제조방법 | |
| WO1992020652A1 (fr) | Procede de production d'un compose de pyrrolidine ou de son sel | |
| Baek et al. | A Facile Synthesis of (-)-Cucurbitine | |
| HK1160105A (en) | Process for producing optically active carboxylic acid | |
| JPWO1999033817A1 (ja) | β−ヒドロキシ−γ−ブチロラクトン類およびβ−(メタ)アクリロイルオキシ−γ−ブチロラクトン類の製造方法 |