ES2900863T3 - Derivados de ciclohexeno y su uso como odorante - Google Patents
Derivados de ciclohexeno y su uso como odorante Download PDFInfo
- Publication number
- ES2900863T3 ES2900863T3 ES16181761T ES16181761T ES2900863T3 ES 2900863 T3 ES2900863 T3 ES 2900863T3 ES 16181761 T ES16181761 T ES 16181761T ES 16181761 T ES16181761 T ES 16181761T ES 2900863 T3 ES2900863 T3 ES 2900863T3
- Authority
- ES
- Spain
- Prior art keywords
- hydrogen
- methyl
- alkyl
- alkenyl
- formula
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000003205 fragrance Substances 0.000 title claims description 29
- 125000000596 cyclohexenyl group Chemical class C1(=CCCCC1)* 0.000 title description 2
- 150000001875 compounds Chemical class 0.000 claims abstract description 118
- 229910052739 hydrogen Inorganic materials 0.000 claims abstract description 103
- 239000001257 hydrogen Substances 0.000 claims abstract description 102
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims abstract description 55
- 238000000034 method Methods 0.000 claims abstract description 53
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims abstract description 37
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 claims abstract description 29
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 claims abstract description 27
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 claims abstract description 22
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims abstract description 17
- 150000001993 dienes Chemical class 0.000 claims abstract description 10
- 239000003054 catalyst Substances 0.000 claims abstract description 6
- 238000011065 in-situ storage Methods 0.000 claims abstract description 4
- 150000002431 hydrogen Chemical group 0.000 claims description 69
- -1 carboxylic acid halide Chemical class 0.000 claims description 33
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 16
- 229910052799 carbon Inorganic materials 0.000 claims description 16
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 claims description 15
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 claims description 15
- 150000001721 carbon Chemical group 0.000 claims description 14
- 125000006527 (C1-C5) alkyl group Chemical group 0.000 claims description 13
- 125000006729 (C2-C5) alkenyl group Chemical group 0.000 claims description 13
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 11
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 claims description 11
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 11
- 238000006243 chemical reaction Methods 0.000 claims description 10
- 150000001299 aldehydes Chemical class 0.000 claims description 9
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 claims description 8
- WNXJIVFYUVYPPR-UHFFFAOYSA-N 1,3-dioxolane Chemical compound C1COCO1 WNXJIVFYUVYPPR-UHFFFAOYSA-N 0.000 claims description 7
- HCJAFBYGZGXACK-UHFFFAOYSA-N 1-ethenylcyclohex-3-ene-1-carbaldehyde Chemical compound C=CC1(C=O)CCC=CC1 HCJAFBYGZGXACK-UHFFFAOYSA-N 0.000 claims description 7
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 claims description 7
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 claims description 7
- LTSTZDGSNJVQKU-UHFFFAOYSA-N 1-ethenyl-3-methylcyclohex-3-ene-1-carbaldehyde Chemical compound CC1=CCCC(C=O)(C=C)C1 LTSTZDGSNJVQKU-UHFFFAOYSA-N 0.000 claims description 6
- QLHHGSKVTLQUKC-UHFFFAOYSA-N (1-ethenyl-2,4-dimethylcyclohex-3-en-1-yl)methanol Chemical compound CC1C=C(C)CCC1(CO)C=C QLHHGSKVTLQUKC-UHFFFAOYSA-N 0.000 claims description 5
- JJUIXSDDQNOAKL-UHFFFAOYSA-N 1-(1-ethenyl-2,4-dimethylcyclohex-3-en-1-yl)but-3-en-1-ol Chemical compound CC1C=C(C)CCC1(C=C)C(O)CC=C JJUIXSDDQNOAKL-UHFFFAOYSA-N 0.000 claims description 5
- CUUQGRRTJCGPEG-UHFFFAOYSA-N 1-(1-ethenyl-2,4-dimethylcyclohex-3-en-1-yl)ethanol Chemical compound CC(O)C1(C=C)CCC(C)=CC1C CUUQGRRTJCGPEG-UHFFFAOYSA-N 0.000 claims description 5
- MZVUQLFYBIIVGJ-UHFFFAOYSA-N 1-(1-ethenyl-2,4-dimethylcyclohex-3-en-1-yl)but-3-en-1-one Chemical compound CC1C=C(C)CCC1(C=C)C(=O)CC=C MZVUQLFYBIIVGJ-UHFFFAOYSA-N 0.000 claims description 4
- UTFFKDUFBDMQIQ-UHFFFAOYSA-N 1-(1-ethenyl-2,4-dimethylcyclohex-3-en-1-yl)ethanone Chemical compound CC1C=C(C)CCC1(C=C)C(C)=O UTFFKDUFBDMQIQ-UHFFFAOYSA-N 0.000 claims description 4
- HDXXCVSLLOOHCF-UHFFFAOYSA-N n-[(1-ethenyl-3-methylcyclohex-3-en-1-yl)methylidene]hydroxylamine Chemical compound CC1=CCCC(C=NO)(C=C)C1 HDXXCVSLLOOHCF-UHFFFAOYSA-N 0.000 claims description 4
- MLJRXERKGLELMB-UHFFFAOYSA-N n-[(1-ethenyl-4-methylcyclohex-3-en-1-yl)methylidene]hydroxylamine Chemical compound CC1=CCC(C=NO)(C=C)CC1 MLJRXERKGLELMB-UHFFFAOYSA-N 0.000 claims description 4
- ULDKKODFYNVPMS-UHFFFAOYSA-N 1-(cyclopenten-1-yl)-2,4-dimethylcyclohex-3-ene-1-carbaldehyde Chemical compound C1(=CCCC1)C1(C(C=C(CC1)C)C)C=O ULDKKODFYNVPMS-UHFFFAOYSA-N 0.000 claims description 3
- BLEKWGULEIACGA-UHFFFAOYSA-N 1-but-1-enyl-2,4-dimethylcyclohex-3-ene-1-carbaldehyde Chemical compound CCC=CC1(C=O)CCC(C)=CC1C BLEKWGULEIACGA-UHFFFAOYSA-N 0.000 claims description 3
- WLWBKMODJZUPHC-UHFFFAOYSA-N 1-buta-1,3-dienyl-2,4-dimethylcyclohex-3-ene-1-carbaldehyde Chemical compound CC1C=C(C)CCC1(C=O)C=CC=C WLWBKMODJZUPHC-UHFFFAOYSA-N 0.000 claims description 3
- PTRRFJIJMLKTET-UHFFFAOYSA-N 1-ethenyl-2-methyl-4-(4-methylpent-3-enyl)cyclohex-3-ene-1-carbaldehyde Chemical compound CC1C=C(CCC=C(C)C)CCC1(C=C)C=O PTRRFJIJMLKTET-UHFFFAOYSA-N 0.000 claims description 3
- KVPRTQWFMOYROG-UHFFFAOYSA-N 2-methyl-1-(2-methylprop-1-enyl)cyclohex-3-ene-1-carbaldehyde Chemical compound CC1C=CCCC1(C=O)C=C(C)C KVPRTQWFMOYROG-UHFFFAOYSA-N 0.000 claims description 3
- AVXURJPOCDRRFD-UHFFFAOYSA-N Hydroxylamine Chemical compound ON AVXURJPOCDRRFD-UHFFFAOYSA-N 0.000 claims description 3
- 125000000217 alkyl group Chemical group 0.000 claims description 3
- 150000002009 diols Chemical class 0.000 claims description 3
- 230000032050 esterification Effects 0.000 claims description 3
- 238000005886 esterification reaction Methods 0.000 claims description 3
- 239000007800 oxidant agent Substances 0.000 claims description 3
- 230000003647 oxidation Effects 0.000 claims description 3
- 238000007254 oxidation reaction Methods 0.000 claims description 3
- 125000006273 (C1-C3) alkyl group Chemical group 0.000 claims description 2
- ZIWXFYOINQODEF-UHFFFAOYSA-N 1-[2,4-dimethyl-1-(2-methylprop-1-enyl)cyclohex-3-en-1-yl]ethanol Chemical compound CC(C)=CC1(C(O)C)CCC(C)=CC1C ZIWXFYOINQODEF-UHFFFAOYSA-N 0.000 claims description 2
- WMJWVVTZKVBZIN-UHFFFAOYSA-N COC(C1(CC=C(CC1)C)C=C)OC Chemical compound COC(C1(CC=C(CC1)C)C=C)OC WMJWVVTZKVBZIN-UHFFFAOYSA-N 0.000 claims description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 2
- 125000004429 atom Chemical group 0.000 claims 1
- 125000002485 formyl group Chemical class [H]C(*)=O 0.000 abstract description 6
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 64
- 239000000203 mixture Substances 0.000 description 50
- 238000005160 1H NMR spectroscopy Methods 0.000 description 44
- 238000002290 gas chromatography-mass spectrometry Methods 0.000 description 44
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 26
- 239000000047 product Substances 0.000 description 18
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 14
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 14
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 14
- KAKZBPTYRLMSJV-UHFFFAOYSA-N Butadiene Chemical class C=CC=C KAKZBPTYRLMSJV-UHFFFAOYSA-N 0.000 description 12
- MLUCVPSAIODCQM-NSCUHMNNSA-N crotonaldehyde Chemical compound C\C=C\C=O MLUCVPSAIODCQM-NSCUHMNNSA-N 0.000 description 11
- MLUCVPSAIODCQM-UHFFFAOYSA-N crotonaldehyde Natural products CC=CC=O MLUCVPSAIODCQM-UHFFFAOYSA-N 0.000 description 11
- 239000000243 solution Substances 0.000 description 11
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 10
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 9
- YQYKLWIDPWLECV-UHFFFAOYSA-N 4-ethenylcyclohexene-1-carbaldehyde Chemical compound C=CC1CCC(C=O)=CC1 YQYKLWIDPWLECV-UHFFFAOYSA-N 0.000 description 8
- 235000011430 Malus pumila Nutrition 0.000 description 8
- 235000015103 Malus silvestris Nutrition 0.000 description 8
- ZSWFCLXCOIISFI-UHFFFAOYSA-N cyclopentadiene Chemical compound C1C=CC=C1 ZSWFCLXCOIISFI-UHFFFAOYSA-N 0.000 description 8
- FLKPEMZONWLCSK-UHFFFAOYSA-N diethyl phthalate Chemical compound CCOC(=O)C1=CC=CC=C1C(=O)OCC FLKPEMZONWLCSK-UHFFFAOYSA-N 0.000 description 8
- 239000000796 flavoring agent Substances 0.000 description 8
- 235000019634 flavors Nutrition 0.000 description 8
- 239000002904 solvent Substances 0.000 description 8
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 description 7
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 7
- RCJMVGJKROQDCB-SNAWJCMRSA-N (3e)-2-methylpenta-1,3-diene Chemical compound C\C=C\C(C)=C RCJMVGJKROQDCB-SNAWJCMRSA-N 0.000 description 6
- RCJMVGJKROQDCB-UHFFFAOYSA-N 1,3-dimethyl-1,3-butadiene Natural products CC=CC(C)=C RCJMVGJKROQDCB-UHFFFAOYSA-N 0.000 description 6
- RRHGJUQNOFWUDK-UHFFFAOYSA-N Isoprene Chemical compound CC(=C)C=C RRHGJUQNOFWUDK-UHFFFAOYSA-N 0.000 description 6
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 6
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 6
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 6
- RUMOYJJNUMEFDD-UHFFFAOYSA-N perillyl aldehyde Chemical compound CC(=C)C1CCC(C=O)=CC1 RUMOYJJNUMEFDD-UHFFFAOYSA-N 0.000 description 6
- LEHBURLTIWGHEM-UHFFFAOYSA-N pyridinium chlorochromate Chemical compound [O-][Cr](Cl)(=O)=O.C1=CC=[NH+]C=C1 LEHBURLTIWGHEM-UHFFFAOYSA-N 0.000 description 6
- RUMOYJJNUMEFDD-SNVBAGLBSA-N (R)-(+)-Perillaldehyde Natural products CC(=C)[C@H]1CCC(C=O)=CC1 RUMOYJJNUMEFDD-SNVBAGLBSA-N 0.000 description 5
- ARXWAZQEZBTNIM-UHFFFAOYSA-N 1-ethenyl-2,4-dimethylcyclohex-3-ene-1-carbaldehyde Chemical compound CC1C=C(C)CCC1(C=C)C=O ARXWAZQEZBTNIM-UHFFFAOYSA-N 0.000 description 5
- SEPQTYODOKLVSB-UHFFFAOYSA-N 3-methylbut-2-enal Chemical compound CC(C)=CC=O SEPQTYODOKLVSB-UHFFFAOYSA-N 0.000 description 5
- 239000012267 brine Substances 0.000 description 5
- 238000004587 chromatography analysis Methods 0.000 description 5
- 239000003921 oil Substances 0.000 description 5
- 235000019198 oils Nutrition 0.000 description 5
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 5
- NPBIJNXYQJVUNF-UHFFFAOYSA-N 1-(2,4-dimethyl-1-prop-1-en-2-ylcyclohex-3-en-1-yl)ethanol Chemical compound CC(O)C1(C(C)=C)CCC(C)=CC1C NPBIJNXYQJVUNF-UHFFFAOYSA-N 0.000 description 4
- NDUZIMWWLPFMTD-UHFFFAOYSA-N 2,4-dimethyl-1-prop-1-en-2-ylcyclohex-3-ene-1-carbaldehyde Chemical compound CC1C=C(C)CCC1(C=O)C(C)=C NDUZIMWWLPFMTD-UHFFFAOYSA-N 0.000 description 4
- MBDOYVRWFFCFHM-UHFFFAOYSA-N 2-hexenal Chemical compound CCCC=CC=O MBDOYVRWFFCFHM-UHFFFAOYSA-N 0.000 description 4
- 244000241257 Cucumis melo Species 0.000 description 4
- GLZPCOQZEFWAFX-UHFFFAOYSA-N Geraniol Chemical compound CC(C)=CCCC(C)=CCO GLZPCOQZEFWAFX-UHFFFAOYSA-N 0.000 description 4
- UAHWPYUMFXYFJY-UHFFFAOYSA-N beta-myrcene Chemical compound CC(C)=CCCC(=C)C=C UAHWPYUMFXYFJY-UHFFFAOYSA-N 0.000 description 4
- RRAFCDWBNXTKKO-UHFFFAOYSA-N eugenol Chemical compound COC1=CC(CC=C)=CC=C1O RRAFCDWBNXTKKO-UHFFFAOYSA-N 0.000 description 4
- 239000004615 ingredient Substances 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- NDTYTMIUWGWIMO-UHFFFAOYSA-N perillyl alcohol Chemical compound CC(=C)C1CCC(CO)=CC1 NDTYTMIUWGWIMO-UHFFFAOYSA-N 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 4
- OQJYBQXYFOQAES-UHFFFAOYSA-N 1-(2,4-dimethyl-1-prop-1-en-2-ylcyclohex-3-en-1-yl)but-3-en-1-ol Chemical compound CC1C=C(C)CCC1(C(O)CC=C)C(C)=C OQJYBQXYFOQAES-UHFFFAOYSA-N 0.000 description 3
- XEMDJTWRJXQQRA-UHFFFAOYSA-N 1-(2,4-dimethyl-1-prop-1-en-2-ylcyclohex-3-en-1-yl)but-3-en-1-one Chemical compound CC1C=C(C)CCC1(C(C)=C)C(=O)CC=C XEMDJTWRJXQQRA-UHFFFAOYSA-N 0.000 description 3
- HPNYRWXBUHDLFO-UHFFFAOYSA-N 1-(3a,4,7,7a-tetrahydro-3h-inden-5-yl)ethanone Chemical compound C1C(C(=O)C)=CCC2C=CCC21 HPNYRWXBUHDLFO-UHFFFAOYSA-N 0.000 description 3
- IMUMRIXLOYBAMK-UHFFFAOYSA-N 1-ethenyl-4-methylcyclohex-3-ene-1-carbaldehyde Chemical compound CC1=CCC(C=O)(C=C)CC1 IMUMRIXLOYBAMK-UHFFFAOYSA-N 0.000 description 3
- SDJHPPZKZZWAKF-UHFFFAOYSA-N 2,3-dimethylbuta-1,3-diene Chemical compound CC(=C)C(C)=C SDJHPPZKZZWAKF-UHFFFAOYSA-N 0.000 description 3
- OZAUVUBFUFWDRD-UHFFFAOYSA-N 3-methyl-1-prop-1-en-2-ylcyclohex-3-ene-1-carbaldehyde Chemical compound CC(=C)C1(C=O)CCC=C(C)C1 OZAUVUBFUFWDRD-UHFFFAOYSA-N 0.000 description 3
- JZLKKMAUZMMUMS-UHFFFAOYSA-N 4-(6-methylhepta-1,5-dien-2-yl)cyclohexene-1-carbaldehyde Chemical compound CC(C)=CCCC(=C)C1CCC(C=O)=CC1 JZLKKMAUZMMUMS-UHFFFAOYSA-N 0.000 description 3
- YJYQQKJSOQDCNY-UHFFFAOYSA-N 4-ethenyl-2-methylcyclohexene-1-carbaldehyde Chemical compound CC1=C(C=O)CCC(C=C)C1 YJYQQKJSOQDCNY-UHFFFAOYSA-N 0.000 description 3
- TYVGPQBBYDIUFO-UHFFFAOYSA-N 4-methyl-1-prop-1-en-2-ylcyclohex-3-ene-1-carbaldehyde Chemical compound CC(=C)C1(C=O)CCC(C)=CC1 TYVGPQBBYDIUFO-UHFFFAOYSA-N 0.000 description 3
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 3
- 240000000560 Citrus x paradisi Species 0.000 description 3
- 235000015510 Cucumis melo subsp melo Nutrition 0.000 description 3
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 3
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- FJJCIZWZNKZHII-UHFFFAOYSA-N [4,6-bis(cyanoamino)-1,3,5-triazin-2-yl]cyanamide Chemical compound N#CNC1=NC(NC#N)=NC(NC#N)=N1 FJJCIZWZNKZHII-UHFFFAOYSA-N 0.000 description 3
- 150000001241 acetals Chemical class 0.000 description 3
- RMRFFCXPLWYOOY-UHFFFAOYSA-N allyl radical Chemical group [CH2]C=C RMRFFCXPLWYOOY-UHFFFAOYSA-N 0.000 description 3
- 125000003118 aryl group Chemical group 0.000 description 3
- QMVPMAAFGQKVCJ-UHFFFAOYSA-N citronellol Chemical compound OCCC(C)CCC=C(C)C QMVPMAAFGQKVCJ-UHFFFAOYSA-N 0.000 description 3
- 239000012230 colorless oil Substances 0.000 description 3
- 239000003599 detergent Substances 0.000 description 3
- SZXQTJUDPRGNJN-UHFFFAOYSA-N dipropylene glycol Chemical compound OCCCOCCCO SZXQTJUDPRGNJN-UHFFFAOYSA-N 0.000 description 3
- 238000004821 distillation Methods 0.000 description 3
- 150000002576 ketones Chemical class 0.000 description 3
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 3
- 235000019341 magnesium sulphate Nutrition 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 239000002304 perfume Substances 0.000 description 3
- 239000000341 volatile oil Substances 0.000 description 3
- FINOAUDUYKVGDS-UHFFFAOYSA-N (2-tert-butylcyclohexyl) acetate Chemical compound CC(=O)OC1CCCCC1C(C)(C)C FINOAUDUYKVGDS-UHFFFAOYSA-N 0.000 description 2
- MCRYLYSUOCEFGK-UHFFFAOYSA-N (4-ethenyl-2-methylcyclohexen-1-yl)methanol Chemical compound CC1=C(CO)CCC(C=C)C1 MCRYLYSUOCEFGK-UHFFFAOYSA-N 0.000 description 2
- VSROEIKVPHHBSR-UHFFFAOYSA-N (4-ethenylcyclohexen-1-yl)methanol Chemical compound OCC1=CCC(C=C)CC1 VSROEIKVPHHBSR-UHFFFAOYSA-N 0.000 description 2
- BVDMQAQCEBGIJR-UHFFFAOYSA-N 1-(2,2,6-trimethylcyclohexyl)hexan-3-ol Chemical compound CCCC(O)CCC1C(C)CCCC1(C)C BVDMQAQCEBGIJR-UHFFFAOYSA-N 0.000 description 2
- PQTQALPIDVGBOL-UHFFFAOYSA-N 1-(2,4-dimethyl-1-prop-1-en-2-ylcyclohex-3-en-1-yl)-2-methylpropan-1-ol Chemical compound CC(C)C(O)C1(C(C)=C)CCC(C)=CC1C PQTQALPIDVGBOL-UHFFFAOYSA-N 0.000 description 2
- KEQFMNVNGVFWID-UHFFFAOYSA-N 1-(2,4-dimethyl-1-prop-1-en-2-ylcyclohex-3-en-1-yl)-2-methylpropan-1-one Chemical compound CC(C)C(=O)C1(C(C)=C)CCC(C)=CC1C KEQFMNVNGVFWID-UHFFFAOYSA-N 0.000 description 2
- ATRBOFYZSKBXFV-UHFFFAOYSA-N 1-(2,4-dimethyl-1-prop-1-en-2-ylcyclohex-3-en-1-yl)ethanone Chemical compound CC1C=C(C)CCC1(C(C)=C)C(C)=O ATRBOFYZSKBXFV-UHFFFAOYSA-N 0.000 description 2
- XDSUUYDJCAZDMC-UHFFFAOYSA-N 1-(2,4-dimethyl-1-prop-1-en-2-ylcyclohex-3-en-1-yl)ethyl acetate Chemical compound CC(=O)OC(C)C1(C(C)=C)CCC(C)=CC1C XDSUUYDJCAZDMC-UHFFFAOYSA-N 0.000 description 2
- KVPDELIBSYIBGK-UHFFFAOYSA-N 1-(4-ethenylcyclohexen-1-yl)ethanol Chemical compound CC(O)C1=CCC(C=C)CC1 KVPDELIBSYIBGK-UHFFFAOYSA-N 0.000 description 2
- MBDOYVRWFFCFHM-SNAWJCMRSA-N 2-Hexenal Natural products CCC\C=C\C=O MBDOYVRWFFCFHM-SNAWJCMRSA-N 0.000 description 2
- WRMNZCZEMHIOCP-UHFFFAOYSA-N 2-phenylethanol Chemical compound OCCC1=CC=CC=C1 WRMNZCZEMHIOCP-UHFFFAOYSA-N 0.000 description 2
- XPCTZQVDEJYUGT-UHFFFAOYSA-N 3-hydroxy-2-methyl-4-pyrone Chemical compound CC=1OC=CC(=O)C=1O XPCTZQVDEJYUGT-UHFFFAOYSA-N 0.000 description 2
- XPPGFLPECUDBQG-UHFFFAOYSA-N 3a,4,7,7a-tetrahydro-3h-indene-5-carbaldehyde Chemical compound C1C(C=O)=CCC2C=CCC21 XPPGFLPECUDBQG-UHFFFAOYSA-N 0.000 description 2
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 2
- HIQIXEFWDLTDED-UHFFFAOYSA-N 4-hydroxy-1-piperidin-4-ylpyrrolidin-2-one Chemical compound O=C1CC(O)CN1C1CCNCC1 HIQIXEFWDLTDED-UHFFFAOYSA-N 0.000 description 2
- RIWPMNBTULNXOH-ARJAWSKDSA-N 4-methyl-2-pentenal Chemical compound CC(C)\C=C/C=O RIWPMNBTULNXOH-ARJAWSKDSA-N 0.000 description 2
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 2
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 2
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 2
- 235000004936 Bromus mango Nutrition 0.000 description 2
- 125000006519 CCH3 Chemical group 0.000 description 2
- NPBVQXIMTZKSBA-UHFFFAOYSA-N Chavibetol Natural products COC1=CC=C(CC=C)C=C1O NPBVQXIMTZKSBA-UHFFFAOYSA-N 0.000 description 2
- 244000223760 Cinnamomum zeylanicum Species 0.000 description 2
- 240000008067 Cucumis sativus Species 0.000 description 2
- 235000010799 Cucumis sativus var sativus Nutrition 0.000 description 2
- NUPSHWCALHZGOV-UHFFFAOYSA-N Decyl acetate Chemical compound CCCCCCCCCCOC(C)=O NUPSHWCALHZGOV-UHFFFAOYSA-N 0.000 description 2
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 2
- 238000005698 Diels-Alder reaction Methods 0.000 description 2
- 239000005770 Eugenol Substances 0.000 description 2
- WTDHULULXKLSOZ-UHFFFAOYSA-N Hydroxylamine hydrochloride Chemical compound Cl.ON WTDHULULXKLSOZ-UHFFFAOYSA-N 0.000 description 2
- 229910010084 LiAlH4 Inorganic materials 0.000 description 2
- 235000014826 Mangifera indica Nutrition 0.000 description 2
- 240000007228 Mangifera indica Species 0.000 description 2
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 2
- LQKRYVGRPXFFAV-UHFFFAOYSA-N Phenylmethylglycidic ester Chemical compound CCOC(=O)C1OC1(C)C1=CC=CC=C1 LQKRYVGRPXFFAV-UHFFFAOYSA-N 0.000 description 2
- UVMRYBDEERADNV-UHFFFAOYSA-N Pseudoeugenol Natural products COC1=CC(C(C)=C)=CC=C1O UVMRYBDEERADNV-UHFFFAOYSA-N 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- 235000009184 Spondias indica Nutrition 0.000 description 2
- DOOTYTYQINUNNV-UHFFFAOYSA-N Triethyl citrate Chemical compound CCOC(=O)CC(O)(C(=O)OCC)CC(=O)OCC DOOTYTYQINUNNV-UHFFFAOYSA-N 0.000 description 2
- 229940022663 acetate Drugs 0.000 description 2
- 230000001476 alcoholic effect Effects 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- 125000003342 alkenyl group Chemical group 0.000 description 2
- VYBREYKSZAROCT-UHFFFAOYSA-N alpha-myrcene Natural products CC(=C)CCCC(=C)C=C VYBREYKSZAROCT-UHFFFAOYSA-N 0.000 description 2
- 235000019270 ammonium chloride Nutrition 0.000 description 2
- QUKGYYKBILRGFE-UHFFFAOYSA-N benzyl acetate Chemical compound CC(=O)OCC1=CC=CC=C1 QUKGYYKBILRGFE-UHFFFAOYSA-N 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- HQKQRXZEXPXXIG-VJOHVRBBSA-N chembl2333940 Chemical compound C1[C@]23[C@H](C)CC[C@H]3C(C)(C)[C@H]1[C@@](OC(C)=O)(C)CC2 HQKQRXZEXPXXIG-VJOHVRBBSA-N 0.000 description 2
- 235000017803 cinnamon Nutrition 0.000 description 2
- JOZKFWLRHCDGJA-UHFFFAOYSA-N citronellol acetate Chemical compound CC(=O)OCCC(C)CCC=C(C)C JOZKFWLRHCDGJA-UHFFFAOYSA-N 0.000 description 2
- 238000004140 cleaning Methods 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 239000002537 cosmetic Substances 0.000 description 2
- MGNZXYYWBUKAII-UHFFFAOYSA-N cyclohexa-1,3-diene Chemical compound C1CC=CC=C1 MGNZXYYWBUKAII-UHFFFAOYSA-N 0.000 description 2
- 239000002781 deodorant agent Substances 0.000 description 2
- 238000006471 dimerization reaction Methods 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- 238000002330 electrospray ionisation mass spectrometry Methods 0.000 description 2
- CBOQJANXLMLOSS-UHFFFAOYSA-N ethyl vanillin Chemical compound CCOC1=CC(C=O)=CC=C1O CBOQJANXLMLOSS-UHFFFAOYSA-N 0.000 description 2
- 229960002217 eugenol Drugs 0.000 description 2
- 239000000284 extract Substances 0.000 description 2
- 239000002979 fabric softener Substances 0.000 description 2
- WPFVBOQKRVRMJB-UHFFFAOYSA-N hydroxycitronellal Chemical compound O=CCC(C)CCCC(C)(C)O WPFVBOQKRVRMJB-UHFFFAOYSA-N 0.000 description 2
- 239000000543 intermediate Substances 0.000 description 2
- 150000002596 lactones Chemical class 0.000 description 2
- 239000010410 layer Substances 0.000 description 2
- CDOSHBSSFJOMGT-UHFFFAOYSA-N linalool Chemical compound CC(C)=CCCC(C)(O)C=C CDOSHBSSFJOMGT-UHFFFAOYSA-N 0.000 description 2
- UWKAYLJWKGQEPM-LBPRGKRZSA-N linalyl acetate Chemical compound CC(C)=CCC[C@](C)(C=C)OC(C)=O UWKAYLJWKGQEPM-LBPRGKRZSA-N 0.000 description 2
- 239000012280 lithium aluminium hydride Substances 0.000 description 2
- CYSFUFRXDOAOMP-UHFFFAOYSA-M magnesium;prop-1-ene;chloride Chemical compound [Mg+2].[Cl-].[CH2-]C=C CYSFUFRXDOAOMP-UHFFFAOYSA-M 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 229930014626 natural product Natural products 0.000 description 2
- ZRSNZINYAWTAHE-UHFFFAOYSA-N p-methoxybenzaldehyde Chemical compound COC1=CC=C(C=O)C=C1 ZRSNZINYAWTAHE-UHFFFAOYSA-N 0.000 description 2
- PMJHHCWVYXUKFD-UHFFFAOYSA-N penta-1,3-diene Chemical compound CC=CC=C PMJHHCWVYXUKFD-UHFFFAOYSA-N 0.000 description 2
- 239000012071 phase Substances 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- 239000011541 reaction mixture Substances 0.000 description 2
- CZCBTSFUTPZVKJ-UHFFFAOYSA-N rose oxide Chemical compound CC1CCOC(C=C(C)C)C1 CZCBTSFUTPZVKJ-UHFFFAOYSA-N 0.000 description 2
- 150000003335 secondary amines Chemical class 0.000 description 2
- 125000003396 thiol group Chemical group [H]S* 0.000 description 2
- 230000009466 transformation Effects 0.000 description 2
- 239000001069 triethyl citrate Substances 0.000 description 2
- VMYFZRTXGLUXMZ-UHFFFAOYSA-N triethyl citrate Natural products CCOC(=O)C(O)(C(=O)OCC)C(=O)OCC VMYFZRTXGLUXMZ-UHFFFAOYSA-N 0.000 description 2
- 235000013769 triethyl citrate Nutrition 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- PHXATPHONSXBIL-UHFFFAOYSA-N xi-gamma-Undecalactone Chemical compound CCCCCCCC1CCC(=O)O1 PHXATPHONSXBIL-UHFFFAOYSA-N 0.000 description 2
- WTFNSXYULBQCQV-UHFFFAOYSA-N $l^{1}-oxidanyloxymethane Chemical compound CO[O] WTFNSXYULBQCQV-UHFFFAOYSA-N 0.000 description 1
- NOOLISFMXDJSKH-UTLUCORTSA-N (+)-Neomenthol Chemical compound CC(C)[C@@H]1CC[C@@H](C)C[C@@H]1O NOOLISFMXDJSKH-UTLUCORTSA-N 0.000 description 1
- WTOYNNBCKUYIKC-JMSVASOKSA-N (+)-nootkatone Chemical compound C1C[C@@H](C(C)=C)C[C@@]2(C)[C@H](C)CC(=O)C=C21 WTOYNNBCKUYIKC-JMSVASOKSA-N 0.000 description 1
- ORHSGDMSYGKJJY-SAIIYOCFSA-N (1'r,6's)-2,2,4',7',7'-pentamethylspiro[1,3-dioxane-5,5'-bicyclo[4.1.0]heptane] Chemical compound C12([C@H]3[C@H](C3(C)C)CCC2C)COC(C)(C)OC1 ORHSGDMSYGKJJY-SAIIYOCFSA-N 0.000 description 1
- VPNOCQFVZBZIMQ-UHFFFAOYSA-N (1-ethenyl-2,4-dimethylcyclohex-3-en-1-yl)methyl acetate Chemical compound CC1C=C(C)CCC1(COC(C)=O)C=C VPNOCQFVZBZIMQ-UHFFFAOYSA-N 0.000 description 1
- CRDAMVZIKSXKFV-FBXUGWQNSA-N (2-cis,6-cis)-farnesol Chemical compound CC(C)=CCC\C(C)=C/CC\C(C)=C/CO CRDAMVZIKSXKFV-FBXUGWQNSA-N 0.000 description 1
- 239000000260 (2E,6E)-3,7,11-trimethyldodeca-2,6,10-trien-1-ol Substances 0.000 description 1
- AVJMJMPVWWWELJ-DHZHZOJOSA-N (2e)-1-methoxy-3,7-dimethylocta-2,6-diene Chemical compound COC\C=C(/C)CCC=C(C)C AVJMJMPVWWWELJ-DHZHZOJOSA-N 0.000 description 1
- 239000001490 (3R)-3,7-dimethylocta-1,6-dien-3-ol Substances 0.000 description 1
- GQVMHMFBVWSSPF-SOYUKNQTSA-N (4E,6E)-2,6-dimethylocta-2,4,6-triene Chemical compound C\C=C(/C)\C=C\C=C(C)C GQVMHMFBVWSSPF-SOYUKNQTSA-N 0.000 description 1
- NVIPUOMWGQAOIT-UHFFFAOYSA-N (E)-7-Hexadecen-16-olide Natural products O=C1CCCCCC=CCCCCCCCCO1 NVIPUOMWGQAOIT-UHFFFAOYSA-N 0.000 description 1
- OOCCDEMITAIZTP-QPJJXVBHSA-N (E)-cinnamyl alcohol Chemical compound OC\C=C\C1=CC=CC=C1 OOCCDEMITAIZTP-QPJJXVBHSA-N 0.000 description 1
- BATOPAZDIZEVQF-MQQKCMAXSA-N (E,E)-2,4-hexadienal Chemical compound C\C=C\C=C\C=O BATOPAZDIZEVQF-MQQKCMAXSA-N 0.000 description 1
- DCSCXTJOXBUFGB-JGVFFNPUSA-N (R)-(+)-Verbenone Natural products CC1=CC(=O)[C@@H]2C(C)(C)[C@H]1C2 DCSCXTJOXBUFGB-JGVFFNPUSA-N 0.000 description 1
- QMVPMAAFGQKVCJ-SNVBAGLBSA-N (R)-(+)-citronellol Natural products OCC[C@H](C)CCC=C(C)C QMVPMAAFGQKVCJ-SNVBAGLBSA-N 0.000 description 1
- DCSCXTJOXBUFGB-SFYZADRCSA-N (R)-(+)-verbenone Chemical compound CC1=CC(=O)[C@H]2C(C)(C)[C@@H]1C2 DCSCXTJOXBUFGB-SFYZADRCSA-N 0.000 description 1
- CDOSHBSSFJOMGT-JTQLQIEISA-N (R)-linalool Natural products CC(C)=CCC[C@@](C)(O)C=C CDOSHBSSFJOMGT-JTQLQIEISA-N 0.000 description 1
- UFLHIIWVXFIJGU-ARJAWSKDSA-N (Z)-hex-3-en-1-ol Chemical compound CC\C=C/CCO UFLHIIWVXFIJGU-ARJAWSKDSA-N 0.000 description 1
- YYMCVDNIIFNDJK-XFQWXJFMSA-N (z)-1-(3-fluorophenyl)-n-[(z)-(3-fluorophenyl)methylideneamino]methanimine Chemical compound FC1=CC=CC(\C=N/N=C\C=2C=C(F)C=CC=2)=C1 YYMCVDNIIFNDJK-XFQWXJFMSA-N 0.000 description 1
- RNLHVODSMDJCBR-VURMDHGXSA-N (z)-3-methyl-5-(2,2,3-trimethylcyclopent-3-en-1-yl)pent-4-en-2-ol Chemical compound CC(O)C(C)\C=C/C1CC=C(C)C1(C)C RNLHVODSMDJCBR-VURMDHGXSA-N 0.000 description 1
- WCIIQJJGGQSZCM-UHFFFAOYSA-N 1,4,4a,7,8,8a-hexahydronaphthalene-2-carbaldehyde Chemical compound C1=CCCC2CC(C=O)=CCC21 WCIIQJJGGQSZCM-UHFFFAOYSA-N 0.000 description 1
- LVXZHHVKUFRLBX-UHFFFAOYSA-N 1-(2,4-dimethyl-1-prop-1-en-2-ylcyclohex-3-en-1-yl)but-2-en-1-one Chemical compound CC=CC(=O)C1(C(C)=C)CCC(C)=CC1C LVXZHHVKUFRLBX-UHFFFAOYSA-N 0.000 description 1
- VPKMGDRERYMTJX-CMDGGOBGSA-N 1-(2,6,6-Trimethyl-2-cyclohexen-1-yl)-1-penten-3-one Chemical compound CCC(=O)\C=C\C1C(C)=CCCC1(C)C VPKMGDRERYMTJX-CMDGGOBGSA-N 0.000 description 1
- SACCSWOIHPVKPO-UHFFFAOYSA-N 1-(3a,4,7,7a-tetrahydro-3h-inden-5-yl)ethanol Chemical compound C1C(C(O)C)=CCC2C=CCC21 SACCSWOIHPVKPO-UHFFFAOYSA-N 0.000 description 1
- QMAIRFRHEGKGDA-UHFFFAOYSA-N 1-(4-prop-1-en-2-ylcyclohexen-1-yl)ethanol Chemical compound CC(O)C1=CCC(C(C)=C)CC1 QMAIRFRHEGKGDA-UHFFFAOYSA-N 0.000 description 1
- OEVIJAZJVZDBQL-UHFFFAOYSA-N 1-(5,5-dimethylcyclohexen-1-yl)pent-4-en-1-one Chemical compound CC1(C)CCC=C(C(=O)CCC=C)C1 OEVIJAZJVZDBQL-UHFFFAOYSA-N 0.000 description 1
- ZXOPLLGTQJCNDX-UHFFFAOYSA-N 1-methyl-3a,4,7,7a-tetrahydro-3h-indene-5-carbaldehyde Chemical compound C1C(C=O)=CCC2C(C)=CCC21 ZXOPLLGTQJCNDX-UHFFFAOYSA-N 0.000 description 1
- RYFTZGITMYBDHI-UHFFFAOYSA-N 1-prop-1-en-2-ylcyclohex-3-ene-1-carbaldehyde Chemical compound CC(=C)C1(C=O)CCC=CC1 RYFTZGITMYBDHI-UHFFFAOYSA-N 0.000 description 1
- GMVANJWNDFADSN-UHFFFAOYSA-N 2,4-dimethyl-1-(2-methylprop-1-enyl)cyclohex-3-ene-1-carbaldehyde Chemical compound CC1C=C(C)CCC1(C=O)C=C(C)C GMVANJWNDFADSN-UHFFFAOYSA-N 0.000 description 1
- FLUWAIIVLCVEKF-UHFFFAOYSA-N 2-Methyl-1-phenyl-2-propanyl acetate Chemical compound CC(=O)OC(C)(C)CC1=CC=CC=C1 FLUWAIIVLCVEKF-UHFFFAOYSA-N 0.000 description 1
- NAMYKGVDVNBCFQ-UHFFFAOYSA-N 2-bromopropane Chemical compound CC(C)Br NAMYKGVDVNBCFQ-UHFFFAOYSA-N 0.000 description 1
- YCOLTBFWHMEGQK-UHFFFAOYSA-N 2-cyclopentylideneacetaldehyde Chemical compound O=CC=C1CCCC1 YCOLTBFWHMEGQK-UHFFFAOYSA-N 0.000 description 1
- NBUOSBPWABUQEX-UHFFFAOYSA-N 2-methyl-3a,4,7,7a-tetrahydro-3h-indene-5-carbaldehyde Chemical compound C1C=C(C=O)CC2CC(C)=CC21 NBUOSBPWABUQEX-UHFFFAOYSA-N 0.000 description 1
- NFAVNWJJYQAGNB-UHFFFAOYSA-N 2-methylundecanal Chemical compound CCCCCCCCCC(C)C=O NFAVNWJJYQAGNB-UHFFFAOYSA-N 0.000 description 1
- MIDXCONKKJTLDX-UHFFFAOYSA-N 3,5-dimethylcyclopentane-1,2-dione Chemical compound CC1CC(C)C(=O)C1=O MIDXCONKKJTLDX-UHFFFAOYSA-N 0.000 description 1
- NGYMOTOXXHCHOC-UHFFFAOYSA-N 3-methyl-5-(2,2,3-trimethylcyclopent-3-en-1-yl)pentan-2-ol Chemical compound CC(O)C(C)CCC1CC=C(C)C1(C)C NGYMOTOXXHCHOC-UHFFFAOYSA-N 0.000 description 1
- NAIVNFKASRRQMZ-UHFFFAOYSA-N 3-methylidenepent-4-en-2-one Chemical compound CC(=O)C(=C)C=C NAIVNFKASRRQMZ-UHFFFAOYSA-N 0.000 description 1
- SSJSDJGZGJAPQL-UHFFFAOYSA-N 3a,4,7,7a-tetrahydro-3h-inden-5-ylmethanol Chemical compound C1C(CO)=CCC2C=CCC21 SSJSDJGZGJAPQL-UHFFFAOYSA-N 0.000 description 1
- 229960000549 4-dimethylaminophenol Drugs 0.000 description 1
- QWRGOHMKGNCVAC-UHFFFAOYSA-N 5,6,7-trimethylocta-2,5-dien-4-one Chemical compound CC=CC(=O)C(C)=C(C)C(C)C QWRGOHMKGNCVAC-UHFFFAOYSA-N 0.000 description 1
- WXACXMWYHXOSIX-UHFFFAOYSA-N 5-propan-2-ylidenecyclopenta-1,3-diene Chemical compound CC(C)=C1C=CC=C1 WXACXMWYHXOSIX-UHFFFAOYSA-N 0.000 description 1
- AUBLFWWZTFFBNU-UHFFFAOYSA-N 6-butan-2-ylquinoline Chemical compound N1=CC=CC2=CC(C(C)CC)=CC=C21 AUBLFWWZTFFBNU-UHFFFAOYSA-N 0.000 description 1
- NVIPUOMWGQAOIT-DUXPYHPUSA-N 7-hexadecen-1,16-olide Chemical compound O=C1CCCCC\C=C\CCCCCCCCO1 NVIPUOMWGQAOIT-DUXPYHPUSA-N 0.000 description 1
- 235000009051 Ambrosia paniculata var. peruviana Nutrition 0.000 description 1
- 235000003097 Artemisia absinthium Nutrition 0.000 description 1
- 240000001851 Artemisia dracunculus Species 0.000 description 1
- 235000017731 Artemisia dracunculus ssp. dracunculus Nutrition 0.000 description 1
- 235000003261 Artemisia vulgaris Nutrition 0.000 description 1
- 240000007436 Cananga odorata Species 0.000 description 1
- WTEVQBCEXWBHNA-UHFFFAOYSA-N Citral Natural products CC(C)=CCCC(C)=CC=O WTEVQBCEXWBHNA-UHFFFAOYSA-N 0.000 description 1
- JOZKFWLRHCDGJA-LLVKDONJSA-N Citronellyl acetate Natural products CC(=O)OCC[C@H](C)CCC=C(C)C JOZKFWLRHCDGJA-LLVKDONJSA-N 0.000 description 1
- 235000009847 Cucumis melo var cantalupensis Nutrition 0.000 description 1
- FKUPPRZPSYCDRS-UHFFFAOYSA-N Cyclopentadecanolide Chemical compound O=C1CCCCCCCCCCCCCCO1 FKUPPRZPSYCDRS-UHFFFAOYSA-N 0.000 description 1
- NOOLISFMXDJSKH-UHFFFAOYSA-N DL-menthol Natural products CC(C)C1CCC(C)CC1O NOOLISFMXDJSKH-UHFFFAOYSA-N 0.000 description 1
- GSNUFIFRDBKVIE-UHFFFAOYSA-N DMF Natural products CC1=CC=C(C)O1 GSNUFIFRDBKVIE-UHFFFAOYSA-N 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- XRHCAGNSDHCHFJ-UHFFFAOYSA-N Ethylene brassylate Chemical compound O=C1CCCCCCCCCCCC(=O)OCCO1 XRHCAGNSDHCHFJ-UHFFFAOYSA-N 0.000 description 1
- 238000005727 Friedel-Crafts reaction Methods 0.000 description 1
- 239000005792 Geraniol Substances 0.000 description 1
- GLZPCOQZEFWAFX-YFHOEESVSA-N Geraniol Natural products CC(C)=CCC\C(C)=C/CO GLZPCOQZEFWAFX-YFHOEESVSA-N 0.000 description 1
- 239000007818 Grignard reagent Substances 0.000 description 1
- 240000004533 Hesperis matronalis Species 0.000 description 1
- 235000015847 Hesperis matronalis Nutrition 0.000 description 1
- 241001632576 Hyacinthus Species 0.000 description 1
- 235000010254 Jasminum officinale Nutrition 0.000 description 1
- 240000005385 Jasminum sambac Species 0.000 description 1
- 244000178870 Lavandula angustifolia Species 0.000 description 1
- 235000010663 Lavandula angustifolia Nutrition 0.000 description 1
- 241000234269 Liliales Species 0.000 description 1
- HYMLWHLQFGRFIY-UHFFFAOYSA-N Maltol Natural products CC1OC=CC(=O)C1=O HYMLWHLQFGRFIY-UHFFFAOYSA-N 0.000 description 1
- 241000220225 Malus Species 0.000 description 1
- 240000009023 Myrrhis odorata Species 0.000 description 1
- 235000007265 Myrrhis odorata Nutrition 0.000 description 1
- 240000005125 Myrtus communis Species 0.000 description 1
- 235000013418 Myrtus communis Nutrition 0.000 description 1
- 238000005481 NMR spectroscopy Methods 0.000 description 1
- 241000030602 Neocallitropsis pancheri Species 0.000 description 1
- GLZPCOQZEFWAFX-JXMROGBWSA-N Nerol Natural products CC(C)=CCC\C(C)=C\CO GLZPCOQZEFWAFX-JXMROGBWSA-N 0.000 description 1
- 235000004347 Perilla Nutrition 0.000 description 1
- 241000229722 Perilla <angiosperm> Species 0.000 description 1
- 235000012550 Pimpinella anisum Nutrition 0.000 description 1
- 235000008184 Piper nigrum Nutrition 0.000 description 1
- 244000203593 Piper nigrum Species 0.000 description 1
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- 235000009827 Prunus armeniaca Nutrition 0.000 description 1
- 244000018633 Prunus armeniaca Species 0.000 description 1
- 241000220317 Rosa Species 0.000 description 1
- AWXTUFPUJSQYGO-OAHLLOKOSA-N [(4s)-4-(6-methylhepta-1,5-dien-2-yl)cyclohexen-1-yl]methanol Chemical compound CC(C)=CCCC(=C)[C@H]1CCC(CO)=CC1 AWXTUFPUJSQYGO-OAHLLOKOSA-N 0.000 description 1
- KGDJMNKPBUNHGY-RMKNXTFCSA-N [(e)-3-phenylprop-2-enyl] propanoate Chemical compound CCC(=O)OC\C=C\C1=CC=CC=C1 KGDJMNKPBUNHGY-RMKNXTFCSA-N 0.000 description 1
- AWXTUFPUJSQYGO-UHFFFAOYSA-N [4-(6-methylhepta-1,5-dien-2-yl)cyclohexen-1-yl]methanol Chemical compound CC(C)=CCCC(=C)C1CCC(CO)=CC1 AWXTUFPUJSQYGO-UHFFFAOYSA-N 0.000 description 1
- 239000002250 absorbent Substances 0.000 description 1
- 230000002745 absorbent Effects 0.000 description 1
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 description 1
- TUCNEACPLKLKNU-UHFFFAOYSA-N acetyl Chemical compound C[C]=O TUCNEACPLKLKNU-UHFFFAOYSA-N 0.000 description 1
- OOCCDEMITAIZTP-UHFFFAOYSA-N allylic benzylic alcohol Natural products OCC=CC1=CC=CC=C1 OOCCDEMITAIZTP-UHFFFAOYSA-N 0.000 description 1
- HMKKIXGYKWDQSV-KAMYIIQDSA-N alpha-Amylcinnamaldehyde Chemical compound CCCCC\C(C=O)=C\C1=CC=CC=C1 HMKKIXGYKWDQSV-KAMYIIQDSA-N 0.000 description 1
- WUOACPNHFRMFPN-UHFFFAOYSA-N alpha-terpineol Chemical compound CC1=CCC(C(C)(C)O)CC1 WUOACPNHFRMFPN-UHFFFAOYSA-N 0.000 description 1
- YPZUZOLGGMJZJO-UHFFFAOYSA-N ambrofix Natural products C1CC2C(C)(C)CCCC2(C)C2C1(C)OCC2 YPZUZOLGGMJZJO-UHFFFAOYSA-N 0.000 description 1
- YPZUZOLGGMJZJO-LQKXBSAESA-N ambroxan Chemical compound CC([C@@H]1CC2)(C)CCC[C@]1(C)[C@@H]1[C@]2(C)OCC1 YPZUZOLGGMJZJO-LQKXBSAESA-N 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- 239000001138 artemisia absinthium Substances 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 239000012752 auxiliary agent Substances 0.000 description 1
- 239000010619 basil oil Substances 0.000 description 1
- 229940018006 basil oil Drugs 0.000 description 1
- 229940007550 benzyl acetate Drugs 0.000 description 1
- JGQFVRIQXUFPAH-UHFFFAOYSA-N beta-citronellol Natural products OCCC(C)CCCC(C)=C JGQFVRIQXUFPAH-UHFFFAOYSA-N 0.000 description 1
- 235000013614 black pepper Nutrition 0.000 description 1
- 239000007844 bleaching agent Substances 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 235000013736 caramel Nutrition 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 239000012876 carrier material Substances 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- WBLIXGSTEMXDSM-UHFFFAOYSA-N chloromethane Chemical compound Cl[CH2] WBLIXGSTEMXDSM-UHFFFAOYSA-N 0.000 description 1
- GQVMHMFBVWSSPF-UHFFFAOYSA-N cis-alloocimene Natural products CC=C(C)C=CC=C(C)C GQVMHMFBVWSSPF-UHFFFAOYSA-N 0.000 description 1
- 229940043350 citral Drugs 0.000 description 1
- 235000000484 citronellol Nutrition 0.000 description 1
- 239000001111 citrus aurantium l. leaf oil Substances 0.000 description 1
- 239000001926 citrus aurantium l. subsp. bergamia wright et arn. oil Substances 0.000 description 1
- 239000001071 citrus reticulata blanco var. mandarin Substances 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- OANSOJSBHVENEI-UHFFFAOYSA-N cyclohexene-1-carbaldehyde Chemical class O=CC1=CCCCC1 OANSOJSBHVENEI-UHFFFAOYSA-N 0.000 description 1
- IYDGMSRMAPNCSD-UHFFFAOYSA-N cyclopenta[g]isochromene Chemical compound C1=C2C=COC=C2C=C2C1=CC=C2 IYDGMSRMAPNCSD-UHFFFAOYSA-N 0.000 description 1
- 239000001939 cymbopogon martini roxb. stapf. oil Substances 0.000 description 1
- SQIFACVGCPWBQZ-UHFFFAOYSA-N delta-terpineol Natural products CC(C)(O)C1CCC(=C)CC1 SQIFACVGCPWBQZ-UHFFFAOYSA-N 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 229940095104 dimethyl benzyl carbinyl acetate Drugs 0.000 description 1
- CJSBUWDGPXGFGA-UHFFFAOYSA-N dimethyl-butadiene Natural products CC(C)=CC=C CJSBUWDGPXGFGA-UHFFFAOYSA-N 0.000 description 1
- IPZJQDSFZGZEOY-UHFFFAOYSA-N dimethylmethylene Chemical compound C[C]C IPZJQDSFZGZEOY-UHFFFAOYSA-N 0.000 description 1
- 238000004851 dishwashing Methods 0.000 description 1
- WTOYNNBCKUYIKC-UHFFFAOYSA-N dl-nootkatone Natural products C1CC(C(C)=C)CC2(C)C(C)CC(=O)C=C21 WTOYNNBCKUYIKC-UHFFFAOYSA-N 0.000 description 1
- 235000013399 edible fruits Nutrition 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 239000003480 eluent Substances 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- XYIBRDXRRQCHLP-UHFFFAOYSA-N ethyl acetoacetate Chemical compound CCOC(=O)CC(C)=O XYIBRDXRRQCHLP-UHFFFAOYSA-N 0.000 description 1
- 229940093858 ethyl acetoacetate Drugs 0.000 description 1
- 229940073505 ethyl vanillin Drugs 0.000 description 1
- 229940093468 ethylene brassylate Drugs 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 239000004744 fabric Substances 0.000 description 1
- 229930002886 farnesol Natural products 0.000 description 1
- 229940043259 farnesol Drugs 0.000 description 1
- 239000010408 film Substances 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- ONKNPOPIGWHAQC-UHFFFAOYSA-N galaxolide Chemical compound C1OCC(C)C2=C1C=C1C(C)(C)C(C)C(C)(C)C1=C2 ONKNPOPIGWHAQC-UHFFFAOYSA-N 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- WTEVQBCEXWBHNA-JXMROGBWSA-N geranial Chemical compound CC(C)=CCC\C(C)=C\C=O WTEVQBCEXWBHNA-JXMROGBWSA-N 0.000 description 1
- HIGQPQRQIQDZMP-UHFFFAOYSA-N geranil acetate Natural products CC(C)=CCCC(C)=CCOC(C)=O HIGQPQRQIQDZMP-UHFFFAOYSA-N 0.000 description 1
- 229940113087 geraniol Drugs 0.000 description 1
- HIGQPQRQIQDZMP-DHZHZOJOSA-N geranyl acetate Chemical compound CC(C)=CCC\C(C)=C\COC(C)=O HIGQPQRQIQDZMP-DHZHZOJOSA-N 0.000 description 1
- HNZUNIKWNYHEJJ-UHFFFAOYSA-N geranyl acetone Natural products CC(C)=CCCC(C)=CCCC(C)=O HNZUNIKWNYHEJJ-UHFFFAOYSA-N 0.000 description 1
- HNZUNIKWNYHEJJ-FMIVXFBMSA-N geranyl acetone Chemical compound CC(C)=CCC\C(C)=C\CCC(C)=O HNZUNIKWNYHEJJ-FMIVXFBMSA-N 0.000 description 1
- 150000004795 grignard reagents Chemical class 0.000 description 1
- 125000005842 heteroatom Chemical group 0.000 description 1
- 125000000623 heterocyclic group Chemical group 0.000 description 1
- UFLHIIWVXFIJGU-UHFFFAOYSA-N hex-3-en-1-ol Natural products CCC=CCCO UFLHIIWVXFIJGU-UHFFFAOYSA-N 0.000 description 1
- 125000004356 hydroxy functional group Chemical group O* 0.000 description 1
- 239000010656 jasmine oil Substances 0.000 description 1
- 239000001102 lavandula vera Substances 0.000 description 1
- 235000018219 lavender Nutrition 0.000 description 1
- SDQFDHOLCGWZPU-UHFFFAOYSA-N lilial Chemical compound O=CC(C)CC1=CC=C(C(C)(C)C)C=C1 SDQFDHOLCGWZPU-UHFFFAOYSA-N 0.000 description 1
- 229930007744 linalool Natural products 0.000 description 1
- UWKAYLJWKGQEPM-UHFFFAOYSA-N linalool acetate Natural products CC(C)=CCCC(C)(C=C)OC(C)=O UWKAYLJWKGQEPM-UHFFFAOYSA-N 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 150000002678 macrocyclic compounds Chemical class 0.000 description 1
- NXPHGHWWQRMDIA-UHFFFAOYSA-M magnesium;carbanide;bromide Chemical compound [CH3-].[Mg+2].[Br-] NXPHGHWWQRMDIA-UHFFFAOYSA-M 0.000 description 1
- 229940043353 maltol Drugs 0.000 description 1
- 239000013521 mastic Substances 0.000 description 1
- 229940041616 menthol Drugs 0.000 description 1
- MARRJGBPDCCAEK-FSAOVCISSA-N methyl (1r,4ar,4bs,8as,10ar)-1,4a-dimethyl-7-propan-2-yl-2,3,4,4b,5,6,8a,9,10,10a-decahydrophenanthrene-1-carboxylate Chemical compound C1CC(C(C)C)=C[C@@H]2CC[C@H]3[C@@](C(=O)OC)(C)CCC[C@]3(C)[C@H]21 MARRJGBPDCCAEK-FSAOVCISSA-N 0.000 description 1
- KVWWIYGFBYDJQC-UHFFFAOYSA-N methyl dihydrojasmonate Chemical compound CCCCCC1C(CC(=O)OC)CCC1=O KVWWIYGFBYDJQC-UHFFFAOYSA-N 0.000 description 1
- YAHNYLGSSPTTAG-UHFFFAOYSA-N methyl n-(3,4-dichlorophenyl)carbamodithioate Chemical compound CSC(=S)NC1=CC=C(Cl)C(Cl)=C1 YAHNYLGSSPTTAG-UHFFFAOYSA-N 0.000 description 1
- NFWSQSCIDYBUOU-UHFFFAOYSA-N methylcyclopentadiene Chemical compound CC1=CC=CC1 NFWSQSCIDYBUOU-UHFFFAOYSA-N 0.000 description 1
- 239000003094 microcapsule Substances 0.000 description 1
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 1
- 239000002088 nanocapsule Substances 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 229920001542 oligosaccharide Polymers 0.000 description 1
- 238000005580 one pot reaction Methods 0.000 description 1
- 239000012044 organic layer Substances 0.000 description 1
- 239000012074 organic phase Substances 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 238000006362 organocatalysis Methods 0.000 description 1
- 150000002923 oximes Chemical class 0.000 description 1
- SVMGVNXXUVNGRK-UHFFFAOYSA-N oxomethylideneiron Chemical class O=C=[Fe] SVMGVNXXUVNGRK-UHFFFAOYSA-N 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 229940067107 phenylethyl alcohol Drugs 0.000 description 1
- 150000003003 phosphines Chemical class 0.000 description 1
- 239000001738 pogostemon cablin oil Substances 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- QWRGOHMKGNCVAC-KQHSAVHASA-N pomarose Chemical compound C\C=C\C(=O)C(\C)=C(\C)C(C)C QWRGOHMKGNCVAC-KQHSAVHASA-N 0.000 description 1
- 150000003141 primary amines Chemical class 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 235000019719 rose oil Nutrition 0.000 description 1
- 239000010666 rose oil Substances 0.000 description 1
- 229930007790 rose oxide Natural products 0.000 description 1
- 239000010671 sandalwood oil Substances 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 229930004725 sesquiterpene Natural products 0.000 description 1
- 239000002453 shampoo Substances 0.000 description 1
- 239000000741 silica gel Substances 0.000 description 1
- 229910002027 silica gel Inorganic materials 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- BATOPAZDIZEVQF-UHFFFAOYSA-N sorbic aldehyde Natural products CC=CC=CC=O BATOPAZDIZEVQF-UHFFFAOYSA-N 0.000 description 1
- VRQDPNKOUPEWOC-UHFFFAOYSA-N spiro[bicyclo[2.2.2]octane-3,3'-piperidine] Chemical compound C1CCNCC21C(CC1)CCC1C2 VRQDPNKOUPEWOC-UHFFFAOYSA-N 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N succinic acid Chemical compound OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 229940116411 terpineol Drugs 0.000 description 1
- LFSYLMRHJKGLDV-UHFFFAOYSA-N tetradecanolide Natural products O=C1CCCCCCCCCCCCCO1 LFSYLMRHJKGLDV-UHFFFAOYSA-N 0.000 description 1
- CRDAMVZIKSXKFV-UHFFFAOYSA-N trans-Farnesol Natural products CC(C)=CCCC(C)=CCCC(C)=CCO CRDAMVZIKSXKFV-UHFFFAOYSA-N 0.000 description 1
- MWOOGOJBHIARFG-UHFFFAOYSA-N vanillin Chemical compound COC1=CC(C=O)=CC=C1O MWOOGOJBHIARFG-UHFFFAOYSA-N 0.000 description 1
- FGQOOHJZONJGDT-UHFFFAOYSA-N vanillin Natural products COC1=CC(O)=CC(C=O)=C1 FGQOOHJZONJGDT-UHFFFAOYSA-N 0.000 description 1
- 235000012141 vanillin Nutrition 0.000 description 1
- DCSCXTJOXBUFGB-UHFFFAOYSA-N verbenone Natural products CC1=CC(=O)C2C(C)(C)C1C2 DCSCXTJOXBUFGB-UHFFFAOYSA-N 0.000 description 1
- 239000002023 wood Substances 0.000 description 1
- 239000010457 zeolite Substances 0.000 description 1
- IHPKGUQCSIINRJ-UHFFFAOYSA-N β-ocimene Natural products CC(C)=CCC=C(C)C=C IHPKGUQCSIINRJ-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C45/00—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds
- C07C45/61—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups
- C07C45/67—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton
- C07C45/68—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton by increase in the number of carbon atoms
- C07C45/72—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by reactions not involving the formation of >C = O groups by isomerisation; by change of size of the carbon skeleton by increase in the number of carbon atoms by reaction of compounds containing >C = O groups with the same or other compounds containing >C = O groups
- C07C45/75—Reactions with formaldehyde
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES, NOT OTHERWISE PROVIDED FOR; PREPARATION OR TREATMENT THEREOF
- A23L27/00—Spices; Flavouring agents or condiments; Artificial sweetening agents; Table salts; Dietetic salt substitutes; Preparation or treatment thereof
- A23L27/20—Synthetic spices, flavouring agents or condiments
- A23L27/202—Aliphatic compounds
- A23L27/2024—Aliphatic compounds having oxygen as the only hetero atom
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES, NOT OTHERWISE PROVIDED FOR; PREPARATION OR TREATMENT THEREOF
- A23L27/00—Spices; Flavouring agents or condiments; Artificial sweetening agents; Table salts; Dietetic salt substitutes; Preparation or treatment thereof
- A23L27/20—Synthetic spices, flavouring agents or condiments
- A23L27/202—Aliphatic compounds
- A23L27/2024—Aliphatic compounds having oxygen as the only hetero atom
- A23L27/2026—Hydroxy compounds
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES, NOT OTHERWISE PROVIDED FOR; PREPARATION OR TREATMENT THEREOF
- A23L27/00—Spices; Flavouring agents or condiments; Artificial sweetening agents; Table salts; Dietetic salt substitutes; Preparation or treatment thereof
- A23L27/20—Synthetic spices, flavouring agents or condiments
- A23L27/202—Aliphatic compounds
- A23L27/2024—Aliphatic compounds having oxygen as the only hetero atom
- A23L27/2028—Carboxy compounds
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES, NOT OTHERWISE PROVIDED FOR; PREPARATION OR TREATMENT THEREOF
- A23L27/00—Spices; Flavouring agents or condiments; Artificial sweetening agents; Table salts; Dietetic salt substitutes; Preparation or treatment thereof
- A23L27/20—Synthetic spices, flavouring agents or condiments
- A23L27/203—Alicyclic compounds
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES, NOT OTHERWISE PROVIDED FOR; PREPARATION OR TREATMENT THEREOF
- A23L27/00—Spices; Flavouring agents or condiments; Artificial sweetening agents; Table salts; Dietetic salt substitutes; Preparation or treatment thereof
- A23L27/20—Synthetic spices, flavouring agents or condiments
- A23L27/205—Heterocyclic compounds
- A23L27/2052—Heterocyclic compounds having oxygen or sulfur as the only hetero atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C251/00—Compounds containing nitrogen atoms doubly-bound to a carbon skeleton
- C07C251/32—Oximes
- C07C251/34—Oximes with oxygen atoms of oxyimino groups bound to hydrogen atoms or to carbon atoms of unsubstituted hydrocarbon radicals
- C07C251/44—Oximes with oxygen atoms of oxyimino groups bound to hydrogen atoms or to carbon atoms of unsubstituted hydrocarbon radicals with the carbon atom of at least one of the oxyimino groups being part of a ring other than a six-membered aromatic ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C33/00—Unsaturated compounds having hydroxy or O-metal groups bound to acyclic carbon atoms
- C07C33/05—Alcohols containing rings other than six-membered aromatic rings
- C07C33/14—Alcohols containing rings other than six-membered aromatic rings containing six-membered rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C403/00—Derivatives of cyclohexane or of a cyclohexene or of cyclohexadiene, having a side-chain containing an acyclic unsaturated part of at least four carbon atoms, this part being directly attached to the cyclohexane or cyclohexene or cyclohexadiene rings, e.g. vitamin A, beta-carotene, beta-ionone
- C07C403/02—Derivatives of cyclohexane or of a cyclohexene or of cyclohexadiene, having a side-chain containing an acyclic unsaturated part of at least four carbon atoms, this part being directly attached to the cyclohexane or cyclohexene or cyclohexadiene rings, e.g. vitamin A, beta-carotene, beta-ionone having side-chains containing only carbon and hydrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C45/00—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds
- C07C45/27—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by oxidation
- C07C45/29—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by oxidation of hydroxy groups
- C07C45/292—Preparation of compounds having >C = O groups bound only to carbon or hydrogen atoms; Preparation of chelates of such compounds by oxidation of hydroxy groups with chromium derivatives
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C47/00—Compounds having —CHO groups
- C07C47/38—Unsaturated compounds having —CHO groups bound to carbon atoms of rings other than six—membered aromatic rings
- C07C47/44—Unsaturated compounds having —CHO groups bound to carbon atoms of rings other than six—membered aromatic rings polycyclic
- C07C47/445—Unsaturated compounds having —CHO groups bound to carbon atoms of rings other than six—membered aromatic rings polycyclic containing a condensed ring system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C47/00—Compounds having —CHO groups
- C07C47/38—Unsaturated compounds having —CHO groups bound to carbon atoms of rings other than six—membered aromatic rings
- C07C47/45—Unsaturated compounds having —CHO groups bound to carbon atoms of rings other than six—membered aromatic rings having unsaturation outside the rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C49/00—Ketones; Ketenes; Dimeric ketenes; Ketonic chelates
- C07C49/527—Unsaturated compounds containing keto groups bound to rings other than six-membered aromatic rings
- C07C49/553—Unsaturated compounds containing keto groups bound to rings other than six-membered aromatic rings polycyclic
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C49/00—Ketones; Ketenes; Dimeric ketenes; Ketonic chelates
- C07C49/527—Unsaturated compounds containing keto groups bound to rings other than six-membered aromatic rings
- C07C49/557—Unsaturated compounds containing keto groups bound to rings other than six-membered aromatic rings having unsaturation outside the rings
-
- C—CHEMISTRY; METALLURGY
- C11—ANIMAL OR VEGETABLE OILS, FATS, FATTY SUBSTANCES OR WAXES; FATTY ACIDS THEREFROM; DETERGENTS; CANDLES
- C11B—PRODUCING, e.g. BY PRESSING RAW MATERIALS OR BY EXTRACTION FROM WASTE MATERIALS, REFINING OR PRESERVING FATS, FATTY SUBSTANCES, e.g. LANOLIN, FATTY OILS OR WAXES; ESSENTIAL OILS; PERFUMES
- C11B9/00—Essential oils; Perfumes
- C11B9/0026—Essential oils; Perfumes compounds containing an alicyclic ring not condensed with another ring
- C11B9/0034—Essential oils; Perfumes compounds containing an alicyclic ring not condensed with another ring the ring containing six carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C11—ANIMAL OR VEGETABLE OILS, FATS, FATTY SUBSTANCES OR WAXES; FATTY ACIDS THEREFROM; DETERGENTS; CANDLES
- C11B—PRODUCING, e.g. BY PRESSING RAW MATERIALS OR BY EXTRACTION FROM WASTE MATERIALS, REFINING OR PRESERVING FATS, FATTY SUBSTANCES, e.g. LANOLIN, FATTY OILS OR WAXES; ESSENTIAL OILS; PERFUMES
- C11B9/00—Essential oils; Perfumes
- C11B9/0042—Essential oils; Perfumes compounds containing condensed hydrocarbon rings
-
- C—CHEMISTRY; METALLURGY
- C11—ANIMAL OR VEGETABLE OILS, FATS, FATTY SUBSTANCES OR WAXES; FATTY ACIDS THEREFROM; DETERGENTS; CANDLES
- C11B—PRODUCING, e.g. BY PRESSING RAW MATERIALS OR BY EXTRACTION FROM WASTE MATERIALS, REFINING OR PRESERVING FATS, FATTY SUBSTANCES, e.g. LANOLIN, FATTY OILS OR WAXES; ESSENTIAL OILS; PERFUMES
- C11B9/00—Essential oils; Perfumes
- C11B9/0042—Essential oils; Perfumes compounds containing condensed hydrocarbon rings
- C11B9/0046—Essential oils; Perfumes compounds containing condensed hydrocarbon rings containing only two condensed rings
- C11B9/0049—Essential oils; Perfumes compounds containing condensed hydrocarbon rings containing only two condensed rings the condensed rings sharing two common C atoms
-
- C—CHEMISTRY; METALLURGY
- C11—ANIMAL OR VEGETABLE OILS, FATS, FATTY SUBSTANCES OR WAXES; FATTY ACIDS THEREFROM; DETERGENTS; CANDLES
- C11B—PRODUCING, e.g. BY PRESSING RAW MATERIALS OR BY EXTRACTION FROM WASTE MATERIALS, REFINING OR PRESERVING FATS, FATTY SUBSTANCES, e.g. LANOLIN, FATTY OILS OR WAXES; ESSENTIAL OILS; PERFUMES
- C11B9/00—Essential oils; Perfumes
- C11B9/0042—Essential oils; Perfumes compounds containing condensed hydrocarbon rings
- C11B9/0046—Essential oils; Perfumes compounds containing condensed hydrocarbon rings containing only two condensed rings
- C11B9/0049—Essential oils; Perfumes compounds containing condensed hydrocarbon rings containing only two condensed rings the condensed rings sharing two common C atoms
- C11B9/0053—Essential oils; Perfumes compounds containing condensed hydrocarbon rings containing only two condensed rings the condensed rings sharing two common C atoms both rings being six-membered
-
- C—CHEMISTRY; METALLURGY
- C11—ANIMAL OR VEGETABLE OILS, FATS, FATTY SUBSTANCES OR WAXES; FATTY ACIDS THEREFROM; DETERGENTS; CANDLES
- C11B—PRODUCING, e.g. BY PRESSING RAW MATERIALS OR BY EXTRACTION FROM WASTE MATERIALS, REFINING OR PRESERVING FATS, FATTY SUBSTANCES, e.g. LANOLIN, FATTY OILS OR WAXES; ESSENTIAL OILS; PERFUMES
- C11B9/00—Essential oils; Perfumes
- C11B9/0042—Essential oils; Perfumes compounds containing condensed hydrocarbon rings
- C11B9/0046—Essential oils; Perfumes compounds containing condensed hydrocarbon rings containing only two condensed rings
- C11B9/0057—Spiro compounds
-
- C—CHEMISTRY; METALLURGY
- C11—ANIMAL OR VEGETABLE OILS, FATS, FATTY SUBSTANCES OR WAXES; FATTY ACIDS THEREFROM; DETERGENTS; CANDLES
- C11B—PRODUCING, e.g. BY PRESSING RAW MATERIALS OR BY EXTRACTION FROM WASTE MATERIALS, REFINING OR PRESERVING FATS, FATTY SUBSTANCES, e.g. LANOLIN, FATTY OILS OR WAXES; ESSENTIAL OILS; PERFUMES
- C11B9/00—Essential oils; Perfumes
- C11B9/0069—Heterocyclic compounds
- C11B9/0073—Heterocyclic compounds containing only O or S as heteroatoms
- C11B9/0076—Heterocyclic compounds containing only O or S as heteroatoms the hetero rings containing less than six atoms
-
- C—CHEMISTRY; METALLURGY
- C11—ANIMAL OR VEGETABLE OILS, FATS, FATTY SUBSTANCES OR WAXES; FATTY ACIDS THEREFROM; DETERGENTS; CANDLES
- C11B—PRODUCING, e.g. BY PRESSING RAW MATERIALS OR BY EXTRACTION FROM WASTE MATERIALS, REFINING OR PRESERVING FATS, FATTY SUBSTANCES, e.g. LANOLIN, FATTY OILS OR WAXES; ESSENTIAL OILS; PERFUMES
- C11B9/00—Essential oils; Perfumes
- C11B9/0069—Heterocyclic compounds
- C11B9/0073—Heterocyclic compounds containing only O or S as heteroatoms
- C11B9/008—Heterocyclic compounds containing only O or S as heteroatoms the hetero rings containing six atoms
-
- C—CHEMISTRY; METALLURGY
- C11—ANIMAL OR VEGETABLE OILS, FATS, FATTY SUBSTANCES OR WAXES; FATTY ACIDS THEREFROM; DETERGENTS; CANDLES
- C11B—PRODUCING, e.g. BY PRESSING RAW MATERIALS OR BY EXTRACTION FROM WASTE MATERIALS, REFINING OR PRESERVING FATS, FATTY SUBSTANCES, e.g. LANOLIN, FATTY OILS OR WAXES; ESSENTIAL OILS; PERFUMES
- C11B9/00—Essential oils; Perfumes
- C11B9/0069—Heterocyclic compounds
- C11B9/0073—Heterocyclic compounds containing only O or S as heteroatoms
- C11B9/0088—Spiro compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/12—Systems containing only non-condensed rings with a six-membered ring
- C07C2601/16—Systems containing only non-condensed rings with a six-membered ring the ring being unsaturated
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2602/00—Systems containing two condensed rings
- C07C2602/02—Systems containing two condensed rings the rings having only two atoms in common
- C07C2602/04—One of the condensed rings being a six-membered aromatic ring
- C07C2602/08—One of the condensed rings being a six-membered aromatic ring the other ring being five-membered, e.g. indane
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2602/00—Systems containing two condensed rings
- C07C2602/02—Systems containing two condensed rings the rings having only two atoms in common
- C07C2602/04—One of the condensed rings being a six-membered aromatic ring
- C07C2602/10—One of the condensed rings being a six-membered aromatic ring the other ring being six-membered, e.g. tetraline
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Wood Science & Technology (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Polymers & Plastics (AREA)
- Food Science & Technology (AREA)
- Health & Medical Sciences (AREA)
- Nutrition Science (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Fats And Perfumes (AREA)
- Cosmetics (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Abstract
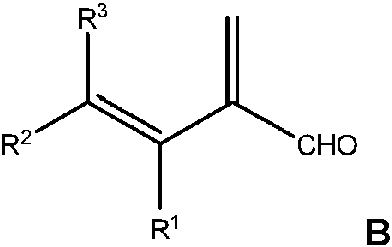
Un proceso que comprende hacer reaccionar formilbutadieno de fórmula B **(Ver fórmula)** en donde R1 es hidrógeno, metilo o etilo; R2 es hidrógeno, alquilo C1-C6, o alquenilo C2-C6; R3 es hidrógeno, metilo o etilo; con un dieno de fórmula C **(Ver fórmula)** en donde R4, R5, R6, R7, R8 y R9 se seleccionan independientemente de hidrógeno, alquilo C1-C6, o alquenilo C2-C6; resultando en compuestos de fórmulas (Ia) y (Ib) **(Ver fórmula)** caracterizado por que en presencia de un catalizador de metilenación y formalina, el formilbutadieno de fórmula B se prepara in situ a partir de un aldehído α, β-insaturado de fórmula A
Description
DESCRIPCIÓN
Derivados de ciclohexeno y su uso como odorante
La presente invención se refiere a un nuevo proceso para la producción de derivados de formil ciclohexeno que son adecuados para su uso como odorantes como tales o como intermedios para la preparación de otros odorantes. En particular, la presente invención se refiere a una reacción de domino-metilenación-Diels-Alder de aldehídos a, pinsaturados usando formaldehído en presencia de 1,3-butadienos.
Se sabe desde hace mucho tiempo que los aldehídos a, p-insaturados pueden metilenarse con formaldehído a dienos de fórmula
Sin embargo, estos dienos son inestables y se dimerizan rápidamente. Por ejemplo, R. Pummerer et al. (Liebigs Ann.
1953, 583, 161) describen la dimerización de un formilbutadieno. De manera similar, la reacción de formilbutadieno con diferentes dienófilos pobres en electrones se describió en JP Kokoku 50-16791 de Daiichi Seiyaku Co. Debido a la inestabilidad de los dienos, hasta ahora solo ha sido posible preparar derivados de formilciclohexeno en forma de cangrejo. Por ejemplo, la preparación de 2-acetilbuta-1,3-dieno mediante la reacción de Friedel-Crafts de complejos de carboniliron y la reacción posterior con ciclopentadieno fue descrita por F. Brion (Angew. Chem. 1981, 93, pág.
900).
Sorprendentemente, los inventores han descubierto ahora que los aldehídos a, p-insaturados se someten a una metilenación in situ utilizando formaldehído y que los formilbutadienos resultantes se someten a una reacción de Diels-Alder organocatalizada con 1,3-butadienos, es decir, un proceso basado en una síntesis one-pot, en la que se suprime la dimerización de los formilbutadienos.
Por consiguiente, la presente invención se refiere en uno de sus aspectos a un proceso que comprende hacer reaccionar formilbutadieno de fórmula B
en donde
R1 es hidrógeno, metilo o etilo;
R2 es hidrógeno, alquilo C1-C6 (por ejemplo, etilo, isopropilo) o alquenilo C2-C6 (por ejemplo, 1 -but-1 -enilo);
R3 es hidrógeno, metilo o etilo;
con un dieno de fórmula C
en donde
R4, R5, R6, R7, R8 y R9 se seleccionan independientemente de hidrógeno, alquilo C1-C6 (por ejemplo, metilo, isopropilo, terc-butilo, pentilo) o alquenilo C2-C6 (por ejemplo, 2-metil-pent-2-en-5-il, 2-metil-prop-2-en-3-ilo, 2-metil-pent-2-en-5-ilo);
resultando en compuestos de fórmulas (Ia) y (Ib)
caracterizado por que en presencia de un catalizador de metilenación y formalina, el formilbutadieno de fórmula B se prepara in situ a partir de un aldehído a, p-insaturado de fórmula A
Dependiendo de las propiedades específicas del dieno de fórmula C utilizado, se pueden preparar compuestos de fórmula (Ia) o (Ib) o mezclas de los mismos. Por ejemplo, los compuestos de fórmula (Ia) se pueden preparar selectivamente partiendo de dienos ricos en electrones, tal como dimetilbutadieno, mientras que se pueden preparar mezclas de compuestos de fórmulas (Ia) y (Ib) si los dienos pobres en electrones, tal como butadieno, isopreno o mirceno, como se ejemplifica en el Esquema 1 a continuación. En los últimos casos, el contenido de compuestos (Ib) en la mezcla de compuestos de fórmulas (Ia) y (Ib) puede variar de 5%-40% en peso basado en la cantidad total de la mezcla.
Esquema 1
formalina aq
Los catalizadores de metilenación son bien conocidos en la técnica. Por ejemplo, se puede usar una mezcla de aminas secundarias y ácido carboxílico, como se describe, por ejemplo, por Anniina Erkkila et al. en el Journal of Organic Chemistry, Vol 71, página 2538 - 2541. También se pueden usar aminoácidos, tales como prolina o derivados de los mismos. El catalizador se puede usar en cantidades de aproximadamente 1% en moles a aproximadamente 100% en moles basado en el aldehído a, p-insaturado (A), preferiblemente de aproximadamente 5% en moles a aproximadamente 50% en moles, p. ej., 20% en moles.
Además del catalizador de metilenación, un cocatalizador tal como trifenilfosfina u otro terc. Opcionalmente se pueden añadir fosfinas, o mezclas de las mismas, que pueden ayudar a incrementar la selectividad de la reacción y reducir el tiempo de reacción.
Preferiblemente, el nuevo proceso se lleva a cabo a una temperatura de aproximadamente 0 °C a aproximadamente 120 °C, p. ej., de aproximadamente 20 °C a aproximadamente 80 °C, durante aproximadamente 2 a 60 horas. Sin embargo, mediante la adición de un cocatalizador, la temperatura de trabajo puede reducirse en comparación con la temperatura de reacción de un proceso sin un cocatalizador.
A veces también es práctico añadir un disolvente adicional tal como tolueno, DMSO, DMF u otros disolventes
orgánicos. Por ejemplo, en el caso de que se utilice 1,3-butadieno como dieno (C), la presión que puede surgir durante la reacción se puede reducir añadiendo un disolvente adicional. Sin embargo, desde un punto de vista ecológico, se prefiere un proceso en el que se utiliza agua como disolvente.
El proceso de reacción de la presente invención se puede llevar a cabo en un matraz de reacción o en un autoclave. Los compuestos de fórmulas (Ia) y (Ib) pueden purificarse por medios conocidos por el experto en la materia, por ejemplo, simplemente por separación de la fase orgánica seguida de destilación o por extracción de la mezcla de reacción con disolventes orgánicos, tales como como MTBE (metil terc-butil éter), tolueno o acetato de etilo. La fase acuosa restante se puede reutilizar en reacciones posteriores después de que se haya enriquecido con formaldehído. Alternativamente, los compuestos de fórmulas (Ia) y (Ib) pueden separarse mediante cromatografía, p. ej. sobre gel de sílice.
Los compuestos de fórmulas (Ia) y (Ib) pueden usarse como aromas o fragancias o pueden usarse como intermedios para la producción de alcoholes de aromas y fragancias adicionales, y derivados de los mismos por reducción de los aldehídos de fórmulas (Ia) y (Ib) en presencia de un reactivo reductor, tal como LiAlH4 o un reactivo de Grignard, dando como resultado compuestos de fórmulas (IIa) y (IIb) en donde R11 es hidrógeno, seguido opcionalmente por esterificación en presencia de haluros de ácido carboxílico y una base, en condiciones conocidas por el experto en la técnica, dando como resultado otros compuestos de fórmulas (IIa) y (IIb)
en donde
R1 a R9 tienen el mismo significado que el dado para las fórmulas (Ia) y (Ib);
R10 es hidrógeno, alquilo C1-C5 lineal o ramificado (p. ej., metilo, etilo, isopropilo) o alquenilo C2-C5 lineal o ramificado (p. ej., prop-2-en-3-ilo, prop-1-en-3-ilo); y R11 es hidrógeno o COR12, en donde R12 es hidrógeno, o alquilo C1-C3 lineal o ramificado (p. ej., etilo, isopropilo).
La oxidación de los compuestos de fórmulas (IIa) y (IIb) en donde R11 = hidrógeno en presencia de un agente oxidante tal como el PCC (cloro cromato de piridinio) da como resultado compuestos de sabor y fragancia de fórmulas (IIIa) y (IIIb)
en donde
R1 a R9 tienen el mismo significado que se dio anteriormente;
R10 es alquilo C1-C5 lineal o ramificado (p. ej., metilo, etilo, isopropilo) o alquenilo C2-C5 lineal o ramificado (p. ej., prop-2-en-3-ilo, prop-1-en-3-ilo).
La transformación del grupo carbonilo de los compuestos de fórmulas (Ia), (Ib), (IIIa) y (IIIb) en presencia de a) hidroxilamina en un disolvente alcohólico, tal como metanol, b) metanol o etanol, o c) dioles, tales como etilenglicol o propilenglicol, dan como resultado compuestos de aroma y fragancia adicionales de fórmulas (IVa) y (IVb) que se describen a continuación en el presente documento. La transformación del grupo carbonilo tiene lugar en condiciones conocidas por el experto en la materia. Los compuestos de fórmula (Ib), (IIIb) y (IVb) tomados solos no constituyen
parte de la presente invención.
Usando el método descrito anteriormente, fue posible producir compuestos nuevos y conocidos adecuados para el uso como aromas y/o fragancias. Por ejemplo, fue posible producir aldehído de perilla (4-(prop-1-en-2-il)ciclohex-1-enecarbaldehído) y alcohol de perilla (1-(4-(prop-1-en-2-il)ciclohex-1-enil) etanol) de una manera ecológicamente ventajosa, es decir, por un método organocatalítico utilizando agua como disolvente. Se describen el alcohol de perilla, el aldehído de perilla así como sus acetales, p. ej., en los documentos EP 1214879 y JP 63 126839 A. Otro ejemplo es el 4-acetoximeta-1,8-dieno, que fue identificado por P. Schreier et al., Deutsche Lebensmittel-Rundschau 1984, 80, 335, como componente volátil en la licuefacción enzimática de pulpa de mango. Sin embargo, además del hecho de que los compuestos recién encontrados son volátiles, no se dan otras propiedades. Bisabolenol ((4-(6-metilhepta-1,5-dien-2-il)ciclohex-1-enil)metanol) y bisabolenal (4-(6-Metilhepta-1,5-dien-2-il)ciclohex-1-enecarbaldehído) se encontraron por primera vez en el aceite esencial de madera de Neocallitropsis pancheri por Raharivelomanana et al. (Journal of Natural Products, vol. 56 (2), 1993, 272-274). Sin embargo, nada en la literatura indica que los compuestos sean adecuados como principio de aroma o fragancia. Solo se conoce por el estado de la técnica que los alcoholes sesquiterpénicos poseen propiedades antibacterianas, por lo que pueden utilizarse, por ejemplo, para la preparación de desodorantes secos (documento WO 2005/087181).
Mientras que algunos compuestos se conocen como aromas o fragancias, para la mayoría de los compuestos no se dan propiedades organolépticas en la técnica anterior y, por lo tanto, constituyen un aspecto adicional de la presente invención.
Por consiguiente, la presente invención se refiere en una realización adicional al uso como aroma o fragancia de un compuesto seleccionado entre 1 -ciclopentenil-2,4-dimetilciclohex-3-enocarbaldehído y un compuesto de fórmula (Iva)
en donde
R1 es hidrógeno o etilo;
R2 es hidrógeno, alquilo C1-C6 (p. ej., etilo, isopropilo) o alquenilo C2-C6 (p. ej., 1 -but-1 enilo);
R3 es hidrógeno, metilo o etilo;
R4 , R5 , R6 , R7 , R8 y R9 se seleccionan independientemente de hidrógeno, alquilo C1-C6 lineal o ramificado (p. ej., metilo, isopropilo, terc-butilo, pentilo) o alquenilo C2-C6 lineal o ramificado (p. ej., 2-metil-pent-2-en-5-ilo, 2-metil-prop-2-en-3-ilo);
R10 es hidrógeno, alquilo C1-C5 (p. ej., metilo, isopropilo, pentilo) o alquenilo C2-C5 (p. ej., prop-1 -en-3-il prop-2-en-3-ilo, 2-metil-prop-1 -en-3-ilo); y
R es hidrógeno y R' es hidroxilo,
R y R ‘se seleccionan de entre metoxi y etoxi, o
R y R' se forman junto con el átomo de carbono al que están unidos dioxolan, dioxano, carbonilo o C=N-OH; con la condición de que el (los) compuesto (s) de fórmula (IVa) en donde R1, R4 a R6 , R8 y R9 son hidrógeno, R7 es metilo y las formas R+R 'junto con el átomo de carbono al que están unidos se excluyen carbonilo o R es hidrógeno y R' es hidroxilo.
Los ejemplos no limitantes son aquellos compuestos de fórmula (IVa) en donde al menos dos de R4 , R5 , R6 , R7 , R8 y R9 no son hidrógeno, por ejemplo, compuestos de fórmula (IVa) en donde R4 y R7 son metilo y R5 , R6 , R8 y R9 son hidrógeno.
Otros ejemplos no limitantes son aquellos compuestos de fórmula (IVa) en donde dos de R4 , R5 , R6 , R7 , R8 y R9 son metilo, preferiblemente R4 y R7 son metilo y R1 es hidrógeno.
Otros ejemplos no limitantes son aquellos compuestos de fórmula (IVa) en donde R1 es hidrógeno y R2 es alquilo C1-C6 (p. ej., etilo, isopropilo) o alquenilo C2-C6 (por ejemplo, 1 -but-1 enilo), preferiblemente metilo, y R3 es hidrógeno o
metilo.
Los compuestos de fórmula (IVa) poseen notas olfativas florales y afrutadas.
En realizaciones particulares, los compuestos de fórmula (IVa) pueden seleccionarse de
2.4- dimetil-1-vinilciclohex-3-enocarbaldehído,
(2,4-dimetil-1-vinilciclohex-3-enil)metanol,
(2,4-dimetil-1-vinilciclohex-3-enil)etanol,
1 -(2,4-dimetil-1 -vinilciclohex-3-enil)etanona,
(2,4-dimetil-1 -vinilciclohex-3-enil)but-3-en-1 -ol,
(2,4-dimetil-1 -vinilciclohex-3-enil)but-3-en-1 -ona,
1 -(buta-1,3-dienil)-2,4-dimetilciclohex-3-enocarbaldehído,
3.4- dimetil-1-vinilciclohex-3-enocarbaldehído,
2-metil-1 -(2-metilprop-1 -enil)ciclohex-3-enocarbaldehído,
2.4- dimetil-1 -(2-metilprop-1 -enil)ciclohex-3-enocarbaldehído,
1 -(2,4-dimetil-1 -(2-metilprop-1 -enil)ciclohex-3-enil)etanol,
4.5- dimetil-2-(2-metilprop-1-enil)-1-vinilciclohex-3-enocarbaldehído,
2- metil-4-(4-metilpent-3-enil)-1-vinilciclohex-3-enocarbaldehído,
3- metil-1-vinil-ciclohex-3-eno-carbaldehído,
oxima de 4-metil-1 -vinil-ciclohex-3-enocarbaldehído,
oxima de 3-metil-1 -vinil-ciclohex-3-eno-carbaldehído,
1 -(but-1 -enil)-2,4-dimetilciclohex-3-enocarbaldehído, y
1-vinilciclohex-3-eno carbaldehído, o mezclas de los mismos.
Los compuestos de fórmula (IVb) adecuados como aroma o fragancia (que tomados solos no constituyen parte de la presente invención) son compuestos de fórmula (IVb)
en donde
R1 es hidrógeno, metilo o etilo;
R2 es hidrógeno, alquilo C1-C6 (p. ej., etilo, isopropilo) o alquenilo C2-C6 (p. ej., 1 -but-1 enilo);
R3 es hidrógeno o metilo;
R4 , R5 y R6 son hidrógeno;
R7 y R8 son independientemente hidrógeno, alquilo C1-C6 (p. ej., metilo, terc-butilo, pentilo) o alquenilo C2-C6 (p. ej., 2-metil-pent-2-en-5il);
R9 es hidrógeno, metilo o etilo; o
R4 + R9 juntos es un residuo bivalente seleccionado de -(CH2)n- en donde n es 1 o 2, -C(=C(CH3)2)- y C(=C(CH2CH3)2)-;
R10 es alquilo C1-C5 (p. ej., metilo, etilo, isopropilo, pentilo) o alquenilo C2-C5 (p. ej., prop-1-en-3-ilo, prop-2-en-3-ilo, 2-metil-prop-1-en-3-ilo); y
R es hidrógeno y R' es hidroxilo;
R y R 'se seleccionan entre metoxi y etoxi, o
R y R' se forman junto con el átomo de carbono al que están unidos dioxolan, dioxano o C=N-OH;
siempre que los compuestos de fórmula (IVb) en donde R1 - R6 , R8 y R9 son hidrógeno y R7 es metilo estén excluidos. Son ejemplos los compuestos de fórmula (IVb) en donde R3 , R4 , R5 y R9 son hidrógeno, y R y R' se forman junto con el átomo de carbono al que están unidos carbonilo o R es hidrógeno y R' es hidroxilo.
Otros ejemplos son aquellos compuestos de fórmula (IVb) en donde R3 y R5 son hidrógeno, R6 y R7 se seleccionan independientemente de hidrógeno y metilo, y R4 + R9 juntos es un residuo bivalente seleccionado de -(CH2)n- en donde n es 1 o 2, -C(=C(CH3)2)-.
Otros ejemplos son aquellos compuestos de fórmula (IVb) en donde R10 es hidrógeno o metilo y R y R' forman junto con el átomo de carbono al que están unidos carbonilo o C=N-OH.
Otros ejemplos son aquellos compuestos de fórmula (IVb) en donde R10 y R se seleccionan independientemente de hidrógeno o metilo, y R' es hidroxilo.
Los compuestos de fórmula (IVb) poseen notas de olor verde.
Los compuestos de fórmula (IVa) se pueden seleccionar de
4- vinilciclohex-1 -eno carbaldehído,
(4-vinilciclohex-1 -enil) metanol,
1 -(4-vinilciclohex-1 -enil) etanol,
2-metil-4-vinilciclohex-1 -eno carbaldehído,
(2-metil-4-vinilciclohex-1 -enil) metanol,
3a,4,7,7a-tetrahidro-1 H-indeno-6-carbaldehído,
oxima de 3a,4,7,7a-tetrahidro-1H-indeno-6-carbaldehído,
(3a,4,7,7a-tetrahidro-1 H-inden-6-il) metanol,
1 -(3a,4,7,7a-tetrahidro-1 H-inden-6il) etanona,
5- metil-3a,4,7,7a-tetrahidro-1 H-indeno-6-carbaldehído,
(5-metil-3a,4,7,7a-tetrahidro-1 H-indeno-6-il) metanol,
1- (propan-2-ilideno)-3a,4,7,7a-tetrahidro-1 H-indeno-6-carbaldehído,
2- metil-3a,4,7,7a-tetrahidro-1H-indeno-6-carbaldehído,
3- metil-3a,4,7,7a-tetrahidro-1H-indeno-6-carbaldehído,
4- etil-3a,4,7,7a-tetrahidro-1 H-indeno-6-carbaldehído,
1,4,4a,7,8,8a-hexahidronaftalen-2-carbaldehído, y
4-(6-metilhepta-1,5-dien-2-il)ciclohex-1-enocarbaldehído, o mezclas de los mismos.
Mientras que algunos compuestos que pertenecen a la fórmula general (IVa) o (IVb) se han descrito en la bibliografía, la mayoría de ellos no lo han hecho y, por lo tanto, son nuevos. Por ejemplo, la preparación de 1 -(3a,4,7,7a-tetrahidro-1 H-inden-6il)etanona, es decir, un compuesto de fórmula (IVb) en donde R1 a R8 y R10 son hidrógeno, R y R‘ se forman junto con el átomo de carbono al que están unidos carbonilo, y R4 + R9 juntos es metileno, se describe por F. Brion et al. (Angew. Chem, 1981, 93, 900). Sin embargo, la técnica anterior permanece en silencio con respecto a las propiedades organolépticas.
Por tanto, en otro aspecto de la invención, se proporciona un compuesto de fórmula (IVa)
en donde
R1 es hidrógeno o etilo;
R2 es hidrógeno, alquilo C1-C6 (por ejemplo, etilo, isopropilo) o alquenilo C2-C6 (por ejemplo, 1 -but-1 enilo);
R3 es hidrógeno, metilo o etilo;
R4 , R5 , R6 , R7 , R8 y R9 se seleccionan independientemente de hidrógeno, alquilo C1-C6 lineal o ramificado (p. ej., metilo, isopropilo, terc-butilo, pentilo) o alquenilo C2-C6 lineal o ramificado (p. ej., 2-metil-pent-2-en-5-ilo, 2-metil-prop-2-en-3-ilo);
R10 es hidrógeno, alquilo C1-C5 (p. ej., metilo, isopropilo, pentilo) o C2-C5 alquenilo (por ejemplo, prop-1 -en-3-il prop-2-en-3-ilo, 2-metil-prop-1-en-3-ilo); y
R es hidrógeno y R 'es hidroxilo; R y R 'se seleccionan entre metoxi y etoxi, o R y R' forman junto con el átomo de carbono al que están unidos dioxolan, dioxano, carbonilo o C=N-OH;
con la condición de que 1-formil-3-metil-1-vinilciclohex-3-eno, 4-(dimetoximetil)-1-metil-4-vinilciclohex-1-eno y compuesto (s) de fórmula (IVa) en donde R1, R4 a R6 , R8 y R9 son hidrógeno, R7 es metilo y R R' forman junto con el átomo de carbono al que están unidos carbonilo o R es hidrógeno y R' es hidroxilo quedan excluidos.
Como se usa en relación con los compuestos de fórmulas (Ia) a (IVa) y (Ib) a (IVb) a menos que se indique lo contrario, "alquilo" y "alquenilo" se refiere a alquilos y alquenilos lineales y ramificados.
Los compuestos de fórmulas (IVa) y (IVb) pueden usarse solos o en combinación con un material base. Como se usa en este documento, el "material base" incluye todas las moléculas aromáticas conocidas seleccionadas de la amplia gama de moléculas naturales y sintéticas actualmente disponibles, tales como aceites esenciales y extractos, alcoholes, aldehídos y cetonas, éteres y acetales, ésteres y lactonas, macrociclos y heterociclos, y/o en mezcla con uno o más principios o excipientes usados convencionalmente junto con odorantes en composiciones de fragancias, por ejemplo, materiales portadores y otros agentes auxiliares comúnmente usados en la técnica, p. ej., solventes tales como dipropilenglicol, miristato de isopropilo y citrato de trietilo.
Como se usa en este documento, "composición de fragancia" significa cualquier composición que comprende al menos un compuesto seleccionado de compuestos de fórmulas (IVa) y (IVb) y un material base, p. ej. un diluyente usado convencionalmente junto con odorantes, tales como dipropilenglicol (DPG), miristato de isopropilo (IMP), citrato de trietilo (REC), ftalato de dietilo (DEP) y alcohol (p. ej., etanol).
La siguiente lista comprende ejemplos de moléculas aromáticas conocidas, que pueden combinarse con los compuestos de la presente invención:
- aceites y extractos esenciales, p. ej. absoluto de musgo de roble, aceite de albahaca, aceites de frutas tropicales, tales como aceite de bergamota y aceite de mandarina, absoluto de masilla, aceite de mirto, aceite de palmarosa, aceite de pachulí, aceite de petitgrain, aceite de ajenjo, aceite de lavanda, aceite de rosa, aceite de jazmín, aceite de ylang-ylang y aceite de sándalo.
- alcoholes, p. ej. cis-3-hexenol, alcohol cinámico, citronelol, Ebanol®, eugenol, farnesol, geraniol, mentol, nerol, rodinol, Super Muguet™, linalol, alcohol feniletílico, Sandalore®, terpineol y Timberol® (1-(2,2,6-trimetilciclohexil)hexan-3-ol).
- aldehídos y cetonas, p. ej. citral, hidroxicitronelal, Lilial®, metilnonilacetaldehído, anisaldehído, alilionona, verbenona, nootkatona, geranilacetona, a-aldehído amilcinámico, Georgywood ™, hidroxicitronelal, Iso E Super®, Isoraldeine® (metilionona), Hedione®, maltol, metil cedril cetona y vainillina.
- éteres y acetales, p. ej. Ambrox®, geranil metil éter, óxido de rosa o Spirambrene®.
- ásteres y lactonas, p. ej. acetato de bencilo, acetato de cedrilo, Y -decalactona, Helvetolide®, y-undecalactona, acetato de vetivenilo, propionato de cinamilo, acetato de citronelilo, acetato de decilo, acetato de dimetilbencilcarbinilo, acetoacetato de etilo, isobutirato de cis-3-hexenilo, acetato de linalilo y acetato de geranilo.
- macrociclos, p. ej. ambrettolida, brasilato de etileno o Exaltolide®.
- heterociclos, p.ej. isobutilquinolina.
Los compuestos de fórmulas (IVa) pueden usarse en una amplia gama de aplicaciones de fragancias, p. ej. en cualquier campo de la perfumería fina y funcional, tales como perfumes, productos para el hogar, productos de lavandería, productos para el cuidado corporal y cosméticos. Los compuestos se pueden emplear en cantidades muy variables, dependiendo de la aplicación específica y de la naturaleza y cantidad de otros principios aromáticos. La proporción es típicamente de 0,0001 a 2 por ciento en peso de la aplicación. En una realización, los compuestos de la presente invención pueden emplearse en un suavizante de telas en una cantidad de 0,0001 a 0,005 por ciento en peso. En otra realización, los compuestos se pueden usar en una solución alcohólica en cantidades del 0,01 al 3 por ciento en peso, más preferiblemente entre el 0,5 y el 2 por ciento en peso. Sin embargo, estos valores se dan solo a modo de ejemplo, ya que el perfumista experimentado también puede lograr efectos o puede crear nuevos acuerdos con concentraciones más bajas o más altas, p. ej., hasta aproximadamente el 20 por ciento en peso basado en la composición de la fragancia.
Los compuestos de fórmulas (IVa) pueden emplearse en una base de producto de consumo mezclando directamente el compuesto, una mezcla de los mismos o una composición de fragancia con la base de producto de consumo, o pueden, en una etapa anterior, quedar atrapado con un material de atrapamiento. tales como polímeros, cápsulas, microcápsulas y nanocápsulas, liposomas, formadores de película, absorbentes tales como carbono o zeolitas, oligosacáridos cíclicos y mezclas de los mismos, o pueden unirse químicamente a sustratos, que están adaptados para liberar la molécula de fragancia tras la aplicación de una sustancia externa. estímulo como luz, enzima o similar, y después se mezcla con la aplicación.
Por lo tanto, la divulgación proporciona adicionalmente un método para fabricar una aplicación de fragancia, que comprende la incorporación de un compuesto de fórmula (IVa), como principio de fragancia, ya sea mezclando directamente el compuesto con la base del producto de consumo o mezclando una composición de fragancia que comprende un compuesto de fórmula (IVa), o precursores del mismo, que después se pueden mezclar con una base de producto de consumo, usando técnicas y métodos convencionales.
Mediante la adición de una cantidad olfativamente aceptable de un compuesto de fórmula (IVa), se mejorarán, mejorarán o modificarán las notas de olor de una base de producto de consumo. Por "precursores" se entiende, en particular, los productos de reacción de un compuesto de fórmula (IVa) con un compuesto que comprende al menos un grupo funcional seleccionado del grupo de amina primaria, amina secundaria, sulfhidrilo (tiol), hidroxilo y carboxilo, en el que se forma un enlace covalente entre al menos un átomo de carbono del compuesto de fórmulas (IVa) respectivamente y al menos uno de los heteroátomos (N, S y O) de dichos compuestos que comprenden al menos un funcional.
En un aspecto adicional, la divulgación proporciona un método para mejorar, potenciar o modificar una base de producto de consumo mediante la adición a la misma de una cantidad olfativamente aceptable de un compuesto seleccionado de compuestos de fórmulas (IVa).
La divulgación también proporciona una aplicación de fragancia que comprende:
a) como odorante un compuesto seleccionado de compuestos de fórmulas (IVa) y mezclas de los mismos; y
b) una base de productos de consumo.
Como se usa en este documento, "base de producto de consumo" significa una composición para su uso como producto de consumo para realizar acciones específicas, tales como limpiar, suavizar y cuidar o similares. Los ejemplos de tales productos incluyen perfumería fina, p. ej., perfume y eau de toilette; cuidado de telas, productos para el hogar y productos para el cuidado personal tales como detergentes para el cuidado de la ropa, acondicionador de aclarado, composición de limpieza personal, detergente para lavavajillas, limpiador de superficies; productos de lavandería, p. ej. suavizante, lejía, detergente; productos para el cuidado del cuerpo, p. ej. champú, gel de ducha; productos para el cuidado del aire y cosméticos, p. ej. desodorante, crema que desaparece.
La invención se describe ahora adicionalmente con referencia a los siguientes ejemplos. Los ejemplos marcados con * no forman parte de la presente invención. Los compuestos de los ejemplos marcados con ** tomados solos no forman parte de la presente invención.
Ejemplo 1: 2.4-dimetil-1-vinilciclohex-3-enocarbaldehído
A una mezcla de aldehído crotónico (165,2 g, 2,36 mol), 2-metil-penta-1,3-dieno (361,6 g, 4,41 mol) y formalina (37% en agua (200 g, 2,46 mol) se añadió una mezcla de pirrolidina (16,0 g, 0,22 mol) y ácido propiónico (17,0 g, 0,23 mol).
La mezcla se colocó en un autoclave y se calentó a 60-1002C durante 8 h. La mezcla de reacción se enfrió a temperatura ambiente, se diluyó con una disolución sat. de NaHCO3 y se extrajo 3 veces con MTBE (200 ml). Las capas org combinada se lavaron con salmuera (200 ml), se secaron (MgSO4) y se evaporó al vacío. El residuo se purificó por destilación para dar 2,4-dimetil-1-vinilciclohex-3-enocarbaldehído (rendimiento del 50%). Punto de ebullición: 50-53 °C/0,15 mbar.
Descripción del olor: verde, fresco, alcanforado.
1H-NMR (300 MHz, CDCh): 9.52 (s, 1H, CHO), 5.79 (dd, J = 10.9, 17.7 Hz, 1H, CH= CH2), 5.36 (sa, 1H, 3-H), 5.30 (d, J = 10.9 Hz, 1H, CH = CHcHt), 5.11 (d, J = 17.7Hz, 1H, CH = CHcHt), 2,49 (sa, 1H, 2-H), 2,01 -1,90 (m, 2H), 1,74 1,59 (m, 2H), 1,66 (sa, 3H, 4-CHa), 1.02 (d, J = 7.1 Hz, 3H, 2-CHa) ppm. 13C-NMR (75 MHz, CDCla): 202,9 (d, CHO), 138,4 (d, CH = CH2), 134,0 (s, C-4), 124,7 (d, C-3), 177,6 (t, CH =CHz), 54,2 (s, C-1), 34,8 (d, C-2), 27,1 (t, C-5), 24,9 (t, C-6), 23,3 (q, 4-CHa), 17,1 (q, 2-CHa) ppm. GC/MS (EI), endo-isómero (principal): 164 (M+, 11), 149 (10), 135 (22), 107 (51), 93 (38), 82 (100), 67 (86), 55 (24), 41 (26). IR (limpio, v/cm-1): 2965s, 2933s, 2729w, 1722s, 1631w, 1451m, 921 m.
Ejemplo 2: (2.4-dimetil-1-vinilciclohex-3-enil) metanol
A una suspensión de LiAlH4 (0,114g, 30 mmol) en dietiléter (20 ml) se añadió una disolución de 2,4-dimetil-1-vinilciclohex-3-enocarbaldehído (56 mmol) en dietiléter (10 ml) a 5°C. La mezcla se agitó a temperatura ambiente durante 1 hora. Se añadieron 0,1 ml de agua, 0,1 ml de solución acuosa de NaOH al 16% y 0,3 ml de agua gota a gota con cuidado. La mezcla se agitó durante 2 h, despuésse filtró y se concentró a vacío. El residuo se purificó mediante cromatografía para dar (2,4-dimetil-1 -vinilciclohex-3-enil) metanol (rendimiento del 76%).
Descripción del olor: floral, similar al iris, amaderado.
1H-NMR (300 MHz, CDCh): 5,75 (dd, J = 10.9, 17.7 Hz, 1H, CH= CH2), 5.23 (sa, 1H, 3-H), 5.19 (d, J = 10.9 Hz, 1H, CH = CHcHt), 5,13 (d, J = 17.7Hz, 1H, CH = CHcHt), 3,50 (d, J = 10.9 Hz, 1H, CHaHbO), 3,42 (d, J = 10.9 Hz, 1H, CHaHbO), 2,21 (sa, 1H, 2-H), 2,02-1,86 (m, 3H), 1,74-1,55 (m, 1H), 1,62 (s, 3H), 1,42-1,32 (m, 1H), 0,91 ( d, J = 7,2 Hz, 3H, 2 -CH3) ppm. GC/MS (EI): 166 (M+, 2), 148 (11), 135 (28), 120 (11), 107 (27), 91 (27), 82 (100), 67 (59), 55 (14), 41 (15).
Ejemplo 3: (2.4-dimetil-1-vinilciclohex-3-enil) etanol
A una solución de bromuro de metilmagnesio (40 mmol, 1 M en THF) se le añadió gota a gota una disolución de 2,4-dimetil-1-vinilciclohex-3-enocarbaldehído (34 mmol) a 10°C. La mezcla se agitó a temperatura ambiente durante 1 hora y después se enfrió a 5°C. Se añadió una disolución sat. de NH4Cl gota a gota y la mezcla se extrajo con MTBE (3 x 50 ml). La. Las fases org combinadas se lavaron con agua y salmuera, se secaron (MgSO4) y se concentraron a vacío. El residuo se purificó por cromatografía para dar (2,4-dimetil-1 -vinilciclohex-3-enil) etanol (rendimiento del 53%).
Descripción del olor: alcanforado, amaderado.
2 Isómeros en una proporción de 1:1. 1H-NMR (300 MHz, CDCl3): 5.66, 5.61 (2dd, J = 17.7, 10.9 Hz, 1H), 5.37-5.35 (m, 1H), 5.22, 5.20 (2d, J= 10.9 Hz, 1H), 5.10, 5.09 (2d, J= 17.7 Hz, 1H), 3.66, 3.54 (2dq, J = 6.8, 6.8 Hz, 1H), 2.46 1.6 (m, 4H), 1.57 (s, 3H), 1.53-1.17 (m, 2H), 1.12, 1.07, 1.01,0.90 (4d, J = 6.8 Hz) ppm. GC/MS (EI): 180 (M+, 2), 162 (18), 147 (15), 136 (40), 121 (70), 107 (100), 93 (61), 82 (72), 67 (43), 55 (22), 41 (20)..
Ejemplo 4: 1-(2.4-dimetil-1-vinilciclohex-3-enil) etanona
A una solución de (2,4-dimetil-1 -vinilciclohex-3-enil) etanol (20 mmol) en CH2CL (40 ml) a temperatura ambiente se añadió PCC (40 mmol). La mezcla se agitó a temperatura ambiente durante la noche y después se diluyó con hexano, se filtró a través de un lecho corto de celite y se concentró al vacío. El residuo se purificó mediante cromatografía para dar 1 -(2,4-dimetil-1 -vinilciclohex-3-enil) etanona (rendimiento del 83%).
Descripción del olor: verde, floral, amaderado.
Isómero principal (endo):
1H-NMR (300 MHz, CDCl3): 5.74 (dd, J = 10.6, 17.7 Hz, 1H, CH=CH2), 5.34 (bs, 1H, 3-H), 5.29 (d, J= 10.6 Hz, 1H, CH=CHcHt ), 5.09 (d, J= 17.7Hz, 1H, CH=CHcHt ), 2.54-2.43 (m, 1H, 2-H), 2.05 (s, 3H, CH3CO), 1.85-1.60 (m, 4H), 1.58 (s, 3H), 0.81 (d, J = 6.8 Hz, 3H) ppm. GC/MS (EI): 178 (M+, 9), 163 (6), 145 (26), 135 (98), 120 (40), 107 (100), 93 (91), 82 (55), 67 (42), 55 (46), 43 (86). IR (limpio, v/cm-1): 3082w, 2963s, 1708s, 1633w, 1451m, 1355m, 1217m, 917m.
Ejemplo 5: acetato de (2.4-dimetil-1-vinilciclohex-3-enil) metilo *
A una solución de (2,4-dimetil-1 -vinilciclohex-3-enil) metanol (3,50 g, 21,1 mmol), trietilamina (3,83 g, 38 mmol) y una cantidad catalítica de DMAP en Et2O (30 ml) se añadió Ac2O (3,22 g, 31,6 mmol). La mezcla se agitó durante 5 h, se vertió sobre agua y se extrajo con Et2O. Las capas orgánicas combinadas se lavaron con agua y salmuera, se secaron
y se evaporaron al vacío. El residuo se destiló bulbo a bulbo para producir acetato de (2,4-dimetil-1 -vinMciclohex-3-enil) metilo (3,81 g, 86%) como un aceite incoloro.
Descripción del olor: floral, jazmín, pomelo
1H-NMR (300 MHz, CDCl3): 5.76 (dd, J = 10.9, 17.7 Hz, 1H, CH=CH2), 5.18 (bs, 1H, 3-H), 5.07 (d, J= 10.9 Hz, 1H, CH=CHcHt ), 5.02 (d, J= 17.7Hz, 1H, CH=CHcHt ), 4.01 (d, J= 10.9 Hz, 1H, CHaHbO), 3.96 (d, J= 10.9 Hz, 1H, CHaHbO), 2.22 (bs, 1H, 2-H), 2.01 (s, 3H, CH3O2), 1.91-1.79 (m, 2H), 1.76-1.66 (m, 1H), 1.61 (s, 3H), 1.46-1.37 (m, 1H), 0.88 (d, J= 7.5 Hz, 3H) ppm. GC/MS (EI): 208 (M+, 1), 166 (1), 148 (18), 133 (16), 120 (14), 107 (21), 91 (19), 82 (100), 67 (55), 55 (8), 43 (31).
Ejemplo 6: (2.4-dimetil-1-vinilciclohex-3-enil) but-3-en-1-ol
De manera análoga al Ejemplo 3, se preparó (2,4-dimetil-1-vinilciclohex-3-enil)but-3-en-1-ol (rendimiento del 78%) partiendo de 2,4-dimetil-1 -vinilciclohex-3 -enecarbaldehído y cloruro de alilmagnesio.
Descripción del olor: verde, floral amaderado.
2 Isómeros en una proporción de 1: 1. 1H-NMR (300 MHz, CDCl3): 6.00-5.78 (m, 1H), 5.74-5.60 (m, 1H), 5.74- 5.60 (m, 1H), 5.36 (bs, 1H), 5.25-5.00 (m, 4H), 3.47-3.38 (m, 1H), 2.54-1.43 (m, 8H), 1.58 (s, 3H), 1.02, 0.92 (2d, J = 6.8 Hz, 3H) ppm. GC/MS (EI): 206 (M+, 1), 188 (3), 165 (40), 147 (41), 136 (39), 121 (91), 107 (100), 93 (57), 82 (63), 67 (46), 55 (36), 42 (41).
Ejemplo 7: (2.4-dimetil-1-vinilciclohex-3-enil) but-3-en-1-ona
Siguiendo el procedimiento general descrito en el Ejemplo 4, se preparó (2,4-dimetil-1 -vinilciclohex-3-enil) but-3-en-1 -ona (rendimiento del 56%) partiendo de (2,4-dimetil- 1-vinilciclohex-3-enil)but-3-en-1-ol.
Descripción del olor: verde, floral, amaderado.
1H-NMR (300 MHz, CDCl3): 6.00-5.87 (m, 1H), 5.76 (d, J= 10.9, 17.7 Hz, 1H), 5.39-5.33 (m, 1H), 5.24 (d, J= 10.9 Hz, 1H), 5.13 (d, J= 17.7 Hz, 1H), 5.16-5.03 (m, 2H), 3.32-3.31 (m, 2H), 2.60-2.48 (m, 1H), 1.96-1.65 (m, 4H), 1.61 (s, 3H), 0.83 (d, J = 6.8 Hz, 3H) ppm. GC/MS (EI): (M+, 2), 189 (3), 163 (29), 145 (19), 135 (100), 120 (32), 107 (83), 93 (73), 79 (36), 69 (40), 55 (34), 41 (54). IR (neat, v/cm-1): 3081m, 2966s, 1710s, 1631m, 1449m, 1378w, 1141m, 917m. Ejemplo 8: 2.4-dimetil-1-(prop-1-en-2-il)ciclohex-3-enocarbaldehído *
Siguiendo el procedimiento general descrito en el Ejemplo 1 ,2,4-dimetil-1-(prop-1-en-2-il)ciclohex-3-enocarbaldehído (rendimiento del 52%; punto de ebullición 62-65 °C/0,15 mbar) se preparó a partir de 2-metil-penta-1,3-dieno y prenal. Descripción del olor: floral, amaderado, terroso.
1H-NMR (300 MHz, CDCl3): 9.40 (s, 1H), 5.34 (bs, 1H), 5.15 (s, 1H), 4.89 (s, 1H), 2.75-2.63 (m, 1H), 2.07-1.70 (m, 4H), 1.70 (s, 3H), 1.60 (s, 3H), 1.00 (d, J = 7.1 Hz) ppm. 13C-NMR (75 MHz, CDCl3): 202.8 (d, CHO), 141.8 (s, CH2=CCH3), 133.5 (s, 4-C), 124.9 (d, 3-C), 116.0 (t, CH2=CCH3), 57.6 (s, 1-C), 32.0 (d, 2-C), 27.2 (t, 5-C), 23.2 (q, 4-CH3), 22.8 (t, 6-C), 20.0 (CH2=CCH3), 17.3 (q, 2-CH3) ppm. GC/MS (EI): 178 (M+, 54), 163 (28), 149 (74), 136 (35), 121 (58), 107 (60), 91 (53), 82 (100), 67 (84), 55 (15), 41 (33).IR (limpio, v/cm-1): 2966s, 2693w, 1721 s, 1636w, 1447m, 1378m, 900m.
Ejemplo 9: 1-(2.4-Dimetil-1-(prop-1-en-2-il)ciclohex-3-enil) etanol *
Siguiendo el procedimiento general descrito en el Ejemplo 3, se preparó 1-(2,4-dimetil-1-(prop-1-en-2-il)ciclohex-3-enil) etanol con un rendimiento del 92% a partir de 2,4-dimetil-1-(prop-1-en-2-il)ciclohex-3-enocarbaldehído.
Descripción del olor: fresco, verde, amaderado.
Mezcla de 2 isómeros en una proporción de 6: 4. 1H-NMR (300 MHz, CDCl3): 5.45-5.37 (m, 1H), 5.18, 5.12 (2s, 1H), 4.84, 4.77 (2s, 1H), 3.74, 3.57 (2dq, J1 = 6.4, 6.4 Hz, J2 = 11.0, 6.4 Hz, 1H), 2.76-2.66, 2.48-2.39 (2m, 1H), 2.07-1.23 (m, 4H), 1.84 (s, 3H), 1.59 (s, 3H), 1.14, 1.09 (2d, J = 6.4 Hz, 3H), 1.06, 0.95 (2s, J = 6.4 Hz, 3H) ppm. GC/MS (EI): 194 (M+, 1), 176 (10), 161 (15), 150 (31), 135 (100), 121 (45), 107 (98), 91 (47), 82 (32), 67 (27), 55 (16), 41 (29).IR (limpio, v/cm-1): 3437br, 3085w, 2964s, 1631w, 1451m, 1373m, 833m.
Ejemplo 10: acetato de 1-(2.4-dimetil-1-(prop-1-en-2-il)ciclohex-3-enil) etilo *
De manera análoga al Ejemplo 5, se preparó acetato de 1-(2,4-dimetil-1-(prop-1-en-2-il)ciclohex-3-enil) etilo partiendo de 1-(2,4-dimetil-1-(prop-1-en-2-il)ciclohex-3-enil) etanol.
Descripción del olor: floral, especiado, eugenol
Mezcla de 2 isómeros en una proporción de 6: 4. 1H-NMR (300 MHz, CDCl3): 5.41-5.36, 5.32-5.28 (2m, 1H), 5.12,
5.10 (2s, 1H), 4.84, 4.77 (2s, 1H), 5.01,4.86 (2q, J1 = 6.4 Hz, J2 = 6.4 Hz, 1H), 2.64-2.55, 2.48-2.38 (2m, 1H), 2.06, 2.04 (2s, 3H), 2.00-1.44 (m, 4H), 1.87, 1.84 (2s, 3H), 1.59, 1.58 (2s, 3H), 1.14, 1.10, 0.99, 0.93 (4d, J= 6.4 Hz, 6H) ppm. GC/MS (EI): 236 (M+, 1), 194 (1), 176 (37), 161 (76), 147 (24), 134 (49), 119 (75), 107 (89), 91 (46), 82 (55). IR (limpio, v/cm-1): 2963s, 1738s, 1633m, 1451m, 1374m, 1247s.
Ejemplo 11: 1 -(2.4-Dimetil-1 -(prop-1 -en-2-il)ciclohex-3-enil) -2-metilpropan-1 -ol *
A una mezcla de Mg (1,2 g, 50 mmol), Li (0,35 g, 50 mmol) y 2,4-dimetil-1 -(prop-1 -en-2-il)ciclohex-3-enocarbaldehído (8,9 g, 50 mmol) se añadió 2-bromopropano (7,5 g, 60 mmol). La mezcla se agitó durante 24 h bajo una atmósfera de argón y después se vertió en una disolución sat. de NH4Cl em hielo. La mezcla se extrajo con MTBE (3 x 50 ml). Las fases org combinadas se lavaron con agua y salmuera, se secaron (MgSÜ4) y se concentró al vacío. El residuo se destiló en un horno Kugelrohr para producir 8,0 g (72%) de un aceite incoloro.
Descripción del olor: afrutado, verde, pomelo, potente.
1H-NMR (300 MHz, CDCl3): 5.38 (bs, 1H), 5.11,4.99 (2s, 1 H), 4.93, 4.85 (2s, 1H), 3.30-3.22 (m, 1H), 2.74-2.65, 2.58 2.50 (2m, 1H), 2.23-2.47 (m, 5H), 1.85, 1.83 (2s, 3H), 1.58 (s, 3H), 1.05, 1.01, 0.99, 0.93, 0.86, 0.77 (6d, J = 6.8 Hz, 9H) ppm. GC/MS (EI): 222 (M+, 1), 204 (1), 189 (1), 179 (3) 161 (6), 150 (29), 135 (100), 122 (53), 107 (66), 93 (26), 82 (18), 67 (15), 55 (12), 41 (24). IR (limpio, v/cm -1): 3501br, 2962s, 1453m, 1374m, 1003m, 888m.
Ejemplo 12: 1-(2.4-Dimetil-1-(prop-1-en-2-il)ciclohex-3-enil)-2-metilpropan-1-ona *
Siguiendo el procedimiento general descrito en el Ejemplo 4, se preparó 1-(2,4-dimetil-1-(prop-1-en-2-il)ciclohex-3-enil)-2-metilpropan-1-ona (rendimiento del 75%) partiendo de 1-(2,4-dimetil-1-(prop-1-en-2-il)ciclohex-3-enil)-2-metilpropan-1-ol.
Descripción del olor: afrutado, pomelo, amaderado.
Isómero principal (endo):
1H-NMR (300 MHz, CDCl3): 5.34-5.31 (m, 1H), 5.15 (s, 1H), 5.04 (s, 1H), 2.99 (sept, J = 6.8 Hz, 1H), 2.87-2.75 (m, 1H), 1.94-1.70 (m, 4H), 1.66 (s, 3H), 1.57 (s, 3H), 1.04 (d, J = 6.8 Hz, 3H), 1.00 (d, J = 6.8 Hz, 3H), 0.85 (d, J = 6.8 Hz, 3H) ppm. 13C-NMR (75 MHz, CDCl3): 217.5 (s), 142.5 (s), 132.3 (s), 125.0 (d), 115.8 (t), 60.3 (s), 35.3 (d), 32.9 (d), 27.4 (t), 23.1 (q), 22.3 (q), 21.5 (t), 20.7 (q), 20.1 (q), 18.7 (q) ppm. GC/MS (EI): 220 (M+, 2), 205 (3), 187 (11), 177 (10), 159 (43), 149 (73), 121 (77), 107 (100), 91 (48), 71 (54), 55 (14), 43 (78). I IR (limpio, v/cm-1): 2969s, 1705s, 1637m, 1447s, 1379m, 896m.
Ejemplo 13: 1-(2.4-Dimetil-1-(prop-1-en-2-il)ciclohex-3-enil) etanona *
Siguiendo el procedimiento general descrito en el Ejemplo 4, se preparó 1-(2,4-dimetil-1-(prop-1-en-2-il)ciclohex-3-enil) etanona (rendimiento del 70%) partiendo de 1-(2,4-dimetil-1-(prop-1-en-2-il)ciclohex-3-enil) etanol.
Descripción del olor: verde, afrutado, amaderado.
1H-NMR (300 MHz, CDCl3): 5.33-5.28 (m, 1H), 5.10 (s, 1H), 5.00 (s, 1H), 2.71-2.61 (m, 1H), 2.02 (s, 3H), 1.91- 1.62 (m, 4H), 1.62 (s, 3H), 1.56 (s, 3H), 0.82 (s, J= 6.7 Hz, 3H) ppm. GC/MS (EI): 192 (M+, 7), 177 (14), 150 (56), 135 (47), 121 (82), 107 (100), 91 (51), 83 (29), 77 (24), 67 (22), 55 (15), 43 (56). IR (limpio, v/cm-1): 3091w, 2964s, 1708s, 1639m, 1446s, 1378m, 1354m, 1211m, 1155m, 898m.
Ejemplo 14: 1-(2.4-Dimetil-1-(prop-1-en-2-il)ciclohex-3-enil) but-3-en-1-ol *
De manera análoga al Ejemplo 3, se preparó 1-(2,4-dimetil-1-(prop-1-en-2-il)ciclohex-3-enil)but-3-en-1-ol (rendimiento del 91%) a partir de 2,4-dimetil-1 -(prop-1 -en-2-il)ciclohex-3-enocarbaldehído y cloruro de alilmagnesio Descripción del olor: afrutado, fresco, amaderado.
Mezcla de 4 isómeros. 1H-NMR (300 MHz, CDCla) 6,00-5,78 (m, 1H), 5,53-5,36 (m, 1H), 5,17-4,71 (m, 4H), 3,52-3,38 (m, 1H), 2,81 -1,50 (m, 7H), 1,85, 1,83 ( 4 s, 3H), 1,65, 1,64, 1,59, 1,58 (4 s, 3H), 1,06, 0,96, 0,85, 0,80 (4d, J = 6.8 Hz, 3H) ppm. GC/MS (EI): isómero principal: 220 (M+, 1), 202 (1), 179 (12), 161 (17), 150 (25), 135 (100), 121 (43), 107 (87), 93 (40), 91 (39), 82 (22), 67 (25), 55 (17), 41 (45). IR (limpio, v/cm-1): 3487br, 3079m, 2962s, 1449m, 992m, 910m.
Ejemplo 15: 1-(2.4-Dimetil-1-(prop-1-en-2-il)ciclohex-3-enil) but-3-en-1-ona *
Siguiendo el procedimiento general descrito en el Ejemplo 4, se preparó 1-(2,4-dimetil-1-(prop-1-en-2-il)ciclohex-3-enil) but-3-en-1-ona partiendo de 1-(2,4-dimetil-1-(prop-1-en-2-il)ciclohex-3-enil) but-3-en-1-ol como una mezcla de 2 isómeros en una proporción de 8:2.
Descripción del olor: afrutado, picante, fresco, amaderado.
1H-NMR (300 MHz, CDCI3): 6.03-5.88 (m, 1H), 5.47-5.31 (m, 1H), 5.15-5.02 (m, 4H), 3.24-3.15 (m, 2H), 2.85-2.65 (m, 1H), 2.13-1.56 (m, 4H), 1.64 (s, 3H), 1.59 (s, 3H), 0.83, 0.73 (2d, J = 6.8 Hz, 3H) ppm. GC/MS (EI): 218 (M+, 5), 203 (5), 177 (26), 159 (17), 149 (77), 135 (36), 121 (82), 107 (100), 91 (42), 69 (38), 41 (52). IR (limpio, v/cm-1): 2962s, 1710s, 1631 s, 1446m, 1139w, 897m.
Ejemplo 16: 1-(2.4-Dimetil-1-(prop-1-en-2-il)ciclohex-3-enil) but-2-en-1-ona *
Una disolución de 1 -(2,4-dimetil-1 -(prop-1 -en-2-il)ciclohex-3-enil) but-3-en-1 -ona (2,5 g, 11,5 mmol) y trietilamina (2 g) en CH2Cl2 se agitó a temperatura ambiente durante la noche. El disolvente y el exceso de trietilamina se evaporaron y el residuo se destiló bulbo a bulbo para producir el compuesto del título (80%) como un aceite ligeramente amarillo.
Descripción del olor: especiado, pimienta negra, damascona, afrutado.
Mezcla de 4 isómeros, Isómero principal: : 1H-NMR (300 MHz, CDCl3): 6.94 (dq, J = 15.5, 7.1 Hz, 1H), 6.37 (d, J = 15.5 Hz, 1H), 5.31 (bs, 1H), 5.12 (s, 1H), 5.03 (s, 1H), 2.68-2.55 (m, 1H), 1.85-1.53 (m, 13H), 0.80 (d, J = 7.1 Hz, 3H) ppm. 13C-NMR (75 MHz, CDCl3): 201.2 (s), 143.0 (s), 141.9 (d), 132.6 (s), 127.0 (d), 124.6 (d), 115.1 (t), 58.2 (s), 32.8 (d), 27.3 (t), 23.2 (q), 21.1 (t), 19.9 (q), 18.2 (q), 18.1 (q) ppm. GGC/MS (EI): 218 (M+, 5), 203 (8), 176 (24), 133 (57), 121 (59), 107 (72), 91 (37), 69 (100), 41 (49). IR (limpio, v/cm-1): 3089m, 2968s, 1696s, 1631 s, 1445s, 1377m, 1142m, 895s.
Ejemplo 17: 1 -(buta-1 ,3-dienil)-2,4-dimetilciclohex-3-enocarbaldehiído
Siguiendo el procedimiento general descrito en el Ejemplo 1, se preparó el compuesto del título (rendimiento del 50%) partiendo de 2-metil-penta-1,3-dieno y aldehido sórbico.
Descripción del olor: afrutado, manzana, floral suave
4 Isómeros en una proporción de 9:5:2:1.1H-NMR (300 MHz, CDCh): 9.62, 9.51, 9.47, 9.39 (4s, 1H), 6.44-6.01 (m, 2H), 5.63-5.05 (m, 4H), 2.62-2.40 (m, 1H), 1.95-1.60 (m, 7H), 0.99, 0.98, 0.92, 0.91 (4d, J= 7.1Hz, 3H) ppm. Isómero principal: 13C-NMR (75 MHz, CDCl3): 202.1 (d), 136.7 (d), 134.1 (s), 134.0 (d), 133.3 (d), 124.6 (d), 117.4 (t), 53.6 (s), 35.2 (d), 27.1 (t), 25.0 (t), 23.3 (q), 17.16 (q) ppm. GC/MS (EI): 190 (M+, 37). 175 (5), 161 (16), 147 (12), 133 (12), 119 (27), 105 (40), 91 (45), 82 (100), 67 (65), 55 (13), 41 (20). IR (limpio, v/cm-1): 2963s, 2710m, 1718s, 1449m, 1378m, 1006m, 907m.
Ejemplo 18: 3.4-dimetiI-1-viniIcicIohex-3-enocarbaIdehído
Siguiendo el procedimiento general descrito en el Ejemplo 1, se preparó el compuesto del título partiendo de 2,3-dimetil-buta-1,3-dieno y aldehído crotónico.
Descripción del olor: fresco, verde, terpénico, afrutado, alcanforado
1H-NMR (300 MHz, CDCla): 9.33 (s, 1H), 5.67 (dd, J = 17.6, 10.5 Hz, 1H), 5.23 (d, J= 10.5 Hz, 1H), 5.09 (d, J = 17.6 Hz, 1H), 2.36-1.60 (m, 6H), 1.66 (s, 3H), 1.57 (s, 3H) ppm. 13C-NMR (75 MHz, CDCl3): 202.1 (d), 138.1 (d), 125.7 (s), 122.8 (s), 116.7 (t), 52.4 (s), 35.8 (t), 28.4 (t), 27.6 (t), 19.2 (q), 18.8 (q) ppm. GC/MS (EI): 164 (M+, 32), 149 (23), 135 (71), 121 (42), 107 (93), 91 (100), 79 (86), 67 (80), 55 (41), 41 (56). IIR (limpio, v/cm-1): 2920s, 1729s, 1441m, 997w, 921 m.
Ejemplo 19: 2-metil-1-(2-metilprop-1-enil)ciclohex-3-enocarbaldehído
Siguiendo el procedimiento general descrito en el Ejemplo 1, se preparó el compuesto del título partiendo de penta-1,3-dieno y 4-metil-pent-2-enal.
Ejemplo 20: 2,4-dimetil-1 -(2-metilprop-1 -enil)ciclohex-3-enocarbaldehído
Siguiendo el procedimiento general descrito en el Ejemplo 1, se preparó el compuesto del título partiendo de 2-metilpenta-1,3-dieno y 4-metil-pent-2-enal. 2 isómeros en una proporción de 9: 1.
Descripción del olor: afrutado, manzana, pétalo de rosa, acuoso
1H-NMR (300 MHz, CDCla): 9.41 (s, 1H), 5.28 (s, 1H), 4.95 (s, 1H), 2.34-2.24 (m, 1H), 1.90-1.70 (m, 4H), 1.71 (s, 3H), 1.61 (s, 3H), 1.49 (s, 3H), 0.85 (d, J= 7.1 Hz, 3H) ppm. 13C-NMR (75 MHz, CDCl3): 203.3 (d), 137.6 (s), 134.6 (s), 124.8 (d), 124.1 (d), 52.9 (s), 36.9 (d), 27.4 (t), 27.1 (q), 23.3 (q), 21.9 (t), 18.6 (q), 17.3 (q) ppm. GC/MS (EI): 192 (M+, 63), 177 (21), 163 (31), 135 (19), 121 (27), 107 (69), 95 (35), 82 (100), 67 (46), 55 (14), 41 (23). IR (limpio, v/cm-1): 2912s, 2712m, 1721 s, 1449m, 1378m, 821w.
Ejemplo 21: 1-(2.4-DimetiI-1-(2-metiIprop-1-eniI)cicIohex-3-eniI)etanoI
Siguiendo el procedimiento general descrito en el Ejemplo 3, se preparó el compuesto del título partiendo de 2,4-dimetil-1-(2-metilprop-1-enil)ciclohex-3-enocarb-aldehído. 2 isómeros en la proporción de 1:1.
Descripción del olor: terroso, seco leñoso, alcanforado
1H-NMR (300 MHz, CDCh): 5.33-5.20 (m, 1H), 4.81,4.76 (2bs, 1H), 2.80-3.70, 3.61-3.52 (2m, 1H), 2.41-2.31 (m, 1H), 1.84, 1.76, 1.75, 1.73, 1.60, 1.60 (6s, 9H), 2.01-1.39 (m, 5H), 1.18, 1.10 (2d, J = 6.4 Hz, 3H), 1.00, 0.87 (2d, J= 7.2 Hz, 3H) ppm. GC/MS (EI): 208 (M+, 5), 190 (4), 175 (5), 163 (61), 135 (20), 121 (42), 107 (100), 93 (52), 83 (34), 69 (30), 55 (23), 41 (22). IR (limpio, v/cm-1): 3422br, 2967s, 1451m, 1374m, 1102m.
Ejemplo 22: 1 -ciclopentenil-2.4-dimetilciclohex-3-enocarbaldehído
Siguiendo el procedimiento general descrito en el Ejemplo 1, se preparó el compuesto del título (20%) partiendo de 2-metilpenta-1,3-dieno y 2-ciclopentiliden-acetaldehído. 2 isómeros en una proporción de 8:2.
Descripción del olor: muguet, afrutado
Isómero principal: 1H-NMR (300 MHz, CDCla): 9.40 (s, 1H), 5.58 (s, 1H), 5.33 (s, 1H), 2.67 (bs, 1H), 2.36-1.70 (m, 10H), 1.60 (s, 3H), 0.98 (d, J = 6.9 Hz, 3H) ppm. 13C-NMR (75 MHz, CDCl3): 202.2 (d), 141.5 (s), 133.4 (s), 129.5 (d), 125.0 (d), 54.6 (s), 33.0 (d), 32.8 (t), 32.0 (t), 27.3 (t), 23.3 (q), 23.2 (2t), 17.3 (q) ppm. GC/MS (EI): 204 (M+, 30), 189 (4), 175 (10), 147 (19), 133 (10), 119 (14), 105 (20), 91 (31), 82 (100), 67 (49), 55 (10), 41 (23).
Ejemplo 23: 4.5-dimetil-2-(2-metilprop-1 -enil)-1 -vinilciclohex-3-enocarbaldehído
Siguiendo el procedimiento general descrito en el Ejemplo 1, se preparó el compuesto del título partiendo de aloocimeno y aldehído crotónico. (2 isómeros en una proporción de 85:15.
Descripción del olor: ligeramente afrutado, verde, débil
Isómero principal: 1H-NMR (300 MHz, CDCla): 9.13 (s, 1H), 5.70-5.59 (m, 1H), 5.24-4.76 (m, 4H), 3.32-3.19 (m, 1H), 2.12-1.15 (m, 4H), 1.63, 1.59, 1.59 (3s, 9H), 0.99 (d, J = 6.8 Hz, 3H) ppm. 13C-NMR (75 MHz, CDCl3): 201.4 (d), 138.2 (s), 137.9 (d), 133.6 (s), 123.7 (d), 121.5 (d), 118.0 (t), 55.4 (s), 38.8 (d), 32.7 (t), 30.6 (d), 25.9 (q), 21.1 (q), 19.3 (q), 18.3 (q) ppm. GC/MS (EI): 218 (M+, 4), 203 (1), 189 (2), 175 (1), 161 (1), 147 (3), 136 (56), 121 (100), 105 (12), 91 (12), 77 (6), 67 (2), 55 (4), 41 (5). IR (limpio, v/cm- 1): 2967s, 1725s, 1445m, 1377m, 921w.
Ejemplo 24: 2-metil-4-(4-metilpent-3-enil)-1 -vinilciclohex-3-enocarbaldehído
Siguiendo el procedimiento general descrito en el Ejemplo 1, se preparó el compuesto del título (50% de rendimiento) partiendo de 2-metil-6-metilenenona-2,7-dieno y aldehído crotónico.
Descripción del olor: muguet, afrutado.
(Endo: exo-isómeros en una proporción de 8: 2). Endo-isómero: 1H-NMR (300 MHz, CDCh): 9.49 (s, 1H), 5.76 (dd, J = 17.7, 10.9 Hz, 1H), 5.37-5.33 (m, 2H), 5.27 (d, J =10.9 Hz, 1H), 5.08 (d, J= 17.7 Hz, 1H), 2.55-2.43 (m, 1H), 2.09 2.65 (m, 8H), 1.67 (s, 3H), 1.58 (s, 3H), 1.00 (d, J= 7.1Hz, 3H) ppm. 13C-NMR (75 MHz, CDCl3): 203.0 (d), 138.3 (d), 137.5 (s), 131.4 (s), 124.4 (d), 124.0 (d), 117.4 (t), 54.3 (s), 37.3 (t), 34.7 (d), 26.4 (t), 25.7 (q), 25.3 (t), 25.0 (t), 17.7 (q), 17.2 (q) ppm. GC/MS (EI): 232 (M+, 5), 217 (6), 203 (14), 189 (12), 171 (6), 150 (22), 135 (20), 119 (23), 107 (100), 91 (35), 79 (30), 69 (92), 55 (28), 41 (68).
Ejemplo 25: 4-metil-1-vinil-ciclohex-3-enocarbaldehído. 3-metil-1-vinil-ciclohex-3-eno-carbaldehído y aldehído de Perilla (relación 5,5:3:1,5)
Siguiendo el procedimiento general descrito en el Ejemplo 1, una mezcla de 4-metil-1-vinil-ciclohex-3-enocarbaldehído, 3-metil-1 -vinil-ciclohex-3-eno-carbaldehído y aldehído de Perilla (relación 5,5:3:1.5) (rendimiento del 31%) a partir de isopreno y aldehído crotónico. Los componentes se separaron por cromatografía (eluyente hexano: MTBE 50:1 a 10:1). Los datos analíticos del aldehído racémico de Perilla obtenidos de esta manera fueron idénticos a los de una muestra auténtica.
Descripción del olor de la mezcla: potente, verde fresco, afrutado, especiado.
4-Metil-1-vinil-ciclohex-3-enocarbaldehído: 1H-NMR (300 MHz, CDCh): 9.35 (s, 1H), 5.69 (dd, J= 17.7, 10.7 Hz, 1H), 5.40 (bs, 1H), 5.26 (d, J=10.7 Hz, 1H), 5.13 (d, J = 17.7 Hz, 1H), 2.44 (bs, 1H), 2.41 (bs, 1H), 2.10-1.64 (m, 5H), 1.63 (s, 3H) ppm. 13C-NMR (75 MHz, CDCl3): 202.0 (d), 138 (d), 134.4 (s), 118.0 (d), 116.9 (t), 51.4 (s), 29.8 (t), 27.3 (t), 26.9 (t), 22.0 (q) ppm. GC/MS (EI): 150 (M+, 23), 135 (24), 121 (45), 107 (33), 93 (100), 79 (98), 67 (54), 55 (37), 39 (38).
3-Metil-1-vinil-ciclohex-3-enocarbaldehído: 1H-NMR (300 MHz, CDCta): 9.36 (s, 1H), 5.71 (dd, J= 10.7, 17.7 Hz, 1H), 5.37 (bs, 1H), 5.27 (d, J= 10.7 Hz, 1H), 5.12 (d, J = 17.7 Hz, 1H), 2.37 (bs, 1H), 2.33 (bs, 1H), 2.10-1.64 (m, 5H), 1.72 (s, 3H) ppm. 13C-NMR (75 MHz, CDCl3): 201.7 (d), 137.9 (d), 131.2 (s), 120.9 (d), 116.8 (t), 52.2 (s), 34.1 (t), 26.7 (t), 23.6 (q), 22.2 (t) ppm. GC/MS (EI): 150 (M+, 10), 135 (16), 121 (78), 107 (29), 93 (100), 79 (88), 67 (32), 55 (31), 39 (32). IR (limpio, v/cm-1): 2917s, 2854m, 2707w, 1726s, 1632w, 1439m, 921m.
Ejemplo 26: oxima de 4-metil-1-vinil-ciclohex-3-enocarbaldehído. oxima de 3-metil-1-vinil-ciclohex-3-eno-carbaldehído (relación 6:4)
Una solución de una mezcla de 4-metil-1-vinil-ciclohex-3-enocarbaldehído y 3-metil-1-vinil-ciclohex-3-enocarbaldehído (6:4. 1.5 g. 10 mmol). hidrocloruro de hidroxilamina (1.04 g. 15 mmol) y NaHCÜ3 (1.26 g. 15 mmol) en EtOH/agua (20 ml. 3:1) se agitó a 50 °C durante 4 h. La mezcla se diluyó con agua y se extrajo 3 veces con MTBE. . Las capas org combinadas se lavaron con agua y salmuera. se secaron (MgSO4) y se evaporó al vacío. La oxima de 4-metil-1-vinil-ciclohex-3-enocarbaldehído y la oxima de 3-metil-1-vinil-ciclohex-3-eno-carbaldehído se obtuvieron después de la destilación de bulbo a bulbo (proporción 6:4. rendimiento del 70%) como aceite incoloro.
Descripción del olor de la mezcla: floral. hoja violeta. verde
1H-NMR (300 MHz. CDCla): 8.43. 8.35 (2bs. 1H). 7.32 (s. 1H). 5.82 (dd. J = 17.7. 10.6 Hz. 1H). 5.38 (bs. 1H). 5.14 5.01 (m. 2H). 2.28-1.64 (m. 6H). 1.70. 1.65 (2s. 3H) ppm. GC/MS (EI): 165 (M+. 2). 148 (24). 131 (24). 120 (25). 105 (100). 91 (44). 79 (30). 68 (96). 53 (28). 39 (25). IR (limpio. v/cm-1): 3315 br. 2927 s. 1635 m. 1439 s. 922 s.
Ejemplo 27: 1-(prop-1-en-2-il)ciclohex-3-enecarbaldehído *
Siguiendo el procedimiento general descrito en el Ejemplo 1. se preparó el compuesto del título (rendimiento del 31%) partiendo de 1.3-butadieno y prenal.
Descripción del olor: fresco. verde. alcanforado. similar al aldehído de la perilla
1H-NMR (300 MHz. CDCla): 9.23 (s. 1H). 5.72-5.60 (m. 2H). 5.07 (s. 1H). 4.91 (s. 1H). 2.54-2.44 (m. 1H). 2.18-2.71 (m. 5H). 1.68 (s. 3H) ppm. 13C-NMR (75 MHz. CDCl3): 201.4 (d). 143.0 (s). 126.8 (d). 124.4 (d). 114.4 (t). 54.4 (s).
29.0 (t). 25.5 (t). 22.4 (t). 19.5 (q) ppm. GC/MS (EI): 150 (M+. 9). 135 (17). 121 (36). 107 (21). 93 (73). 79 (100). 67 (21). 55 (24). 41 (27). IR (limpio. v/cm-1): 3028w. 2923s. 2698m. 1725s. 1668m. 1634m. 1440m. 1377m. 901m.
Ejemplo 28: 1 -(but-1 -enil)-2.4-dimetilciclohex-3-enocarbaldehído
Siguiendo el procedimiento general descrito en el Ejemplo 1. se preparó el compuesto del título (rendimiento del 71%) partiendo de 2-metil-penta-1.3-dieno y 2-hexenal.
Descripción del olor: afrutado. parecido a la manzana. floral.
4 isómeros en una proporción de 5:2:7:1. 1H-NMR (300 MHz. CDCh): 9.62. 9.53. 9.45. 9.36 (4s. 1H). 5.60-5.14 (m.
3H). 2.63-2.33 (m. 1H). 2.13-1.61 (m. 9H). 1.01-0.90 (m. 6H) ppm. 13C-NMR (75 MHz. CDCls): Isómero principal: 203.3 (d). 137.3 (d). 134.6 (s). 129.0 (d). 124.1 (d). 53.3 (s). 36.6 (d). 27.3 (t). 27.1 (t). 23.3 (q). 22.7 (t). 17.2 (q). 14.1 (q) ppm. GC/MS (EI): 192 (M+. 20). 163 (20). 135 (13). 121 (16). 107 (35). 93 (24). 82 (100). 67 (46). 55 (18). 41 (20). IR (limpio. v/cm-1): 1964. 2874 m. 2711 w. 1721. 1451 m.
Ejemplo 29: 4-metil-1-(prop-1-en-2-il)ciclohex-3-enocarbaldehído y 3-metil-1-(prop-1-en-2-il)ciclohex-3-enocarbaldehído *
Siguiendo el procedimiento general descrito en el Ejemplo 1. se preparó una mezcla de 4-metil-1-(prop-1-en-2-il)ciclohex-3-enocarbaldehído y 3-metil-1-(prop-1-en-2-il)ciclohex-3-enecarbaldehído (rendimiento del 31%) a partir de isopreno y prenal.
Descripción del olor: verde. afrutado. mango. damascona. ciruela.
Mezcla de isómeros en una proporción de 6: 4. 1H-NMR (300 MHz. CDCl3): 9.22. 9.21 (2s. 1H). 5.04-4.83 (m. 3H).
2.51-2.33 (m. 2H). 2.17-1.72 (m. 5H). 1.70. 1.68. 1.67. 1.60 (4s. 6H) ppm. 4-metil-1-(prop-1-en-2-il)ciclohex-3-enecarbaldehído: 13C-NMR (75 MHz. CDCL): 201.7 (d). 143.0 (s). 134.0 (s). 118.4 (d). 114.4 (t). 54.2 (s). 29.3 (t). 27.2 (t). 26.0 (t). 23.2 (q). 19.6 (q) ppm. GC/MS (EI): 164 (M+. 20). 149 (31). 135 (68). 121 (35). 107 (71). 93 (100). 79 (64).
67 (40). 55 (28). 41 (38). 3-metil-1-(prop-1-en-2-il)ciclohex-3-enecarbaldehído: 13C-NMR (75 MHz. CDCh): 201.5 (d).
143.0 (s). 131.6 (s). 120.6 (d). 114.3 (t). 55.0 (s). 33.7 (t). 25.4 (t). 23.6 (q). 22.4 (t). 19.6 (q) ppm. GC/MS (EI): 164 (M+.
18). 149 (32). 135 (68). 121 (34). 107 (72). 93 (100). 79 (64). 67 (41). 55 (27). 41 (38). IR (limpio. v/cm-1): 2967m.
2921 s. 1726s. 1635m. 1441m. 1377m. 899m.
Ejemplo 30: 1-vinilciclohex-3-eno carbaldehído y 4-vinilciclohex-1-eno carbaldehído **
Siguiendo el procedimiento general descrito en el Ejemplo 1. se preparó una mezcla de 1-vinilciclohex-3-eno carbaldehído y 4-vinilciclohex-1-eno carbaldehído (rendimiento del 42%) a partir de 1.3-butadieno y aldehído crotónico.
Descripción del olor de la mezcla: verde. afrutado. manzana. melón. floral. violeta.
1-Vinilciclohex-3-eno carbaldehído: 1H-NMR (300 MHz. CDCL): 9.38 (s. 1H). 5.77-5.63 (m. 3H). 5.29 (d. J= 10.6 Hz.
1H). 5.16 (d. J= 17.7 Hz. 1H). 2.53-1.67 (m. 6H) ppm. 13C-NMR (75 MHz. CDCl3): 201.8 (d). 137.9 (d). 127.1 (d). 123.9 (d). 117.0 (t). 51.7 (s). 29.4 (t). 26.9 (t). 22.0 (t) ppm. GC/MS (EI): 136 (M+. 5). 118 (17). 107 (28). 91 (46). 79 (100).
67 (9), 53 (14), 39 (23).
4-Vinilciclohex-l-eno carbaldehído: 1H-NMR (300 MHz, CDCI3): 9.41 (s, 1H), 6.79 (bs, 1H), 5.81 (ddd, J= 17.0, 10.2, 6.6 Hz, 1H), 5.04 (d, J= 17.0 Hz, 1H), 4.99 (d, J = 10.2 Hz, 1H), 2.55-2.05 (m, 5H), 1.91-1.83 (m, 1H), 1.44-1.30 (m, 1H) ppm. 13C-NMR (75 MHz, CDCl3): 194.0 (d), 150.1 (d), 142.0 (d), 141.3 (s), 113.5 (t), 37.1 (d), 32.0 (t), 27.2 (t), 20.8 (t) ppm.GC/MS (EI): 136 (M+, 21), 121 (14), 107 (60), 91 (41), 79 (88), 67 (27), 54 (100), 39 (49). IR (limpio, v/cm-1): 2928s, 1686s, 1643m, 1420w, 1178w, 916w.
Ejemplo 31: (4-vinilciclohex-1-enil) metanol **
Siguiendo el procedimiento general descrito en el Ejemplo 2, se preparó el compuesto del título (rendimiento del 85%) partiendo de 4-vinilciclohex-1-eno carbaldehído.
Descripción del olor: especiado, canela, rosado, afrutado, verde.
1H-NMR (300 MHz, CDCla): 5.48 (ddd, J= 17.0, 10.2, 6.4 Hz, 1H), 5.68 (bs, 1H), 5.03 (d, J = 17.0 Hz, 1H), 4.96 (d, J = 10.2 Hz, 1H), 4.00 (s, 2H), 2.27-1.81 (m, 6H), 1.60 (bs, OH), 1.48-1.35 (m, 1H) ppm. GC/MS (EI): 138 (M+, 9), 120 (26), 105 (58), 91 (64), 79 (100), 67 (33), 55 (57), 41 (35). IR (limpio, v/cm -1): 3332br, 3079m, 2914s, 1640m, 1435m, 995s, 912s.
Ejemplo 32: 1-(4-vinilciclohex-1-enil) etanol **
Siguiendo el procedimiento general descrito en el Ejemplo 3, se preparó el compuesto del título (rendimiento del 66%) partiendo de 4-vinilciclohex-1-eno carbaldehído.
Descripción del olor: cinámico, afrutado, manzana, verde
Mezcla de 2 isómeros en la proporción de 1:1. 1H-NMR (300 MHz, CDCl3): 5.92-5.80 (m, 1H), 5.66 (sa, 1H), 5.05 4.93 (m, 2H), 4.24-4.12 (m, 1H), 2.32-1.79 (m, 6H), 1.48-1.31 (m , 1H), 1,25 (2d, J = 6.5 Hz, 3H) ppm. GC/MS (EI): isómero principal: 152 (M+, 9), 134 (35), 119 (33), 105 (53), 91 (60), 79 (100), 67 (34), 55 (24), 43 (68). IR (limpio, v/cm-1): 3369br, 3080m, 2973m, 2925s, 1436m, 1071m, 912m.
Ejemplo 33: 2-metil-4-vinilciclohex-1-eno carbaldehído **
Siguiendo el procedimiento general descrito en el Ejemplo 1, se preparó el compuesto del título (rendimiento del 12%) partiendo de 1,3-butadieno y prenal.
Descripción del olor: verde, afrutado, canela.
1H-NMR (300 MHz, CDCla): 10.12 (s, 1H), 5.79 (ddd, J = 17.0, 10.2, 6.1 Hz, 1H), 5.06-4.95 (m, 2H), 2.48-1.22 (m, 7H), 2.14 (s, 3H) ppm. 13C-NMR (75 MHz, CDCl3): 191.0 (d), 155.2 (s), 142.2 (d), 133.3 (s), 113.4 (t), 39.2 (t), 37.0 (d), 27.5 (t), 21.9 (t), 18.3 (q) ppm. GC/MS (EI): 150 (M+, 42), 135 (45), 121 (47), 107 (55), 93 (87), 79 (100), 67 (94), 54 (57), 41 (54). IR (limpio, v/cm-1): 2921s, 1714s, 1666s, 1440m, 1379m, 1244m, 914m.
Ejemplo 34: (2-metil-4-vinilciclohex-1-enil) metanol **
Siguiendo el procedimiento general descrito en el Ejemplo 2, se preparó el compuesto del título (rendimiento del 92%) partiendo de 2-metil-4-vinilciclohex-1-eno carbaldehído.
Descripción del olor: metálico, floral, rosado.
1H-NMR (300 MHz, CDCls): 5.82 (ddd, J= 17.0, 10.2, 6.4 Hz, 1H), 5.01 (d, J= 17.0 Hz, 1H), 4.95 (d, J= 10.2 Hz, 1H), 4.16 (d, J= 10.9 Hz, 1H), 4.07 (d, J= 10.9 Hz, 1H), 2.26-1.92 (m, 7H), 1.71 (s, 3H) ppm. GC/MS (EI): 152 (M+, 7), 134 (43), 119 (77), 93 (100), 91 (98), 79 (94), 69 (43), 55 (36), 41 (54). IR (limpio, v/cm-1): 3349br, 3079w, 2920s, 1640w, 1436s, 995s, 910m.
Ejemplo 35: 3a, 4.7.7a-tetrahidro-1H-indeno-6-carbaldehído **
Siguiendo el procedimiento general descrito en el Ejemplo 1, se preparó el compuesto del título (rendimiento del 40%; punto de ebullición: 65-70°C/0,54 mbar) partiendo de ciclopentadieno y aldehído crotónico.
Descripción del olor: verde, melón, pepino, manzana, marino, floral.
1H-NMR (300 MHz, CDCls): 9.40 (s, 1H), 6.93 (dd, J= 4.9, 4.9 Hz, 1H), 5.65-5.53 (m, 2H), 2.99-2.91 (m, 1H), 2.58 2.35 (m, 4H), 2.23-2.13 (m, 1H), 2.05-1.91 (m, 2H) ppm. 13C-NMR (75 MHz, CDCl3): 192.7 (d), 152.4 (d), 142.7 (s), 134.9 (d), 130.4 (d), 43.0 (d), 39.8 (t), 34.6 (d), 29.3 (t), 24.3 (t) ppm. GC/MS (EI): 148 (M+, 26), 133 (6), 120 (10), 105 (6), 91 (18), 77 (13), 66 (100), 55 (6), 39 (12). IR (limpio, v/cm-1): Los 3050m, 2924s, 2717m, 1678s, 1171m.
Ejemplo 36: 3a, 4.7.7a-tetrahidro-1 H-indeno-6-carbaldehvde oxima **
De manera análoga al Ejemplo 26, el compuesto del título se preparó partiendo de 3a,4,7,7a-tetrahidro-1 H-indeno-6-carbaldehído con un rendimiento del 65%.
Descripción del olor: especiado, floral, débil.
1H-NMR (300 MHz, CDCls): 8,85 (ancho, OH), 7,74 (s, 1 H), 6,16 (dd, J = 5.1,5.1 Hz, 1 H), 5,69-5,66 (m, 1 H), 5,59 5,56 (m, 1 H), 2,90 (sa, 1 H), 2,57-2,35 (m, 4 H), 2,15-1,96 (m, 3H) ppm. 13C-NMR (75 MHz, CDCls): 152.5 (d), 136.3 (s), 135.2 (d), 134.2 (s), 130.2 (d), 42.8 (d), 39.8 (d), 34.7 (t), 28.5 (t), 26.6 (t ) ppm. GC/MS (EI): 163 (M+, 17), 146 (18), 129 (6), 115 (7), 91 (9), 77 (9), 66 (100), 39 (8). IR (limpio, v/cm-1): 3302br, 3047m, 2924s, 1631m, 1446m, 1311w, 953s.
Ejemplo 37: (3a, 4.7.7a-Tetrahydro-1 H-inden-6-il) metanol **
Siguiendo el procedimiento general descrito en el Ejemplo 2, se preparó el compuesto del título (rendimiento del 53%) partiendo de 3a, 4,7,7a-tetrahidro-1 H-indeno-6-carbaldehído.
Descripción del olor: pepino, verde, nonadienol.
1H-NMR (300 MHz, CDCla): 5.78-5.73 (m, 1H), 5.65-5.53 (m, 2H), 3.97 (s, 2H), 2.88-2.78 (m, 1H), 2.56-1.79 (m, 8H) ppm. GC/MS (EI): 150 (M+, 1), 132 (30), 117 (25), 104 (4), 91 (16), 79 (14), 66 (100), 55 (5), 39 (9).
Ejemplo 38: 1-(3a, 4,7,7a-tetrahidro-1 H-inden-6il) etanona **
Siguiendo el procedimiento general descrito en el Ejemplo 4, se preparó el compuesto del título (rendimiento del 30%) partiendo de 1-(3a, 4,7,7a-tetrahidro-1 H-inden-6-il) etanol.
Descripción del olor: verde, afrutado, floral, melón.
1H-NMR (300 MHz, CDCls): 7.05 (dd, J = 5.3, 5.3 Hz, 1H), 5.67-5.63 (m, 1H), 5.56-5.51 (m, 1H), 2.97-2.88 (m, 1H), 2.70-2.34 (m, 4H), 2.28 (s, 3H), 2.11-1.92 (m, 3H) ppm. GC/MS (EI): 162 (M+, 27), 147 (6), 119 (26), 97 (20), 91 (18), 77 (9), 66 (100), 53 (8), 43 (40).
Ejemplo 39: 5-Metil-3a, 4,7,7a-tetrahidro-1 H-indeno-6-carbaldehído **
Siguiendo el procedimiento general descrito en el Ejemplo 1, se preparó el compuesto del título (rendimiento del 35%; punto de ebullición: 90°C/0,41 mbar) partiendo de ciclopentadieno y prenal.
Descripción del olor: verde, afrutado, melón.
1H-NMR (300 MHz, CDCls): 10.04 (s, 1H), 5.61-5.58 (m, 1H), 5.46-5.43 (m, 1H), 3.04-2.94 (m, 1H), 2.59-2.46 (m, 2H), 2.40-2.28 (m, 2H), 2.16 (s, 3H), 2.13-2.00 (m, 2H), 1.93-1.81 (m, 1H) ppm. 13C-NMR (75 MHz, CDCl3): 188.8 (d), 159.7 (s), 135.0 (s), 133.3 (d), 130.9 (d), 44.1 (d), 40.0 (t), 37.7 (t), 34.4 (d), 25.6 (t), 18.8 (q) ppm. GC/MS (EI): 162 (M+, 46), 147 (22), 131 (10), 115 (6), 105 (9), 91 (20), 77 (14), 66 (100), 51 (6), 39 (12). IR (limpio, v/cm-1): Los 3048m, 2925s, 2848s, 1665s, 1632m, 1434m, 1377m.
Ejemplo 40: (5-Metil-3a, 4.7.7a-tetrahidro-1H-indeno-6-vl) metanol **
Siguiendo el procedimiento general descrito en el Ejemplo 2, se preparó el compuesto del título (rendimiento del 98%) partiendo de 5-metil-3a, 4,7,7a-tetrahidro-1H-indeno-6-carbaldehído.
Descripción del olor: especiado, jacinto, afrutado, manzana, verde.
1H-NMR (300 MHz, CDCls): 5.67-5.63 (m, 1H), 5.53-5.47 (m, 1H), 5.17-4.08 (m, 2H), 2.96-2.85 (m, 1H), 2.61-2.44 (m, 2H), 2.27-2.15 (m, 2H), 2.04-1.82 (m, 4H), 1.75 (s, 3H) ppm.GC/MS (EI): 164 (M+, 1), 146 (69), 131 (87), 117 (19), 105 (30), 91 (40), 79 (33), 66 (100), 53 (7), 41 (13). IR (limpio, v/cm-1): 3327br, 3047m, 2925s, 1668w, 1444m, 996s. Ejemplo 41: rac-1-(propan-2-ilideno)-3a, 4.7.7a-tetrahidro-1H-indeno-6-carbaldehído **
Siguiendo el procedimiento general descrito en el Ejemplo 1, se preparó el compuesto del título (rendimiento del 42%) partiendo de 6,6-dimetil fulveno y aldehído crotónico.
Descripción del olor: afrutado, verde, amaderado.
1H-NMR (300 MHz, CDCls): 9.44 (s, 1H, CHO), 6.95 (ddd, J = 5.9, 4.5, 1.5 Hz, 1H, 5-H), 6.34 (dd, J = 5.7, 2.3 Hz, 1H, 2-H), 5.70 (bd, J = 5.7 Hz, 1H, 3-H), 3.24-3.17 (m, 1H, 3aH), 2.92 (ddd, J = 7.5, 7.5, 7.5 Hz, 1H, 7a-H), 2.72-2.62 (m, 2H, 4-Ha, 7-Ha), 2.27-2.17 (dddd, J = 16.6, 6.1,4.5, 1.5 Hz, 1H, 4-Hb), 1.91 (dd, J = 15.5 Hz, 8.3 Hz, 1H, 7-Hb), 1.79 (s, 3H, (CH3)a), 1.74 (s, H, CH3)b) ppm. 13C-NMR (75 MHz, CDCl3): 192.1 (d, CHO), 151.8 (d, C-5), 143.7 (s, C-6), 142.9 (s, C-1), 136.7 (d, C-3), 131.4 (d, C-2), 122.6 (s, C(CH3)2), 43.4 (d, C-3a), 39.4 (d, C-7a), 29.3 (t, C-4), 23.8 (t,
C-7), 21.1 (q, (CH3)a), 21.0 (q, (CH3)b) ppm. GC/MS (EI): 188 (M+, 30), 173 (4), 159 (2), 145 (5), 128 (6), 115 (7), 106 (100), 91 (40), 77 (7), 65 (6), 53 (4), 39 (5). IR (limpio, v/cm-1): 2910s, 2716m, 1681 s, 1443m, 1374m.
Ejemplo 42: 2-metil-3a, 4.7,7a-tetrahidro-1H-indeno-6-carbaldehído y 3-metil-3a, 4,7,7a-tetrahidro-1H-indeno-6-carbaldehído (mezcla con una proporción de 2:1). **
Siguiendo el procedimiento general descrito en el Ejemplo 1, una mezcla de 2-metil-3a, 4,7,7a-tetrahidro-1H-indeno-6-carbaldehído y 3-metil-3a, 4,7,7a-tetrahidro-1H- Se preparó indeno-6-carbaldehído (rendimiento del 35%) partiendo de metil ciclopentadieno y aldehído crotónico.
Descripción del olor: verde, fresco, especiado, afrutado, comínico, anís.
1H-NMR (300 MHz, CDCla): 9.45, 9.44 (2s, 1H), 6.99-6.96 (m, 1H), 5.28-5.27, 5.18-5.17 (2m, 1H), 2.98-2.93, 2.74 2.68 (2m, 1H), 2.59-2.39 (m, 4H), 2.24-2.16 (m, 1H), 2.07-2.02 (m, 1H), 1.94-1.85 (m, 1H), 1.69, 1.67 (2s, 3H) ppm. GC/MS (EI): Isómero principal: 162 (M+, 21), 147 (5), 134 (6), 115 (5), 105 (5), 91 (13), 80 (100), 65 (6), 53 (7), 39 (10). IR (limpio, v/cm-1): Los 3037m, 2917s, 2842m, 1679s, 1442m, 1377m, 1176m, 831m.
Ejemplo 43: 4-etil-3a, 4.7.7a-tetrahydro-1H-indeno-6-carbaldehído **
Siguiendo el procedimiento general descrito en el Ejemplo 1, se preparó el compuesto del título (rendimiento del 42%) partiendo de ciclopentadieno y 2-hexenal.
Descripción del olor: verde, afrutado, débil.
1H-NMR (300 MHz, CDCla): 9.42, 9.40 (2s, 1H), 6.84-6.83, 6.74-6.72 (2m, 1H), 5.74-5.53 (m, 2H), 3.26-3.13 (m, 1H), 2.87-2.75 (m, 1H), 2.66-1.46 (m, 7H), 1.06, 1.02 (2t, J = 7.5 Hz, 3H) ppm. Isómero principal: 13C-NMR (75 MHz, CDCL) 192.7 (d), 157.3 (d), 142.4 (s), 132.5 (d), 130.3 (d), 49.1 (d), 41.2 (d), 41.0 (t), 34.4 (d), 25.1 (t), 24.9 (t), 12.44 (q) ppm. GC/MS (EI): 176 (M+, 28), 147 (23), 117 (13), 105 (8), 91 (21), 77 (14), 66 (100), 41 (10). Isómero minoritario: 13C-NMR (75 MHz, CDCh): 192.7 (d), 156.3 (d), 142.5 (s), 133.9 (d), 130.2 (d), 49.4 (d), 41.9 (d), 39.4 (t), 35.5 (d), 27.1 (t), 24.7 (t), 11.63 (q) ppm. IR (limpio, v/cm-1): 3054 m, 2961 s, 2929 s, 1683 s, 1447 m.
Ejemplo 44: 1,4,4a, 7.8.8a-hexahidronaftalen-2-carbaldehído **
Siguiendo el procedimiento general descrito en el Ejemplo 1, se preparó el compuesto del título (rendimiento del 19%) partiendo de ciclohexadieno y aldehído crotónico.
Descripción del olor: floral, verde, especiado, amaderado.
1H-NMR (300 MHz, CDCL): 9.39 (s, 1H), 6.70 (s, 1H), 5.59 (s, 2H), 2.60-2.49 (m, 1H), 2.39-1.98 (m, 7H), 1.54 (d, J = 12.8 Hz, 1H), 1.51 (d, J = 12.8 Hz, 1H) ppm. 13C-NMR (75 MHz, CDCl3): 194.4 (d), 149.1 (d), 140.1 (s), 131.0 (d), 127.1 (d), 32.1 (d), 31.5 (t), 29.5 (d), 25.0 (t), 24.6 (t), 24.1 (t) ppm. GGC/MS (EI): 162 (M+, 53), 147 (9), 133 (16), 139 (15), 115 (6), 105 (12), 91 (39), 80 (100), 65 (9), 53 (9), 39 (13). IR (limpio, v/cm-1): Los 3018m, 2923s, 2719w, 1684s, 1647m, 1455m, 1175m.
Ejemplo 45: 4-(6-Metilhepta-1.5-dien-2-il)ciclohex-1-enocarbaldehído **
Siguiendo el procedimiento general descrito en el Ejemplo 1, se preparó el compuesto del título (rendimiento del 10%) partiendo de mirceno y aldehído crotónico.
Descripción del olor: verde, afrutado, graso.
Los datos analíticos están de acuerdo con los datos de referencia de Raharivelomanana et al., Journal of Natural Products, vol. 56 (2), 1993, 272-274.
Ejemplo 46: Composición de la fragancia
Una composición de fragancia con carácter afrutado, de manzana y especiado.
Agrumex (acetato de 2-terc-butilciclohexilo) 300 1-Vinilciclohex-3-eno carbaldehído 13 4-Vinilciclohex-1-eno carbaldehído 7 Belambre (1,7,7-trimetil-2 '-(1 -metiletil) espiro [biciclo [2.2.1]
heptano-2,4 '-[1,3] dioxano]) 50% en IPM 10
Propionato de alil ciclohexilo 15 Etil vainillina 1 Fraise pure (etil metil fenil glicidato) 3 Galaxolida (ciclopenta [g] -2-benzopirano, 1,3,4,6,7,8-hexahidro-4,6,6,7,8,8-hexametil) 66% en DEP 200 Galbanona 10 (1 -(5,5-dimetilciclohex-1-enil) pent-4-en-1 -ona) 50 Jasmacicleno (4,7-metano-1H-inden-6-ol, 3a, 4,5,6,7,7a-hexahidro-, acetato) 50 Peche puro (5-heptildihidrofuran-2 (3H) -ona) 50 Dietilftalato 50 Pomarosa (5,6,7-trimetilocta-2,5-dien-4-ona) 1 Hercolyn DW (dihidroabietato de metilo) 250
1000
En este perfume, 1-vinilciclohex-3-eno carbaldehído y 4-vinilciclohex-1-eno carbaldehído imparten un sabor afrutado fresco natural con una nota de salida brillante.
Claims (13)
1. Un proceso que comprende hacer reaccionar formilbutadieno de fórmula B
en donde
R1 es hidrógeno, metilo o etilo;
R2 es hidrógeno, alquilo C1-C6, o alquenilo C2-C6;
R3 es hidrógeno, metilo o etilo;
con un dieno de fórmula C
en donde
R4, R5, R6, R7, R8 y R9 se seleccionan independientemente de hidrógeno, alquilo C1-C6, o alquenilo C2-C6; resultando en compuestos de fórmulas (Ia) y (Ib)
caracterizado por que en presencia de un catalizador de metilenación y formalina, el formilbutadieno de fórmula B se prepara in situ a partir de un aldehído a, p-insaturado de fórmula A
2. Un proceso de acuerdo con la reivindicación 1 que comprende la posterior reducción de un compuesto de fórmula (Ia) dando como resultado compuestos de fórmula (IIa)
en donde
R1 es hidrógeno, metilo o etilo;
R2 es hidrógeno, alquilo C1-C6, o alquenilo C2-C6;
R3 es hidrógeno, metilo o etilo;
R4 , R5 , R6 , R7 , R8 y R9 se seleccionan independientemente de hidrógeno, alquilo C1-C6, o alquenilo C2-C6;
R10 es hidrógeno, alquilo C1-C5 lineal o ramificado, o alquenilo C2-C5 lineal o ramificado; y
R11 es hidrógeno.
3. Un proceso de acuerdo con la reivindicación 2 que comprende la esterificación posterior de un compuesto de fórmula (IIa) en presencia de un haluro de ácido carboxílico y una base que da como resultado compuestos de fórmula (IIa) en donde R11 es COR12, en donde R12 es hidrógeno, o alquilo C1-C3 C lineal o ramificado.
4. Un proceso de acuerdo con la reivindicación 2 que comprende la oxidación posterior de un compuesto de fórmula (IIa) en presencia de un agente oxidante que da como resultado compuestos de fórmula (IIIa).
en donde
R1 es hidrógeno, metilo o etilo;
R2 es hidrógeno, alquilo C1-C6, o alquenilo C2-C6;
R3 es hidrógeno, metilo o etilo;
R4 , R5 , R6 , R7 , R8 y R9 se seleccionan independientemente de hidrógeno, alquilo C1-C6, o alquenilo C2-C6; y R10 es alquilo C1-C5 lineal o ramificado, o alquenilo C2-C5 lineal o ramificado.
5. Un proceso de acuerdo con la reivindicación 1 o la reivindicación 4 que comprende la transformación posterior del grupo carbonilo de un compuesto seleccionado entre compuestos de fórmulas (Ia) y (IIIa) en presencia de a) hidroxilamina;
b) metanol o etanol; o
c) un diol;
dando como resultado compuestos de fórmula (IVa)
en donde
R1 es hidrógeno, metilo o etilo;
R2 es hidrógeno, alquilo C1-C6, o alquenilo C2-C6;
R3 es hidrógeno, metilo o etilo;
R4 , R5 , R6 , R7 , R8 y R9 se seleccionan independientemente de hidrógeno, alquilo C1-C6, o alquenilo C2-C6; y R10 es hidrógeno, alquilo C1-C5 lineal o ramificado, o alquenilo C2-C5 lineal o ramificado; R y R 'se seleccionan entre metoxi y etoxi; o
R y R' se forman junto con el átomo de carbono al que están unidos dioxolan, dioxano o C=N-OH.
6. Un proceso de acuerdo con la reivindicación 1 que comprende la posterior reducción de un compuesto de fórmula (Ib) dando como resultado compuestos de fórmula (IIb)
en donde
R1 es hidrógeno, metilo o etilo;
R2 es hidrógeno, alquilo C1-C6, o alquenilo C2-C6;
R3 es hidrógeno, metilo o etilo;
R4 , R5 , R6 , R7 , R8 y R9 se seleccionan independientemente de hidrógeno, alquilo C1-C6, o alquenilo C2-C6;
R10 es hidrógeno, alquilo C1-C5 lineal o ramificado, o alquenilo C2-C5 lineal o ramificado; y R11 es hidrógeno.
7. Un proceso de acuerdo con la reivindicación 6 que comprende la esterificación posterior de un compuesto de fórmula (IIb) en el que R11 es hidrógeno en presencia de haluros de ácido carboxílico y una base que da como resultado compuestos de fórmula (IIb) en donde R11 es COR12, en donde R12 es hidrógeno, o alquilo C1-C3 lineal o ramificado.
8. Un proceso de acuerdo con la reivindicación 6 que comprende la oxidación posterior de un compuesto de fórmula (IIb) en presencia de un agente oxidante que da como resultado compuestos de fórmula (IIIb).
en donde
R1 es hidrógeno, metilo o etilo;
R2 es hidrógeno, alquilo C1-C6, o alquenilo C2-C6;
R3 es hidrógeno, metilo o etilo;
R4 , R5 , R6 , R7 , R8 y R9 se seleccionan independientemente de hidrógeno, alquilo C1-C6, o alquenilo C2-C6; y R10 es lineal o ramificado alquilo C1-C5, o alquenilo C2-C5 lineal o ramificado.
9. Un proceso de acuerdo con la reivindicación 1 o la reivindicación 8 que comprende la transformación posterior del grupo carbonilo de un compuesto seleccionado entre compuestos de fórmulas (Ib) y (IIIb) en presencia de a) hidroxilamina;
b) metanol o etanol; o
c) un diol;
dando como resultado compuestos de fórmula (IVb)
en donde
R1 es hidrógeno, metilo o etilo;
R2 es hidrógeno, alquilo C1-C6, o alquenilo C2-C6;
R3 es hidrógeno, metilo o etilo;
R4 , R5 , R6 , R7 , R8 y R9 se seleccionan independientemente de hidrógeno, alquilo C1-C6, o alquenilo C2-C6; y R10 es hidrógeno, alquilo C1-C5 lineal o ramificado, o alquenilo C2-C5 lineal o ramificado;
R y R 'se seleccionan entre metoxi y etoxi; o
R y R' se forman junto con el átomo de carbono al que están unidos dioxolan, dioxano o C=N-OH.
10. Compuestos de fórmula (IVa)
en donde
R1 es hidrógeno o etilo;
R2 es hidrógeno, alquilo C1-C6, o alquenilo C2-C6;
R3 es hidrógeno, metilo o etilo;
R4 , R5 , R6 , R7 , R8 y R9 se seleccionan independientemente de hidrógeno, alquilo C1-C6, o alquenilo C2-C6; y R10 es hidrógeno, alquilo C1-C5 lineal o ramificado, o alquenilo C2-C5 lineal o ramificado;
R es hidrógeno y R 'es hidroxilo;
R y R 'se seleccionan entre metoxi y etoxi; o
R y R ' se forman junto con el átomo de carbono al que están unidos dioxolan, dioxano, carbonilo o C=N-OH; con la condición de que 1-formil-3-metil-1-vinilciclohex-3-eno, 4-(dimetoximetil)-1-metil-4-vinilciclohex-1-eno y compuesto (s) de fórmula (IVa) en donde R1, R4 a R6, R8 y R9 son hidrógeno, R7 es metilo y las formas R R' junto con el átomo de carbono al que están unidos se excluyen de un grupo carbonilo o R es hidrógeno y R' es hidroxilo.
11. Compuestos de fórmula (IVa) según la reivindicación 10 seleccionados entre
2.4- dimetil-1-vinilciclohex-3-enocarbaldehído,
(2,4-dimetil-1 -vinilciclohex-3-enil) metanol,
(2,4-dimetil-1 -vinilciclohex-3-enil) etanol,
1 -(2,4-dimetil-1 -vinilciclohex-3-enil) etanona,
(2,4-dimetil-1 -vinilciclohex-3-enil) but-3-en-1 -ol,
(2,4-dimetil-1 -vinilciclohex-3-enil) but-3-en-1 -ona,
1 -(buta-1,3-dienil) -2,4-dimetilciclohex-3-enocarbaldehído,
3.4- dimetil-1-vinilciclohex-3-enocarbaldehído,
2-metil-1 -(2-metilprop-1 -enil)ciclohex-3-enocarbaldehído,
2.4- dimetil-1 -(2-metilprop-1 -enil)ciclohex-3-enocarbaldehído,
1 -(2,4-dimetil-1 -(2-metilprop-1 -enil)ciclohex-3-enil) etanol,
4.5- dimetil-2-(2-metilprop-1 -enil) -1 -vinilciclohex-3-enocarbaldehído,
2-metil-4-(4-metilpent-3-enil) -1-vinilciclohex-3-enocarbaldehído,
oxima de 4-metil-1 -vinil-ciclohex-3-enocarbaldehído,
oxima de 3-metil-1 -vinil-ciclohex-3-eno-carbaldehído,
1 -(but-1 -enil) -2,4-dimetilciclohex-3-enocarbaldehído,
y 1-vinilciclohex-3-eno carbaldehído.
12. 1 -ciclopentenil-2,4-dimetilciclohex-3-enocarbaldehído.
13. El uso como aroma o fragancia de un compuesto seleccionado entre 1-ciclopentenil-2,4-dimetilciclohex-3-enocarbaldehído y un compuesto de fórmula (IVa)
en donde
R1 es hidrógeno o etilo;
R2 es hidrógeno, alquilo C1-C6, o alquenilo C2-C6;
R3 es hidrógeno, metilo o etilo;
R4, R5, R6, R7, R8 y R9 se seleccionan independientemente de hidrógeno, alquilo C1-C6, o alquenilo C2-C6; y
R10 es hidrógeno, alquilo C1-C5 lineal o ramificado, o alquenilo C2-C5 lineal o ramificado;
R es hidrógeno y R 'es hidroxilo;
R y R' se seleccionan entre metoxi y etoxi; o
R y R' se forman junto con el átomo de carbono al que están unidos dioxolan, carbonilo, dioxano o C=N-OH; con la condición de que el (los) compuesto (s) de fórmula (IVa) en donde R1, R4 a R6 , R8 y R9 son hidrógeno, R7 es metilo y las formas R R' junto con el átomo de carbono al que están unidos se excluyen de un grupo carbonilo o R es hidrógeno y R' es hidroxilo.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB0715496.6A GB0715496D0 (en) | 2007-08-10 | 2007-08-10 | Novel process |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2900863T3 true ES2900863T3 (es) | 2022-03-18 |
Family
ID=38543274
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES16181761T Active ES2900863T3 (es) | 2007-08-10 | 2008-08-07 | Derivados de ciclohexeno y su uso como odorante |
Country Status (9)
| Country | Link |
|---|---|
| US (2) | US8304380B2 (es) |
| EP (2) | EP3112338B1 (es) |
| JP (1) | JP5563454B2 (es) |
| CN (1) | CN101796013B (es) |
| BR (1) | BRPI0815373B1 (es) |
| ES (1) | ES2900863T3 (es) |
| GB (1) | GB0715496D0 (es) |
| MX (1) | MX2010001478A (es) |
| WO (1) | WO2009021342A2 (es) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB0715496D0 (en) * | 2007-08-10 | 2007-09-19 | Givauden Sa | Novel process |
| GB201013474D0 (en) * | 2010-08-11 | 2010-09-22 | Givaudan Sa | Organic compounds |
| DE102011005947A1 (de) * | 2011-03-23 | 2012-09-27 | Henkel Ag & Co. Kgaa | Diels-Alder-Addukte als thermisch spaltbare Riechstoffvorläufer |
| GB201201287D0 (en) * | 2012-01-26 | 2012-03-07 | Givaudan Sa | Compositions |
| WO2015148743A1 (en) * | 2014-03-26 | 2015-10-01 | The Procter & Gamble Company | Perfume systems |
| CN104433927B (zh) * | 2014-10-23 | 2017-11-10 | 广东比伦生活用纸有限公司 | 一种手帕纸的加香工艺及制得的香味手帕纸 |
| GB201613013D0 (en) * | 2016-07-27 | 2016-09-07 | Givaudan Sa | Organic compound |
| CN109651149B (zh) * | 2017-10-11 | 2021-06-01 | 中国科学院大连化学物理研究所 | 一种制备1,2-环己烷二甲酸酯或邻苯二甲酸酯的方法 |
| CN111495289B (zh) * | 2020-04-27 | 2021-01-12 | 肇庆市高要华新香料有限公司 | 一种气液两相连续反应装置及山梨醛的制备方法 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3067244A (en) * | 1958-03-06 | 1962-12-04 | Shell Oil Co | Process for the production of dielsalder adducts |
| US3641156A (en) * | 1968-04-29 | 1972-02-08 | Hoffmann La Roche | Juvabione and derivatives thereof |
| NL7304990A (es) | 1972-05-01 | 1973-11-05 | ||
| US4010207A (en) | 1976-01-15 | 1977-03-01 | International Flavors & Fragrances Inc. | Process for the alkylation of α, β-unsaturated aldehydes |
| GB1591342A (en) | 1976-08-11 | 1981-06-17 | Int Flavors & Fragrances Inc | Carbonyl compounds processes for preparing same and uses of such carbonyl compounds in affecting the aroma and taste of foodstuffs robaccos beverages perfumes and perfumed articles |
| JPH0657120B2 (ja) * | 1986-11-18 | 1994-08-03 | 長谷川香料株式会社 | 持続性紫蘇フレーバー剤 |
| DE19961030A1 (de) | 1999-12-16 | 2001-06-21 | Haarmann & Reimer Gmbh | Aromen und Aromakompositionen enthaltend 4,8-Dimethyl-3,7-nonadien-2-on und ein Verfahren zu dessen Herstellung |
| JP2002179509A (ja) | 2000-12-12 | 2002-06-26 | Takasago Internatl Corp | 抗カビ香料組成物 |
| US20050191257A1 (en) | 2004-02-27 | 2005-09-01 | John Brahms | Dry deodorant containing a sesquiterpene alcohol and zinc oxide |
| GB0715496D0 (en) * | 2007-08-10 | 2007-09-19 | Givauden Sa | Novel process |
-
2007
- 2007-08-10 GB GBGB0715496.6A patent/GB0715496D0/en not_active Ceased
-
2008
- 2008-08-07 EP EP16181761.4A patent/EP3112338B1/en active Active
- 2008-08-07 JP JP2010519318A patent/JP5563454B2/ja active Active
- 2008-08-07 BR BRPI0815373-6A patent/BRPI0815373B1/pt active IP Right Grant
- 2008-08-07 CN CN200880102957XA patent/CN101796013B/zh active Active
- 2008-08-07 MX MX2010001478A patent/MX2010001478A/es active IP Right Grant
- 2008-08-07 ES ES16181761T patent/ES2900863T3/es active Active
- 2008-08-07 WO PCT/CH2008/000337 patent/WO2009021342A2/en not_active Ceased
- 2008-08-07 EP EP08772908A patent/EP2188242A2/en not_active Withdrawn
- 2008-08-07 US US12/672,603 patent/US8304380B2/en not_active Expired - Fee Related
-
2012
- 2012-10-08 US US13/647,161 patent/US8691746B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| MX2010001478A (es) | 2010-03-01 |
| US20130035278A1 (en) | 2013-02-07 |
| US8304380B2 (en) | 2012-11-06 |
| EP2188242A2 (en) | 2010-05-26 |
| GB0715496D0 (en) | 2007-09-19 |
| BRPI0815373B1 (pt) | 2018-01-02 |
| US20100204084A1 (en) | 2010-08-12 |
| BRPI0815373A2 (pt) | 2015-02-10 |
| US8691746B2 (en) | 2014-04-08 |
| EP3112338A2 (en) | 2017-01-04 |
| WO2009021342A3 (en) | 2009-07-30 |
| EP3112338B1 (en) | 2021-09-29 |
| JP2010535718A (ja) | 2010-11-25 |
| EP3112338A3 (en) | 2017-03-22 |
| CN101796013A (zh) | 2010-08-04 |
| CN101796013B (zh) | 2013-09-04 |
| WO2009021342A2 (en) | 2009-02-19 |
| JP5563454B2 (ja) | 2014-07-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2900863T3 (es) | Derivados de ciclohexeno y su uso como odorante | |
| JP6423972B2 (ja) | シクロヘキセノンの合成方法および香料製造におけるその使用 | |
| CN1333059C (zh) | 用作发香成分的螺环化合物 | |
| US7687452B2 (en) | Organic compounds | |
| US7812195B2 (en) | Cyclohexenyl butenones and fragrance compositions comprising them | |
| US6177400B1 (en) | Unsaturated ketones and their use in perfumery | |
| BRPI0812460B1 (pt) | "organic compounds". | |
| US20260078080A1 (en) | Dimethylbicycloheptenyl and dimethylbicycloheptanyl derivatives and their use as odorants | |
| EP1706366B1 (en) | BICYCLO[3.3.1]NONANES AND BICYCLO[3.3.1ßNONENES AND THEIR USE AS FLAVOUR OR FRAGRANCE INGREDIENT | |
| CN102369179B (zh) | 作为紫罗兰和/或木质添味剂的羧酸衍生物 | |
| HK1064699B (en) | Spiro compounds as perfuming ingredients |