ES2901712T3 - Combinación de un inhibidor de pi3k y un inhibidor de c-met. - Google Patents
Combinación de un inhibidor de pi3k y un inhibidor de c-met. Download PDFInfo
- Publication number
- ES2901712T3 ES2901712T3 ES13751058T ES13751058T ES2901712T3 ES 2901712 T3 ES2901712 T3 ES 2901712T3 ES 13751058 T ES13751058 T ES 13751058T ES 13751058 T ES13751058 T ES 13751058T ES 2901712 T3 ES2901712 T3 ES 2901712T3
- Authority
- ES
- Spain
- Prior art keywords
- met
- pharmaceutically acceptable
- combination
- compound
- hgf
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000003112 inhibitor Substances 0.000 title claims description 39
- 229940043441 phosphoinositide 3-kinase inhibitor Drugs 0.000 title description 25
- 239000012828 PI3K inhibitor Substances 0.000 title description 11
- 150000001875 compounds Chemical class 0.000 claims abstract description 140
- 150000003839 salts Chemical class 0.000 claims abstract description 83
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims abstract description 73
- 201000010099 disease Diseases 0.000 claims abstract description 69
- 238000011282 treatment Methods 0.000 claims abstract description 66
- 230000002062 proliferating effect Effects 0.000 claims abstract description 64
- 230000001419 dependent effect Effects 0.000 claims abstract description 47
- 230000004913 activation Effects 0.000 claims abstract description 37
- 230000019491 signal transduction Effects 0.000 claims abstract description 23
- 230000003321 amplification Effects 0.000 claims abstract description 22
- 238000003199 nucleic acid amplification method Methods 0.000 claims abstract description 22
- 230000035772 mutation Effects 0.000 claims abstract description 20
- 230000003305 autocrine Effects 0.000 claims abstract description 17
- 230000003076 paracrine Effects 0.000 claims abstract description 17
- 125000000339 4-pyridyl group Chemical group N1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 claims abstract description 15
- 230000008482 dysregulation Effects 0.000 claims abstract description 15
- 230000001747 exhibiting effect Effects 0.000 claims abstract description 15
- 230000002018 overexpression Effects 0.000 claims abstract description 15
- OAWXZFGKDDFTGS-BYPYZUCNSA-N (2s)-pyrrolidine-1,2-dicarboxylic acid Chemical compound OC(=O)[C@@H]1CCCN1C(O)=O OAWXZFGKDDFTGS-BYPYZUCNSA-N 0.000 claims abstract description 7
- 229940124617 receptor tyrosine kinase inhibitor Drugs 0.000 claims abstract description 7
- 206010028980 Neoplasm Diseases 0.000 claims description 131
- KXDAEFPNCMNJSK-UHFFFAOYSA-N Benzamide Chemical compound NC(=O)C1=CC=CC=C1 KXDAEFPNCMNJSK-UHFFFAOYSA-N 0.000 claims description 70
- 239000003814 drug Substances 0.000 claims description 60
- 229940124597 therapeutic agent Drugs 0.000 claims description 47
- 229940121358 tyrosine kinase inhibitor Drugs 0.000 claims description 37
- 239000005483 tyrosine kinase inhibitor Substances 0.000 claims description 37
- 150000004917 tyrosine kinase inhibitor derivatives Chemical class 0.000 claims description 37
- 201000011510 cancer Diseases 0.000 claims description 35
- 238000000034 method Methods 0.000 claims description 30
- 208000005017 glioblastoma Diseases 0.000 claims description 25
- 208000002154 non-small cell lung carcinoma Diseases 0.000 claims description 25
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 claims description 24
- 239000008194 pharmaceutical composition Substances 0.000 claims description 23
- 208000020816 lung neoplasm Diseases 0.000 claims description 16
- 206010058467 Lung neoplasm malignant Diseases 0.000 claims description 15
- 201000005202 lung cancer Diseases 0.000 claims description 15
- 108090000623 proteins and genes Proteins 0.000 claims description 15
- 125000000437 thiazol-2-yl group Chemical group [H]C1=C([H])N=C(*)S1 0.000 claims description 14
- 206010027476 Metastases Diseases 0.000 claims description 10
- 239000003937 drug carrier Substances 0.000 claims description 10
- 230000015572 biosynthetic process Effects 0.000 claims description 9
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 claims description 8
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 claims description 8
- 206010039491 Sarcoma Diseases 0.000 claims description 6
- 230000002401 inhibitory effect Effects 0.000 claims description 6
- 230000002496 gastric effect Effects 0.000 claims description 4
- 210000004072 lung Anatomy 0.000 claims description 4
- 201000001441 melanoma Diseases 0.000 claims description 4
- 208000031261 Acute myeloid leukaemia Diseases 0.000 claims description 3
- 208000009746 Adult T-Cell Leukemia-Lymphoma Diseases 0.000 claims description 3
- 208000016683 Adult T-cell leukemia/lymphoma Diseases 0.000 claims description 3
- 206010003571 Astrocytoma Diseases 0.000 claims description 3
- 208000032791 BCR-ABL1 positive chronic myelogenous leukemia Diseases 0.000 claims description 3
- 208000010833 Chronic myeloid leukaemia Diseases 0.000 claims description 3
- 206010025323 Lymphomas Diseases 0.000 claims description 3
- 206010027406 Mesothelioma Diseases 0.000 claims description 3
- 208000034578 Multiple myelomas Diseases 0.000 claims description 3
- 208000033761 Myelogenous Chronic BCR-ABL Positive Leukemia Diseases 0.000 claims description 3
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 claims description 3
- 206010035226 Plasma cell myeloma Diseases 0.000 claims description 3
- 208000008383 Wilms tumor Diseases 0.000 claims description 3
- 201000006966 adult T-cell leukemia Diseases 0.000 claims description 3
- 210000000481 breast Anatomy 0.000 claims description 3
- 210000003679 cervix uteri Anatomy 0.000 claims description 3
- 208000006990 cholangiocarcinoma Diseases 0.000 claims description 3
- 230000002357 endometrial effect Effects 0.000 claims description 3
- 210000003734 kidney Anatomy 0.000 claims description 3
- 210000004185 liver Anatomy 0.000 claims description 3
- 230000002611 ovarian Effects 0.000 claims description 3
- 210000002307 prostate Anatomy 0.000 claims description 3
- 210000001685 thyroid gland Anatomy 0.000 claims description 3
- 210000003932 urinary bladder Anatomy 0.000 claims description 3
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 claims description 2
- UTCSSFWDNNEEBH-UHFFFAOYSA-N imidazo[1,2-a]pyridine Chemical compound C1=CC=CC2=NC=CN21 UTCSSFWDNNEEBH-UHFFFAOYSA-N 0.000 claims description 2
- 210000002346 musculoskeletal system Anatomy 0.000 claims description 2
- 210000003238 esophagus Anatomy 0.000 claims 2
- 210000003128 head Anatomy 0.000 claims 2
- 210000003739 neck Anatomy 0.000 claims 2
- 102000005962 receptors Human genes 0.000 abstract description 24
- 108020003175 receptors Proteins 0.000 abstract description 24
- 108010089836 Proto-Oncogene Proteins c-met Proteins 0.000 abstract description 7
- 102000008022 Proto-Oncogene Proteins c-met Human genes 0.000 abstract description 7
- 108090000100 Hepatocyte Growth Factor Proteins 0.000 description 62
- 102000003745 Hepatocyte Growth Factor Human genes 0.000 description 61
- 241001465754 Metazoa Species 0.000 description 48
- 210000004027 cell Anatomy 0.000 description 41
- 230000000694 effects Effects 0.000 description 37
- 239000003795 chemical substances by application Substances 0.000 description 27
- 230000034994 death Effects 0.000 description 27
- 231100000517 death Toxicity 0.000 description 27
- 238000009097 single-agent therapy Methods 0.000 description 26
- 238000012360 testing method Methods 0.000 description 22
- 230000037396 body weight Effects 0.000 description 21
- 239000003981 vehicle Substances 0.000 description 18
- 239000002552 dosage form Substances 0.000 description 17
- 239000000203 mixture Substances 0.000 description 17
- 241000699670 Mus sp. Species 0.000 description 16
- 238000005259 measurement Methods 0.000 description 16
- 230000004083 survival effect Effects 0.000 description 15
- 230000005764 inhibitory process Effects 0.000 description 14
- 239000002935 phosphatidylinositol 3 kinase inhibitor Substances 0.000 description 14
- 230000004614 tumor growth Effects 0.000 description 14
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 14
- 230000004044 response Effects 0.000 description 12
- 108091007960 PI3Ks Proteins 0.000 description 11
- 102000038030 PI3Ks Human genes 0.000 description 11
- 238000002474 experimental method Methods 0.000 description 11
- 230000002195 synergetic effect Effects 0.000 description 11
- 239000002253 acid Substances 0.000 description 10
- 239000008367 deionised water Substances 0.000 description 10
- 229910021641 deionized water Inorganic materials 0.000 description 10
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 9
- 108090000430 Phosphatidylinositol 3-kinases Proteins 0.000 description 9
- 229940079593 drug Drugs 0.000 description 9
- 239000012458 free base Substances 0.000 description 9
- 239000000725 suspension Substances 0.000 description 9
- 210000004881 tumor cell Anatomy 0.000 description 9
- 230000009286 beneficial effect Effects 0.000 description 8
- 238000004364 calculation method Methods 0.000 description 8
- 230000012010 growth Effects 0.000 description 8
- 238000001325 log-rank test Methods 0.000 description 8
- 108010011536 PTEN Phosphohydrolase Proteins 0.000 description 7
- 102000014160 PTEN Phosphohydrolase Human genes 0.000 description 7
- 239000011159 matrix material Substances 0.000 description 7
- 229920000609 methyl cellulose Polymers 0.000 description 7
- 239000001923 methylcellulose Substances 0.000 description 7
- 229920000136 polysorbate Polymers 0.000 description 7
- 239000000243 solution Substances 0.000 description 7
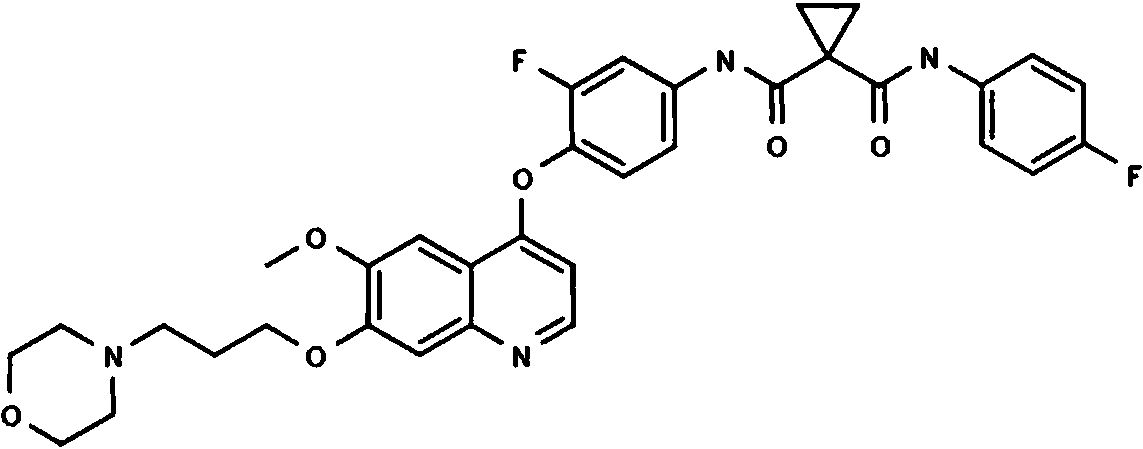
- CXQHYVUVSFXTMY-UHFFFAOYSA-N N1'-[3-fluoro-4-[[6-methoxy-7-[3-(4-morpholinyl)propoxy]-4-quinolinyl]oxy]phenyl]-N1-(4-fluorophenyl)cyclopropane-1,1-dicarboxamide Chemical compound C1=CN=C2C=C(OCCCN3CCOCC3)C(OC)=CC2=C1OC(C(=C1)F)=CC=C1NC(=O)C1(C(=O)NC=2C=CC(F)=CC=2)CC1 CXQHYVUVSFXTMY-UHFFFAOYSA-N 0.000 description 6
- 230000008859 change Effects 0.000 description 6
- 238000002648 combination therapy Methods 0.000 description 6
- 238000009472 formulation Methods 0.000 description 6
- 230000035755 proliferation Effects 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- 208000024891 symptom Diseases 0.000 description 6
- 230000001225 therapeutic effect Effects 0.000 description 6
- 206010053759 Growth retardation Diseases 0.000 description 5
- 241000699666 Mus <mouse, genus> Species 0.000 description 5
- 241000699660 Mus musculus Species 0.000 description 5
- 102000001253 Protein Kinase Human genes 0.000 description 5
- BPEGJWRSRHCHSN-UHFFFAOYSA-N Temozolomide Chemical compound O=C1N(C)N=NC2=C(C(N)=O)N=CN21 BPEGJWRSRHCHSN-UHFFFAOYSA-N 0.000 description 5
- 238000012054 celltiter-glo Methods 0.000 description 5
- 230000003831 deregulation Effects 0.000 description 5
- 235000005911 diet Nutrition 0.000 description 5
- 230000037213 diet Effects 0.000 description 5
- 230000014509 gene expression Effects 0.000 description 5
- 230000009036 growth inhibition Effects 0.000 description 5
- 231100000001 growth retardation Toxicity 0.000 description 5
- 229940043355 kinase inhibitor Drugs 0.000 description 5
- 231100000682 maximum tolerated dose Toxicity 0.000 description 5
- 238000011580 nude mouse model Methods 0.000 description 5
- 230000037361 pathway Effects 0.000 description 5
- 239000003757 phosphotransferase inhibitor Substances 0.000 description 5
- 108060006633 protein kinase Proteins 0.000 description 5
- 241000282412 Homo Species 0.000 description 4
- 241000124008 Mammalia Species 0.000 description 4
- 238000004458 analytical method Methods 0.000 description 4
- 230000001028 anti-proliverative effect Effects 0.000 description 4
- 239000002775 capsule Substances 0.000 description 4
- 239000012050 conventional carrier Substances 0.000 description 4
- KTEIFNKAUNYNJU-GFCCVEGCSA-N crizotinib Chemical compound O([C@H](C)C=1C(=C(F)C=CC=1Cl)Cl)C(C(=NC=1)N)=CC=1C(=C1)C=NN1C1CCNCC1 KTEIFNKAUNYNJU-GFCCVEGCSA-N 0.000 description 4
- 239000007884 disintegrant Substances 0.000 description 4
- 208000035475 disorder Diseases 0.000 description 4
- 238000003208 gene overexpression Methods 0.000 description 4
- 239000000314 lubricant Substances 0.000 description 4
- 210000000056 organ Anatomy 0.000 description 4
- -1 pyridin-4-yl (S)-pyrrolidine-1,2-dicarboxylic acid Chemical compound 0.000 description 4
- 230000011664 signaling Effects 0.000 description 4
- 229960004964 temozolomide Drugs 0.000 description 4
- 238000002560 therapeutic procedure Methods 0.000 description 4
- 210000001519 tissue Anatomy 0.000 description 4
- 231100000419 toxicity Toxicity 0.000 description 4
- 230000001988 toxicity Effects 0.000 description 4
- 230000003442 weekly effect Effects 0.000 description 4
- CWHUFRVAEUJCEF-UHFFFAOYSA-N BKM120 Chemical compound C1=NC(N)=CC(C(F)(F)F)=C1C1=CC(N2CCOCC2)=NC(N2CCOCC2)=N1 CWHUFRVAEUJCEF-UHFFFAOYSA-N 0.000 description 3
- 238000000846 Bartlett's test Methods 0.000 description 3
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 3
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 3
- 241000282320 Panthera leo Species 0.000 description 3
- 229920002472 Starch Polymers 0.000 description 3
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 3
- 230000002159 abnormal effect Effects 0.000 description 3
- 230000009471 action Effects 0.000 description 3
- 239000000654 additive Substances 0.000 description 3
- 230000000996 additive effect Effects 0.000 description 3
- 238000000540 analysis of variance Methods 0.000 description 3
- 230000019552 anatomical structure morphogenesis Effects 0.000 description 3
- IMHBYKMAHXWHRP-UHFFFAOYSA-N anilazine Chemical compound ClC1=CC=CC=C1NC1=NC(Cl)=NC(Cl)=N1 IMHBYKMAHXWHRP-UHFFFAOYSA-N 0.000 description 3
- 230000000259 anti-tumor effect Effects 0.000 description 3
- 238000003556 assay Methods 0.000 description 3
- 239000011230 binding agent Substances 0.000 description 3
- 239000000969 carrier Substances 0.000 description 3
- 230000003833 cell viability Effects 0.000 description 3
- 238000003570 cell viability assay Methods 0.000 description 3
- 230000001413 cellular effect Effects 0.000 description 3
- 235000019784 crude fat Nutrition 0.000 description 3
- JOGKUKXHTYWRGZ-UHFFFAOYSA-N dactolisib Chemical compound O=C1N(C)C2=CN=C3C=CC(C=4C=C5C=CC=CC5=NC=4)=CC3=C2N1C1=CC=C(C(C)(C)C#N)C=C1 JOGKUKXHTYWRGZ-UHFFFAOYSA-N 0.000 description 3
- 239000008121 dextrose Substances 0.000 description 3
- 239000003085 diluting agent Substances 0.000 description 3
- 239000000945 filler Substances 0.000 description 3
- 239000007903 gelatin capsule Substances 0.000 description 3
- 238000002513 implantation Methods 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- 239000003446 ligand Substances 0.000 description 3
- 230000009401 metastasis Effects 0.000 description 3
- 239000008108 microcrystalline cellulose Substances 0.000 description 3
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 3
- 229940016286 microcrystalline cellulose Drugs 0.000 description 3
- 150000007522 mineralic acids Chemical class 0.000 description 3
- 239000006186 oral dosage form Substances 0.000 description 3
- 238000003305 oral gavage Methods 0.000 description 3
- 150000007524 organic acids Chemical class 0.000 description 3
- 230000036961 partial effect Effects 0.000 description 3
- 239000000546 pharmaceutical excipient Substances 0.000 description 3
- 241000894007 species Species 0.000 description 3
- 235000019698 starch Nutrition 0.000 description 3
- GLBZSOQDAOLMGC-UHFFFAOYSA-N 1-(2-hydroxy-2-methylpropyl)-n-[5-(7-methoxyquinolin-4-yl)oxypyridin-2-yl]-5-methyl-3-oxo-2-phenylpyrazole-4-carboxamide Chemical compound C=1C=NC2=CC(OC)=CC=C2C=1OC(C=N1)=CC=C1NC(=O)C(C1=O)=C(C)N(CC(C)(C)O)N1C1=CC=CC=C1 GLBZSOQDAOLMGC-UHFFFAOYSA-N 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- 206010006187 Breast cancer Diseases 0.000 description 2
- 208000026310 Breast neoplasm Diseases 0.000 description 2
- 235000019750 Crude protein Nutrition 0.000 description 2
- 230000004544 DNA amplification Effects 0.000 description 2
- 206010061818 Disease progression Diseases 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- 206010064571 Gene mutation Diseases 0.000 description 2
- 101000973623 Homo sapiens Neuronal growth regulator 1 Proteins 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 2
- 208000007766 Kaposi sarcoma Diseases 0.000 description 2
- 239000002146 L01XE16 - Crizotinib Substances 0.000 description 2
- UCEQXRCJXIVODC-PMACEKPBSA-N LSM-1131 Chemical compound C1CCC2=CC=CC3=C2N1C=C3[C@@H]1C(=O)NC(=O)[C@H]1C1=CNC2=CC=CC=C12 UCEQXRCJXIVODC-PMACEKPBSA-N 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- 102100022223 Neuronal growth regulator 1 Human genes 0.000 description 2
- 229910019142 PO4 Inorganic materials 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- 206010041067 Small cell lung cancer Diseases 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 231100000230 acceptable toxicity Toxicity 0.000 description 2
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 2
- 208000026935 allergic disease Diseases 0.000 description 2
- 238000010171 animal model Methods 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 208000035269 cancer or benign tumor Diseases 0.000 description 2
- 239000001768 carboxy methyl cellulose Substances 0.000 description 2
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 2
- 150000001735 carboxylic acids Chemical class 0.000 description 2
- 230000003197 catalytic effect Effects 0.000 description 2
- 238000004113 cell culture Methods 0.000 description 2
- 230000010261 cell growth Effects 0.000 description 2
- 239000001913 cellulose Substances 0.000 description 2
- 235000010980 cellulose Nutrition 0.000 description 2
- 229920002678 cellulose Polymers 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 229960005061 crizotinib Drugs 0.000 description 2
- 230000001086 cytosolic effect Effects 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 230000002950 deficient Effects 0.000 description 2
- 230000005750 disease progression Effects 0.000 description 2
- 239000000890 drug combination Substances 0.000 description 2
- 230000008029 eradication Effects 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 239000012091 fetal bovine serum Substances 0.000 description 2
- 239000000835 fiber Substances 0.000 description 2
- 229950008692 foretinib Drugs 0.000 description 2
- 230000004077 genetic alteration Effects 0.000 description 2
- 231100000118 genetic alteration Toxicity 0.000 description 2
- 210000004602 germ cell Anatomy 0.000 description 2
- 150000004676 glycans Chemical class 0.000 description 2
- 239000003102 growth factor Substances 0.000 description 2
- 239000001963 growth medium Substances 0.000 description 2
- 150000003840 hydrochlorides Chemical class 0.000 description 2
- 239000007943 implant Substances 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 2
- 230000003834 intracellular effect Effects 0.000 description 2
- 230000031146 intracellular signal transduction Effects 0.000 description 2
- 230000009545 invasion Effects 0.000 description 2
- 238000012417 linear regression Methods 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- 239000011777 magnesium Substances 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 230000036210 malignancy Effects 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 239000002609 medium Substances 0.000 description 2
- 238000012544 monitoring process Methods 0.000 description 2
- FVLVBVSILSHUAF-UHFFFAOYSA-N n-benzyl-3,5-dimethyl-n-propan-2-ylbenzamide Chemical compound C=1C(C)=CC(C)=CC=1C(=O)N(C(C)C)CC1=CC=CC=C1 FVLVBVSILSHUAF-UHFFFAOYSA-N 0.000 description 2
- 231100000252 nontoxic Toxicity 0.000 description 2
- 230000003000 nontoxic effect Effects 0.000 description 2
- 238000007911 parenteral administration Methods 0.000 description 2
- 239000010452 phosphate Substances 0.000 description 2
- 150000003905 phosphatidylinositols Chemical class 0.000 description 2
- 229920001282 polysaccharide Polymers 0.000 description 2
- 239000005017 polysaccharide Substances 0.000 description 2
- 238000010837 poor prognosis Methods 0.000 description 2
- 229920003124 powdered cellulose Polymers 0.000 description 2
- 235000019814 powdered cellulose Nutrition 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 102000004169 proteins and genes Human genes 0.000 description 2
- 230000008707 rearrangement Effects 0.000 description 2
- 238000011069 regeneration method Methods 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 230000008844 regulatory mechanism Effects 0.000 description 2
- 238000001223 reverse osmosis Methods 0.000 description 2
- 238000005070 sampling Methods 0.000 description 2
- 238000013207 serial dilution Methods 0.000 description 2
- 208000000587 small cell lung carcinoma Diseases 0.000 description 2
- 230000000392 somatic effect Effects 0.000 description 2
- 230000003068 static effect Effects 0.000 description 2
- 238000007619 statistical method Methods 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 229960004793 sucrose Drugs 0.000 description 2
- 230000009044 synergistic interaction Effects 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 239000003826 tablet Substances 0.000 description 2
- 239000000454 talc Substances 0.000 description 2
- 235000012222 talc Nutrition 0.000 description 2
- 229910052623 talc Inorganic materials 0.000 description 2
- 238000010998 test method Methods 0.000 description 2
- 230000017423 tissue regeneration Effects 0.000 description 2
- 229950005976 tivantinib Drugs 0.000 description 2
- WEEMDRWIKYCTQM-UHFFFAOYSA-N 2,6-dimethoxybenzenecarbothioamide Chemical compound COC1=CC=CC(OC)=C1C(N)=S WEEMDRWIKYCTQM-UHFFFAOYSA-N 0.000 description 1
- 208000010507 Adenocarcinoma of Lung Diseases 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 201000001320 Atherosclerosis Diseases 0.000 description 1
- 238000012935 Averaging Methods 0.000 description 1
- 241000605059 Bacteroidetes Species 0.000 description 1
- 206010005003 Bladder cancer Diseases 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- 208000024172 Cardiovascular disease Diseases 0.000 description 1
- 206010008342 Cervix carcinoma Diseases 0.000 description 1
- 108091007958 Class I PI3Ks Proteins 0.000 description 1
- 206010009944 Colon cancer Diseases 0.000 description 1
- 108010071942 Colony-Stimulating Factors Proteins 0.000 description 1
- 208000001333 Colorectal Neoplasms Diseases 0.000 description 1
- 229920002785 Croscarmellose sodium Polymers 0.000 description 1
- 108010009392 Cyclin-Dependent Kinase Inhibitor p16 Proteins 0.000 description 1
- 102000009503 Cyclin-Dependent Kinase Inhibitor p18 Human genes 0.000 description 1
- 108010009367 Cyclin-Dependent Kinase Inhibitor p18 Proteins 0.000 description 1
- 102100024458 Cyclin-dependent kinase inhibitor 2A Human genes 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 239000004375 Dextrin Substances 0.000 description 1
- 229920001353 Dextrin Polymers 0.000 description 1
- 206010013710 Drug interaction Diseases 0.000 description 1
- 238000001061 Dunnett's test Methods 0.000 description 1
- 102000009024 Epidermal Growth Factor Human genes 0.000 description 1
- 101800003838 Epidermal growth factor Proteins 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 201000008808 Fibrosarcoma Diseases 0.000 description 1
- 206010016654 Fibrosis Diseases 0.000 description 1
- 102000003688 G-Protein-Coupled Receptors Human genes 0.000 description 1
- 108090000045 G-Protein-Coupled Receptors Proteins 0.000 description 1
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 1
- 229930182566 Gentamicin Natural products 0.000 description 1
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 description 1
- 229920002907 Guar gum Polymers 0.000 description 1
- SQUHHTBVTRBESD-UHFFFAOYSA-N Hexa-Ac-myo-Inositol Natural products CC(=O)OC1C(OC(C)=O)C(OC(C)=O)C(OC(C)=O)C(OC(C)=O)C1OC(C)=O SQUHHTBVTRBESD-UHFFFAOYSA-N 0.000 description 1
- 238000012893 Hill function Methods 0.000 description 1
- 101000605639 Homo sapiens Phosphatidylinositol 4,5-bisphosphate 3-kinase catalytic subunit alpha isoform Proteins 0.000 description 1
- 101001059454 Homo sapiens Serine/threonine-protein kinase MARK2 Proteins 0.000 description 1
- 101000727826 Homo sapiens Tyrosine-protein kinase RYK Proteins 0.000 description 1
- 229920000663 Hydroxyethyl cellulose Polymers 0.000 description 1
- 239000004354 Hydroxyethyl cellulose Substances 0.000 description 1
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 1
- 108090001061 Insulin Proteins 0.000 description 1
- 102000004877 Insulin Human genes 0.000 description 1
- 108090000723 Insulin-Like Growth Factor I Proteins 0.000 description 1
- 206010069755 K-ras gene mutation Diseases 0.000 description 1
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 208000018142 Leiomyosarcoma Diseases 0.000 description 1
- 206010050017 Lung cancer metastatic Diseases 0.000 description 1
- 208000007433 Lymphatic Metastasis Diseases 0.000 description 1
- 229940125895 MET kinase inhibitor Drugs 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 229920003091 Methocel™ Polymers 0.000 description 1
- HSHXDCVZWHOWCS-UHFFFAOYSA-N N'-hexadecylthiophene-2-carbohydrazide Chemical compound CCCCCCCCCCCCCCCCNNC(=O)c1cccs1 HSHXDCVZWHOWCS-UHFFFAOYSA-N 0.000 description 1
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 1
- 206010061309 Neoplasm progression Diseases 0.000 description 1
- 206010029113 Neovascularisation Diseases 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 206010033128 Ovarian cancer Diseases 0.000 description 1
- 206010061535 Ovarian neoplasm Diseases 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Natural products N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 239000004107 Penicillin G sodium Substances 0.000 description 1
- 102100038332 Phosphatidylinositol 4,5-bisphosphate 3-kinase catalytic subunit alpha isoform Human genes 0.000 description 1
- 108091000080 Phosphotransferase Proteins 0.000 description 1
- 101150063858 Pik3ca gene Proteins 0.000 description 1
- 108010038512 Platelet-Derived Growth Factor Proteins 0.000 description 1
- 102000010780 Platelet-Derived Growth Factor Human genes 0.000 description 1
- 102000010995 Pleckstrin homology domains Human genes 0.000 description 1
- 108050001185 Pleckstrin homology domains Proteins 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 1
- 102000001708 Protein Isoforms Human genes 0.000 description 1
- 108010029485 Protein Isoforms Proteins 0.000 description 1
- 108091008611 Protein Kinase B Proteins 0.000 description 1
- 108700020978 Proto-Oncogene Proteins 0.000 description 1
- 102000052575 Proto-Oncogene Human genes 0.000 description 1
- 239000012980 RPMI-1640 medium Substances 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 229940127361 Receptor Tyrosine Kinase Inhibitors Drugs 0.000 description 1
- 208000006265 Renal cell carcinoma Diseases 0.000 description 1
- 102000004495 STAT3 Transcription Factor Human genes 0.000 description 1
- 108010017324 STAT3 Transcription Factor Proteins 0.000 description 1
- 102100028904 Serine/threonine-protein kinase MARK2 Human genes 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 102000013275 Somatomedins Human genes 0.000 description 1
- 208000005718 Stomach Neoplasms Diseases 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 102100029759 Tyrosine-protein kinase RYK Human genes 0.000 description 1
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 description 1
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 description 1
- 240000008042 Zea mays Species 0.000 description 1
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 1
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 230000001133 acceleration Effects 0.000 description 1
- 239000008351 acetate buffer Substances 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 208000037844 advanced solid tumor Diseases 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 150000001447 alkali salts Chemical class 0.000 description 1
- 230000000172 allergic effect Effects 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- CEGOLXSVJUTHNZ-UHFFFAOYSA-K aluminium tristearate Chemical compound [Al+3].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CEGOLXSVJUTHNZ-UHFFFAOYSA-K 0.000 description 1
- 229940063655 aluminum stearate Drugs 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 230000033115 angiogenesis Effects 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 208000010668 atopic eczema Diseases 0.000 description 1
- 230000035578 autophosphorylation Effects 0.000 description 1
- 230000006399 behavior Effects 0.000 description 1
- FCPVYOBCFFNJFS-LQDWTQKMSA-M benzylpenicillin sodium Chemical compound [Na+].N([C@H]1[C@H]2SC([C@@H](N2C1=O)C([O-])=O)(C)C)C(=O)CC1=CC=CC=C1 FCPVYOBCFFNJFS-LQDWTQKMSA-M 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000008827 biological function Effects 0.000 description 1
- 230000031018 biological processes and functions Effects 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 230000036765 blood level Effects 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- CJZGTCYPCWQAJB-UHFFFAOYSA-L calcium stearate Chemical compound [Ca+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CJZGTCYPCWQAJB-UHFFFAOYSA-L 0.000 description 1
- 239000008116 calcium stearate Substances 0.000 description 1
- 235000013539 calcium stearate Nutrition 0.000 description 1
- 239000007894 caplet Substances 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 239000012876 carrier material Substances 0.000 description 1
- 239000006143 cell culture medium Substances 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 230000032823 cell division Effects 0.000 description 1
- 230000004709 cell invasion Effects 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 230000010307 cell transformation Effects 0.000 description 1
- 230000033077 cellular process Effects 0.000 description 1
- 230000036755 cellular response Effects 0.000 description 1
- 208000026106 cerebrovascular disease Diseases 0.000 description 1
- 201000010881 cervical cancer Diseases 0.000 description 1
- 230000035605 chemotaxis Effects 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 239000008119 colloidal silica Substances 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 235000005822 corn Nutrition 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 229960001681 croscarmellose sodium Drugs 0.000 description 1
- 229960000913 crospovidone Drugs 0.000 description 1
- 229920006037 cross link polymer Polymers 0.000 description 1
- 235000010947 crosslinked sodium carboxy methyl cellulose Nutrition 0.000 description 1
- 239000000824 cytostatic agent Substances 0.000 description 1
- 230000001085 cytostatic effect Effects 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- 229940127089 cytotoxic agent Drugs 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 229950006418 dactolisib Drugs 0.000 description 1
- 238000007405 data analysis Methods 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 229940096516 dextrates Drugs 0.000 description 1
- 235000019425 dextrin Nutrition 0.000 description 1
- 235000013681 dietary sucrose Nutrition 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- GXGAKHNRMVGRPK-UHFFFAOYSA-N dimagnesium;dioxido-bis[[oxido(oxo)silyl]oxy]silane Chemical compound [Mg+2].[Mg+2].[O-][Si](=O)O[Si]([O-])([O-])O[Si]([O-])=O GXGAKHNRMVGRPK-UHFFFAOYSA-N 0.000 description 1
- 238000006471 dimerization reaction Methods 0.000 description 1
- 239000001177 diphosphate Substances 0.000 description 1
- 239000008298 dragée Substances 0.000 description 1
- 230000000857 drug effect Effects 0.000 description 1
- 229940126534 drug product Drugs 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 229940116977 epidermal growth factor Drugs 0.000 description 1
- 102000052116 epidermal growth factor receptor activity proteins Human genes 0.000 description 1
- 108700015053 epidermal growth factor receptor activity proteins Proteins 0.000 description 1
- 230000007705 epithelial mesenchymal transition Effects 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 230000004761 fibrosis Effects 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 206010017758 gastric cancer Diseases 0.000 description 1
- 238000012224 gene deletion Methods 0.000 description 1
- 229960002518 gentamicin Drugs 0.000 description 1
- 210000004907 gland Anatomy 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 238000000227 grinding Methods 0.000 description 1
- 239000000665 guar gum Substances 0.000 description 1
- 235000010417 guar gum Nutrition 0.000 description 1
- 229960002154 guar gum Drugs 0.000 description 1
- 201000010536 head and neck cancer Diseases 0.000 description 1
- 208000014829 head and neck neoplasm Diseases 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 230000002489 hematologic effect Effects 0.000 description 1
- 206010073071 hepatocellular carcinoma Diseases 0.000 description 1
- 231100000844 hepatocellular carcinoma Toxicity 0.000 description 1
- 239000000833 heterodimer Substances 0.000 description 1
- 230000003054 hormonal effect Effects 0.000 description 1
- 235000019447 hydroxyethyl cellulose Nutrition 0.000 description 1
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 1
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 1
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 1
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 1
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 1
- 208000026278 immune system disease Diseases 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 208000027866 inflammatory disease Diseases 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- CDAISMWEOUEBRE-GPIVLXJGSA-N inositol Chemical compound O[C@H]1[C@H](O)[C@@H](O)[C@H](O)[C@H](O)[C@@H]1O CDAISMWEOUEBRE-GPIVLXJGSA-N 0.000 description 1
- 229960000367 inositol Drugs 0.000 description 1
- 229940125396 insulin Drugs 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 235000015110 jellies Nutrition 0.000 description 1
- 239000008274 jelly Substances 0.000 description 1
- 230000003907 kidney function Effects 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 208000019423 liver disease Diseases 0.000 description 1
- 230000003908 liver function Effects 0.000 description 1
- 230000004807 localization Effects 0.000 description 1
- 238000011866 long-term treatment Methods 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- 201000005249 lung adenocarcinoma Diseases 0.000 description 1
- 208000037841 lung tumor Diseases 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- ZLNQQNXFFQJAID-UHFFFAOYSA-L magnesium carbonate Chemical compound [Mg+2].[O-]C([O-])=O ZLNQQNXFFQJAID-UHFFFAOYSA-L 0.000 description 1
- 239000001095 magnesium carbonate Substances 0.000 description 1
- 229910000021 magnesium carbonate Inorganic materials 0.000 description 1
- 239000000391 magnesium silicate Substances 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 235000019793 magnesium trisilicate Nutrition 0.000 description 1
- 229940099273 magnesium trisilicate Drugs 0.000 description 1
- 229910000386 magnesium trisilicate Inorganic materials 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 230000010311 mammalian development Effects 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 238000002483 medication Methods 0.000 description 1
- 238000007909 melt granulation Methods 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 230000004066 metabolic change Effects 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 230000004899 motility Effects 0.000 description 1
- YOHYSYJDKVYCJI-UHFFFAOYSA-N n-[3-[[6-[3-(trifluoromethyl)anilino]pyrimidin-4-yl]amino]phenyl]cyclopropanecarboxamide Chemical compound FC(F)(F)C1=CC=CC(NC=2N=CN=C(NC=3C=C(NC(=O)C4CC4)C=CC=3)C=2)=C1 YOHYSYJDKVYCJI-UHFFFAOYSA-N 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 210000005170 neoplastic cell Anatomy 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 102000037979 non-receptor tyrosine kinases Human genes 0.000 description 1
- 108091008046 non-receptor tyrosine kinases Proteins 0.000 description 1
- 231100000590 oncogenic Toxicity 0.000 description 1
- 230000002246 oncogenic effect Effects 0.000 description 1
- 238000011275 oncology therapy Methods 0.000 description 1
- 238000001543 one-way ANOVA Methods 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 201000008968 osteosarcoma Diseases 0.000 description 1
- 201000010279 papillary renal cell carcinoma Diseases 0.000 description 1
- 235000019369 penicillin G sodium Nutrition 0.000 description 1
- 229940056360 penicillin g Drugs 0.000 description 1
- 229940124531 pharmaceutical excipient Drugs 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 230000003285 pharmacodynamic effect Effects 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 238000009520 phase I clinical trial Methods 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 125000001095 phosphatidyl group Chemical group 0.000 description 1
- 150000003904 phospholipids Chemical class 0.000 description 1
- DCWXELXMIBXGTH-QMMMGPOBSA-N phosphonotyrosine Chemical group OC(=O)[C@@H](N)CC1=CC=C(OP(O)(O)=O)C=C1 DCWXELXMIBXGTH-QMMMGPOBSA-N 0.000 description 1
- 230000026731 phosphorylation Effects 0.000 description 1
- 238000006366 phosphorylation reaction Methods 0.000 description 1
- 102000020233 phosphotransferase Human genes 0.000 description 1
- 230000035790 physiological processes and functions Effects 0.000 description 1
- 230000036470 plasma concentration Effects 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 235000013809 polyvinylpolypyrrolidone Nutrition 0.000 description 1
- 229920000523 polyvinylpolypyrrolidone Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 208000005069 pulmonary fibrosis Diseases 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 238000001959 radiotherapy Methods 0.000 description 1
- 102000027426 receptor tyrosine kinases Human genes 0.000 description 1
- 108091008598 receptor tyrosine kinases Proteins 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 230000008929 regeneration Effects 0.000 description 1
- 230000012760 regulation of cell migration Effects 0.000 description 1
- 201000009410 rhabdomyosarcoma Diseases 0.000 description 1
- 238000009666 routine test Methods 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- CDAISMWEOUEBRE-UHFFFAOYSA-N scyllo-inosotol Natural products OC1C(O)C(O)C(O)C(O)C1O CDAISMWEOUEBRE-UHFFFAOYSA-N 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 230000000391 smoking effect Effects 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- 239000008279 sol Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 235000010356 sorbitol Nutrition 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 201000011549 stomach cancer Diseases 0.000 description 1
- 229960002385 streptomycin sulfate Drugs 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 239000007940 sugar coated tablet Substances 0.000 description 1
- 238000009495 sugar coating Methods 0.000 description 1
- 150000003460 sulfonic acids Chemical class 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 206010042863 synovial sarcoma Diseases 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 229940061353 temodar Drugs 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 238000010361 transduction Methods 0.000 description 1
- 230000026683 transduction Effects 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 230000009261 transgenic effect Effects 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- 230000014616 translation Effects 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- 238000011269 treatment regimen Methods 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- 235000019731 tricalcium phosphate Nutrition 0.000 description 1
- 239000001226 triphosphate Substances 0.000 description 1
- 230000005751 tumor progression Effects 0.000 description 1
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 1
- 201000005112 urinary bladder cancer Diseases 0.000 description 1
- VBEQCZHXXJYVRD-GACYYNSASA-N uroanthelone Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CS)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)C(C)C)[C@@H](C)O)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CCSC)NC(=O)[C@H](CS)NC(=O)[C@@H](NC(=O)CNC(=O)CNC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CS)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CS)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O)C(C)C)[C@@H](C)CC)C1=CC=C(O)C=C1 VBEQCZHXXJYVRD-GACYYNSASA-N 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
- 238000003026 viability measurement method Methods 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/53—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with three nitrogens as the only ring hetero atoms, e.g. chlorazanil, melamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4738—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4745—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems condensed with ring systems having nitrogen as a ring hetero atom, e.g. phenantrolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/427—Thiazoles not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/4439—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. omeprazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/4545—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a six-membered ring with nitrogen as a ring hetero atom, e.g. pipamperone, anabasine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4709—Non-condensed quinolines and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene or sparfloxacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Landscapes
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Oncology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Hematology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
Una combinación farmacéutica que comprende (a) la 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1- dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (S)-pirrolidin-1,2-dicarboxílico (COMPUESTO D), o una sal farmacéuticamente aceptable de esta, y (b) al menos un inhibidor de la tirosina cinasa de tipo receptor c-Met, o una sal farmacéuticamente aceptable de este, para su uso en el tratamiento de una enfermedad proliferativa que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met mediante la sobreexpresión o amplificación del gen HGF / c-Met, la activación paracrina y autocrina dependiente de HGF y/o la activación del receptor c-Met mediante una mutación genética.
Description
DESCRIPCIÓN
Combinación de un inhibidor de PI3K y un inhibidor de c-Met
Campo de la invención
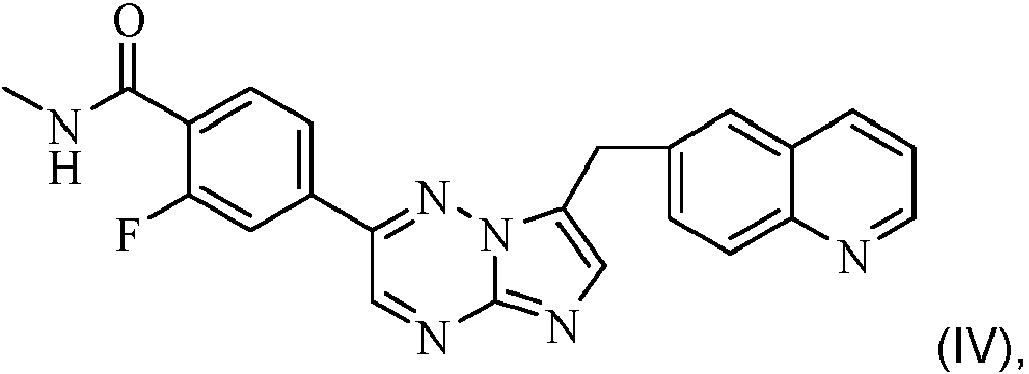
La presente invención se refiere a una combinación farmacéutica que comprende (a) un inhibidor de fosfatidilinositol 3-cinasa, la 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (SJ-pirrolidin-1,2-dicarboxílico (COMPUESTO D), o una sal farmacéuticamente aceptable de esta, y (b) al menos un inhibidor de la tirosina cinasa de tipo receptor c-Met, o una sal farmacéuticamente aceptable de este, para su uso en el tratamiento de una enfermedad proliferativa que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met mediante la sobreexpresión o amplificación del gen HGF / c-Met, la activación paracrina y autocrina dependiente de HGF y/o la activación del receptor c-Met mediante una mutación genética. La presente invención también se refiere a una composición farmacéutica que comprende tal combinación farmacéutica y un portador farmacéuticamente aceptable; una combinación farmacéutica que comprende el COMPUESTO D, o una sal farmacéuticamente aceptable de este, y 2-fluoro-N-metil-4-[7-quinolin-6-il-metil)imidazo[1,2-b][1,2,4]triazin-2-il]benzamida, o una sal farmacéuticamente aceptable de esta; y el COMPUESTO D para su uso en el tratamiento de una enfermedad proliferativa que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met mediante la sobreexpresión o amplificación del gen HGF / c-Met, la activación paracrina y autocrina dependiente de HGF y/o la activación del receptor c-Met mediante una mutación genética en combinación con al menos un inhibidor de la tirosina cinasa de tipo receptor c-Met, o una sal farmacéuticamente aceptable de este. También se refiere a un inhibidor de la tirosina cinasa de tipo receptor c-Met que es 2-fluoro-N-metil-4-[7-quinolin-6-il-metil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida, o una sal farmacéuticamente aceptable de esta, para su uso en el tratamiento de una enfermedad proliferativa que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met mediante la sobreexpresión o amplificación del gen HGF / c-Met, la activación paracrina y autocrina dependiente de HGF y/o la activación del receptor c-Met mediante una mutación genética, en combinación con el COMPUESTO D, o una sal farmacéuticamente aceptable de este.
Antecedentes
Las proteínas cinasas (PK, por sus siglas en inglés) son un grupo de enzimas que regulan diversos e importantes procesos biológicos que incluyen el crecimiento, supervivencia y diferenciación celulares, formación y morfogénesis de órganos, neovascularización, reparación y regeneración de tejidos, entre otros. Las proteínas cinasas ejercen sus funciones fisiológicas catalizando la fosforilación de proteínas (o sustratos) y de este modo modulan las actividades celulares de los sustratos en varios contextos biológicos.
Las proteínas cinasas se pueden clasificar como de tipo receptor y de tipo no receptor. Las tirosina cinasas de tipo receptor (RTK, por sus siglas en inglés) poseen una porción extracelular, un dominio de transmembrana y una porción intracelular, mientras que las tirosina cinasas de tipo no receptor son completamente intracelulares. La transducción de señales mediada por RTK se inicia normalmente mediante una interacción extracelular con un factor de crecimiento específico (ligando), que normalmente va seguida por una dimerización del receptor, estimulación de la actividad de la proteína tirosina cinasa intrínseca y transfosforilación del receptor. Por lo tanto, se crean sitios de unión para las moléculas de transducción de señales intracelulares y esto conduce a la formación de complejos con una gama de moléculas de señalización citoplásmicas que facilitan la respuesta celular adecuada tal como la división y diferenciación celular, efectos metabólicos y cambios en el microentorno extracelular. Las tirosina cinasas de tipo no receptor también se componen de numerosas subfamilias, que incluyen Src, Btk, Abl, Fak y Jak.
c-Met, un protooncogén, es un miembro de una subfamilia distintiva de tirosina cinasas de tipo receptor heterodiméricas que incluyen Met, Ron y Sea (Birchmeier, C. et al., Nat. Rev. Mol. Cell Biol. 2003, 4(12):915-925; Christensen, J. G. et al., Cáncer Lett. 2005, 225(1):1-26). El único ligando de alta afinidad para c-Met es el factor de crecimiento de hepatocitos (HGF), también conocido como factor disperso (SF). La unión de HGF a c-Met induce la activación del receptor mediante la autofosforilación, lo cual provoca un incremento de la señalización dependiente del receptor. Tanto c-Met como HGF se expresan de forma generalizada en varios órganos, pero su expresión se encuentra normalmente confinada a las células de origen epitelial y mesenquimal, respectivamente. Las funciones biológicas de c-MET (o vía de señalización de c-MET) en tejidos normales y neoplasias malignas humanas tales como el cáncer se han documentado extensivamente (Christensen, J.G. et al., Cáncer Lett. 2005, 225(1):1-26; Corso, S. et al., Trends in Mol. Med. 2005, 11(6):284-292).
Tanto HGF como c-Met son necesarios para el desarrollo normal de los mamíferos y las anomalías manifestadas en ratones con supresión tanto de HGF como de c-Met son coherentes con la proximidad de la expresión embriónica y defectos de transición epithelial-mesenquimales durante la morfogénesis de los órganos (Christensen, J.G. et al., Cancer Lett. 2005, 225(1):1-26). De forma coherente con estas observaciones, se ha demostrado que la transducción de la señalización y los efectos biológicos posteriores de la vía de HGF/c-Met son importantes para la interacción epitelialmesenquimal y la regulación de la migración e invasión celular, la proliferación y supervivencia celular, angiogénesis, morfogénesis y organización de las estructuras tubulares tridimensionales (por ejemplo, formación de glándulas, células
tubulares renales) durante el desarrollo. Las consecuencias específicas de la activación de la vía de c-Met en una célula/tejido determinado dependen en gran medida del contexto.
Los datos muestran que una vía de c-Met desregulada desempeña una función importante y, a veces, es la causante (en el caso de alteraciones genéticas) de la formación, crecimiento, mantenimiento y evolución de los tumores (Birchmeier, C. et al., Nat. Rev. Mol. Cell. Biol. 2003, 4(12):915-925; Boccaccio, C. et al., Nat. Rev. Cáncer 2006, 6(8):637-645; Christensen, J.G. et al., Cancer Lett. 2005, 225(1):1-26). HGF y/o c-Met se sobreexpresan en porciones significativas de la mayoría de los cánceres humanos y, a menudo, se asocian con resultados clínicos deficientes, tales como una enfermedad más agresiva, progresión de la enfermedad, metástasis tumorales y una menor supervivencia del paciente. Además, los pacientes con niveles elevados de proteínas HGF/c-Met son más resistentes a la quimioterapia y radioterapia. Además de la expresión anómala de HGF/c-Met, el receptor c-Met también se puede activar en pacientes con cáncer a través de mutaciones genéticas (tanto de la línea germinal como somática) y amplificación de genes. Aunque la amplificación y las mutaciones de genes son las alteraciones genéticas más comunes que han sido reseñadas en los pacientes, el receptor también puede activarse mediante deleciones, truncamientos y reordenamiento de genes, así como mediante mecanismos reguladores negativos defectuosos y un procesamiento anómalo del receptor.
Además, tras su activación, c-MET activa un número diverso de vías de señalización intracelulares, que incluyen, sin carácter limitante, la vía de fosfatidilinositol 3-cinasa (PI3K) / Akt, ERK 1 / 2, p38 y STAT3. Las PI3K comprenden una familia de serina/treonina cinasas lipídicas que catalizan la transferencia de fosfato a la posición D-3' de lípidos con inositol para producir fosfoinositol-3-fosfato (PIP), fosfoinositol-3,4-difosfato (PIP2) y fosfoinositol-3,4,5-trifosfato (PIP3) que, a su vez, actúan como segundos mensajeros en las cascadas de señalización acoplando proteínas que contienen dominios de homología de pleckstrina, FYVE, Phox y otros dominios de unión a fosfolípidos en una diversidad de complejos de señalización a menudo en la membrana plasmática (Vanhaesebroeck et al., Annu. Rev. Biochem 70:535 (2001); Katso et al., Annu. Rev. Cell Dev. Biol. 17:615 (2001)). De las dos PI3K de clase 1, las PI3K de clase 1A son heterodímeros compuestos de una subunidad catalítica p110 (isoformas a, p, 5) asociada constitutivamente con una subunidad reguladora que puede ser p85a, p55a, p50a, p85p o p55Y. La subclase clase 1B tiene un miembro en la familia, un heterodímero compuesto por una subunidad catalítica p110y asociada con una de las dos subunidades reguladoras, ya sea p101 o p84 (Fruman et al., Annu Rev. Biochem. 67:481 (1998); Suire et al., Curr. Biol. 15:566 (2005)). Los dominios modulares de las subunidades p85/55/50 incluyen dominios de homología de Src (SH2) que se unen a residuos de fosfotirosina en un contexto de secuencia específico en tirosina cinasas citoplasmáticas y receptoras activadas, lo que provoca la activación y localización de las PI3K de clase 1A. La PI3K de clase 1B se activa directamente mediante receptores acoplados a proteína G que se unen a un repertorio diverso de ligandos peptídicos y no peptídicos (Stephens et al., Cell 89:105 (1997)); Katso et al., Annu. Rev. Cell Dev. Biol. 17:615-675 (2001)). La vía de Pl3K es un regulador crucial de procesos celulares clave que incluyen la proliferación, supervivencia, quimiotaxis, tráfico celular, motilidad, metabolismo, respuestas inflamatorias y alérgicas, transcripción y traducción (Cantley et al., Cell64:281 (1991); Escobedo y Williams, Nature 335: 85 (1988); Fantl et al., Cell., 69: 413 (1992). Se ha demostrado que derivados de cicloaminourea 2-carboxamídicos, tales como la 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (§)-pirrolidin-1,2-dicarboxílico (COMPUESTO D), ejercen un efecto en modelos de cáncer de mama BT474 y HBCx-5 y de xenoinjerto gástrico NCI-N87 (WO2012/062694). Bartholomeusz et al. han descrito en Expert Opin. Ther. Targets 2012, 16(1), 121 que el COMPUESTO D se encuentra en ensayos clínicos de fase I en los que participan pacientes con tumores sólidos avanzados con una mutación del gen PIK3CA. Gong et al. han descrito en International journal of proteomics 2011,2011, 1, que la inhibición del crecimiento de células tumorales de pulmón H1993 se puede incrementar combinando BEZ-235 y p F-2341066. El documento US2010/267742 ha descrito una composición farmacéutica que incluye un inhibidor de la cinasa PKCp y un inhibidor de la cinasa c-met que es útil en el tratamiento del cáncer, por ejemplo, el cáncer de pulmón.
A pesar de los avances significativos en medicina y las numerosas opciones de tratamiento para pacientes con cáncer, siguen siendo necesarios agentes terapéuticos eficaces y seguros, y siguen siendo necesarias nuevas terapias combinadas que se puedan administrar para un tratamiento eficaz a largo plazo del cáncer.
Se ha descubierto ahora que una combinación farmacéutica que comprende (a) un inhibidor de fosfatidilinositol 3-cinasa, la 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (S)-pirrolidin-1,2-dicarboxílico (COMPUESTO D), o una sal farmacéuticamente aceptable de esta, y (b) al menos un inhibidor de la tirosina cinasa de tipo receptor c-Met, en particular 2-fluoro-N-meti-4-[7-quinolin-6-ilmetil)imidazo[1,2-¿][1,2,4]triazin-2il]benzamida, o una sal farmacéuticamente aceptable de esta, es particularmente eficaz para el tratamiento de una enfermedad proliferativa que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met.
Cabe esperar que el efecto antiproliferativo de esta combinación sea superior al efecto máximo que se puede conseguir con cada tipo de ingrediente por sí solo.
Compendio de la invención
La presente invención se refiere en un primer aspecto a una combinación farmacéutica que comprende (a) un inhibidor de fosfatidilinositol 3-cinasa, la 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del
ácido (SJ-pi rrolidin-1,2-dicarboxílico (COMPUESTO D), o una sal farmacéuticamente aceptable de esta, y (b) al menos un inhibidor de la tirosina cinasa de tipo receptor c-Met, o una sal farmacéuticamente aceptable de este, para su uso en el tratamiento (mediante la administración simultánea, por separado o secuencial) de una enfermedad proliferativa que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met mediante la sobreexpresión o amplificación del gen HGF / c-Met, la activación paracrina y autocrina dependiente de HGF y/o la activación del receptor c-Met mediante una mutación genética. La combinación de la invención es particularmente útil para el tratamiento del cáncer de pulmón (por ejemplo, cáncer de pulmón no microcítico) o glioblastoma.
En una realización preferida, el inhibidor de la tirosina cinasa de tipo receptor c-Met es 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-jb][1,2,4]triazin-2il]benzamida o una sal farmacéuticamente aceptable de esta.
En otro aspecto, la presente invención se refiere a la 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (SJ-pirrolidin-1,2-dicarboxílico (COMPUESTO D) para su uso en el tratamiento de una enfermedad proliferativa que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met mediante la sobreexpresión o amplificación del gen HGF / c-Met, la activación paracrina y autocrina dependiente de HGF y/o la activación del receptor c-Met mediante una mutación genética, en combinación con al menos un inhibidor de la tirosina cinasa de tipo receptor c-Met, o una sal farmacéuticamente aceptable de este.
En otro aspecto, la presente invención se refiere a un inhibidor de la tirosina cinasa de tipo receptor c-Met que es 2-fluoro-N-metil-4-[7-quinolin-6-il-metil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida, o una sal farmacéuticamente aceptable de esta, para su uso en el tratamiento de una enfermedad proliferativa que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met mediante la sobreexpresión o amplificación del gen HGF/c-Met, la activación paracrina y autocrina dependiente de HGF y/o la activación del receptor c-Met mediante una mutación genética, en combinación con la 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (SJ-pirrolidin-1,2-dicarboxílico (COMPUESTO D), o una sal farmacéuticamente aceptable de esta.
El tratamiento de una enfermedad proliferativa puede comprender inhibir la formación de metástasis. En una realización preferida, la enfermedad proliferativa es un cáncer.
En un aspecto, la invención proporciona una composición farmacéutica que comprende una cantidad, que es eficaz terapéuticamente de forma conjunta contra una enfermedad proliferativa dependiente de c-Met, de la combinación del COMPUESTO D y al menos un inhibidor de la tirosina cinasa de tipo receptor c-Met o una sal farmacéuticamente aceptable de este y uno o más portadores farmacéuticamente aceptables. Esta composición farmacéutica se puede administrar a un sujeto como una combinación fija en una única formulación o forma farmacéutica unitaria mediante cualquier vía adecuada. Como alternativa, los agentes terapéuticos se pueden administrar a un sujeto como una combinación no fija en formulaciones o composiciones farmacéuticas o formas farmacéuticas unitarias por separado y se pueden administrar ya sea de forma simultánea, concurrente o secuencial sin límites de tiempo específicos.
En un aspecto, la presente invención proporciona un envase comercial que comprende como agentes terapéuticos una combinación farmacéutica del Compuesto D y al menos una sobreexpresión o amplificación del gen c-Met, activación paracrina y autocrina dependiente de HGF y/o activación del receptor c-Met mediante una mutación genética, junto con instrucciones para la administración simultánea, por separado o secuencial de estos en el tratamiento de una enfermedad proliferativa que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met mediante la sobreexpresión o amplificación del gen HGF/c-Met, la activación paracrina y autocrina dependiente de HGF y/o la activación del receptor c-Met mediante una mutación genética. En una realización, la enfermedad proliferativa es un cáncer de pulmón (por ejemplo, cáncer de pulmón no microcítico) o glioblastoma.
En otro aspecto, la presente invención proporciona una composición farmacéutica que comprende la combinación del COMPUESTO D y al menos un inhibidor de la tirosina cinasa de tipo receptor c-Met o una sal farmacéuticamente aceptable de este y al menos un portador farmacéuticamente aceptable.
En otro aspecto más, la presente invención proporciona una combinación farmacéutica que comprende la 2-amida y 1-({4-metil-5-[2-(2,2,2-trifl uoro-1, 1 -dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (S)-pi rrolidin-1,2-dicarboxílico (COMPUESTO D) o una sal farmacéuticamente aceptable de esta y un inhibidor de la tirosina cinasa de tipo receptor c-Met, la 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)-imidazo[1,2-b][1,2,4]triazin-2il]benzamida o una sal farmacéuticamente aceptable de esta.
En otro aspecto más, la presente invención proporciona el Compuesto D para su uso en el tratamiento de una enfermedad proliferativa que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met mediante la sobreexpresión o amplificación del gen HGF/c-Met, la activación paracrina y autocrina dependiente de HGF y/o la activación del receptor c-Met mediante una mutación genética, en combinación con al menos un inhibidor de la tirosina cinasa de tipo receptor c-Met, o una sal farmacéuticamente aceptable de este.
Descripción detallada de las figuras
La Figura 1 muestra los efectos de combinar dosis del COMPUESTO C y 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida en la proliferación de modelos de tumor de glioblastoma humano H4.
La Figura 2 muestra los efectos de combinar dosis del COMPUESTO C y 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida en la proliferación de modelos de tumor de glioblastoma humano U87-MG.
La Figura 3 muestra los efectos de combinar dosis del COMPUESTO C y 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida en la proliferación de modelos de tumor de glioblastoma humano A172.
La Figura 4 muestra los efectos de combinar dosis del COMPUESTO C y 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida en la proliferación de modelos de tumor de glioblastoma humano LN229.
La Figura 5 muestra los efectos sobre el crecimiento antitumoral medio comparativo para la combinación de 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida y el COMPUESTO D en modelos de xenoinjerto de cáncer de pulmón no microcítico humano NCI-H1993 en comparación con un control de vehículo y ambas monoterapias.
Descripción detallada
La presente invención se refiere a una combinación farmacéutica que comprende (a) un inhibidor de fosfatidilinositol 3-cinasa, la 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (SJ-pirrolidin-1,2-dicarboxílico (COMPUESTO D), o una sal farmacéuticamente aceptable de esta, y (b) al menos un inhibidor de la tirosina cinasa de tipo receptor c-Met, o una sal farmacéuticamente aceptable de este, para su uso (mediante la administración simultánea, por separado o secuencial) en el tratamiento de una enfermedad proliferativa que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met mediante la sobreexpresión o amplificación del gen HGF/c-Met, la activación paracrina y autocrina dependiente de HGF y/o la activación del receptor c-Met mediante una mutación genética. La combinación de la invención es particularmente útil para el tratamiento del cáncer de pulmón (por ejemplo, cáncer de pulmón no microcítico) o glioblastoma.
Los términos generales utilizados en la presente se definen con los siguientes significados, a menos que se indique explícitamente lo contrario:
Las expresiones «que comprende» y «que incluye» se utilizan en la presente en su sentido abierto y no limitante, a menos que se indique lo contrario.
Se debe interpretar que los términos «un», «una», «el», «la» y referencias similares que se utilizan en el contexto de la descripción de la invención (especialmente en el contexto de las reivindicaciones adjuntas) cubren tanto el singular como el plural a menos que se indique lo contrario en la presente o se contradiga claramente por el contexto. Cuando se utiliza la forma del plural para compuestos, sales y similares, se considera que esto significa también un único compuesto o sal.
El término «combinación» o «combinación farmacéutica» se define en la presente de modo que se refiera a una combinación fija en una forma farmacéutica unitaria, una combinación no fija o un kit de partes para la administración combinada donde el inhibidor de fosfatidilinositol 3-cinasa 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (S)-pirrolidin-l ,2-dicarboxílico (COMPUESTO D) y el inhibidor de la tirosina cinasa de tipo receptor c-Met o una sal farmacéuticamente aceptable de este se pueden administrar independientemente al mismo tiempo o por separado dentro de intervalos de tiempo que permitan que los agentes terapéuticos muestren un efecto cooperativo, por ejemplo, sinérgico.
La expresión «combinación fija» significa que los agentes terapéuticos, por ejemplo, el inhibidor de fosfatidilinositol 3-cinasa 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (S)-pirrolidin-l,2-dicarboxílico (COMPUESTO D) y el inhibidor de la tirosina cinasa de tipo receptor c-Met, se administran a un sujeto simultáneamente en forma de una única entidad o forma farmacéutica.
La expresión «combinación no fija» significa que los agentes terapéuticos, por ejemplo, el inhibidor de fosfatidilinositol 3-cinasa 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (S)-pirrolidin-l,2-dicarboxílico (COMPUESTO D) y el inhibidor de la tirosina cinasa de tipo receptor c-Met o una sal farmacéuticamente aceptable de este, se administran ambos a un paciente como entidades o formas farmacéuticas separadas, ya sea de forma simultánea, concurrente o secuencial sin límites de tiempo específicos, donde tal administración proporciona unos niveles terapéuticamente eficaces de los compuestos en el cuerpo del sujeto, por ejemplo, un mamífero o ser humano, que lo necesite.
El término «kit de partes» se refiere a los agentes terapéuticos (a) y (b) tal como se han definido anteriormente que se dosifican independientemente o mediante el uso de diferentes combinaciones fijas con cantidades diferenciadas de los
agentes terapéuticos (a) y (b), es decir, simultáneamente o en diferentes puntos de tiempo. Las partes del kit de partes pueden administrarse entonces, por ejemplo, simultáneamente o de forma escalonada cronológicamente, es decir, en diferentes puntos de tiempo y con intervalos de tiempo iguales o diferentes para cualquier parte del kit de partes. La proporción de las cantidades totales del agente terapéutico (a) respecto al agente terapéutico (b) que se ha de administrar en el preparado combinado se puede modificar, por ejemplo, para hacer frente a las necesidades de una subpoblación de pacientes que se ha de tratar o las necesidades del paciente individual.
La expresión «un inhibidor de fosfatidilinositol 3-cinasa» o «inhibidor de PI3K» se define en la presente de modo que se refiera a un compuesto que tiene como diana, reduce o inhibe la fosfatidilinositol 3-cinasa. Se ha demostrado que la actividad de la fosfatidilinositol 3-cinasa aumenta como respuesta a una serie de estímulos hormonales y de factores de crecimiento, que incluyen la insulina, el factor de crecimiento derivado de plaquetas, factor de crecimiento similar a la insulina, factor de crecimiento epidérmico, factor estimulador de colonias y factor de crecimiento de hepatocitos, y se ha implicado en procesos relacionados con el crecimiento y la transformación celular.
La expresión «inhibidor de la tirosina cinasa de tipo receptor c-Met» se define en la presente de modo que se refiera a un compuesto que tiene como diana, reduce o inhibe la actividad de la tirosina cinasa de tipo receptor c-Met.
La expresión «enfermedad proliferativa dependiente de c-Met» o «cáncer dependiente de c-Met» se refiere a aquellas enfermedades proliferativas que presentan una desregulación de c-Met y/o la vía de señalización de HGF/c-Met, en particular una sobreexpresión y amplificación del gen HGF/c-Met, activación paracrina y autocrina dependiente de HGF y/o mutaciones genéticas del receptor c-Met (tanto de la línea germinal como somáticas). En una realización preferida, la enfermedad proliferativa es un cáncer que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met. Se pretende que la «desregulación de c-Met y/o la vía de señalización de HGF/c-Met» incluya la activación de la clase c-Met de tirosina cinasas de tipo receptor a través de varios mecanismos que incluyen, sin carácter limitante, activación paracrina y autocrina dependiente de HGF, sobreexpresión y amplificación del gen HGF/c-met, mutaciones puntuales, deleciones, truncamientos, reordenamiento, así como también procesamiento anómalo del receptor c-Met y mecanismos reguladores negativos defectuosos. En una realización preferida, la expresión «enfermedad proliferativa dependiente de c-Met» o «cáncer dependiente de c-Met» incluye la sobreexpresión y amplificación del gen HGF/c-Met.
La expresión «composición farmacéutica» se define en la presente como referente a una mezcla o solución que contiene al menos un agente terapéutico que se ha de administrar a un sujeto, por ejemplo, un mamífero o ser humano, para tratar una enfermedad o afección particular que afecta al sujeto de esta.
La expresión «farmacéuticamente aceptable» se define en la presente como referente a aquellos compuestos, materiales, composiciones y/o formas farmacéuticas que son, dentro del alcance del juicio médico razonable, adecuados para entrar en contacto con los tejidos de un sujeto, por ejemplo, un mamífero o ser humano, sin excesiva toxicidad, irritación, respuesta alérgica y otras complicaciones problemáticas proporcionales a una relación de beneficio/riesgo razonable.
El término «tratar» o «tratamiento», tal como se utiliza en la presente, comprende un tratamiento que atenúa, reduce o alivia al menos un síntoma en un sujeto o que produce un retraso del avance de una enfermedad. Por ejemplo, el tratamiento puede ser la disminución de uno o varios síntomas de un trastorno o la erradicación completa de un trastorno, tal como el cáncer. Dentro del significado de la presente invención, el término «tratar» también denota detener, retrasar el inicio (es decir, el periodo previo a la manifestación clínica de una enfermedad) y/o reducir el riesgo de desarrollar o empeorar una enfermedad.
La expresión «terapéuticamente activo de forma conjunta» o «efecto terapéutico conjunto», tal como se utiliza en la presente, significa que los agentes terapéuticos pueden administrarse por separado (de una manera escalonada cronológicamente, especialmente de una manera que siga una secuencia específica) en los intervalos de tiempo que se prefieran, en el animal de sangre caliente, especialmente un ser humano, que ha de ser tratado, y mostrar aún así una interacción (preferentemente sinérgica) (efecto terapéutico conjunto). Se puede determinar si este es el caso, entre otros, siguiendo los niveles en sangre, mostrando que ambos agentes terapéuticos están presentes en la sangre del ser humano que se ha de tratar al menos durante ciertos intervalos de tiempo.
La expresión «cantidad farmacéuticamente eficaz» o «cantidad clínicamente eficaz» de una combinación farmacéutica de agentes terapéuticos es una cantidad suficiente para proporcionar una mejora observable respecto a los signos y síntomas clínicamente observables de la línea base de la enfermedad proliferativa tratada con la combinación.
La expresión «efecto sinérgico», tal como se utiliza en la presente, se refiere a la acción de dos agentes terapéuticos tales como, por ejemplo, el COMPUESTO D o una sal farmacéuticamente aceptable de este y un inhibidor de la tirosina cinasa de tipo receptor c-Met o una sal farmacéuticamente aceptable de este, que produce un efecto, por ejemplo, la ralentización del avance sintomático de una enfermedad proliferativa, particularmente el cáncer, o sus síntomas, que es mayor que la simple adición de los efectos de cada agente terapéutico administrado por sí solo. Se puede calcular un efecto sinérgico, por ejemplo, utilizando métodos adecuados tales como la ecuación sigmoide de Emáx (Holford, N. H. G. y Scheiner, L. B., Clin. Pharmacokinet. 6: 429-453 (1981)), la ecuación de la aditividad de Loewe (Loewe, S. y Muischnek, H., Arch. Exp.
Pathol Pharmacol. 114: 313-326 (1926)) y la ecuación del efecto mediano (Chou, T. C. y Talalay, P., Adv. Enzyme Regul.
22: 27-55 (1984)). Cada ecuación mencionada anteriormente se puede aplicar a los datos experimentales para generar una gráfica correspondiente con el fin de ayudar a evaluar los efectos de la combinación farmacológica. Las gráficas correspondientes asociadas con las ecuaciones mencionadas anteriormente son la curva de concentración-efecto, la curva de isobolograma y la curva del índice de combinación, respectivamente.
El término «sujeto» o «paciente», tal como se utiliza en la presente, incluye animales que pueden padecer o estar afectados por una enfermedad proliferativa o cualquier trastorno que implique, directa o indirectamente, un tumor. Los ejemplos de sujetos incluyen mamíferos, por ejemplo, seres humanos, perros, vacas, caballos, cerdos, ovejas, cabras, gatos, ratones, conejos, ratas y animales no humanos transgénicos. En la realización preferida, el sujeto es un ser humano, por ejemplo, un ser humano que padece, que corre el riesgo de padecer o que puede padecer potencialmente una enfermedad proliferativa.
El término «aproximadamente» o «alrededor de» tendrá el significado de dentro de un 10%, más preferentemente dentro de un 5%, de un valor o intervalo dado.
Las combinaciones de la presente invención incluyen un inhibidor de PI3K, la 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (S)-pirrolidin-1,2-dicarboxílico (COMPUESTO d ) o una sal farmacéuticamente aceptable de esta.
El documento WO2010/029082 describe derivados de cicloaminourea 2-carboxamídicos específicos, que se ha descubierto que tienen una actividad inhibidora para la isoforma a de PI3K. En el documento WO2010/029082 se describe un derivado de cicloaminourea 2-carboxamídico específico, la 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (S)-pirrolidin-1,2-dicarboxílico (COMPUESTO D), que es adecuado para la combinación de la presente invención, su preparación y formulaciones adecuadas que lo contienen.
La síntesis del COMPUESTO D se describe en el documento WO2010/029082 como el Ejemplo 15.
El COMPUESTO D se puede utilizar en forma de base libre o como una sal farmacéuticamente aceptable de este. Las sales adecuadas incluyen las que se forman, por ejemplo, como sales de adición de ácido, preferentemente con ácidos orgánicos o inorgánicos, con un átomo de nitrógeno básico. Los ácidos inorgánicos adecuados son, por ejemplo, ácidos halhídricos tales como el ácido clorhídrico, ácido sulfúrico o ácido fosfórico. Los ácidos orgánicos adecuados son, por ejemplo, ácidos carboxílicos o ácidos sulfónicos, tales como el ácido fumárico o ácido metanosulfónico.
Las combinaciones de la presente invención incluyen además al menos un inhibidor de la tirosina cinasa de tipo receptor c-Met o una sal farmacéuticamente aceptable de este. Los ejemplos de un inhibidor de la tirosina cinasa de tipo receptor c-Met adecuados incluyen, sin carácter limitante, 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida, ARQ197 (tavantinib), AMG458, GSK1363089 (XL880 o foretinib), PF2341066 (crizotinib), o una sal farmacéuticamente aceptable de estos.
Preferentemente, el inhibidor de la tirosina cinasa de tipo receptor c-Met para su uso en la combinación de la presente invención es un compuesto de fórmula (IV)
o una sal farmacéuticamente aceptable de este. El compuesto de fórmula (IV) tiene el nombre químico de 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida. Este compuesto y el método para la síntesis de este compuesto se divulgan en el Ejemplo 7 de la solicitud de patente de PCT internacional WO2008/064157.
El compuesto de fórmula (IV) se puede utilizar en forma de base libre o como una sal farmacéuticamente aceptable de este. Las sales adecuadas de la 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida incluyen sales de adición de ácidos orgánicos o minerales de residuos básicos tales como aminas; sales orgánicas o alcalinas de residuos ácidos tales como ácidos carboxílicos; y similares. Las sales farmacéuticamente aceptables de la presente invención incluyen las sales atóxicas convencionales del compuesto original que se forman, por ejemplo, a partir de ácidos orgánicos o inorgánicos atóxicos. Preferentemente, el compuesto de fórmula (IV) es una forma salina divulgada en la solicitud de patente de PCT WO2009/143211. Las formas salinas preferidas del compuesto de fórmula (IV) incluyen la
forma salina de ácido diclorhídrico y la forma salina de ácido dibencenosulfónico de la 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida
Los inhibidores adecuados de la tirosina cinasa de tipo receptor c-Met incluyen además:
(i.) ARQ197 (tavantinib) (desarrollado por Daiichi Sankyo y ArQule) que tiene la estructura química:
(ii.) AMG458 (desarrollado por Amgen) que tiene la estructura química:
(iii.) GSK1363089 (también conocido como XL880 o foretinib) (desarrollado por GlaxoSmithKline) que tiene la estructura química:
y
(iv.) PF2341066 (también conocido como crizotinib) (desarrollado por Pfizer) que tiene la estructura química:
La estructura de los agentes terapéuticos identificados con números de código, denominaciones comerciales o genéricas se puede consultar en la edición actual del compendio estándar «The Merck Index» o en bases de datos, por ejemplo, Patents International (por ejemplo, IMS World Publications).
Una combinación farmacéutica que comprende (a) un inhibidor de fosfatidilinositol 3-cinasa, la 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (S)-pirrolidin-1,2-dicarboxílico (COMPUESTO D) o una sal farmacéuticamente aceptable de esta, y (b) al menos un inhibidor de la tirosina cinasa de tipo receptor c-Met o una sal farmacéuticamente aceptable de este, se denominará en lo sucesivo en la presente COMBINACIÓN DE LA INVENCIÓN.
A menos que se especifique de otro modo o que lo indique claramente el texto o que no sea aplicable, la referencia a los agentes terapéuticos útiles en la COMBINACIÓN DE LA INVENCIÓN incluye tanto la base libre de los compuestos como todas las sales farmacéuticamente aceptables de los compuestos.
En una realización preferida de la presente invención, la combinación comprende (a) un inhibidor de fosfatidilinositol 3-cinasa, el COMPUESTO D o una sal farmacéuticamente aceptable de este, y (b) 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2-il]benzamida o una sal farmacéuticamente aceptable de esta.
La COMBINACIÓN DE LA INVENCIÓN es útil para el tratamiento de una enfermedad proliferativa que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met mediante la sobreexpresión o amplificación del gen HGF/c-Met, la activación paracrina y autocrina dependiente de HGF y/o la activación del receptor c-Met mediante una mutación genética en un sujeto que lo necesite. La COMBINACIÓN DE LA INVENCIÓN se puede utilizar para el tratamiento de una enfermedad proliferativa en un sujeto que lo necesite administrando al sujeto una combinación farmacéutica que comprenda (a) una cantidad eficaz de la 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (S)-pirrolidin-l ,2-dicarboxílico (COMPUESTO D) o una sal farmacéuticamente aceptable de esta y (b) una cantidad eficaz de al menos un inhibidor de la tirosina cinasa de tipo receptor c-Met tal como 2-fluoro-N-metil-4-[7-quinolin-6-il-metil)imidazo[1,2-b][1,2,4]triazin-2-il]benzamida o una sal farmacéuticamente aceptable de esta. Preferentemente, estos agentes terapéuticos se administran con dosis terapéuticamente eficaces, las cuales, cuando se combinan, proporcionan un efecto beneficioso de forma conjunta. La administración puede ser por separado, simultánea o secuencial.
La naturaleza de las enfermedades proliferativas, particularmente enfermedades proliferativas dependientes de c-Met, es multifactorial. En ciertas circunstancias, se pueden combinar fármacos con diferentes mecanismos de acción. Sin embargo, tan solo el hecho de considerar cualquier combinación de fármacos que tengan un modo de acción diferente no conduce necesariamente a combinaciones con efectos ventajosos.
Se ha establecido que la administración de la COMBINACIÓN DE LA INVENCIÓN se puede utilizar para tratar a un sujeto que padece una enfermedad proliferativa, particularmente cáncer de pulmón (por ejemplo, cáncer de pulmón no microcítico) o glioblastoma. En la presente invención, la administración de la COMBINACIÓN De LA INVENCIÓN da como resultado un tratamiento más beneficioso, por ejemplo, un efecto antiproliferativo sinérgico o mejorado, por ejemplo, respecto al retraso del avance de una enfermedad proliferativa o respecto a un cambio en el volumen del tumor, en comparación con cualquiera de las monoterapias.
En una realización, la enfermedad proliferativa que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met es un cáncer que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met. En una realización adicional, esta enfermedad proliferativa es un cáncer que presenta una sobreexpresión y/o amplificación del gen HGF/c-Met.
Las enfermedades proliferativas dependientes de c-Met, adecuadas para el tratamiento con la COMBINACIÓN DE LA INVENCIÓN incluyen, sin carácter limitante, cánceres, aterosclerosis, fibrosis pulmonar, regeneración y fibrosis renal, enfermedades hepáticas, trastornos alérgicos, trastornos inmunitarios e inflamatorios, enfermedades cerebrovasculares, enfermedades cardiovasculares y afecciones asociadas con el trasplante de órganos.
En una realización, la enfermedad proliferativa dependiente de c-Met es cáncer. El término «cáncer» se utiliza en la presente para referirse a un espectro amplio de tumores, incluidas todas las neoplasias malignas hematológicas y sólidas. Los ejemplos de tales tumores incluyen, sin carácter limitante, tumores benignos y malignos de mama, vejiga, cuello uterino, colangiocarcinoma, colorrectales, de esófago, gástricos, de cabeza y cuello, de riñón (por ejemplo, carcinoma de células renales papilares), de hígado (por ejemplo, carcinoma hepatocelular), de pulmón (por ejemplo, cáncer de pulmón no microcítico y cáncer de pulmón microcítico), nasofaríngeo, de ovario, páncreas, próstata, tiroides, endometrio, sarcomas del sistema musculoesquelético (por ejemplo, osteosarcoma, sarcoma sinovial, rabdomiosarcoma), sarcomas de los tejidos blandos (por ejemplo, MFH/fibrosarcoma, leiomiosarcoma, sarcoma de Kaposi), mieloma múltiple, linfomas, leucemia de linfocitos T en adultos, leucemia mielógena aguda, leucemia mieloide crónica, glioblastomas, astrocitomas, melanoma, mesotelioma y tumor de Wilm y similares.
En una realización adicional de la presente invención, la enfermedad proliferativa dependiente de c-Met es un tumor sólido. La expresión «tumor sólido» significa especialmente cáncer de mama, cáncer de vejiga, cáncer de ovario, cáncer colorrectal, melanoma, cáncer gástrico, cáncer cervicouterino, cáncer de pulmón (por ejemplo, cáncer de pulmón microcítico y cáncer de pulmón no microcítico), cáncer de cabeza y cuello, cáncer de próstata o sarcoma de Kaposi. La presente combinación inhibe el crecimiento de tumores sólidos y también tumores líquidos.
En una realización adicional de la presente invención, la enfermedad proliferativa dependiente de c-Met es un cáncer de pulmón (por ejemplo, cáncer de pulmón no microcítico), o glioblastoma.
En una realización adicional, la presente invención se refiere a la COMBINACIÓN DE LA INVENCIÓN para su uso en el tratamiento de una enfermedad proliferativa dependiente de c-Met, que es resistente al tratamiento con un inhibidor de la tirosina cinasa de tipo receptor c-Met, particularmente la 2-fluoro-N-metil-4-[7-quinolin-6-il-metil)imidazo[1,2-b][1,2,4]triazin-2-il]benzamida o una sal farmacéuticamente aceptable de esta. Tal como se utiliza en la presente, el término «resistente» significa tumores previamente sensibles que, en la presencia continuada de un inhibidor de la tirosina cinasa de tipo receptor c-Met, o bien han vuelto a crecer después de su contracción debida al tratamiento, o han reaparecido después de haber sido eliminados temporalmente debido al tratamiento. El tratamiento con éxito de tumores resistentes puede provocar, por ejemplo, una mayor sensibilidad de una célula tumoral frente a agentes quimioterapéuticos y/o terapias contra el cáncer que se hayan intentado previamente o que sean novedosos y puede dar como resultado, por ejemplo, la posterior muerte de las células tumorales y prevención de la metástasis.
En una realización adicional, la presente invención se refiere a una COMBINACIÓN DE LA INVENCIÓN para su uso en la inhibición del crecimiento y/o la propagación de metástasis de cánceres dependientes de c-Met, particularmente tumores dependientes de c-Met. La COMBINACIÓN DE LA INVENCIÓN es adecuada para el tratamiento de pacientes con un pronóstico desfavorable, padeciendo especialmente tales pacientes con un pronóstico desfavorable cáncer de pulmón metastásico (por ejemplo, cáncer de pulmón no microcítico) o glioblastoma.
En una realización adicional, la presente invención se refiere a una combinación farmacéutica que comprende (a) un inhibidor de fosfatidilinositol 3-cinasa, el COMPUESTO D o una sal farmacéuticamente aceptable de este, y (b) el inhibidor de la tirosina cinasa de tipo receptor c-Met 2-fluoro-N-metil-4-[7-quinolin-6-il-metil)imidazo[1,2-b][1,2,4]triazin-2-il]benzamida o una sal farmacéuticamente aceptable de esta para su uso en el tratamiento de una enfermedad proliferativa, en particular una enfermedad proliferativa dependiente de c-Met. Preferentemente, la enfermedad proliferativa es un cáncer, de la forma más preferida cáncer de pulmón (por ejemplo, cáncer de pulmón no microcítico) o glioblastoma.
A un paciente que padezca una enfermedad proliferativa dependiente de c-Met, en particular cáncer de pulmón (por ejemplo, cáncer de pulmón no microcítico) o glioblastoma, se le puede administrar por separado, de forma simultánea o secuencial una combinación que comprenda (a) un inhibidor de fosfatidilinositol 3-cinasa, la 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (S)-pirrolidin-l ,2-dicarboxílico (COMPUESTO D) o una sal farmacéuticamente aceptable de esta, y (b) al menos un inhibidor de la tirosina cinasa de tipo receptor c-Met o una sal farmacéuticamente aceptable de este, para el tratamiento de dicha enfermedad proliferativa dependiente de c-Met de acuerdo con la presente invención.
En una realización adicional, la presente invención divulga el COMPUESTO D para su uso en un método para tratar una enfermedad proliferativa dependiente de c-Met, comprendiendo el método administrar a un sujeto que lo necesite una combinación de (a) un inhibidor de fosfatidilinositol 3-cinasa, el COMPUESTO D o una sal farmacéuticamente aceptable de este, y (b) el inhibidor de la tirosina cinasa de tipo receptor c-Met 2-fluoro-N-metil-4-[7-quinolin-6-il-metil)imidazo[1,2-b][1,2,4]triazin-2-il]benzamida o una sal farmacéuticamente aceptable de esta, en una cantidad que sea terapéuticamente eficaz de forma conjunta contra dicha enfermedad proliferativa. Preferentemente, la enfermedad proliferativa dependiente de c-Met es un cáncer, de la forma más preferida cáncer de pulmón (por ejemplo, cáncer de pulmón no microcítico) o glioblastoma.
En una realización adicional, la presente invención se refiere a un COMPUESTO D para su uso en un método para inhibir la formación de metástasis en un sujeto que padece un cáncer dependiente de c-Met, que comprende administrar a un sujeto que lo necesite una combinación de (a) una inhibidor de fosfatidilinositol 3-cinasa, la 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (S)-pirrolidin-l,2-dicarboxílico (COMPUESTO D) o una sal farmacéuticamente aceptable de esta, y (b) al menos un inhibidor de la tirosina cinasa de tipo receptor c-Met o una sal farmacéuticamente aceptable de este, en una cantidad que sea terapéuticamente eficaz de forma conjunta contra dicho cáncer. Los cánceres adecuados son los que se han expuesto en las realizaciones anteriormente.
En una realización preferida, los métodos y realizaciones de la presente se pueden utilizar para tratar un cáncer de pulmón (por ejemplo, cáncer de pulmón no microcítico) o glioblastoma.
En una realización adicional, la presente invención se refiere a un inhibidor de fosfatidilinositol 3-cinasa, el COMPUESTO D o una sal farmacéuticamente aceptable de este, en combinación con el inhibidor de la tirosina cinasa de tipo receptor
c-Met 2-fluoro-N-met¡l-4-[7-qu¡nol¡n-6-¡l-met¡l)¡m¡dazo[1,2-jb][1,2,4]tr¡az¡n-2-¡l]benzam¡da o una sal farmacéuticamente aceptable de esta para su uso en el tratam¡ento de una enfermedad prol¡ferat¡va depend¡ente de c-Met. En una real¡zac¡ón prefer¡da, la enfermedad prol¡ferat¡va depend¡ente de c-Met es un cáncer, en part¡cular cáncer de pulmón (por ejemplo, cáncer de pulmón no m¡crocít¡co) o gl¡oblastoma.
La adm¡n¡strac¡ón de una COMBINACIÓN DE LA INVENCIÓN puede dar como resultado no solo un efecto benef¡c¡oso, por ejemplo, un efecto terapéut¡co en comparac¡ón con la monoterap¡a de los agentes terapéut¡cos ¡nd¡v¡duales de la comb¡nac¡ón, por ejemplo, un efecto terapéut¡co s¡nérg¡co, por ejemplo, respecto al al¡v¡o, retraso de la evoluc¡ón o ¡nh¡b¡c¡ón de los síntomas, s¡no tamb¡én efectos benef¡c¡osos sorprendentes ad¡c¡onales, por ejemplo, menos efectos secundar¡os, una cal¡dad de v¡da mejorada o una morb¡l¡dad reduc¡da, en comparac¡ón con una monoterap¡a que apl¡ca solo uno de los agentes farmacéut¡camente terapéut¡cos ut¡l¡zados en la comb¡nac¡ón de la ¡nvenc¡ón.
Un benef¡c¡o ad¡c¡onal cons¡ste en que se pueden ut¡l¡zar dos¡s más bajas de los agentes terapéut¡cos de la COMBINACIÓN DE LA INVENCIÓN, por ejemplo, de modo que las dos¡s no solo pueden ser a menudo más pequeñas, s¡no que tamb¡én se pueden apl¡car con menos frecuenc¡a o se pueden ut¡l¡zar para d¡sm¡nu¡r la ¡nc¡denc¡a de efectos secundar¡os observados solo con uno de los agentes terapéut¡cos por sí solo. Esto está de acuerdo con los deseos y requ¡s¡tos de los pac¡entes que se han de tratar.
Puede demostrarse med¡ante modelos de prueba estableados que una COMBINACIÓN DE LA INVENCIÓN da como resultado los efectos benef¡c¡osos descr¡tos anter¡ormente en la presente. El experto en la técn¡ca está totalmente capac¡tado para selecc¡onar un modelo de prueba relevante para demostrar tales efectos benef¡c¡osos. La act¡v¡dad farmacológ¡ca de una COMBINACIÓN DE LA INVENCIÓN puede, por ejemplo, demostrarse en un estud¡o clín¡co o en un proced¡m¡ento de prueba in vitro tal como se descr¡be esenc¡almente más adelante en la presente.
Los estud¡os clín¡cos adecuados son en part¡cular, por ejemplo, estud¡os de escalada de la dos¡s s¡n enmascaramiento en pac¡entes con una enfermedad prol¡ferat¡va depend¡ente de c-Met, en part¡cular cáncer de pulmón (por ejemplo, cáncer de pulmón no m¡crocít¡co) o gl¡oblastoma. Tales estud¡os demuestran en part¡cular la s¡nerg¡a de los agentes terapéut¡cos de la comb¡nac¡ón de la ¡nvenc¡ón. Los efectos benef¡c¡osos sobre enfermedades prol¡ferat¡vas depend¡entes de c-Met se pueden determ¡nar d¡rectamente med¡ante los resultados de estos estud¡os, los cuales son conoc¡dos de por sí por un experto en la técn¡ca. Tales estud¡os pueden ser adecuados, en part¡cular, para comparar los efectos de una monoterap¡a que ut¡l¡za cualqu¡era de los agentes terapéut¡cos y una comb¡nac¡ón farmacéut¡ca de la ¡nvenc¡ón. En una real¡zac¡ón, la dos¡s del ¡nh¡b¡dor de fosfat¡d¡l¡nos¡tol 3-c¡nasa, la 2-am¡da y 1-({4-met¡l-5-[2-(2,2,2-tr¡fluoro-1,1-d¡met¡let¡l)p¡r¡d¡n-4-¡l]t¡azol-2-¡l}am¡da) del ác¡do (S)-p¡rrol¡d¡n-1,2-d¡carboxíl¡co (COMPUESTO D), se escala hasta que se alcanza la dos¡s máx¡ma tolerada y el ¡nh¡b¡dor de la t¡ros¡na c¡nasa de t¡po receptor c-Met, por ejemplo, la 2-fluoro-N-met¡l-4-[7-qu¡nol¡n-6-¡lmet¡l)-¡m¡dazo[1,2-jb][1,2,4]tr¡az¡n-2¡l]benzam¡da, se adm¡n¡stra con una dos¡s f¡ja. Como alternat¡va, el ¡nh¡b¡dor de fosfat¡d¡l¡nos¡tol 3-c¡nasa, la 2-am¡da y 1-({4-met¡l-5-[2-(2,2,2-tr¡fluoro-1,1-d¡met¡let¡l)p¡r¡d¡n-4-¡l]t¡azol-2-¡l}am¡da) del ác¡do (S)-p¡rrol¡d¡n-1,2-d¡carboxíl¡co (COMPUESTO D), se puede adm¡n¡strar con una dos¡s f¡ja y la dos¡s del ¡nh¡b¡dor de la t¡ros¡na c¡nasa de t¡po receptor c-Met, por ejemplo, la 2-fluoro-N-met¡l-4-[7-qu¡nol¡n-6-¡lmet¡l)-¡m¡dazo[1,2-b][1,2,4]tr¡az¡n-2¡l]benzam¡da, se puede escalar. Cada pac¡ente puede rec¡b¡r dos¡s del ¡nh¡b¡dor de fosfat¡d¡l¡nos¡tol 3-c¡nasa, la 2-am¡da y 1-({4-met¡l-5-[2-(2,2,2-tr¡fluoro-1,1-d¡met¡let¡l)p¡r¡d¡n-4-¡l]t¡azol-2-¡l}am¡da) del ác¡do (S)-p¡ rrol¡d¡ n-1,2-d¡carboxíl¡co (COMPUESTO D), ya sea a d¡ar¡o o de forma ¡nterm¡tente. La ef¡cac¡a del tratam¡ento se puede determinar en tales estud¡os, por ejemplo, después de 12, 18 o 24 semanas med¡ante la evaluac¡ón de las puntuac¡ones de los síntomas cada 6 semanas.
La determ¡nac¡ón de una ¡nteracc¡ón s¡nérg¡ca entre uno o más componentes, el ¡ntervalo ópt¡mo para el efecto y los ¡ntervalos de dos¡s absolutas de cada componente para el efecto se puede med¡r def¡n¡t¡vamente med¡ante la adm¡n¡strac¡ón de los componentes en d¡ferentes ¡ntervalos de relac¡ones p/p y dos¡s para pac¡entes que neces¡ten tratam¡ento. Para los seres humanos, la complej¡dad y el coste de llevar a cabo estud¡os clín¡cos en pac¡entes pueden hacer poco práct¡co el uso de esta forma de prueba como modelo pr¡mar¡o para la s¡nerg¡a. S¡n embargo, la observac¡ón de la s¡nerg¡a en una espec¡e puede ser pred¡ct¡va del efecto en otras espec¡es y ex¡sten modelos con an¡males, tal como se descr¡ben en la presente, para med¡r un efecto s¡nérg¡co y los resultados de tales estud¡os tamb¡én se pueden ut¡l¡zar para predec¡r ¡ntervalos de relac¡ones de dos¡s ef¡caces y las dos¡s absolutas y concentrac¡ones en plasma requer¡das en otras espec¡es med¡ante la apl¡cac¡ón de métodos farmacoc¡nét¡cos/farmacod¡nám¡cos. Las correlac¡ones estableadas entre modelos tumorales y efectos observados en seres humanos sug¡eren que se puede demostrar la s¡nerg¡a en an¡males, por ejemplo, med¡ante modelos de xeno¡njerto o en líneas celulares adecuadas.
C¡ertos aspectos de la presente ¡nvenc¡ón pueden emplear comb¡nac¡ones de un ¡nh¡b¡dor de fosfat¡d¡l¡nos¡tol 3-c¡nasa, la 2-am¡da y 1-({4-met¡l-5-[2-(2,2,2-tr¡fluoro-1,1-d¡met¡let¡l)p¡r¡d¡n-4-¡l]t¡azol-2-¡l}am¡da) del ác¡do (S)-p¡rrol¡d¡n-1,2-d¡carboxíl¡co (COMPUESTO D), que se formulan como una compos¡c¡ón farmacéut¡ca que comprende uno o más portadores farmacéut¡camente aceptables.
En un aspecto, la ¡nvenc¡ón proporc¡ona una compos¡c¡ón farmacéut¡ca que comprende una cant¡dad, que es ef¡caz terapéut¡camente de forma conjunta contra una enfermedad prol¡ferat¡va depend¡ente de c-Met, de una COMBINACIÓN DE LA INVENCIÓN y uno o más portadores farmacéut¡camente aceptables. Esta compos¡c¡ón farmacéut¡ca puede estar
constituida por los agentes terapéuticos (a) y (b) que se han de administrar a un paciente como una combinación fija en una única formulación o forma farmacéutica unitaria mediante cualquier vía adecuada. Como alternativa, los agentes terapéuticos, por ejemplo, el inhibidor de fosfatidilinositol 3-cinasa, la 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (S)-pirrolidin-1,2-dicarboxílico (COMPUESTO D), y el inhibidor de la tirosina cinasa de tipo receptor c-Met o una sal farmacéuticamente aceptable de este se administran ambos a un paciente como una combinación no fija en formulaciones o composiciones farmacéuticas o formas farmacéuticas unitarias por separado y se administran ya sea de forma simultánea, concurrente o secuencial sin límites de tiempo específicos.
En una realización preferida, la invención proporciona composiciones farmacéuticas que comprenden por separado una cantidad, que es terapéuticamente eficaz de forma conjunta contra una enfermedad proliferativa dependiente de c-Met, del agente terapéutico (a) y el agente terapéutico (b), los cuales se administran de forma concurrente pero por separado, o se administran de forma secuencial a un sujeto que lo necesite.
Las composiciones farmacéuticas para la administración separada de los agentes terapéuticos o para la administración de los agentes terapéuticos en una combinación fija, es decir, una única composición farmacéutica que comprende la COMBINACIÓN DE LA INVENCIÓN, se pueden preparar de una manera conocida de por sí y son aquellas adecuadas para una administración enteral, tal como oral o rectal, y parenteral a sujetos (animales de sangre caliente), incluidos los seres humanos, que comprenden una cantidad terapéuticamente eficaz de al menos un agente terapéutico farmacológicamente activo por sí solo, por ejemplo, como se ha indicado anteriormente, o en combinación con uno o más portadores farmacéuticamente aceptables, especialmente adecuados para una aplicación enteral o parenteral.
La composición farmacéutica novedosa puede contener de aproximadamente un 0,1% a aproximadamente un 99,9%, preferentemente de aproximadamente un 1% a aproximadamente un 60%, del(de los) agente(s) terapéutico(s).
Las composiciones farmacéuticas para la terapia combinada, incluidas las combinaciones fijas y combinaciones no fijas, para administración enteral o parenteral son, por ejemplo, aquellas en formas farmacéuticas unitarias, tales como comprimidos recubiertos de azúcar, comprimidos, cápsulas o supositorios, o ampollas. Si no se indica lo contrario, estas se preparan de una manera conocida de por sí, por ejemplo, por medio de diversos procesos convencionales de mezcla, trituración, granulación, recubrimiento con azúcar, disolución, liofilización o técnicas de fabricación muy evidentes para los expertos en la técnica. Se apreciará que el contenido unitario de un agente terapéutico contenido en una dosis individual de cada forma farmacéutica no necesita constituir en sí mismo una cantidad eficaz ya que la cantidad eficaz necesaria puede alcanzarse mediante la administración de una pluralidad de unidades de dosificación.
Una forma farmacéutica unitaria que contiene la combinación de agentes o los agentes individuales de la combinación de agentes pueden estar en forma de microcomprimidos contenidos dentro de una cápsula, por ejemplo, una cápsula de gelatina. Para esto, se puede utilizar una cápsula de gelatina como la que se emplea en las formulaciones farmacéuticas, tal como la cápsula de gelatina dura conocida como CAPSUGEL, que se puede adquirir de Pfizer.
Las formas farmacéuticas unitarias de la presente invención pueden comprender opcionalmente además portadores o excipientes convencionales adicionales utilizados para productos farmacéuticos. Los ejemplos de tales portadores incluyen, sin carácter limitante, desintegrantes, aglutinantes, lubricantes, deslizantes, estabilizantes y rellenos, diluyentes, colorantes, sabores y conservantes. Un experto en la técnica puede seleccionar uno o más de los portadores mencionados anteriormente con respecto a las propiedades particulares deseadas de la forma farmacéutica mediante experimentación rutinaria y sin ninguna dificultad excesiva. La cantidad de cada uno de los portadores utilizados puede variar dentro de los intervalos convencionales en la técnica. Las siguientes referencias divulgan técnicas y excipientes utilizados para formular formas farmacéuticas orales. Remítase a The Handbook of Pharmaceutical Excipients, 4.a edición, Rowe et al., Eds., American Pharmaceuticals Association (2003); y Remington: the Science and Practice of Pharmacy, 20.a edición, Gennaro, Ed., Lippincott Williams & Wilkins (2003).
Estos portadores convencionales adicionales opcionales pueden incorporarse en la forma farmacéutica oral incorporando dicho uno o más portadores convencionales en la mezcla inicial antes o durante la granulación de la masa fundida o combinando dicho uno o más portadores convencionales con los gránulos en la forma farmacéutica oral. En la última realización, la mezcla combinada puede mezclarse adicionalmente, por ejemplo, en un mezclador en forma de V, y posteriormente prensarse o moldearse para obtener un comprimido, por ejemplo, un comprimido monolítico, encapsulado en una cápsula o introducido en un sobre.
Los ejemplos de desintegrantes farmacéuticamente aceptables incluyen, sin carácter limitante, almidones; arcillas; celulosas; alginatos; gomas; polímeros reticulados, por ejemplo, polivinilpirrolidona o crospovidona reticulada, por ejemplo, POLYPLASDONE XL de International Specialty Products (Wayne, NJ); carboximetilcelulosa sódica o croscarmelosa sódica reticulada, por ejemplo, AC-DI-SOL de FMC; y carboximetilcelulosa cálcica reticulada; polisacáridos de soja; y goma guar. El desintegrante puede estar presente en una cantidad de aproximadamente un 0% a aproximadamente un 10% en peso de la composición. En una realización, el desintegrante está presente en una cantidad de aproximadamente un 0,1% a aproximadamente un 5% en peso de la composición.
Los ejemplos de aglutinantes farmacéuticamente aceptables incluyen, sin carácter limitante, almidones; celulosas y derivados de estas, por ejemplo, celulosa microcristalina, por ejemplo, AVICEL PH de FMC (Filadelfia, PA), hidroxipropilcelulosa, hidroxiletilcelulosa e hidroxipropilmetilcelulosa METHOCEL de Dow Chemical Corp. (Midland, MI); sacarosa; dextrosa; jarabe de maíz; polisacáridos; y gelatina. El aglutinante puede estar presente en una cantidad de aproximadamente un 0% a aproximadamente un 50%, por ejemplo, 2-20% en peso de la composición.
Los ejemplos de lubricantes farmacéuticamente aceptables y deslizantes farmacéuticamente aceptables incluyen, sin carácter limitante, sílice coloidal, trisilicato de magnesio, almidones, talco, fosfato de calcio tribásico, estearato de magnesio, estearato de aluminio, estearato de calcio, carbonato de magnesio, óxido de magnesio, polietilenglicol, celulosa en polvo y celulosa microcristalina. El lubricante puede estar presente en una cantidad de aproximadamente un 0% a aproximadamente un 10% en peso de la composición. En una realización, el lubricante puede estar presente en una cantidad de aproximadamente un 0,1% a aproximadamente un 1,5% en peso de la composición. El deslizante puede estar presente en una cantidad de aproximadamente un 0,1% a aproximadamente un 10% en peso.
Los ejemplos de rellenos farmacéuticamente aceptables y diluyentes farmacéuticamente aceptables incluyen, sin carácter limitante, azúcar de repostería, azúcar comprimible, dextratos, dextrina, dextrosa, lactosa, manitol, celulosa microcristalina, celulosa en polvo, sorbitol, sacarosa y talco. El relleno y/o el diluyente, por ejemplo, pueden estar presentes en una cantidad de aproximadamente un 0% a aproximadamente un 80% en peso de la composición.
En una realización, la composición farmacéutica comprende una cantidad que es terapéuticamente eficaz de forma conjunta contra una enfermedad proliferativa dependiente de c-Met, de una COMBINACIÓN DE LA INVENCIÓN y uno o más portadores farmacéuticamente aceptables, donde el inhibidor de fosfatidilinositol 3-cinasa es el COMPUESTO D o una sal farmacéuticamente aceptable de este.
En una realización adicional, la composición farmacéutica comprende una cantidad que es terapéuticamente eficaz de forma conjunta contra una enfermedad proliferativa de una COMBINACIÓN DE LA INVENCIÓN y uno o más portadores farmacéuticamente aceptables, donde el inhibidor de c-Met es 2-fluoro-N-metil-4-[7-quinolin-6-il-metil)imidazo[1,2-jb][1,2,4]triazin-2-il]benzamida o una sal farmacéuticamente aceptable de esta.
En una realización adicional, la composición farmacéutica comprende una cantidad que es terapéuticamente eficaz de forma conjunta contra una enfermedad proliferativa de una COMBINACIÓN DE LA INVENCIÓN y uno o más portadores farmacéuticamente aceptables, donde el inhibidor de fosfatidilinositol 3-cinasa es el COMPUESTO D o una sal farmacéuticamente aceptable de este y el inhibidor de c-Met es 2-fluoro-N-metil-4-[7-quinolin-6-il-metil)imidazo[1,2-b][1,2,4]triazin-2-il]benzamida o una sal farmacéuticamente aceptable de esta.
De acuerdo con la presente invención, una cantidad terapéuticamente eficaz de cada uno de los agentes terapéuticos de la combinación de la invención se puede administrar de forma simultánea o secuencial y en cualquier orden, y los componentes se pueden administrar por separado o como una combinación fija. Por ejemplo, la composición farmacéutica para su uso en un método de tratamiento de una enfermedad proliferativa de acuerdo con la invención puede comprender (i) la administración del primer agente terapéutico (a) en forma libre o de sal farmacéuticamente aceptable , y (ii) la administración de un agente terapéutico (b) en forma libre o de sal farmacéuticamente aceptable, de forma simultánea o secuencial en cualquier orden, en cantidades terapéuticamente eficaces de forma conjunta, preferentemente en cantidades sinérgicamente eficaces, por ejemplo, con dosificaciones diarias o intermitentes correspondientes a las cantidades descritas en la presente. Los agentes terapéuticos individuales de la COMBINACIÓN DE lA INVENCIÓN se pueden administrar por separado en diferentes momentos durante el transcurso de una terapia o de forma concurrente en formas combinadas únicas o divididas. Por consiguiente, se debe entender que la presente invención engloba todos estos regímenes de tratamiento simultáneo o alternante y el término «administrar» se debe interpretar de forma correspondiente.
La dosis eficaz de cada uno de los agentes terapéuticos empleados en la COMBINACIÓN DE LA INVENCIÓN puede variar dependiendo del compuesto particular o la composición farmacéutica empleada, el modo de administración, la afección que se esté tratando y la gravedad de la afección que se esté tratando. Por lo tanto, el régimen de dosificación de la combinación de la invención se selecciona de acuerdo con una variedad de factores que incluyen la vía de administración y la función renal y hepática del paciente. Un médico o facultativo experto puede determinar y recetar fácilmente la cantidad eficaz de los agentes terapéuticos individuales requerida para aliviar, contrarrestar o detener el avance de la afección.
La dosificación eficaz de cada uno de los agentes terapéuticos de la combinación puede requerir la administración más frecuente de uno de los compuestos en comparación con el(los) otro(s) compuesto(s) de la combinación. Por lo tanto, para permitir una dosificación adecuada, los productos farmacéuticos envasados pueden contener una o más formas farmacéuticas que contienen la combinación de compuestos, y una o más formas farmacéuticas que contienen uno de los compuestos de la combinación, pero no el(los) otro(s) compuesto(s) de la combinación.
Cuando los agentes terapéuticos, que se emplean en la COMBINACIÓN DE LA INVENCIÓN, se aplican en la forma comercializada como fármacos individuales, su dosificación y modo de administración pueden estar de acuerdo con la información proporcionada en el prospecto del envase del fármaco comercializado respectivo, si no se menciona en la presente lo contrario.
La dosis del COMPUESTO D se administra preferentemente a diario con una dosis comprendida en el intervalo de aproximadamente 0,05 a aproximadamente 50 mg por kilogramo de peso corporal del receptor al día; preferentemente aproximadamente 0.1-25 mg/kg/día, más preferentemente de aproximadamente 0,5 a 10 mg/kg/día. De este modo, para la administración a una persona de 70 kg, el intervalo de dosificación sería de la forma más preferente de aproximadamente 35-700 mg al día.
El inhibidor de la tirosina cinasa de tipo receptor c-Met, especialmente la 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-jb][1,2,4]triazin-2-il]benzamida, se administra preferentemente a diario con una dosis comprendida en el intervalo de aproximadamente 0,01 mg/kg a aproximadamente 100 mg/kg de peso corporal al día. De este modo, para la administración a una persona de 70 kg, el intervalo de dosificación sería de la forma más preferente de aproximadamente 0,7 mg a 7 g al día, más preferentemente de 50 mg a 300 mg al día.
La dosificación óptima de cada agente terapéutico para el tratamiento de una enfermedad proliferativa se puede determinar empíricamente para cada individuo utilizando métodos conocidos y dependerá de una variedad de factores, que incluyen, sin carácter limitante, el grado de avance de la enfermedad; la edad, el peso corporal, la salud general, el género y la dieta del individuo; el tiempo y la vía de administración; y otros medicamentos que el individuo esté tomando. Las dosificaciones óptimas se pueden establecer utilizando pruebas y procedimientos rutinarios que son muy conocidos en la técnica.
La cantidad de cada agente terapéutico que puede combinarse con los materiales portadores para producir una única forma farmacéutica variará dependiendo del individuo tratado y el modo particular de administración. En algunas realizaciones, las formas farmacéuticas unitarias que contienen la combinación de agentes tal como se describe en la presente contendrán las cantidades de cada agente de la combinación que se administran habitualmente cuando los agentes se administran solos.
La frecuencia de la dosificación puede variar dependiendo del compuesto utilizado y la afección particular que se ha de tratar. En general, se prefiere el uso de la dosificación mínima que sea suficiente para proporcionar una terapia eficaz. En general, se puede monitorizar a los pacientes para determinar la efectividad terapéutica utilizando ensayos adecuados para la afección que se esté tratando, con lo que estarán familiarizados los expertos en la técnica.
En una realización preferida, la presente invención proporciona una combinación farmacéutica de los agentes terapéuticos COMPUESTO D o una sal farmacéuticamente aceptable de este y un inhibidor de la tirosina cinasa de tipo receptor c-Met, preferentemente 2-fluoro-N-metil-4-[7-quinolin-6-il-metil)imidazo[1,2-b][1,2,4]triazin-2-il]benzamida, o una sal farmacéuticamente aceptable de esta, que están presentes con una proporción de dosificación comprendida en el intervalo de 8:1 a 1:1, más preferentemente de 4:1 a 2:1 a 1:1, respectivamente, a diario.
Las proporciones, dosificaciones individuales y combinadas, y concentraciones óptimas de los compuestos farmacológicos que producen eficacia sin toxicidad se basan en la cinética de la disponibilidad de los agentes terapéuticos en los sitios diana, y se determinan utilizando métodos conocidos por los expertos en la técnica.
Además, la presente invención proporciona un envase comercial que comprende como agentes terapéuticos la COMBINACIÓN DE LA INVENCIÓN, junto con instrucciones para la administración simultánea, por separado o secuencial de estos en el tratamiento de una enfermedad proliferativa dependiente de c-Met. En una realización preferida, la enfermedad proliferativa es un cáncer de pulmón (por ejemplo, cáncer de pulmón no microcítico) o glioblastoma.
Los siguientes Ejemplos ilustran la invención descrita anteriormente; sin embargo, no se pretende que limiten el alcance de la invención de ningún modo. Los efectos beneficiosos de la combinación farmacéutica de la presente invención también se pueden determinar mediante otros modelos de prueba conocidos de por sí por el experto en la técnica pertinente.
La utilidad de la COMBINACIÓN DE LA PRESENTE INVENCIÓN, tal como se describe en la presente, se puede demostrar in vitro, en métodos de prueba con animales, así como también en estudios clínicos.
Ejemplo de referencia 1: Combinaciones con el COMPUESTO A en cáncer de pulmón no microcítico
Materiales y métodos
El inhibidor de PI3K 2-metil-2-[4-(3-metil-2-oxo-8-quinolin-3-il-2,3-dihidroimidazo[4,5-c]quinolin-1-il)fenil]propionitrilo (COMPUESTO A) y el inhibidor de la tirosina cinasa de tipo receptor c-MET 2-fluoro-W-metil-4-[7-quinolin-6
ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida se evalúan combinados en modelos de cáncer de pulmón no microcítico. Se preparan individualmente patrones de los compuestos para ambos compuestos en DMSO. Los compuestos se diluyen en serie utilizando un dispensador Tecan para cubrir un intervalo de concentraciones de ~1000x. Las concentraciones más elevadas utilizadas para el experimento son las siguientes: COMPUESTO A = 2,7 |jM y 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida = 0,27 j M. Tanto el agente individual como las combinaciones se evalúan en múltiples concentraciones, junto con controles y un autocruzamiento.
Cultivo celular y mediciones de viabilidad
Las líneas celulares utilizadas en este estudio se adquieren de la Colección de Cultivos Tipo Estadounidense, e incluyen las líneas celulares de cáncer de pulmón no microcítico humano EBC-1 (que contiene una amplificación de c-Met), NCI-H1993 (que contiene c-MET amplificado), NCI-H1648 (que contiene una amplificación de c-Met), NCI-H1573 (que contiene una amplificación de c-Met y una mutación de KRAS) y HCC2935 (mutación de EGFR). Todas las líneas celulares se mantienen en su medio de cultivo respectivo tal y como especifica el proveedor.
Para la evaluación de los efectos de la combinación, las células se siembran en placas de 384 pocillos con una densidad de 500 células/pocillo y se incuban durante toda la noche. El contenido de las placas maestras de compuesto se diluye previamente con un factor de 1:200 (1 j L de solución de compuesto a 200 j L de medio de cultivo RPMI-160 que contiene un 10% de suero bovino fetal) antes de transferir 5 j L de esta predilución a las placas de células que contienen 20 j L de medio de cultivo celular, para conseguir las concentraciones finales de los compuestos objetivo, así como una concentración de vehículo (DMSO) de un 0,09%.
Los efectos de los agentes individuales, así como de su combinación, sobre la viabilidad celular se evalúa después de 72 horas de incubación a 37 °C/5% de CO2 mediante la cuantificación de los niveles de ATP celular (CellTiterGlo, Promega) utilizando 25 j L de reactivo/pocillo y placas replicadas n=2 para cada condición. El número/viabilidad de las células en el momento de la adición del compuesto se evalúa del mismo modo y se utiliza para estimar el tiempo de duplicación de la población para una línea celular.
Para los niveles no tratados y tratados U y T , la inhibición se calcula utilizando la fórmula I = 1-T/U, que varía desde un 0% hasta un 100% para una inhibición completa. La «inhibición del crecimiento» GI = 1 -( T -Uq)/Vq cuando T <Uq y 1 -(T-U 0)/(U-U 0) en los otros casos, donde U 0 es el nivel no tratado en el tiempo cero . Unos niveles de GI de un 0, 100% y 200% corresponden a compuestos inactivos, citostáticos y citotóxicos.
Cálculos de la actividad, sinergia y selectividad de los compuestos
La actividad del agente individual para cada compuesto se caracteriza mediante un ajuste a una función de Hill sigmoidal de la forma I = fmáxCa/[Ca+CE50a], donde C es la concentración, CE 50 es el punto de inflexión y a es la sigmoidicidad. El punto de cruce CI 50 se calcula donde la curva ajustada alcanza un 50% de inhibición.
Para las combinaciones, los cálculos de sinergia se refieren al modelo aditivo de Loewe (la expectación del «fármaco consigo mismo» que se obtiene como resultado de la adición de dosis eficaces). La expectación de Loewe [Loewe S., Ergebn Physiol 27: 47-187 (1928)) se calcula para cada par de dosis Cx,y ajustando la inhibición ILoewe de modo que (Cx/ICx) (Cy/ICy) = 1, y ICx,y son las concentraciones eficaces en ILoewe para las curvas ajustadas del agente individual, utilizando una optimización numérica [Berenbaum MC, J Theor Biol 114: 413-431 (1985)]. La «puntuación de sinergia» S se calcula promediando la diferencia entre Idatos e ILoewe para todos los puntos de dosis de la combinación evaluados, excluyendo el punto de concentración más elevada en la matriz de dosis, que lo más probable es que esté dominado por efectos del fármaco fuera de la diana. El valor de GImáx corresponde a la inhibición máxima del crecimiento en la matriz (excluyendo el par de dosis más elevado), como una medida de la eficacia global de la combinación.
La sinergia selectiva se evalúa comparando las puntuaciones de sinergia para una combinación en todas las líneas celulares evaluadas. La «puntuación de selectividad» para esa combinación en una línea celular individual se calcula como SS = abs( S ) * GImáx * (S - y )/a , donde y es la mediana y a es la desviación absoluta de la mediana de S en todas las líneas celulares. Esta puntuación Z ponderada resalta combinaciones que son excepcionalmente sinérgicas en una línea celular y que son de por sí tanto eficaces como sinérgicas.
Todos los cálculos se realizan utilizando el software Chalice (CombinatoRx, Cambridge MA). En este experimento, los datos de GImáx se interpretan en una escala tal como se indica a continuación: (a) GImáx = «0» indica una inhibición nula, (b) GImáx = aproximadamente «1» indica estasis e inhibición de un 100%, y (c) GImáx = 2 indica una inhibición de un 200% y la erradicación total o muerte de las células cancerosas. Utilizando este procedimiento, se muestra que la eficacia de la combinación^GImáx exclu endo la concentración más elevada es la si uiente:
En este experimento, la puntuación de sinergia (SS) se interpreta de la siguiente manera: (a) SS = «0» indica sinergia, (b) SS = «0,1» indica una sinergia elevada y (c) SS = valor negativo de «-0.01 a -0.07» indica aditividad. Se muestra que la puntuación de sinergia selectiva que se obtiene para la combinación, excluyendo la concentración más elevada, es la siguiente: _______________________________________________________________________________
SS EBC-1 H1993 H1648 H1573 HCC2935
COMPUESTO A 0,06 0,07 0,07 0,00 0,04
Ejemplo de referencia 2: Combinaciones con el COMPUESTO C en cáncer de pulmón no microcítico
Siguiendo el procedimiento experimental descrito en el Ejemplo 1 anterior, la eficacia y sinergia de la combinación del inhibidor de PI3K 5-(2,6-dimorfolin-4-ilpirimidin-4-il)-4-trifluorometilpiridin-2-ilamina (COMPUESTO C) y el inhibidor de la tirosina cinasa de tipo receptor c-MET 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida se evalúan de forma combinada en modelos de cáncer de pulmón no microcítico. Los compuestos se diluyen en serie utilizando un dispensador Tecan para cubrir un intervalo de concentraciones de ~1000x. Las concentraciones más elevadas utilizadas para el experimento son las siguientes: COMPUESTO C = 11 |jM y 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida = 0,27 j M. Tanto el agente individual como las combinaciones se evalúan en múltiples concentraciones, junto con controles y un autocruzamiento.
Todos los cálculos se realizan utilizando el software Chalice (CombinatoRx, Cambridge MA). Utilizando este procedimiento, se muestra que la eficacia de la combinación (GImáx), excluyendo la concentración más elevada, es la siguiente: _______________________________________________________________________________
GIMáx EBC-1 H1993 H1648 H1573 HCC2935
COMPUESTO C 1,83 1,67 1,78 1,54 1,37
Además, se muestra que la puntuación de sinergia selectiva para la combinación, excluyendo la concentración más elevada, es la siguiente:
COMPUESTO C 0,07 0,05 -0,01 -0,03 -0,07
Ejemplo 3: Combinaciones con el COMPUESTO D en cáncer de pulmón no microcítico
Siguiendo el procedimiento experimental descrito en el Ejemplo 1 anterior, la eficacia y sinergia de la combinación del inhibidor de PI3K COMPUESTO D y el inhibidor de la tirosina cinasa de tipo receptor c-MET 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida se evalúan de forma combinada en modelos de cáncer de pulmón no microcítico. Los compuestos se diluyen en serie utilizando un dispensador Tecan para cubrir un intervalo de concentraciones de ~1000x. Las concentraciones más elevadas utilizadas para el experimento son las siguientes: COMPUESTO D = 11 j M y 2-fluoro-W-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida = 0,27 j M. Las concentraciones más bajas utilizadas para el experimento son las siguientes: COMPUESTO D = 0,15 j M y 2-fluoro-W-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida = 0,0003 j M. Tanto el agente individual como las combinaciones se evalúan en múltiples concentraciones, junto con controles y un autocruzamiento.
Todos los cálculos se realizan utilizando el software Chalice (CombinatoRx, Cambridge MA). Utilizando este procedimiento, se muestra que la eficacia de la combinación (GImáx), excluyendo la concentración más elevada, es la siguiente:
COMPUESTO D 1,87 1,21 1,37 0,57 0,77
Además, se muestra que la puntuación de sinergia selectiva para la combinación, excluyendo la concentración más elevada, es la siguiente: _______________________________________________________________________________
EBC-1 H1993 H1648 H1573 HCC2935
COMPUESTO D 0,12 0,11 0,16 0,00 0,00
Ejemplo de referencia 4: Combinaciones con el COMPUESTO C en glioblastoma
Métodos
El inhibidor de PI3K 5-(2,6-dimorfolin-4-ilpirimidin-4-il)-4-trifluorometilpiridin-2-ilamina (COMPUESTO C) y el inhibidor de la tirosina cinasa de tipo receptor c-MET 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-jb][1,2,4]triazin-2il]benzamida se evalúan combinados en modelos tumorales de glioblastoma. El COMPUESTO C (10 mM) y la 2-fluoro-Ñ-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-jb][1,2,4]triazin-2il]benzamida (10 mM) se disuelven en DMSO y se almacenan en alícuotas a -20 °C.
Cultivo celular y ensayo de viabilidad celular
Se adquieren líneas celulares de glioblastoma humano, U-87 MG (línea que expresa HGF y PTEN mutado), H4 (línea que expresa HGF y PTEN mutado), A172 (línea con PTEN mutado y nivel de expresión bajo de HGF) y LN-229 (PTEN de origen natural y HGF bajo) de la Colección de Cultivos Tipo Estadounidense y se mantienen en una incubadora humidificada a 37 °C en un 5% de CO2 en los medios recomendados. Las cuatro líneas celulares expresan MET detectado a nivel de ARNm.
Las células se someten a pasaje dos veces a la semana y el medio se cambia cada 2-3 días. Para el ensayo de viabilidad celular, las células se tripsinizan utilizando TryPLE Express y se siembran (4000 células/pocillo) en placas negras de 96 pocillos de fondo transparente (Costar, #3904) por triplicado, y se permite que se adhieran durante toda la noche, a continuación se incuban durante 72 horas con varias concentraciones de agentes inhibidores o combinaciones de agentes.
La viabilidad celular se determina midiendo el contenido de ATP celular utilizando el ensayo de viabilidad celular luminiscente CellTiter-Glo® (CTG) (Promega). El tratamiento de las células con una combinación y con cada agente individual se compara con los controles o células tratadas con un volumen equivalente de medio. Se añade un volumen equivalente de los reactivos CTG a cada pocillo al final del tratamiento con el compuesto y se registra la luminiscencia en un lector de placas Envision (Perkin Elmer). Se calculan los valores de las señales luminiscentes reducidas y aumentadas (respuestas) respecto a las células no tratadas (control).
Método para calcular el efecto de las combinaciones
Para evaluar la actividad antiproliferativa de este inhibidor de PI3K con este inhibidor de cMET de manera imparcial, así como también para identificar el efecto sinérgico de todas las concentraciones posibles, los estudios se llevan a cabo con una «matriz de dosis». Esta utiliza todas las permutaciones posibles del agente individual diluido en serie y la matriz de dosis, que consisten en lo siguiente:
□ COMPUESTO C, que se somete a una dilución en serie X2 de 5 dosis, con una dosis elevada de 2,4 |jM y una dosis baja de aproximadamente 150 nM
□ Este inhibidor de c-MET, que se somete a una dilución en serie X2 de 5 dosis, con una dosis elevada de 1 j M y una dosis baja de aproximadamente 12 nM
La interacción sinérgica (analizada utilizando el software Chalice [CombinatoRx, Cambridge MA]) se calcula comparando la respuesta de una combinación respecto a la respuesta del agente actuando por sí solo, frente al modelo de referencia de dosis aditiva del fármaco consigo mismo. Las desviaciones de las dosis aditivas se pueden evaluar numéricamente
con un Índice de combinación (IC), el cual cuantifica la fuerza global del efecto de la combinación. Este cálculo (esencialmente una puntuación volumétrica) es como se indica a continuación:
Vhsa=Xx,y ln/X ln/Y (/datos - /hsa)
De forma adicional, el IC se calcula entre los datos y la superficie del agente individual más elevada, que se normaliza respecto a los factores de dilución del agente individual (Lehar J et al. (2009), «Synergistic drug combinations tend to improve therapeutically relevant selectivity», Nature Biotechnology 27: 659 - 66 (2009)).
Análisis de los datos
El análisis de los datos y la generación de las gráficas se llevan a cabo utilizando el software Microsoft Excel y el software Chalice.
Resultados
El efecto del COMPUESTO C y la 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida se evalúa en el esquema de «matriz de dosis» tal y como se ha expuesto anteriormente. Las cuatro líneas celulares se tratan en un formato de 96 pocillos durante 2 días con el COMPUESTO C y la 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida. La viabilidad celular se mide utilizando el ensayo CellTiter-Glo y los datos de % de inhibición se muestran numéricamente como una matriz de dosis 6X6. Las Figuras 1 a 4 de la presente proporcionan un resumen de los resultados del procedimiento anterior. Cada punto de evaluación representa los datos promediados de 3 pocillos y el espectro de colores también representa el nivel de inhibición. Los rectángulos en negrita resaltan la región en la que la combinación es más eficaz que los agentes individuales con la misma dosis.
En las Figuras 1 a 4 de la presente se muestra el porcentaje de inhibición en toda la matriz de dosis. El COMPUESTO C presenta actividad antiproliferativa dependiente de la concentración en las cuatro líneas celulares, y es menos activo en la línea celular que contiene PTEN de origen natural (LN229). La 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida presenta únicamente actividades moderadas en las dos líneas celulares con HGF elevado (U87 MG y H4) y es completamente inactiva en las otras dos (A172 y LN229). Cuando se utilizan conjuntamente, se observa sinergia tanto en H4 como en U87-MG, pero no en A172 ni en LN229, lo que se pone de manifiesto mediante una mayor inhibición del crecimiento en comparación con cada uno de los agentes individuales en las áreas resaltadas, así como también los isobologramas que se muestran en las Figuras 1 a 4 de la presente.
Estos datos sugieren que esta combinación inhibe de forma sinérgica el crecimiento de una subpoblación de las líneas celulares de glioblastoma, las líneas celulares con PTEN mutado así como HGF elevado parecen ser más sensibles a cada uno de los agentes individuales y la combinación da como resultado una inhibición del crecimiento más pronunciada.
Ejemplo de referencia 5: Combinaciones con el COMPUESTO C en modelos de xenoinjerto de glioblastoma
En este experimento, se utiliza el modelo de xenoinjerto de glioblastoma humano U-87 MG para evaluar la eficacia antitumoral del inhibidor de PI3K 5-(2,6-dimorfolin-4-ilpirimidin-4-il)-4-trifluorometilpiridin-2-ilamina (COMPUESTO C) y el inhibidor de c-Met 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida como agentes individuales o combinados. Se ha descrito que las células tumorales U-87 Mg obtenidas del Instituto Nacional contra el Cáncer son homocigotas para las variantes oncogénicas probables de CDKN2A, CDKN2C, CDKN2a y PTEN; no se detectan mutaciones en MET, PIK3CA ni en otros 58 genes que se encuentran alterados con frecuencia en células neoplásicas; y expresan HGF.
Se tratan ratones a diario durante 21 días con monoterapias de 17,7 y 35,3 mg/kg del inhibidor de c-Met y 32,7 mg/kg del COMPUESTO C, y con una terapia dual del inhibidor de c-Met/COMPUESTO C de 17,7:32,7. En el estudio, se incluyó una combinación del inhibidor de c-Met / COMPUESTO C con una proporción de dosis de 58,8:5,4 mg/kg. Los ratones de control recibieron ambos vehículos y un comportamiento monitorizado del modelo tumoral con régimen de temozolomida preclínico estándar. Los tratamientos orales empezaron el Día 1 (D1) en ratones atímicos con tumores subcutáneos establecidos. Cada animal se sometió a eutanasia cuando su tumor alcanzó un volumen predeterminado de criterio de valoración de 2000 mm3, o el D60, el que se produjera en primer lugar. El estudio finalizó el D51. La eficacia a corto plazo se determinó a partir de la media y la mediana de los cambios del volumen tumoral el D13, el último día antes de que más de un 50% de los ratones en cualquier grupo saliera del estudio. La eficacia global se determinó a partir de los tiempos requeridos para que los tumores evolucionaran hasta el criterio de valoración del volumen y a partir de la supervivencia el D51 y las tasas de remisión. Este informe describe los métodos y resultados del experimento de ralentización del crecimiento del tumor U87MG-e326.
Ratones
Los ratones atímicos hembra (nu/nu, Charles River) tienen 10 semanas de edad y tienen un peso corporal (BW, por sus siglas en inglés) comprendido en el intervalo de 15,5-273 g, el D1 del estudio. Los animales se alimentan con agua (ósmosis inversa, 1 ppm de Cl) y la dieta de laboratorio modificada e irradiada Lab Diet® NIH 31 constituida por un 18,0% de proteína cruda, un 5,0% de grasa cruda y un 5,0% de fibra cruda, de acceso libre. Los ratones se alojan en lechos para animales de laboratorio Enrich-o'cobs™ irradiados en microaisladores estáticos siguiendo un ciclo de luz de 12 horas a 20-22 °C (68-72 °F) y con un 40-60% de humedad.
Implante y medición del tumor
Se obtiene la línea tumoral U-87 MG de la Colección de Cultivos Tipo Estadounidense y se mantiene mediante un injerto en serie en ratones atímicos. Se implanta un fragmento del tumor (1 mm3) por vía subcutánea en el flanco derecho de cada ratón de prueba. Los tumores se miden con un calibre en dos dimensiones para monitorizar el crecimiento a medida que el volumen medio se acerca al intervalo deseado de 100-150 mm3. El tamaño del tumor, en mm3, se calculó a partir de: Volumen del tumor = (anchura2 x longitud)/ 2, donde la anchura y la longitud (en mm) son mediciones del tumor. Se puede estimar el peso del tumor asumiendo que 1 mg es equivalente a 1 mm3 de volumen del tumor. Catorce días después de la implantación de las células tumorales, el D1 del estudio, los ratones con volúmenes tumorales individuales de 63 196 mm3 se clasifican en siete grupos, con volúmenes tumorales medios del grupo de 122-127 mm3.
Artículos de prueba
El inhibidor de c-Met 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-jb][1,2,4]triazin-2il]benzamida (sal de di-HCl, 84,98% de base libre) se almacena a 4 °C y se añade a agua desionizada a 2X la concentración final y se somete a sonicación hasta que se disuelve. Se añade un volumen equivalente de metilcelulosa al 0,5% y Tween® 80 al 0,1% en agua desionizada para proporcionar una solución de dosificación de 5,884 mg/mL en metilcelulosa al 0,25% y Tween® 80 al 0,05% en agua desionizada (Vehículo 1). Se diluyen porciones de esta solución con el Vehículo 1 para proporcionar soluciones de dosificación de 3,53 y 1,765 mg/mL.
El COMPUESTO C (sal de HCl, 91,85% de base libre) se almacena a -20 °C y se añade a Tween® 80 al 1% en agua desionizada y se somete a sonicación para obtener una suspensión uniforme de 2X la concentración final. Se añade un volumen equivalente de metilcelulosa al 1% en agua desionizada y la mezcla se agita y se somete a sonicación para obtener una suspensión de dosificación incolora opaca de 3,266 mg/mL en metilcelulosa al 0,5% y Tween® 80 al 0,5% en agua desionizada (Vehículo 2). La suspensión de dosificación de 0,544 mg/mL se obtiene diluyendo una porción de la primera suspensión con el Vehículo 2.
La temozolomida (Temodar®, Schering Corporation, cápsula de 100 mg, Lote # IRSA001) se prepara una vez, por suspensión en agua desionizada, y se almacena a 4 °C.
Plan de tratamiento
Ambos agentes de prueba y los vehículos se administran mediante una sonda oral (p.o.) una vez al día durante 21 días consecutivos (qd x 21). En las terapias combinadas, se administra 2-metil-2-[4-(3-metil-2-oxo-8-quinolin-3-il-2,3-dihidroimidazo[4,5-c]quinolin-1-il)fenil]propionitrilo (COMPUESTO A) dentro de un periodo de 60 minutos después del inhibidor de c-Met. La temozolomida se administra p.o. una vez al día durante cinco días consecutivos (qd x 5). En todos los grupos, el volumen de dosificación de 10 mL/kg (0,2 mL/20 g de ratón) se escala hasta el peso de cada animal que se determina el día de la dosificación, con la excepción de los fines de semana, cuando se prosigue con el BW previo.
Se tratan siete grupos de ratones atímicos (n = 10/grupo) como se indica a continuación. Los ratones del Grupo 1 reciben los Vehículos 1 y 2, y sirvieron como controles para todos los análisis. El D7, este grupo recibe de forma inadvertida una dosis de un anticuerpo de control negativo de IgG; se llegó a la conclusión de que este error no tuvo ningún impacto sobre el crecimiento tumoral de control. Los Grupos 2 y 3 reciben las monoterapias de c-Met con dosis de 17,7 y 35,3 mg/kg (equivalentes a 15 y 30 mg/kg de base libre), respectivamente. El Grupo 4 recibió una monoterapia del COMPUESTO C con una dosis de 32,7 mg/kg (30 mg/kg de base libre). El Grupo 5 recibió 17,7 mg/kg del inhibidor de c-Met en combinación con 32,7 mg/kg del COMPUESTO C. El Grupo 6 recibió 58,8 mg/kg del inhibidor de c-Met en combinación con 5,4 mg/kg del COMPUESTO C (equivalentes a 50 y 5 mg/kg de base libre, respectivamente). El Grupo 7, el grupo de referencia, recibió una monoterapia de temozolomida con una dosis de 100 mg/kg.
Inhibición del crecimiento tumoral
Se determina la eficacia a corto plazo el D13. Antes del D13, un animal del Grupo 1 con un doblete tumoral abandona el estudio cuando la suma de sus volúmenes tumorales evolucionó hasta el criterio de valoración. El último volumen tumoral registrado para este animal se incluye en los datos del D13. Se determinó ATV, la diferencia en el volumen tumoral entre el D1 (el inicio de la dosificación) y el día del criterio de valoración, para cada animal. Para cada grupo de tratamiento, la respuesta en el día del criterio de valoración se calculó mediante una de las siguientes relaciones:
T/C (%) = 100 x AT/AC, para AT > 0
T/T0 (%) = 100 x AT/T0, para AT < 0,
donde
AT = (volumen tumoral medio del grupo tratado en el día del criterio de valoración) - (volumen tumoral medio del grupo tratado en el D1),
AC = (volumen tumoral medio del grupo de control en el día del criterio de valoración) - (volumen tumoral medio del grupo de control en el D1), y
T0 = volumen tumoral medio del grupo tratado en el D1.
Un valor de T/T0 negativo representa una reducción neta del tumor para un grupo. Un valor de T/C de un 40% o inferior sugiere una actividad terapéutica potencial.
Retraso del crecimiento tumoral
Cada animal se somete a eutanasia cuando su neoplasma alcanza el volumen del criterio de valoración (2000 mm3) o en el último día del estudio (D51). Para cada animal cuyo tumor alcanza el volumen del criterio de valoración, el tiempo hasta el criterio de valoración (TTE, por sus siglas en inglés) se calcula mediante la siguiente ecuación:
TTE = (logi0 (volumen del criterio de valoración) - b)/ m
donde TTE se expresa en días, el volumen del criterio de valoración está en mm3, b es la intersección y m es la pendiente de la recta obtenida mediante una regresión linear del conjunto de datos de crecimiento tumoral transformados logarítmicamente. El conjunto de datos comprende la primera observación que excede el volumen del criterio de valoración del estudio y las tres observaciones consecutivas que preceden inmediatamente a la consecución del volumen del criterio de valoración. A cualquiera animal con un tumor que no alcance el criterio de valoración, se le asigna un valor de TTE equivalente al del último día del estudio. A cualquier animal que se clasifique como que ha fallecido por causas TR, se le asigna un valor de TTE equivalente al del día del fallecimiento. Cualquier animal que se clasifique como que ha fallecido por causas NTR (distintas de metástasis) se excluye de los cálculos de TTE.
La eficacia del tratamiento se determina a partir del retraso del crecimiento tumoral (TGD, por sus siglas en inglés), que se define como el incremento en la mediana de TTE para un grupo de tratamiento en comparación con el grupo de control:
TGD = T - C,
que se expresa en días o como un porcentaje de la mediana de TTE del grupo de control:
% de TGD = [(T-C) C] x 100
donde:
T = mediana de TTE para un grupo de tratamiento,
C = mediana de TTE para el grupo de control designado.
MTV y criterios para las respuestas de remisión
La eficacia del tratamiento también se puede determinar a partir de los volúmenes tumorales de los animales que permanecen en el estudio en el último día y a partir del número de respuestas de remisión. El MTV(n) se define como la mediana del volumen tumoral en el D51 en el número de animales que permanecen, n, cuyos tumores no han alcanzado el volumen del criterio de valoración. El tratamiento puede provocar una remisión parcial (PR, por sus siglas en inglés) o una remisión completa (CR, por sus siglas en inglés) del tumor en un animal. Una PR indica que el volumen tumoral es un 50% o menos de su volumen en el D1 para tres mediciones consecutivas durante el transcurso del estudio y superior o igual a 13,5 mm3 para una o más de estas tres mediciones. Una CR indica que el volumen tumoral es inferior a 13.5 mm3 para tres mediciones consecutivas durante el transcurso del estudio. Cualquier animal que presente una respuesta CR en el último día del estudio se clasifica adicionalmente como un superviviente exento de tumor (TFS, por sus siglas en inglés).
Toxicidad
Los animales se pesaron los Días 1-5, en cada día de tratamiento (excepto los fines de semana), y dos veces a la semana a partir de entonces, hasta el final del estudio. Las determinaciones nadir del BW medio del grupo excluyen las mediciones tomadas después de que más de un 50% de los ratones evaluables en el grupo hayan abandonado el estudio y también excluyen cualquier animal que se haya clasificado como un fallecimiento NTR durante el estudio. La toxicidad aceptable para la dosis máxima tolerada (MTD, por sus siglas en inglés) se define como una pérdida de BW media del grupo inferior a un 15% durante la prueba y no más de un fallecimiento TR entre 10 animales. Cualquier animal con pérdidas de BW que excedan un 15% para tres mediciones consecutivas o una pérdida de BW que exceda un 20% para una medición, se somete a eutanasia y se clasifica como un fallecimiento TR a menos que sea el primer fallecimiento en el grupo. Un fallecimiento se clasifica como no relacionado con el tratamiento (NTR, por sus siglas en inglés) si no existe ninguna evidencia de que el fallecimiento esté relacionado con los efectos secundarios del tratamiento y el fallecimiento se produce más de 14 días después de que finalice la dosificación. Los fallecimientos NTR se clasifican como NTRa (debidos a un accidente o error), NTRu (debidos a causas desconocidas) o NTRm (diseminación del tumor confirmada por necropsia mediante invasión y/o metástasis). Para preservar los animales a la vez que se proporciona el máximo de información, el primer fallecimiento en un grupo se clasifica como NTRu; un fallecimiento NTR de este tipo se debe reclasificar como TR si se registran dos fallecimientos TR posteriores en el mismo grupo.
Análisis gráficos y estadísticos
Todos los análisis gráficos y estadísticos se realizan con Prism 3.03 (GraphPad) para Windows. Los cambios en el volumen tumoral medio para los Grupos 1-7 se comparan en primer lugar con un análisis de varianza (ANOVA), con la prueba de Bartlett. Cuando la prueba de Bartlett indica diferencias significativas entre las varianzas (P < 0,0001), los grupos se comparan con un análisis de Kruskal-Wallis, el cual muestra diferencias significativas entre los cambios en la mediana del volumen tumoral (P < 0,0001). Una prueba de comparación múltiple de Dunn post hoc compara los grupos tratados con el fármaco con el Grupo de control 1. Estas pruebas no paramétricas se repiten una vez para comparar uno de los grupos de terapia combinada con sus mono terapias correspondientes.
La supervivencia se analiza con el método de Kaplan-Meier. La prueba de rango logarítmico (Mantel-Cox) se emplea para analizar la significancia de la diferencia entre las experiencias de supervivencia global (curvas de supervivencia) de dos grupos. La prueba de rango logarítmico analiza los valores individuales de TTE para todos los animales en un grupo, excepto los excluidos como fallecimientos no relacionados con el tratamiento (NTR). Los análisis estadísticos de dos colas se llevan a cabo con P = 0,05. Prism resume los resultados de la prueba como no significativos (ns) para P > 0,05, significativos (simbolizados con «*») para 0,01 < P < 0,05, muy significativos («**») para 0,001 < P < 0,01 y extremadamente significativos («***») para P < 0,001. Debido a que las pruebas de significancia estadística no proporcionan una estimación de la magnitud de la diferencia entre los grupos, todos los niveles de significancia se describen como significativos o no significativos en el texto de este informe.
Resultados
i i n l r imi n n ri r i n n l i i n r l n l i :
Criterio de valoración del estudio = 2000 mm3, actividad a corto plazo = 13 días, días en evolución 51.
N = número de animales en un grupo no fallecidos por causas accidentales o desconocidas, o sometidos a eutanasia para muestreo.
T/C = 100 x (AT/ AC) = % de cambio entre el D1 y el D13 en el volumen tumoral medio de un grupo tratado en comparación con un grupo de control.
T/To= 100 x (AT/T0) = % de cambio entre el D1 y el D13 en el volumen tumoral medio de un grupo tratado en comparación con su volumen inicial, cuando AT = 0.
Significancia estadística (prueba de Dunn) = valor P de la prueba de comparación múltiple de Kruskal-Wallis Dunn: ns = no significativo = P > 0,05, en comparación con el grupo indicado
Significancia estadística (prueba de rango logarítmico) = valor P de la prueba de rango logarítmico en comparación con el grupo indicado: ns = no significativo; los resultados se consideran significativos para P < 0,05.
Las monoterapias con inhibidor de c-Met con dosis de 15 mg/kg y 30 mg/kg dieron como resultado un 5% y un 1% de T/C, respectivamente. El COMPUESTO C con dosis de 30 mg/kg dio como resultado un T/C de un 31%. La combinación del inhibidor de c-Met con dosis de 15 mg/kg y el COMPUESTO C con dosis de 30 mg/kg consiguió una remisión tumoral con T/T0: -83%, que es significativamente mejor que cualquiera de los agentes individuales por sí sólo.
Después de finalizar el tratamiento, se evalúa el porcentaje de retraso del crecimiento tumoral (% de TGD) monitorizando el crecimiento tumoral y registrando el tiempo necesario para alcanzar el criterio de valoración (TTE). El grupo tratado con vehículo alcanzó el criterio de valoración a los 11,7 días. El inhibidor de c-Met con dosis de 15 mg/kg y 30 mg/kg incrementa la mediana de TTE en 21,4 días (183% de TGD) y 23.4 días (200% de TGD), respectivamente. El COMPUESTO C con dosis de 30 mg/kg incrementó la mediana de TTE en 9,3 días (79% de TGD). La combinación del inhibidor de c-Met con dosis de 15 mg/kg y el COMPUESTO C con dosis de 30 mg/kg presentó la mediana de TTE en 28,7 días, lo que supone un 245% de TGD.
Ejemplo 6: Combinaciones con el COMPUESTO D en modelos de xenoinjerto de cáncer de pulmón no microcítico
En este experimento, se utiliza el modelo de xenoinjerto de carcinoma pulmonar no microcítico humano NCI-H1993 para evaluar la eficacia antitumoral del inhibidor de PI3K COMPUESTO D y el inhibidor de c-Met 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-jb][1,2,4]triazin-2il]benzamida como agentes individuales o combinados. Las células tumorales NCI-H1993 obtenidas de la Colección de Cultivos Tipo Estadounidense (ATCC) derivan de una metástasis de los ganglios linfáticos de un paciente que padece un adenocarcinoma pulmonar de estadio 3A y que tienen un historial de fumador.
Ratones
Los ratones atímicos sin pelaje hembra (Crl:NU (Ncr)-Foxnf"u, Charles River) tienen 8 semanas de edad y tienen un peso corporal (BW) comprendido en el intervalo de 16,1-26,2 g, el D1 del estudio. Los animales se alimentan con agua (ósmosis inversa, 1 ppm de Cl) y la dieta de laboratorio modificada e irradiada Lab Diet® NIH 31 constituida por un 18,0% de proteína cruda, un 5,0% de grasa cruda y un 5,0% de fibra cruda, de acceso libre. Los ratones se alojan en lechos para animales de laboratorio Enrich-o'cobs™ irradiados en microaisladores estáticos siguiendo un ciclo de luz de 12 horas a 20-22 °C (68-72 °F) y con un 40-60% de humedad.
Implante y medición del tumor
La línea tumoral NCI-H1993 se obtiene de la Colección de Cultivos Tipo Estadounidense y se mantiene a DRS_NC en medio RPMI-1640 que contiene 100 unidades/ penicilina G sódica, 100 |jg/mL de sulfato de estreptomicina, 25 |jg/mL de gentamicina, 10% de suero bovino fetal y glutamina 2 mM. Las células tumorales se cultivan en frascos de cultivo tisular en una incubadora humidificada a 37 °C en una atmósfera de un 5% de CO2 y un 95% de aire.
Las células tumorales utilizadas para el implante se recolectan durante la fase de crecimiento logarítmico y se suspenden de nuevo en PBS frío que contiene un 50% de Matrigel™ (BD Biosciences). Se inyectan 1 x 107 células (0,2 mL de suspensión celular) a cada ratón por vía subcutánea en el flanco derecho. Los tumores se miden con un calibre en dos dimensiones para monitorizar el crecimiento a medida que el volumen medio se acerca al intervalo deseado de 200-250 mm3. El tamaño del tumor, en mm3, se calculó a partir de: Volumen del tumor = (anchura2 x longitud)/2, donde la anchura y la longitud (en mm) son mediciones del tumor. Se puede estimar el peso del tumor asumiendo que 1 mg es equivalente a 1 mm3 de volumen del tumor. Catorce días después de la implantación de las células tumorales, el D1 del estudio, los ratones con volúmenes tumorales individuales de 172-256 mm3 se clasifican en grupos de 10 ratones, con volúmenes tumorales medios del grupo de 206-215 mm3.
Artículos de prueba
El inhibidor de c-Met 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida (sal de HCl, 84,98% de base libre) se almacena a 4 °C y se añade a un volumen de agua desionizada equivalente a 1/2 del volumen final y se somete a sonicación hasta que se disuelve para obtener una suspensión uniforme 2X. Se añade un volumen equivalente de metilcelulosa al 0,5%: Tween® 80 al 0,1% para proporcionar una solución de 1,77 mg/mL con concentraciones finales de vehículo de metilcelulosa al 0,25% y Tween® 80 al 0,05% en agua desionizada (Vehículo 1). Se preparan soluciones frescas una vez al día para la dosificación de la tarde y se almacenan a temperatura ambiente hasta la dosificación de la mañana.
El COMPUESTO D se suspende con una concentración de 3.0 mg/mL en metilcelulosa al 0,5% en agua desionizada. El vehículo se añade en porciones equivalentes a 1/3 del volumen final. La suspensión se agita con vórtex después de cada adición y a continuación se somete finalmente a una sonicación con sonda sobre hielo para preparar una suspensión blanca homogénea. Se prepara una suspensión fresca cada semana, se almacena a 4 °C y se suspende de nuevo antes de su dosificación.
El Vehículo 2 se prepara con una concentración final de vehículo de un 35% de D5W (dextrosa al 5% en agua): un 5% de Tween® 80 al 10% (concentración final de un 0,05%): un 60% de tampón de acetato 100 mM de pH 4,5.
Plan de tratamiento
El inhibidor de c-MET y el vehículo se administran cada uno mediante una sonda oral (p.o.) dos veces al día durante todo el estudio (b.i.d. hasta el final). El COMPUESTO D se administra mediante una sonda oral (p.o.) una vez al día durante todo el estudio (qd hasta el final). En las terapias combinadas, el COMPUESTO D se administra dentro de un periodo de 30 minutos después del inhibidor de c-Met. En todos los grupos, el volumen de dosificación de 10 mL/kg (0,2 mL/20 g de ratón) se escala hasta el peso de cada animal que se determina el día de la dosificación, con la excepción de los fines de semana, cuando se prosigue con el BW previo.
Los grupos de ratones atímicos (n = 10/grupo) se tratan como se indica a continuación. El Grupo 1 recibe el Vehículo 1 y el Vehículo 2 y sirven como controles para el estudio. El Grupo 2 recibe 17,7 mg/kg de la monoterapia del inhibidor de c-MET dos veces al día durante todo el estudio (b.i.d. hasta el final). El Grupo 3 recibe 30 mg/kg de la monoterapia del COMPUESTO D una vez al día durante todo el estudio (qd hasta el final). El Grupo 4 recibe 17,7 mg/kg del inhibidor de c-MET b.i.d. hasta el final en combinación con 30 mg/kg del COMPUESTO D qd hasta el final.
Inhibición del crecimiento tumoral
La eficacia a corto plazo se determina el Día 20 (D20). Antes del D20, un animal en el Grupo 1 y un animal en el Grupo 3 han abandonado el estudio debido al avance del tumor; se prosigue con el volumen tumoral final de cada uno y se incluye en el volumen medio del grupo.
Se determinó ATV, la diferencia en el volumen tumoral entre el D1 (el inicio de la dosificación) y el día del criterio de valoración, para cada animal. Para cada grupo de tratamiento, la respuesta en el día del criterio de valoración se calculó mediante una de las siguientes relaciones:
T/C (%) = 100 x AT/AC, para AT > 0
T/T0 (%) = 100 x AT/T0, para AT < 0,
donde
AT = (volumen tumoral medio del grupo tratado en el día del criterio de valoración) - (volumen tumoral medio del grupo tratado en el D1),
AC = (volumen tumoral medio del grupo de control en el día del criterio de valoración) - (volumen tumoral medio del grupo de control en el D1), y
T0 = volumen tumoral medio del grupo tratado en el D1.
Un valor de T/T0 negativo representa una reducción neta del tumor para un grupo. Un valor de T/C de un 40% o inferior sugiere una actividad terapéutica potencial.
Retraso del crecimiento tumoral
Los tumores se miden con un calibre dos veces a la semana y cada animal se somete a eutanasia cuando su neoplasma alcanza el volumen del criterio de valoración (600 mm3) o en el último día del estudio (D71), el que se produzca en primer
lugar. El tiempo transcurrido hasta alcanzar el criterio de valoración (TTE) para cada ratón se calcula con la siguiente ecuación:
TTE = (log10 (volumen del criterio de valoración) - b)/ m
donde TTE se expresa en días, el volumen del criterio de valoración está en mm3, b es la intersección y m es la pendiente de la recta obtenida mediante una regresión linear del conjunto de datos de crecimiento tumoral transformados logarítmicamente. Cada conjunto de datos comprende la primera observación que excede el volumen del criterio de valoración del estudio y las tres observaciones consecutivas que preceden inmediatamente a la consecución del volumen del criterio de valoración. A cualquiera animal con un tumor que no alcance el criterio de valoración, se le asigna un valor de TTE equivalente al del último día del estudio. A cualquier animal que se clasifique como que ha fallecido por causas relacionadas con el tratamiento (TR), se le asigna un valor de TTE equivalente al del día del fallecimiento. Cualquier animal que se clasifique como que ha fallecido por causas no relacionadas con el tratamiento (NTR) (distintas de metástasis) se excluye de los cálculos de TTE.
La eficacia del tratamiento se determina a partir del retraso del crecimiento tumoral (TGD, por sus siglas en inglés), que se define como el incremento en la mediana de TTE para un grupo de tratamiento en comparación con el grupo de control:
TGD = T - C,
que se expresa en días o como un porcentaje de la mediana de TTE del grupo de control:
% de TGD = [(T-C) C] x 100
donde:
T = mediana de TTE para un grupo de tratamiento,
C = mediana de TTE para el grupo de control designado.
MTV y criterios para las respuestas de remisión
La eficacia del tratamiento también se puede determinar a partir de los volúmenes tumorales de los animales que permanecen en el estudio en el último día y a partir del número de respuestas de remisión. El MTV(n) se define como la mediana del volumen tumoral en el D71 en el número de animales que permanecen, n, cuyos tumores no han alcanzado el volumen del criterio de valoración.
El tratamiento puede provocar una remisión parcial (PR) o una remisión completa (CR) del tumor en un animal. Una PR indica que el volumen tumoral es un 50% o menos de su volumen en el D1 para tres mediciones consecutivas durante el transcurso del estudio y superior o igual a 13,5 mm3 para una o más de estas tres mediciones. Una CR indica que el volumen tumoral es inferior a 13.5 mm3 para tres mediciones consecutivas durante el transcurso del estudio.
Toxicidad
Los animales se pesaron los Días 1-5, en cada día de tratamiento (excepto los fines de semana), y dos veces a la semana a partir de entonces, hasta el final del estudio. La pérdida de peso corporal (BW) media máxima del grupo se determina para el intervalo entre el D1 y el D20, así como para la totalidad del estudio. Las determinaciones nadir del BW medio del grupo excluyen las mediciones tomadas después de que más de un 50% de los ratones evaluables en el grupo hayan abandonado el estudio y también excluyen cualquier animal que se haya clasificado como un fallecimiento no relacionado con el tratamiento (NTR) durante el estudio. La toxicidad aceptable para la dosis máxima tolerada (MTD, por sus siglas en inglés) se define como una pérdida de BW media del grupo inferior a un 15% durante la prueba y no más de un fallecimiento TR entre 10 animales. Cualquier animal con pérdidas de BW que excedan un 15% para tres mediciones consecutivas o una pérdida de BW que exceda un 20% para una medición, se somete a eutanasia y se clasifica como un fallecimiento TR a menos que sea el primer fallecimiento en el grupo. Un fallecimiento se clasifica como NTR si no existe ninguna evidencia de que el fallecimiento esté relacionado con los efectos secundarios del tratamiento y el fallecimiento se produce más de 14 días después de que finalice la dosificación. Los fallecimientos NTR se clasifican como NTRa (debidos a un accidente o error), NTRu (debidos a causas desconocidas) o NTRm (diseminación del tumor confirmada por necropsia mediante invasión y/o metástasis). Para preservar los animales a la vez que se proporciona el máximo de información, el primer fallecimiento en un grupo se clasifica como NTRu; un fallecimiento NTR de este tipo se debe reclasificar como TR si se registran dos fallecimientos TR posteriores en el mismo grupo.
Análisis gráficos y estadísticos
Los análisis gráficos y estadísticos se realizan con Prism 3.03 (GraphPad) para Windows. Los cambios en el volumen tumoral medio para todos los grupos se comparan con un análisis de varianza de una vía (ANOVA), con la prueba de Bartlett para una varianza equivalente. Debido a que las diferencias entre las varianzas son significativas (P < 0,01), los grupos se comparan con el análisis de Kruskal-Wallis y la prueba de comparación múltiple post hoc de Dunn. Estas últimas pruebas se repiten para comparar la combinación con las monoterapias de sus componentes.
La supervivencia se analiza mediante el método de Kaplan-Meier basado en los valores de TTE. La prueba de rango logarítmico se emplea para determinar la significancia de la diferencia entre las experiencias de supervivencia global (curvas de supervivencia) de dos grupos. Los análisis estadísticos de dos colas se llevan a cabo con P = 0,05. Prism resume los resultados de la prueba como no significativos (ns) para P > 0,05, significativos (simbolizados con «*») para 0,01 < P < 0,05, muy significativos («**») para 0,001 < P < 0,01 y extremadamente significativos («***») para P < 0,001. Debido a que las pruebas de significancia estadística no proporcionan una estimación de la magnitud de la diferencia entre los grupos, todos los niveles de significancia se describen como significativos o no significativos en el texto de este informe.
Resultados
Siguiendo el procedimiento anterior, se obtienen los siguientes resultados al final del estudio tal como se ha definido anteriormente:
N = número de animales en un grupo no fallecidos por causas relacionadas con el tratamiento, accidentales o desconocidas, o sometidos a eutanasia para muestreo.
T/C = 100 x (AT/ AC) = % de cambio entre el D1 y el D20 en el volumen tumoral medio de un grupo tratado en comparación con un grupo de control.
T/To= 100 x (AT/T0) = % de cambio entre el D1 y el D20 en el volumen tumoral medio de un grupo tratado en comparación con su volumen inicial, cuando AT = 0.
Significancia estadística (prueba de Dunn) = valor P de la prueba de comparación múltiple de Kruskal-Wallis Dunn: ns = no significativo = P > 0,05, en comparación con el grupo indicado
Significancia estadística (prueba de rango logarítmico) = valor P de la prueba de rango logarítmico en comparación con el grupo indicado: ns = no significativo; los resultados se consideran significativos para P < 0,05.
La monoterapia del inhibidor de c-Met con dosis de 17,7 mg/kg p.o bid hasta el final no consigue una inhibición significativa respecto al control ( Grupo 1) debido a una respuesta variable y al solapamiento del cambio en los intervalos de los volúmenes tumorales. La monoterapia del COMPUESTO D con dosis de 30 mg/kg p.o. qd hasta el final da como resultado una mediana de la aceleración del crecimiento tumoral no significativa. La combinación del inhibidor de c-Met y el COMPUESTO D da como resultado un -17% de T/T0 y medianas de las actividades significativas (P < 0,01, prueba de Dunnett), pero no mejora de forma significativa en comparación con la monoterapia del inhibidor de c-Met el Día 20.
En general, la monoterapia del inhibidor de c-Met incrementa la mediana de TTE en un 97% y extiende de forma significativa la supervivencia (P < 0,001, prueba de rango logarítmico), proporcionando cuatro supervivientes el D71 y una PR. La monoterapia del COMPUESTO D bien tolerada da como resultado una supervivencia global que no es significativamente más corta que la del control (Grupo 1).
La combinación del inhibidor de c-Met y el COMPUESTO D incrementa la mediana de TTE en el máximo posible de un 184%. El grupo de la combinación tiene 8 supervivientes y 1 remisión parcial. La combinación mejora significativamente ambas monoterapias. La Figura 5 de la presente proporciona un resumen de los resultados.
En resumen, la monoterapia del inhibidor de c-Met con dosis de 17,7 mg/kg b.i.d. hasta el final produce un 15% de T/C y una inhibición del crecimiento tumoral el D20 no significativa, pero proporciona un incremento de un 97% en la mediana de TTE y una extensión significativa de la supervivencia. La monoterapia del COMPUESTO D con dosis de 30 mg/kg qd hasta el final no es significativamente activa (inactiva). La combinación presenta interacciones farmacológicas favorables al provocar una reducción del tumor en el D20 y producir el incremento máximo posible de un 184% en la mediana de TTE. No se observan mejoras significativas respecto a la monoterapia del inhibidor de c-Met en el D20; sin embargo, la combinación extiende significativamente la supervivencia con respecto a ambas monoterapias correspondientes. Un fallecimiento durante la monoterapia del inhibidor de c-Met y 2 fallecimientos durante la terapia combinada son debidos a pérdidas individuales de peso corporal. Ya que las pérdidas de peso corporal medias del grupo son nulas o despreciables, no está claro si la monoterapia del inhibidor de c-Met se encuentra en la dosis máxima terminal y si la combinación excede la dosis máxima terminal para el modelo.
Claims (14)
1. Una combinación farmacéutica que comprende (a) la 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (s)-pirrolidin-1,2-dicarboxílico (COMPUESTO D), o una sal farmacéuticamente aceptable de esta, y (b) al menos un inhibidor de la tirosina cinasa de tipo receptor c-Met, o una sal farmacéuticamente aceptable de este, para su uso en el tratamiento de una enfermedad proliferativa que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met mediante la sobreexpresión o amplificación del gen HGF / c-Met, la activación paracrina y autocrina dependiente de HGF y/o la activación del receptor c-Met mediante una mutación genética.
2. La combinación farmacéutica para su uso de acuerdo con la reivindicación 1, donde el inhibidor de la tirosina cinasa de tipo receptor c-Met es 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-jb][1,2,4]triazin-2il]benzamida , o una sal farmacéuticamente aceptable de esta.
3. La combinación farmacéutica para su uso de acuerdo con la reivindicación 1 o la reivindicación 2, donde la enfermedad proliferativa es un cáncer.
4. La combinación farmacéutica para su uso de acuerdo con cualquiera de las reivindicaciones 1 a 3, donde la enfermedad proliferativa es un cáncer seleccionado del grupo constituido por tumores benignos y malignos de mama, vejiga, cuello uterino, colangiocarcinoma, colorrectales, de esófago, gástricos, de cabeza y cuello, de riñón, hígado, pulmón, nasofaríngeos, de ovario, páncreas, próstata, tiroides, endometrio, sarcomas del sistema musculoesquelético, sarcomas de los tejidos blandos, mieloma múltiple, linfomas, leucemia de linfocitos T en adultos, leucemia mielógena aguda, leucemia mieloide crónica, glioblastomas, astrocitomas, melanoma, mesotelioma y tumor de Wilm.
5. La combinación farmacéutica para su uso de acuerdo con cualquiera de las reivindicaciones 1 a 4, donde la enfermedad proliferativa es cáncer de pulmón (por ejemplo, cáncer de pulmón no microcítico) o glioblastoma.
6. La combinación farmacéutica para su uso de acuerdo con cualquiera de las reivindicaciones 1 a 5, donde la administración de la combinación es simultánea, por separado o secuencial.
7. Una composición farmacéutica que comprende una combinación farmacéutica de acuerdo con la reivindicación 1 o la reivindicación 2 y al menos un portador farmacéuticamente aceptable.
8. La combinación farmacéutica para su uso de acuerdo con la reivindicación 1 en un método para inhibir la formación de metástasis en un sujeto que padece cáncer, que comprende administrar a un sujeto que lo necesite una cantidad farmacéuticamente eficaz de una combinación farmacéutica de acuerdo con la reivindicación 1.
9. La combinación farmacéutica para su uso en un método de acuerdo con la reivindicación 8, donde la enfermedad proliferativa o cáncer es un cáncer seleccionado del grupo constituido por tumores benignos y malignos de mama, vejiga, cuello uterino, colangiocarcinoma, colorrectales, de esófago, gástricos, de cabeza y cuello, de riñón, hígado, pulmón, nasofaríngeos, de ovario, páncreas, próstata, tiroides, endometrio, sarcomas del sistema musculoesquelético, sarcomas de los tejidos blandos, mieloma múltiple, linfomas, leucemia de linfocitos T en adultos, leucemia mielógena aguda, leucemia mieloide crónica, glioblastomas, astrocitomas, melanoma, mesotelioma y tumor de Wilm.
10. La combinación farmacéutica para su uso en un método de acuerdo con la reivindicación 9, donde el tratamiento comprende administrar la cantidad del agente terapéutico (a) y la cantidad del agente terapéutico (b) por separado o de forma secuencial.
11. Una combinación farmacéutica que comprende la 2-amida y 1 -({4-metil-5-[2-(2,2,2-trifl uoro-1, 1 -dimetiletil)pi ridin-4-il]tiazol-2-il}amida) del ácido (S)-pirrolidin-1,2-dicarboxílico (COMPUESTO D), o una sal farmacéuticamente aceptable de esta, y un inhibidor de la tirosina cinasa de tipo receptor c-Met, la 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)-imidazo[1,2-¿][1,2,4]triazin-2il]benzamida o una sal farmacéuticamente aceptable de esta.
12. La 2-amida y 1-({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (S)-pirrolidin-1,2-dicarboxílico (COMPUESTO D), o una sal farmacéuticamente aceptable de esta, para su uso en el tratamiento de una enfermedad proliferativa que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met mediante la sobreexpresión o amplificación del gen HGF / c-Met, la activación paracrina y autocrina dependiente de HGF y/o la activación del receptor c-Met mediante una mutación genética, en combinación con al menos un inhibidor de la tirosina cinasa de tipo receptor c-Met, o una sal farmacéuticamente aceptable de este.
13. El compuesto para su uso de acuerdo con la reivindicación 12, donde el inhibidor de la tirosina cinasa de tipo receptor c-Met es 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2il]benzamida , o una sal farmacéuticamente aceptable de esta.
14. Un inhibidor de la tirosina cinasa de tipo receptor c-Met que es 2-fluoro-N-metil-4-[7-quinolin-6-ilmetil)imidazo[1,2-jb][1,2,4]triazin-2il]benzamida, o una sal farmacéuticamente aceptable de esta, para su uso en el tratamiento de una enfermedad proliferativa que presenta una desregulación de c-Met y/o la vía de señalización de HGF/c-Met mediante la sobreexpresión o amplificación del gen HGF / c-Met, la activación paracrina y autocrina dependiente de HGF y/o la activación del receptor c-Met mediante una mutación genética, en combinación con la 2-amida y 1 -({4-metil-5-[2-(2,2,2-trifluoro-1,1-dimetiletil)piridin-4-il]tiazol-2-il}amida) del ácido (S)-pirrolidin-l,2-dicarboxílico (COMPUESTO D), o una sal farmacéuticamente aceptable de esta.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201261683790P | 2012-08-16 | 2012-08-16 | |
| PCT/US2013/054848 WO2014028566A1 (en) | 2012-08-16 | 2013-08-14 | Combination of pi3k inhibitor and c-met inhibitor |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2901712T3 true ES2901712T3 (es) | 2022-03-23 |
Family
ID=49004065
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES13751058T Active ES2901712T3 (es) | 2012-08-16 | 2013-08-14 | Combinación de un inhibidor de pi3k y un inhibidor de c-met. |
Country Status (14)
| Country | Link |
|---|---|
| US (5) | US20150216870A1 (es) |
| EP (1) | EP2885003B1 (es) |
| JP (3) | JP2015529194A (es) |
| KR (2) | KR102245985B1 (es) |
| CN (1) | CN105050623B (es) |
| AU (4) | AU2013302702A1 (es) |
| BR (1) | BR112015002528A2 (es) |
| CA (1) | CA2879704A1 (es) |
| ES (1) | ES2901712T3 (es) |
| HK (1) | HK1211476A1 (es) |
| IN (1) | IN2015DN00528A (es) |
| MX (1) | MX369518B (es) |
| RU (1) | RU2705095C2 (es) |
| WO (1) | WO2014028566A1 (es) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PH12014500682A1 (en) | 2011-09-27 | 2014-05-12 | Novartis Ag | 3-pyrimidin-4-yl-oxazolidin-2-ones as inhibitors of mutant idh |
| UY34632A (es) | 2012-02-24 | 2013-05-31 | Novartis Ag | Compuestos de oxazolidin- 2- ona y usos de los mismos |
| EP2834246B1 (en) | 2012-04-03 | 2021-07-28 | Novartis AG | Combination products with tyrosine kinase inhibitors and their use |
| US9296733B2 (en) | 2012-11-12 | 2016-03-29 | Novartis Ag | Oxazolidin-2-one-pyrimidine derivative and use thereof for the treatment of conditions, diseases and disorders dependent upon PI3 kinases |
| GEP201706699B (en) | 2013-03-14 | 2017-07-10 | Novartis Ag | 3-pyrimidin-4-yl-oxazolidin-2-ones as inhibitors of mutant idh |
| CN105338980A (zh) * | 2013-06-18 | 2016-02-17 | 诺华股份有限公司 | 药物组合 |
| KR20160037989A (ko) | 2013-08-02 | 2016-04-06 | 아두로 바이오테크 홀딩스, 유럽 비.브이. | 면역 자극을 위한 cd27 효능제와 면역 체크포인트 억제의 조합 |
| ES2857523T3 (es) | 2014-07-25 | 2021-09-29 | Novartis Ag | Formulación en comprimido de 2-fluoro-N-metil-4-[7-(quinolin-6-ilmetil)imidazo[1,2-b][1,2,4]triazin-2-il]benzamida |
| JP6847835B2 (ja) | 2014-12-12 | 2021-03-24 | ザ ジェネラル ホスピタル コーポレイション | 乳がん脳転移の処置 |
| GB201516504D0 (en) | 2015-09-17 | 2015-11-04 | Astrazeneca Ab | Imadazo(4,5-c)quinolin-2-one Compounds and their use in treating cancer |
| WO2021127041A1 (en) * | 2019-12-20 | 2021-06-24 | Recurium Ip Holdings, Llc | Combinations |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB0211649D0 (en) * | 2002-05-21 | 2002-07-03 | Novartis Ag | Organic compounds |
| GB0510390D0 (en) * | 2005-05-20 | 2005-06-29 | Novartis Ag | Organic compounds |
| JO2660B1 (en) * | 2006-01-20 | 2012-06-17 | نوفارتيس ايه جي | Pi-3 inhibitors and methods of use |
| GEP20125658B (en) * | 2006-11-22 | 2012-10-10 | Incyte Corp | Imidazotriazines and imidazo pyrimidines as kinase inhibitors |
| BRPI0807893A2 (pt) * | 2007-02-20 | 2014-06-17 | Novartis Ag | Imidazoquinolinas como inibidores duais de lipídio quinase e mtor. |
| AU2009221164B2 (en) * | 2008-03-05 | 2012-07-26 | Novartis Ag | Use of pyrimidine derivatives for the treatment of EGFR dependent diseases or diseases that have acquired resistance to agents that target EGFR family members |
| DK2300455T3 (en) * | 2008-05-21 | 2017-10-30 | Incyte Holdings Corp | SALTS OF 2-FLUORO-N-METHYL-4- [7- (QUINOLIN-6-YL-METHYL) - IMIDAZO [1,2-B] [1,2,4] TRIAZIN-2-YL] BENZAMIDE AND PROCEDURES WITH THE PREPARATION THEREOF |
| KR20110028651A (ko) * | 2008-07-11 | 2011-03-21 | 노파르티스 아게 | (a) 포스포이노시타이드 3-키나제 억제제 및 (b) ras/raf/mek 경로의 조절제의 조합물 |
| UA104147C2 (uk) * | 2008-09-10 | 2014-01-10 | Новартис Аг | Похідна піролідиндикарбонової кислоти та її застосування у лікуванні проліферативних захворювань |
| WO2010121175A1 (en) * | 2009-04-17 | 2010-10-21 | Rush University Medical Center | Combination targeted therapy for lung cancer |
| AR083267A1 (es) * | 2010-10-04 | 2013-02-13 | Novartis Ag | Combinaciones farmaceuticas |
| JP2013542228A (ja) * | 2010-11-08 | 2013-11-21 | ノバルティス アーゲー | Egfr依存性疾患またはegfrファミリーメンバーを標的とする薬剤に対して獲得耐性を有する疾患の治療における2−カルボキサミドシクロアミノウレア誘導体の使用 |
-
2013
- 2013-08-14 US US14/420,792 patent/US20150216870A1/en not_active Abandoned
- 2013-08-14 AU AU2013302702A patent/AU2013302702A1/en not_active Abandoned
- 2013-08-14 CN CN201380043882.3A patent/CN105050623B/zh not_active Expired - Fee Related
- 2013-08-14 HK HK15112283.4A patent/HK1211476A1/xx unknown
- 2013-08-14 IN IN528DEN2015 patent/IN2015DN00528A/en unknown
- 2013-08-14 CA CA2879704A patent/CA2879704A1/en not_active Abandoned
- 2013-08-14 MX MX2015002005A patent/MX369518B/es active IP Right Grant
- 2013-08-14 EP EP13751058.2A patent/EP2885003B1/en not_active Not-in-force
- 2013-08-14 KR KR1020157003716A patent/KR102245985B1/ko not_active Expired - Fee Related
- 2013-08-14 JP JP2015527558A patent/JP2015529194A/ja not_active Withdrawn
- 2013-08-14 ES ES13751058T patent/ES2901712T3/es active Active
- 2013-08-14 KR KR1020217012172A patent/KR20210049187A/ko not_active Ceased
- 2013-08-14 RU RU2015108755A patent/RU2705095C2/ru active
- 2013-08-14 BR BR112015002528-5A patent/BR112015002528A2/pt not_active Application Discontinuation
- 2013-08-14 WO PCT/US2013/054848 patent/WO2014028566A1/en not_active Ceased
-
2016
- 2016-10-06 AU AU2016238903A patent/AU2016238903A1/en not_active Abandoned
-
2017
- 2017-10-18 JP JP2017201774A patent/JP6644042B2/ja not_active Expired - Fee Related
-
2018
- 2018-03-09 AU AU2018201725A patent/AU2018201725A1/en not_active Abandoned
- 2018-10-11 US US16/157,333 patent/US20190083500A1/en not_active Abandoned
-
2019
- 2019-07-30 US US16/526,027 patent/US20190350935A1/en not_active Abandoned
- 2019-09-05 AU AU2019226212A patent/AU2019226212B2/en not_active Ceased
-
2020
- 2020-01-07 JP JP2020000928A patent/JP6970217B2/ja not_active Expired - Fee Related
- 2020-03-17 US US16/820,886 patent/US20200253980A1/en not_active Abandoned
-
2021
- 2021-12-15 US US17/644,491 patent/US20220280523A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| RU2705095C2 (ru) | 2019-11-05 |
| MX2015002005A (es) | 2015-10-08 |
| EP2885003B1 (en) | 2021-09-29 |
| WO2014028566A1 (en) | 2014-02-20 |
| US20220280523A1 (en) | 2022-09-08 |
| US20190083500A1 (en) | 2019-03-21 |
| KR102245985B1 (ko) | 2021-04-30 |
| US20190350935A1 (en) | 2019-11-21 |
| CA2879704A1 (en) | 2014-02-20 |
| IN2015DN00528A (es) | 2015-06-26 |
| MX369518B (es) | 2019-11-11 |
| BR112015002528A2 (pt) | 2018-05-22 |
| KR20210049187A (ko) | 2021-05-04 |
| HK1211476A1 (en) | 2016-05-27 |
| AU2018201725A1 (en) | 2018-04-05 |
| AU2016238903A1 (en) | 2016-10-27 |
| EP2885003A1 (en) | 2015-06-24 |
| JP6970217B2 (ja) | 2021-11-24 |
| CN105050623A (zh) | 2015-11-11 |
| US20200253980A1 (en) | 2020-08-13 |
| JP6644042B2 (ja) | 2020-02-12 |
| AU2019226212B2 (en) | 2020-05-14 |
| US20150216870A1 (en) | 2015-08-06 |
| JP2020079243A (ja) | 2020-05-28 |
| CN105050623B (zh) | 2018-06-12 |
| RU2015108755A (ru) | 2016-10-10 |
| AU2019226212A1 (en) | 2019-09-26 |
| AU2013302702A1 (en) | 2015-02-19 |
| KR20150043328A (ko) | 2015-04-22 |
| JP2015529194A (ja) | 2015-10-05 |
| JP2018035188A (ja) | 2018-03-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2901712T3 (es) | Combinación de un inhibidor de pi3k y un inhibidor de c-met. | |
| ES2952265T3 (es) | Terapia combinada que comprende un inhibidor de Raf y trametinib | |
| US9675595B2 (en) | Synergistic combinations of PI3K- and MEK-inhibitors | |
| US20160129003A1 (en) | Pharmaceutical Combinations | |
| CN107427522A (zh) | 用于治疗黑素瘤的阿吡莫德 | |
| JP2016520662A (ja) | Pi3k阻害剤および微小管不安定化剤の医薬組み合わせ | |
| US20180280370A1 (en) | Dosage regimen for a phosphatidylinositol 3-kinase inhibitor | |
| EP4203963B1 (en) | Combination therapy of naporafenib and trametinib for use in the treatment of sarcoma |