ES2905409T3 - Colorantes trisazoicos negros, su preparación y uso - Google Patents
Colorantes trisazoicos negros, su preparación y uso Download PDFInfo
- Publication number
- ES2905409T3 ES2905409T3 ES15791670T ES15791670T ES2905409T3 ES 2905409 T3 ES2905409 T3 ES 2905409T3 ES 15791670 T ES15791670 T ES 15791670T ES 15791670 T ES15791670 T ES 15791670T ES 2905409 T3 ES2905409 T3 ES 2905409T3
- Authority
- ES
- Spain
- Prior art keywords
- group
- general formula
- carbon atoms
- coom
- dye
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000000975 dye Substances 0.000 title claims description 102
- 238000002360 preparation method Methods 0.000 title claims description 31
- 125000004432 carbon atom Chemical group C* 0.000 claims abstract description 39
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims abstract description 34
- 125000001424 substituent group Chemical group 0.000 claims abstract description 22
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 claims abstract description 17
- 150000001408 amides Chemical class 0.000 claims abstract description 16
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 15
- 125000000565 sulfonamide group Chemical class 0.000 claims abstract description 15
- 125000003545 alkoxy group Chemical group 0.000 claims abstract description 13
- 229940124530 sulfonamide Drugs 0.000 claims abstract description 7
- 150000003456 sulfonamides Chemical class 0.000 claims abstract description 7
- 150000001768 cations Chemical class 0.000 claims abstract description 6
- 125000004185 ester group Chemical group 0.000 claims abstract description 6
- 125000005843 halogen group Chemical group 0.000 claims abstract description 6
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 claims abstract description 5
- 125000003368 amide group Chemical group 0.000 claims abstract description 5
- -1 atom hydrogen Chemical class 0.000 claims abstract description 4
- 229910052751 metal Inorganic materials 0.000 claims abstract description 4
- 239000002184 metal Substances 0.000 claims abstract description 4
- 125000003277 amino group Chemical group 0.000 claims abstract description 3
- 125000001174 sulfone group Chemical class 0.000 claims abstract 5
- 229910052739 hydrogen Inorganic materials 0.000 claims abstract 3
- 125000001931 aliphatic group Chemical group 0.000 claims abstract 2
- 125000002560 nitrile group Chemical group 0.000 claims abstract 2
- 229920006395 saturated elastomer Polymers 0.000 claims abstract 2
- 239000000976 ink Substances 0.000 claims description 27
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 26
- 239000003086 colorant Substances 0.000 claims description 19
- 239000007788 liquid Substances 0.000 claims description 16
- 238000007641 inkjet printing Methods 0.000 claims description 13
- 238000000034 method Methods 0.000 claims description 11
- 239000000203 mixture Substances 0.000 claims description 11
- 238000004043 dyeing Methods 0.000 claims description 7
- 239000002253 acid Substances 0.000 claims description 6
- 230000015572 biosynthetic process Effects 0.000 claims description 6
- 230000003287 optical effect Effects 0.000 claims description 6
- 239000000758 substrate Substances 0.000 claims description 6
- ZUQOBHTUMCEQBG-UHFFFAOYSA-N 4-amino-5-hydroxynaphthalene-1,7-disulfonic acid Chemical compound OS(=O)(=O)C1=CC(O)=C2C(N)=CC=C(S(O)(=O)=O)C2=C1 ZUQOBHTUMCEQBG-UHFFFAOYSA-N 0.000 claims description 5
- 230000007935 neutral effect Effects 0.000 claims description 5
- 239000012530 fluid Substances 0.000 claims description 4
- 239000000463 material Substances 0.000 claims description 4
- 230000002378 acidificating effect Effects 0.000 claims description 3
- 150000001450 anions Chemical class 0.000 claims description 3
- 150000001875 compounds Chemical class 0.000 claims description 3
- 238000006193 diazotization reaction Methods 0.000 claims description 3
- 239000010985 leather Substances 0.000 claims description 3
- 238000007639 printing Methods 0.000 claims description 3
- 239000002904 solvent Substances 0.000 claims description 3
- 229910052782 aluminium Inorganic materials 0.000 claims description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 claims description 2
- 150000001412 amines Chemical class 0.000 claims description 2
- 239000012736 aqueous medium Substances 0.000 claims description 2
- 125000006367 bivalent amino carbonyl group Chemical group [H]N([*:1])C([*:2])=O 0.000 claims description 2
- 238000005859 coupling reaction Methods 0.000 claims description 2
- 230000005693 optoelectronics Effects 0.000 claims description 2
- 229920002994 synthetic fiber Polymers 0.000 claims description 2
- 239000012209 synthetic fiber Substances 0.000 claims description 2
- 239000007791 liquid phase Substances 0.000 claims 5
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 claims 2
- 229940083957 1,2-butanediol Drugs 0.000 claims 1
- 229940015975 1,2-hexanediol Drugs 0.000 claims 1
- CUVLMZNMSPJDON-UHFFFAOYSA-N 1-(1-butoxypropan-2-yloxy)propan-2-ol Chemical compound CCCCOCC(C)OCC(C)O CUVLMZNMSPJDON-UHFFFAOYSA-N 0.000 claims 1
- WDQFELCEOPFLCZ-UHFFFAOYSA-N 1-(2-hydroxyethyl)pyrrolidin-2-one Chemical compound OCCN1CCCC1=O WDQFELCEOPFLCZ-UHFFFAOYSA-N 0.000 claims 1
- COBPKKZHLDDMTB-UHFFFAOYSA-N 2-[2-(2-butoxyethoxy)ethoxy]ethanol Chemical compound CCCCOCCOCCOCCO COBPKKZHLDDMTB-UHFFFAOYSA-N 0.000 claims 1
- MRABAEUHTLLEML-UHFFFAOYSA-N Butyl lactate Chemical compound CCCCOC(=O)C(C)O MRABAEUHTLLEML-UHFFFAOYSA-N 0.000 claims 1
- ZJCCRDAZUWHFQH-UHFFFAOYSA-N Trimethylolpropane Chemical compound CCC(CO)(CO)CO ZJCCRDAZUWHFQH-UHFFFAOYSA-N 0.000 claims 1
- 150000007513 acids Chemical class 0.000 claims 1
- 230000003115 biocidal effect Effects 0.000 claims 1
- 239000003139 biocide Substances 0.000 claims 1
- BMRWNKZVCUKKSR-UHFFFAOYSA-N butane-1,2-diol Chemical compound CCC(O)CO BMRWNKZVCUKKSR-UHFFFAOYSA-N 0.000 claims 1
- 239000001191 butyl (2R)-2-hydroxypropanoate Substances 0.000 claims 1
- 150000001989 diazonium salts Chemical class 0.000 claims 1
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 claims 1
- 229940028356 diethylene glycol monobutyl ether Drugs 0.000 claims 1
- 239000004210 ether based solvent Substances 0.000 claims 1
- 235000011187 glycerol Nutrition 0.000 claims 1
- FHKSXSQHXQEMOK-UHFFFAOYSA-N hexane-1,2-diol Chemical compound CCCCC(O)CO FHKSXSQHXQEMOK-UHFFFAOYSA-N 0.000 claims 1
- 239000007783 nanoporous material Substances 0.000 claims 1
- JCGNDDUYTRNOFT-UHFFFAOYSA-N oxolane-2,4-dione Chemical compound O=C1COC(=O)C1 JCGNDDUYTRNOFT-UHFFFAOYSA-N 0.000 claims 1
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 claims 1
- HXJUTPCZVOIRIF-UHFFFAOYSA-N sulfolane Chemical compound O=S1(=O)CCCC1 HXJUTPCZVOIRIF-UHFFFAOYSA-N 0.000 claims 1
- 150000003457 sulfones Chemical class 0.000 claims 1
- 229940113165 trimethylolpropane Drugs 0.000 claims 1
- 239000001257 hydrogen Substances 0.000 abstract 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 abstract 1
- 239000000725 suspension Substances 0.000 description 26
- 125000000664 diazo group Chemical group [N-]=[N+]=[*] 0.000 description 19
- ALYNCZNDIQEVRV-UHFFFAOYSA-N 4-aminobenzoic acid Chemical compound NC1=CC=C(C(O)=O)C=C1 ALYNCZNDIQEVRV-UHFFFAOYSA-N 0.000 description 18
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 15
- 239000000243 solution Substances 0.000 description 13
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 10
- 229960004050 aminobenzoic acid Drugs 0.000 description 9
- JJYPMNFTHPTTDI-UHFFFAOYSA-N 3-methylaniline Chemical compound CC1=CC=CC(N)=C1 JJYPMNFTHPTTDI-UHFFFAOYSA-N 0.000 description 8
- 239000007864 aqueous solution Substances 0.000 description 8
- 150000008049 diazo compounds Chemical class 0.000 description 8
- WXWCDTXEKCVRRO-UHFFFAOYSA-N para-Cresidine Chemical compound COC1=CC=C(C)C=C1N WXWCDTXEKCVRRO-UHFFFAOYSA-N 0.000 description 8
- 238000003756 stirring Methods 0.000 description 8
- YDUSPRIPZPLXMR-UHFFFAOYSA-N 4-(4-amino-3-nitroanilino)-4-oxobutanoic acid Chemical compound NC1=C(C=C(C=C1)NC(CCC(=O)O)=O)[N+](=O)[O-] YDUSPRIPZPLXMR-UHFFFAOYSA-N 0.000 description 6
- LPXPTNMVRIOKMN-UHFFFAOYSA-M sodium nitrite Chemical compound [Na+].[O-]N=O LPXPTNMVRIOKMN-UHFFFAOYSA-M 0.000 description 6
- LTASFWDWBYFZQQ-UHFFFAOYSA-N 2-amino-5-nitrobenzenesulfonic acid Chemical compound NC1=CC=C([N+]([O-])=O)C=C1S(O)(=O)=O LTASFWDWBYFZQQ-UHFFFAOYSA-N 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 238000001035 drying Methods 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- IOVCWXUNBOPUCH-UHFFFAOYSA-N Nitrous acid Chemical compound ON=O IOVCWXUNBOPUCH-UHFFFAOYSA-N 0.000 description 3
- CBENFWSGALASAD-UHFFFAOYSA-N Ozone Chemical compound [O-][O+]=O CBENFWSGALASAD-UHFFFAOYSA-N 0.000 description 3
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 3
- LNOPIUAQISRISI-UHFFFAOYSA-N n'-hydroxy-2-propan-2-ylsulfonylethanimidamide Chemical compound CC(C)S(=O)(=O)CC(N)=NO LNOPIUAQISRISI-UHFFFAOYSA-N 0.000 description 3
- 239000003960 organic solvent Substances 0.000 description 3
- 235000010288 sodium nitrite Nutrition 0.000 description 3
- 238000003860 storage Methods 0.000 description 3
- 239000004753 textile Substances 0.000 description 3
- VZLLZDZTQPBHAZ-UHFFFAOYSA-N 2-nitroaniline-4-sulfonic acid Chemical compound NC1=CC=C(S(O)(=O)=O)C=C1[N+]([O-])=O VZLLZDZTQPBHAZ-UHFFFAOYSA-N 0.000 description 2
- ZAJAQTYSTDTMCU-UHFFFAOYSA-N 3-aminobenzenesulfonic acid Chemical compound NC1=CC=CC(S(O)(=O)=O)=C1 ZAJAQTYSTDTMCU-UHFFFAOYSA-N 0.000 description 2
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 2
- 229920000742 Cotton Polymers 0.000 description 2
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 2
- 229920000297 Rayon Polymers 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- UZZFFIUHUDOYPS-UHFFFAOYSA-L disodium 4-amino-3,6-bis[[4-[(2,4-diaminophenyl)diazenyl]phenyl]diazenyl]-5-oxido-7-sulfonaphthalene-2-sulfonate Chemical compound [Na+].[Na+].Nc1ccc(N=Nc2ccc(cc2)N=Nc2c(N)c3c(O)c(N=Nc4ccc(cc4)N=Nc4ccc(N)cc4N)c(cc3cc2S([O-])(=O)=O)S([O-])(=O)=O)c(N)c1 UZZFFIUHUDOYPS-UHFFFAOYSA-L 0.000 description 2
- 238000007654 immersion Methods 0.000 description 2
- NCBZRJODKRCREW-UHFFFAOYSA-N m-anisidine Chemical compound COC1=CC=CC(N)=C1 NCBZRJODKRCREW-UHFFFAOYSA-N 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 239000002609 medium Substances 0.000 description 2
- TWNQGVIAIRXVLR-UHFFFAOYSA-N oxo(oxoalumanyloxy)alumane Chemical class O=[Al]O[Al]=O TWNQGVIAIRXVLR-UHFFFAOYSA-N 0.000 description 2
- 238000004806 packaging method and process Methods 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- ASGMFNBUXDJWJJ-JLCFBVMHSA-N (1R,3R)-3-[[3-bromo-1-[4-(5-methyl-1,3,4-thiadiazol-2-yl)phenyl]pyrazolo[3,4-d]pyrimidin-6-yl]amino]-N,1-dimethylcyclopentane-1-carboxamide Chemical compound BrC1=NN(C2=NC(=NC=C21)N[C@H]1C[C@@](CC1)(C(=O)NC)C)C1=CC=C(C=C1)C=1SC(=NN=1)C ASGMFNBUXDJWJJ-JLCFBVMHSA-N 0.000 description 1
- ABJSOROVZZKJGI-OCYUSGCXSA-N (1r,2r,4r)-2-(4-bromophenyl)-n-[(4-chlorophenyl)-(2-fluoropyridin-4-yl)methyl]-4-morpholin-4-ylcyclohexane-1-carboxamide Chemical compound C1=NC(F)=CC(C(NC(=O)[C@H]2[C@@H](C[C@@H](CC2)N2CCOCC2)C=2C=CC(Br)=CC=2)C=2C=CC(Cl)=CC=2)=C1 ABJSOROVZZKJGI-OCYUSGCXSA-N 0.000 description 1
- IUSARDYWEPUTPN-OZBXUNDUSA-N (2r)-n-[(2s,3r)-4-[[(4s)-6-(2,2-dimethylpropyl)spiro[3,4-dihydropyrano[2,3-b]pyridine-2,1'-cyclobutane]-4-yl]amino]-3-hydroxy-1-[3-(1,3-thiazol-2-yl)phenyl]butan-2-yl]-2-methoxypropanamide Chemical compound C([C@H](NC(=O)[C@@H](C)OC)[C@H](O)CN[C@@H]1C2=CC(CC(C)(C)C)=CN=C2OC2(CCC2)C1)C(C=1)=CC=CC=1C1=NC=CS1 IUSARDYWEPUTPN-OZBXUNDUSA-N 0.000 description 1
- STBLNCCBQMHSRC-BATDWUPUSA-N (2s)-n-[(3s,4s)-5-acetyl-7-cyano-4-methyl-1-[(2-methylnaphthalen-1-yl)methyl]-2-oxo-3,4-dihydro-1,5-benzodiazepin-3-yl]-2-(methylamino)propanamide Chemical compound O=C1[C@@H](NC(=O)[C@H](C)NC)[C@H](C)N(C(C)=O)C2=CC(C#N)=CC=C2N1CC1=C(C)C=CC2=CC=CC=C12 STBLNCCBQMHSRC-BATDWUPUSA-N 0.000 description 1
- HUWSZNZAROKDRZ-RRLWZMAJSA-N (3r,4r)-3-azaniumyl-5-[[(2s,3r)-1-[(2s)-2,3-dicarboxypyrrolidin-1-yl]-3-methyl-1-oxopentan-2-yl]amino]-5-oxo-4-sulfanylpentane-1-sulfonate Chemical compound OS(=O)(=O)CC[C@@H](N)[C@@H](S)C(=O)N[C@@H]([C@H](C)CC)C(=O)N1CCC(C(O)=O)[C@H]1C(O)=O HUWSZNZAROKDRZ-RRLWZMAJSA-N 0.000 description 1
- XGLVDUUYFKXKPL-UHFFFAOYSA-N 2-(2-methoxyethoxy)-n,n-bis[2-(2-methoxyethoxy)ethyl]ethanamine Chemical compound COCCOCCN(CCOCCOC)CCOCCOC XGLVDUUYFKXKPL-UHFFFAOYSA-N 0.000 description 1
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 1
- ASDQMECUMYIVBG-UHFFFAOYSA-N 2-[2-(2-aminoethoxy)ethoxy]ethanol Chemical compound NCCOCCOCCO ASDQMECUMYIVBG-UHFFFAOYSA-N 0.000 description 1
- AJHPGXZOIAYYDW-UHFFFAOYSA-N 3-(2-cyanophenyl)-2-[(2-methylpropan-2-yl)oxycarbonylamino]propanoic acid Chemical compound CC(C)(C)OC(=O)NC(C(O)=O)CC1=CC=CC=C1C#N AJHPGXZOIAYYDW-UHFFFAOYSA-N 0.000 description 1
- BFQFAPOGSIVDJL-UHFFFAOYSA-N 3-[3-(4-amino-3-nitroanilino)-3-oxopropoxy]propanoic acid Chemical compound NC1=C(C=C(C=C1)NC(CCOCCC(=O)O)=O)[N+](=O)[O-] BFQFAPOGSIVDJL-UHFFFAOYSA-N 0.000 description 1
- AOMZHDJXSYHPKS-DROYEMJCSA-L Amido Black 10B Chemical compound [Na+].[Na+].[O-]S(=O)(=O)C1=CC2=CC(S([O-])(=O)=O)=C(\N=N\C=3C=CC=CC=3)C(O)=C2C(N)=C1\N=N\C1=CC=C(N(=O)=O)C=C1 AOMZHDJXSYHPKS-DROYEMJCSA-L 0.000 description 1
- BQXUPNKLZNSUMC-YUQWMIPFSA-N CCN(CCCCCOCC(=O)N[C@H](C(=O)N1C[C@H](O)C[C@H]1C(=O)N[C@@H](C)c1ccc(cc1)-c1scnc1C)C(C)(C)C)CCOc1ccc(cc1)C(=O)c1c(sc2cc(O)ccc12)-c1ccc(O)cc1 Chemical compound CCN(CCCCCOCC(=O)N[C@H](C(=O)N1C[C@H](O)C[C@H]1C(=O)N[C@@H](C)c1ccc(cc1)-c1scnc1C)C(C)(C)C)CCOc1ccc(cc1)C(=O)c1c(sc2cc(O)ccc12)-c1ccc(O)cc1 BQXUPNKLZNSUMC-YUQWMIPFSA-N 0.000 description 1
- 229940127007 Compound 39 Drugs 0.000 description 1
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical class [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- SMNRFWMNPDABKZ-WVALLCKVSA-N [[(2R,3S,4R,5S)-5-(2,6-dioxo-3H-pyridin-3-yl)-3,4-dihydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl] [[[(2R,3S,4S,5R,6R)-4-fluoro-3,5-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-hydroxyphosphoryl]oxy-hydroxyphosphoryl] hydrogen phosphate Chemical compound OC[C@H]1O[C@H](OP(O)(=O)OP(O)(=O)OP(O)(=O)OP(O)(=O)OC[C@H]2O[C@H]([C@H](O)[C@@H]2O)C2C=CC(=O)NC2=O)[C@H](O)[C@@H](F)[C@@H]1O SMNRFWMNPDABKZ-WVALLCKVSA-N 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 239000004411 aluminium Substances 0.000 description 1
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 239000013011 aqueous formulation Substances 0.000 description 1
- 229910052788 barium Inorganic materials 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- CRVGTESFCCXCTH-UHFFFAOYSA-O bis(2-hydroxyethyl)-methylazanium Chemical compound OCC[NH+](C)CCO CRVGTESFCCXCTH-UHFFFAOYSA-O 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-O bis(2-hydroxyethyl)azanium Chemical compound OCC[NH2+]CCO ZBCBWPMODOFKDW-UHFFFAOYSA-O 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 229910052792 caesium Inorganic materials 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 238000004040 coloring Methods 0.000 description 1
- 229940125878 compound 36 Drugs 0.000 description 1
- 229940125807 compound 37 Drugs 0.000 description 1
- 229940127573 compound 38 Drugs 0.000 description 1
- 238000010924 continuous production Methods 0.000 description 1
- 238000012864 cross contamination Methods 0.000 description 1
- 239000008367 deionised water Substances 0.000 description 1
- 229910021641 deionized water Inorganic materials 0.000 description 1
- 238000010612 desalination reaction Methods 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- 238000011026 diafiltration Methods 0.000 description 1
- 239000000982 direct dye Substances 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 238000005562 fading Methods 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 159000000011 group IA salts Chemical class 0.000 description 1
- 150000002484 inorganic compounds Chemical class 0.000 description 1
- 229910010272 inorganic material Inorganic materials 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 150000001457 metallic cations Chemical class 0.000 description 1
- 231100000219 mutagenic Toxicity 0.000 description 1
- 230000003505 mutagenic effect Effects 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- PIDFDZJZLOTZTM-KHVQSSSXSA-N ombitasvir Chemical compound COC(=O)N[C@@H](C(C)C)C(=O)N1CCC[C@H]1C(=O)NC1=CC=C([C@H]2N([C@@H](CC2)C=2C=CC(NC(=O)[C@H]3N(CCC3)C(=O)[C@@H](NC(=O)OC)C(C)C)=CC=2)C=2C=CC(=CC=2)C(C)(C)C)C=C1 PIDFDZJZLOTZTM-KHVQSSSXSA-N 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 229910052701 rubidium Inorganic materials 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 235000012239 silicon dioxide Nutrition 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 229910052712 strontium Inorganic materials 0.000 description 1
- 125000000547 substituted alkyl group Chemical group 0.000 description 1
- 238000004381 surface treatment Methods 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 125000005207 tetraalkylammonium group Chemical group 0.000 description 1
- DZLFLBLQUQXARW-UHFFFAOYSA-N tetrabutylammonium Chemical compound CCCC[N+](CCCC)(CCCC)CCCC DZLFLBLQUQXARW-UHFFFAOYSA-N 0.000 description 1
- QEMXHQIAXOOASZ-UHFFFAOYSA-N tetramethylammonium Chemical compound C[N+](C)(C)C QEMXHQIAXOOASZ-UHFFFAOYSA-N 0.000 description 1
- 210000002268 wool Anatomy 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B31/00—Disazo and polyazo dyes of the type A->B->C, A->B->C->D, or the like, prepared by diazotising and coupling
- C09B31/16—Trisazo dyes
- C09B31/26—Trisazo dyes from other coupling components "D"
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B41—PRINTING; LINING MACHINES; TYPEWRITERS; STAMPS
- B41J—TYPEWRITERS; SELECTIVE PRINTING MECHANISMS, i.e. MECHANISMS PRINTING OTHERWISE THAN FROM A FORME; CORRECTION OF TYPOGRAPHICAL ERRORS
- B41J2/00—Typewriters or selective printing mechanisms characterised by the printing or marking process for which they are designed
- B41J2/005—Typewriters or selective printing mechanisms characterised by the printing or marking process for which they are designed characterised by bringing liquid or particles selectively into contact with a printing material
- B41J2/01—Ink jet
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B33/00—Disazo and polyazo dyes of the types A->K<-B, A->B->K<-C, or the like, prepared by diazotising and coupling
- C09B33/18—Trisazo or higher polyazo dyes
- C09B33/22—Trisazo dyes of the type A->B->K<-C
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B67/00—Influencing the physical, e.g. the dyeing or printing properties of dyestuffs without chemical reactions, e.g. by treating with solvents grinding or grinding assistants, coating of pigments or dyes; Process features in the making of dyestuff preparations; Dyestuff preparations of a special physical nature, e.g. tablets, films
- C09B67/0033—Blends of pigments; Mixtured crystals; Solid solutions
- C09B67/0046—Mixtures of two or more azo dyes
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D11/00—Inks
- C09D11/02—Printing inks
- C09D11/03—Printing inks characterised by features other than the chemical nature of the binder
- C09D11/037—Printing inks characterised by features other than the chemical nature of the binder characterised by the pigment
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D11/00—Inks
- C09D11/16—Writing inks
- C09D11/17—Writing inks characterised by colouring agents
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D11/00—Inks
- C09D11/30—Inkjet printing inks
- C09D11/32—Inkjet printing inks characterised by colouring agents
- C09D11/328—Inkjet printing inks characterised by colouring agents characterised by dyes
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Materials Engineering (AREA)
- Wood Science & Technology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Inks, Pencil-Leads, Or Crayons (AREA)
- Ink Jet Recording Methods And Recording Media Thereof (AREA)
- Manufacturing & Machinery (AREA)
- Coloring (AREA)
- Optical Filters (AREA)
Abstract
Colorante trisazoico de fórmula general (V) **(Ver fórmula)** donde M se selecciona del grupo que consiste en H, un catión metálico, un catión amonio N(HkR5 m), en donde cada R5 se selecciona del grupo que consiste en -H, un grupo alifático sustituido o sin sustituir, saturado o insaturado que tiene de 1 a 18 átomos de carbono, y k es un número entero seleccionado de 0, 1, 2, 3, 4 y m = 4 - k, donde R1, R2 representan independientemente un átomo de hidrógeno, un grupo SO3M, un grupo COOM, un átomo de halógeno, un grupo NO2, un grupo éster, un grupo alquilo o alcoxi, teniendo cada uno de 1 a 6 átomos de carbono, un grupo amida o sulfonamida sin sustituir o sustituido o un grupo sulfona, teniendo cada uno hasta 12 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, OH, OCH3, NH2, Cl, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM, donde R3, R4 representan independientemente un átomo de hidrógeno, un grupo alquilo o alcoxi, teniendo cada uno de 1 a 6 átomos de carbono, un grupo amida o sulfonamida sin sustituir o sustituido, teniendo cada uno hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, OH, OCH3, NH2, Cl, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM donde o A representa un resto de fórmula general (VI) **(Ver fórmula)** en la que R6, R7, R8, R9, R10 representan independientemente un átomo de hidrógeno, un grupo SO3M, un grupo NO2, un grupo nitrilo, un grupo amino, un grupo COOM, un átomo de halógeno, un grupo éster, un grupo alquilo o alcoxi, teniendo cada uno de 1 a 2 átomos de carbono, un grupo amida o sulfonamida sin sustituir o sustituido o un grupo sulfona, teniendo cada uno hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, Cl, OH, OCH3, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM; o A representa un resto de fórmula general (VII) **(Ver fórmula)** en la que o es 0 o 1 y R11, R12, R13, R14 representan independientemente un átomo de hidrógeno, un grupo SO3M, un grupo NO2, un grupo COOM, un grupo amida o sulfonamida sin sustituir o sustituido que tiene hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, OH, OCH3, NH2, Cl, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM;
Description
DESCRIPCIÓN
Colorantes trisazoicos negros, su preparación y uso
Campo de la invención
La invención se refiere a nuevos colorantes trisazoicos negros y sus sales, un método para su preparación y su uso en operaciones de teñido e impresión. También se refiere a preparaciones de colorantes líquidos que contienen estos colorantes trisazoicos, en particular a fluidos acuosos de registro para impresión por chorro de tinta y para utensilios de escritura.
Antecedentes de la invención
La velocidad de las modernas impresoras de chorro de tinta tiene que aumentar constantemente por razones económicas. Las hojas de registro especialmente adecuadas para tales impresoras comprenden compuestos inorgánicos nanoporosos tales como por ejemplo dióxido de silicio, hidróxido/óxido de aluminio, óxido de aluminio o sus mezclas. Tales hojas de registro se conocen como "hojas de registro nanoporosas". Las imágenes impresas en estas hojas de registro deben tener una buena estabilidad de almacenamiento incluso en condiciones adversas. Esto solo se puede lograr mediante el uso de un sistema de tintas finamente ajustado, respectivamente, los colorantes que contiene.
Hasta el momento, estas imágenes no cumplen con todas las propiedades requeridas. En particular, la inalterabilidad frente al agua, la estabilidad frente a la luz, la estabilización frente al ozono, la tonalidad y el brillo de las imágenes impresas en estas hojas de registro no son satisfactorias. Así, se buscan nuevos colorantes que mejoren las propiedades mencionadas anteriormente de las imágenes impresas sobre estas hojas de registro, en particular en las zonas con tonalidad negra.
Además de esto, la impresión con chorro de tinta industrial es cada vez más importante en la industria del envasado y el envasado de alimentos. En ese segmento, la inalterabilidad frente al agua, la inalterabilidad frente a la luz y el uso de componentes seguros son imprescindibles. También se requiere que estas propiedades sean las mismas independientemente del medio de registro utilizado.
Aun así ya se han propuesto bastantes colorantes negros como colorantes negros para la impresión por chorro de tinta. Sin embargo, ninguno satisface todas las propiedades requeridas.
Además de esto los colorantes deben presentar una buena solubilidad en agua y ser seguros para el ser humano y desde el punto de vista ecológico.
Los siguientes colorantes negros se utilizan frecuentemente en impresoras industriales de chorro de tinta:
C.I. Acid Black 1 con la fórmula (I)
estándar.
(II) C.I. Direct Black 19
El Direct black 19 que presenta una buena inalterabilidad frente al agua generalmente está disponible como una mezcla que contiene diferentes productos secundarios y ha demostrado ser mutagénico (Patente de los Estados Unidos 5.340.929).
Aun así ya se han propuesto bastantes colorantes negros como colorantes negros para la impresión por chorro de tinta como en la patente de los Estados Unidos 5.423.906 y US 2012/0090503 A1. Sin embargo, ninguno satisface todas las propiedades requeridas.
Se han propuesto varios tipos de composiciones de tinta. Las tintas típicas comprenden uno o más colorantes o pigmentos, agua, codisolventes orgánicos y otros aditivos.
Las tintas deben satisfacer los siguientes criterios:
(1) La tinta debe dar imágenes de excelente calidad en cualquier tipo de hoja de registro.
(2) La tinta debe dar imágenes impresas que presenten buena inalterabilidad frente al agua.
(3) La tinta debe dar imágenes impresas que presenten buena estabilidad frente a la luz.
(4) La tinta debe dar imágenes impresas que presenten buena inalterabilidad frente al ozono.
(5) La tinta debe dar imágenes impresas que presenten una resistencia frente a los borrones excelente.
(6) La tinta debe proporcionar imágenes impresas que presenten una excelente estabilidad de almacenamiento en condiciones de alta temperatura y humedad.
(7) La tinta no debe obstruir las boquillas de chorro de las impresoras de chorro de tinta incluso cuando se mantiene destapada cuando el registro está suspendido durante largos períodos.
(8) La tinta debe poder almacenarse durante largos períodos sin deterioro de su calidad.
(9) La tinta debe ser no tóxica, no inflamable y segura.
Sumario de la invención
Un objetivo de la invención es la provisión de nuevos colorantes trisazoicos negros con tonalidad negra, en la medida de lo posible neutra, y su uso en tintas acuosas, en particular en fluidos de registro para impresión por chorro de tinta y para utensilios de escritura. Son particularmente ventajosos en la impresión por chorro de tinta para la preparación de imágenes o aplicación de color en hojas de registro nanoporosas de secado rápido. Estos nuevos colorantes trisazoicos negros con alto poder colorante tienen una excelente solubilidad en formulaciones acuosas, dan imágenes o coloraciones que tienen buenas propiedades generales, en particular en la impresión por chorro de tinta, donde proporcionan imágenes con tonalidad brillante, donde la nitidez de las imágenes no se deteriora o solo se deteriora ligeramente después de largos períodos de almacenamiento en condiciones de alta temperatura y humedad. Las imágenes también muestran una buena estabilidad frente a la luz y una excelente inalterabilidad frente al ozono y poco desteñido.
Un objetivo adicional de la invención es la provisión de preparaciones colorantes líquidas, en particular de tintas para impresión por chorro de tinta y para utensilios de escritura, dando una tonalidad espectralmente invariable en cualquier
tipo de hoja de registro.
Es otro objetivo de la invención proporcionar un método de fabricación de colorantes y/o composiciones de colorantes, tales como tintas, líquidos para registro, colorantes textiles y soluciones colorantes para fabricar filtros de color para aplicaciones ópticas y/u optoelectrónicas, todas las cuales tienen al menos algunas, preferentemente todas las propiedades ventajosas antes mencionadas. Además, es un objetivo de la invención proporcionar un método de aplicación de una composición colorante, tal como una tinta, un líquido de registro, o un colorante textil con al menos uno de los colorantes a un sustrato, preferentemente sin usar disolventes orgánicos volátiles.
Otro objetivo de la invención es la provisión de tintas que tengan todas las propiedades requeridas mencionadas anteriormente.
Descripción de la invención
La presente invención se refiere a colorantes trisazoicos novedosos de fórmula general (V)
donde
M representa un átomo de hidrógeno, un catión metálico o un catión amonio, que opcionalmente puede estar sustituido por uno o más grupos alquilo o alquilo sustituido teniendo cada uno de 1 a 18 átomos de C; donde
R1, R2 representan independientemente un átomo de hidrógeno, un grupo SO3M, un grupo COOM, un átomo de halógeno, un grupo NO2, un grupo éster, un grupo alquilo o alcoxi teniendo cada uno de 1 a 6 átomos de carbono, un grupo amida o sulfonamida sin sustituir o sustituido teniendo cada uno hasta 12 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, OH, OCH3, NH2, Cl, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM,
donde
R3, R4 representan independientemente un átomo de hidrógeno, un grupo alquilo o alcoxi teniendo cada uno de 1 a 6 átomos de carbono, un grupo amida o sulfonamida sin sustituir o sustituido teniendo cada uno hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, OH, OCH3, NH2, Cl, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM, donde
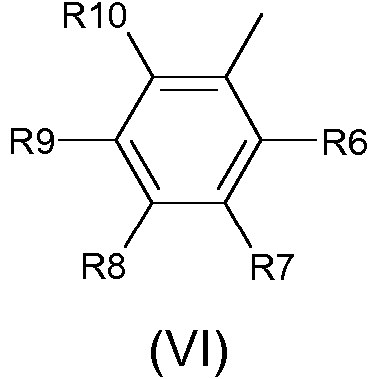
o A representa un resto de fórmula general (VI)
donde
R6, R7, R8, R9, R10 representan independientemente un átomo de hidrógeno, un grupo SO3M, un grupo NO2, un grupo amino, un grupo COOM, un átomo de halógeno, un grupo éster, un grupo alquilo o alcoxi teniendo cada uno de 1 a 2 átomos de carbono, un grupo amida o sulfonamida sin sustituir o sustituido teniendo cada uno hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, OH, OCH3, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM; o A representa un resto de fórmula general (VII)
en donde
o es 0 o 1 y
R11, R12, R13, R14 representan independientemente un átomo de hidrógeno, un grupo SO3M, un grupo NO2, un grupo COOM, un grupo amida o sulfonamida sin sustituir o sustituido teniendo hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, OH, OCH3, NH2, Cl, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM.
Los colorantes trisazoicos preferidos son de fórmula general (V), en donde M es como se ha definido anteriormente, R1, R2 representan independientemente un átomo de hidrógeno, un grupo SO3M, o un grupo COOM, un grupo amida o sulfonamida sin sustituir o sustituido teniendo hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, OH, OCH3, NH2, Cl, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM;
R3,R4 representan independientemente un átomo de hidrógeno, un grupo alquilo o alcoxi teniendo cada uno de 1 a 2 átomos de carbono, un grupo amida o sulfonamida sin sustituir o sustituido teniendo hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, OH, OCH3, NH2, Cl, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM;
A representa un resto de fórmula general (VI) como se ha descrito anteriormente
donde
R6, Rio representan independientemente un átomo de hidrógeno, un grupo SO3M, un grupo NO2, un grupo COOM (más particularmente independientemente un átomo de hidrógeno, un grupo SO3M, un grupo NO2) y
R7, R9 representan independientemente un átomo de hidrógeno, un grupo COOM (más preferentemente ambos representan un átomo de hidrógeno) y
R8, representa un grupo hidrógeno, un grupo SO3M, un grupo NO2, un grupo amida o sulfonamida sustituido teniendo hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, OH, OCH3, NH2, Cl, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM (más preferentemente un grupo SO3M, un grupo NO2, un grupo amida o sulfonamida sustituido como se ha descrito).
Incluso más particularmente preferidos son los colorantes trisazoicos de fórmula general (V), en donde M es como se ha definido anteriormente,
R1, R2 representan independientemente un átomo de hidrógeno o un grupo COOM;
R3,R4 representan independientemente un átomo de hidrógeno, un grupo alquilo o alcoxi teniendo cada uno de 1 a 2 átomos de carbono;
A representa un resto de fórmula general (VI) como se ha descrito anteriormente
donde
R6, R10 representan independientemente un átomo de hidrógeno, un grupo SO3M, o un grupo NO2, R7, R9 representan un átomo de hidrógeno, y
R8, representa un grupo SO3M, un grupo NO2 amida o sulfonamida sustituido teniendo hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM (lo más preferentemente R8 representa un grupo NO2, un grupo NHCOCH3, un grupo NHCOCH2CH2COOM, un grupo NHCO(CH2)3COOM o un grupo NHCOCH2OCH2COOM).
Como cationes metálicos, se prefieren los cationes de los metales alcalinos (Li, Na, K, Rb, Cs), de los metales alcalinotérreos (Mg, Ca, Sr, Ba) y el catión amonio, opcionalmente sustituidos con uno o más grupos alquilo teniendo cada uno de 1 a 4 átomos de carbono o con alquilo sustituido con hidroxi teniendo cada uno de 1 a 6 átomos de carbono.
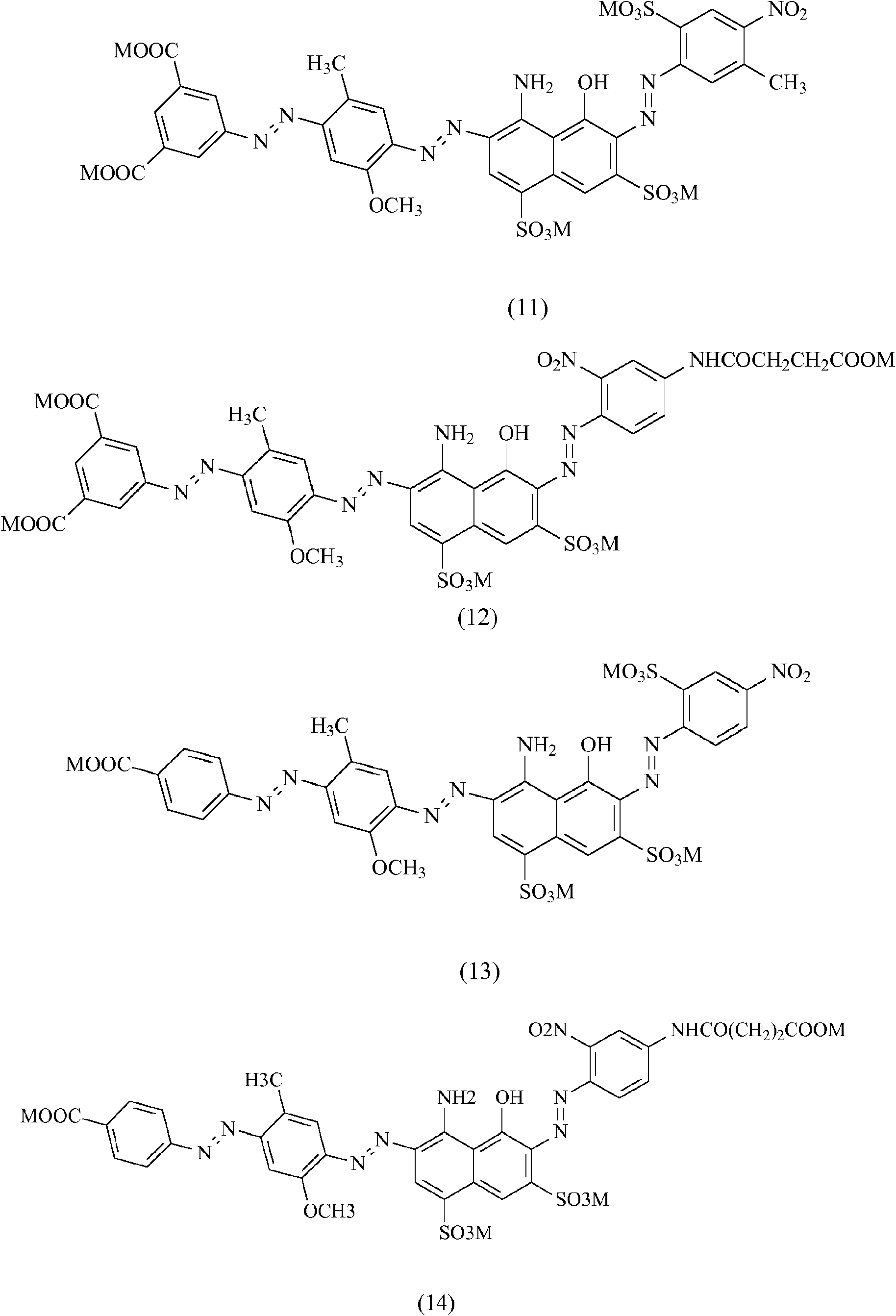
Ejemplos específicos de colorantes trisazoicos de fórmula general (IV) son los siguientes, donde el sustituyente M se define en la Tabla 1.
Los colorantes trisazoicos preparados de fórmula general (V) se enumeran en la Tabla 1 junto con su máximo de absorción en solución acuosa:
Tabla 1
continuación
Los colorantes trisazoicos de fórmula general (V) pueden estar en forma de ácido libre o en forma de sales inorgánicas u orgánicas de los mismos. Preferentemente, están en forma de sus sales alcalinas o de amonio, en donde el catión amonio puede estar sustituido. Ejemplos de tales cationes amonio sustituidos son 2-hidroxietilamonio, bis-(2-hidroxietil)-amonio, tris-(2-hidroxietil)-amonio, bis-(2-hidroxietil)-metilamonio, tris-[2 -(2 -metoxietoxi)-etil]-amonio, 8-hidroxi-3,6-dioxaoctilamonio y tetraalquilamonio tal como tetrametilamonio o tetrabutilamonio.
La invención no se refiere únicamente a colorantes trisazoicos puros de fórmula general (V), sino también a mezclas de estos colorantes trisazoicos.
La invención también se refiere a un método de preparación de los colorantes trisazoicos de fórmula general (V) de acuerdo con la invención, en donde una amina de fórmula general (VIII),
donde R1 y R2 son como se ha definido anteriormente, se diazota y posteriormente se acopla con un compuesto de fórmula general (IX),
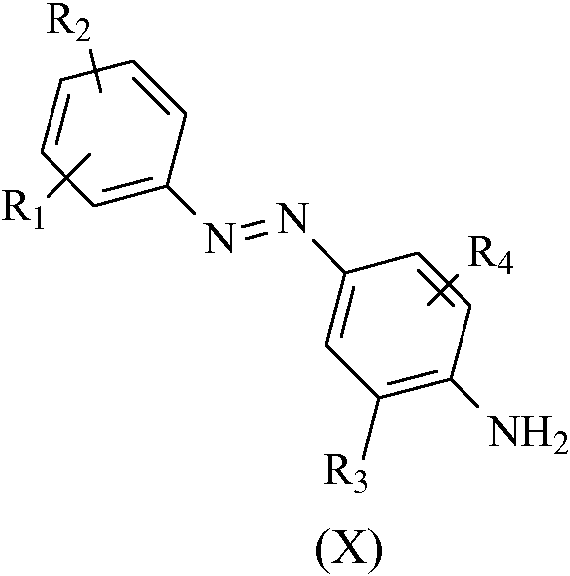
donde R3 y R4 son como se ha definido anteriormente, con un valor de pH ácido situado entre aproximadamente 1,0 y 3,0 con formación del colorante intermedio de fórmula general (X).
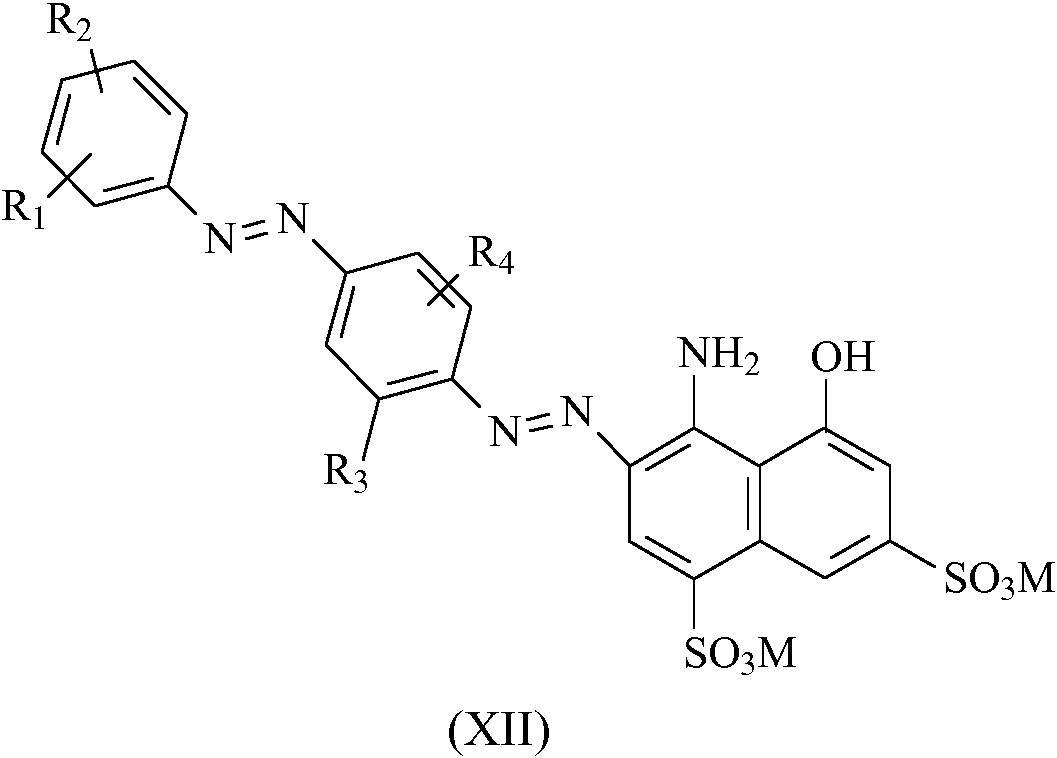
El colorante intermedio de fórmula general (X), en donde Ri, R2, R3 y R4 son como se han definido anteriormente, se diazota y posteriormente se acopla con K-Acid a un pH ácido situado entre un valor de 0,5 y 2,0 con formación del colorante intermedio de fórmula general (XII) donde R1, R2, R3 y R4 son como se han definido anteriormente y M es el catión metálico de la base utilizado para mantener el pH durante la reacción de acoplamiento.
El colorante intermedio de fórmula general (XII) se acopla además con un compuesto diazoico de fórmula general (XIII)
donde R6, R7, R8, R9 y R10 son como se han definido anteriormente,
o de fórmula general (XIV)
donde o, R11, R12, R13 y R14 son como se ha definido anteriormente y X es el anión del ácido usado durante la diazotización, a un pH más o menos neutro situado entre un valor de 5,0 y 9,0 con formación de los colorantes de fórmula general (V) de acuerdo con la invención.
Los colorantes trisazoicos de fórmula general (V) de acuerdo con la invención se usan para la tinción de materiales que contienen celulosa, papel, algodón, viscosa, cuero y lana para proporcionar materiales teñidos con buena inalterabilidad frente al agua y estabilidad frente a la luz.
Todos los métodos bien conocidos en las industrias textil y papelera para la tinción con colorantes sustantivos pueden usarse con los colorantes trisazoicos, preferentemente para el tratamiento de volumen o superficial de papel encolado o sin encolar. Los colorantes también se pueden usar en el teñido de hilos y piezas de algodón, viscosa y lino por el proceso de agotamiento de un licor largo o en un proceso continuo.
Los colorantes trisazoicos de acuerdo con la invención son particularmente adecuados para registrar texto e imágenes en hojas de registro, papel estucado o no estucado, para la tinción o impresión de materiales de fibra naturales o sintéticos, hojas de registro nanoporosas, cuero y aluminio.
La invención se refiere además a preparaciones colorantes líquidas que contienen al menos un colorante trisazoico de fórmula general (V). El uso de dichas preparaciones colorantes líquidas es particularmente preferido para la tinción de papel. Dichas preparaciones de colorantes concentradas estables, líquidas, preferentemente acuosas, pueden obtenerse utilizando métodos bien conocidos en la técnica, preferentemente por disolución en disolventes adecuados. Es especialmente ventajosa la posibilidad de preparar dichas preparaciones concentradas, acuosas y estables en el transcurso de la propia síntesis del colorante, sin aislamiento intermedio del colorante, por ejemplo después de una etapa de desalinización mediante diafiltración de la solución de reacción.
Los colorantes trisazoicos o mezclas de colorantes trisazoicos de fórmula general (V) son colorantes excelentes para la preparación de tintas para impresión por chorro de tinta y para utensilios de escritura.
Los colorantes trisazoicos de fórmula general (V) de acuerdo con la invención pueden combinarse con colorantes tonificantes, en particular colorantes como los descritos en las solicitudes de patente EP 0.755.984, EP 1.219.682, así como en las patentes US 5.074.914, US 5.684.140 y US 5.824.785, para obtener un tono negro aún más neutro.
Una tinta de este tipo comprende uno o varios de los colorantes trisazoicos de acuerdo con la invención en un medio acuoso líquido. La tinta contiene de 0,5 por ciento en peso a 20 por ciento en peso, preferentemente de 0,5 por ciento en peso a 8 por ciento en peso, de estos colorantes trisazoicos, basado en el peso total de la tinta. El medio líquido es preferentemente agua o una mezcla de agua y disolventes orgánicos miscibles en agua. Los disolventes orgánicos se citan por ejemplo en las patentes de Estados Unidos N.° 4.626.284, US 4.703.113, US 4.963.189 y solicitudes de patente GB 2.289.473, EP 0.425.150 y EP 0.597.672.
La presente invención se ilustrará con más detalle mediante los siguientes ejemplos sin limitar de ningún modo el alcance de los compuestos reivindicados.
Ejemplos
Ejemplo 1
El colorante trisazoico N.° 17 se preparó de la siguiente manera:
Componente diazoico del colorante
Suspensión diazoica A
Se suspendieron 30,8 g (0,22 Mol) de ácido 4-aminobenzoico (al 98 %) a temperatura ambiente en 200 ml de agua
y a continuación se enfriaron a una temperatura entre 0 °C y 5 °C y se añadió gota a gota una solución acuosa de ácido clorhídrico (37 %) durante un período de 10 minutos a una temperatura entre 0 °C y 10 °C con agitación y se añadieron lentamente 55 ml de una solución acuosa (4 N) de nitrito de sodio manteniendo la temperatura por debajo de 10 °C. Posteriormente, se continuó agitando durante 1 hora a una temperatura entre 0 °C y 5 °C. El exceso de ácido nitroso se eliminó posteriormente por reacción con ácido sulfámico.
Preparación del colorante de fórmula (XXV)
Se suspendieron 28,3 g (0,2 Mol) de 5-metil-o-anisidina (97 %) en 200 ml de agua y 22 ml de una solución acuosa de ácido clorhídrico (37 %) y la suspensión se agitó durante 2 h a temperatura ambiente. Posteriormente, la suspensión se enfrió hasta una temperatura entre 5 y 10 °C.
La suspensión diazoica A se añadió durante un período de 30 minutos a una temperatura interna entre 5 °C y 10 °C a la suspensión de la 5-metil-o-anisidina manteniendo el pH en un valor entre 0,5 y 1 mediante la adición de una solución de hidróxido de sodio (30 %). Terminada la adición, la agitación se continuó durante 18 horas a temperatura ambiente. El precipitado se filtró y se lavó con 50 ml de una solución de ácido clorhídrico al 3,5%. Después del secado, se obtuvieron 45,7 g del colorante de fórmula (XXV).
Suspensión diazoica B
Se disolvieron 14,3 g (50 mMol) de colorante de fórmula (XXV) en 100 ml de agua y 10 ml de N-metilpirrolidona a 80 °C ajustando el pH a un valor de 9,0 con la adición de una solución de NaOH al 30 %.
A continuación, la solución obtenida se enfrió hasta 0 °C a 5 °C y se añadieron 12,5 ml de una solución acuosa (4N) de nitrito de sodio. Con agitación, se añadieron gota a gota lentamente 13 ml de una solución acuosa de ácido clorhídrico (37 %) durante un período de 10 minutos a una temperatura entre 0 °C y 10 °C. Terminada la adición, la agitación se continuó durante 2 horas a esta temperatura. El exceso de ácido nitroso se eliminó posteriormente por reacción con ácido sulfámico.
Preparación del colorante diazoico de fórmula (XXVI)
Se suspendieron 21,3 g (50 mMol) de K-acid (CAS: 130-23-4) (75 %) en 200 ml de agua y 5 ml de una solución acuosa de hidróxido de sodio (30 %). A continuación, la suspensión se agitó durante 30 minutos a temperatura ambiente y a continuación se enfrió hasta 5 °C.
A esta suspensión se le añadió la suspensión diazoica B durante un período de 30 minutos a una temperatura interna entre 5 °C y 10 °C manteniendo el pH en un valor entre 1 y 2 mediante la adición simultánea de una solución saturada de acetato de sodio. Terminada la adición, la agitación se continuó durante 18 horas a temperatura ambiente. A continuación, la suspensión espesa se calentó a 80 °C y se disolvió mediante la adición de una solución de hidróxido de sodio (30 %) ajustando el pH a un valor de 9. A continuación, la solución caliente se filtró hasta la transparencia sobre celita. A continuación, precipitó el colorante (XXVI) disminuyendo el pH a un valor de 6 con la adición de ácido acético y con la adición de 10 g de cloruro sódico.
A continuación, se filtró el colorante intermedio (XXVI) y se lavó con 50 ml de agua. Después de secar se obtuvieron 26,4 g del colorante de fórmula (XXVI).
Suspensión diazoica C
Se suspendieron 30,8 g (0,22 Mol) de ácido 4-aminobenzoico (98 %) en 200 ml de agua y a continuación se enfriaron a una temperatura entre 5 °C y 10 °C. A la suspensión se le añadió gota a gota 50 ml de una solución acuosa de ácido clorhídrico (37 %) durante un período de 10 minutos con agitación y lentamente se añadieron 55 ml de una solución acuosa (4 N) de nitrito de sodio manteniendo la temperatura entre 0 °C y 10 °C. El exceso de ácido nitroso se eliminó por reacción con ácido sulfámico.
Preparación del colorante trisazoico N.° 17 (17)
Se suspendieron 7,4 g (12 mMol) de colorante de fórmula (XXVI) en 100 ml de agua y se enfriaron entre 0 °C y 5 °C. Posteriormente, se añadieron lentamente a la suspensión 12 mMol de la suspensión diazoica C durante un período de 30 min manteniendo la temperatura por debajo de 5 °C y manteniendo el pH en un valor de 6,0 a 7,5 mediante la adición simultánea de una solución de hidróxido de sodio (20 %).
Terminada la adición, se continuó agitando durante 2 horas a una temperatura entre 0 °C y 5 °C y a continuación se dejó calentar a temperatura ambiente. Después de 2 horas, la solución oscura se filtró hasta la transparencia y el filtrado se concentró con un evaporador rotatorio. A continuación, el colorante N.° 17 precipitó mediante la adición de metanol y se filtró.
El colorante bruto se purificó con 60 ml de una solución acuosa (80 %) de etanol. Después del secado, se obtuvieron 6 g del colorante 17 en forma de su sal sódica.
Los colorantes trisazoicos números (10) a (16) y (18) a (40) de acuerdo con la invención se pueden preparar de manera similar usando materiales de partida apropiados, por ejemplo, como se describe a continuación con respecto a los colorantes trisazoicos números (31) a (40):
Preparación de (A) preparación igual a la del colorante de fórmula (XXVI). Sin embargo, se utilizaron ácido 3-aminobenzoico y m-toluidina en lugar de ácido 4-aminobenzoico y 5-metil-o-anisidina, respectivamente.
Preparación de (B) preparación igual a la del colorante de fórmula (XXVI). Sin embargo, se utilizó m-toluidina en lugar de 5-metil-o-anisidina.
Preparación de (C) preparación igual a la del colorante de fórmula (XXVI). Sin embargo, se usó anilina 2,5-disulfónica en lugar de ácido 4-aminobenzoico.
Preparación de (D) preparación igual a la del colorante de fórmula (XXVI). Sin embargo, se utilizaron ácido 3-aminobencenosulfónico y m-metoxianilina en lugar de ácido 4-aminobenzoico y 5-metil-o-anisidina, respectivamente.
Preparación de (E) preparación igual a la del colorante de fórmula (XXVI). Sin embargo, se utilizaron ácido 4-[(4-amino-3-nitrofenil)amino]-4-oxobutanoico y m-toluidina en lugar de ácido 4-aminobenzoico y 5-metil-o-anisidina, respectivamente.
Se usó la suspensión diazoica (C) y ácido 4-nitroanilina-2-sulfónico en lugar del compuesto diazoico (XXVI) y ácido 4-aminobenzoico del ejemplo 1.
Preparación de (D) preparación igual a la del colorante de fórmula (XXVI). Sin embargo, se utilizaron ácido 3-aminobencenosulfónico y m-metoxianilina en lugar de ácido 4-aminobenzoico y 5-metil-o-anisidina, respectivamente.
Preparación de (E) preparación igual a la del colorante de fórmula (XXVI). Sin embargo, se utilizaron ácido 4-[(4-amino-3-nitrofenil)amino]-4-oxobutanoico y m-toluidina en lugar de ácido 4-aminobenzoico y 5-metil-o-anisidina, respectivamente.
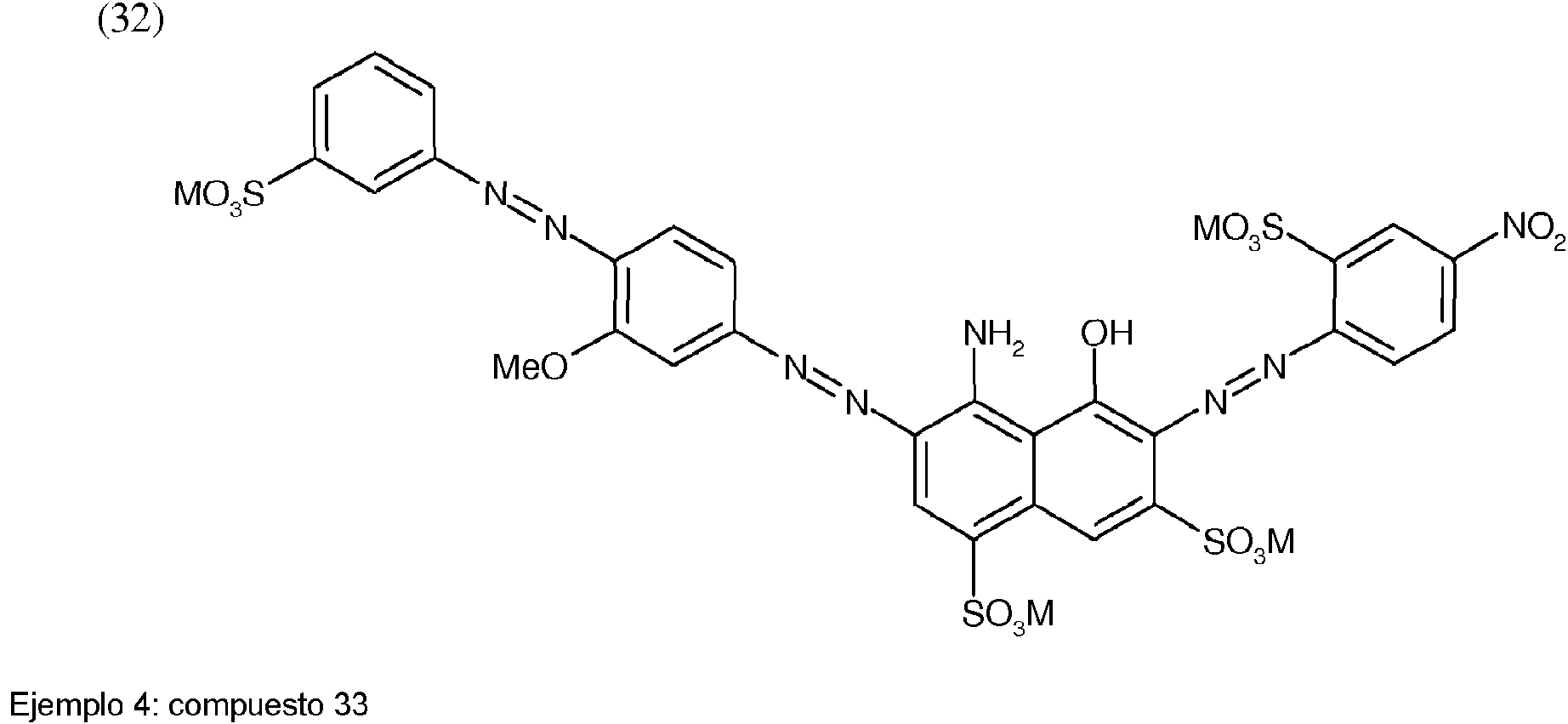
Ejemplo 3: compuesto 32
Se usó la suspensión diazoica (D) en lugar de la suspensión diazoica (C) del ejemplo 2.
Se usó la suspensión diazoica (A) en lugar de la suspensión diazoica (C) del ejemplo 2.
Ejemplo 5: compuesto 34
Se utilizó ácido 4-[(4-amino-3-nitrofenil)amino]-4-oxobutanoico en lugar del ácido 4-nitroanilina-2-sulfónico del ejemplo 4.
Ejemplo 6: compuesto 35
Se usó la suspensión diazoica (E) en lugar de la suspensión diazoica (A) del ejemplo 5.
Ejemplo 7: compuesto 36
Se usó la suspensión diazoica (B) en lugar de la suspensión diazoica (A) del ejemplo 5.
Ejemplo 8: compuesto 37
Se usó ácido 4-nitroanilina-2-sulfónico en lugar del ácido 4-[(4-amino-3-nitrofenil)amino]-4-oxobutanoico del ejemplo 7.
Ejemplo 9: compuesto 38
Se usó la suspensión diazoica (A) y ácido 2-nitroanilina-4-sulfónico en lugar de la suspensión diazoica (B) y ácido 4-nitroanilina-2-sulfónico del ejemplo 8, respectivamente.
Ejemplo 10: compuesto 39
Se utilizó ácido 4-[(4-amino-3-nitrofenil)amino]-4-oxobutanoico en lugar del ácido 2-nitroanilina-4-sulfónico del ejemplo 9.
Ejemplo 11: compuesto 40
Se utilizó ácido 3-{3-[(4-amino-3-nitrofenil)amino]-3-oxopropoxi}propanoico en lugar del ácido 4-[(4-amino-3-nitrofenil)amino]-4-oxobutanoico del ejemplo 7.
(C) Inalterabilidad frente al agua
Los patrones se imprimieron en los medios de registro 1 y 2 y se probaron como se describe en la prueba ISO 18935:2005(E), Método 3 - Remojo en agua, con las siguientes diferencias:
a. el tiempo de inmersión en las presentes pruebas se fijó en 1 minuto a diferencia de la norma ISO 18935:2005(E), en la que el tiempo de inmersión establecido es de 1 hora;
b. solo el patrón negro se prepara de acuerdo con el procedimiento descrito anteriormente.
En primer lugar, se midió la densidad óptica (DO Patrón no empapado) de los patrones de color en las muestras con un densitómetro Spectrolino® 1 día después de haber sido impreso. A continuación, las muestras con los patrones se sumergieron en agua desionizada a temperatura ambiente durante 1 minuto. A continuación, las muestras con los patrones se retiraron y se colgaron verticalmente para que se secaran durante 1 hora. Se utilizaron recipientes separados para cada muestra para evitar la contaminación cruzada. La densidad óptica (DO Patrón empapado) de los patrones de color, tratados con agua se midió con un densitómetro Spectrolino®. El porcentaje calculado de inalterabilidad frente al agua se expresa de acuerdo con la siguiente fórmula:
¡ DO Patrón empapado \
Pérdida de densidad óptica = 11 -------------- ;-------------------— I * 100%
V DO Patrón no empapado/
Los valores bajos de pérdida de densidad óptica indican una buena inalterabilidad frente al agua de un colorante.
Resultados
Los valores medidos de L*a*b* (iluminante D65) de los colorantes trisazoicos de acuerdo con la invención y los colorantes trisazoicos (I) y (II) que representan el estado de la técnica se enumeran en la Tabla 2.
Tabla 2
_____ _____
Una comparación de los valores L*a*b* medidos en la Tabla 2 muestra inmediatamente que las tintas que contienen los colorantes trisazoicos de acuerdo con la invención dan regiones de imagen negras que tienen valores más bajos de b* en comparación con regiones de imagen impresas con tintas que contienen el colorante trisazoico (I). Los colorantes trisazoicos de acuerdo con la invención son por lo tanto particularmente adecuados en la impresión por chorro de tinta, porque permiten una reproducción de los negros más neutra comparable al colorante (II) que representa el estado de la técnica.
Una comparación de las pérdidas de densidad medidas de las muestras impresas en la Tabla 3 muestra inmediatamente que los colorantes trisazoicos (12) y (14) de acuerdo con la invención tienen una estabilidad frente a la luz considerablemente mejorada en comparación con los colorantes trisazoicos (I) y (II) que representan el estado de la técnica.
Tabla 3
____ ___
La inalterabilidad frente al agua (WF) de las hojas de registro 1 y 2 se enumera en la Tabla 4
Tabla 4
___ ___
Con respecto a la inalterabilidad frente a la luz y al agua indicadas respectivamente en las Tablas 3 y 4, los colorantes 12 y 14 tienen una inalterabilidad frente a la luz y al agua considerablemente mejor que el colorante comercial (I) y una inalterabilidad frente a la luz mucho mejor que el colorante comercial (II) que representa el estado de la técnica.
Esto significa que las imágenes negras impresas por chorro de tinta resistente al agua usando los colorantes trisazoicos de acuerdo con la invención se desvanecen mucho menos que las imágenes negras que contienen los colorantes trisazoicos conocidos que representan el estado de la técnica.
Claims (15)
1. Colorante trisazoico de fórmula general (V)
donde
M se selecciona del grupo que consiste en H, un catión metálico, un catión amonio N(HkR5 m), en donde cada R5 se selecciona del grupo que consiste en -H, un grupo alifático sustituido o sin sustituir, saturado o insaturado que tiene de 1 a 18 átomos de carbono, y
k es un número entero seleccionado de 0, 1, 2, 3, 4 y
m = 4 - k,
donde
R1, R2 representan independientemente un átomo de hidrógeno, un grupo SO3M, un grupo COOM, un átomo de halógeno, un grupo NO2, un grupo éster, un grupo alquilo o alcoxi, teniendo cada uno de 1 a 6 átomos de carbono, un grupo amida o sulfonamida sin sustituir o sustituido o un grupo sulfona, teniendo cada uno hasta 12 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, OH, OCH3, NH2, Cl, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM,
donde
R3, R4 representan independientemente un átomo de hidrógeno, un grupo alquilo o alcoxi, teniendo cada uno de 1 a 6 átomos de carbono, un grupo amida o sulfonamida sin sustituir o sustituido, teniendo cada uno hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, OH, OCH3, NH2, Cl, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM
donde
o A representa un resto de fórmula general (VI)
en la que
R6, R7, R8, R9, R10 representan independientemente un átomo de hidrógeno, un grupo SO3M, un grupo NO2,
un grupo nitrilo, un grupo amino, un grupo COOM, un átomo de halógeno, un grupo éster, un grupo alquilo o alcoxi, teniendo cada uno de 1 a 2 átomos de carbono, un grupo amida o sulfonamida sin sustituir o sustituido o un grupo sulfona, teniendo cada uno hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, Cl, OH, OCH3, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM;
o A representa un resto de fórmula general (VII)
en la que
o es 0 o 1
y
R11, R12, R13, R14 representan independientemente un átomo de hidrógeno, un grupo SO3M, un grupo NO2, un grupo COOM, un grupo amida o sulfonamida sin sustituir o sustituido que tiene hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, OH, OCH3, NH2, Cl, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM;
2. Colorante trisazoico de fórmula general (V) de acuerdo con la reivindicación 1, en donde
M es como se define en la reivindicación 1,
R1, R2 representan independientemente un átomo de hidrógeno, un grupo SO3M, un grupo COOM, un grupo amida o sulfonamida sin sustituir o sustituido, teniendo cada uno hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3c Oo M y CH2OCH2COOM,
R3, R4 representan independientemente un átomo de hidrógeno, un grupo alquilo o alcoxi, teniendo cada uno de 1 a 2 átomos de carbono, un grupo amida o sulfonamida sin sustituir o sustituido, teniendo cada uno hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, OH, OCH3, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM,
A representa un resto de fórmula general (VI)
donde
R6, R10 representan independientemente un átomo de hidrógeno, un grupo SO3M, un grupo NO2, un grupo COOM, y
R7, R9 representan independientemente un átomo de hidrógeno, un grupo COOM
y
R8, representa un átomo de hidrógeno, un grupo SO3M, un grupo NO2, un grupo amida o sulfonamida sustituido o un grupo sulfona que tiene hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, OH, OCH3, NH2, Cl, COOCH3, COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y
CH2OCH2C00 M.
3. Colorante trisazoico de fórmula general (V) de acuerdo con la reivindicación 1 o la reivindicación 2, en donde M, R1, R2, R3, R4 son como se ha definido en la reivindicación 2
A o representa un resto de fórmula general (VI)
donde
R6, R10 representan independientemente un átomo de hidrógeno, un grupo SO3M, un grupo NO2,
y
R7, R9 representa un átomo de hidrógeno,
y
R8, representa un grupo SO3M, un grupo NO2, un grupo amida o sulfonamida sustituido que tiene hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en COOM, COOCH3 COOCH2CH3, CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM.
4. Colorante trisazoico de fórmula general (V) de acuerdo con una cualquiera de las reivindicaciones 1 a 3, en donde M es como se define en la reivindicación 1,
R1, R2 representan independientemente un átomo de hidrógeno, o un grupo COOM,
R3, R4 representan independientemente un átomo de hidrógeno, un grupo alquilo o alcoxi, teniendo cada uno de 1 a 2 átomos de carbono,
A representa un resto de fórmula general (VI)
donde
R6, R10 representan independientemente un átomo de hidrógeno, un grupo SO3M, o un grupo NO2,
y
R7, R9 representan un átomo de hidrógeno,
y
R8, representa un grupo SO3M, un grupo NO2, un grupo amida o sulfonamida sustituido o un grupo sulfona que tiene hasta 6 átomos de carbono, en donde los sustituyentes se seleccionan del grupo que consiste en CH3, CH2CH2COOM, (CH2)3COOM y CH2OCH2COOM.
5. Colorante trisazoico de fórmula general (V) de acuerdo con una cualquiera de las reivindicaciones 1 a 4, en donde M es como se define en la reivindicación 1,
R1, R2, R3, R4 son como se ha definido en la reivindicación 4,
A representa un resto de fórmula general (VI) y R6, R7, R9, R10 son como se ha definido en la reivindicación 4 y
R8, representa un grupo NO2, un grupo NHCOCH3, un grupo NHCOCH2CH2COOM, un grupo NHCO(CH2)3COOM
o un grupo NHCOCH2OCH2COOM.
6. Método de preparación de los colorantes trisazoicos de acuerdo con la invención de fórmula general (V) de acuerdo con la reivindicación 1 , en donde
una amina de fórmula general (VIII)
donde R1 y R2 son como se han definido en la reivindicación 1
se diazota y posteriormente se acopla con un compuesto de fórmula general (IX),
donde R3 y R4 son como se han definido en la reivindicación 1,
con un valor de pH ácido situado entre 1,0 y 3,0, con formación del colorante intermedio de fórmula general (X),
en donde el colorante intermedio de fórmula general (X), donde R1, R2, R3 y R4 son como se han definido en la reivindicación 1, se diazota y posteriormente se acopla con K-Acid (CAS: 130-23-4) a un valor de pH ácido situado entre 0,5 y 2,0 con formación del colorante intermedio de fórmula general (XII), en donde
R1, R2, R3 y R4 son como se han definido en la reivindicación 1 y M el catión de la base utilizada durante la reacción de acoplamiento para mantener el valor de pH en el intervalo de pH definido,
en donde este colorante intermedio de fórmula general (XII) se acopla posteriormente con un compuesto diazonio de fórmula general (XIII)
donde R6, R7, R8, R9 y R10 son como se han definido en la reivindicación 1 y X es el anión del ácido usado durante la diazotización,
o de fórmula general (XIV)
donde o, R11, R12, R13 y R14 son como se han definido en la reivindicación 1 y X es el anión del ácido usado durante la diazotización,
a un valor de pH más o menos neutro situado entre aproximadamente 5,0 y 9,0 dando el colorante de fórmula general (V).
7. Proceso para el registro de texto e imágenes en hojas de registro y para la tinción e impresión de materiales de fibra natural o sintética, materiales nanoporosos, cuero y aluminio mediante la aplicación a los mismos de un colorante trisazoico negro o una mezcla de colorantes trisazoicos negros, de acuerdo con una cualquiera de las reivindicaciones 1 a 5.
8. Líquidos de registro para impresión por chorro de tinta y para utensilios de escritura que comprenden al menos un colorante trisazoico o una mezcla de colorantes trisazoicos de acuerdo con una cualquiera de las reivindicaciones 1 a 5.
9. Líquidos de registro para impresión por chorro de tinta y para utensilios de escritura de acuerdo con la reivindicación 8 que comprenden además uno o más de otros colorantes.
10. Preparación de colorante líquido que comprende al menos un colorante trisazoico o una mezcla de colorantes trisazoicos de acuerdo con una cualquiera de las reivindicaciones 1 a 5.
11. La preparación de colorante líquido de acuerdo con la reivindicación 10, en donde la fase líquida comprende dichos uno o más colorantes trisazoicos y en donde la cantidad de dichos colorantes en la fase líquida está en el intervalo del 0,5 % al 20 % en peso, basado en el peso total de la fase líquida.
12. La preparación de colorante líquido de acuerdo con las reivindicaciones 10 u 11, en donde la fase líquida comprende además uno o más de los siguientes componentes: W-metil-2-pirrolidona, 2-pirrolidona, 2-hexilpirrolidona, hidroxietil-pirrolidona, 1,2-hexanodiol, 1,2-butanodiol, trimetilolpropano, dietilenglicol-monobutiléter, trietilenglicolmonobutiléter, dipropilenglicol-monobutiléter, glicerina, lactato de butilo, sulfolano, disolventes glicol éter, biocida en un intervalo del 0,01 % al 50 % en peso, basado en el peso total de la fase líquida.
13. Un método para aplicar un líquido que comprende uno o más de los colorantes trisazoicos de acuerdo con una cualquiera de las reivindicaciones 1 a 5 en un medio acuoso líquido sobre un sustrato que comprende al menos las siguientes etapas
a) Proporcionar un sustrato, y
p) Proporcionar un depósito que comprende el líquido que contiene el colorante,
Y) Transferir al menos una parte del líquido que contiene colorante del depósito al sustrato, y
8) Eliminar del sustrato el agua, y si es aplicable otros disolventes opcionales,.
14. Un artículo impreso, que comprende
A. un sustrato, y
B. una capa que comprende al menos un colorante trisazoico de acuerdo con una cualquiera de las reivindicaciones 1 a 5.
15. Un uso de un colorante de acuerdo con una cualquiera de las reivindicaciones 1 a 5 en tintas para impresión por chorro de tinta, utensilios de escritura o en soluciones colorantes para fabricar filtros de color para aplicaciones ópticas y optoelectrónicas.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP14020086.6A EP3020770A1 (en) | 2014-11-17 | 2014-11-17 | Black trisazo dyes, their preparation and their use |
| PCT/EP2015/076355 WO2016078988A1 (en) | 2014-11-17 | 2015-11-11 | Black trisazo dyes, their preparation and their use |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2905409T3 true ES2905409T3 (es) | 2022-04-08 |
Family
ID=52338803
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES15791670T Active ES2905409T3 (es) | 2014-11-17 | 2015-11-11 | Colorantes trisazoicos negros, su preparación y uso |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US10259942B2 (es) |
| EP (2) | EP3020770A1 (es) |
| JP (1) | JP6748093B2 (es) |
| CN (2) | CN114656799A (es) |
| DK (1) | DK3221406T3 (es) |
| ES (1) | ES2905409T3 (es) |
| HU (1) | HUE060874T2 (es) |
| PL (1) | PL3221406T3 (es) |
| WO (1) | WO2016078988A1 (es) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA3142257A1 (en) * | 2019-06-06 | 2020-12-10 | Lanxess Deutschland Gmbh | Trisazo compounds |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CH588535A5 (es) * | 1974-06-17 | 1977-06-15 | Sandoz Ag | |
| CH671023A5 (es) * | 1987-02-10 | 1989-07-31 | Ciba Geigy Ag | |
| GB9217964D0 (en) | 1992-08-24 | 1992-10-07 | Ici Plc | Compound |
| JP2002003740A (ja) * | 2000-06-21 | 2002-01-09 | Kiriya Kagaku Kk | 黒色染料組成物及びその製造方法 |
| JP2002003742A (ja) * | 2000-06-21 | 2002-01-09 | Kiriya Kagaku Kk | 染料組成物の製造方法 |
| KR100510133B1 (ko) * | 2003-02-08 | 2005-08-26 | 삼성전자주식회사 | 내광성 착색제 및 이를 포함하는 내광성 잉크 조성물 |
| DE10337636A1 (de) * | 2003-08-16 | 2005-03-17 | Dystar Textilfarben Gmbh & Co. Deutschland Kg | Farbstoffmischungen von faserreaktiven Azofarbstoffen, ihre Herstellung und ihre Verwendung |
| JP4502274B2 (ja) * | 2003-12-02 | 2010-07-14 | 日本化薬株式会社 | トリスアゾ化合物、インク組成物及び着色体 |
| CN1886467A (zh) * | 2003-12-02 | 2006-12-27 | 日本化药株式会社 | 三偶氮化合物、油墨组合物和着色体 |
| WO2010057830A1 (en) * | 2008-11-20 | 2010-05-27 | Dystar Colours Deutschland Gmbh | Ring fluorinated reactive dyes |
-
2014
- 2014-11-17 EP EP14020086.6A patent/EP3020770A1/en not_active Withdrawn
-
2015
- 2015-11-11 CN CN202210335087.2A patent/CN114656799A/zh active Pending
- 2015-11-11 ES ES15791670T patent/ES2905409T3/es active Active
- 2015-11-11 US US15/527,175 patent/US10259942B2/en active Active
- 2015-11-11 PL PL15791670T patent/PL3221406T3/pl unknown
- 2015-11-11 JP JP2017544831A patent/JP6748093B2/ja active Active
- 2015-11-11 DK DK15791670.1T patent/DK3221406T3/da active
- 2015-11-11 WO PCT/EP2015/076355 patent/WO2016078988A1/en not_active Ceased
- 2015-11-11 EP EP15791670.1A patent/EP3221406B1/en active Active
- 2015-11-11 HU HUE15791670A patent/HUE060874T2/hu unknown
- 2015-11-11 CN CN201580062535.4A patent/CN107087414A/zh active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| CN107087414A (zh) | 2017-08-22 |
| DK3221406T3 (da) | 2022-03-21 |
| JP6748093B2 (ja) | 2020-08-26 |
| EP3221406A1 (en) | 2017-09-27 |
| EP3221406B1 (en) | 2022-01-05 |
| US20170335110A1 (en) | 2017-11-23 |
| US10259942B2 (en) | 2019-04-16 |
| EP3020770A1 (en) | 2016-05-18 |
| HUE060874T2 (hu) | 2023-04-28 |
| JP2018501387A (ja) | 2018-01-18 |
| CN114656799A (zh) | 2022-06-24 |
| PL3221406T3 (pl) | 2022-04-19 |
| WO2016078988A1 (en) | 2016-05-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US6302949B1 (en) | Metallized bisazo dyes, their preparation and use | |
| TW201141959A (en) | Water-soluble azo compound or salt thereof, ink composition and colored body | |
| US6068687A (en) | Azo dyes and their preparation and use | |
| TW201708406A (zh) | 化合物、著色組成物、噴墨記錄用墨水、噴墨記錄方法、噴墨印表機墨水匣以及噴墨記錄物 | |
| US6562115B2 (en) | Azo dyes and their preparation and use | |
| CN102558899B (zh) | 黑色三偶氮染料,其制备及其用途 | |
| JP2009185133A (ja) | インク組成物、インクジェット記録方法及び着色体 | |
| US20150062265A1 (en) | Ink composition, inkjet recording ink, and inkjet recording method | |
| US6709502B2 (en) | Monoazo dyes and their preparation and use | |
| ES2905409T3 (es) | Colorantes trisazoicos negros, su preparación y uso | |
| US6320031B1 (en) | Monoazo dyes and their preparation and use | |
| JP4941785B2 (ja) | インクジェット記録用水性インク、インクカートリッジおよびインクジェット記録装置 | |
| US7060105B2 (en) | Copper complex monazo dyes and their preparation and use | |
| ES2998468T3 (en) | Trisazo compounds for ink-jet printing | |
| ES2692440T3 (es) | Colorantes ácidos | |
| CN105452396B (zh) | 水性油墨组合物、喷墨记录方法及着色体 | |
| US6929688B2 (en) | Monoazo dyes and their preparation and use | |
| JP5637938B2 (ja) | インク組成物、インクジェット記録用インク及びインクジェット記録方法 | |
| JP2019501248A (ja) | アントラピリドンアゾ染料、それらの調製および使用 | |
| JP2013253218A (ja) | 着色組成物、インク組成物、インクジェット記録用インク及びインクジェット記録方法 | |
| JP2012149213A (ja) | インク組成物、インクジェット記録用インク及びインクジェット記録方法 |