ES2906222T3 - Productos químicos agrícolas - Google Patents
Productos químicos agrícolas Download PDFInfo
- Publication number
- ES2906222T3 ES2906222T3 ES19701697T ES19701697T ES2906222T3 ES 2906222 T3 ES2906222 T3 ES 2906222T3 ES 19701697 T ES19701697 T ES 19701697T ES 19701697 T ES19701697 T ES 19701697T ES 2906222 T3 ES2906222 T3 ES 2906222T3
- Authority
- ES
- Spain
- Prior art keywords
- alkyl
- haloalkyl
- independently selected
- compound
- halo
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D235/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings
- C07D235/02—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings condensed with carbocyclic rings or ring systems
- C07D235/04—Benzimidazoles; Hydrogenated benzimidazoles
- C07D235/06—Benzimidazoles; Hydrogenated benzimidazoles with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached in position 2
- C07D235/08—Radicals containing only hydrogen and carbon atoms
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/48—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with two nitrogen atoms as the only ring hetero atoms
- A01N43/50—1,3-Diazoles; Hydrogenated 1,3-diazoles
- A01N43/52—1,3-Diazoles; Hydrogenated 1,3-diazoles condensed with carbocyclic rings, e.g. benzimidazoles
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/48—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with two nitrogen atoms as the only ring hetero atoms
- A01N43/54—1,3-Diazines; Hydrogenated 1,3-diazines
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/48—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with two nitrogen atoms as the only ring hetero atoms
- A01N43/58—1,2-Diazines; Hydrogenated 1,2-diazines
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/64—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with three nitrogen atoms as the only ring hetero atoms
- A01N43/647—Triazoles; Hydrogenated triazoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D249/00—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms
- C07D249/16—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms condensed with carbocyclic rings or ring systems
- C07D249/18—Benzotriazoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Dentistry (AREA)
- Wood Science & Technology (AREA)
- Plant Pathology (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Agronomy & Crop Science (AREA)
- General Health & Medical Sciences (AREA)
- Pest Control & Pesticides (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- Plural Heterocyclic Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
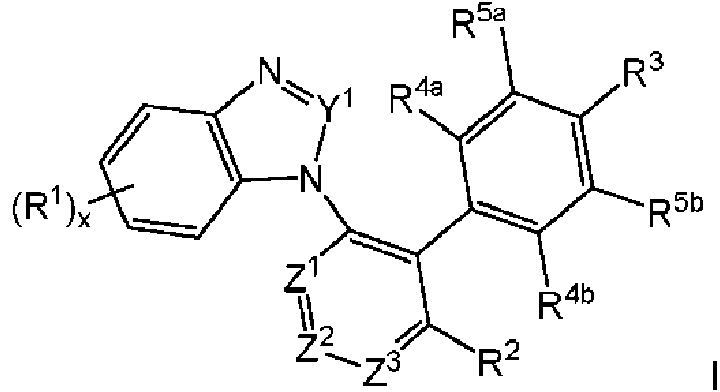
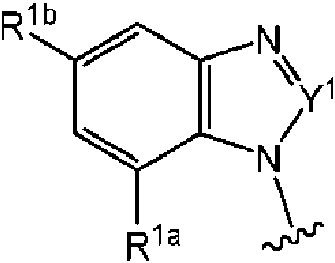
Un compuesto de fórmula I, o una sal o N-óxido agronómicamente aceptable del mismo: **(Ver fórmula)** Y1 se selecciona de CH y N; Z1, Z2 y Z3 se seleccionan cada uno independientemente de N y CR6; en la que al menos uno de Z1, Z2 y Z3 es CR6; R1 y R10 se seleccionan cada uno independientemente en cada ocurrencia de: alquilo C1-C6, haloalquilo C1-C6, cicloalquilo C3-C6, halo, nitro, OR7, SR8, OS(O)2R8, S(O)2R8, C(O)OR8, C(O)NR8R8, C(O)R8, S(O)2NR8R8, S(O)(NR8)R8, S(O)R8, ciano, alquenilo C2-C6, alquinilo C2-C6 y NR8R9; R2 y R6 se seleccionan cada uno independientemente en cada ocurrencia de H, halo, nitro, ciano, alquilo C1-C6, cicloalquilo C3-C6 y haloalquilo C1-C6; R3, R4a, R4b, R5a y R5b se seleccionan independientemente en cada ocurrencia de H, alquilo C1-C6, haloalquilo C1-C6, cicloalquilo C3-C6, halo, nitro, OR7, SR8, OS(O)2R8, S(O)2R8, C(O)OR8, C(O)NR8R8, C(O)R8, S(O)2NR8R8, S(O)(NR8)R8, S(O)R8, ciano, alquenilo C2-C6, alquinilo C2-C6 y NR8R9; o en la que R4b y R5b junto con los átomos de carbono a los que están unidos forman un anillo seleccionado de: fenilo, heteroarilo de 5 o 6 miembros, anillo de heterocicloalquilo de 5, 6 o 7 miembros y cicloalquilo C5-C7; estando dicho anillo de heteroarilo o fenilo opcionalmente sustituido con desde 1 a 4 grupos R10 o estando dicho anillo heterocicloalquilo o cicloalquilo opcionalmente sustituido con desde 1 a 4 grupos R11; con la condición de que ya sea al menos uno de R4a y R4b se seleccione de alquilo C1-C6, haloalquilo C1-C6, halo, nitro, O-alquilo C1-C6, SR8, OS(O)2R8, S(O)2R8, S(O)2NR8R8, S(O)(NR8)R8, S(O)R8, ciano, alquenilo C2-C6, alquinilo C2-C6 y NR8R9; o R4b y R5b juntos forman un anillo; R7 se selecciona independientemente en cada ocurrencia de: H, alquilo C1-C6, alquenilo C3-C6, alquinilo C3-C6, cicloalquilo C3-C6 y haloalquilo C1-C6; R8 se selecciona independientemente en cada ocurrencia de: H, cicloalquilo C3-C6 y alquilo C1-C6; o en el que dos grupos R8 están unidos al mismo átomo de nitrógeno, dichos grupos R8, junto con dicho átomo de nitrógeno forman un anillo heterocicloalquilo de 4, 5, 6 o 7 miembros; R9 se selecciona independientemente en cada ocurrencia de; H, alquilo C1-C6, C(O)-alquilo C1-C6 y S(O)2-alquilo C1- C6; o donde un grupo R8 y un grupo R9 están unidos al mismo átomo de nitrógeno, dichos grupos R8 y R9, junto con dicho átomo de nitrógeno forman un anillo heterocicloalquilo de 4, 5, 6 o 7 miembros; R11 se selecciona independientemente en cada ocurrencia de: =O, =S, alquilo C1-C6, haloalquilo C1-C6, halo, nitro, OR8, SR8, OS(O)2R8, S(O)2R8, S(O)2NR8R8, S(O)(NR8)R8, S(O)R8, ciano, alquenilo C2-C6, alquinilo C2-C6 y NR8R9; y x es un número entero desde 0 a 4; en la que para cualquier grupo R1, R2, R3, R4a, R4b, R5a, R5b, R6, R7, R8, R9, R10, o R11 que es alquilo, alquenilo, cicloalquilo, heterocicloalquilo (incluso cuando dos grupos R8 o un grupo R8 y un grupo R9 junto con un nitrógeno al que están unidos forman un anillo heterocicloalquilo), alquinilo, C(O)-alquilo o S(O)2- alquilo está opcionalmente sustituido, cuando sea químicamente posible, con 1 a 4 sustituyentes, cada uno de los cuales se selecciona independientemente en cada ocurrencia del grupo que consiste en: =O; =NRa, =NORa, alquilo C1-C4, halo, nitro, ciano, haloalquilo C1-C4, alquenilo C2-C4, alquinilo C2-C4, NRaRb, S(O)2Ra, S(O)Ra, S(O)(NRa)Ra, S(O)2NRaRa, CO2Ra, C(O)Ra, CONRaRa y ORa; en la que Ra se selecciona independientemente de H y alquilo C1-C4; y Rb es independientemente H, alquilo C1-C4, C(O)-alquilo C1-C4, S(O)2-alquilo C1-C4.
Description
DESCRIPCIÓN
Productos químicos agrícolas
La presente invención se refiere a compuestos de benzimidazol y benzotriazol que son útiles en el campo de la agricultura como fungicidas.
Dado el aumento mundial de la demanda de alimentos, existe una necesidad internacional de nuevos tratamientos para reducir las pérdidas de cultivos alimentarios por enfermedades, insectos y malas hierbas. Más del 40 % de los cultivos se pierden antes de la cosecha y el 10 % después de la cosecha en todo el mundo. De hecho, las pérdidas han aumentado desde mediados de la década de 1990.
Una nueva amenaza que contribuye a esto es la ocurrencia de organismos resistentes a los productos químicos, por ejemplo, malas hierbas resistentes al glifosato en EE. UU. y cepas de especies de hongos Septoria resistentes a la estrobilurina.
Investigaciones recientes también sugieren que la propagación geográfica de muchas plagas y enfermedades de los cultivos está aumentando, posiblemente como resultado del calentamiento global.
Un objetivo de determinadas realizaciones de la presente invención es proporcionar pesticidas (por ejemplo, fungicidas) que tengan actividad no selectiva, es decir, actividad de amplio espectro, o que sean activos específicamente frente a organismos diana selectivos.
Un objetivo de determinadas realizaciones de la presente invención es proporcionar compuestos que sean menos persistentes en el medio ambiente después de su uso que los compuestos de la técnica anterior. Como alternativa o adicionalmente, los compuestos de la presente invención son menos propensos a la bioacumulación una vez en la cadena alimentaria que los compuestos de la técnica anterior.
Otro objetivo de determinadas realizaciones de la invención es proporcionar compuestos que sean menos dañinos para los seres humanos que los compuestos de la técnica anterior. Como alternativa o adicionalmente, los compuestos de la invención pueden ser menos dañinos que los compuestos de la técnica anterior para uno o más de los siguientes grupos: anfibios, peces, mamíferos (incluyendo animales domésticos tales como perros, gatos, vacas, ovejas, cerdos, cabras, etc.), reptiles, aves e invertebrados beneficiosos (por ejemplo, abejas y otros insectos o gusanos), nematodos beneficiosos, hongos beneficiosos y bacterias fijadoras de nitrógeno.
Los compuestos de la invención pueden ser tan activos o más activos que los compuestos de la técnica anterior. Pueden tener actividad frente a organismos que han desarrollado una resistencia a los compuestos de la técnica anterior. Sin embargo, la presente invención también puede referirse a compuestos que tienen sólo un bajo nivel de actividad en relación con los compuestos de la técnica anterior. Estos compuestos de menor actividad siguen siendo eficaces como fungicidas, pero pueden tener otras ventajas en relación con los compuestos existentes tales como, por ejemplo, un impacto ambiental reducido.
Los compuestos de la invención pueden ser más selectivos que los compuestos de la técnica anterior, es decir, pueden tener una actividad mejor, similar o incluso ligeramente menor que los compuestos de la técnica anterior frente a las especies diana, pero tienen una actividad significativamente menor frente a las especies no diana (por ejemplo, los cultivos que no se protegen).
Ciertas realizaciones de la invención proporcionan compuestos que logran uno o más de los objetivos anteriores. Los compuestos pueden ser activos por sí mismos o pueden metabolizarse o reaccionar en medios acuosos para producir un compuesto activo.
Fatima Al-omran et al: "synthesis of polyfunctionally substituted heteroaromatic compounds via benzotriazolyl chalcones with antimicrobial and antifungal activities", Journal of Heterocyclic Chemistry, 1 May 2004 (2004-05-01), pages 327-333, informa de la utilidad de tanto los derivados de 3-(1-benzotriazolil) chalcona como la 2-(1-benzotriazolil)-1,4-pentadien-3-ona en la síntesis de 2-(1 H)-piridona, piridina, pirazol y derivados de isoxazol.
Sumario de la invención
En un primer aspecto de la invención se proporciona un compuesto de fórmula I, o una sal o N-óxido agronómicamente aceptables del mismo:
Y1 se selecciona de CH y N;
Z1, Z2 y Z3 se seleccionan cada uno independientemente de N y CR6; en el que al menos uno de Z1, Z2 y Z3 es CR6; R1 y R10 se seleccionan cada uno independientemente en cada ocurrencia de: alquilo C1-C6, haloalquilo C1-C6, cicloalquilo C3-C6, halo, nitro, OR7, SR8, OS(O)2R8, S(O)2R8, C(O)OR8, C(O)NR8R8, C(O)R8, S(O)2NR8R8, S(O)(NR8)R8, S(O)R8, ciano, alquenilo C2-C6, alquinilo C2-C6 y NR8R9;
R2 y R6 se seleccionan cada uno independientemente en cada ocurrencia de H, halo, nitro, ciano, alquilo C1-C6, cicloalquilo C3-C6 y haloalquilo C1-C6;
R3, R4a, R4b, R5a y R5b se seleccionan independientemente en cada ocurrencia de H, alquilo C1-C6, haloalquilo C1-C6, cicloalquilo C3-C6, halo, nitro, OR7, SR8, OS(O)2R8, S(O)2R8, C(O)RO8, C(O)NR8R8, C(O)R8, S(O)2NR8R8, S(O)(NR8)R8, S(O)R8, ciano, alquenilo C2-C6, alquinilo C2-C6 y NR8R9; o en la que R4b y R5b junto con los átomos de carbono a los que están unidos forman un anillo seleccionado de: fenilo, heteroarilo de 5 o 6 miembros, anillo de heterocicloalquilo de 5, 6 o 7 miembros y cicloalquilo C5-C7; estando dicho anillo de heteroarilo o fenilo opcionalmente sustituido con desde 1 a 4 grupos R10 o estando dicho anillo heterocicloalquilo o cicloalquilo opcionalmente sustituido con desde 1 a 4 grupos R11;
con la condición de que al menos uno de R4a y R4b se seleccione de alquilo C1-C6, haloalquilo C1-C6, halo, nitro, O alquilo C1-C6, SR8, OS(O)2R8, S(O)2R8, S(O)2NR8R8, S(O)(NR8)R8, S(O)R8, ciano, alquenilo C2-C6, alquinilo C2-C6 y nR8R9; o R4b y R5b juntos forman un anillo;
R7 se selecciona independientemente en cada ocurrencia de: H, alquilo C1-C6, alquenilo C3-C6, alquinilo C3-C6, cicloalquilo C3-C6 y haloalquilo C1-C6;
R8 se selecciona independientemente en cada ocurrencia de: H, cicloalquilo C3-C6 y alquilo C1-C6;
o donde dos grupos R8 están unidos al mismo átomo de nitrógeno, dichos grupos R8, junto con dicho átomo de nitrógeno forman un anillo heterocicloalquilo de 4, 5, 6 o 7 miembros;
R9 se selecciona independientemente en cada ocurrencia de; H, alquilo C1-C6, C(O)-alquilo C1-C6 y S(O)2-alquilo C1-C6;
o donde un grupo R8 y un grupo R9 están unidos al mismo átomo de nitrógeno, dichos grupos R8 y R9, junto con dicho átomo de nitrógeno forman un anillo heterocicloalquilo de 4, 5, 6 o 7 miembros;
R11 se selecciona independientemente en cada ocurrencia de: =O, =S, alquilo C1-C6, haloalquilo C1-C6, halo, nitro, OR8, SR8, OS(O)2R8, S(O)2R8, S(O)2NR8R8, S(O)(NR8)R8, S(O)R8, ciano, alquenilo C2-C6, alquinilo C2-C6 y NR8R9; y x es un número entero desde 0 a 4; en el que para cualquier grupo R1, R2, R3, R4a, R4b, R5a, R5b, R6, R7, R8, R9, R10, o R11 que es alquilo, alquenilo, cicloalquilo, heterocicloalquilo (incluso cuando dos grupos R8 o un grupo R8 y un grupo R9 junto con un nitrógeno al que están unidos forman un anillo heterocicloalquilo), alquinilo, C(O)-alquilo o S(O)2-alquilo está opcionalmente sustituido, cuando sea químicamente posible, con 1 a 4 sustituyentes, cada uno de los cuales se selecciona independientemente en cada ocurrencia del grupo que consiste en: =O; =NRa, =NORa, alquilo C1-C4, halo, nitro, ciano, haloalquilo C1-C4, alquenilo C2-C4, alquinilo C2-C4, NRaRB, S(O)2Ra, S(O)Ra, S(O)(NRa)Ra, S(O)2NRaRa, CO2Ra, C(O)Ra, CONRaRa y ORa;
en el que Ra se selecciona independientemente de H y alquilo C1-C4; y Rb es independientemente H, alquilo C1-C4, C(O) -alquilo C1-C4, S(O)2-alquilo C1-C4.
En una realización, el compuesto de fórmula I es un compuesto de fórmula II:
En una realización, el compuesto de fórmula I es un compuesto de fórmula III:
en la que Y1, R1, R2, R3, R4a, R4b, R5a, R5b, R6 y x son como se describe arriba para la fórmula I. Puede ser que Y1 sea
CH.
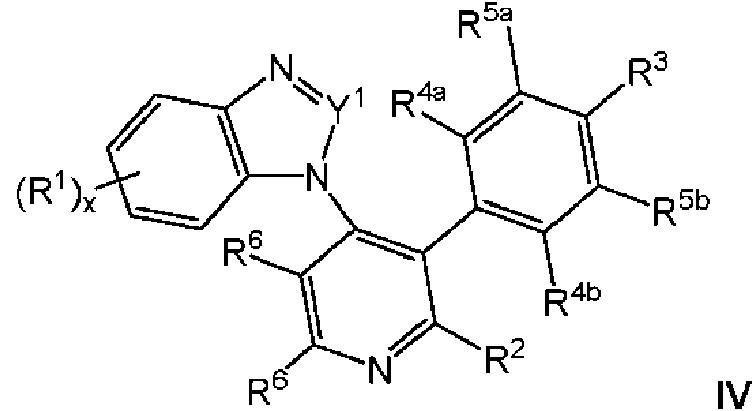
En una realización, el compuesto de fórmula I es un compuesto de fórmula IV:
en la que Y1, R1, R2, R3, R4a, R4b, R5a, R5b, R6 y x son como se describe arriba para la fórmula I. Puede ser que Y1 sea
CH.
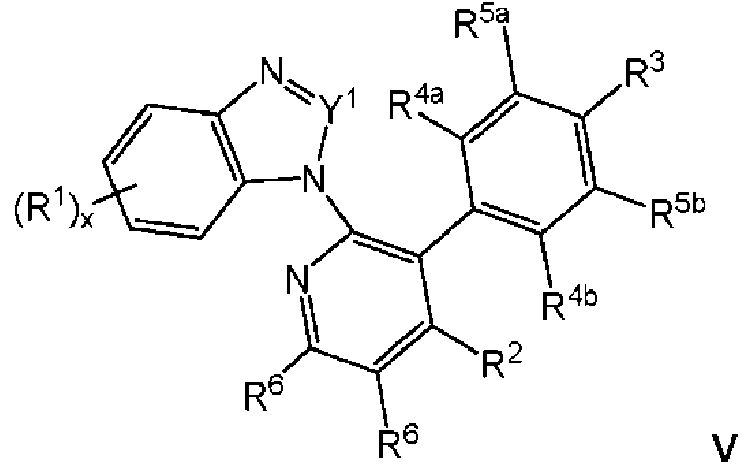
En una realización, el compuesto de fórmula I es un compuesto de fórmula V:
en la que Y1, R1, R2, R3, R4a, R4b, R5a, R5b, R6 y x son como se describe arriba para la fórmula I. Puede ser que Y1 sea
CH.
En una realización, el compuesto de fórmula I es un compuesto de fórmula VI:
en la que Y1, R1, R2, R3, R4a, R4b, R5a, R5b, R6 y x son como se describe arriba para la fórmula I. Puede ser que Y1 sea
CH.
En una realización, el compuesto de fórmula I es un compuesto de fórmula VII:
en la que Z1, Z2, Z3, R1, R2, R3, R4a, R4b, R5a, R5b y x son como se describe arriba para la fórmula I.
En una realización, el compuesto de fórmula I es un compuesto de fórmula VIII:
en la que Z1, Z2, Z3, R1, R2, R3, R4a, R4b, R5a, R5b y x son como se describe arriba para la fórmula I.
Las siguientes realizaciones se aplican a compuestos de cualquiera de las fórmulas (I)-(VIII). Estas realizaciones son independientes e intercambiables. Una cualquiera realización puede combinarse con cualquier otra realización, cuando se permita químicamente. En otras palabras, cualquiera de las características descritas en las siguientes realizaciones puede combinarse (cuando sea químicamente permisible) con las características descritas en una o más realizaciones. En particular, cuando se ejemplifica o ilustra un compuesto en esta memoria descriptiva, cualquiera dos o más de las realizaciones enumeradas a continuación, expresadas en cualquier nivel de generalidad, que abarcan ese compuesto pueden combinarse para proporcionar una realización adicional que forma parte de la presente divulgación.
Puede ser que Y1 se CH. Puede ser que Y1 sea n
Puede ser que Z2 sea CR6.
Puede ser que Z1 sea N. Puede ser que Z1 sea CR6
Puede ser que Z3 sea N. Puede ser que Z3 sea CR6.
Puede ser que Z1 y Z3 son cada N y Z2 es CR6. Puede ser que Z1 y Z2 sean cada CR6 y Z3 sea N. Puede ser que Z2 y Z3 sean cada CR6 y Z1 sea N. Puede ser que Z1, Z2 y Z3 sean cada CR6.
Puede ser que x sea un número entero seleccionado entre 1 y 2.
Puede ser que R1 se seleccione independientemente en cada ocurrencia de alquilo C1-C6, haloalquilo C1-C6, halo, nitro, OR7 y ciano. Puede ser que R1 se seleccione independientemente en cada ocurrencia de alquilo C1-C6, haloalquilo C1-C6, halo, nitro, OR7y ciano. Puede ser que R1 se seleccione independientemente en cada ocurrencia
de halo, nitro, OR7y ciano. Puede ser que R1 sea independiente en cada ocurrencia OR7 R1 puede ser al menos una ocurrencia O-C3-alquinilo, por ejemplo, O-propargilo. R1 puede ser al menos una ocurrencia O-alquilo C1-C4, por ejemplo, OMe. Puede ser que R1 sea independientemente en cada ocurrencia halo, por ejemplo, flúor o cloro.
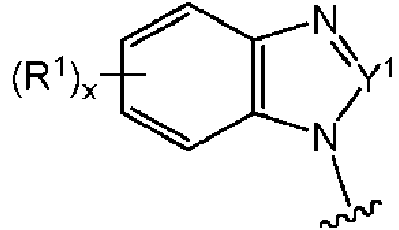
Puede ser que
tenga la estructura:
en la que y es un número entero de 0 a 3; y en la que R1a se selecciona de halo y OR7, por ejemplo, OH, O-alquilo C1-C4 u O-alquinilo C3.
Puede ser que
tenga la estructura:
Puede ser que
tenga la estructura:
Puede ser que
tenga la estructura:
en la que R1a y R1b se seleccionan cada uno de halo y OR7, por ejemplo, OH, O-alquilo C1-C4 u O-alquinilo C3. Puede ser que
tenga la estructura:
Puede ser que
tenga la estructura:
Puede ser que R1a sea OR7, por ejemplo, OH, O-alquilo C1-C4 u O-alquinilo C3. Puede ser que R1a sea O-alquilo C1-C4, por ejemplo, OMe. Puede ser que R1a sea halo. Puede ser que R1a sea flúor.
Puede ser que R1b es OR7, por ejemplo, OH, O-alquilo C1-C4 u O-alquinilo C3. Puede ser que R1b sea O-alquilo C1-C4, por ejemplo, OMe. Puede ser que R1b sea halo, por ejemplo, cloro o flúor.
Puede ser que y sea 0. Puede ser que y sea 1.
En realizaciones ilustrativas,
puede tener una estructura seleccionada de:
R2 se puede seleccionar independientemente de halo, alquilo C1-C2 y haloalquilo C1-C2. R2 se puede seleccionar independientemente de cloro, alquilo C1-C2 y haloalquilo C1-C2. R2 se puede seleccionar independientemente de alquilo C1-C2 y haloalquilo C1-C2. R2 puede ser alquilo C1-C2, por ejemplo, metilo o etilo. R2 puede ser haloalquilo C1-C2, por ejemplo, CF3. R2 puede ser halo, por ejemplo, cloro.
Puede ser que R3, R4a, R4b, R5a y R5b se seleccionen cada uno independientemente de H, halo, alquilo C1-C6, haloalquilo C1-C6, O-alquilo C1-C6 y O-haloalquilo C1-C6.
Puede ser que R3 sea H. Alternativamente, puede ser que R3 se seleccione independientemente de halo, alquilo C1-Ce, haloalquilo C1-C6, O-alquilo C1-C6 y O-haloalquilo C1-C6. Puede ser que R3 se seleccione independientemente de halo, alquilo C1-C6, haloalquilo C1-C6, OH y O-alquilo C1-C4. Puede ser que R3 sea halo, por ejemplo, fluoro o cloro. Puede ser que R3 sea O-alquilo C1-C4, por ejemplo, OMe.
Puede ser que R4a se seleccione dependientemente de halo, alquilo C1-C6, haloalquilo C1-C6, O-alquilo C1-C6 y O-haloalquilo C1-C6. Puede ser que R4a sea halo, por ejemplo, cloro.
Puede ser que R4b sea H. Alternativamente, puede ser que R4b se seleccione independientemente de halo, alquilo C1-Ce, haloalquilo C1-C6, O-alquilo C1-C6 y O- haloalquilo C1-C6. Puede ser que R4b sea halo, por ejemplo, cloro.
Puede ser que R5a sea H. Alternativamente, puede ser que R5a se seleccione independientemente de halo, alquilo C i Ca, haloalquilo C1-C6, O-alquilo C1-C6 y O-haloalquilo C1-C6.
Puede ser que ni R4a ni R4b sean H
Puede ser que tanto R4a como R4b se seleccionen cada uno independientemente de halo, alquilo Ci-Ca, haloalquilo Ci-Ca, O-alquilo Ci-Ca y O-haloalquilo Ci-Ca. Puede ser que tanto R4a como R4b sean halo, por ejemplo, cloro.
Puede ser que R5b sea H. Alternativamente, puede ser que R5b se seleccione independientemente de halo, alquilo C i Ca, haloalquilo Ci-Ca, O-alquilo Ci-Ca y O-haloalquilo Ci-Ca.
Puede ser que R5a y R5b sean cada H. Puede ser que R4b y R5b sean cada H. Puede ser que R4b, R5a y R5b sean cada uno H.
Puede ser que ninguno de R3, R4a y R4b sea H
Puede ser que R3, R4a y R4b se seleccionen cada uno independientemente de halo, alquilo Ci-Ca, haloalquilo Ci-Ca, O-alquilo Ci-Ca y O-haloalquilo Ci-Ca.
Puede ser que al menos uno de R4a y R4b se seleccione de alquilo Ci-Ca, haloalquilo Ci-Ca, cloro, bromo, yodo, nitro, O-alquilo Ci-Ca, ciano, alquenilo C2-Ca y alquinilo C2-Ca. Puede ser que al menos uno de R4a y R4b se seleccione de alquilo Ci-Ca, haloalquilo Ci-Ca, cloro, bromo, yodo, O-alquilo Ci-Ca, alquenilo C2-Ca y alquinilo C2-Ca.
El compuesto de fórmula (I) se puede seleccionar de:
Descripción detallada
El término Cm-Cn se refiere a un grupo con m a n átomos de carbono.
El término "alquilo" se refiere a una cadena hidrocarburo monovalente saturada lineal o ramificada. Por ejemplo, alquilo C1-C6 puede referirse a metilo, etilo, n-propilo, iso-propilo, n-butilo, sec-butilo, ferf-butilo, n-pentilo o n-hexilo. Los grupos alquilo pueden estar sustituidos o no sustituidos por uno o más sustituyentes. Los sustituyentes específicos para cada grupo alquilo independientemente pueden ser flúor, ORa o NHRa.
El término "haloalquilo" se refiere a un grupo hidrocarburo sustituido con al menos un átomo de halógeno elegido independientemente en cada ocurrencia entre: flúor, cloro, bromo y yodo. El átomo de halógeno puede estar presente en cualquier posición de la cadena hidrocarburo. Por ejemplo, haloalquilo C1-C6 puede referirse a clorometilo, fluorometilo, trifluorometilo, cloroetilo, por ejemplo, 1-clorometilo y 2-cloroetilo, tricloroetilo, por ejemplo, 1,2,2-tricloroetilo, 2.2,2-tricloroetilo, fluoroetilo, por ejemplo, 1 -fluoroetilo y 2-fluoroetilo, trifluoroetilo por ejemplo, 1,2,2-trifluoroetilo y 2.2,2-trifluoroetilo, cloropropilo, tricloropropilo, fluoropropilo, trifluoropropilo. Un grupo haloalquilo puede ser un grupo fluoroalquilo, es decir, una cadena hidrocarburo sustituida con al menos un átomo de flúor. De este modo, un grupo haloalquilo puede tener cualquier cantidad de sustituyentes halógeno. El grupo puede contener un solo sustituyente halógeno, puede tener dos o tres sustituyentes halógeno o puede estar saturado con sustituyentes halógeno.
El término "alquenilo" se refiere a un grupo hidrocarburo ramificado o lineal que contiene al menos un doble enlace. El(los) doble(s) enlace(s) puede(n) estar presente(s) como el isómero E o Z. El doble enlace puede estar en cualquier posición posible de la cadena hidrocarburo. Por ejemplo, " alquenilo C2-C6" puede referirse a etenilo, propenilo, butenilo, butadienilo, pentenilo, pentadienilo, hexenilo y hexadienilo. Los grupos alquenilo pueden estar sustituidos o
no sustituidos por uno o más sustituyentes. Los sustituyentes específicos para cualquier átomo de carbono saturado en cada grupo alquenilo pueden ser independientemente flúor, ORa o NHRa.
El término "alquinilo" se refiere a una cadena hidrocarburo ramificada o lineal que contiene al menos un triple enlace. El triple enlace puede estar en cualquier posición posible de la cadena hidrocarburo. Por ejemplo, "alquinilo C2-C6" puede referirse a etinilo, propinilo, butinilo, pentinilo y hexinilo. Los grupos alquinilo pueden estar sustituidos o no sustituidos por uno o más sustituyentes. Los sustituyentes específicos para cualquier átomo de carbono saturado en cada grupo alquinilo pueden ser independientemente flúor, ORa o NHRa.
El término "cicloalquilo" se refiere a un sistema de anillo de hidrocarburo saturado que contiene, por ejemplo, 3, 4, 5 o 6 átomos de carbono. Por ejemplo, "cicloalquilo C3-C6" puede referirse a ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo. Los grupos cicloalquilo pueden estar sustituidos o no sustituidos por uno o más sustituyentes. Los sustituyentes específicos para cada grupo cicloalquilo independientemente pueden ser flúor, ORa o NHRa.
El término heterocicloalquilo puede referirse a un grupo monocíclico o bicíclico saturado o parcialmente saturado que tiene el número indicado de átomos en el sistema de anillos y que comprende 1 o 2 heteroátomos seleccionados independientemente entre O, S y N en el sistema de anillos (en otras palabras, 1 o 2 de los átomos que forman el sistema de anillo se seleccionan de O, S y N). Por parcialmente saturado se entiende que el anillo puede comprender uno o dos dobles enlaces. Esto se aplica particularmente a anillos monocíclicos de 5 a 6 miembros. El doble enlace estará por lo general entre dos átomos de carbono, pero puede estar entre un átomo de carbono y un átomo de nitrógeno. Los ejemplos de grupos heterocicloalquilo incluyen; piperidina, piperazina, morfolina, tiomorfolina, pirrolidina, tetrahidrofurano, tetrahidrotiofeno, dihidrofurano, tetrahidropirano, dihidropirano, dioxano y azepina. Un grupo heterocicloalquilo puede no estar sustituido o estar sustituido con uno o más sustituyentes. Los sustituyentes específicos para cualquier átomo de carbono saturado en cada grupo heterocicloalquilo pueden ser independientemente flúor, ORa o NHRa.
Los grupos arilo pueden ser cualquier sistema de anillo carbocíclico aromático (es decir, un sistema de anillo que contiene 2(2n 1) electrones n). Los grupos arilo pueden tener de 6 a 12 átomos de carbono en el sistema de anillos. Los grupos arilo serán por lo general grupos fenilo. Los grupos arilo pueden ser grupos naftilo o grupos bifenilo.
En cualquiera de los aspectos y realizaciones anteriores, los grupos heteroarilo pueden ser cualquier sistema de anillo aromático (es decir, un sistema de anillo que contiene 2(2n+1) electrones n) de 5 a 10 miembros que comprende desde 1 a 4 heteroátomos seleccionados independientemente de O, S y N (en otras palabras, desde 1 a 4 de los átomos que forman el sistema de anillo se seleccionan de O, S y N). De este modo, cualquier grupo heteroarilo se puede seleccionar independientemente de: grupos heteroarilo de 5 miembros en los que el anillo heteroaromático está sustituido con 1-4 heteroátomos seleccionados independientemente entre O, S y N; y grupos heteroarilo de 6 miembros en los que el anillo heteroaromático está sustituido con 1-3 (por ejemplo, 1-2) átomos de nitrógeno; grupos heteroarilo bicíclicos de 9 miembros en los que el sistema heteroaromático está sustituido con 1-4 heteroátomos seleccionados independientemente entre O, S y N; grupos heteroarilo bicíclicos de 10 miembros en los que el sistema heteroaromático está sustituido con 1-4 átomos de nitrógeno. Específicamente, los grupos heteroarilo pueden seleccionarse independientemente de: pirrol, furano, tiofeno, pirazol, imidazol, oxazol, isoxazol, triazol, oxadiazol, tiadiazol, tetrazol; piridina, piridazina, pirimidina, pirazina, triazina, indol, isoindol, benzofurano, isobenzofurano, benzotiofeno, indazol, benzimidazol, benzoxazol, benzotiazol, bencisoxazol, purina, quinolina, isoquinolina, cinolina, quinazolina, quinoxalina, pteridina, ftalazina y naftiridina.
Puede ser que, en cualquier grupo que sea un grupo arilo o heteroarilo, ese grupo arilo o heteroarilo no esté sustituido o esté opcionalmente sustituido, cuando sea químicamente posible, por 1 a 5 sustituyentes, cada uno de los cuales se selecciona independientemente en cada ocurrencia de: halo, nitro, ciano, NRaRa, NRaS(O)2Ra, NRaC(O)Ra, NRaCONRaRa, NRaCO2Ra, ORa, SRa, S(O)Ra, S(O)2ORa, S(O)2Ra, S(O)2NRaRa, CO2RaC(O)Ra, CONRaRa, CRbRbNRaRa, CRbRbOa, alquilo C1-C4, alquenilo C2-C4, alquinilo C2-C4 y haloalquilo C1-C4; en el que Ra y Rb son como se describieron anteriormente para la fórmula I.
Los compuestos de la invención que contienen uno o más átomos de carbono asimétricos pueden existir como dos o más estereoisómeros (por ejemplo, enantiómeros o diastereoisómeros).
Cuando un compuesto de la invención contiene un doble enlace tal como un grupo C=C o C=N, son posibles los isómeros geométricos cis/trans (o Z/E). Cuando los isómeros estructurales son interconvertibles a través de una barrera de baja energía, puede ocurrir isomería tautomérica ("tautomerismo"). Esto puede tomar la forma de tautomerismo de protones en compuestos de la invención que contienen, por ejemplo, un grupo imino, ceto u oxima, o el llamado tautomerismo de valencia en compuestos que contienen una unidad estructural aromática. De ello se deduce que un solo compuesto puede exhibir más de un tipo de isomería.
Incluidos dentro del alcance de la presente invención están todos los estereoisómeros, isómeros geométricos y formas tautoméricas de los compuestos de la invención, incluidos los compuestos que exhiben más de un tipo de isomería y mezclas de uno o más de los mismos.
Los compuestos de la invención se pueden obtener, almacenar y/o usar en forma de una sal agronómicamente aceptable. Las sales apropiadas incluyen, pero no se limitan a, sales de ácidos inorgánicos aceptables tales como los
ácidos clorhídrico, sulfúrico, fosfórico, nítrico, carbónico, bórico, sulfámico y bromhídrico, o sales de ácidos orgánicos agronómicamente aceptables tales como ácidos acético, propiónico, butírico, tartárico, maleico, hidroximaleico, fumárico, málico, cítrico, láctico, mucico, glucónico, benzoico, succínico, oxálico, fenilacético, metanosulfónico, toluenosulfónico, bencenosulfónico, salicílico, sulfanílico, aspártico, glutámico, edético, esteárico, palmítico, oleico, láurico, pantoténico, tánico, ascórbico y valérico. Las sales apropiadas también incluyen sales de bases inorgánicas y orgánicas, por ejemplo, contraiones tales como Na, Ca, K, Li, Mg, amonio, trimetilsulfonio. Los compuestos también se pueden obtener, almacenar y/o usar en forma de N-óxido. También se incluyen sales de adición de ácido o sales de base en las que el contraión es ópticamente activo, por ejemplo, d-lactato o l-lisina, o racémico, por ejemplo, dltartrato o dl-arginina.
Los isómeros cis/trans pueden separarse mediante técnicas convencionales bien conocidas para los expertos en la técnica, por ejemplo, cromatografía y cristalización fraccionada.
Las técnicas convencionales para la preparación/aislamiento de enantiómeros individuales cuando sea necesario incluyen la síntesis quiral a partir de un precursor ópticamente puro apropiado o la resolución del racemato (o el racemato de una sal o derivado) usando, por ejemplo, cromatografía líquida de alta presión (HPLC) quiral. De este modo, los compuestos quirales de la invención (y los precursores quirales de los mismos) pueden obtenerse en forma enantioméricamente enriquecida usando cromatografía, por lo general HPLC, en una resina asimétrica con una fase móvil que consiste en un hidrocarburo, por lo general heptano o hexano, que contiene de 0 a 50 % en volumen de isopropanol, por lo general desde 2 % a 20 %, y para ejemplos específicos, de 0 a 5 % en volumen de una alquilamina, por ejemplo, dietilamina al 0.1 %. La concentración del eluido proporciona la mezcla enriquecida.
Alternativamente, el racemato (o un precursor racémico) se puede hacer reaccionar con un compuesto ópticamente activo apropiado, por ejemplo, un alcohol o, en el caso de que el compuesto de la invención contenga una unidad estructural ácida o básica, una base o un ácido tal como 1 -feniletilamina o ácido tartárico. La mezcla diastereoisómera resultante puede separarse por cromatografía y/o cristalización fraccionada y uno o ambos de los diastereoisómeros convertidos en el o los enantiómeros puros correspondientes por medios bien conocidos para un experto en la técnica.
Cuando cualquier racemato cristaliza, son posibles cristales de dos tipos diferentes. El primer tipo es el compuesto racémico (racemato verdadero) al que se hace referencia anteriormente, en el que se produce una forma homogénea de cristal que contiene ambos enantiómeros en cantidades equimolares. El segundo tipo es la mezcla racémica o conglomerado en el que se producen dos formas de cristal en cantidades equimolares, cada una de las cuales comprende un solo enantiómero.
Si bien las dos formas cristalinas presentes en una mezcla racémica tienen propiedades físicas idénticas, pueden tener propiedades físicas diferentes en comparación con el verdadero racemato. Las mezclas racémicas pueden separarse mediante técnicas convencionales conocidas para los expertos en la técnica; véase, por ejemplo, "Stereochemistry of Organic Compounds" de E. L. Eliel and S. H. Wilen (Wiley, 1994).
La actividad de los compuestos de la presente invención puede evaluarse mediante una variedad de ensayos in silico, in vitro e in vivo. Se ha demostrado que el análisis in silico de una variedad de compuestos predice la actividad final in vitro e incluso in vivo.
La presente invención también incluye todos los compuestos marcados con isótopos ambientalmente aceptables de fórmulas I a VIII y sus síntesis, en las que uno o más átomos son reemplazados por átomos que tienen el mismo número atómico, pero una masa atómica o número de masa diferente de la masa atómica o número de masa que normalmente se encuentra en la naturaleza.
Los ejemplos de isótopos apropiados para su inclusión en los compuestos de la invención incluyen isótopos de hidrógeno, tales como 2H, 3H, carbono, tales como 11C, 13C y 14C, cloro, tales como 36Cl, flúor, tales como 18F, yodo, tales como 123I y 125I, nitrógeno, tales como 13N y 15N, oxígeno, tales como 15O, 17O y 18O, fósforo, tales como 32P y azufre, tales como 35S.
Los compuestos marcados isotópicamente pueden prepararse generalmente mediante técnicas convencionales conocidas para los expertos en la técnica o mediante procesos análogos a los descritos usando un reactivo marcado isotópicamente adecuado en lugar del reactivo no marcado empleado anteriormente.
A lo largo de la descripción y las reivindicaciones de esta memoria descriptiva, las palabras "comprende" y "contiene" y las variaciones de las palabras, por ejemplo, "que comprende" y "comprende", significan "que incluye pero no se limita a", y no pretende (y no) excluye otras unidades estructurales, aditivos, componentes, números enteros o etapas.
A lo largo de la descripción y las reivindicaciones de esta memoria descriptiva, el singular abarca el plural a menos que el contexto requiera lo contrario. En particular, cuando se usa el artículo indefinido, la memoria descriptiva debe entenderse que contempla tanto la pluralidad como la singularidad, a menos que el contexto requiera lo contrario.
Debe entenderse que los rasgos, números enteros, características, compuestos, unidades estructurales químicas o grupos descritos junto con un aspecto, realización o ejemplo particular de la invención son aplicables a cualquier otro aspecto, realización o ejemplo descrito en este documento a menos que sea incompatible con el mismo.
Si es adecuado, los compuestos de la invención pueden, a determinadas concentraciones o tasas de aplicación, usarse como fungicidas.
Según otro aspecto de la presente invención, se proporciona un método de control de enfermedades fúngicas, comprendiendo el método la aplicación de una cantidad agronómicamente eficaz y sustancialmente no fitotóxica (para la planta de cultivo) de un compuesto de la invención a las semillas de las plantas, a las propias plantas o al área en la que se pretende que crezcan las plantas.
El plaguicida se puede aplicar como tratamiento de semillas, aplicación foliar, aplicación al tallo, aplicación por inmersión o goteo (quimigación) a la semilla, la planta o al fruto de la planta o al suelo o al sustrato inerte (por ejemplo, sustratos inorgánicos como arena, lana de roca, lana de vidrio, minerales expandidos como perlita, vermiculita, zeolita o arcilla expandida), Pumbe, materiales piroclásticos o similares, sustratos orgánicos sintéticos (por ejemplo, poliuretano), sustratos orgánicos (por ejemplo, turba, compost, productos de desecho de árboles como fibra de coco, fibra de madera o astillas, corteza de árbol) o a un sustrato líquido (por ejemplo, sistemas hidropónicos flotantes, Nutrient Film Technique, Aeroponics).
En un aspecto adicional, la presente invención también se refiere a una composición fungicida que comprende una cantidad eficaz y no fitotóxica de un compuesto activo de la invención. La composición puede comprender además uno o más fungicidas adicionales.
El término "cantidad eficaz y no fitotóxica" significa una cantidad de plaguicida según la invención que es suficiente para controlar o destruir cualquiera de las plagas diana presentes o que pueden aparecer en los cultivos y que no tiene ningún efecto perjudicial significativo sobre el cultivos o, de hecho, tiene un efecto positivo sobre el vigor y el rendimiento de la planta en ausencia del organismo diana.
La cantidad variará dependiendo de la plaga que se va a controlar, el tipo de cultivo, las condiciones climáticas y los compuestos incluidos en la composición de plaguicida. Esta cantidad puede determinarse mediante ensayos de campo sistemáticos, que están dentro de las capacidades de un experto en la técnica.
Dependiendo de sus propiedades físicas y/o químicas particulares, los compuestos activos de la invención pueden formularse como soluciones, emulsiones, suspensiones, polvos, espumas, pastas, gránulos, aerosoles, microencapsulados en sustancias poliméricas y en materiales de recubrimiento para semillas, y también como formulaciones de nebulización fría y caliente ULV.
Los compuestos activos se pueden usar puros o en forma de una formulación, por ejemplo, soluciones listas para su uso, emulsiones, suspensiones a base de agua o aceite, polvos, polvos humectables, pastas, polvos solubles, polvos, gránulos solubles, gránulos para administración por difusión, suspoemulsiones concentradas, sustancias naturales impregnadas de principio activo, sustancias sintéticas impregnadas de principio activo, fertilizantes y también microencapsulados en sustancias poliméricas. La aplicación se puede realizar, por ejemplo, mediante riego, pulverización, atomización, difusión, espolvoreado, espumado, esparcido, etc. También es posible aplicar los compuestos activos por el método de volumen ultrabajo o inyectar la preparación del compuesto activo o el propio compuesto activo en el suelo. También es posible tratar la semilla de las plantas.
Las formulaciones que contienen los compuestos de la invención se producen de manera conocida, por ejemplo, mezclando los compuestos con diluyentes (por ejemplo, disolventes líquidos y/o portadores sólidos), opcionalmente con el uso de surfactantes (por ejemplo, emulsionantes y/o dispersantes y/o formadores de espuma). Las formulaciones se preparan ya sea en fábricas/plantas de producción o alternativamente antes o durante la aplicación.
Los auxiliares son sustancias que son apropiadas para conferir a la propia composición y/o a las preparaciones derivadas de la misma (por ejemplo, licores de pulverización, abonos de semillas) propiedades particulares tales como determinadas propiedades técnicas y/o también propiedades biológicas particulares. Los auxiliares apropiados típicos son: diluyentes, disolventes y portadores.
Los diluyentes apropiados son, por ejemplo, agua, líquidos químicos orgánicos polares y no polares, por ejemplo, de las clases de hidrocarburos aromáticos y no aromáticos (tales como parafinas, alquilbencenos, alquilnaftalenos, clorobencenos), los alcoholes y polioles (que, si es adecuado, también pueden estar sustituidos, eterificados y/o esterificados), las cetonas (tales como acetona, ciclohexanona), ésteres (incluyendo grasas y aceites) y (poli)éteres, las aminas no sustituidas y sustituidas, amidas, lactamas (tales como N- alquilpirrolidonas) y lactonas, las sulfonas y los sulfóxidos (tales como el dimetilsulfóxido).
Si el diluyente usado es agua, también es posible usar, por ejemplo, disolventes orgánicos como disolventes auxiliares. Esencialmente, los disolventes líquidos apropiados son: compuestos aromáticos tales como xileno, tolueno o alquilnaftalenos, compuestos aromáticos clorados e hidrocarburos alifáticos clorados tales como clorobencenos, cloroetilenos o cloruro de metileno, hidrocarburos alifáticos tales como ciclohexano o parafinas, por ejemplo, fracciones de petróleo, alcoholes tales como butanol o glicol y también sus éteres y ésteres, cetonas tales como acetona, metiletilcetona, metilisobutilcetona o ciclohexanona, disolventes fuertemente polares tales como dimetilformamida y dimetilsulfóxido.
Los portadores sólidos apropiados son: por ejemplo, sales de amonio y minerales naturales molidos tales como caolines, arcillas, talco, creta, cuarzo, atapulgita, montmorillonita o tierra de diatomeas, y minerales sintéticos molidos, tales como sílice, alúmina y silicatos finamente divididos; portdores sólidos apropiados para gránulos son: por ejemplo, rocas naturales trituradas y fraccionadas tales como calcita, mármol, piedra pómez, sepiolita y dolomita, y también gránulos sintéticos de harinas inorgánicas y orgánicas, y gránulos de material orgánico tales como papel, aserrín, cáscaras de coco, mazorcas de maíz y tallos de tabaco; emulsionantes y/o formadores de espuma apropiados son: por ejemplo, emulsionantes no iónicos y aniónicos, tales como ésteres de polioxietileno de ácidos grasos, éteres de polioxietileno de alcoholes grasos, por ejemplo, alquilaril poliglicol éteres, alquilsulfonatos, alquilsulfatos, arilsulfonatos y también hidrolizados de proteínas; los dispersantes apropiados son sustancias no iónicas y/o iónicas, por ejemplo, de las clases de alcohol-POE y/o -POP éteres, ácidos y/o POP-POE ésteres, alquilarilo y/o POP-POE éteres, aductos de grasas- y/o POP-POE, derivados de POE y/o POP-poliol, aductos de POE y/o POP-sorbitán o azúcar, sulfatos de alquilo o arilo, sulfonatos de alquilo o arilo y fosfatos de alquilo o arilo o los correspondientes aductos de PO-éter. Adicionalmente, oligo- o polímeros apropiados, por ejemplo, los derivados de monómeros vinílicos, de ácido acrílico, de EO y/o PO solos o en combinación con, por ejemplo, (poli)alcoholes o (poli)aminas. También es posible emplear lignina y sus derivados de ácido sulfónico, celulosas no modificadas y modificadas, ácidos sulfónicos aromáticos y/o alifáticos y sus aductos con formaldehído.
Los agentes de pegajosidad tales como la carboximetilcelulosa y los polímeros naturales y sintéticos en forma de polvos, gránulos o látex, tales como la goma arábiga, el alcohol polivinílico y el acetato de polivinilo, así como los fosfolípidos naturales tales como las cefalinas y las lecitinas y los fosfolípidos sintéticos, se pueden usar en la formulaciones.
Otros aditivos pueden ser aceites minerales y vegetales. También es posible agregar colorantes tales como pigmentos inorgánicos, por ejemplo, óxido de hierro, óxido de titanio y azul de Prusia, y colorantes orgánicos, tales como colorantes de alizarina, colorantes azoicos y colorantes de ftalocianina metálica, y nutrientes de oligoelementos tales como sales de hierro, manganeso, boro, cobre, cobalto, molibdeno y zinc. Otros posibles aditivos son perfumes, minerales o vegetales, opcionalmente aceites y ceras modificados.
Las formulaciones también pueden comprender estabilizantes, por ejemplo, estabilizantes de baja temperatura, conservantes, antioxidantes, estabilizantes de luz u otros agentes que mejoran la estabilidad química y/o física.
Las formulaciones contienen generalmente entre 0.01 y 98 % en peso de principio activo, preferiblemente entre 0.1 y 95 % y en particular preferiblemente entre 0.5 y 90 %.
Los compuestos activos de la invención también se pueden usar en mezcla con otros fungicidas conocidos, por ejemplo, para mejorar el espectro de actividad o para reducir o retardar el desarrollo de resistencia. También es posible una mezcla con otros compuestos activos conocidos tales como nematicidas, herbicidas, insecticidas, acaricidas o bactericidas, o con fertilizantes y reguladores del crecimiento, protectores o semioquímicos.
Ejemplos de tasas de aplicación de los compuestos activos según la invención son: cuando se tratan las hojas: desde 0.1 a 10000 g/ha, preferiblemente desde 10 a 1000 g/ha, en particular preferiblemente desde 50 a 300 g/ha (cuando la aplicación se realiza por riego o por goteo, incluso es posible reducir la tasa de aplicación, especialmente cuando se usan sustratos inertes tales como lana de roca o perlita); en el tratamiento de semillas: desde 2 a 200 g por 100 kg de semillas, preferiblemente de 2.5 a 150 g por 100 kg de semillas, y en particular preferiblemente desde 2.5 a 25 g por 100 kg de semillas, en particular muy preferiblemente desde 2.5 a 12.5 g por 100 kg de semilla; al tratar el suelo: desde 0.1 a 10000 g/ha, preferiblemente desde 1 a 5000 g/ha.
Las composiciones según la invención son apropiadas para proteger cualquier variedad vegetal que se utilice en agricultura, en invernadero, en bosques o en horticultura y, en particular, cereales (por ejemplo, trigo, cebada, centeno, mijo y avena), maíz, algodón, soja, arroz, patatas, girasoles, judías, café, remolacha (por ejemplo, remolacha azucarera y remolacha forrajera), cacahuetes, hortalizas (por ejemplo, tomates, pepinos, cebollas y lechuga), césped, árboles frutales y de frutos secos (por ejemplo, manzanas, peras, melocotones nectarinas, albaricoques, avellanas, pacanas, macadamia, pistachos), frutos rojos (por ejemplo, fresas, frambuesas, grosellas negras, grosellas rojas), vides, plátanos, cacao y plantas ornamentales.
Los compuestos activos de la invención, en combinación con una buena tolerancia de las plantas y una toxicidad favorable para los animales de sangre caliente y siendo bien tolerados por el medio ambiente, son apropiados para proteger las plantas y los órganos de las plantas, para aumentar los rendimientos de las cosechas, para mejorar la calidad del material cosechado y para el control de plagas, en particular enfermedades fúngicas, que se encuentran en la agricultura, en la horticultura, en la ganadería, en los bosques, en jardines e instalaciones de ocio, en la protección de productos almacenados y de materiales, y en el sector de la higiene. Pueden emplearse preferiblemente como agentes de protección de cultivos.
Uso como fungicidas
Los compuestos de la invención tienen actividad como fungicidas.
Los siguientes son ejemplos ilustrativos de plagas agrícolas que pueden ser controladas por compuestos fungicidas:
Enfermedades por mildiú pulverulento tales como: enfermedades por Blumeria, causadas por ejemplo, por Blumeria graminis; enfermedades por Podosphaera, causadas por ejemplo, por Podosphaera leucotheca; enfermedades por Sphaerotheca, causadas por ejemplo, por Sphaerotheca fuliginea; enfermedades por Uncinula, causadas por ejemplo, por Uncinula necator;
Enfermedades por roya tales como: enfermedades por Gymnosporangium, causadas por ejemplo, por Gymnosporangium sabinae; enfermedades por Hemileia, causadas por ejemplo, por Hemileia vastatix; enfermedades causadas por Phakopsora, causadas por ejemplo, por Phakopsora pachyrhizi o Phakopsora meibomiae; enfermedades por Puccinia, causadas por ejemplo, por Puccinia recondita; enfermedades por Uromyces, causadas por ejemplo, por Uromyces appendiculatus;
Enfermedades por oomicetos tales como: enfermedades por Albugo causadas por ejemplo, por Albugo Candida; enfermedades por Bremia, causadas por ejemplo, por Bremia lactucae; enfermedades por Peronospora, causadas por ejemplo, por Peronospora pisi o P. brassicae; enfermedades por Phytophthora, causadas por ejemplo, por Phytophthora infestans; enfermedades por Plasmopara, causadas por ejemplo, por Plasmopara viticola; enfermedades por pseudoperonospora, causadas por ejemplo, por Pseudoperonospora humuli o Pseudoperonospora cubensis; enfermedades por Pythium, causadas por ejemplo, por Pythium ultimum; enfermedades por mancha foliar, mancha de la hoja y tizón foliar tales como: enfermedades por Alternaria, causadas por ejemplo, por Alternaria solani; enfermedades por Cercospora, causadas por ejemplo, por Cercospora beticola; enfermedades por Cladiosporum, por ejemplo, causadas por Cladiosporium cucumerinum; enfermedades por Cochliobolus, causadas por ejemplo, por Cochliobolus sativus; enfermedades por Colletotrichum, causadas por ejemplo, por Colletotrichum lindemuthanium; enfermedades por Cycloconium, causadas por ejemplo, por Cyclconium oleaginum; enfermedades por Diaporthe, causadas por ejemplo, por Diaporthe citri; Drechslera, Syn: Helminthosporium) o Cochliobolus miyabeanus; enfermedades por Elsinoe, causadas por ejemplo, por Elsinoe fawcettii; enfermedades por Gloeosporium, causadas por ejemplo, por Gloeosporium laeticolor; enfermedades por Glomerella, causadas por ejemplo, por Glomerella cingulata; enfermedades por Guignardia, causadas por ejemplo, por Guignardia bidwelli; enfermedades por Leptosphaeria, causadas por ejemplo, por Leptosphaeria maculans; Leptosphaeria nodorum; enfermedades por Magnaporthe, causadas por ejemplo, por Magnaporthe grisea; enfermedades por Mycosphaerella, causadas por ejemplo, por Mycosphaerella graminicola; Mycosphaerella arachidtola; Mycosphaerella fibensis; enfermedades por Phaeosphaera, causadas por ejemplo, por Phaeosphaera nodorum;
Enfermedades por Pyrenophora, causadas por ejemplo, por Pyrenophora teres; enfermedades por Ramularia, causadas por ejemplo, por Ramularia collo-cygni; enfermedades por Rhynchosporium, causadas por ejemplo, por Rhynchosporium secalis; enfermedades por Septoria, causadas por ejemplo, por Septoria apii o Septoria lycopercisi; enfermedades por Typhula, causadas por ejemplo, por Typhula incarnata; enfermedades por Venturia, causadas por ejemplo, por Venturia inaequalis;
Enfermedades de raíces y tallos tales como: enfermedades por Corticium, causadas por ejemplo, por Corticium graminearum; enfermedades por Fusarium, causadas por ejemplo, por Fusarium oxysporum; enfermedades por Gaeumannomyces, causadas por ejemplo, por Gaeumannomyces graminis; enfermedades por Rhizoctonia, causadas por ejemplo, por Rhizoctonia solani; enfermedades por Sarocladium causadas, por ejemplo, por Sarocladium oryzae; enfermedades por Sclerotium causadas, por ejemplo, por Sclerotium oryzae; enfermedades por Tapesia, causadas por ejemplo, por Tapesia acuformis; enfermedades por Thielavbpsis, causadas por ejemplo, por Thielaviopsis basicola;
Enfermedades de la espiga y la panícula, incluida la mazorca de maíz, tales como: enfermedades por Alternaria, causadas por ejemplo, por Alternaria spp.; enfermedades por Aspergillus, causadas por ejemplo, por Aspergillus flavus; enfermedades por Cladosporium, causadas por ejemplo, por Cladosporium spp.; enfermedades por Claviceps, causadas por ejemplo, por Claviceps purpurea; enfermedades por Fusarium, causadas por ejemplo, por Fusarium culmorum; enfermedades por Gibberella, causadas por ejemplo, por Gibberella zeae; enfermedades por Monographella, causadas por ejemplo, por Monographella nivalis;
Enfermedades del tizón y del hollín tales como: enfermedades por Sphacelotheca, causadas por ejemplo, por Sphacelotheca reiliana; enfermedades por Tilletia, causadas por ejemplo, por Tilletia caries; enfermedades por Urocystis, causadas por ejemplo, por Urocystis occulta; enfermedades por Ustilago, causadas por ejemplo, por Ustilago nuda;
Enfermedades de pudrición y moho de la fruta tales como: enfermedades por Aspergillus, causadas por ejemplo, por Aspergillus flavus; enfermedades por Botrytis, causadas por ejemplo, por Botrytis cinerea; enfermedades por Penicillium, causadas por ejemplo, por Penicillium expansum; enfermedades por Rhizopus causadas por ejemplo, por Rhizopus stolonifer; enfermedades por Sclerotinia, causadas por ejemplo, por Sclerotinia sclerotiorum;
Enfermedades por Verticilium, causadas por ejemplo, por Verticilium alboatrum;
Enfermedades transmitidas por la semilla y el suelo, moho, marchitamiento, pudrición y marchitamiento fúngico tales como: enfermedades por Alternaria, causadas por ejemplo, por Alternaria brassicicola; enfermedades por Aphanomyces, causadas por ejemplo, por Aphanomyces euteiches; enfermedades por Ascochyta, causadas por ejemplo, por Ascochyta lentis; enfermedades por Aspergillus, causadas por ejemplo, por Aspergillus flavus;
enfermedades por Cladosporium, causadas por ejemplo, por Cladosporium herbarum; Enfermedades por Cochliobolus, causadas por ejemplo, por Cochliobolus sativus (Conidiaform: Drechslera, Bipolaris Syn: helmintosporium);
Enfermedades por Colletotrichum, causadas por ejemplo, por Colletotrichum coccodes; enfermedades por Fusarium, causadas por ejemplo, por Fusarium culmorum; enfermedades por Gibberella, causadas por ejemplo, por Gibberella zeae; enfermedades por Macrophomina, causadas por ejemplo, enfermedades por Macrophomina phaseolina, Monographella, causadas por ejemplo, por Monographella nivalis; enfermedades por Penicillium, causadas por ejemplo, por Penicillium expansum; enfermedades por Phoma, causadas por ejemplo, por Phoma lingam; enfermedades por Phomopsis, causadas por ejemplo, por Phomopsis sojae; enfermedades por Phytophthora, causadas por ejemplo, por Phytophthora cactorum; enfermedades por Pyrenophora, causadas por ejemplo, por Pyrenophora graminea; enfermedades por Pyricularia, causadas por ejemplo, por Pyricularia oryzae; enfermedades por Pythium, causadas por ejemplo, por Pythium ultimum; enfermedades por Rhizoctonia, causadas por ejemplo, por Rhizoctonia solani; enfermedades por Rhizopus, causadas por ejemplo, por Rhizopus oryzae; enfermedades por Sclerotium, causadas por ejemplo, por Sclerotium rolfsii; enfermedades de Septoria, causadas por ejemplo, por Septoria nodorum; enfermedades por Typhula, causadas por ejemplo, por Typhula incarnata; enfermedades por Verticillium, causadas por ejemplo, por Verticillium dahliae; enfermedades de cancro, escoba y de acrenosis tales como: enfermedades por Nectria, causadas por ejemplo, por Nectria galligena;
Afecta enfermedades como:
enfermedades por Monilinia, causadas por ejemplo, por Monilinia laxa; enfermedades de ampollas de hojas o rizos de hojas tales como: enfermedades por Exobasidium causadas por ejemplo, por
Exobasidium vexans; enfermedades por Taphrina, causadas por ejemplo, por Taphrina deformans; -Enfermedades de disminución de plantas de madera tales como:
Enfermedades por Esca, causadas por ejemplo, por Phaemoniella clamydospora, Phaeomoniella clamydospora, Phaeoacremonium aleophilum y Fomitiporia mediterranea;
Eutypa dyeback, causada por ejemplo, por Eutypa lata; enfermedad del olmo holandés, causada por ejemplo, por Ceratocystsc ulmi; enfermedades por Ganoderma causadas por ejemplo, por Ganoderma boninense; enfermedades de flores y semillas tales como: enfermedades por Botrytis, causadas por ejemplo, por Botrytis cinerea;
Enfermedades de los tubérculos tales como: enfermedades por Rhizoctonia, causadas por ejemplo, por Rhizoctonia solani; enfermedades por Helminthosporium, causadas por ejemplo, por Helminthospohum solani.
Enfermedades de los tubérculos tales como
enfermedades por Rhizoctonia causadas, por ejemplo, por Rhizoctonia solani; enfermedades por Helminthosporium, causadas por ejemplo, por Helminthospohum solani;
Enfermedades de la raíz del club tales como
Enfermedades por Plasmodiophora, causadas por ejemplo, por Plamodiophora brassicae.
Los compuestos de la invención pueden ser activos frente a un amplio espectro de enfermedades fúngicas de las plantas. Alternativamente, pueden ser activos específicamente frente a enfermedades fúngicas de cereales o pueden ser específicamente activos frente a enfermedades de oomicetos.
Los patógenos fúngicos de cereales notables son:
Erisyphe graminis (now Blumeria)
Septoria nodorum
Septoria tritici
Fusarium oxysporum
Rhychosporium secalis
Pyrenophora teres
Puede ser que los compuestos de la invención sean para su uso en el tratamiento de una enfermedad fúngica causada por un patógeno seleccionado de Botrytis cinerea, una especie Alternaría, Septoria tritici y Rhizoctonia cerealis. Los patógenos fúngicos oomicetos notables son:
Plasmopara vitícola
Phytophthora infestans
Pythium ultimum
Bremia lactuca
Peronospora spp
Además de su actividad fungicida, pero sin pretender que sean parte de la invención, los compuestos de la invención también pueden tener actividad frente a otros microbios, por ejemplo, bacterias.
Aunque no forman parte de la invención, los compuestos fungicidas de la invención también se pueden usar en el tratamiento de enfermedades fúngicas de seres humanos y animales (por ejemplo, mamíferos). Asimismo, los compuestos bactericidas de la invención pueden usarse en el tratamiento de enfermedades bacterianas de humanos y animales.
Descripción detallada - Síntesis
El experto en la técnica apreciará que la adaptación de los métodos conocidos en la técnica podría aplicarse en la fabricación de los compuestos de la presente invención.
Por ejemplo, el experto en la técnica se familiarizará de inmediato con libros de texto estándar tales como Comprehensive Organic Transformations - A Guide to Functional Group Transformations", RC Larock, Wiley-VCH (1999 or later editions); "March's Advanced Organic Chemistry - Reactions, Mechanisms and Structure", MB Smith, J. March, Wiley, (5th edition or later); "Advanced Organic Chemistry, Part B, Reactions and Synthesis", FA Carey, RJ Sundberg, Kluwer Academic/Plenum Publications, (2001 or later editions); "Organic Synthesis - The Disconnection Approach", S Warren (Wiley), (1982 or later editions); "Designing Organic Syntheses" S Warren (Wiley) (1983 or later editions); "Heterocyclic Chemistry", J. Joule (Wiley 2010 edition or later); ("Guidebook To Organic Synthesis" RK Mackie and DM Smith (Longman) (1982 or later editions), etc., y las referencias que contienen como guía.
El experto en la técnica está familiarizado con una variedad de estrategias para sintetizar moléculas orgánicas y particularmente heterocíclicas y éstas representan un conocimiento general común como se establece en libros de texto tales como Warren "Organic Synthesis: The Disconnection Approach"; Mackie and Smith "Guidebook to Organic Chemistry"; y Clayden, Greeves, Warren and Wothers "Organic Chemistry".
El experto ejercerá su juicio y habilidad en cuanto a la secuencia de reacciones más eficiente para la síntesis de un compuesto diana dado y empleará grupos protectores según sea necesario. Esto dependerá, inter alia, de factores tales como la naturaleza de otros grupos funcionales presentes en un sustrato particular. Claramente, el tipo de química implicada influirá en la elección del reactivo que se utilice en dichas etapas de síntesis, la necesidad y el tipo de grupos protectores que se empleen y la secuencia para realizar de protección/desprotección. Estos y otros parámetros de reacción serán evidentes para el experto en la técnica con referencia a los libros de texto estándar ya los ejemplos proporcionados en este documento.
Puede ser necesario proteger y desproteger los grupos funcionales sensibles durante la síntesis de un compuesto de la invención. Esto se puede lograr mediante métodos convencionales, por ejemplo, como se describe en “Protective Groups in Organic Synthesis” de TW Greene and PGM Wuts, John Wiley & Sons Inc. (1999), y las referencias en este.
A lo largo de esta memoria descriptiva, estas abreviaturas tienen los siguientes significados:
Se puede acceder a determinados compuestos de la invención según los siguientes esquemas de síntesis generales o de forma análoga a estos. Se puede acceder a determinados compuestos de la invención a través de los productos intermedios sintéticos descritos en los ejemplos 1 a 27 a continuación.
Esquemas de síntesis generales
Determinados compuestos de la invención se pueden hacer según el esquema A. Reacción de Suzuki entre yoduro A y ácido borónico B (por ejemplo, usando Na2¿O3, Pd(PPh3)4 en dioxano/agua a 90 °C) puede proporcionar biarilo C que puede combinarse con benzimidazol/benzotriazol D (Pd2dba3, Xantphos, Cs2CO3 en dioxano a 100 °C) para proporcionar compuestos de fórmula E. Esto se puede usar para producir los compuestos en los que Y1 es ya sea CH o N.
Determinados compuestos de piridazina de la invención se pueden preparar según el esquema B. Benzimidazol/benzotriazol D se puede convertir en bromuro F (por ejemplo, por reacción con cloruro de bromoacetilo en acetona en presencia de K2CO3 a reflujo). Reacción de bromuro F con ácido carboxílico G en presencia de una base (por ejemplo, Et3N y DBU en presencia de aire) puede proporcionar butanolida H. El tratamiento posterior con hidrazina seguido de POCh puede proporcionar piridazina J (un subconjunto de compuestos de fórmula I). Esto se puede usar para producir los compuestos en los que Y1 es ya sea CH o N.
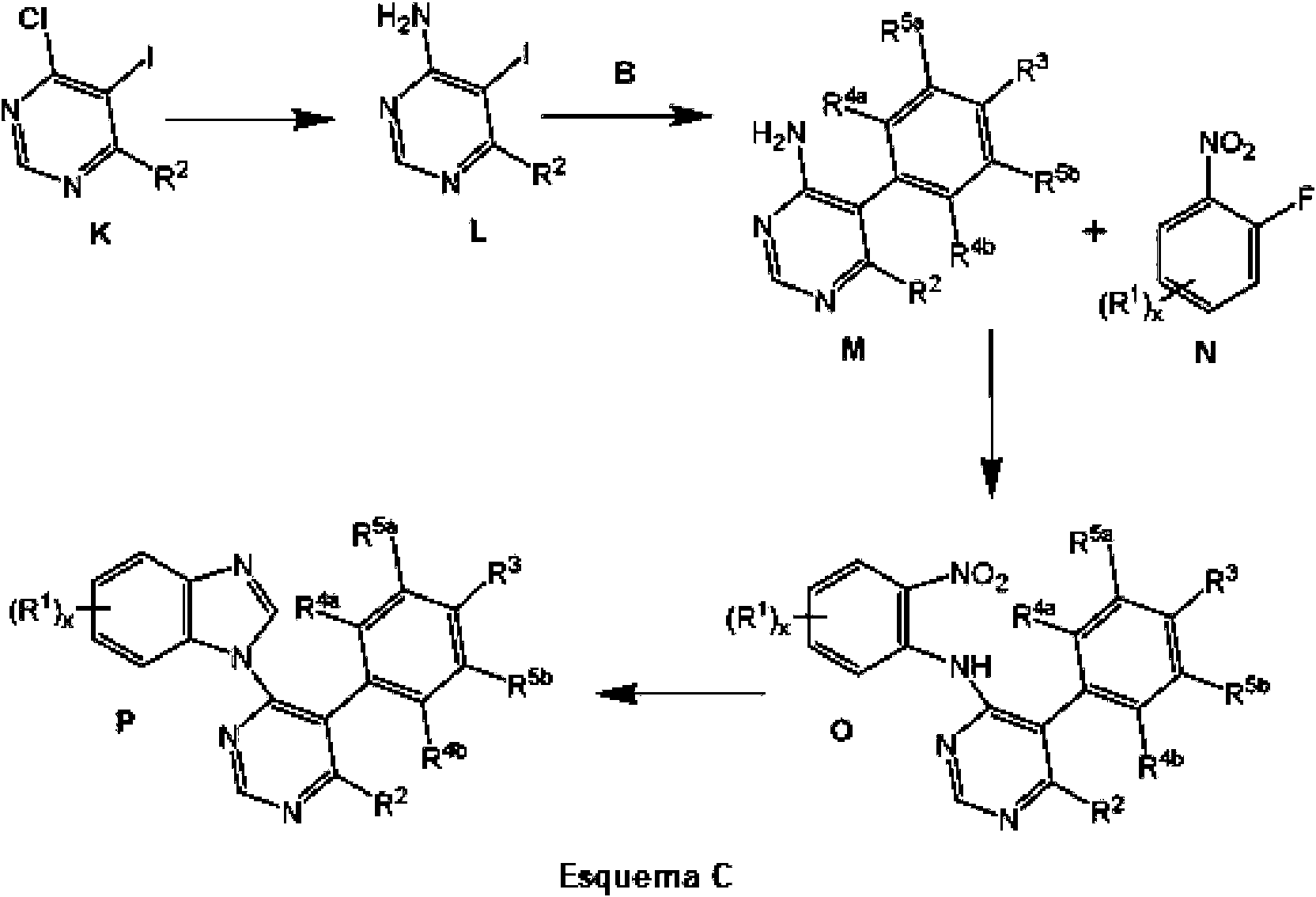
Determinados compuestos de pirimidina de la invención se pueden preparar según el esquema C. Cloro pirimidina K se puede convertir en amino pirimidina L (por ejemplo, calentando con NH4OH). La reacción de Suzuki entre aminopirimidina L y ácido borónico B (por ejemplo, usando Na2CO3, Pd(PPh3)4 en dioxano/agua a 90 °C) puede proporcionar biarilo M que puede acoplarse con nitrobenceno D (por ejemplo, desprotonando el grupo amina de la pirimidina L con NaH y haciéndolo reaccionar con nitrobenceno N en DMF a temperatura ambiente) para proporcionar los compuestos de fórmula O. La reducción del grupo nitro (por ejemplo, usando Fe, NH4O en THF/agua/metanol a 60 °C) seguido de la reacción con ortoformiato de metilo en presencia de un ácido (por ejemplo, HCl) y a alta temperatura (por ejemplo, 100 °C) puede proporcionar la pirimidina P (un subconjunto de compuestos de fórmula I).
Determinados compuestos de pirimidina de la invención se pueden preparar según el esquema D. La reducción de nitrato O (por ejemplo, usando Fe, NH4Cl en THF, MeOH, H2O) seguido de la formación de triazol (por ejemplo, usando NaNO2 y HCI) puede proporcionar el triazol.
Ejemplos
Métodos generales
La cromatografía instantánea se llevó a cabo usando un Biotage Isolera 4, con cartuchos Biotage® SNAP KP-Sil, empacados con partículas de sílice de 50 |jm con un área superficial de 500 m2/g, o cartuchos alternativos (por ejemplo, Puriflash, producido por Interchim) donde se indique, o usando gel de sílice (partículas de 40-63 jm ). La visualización se llevó a cabo con luz ultravioleta (254 nm) y mediante tinción con soluciones de permanganato de potasio, ácido fosfomolíbdico (PMA) o ninhidrina.
Todos los espectros de 1H RMN se obtuvieron en un Bruker AVIII 400 con QNP de 5 mm o Bruker AVI 500 con QNP de 5 mm. Los cambios químicos se expresan en partes por millón (8) y se refieren al solvente. Las constantes de acoplamiento j se expresan en hercios (Hz).
La MS se llevó a cabo en un Waters Alliance ZQ MS, usando una columna LC YMC-Triart C18 de 50 x 2 mm de 5 micrómetros (disolvente: 5-90 % de gradiente de acetonitrilo en agua (con 1 % en volumen de solución acuosa de amoníaco al 28 % (en peso)) por el método A. Velocidad de flujo 0.8 mL/min. Las longitudes de onda fueron 254 y 210 nM.
Método A (pH básico de 5 minutos)
Columna: YMC-Triart C1850 x 2 mm, 5 jm . Velocidad de flujo: 0.8 mL/min. Volumen de inyección: 5 jL .
Fase móvil A H2O
B CH3CN
C 50 % H2O / 50 % CH3CN 1.0 % amoníaco (ac.)
Método E (pH básico de 3.5 minutos)
Fases móviles: Agua (A)/Acetonitrilo (B) ambos con 0.1 % (v/v) de amoníaco
Columna: BEH C182.1 x 50 mm, 1.7 pm a 50 °C
Método F (pH ácido de 3.5 minutos)
Fases móviles: Agua (A)/Acetonitrilo (B) ambos con 0.1 % (v/v) de ácido fórmico
Columna: CSH C182.1 x 50 mm, 1.7 pm a 50 °C
Todos los reactivos se obtuvieron de proveedores comerciales y se usaron como se suministraron a menos que se indique lo contrario.
Todos los compuestos se nombran usando ChemBioDraw Ultra 14.0.
Producto intermedio A: 5-Yodo-6-metilpirimidin-4-amina
Una suspensión de 4-cloro-5-yodo-6-metilpirimidina (170 mg, 0.668 mmol) en hidróxido de amonio (28 %, 2 mL) se calentó a 100 °C en un tubo sellado durante 3 h. Después de enfriar a temperatura ambiente, la suspensión se filtró y el sólido se lavó (agua) y se secó al vacío para producir el compuesto base como un sólido de color naranja pálido (90 mg, 57 %).1H RMN 8h (500 MHz, CDCla) 8.33 (s, 1H), 5.46 (br s, 2H), 2.64 (s, 3H). LCMS (Método A): 1.66 min (236.0, MH+).
Producto intermedio B: 5-(2-Cloro-4-fluorofenil)-6-metilpirimidin-4-amina
El producto intermedio A (90 mg, 0.38 mmol) y acido 2-cloro-4-fluorofenilboromco (100 mg, 0.57 mmol) se disolvieron en 1,4-dioxano (3 mL). Se agregó carbonato de sodio (ac. 2 M) (0.78 mL, 1.5 mmol) y la mezcla se desgasificó burbujeando nitrógeno durante 5 min. Se agregó tetrakis(trifenilfosfina)paladio (22 mg, 20 |jmol) y la reacción se calentó a 90 °C, durante 16 h. La reacción se filtró a través de decalite®, eluyendo con EtOAc y concentrando al vacío. El residuo se purificó por cromatografía (SiO2, 0-100 % de EtOAc en PE) y el compuesto base se aisló como un sólido de color naranja (82 mg, 90 %). 1H RMN 8h (500 MHz, CDCh) 8.53 (s, 1H), 7.34 (dd, j= 8.4, 2.6 Hz, 1H), 7.29 - 7.24 (m, 1H), 7.15 (td, j= 8.2, 2.6 Hz, 1H),4.62 (br s, 2H), 2.13 (s, 3H). LCMS (Método A): 2.22 min (238.1, MH+).
Productos intermedios C-G:
Los siguientes productos intermedios se prepararon usando el método general descrito para el producto intermedio B a partir del acido halo (hetero)-aromatico y borónico adecuado.
Producto intermedio H: 5-(2-Cloro-4-fluorofenil)-N-(2,4-difluoro-6-nitrofenil)-6-metilpirimidin-4-amina
Se agrego hidruro de sodio (60 %, 55 mg, 1.4 mmol) a una solución del producto intermedio B en DMF (2 mL). Después de agitar a temperatura ambiente durante 15 min, se agregó 1,2,5-trifluoro-3-nitrobenceno (63 j L, 0.56 mmol) y se continuó agitando durante 90 min. La mezcla de reacción se inactivo cuidadosamente con agua y se extrajo con EtOAc (x 3). Las fases orgánicas combinadas se lavaron con salmuera, se secaron (MgSO4) y se concentraron al vacío. El residuo se purificó por cromatografía (SiO2, 0-50 % de EtOAc en PE) y el compuesto base se aisló como un sólido de color amarillo (129 mg, 70%). 1H RMN 8h (500 MHz, CDCls) 8.61 (s, 1H), 7.66 -7.61 (m, 1H), 7.41 (dd, j= 8.3, 2.5 Hz, 1H), 7.37 (dd, j= 8.5, 5.9 Hz, 1H), 7.25 -7.21 (m, 2H), 7.13 (br s, 1H), 2.23 (s, 3H).
LCMS (Método A): 3.17 min (395.3, MH+).
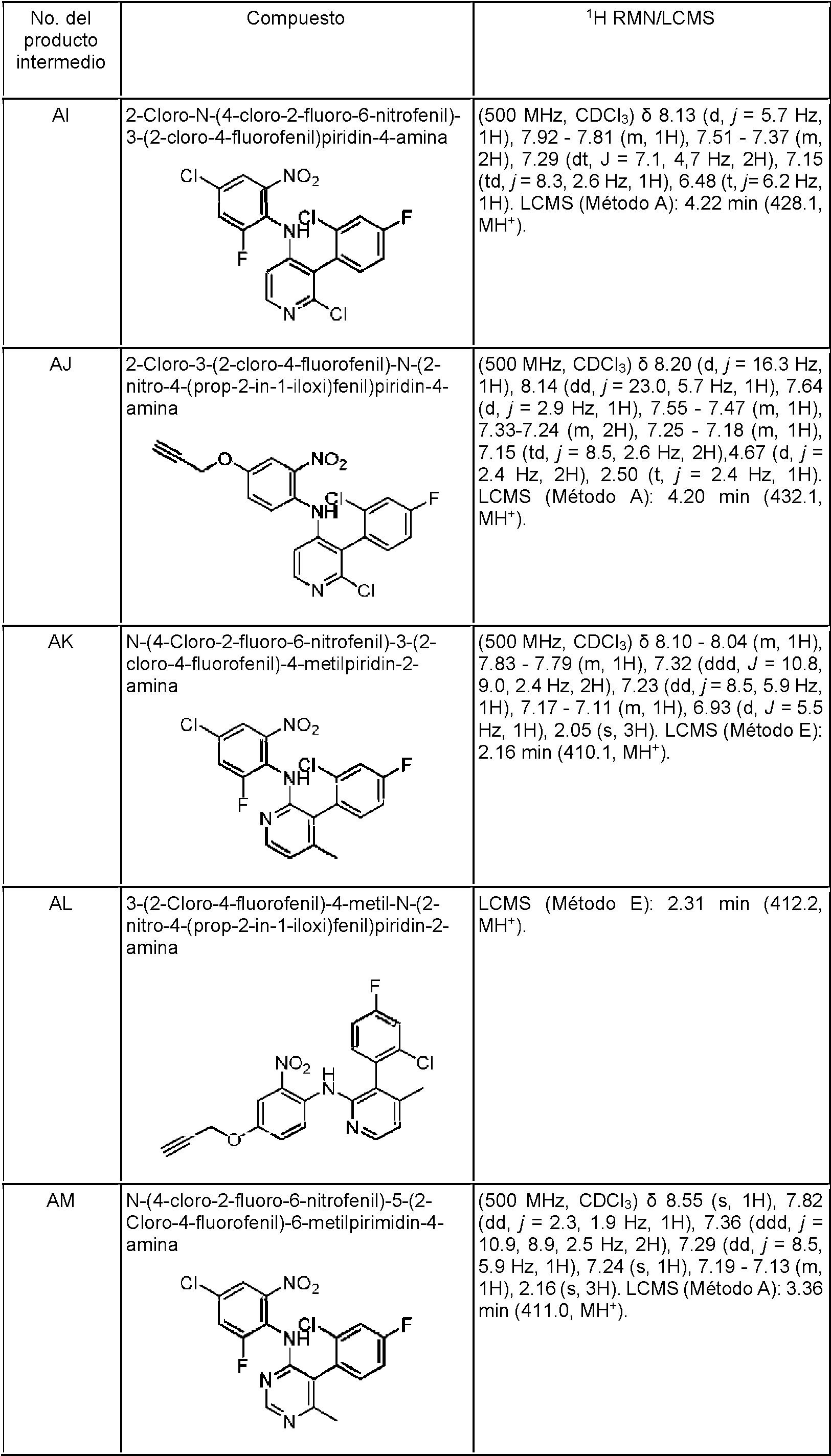
Productos intermedios I-L:
Los siguientes productos intermedios se prepararon usando el método general descrito para el producto intermedio H a partir del producto intermedio adecuado (C-F) y 1,2,5-trifluoro-3-nitrobenceno.
Producto intermedio M: 2'-Cloro-N-(2,4-difluoro-6-nitrofenil)-4'-fluoro-6-metil-[1,1'-bifenil]-2-amina
Producto intermedio G (90 mg, 0.38 mmol), 2-bromo-1,5-difluoro-3-nitrobenceno (57 pL, 0.46 mmol), carbonato de cesio (174 mg, 0.535 mmol) y 4,5-bis(difenilfosfino)-9,9-dimetilxanteno (44 mg, 0.08 mmol) se disolvieron en 1,4-dioxano (1 mL). La mezcla se desgasificó por burbujeo de nitrógeno durante 5 min. Se agregó tris(dibencilidenacetona)dipaladio(0) (70 mg, 0.08 mmol) y la reacción se calentó a 100 °C, durante 16 h. Después de enfriar a temperatura ambiente, la mezcla se repartió entre EtOAc y agua. La capa acuosa se extrajo con EtOAc. Las capas orgánicas combinadas se lavaron (salmuera), se secaron (MgSO4) y se concentraron al vacío. El residuo se purificó por cromatografía (SiO2, 0-100 % de EtOAc en PE) y el compuesto base se aisló como un aceite de color rojo (111 mg, 74 %). 1H RMN 8h (500 MHz, CDCls) 7.87 (br s, 1H), 7.66 (ddd, J = 8.5, 3.0, 2.0 Hz, 1H), 7.49 (ddd, J = 7.5, 2.8, 2.0 Hz, 1H), 7.32 (dd, j= 8.5, 2.6 Hz, 1H), 7.27 - 7.22 (m, 1H), 7.20 (td, j= 7.8, 2.9 Hz, 1H), 7.17 - 7.10 (m, 1H), 7.10 -7.05 (m, 1H), 6.78 (dd, j = 8.0, 5.2 Hz, 1H), 2.07 (s, 3H).
Producto intermedio N: N1-(5-(2-Cloro-4-fluorofenil)-6-metilpirimidin-4-il)-4,6-difluorobenceno-1,2-diamina
Se agregó una solución de cloruro de amonio (51 mg, 0.95 mmol) en agua (0.4 mL) a una solución del producto intermedio H (125 mg, 0.317 mmol) en THF (2 mL)/metanol (1 mL). Se agregó polvo de hierro (53 mg, 0.95 mmol) y la mezcla se calentó a 65 °C, durante 18 h. Después de enfriar a temperatura ambiente, la mezcla se filtró a través de decalite®, eluyendo con EtOAc. El filtrado se lavó (agua, salmuera), se secó (MgSO4) y concentró al vacío para producir el compuesto base como un sólido blanquecino (116 mg, cuant.). 1H RMN 8h (500 MHz, CDCh) 8.61 (s, 1 H), 7.44 7.33 (m, 2H), 7.24-7.17 (m, 1H), 6.35-6.20 (m, 2H), 5.29 (s, 1H), 4.13 (br s, 2H), 2.18 (s, 3H). LCMS (Método A): 2.84 min (365.3, MH+).
Productos intermedios O-S:
Los siguientes productos intermedios se prepararon usando el método general descrito para el producto intermedio N a partir del producto intermedio adecuado (I-M).
Producto intermedio T: 3-Metil-2-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)anilina
A una solución de 2-bromo-3-metilanilina (0.34 mL, 2.7 mmol) en 1,4-dioxano (12 mL) se le agregó acetato de potasio (527 mg, 5.37 mmol), bis(pinacolato)diboro (1365 mg, 5.37 mmol) y la solución se desgasificó durante 10 min. Se agregó complejo de [1,1'-bis(difenilfosfino)ferroceno]dicloropaladio(II) con diclorometano (219 mg, 0.269 mmol) y la suspensión se calentó a 90 °C, durante 18 h en un recipiente cerrado. La mezcla de reacción se dejó enfriar, se diluyó con EtOAc y luego se lavó con salmuera. La capa orgánica se secó sobre MgSO4, y se concentró al vacío. El residuo se purificó por cromatografía (SiO2, 0-20 % de EtOAc en PE) y el compuesto base se aisló como un sólido de color blanco (742 mg, 65 %). 1H RMN 8h (500 MHz, CDCla) 7.04 (t, J = 7.7 Hz, 1H), 6.49 (m, 2H), 4.20 (s, 2H), 2.44 (s, 3H), 1.34 (s, 12H). LCMS (Método A): 4.15 min (234.2, MH+).
Producto intermedio U: 2'-Cloro-4'-fluoro-6-metil-N-(2-nitrofenil)-[1,1'-bifenil]-2-amina
Producto intermedio G (50 mg, 0.21 mmol), 4,5-bis(difenilfosfino)-9,9-dimetilxanteno (24,55 mg, 0.042 mmol), carbonato de cesio (97 mg, 0.297 mmol) y 1-bromo-2-nitrobenceno (47.1 mg, 0.233 mmol) se disolvieron en 1,4-dioxano (8 mL). La solución se purgó con N2 durante 5 min y se agregó tris(dibencilidenacetona)dipaladio (0) (38.9 mg, 0.042 mmol). La solución se calentó a 100 °C, durante 18 h. La mezcla de reacción se dejó enfriar, se agregó agua y el producto se extrajo con EtOAc. Las capas orgánicas combinadas se lavaron con salmuera, se secaron (MgSO4) y se concentraron al vacío. El residuo se purificó por cromatografía (SO 2, 0-20 % de EtOAc en PE) y el compuesto base se aisló como un sólido de color naranja (67 mg, 71 %). 1H r Mn 8h (500 MHz, CDCh) 9.00 (s, 1H), 8.08 (dd, J = 8.6, 1.5 Hz, 1H), 7.38-7.30 (m, 3H), 7.23 (dt, j= 8.7, 2.1 Hz, 2H), 7.20 -7.17 (m, 1H), 7.16 (dd, j= 8.5, 6.1 Hz, 1H), 7.06 -7.02 (m, 1H), 6.71 (ddd, j= 8.4, 6.9, 1.3 Hz, 1H), 2.09 (s, 3H). LCMS (Método A): 4.49 min (357.0, MH+).
Producto intermedio V: 1-Fluoro-2-nitro-4-(prop-2-in-1 -iloxi) benceno
Se agregó bromuro de propargilo (80 % en PhMe, 0.355 mL, 3.18 mmol) a una solución de 4-fluoro-3-nitrofenol (0.500 g, 3.2 mmol) y carbonato de potasio (0.440 g, 3.18 mmol) en DMF (10 mL) a r.t. y la mezcla de reacción se agitó durante 3 días. Luego, la mezcla de reacción se diluyó con agua y se extrajo en EtOAc antes de secarse (MgSO4) y concentrar al vacío. El residuo se purificó por cromatografía (SiO2, 0-20 % de EtOAc en PE) y el compuesto base se aisló como un aceite de color marrón (0.620 g, 100 %). 1H RMN 8h (500 MHz, CDCla) 87.67 (dd, j= 5.0, 2.1 Hz, 1H), 7.26 (dd, j= 5.2, 2.4 Hz, 2H), 4.77 (d, j= 2.4 Hz, 2H), 2.60 (t, J = 2.4 Hz, 1H).
Producto intermedio W:
El siguiente producto intermedio se preparó usando el método general descrito para el producto intermedio B a partir de 2-bromo-1,3-difluoro-5-metoxibenceno y el producto intermedio T.
Productos intermedios X-Y:
Los siguientes productos intermedios se prepararon usando el método general descrito para el producto intermedio B a partir del ácido halo (hetero)-aromático y borónico adecuados.
Producto intermedio Z: 2-(2,6-difluoro-4-metoxifenil)-3-oxobutanonitrilo
Se agregaron hidruro de sodio (177 mg, 4.42 mmol) y THF anhidro (5.9 mL) a un vial de microondas de 20 mL que luego se tapó y se purgó con nitrógeno. Luego se agregó gota a gota 2-Cloro-4-fluorofenilacetonitrilo (500 mg, 2.95 mmol) como una solución en THF (1 mL) y la reacción se agitó a r.t., durante 5 minutos. Luego se agregó EtOAc (2.88 mL, 29.5 mmol) y la reacción se calentó a 65 °C, durante 1 hora. Se agregaron agua (25 mL) y EtOAc (25 mL) a la mezcla de reacción y las capas se separaron. La capa acuosa se acidificó a pH 6 usando HCl 1 M ac. y se extrajo con EtOAc (3 x 10 mL). Las capas orgánicas combinadas se secaron usando MgSO4 y se concentraron a presión reducida para producir el compuesto base como un sólido de color amarillo (614 mg, 98 %). LCMS (Método F): 1.63 min (210.0, MH-).
Producto intermedio AA: 5-(2,6-difluoro-4-metoxifenil)-6-metilpirimidin-4-amina
Se agregó lentamente (trimetilsilil) diazometano (0.89 mL, 1.8 mmol) a una solución del producto intermedio Z (200 mg, 0.888 mmol) en DCM anhidro (1.8 mL) y se agitó durante 18 horas a r.t. Se agregó ácido acético gota a gota hasta que cesó el desprendimiento de gas, lo que indica la extinción del (trimetilsilil) diazometano restante. Luego se concentró la solución al vacío para proporcionar un aceite en bruto. Después, el residuo se disolvió en etanol (5.00 mL) y se agregó a una solución preformada de clorhidrato de formimidamida (79.0 mg, 0.98 mmol) en etóxido de sodio al 30 % en EtOH (829 pl, 2.22 mmol). A continuación, la reacción se calentó a 80 °C, durante 17 horas. La mezcla de reacción se dejó enfriar a r.t. y la solución se neutralizó usando ácido acético y se concentró al vacío para producir un sólido de color negro en bruto. El residuo en bruto se purificó mediante cromatografía (SiO2, 50-100 % de EtOAc en PE). Esto proporcionó el compuesto base como un sólido de color amarillo (27.5 mg, 12 % de rendimiento). 1H RMN 8h (500 MHz, DMSO-d6) 88.27 (s, 1H), 6.88 (d, J = 9,6 Hz, 2H), 6.53 (br. s, 2H), 3.96 - 3.61 (s, 3H), 2.06 - 1.83 (s, 3H).
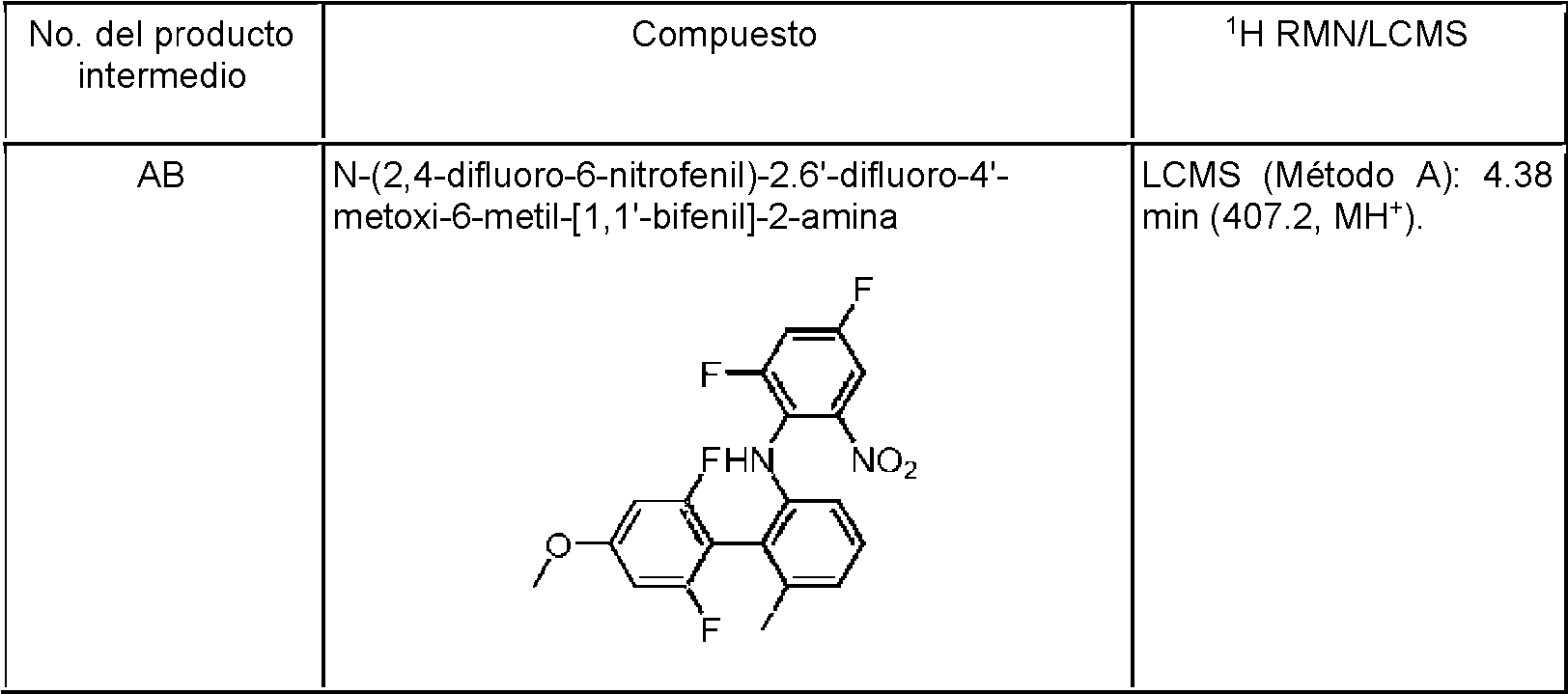
Producto intermedio AB
El siguiente producto intermedio se preparó usando el método general descrito para el producto intermedio H a partir del producto intermedio adecuado (W), 1,2,5-trifluoro-3-nitrobenceno y tert-butóxido de potasio (2 equivalentes) en lugar de NaH como base.
Productos intermedios AC-AD
Los siguientes productos intermedios se prepararon usando el método general descrito para el producto intermedio U a partir del producto intermedio adecuado y el bromonitrobenceno sustituido adecuado.
Producto intermedio AE: N-(4-cloro-2-fluoro-6-nitrofenil)-5-(2,6-difluoro-4-metoxifenil)-6-metilpirimidin-4-amina
El producto intermedio AA (176 mg, 0.701 mmol) se disolvió en THF anhidro (3.5 mL) y el matraz se selló y purgó con nitrógeno. A continuación, se agregó gota a gota solución de bis(trimetilsilM)amida sódica 2 M en THF (525 pl, 1.05 mmol) y la reacción se dejó en agitación durante 15 minutos a r.t. Luego se agregó 5-cloro-1,2-difluoro-3-nitrobenceno (136 mg, 0.701 mmol) como una solución en THF anhidro (0.5 mL) y se dejó que la reacción prosiguiera durante aprox.
16 horas. La mezcla de reacción se diluyó con agua (10 mL), se neutralizó usando HCl AC. 1 M y se extrajo con EtOAc (3 x 10 mL). Las fases orgánicas combinadas se secaron sobre MgSO4 y se concentraron al vacío para producir un sólido en bruto que se purificó mediante cromatografía (SiO2, 0-100 % de EtOAc en PE) para producir el compuesto base como un aceite de color amarillo (80 mg, 27 % de rendimiento). 1H RMN 8h (500 MHz, DMsO-d6) 58.49 (s, 1H), 8.40 (s, 1H), 8.03-7.95 (m, 2H), 6.97 (d, J = 9.8 Hz, 2H), 3.86 (s, 3H), 2.10 (d, J = 17.0 Hz, 3H).
Productos intermedios AF-AN
Los siguientes productos intermedios se prepararon usando el método general descrito para intermedio AE a partir del producto intermedio adecuado y fluoro-nitrobenceno sustituido.
Productos intermedios AO-BB:
Los siguientes productos intermedios se prepararon usando el método general descrito para el intermedio N a partir del producto intermedio adecuado.
Producto intermedio BC:
El siguiente producto intermedio se preparó usando el método general descrito para el producto intermedio B a partir de 5,6-dicloropiridazin-4-amina y ácido 2-cloro-4-fluorofenilborónico.
Producto intermedio BD;
El siguiente producto intermedio se preparó usando el método general descrito para el producto intermedio H a partir del producto intermedio adecuado (BC) y 2.5-difluoronitrobenceno.
Producto intermedio BE
El siguiente producto intermedio se preparó usando el método general descrito para el producto intermedio N a partir del producto intermedio BD adecuado.
Ejemplo 1: 1-(5-(2-Cloro-4-fluorofenil)-6-metilpirimidin-4-il)-5,7-difluoro-1H-benzo[d]imidazol
Se agregó HCl concentrado (2.0 j l, 16 |jmol) a una solución del producto intermedio L (116 mg, 0.318 mmol) en ortoformiato de trimetilo (522 jl, 4.77 mmol) y la mezcla se agitó a 100 °C, durante 3 h. Después de enfriar a temperatura ambiente, la mezcla de reacción se repartió entre agua y EtOAc. La capa acuosa se extrajo con EtOAc (x3). Las fases orgánicas combinadas se lavaron con salmuera, se secaron (MgSO4) y se concentraron al vacío. El residuo se purificó por cromatografía (SiO2, 0-60 % de EtOAc en PE) y el compuesto base se aisló como un sólido de color naranja pálido (94 mg, 79 %). 1H RMN 8h (500 MHz, CDCl3) 9.18 (s, 1H), 7.62 (s, 1H), 7.26-7.16 (m, 3H), 7.03 (td, y = 8.2, 2.5 Hz, 1H), 6.91 -6.82 (m, 1H), 2.48 (s, 3H). LCMS (Método A): 3.15 min (375.2, MH+).
Ejemplos 2-6:
Los siguientes ejemplos se prepararon usando el método general descrito en el ejemplo 1 a partir de los productos intermedios O-S.
Ejemplos 7-19:
Los siguientes ejemplos se prepararon usando el método general descrito en el ejemplo 1 a partir de los productos intermedios AO-BB.
Ejemplo 20: 5-Cloro-1-(2-cloro-3-(2-cloro-4-metoxifenil)piridin-4-il)-7-fluoro-1H-benzo[d][1,2,3]triazol
Se agregó ácido clorhídrico (3 M, 3 mL) al intermedio AU (0.112 g, 0.271 mmol) y la mezcla se sometió a ultrasonido hasta que fue una suspensión. Luego se agregó gota a gota una solución de nitrito de sodio (0.028 g, 0.41 mmol) en agua (0.25 mL) y la mezcla de reacción se agitó a r.t. por 1 hora A continuación, la mezcla de reacción se diluyó con EtOAc y agua y las fases se separaron. A continuación, la mezcla de reacción se secó (MgSO4) y se concentró al vacío para dar el compuesto base como un sólido de color naranja (91 mg, 79 %). 1H RMN (500 MHz,_DMSO-d6) 8h 8.84 (d, j = 5.2 Hz, 1H), 8.18 (d, j = 1.6 Hz, 1H), 8.09 (dd, j = 5.2, 2.8 Hz, 1H), 7.80 (dd, j = 10.2, 1.5 Hz, 1H), 7.29 (d, j = 8.6 Hz, 1H), 6.99 (d, j = 2.5 Hz, 1H), 6.89 (dd, j = 8.6, 2.5 Hz, 1H), 3.74 (s, 3H).
Ejemplos 21-26:
Los siguientes ejemplos se prepararon usando el método general descrito en el ejemplo 20 a partir del producto intermedio adecuado.
Ejemplo 27:
El siguiente ejemplo se preparó usando el método general descrito en el ejemplo 1 a partir del Intermedio BE.
Ejemplo 28: Prueba de la actividad fungicida de los compuestos de la invención
Los compuestos se cribaron en placas de 96 pocillos con 10 compuestos por placa. Cada compuesto se seleccionó usando agar enmendado a 20, 2, 0.2 y 0.02 ppm del material de prueba. Se usaron prolina a 50 y 10 ppm y DMSO al 0.2 % respectivamente como controles positivo y negativo. Cada concentración de prueba y estándar se probaron dos veces en una placa.
Los compuestos se examinaron frente a los siguientes tres patógenos fúngicos: Botrytis cinerea, Alternaría. alternata y Zymoseptoria tritici. El agar usado en la prueba varió dependiendo del patógeno con el medio N usado para B. cinerea y A. alternata y agar patata dextrosa al 1 % para Z. tritici. Para cada patógeno se agregaron suficientes esporas al agar apropiado para dar 1,000 esporas/mL de agar de A. alternata, 5,000 esporas/mL de agar de B. cinerea y 10,000 esporas/mL de agar de Z. tritici.
Se produjo una solución madre x10 en DMSO al 2 % para cada dosis, es decir, 200, 20, 2 y 0.2 ppm, y se agregaron 10 |jl de esta a los pocillos adecuados de la placa. Se agregó una cantidad equivalente de DMSo al 2 % y solución madre de prolina a 500 y 100 ppm para los controles. A cada pocillo se le agregaron 90 j l de la suspensión de esporas de agar adecuada para dar las concentraciones de pocillo finales descritas en el primer párrafo.
Las placas se incubaron a temperatura ambiente (18 °C) y se evaluaron después
a) 3 a 4 días A. alternata y B. cinerea
b) 7 días para Z. tritici
La cantidad de crecimiento fúngico en cada pocillo se comparó con los controles de DMSO y se calificó según la siguiente clave
0 - sin crecimiento (100 % de control)
1 - crecimiento reducido en un 75 % en comparación con el control DMSO (25 % de crecimiento)
2 - crecimiento reducido en un 50 % en comparación con el control DMSO (50 % de crecimiento)
3 - crecimiento reducido en un 25 % en comparación con el crecimiento del control DMSO (75 % de crecimiento) 4 - ninguna reducción en el crecimiento en comparación con el crecimiento de control de DMSO (100 % de crecimiento) A continuación, se usaron esos números para dar una EC50. La clasificación en la tabla es:
A) EC50<20 ppm, B) EC50>20ppm
Claims (16)
1. Un compuesto de fórmula I, o una sal o N-óxido agronómicamente aceptable del mismo:
Y1 se selecciona de CH y N;
Z1, Z2 y Z3 se seleccionan cada uno independientemente de N y CR6; en la que al menos uno de Z1, Z2 y Z3 es CR6;
R1 y R10 se seleccionan cada uno independientemente en cada ocurrencia de: alquilo C1-C6, haloalquilo C1-C6, cicloalquilo C3-C6, halo, nitro, OR7, SR8, OS(O)2R8, S(O)2R8, C(O)OR8, C(O)NR8R8, C(O)R8, S(O)2NR8R8, S(O)(NR8)R8, S(O)R8, ciano, alquenilo C2-C6, alquinilo C2-C6 y NR8R9;
R2 y R6 se seleccionan cada uno independientemente en cada ocurrencia de H, halo, nitro, ciano, alquilo C1-C6, cicloalquilo C3-C6 y haloalquilo C1-C6;
R3, R4a, R4b, R5a y R5b se seleccionan independientemente en cada ocurrencia de H, alquilo C1-C6, haloalquilo C1-C6, cicloalquilo C3-C6, halo, nitro, OR7, SR8, OS(O)2R8, S(O)2R8, C(O)OR8, C(O)NR8R8, C(O)R8, S(O)2NR8R8, S(O)(NR8)R8, S(O)R8, ciano, alquenilo C2-C6, alquinilo C2-C6 y NR8R9; o en la que R4b y R5b junto con los átomos de carbono a los que están unidos forman un anillo seleccionado de: fenilo, heteroarilo de 5 o 6 miembros, anillo de heterocicloalquilo de 5, 6 o 7 miembros y cicloalquilo C5-C7; estando dicho anillo de heteroarilo o fenilo opcionalmente sustituido con desde 1 a 4 grupos R10 o estando dicho anillo heterocicloalquilo o cicloalquilo opcionalmente sustituido con desde 1 a 4 grupos R11;
con la condición de que ya sea al menos uno de R4a y R4b se seleccione de alquilo C1-C6, haloalquilo C1-C6, halo, nitro,
O-alquilo C1-C6, SR8, OS(O)2R8, S(O)2R8, S(O)2NR8R8, S(O)(NR8)R8, S(O)R8, ciano, alquenilo C2-C6, alquinilo C2-C NR8R9; o R4b y R5b juntos forman un anillo;
R7 se selecciona independientemente en cada ocurrencia de: H, alquilo C1-C6, alquenilo C3-C6, alquinilo C3-C6, cicloalquilo C3-C6 y haloalquilo C1-C6;
R8 se selecciona independientemente en cada ocurrencia de: H, cicloalquilo C3-C6 y alquilo C1-C6; o en el que dos grupos R8 están unidos al mismo átomo de nitrógeno, dichos grupos R8, junto con dicho átomo de nitrógeno forman un anillo heterocicloalquilo de 4, 5, 6 o 7 miembros;
R9 se selecciona independientemente en cada ocurrencia de; H, alquilo C1-C6, C(O)-alquilo C1-C6 y S(O)2-alquilo C1-C6; o donde un grupo R8 y un grupo R9 están unidos al mismo átomo de nitrógeno, dichos grupos R8 y R9, junto con dicho átomo de nitrógeno forman un anillo heterocicloalquilo de 4, 5, 6 o 7 miembros;
R11 se selecciona independientemente en cada ocurrencia de: =O, =S, alquilo C1-C6, haloalquilo C1-C6, halo, nitro, OR8, SR8, OS(O)2R8, S(O)2R8, S(O)2NR8R8, S(O)(NR8)R8, S(O)R8, ciano, alquenilo C2-C6, alquinilo C2-C6 y NR8R x es un número entero desde 0 a 4; en la que para cualquier grupo R1, R2, R3, R4a, R4b, R5a, R5b, R6, R7, R8, R9, R10, o
R11 que es alquilo, alquenilo, cicloalquilo, heterocicloalquilo (incluso cuando dos grupos R8 o un grupo R8 y un grupo
R9 junto con un nitrógeno al que están unidos forman un anillo heterocicloalquilo), alquinilo, C(O)-alquilo o S(O)2-alquilo está opcionalmente sustituido, cuando sea químicamente posible, con 1 a 4 sustituyentes, cada uno de los cuales se selecciona independientemente en cada ocurrencia del grupo que consiste en: =O; =NRa, =NORa, alquilo
C1-C4, halo, nitro, ciano, haloalquilo C1-C4, alquenilo C2-C4, alquinilo C2-C4, NRaRb, S(O)2Ra, S(O)Ra, S(O)(NRa)Ra, S(O)2NRaRa, CO2Ra, C(O)Ra, CONRaRa y ORa;
en la que Ra se selecciona independientemente de H y alquilo C1-C4; y Rb es independientemente H, alquilo C1-C4, C(O)-alquilo C1-C4, S(O)2-alquilo C1-C4.
2. Un compuesto de la reivindicación 1, en el que Y1 es CH o Y1 es N.
3. Un compuesto de una cualquiera de las reivindicaciones 1 a 2, en el que Z2 es CR6.
4. Un compuesto de una cualquiera de las reivindicaciones 1 a 3, en el que: (a) Z1 y Z3 son cada uno N; (b) Z1 es CR6 y Z3 es N; (c) Z3 es CR6 y Z1 es N; o (d) Z1 y Z3 son cada uno CR6.
5. Un compuesto de una cualquiera de las reivindicaciones 1 a 4, en el que x es un número entero seleccionado de 1 y 2 y R1 se selecciona independientemente en cada ocurrencia de alquilo C1-C4, haloalquilo C1-C4, halo, nitro, OR7y ciano.
6. Un compuesto de una cualquiera de las reivindicaciones 1 a 5, en el que R2 se selecciona independientemente de alquilo C1-C2 y haloalquilo C1-C2.
7. Un compuesto de una cualquiera de las reivindicaciones 1 a 6, en el que R4a se selecciona independientemente de halo, alquilo C1-C4, haloalquilo C1-C4, O-alquilo C1-C4 y O-haloalquilo C1-C4.
8. Un compuesto de una cualquiera de las reivindicaciones 1 a 7, en el que R4b se selecciona independientemente de halo, alquilo C1-C4, haloalquilo C1-C4, O-alquilo C1-C4 y O-haloalquilo C1-C4.
9. Un compuesto de una cualquiera de las reivindicaciones 1 a 8, en el que ni R4a ni R4b son H.
10. Un compuesto de una cualquiera de las reivindicaciones 1 a 7, en el que R4b es H.
11. Un compuesto de una cualquiera de las reivindicaciones 1 a 10, en el que R5a es H y/o R5b es H.
12. Un compuesto de una cualquiera de las reivindicaciones 1 a 11, en el que R3 se selecciona independientemente de halo, alquilo C1-C4, haloalquilo C1-C4, O-alquilo C1-C4 y O-haloalquilo C1-C4.
14. Un método de control de enfermedades fúngicas, comprendiendo el método aplicar una cantidad agronómicamente eficaz y sustancialmente no fitotóxica de un compuesto de una cualquiera de las reivindicaciones 1 a 13 a semillas de plantas, a las propias plantas o a un área donde se pretende que las plantas crezcan.
15. Un uso de un compuesto de una cualquiera de las reivindicaciones 1 a 13 para controlar enfermedades fúngicas de las plantas.
16. Una composición fungicida que comprende una cantidad eficaz y no fitotóxica de un compuesto activo de una cualquiera de las reivindicaciones 1 a 13.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB1800688.2A GB201800688D0 (en) | 2018-01-16 | 2018-01-16 | Agricultural chemicals |
| PCT/GB2019/050097 WO2019141972A1 (en) | 2018-01-16 | 2019-01-15 | Agricultural chemicals |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2906222T3 true ES2906222T3 (es) | 2022-04-13 |
Family
ID=61256257
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES19701697T Active ES2906222T3 (es) | 2018-01-16 | 2019-01-15 | Productos químicos agrícolas |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US11440900B2 (es) |
| EP (1) | EP3740474B1 (es) |
| CN (1) | CN111601796A (es) |
| BR (1) | BR112020014319A2 (es) |
| DK (1) | DK3740474T3 (es) |
| ES (1) | ES2906222T3 (es) |
| GB (1) | GB201800688D0 (es) |
| WO (1) | WO2019141972A1 (es) |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20050038041A1 (en) | 2003-08-15 | 2005-02-17 | Yuki Nakagawa | Fungicidal pyrimidine derivatives |
| WO2009000413A1 (en) | 2007-06-26 | 2008-12-31 | Sanofi-Aventis | A regioselective copper catalyzed synthesis of benzimidazoles and azabenzimidazoles |
-
2018
- 2018-01-16 GB GBGB1800688.2A patent/GB201800688D0/en not_active Ceased
-
2019
- 2019-01-15 US US16/962,184 patent/US11440900B2/en active Active
- 2019-01-15 EP EP19701697.5A patent/EP3740474B1/en not_active Not-in-force
- 2019-01-15 WO PCT/GB2019/050097 patent/WO2019141972A1/en not_active Ceased
- 2019-01-15 BR BR112020014319-7A patent/BR112020014319A2/pt not_active Application Discontinuation
- 2019-01-15 DK DK19701697.5T patent/DK3740474T3/da active
- 2019-01-15 ES ES19701697T patent/ES2906222T3/es active Active
- 2019-01-15 CN CN201980008704.4A patent/CN111601796A/zh active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| BR112020014319A2 (pt) | 2020-12-08 |
| CN111601796A (zh) | 2020-08-28 |
| US20200339543A1 (en) | 2020-10-29 |
| EP3740474B1 (en) | 2022-01-05 |
| GB201800688D0 (en) | 2018-02-28 |
| US11440900B2 (en) | 2022-09-13 |
| DK3740474T3 (da) | 2022-02-14 |
| EP3740474A1 (en) | 2020-11-25 |
| WO2019141972A1 (en) | 2019-07-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2019141980A1 (en) | Agricultural chemicals | |
| WO2017178819A1 (en) | Agricultural chemicals | |
| WO2016055802A1 (en) | Agricultural chemicals | |
| ES2987449T3 (es) | Derivados de picolinamida útiles como fungicidas agrícolas | |
| WO2019020981A1 (en) | PYRAZOLE, ISOTHIAZOLE AND ISOXAZOLE DERIVATIVES USEFUL AS AGRICULTURAL FUNGICIDES | |
| ES3037308T3 (en) | Pyrido[2,3-e]oxazine derivatives as agricultural chemicals | |
| AU2014322853B2 (en) | Agricultural chemicals | |
| AU2017388277A1 (en) | Agricultural chemicals | |
| ES2906222T3 (es) | Productos químicos agrícolas | |
| WO2015040352A1 (en) | Agricultural chemicals | |
| WO2016055801A2 (en) | Agricultural chemicals | |
| RU2826642C2 (ru) | Производные пиколинамида, пригодные в качестве сельскохозяйственных фунгицидов | |
| EA047275B1 (ru) | ПИРИДО[2,3-е]ОКСАЗИНОВЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ХИМИЧЕСКИХ ВЕЩЕСТВ | |
| GB2587787A (en) | Agricultural chemicals |