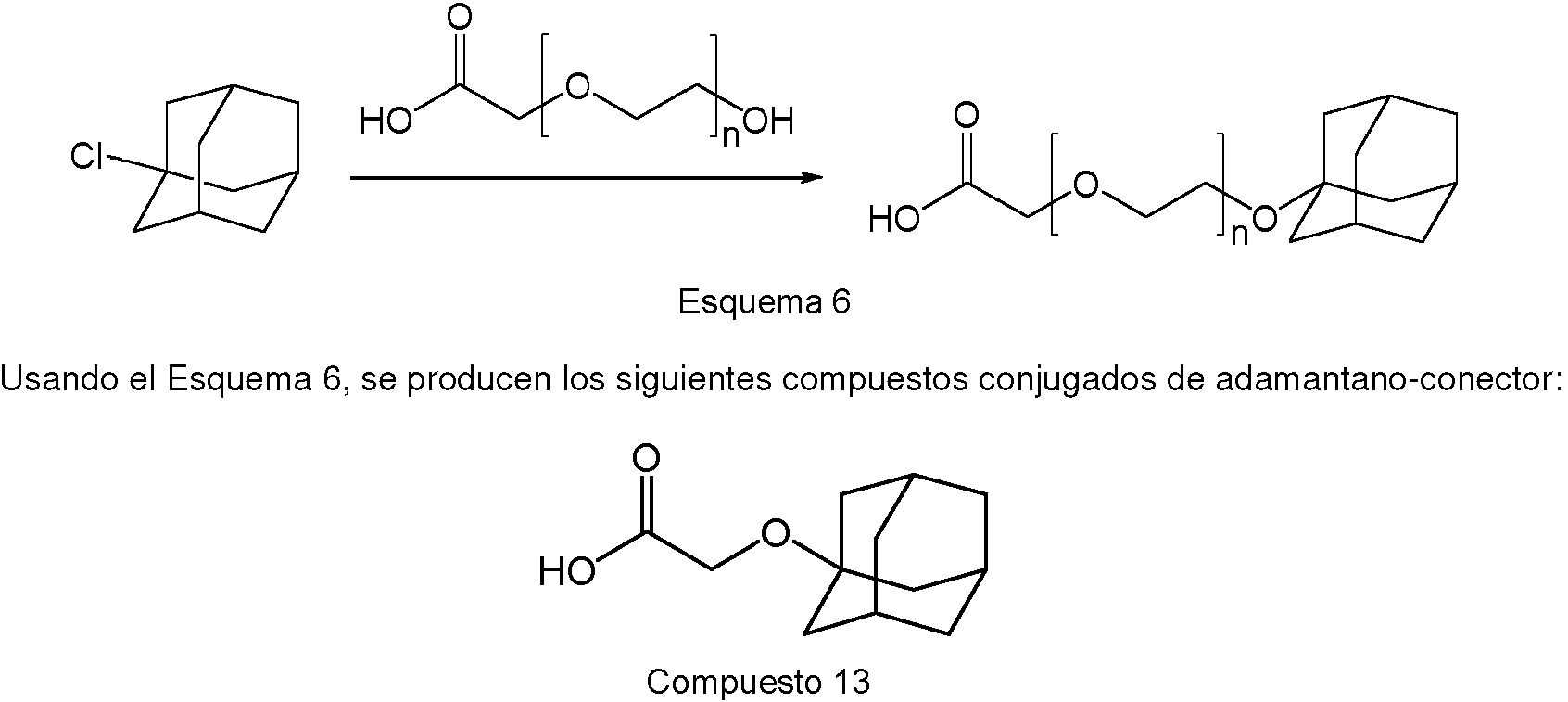
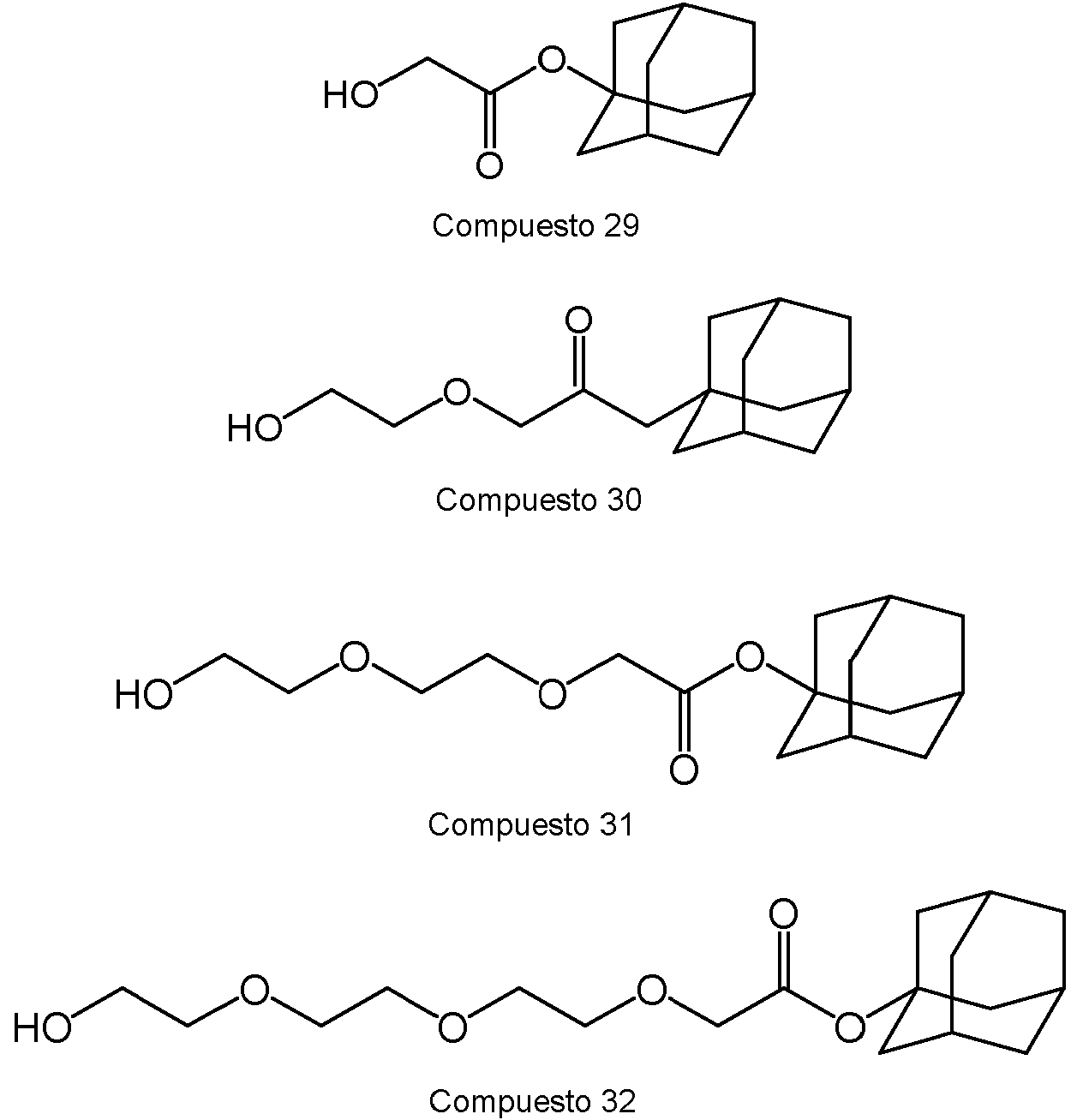
ES2910976T3 - Eliminadores de receptores de andrógenos tripartitos, métodos y usos de los mismos - Google Patents
Eliminadores de receptores de andrógenos tripartitos, métodos y usos de los mismos Download PDFInfo
- Publication number
- ES2910976T3 ES2910976T3 ES18794821T ES18794821T ES2910976T3 ES 2910976 T3 ES2910976 T3 ES 2910976T3 ES 18794821 T ES18794821 T ES 18794821T ES 18794821 T ES18794821 T ES 18794821T ES 2910976 T3 ES2910976 T3 ES 2910976T3
- Authority
- ES
- Spain
- Prior art keywords
- day
- hair
- disclosed
- aspects
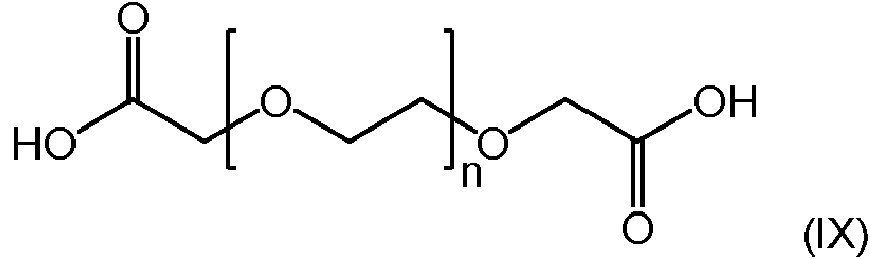
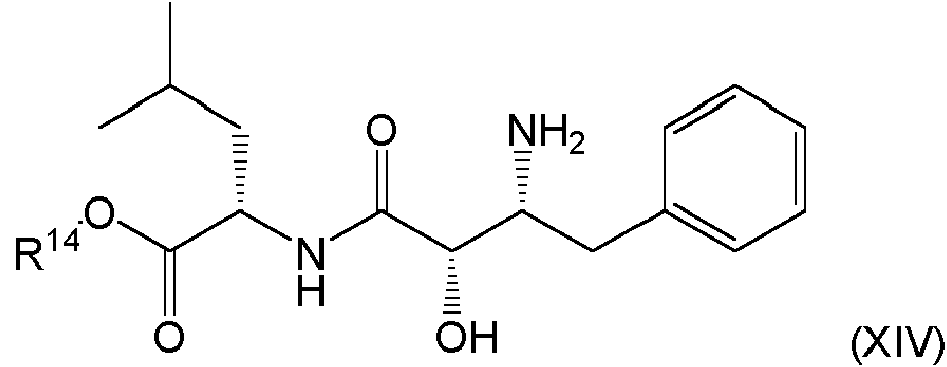
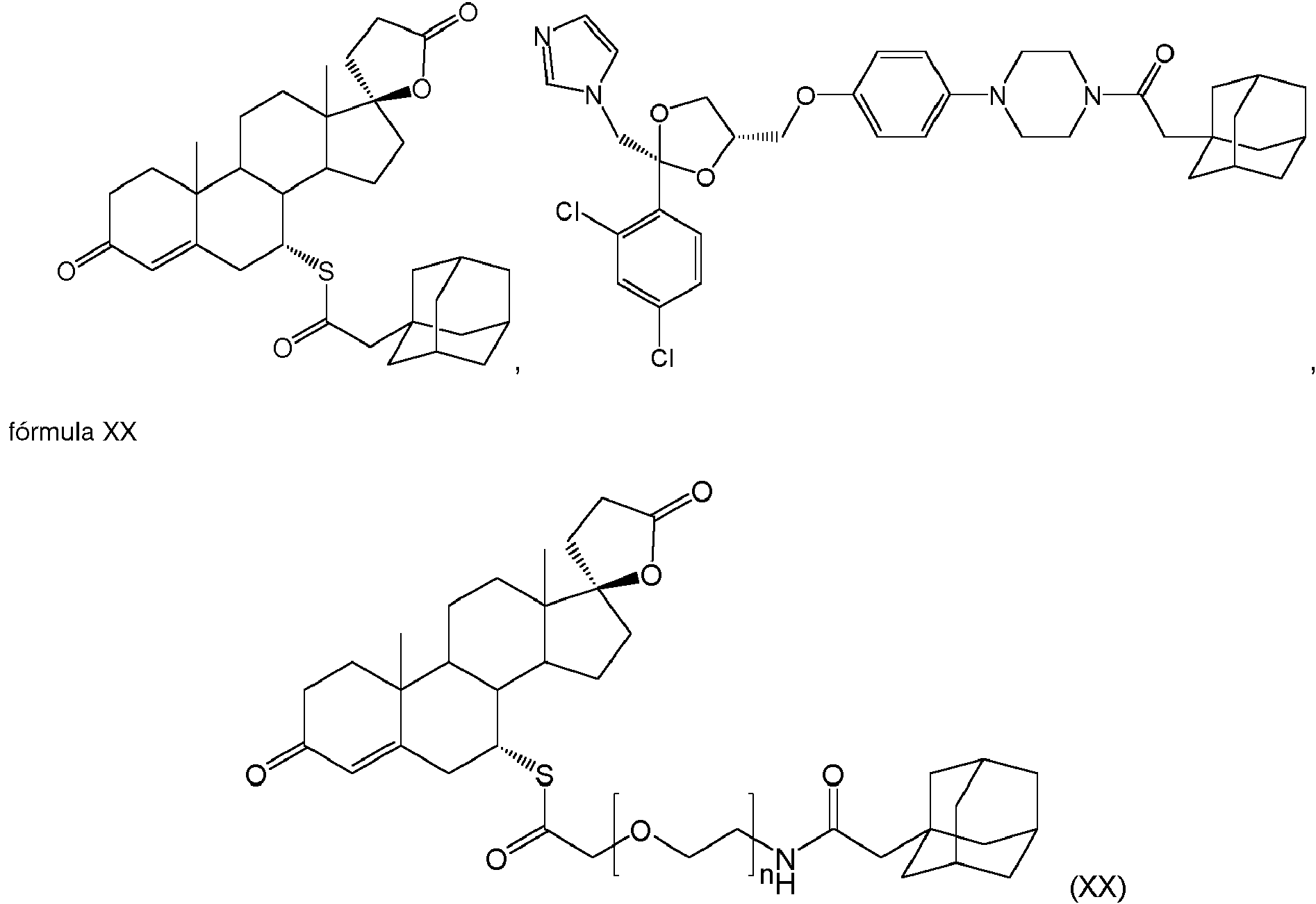
- formula
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 108010080146 androgen receptors Proteins 0.000 title description 136
- 238000000034 method Methods 0.000 title description 24
- 102000001307 androgen receptors Human genes 0.000 title description 4
- 150000001875 compounds Chemical class 0.000 claims abstract description 95
- 210000004209 hair Anatomy 0.000 claims description 131
- 201000004384 Alopecia Diseases 0.000 claims description 121
- 210000003780 hair follicle Anatomy 0.000 claims description 88
- 239000008194 pharmaceutical composition Substances 0.000 claims description 68
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 62
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 54
- 230000003676 hair loss Effects 0.000 claims description 36
- 238000011282 treatment Methods 0.000 claims description 35
- 208000024963 hair loss Diseases 0.000 claims description 24
- 206010000496 acne Diseases 0.000 claims description 22
- 208000002874 Acne Vulgaris Diseases 0.000 claims description 21
- XXJWXESWEXIICW-UHFFFAOYSA-N diethylene glycol monoethyl ether Chemical compound CCOCCOCCO XXJWXESWEXIICW-UHFFFAOYSA-N 0.000 claims description 19
- 238000004519 manufacturing process Methods 0.000 claims description 18
- 230000003412 degenerative effect Effects 0.000 claims description 17
- HIQIXEFWDLTDED-UHFFFAOYSA-N 4-hydroxy-1-piperidin-4-ylpyrrolidin-2-one Chemical compound O=C1CC(O)CN1C1CCNCC1 HIQIXEFWDLTDED-UHFFFAOYSA-N 0.000 claims description 16
- 210000002374 sebum Anatomy 0.000 claims description 15
- 239000011928 denatured alcohol Substances 0.000 claims description 13
- 239000003937 drug carrier Substances 0.000 claims description 12
- 201000002996 androgenic alopecia Diseases 0.000 claims description 11
- 230000037308 hair color Effects 0.000 claims description 10
- 206010020112 Hirsutism Diseases 0.000 claims description 4
- 208000027418 Wounds and injury Diseases 0.000 claims description 4
- 230000036573 scar formation Effects 0.000 claims description 4
- 206010052428 Wound Diseases 0.000 claims description 3
- 230000001815 facial effect Effects 0.000 claims description 3
- 230000005808 skin problem Effects 0.000 claims description 3
- 102100032187 Androgen receptor Human genes 0.000 description 133
- 239000000203 mixture Substances 0.000 description 114
- 230000001965 increasing effect Effects 0.000 description 82
- 210000003491 skin Anatomy 0.000 description 74
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 63
- 210000004027 cell Anatomy 0.000 description 60
- 231100000360 alopecia Toxicity 0.000 description 53
- 210000004919 hair shaft Anatomy 0.000 description 49
- ORILYTVJVMAKLC-UHFFFAOYSA-N adamantane Chemical group C1C(C2)CC3CC1CC2C3 ORILYTVJVMAKLC-UHFFFAOYSA-N 0.000 description 47
- 125000000896 monocarboxylic acid group Chemical group 0.000 description 45
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 39
- 238000006243 chemical reaction Methods 0.000 description 39
- 230000000694 effects Effects 0.000 description 38
- 229910052736 halogen Inorganic materials 0.000 description 37
- 150000002367 halogens Chemical class 0.000 description 37
- 230000009467 reduction Effects 0.000 description 33
- 208000035475 disorder Diseases 0.000 description 32
- 108700008625 Reporter Genes Proteins 0.000 description 29
- MUMGGOZAMZWBJJ-DYKIIFRCSA-N Testostosterone Chemical compound O=C1CC[C@]2(C)[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 MUMGGOZAMZWBJJ-DYKIIFRCSA-N 0.000 description 28
- 229940123407 Androgen receptor antagonist Drugs 0.000 description 27
- 239000002243 precursor Substances 0.000 description 26
- 230000003698 anagen phase Effects 0.000 description 25
- 238000009472 formulation Methods 0.000 description 25
- 230000005764 inhibitory process Effects 0.000 description 23
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 22
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 21
- 230000003779 hair growth Effects 0.000 description 20
- 239000002609 medium Substances 0.000 description 20
- 229960002256 spironolactone Drugs 0.000 description 20
- 201000010099 disease Diseases 0.000 description 19
- LXMSZDCAJNLERA-ZHYRCANASA-N spironolactone Chemical compound C([C@@H]1[C@]2(C)CC[C@@H]3[C@@]4(C)CCC(=O)C=C4C[C@H]([C@@H]13)SC(=O)C)C[C@@]21CCC(=O)O1 LXMSZDCAJNLERA-ZHYRCANASA-N 0.000 description 19
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 18
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 18
- 238000007792 addition Methods 0.000 description 18
- 230000003797 telogen phase Effects 0.000 description 18
- 210000001519 tissue Anatomy 0.000 description 17
- -1 Boc-protected amino Chemical group 0.000 description 16
- 238000003556 assay Methods 0.000 description 16
- XMAYWYJOQHXEEK-OZXSUGGESA-N (2R,4S)-ketoconazole Chemical compound C1CN(C(=O)C)CCN1C(C=C1)=CC=C1OC[C@@H]1O[C@@](CN2C=NC=C2)(C=2C(=CC(Cl)=CC=2)Cl)OC1 XMAYWYJOQHXEEK-OZXSUGGESA-N 0.000 description 15
- 239000012267 brine Substances 0.000 description 15
- 229960004125 ketoconazole Drugs 0.000 description 15
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 15
- 229910052801 chlorine Inorganic materials 0.000 description 14
- 239000000460 chlorine Substances 0.000 description 14
- 230000001404 mediated effect Effects 0.000 description 14
- 230000011664 signaling Effects 0.000 description 14
- 229960003604 testosterone Drugs 0.000 description 14
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 description 13
- 125000003601 C2-C6 alkynyl group Chemical group 0.000 description 13
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 13
- 229910052794 bromium Inorganic materials 0.000 description 13
- 229910052731 fluorine Inorganic materials 0.000 description 13
- 210000002510 keratinocyte Anatomy 0.000 description 13
- 125000005543 phthalimide group Chemical group 0.000 description 13
- 230000007704 transition Effects 0.000 description 13
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 12
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 12
- 239000003098 androgen Substances 0.000 description 12
- 230000002500 effect on skin Effects 0.000 description 12
- 238000002474 experimental method Methods 0.000 description 12
- 230000002209 hydrophobic effect Effects 0.000 description 12
- 239000011159 matrix material Substances 0.000 description 12
- NGNBDVOYPDDBFK-UHFFFAOYSA-N 2-[2,4-di(pentan-2-yl)phenoxy]acetyl chloride Chemical compound CCCC(C)C1=CC=C(OCC(Cl)=O)C(C(C)CCC)=C1 NGNBDVOYPDDBFK-UHFFFAOYSA-N 0.000 description 11
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 11
- 239000003814 drug Substances 0.000 description 11
- 229910052938 sodium sulfate Inorganic materials 0.000 description 11
- 235000011152 sodium sulphate Nutrition 0.000 description 11
- 239000000243 solution Substances 0.000 description 11
- 102000006275 Ubiquitin-Protein Ligases Human genes 0.000 description 10
- 108010083111 Ubiquitin-Protein Ligases Proteins 0.000 description 10
- 125000000304 alkynyl group Chemical group 0.000 description 10
- 230000027455 binding Effects 0.000 description 10
- 229940079593 drug Drugs 0.000 description 10
- 210000002615 epidermis Anatomy 0.000 description 10
- 229920001184 polypeptide Polymers 0.000 description 10
- 238000002360 preparation method Methods 0.000 description 10
- 102000004196 processed proteins & peptides Human genes 0.000 description 10
- 108090000765 processed proteins & peptides Proteins 0.000 description 10
- 230000002829 reductive effect Effects 0.000 description 10
- 230000037390 scarring Effects 0.000 description 10
- 125000000008 (C1-C10) alkyl group Chemical group 0.000 description 9
- 206010068168 androgenetic alopecia Diseases 0.000 description 9
- 230000015556 catabolic process Effects 0.000 description 9
- 230000003778 catagen phase Effects 0.000 description 9
- 238000006731 degradation reaction Methods 0.000 description 9
- 239000000499 gel Substances 0.000 description 9
- 238000005259 measurement Methods 0.000 description 9
- 230000035515 penetration Effects 0.000 description 9
- 210000004761 scalp Anatomy 0.000 description 9
- 239000002904 solvent Substances 0.000 description 9
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 9
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 8
- VGGGPCQERPFHOB-MCIONIFRSA-N Bestatin Chemical group CC(C)C[C@H](C(O)=O)NC(=O)[C@@H](O)[C@H](N)CC1=CC=CC=C1 VGGGPCQERPFHOB-MCIONIFRSA-N 0.000 description 8
- 125000006374 C2-C10 alkenyl group Chemical group 0.000 description 8
- 208000012641 Pigmentation disease Diseases 0.000 description 8
- 239000003153 chemical reaction reagent Substances 0.000 description 8
- 210000004207 dermis Anatomy 0.000 description 8
- 230000012010 growth Effects 0.000 description 8
- 230000019612 pigmentation Effects 0.000 description 8
- 102200025788 rs179363875 Human genes 0.000 description 8
- 102200001405 rs377584435 Human genes 0.000 description 8
- 102220087975 rs777340009 Human genes 0.000 description 8
- 102220094037 rs864622206 Human genes 0.000 description 8
- 239000000126 substance Substances 0.000 description 8
- 229910052789 astatine Inorganic materials 0.000 description 7
- 239000003795 chemical substances by application Substances 0.000 description 7
- 231100000673 dose–response relationship Toxicity 0.000 description 7
- 230000002401 inhibitory effect Effects 0.000 description 7
- 108090000623 proteins and genes Proteins 0.000 description 7
- 125000006656 (C2-C4) alkenyl group Chemical group 0.000 description 6
- 241001465754 Metazoa Species 0.000 description 6
- 241000699666 Mus <mouse, genus> Species 0.000 description 6
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 6
- 229910003204 NH2 Inorganic materials 0.000 description 6
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical class [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 6
- 239000000556 agonist Substances 0.000 description 6
- 235000001014 amino acid Nutrition 0.000 description 6
- 229940024606 amino acid Drugs 0.000 description 6
- 229940030486 androgens Drugs 0.000 description 6
- 239000005557 antagonist Substances 0.000 description 6
- 230000006907 apoptotic process Effects 0.000 description 6
- 239000002585 base Substances 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 6
- 230000002708 enhancing effect Effects 0.000 description 6
- 239000003446 ligand Substances 0.000 description 6
- 230000002441 reversible effect Effects 0.000 description 6
- 235000002639 sodium chloride Nutrition 0.000 description 6
- 239000007787 solid Substances 0.000 description 6
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 6
- 125000006650 (C2-C4) alkynyl group Chemical group 0.000 description 5
- 206010016936 Folliculitis Diseases 0.000 description 5
- 108700028146 Genetic Enhancer Elements Proteins 0.000 description 5
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 5
- 108090000848 Ubiquitin Proteins 0.000 description 5
- 102000044159 Ubiquitin Human genes 0.000 description 5
- 239000003936 androgen receptor antagonist Substances 0.000 description 5
- 210000000805 cytoplasm Anatomy 0.000 description 5
- 238000012217 deletion Methods 0.000 description 5
- 230000037430 deletion Effects 0.000 description 5
- 210000004709 eyebrow Anatomy 0.000 description 5
- 210000004907 gland Anatomy 0.000 description 5
- 230000003648 hair appearance Effects 0.000 description 5
- 230000003803 hair density Effects 0.000 description 5
- 238000001727 in vivo Methods 0.000 description 5
- 210000002752 melanocyte Anatomy 0.000 description 5
- 230000004048 modification Effects 0.000 description 5
- 238000012986 modification Methods 0.000 description 5
- 210000003205 muscle Anatomy 0.000 description 5
- 230000008569 process Effects 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 235000018102 proteins Nutrition 0.000 description 5
- 102000004169 proteins and genes Human genes 0.000 description 5
- 150000003839 salts Chemical class 0.000 description 5
- 238000012360 testing method Methods 0.000 description 5
- 230000003813 thin hair Effects 0.000 description 5
- KLDLRDSRCMJKGM-UHFFFAOYSA-N 3-[chloro-(2-oxo-1,3-oxazolidin-3-yl)phosphoryl]-1,3-oxazolidin-2-one Chemical compound C1COC(=O)N1P(=O)(Cl)N1CCOC1=O KLDLRDSRCMJKGM-UHFFFAOYSA-N 0.000 description 4
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 4
- 208000006926 Discoid Lupus Erythematosus Diseases 0.000 description 4
- 108010076876 Keratins Proteins 0.000 description 4
- 102000011782 Keratins Human genes 0.000 description 4
- XUMBMVFBXHLACL-UHFFFAOYSA-N Melanin Chemical compound O=C1C(=O)C(C2=CNC3=C(C(C(=O)C4=C32)=O)C)=C2C4=CNC2=C1C XUMBMVFBXHLACL-UHFFFAOYSA-N 0.000 description 4
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 4
- 102000004245 Proteasome Endopeptidase Complex Human genes 0.000 description 4
- 108090000708 Proteasome Endopeptidase Complex Proteins 0.000 description 4
- 239000000872 buffer Substances 0.000 description 4
- 238000004587 chromatography analysis Methods 0.000 description 4
- 208000004921 cutaneous lupus erythematosus Diseases 0.000 description 4
- UWFYSQMTEOIJJG-FDTZYFLXSA-N cyproterone acetate Chemical compound C1=C(Cl)C2=CC(=O)[C@@H]3C[C@@H]3[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(C)=O)(OC(=O)C)[C@@]1(C)CC2 UWFYSQMTEOIJJG-FDTZYFLXSA-N 0.000 description 4
- 229960000978 cyproterone acetate Drugs 0.000 description 4
- 230000006378 damage Effects 0.000 description 4
- 230000003325 follicular Effects 0.000 description 4
- 230000006870 function Effects 0.000 description 4
- 230000031774 hair cycle Effects 0.000 description 4
- 230000003646 hair health Effects 0.000 description 4
- BXWNKGSJHAJOGX-UHFFFAOYSA-N hexadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCO BXWNKGSJHAJOGX-UHFFFAOYSA-N 0.000 description 4
- 238000013537 high throughput screening Methods 0.000 description 4
- 108020001756 ligand binding domains Proteins 0.000 description 4
- 230000000670 limiting effect Effects 0.000 description 4
- 238000003670 luciferase enzyme activity assay Methods 0.000 description 4
- RJMUSRYZPJIFPJ-UHFFFAOYSA-N niclosamide Chemical compound OC1=CC=C(Cl)C=C1C(=O)NC1=CC=C([N+]([O-])=O)C=C1Cl RJMUSRYZPJIFPJ-UHFFFAOYSA-N 0.000 description 4
- 229960001920 niclosamide Drugs 0.000 description 4
- CTSLXHKWHWQRSH-UHFFFAOYSA-N oxalyl chloride Chemical compound ClC(=O)C(Cl)=O CTSLXHKWHWQRSH-UHFFFAOYSA-N 0.000 description 4
- 230000037361 pathway Effects 0.000 description 4
- 239000002953 phosphate buffered saline Substances 0.000 description 4
- 210000004918 root sheath Anatomy 0.000 description 4
- 239000000523 sample Substances 0.000 description 4
- 210000001732 sebaceous gland Anatomy 0.000 description 4
- 230000004936 stimulating effect Effects 0.000 description 4
- 239000011550 stock solution Substances 0.000 description 4
- 208000024891 symptom Diseases 0.000 description 4
- 208000011580 syndromic disease Diseases 0.000 description 4
- 230000000699 topical effect Effects 0.000 description 4
- 230000002103 transcriptional effect Effects 0.000 description 4
- IUSARDYWEPUTPN-OZBXUNDUSA-N (2r)-n-[(2s,3r)-4-[[(4s)-6-(2,2-dimethylpropyl)spiro[3,4-dihydropyrano[2,3-b]pyridine-2,1'-cyclobutane]-4-yl]amino]-3-hydroxy-1-[3-(1,3-thiazol-2-yl)phenyl]butan-2-yl]-2-methoxypropanamide Chemical compound C([C@H](NC(=O)[C@@H](C)OC)[C@H](O)CN[C@@H]1C2=CC(CC(C)(C)C)=CN=C2OC2(CCC2)C1)C(C=1)=CC=CC=1C1=NC=CS1 IUSARDYWEPUTPN-OZBXUNDUSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- 239000004215 Carbon black (E152) Substances 0.000 description 3
- 206010007882 Cellulitis Diseases 0.000 description 3
- 108020004414 DNA Proteins 0.000 description 3
- 208000003024 Diffuse alopecia Diseases 0.000 description 3
- 238000002965 ELISA Methods 0.000 description 3
- 208000003794 Follicular Mucinosis Diseases 0.000 description 3
- 206010021143 Hypoxia Diseases 0.000 description 3
- 208000011738 Lichen planopilaris Diseases 0.000 description 3
- 206010028980 Neoplasm Diseases 0.000 description 3
- 229930182555 Penicillin Natural products 0.000 description 3
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 3
- 206010036049 Polycystic ovaries Diseases 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 102000040945 Transcription factor Human genes 0.000 description 3
- 108091023040 Transcription factor Proteins 0.000 description 3
- 238000010521 absorption reaction Methods 0.000 description 3
- 208000010640 alopecia mucinosa Diseases 0.000 description 3
- 150000001413 amino acids Chemical class 0.000 description 3
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 3
- 230000003833 cell viability Effects 0.000 description 3
- 229940125807 compound 37 Drugs 0.000 description 3
- 230000008602 contraction Effects 0.000 description 3
- 125000004122 cyclic group Chemical group 0.000 description 3
- 231100000433 cytotoxic Toxicity 0.000 description 3
- 230000001472 cytotoxic effect Effects 0.000 description 3
- 230000003247 decreasing effect Effects 0.000 description 3
- 230000001419 dependent effect Effects 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 230000018109 developmental process Effects 0.000 description 3
- 210000000720 eyelash Anatomy 0.000 description 3
- 239000006260 foam Substances 0.000 description 3
- 125000000524 functional group Chemical group 0.000 description 3
- 230000014509 gene expression Effects 0.000 description 3
- 230000036541 health Effects 0.000 description 3
- 229940088597 hormone Drugs 0.000 description 3
- 239000005556 hormone Substances 0.000 description 3
- 229930195733 hydrocarbon Natural products 0.000 description 3
- 150000002430 hydrocarbons Chemical class 0.000 description 3
- 230000000977 initiatory effect Effects 0.000 description 3
- 210000001208 inner root sheath cell Anatomy 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- 229910052740 iodine Inorganic materials 0.000 description 3
- 230000002427 irreversible effect Effects 0.000 description 3
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 3
- 201000011486 lichen planus Diseases 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 230000008099 melanin synthesis Effects 0.000 description 3
- 229940105132 myristate Drugs 0.000 description 3
- 239000002674 ointment Substances 0.000 description 3
- 229940049954 penicillin Drugs 0.000 description 3
- 201000010065 polycystic ovary syndrome Diseases 0.000 description 3
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 3
- 229920000053 polysorbate 80 Polymers 0.000 description 3
- 230000003389 potentiating effect Effects 0.000 description 3
- 239000002244 precipitate Substances 0.000 description 3
- 230000002028 premature Effects 0.000 description 3
- 239000003755 preservative agent Substances 0.000 description 3
- 102000005962 receptors Human genes 0.000 description 3
- 108020003175 receptors Proteins 0.000 description 3
- 229960005322 streptomycin Drugs 0.000 description 3
- 230000035882 stress Effects 0.000 description 3
- 238000003786 synthesis reaction Methods 0.000 description 3
- 230000008685 targeting Effects 0.000 description 3
- 201000001297 telogen effluvium Diseases 0.000 description 3
- TUNFSRHWOTWDNC-UHFFFAOYSA-N tetradecanoic acid Chemical compound CCCCCCCCCCCCCC(O)=O TUNFSRHWOTWDNC-UHFFFAOYSA-N 0.000 description 3
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 description 2
- UDQTXCHQKHIQMH-KYGLGHNPSA-N (3ar,5s,6s,7r,7ar)-5-(difluoromethyl)-2-(ethylamino)-5,6,7,7a-tetrahydro-3ah-pyrano[3,2-d][1,3]thiazole-6,7-diol Chemical compound S1C(NCC)=N[C@H]2[C@@H]1O[C@H](C(F)F)[C@@H](O)[C@@H]2O UDQTXCHQKHIQMH-KYGLGHNPSA-N 0.000 description 2
- NVKAWKQGWWIWPM-ABEVXSGRSA-N 17-β-hydroxy-5-α-Androstan-3-one Chemical compound C1C(=O)CC[C@]2(C)[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CC[C@H]21 NVKAWKQGWWIWPM-ABEVXSGRSA-N 0.000 description 2
- YCNCRLKXSLARFT-UHFFFAOYSA-N 2-hydroxy-2-methyl-n-[4-nitro-3-(trifluoromethyl)phenyl]-3-[(2,2,2-trifluoroacetyl)amino]propanamide Chemical compound FC(F)(F)C(=O)NCC(O)(C)C(=O)NC1=CC=C([N+]([O-])=O)C(C(F)(F)F)=C1 YCNCRLKXSLARFT-UHFFFAOYSA-N 0.000 description 2
- FJKROLUGYXJWQN-UHFFFAOYSA-N 4-hydroxybenzoic acid Chemical compound OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 2
- 208000005676 Adrenogenital syndrome Diseases 0.000 description 2
- 206010001765 Alopecia syphilitic Diseases 0.000 description 2
- 206010001766 Alopecia totalis Diseases 0.000 description 2
- 206010001767 Alopecia universalis Diseases 0.000 description 2
- 208000019901 Anxiety disease Diseases 0.000 description 2
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 description 2
- 206010006187 Breast cancer Diseases 0.000 description 2
- 208000026310 Breast neoplasm Diseases 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- 208000008448 Congenital adrenal hyperplasia Diseases 0.000 description 2
- 230000004568 DNA-binding Effects 0.000 description 2
- 241001635598 Enicostema Species 0.000 description 2
- 102100023600 Fibroblast growth factor receptor 2 Human genes 0.000 description 2
- 101710182389 Fibroblast growth factor receptor 2 Proteins 0.000 description 2
- 102100034051 Heat shock protein HSP 90-alpha Human genes 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- 206010022489 Insulin Resistance Diseases 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 2
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 2
- 108060001084 Luciferase Proteins 0.000 description 2
- 239000005089 Luciferase Substances 0.000 description 2
- 206010027626 Milia Diseases 0.000 description 2
- 101100236865 Mus musculus Mdm2 gene Proteins 0.000 description 2
- 241000699670 Mus sp. Species 0.000 description 2
- 239000004372 Polyvinyl alcohol Substances 0.000 description 2
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M Potassium chloride Chemical compound [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 description 2
- 229940124158 Protease/peptidase inhibitor Drugs 0.000 description 2
- 206010039792 Seborrhoea Diseases 0.000 description 2
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 2
- GLNADSQYFUSGOU-GPTZEZBUSA-J Trypan blue Chemical compound [Na+].[Na+].[Na+].[Na+].C1=C(S([O-])(=O)=O)C=C2C=C(S([O-])(=O)=O)C(/N=N/C3=CC=C(C=C3C)C=3C=C(C(=CC=3)\N=N\C=3C(=CC4=CC(=CC(N)=C4C=3O)S([O-])(=O)=O)S([O-])(=O)=O)C)=C(O)C2=C1N GLNADSQYFUSGOU-GPTZEZBUSA-J 0.000 description 2
- 210000001015 abdomen Anatomy 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- 239000004480 active ingredient Substances 0.000 description 2
- 230000002411 adverse Effects 0.000 description 2
- 230000032683 aging Effects 0.000 description 2
- 125000000217 alkyl group Chemical group 0.000 description 2
- 230000003281 allosteric effect Effects 0.000 description 2
- 208000004631 alopecia areata Diseases 0.000 description 2
- 208000032775 alopecia universalis congenita Diseases 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 239000003963 antioxidant agent Substances 0.000 description 2
- 230000036506 anxiety Effects 0.000 description 2
- 235000009582 asparagine Nutrition 0.000 description 2
- 229960001230 asparagine Drugs 0.000 description 2
- 230000036621 balding Effects 0.000 description 2
- 230000004888 barrier function Effects 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 229960000686 benzalkonium chloride Drugs 0.000 description 2
- CADWTSSKOVRVJC-UHFFFAOYSA-N benzyl(dimethyl)azanium;chloride Chemical compound [Cl-].C[NH+](C)CC1=CC=CC=C1 CADWTSSKOVRVJC-UHFFFAOYSA-N 0.000 description 2
- 230000033228 biological regulation Effects 0.000 description 2
- 210000000988 bone and bone Anatomy 0.000 description 2
- 239000004067 bulking agent Substances 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 201000011510 cancer Diseases 0.000 description 2
- 235000011089 carbon dioxide Nutrition 0.000 description 2
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 2
- 229960000541 cetyl alcohol Drugs 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- OSASVXMJTNOKOY-UHFFFAOYSA-N chlorobutanol Chemical compound CC(C)(O)C(Cl)(Cl)Cl OSASVXMJTNOKOY-UHFFFAOYSA-N 0.000 description 2
- 230000002860 competitive effect Effects 0.000 description 2
- 208000012482 complete androgen insensitivity syndrome Diseases 0.000 description 2
- 229940125936 compound 42 Drugs 0.000 description 2
- 230000003013 cytotoxicity Effects 0.000 description 2
- 231100000135 cytotoxicity Toxicity 0.000 description 2
- 230000034994 death Effects 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- FMGSKLZLMKYGDP-USOAJAOKSA-N dehydroepiandrosterone Chemical compound C1[C@@H](O)CC[C@]2(C)[C@H]3CC[C@](C)(C(CC4)=O)[C@@H]4[C@@H]3CC=C21 FMGSKLZLMKYGDP-USOAJAOKSA-N 0.000 description 2
- 230000008021 deposition Effects 0.000 description 2
- 238000009792 diffusion process Methods 0.000 description 2
- 238000007865 diluting Methods 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 239000012153 distilled water Substances 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 210000005175 epidermal keratinocyte Anatomy 0.000 description 2
- 210000005081 epithelial layer Anatomy 0.000 description 2
- 230000007717 exclusion Effects 0.000 description 2
- 210000000744 eyelid Anatomy 0.000 description 2
- 238000005562 fading Methods 0.000 description 2
- 208000015707 frontal fibrosing alopecia Diseases 0.000 description 2
- 230000002068 genetic effect Effects 0.000 description 2
- 235000011187 glycerol Nutrition 0.000 description 2
- YMAWOPBAYDPSLA-UHFFFAOYSA-N glycylglycine Chemical compound [NH3+]CC(=O)NCC([O-])=O YMAWOPBAYDPSLA-UHFFFAOYSA-N 0.000 description 2
- 230000003662 hair growth rate Effects 0.000 description 2
- 230000003659 hair regrowth Effects 0.000 description 2
- 230000003760 hair shine Effects 0.000 description 2
- 210000003128 head Anatomy 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 229920002674 hyaluronan Polymers 0.000 description 2
- 229960003160 hyaluronic acid Drugs 0.000 description 2
- 238000011065 in-situ storage Methods 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 230000016507 interphase Effects 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 2
- 230000003780 keratinization Effects 0.000 description 2
- 210000002414 leg Anatomy 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- 238000001294 liquid chromatography-tandem mass spectrometry Methods 0.000 description 2
- 230000033001 locomotion Effects 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- 238000012423 maintenance Methods 0.000 description 2
- 229920000609 methyl cellulose Polymers 0.000 description 2
- 239000001923 methylcellulose Substances 0.000 description 2
- 239000013642 negative control Substances 0.000 description 2
- 210000000056 organ Anatomy 0.000 description 2
- 230000008506 pathogenesis Effects 0.000 description 2
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 2
- 230000004962 physiological condition Effects 0.000 description 2
- 230000035479 physiological effects, processes and functions Effects 0.000 description 2
- 239000000049 pigment Substances 0.000 description 2
- 239000013612 plasmid Substances 0.000 description 2
- 239000004033 plastic Substances 0.000 description 2
- 229920003023 plastic Polymers 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 229920002451 polyvinyl alcohol Polymers 0.000 description 2
- 239000013641 positive control Substances 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 230000002062 proliferating effect Effects 0.000 description 2
- 230000002035 prolonged effect Effects 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 231100000241 scar Toxicity 0.000 description 2
- 238000012216 screening Methods 0.000 description 2
- 230000001568 sexual effect Effects 0.000 description 2
- 238000004904 shortening Methods 0.000 description 2
- 230000037384 skin absorption Effects 0.000 description 2
- 231100000274 skin absorption Toxicity 0.000 description 2
- 210000004927 skin cell Anatomy 0.000 description 2
- 208000017520 skin disease Diseases 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- 239000007921 spray Substances 0.000 description 2
- 238000005507 spraying Methods 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 239000013589 supplement Substances 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 230000002459 sustained effect Effects 0.000 description 2
- 231100000331 toxic Toxicity 0.000 description 2
- 230000002588 toxic effect Effects 0.000 description 2
- 239000012096 transfection reagent Substances 0.000 description 2
- 208000002271 trichotillomania Diseases 0.000 description 2
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 2
- 229950009811 ubenimex Drugs 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- ASGMFNBUXDJWJJ-JLCFBVMHSA-N (1R,3R)-3-[[3-bromo-1-[4-(5-methyl-1,3,4-thiadiazol-2-yl)phenyl]pyrazolo[3,4-d]pyrimidin-6-yl]amino]-N,1-dimethylcyclopentane-1-carboxamide Chemical compound BrC1=NN(C2=NC(=NC=C21)N[C@H]1C[C@@](CC1)(C(=O)NC)C)C1=CC=C(C=C1)C=1SC(=NN=1)C ASGMFNBUXDJWJJ-JLCFBVMHSA-N 0.000 description 1
- RDEIXVOBVLKYNT-VQBXQJRRSA-N (2r,3r,4r,5r)-2-[(1s,2s,3r,4s,6r)-4,6-diamino-3-[(2r,3r,6s)-3-amino-6-(1-aminoethyl)oxan-2-yl]oxy-2-hydroxycyclohexyl]oxy-5-methyl-4-(methylamino)oxane-3,5-diol;(2r,3r,4r,5r)-2-[(1s,2s,3r,4s,6r)-4,6-diamino-3-[(2r,3r,6s)-3-amino-6-(aminomethyl)oxan-2-yl]o Chemical compound OS(O)(=O)=O.O1C[C@@](O)(C)[C@H](NC)[C@@H](O)[C@H]1O[C@@H]1[C@@H](O)[C@H](O[C@@H]2[C@@H](CC[C@@H](CN)O2)N)[C@@H](N)C[C@H]1N.O1C[C@@](O)(C)[C@H](NC)[C@@H](O)[C@H]1O[C@@H]1[C@@H](O)[C@H](O[C@@H]2[C@@H](CC[C@H](O2)C(C)N)N)[C@@H](N)C[C@H]1N.O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N RDEIXVOBVLKYNT-VQBXQJRRSA-N 0.000 description 1
- HUWSZNZAROKDRZ-RRLWZMAJSA-N (3r,4r)-3-azaniumyl-5-[[(2s,3r)-1-[(2s)-2,3-dicarboxypyrrolidin-1-yl]-3-methyl-1-oxopentan-2-yl]amino]-5-oxo-4-sulfanylpentane-1-sulfonate Chemical compound OS(=O)(=O)CC[C@@H](N)[C@@H](S)C(=O)N[C@@H]([C@H](C)CC)C(=O)N1CCC(C(O)=O)[C@H]1C(O)=O HUWSZNZAROKDRZ-RRLWZMAJSA-N 0.000 description 1
- LKJPYSCBVHEWIU-KRWDZBQOSA-N (R)-bicalutamide Chemical compound C([C@@](O)(C)C(=O)NC=1C=C(C(C#N)=CC=1)C(F)(F)F)S(=O)(=O)C1=CC=C(F)C=C1 LKJPYSCBVHEWIU-KRWDZBQOSA-N 0.000 description 1
- IYDMGGPKSVWQRT-IHLOFXLRSA-N 1-[4-[(4r,5s)-4,5-bis(4-chlorophenyl)-2-(4-methoxy-2-propan-2-yloxyphenyl)-4,5-dihydroimidazole-1-carbonyl]piperazin-1-yl]ethanone Chemical group CC(C)OC1=CC(OC)=CC=C1C1=N[C@H](C=2C=CC(Cl)=CC=2)[C@H](C=2C=CC(Cl)=CC=2)N1C(=O)N1CCN(C(C)=O)CC1 IYDMGGPKSVWQRT-IHLOFXLRSA-N 0.000 description 1
- UEJJHQNACJXSKW-UHFFFAOYSA-N 2-(2,6-dioxopiperidin-3-yl)-1H-isoindole-1,3(2H)-dione Chemical compound O=C1C2=CC=CC=C2C(=O)N1C1CCC(=O)NC1=O UEJJHQNACJXSKW-UHFFFAOYSA-N 0.000 description 1
- LCQXXVFFJHBYME-UHFFFAOYSA-N 2-butyl-4-hydroxybenzoic acid Chemical compound CCCCC1=CC(O)=CC=C1C(O)=O LCQXXVFFJHBYME-UHFFFAOYSA-N 0.000 description 1
- BGAJNPLDJJBRHK-UHFFFAOYSA-N 3-[2-[5-(3-chloro-4-propan-2-yloxyphenyl)-1,3,4-thiadiazol-2-yl]-3-methyl-6,7-dihydro-4h-pyrazolo[4,3-c]pyridin-5-yl]propanoic acid Chemical compound C1=C(Cl)C(OC(C)C)=CC=C1C1=NN=C(N2C(=C3CN(CCC(O)=O)CCC3=N2)C)S1 BGAJNPLDJJBRHK-UHFFFAOYSA-N 0.000 description 1
- 102100033875 3-oxo-5-alpha-steroid 4-dehydrogenase 2 Human genes 0.000 description 1
- ARBYGDBJECGMGA-UHFFFAOYSA-N 4-[3-(4-hydroxybutyl)-4,4-dimethyl-2,5-dioxoimidazolidin-1-yl]-2-(trifluoromethyl)benzonitrile Chemical compound O=C1C(C)(C)N(CCCCO)C(=O)N1C1=CC=C(C#N)C(C(F)(F)F)=C1 ARBYGDBJECGMGA-UHFFFAOYSA-N 0.000 description 1
- 229940090248 4-hydroxybenzoic acid Drugs 0.000 description 1
- SQDAZGGFXASXDW-UHFFFAOYSA-N 5-bromo-2-(trifluoromethoxy)pyridine Chemical compound FC(F)(F)OC1=CC=C(Br)C=N1 SQDAZGGFXASXDW-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- 208000030507 AIDS Diseases 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 201000010028 Acrocephalosyndactylia Diseases 0.000 description 1
- APKFDSVGJQXUKY-KKGHZKTASA-N Amphotericin-B Natural products O[C@H]1[C@@H](N)[C@H](O)[C@@H](C)O[C@H]1O[C@H]1C=CC=CC=CC=CC=CC=CC=C[C@H](C)[C@@H](O)[C@@H](C)[C@H](C)OC(=O)C[C@H](O)C[C@H](O)CC[C@@H](O)[C@H](O)C[C@H](O)C[C@](O)(C[C@H](O)[C@H]2C(O)=O)O[C@H]2C1 APKFDSVGJQXUKY-KKGHZKTASA-N 0.000 description 1
- 206010056292 Androgen-Insensitivity Syndrome Diseases 0.000 description 1
- 208000025490 Apert syndrome Diseases 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 206010053555 Arthritis bacterial Diseases 0.000 description 1
- 206010004146 Basal cell carcinoma Diseases 0.000 description 1
- VGGGPCQERPFHOB-UHFFFAOYSA-N Bestatin Natural products CC(C)CC(C(O)=O)NC(=O)C(O)C(N)CC1=CC=CC=C1 VGGGPCQERPFHOB-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- 239000004255 Butylated hydroxyanisole Substances 0.000 description 1
- 239000004322 Butylated hydroxytoluene Substances 0.000 description 1
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 1
- 238000011740 C57BL/6 mouse Methods 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 101100507655 Canis lupus familiaris HSPA1 gene Proteins 0.000 description 1
- 241000499489 Castor canadensis Species 0.000 description 1
- 102100025064 Cellular tumor antigen p53 Human genes 0.000 description 1
- 101710150820 Cellular tumor antigen p53 Proteins 0.000 description 1
- 241000700112 Chinchilla Species 0.000 description 1
- GHXZTYHSJHQHIJ-UHFFFAOYSA-N Chlorhexidine Chemical compound C=1C=C(Cl)C=CC=1NC(N)=NC(N)=NCCCCCCN=C(N)N=C(N)NC1=CC=C(Cl)C=C1 GHXZTYHSJHQHIJ-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- QMBJSIBWORFWQT-DFXBJWIESA-N Chlormadinone acetate Chemical compound C1=C(Cl)C2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(C)=O)(OC(=O)C)[C@@]1(C)CC2 QMBJSIBWORFWQT-DFXBJWIESA-N 0.000 description 1
- 229920001287 Chondroitin sulfate Polymers 0.000 description 1
- 208000032544 Cicatrix Diseases 0.000 description 1
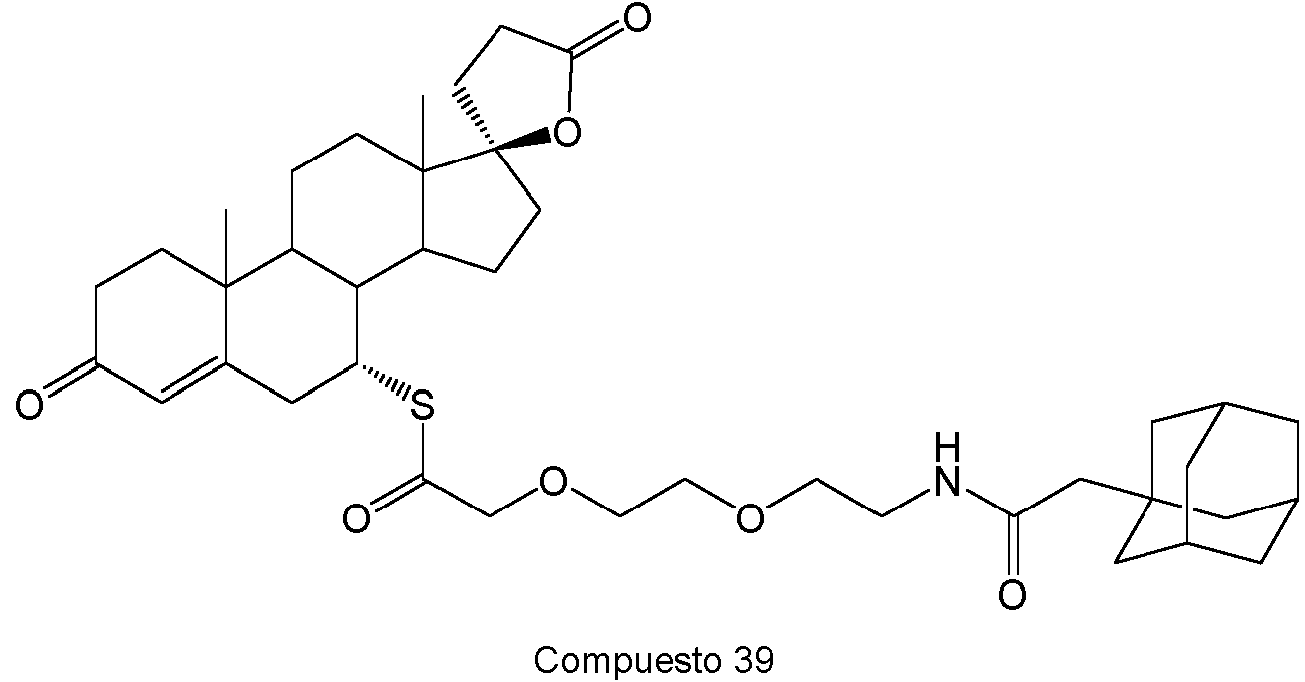
- 229940127007 Compound 39 Drugs 0.000 description 1
- 241000699800 Cricetinae Species 0.000 description 1
- IGXWBGJHJZYPQS-SSDOTTSWSA-N D-Luciferin Chemical compound OC(=O)[C@H]1CSC(C=2SC3=CC=C(O)C=C3N=2)=N1 IGXWBGJHJZYPQS-SSDOTTSWSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- 102000012199 E3 ubiquitin-protein ligase Mdm2 Human genes 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 102000016942 Elastin Human genes 0.000 description 1
- 108010014258 Elastin Proteins 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 206010053487 Exposure to toxic agent Diseases 0.000 description 1
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 1
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- 229920002683 Glycosaminoglycan Polymers 0.000 description 1
- 108010008488 Glycylglycine Proteins 0.000 description 1
- 102000011733 Hair-Specific Keratins Human genes 0.000 description 1
- 108010037031 Hair-Specific Keratins Proteins 0.000 description 1
- 101710113864 Heat shock protein 90 Proteins 0.000 description 1
- 108010004889 Heat-Shock Proteins Proteins 0.000 description 1
- 102000002812 Heat-Shock Proteins Human genes 0.000 description 1
- 208000028782 Hereditary disease Diseases 0.000 description 1
- 102100032742 Histone-lysine N-methyltransferase SETD2 Human genes 0.000 description 1
- 101000640851 Homo sapiens 3-oxo-5-alpha-steroid 4-dehydrogenase 2 Proteins 0.000 description 1
- 101001016865 Homo sapiens Heat shock protein HSP 90-alpha Proteins 0.000 description 1
- 101000654725 Homo sapiens Histone-lysine N-methyltransferase SETD2 Proteins 0.000 description 1
- 101000581514 Homo sapiens Membrane-bound transcription factor site-2 protease Proteins 0.000 description 1
- 101000974343 Homo sapiens Nuclear receptor coactivator 4 Proteins 0.000 description 1
- 101000583175 Homo sapiens Prolactin-inducible protein Proteins 0.000 description 1
- 101000836268 Homo sapiens U4/U6.U5 tri-snRNP-associated protein 1 Proteins 0.000 description 1
- 206010020880 Hypertrophy Diseases 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 208000024502 Keratosis follicularis spinulosa decalvans Diseases 0.000 description 1
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 1
- PWKSKIMOESPYIA-BYPYZUCNSA-N L-N-acetyl-Cysteine Chemical compound CC(=O)N[C@@H](CS)C(O)=O PWKSKIMOESPYIA-BYPYZUCNSA-N 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 1
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 206010027145 Melanocytic naevus Diseases 0.000 description 1
- 102100027382 Membrane-bound transcription factor site-2 protease Human genes 0.000 description 1
- 235000011779 Menyanthes trifoliata Nutrition 0.000 description 1
- 241000699673 Mesocricetus auratus Species 0.000 description 1
- 102000005431 Molecular Chaperones Human genes 0.000 description 1
- 108010006519 Molecular Chaperones Proteins 0.000 description 1
- QPCDCPDFJACHGM-UHFFFAOYSA-N N,N-bis{2-[bis(carboxymethyl)amino]ethyl}glycine Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(=O)O)CCN(CC(O)=O)CC(O)=O QPCDCPDFJACHGM-UHFFFAOYSA-N 0.000 description 1
- 125000001429 N-terminal alpha-amino-acid group Chemical group 0.000 description 1
- 229910002651 NO3 Inorganic materials 0.000 description 1
- 108020000002 NR3 subfamily Proteins 0.000 description 1
- 206010029098 Neoplasm skin Diseases 0.000 description 1
- 241000772415 Neovison vison Species 0.000 description 1
- 208000007256 Nevus Diseases 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- 102100022927 Nuclear receptor coactivator 4 Human genes 0.000 description 1
- BDUHCSBCVGXTJM-IZLXSDGUSA-N Nutlin-3 Chemical group CC(C)OC1=CC(OC)=CC=C1C1=N[C@H](C=2C=CC(Cl)=CC=2)[C@H](C=2C=CC(Cl)=CC=2)N1C(=O)N1CC(=O)NCC1 BDUHCSBCVGXTJM-IZLXSDGUSA-N 0.000 description 1
- 206010031149 Osteitis Diseases 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 102100025803 Progesterone receptor Human genes 0.000 description 1
- 102100030350 Prolactin-inducible protein Human genes 0.000 description 1
- 201000004681 Psoriasis Diseases 0.000 description 1
- 108091027981 Response element Proteins 0.000 description 1
- 201000000860 Secondary syphilis Diseases 0.000 description 1
- 208000000453 Skin Neoplasms Diseases 0.000 description 1
- 102100032250 Trichohyalin Human genes 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 102100027244 U4/U6.U5 tri-snRNP-associated protein 1 Human genes 0.000 description 1
- 241000282485 Vulpes vulpes Species 0.000 description 1
- 239000004164 Wax ester Substances 0.000 description 1
- SPXSEZMVRJLHQG-XMMPIXPASA-N [(2R)-1-[[4-[(3-phenylmethoxyphenoxy)methyl]phenyl]methyl]pyrrolidin-2-yl]methanol Chemical compound C(C1=CC=CC=C1)OC=1C=C(OCC2=CC=C(CN3[C@H](CCC3)CO)C=C2)C=CC=1 SPXSEZMVRJLHQG-XMMPIXPASA-N 0.000 description 1
- PVRYEWOXWGDQHA-URLMMPGGSA-N [(4s,5r)-4,5-bis(4-bromophenyl)-2-(2-ethoxy-4-methoxyphenyl)-4,5-dihydroimidazol-1-yl]-[4-(2-hydroxyethyl)piperazin-1-yl]methanone Chemical group CCOC1=CC(OC)=CC=C1C1=N[C@@H](C=2C=CC(Br)=CC=2)[C@@H](C=2C=CC(Br)=CC=2)N1C(=O)N1CCN(CCO)CC1 PVRYEWOXWGDQHA-URLMMPGGSA-N 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 201000010272 acanthosis nigricans Diseases 0.000 description 1
- 239000008351 acetate buffer Substances 0.000 description 1
- XVIYCJDWYLJQBG-UHFFFAOYSA-N acetic acid;adamantane Chemical compound CC(O)=O.C1C(C2)CC3CC1CC2C3 XVIYCJDWYLJQBG-UHFFFAOYSA-N 0.000 description 1
- 229960004308 acetylcysteine Drugs 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 239000008186 active pharmaceutical agent Substances 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 210000000577 adipose tissue Anatomy 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 239000004479 aerosol dispenser Substances 0.000 description 1
- 125000003342 alkenyl group Chemical group 0.000 description 1
- 230000000172 allergic effect Effects 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 150000003927 aminopyridines Chemical class 0.000 description 1
- APKFDSVGJQXUKY-INPOYWNPSA-N amphotericin B Chemical compound O[C@H]1[C@@H](N)[C@H](O)[C@@H](C)O[C@H]1O[C@H]1/C=C/C=C/C=C/C=C/C=C/C=C/C=C/[C@H](C)[C@@H](O)[C@@H](C)[C@H](C)OC(=O)C[C@H](O)C[C@H](O)CC[C@@H](O)[C@H](O)C[C@H](O)C[C@](O)(C[C@H](O)[C@H]2C(O)=O)O[C@H]2C1 APKFDSVGJQXUKY-INPOYWNPSA-N 0.000 description 1
- 229960003942 amphotericin b Drugs 0.000 description 1
- 239000012491 analyte Substances 0.000 description 1
- 230000001548 androgenic effect Effects 0.000 description 1
- AEMFNILZOJDQLW-QAGGRKNESA-N androst-4-ene-3,17-dione Chemical compound O=C1CC[C@]2(C)[C@H]3CC[C@](C)(C(CC4)=O)[C@@H]4[C@@H]3CCC2=C1 AEMFNILZOJDQLW-QAGGRKNESA-N 0.000 description 1
- 229960005471 androstenedione Drugs 0.000 description 1
- AEMFNILZOJDQLW-UHFFFAOYSA-N androstenedione Natural products O=C1CCC2(C)C3CCC(C)(C(CC4)=O)C4C3CCC2=C1 AEMFNILZOJDQLW-UHFFFAOYSA-N 0.000 description 1
- 230000003466 anti-cipated effect Effects 0.000 description 1
- HJBWBFZLDZWPHF-UHFFFAOYSA-N apalutamide Chemical compound C1=C(F)C(C(=O)NC)=CC=C1N1C2(CCC2)C(=O)N(C=2C=C(C(C#N)=NC=2)C(F)(F)F)C1=S HJBWBFZLDZWPHF-UHFFFAOYSA-N 0.000 description 1
- 229950007511 apalutamide Drugs 0.000 description 1
- 230000001640 apoptogenic effect Effects 0.000 description 1
- 238000003782 apoptosis assay Methods 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 235000009697 arginine Nutrition 0.000 description 1
- 125000000637 arginyl group Chemical group N[C@@H](CCCNC(N)=N)C(=O)* 0.000 description 1
- 210000000617 arm Anatomy 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- 239000012131 assay buffer Substances 0.000 description 1
- RYXHOMYVWAEKHL-UHFFFAOYSA-N astatine atom Chemical compound [At] RYXHOMYVWAEKHL-UHFFFAOYSA-N 0.000 description 1
- 208000010668 atopic eczema Diseases 0.000 description 1
- 208000025255 bacterial arthritis Diseases 0.000 description 1
- 208000003373 basosquamous carcinoma Diseases 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- 229960000997 bicalutamide Drugs 0.000 description 1
- 238000012925 biological evaluation Methods 0.000 description 1
- 230000008827 biological function Effects 0.000 description 1
- 230000008512 biological response Effects 0.000 description 1
- 230000002051 biphasic effect Effects 0.000 description 1
- 239000012496 blank sample Substances 0.000 description 1
- 208000002352 blister Diseases 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 208000018339 bone inflammation disease Diseases 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 239000007975 buffered saline Substances 0.000 description 1
- SKKTUOZKZKCGTB-UHFFFAOYSA-N butyl carbamate Chemical compound CCCCOC(N)=O SKKTUOZKZKCGTB-UHFFFAOYSA-N 0.000 description 1
- 235000019282 butylated hydroxyanisole Nutrition 0.000 description 1
- 229940043253 butylated hydroxyanisole Drugs 0.000 description 1
- CZBZUDVBLSSABA-UHFFFAOYSA-N butylated hydroxyanisole Chemical compound COC1=CC=C(O)C(C(C)(C)C)=C1.COC1=CC=C(O)C=C1C(C)(C)C CZBZUDVBLSSABA-UHFFFAOYSA-N 0.000 description 1
- 235000010354 butylated hydroxytoluene Nutrition 0.000 description 1
- 229940095259 butylated hydroxytoluene Drugs 0.000 description 1
- BHRQIJRLOVHRKH-UHFFFAOYSA-L calcium;2-[bis[2-[bis(carboxylatomethyl)amino]ethyl]amino]acetate;hydron Chemical compound [Ca+2].OC(=O)CN(CC(O)=O)CCN(CC([O-])=O)CCN(CC(O)=O)CC([O-])=O BHRQIJRLOVHRKH-UHFFFAOYSA-L 0.000 description 1
- UJVLDDZCTMKXJK-WNHSNXHDSA-N canrenone Chemical compound C([C@H]1[C@H]2[C@@H]([C@]3(CCC(=O)C=C3C=C2)C)CC[C@@]11C)C[C@@]11CCC(=O)O1 UJVLDDZCTMKXJK-WNHSNXHDSA-N 0.000 description 1
- 229960005057 canrenone Drugs 0.000 description 1
- 230000034303 cell budding Effects 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 230000005889 cellular cytotoxicity Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 239000003610 charcoal Substances 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 210000000038 chest Anatomy 0.000 description 1
- 229960003260 chlorhexidine Drugs 0.000 description 1
- 229960001616 chlormadinone acetate Drugs 0.000 description 1
- 229960004926 chlorobutanol Drugs 0.000 description 1
- 229940059329 chondroitin sulfate Drugs 0.000 description 1
- 208000011830 chronic cutaneous lupus erythematosus Diseases 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- CCGSUNCLSOWKJO-UHFFFAOYSA-N cimetidine Chemical compound N#CNC(=N/C)\NCCSCC1=NC=N[C]1C CCGSUNCLSOWKJO-UHFFFAOYSA-N 0.000 description 1
- 229960001380 cimetidine Drugs 0.000 description 1
- 239000007979 citrate buffer Substances 0.000 description 1
- 210000001520 comb Anatomy 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 229940127271 compound 49 Drugs 0.000 description 1
- 230000003750 conditioning effect Effects 0.000 description 1
- 210000002808 connective tissue Anatomy 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 239000002537 cosmetic Substances 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 230000001186 cumulative effect Effects 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 1
- 235000018417 cysteine Nutrition 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 238000013480 data collection Methods 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 230000001934 delay Effects 0.000 description 1
- 230000002939 deleterious effect Effects 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- METQSPRSQINEEU-UHFFFAOYSA-N dihydrospirorenone Natural products CC12CCC(C3(CCC(=O)C=C3C3CC33)C)C3C1C1CC1C21CCC(=O)O1 METQSPRSQINEEU-UHFFFAOYSA-N 0.000 description 1
- 238000006471 dimerization reaction Methods 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 230000008034 disappearance Effects 0.000 description 1
- 208000037765 diseases and disorders Diseases 0.000 description 1
- 238000010494 dissociation reaction Methods 0.000 description 1
- 230000005593 dissociations Effects 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 229960004845 drospirenone Drugs 0.000 description 1
- METQSPRSQINEEU-HXCATZOESA-N drospirenone Chemical compound C([C@]12[C@H]3C[C@H]3[C@H]3[C@H]4[C@@H]([C@]5(CCC(=O)C=C5[C@@H]5C[C@@H]54)C)CC[C@@]31C)CC(=O)O2 METQSPRSQINEEU-HXCATZOESA-N 0.000 description 1
- 238000009510 drug design Methods 0.000 description 1
- 229940088679 drug related substance Drugs 0.000 description 1
- 229920002549 elastin Polymers 0.000 description 1
- 239000003974 emollient agent Substances 0.000 description 1
- 230000002996 emotional effect Effects 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 229960004671 enzalutamide Drugs 0.000 description 1
- WXCXUHSOUPDCQV-UHFFFAOYSA-N enzalutamide Chemical compound C1=C(F)C(C(=O)NC)=CC=C1N1C(C)(C)C(=O)N(C=2C=C(C(C#N)=CC=2)C(F)(F)F)C1=S WXCXUHSOUPDCQV-UHFFFAOYSA-N 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 210000001339 epidermal cell Anatomy 0.000 description 1
- 210000000918 epididymis Anatomy 0.000 description 1
- 201000010063 epididymitis Diseases 0.000 description 1
- 210000000981 epithelium Anatomy 0.000 description 1
- DEFVIWRASFVYLL-UHFFFAOYSA-N ethylene glycol bis(2-aminoethyl)tetraacetic acid Chemical compound OC(=O)CN(CC(O)=O)CCOCCOCCN(CC(O)=O)CC(O)=O DEFVIWRASFVYLL-UHFFFAOYSA-N 0.000 description 1
- 201000010934 exostosis Diseases 0.000 description 1
- 210000002744 extracellular matrix Anatomy 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 239000004744 fabric Substances 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- MKXKFYHWDHIYRV-UHFFFAOYSA-N flutamide Chemical compound CC(C)C(=O)NC1=CC=C([N+]([O-])=O)C(C(F)(F)F)=C1 MKXKFYHWDHIYRV-UHFFFAOYSA-N 0.000 description 1
- 229960002074 flutamide Drugs 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 239000012458 free base Substances 0.000 description 1
- 239000012737 fresh medium Substances 0.000 description 1
- 108020001507 fusion proteins Proteins 0.000 description 1
- 102000037865 fusion proteins Human genes 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 235000004554 glutamine Nutrition 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- 229940043257 glycylglycine Drugs 0.000 description 1
- 230000003793 hair pigmentation Effects 0.000 description 1
- 201000010066 hyperandrogenism Diseases 0.000 description 1
- 201000010930 hyperostosis Diseases 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 239000005414 inactive ingredient Substances 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 208000000509 infertility Diseases 0.000 description 1
- 230000036512 infertility Effects 0.000 description 1
- 208000021267 infertility disease Diseases 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 230000028709 inflammatory response Effects 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 238000007689 inspection Methods 0.000 description 1
- 210000001613 integumentary system Anatomy 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 235000015110 jellies Nutrition 0.000 description 1
- 239000008274 jelly Substances 0.000 description 1
- 229960004942 lenalidomide Drugs 0.000 description 1
- GOTYRUGSSMKFNF-UHFFFAOYSA-N lenalidomide Chemical compound C1C=2C(N)=CC=CC=2C(=O)N1C1CCC(=O)NC1=O GOTYRUGSSMKFNF-UHFFFAOYSA-N 0.000 description 1
- 210000003041 ligament Anatomy 0.000 description 1
- 229940040145 liniment Drugs 0.000 description 1
- 239000000865 liniment Substances 0.000 description 1
- 210000000088 lip Anatomy 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 239000008263 liquid aerosol Substances 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 235000018977 lysine Nutrition 0.000 description 1
- 239000012139 lysis buffer Substances 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 210000005075 mammary gland Anatomy 0.000 description 1
- 238000007726 management method Methods 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- KJLLKLRVCJAFRY-UHFFFAOYSA-N mebutizide Chemical compound ClC1=C(S(N)(=O)=O)C=C2S(=O)(=O)NC(C(C)C(C)CC)NC2=C1 KJLLKLRVCJAFRY-UHFFFAOYSA-N 0.000 description 1
- RQZAXGRLVPAYTJ-GQFGMJRRSA-N megestrol acetate Chemical compound C1=C(C)C2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(C)=O)(OC(=O)C)[C@@]1(C)CC2 RQZAXGRLVPAYTJ-GQFGMJRRSA-N 0.000 description 1
- 229960004296 megestrol acetate Drugs 0.000 description 1
- 210000004379 membrane Anatomy 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 201000002266 mite infestation Diseases 0.000 description 1
- 230000004660 morphological change Effects 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 210000004165 myocardium Anatomy 0.000 description 1
- IOMMMLWIABWRKL-WUTDNEBXSA-N nazartinib Chemical compound C1N(C(=O)/C=C/CN(C)C)CCCC[C@H]1N1C2=C(Cl)C=CC=C2N=C1NC(=O)C1=CC=NC(C)=C1 IOMMMLWIABWRKL-WUTDNEBXSA-N 0.000 description 1
- 210000005036 nerve Anatomy 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- XWXYUMMDTVBTOU-UHFFFAOYSA-N nilutamide Chemical compound O=C1C(C)(C)NC(=O)N1C1=CC=C([N+]([O-])=O)C(C(F)(F)F)=C1 XWXYUMMDTVBTOU-UHFFFAOYSA-N 0.000 description 1
- 229960002653 nilutamide Drugs 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 108091008581 nuclear androgen receptors Proteins 0.000 description 1
- 102000006255 nuclear receptors Human genes 0.000 description 1
- 108020004017 nuclear receptors Proteins 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 230000037312 oily skin Effects 0.000 description 1
- 125000005430 oxychloro group Chemical group 0.000 description 1
- 230000003076 paracrine Effects 0.000 description 1
- 230000037368 penetrate the skin Effects 0.000 description 1
- 230000000149 penetrating effect Effects 0.000 description 1
- 239000003961 penetration enhancing agent Substances 0.000 description 1
- 239000002304 perfume Substances 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 1
- 235000008729 phenylalanine Nutrition 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 230000026731 phosphorylation Effects 0.000 description 1
- 238000006366 phosphorylation reaction Methods 0.000 description 1
- XKJCHHZQLQNZHY-UHFFFAOYSA-N phthalimide Chemical compound C1=CC=C2C(=O)NC(=O)C2=C1 XKJCHHZQLQNZHY-UHFFFAOYSA-N 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 210000004694 pigment cell Anatomy 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 150000003077 polyols Chemical class 0.000 description 1
- 239000000244 polyoxyethylene sorbitan monooleate Substances 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 229940068968 polysorbate 80 Drugs 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 229960000688 pomalidomide Drugs 0.000 description 1
- UVSMNLNDYGZFPF-UHFFFAOYSA-N pomalidomide Chemical compound O=C1C=2C(N)=CC=CC=2C(=O)N1C1CCC(=O)NC1=O UVSMNLNDYGZFPF-UHFFFAOYSA-N 0.000 description 1
- 239000001103 potassium chloride Substances 0.000 description 1
- 235000011164 potassium chloride Nutrition 0.000 description 1
- 239000000583 progesterone congener Substances 0.000 description 1
- 108090000468 progesterone receptors Proteins 0.000 description 1
- 230000005522 programmed cell death Effects 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 125000001500 prolyl group Chemical class [H]N1C([H])(C(=O)[*])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 210000002307 prostate Anatomy 0.000 description 1
- 230000007319 proteasomal degradation pathway Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 230000017854 proteolysis Effects 0.000 description 1
- 208000009954 pyoderma gangrenosum Diseases 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 238000010791 quenching Methods 0.000 description 1
- 239000002516 radical scavenger Substances 0.000 description 1
- 238000001959 radiotherapy Methods 0.000 description 1
- 229940044551 receptor antagonist Drugs 0.000 description 1
- 239000002464 receptor antagonist Substances 0.000 description 1
- 230000007115 recruitment Effects 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 230000001850 reproductive effect Effects 0.000 description 1
- 210000004994 reproductive system Anatomy 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 230000037387 scars Effects 0.000 description 1
- 210000004378 sebocyte Anatomy 0.000 description 1
- 208000008742 seborrheic dermatitis Diseases 0.000 description 1
- 210000001625 seminal vesicle Anatomy 0.000 description 1
- 239000002453 shampoo Substances 0.000 description 1
- 210000002027 skeletal muscle Anatomy 0.000 description 1
- 230000008470 skin growth Effects 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 239000000344 soap Substances 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- HRZFUMHJMZEROT-UHFFFAOYSA-L sodium disulfite Chemical compound [Na+].[Na+].[O-]S(=O)S([O-])(=O)=O HRZFUMHJMZEROT-UHFFFAOYSA-L 0.000 description 1
- 229940001584 sodium metabisulfite Drugs 0.000 description 1
- 235000010262 sodium metabisulphite Nutrition 0.000 description 1
- AKHNMLFCWUSKQB-UHFFFAOYSA-L sodium thiosulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=S AKHNMLFCWUSKQB-UHFFFAOYSA-L 0.000 description 1
- 229940001474 sodium thiosulfate Drugs 0.000 description 1
- 235000019345 sodium thiosulphate Nutrition 0.000 description 1
- 239000008279 sol Substances 0.000 description 1
- 239000008247 solid mixture Substances 0.000 description 1
- 238000000527 sonication Methods 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- 230000003068 static effect Effects 0.000 description 1
- 239000003270 steroid hormone Substances 0.000 description 1
- 230000010009 steroidogenesis Effects 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 210000004003 subcutaneous fat Anatomy 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 210000000106 sweat gland Anatomy 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 201000004595 synovitis Diseases 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 108010067247 tacrolimus binding protein 4 Proteins 0.000 description 1
- 230000002123 temporal effect Effects 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 210000001550 testis Anatomy 0.000 description 1
- 210000000531 tether cell Anatomy 0.000 description 1
- 229960003433 thalidomide Drugs 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- RTKIYNMVFMVABJ-UHFFFAOYSA-L thimerosal Chemical compound [Na+].CC[Hg]SC1=CC=CC=C1C([O-])=O RTKIYNMVFMVABJ-UHFFFAOYSA-L 0.000 description 1
- 229940033663 thimerosal Drugs 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- 229950010529 topilutamide Drugs 0.000 description 1
- 238000001890 transfection Methods 0.000 description 1
- 230000001052 transient effect Effects 0.000 description 1
- 108010031667 trichohyalin Proteins 0.000 description 1
- 230000001960 triggered effect Effects 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- GPRLSGONYQIRFK-MNYXATJNSA-N triton Chemical compound [3H+] GPRLSGONYQIRFK-MNYXATJNSA-N 0.000 description 1
- 230000034512 ubiquitination Effects 0.000 description 1
- 238000010798 ubiquitination Methods 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- 201000010653 vesiculitis Diseases 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
- 210000001835 viscera Anatomy 0.000 description 1
- 238000011179 visual inspection Methods 0.000 description 1
- 235000019386 wax ester Nutrition 0.000 description 1
- 238000004018 waxing Methods 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J31/00—Normal steroids containing one or more sulfur atoms not belonging to a hetero ring
- C07J31/003—Normal steroids containing one or more sulfur atoms not belonging to a hetero ring the S atom directly linked to a ring carbon atom of the cyclopenta(a)hydrophenanthrene skeleton
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/427—Thiazoles not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene or sparfloxacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/58—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids containing heterocyclic rings, e.g. danazol, stanozolol, pancuronium or digitogenin
- A61K31/585—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids containing heterocyclic rings, e.g. danazol, stanozolol, pancuronium or digitogenin containing lactone rings, e.g. oxandrolone, bufalin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/10—Anti-acne agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/14—Drugs for dermatological disorders for baldness or alopecia
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C233/00—Carboxylic acid amides
- C07C233/01—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms
- C07C233/16—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having the nitrogen atom of at least one of the carboxamide groups bound to a carbon atom of a hydrocarbon radical substituted by singly-bound oxygen atoms
- C07C233/17—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having the nitrogen atom of at least one of the carboxamide groups bound to a carbon atom of a hydrocarbon radical substituted by singly-bound oxygen atoms with the substituted hydrocarbon radical bound to the nitrogen atom of the carboxamide group by an acyclic carbon atom
- C07C233/21—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having the nitrogen atom of at least one of the carboxamide groups bound to a carbon atom of a hydrocarbon radical substituted by singly-bound oxygen atoms with the substituted hydrocarbon radical bound to the nitrogen atom of the carboxamide group by an acyclic carbon atom having the carbon atom of the carboxamide group bound to an acyclic carbon atom of an unsaturated carbon skeleton containing rings other than six-membered aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C43/00—Ethers; Compounds having groups, groups or groups
- C07C43/02—Ethers
- C07C43/18—Ethers having an ether-oxygen atom bound to a carbon atom of a ring other than a six-membered aromatic ring
- C07C43/196—Ethers having an ether-oxygen atom bound to a carbon atom of a ring other than a six-membered aromatic ring containing hydroxy or O-metal groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C53/00—Saturated compounds having only one carboxyl group bound to an acyclic carbon atom or hydrogen
- C07C53/132—Saturated compounds having only one carboxyl group bound to an acyclic carbon atom or hydrogen containing rings
- C07C53/136—Saturated compounds having only one carboxyl group bound to an acyclic carbon atom or hydrogen containing rings containing condensed ring systems
- C07C53/138—Saturated compounds having only one carboxyl group bound to an acyclic carbon atom or hydrogen containing rings containing condensed ring systems containing an adamantane ring system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C69/00—Esters of carboxylic acids; Esters of carbonic or haloformic acids
- C07C69/66—Esters of carboxylic acids having esterified carboxylic groups bound to acyclic carbon atoms and having any of the groups OH, O—metal, —CHO, keto, ether, acyloxy, groups, groups, or in the acid moiety
- C07C69/67—Esters of carboxylic acids having esterified carboxylic groups bound to acyclic carbon atoms and having any of the groups OH, O—metal, —CHO, keto, ether, acyloxy, groups, groups, or in the acid moiety of saturated acids
- C07C69/708—Ethers
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D207/00—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D207/02—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D207/18—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having one double bond between ring members or between a ring member and a non-ring member
- C07D207/22—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having one double bond between ring members or between a ring member and a non-ring member with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D207/24—Oxygen or sulfur atoms
- C07D207/26—2-Pyrrolidones
- C07D207/273—2-Pyrrolidones with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to other ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/06—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J21/00—Normal steroids containing carbon, hydrogen, halogen or oxygen having an oxygen-containing hetero ring spiro-condensed with the cyclopenta(a)hydrophenanthrene skeleton
- C07J21/001—Lactones
- C07J21/003—Lactones at position 17
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J41/00—Normal steroids containing one or more nitrogen atoms not belonging to a hetero ring
- C07J41/0033—Normal steroids containing one or more nitrogen atoms not belonging to a hetero ring not covered by C07J41/0005
- C07J41/0044—Normal steroids containing one or more nitrogen atoms not belonging to a hetero ring not covered by C07J41/0005 with an estrane or gonane skeleton, including 18-substituted derivatives and derivatives where position 17-beta is substituted by a carbon atom not directly bonded to another carbon atom and not being part of an amide group
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J43/00—Normal steroids having a nitrogen-containing hetero ring spiro-condensed or not condensed with the cyclopenta(a)hydrophenanthrene skeleton
- C07J43/003—Normal steroids having a nitrogen-containing hetero ring spiro-condensed or not condensed with the cyclopenta(a)hydrophenanthrene skeleton not condensed
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J71/00—Steroids in which the cyclopenta(a)hydrophenanthrene skeleton is condensed with a heterocyclic ring
- C07J71/0005—Oxygen-containing hetero ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K5/00—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof
- C07K5/04—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof containing only normal peptide links
- C07K5/06—Dipeptides
- C07K5/06008—Dipeptides with the first amino acid being neutral
- C07K5/06017—Dipeptides with the first amino acid being neutral and aliphatic
- C07K5/06034—Dipeptides with the first amino acid being neutral and aliphatic the side chain containing 2 to 4 carbon atoms
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Dermatology (AREA)
- Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Plural Heterocyclic Compounds (AREA)
- Pyrrole Compounds (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Steroid Compounds (AREA)
Abstract
Un compuesto seleccionado del grupo que consiste de: **(Ver fórmula)** fórmula XX **(Ver fórmula)** donde n es cualquier número entero de 0 a 10, y fórmula XXI **(Ver fórmula)** donde n es cualquier número entero de 0 a 10.
Description
DESCRIPCIÓN
Eliminadores de receptores de andrógenos tripartitos, métodos y usos de los mismos
Los andrógenos son bien conocidos por controlar el desarrollo y las funciones del sistema reproductor tanto en hombres como en mujeres. El principal andrógeno circulante es la testosterona. La testosterona puede ser metabolizada por las 5a-reductasas en un andrógeno más potente, la 5a-dihidrotestosterona (DHT). Tanto la testosterona como la DHT pueden unirse a los receptores de andrógenos, pero la DHT tiene una afinidad diez veces mayor por los receptores de andrógenos en comparación con la testosterona.
Los dermatólogos reconocen muchos tipos diferentes de afecciones, enfermedades y trastornos relacionados con la piel que afectan a la salud de la piel y/o el cabello. El papel de la señalización de los receptores de andrógenos se ha implicado en la fisiología y patogenia de la piel y el cabello basándose en el hecho de que los receptores de andrógenos y muchas enzimas de esteroidogénesis androgénica se expresan en la piel, y la presencia de dimorfismo sexual en la etiología y las enfermedades de la piel y el cabello. Aunque la piel no es la principal fuente de síntesis de andrógenos, en los sebocitos, las glándulas sudoríparas y las células de la papila dérmica del cabello, las prohormonas androgénicas circulantes, la dehidroepiandrosterona (DHEA) y la androstenediona, pueden convertirse en testosterona y DHT. Estos potentes andrógenos regulan subsecuentemente la fisiología dérmica a través de formas intracrinas o paracrinas. Se ha demostrado que la sobreactivación del receptor de andrógenos por DHT desempeña un papel crítico en la pérdida de cabello (alopecia) en los hombres, crecimiento excesivo de vello (hirsutismo) en las mujeres. Además, la señalización del receptor de andrógenos está implicada en la producción excesiva de sebo y parece promover las respuestas inflamatorias anormales o excesivas que se observan en muchas enfermedades cutáneas, como el acné y la psoriasis.
La presente memoria divulga describe nuevos compuestos, composiciones farmacéuticas que comprenden estos compuestos y métodos y usos para dirigirse al receptor de andrógenos usando estos compuestos y composiciones para tratar una afección, enfermedad o trastorno relacionado con la piel mediado por la señal del receptor de andrógenos que afecta a la salud de la piel y/o el cabello. Tales tratamientos promueven de manera segura y eficaz la salud de la piel y el cabello de un individuo.
SUMARIO
La presente memoria descriptiva divulga de manera general un compuesto de fórmula I
ARA -L-EE (I)
en donde ARA es un antagonista del receptor de andrógenos (AR), L es una molécula conectora y EE es un promotor de la eliminación o un elemento potenciador de la eliminación de AR. Un antagonista de AR divulgado en la presente puede ser cualquier molécula que reduzca o prevenga las respuestas mediadas por agonistas a través de un AR, incluyendo un antagonista de AR ortostérico, un antagonista de AR alostérico o un antagonista de AR que interactúe en uno o más sitios de unión únicos que normalmente no están implicados en la regulación biológica de la actividad de AR. Un antagonista de AR divulgado en la presente puede ser reversible o irreversible. Un conector divulgado en la presente puede ser de fórmula II
R3NH(CO)R4, R3NH(CO)R4OH, R3NH(CO)R4COOH; R3 y R4 son cada uno independientemente alquilo C1-10, alquenilo C2-10 o alquinilo C2-10; y n cualquier número entero de 0 a 10. Un promotor de la eliminación o un elemento potenciador de la eliminación de AR divulgado en la presente puede ser una etiqueta hidrófoba o una fracción reclutadora de ligasa E3. Una etiqueta hidrófoba incluye, sin limitación, una fracción de adamantano o un aminoácido protegido por Boc. Una fracción reclutadora de ligasa E3 incluye, sin limitación, una fracción de factor 1a inducible por hipoxia (HIF-1a), una fracción de Nutlin, una fracción de bestatina o una fracción de ftalimida.
En un aspecto, la invención reivindicada proporciona un compuesto seleccionado del grupo que consiste de:
fórmula XX
donde n es cualquier número entero de 0 a 10, y fórmula XXI
donde n es cualquier número entero de 0 a 10.
Otros aspectos de la invención reivindicada proporcionan una composición farmacéutica que comprende uno o más compuestos divulgados en la presente.
También se divulga, pero no se reivindica, un kit que comprende uno o más compuestos divulgados en la presente o una o más composiciones farmacéuticas divulgadas en la presente.
Los aspectos de la presente invención también proporcionan un compuesto divulgado en la presente o una composición farmacéutica divulgada en la presente para su uso en el tratamiento de la caída del cabello.
Los aspectos de la presente invención también proporcionan un compuesto divulgado en la presente o una composición farmacéutica divulgada en la presente para su uso en el tratamiento del debilitamiento del cabello.
Los aspectos de la presente invención también proporcionan un compuesto divulgado en la presente o una composición farmacéutica divulgada en la presente para su uso en el tratamiento de la pérdida del color del cabello.
Los aspectos de la presente invención también proporcionan un compuesto divulgado en la presente o una
composición farmacéutica divulgada en la presente para su uso en el tratamiento de una afección asociada con un trastorno degenerativo del folículo piloso.
También se divulga, pero no se reivindica, un método para mejorar la apariencia del cabello en un individuo que comprende el paso de administrar una cantidad terapéuticamente eficaz de un compuesto divulgado en la presente o una composición farmacéutica divulgada en la presente. También se divulga, pero no se reivindica, un compuesto divulgado en la presente o una composición farmacéutica divulgada en la presente para su uso en la mejora de la apariencia del cabello; el uso de un compuesto divulgado en la presente o una composición farmacéutica divulgada en la presente para mejorar la apariencia del cabello; y el uso de un compuesto divulgado en la presente o una composición farmacéutica divulgada en la presente en la fabricación de un medicamento para mejorar la apariencia del cabello.
Los aspectos de la presente invención también proporcionan un compuesto divulgado en la presente o una composición farmacéutica divulgada en la presente para su uso en el tratamiento de problemas del cabello, preferiblemente alopecia androgénica e hirsutismo facial.
Los aspectos de la presente invención también proporcionan un compuesto divulgado en la presente o una composición farmacéutica divulgada en la presente para su uso en el tratamiento de problemas de la piel, preferiblemente acné, producción excesiva de sebo y formación de cicatrices posteriores a heridas.
DESCRIPCIÓN DETALLADA
La piel es la cubierta exterior del cuerpo de un mamífero y protege los músculos, huesos, ligamentos y órganos internos subyacentes. Típicamente, el órgano más grande del sistema tegumentario, la piel se compone de tres capas principales: la epidermis, la dermis y la hipodermis. La epidermis es la capa epitelial más externa de la piel y forma la envoltura protectora e impermeable sobre la superficie del cuerpo que también sirve como barrera contra las infecciones. La dermis es una capa epitelial de piel debajo de la epidermis y sirve para proteger al cuerpo del estrés y la tensión. La hipodermis se encuentra debajo de la dermis y comprende tejido conectivo laxo, tejido adiposo y elastina. Aunque no está compuesta por tejido epitelial y, por tanto, no forma parte de la piel, la hipodermis une la piel al hueso y al músculo subyacentes, además de suministrarle vasos sanguíneos y nervios.
Cada cabello comprende dos estructuras: el tallo del cabello y el folículo piloso. El tallo del cabello está compuesto principalmente de queratina que se organiza en tres capas llamadas médula, corteza y cutícula. La médula es la capa interna y no está necesariamente presente en todos los tipos de cabello. La siguiente capa de queratina es la corteza, la capa intermedia que constituye la mayor parte del tallo del cabello. La capa externa es la cutícula, que está formada por escamas estrechamente apretadas en una estructura superpuesta similar a las tejas del techo y se continúa con la vaina de la raíz. La mayoría de los productos acondicionadores para el cabello intentan afectar a la cutícula. Las células pigmentarias, o melanocitos, se distribuyen por la corteza y la médula dando al cabello su color característico. Para los propósitos de la presente divulgación, es necesario considerar varios tipos de cabello, incluyendo, pelos terminales y pelos vellosos y pelos terminales modificados, como los que se ven en las pestañas y las cejas. Los pelos terminales son pelos gruesos, pigmentados y largos en los que el bulbo del folículo piloso se asienta profundamente en la dermis. Los pelos vellosos, por el contrario, son pelos cortos finos, delgados y no pigmentados en los que el bulbo piloso está localizado superficialmente en la dermis. A medida que avanza la alopecia, se produce una transición en el área de calvicie próxima en la que los propios pelos están cambiando del tipo terminal al velloso.
Situado en la capa dérmica de la piel, el folículo piloso puede reconocerse como una entidad separada dentro de la piel cuya formación y mantenimiento se basan en la interacción entre los componentes dérmicos y epidérmicos. El folículo comprende varios componentes. En la base del folículo hay una proyección llamada papila dérmica, que contiene capilares que suministran nutrientes a la porción del folículo llamada bulbo. El bulbo puede dividirse en dos regiones: una región inferior de células indiferenciadas y una región superior de células en proliferación activa, llamada células de matriz, que se diferenciaron para formar la vaina interna y el tallo del cabello. Las células de la matriz son células en proliferación activa que se diferencian y se queratinizan para formar el tallo del cabello. Durante la diferenciación de las células epidérmicas (fase anágena), las células de la matriz se dividen cada de 23 a 72 horas, más rápido que cualquier otra célula del cuerpo. Las células de la matriz localizadas en las inmediaciones inmediatas de la papila dérmica se diferencian y se queratinizan para formar el tallo del cabello, mientras que las células de la matriz hacia la periferia de un folículo piloso proliferan y producen la vaina radicular interna. El folículo también contiene dos capas epidérmicas denominadas vaina radicular interna y vaina radicular externa. Estas vainas protegen y moldean el tallo del cabello en crecimiento. La vaina radicular interna puede dividirse en tres capas (cutícula, capa de Huxley y capa de Henle) en base a la estructura, los patrones de queratinización y la incorporación de tricohialina. La vaina interna sigue el tallo del cabello hasta que termina justo debajo del nivel de una glándula sebácea para dejar que solo el tallo del cabello sobresalga por encima de la epidermis. La vaina radicular externa continúa hasta la glándula y se diferencia de otros componentes epidérmicos del folículo piloso en que es continúa con la epidermis. La glándula sebácea produce sebo, un aceite natural que acondiciona el tallo del cabello y, algunas veces, una glándula apocrina (olor). Un músculo erector del pelo se
adhiere debajo de la glándula a una capa fibrosa alrededor de la vaina exterior. La contracción del músculo tira tanto del cabello para hacerlo erguido como de la piel formando una superficie rugosa. El color del cabello es causado por un pigmento (melanina) que es producido por el folículo piloso.
En circunstancias normales, el crecimiento del cabello en cada folículo piloso se produce en un ciclo que puede comprender por lo menos cuatro fases: anágena (fase de crecimiento), catágena (fase de regresión), telógena (fase de reposo) y exógena (fase de muda). La fase anágena es la fase de crecimiento activo del cabello durante la cual las células de la matriz en la raíz del cabello se dividen rápidamente. Aproximadamente el 80-90% de todos los cabellos se encuentran en esta fase en cualquier momento. Los pelos anágenos están anclados profundamente en la grasa subcutánea y no pueden sacarse fácilmente. Cuando se forma un cabello nuevo, empuja el cabello en maza hacia arriba del folículo y eventualmente lo expulsa. Durante esta fase el cabello crece aproximadamente 0,35 mm por día (1 cm cada 28 días), pero este ritmo varía dependiendo del sitio del folículo piloso y la edad y el sexo del individuo. El cabello del cuero cabelludo humano permanece en la fase anágena activa de crecimiento durante 2-6 años, en comparación con otros sitios como en la pierna (que permanece en fase anágena de 19 a 26 semanas), en el brazo (de 6 a 12 semanas) y en el área del bigote, pestañas y cejas (de 4 a 14 semanas).). Los sujetos humanos que tienen dificultad para hacer crecer su cabello más allá de una cierta longitud tienen una fase activa de crecimiento corta. Los sujetos humanos que tienen el pelo muy largo tienen una fase activa de crecimiento larga.
La fase catágena es una breve fase de transición entre las fases anágena y telógena que dura solo aproximadamente 7-21 días. Aunque breve, esta fase puede dividirse en ocho subfases que comienzan con la anágena tardía y terminan con la telógena temprana. Aproximadamente el 1-3% de todos los cabellos están en esta fase en cualquier momento. Es un período de regresión controlada en la que el folículo piloso retrocede y desmantela la parte del folículo piloso en crecimiento del cabello, en parte, a través de la apoptosis. Durante esta fase hay una involución del folículo piloso y una reestructuración fundamental de la matriz extracelular por 1) la retirada de la papila dérmica y la detención del crecimiento del cabello, 2) el cese de la proliferación celular de la matriz y la síntesis de melanina de los melanocitos, 3) la contracción de la capa externa vaina de la raíz y la unión al tallo del cabello, 4) movimiento del folículo piloso inferior al nivel del músculo erector del pelo, 5) movimiento de la papila dérmica hacia arriba a través de la piel, deteniéndose por debajo de la protuberancia del folículo piloso, y 6) cese de la producción de proteínas y pigmentos mediante muerte celular de queratinocitos y melanocitos. Además, hay una apoptosis masiva en la parte bulbar, transitoria, del folículo piloso que contribuye a la regresión del folículo piloso ya la formación de una serpentina fibrosa en la piel. El inicio de estos eventos apoptóticos parece estar predeterminado y finamente orquestado, y como tal, los eventos en esta fase pueden describirse más apropiadamente con el término "muerte celular programada".
La tercera fase es la fase telógena que, a todos los efectos prácticos, puede denominarse "fase de reposo". Aproximadamente el 10-15% de todos los cabellos se encuentran en esta fase en cualquier momento. Durante esta fase, el folículo piloso deja de dividirse y el tallo piloso deja de crecer, el cabello telógeno completa la diferenciación y las últimas células de crecimiento piloso se agrupan en la base del tallo piloso para formar una estructura de maza que comprende un cepillo que reside centralmente de células queratinizadas rodeadas de células de amarre aparentes que contienen núcleos discretos fáciles de encontrar y abundante citoplasma. Denominado un pelo en maza, el grupo de células en realidad mantiene el tallo del cabello en el tubo del folículo piloso. En el aspecto final de la fase telógena, una señal química hace que las células de la matriz inicien el crecimiento de un nuevo tallo piloso a partir del mismo folículo piloso y el ciclo comienza de nuevo con una nueva fase anágena. Aunque un cabello telógeno se encuentra cerca de la superficie de la piel, permanece firmemente anclado al folículo piloso. Un cabello telógeno finalmente se desprende en la fase exógena y es reemplazado por el siguiente cabello anágeno en ciernes. Pasan aproximadamente 30-90 días antes de que el pelo telógeno del cuero cabelludo se desprenda. El período de tiempo es mucho más largo para los pelos de las cejas, las pestañas, los brazos y las piernas.
La fase final es la exógena, una fase marcada por un proceso activo altamente controlado en el que un cabello telógeno se desprende del folículo. El cabello exógeno desprendido tiene una base contraída que tiene una forma más alargada y tiene un margen festoneado y picado. Dentro de esta base del tallo hay poco citoplasma asociado y muy pocos núcleos contraídos y fragmentados. Se cree que la contracción del mazo de cabello y la desaparición del amarre del cepillo permiten que el cabello exógeno se desprenda del folículo. Normalmente, cada día se desprenden aproximadamente de 25 a 150 cabellos exógenos.
Recientemente, se ha propuesto una fase de adición denominada kenógena. Esta fase describe el intervalo del ciclo capilar en el que el folículo piloso permanece vacío después de que se haya extruido el cabello telógeno, pero antes de que reaparezca un nuevo cabello anágeno.
Los andrógenos, principalmente la testosterona y la 5a-dihidrotestosterona (DHT) desempeñan un papel importante en el crecimiento y desarrollo de los órganos reproductores masculinos. Estas hormonas esteroides realizan sus funciones biológicas a través de sus asociaciones con el receptor de andrógenos (AR). También conocido como subfamilia de receptores nucleares 3, grupo C, miembro 4 (NR3C4), el AR es un factor de transcripción dependiente de ligando de 110 KDa que se incluye en el grupo de la superfamilia de receptores nucleares. El AR tiene cuatro dominios funcionales, un dominio N terminal (NTD), un dominio de unión a ADN (DBD),
una región bisagra y un dominio de unión a ligando (LBD). El DBD tiene motivos ZNF que le permiten unirse al ADN. El resto de los dominios están implicados en la dimerización y unión de ligandos. Un AR está más estrechamente relacionado con el receptor de progesterona, y las progestinas en dosificaciones más altas pueden bloquear el AR. El AR se expresa en una serie de tejidos y células que incluyen la próstata, los testículos, la vesícula seminal, el epidídimo, la piel, el músculo esquelético, el músculo cardíaco, el hígado y el sistema nervioso central. La función principal del receptor de AR es como un factor de transcripción de unión al ADN que regula la expresión génica, incluyendo los genes críticos para el desarrollo y mantenimiento del fenotipo sexual masculino.
En el estado no unido al ligando, un AR es una proteína citosólica inactiva, que forma complejos con varias proteínas de choque térmico, incluyendo Hsp70, Hsp90 y Hsp 56, así como p23. Tras unirse al ligando, dos eventos críticos de fosforilación promueven un cambio conformacional en un AR, lo que da como resultado la liberación del LBD para la unión de la hormona y la disociación del AR unido al ligando del complejo Hsp. El AR unido a ligando libre de complejos se traslada al núcleo, forma homodímeros y se une a los elementos de respuesta a andrógenos (ARE) presentes en varios genes objetivo, activando de este modo la expresión génica. La expresión temporal y espacial puede regularse en parte por muchos coreguladores que se unen a homodímeros de AR unidos a ligando en diferentes puntos temporales y en diferentes tipos de células. Por ejemplo, la modulación de la actividad de AR puede llevarse a cabo mediante varios factores de transcripción como ARA70, TR4, miembros de la familia SRC y CBP/p300 y otras proteínas asociadas. Los motivos FXXLF y WXXLF que contienen coactivadores como los miembros p160 se unen con la región AF2 del LBD de un AR.
La actividad de AR también impulsa la pérdida de cabello, el debilitamiento del cabello o la pérdida de color del cabello. Por ejemplo, la papila dérmica es el principal regulador del ciclo del cabello y esta estructura tiene AR. La exposición de DHT a los folículos en el vértice y la región frontal del cuero cabelludo puede suprimir el crecimiento del cabello en parte al acortar drásticamente la longitud del anágeno hasta el punto en que el folículo piloso existe solo en un estado miniaturizado de telógeno extendido. Además, la testosterona se convierte en DHT en el folículo a través de la actividad enzimática de la 5-alfa reductasa tipo II. Además, la alopecia androgénica es una forma común de pérdida de cabello que comienza a manifestarse en los hombres después del inicio de la pubertad y aumenta en frecuencia con cada década de vida. En el cuero cabelludo con calvicie de los hombres, los niveles de tanto AR como DHT son aproximadamente 2 veces más altos que los niveles de AR y DHT observados en el cuero cabelludo sin calvicie. Por tanto, aunque modulado por variables genéticas y ambientales, el atributo principal de la alopecia androgénica es el aumento de la señalización de AR que da como resultado el acortamiento progresivo del ciclo de crecimiento del cabello en el folículo piloso. Cabe señalar que la alopecia femenina también se produce y se cree que está regulada por factores similares a los implicados en la alopecia androgénica. Por tanto, enfocarse en AR de una manera que reduzca, suprima o elimine sus capacidades de señalización evitará la progresión de los factores que impulsan la caída del cabello, el debilitamiento del cabello o la pérdida del color del cabello.
La actividad de AR también impulsa ciertas afecciones, enfermedades y trastornos de la piel como, por ejemplo, el acné. El acné, también conocido como acné vulgar, es una enfermedad de la piel a largo plazo que se produce cuando los folículos pilosos se obstruyen con células muertas y grasa de la piel. Se caracteriza por puntos negros o puntos blancos, espinillas, piel grasa y posibles cicatrices. El acné afecta principalmente a áreas de la piel con una cantidad relativamente alta de glándulas sebáceas, incluyendo la cara, la parte superior del pecho y la espalda. La apariencia resultante puede provocar ansiedad, reducción de la autoestima y, en casos extremos, depresión o pensamientos suicidas. Durante la pubertad, un aumento de los andrógenos tanto en hombres como en mujeres hace que las glándulas de los folículos de la piel crezcan más y produzcan más sebo aceitoso. El acné se ha relacionado con una mayor exposición a la testosterona, DHT y dehidroepiandrosterona (DHEA), y tales andrógenos parecen ser esenciales para que se produzca el acné, ya que el acné no se desarrolla en individuos con síndrome de insensibilidad completa a los andrógenos (CAIS). Por tanto, dirigirse a AR de una manera que reduzca, suprima o elimine sus capacidades de señalización evitará la progresión de factores que impulsan afecciones, enfermedades y trastornos de la piel, como el acné u otra afección, enfermedad o trastorno de la piel mediada por señales de AR.
Además de ser uno de los trastornos de la piel más comunes, el acné también es un componente cardinal de muchas enfermedades o síndromes sistémicos. Su asociación ilustra la naturaleza de estas enfermedades y es indicativa de la patogenia del acné. La hiperplasia suprarrenal congénita (CAH) y el síndrome de seborrea-acnéhirsutismo-alopecia androgenética (SAHA) destacan el papel de los esteroides andrógenos, mientras que los síndromes de ovario poliquístico (PCO) e hiperandrogenismo-resistencia a la insulina-acantosis nigricans (HAIR-AN) indican resistencia a la insulina en acné. El síndrome de Apert con señalización del receptor 2 del factor de crecimiento de fibroblastos (FGFR2) aumentado produce hiperqueratinización folicular e hipertrofia de las glándulas sebáceas en el acné. Los síndromes de sinovitis-acné-pustulosis-hiperostosis-osteítis (SAPHO) y artritis piógenapioderma gangrenoso-acné (PAPA) destacan los atributos de la inflamación para la formación del acné.
La presente memoria descriptiva divulga eliminadores de receptores de andrógenos (ARE) tripartitos que comprenden un antagonista de AR enlazado a una molécula que marca el antagonista de AR para la degradación de la proteasoma. Por tanto, los ARE divulgados tienen la capacidad tanto de antagonizar la actividad de AR como de
desencadenar la degradación de este receptor. Los ARE divulgados en la presente penetran eficazmente en la piel y/o el cuero cabelludo cuando se aplican tópicamente para desencadenar la depuración celular de AR, dando como resultado de este modo el tratamiento de afecciones, enfermedades y trastornos de la piel y el cabello mediados por la señalización de AR incluyendo, sin limitación, problemas del cabello como la alopecia androgénica e hirsutismo facial y/o problemas de la piel como acné, producción excesiva de sebo y formación de cicatrices posteriores a la herida.
Sin querer estar limitados por ninguna teoría en particular, se cree que los ARE divulgados, las composiciones que comprenden uno o más ARE y los métodos y usos de tales composiciones reducen o previenen una afección, enfermedad o trastorno del cabello mediado por la señalización de AR para reducir o prevenir la caída del cabello, el debilitamiento del cabello y/o la pérdida del color del cabello mediada por la señalización AR. Esto puede lograrse, sin limitación, reduciendo, suprimiendo o inhibiendo la señalización de AR en un folículo piloso, reduciendo o eliminando AR en el citoplasma de un folículo y/o papila dérmica, induciendo un folículo piloso en la fase anágena y/o estimulando las células de la matriz para formar un nuevo tallo piloso, prolongando el período de tiempo que un folículo piloso permanece en fase anágena permitiendo de este modo que el folículo produzca un tallo piloso más largo y/o más grueso, aumentando el depósito de queratina produciendo de este modo un cabello más largo y/o más grueso, aumentando el depósito de melanina oscureciendo de este modo el color del tallo del cabello, previniendo o prolongando la fase catágena aumentando de este modo el tiempo que un cabello permanece en un folículo, prolongando el período de tiempo que un folículo capilar permanece en fase telógena aumentando de este modo el tiempo que un cabello permanece en un folículo, evitando que el folículo entre en la fase exógena, deteniendo de este modo la liberación del tallo piloso, deteniedo la liberación del tallo piloso en la fase exógena aumentando de este modo el número de cabellos y /o estimulando el crecimiento de nuevos cabellos permitiendo de este modo la producción de dos o más cabellos por folículo, y/o aumentando la conversión de cabellos intermedios en cabellos terminales. Por lo tanto, en cualquier momento dado durante el tratamiento, hay más pelos en los folículos y disminución de la caída del cabello. El resultado no es solo un aumento en la longitud, espesor y/u oscuridad de los cabellos, sino también un aumento en el número y/o densidad de los pelos.
Además, sin desear estar limitados por ninguna teoría en particular, se cree que los ARE divulgados, las composiciones que comprenden uno o más ARE y los métodos y usos de tales composiciones reducen o previenen una afección, enfermedad o trastorno de la piel mediado por la señalización de AR. Esto puede lograrse, sin limitación, reduciendo, suprimiendo o inhibiendo la señalización de AR en un folículo piloso y reduciendo o eliminando AR en el citoplasma de una célula. Por lo tanto, en cualquier momento dado durante el tratamiento, los síntomas o atributos no deseados de una afección, enfermedad o trastorno de la piel se reducen, suprimen o eliminan.
La presente memoria descriptiva divulga, en parte, un eliminador del receptor de andrógenos tripartito (ARE). Un ARE comprende un antagonista de AR, una molécula conectora y un promotor de la eliminación o elemento potenciador de la eliminación de AR. Como se divulga en general en la presente, un ARE tiene la fórmula I:
ARA-L-EE (I)
en donde ARA es un antagonista de AR, L es una molécula conectora y EE es un promotor de la eliminación o un elemento potenciador de la eliminación de AR.
La presente memoria descriptiva divulga, en parte, un antagonista del receptor de AR. Un antagonista de AR, también llamado bloqueador de AR, reduce o previene las respuestas mediadas por agonistas mediadas por un AR, en lugar de provocar una respuesta biológica por sí mismo tras unirse a un AR. Por tanto, un antagonista de AR tiene afinidad pero no eficacia por su AR afín, y la unión alterará la interacción e inhibirá la función de un agonista de AR o un agonista de AR inverso en un AR. Un antagonista de AR divulgado en la presente puede mediar sus efectos uniéndose a un sitio ortostérico activo o uniéndose a un sitio alostérico en un AR, o un antagonista de AR divulgado en la presente puede interactuar en sitios de unión únicos que normalmente no están implicados en la regulación biológica de la actividad de AR. Un antagonista de AR divulgado en la presente puede ser reversible o irreversible dependiendo de la longevidad del complejo antagonista-receptor que, a su vez, depende de la naturaleza de la unión del antagonista-receptor. Sin desear estar limitados por ninguna teoría, la degradación de AR en las células puede desencadenarse alterando el complejo HSP90/AR en el citoplasma, provocando de este modo la depuración de AR a través de la proteasoma.
Un antagonista de AR divulgado en la presente es flutamida, nilutamida, bicalutamida, enzalutamida, apalutamida, acetato de ciproterona, acetato de megestrol, acetato de clormadinona, espironolactona, canrenona, drospirenona, cetoconazol, topilutamida (fluridil) o cimetidina. Un antagonista de AR divulgado en la presente es espironolactona, cetoconazol, metoxibencil lactama, RU58841 o Compuesto ARA1. En los compuestos de la invención reivindicada, un antagonista de AR es espironolactona o cetoconazol.
Otros antagonistas útiles como antagonista de AR divulgados en la presente se describen, por ejemplo, en la Patente de Estados Unidos 6.790.979; Patente de Estados Unidos 8.198.323; Hu, et al., Synthesis and Biological Evaluation of Amino-Pyridines as Androgen Receptor Antagonists for Stimulating Hair Growth and Reducing Sebum Production, Bioorg. Med. Chem. Lett. 17: 5693-5697 (2007); Hu, et al., (1R,2S)-4-(2-Cyano-cydohexyl-oxy)-2-trifluoromethy 1-benzonittile, a Potent Androgen Receptor Antagonists for Stimulating Hair Growth and Reducing Sebum Production, Bioorg. Med. Chem. Lett. 17: 5983-5988 (2007); Mitchell, et al., Rational Design of a Topical Androgen Receptor Antagonist for the Suppression of Sebum. Production with Properties Suitable for Follicular Delivery, J. Med. Chem. 53: 4422-4427 (2010). También hay que señalar que M. Toure, Angew. Chemie, 2015, 55(6), págs. 1966-1973 divulga un compuesto tripartito que comprende un agonista de AR RU59063, acoplado por un conector PEG a una fracción de adamantano como promotor de la eliminación o elemento potenciador de la eliminación de AR para su uso en el tratamiento del cáncer.
La presente memoria descriptiva divulga, en parte, un conector. Un conector divulgado en la presente es una molécula que une directa o indirectamente un antagonista del receptor de andrógenos a un promotor de la eliminación o un elemento potenciador de la eliminación de AR. Típicamente, esta unión es una unión covalente.
Una molécula conectora puede ser de fórmula II:
donde R1 y R2 son cada uno independientemente H, OH, COOH, NH2, R3OH, R3COOH, OR3OH, OR3COOH, R3NH(CO)R4, R3NH(CO)R4OH, R3NH(CO)R4COOH; R3 y R4 son cada uno independientemente alquilo C1-10, alquenilo C2-10 o alquinilo C2-10; y n cualquier número entero de 0 a 10. Un grupo funcional alquilo que comprende un hidrocarburo de cadena lineal o de cadena ramificada enlazado exclusivamente por enlaces simples y que no tiene ninguna estructura cíclica. Un grupo funcional alquenilo que comprende un hidrocarburo de cadena lineal o de cadena ramificada que tiene uno o más enlaces dobles carbono-carbono y que no tiene ninguna estructura cíclica. Un grupo funcional alquinilo que comprende un hidrocarburo de cadena lineal o de cadena ramificada que tiene uno o más enlaces triples carbono-carbono y que no tiene ninguna estructura cíclica.
Una molécula conectora divulgada en la presente es de fórmula II, en donde R1 y R2 son cada uno independientemente H, OH, COOH, NH2, R3OH, R3COOH, OR3OH, OR3COOH, R3NH(CO)R4, R3NH(CO)R4OH, o R3NH(CO)R4COOH; R3 y R4 son cada uno independientemente alquilo C1-6, alquenilo C2-6 o alquinilo C2-6; y n cualquier número entero de 0 a 10. Una molécula conectora divulgada en la presente es de fórmula II, en donde R1 y R2 son cada uno independientemente H, OH, COOH, NH2, R3OH, R3COOH, OR3OH, OR3COOH, R3NH(CO)R4, R3NH(CO)R4OH, o R3Nh (CO)R4COOH; R3 y R4 son cada uno independientemente alquilo C1-4, alquenilo C2-4 o alquinilo C2-4; y n cualquier número entero de 0 a 5. Una molécula divulgada en la presente es de fórmula II, en donde R1 y R2 son cada uno independientemente H, OH, COOH, NH2, R3OH, R3COOH, OR3OH, OR3COOH, o R3NH(CO)R4OH; R3 y R4 son cada uno independientemente alquilo C1-10; y n cualquier número entero de 0 a 10. En otros aspectos más de esta realización, una molécula conectora divulgada en la presente es de fórmula II, en donde R1 y R2 son cada uno independientemente H, OH, COOH, NH2, R3OH, R3COOH, OR3OH, OR3COOH, o R3NH(CO)R4OH; R3 y R4 son cada uno independientemente alquilo C1-6; y n cualquier número entero de 0 a 10. En otros aspectos de esta realización, una molécula conectora divulgada en la presente es de fórmula II, en donde R1 y R2 son cada uno independientemente H, OH, COOH, NH2, R3OH, R3COOH, OR3OH, OR3COOH, o R3NH(CO)R4OH; R3 y R4 son cada uno independientemente alquilo C1-6;y n cualquier número entero de 0 a 5.
Una molécula conectora divulgada en la presente puede ser de fórmula II, en donde R1 es OH, COOH, NH2, R3OH, R3COOH o R3NH(CO)R4OH; R2 es OH, COOH, NH2, R3COOH o OR3COOH, R3 y R4 son cada uno independientemente alquilo C1-10; y n cualquier número entero de 0 a 10. Una molécula conectora divulgada en la presente es de fórmula II, en donde R1 es OH, COOH, NH2, R3OH, R3COOH o R3NH(CO)R4OH; R2 es OH, COOH, NH2, R3COOH, o OR3COOH, R3 y R4 son cada uno independientemente alquilo C1-6; y n cualquier número entero de 0 a 10. Una molécula conectora divulgada en la presente es de fórmula II, en donde R1 es OH, COOH, NH2, R3OH, R3COOH o R3NH(CO)R4OH; R2 es OH, COOH, NH2, R3COOH o OR3COOH, R3 y R4 son cada uno independientemente alquilo C1-6; y n cualquier número entero de 0 a 5. Una molécula conectora divulgada en la presente es de fórmula II, en donde R1 es OH, R3OH, R3COOH o R3NH(CO)R4OH; R2 es OH, COOH, NH2, R3COOH o OR3COOH, R3 y R4 son cada uno independientemente alquilo C1-6; y n cualquier número entero de 0 a 5. Una molécula conectora divulgada en la presente es de fórmula II, en donde R1 es OH, R3OH, R3COOH o R3NH(CO)R4OH; R2 es OH, COOH, NH2, R3COOH, o OR3COOH, R3 y R4 son cada uno independientemente alquilo C1-4; y n cualquier número entero de 0 a 4.
Una molécula conectora divulgada en la presente es de fórmula II, en donde R1 es OH, C-C-OH, C-COOH o C-C-NH-CO-CCC-OH; R2 es OH, COOH, NH2, C-COOH u O-C-COOH; y n cualquier número entero de 0 a 10. Una
molécula conectora divulgada en la presente es de fórmula II, en donde R1 es OH, C-C-O H , C-CO O H o C -C -N H -C O -C -C -C -O H ; R2 es OH, COOH, NH2, C-CO O H u O C-CO O H; y n cualquier número entero de 0 a 8. Una molécula conectora divulgada en la presente es de fórmula II, en donde R1 es OH, C-C-O H , C-CO O H o C -C -N H -C O -C -C -C -OH; R2 es OH, COOH, NH2, C-CO O H u O -C-CO O H; y n cualquier número entero de 0 a 6. Una molécula conectora divulgada en la presente es de fórmula II, en donde R1 es OH, C-C-O H , C-CO O H o C -C -N H -C O -C -C -C -O H ; R2 es OH, COOH, NH, C-CO O H u O -C-CO O H ; y n cualquier número entero de 0 a 4.
Una molécula conectora divulgada en la presente es de fórmula III:
en donde n cualquier número entero de 0 a 10. Una molécula conectora divulgada en la presente es de fórmula III, en donde n cualquier número entero de 0 a 8. Una molécula conectora divulgada en la presente es de fórmula III, en donde n es cualquier número entero de 0 a 6. Una molécula conectora divulgada en la presente es de fórmula III, en donde n es cualquier número entero de 0 a 4. Una molécula conectora divulgada en la presente de fórmula III es
Una molécula conectora divulgada en la presente es de fórmula IV:
en donde n es cualquier número entero de 0 a 10. Una molécula conectora divulgada en la presente es de fórmula IV, en donde n es cualquier número entero de 0 a 8. Una molécula conectora divulgada en la presente es de fórmula IV, en donde n es cualquier número entero de 0 a 6. Una molécula conectora divulgada en la presente es de fórmula IV, en donde n es cualquier número entero de 0 a 4. Una molécula conectora divulgada en la presente de fórmula IV es
Una molécula conectora divulgada en la presente es de fórmula V:
en donde n es cualquier número entero de 0 a 10. Una molécula conectora divulgada en la presente es de fórmula V, en donde n es cualquier número entero de 0 a 8. Una molécula conectora divulgada en la presente es de fórmula V, en donde n es cualquier número entero de 0 a 6. Una molécula conectora divulgada en la presente es de fórmula V,
en donde n es cualquier número entero de 0 a 4. Una molécula conectora divulgada en la presente de fórmula V es
Una molécula conectora divulgada en la presente es de fórmula VI:
en donde n es cualquier número entero de 0 a 10. Una molécula conectora divulgada en la presente es de fórmula
VI, en donde n es cualquier número entero de 0 a 8. Una molécula conectora divulgada en la presente es de fórmula VI, en donde n es cualquier número entero de 0 a 6. Una molécula conectora divulgada en la presente es de fórmula VI, en donde n es cualquier número entero de 0 a 4. Una molécula conectora divulgada en la presente de fórmula VI es
Una molécula conectora divulgada en la presente es de fórmula VII:
en donde n es cualquier número entero de 0 a 10. Una molécula conectora divulgada en la presente es de fórmula
VII, en donde n es cualquier número entero de 0 a 8. Una molécula conectora divulgada en la presente es de fórmula
VII, en donde n es cualquier número entero de 0 a 6. Una molécula conectora divulgada en la presente es de fórmula
VII, en donde n es cualquier número entero de 0 a 4. Una molécula conectora divulgada en la presente de fórmula
VII es
o
Una molécula conectora divulgada en la presente es de fórmula VIII:
en donde n es cualquier número entero de 0 a 10. Una molécula conectora divulgada en la presente es de fórmula VIII, en donde n es cualquier número entero de 0 a 8. Una molécula conectora divulgada en la presente es de fórmula VIII, en donde n es cualquier número entero de 0 a 6. Una molécula conectora divulgada en la presente es de fórmula VIII, en donde n es cualquier número entero de 0 a 4. Una molécula conectora divulgada en la presente de fórmula VIII es
Una molécula conectora divulgada en la presente es de fórmula IX:
en donde n es cualquier número entero de 0 a 10. Una molécula conectora divulgada en la presente es de fórmula IX, en donde n es cualquier número entero de 0 a 8. Una molécula conectora divulgada en la presente es de fórmula IX, en donde n es cualquier número entero de 0 a 6. Una molécula conectora divulgada en la presente es de fórmula IX, en donde n es cualquier número entero de 0 a 4. Una molécula conectora divulgada en la presente de fórmula IX es
o
Una molécula conectora divulgada en la presente tiene la fórmula X:
en donde n es cualquier número entero de 0 a 10 Una molécula conectora divulgada en la presente es de fórmula X, en donde n es cualquier número entero de 0 a 8. Una molécula conectora divulgada en la presente es de fórmula X, en donde n es cualquier número entero de 0 a 6. Una molécula conectora divulgada en la presente es de fórmula X, en donde n es cualquier número entero de 0 a 4. Una molécula conectora divulgada en la presente de fórmula X es
La presente memoria descriptiva divulga, en parte, un promotor de la eliminación o un elemento potenciador de la eliminación de AR. Un promotor de la eliminación o elemento potenciador de la eliminación de AR divulgado en la presente se dirige, induce, facilita o marca de otro modo un polipéptido enlazado al promotor de la eliminación o elemento potenciador de la eliminación de AR como un polipéptido que debe degradarse, destruirse o volverse de otro modo inactivo o no funcional. En una realización, un promotor de la eliminación o un elemento potenciador de la eliminación de AR divulgado en la presente se dirige, facilita o marca de otro modo un polipéptido para la vía de degradación proteasómica. En un aspecto de esta realización, un promotor de la eliminación o un elemento potenciador de la eliminación de AR divulgado en la presente se dirige, facilita o marca de otro modo un polipéptido para la degradación por una proteasoma usando una vía independiente de ubiquitina. En otro aspecto de esta realización, un promotor de la eliminación o un elemento potenciador de la eliminación de AR divulgado en la presente se dirige, facilita o marca de otro modo un polipéptido para la degradación por una proteasoma usando una vía dependiente de ubiquitina.
Un promotor de la eliminación o un elemento potenciador de la eliminación de AR puede ser una etiqueta hidrófoba. Una etiqueta hidrófoba es una molécula que parece desestabilizar un polipéptido, dando como resultado de este modo el reclutamiento de una o más chaperonas en un polipéptido desplegado. La proteína desestabilizada luego se transporta a los proteosomas donde se degrada. La degradación usando una etiqueta hidrófoba parece ser un proceso independiente de la ubiquitina. Los ejemplos de una etiqueta hidrófoba son una fracción de adamantano y un aminoácido protegido con carbamato de butilo (Boc).
Una etiqueta hidrófoba es una fracción de adamantano. Una fracción de adamantano divulgada en la presente comprende un cicloalcano C10H16 dispuesto en una configuración de "sillón" de cuatro anillos de ciclohexano conectados. También puede existir una configuración en forma de barco. En aspectos de esta realización, un adamantano es de fórmula XI:
en donde R5 es H, OH, COOH, NH2, un halógeno, R6OH, R6COOH, R6C(O)NH2, o R6C(O)R7; R6 es alquilo C1-10,
alquenilo C2-10 o alquinilo C2-10; y R7 es un halógeno. Un halógeno se refiere a un elemento no metálico que incluye flúor (F), cloro (CI), bromo (Br), yodo (I), astato (At) y ununseptio (Uus). Una fracción de adamantano divulgada en la presente tiene la fórmula XI, en donde R5 es H, Oh , Co Oh , NH2, un halógeno, R6OH, R6COOH, R6C(O)NH2 o R6C(O)R7; R6 es alquilo C1-6, alquenilo C2-6 o alquinilo C2-6; y R7 es un halógeno. Una fracción de adamantano divulgada en la presente tiene la fórmula XI, en donde R5 es H, OH, COOH, NH2, un halógeno, R6OH, R6COOH, R6C(O)NH2 o R6C(O)R7; R6 es alquilo C1-4, alquenilo C2-4 o alquinilo C2-4; y R7 es un halógeno. Una fracción de adamantano divulgada en la presente tiene la fórmula XI, en donde R5 es H, OH, COOH, NH2, F, Br, CI, I, R6OH, R6COOH, R6C(O)NH2 o R6C(O)R7; R6 es alquilo C1-6, alquenilo C2-6 o alquinilo C2-6; y R7 es un F, Br, CI o I. Una fracción de adamantano divulgada en la presente de fórmula XI es
Una etiqueta hidrófoba divulgada pero no reivindicada es un aminoácido protegido con Boc. Un aminoácido protegido con Boc induce la degradación de proteínas aprovechando la vía de la regla del extremo N, donde la vida media de un polipéptido está determinada por el aminoácido N-terminal específico presente. Los siguientes aminoácidos confieren todos una vida media de menos de 90 minutos a un polipéptido: glutamina, arginina, ácido glutámico, fenilalanina, ácido aspártico, cisteína, lisina y asparagina. En aspectos de esta realización, una etiqueta hidrófoba es una fracción de arginina protegida con carbamato de terc-butilo (BOC3Arg), una fracción de lisina protegida con carbamato de isobutilo (BOC2Lys), una fracción de ácido aspártico protegida con carbamato de isobutilo (BOC2Asp), una asparagina protegida con carbamato de iso-butilo (BOC2Asn), una fracción de ácido glutámico protegido con carbamato de isobutilo (BOC2Glu) y una fracción de glutamina protegida con carbamato de isobutilo (BOC2Gln). En aspectos de esta realización, una etiqueta hidrófoba es
Etiquetas hidrófobas adicionales útiles como promotores de la eliminación o elementos potenciadores de la eliminación de AR descritos en la presente se describen, por ejemplo, en Neklesa, et al., Small-Molecule Hydrophobic Tagging Induced Degradation of HaloTag Fusion Proteins, Nat. Chem. Biol. 7(8): 538-543 (2012).
Como se divulga pero no se reivindica en la presente, un promotor de la eliminación o un elemento potenciador de la eliminación de AR es una fracción reclutadora de ligasa E3. Una fracción reclutadora de ligasa E3 recluta una ligasa E3 de ubiquitina para ubiquitilar un polipéptido de interés, lo que hace que todo el complejo se degrade a través de la vía de ubiquitinación. La degradación usando una fracción reclutadora de ligasa E3 es un proceso dependiente de la ubiquitina.
Como se divulga pero no se reivindica en la presente, una fracción reclutadora de ligasa E3 es un factor 1a inducible por hipoxia (HIF-1a). Una fracción HIF-1a reconoce una prolina central hidroxilada en una secuencia de reconocimiento de siete aminoácidos del factor 1a inducible por hipoxia (HIF-1a). La fracción AHIF-1a es la fórmula XII
en donde R8 es H, OH, COOH, NH2, un halógeno, R9OH, R9COOH, R9C(O)NH2, o R9C(O)R10; R9 es alquilo C1-10, alquenilo C2-10 o alquinilo C2-10; y R10 es un halógeno. Una fracción de HIF-1a divulgada en la presente tiene la fórmula XII, en donde R8 es H, OH, COOH, NH2, un halógeno, R9OH, R9COOH, R9C(O)NH2, o R9C(O)R10; R9 es alquilo C1-6, alquenilo C2-6 o alquinilo C2-6; y R10 es un halógeno. Una fracción de HIF-1a divulgada en la presente tiene la fórmula XII, en donde R8 es H, OH, COOH, NH2, un halógeno, R9OH, R9COOH, R9C(O)NH2, o R9C(O)R10; R9 es alquilo C1-4, alquenilo C2-4 o alquinilo C 2-4; y R10 es un halógeno. Una fracción de HIF-1 a divulga en la presente es de fórmula XII, en donde R8 es H, OH, COOH, NH2, F, Br, CI, I, R9OH, R9COOH, R9C(O)NH2 o R9C(O)R10; R9 es alquilo C1-6, alquenilo C2-6 o alquinilo C2-6; y R10 es un F, Br, CI o I. Una fracción de HIF-1 a divulgada en la presente de fórmula XII es
Como se divulga pero no se reivindica en la presente, una fracción reclutadora de ligasa E3 es una fracción Nutlin. Una fracción de Nutlin es un análogo de cis-imidazolina que inhibe la interacción entre el doble minuto 2 de ratón (MDM2) y el supresor tumoral p53. Una fracción Nutlin incluye una fracción Nutlin-1, una fracción Nutlin-2 y una fracción Nutlin-3. Una fracción de Nutlin es la fórmula XIII
en donde R11 es H, OH, COOH, NH2, un halógeno, R12OH, R12COOH, R12C(O)NH2, o R12C(O)R13; R12 es alquilo Ci-10, alquenilo C2-10 o alquinilo C2-10; y R13 es un halógeno. Una fracción Nutlin divulgada en la presente es de fórmula XIII, en donde R11 es H, OH, COOH, NH2, un halógeno, R12OH, R12COOH, R12C(O)NH2, o R12C(O)R13; R12 es alquilo C1-6, alquenilo C2-6 o alquinilo C2-6; y R13 es un halógeno. Una fracción Nutlin divulgada en la presente es de fórmula XIII, en donde R11 es H, OH, COOH, NH2, un halógeno, R12OH, R12COOH, R12C(O)NH2, o R12C(O)R13; R12 es alquilo C1-4, alquenilo C2-4 o alquinilo C2-4; y R13 es un halógeno. Una fracción Nutlin divulgada en la presente es de fórmula XIII, en donde R11 es H, OH, COOH, NH2, F, Br, CI, I, R12OH, R12COOH, R12C(O)NH2 o R12C(O)R13; R12 es alquilo C1-6, alquenilo C2-6 o alquinilo C2-6; y R13 es un F, Br, CI o I.
Como se divulga pero no se reivindica en la presente, una fracción reclutadora de ligasa E3 es una fracción de bestatina. Una fracción de bestatina (también conocida como ubenimex) es un inhibidor de proteasa competitivo y reversible. En un aspecto de esta realización, una fracción de bestatina es la fórmula XIV
en donde R14 es H, OH, COOH, NH2, un halógeno, R15OH, R15COOH, R15C(O)NH2, o R15C(O)R16; R15 es alquilo C1-10, alquenilo C2-10 o alquinilo C2-10; y R16 es un halógeno. Una fracción de bestatina divulgada en la presente es de fórmula XIV, en donde R14 es H, OH, COOH, NH2, un halógeno, R15OH, R15COOH, R15C(O)NH2, o R15C(O)R16; R15 es alquilo C1-6, alquenilo C2-6 o alquinilo C2-6; y R16 es un halógeno. Una fracción de bestatina divulgada en la presente es de fórmula XIV, en donde R14 es H, OH, COOH, NH2, un halógeno, R15OH, R15COOH, R15C(O)NH2, o R15C(O)R16; R15 es alquilo C1-4, alquenilo C2-4 o alquinilo C2-4; y R16 es un halógeno. Una fracción de bestatina divulgada en la presente es de fórmula XIV, en donde R14 es H, OH, COOH, NH2, F, Br, Cl, I, R15OH, R15COOH, R15C(O)NH2, o R15C(O)R16; R15 es alquilo C1-6, alquenilo C2-6 o alquinilo C2-6; y R16 es F, Br, Cl o I.
Como se divulga pero no se reivindica en la presente, una fracción reclutadora de ligasa E3 es una fracción de ftalimida. Una fracción de ftalimida es un inhibidor de proteasa reversible y competitivo. Una fracción de ftalimida es una molécula que comprende una ftalimida, C6H4(CO)2NH. Una fracción de ftalimida incluye talidomida, lenalidomida y pomalidomida. Una fracción de ftalimida es la fórmula XV
en donde R17 es H, OH, COOH, NH2, un halógeno, R19OH, R19COOH, R19C(O)NH2, o R19C(O)R20, NHR19OH,
NHR19COOH, NHR19C(O)NH2, o NHR19C(O)R20; R18 es H, OH, O, COOH o Ci -6; R19 es alquilo C1-10, alquenilo C2-10 o alquinilo C2-10; y R20 es un halógeno. Una fracción de ftalimida divulgada en la presente tiene la fórmula XV, en donde R17 es H, OH, COOH, NH2, un halógeno, R19OH, R19COOH, R19C(O)NH2, o R19C(O)R20, NHR19OH, NHR19COOH, NHR19C(O)NH2 o NHR19C(O)R20; R18 es H, OH, O, COOH o C1-6; R19 es alquilo C1-6, alquenilo C2-6 o alquinilo C2-6; y R20 es un halógeno. Una fracción de ftalimida divulgada en la presente tiene la fórmula XV, en donde R17 es H, OH, COOH, NH2, un halógeno, R19OH, R19COOH, R19C(O)NH2, o R19C(O)R20, NHR19OH, NHR19COOH, NHR19C(O)NH2 o NHR19C(O)R20; R18 es H, OH, O, COOH o C1-6; R19 es alquilo C1-4, alquenilo C2-4 o alquinilo C2-4; y R20 es un halógeno. Una fracción de ftalimida divulgada en la presente tiene la fórmula XV, en donde R17 es H, OH, COOH, NH2, F, Br, CI, I, R19OH, R19COOH, R19C(O)NH2, o R19C(O)R20, NHR19OH, NHR19COOH, NHR19C(O)NH2 o NHR19C(O)R20; R18 es H, OH, O, COOH o C1-6; R19 es alquilo C1-6, alquenilo C2-6 o alquinilo C2-6; y R20 es un F, Br, CI o I.
Una fracción de ftalimida es cualquiera de las fórmulas XVI, XVII, XVIII o XIX.
en donde R20 es H, OH, COOH, NH2, un halógeno, R21OH, R21COOH, R21C(O)NH2, o R21C(O)R22; R21 es alquilo C1-10, alquenilo C2-10 o alquinilo C2-10; y R22 es un halógeno. En aspectos de esta realización, una fracción de ftalimida divulgada en la presente es cualquiera de las fórmulas XVI, XVII, XVIII o XIX, en donde R20 es H, OH, COOH, NH2, un halógeno, R21OH, R21COOH, R21C(O)NH2, o R21C(O)R22; R21 es alquilo C1-6, alquenilo C2-6 o alquinilo C2-6; y R22 es un halógeno. En otros aspectos de esta realización, una fracción de ftalimida divulgada en la presente es cualquiera de las fórmulas XVI, XVII, XVIII o XIX, en donde R20 es H, OH, COOH, NH2, un halógeno, R21OH, R21COOH, R21C(O)NH2, o R21C(O)R22; y R21 es alquilo C1-4, alquenilo C2-4 o alquinilo C2-4; y R22 es un halógeno. En otros aspectos más de esta realización, una fracción de ftalimida divulgada en la presente es cualquiera de las fórmulas XVI, XVII, XVIII o XIX, en donde R20 es H, OH, COOH, NH2, F, Br, CI, I, R21OH, R21COOH, R21C(O)NH2, o R21C(O)R22; y R21 es alquilo C1-6, alquenilo C2-6 o alquinilo C2-6; y R22 es un F, Br, CI o I.
En una realización de la invención reivindicada, un ARE divulgado en la presente tiene la fórmula XX:
en donde n es cualquier número entero de 0 a 10. En aspectos de esta realización, un ARE divulgado en la presente
tiene la fórmula XX, en donde n es cualquier número entero de 0 a 8. En otros aspectos más de esta realización, un ARE divulgado en la presente tiene la fórmula XX, en donde n es cualquier número entero de 0 a 6. En otros aspectos más de esta realización, un ARE divulgado en la presente tiene la fórmula XX, en donde n es cualquier número entero de 0 a 4. En otros aspectos de esta realización, un ARE divulgado en la presente es
En una realización de la invención reivindicada, un ARE divulgado en la presente es:
En una realización de la invención reivindicada, un ARE divulgado en la presente tiene la fórmula XXI:
en donde n es cualquier número entero de 0 a 10. En aspectos de esta realización, un ARE divulgado en la presente tiene la fórmula XXI, en donde n es cualquier número entero de 0 a 8. En otros aspectos más de esta realización, un ARE divulgado en la presente tiene la fórmula XXI, en donde n es cualquier número entero de 0 a 6. En otros aspectos más de esta realización, un ARE divulgado en la presente tiene la fórmula XXI, en donde n es cualquier número entero de 0 a 4. En otros aspectos de esta realización, un ARE divulgado en la presente es
En una realización de la invención reivindicada, un ARE divulgado en la presente es:
Un ARE divulgado pero no reivindicado en la presente es de fórmula XXII:
en donde n es cualquier número entero de 0 a 10. En aspectos de esta realización, un ARE divulgado en la presente tiene la fórmula XXII, en donde n es cualquier número entero de 0 a 8. En otros aspectos más de esta realización, un ARE divulgado en la presente tiene la fórmula XXII, en donde n es cualquier número entero de 0 a 6. En otros aspectos más de esta realización, un ARE divulgado en la presente tiene la fórmula XXII, en donde n es cualquier número entero de 0 a 4. En otros aspectos de esta realización, un ARE divulgado en la presente es
Un ARE divulgado pero no reivindicado en la presente es de fórmula XXIII:
(XXIII)
en donde n es cualquier número entero de 0 a 10. En aspectos de esta realización, un ARE divulgado en la presente tiene la fórmula XXIII, en donde n es cualquier número entero de 0 a 8. En otros aspectos más de esta realización, un ARE divulgado en la presente tiene la fórmula XXIII, en donde n es cualquier número entero de 0 a 6. En otros aspectos más de esta realización, un ARE divulgado en la presente tiene la fórmula XXIII, en donde n es cualquier número entero de 0 a 4. En otros aspectos de esta realización, un ARE divulgado en la presente es
o
Los aspectos de la presente memoria divulgan, en parte, una composición farmacéutica. Una composición farmacéutica se refiere a una concentración terapéuticamente eficaz de un ingrediente activo como, por ejemplo, cualquiera de los ARE divulgados en la presente. Como se reivindica, una composición farmacéutica comprende un compuesto de la invención. Preferiblemente, la composición farmacéutica no produce una reacción adversa, alérgica u otra reacción inconveniente o no deseada cuando se administra a un individuo. Una composición farmacéutica como se divulga en la presente es útil para aplicaciones médicas y veterinarias. Una composición farmacéutica puede administrarse a un individuo sola o en combinación con otros compuestos activos, agentes, fármacos u hormonas complementarios.
En una realización, una composición puede comprender un único ARE divulgado en la presente. En otra realización, una composición puede comprender un solo ARE divulgado en la presente. En aspectos de esta realización, una composición divulgada en la presente comprende, por ejemplo, uno o más ARE, dos o más ARE, tres o más ARE, cuatro o más ARE o cinco o más ARE. En otros aspectos de esta realización, una composición divulgada en la presente comprende, por ejemplo, solo un ARE, como máximo dos ARE, como máximo tres ARE, como máximo cuatro ARE o como máximo cinco ARE. En otros aspectos más de esta realización, una composición divulgada en la presente comprende, por ejemplo, de 1 a 2 ARE, de 1 a 3 ARE, de 1 a 4 ARE, de 1 a 5 ARE, de 2 a 3 ARE, de 2 a 4 ARE, de 2 a 5 ARE, de 3 a 4 ARE, de 3 a 5 ARE o de 4 a 5 ARE.
La cantidad de uno o más ARE en una composición farmacéutica divulgada en la presente variará generalmente de aproximadamente un 0,01% a aproximadamente un 50% en peso de la composición total, preferiblemente de aproximadamente un 0,1% a aproximadamente un 50% en peso de la composición total, más preferiblemente de aproximadamente un 1% a aproximadamente un 50% en peso de la composición total.
En aspectos de esta realización, una composición divulgada en la presente comprende un ARE en una cantidad de, por ejemplo, el 0,01%, 0,025%, 0,05%, 0,075%, 0,1%, 0,2%, 0,25%, 0,3%, 0,4%, 0,5%, 0,6%, 0,7%, 0,75%, 0,8%, 0,9%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% o 50% en peso de la composición. En otros aspectos de esta realización, una composición divulgada en la presente comprende un ARE en una cantidad de, por ejemplo, por lo menos 0,01%, por lo menos el 0,025%, por lo menos el 0,05%, por lo menos el 0,075%, por lo menos el 0,1%, por lo menos el 0,25%, por lo menos el 0,5%, por lo menos el 0,75%, por lo menos el 1%, por lo menos el 2%, por lo menos el 3%, por lo menos el 4%, por lo menos el 5%, por lo menos el 6%, por lo menos el 7%, por lo menos el 8%, por lo menos el 9%, por lo menos el 10%, por lo menos el 15%, por lo menos el 20%, por lo menos el 25%, por lo menos el 30%, por lo menos el 35%, por lo menos el 40%, por lo menos el 45% o por lo menos el 50% en peso de la composición. En otros aspectos más de esta realización, una composición divulgada en la presente comprende un ARE en una cantidad de, por ejemplo, como máximo el 0,01%, como máximo el 0,025%, como máximo el 0,05%, como máximo el 0,075%, como máximo el 0,1%, como máximo el 0,25%, como máximo el 0,5%, como máximo el 0,75%, como máximo el 1%, como máximo el 2%, como máximo el 3%, como máximo el 4%, como máximo el 5%, como máximo el 6%, como máximo el 7%, como máximo el 8%, como máximo el 9%, como máximo el 10%, como máximo el 15%, como máximo el 20%, como máximo el 25%, como máximo el 30%, como máximo el 35%, como máximo el 40%, como máximo el 45%, o como máximo el 50% en peso de la composición
En otros aspectos más de esta realización, una composición divulgada en la presente comprende un ARE en una cantidad de, por ejemplo, del 0,01% a aproximadamente el 0,05%, 0,01% a aproximadamente el 0,075%, 0,01% a aproximadamente el 0,1%, de aproximadamente el 0,1% a aproximadamente el 0,5%, de aproximadamente el 0,1% a aproximadamente el 0,75%, de aproximadamente el 0,1% a aproximadamente el 1%, de aproximadamente el 0,1% a aproximadamente el 2%, de aproximadamente el 0,1% a aproximadamente el 3%, de aproximadamente el 0,1% a aproximadamente el 4%, de aproximadamente el 0,1% a aproximadamente el 5%, de aproximadamente el 0,1% a aproximadamente el 6%, de aproximadamente el 0,1% a aproximadamente el 7%, de aproximadamente el 0,1% a aproximadamente el 8%, de aproximadamente el 0,1% a aproximadamente el 9%, de aproximadamente el 0,1% a aproximadamente el 10%, de aproximadamente el 0,1% a aproximadamente el 15%, de aproximadamente el 0,1% a aproximadamente el 20%, de aproximadamente el 0,1% a aproximadamente el 25%, de aproximadamente el 0,1% a aproximadamente el 30%, de aproximadamente el 0,1% a aproximadamente el 35%, de aproximadamente el 0,1% a aproximadamente el 40%, de aproximadamente el 0,25% a aproximadamente el 0,5%,
de aproximadamente el 0,25% a aproximadamente el 0,75%, de aproximadamente el 0,25% a aproximadamente el 1%, de aproximadamente el 0,25% a aproximadamente el 2%, de aproximadamente el 0,25% a aproximadamente el 3%, de aproximadamente el 0,25% a aproximadamente el 4%, de aproximadamente el 0,25% a aproximadamente el 5%, de aproximadamente el 0,25% a aproximadamente el 6%, de aproximadamente el 0,25% a aproximadamente el 7%, de aproximadamente el 0,25% a aproximadamente el 8%, de aproximadamente el 0,25% a aproximadamente el 9%, de aproximadamente el 0,25% a aproximadamente el 10%, de aproximadamente el 0,25% a aproximadamente el 15%, de aproximadamente el 0,25% a aproximadamente el 20%, de aproximadamente el 0,25% a aproximadamente el 25%, de aproximadamente el 0,25% a aproximadamente el 30%, de aproximadamente el 0,25% a aproximadamente el 35%, de aproximadamente el 0,25% a aproximadamente el 40%, de aproximadamente el 0,5% a aproximadamente el 0,75%, de aproximadamente el 0,5% a aproximadamente el 1%, de aproximadamente el 0,5% a aproximadamente el 2%, de aproximadamente el 0,5% a aproximadamente el 3%, de aproximadamente el 0,5% a aproximadamente el 4%, de aproximadamente el 0,5% a aproximadamente el 5%, de aproximadamente el 0,5% a aproximadamente el 6%, de aproximadamente el 0,5% a aproximadamente el 7%, de aproximadamente el 0,5% a aproximadamente el 8%, de aproximadamente el 0,5% a aproximadamente el 9%, de aproximadamente el 0,5% a aproximadamente el 10%, de aproximadamente el 0,5% a aproximadamente el 15%, de aproximadamente el 0,5% a aproximadamente el 20%, de aproximadamente el 0,5% a aproximadamente el 25% de aproximadamente el 0,5% a aproximadamente el 30%, de aproximadamente el 0,5% a aproximadamente el 35% de aproximadamente el 0,5% a aproximadamente el 40%, de aproximadamente el 0,75% a aproximadamente el 1% de aproximadamente el 0,75% a aproximadamente el 2%, de aproximadamente el 0,75% a aproximadamente el 3% de aproximadamente el 0,75% a aproximadamente el 4%, de aproximadamente el 0,75% a aproximadamente el 5% de aproximadamente el 0,75% a aproximadamente el 6%, de aproximadamente el 0,75% a aproximadamente el 7% de aproximadamente el 0,75% a aproximadamente el 8% de aproximadamente el 0,75% a aproximadamente el 9% de aproximadamente el 0,75% a aproximadamente el 10%, de aproximadamente el 0,75% a aproximadamente el 15%, de aproximadamente el 0,75% a aproximadamente el 20%, de aproximadamente el 0,75% a aproximadamente el 25%, de aproximadamente el 0,75% a aproximadamente el 30%, de aproximadamente el 0,75% a aproximadamente el 35%, de aproximadamente el 0,75% a aproximadamente el 40%, de aproximadamente el 1% a aproximadamente el 2%, de aproximadamente el 1% a aproximadamente el 3%, de aproximadamente el 1% a aproximadamente el 4%, de aproximadamente el 1% a aproximadamente el 5%, de aproximadamente el 1% a aproximadamente el 6%, de aproximadamente el 1% a aproximadamente el 7%, de aproximadamente el 1% a aproximadamente el 8%, de aproximadamente el 1% a el 9%, de aproximadamente el 1% a aproximadamente el 10%, de
aproximadamente el 7% a aproximadamente el 20%, de aproximadamente el 7% a aproximadamente el 25%, de aproximadamente el 7% a aproximadamente el 30%, de aproximadamente el 7% a aproximadamente el 35%, de aproximadamente el 7% a aproximadamente el 40%, de aproximadamente el 8% a aproximadamente el 9%, de aproximadamente el 8% a aproximadamente el 10%, de aproximadamente el 8% a aproximadamente el 15%, de aproximadamente el 8% a aproximadamente el 20%, de aproximadamente el 8% a aproximadamente el 25%, de aproximadamente el 8% a aproximadamente el 30%, de aproximadamente el 8% a aproximadamente el 35%, de aproximadamente el 8% a aproximadamente el 40%, de aproximadamente el 9% a aproximadamente el 10%, de aproximadamente el 9% a aproximadamente el 15%, de aproximadamente el 9% a aproximadamente el 20%, de aproximadamente el 9% a aproximadamente el 25%, de aproximadamente el 9% a aproximadamente el 30%, de aproximadamente el 9% a aproximadamente el 35%, de aproximadamente el 9% a aproximadamente el 40%, de aproximadamente el 10% a aproximadamente el 15%, de aproximadamente el 10% a aproximadamente el 20%, de aproximadamente el 10% a aproximadamente el 25%, de aproximadamente el 10% a aproximadamente el 30%, de aproximadamente el 10% a aproximadamente el 35%, de aproximadamente el 10% a aproximadamente el 40%, de aproximadamente el 10% a aproximadamente el 45%, de aproximadamente el 10% a aproximadamente el 50%, de aproximadamente el 15% a aproximadamente el 20%, de aproximadamente el 15% a aproximadamente el 25%, de aproximadamente el 15% a aproximadamente el 30%, de aproximadamente el 15% a aproximadamente el 35%, de aproximadamente el 15% a aproximadamente el 40%, de aproximadamente el 15% a aproximadamente el 45%, de aproximadamente el 15% a aproximadamente el 50%, de aproximadamente el 20% a aproximadamente el 25%, de aproximadamente el 20% a aproximadamente el 30%, de aproximadamente el 20% a aproximadamente el 35%, de aproximadamente el 20% a aproximadamente el 40%, de aproximadamente el 20% a aproximadamente el 45%, de aproximadamente el 20% a aproximadamente el 50%, de aproximadamente el 25% a aproximadamente el 30%, de aproximadamente el 25% a aproximadamente el 35%, de aproximadamente el 25% a aproximadamente el 40%, de aproximadamente el 25% a aproximadamente el 45%, de aproximadamente el 30% a aproximadamente el 25%, de aproximadamente el 30% a aproximadamente el 35%, de aproximadamente el 30% a aproximadamente el 40%, de aproximadamente el 30% a aproximadamente el 45%, de aproximadamente el 30% a aproximadamente el 50%, de aproximadamente el 35% a aproximadamente el 40%, de aproximadamente el 35% a aproximadamente el 45%, de aproximadamente el 35% a aproximadamente el 50%, de aproximadamente el 40% a aproximadamente el 45%, de aproximadamente el 40% a aproximadamente el 50%, o de aproximadamente el 45% a aproximadamente el 50%, en peso de la composición.
En aspectos de esta realización, una composición divulgada en la presente comprende un ARE en una cantidad de, por ejemplo, aproximadamente 1 pg, aproximadamente 2 pg, aproximadamente 3 pg, aproximadamente 4 pg, aproximadamente 5 pg, aproximadamente 6 pg, aproximadamente 7 pg, aproximadamente 8 pg, aproximadamente 9 pg, aproximadamente 10 pg, aproximadamente 15 pg, aproximadamente 20 pg, aproximadamente 25 pg, aproximadamente 30 pg, aproximadamente 35 pg, aproximadamente 40 pg, aproximadamente 45 pg, aproximadamente 50 pg, aproximadamente 55 pg, aproximadamente 60 pg, aproximadamente 65 pg, aproximadamente 70 pg, aproximadamente 75 pg, aproximadamente 80 pg, aproximadamente 85 pg, aproximadamente 90 pg, aproximadamente 95 pg, aproximadamente 100 pg, aproximadamente 110 pg, aproximadamente 120 pg, aproximadamente 130 pg, aproximadamente 140 pg, aproximadamente 150 pg, aproximadamente 160 pg, aproximadamente 170 pg, aproximadamente 180 pg, aproximadamente 190 pg, aproximadamente 200 pg, aproximadamente 210 pg, aproximadamente 220 pg, aproximadamente 230 pg, aproximadamente 240 pg, aproximadamente 250 pg, 260 pg, aproximadamente 270 pg, aproximadamente 280 pg, aproximadamente 290 pg, aproximadamente 300 pg, aproximadamente 310 pg, aproximadamente 320 pg, aproximadamente 330 pg, aproximadamente 340 pg, aproximadamente 350 pg, 360 pg, aproximadamente 370 pg, aproximadamente 380 pg, aproximadamente 390 pg, aproximadamente 400 pg, aproximadamente 410 pg, aproximadamente 420 pg, aproximadamente 430 pg, aproximadamente 440 pg, aproximadamente 450 pg, 460 pg, aproximadamente 470 pg, aproximadamente 480 pg, aproximadamente 490 pg, aproximadamente 500 pg, aproximadamente 510 pg, aproximadamente 520 pg, aproximadamente 530 pg, aproximadamente 540 pg, aproximadamente 550 pg, 560 pg, aproximadamente 570 pg, aproximadamente 580 pg, aproximadamente 590 pg, aproximadamente 600 pg, aproximadamente 610 pg, aproximadamente 620 pg, aproximadamente 630 pg, aproximadamente 640 pg, aproximadamente 650 pg, 660 pg, aproximadamente 670 pg, aproximadamente 680 pg, aproximadamente 690 pg, aproximadamente 700 pg, aproximadamente 710 pg, aproximadamente 720 pg, aproximadamente 730 pg, aproximadamente 740 pg, aproximadamente 750 pg, 760 pg, aproximadamente 770 pg, aproximadamente 780 pg, aproximadamente 790 pg, aproximadamente 800 pg, aproximadamente 810 pg, aproximadamente 820 pg, aproximadamente 830 pg, aproximadamente 840 pg, aproximadamente 850 pg, 860 pg, aproximadamente 870 pg, aproximadamente 880 pg, aproximadamente 890 pg, aproximadamente 900 pg, aproximadamente 910 pg, aproximadamente 920 pg, aproximadamente 930 pg, aproximadamente 940 pg, aproximadamente 950 pg, 960 pg, aproximadamente 970 pg, aproximadamente 980 pg, aproximadamente 990 pg, o aproximadamente 1.000 pg.
En otros aspectos de esta realización, una composición divulgada en la presente comprende un ARE en una cantidad de, por ejemplo, por lo menos 1 pg, por lo menos 2 pg, por lo menos 3 pg, por lo menos 4 pg, por lo menos 5 pg, por lo menos 6 pg, por lo menos 7 pg, por lo menos 8 pg, por lo menos 9 pg, por lo menos 10 pg, por lo menos 15 pg, por lo menos 20 pg, por lo menos 25 pg, por lo menos 30 pg, por lo menos 35 pg, por lo menos 40 pg, por lo menos 45 pg, por lo menos 50 pg, por lo menos 55 pg, por lo menos 60 pg, por lo menos 65 pg, por lo menos
70 gg, por lo menos 75 gg, por lo menos 80 gg, por lo menos 85 gg, por lo menos 90 gg, por lo menos 95 gg, por lo menos 100 gg, por lo menos 110 gg, por lo menos 120 gg, por lo menos 130 gg, por lo menos 140 gg, por lo menos 150 gg, por lo menos 160 gg, por lo menos 170 gg, por lo menos 180 gg, por lo menos 190 gg, por lo menos 200 gg, por lo menos 210 gg, por lo menos 220 gg, por lo menos 230 gg, por lo menos 240 gg, por lo menos 250 gg, 260 gg, por lo menos 270 gg, por lo menos 280 gg, por lo menos 290 gg, por lo menos 300 gg, por lo menos 310 gg, por lo menos 320 gg, por lo menos 330 gg, por lo menos 340 gg, por lo menos 350 gg, 360 gg, por lo menos 370 gg, por lo menos 380 gg, por lo menos 390 gg, por lo menos 400 gg, por lo menos 410 gg, por lo menos 420 gg, por lo menos 430 gg, por lo menos 440 gg, por lo menos 450 gg, 460 gg, por lo menos 470 gg, por lo menos 480 gg, por lo menos 490 gg, por lo menos 500 gg, por lo menos 510 gg, por lo menos 520 gg, por lo menos 530 gg, por lo menos 540 gg, por lo menos 550 gg, 560 gg, por lo menos 570 gg, por lo menos 580 gg, por lo menos 590 gg, por lo menos 600 gg, por lo menos 610 gg, por lo menos 620 gg, por lo menos 630 gg, por lo menos 640 gg, por lo menos 650 gg, 660 gg, por lo menos 670 gg, por lo menos 680 gg, por lo menos 690 gg, por lo menos 700 gg, por lo menos 710 gg, por lo menos 720 gg, por lo menos 730 gg, por lo menos 740 gg, por lo menos 750 gg, 760 gg, por lo menos 770 gg, por lo menos 780 gg, por lo menos 790 gg, por lo menos 800 gg, por lo menos 810 gg, por lo menos 820 gg, por lo menos 830 gg, por lo menos 840 gg, por lo menos 850 gg, 860 gg, por lo menos 870 gg, por lo menos 880 gg, por lo menos 890 gg, por lo menos 900 gg, por lo menos 910 gg, por lo menos 920 gg, por lo menos 930 gg, por lo menos 940 gg, por lo menos 950 gg, 960 gg, por lo menos 970 gg, por lo menos 980 gg, por lo menos 990 gg, o por lo menos 1,000 gg.
En otros aspectos más de esta realización, una composición divulgada en la presente comprende un ARE en una cantidad de, por ejemplo, como máximo 1 gg, como máximo 2 gg, como máximo 3 gg, como máximo 4 gg, como máximo 5 gg, como máximo 6 gg, como máximo 7 gg, como máximo 8 gg, como máximo 9 gg, como máximo 10 gg, como máximo 15 gg, como máximo 20 gg, como máximo 25 gg, como máximo 30 gg, como máximo 35 gg, como máximo 40 gg, como máximo 45 gg, como máximo 50 gg, como máximo 55 gg, como máximo 60 gg, como máximo 65 gg, como máximo 70 gg, como máximo 75 gg, como máximo 80 gg, como máximo 85 gg, como máximo 90 gg, como máximo 95 gg, como máximo 100 gg, como máximo 110 gg, como máximo 120 gg, como máximo 130 gg, como máximo 140 gg, como máximo 150 gg, como máximo 160 gg, como máximo 170 gg, como máximo 180 gg, como máximo 190 gg, como máximo 200 gg, como máximo 210 gg, como máximo 220 gg, como máximo 230 gg, como máximo 240 gg, como máximo 250 gg, 260 gg, como máximo 270 gg, como máximo 280 gg, como máximo 290 gg, como máximo 300 gg, como máximo 310 gg, como máximo 320 gg, como máximo 330 gg, como máximo 340 gg, como máximo 350 gg, 360 gg, como máximo 370 gg, como máximo 380 gg, como máximo 390 gg, como máximo 400 gg, como máximo 410 gg, como máximo 420 gg, como máximo 430 gg, como máximo 440 gg, como máximo 450 gg, 460 gg, como máximo 470 gg, como máximo 480 gg, como máximo 490 gg, como máximo 500 gg, como máximo 510 gg, como máximo 520 gg, como máximo 530 gg, como máximo 540 gg, como máximo 550 gg, 560 gg, como máximo 570 gg, como máximo 580 gg, como máximo 590 gg, como máximo 600 gg, como máximo 610 gg, como máximo 620 gg, como máximo 630 gg, como máximo 640 gg, como máximo 650 gg, 660 gg, como máximo 670 gg, como máximo 680 gg, como máximo 690 gg, como máximo 700 gg, como máximo 710 gg, como máximo 720 gg, como máximo 730 gg, como máximo 740 gg, como máximo 750 gg, 760 gg, como máximo 770 gg, como máximo 780 gg, como máximo 790 gg, como máximo 800 gg, como máximo 810 gg, como máximo 820 gg, como máximo 830 gg, como máximo 840 gg, como máximo 850 gg, 860 gg, como máximo 870 gg, como máximo 880 gg, como máximo 890 gg, como máximo 900 gg, como máximo 910 gg, como máximo 920 gg, como máximo 930 gg, como máximo 940 gg, como máximo 950 gg, 960 gg, como máximo 970 gg, como máximo 980 gg, como máximo 990 gg, o como máximo 1.000 gg.
En otros aspectos más de esta realización, una composición divulgada en la presente comprende un ARE en una cantidad de, por ejemplo, de aproximadamente 1 gg a aproximadamente 10 gg, de aproximadamente 1 gg a aproximadamente 20 gg, de aproximadamente 1 gg a aproximadamente 30 gg, de aproximadamente 1 gg a aproximadamente 40 gg, de aproximadamente 1 gg a aproximadamente 50 gg, de aproximadamente 1 gg a aproximadamente 60 gg, de aproximadamente 1 gg a aproximadamente 70 gg, de aproximadamente 1 gg a aproximadamente 80 gg, de aproximadamente 1 gg a aproximadamente 90 gg, de aproximadamente 1 gg a aproximadamente 100 gg, de aproximadamente 1 gg a aproximadamente 110 gg, de aproximadamente 1 gg a aproximadamente 120 gg, de aproximadamente 1 gg a aproximadamente 130 gg, de aproximadamente 1 gg a aproximadamente 140 gg, de aproximadamente 1 gg a aproximadamente 150 gg, de aproximadamente 5 gg a aproximadamente 10 gg, de aproximadamente 5 gg a aproximadamente 20 gg, de aproximadamente 5 gg a aproximadamente 30 gg, de aproximadamente 5 gg a aproximadamente 40 gg, de aproximadamente 5 gg a aproximadamente 50 gg, de aproximadamente 5 gg a aproximadamente 60 gg, de aproximadamente 5 gg a aproximadamente 70 gg, de aproximadamente 5 gg a aproximadamente 80 gg, de aproximadamente 5 gg a aproximadamente 90 gg, de aproximadamente 5 gg a aproximadamente 100 gg, de aproximadamente 5 gg a aproximadamente 110 gg, de aproximadamente 5 gg a aproximadamente 120 gg, de aproximadamente 5 gg a aproximadamente 130 gg, de aproximadamente 5 gg a aproximadamente 140 gg, de aproximadamente 5 gg a aproximadamente 150 gg, de aproximadamente 10 gg a aproximadamente 20 gg, de aproximadamente 10 gg a aproximadamente 30 gg, de aproximadamente 10 gg a aproximadamente 40 gg, de aproximadamente 10 gg a aproximadamente 50 gg, de aproximadamente 10 gg a aproximadamente 60 gg, de aproximadamente 10 gg a aproximadamente 70 gg, de aproximadamente 10 gg a aproximadamente 80 gg, de aproximadamente 10 gg a aproximadamente 90 gg, de aproximadamente 10 gg a aproximadamente 100 gg, de aproximadamente 10 gg a
aproximadamente 110 gg, de aproximadamente 10 gg a aproximadamente 120 gg, de aproximadamente 10 gg a aproximadamente 130 gg, de aproximadamente 10 gg a aproximadamente 140 gg, de aproximadamente 10 gg a aproximadamente 150 gg, de aproximadamente 10 gg a aproximadamente 175 gg, de aproximadamente 10 gg a aproximadamente 200 gg, de aproximadamente 10 gg a aproximadamente 225 gg, de aproximadamente 10 gg a aproximadamente 250 gg, de aproximadamente 25 gg a aproximadamente 50 gg, de aproximadamente 25 gg a aproximadamente 75 gg, de aproximadamente 25 gg a aproximadamente 100 gg, de aproximadamente 25 gg a aproximadamente 125 gg, de aproximadamente 25 gg a aproximadamente 150 gg, de aproximadamente 25 gg a aproximadamente 175 gg, de aproximadamente 25 gg a aproximadamente 200 gg, de aproximadamente 25 gg a aproximadamente 225 gg, de aproximadamente 25 gg a aproximadamente 250 gg, de aproximadamente 50 gg a aproximadamente 75 gg, de aproximadamente 50 gg a aproximadamente 100 gg, de aproximadamente 50 gg a aproximadamente 125 gg, de aproximadamente 50 gg a aproximadamente 150 gg, de aproximadamente 50 gg a aproximadamente 175 gg, de aproximadamente 50 gg a aproximadamente 200 gg, de aproximadamente 50 gg a aproximadamente 225 gg, de aproximadamente 50 gg a aproximadamente 250 gg, de aproximadamente 75 gg a aproximadamente 100 gg, de aproximadamente 75 gg a aproximadamente 125 gg, de aproximadamente 75 gg a aproximadamente 150 gg, de aproximadamente 75 gg a aproximadamente 175 gg, de aproximadamente 75 gg a aproximadamente 200 gg, de aproximadamente 75 gg a aproximadamente 225 gg, o de aproximadamente 75 gg a aproximadamente 250 gg.
En otros aspectos más de esta realización, una composición divulgada en la presente comprende un ARE en una cantidad de, por ejemplo, de aproximadamente 100 gg a aproximadamente 125 gg, de aproximadamente 100 gg a aproximadamente 150 gg de aproximadamente 100 gg a aproximadamente 175 gg de aproximadamente 100 gg a aproximadamente 200 gg de aproximadamente 100 gg a aproximadamente 225 gg de aproximadamente 100 gg a aproximadamente 250 gg de aproximadamente 100 gg a aproximadamente 275 gg de aproximadamente 100 gg a aproximadamente 300 gg de aproximadamente 100 gg a aproximadamente 325 gg de aproximadamente 100 gg a aproximadamente 350 gg de aproximadamente 100 gg a aproximadamente 375 gg de aproximadamente 100 gg a aproximadamente 400 gg de aproximadamente 100 gg a aproximadamente 425 gg de aproximadamente 100 gg a aproximadamente 450 gg de aproximadamente 100 gg a aproximadamente 475 gg de aproximadamente 100 gg a aproximadamente 500 gg de aproximadamente 100 gg a aproximadamente 525 gg de aproximadamente 100 gg a aproximadamente 550 gg de aproximadamente 100 gg a aproximadamente 575 gg de aproximadamente 100 gg a aproximadamente 600 gg de aproximadamente 125 gg a aproximadamente 150 gg de aproximadamente 125 gg a aproximadamente 175 gg de aproximadamente 125 gg a aproximadamente 200 gg de aproximadamente 125 gg a aproximadamente 225 gg de aproximadamente 125 gg a aproximadamente 250 gg de aproximadamente 125 gg a aproximadamente 275 gg de aproximadamente 125 gg a aproximadamente 300 gg de aproximadamente 125 gg a aproximadamente 325 gg de aproximadamente 125 gg a aproximadamente 350 gg de aproximadamente 125 gg a aproximadamente 375 gg de aproximadamente 125 gg a aproximadamente 400 gg de aproximadamente 125 gg a aproximadamente 425 gg de aproximadamente 125 gg a aproximadamente 450 gg de aproximadamente 125 gg a aproximadamente 475 gg de aproximadamente 125 gg a aproximadamente 500 gg de aproximadamente 125 gg a aproximadamente 525 gg de aproximadamente 125 gg a aproximadamente 550 gg de aproximadamente 125 gg a aproximadamente 575 gg de aproximadamente 125 gg a aproximadamente 600 gg de aproximadamente 150 gg a aproximadamente 175 gg de aproximadamente 150 gg a aproximadamente 200 gg de aproximadamente 150 gg a aproximadamente 225 gg de aproximadamente 150 gg a aproximadamente 250 gg de aproximadamente 150 gg a aproximadamente 275 gg de aproximadamente 150 gg a aproximadamente 300 gg de aproximadamente 150 gg a aproximadamente 325 gg de aproximadamente 150 gg a aproximadamente 350 gg de aproximadamente 150 gg a aproximadamente 375 gg de aproximadamente 150 gg a aproximadamente 400 gg de aproximadamente 150 gg a aproximadamente 425 gg de aproximadamente 150 gg a aproximadamente 450 gg de aproximadamente 150 gg a aproximadamente 475 gg de aproximadamente 150 gg a aproximadamente 500 gg de aproximadamente 150 gg a aproximadamente 525 gg de aproximadamente 150 gg a aproximadamente 550 gg de aproximadamente 150 gg a aproximadamente 575 gg de aproximadamente 150 gg a aproximadamente 600 gg de aproximadamente 200 gg a aproximadamente 225 gg de aproximadamente 200 gg a aproximadamente 250 gg de aproximadamente 200 gg a aproximadamente 275 gg de aproximadamente 200 gg a aproximadamente 300 gg de aproximadamente 200 gg a aproximadamente 325 gg de aproximadamente 200 gg a aproximadamente 350 gg de aproximadamente 200 gg a aproximadamente 375 gg de aproximadamente 200 gg a aproximadamente 400 gg de aproximadamente 200 gg a aproximadamente 425 gg de aproximadamente 200 gg a aproximadamente 450 gg de aproximadamente 200 gg a aproximadamente 475 gg de aproximadamente 200 gg a aproximadamente 500 gg de aproximadamente 200 gg a aproximadamente 525 gg de aproximadamente 200 gg a aproximadamente 550 gg de aproximadamente 200 gg a aproximadamente 575 gg de aproximadamente 200 gg a aproximadamente 600 gg de aproximadamente 200 gg a aproximadamente 625 gg de aproximadamente 200 gg a aproximadamente 650 gg de aproximadamente 200 gg a aproximadamente 675 gg de aproximadamente 200 gg a aproximadamente 700 gg de aproximadamente 200 gg a aproximadamente 725 gg de aproximadamente 200 gg a aproximadamente 750 gg de aproximadamente 200 gg a aproximadamente 775 gg de aproximadamente 200 gg a aproximadamente 800 gg de aproximadamente 200 gg a aproximadamente 825 gg de aproximadamente 200 gg a aproximadamente 850 gg de aproximadamente 200 gg a aproximadamente 875 gg de aproximadamente 200 gg a aproximadamente 900 gg de aproximadamente 200 gg a aproximadamente 925 gg de aproximadamente 200 gg a aproximadamente 950 gg de aproximadamente 200 gg a aproximadamente 975 gg, o de aproximadamente 200 gg a aproximadamente 1.000 gg.
En otros aspectos más de esta realización, una composición divulgada en la presente comprende un ARE
en una cantidad de, por ejemplo, de aproximadamente 250 gg a aproximadamente 275 gg, de aproximadamente 250
adamente adamente adamente adamente adamente adamente adamente adamente adamente adamente adamente adamente adamente
de aproximadamente 400 gg a aproximadamente 1.000 gg.
En otros aspectos más de esta realización, una composición divulgada en la presente comprende un ARE
en una cantidad de, por ejemplo, de aproximadamente 500 gg a aproximadamente 525 gg, de aproximadamente 500
adamente adamente adamente adamente adamente adamente adamente
aproximadamente 700 gg a aproximadamente 800 gg, de aproximadamente 700 gg a ap aproximadamente 700 gg a aproximadamente 850 gg, de aproximadamente 700 gg a ap aproximadamente 700 gg a aproximadamente 900 gg, de aproximadamente 700 gg a ap aproximadamente 700 gg a aproximadamente 950 gg, de aproximadamente 700 gg a ap aproximadamente 700 gg a aproximadamente 1,000 gg, de aproximadamente 800 gg a de aproximadamente 800 gg a aproximadamente 850 gg, de aproximadamente adamente 8 de aproximadamente 800 gg a aproximadamente 900 gg, de aproximadamente adamente 9 de aproximadamente 800 gg a aproximadamente 950 gg, de aproximadamente adamente 9 o de aproximadamente 800 gg a aproximadamente 1.000 gg.
En aspectos de esta realización, una composición divulgada en la presente comprende un ARE en una cantidad de, por ejemplo, aproximadamente 1 mg, aproximadamente 2 mg, aproximadamente 3 mg, aproximadamente 4 mg, aproximadamente 5 mg, aproximadamente 6 mg, a aproximadamente 8 mg, aproximadamente 9 mg, aproximadamente 10 mg, aproximadamente 20 mg, aproximadamente 25 mg, aproximadamente 30 mg, a aproximadamente 40 mg, aproximadamente 45 mg, aproximadamente 50 mg, a aproximadamente 60 mg, aproximadamente 65 mg, aproximadamente 70 mg, a aproximadamente 80 mg, aproximadamente 85 mg, aproximadamente 90 mg, a aproximadamente 100 mg, aproximadamente 110 mg, aproximadamente 120 mg, a aproximadamente 140 mg, aproximadamente 150 mg, aproximadamente 160 mg, a aproximadamente 180 mg, aproximadamente 190 mg, aproximadamente 200 mg, a aproximadamente 220 mg, aproximadamente 230 mg, aproximadamente 240 mg, 260 mg, aproximadamente 270 mg, aproximadamente 280 mg, aproximadamente 290 mg, aproximadamente 310 mg, aproximadamente 320 mg, aproximadamente 330 mg, aproximadamente 350 mg, 360 mg, aproximadamente 370 mg, aproximadamente 380 mg, aproximadamente 400 mg, aproximadamente 410 mg, aproximadamente 420 430 mg, aproximadamente 440 mg, aproximadamente 450 mg, 460 mg, aproximadamente ente 480 mg, aproximadamente 490 mg, aproximadamente 500 mg, aproximadamente 510 mg, aproximadamente 530 mg, aproximadamente 540 mg, aproximadamente 550 mg, 570 mg, aproximadamente 580 mg, aproximadamente 590 mg, aproximadamente 600 mg, aproximadamente 620 mg, aproximadamente 630 mg, aproximadamente 640 mg, 660 mg, aproximadamente 670 mg, aproximadamente 680 mg, aproximadamente 690 mg, aproximadamente 710 mg, aproximadamente 720 mg, aproximadamente 730 mg, aproximadamente 750 mg, 760 mg, aproximadamente 770 mg, aproximadamente 780 mg, aproximadamente 800 mg, aproximadamente 810 mg, aproximadamente 820 830 mg, aproximadamente 840 mg, aproximadamente 850 mg, 860 mg, aproximadamente ente 880 mg, aproximadamente 890 mg, aproximadamente 900 mg, aproximadamente 910 920 mg, aproximadamente 930 mg, aproximadamente 940 mg, aproximadamente 950 mg ximadamente mg, aproximadamente 980 mg, aproximadamente 990 mg, o aproximadamente 1.000 mg.
En otros aspectos de esta realización, una composición divulgada en la presente comprende un ARE en una cantidad de, por ejemplo, por lo menos 1 mg, por lo menos 2 mg, por lo menos 3 mg, por lo menos 4 mg, por lo menos 5 mg, por lo menos 6 mg, por lo menos 7 mg, por lo menos 8 mg, por lo menos 9 mg, por lo menos 10 mg, por lo menos 15 mg, por lo menos 20 mg, por lo menos 25 mg, por lo menos 30 mg, por lo menos 35 mg, por lo menos 40 mg, por lo menos 45 mg, por lo menos 50 mg, por lo menos 55 mg, por lo menos 60 mg, por lo menos 65 mg, por lo menos 70 mg, por lo menos 75 mg, por lo menos 80 mg, por lo menos 85 mg, por lo menos 90 mg, por lo menos 95 mg, por lo menos 100 mg, por lo menos 110 mg, por lo menos 120 mg, por lo menos 130 mg, por lo menos 140 mg, por lo menos 150 mg, por lo menos 160 mg, por lo menos 170 mg, por lo menos 180 mg, por lo menos 190 mg, por lo menos 200 mg, por lo menos 210 mg, por lo menos 220 mg, por lo menos 230 mg, por lo menos 240 mg, por lo menos 250 mg, 260 mg, por lo menos 270 mg, por lo menos 280 mg, por lo menos 290 mg, por lo menos 300 mg, por lo menos 310 mg, por lo menos 320 mg, por lo menos 330 mg, por lo menos 340 mg, por lo menos 350 mg, 360 mg, por lo menos 370 mg, por lo menos 380 mg, por lo menos 390 mg, por lo menos 400 mg, por lo menos 410 mg, por lo menos 420 mg, por lo menos 430 mg, por lo menos 440 mg, por lo menos 450 mg, 460 mg, por lo menos 470 mg, por lo menos 480 mg, por lo menos 490 mg, por lo menos 500 mg, por lo menos 510 mg, por lo menos 520 mg, por lo menos 530 mg, por lo menos 540 mg, por lo menos 550 mg, 560 mg, por lo menos 570 mg, por lo menos 580 mg, por lo menos 590 mg, por lo menos 600 mg, por lo menos 610 mg, por lo menos 620 mg, por lo menos 630 mg, por lo menos 640 mg, por lo menos 650 mg, 660 mg, por lo menos 670 mg, por lo menos 680 mg, por lo menos 690 mg, por lo menos 700 mg, por lo menos 710 mg, por lo menos 720 mg, por lo menos 730 mg, por lo menos 740 mg, por lo menos 750 mg, 760 mg, por lo menos 770 mg, por lo menos 780 mg, por lo menos 790 mg, por lo menos 800 mg, por lo menos 810 mg, por lo menos 820 mg, por lo menos 830 mg, por lo menos 840 mg, por lo menos 850 mg, 860 mg, por lo menos 870 mg, por lo menos 880 mg, por lo menos 890 mg, por lo menos 900 mg, por lo menos 910 mg, por lo menos 920 mg, por lo menos 930 mg, por lo menos 940 mg, por lo menos 950 mg,
960 mg, por lo menos 970 mg, por lo menos 980 mg, por lo menos 990 mg, o por lo menos 1.000 mg.
En otros aspectos más de esta realización, una composición divulgada en la presente comprende un ARE
en una cantidad de, por ejemplo, como máximo 1 mg, como máximo 2 mg, como máximo 3 mg, como máximo 4 mg, como máximo 5 mg, como máximo 6 mg, como máximo 7 mg, como máximo 8 mg, como máximo 9 mg, como máximo 10 mg, como máximo 15 mg, como máximo 20 mg, como máximo 25 mg, como máximo 30 mg, como máximo 35 mg, como máximo 40 mg, como máximo 45 mg, como máximo 50 mg, como máximo 55 mg, como máximo 60 mg, como máximo 65 mg, como máximo 70 mg, como máximo 75 mg, como máximo 80 mg, como máximo 85 mg, como máximo 90 mg, como máximo 95 mg, como máximo 100 mg, como máximo 110 mg, como máximo 120 mg, como máximo 130 mg, como máximo 140 mg, como máximo 150 mg, como máximo 160 mg, como máximo 170 mg, como máximo 180 mg, como máximo 190 mg, como máximo 200 mg, como máximo 210 mg, como máximo 220 mg, como máximo 230 mg, como máximo 240 mg, como máximo 250 mg, 260 mg, como máximo 270 mg, como máximo 280 mg, como máximo 290 mg, como máximo 300 mg, como máximo 310 mg, como máximo 320 mg, como máximo 330 mg, como máximo 340 mg, como máximo 350 mg, 360 mg, como máximo 370 mg, como máximo 380 mg, como máximo 390 mg, como máximo 400 mg, como máximo 410 mg, como máximo 420 mg, como máximo 430 mg, como máximo 440 mg, como máximo 450 mg, 460 mg, como máximo 470 mg, como máximo 480 mg, como máximo 490 mg, como máximo 500 mg, como máximo 510 mg, como máximo 520 mg, como máximo 530 mg, como máximo 540 mg, como máximo 550 mg, 560 mg, como máximo 570 mg, como máximo 580 mg, como máximo 590 mg, como máximo 600 mg, como máximo 610 mg, como máximo 620 mg, como máximo 630 mg, como máximo 640 mg, como máximo 650 mg, 660 mg, como máximo 670 mg, como máximo 680 mg, como máximo 690 mg, como máximo 700 mg, como máximo 710 mg, como máximo 720 mg, como máximo 730 mg, como máximo 740 mg, como máximo 750 mg, 760 mg, como máximo 770 mg, como máximo 780 mg, como máximo 790 mg, como máximo 800 mg, como máximo 810 mg, como máximo 820 mg, como máximo 830 mg, como máximo 840 mg, como máximo 850 mg, 860 mg, como máximo 870 mg, como máximo 880 mg, como máximo 890 mg, como máximo 900 mg, como máximo 910 mg, como máximo 920 mg, como máximo 930 mg, como máximo 940 mg, como máximo 950 mg, 960 mg, como máximo 970 mg, como máximo 980 mg, como máximo 990 mg, o como máximo 1.000 mg.
En otros aspectos más de esta realización, una composición divulgada en la presente comprende un ARE en una cantidad de, por ejemplo, de aproximadamente 1 mg a aproximadamente 10 mg, de aproximadamente 1 mg a aproximadamente 20 mg, de aproximadamente 1 mg a aproximadamente 30 mg, de aproximadamente 1 mg a aproximadamente 40 mg, de aproximadamente 1 mg a aproximadamente 50 mg, de aproximadamente 1 mg a aproximadamente 60 mg, de aproximadamente 1 mg a aproximadamente 70 mg, de aproximadamente 1 mg a aproximadamente 80 mg, de aproximadamente 1 mg a aproximadamente 90 mg, de aproximadamente 1 mg a aproximadamente 100 mg, de aproximadamente 1 mg a aproximadamente 110 mg, de aproximadamente 1 mg a aproximadamente 120 mg, de aproximadamente 1 mg a aproximadamente 130 mg, de aproximadamente 1 mg a aproximadamente 140 mg, de aproximadamente 1 mg a aproximadamente 150 mg, de aproximadamente 5 mg a aproximadamente 10 mg, de aproximadamente 5 mg a aproximadamente 20 mg, de aproximadamente 5 mg a aproximadamente 30 mg, de aproximadamente 5 mg a aproximadamente 40 mg, de aproximadamente 5 mg a aproximadamente 50 mg, de aproximadamente 5 mg a aproximadamente 60 mg, de aproximadamente 5 mg a aproximadamente 70 mg, de aproximadamente 5 mg a aproximadamente 80 mg, de aproximadamente 5 mg a aproximadamente 90 mg, de aproximadamente 5 mg a aproximadamente 100 mg, de aproximadamente 5 mg a aproximadamente 110 mg, de aproximadamente 5 mg a aproximadamente 120 mg, de aproximadamente 5 mg a aproximadamente 130 mg, de aproximadamente 5 mg a aproximadamente 140 mg, de aproximadamente 5 mg a aproximadamente 150 mg, de aproximadamente 10 mg a aproximadamente 20 mg, de aproximadamente 10 mg a aproximadamente 30 mg, de aproximadamente 10 mg a aproximadamente 40 mg, de aproximadamente 10 mg a aproximadamente 50 mg, de aproximadamente 10 mg a aproximadamente 60 mg, de aproximadamente 10 mg a aproximadamente 70 mg, de aproximadamente 10 mg a aproximadamente 80 mg, de aproximadamente 10 mg a aproximadamente 90 mg, de aproximadamente 10 mg a aproximadamente 100 mg, de aproximadamente 10 mg a aproximadamente 110 mg, de aproximadamente 10 mg a aproximadamente 120 mg, de aproximadamente 10 mg a aproximadamente 130 mg, de aproximadamente 10 mg a aproximadamente 140 mg, de aproximadamente 10 mg a aproximadamente 150 mg, de aproximadamente 10 mg a aproximadamente 175 mg, de aproximadamente 10 mg a aproximadamente 200 mg, de aproximadamente 10 mg a aproximadamente 225 mg, de aproximadamente 10 mg a aproximadamente 250 mg, de aproximadamente 25 mg a aproximadamente 50 mg, de aproximadamente 25 mg a aproximadamente 75 mg, de aproximadamente 25 mg a aproximadamente 100 mg, de aproximadamente 25 mg a aproximadamente 125 mg, de aproximadamente 25 mg a aproximadamente 150 mg, de aproximadamente 25 mg a aproximadamente 175 mg, de aproximadamente 25 mg a aproximadamente 200 mg, de aproximadamente 25 mg a aproximadamente 225 mg, de aproximadamente 25 mg a aproximadamente 250 mg, de aproximadamente 50 mg a aproximadamente 75 mg, de aproximadamente 50 mg a aproximadamente 100 mg, de aproximadamente 50 mg a aproximadamente 125 mg, de aproximadamente 50 mg a aproximadamente 150 mg, de aproximadamente 50 mg a aproximadamente 175 mg, de aproximadamente 50 mg a aproximadamente 200 mg, de aproximadamente 50 mg a aproximadamente 225 mg, de aproximadamente 50 mg a aproximadamente 250 mg, de aproximadamente 75 mg a aproximadamente 100 mg, de aproximadamente 75 mg a aproximadamente 125 mg, de aproximadamente 75 mg a aproximadamente 150 mg, de aproximadamente 75 mg a aproximadamente 175 mg, de aproximadamente 75 mg a aproximadamente 200 mg, de aproximadamente 75 mg a aproximadamente 225 mg, o de aproximadamente 75 mg a aproximadamente 250 mg.
En otros aspectos más de esta realización, una composición divulgada en la presente comprende un ARE en una cantidad de, por ejemplo, de aproximadamente 100 mg a aproximadamente 125 mg, de aproximadamente
100 mg a aproximadamente 150 mg, de aproximadamente 100 mg a aproximadamente 175 mg, de aproximadamente 100 mg a aproximadamente 200 mg, de aproximadamente 100 mg a aproximadamente 225 mg, de aproximadamente 100 mg a aproximadamente 250 mg, de aproximadamente 100 mg a aproximadamente 275 mg, de aproximadamente 100 mg a aproximadamente 300 mg, de aproximadamente 100 mg a aproximadamente 325 mg, de aproximadamente 100 mg a aproximadamente 350 mg, de aproximadamente 100 mg a aproximadamente 375 mg, de aproximadamente 100 mg a aproximadamente 400 mg, de aproximadamente 100 mg a aproximadamente 425 mg, de aproximadamente 100 mg a aproximadamente 450 mg, de aproximadamente 100 mg a aproximadamente 475 mg, de aproximadamente 100 mg a aproximadamente 500 mg, de aproximadamente 100 mg a aproximadamente 525 mg, de aproximadamente 100 mg a aproximadamente 550 mg, de aproximadamente 100 mg a aproximadamente 575 mg, de aproximadamente 100 mg a aproximadamente 600 mg, de aproximadamente 125 mg a aproximadamente 150 mg, de aproximadamente 125 mg a aproximadamente 175 mg, de aproximadamente 125 mg a aproximadamente 200 mg, de aproximadamente 125 mg a aproximadamente 225 mg, de aproximadamente 125 mg a aproximadamente 250 mg, de aproximadamente 125 mg a aproximadamente 275 mg, de aproximadamente 125 mg a aproximadamente 300 mg, de aproximadamente 125 mg a aproximadamente 325 mg, de aproximadamente 125 mg a aproximadamente 350 mg, de aproximadamente 125 mg a aproximadamente 375 mg, de aproximadamente 125 mg a aproximadamente 400 mg, de aproximadamente 125 mg a aproximadamente 425 mg, de aproximadamente 125 mg a aproximadamente 450 mg, de aproximadamente 125 mg a aproximadamente 475 mg, de aproximadamente 125 mg a aproximadamente 500 mg, de aproximadamente 125 mg a aproximadamente 525 mg, de aproximadamente 125 mg a aproximadamente 550 mg, de aproximadamente 125 mg a aproximadamente 575 mg, de aproximadamente 125 mg a aproximadamente 600 mg, de aproximadamente 150 mg a aproximadamente 175 mg, de aproximadamente 150 mg a aproximadamente 200 mg, de aproximadamente 150 mg a aproximadamente 225 mg, de aproximadamente 150 mg a aproximadamente 250 mg, de aproximadamente 150 mg a aproximadamente 275 mg, de aproximadamente 150 mg a aproximadamente 300 mg, de aproximadamente 150 mg a aproximadamente 325 mg, de aproximadamente 150 mg a aproximadamente 350 mg, de aproximadamente 150 mg a aproximadamente 375 mg, de aproximadamente 150 mg a aproximadamente 400 mg, de aproximadamente 150 mg a aproximadamente 425 mg, de aproximadamente 150 mg a aproximadamente 450 mg, de aproximadamente 150 mg a aproximadamente 475 mg, de aproximadamente 150 mg a aproximadamente 500 mg, de aproximadamente 150 mg a aproximadamente 525 mg, de aproximadamente 150 mg a aproximadamente 550 mg, de aproximadamente 150 mg a aproximadamente 575 mg, de aproximadamente 150 mg a aproximadamente 600 mg, de aproximadamente 200 mg a aproximadamente 225 mg, de aproximadamente 200 mg a aproximadamente 250 mg, de aproximadamente 200 mg a aproximadamente 275 mg, de aproximadamente 200 mg a aproximadamente 300 mg, de aproximadamente 200 mg a aproximadamente 325 mg, de aproximadamente 200 mg a aproximadamente 350 mg, de aproximadamente 200 mg a aproximadamente 375 mg, de aproximadamente 200 mg a aproximadamente 400 mg, de aproximadamente 200 mg a aproximadamente 425 mg, de aproximadamente 200 mg a aproximadamente 450 mg, de aproximadamente 200 mg a aproximadamente 475 mg, de aproximadamente 200 mg a aproximadamente 500 mg, de aproximadamente 200 mg a aproximadamente 525 mg, de aproximadamente 200 mg a aproximadamente 550 mg, de aproximadamente 200 mg a aproximadamente 575 mg, de aproximadamente 200 mg a aproximadamente 600 mg, de aproximadamente 200 mg a aproximadamente 625 mg, de aproximadamente 200 mg a aproximadamente 650 mg, de aproximadamente 200 mg a aproximadamente 675 mg, de aproximadamente 200 mg a aproximadamente 700 mg, de aproximadamente 200 mg a aproximadamente 725 mg, de aproximadamente 200 mg a aproximadamente 750 mg, de aproximadamente 200 mg a aproximadamente 775 mg, de aproximadamente 200 mg a aproximadamente 800 mg, de aproximadamente 200 mg a aproximadamente 825 mg, de aproximadamente 200 mg a aproximadamente 850 mg, de aproximadamente 200 mg a aproximadamente 875 mg, de aproximadamente 200 mg a aproximadamente 900 mg, de aproximadamente 200 mg a aproximadamente 925 mg, de aproximadamente 200 mg a aproximadamente 950 mg, de aproximadamente 200 mg a aproximadamente 975 mg, o de aproximadamente 200 mg a aproximadamente 1.000 mg.
En otros aspectos más de esta realización, una composición divulgada en la presente comprende un ARE en una cantidad de, por ejemplo, de aproximadamente 250 mg a aproximadamente 275 mg, de aproximadamente 250 mg a aproximadamente 300 mg, de aproximadamente 250 mg a aproximadamente 325 mg, de aproximadamente 250 mg a aproximadamente 350 mg, de aproximadamente 250 mg a aproximadamente 375 mg, de aproximadamente 250 mg a aproximadamente 400 mg, de aproximadamente 250 mg a aproximadamente 425 mg, de aproximadamente 250 mg a aproximadamente 450 mg, de aproximadamente 250 mg a aproximadamente 475 mg, de aproximadamente 250 mg a aproximadamente 500 mg, de aproximadamente 250 mg a aproximadamente 525 mg, de aproximadamente 250 mg a aproximadamente 550 mg, de aproximadamente 250 mg a aproximadamente 575 mg, de aproximadamente 250 mg a aproximadamente 600 mg, de aproximadamente 250 mg a aproximadamente 625 mg, de aproximadamente 250 mg a aproximadamente 650 mg, de aproximadamente 250 mg a aproximadamente 675 mg, de aproximadamente 250 mg a aproximadamente 700 mg, de aproximadamente 250 mg a aproximadamente 725 mg, de aproximadamente 250 mg a aproximadamente 750 mg, de aproximadamente 250 mg a aproximadamente 775 mg, de aproximadamente 250 mg a aproximadamente 800 mg, de aproximadamente 250 mg a aproximadamente 825 mg, de aproximadamente 250 mg a aproximadamente 850 mg, de aproximadamente 250 mg a aproximadamente 875 mg, de aproximadamente 250 mg a aproximadamente 900 mg, de aproximadamente 250 mg a aproximadamente 925 mg, de aproximadamente 250 mg a aproximadamente 950 mg, de aproximadamente 250 mg a aproximadamente 975 mg, de aproximadamente 250
mg a aproximadamente 1,000 mg, de aproximadamente 300 mg a aproximadamente 325 mg, de aproximadamente 300 mg a aproximadamente 350 mg, de aproximadamente 300 mg a aproximadamente 375 mg, de aproximadamente 300 mg a aproximadamente 400 mg, de aproximadamente 300 mg a aproximadamente 425 mg, de aproximadamente 300 mg a aproximadamente 450 mg, de aproximadamente 300 mg a aproximadamente 475 mg, de aproximadamente 300 mg a aproximadamente 500 mg, de aproximadamente 300 mg a aproximadamente 525 mg, de aproximadamente 300 mg a aproximadamente 550 mg, de aproximadamente 300 mg a aproximadamente 575 mg, de aproximadamente 300 mg a aproximadamente 600 mg, de aproximadamente 300 mg a aproximadamente 625 mg, de aproximadamente 300 mg a aproximadamente 650 mg, de aproximadamente 300 mg a aproximadamente 675 mg, de aproximadamente 300 mg a aproximadamente 700 mg, de aproximadamente 300 mg a aproximadamente 725 mg, de aproximadamente 300 mg a aproximadamente 750 mg, de aproximadamente 300 mg a aproximadamente 775 mg, de aproximadamente 300 mg a aproximadamente 800 mg, de aproximadamente 300 mg a aproximadamente 825 mg, de aproximadamente 300 mg a aproximadamente 850 mg, de aproximadamente 300 mg a aproximadamente 875 mg, de aproximadamente 300 mg a aproximadamente 900 mg, de aproximadamente 300 mg a aproximadamente 925 mg, de aproximadamente 300 mg a aproximadamente 950 mg, de aproximadamente 300 mg a aproximadamente 975 mg, de aproximadamente 300 mg a aproximadamente 1,000 mg, de aproximadamente 400 mg a aproximadamente 425 mg, de aproximadamente 400 mg a aproximadamente 450 mg, de aproximadamente 400 mg a aproximadamente 475 mg, de aproximadamente 400 mg a aproximadamente 500 mg, de aproximadamente 400 mg a aproximadamente 525 mg, de aproximadamente 400 mg a aproximadamente 550 mg, de aproximadamente 400 mg a aproximadamente 575 mg, de aproximadamente 400 mg a aproximadamente 600 mg, de aproximadamente 400 mg a aproximadamente 625 mg, de aproximadamente 400 mg a aproximadamente 650 mg, de aproximadamente 400 mg a aproximadamente 675 mg, de aproximadamente 400 mg a aproximadamente 700 mg, de aproximadamente 400 mg a aproximadamente 725 mg, de aproximadamente 400 mg a aproximadamente 750 mg, de aproximadamente 400 mg a aproximadamente 775 mg, de aproximadamente 400 mg a aproximadamente 800 mg, de aproximadamente 400 mg a aproximadamente 825 mg, de aproximadamente 400 mg a aproximadamente 850 mg, de aproximadamente 400 mg a aproximadamente 875 mg, de aproximadamente 400 mg a aproximadamente 900 mg, de aproximadamente 400 mg a aproximadamente 925 mg, de aproximadamente 400 mg a aproximadamente 950 mg, de aproximadamente 400 mg a aproximadamente 975 mg, o de aproximadamente 400 mg a aproximadamente 1.000 mg.
En otros aspectos más de esta realización, una composición divulgada en la presente comprende un ARE en una cantidad de, por ejemplo, de aproximadamente 500 mg a aproximadamente 525 mg, de aproximadamente 500 mg a aproximadamente 550 mg, de aproximadamente 500 mg a aproximadamente 575 mg, de aproximadamente 500 mg a aproximadamente 600 mg, de aproximadamente 500 mg a aproximadamente 625 mg, de aproximadamente 500 mg a aproximadamente 650 mg, de aproximadamente 500 mg a aproximadamente 675 mg, de aproximadamente 500 mg a aproximadamente 700 mg, de aproximadamente 500 mg a aproximadamente 725 mg, de aproximadamente 500 mg a aproximadamente 750 mg, de aproximadamente 500 mg a aproximadamente 775 mg, de aproximadamente 500 mg a aproximadamente 800 mg, de aproximadamente 500 mg a aproximadamente 825 mg, de aproximadamente 500 mg a aproximadamente 850 mg, de aproximadamente 500 mg a aproximadamente 875 mg, de aproximadamente 500 mg a aproximadamente 900 mg, de aproximadamente 500 mg a aproximadamente 925 mg, de aproximadamente 500 mg a aproximadamente 950 mg, de aproximadamente 500 mg a aproximadamente 975 mg, de aproximadamente 500 mg a aproximadamente 1,000 mg, de aproximadamente 600 mg a aproximadamente 625 mg, de aproximadamente 600 mg a aproximadamente 650 mg, de aproximadamente 600 mg a aproximadamente 675 mg, de aproximadamente 600 mg a aproximadamente 700 mg, de aproximadamente 600 mg a aproximadamente 725 mg, de aproximadamente 600 mg a aproximadamente 750 mg, de aproximadamente 600 mg a aproximadamente 775 mg, de aproximadamente 600 mg a aproximadamente 800 mg, de aproximadamente 600 mg a aproximadamente 825 mg, de aproximadamente 600 mg a aproximadamente 850 mg, de aproximadamente 600 mg a aproximadamente 875 mg, de aproximadamente 600 mg a aproximadamente 900 mg, de aproximadamente 600 mg a aproximadamente 925 mg, de aproximadamente 600 mg a aproximadamente 950 mg, de aproximadamente 600 mg a aproximadamente 975 mg, de aproximadamente 600 mg a aproximadamente 1,000 mg, de aproximadamente 700 mg a aproximadamente 725 mg, de aproximadamente 700 mg a aproximadamente 750 mg, de aproximadamente 700 mg a aproximadamente 775 mg, de aproximadamente 700 mg a aproximadamente 800 mg, de aproximadamente 700 mg a aproximadamente 825 mg, de aproximadamente 700 mg a aproximadamente 850 mg, de aproximadamente 700 mg a aproximadamente 875 mg, de aproximadamente 700 mg a aproximadamente 900 mg, de aproximadamente 700 mg a aproximadamente 925 mg, de aproximadamente 700 mg a aproximadamente 950 mg, de aproximadamente 700 mg a aproximadamente 975 mg, de aproximadamente 700 mg a aproximadamente 1,000 mg, de aproximadamente 800 mg a aproximadamente 825 mg, de aproximadamente 800 mg a aproximadamente 850 mg, de aproximadamente 800 mg a aproximadamente 875 mg, de aproximadamente 800 mg a aproximadamente 900 mg, de aproximadamente 800 mg a aproximadamente 925 mg, de aproximadamente 800 mg a aproximadamente 950 mg, de aproximadamente 800 mg a aproximadamente 975 mg, o de aproximadamente 800 mg a aproximadamente 1.000 mg.
Una composición farmacéutica divulgada en la presente puede incluir opcionalmente un portador farmacéuticamente aceptable que facilita el procesamiento de un ARE en composiciones farmacéuticamente
aceptables. Un portador farmacológicamente aceptable es sinónimo de "vehículo farmacológico" y se refiere a cualquier portador que sustancialmente no tiene efectos perjudiciales a largo plazo o permanentes cuando se administra y abarca términos como vehículo, estabilizador, diluyente, aditivo, auxiliar o excipiente farmacológicamente aceptable. Dicho portador generalmente se mezcla con un compuesto activo o se permite que se diluya o encierre el compuesto activo y puede ser un agente sólido, semisólido o líquido. Se entiende que los ingredientes activos pueden ser solubles o pueden administrarse como una suspensión en el portador o diluyente deseado.
En una realización, solo hay un único portador farmacéuticamente aceptable en una composición divulgada en la presente. En otra realización, hay una pluralidad de portadores farmacéuticamente aceptables en una composición divulgada en la presente. En aspectos de esta realización, una composición divulgada en la presente comprende, por ejemplo, uno o más, dos o más, tres o más, cuatro o más o cinco o más portadores farmacéuticamente aceptables. En otros aspectos de esta realización, una composición divulgada en la presente comprende, por ejemplo, solo uno, como máximo dos, como máximo tres, como máximo cuatro o como máximo cinco portadores farmacéuticamente aceptables. En otros aspectos más de esta realización, una composición divulgada en la presente comprende, por ejemplo, de 1 a 2, de 1 a 3, de 1 a 4, de 1 a 5, de 2 a 3, de 2 a 4, de 2 a 5, de 3 a 4, de 3 a 5 o de 4 a 5 portadores farmacéuticamente aceptables.
En otra realización, una composición divulgada en la presente comprende una cantidad de portador farmacéuticamente aceptable que proporciona un efecto formulativo o beneficioso deseado a una composición farmacéutica divulgada en la presente. En aspectos de esta realización, una composición divulgada en la presente comprende un portador farmacéuticamente aceptable en una cantidad de, por ejemplo, por lo menos el 25%, por lo menos el 30%, por lo menos el 35%, por lo menos el 40%, por lo menos el 45%, por lo menos el 50%, por lo menos 55%, por lo menos el 60%, por lo menos el 65%, por lo menos el 70%, por lo menos el 75%, por lo menos el 80%, por lo menos el 85%, por lo menos el 90%, por lo menos el 95%, por lo menos el 96%, por lo menos el 97%, por lo menos el 98% o por lo menos el 99% en peso de la composición. En otros aspectos de esta realización, una composición divulgada en la presente comprende un portador farmacéuticamente aceptable en una cantidad de, por ejemplo, como máximo 25%, como máximo el 30%, como máximo el 35%, como máximo el 40%, como máximo el 45%, como máximo el 50%, como máximo el 55%, como máximo el 60%, como máximo el 65%, como máximo el 70%, como máximo el 75%, como máximo el 80%, como máximo el 85%, como máximo el 90%, como máximo el 95%, como máximo el 96%, como máximo el 97%, como máximo el 98% o como máximo el 99% en peso de la composición. En otros aspectos más de esta realización, una composición divulgada en la presente comprende un portador farmacéuticamente aceptable en una cantidad de, por ejemplo, de aproximadamente el 25% a aproximadamente el 50% de aproximadamente el 25% a aproximadamente e 75%, de aproximadamente e 25% aproximadamente el 90% de aproximadamente el 25% a aproximadamente e 95%, de aproximadamente e 25% aproximadamente el 96%. de aproximadamente el 25% a aproximadamente e 97%, de aproximadamente e 25% aproximadamente el 98%. de aproximadamente el 25% a aproximadamente e 99%, de aproximadamente e 50% aproximadamente el 75%. de aproximadamente el 50% a aproximadamente e 90%, de aproximadamente e 50% aproximadamente el 95%. de aproximadamente el 50% a aproximadamente e 96%, de aproximadamente e 50% aproximadamente el 97%. de aproximadamente el 50% a aproximadamente e 98%, de aproximadamente e 50% aproximadamente el 99%. de aproximadamente el 75% a aproximadamente e 80%, de aproximadamente e 75% aproximadamente el 85%. de aproximadamente el 75% a aproximadamente e 90%, de aproximadamente e 75% aproximadamente el 95%. de aproximadamente el 75% a aproximadamente e 96%, de aproximadamente e 75% aproximadamente el 97%. de aproximadamente el 75% a aproximadamente e 98%, de aproximadamente e 75% aproximadamente el 99%. de aproximadamente el 80% a aproximadamente e 85%, de aproximadamente e 80% aproximadamente el 90%. de aproximadamente el 80% a aproximadamente e 95%, de aproximadamente e 80% aproximadamente el 96%. de aproximadamente el 80% a aproximadamente e 97%, de aproximadamente e 80% aproximadamente el 98%. de aproximadamente el 80% a aproximadamente e 99%, de aproximadamente e 85% aproximadamente el 90%. de aproximadamente el 85% a aproximadamente e 95%, de aproximadamente e 85% aproximadamente el 96%. de aproximadamente el 85% a aproximadamente e 97%, de aproximadamente e 85% aproximadamente el 98%. de aproximadamente el 85% a aproximadamente e 99%, de aproximadamente e 90% aproximadamente el 95%. de aproximadamente el 90% a aproximadamente e 96%, de aproximadamente e 90% aproximadamente el 97%. de aproximadamente el 90% a aproximadamente e 98%, de aproximadamente e 90% aproximadamente el 99%, o de aproximadamente el 95% a aproximadamente el 99%, en peso de la composición.
Una composición farmacéutica divulgada en la presente puede comprender además uno o más componentes farmacéuticamente aceptables (o componentes farmacéuticos) incluyendo, sin limitación, tampones, conservantes, ajustadores de tonicidad, sales, antioxidantes, agentes de ajuste de osmolalidad, sustancias fisiológicas, sustancias farmacológicas, agentes de carga, agentes de viscosidad, surfactantes, agentes emulsionantes, agentes humectantes, agentes edulcorantes o aromatizantes, y similares. Pueden usarse varios tampones y medios para ajustar el pH para preparar una composición farmacéutica divulgada en la presente, siempre que la preparación resultante sea farmacéuticamente aceptable. Tales tampones incluyen, sin limitación, tampones de acetato, tampones de citrato, tampones de fosfato, solución salina tamponada neutra, solución salina tamponada con fosfato y tampones de borato. Se entiende que pueden usarse ácidos o bases para ajustar el pH de una composición según sea necesario. Los antioxidantes farmacéuticamente aceptables incluyen, sin limitación,
metabisulfito de sodio, tiosulfato de sodio, acetilcisteína, hidroxianisol butilado e hidroxitolueno butilado. Los conservantes útiles incluyen, sin limitación, cloruro de benzalconio, clorobutanol, clorhexidina, timerosal, un ácido parahidroxibenzoico como, por ejemplo, ácido metil-, propil- o butil-parahidroxibenzoico, una sal fenilmercúrica como, por ejemplo, nitrato, cloruro, acetato y borato, una composición de oxicloro estabilizada, como, por ejemplo, PURiTe® y quelantes como, por ejemplo, EDTA, DTPA o DTPA-bisamida, calcio DTPA y CaNaDTPA-bisamida. Los ajustadores de tonicidad útiles en una composición farmacéutica incluyen, sin limitación, sales como, por ejemplo, cloruro de sodio, cloruro de potasio, manitol o glicerina y otros ajustadores de tonicidad farmacéuticamente aceptables. Un agente de carga o agente de viscosidad útil en una composición farmacéutica incluye, sin limitación, un polisacárido como, por ejemplo, metilcelulosa, mucopolisacáridos, por ejemplo, ácido hialurónico y sulfato de condroitina, o polialcohol, por ejemplo, alcohol polivinílico. También pueden emplearse varios geles y matrices de liberación lenta, así como insertos oculares solubles e insolubles, por ejemplo, a base de sustancias que se forman geles in s itu . La composición farmacéutica puede proporcionarse como una sal y puede formarse con muchos ácidos, que incluyen pero no se limitan a, clorhídrico, sulfúrico, acético, láctico, tartárico, málico, succínico, etc. Las sales tienden a ser más solubles en solventes acuosos u otros protónicos que las formas de base libre correspondientes. Se entiende que estas y otras sustancias conocidas en el campo de la farmacología pueden incluirse en una composición farmacéutica.
Una composición farmacéutica divulgada en la presente puede formularse en cualquier forma que permita la aplicación tópica de un ARE divulgado en la presente de una manera que logre un efecto beneficioso deseado. Una aplicación tópica se refiere al uso de por lo menos un ARE descrito en la presente, incorporado en un portador farmacéutico adecuado y aplicado en un sitio de piel y/o debilitamiento del cabello o calvicie para el ejercicio de acción local. Por consiguiente, tales composiciones tópicas incluyen aquellas formas farmacéuticas en las que el por lo menos un ARE se aplica externamente por contacto directo con la superficie de la piel a tratar.
En una realización, una composición divulgada en la presente puede formularse en, por ejemplo, una formulación de una sola fase o una formulación bifásica que comprende una fase media y una fase dispersa. En otra realización, una composición divulgada en la presente se puede formular en, por ejemplo, una composición líquida, una composición coloidal, una composición semisólida o una composición sólida. En otra realización, una composición divulgada en la presente puede formularse en, por ejemplo, un aerosol líquido, una espuma, una emulsión, un gel, una sol. o una sol. sólida. En otra realización, una composición divulgada en la presente puede formularse en, por ejemplo, una pulverización, un aerosol líquido, un lavado, una loción para después del afeitado, un perfume, una loción, una crema, un ungüento, una composición de cera, una espuma, un champú, un acondicionador, una pomada, un linimento, una pasta, una jalea, un jabón, una suspensión o un emoliente. También pueden emplearse varios geles y matrices para la administración de liberación lenta, así como insertos oculares solubles e insolubles, por ejemplo, basados en sustancias que forman geles in situ.
En una realización, una composición farmacéutica divulgada en la presente se mezcla con un vehículo o portador dermatológicamente compatible. El vehículo que puede emplearse para preparar composiciones puede comprender, por ejemplo, soluciones acuosas como, por ejemplo, soluciones salinas fisiológicas, soluciones oleosas o pomadas. El vehículo además puede contener conservantes dermatológicamente compatibles como, por ejemplo, cloruro de benzalconio, surfactantes como, por ejemplo, polisorbato 80, liposomas o polímeros, por ejemplo, metilcelulosa, alcohol polivinílico, polivinilpirrolidona y ácido hialurónico; estos pueden usarse para aumentar la viscosidad. Además, también es posible usar insertos farmacológicos solubles o insolubles cuando se va a administrar el fármaco.
En una realización, una composición farmacéutica divulgada en la presente comprende del 0,1% al 10% de un compuesto divulgado en la presente, del 20% al 40% de alcohol desnaturalizado, del 40% al 60% de miristato de isopropilo y del 10% al 30% de Transcutol. En aspectos de esta realización, una composición farmacéutica divulgada en la presente comprende del 0,25% al 8% de un compuesto divulgado en la presente, del 23% al 37% de alcohol desnaturalizado, del 43% al 57% de miristato de isopropilo y del 13% al 27% de Transcutol. En otros aspectos de esta realización, una composición farmacéutica divulgada en la presente comprende del 0,5% al 5% de un compuesto divulgado en la presente, del 25% al 35% de alcohol desnaturalizado, del 45% al 55% de miristato de isopropilo y del 15% al 25% de Transcutol. En otros aspectos más de esta realización, una composición farmacéutica divulgada en la presente que comprende del 0,75% al 3% de un compuesto divulgado en la presente, del 27% al 32% de alcohol desnaturalizado, del 47% al 52% de miristato de isopropilo, y 17% a 22% Transcutol. En otros aspectos más de esta realización, una composición farmacéutica divulgada en la presente comprende del 1% al 2% de un compuesto divulgado en la presente, del 29% al 31% de alcohol desnaturalizado, del 48% al 50% de miristato de isopropilo y del 19% al 21% de Transcutol.
En una realización, una composición farmacéutica divulgada en la presente comprende del 0,1% al 10% de cualquiera de los Compuestos 37 a 52, o cualquier combinación de los mismos, del 20% al 40% de alcohol desnaturalizado, del 40% al 60% de miristato de isopropilo y del 10% al 30% de Transcutol. En aspectos de esta realización, una composición farmacéutica divulgada en la presente comprende del 0,25% al 8% de cualquiera de los Compuestos 37 a 52, o cualquier combinación de los mismos, del 23% al 37% de alcohol desnaturalizado, del 43% al 57% de miristato de isopropilo y del 13% al 27% Transcutol. En otros aspectos de esta realización, una
composición farmacéutica divulgada en la presente comprende del 0,5% al 5% de cualquiera de los Compuestos 37
a 52, o cualquier combinación de los mismos, del 25% al 35% de alcohol desnaturalizado, del 45% al 55% de
miristato de isopropilo y del 15% al 25% de Transcutol. En otros aspectos más de esta realización, una composición
farmacéutica divulgada en la presente comprende del 0,75% al 3% de cualquiera de los Compuestos 37 a 52, o
cualquier combinación de los mismos, del 27% al 32% de alcohol desnaturalizado, del 47% al 52% de miristato de
isopropilo y del 17% al 22% de Transcutol. En otros aspectos más de esta realización, una composición
farmacéutica divulgada en la presente comprende del 1% al 2% de cualquiera de los Compuestos 37 a 52, o
cualquier combinación de los mismos, del 29% al 31% de alcohol desnaturalizado, del 48% al 50% de miristato de
isopropilo y del 19% al 21% Transcutol.
En una realización, una composición farmacéutica divulgada en la presente puede alojarse en recipientes
adecuados para dispensar la composición. El recipiente puede ser un vial, una botella, un tubo, etc. En ciertas
realizaciones, el recipiente se podrá apretar para liberar la composición en el mismo. El recipiente puede tener una
tapa, que puede romperse, torcerse, etc. para abrir y cerrar. El recipiente debe ser tal que se mantenga la esterilidad
de la composición en el mismo. En ciertas realizaciones, el recipiente tendrá un precinto de seguridad antes de
abrirlo. En una realización, un recipiente puede contener de aproximadamente 1 ml a aproximadamente 50 ml de la
composición divulgada en la presente. En aspectos de esta realización, un recipiente puede contener, por ejemplo,
de 1 ml a 5 ml, de 1 ml a 10 ml, de 1 ml a 15 ml, de 1 ml a 20 ml, de 1 ml a 25 ml, de 1 ml a 30 ml, de 1 ml a 35 ml,
de 1 ml a 40 ml, de 1 ml a 45 ml, de 1 ml a 50 ml, de 2 ml a 5 ml, de 2 ml a 10 ml, de 2 ml a 15 ml, de 2 ml a 20 ml,
de 2 ml a 25 ml, de 2 ml a 30 ml, de 2 ml a 35 ml, de 2 ml a 40 ml, de 2 ml a 45 ml, de 2 ml a 50 ml, de 3 ml a ml, de 3 ml a 15 ml, de 3 ml a 20 ml, de 3 ml a 25 ml, de 3 ml a 30 ml, de 3 ml a 35 ml, d ml, de 3 ml a 50 ml, de 5 ml a 10 ml, de 5 ml a 15 ml, de 5 ml a 20 ml, de 5 ml a 25 ml, d de 5 ml a 35 ml, de 5 ml a 40 ml, de 5 ml a 45 ml, de 5 ml a 50 ml, de 10 ml a 20 ml, de 10 ml a 30 ml, ml, de 10 ml a 50 ml, de 20 ml a 30 ml, de 20 ml a 40 ml, de 20 ml a 50 ml, de 30 ml a 40 ml, de 30 ml a 50 ml, o de
40 ml a 50 ml.
Una composición farmacéutica divulgada pero no reivindicada en la presente se puede proporcionar en un
kit. Un kit puede comprender un sistema de administración que tenga uno o más de un cepillo aplicador, un hisopo o
almohadilla de espuma porosa, un tubo hueco, una varilla medidora o una combinación de los mismos. En ciertas
realizaciones, el sistema de administración comprende una pluralidad de cepillos aplicadores que tienen filamentos
recubiertos con un agente potenciador de la lubricidad. El agente potenciador de la lubricidad puede ser un polímero
que se recubre sobre los filamentos para controlar la liberación de la composición del cepillo, es decir, la
composición no se libera del cepillo hasta que entra en contacto con la superficie de la piel y la velocidad de la
liberación es tal que se libera del cepillo una cantidad terapéuticamente apropiada de una composición sobre la
superficie de la piel. Los cepillos aplicadores del kit son útiles para aplicar la composición potenciadora del
crecimiento del cabello en el sitio de interés, es decir, por lo menos una región de la piel. Puede haber una pluralidad
de cepillos aplicadores en un kit. Por ejemplo, en un kit de administración para 30 días, puede haber 60 aplicadores,
de tal manera que haya un aplicador para cada ojo, por aplicación, durante 30 días. Alternativamente, puede haber
2, 10, 20, 30, 40, 50, 60, 90, 120, etc. aplicadores por kit. Dentro del kit, los cepillos aplicadores pueden
empaquetarse individualmente o en juegos de 2 o más. Los cepillos aplicadores se envasan de tal manera que
permanezcan estériles hasta su uso. En ciertas realizaciones, los cepillos aplicadores pueden envasarse en fundas
de plástico. Además, para evitar la contaminación del ojo, son preferiblemente aplicadores desechables de un solo
uso.
El kit también puede comprender un conjunto de instrucciones. Las instrucciones pueden incluir información
útil para el usuario final como, por ejemplo, cómo utilizar el sistema de administración y la composición potenciadora
del crecimiento del cabello, con qué frecuencia usarla, etc.
El contenido del kit, los cepillos aplicadores, el recipiente de la composición y las instrucciones, están
encerrados en una carcasa exterior. La carcasa exterior puede ser una caja, una bolsa sellada, una bolsa de
aluminio, etc. En ciertas realizaciones, el sistema de administración, el recipiente y las instrucciones están
encerrados en una caja. En otras realizaciones del kit, el recipiente y las instrucciones están contenidos en una
primera caja, el sistema de administración está contenido en una segunda caja, y la primera y la segunda cajas
están contenidas juntas en una tercera caja.
Los aspectos de la presente memoria descriptiva divulgan, en parte, compuestos o composiciones de la
invención para tratar la caída del cabello. Dicho tratamiento implica la administración de una cantidad eficaz de uno o
más ARE o composición farmacéutica divulgada en la presente a por lo menos una región del cabello o una parte del
mismo asociada con la caída del cabello, en donde la administración da como resultado una reducción en el atributo
asociado con la caída del cabello. El término "caída del cabello" es sinónimo de "alopecia" y se refiere a la ausencia
o pérdida de cabello en la superficie de la piel, lo que incluye sin limitación, la pérdida de cabello en el cuero
cabelludo, la cara, la barba, la cabeza, la zona púbica, el labio superior y las cejas y/o los párpados.
Los aspectos de la presente memoria descriptiva divulgan, en parte, compuestos o composiciones de la
invención para tratar el debilitamiento del cabello. Dicho tratamiento implica la administración de una cantidad eficaz
de uno o más ARE o composición farmacéutica divulgada en la presente a por lo menos una región del cabello o una parte de la misma asociada con el debilitamiento del cabello, en donde la administración da como resultado una reducción en el atributo asociado con el debilitamiento del cabello. El término "debilitamiento del cabello" se refiere a una condición relacionada con la edad en donde los folículos pilosos producen cabellos que son más cortos en longitud, de menor diámetro, de color más claro y más frágiles en lugar de no producir cabello en absoluto. El debilitamiento del cabello es una afección en donde el tallo de cada cabello se vuelve más corto en longitud, más pequeño en diámetro (más fino), menos pigmentado y/o más frágil. Como tal, el debilitamiento del cabello es distinto de la caída del cabello, una afección en donde el folículo piloso deja de producir un tallo piloso por completo. Como se ha analizado anteriormente, el folículo piloso es un mini órgano complejo. Pero como todos los sistemas biológicos, la parte biológicamente activa del folículo piloso sufre un proceso de envejecimiento. Este proceso de envejecimiento se caracteriza por 1) la migración de la base del folículo piloso hacia arriba hacia la superficie de la piel, una disminución en la síntesis de queratinas capilares y una pérdida de pigmentación. Aunque producen pelos, los folículos pilosos más viejos producen pelos más cortos, de menor diámetro, de color más claro y más frágiles. En conjunto, este cambio relacionado con la edad en las características del cabello se manifiesta como debilitamiento del cabello. El debilitamiento del cabello afecta aproximadamente a 40 millones de hombres y 25 millones de mujeres en los Estados Unidos. El impacto emocional de la caída del cabello puede provocar ansiedad, estrés, depresión, y autoestima más baja.
Los aspectos de la presente memoria descriptiva divulgan, en parte, compuestos o composiciones de la invención para tratar la pérdida de color del cabello. Dicho tratamiento implica la administración de una cantidad eficaz de uno o más ARE o composición farmacéutica divulgada en la presente a por lo menos una región del cabello o una parte de la misma asociada con la pérdida del color del cabello, en donde la administración da como resultado una reducción en el atributo asociado con la pérdida del color del cabello. El término "pérdida de color del cabello" se refiere a la reducción de la pigmentación del tallo del cabello.
El cabello incluye el de las especies de mamíferos, incluyendo tanto humanos como animales. En los humanos, el cabello incluye el cabello del cuero cabelludo, la cara, la barba, la cabeza, la zona púbica, el labio superior, las cejas y los párpados. En los animales, el pelo incluye el pelo de toda la superficie del cuerpo. Por ejemplo, para animales criados por su piel, como, por ejemplo, un visón, una chinchilla, un zorro o un castor, los compuestos pueden aplicarse sobre toda la superficie del cuerpo para mejorar el pelaje general por razones comerciales. El proceso también puede usarse por razones cosméticas en animales, por ejemplo, aplicado a la piel de perros y gatos que tienen calvas debido a la sarna u otras enfermedades que provocan cierto grado de aparición de pelo.
Los aspectos de la presente memoria descriptiva divulgan, en parte, compuestos y composiciones de la invención para tratar una afección asociada con un trastorno degenerativo del folículo piloso. Dicho tratamiento implica la administración de una cantidad eficaz de uno o más ARE o la composición farmacéutica divulgada en la presente a por lo menos una región del cabello o una parte de la misma asociada con un trastorno degenerativo del folículo piloso, en donde la administración da como resultado una reducción en el atributo asociado con el trastorno degenerativo del folículo piloso. Un trastorno degenerativo del folículo piloso es una afección en donde la función o estructura de un folículo piloso se deteriora progresivamente con el tiempo. Un trastorno degenerativo del folículo piloso provoca la caída del cabello, debilitamiento del cabello y/o pérdida del color del cabello. Por ejemplo, un trastorno degenerativo del folículo piloso incluye alopecia que incluye alopecias por cicatrización y alopecias que no sean por cicatrización.
En un aspecto de esta realización, una composición divulgada en la presente se administra a un individuo para tratar un trastorno degenerativo del folículo piloso asociado con la pérdida de cabello, debilitamiento del cabello, pérdida del color del cabello, falta de crecimiento del cabello nuevo, tasa reducida de crecimiento del tallo del cabello, diámetro del tallo del cabello reducido (grosor), reducción de la longitud del tallo del cabello, reducción de la densidad del cabello, reducción de la queratinización del tallo del cabello, aumento de la fragilidad, reducción de la pigmentación del cabello, reducción del brillo del tallo del cabello, reducción de la salud del cabello, reducción del tiempo que un folículo piloso pasa en fase anágena, reducción del tiempo un folículo piloso pasa en fase catágena, reducción del tiempo que un folículo piloso pasa en fase telógena, liberación prematura del tallo piloso del folículo piloso, inicio prematuro de la apoptosis en el folículo piloso, conversión prematura de un cabello terminal en cabello velloso.
La alopecia puede estar provocada por una multitud de factores que incluyen, sin limitación, composición genética, trastorno funcional, trastorno hereditario, disposición hereditaria del tallo del cabello o genodermatosis, rotura química como sobreprocesamiento o uso frecuente de alisadores químicos, daño por calor como por el uso repetido de peines calientes, la exposición crónica a la tracción en el tallo del cabello, el arrancamiento compulsivo del cabello, el efluvio telógeno resultante del estrés físico o psicológico, la sífilis secundaria puede provocar "pérdida de cabello apolillado", lupus eritematoso discoide o lupus eritematoso cutáneo crónico, liquenplanopilaris, pseudopelade de Brocq, foliculitis en penacho, celulitis disecante, alopecia mucinosa, queratosis folicularis spinulosa decalvans, efecto adverso de ciertos medicamentos como quimioterapia, radioterapia y comprimidos de refuerzo de testosterona. La alopecia se produce con frecuencia en pacientes sometidos a tratamiento para cáncer o que
padecen otras enfermedades, como el SIDA, en donde se usan fármacos citotóxicos o destructores de células.
La alopecia se clasifica típicamente como por cicatrices o sin cicatrices. La alopecia por cicatrices, también conocida como "alopecia cicatrisata" o "alopecia cicatricial", se refiere a la pérdida de cabello caracterizada por la destrucción potencialmente permanente e irreversible de los folículos pilosos y su sustitución por tejido cicatricial. Los ejemplos no limitativos de alopecia cicatricial incluyen enfermedades ampollosas, alopecia química, lupus eritematoso discoide, foliculitis severa, liquen planopilaris, celulitis disecante, alopecia cicatricial centrífuga central, alopecia fibrosante frontal posmenopáusica y tumores y excrecencias cutáneas, como, por ejemplo, nevus sebáceo, carcinoma de células basales y carcinoma de células escamosas.
La alopecia sin cicatrices se refiere a la pérdida de cabello sin destrucción permanente del folículo piloso. Los ejemplos no limitativos de alopecia sin cicatrices incluyen efluvio anágeno, alopecia adnata, alopecia androgenética, alopecia AREata, alopecia congénita, alopecia diffusa, alopecia diseminada, alopecia folicular, alopecia leprotica, alopecia marginalis, alopecia medicamentosa, alopecia mucinosa, alopecia neurótica, alopecia pityrodes, alopecia presenili, alopecia senilis, alopecia sintomática, alopecia sifilítica, alopecia totalis, alopecia tóxica, alopecia triangularis, alopecia triangularis congenitalis, alopecia universalis, foliculitis, olliculitis decalvans, alopecia por tracción, tricotilomanía, efluvio telógeno y trastornos heredados del tallo del cabello.
Una composición farmacéutica divulgada en la presente puede administrarse a un individuo para tratar un trastorno degenerativo del folículo piloso asociado con la alopecia por cicatrices. Una composición divulgada en la presente puede administrarse a un individuo para tratar un trastorno degenerativo del folículo piloso asociado con una enfermedad ampollosa, una exposición química, un lupus eritematoso discoide, una foliculitis grave, un liquen planopilaris, una celulitis disecante, una alopecia cicatricial centrífuga central, una alopecia fibrosante frontal posmenopáusica, un tumor o una excrecencia de la piel.
Una composición farmacéutica divulgada en la presente puede administrarse a un individuo para tratar una alopecia no por cicatrices. Una composición divulgada en la presente puede administrarse a un individuo para tratar un trastorno degenerativo del folículo piloso asociado con efluvio anágeno, alopecia adnata, alopecia androgenética, alopecia AREata, alopecia congénita, alopecia diffusa, alopecia diseminada, alopecia folicular, alopecia leprotica, alopecia marginalis, alopecia medicamentosa, alopecia mucinosa, alopecia neurótica, alopecia pityrodes, alopecia presenili, alopecia senilis, alopecia sintomática, alopecia sifilítica, alopecia totalis, alopecia tóxica, alopecia triangularis, alopecia triangularis congenitalis, alopecia universalis, foliculitis, olliculitis decalvans, alopecia por tracción, tricotilomanía, efluvio telógeno, o trastorno heredado del tallo del cabello.
Un trastorno degenerativo del folículo piloso asociado con la pérdida de cabello en un individuo puede tratarse reduciendo un atributo asociado con la pérdida de cabello. La reducción del atributo asociado con la caída del cabello puede lograrse aumentando la tasa de crecimiento del cabello, aumentando el grosor del cabello, aumentando la longitud del cabello, aumentando la densidad del cabello, aumentando el número de cabellos producidos por folículo, aumentando la pigmentación del cabello, aumentando el brillo del cabello, convirtiendo el cabello intermedio o cabello velloso en cabello terminal, aumentando la salud del cabello, aumentando el tiempo que un folículo piloso permanece en fase anágena, aumentando el tiempo que un folículo piloso permanece en fase catágena, aumentando el tiempo que un folículo piloso permanece en fase telógena, prolongando o previniendo la liberación del tallo piloso del folículo piloso, o prolongando o previniendo el inicio de la apoptosis en un folículo piloso.
La reducción del atributo asociado con un trastorno degenerativo del folículo piloso asociado con el debilitamiento del cabello puede lograrse aumentando la tasa de crecimiento del cabello, aumentando el grosor del cabello, aumentando la longitud del cabello, aumentando la densidad del cabello, aumentando el número de cabellos producidos por folículo, aumentando la producción de queratina en el tallo del cabello, aumentando la pigmentación del tallo del cabello, aumentando el brillo del tallo del cabello, convirtiendo el cabello intermedio o velloso en cabello terminal, aumentando la salud del cabello, aumentando el tiempo que un folículo piloso permanece en fase anágena, aumentando el tiempo que un folículo piloso permanece en fase catágena, o aumentando el tiempo que un folículo piloso permanece en fase telógena.
Una composición farmacéutica divulgada en la presente puede administrarse a un individuo para tratar un trastorno degenerativo del folículo piloso asociado con la pérdida del color del cabello. Una composición divulgada en la presente puede administrarse a un individuo para tratar un trastorno degenerativo del folículo piloso asociado con una disminución de la pigmentación del tallo del cabello, disminución de la producción de melanina, aumento de la muerte de melanocitos asociada con la apoptosis o cualquier otra causa.
La reducción del atributo asociado con un trastorno degenerativo del folículo piloso asociado con la pérdida del color del cabello puede lograrse aumentando la pigmentación del tallo del cabello, aumentando la producción de melanina, aumentando el brillo del cabello, convirtiendo el cabello intermedio o velloso en cabello terminal, aumentando la salud del cabello, aumentando el tiempo que un folículo piloso permanece en fase anágena, aumentando el tiempo que un folículo piloso permanece en fase catágena, aumentando el tiempo que un folículo
piloso permanece en fase telógena, prolongando o previniendo la muerte de melanocitos, o prolongando o previniendo el inicio de la apoptosis en un folículo piloso.
También se divulga, pero no se reivindica, un método para mejorar la apariencia del cabello. Dichos métodos implican la administración de una cantidad eficaz de uno o más ARE o composición farmacéutica divulgada en la presente a por lo menos una región del cabello o una parte de la misma, en donde la administración mejora un atributo de la apariencia del cabello. Esta administración da como resultado una mejora de por lo menos un atributo del cabello que incluye, sin limitación, aumento de la longitud del cabello, aumento del grosor del cabello, aumento del crecimiento de cabello nuevo, aumento de la velocidad de crecimiento del cabello, aumento del número de cabellos, aumento de la conversión de cabello intermedio en cabello terminal, aumento de la densidad del cabello, aumento del número de cabellos por folículo y/o aumento del color u oscuridad del cabello.
Los aspectos de la presente memoria descriptiva divulgan, en parte, compuestos y composiciones de la invención para tratar una afección, enfermedad o trastorno de la piel. Dicho tratamiento implica la administración de una cantidad eficaz de un ARE o una composición farmacéutica divulgada en la presente en por lo menos una región de la piel o una parte de la misma asociada con una afección, enfermedad o trastorno de la piel. Como se usa en la presente, el término "región de la piel" es sinónimo de "región epidérmica". En aspectos de esta realización, una afección, enfermedad o trastorno de la piel incluye, sin limitación, acné, producción excesiva de sebo, formación de una cicatriz después de una herida o un problema dermatológico asociado con la enfermedad de ovario poliquístico.
Una cantidad eficaz (o una cantidad terapéuticamente eficaz) del por lo menos un ARE divulgado en la presente es una que reduce o inhibe una o más afecciones fisiológicas, atributos o síntomas de una afección, trastorno o enfermedad de la piel o el cabello asociados con la señalización mediada por AR. Un experto en la materia puede determinar una cantidad eficaz, pero variará dependiendo del ARE empleado, la frecuencia de la aplicación y el resultado deseado.
En aspectos de esta realización, una cantidad terapéuticamente eficaz de por lo menos un ARE divulgado en la presente reduce o inhibe una o más afecciones fisiológicas, atributos o síntomas de una afección, trastorno o enfermedad de la piel o el cabello asociados con la señalización mediada por AR en , por ejemplo, por lo menos un 10%, por lo menos un 20%, por lo menos un 30%, por lo menos un 40%, por lo menos un 50%, por lo menos un 60%, por lo menos un 70%, por lo menos un 80%, por lo menos un 90% o por lo menos un 95%. En otros aspectos más de esta realización, una cantidad terapéuticamente eficaz del por lo menos un compuesto mejora un atributo asociado con el cabello en, por ejemplo, de aproximadamente un 10% a aproximadamente un 100%, de aproximadamente un 10% a aproximadamente un 90%, de aproximadamente un 10% a aproximadamente un 80%, de aproximadamente 20% a aproximadamente un 70%, de aproximadamente un 20% a aproximadamente un 60%, de aproximadamente un 20% a aproximadamente un 50%, de aproximadamente un 20% a aproximadamente un 40%, de aproximadamente un 30% a aproximadamente un 100%, de aproximadamente un 30% a aproximadamente un 90%, de aproximadamente un 30% a aproximadamente un 80%, de aproximadamente un 30% a aproximadamente un 70%, de aproximadamente un 30% a aproximadamente un 60%, o de aproximadamente un 30% a aproximadamente un 50%. En aspectos de esta realización, una dosis terapéuticamente eficaz es la dosificación suficiente para lograr el efecto terapéutico deseado durante, por ejemplo, por lo menos un día, por lo menos dos días, por lo menos tres días, por lo menos cuatro días, por lo menos cinco días, por lo menos por lo menos seis días, por lo menos siete días, por lo menos una semana, por lo menos dos semanas, por lo menos tres semanas, por lo menos cuatro semanas, por lo menos un mes, por lo menos dos meses, por lo menos tres meses, por lo menos cuatro meses, por lo menos por lo menos cinco meses, por lo menos seis meses, por lo menos siete meses, por lo menos ocho meses, por lo menos nueve meses, por lo menos diez meses, por lo menos once meses o por lo menos doce meses.
En aspectos de esta realización, una cantidad eficaz de un ARE divulgado en la presente generalmente está en el intervalo de aproximadamente 0, 001 mg/kg/día a aproximadamente 100 mg/kg/día. En aspectos de esta realización, una cantidad eficaz de un ARE divulgado en la presente puede ser, por ejemplo, por lo menos 0,001 mg/kg/día, por lo menos 0,01 mg/kg/día, por lo menos 0,1 mg/kg/día, por lo menos 1,0 mg /kg/día, por lo menos 5,0 mg/kg/día, por lo menos 10 mg/kg/día, por lo menos 15 mg/kg/día, por lo menos 20 mg/kg/día, por lo menos 25 mg/kg/día, por lo menos 30 mg/kg/día, por lo menos 35 mg/kg/día, por lo menos 40 mg/kg/día, por lo menos 45 mg/kg/día, o por lo menos 50 mg/kg/día. En otros aspectos de esta realización, una cantidad eficaz de un ARE divulgado en la presente puede ser, por ejemplo, como máximo 0,001 mg/kg/día, como máximo 0,01 mg/kg/día, como máximo 0,1 mg/kg/día, como máximo 1,0 mg/kg/día, como máximo 5,0 mg/kg/día, como máximo 10 mg/kg/día, como máximo 15 mg/kg/día, como máximo 20 mg/kg/día, como máximo 25 mg/kg/día, como máximo 30 mg/kg/día, como máximo 35 mg/kg/día, como máximo 40 mg/kg/día, como máximo 45 mg/kg/día, o como máximo 50 mg/kg/día.
En otros aspectos de esta realización, una cantidad eficaz de un ARE divulgado en la presente puede estar en el intervalo de, por ejemplo, de aproximadamente 0,001 mg/kg/día a aproximadamente 10 mg/kg/día, de aproximadamente 0,001 mg/kg/día a aproximadamente 15 mg/kg/día, de aproximadamente 0,001 mg/kg/día a aproximadamente 20 mg/kg/día, de aproximadamente 0,001 mg/kg/día a aproximadamente 25 mg/kg/día, de aproximadamente 0,001 mg/kg/día a aproximadamente 30 mg/kg/día, de aproximadamente 0,001 mg/kg/día a
aproximadamente 35 mg/kg/día, de aproximadamente 0,001 mg/kg/día a aproximadamente 40 mg/kg/día, de aproximadamente 0,001 mg/kg/día a aproximadamente 45 mg/kg/día, de aproximadamente 0,001 mg/kg/día a aproximadamente 50 mg/kg/día, de aproximadamente 0,001 mg/kg/día a aproximadamente 75 mg/kg/día, o de aproximadamente 0,001 mg/kg/día a aproximadamente 100 mg/kg/día, En otros aspectos más de esta realización, una cantidad eficaz de una ARE divulgado en la presente puede estar en el intervalo de, por ejemplo, de aproximadamente 0,01 mg/kg/día a aproximadamente 10 mg/kg/día, de aproximadamente 0,01 mg/kg/día a aproximadamente 15 mg/kg/día, de aproximadamente 0,01 mg/kg/día a aproximadamente 20 mg/kg/día, de aproximadamente 0,01 mg/kg/día a aproximadamente 25 mg/kg/día, de aproximadamente 0,01 mg/kg/día a aproximadamente 30 mg/kg/día, de aproximadamente 0,01 mg/kg/día a aproximadamente 35 mg/kg/día, de aproximadamente 0,01 mg/kg/día a aproximadamente 40 mg/kg/día, de aproximadamente 0,01 mg/kg/día a aproximadamente 45 mg/kg/día, de aproximadamente 0,01 mg/kg/día a aproximadamente 50 mg/kg/día, de aproximadamente 0,01 mg/kg/día a aproximadamente 75 mg/kg/día, o de aproximadamente 0,01 mg/kg/día a aproximadamente 100 mg/kg/día, En otros aspectos más de esta realización, una cantidad eficaz de un ARE divulgado en la presente puede estar en el intervalo de, por ejemplo, de aproximadamente 0,1 mg/kg/día a aproximadamente 10 mg/kg/día, de aproximadamente 0,1 mg/kg/día a aproximadamente 15 mg/kg/día, de aproximadamente 0,1 mg/kg/día a aproximadamente 20 mg/kg/día, de aproximadamente 0,1 mg/kg/día a aproximadamente 25 mg/kg/día, de aproximadamente 0,1 mg/kg/día a aproximadamente 30 mg/kg/día, de aproximadamente 0,1 mg/kg/día a aproximadamente 35 mg/kg/día, de aproximadamente 0,1 mg/kg/día a aproximadamente 40 mg/kg/día, de aproximadamente 0,1 mg/kg/día a aproximadamente 45 mg/kg/día, de aproximadamente 0,1 mg/kg/día a aproximadamente 50 mg/kg/día, de aproximadamente 0,1 mg/kg/día a aproximadamente 75 mg/kg/día, o de aproximadamente 0,1 mg/kg/día a aproximadamente 100 mg/kg/día.
En otros aspectos de esta realización, una cantidad eficaz de un ARE divulgado en la presente puede estar en el intervalo de, por ejemplo, de aproximadamente 1 mg/kg/día a aproximadamente 10 mg/kg/día, de aproximadamente 1 mg/kg/día a aproximadamente 15 mg/kg/día, de aproximadamente 1 mg/kg/día a aproximadamente 20 mg/kg/día, de aproximadamente 1 mg/kg/día a aproximadamente 25 mg/kg/día, de aproximadamente 1 mg/kg/día a aproximadamente 30 mg/kg/día, de aproximadamente 1 mg/kg/día a aproximadamente 35 mg/kg/día, de aproximadamente 1 mg/kg/día a aproximadamente 40 mg/kg/día, de aproximadamente 1 mg/kg/día a aproximadamente 45 mg/kg/día, de aproximadamente 1 mg/kg/día a aproximadamente 50 mg/kg/día, de aproximadamente 1 mg/kg/día a aproximadamente 75 mg/kg/día, o de aproximadamente 1 mg/kg/día a aproximadamente 100 mg/kg/día. En otros aspectos más de esta realización, una cantidad eficaz de un ARE divulgado en la presente puede estar en el intervalo de, por ejemplo, de aproximadamente 5 mg/kg/día a aproximadamente 10 mg/kg/día, de aproximadamente 5 mg/kg/día a aproximadamente 15 mg/kg/día, de aproximadamente 5 mg/kg/día a aproximadamente 20 mg/kg/día, de aproximadamente 5 mg/kg/día a aproximadamente 25 mg/kg/día, de aproximadamente 5 mg/kg/día a aproximadamente 30 mg/kg/día, de aproximadamente 5 mg/kg/día a aproximadamente 35 mg/kg/día, de aproximadamente 5 mg/kg/día a aproximadamente 40 mg/kg/día, de aproximadamente 5 mg/kg/día a aproximadamente 45 mg/kg/día, de aproximadamente 5 mg/kg/día a aproximadamente 50 mg/kg/día, de aproximadamente 5 mg/kg/día a aproximadamente 75 mg/kg/día, o de aproximadamente 5 mg/kg/día a aproximadamente 100 mg/kg/día.
En otros aspectos de esta realización, una cantidad eficaz de un ARE divulgado en la presente generalmente está en el intervalo de aproximadamente 0, 001 mg/día a aproximadamente 100 mg/día. En aspectos de esta realización, una cantidad eficaz de un ARE divulgado en la presente puede ser de, por ejemplo, por lo menos 0,001 mg/día, por lo menos 0,01 mg/día, por lo menos 0,1 mg/día, por lo menos 1,0 mg/día, por lo menos 5,0 mg/día, por lo menos 10 mg/día, por lo menos 15 mg/día, por lo menos 20 mg/día, por lo menos 25 mg/día, por lo menos 30 mg/día, por lo menos 35 mg/día, por lo menos 40 mg /día, por lo menos 45 mg/día, o por lo menos 50 mg/día. En otros aspectos de esta realización, una cantidad eficaz de un ARE divulgado en la presente puede ser de, por ejemplo, como máximo 0,001 mg/día, como máximo 0,01 mg/día, como máximo 0,1 mg/día, como máximo 1,0 mg/día, como máximo 5,0 mg/día, como máximo 10 mg/día, como máximo 15 mg/día, como máximo 20 mg/día, como máximo 25 mg/día, como máximo 30 mg/día, como máximo 35 mg/día, como máximo 40 mg/día, como máximo 45 mg/día, o como máximo 50 mg/día.
En otros aspectos de esta realización, una cantidad eficaz de un ARE divulgado en la presente puede estar en el intervalo de, por ejemplo, de aproximadamente 0,001 mg/día a aproximadamente 10 mg/día, de aproximadamente 0,001 mg/día a aproximadamente 15 mg/día, de aproximadamente 0,001 mg/día a aproximadamente 20 mg/día, de aproximadamente 0,001 mg/día a aproximadamente 25 mg/día, de aproximadamente 0,001 mg/día a aproximadamente 30 mg/día, de aproximadamente 0,001 mg/día a aproximadamente 35 mg/día, de aproximadamente 0,001 mg/día a aproximadamente 40 mg/día, de aproximadamente 0,001 mg/día a aproximadamente 45 mg/día, de aproximadamente 0,001 mg/día a aproximadamente 50 mg/día, de aproximadamente 0,001 mg/día a aproximadamente 75 mg/día, o de aproximadamente 0,001 mg/día a aproximadamente 100 mg/día. En otros aspectos más de esta realización, una cantidad eficaz de un ARE divulgado en la presente puede estar en el intervalo de, por ejemplo, de aproximadamente 0,01 mg/día a aproximadamente 10 mg/día, de aproximadamente 0,01 mg/día a aproximadamente 15 mg/día, de aproximadamente 0,01 mg/día a aproximadamente 20 mg/día, de
aproximadamente 0,01 mg/día a aproximadamente 25 mg/día, de aproximadamente 0,01 mg/día a aproximadamente 30 mg/día, de aproximadamente 0,01 mg/día a aproximadamente 35 mg/día, de aproximadamente 0,01 mg/día a aproximadamente 40 mg/día, de aproximadamente 0,01 mg/día a aproximadamente 45 mg/día, de aproximadamente 0,01 mg/día a aproximadamente 50 mg/día, de aproximadamente 0,01 mg/día a aproximadamente 75 mg/día, o de aproximadamente 0,01 mg/día a aproximadamente 100 mg/día. En otros aspectos más de esta realización, una cantidad eficaz de un ARE divulgado en la presente puede estar en el intervalo de, por ejemplo, de aproximadamente 0,1 mg/día a aproximadamente 10 mg/día, de aproximadamente 0,1 mg/día a aproximadamente 15 mg/día, de aproximadamente 0,1 mg/día a aproximadamente 20 mg/día, de aproximadamente 0,1 mg/día a aproximadamente 25 mg/día, de aproximadamente 0,1 mg/día a aproximadamente 30 mg/día, de aproximadamente 0,1 mg/día a aproximadamente 35 mg/día, de aproximadamente 0,1 mg/día a aproximadamente 40 mg/día, de aproximadamente 0,1 mg/día a aproximadamente 45 mg/día, de aproximadamente 0,1 mg/día a aproximadamente 50 mg/día, de aproximadamente 0,1 mg/día a aproximadamente 75 mg/día, o de aproximadamente 0,1 mg/día a aproximadamente 100 mg/día.
En otros aspectos de esta realización, una cantidad eficaz de un ARE divulgado en la presente puede estar en el intervalo de, por ejemplo, de aproximadamente 1 mg/día a aproximadamente 10 mg/día, de aproximadamente 1 mg/día a aproximadamente 15 mg/día, de aproximadamente 1 mg/día a aproximadamente 20 mg/día, de aproximadamente 1 mg/día a aproximadamente 25 mg/día, de aproximadamente 1 mg/día a aproximadamente 30 mg/día, de aproximadamente 1 mg/día a aproximadamente 35 mg/día, de aproximadamente 1 mg/día a aproximadamente 40 mg/día, de aproximadamente 1 mg/día a aproximadamente 45 mg/día, de aproximadamente 1 mg/día a aproximadamente 50 mg/día, de aproximadamente 1 mg/día a aproximadamente 75 mg/día, o de aproximadamente 1 mg/día a aproximadamente 100 mg/día. En otros aspectos más de esta realización, una cantidad eficaz de un ARE divulgado en la presente puede estar en el intervalo de, por ejemplo, de aproximadamente 5 mg/día a aproximadamente 10 mg/día, de aproximadamente 5 mg/día a aproximadamente 15 mg/día, de aproximadamente 5 mg/día a aproximadamente 20 mg/día, de aproximadamente 5 mg/día a aproximadamente 25 mg/día, de aproximadamente 5 mg/día a aproximadamente 30 mg/día, de aproximadamente 5 mg/día a aproximadamente 35 mg/día, de aproximadamente 5 mg/día a aproximadamente 40 mg/día, de aproximadamente 5 mg/día a aproximadamente 45 mg/día, de aproximadamente 5 mg/día a aproximadamente 50 mg/día, de aproximadamente 5 mg/día a aproximadamente 75 mg/día, o de aproximadamente 5 mg/día a aproximadamente 100 mg/día.
La dosificación puede ser una única dosificación o acumulativa (dosificación en serie), y un experto en la técnica puede determinarla fácilmente. Por ejemplo, el método de tratamiento divulgado en la presente puede comprender una administración individual de una cantidad eficaz de un ARE o composición farmacéutica divulgada en la presente. Como ejemplo no limitativo, una cantidad eficaz de un ARE o una composición farmacéutica divulgada en la presente puede administrarse una vez a un individuo, por ejemplo, como una única inyección o depósito. Alternativamente, un método de tratamiento divulgado en la presente puede comprender administraciones múltiples de una cantidad eficaz de un ARE o una composición farmacéutica divulgada en la presente durante un intervalo de períodos de tiempo, como, por ejemplo, diariamente, cada dos días, cada tercer día, una vez a la semana, varias veces a la semana, una vez al mes, varias veces al mes, una vez al año o varias veces al año. Una composición farmacéutica divulgada en la presente puede administrarse varias veces al día, por ejemplo, dos veces al día, tres veces al día, cuatro veces al día, cinco veces al día o seis veces al día. La periodicidad de la administración puede variar de un individuo a otro, dependiendo de factores como la gravedad de los síntomas de un individuo. Por ejemplo, una cantidad eficaz de un ARE o una composición farmacéutica divulgada en la presente puede administrarse a un individuo de 1 a 5 veces al día durante un período de tiempo indefinido, o hasta que el individuo ya no necesite terapia, por ejemplo, durante un período de tratamiento de por lo menos una semana, más preferiblemente por lo menos un mes, más preferiblemente por lo menos tres meses y lo más preferible por lo menos seis meses. Un experto en la técnica reconocerá que el estado del individuo puede monitorizarse a lo largo del curso del tratamiento y que la cantidad eficaz de una composición farmacéutica divulgada en la presente que se administra puede ajustarse en consecuencia.
En aspectos de esta realización, la longitud del cabello de una región tratada aumenta con respecto a una región no tratada, por ejemplo, por lo menos un 5%, por lo menos un 10%, por lo menos un 15%, por lo menos un 20%, por lo menos un 25%, por lo menos un 30%, por lo menos un 40%, por lo menos un 50%, por lo menos un 60%, por lo menos un 70%, por lo menos un 80%, por lo menos un 90% o por lo menos un 95%. En otros aspectos más de esta realización, la longitud del cabello aumenta con respecto a una región no tratada, por ejemplo, de aproximadamente el 5% a aproximadamente el 100%, de aproximadamente el 15% a aproximadamente el 100%, de aproximadamente el 25% a aproximadamente el 100%, de aproximadamente el 35% a aproximadamente el 100%, o de aproximadamente el 45% a aproximadamente el 100%. En otros aspectos más de esta realización, la longitud del cabello de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, de aproximadamente 1 mm a aproximadamente 500 mm, de aproximadamente 10 mm a aproximadamente 500 mm, o de aproximadamente 100 mm a aproximadamente 500 mm. En aspectos adicionales de esta realización, la longitud del cabello de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, por lo menos 1 mm, por lo menos, 2 mm, por lo menos, 3 mm, por lo menos 4 mm, por lo menos 5 mm, por lo menos 6 mm, por lo menos 7 mm, por lo menos 8 mm, por lo menos 9 mm, o por lo menos 10 mm.
En otros aspectos de esta realización, el grosor del cabello de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, por lo menos un 5 % , por lo menos un 10 % , por lo menos un 15 % , por lo menos un 20 % , por lo menos un 25 % , por lo menos un 30 % , por lo menos un 40 %, por lo menos un 50 % , por lo menos un 60%, por lo menos un 70 % , por lo menos un 80%, por lo menos un 90% o por lo menos un 95%. En otros aspectos más de esta realización, el grosor del cabello de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, de aproximadamente el 5 % a aproximadamente el 100 %, de aproximadamente el 15 % a aproximadamente el 100 %, de aproximadamente el 25 % a aproximadamente el 100 %, de aproximadamente el 35 % a aproximadamente el 100 %, o de aproximadamente el 45 % a aproximadamente el 100 %. En otros aspectos más de esta realización, el grosor del cabello de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, de aproximadamente 1 gm2 a aproximadamente 1 mm2, de aproximadamente 10 gm2 a aproximadamente 1 mm2, de aproximadamente 100 gm2 a aproximadamente 1 mm2, o de aproximadamente 100 gm2 a aproximadamente 2 mm2. En aspectos adicionales de esta realización, el grosor del cabello de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, por lo menos 100 gm2, por lo menos 200 gm2, por lo menos 300 gm2, por lo menos 400 gm2, por lo menos 500 gm2, por lo menos 600 gm2, por lo menos 700 gm2, por lo menos 800 gm2, por lo menos 900 gm2, por lo menos 1 mm2, por lo menos 2 mm2, o por lo menos 3 mm2.
En aspectos de esta realización, el crecimiento de cabello nuevo de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, por lo menos un 5 % , por lo menos un 10 % , por lo menos un 15 % , por lo menos un 20 % , por lo menos un 25 % , por lo menos un 30 %, por lo menos un 40%, por lo menos un 50 %, por lo menos un 60%, por lo menos un 70 % , por lo menos un 80%, por lo menos un 90 % o por lo menos un 95%. En otros aspectos de esta realización, el crecimiento de cabello nuevo de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, de aproximadamente el 5 % a aproximadamente el 100 %, de aproximadamente el 15 % a aproximadamente el 100 %, de aproximadamente el 25 % a aproximadamente el 100 %, de aproximadamente el 35 % a aproximadamente el 100 %, o de aproximadamente el 45 % a aproximadamente el 100 %.
En otros aspectos de esta realización, la tasa de crecimiento del cabello de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, por lo menos un 5 % , por lo menos un 10 % , por lo menos un 15 % , por lo menos un 20 % , por lo menos un 25 % , por lo menos un 30 %, por lo menos un 40%, por lo menos un 50 %, por lo menos un 60%, por lo menos un 70 % , por lo menos un 80%, por lo menos un 90 % o por lo menos un 95%. En otros aspectos más de esta realización, la tasa de crecimiento del cabello de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, de aproximadamente el 5 % a aproximadamente el 100 %, de aproximadamente el 15 % a aproximadamente el 100 %, de aproximadamente el 25 % a aproximadamente el 100 %, de aproximadamente el 35 % a aproximadamente el 100 %, o de aproximadamente el 45 % a aproximadamente el 100 %.
En otros aspectos de esta realización, el número de cabellos de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, por lo menos un 5 % , por lo menos un 10 % , por lo menos un 15 % , por lo menos un 20 % , por lo menos un 25 % , por lo menos un 30 %, por lo menos un 40%, por lo menos un 50 %, por lo menos un 60%, por lo menos un 70 % , por lo menos un 80%, por lo menos un 90% o por lo menos un 95%. En otros aspectos más de esta realización, el número de cabellos de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, de aproximadamente el 5 % a aproximadamente el 100 %, de aproximadamente el 15 % a aproximadamente el 100 %, de aproximadamente el 25 % a aproximadamente el 100 %, de aproximadamente el 35 % a aproximadamente el 100 %, o de aproximadamente el 45 % a aproximadamente el 100 %.
En otros aspectos de esta realización, la conversión de cabellos intermedios en cabellos terminales de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, por lo menos un 5 % , por lo menos un 10 % , por lo menos un 15 % , por lo menos un 20 % , por lo menos por lo menos un 25 % , por lo menos un 30 %, por lo menos un 40%, por lo menos un 50 %, por lo menos un 60%, por lo menos un 70 % , por lo menos un 80%, por lo menos un 90 % o por lo menos un 95%. En otros aspectos más de esta realización, la conversión de cabellos intermedios en cabellos terminales de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, de aproximadamente el 5 % a aproximadamente el 100 %, de aproximadamente el 15 % a aproximadamente el 100 %, de aproximadamente el 25 % a aproximadamente el 100 %, de aproximadamente el 35 % a aproximadamente el 100 %, o de aproximadamente el 45 % a aproximadamente el 100 %.
En otros aspectos de esta realización, la densidad del cabello de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, por lo menos un 5 % , por lo menos un 10 % , por lo menos un 15 % , por lo menos un 20 % , por lo menos un 25 % , por lo menos un 30 %, por lo menos un 40%, por lo menos un 50 %, por lo menos un 60%, por lo menos un 70 % , por lo menos un 80%, por lo menos un 90% o por lo menos un 95%. En otros aspectos más de esta realización, la densidad del cabello de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, de aproximadamente el 5 % a aproximadamente el 100 %, de aproximadamente el 15 % a aproximadamente el 100 %, de aproximadamente el 25 % a aproximadamente el 100 %, de aproximadamente el 35 % a aproximadamente el 100 %, o de aproximadamente el 45 % a aproximadamente el 100 %.
En otros aspectos de esta realización, el número de cabellos producidos por folículo piloso de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, por lo menos un 5%, por lo menos un 10%, por lo menos un 15%, por lo menos un 20%, por lo menos un 25%, por lo menos un 30%, por lo menos un 40%, por lo menos un 50%, por lo menos un 60%, por lo menos un 70%, por lo menos un 80%, por lo menos un 90% o por lo menos un 95%. En otros aspectos más de esta realización, el número de cabellos producidos por folículo piloso de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, de aproximadamente el 5% a aproximadamente el 100%, de aproximadamente el 15% a aproximadamente el 100%, de aproximadamente el 25% a aproximadamente el 100%, de aproximadamente el 35% a aproximadamente el 100%, o de aproximadamente el 45% a aproximadamente el 100%. En otros aspectos más de esta realización, el número de cabellos producidos por folículo piloso de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, 2 o más tallos de cabello/folículo, 3 o más tallos de cabello/folículo, 4 o más tallos de cabello/folículo, o 5 o más tallos de cabello/folículo. En aspectos adicionales de esta realización, el número de cabellos producidos por folículo piloso de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, 2 tallos de cabello/folículo, 3 tallos de cabello/folículo, 4 tallos de cabello/folículo, o 5 tallos de cabello/folículo. En otros aspectos más de esta realización, el número de cabellos producidos por folículo piloso de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, de 2 a 5 tallos de cabello/folículo, de 3 a 5 tallos de cabello/folículo, de 2 a 4 tallos de cabello/folículo, o de 2 a 3 tallos de cabello/folículo.
En otros aspectos de esta realización, el color del cabello de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, por lo menos un 5%, por lo menos un 10%, por lo menos un 15%, por lo menos un 20%, por lo menos un 25%, por lo menos un 30%, por lo menos un 40%, por lo menos un 50%, por lo menos un 60%, por lo menos un 70%, por lo menos un 80%, por lo menos un 90% o por lo menos un 95%. En otros aspectos de esta realización, el color del cabello de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, de aproximadamente el 5% a aproximadamente el 100%, de aproximadamente el 15% a aproximadamente el 100%, de aproximadamente el 25% a aproximadamente el 100%, de aproximadamente el 35% a aproximadamente el 100%, o de aproximadamente el 45% a aproximadamente el 100%.
En otros aspectos de esta realización, la pigmentación y/o melanización del cabello de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, por lo menos un 5%, por lo menos un 10%, por lo menos un 15%, por lo menos un 20%, por lo menos un 25%, por lo menos un 30%, por lo menos un 40%, por lo menos un 50%, por lo menos un 60%, por lo menos un 70%, por lo menos un 80%, por lo menos un 90% o por lo menos un 95%. En otros aspectos de esta realización, la pigmentación y/o melanización del cabello de una región tratada aumenta con respecto a una región no tratada en, por ejemplo, de aproximadamente el 5% a aproximadamente el 100%, de aproximadamente el 15% a aproximadamente el 100%, de aproximadamente el 25% a aproximadamente el 100%, de aproximadamente el 35% a aproximadamente el 100%, o de aproximadamente el 45% a aproximadamente el 100%.
Una composición farmacéutica divulgada en la presente puede aplicarse de acuerdo con un método divulgado en la presente a un sitio de piel y/o debilitamiento del cabello o calvicie. La aplicación de una de las composiciones divulgadas en la presente puede ser frotando, vertiendo, rociando o pulverizando, o aplicarse de otro modo a un sitio de la piel y/o debilitamiento del cabello o calvicie. Una composición farmacéutica divulgada en la presente puede aplicarse introduciendo o impregnando una composición en o sobre un soporte sólido como, por ejemplo, un vendaje, un trapo, una toallita, una toalla, una manopla, un guante o una mascarilla y luego aplicando la composición a un sitio de la piel y/o debilitamiento del cabello o calvicie. Una composición farmacéutica divulgada en la presente puede aplicarse usando un dispositivo de administración como, por ejemplo, un dispensador de aerosoles, un pulverizador de bomba, un pulverizador de gatillo o una botella exprimible, para aplicar una composición a un sitio de la piel y/o debilitamiento del cabello o calvicie.
EJEMPLOS
Los siguientes ejemplos no limitativos se proporcionan solo con propósitos ilustrativos para facilitar una comprensión más completa de las realizaciones representativas contempladas ahora. No debe interpretarse que estos ejemplos limitan ninguna de las realizaciones descritas en la presente memoria descriptiva, incluyendo las concernientes a los compuestos, las composiciones farmacéuticas o los métodos y usos divulgados en la presente.
Ejemplo 1
Preparación del precursor de adamantano
Este ejemplo ilustra cómo preparar precursores de adamantano para la unión posterior a una molécula conectora divulgada en la presente.
Esquema 1. Se disolvió ácido acético de adamantano (1,6 g, 8,2 mmol) en 20 ml de diclorometano y se trató gota a gota con dimetilformamida (2 gotas) y cloruro de oxalilo (2,1 ml, 24,7 mmol). La reacción se agitó a temperatura ambiente durante 18 horas, se concentró al vacío y se colocó bajo vacío fuerte durante la noche para
proporcionar el producto como un aceite (cuant.).
Esquema 2. Se disolvió adamantano-OH (1,6 g, 8,2 mmol) en 20 ml de diclorometano y se trató gota a gota con dimetilformamida (2 gotas) y cloruro de oxalilo (2,1 ml, 24,7 mmol). La reacción se agitó a temperatura ambiente durante 18 horas, se concentró al vacío y se colocó bajo vacío fuerte durante la noche para proporcionar el producto como un aceite (cuant.).
Ejemplo 2
Preparación del conjugado Adamantano-Conector
Esquema 3. El precursor de adamantano del esquema 1 y el conector se suspendieron en acetonitrilo y se trataron con 3 equivalentes de trietanolamina seguido de la adición de 1 equivalente de cloruro de ácido. La reacción se agitó durante 3 horas, se diluyó con acetato de etilo y se lavó con ácido clorhídrico 1 N y salmuera, se secó sobre sulfato de sodio, se concentró y se colocó a vacío alto durante la noche. Los compuestos conjugados de adamantano-conector resultantes se muestran a continuación en el esquema 3, donde n es de 0 a 10.
Esquema 4. El precursor de adamantano del esquema 1 y el conector se suspendieron en acetonitrilo y se trataron con 3 equivalentes de trietanolamina seguido de la adición de 1 equivalente de cloruro de ácido. La reacción se agitó durante 3 horas, se diluyó con acetato de etilo y se lavó con ácido clorhídrico 1 N y salmuera, se secó sobre sulfato de sodio, se concentró y se colocó a vacío alto durante la noche. Los compuestos conjugados de adamantano-conector resultantes se muestran a continuación en el esquema 4, donde n es de 0 a 10.
Esquema 5. El precursor de adamantano del esquema 2 y el conector se suspendieron en acetonitrilo y se trataron con 3 equivalentes de trietanolamina seguido de la adición de 1 equivalente de cloruro de ácido. La reacción se agitó durante 3 horas, se diluyó con acetato de etilo y se lavó con ácido clorhídrico 1 N y salmuera, se secó sobre sulfato de sodio, se concentró y se colocó a vacío alto durante la noche. Los compuestos conjugados de adamantano-conector resultantes se muestran a continuación en el esquema 5, donde n es de 0 a 10.
Usando el Esquema 5, se producen los siguientes compuestos conjugados de adamantano-conector:
Esquema 6. El precursor de adamantano del esquema 2 y el conector se suspendieron en acetonitrilo y se trataron con 3 equivalentes de trietanolamina seguido de la adición de 1 equivalente de cloruro de ácido. La reacción se agitó durante 3 horas, se diluyó con acetato de etilo y se lavó con ácido clorhídrico 1 N y salmuera, se secó sobre sulfato de sodio, se concentró y se colocó a vacío alto durante la noche. Los compuestos conjugados de adamantano-conector resultantes se muestran a continuación en el esquema 6, donde n es de 0 a 10.
Esquema 7. El precursor de adamantano del esquema 2 y el conector se suspendieron en acetonitrilo y se trataron con 3 equivalentes de trietanolamina seguido de la adición de 1 equivalente de cloruro de ácido. La reacción se agitó durante 3 horas, se diluyó con acetato de etilo y se lavó con ácido clorhídrico 1 N y salmuera, se secó sobre sulfato de sodio, se concentró y se colocó a vacío alto durante la noche. Los compuestos conjugados de adamantano-conector resultantes se muestran a continuación en el esquema 7, donde n es de 0 a 10.
Usando el Esquema 7, se producen los siguientes compuestos conjugados de adamantano-conector:
Esquema 8. El precursor de adamantano del esquema 2 y el conector se suspendieron en acetonitrilo y se trataron con 3 equivalentes de trietanolamina seguido de la adición de 1 equivalente de cloruro de ácido. La reacción se agitó durante 3 horas, se diluyó con acetato de etilo y se lavó con ácido clorhídrico 1 N y salmuera, se secó sobre sulfato de sodio, se concentró y se colocó a vacío alto durante la noche. Los compuestos conjugados de adamantano-conector resultantes se muestran a continuación en el esquema 8, donde n es de 0 a 10.
Usando el Esquema 8, se producen los siguientes compuestos conjugados de adamantano-conector:
Esquema 9. El precursor de adamantano del esquema 2 y el conector se suspendieron en acetonitrilo y se trataron con 3 equivalentes de trietanolamina seguido de la adición de 1 equivalente de cloruro de ácido. La reacción se agitó durante 3 horas, se diluyó con acetato de etilo y se lavó con ácido clorhídrico 1 N y salmuera, se secó sobre sulfato de sodio, se concentró y se colocó a vacío alto durante la noche. Los compuestos conjugados de adamantano-conector resultantes se muestran a continuación en el esquema 9, donde n es de 0 a 10.
Usando el Esquema 9, se produjeron los siguientes compuestos conjugados de adamantano-conector:
Esquema 10. El precursor de adamantano del esquema 2 y el conector se suspendieron en acetonitrilo y se trataron con 3 equivalentes de trietanolamina seguido de la adición de 1 equivalente de cloruro de ácido. La reacción se agitó durante 3 horas, se diluyó con acetato de etilo y se lavó con ácido clorhídrico 1 N y salmuera, se secó sobre sulfato de sodio, se concentró y se colocó a vacío alto durante la noche. Los compuestos conjugados de adamantano-conector resultantes se muestran a continuación en el esquema 10, donde n es de 0 a 10.
Pueden realizarse esquemas de reacción similares a los esquemas 3-10 excepto que puede sustituirse un HIF-1a por el precursor de adamantano del esquema 1 o 2.
Ejemplo 3
Preparación del conjugado HIF-1a-Conector
Esquema 11. Se suspendieron HIF-1a y el conector en acetonitrilo y se trataron con 3 equivalentes de trietanolamina seguido de la adición de 1 equivalente de cloruro de ácido. La reacción se agitó durante 3 horas, se diluyó con acetato de etilo y se lavó con ácido clorhídrico 1 N y salmuera, se secó sobre sulfato de sodio, se concentró y se colocó a vacío alto durante la noche. Los compuestos conjugados HIF-1a-conector resultantes se muestran a continuación en el esquema 11, donde n es de 0 a 10.
Pueden realizarse esquemas de reacción similares al esquema 11 excepto que puede usarse cualquiera de los otros conectores de los esquemas 3-8 o 10.
Ejemplo 4
Preparación del precursor del antagonista del receptor de andrógenos
Este ejemplo ilustra cómo preparar un antagonista de AR divulgado en la presente para la unión posterior a una molécula conectora divulgada en la presente.
El esquema 12 muestra la producción de un precursor de espironolactona reactivo. Se burbujeó metanol (50 ml) con nitrógeno durante 15 minutos, se trató con espironolactona (5 g, 12 mmol), se enfrió sobre hielo y se trató gota a gota con metóxido de sodio 5,4 M/metanol (5 ml, 27 mmol). Se retiró el baño de hielo y la reacción se agitó durante 40 minutos. La reacción se colocó en un baño de hielo y se neutralizó con ácido acético (1,5 ml) para formar un precipitado. Se añadió más metanol y la mezcla se sonicó y se filtró. Se filtró una segunda cosecha. El sólido se secó a vacío alto durante la noche y se almacenó en el congelador.
El Esquema 13 muestra la producción de un precursor de Cetoconazol reactivo. Se calentaron cetoconazol (800 mg) e hidróxido de sodio al 20% (2 ml) a reflujo en metanol (20 ml) durante la noche. La solución se enfrió a temperatura ambiente y se añadió agua. El precipitado resultante se filtró, se lavó con agua y se secó a vacío alto durante la noche para dar 700 mg.
Ejemplo 5
Preparación del conjugado antagonista de AR-adamantano-conector
Esquema 14. El precursor de espironolactona reactivo (70 mg, 0,18 mg) del esquema 12 y el precursor de adamantano del esquema 1 se disolvieron en acetonitrilo y se trataron con N,N-diisopropiletilamina (78 pl, 0,45 mmol). Se añadió cloruro de ácido (47 mg, 0,22 mmol) y la reacción se agitó durante 8 horas. La reacción se diluyó con acetato de etilo y se lavó con ácido clorhídrico 1 N y salmuera, se secó sobre sulfato de sodio y se concentró. El residuo se cristalizó a partir de acetato de etilo. Se produjo el siguiente compuesto conjugado antagonista de AR-adamantano-conector.
Esquema 15. El precursor de espironolactona reactivo (55 mg, 0,15 mmol) del esquema 12 y el conjugado de adamantano-conector (55 mg, 0,16 mmol) del esquema 4 se disolvieron en diclorometano (4 ml) y se trataron con trietanolamina (63 pl, 0,45 mmol) y cloruro de bis(2-oxo-3-oxazolidinil)fosfínico (41 mg, 0,16 mmol). La reacción se agitó durante 2 horas. Se había formado un producto mínimo. Se añadió 4-dimetilaminopiridina y se continuó agitando durante la noche. La reacción se diluyó con acetato de etilo y se lavó con bicarbonato de sodio saturado con ácido cítrico y salmuera. Se purificó por cromatografía Si Gel usando acetato de etilo. Se producen los siguientes compuestos conjugados antagonista de AR-adamantano-conector, donde n es de 0 a 10.
Usando el Esquema 15, se produjeron los siguientes compuestos conjugados de antagonista de AR-adamantano-conector:
Pueden realizarse esquemas de reacción similares al esquema 15, excepto que en lugar del precursor de adamantano del esquema 4, puede usarse cualquiera de los otros precursores de adamantano de los esquemas 3 o 5-10.
Ejemplo 6
Preparación del conjugado antagonista de AR-adamantano-conector
Esquema 16. El precursor de cetoconazol reactivo (70 mg, 0,18 mg) del esquema 13 y el precursor de adamantano del esquema 1 se disolvieron en acetonitrilo y se trataron con N,N-diisopropiletilamina (78 gl, 0,45 mmol). Se añadió cloruro de ácido (47 mg, 0,22 mmol) y la reacción se agitó durante 8 horas. La reacción se diluyó con acetato de etilo y se lavó con ácido clorhídrico 1 N y salmuera, se secó sobre sulfato de sodio y se concentró. El residuo se cristalizó a partir de acetato de etilo. Se produjo el siguiente compuesto conjugado de antagonista de AR-adamantano-conector.
Esquema 17. El precursor de cetoconazol reactivo (55 mg, 0,15 mmol) del esquema 13 y el conjugado de adamantano-conector (55 mg, 0,16 mmol) del esquema 4 se disolvieron en diclorometano (4 ml) y se trataron con 3 equivalentes de trietanolamina y 1,2 equivalentes de cloruro de bis(2-oxo-3-oxazolidinil)fosfínico. La reacción se agitó durante 2 horas. La reacción se diluyó con acetato de etilo y se lavó con bicarbonato de sodio y salmuera. Se purificó por cromatografía Si Gel usando acetato de etilo. Se producen los siguientes compuestos conjugados antagonista de AR-adamantano-conector, donde n es de 0 a 10.
Usando el Esquema 17, se produjeron los siguientes compuestos conjugados antagonista de AR-adamantano-conector:
Pueden realizarse esquemas de reacción similares al esquema 17, excepto que en lugar del precursor de adamantano del esquema 4, puede usarse cualquiera de los otros precursores de adamantano de los esquemas 3 o 5-10.
Ejemplo 7
Preparación del conjugado de AR-antagonista-HIF-1a-conector
Esquema 18. El precursor de espironolactona reactivo (55 mg, 0,15 mmol) del esquema 12 y el conjugado de HIF-1a-conector (55 mg, 0,16 mmol) del esquema 11 se disolvieron en diclorometano (4 ml) y se trataron con trietanolamina (63 pl, 0,45 mmol) y cloruro de bis(2-oxo-3-oxazolidinil)fosfínico (41 mg, 0,16 mmol). La reacción se agitó durante 2 horas. Se había formado un producto mínimo. Se añadió 4-dimetilaminopiridina y se continuó agitando durante la noche. La reacción se diluyó con acetato de etilo y se lavó con bicarbonato de sodio saturado con ácido cítrico y salmuera. Se purificó por cromatografía Si Gel usando acetato de etilo. Se producen los siguientes compuestos conjugados antagonista de AR-HIF-1a-conector, donde n es de 0 a 10.
Usando el Esquema 18, se produjeron los siguientes compuestos conjugados antagonista de AR-HIF-1aconector:
Pueden realizarse esquemas de reacción similares al esquema 18 excepto que puede usarse HIF-1a unido a cualquiera de los otros conectores de los esquemas 3-8 o 10.
Ejemplo 8
Preparación del conjugado antagonista de AR-HIF-1a-conector
Esquema 19. El precursor de cetoconazol reactivo (55 mg, 0,15 mmol) del esquema 13 y el conjugado de HIF-1a-conector (55 mg, 0,16 mmol) del esquema 11 se disolvieron en diclorometano (4 ml) y se trataron con 3 equivalentes de trietanolamina y 1,2 equivalentes de cloruro de bis(2-oxo-3-oxazolidinil)fosfínico. La reacción se agitó durante 2 horas. La reacción se diluyó con acetato de etilo y se lavó con bicarbonato de sodio y salmuera. Se purificó por cromatografía Si Gel usando acetato de etilo. Se producen los siguientes compuestos conjugados de antagonista de AR-HIF-1a-conector, donde n es de 0 a 10.
Usando el Esquema 19, se produjeron los siguientes compuestos conjugados de antagonista de AR-HIF-la-conector:
Pueden realizarse esquemas de reacción similares al esquema 19 excepto que puede usarse HIF-1a unido a cualquiera de los otros conectores de los esquemas 3-8 o 10.
Ejemplo 9
Preparación de ARE Adicionales
Usando los procedimientos descritos en los Ejemplos 4-8, se producen los siguientes ARE adicionales que comprenden metoxibencil lactama:
Pueden realizarse esquemas de reacción similares a los descritos en los Ejemplos 4-8 excepto que puede
usarse adamantano o H IF-1a unido a cualquiera de los otros conectores de los esquemas 3-9.
Ejemplo 10
Ensayo de inhibición
Este ejemplo ilustra cómo determinar la actividad inhibidora de un ARE divulgado en la presente usando un ensayo informador transcripcional del receptor de andrógenos basado en células usando una línea celular modificada.
Para el ensayo MDA-kb2, se mantuvo la línea celular de cáncer de mama de glándula mamaria MDA-kb2 en medio L-15 (Gibco) suplementado con 10 % de FBS, 100 U/ml de penicilina, 100 qg/ml de estreptomicina y 0,25 qg/ml de anfotericina B a 37° C, sin CO 2. Para los experimentos, las células se colocaron en placas a 1,0 x 104 células (50% de confluencia) por pocillo en 100 ql de medio en placas de 96 pocillos. Cuando se unieron las células (después de 6 horas), se retiró el medio y se reemplazó con medio de dosificación que contenía 10 % de FBS desprovisto de carbón vegetal.
Para el ensayo de queratinocitos, se mantuvo la línea celular normal de queratinocitos epidérmicos primarios humanos adultos (ATCC PCS-200-011) en medio EPIUFE®, con calcio 60 qM (Thermo MEPISOOCA) suplementado con suplemento de crecimiento de queratinocitos humanos, 100 U/ml de penicilina y 100 qg/ml de estreptomicina a 37° C con 5 % de CO 2. Para los experimentos, las células se sembraron al 70 % de confluencia por pocillo en 100 ql de medio en placas de 96 pocillos. La transfección inversa se realizó en las células usando Lipofectamine 3000 (Life Technologies) con plásmidos de acuerdo con las instrucciones del fabricante. Brevemente, se incubaron 0,3 ql de reactivo de transfección por 100 ng de ADN con reactivo P3000 y Opti-Mem antes de la adición de células. Después de 16 horas, se retiró el medio y se reemplazó con medio de dosificación.
Se preparó una solución madre de 5a-androstan-17p-ol-3-ona (DHT) a 1000x en etanol. Cada ARE probado se preparó en DMSO. El medio de dosificación se preparó en el momento del tratamiento diluyendo en serie la solución madre en el medio. Las concentraciones de etanol en los medios nunca superaron el 0 ,1% . SPG-001 es espironolactona; SPG-002 es cetoconazol; SPG-003 es espironolactona-adamantano ARE (Compuesto 37); SP G -004 es espironolactona-adamantano ARE (Compuesto 39); SPG-005 es cetoconazol-adamantano ARE (Compuesto 42); y SPG-006 es cetoconazol-adamantano ARE (Compuesto 40). Los pocillos de control negativo contenían 100 ql de medio/pocillo con 1 ql de etanol/ml de medio y una cantidad adecuada de DMSO. Cada placa también contenía DHT 1,0 nM con un ARE o sin un ARE como control positivo. Las células se incubaron 24 horas a 37° C sin CO 2.
Para evaluar la viabilidad celular, primero se examinaron visualmente las células bajo un microscopio de contraste de fase para registrar la confluencia celular, los cambios morfológicos y la presencia de cristalización del fármaco, así como para observar signos de citotoxicidad como por ejemplo, desprendimiento, vacuolización, degradación de la membrana o falta de brillo de fase. Después de la inspección microscópica, se realizó un ensayo de exclusión con azul de tripano para evaluar la viabilidad celular y el número de células de cada pocillo. Cada pocillo se lavó con un volumen de 0,5 ml de PBS. Se añadieron 30 ql de azul de tripano a cada pocillo durante 5-10 minutos. El número total de células y el número total de células viables se contarán a partir de 1 número de campos por pocillo, por triplicado.
Para evaluar la inhibición mediada por ARE, se realizó un ensayo de luciferasa de AR. Después de lavar las células con 1 x PBS, se añadieron 20 ql de tampón de lisis (Tris/fosfato 25 mM, EGTA 4 mM, Triton al 1 % , glicerol al 10 % , DTT 2 mM) por pocillo, se incubó durante 5 minutos con agitación suave y se almacenó a -80° C. El día del ensayo, las placas se descongelaron a temperatura ambiente y se añadieron 80 ql de tampón de ensayo (glicilglicina 25 mM, MgCl2 15 mM. ATP 5 mM, BSA 0,1 mg/ml) a cada pocillo. Luego, las placas se procesan en un lector de microplacas (POLARstar Omega) inyectando 100 ql de D-luciferina 1 mM por pocillo, seguido de una medición de quimioluminiscencia de 3 segundos al inicio de la inyección. La actividad de luciferasa se determinó, midió y normalizó a unidades de luz relativas (RLU). Los valores de reducción de la actividad del gen informador de AR se calcularon de la siguiente manera: actividad del gen informador de AR = 1 - (señal media (grupo de tratamiento) / señal media (grupo de tratamiento sin fármaco).
Para evaluar los niveles de AR, se realizó un ELISA.
En la Tabla 1 se muestran los resultados de dos ensayos independientes de MDA-kb2. Se observó una inhibición dependiente de la dosis de la actividad del gen informador de AR para todos los compuestos probados. Además, la adición de un promotor de la eliminación o un elemento potenciador de la eliminación de AR aumentó significativamente el grado de inhibición observado. Por ejemplo, la espironolactona demostró una reducción del 4 1 % en la actividad del gen informador de AR a 10 qM, mientras que SPG-003 mostró una reducción del 90 % en la actividad del gen informador de AR a 10 qM (Tabla 1). De manera similar, el cetoconazol demostró una reducción del 43 % en la actividad del gen informador de AR a 10 qM, mientras que SPG-005 mostró una reducción del 80 % en la actividad del gen informador de AR a 10 qM (Tabla 1). También se observó una reducción dependiente de la dosis
en los niveles de proteína de AR para todos los compuestos probados. Además, la adición de un promotor de la eliminación o un elemento potenciador de la eliminación de AR aumentó significativamente el grado de inhibición observado. Por ejemplo, la espironolactona demostró una reducción del 35% en el nivel de proteína de AR a 10 pM, mientras que SPG-003 mostró una reducción del 71% en el nivel de proteína de AR a 10 pM (Tabla 1). De manera similar, el cetoconazol demostró una reducción del 10% en el nivel de proteína de AR a 10 pM, mientras que SPG-005 mostró una reducción del 54% en el nivel de proteína de AR a 10 pM (Tabla 1).
En la Tabla 2 se muestran los resultados de los ensayos de queratinocitos. Se observó una inhibición dependiente de la dosis de la actividad del gen informador de AR para todos los compuestos probados. Además, la adición de un promotor de la eliminación o un elemento potenciador de la eliminación de AR aumentó significativamente el grado de inhibición observado. Por ejemplo, la espironolactona demostró una reducción del 59% en la actividad del gen informador de AR a 10 pM, mientras que SPG-003 mostró una reducción del 93% en la actividad del gen informador de AR a 10 pM (Tabla 2). De manera similar, el cetoconazol demostró una reducción del 56% en la actividad del gen informador de AR a 10 pM, mientras que SPG-005 mostró una reducción del 90% en la actividad del gen informador de AR a 10 pM (Tabla 2). También se observó una reducción dependiente de la dosis en los niveles de proteína de AR para todos los compuestos probados. Además, la adición de un promotor de la eliminación o un elemento potenciador de la eliminación de AR aumentó significativamente el grado de inhibición observado. Por ejemplo, la espironolactona demostró una reducción del 51% en el nivel de proteína de AR a 10 pM, mientras que SPG-003 mostró una reducción del 65% en el nivel de proteína de AR a 10 pM (Tabla 2). De manera similar, el cetoconazol demostró una reducción del 20% en el nivel de proteína de AR a 10 pM, mientras que SPG-005 mostró una reducción del 65% en el nivel de proteína de AR a 10 pM (Tabla 2).
continuación
Ejemplo 11
Ensayo de inhibición
Este ejemplo ilustra cómo determinar la actividad inhibidora de un ARE divulgado en la presente usando un ensayo informador transcripcional del receptor de andrógenos basado en células usando queratinocitos humanos primarios.
Para el ensayo de queratinocitos, se mantuvo la línea celular normal de queratinocitos epidérmicos primarios humanos adultos (ATCC PCS-200-011) en medio EPIUFE®, con calcio 60 pM (Thermo MEPISOOCA) suplementado con suplemento de crecimiento de queratinocitos humanos, 100 U/ml de penicilina y 100 pg/ml de estreptomicina a 37° C con 5% de C02. Para los experimentos, las células se sembraron al 70% de confluencia por pocillo en 100 pl de medio en placas de 96 pocillos. Se realizó transfección inversa en las células usando Lipofectamine 3000 (Life Technologies) con plásmidos de acuerdo con las instrucciones del fabricante. Brevemente, se incubaron 0,3 pl de reactivo de transfección por 100 ng de ADN con reactivo P3000 y Opti-Mem antes de la adición de células. Después de 16 horas, se retiró el medio y se reemplazó con medio de dosificación.
Para evaluar la inhibición mediada por ARE, se realizó un ensayo de luciferasa de AR como se describe en el Ejemplo 10. Para evaluar los niveles de AR, se realizó un ELISA como se describe en el Ejemplo 10.
Se preparó una solución madre de niclosamida a 1000x en etanol. Cada ARE probado se preparó en DMSO. El medio de dosificación se preparó en el momento del tratamiento diluyendo en serie la solución madre en el medio. Las concentraciones de etanol en los medios nunca superaron el 0,1%. SPG-001 es espironolactona; SPG-002 es cetoconazol; SPG-003 es espironolactona-adamantano ARE (Compuesto 37); y SPG-005 es cetoconazol-adamantano ARE (Compuesto 42). Los pocillos de control negativo contenían 100 pl de medio/pocillo con 1 pl de etanol/ml de medio y una cantidad adecuada de DMSO. Cada ARE se aplicó a los queratinocitos en concentraciones de hasta 50 pM. Cada placa también contenía niclosamida 1,0 nM con un ARE o sin un ARE como control positivo. Las células se incubaron 72 horas a 37° C sin CO2.
Los resultados se muestran en la Tabla 3. Los valores de IC50 se calcularon de la siguiente manera: SPG-001: 50 pM; SPG-002: 11 pM; SPG-003: aproximadamente 50 pM; SPG-005: 2 pM; y niclosamida: <0,2 pM. Los resultados mostraron que tanto SPG-001 como SPG-003 tenían esencialmente los mismos efectos citotóxicos con valores de IC50 equivalentes cuando se aplicaban 50 pM de cada uno a los queratinocitos. La niclosamida, un
fármaco que previamente se había demostrado que era citotóxico para estas células, tenía una IC50 por debajo de 0,2 pM. Estos resultados indican que SPG-003 tenía una citotoxicidad en las células de la piel comparable a la de su compuesto original, el antagonista de AR, espironolactona (Tabla 3).
Ejemplo 12
Ensayo de inhibición
Este ejemplo ilustra cómo determinar la actividad inhibidora de un ARE divulgado en la presente usando un ensayo informador transcripcional del receptor de andrógenos basado en células usando queratinocitos humanos primarios.
Para evaluar la inhibición mediada por ARE, se realizó un ensayo de luciferasa de R como se describe en el Ejemplo 10 para examinar los efectos de SPG-001 (espironolactona), SPG-002 (cetoconazol), SPG-003 (un espironolactona-adamantano ARE, compuesto 37), SPG-007 (un cetoconazol-HIF-1a ARE, Compuesto 47), SPG-008 (un cetoconazol-HIF-1a ARE, Compuesto 49) y SPG-009 (un espironolactona-HIF-1a ARE, Compuesto 43) después de exposición continua durante 24 y 72 horas. Para evaluar los niveles de AR, se realizó un ELISA como se describe en el Ejemplo 10. Los resultados se analizaron para los valores de IC50 e IC90 en GraphPad Prism usando una ecuación de curva logística de cuatro parámetros. Las restricciones inferiores se establecieron en 1 (nivel de control no inducido). Todos los valores informados tenían un valor R-cuadrado superior a 0,96.
En ambos puntos temporales de este experimento, SPG-003 fue superior a SPG-001 (Tabla 4). Por ejemplo, la inhibición máxima observada de la actividad del gen informador fue del 65% para SPG-001 y del 91% para SPG-003 después de 24 horas de tratamiento. La IC50 para SPG-003 para el tratamiento de 24 horas fue de 3,7 pM y la IC90 fue de 7 pM. Ninguno de los parámetros pudo calcularse para SPG-001 en este experimento. SPG-003 fue el compuesto con mejor rendimiento del grupo probado en este estudio.
Como se vio en el tratamiento de 24 horas, SPG-003 fue superior a SPG-001 tanto en IC50 como en IC90 , así como en la inhibición máxima observada de la actividad del gen informador después del tratamiento de 72 horas. Curiosamente, la IC50 calculada de SPG-003 se redujo de 3,7 pM a 2,5 pM (Tabla 4). La IC90 calculada de SPG-003 también se redujo de 7 pM a 5,7 pM (Tabla 4). Esto sugiere que el tratamiento prolongado con SPG-003 da como resultado una mejor inhibición del gen informador de AR objetivo. Se observó una inhibición dependiente de la dosis de la actividad del gen informador de AR para SPG-003. SPG-003 aumentó la potencia y la inhibición de la actividad del gen informador de AR con un tratamiento prolongado, mientras que la citotoxicidad celular fue mínima en los queratinocitos humanos.
Los efectos sostenidos de SPG-001 frente a SPG-003 también se examinaron en queratinocitos humanos transfectados con un gen informador de luciferasa de AR. Las células se transfectaron con el gen informador y luego se trataron con SPG-001 7 pM o SPG-0037 pM durante 24 horas. Después de 24 horas, se lavaron las células y se reemplazó el medio por medio nuevo que no contenía ningún antagonista de AR. La actividad del gen informador se midió después de dos días o tres días de cultivo celular adicional en ausencia de antagonistas de AR. La reducción
de la actividad del gen informador de AR se calculó de la siguiente manera: 1-(señal media (grupo de tratamiento)/(señal media (grupo de tratamiento, sin fármaco, mismo período de lavado).
Los resultados de ese experimento mostraron que SPG-003 tenía una inhibición sostenida de la actividad del gen informador durante tres días que fue significativamente mejor que lo que se observó con las células tratadas con SPG-001. Por ejemplo, como se ve en la Tabla 5, tres días después de la eliminación de SPG-003, la actividad del gen informador se suprimió en un 48% en las células tratadas con SPG-003. Sin embargo, las células tratadas con SPG-001 a esa misma concentración solo mostraron una inhibición del 24% del gen informador. Estos datos destacan nuevamente la superioridad de SPG-003 como antagonista de AR en comparación con su compuesto original SPG-001 (espironolactona). La viabilidad celular estuvo entre el 90% y el 100% para ambos compuestos durante la duración de este estudio.
Ejemplo 13
Ensayo de inhibición
Este ejemplo ilustra cómo determinar la actividad inhibidora de un ARE divulgado en la presente usando un ensayo indicador transcripcional del receptor de andrógenos basado en células usando queratinocitos humanos primarios.
Para determinar la eficacia de un compuesto, se realizó un ensayo de MDA-kb2 como se describe en el Ejemplo 10. Las células se trataron con compuestos durante 24 horas antes de medir la actividad del gen informador. La IC50 y la IC90 de SPG-001 y SPG-003 se determinaron en células MDA-kb2 tratadas con DHT 0,1 nM durante 24 horas. Los resultados del ensayo de luciferasa de AR se analizaron utilizando GraphPad Prism usando una ecuación de curva logística de cuatro parámetros. Las restricciones inferiores se establecieron en 1 (nivel de control no inducido).
A pesar de que los niveles hormonales se redujeron para modelar mejor los parámetros de la piel humana femenina, la actividad del gen informador seguía siendo bastante significativa con una inducción de 12 veces con respecto a las células de control no expuestas a DHT. En este experimento, SPG-001 no tenía capacidad aparente para inhibir la actividad del gen informador. El acetato de ciproterona, un antagonista de AR aprobado demostró en realidad actividad agonista de AR en concentraciones superiores a 3,3 pM con actividad antagonista limitada a concentraciones inferiores a 1 pM. SPG-003 mostró una inhibición máxima de la actividad del gen informador del 95%, una IC50 de 789 nM, una IC90 de 2,71 pM. La viabilidad de las células de cáncer de mama MDA-kb2 comenzó a disminuir del 80% al 50% con el tratamiento con 6 pM a 10 pM de SPG-003, aunque este fenómeno no se había visto anteriormente en experimentos similares con esta línea celular y debe investigarse más detenidamente. Estos experimentos demostraron una inhibición dependiente de la dosis de la actividad del gen informador de AR para SPG-003. Esta inhibición dependiente de la dosis no se observó para SPG-001 o acetato de ciproterona en condiciones de niveles de DHT reducidos (relatividad de 10 veces en experimentos anteriores).
Ejemplo 14
Estudios de Formulación
Se realizó un estudio para desarrollar una formulación experimental para la administración tópica de SPG-003 a piel humana y de ratón. Los resultados de esos estudios identificaron formulaciones experimentales que luego se aplicaron a la piel humana y de ratón usando cámaras de FDC estándar. A partir de estos estudios de formulación se identificó como óptima una formulación que consiste de IPM/Etanol/Transcutol/49.8/30/20 p/p/p. Estos estudios
demostraron una penetración significativa en la dermis y la epidermis de SPG-003 y sugirieron que estas formulaciones podrían usarse para inhibir eficazmente la AR in vivo cuando se aplican tópicamente.
Se realizaron pruebas de detección de solubilidad en 8 sistemas de solventes: (1) Transcutol:Etanol: miristato de isopropilo (IPM) 2:3:5 (v:v); (2) Transcutol:Etanol 3:7 (v:v); (3) Etanol:propilenglicol 1:1 (v:v); (4) Etanol:H2O 7:3 (v:v); (5) IMP; (6) Etanol:Tween 80:Alcohol cetílico 90:5:5(p:p); (7) C C T: Tween 80: alcohol cetílico 90:5:5 (p:p); y (8) CCT:isopropanol 1 :1 (v:v). Estos sistemas de solventes se seleccionaron de la base de datos de ingredientes inactivos (IIG) de la FDA. Uno de los objetivos era identificar sistemas de solventes para la formulación de soluciones con una concentración API objetivo del 1 % en peso. Otro objetivo era identificar solventes que fuesen potencialmente buenos potenciadores de la penetración y, sin embargo, clínicamente viables. Como el alcohol cetílico es sólido, los sistemas solventes con ellos se prepararon en proporciones ponderadas.
Para los sistemas de solventes (3), (4), (5) y (7), SPG-003 no fue soluble después de una sonicación extensa. Para el solvente (1), (2), (6) y (8), SPG-003 tuvo buena solubilidad en esos sistemas de solventes. Se seleccionó Transcutol:Etanol:IPM 2:3:5 (v:v) como formulación de solución ya que tiene un buen potenciador de la penetración (Transcutol) y un IPM de lípidos (clínicamente viable).
Para examinar la capacidad de penetración de la formulación SPG-003, se realizaron dos ensayos diferentes. La formulación de SPG-003 se preparó añadiendo SPG-003 (concentración final del 1 ,0 % en peso) a una mezcla que comprendía 30 % de alcohol desnaturalizado. 49 de IPM, 20 % de Transcutol y sonicando esta mezcla hasta que se disolvió el compuesto.
Se adquirió tejido de piel de cadáver humano de un banco de tejidos en los Estados Unidos. Se usaron dos lotes de tejido de piel dermatomado. Datos demográficos del donante: tejido 08033 (espesor medio: 397 pm): sexo = masculino, edad = 58, raza = caucásico y sitio anatómico = abdomen; tejido 08696 (espesor medio: 1040 pm): sexo = masculino, edad = 50, raza = caucásico y sitio anatómico = abdomen. El espesor se midió usando un calibre de presión digital. Duplicado para cada donante (N = 2). El tejido se recibió en envases de hielo seco. Se almacenó a -20° C hasta su uso.
Después de pasar la inspección visual inicial, se evaluó la integridad de la barrera del tejido de la piel usando medición de la resistencia eléctrica transepidérmica (medición TEER). La medición se realizó usando un medidor LCR a una frecuencia de 100 Hz a temperatura ambiente. El medio de medición fue una solución de NaCl al 0,9%, usando un par de electrodos de acero inoxidable. Antes del estudio de absorción y penetración en la piel, se evaluó el valor de la resistencia eléctrica de cada lote de tejido de piel humana. Debido a la posible variación de lote a lote en la edad, el sexo, la raza y el sitio anatómico del donante, el objetivo de la medición fue establecer el valor umbral para el tejido de cadáver intacto para cada lote que se usará en el presente estudio de absorción y penetración en la piel. Se tomaron seis (6) muestras de tejido de puntos seleccionados de cada lote. Se midió el valor de resistencia eléctrica transepidérmica (medida TEER, valor Z). Todos los valores de TEE R informados son valores netos después de restar la muestra en blanco del medio de medición (aproximadamente 1,3 KOhms). Se determinó que el valor de TEE R umbral era de 6,0 KOhms para el donante 08033 y de 10 KOhms para el donante 08696. Para aquellos tejidos con defectos visibles, el valor de TEE R se encontró en el intervalo de 0,1 KOhms a 0,5 KOhms.
El estudio de selección de la formulación se llevó a cabo en una estación de selección de alto rendimiento (HTS). Las muestras de tejido de la piel (después de lavarlas con PBS 1x, pH 7,4) se montaron en celdas de difusión en la estación de HTS. En el estudio se usaron un total de 4 celdas. Cada celda de la estación tiene un área de difusión de 0,503 cm2 (8 mm de diámetro). Cada celda individual es de tipo Franz-Cell estático. La cámara receptora se llenó con 3,0 ml de BSA al 4 % en agua, suplementada con sulfato de gentamicina al 0 ,01% , que se mezcló enérgica y continuamente. La temperatura se estableció en 32 ± 0,1° C. Las muestras de tejido en las células HTS se equilibraron a 32 ± 0 ,1° C durante 1 hora antes de la dosificación. La dosis de formulación de SPG-003 aplicada para cada muestra fue de 5,0 pl y cada muestra se procesó en dos repeticiones.
El punto temporal de recopilación de datos fue 8 horas. Al final del intervalo de tiempo, se retiraron los tejidos de la piel de las celdas. La superficie del tejido se limpió cuidadosamente con un hisopo humedecido con agua destilada, seguido de una limpieza con un hisopo seco una vez; luego, se limpió con un hisopo humedecido con agua destilada, y luego se limpió con un hisopo seco una vez más. Luego, se realizaron dos ciclos de desprendimiento con cinta para eliminar la formulación residual que quedaba en la superficie de la piel (no absorbida/no penetrada). Luego, se usó el método estándar de desprendimiento con cinta para eliminar la capa de SC. Se usó cinta Scotch en el proceso de desprendimiento con de cinta. El ciclo de desprendimiento con cinta se repitió un total de 15 veces. Se ha establecido en nuestro laboratorio que 15 ciclos de desprendimiento son suficientes para eliminar completamente la capa de S C de la piel de un cadáver humano. Las tiras de cinta recogidas se desecharon. Después de retirar la capa de SC, la epidermis y la capa dérmica se cortaron en pedazos y se extrajeron con 7,0 ml de DMSO/ACN = 1 :1 v/v durante la noche a temperatura ambiente usando un agitador orbital. Los extractos fueron recolectados y estaban listos para el análisis. El fluido receptor se recogió y preparó para el análisis. Se desarrolló un método de cromatografía líquida-espectrometría de masas en tándem (LC-MS/MS) para la
cuantificación de SPG-003 en BSA y piel humana empapada en muestras de matriz DMSO/ACN=1:1 v/v. El intervalo de concentración de la calibración SPG-003 fue de 1 ng/ml a 120 ng/ml para la matriz BSA y de 10 ng/ml a 1000 ng/ml para la piel del oído humano empapada en muestras de matriz DMSO/ACN=1:1 v/v.
El compuesto SPG-003 muestra una cantidad limitada de penetración en la piel, pero una buena cantidad de retención en la piel en la epidermis y la dermis después de 8 horas de exposición.
En base a los resultados anteriores, se realizó un estudio similar de penetración en la piel usando un modelo de piel de hámster. Tanto SPG-003 como la espironolactona se formularon con Transcutol:Etanol:IPM 2:3:5 (v:v) como se ha descrito anteriormente. La dosis de formulación aplicada para cada muestra fue de 10,0 pl y cada muestra se procesó en cuatro repeticiones. Las muestras se evaluaron en el punto temporal de 8 horas para determinar la absorción del compuesto en las capas epidérmica y dérmica y la penetración en el medio receptor.
El compuesto SPG-003 tiene una cantidad limitada de penetración en la piel, pero tiene una buena cantidad de absorción en la piel. En otras palabras, se retuvo principalmente en la capa de epidermis/dermis. El compuesto de espironolactona tiene una buena cantidad de penetración y absorción en la piel.
Ejemplo 15
Estudios de alopecia androgenética in vivo
Estos experimentos probaron la estabilidad de la formulación SPG-003 en una solución así como homogeneizado de piel de ratón.
Para probar la estabilidad de la formulación en solución, se pesaron aproximadamente 100 mg de la formulación de SPG-003 en un vial de 4 ml y se añadieron 3 ml de etanol para disolver completamente la formulación. Luego se añadieron 300 pl de solución de etanol a 700 pl de acetonitrilo/HLO (70/30 v/v) para hacer 1 ml de solución final y se mezcló bien para el análisis HPLC. Las formulaciones en solución de SPG-003 se almacenaron a temperatura ambiente (20° C) y 4° C hasta 21 días y la potencia se probó en T0 y 21 días.
Para probar la estabilidad de la formulación en un homogeneizado de tejido, la formulación de SPG-003 se incubó en un homogeneizado de piel de ratón a 32° C durante 24 horas. Después de este período de incubación, se añadió 10 veces el volumen de acetonitrilo a las muestras de homogeneizado para inactivar la reacción y precipitar la proteína. Luego, las muestras se centrifugaron y el sobrenadante claro se analizó por HPLC.
Estos experimentos indican que la formulación de SPG-003 muestra una buena estabilidad en solución durante por lo menos hasta 21 días de almacenamiento tanto a temperatura ambiente como a 4° C. Además, esta formulación es estable en homogeneizado de piel de ratón hasta 24 horas de incubación a 32° C.
Ejemplo 16
Estudios de alopecia androgenética in vivo
Se utilizará un modelo de ratón de alopecia androgenética para demostrar la actividad de un ARE divulgado en la presente. Se afeitará y depilará el dorso de ratones C57BL/6 macho de 7 semanas de edad al comienzo del estudio y se aplicarán 100 ul de testosterona al 1% en el dorso de cada ratón diariamente para suprimir el rebrote del cabello. También se aplicarán 10 ul de cada ARE tópicamente diariamente a ratones en presencia de testosterona al 1%. La depilación sincronizará todos los folículos pilosos en la fase de crecimiento o anágena del ciclo del cabello, mientras que la testosterona exógena actuará para suprimir el crecimiento del cabello. En ausencia de testosterona, el nuevo crecimiento completo del cabello generalmente se produce en el plazo de 14 días. La presencia de testosterona retrasa el crecimiento del cabello durante unos 7 días. Hasta la adición de un ARE, se revertirá el retraso en el rebrote, demostrando de este modo la capacidad del compuesto para bloquear los efectos inhibidores del crecimiento del cabello de los andrógenos in vivo. Cada grupo de tratamiento experimental de ratones consistirá de 8-10 animales.
Ejemplo 17
Modelo de reducción de sebo in vivo
Se usará el modelo de oreja de hámster sirio para demostrar la capacidad de un ARE divulgado en la presente de suprimir la producción de sebo cuando se aplica tópicamente. Cada ARE se aplicará durante dos semanas. Al finalizar el estudio, se sacrificarán los animales, se extraerán los ésteres de cera y se analizará el contenido de lípidos, ya que se ha demostrado que se correlaciona muy bien con la producción de sebo. Además, se evaluará histológicamente el tamaño de las glándulas sebáceas como una medida independiente de la producción de sebo. Se ha demostrado que los antagonistas orales de AR, como la espironolactona y el acetato de ciproterona, son eficaces para reducir la producción de sebo y la gravedad del acné en las mujeres.
Para terminar, debe entenderse que aunque los aspectos de la presente memoria descriptiva se destacan haciendo referencia a realizaciones específicas, un experto en la técnica apreciará fácilmente que estas realizaciones descritas son solo ilustrativas de los principios de la materia divulgada en la presente. Por lo tanto, debe entenderse que la materia divulgada no se limita de ninguna manera a un compuesto, composición, artículo, aparato, metodología, protocolo y/o reactivo, etc., particular descrito en la presente, a menos que se indique expresamente como tal. Además, los expertos en la técnica reconocerán que pueden realizarse ciertos cambios, modificaciones, permutaciones, alteraciones, adiciones, sustracciones y subcombinaciones de los mismos de acuerdo con las enseñanzas de la presente.
En la presente se describen ciertas realizaciones de la presente invención, incluyendo el mejor modo conocido por los inventores para llevar a cabo la invención. Por supuesto, las variaciones de estas realizaciones descritas resultarán evidentes para los expertos en la técnica tras leer la descripción anterior. El inventor espera que los expertos en la técnica empleen tales variaciones según sea apropiado, y los inventores pretenden que la presente invención sea puesta en práctica de maneras distintas a la descrita específicamente en la presente. Por consiguiente, esta invención incluye todas las modificaciones y equivalentes de la materia enumerada en las reivindicaciones adjuntas según lo permitido por la ley aplicable. Además, cualquier combinación de las realizaciones descritas anteriormente en todas las posibles variaciones de las mismas está abarcada por la invención a menos que se indique lo contrario en la presente o se contradiga claramente por el contexto.
Las agrupaciones de realizaciones, elementos o pasos alternativos de la presente invención no deben interpretarse como limitaciones. Se puede hacer referencia a cada miembro del grupo y reivindicarlo individualmente o en cualquier combinación con otros miembros del grupo divulgados en la presente. Se anticipa que uno o más miembros de un grupo pueden incluirse o eliminarse de un grupo por razones de conveniencia y/o patentabilidad. Cuando se produce dicha inclusión o eliminación, se considera que la memoria descriptiva contiene el grupo modificado, cumpliendo por tanto la descripción escrita de todos los grupos Markush usados en las reivindicaciones adjuntas.
A menos que se indique lo contrario, todos los números que expresan una característica, artículo, cantidad, parámetro, propiedad, término, y demás usados en la presente memoria descriptiva y reivindicaciones, deben entenderse modificados en todos los casos por el término "aproximadamente". Como se usa en el presente, el término "aproximadamente" significa que la característica, el artículo, la cantidad, el parámetro, la propiedad o el término así calificado abarca un intervalo de más o menos el diez por ciento por encima y por debajo del valor de la
característica, el artículo, la cantidad o el parámetro, propiedad o término expuestos. Por consiguiente, a menos que se indique lo contrario, los parámetros numéricos expuestos en la memoria descriptiva y reivindicaciones adjuntas son aproximaciones que pueden variar. Por ejemplo, como los instrumentos de espectrometría de masas pueden variar ligeramente en la determinación de la masa de un analito dado, el término "aproximadamente" en el contexto de la masa de un ion o la relación masa/carga de un ion se refiere a /-0,50 unidades de masa atómica. Como mínimo, y no como un intento de limitar la aplicación de la doctrina de los equivalentes al alcance de las reivindicaciones, cada indicación numérica debe interpretarse por lo menos a la luz del número de dígitos significativos informados y aplicando técnicas ordinarias de redondeo.
El uso de los términos "podría" o "puede" en referencia a una realización o aspecto de una realización también conlleva el significado alternativo de "no podría" o "no puede". Como tal, si la presente memoria descriptiva divulga que una realización o un aspecto de una realización puede incluirse como parte de la materia de la invención, entonces la limitación negativa o condición de exclusión también se entiende explícitamente, lo que significa que una realización o un aspecto de una realización podría no ser o no puede ser incluido como parte de la materia inventiva. De manera similar, el uso del término "opcionalmente" en referencia a una realización o aspecto de una realización significa que dicha realización o aspecto de la realización podría incluirse como parte del objeto de la invención o puede no estar incluido como parte del objeto de la invención. La aplicación de dicha limitación negativa o condición de exclusión se basará en si la limitación negativa o la condición de exclusión se enumeran en la materia reivindicada.
A pesar de que los intervalos y valores numéricos que establecen el amplio alcance de la invención son aproximaciones, los intervalos y valores numéricos expuestos en los ejemplos específicos se informan con la mayor precisión posible. Sin embargo, cualquier intervalo o valor numérico contiene inherentemente ciertos errores que resultan necesariamente de la desviación estándar encontrada en sus respectivas mediciones de prueba. La enumeración de intervalos numéricos de valores en la presente tiene la intención de servir simplemente como un método abreviado para referirse individualmente a cada valor numérico separado que se encuentra dentro del intervalo. A menos que se indique lo contrario en la presente, cada valor individual de un intervalo numérico se incorpora en la presente memoria descriptiva como si se mencionara individualmente en la presente.
Debe interpretarse que los términos "un", "uno", "el" y referencias similares usadas en el contexto de la descripción de la presente invención (especialmente en el contexto de las siguientes reivindicaciones) cubren tanto el singular como el plural, a menos que se indique lo contrario en la presente o se contradiga claramente por el contexto. Además, los indicadores ordinales, como "primero", "segundo", "tercero", etc., para elementos identificados se usan para distinguir entre los elementos, y no indican ni implican un número requerido o limitado de tales elementos, y no indican una posición u orden particular de dichos elementos a menos que se indique específicamente lo contrario. Todos los métodos descritos en la presente pueden realizarse en cualquier orden adecuado a menos que se indique lo contrario en la presente o que el contexto lo contradiga claramente. El uso de cualquiera y todos los ejemplos, o el lenguaje de ejemplo (por ejemplo, "como") que se proporciona en la presente pretende simplemente ilustrar mejor la presente invención y no supone una limitación del alcance de la invención reivindicada de otro modo. Ningún lenguaje en la presente memoria descriptiva debe interpretarse como indicación de cualquier elemento no reivindicado esencial para la puesta en práctica de la invención.
Cuando se usa en las reivindicaciones, ya sea como se presentó o se añadió por modificación, el término de transición abierto "que comprende" (y las frases de transición abiertas equivalentes del mismo, como que incluye, que contiene y que tiene) abarca todos los elementos, limitaciones, pasos y características enumerados expresamente solos o en combinación con una materia no enumerada; los elementos, limitaciones y/o características nombradas son esenciales, pero pueden añadirse otros elementos, limitaciones y/o características no nombrados y seguir formando un constructo dentro del alcance de la reivindicación. Las realizaciones específicas divulgadas en la presente pueden estar más limitadas en las reivindicaciones usando las frases de transición cerradas "que consiste de" o "que consiste esencialmente de" en lugar de o como una modificación de "que comprende". Cuando se usa en las reivindicaciones, ya sea como se presentó o se añadió por modificación, la frase de transición cerrada "que consiste de" excluye cualquier elemento, limitación, paso o característica que no se enumere expresamente en las reivindicaciones. La frase de transición cerrada "que consiste esencialmente de" limita el alcance de una reivindicación a los elementos, limitaciones, pasos y/o características expresamente enumerados y a cualquier otro elemento, limitación, paso y/o característica que no afecte materialmente a la característica o características básicas y novedosas de la materia reivindicada. Por tanto, el significado de la frase de transición abierta "que comprende" se define como que abarca todos los elementos, limitaciones, pasos y/o características enumerados específicamente, así como cualquiera de ellos opcional adicional no especificado. El significado de la frase de transición cerrada "que consiste de" se define como que solo incluye esos elementos, limitaciones, pasos y/o características enumerados específicamente en la reivindicación, mientras que el significado de la frase de transición cerrada "que consiste esencialmente de" se define como que solo incluye aquellos elementos, limitaciones, pasos y/o características enumerados específicamente en la reivindicación y aquellos elementos, limitaciones, pasos y/o características que no afectan materialmente a las características básicas y novedosas de la materia reivindicada. Por lo tanto, la frase de transición abierta "que comprende" (y las frases de transición abiertas equivalentes de la misma) incluye dentro de su significado, como caso limitante, la materia
reivindicada especificada por las frases de transición cerrada "que consiste de" o "que consiste esencialmente de". Como tales realizaciones descritas en la presente o reivindicadas con la frase "que comprende" se describen, habilitan o respaldan expresa o inherentemente de manera inequívoca en la presente las frases “que consiste esencialmente de” y “que consiste de”.
Todas las patentes, publicaciones de patentes y otras publicaciones a las que se hace referencia e identifican en la presente memoria descriptiva se proporcionan únicamente para su divulgación antes de la fecha de presentación de la presente solicitud. Nada en este sentido debe interpretarse como una admisión de que los inventores no tienen derecho a anteceder dicha divulgación en virtud de una invención anterior o por cualquier otra razón. Todas las exposiciones en cuanto a la fecha o representación en cuanto al contenido de estos documentos se basan en la información disponible para los solicitantes y no constituye ninguna admisión en cuanto a la exactitud de las fechas o el contenido de estos documentos.
Por último, la terminología usada en la presente tiene el propósito de describir realizaciones particulares únicamente, y no se pretende que limite el alcance de la presente invención, que se define únicamente por las reivindicaciones. Por consiguiente, la presente invención no se limita precisamente a lo que se muestra y describe.
Claims (1)
- REIVINDICACIONES1. Un compuesto seleccionado del grupo que consiste de:donde n es cualquier número entero de 0 a 10, yfórmula XXIdonde n es cualquier número entero de 0 a 10.2. El compuesto de la reivindicación 1, en donde n es cualquier número entero de 0 a 6 para la fórmula XX. 3. El compuesto de la reivindicación 2, en donde n es cualquier número entero de 0 a 4 para la fórmula XX. 4. El compuesto de la reivindicación 3, en donde la fórmula XX es5. El compuesto de la reivindicación 1, en donde n es cualquier número entero de 0 a 6 para la fórmula XXI.6. El compuesto de la reivindicación 5, en donde n es cualquier número entero de 0 a 4 para la fórmula XXI.7. El compuesto de la reivindicación 6, en donde la fórmula XXI eso9. La composición farmacéutica de acuerdo con la reivindicación 8, que comprende además uno o más portadores farmacéuticamente aceptables y/o uno o más componentes farmacéuticamente aceptables.10. La composición farmacéutica de acuerdo con la reivindicación 9, que comprende del 0,1% al 10% de un compuesto de acuerdo con cualquiera de las reivindicaciones 1-7, del 20% al 40% de alcohol desnaturalizado, del 40% al 60% de miristato de isopropilo y del 10% al 30% de Transcutol.11. La composición farmacéutica de acuerdo con la reivindicación 10, que comprende del 0,5% al 5% de un compuesto de acuerdo con cualquiera de las reivindicaciones 1-7, del 25% al 35% de alcohol desnaturalizado, del 45% al 55% de miristato de isopropilo y del 15% al 25% de Transcutol.12. Un compuesto de cualquiera de las reivindicaciones 1-7 o una composición farmacéutica de cualquiera de las reivindicaciones 8-11 adecuada para su uso en el tratamiento de la caída del cabello, debilitamiento del cabello, pérdida del color del cabello.13. Un compuesto de cualquiera de las reivindicaciones 1-7 o una composición farmacéutica de cualquiera de las reivindicaciones 8-11 para su uso en el tratamiento del trastorno degenerativo de folículos pilosos.14. Un compuesto de cualquiera de las reivindicaciones 1-7 o una composición farmacéutica de cualquiera de las reivindicaciones 8-11 adecuada para su uso en el tratamiento de problemas del cabello, preferiblemente alopecia androgénica e hirsutismo facial.15. Un compuesto de cualquiera de las reivindicaciones 1-7 o una composición farmacéutica de cualquiera de las reivindicaciones 8-11 adecuada para su uso en el tratamiento de problemas de la piel preferiblemente acné, producción excesiva de sebo y formación de cicatrices después de heridas.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762492822P | 2017-05-01 | 2017-05-01 | |
| PCT/US2018/030538 WO2018204422A1 (en) | 2017-05-01 | 2018-05-01 | Tripartite androgen receptor eliminators, methods and uses thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2910976T3 true ES2910976T3 (es) | 2022-05-17 |
Family
ID=64016717
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES18794821T Active ES2910976T3 (es) | 2017-05-01 | 2018-05-01 | Eliminadores de receptores de andrógenos tripartitos, métodos y usos de los mismos |
Country Status (9)
| Country | Link |
|---|---|
| US (2) | US11447483B2 (es) |
| EP (1) | EP3618833B1 (es) |
| JP (1) | JP7061135B2 (es) |
| KR (1) | KR102746106B1 (es) |
| CN (1) | CN110831601B (es) |
| AU (1) | AU2018261331C1 (es) |
| CA (1) | CA3062161A1 (es) |
| ES (1) | ES2910976T3 (es) |
| WO (1) | WO2018204422A1 (es) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018071606A1 (en) | 2016-10-11 | 2018-04-19 | Arvinas, Inc. | Compounds and methods for the targeted degradation of androgen receptor |
| BR112019015484A2 (pt) | 2017-01-31 | 2020-04-28 | Arvinas Operations Inc | ligantes de cereblon e compostos bifuncionais compreendendo os mesmos |
| CN110746399B (zh) * | 2018-07-23 | 2022-04-22 | 上海美志医药科技有限公司 | 具有降解雄激素受体活性的化合物 |
| CN109762045A (zh) * | 2018-12-14 | 2019-05-17 | 中山大学附属第一医院 | 一种双靶点构建protac的方法及其用途 |
| CA3165168A1 (en) | 2019-12-19 | 2021-06-24 | Arvinas Operations, Inc. | Compounds and methods for the targeted degradation of androgen receptor |
| CN115996918A (zh) | 2020-05-09 | 2023-04-21 | 阿尔维纳斯运营股份有限公司 | 制造双官能团化合物的方法、双官能团化合物的超纯形式以及包括所述双官能团化合物的剂型 |
| US12496301B2 (en) | 2023-12-08 | 2025-12-16 | Arvinas Operations, Inc. | Use of androgen receptor degrader for the treatment of spinal and bulbar muscular atrophy |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3013012A (en) * | 1960-12-22 | 1961-12-12 | Searle & Co | Alkanoylthio-17alpha-carboxyethyl-17beta-hydroxyandrosten-3-one lactones |
| US7355081B2 (en) | 2002-04-17 | 2008-04-08 | The University Of North Carolina At Chapel Hill | Curcumin analogues and uses thereof |
| US6790979B2 (en) | 2002-04-17 | 2004-09-14 | University Of North Carolina At Chapel Hill | Curcumin analogues and uses thereof |
| CA2861066C (en) * | 2012-01-12 | 2024-01-02 | Yale University | Compounds and methods for the enhanced degradation of targeted proteins and other polypeptides by an e3 ubiquitin ligase |
| US20150119435A1 (en) * | 2012-05-11 | 2015-04-30 | Yale University | Compounds useful for promoting protein degradation and methods using same |
| SI2900277T1 (sl) * | 2012-12-13 | 2022-05-31 | Immunomedics, Inc. | Odmerki imunokonjugatov protiteles in SN-38 za boljšo učinkovitost in zmanjšano toksičnost |
| JP6817962B2 (ja) | 2015-01-20 | 2021-01-20 | アルビナス・オペレーションズ・インコーポレイテッドArvinas Operations, Inc. | ターゲティングされたアンドロゲン受容体分解のための化合物および方法 |
| CA2983426C (en) | 2015-04-21 | 2023-10-17 | Gtx, Inc. | Selective androgen receptor degrader (sard) ligands and methods of use thereof |
| WO2016197114A1 (en) | 2015-06-05 | 2016-12-08 | Arvinas, Inc. | Tank-binding kinase-1 protacs and associated methods of use |
| PL3316885T3 (pl) | 2015-07-01 | 2021-12-06 | Immunomedics, Inc. | Immunokoniugaty przeciwciało-sn-38 z linkerem cl2a |
-
2018
- 2018-05-01 AU AU2018261331A patent/AU2018261331C1/en active Active
- 2018-05-01 JP JP2019559295A patent/JP7061135B2/ja active Active
- 2018-05-01 WO PCT/US2018/030538 patent/WO2018204422A1/en not_active Ceased
- 2018-05-01 KR KR1020197034692A patent/KR102746106B1/ko active Active
- 2018-05-01 US US16/608,749 patent/US11447483B2/en active Active
- 2018-05-01 CA CA3062161A patent/CA3062161A1/en active Pending
- 2018-05-01 ES ES18794821T patent/ES2910976T3/es active Active
- 2018-05-01 CN CN201880044734.6A patent/CN110831601B/zh active Active
- 2018-05-01 EP EP18794821.1A patent/EP3618833B1/en active Active
-
2022
- 2022-09-13 US US17/931,773 patent/US12319681B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| EP3618833B1 (en) | 2022-01-19 |
| US11447483B2 (en) | 2022-09-20 |
| JP2020518580A (ja) | 2020-06-25 |
| US12319681B2 (en) | 2025-06-03 |
| US20200207753A1 (en) | 2020-07-02 |
| EP3618833A1 (en) | 2020-03-11 |
| AU2018261331B2 (en) | 2022-03-03 |
| KR102746106B1 (ko) | 2024-12-24 |
| AU2018261331A1 (en) | 2019-12-19 |
| EP3618833A4 (en) | 2021-01-13 |
| CN110831601A (zh) | 2020-02-21 |
| CA3062161A1 (en) | 2018-11-08 |
| KR20200014295A (ko) | 2020-02-10 |
| JP7061135B2 (ja) | 2022-04-27 |
| WO2018204422A1 (en) | 2018-11-08 |
| AU2018261331C1 (en) | 2022-08-04 |
| CN110831601B (zh) | 2023-10-27 |
| US20230092979A1 (en) | 2023-03-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2910976T3 (es) | Eliminadores de receptores de andrógenos tripartitos, métodos y usos de los mismos | |
| Meidan et al. | Treatments for androgenetic alopecia and alopecia areata: current options and future prospects | |
| EP2250996A2 (en) | Method of enhancing hair growth | |
| ES2366609T3 (es) | Utilización de un derivado de ácido piridinodicarboxílico o de una de sus sales para estimular o inducir el crecimiento de las fibras queratínicas y/o detener su caída. | |
| CN106176261A (zh) | 用于刺激毛发生长的组合物和方法 | |
| US9248167B2 (en) | Exfoliative hair retention-promoting formulation | |
| ES2603390T3 (es) | Compuestos para la piel seca y aplicación antienvejecimiento | |
| CN105263469A (zh) | 包含比马前列素的局部组合物和利用其刺激毛发生长的方法 | |
| JP2003500432A (ja) | ジフェニルエーテル誘導体を用いて脱毛症を処置する方法 | |
| US10016351B2 (en) | Composition for promoting hair growth or preventing hair loss | |
| PT1558203E (pt) | Composição capilar contendo um composto estiril-pirazolo | |
| US20160136071A1 (en) | Topical bimatoprost for promoting hair growth containing formulations | |
| ES2657376T3 (es) | Composición que contiene la asociación de madecasósido y/o de terminolósido y de una arginina y/o una de sus sales y/o uno de sus derivados; utilización de la asociación para inducir y/o estimular el crecimiento de estas fibras queratínicas humanas y/o frenar su caída | |
| Razi-Khosroshahi et al. | Latanoprost in treatment of alopecia areata and androgenic alopecia: A comprehensive review | |
| EP2735303A1 (en) | Hair growth compositions and methods | |
| ES2648872T3 (es) | Uso cosmético de un derivado de ácido jasmónico para tratar el cabello y el cuero cabelludo | |
| HK1206598A1 (en) | Eprotirome for use in the prevention and/or treatment of hair disorders and compositions thereof | |
| JP2008530181A (ja) | 少なくとも1種類の天然Ac−N−Ser−Asp−Lys−Proテトラペプチドまたはその類似体の1つの、毛髪喪失を遅延させ、かつ/または毛髪成長を刺激するための薬剤としての化粧料的使用 | |
| Islam et al. | A guide to diagnosis and management of hypertrichosis | |
| US20250170150A1 (en) | Olfactory receptor 2a4/7 agonist for promoting hair growth and improving aesthetic aspect | |
| WO2025133899A1 (en) | Topical composition comprising dutasteride and latanoprost for alopecia | |
| US8679513B2 (en) | Cosmetic use of a jasmonic acid derivative for treating the hair and the scalp | |
| JP2015514740A (ja) | 色素沈着阻害剤としてのリケステリン酸およびその誘導体 | |
| HK1231769A1 (en) | Compositions and methods for stimulating hair growth |