ES2928636T3 - Compuestos de diariloxibenzoheterodiazol disustituidos - Google Patents
Compuestos de diariloxibenzoheterodiazol disustituidos Download PDFInfo
- Publication number
- ES2928636T3 ES2928636T3 ES19795661T ES19795661T ES2928636T3 ES 2928636 T3 ES2928636 T3 ES 2928636T3 ES 19795661 T ES19795661 T ES 19795661T ES 19795661 T ES19795661 T ES 19795661T ES 2928636 T3 ES2928636 T3 ES 2928636T3
- Authority
- ES
- Spain
- Prior art keywords
- aldrich
- formula
- hydrogen atom
- mmol
- represent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent materials, e.g. electroluminescent or chemiluminescent
- C09K11/06—Luminescent materials, e.g. electroluminescent or chemiluminescent containing organic luminescent materials
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- H—ELECTRICITY
- H02—GENERATION; CONVERSION OR DISTRIBUTION OF ELECTRIC POWER
- H02S—GENERATION OF ELECTRIC POWER BY CONVERSION OF INFRARED RADIATION, VISIBLE LIGHT OR ULTRAVIOLET LIGHT, e.g. USING PHOTOVOLTAIC [PV] MODULES
- H02S40/00—Components or accessories in combination with PV modules, not provided for in groups H02S10/00 - H02S30/00
- H02S40/20—Optical components
- H02S40/22—Light-reflecting or light-concentrating means
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10F—INORGANIC SEMICONDUCTOR DEVICES SENSITIVE TO INFRARED RADIATION, LIGHT, ELECTROMAGNETIC RADIATION OF SHORTER WAVELENGTH OR CORPUSCULAR RADIATION
- H10F77/00—Constructional details of devices covered by this subclass
- H10F77/40—Optical elements or arrangements
- H10F77/42—Optical elements or arrangements directly associated or integrated with photovoltaic cells, e.g. light-reflecting means or light-concentrating means
- H10F77/45—Wavelength conversion means, e.g. by using luminescent material, fluorescent concentrators or up-conversion arrangements
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/655—Aromatic compounds comprising a hetero atom comprising only sulfur as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1007—Non-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K30/00—Organic devices sensitive to infrared radiation, light, electromagnetic radiation of shorter wavelength or corpuscular radiation
- H10K30/80—Constructional details
- H10K30/87—Light-trapping means
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Electromagnetism (AREA)
- Electroluminescent Light Sources (AREA)
- Photovoltaic Devices (AREA)
- Plural Heterocyclic Compounds (AREA)
- Steroid Compounds (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
Abstract
Un compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I): en la que: R1, R2 y R3, que son iguales o diferentes entre sí, representan un átomo de hidrógeno; o representan un átomo de halógeno tal como, por ejemplo, cloro, bromo, flúor, yodo, preferentemente flúor; o se seleccionan de grupos alquilo C1-C12, preferiblemente C1-C8, lineales o ramificados opcionalmente halogenados, grupos fenoxi opcionalmente sustituidos, siempre que al menos uno de R1, R2 y R3 sea un grupo fenoxi opcionalmente sustituido y, si R3 es un grupo fenoxi opcionalmente sustituido grupo fenoxi sustituido, al menos uno de R1, R2 es diferente de hidrógeno; R4, que son iguales o diferentes entre sí, representan un átomo de hidrógeno; o se seleccionan de grupos -COOR en los que R se selecciona de grupos alquilo C1-C8, preferiblemente C1-C4, lineales o ramificados. Este compuesto de diariloxibenzoheterodiazol disustituido de fórmula general (I) puede ser utilizado ventajosamente como convertidor de espectro en concentradores solares luminiscentes ("Luminescent Solar Concentrators" - LSCs) que, a su vez, son capaces de mejorar el rendimiento de los dispositivos fotovoltaicos (o dispositivos solares) seleccionados, por ejemplo, de células fotovoltaicas (o células solares), módulos fotovoltaicos (o módulos solares), sobre soporte rígido o flexible. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Compuestos de diariloxibenzoheterodiazol disustituidos
La presente invención se relaciona con un compuesto de diariloxibenzoheterodiazol disustituido.
Más específicamente, la presente invención se relaciona con un compuesto de diariloxibenzoheterodiazol disustituido con grupos tiofeno sustituidos con un grupo fenilo, estando dicho grupo fenilo sustituido con al menos un grupo fenoxilo.
Dicho compuesto de diariloxibenzoheterodiazol disustituido con grupos tiofeno sustituidos con un grupo fenilo, estando dicho grupo fenilo sustituido con al menos un grupo fenoxilo, puede ser usado ventajosamente como un convertidor de espectro en concentradores solares luminiscentes (“Concentradores Solares Luminiscentes” - LSC, por sus siglas en inglés) que, a su vez, son capaces de mejorar el rendimiento de dispositivos fotovoltaicos (o dispositivos solares) seleccionados, por ejemplo, de celdas fotovoltaicas (o celdas solares), módulos fotovoltaicos (o módulos solares), ya sea sobre un soporte rígido o flexible.
La presente invención también se relaciona con un concentrador solar luminiscente (“Concentrador Solar Luminiscente” -LSC) que incluye al menos un compuesto de diariloxibenzoheterodiazol disustituido con grupos tiofeno sustituidos con un grupo fenilo, estando dicho grupo fenilo sustituido con al menos un grupo fenoxilo, así como un dispositivo fotovoltaico (o dispositivo solar), que comprende dicho concentrador solar luminiscente (“Concentrador Solar Luminiscente” - LSC).
Una de las principales limitaciones para el uso de la energía solar es la capacidad de los dispositivos fotovoltaicos (o dispositivos solares) para absorber de manera óptima solamente la radiación con longitudes de onda que caen dentro de un rango estrecho de espectros.
Con un rango de espectros de radiación solar que se extiende de longitudes de onda de aproximadamente 300 nm a longitudes de onda de aproximadamente 2500 nm, las celdas fotovoltaicas (o celdas solares) basadas en silicio cristalino, por ejemplo, tienen una zona de absorción óptima (espectro efectivo) en el rango de 900 nm-1100 nm, mientras que las celdas fotovoltaicas de polímero (o celdas solares) son susceptibles a daño cuando se exponen a una radiación de longitud de onda menor a aproximadamente 500 nm, debido a fenómenos de fotodegradación inducida que se vuelven significativos por debajo de este límite. Por lo general, la eficiencia de los dispositivos fotovoltaicos (o dispositivos solares) de vanguardia es máxima en la región del espectro en el rango de 570 nm a 680 nm (amarillo-naranja).
Los inconvenientes mencionados anteriormente resultan en que los dispositivos fotovoltaicos (o dispositivos solares) tengan una eficiencia cuántica externa (EQE, por sus siglas en inglés) limitada, definida como la relación entre el número de pares electrón-hueco generados en el material semiconductor de los dispositivos fotovoltaicos (o dispositivos solares) y el número de fotones incidentes en tales dispositivos fotovoltaicos (o dispositivos solares). Para mejorar la eficiencia cuántica externa (EQE) de los dispositivos fotovoltaicos (o dispositivos solares), se han desarrollado instrumentos que, cuando son colocados entre la fuente de radiación luminosa (el sol) y los dispositivos fotovoltaicos (o dispositivos solares), absorben selectivamente la radiación incidente teniendo longitudes de onda fuera del espectro efectivo de estos dispositivos fotovoltaicos (o dispositivos solares), emitiendo la energía absorbida en forma de fotones de longitud de onda dentro del espectro efectivo. Dichos instrumentos se denominan concentradores solares luminiscentes (“Concentradores solares luminiscentes” - LSC). Cuando la energía de los fotones reemitidos por los concentradores solares luminiscentes (“Concentradores Solares Luminiscentes” - LSC) es más alta a la de los fotones incidentes, el proceso de fotoluminiscencia, que incluye la absorción de la radiación solar y la subsecuente reemisión de fotones con una longitud de onda más corta, también es referido como proceso de “conversión ascendente”. Por el contrario, cuando la energía de los fotones emitidos por los concentradores solares luminiscentes (“Concentradores solares luminiscentes” - LSC) es más baja que la de los fotones incidentes, el proceso de fotoluminiscencia es referido como proceso de “conversión descendente” (o “desplazamiento descendente”).
Generalmente, dichos concentradores solares luminiscentes (“Concentradores Solares Luminiscentes” - LSC) consisten en grandes láminas de un material transparente a la radiación solar (por ejemplo, vidrios poliméricos o inorgánicos), dentro de las cuales los compuestos fluorescentes, que actúan como convertidores de espectros, se dispersan o se unen químicamente a dicho material. Como resultado del fenómeno óptico de reflexión total, la radiación emitida por los compuestos fluorescentes es “guiada” hacia los delgados bordes de la placa, en donde se concentra en las celdas fotovoltaicas (o celdas solares) colocadas ahí. De este modo, se pueden usar grandes áreas de materiales de bajo costo (láminas fotoluminiscentes) para concentrar la luz en pequeñas áreas de materiales de alto costo [celdas fotovoltaicas (o celdas solares)]. Los compuestos fluorescentes se pueden depositar sobre el soporte de vidrio en forma de una película delgada o, como en el caso de los materiales poliméricos, se pueden dispersar dentro de la matriz polimérica. Alternativamente, la matriz polimérica se puede funcionalizar directamente con grupos cromóforos fluorescentes.
Idealmente, para ser usados en convertidores de espectros, los compuestos fluorescentes deben tener las siguientes características:
- alta eficiencia cuántica de luminiscencia (O) [(O) se define de acuerdo con la ecuación (1), reportada a continuación como la relación entre el número de fotones emitidos y el número de fotones absorbidos por una molécula luminiscente
por unidad de tiempo], y tiene un máximo valor de 1:
(O) = número de fotones emitidos/número de fotones absorbidos (1);
- amplia banda de absorción en la región del espectro, en donde el dispositivo fotovoltaico (o dispositivo solar) es poco eficiente;
- alto coeficiente de absorción;
- banda de emisión estrecha en la región del espectro, en donde el dispositivo fotovoltaico (o dispositivo solar) es más eficiente;
- bandas de absorción y emisión bien separadas para evitar o minimizar los fenómenos de autoabsorción.
Es bien sabido que algunos compuestos de benzotiadiazol, en particular el 4,7-di(tien-2'-il)-2,1,3-benzotiadiazol (DTB, por sus siglas en inglés), son compuestos fluorescentes que se pueden usar en la construcción de concentradores solares luminiscentes (“Concentradores solares luminiscentes” - LSC). Tales compuestos han sido descritos en la solicitud de patente internacional WO 2011/048458 a nombre del Solicitante.
El 4,7-di(tien-2'-il)-2,1,3-benzotiadiazol (DTB) se caracteriza por una emisión centrada en alrededor de 579 nm, valor que corresponde a una energía muy por encima del umbral mínimo de operación de las celdas fotovoltaicas (o celdas solares), un umbral que, por ejemplo, corresponde a una longitud de onda de aproximadamente 1100 nm para las celdas fotovoltaicas (o celdas solares) más populares, basadas en silicio. Además, su absorción de la radiación luminosa es intensa y se extiende a lo largo de un rango de longitud de onda relativamente amplio, en el rango de aproximadamente 550 nm (la longitud de onda de la radiación verde) y el ultravioleta. Finalmente, en solución de diclorometano, el 4,7-di(tien-2'-il)-2,1,3-benzotiadiazol (DTB) tiene un desplazamiento de Stokes de 134 nm, mucho más alto que el de la mayoría de los productos comerciales propuestos hasta ahora para su uso en concentradores solares luminiscentes (“Concentradores solares luminiscentes” - LSC).
Por estas razones, el uso de 4,7-di(tien-2'-il)-2,1,3-benzotiadiazol (DTB) ha hecho posible la producción de concentradores solares luminiscentes (“Concentradores Solares Luminiscentes” - LSC) de excelente calidad.
Sin embargo, aunque absorbe una parte significativa del espectro solar, el 4,7-di(tien-2'-il)-2,1,3-benzotiadiazol (DTB) tiene una absorción modesta en regiones con longitudes de onda más largas, correspondientes al amarillo y las radiaciones rojas, que, por lo tanto, no se pueden convertir en otras radiaciones que la celda fotovoltaica (o celda solar) pueda aprovechar más eficazmente.
La solicitud de patente internacional WO 2016/046319 a nombre del Solicitante describe un compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I):
en donde:
- Z representa un átomo de azufre, un átomo de oxígeno, un átomo de selenio; o un grupo NR5 , en donde R5 se selecciona de grupos alquilo de C1-C20, preferiblemente de C1-C8, lineales o ramificados, o de grupos arilo opcionalmente sustituidos;
- R1, R2 y R3, que son iguales o diferentes entre sí, representan un átomo de hidrógeno; o se seleccionan de grupos alquilo de C1-C20, preferiblemente de C1-C8, lineales o ramificados, que contienen opcionalmente heteroátomos, grupos cicloalquilo opcionalmente sustituidos, grupos arilo opcionalmente sustituidos, grupos alcoxilo de C1-C20, preferiblemente de C1-C8, lineales o ramificados, opcionalmente sustituidos, grupos fenoxilo opcionalmente sustituidos, grupos -COOR6 , en donde R6 se selecciona de grupos alquilo de C1-C20, preferiblemente de C1-C8 , lineales o ramificados, o es un grupo cianuro;
- o R1 y R2 pueden estar unidos entre sí para formar, junto con los átomos de carbono a los que están unidos, un sistema cíclico o policíclico saturado, insaturado o aromático, que contiene de 3 a 14 átomos de carbono, preferiblemente de 4 a 6 átomos de carbono, que contiene opcionalmente uno o más heteroátomos, tales como, por ejemplo, oxígeno, azufre, nitrógeno, silicio, fósforo, selenio;
- o R2 y R3 pueden estar unidos entre sí para formar, junto con los átomos de carbono a los que están unidos, un sistema cíclico o policíclico saturado, insaturado o aromático, que contiene de 3 a 14 átomos de carbono, preferiblemente de 4 a 6 átomos de carbono, que contiene opcionalmente uno o más heteroátomos, tales como, por ejemplo, oxígeno, azufre, nitrógeno, silicio, fósforo, selenio;
- R4, que son iguales o diferentes entre sí, se seleccionan de grupos arilo opcionalmente sustituidos.
Se dice que el compuesto de diariloxibenzoheterodiazol disustituido, mencionado anteriormente, se usa ventajosamente en la construcción de concentradores solares luminiscentes (“Concentradores solares luminiscentes” - LSC).
Por lo tanto, el Solicitante se enfrentó al problema de encontrar compuestos capaces de proporcionar un rendimiento comparable o incluso superior, en particular en términos de potencia generada por los dispositivos fotovoltaicos (o dispositivos solares), en donde se usan, tanto en comparación con los compuestos de benzotiadiazol conocidos, y en comparación con los compuestos de dibenzoheterodiazol disustituidos específicamente descritos en la solicitud de patente internacional WO 2016/046319, mencionada anteriormente.
El Solicitante ha encontrado que algunos de los compuestos de diariloxibenzoheterodiazol disustituidos no descritos específicamente en la solicitud de patente internacional WO 2016/046319, mencionada anteriormente, en particular compuestos de diariloxibenzoheterodiazol disustituidos con grupos tiofeno sustituidos con un grupo fenilo, dicho grupo fenilo siendo sustituido con al menos un grupo fenoxilo, que tiene la fórmula general específica (I) que se reporta a continuación, puede proporcionar el rendimiento mencionado anteriormente. Dichos compuestos de diariloxibenzoheterodiazol disustituidos pueden ser usados ventajosamente como convertidores de espectros en concentradores solares luminiscentes (“Concentradores Solares Luminiscentes” - LSC) que, a su vez, son capaces de mejorar el rendimiento de dispositivos fotovoltaicos (o solares) seleccionados, por ejemplo, de celdas fotovoltaicas (o celdas solares), módulos fotovoltaicos (o módulos solares), sobre un soporte rígido o flexible. Más específicamente, estos compuestos de diariloxibenzoheterodiazol disustituidos son capaces de proporcionar un rendimiento comparable o incluso más alto, particularmente en términos de potencia generada por los dispositivos fotovoltaicos, en donde se usan, en comparación con los compuestos de benzotiadiazol conocidos y los compuestos de diariloxibenzoheterodiazol disustituidos específicamente descritos en la solicitud de patente internacional WO 2016/046319, mencionada anteriormente.
WO 2018/055074 proporciona ejemplos adicionales de compuestos de diariloxibenzotiadiazol sustituidos para usar en un concentrador solar luminiscente.
Por lo tanto, el objeto de la presente invención es un compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I):
en donde:
- R1, R2 y R3 , que son iguales o diferentes entre sí, representan un átomo de hidrógeno; o representan un átomo de halógeno, tal como, por ejemplo, cloro, bromo, flúor, yodo, preferentemente flúor; o se seleccionan de grupos alquilo de C1-C12, preferiblemente de C1-C8 , lineales o ramificados, opcionalmente halogenados, grupos fenoxilo opcionalmente sustituidos, siempre que al menos uno de R1, R2 o R3 sea un grupo fenoxilo opcionalmente sustituido y, si R3 es un grupo fenoxilo opcionalmente sustituido, al menos uno de R1 o R2 es diferente de hidrógeno;
- R4 , que son iguales o diferentes entre sí, representan un átomo de hidrógeno; o se seleccionan de grupos -COOR, en donde R se selecciona de grupos alquilo de C1-C8 , preferiblemente de C1-C4 , lineales o ramificados.
Para los propósitos de la presente descripción y de las siguientes reivindicaciones, las definiciones de rangos numéricos siempre incluirán los miembros extremos, a menos que se especifique lo contrario.
Para los propósitos de la presente descripción y de las siguientes reivindicaciones, el término “que comprende” también incluirá los términos “que consiste esencialmente en” o “que consiste en”.
El término “grupos alquilo de C1-C8” significa grupos alquilo lineales o ramificados que tienen de 1 a 8 átomos de carbono. Los ejemplos específicos de grupos alquilo de C1-C8 son: metilo, etilo, n-propilo, isopropilo, n-butilo, isobutilo, tere-butilo.
El término “grupos alquilo de C1-C8 opcionalmente halogenados” significa grupos alquilo lineales o ramificados, saturados o insaturados que tienen de 1 a 8 átomos de carbono, en donde al menos uno de los átomos de hidrógeno está
reemplazado por un átomo de halógeno, tal como, por ejemplo, flúor, cloro, preferiblemente flúor. Los ejemplos específicos de grupos alquilo de C1-C8 opcionalmente halogenados son: fluorometilo, difluorometilo, trifluorometilo, triclorometilo, 2,2,2-trifluoroetilo, 2,2,2-tricloroetilo, 2,2,3,3-tetrafluoropropilo, 2,2,3,3,3-pentafluoropropilo, perfluoropentilo, perfluorooctilo.
El término “grupos fenoxilo opcionalmente sustituidos” significa grupos fenoxilo de C6H5O opcionalmente sustituidos con uno o más grupos, que son iguales o diferentes entre sí, seleccionados de: átomos de halógeno, tales como, por ejemplo, flúor, cloro, preferiblemente flúor; grupos alquilo de C1-C20; grupos alcoxilo de C1-C20; grupos cianuro; grupos amina; grupos nitro; grupos éster. Los ejemplos específicos de grupos fenoxilo de C6H5O son: fenoxilo, 4-octilfenoxilo, 4-trifluorometilfenoxilo, 2-trifluorometilfenoxilo, 6-trifluorometilfenoxilo.
De acuerdo con una realización preferida de la presente invención, en dicha fórmula general (I):
- R1, R2 y R3 , que son iguales entre sí, se seleccionan de grupos fenoxilo opcionalmente sustituidos, preferiblemente un grupo fenoxilo; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R1 y R3 , que son iguales entre sí, representan un átomo de hidrógeno, y R2 se selecciona de grupos fenoxilo opcionalmente sustituidos, preferiblemente
- son un grupo fenoxilo; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R1 y R2 , que son iguales entre sí, se seleccionan de grupos fenoxilo opcionalmente sustituidos, son preferiblemente un grupo fenoxilo, y R3 representa un átomo de hidrógeno; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R2 y R3 , que son iguales entre sí, se seleccionan de grupos fenoxilo opcionalmente sustituidos, son preferiblemente un grupo fenoxilo, y R1 representa un átomo de hidrógeno; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R1 representa un átomo de hidrógeno, R2 se selecciona de grupos alquilo de C1-C8 , preferiblemente de C1-C4 , lineales o ramificados opcionalmente halogenados, preferiblemente es metilo, y R3 se selecciona de grupos fenoxilo opcionalmente sustituidos, preferiblemente es un grupo fenoxilo; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R1 se selecciona de grupos alquilo de C1-C8 , preferiblemente de C1-C4 , lineales o ramificados opcionalmente halogenados, preferiblemente es trifluorometilo, R2 se selecciona de grupos fenoxilo opcionalmente sustituidos, preferiblemente es un grupo fenoxilo, y R3 representa un átomo de hidrógeno; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R1 y R3 , que son iguales entre sí, representan un átomo de hidrógeno, y R2 se selecciona de grupos fenoxilo opcionalmente sustituidos, preferiblemente es un grupo 4-trifluorometilfenoxilo; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R1 y R3 , que son iguales entre sí, representan un átomo de hidrógeno; R2 se selecciona de grupos fenoxilo opcionalmente sustituidos, preferiblemente es un grupo 2-trifluorometilfenoxilo; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R1 y R2 , que son iguales entre sí, se seleccionan de grupos fenoxilo opcionalmente sustituidos, preferiblemente son un grupo 4-octilfenoxilo, y R3 representa un átomo de hidrógeno; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R1 y R2 , que son iguales entre sí, se seleccionan de grupos fenoxilo opcionalmente sustituidos, preferiblemente son un grupo 4-octilfenoxilo, y R3 representa un átomo de hidrógeno; y
- R4 , que son iguales entre sí, se seleccionan de grupos -COOr , en donde R se selecciona de grupos alquilo de C1-C8, preferiblemente de C1-C4 , lineales o ramificados, preferiblemente representan un grupo -COOCH3 ; o
- R1 y R3 , que son iguales entre sí, representan un átomo de hidrógeno, y R2 se selecciona de grupos fenoxilo opcionalmente sustituidos, preferiblemente es un grupo fenoxilo; y
- R4 , que son iguales entre sí, se seleccionan de grupos -COOR, en donde R se selecciona de grupos alquilo de C1-C8, preferiblemente de C1-C4 , lineales o ramificados, preferiblemente representan un grupo -COOCH3 ; o
- R1, que son iguales entre sí, representan un átomo de halógeno, tal como cloro, bromo, flúor, yodo, preferiblemente representan un átomo de flúor, R2 se selecciona de grupos fenoxilo opcionalmente sustituidos, preferiblemente es un grupo fenoxilo, y R3 , que son iguales entre sí, representan un átomo de hidrógeno; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno.
Se dan ejemplos específicos de compuestos que tienen la fórmula general (I) útiles para el propósito de la presente invención en la Tabla 1.
Tabla 1:
El compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I), objeto de la presente invención, se puede obtener por medio de un proceso conocido en la técnica por la operación, por ejemplo, como se describe en la solicitud de patente internacional WO 2016/046319 o en la solicitud de patente italiana MI201800000000667, ambas a nombre del Solicitante.
Los detalles adicionales sobre el proceso para la preparación de dicho compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I) se pueden encontrar en los siguientes ejemplos.
Como se describe anteriormente, dicho compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I) puede ser usado ventajosamente como un convertidor de espectros en concentradores solares luminiscentes (“Concentradores Solares Luminiscentes” - LSC) que, a su vez, son capaces de mejorar el rendimiento de los dispositivos fotovoltaicos (o dispositivos solares), tales como, por ejemplo, celdas fotovoltaicas (o celdas solares), módulos fotovoltaicos (o módulos solares), ya sea sobre un soporte rígido o flexible.
Dichos concentradores solares luminiscentes (“Concentradores Solares Luminiscentes” - LSC) se pueden preparar, por ejemplo, por la dispersión fundida de dicho compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I) en materiales poliméricos, tales como, por ejemplo, polimetilmetacrilato (PMMA, por sus siglas en inglés), poliestireno (PS, por sus siglas en inglés), polivinilacetato (PVA, por sus siglas en inglés). En consecuencia, un objeto adicional de la presente invención es un concentrador solar luminiscente (“Concentrador solar luminiscente” - LSC) que incluye al menos un compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I).
El compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I) puede ser usado en dicho concentrador solar luminiscente (“Concentrador Solar Luminiscente” - LSC) en las siguientes formas: disperso en polímero o en vidrio, unido químicamente a un polímero o a vidrio, en solución, o en forma de gel.
Por ejemplo, el concentrador solar luminiscente (“Concentrador Solar Luminiscente” - LSC) puede contener una matriz transparente, en donde el término matriz transparente significa cualquier material transparente usado en forma de soporte, de aglutinante o de material, en donde al menos un compuesto de diariloxibenzoheterodiazol disustituido que tiene fórmula general, se dispersa o se incorpora. El material usado para la matriz es, como tal, transparente a la radiación de interés y en particular a la radiación que tiene una frecuencia incluida en el espectro efectivo del dispositivo fotovoltaico (o dispositivo solar), tal como, por ejemplo, la celda fotovoltaica (o celda solar) en donde se usa. Por lo tanto, los materiales adecuados para el propósito de la presente invención se pueden seleccionar de materiales que son transparentes al menos a la radiación que tiene una longitud de onda en el rango de 250 nm a 1100 nm.
La matriz transparente que se puede usar para los propósitos de la presente invención se puede seleccionar, por ejemplo, de materiales poliméricos o materiales vítreos. Dicha matriz se caracteriza por una alta transparencia y una larga vida útil en términos de calor y luz. Los materiales poliméricos que se pueden usar ventajosamente para el propósito de la presente invención son, por ejemplo, polimetilmetacrilato (PMMA), resinas epóxicas, resinas de silicio, tereftalatos de polialquileno, policarbonatos, poliestireno, polipropileno. Los materiales vítreos que se pueden usar ventajosamente para el propósito de la presente invención son, por ejemplo, sílice.
En el caso en donde la matriz sea de tipo polimérico, dicho al menos un compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I) se puede dispersar en el polímero de dicha matriz por medio de, por ejemplo, la dispersión en forma fundida y la subsecuente formación de una lámina, que comprende dicho polímero y dicho al menos un compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I), operando, por ejemplo, de acuerdo con la técnica conocida como “moldeado por fundición”. Alternativamente, dicho al menos un compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general, y el polímero de dicha matriz se pueden solubilizar en al menos un disolvente, obteniendo una solución que se deposita sobre una lámina de dicho polímero, formando una película que incluye dicho al menos un compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I), y dicho polímero, operando, por ejemplo, a través del uso de un aplicador de película tipo “Doctor Blade”, subsecuentemente se deja evaporar dicho disolvente.
En el caso de que la matriz sea de tipo vitreo, dicho al menos un compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I) se puede solubilizar en al menos un disolvente obteniendo una solución que se deposita sobre una lámina de dicha matriz de tipo vítreo, formando un película que incluye dicho al menos un compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I), operando, por ejemplo, a través del uso de un aplicador de película tipo “Doctor Blade”, subsecuentemente se deja evaporar dicho disolvente.
Un dispositivo fotovoltaico (o dispositivo solar) que comprende al menos una celda fotovoltaica (o celda solar) y al menos un concentrador solar luminiscente (“Concentrador solar luminiscente” - LSC), que comprende al menos un compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I) es también objeto de la presente invención.
Dicho dispositivo fotovoltaico (o dispositivo solar) se puede obtener, por ejemplo, por el ensamblaje del mencionado concentrador solar luminiscente con una celda fotovoltaica (o celda solar). De acuerdo con una realización preferida de la presente invención, el concentrador solar mencionado anteriormente se puede construir en forma de una lámina transparente obtenida por la solubilización de dicho al menos un compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I) y el polímero de la matriz polimérica en al menos un disolvente, obteniendo una solución que se deposita sobre una lámina de dicho polímero, formando una película que comprende al menos un compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I) y dicho polímero, por ejemplo, usando un aplicador de película tipo “Doctor Blade”, subsecuentemente se deja evaporar dicho disolvente. En dichos dispositivos fotovoltaicos (o dispositivos solares), dichas láminas se pueden acoplar subsecuentemente a una celda fotovoltaica (o celda solar).
Para una mejor comprensión de la presente invención y para poner la misma en práctica, se describen a continuación algunos ejemplos ilustrativos y no limitativos de la misma.
El 4,7-di(tien-2'-il)-2,1,3-benzotiadiazol (DTB) se obtuvo como se describe en el Ejemplo 1 de la solicitud de patente internacional WO 2012/007834 a nombre del Solicitante.
Ejemplo 1 (invención)
Síntesis de 2-POP-DTBOP (por sus siglas en inglés) que tiene la fórmula (1)
(1) Síntesis de 4,7-dibromo-5,6-difenoxibenzotiadiazol que tiene la fórmula (a)
Se adicionaron fenol (Aldrich), (2,9 g; 2,8 mL; 31,6 mmol) y carbonato de potasio (Aldrich), (4,4 g; 31,6 mmol) a una solución 0,3 M de 4,7-dibromo-5,6-difluorobenzotiadiazol (Sunatech), (4,35 g; 13,2 mmol) en N,N-dimetilformamida anhidra (Aldrich), (44 mL) a un matraz de 250 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración, la mezcla de reacción obtenida se calentó a 82°C y se mantuvo, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, después de la adición de 100 mL de agua destilada, se obtuvo un precipitado que se recuperó por filtración, se lavó con agua destilada (30 mL) y se secó bajo vacío, obteniendo 6,3 g de 4,7-dibromo-5,6-difenoxibenzotiadiazol que tiene la fórmula (a), (productividad = 100%).
(2) Síntesis de 4,7-ditienil-5,6-difenoxibenzotiadiazol que tiene la fórmula (b)
Se adicionó 2-tributilestanniltiofeno (Aldrich), (11,8 g; 10,1 mL; 31,7 mmol), bajo una atmósfera inerte, a una solución 0,1 M de 4,7-dibromo-5,6-difenoxibenzotiadiazol que tiene la fórmula (a) obtenido como se describe anteriormente (6,3 g; 13,2 mmol) en tolueno anhidro (Aldrich), (132 mL) en un matraz de 250 mL magnéticamente agitado, provisto de un termómetro y un sistema de refrigeración. Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,352 g; 0,4 mmol) y tris-o-tolilfosfina (Aldrich), (0,441 g; 1,45 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C y se mantuvo, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 100 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente graduado: mezcla de n-heptano (Aldrich)/diclorometano (Aldrich), de la relación 9/1 (v/v) a la relación 8/2 (v/v) a la relación 6/4 (v(v)]. El producto obtenido se recristalizó en una mezcla de n-heptano (Aldrich)/diclorometano (Aldrich), (relación 9/1 (v/v)), obteniendo 5,7 g de 4,7-ditienil-5,6-difenoxibenzotiadiazol que tiene la fórmula (b), (productividad = 89%).
(3) Síntesis de 4,7-bis-(5-bromo-2-tienil)-5,6-difenoxibenzotiadiazol que tiene la fórmula (c)
Se adicionó W-bromosuccinimida (Aldrich), (4,7 g; 26,3 mmol), bajo una atmósfera inerte, a una solución 0,05 M de 4,7-ditienil-5,6-difluorobenzotiadiazol que tiene la fórmula (b), obtenido como se describe anteriormente (5,7 g; 11,8 mmol) en tetrahidrofurano anhidro (Aldrich), (230 mL) en un matraz de 500 mL magnéticamente agitado, equipado con un termómetro y un sistema de enfriamiento, la mezcla de reacción obtenida se mantuvo bajo agitación, en la oscuridad a temperatura ambiente (25°C), por 12 horas. Subsecuentemente, después de la adición de 200 mL de agua destilada, se obtuvo un precipitado que se recuperó por filtración, se lavó con metanol (Aldrich), (200 mL) y se recristalizó en una mezcla de n-heptano (Aldrich)/diclorometano (Aldrich) [relación 9 /1 (v/v)], obteniendo 7,4 g de 4,7-bis-(5-bromo-2-tienil)-5,6-difenoxibenzotiadiazol que tiene la fórmula (c), (productividad = 98%).
(4) Síntesis de 2-POP-DTBOP (1)
Se adicionaron ácido 2-fenoxifenilborónico (Aldrich), (3,1 g; 14,7 mmol) y una solución acuosa 2,1 M de carbonato de potasio (Aldrich), (6 g en 22 mL de agua destilada; 43,4 mmol), bajo una atmósfera inerte, a una solución 0,08 M de 4,7-bis-(5-bromo-2-tienil)-5,6-difenoxibenzotiadiazol que tiene la fórmula (c), obtenido como se describe anteriormente (3,5 g; 5,5 mmol) en 1,4-dioxano anhidro (Aldrich), (66 mL) en un matraz de 250 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración. Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionó tetrakis(fenilfosfina)paladio (Aldrich), (0,308 g; 0,27 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 85°C y se mantuvo, a dicha temperatura, bajo agitación, por 12 horas.
Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 100 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente graduado: mezcla de n-heptano (Aldrich)/diclorometano (Aldrich), de la relación 9/1 (v/v) a la relación 8/2 (v/v) a la relación 6/4 (v(v)]. El producto obtenido se recristalizó en una mezcla de n-heptano (Aldrich)/diclorometano (Aldrich) [relación 9/1 (v/v)], obteniendo 4,1 g de 2-POP-DTBOP que tiene la fórmula (1), (productividad = 90 %).
Ejemplo 2 (invención)
Síntesis de 2-POP-6-F-DTBOP (por sus siglas en inglés) que tiene la fórmula (12)
(1) Síntesis de 2-fenoxi-6-fluoro-1-bromobenceno que tiene la fórmula (I')
Lo siguiente se colocó en un vial de microondas: 2,4-difluoro-1-bromobenceno (Aldrich), (0,75 g; 3,9 mmol), fenol (0,365 g; 3,9 mmol), carbonato de potasio (Aldrich), (1,5 g; 10,8 mmol) y W-metilpirrolidona (Aldrich), (15 mL). Después de agitar la mezcla de reacción obtenida, bajo un flujo de argón, el vial se cerró con su tapón especial, y se colocó en un reactor de 50 mL, se ajustó el gradiente de reacción de 25°C a 200°C por 4 minutos. La mezcla de reacción se mantuvo en el reactor a 200°C por 40 minutos, subsecuentemente se recuperó, se vertió en agua destilada (50 mL), y se extrajo con éter etílico (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover el disolvente residual por destilación bajo presión reducida, el residuo obtenido se purificó por elución en una columna de cromatografía de gel de sílice [eluyente: n-heptano (Aldrich)], obteniendo 0,816 g de 2-fenoxi-6-fluoro-1-bromobenceno que tiene fórmula (I'), (productividad = 78%).
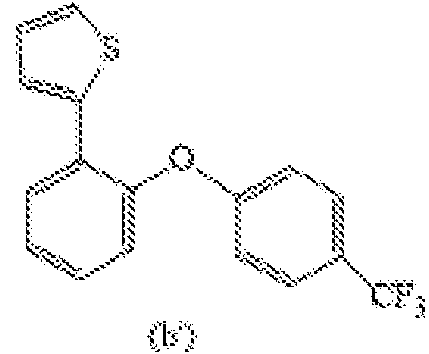
(2) Síntesis de 2-fenoxi-6-fluoro-1-(2-tienil)benceno que tiene la fórmula (m')
Se adicionó 2-tributilestanniltiofeno (Aldrich), (1,37 g; 1,14 mL; 3,67 mmol), bajo una atmósfera inerte, a una solución 0,1 M de 2-fenoxi-6-fluoro-1-bromobenceno que tiene la fórmula (I'), obtenido como se describe anteriormente (0,816 g; 3,06 mmol) en tolueno anhidro (Aldrich), (30,6 mL), en un matraz de 100 mL magnéticamente agitado, equipado con un termómetro y un sistema de refrigeración. Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno,
se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,042 g; 0,04 mmol) y tris-o-tolilfosfina (Aldrich), (0,051 g; 0,15 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C, y se mantuvo, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover el disolvente residual por destilación bajo presión reducida, el residuo obtenido se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)], obteniendo 0,8 g de 2-fenoxi-6-fluoro-1-(2-tienil)benceno que tiene la fórmula (m'), (productividad = 95%).
(3) Síntesis de 2-POP-6-F-DTBOP que tiene la fórmula (12)
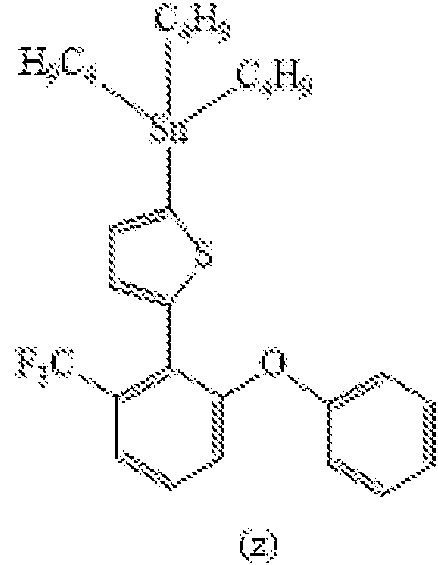
Se adicionó gota a gota n-butillitio (Aldrich), (solución 1,6 M en hexano), (2 mL; 3,2 mmol), bajo una atmósfera inerte, a una solución 0,1 M de 2-fenoxi-6-fluoro-1-(2-tienil)benceno que tiene la fórmula (m'), obtenido como se describe anteriormente (0,79 g; 2,9 mmol) en tetrahidrofurano anhidro (Aldrich), (30 mL), a -78°C, en un matraz de 100 mL equipado con un agitador magnético y un termómetro, la reacción de la mezcla obtenida se mantuvo bajo agitación, y se elevó la temperatura a -50°C por 3 horas. Subsecuentemente, después de colocar el matraz en un baño con acetona y hielo seco a -78°C, se adicionó gota a gota cloruro de tributilestannilo (Aldrich), (1,14 g; 0,953 mL; 3,5 mmol). Después de 15 minutos, se retiró el matraz del baño, se permitió que la temperatura se eleve hasta 20°C, y se mantuvo la mezcla de reacción, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, después de la adición de una solución saturada de bicarbonato de sodio (Aldrich), (20 mL), la mezcla de reacción se extrajo con éter etílico (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó con una solución saturada de bicarbonato de sodio (Aldrich), (1 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover el disolvente residual por destilación bajo presión reducida, se obtuvo el residuo que comprende 2-fenoxi-6-fluoro-1[2'(5'-tributilestannil)tienil]benceno que tiene la fórmula (n'):
se usó de la siguiente manera.
En un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración, el residuo que comprende 2-fenoxi-6-fluoro-1[2'(5'-tributilestannil)tienil]benceno que tiene la fórmula (n') se obtiene como se describe anterior, se disolvió en tolueno anhidro (Aldrich), (26 mL) obteniendo una solución a la que se adicionó 4,7-dibromo-5,6-difenoxibenzotiadiazol que tiene la fórmula (a), obtenido como se describe en el Ejemplo 1 (0,48 g); 1 mmol), bajo una atmósfera inerte. Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,03 g; 0,03 mmol) y tris-o-tolilfosfina (Aldrich), (0,04 g; 0,13 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C, y se mantuvo, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)/diclorometano (Aldrich)/acetato de etilo (Aldrich) mezcla 85/10/5 (v/v/v). El producto obtenido se recristalizó en una mezcla de n-heptano (Aldrich)/diclorometano (Aldrich) [relación 9/1 (v/v)], obteniendo 0,7 g de 2-POP-6-F-DTBOP que tiene la fórmula (12), (productividad = 80%).
Ejemplo 3 (invención)
Síntesis de 2-POP-(DTBOP-4-COOCH3), (por sus siglas en inglés) que tiene fórmula (11)
(1) Síntesis de 4,7-dibromo-5,6-di-(4'-carbometoxifenoxi)benzotiadiazol que tiene la fórmula (d)
Se adicionaron 4-carbometoxifenol (Aldrich), (1,1 g; 7,1 mmol) y carbonato de potasio (Aldrich), (0,98 g; 7,1 mmol), bajo una atmósfera inerte, a una solución 0,3 M de 4,7-dibromo-5,6- difluorobenzotiadiazol (Sunatech), (1 g; 3 mmol) en N,N-dimetilformamida anhidra (Aldrich), (15 mL) en un matraz de 250 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración, la mezcla de reacción obtenida se calentó a 82°C, y se mantuvo, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, después de la adición de 100 mL de agua destilada, se obtuvo un precipitado que se recuperó por filtración, se lavó con agua destilada (30 mL) y se secó bajo vacío, obteniendo 1,75 g de 4,7-dibromo-5,6-di-(4'-carbometoxifenoxi)benzotiadiazol que tiene la fórmula (d), (productividad = 98%).
(2) Síntesis de 4,7-ditienil-5,6-di-(4'-carbometoxifenoxi)benzotiadiazol que tiene la fórmula (e)
Se adicionó 2-tributilestanniltiofeno (Aldrich), (1,5 g; 1,3 mL; 4,1 mmol), bajo una atmósfera inerte, a una solución 0,1 M de 4,7-dibromo-5,6-di-(4'-carbometoxifenoxi)benzotiadiazol que tiene la fórmula (d), obtenido como se describe anteriormente (1 g; 1,7 mmol) en tolueno anhidro (Aldrich), (17 mL) en un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración. Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,0454 g; 0,05 mmol) y tris-o-tolilfosfina
(Aldrich), (0,0547 g; 0,18 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C, y se mantuvo, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente graduado: mezcla de n-heptano (Aldrich)/diclorometano (Aldrich) de la relación 9/1 (v/v) a la relación 8/2 (v/v) a la relación 6/4 (v/v)]. El producto obtenido se recristalizó en una mezcla de n-heptano (Aldrich)/diclorometano (Aldrich) [relación 9/1 (v/v)] para producir 0,9 g de 4,7-d itienil-5,6-di-(4'-carbometoxifenoxi)benzotiadiazol que tiene la fórmula (e), (productividad = 88%).
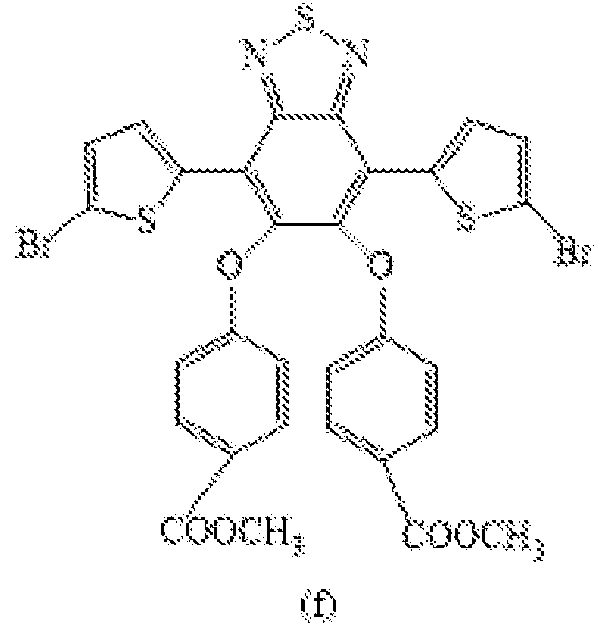
(3) Síntesis de 4,7-bis-(5-bromo-2-tienil)-5,6-di-(4'-carbometoxifenoxi)-benzotiadiazol que tiene la fórmula (f)
Se adicionó W-bromosuccinimida (Aldrich), (0,592 g; 3,3 mmol), bajo una atmósfera inerte, a una solución 0,05 M de 4,7-ditienil-5,6-di-(4'-carbometoxifenoxi)benzotiadiazol que tiene la fórmula (e), obtenido como se describe anteriormente (0,9 g; 1,5 mmol) en tetrahidrofurano anhidro (Aldrich), (30 mL) en un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración, la mezcla de reacción obtenida se mantuvo bajo agitación, en la oscuridad, a temperatura ambiente (25°C), por 12 horas. Subsecuentemente, después de la adición de 50 mL de agua destilada, se obtuvo un precipitado que se recuperó por filtración, se lavó con metanol (Aldrich), (200 mL), y se recristalizó en una mezcla de n-heptano (Aldrich)/diclorometano (Aldrich) [relación 9 /1 (v/v)] para producir 1,1 g de 4,7-bis-(5-bromo-2-tienil)-5,6-di-(4'-carbometoxifenoxi)benzotiazol que tiene la fórmula (f), (productividad = 98 %).
(4) Síntesis de 2-POP-(DTBOP-4-COOCH3) que tiene fórmula (11)
Se adicionaron ácido 2-fenoxifenilborónico (Aldrich), (0,86 g; 4 mmol) y una solución acuosa 2 M de carbonato de potasio (Aldrich), (1,66 g en 6 mL de agua destilada; 12 mmol), bajo una atmósfera inerte, a una solución 0,08 M de 4,7-bis-(5-bromo-2-tienil)-5,6-di-(4'-carbometoxifenoxi)benzotiadiazol que tiene la fórmula (f), obtenido como se describe anteriormente (1,1 g; 5,5 mmol) en 1,4-dioxano anhidro (Aldrich), (18 mL) en un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración. Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionó tetrakis(fenilfosfina)paladio (Aldrich), (0,084 g; 0,07 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 85°C, y se mantuvo a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)/mezcla de diclorometano (Aldrich)/acetato de etilo (Aldrich), relación 8/1/1 (v/v/v)]. El producto obtenido se recristalizó en una mezcla de n-heptano (Aldrich)/diclorometano (Aldrich) [relación 9/1 (v/v)], obteniendo 1,1 g de 2-POP-(DTBOP-4-COOCH3) que tiene la fórmula (11), (productividad = 78%).
Ejemplo 4 (invención)
Síntesis de 2,6-POP-DTBOP que tiene la fórmula (3)
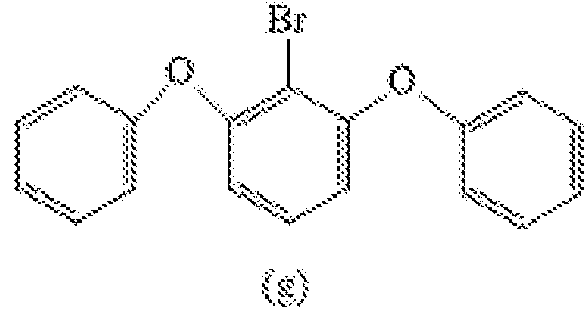
(1) Síntesis de 2,6-difenoxM-bromobenceno que tiene la fórmula (g)
Lo siguiente se colocó en un vial de microondas: 2,6-difluoro-1-bromobenceno (Aldrich), (0,85 g; 4,3 mmol), fenol (Aldrich), (1,9 g; 1,8 mL; 20 mmol), carbonato de potasio (Aldrich), (2 g; 14,5 mmol) y N-metilpirrolidona (Aldrich), (10 mL). Después de agitar la mezcla de reacción obtenida bajo un flujo de argón, se cerró el vial con su tapón especial, y se colocó en un reactor de 50 mL, se ajustó el gradiente de reacción de 25°C a 210°C por 4 minutos. La mezcla de reacción se mantuvo en el reactor a 210°C por 2 horas, subsecuentemente se recuperó, se vertió en agua destilada (50 mL), y se extrajo con éter etílico (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover el disolvente residual por destilación bajo presión reducida, el residuo obtenido se purificó por elución en una columna de cromatografía de gel de sílice [eluyente: n-heptano (Aldrich)], obteniendo 1,2 g de 2,6-difenoxi-1-bromobenceno que tiene la fórmula (g), (productividad = 82%).
(2) Síntesis de 2,6-difenoxi-1-(2-tienil)benceno que tiene la fórmula (h)
Se adicionó 2-tributilestanniltiofeno (Aldrich), (1,3 g; 1,1 mL; 3,5 mmol), bajo una atmósfera inerte, a una solución 0,1 M de 2,6-difenoxi-1-bromobenceno que tiene la fórmula (g), obtenido como se describe anteriormente (1 g; 2,9 mmol) en tolueno anhidro (Aldrich), (29 mL) en un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración. Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,04 g; 0,04 mmol) y tris-o-tolilfosfina (Aldrich), (0,046 g; 0,15 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C, y se mantuvo bajo agitación, a dicha temperatura, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)] obteniendo 0,95 g de 2,6-difenoxi-1(2-tienil)benceno que tiene la fórmula (h), (productividad = 95%).
(3) Síntesis de 2,6-POP-DTBOP que tiene la fórmula (3)
Se adicionó gota a gota n-butiMitio (Aldrich), (solución 1,6 M en hexano), (1,9 mL; 3 mmol), bajo una atmósfera inerte, a una solución 0,1 M de 2,6-difenoxi-1(2-tienil)benceno que tiene fórmula (h), obtenido como se describe anteriormente (0,95 g; 2,7 mmol) en tetrahidrofurano anhidro (Aldrich), (27 mL), a -78°C, en un matraz de 100 mL equipado con un agitador magnético y un termómetro, la mezcla de reacción obtenida se mantuvo bajo agitación, y se elevó la temperatura a -50°C en 3 horas. Subsecuentemente, después de colocar el matraz en un baño con acetona y hielo seco a -78°C, se adicionó gota a gota cloruro de tributilestannilo (Aldrich), (1,1 g; 0,9 mL; 3,3 mmol). Después de 15 minutos, se retiró el matraz del baño, se permitió que la temperatura se eleve hasta 20°C, y se mantuvo la mezcla de reacción, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, después de adicionar una solución saturada de bicarbonato de sodio (Aldrich), (20 mL), la mezcla de reacción se extrajo con éter etílico (Aldrich), (20 mL), la fase orgánica obtenida se lavó con una solución saturada de bicarbonato de sodio (Aldrich), (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover el disolvente residual por destilación bajo presión reducida, se obtuvo el residuo que comprende 2,6-difenoxi-1[2'(5'-tributilestannil)tienil]benceno que tiene la fórmula (i):
se usó de la siguiente manera.
El residuo que comprende 2,6-difenoxi-1[2'(5'-tributilestannil)tienil]benceno que tiene la fórmula (i), obtenido como se describe anteriormente se disolvió en tolueno anhidro (Aldrich), (25 mL), obteniendo una solución a la cual se le adicionó, bajo una atmósfera inerte, 4,7-dibromo-5,6-difenoxibenzotiadiazol que tiene la fórmula (a), obtenido como se describe en el Ejemplo 1 (0,6 g; 1,25 mmol), en un matraz de 100 mL equipado con un agitador magnético y un termómetro. Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,034 g; 0,04 mmol) y tris-o-tolilfosfina (Aldrich), (0,043 g; 0,14 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C, y se mantuvo bajo agitación, a dicha temperatura, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)/diclorometano (Aldrich) relación de mezcla 9/1 (v/v)]. El producto obtenido se recristalizó en una mezcla de n-heptano (Aldrich)/diclorometano (Aldrich) [relación 9/1 (v/v)], obteniendo 1 g de 2,6-POP-DTBOP que tiene la fórmula (3), (productividad = 80%).
Ejemplo 5 (invención)
Síntesis de 2,4-POP-DTBOP que tiene la fórmula (4)
(1) Síntesis de 2,4-difenoxM-bromobenceno que tiene la fórmula (I)
Lo siguiente se colocó en un vial de microondas: 2,4-difluoro-1-bromobenceno (Aldrich), (2 g; 10,4 mmol), fenol (Aldrich), (3,2 g; 3 mL; 34,1 mmol), carbonato de potasio (Aldrich), (5,7 g; 41,3 mmol) y N-metilpirrolidona (Aldrich), (26 mL). Después de agitar la mezcla de reacción obtenida bajo un flujo de argón, se cerró el vial con su tapón especial, y se colocó en un reactor de 50 mL, se ajustó el gradiente de reacción de 25°C a 220°C por 4 minutos. La mezcla de reacción se mantuvo en el reactor a 220°C por 1 hora, subsecuentemente se recuperó, se vertió en agua destilada (50 mL), y se extrajo con éter etílico (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover el disolvente residual por destilación bajo presión reducida, el residuo obtenido se purificó por elución en una columna de cromatografía de gel de sílice [eluyente: n-heptano (Aldrich)], para obtener 3,4 g de 2,4-difenoxi-1-bromobenceno que tiene la fórmula (I), (productividad = 96%).
(2) Síntesis de 2,4-difenoxi-1-(2-tienil)benceno que tiene la fórmula (m)
Se adicionó 2-tributilestanniltiofeno (Aldrich), (1,2 g; 1 mL; 3,2 mmol), bajo una atmósfera inerte, a una solución 0,1 M de 2,4-difenoxi-1-bromobenceno que tiene la fórmula (I), obtenido como se describe anteriormente (0,91 g; 3,2 mmol) en tolueno anhidro (Aldrich), (27 mL), en un matraz de 100 mL equipado con un agitador magnético y un termómetro. Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich)
(0,0364 g; 0,04 mmol) y tris-o-tolilfosfina (Aldrich), (0,0462 g; 0,15 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C, y se mantuvo bajo agitación, a dicha temperatura, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente
se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)], para obtener 0,88 g de 2,4-difenoxi-1-(2-tienil)benceno que tiene la fórmula (m), (productividad = 95%).
(3) Síntesis de 2,4-POP-DTBOP que tiene la fórmula (4)
Se adicionó gota a gota n-butillitio (Aldrich), (solución 1,6 M en hexano), (1,7 mL; 2,7 mmol), bajo una atmósfera inerte, a una solución 0,1 M de 2,4-difenoxi-1(2-tienil)benceno que tiene fórmula (m), obtenido como se describe anteriormente (0,87 g; 2,5 mmol) en tetrahidrofurano anhidro (Aldrich), (25 mL) a -78°C, en un matraz de 100 mL equipado con un agitador magnético y un termómetro, la mezcla de reacción obtenida se mantuvo bajo agitación, y se elevó la temperatura a -50°C por 3 horas. Después de colocar el matraz en un baño con acetona y hielo seco a -78°C, se adicionó gota a gota cloruro de tributilestannilo (Aldrich), (0,98 g; 0,8 mL; 3 mmol). Después de 15 minutos, se retiró el matraz del baño, se permitió que la temperatura se eleve hasta 20°C, y se mantuvo la mezcla de reacción, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, después de la adición de una solución saturada de bicarbonato de sodio (Aldrich), (20 mL), la mezcla de reacción se extrajo con éter etílico (Aldrich), (20 mL), la fase orgánica obtenida se lavó con una solución saturada de bicarbonato de sodio (Aldrich), (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover el disolvente residual por destilación bajo presión reducida, se obtuvo el residuo que comprende 2,4-fenoxi-1[2'(5'-tributilestannil)tienil]benceno que tiene la fórmula (n):
se usó de la siguiente manera.
El residuo que comprende 2,4-difenoxi-1[2'(5'-tributilestannil)tienil]benceno que tiene la fórmula (n), obtenido como se describe anteriormente se disolvió en tolueno anhidro (Aldrich), (25 mL), en un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de enfriamiento, bajo una atmósfera inerte, y a esto se le adicionó 4,7-dibromo-5,6-difenoxibenzotiadiazol que tiene la fórmula (a), obtenido como se describe en el Ejemplo 1 (0,5 g; 1,04 mmol). Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,03 g; 0,03 mmol) y tris-o-tolilfosfina (Aldrich), (0,04 g; 0,13 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C, y se mantuvo, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)/diclorometano (Aldrich) relación de mezcla 9/1 (v/v)]. El producto obtenido se recristalizó en una mezcla de n-heptano (Aldrich)/diclorometano (Aldrich) [relación 9/1 (v/v)], obteniendo 0,83 g de 2,4-POP-DTBOP que tiene la fórmula (4), (productividad = 80%).
Ejemplo 6 (invención)
Síntesis de 2,4,6-POP-DTBOP que tiene la fórmula (2)
(1) Síntesis de 2,4,6-trifenoxi-1-bromobenceno que tiene la fórmula (o)
Lo siguiente se colocó en un vial de microondas: 2,4,6-trifluoro-1-bromobenceno (Aldrich), (1,6 g; 0,9 mmol), fenol (Aldrich), (3,4 g; 3,2 mL; 36,2 mmol), carbonato de potasio (Aldrich), (5 g; 36,2 mmol) y W-metilpirrolidona (Aldrich), (26 mL). Después de agitar la mezcla de reacción obtenida bajo un flujo de argón, se cerró el vial con su tapón especial, y se colocó en un reactor de 50 mL, se ajustó el gradiente de reacción de 25°C a 220°C por 4 minutos. La mezcla de reacción se mantuvo en el reactor a 220°C por 3 horas, subsecuentemente se recuperó, se vertió en agua destilada (50 mL), y se extrajo con éter etílico (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)], obteniendo 2,3 g de 2,4,6-trifenoxi-1-bromobenceno que tiene la fórmula (o), (productividad = 70%).
(2) Síntesis de 2,4,6-trifenoxi-1-(2-tienil)benceno que tiene la fórmula (p)
Se adicionó 2-tributilestanniltiofeno (Aldrich), (1,5 g; 1,3 mL; 4,2 mmol), bajo una atmósfera inerte, a una solución 0,1 M de 2,4,6-trifenoxi-1-bromobenceno que tiene la fórmula (o), obtenido como se describe anteriormente (1,5 g; 3,5 mmol) en tolueno anhidro (Aldrich), (35 mL), en un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración. Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,048 g; 0,05 mmol) y tris-o-tolilfosfina (Aldrich), (0,06 g; 0,19 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C, y se mantuvo bajo agitación, a dicha temperatura, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol,
obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)], obteniendo 1,1 g de 2,4,6-trifenoxi-1(2-tienil)benceno que tiene la fórmula (p), (productividad = 72%).
(4) Síntesis de 2,4,6-POP-DTBOP que tiene la fórmula (2)
Se adicionó gota a gota n-butillitio (Aldrich), (solución 1,6 M en hexano), (0,8 mL; 1,3 mmol), bajo una atmósfera inerte, a una solución 0,1 M de 2,4,6-trifenoxi-1(2-tienil)benceno que tiene la fórmula (p), obtenido como se describe anteriormente (0,5 g; 1,15 mmol), en tetrahidrofurano anhidro (Aldrich), (11 mL), a -78°C, en un matraz de 100 mL equipado con un agitador magnético y un termómetro, la reacción la mezcla obtenida se mantuvo bajo agitación, y se elevó la temperatura a -50°C por 3 horas. Subsecuentemente, después de colocar el matraz en un baño con acetona y hielo seco a -78°C, se adicionó gota a gota cloruro de tributilestannilo (Aldrich), (0,5 g; 0,4 mL; 1,4 mmol), a los 15 minutos se retiró el matraz del baño, se permitió que la temperatura se eleve hasta 20°C, y la mezcla de reacción se mantuvo, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, después de la adición de una solución saturada de bicarbonato de sodio (Aldrich), (30 mL), la mezcla de reacción se extrajo con éter etílico (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó con una solución saturada de bicarbonato de sodio bicarbonato (Aldrich), (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover el disolvente residual por destilación bajo presión reducida, se obtuvo el residuo que comprende 2,4,6-trifenoxi-1[2'(5'-tributilestannil)tienil]benceno que tiene la fórmula (q):
se usó de la siguiente manera.
El residuo que comprende 2,4,6-trifenoxi-1[2'(5'-tributilestannil)tienil]benceno que tiene la fórmula (q), obtenido como se describe anteriormente se disolvió en tolueno anhidro (Aldrich), (11,5 mL), en 100 mL matraz equipado con un agitador magnético, un termómetro y un sistema de refrigeración, bajo una atmósfera inerte, y se le adicionó 4,7-dibromo-5,6-difenoxibenzotiadiazol que tiene la fórmula (a), obtenido como se describe en el Ejemplo 1 (0,24 g; 0,5 mmol). Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,0136 g; 0,015 mmol) y tris-o-tolilfosfina (Aldrich), (0,0182 g; 0,06 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C, y se mantuvo, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)/diclorometano (Aldrich) relación de mezcla 9/1 (v/v)]. El producto obtenido se recristalizó en una mezcla de n-heptano (Aldrich)/diclorometano (Aldrich) [relación 9/1 (v/v)], obteniendo 0,44 g de 2,4,6-POP-DTBOP que tiene la fórmula (2), (productividad = 75%).
Ejemplo 7 (invención)
Síntesis de 2-CH3-4-POP-DTBOP que tiene la fórmula (5)
3-CH;4-P0F-DTB0P {$)
(1) Síntesis de 2-metil-4-fenoxi-1-bromobenceno que tiene la fórmula (r)
Lo siguiente se colocó en un vial de microondas: 2-metil-4-fluoro-1-bromobenceno (Aldrich), (1 g; 5,3 mmol), fenol (Aldrich), (2,1 g; 2 mL; 22,8 mmol), carbonato de potasio (Aldrich), (1,4 g; 10,1 mmol) y N-metilpirrolidona (Aldrich), (12 mL). Después de agitar la mezcla de reacción obtenida bajo un flujo de argón, se cerró el vial con su tapón especial, y se colocó en un reactor de 50 mL, se ajustó el gradiente de reacción de 25°C a 220°C por 4 minutos. La mezcla de reacción se mantuvo en el reactor a 220°C por 3 horas, subsecuentemente se recuperó, se vertió en agua destilada (50 mL), y se extrajo con éter etílico (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover el disolvente residual por destilación bajo presión reducida, el residuo obtenido se purificó por elución en una columna de cromatografía de gel de sílice [eluyente: n-heptano (Aldrich)], obteniendo 0,7 g de 2-metil-4-fenoxi-1-bromobenceno que tiene fórmula (r), (productividad = 51%).
(2) Síntesis de 2-metil-4-fenoxi-1-(2'-tienil)benceno que tiene la fórmula(s)
Se adicionó 2-tributilestanniltiofeno (Aldrich), (1 g; 0,9 mL; 3,2 mmol), bajo una atmósfera inerte, a una solución 0,2 M de 2-metil-4-fenoxi-1-bromobenceno que tiene la fórmula (r), obtenido como se describe anteriormente (0,7 g; 2,7 mmol) en tolueno anhidro (Aldrich), (13 mL), en un matraz de 100 mL equipado con un agitador magnético y un termómetro. Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,0364 g; 0,04 mmol) y tris-o-tolilfosfina (Aldrich), (0,0462 g; 0,15 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C, y se mantuvo bajo agitación, a dicha temperatura, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 30 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)], obteniendo 1,1 g de 2-metil-4-fenoxi-1(2'-tienil)benceno que tiene la fórmula (s), (productividad =
98%).
(3) Síntesis de 2-CH3-4-POP-DTBOP que tiene la fórmula (5)
Se adicionó gota a gota n-butiNitio (Aldrich), (solución 1,6 M en hexano), (1,9 mL; 3 mmol), bajo una atmósfera inerte, a una solución 0,1 M de 2-metil-4-fenoxi-1(2'-tienil)benceno que tiene la fórmula (s), obtenido como se describe anteriormente (0,7 g; 2,7 mmol) en tetrahidrofurano anhidro (Aldrich), (27 mL) a -78°C, en un matraz de 100 mL equipado con un agitador magnético y un termómetro, la mezcla de reacción obtenida se mantuvo bajo agitación, y se elevó la temperatura a -50°C por 3 horas. Subsecuentemente, después de colocar el matraz en un baño con acetona y hielo seco a -78°C, se adicionó gota a gota cloruro de tributilestannilo (Aldrich), (0,5 g; 0,4 mL; 1,4 mmol). Después de 15 minutos, se retiró el matraz del baño, se permitió que la temperatura se eleve hasta 20°C, y se mantuvo la mezcla de reacción, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, después de la adición de una solución saturada de bicarbonato de sodio (Aldrich), (30 mL), la mezcla de reacción se extrajo con éter etílico (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó con una solución saturada de bicarbonato de sodio bicarbonato (Aldrich), (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover el disolvente residual por destilación bajo presión reducida, se obtuvo el residuo que comprende 2-metil-4-fenoxi-1[2'(5'-tributilestannil)tienil]benceno que tiene la fórmula (t):
se usó de la siguiente manera.
En un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración, bajo una atmósfera inerte, se disolvió el residuo que comprende 2-metil-4-fenoxi-1[2'(5'-tributilestannil)tienil]benceno que tiene la fórmula (t), obtenido como se describe anteriormente en tolueno anhidro (Aldrich), (27 mL) al que se adicionó 4,7-dibromo-5,6-difenoxibenzotiadiazol que tiene la fórmula (a), obtenido como se describe en el Ejemplo 1 (0,525 g; 1,1 mmol). Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,03 g; 0,033 mmol) y tris-o-tolilfosfina (Aldrich), (0,04 g; 0,13 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C, y se mantuvo, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)/mezcla de diclorometano (Aldrich), relación 9/1 (v/v)]. El producto obtenido se recristalizó en una mezcla de n-heptano (Aldrich)/diclorometano (Aldrich) [relación 9/1 (v/v)], obteniendo 0,74 g de 2-CH3-POP-DTBOP que tiene la fórmula (5), (productividad = 80%).
Ejemplo 8 (invención)
Síntesis de 6-CF3-2-POP-DTBOP que tiene la fórmula (6)
(1) Síntesis de 6-trifluorometil-2-fenoxi-1-bromobenceno que tiene la fórmula (u)
Lo siguiente se colocó en un vial de microondas: 6-trifluorometil-2-fluoro-1-bromobenceno (Aldrich), (1 g; 4,1 mmol), fenol (Aldrich), (0,8 g; 0,7 mL; 8,2 mmol), carbonato de potasio (Aldrich), (1,1 g; 8,2 mmol) y dimetilformamida (Aldrich), (20 mL). Después de agitar la mezcla de reacción obtenida bajo un flujo de argón, se cerró el vial con su tapón especial, y se colocó en un reactor de 50 mL, se ajustó el gradiente de reacción de 25°C a 150°C por 4 minutos. La mezcla de reacción se mantuvo en el reactor a 150°C por 45 minutos, subsecuentemente se recuperó, se vertió en agua destilada (50 mL), y se extrajo con éter etílico (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover el disolvente residual por destilación bajo presión reducida, el residuo obtenido se purificó por elución en una columna de cromatografía de gel de sílice [eluyente: n-heptano (Aldrich)], para obtener 1 g de 6-trifluorometil-2-fenoxi-1-bromobenceno fórmula (u), (productividad = 77%).
(2) Síntesis de 6-trifluorometil-2-fenoxi-1-(2'-tienil)benceno que tiene la fórmula (v)
Se adicionó 2-tributilestanniltiofeno (Aldrich), (1,4 g; 1,2 mL; 3,8 mmol), bajo una atmósfera inerte, a una solución 0,2 M de 6-trifluorometil-2-fenoxi-1-bromobenceno que tiene la fórmula (u), obtenido como se describe anteriormente (1 g; 3,1 mmol) en tolueno anhidro (Aldrich), (21 mL), en un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración. Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,0435 g; 0,05 mmol) y tris-o-tolilfosfina (Aldrich), (0,0535 g; 0,18 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C, y se mantuvo, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)] para obtener 0,7 g de 6-trifluorometil-2-fenoxi-1(2'-tienil)benceno que tiene la fórmula (v), (productividad = 71%).
(3) Síntesis de 6-CF3-2-POP-DTBOP que tiene la fórmula (6)
Se adicionó gota a gota n-butillitio (Aldrich), (solución 1,6 M en hexano), (1,5 mL; 2,4 mmol), bajo una atmósfera inerte, a
una solución 0,1 M de 6-trifluorometil-2-fenoxi-1(2'-tienil)benceno que tiene la fórmula (v), obtenido como se describe anteriormente (0,7 g; 2,2 mmol) en tetrahidrofurano anhidro (Aldrich), (22 mL), a -78°C, en un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración, la mezcla de reacción obtenida se mantuvo bajo agitación, y se elevó la temperatura a -50°C por 3 horas. Subsecuentemente, después de colocar el matraz en un baño con acetona y hielo seco a -78°C, se adicionó gota a gota cloruro de tributilestannilo (Aldrich), (0,9 g; 0,7 mL; 2,6 mmol). Después de 15 minutos, se retiró el matraz del baño, se permitió que la temperatura se eleve hasta 20°C, y se mantuvo la mezcla de reacción, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, después de la adición de una solución saturada de bicarbonato de sodio (Aldrich), (20 mL), la mezcla de reacción se extrajo con éter etílico (Aldrich), (3 x 25 mL): la fase orgánica obtenida se lavó con una solución saturada de bicarbonato de sodio (Aldrich), (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover el disolvente residual por destilación bajo presión reducida, se obtuvo el residuo que comprende 6-trifluorometil-2-fenoxi-1[2'(5'-tributilestannil)tienil]benceno que tiene la fórmula (z):
se usó de la siguiente manera.
En un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración, bajo una atmósfera inerte, el residuo que comprende 6-trifluorometil-2-fenoxi-1[2'(5'-tributilestannil)tienil)]benceno que tiene la fórmula (z), obtenido como se describe anteriormente, se disolvió en tolueno anhidro (Aldrich), (22 mL), obteniendo una solución a la que se le adicionó 4,7-dibromo-5,6-difenoxibenzotiadiazol que tiene la fórmula (a), obtenido como se describe en el Ejemplo 1 (0,449 g; 0,9 mmol). Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,027 g; 0,03 mmol) y tris-o-tolilfosfina (Aldrich), (0,034 g; 0,11 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C, y se mantuvo, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)/mezcla de diclorometano (Aldrich), relación 9/1 (v/v)]. El producto obtenido se recristalizó en una mezcla de n-heptano (Aldrich)/diclorometano (Aldrich) [relación 9/1 (v/v)], obteniendo 0,6 g de 6-CF3-2-POP-DTBOP que tiene la fórmula (6), (productividad = 70%).
Ejemplo 9 (invención)
Síntesis de 2-(POP-4-CF3)-DTBOP que tiene la fórmula (7)
(1) Síntesis de 2-(4'-trifluorometilfenoxi)-1-bromobenceno que tiene la fórmula (a')
Lo siguiente se colocó en un vial de microondas: 2-bromofenol (Aldrich), (0,57 g; 0,38 mL; 3,3 mmol), 4-fluoro-1-trifluorometilbenceno (Aldrich), (0,54 g; 0,42 mL; 3,3 mmol), carbonato de potasio (Aldrich), (0,5 g; 3,6 mmol) y dimetilformamida (Aldrich), (5 mL). Después de agitar la mezcla de reacción obtenida bajo un flujo de argón, se cerró el vial con su tapón especial, y se colocó en un reactor de 50 mL, se ajustó el gradiente de reacción de 25°C a 190°C por 4 minutos. La mezcla de reacción se mantuvo en el reactor a 190°C por 45 minutos, subsecuentemente se recuperó, se vertió en agua destilada (50 mL), y se extrajo con éter etílico (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)], obteniendo 0,5 g de 2(4'-trifluorometilfenoxi)-1-bromobenceno que tiene la fórmula (a'), (productividad = 50%).
(2) Síntesis de 2-(4'-trifluorometilfenoxi)-1-(2'-tienil)benceno que tiene la fórmula (b')
Se adicionaron ácido 2-tienilborónico (Aldrich), (0,33 g; 2,6 mmol) y una solución acuosa 2 M de carbonato de potasio (Aldrich), (1,18 g en 4,3 mL de agua destilada; 8,6 mmol), bajo una atmósfera inerte, a una solución 0,2 M de 2(4-trifluorometilfenoxi)-1-bromobenceno que tiene la fórmula (a'), obtenido como se describe anteriormente (0,67 g; 2,1 mmol) en 1,4-dioxano anhidro (Aldrich), (16 mL), en un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración. Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionó tetrakis(trifenilfosfina)paladio (Aldrich), (0,05 g; 0,04 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 85°C, y se mantuvo a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)], para obtener 0,35 g de 2(4'-trifluorometilfenoxi)-1(2'-tienil)benceno que tiene la fórmula (b'), (productividad = 52%).
(3) Síntesis de 2-(POP-4-CF3)-DTBOP que tiene la fórmula (7)
Se adicionó gota a gota n-butillitio (Aldrich), (solución 1,6 M en hexano), (0,75 mL; 1,2 mmol), bajo una atmósfera inerte, a una solución 0,1 M de 2(4-trifluorometilfenoxi)-1(2'-tienil)benceno que tiene la fórmula (b'), obtenido como se describe anteriormente (0,35 g; 1,1 mmol) en tetrahidrofurano anhidro (Aldrich), (10 mL), a -78°C, en un matraz de 100 mL equipado con un agitador magnético y un termómetro, la mezcla de reacción obtenida se mantuvo bajo agitación, y se elevó la temperatura a -50°C por 3 horas. Después de colocar el matraz en un baño con acetona y hielo seco a -78°C, se adicionó gota a gota cloruro de tributilestannilo (Aldrich), (0,43 g; 0,4 mL; 1,3 mmol). Después de 15 minutos, se retiró el matraz del baño, se permitió que la temperatura se eleve hasta 20°C, y se mantuvo la mezcla de reacción, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, después de la adición de una solución saturada de bicarbonato de sodio (Aldrich), (20 mL), la mezcla de reacción se extrajo con éter etílico (Aldrich), (3 x 25 mL): la fase orgánica obtenida se lavó con una solución saturada de bicarbonato de sodio (Aldrich), (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover el disolvente residual por destilación bajo presión reducida, se obtuvo el residuo que comprende 2(4'-trifluorometilfenoxi)-1(2'(5'-tributilestannil)tienil)benceno que tiene la fórmula (c'):
se usó de la siguiente manera.
El residuo que comprende 2(4'-trifluorometilfenoxi)-1[2'(5'-tributilestannil)tienil]benceno que tiene la fórmula (c'), obtenido como se describe anteriormente se disolvió en tolueno anhidro (Aldrich), (11 mL), en un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de enfriamiento, bajo una atmósfera inerte, obteniendo una solución a la que se le adicionó 4,7-dibromo-5,6-difenoxibenzotiadiazol que tiene la fórmula (a), obtenido como se describe en el Ejemplo 1 (0,207 g; 0,43 mmol). Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,027 g; 0,03 mmol) y tris-o-tolilfosfina (Aldrich), (0,0125 g; 0,041 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C, y se mantuvo bajo agitación, a dicha temperatura, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)/mezcla de diclorometano (Aldrich), relación 9/1 (v/v)]. El producto obtenido se recristalizó en una mezcla de n-heptano (Aldrich)/diclorometano (Aldrich), (relación 9/1 (v/v)), obteniendo 0,29 g de 2-(POP-4-CF3)-DTBOP que tiene la fórmula (7), (productividad = 70%).
Ejemplo 10 (invención)
Síntesis de 2-(POP-2-CF3)-DTBOP que tiene la fórmula (8)
(1) Síntesis de 2-(2'-trifluorometilfenoxi)-1-bromobenceno que tiene la fórmula (d')
Lo siguiente se colocó en un vial de microondas: 2-bromofenol (Aldrich), (0,57 g; 0,38 mL; 3,3 mmol), 2-fluoro-1-trifluorometilbenceno (Aldrich), (0,54 g; 0,42 mL; 3,3 mmol), carbonato de potasio (Aldrich), (0,5 g; 3,6 mmol) y dimetilformamida (Aldrich), (5 mL). Después de agitar la mezcla de reacción obtenida bajo un flujo de argón, se cerró el vial con su tapón especial, y se colocó en un reactor de 50 mL, se ajustó el gradiente de reacción de 25°C a 190°C por 4
minutos. La mezcla de reacción se mantuvo en el reactor a 190°C por 45 minutos, subsecuentemente se recuperó, se vertió en agua destilada (50 mL), y se extrajo con éter etílico (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)] para obtener 0,5 g de 2(2'-trifluorometilfenoxi)-1-bromobenceno que tiene la fórmula (d'), (productividad = 50%).
(2) Síntesis de 2-(2'-trifluorometilfenoxi)-1-(2'-tienil)benceno que tiene la fórmula (e')
Se adicionaron ácido 2-tienilborónico (Aldrich), (0,33 g; 2,6 mmol) y una solución acuosa 2 M de carbonato de potasio (Aldrich), (1,18 g en 4,3 mL de agua destilada; 8,6 mmol), bajo una atmósfera inerte, a una solución 0,13 M de 2(2'-trifluorometilfenoxi)-1-bromobenceno que tiene la fórmula (d'), obtenido como se describe anteriormente (0,67 g; 2,1 mmol) en 1,4-dioxano anhidro (Aldrich), (16 mL), en un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración. Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionó tetrakis(trifenilfosfina)paladio (Aldrich), (0,05 g; 0,04 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 85°C, y se mantuvo a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)], para obtener 0,35 g de 2(2'-trifluorometilfenoxi)-1(2'-tienil)benceno que tiene la fórmula (e'), (productividad = 52%).
(3) Síntesis de 2-(POP-6-CF3)-DTBOP que tiene la fórmula (8)
Se adicionó gota a gota n-butillitio (Aldrich), (solución 1,6 M en hexano), (0,75 mL; 1,2 mmol), bajo una atmósfera inerte, a una solución 0,1 M de 2(2'-trifluorometilfenoxi)-1(2'-tienil)benceno que tiene la fórmula (e'), obtenido como se describe anteriormente (0,35 g; 1,1 mmol) en tetrahidrofurano anhidro (Aldrich), (10 mL), a -78°C, en un matraz de 100 mL equipado con un agitador magnético y un termómetro, la reacción la mezcla obtenida se mantuvo bajo agitación, y se elevó la temperatura a -50°C por 3 horas. Después de colocar el matraz en un baño con acetona y hielo seco a -78°C, se adicionó gota a gota cloruro de tributilestannilo (Aldrich), (0,43 g; 0,4 mL; 1,3 mmol). Después de 15 minutos, se retiró el matraz del baño, se permitió que la temperatura se eleve hasta 20°C, y se mantuvo la mezcla de reacción, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, después de la adición de una solución saturada de bicarbonato de sodio (Aldrich), (20 mL), la mezcla de reacción se extrajo con éter etílico (Aldrich), (3 x 25 mL): la fase orgánica obtenida se lavó con una solución saturada de bicarbonato de sodio (Aldrich), (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover el disolvente residual por destilación bajo presión reducida, se obtuvo el residuo que comprende 2(2'-trifluorometilfenoxi)-1[2'(5'-tributilestannil)tienil]benceno que tiene la fórmula (f'):
se usó de la siguiente manera.
En un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración, bajo una atmósfera inerte, el residuo que comprende 2(2'-trifluorometilfenoxi)-1[2'(5'-tributilestannil)tienil]benceno que tiene la
fórmula (f), obtenido como se describe anteriormente se disolvió en tolueno anhidro (Aldrich), (11 mL), a lo que se le adicionó 4,7-dibromo-5,6-difenoxibenzotiadiazol que tiene la fórmula (a), obtenido como se describe en el Ejemplo 1 (0,207 g; 0,43 mmol). Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,010 g; 0,011 mmol) y tris-o-tolilfosfina (Aldrich), (0,0125 g; 0,041 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C, y se mantuvo, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)/diclorometano (Aldrich) relación de mezcla 9/1 (v/v)]. El producto obtenido se recristalizó en una mezcla de n-heptano (Aldrich)/diclorometano (Aldrich) [relación 9/1 (v/v)], obteniendo 0,27 g de 2-(POP-6-CF3)-DTBOP que tiene la fórmula (8), (productividad = 66%).
Ejemplo 11 (invención)
Síntesis de 2,6-(POP-4-C8H17)-DTBOP que tiene la fórmula (9)
(1) Síntesis de 2,6-di-(4'-octilfenoxi)-1-bromobenceno que tiene la fórmula (g')
Lo siguiente se colocó en un vial de microondas: 2,6-difluoro-1-bromobenceno (Aldrich), (0,5 g; 2,6 mmol), 4-octilfenol (1,2 g; 5,8 mmol), carbonato de potasio (Aldrich), (1 g; 7,6 mmol) y N-metilpirrolidona (Aldrich), (10 mL). Después de agitar la mezcla de reacción obtenida bajo un flujo de argón, se cerró el vial con su tapón especial, y se colocó en un reactor de 50 mL, se ajustó el gradiente de reacción de 25°C a 220°C por 4 minutos. La mezcla de reacción se mantuvo en el reactor a 220°C por 2 horas, subsecuentemente se recuperó, se vertió en agua destilada (50 mL), y se extrajo con éter etílico (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover el disolvente residual por destilación bajo presión reducida, el residuo obtenido se purificó por elución en una columna de cromatografía de gel de sílice [eluyente: n-heptano (Aldrich)], para obtener 0,57 g de 2,6-di-(4'-octilfenoxi)-1-bromobenceno que tiene la fórmula (g'), (productividad = 38%).
(2) Síntesis de 2,6-(4'-octilfenoxi)-1-(2'-tienil)benceno que tiene la fórmula (h')
Se adicionó 2-tributilestanniltiofeno (Aldrich), (0,45 g; 0,4 mL; 1,2 mmol), bajo una atmósfera inerte, a una solución 0,13 M de 2,6-di-(4'-octilfenoxi)-1-bromobenceno que tiene la fórmula (g'), obtenido como se describe anteriormente (0,57 g; 1 mmol) en tolueno anhidro (Aldrich), (10 mL), en un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración. Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,015 g; 0,016 mmol) y tris-o-tolilfosfina (Aldrich), (0,019 g; 0,06 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 85°C, y se mantuvo bajo agitación, a dicha temperatura, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 200 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)], para obtener 0,47 g de 2,6(4'-octilfenoxi)-1(2'-tienil)benceno que tiene la fórmula (h'), (productividad = 83%).
(3) Síntesis de 2,6-(POP-4-CsH17)-DTBOP que tiene la fórmula (9)
Se adicionó gota a gota n-butillitio (Aldrich), (solución 1,6 M en hexano), (1,4 mL; 2,2 mmol), bajo una atmósfera inerte, a una solución 0,1 M de 2,6(4'-octilfenoxi)-1(2'-tienil)benceno que tiene la fórmula (h'), obtenido como se describe anteriormente (1,16 g; 2,04 mmol) en tetrahidrofurano anhidro (Aldrich), (20,4 mL), a -78°C, en un matraz de 100 mL equipado con un agitador magnético y un termómetro, la mezcla de reacción obtenida se mantuvo bajo agitación, y se elevó la temperatura a -50°C por 3 horas. Después de colocar el matraz en un baño con acetona y hielo seco a -78°C, se adicionó gota a gota cloruro de tributilestannilo (Aldrich), (0,8 g; 0,66 mL; 2,45 mmol). Después de 15 minutos, se retiró el matraz del baño, se permitió que la temperatura se eleve hasta 20°C, y se mantuvo la mezcla de reacción, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, después de la adición de una solución saturada de bicarbonato de sodio (Aldrich), (20 mL), la mezcla de reacción se extrajo con éter etílico (Aldrich), (3 x 25 mL): la fase orgánica obtenida se lavó con una solución saturada de bicarbonato de sodio (Aldrich), (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover el disolvente residual por destilación bajo presión reducida, se obtuvo el residuo que comprende 2,6(4'-octilfenoxi)-1[2'(5'-tributilestannil)tienil]benceno que tiene la fórmula (i'):
se usó de la siguiente manera.
En un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración, bajo una atmósfera inerte, el residuo que comprende 2,6(4'-octilfenoxi)-1(2'(5'-tributilestannil)tienil)benceno con fórmula (i'), obtenido como se describe anteriormente se disolvió en tolueno anhidro (Aldrich), (10 mL) obteniendo una solución a la que se le adicionó 4,7-dibromo-5,6-difenoxibenzotiadiazol que tiene la fórmula (a), obtenido como se describe en Ejemplo 1 (0,207 g; 0,43 mmol). Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,012 g; 0,013 mmol) y tris-o-tolilfosfina (Aldrich), (0,015 g; 0,05 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C, y se mantuvo bajo agitación, a dicha temperatura, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del
disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: n-heptano (Aldrich)/diclorometano (Aldrich)/acetato de etilo (Aldrich) mezcla 9/0,97/0,03 (v/v/v)]. El producto obtenido se recristalizó en una mezcla de n-heptano (Aldrich)/diclorometano (Aldrich) [relación 9/1 (v/v)], para obtener 0,4 g de 2,6-(POP-4-C8 H17)-DTBOP que tiene la fórmula (9), (productividad = 69%).
Ejemplo 12 (invención)
Síntesis de 2,6-(POP-4-C8H17)-(DTBOP-4-COOCH3) que tiene la fórmula (10)
Se adicionó gota a gota n-butillitio (Aldrich), (solución 1,6 M en hexano), (1,4 mL; 2,2 mmol), bajo una atmósfera inerte, a una solución 0,1 M de 2,6(4'-octilfenoxi)-1(2'-tienil)benceno que tiene la fórmula (h'), obtenido como se describe anteriormente (1,16 g; 2,04 mmol) en tetrahidrofurano anhidro (Aldrich), (20,4 mL), a -78°C, en un matraz de 100 mL equipado con un agitador magnético y un termómetro, la mezcla de reacción obtenida se mantuvo bajo agitación, y se elevó la temperatura a -50°C por 3 horas. Subsecuentemente se colocó el matraz en un baño con acetona y hielo seco a -78°C, se adicionó gota a gota cloruro de tributilestannilo (Aldrich), (0,8 g; 0,66 mL; 2,45 mmol). Después de 15 minutos, se retiró el matraz del baño, se permitió que la temperatura se eleve hasta 20°C, y se mantuvo la mezcla de reacción, a dicha temperatura, bajo agitación, por 12 horas. Subsecuentemente, después de la adición de una solución saturada de bicarbonato de sodio (Aldrich), (20 mL), la mezcla de reacción se extrajo con éter etílico (Aldrich), (3 x 25 mL): la fase orgánica obtenida se lavó con una solución saturada de bicarbonato de sodio (Aldrich), (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover el disolvente residual por destilación bajo presión reducida, se obtuvo el residuo que comprende 2,6(4'-octilfenoxi)-1[2'(5'-tributilestannil)tienil]benceno que tiene la fórmula (i'):
se usó de la siguiente manera.
En un matraz de 100 mL equipado con un agitador magnético, un termómetro y un sistema de refrigeración, bajo una atmósfera inerte, el residuo que comprende 2,6(4'-octilfenoxi)-1(2'(5'-tributilestannil)tienil)benceno con fórmula (i'), obtenido como se describe anteriormente se disolvió en tolueno anhidro (Aldrich), (10 mL), obteniendo una solución a la que se le adicionó 4,7-dibromo-5,6-di-(4'-carbometoxifenoxi)benzotiadiazol que tiene fórmula (d), obtenido como se
describe en el Ejemplo 3 (0,237 g; 0,4 mmol). Después de remover el aire presente a través de 3 ciclos de vacío/nitrógeno, se adicionaron tris(dibencilidenacetona)dipaladio (Aldrich), (0,012 g; 0,013 mmol) y tris-o-tolilfosfina (Aldrich), (0,015 g; 0,05 mmol), obteniendo una mezcla de reacción que se sumergió en un baño precalentado a 110°C, y se mantuvo bajo agitación, a dicha temperatura, por 12 horas. Subsecuentemente, la mezcla de reacción se vertió en agua destilada (50 mL) y se extrajo con diclorometano (Aldrich), (3 x 25 mL), la fase orgánica obtenida se lavó hasta la neutralidad con agua destilada (3 x 25 mL), y subsecuentemente se deshidrató sobre sulfato de sodio (Aldrich). Después de remover la mayor parte del disolvente residual por destilación bajo presión reducida, se adicionó gota a gota el residuo obtenido a 50 mL de metanol, obteniendo un precipitado que se recuperó por filtración, y subsecuentemente se purificó por elución en columna de cromatografía en gel de sílice [eluyente: mezcla n-heptano (Aldrich)/diclorometano (Aldrich)/acetato de etilo (Aldrich) 9/0,97/0,03 (v/v/v)]. El producto obtenido se recristalizó en una mezcla de n-heptano (Aldrich)/diclorometano (Aldrich) [relación 9/1 (v/v)], para obtener 0,4 g de 2,6-(POP-4-C8 H17)-(DT-BOP-4-COOCH3) que tiene la fórmula (10), (productividad = 64%).
Ejemplo 13 (comparativo)
Se disolvieron 6 g de polimetilmetacrilato Altuglas VSUVT 100 (PMMA) y 49,5 mg de 4,7-di(tien-2'-il)-2,1,3-benzotiadiazol (DTB) en 30 mL de 1,2-diclorobenceno (Aldrich). Subsecuentemente, la solución obtenida se depositó uniformemente sobre una lámina de polimetilmetacrilato (dimensiones 300 mm x 90 mm x 6 mm) usando un aplicador de película tipo “Doctor Blade”, y se permitió que el disolvente se evapore a temperatura ambiente (25°C), en una ligera corriente de aire, por 24 horas. El resultado es una lámina transparente de color amarillo proporcionada por la película, cuyo espesor está en el rango de 100 |jm a 50 |jm.
Subsecuentemente se aplicó una celda fotovoltaica IXYS-KXOB22-12 con un área superficial de 1,2 cm2 en uno de los bordes de la lámina del polímero.
La cara principal de la placa del polímero [la recubierta con la película delgada que contiene 4,7-di(tien-2'-il)-2,1,3-benzotiadiazol (DTB)] se iluminó subsecuentemente con una fuente de luz con una potencia de 1000 W/m2 (1 sol), y se midió la potencia eléctrica generada por el efecto de iluminación.
La potencia (P) se midió iluminando una porción de la placa con dimensiones de 100 mm x 90 mm a una distancia (d) creciente desde el borde al cual la celda fotovoltaica está fija. La contribución de los efectos de la guía de ondas, del borde y de la autoabsorción se podría cuantificar a través de estas mediciones a una distancia variable de la celda fotovoltaica.
La figura 1 muestra la curva relativa a la potencia (P) generada, expresada en mW (representada en las ordenadas), en función de la distancia (d) desde el borde al cual la celda fotovoltaica está fija, expresada en cm (representada en las abscisas).
Se puede observar que, en ausencia de los efectos del borde, la potencia promedio generada es de 5,69 mW (figura 1).
La figura 2 muestra la potencia (P) generada, expresada en mW (en las ordenadas), (en las abscisas se muestra el número de Ejemplo).
Ejemplo 14 (comparativo)
Se disolvieron 6 g de polimetilmetacrilato Altuglas VSUVT 100 (PMMA) y 87,1 mg de 5,6-difenoxi-4,7-bis-(2-tienil)-2,1,3-benzotiadiazol que tiene la fórmula (la), (DTBOP), obtenido como se describe en el Ejemplo 1 de la solicitud de patente internacional Wo 2016/046319 mencionada anteriormente, en 30 mL de 1,2-diclorobenceno (Aldrich). Subsecuentemente, la solución obtenida se depositó uniformemente sobre una lámina de polimetilmetacrilato (dimensiones 300 mm x 90 mm x 6 mm) usando un aplicador de película tipo “Doctor Blade”, y se permitió que el disolvente se evapore a temperatura ambiente (25°C), en una ligera corriente de aire, por 24 horas. El resultado es una lámina transparente de color naranja proporcionada por la película, cuyo espesor está en el rango de 100 jm a 50 jm .
Subsecuentemente se aplicó una celda fotovoltaica IXYS-KXOB22-12 con un área superficial de 1,2 cm2 en uno de los bordes de la lámina del polímero.
La cara principal de la placa de polímero [la recubierta con la película delgada que contiene 5,6-difenoxi-4,7-bis(2-tienil)-2,1,3-benzotiadiazol que tiene la fórmula (la)] se iluminó subsecuentemente con una fuente de luz con una potencia de 1000 W/m2 (1 sol), y se midió la potencia eléctrica generada por el efecto de iluminación.
La potencia (P) se midió iluminando una porción de la placa con dimensiones de 100 mm x 90 mm a una distancia (d) creciente desde el borde al cual la celda fotovoltaica está fija. La contribución de los efectos de la guía de ondas, del borde y de la autoabsorción se podría cuantificar a través de estas mediciones a una distancia variable de la celda fotovoltaica.
La figura 1 muestra la curva relativa a la potencia (P) generada, expresada en mW (representada en las ordenadas), en función de la distancia (d) desde el borde al cual la celda fotovoltaica está fija, expresada en cm (representada en las abscisas).
Se puede observar que, en ausencia de los efectos del borde, la potencia promedio generada es de 8,49 mW (figura 1).
La figura 2 muestra la potencia (P) generada, expresada en mW (en las ordenadas), (en las abscisas se muestra el número de Ejemplo).
Ejemplo 15 (invención)
Se disolvieron 6 g de polimetilmetacrilato Altuglas VSUVT 100 (PMMA) y 85,2 mg de 2-POP-DTBOP que tiene la fórmula, obtenido como se describe en el Ejemplo 1, en 30 mL de 1,2-diclorobenceno (Aldrich). Subsecuentemente, la solución obtenida se depositó uniformemente sobre una lámina de polimetilmetacrilato (dimensiones 300 mm x 90 mm x 6 mm) usando un aplicador de película tipo “Doctor Blade”, y se permitió que el disolvente se evapore a temperatura ambiente (25°C), en una ligera corriente de aire, por 24 horas. El resultado es una lámina transparente de color naranja proporcionada por la película, cuyo espesor está en el rango de 100 |jm a 50 |jm. Subsecuentemente se aplicó una celda fotovoltaica IXYS-KXOB22-12 con un área superficial de 1,2 cm2 en uno de los bordes de la lámina del polímero.
La cara principal de la placa de polímero [la recubierta con la película delgada que contiene 2-POP-DTBOP que tiene la fórmula (1)] se iluminó subsecuentemente con una fuente de luz con una potencia de 1000 W/m2 (1 sol), y se midió la potencia eléctrica generada por el efecto de iluminación. La potencia (P) se midió iluminando una porción de la placa con dimensiones de 100 mm x 90 mm a una distancia (d) creciente desde el borde al cual la celda fotovoltaica está fija. La contribución de los efectos de la guía de ondas, del borde y de la autoabsorción se podría cuantificar a través de estas mediciones a una distancia variable de la celda fotovoltaica.
La figura 1 muestra la curva relativa a la potencia (P) generada, expresada en mW (representada en las ordenadas), en función de la distancia (d) desde el borde al cual la celda fotovoltaica está fija, expresada en cm (representada en las abscisas).
Se puede observar que, en ausencia de los efectos del borde, la potencia promedio generada es de 12,76 mW (figura 1).
La figura 2 muestra la potencia (P) generada, expresada en mW (en las ordenadas), (en las abscisas se muestra el número de Ejemplo).
Ejemplo 16 (invención)
Se disolvieron 6 g de polimetilmetacrilato Altuglas VSUVT 100 (PMMA) y 164,2 mg de 2-POP-DTBOP que tiene la fórmula (1), obtenido como se describe en el Ejemplo 1, en 30 mL de 1,2-diclorobenceno (Aldrich). Subsecuentemente, la solución obtenida se depositó uniformemente sobre una lámina de polimetilmetacrilato (dimensiones 300 mm x 90 mm x 6 mm) usando un aplicador de película tipo “Doctor Blade”, y se permitió que el disolvente se evapore a temperatura ambiente (25°C), en una ligera corriente de aire, por 24 horas. El resultado es una lámina transparente de color naranja proporcionada por la película, cuyo espesor está en el rango de 100 jm a 50 jm . Subsecuentemente se aplicó una celda fotovoltaica IXYS-KXOB22-12 con un área superficial de 1,2 cm2 en uno de los bordes de la lámina del polímero.
La cara principal de la placa de polímero [la recubierta con la película delgada que contiene 2-POP-DTBOP que tiene la fórmula (1)] se iluminó subsecuentemente con una fuente de luz con una potencia de 1000 W/m2 (1 sol), y se midió la potencia eléctrica generada por el efecto de iluminación. La potencia (P) se midió iluminando una porción de la placa con dimensiones de 100 mm x 90 mm a una distancia (d) creciente desde el borde al cual la celda fotovoltaica está fija. La contribución de los efectos de la guía de ondas, del borde y de la autoabsorción se podría cuantificar a través de estas mediciones a una distancia variable de la celda fotovoltaica.
La figura 1 muestra la curva relativa a la potencia (P) generada, expresada en mW (representada en las ordenadas), en función de la distancia (d) desde el borde al cual la celda fotovoltaica está fija, expresada en cm (representada en las abscisas).
Se puede observar que, en ausencia de los efectos del borde, la potencia promedio generada es de 14,52 mW (figura 1).
La figura 2 muestra la potencia (P) generada, expresada en mW (en las ordenadas), (en las abscisas se muestra el número de Ejemplo).
Ejemplo 17 (invención)
Se disolvieron 6 g de polimetilmetacrilato Altuglas VSUVT 100 (PMMA) y 165,2 mg de 2-POP-(DTBOP-4-COOCH3) que tiene la fórmula (11), obtenido como se describe en el Ejemplo 3, en 30 mL de 1,2-diclorobenceno (Aldrich). Subsecuentemente, la solución obtenida se depositó uniformemente sobre una lámina de polimetilmetacrilato (dimensiones 300 mm x 90 mm x 6 mm) usando un aplicador de película tipo “Doctor Blade”, y se permitió que el disolvente se evapore a temperatura ambiente (25°C), en una ligera corriente de aire, por 24 horas. El resultado es una lámina transparente de color naranja proporcionada por la película, cuyo espesor está en el rango de 100 jm a 50 jm .
Subsecuentemente se aplicó una celda fotovoltaica IXYS-KXOB22-12 con un área superficial de 1,2 cm2 en uno de los bordes de la lámina del polímero.
La cara principal de la placa de polímero [la recubierta con la película delgada que contiene 2-POP-(DTBOP-4-COOCH3) que tiene la fórmula (11)], se iluminó subsecuentemente con una fuente de luz con una potencia de 1000 W/m2 (1 sol), y se midió la potencia eléctrica generada por el efecto de iluminación.
La potencia (P) se midió iluminando una porción de la placa con dimensiones de 100 mm x 90 mm a una distancia (d) creciente desde el borde al cual la celda fotovoltaica está fija. La contribución de los efectos de la guía de ondas, del borde y de la autoabsorción se podría cuantificar a través de estas mediciones a una distancia variable de la celda fotovoltaica.
La figura 1 muestra la curva relativa a la potencia (P) generada, expresada en mW (representada en las ordenadas), en función de la distancia (d) desde el borde al cual la celda fotovoltaica está fija, expresada en cm (representada en las abscisas).
Se puede observar que, en ausencia de los efectos del borde, la potencia promedio generada es de 12,74 mW (figura 1).
La figura 2 muestra la potencia (P) generada, expresada en mW (en las ordenadas), (en las abscisas se muestra el número de Ejemplo).
Ejemplo 18 (invención)
Se disolvieron 6 g de polimetilmetacrilato Altuglas VSUVT 100 (PMMA) y 190,4 mg de 2,6-POP-DTBOP que tiene la fórmula (3), obtenido como se describe en el Ejemplo 4, en 30 mL de 1,2-diclorobenceno (Aldrich). Subsecuentemente, la solución obtenida se depositó uniformemente sobre una lámina de polimetilmetacrilato (dimensiones 300 mm x 90 mm x 6 mm) usando un aplicador de película tipo “Doctor Blade”, y se permitió que el disolvente se evapore a temperatura ambiente (25°C), en una ligera corriente de aire, por 24 horas. El resultado es una lámina transparente de color naranja proporcionada por la película, cuyo espesor está en el rango de 100 |jm a 50 |jm. Subsecuentemente se aplicó una celda fotovoltaica IXYS-KXOB22-12 con un área superficial de 1,2 cm2 en uno de los bordes de la lámina del polímero.
La cara principal de la placa de polímero [la recubierta con la película delgada que contiene 2,6-POP-DTBOP que tiene la fórmula (3)] se iluminó subsecuentemente con una fuente de luz con una potencia de 1000 W/m2 (1 sol), y se midió la potencia eléctrica generada por el efecto de iluminación. La potencia (P) se midió iluminando una porción de la placa con dimensiones de 100 mm x 90 mm a una distancia (d) creciente desde el borde al cual la celda fotovoltaica está fija. La contribución de los efectos de la guía de ondas, del borde y de la autoabsorción se podría cuantificar a través de estas mediciones a una distancia variable de la celda fotovoltaica.
La figura 1 muestra la curva relativa a la potencia (P) generada, expresada en mW (representada en las ordenadas), en función de la distancia (d) desde el borde al cual la celda fotovoltaica está fija, expresada en cm (representada en las abscisas).
Se puede observar que, en ausencia de los efectos del borde, la potencia promedio generada es de 13,06 mW (figura 1).
La figura 2 muestra la potencia (P) generada, expresada en mW (en las ordenadas), (en las abscisas se muestra el número de Ejemplo).
Ejemplo 19 (invención)
Se disolvieron 6 g de polimetilmetacrilato Altuglas VSUVT 100 (PMMA) y 180 mg de 2,4-POP-DTBOP que tiene la fórmula (4), obtenido como se describe en el Ejemplo 5, en 30 mL de 1,2-diclorobenceno (Aldrich). Subsecuentemente, la solución obtenida se depositó uniformemente sobre una lámina de polimetilmetacrilato (dimensiones 300 mm x 90 mm x 6 mm) usando un aplicador de película tipo “Doctor Blade”, y se permitió que el disolvente se evapore a temperatura ambiente (25°C), en una ligera corriente de aire, por 24 horas. El resultado es una lámina transparente de color naranja proporcionada por la película, cuyo espesor está en el rango de 100 jm a 50 jm . Subsecuentemente se aplicó una celda fotovoltaica IXYS-KXOB22-12 con un área superficial de 1,2 cm2 en uno de los bordes de la lámina del polímero.
La cara principal de la placa de polímero [la recubierta con la película delgada que contiene 2,4-POP-DTBOP que tiene la fórmula (4)] se iluminó subsecuentemente con una fuente de luz con una potencia de 1000 W/m2 (1 sol), y se midió la potencia eléctrica generada por el efecto de iluminación. La potencia (P) se midió iluminando una porción de la placa con dimensiones de 100 mm x 90 mm a una distancia (d) creciente desde el borde al cual la celda fotovoltaica está fija. La contribución de los efectos de la guía de ondas, del borde y de la autoabsorción se podría cuantificar a través de estas mediciones a una distancia variable de la celda fotovoltaica.
La figura 1 muestra la curva relativa a la potencia (P) generada, expresada en mW (representada en las ordenadas), en función de la distancia (d) desde el borde al cual la celda fotovoltaica está fija, expresada en cm (representada en las
abscisas).
Se puede observar que, en ausencia de los efectos del borde, la potencia promedio generada es de 13,23 mW (figura 1).
La figura 2 muestra la potencia (P) generada, expresada en mW (en las ordenadas), (en las abscisas se muestra el número de Ejemplo).
Ejemplo 20 (invención)
Se disolvieron 6 g de polimetilmetacrilato Altuglas VSUVT 100 (PMMA) y 112 mg de 2,4,6-POP-DTBOP que tiene la fórmula (2), obtenido como se describe en el Ejemplo 6, en 30 mL de 1,2-diclorobenceno (Aldrich). Subsecuentemente, la solución obtenida se depositó uniformemente sobre una lámina de polimetilmetacrilato (dimensiones 300 mm x 90 mm x 6 mm) usando un aplicador de película tipo “Doctor Blade”, y se permitió que el disolvente se evapore a temperatura ambiente (25°C), en una ligera corriente de aire, por 24 horas. El resultado es una lámina transparente de color naranja proporcionada por la película, cuyo espesor está en el rango de 100 |jm a 50 |jm. Subsecuentemente se aplicó una celda fotovoltaica IXYS-KXOB22-12 con un área superficial de 1,2 cm2 en uno de los bordes de la lámina del polímero.
La cara principal de la placa de polímero [la recubierta con la película delgada que contiene 2,4,6-POP-DTBOP que tiene la fórmula (2)] se iluminó subsecuentemente con una fuente de luz con una potencia de 1000 W/m2 (1 sol), y se midió la potencia eléctrica generada por el efecto de iluminación.
La potencia (P) se midió iluminando una porción de la placa con dimensiones de 100 mm x 90 mm a una distancia (d) creciente desde el borde al cual la celda fotovoltaica está fija. La contribución de los efectos de la guía de ondas, del borde y de la autoabsorción se podría cuantificar a través de estas mediciones a una distancia variable de la celda fotovoltaica.
La figura 1 muestra la curva relativa a la potencia (P) generada, expresada en mW (representada en las ordenadas), en función de la distancia (d) desde el borde al cual la celda fotovoltaica está fija, expresada en cm (representada en las abscisas).
Se puede observar que, en ausencia de los efectos del borde, la potencia promedio generada es de 11,88 mW (figura 1).
La figura 2 muestra la potencia (P) generada, expresada en mW (en las ordenadas), (en las abscisas se muestra el número de Ejemplo).
Ejemplo 21 (invención)
Se disolvieron 6 g de polimetilmetacrilato Altuglas VSUVT 100 (PMMA) y 206 mg de 2,4,6-POP-DTBOP que tiene la fórmula (2), obtenido como se describe en el Ejemplo 6, en 30 mL de 1,2-diclorobenceno (Aldrich). Subsecuentemente, la solución obtenida se depositó uniformemente sobre una lámina de polimetilmetacrilato (dimensiones 300 mm x 90 mm x 6 mm) usando un aplicador de película tipo “Doctor Blade”, y se permitió que el disolvente se evapore a temperatura ambiente (25°C), en una ligera corriente de aire, por 24 horas. El resultado es una lámina transparente de color naranja proporcionada por la película, cuyo espesor está en el rango de 100 jm a 50 jm . Subsecuentemente se aplicó una celda fotovoltaica IXYS-KXOB22-12 con un área superficial de 1,2 cm2 en uno de los bordes de la lámina del polímero.
La cara principal de la placa de polímero [la recubierta con la película delgada que contiene 2,4,6-POP-DTBOP que tiene la fórmula (2)] se iluminó subsecuentemente con una fuente de luz con una potencia de 1000 W/m2 (1 sol), y se midió la potencia eléctrica generada por el efecto de iluminación.
La potencia (P) se midió iluminando una porción de la placa con dimensiones de 100 mm x 90 mm a una distancia (d) creciente desde el borde al cual la celda fotovoltaica está fija. La contribución de los efectos de la guía de ondas, del borde y de la autoabsorción se podría cuantificar a través de estas mediciones a una distancia variable de la celda fotovoltaica.
La figura 1 muestra la curva relativa a la potencia (P) generada, expresada en mW (representada en las ordenadas), en función de la distancia (d) desde el borde al cual la celda fotovoltaica está fija, expresada en cm (representada en las abscisas).
Se puede observar que, en ausencia de los efectos del borde, la potencia promedio generada es de 14,9 mW (figura 1).
La figura 2 muestra la potencia (P) generada, expresada en mW (en las ordenadas), (en las abscisas se muestra el número de Ejemplo).
Ejemplo 22 (invención)
Se disolvieron 6 g de polimetilmetacrilato Altuglas VSUVT 100 (PMMA) y 148,9 mg de 2-CH3-4-POP-DTBOP que tiene la fórmula (5), obtenido como se describe en el Ejemplo 7, en 30 mL de 1,2-diclorobenceno (Aldrich). Subsecuentemente, la solución obtenida se depositó uniformemente sobre una lámina de polimetilmetacrilato (dimensiones 300 mm x 90 mm
x 6 mm) usando un aplicador de película tipo “Doctor Blade”, y se permitió que el disolvente se evapore a temperatura ambiente (25°C), en una ligera corriente de aire, por 24 horas. El resultado es una lámina transparente de color naranja proporcionada por la película, cuyo espesor está en el rango de 100 |jm a 50 |jm. Subsecuentemente se aplicó una celda fotovoltaica IXYS-KXOB22-12 con un área superficial de 1,2 cm2 en uno de los bordes de la lámina del polímero.
La cara principal de la placa de polímero [la recubierta con la película delgada que contiene 2-CH3-4-POP-DTBOP que tiene la fórmula (5)] se iluminó subsecuentemente con una fuente de luz con una potencia de 1000 W/m2 (1 sol), y se midió la potencia eléctrica generada por el efecto de iluminación.
La potencia (P) se midió iluminando una porción de la placa con dimensiones de 100 mm x 90 mm a una distancia (d) creciente desde el borde al cual la celda fotovoltaica está fija. La contribución de los efectos de la guía de ondas, del borde y de la autoabsorción se podría cuantificar a través de estas mediciones a una distancia variable de la celda fotovoltaica. La figura 1 muestra la curva relativa a la potencia (P) generada, expresada en mW (representada en las ordenadas), en función de la distancia (d) desde el borde al cual la celda fotovoltaica está fija, expresada en cm (representada en las abscisas).
Se puede observar que, en ausencia de los efectos del borde, la potencia promedio generada es de 13,48 mW (figura 1). La figura 2 muestra la potencia (P) generada, expresada en mW (en las ordenadas), (en las abscisas se muestra el número de Ejemplo).
Ejemplo 23 (invención)
Se disolvieron 6 g de polimetilmetacrilato Altuglas VSUVT 100 (PMMA) y 173,5 mg de 6-CF3-2-POP-DTBOP que tiene la fórmula (6), obtenido como se describe en el Ejemplo 8, en 30 mL de 1,2-diclorobenceno (Aldrich). Subsecuentemente, la solución obtenida se depositó uniformemente sobre una lámina de polimetilmetacrilato (dimensiones 300 mm x 90 mm x 6 mm) usando un aplicador de película tipo “Doctor Blade”, y se permitió que el disolvente se evapore a temperatura ambiente (25°C), en una ligera corriente de aire, por 24 horas. El resultado es una lámina transparente de color amarillo proporcionada por la película, cuyo espesor está en el rango de 100 jm a 50 jm .
Subsecuentemente se aplicó una celda fotovoltaica IXYS-KXOB22-12 con un área superficial de 1,2 cm2 en uno de los bordes de la lámina del polímero.
La cara principal de la placa de polímero [la recubierta con la película delgada que contiene 6-CF3-2-POP-DTBOP que tiene la fórmula (6)] se iluminó subsecuentemente con una fuente de luz con una potencia de 1000 W/m2 (1 sol), y se midió la potencia eléctrica generada por el efecto de iluminación.
La potencia (P) se midió iluminando una porción de la placa con dimensiones de 100 mm x 90 mm a una distancia (d) creciente desde el borde al cual la celda fotovoltaica está fija. La contribución de los efectos de la guía de ondas, del borde y de la autoabsorción se podría cuantificar a través de estas mediciones a una distancia variable de la celda fotovoltaica. La figura 1 muestra la curva relativa a la potencia (P) generada, expresada en mW (representada en las ordenadas), en función de la distancia (d) desde el borde al cual la celda fotovoltaica está fija, expresada en cm (representada en las abscisas).
Se puede observar que, en ausencia de los efectos del borde, la potencia promedio generada es de 9,22 mW (figura 1). La figura 2 muestra la potencia (P) generada, expresada en mW (en las ordenadas), (en las abscisas se muestra el número de Ejemplo).
Ejemplo 24 (invención)
Se disolvieron 6 g de polimetilmetacrilato Altuglas VSUVT 100 (PMMA) y 170,6 mg de 2-(POP-4-CF3)-DTBOP que tiene la fórmula (7), obtenido como se describe en el Ejemplo 9, en 30 mL de 1,2-diclorobenceno (Aldrich). Subsecuentemente, la solución obtenida se depositó uniformemente sobre una lámina de polimetilmetacrilato (dimensiones 300 mm x 90 mm x 6 mm) usando un aplicador de película tipo “Doctor Blade”, y se permitió que el disolvente se evapore a temperatura ambiente (25°C), en una ligera corriente de aire, por 24 horas. El resultado es una lámina transparente de color naranja proporcionada por la película, cuyo espesor está en el rango de 100 jm a 50 jm .
Subsecuentemente se aplicó una celda fotovoltaica IXYS-KXOB22-12 con un área superficial de 1,2 cm2 en uno de los bordes de la lámina del polímero.
La cara principal de la placa de polímero [la recubierta con la película delgada que contiene 2-(POP-4-CF3-)-DTBOP que tiene la fórmula (7)] se iluminó subsecuentemente con una fuente de luz con una potencia de 1000 W/m2 (1 sol), y se midió la potencia eléctrica generada por el efecto de iluminación.
La potencia (P) se midió iluminando una porción de la placa con dimensiones de 100 mm x 90 mm a una distancia (d) creciente desde el borde al cual la celda fotovoltaica está fija. La contribución de los efectos de la guía de ondas, del borde y de la autoabsorción se podría cuantificar a través de estas mediciones a una distancia variable de la celda fotovoltaica. La figura 1 muestra la curva relativa a la potencia (P) generada, expresada en mW (representada en las ordenadas), en función de la distancia (d) desde el borde al cual la celda fotovoltaica está fija, expresada en cm (representada en las abscisas).
Se puede observar que, en ausencia de los efectos del borde, la potencia promedio generada es de 12,56 mW (figura 1). La figura 2 muestra la potencia (P) generada, expresada en mW (en las ordenadas), (en las abscisas se muestra el número de Ejemplo).
Ejemplo 25 (invención)
Se disolvieron 6 g de polimetilmetacrilato Altuglas VSUVT 100 (PMMA) y 170,6 mg de 2-(POP-2-CF3)-DTBOP que tiene la fórmula (8), obtenido como se describe en el Ejemplo 10, en 30 mL de 1,2-diclorobenceno (Aldrich). Subsecuentemente, la solución obtenida se depositó uniformemente sobre una lámina de polimetilmetacrilato (dimensiones 300 mm x 90 mm x 6 mm) usando un aplicador de película tipo “Doctor Blade”, y se permitió que el disolvente se evapore a temperatura ambiente (25°C), en una ligera corriente de aire, por 24 horas. El resultado es una lámina transparente de color naranja proporcionada por la película, cuyo espesor está en el rango de 100 |jm a 50 |jm.
Subsecuentemente se aplicó una celda fotovoltaica IXYS-KXOB22-12 con un área superficial de 1,2 cm2 en uno de los bordes de la lámina del polímero.
La cara principal de la placa de polímero [la recubierta con la película delgada que contiene 2-(POP-2-CF3)-DTBOP que tiene la fórmula (8)] se iluminó subsecuentemente con una fuente de luz con una potencia de 1000 W/m2 (1 sol), y se midió la potencia eléctrica generada por el efecto de iluminación.
La potencia (P) se midió iluminando una porción de la placa con dimensiones de 100 mm x 90 mm a una distancia (d) creciente desde el borde al cual la celda fotovoltaica está fija. La contribución de los efectos de la guía de ondas, del borde y de la autoabsorción se podría cuantificar a través de estas mediciones a una distancia variable de la celda fotovoltaica. La figura 1 muestra la curva relativa a la potencia (P) generada, expresada en mW (representada en las ordenadas), en función de la distancia (d) desde el borde al cual la celda fotovoltaica está fija, expresada en cm (representada en las abscisas).
Se puede observar que, en ausencia de los efectos del borde, la potencia promedio generada es de 12,35 mW (figura 1). La figura 2 muestra la potencia (P) generada, expresada en mW (en las ordenadas), (en las abscisas se muestra el número de Ejemplo).
Ejemplo 26 (invención)
Se disolvieron 6 g de polimetilmetacrilato Altuglas VSUVT 100 (PMMA) y 292 mg de 2,6-(POP-4-Cs H17)-DTBOP que tiene la fórmula (9), obtenido como se describe en el Ejemplo 11, en 30 mL de 1,2-diclorobenceno (Aldrich). Subsecuentemente, la solución obtenida se depositó uniformemente sobre una lámina de polimetilmetacrilato (dimensiones 300 mm x 90 mm x 6 mm) usando un aplicador de película tipo “Doctor Blade”, y se permitió que el disolvente se evapore a temperatura ambiente (25°C), en una ligera corriente de aire, por 24 horas. El resultado es una lámina transparente de color naranja proporcionada por la película, cuyo espesor está en el rango de 100 jm a 50 jm .
Subsecuentemente se aplicó una celda fotovoltaica IXYS-KXOB22-12 con un área superficial de 1,2 cm2 en uno de los bordes de la lámina del polímero.
La cara principal de la placa de polímero [la recubierta con la película delgada que contiene 2,6-(POP-4-Cs H17)-DTBOP que tiene la fórmula (9)] se iluminó subsecuentemente con una fuente de luz con una potencia de 1000 W/m2 (1 sol), y se midió la potencia eléctrica generada por el efecto de iluminación.
La potencia (P) se midió iluminando una porción de la placa con dimensiones de 100 mm x 90 mm a una distancia (d) creciente desde el borde al cual la celda fotovoltaica está fija. La contribución de los efectos de la guía de ondas, del borde y de la autoabsorción se podría cuantificar a través de estas mediciones a una distancia variable de la celda fotovoltaica. La figura 1 muestra la curva relativa a la potencia (P) generada, expresada en mW (representada en las ordenadas), en función de la distancia (d) desde el borde al cual la celda fotovoltaica está fija, expresada en cm (representada en las abscisas).
Se puede observar que, en ausencia de los efectos del borde, la potencia promedio generada es de 9,01 mW (figura 1). La figura 2 muestra la potencia (P) generada, expresada en mW (en las ordenadas), (en las abscisas se muestra el número de Ejemplo).
Ejemplo 27 (invención)
Se disolvieron6 g de polimetilmetacrilato Altuglas VSUVT 100 (PMMA) y 260 mg de 2,6-(POP-4-C8H17)-(DTBOP-4-COOCH3) que tiene la fórmula (10), obtenido como se describe en el Ejemplo 12, en 30 mL de 1,2-diclorobenceno (Aldrich). Subsecuentemente, la solución obtenida se depositó uniformemente sobre una lámina de polimetilmetacrilato (dimensiones 300 mm x 90 mm x 6 mm) usando un aplicador de película tipo “Doctor Blade”, y se permitió que el disolvente se evapore a temperatura ambiente (25°C), en una ligera corriente de aire, por 24 horas. El resultado es una lámina transparente de color naranja proporcionada por la película, cuyo espesor está en el rango de 100 |jm a 50 |jm.
Subsecuentemente se aplicó una celda fotovoltaica IXYS-KXOB22-12 con un área superficial de 1,2 cm2 en uno de los bordes de la lámina del polímero.
La cara principal de la placa de polímero [la recubierta con la película delgada que contiene 2,6-(POP-4-C8H17)-(DTBOP-4 -COOCH3) que tiene la fórmula (10)] se iluminó subsecuentemente con una fuente de luz con una potencia de 1000 W/m2 (1 sol), y se midió la potencia eléctrica generada por el efecto de iluminación.
La potencia (P) se midió iluminando una porción de la placa con dimensiones de 100 mm x 90 mm a una distancia (d) creciente desde el borde al cual la celda fotovoltaica está fija. Estas medidas a una distancia variable de la celda fotovoltaica permiten cuantificar la contribución de los efectos de la guía de onda, del borde, de la difusión y de la autoabsorción.
La figura 1 muestra la curva relativa a la potencia (P) generada, expresada en mW (representada en las ordenadas), en función de la distancia (d) desde el borde al cual la celda fotovoltaica está fija, expresada en cm (representada en las abscisas).
Se puede observar que, en ausencia de los efectos del borde, la potencia promedio generada es de 10,54 mW (figura 1). La figura 2 muestra la potencia (P) generada, expresada en mW (en las ordenadas), (en las abscisas se muestra el número de Ejemplo).
Ejemplo 28 (invención)
Se disolvieron 6 g de polimetilmetacrilato Altuglas VSUVT 100 (PMMA) y 151 mg de 2-POP-6-F-DTBOP que tiene la fórmula (12), obtenido como se describe en el Ejemplo 2, en 30 mL de 1,2-diclorobenceno (Aldrich). Subsecuentemente, la solución obtenida se depositó uniformemente sobre una lámina de polimetilmetacrilato (dimensiones 300 mm x 90 mm x 6 mm) usando un aplicador de película tipo “Doctor Blade”, y se permitió que el disolvente se evapore a temperatura ambiente (25°C), en una ligera corriente de aire, por 24 horas. El resultado es una lámina transparente de color naranja proporcionada por la película, cuyo espesor está en el rango de 100 jm a 50 jm . Subsecuentemente se aplicó una celda fotovoltaica IXYS-KXOB22-12 con un área superficial de 1,2 cm2 en uno de los bordes de la lámina del polímero.
La cara principal de la placa de polímero [la recubierta con la película delgada que contiene 2-POP-6-F-DTBOP que tiene la fórmula (12)] se iluminó subsecuentemente con una fuente de luz con una potencia de 1000 W/m2 (1 sol), y se midió la potencia eléctrica generada por el efecto de iluminación. La potencia (P) se midió iluminando una porción de la placa con dimensiones de 100 mm x 90 mm a una distancia (d) creciente desde el borde al cual la celda fotovoltaica está fija. La contribución de los efectos de la guía de ondas, del borde y de la autoabsorción se podría cuantificar a través de estas mediciones a una distancia variable de la celda fotovoltaica.
La figura 1 muestra la curva relativa a la potencia (P) generada, expresada en mW (representada en las ordenadas), en función de la distancia (d) desde el borde al cual la celda fotovoltaica está fija, expresada en cm (representada en las abscisas).
Se puede observar que, en ausencia de los efectos del borde, la potencia promedio generada es de 10,46 mW (figura 1). La figura 2 muestra la potencia (P) generada, expresada en mW (en las ordenadas), (en las abscisas se muestra el número de Ejemplo).
Claims (4)
1. Un compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I):
en donde:
- R1, R2 y R3 , que son iguales o diferentes entre sí, representan un átomo de hidrógeno; o representan un átomo de halógeno, tal como cloro, bromo, flúor, yodo, preferiblemente flúor; o se seleccionan de grupos alquilo de C1-C12, preferiblemente de C1-C8 , lineales o ramificados opcionalmente halogenados, grupos fenoxilo opcionalmente sustituidos, siempre que al menos uno de R1, R2 o R3 sea un grupo fenoxilo opcionalmente sustituido y, si R3 es un grupo fenoxilo opcionalmente sustituido, al menos uno de R1 o R2 es diferente de hidrógeno;
- R4 , que son iguales o diferentes entre sí, representan un átomo de hidrógeno; o se seleccionan de grupos -COOR, en donde R se selecciona de grupos alquilo de C1-C8 , preferiblemente de C1-C4 , lineales o ramificados.
2. Un compuesto de diariloxibenzoheterodiazol disustituido de acuerdo con la reivindicación 1, en donde en dicha fórmula general (I):
- R1, R2 y R3 , que son iguales entre sí, se seleccionan de grupos fenoxilo opcionalmente sustituidos, preferiblemente son un grupo fenoxilo; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R1 y R3 , que son iguales entre sí, representan un átomo de hidrógeno, y R2 se selecciona de grupos fenoxilo opcionalmente sustituidos, preferiblemente es un grupo fenoxilo; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R1 y R2 , que son iguales entre sí, se seleccionan de grupos fenoxilo opcionalmente sustituidos, preferiblemente son un grupo fenoxilo, y R3 representa un átomo de hidrógeno; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R2 y R3 , que son iguales entre sí, se seleccionan de grupos fenoxilo opcionalmente sustituidos, preferiblemente son un grupo fenoxilo, y R1 representa un átomo de hidrógeno; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R1 representa un átomo de hidrógeno, R2 se selecciona de un grupo alquilo de C1-C8, preferiblemente de C1-C4 , lineal o ramificado opcionalmente halogenado, preferiblemente es un metilo, y R3 se selecciona de grupos fenoxilo opcionalmente sustituidos, preferiblemente es un grupo fenoxilo; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R1 se selecciona de un grupo alquilo de C1-C8 , preferiblemente de C1-C4 , lineal o ramificado opcionalmente halogenado, preferiblemente es trifluorometilo, R2 se selecciona de grupos fenoxilo opcionalmente sustituidos, preferiblemente es un grupo fenoxilo, y R3 representa un átomo de hidrógeno; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R1 y R3 , que son iguales entre sí, representan un átomo de hidrógeno, y R2 se selecciona de grupos fenoxilo opcionalmente sustituidos, preferiblemente es un grupo 4-trifluorometilfenoxilo; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R1 y R3 , que son iguales entre sí, representan un átomo de hidrógeno; R2 se selecciona de grupos fenoxilo opcionalmente sustituidos, preferiblemente es un grupo 2-trifluorometilfenoxilo; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R1 y R2 , que son iguales entre sí, se seleccionan de grupos fenoxilo opcionalmente sustituidos, preferiblemente son un grupo 4-octilfenoxilo, y R3 representa un átomo de hidrógeno; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno; o
- R1 y R2 , que son iguales entre sí, se seleccionan de grupos fenoxilo opcionalmente sustituidos, preferiblemente son un grupo 4-octilfenoxilo, y R3 representa un átomo de hidrógeno; y
- R4 , que son iguales entre sí, se seleccionan de grupos -COOr , en donde R se selecciona de grupos alquilo de C1-C8, preferiblemente de C1-C4 , lineales o ramificados, preferiblemente representan un grupo -COOCH3 ; o
- R1 y R3 , que son iguales entre sí, representan un átomo de hidrógeno, y R2 se selecciona de grupos fenoxilo
opcionalmente sustituidos, preferiblemente es un grupo fenoxilo; y
- R4 , que son iguales entre sí, se seleccionan de grupos -COOR, en donde R se selecciona de grupos alquilo de C1-C8 , preferiblemente de C1-C4 , lineales o ramificados, preferiblemente representan un grupo -COOCH3 ; o
- R1, que son iguales entre sí, representan un átomo de halógeno, tal como cloro, bromo, flúor, yodo, preferiblemente representan un átomo de flúor, R2 se selecciona de grupos fenoxilo opcionalmente sustituidos, preferiblemente un grupo fenoxilo, y R3, que son los iguales entre sí, representan un átomo de hidrógeno; y
- R4 , que son iguales entre sí, representan un átomo de hidrógeno.
3. Un concentrador solar luminiscente (LSC) que incluye al menos un compuesto de diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I) de acuerdo con las reivindicaciones 1 ó 2.
4. Un dispositivo fotovoltaico (o dispositivo solar) que comprende al menos una celda fotovoltaica (o celda solar), y al menos un concentrador solar luminiscente (LSC) que incluye al menos un compuesto diariloxibenzoheterodiazol disustituido que tiene la fórmula general (I) de acuerdo con la reivindicación 3.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IT102018000009633A IT201800009633A1 (it) | 2018-10-19 | 2018-10-19 | Composti diarilossibenzoeterodiazolici disostituiti |
| PCT/IB2019/058892 WO2020079654A1 (en) | 2018-10-19 | 2019-10-18 | Disubstituted dl aryloxybenzoh eterodi azole compounds |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2928636T3 true ES2928636T3 (es) | 2022-11-21 |
Family
ID=67875790
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES19795661T Active ES2928636T3 (es) | 2018-10-19 | 2019-10-18 | Compuestos de diariloxibenzoheterodiazol disustituidos |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US11856806B2 (es) |
| EP (1) | EP3867333B1 (es) |
| CN (1) | CN113166138A (es) |
| CA (1) | CA3116657A1 (es) |
| DK (1) | DK3867333T3 (es) |
| ES (1) | ES2928636T3 (es) |
| IT (1) | IT201800009633A1 (es) |
| PL (1) | PL3867333T3 (es) |
| SA (1) | SA521421782B1 (es) |
| WO (1) | WO2020079654A1 (es) |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IT1396026B1 (it) | 2009-10-19 | 2012-11-09 | Eni Spa | Composizioni fotoluminescenti per convertitori di spettro a migliorata efficienza |
| IT1401129B1 (it) | 2010-07-16 | 2013-07-12 | Eni Spa | Processo per la sintesi di composti benzotiadiazolici |
| US8866997B2 (en) * | 2010-11-02 | 2014-10-21 | Arizona Board Of Regents On Behalf Of The University Of Arizona | Patterned electronic and polarization optical devices |
| US10312395B2 (en) | 2014-09-25 | 2019-06-04 | Eni S.P.A. | Luminescent solar concentrator comprising disubstituted benzoheterodiazole compounds |
| US11133474B2 (en) * | 2014-09-25 | 2021-09-28 | Eni S.P.A. | Disubstituted diaryloxybenzoheterodiazole compounds |
| ITUB20155558A1 (it) * | 2015-11-13 | 2017-05-13 | Eni Spa | Composti diarilossibenzoeterodiazolici disostituiti |
| IT201600095693A1 (it) * | 2016-09-23 | 2018-03-23 | Eni Spa | Concentratore solare luminescente |
-
2018
- 2018-10-19 IT IT102018000009633A patent/IT201800009633A1/it unknown
-
2019
- 2019-10-18 WO PCT/IB2019/058892 patent/WO2020079654A1/en not_active Ceased
- 2019-10-18 DK DK19795661.8T patent/DK3867333T3/da active
- 2019-10-18 ES ES19795661T patent/ES2928636T3/es active Active
- 2019-10-18 CN CN201980068884.5A patent/CN113166138A/zh active Pending
- 2019-10-18 EP EP19795661.8A patent/EP3867333B1/en active Active
- 2019-10-18 CA CA3116657A patent/CA3116657A1/en active Pending
- 2019-10-18 US US17/286,621 patent/US11856806B2/en active Active
- 2019-10-18 PL PL19795661.8T patent/PL3867333T3/pl unknown
-
2021
- 2021-04-18 SA SA521421782A patent/SA521421782B1/ar unknown
Also Published As
| Publication number | Publication date |
|---|---|
| US11856806B2 (en) | 2023-12-26 |
| IT201800009633A1 (it) | 2020-04-19 |
| EP3867333B1 (en) | 2022-09-14 |
| CN113166138A (zh) | 2021-07-23 |
| SA521421782B1 (ar) | 2024-07-15 |
| DK3867333T3 (da) | 2022-10-17 |
| WO2020079654A1 (en) | 2020-04-23 |
| EP3867333A1 (en) | 2021-08-25 |
| US20210367176A1 (en) | 2021-11-25 |
| PL3867333T3 (pl) | 2022-12-12 |
| CA3116657A1 (en) | 2020-04-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2719751T3 (es) | Compuestos de diariloxibenzoheterodiazol disustituido | |
| ES2436743T3 (es) | Concentrador solar luminiscente que comprende compuestos de benzotiadiazol disustituidos | |
| ES2712161T3 (es) | Concentrador solar luminiscente que comprende compuestos benzoheterodiazol disustituidos | |
| ITMI20111268A1 (it) | Concentratore solare luminescente comprendente composti benzoselenadiazolici disostituiti | |
| ES2764558T3 (es) | Compuestos de diarioloxibenzoheterodiazolo disustituidos | |
| ES2928636T3 (es) | Compuestos de diariloxibenzoheterodiazol disustituidos | |
| ITMI20131620A1 (it) | Concentratore solare luminescente comprendente composti benzoeterodiazolici tetrasostituiti | |
| ES2989903T3 (es) | Compuestos de diariloxibenzoheterodiazol disustituidos con grupos tienotiofénicos | |
| ES2990221T3 (es) | Concentrador solar luminiscente que comprende compuestos de ditienilpiridintiadiazol | |
| ES2989502T3 (es) | Compuestos de fluoroariloxibenzoheterodiazol disustituidos | |
| WO2014128648A1 (en) | Luminescent solar concentrator comprising disubstituted naphthothiadiazole compounds |