ES2929305T3 - Uso de un catalizador metálico en polvo que comprende una aleación de CoCrMo - Google Patents
Uso de un catalizador metálico en polvo que comprende una aleación de CoCrMo Download PDFInfo
- Publication number
- ES2929305T3 ES2929305T3 ES13706241T ES13706241T ES2929305T3 ES 2929305 T3 ES2929305 T3 ES 2929305T3 ES 13706241 T ES13706241 T ES 13706241T ES 13706241 T ES13706241 T ES 13706241T ES 2929305 T3 ES2929305 T3 ES 2929305T3
- Authority
- ES
- Spain
- Prior art keywords
- weight
- metal alloy
- catalyst
- respect
- total weight
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/70—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper
- B01J23/89—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with noble metals
- B01J23/8933—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with noble metals also combined with metals, or metal oxides or hydroxides provided for in groups B01J23/02 - B01J23/36
- B01J23/8993—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with noble metals also combined with metals, or metal oxides or hydroxides provided for in groups B01J23/02 - B01J23/36 with chromium, molybdenum or tungsten
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/02—Impregnation, coating or precipitation
- B01J37/0215—Coating
- B01J37/0225—Coating of metal substrates
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/38—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of noble metals
- B01J23/40—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of noble metals of the platinum group metals
- B01J23/44—Palladium
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/38—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of noble metals
- B01J23/54—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of noble metals combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36
- B01J23/56—Platinum group metals
- B01J23/60—Platinum group metals with zinc, cadmium or mercury
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/38—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of noble metals
- B01J23/54—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of noble metals combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36
- B01J23/56—Platinum group metals
- B01J23/64—Platinum group metals with arsenic, antimony, bismuth, vanadium, niobium, tantalum, polonium, chromium, molybdenum, tungsten, manganese, technetium or rhenium
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J35/00—Catalysts, in general, characterised by their form or physical properties
- B01J35/30—Catalysts, in general, characterised by their form or physical properties characterised by their physical properties
- B01J35/391—Physical properties of the active metal ingredient
- B01J35/393—Metal or metal oxide crystallite size
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/02—Impregnation, coating or precipitation
- B01J37/0201—Impregnation
- B01J37/0207—Pretreatment of the support
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/02—Impregnation, coating or precipitation
- B01J37/0215—Coating
- B01J37/0225—Coating of metal substrates
- B01J37/0226—Oxidation of the substrate, e.g. anodisation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C29/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring
- C07C29/17—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring by hydrogenation of carbon-to-carbon double or triple bonds
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Catalysts (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
- Crystallography & Structural Chemistry (AREA)
Abstract
La presente invención se relaciona con un nuevo sistema catalítico de polvo metálico (catalizador) que comprende una aleación de cobalto/cromo como vehículo, su producción y su uso en procesos de hidrogenación. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Uso de un catalizador metálico en polvo que comprende una aleación de CoCrMo
La presente invención se refiere a un nuevo sistema catalítico metálico en polvo que comprende una aleación de cobalto/cromo como soporte y a su uso en procesos de hidrogenación.
Los catalizadores en polvo son bien conocidos y se utilizan en reacciones químicas. Algunos tipos importantes dichos tales catalizadores son, por ejemplo, los catalizadores de Lindlar.
Un catalizador de Lindlar es un catalizador heterogéneo que consiste en paladio depositado sobre un soporte de carbonato de calcio que está también tratado con varias formas de plomo.
Dichos catalizadores tienen tanta importancia que siempre existe la necesidad de mejorarlos.
El documento WO 2012/001166 A1 divulga un catalizador de hidrogenación que comprende fibras de metal sinterizado como soporte.
El objetivo de la presente invención era descubrir un catalizador en polvo con propiedades mejoradas.
El sistema catalítico en polvo según la presente invención presenta un metal (o aleación metálica) como material de soporte, en lugar de un soporte de carbonato de calcio.
Esta aleación metálica está recubierta por una capa de óxido metálico sobre la que se deposita paladio (Pd).
Además, el nuevo sistema catalítico en polvo según la presente invención está exento de plomo (Pb).
Los componentes principales de la aleación metálica en polvo son el cobalto (Co), el cromo (Cr) y el molibdeno (Mo). Por lo tanto, la presente invención se refiere a un sistema catalítico en polvo que comprende un soporte de aleación metálica que comprende
(i) del 55% en peso al 80% en peso, con respecto al peso total de la aleación metálica, de Co, y
(ii) del 20% en peso al 40% en peso, con respecto al peso total de la aleación metálica, de Cr, y
(iii) del 2% en peso al 10% en peso, con respecto al peso total de la aleación metálica, de Mo, y
en el que dicha aleación metálica está recubierta por una capa de óxido metálico e impregnada con Pd según la reivindicación 1.
Es obvio que todos los porcentajes suman siempre 100.
El sistema catalítico se encuentra en forma de polvo.
Este nuevo sistema catalítico en polvo presenta numerosas ventajas:
° El catalizador es fácil de reciclar (y de eliminar) después de la reacción. Esto se puede realizar, por ejemplo, por filtración.
° El catalizador se puede utilizar más de una vez (reutilizable).
° El catalizador como tal es un sistema muy estable. Por ejemplo, es estable con respecto a los ácidos y al agua. ° El catalizador es fácil de producir.
° El catalizador es fácil de manipular.
° La hidrogenación se puede llevar a cabo sin disolventes.
° El catalizador está exento de plomo.
° El catalizador muestra una alta selectividad en reacciones de hidrogenación.
Las aleaciones metálicas utilizadas como soporte se conocen como aleación de cobalto/cromo/molibdeno. Dichas
aleaciones están disponibles comercialmente, por ejemplo de EOS GMBH, Alemania (EOS CobaltChrome MP1®), de Attenborough Dental, Reino Unido (Megallium ®) y de International Nickel.
Este tipo de aleaciones se utilizan habitualmente en el campo de la odontología. Especialmente, se utilizan en la producción de prótesis dentales.
Por lo tanto, es sorprendente que dichos materiales presenten excelentes propiedades cuando se utilizan como catalizadores en hidrogenaciones.
Preferentemente, la presente invención se refiere a un sistema catalítico en polvo, en el que la aleación metálica comprende
(i) del 55% en peso al 70% en peso, con respecto al peso total de la aleación metálica, de Co, y
(ii) del 20% en peso al 35% en peso, con respecto al peso total de la aleación metálica, de Cr, y
(iii) del 4% en peso al 10% en peso, con respecto al peso total de la aleación metálica, de Mo, y
en el que dicha aleación metálica está recubierta por una capa de óxido metálico impregnada con Pd según la reivindicación 1.
La aleación metálica puede comprender otros metales, tales como, por ejemplo, Cu, Fe, Ni, Mn, Si, Ti, Al y/o Nb. Por lo tanto, la presente invención también se refiere a un sistema catalítico en polvo, en el que la aleación comprende otros metales, tales como, por ejemplo, Cu, Fe, Ni, Mn, Si, Ti, Al y/o Nb.
Además, la aleación metálica también puede comprender carbono.
Por tanto, la presente invención también se refiere a un catalizador en polvo, en el que la aleación comprende carbono. La capa de óxido metálico, que recubre la aleación metálica, no es ácida (siendo preferentemente básica o anfótera). La capa de óxido comprende ZnO y Al.
También se prefiere un sistema catalítico en polvo en el que la capa de óxido metálico no ácida está esencialmente exenta de Pb.
La aleación metálica se recubre preferentemente con una capa fina de ZnO (0,5 - 3,5 pm de espesor) y opcionalmente al menos un óxido de metal (Cr, Mn, Mg, Cu y/o Al) adicional.
El recubrimiento de la aleación metálica se realiza mediante procesos comúnmente conocidos, tales como, por ejemplo, recubrimiento por inmersión.
Generalmente, el sistema catalítico en polvo de la presente invención comprende entre el 0,1% en peso y el 50% en peso, con respecto al peso total del catalizador, de ZnO, preferentemente entre el 0,1% en peso y el 30% en peso, de forma más preferida entre el 1,5% en peso y el 10% en peso y de la forma más preferida entre el 2% en peso y el 8% en peso.
La presente invención se refiere a un sistema catalítico en polvo, en el que la capa de óxido metálico no ácida comprende ZnO y Al2O3 y en el que la relación de ZnO:Al2O3 es de 2:1 a 1:2 (preferentemente 1:1).
A continuación, las aleaciones metálicas recubiertas se impregnan con nanopartículas de paladio. Las nanopartículas se sintetizan mediante procedimientos comúnmente conocidos, por ejemplo utilizando PdCl2 como precursor, que después se reduce con hidrógeno.
Las nanopartículas de Pd, que se encuentran sobre la capa de óxido metálico no ácida, tienen un tamaño de partícula promedio de entre 0,5 y 20 nm, preferentemente de entre 2 y 15 nm, de forma más preferida de entre 5 y 12 nm y de la forma más preferida de entre 7 y 10 nm. (El tamaño se mide mediante procedimientos de dispersión de luz). El sistema catalítico en polvo según la presente invención comprende entre el 0,001% en peso y el 5% en peso, con respecto al peso total del catalizador, de nanopartículas de Pd, preferentemente entre el 0,01% en peso y el 2% en peso, de forma más preferida entre el 0,05% en peso y el 1% en peso.
El sistema catalítico en polvo se activa generalmente antes de su uso. La activación se realiza mediante procesos bien conocidos, tales como termoactivación en H2.
El sistema catalítico en polvo de la presente invención se usa en la hidrogenación catalítica selectiva de material de
partida orgánico, especialmente de material de partida orgánico que comprende un triple enlace carbono-carbono, más especialmente de compuestos de alquinol.
Preferentemente, la presente invención se refiere a un proceso de reacción de un compuesto de fórmula (I)
OH
H C = C ---- C-----R2 (I)
Rt
en la que
R1 es alquilo C5-C35 lineal o ramificado o un resto alquenilo C5-C35 lineal o ramificado, en los que la cadena de C puede estar sustituida, y
R2 es alquilo C1 -C4 lineal o ramificado, en el que la cadena de C puede estar sustituida.
con hidrógeno en presencia de un catalizador (I), (II), (III), (IV) (V), (V'), (V"), (VI), (VII), (VIII), (VIII'), (IX) y/o (X). El hidrógeno se utiliza generalmente en la forma de H2 gaseoso.
Los compuestos preferidos de fórmula (I) son los siguientes:
, y
Los ejemplos siguientes sirven para ilustrar la invención. Todos los porcentajes se refieren al peso y las temperaturas se proporcionar en grados Celsius, si no se indica lo contrario.
Ejemplo 1: Síntesis del sistema catalítico en polvo (aleación de cobalto/cromo/molibdeno recubierta por deposición de Al2 Ü3/ZnO y Pd)
Etapa 1: Pretratamiento térmico
El polvo de aleación metálica (EOS CobaltChrome MP1® comercialmente disponible de EOS GmbH, Alemania) se sometió a un pretratamiento térmico a 450 °C durante 3 h.
Etapa 2: Deposición de ZnO + A2O3 (recubrimiento del soporte de aleación metálica)
A un matraz de 100 ml se añadieron 20,0 g (53,3 mmol) de Al(NO3)3-9H2O y 70 ml de agua. La mezcla se agitó hasta que el Al(NO3)3-9H2O se disolvió por completo. La solución se calentó hasta 95 °C. Después se añadieron lentamente 4,34 g (53,3 mmol) de polvo de ZnO a la solución de reacción. Se mantuvo el calentamiento y la agitación hasta que el ZnO se disolvió por completo. A continuación, la solución se enfrió a temperatura ambiente y se filtró a través de un filtro de membrana.
La deposición de ZnO/Al2O3 se realizó añadiendo el polvo de aleación metálica oxidado (10,0 g) de la etapa 1 a la solución precursora y agitando la mezcla a temperatura ambiente durante 15 min.
A continuación, el polvo se retiró por filtración a través de un filtro de membrana y se secó al aire a 40 °C y 125 mbar durante 2 horas, operación seguida de una etapa de calcinación a 450 °C durante 1 hora. El ciclo de agitación-secadocalcinación se repitió 3 veces. Finalmente, el soporte en polvo se calcinó al aire a 550 °C durante 1 h.
Se obtuvieron 9,38 g de polvo de aleación metálica recubierto.
Etapa 3: Preparación y deposición de las nanopartículas de Pd
Se añadieron 318 mg (1,31 mmol) de molibdato de sodio dihidratado y 212 mg (1,20 mmol) de cloruro de paladio (II) anhidro a 60 ml de agua desionizada con calentamiento (aproximadamente 95 °C). La mezcla se agitó. El calentamiento y la agitación continuaron hasta la completa evaporación del agua (se formó un residuo sólido). Posteriormente, se añadieron al residuo 60 ml de agua desionizada con agitación. El ciclo de evaporación-disolución se repitió dos veces a fin de disolver completamente el PdCl2. Finalmente, se añadieron al residuo sólido 100 ml de agua caliente. La solución de color marrón oscuro se enfrió a temperatura ambiente y se filtró a través de un filtro de papel. El filtro se lavó con agua hasta que el volumen final de la solución precursora fuera de 120 ml.
Posteriormente se formó la suspensión de Pd° borboteando hidrógeno a través de la solución precursora durante 1 h en un cilindro de vidrio a temperatura ambiente.
La suspensión de Pd° así obtenida y 9,38 g del polvo de aleación metálica recubierto (de la etapa 2) se añadieron a un matraz de 200 ml. La mezcla se agitó a temperatura ambiente durante 15 min. El polvo se retiró por filtración a través de un papel de filtro y se secó al aire a 40 °C y 125 mbar durante 2 h. Este proceso se repitió dos veces. Etapa 4: Termoactivación del catalizador en H2
El catalizador en polvo obtenido en la etapa 3 se sometió a un tratamiento de temperatura a 300 °C durante 4 h bajo flujo de H2-Ar. A continuación, se enfrió a temperatura ambiente bajo el mismo flujo de H2-Ar.
Se obtuvieron 8,85 g del sistema catalítico en polvo según la presente invención.
Ejemplo 2a:
Hidrogenación selectiva de MBY a MBE
A 285 g (3,38 mol) de MBY se añadieron 1,5 g del catalizador del ejemplo 1 con agitación. La reacción se llevó a cabo a 65 °C y 4 bar de presión durante aproximadamente 7 horas.
Al final de la reacción la selectividad de la reacción fue del 96,42% y la conversión del 99,43%.
Se puede observar que el nuevo catalizador en polvo tiene excelentes propiedades como catalizador para hidrogenaciones selectivas.
Ejemplo 2b:
Hidrogenación selectiva repetida de MBY a MBE
Se utilizaron las mismas condiciones de reacción que en el ejemplo 2a. Al final de la reacción (después de aproximadamente 7 - 9 horas), la mezcla de reacción se enfrió en atmósfera inerte y la solución de reacción se intercambió por MBY nuevo (nuevamente 285 g) y se inició de nuevo la hidrogenación.
Se llevaron a cabo 11 ciclos. La tabla siguiente muestra los resultados de los ciclos.
Se puede observar que el nuevo catalizador en polvo mantiene las excelentes propiedades catalíticas incluso después de 11 ciclos (sin tratar el catalizador).
Ejemplo 3a - 3d: Hidrogenación selectiva de deshidrooisofitol (DIP)
A 285 g (0,97 mol) de DIP se añadieron 1,5 g del catalizador del ejemplo 1 con agitación. La reacción se llevó a cabo a 85 °C y 4 bar de presión durante aproximadamente 4,5 horas.
Al final de la reacción, la selectividad de la reacción fue del 81,76% y la conversión del 87,15%.
Este ejemplo se repitió 3 veces, dando como resultado los siguientes valores de conversión y selectividad:
Se puede observar que el nuevo sistema catalítico en polvo presenta excelentes propiedades como catalizador para hidrogenaciones selectivas.
Ejemplo 3e - 3i: Hidrogenación selectiva de deshidrooisofitol (DIP) con un modificador básico
A 285 g (0,97 mol) de DIP se añadieron 1,5 g del catalizador del ejemplo 1 y un modificador básico (Tegochrome 22 = 2,2-etilenditiodietanol) con agitación. La reacción se llevó a cabo a 85 °C y 4 bar de presión durante unas 7 horas. Al final de la reacción la selectividad de la reacción fue del 82,02% y la conversión del 87,51%.
Este ejemplo se repitió 4 veces, dando como resultado los siguientes valores de conversión y selectividad:
Ejemplo 3k: Hidrogenación selectiva repetida de deshidrooisofitol (DIP) con un modificador básico
Se utilizaron las mismas condiciones de reacción que en los ejemplos 3e - 3i.
Al final de la reacción (después de aproximadamente 2,5 - 3 horas), la mezcla de reacción se enfrió en atmósfera inerte y la solución de reacción se intercambió por DIP nuevo (nuevamente 285 g) y se inició de nuevo la hidrogenación.
Se llevaron a cabo 5 ciclos. La tabla siguiente muestra los resultados de los ciclos.
Se puede observar que el nuevo sistema catalítico en polvo mantiene las excelentes propiedades catalíticas incluso después de 5 ciclos (sin tratar el catalizador).
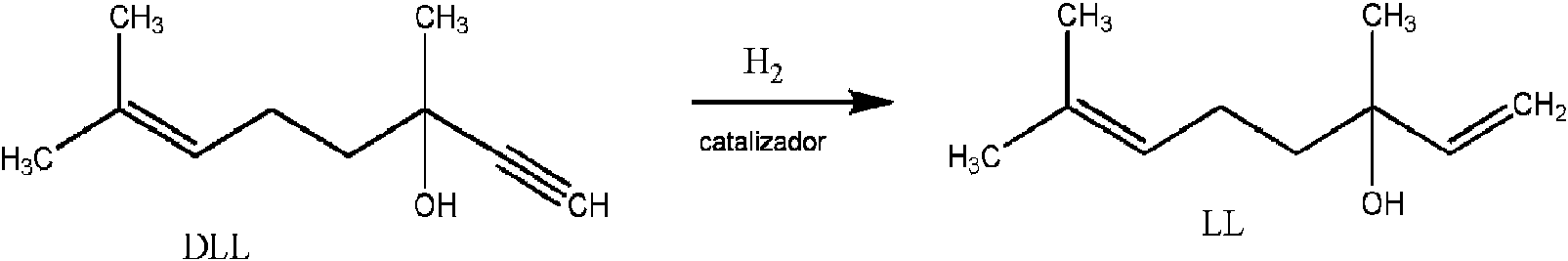
Ejemplo 4: Hidrogenación selectiva de deshidrolinalool (DLL).
A 285 g (1,87 mol) de DLL se añadieron 1,5 g del catalizador del ejemplo 1 con agitación. La reacción se llevó a cabo a 55 °C y 4 bar de presión durante aproximadamente 6 horas.
Al final de la reacción la selectividad de la reacción fue del 92,08% y la conversión del 99,38%.
Ejemplo 5: Hidrogenación selectiva de acetato de deshidrolinalilo (DLA)
A 285 g (1,45 mol) de DLA se añadieron 1,5 g del catalizador del ejemplo 1 con agitación. La reacción se llevó a cabo a 40 °C y 4 bar de presión durante unas 7 horas.
Al final de la reacción, la selectividad de la reacción fue del 88,22% y la conversión del 94,98%.
Claims (7)
1. Uso de un sistema catalítico en polvo que comprende
un soporte de aleación metálica que comprende
(i) del 55% en peso al 80% en peso, con respecto al peso total de la aleación metálica, de Co, y
(ii) del 20% en peso al 40% en peso, con respecto al peso total de la aleación metálica, de Cr, y
(iii) del 2% en peso al 10% en peso, con respecto al peso total de la aleación metálica, de Mo, y
en el que dicha aleación metálica está recubierta por una capa de óxido metálico, que es una mezcla de ZnO y AbO3 en una relación de 2:1 a 1:2, e impregnada con nanopartículas de Pd, en la que las nanopartículas de Pd presentan un tamaño de partícula promedio de entre 0,5 y 20 nm (el tamaño se mide mediante procedimientos de dispersión de luz) en la hidrogenación catalítica selectiva de
un compuesto de fórmula (I)
OH
H C = C ---- C-----R2 (I)
Ri
en la que
R1 es alquilo C5-C35 lineal o ramificado o un resto alquenilo C5-C35 lineal o ramificado, en los que la cadena de C puede estar sustituida, y
R2 es alquilo C1-C4 lineal o ramificado, en el que la cadena de C puede estar sustituida.
2. Uso según la reivindicación 1, en el que la aleación metálica comprende otros metales.
3. Uso según cualquiera de las reivindicaciones anteriores, en el que la aleación metálica comprende carbono.
4. Uso según cualquiera de las reivindicaciones anteriores, en el que la aleación metálica comprende
del 55% en peso al 70% en peso, con respecto al peso total de la aleación metálica, de Co, y
del 20% en peso al 35% en peso, con respecto al peso total de la aleación metálica, de Cr, y
del 4% en peso al 10% en peso, con respecto al peso total de la aleación metálica, de Mo.
5. Uso según cualquiera de las reivindicaciones anteriores que comprende entre el 0,1% en peso y el 50% en peso, con respecto al peso total del catalizador, de la capa de óxido metálico no ácido.
6. Uso según cualquiera de las reivindicaciones anteriores, en el que el óxido metálico es una mezcla de ZnO y Al2O3 en una relación de, preferentemente, 1:1.
7. Uso según cualquiera de las reivindicaciones anteriores, en el que el catalizador comprende entre el 0,001% en peso y el 5% en peso, con respecto al peso total del catalizador, de las nanopartículas de Pd.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP12156805 | 2012-02-24 | ||
| PCT/EP2013/053511 WO2013124391A1 (en) | 2012-02-24 | 2013-02-22 | Metal powderdous catalyst comprising a cocrmo-alloy |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2929305T3 true ES2929305T3 (es) | 2022-11-28 |
Family
ID=47750674
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES13706241T Active ES2929305T3 (es) | 2012-02-24 | 2013-02-22 | Uso de un catalizador metálico en polvo que comprende una aleación de CoCrMo |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US9283549B2 (es) |
| EP (1) | EP2817095B1 (es) |
| JP (1) | JP6202577B2 (es) |
| KR (1) | KR102103039B1 (es) |
| CN (1) | CN104136120B (es) |
| BR (1) | BR112014020918B1 (es) |
| ES (1) | ES2929305T3 (es) |
| IN (1) | IN2014DN07059A (es) |
| WO (1) | WO2013124391A1 (es) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN110582351B (zh) * | 2017-05-01 | 2023-02-28 | 帝斯曼知识产权资产管理有限公司 | 用于氢化工艺的金属粉末催化剂 |
| PL3618957T3 (pl) * | 2017-05-01 | 2024-03-11 | Dsm Ip Assets B.V. | Metalowy sproszkowany katalizator do sposobów uwodorniania |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1578122A (en) * | 1976-02-11 | 1980-11-05 | Johnson Matthey Co Ltd | Catalytic hydrogenation of fatty oils |
| CN101616733B (zh) * | 2007-02-19 | 2013-05-15 | 帝斯曼知识产权资产管理有限公司 | 基于包覆有经钯纳米颗粒浸渍的氧化锌层的经烧结金属纤维的用于炔醇氢化的催化剂 |
| EP2528882B1 (en) * | 2010-01-28 | 2016-11-30 | DSM IP Assets B.V. | Hydrogenation process |
| CN107262112A (zh) * | 2010-07-01 | 2017-10-20 | 帝斯曼知识产权资产管理有限公司 | 新的结构化催化剂 |
-
2013
- 2013-02-22 BR BR112014020918-9A patent/BR112014020918B1/pt active IP Right Grant
- 2013-02-22 IN IN7059DEN2014 patent/IN2014DN07059A/en unknown
- 2013-02-22 JP JP2014558109A patent/JP6202577B2/ja active Active
- 2013-02-22 CN CN201380010930.9A patent/CN104136120B/zh active Active
- 2013-02-22 WO PCT/EP2013/053511 patent/WO2013124391A1/en not_active Ceased
- 2013-02-22 EP EP13706241.0A patent/EP2817095B1/en active Active
- 2013-02-22 KR KR1020147026537A patent/KR102103039B1/ko active Active
- 2013-02-22 ES ES13706241T patent/ES2929305T3/es active Active
- 2013-02-22 US US14/380,195 patent/US9283549B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US20150018585A1 (en) | 2015-01-15 |
| IN2014DN07059A (es) | 2015-04-10 |
| US9283549B2 (en) | 2016-03-15 |
| EP2817095A1 (en) | 2014-12-31 |
| EP2817095B1 (en) | 2022-09-14 |
| CN104136120B (zh) | 2017-02-22 |
| KR102103039B1 (ko) | 2020-04-22 |
| JP6202577B2 (ja) | 2017-09-27 |
| BR112014020918A8 (pt) | 2020-09-24 |
| KR20140134301A (ko) | 2014-11-21 |
| BR112014020918B1 (pt) | 2024-02-27 |
| CN104136120A (zh) | 2014-11-05 |
| JP2015513455A (ja) | 2015-05-14 |
| WO2013124391A1 (en) | 2013-08-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2616741T3 (es) | Procedimiento de hidrogenación | |
| JP6312609B2 (ja) | 水素化プロセスのための金属粉末状触媒 | |
| WO2018164182A1 (ja) | アンモニア合成用触媒、及びその利用 | |
| JP2021130100A (ja) | アンモニア分解触媒 | |
| ES2929305T3 (es) | Uso de un catalizador metálico en polvo que comprende una aleación de CoCrMo | |
| ITFI20080210A1 (it) | Catalizzatori a base di metalli non nobili per la decomposizione dell'ammoniaca e loro preparazione | |
| ES2937148T3 (es) | Catalizador metálico pulverulento que comprende una aleación de Fe | |
| ES2962290T3 (es) | Catalizador metálico en polvo para procesos de hidrogenación | |
| JP3834776B2 (ja) | ゲルマニウムナイトライド構造を含む光水分解用触媒 | |
| JP2012223768A (ja) | アンモニア分解触媒及びアンモニア分解方法 | |
| JP6937013B2 (ja) | ベンゼン化合物の製造方法及びベンゼン化合物製造用の触媒 | |
| JP6209778B2 (ja) | 特定のイソプレノイドの段階的水素化 | |
| CN119176774A (zh) | N-烷基咔唑的合成方法 | |
| JP2021181417A (ja) | プロリノールの製造方法、複合金属化合物およびその製造方法 | |
| JP2008274010A (ja) | 蛍光体前駆体及び蛍光体の製造方法 |