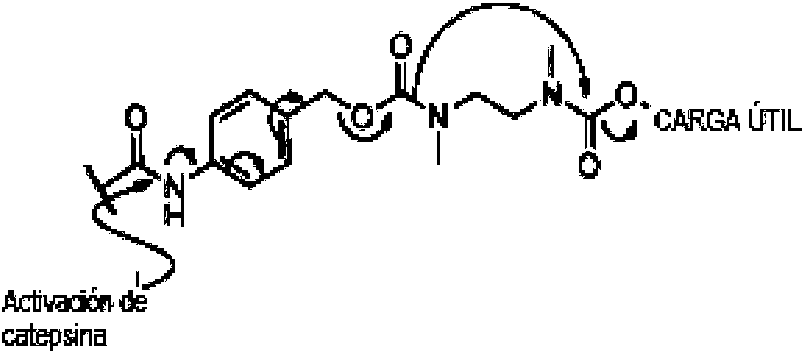ES2929333T3 - Compuestos de aminotioléster y usos de los mismos - Google Patents
Compuestos de aminotioléster y usos de los mismos Download PDFInfo
- Publication number
- ES2929333T3 ES2929333T3 ES20749897T ES20749897T ES2929333T3 ES 2929333 T3 ES2929333 T3 ES 2929333T3 ES 20749897 T ES20749897 T ES 20749897T ES 20749897 T ES20749897 T ES 20749897T ES 2929333 T3 ES2929333 T3 ES 2929333T3
- Authority
- ES
- Spain
- Prior art keywords
- methyl
- branched
- inthioate
- linear
- amino
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C327/00—Thiocarboxylic acids
- C07C327/20—Esters of monothiocarboxylic acids
- C07C327/22—Esters of monothiocarboxylic acids having carbon atoms of esterified thiocarboxyl groups bound to hydrogen atoms or to acyclic carbon atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
- A61K31/22—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acyclic acids, e.g. pravastatin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
- A61K31/22—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acyclic acids, e.g. pravastatin
- A61K31/222—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acyclic acids, e.g. pravastatin with compounds having aromatic groups, e.g. dipivefrine, ibopamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/265—Esters, e.g. nitroglycerine, selenocyanates of carbonic, thiocarbonic, or thiocarboxylic acids, e.g. thioacetic acid, xanthogenic acid, trithiocarbonic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/27—Esters, e.g. nitroglycerine, selenocyanates of carbamic or thiocarbamic acids, meprobamate, carbachol, neostigmine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4402—Non condensed pyridines; Hydrogenated derivatives thereof only substituted in position 2, e.g. pheniramine, bisacodyl
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4406—Non condensed pyridines; Hydrogenated derivatives thereof only substituted in position 3, e.g. zimeldine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/545—Heterocyclic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6849—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a receptor, a cell surface antigen or a cell surface determinant
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6851—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C213/00—Preparation of compounds containing amino and hydroxy, amino and etherified hydroxy or amino and esterified hydroxy groups bound to the same carbon skeleton
- C07C213/08—Preparation of compounds containing amino and hydroxy, amino and etherified hydroxy or amino and esterified hydroxy groups bound to the same carbon skeleton by reactions not involving the formation of amino groups, hydroxy groups or etherified or esterified hydroxy groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C219/00—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton
- C07C219/02—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton having esterified hydroxy groups and amino groups bound to acyclic carbon atoms of the same carbon skeleton
- C07C219/20—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton having esterified hydroxy groups and amino groups bound to acyclic carbon atoms of the same carbon skeleton the carbon skeleton being unsaturated
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/24—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D213/28—Radicals substituted by singly-bound oxygen or sulphur atoms
- C07D213/32—Sulfur atoms
- C07D213/34—Sulfur atoms to which a second hetero atom is attached
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/24—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D213/54—Radicals substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
- C07D213/59—Radicals substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals with at least one of the bonds being to sulfur
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/06—Systems containing only non-condensed rings with a five-membered ring
- C07C2601/08—Systems containing only non-condensed rings with a five-membered ring the ring being saturated
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/12—Systems containing only non-condensed rings with a six-membered ring
- C07C2601/16—Systems containing only non-condensed rings with a six-membered ring the ring being unsaturated
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Cell Biology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Emergency Medicine (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Hematology (AREA)
- Oncology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Steroid Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Pyridine Compounds (AREA)
- Medicinal Preparation (AREA)
Abstract
La presente invención se refiere a nuevos compuestos de aminoésteres o sus sales o isómeros ópticos, racematos, diastereoisómeros, enantiómeros o tautómeros farmacéuticamente aceptables. La presente invención también se refiere a su proceso de preparación ya estos compuestos para su uso como medicamento, en particular para el tratamiento o la prevención del cáncer. La presente invención se refiere además a un conjugado de anticuerpo y fármaco que comprende dichos compuestos. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Compuestos de aminotioléster y usos de los mismos
[0001] La presente invención se refiere a compuestos de aminoésteres novedosos o sus sales farmacéuticamente aceptables o isómeros ópticos, racematos, diastereoisómeros, enantiómeros o tautómeros. La presente invención también se refiere a sus procesos de preparación y a aquellos compuestos para su uso como un medicamento, en particular, para la prevención o el tratamiento de cáncer. La presente invención se refiere adicionalmente a un conjugado anticuerpo-fármaco que comprende tales compuestos.
Antecedentes de la Invención
[0002] El cáncer es actualmente uno de los problemas principales de salud en los países desarrollados. El cáncer es una proliferación no regulada de células debido a la pérdida de controles normales, lo que da lugar a un crecimiento no regulado, falta de diferenciación, invasión de tejido local y, a menudo, metástasis. El cáncer puede desarrollarse en cualquier tejido u órgano a cualquier edad.
[0003] Algunos cánceres son curables, si se detectan durante las etapas tempranas, y a largo plazo también se pueden curar en etapas más tardías. Sin embargo, la cura no siempre es posible y no se intenta en algunos casos avanzados en los que los cuidados paliativos proporcionan mejor calidad de vida que un tratamiento agresivo, particularmente, en personas de edad avanzada o en pacientes con trastornos comórbidos subyacentes.
[0004] La apoptosis está involucrada en el desarrollo, diferenciación y renovación de tejidos. Por lo tanto, la inducción de apoptosis es de mayor interés desde un punto de vista terapéutico.
[0005] Una variedad muy grande de productos medicinales anticáncer naturales o sintéticos disponible actualmente son compuestos que inducen apoptosis.
[0006] Entre estos productos medicinales antineoplásicos, se puede hacer mención de agentes alquilantes, tales como ciclofosfamida, nitrosoureas, tales como 1,3-bis(2-cloroetil)-1-nitrosourea (BCNU), agentes intercalantes, tales como actinomicina D o adriamicina, análogos de base purina o pirimidina, tales como 6-tioguanina y 5-fluorouracilo, inhibidores de la síntesis de novo de bases purina, tales como metotrexato, y, finalmente, inhibidores de polimerización de tubulina, tales como Taxol(R).
[0007] Una de las principales desventajas en el uso de estas sustancias es la ausencia de actividad apoptótica selectiva en células tumorales.
[0008] Por tanto, sigue siendo necesario tener moléculas disponibles que inducen la apoptosis máxima en tejido tumoral, causando el menor daño posible, y de un modo reversible, a los tejidos sanos del cuerpo.
[0009] QUASH G ET AL ("Aldehyde dehydrogenase inhibitors: alpha,beta-Acetylenic N-substituted aminothiolesters are reversible growth inhibitors of normal epithelial but irreversible apoptogens for cancer epithelial cells from human prostate in culture", European Journal Of Medicinal Chemistry, volumen 43, número 5, (2008), páginas 906-916) describe los compuestos de éster S-metílico del ácido 4-metil- 2-pentinetioico como inductores de apoptosis que se utilizan en el tratamiento de cánceres.
[0010] Los compuestos de aminotiolésteres y su aplicación, en particular en el tratamiento de cáncer, también se describen en US2007/0032476.
[0011] WO2017/064241 describe el uso de tales compuestos de aminotiolésteres en combinación con un compuesto que es capaz de aumentar el nivel de H2O2 en células cancerígenas de un sujeto.
Descripción de la invención
[0012] Los inventores de la presente invención han identificado nuevos compuestos de fórmula (I), que poseen propiedades de interés en la prevención o el tratamiento de cáncer.
[0013] La presente invención es como se define en las reivindicaciones.
[0014] Se refiere a un compuesto de fórmula (I):
[0015] En la que:
-X es S;
- R1 es alquilo (C1-C7) lineal o ramificado,
- R2 es CHR5CHR6OR4 o (CHR5VOR4,
- v se selecciona de 2 a 4;
- R3 es alquilo (C1-C7) lineal o ramificado,
- R4 se selecciona entre: H, alquilo (C2-C7) lineal o ramificado, alquenilo (C2-C7) lineal o ramificado, -CONR7R8, arilo, heteroarilo, cicloalquilo (C2-C7), alquil (C1-C7)-arilo lineal o ramificado o alquil (C1-C7)-heteroarilo lineal o ramificado; estando dicho arilo, cicloalquilo (C2-C7) y heteroarilo opcionalmente sustituidos por uno o más sustituyentes que se seleccionan entre: halógeno, alquilo (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, alcoxi (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, -COOH, arilo, -NRR', -NO2, o estando dicho arilo y heteroarilo opcionalmente fusionados para formar un heterocicloalquilo; - R5 y R6 se seleccionan entre:
• H, o
• R5 es H y R1 y R6 están unidos para formar con el átomo de nitrógeno unido a R1 un heterocicloalquilo, o • R6 es H y R1 y R5 están unidos a R1 para formar con el átomo de nitrógeno unido a R1 un heterocicloalquilo; - R7 es alquilo -(C1-C3);
- R8 es alquilo -(C1-C3)-NRR';
- R y R', idénticos o diferentes, se seleccionan de manera independiente entre H y alquilo (C1-C7) lineal o ramificado, o sus sales farmacéuticamente aceptables o isómeros ópticos, racematos, diastereoisómeros, enantiómeros o tautómeros.
[0016] En una realización, un compuesto descrito es un compuesto de fórmula (I), tal como se menciona anteriormente, en el que:
- X es un átomo que se selecciona entre O y S;
- R1 y R2, idénticos o diferentes, se seleccionan de manera independiente entre: alquilo (C1-C7) lineal o ramificado, alquenilo (C2-C7) lineal o ramificado, arilo, heteroarilo, CHR5CHR6OR4 y (CHR5VOR4,
estando dicho arilo y heteroarilo opcionalmente sustituidos por uno o más sustituyentes que se seleccionan entre: alquilo (C1-C7) lineal o ramificado, halógeno, NO2 y CONH2;
- v se selecciona de 2 a 4;
- R3 se selecciona entre alquilo (C1-C7) lineal o ramificado o alquilo (C1-C7)-NY1Y2 lineal o ramificado; estando dicho alquilo (C1-C7)-NY1Y2 lineal o ramificado opcionalmente sustituido por alquilo (C1-C7)-CO2Z;
- R4 se selecciona entre: H, alquilo (C2-C7) lineal o ramificado, alquenilo (C2-C7) lineal o ramificado, arilo, heteroarilo, alquil (C1-C7)-arilo lineal o ramificado y alquil (C1-C7)-heteroarilo lineal o ramificado;
estando dicho arilo y heteroarilo opcionalmente sustituidos por uno o más sustituyentes que se seleccionan entre: alquilo (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, alcoxi (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, -COOH, arilo, -NRR', -NO2, o estando dicho arilo y heteroarilo opcionalmente fusionados para formar un heterocicloalquilo;
- R5 y Ra, idénticos o diferentes, se seleccionan de manera independiente entre:
• H y alquilo (C1-C7) lineal o ramificado, o
• R5 y Ra están unidos para formar con los átomos de carbono a los que se acoplan un cicloalquilo, arilo o heteroarilo, o
• R5 es H y R1 y Ra están unidos para formar con el átomo de nitrógeno unido a R1 un heterocicloalquilo o heteroarilo, o
• Ra es H y R1 y R5 están unidos a R1 para formar con el átomo de nitrógeno unido a R1 un heterocicloalquilo; - R y R', idénticos o diferentes, se seleccionan de manera independiente entre H y alquilo (C1-C7) lineal o ramificado, - Y1 e Y2, idénticos o diferentes, se seleccionan de manera independiente entre H y alquilo -CO-(Ci-C7);
- Z se selecciona entre H y alquilo (C1-C7) lineal o ramificado;
y en el que, como mínimo uno de R1 y R2 es CHR5CHRaOR4 o (CHR5VOR4 cuando X es S y R3 es alquilo (C1-C7) lineal o ramificado;
o sus sales farmacéuticamente aceptables o isómeros ópticos, racematos, diastereoisómeros, enantiómeros o tautómeros.
[0017] De acuerdo con otra realización, un compuesto de acuerdo con la invención es un compuesto de fórmula (I), tal como se menciona anteriormente, en el que R3 es metilo, R1 es metilo, R2 es CHR5CHR6OR4 o (CHR5VOR4 y R5 y R6 son:
- H, o
- R5 es H y R1 y R6 están unidos para formar con el átomo de nitrógeno unido a R1 un pirrolidinilo, o
- R6 es H y R1 y R5 están unidos a R1 para formar con el átomo de nitrógeno unido a R1 un pirrolidinilo.
[0018] En particular, R4 se selecciona entre H, alquilo (C2-C7) lineal o ramificado, alquenilo (C2-C7) lineal o ramificado, -CONR7R8, cicloalquilo (C2-C7), alquil (C1-C7)-heteroarilo lineal o ramificado, arilo o bencilo; estando dicho cicloalquilo (C2-C7) sustituido por uno o más sustituyentes seleccionados entre: alquilo (C1-C7) lineal o ramificado; estando dicho bencilo opcionalmente sustituido por uno o más sustituyentes seleccionados entre: alquilo (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, alcoxi (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, halógeno o estando dicho bencilo opcionalmente fusionado para formar 1,3-benzodioxol.
[0019] Alternativamente, en particular, R4 se selecciona entre H, alquilo (C2-C7) lineal o ramificado, alquenilo (C2-C7) lineal o ramificado, alquil (C1-C7)-heteroarilo lineal o ramificado, arilo, alquil (C1-C7)-arilo lineal o ramificado o bencilo; estando dicho bencilo opcionalmente sustituido por uno o más sustituyentes seleccionados entre: alquilo (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, alcoxi (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, halógeno o piridilo, o estando dicho bencilo opcionalmente fusionado para formar 1,3-benzodioxol.
[0020] Más particularmente, R5 y R6 son H y R4 se selecciona entre H, alquilo (C2-C7) lineal o ramificado, alquenilo (C2-C7) lineal o ramificado, CONR7R8, cicloalquilo (C2-C7), alquil (C1-C7)-heteroarilo lineal o ramificado o bencilo; estando dicho cicloalquilo (C2-C7) opcionalmente sustituido por uno o más sustituyentes seleccionados entre: alquilo (C1-C7) lineal o ramificado; estando dicho bencilo opcionalmente sustituido por uno o más sustituyentes seleccionados entre: alquilo (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, alcoxi (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, halógeno.
[0021] Alternativamente, más particularmente, R5 y R6 son H y R4 se selecciona entre H, alquilo (C2-C7) lineal o ramificado, alquenilo (C2-C7) lineal o ramificado, alquil (C1-C7)-heteroarilo lineal o ramificado, alquil (C1-C7)-arilo lineal o ramificado o bencilo; estando dicho bencilo opcionalmente sustituido por uno o más sustituyentes seleccionados entre: alquilo (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, alcoxi (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, halógeno.
[0022] Incluso más particularmente, R1 es metilo y R4 se selecciona entre: H, CONR7R8 siendo R7 un metilo y siendo R8 NRR' con R y R' siendo metilo, etilo, propeno, bencilo, piridilo, benciloxibutilo, metil-ciclohexenilo sustituido por uno o más de metilo y bencilo sustituido por uno o más de flúor, cloro, metoxi o metilo.
[0023] Alternativamente, incluso más particularmente, R1 es metilo y R4 se selecciona entre: H, etilo, propeno, bencilo, piridilo, benciloxibutilo y bencilo sustituido por uno o más de flúor, cloro, metoxi o metilo.
[0024] De acuerdo con una realización específica, un compuesto de fórmula (I) se selecciona entre:
- 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo;
- 4-[2-aliloxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo;
- 4-[2-benciloxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo;
- 4-metil-4-[metil-[2-(m-tolilmetoxi)etil]amino]pent-2-intioato de S-metilo;
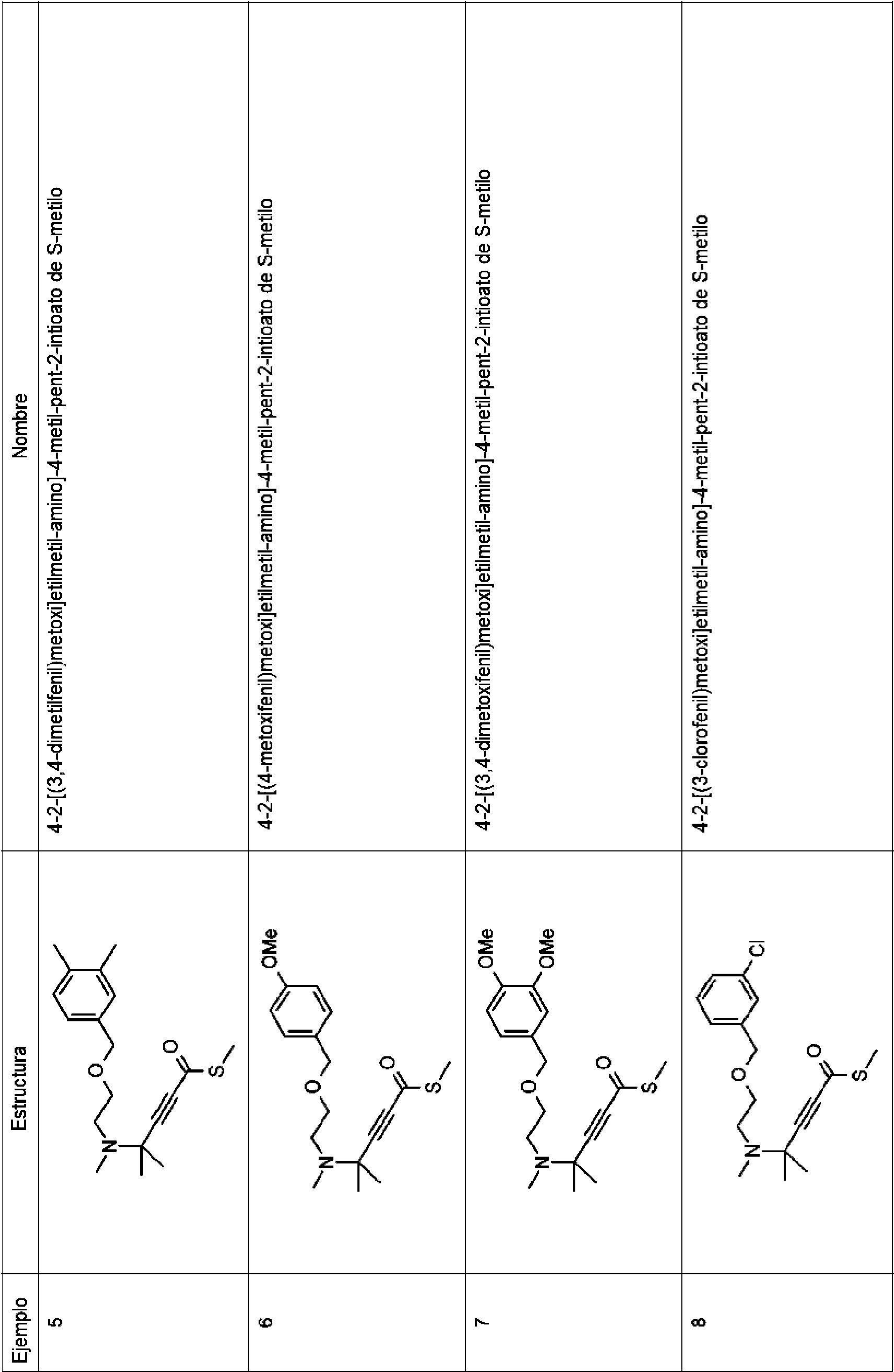
- 4-[2-[(3,4-dimetilfenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo;
- 4-[2-[(4-metoxifenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo;
- 4-[2-[(3,4-dimetoxifenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo;
- 4-[2-[(3-clorofenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo;
- 4-[2-[(3-fluorofenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo;
- 4-metil-4-[metil-[2-(2-piridilmetoxi)etil]amino]pent-2-intioato de S-metilo;
- 4-metil-4-[metil-[2-(3-piridilmetoxi)etil]amino]pent-2-intioato de S-metilo;
- 4-metil-4-[metil-[2-(4-piridilmetoxi)etil]amino]pent-2-intioato de S-metilo;
- Ácido 2-amino-3-((4-(dimetilamino)-4-metilpent-2inil)tio)propanoico;
- Ácido 2-amino-4-((4-(dimetilamino)-4-metilpentil-2-inil)tio)butanoico;
- etil-2-acetamido-3-((4-(dimetilamino)-4-metilpent-2-inil)tio)propanoato;
- 4-((4-(benciloxi)butil)(metil)amino)-4-metilpent-2-intioato de S-metilo;
- 4-((2-hidroxietil)(metil)amino)-4-metilpent-2-intioato de S-metilo;
- 4-metil-4-[metil-[2-(2-naftilmetoxi)etil]amino]pent-2-intioato de S-metilo;
- 4-metil-4-[metil-[2-[(2,6,6-trimetilciclohexen-1-il)metoxi]etil]amino]pent-2-intioato de S-metilo;
- 2-[(1,1-dimetil-4-metilsulfanil-4-oxo-but-2-inil)-metilamino] etil-3,4-dimetoxibenzoato;
- acetato de 2[(1,1-dimetil-4-metilsulfanil-4-oxo-but-2-inil)-metilamino]etilo;
- 2,5,10,11,11-pentametil-6-oxo-7-oxa-2,5,10-triazatetradec-12-in-14-tioato de S-metilo;
- 4-[2-(metoximetil)pirrolidin-1-il]-4-metilpent-2-intioato de S-metilo;
- 4-(3-metoxipirrolidin-1-il)-4-metilpent-2-intioato de S-metilo;
- 4-metil-4-[metil(2-fenoxiciclopentil)amino]pent-2-intioato de S-metilo;
- 4-(2-((benciloxi)metil)pirrolidin-1-il)-4-metilpent-2-intioato de (S)-S-metilo;
- 4-[(3(benciloxi)-1pirrolidinil])-4-metilpent-2-intioato de S-metilo;
o sus sales farmacéuticamente aceptables o isómeros ópticos, racematos, diastereoisómeros, enantiómeros o tautómeros.
[0025] De acuerdo con una realización específica, un compuesto de fórmula (I) se selecciona entre:
- 4-[2-benciloxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo; y
- 4-[2-[(3,4-dimetilfenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo;
o sus sales farmacéuticamente aceptables o isómeros ópticos, racematos, diastereoisómeros, enantiómeros o tautómeros.
[0026] En otra realización, un compuesto de acuerdo con la invención es un compuesto de fórmula (I) tal como se menciona anteriormente, en el que:
-X es S;
- R1 es alquilo (C1-C7) lineal o ramificado;
- R2 es CHR5CHR6OR4 o (CHR5)vOR4,
- R4 se selecciona entre H, arilo, heteroarilo, alquil (Ci-C7)-arilo lineal o ramificado o alquil (Ci-C7)-heteroarilo lineal o ramificado;
estando dicho arilo y heteroarilo opcionalmente sustituidos por uno o más sustituyentes que se seleccionan entre: -COOH, -NRR' y -NO2; y
- R y R' idénticos, son H.
[0027] La presente invención también se refiere a un proceso de preparación de un compuesto de fórmula (I), tal como se describe en el presente documento, que comprende:
a) hacer reaccionar un compuesto de fórmula (II) con un ácido orgánico o inorgánico
b) hacer reaccionar el compuesto obtenido en la etapa a) con una base;
c) hacer reaccionar el compuesto obtenido en la etapa b) con CO2;
d) hacer reaccionar el compuesto obtenido en la etapa c) con cloroformiato de alquilo, un reactivo capaz de formar, con el compuesto obtenido en la etapa c), un haluro de ácido o un reactivo capaz de formar, con el compuesto obtenido en la etapa c), un anhídrido mixto;
e) hacer reaccionar el compuesto obtenido en la etapa d) con un compuesto precursor de anión SMe-; en el que R1 y R2 se definen en el presente documento.
[0028] En particular, se refiere a un proceso, tal como se menciona anteriormente, en el que la base de la etapa b) tiene un pKa superior a 25, de manera preferente la base utilizada en la etapa b) se selecciona entre bases de litio o magnesio, de manera preferente la base se selecciona entre butil litio o hexil litio.
[0029] La presente invención también se refiere a una composición farmacéutica que comprende un compuesto de fórmula (I), tal como se describe en el presente documento, y un excipiente farmacéutico aceptable.
[0030] Se refiere adicionalmente a un compuesto de fórmula (I), tal como se describe en el presente documento, para su uso como un medicamento.
[0031] De manera particular, se refiere a un compuesto de fórmula (I), tal como se describe en el presente documento, para su uso para la prevención o el tratamiento de cáncer.
[0032] Más particularmente, la presente invención se refiere a un compuesto de fórmula (I), tal como se describe en el presente documento, para su uso para la prevención o el tratamiento de leucemia.
[0033] La presente invención se refiere también a un conjugado anticuerpo-fármaco de fórmula: B-L-Ab, en la que: - B es un compuesto de fórmula (I), tal como se menciona anteriormente, en el que:
-X es S;
- R1 es alquilo (C1-C7) lineal o ramificado;
- R2 es CHR5CHR6OR4 o (CHR5VOR4;
- R4 se selecciona entre H, arilo, heteroarilo, alquil (C1-C7)-arilo lineal o ramificado o alquil (C1-C7)-heteroarilo lineal o ramificado;
estando dicho arilo y heteroarilo opcionalmente sustituidos por uno o más sustituyentes que se seleccionan entre: -COOH, -NRR' y -NO2; y
- R y R' idénticos, son H;
- L es un resto químico que comprende un enlace covalente o una cadena de átomos que acopla de manera covalente el Ab al compuesto de fórmula (I); y
- Ab es un anticuerpo que se selecciona entre: rituximab, trastuzumab, alemtuzumab, ibritumomab, tiuxetano, tositumomab, brevacizumab, cetuximab, panitumumab, ofatumumab, ipilimumab y obinutuzumab.
[0034] Un compuesto de fórmula (I) de acuerdo con la invención es tal como se menciona anteriormente.
[0035] En una realización, R3 es metilo.
[0036] En otra realización, R1 es un metilo y R2 es CHR5CHR6OR4 o (CHR5VOR4.
[0037] En una realización, R4 se selecciona entre H, alquilo (C2-C7) lineal o ramificado, alquenilo (C2-C7) lineal o ramificado, alquil (Ci-C7)-heteroarilo lineal o ramificado, arilo, alquil (Ci-C7)-arilo lineal o ramificado o bencilo; estando dicho bencilo opcionalmente sustituido por uno o más sustituyentes que se seleccionan entre: alquilo (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, alcoxi (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, halógeno o piridilo, o estando dicho bencilo opcionalmente fusionado para formar 1,3-benzodioxol, en particular R4 se selecciona entre H, alquilo (C2-C7) lineal o ramificado, alquenilo (C2-C7) lineal o ramificado, alquil (C1-C7)-heteroarilo lineal o ramificado, alquil (C1-C7)-arilo lineal o ramificado o bencilo; estando dicho bencilo opcionalmente sustituido por uno o más sustituyentes que se seleccionan entre: alquilo (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, alcoxi (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno o halógeno, y más particularmente, R4 se selecciona entre: H, etilo, propenilo, bencilo, piridilo, benciloxibutilo y bencilo sustituidos por uno o más de flúor, cloro, metoxi o metilo.
[0038] A menos que se indique lo contrario, los términos utilizados anteriormente o a continuación en referencia a los compuestos de fórmula (I) tienen el significado atribuido a ellos a continuación:
- v se selecciona de 2 a 4, significa que el sustituyente “CHR5” se repite dos veces CHR5CHR5OR4, tres veces CHR5CHR5CHR5OR4 o cuatro veces CHR5CHR5CHR5CHR5OR4;
- “halógeno” hace referencia a átomo de flúor, cloro, bromo o yodo, en particular a átomo de flúor o cloro.
- “alquilo” representa un grupo de hidrocarburo alifático que puede ser lineal o ramificado, que tiene de 1 a 7 o de 2 a 7 átomos de carbono en la cadena de alquilo (C1-C7) o alquilo (C2-C7), a menos que se indique lo contrario. En particular, los grupos alquilo tienen de 1 a 3 átomos de carbono en la cadena de alquilo (C1-C3). Ramificado significa que uno o más grupos alquilo, tales como metilo, etilo o propilo, se unen a una cadena de alquilo lineal. Los grupos alquilo de ejemplo incluyen metilo, etilo, n-propilo, i-propilo, n-butilo, t-butilo, 2,2-dimetilbutilo, n-pentilo, n-hexilo, nheptilo, en particular, metilo o etilo.
- “alquenilo” hace referencia a un grupo de hidrocarburo alifático que contiene un doble enlace carbono-carbono y que puede ser lineal o ramificado que tiene de 2 a 7 átomos de carbono en la cadena de alquenilo (C2-C7), a menos que se especifique lo contrario. Los grupos alquenilo preferidos tienen de 2 a 3 átomos de carbono en la cadena de alquenilo (C2-C3). Los grupos alquenilo de ejemplo incluyen etenilo, n-propenilo, i-propenilo, n-butenilo, i-butenilo, 2,2-dimetilbut-1-enilo, n-pentenilo, en particular propenilo.
- “alcoxi” representa un grupo alquilo, tal como se ha definido previamente, de enlace simple con oxígeno. Los ejemplos de alcoxi (C1-C7) lineal o ramificado incluyen metoxi (CH3O-) y etoxi (CH3CH2O-).
- “arilo” se refiere a un sistema de anillos de hidrocarburo monocíclico o multicíclico aromático de 6 a 14 átomos de carbono, de manera preferente, de 6 a 10 átomos de carbono. Los grupos arilo de ejemplo incluyen fenilo, naftilo, bencilo, fenantrilo, bifenilo, en particular, fenilo.
- “heteroarilo” se refiere a un anillo monocíclico, bicíclico o multicíclico aromático de 5 a 14 miembros, de manera preferente, de 5 a 10, en donde, como mínimo, un miembro del anillo es un heteroátomo. Los heteroátomos pueden ser O o N, en particular N. En particular, cada anillo comprende de 1 a 3 heteroátomos. Los ejemplos incluyen pirrolilo, piridilo, piperidinilo, pirazolilo, pirimidinilo, pirazinilo, indolilo, imidazolilo, en particular piridilo.
- “cicloalquilo” hace referencia a un anillo de hidrocarburo no aromático monocíclico o bicíclico saturado de 2 a 7 átomos de carbono, de manera preferente de 3 a 6 átomos de carbono, que puede comprender una o más insaturaciones. Los ejemplos específicos de grupos cicloalquilo monocíclicos incluyen ciclopropilo, ciclobutilo, ciclopentilo, ciclopentenilo, ciclohexilo, ciclohexenilo.
[0039] De manera preferente, el grupo cicloalquilo es ciclohexenilo.
- “alquil (C1-C7)-arilo” o “alquil (C1-C7)-heteroarilo” significa que R4 está unido al átomo de oxígeno mediante el carbono del grupo alquilo; en particular alquil (C1-C7)-arilo es bencilo.
- “heterociclo” o “heterocicloalquilo” hace referencia a anillos monocíclicos, bicíclicos o multicíclicos de 3 a 14, de
manera preferente, de 5 a 10 miembros, estable no aromático saturado o parcialmente insaturado, que puede opcionalmente formar puentes y en donde, como mínimo, un miembro del anillo es un heteroátomo. Típicamente, los heteroátomos incluyen, pero no se limitan a, O o N. En particular, cada anillo comprende de 1 a 3 heteroátomos. Los heterociclos adecuados también se dan a conocer en the Handbook of Chemistry and Physics, 76a Edición, CRC Press, Inc., 1995-1996, páginas 225 a 226, la divulgación del cual se incorpora en el presente documento por referencia. Los ejemplos de heterocicloalquilo incluyen, pero no se limitan a, tetrahidropiridilo, tetrahidropiranilo, pirrolidinilo, piperidilo, morfolinilo, imidazolidinilo o benzodioxol, en particular 1,3 benzodioxol.
- El término “sustituido” hace referencia a, a menos que se especifique lo contrario, una sustitución con uno o más sustituyentes, que pueden ser idénticos o diferentes, por ejemplo, seleccionados entre alquilo (C1-C7) lineal o ramificado, halógeno, NO2 y CONH2, alquilo (C1-C7) lineal o ramificado sustituido por uno o más átomos de halógeno, alcoxi (C1-C7) lineal o ramificado, alcoxi (C1-C7) lineal o ramificado sustituido por uno o más átomos de halógeno, arilo, - COOH, -COOCH2CH3, -NRR', NH2, NHalquilo y N(alquilo)2. Los ejemplos incluyen, en particular, metilo, metoxi, cloro, flúor, CF3 y OCF3.
[0040] Los compuestos de fórmula (I), tal como como se describen en el presente documento, pueden comprender uno o más átomos de carbono asimétricos. Por lo tanto, pueden existir en forma de enantiómeros o diastereoisómeros. Estos enantiómeros y diastereoisómeros, así como sus mezclas, incluyendo mezclas racémicas, forman parte de la presente invención.
[0041] Los compuestos de fórmula (I), tal como se describen en el presente documento, se pueden proporcionar en forma de una base libre o en forma de sales de adición con ácidos, que también forman parte de la presente invención.
[0042] Estas sales se preparan de manera ventajosa con ácidos farmacéuticamente aceptables, pero las sales con otros ácidos útiles, por ejemplo, para la purificación o para el aislamiento de los compuestos de fórmula (I), tal como se describen en el presente documento, también forman parte de la presente invención.
[0043] Tal como se utiliza en el presente documento, la expresión “farmacéuticamente aceptable” hace referencia a aquellos compuestos, materiales, excipientes, composiciones o formas de administración que están dentro del alcance del criterio médico, adecuados para el contacto con los tejidos de seres humanos y animales sin toxicidad excesiva, irritación, respuesta alérgica u otras complicaciones problemáticas proporcionales con una relación de beneficio/riesgo razonable.
[0044] Tal como se utiliza en el presente documento, “sales farmacéuticamente aceptables” hace referencia a derivados de los compuestos divulgados, en los que el compuesto original se modifica preparando sales ácidas o básicas de los mismos. Las sales farmacéuticamente aceptables incluyen las sales no tóxicas convencionales o las sales de amonio cuaternario del compuesto original formadas, por ejemplo, a partir de ácidos inorgánicos u orgánicos no tóxicos. Por ejemplo, tales sales no tóxicas convencionales incluyen aquellas derivadas de ácidos inorgánicos, tales como clorhídrico, bromhídrico, sulfúrico, sulfámico, fosfórico, nítrico y similares, que incluyen monosales, disales o trisales de los mismos; y las sales preparadas a partir de los ácidos orgánicos, tales como acético, propiónico, succínico, tartárico, cítrico, metanosulfónico, bencenosulfónico, glucurónico, glutámico, benzoico, salicílico, toluenosulfónico, oxálico, fumárico, maleico, láctico y similares. Otras sales de adición incluyen sales de amonio, tales como trometamina, meglumina, epolamina, etc., sales metálicas, tales como de sodio, potasio, calcio, zinc o magnesio.
[0045] Las sales farmacéuticamente aceptables de la presente invención pueden sintetizarse a partir del compuesto original que contiene un resto básico o ácido mediante procedimientos químicos convencionales. Generalmente, tales sales se pueden preparar haciendo reaccionar las formas de ácido o base libre de dichos compuestos con una cantidad estequiométrica de la base o el ácido apropiado en agua o en un disolvente orgánico o en una mezcla de los dos. Generalmente, se prefieren medios no acuosos, tales como éter, acetato de etilo, etanol, isopropanol o acetonitrilo. Las listas de sales adecuadas se encuentran en Remington's Pharmaceutical Sciences, 20a edición, Mack Publishing Company, Easton, PA, 2000, la divulgación de las cuales se incorporan en el presente documento por referencia.
Proceso
[0046] La presente invención se refiere también al proceso de preparación de los compuestos de fórmula (I), tal como se describe en el presente documento.
[0047] Los compuestos y el proceso de la presente invención se pueden preparar mediante un conjunto de procedimientos bien conocidos por los expertos en la técnica. Se pueden sintetizar los compuestos, por ejemplo, mediante la aplicación o la adaptación de los procedimientos descritos a continuación o variaciones a partir de los mismos reconocidas por el experto. Las modificaciones y las sustituciones apropiadas resultarán fácilmente obvias y bien conocidas o fácilmente obtenibles a partir de la literatura científica por los expertos en la técnica.
[0048] Se entenderá que los compuestos de la presente invención pueden contener uno o más átomos de carbono sustituidos de manera asimétrica y se pueden aislar en formas ópticamente activas o racémicas. Por lo tanto, se prevén todas las formas quirales, diaestereoméricas, racémicas, formas isoméricas de una estructura, a menos que la estereoquímica o forma isomérica específicas se indique de manera específica. Se conoce bien en la técnica como
preparar y aislar tales formas ópticamente activas.
[0049] Por ejemplo, se pueden separar las mezclas de estereoisómeros mediante técnicas estándar que incluyen, pero no se limitan a, resolución de formas racémicas, cromatografía normal, de fase reversa y quiral, formación de sal preferencial, recristalización y similares o mediante síntesis quiral a partir de materiales iniciales quirales o mediante síntesis deliberada de centros diana quirales.
[0050] Los compuestos de la presente invención se pueden preparar mediante una variedad de rutas sintéticas. Los reactivos y los materiales iniciales están disponibles comercialmente o se sintetizan fácilmente mediante técnicas bien conocidas por un experto en la técnica. Todos los sustituyentes, a menos que se indique lo contrario, son como se definen previamente.
[0051] En las reacciones descritas de aquí en adelante en el presente documento, puede ser necesario proteger grupos funcionales reactivos, por ejemplo, grupos hidroxilo, amino, imino, tio o carboxilo, donde estos grupos son necesarios para el producto final, para evitar su participación no deseada en las reacciones. Los grupos protectores convencionales pueden utilizarse de acuerdo con la práctica estándar, por ejemplo, véanse, T.W. Greene y P. G. M. Wuts en Protective Groups in Organic, 4a edición (2007) John Wiley & Sons Inc., 1999; J. F. W. McOmie en Protective Groups in Organic Chemistry, Plenum Press, 1973.
[0052] Algunas reacciones se pueden llevar a cabo en presencia de una base. No existe ninguna restricción particular sobre la naturaleza de la base que se utiliza en esta reacción, y cualquier base utilizada de manera convencional en reacciones de este tipo se puede utilizar igualmente en el presente documento, siempre y cuando no tenga ningún efecto adverso sobre otras partes de la molécula, y a menos que se indique lo contrario. Los ejemplos de bases adecuadas incluyen: hidróxido de sodio, carbonato de potasio, trietilamina, hidruros de metal alcalino, tales como hidruro de sodio e hidruro de potasio; compuestos de alquil litio, tales como metil litio y butil litio; y alcóxidos de metal alcalino, tales como metóxido de sodio y etóxido de sodio.
[0053] Normalmente, las reacciones se llevan a cabo en un disolvente adecuado. Se puede utilizar una variedad de disolventes, siempre y cuando no tengan ningún efecto adverso sobre la reacción o sobre los reactivos involucrados. Los ejemplos de disolventes adecuados incluyen: hidrocarburos, que pueden ser hidrocarburos aromáticos, alifáticos o cicloalifáticos, tales como hexano, ciclohexano, benceno, tolueno y xileno; amidas, tales como dimetilformamida; alcoholes, tales como etanol y metanol y éteres, tales como dietil éter y tetrahidrofurano.
[0054] Las reacciones pueden tener lugar en un rango amplio de temperaturas. En general, se considera conveniente llevar a cabo la reacción a una temperatura desde 0 °C hasta 150 °C (de manera más preferente, desde aproximadamente temperatura ambiente hasta 100 °C). El tiempo necesario para la reacción también puede variar considerablemente, dependiendo de muchos factores, especialmente de la temperatura de reacción y del origen de los reactivos. Sin embargo, dado que la reacción se realiza bajo las condiciones preferidas indicadas anteriormente, un periodo desde 3 horas hasta 20 horas será normalmente suficiente.
[0055] Se puede recuperar el compuesto preparado de este modo de la mezcla de reacción utilizando métodos convencionales. Por ejemplo, los compuestos se pueden recuperar separando por destilación el disolvente de la mezcla de reacción o, si es necesario, después de separar por destilación el disolvente de la mezcla de reacción, vertir el residuo en agua, seguido de la extracción con un disolvente orgánico inmiscible en agua y separar por destilación el disolvente del extracto. Adicionalmente, el producto, si se desea, puede purificarse de forma adicional mediante varias técnicas bien conocidas, tales como la recristalización, la reprecipitación o varias técnicas de cromatografía, especialmente, cromatografía en columna o cromatografía en capa fina preparativa.
[0056] Los procesos de preparación de un compuesto de fórmula (I) de la presente invención es un objeto adicional de la presente invención.
[0057] De acuerdo con un primer aspecto, un compuesto de la presente invención de fórmula (I) puede obtenerse a) haciendo reaccionar un compuesto de fórmula (II) con un ácido orgánico o inorgánico
b) haciendo reaccionar el compuesto obtenido en la etapa a) con una base;
c) haciendo reaccionar el compuesto obtenido en la etapa b) con CO2;
d) haciendo reaccionar el compuesto obtenido en la etapa c) con cloroformiato de alquilo, un reactivo capaz de formar, con el compuesto obtenido en la etapa c), un haluro de ácido o un reactivo capaz de formar, con el
compuesto obtenido en la etapa c), un anhídrido mixto;
e) haciendo reaccionar un compuesto obtenido en la etapa d) con un compuesto precursor de anión SMe-; en donde R1 y R2 son tal como se definen en el presente documento.
[0058] En particular, la base de la etapa b) tiene un pKa superior a 25, de manera preferente la base utilizada en la etapa b) se selecciona entre bases de litio o magnesio, de manera preferente la base se selecciona entre butil litio o hexil litio.
[0059] En particular, el compuesto de fórmula (II) se obtiene mediante una etapa a1) de reacción entre 3-cloro-3-metilbut-1-ino con R1R2NH en un medio acuoso.
[0060] En particular, dicho compuesto obtenido en la etapa a1) se purifica mediante una o más filtraciones, por ejemplo, en filtración o en una serie de 2 hasta 10 filtraciones, de manera preferente en una serie de 2 hasta 5 filtraciones, por ejemplo, en 4 filtraciones.
[0061] En una realización, se obtiene 3-cloro-3-metilbut-1-ino mediante una etapa de reacción de hacer reaccionar 2-metilbut-3-in-2-ol con ácido clorhídrico en presencia de un catalizador de cobre.
[0062] En otra realización, el ácido es un ácido inorgánico seleccionado entre ácido clorhídrico, ácido fosfórico, ácido nítrico, ácido sulfúrico, de manera preferente ácido clorhídrico.
[0063] En otra realización, la etapa d) se lleva a cabo con:
- un cloroformiato de alquilo que tiene un alquilo (C-i-Ca), que puede comprender como mínimo un doble enlace, de manera preferente, cloroformiato de metilo, etilo, isoprenilo, terc-butilo o isobutilo, de manera preferente cloroformiato de isobutilo; o
- un reactivo capaz de formar con el compuesto obtenido en la etapa c) un anhídrido mixto seleccionado entre cloruros de ácido, por ejemplo, cloruro de pivaloílo; o
- un reactivo capaz de formar, con el compuesto obtenido en la etapa c), un haluro de ácido seleccionado entre SOCh, COCl2, PCla, PCla, PBr3 o PPh3 Br2.
[0064] En una realización, los compuestos precursores de aniones SMe- se seleccionan entre las sales de fórmula XSMe, en la que X representa un metal alcalino o metal alcalinotérreo, por ejemplo, Na, metil mercaptano, o (SMe)2, de manera preferente NaSMe.
[0065] Este proceso se describe en detalle en las solicitudes de patentes FR 1651283 y PCT/EP2017/053457, de las cuales el contenido se incorpora por referencia.
[0066] Alternativamente, un compuesto de acuerdo con la invención puede prepararse a partir de la amina acetilénica correspondiente tratada sucesivamente mediante BuLi, COS y Mel. Se puede encontrar un proceso detallado de preparación, por ejemplo, en G.Quash et al., European Journal of Medicinal Chemistry 43 (2008) 906-916, del cual el contenido se incorpora por referencia, en particular, en la parte 2 del apartado Material y Procedimientos.
[0067] Las reacciones anteriores se pueden llevar a cabo por el experto en la materia mediante la aplicación o la adaptación de los procedimientos ilustrados en los ejemplos que se describen en el presente documento a continuación.
[0068] Además, el proceso de la invención puede comprender también la etapa adicional de aislar el compuesto de fórmula (I) o (II). Esto se puede realizar por el experto en la técnica mediante cualquiera de los medios convencionales conocidos, tales como los procedimientos de recuperación descritos anteriormente.
[0069] De manera general, los productos de partida están disponibles comercialmente en Aldrich o Acros u otro proveedor químico habitual o pueden obtenerse mediante la aplicación o la adaptación de cualquier procedimiento conocido o aquellos descritos en los ejemplos.
Uso
[0070] Tal como ya se ha mencionado, la presente invención también se refiere a un compuesto de fórmula (I), tal como se describe en el presente documento, para su uso como un medicamento.
[0071] Más particularmente, se refiere a un compuesto de fórmula (I), tal como se describe en el presente documento, para la prevención y/o el tratamiento de cáncer.
[0072] La presente invención también se refiere a un procedimiento para la prevención y/o el tratamiento de un cáncer, que comprende la administración a un sujeto que lo necesita de una cantidad eficaz de un compuesto de la fórmula (I) tal como se describe en el presente documento.
[0073] Los términos “tratar”, “que trata”, “tratado” o “tratamiento”, tal como se usan en el contexto de la presente invención, se refieren al tratamiento terapéutico, en el que el objetivo es eliminar o disminuir los síntomas. Los resultados clínicos beneficiosos o deseados incluyen, pero no se limitan a, la eliminación de síntomas, el alivio de síntomas, la disminución del alcance de la afección, estado estabilizado (es decir, no empeoramiento) de la afección, retraso o disminución de progresión de la afección.
[0074] Los términos “prevenir”, “prevención”, “que previene” o “prevenido”, tal como se utilizan en el contexto de la presente invención, hacen referencia a la prevención de la aparición, reaparición o propagación de una enfermedad o trastorno, o de uno o más síntomas de los mismos. En determinadas realizaciones, los términos hacen referencia al tratamiento con o la administración de un compuesto proporcionado en el presente documento antes de la aparición de síntomas, particularmente en pacientes en riesgo de enfermedad o trastornos proporcionados en el presente documento. Los términos abarcan la inhibición o la reducción de un síntoma de la enfermedad particular. Los sujetos con historial familiar de una enfermedad en particular son candidatos para regímenes preventivos en determinadas realizaciones. Adicionalmente, los sujetos que tienen un historial de síntomas recurrentes son también candidatos potenciales para la prevención. A este respecto, el término “prevención” se puede usar de manera intercambiable con el término “tratamiento profiláctico”.
[0075] Tal como se utiliza en el presente documento y a menos que se indique lo contrario, “cáncer” se refiere al crecimiento, división o proliferación de células anormales en el cuerpo. Se refiere a cualquier tipo de tumor maligno (es decir, no benigno). El tumor maligno puede corresponder a un tumor primario o a un tumor secundario (es decir, una metástasis). Además, el tumor puede corresponder a un tumor maligno sólido, que incluye, por ejemplo, carcinomas, adenocarcinomas, sarcomas, melanomas, mesoteliomas, blastomas, o a un cáncer de la sangre, tal como leucemias, linfomas y mielomas. El cáncer puede, por ejemplo, corresponder a un carcinoma sólido, un melanoma, un cáncer de pulmón (que incluye, pero no se limita a, carcinomas de pulmón de células no pequeñas (NSCLC), carcinoma de pulmón de células pequeñas (SCLC), carcinomas de células pequeñas combinados, blastomas pleuropulmonares, tumores carcinoides, carcinomas sarcomatoides, tumores carcinoides, carcinomas adenoescamosos, carcinomas de pulmón de células escamosas, adenocarcinomas y carcinomas de pulmón de células grandes), un cáncer cerebral (que incluye, pero no se limita a gliomas, glioblastomas, astrocitomas, oligoastrocitomas, oligodendrogliomas y ependimomas), cáncer de riñón, cáncer de próstata, cáncer de mama, síndrome mielodisplásico y leucemia.
[0076] En particular, la presente invención se refiere a un compuesto de fórmula (I), tal como se describe en el presente documento, para la prevención y/o el tratamiento de leucemia.
[0077] En particular, el sujeto que necesita un tratamiento contra el cáncer es un sujeto afectado por dicha enfermedad.
[0078] En el contexto de la presente invención, la identificación de los sujetos que necesitan tratamiento de las enfermedades y afecciones descritas en el presente documento se lleva a cabo tal como se menciona anteriormente y está dentro de la capacidad y el conocimiento de un experto en la técnica. Un experto clínico en la técnica puede identificar fácilmente, utilizando las técnicas mencionadas anteriormente, a aquellos sujetos que necesitan dicho tratamiento.
[0079] Una cantidad terapéuticamente eficaz se puede determinar fácilmente por el especialista responsable, como un experto en la técnica, mediante el uso de técnicas convencionales y observando los resultados obtenidos en circunstancias análogas. Para determinar la cantidad terapéuticamente eficaz se considera un número de factores por el especialista responsable, que incluyen, pero no se limitan a: los tipos de sujeto; su tamaño, edad y salud general; la enfermedad específica involucrada; el nivel de implicación o la gravedad de la enfermedad; la respuesta del sujeto individual; el compuesto particular administrado; el modo de administración; la característica de biodisponibilidad de la preparación administrada; el régimen de dosis seleccionado; el uso de medicación que se administra simultáneamente; y otras circunstancias relevantes.
[0080] Tal como se utiliza en el presente documento, una “cantidad eficaz” se refiere a una cantidad que es eficaz en la reducción, la eliminación, el tratamiento o el control de los síntomas de las enfermedades y las afecciones descritas en el presente documento. El término “que controla” pretende referirse a todos los procesos en los que pueda haber retraso, interrupción, detención o suspensión de la progresión de las enfermedades y las afecciones descritas en el presente documento, pero no necesariamente indica una eliminación total de todos los síntomas de enfermedad y afección y pretende incluir tratamiento profiláctico y uso crónico.
[0081] El término “paciente” o “sujeto” se refiere a un animal de sangre caliente, tal como un mamífero, en particular, un ser humano, hombre o mujer, a menos que se indique lo contrario, que está afectado por o tiene potencial de estar afectado por una o más enfermedades y afecciones descritas en el presente documento.
[0082] La cantidad del compuesto de acuerdo con la presente invención, que se necesita para conseguir el efecto biológico deseado, variará dependiendo de un conjunto de factores, que incluyen la dosis del fármaco a administrar, las características químicas (por ejemplo, hidrofobicidad) de los compuestos empleados, la potencia de los compuestos, el tipo de enfermedad, el estado de enfermedad del paciente y la vía de administración.
[0083] Los compuestos proporcionados en el presente documento se pueden formular en composiciones farmacéuticas mezclándolos opcionalmente con uno o más excipientes farmacéuticamente aceptables.
[0084] Tales composiciones se pueden preparar para su uso en administración oral, particularmente, en forma de comprimidos o cápsulas, en particular, comprimidos bucodispersables (lyoc); o administración parenteral, particularmente, en forma de soluciones, suspensiones o emulsiones líquidas.
[0085] Se puede preparar mediante cualquier procedimiento bien conocido en la técnica farmacéutica, por ejemplo, tal como se describe en Remington: The Science and Practice of Pharmacy, 20a edición; Gennaro, A. R., Ed.; Lippincott Williams & Wilkins: Filadelfia, PA, 2000. Se pueden incluir agentes aglutinantes y/o materiales adyuvantes compatibles farmacéuticamente como parte de la composición. Las composiciones orales incluirán de manera general un portador diluyente o un portador comestible inerte. Se pueden administrar en formas de dosis unitaria, en donde el término “dosis unitaria” significa una dosis única que es capaz de ser administrada a un paciente y que se puede manipular y empaquetar fácilmente, permaneciendo como una dosis unitaria física y químicamente estable, que comprende el compuesto activo en sí o como una composición farmacéuticamente aceptable.
[0086] Los comprimidos, píldoras, polvos, cápsulas, trociscos y similares pueden contener uno o más de cualquiera de los siguientes ingredientes o compuestos de una naturaleza similar: un aglutinante, tal como celulosa microcristalina o goma tragacanto; un diluyente, tal como almidón o lactosa; un disgregante, tal como almidón y derivados de celulosa; un lubricante, tal como estearato de magnesio; un glidante, tal como dióxido de silicio coloidal; un agente edulcorante, tal como sacarosa o sacarina; o un agente aromatizante, tal como menta o salicilato de metilo. Las cápsulas pueden tener forma de una cápsula dura o una cápsula blanda, que se fabrican generalmente a partir de mezclas de gelatina mezcladas opcionalmente con plastificantes, así como también una cápsula de almidón. Adicionalmente, las formas de unidades de dosificación pueden contener otros materiales diferentes que modifican la forma física de la unidad de dosificación, por ejemplo, recubrimientos de azúcar, goma laca o agentes entéricos. Otras formas de dosificación oral, tales como jarabe o elixir, pueden contener agentes edulcorantes, conservantes, colorantes, pigmentos y aromatizantes. Adicionalmente, los compuestos activos se pueden incorporar en preparaciones y formulaciones de disolución rápida, liberación modificada o liberación sostenida y en donde dichas formulaciones de liberación sostenida son de manera preferente bimodales.
[0087] Las preparaciones líquidas para administración incluyen soluciones, suspensiones y emulsiones estériles acuosas o no acuosas. Las composiciones líquidas pueden incluir también aglutinantes, tampones, conservantes, agentes quelantes, edulcorantes, agentes aromatizantes y colorantes y similares. Los disolventes no acuosos incluyen alcoholes, propilenglicol, polietilenglicol, copolímeros de acrilatos, aceites vegetales, tales como aceite de oliva y ésteres orgánicos, tal como oleato de etilo. Los portadores acuosos incluyen mezclas de alcoholes y agua, hidrogeles, medios tamponados y solución salina. En particular, polímero biocompatible, biodegradable de láctido, copolímero de láctido/glicólido o copolímeros de polioxietileno-polioxipropileno pueden ser excipientes útiles para controlar la liberación de los compuestos activos. Los vehículos intravenosos pueden incluir rellenos fluidos y nutrientes, rellenos de electrolitos, tales como aquellos basados en dextrosa de Ringer y similares.
[0088] Los ejemplos de vías de administración incluyen parental, por ejemplo, subcutánea, intramuscular, intravenosa, intradérmica, así como administración oral.
Conjugados Anticuerpo-Fármaco
[0089] Tal como se ha mencionado, la presente invención se refiere también a un conjugado anticuerpo-fármaco de fórmula: B-L-Ab, en donde:
- B es un compuesto de fórmula (I), tal como se menciona anteriormente, en la que:
-X es S;
- R1 es alquilo (C1-C7) lineal o ramificado;
- R2 es CHR5CHR6OR4 o (CHR5VOR4;
- R4 se selecciona entre H, arilo, heteroarilo, alquil (Ci-C7)-arilo lineal o ramificado o alquil (Ci-C7)-heteroarilo lineal o ramificado;
estando dicho arilo y heteroarilo opcionalmente sustituidos por uno o más sustituyentes que se seleccionan entre: -COOH, -NRR' y -NO2; y
- R y R' idénticos, son H;
- L es un resto químico que comprende un enlace covalente o una cadena de átomos que acopla de manera covalente el Ab al compuesto de fórmula (I); y
- Ab es un anticuerpo que se selecciona entre: rituximab, trastuzumab, alemtuzumab, ibritumomab, tiuxetano, tositumomab, brevacizumab, cetuximab, panitumumab, ofatumumab, ipilimumab y obinutuzumab.
[0090] Por “conjugado anticuerpo-fármaco” o ADC se entiende una clase importante de fármacos biofarmacéuticos altamente potentes diseñados como una terapia dirigida para el tratamiento de personas con cáncer. A diferencia de la quimioterapia, los ADCs pretenden dirigirse y eliminar solamente las células cancerígenas y salvar las células sanas. Los ADCs son moléculas compuestos por un anticuerpo unido a una carga útil o fármaco citotóxico (anticáncer)
biológicamente activo. En el contexto de la presente invención, el fármaco citotóxico es el compuesto de la fórmula (I) mencionado anteriormente. Este compuesto se une al anticuerpo mediante un enlazador.
[0091] “Enlazador”, tal como se utiliza en el presente documento, significa un resto químico que comprende un enlace covalente o una cadena de átomos que acopla de manera covalente el anticuerpo al compuesto de fórmula (I), tal como se menciona anteriormente.
[0092] El enlazador del conjugado anticuerpo-fármaco puede ser cualquier enlazador capaz de conjugar el anticuerpo y el compuesto de fórmula (I) mencionado anteriormente. Los grupos enlazadores adecuados se conocen bien en la técnica. En particular, puede ser un enlazador biodegradable.
[0093] Más particularmente, el compuesto de acuerdo con la presente invención, tal como se menciona anteriormente, se acopla a un anticuerpo a través de un grupo de acoplamiento (maleimida, éster de succinimidilo, sustrato de enzimas de secuencia peptídica específica, etc ...), unido a un enlazador escindible (sitio de proteasa, hidracina, disulfuro) o un enlazador no escindible y con o sin un espaciador autoinmolativo.
[0094] En la definición anterior del conjugado anticuerpo-fármaco B-L-Ab, el enlazador L, por tanto, incluye tanto el enlazador y finalmente el enlazador unido a un grupo de acoplamiento tal como se define en el presente documento.
[0095] Los enlazadores de dipéptido escindibles de tipo Val-Ala y Val-Cit pueden mencionarse como ejemplos. Se aprovechan del mecanismo de direccionamiento de conjugado anticuerpo-fármaco que involucra la unión secuencial del conjugado anticuerpo-fármaco a su antígeno afín en la superficie de las células cancerígenas diana, y la internalización de los complejos ADC-antígeno a través de la vía endosomal-lisosomal.
[0096] En estos casos, la liberación intracelular del fármaco anticáncer citotóxico se basa en el hecho de que los endosomas/lisosomas son compartimentos ácidos que facilitarán la escisión de enlaces químicos lábiles a los ácidos, tales como hidrazona. Además, si el sitio de escisión de proteasa específico lisosomal se modifica en el enlazador, por ejemplo, el sitio de catepsina B en vcMMAE, las citotoxinas se liberarán en la proximidad de sus dianas intracelulares.
[0097] Alternativamente, los enlazadores que contienen disulfuros mixtos proporcionan otro enfoque mediante el cual las cargas útiles citotóxicas pueden liberarse de manera intracelular a medida que se escinden de manera selectiva en el entorno reductor de la célula, pero no en el entorno enriquecido con oxígeno en el torrente sanguíneo.
[0098] Estos enlazadores se pueden preparar mediante los procedimientos bien conocidos por el experto en la técnica.
[0099] En particular, el enlazador de acuerdo con la presente invención es el maleimidocaproil-Val-Cit descrito en la sección experimental.
[0100] Otros ejemplos de los enlazadores que pueden utilizarse en el contexto de la invención, así como los procedimientos de preparación de los mismos pueden ser enlazador de maleimidocaproilo, mercaptoacetamidocaproilo, enlazador de hidrazona y glucurónido combinado con un enlazador autoinmolativo de alcohol p-aminobencílico (PAB), tal como se menciona en Perez et al.: "Antibody-drug conjugates: current status and future directions"; Drug Discovery Today, Volumen 00, Número 00, diciembre de 2013 y en McCombs y Shawn: "Antibody Drug Conjugates: Design and Selection of Linker, Payload and Conjugation Chemistry", The AAPS Journal, Volumen 17, Número 2, marzo de 2015.
[0101] Los anticuerpos están disponibles comercialmente y se conocen bien por el experto en la técnica.
[0102] Más información acerca de estos anticuerpos se proporciona en la tabla 1 a continuación.
[0103] El procedimiento para preparar el conjugado de anticuerpo-fármaco de acuerdo con la invención se adaptará por el experto en la técnica en función del enlazador y el anticuerpo seleccionados. El experto en la técnica será capaz de preparar el conjugado anticuerpo-fármaco basándose en su conocimiento general. Se proporciona un ejemplo en la sección experimental de la presente invención.
[0104] La presente invención también se refiere al conjugado anticuerpo-fármaco, tal como se define anteriormente, para su uso como un medicamento, en particular, para su uso en la prevención y/o el tratamiento de cáncer.
[0105] Los ejemplos de cáncer a tratar son linfoma de células B, cáncer de mama, leucemia linfocítica crónica, cáncer de colon, cáncer de pulmón, cáncer de mama, cáncer renal y melanoma.
[0106] La presente invención se refiere adicionalmente a una composición farmacéutica que comprende un conjugado anticuerpo-fármaco de acuerdo con la presente invención.
[0107] Los términos “tratar”, “que trata”, “tratado” o “tratamiento”, tal como se usan en el contexto de la presente invención, se refieren al tratamiento terapéutico, en el que el objetivo es eliminar o disminuir los síntomas. Los resultados clínicos beneficiosos o deseados incluyen, pero no se limitan a, eliminación de síntomas, alivio de síntomas, disminución del alcance de afección, estado estabilizado (es decir, no empeoramiento) de la afección, retraso o disminución de progresión de la afección.
[0108] Los términos “prevenir”, “prevención”, “que previene” o “prevenido”, tal como se utilizan en el contexto de la presente invención, hacen referencia a la prevención de la aparición, reaparición o propagación de una enfermedad o trastorno, o de uno o más síntomas de los mismos. En determinadas realizaciones, los términos hacen referencia al tratamiento con o la administración de un compuesto proporcionado en el presente documento antes de la aparición de síntomas, particularmente en pacientes en riesgo de enfermedad o trastornos proporcionados en el presente documento. Los términos abarcan la inhibición o la reducción de un síntoma de la enfermedad particular. Los sujetos con historial familiar de una enfermedad en particular son candidatos para regímenes preventivos en determinadas realizaciones. Adicionalmente, los sujetos que tienen un historial de síntomas recurrentes son también candidatos potenciales para la prevención. A este respecto, el término “prevención” se puede usar de manera intercambiable con el término “tratamiento profiláctico”.
[0109] Tal como se utiliza en el presente documento y a menos que se indique lo contrario, “cáncer” se refiere al crecimiento, división o proliferación de células anormales en el cuerpo. Se refiere a cualquier tipo de tumor maligno (es decir, no benigno). El tumor maligno puede corresponder a un tumor primario o a un tumor secundario (es decir, una metástasis).
[0110] En particular, el sujeto que necesita un tratamiento contra el cáncer es un sujeto afectado por dicha enfermedad.
[0111] En el contexto de la presente invención, la identificación de los sujetos que necesitan tratamiento de enfermedades y afecciones descritas en el presente documento se lleva a cabo, tal como se menciona anteriormente, y está dentro de la capacidad y el conocimiento de un experto en la técnica. Un experto clínico en la técnica puede identificar fácilmente, mediante las técnicas mencionadas anteriormente, a aquellos sujetos que necesitan dicho tratamiento.
[0112] Una cantidad terapéuticamente eficaz se puede determinar fácilmente por el especialista responsable, como un experto en la técnica, mediante el uso de técnicas convencionales y observando los resultados obtenidos en circunstancias análogas. Para determinar la cantidad terapéuticamente eficaz se considera un número de factores por el especialista responsable, que incluyen, pero no se limitan a: los tipos de sujeto; su tamaño, edad y salud general; la enfermedad específica involucrada; el nivel de implicación o la gravedad de la enfermedad; la respuesta del sujeto individual; el compuesto particular administrado; el modo de administración; la característica de biodisponibilidad de la preparación administrada; el régimen de dosis seleccionado; el uso de medicación que se administra simultáneamente; y otras circunstancias relevantes.
[0113] Tal como se utiliza en el presente documento, una “cantidad eficaz” se refiere a una cantidad que es eficaz en la reducción, la eliminación, el tratamiento o el control de los síntomas de las enfermedades y las afecciones descritas en el presente documento. El término “que controla” pretende referirse a todos los procesos en los que pueda haber retraso, interrupción, detención o suspensión de la progresión de las enfermedades y las afecciones descritas en el
presente documento, pero no necesariamente indica una eliminación total de todos los síntomas de enfermedad y afección y pretende incluir tratamiento profiláctico y uso crónico.
[0114] El término “paciente” o “sujeto” se refiere a un animal de sangre caliente, tal como un mamífero, en particular, un ser humano, hombre o mujer, a menos que se indique lo contrario, que está afectado por o tiene potencial de estar afectado por una o más enfermedades y afecciones descritas en el presente documento.
[0115] La cantidad del conjugado anticuerpo-fármaco de acuerdo con la presente invención, que se necesita para conseguir el efecto biológico deseado, variará dependiendo de un conjunto de factores, que incluyen la dosis a administrar, las características químicas y biológicas (por ejemplo, hidrofobicidad) de los compuestos empleados, la potencia de los compuestos, el tipo de enfermedad, el estado de la enfermedad del paciente y la vía de administración.
[0116] El conjugado anticuerpo-fármaco proporcionado en el presente documento se puede formular en composiciones farmacéuticas mezclándolo opcionalmente con uno o más excipientes farmacéuticamente aceptables.
[0117] Tales composiciones se pueden preparar para su uso en la administración oral, particularmente, en forma de comprimidos o cápsulas, en particular, comprimidos bucodispersables (lyoc); o administración parenteral, particularmente, en forma de soluciones, suspensiones o emulsiones líquidas.
[0118] Se puede preparar mediante cualquier procedimiento bien conocido en la técnica farmacéutica, por ejemplo, tal como se describe en Remington: The Science and Practice of Pharmacy, 20a edición; Gennaro, A. R., Ed.; Lippincott Williams & Wilkins: Filadelfia, PA, 2000. Se pueden incluir agentes aglutinantes y/o materiales adyuvantes compatibles farmacéuticamente como parte de la composición. Las composiciones orales incluirán de manera general un portador diluyente o un portador comestible inerte. Se pueden administrar en formas de dosis unitaria, en donde el término “dosis unitaria” significa una dosis única que es capaz de ser administrada a un paciente y que se puede manipular y empaquetar fácilmente, permaneciendo como una dosis unitaria física y químicamente estable, que comprende el compuesto activo en sí o como una composición farmacéuticamente aceptable.
[0119] Los comprimidos, píldoras, polvos, cápsulas, trociscos y similares pueden contener uno o más de cualquiera de los siguientes ingredientes o compuestos de una naturaleza similar: un aglutinante, tal como celulosa microcristalina o goma tragacanto; un diluyente, tal como almidón o lactosa; un disgregante, tal como almidón y derivados de celulosa; un lubricante, tal como estearato de magnesio; un glidante, tal como dióxido de silicio coloidal; un agente edulcorante, tal como sacarosa o sacarina; o un agente aromatizante, tal como menta o salicilato de metilo. Las cápsulas pueden tener forma de una cápsula dura o una cápsula blanda, que se fabrican generalmente a partir de mezclas de gelatina mezcladas opcionalmente con plastificantes, así como también una cápsula de almidón. Adicionalmente, las formas de unidades de dosificación pueden contener otros materiales diferentes que modifican la forma física de la unidad de dosificación, por ejemplo, recubrimientos de azúcar, goma laca o agentes entéricos. Otras formas de dosificación oral, tales como jarabe o elixir, pueden contener agentes edulcorantes, conservantes, colorantes, pigmentos y aromatizantes. Adicionalmente, los compuestos activos se pueden incorporar en preparaciones y formulaciones de disolución rápida, liberación modificada o liberación sostenida y en donde dichas formulaciones de liberación sostenida son de manera preferente bimodales.
[0120] Las preparaciones líquidas para administración incluyen soluciones, suspensiones y emulsiones estériles acuosas o no acuosas. Las composiciones líquidas pueden incluir también aglutinantes, tampones, conservantes, agentes quelantes, edulcorantes, agentes aromatizantes y colorantes y similares. Los disolventes no acuosos incluyen alcoholes, propilenglicol, polietilenglicol, copolímeros de acrilatos, aceites vegetales, tales como aceite de oliva y ésteres orgánicos, tal como oleato de etilo. Los portadores acuosos incluyen mezclas de alcoholes y agua, hidrogeles, medios tamponados y solución salina. En particular, polímero biocompatible, biodegradable de láctido, copolímero de láctido/glicólido o copolímeros de polioxietileno-polioxipropileno pueden ser excipientes útiles para controlar la liberación de los compuestos activos. Los vehículos intravenosos pueden incluir rellenos fluidos y nutrientes, rellenos de electrolitos, tales como aquellos basados en dextrosa de Ringer y similares.
[0121] Los ejemplos de vías de administración incluyen parental, por ejemplo, subcutánea, intramuscular, intravenosa, intradérmica, así como administración oral.
[0122] En el alcance de la presente invención, se debe entender que “un compuesto para su uso en el tratamiento o la prevención de” es equivalente a “el uso de un compuesto para el tratamiento o la prevención de” y a “el uso de un compuesto para la producción de un medicamento destinado al tratamiento o la prevención de”.
[0123] La presente invención se ilustrará adicionalmente mediante la siguiente figura y ejemplos.
FIGURA
[0124] Figura 1: La viabilidad media de células Raji en porcentaje en comparación con las células no tratadas después de un tratamiento con 50 pg/ml de Rituximab (85,50 % ± 2,268 %) y Rituximab (102,9 % ± 1,789 %) acoplados con el compuesto 5. La diferencia entre las dos medias fue significativa utilizando la prueba t no emparejada (P < 0,01, **).
EJEMPLOS
[0125] Los compuestos representativos de la presente invención (excepto los compuestos 13, 14, 15 y 16 que no forman parte de la presente invención), se resumen en la tabla 2 a continuación:
[0126] Los compuestos representativos de la presente invención (excepto los compuestos 13, 14, 15 y 16 que no forman parte de la presente invención) pueden sintetizarse de acuerdo con los siguientes procedimientos.
Procedimientos analíticos generales
[0127] El espectro de RMN 1H y 13C se registraron en un Bruker Advance ALS300 y DRX400 MHz de Bruker. Los desplazamientos químicos se presentan en ppm (8) e hicieron referencia a DMSO-d6 (1H, 2,50 ppm; 13C, 39,52 ppm) o CDCl3 (7,26 ppm). Las constantes de acoplamiento (J) se indicaron en Hz.
[0128] Los espectros de masas de HRMS-ESI se registraron en modo de iones positivos en un espectrómetro de masas híbrido con analizador cuadrupolo de tiempo de vuelo (MicroTOFQ-II, Bruker Daltonics, Bremen) con una fuente de iones de Ionización por Electrospray (ESI). Para la espectrometría de masas de baja resolución, se registraron los espectros de masas de LRMS-ESI en un espectrómetro Thermo Finnigan MAT 95 XL.
Parte 1: Preparación de los compuestos de acuerdo con la presente invención
Ejemplo 1: 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo
[0129] Preparación de N-(2-etoxietil)-N,2-dimetil-but-3-in-2-amina: A una solución de N-metil-N-(2'hidroxiyetil)-3-amino-3metil-1-butino (Easton, Nelson R.; Hennion, George F. EE. UU. (1967), US 3337625 19670822.) (1,0 g, 7,08 mmol) y yodoetano (0,98 ml, 7,6 mmol) en THF (12 ml) se añadió NaH (0,459 g, 11,5 mmol) a temperatura ambiente y la mezcla se puso a reflujo durante 3 horas. A continuación, la mezcla se hidrolizó con precaución a temperatura ambiente con agua y se extrajo mediante EtOAc (3x25 ml). Las capas orgánicas se lavaron con una solución acuosa saturada de cloruro sódico, se secaron sobre Na2SO4 y se concentraron al vacío. La purificación del producto en bruto mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=70/30) generó N-(2- etoxietil)-N,2-dimetil-but-3-in-2-amina pura (0,479 g, 40 %).
[0130] RMN 1H (300 MHz, DMSO) 83,45 - 3,36 (m, 4H), 3,11 (s, 1H), 2,51 (t, J = 6,7 Hz,. 2H), 2,20 (s, 3H), 1,27 (s, 6H), 1,09 (t, J = 7,0 Hz, 3H).
[0131] ESI-LRMS 170,0 [M+H]+.
[0132] Preparación de 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo: A N-(2-etoxietil)-N,2-dimetilbut-3-in-2-amina (0,367 g, 2,17 mmol) en THF (11 ml) se añadió gota a gota una solución de n-BuLi 2,28 M en hexano (1,14 ml, 2,60 mmol) a -70 °C. Después de 5 minutos a -70 °C, la mezcla de reacción se calentó hasta 0 °C, se mantuvo 10 minutos a esta temperatura, a continuación, se enfrió a -70 °C antes de burbujear durante 30 minutos con sulfuro de carbonilo (COS) a través de la solución. La solución amarilla se calentó hasta 0 °C, se agitó durante un periodo adicional de 10 minutos a esta temperatura antes de añadir gota a gota yodometano (0,162 ml, 2,60 mmol). La mezcla se agitó durante 2 horas, se hidrolizó con precaución a 0 °C con agua y se extrajo con éter. Las capas orgánicas se lavaron con una solución acuosa saturada de cloruro sódico, se secaron sobre Na2SO4 y se concentraron al vacío. La purificación del producto en bruto mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=90/10) generó 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo (0,369 g, 70 %) como un aceite casi incoloro.
[0133] RMN 1H (300 MHz, DMSO) 83,42 (t, J = 6,3 Hz, 2H), 3,42 (q, J = 7,0 Hz, 2H), 2,56 (t, J= 6,3 Hz, 2H), 2,39 (s, 3H), 2,25 (s, 3H), 1,36 (s, 6H), 1,10 (t, J = 7,0 Hz, 3H).
[0134] ESI- HRMS calculado para C12H22NO2S [M+H]+: 244,1366, encontrado: 244,1362.
Ejemplo 2: 4-[2-aliloxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo
[0135] Preparación de N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina: A N-metil-N-(2'hidroxietil)-3-amino-3-metil-1-butino (Easton, Nelson R.; Hennion, George F. EE. UU. (1967), US 3337625 19670822.)) (1,0 g, 7,08 mmol) en THF (12 ml) se añadió NaH (0,40 g, 8,50 mmol) a 0 °C. Después de 15 minutos a 0 °C y 15 minutos a temperatura ambiente, se añadió de golpe n-Bu4NI (0,026 g, 0,071 mmol) a 0 °C seguido de la adición gota a gota de bromuro de alilo (0,735 ml, 8,50 mmol). Se dejó que la mezcla de reacción alcanzara la temperatura ambiente, se agitó durante la noche, a continuación, se hidrolizó con precaución con agua y se extrajo con éter (3x25 ml). Las capas orgánicas se lavaron con una solución acuosa saturada de cloruro sódico (25 ml), se secaron sobre Na2SO4 y se concentraron al vacío. La purificación mediante cromatografía en gel de sílice (éter de petróleo/éter = 80/20 a 70/30) generó N-(2- aliloxietil)-N,2-dimetil-but-3-in-2-amina (0,941 g, 73 %) como un aceite.
[0136] RMN 1H (300 MHz, DMSO) 85,88 (ddt, J = 17,3, 10,5, 5,3 Hz, 1H), 5,24 (ddd, J = 17,3, 3,8, 1,7 Hz, 1 H), 5,16- 5,09 (m, 1H), 3,93 (dt, J = 5,3, 1,6 Hz, 2H), 3,43 (t, J = 6,4 Hz, 2H), 3,12 (s, 1H), 2,55 (t, J = 6,4 Hz, 2H), 2,21 (s, 3H), 1,27 (s, 6H).
[0137] ESI-LRMS 182,0 [M+H]+.
[0138] Preparación de 4-[2-aliloxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo: El compuesto se obtiene utilizando el mismo proceso que el que se describe para el 4-[2-etoxietil(metil)amino]-4-metil-pent- 2-intioato de S-metilo [ejemplo 1] empezando a partir de N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina. Escala: 2,2 mmol. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=90/10 a 80/20). Rendimiento: 65 %. Aceite casi incoloro.
[0139] RMN 1H (300 MHz, DMSO) 85,88 (ddt, J = 17,3, 10,5, 5,3 Hz, 1H), 5,24 (ddd, J = 17,3, 3,8, 1,7 Hz, 1H), 5,17 - 5,10 (m, 1H), 3,94 (dt, J = 5,3, 1,5 Hz, 2H), 3,45 (t, J = 6,2 Hz, 2H), 2,58 (t, J= 6,2 Hz, 2H), 2,39 (s, 3H), 2,26 (s, 3H), 1,36 (s, 6 H).
[0140] ESI-HRMS calculado para C13H22NO2S [M+H]+: 256,1366, encontrado: 256,1364.
Ejemplo 3: 4-[2-benciloxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo
[0141] Preparación de N-(2-benciloxietil)-N,2-dimetil-but-3-in-2-amina: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina [ejemplo 2] utilizando 1,015 equivalentes de NaH y 1,01 equivalentes de bromuro de bencilo. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=90/10). Rendimiento: 81 %. Aceite incoloro.
[0142] RMN 1H (300 MHz, DMSO) 87,39 - 7,24 (m, 5H), 4,47 (s, 2H), 3,49 (t, J = 6,3 Hz, 2H), 3,12 (s, 1H), 2,58 (t, J= 6,3 Hz, 2H), 2,21 (s, 3H), 1,27 (s, 6 H). ESI-LRMS 232,0 [M+H]+.
[0143] Preparación de 4-[2-benciloxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo: El compuesto se obtiene utilizando el mismo proceso que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo [ejemplo 1] empezando a partir de N-(2-benciloxietil)-N,2-dimetil-but-3-in-2-amina. Escala: 2,2 mmol. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=90/10). Rendimiento: 79 %. Aceite incoloro.
[0144] RMN 1H (300 MHz, DMSO) 87,37 - 7,26 (m, 5H), 4,48 (s, 2H), 3,52 (t, J = 6,1 Hz, 2H), 2,62 (t, J = 6,1 Hz, 2H), 2,38 (s, 3H), 2,26 (s, 3H), 1,36 (s, 6H).
[0145] ESI- HRMS calculado para C17H24NO2S [M+H]+: 306,1522, encontrado: 306,1514.
[0146] Protocolo alternativo: A N-(2-benciloxietil)-N,2-dimetil-but-3-in-2-amina (0,650 g, 2,81 mmol) en THF (8 ml) se añadió gota a gota una solución de n-BuLi 2,28 M en hexano (1,36 ml, 3,09 mmol) a -70 °C. Después de 5 minutos a -70°C, la mezcla de reacción se calentó hasta 0°C, se mantuvo 30 minutos a esta temperatura y se burbujeó CO2 a través de la solución durante 30 minutos. La mezcla se calentó hasta la temperatura ambiente dentro de un periodo de 5 minutos, a continuación, se volvió a enfriar a 0 °C. Se añadió gota a gota cloroformiato de isobutilo (0,40 ml, 3,08 mmol) y la mezcla se agitó durante 10 minutos antes de la adición de metóxido de sodio (0,236 g, 3,37 mmol) de golpe. La mezcla se calentó hasta la temperatura ambiente, se agitó durante 15 min adicionales a esta temperatura, a continuación, se hidrolizó con precaución a 0 °C con agua y se extrajo con éter. Las capas orgánicas se lavaron con una solución acuosa saturada de cloruro sódico, se secaron sobre Na2SO4 y se concentraron al vacío. La purificación del producto en bruto mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=90/10) generó 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo (0,307 g, 36 %).
Ejemplo 4: 4-metil-4-[metil-[2-(m-tolilmetoxi)etil]amino]pent -2-intioato de S-metilo
[0147] Preparación de N-2-dimetil-N-[2-(m-tolilmetoxi)etil]but-3-in-2-amina: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina [ejemplo 2] utilizando bromuro de 3-metilbencilo. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=90/10). Escala: 4,5 mmol. Rendimiento: 79 %. Aceite incoloro.
[0148] RMN 1H (300 MHz, DMSO) 87,26 - 7,19 (m, 1H), 7,16 - 7,05 (m, 3H), 4,43 (s, 2H), 3,48 (t, J = 6,3 Hz, 2H), 3,12 (s, 1H), 2,57 (t, J = 6,3 Hz, 2H), 2,30 (s, 3H), 2,21 (s, 3H), 1,27 (s, 6 H).
[0149] ESI-LRMS 246,1 [M+H]+.
[0150] Preparación de 4-metil-4-[metil-[2-(m-tolilmetoxi)etil]amino]pent -2-intioato de S-metilo: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent- 2-intioato de S-metilo [ejemplo 1] empezando a partir de N-2-dimetil-N-[2-(m-tolilmetoxi)etil]but-3-in-2-amina. Escala: 1,3 mmol. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=90/10). Rendimiento: 77 %. Aceite incoloro.
[0151] RMN 1H (300 MHz, DMSO) 87,26 - 7,19 (m, 1H), 7,16 - 7,05 (m, 3H), 4,44 (s, 2H), 3,50 (t, J = 6,1 Hz, 2H), 2,62 (t, J = 6,1 Hz, 2H), 2,38 (s, 3H), 2,30 (s, 3H), 2,26 (s, 3H), 1,36 (s, 6H).
[0152] ESI- HRMS calculado para C18H26NO2S [M+H]+: 320,1679, encontrado: 320,1667.
Ejemplo 5: 4-[2-[(3,4-dimetilfenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo
[0153] Preparación de N-[2-[(3,4-dimetilfenil)metoxi]etil]-N,2-dimetil-but-3-in-2-amina : El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina [ejemplo 2] utilizando bromuro de 3,4-dimetilbencilo. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=60/40). Escala: 3,8 mmol. Rendimiento: 60 %. Aceite incoloro.
[0154] RMN 1H (300 MHz, DMSO) 87,12 -7,06 (m, 2H), 7,04 -6,99 (m, 1H), 4,39 (s, 2H), 3,45 (t, J = 6,3 Hz, 2H), 3,12 (s 1H), 2,56 (t, J = 6,3 Hz, 2H), 2,20 (s, 6H), 2,19 (s, 3H), 1,27 (s, 6H).
[0155] ESI-LRMS 182,0 [M+H]+. ESI-LRMS 260,0 [M+H]+.
[0156] Preparación de 4-[2-[(3,4-dimetilfenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent- 2-intioato de S-metilo [ejemplo 1] empezando a partir de N-[2-[(3,4-dimetilfenil)metoxi]etil]-N,2-dimetil-but-3-in-2-amina. Escala: 1,3 mmol. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=90/10). Rendimiento: 77 %. Aceite casi incoloro.
[0157] RMN 1H (300 MHz, DMSO) 87,12 -7,06 (m, 2H), 7,05 -6,99 (m, 1H), 4,40 (s, 2H), 3,48 (t, J = 6,2 Hz, 2H), 2,60 (t, J = 6,2 Hz, 2H), 2,38 (s, 3H), 2,25 (s, 3H), 2,20 (s, 3H), 2,19 (s, 3H), 1,36 (s, 6H).
[0158] ESI- HRMS calculado para C19H28NO2S [M+H]+: 334,1835, encontrado: 334,1825.
Ejemplo 6: 4-[2-[(4-metoxifenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo
[0159] Preparación de N-[2-[(4-metoxifenil)metoxi]etil]-N,2-dimetil-but-3-in-2-amina: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina [ejemplo 2] utilizando 1-(bromometil)-4-metoxibenceno. Purificación mediante cromatografía en gel de sílice (DCM/MeOH = 99/1 a 97,5/2,5). Escala: 4,0 mmol. Rendimiento: 53 %. Aceite incoloro.
[0160] RMN 1H (300 MHz, DMSO) 87,27 - 7,20 (m, 2H), 6,93 - 6,86 (m, 2H), 4,39 (s, 2H), 3,74 (s, 3H), 3,45 (t, J = 6,3 Hz, 2H), 3,12 (s, 1H), 2,55 (t, J = 6,4 Hz, 2H), 2,20 (s, 3H), 1,27 (s, 6H).
[0161] ESI-LRMS 261,9 [M+H]+.
[0162] Preparación de 4-[2-[(4-metoxifenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent- 2-intioato de S-metilo [ejemplo 1] empezando a partir de N-[2-[(4-metoxifenil)metoxi]etil]-N,2-dimetil-but-3-in-2-amina. Escala: 1,3 mmol. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=80/20). Rendimiento: 74%. Aceite casi incoloro.
[0163] RMN 1H (300 MHz, DMSO) 87,27 - 7,21 (m, 2H), 6,93 - 6,87 (m, 2H), 4,40 (s, 2H), 3,74 (s, 3H), 3,48 (t, J = 6,2 Hz, 2H), 2,60 (t, J = 6,2 Hz, 2H), 2,38 (s, 3H), 2,25 (s, 3H), 1,36 (s, 6H).
[0164] ESI- HRMS calculado para C18H26NO3S [M+H]+: 336,1628, encontrado: 336,1613.
Ejemplo 7: 4-[2-[(3,4-dimetoxifenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo
[0165] Preparación de N-[2-[(3,4-dimetoxifenil)metoxi]etil]-N,2-dimetil-but-3-in-2-amina: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina [ejemplo 2] utilizando 4-(bromometil)-1,2-dimetoxibenceno. Purificación mediante cromatografía en gel de sílice (DCM/MeOH=99/1 a 97,5/2,5). Escala: 4,0 mmol. Rendimiento: 67 %. Aceite incoloro.
[0166] RMN 1H (300 MHz, DMSO) 86,94 -6,88 (m, 2H), 6,87 -6,80 (m, 1H), 4,39 (s, 2H), 3,74 (s, 3H), 3,73 (s, 3H), 3,46 (t , J = 6,3 Hz, 2H), 3,12 (s, 1H), 2,56 (t, J = 6,3 Hz, 2H), 2,21 (s, 3H), 1,27 (s, 6H).
[0167] ESI-LRMS 292,0 [M+H]+.
[0168] Preparación de 4-[2-[(3,4-dimetoxifenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo [ejemplo 1] empezando a partir de N-[2-[(3,4-dimetoxifenil)metoxi]etil]-N,2-dimetil-but-3-in-2-amina. Escala: 1,0 mmol. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=90/10). Rendimiento: 67 %. Aceite casi incoloro.
[0169] RMN 1H (300 MHz, DMSO) 56,94 - 6,87 (m, 1H), 6,87 - 6,81 (m, 1H), 4,40 (s, 2H), 3,74 (s, 3H), 3,73 (s, 3H), 3,48 (t, J = 6., Hz, 2H), 2,61 (t, J = 6,2 Hz, 2H), 2,38 (s, 3H), 2,26 (s, 3H), 1,36 (s, 6 H).
[0170] ESI- HRMS calculado para C19H28NO4S [M+H]+: 366,1734, encontrado: 336,1720.
Ejemplo 8: 4-[2-[(3-clorofenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo
[0171] Preparación de N-[2-[(3-clorofenil)metoxi]etil]-N,2-dimetil-but-3-in-2-amina: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina [ejemplo 2] utilizando bromuro de 3-clorobencilo. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=70/30). Escala: 4,0 mmol. Rendimiento: 71%. Aceite incoloro.
[0172] RMN 1H (300 MHz, DMSO) 57,43 - 7,25 (m, 4H), 4,49 (s, 2H), 3,50 (t, J = 6,2 Hz, 2H), 3,12 (s, 1H), 2,58 (t, J = 6,2 Hz, 2H), 2,22 (s, 3H), 1,28 (s, 6H).
[0173] ESI-LRMS 266,0 [M+H]+.
[0174] Preparación de 4-[2-[(3-clorofenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo [ejemplo 1] empezando a partir de N-[2-[(3-clorofenil)metoxi]etil]-N,2-dimetil-but-3-in-2-amina, a excepción de que la mezcla de reacción se mantuvo a -70 °C después de la adición de n-BuLi durante 30 minutos antes del burbujeo con COS. Escala: 1,3 mmol. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=75/25). Rendimiento: 63 %. Aceite casi incoloro.
[0175] RMN 1H (300 MHz, DMSO) 57,44 - 7,24 (m, 4H), 4,50 (s, 2H), 3,52 (t, J = 6,0 Hz, 2H), 2,63 (t, J = 6,0 Hz, 2H), 2,38 (s, 3H), 2,27 (s, 3H), 1,37 (s, 6H).
[0176] ESI- HRMS calculado para C1yH2aClNO2S [M+H]+: 340,1133, encontrado: 340,1120.
Ejemplo 9: 4-[2-[(3-fluorofenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo
[0177] Preparación de N-[2-[(3-fluorofenil)metoxi]etil]-N,2-dimetil-but-3-in-2-amina: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina [ejemplo 2] utilizando bromuro de 3-fluorobencilo. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=80/20). Escala: 4,0 mmol. Rendimiento: 71 %. Aceite incoloro.
[0178] Preparación de 4-[2-[(3-fluorofenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo [ejemplo 1] empezando a partir de N-[2-[(3-fluorofenil)metoxi]etil]-N,2-dimetil-but-3-in-2-amina, a excepción de que la mezcla de reacción se mantuvo a -70 °C después de la adición de n-BuLi durante 30 minutos antes del burbujeo con COS. Escala: 1,3 mmol. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=70/30). Rendimiento: 87 %. Aceite casi incoloro.
[0179] RMN 1H (300 MHz, DMSO) 57,44 -7,34 (m, 1H), 7,20 -7,05 (m, 3H), 4,51 (s, 2H), 3,53 (t, J = 6,1 Hz, 2H), 2,63 (t, J = 6,1 Hz, 2H), 2,38 (s, 3H), 2,27 (s, 3H), 1,37 (s, 6 H).
[0180] ESI- HRMS calculado para C17H23NO2S [M+H]+: 324,1428, encontrado: 324,1415
Ejemplo 10: 4-metil-4-[metil-[2-(2-piridilmetoxi)etil]amino]pent-2-intioato de S-metilo
[0181] Preparación de N-2-dimetil-N-[2-(2-piridilmetoxi)etil]but-3-in-2-amina: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina [ejemplo 2] empezando a partir de bromhidrato de 2-(bromometil)piridina y utilizando 4 equivalentes de NaH. Purificación mediante cromatografía en gel de sílice (DCM/MeOH=99/1 a 95/5). Escala: 2,1 mmol. Rendimiento: 71 %. Aceite amarillo.
[0182] RMN 1H (300 MHz, DMSO) 58,50 (ddd, J = 4,8, 1,8, 0,9 Hz, 1H), 7,80 (td, J = 7,7, 1,8 Hz, 1H), 7,44 (d, J = 7,8 Hz, 1H), 7,32 - 7,24 (m, 1H), 4,55 (s, 2H), 3,56 (t, J = 6,2 Hz, 2H), 3,13 (s, 1H), 2,61 (t, J = 6,2 Hz, 2H), 2,23 (s, 3H), 1,28 (s, 6 H).
[0183] ESI-LRMS 233,1 [M+H]+.
[0184] Preparación de 4-metil-4-[metil-[2-(2-piridilmetoxi)etil]amino]pent-2-intioato de S-metilo: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo [ejemplo 1] empezando a partir de N-2-dimetil-N-[2-(2-piridilmetoxi)etil]but-3-in-2-amina y utilizando 1,5 equivalentes de extracciones de n-BuLi, 1,5 equivalentes de Mel y d Cm . Escala: 0,9 mmol. Purificación mediante cromatografía en gel de sílice (DCM/MeOH=99/1 a 90/10). Rendimiento: 18 %. Aceite amarillo.
[0185] RMN 1H (300 MHz, DMSO) 58,54 - 8,48 (m, 1H), 7,80 (td, J = 7,7, 1,8 Hz, 1H), 7,44 (d, J = 7,8 Hz, 1H), 7,28 (dd, J = 6,7, 5,1 Hz, 1H), 4,56 (s, 2H), 3,59 (t, J = 6,1 Hz, 2H), 2,65 (t, J = 6,1 Hz, 2H), 2,38 (s, 3H), 2,28 (s, 3H), 1,37 (s, 6H).
[0186] ESI- HRMS calculado para C16H23N2O2S [M+H]+: 3071475, encontrado: 307,1471.
Ejemplo 11: 4-metil-4-[metil-[2-(2-piridilmetoxi)etil]amino]pent-2-intioato de S-metilo
[0187] Preparación de N-2-dimetil-N-[2-(2-piridilmetoxi)etil]but-3-in-2-amina: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina [ejemplo 2] empezando a partir de bromhidrato de 3-(bromometil)piridina y utilizando 4 equivalentes de NaH. Purificación mediante cromatografía en gel de sílice (DCM/MeOH=99/1 a 95/5). Escala: 2,1 mmol. Rendimiento: 67 %. Aceite amarillo.
[0188] RMN 1H (300 MHz, DMSO) 58,56 - 8,52 (m, 1H), 8,49 (dd, J = 4,8, 1,7 Hz, 1H), 7,78 - 7,70 (m, 1H), 7,38 (ddd, J = 7,8, 4,8, 0,8 Hz, 1H), 4,52 (s, 2H), 3,52 (t, J = 6,2 Hz, 2H), 3,12 (s, 1H), 2,58 (t, J = 6,2 Hz, 2H), 2,21 (s, 3H), 1,27 (s, 6H).
[0189] ESI-LRMS 233,1 [M+H]+.
[0190] Preparación de 4-metil-4-[metil-[2-(3-piridilmetoxi)etil]amino]pent-2-intioato de S-metilo: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo [ejemplo 1] empezando a partir de N-2-dimetil-N-[2-(3-piridilmetoxi)etil]but-3-in-2-amina y utilizando 1.5 equivalentes de extracciones de n-BuLi, 1,5 equivalentes de Mel y d Cm . Escala: 0,4 mmol. Purificación mediante cromatografía en gel de sílice (DCM/MeOH=99/1 a 95/5). Rendimiento: 15 %. Aceite amarillo.
[0191] RMN 1H (300 MHz, DMSO) 58,54 (d, J = 1,5 Hz, 1H), 8,49 (dd, J = 4,8, 1,7 Hz, 1H), 7,78 - 7,70 (m, 1H), 7,38 (ddd, J = 7,8, 4,8, 0,8 Hz, 1H), 4,53 (s, 2H), 3,54 (t, J = 6,1 Hz, 2H), 2,63 (t, J = 6,1 Hz, 2H), 2,38 (s, 3H), 2,26 (s, 3H), 1,36 (s, 6H).
[0192] ESI- HRMS calculado para C16H23N2O2S [M+H]+: 3071475, encontrado: 307,1474.
Ejemplo 12: 4-metil-4-[metil-[2-(4-piridilmetoxi)etil]amino]pent-2-intioato de S-metilo
[0193] Preparación de N-2-dimetil-N-[2-(4-piridilmetoxi)etil]but-3-in-2-amina: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina [ejemplo 2] empezando a partir de bromhidrato de 4-(bromometil)piridina y utilizando 4 equivalentes de NaH. Purificación mediante cromatografía en gel de sílice (DCM/MeOH=99/1 a 95/5). Escala: 2,1 mmol. Rendimiento: 95 %. Aceite amarillo.
[0194] RMN 1H (300 MHz, DMSO) 58,56 - 8,49 (m, 2H), 7,38 - 7,27 (m, 2H), 4,54 (s, 2H), 3,53 (t, J = 6,2 Hz, 2H), 3,13 (s, 1H), 2,61 (t, J = 6,2 Hz, 2H), 2,23 (s, 3H), 1,28 (s, 6H). ESI-LRMS 233,1 [M+H]+.
[0195] Preparación de 4-metil-4-[metil-[2-(4-piridilmetoxi)etil]amino]pent-2-intioato de S-metilo: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo [ejemplo 1] empezando a partir de N-2-dimetil-N-[2-(4-piridilmetoxi)etil]but-3-in-2-amina y utilizando 1.5 equivalentes de n-BuLi, 1,5 equivalentes de Mel y extracciones con DCM. Escala: 1,0 mmol. Purificación mediante cromatografía en gel de sílice (DCM/MeOH=99/1 a 95/15). Rendimiento: 24 %. Aceite amarillo.
[0196] RMN 1H (300 MHz, DMSO) 58,60 - 8,45 (m, 2H), 7,37 - 7,26 (m, 2H), 4,55 (s, 2H), 3,56 (t, J = 6,0 Hz, 2H), 2,65 (t, J = 6,0 Hz, 2H), 2,38 (s, 3H), 2,28 (s, 3H), 1,37 (s, 6H).
[0197] ESI- HRMS calculado para C16H23N2O2S [M+H]+: 3071475, encontrado: 307,1470.
Ejemplo 13: 4-(dimetilamino)-4-metil-pent-2-inoato de metilo (no forma parte de la presente invención)
[0198] Preparación de clorhidrato de ácido 4-(dimetilamino)-4-metil-pent-2-inoico: A N,N,2-trimetilbut-3-in-2-amina (0,928 g, 8,35 mmol) en THF (42 ml) se añadió gota a gota una solución de n-BuLi 2,35 M en hexano (3,73 ml, 8,76 mmol) a -70 °C. Después de 5 minutos a -70 °C, la mezcla de reacción se calentó hasta 0 °C, se mantuvo 10 minutos a esta temperatura, a continuación, se enfrió a -70 °C antes de burbujear durante 45 minutos con dióxido de carbono. La mezcla se calentó a 0 °C dentro de 2 horas, a continuación, se hidrolizó con precaución a 0 °C con agua y se lavó (2x 25 ml) con éter. Las capas acuosas se acidificaron (pH 1-2) con HCI 6 N, a continuación, se concentraron al vacío. El sólido obtenido se trituró y se lavó dos veces con MeOH. El clorhidrato de ácido 4-(dimetilamino)-4-metilpent-2-inoico en bruto (0,721 g, 45 %) obtenido como un sólido blanco se utilizó en la siguiente etapa sin purificación.
[0199] RMN 1H (300 MHz, D2O) 2,94 (s, 6H), 1,70 (s, 6H). 13C RMN (75 MHz, D2O) 5158,97 (C), 83,64 (C), 76,05 (C), 60,35 (C), 38,46 (2 CH3), 23,66 (2 CH3).
[0200] Preparación de 4-(dimetilamino)-4-metil-pent-2-inoato de metilo: Se trató clorhidrato de ácido 4-(dimetilamino)-4-metil-pent-2-inoico (0,500 g, 2,61 mmol) en MeOH (10 ml) con H2SO4 concentrado (0,15 ml) a 0 °C, a continuación, se agitó durante la noche a temperatura ambiente. Después de la concentración al vacío el residuo se diluyó en AcOEt. La capa orgánica se lavó con una solución NaHCO3 y solución acuosa saturada de cloruro sódico, se secó sobre Na2SO4 y el disolvente se evaporó al vacío para generar (rendimiento <10 %, no optimizado) al éster de metilo como un aceite casi incoloro.
[0201] RMN 1H (300 MHz, DMSO) 83,71 (s, 3H), 2,19 (s, 6 H), 1,35 (s, 6 H).
[0202] ESI-LRMS [M+H]+ calculado para C9H15NO2 [M+H]+: 170,11, encontrado: 170,1.
Ejemplo 14: 4-(dimetilamino)-4-metil-pent-2-inoato de etilo (no forma parte de la presente invención):
[0203] El compuesto se obtiene mediante el mismo procedimiento que el que se describe en el ejemplo 13 utilizando EtOH en la etapa de esterificación. Escala 5,22 mmol. Rendimiento: 73 %. Aceite incoloro.
[0204] RMN 1H (300 MHz, DMSO) 84,17 (q, J = 7,1 Hz, 2H), 2,19 (s, 6 H), 1,34 (s, 6 H), 1,22 (t, J = 7,1 Hz, 3H).
[0205] ESI- HRMS calculado para C10H18NO2 [M+H]+: 184,1332, encontrado: 184,1326.
Ejemplo 15: 2-((4-(dimetilamino)-4-metilpent-2-inil)tio)acetato de terc-butilo (no forma parte de la presnte invención):
[0206] El compuesto se obtuvo utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo [ejemplo 1] empezando a partir de N,N,2-trimetilbut-3-in-2-amina y utilizando yodoacetato de terc-butilo en lugar de yodometano. Purificación mediante cromatografía en gel de sílice (ciclohexano/EtOAc=70/30). Escala 3 mmol. Rendimiento: 57 %. Aceite rojo.
[0207] RMN 1H (300MHz, DMSO) 83,82 (s, 2H), 2,21 (s, 6 H), 1,41 (s, 9H), 1,37 (s, 6 H).
[0208] ESI- HRMS: calculado para C14H24NO3S [M+H]+: 286,1471, encontrado: 286,1472.
Ejemplo 16: Ácido 2-((4-(dimetilamino)-4-metilpent-2-inil)tio)acético (no forma parte de la presente invención)
[0209] A una solución de 2-((4-(dimetilamino)-4-metilpent-2-inil)tio)acetato de terc-butilo (200 mg, 0,7 mmol) en diclorometano (3,6 ml) se añade ácido trifluoroacético (0,36 ml). La mezcla se agita durante la noche en oscuridad. Después de la evaporación bajo presión reducida, el producto en bruto se trituró y se lavó con Et2O. Se obtuvo la sal de TFA como un sólido amorfo. Rendimiento: 84 %.
[0210] RMN 1H (300MHz, acetona) 8 12,14 (s, 1H), 3,95 (s, 2H), 2,99 (s, 6 H), 1,87 (s, 6 H).
[0211] ESI- HRMS: calculado para C10H16NO3S [M+H]+ 230,0845, encontrado: 230,0847.
Ejemplo 17: 4-((4-(benciloxi)butil)(metil)amino)-4-metilpent-2-intioato de S-metilo
[0212] Preparación de 4-(metil(2-metilbut-3-in-2-il)amino)butan-1-ol: Este compuesto se preparó mediante los protocolos estándares descritos previamente para la síntesis de N-metil-N-(2'hidroxietil)-3-amino-3-metil-1-butino (Easton, Nelson R.; Hennion, George F. EE. UU. (1967), patentes de Estados Unidos 3337625 19670822) empezando a partir de 4-(metil-amino)butan-1-ol comercialmente disponible. Se obtuvo 4-(metil(2-metilbut-3-in-2-il)amino)butan-1 -ol como un aceite amarillo claro. Escala 3 mmol. Rendimiento: 99 %.
[0213] RMN 1H (300MHz, DMSO) 84,41 (t, J = 5,2Hz, 1H), 3,42 -3,33 (m, 2H), 3,09 (s, 1H), 2,38 -2,29 (m, 2H), 2,14 (s, 3H), 1,45 - 1,36 (m, 4H), 1,27 (s, 6H).
[0214] ESI - LRMS: 170,1 [M+H]+
[0215] Preparación de N-(4-benciloxil)butil)-N,2-dimetilbut-3-in-2-amina: El compuesto se obtuvo utilizando el mismo procedimiento que el que se describe para N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina [ejemplo 2] empezando a partir de 4-(metil(2-metilbut-3-in-2-il)amino)butan-1-ol y utilizando 1,015 equivalentes de NaH y 1,01 equivalentes de bromuro de bencilo. Purificación mediante cromatografía en gel de sílice (ciclohexano/EtOAc=80/20). Escala 2,4 mmol. Rendimiento: 55 %. Aceite amarillo.
[0216] RMN 1H (300 MHz, DMSO) 87,39 - 7,22 (m, 5H), 4,44 (s, 2H), 3,42 (t, J = 6,3 Hz, 2H), 3,08 (s, 1H), 2,34 (t, J = 6,9Hz, 2H), 2,13 (s, 3H), 1,60 - 1,37 (m, 4H), 1,26 (s, 6H).
[0217] ESI - LRMS: 260,2 [M+H]+
[0218] Preparación de 4-((4-(benciloxi)butil)(metil)amino)-4-metilpent-2-intioato de S-metilo: El compuesto se obtuvo utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent- 2-intioato de S-metilo [ejemplo 1] empezando a partir de N-(4-benciloxibutil)-N,2-dimetil-but-3-in-2-amina. Purificación mediante cromatografía en gel de sílice (ciclohexano/EtOAc=90/10). Escala 0,77 mmol. Rendimiento: 80 %. Aceite amarillo.
[0219] RMN 1H (300MHz, CDCl3) 87,38 - 7,19 (m, 5H), 4,48 (s, 2H), 3,47 (t, J = 6,1 Hz, 2H), 2,45 (t, J = 6,9Hz, 2H), 2,35 (s, 3H), 2,26 (s, 3H), 1,73 - 1,48 (m, 4H), 1,39 (s, 6 H).
[0220] ESI- HRMS: calculado para C19H28NO2S [M+H]+ 334,1835, encontrado: 334,1840.
Ejemplo 18: 4-((2-hidroxietil)(metil)amino)-4-metilpent-2-intioato de S-metilo
a) véanse Easton, Nelson R.; Hennion, George F., EE. UU. (1966), patente de Estados Unidos 3285913 b) 3,4-DHP, pTSA, DCM (70 %) c) nBuLi, THF, -70 °C, sulfuro de carbonilo, a continuación, Mel 0 °C (59 %) d) pTSA, MeOH, temperatura ambiente (90 %)
[0222] Preparación del Compuesto 3: N,2-dimetil-N-(2-((tetrahidro-2H-piran-2-il)oxi)etil)but-3-in-2-amina: A 2-(metil(2-metilbut-3-in-2-il)amino)etanol 2 (3,00 g, 21,2 mmol) y 3,4-dihidro-2H-pirano (5,0 equivalentes) en DCM anhidro (135 ml) se añadió ácido p-toluenosulfónico (0,1 equivalentes) a temperatura ambiente. La mezcla de reacción se agitó durante la noche, se lavó con una disolución acuosa saturada de NaHcO3 (30 ml), a continuación, con solución acuosa saturada de cloruro sódico (30 ml). La capa orgánica se secó sobre sulfato de sodio, se filtró y se concentró al vacío. En primer lugar, el residuo se purificó mediante destilación de vía corta utilizando el aparato de Kugelrohr (10 12 Torrs, horno 155 °C), a continuación, mediante cromatografía “flash” en gel de sílice (éter de petróleo/acetato de etilo 95/5 a 60/40) para generar el compuesto 3 como un aceite (rendimiento del 70 %).
[0223] RMN 1H (300 MHz, DMSO) 84,60 -4,50 (m, 1H), 3,82-3,70 (m, 1H), 3,59-3,56 (m, 1H), 3,49 -3,35 (m, 2H), 3,12 (s, 1H), 2,55 (t, J = 6,5 Hz, 2H), 2,21 (s, 3H), 1,77 - 1,35 (m, 6 H), 1,27 (s, 6 H).
[0224] Preparación del Compuesto 4: 4-metil-4-(metil(2-((tetrahidro-2H-piran-2-il)oxi) etil) amino) pent-2-intioato de S-metilo: A la amina acetilénica 3 (1,00 g, 4,44 mmol) en THF anhidro (22 ml) se añadió gota a gota una solución de n-butil litio (2,2 M en hexanos, 1,5 equivalentes). Se dejó que la mezcla alcanzara 0 °C en un periodo de 10 minutos, a continuación, se volvió a enfriar hasta - 70 °C antes del burbujeo con sulfuro de carbonilo. Después de 30 minutos, la solución amarilla brllante se calentó con precaución hasta 0 °C, se agitó durante 30 minutos a esta temperatura y se añadió gota a gota yoduro de etilo (1,2 equivalentes). La mezcla de reacción se agitó durante 2 horas a 0 °C antes de la hidrólisis mediante agua. El tratamiento final de extracción mediante DCM (lavado con solución acuosa saturada de cloruro sódico, secado con sulfato de sodio y concentración bajo presión reducida) produjo un producto en bruto que se purificó mediante cromatografía en gel de sílice (éter de petróleo/acetato de etilo 90/10 a 60/40) para generar el compuesto 4 como un aceite (rendimiento del 59 %).
[0225] RMN 1H (300 MHz, DMSO) 84,58 (t, J = 3,2 Hz, 1H), 3,75 (ddd, J= 11,4, 7,9, 3,3 Hz, 1H), 3,70 - 3,60 (m, 1H), 3,49 - 3,38 (m, 2H), 2,59 (t, J = 6,3 Hz, 2H), 2,39 (s, 3H), 2,27 (s, 3H), 1,77 - 1,39 (m, 6 H), 1,36 (s, 6 H). RMN 13C (75 MHz, CDCla) 8 176,62 (C=O), 98,94 (CH), 96,46 (C), 80,97 (C), 66,55 (CH2), 62,37 (CH2), 55,19 (C), 52,43 (CH2), 37,92 (CH3), 30,75 (CH2), 28,01(2xCHa), 25,59 (CH2), 19,63 (CH2), 12,61 (CH3).
[0226] Preparación del Compuesto 5: 4-((2-hidroxietil)(metil)amino)-4-metilpent-2-intioato de S-metilo: Al aminotioléster 4 (1,00 g, 3,34 mmol) en metanol (15 ml) se añadió ácido p-toluenosulfónico (1,1 equivalentes) a temperatura ambiente. La mezcla de reacción se agitó durante la noche, se lavó con una solución acuosa saturada de NaHCO3 (30 ml), a continuación, con solución acuosa saturada de cloruro sódico (30 ml). La capa orgánica se secó sobre sulfato de sodio, se filtró y se concentró al vacío. El residuo se purificó mediante cromatografía en gel de sílice (éter de petróleo/acetato de etilo 80/20 a 20/80) para generar el compuesto 5 como un aceite (rendimiento del 90 %).
[0227] RMN 1H (300 MHz, DMSO) 54,42 (t, J = 5,6 Hz, 1H), 3,44 (td, J = 6,7, 5,6 Hz, 2H), 2,46 (, J = 6,7 Hz, 2H), 2,39 (s, 3H), 2,24 (s, 3H), 1,36 (s, 6H). 13C RMN (75 MHz, CDCI3) 5176,46 (C=O), 95,56 (C), 80,89 (C), 58,92 (CH2), 54,99 (C) , 53,52 (CH2), 36,12 (CH3), 27,88 (2xCH3), 12,53(CH3). ESI-HRMS: Calculado para C10H18 NO2S [M+H]+, 216,1053 encontrado 216,1043.
Ejemplo 19. 4-metil-4-[metil-[2-(2-naftilmetoxi)etil]amino]pent-2-intioato de S-metilo
[0228] Preparación de N,2-dimetil-N-[2-(2-naftilmetoxi)etil]but-3-in-2-amina: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina [ejemplo 2] utilizando 1,015 equivalentes de NaH y 1,01 equivalentes de bromuro de 2-naftilo. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=90/10). Rendimiento: 61 %. Aceite naranja.
[0229] RMN 1H (300 MHz, DMSO) 57,91 - 7,88 (m, 4H), 7,50 - 7,48 (m, 3H), 4,65 (s, 2H), 3,55 (t, 6,1Hz, 2H), 3,13 (s, 1H), 2,62 (t, 6,2Hz, 2H), 2,23 (s, 3H), 1,28 (s, 6H).
[0230] Preparación de 4-metil-4-[metil-[2-(2-naftilmetoxi)etil]amino]pent -2-intioato de S-metilo: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo [ejemplo 1] empezando a partir de N,2-dimetil-N-[2-(2-naftilmetoxi)etil]but-3-in-2-amina. Escala: 0,65 mmol. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc = 85/15). Rendimiento: 28 %. Aceite amarillo.
[0231] RMN 1H (300 MHz, DMSO) 57,95 - 7,82 (m, 4H), 7,55 - 7,41 (m, 3H), 4,66 (s, 2H), 3,57 (t, J = 6,2Hz, 2H), 2,66 (t, J = 6,1 Hz, 2H), 2,38 (s, 3H), 2,28 (s, 3H), 1,37 (s, 6H).
[0232] ESI- HRMS calculado para C21H26NO2S 356,1683, encontrado 356,1679 [M+H]+
Ejemplo 20: 4-metil-4-[metil-[2-[(2,6,6-trimetilciclohexen-1-il)metoxi]etil]amino]pent-2-intioato de S-metilo [0233] Preparación de N,2-dimetil-N-[2[(2,6, 6-trimetilciclohexen-1-il)-metoxi]etil]but-3-in-2-amina: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina [ejemplo 2] utilizando 1,015 equivalentes de NaH y 1,01 equivalentes de 2-(bromometil)-1,3,3-trimetil-1-ciclohexeno (preparado a partir de p-ciclocitral mediante protocolos conocidos (documento WO 2015048363)). Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=95/05). Rendimiento: 67 %. Aceite amarillo pálido.
[0234] 3,86 (s, 2H), 3,41 (t, J = 6,5Hz, 2H), 3,12 (s, 1H), 2,53 (t, J = 6,4Hz, 2H), 2,20 (s, 3H), 1,90 (t, J = 5,9Hz, 2H), 1,62 (s, 3H), 1,57 - 1,49 (m, 2H), 1,41 -1,33 (s, 2H), 1,27 (s, 6H), 0,97 (s, 6H).
[0235] Preparación de 4-metil-4-[metil-[2-[(2,6,6-trimetilciclohexen-1-il)metoxi]etil]-amino]pent-2-intioato de S-metilo: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo [ejemplo 19] empezando a partir de N,2-dimetil-N-[2-[(2,6,6-trimetilciclohexen-1-il)metoxi]etil]but-3-in-2-amina. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=90/10). Rendimiento: 63 %. Aceite amarillo.
[0236] RMN 1H (300 MHz, DMSO) 53,87 (s, 2H), 3,44 (t, J = 6,3 Hz, 2H), 2,57 (t, J = 6,3 Hz, 2H), 2,38 (s, 3H), 2,26 (s, 3H), 1,91 (t, J = 6,2 Hz, 2H), 1,62 (s, 3H), 1,57 - 1,49 (m, 2H), 1,36 (s, 6H), 1,39 - 1,34 (m, 2H), 0,97 (s, 6H).
[0237] ESI- HRMS calculado para C20H34NO2S [M+H]+: 352,2305, encontrado: 352,2289.
[0238] Ejemplo 21: Acetato de 2-[(1,1-dimetil-4-metilsulfanil-4-oxo-but-2-inil)-metilamino] etilo:
[0239] A 4-[2-hidroxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo (100 mg, 0,46 mmol) y diisopropiletilamina (1,2 equivalentes) en diclorometano (2,3 ml) se añadió gota a gota cloruro de acetilo (1,2 equivalentes) a 0 °C. Después de 10 minutos a 0 °C, la mezcla de reacción se calentó hasta temperatura ambiente y se agitó hasta su completa conversión (control mediante CCF). A continuación, la mezcla se diluyó en diclorometano (30 ml), se lavó con solución acuosa saturada de cloruro sódico (40 ml), se secó sobre sulfato de sodio y el disolvente se evaporó bajo presión reducida. El producto en bruto se purificó mediante cromatografía en gel de sílice (éter de petróleo/acetato de etilo 75/25) para generar el producto 21 como un aceite amarillo. Rendimiento 58 %.
[0240] RMN 1H (300MHz, DMSO) 54,05 (t, J = 6,1Hz, 2H), 2,62 (t, J = 6,1Hz, 2H), 2,39 (s, 3H), 2,26 (s, 3H), 2,01 (s,3H), 1,36 (s, 6H).
[0241] ESI- HRMS calculado para C12H19NO3S [M+H]+: 258,1086, encontrado: 258,1150.
Ejemplo 22: 2-[(1,1-dimetil-4-metilsulfanil-4-oxo-but-2-inil)-metilamino]etil-3,4-dimetoxibenzoato:
[0242] El compuesto se obtiene mediante el mismo procedimiento que el que se describe para el acetato de 2-[(1,1-dimetil-4-metilsulfanil-4-oxo-but-2-inil)-metilamino]etilo [ejemplo 21] empezando a partir de cloruro de 3,4-dimetoxibenzoílo. Escala: 0,46 mmol. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=60/40). Rendimiento: < 10 %. Aceite amarillo.
[0243] RMN 1H (300 MHz, DMSO) 87,59 (dd, J = 8,4, 2,0Hz, 1H), 7,45 (d, J = 2,0Hz, 1H), 7,08 (d,J = 8,5Hz, 1H), 4,28 (t, J = 7,1Hz, 2H), 3,83 (s, 3H), 3,80 (s, 3H), 2,72 (t, J = 7,1Hz, 2H), 2,38(s, 3H), 2,33 (s, 3H), 1,39 (s, 6 H). Ejemplo 23: 2,5,10,11,11-pentametil-6-oxo-7-oxa-2,5,10-triazatetradec-12-ine-14-tioato de S-metilo
[0244] El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para 4-metil-4-[metil-[2-[metil-[2-(metilamino)etil]carbamoil]oxietil]amino]pent-2-intioato [compuesto 7/Ejemplo 29] empezando a partir de N,N,N'-trimetiletilenediamina. Purificación mediante cromatografía en gel de sílice DCM/MeOH (85/15). Rendimiento: 34 %. Aceite amarillo. RMN 1H (300 MHz, DMSO) 84,01 (t, J = 5,9Hz, 2H), 3,32-3,25 (m, 2H), 2,83 (s grande, 3H), 2,62 (t, J = 5,8Hz, 2H), 2,6-2,5 (m parcialmente oculto por el pico del disolvente, 2H), 2,39 (s, 3H), 2,27 (s,3H), 2,17 (s grande, 6 H), 1,36 (s, 6 H).
[0245] ESI- HRMS calculado para C16H30N3O3S [M+H]+: 344,1992, encontrado: 344,1993.
Ejemplo 24: 4-(2-(metoximetil)pirrolidin-1-il)-4-metilpent-2-intioato de (S)-S-metilo
[0246] Preparación de (S)-2-(metoximetil)-1-(2-metilbut-3-in-2-il)pirrolidina: El compuesto se obtuvo utilizando el mismo procedimiento que el que se describe para N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina [ejemplo 2] utilizando 1 equivalente de NaH y 1,01 equivalentes de yodometano. Purificación mediante cromatografía en gel de sílice (diclorometano/metanol=90/10). Escala 3,0 mmol. Rendimiento: 61 %. Aceite naranja. RMN 1H (300 MHz, DMSO) 8 3,23 (s, 3H), 3,16 -3,06 (m, 2H), 3,05 (s, 1H), 3,03 -2,91 (m, 1H), 2,91 -2,80 (m, 1H), 2,67 -2,54 (m, 1H), 1,77 -1,49 (m, 4H), 1,30 (s, 3H), 1,24 (s, 3H).
[0247] ESI - LRMS: 182,2 [M+H]+.
[0248] Preparación de 4-(2-(metoximetil)pirrolidin-1-il)-4-metilpent-2-intioato de (S)-S-metilo: El compuesto se obtiene utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo [ejemplo 1 ] empezando a partir de (S)-2-(metoximetil)-1-(2-metilbut-3-in-2-il)pirrolidina. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=80/20). Escala 0,8 mmol. Rendimiento: 57 %. Aceite amarillo.
[0249] RMN 1H (300 MHz, DMSO) 83,24 (s, 3H), 3,19 - 2,89 (m, 4H), 2,67 -2,53 (m, 1H), 2,38 (s, 3H), 1,83 - 1,50 (m, 4H), 1,39 (s, 3H), 1,33 (s, 3H).
[0250] ESI- HRMS calculado para C13H22NO2S [M+H]+: 256,1366, encontrado: 256,1363.
Ejemplo 25: 4-[(3R)-3-metoxipirrolidin-1-il]-4-metil-pent-2-intioato de S-metilo
[0251] Preparación de (R)-3-metoxi-1-(2-metilbut-3-in-2-il)pirrolidina: El compuesto se obtuvo utilizando el mismo procedimiento que el que se describe para N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina [ejemplo 2] empezando a partir de (R)-1-(2-metilbut-3-in-2-il)pirrolidin-3-ol utilizando 1,015 equivalentes de NaH y 1,01 equivalentes de yodometano. Purificación mediante cromatografía en gel de sílice (diclorometano/metanol=90/10). Escala 3,3 mmol. Rendimiento: 30 %. Aceite amarillo.
[0252] RMN 1H (300 MHz, DMSO) 83,85 (ddd, J = 10,8, 7,2, 3,6 Hz, 1H), 3,17 (s, 3H), 3,13 (s, 1H) 2,82 (dd, J = 9,8, 6,5 Hz, 1H), 2,66 - 2,60 (m, 1H), 2,56 - 2,50 (m, 2H), 2,01 - 1,87 (m, 1H), 1,73 - 1,55 (m, 1H), 1,28 (s, 6H).
[0253] ESI - LRMS: 168,0 [M+H]+.
[0254] Preparación de 4-(3-metoxipirrolidin-1-il)-4-metilpent-2-intioato de (R)-S-metilo: El compuesto se obtuvo utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo [ejemplo 1] empezando a partir de (R)-3-metoxi-1-(2-metilbut-3-in-2-il)pirrolidina. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc=60/40). Escala 0,8 mmol. Rendimiento: 55 %. Aceite amarillo.
[0255] RMN 1H (300 MHz, DMSO) 83,87 (ddd, J = 10,5, 6,9, 3,4 Hz, 1H), 3,18 (s, 3H), 2,90 -2,76 (m, 1H), 2,77 -2,65 (m, 1H), 2,65 - 2,54 (m, 2H), 2,38 (s, 3H), 2,07 - 1,86 (m, 1H), 1,76 - 1,60 (m, 1H), 1,36 (s, 6H).
Ejemplo 26: 4-(((1R,2R)-2-(benciloxi)ciclopentil)(metil)amino)-4-metilpent-2-intioato de S-metilo
[0256] Preparación de (1R, 2R)-2-benciloxi-N-(1,1-dimetilprop-2-inil)ciclopentanamina: A una solución de (1R,2R)-2-(benciloxi)ciclopentanamina (0,93 g, 4,86 mmol), 3-cloro-3-metilbut-1-ino (1,3 equivalentes) y trietilamina
(1,3 equivalentes) disponibles comercialmente en THF (20 ml) se añadió Cul (8 % molar) a temperatura ambiente. La mezcla se agitó durante la noche. El disolvente se evaporó bajo presión reducida y a continuación, el producto en bruto se diluyó en solución acuosa saturada de NaHCÜ3, se extrajo con acetato de etilo. Las capas orgánicas se lavaron con una solución acuosa al 2 % de NH4OH, a continuación, con una solución acuosa saturada de cloruro sódico, se secaron sobre Na2SO4 y el disolvente se evaporó bajo presión reducida. Se obtuvo (1R, 2R)-2-benciloxi-N-(1,1-dimetilprop-2-inil)ciclopentanamina como un aceite marrón. Rendimiento: 99 %.
[0257] RMN 1H (300 MHz, DMSO) 87,37 - 7,16 (m, 5H), 4,56-4,36 (m, 2H), 3,72 -3,58 (m, 1H), 3,28 - 3,19 (m, 1H), 3,08 (s, 1H), 2,00 - 1,88 (m, 1H), 1,86- 1,67 (m, 2H), 1,65- 1,49 (m, 3H), 1,40 - 1,28 (m, 1H), 1,25 (s, 3H), 1,25 (s, 3H).
[0258] Preparación de (1R, 2R)-2-(benciloxi)-N-metil-N-(2-metilbut-3-in-2-il)ciclopentanamina: A (1R,2R)-2-(benciloxi)-N-(2-metilbut-3-in-2-il)ciclopentanamina (0,25 g, 0,97 mmol) se añadieron 5 equivalentes de ácido fórmico y 1,5 equivalentes de formaldehído (37 % en agua). La mezcla se puso a reflujo durante la noche, a continuación, se añadió HCI 2 N hasta que se alcanzó pH 1 y se lavó con éter. La capa acuosa se basificó con NaOH 1 N y se extrajo con DCM. La capa orgánica se lavó con una solución acuosa saturada de cloruro sódico, se secó sobre Na2SO4 y los disolventes se evaporaron bajo presión reducida. A continuación, el producto en bruto se purificó mediante cromatografía en gel de sílice (éter de petróleo/ EtOAc = 80/20) para generar como un aceite amarillo. Rendimiento: 68 %.
[0259] RMN 1H (300 MHz, DMSO) 87,43 -7,17 (m, 5H), 4,52 (m, 2H), 3,94 -3,78 (m, 1H), 3,62 -3,49 (m, 1H), 3,11 (s, 1H), 2,20 (s, 3H), 1,78 - 1,45 (m, 6H), 1,37 (s, 3H), 1,34 (s, 3H). ESI-LRMS: 272,1 [M+H]+.
[0260] Preparación de 4-(((1R,2R)-2-(benciloxi)cidopentil)(metil)amino)-4-metilpent-2-intioato de S-metilo: El compuesto se obtuvo utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metilpent- 2-intioato de S-metilo [ejemplo 1] empezando a partir de (1R, 2R)-2-(benciloxi)-N-metil-N-(2-metil-but-3-in-2-il)-ciclopentanamina. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc = 80/20, a continuación, DCM = 100). Escala 0,64 mmol. Rendimiento: 47 %. Aceite amarillo.
[0261] RMN 1H (300 MHz, DMSO) 87,35 - 7,20 (m, 5H), 4,51 (s, 2H), 3,92 - 3,80 (m, 1H), 3,59 - 3,45 (m, 1H), 2,36 (s, 3H), 2,24 (s, 3H), 1,78 - 1,49 (m, 6H), 1,45 (s, 3H), 1,42 (s, 3H). ESI- HRMS calculado para C29H23NO2S [M+H]+: 346,1835 encontrado: 346,1824.
Ejemplo 27: 4-(2-((benciloxi)metil)pirrolidin-1-il)-4-metilpent-2-intioato de (S)-S-metilo:
[0262] Preparación de (S)-2-(benciloxi)metil)-1-(2-metilbut-3-in-2-il)pirrolidina: El compuesto se obtuvo utilizando el mismo procedimiento que el que se describe para N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina [ejemplo 2] empezando a partir de (S)-(1-(2-metilbut-3-in-2-il)pirrolidin-2-il)metanol utilizando 1,015 equivalentes de NaH y 1,01 equivalentes de bromuro de bencilo. Purificación mediante cromatografía en gel de sílice (diclorometano/metanol = 95/5). Escala 3,0 mmol. Rendimiento: 60 %. Aceite naranja.
[0263] RMN 1H (300 MHz, DMSO) 87,41 - 7,19 (m, 5H), 4,46 (s, 2H), 3,24 (dd, J = 8,3, 2,7 Hz, 1H), 3,14 (dd, J = 7,6, 3,2 Hz, 1H), 3,11 - 3,02 (m, 2H), 2,86 (dd, J = 8,4, 6,0 Hz, 1H), 2,65 -2,54 (m, 1H), 1,81 - 1,51 (m, 4H), 1,25 (s, 3H), 1,23 (s, 3H).
[0264] ESI - LRMS: 258,1 [M+H]+.
[0265] Preparación de 4-(2-((benciloxi)metil)pirrolidin-1-il) -4-metilpent-2-intioato de (S)-S-metilo: El compuesto se obtuvo utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent- 2-intioato de S-metilo [ejemplo 1] empezando a partir de (S)-2-((benciloxi)metil)-1-(2-metilbut-3-in-2-il)pirrolidina. Purificación mediante cromatografía en gel de sílice (éter de petróleo/EtOAc = 80/20). Escala 1,2 mmol. Rendimiento: 50 %. Aceite naranja.
[0266] RMN 1H (300 MHz, DMSO) 87,46 - 7,18 (m, 5H), 4,47 (s, 2H), 3,29 - 3,23 (m, 1H), 3,17 - 3,03 (m, 2H), 2,94 (dd, J = 8,5, 5,7 Hz, 1H), 2,62 -2,53 (m, 1H), 2,38 (s, 3H), 1,85 - 1,58 (m, 4H), 1,34 (s, 3H), 1,32 (s, 3H).
Ejemplo 28: 4-(3-(benciloxi)pirrolidin-1-il)-4-metilpent-2-intioato de (R)-S-metilo:
[0267] Preparación de (R)-3-(benciloxi)-1-(2-metilbut-3-in-2-il)pirrolidina: El compuesto se obtuvo utilizando el mismo procedimiento que el que se describe para N-(2-aliloxietil)-N,2-dimetil-but-3-in-2-amina [ejemplo 2] empezando a partir de (R)-1-(2-metilbut-3-in-2-il)pirrolidin-3-ol utilizando 1,01 equivalentes de NaH y 1,01 equivalentes de bromuro de bencilo. Purificación mediante cromatografía en gel de sílice (diclorometano/metanol = 98/2). Escala 3,3 mmol. Rendimiento: 69 %. Aceite naranja.
[0268] RMN 1H (300 MHz, DMSO) 87,40 - 7,17 (m, 5H), 4,42 (s, 2H), 4,07 (tt, J = 7,3, 3,7Hz, 1H) 3,13 (s, 1H), 2,86 (dd, J = 9,6, 6,7 Hz, 1H), 2,75 -2,65 (m, 2H), 2,60 -2,53 (m, 1H), 2,06 - 1,95 (m, 1H), 1,75 - 1,65 (m, 1H), 1,29 (s, 6H).
[0269] ESI-LRMS 244,1 [M+H]+.
[0270] Preparación de 4-(3-(benciloxi)pirrolidin-1-il)-4-metilpent-2-intioato de (R)-S-metilo: El compuesto se obtuvo utilizando el mismo procedimiento que el que se describe para 4-[2-etoxietil(metil)amino]-4-metil-pent- 2-intioato de S-metilo [ejemplo 1] empezando a partir de (R)-3-(benciloxi)-1-(2-metilbut-3-in-2-il)pirrolidina. Purificación mediante cromatografía en gel de sílice (diclorometano/metanol = 98/2). Escala 1,2 mmol. Rendimiento: 69 %. Aceite naranja.
[0271] RMN 1H (300 MHz, DMSO) 87,32 (m, 5H), 4,44 (s, 2H), 4,09 (dq, J = 10,2, 3,5 Hz, 1H), 2,97 - 2,83 (m, 1H), 2,80 -2,65 (m, 2H), 2,65 -2,55 (m, 1H), 2,37 (s, 3H), 2,11 -1,90 (m, 1H), 1,83 - 1,67 (m, 1H), 1,37 (s, 6 H).
[0272] ESI- HRMS calculado para C18H24NO2S [M+H]+: 318,1522, encontrado: 318,1518.
Ejemplo 29: Compuesto ADC (sin anticuerpo)
[0273] Preparación de un enlazador (Mc-Val-Cit-PAB-PNP): El enlazador seleccionado para la preparación de conjugado se diseñó sobre una plataforma conocida y ya utilizada en Rituximab y otros, que comprende la maleimida para el acoplamiento al Anticuerpo, el grupo escindible de Catepsina y el sistema de p-amino bencilo para la eliminación 1,6: Mc-Val-Cit-PAB-PNP, CAS 159857-81-5.
[0274] Se preparó utilizando los protocolos estándares empezando a partir de Fmoc-Val-OSu [CAS 3392-12-9] o se puede comprar en distribuidores comerciales (por ejemplo, biolaboratorios creativos, ALB technology, Carbosynth etc.).
[0275] La fórmula general del enlazador se indica a continuación:
Preparación del compuesto de los compuestos de acuerdo con la presente invención (ejemplo 18) acoplado a Mc-Val-Cit-PAB-PNP
[0276]
Compuesto 6
[0277] A p-nitrocloroformiato (140 mg, 0,70mmol, 1,5 equivalentes) en DCM (2,5 ml) se añadió gota a gota una solución de compuesto 5 (100 mg, 0,46 mmol) y TEA (1,5 equivalentes) en DCM (1,5 ml) a 0 °C. Después de 10 minutos a 0 °C, la mezcla de reacción se calentó hasta temperatura ambiente y se agitó hasta su conversión completa (comprobación mediante CCF, 1 hora). A continuación, la mezcla se diluye en DCM (30 ml), se lava con una solución acuosa saturada de cloruro sódico (40 ml), se seca sobre Na2SO4 y el disolvente se evapora bajo presión reducida. El producto en bruto se purificó mediante cromatografía en gel de sílice (éter de petróleo/acetato de etilo 100/ a 70/30) para generar el compuesto 6 como un sólido amorfo (rendimiento del 82 %). RMN 1H (300 MHz, DMSO): 8 (ppm) 8,35 8,30 (m, 2H), 7,59-7,53 (m, 2H), 4,30 (t, J = 5,7 Hz, 2H), 2,75 (t, J= 5,7 Hz, 2H), 2,39 (s, 3H), 2,30 (s, 3H), 1,39 (s, 6H).
Compuesto 7
[0278] Al compuesto 6 (200mg, 0,53 mmol) en DCM (3 ml) se añade TEA (1,2 equivalentes) a temperatura ambiente. A continuación, se añade una solución de N-metil-N-[2-(metilamino)etil]carbamato de terc-butilo (1,2 equivalentes) en DCM (2,3 ml) a 0 °C. La mezcla de reacción amarilla brillante obtenida se calentó hasta temperatura ambiente y se agitó durante la noche. La mezcla se diluyó en 30 ml de DCM, se lavó con 40 ml de una solución acuosa saturada de cloruro sódico, se secó sobre Na2SO4 y el disolvente se evaporó bajo presión reducida. El producto en bruto se purificó mediante cromatografía en gel de sílice (éter de petróleo/acetato de etilo 75/25 a 20/80) para generar el compuesto 7 como un aceite viscoso (rendimiento 70 %).
[0279] RMN 1H (300MHz, DMSO): 8(ppm) 3,99 (t, J = 5,7Hz, 2H), 3,30 (s, 3H), 2,85-2,70 (m, 7H), 2,66-2,58 (m, 2H), 2,38 (s, 3H), 2,26 (s, 3H), 1,37 (s, 9H), 1,36 (s, 6H). ESI-LRMS: Calculado para C20H36N3O5S [M+H]+: 430,2; encontrado: 430,2.
Compuesto 8
[0280] Al compuesto 7 (44,5 mg, 0,104 mmol) en 4,5 ml de DCM (4,5 ml) se añadió TFA (0,5 ml) a 0 °C. A continuación, la mezcla se dejó a calentar hasta temperatura ambiente y se agitó durante la noche. Después de la concentración al vacío (Temperatura de baño en °C < 45 °C). El residuo oleoso se trituró y se sometió a ultrasonidos en Et2O. El sólido pegajoso resultante (sal de bis trifluoroacetato) se lavó con Et2O y se secó. Rendimiento: 67 %.
[0281] RMN 1H (300 MHz, D2O) 84,57 - 4,44 (m, 2H), 3,73 - 3,69 (m, 2H), 3,62 (t, J = 5,7 Hz, 2H), 3,30 - 3,19 (t, J = 5,8 Hz, 2H), 3,05 - 2,99 (m, 3H), 2,99 - 2,90 (m, 3H), 2,73 (s, 3H), 2,45 (s, 3H), 1,79 (s, 6H). ESI-LRMS: Calculado para C15H28N3O3S [M+H]+: 330,2; encontrado: 330,1.
Compuesto 9
[0282] A MC-Val-Cit-PABC-PNP (52 mg, 0,07 mmol) y el compuesto 8 (1,06 equivalentes) en DMF (1,4 ml) se añadieron de manera secuencial a 0 °C: HOBt (1 equivalente) en una parte, a continuación, DIPEA (3 equivalentes) gota a gota. Después de 5 minutos a 0 °C, la mezcla se calentó hasta temperatura ambiente y se agitó durante la noche. A continuación, la mezcla se concentró al vacío (3/4 eliminación por evaporación, T del baño en °C < 45 °C) y se floculó con Et2O. Se obtuvo un sólido en bruto blanco después de lavados/trituraciones (x3) en Et2O. Una
purificación final mediante cromatografía en sílice (MeOH/DCM 95/5 a 90/10 %) produjo el producto final (compuesto 9) como un sólido blanco. Rendimiento: 75 %.
[0283 ] RMN 1H (300 MHz, DMSO) 89,99 (s, 1H), 8,08 (d, J = 7,4 Hz, 1H), 7,80 (d, J = 8,6 Hz, 1H), 7,59 (d, J = 8,5 Hz, 2H), 7,35 - 7,22 (m, 2H), 7,01 (s, 2H), 5,97 (t, J = 5,8 Hz, 1H), 5,41 (s, 2H), 4,98 (s, 2H), 4,44 - 4,32 (m, 1 H), 4,25 -4,14 (m, 1H), 3,99 (s, 2H), 3,45 -3,33 (m, 4H), 3,09 -2,89 (m, 2H), 2,89 -2,70 (m, 6 H), 2,65 -2,56 (m, 2H), 2,38 (s, 3H), 2,30 -2,11 (m, 5H), 2,10-1,90 (m, 1H), 1,77 - 1,09 (m, 18H), 0,84 (dd, J = 9,5, 6,8 Hz, 6 H).
[0284 ] LC Zorbax, ACN/TFA al 0,1 % en H2O, 254 nm, 96 %.
[0285 ] ESI - HRMS: Calculado para C44H66N9O11S [M+H]+ 928,4597 encontrado 928,4586.
P a r te 2 : U s o d e u n c o m p u e s to d e a c u e r d o c o n la p re s e n te in v e n c ió n
E je m p lo 1: a c t iv id a d d e lo s c o m p u e s to s d e a c u e r d o c o n la p re s e n te in v e n c ió n Material y Procedimientos [0286 ] L ín e a s c e lu la r e s . Se utilizó la línea celular de leucemia, HL-60 (derivada de una mujer de 36 años con AML-M2) para determinar la eficacia de fármaco. Las células se obtuvieron de la Colección Europea de Cultivos Celulares (ECACC). Todas las células se cultivaron en un medio adecuado de acuerdo con las recomendaciones del fabricante.
[0287 ] E n s a y o d e V ia b il id a d C e lu la r , fo r m a to d e 96 p o c il lo s . Las células se sembraron en placas de cultivo celular de 96 pocillos a concentraciones necesarias para asegurar aproximadamente el 80 % de confluencia en el control (células no tratadas) al final del experimento (0,5 x 104 - 5 x 104 células/pocillo).
[0288 ] La sensibilidad hacia los compuestos de acuerdo con la presente invención se determinó utilizando diferentes concentraciones de cada compuesto que oscilaban entre 0,5 y 100 jM (0,5, 1, 2, 5, 10, 15, 20, 25, 30, 40, 50, 100 |jM). Después de 48 horas de incubación a 37 °C en una atmósfera humidificada que contenía 5 % de CO2, el efecto inhibidor del crecimiento de los compuestos se analizó utilizando Resazurina, de acuerdo con las instrucciones del fabricante.
[0289 ] Para asegurar la buena calidad de datos y para minimizar el impacto de errores de pipeteo, cada concentración de compuestos se evaluó basándose en la intensidad media de fluorescencia de 8 pocillos separados. Las respuestas de los compuestos se cuantificaron mediante la concentración inhibitoria media máxima (IC50) para cada línea celular particular, y se determinaron mediante el análisis de regresión no lineal de curvas logarítmica de dosis/respuesta.
[0290 ] A n á l is is E s ta d ís t ic o . Los valores se expresaron como una media ± DE o frecuencias y proporciones. Las curvas de viabilidad celular se determinaron utilizando una línea de regresión de cuatro parámetros. Las diferencias entre los grupos se determinaron mediante prueba t no emparejada, Chi cuadrado, prueba exacta de Fisher o ANOVA, según proceda. P < 0,05 se consideró estadísticamente significativa. El análisis se realizó utilizando la versión 5.0 de prisma de GraphPad (software GraphPad, San Diego California EE. UU.).
Resultados
[0291 ] La IC50 obtenida mediante el ensayo de la actividad citotóxica de los compuestos de acuerdo con la presente invención (excepto los compuestos 13, 14, 15 y 16 que no forman parte de la presente invención) en células HL60 se mencionan en la tabla 3 a continuación.
T a b la 3
Ejemplo 2: actividad de los compuestos 3 y 5 en ensayos enzimáticos con ALDH1A1, ALDH1A2, ALDH1A3, ALDH2 y ALDH3A1 recombinante humana
Material y Procedimientos
[0292] Se prepararon ALDH1A1, ALDH1A2, ALDH1A3, ALDH2 recombinantes humanas (Creative BioMart, NY, EE. UU.) a una concentración de 1 mg/ml. Las reacciones enzimáticas se llevaron a cabo utilizando las concentraciones saturantes de sustrato. Para probar la actividad enzimática de las enzimas, se añadieron 10 j l de enzima a un tampón
de reacción que contenía 50 mM de HEPES pH 7,2, 30 mM de MgCh, más 20 mM de cofactor de NAD+ y 2 mM de Hexanal (Sigma-Aldrich, St. Louis, Missouri, EE. UU.) en presencia o ausencia de los diferentes compuestos de prueba. Los patrones internos se prepararon con forma reducida del Nicotinamida adenina dinucleótido (NADH, 500 |jM, Sigma-Aldrich) en Tampón de Reacción (50 mM de HEPES pH 7,2, 30 mM de MgCh).
[0293] Para ALDH3A1 (1 mg/ml), se añadieron 10 j l de enzima a un tampón de reacción que contenía 50 mM de Tris, 5 mM de DTT, pH 8, más 40 mM de Nicotinamida adenina dinucleótido fosfato (forma oxidada, NADP+) y 4-Nitrobenzaldehído (4-NBA) (Sigma-.Aldrich). Los patrones internos se prepararon con forma reducida de Nicotinamida adenina dinucleótido fosfato (NADPH, 5 jM , Sigma-Aldrich) en Tampón de Reacción (50 mM de Tris, 5 mM de DTT, pH 8). Los ensayos de inhibición dependientes de tiempo se llevaron a cabo durante 0-2-5-10-15-20-30-45-60 minutos a 37 °C en una cubeta de cuarzo de 1 ml. La formación de NADH se controló con la lectura de muestras a una longitud de onda de excitación = 340 nm/longitud de onda de emisión = 460 nm (fluorescencia) durante como mínimo 600 segundos utilizando fluorímetro Varian Cary Eclipse.
[0294] El control negativo consistió en las mismas reacciones a excepción de que no se añadió la enzima (blanco de enzima). Para determinar la pendiente para el blanco de enzima y calcular la concentración de producto (Unidad de fluorescencia) se utilizó la siguiente fórmula:
dF Cst
v = — x -—
dt Fst
donde Cst es la concentración de NADH patrón, Fst es la fluorescencia del patrón y dF/dt es la pendiente de la fluorescencia dependiente de tiempo (S. Sotobodowska et al, 2012).
[0295] La actividad específica de las enzimas (jm ol/m inm g - U/mg) en ausencia o presencia de inhibidores se calculó de la siguiente manera:
Actividad específica
Pendiente ajustada (|imol NADH/s) x tiempo (60 s/min) x factor de dilución
Volumen final de ensayo (1000 |il) x volumen de enzima (0,01 |il) x concentración de enzima (mg/ml)
Actividad específica
Pendiente ajustada (|imol NADPH/s) x tiempo (60 s/min) x factor de dilución
Volumen final de ensayo (1000 |il) x volumen de enzima (0,01 |il) x concentración de enzima (mg/ml)
[0296] En dichas reacciones, la actividad de los compuestos 3 y 5 de acuerdo con la presente invención se comparó con la de DIMATE (4-(dimetilamino)-4-metilpent-2-intioato de S-metilo, descrito en el documento EP 1296946).
Resultados
[0297] Las IC50 obtenidas se mencionan en la tabla 4 a continuación.
T l 4
[0298] Los compuestos 3 y 5 mostraron una inhibición más alta de las enzimas ALDH de clase 1 que la de DIMATE.
Ejemplo 3: Parámetros cinéticos de los compuestos 3 y 5 en reacciones con ALDH1A1, ALDH1A2, ALDH1A3, ALDH2 y ALDH3A1 recombinantes humanas
Material y Procedimientos
[0299] Los datos cinéticos se expresan como la media ± error estándar a partir de tres determinaciones independientes. Kinact/Ki se determinó a partir de las representaciones de Kobs frente a la concentración de inhibidor [I]. Kobs se determinó a partir de la representación de la concentración de producto frente al tiempo de incubación de las enzimas con los compuestos 3 y 5 o DIMATE a concentraciones diferentes (es decir, 300 ji M, 200 ji M, 100 ji M, 50 |jM, 20 jiM y 10 jiM de inhibidores). Las Kobs se obtuvieron a partir del ajuste exponencial negativo utilizando el programa de regresión no lineal GraFit 5.0 (software Erithacus).
Resultados
[0300] Los parámetros obtenidos se mencionan en la tabla 5 a continuación.
Tabla 5
[0301] La potencia inhibitoria de los compuestos 3 y 5 es entre 4 y 20 veces más alta que la de DIMATE para enzimas recombinantes de ALDH de clase 1, en particular, ALDH1A2 y ALDH1A3.
Ejemplo 4: Tipo de inhibición después de la caracterización enzimática y bioquímica completa de los compuestos 3 y 5
Material y Procedimientos
[0302] Para determinar los mecanismos de inhibición de los compuestos analizados para cada isoenzima, se calcularon las Kobs correspondientes tal como se menciona anteriormente, representando la concentración de producto frente al tiempo de incubación de las enzimas con los compuestos de prueba a 300 ji M, 200 ji M, 100 ji M, 50 ji M, 20 ji M y 10 ji M. Las Kobs se obtuvieron para cada concentración de inhibidor ensayada, a partir del ajuste exponencial negativo utilizando el programa de regresión no lineal GraFit 5.0 (software Erithacus). Finalmente, se determinó el parámetro cinético de kinact/Ki a partir del gráfico de kobs frente a la concentración correspondiente de inhibidor. La pendiente del ajuste lineal de datos indicó la constante de velocidad en jiM-1min-1. Basándose en los gráficos diferentes obtenidos, la inhibición irreversible se caracterizó como Marcaje de Afinidad Específico o No Específico.
[0303] En el caso de Marcaje de Afinidad Específica, el gráfico muestra un diagrama de kobs saturada frente a la concentración de inhibidor (similar a una representación de inhibición reversible), alcanzando el nivel plano a concentraciones elevadas de inhibidor. En el Marcaje de Afinidad No Específica, la dependencia de kobs sobre la concentración de inhibidor aparece como no saturante.
[0304] En dicho experimento, los compuestos 3 y 5 se compararon con Dimate.
Resultados
[0305] Los resultados obtenidos se mencionan en la tabla 6 a continuación.
Tabla 6
[0306] Aunque todos los compuestos caracterizados mostraron una inhibición irreversible, el tipo de inactivación observada para las isoenzimas diferentes varió entre el marcaje de afinidad específica y no específica. Especialmente, los compuestos 3 y 5 interactúan con una especificidad más alta con ALDH1A3, mientras que para DIMATE, esa inhibición tiene lugar mediante un mecanismo de una etapa única de inactivación, tal como se describe para inhibidores irreversibles con marcaje de afinidad no específica.
Parte 3: Preparación de un conjugado anticuerpo-fármaco (ADC) de acuerdo con la presente invención
[0307] ADC es un sistema de tres componentes que incluye un agente citotóxico unido a través de un enlazador biodegradable a un anticuerpo. El anticuerpo se une a marcadores específicos (antígenos o receptores) en la superficie de la célula es cancerígena. A continuación, el conjugado anticuerpo-fármaco completo se interioriza dentro de la célula cancerígena, donde el enlazador se degrada y el fármaco activo se libera.
[0308] En el contexto de la presente invención, agente citotóxico, un compuesto de acuerdo con la presente invención, se acopla a un anticuerpo a través de un grupo de acoplamiento (maleimida, éster de succinimidilo, sustrato de enzimas de secuencia peptídica específica, etc ...), unido a un enlazador escindible (sitio de proteasa, hidracina, disulfuro) o un enlazador no escindible y con o sin un espaciador autoinmolativo.
Síntesis del compuesto de acuerdo con la presente invención
[0309] Se hace la referencia a la parte 1 del ejemplo 29.
Conjugación con el anticuerpo rituximab
[0310] El anticuerpo rituximab (Roche®) se mezcló con DTT a 37 °C durante 30 minutos y, a continuación, se diafiltró contra PBS que contenía 1 mmol/l de EDTA utilizando Amicon Ultra-15, MWCO 30kDa, Merck-Millipore. La concentración de tiol se cuantificó mediante el reactivo de Ellman, ácido 5,5'-ditiobis(2-nitrobenzoico) [DTNB]. Se añadió un exceso molar de 50 veces del compuesto 9 final obtenido en el párrafo anterior disuelto en DMF al anticuerpo reducido a 4 °C durante 1 hora. El conjugado anticuerpo-fármaco se diafiltró en PBSx1 utilizando Amicon Ultra-15, MWCO 30kDa, Merck-Millipore. Para determinar la relación fármaco-anticuerpo (DAR), la concentración de tiol del anticuerpo modificado después del acoplamiento se cuantificó mediante el reactivo de Ellman.
[0311] El mecanismo de liberación del compuesto de acuerdo con la presente invención, seguido del grupo de escisión de catepsina, se muestra en el esquema a continuación:
[0312] Fragmentos liberados:
Parte 4: Uso de un ADC de acuerdo con la presente invención
Determinación de Relación Fármacos/Anticuerpo (DAR)
[0313] La DAR del Conjugado Anticuerpo-Fármaco mencionado en la parte 3 se controló mediante la diferencia entre la cuantificación de tiol utilizando el Reactivo de Ellman, después de la tiolación suave de rituximab mediante ditiotreitol (DTT) y la inactivación de estos tioles libres mediante el acoplamiento del grupo maleimida. Después de la tiolación de DTT, se generaron 10 nuevos grupos tiol mediante la molécula de Rituximab. Después del acoplamiento del producto final 9, la totalidad de estos nuevos grupos tiol libres se inactivaron dando lugar a un acoplamiento de 10 compuestos 9 por molécula de Rituximab.
Citotoxicidad Celular por Rituximab-compuesto 9.
[0314] Se colocaron en placas 50.000 células Raji viables por triplicado. A continuación, se añadieron diluciones 1:2 en serie de Rituximab-compuesto 9 o Rituximab de control para generar las concentraciones finales (concentraciones de partida de 50 pg/ml). Las células se incubaron durante un periodo de 48 horas durante el cual se añadieron 20 pl de Azul de Alamar (Thermo Fisher Scientific) a cada pocillo. Las placas se incubaron durante cuatro horas adicionales y se leyó la intensidad de flureoscencia en un lector de placas utilizando una longitud de onda de excitación de 540 nm y una longitud de onda de emisión de 620 nm.
[0315] Los resultados muestran que la viabilidad de células Raji fue significativamente menor (figura 1; valor p < 0,01; **) utilizando un tratamiento con 500 pg/ml de Rituximab-compuesto 9 durante 48 horas que Rituximab per se.
Claims (12)
1. Compuesto de fórmula (I):
en la que:
-X es S;
- R1 es alquilo (C1-C7) lineal o ramificado,
- R2 es CHR5CHR6OR4 o (CHR5VOR4,
- v se selecciona de 2 a 4;
- R3 es alquilo (C1-C7) lineal o ramificado,
- R4 se selecciona entre: H, alquilo (C2-C7) lineal o ramificado, alquenilo (C2-C7) lineal o ramificado, -CONR7R8, arilo, heteroarilo, cicloalquilo (C2-C7), alquil (C1-C7)-arilo lineal o ramificado o alquil (C1-C7)-heteroarilo lineal o ramificado; estando dicho arilo, cicloalquilo (C2-C7) y heteroarilo opcionalmente sustituidos por uno o más sustituyentes que se seleccionan entre: halógeno, alquilo (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, alcoxi (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, -COOH, arilo, -NRR', -NO2, o estando dicho arilo y heteroarilo opcionalmente fusionados para formar un heterocicloalquilo; - R5 y R6 se seleccionan entre:
• H, o
• R5 es H y R1 y R6 están unidos para formar con el átomo de nitrógeno unido a R1 un heterocicloalquilo, o
• R6 es H y R1 y R5 están unidos a R1 para formar con el átomo de nitrógeno unido a R1 un heterocicloalquilo;
- R7 es alquilo -(C1-C3);
- R8 es alquilo -(C1-C3)-NRR';
- R y R', idénticos o diferentes, se seleccionan de manera independiente entre H y alquilo (C1-C7) lineal o ramificado, o sus sales farmacéuticamente aceptables o isómeros ópticos, racematos, diastereoisómeros, enantiómeros o tautómeros.
2. Compuesto, según la reivindicación 1, en el que R3 es metilo, R1 es metilo, R2 es CHR5CHR6OR4 o (CHR5VOR4 y R5 y R6 son:
- H, o
- R5 es H y R1 y R6 están unidos para formar con el átomo de nitrógeno unido a R1 un pirrolidinilo, o
- R6 es H y R1 y R5 están unidos a R1 para formar con el átomo de nitrógeno unido a R1 un pirrolidinilo.
3. Compuesto, según la reivindicación 1 o 2, en el que R4 se selecciona entre alquilo (C2-C7) lineal o ramificado, alquenilo (C2-C7) lineal o ramificado, -CONR7R8, cicloalquilo (C2-C7), alquil (C1-C7)-heteroarilo lineal o ramificado, arilo o bencilo; estando dicho cicloalquilo (C2-C7) sustituido por uno o más sustituyentes seleccionados entre: alquilo (C1-C7) lineal o ramificado, estando dicho bencilo opcionalmente sustituido por uno o más sustituyentes seleccionados entre: alquilo (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, alcoxi (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, halógeno o estando dicho bencilo opcionalmente fusionado para formar 1,3-benzodioxol.
4. Compuesto, según la reivindicación 1 o 2, en el que R5 y R6 son H y R4 se selecciona entre alquilo (C2-C7) lineal o ramificado, alquenilo (C2-C7) lineal o ramificado, CONR7R8, cicloalquilo (C2-C7), alquil (C1-C7)-heteroarilo lineal o ramificado o bencilo; estando dicho cicloalquilo (C2-C7) opcionalmente sustituido por uno o más sustituyentes seleccionados entre: alquilo (C1-C7) lineal o ramificado, estando dicho bencilo opcionalmente sustituido por uno o más sustituyentes seleccionados entre: alquilo (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, alcoxi (C1-C7) lineal o ramificado opcionalmente sustituido por uno o más átomos de halógeno, halógeno.
5. Compuesto, según la reivindicación 4, en el que R1 es metilo y R4 se selecciona entre: -CONR7R8, siendo R7 un metilo y siendo R8 NRR' con R y R' siendo metilo, etilo, propeno, bencilo, piridilo, benciloxibutilo, metil-ciclohexenilo
sustituido por uno o más de metilo y bencilo sustituido por uno o más de flúor, cloro, metoxi o metilo.
6. Compuesto, según cualquiera de las reivindicaciones 1 a 5, seleccionado del grupo que consiste en:
- 4-[2-etoxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo;
- 4-[2-aliloxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo;
- 4-[2-benciloxietil(metil)amino]-4-metil-pent-2-intioato de S-metilo;
- 4-metil-4-[metil-[2-(m-tolilmetoxi)etil]amino]pent-2-intioato de S-metilo;
- 4-[2-[(3,4-dimetilfenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo;
- 4-[2-[(4-metoxifenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo;
- 4-[2-[(3,4-dimetoxifenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo;
- 4-[2-[(3-clorofenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo;
- 4-[2-[(3-fluorofenil)metoxi]etil-metil-amino]-4-metil-pent-2-intioato de S-metilo;
- 4-metil-4-[metil-[2-(2-piridilmetoxi)etil]amino]pent-2-intioato de S-metilo;
- 4-metil-4-[metil-[2-(3-piridilmetoxi)etil]amino]pent-2-intioato de S-metilo;
- 4-metil-4-[metil-[2-(4-piridilmetoxi)etil]amino]pent-2-intioato de S-metilo;
- 4-((4-(benciloxi)butil)(metil)amino)-4-metilpent-2-intioato de S-metilo;
- 4-((2-hidroxietil)(metil)amino)-4-metilpent-2-intioato de S-metilo;
- 4-metil-4-[metil-[2-(2-naftilmetoxi)etil]amino]pent-2-intioato de S-metilo;
- 4-metil-4-[metil-[2-[(2,6,6-trimetilciclohexen-1-il)metoxi]etil]amino]pent-2-intioato de S-metilo;
- 2-[(1,1-dimetil-4-metilsulfanil-4-oxo-but-2-inil)-metilamino] etil-3,4-dimetoxibenzoato;
- acetato de 2[(1,1-dimetil-4-metilsulfanil-4-oxo-but-2-inil)-metilamino]etilo;
- 2,5,10,11,11-pentametil-6-oxo-7-oxa-2,5,10-triazatetradec-12-in-14-tioato de S-metilo;
- 4-[2-(metoximetil)pirrolidin-1-il]-4-metilpent-2-intioato de S-metilo;
- 4-(3-metoxipirrolidin-1-il)-4-metilpent-2-intioato de S-metilo;
- 4-metil-4-[metil(2-fenoxiciclopentil)amino]pent-2-intioato de S-metilo;
- 4-(2-((benciloxi)metil)pirrolidin-1-il)-4-metilpent-2-intioato de (S)-S-metilo;
- 4-[(3(benciloxi)-1pirrolidinil])-4-metilpent-2-intioato de S-metilo;
o sus sales farmacéuticamente aceptables o isómeros ópticos, racematos, diastereoisómeros, enantiómeros o tautómeros.
7. Compuesto, según la reivindicación 1, en el que:
-X es S;
- R1 es alquilo (C1-C7) lineal o ramificado;
- R2 es CHR5CHR6OR4 o (CHR5VOR4,
- R4 se selecciona entre H, arilo, heteroarilo, alquil (C1-C7)-arilo lineal o ramificado o alquil (C1-C7)-heteroarilo lineal o ramificado;
estando dicho arilo y heteroarilo opcionalmente sustituidos por uno o más sustituyentes que se seleccionan entre: -COOH, -NRR' y -NO2; y
- R y R' idénticos, son H.
8. Proceso de preparación de un compuesto, según cualquiera de las reivindicaciones 1 a 7, que comprende: a) hacer reaccionar un compuesto de fórmula (II) con un ácido orgánico o inorgánico
b) hacer reaccionar el compuesto obtenido en la etapa a) con una base;
c) hacer reaccionar el compuesto obtenido en la etapa b) con CO2;
d) hacer reaccionar el compuesto obtenido en la etapa c) con cloroformiato de alquilo, un reactivo capaz de formar, con el compuesto obtenido en la etapa c), un haluro de ácido o un reactivo capaz de formar, con el compuesto obtenido en la etapa c), un anhídrido mixto;
e) hacer reaccionar el compuesto obtenido en la etapa d) con un compuesto precursor de anión SMe-;
en el que R1 y R2 se definen, según cualquiera de las reivindicaciones 1 a 7.
9. Composición farmacéutica que comprende un compuesto, según cualquiera de las reivindicaciones 1 a 7, y un excipiente farmacéutico aceptable.
10. Compuesto, según cualquiera de las reivindicaciones 1 a 7, para su uso como un medicamento.
11. Compuesto, según cualquiera de las reivindicaciones 1 a 7, para su uso para la prevención o el tratamiento de
cáncer, en particular, leucemia.
12. Conjugado anticuerpo-fármaco de fórmula: B-L-Ab, en la que:
- B es un compuesto de fórmula (I), tal como se define en la reivindicación 7;
- L es un resto químico que comprende un enlace covalente o una cadena de átomos que acopla de manera covalente el Ab al compuesto de fórmula (I); y
- Ab es un anticuerpo que se selecciona entre: rituximab, trastuzumab, alemtuzumab, ibritumomab, gemtuzumab, tiuxetano, tositumomab, brevacizumab, cetuximab, panitumumab, ofatumumab y obinutuzumab.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP19305989 | 2019-07-31 | ||
| PCT/EP2020/071640 WO2021019071A1 (en) | 2019-07-31 | 2020-07-31 | Aminothiolester compounds and uses thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2929333T3 true ES2929333T3 (es) | 2022-11-28 |
Family
ID=67659156
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES20749897T Active ES2929333T3 (es) | 2019-07-31 | 2020-07-31 | Compuestos de aminotioléster y usos de los mismos |
Country Status (21)
| Country | Link |
|---|---|
| US (1) | US20220265845A1 (es) |
| EP (1) | EP3833657B1 (es) |
| JP (1) | JP7681566B2 (es) |
| KR (1) | KR102941434B1 (es) |
| CN (1) | CN114341110A (es) |
| AU (1) | AU2020322170C1 (es) |
| BR (1) | BR112022001620A2 (es) |
| CA (1) | CA3145268A1 (es) |
| DK (1) | DK3833657T3 (es) |
| ES (1) | ES2929333T3 (es) |
| HR (1) | HRP20220961T1 (es) |
| HU (1) | HUE059240T2 (es) |
| IL (1) | IL290031B2 (es) |
| LT (1) | LT3833657T (es) |
| MA (1) | MA57224B1 (es) |
| MX (1) | MX2022001023A (es) |
| PL (1) | PL3833657T3 (es) |
| PT (1) | PT3833657T (es) |
| SI (1) | SI3833657T1 (es) |
| WO (1) | WO2021019071A1 (es) |
| ZA (1) | ZA202201239B (es) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP4035666A1 (en) * | 2021-01-29 | 2022-08-03 | Advanced Biodesign | Aminothiolester compound or derivative thereof for use as an immunomodulatory agent |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3337625A (en) | 1961-09-18 | 1967-08-22 | Lilly Co Eli | Amino-acetylenic compounds |
| US3285913A (en) | 1963-08-28 | 1966-11-15 | Lilly Co Eli | Metal catalyst process for preparing alpha-amino-acetylenes |
| FR2809727B1 (fr) * | 2000-05-31 | 2002-07-26 | Galderma Res & Dev | Nouveaux composes aminothiolesters, compositions pharmaceutiques et cosmetiques les contenant et utilisations |
| US7078402B2 (en) * | 2000-05-31 | 2006-07-18 | Centre National De La Recherche Scientifique (Cnrs) | Aminothiol ester compounds, pharmaceutical and cosmetics compositions containing same and uses thereof |
| FR2983492B1 (fr) * | 2011-12-06 | 2015-10-30 | Advanced Biodesign | Procede ex vivo de purge tumorale d'un echantillon biologique |
| GB201309807D0 (en) * | 2013-05-31 | 2013-07-17 | Pharma Mar Sau | Antibody drug conjugates |
| MD4794B1 (ro) | 2013-09-27 | 2022-02-28 | Merck Sharp & Dohme Corp | Derivaţi de chinolizină substituiţi utili ca inhibitori de integrază HIV |
| CN104761544B (zh) * | 2014-01-03 | 2019-03-15 | 北京轩义医药科技有限公司 | Egfr酪氨酸激酶的临床重要突变体的选择性抑制剂 |
| MX377725B (es) * | 2015-10-15 | 2025-03-11 | Advanced Biodesign | Combinación que comprende un compuesto de aminotioléster o una de sus sales farmacéuticamente aceptables y un compuesto capaz de aumentar el nivel de peróxido de hidrógeno (h2o2) en las células cancerosas de un sujeto. |
| PL3362056T3 (pl) * | 2015-10-15 | 2021-09-27 | Advanced Biodesign | Związki aminotioestrowe lub ich farmaceutycznie dopuszczalne sole do stosowania w leczeniu nowotworu |
-
2020
- 2020-07-31 MA MA57224A patent/MA57224B1/fr unknown
- 2020-07-31 CA CA3145268A patent/CA3145268A1/en active Pending
- 2020-07-31 CN CN202080062104.9A patent/CN114341110A/zh active Pending
- 2020-07-31 IL IL290031A patent/IL290031B2/en unknown
- 2020-07-31 WO PCT/EP2020/071640 patent/WO2021019071A1/en not_active Ceased
- 2020-07-31 SI SI202030083T patent/SI3833657T1/sl unknown
- 2020-07-31 AU AU2020322170A patent/AU2020322170C1/en active Active
- 2020-07-31 EP EP20749897.3A patent/EP3833657B1/en active Active
- 2020-07-31 BR BR112022001620A patent/BR112022001620A2/pt unknown
- 2020-07-31 HR HRP20220961TT patent/HRP20220961T1/hr unknown
- 2020-07-31 JP JP2022506239A patent/JP7681566B2/ja active Active
- 2020-07-31 PT PT207498973T patent/PT3833657T/pt unknown
- 2020-07-31 DK DK20749897.3T patent/DK3833657T3/da active
- 2020-07-31 US US17/631,046 patent/US20220265845A1/en active Pending
- 2020-07-31 LT LTEPPCT/EP2020/071640T patent/LT3833657T/lt unknown
- 2020-07-31 KR KR1020227003281A patent/KR102941434B1/ko active Active
- 2020-07-31 HU HUE20749897A patent/HUE059240T2/hu unknown
- 2020-07-31 ES ES20749897T patent/ES2929333T3/es active Active
- 2020-07-31 PL PL20749897.3T patent/PL3833657T3/pl unknown
- 2020-07-31 MX MX2022001023A patent/MX2022001023A/es unknown
-
2022
- 2022-01-26 ZA ZA2022/01239A patent/ZA202201239B/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| IL290031B1 (en) | 2025-12-01 |
| PT3833657T (pt) | 2022-09-28 |
| JP7681566B2 (ja) | 2025-05-22 |
| EP3833657A1 (en) | 2021-06-16 |
| LT3833657T (lt) | 2022-10-10 |
| HRP20220961T1 (hr) | 2022-11-11 |
| AU2020322170B2 (en) | 2025-12-18 |
| DK3833657T3 (da) | 2022-08-15 |
| KR102941434B1 (ko) | 2026-03-19 |
| EP3833657B1 (en) | 2022-07-27 |
| AU2020322170A1 (en) | 2022-02-24 |
| IL290031A (en) | 2022-03-01 |
| BR112022001620A2 (pt) | 2022-03-22 |
| CA3145268A1 (en) | 2021-02-04 |
| WO2021019071A1 (en) | 2021-02-04 |
| CN114341110A (zh) | 2022-04-12 |
| AU2020322170C1 (en) | 2026-04-09 |
| SI3833657T1 (sl) | 2022-09-30 |
| JP2022542607A (ja) | 2022-10-05 |
| IL290031B2 (en) | 2026-04-01 |
| MX2022001023A (es) | 2022-02-22 |
| HUE059240T2 (hu) | 2022-11-28 |
| PL3833657T3 (pl) | 2022-09-19 |
| US20220265845A1 (en) | 2022-08-25 |
| ZA202201239B (en) | 2022-09-28 |
| MA57224B1 (fr) | 2022-10-31 |
| KR20220039722A (ko) | 2022-03-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7551056B2 (ja) | プログラマブルなポリマー薬物 | |
| ES2975183T3 (es) | Inhibidores de ENPP1 y su uso para el tratamiento del cáncer | |
| ES2905318T3 (es) | Profármacos de riluzol y su uso | |
| JP2024040167A (ja) | 生物学的に活性な化合物を含むホスホアルキルリボースポリマー | |
| JP2024028303A (ja) | 生物学的に活性な化合物を含むホスホアルキルポリマー | |
| JP2024050717A (ja) | 生物学的に活性な化合物を含むイオン性ポリマー | |
| JP2020536845A (ja) | プログラマブルな樹枝状薬物 | |
| ES3010655T3 (en) | Haloallylamine sulfone derivative inhibitors of lysyl oxidases and uses thereof | |
| ES2314446T3 (es) | Derivados de tetrahidrocarbazol y su uso farmaceutico. | |
| ES2929333T3 (es) | Compuestos de aminotioléster y usos de los mismos | |
| ES2609084T3 (es) | Derivados de fenoxi y feniltio sustituidos para tratar trastornos proliferativos | |
| ES2621802T3 (es) | Sulfóxidos alfa, beta-insaturados para tratar trastornos proliferativos | |
| RU2833575C2 (ru) | Аминотиолэфирные соединения и их применение | |
| EP3659307A1 (en) | Anticancer Drugs and Methods of Making and Using Same | |
| HK40050232A (en) | Aminothiolester compounds and uses thereof | |
| HK40050232B (en) | Aminothiolester compounds and uses thereof | |
| US12600738B2 (en) | Quinolinone derivative compound selectively binding to cysteine, peptide conjugate thereof, and antibody-drug conjugate comprising same | |
| US8735620B2 (en) | Processes for preparing (E)-styrylbenzylsulfone compounds and uses thereof for treating proliferative disorders | |
| JP2008127393A (ja) | 新規なアミド構造を有するピリミジン化合物及びこれを含有する医薬 | |
| HK1194308A1 (zh) | 双功能酶制钳型分子的方法和用途 |