ES2929470T3 - Procedimiento de purificación de moléculas biológicas tales como ADN plasmídico utilizando cromatografía de intercambio aniónico - Google Patents
Procedimiento de purificación de moléculas biológicas tales como ADN plasmídico utilizando cromatografía de intercambio aniónico Download PDFInfo
- Publication number
- ES2929470T3 ES2929470T3 ES19160132T ES19160132T ES2929470T3 ES 2929470 T3 ES2929470 T3 ES 2929470T3 ES 19160132 T ES19160132 T ES 19160132T ES 19160132 T ES19160132 T ES 19160132T ES 2929470 T3 ES2929470 T3 ES 2929470T3
- Authority
- ES
- Spain
- Prior art keywords
- plasmid dna
- optionally
- nucleic acid
- interest
- salt
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/10—Processes for the isolation, preparation or purification of DNA or RNA
- C12N15/1003—Extracting or separating nucleic acids from biological samples, e.g. pure separation or isolation methods; Conditions, buffers or apparatuses therefor
- C12N15/1006—Extracting or separating nucleic acids from biological samples, e.g. pure separation or isolation methods; Conditions, buffers or apparatuses therefor by means of a solid support carrier, e.g. particles, polymers
- C12N15/101—Extracting or separating nucleic acids from biological samples, e.g. pure separation or isolation methods; Conditions, buffers or apparatuses therefor by means of a solid support carrier, e.g. particles, polymers by chromatography, e.g. electrophoresis, ion-exchange, reverse phase
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/26—Selective adsorption, e.g. chromatography characterised by the separation mechanism
- B01D15/36—Selective adsorption, e.g. chromatography characterised by the separation mechanism involving ionic interaction, e.g. ion-exchange, ion-pair, ion-suppression or ion-exclusion
- B01D15/361—Ion-exchange
- B01D15/363—Anion-exchange
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biomedical Technology (AREA)
- Genetics & Genomics (AREA)
- Analytical Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biotechnology (AREA)
- General Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- General Health & Medical Sciences (AREA)
- Biophysics (AREA)
- Microbiology (AREA)
- Plant Pathology (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Physics & Mathematics (AREA)
- Crystallography & Structural Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Peptides Or Proteins (AREA)
- Immunology (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Saccharide Compounds (AREA)
Abstract
La presente invención proporciona métodos nuevos y mejorados para la purificación o el aislamiento de una molécula biológica de interés, como el ADN plasmídico (pDNA) que implica un paso de cromatografía de intercambio aniónico (AEX). El método logra la eliminación simple y efectiva de impurezas como ARN, ADN genómico, proteínas, fracciones celulares o combinaciones de los mismos. Los métodos novedosos de la presente invención son particularmente adecuados para plantas de producción a gran escala y proporcionan biomoléculas purificadas (como pDNA) con excelente calidad y buenos rendimientos, al mismo tiempo que permiten tiempos de procesamiento más rápidos y costos reducidos. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Procedimiento de purificación de moléculas biológicas tales como ADN plasmídico utilizando cromatografía de intercambio aniónico
CAMPO DE LA INVENCIÓN
La presente invención proporciona nuevos métodos mejorados para la purificación o el aislamiento de ADN plasmídico (ADNp). El método incluye la eliminación simple y efectiva de impurezas tales como ARN, ADN genómico, proteínas, fracciones celulares o combinaciones de los mismos. Los métodos novedosos de la presente invención son particularmente adecuados para plantas de producción a gran escala y proporcionan ADNp purificado con excelente calidad y buenos rendimientos, al mismo tiempo que permiten tiempos de procesamiento más rápidos y costos reducidos.
El ADNp purificado obtenido por el método de la presente invención es particularmente adecuado para aplicaciones en sectores tales como la producción transitoria sintética, la terapia génica ex vivo, agentes terapéuticos de ARN, vacunas de ADN, anticuerpos de ADN, terapia génica no viral y vectores virales. El ADNp purificado obtenido a través del método de la presente invención también se puede usar, por ejemplo, en vacunas, terapia viral, terapia génica y celular, producción de moléculas tales como ARN y polipéptidos in vivo o in vitro, o en la terapia de células T con receptor de antígeno quimérico (CAR).
La presente invención también describe el uso novedoso de un recipiente en forma de tulipán que se puede usar favorablemente durante la clarificación de una muestra que comprende la molécula biológica de interés. El recipiente o tanque en forma de tulipán se puede usar ventajosamente durante la separación de fases para separar componentes sólidos de la mezcla que contiene la molécula biológica. Más específicamente, la presente invención proporciona el uso novedoso de un recipiente o tanque en forma de tulipán para recoger la fase inferior (es decir, más densa) de la mezcla que contiene la molécula biológica durante la separación de fases.
ANTECEDENTES DE LA INVENCIÓN
El ADN plasmídico es una pequeña molécula separada físicamente del ADN cromosómico y puede replicarse de forma independiente. El ADN plasmídico existe típicamente en tres conformaciones diferentes: ADNp superenrollado, ADNp circular abierto y ADNp lineal. Dadas las diversas aplicaciones terapéuticas de ADNp, que incluyen, pero no se limitan a la producción de proteínas transitorias sintéticas, terapia génica ex vivo, agentes terapéuticos de ARN, vacunas de ADN, anticuerpos de ADN, terapia génica no viral y vectores virales, los expertos en la técnica apreciarán que son altamente deseables métodos mejorados de purificación o aislamiento de ADNp.
Teniendo en cuenta la alta carga negativa del ADNp, la cromatografía de intercambio aniónico se usa con frecuencia en métodos para purificar o aislar el ADNp. El material de intercambio aniónico contiene grupos cargados positivamente. Por lo tanto, la cromatografía de intercambio aniónico separa moléculas tales como proteínas contenidas en solución de acuerdo con sus cargas mediante el uso de un material de intercambio aniónico. Como apreciarán los expertos en la técnica, la concentración de las sales utilizadas durante la cromatografía de intercambio aniónico variará dependiendo de la sustancia que se ha de eluir. Ejemplos de materiales de intercambio aniónico típicos incluyen diversos tipos de membranas, perlas y resinas de intercambio aniónico. Las proteínas unidas al material de intercambio aniónico se eluyen luego mediante el uso de un gradiente de concentraciones crecientes de sal incluidas con una solución tampón apropiada. Así, en métodos de cromatografía de intercambio aniónico conocidos, la carga de la muestra se lleva a cabo típicamente con un tampón que tiene una baja concentración de sal, y la concentración de sal se incrementa posteriormente durante la etapa de elución.
Al purificar ADNp mediante cromatografía de intercambio aniónico, particularmente a escala industrial, hay varias etapas aguas arriba que típicamente ocurren antes de cargar la solución que contiene ADNp en la columna de intercambio de aniones. Estas etapas incluyen normalmente la fermentación por lotes alimentados, la recogida y el lavado de células, la lisis celular continua, la neutralización, la eliminación de ARN, la filtración profunda de eliminación de floculados, la concentración de plásmidos y la diafiltración. Posteriormente, el proceso de purificación de ADNp incluye típicamente el uso de cromatografía de intercambio aniónico (AEX), que incluye la unión del ADNp al material de intercambio aniónico usando una sal de baja conductividad, seguida de la elución del ADNp con una sal de mayor conductividad, filtración por flujo tangencial con intercambio de tampón, y luego someter las fracciones que contienen ADNp a una etapa de purificación adicional para enriquecer aún más el ADNp superenrollado, p. ej., por cromatografía PlasmidSelect Xtra® (PSX) (disponible, p. ej., de GE Healthcare Technology), a menudo seguida de una etapa adicional de filtración por flujo tangencial con un intercambio de tampón utilizando un tampón de llenado final. En estos métodos conocidos para purificar o aislar ADNp usando cromatografía de intercambio aniónico, la etapa de elución se logra típicamente aumentando gradualmente la concentración de sal en el tampón de elución.
Por ejemplo, Franco-Medrano et al., Bioprocess and Biosystems Engineering (2017), vol. 40, páginas 463-471 describe una purificación de un vector de ADNp específico usando, entre otros, cromatografía de intercambio aniónico utilizando elución en gradiente de cloruro de sodio convencional. Similarmente, Syren et al., Journal of Chromatography B (2007), vol. 856, páginas 68-74 describe la purificación de ADN plasmídico usando "Sartobind Q" (un material de cromatografía de intercambio aniónico comercial), eluyendo el ADN plasmídico con altas concentraciones de cloruro sódico. También, Eon-Duval et al., Journal of Chromatography B, 2004, vol. 804(2), páginas 327-335 describen un método para la purificación de
ADN plasmídico de calidad farmacéutica a partir de cultivo celular empleando una etapa de cromatografía de intercambio aniónico usando elución de gradiente salino convencional con cloruro de sodio.
Después de las etapas iniciales de unión y elución, se requieren etapas adicionales con el fin de obtener el ADNp con una pureza y un rendimiento aceptables, como se mencionó anteriormente. Aún más, se sabe que los métodos existentes de purificación de ADNp dan como resultado una escasa selectividad y una mala recuperación. Los métodos conocidos son, por lo tanto, incapaces de proporcionar una separación eficiente y rentable del ADNp. También vale la pena señalar que muchos de estos métodos conocidos adolecen de la desventaja de usar PEG u otros aditivos, que pueden no ser deseables en la preparación de ADN plasmídico, ya que requieren etapas adicionales de separación, eliminación y control de calidad. Éstas pueden ser difíciles, consumen más tiempo y son más costosas. Como estas etapas adicionales agregan costos al proceso de purificación y aumentan el tiempo necesario para la purificación, existe la necesidad de un método para la purificación o el aislamiento de ADNp que elimine la necesidad de muchas de las etapas adicionales durante la purificación, reduciendo así la cantidad de tiempo requerido para la purificación, sin comprometer la pureza o el rendimiento del ADNp.
Como apreciarán los expertos en la técnica, aún otro inconveniente de los procesos conocidos para la purificación de biomoléculas (tales como ADNp) es la dificultad de aplicar métodos de este tipo en la producción a gran escala, en particular la producción a gran escala de ADNp de calidad farmacéutica. Hay muchas restricciones existentes en la producción a gran escala, por ejemplo, problemas de seguridad personal y consideraciones sobre residuos peligrosos. Además, la aplicación de procesos de purificación a escala de laboratorio de ADNp a mayor escala casi siempre da como resultado una disminución del rendimiento del ADNp purificado. Dadas estas limitaciones, sería deseable proporcionar un método de purificación o aislamiento de ADNp que no solo proporcione ADNp con una pureza mejorada y un alto rendimiento, sino que también pueda usarse para la producción a gran escala.
SUMARIO DE LA INVENCIÓN
Un primer aspecto de la presente invención se refiere a un método para aislar o purificar ADN plasmídico ("ADNp") de interés a partir de una mezcla, comprendiendo el método poner en contacto la mezcla que comprende el ADN plasmídico de interés con un material de intercambio aniónico (AEX) en presencia de una solución que comprende una sal cosmotrópica a una concentración que permite la unión selectiva del ADN plasmídico de interés al material de intercambio aniónico; y eluir el ADN plasmídico de interés con un eluyente que comprende una sal caotrópica a una concentración que proporciona un eluyente que contiene el ADNp purificado. La sal cosmotrópica de este método se selecciona del grupo que consiste en: sulfato de amonio, citrato de amonio, fosfato de amonio, fosfato de potasio, citrato de sodio, fosfato de sodio y mezclas de los mismos, y
en el que la concentración de la sal cosmotrópica es superior a aproximadamente 0,5 M. En algunas realizaciones, la fracción o fracciones que comprenden dicho ADN plasmídico de interés en el eluyente se recoge o recogen opcionalmente. El ADN plasmídico purificado de interés puede, en algunos casos, aislarse posteriormente de una cualquiera de las fracciones recogidas o de todas ellas.
En algunas realizaciones, la sal utilizada a una concentración que permite la unión selectiva de la biomolécula de interés al material AEX es una sal cosmotrópica, por ejemplo, citrato de amonio, sulfato de amonio, fosfato de amonio, fosfato de potasio, citrato de sodio, fosfato de sodio o mezclas de dichas sales.
En algunas realizaciones, la sal caotrópica que está presente en el eluyente a una concentración que proporciona un eluyente que contiene el ADN plasmídico purificado se selecciona de cloruro de amonio, cloruro de potasio, cloruro de sodio, sulfato de magnesio, cloruro de magnesio, nitrato de magnesio, hidrocloruro de guanidinio o mezclas de los mismos.
El ADN plasmídico a purificar mediante los métodos de la invención es típicamente una biomolécula altamente polar / cargada. Se encontró que el nuevo método descrito en este documento es particularmente adecuado para una purificación rápida y altamente efectiva de ADN plasmídico, en particular ADN plasmídico superenrollado de calidad farmacéutica (ADNp sc), que debe estar libre de ADN genómico bacteriano, ARN, proteína y endotoxinas.
La presente invención también describe una etapa ventajosa de preparación de muestras que puede usarse ventajosamente antes de poner en contacto la mezcla que contiene el ADN plasmídico de interés con el material AEX.
En esta etapa de preparación de la muestra, los componentes sólidos (tales como residuos celulares u otros materiales insolubles en el sistema tampón) de la mezcla que comprende el ADN plasmídico de interés se separan convenientemente mediante separación de fases y/o filtración. En algunos casos, la eliminación de los componentes sólidos se logra a través de una simple separación de dos fases, en la que se agrega un tampón para aumentar la densidad de la mezcla a más de aproximadamente 1,1 kg/L. El aumento en la densidad de la mezcla hace que los componentes sólidos floten en la parte superior, y la parte líquida de la mezcla (que comprende el ADN plasmídico de interés) puede luego drenarse convenientemente, sin requerir una etapa de filtración (o al menos ofreciendo una mayor capacidad de filtración debido al contenido de material sólido significativamente reducido, lo que permite la escalabilidad del proceso, es decir, lo hace útil para la producción a gran escala). Esta etapa de preparación de la muestra puede combinarse ventajosamente en algunos casos con el nuevo método de purificación descrito en este documento.
Relacionado con lo anterior, la presente invención también describe el uso de un recipiente o tanque en forma de tulipán para la etapa de separación de fases anterior. Se encontró que el recipiente en forma de tulipán era particularmente
ventajoso para la separación conveniente y eficaz de los componentes sólidos de la parte líquida de la mezcla que comprende el ADN plasmídico de interés.
BREVE DESCRIPCIÓN DE LOS DIBUJOS
La Figura 1 representa una vista esquemática del vector plásmido pUC19 utilizado como una biomolécula de muestra para ser purificada en los ejemplos de trabajo.
La Figura 2A - D muestra datos de electroforesis en gel de agarosa (AGE) en los resultados de una detección de tampón de unión utilizando Sartobind Q como material AEX.
La Figura 3A - D muestra datos de electroforesis en gel de agarosa (AGE) en los resultados de una detección de tampón de unión utilizando Sartobind Q como material AEX.
La Figura 4 representa un perfil de cromatografía de la unidad de cromatografía AEX (Sartobind Q) ampliado en el gradiente de elución.
La Figura 5 muestra datos de electroforesis en gel de agarosa de fracciones de la etapa de cromatografía AEX (Sartobind Q).
La Figura 6 muestra trazas de AEX-HPLC del material eluido 1 de Sartobind Q como se representa en la Figura 3 (línea discontinua) y el patrón (línea continua).
La Figura 7 muestra datos de análisis SDS-PAGE de la carga y el material eluido de la etapa de cromatografía Sartobind Q.
La Figura 8 incluye una representación esquemática del proceso de recuperación primaria, incluida la etapa de cromatografía AEX.
La Figura 9 muestra un perfil de cromatografía de la unidad AEX utilizando Sartobind Q.
DESCRIPCIÓN DETALLADA DE LA INVENCIÓN
Como apreciarán los expertos en la técnica, a la vista de las diversas aplicaciones terapéuticas para el ADN plasmídico, es muy deseable desarrollar un método simple y escalable para purificar el ADN plasmídico con una pureza excelente y en gran cantidad, en particular debido a que muchas etapas de aislamiento/purificación conocidas que típicamente son más adecuadas para la producción a pequeña escala, tales como la producción a escala de laboratorio y de sobremesa, no se pueden traducir adecuadamente a una escala mayor.
La presente invención proporciona métodos para el aislamiento o la purificación de ADN plasmídico como se define en las reivindicaciones adjuntas. En algunas realizaciones, la presente invención incluye métodos de purificación o aislamiento de ADN plasmídico superenrollado libre de impurezas, incluidos ADNp circular abierto, ADNp lineal, endotoxinas, ARN, lipopolisacáridos, ADN genómico, proteínas y/o combinaciones de los mismos mediante el uso de cromatografía de intercambio aniónico en condiciones inusuales definidas. Los métodos de la presente invención son particularmente adecuados para el aislamiento o la purificación a gran escala de ADN plasmídico (en particular ADN plasmídico superenrollado), en un número limitado de etapas, con alta pureza y excelentes rendimientos. En particular, los métodos de purificación de la presente invención pueden usarse ventajosamente para la producción a gran escala para volúmenes de hasta 10.000 litros de volumen de trabajo de fermentación.
Se apreciará que las expresiones "ADN plasmídico de interés", "ADN plasmídico", "molécula diana" se utilizan todas como sinónimos, refiriéndose a la molécula que se ha de purificar de otros componentes o impurezas presentes en la mezcla sometida al método de purificación.
Las impurezas incluyen, pero no se limitan a proteínas de células huésped, endotoxinas, ADN y/o ARN de células huésped. Se apreciará que lo que se considera una impureza puede depender del contexto en el que se pongan en práctica los métodos de la invención. Una "impureza" puede derivar o no de una célula huésped, es decir, puede ser o no una impureza de la célula huésped.
"Aislar” o "purificar" el ADN plasmídico significa el enriquecimiento de la molécula diana a partir de otros componentes con los que la molécula diana está inicialmente asociada. En el presente documento se proporcionan los grados de purificación deseados y/u obtenibles. Preferiblemente, los métodos de la invención dan como resultado un enriquecimiento de aproximadamente cinco veces, preferiblemente un enriquecimiento de aproximadamente 10 veces, preferiblemente un enriquecimiento de aproximadamente 20 veces, preferiblemente un enriquecimiento de aproximadamente 50 veces, preferiblemente un enriquecimiento de aproximadamente 100 veces, preferiblemente un enriquecimiento de aproximadamente 200 veces, preferiblemente un enriquecimiento de aproximadamente 500 veces, preferiblemente un enriquecimiento de aproximadamente 1000 veces. Alternativamente, el grado de purificación puede expresarse como un porcentaje del primer componente con respecto a otro componente, o con respecto a la preparación resultante. En el presente documento se proporcionan ejemplos de porcentajes de este tipo.
Los inventores descubrieron sorprendentemente que es posible purificar el ADN plasmídico, tal como el ADN plasmídico (superenrollado), de una manera rápida, sencilla y directa. Esto se logra poniendo en contacto la mezcla que comprende el ADN plasmídico de interés con un material de cromatografía de intercambio aniónico (AEX) en condiciones que producen una unión altamente selectiva de la molécula biológica a purificar, mientras que los demás componentes de la mezcla no se unen al material AEX.
A este respecto, los inventores encontraron que cargar la mezcla que comprende la biomolécula a purificar con el material AEX en una solución que tiene una concentración bastante alta (> 0,5 M) de una sal cosmotrópica da como resultado una unión altamente específica de la biomolécula deseada al material AEX, es decir, la mayoría de los componentes de la solución no están unidos al material AEX. Se cree que estas condiciones de carga son bastante inusuales para la cromatografía AEX, en donde la muestra que se ha de purificar típicamente se pone en contacto con el material AEX en condiciones de baja fuerza iónica y, posteriormente, se eluye (gradualmente o por etapas) aumentando la concentración de sal/fuerza iónica del tampón de elución. En otras palabras, las condiciones de carga específicas identificadas por los presentes inventores permiten un enriquecimiento efectivo de la molécula fijadora de objetivo ya durante la fase de carga de la etapa de cromatografía AEX, con una purificación adicional posible durante condiciones de elución seleccionadas adecuadamente, como se describirá en detalle a continuación.
Por lo tanto, la etapa de cromatografía AEX, cuando se emplea en las condiciones identificadas por los presentes inventores, permite separar el ADN plasmídico deseado de esencialmente todos los contaminantes no deseados en una sola etapa de purificación. De hecho, las condiciones encontradas por los inventores permiten incluso prescindir de una serie de etapas preparatorias pre-purificación comúnmente aplicadas en la purificación del ADN plasmídico de interés debido a su unión eficaz y altamente selectiva de la molécula diana al material AEX, ya que muchos de los contaminantes simplemente no se unen en esas condiciones cuidadosamente seleccionadas, como se explicará con mayor detalle más adelante.
La presente invención generalmente se refiere a un método para aislar o purificar un ADN plasmídico de interés de una mezcla, en el que el método comprende poner en contacto la mezcla que contiene la molécula biológica de interés con un material de intercambio aniónico (AEX) en presencia de una solución que comprende una sal cosmotrópica seleccionada del grupo que consiste en sulfato de amonio, citrato de amonio, fosfato de amonio, fosfato de potasio, citrato de sodio, fosfato de sodio, y mezclas de los mismos, a una concentración superior a aproximadamente 0,5 M, que permite la unión selectiva del ADN plasmídico de interés al material de intercambio aniónico; y eluir el ADN plasmídico de interés del material AEX con un eluyente que comprende una sal caotrópica a una concentración que proporciona un eluyente que contiene el ADN plasmídico de interés purificado.
"Unión selectiva" en el contexto de la presente invención significa que la gran mayoría de los demás componentes de la mezcla no se unen al material AEX cuando se ponen en contacto con una solución que comprende la sal cosmotrópica a la concentración adecuada. Un experto en la técnica apreciará que en biología (y química) la unión, elución, etc., nunca será 100 % exclusiva, pero para los propósitos de la presente invención, "unión selectiva" significa que al menos el 70 %, el 80 %, el 85 %, el 90 % o incluso el 95 % de los otros componentes ("contaminantes") en presencia de la solución salina cosmotrópica no se unirá al material AEX tras el contacto. En aras de la conveniencia, al contacto de la mezcla con el material AEX también puede aludirse aquí como una "etapa de carga" (como se usa comúnmente en la cromatografía en columna, aunque el presente método, por supuesto, no se limita a la cromatografía en columna), y a la solución salina cosmotrópica que incluye la mezcla a purificar también se la alude como "tampón de carga" o "solución de carga". A la propia solución salina cosmotrópica también se la puede aludir en este documento como "tampón de unión".
Típicamente, se recoge o recogen la fracción o fracciones que comprenden el ADN plasmídico purificado de interés en el eluyente, aunque esto no siempre es necesario (por ejemplo, en procesos de purificación analítica en donde la concentración / pureza de la molécula de interés se puede medir directamente en la solución), p. ej., por espectroscopia UV). Asimismo, en la mayoría de los casos, el ADN plasmídico de interés se aísla luego de una cualquiera o de todas las fracciones recogidas para su uso posterior, como se describe más adelante en el presente documento.
Para la mayoría de las biomoléculas, el aislamiento no significa necesariamente la precipitación y el secado, sino más bien mantener la molécula purificada en una solución, típicamente tamponada, que garantiza la estabilidad frente a la degradación, p. ej., en almacenamiento a largo plazo. Por tanto, el aislamiento también puede incluir la concentración, es decir, la eliminación de parte del disolvente para aumentar la concentración de la molécula diana. Como es bien sabido en la técnica, las soluciones que comprenden una biomolécula (ya sean biomoléculas basadas en proteínas o ácidos nucleicos) en muchos casos pueden almacenarse ventajosamente en una solución congelada, aunque en algunos casos, también se puede eliminar el disolvente, p. ej., por liofilización.
La cromatografía AEX se caracteriza típicamente por cargar la mezcla que se ha de purificar en el material AEX en un tampón que comprende una sal/tampón con baja fuerza iónica, es decir, a concentraciones de sal más bien bajas. Estas condiciones permiten que las moléculas altamente polares y/o cargadas se unan a los grupos cargados en el material AEX, mientras que los componentes que tienen una polaridad / hidrofilicidad más baja no se unirán en tales condiciones. A continuación, la molécula de interés se eluye típicamente de la columna aumentando sucesivamente la concentración de la sal/tampón de modo que el mayor número de iones compita con la unión de las moléculas aún unidas al material AEX. Con el fin de lograr el alto grado de pureza deseado, se utiliza típicamente un gradiente que aumenta la fuerza iónica del tampón de elución para las purificaciones mediante cromatografía AEX. En muchos casos, sin embargo, la cromatografía
AEX convencional no logra una pureza lo suficientemente alta porque demasiados contaminantes (especialmente contaminantes cargados/altamente polares) también se unen al material AEX durante la fase de carga y luego se eluyen al mismo tiempo que la molécula de interés.
Los inventores han encontrado sorprendentemente que es posible llevar a cabo la etapa de carga (es decir, el contacto inicial de la mezcla con el material AEX) en soluciones que comprenden sales cosmotrópicas a concentraciones relativamente altas (superiores a aproximadamente 0,5 M). Sales cosmotrópicas contribuyen a la estabilidad y estructura de las interacciones agua-agua ("generadoras de orden") al hacer que las moléculas de agua interactúen favorablemente, lo que también conduce a una estabilización de las interacciones intramoleculares en macromoléculas como las proteínas. Los cosmótropos iónicos se caracterizan por una fuerte energía de solvatación que típicamente conduce a un aumento de la cohesión general de la solución (como se indica a menudo por un aumento de la viscosidad y densidad de la solución). En contraste, los agentes/sales caotrópicos (generadores de desorden) tienen el efecto opuesto, alterando la estructura del agua, aumentando la solubilidad de las partículas de disolvente no polares y desestabilizando los agregados de soluto.
Los inventores han descubierto que el uso de una sal cosmotrópica de este tipo en la solución en contacto con el material AEX a una concentración suficientemente alta conduce a una unión altamente selectiva de determinadas biomoléculas (en particular, biomoléculas que tienen una alta densidad de carga, como el ADN plasmídico), al tiempo que evita que otros componentes se unan a dicho material AEX. Por lo tanto, en algunos casos, el "flujo continuo" de la etapa de carga en una solución que comprende una sal cosmotrópica a una concentración suficientemente alta ya contendrá la mayoría, si no esencialmente todos los contaminantes de la mezcla que comprende la biomolécula de interés.
Se apreciará que la propiedad de ser cosmotrópico o caotrópico se atribuye especialmente al ion específico y no a una sal (que comprende un contraión). Por lo tanto, bien puede ser que una sal comprenda un anión que se sabe que es cosmotrópico, mientras que se sabe que el contraión es más bien caotrópico. Sales de este tipo pueden funcionar (o no) en la unión selectiva de la molécula diana al material AEX. Sin embargo, los expertos en la técnica podrán averiguar si una sal dada, a altas concentraciones, asegurará la unión selectiva de la molécula diana al material AEX simplemente realizando experimentos de rutina.
En la mayoría de las realizaciones, la elución de la molécula diana del material AEX se puede lograr mediante un eluyente (es decir, una solución o tampón que se usa para separar los componentes unidos al material AEX) que comprende una sal caotrópica en una concentración suficientemente alta para eluir la molécula biológica de interés. Por lo tanto, la fase de elución en muchas realizaciones no es materialmente diferente de la cromatografía AEX convencional, pero debido a la mayor especificidad en la unión al material AEX durante la fase de carga, la pureza del eluyente a menudo aumenta significativamente.
En los métodos de la presente invención, la molécula biológica a purificar es ADN plasmídico. El ADN plasmídico existe a menudo en diferentes conformaciones: además de la conformación superenrollada (SC) "nativa", el ADN plasmídico también puede estar presente en forma circular abierta (OC), o incluso en forma lineal. Dado que el ADN plasmídico superenrollado (ADNp sc) representa típicamente la conformación deseada (y comercialmente relevante) para el ADN plasmídico, la biomolécula de interés en algunas realizaciones de este aspecto de la presente invención es ADNp sc.
El ADN plasmídico a purificar/aislar puede comprender típicamente ADN de mamífero, ADN bacteriano, ADN no codificante o ADN viral. En algunos casos, el ADN plasmídico comprenderá ADN capaz de expresar un polipéptido de interés. El método de purificación no dependerá generalmente del tamaño del ADN plasmídico, es decir, los minivectores con solo 350 pb, así como los vectores de plásmido grandes que comprenden hasta 20 genes (35 kpb), y cualquier elemento intermedio puede purificarse de manera efectiva mediante el método descrito en este documento.
El método de la presente invención permite la purificación eficaz de ADN plasmídico de otros contaminantes. En consecuencia, en determinadas realizaciones, la pureza resultante del ADN plasmídico es al menos el 90 %, o al menos el 93 %, o al menos el 95 %, o al menos el 97 %, o al menos el 98 % o al menos el 99 %.
En algunas realizaciones, el método incluso logra el fraccionamiento de ADN plasmídico superenrollado a partir de otras formas de ADN plasmídico, tales como ADN plasmídico lineal, ADN plasmídico circular abierto y, opcionalmente, otras moléculas de ácido nucleico.
Dado que el ADN plasmídico de interés se obtiene típicamente mediante procesos biológicos (tales como procesos de cultivo/fermentación celular), la mezcla que comprende la molécula diana incluirá en muchas realizaciones ADN plasmídico (incluido el ADNp superenrollado, el ADNp circular abierto y el ADNp lineal), ADN genómico, ARN, lipopolisacáridos, endotoxinas, proteínas o cualquier combinación de los componentes anteriores.
Se apreciará que la concentración de la sal cosmotrópica que permite la unión selectiva de la molécula biológica de interés al material AEX durante la etapa de carga depende típicamente de la naturaleza de la molécula diana y del material AEX elegido. En algunas realizaciones, la unión altamente selectiva de la molécula diana se ha logrado con concentraciones de sal mayores que aproximadamente 0,5 M, o mayores que 0,6 M o mayores que 0,8 M. En determinadas realizaciones, la concentración de sal de la solución que permite la unión selectiva de la molécula diana está entre aproximadamente 0,5 M y aproximadamente 4,0 M, o entre aproximadamente 0,8 M y aproximadamente 2,0 M, o entre aproximadamente 1,0 M y aproximadamente 2,0 M, tal como 1,5 M.
El término "aproximadamente" se usa en este documento para significar aproximadamente, en la región de, apenas o alrededor. Cuando el término "aproximadamente" se usa junto con un intervalo numérico, modifica ese intervalo al extender los límites por encima y por debajo de los valores numéricos establecidos. En general, el término "aproximadamente" se usa en este documento para modificar un valor numérico por encima y por debajo del valor establecido en una varianza del 10 %.
Como se indicó anteriormente, las sales cosmotrópicas en las concentraciones anteriores se emplean para la etapa de carga del presente método de purificación. En cualquier caso, la concentración ideal de dicha sal para la etapa de carga depende de las propiedades reales de la molécula diana y del material AEX, pero un experto en la técnica puede determinarla fácilmente mediante experimentos de rutina. Una vez que se ha determinado una concentración adecuada, puede ser útil para una unión consistente y reproducible equilibrar el material AEX con un tampón que comprenda la sal cosmotrópica a la misma concentración que en la solución de carga que comprende la molécula diana a purificar.
En cualquier caso, ejemplos de sales cosmotrópicas adecuadas incluyen sulfato de amonio, citrato de amonio, fosfato de amonio, fosfato de potasio, citrato de potasio, citrato de sodio, fosfato de sodio o mezclas de los mismos. Por ejemplo, se encontró que el sulfato de amonio es una sal cosmotrópica particularmente útil para la fase de carga cuando la molécula diana a purificar es ADN plasmídico.
Como puede verse en el Ejemplo 1, la carga de la mezcla en una membrana AEX pre-equilibrada opcionalmente en una solución que comprende altas concentraciones (> 0,5 M) de sulfato de amonio aseguró una unión altamente selectiva del ADNp al material AEX, mientras que el ARN y otros contaminantes no se unió a la membrana AEX (véanse las Fig. 2A y 2B). En consecuencia, una concentración útil de sulfato de amonio en la solución de carga es en determinadas realizaciones de aproximadamente 0,5 M a aproximadamente 2,0 M.
Un experto en la técnica apreciará que otros factores pueden ejercer una influencia sobre el comportamiento de unión de los componentes en la mezcla. Uno de estos factores es el pH de la solución. Para las biomoléculas, el intervalo de pH disponible para las purificaciones es, naturalmente, bastante limitado. Con el fin de evitar condiciones de pH que puedan afectar negativamente a la estabilidad de la molécula diana (p. ej., al fomentar la hidrólisis de la biomolécula), los valores de pH durante la carga y elución de la biomolécula de interés oscila típicamente entre pH 2 y pH 11, aunque los valores de pH generalmente se preferirán más cercanos a neutros, especialmente para biomoléculas que son sensibles a la degradación en condiciones ácidas o alcalinas. Por ejemplo, en algunas realizaciones, el pH de la solución que comprende la sal cosmotrópica en contacto con el material AEX (es decir, el "tampón de carga") está entre pH 4 y pH 9, o entre pH 5 y pH 8, o entre pH 6 y pH 10, o entre pH 6,0 y 8,0, p. ej., alrededor de pH 7,0. Los expertos en la técnica apreciarán que un experto en la técnica puede determinar las condiciones óptimas de pH mediante experimentos de rutina.
Se apreciará además que un cambio de pH, por ejemplo, durante la etapa de elución, puede cambiar el comportamiento/la fuerza de unión de las biomoléculas unidas al material AEX y, por lo tanto, puede usarse en algunas realizaciones para la liberación controlada y selectiva de la molécula diana del material AEX. Sin embargo, en otros casos, la unión de la molécula diana al material AEX será esencialmente independiente del pH. Por ejemplo, la unión del ADN plasmídico no cambió dentro de un amplio intervalo de pH (tan bajo como pH 2).
Con respecto a las condiciones seleccionadas para la elución de la molécula diana, la concentración de la sal caotrópica que proporciona un eluyente que contiene la molécula biológica purificada de interés es típicamente de aproximadamente 0,25 M a aproximadamente 4,0 M, o de aproximadamente 0,4 M a aproximadamente 3,0 M, o de aproximadamente 0,5 M a 2,0 M. Como es bien sabido en la técnica, la etapa de elución puede incluir una elución en gradiente variando la concentración de la sal (preferiblemente caotrópica) en el eluyente, lo que generalmente implica aumentar (continuamente o por etapas) la concentración de la sal caotrópica en el eluyente.
En algunas realizaciones, la sal caotrópica para la etapa de elución se selecciona del grupo que consiste en: cloruro de amonio, cloruro de potasio, cloruro de sodio, sulfato de magnesio, cloruro de magnesio, nitrato de magnesio, hidrocloruro de guanidinio y mezclas de los mismos. Una sal particularmente útil, especialmente para la purificación de ADN plasmídico, es sulfato de magnesio. En estas realizaciones, la concentración de sal caotrópica, p. ej., sulfato de magnesio o cloruro de sodio, es típicamente de al menos aproximadamente 0,5 M y, en algunos casos, puede variar de 0,5 M a aproximadamente 2,0 M o de aproximadamente 0,5 M a aproximadamente 1,0 M.
Nuevamente, como en el caso de la sal cosmotrópica contenida en el tampón de carga, la sal caotrópica y su concentración óptima para la elución de la molécula diana depende de la naturaleza de la molécula biológica de interés y del material AEX específico elegido para la purificación y puede determinarse fácilmente por un experto en la técnica a través de la experimentación de rutina (véanse los Ejemplos). Dado que el material AEX se puede reutilizar típicamente para otro proceso de purificación, puede ser útil agregar una elución de alta concentración de sal al final (p. ej., con NaCl aproximadamente 2,0 a 4,0 M) que eliminará esencialmente cualquier material unido del material AEX.
En principio, cualquier material AEX disponible puede usarse en el contexto del método de la presente invención. Por ejemplo, el método se puede aplicar con configuraciones AEX débiles y fuertes, con densidad de ligando alta y baja, con diferentes químicas de perlas y/o enlazadores. Materiales AEX adecuados están disponibles, por ejemplo, como una membrana de intercambio aniónico, una resina de intercambio aniónico, una estructura de hidrogel microporoso tridimensional, un lecho empaquetado de perlas superporosas, perlas macroporosas, un monolito, perlas de agarosa,
agarosa reticulada, perlas de sílice, geles de poros grandes, perlas a base de metacrilato, perlas a base de poliestireno, perlas a base de celulosa, perlas a base de dextrano, perlas a base de bisacrilamida, perlas a base de poliviniléter, perlas a base de material cerámico o perlas a base de polímeros. Ejemplos de materiales AEX disponibles comercialmente incluyen, entre otros, Sartobind Q®, Mustang Q®, Mustang E®, Poros XQ®, Poros HQ®, Nuvia Q®, Capt PolyQuat®, DEAE Sepharose®, NH2-750F®, Q Sepharose®, Giga Cap® Q-650M, Fractogel® EMD COO, NatriFlo® HD-Q y
3M™ Emphaze™ Purificador híbrido AEX (todos los nombres de marcas registradas).
Particularmente para purificaciones a mayor escala industrial, el método puede llevarse a cabo usando cromatografía de membrana AEX o cromatografía de lecho de resina. En algunas realizaciones, la membrana de intercambio aniónico tiene
un tamaño medio de poros de aproximadamente 3,0 gm a aproximadamente 5,0 gm, preferiblemente el tamaño medio de
poros es de aproximadamente 3,0 gm.
Alternativamente, el método puede llevarse a cabo usando cromatografía en columna AEX. En estas realizaciones, la resina de intercambio aniónico tiene preferiblemente un diámetro medio de partícula de aproximadamente 30 gm a aproximadamente 300 gm.
En cualquier caso, los expertos en la técnica apreciarán que el método descrito en este documento no requiere que el material AEX esté en una forma específica, es decir, otros materiales AEX en cualquier forma, como las otras alternativas mencionadas anteriormente, pueden también puede emplearse como el agente de purificación en el método de purificación descrito en este documento.
Dado que el método proporciona excelentes capacidades de purificación, típicamente se puede llevar a cabo en ausencia
de cualesquiera disolventes orgánicos, detergentes, glicoles, hexamina cobalto, espermidina y/o polivinilpirrolidona, por lo que ya no es necesario eliminar dichos agentes antes de proporcionar la molécula diana final en forma aislada.
Si bien la etapa de purificación AEX representa el aspecto principal de la presente invención, se apreciará que un método
de purificación para una biomolécula de interés incluirá típicamente más etapas del método, incluidas las etapas llevadas a cabo antes de la etapa de cromatografía AEX, pero también, opcionalmente, etapas adicionales realizadas después de la etapa de cromatografía AEX.
Como se señaló anteriormente, las moléculas biológicas de interés, como el ADN plasmídico, a menudo se obtienen a partir de células cultivadas en un denominado cultivo celular. En determinados casos, la molécula biológica de interés puede obtenerse del cultivo celular de una manera bastante directa cuando las células secretan la molécula en el medio
de cultivo celular circundante. Sin embargo, en la mayoría de los casos será necesario liberar la molécula diana de las células mediante la destrucción de las células vía lisis celular, lo que puede lograrse por medios físicos y/o químicos, como
es bien conocido en la técnica. La lisis celular producirá típicamente la molécula diana junto con un gran número de contaminantes solubles e insolubles en agua derivados de la célula huésped, tales como membranas celulares, organelas celulares, ADN genómico, ARN y proteínas de la célula huésped. Por lo tanto, una purificación de una molécula diana requerirá típicamente la eliminación de estos contaminantes, donde en particular los contaminantes sólidos (es decir, no solubles) se eliminan antes de la etapa de cromatografía AEX, típicamente por medios mecánicos.
En consecuencia, en algunas realizaciones de la presente invención, el método comprende, además, separar los componentes sólidos de la mezcla que comprende el ADN plasmídico de interés antes de poner en contacto la mezcla con
un material AEX.
La eliminación de los componentes sólidos de la mezcla a purificar puede lograrse, por ejemplo, mediante filtración o separación de fases. En algunos casos, esta etapa del método logra la eliminación de componentes sólidos a través de
una separación de dos fases tal como una separación de fase sólida-líquida.
Con el fin de lograr una mejor separación, la mezcla que comprende componentes sólidos puede modificarse en algunas realizaciones, por ejemplo, aumentando la densidad de la mezcla, por ejemplo a una densidad superior a aproximadamente
1,1 kg/L. Este aumento en la densidad de la mezcla da como resultado que los componentes sólidos (tales como residuos celulares u otra materia precipitada) floten sobre la mezcla. La solución que comprende el ADN plasmídico de interés se puede drenar convenientemente desde la parte inferior del recipiente/tanque que contiene la mezcla. El ajuste de la densidad, tal como por lo menos a aproximadamente 1,1 kg/L, por lo tanto produce una mezcla en la que no se requiere filtración para obtener una mezcla clarificada que puede someterse posteriormente a cromatografía AEX. La densidad de
la solución se puede aumentar generalmente mediante una diversidad de operaciones. Por ejemplo, una sal hidrosoluble, un carbohidrato (p. ej., glucosa, sacarosa, glicerol, etc.), urea u otros componentes que aumentan la densidad de una solución acuosa. Sin embargo, en particular en el contexto del método de purificación de la presente invención, puede ser ventajoso emplear una sal cosmotrópica que también sea adecuada para la etapa de carga de la etapa de cromatografía
AEX, tales como cualquiera de las sales cosmotrópicas descritas anteriormente en este documento.
Alternativamente, también se pueden lograr técnicas de separación de fases para eliminar contaminantes insolubles modificando la densidad de la mezcla de otras formas. Por ejemplo, al agregar alcoholes (p. ej., etanol, metanol, isopropanol, etc.) a la mezcla, la densidad disminuiría, lo que provocaría que los componentes sólidos sedimentaran en el fondo del recipiente o tanque (opcionalmente, la sedimentación podría ser asistida por centrifugación). Otra opción sería agregar compuestos líquidos no acuosos a la mezcla para establecer un sistema de dos fases líquido/líquido, p. ej., un sistema de dos fases PEG/sal, en donde las partículas insolubles estarán en la fase PEG y el ADN plasmídico en la fase
salina.
Además, se entenderá que en determinados casos aún se puede aplicar una filtración ligera, por ejemplo, una filtración de profundidad, ya sea para la parte líquida drenada de la mezcla y/o para el volumen restante final de la mezcla (para maximizar rendimientos). La etapa de filtración adicional opcional asegura la eliminación de cualquier partícula sólida restante en la parte líquida de la mezcla. En cualquier caso, se apreciará que una filtración de este tipo será mucho más rápida y no obstruirá el filtro debido al contenido de sólidos mucho más bajo en la mezcla. Los dispositivos de filtración de profundidad están disponibles comercialmente, por ejemplo, bajo el nombre de filtro de profundidad Clarisolve® de Merck-Millipore.
Dado que esta etapa del método también se puede utilizar en la fase preparatoria de otros métodos de purificación, la presente divulgación también describe las dos separaciones de fase anteriores per se, es decir, no seguida o no seguida necesariamente por la etapa de cromatografía AEX de la presente invención.
Los inventores también han encontrado que un recipiente o tanque en forma de tulipán es particularmente útil para la eliminación de componentes sólidos en la mezcla, particularmente cuando la densidad se ajusta a por lo menos aproximadamente 1,1 kg/L, lo que asegura que los componentes sólidos flotarán en la parte superior de la mezcla de dos fases sólido/líquido, es decir, en donde el diámetro del recipiente/tanque es mayor que en la parte inferior del recipiente del que se drena la fase líquida (véase, por ejemplo, el recipiente en forma de tulipán en la Figura 8). En consecuencia, el uso de un tanque o recipiente en forma de tulipán para la separación de dos fases descrita anteriormente representa otra parte de la presente divulgación.
La separación en dos fases descrita anteriormente representa un método altamente eficaz, rápido, reproducible y económico para preparar la solución que comprende la molécula biológica de interés para cualquier etapa de purificación posterior, como la etapa de cromatografía AEX de la presente invención. Particularmente cuando el ajuste de densidad ya se logra con una concentración relativamente alta de la sal cosmotrópica como se usa en la etapa de cromatografía AEX subsiguiente (p. ej., sulfato de amonio), la separación de dos fases puede ser la única etapa (posiblemente combinada con una filtración de profundidad antes de poner en contacto la mezcla con el material AEX) requerida después de recoger el sobrenadante celular. Dado que algunas de las sales cosmotrópicas actúan como tampón, otra ventaja de ajustar la densidad de la mezcla con dichas sales cosmotrópicas es que se requiere menos tampón de neutralización (para evitar la posible degradación de la molécula diana) inmediatamente después de la lisis celular.
Además, la eliminación conveniente de los componentes sólidos mediante el simple drenaje de la solución más densa que contiene la molécula diana es muy ventajosa para la filtración de profundidad posterior (aunque opcional), sobre todo porque el área de filtro requerida se reduce en gran medida como solo una pequeña fracción de las partículas insolubles se procesan sobre el filtro.
El método de cromatografía AEX de la presente invención puede contener, en algunas realizaciones, etapas adicionales después de la elución del ADN plasmídico purificado de interés. Por ejemplo, en algunos casos, el método comprende además la etapa de precipitar el ADN plasmídico de interés del eluyente. La precipitación se puede lograr mediante una diversidad de métodos generalmente conocidos en la técnica, tales como cambiar el pH de las fracciones de eluyente que comprenden la molécula diana o agregar antidisolventes u otros aditivos al eluyente, provocando así que la molécula diana precipite del eluyente.
Después de la precipitación, el método puede comprender, en algunos casos, además, filtrar el eluyente mediante filtración de flujo tangencial para aislar el ADN plasmídico precipitado. Por ejemplo, en algunos casos, el tamaño medio de los poros de la membrana de filtración utilizada en la etapa de filtración de flujo tangencial será < 0,45 gm o incluso < 0,2 gm.
En algunos casos, el método puede incluir, además, la liofilización del ADN plasmídico purificado de interés, opcionalmente en presencia de un carbohidrato que puede estabilizar el ADN plasmídico en forma liofilizada durante el almacenamiento. Se pueden usar muchos monosacáridos o disacáridos para dicho propósito, como se sabe generalmente en la técnica.
En otras realizaciones, el método incluirá, además. la dilución, concentración o intercambio de tampón de la(s) fracción(es) que comprende(n) la molécula diana purificada. En determinados casos, la molécula diana puede modificarse químicamente (p. ej., biotinilación, metilación, acetilación) o cortarse en trozos más pequeños (p. ej., digestión por enzimas de restricción en el caso de los ácidos nucleicos).
Dependiendo del problema de purificación específico y de la fuente de la molécula diana, en algunos casos puede ser útil recoger adicionalmente el flujo de la etapa de carga (es decir, la etapa de poner en contacto la mezcla con un material AEX en presencia de la solución que comprende la sal cosmotrópica a una concentración superior a aproximadamente 0,5 M, lo que permite la unión selectiva del ADN plasmídico al material de intercambio aniónico).
Como se comenta en este documento, la etapa de cromatografía AEX es capaz de unir selectivamente un ADN plasmídico de interés al material AEX, es decir, la mayoría de los componentes no deseados de la mezcla no se unirán al material AEX en estas condiciones de carga. Por ejemplo, para la purificación de ADN plasmídico de un cultivo celular, el flujo continuo puede comprender ARN, ADN genómico, proteínas, fracciones celulares o combinaciones de los mismos. En algunas realizaciones, el flujo continuo comprenderá sustancialmente todo (es decir, al menos el 80 %, al menos el 90 % o incluso al menos el 95 %) el ARN que estaba presente en la mezcla en contacto con el material AEX.
En algunos casos, la purificación puede mejorarse incluyendo, además, una etapa de lavado. Por lo tanto, en algunas realizaciones, el método comprenderá además lavar el material AEX con una solución tampón de lavado antes de la elución del ADN plasmídico de interés. En algunos casos, el lavado puede continuar con un tampón de "carga" limpio adicional (es decir, que comprende una sal cosmotrópica en una concentración relativamente alta). En otros casos, una solución tampón de lavado puede comprender una sal caotrópica en una concentración inferior a la concentración requerida para la elución de la molécula biológica de interés.
En estos casos, el tampón de lavado también puede comprender todavía la sal cosmotrópica (posiblemente en menor concentración que en el tampón de carga), o puede comprender solo la sal caotrópica. La sal caotrópica para el tampón de lavado se selecciona preferiblemente del grupo que consiste en: cloruro de amonio, cloruro de potasio, cloruro de sodio, sulfato de magnesio, cloruro de magnesio, nitrato de magnesio y mezclas de los mismos. En particular, cuando la sal caotrópica no tiene capacidad tampón, el tampón de lavado puede comprender, además, una sustancia tampón adecuada para mantener el pH en el nivel deseado. Para simplificar, el tampón de lavado comprenderá en muchos casos la misma sal caotrópica que el eluyente, aunque esto puede no ser necesario en términos de eficiencia de purificación.
Se apreciará, además, que, particularmente cuando la purificación de la molécula diana debe producir el producto a un nivel muy alto de pureza, el método de la presente invención puede comprender, además, una etapa de purificación adicional, que típicamente sigue a la etapa de elución y, opcionalmente, aislar la molécula biológica de la etapa de cromatografía AEX. En algunas realizaciones en las que la molécula diana a purificar es ADN plasmídico superenrollado, la segunda etapa de purificación puede implicar, por lo tanto, el uso de un medio de cromatografía de adsorción aromática tiofílico, disponible por ejemplo de GE Healthcare Life Sciences con el nombre comercial PlasmidSelect Xtra®, o abreviado "PSX"). Se sabe que esta resina particular tiene una excelente selectividad para separar el ADN plasmídico superenrollado del ADN plasmídico lineal y/o circular abierto y, por lo tanto, puede usarse para el enriquecimiento final de la conformación superenrollada del ADN de calidad farmacéutica.
En algunas realizaciones, el método comprenderá, además, después de la purificación y el aislamiento del ADN plasmídico, una etapa adicional de utilizar dicho ADN plasmídico para la expresión de un polipéptido de interés codificado por dicho ADN plasmídico. El polipéptido producido a través del ADN plasmídico típicamente se recogerá y, opcionalmente, se purificará. Finalmente, el método puede incluso, en algunos casos, incluir la formulación del polipéptido (obtenido mediante la expresión del ADN plasmídico purificado) en una composición farmacéutica que puede comprender opcionalmente uno o más excipientes farmacéuticamente aceptables.
Alternativamente, cuando el ADN plasmídico está destinado al uso farmacéutico directamente, el método puede incluir la formulación del ácido nucleico en una composición farmacéutica, que nuevamente puede comprender opcionalmente uno o más excipientes farmacéuticamente aceptables. El ADN plasmídico purificado por el método de la presente invención se puede usar como una vacuna basada en ADN o se puede usar como un "profármaco" en el que el plásmido luego involucrará el aparato de transcripción y traducción de la célula para biosintetizar la entidad terapéutica in situ.
En aún otras realizaciones, el método comprenderá, además, el uso del ADN plasmídico purificado para la producción de ARN, incluidos fármacos basados en ARN, para la producción de oligonucleótidos más cortos, tales como ARNip o aptámeros (segmentos cortos de ácido nucleico monocatenario (típicamente 20-60 nucleótidos), o para la producción de ADNzimas (análogos de ribozima con una cadena principal de ARN reemplazada por motivos de ADN que confieren una estabilidad biológica mejorada).
Una variante preferida del método de purificación que implica cromatografía AEX comprende, antes de dicha etapa de cromatografía AEX, las etapas de recolección y lavado de células, lisis celular, neutralización y eliminación de floculados antes de poner en contacto la solución que comprende el ADN plasmídico de interés con el material AEX.
Como se indicó anteriormente, las condiciones identificadas para la etapa de carga de AEX permiten la unión selectiva del ADN plasmídico al material AEX. Por lo tanto, el ARN, que típicamente también se une al material AEX en condiciones estándar bajas en sal, no se une o no se une sustancialmente al material AEX en las condiciones de carga descritas en este documento y, por lo tanto, puede eliminarse cuantitativamente de la molécula diana en una sola etapa.
El método descrito en este documento tiene la gran ventaja de que no es necesario eliminar el ARN con una etapa de precipitación de cloruro de calcio (CaCk). Por supuesto, evitar etapas de purificación adicionales es beneficioso en términos de rendimiento, costos y duración del método de purificación global. En consecuencia, el método en determinadas realizaciones se caracteriza, además, porque no comprende una etapa de precipitación de cloruro de calcio (CaCk).
Lo mismo es cierto para las proteínas que tampoco se unen al material AEX en las condiciones identificadas en este documento. Dado que el ADNp circular abierto, el ADNp lineal y el ADN genómico tienen todos una fuerza de interacción diferente con los ligandos AEX en comparación con el ADN plasmídico superenrollado, sus niveles pueden reducirse considerablemente durante la etapa de cromatografía AEX. En consecuencia, el método como se describe y reivindica en este documento permite la purificación simple, rápida, altamente efectiva y económica de ADN plasmídico de interés que involucra esencialmente solo una única etapa cromatográfica que involucra materiales que tienen ligandos AEX.
Muchas etapas adicionales comúnmente necesarias en los procedimientos de purificación de ADN plasmídico descritos en la técnica anterior, tales como el intercambio de tampón, filtraciones de profundidad (múltiples), se puede evitar la precipitación de CaCl2 o etapas cromatográficas adicionales, tales como la cromatografía PSX (dependiendo del contenido
requerido de ADNp sc). Finalmente, el método descrito en este documento permite escalarlo para grandes plantas de producción.
Habiendo descrito los diversos aspectos de la presente invención en términos generales, será evidente para los expertos en la técnica que son posibles muchas modificaciones y ligeras variaciones sin apartarse del alcance de la presente invención.
EJEMPLOS
Ejemplo 1: Detecciónde las condiciones de unión y elución con material de intercambio aniónico Sartobind Q para una muestra de ADN plasmídico (pUC19)
Todos los tampones utilizados durante todo el proceso se filtraron a través de filtros de 0,2 gm antes de su uso. Se cultivaron, lisaron y aclararon células de E. coli que albergaban el plásmido pUC19 (una descripción esquemática de este ADN plasmídico se encuentra en la Fig. 1) mediante métodos de filtración como se describe con más detalle a continuación.
Las células se cultivaron en biorreactores a pequeña escala en condiciones de lote alimentado hasta una densidad óptica de 65 - 90, medida a 600 nm (DO600). Las células se recogieron por centrifugación (4.400 - 4.800, 45 minutos). Las células recogidas al final del crecimiento celular se resuspendieron en tampón P1 (Tris 50 mM, EDTA 10 mM; pH 7,4). Luego se añadió tampón P2 (NaOH 0,2 M, SDS al 1% (p/v)) en una relación 1:1 (v/v), con el fin de realizar la lisis alcalina de las células. La mezcla se homogeneizó suavemente y se dejó reposar a temperatura ambiente durante 5 minutos. Para detener la lisis celular y neutralizar la mezcla, se añadió el volumen adecuado de tampón P3 frío (acetato de potasio 5 M, ácido acético, 4 °C), aproximadamente el 25 % en volumen de los demás tampones. Después de una suave homogeneización, se añadió el tampón de acondicionamiento que contenía sulfato de amonio 3 M en una relación de 1:1 (v/v), con el fin de cambiar la densidad de la solución, lo que provocó que los restos celulares flotaran en la parte superior de la solución. A continuación, la solución se sometió a una filtración de profundidad final (filtro de profundidad Clarisolve, Merck-Millipore, con tamaños de poro de 40 a 0,5 gm) para eliminar cualquier residuo celular restante, así como algunas proteínas y ADN genómico precipitados. Después de la filtración, el pH de la solución filtrada se ajustó a pH 7,0 añadiendo un volumen apropiado de NaOH 1 M al filtrado.
La detección de las condiciones de unión y elución se realizó en un robot de manipulación de líquidos (Freedom Evo 150; Tecan) y permitió ejecutar 96 etapas de cromatografía en paralelo. Se usaron placas de pocillos Sartobind Q 96 (Cat n°: 991EXQ42GC — V, Sartorius) para la detección. El acondicionamiento de la carga se realizó cambiando el tampón con la ayuda de placas desaladoras Zeba Spin (Cat n° 89808, ThermoScientific) y el respectivo tampón de unión. Las unidades Sartobind Q se equilibraron con el tampón de unión antes de aplicar 2,0 mL de la solución de carga. La membrana se lavó con 1 mL del respectivo tampón de unión y 1 mL de tampón de lavado (fosfato sódico 20 mM, pH 7,5). El material se eluyó aplicando 1 mL de tampón de elución seguido de una etapa de extracción con 1 mL de NaCl 4 M. Los análisis de las muestras se realizaron por electroforesis en gel de agarosa (AGE), en donde se pueden estimar cantidades y calidades.
a) Detección de tampón de unión
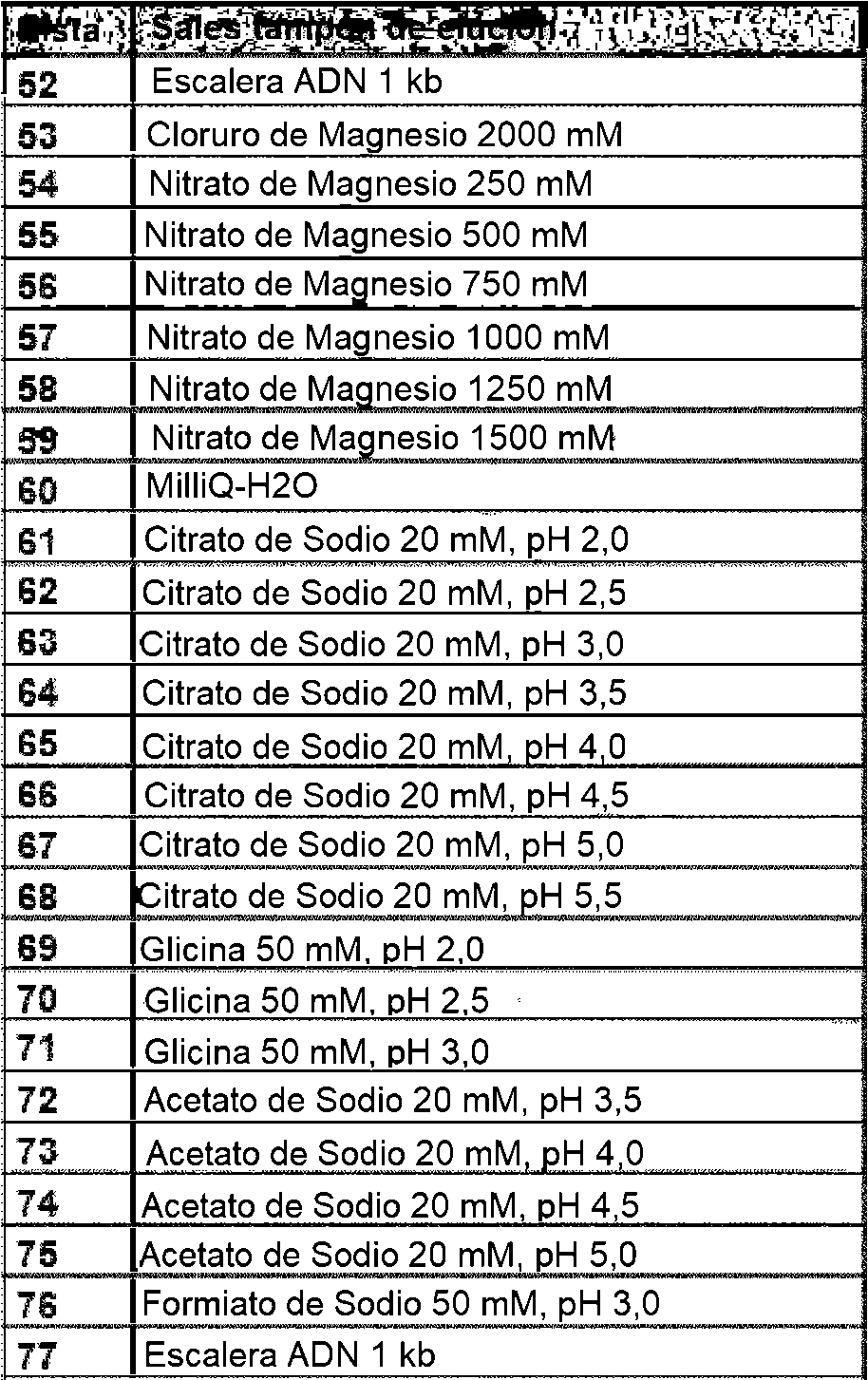
En una primera ronda, se detectaron varios tampones de unión a diferentes concentraciones y la elución se realizó con un tampón de elución que comprendía NaCl 2 M en fosfato sódico 20 mM a pH 7,5. Los geles de agarosa se cargaron con productos eluidos de acuerdo con Tabla 1 que figura más adelante. Las sales tampón de unión enumeradas en la tabla se usaron junto con fosfato de sodio 20 mM a pH 7,0, a menos que se indique lo contrario.
Tabla 1. Esquema de carga de muestras sometidas a diferentes condiciones de tampón de unión
!
Los resultados del esfuerzo de detección del tampón de unión se muestran en las Figuras 2A a 2D, en donde el panel superior e inferior muestran el mismo gel después de diferentes tiempos de exposición (panel superior = tiempo de exposición más corto; panel inferior = tiempo de exposición más largo). El marcaje en el lado derecho del gel representa las bandas de impurezas de ADN plasmídico pUC19 y ARN pUC19 circulares abiertas (oc) y superenrolladas (sc) dentro del gel de agarosa.
Los resultados sugieren que la unión a altas concentraciones de sal es factible, particularmente cuando se usan sales cosmotrópicas (p. ej., citrato de amonio, sulfato de amonio, fosfato de amonio, citrato de potasio, fosfato de potasio, citrato de sodio, fosfato de sodio, etc.), y es esencialmente independiente del pH del tampón de unión. Los resultados también demuestran que, particularmente a concentraciones de sal más altas, la unión de ARN se reduce notablemente en comparación con la carga (véanse las pistas 50 y 101) o no se une en absoluto (p. ej., pistas 10 - 15).
b) Detección del tampón de elución
En una segunda ronda, se examinaron varios tampones de elución a diferentes concentraciones y la unión de la mezcla de muestra se logró con un tampón de unión que comprendía fosfato de Na 20 mM y sulfato de amonio 1,5 M a pH 7,0. Los geles de agarosa se cargaron con productos eluidos de acuerdo con la Tabla 2 que figura más adelante. Las sales de tampón de elución enumeradas en la tabla se usaron junto con fosfato de Na 20 mM a pH 7,0, a menos que se indique lo contrario.
Tabla 2. Esquema de carga de muestras sometidas a diferentes condiciones de tampón de elución
Los resultados del esfuerzo de detección del tampón de elución se muestran en las Figuras 3A a 3D, en las que el panel superior e inferior muestran el mismo gel después de diferentes tiempos de exposición (panel superior = tiempo de exposición más corto; panel inferior = tiempo de exposición más largo). El marcaje en el lado derecho del gel representa las bandas de impurezas de ADN plasmídico de pUC19 y ARN circulares abiertas (oc) y superenrolladas (sc) dentro del gel de agarosa.
Los resultados demuestran que el ADN plasmídico se puede eluir de la resina AEX cuando se usan sales caotrópicas (p. ej., cloruro de amonio, cloruro de potasio, cloruro de sodio, sulfato de magnesio, cloruro de magnesio, nitrato de magnesio, etc.), incluso en los casos en los que la conductividad del tampón de elución es significativamente menor que la conductividad del tampón de unión. Además, la mayoría de los tampones de elución testados eluyen el ADNp sc mejor que el ADNp oc y no eluyen el ARN. Sin embargo, se observó que determinadas sales caotrópicas, p. ej., nitrato de magnesio, preferentemente ADNp oc eluido frente a ADNp sc (véase la Fig. 3C).
Ejemplo 2: Purificación de pUC19 utilizando Sartobind Q y sulfato de magnesio para la elución con un sistema tampón fosfato
a) Procedimiento de purificación
Todos los tampones utilizados durante todo el proceso se filtraron a través de filtros de 0,2 gm. Se cultivaron y lisaron células de E. coli que albergaban el plásmido pUC19 como se describe en el Ejemplo 1.
La solución de 150 mL que contenía pUC19 se acondicionó con 150 mL de tampón acondicionador (fosfato de Na 40 mM, pH 7,0, sulfato de amonio 3 M). La unidad de cromatografía se equilibró con 20 volúmenes de columna (CVs) de fosfato de Na 20 mM, sulfato de amonio 1,5 M, pH 7,0 a un caudal de 4 CVs/min. A continuación, se aplicó la carga acondicionada a la unidad de intercambio de aniones. La unidad se lavó aplicando 20 CVs de tampón de equilibrio seguido de un segundo lavado de 20 CVs de tampón de lavado 2 (fosfato de Na 20 mM, sulfato de magnesio 0,5 M, pH 7,0) que se encontró que eliminaba las impurezas de ARN. A continuación, se eluyó el ADN del plásmido aplicando un gradiente del tampón de lavado 2 al tampón de elución (fosfato de Na 20 mM, sulfato de magnesio 1,0 M, pH 7,0) en 25 CVs. Finalmente, la unidad de cromatografía se depuró aplicando 30 CVs de NaCl 4 M.
Un perfil de cromatografía representativo de la unidad de intercambio de aniones (Sartobind Q) se muestra en la Figura 4 con un zoom en el gradiente de elución. Se establecieron dos grupos: el Grupo 1 que comprende las fracciones 1C2 a 2B4
(recuadro gris claro) y el Grupo 2 que comprende las fracciones 1C4 a 2B2 (recuadro gris oscuro).
b) Evaluación de impurezas residuales
Las fracciones de la etapa de cromatografía AEX con Sartobind Q se analizaron mediante electroforesis en gel de agarosa (véase la Tabla 3 que figura a continuación para el esquema de carga del gel de agarosa) y los resultados se muestran en la Figura 5.
Tabla 3: Esquema de carga de fracciones de la etapa de cromatografía de intercambio aniónico (Sartobind Q) analizadas por electroforesis en gel de agarosa.
Se cargaron grandes cantidades en el gel de agarosa para visualizar las impurezas. La Figura 5 muestra que el ARN se eliminó en gran medida durante la segunda etapa de lavado (véase, p. ej., la pista 4; tampón de lavado: Tris-base 50 mM/TAPS (ácido [tris(hidroximetil)metilamino]propanosulfónico), sulfato de magnesio 0,5 M, pH 7,0). Para el gradiente de elución en las condiciones elegidas, se observó que el ADNp oc tenía un tiempo de retención más bajo que el ADNp SC (véase de nuevo la Figura 5).
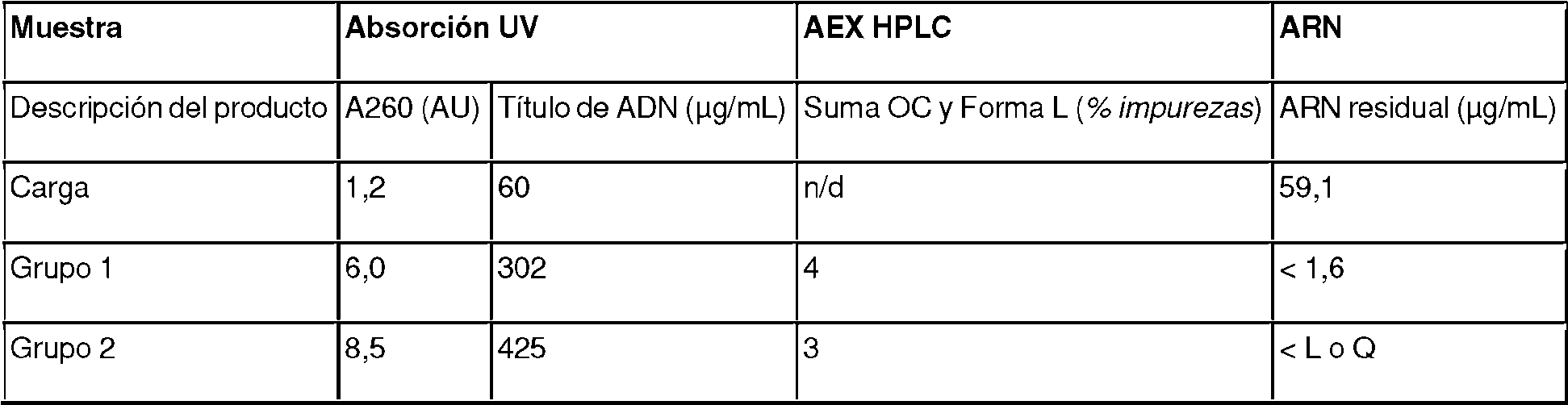
Las fracciones de la etapa de cromatografía AEX (Sartobind Q) también se analizaron por HPLC. Trazas de AEX-HPLC del grupo de elución 1 de Sartobind Q (véase la Figura 4 ; línea discontinua) y un patrón (línea continua) se muestran en la Figura 6 y los resultados se resumen en la Tabla 4 que figura más abajo. Para medir el ARN residual dentro del grupo de carga y elución 1, el ADNp se transfirió al agua realizando una etapa de filtración de flujo tangencial (casete Pellicon 3, 30 kDa, tamiz C, membrana Ultracel, Cat. n°: P3C030C00, Merck Millipore). Dado que el grupo 2 era un subconjunto del grupo 1, no se midió el ARN residual para el grupo 2.
Tabla 4: Resultados analíticos para el funcionamiento de la unidad AEX.
Los resultados resumidos en la Tabla 4 anterior demuestran que el ARN se eliminó cuantitativamente. El ADNp oc y el ADNp lineal se redujeron a niveles bajos de 4 % y 3 % para el Grupo 1 y el Grupo 2, respectivamente. En conjunto, la elución en gradiente permitió la separación del ARN, así como el ADN plasmídico circular abierto (ADNp oc) del ADN plasmídico superenrollado (ADNp sc). El análisis SDS-PAGE (Figura 7) confirmó que las impurezas proteínicas también se eliminaron cuantitativamente mediante la etapa de cromatografía AEX (véase la Tabla 5 para el esquema de carga del gel SDS-PAGE).
Tabla 5: Esquema de carga de muestras analizadas por SDS-PAGE.
Ejemplo 3: Proceso mejorado de recuperación primaria y purificación de ADNp pUC19 utilizando Sartobind Q y sulfato de magnesio para la elución con un sistema tampón Tris
Células de E. coli que albergan el plásmido pUC19 se cultivaron y lisaron como se describe con más detalle a continuación. Todos los tampones utilizados durante todo el proceso se filtraron a través de filtros de 0,2 pm. Una representación esquemática del proceso de recuperación primaria que incluye la etapa de cromatografía AEX se muestra en la Figura 8.
Para la recuperación primaria, se suspendió un sedimento de 76,4 g de E. coli que albergaba el plásmido pUC19 con 764 mL de tampón de suspensión (Tris 50 mM, EDTA 10 mM) durante 1 hora. La adición de 764 mL de tampón de lisis (SDS al 1 %, NaOH 0,2 M) inició la lisis de las células. El proceso de lisis se detuvo después de 4 minutos mediante la adición de 198 mL de tampón de neutralización (acetato de potasio 3 M, ácido acético 2 M, enfriado a 5 °C). Se encontró que 0,26 volúmenes son suficientes para la neutralización.
Se acondicionaron 1800 mL de la solución neutralizada en un tanque con forma de tulipán agregando 1800 mL de tampón acondicionador (Tris-base/TAPS 200 mM, sulfato de amonio 3 M, pH 7,0) para aumentar la densidad de la solución. El tanque en forma de tulipán facilita la eliminación de partículas insolubles y, por lo tanto, mejora el comportamiento de filtración de la solución acondicionada cuando se aplica a un filtro de profundidad (Clarisolve; Cat n°: CS40MS01L3; 40 pm, Merck Millipore). El valor de pH del filtrado se ajustó a 7,0 mediante la adición de 194 mL de NaOH 1 M.
La unidad de cromatografía se equilibró con 20 volúmenes de columna (CVs) de Tris-base/TAPS 50 mM, sulfato de amonio 1,5 M, pH 7,0 a un caudal de 4 CVs/min. A continuación, el filtrado profundo se aplicó a la unidad AEX (Sartobind Q; Catn° 96IEXQ42EUC11-A; volumen de lecho de 3 mL; Sartorius). La unión del ADN plasmídico se realizó a una concentración de sulfato de amonio 1,5 M. El flujo continuo de carga mostró altos valores de absorbancia, lo que indica que las proteínas y una cantidad significativa de especies de ARN no se unieron al material AEX en estas condiciones de carga. A continuación, la unidad se lavó aplicando 20 CVs de tampón de equilibrio seguido de un segundo lavado con 20 CVs de tampón de lavado (Tris-Base/TAPS 50 mM, sulfato de magnesio 0,5 M, pH 7,0) para eliminar las impurezas de ARN. El ADN plasmídico se eluyó aplicando un gradiente de lavado a tampón de elución (Tris-Base/TAPS 50 mM, sulfato de magnesio 1,0 M, pH 7,0) en 25 CVs. La elución en gradiente permitió la separación de principalmente dos especies, en las que el primer pico contenía ADNp oc y el segundo pico contenía ADNp sc. La unidad de cromatografía se depuró finalmente aplicando 30 CVs de NaCl 4 M. Un perfil de cromatografía representativo de la unidad de intercambio de aniones (Sartobind Q) se muestra en la Figura 9.
Claims (15)
1. Un método para aislar o purificar un ADN plasmídico ("ADNp") de interés a partir de una mezcla, comprendiendo el método:
poner en contacto la mezcla con un material de intercambio aniónico en presencia de una solución que comprende una sal cosmotrópica a una concentración que permite la unión selectiva del ADN plasmídico (ADNp) de interés al material de intercambio aniónico;
en el que la sal cosmotrópica se selecciona del grupo que consiste en: sulfato de amonio, citrato de amonio, fosfato de amonio, fosfato de potasio, citrato de sodio, fosfato de sodio y mezclas de los mismos;
en el que la concentración de la sal cosmotrópica es superior a aproximadamente 0,5 M; y
eluir la molécula de ácido nucleico de interés con un eluyente que comprende una sal caotrópica a una concentración que proporciona un eluyente que contiene la molécula de ácido nucleico purificada; opcionalmente en el que
(i) se recoge(n) la(s) fracción(es) que comprende(n) dicha molécula de ácido nucleico en el eluyente; y/o
(ii) dicha molécula de ácido nucleico de interés se aísla de cualquiera o todas las fracciones recogidas; y/o
(iii) el método se lleva a cabo en ausencia de disolventes orgánicos, detergentes, glicoles, hexamina cobalto, espermidina y/o polivinilpirrolidona.
2. El método de la reivindicación 1, en el que
(i) el ADN plasmídico es ADN plasmídico superenrollado (ADNp sc); y/o
(ii) el ADN plasmídico comprende ADN de mamífero, ADN bacteriano, ADN no codificante o ADN viral; opcionalmente en el que el ADN plasmídico comprende ADN capaz de expresar un polipéptido de interés; y/o
(iii) la mezcla comprende ADN plasmídico superenrollado, ADN plasmídico circular abierto, ADN plasmídico lineal, ADN genómico, ARN, lipopolisacáridos, endotoxinas, proteínas o cualquier combinación de los mismos.
3. El método de la reivindicación 1 o la reivindicación 2, en el que la pureza del ADN plasmídico purificado y/o aislado es al menos del 90 %, o al menos del 95 %, o al menos del 98 %.
4. El método de una cualquiera de las reivindicaciones 1 a 3, en el que
(i) la concentración de la sal cosmotrópica es de aproximadamente 0,8 M a aproximadamente 4,0 M; y/o (ii) la concentración de la sal caotrópica que proporciona un eluyente que contiene la molécula de ácido nucleico purificado es de aproximadamente 0,25 M a aproximadamente 4,0 M; y/o
(iii) la etapa de elución comprende una elución en gradiente variando la concentración de la sal caotrópica en el eluyente; opcionalmente en el que se aumenta la concentración de la sal caotrópica en el eluyente.
5. El método de una cualquiera de las reivindicaciones 2 a 4, en el que la etapa de elución incluye el fraccionamiento del ADN plasmídico superenrollado de otras formas de ADN plasmídico, tales como el ADN plasmídico lineal y el ADN plasmídico circular abierto y, opcionalmente, otras moléculas de ácido nucleico.
6. El método de una cualquiera de las reivindicaciones 1 a 5, en el que
(i) la sal cosmotrópica es sulfato de amonio; opcionalmente en el que la concentración de sulfato de amonio es de aproximadamente 0,5 M a aproximadamente 2,0 M; y/o
(ii) en el que la sal caotrópica se selecciona del grupo que consiste en: cloruro de amonio, cloruro de potasio, cloruro de sodio, sulfato de magnesio, cloruro de magnesio, nitrato de magnesio, hidrocloruro de guanidinio y mezclas de los mismos, en el que opcionalmente la sal caotrópica es sulfato de magnesio; además, opcionalmente, en el que la concentración de sulfato de magnesio es de aproximadamente 0,5 M a aproximadamente 1,0 M; y/o
(iii) la solución que comprende la sal cosmotrópica tiene un pH en el intervalo de aproximadamente 5,0 a aproximadamente 10,0, o de aproximadamente 5,0 a aproximadamente 8,0, o de aproximadamente 6,0 a aproximadamente 8,0, o aproximadamente pH 7.
7. El método de una cualquiera de las reivindicaciones 1 a 6, en el que el material de intercambio aniónico se selecciona de una membrana de intercambio aniónico, una resina de intercambio iónico, una estructura de hidrogel microporoso tridimensional, un lecho empaquetado de perlas superporosas, perlas macroporosas, un monolito, perlas de agarosa, agarosa reticulada, perlas de sílice, geles de poros grandes, perlas a base de metacrilato, perlas a base de poliestireno, perlas a base de celulosa, perlas a base de dextrano, perlas a base de bisacrilamida, perlas a base de poliviniléter, perlas a base de cerámica, o perlas a base de polímeros;
opcionalmente en el que el material de intercambio aniónico es
(i) una membrana de intercambio aniónico; opcionalmente en el que la membrana de intercambio aniónico tiene un tamaño medio de poros de aproximadamente 3,0 pm a aproximadamente 5,0 pm; preferiblemente en el que el tamaño medio de los poros es de aproximadamente 3,0 pm; o
(ii) una resina de intercambio iónico, opcionalmente en el que la resina de intercambio iónico tiene un diámetro medio de partícula de aproximadamente 30 pm a aproximadamente 300 pm.
8. El método de una cualquiera de las reivindicaciones 1 a 7, en el que el método comprende, además, separar los componentes sólidos de la mezcla que comprende la molécula de ácido nucleico de interés antes de poner en contacto la mezcla con un material de intercambio aniónico en presencia de la solución que comprende la sal a una concentración que permita la unión selectiva de la molécula de ácido nucleico al material de intercambio aniónico, opcionalmente en el que dicha eliminación de componentes sólidos se logra mediante filtración o separación de fases.
9. El método de la reivindicación 8, en el que la eliminación de componentes sólidos se logra a través de la separación de dos fases,
opcionalmente en el que
(i) se añade un tampón para aumentar la densidad de la mezcla para que sea superior a aproximadamente 1,1 kg/L, opcionalmente en el que el tampón comprende una sal cosmotrópica, preferiblemente en el que la sal cosmotrópica es sulfato de amonio; y/o
(ii) en el que la fase inferior de la mezcla de dos fases que tiene una densidad mayor que la fase superior se somete a una filtración de profundidad.
10. El método de una cualquiera de las reivindicaciones 1 a 9, en el que el método comprende, además, la etapa de (i) precipitar la molécula de ácido nucleico del eluyente; y/o
(ii) filtrar el eluyente por filtración de flujo tangencial para aislar la molécula de ácido nucleico; opcionalmente en el que el tamaño medio de los poros de la membrana de filtración utilizada en la etapa de filtración de flujo tangencial es < 0,2 pm; y/o
(iii) liofilizar la molécula de ácido nucleico purificada de interés, en el que opcionalmente la liofilización se lleva a cabo en presencia de un carbohidrato; y/o
(iv) recoger un flujo continuo tras la etapa de poner en contacto la mezcla con un material de intercambio aniónico en presencia de la solución que comprende la sal a una concentración que permita la unión selectiva de la molécula de ácido nucleico al material de intercambio aniónico; opcionalmente en el que el flujo continuo comprende ARN, ADN genómico, proteínas, fracciones celulares o combinaciones de los mismos, preferiblemente en el que el flujo continuo comprende ARN; y/o
(v) lavar el material de intercambio aniónico con una solución tampón de lavado antes de la elución de la molécula de ácido nucleico de interés; opcionalmente en el que la solución tampón de lavado comprende una sal caotrópica a una concentración inferior a la concentración requerida para la elución de la molécula de ácido nucleico de interés, en el que la sal caotrópica se selecciona preferentemente del grupo que consiste en: cloruro de amonio, cloruro de potasio, cloruro de sodio, sulfato de magnesio, cloruro de magnesio, nitrato de magnesio y mezclas de los mismos.
11. El método de una cualquiera de las reivindicaciones 1 a 10, en el que el método comprende, además, una etapa de purificación adicional que sigue a la etapa de eluir y, opcionalmente, aislar la molécula de ácido nucleico; opcionalmente, en el que la segunda etapa de purificación comprende el uso de un medio de cromatografía de adsorción aromática tiófila que tiene una selectividad que permite separar el ADN plasmídico superenrollado del ADN circular abierto y/o ADN lineal.
12. El método de una cualquiera de las reivindicaciones 1 a 11, en el que el método comprende, además, la etapa de (i) usar el ácido nucleico para expresar un polipéptido de interés; preferiblemente en el que el ácido nucleico es
ADN plasmídico; o
(ii) usar el ácido nucleico para producir y recoger un polipéptido de interés; preferiblemente en el que el ácido nucleico es ADN plasmídico; opcionalmente, en el que el método comprende, además, la etapa de formular el polipéptido de interés en una composición farmacéutica.
13. El método de una cualquiera de las reivindicaciones 2 a 11, en el que el método comprende, además, la etapa de utilizar el ADN plasmídico purificado para la producción de ARN.
14. El método de una cualquiera de las reivindicaciones 1 a 13, en el que el método incluye las etapas de recogida y lavado de células, lisis celular, neutralización y eliminación de floculados antes de poner en contacto la mezcla resultante que comprende la molécula de ácido nucleico de interés con el material de intercambio aniónico.
15. El método de una cualquiera de las reivindicaciones 1 a 14, en el que el método no comprende una etapa de precipitación de CaCl2 para eliminar el ARN.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP19160132.7A EP3663401B1 (en) | 2019-02-28 | 2019-02-28 | Purification process for biological molecules such as plasmid dna using anionic exchange chromatography |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2929470T3 true ES2929470T3 (es) | 2022-11-29 |
Family
ID=65801825
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES19160132T Active ES2929470T3 (es) | 2019-02-28 | 2019-02-28 | Procedimiento de purificación de moléculas biológicas tales como ADN plasmídico utilizando cromatografía de intercambio aniónico |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US20220145283A1 (es) |
| EP (2) | EP3663401B1 (es) |
| JP (1) | JP7566762B2 (es) |
| KR (1) | KR102919038B1 (es) |
| CN (1) | CN113518822A (es) |
| CA (1) | CA3130855A1 (es) |
| DK (1) | DK3663401T3 (es) |
| ES (1) | ES2929470T3 (es) |
| LT (1) | LT3663401T (es) |
| PL (1) | PL3663401T3 (es) |
| SG (1) | SG11202108893SA (es) |
| WO (1) | WO2020174085A1 (es) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN118904316A (zh) | 2018-12-12 | 2024-11-08 | 唐纳森公司 | 亲和膜及其制备方法 |
| CN113388609B (zh) * | 2021-06-21 | 2022-09-13 | 上海碧博生物医药科技有限公司 | 大型质粒dna的纯化方法 |
| EP4234695A1 (en) * | 2022-02-24 | 2023-08-30 | Sartorius BIA Separations d.o.o. | Methods for the selective removal of contaminants during a process of purifying biologic agents |
| CN114907430B (zh) * | 2022-06-21 | 2023-12-01 | 中国科学院过程工程研究所 | 一种mRNA的分离纯化方法 |
| CN115337916B (zh) * | 2022-07-29 | 2023-10-24 | 福建卫生职业技术学院 | 一种水凝胶型细胞膜半制备色谱柱及其制备方法与应用 |
| CN115612684A (zh) * | 2022-11-01 | 2023-01-17 | 北京启辰生生物科技有限公司 | Gmp级质粒dna大规模简化生产方法 |
| KR20260046476A (ko) | 2023-08-02 | 2026-04-07 | 메르크 파텐트 게엠베하 | 플라스미드 dna의 정제 방법 |
| CN116899633B (zh) * | 2023-09-13 | 2023-12-19 | 赛普(杭州)过滤科技有限公司 | 一种亲水阴离子交换层析介质及其制备方法与应用 |
| CN117434180A (zh) * | 2023-10-27 | 2024-01-23 | 苏州百因诺生物科技有限公司 | 可提高细胞裂解液中质粒dna分离度的液相色谱检测方法及质粒dna浓度的检测方法 |
| WO2026037771A1 (en) | 2024-08-12 | 2026-02-19 | F. Hoffmann-La Roche Ag | Method for purifying recombinant plasmid dna |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6214586B1 (en) | 1997-12-08 | 2001-04-10 | Genzyme Corporation | Method for purifying plasmid DNA and plasmid DNA substantially free of genomic DNA |
| US6270970B1 (en) | 1999-05-14 | 2001-08-07 | Promega Corporation | Mixed-bed solid phase and its use in the isolation of nucleic acids |
| EP2246413A3 (en) * | 2004-04-19 | 2011-10-26 | Centelion | Method for purifying plasmid DNA having pharmaceutical quality |
| EP2088196A1 (en) * | 2008-02-08 | 2009-08-12 | Boehringer Ingelheim RCV GmbH & Co KG | Methods and devices for producing biomolecules |
-
2019
- 2019-02-28 LT LTEP19160132.7T patent/LT3663401T/lt unknown
- 2019-02-28 DK DK19160132.7T patent/DK3663401T3/da active
- 2019-02-28 EP EP19160132.7A patent/EP3663401B1/en active Active
- 2019-02-28 PL PL19160132.7T patent/PL3663401T3/pl unknown
- 2019-02-28 ES ES19160132T patent/ES2929470T3/es active Active
-
2020
- 2020-02-28 CN CN202080017232.1A patent/CN113518822A/zh active Pending
- 2020-02-28 JP JP2021550323A patent/JP7566762B2/ja active Active
- 2020-02-28 WO PCT/EP2020/055285 patent/WO2020174085A1/en not_active Ceased
- 2020-02-28 EP EP20706520.2A patent/EP3931320A1/en active Pending
- 2020-02-28 SG SG11202108893SA patent/SG11202108893SA/en unknown
- 2020-02-28 KR KR1020217027475A patent/KR102919038B1/ko active Active
- 2020-02-28 CA CA3130855A patent/CA3130855A1/en active Pending
- 2020-02-28 US US17/434,442 patent/US20220145283A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| JP2022523389A (ja) | 2022-04-22 |
| US20220145283A1 (en) | 2022-05-12 |
| SG11202108893SA (en) | 2021-09-29 |
| EP3663401B1 (en) | 2022-09-21 |
| CA3130855A1 (en) | 2020-09-03 |
| WO2020174085A1 (en) | 2020-09-03 |
| KR20210134639A (ko) | 2021-11-10 |
| CN113518822A (zh) | 2021-10-19 |
| LT3663401T (lt) | 2022-10-25 |
| KR102919038B1 (ko) | 2026-01-27 |
| EP3931320A1 (en) | 2022-01-05 |
| JP7566762B2 (ja) | 2024-10-15 |
| EP3663401A1 (en) | 2020-06-10 |
| PL3663401T3 (pl) | 2023-02-27 |
| DK3663401T3 (da) | 2022-11-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2929470T3 (es) | Procedimiento de purificación de moléculas biológicas tales como ADN plasmídico utilizando cromatografía de intercambio aniónico | |
| ES2328008T5 (es) | Procedimientos de purificación de ADN | |
| US7655794B2 (en) | Nucleic acid purification method | |
| US6821757B2 (en) | Rapid and simple process for isolation of circular nucleic acids | |
| EP2066792B1 (en) | Nucleic acid purification method using anion exchange | |
| KR20100017884A (ko) | 고농도의 생물학적 활성 분자 함유 조성물 및 그 제조 방법 | |
| Freitas et al. | Plasmid purification by hydrophobic interaction chromatography using sodium citrate in the mobile phase | |
| CA2664211A1 (en) | Nucleic acid purification method | |
| Prazeres et al. | Purification of plasmids for gene therapy and DNA vaccination | |
| US6953686B1 (en) | Methods of DNA purification and purified DNA | |
| JP7586936B2 (ja) | 混入dnaをより効果的に除去するための、アデノ随伴ウイルスの精製の強化 | |
| HK40058215A (zh) | 采用阴离子交换色谱法的生物分子(如质粒dna)纯化工艺 | |
| WO2026037771A1 (en) | Method for purifying recombinant plasmid dna | |
| Zhong et al. | Developing an RNase-free bioprocess to produce pharmaceutical-grade plasmid DNA using selective precipitation and membrane chromatography | |
| CN108048456A (zh) | 一种质粒提取方法 | |
| US20250188441A1 (en) | Method for reducing endotoxin levels in nucleic acid purification | |
| Zhong | Downstream Bioprocess Development for a Scalable Production of Pharmaceutical-grade Plasmid DNA | |
| EP1670913A1 (en) | Purification of biological macromolecules | |
| PT109053A (pt) | Suporte cromatográfico para purificação de dna plasmídico por cromatografia de afinidade e respetivo método de purificação |