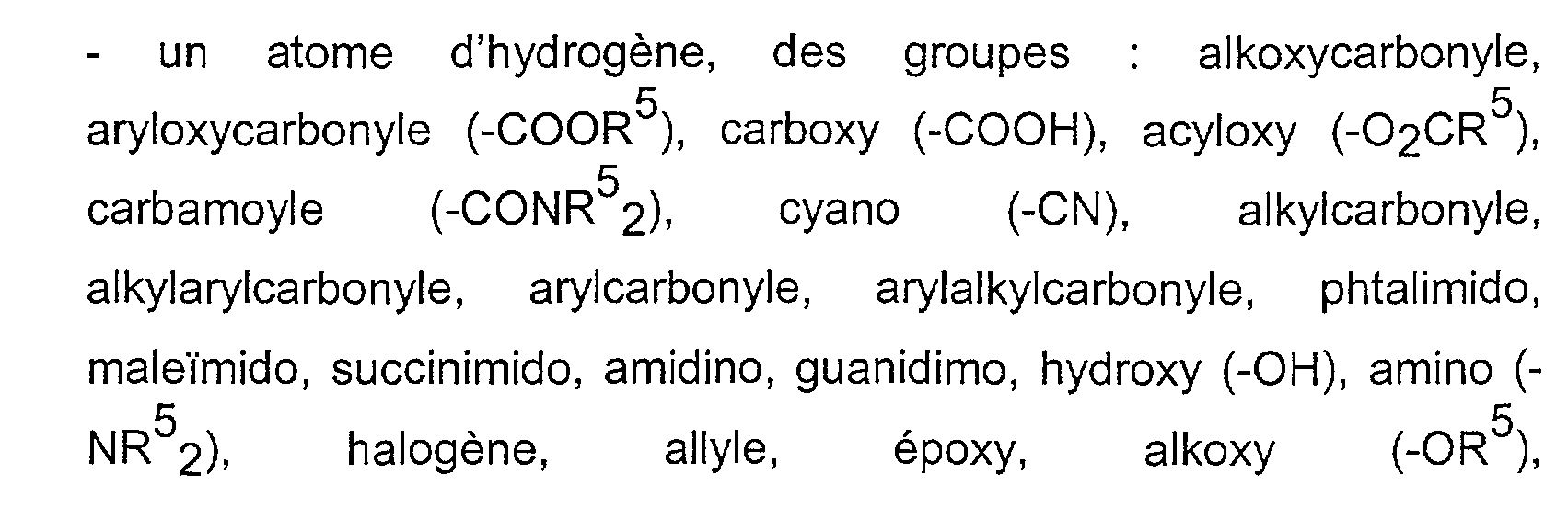FR2829140A1 - Procede de synthese de polymeres a fonctions thiols - Google Patents
Procede de synthese de polymeres a fonctions thiols Download PDFInfo
- Publication number
- FR2829140A1 FR2829140A1 FR0111494A FR0111494A FR2829140A1 FR 2829140 A1 FR2829140 A1 FR 2829140A1 FR 0111494 A FR0111494 A FR 0111494A FR 0111494 A FR0111494 A FR 0111494A FR 2829140 A1 FR2829140 A1 FR 2829140A1
- Authority
- FR
- France
- Prior art keywords
- different
- polymer
- alkyl
- radical
- formula
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 229920000642 polymer Polymers 0.000 title claims abstract description 75
- 238000000197 pyrolysis Methods 0.000 title claims abstract description 13
- 238000004519 manufacturing process Methods 0.000 title claims abstract description 4
- 229920001296 polysiloxane Polymers 0.000 title claims description 13
- ZOOODBUHSVUZEM-UHFFFAOYSA-N ethoxymethanedithioic acid Chemical group CCOC(S)=S ZOOODBUHSVUZEM-UHFFFAOYSA-N 0.000 title abstract description 13
- 125000003396 thiol group Chemical group [H]S* 0.000 title abstract 3
- 239000002537 cosmetic Substances 0.000 title description 2
- 238000000034 method Methods 0.000 claims abstract description 33
- 125000003118 aryl group Chemical group 0.000 claims abstract description 23
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 16
- 125000003710 aryl alkyl group Chemical group 0.000 claims abstract description 8
- 125000002252 acyl group Chemical group 0.000 claims abstract description 7
- 125000000753 cycloalkyl group Chemical group 0.000 claims abstract description 7
- 125000000592 heterocycloalkyl group Chemical group 0.000 claims abstract description 6
- -1 alkyl radical Chemical class 0.000 claims description 46
- 150000003254 radicals Chemical class 0.000 claims description 28
- 125000004432 carbon atom Chemical group C* 0.000 claims description 16
- 229920001577 copolymer Polymers 0.000 claims description 16
- 229910052736 halogen Inorganic materials 0.000 claims description 14
- 150000002367 halogens Chemical class 0.000 claims description 14
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 12
- 125000003545 alkoxy group Chemical group 0.000 claims description 8
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 8
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 8
- 229910052720 vanadium Inorganic materials 0.000 claims description 8
- 150000003573 thiols Chemical group 0.000 claims description 7
- RFFLAFLAYFXFSW-UHFFFAOYSA-N 1,2-dichlorobenzene Chemical compound ClC1=CC=CC=C1Cl RFFLAFLAYFXFSW-UHFFFAOYSA-N 0.000 claims description 6
- 239000004593 Epoxy Substances 0.000 claims description 6
- 150000001336 alkenes Chemical class 0.000 claims description 6
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 claims description 6
- 125000004435 hydrogen atom Chemical class [H]* 0.000 claims description 6
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 6
- 229920006395 saturated elastomer Polymers 0.000 claims description 6
- 229920005573 silicon-containing polymer Polymers 0.000 claims description 6
- 239000002904 solvent Substances 0.000 claims description 6
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 claims description 5
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 claims description 5
- 150000001735 carboxylic acids Chemical class 0.000 claims description 5
- 159000000011 group IA salts Chemical class 0.000 claims description 5
- XFXPMWWXUTWYJX-UHFFFAOYSA-N Cyanide Chemical compound N#[C-] XFXPMWWXUTWYJX-UHFFFAOYSA-N 0.000 claims description 4
- 125000004423 acyloxy group Chemical group 0.000 claims description 4
- 125000004453 alkoxycarbonyl group Chemical group 0.000 claims description 4
- 125000004448 alkyl carbonyl group Chemical group 0.000 claims description 4
- 125000005099 aryl alkyl carbonyl group Chemical group 0.000 claims description 4
- 125000005129 aryl carbonyl group Chemical group 0.000 claims description 4
- 125000005161 aryl oxy carbonyl group Chemical group 0.000 claims description 4
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 4
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 4
- 229920000620 organic polymer Polymers 0.000 claims description 4
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 4
- 125000005544 phthalimido group Chemical group 0.000 claims description 4
- 229920000233 poly(alkylene oxides) Chemical group 0.000 claims description 4
- 229910052721 tungsten Inorganic materials 0.000 claims description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 4
- 229910052727 yttrium Inorganic materials 0.000 claims description 4
- 229910052783 alkali metal Inorganic materials 0.000 claims description 3
- 150000001345 alkine derivatives Chemical class 0.000 claims description 3
- 125000002355 alkine group Chemical group 0.000 claims description 3
- 125000005842 heteroatom Chemical group 0.000 claims description 3
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 claims description 3
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 claims description 3
- 150000003242 quaternary ammonium salts Chemical class 0.000 claims description 3
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 claims description 2
- YUDRVAHLXDBKSR-UHFFFAOYSA-N [CH]1CCCCC1 Chemical compound [CH]1CCCCC1 YUDRVAHLXDBKSR-UHFFFAOYSA-N 0.000 claims description 2
- 125000002877 alkyl aryl group Chemical group 0.000 claims description 2
- 125000004188 dichlorophenyl group Chemical group 0.000 claims description 2
- 239000000839 emulsion Substances 0.000 claims description 2
- 229910052731 fluorine Inorganic materials 0.000 claims description 2
- 239000011737 fluorine Substances 0.000 claims description 2
- 229910052739 hydrogen Inorganic materials 0.000 claims description 2
- 239000001257 hydrogen Substances 0.000 claims description 2
- 239000003960 organic solvent Substances 0.000 claims description 2
- 125000001181 organosilyl group Chemical group [SiH3]* 0.000 claims description 2
- 230000003252 repetitive effect Effects 0.000 claims description 2
- 125000000547 substituted alkyl group Chemical group 0.000 claims description 2
- 125000000623 heterocyclic group Chemical group 0.000 claims 1
- WCYWZMWISLQXQU-UHFFFAOYSA-N methyl Chemical compound [CH3] WCYWZMWISLQXQU-UHFFFAOYSA-N 0.000 claims 1
- 125000003342 alkenyl group Chemical group 0.000 abstract 1
- 125000000304 alkynyl group Chemical group 0.000 abstract 1
- 239000000178 monomer Substances 0.000 description 25
- 238000010526 radical polymerization reaction Methods 0.000 description 21
- 230000008569 process Effects 0.000 description 20
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 8
- 238000006116 polymerization reaction Methods 0.000 description 8
- 239000012991 xanthate Substances 0.000 description 8
- 150000001875 compounds Chemical class 0.000 description 7
- 238000002360 preparation method Methods 0.000 description 7
- 239000000243 solution Substances 0.000 description 7
- 229920001400 block copolymer Polymers 0.000 description 6
- 238000005481 NMR spectroscopy Methods 0.000 description 5
- 239000000203 mixture Substances 0.000 description 5
- 239000002243 precursor Substances 0.000 description 5
- KAKZBPTYRLMSJV-UHFFFAOYSA-N Butadiene Chemical compound C=CC=C KAKZBPTYRLMSJV-UHFFFAOYSA-N 0.000 description 4
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- 238000004132 cross linking Methods 0.000 description 4
- 239000004205 dimethyl polysiloxane Substances 0.000 description 4
- 235000013870 dimethyl polysiloxane Nutrition 0.000 description 4
- 229920000435 poly(dimethylsiloxane) Polymers 0.000 description 4
- 230000002441 reversible effect Effects 0.000 description 4
- 229920002545 silicone oil Polymers 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- 238000005160 1H NMR spectroscopy Methods 0.000 description 3
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 239000012043 crude product Substances 0.000 description 3
- 229920001519 homopolymer Polymers 0.000 description 3
- 238000012690 ionic polymerization Methods 0.000 description 3
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 229910052717 sulfur Inorganic materials 0.000 description 3
- 229920001567 vinyl ester resin Polymers 0.000 description 3
- MYRTYDVEIRVNKP-UHFFFAOYSA-N 1,2-Divinylbenzene Chemical compound C=CC1=CC=CC=C1C=C MYRTYDVEIRVNKP-UHFFFAOYSA-N 0.000 description 2
- OVSKIKFHRZPJSS-UHFFFAOYSA-N 2,4-D Chemical compound OC(=O)COC1=CC=C(Cl)C=C1Cl OVSKIKFHRZPJSS-UHFFFAOYSA-N 0.000 description 2
- KUDUQBURMYMBIJ-UHFFFAOYSA-N 2-prop-2-enoyloxyethyl prop-2-enoate Chemical compound C=CC(=O)OCCOC(=O)C=C KUDUQBURMYMBIJ-UHFFFAOYSA-N 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 2
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 2
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 2
- 150000005840 aryl radicals Chemical class 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 2
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 2
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 2
- 239000007870 radical polymerization initiator Substances 0.000 description 2
- 229920005604 random copolymer Polymers 0.000 description 2
- 239000012429 reaction media Substances 0.000 description 2
- 239000011541 reaction mixture Substances 0.000 description 2
- 230000007420 reactivation Effects 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 159000000000 sodium salts Chemical class 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 239000011593 sulfur Substances 0.000 description 2
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 2
- OCJBOOLMMGQPQU-UHFFFAOYSA-N 1,4-dichlorobenzene Chemical compound ClC1=CC=C(Cl)C=C1 OCJBOOLMMGQPQU-UHFFFAOYSA-N 0.000 description 1
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 1
- ILLHORFDXDLILE-UHFFFAOYSA-N 2-bromopropanoyl bromide Chemical compound CC(Br)C(Br)=O ILLHORFDXDLILE-UHFFFAOYSA-N 0.000 description 1
- KRTGJZMJJVEKRX-UHFFFAOYSA-N 2-phenylethan-1-yl Chemical compound [CH2]CC1=CC=CC=C1 KRTGJZMJJVEKRX-UHFFFAOYSA-N 0.000 description 1
- XVMSFILGAMDHEY-UHFFFAOYSA-N 6-(4-aminophenyl)sulfonylpyridin-3-amine Chemical compound C1=CC(N)=CC=C1S(=O)(=O)C1=CC=C(N)C=N1 XVMSFILGAMDHEY-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- QYKIQEUNHZKYBP-UHFFFAOYSA-N Vinyl ether Chemical compound C=COC=C QYKIQEUNHZKYBP-UHFFFAOYSA-N 0.000 description 1
- CIUQDSCDWFSTQR-UHFFFAOYSA-N [C]1=CC=CC=C1 Chemical compound [C]1=CC=CC=C1 CIUQDSCDWFSTQR-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 239000012267 brine Substances 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 229910052793 cadmium Inorganic materials 0.000 description 1
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 1
- JJWKPURADFRFRB-UHFFFAOYSA-N carbonyl sulfide Chemical compound O=C=S JJWKPURADFRFRB-UHFFFAOYSA-N 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- YACLQRRMGMJLJV-UHFFFAOYSA-N chloroprene Chemical compound ClC(=C)C=C YACLQRRMGMJLJV-UHFFFAOYSA-N 0.000 description 1
- 238000007334 copolymerization reaction Methods 0.000 description 1
- 239000003431 cross linking reagent Substances 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 229940117389 dichlorobenzene Drugs 0.000 description 1
- 150000001993 dienes Chemical class 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- GDNCXORZAMVMIW-UHFFFAOYSA-N dodecane Chemical compound [CH2]CCCCCCCCCCC GDNCXORZAMVMIW-UHFFFAOYSA-N 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- QUPDWYMUPZLYJZ-UHFFFAOYSA-N ethyl Chemical compound C[CH2] QUPDWYMUPZLYJZ-UHFFFAOYSA-N 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 238000013467 fragmentation Methods 0.000 description 1
- 238000006062 fragmentation reaction Methods 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 239000004816 latex Substances 0.000 description 1
- 229920000126 latex Polymers 0.000 description 1
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 1
- 235000019341 magnesium sulphate Nutrition 0.000 description 1
- 125000005395 methacrylic acid group Chemical group 0.000 description 1
- 229920006030 multiblock copolymer Polymers 0.000 description 1
- ZIUHHBKFKCYYJD-UHFFFAOYSA-N n,n'-methylenebisacrylamide Chemical compound C=CC(=O)NCNC(=O)C=C ZIUHHBKFKCYYJD-UHFFFAOYSA-N 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 229910000510 noble metal Inorganic materials 0.000 description 1
- 238000010534 nucleophilic substitution reaction Methods 0.000 description 1
- CXQXSVUQTKDNFP-UHFFFAOYSA-N octamethyltrisiloxane Chemical compound C[Si](C)(C)O[Si](C)(C)O[Si](C)(C)C CXQXSVUQTKDNFP-UHFFFAOYSA-N 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 125000000962 organic group Chemical group 0.000 description 1
- 239000012074 organic phase Substances 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- 230000003071 parasitic effect Effects 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 125000004193 piperazinyl group Chemical group 0.000 description 1
- 125000005936 piperidyl group Chemical group 0.000 description 1
- 238000004987 plasma desorption mass spectroscopy Methods 0.000 description 1
- 238000006068 polycondensation reaction Methods 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 125000003072 pyrazolidinyl group Chemical group 0.000 description 1
- 150000003856 quaternary ammonium compounds Chemical class 0.000 description 1
- 238000007342 radical addition reaction Methods 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 238000001256 steam distillation Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 238000007725 thermal activation Methods 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 238000006276 transfer reaction Methods 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 229960000834 vinyl ether Drugs 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/38—Polysiloxanes modified by chemical after-treatment
- C08G77/382—Polysiloxanes modified by chemical after-treatment containing atoms other than carbon, hydrogen, oxygen or silicon
- C08G77/392—Polysiloxanes modified by chemical after-treatment containing atoms other than carbon, hydrogen, oxygen or silicon containing sulfur
Landscapes
- Chemical & Material Sciences (AREA)
- General Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Silicon Polymers (AREA)
Abstract
La présente invention concerne un procédé de préparation de polymères présentant au moins une fonction thiol, qui comprend la pyrolyse d'au moins un polymère présentant au moins une fonction de formule (1) suivante : dans laquelle R1, R2, R3 et R4 sont tels que définis dans la description.
Description
<Desc/Clms Page number 1>
La présente invention concerne un nouveau procédé de préparation de polymères présentant des extrémités thiols à partir de polymères à architecture contrôlée porteurs de fonctions xanthate particulières, notamment issus d'un procédé de polymérisation radicalaire vivante ou contrôlée.
Les polymères présentant des extrémités thiols peuvent trouver de nombreux domaines d'applications. Ainsi, en cosmétique, ils peuvent être utilisés dans le domaine capillaire (tel que, dans le domaine des permanentes pour les cheveux). Ils peuvent également être utilisés pour générer des couches organisées de polymères sur des substrats métalliques nobles, tels que l'or. En outre, compte tenu de la réactivité des fonctions thiols, les polymères ainsi obtenus permettent d'accéder à d'autres composés polymères, notamment par substitution nucléophile ou par addition radicalaire de ces fonctions.
Les polymères à architecture contrôlée peuvent être des polymères (homopolymères) ou des copolymères (statistiques, diblocs, triblocs, greffés ou en étoile, ou hyperramifiés). De façon plus spécifique, au sens de l'invention, on entend par"polymère à architecture contrôlée" un polymère à base de deux ou plusieurs monomères présentant un agencement contrôlé de ces différentes unités monomères le constituant.
Les polymères à architecture contrôlée sont habituellement préparés par polymérisation ionique vivante. Ce type de polymérisation présente l'inconvénient de ne permettre la polymérisation que de certains types de monomères apolares, notamment le styrène et le butadiène, et de requérir un milieu réactionnel particulièrement pur et des températures souvent inférieures à l'ambiante de manière à minimiser les réactions parasites, d'où des contraintes de mise en oeuvre sévères.
La polymérisation radicalaire présente l'avantage d'être mise en oeuvre facilement sans que des conditions de pureté excessives soient respectées et à des températures égales ou supérieures à l'ambiante. Cependant, jusqu'à
<Desc/Clms Page number 2>
récemment, il n'existait pas de procédé de polymérisation radicalaire permettant d'obtenir des polymères à architecture contrôlée, en particulier des copolymères à blocs. Depuis peu, un nouveau procédé de polymérisation radicalaire s'est développé : il s'agit de la polymérisation radicalaire dite"contrôlée"ou"vivante" (Matyjaszewski, K., Ed. Controlled Radical Polymerization ; ACS Symposium Series 685 ; American Chemical Society : Washington, DC, 1998, et ACS Symposium Series 768,2001). Dans ces systèmes, des réactions de terminaison ou de transfert réversible permettent de maintenir les extrémités actives tout au long de la polymérisation, donnant par conséquent accès à divers polymères à architecture contrôlée.
La polymérisation radicalaire contrôlée présente idéalement les aspects distinctifs suivants :
1. le nombre de chaînes est fixe pendant toute la durée de la réaction,
2. les chaînes croissent toutes à la même vitesse, ce qui se traduit par : - une augmentation linéaire des masses moléculaires avec la conversion, - une distribution des masses resserrée,
3. la masse moléculaire moyenne est contrôlée par le rapport molaire monomère/précurseur de chaîne,
4. la possibilité de préparer des copolymères à blocs.
1. le nombre de chaînes est fixe pendant toute la durée de la réaction,
2. les chaînes croissent toutes à la même vitesse, ce qui se traduit par : - une augmentation linéaire des masses moléculaires avec la conversion, - une distribution des masses resserrée,
3. la masse moléculaire moyenne est contrôlée par le rapport molaire monomère/précurseur de chaîne,
4. la possibilité de préparer des copolymères à blocs.
Le caractère contrôlé est d'autant plus marqué que la vitesse de réactivation des chaînes en radical est très grande devant la vitesse de croissance des chaînes (propagation). Il existe des cas où ce n'est pas toujours vrai (i. e. la vitesse de réactivation des chaînes en radical est inférieure à la vitesse de propagation) et les conditions 1 et 2 ne sont pas observées, néanmoins, il est toujours possible de préparer des copolymères à blocs.
Récemment, des procédés de polymérisation radicalaire vivante par transfert réversible par addition-fragmentation ont été développés. Ce type particulier de polymérisation constitue une des technologies les plus appropriées pour synthétiser des copolymères à blocs par voie radicalaire. Dans ce cadre, les xanthates RSC=SOR'ont été utilisés à titre d'agents de transfert dans les demandes de brevets WO 98/58974, WO 00/75207 et WO 01/042312 de la
<Desc/Clms Page number 3>
société Rhodia Chimie pour synthétiser des polymères à architecture contrôlée.
Un procédé de préparation par polymérisation radicalaire sous activation thermique de copolymères hybrides silicones et organiques a également été décrit dans la demande de brevet français FR 00 09722 déposée par la demanderesse le 25 juillet 2000. Ces copolymères hybrides sont préparés à partir d'un précurseur silicone présentant des fonctions réactives, notamment de type xanthate, d'au moins un monomère éthyléniquement insaturé organique et d'un initiateur de polymérisation radicalaire. Il a été aussi décrit dans la demande de brevet français n 01 05144 déposée par la demanderesse le 13 avril 2001 un procédé de préparation de polymères en forme d'étoiles qui comprend une étape de polymérisation radicalaire d'une composition comprenant : au moins un monomère réticulant, une source de radicaux libres et au moins un polymère de première génération. Ce polymère de première génération est lui-même obtenu par un procédé comprenant une étape de polymérisation radicalaire faisant réagir au moins un monomère réticulant, une source de radicaux libres et au moins un agent de transfert, notamment les xanthates de formule RSC=SOR', tels que décrits dans les demandes de brevets WO 98/58974, WO 00/75207 et WO 01/042312.
Cependant, malgré les avantages apportés par ces procédés de polymérisation radicalaire vivante, les polymères ainsi préparés présentent des extrémités réactives, telles que notamment des fonctions xanthate, qui-sont fragiles, car hydrolysables en milieu basique. lls sont donc susceptibles de libérer des sous-produits soufrés, de bas poids moléculaires, malodorants, et/ou toxiques pour l'environnement et l'être humain.
Dans la suite de la description, le terme polymère est utilisé pour décrire des homopolymères ou des copolymères, sauf indication contraire.
De plus, on entend par polymère à blocs un copolymère comprenant au moins deux enchaînements successifs de blocs d'unités monomères de constitutions chimiques différentes. Les blocs peuvent être constitués d'un
<Desc/Clms Page number 4>
homopolymère ou d'un polymère obtenu à partir d'un mélange de monomères éthyléniquement insaturés. Dans ce cas, le bloc peut être un copolymère statistique. Le copolymère à blocs peut comprendre deux blocs constitués, chacun, de copolymères statistiques. Dans ce cas, les monomères éthyléniquement insaturés sont tels que les blocs obtenus sont de natures différentes. Par natures différentes, on entend des blocs constitués de monomères de types différents, mais aussi des blocs constitués de monomères de même type mais dans des quantités différentes.
Un but de la présente invention est de proposer un procédé simple de mise en oeuvre, mais efficace, permettant de retirer les fonctions xanthates portées par des polymères, généralement obtenus par polymérisation radicalaire.
Un autre but de l'invention est de proposer une nouvelle voie d'accès à des polymères à fonctions thiol.
Ces buts et d'autres qui apparaîtront à la lecture de la description sont atteints par la présente invention qui concerne un procédé de préparation de polymères présentant au moins une fonction thiol, qui comprend la pyrolyse d'au moins un polymère présentant au moins une fonction de formule (1) suivante :
formule (1) dans laquelle R1, R2, R3 et R4, identiques ou différents, représentent un groupe choisi parmi l'atome d'hydrogène, les radicaux alkyle, acyle, aryle, aralkyl, alcène ou alcyne, cycloalkyle ou hétérocycloalkyle, saturé ou non, aromatique, ou une chaîne polymère, RI et R4 ou R1 et R2 pouvant former ensemble un cycloalkyle ou un hétérocycloalkyle.
formule (1) dans laquelle R1, R2, R3 et R4, identiques ou différents, représentent un groupe choisi parmi l'atome d'hydrogène, les radicaux alkyle, acyle, aryle, aralkyl, alcène ou alcyne, cycloalkyle ou hétérocycloalkyle, saturé ou non, aromatique, ou une chaîne polymère, RI et R4 ou R1 et R2 pouvant former ensemble un cycloalkyle ou un hétérocycloalkyle.
La température de pyrolyse mise en oeuvre dans le procédé selon l'invention dépend dans une large mesure de la nature chimique des radicaux R1,
<Desc/Clms Page number 5>
R2, R3 et R4. Cette température de pyrolyse est choisie de telle sorte qu'il y ait transformation de la fonction de formule (1) présentée par les polymères mis en oeuvre en une fonction thiol et de produire du sulfure de carbonyle, de formule COS, et un composé oléfinique de formule (2) suivante : R1 R2=R3R4. Ainsi, il est à la portée de l'homme du métier de définir les conditions de polymérisation de telle sorte que la réaction de pyrolyse n'ait pas lieu lors de cette polymérisation.
Pour donner un ordre de grandeur, la température de pyrolyse est généralement comprise entre 20 et 200 C, de préférence entre 100 et 180 C, plus particulièrement entre 130 et 160 C.
La pyrolyse selon l'invention est généralement mise en oeuvre à pression atmosphérique.
La pyrolyse selon l'invention est généralement mise en oeuvre sur un polymère qui est en solution, en émulsion (sous forme de latex), solide ou à l'état fondu.
Ainsi, lorsqu'elle est mise en oeuvre sur un polymère qui est en solution, le solvant est de préférence un solvant présentant une température d'ébullition supérieure ou égale à la température de pyrolyse. On peut notamment citer l'eau, un solvant organique, tel que notamment le 1, 2-dichlorobenzène.
Les groupes alkyle, acyle, aryle, aralkyle ou alcyne éventuellement substitués présentent généralement 1 à 20 atomes de carbone, de préférence 1 à
12, et plus préférentiellement 1 à 9 atomes de carbone. Ils peuvent être linéaires ou ramifiés. Ils peuvent être également substitués par des atomes d'oxygène, sous forme notamment d'esters, des atomes de soufre ou d'azote.
12, et plus préférentiellement 1 à 9 atomes de carbone. Ils peuvent être linéaires ou ramifiés. Ils peuvent être également substitués par des atomes d'oxygène, sous forme notamment d'esters, des atomes de soufre ou d'azote.
Parmi les radicaux alkyle, on peut notamment citer le radical méthyle, éthyle, propyle, butyle, pentyl, isopropyl, tert-butyle, pentyl, hexyle, octyle, decyle ou dodécyle. On préfère les radicaux méthyle ou éthyle.
Les groupes alcyne sont des radicaux généralement de 2 à 10 atomes de carbone, ils présentent au moins une insaturation acétylénique, tel que le radical acétylényle.
Le groupe acyle est un radical présentant généralement de 1 à 20 atomes de carbone avec un groupement carbonyle.
<Desc/Clms Page number 6>
Parmi les radicaux aryle, on peut notamment citer le radical phényle, éventuellement substitué notamment par une fonction nitro ou hydroxyle.
Parmi les radicaux aralkyl, on peut notamment citer le radical benzyle ou phénéthyle, éventuellement substitué notamment par une fonction nitro ou hydroxyle.
Le radical ! cydoa) kyte (Cg-Cg) est un radical hydrocarboné cyclique, tel que notamment le cyclopropyle, cyclopentyle ou cyclohexyl. De préférence, lorsque R1 et R4 ou R1 et R2 forment un cycloalkyle, celui-ci est le cyclohexyl.
Le radical hétérocycloalkyle est un radical cycloalkyl tel que défini cidessus contenant, à la place d'un ou plusieurs atomes de carbone du cycle, un ou plusieurs hétéroatomes choisis parmi N, 0 et S.
Parmi les radicaux hétérocycloalkyle, on peut donc notamment citer le radical pipéridyle, pyrazolidinyle, pipérazinyle et morpholinyl.
Lorsque R1, R2, R3 ou R4 est une chaîne polymère, cette chaîne polymère peut être issue d'une polymérisation radicalaire ou ionique ou issue d'une polycondensation.
R1, R2, R3 et R4 sont de préférence choisis de telle manière que l'élimination du composé oléfinique de formule (2) produit, indiqué ci-dessus, notamment par évaporation ou entraînement à la vapeur, soit rendue plus facile.
De préférence, R1, R2, R3 et R4 représentent des groupes choisis parmi : l'atome d'hydrogène, le radical méthyle, éthyle et le radical cyclohexyl pour R1 et R4 ou R1 et R2.
Le polymère présentant au moins une fonction de formule (1) mis en oeuvre dans le procédé de la présente invention est de préférence un polymère organique, un polymère de type silicone ou un copolymère hybride d'une part formé par un polymère de type silicone et d'autre part par un polymère organique.
Ces polymères peuvent être obtenus par polymérisation radicalaire et/ou ionique. En effet, même s'il s'est agi au départ de retirer des fonctions réactives obtenues lors de procédé de synthèse de polymères par la voie radicalaire, il s'avère que le procédé selon l'invention s'applique également à des polymères tels que les polymères siliconés présentant au moins une fonction de formule (1).
<Desc/Clms Page number 7>
Selon un mode particulier de réalisation, pour présenter au moins une extrémité de formule (1), les polymères utilisés dans présente invention ont été obtenus par un procédé, tel que décrit dans l'une des demandes de brevets WO 98/58974 et WO 00/75207 de la société Rhodia Chimie, mettant en oeuvre au moins un composé xanthate de formule (2) suivante :
dans laquelle R, R1, R2, R3 et R4, identiques ou différents, ont les significations données pour R1, R2, R3 et R4 et spécifiées ci-dessus.
dans laquelle R, R1, R2, R3 et R4, identiques ou différents, ont les significations données pour R1, R2, R3 et R4 et spécifiées ci-dessus.
Ainsi, les polymères utilisés dans le procédé de l'invention peuvent être par exemple des polymères issus d'un procédé de polymérisation radicalaire contrôlée réalisée par mise en contact d'un ou plusieurs monomère (s) éthyléniquement insaturé (s), d'au moins une source de radicaux libres et d'au moins un agent de transfert réversible de type xanthate de formule (2). De façon plus spécifique, les polymères organiques vivants utilisés dans le procédé de l'invention peuvent être des polymères séquencés issus d'un procédé de copolymérisation comportant N étapes successives de polymérisations radicalaires (N étant supérieur ou égale à 2), la première de ces étapes étant une polymérisation radicalaire contrôlée réalisée par mise en contact d'un ou plusieurs monomère (s) éthyléniquement insaturé (s), d'au moins une source de radicaux libres et d'au moins un agent de transfert réversible du type précité, et les (N-1) étapes suivantes étant des polymérisations radicalaires contrôlées réalisées par mise en contact d'un ou plusieurs monomère (s) éthyléniquement insaturé (s) différents de ceux de l'étape précédente, d'au moins une source de radicaux libres et de la composition de polymère vivante issue de l'étape précédente.
Par exemple, lorsque N est égal à 2, le polymère utilisé dans présente invention peut être un polymère de formule (1) suivante :
<Desc/Clms Page number 8>
, avec m et n, identiques ou différentes, supérieurs ou égaux à 1, de préférence supérieurs à 6, et de préférence inférieurs à 500, l'un des deux (m ou n) pouvant être égal à 0, lorsque m ou n > 1 les motifs unitaires répétitifs d'indice m ou n respectivement sont différents ou avantageusement identiques, - R, R1, R2, R3 et R4, identiques ou différents, ont les significations données ci-dessus pour R1, R2, R3 et R4, - V, V, W et W', identiques ou différents, représentent : H, un groupe alkyle ou un halogène, - X, X', Y et Y', identiques ou différents, représentent H, un halogène ou un groupe Rg, ORs, 02CORs, NHCOH, OH, NH2, NHRg, N (Rs) 2, (rus) 2N+0-, NHCORg, C02H, CO2R5, CN, CONH2, CONHR5 ou
CON (Rs) , dans lesquels rus est choisi parmi les groupes alkyle, aryle, aralkyl, alkylaryle, alcène ou organosilyle, éventuellement perfluorés et éventuellement substitués par un ou plusieurs groupes carboxyle, époxy, hydroxyle, alkoxy, amino, halogène ou sulfonique, et - a et b sont 0 ou 1.
Le polymère présentant au moins une fonction de formule (1) mis en oeuvre dans la présente invention peut correspondre à un polymère en forme d'étoiles. Ainsi, celui-ci peut être obtenu par un procédé tel que décrit dans la demande de brevet français n 01 05144 déposée par la demanderesse le 13 avril 2001. Ce procédé comprend une étape de polymérisation radicalaire d'une
<Desc/Clms Page number 9>
composition comprenant : au moins un monomère réticulant, une source de radicaux libres et au moins un polymère de première génération. Ce polymère de première génération est lui-même obtenu par un procédé comprenant une étape de polymérisation radicalaire faisant réagir au moins un monomère éthyléniquement insaturé, une source de radicaux libres et au moins un composé xanthate de formule (2) tel que précédemment décrit.
Les monomères réticulants sont choisis parmi des composés organiques comportant au moins deux insaturations éthyléniques et au plus 10 insaturations et connus comme étant réactifs par voie radicalaire. De préférence, ces monomères présentent deux insaturations éthyléniques.
Ainsi, on peut notamment citer les dérivés acryliques, méthacryliques, acrylamido, méthacrylamido, ester vinylique, éther vinylique, diénique, styrénique, alpha-méthyl styrénique et allylique. Comme monomères réticulants, on préfère le N, N'-méthylènebisacrylamide, le divinylbenzène et le diacrylate d'éthylène glycol.
Le polymère présentant au moins une fonction de formule (1) mis en oeuvre dans la présente invention peut correspondre, selon un autre mode de réalisation, à des copolymères hybrides silicones et organiques comprenant des motifs (il) :
dans lesquels : - x est égal à 0,1, 2 ou 3, y est égal à 0,1, 2 ou 3 avec 2 : : ; ; (x+y) : : ; ; 3 et y est différent de 0 pour au moins un des motifs du copolymère hybride, les symboles A, identiques ou différents, représentent : un radical alkyle linéaire ou ramifié contenant 1 à 8 atomes de carbone, éventuellement substitué par au moins un halogène, de préférence le fluor, les radicaux alkyle étant de préférence méthyle, éthyle, propyle, octyle et 3,3, 3-trifluoropropyle, un radical cycloalkyle contenant entre 3 et 8 atomes de carbone cycliques, éventuellement substitué,
dans lesquels : - x est égal à 0,1, 2 ou 3, y est égal à 0,1, 2 ou 3 avec 2 : : ; ; (x+y) : : ; ; 3 et y est différent de 0 pour au moins un des motifs du copolymère hybride, les symboles A, identiques ou différents, représentent : un radical alkyle linéaire ou ramifié contenant 1 à 8 atomes de carbone, éventuellement substitué par au moins un halogène, de préférence le fluor, les radicaux alkyle étant de préférence méthyle, éthyle, propyle, octyle et 3,3, 3-trifluoropropyle, un radical cycloalkyle contenant entre 3 et 8 atomes de carbone cycliques, éventuellement substitué,
<Desc/Clms Page number 10>
. un radical aryle contenant entre 6 et 12 atomes de carbone pouvant être substitué, de préférence phényle ou dichlorophényle, . une partie aralkyl ayant une partie alkyle contenant entre 5 et
14 atomes de carbone et une partie aryle contenant entre 6 et
12 atomes de carbone, substituée éventuellement sur la partie aryle par des halogènes, des alkyles et/ou des alkoxyles contenant 1 à
3 atomes de carbone, . les symboles U, identiques ou différents, représentent (III) :
dans lequel : - R1, R2, R3 et R4, identiques ou différents, ont la signification donnée cidessus, - V et V', identiques ou différents, ont les significations données cidessus, - X et X', identiques ou différents, ont les significations données cidessus, - R et R, identiques ou différents, représentent : - un groupe (i) alkyle, acyle, aryle, alcène ou alcyne éventuellement substitué, - un cycle (ii) carboné, saturé ou non, éventuellement substitué et/ou aromatique, - un hétérocycle (iii), saturé ou non, éventuellement substitué,
14 atomes de carbone et une partie aryle contenant entre 6 et
12 atomes de carbone, substituée éventuellement sur la partie aryle par des halogènes, des alkyles et/ou des alkoxyles contenant 1 à
3 atomes de carbone, . les symboles U, identiques ou différents, représentent (III) :
dans lequel : - R1, R2, R3 et R4, identiques ou différents, ont la signification donnée cidessus, - V et V', identiques ou différents, ont les significations données cidessus, - X et X', identiques ou différents, ont les significations données cidessus, - R et R, identiques ou différents, représentent : - un groupe (i) alkyle, acyle, aryle, alcène ou alcyne éventuellement substitué, - un cycle (ii) carboné, saturé ou non, éventuellement substitué et/ou aromatique, - un hétérocycle (iii), saturé ou non, éventuellement substitué,
<Desc/Clms Page number 11>
- un atome d'hydrogène, des groupes alkoxycarbonyle, 5 5 aryloxycarbonyle (-COOR), carboxy (-COOH), acyloxy (-02CR), 5 carbamoyl (-CONR 2), cyano (-CN), alkylcarbonyl, alkylarylcarbonyle, arylcarbonyle, arylalkylcarbonyle, phtalimido, maleïmido, succinimido, amidino, guanidimo, hydroxy (-OH), amino (- 5 5 NR52), halogène, allyle, époxy, alkoxy (-OR5 S-alkyle, S-aryle, des groupes présentant un caractère hydrophile ou ionique tels que les sels alcalins d'acides carboxyliques, les sels alcalins d'acide sulfonique, les chaînes polyoxyde d'alkylène (POE,
POP), les substituants cationiques (sels d'ammonium quaternaires), g R, identiques ou différents, représentant un groupe alkyle ou aryle, et/ou une chaîne polymère, - les radicaux (i), (ii) et (iii) pouvant être substitués avantageusement par : des groupes phényles substitués, des groupes aromatiques substitués, ou des groupes : alkoxycarbonyle, aryloxycarbonyle (-
Cool), carboxy (-COOH), acyloxy (-OCR), carbamoyte (- 5 CONR 52), cyano (-CN), alkylcarbonyl, alkylarylcarbonyle, arylcarbonyle, arylalkylcarbonyle, phtalimido, maleïmido, succinimido, g amidino, guanidimo, hydroxy (-OH), amino (-NR52), halogène, allyle, g époxy, alkoxy (-OR5), S-alkyle, S-aryle, des groupes présentant un caractère hydrophile ou ionique tels que les sels alcalins d'acides carboxyliques, les sels alcalins d'acide sulfonique, les chaînes polyoxyde d'alkylène (POE, POP), les substituants cationiques (sels
5 d'ammonium quaternaires), R5, identiques ou différents, représentant un groupe alkyle ou aryle, et/ou une chaîne polymère, - W, identiques ou différents, représentent un radical divalent choisi parmi - O-,-NRg-,-NH-,-S-, Rg ayant la signification donnée ci-dessus, - Sp, identiques ou différents, représentent une rotule constituée d'un radical divalent organique de formule- (CH- dans lequel x'est compris entre 1 et 20, ce radical pouvant être substitué et/ou contenir au moins un hétéroatome,
<Desc/Clms Page number 12>
- 0 ou 1, - m 2 1, et lorsque m > 1 les motifs unitaires répétitifs d'indice m sont identiques ou différents, m étant de préférence inférieur à 500.
Ces copolymères hybrides peuvent être obtenus par le procédé dans lequel on met en contact : - au moins un monomère éthyléniquement insaturé de formule (IV) :
- un composé silicone précurseur comprenant des motifs, identiques ou différents, de formule (V) :
dans lequel : - A, x et y correspondent aux valeurs données précédemment, et le radical monovalent U'est selon la formule suivante (VI) :
- et un initiateur de polymérisation radicalaire.
- un composé silicone précurseur comprenant des motifs, identiques ou différents, de formule (V) :
dans lequel : - A, x et y correspondent aux valeurs données précédemment, et le radical monovalent U'est selon la formule suivante (VI) :
- et un initiateur de polymérisation radicalaire.
Le composé silicone précurseur de formule générale (V) utilisé au sein du procédé de préparation de ces copolymères hybrides peut être obtenu par réaction : (i) d'une silicone comprenant des motifs de formule (VII) :
RxU"ySiO [4- (x+y)]/2 où le radical monovalent U"est selon la formule suivante (veil) :
RxU"ySiO [4- (x+y)]/2 où le radical monovalent U"est selon la formule suivante (veil) :
<Desc/Clms Page number 13>
dans laquelle : - R2, R3, W et Sp sont de définitions identiques à celles données précédemment, - L est un groupement électrofuge, par exemples : Br, CI-, 1-, OTs-,
OMs-, (C6H6)-(C=O)-O-, (CH3)-(C=O)-O-, (CF3)-(C=O)-O-. (ii) avec un composé choisi parmi ceux de formules générales suivantes (IX), (X) ou (XI) :
dans lesquelles : - R1, R2, R3 et R4, identiques ou différents, ont la signification donnée ci-dessus, - M'+ représente K+, Na+, Nu4+, ou PR'R étant de définition similaire à celle donnée pour R de la formule (1), - M"2+ représente un métal alcalino-terreux tels que Ca2+, Ba2+ et Sr2++,
<Desc/Clms Page number 14>
- Mm représente Zn, Cd, m est égal à 1 ou 2, n est égal à 1,2, 3 ou 4 et de préférence m est égal à 1 et n est égal à 2.
Cette silicone de formule (Vil) peut être notamment obtenue à partir (i) d'une silicone comprenant des motifs de formule (XII) : RXU"lySiO[4- (x+y) ]/2 où le radical monovalent U"'est de formule (X !))) :-Sp-WH et (ii) d'un composé de formule :
Outre des copolymères hybrides comprenant un seul segment organique, les polymères utilisés dans le procédé selon l'invention peuvent correspondre à des polymères hybrides porteurs de groupements organiques à blocs (c'est à dire multiblocs). Pour cela, leur procédé de préparation consiste à répéter la mise en oeuvre du procédé de préparation précédemment décrit en utilisant : - des monomères éthyléniquement insaturés différents de la mise en oeuvre précédente, et - à la place du composé silicone précurseur (V), le copolymère hybride comprenant des motifs (II) à blocs issu de la mise en oeuvre précédente.
Selon ce procédé de préparation de copolymères multiblocs, lorsque l'on souhaite obtenir des copolymères à blocs homogènes et non à gradient de composition, et si toutes les polymérisations successives sont réalisées dans le même réacteur, il est essentiel que tous les monomères utilisés lors d'une étape aient été consommés avant que la polymérisation de l'étape suivante ne commence, donc avant que les nouveaux monomères ne soient introduits.
Ces copolymères hybrides ont été décrits dans la demande de brevet français FR 00 09722 déposée par la demanderesse le 25 juillet 2000.
<Desc/Clms Page number 15>
Tel que mentionné précédemment, le polymère présentant au moins une fonction de formule (1) peut correspondre, selon un autre mode de réalisation, à un polymère de type silicone. Dans ce cas, le polymère de type silicone est de formule générale (V), tel que décrit ci-dessus.
Les monomères éthyléniquement insaturés mentionnés antérieurement sont plus spécifiquement selon l'invention les monomères choisis parmi le styrène ou ses dérivés, le butadiène, le chloroprène, les esters (méth) acryliques, les esters vinyliques, les nitriles vinyliques, les esters vinyliques et les amides des acides carboxyliques insaturés.
Les exemples suivants illustrent l'invention sans toutefois en limiter la portée.
EXEMPLES :
Exemple 1 : - Synthèse du sel de sodium de l'acide 0- (2-propyl) xanthique
1 équivalent de 2-propanol est additionné goutte à goutte, à 0 C, sur une solution (1 M) de 1,1 équivalent de NaH dans le THF. 4 équivalents de CS2 sont ajoutés, et le milieu réactionnel est agité 1 nuit à température ambiante.
Exemple 1 : - Synthèse du sel de sodium de l'acide 0- (2-propyl) xanthique
1 équivalent de 2-propanol est additionné goutte à goutte, à 0 C, sur une solution (1 M) de 1,1 équivalent de NaH dans le THF. 4 équivalents de CS2 sont ajoutés, et le milieu réactionnel est agité 1 nuit à température ambiante.
Le THF est ensuite évaporé, 1 litre d'éther de pétrole est ensuite additionné pour laver le solide obtenu, par filtration. Le solide est ensuite séché sous vide.
<Desc/Clms Page number 16>
2H (1)) ; 0, 93 ppm (trip. 3H (4)) RMN 13C 208,0 ppm C (5) ; 81,5 ppm C (2) ; 28,8 ppm C (3) ; 19,0 ppm C (1) ; 10,0 ppm C (4) - Synthèse d'une huile silicone (polydiméthylsiloxane, DPn=14) a, ro-bis[O- {2- propyl) xanthate
A une solution de 10 g d'huile silicone a, co-hydroxylée (polydiméthylsiloxane, DPn=14) (1 équivalent) et de 2,6 g (4 équivalents) de pyridine dans de l'éther (200 ml), est additionné goutte à goutte et à température ambiante, 1,9 ml (2,4 équivalents) de bromure de 2-bromo-propionyle.
Après une nuit d'agitation à température ambiante, 50 ml d'eau-sont additionnés au mélange réactionnel. La phase aqueuse est ensuite extraite par 2 x 100 ml d'acétate d'éthyle.
Les phases organiques réunies sont ensuite lavées successivement par une solution aqueuse de NaOH (1 M), une solution aqueuse HC110 %, de l'eau et de la saumure, puis séchées sur du sulfate de magnésium. Les solvants sont ensuite évaporés. Le produit brut obtenu est ensuite chromatographié sur colonne de silice (heptane 9/éther 1) pour donner 11 g d'huile silicone bromé.
1 g de l'huile silicone bromé est additionné à une solution de 0,5 g de xanthate 1 (4 éq. ) en solution dans 10 ml de CH3CN. Le mélange réactionnel est
<Desc/Clms Page number 17>
agité durant toute 1 nuit à température ambiante. Le solvant est évaporé, de l'éther est ensuite ajouté, puis une filtration est effectuée pour éliminer l'excès de sel de xanthate et le sel de sodium formé. Sur le spectre du produit brut obtenu, le brome est déplacé totalement par le sel de xanthate.
RMN'H 5,56 ppm (sext. 2H (2')) ; 4,32 ppm (quad. 2H (5)) ; 4,06 ppm (trip. 4H (3)) ; 1,6 à 1,8 ppm (mult. 8H (2, 3')) ; 1,51 ppm (doub. 6H (6)) ; 1,30 ppm (mult. 6H (1')) ; 0,90 ppm (trip. 6H (4')) ; 0,52 ppm (mult. 4H (1)) ; 0,1 ppm (mult. SiMe3) RMN 13C 211,5 ppm C (5') ; 171,4 ppm C (4) ; 82,7 ppm C (2') ; 68,1 ppm C (3) ; 46,9 ppm C (5) ; 28,5 ppm C (3') ; 22,6 ppm C (2) ; 18,7, 17,0 et 9,6 ppm C (1'), C (4') et C (6) ; 14,2 ppm C (1) ; 1,0 et 0,1 ppm (Si-CH3).
3 0,2 g de silicone portant la fonction xanthate 2 est mis en solution dans 1 ml de chlorobenzène, puis mis à reflux. Après 2 heures d'agitation, peu de changement est observé.
En solution dans le dichloro-benzène, les 0,2 g de silicone 2 sont mis à reflux durant 2 heures.
<Desc/Clms Page number 18>
Le solvant est ensuite évaporé avec les produits d'élimination, pour donner un produit brut où les signaux caractéristiques de la fonction xanthate ne sont plus observés par RMN 1H et 13C.
Par contre, on observe toujours par RMN 1H, 1 signal à 3,5 ppm, qui devrait correspondre au H (5). Le déplacement chimique du carbone correspondant en C, nous confirme la même chose.
RMN 1H 4,09 ppm (trip dedoub.
4H (3)) ; 3,50 ppm (mult.
2H (5)) ; 1,72 ppm (mult.
4H (2)) ; 1,50 ppm (doub.
6H (2)) ; 0,55 ppm (mult.
4H (1)) ; 0,1 ppm (mult. SiMe3) RMN 13C 68,0 ppm C (3) ; 48,2 ppm C (5) ; 22,7 ppm C (2) ; 17,0 ppm C (6) ; 14,1 ppm C (1) ; 1,1 et 0,2 ppm (Si-CH3).
Claims (10)
1. Procédé de préparation d'un polymère présentant au moins une fonction thiol, qui comprend la pyrolyse d'au moins un polymère présentant au moins une fonction de formule (1) suivante :
formule (1) dans laquelle R1, R2, R3 et R4, identiques ou différents, représentent un groupe choisi parmi l'atome d'hydrogène, les radicaux alkyle, acyle, aryle, aralkyl, alcène ou alcyne, cycloalkyle ou hétérocycloalkyle, saturé ou non, aromatique, ou une chaîne polymère, R1 et R4 ou R1 et R2 pouvant former ensemble un cycloalkyle ou un hétérocycloalkyle.
2. Procédé selon la revendication 1, caractérisé en ce que la température de pyrolyse est comprise entre 20 et 200 C, de préférence entre 100 et 180 C, plus particulièrement entre 130 et 160 C.
3. Procédé selon la revendication 1 ou 2, caractérisé en ce que la pyrolyse est réalisée sur un polymère en solution, en émulsion ou à l'état fondu.
4. Procédé selon la revendication 3, caractérisé en ce que le solvant est choisi parmi l'eau et un solvant organique, tel que notamment le 1,2dichlorobenzène.
5. Procédé selon l'une des revendications précédentes, caractérisé en ce que R1, R2, R3 et R4 représentent des groupes choisis parmi : l'atome d'hydrogène, le radical méthyle, éthyle et le radical cyclohexyle pour R1 et R4 ou R1 et R2.
6. Procédé selon l'une des revendications précédentes, caractérisé en ce que le polymère présentant au moins une fonction de formule (1) est un polymère
<Desc/Clms Page number 20>
organique, un polymère de type silicone ou un copolymère hybride d'une part formé par un polymère de type silicone et d'autre part par un polymère organique.
7. Procédé selon l'une des revendications précédentes, caractérisé en ce que le polymère présentant au moins une fonction de formule (1) est un polymère de formule (1) suivante :
, avec m et n, identiques ou différentes, supérieurs ou égaux à 1, de préférence supérieurs à 6, l'un des deux (m ou n) pouvant être égal à 0, lorsque m ou n > 1 les motifs unitaires répétitifs d'indice m ou n respectivement sont différents ou avantageusement identiques, - R, R1, R2, R3 et R4, identiques ou différents, ont les significations données pour R1, R2, R3 et R4 à la revendication 1, - V, V, W et W, identiques ou différents, représentent : H, un groupe alkyle ou un halogène,
- X, X', Y et Y', identiques ou différents, représentent H, un halogène ou un groupe Rg, Ours, CCORg, NHCOH, OH, NH2, NHRg, N (rus) 2, (Rs) 2N+0-, NHCORs, C02H, C02Rs, CN, CONH2, CONHRg ou CON (rus) 2, dans lesquels Rg est choisi parmi les groupes alkyle, aryle, aralkyle, alkylaryle, alcène ou organosilyle, éventuellement perfluorés et éventuellement substitués par un ou plusieurs groupes carboxyle, époxy, hydroxyle, alkoxy, amino, halogène ou sulfonique, et - a et b sont 0 ou 1.
<Desc/Clms Page number 21>
8. Procédé selon l'une des revendications précédentes 1 à 6, caractérisé en ce que le polymère est un copolymère hybride silicone et organique comprenant des motifs (li) :
aans lesquels : - x est égal à 0,1, 2 ou 3, y est égal à 0,1, 2 ou 3 avec 2 : : : ; (x+y) # 3 et y est différent de 0 pour au moins un des motifs du copolymère hybride, les symboles A, identiques ou différents, représentent : un radical alkyle linéaire ou ramifié contenant 1 à 8 atomes de carbone, éventuellement substitué par au moins un halogène, de préférence le fluor, les radicaux alkyle étant de préférence méthyle, éthyle, propyle, octyle et 3,3, 3-trifluoropropyle, un radical cycloalkyle contenant entre 3 et 8 atomes de carbone cycliques, éventuellement substitué, un radical aryle contenant entre 6 et 12 atomes de carbone pouvant être substitué, de préférence phényle ou dichlorophényle, une partie aralkyl ayant une partie alkyle contenant entre 5 et
14 atomes de carbone et une partie aryle contenant entre 6 et
12 atomes de carbone, substituée éventuellement sur la partie aryle par des halogènes, des alkyles et/ou des alkoxyles contenant 1 à
3 atomes de carbone, les symboles U, identiques ou différents, représentent (III) :
<Desc/Clms Page number 22>
dans lequel : - R1, R2, R3 et R4, identiques ou différents, ont la signification donnée dans la revendication 1, - V et V', identiques ou différents, ont les significations données dans la revendication 6, - X et X', identiques ou différents, ont les significations données dans la revendication 6,
2 3 R - R2 et R3, identiques ou différents, représentent : - un groupe (i) alkyle, acyle, aryle, alcène ou alcyne éventuellement substitué, - un cycle (ii) carboné, saturé ou non, éventuellement substitué et/ou aromatique, -un hétérocycle (iii), saturé ou non, éventuellement substitué,
- un atome d'hydrogène, des groupes alkoxycarbonyle, aryloxycarbonyle (-COOR), carboxy (-COOH), acyloxy (-02CR), 5 carbamoyl (-CONR 52), cyano (-CN), alkylcarbonyl, alkylarylcarbonyle, arylcarbonyle, arylalkylcarbonyle, phtalimido, maleïmido, succinimido, amidino, guanidimo, hydroxy (-OH), amino (- 5 5 NR52), halogène, allyle, époxy, alkoxy (-OR5), S-alkyle, S-aryle, des groupes présentant un caractère hydrophile ou ionique tels que les sels alcalins d'acides carboxyliques, les sels alcalins d'acide sulfonique, les chaînes polyoxyde d'alkylène (POE, POP), les substituants cationiques (sels d'ammonium quaternaires),
<Desc/Clms Page number 23>
5 R, identiques ou différents, représentant un groupe alkyle ou aryle, et/ou une chaîne polymère, - les radicaux (i), (ii) et (iii) pouvant être substitués avantageusement par : des groupes phényles substitués, des groupes aromatiques substitués, ou des groupes : alkoxycarbonyle, aryloxycarbonyle (- Cool), carboxy (-COOH), acyloxy (-O2CR5), carbamoyle (- 5 CONR 52), cyano (-CN), alkylcarbonyle, alkylarylcarbonyle, arylcarbonyle, arylalkylcarbonyle, phtalimido, maleïmido, succinimido, amidino, guanidimo, hydroxy (-OH), amino (-NR25), halogène, allyle,
5 époxy, alkoxy (-OR5), S-alkyle, S-aryle, des groupes présentant un caractère hydrophile ou ionique tels que les sels alcalins d'acides carboxyliques, les sels alcalins d'acide suifonique, les chaînes
polyoxyde d'alkylène (POE, POP), les substituants cationiques (sels g d'ammonium quaternaires), R, identiques ou différents, représentant un groupe alkyle ou aryle, et/ou une chaîne polymère, - W, identiques ou différents, représentent un radical divalent choisi parmi - O-,-NRg-,-NH-,-S-, Rg ayant la signification donnée dans la revendication 4, - Sp, identiques ou différents, représentent une rotule constituée d'un radical divalent organique de formufe- (CH.- dans fequei x'est compris entre 1 et 20, ce radical pouvant être substitué et/ou contenir au moins un hétéroatome, - a = 0 ou 1, - m 1, et lorsque m > 1 les motifs unitaires répétitifs d'indice m sont identiques ou différents.
9. Procédé selon l'une des revendications 1 à 6, caractérisé en ce que le polymère présentant au moins une fonction de formule (1) est un polymère de type silicone de formule (V) :
<Desc/Clms Page number 24>
5 10 dans laquelle : - A, x et y correspondent aux valeurs données à la revendication 8, et le radical monovalent U'est selon la formule suivante (VI) :
dans laquelle - R1, R2, R3 et R4, identiques ou différents, ont la signification donnée dans la revendication 1, - R2 et R3, W et Sp, identiques ou différents, ont les significations données dans la revendication 8.
10. Procédé selon l'une des revendications 1 à 6, caractérisé en ce le polymère présentant au moins une fonction de formule (1) est un polymère en forme d'étoiles.
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR0111494A FR2829140B1 (fr) | 2001-09-05 | 2001-09-05 | Procede de synthese de polymeres a fonctions thiols |
| KR20037011087A KR20030081462A (ko) | 2001-02-26 | 2002-02-18 | 저에너지 표면의 친수성을 증가시키기 위한 양쪽성 블록코폴리머의 용도 |
| EP02740786A EP1397417A1 (fr) | 2001-05-04 | 2002-05-03 | Procede de synthese de polymeres a fonctions thiols |
| PCT/FR2002/001538 WO2002090424A1 (fr) | 2001-05-04 | 2002-05-03 | Procede de synthese de polymeres a fonctions thiols |
| US10/476,534 US7396901B2 (en) | 2001-05-04 | 2002-05-03 | Method for synthesis of polymers with thiol functions |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR0111494A FR2829140B1 (fr) | 2001-09-05 | 2001-09-05 | Procede de synthese de polymeres a fonctions thiols |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| FR2829140A1 true FR2829140A1 (fr) | 2003-03-07 |
| FR2829140B1 FR2829140B1 (fr) | 2003-12-19 |
Family
ID=8866997
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| FR0111494A Expired - Lifetime FR2829140B1 (fr) | 2001-02-26 | 2001-09-05 | Procede de synthese de polymeres a fonctions thiols |
Country Status (1)
| Country | Link |
|---|---|
| FR (1) | FR2829140B1 (fr) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2021063780A1 (fr) | 2019-10-03 | 2021-04-08 | Rhodia Operations | Dispersions de polymère appropriées pour traitement de conditionnement de tissu |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1223655A (en) * | 1968-02-08 | 1971-03-03 | Goodrich Co B F | Curing |
| US3914214A (en) * | 1973-08-24 | 1975-10-21 | Us Agriculture | Thiolation of polysaccharides |
| GB1508699A (en) * | 1975-07-25 | 1978-04-26 | Ceskoslovenska Akademie Ved | Method of preparing polymeric thiols from polymeric nitroesters |
| WO1998058974A1 (fr) * | 1997-06-23 | 1998-12-30 | Rhodia Chimie | Procede de synthese de polymeres a blocs par polymerisation radicalaire controlee |
| FR2794463A1 (fr) * | 1999-06-04 | 2000-12-08 | Rhodia Chimie Sa | Procede de synthese de polymeres par polymerisation radicalaire controlee a l'aide de xanthates halogenes |
| WO2001042312A1 (fr) * | 1999-12-09 | 2001-06-14 | Rhodia Chimie | Procede de synthese de polymeres par polymerisation radicalaire controlee a l'aide de xanthates |
-
2001
- 2001-09-05 FR FR0111494A patent/FR2829140B1/fr not_active Expired - Lifetime
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1223655A (en) * | 1968-02-08 | 1971-03-03 | Goodrich Co B F | Curing |
| US3914214A (en) * | 1973-08-24 | 1975-10-21 | Us Agriculture | Thiolation of polysaccharides |
| GB1508699A (en) * | 1975-07-25 | 1978-04-26 | Ceskoslovenska Akademie Ved | Method of preparing polymeric thiols from polymeric nitroesters |
| WO1998058974A1 (fr) * | 1997-06-23 | 1998-12-30 | Rhodia Chimie | Procede de synthese de polymeres a blocs par polymerisation radicalaire controlee |
| FR2794463A1 (fr) * | 1999-06-04 | 2000-12-08 | Rhodia Chimie Sa | Procede de synthese de polymeres par polymerisation radicalaire controlee a l'aide de xanthates halogenes |
| WO2000075207A1 (fr) * | 1999-06-04 | 2000-12-14 | Rhodia Chimie | Procede de synthese de polymeres par polymerisation radicalaire controlee a l'aide de xanthates halogenes |
| WO2001042312A1 (fr) * | 1999-12-09 | 2001-06-14 | Rhodia Chimie | Procede de synthese de polymeres par polymerisation radicalaire controlee a l'aide de xanthates |
| FR2802208A1 (fr) * | 1999-12-09 | 2001-06-15 | Rhodia Chimie Sa | Procede de synthese de polymeres par polymerisation radicalaire controlee a l'aide de xanthates |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2021063780A1 (fr) | 2019-10-03 | 2021-04-08 | Rhodia Operations | Dispersions de polymère appropriées pour traitement de conditionnement de tissu |
Also Published As
| Publication number | Publication date |
|---|---|
| FR2829140B1 (fr) | 2003-12-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0991683B2 (fr) | Procede de synthese de polymeres a blocs par polymerisation radicalaire controlee | |
| EP1392737B1 (fr) | Procede de reduction radicalaire de fonctions dithiocarbonylees ou dithiophosphorylees portees par un polymere | |
| EP1044231B1 (fr) | Procede de synthese de polymeres a blocs par polymerisation radicalaire controlee a partir de composes dithioesters | |
| EP1309629B1 (fr) | Procede de synthese de polymeres a blocs par polymerisation radicalaire controlee | |
| EP1319027B1 (fr) | Procede de synthese de polymeres a blocs par polymerisation radicalaire controlee en presence d'un compose disulfure | |
| CA2375849A1 (fr) | Procede de synthese de polymeres par polymerisation radicalaire controlee a l'aide de xanthates halogenes | |
| WO1999035177A1 (fr) | Procede de synthese de polymeres a blocs par polymerisation radicalaire controlee a partir de composes dithiocarbamates | |
| EP1309638B1 (fr) | Procede de synthese de copolymeres hybrides silicones et organiques par polymerisation radicalaire controlee | |
| EP1397403A2 (fr) | Copolymeres a blocs tensioactifs prepares par polymerisation radicalaire controlee | |
| WO2012045944A1 (fr) | Polymérisation radicalaire contrôlée de n-vinyl lactames en milieu aqueux | |
| EP1397417A1 (fr) | Procede de synthese de polymeres a fonctions thiols | |
| EP1913043A1 (fr) | Copolymere a blocs comprenant un bloc lcst presentant une temperature inferieure critique de solubilite, formulations comprenant le copolymere et utilisation pour vectoriser un ingredient actif | |
| FR2829140A1 (fr) | Procede de synthese de polymeres a fonctions thiols | |
| EP2283052A1 (fr) | Copolymère amphiphile à blocs, procédé pour sa préparation | |
| WO2001027176A1 (fr) | Procede de preparation de polymeres greffes | |
| FR2829138A1 (fr) | Procede de reduction radicalaire de fonctions dithiocarbonylees ou dithiophosphorylees portees par un polymere | |
| WO2002036640A1 (fr) | Synthese de polymeres a blocs obtenus par polymerisation radicalaire controlee | |
| FR2840613A1 (fr) | Procede de synthese de polymeres a blocs par polymerisation radicalaire controlee par de nouveaux agents de controle dithiophosphotesters |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PLFP | Fee payment |
Year of fee payment: 16 |
|
| PLFP | Fee payment |
Year of fee payment: 17 |
|
| PLFP | Fee payment |
Year of fee payment: 18 |
|
| PLFP | Fee payment |
Year of fee payment: 19 |
|
| PLFP | Fee payment |
Year of fee payment: 20 |