JP2005220080A - アダマンタン誘導体及びこれを用いた有機電界発光素子 - Google Patents
アダマンタン誘導体及びこれを用いた有機電界発光素子 Download PDFInfo
- Publication number
- JP2005220080A JP2005220080A JP2004029906A JP2004029906A JP2005220080A JP 2005220080 A JP2005220080 A JP 2005220080A JP 2004029906 A JP2004029906 A JP 2004029906A JP 2004029906 A JP2004029906 A JP 2004029906A JP 2005220080 A JP2005220080 A JP 2005220080A
- Authority
- JP
- Japan
- Prior art keywords
- formula
- group
- adamantane derivative
- represented
- adamantane
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 0 c(cc1)cc(C(*23)=C4)c1C2=CC1=*2[Cn]3(*35)*6=C4c4ccccc4C6=CC3=C(C=CC=C3)C3=C5C=C2c2ccccc12 Chemical compound c(cc1)cc(C(*23)=C4)c1C2=CC1=*2[Cn]3(*35)*6=C4c4ccccc4C6=CC3=C(C=CC=C3)C3=C5C=C2c2ccccc12 0.000 description 1
Images
Landscapes
- Electroluminescent Light Sources (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
本発明の実施形態に係るアダマンタン誘導体は、下記式(1)で表されるオルトターフェニル構造、を含むオルトターフェニル構造を含む置換基を有する。また、アダマンタン誘導体は、下記式(2)で表され、
次に、本発明の実施形態1に係るアダマンタン誘導体、を使用した有機EL素子の実施形態について説明する。
)を使用することができる。
<2,2−ビス[4−(o−ターフェニル)]アダマンタンの合成>
IR(KBr):3055,3017,2913,2855,1474,1010,824,764,747,701cm-1
1H−NMR(CDCl3):1.69(d,J=11.3Hz,4H),1.70(s,2H),1.82(s,2H)、1.99(d,J=12.2Hz,4H),3.12(s,2H),6.96(d,J=8.3Hz,4H),7.03(dm,J=8.4Hz,4H),7.08(tm,J=7.5Hz,4H),7.13(tm,J=7.2Hz,2H),7.19(d,J=8.3Hz,4H),7.39(m,8H)ppm
13C−NMR(CDCl3):27.60,32.00,33.38,38.02,50.14,125.38,126.28,127.23,127.34,127.55,129.85,129.87,130.20,130.35,137.62,140.51,140.53,141.44,146.73ppm
<1,3−ジフェニルアダマンタンの合成>
アダマンタン 1.02g(7.49mmol)、塩化鉄六水和物 19.7g(72.9mmol)、K10モンモリロナイト 20gを、ベンゼン100mLに加え、ディーン・スタークトラップを用いて脱水しながら、17時間還流した。反応液をろ過し、残渣をヘキサンで洗浄した。ろ液とヘキサン洗浄液とを合わせて、水洗し、炭酸水素ナトリウム水溶液で洗浄後、無水硫酸ナトリウムで乾燥した。有機層について減圧下、溶媒を留去した後、濃縮物をシリカゲルカラム(クロロホルム:ヘキサン=1:9)で精製した。さらにエタノールで再結晶することにより、下記式(27)に示す1,3−ジフェニルアダマンタンを0.900g(収率41.7%)得た。構造はNMRにより確認した。
1H−NMR(CDCl3):1.79(s,2H),1.96(s,8H),2.05(s,2H),2.31(s,2H),7.19(t,2H),7.32(t,4H),7.40(d,4H)ppm
上記式(27)で示される1,3−ジフェニルアダマンタン 0.577g(2.0mmol)、ヨウ素 0.508g(2.02mmol)を、クロロホルム 11mLに加え、ヨウ素が溶解するまで15分間撹拌した。この溶液に[ビス(トリフルオロアセトキシ)ヨード]ベンゼン 0.860g(2.0mmol)を加え、窒素雰囲気下、室温で24時間撹拌した。この溶液にクロロホルム 20mLを加え、5%亜硝酸ナトリウム水溶液、水、飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥した。有機層について減圧下、溶媒を留去した後、濃縮物をクロロホルム/メタノールで再結晶することにより、下記式(28)で示す1,3−ビス(4−ヨードフェニル)アダマンタンを0.810g(収率75.0%)得た。構造はNMRにより確認した。
1H−NMR(CDCl3):1.77(s,2H),1.90(s,8H),1.94(s,2H),2.31(s,2H),7.13(d,4H),7.63(d,4H)ppm
上記式(28)で示される1,3−ビス(4−ヨードフェニル)アダマンタン 0.500g(0.926mmol)、2−ビフェニルホウ酸 0.403g(2.04mmol)、酢酸パラジウム 0.023g(0.094mmol)、o−トルイルホスフィン 0.086g(0.283mmol)を、ジメトキシエタン 8mLに加えた。この混合溶液に、炭酸カリウム 0.320g(2.32mmol)を水 2.3mLに溶解させた水溶液を加え、窒素雰囲気下で10時間還流した。冷却後、水 50mLを反応液中に加え、クロロホルムで抽出した。有機層を水、飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥した。有機層について減圧下、溶媒を留去した後、シリカゲルカラム(クロロホルム:ヘキサン=1:5〜1:1)で精製し、下記式(10)で示す1,3−ビス[4−(o−ターフェニル)]アダマンタンを0.499g(収率90.9%)得た。構造はNMRにより確認した。
1H−NMR(CDCl3):1.75(s,2H),1.90(s,8H),1.96(s,2H),2.27(s,2H),7.08(d,4H),7.13−7.15(m,4H),7.19−7.24(m,10H),7.38−7.44(m,8H)ppm
13C−NMR(CDCl3):29.52,35.87,37.00,42.20,48.86,124.38,126.34,127.22,127.41,127.79,129.57,129.87,130.61,130.66,138.66,140.37,140.49,141.65,148.83
<1,3−ジフェニル−5,7−ジメチルアダマンタンの合成>
1,3−ジメチルアダマンタン 1.23g(7.49mmol)、塩化鉄 11.83g(72.9mmol)、K10モンモリロナイト 20gを、ベンゼン100mLに加え、ディーン・スタークトラップを用いて脱水しながら、22時間還流した。反応液をろ過し、残渣をヘキサンで洗浄した。ろ液とヘキサン洗浄液とを合わせて、水洗し、炭酸水素ナトリウム水溶液で洗浄後、無水硫酸ナトリウムで乾燥した。有機層について減圧下、溶媒を留去した後、濃縮物をシリカゲルカラム(クロロホルム:ヘキサン=1:10〜1:1)で精製し、下記式(29)で示す1,3−ジフェニル−5,7−ジメチルアダマンタンを0.280g(収率11.8%)得た。構造はNMRにより確認した。
1H−NMR(CDCl3):0.98(s,6H),1.26(s,2H),1.59(q,8H),1.91(s,2H),7.17(t,2H),7.32(t,4H),7.40(d,4H)ppm
上記式(29)で示される1,3−ジフェニル−5,7−ジメチルアダマンタン 0.280g(0.88mmol)、ヨウ素 0.230g(0.906mmol)を、クロロホルム 5mLに加え、ヨウ素が溶解するまで10分間撹拌した。この溶液に[ビス(トリフルオロアセトキシ)ヨード]ベンゼン 0.390g(0.907mmol)を加え、窒素雰囲気下、室温で24時間撹拌した。この溶液にクロロホルム 10mLを加え、5%亜硝酸ナトリウム水溶液、水、飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥した。有機層について減圧下、溶媒を留去した後、濃縮物をシリカゲルカラム(クロロホルム:ヘキサン=0:10〜10:1)で精製することにより、下記式(30)で示す1,3−ビス(4−ヨードフェニル)−5,7−ジメチルアダマンタンを0.380g(収率76.0%)得た。構造はNMRにより確認した。
1H−NMR(CDCl3):0.97(s,6H),1.24(s,2H),1.53(q,8H),1.79(s,2H),7.12(d,4H),7.62(d,4H)ppm
上記式(30)で示される1,3−ビス(4−ヨードフェニル)−5,7−ジメチルアダマンタン 0.200g(0.352mmol)、2−ビフェニルホウ酸 0.153g(0.773mmol)、酢酸パラジウム 0.0086g(0.035mmol)、o−トルイルホスフィン 0.0321g(0.105mmol)を、ジメトキシエタン 3mLに加えた。この混合溶液に、炭酸カリウム 0.122g(0.883mmol)を水 0.9mLに溶解させた水溶液を加え、窒素雰囲気下で10時間還流した。冷却後、水 30mLを反応液中に加え、クロロホルムで抽出した。有機層を水、飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥した。有機層について減圧下、溶媒を留去した後、シリカゲルカラム(クロロホルム:ヘキサン=1:5〜1:1)で精製し、下記式(12)で示す1,3−ビス[4−(o−ターフェニル)]−5,7−ジメチルアダマンタンを0.190g(収率86.9%)得た。構造はNMRにより確認した。
1H−NMR(CDCl3):0.95(s,6H),1.22(s,2H),1.54(q,8H),1.82(s,2H),7.07(d,4H),7.13−7.15(m,4H),7.19−7.22(m,10H),7.38−7.41(m,8H)ppm
13C−NMR(CDCl3):30.55,32.40,38.78,47.60,48.65,50.04,124.51,126.35,127.23,127.41,127.81,129.58,129.87,130.62,130.66,138.73,140.36,140.49,141.65,148.26
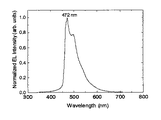
<青色用燐光発光有機電界発光素子の評価>
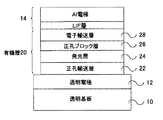
ガラス基板上にITOの透明電極を150nmの膜厚で形成し、有機洗浄、純水洗浄、乾燥、UVオゾン処理を行った。その基板を直ちに真空チャンバへ導入後、ArとO2のプラズマ処理を行った。
ホスト材料を上記式(10)で示した1,3−ビス[4−(o−ターフェニル)]アダマンタン(昇華精製なし)に代えた以外は、実施例4と同様にして有機EL素子を構成した。青色燐光材料(FIrpic)からの青色発光が確認された。外部量子効率は最大8.0%であった。
ホスト材料を上記式(12)で示した1,3−ビス[4−(o−ターフェニル)]−5,7−ジメチルアダマンタン(昇華精製なし)に代えた以外は、実施例4と同様にして有機EL素子を構成した。青色燐光材料(FIrpic)からの青色発光が確認された。外部量子効率は最大7.3%であった。
<PLスペクトルの評価>
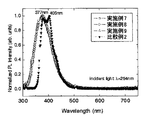
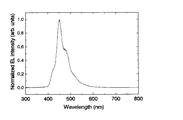
石英基板上に、真空蒸着(真空度5×10-7Torr;1Torr≒133Pa)により、上記式(5)で示した2,2−ビス[4−(o−ターフェニル)]アダマンタンの層を100nmの厚さに形成した。形成した薄膜のPLスペクトルを測定した(励起光波長:254nm)。測定結果を図3に示す。ピーク波長は377nmであった。
2,2−ビス[4−(o−ターフェニル)]アダマンタンを、上記式(10)で示した1,3−ビス[4−(o−ターフェニル)]アダマンタンに代えた以外は、実施例7と同様にして形成した薄膜のPLスペクトルを測定した。測定結果を図3に示す。ピーク波長は377nmであった。
2,2−ビス[4−(o−ターフェニル)]アダマンタンを、上記式(12)で示した1,3−ビス[4−(o−ターフェニル)]−5,7−ジメチルアダマンタンに代えた以外は、実施例7と同様にして形成した薄膜のPLスペクトルを測定した。測定結果を図3に示す。ピーク波長は377nmであった。
<蒸着膜の安定性評価>
実施例7で形成した、2,2−ビス[4−(o−ターフェニル)]アダマンタンの薄膜を形成した基板を室温下、大気中で放置したが、3ヶ月経過後も膜質の変化はなく良好であった。また、実施例4で作成した青色用燐光発光有機EL素子を恒温槽(オーブン)に入れ、室温から10℃刻みで昇温させ、各温度で1時間維持した後、発光効率を測定した。その結果、100℃においても素子の発光効率の急激な低下は観測されなかった。
2,2−ビス[4−(o−ターフェニル)]アダマンタンを、上記式(10)で示した1,3−ビス[4−(o−ターフェニル)]アダマンタンに代えた以外は、実施例10と同様にして形成した薄膜の室温下、大気中での安定性を評価した。3ヶ月経過後も膜質の変化はなく良好であった。
2,2−ビス[4−(o−ターフェニル)]アダマンタンを、上記式(12)で示した1,3−ビス[4−(o−ターフェニル)]−5,7−ジメチルアダマンタンに代えた以外は、実施例10と同様にして形成した薄膜の室温下、大気中での安定性を評価した。3ヶ月経過後も膜質の変化はなく良好であった。
2,2−ビス[4−(o−ターフェニル)]アダマンタンを、上記式(31)で示すCBPに代えた以外は、実施例7と同様にして形成した薄膜のPLスペクトルを測定した。測定結果を図3に示す。ピーク波長は405nmであり、2,2−ビス[4−(o−ターフェニル)]アダマンタンのピーク波長よりも長波長であった。
2,2−ビス[4−(o−ターフェニル)]アダマンタンを、上記式(31)で示すCBPに代えた以外は、実施例10と同様にして形成した薄膜の室温下、大気中での安定性を評価した。室温で1ヶ月経過後に、凝集が起こり膜質の変化が見られた。また、比較例1で作成した青色用燐光発光有機EL素子を恒温槽(オーブン)に入れ、室温から10℃刻みで昇温させ、各温度で1時間維持した後、発光効率を測定した。その結果、80℃以上になると素子の発光効率の急激な低下が観測された。なお、CBPを用いた有機EL素子
の素子温度対外部量子効率の変化及びCBPを用いた有機薄膜の耐熱試験の結果は特開2002−203683号公報に開示されている。
<緑色用燐光発光有機電界発光素子の評価>
ガラス基板上にITOの透明電極を150nmの膜厚で形成し、有機洗浄、純水洗浄、乾燥、UVオゾン処理を行った。その基板を直ちに真空チャンバへ導入後、ArとO2のプラズマ処理を行った。
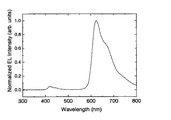
<赤色用燐光発光有機電界発光素子の評価>
ガラス基板上にITOの透明電極を150nmの膜厚で形成し、有機洗浄、純水洗浄、乾燥、UVオゾン処理を行った。その基板を直ちに真空チャンバへ導入後、ArとO2のプラズマ処理を行った。
<青色用蛍光発光有機電界発光素子の評価>
ガラス基板上にITOの透明電極を150nmの膜厚で形成し、有機洗浄、純水洗浄、乾燥、UVオゾン処理を行った。その基板を直ちに真空チャンバへ導入後、ArとO2のプラズマ処理を行った。
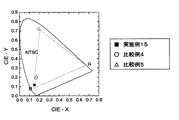
ホスト材料を下記式(33)で示した1,3−ビス[4−(1−ピレニル)フェニル]アダマンタンに代えた以外は、実施例15と同様にして有機EL素子を構成した。青色蛍光材料(式(19)で示される化合物)からの青色発光が確認された。外部量子効率は最大2.9%であった。また、色度はx=0.166、y=0.191であり、青色の色純度は実施例15より劣るものであった。
ガラス基板上にITOの透明電極を150nmの膜厚で形成し、有機洗浄、純水洗浄、乾燥、UVオゾン処理を行った。その基板を直ちに真空チャンバへ導入後、ArとO2のプラズマ処理を行った。
Claims (15)
- 請求項1に記載のアダマンタン誘導体であって、
前記アダマンタン誘導体は、
下記式(2)
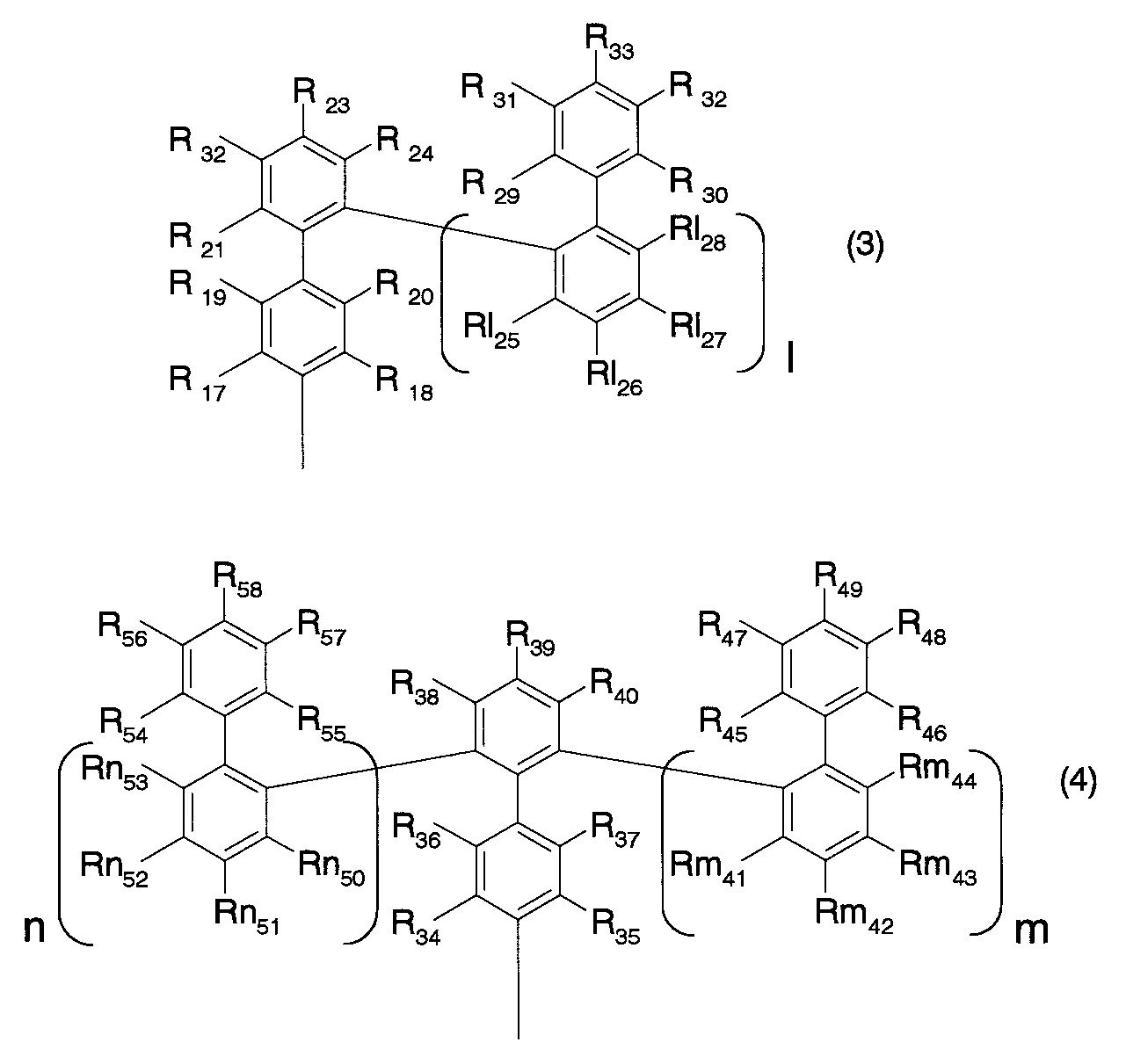
式(2)において、R1〜R16のうち少なくとも1つは下記式(3)または式(4)
で表される置換基であり、
式(2)中のR1〜R16のうち、式(3)または式(4)で表される置換基以外の置換基は、それぞれ水素、炭素数1〜6のアルキル基、炭素数2〜6のアルケニル基、炭素数2〜6のアルキニル基、アリール基、ヘテロアリール基、炭素数1〜6のアルコキシル基、アシル基、アシロキシ基、アミノ基、ニトロ基、シアノ基、エステル基、アミド基、ハロゲン基、炭素数1〜6のパーフルオロアルキル基のいずれかであることを特徴とするアダマンタン誘導体。 - 請求項2に記載のアダマンタン誘導体であって、
前記式(2)において、R1〜R16のうち少なくとも2つは前記式(3)または前記式(4)で表される置換基であることを特徴とするアダマンタン誘導体。 - 請求項3に記載のアダマンタン誘導体であって、
前記式(2)において、R1〜R4のうち少なくとも2つは前記式(3)または前記式(4)で表される置換基であることを特徴とするアダマンタン誘導体。 - 請求項3に記載のアダマンタン誘導体であって、
前記式(2)において、R5〜R16のうち少なくとも2つは前記式(3)または前記式(4)で表される置換基であることを特徴とするアダマンタン誘導体。 - 請求項5に記載のアダマンタン誘導体であって、
前記式(2)において、R5及びR6、あるいはR7及びR8、あるいはR9及びR10、あるいはR11及びR12、あるいはR13及びR14、あるいはR15及びR16、の組み合わせのうちの少なくとも1組は前記式(3)または前記式(4)で表される置換基であることを特徴とするアダマンタン誘導体。 - 請求項3に記載のアダマンタン誘導体であって、
前記式(2)において、R1〜R4のうち少なくとも2つのみが前記式(3)または前記式(4)で表される置換基であることを特徴とするアダマンタン誘導体。 - 請求項3に記載のアダマンタン誘導体であって、
前記式(2)において、R5〜R16のうち少なくとも2つのみが前記式(3)または前記式(4)で表される置換基であることを特徴とするアダマンタン誘導体。 - 請求項2〜8のいずれか1つに記載のアダマンタン誘導体であって、
前記式(3)または前記式(4)において、l,m,nはそれぞれ0であることを特徴とするアダマンタン誘導体。 - 有機層を備える有機電界発光素子であって、
請求項1〜10のいずれか1つに記載のアダマンタン誘導体を前記有機層中に含むことを特徴とする有機電界発光素子。 - 発光層を備える有機電界発光素子であって、
請求項1〜10のいずれか1つに記載のアダマンタン誘導体を前記発光層中に含むことを特徴とする有機電界発光素子。 - 有機電界発光素子であって、
ホスト材料及びドーパント材料を含む発光層を備え、
前記ホスト材料は、請求項1〜10のいずれか1つに記載のアダマンタン誘導体を含むことを特徴とする有機電界発光素子。 - 有機電界発光素子であって、
ホスト材料及び燐光発光性のドーパント材料を含む発光層を備え、
前記ホスト材料は、請求項1〜10のいずれか1つに記載のアダマンタン誘導体を含むことを特徴とする有機電界発光素子。 - 有機電界発光素子であって、
ホスト材料及び青色燐光発光性のドーパント材料を含む発光層を備え、
前記ホスト材料は、請求項1〜10のいずれか1つに記載のアダマンタン誘導体を含むことを特徴とする有機電界発光素子。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004029906A JP4470508B2 (ja) | 2004-02-05 | 2004-02-05 | アダマンタン誘導体及びこれを用いた有機電界発光素子 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004029906A JP4470508B2 (ja) | 2004-02-05 | 2004-02-05 | アダマンタン誘導体及びこれを用いた有機電界発光素子 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2005220080A true JP2005220080A (ja) | 2005-08-18 |
| JP4470508B2 JP4470508B2 (ja) | 2010-06-02 |
Family
ID=34995991
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004029906A Expired - Lifetime JP4470508B2 (ja) | 2004-02-05 | 2004-02-05 | アダマンタン誘導体及びこれを用いた有機電界発光素子 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4470508B2 (ja) |
Cited By (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005294250A (ja) * | 2004-03-10 | 2005-10-20 | Fuji Photo Film Co Ltd | 発光素子 |
| WO2007077456A1 (en) * | 2006-01-06 | 2007-07-12 | Isis Innovation Limited | Branched compounds and their use in sensors |
| WO2009107541A1 (ja) * | 2008-02-25 | 2009-09-03 | パイオニア株式会社 | 有機電界発光素子 |
| US7651789B2 (en) | 2004-03-10 | 2010-01-26 | Fujifilm Corporation | Organic electroluminescent device |
| US20100140605A1 (en) * | 2008-12-10 | 2010-06-10 | Fujifilm Corporation | Organic electroluminescence device and luminescence apparatus |
| WO2010067708A1 (ja) * | 2008-12-08 | 2010-06-17 | 富士フイルム株式会社 | 有機電界発光素子 |
| JP2010161326A (ja) * | 2008-02-28 | 2010-07-22 | Fujifilm Corp | 有機電界発光素子 |
| JP2010161325A (ja) * | 2008-02-28 | 2010-07-22 | Fujifilm Corp | 有機電界発光素子 |
| JP2010245063A (ja) * | 2009-03-31 | 2010-10-28 | Fujifilm Corp | 有機電界発光素子 |
| JP2011071458A (ja) * | 2009-01-07 | 2011-04-07 | Fujifilm Corp | 有機電界発光素子 |
| JP2011100943A (ja) * | 2009-11-09 | 2011-05-19 | Fujifilm Corp | 有機電界発光素子 |
| JP2013501109A (ja) * | 2009-08-04 | 2013-01-10 | メルク パテント ゲーエムベーハー | 多環式炭水化物を含む電子デバイス |
| CN104177264A (zh) * | 2013-05-28 | 2014-12-03 | 海洋王照明科技股份有限公司 | 苯萘胺基蓝光磷光主体材料及其制备方法和有机电致发光器件 |
| JP2015046608A (ja) * | 2009-09-30 | 2015-03-12 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子 |
| WO2016068478A3 (ko) * | 2014-10-30 | 2016-08-04 | 주식회사 엘지화학 | 고리 화합물 및 이를 포함하는 유기 발광 소자 |
| TWI549563B (zh) * | 2008-02-28 | 2016-09-11 | Udc愛爾蘭有限公司 | 有機電致發光裝置 |
| WO2021101112A1 (ko) * | 2019-11-21 | 2021-05-27 | 주식회사 엘지화학 | 화합물 및 이를 포함하는 유기 발광 소자 |
| KR20210095555A (ko) * | 2020-01-23 | 2021-08-02 | 주식회사 엘지화학 | 신규한 화합물 및 이를 포함하는 유기발광 소자 |
| CN116368118A (zh) * | 2020-10-09 | 2023-06-30 | 保土谷化学工业株式会社 | 金刚烷化合物、有机电致发光元件和电子设备 |
| US11997925B2 (en) | 2018-08-31 | 2024-05-28 | Lg Chem, Ltd. | Cyclic compound and organic light emitting device comprising same |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101708176B1 (ko) | 2015-12-31 | 2017-02-20 | 머티어리얼사이언스 주식회사 | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR102096867B1 (ko) | 2016-12-29 | 2020-04-03 | 머티어리얼사이언스 주식회사 | 유기 화합물 및 이를 포함하는 유기전계발광소자 |
| KR20200037732A (ko) | 2018-10-01 | 2020-04-09 | 머티어리얼사이언스 주식회사 | 유기 화합물 및 이를 포함하는 유기전계발광소자 |
-
2004
- 2004-02-05 JP JP2004029906A patent/JP4470508B2/ja not_active Expired - Lifetime
Cited By (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005294250A (ja) * | 2004-03-10 | 2005-10-20 | Fuji Photo Film Co Ltd | 発光素子 |
| US7651789B2 (en) | 2004-03-10 | 2010-01-26 | Fujifilm Corporation | Organic electroluminescent device |
| WO2007077456A1 (en) * | 2006-01-06 | 2007-07-12 | Isis Innovation Limited | Branched compounds and their use in sensors |
| US7812323B2 (en) | 2006-01-06 | 2010-10-12 | Isis Innovation Limited | Branched compounds and their use in sensors |
| WO2009107541A1 (ja) * | 2008-02-25 | 2009-09-03 | パイオニア株式会社 | 有機電界発光素子 |
| JP2010161326A (ja) * | 2008-02-28 | 2010-07-22 | Fujifilm Corp | 有機電界発光素子 |
| JP2010161325A (ja) * | 2008-02-28 | 2010-07-22 | Fujifilm Corp | 有機電界発光素子 |
| TWI549563B (zh) * | 2008-02-28 | 2016-09-11 | Udc愛爾蘭有限公司 | 有機電致發光裝置 |
| WO2010067708A1 (ja) * | 2008-12-08 | 2010-06-17 | 富士フイルム株式会社 | 有機電界発光素子 |
| JP2010161060A (ja) * | 2008-12-08 | 2010-07-22 | Fujifilm Corp | 有機電界発光素子 |
| US20100140605A1 (en) * | 2008-12-10 | 2010-06-10 | Fujifilm Corporation | Organic electroluminescence device and luminescence apparatus |
| US9461253B2 (en) * | 2008-12-10 | 2016-10-04 | Udc Ireland Limited | Organic electroluminescence device and luminescence apparatus |
| JP2015053492A (ja) * | 2009-01-07 | 2015-03-19 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子 |
| JP2011071458A (ja) * | 2009-01-07 | 2011-04-07 | Fujifilm Corp | 有機電界発光素子 |
| JP2010245063A (ja) * | 2009-03-31 | 2010-10-28 | Fujifilm Corp | 有機電界発光素子 |
| JP2015181182A (ja) * | 2009-08-04 | 2015-10-15 | メルク パテント ゲーエムベーハー | 多環式炭水化物を含む電子デバイス |
| JP2013501109A (ja) * | 2009-08-04 | 2013-01-10 | メルク パテント ゲーエムベーハー | 多環式炭水化物を含む電子デバイス |
| JP2015046608A (ja) * | 2009-09-30 | 2015-03-12 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子 |
| JP2011100943A (ja) * | 2009-11-09 | 2011-05-19 | Fujifilm Corp | 有機電界発光素子 |
| CN104177264A (zh) * | 2013-05-28 | 2014-12-03 | 海洋王照明科技股份有限公司 | 苯萘胺基蓝光磷光主体材料及其制备方法和有机电致发光器件 |
| TWI586655B (zh) * | 2014-10-30 | 2017-06-11 | Lg 化學股份有限公司 | 環狀化合物及含有該環狀化合物的有機發光元件 |
| WO2016068478A3 (ko) * | 2014-10-30 | 2016-08-04 | 주식회사 엘지화학 | 고리 화합물 및 이를 포함하는 유기 발광 소자 |
| KR101787195B1 (ko) | 2014-10-30 | 2017-10-18 | 주식회사 엘지화학 | 고리 화합물 및 이를 포함하는 유기 발광 소자 |
| JP2017533893A (ja) * | 2014-10-30 | 2017-11-16 | エルジー・ケム・リミテッド | 環化合物およびこれを含む有機発光素子 |
| US10431748B2 (en) | 2014-10-30 | 2019-10-01 | Lg Chem, Ltd. | Cyclic compound and organic light-emitting element comprising same |
| US11997925B2 (en) | 2018-08-31 | 2024-05-28 | Lg Chem, Ltd. | Cyclic compound and organic light emitting device comprising same |
| WO2021101112A1 (ko) * | 2019-11-21 | 2021-05-27 | 주식회사 엘지화학 | 화합물 및 이를 포함하는 유기 발광 소자 |
| KR20210062556A (ko) * | 2019-11-21 | 2021-05-31 | 주식회사 엘지화학 | 화합물 및 이를 포함하는 유기 발광 소자 |
| KR102669427B1 (ko) * | 2019-11-21 | 2024-05-28 | 주식회사 엘지화학 | 화합물 및 이를 포함하는 유기 발광 소자 |
| KR20210095555A (ko) * | 2020-01-23 | 2021-08-02 | 주식회사 엘지화학 | 신규한 화합물 및 이를 포함하는 유기발광 소자 |
| KR102501262B1 (ko) | 2020-01-23 | 2023-02-17 | 주식회사 엘지화학 | 신규한 화합물 및 이를 포함하는 유기발광 소자 |
| CN116368118A (zh) * | 2020-10-09 | 2023-06-30 | 保土谷化学工业株式会社 | 金刚烷化合物、有机电致发光元件和电子设备 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP4470508B2 (ja) | 2010-06-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4470508B2 (ja) | アダマンタン誘導体及びこれを用いた有機電界発光素子 | |
| JP4545741B2 (ja) | 有機電界発光素子 | |
| TWI429650B (zh) | Organic electroluminescent elements | |
| JP5723764B2 (ja) | 有機電界発光素子 | |
| JP4593470B2 (ja) | 有機電界発光素子 | |
| CN103907217B (zh) | 有机电致发光元件 | |
| TWI477579B (zh) | Organic electroluminescent elements | |
| TWI585091B (zh) | Organic electroluminescent elements | |
| TWI475022B (zh) | Organic electroluminescent elements | |
| JP4630637B2 (ja) | 有機発光素子及び有機化合物 | |
| JPH0812600A (ja) | フェニルアントラセン誘導体および有機el素子 | |
| WO2012035962A1 (en) | New condensed polycyclic compound and organic light-emitting element using the same | |
| JP2004220931A (ja) | 有機電界発光素子 | |
| CN104871335B (zh) | 有机电致发光元件用材料及使用其的有机电致发光元件 | |
| WO2010113726A1 (ja) | 燐光発光素子用材料及びこれを用いた有機電界発光素子 | |
| JP2009269909A (ja) | 新規な電子材料用化合物及びこれを使用する有機電子素子 | |
| JP2012246258A (ja) | 縮合多環化合物及びこれを用いた有機発光素子 | |
| KR20130098413A (ko) | 퀴놀리노[3,2,1-kl]페녹사진 화합물과 이를 사용한 유기 발광 소자 및 조명 장치 | |
| KR100936140B1 (ko) | 발광 특성이 개선된 청색 형광 물질 및 이를 이용한유기전계발광소자 | |
| JP5618647B2 (ja) | 新規有機化合物およびそれを有する有機発光素子 | |
| JP5624518B2 (ja) | 有機電界発光素子、該素子用材料、並びに該素子を用いた発光装置、表示装置及び照明装置 | |
| JP2004155709A (ja) | 有機金属錯体化合物及びこれを用いた有機発光素子 | |
| WO2004065520A1 (ja) | 発光素子、それに用いる縮合多環系化合物及びその製造方法 | |
| KR20160072868A (ko) | 이리듐 착화합물 및 이를 이용한 유기전계 발광소자 | |
| KR20160045019A (ko) | 신규한 화합물 및 이를 포함하는 유기발광소자 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20061004 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20090729 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20090915 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091023 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20091117 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100108 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20100209 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20100222 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130312 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130312 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130312 Year of fee payment: 3 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313532 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130312 Year of fee payment: 3 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |