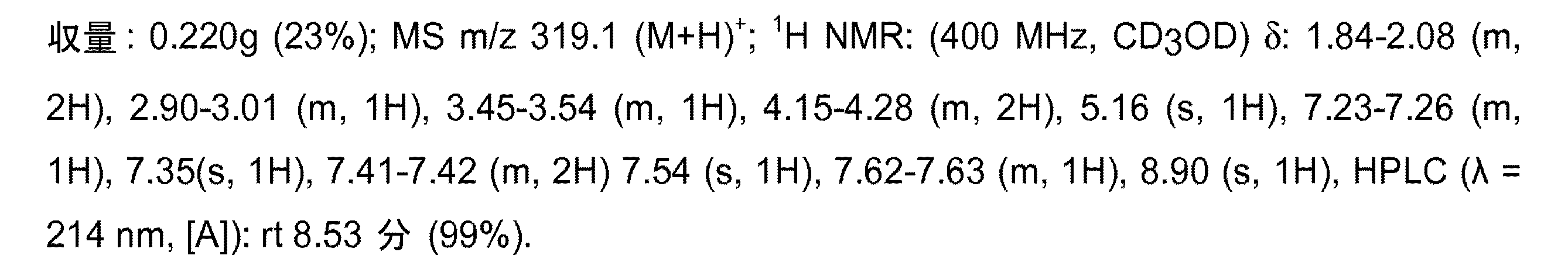JP2012502006A - 新規の阻害剤 - Google Patents
新規の阻害剤 Download PDFInfo
- Publication number
- JP2012502006A JP2012502006A JP2011525556A JP2011525556A JP2012502006A JP 2012502006 A JP2012502006 A JP 2012502006A JP 2011525556 A JP2011525556 A JP 2011525556A JP 2011525556 A JP2011525556 A JP 2011525556A JP 2012502006 A JP2012502006 A JP 2012502006A
- Authority
- JP
- Japan
- Prior art keywords
- alkyl
- imidazol
- compound
- dione
- phenyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 0 *CCNC**CCN*I Chemical compound *CCNC**CCN*I 0.000 description 5
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4178—1,3-Diazoles not condensed 1,3-diazoles and containing further heterocyclic rings, e.g. pilocarpine, nitrofurantoin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/18—Drugs for disorders of the alimentary tract or the digestive system for pancreatic disorders, e.g. pancreatic enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
- A61P15/08—Drugs for genital or sexual disorders; Contraceptives for gonadal disorders or for enhancing fertility, e.g. inducers of ovulation or of spermatogenesis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/20—Hypnotics; Sedatives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/22—Anxiolytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D235/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings
- C07D235/02—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings condensed with carbocyclic rings or ring systems
- C07D235/04—Benzimidazoles; Hydrogenated benzimidazoles
- C07D235/06—Benzimidazoles; Hydrogenated benzimidazoles with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached in position 2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/06—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Immunology (AREA)
- Diabetes (AREA)
- Psychiatry (AREA)
- Reproductive Health (AREA)
- Pain & Pain Management (AREA)
- Rheumatology (AREA)
- Endocrinology (AREA)
- Hematology (AREA)
- Psychology (AREA)
- Cardiology (AREA)
- Gynecology & Obstetrics (AREA)
- Heart & Thoracic Surgery (AREA)
- Vascular Medicine (AREA)
- Obesity (AREA)
- Urology & Nephrology (AREA)
- Hospice & Palliative Care (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Anesthesiology (AREA)
- Pregnancy & Childbirth (AREA)
- Transplantation (AREA)
- Dermatology (AREA)
Abstract
Description
本発明は、グルタミニルシクラーゼ(QC、EC 2.3.2.5)の阻害剤としての新規イミダゾリジン誘導体に関する。QCは、アンモニアの遊離下でのN-末端グルタミン残基のピログルタミン酸(5-オキソ-プロリル、pGlu*)への分子内環化、及び水の遊離下でのN-末端グルタミン酸残基のピログルタミン酸への分子内環化を触媒する。
グルタミニルシクラーゼ(QC, EC 2.3.2.5)は、アンモニアを遊離しながらの、N-末端グルタミン残基のピログルタミン酸(pGlu*)への分子内環化を触媒する。QCは、1963年にMesserにより熱帯植物カリカ・パパイヤ(Carica papaya)のラテックスから最初に単離された(Messer, M.の文献(1963 Nature 4874, 1299))。24年後、対応する酵素活性が、動物の下垂体において発見された(Busby, W. H. J.らの文献(1987 J Biol Chem 262, 8532-8536);Fischer, W. H.及びSpiess, J.の文献(1987 Proc Natl Acad Sci USA 84, 3628-3632))。哺乳動物のQCに関して、QCによるGlnのpGluへの転換が、TRH及びGnRHの前駆体について示すことができた(Busby, W. H. J.らの文献(1987 J Biol Chem 262, 8532-8536);Fischer, W. H.及びSpiess, J.の文献(1987 Proc Natl Acad Sci USA 84, 3628-3632))。加えて、最初のQC局在化実験は、ウシ下垂体におけるQCの触媒の推定生成物との同時局在を明らかにし、ペプチドホルモン合成において示唆された機能を更に改良した(Bockers, T. M.らの文献(1995 J Neuroendocrinol 7, 445-453))。対照的に、植物のQCの生理機能は、余り明確ではない。C.パパイヤ由来の酵素の場合、病原性微生物に対する植物防御における役割が示唆された(El Moussaoui, A.らの文献(2001 Cell Mol Life Sci 58, 556-570))。他の植物に由来する推定上のQCが、配列比較により最近同定された(Dahl, S. W.らの文献(2000 Protein Expr Purif 20, 27-36))。しかしこれらの酵素の生理機能は依然曖昧である。
EP 02 011 349.4は、昆虫グルタミニルシクラーゼをコードするポリヌクレオチドに加え、該ポリヌクレオチドによりコードしたポリペプチド、及びグルタミニルシクラーゼ活性を低下させる作用物質のスクリーニング法におけるそれらの使用を開示している。このような作用物質は、殺虫剤として有用である。
用語「ki」又は「KI」及び「KD」は、結合定数であり、これは阻害剤の酵素への結合及び酵素からのその後の放出を説明している。別の測定値は、「IC50」値であり、これは、所与の基質濃度で、50%の酵素活性を生じる阻害剤濃度を反映している。
本明細書において使用される用語「EC活性」は、QCによるN-末端グルタミン酸残基のピログルタミン酸(pGlu*)への分子内環化として定義される。従ってスキーム3を参照されたい。
好ましい実施態様において、QC阻害との相関関係を考慮し、本対象となる方法及び医学的用途は、QC阻害のIC50が10μM以下、より適切には1μM以下、更により適切には0.1μM以下若しくは0.01μM以下、又は最も適切には0.001μM以下である作用物質を利用する。実際、Ki値が、より低いμM、好ましくはnM、更により適切にはpMの範囲である阻害剤が意図されている。従って、本明細書においては便宜上「QC阻害剤」として本活性作用物質が説明されているが、そのような命名は、本発明の対象を特定の作用機構に限定することを意図するものではないことは理解されるであろう。
一般に、本対象となる方法又は医学的用途のQC阻害剤は、例えば、分子量が500g/モル以下、400g/モル以下、適切には350g/モル以下、更により適切には300g/モル以下、及び更には250g/モル以下である小分子であろう。
本明細書において使用される用語「治療的有効量」は、治療される疾患又は障害の症状を緩和することを含む、研究者、獣医、医師又は他の臨床医により探求される、組織の系、動物又はヒトにおいて生物学的応答又は医学的応答を誘起する活性化合物又は医薬物質の量を意味する。
表現「アルキレン」は、式-(CH2)n-の鎖を意味し、式中nは、特に限定しない限りは、整数であり、例えば2〜5である。
表現「-アルキルヘテロアリール」は、特に限定しない限りは、アルキレン部分、例えばC1-4アルキレン部分を介して結合されているヘテロアリール残基を示す。
用語「アミノ」は、-NH2基を指す。
用語「フェニルによって置換したフェニル」はビフェニルを指す。
主張された化合物の全ての可能性のある立体異性体が、本発明に含まれる。
本発明の化合物が少なくとも1個のキラル中心を有する場合、それに応じて該化合物は鏡像異性体として存在し得る。本化合物が2個以上のキラル中心を有する場合、該化合物は加えてジアステレオマーとして存在し得る。全てのそのような異性体及びそれらの混合物が、本発明の範囲内に包含されることは理解されるべきである。
本発明の化合物の製造プロセスが立体異性体の混合物を生じる場合、これらの異性体は、分取クロマトグラフィーなどの通常の技術により分離されてもよい。本化合物は、ラセミ体の形状で製造されてもよいか、又は個別の鏡像異性体が、鏡像特異的合成によるか若しくは分割によるかのいずれかにより、製造されてもよい。本化合物は、例えば、(-)-ジ-p-トルオイル-d-酒石酸及び/又は(+)-ジ-p-トルオイル-l-酒石酸などの光学活性のある酸との塩形成、それに続く分別結晶及び遊離塩基の再生によるジアステレオマー対の形成などの、標準技術により、該化合物の成分鏡像異性体に分割されてよい。また、本化合物は、ジアステレオマー的エステル又はアミドの形成、それに続くクロマトグラフィーによる分離及びキラル補助基の除去により、分割されてもよい。或いは本化合物は、キラルHPLCカラムを用い、分割されてよい。
遊離化合物とそれらの塩又は溶媒和物の形態の化合物の間の密接な関係を考慮し、化合物がこの文脈において言及される限りは、対応する塩、溶媒和物又は多形体も意図されるが、但しその状況下で可能又は適切であることを条件とする。
本発明の化合物の医薬として許容し得る酸付加塩の形は全て、本発明の範囲により包含されることが意図されている。
更に本化合物の結晶形の一部は、多形体として存在してよく、かつそれ自体、本発明に含まれることが意図されている。加えて一部の本化合物は、水と(すなわち水和物)又は一般的な有機溶媒と溶媒和物を形成することができ、そのような溶媒和物も、本発明の範囲内に包含されることが意図されている。また、本化合物の塩を含む該化合物は、それらの水和物の形で得ることができるか、又はそれらの結晶化に使用される他の溶媒を含むことができる。
本発明は更に、その範囲内に、本発明の化合物のプロドラッグを含む。一般に、そのようなプロドラッグは、所望の治療活性のある化合物へインビボにおいて容易に転換可能である化合物の官能基誘導体(functional derivative)であろう。従ってこれらの場合、本発明の治療法で、用語「投与する」は、主張した化合物1種以上のプロドラッグ型による説明した様々な障害の治療を包含するが、該プロドラッグ型は、対象への投与後に先に明記した化合物に転換する。適切なプロドラッグ誘導体の選択及び製造の通常の手順は、例えば、H. Bundgaardの文献「プロドラッグの設計(Design of Prodrugs)」(Elsevier, 1985)に説明されている。
本発明の化合物の製造プロセスの間に、関心のある任意の分子上の感応性のある基又は反応基を保護することが必要及び/又は望ましいことがある。このことは、J.F.W. McOmieの文献「有機化学における保護基(Protective Groups in Organic Chemistry)」(Plenum Press, 1973);並びに、T.W. Greene及びP. G. M. Wutsの文献「有機合成における保護基(Protective Groups in Organic Synthesis)」(John Wiley & Sons, 1991)に記載されているものなど、通常の保護基により実現することができ、これらの文献は引用により本明細書中に完全に組み込まれている。該保護基は、都合の良い引き続きの工程において、当該技術分野由来の公知の方法を用いて除去することができる。
従って、例えば懸濁液、エリキシル剤、及び溶液などの液体経口製剤に関して、適切な担体及び添加剤には、有利なことに、水、グリコール、油類、アルコール、調味料、保存料、着色料などを含んでもよく;例えば散剤、カプセル剤、ゲルキャップ剤及び錠剤などの固形経口製剤に関しては、適切な担体及び添加剤には、デンプン、糖類、希釈剤、造粒剤、潤滑剤、結合剤、崩壊剤などを含む。
崩壊剤には、デンプン、メチルセルロース、寒天、ベントナイト、キサンタンゴムなどを含むが、これらに限定されるものではない。
本発明に従い、式(I)の化合物、又は、そのすべての互変異性体及び立体異性体、又はそれらの医薬として許容し得る塩、溶媒和物若しくは多形体
R1は、-C3-8カルボシクリル-ヘテロアリール、-C2-6アルケニルヘテロアリール、-C1-6アルキルヘテロアリール、又は(CH2)aCR5R6(CH2)bヘテロアリールを表し、式中、a及びbは独立して、0〜5の整数を表し、但し、a+b=0〜5であり、かつR5及びR6が、それらの結合する炭素原子と共にC3-C5シクロアルキル基又は二環式ヘテロアリール基を形成するアルキレンであり;
ここで、上記のヘテロアリール基のいずれも、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、-C1-6チオアルキル、-SOC1-4アルキル、-SO2C1-4アルキル、C1-6アルコキシ-、-O-C3-8シクロアルキル、C3-8シクロアルキル、-SO2C3-8シクロアルキル、-SOC3-6シクロアルキル、C3-6アルケニルオキシ-、C3-6アルキニルオキシ-、-C(O)C1-6アルキル、-C(O)OC1-6アルキル、C1-6アルコキシ-C1-6アルキル-、ニトロ、ハロゲン、シアノ、ヒドロキシル、-C(O)OH、-NH2、-NHC1-4アルキル、-N(C1-4アルキル)(C1-4アルキル)、-C(O)N(C1-4アルキル)(C1-4アルキル)、-C(O)NH2、-C(O)NH(C1-4アルキル)、及び-C(O)NH(C3-10シクロアルキル)から選択される1つ以上の基によって任意に置換してもよく;
かつここで、上記のカルボシクリル基のいずれも、C1-4アルキル、オキソ、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
R2は、C1-8アルキル、アリール、ヘテロアリール、カルボシクリル、ヘテロシクリル、-C1-4アルキルアリール、-C1-4アルキルヘテロアリール、-C1-4アルキルカルボシクリル、又は-C1-4アルキルヘテロシクリルを表し;
ここで、上記のアリール基及びヘテロアリール基のいずれも、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、-C1-6チオアルキル、-SOC1-4アルキル、-SO2C1-4アルキル、C1-6アルコキシ-、-O-C3-8シクロアルキル、C3-8シクロアルキル、-SO2C3-8シクロアルキル、-SOC3-6シクロアルキル、C3-6アルケニルオキシ-、C3-6アルキニルオキシ-、-C(O)C1-6アルキル、-C(O)OC1-6アルキル、C1-6アルコキシ-C1-6アルキル-、ニトロ、ハロゲン、シアノ、ヒドロキシル、-C(O)OH、-NH2、-NHC1-4アルキル、-N(C1-4アルキル)(C1-4アルキル)、-C(O)N(C1-4アルキル)(C1-4アルキル)、-C(O)NH2、-C(O)NH(C1-4アルキル)、及び-C(O)NH(C3-10シクロアルキル)から選択される1つ以上の基によって任意に置換してもよく;
かつここで、上記のカルボシクリル基及びヘテロシクリル基のいずれも、C1-4アルキル、オキソ、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
或いはR2は、フェニルによって置換したフェニル、単環式ヘテロアリール基によって置換したフェニル、ベンジルオキシによって置換したフェニル、カルボシクリルに縮合したフェニル、ヘテロシクリルに縮合したフェニル、-C1-4アルキル(フェニルによって置換したフェニル)、-C1-4アルキル(単環式ヘテロアリール基によって置換したフェニル)、-C1-4アルキル(ベンジルオキシによって置換したフェニル)、-C1-4アルキル(任意に置換したカルボシクリルに縮合した任意に置換したフェニル)、又はC1-4アルキル(任意に置換したヘテロシクリルに縮合した任意に置換したフェニル)を表し;
ここで、上記のフェニル基、ベンジルオキシ基、及びヘテロアリール基のいずれも、C1-4アルキル、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく、かつここで、上記のカルボシクリル基及びヘテロシクリル基のいずれも、C1-4アルキル、オキソ、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
R3は、H、-C1-4アルキル、又はアリールを表し;
ここで、上記のアリールは、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、-C1-6チオアルキル、-SOC1-4アルキル、-SO2C1-4アルキル、C1-6アルコキシ-、-O-C3-8シクロアルキル、C3-8シクロアルキル、-SO2C3-8シクロアルキル、-SOC3-6シクロアルキル、C3-6アルケニルオキシ-、C3-6アルキニルオキシ-、-C(O)C1-6アルキル、-C(O)OC1-6アルキル、C1-6アルコキシ-C1-6アルキル-、ニトロ、ハロゲン、シアノ、ヒドロキシル、-C(O)OH、-NH2、-NHC1-4アルキル、-N(C1-4アルキル)(C1-4アルキル)、-C(O)N(C1-4アルキル)(C1-4アルキル)、-C(O)NH2、-C(O)NH(C1-4アルキル)、及び-C(O)NH(C3-10シクロアルキル)から選択される1つ以上の基によって任意に置換してもよく;
或いは、R2及びR3は、1つ以上のC1-2アルキル基によって任意に置換したカルボシクリル環を形成するよう結合し;
或いは、R2及びR3は、フェニルに縮合したカルボシクリル環を形成するよう結合し、ここで、上記のカルボシクリル及び/又はフェニルは、C1-4アルキル、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
或いは、R2及びR3は、単環式ヘテロアリールに縮合したカルボシクリル環を形成するよう結合し、ここで、上記のカルボシクリル及び/又はヘテロアリールは、C1-4アルキル、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
R4は、H、-C1-8アルキル、-C(O)C1-6アルキル、又はNH2を表し;
Xは、O又はSを表し;かつ
Yは、O又はSを表す。
例えば、米国特許第6,236,786号及びWO99/06361は両方とも、MMP阻害剤に関し;WO2008/076754は、カンナビノイド阻害剤に関し;WO2008/028032は、高眼圧症を治療するのに有用であるといわれている化合物に関し、並びにWerbelらの文献(J. Med. Chem., 20(12), (1977), 1569-1572)は、マンソン住血吸虫を治療するための化合物に関する。
カルボシクリル及びヘテロシクリルが置換される場合、典型的には、これらは1個又は2個の置換基(例えば、1個の置換基)によって置換される。典型的には、該置換基はメチルである。より典型的には、カルボシクリル基及びヘテロシクリル基は非置換である。
上記のヘテロアリール基は通常、非置換であろうけれども、適切にはアルキル(MeなどのC1-4アルキル)、アルコキシ-(例えば、OMeなどのC1-4アルコキシ-)、及びハロゲン(例えば、F)から選択される1個以上の置換基、適切には1個又は2個の置換基によって置換してもよい。
特に適切な二環式ヘテロアリール基の例には、1H-ベンズイミダゾリル、イミダゾ[1,2-a]ピリジン、及びベンゾ[c][1,25]チアジアゾリルを含む。1H-ベンゾイミダゾール-5-イルが特に適切である。
該実施態様において、R1のヘテロアリール基は、二環式、例えば、先に記載した基のうちの1つであってもよい。しかしながら、より適切なヘテロアリール基は、単環、特に5員環又は6員環、より特別には5員環である。典型的には、該ヘテロアリール基は、窒素含有複素環基であり、より典型的には1〜3個の窒素原子を含む。適切には、ヘテロアリール基はS原子を含まない。上記のヘテロアリール基は、非置換であってもよいか又は、1個以上の置換基、適切にはアルキル(例えば、MeなどのC1-4アルキル)、アルコキシ-(例えば、OMeなどのC1-4アルコキシ-)、及びハロゲン(例えば、F)から選択される1個若しくは2個の置換基によって適切に置換してもよいかのいずれかである。
R1が-C2-6アルケニルヘテロアリールを表す場合、C2-6アルケニルの例には、C2-4アルケニル、特にプロペニルを含む。典型的な-アルケニルヘテロアリール基は、3-イミダゾール-1-イル-プロパ-2-エニル-である。
最も適切には、該アルキル基は、-CH2-、-(CH2)2、又は-(CH2)3-であり、-(CH2)3-が特に適切である。特に適切な-アルキルヘテロアリール基は、3-イミダゾール-1-イル-プロピル-である。
R11、R12、及びR13は独立して、H又はC1-2アルキルを表す。
R14及びR15は独立して、H又はC1-2アルキルを表す。
R16及びR17は独立して、H又はC1-2アルキルを表す。
R18及びR19は独立して、H又はC1-2アルキルを表す。
特に適切な化合物において、R1は下記式を表す
このような化合物において、Bは、結合、-CH2-、又は-CH2-CH2-を表す。特に適切な実施態様において、Bは結合を表す。別の実施態様において、Bは-CH2-を表す。第三の実施態様において、Bは-CH2-CH2-を表す。
R11は適切にはHを表し、
R12は適切にはH又はメチルを表す。
R13は適切にはH又はメチルを表す。
本発明の一実施態様において、R12はHを表し、かつR13はメチルを表す。別の実施態様において、R12はメチルを表し、かつR13はHを表す。第三の実施態様において、R12はHを表し、かつR13はHを表す。
或いは、Aは分岐C2-5アルキレン鎖を表す。
Aが、同じ位置で2個のアルキレン置換基によって置換されるC2-5アルキレン鎖を表す場合(ここで、2個のアルキレン置換基は互いに結合して、C3-5スピロ-シクロアルキル基を形成する。)、該スピロ-シクロアルキル基は適切には、C3スピロ-シクロアルキルである。
一実施態様において、R16はHを表し、かつR17はHを表す。別の実施態様において、R16はHを表し、かつR17はC1-2アルキルを表す。第三の実施態様において、R16はC1-2アルキルを表し、かつR17はHを表す。
適切には、Cは、結合、-CH2-、又は-CH2CH2-を表す。一実施態様において、Cは結合を表す。別の実施態様において、Cは-CH2-を表す。第三の実施態様において、Cは-CH2CH2-を表す。
一実施態様において、R18はHを表し、かつR19はHを表す。別の実施態様において、R18はHを表し、かつR19はC1-2アルキルを表す。第三の実施態様において、R18はC1-2アルキルを表し、かつR19はHを表す。
適切には、Dは、結合、-CH2-、又は-CH2CH2-を表す。一実施態様において、Dは結合を表す。別の実施態様において、Dは-CH2-を表す。第三の実施態様において、Dは-CH2CH2-を表す。
最も適切には、R1は、下記式を表す
特に適切な実施態様において、式(I)の化合物は、下記式によって表される
最も適切には、式(I)の化合物は、下記式によって表される
R2が、(任意に置換してもよい)ヘテロシクリルを表す場合、例には、テトラヒドロフラニル、モルフォリニル、ピペルジニル(piperdinyl)、3,4-ジヒドロ-2H-ピラニル、ピロリジニル、メチルテトラヒドロフラニル-(例えば、5-メチルテトラヒドロフラン-2-イル-)を含む。
R2が、(任意に置換してもよい)-C1-4アルキルヘテロシクリルを表す場合;例には、-メチル-テトラヒドロフラニル(例えば、-メチル-テトラヒドロフラン-2-イル、-メチル-テトラヒドロフラン-3イル)、-エチル-テトラヒドロフラニル、-メチル-ピペリジニルを含む。
R2が、フェニルによって置換したフェニルを表し、ここで、上記のフェニル基のいずれも任意に置換してもよい場合、例には-ビフェニル-4-イルを含む。
R2が、ベンジルオキシによって置換したフェニルを表し、ここで上記フェニル基及びベンジルオキシ基のいずれも任意に置換してもよい場合、例には、4-ベンジルオキシ-フェニル-、4-(3-メチルベンジルオキシ)フェニル-、及び4-(4-メチルベンジルオキシ)フェニル-を含む。
R2が、任意に置換したヘテロシクリルに縮合した任意に置換したフェニルを表す場合、例には、ベンゾ[1,3]ジオキソ-4-イル-及び2,3-ジヒドロ-ベンゾ[1,4]ジオキシン-4-イル-を含む。
R2が、-C1-4アルキル(単環式ヘテロアリール基によって置換したフェニル)を表す場合、例には、4-(オキサゾール-5-イル)フェニル-メチル-を含む。
R2が、-C1-4アルキル(任意に置換したヘテロシクリルに縮合した任意に置換したフェニル)を表す場合;例には、ベンゾ[1,3]ジオキソ-4-イル-メチル-及び2,3-ジヒドロ-ベンゾ[1,4]ジオキシン-4-イル-メチル-を含む。
より適切には、R2は、アリール、ヘテロアリール、フェニルによって置換したフェニル、又はヘテロシクリルに縮合したフェニルを表し、上記アリール基、ヘテロアリール基、フェニル基、及びヘテロシクリル基は任意に置換されている。
一実施態様において、R2がフェニルによって置換したフェニルを表す場合、上記フェニル基は、例えば、同じでも異なってもよくかつハロ、OH、C1-3アルキル、C1-3ハロアルキル、C1-3アルコキシ、C1-3ハロアルコキシから選択される1個以上の置換基によって任意に置換される。R2が、フェニルによって置換したフェニルを表す場合、R2は適切には、-ビフェニル-4-イルを表す。
一実施態様において、R2は、任意に置換したヘテロシクリルに縮合した任意に置換したフェニルを表す。R2が、任意に置換したヘテロシクリルに縮合した任意に置換したフェニルを表す場合、R2は適切には、2,3-ジヒドロ-ベンゾ[1,4]ジオキシン-4-イル-を表す。
特に適切なR2基は、n-プロピルオキシによって置換したフェニル、特に4-n-プロポキシフェニルである。
R3が、任意に置換したアリールを表す場合、アリールは典型的には、フェニルを表し得る。典型的な置換フェニル基には、2,4-ジクロロフェニル-、2,4-ジフルオロロフェニル(difluororophenyl)-、2,4-ジメトキシフェニル-、2,4-ジメチルフェニル-、2,4-ビス(トリフルオロメチル)フェニル-、2,4,6-トリフルオロフェニル-、2,4,6-トリメチルフェニル-、2,6-ジクロロフェニル-、2,6-ジフルオロフェニル-、2,6-ジメトキシフェニル-、2-イソプロピル-6-メチルフェニル-、3-(シクロペンチルオキシ)-4-メトキシフェニル-、3,4,5-トリメトキシフェニル-、3,4-ジメトキシフェニル-、3,4-ジクロロフェニル-、3,4-ジメチルフェニル-、3,4,5-トリフルオロフェニル-、3,5-ビス(トリフルオロロメチル(trifluororophenyl))フェニル-、3,5-ジメトキシフェニル-、3-メトキシフェニル-、4-(トリフルオロメチル)フェニル-、4-ブロモ-2-(トリフルオロメチル)フェニル-、-4-ブロモフェニル-、4-クロロ-3-(トリフルオロメチル)フェニル-、4-クロロフェニル-、4-シアノフェニル-、4-エトキシフェニル-、4-エチルフェニル-、4-フルオロフェニル-、4-イソプロピルフェニル-、4-メトキシフェニル-を含む。或いは、R3は、非置換フェニル-を表してもよい。さらなる典型的な置換フェニル基には、2-ブロモ-4-フルオロフェニル-、2-ブロモ-5-フルオロフェニル-、2-クロロフェニル-、2-フルオロ-5-(トリフルオロメチル)フェニル-、2-ヒドロキシ-3-メトキシフェニル-、2-ヒドロキシ-5-メチルフェニル-、3-クロロフェニル-、3-フルオロ-4-(トリフルオロメチル)フェニル-、3-ヒドロキシ-4-メトキシフェニル-、4-クロロ-3-(トリフルオロメチル)フェニル-、4-クロロフェニル-、4-フルオロフェニル-、及び4-プロポキシフェニル-を含む。
R2及びR3が結合して、フェニルに縮合したカルボシクリル環を形成する場合;例には、インダニル(例えば、インダン-2-イル)及びテトラリニルを含む。
適切には、R3はHを表すか又は、R2及びR3は結合して、フェニルに縮合したカルボシクリル環を形成する。最も適切にはR3はHを表す。
R4が-C(O)C1-6アルキルを表す場合;例には、-C(O)メチル、-C(O)エチル、-C(O)プロピル、及び-C(O)ブチルなどの-C(O)C1-4アルキルを含む。
適切には、R4は、H、-C1-8アルキル、又は-C(O)C1-6アルキルを表す。より適切には、R4はH又は-C1-8アルキル、例えばH又はメチルを表す。最も適切には、R4はHを表す。
一実施態様において、YはOを表す。代替的な実施態様において、YはSを表す。
一実施態様において、XはOを表しかつYはSを表す。代替的な実施態様において、XはSを表しかつYはOを表す。適切には、X及びYは両方ともOを表す。
最も適切には、式(I)の化合物は下記式によって表される
1.5-(ベンゾ[c][1,2,5]チアジアゾール-6-イル)-1-(1H-ベンゾ[d]イミダゾール-5-イル)イミダゾリジン-2,4-ジオン
2.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-フェニルイミダゾリジン-2,4-ジオン
3.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-ヒドロキシ-5-メチルフェニル)イミダゾリジン-2,4-ジオン
4.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-フルオロ-5-トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン
5.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-ブロモ-5-フルオロフェニル)イミダゾリジン-2,4-ジオン
6.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオン
7.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロ-3-トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン
8.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-フルオロ-4-(トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン
9.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-ヒドロキシ-4-メトキシフェニル)イミダゾリジン-2,4-ジオン
10.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-ヒドロキシ-3-メトキシフェニル)イミダゾリジン-2,4-ジオン
11.1-(1H-ベンズイミダゾール-5-イル)-5-(1,1'-ビフェニル-4-イル)イミダゾリジン-2,4-ジオン
12.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-クロロフェニル)イミダゾリジン-2,4-ジオン
13.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロフェニル)イミダゾリジン-2,4-ジオン
14.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-クロロフェニル)イミダゾリジン-2,4-ジオン
15.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-フルオロフェニル)イミダゾリジン-2,4-ジオン
16.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3-ジヒドロベンゾ[b][1,4]ジオキシン-7-イル)イミダゾリジン-2,4-ジオン
17.1-(3-(1H-イミダゾール-1-イル)プロピル)-5-フェニルイミダゾリジン-2,4-ジオン
18.1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(2-ブロモ-4-フルオロフェニル)イミダゾリジン-2,4-ジオン
19. 1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオン
20.1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(3-フルオロ-4-(トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン
21. 1-[3-(1H-イミダゾール-1-イル)プロピル-5-(4-ビフェニル)イミダゾリジン-2,4-ジオン
22. 1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(3-クロロフェニル)イミダゾリジン-2,4-ジオン
23. 1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(2-クロロフェニル)イミダゾリジン-2,4-ジオン
24.1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)-5-フェニルイミダゾリジン-2,4-ジオン
25.5-(2-ブロモ-5-フルオロフェニル)-1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)イミダゾリジン-2,4-ジオン
26.1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオン
27.1-[3-(5-メチル-1H-イミダゾール-1-イル)プロピル]-5-(4-フェニルフェニル)イミダゾリジン-2,4-ジオン
28.5-(3-クロロフェニル)-1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)イミダゾリジン-2,4-ジオン
29.1-(3-(4-メチル-1H-イミダゾール-1-イル)プロピル)-5-フェニルイミダゾリジン-2,4-ジオン
30.1-[3-(4-メチル-1H-イミダゾール-1-イル)プロピル]-5-(4-ビフェニル)イミダゾリジン-2,4-ジオン
31.5-(3-クロロフェニル)-1-(3-(4-メチル-1H-イミダゾール-1-イル)プロピル)イミダゾリジン-2,4-ジオン
32. 3-(1H-ベンズイミダゾール-5-イル)-1',3'-ジヒドロ-2H,5H-スピロ[イミダゾリジン-4,2'-インデン]-2,5-ジオン
33.5-(ベンゾ[c][1,2,5]チアジアゾール-6-イル)-1-(1H-ベンゾ[d]イミダゾール-5-イル)-2-チオキソイミダゾリジン-4-オン
34.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-フェニル-2-チオキソイミダゾリジン-4-オン
35.1-(1H-ベンズイミダゾール-5-イル)-5-(1,1'-ビフェニル-4-イル)-2-チオキソイミダゾリジン-4-オン
36.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-ヒドロキシ-4-メトキシフェニル)-2-チオキソイミダゾリジン-4-オン
37.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-フェニル-4-チオキソイミダゾリジン-2-オン
38.1-(1H-ベンズイミダゾール-5-イル)-5-(1,1'-ビフェニル-4-イル)-4-チオキソイミダゾリジン-2-オン
39. 3-(1H-ベンズイミダゾール-5-イル)-5-チオキソ-1',3'-ジヒドロ-2H-スピロ[イミダゾリジン-4,2'-インデン]-2-オン
40. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロフェニル)-4-チオキソイミダゾリジン-2-オン
41. 1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3,4-トリフルオロフェニル)-4-チオキソイミダゾリジン-2-オン
42.1-(1H-ベンゾ[d]イミダゾール-6-イル)-5-(4-ブロモ-2-フルオロフェニル)-4-チオキソイミダゾリジン-2-オン
43.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3-ジフルオロ-4-メチルフェニル)-4-チオキソイミダゾリジン-2-オン
44.1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロ-3-メチルフェニル)-4-チオキソイミダゾリジン-2-オン
45.1-(1H-ベンゾ[d]イミダゾール-5-イル)-3-メチル-5-フェニルイミダゾリジン-2,4-ジオン
46. 1-(H-イミダゾ[1,2-a]ピリジン-7-イル)-5-フェニルイミダゾリジン-2,4-ジオン;
又はそのすべての互変異性体及び立体異性体を含むそれらの医薬として許容し得る塩、溶媒和物、若しくは多形体。
式(I)の化合物
XがSを表す場合、該転換は、(II)と硫化物イオン源、例えば硫化ナトリウムの反応を含む。該反応は、適切には高い温度で、適切にはマイクロ波条件下で実施される。該反応は典型的には、酸(例えば、塩酸)の存在下で極性プロトン性溶媒(例えば、メタノール)において実施される。
前記反応は適切には、酸触媒(例えば、塩酸ピリジニウム)の存在下で実施される。前記反応は典型的には、極性プロトン性溶媒(例えば、無水エタノール)において実施される。
該反応は、当業者に公知のイミン形成のための従来条件の下で実施してもよい。
該反応は典型的には、HCl:AcOH(1:40(v/v))の混合物において実施される。
J及びKが両方ともHを表す場合、該反応は典型的には、高い温度で実施される。
J及びKが両方とも脱離基を表す場合、該反応は典型的には、塩基(例えば、トリエチルアミン)の存在下で高い温度で実施される。
式(XV)の化合物は、式(VI)の化合物と式(VII)の化合物及びシアン化物源(例えば、トリメチルシリルシアニド)の反応によって製造してもよい。
式(IV)、(V)、(VI)、(VII)、(IX)、(X)、(XI)、(XII)、及び(XIV)の化合物は、公知でありかつ容易に入手可能であるか又は、それ自体知られている従来の方法によって製造してもよいかのいずれかである。
哺乳動物におけるQC(EC)の生理的基質は、例えば、アミロイドβ-ペプチド(3-40)、(3-42)、(11-40)及び(11-42)、ABri、ADan、ガストリン、ニューロテンシン、FPP、CCL2、CCL7、CCL8、CCL16、CCL18、フラクタルキン、オレキシンA、[Gln3]-グルカゴン(3-29)、[Gln5]-サブスタンスP(5-11)及びペプチドQYNADである。更なる詳細については、表1を参照されたい。本発明記載の化合物及び/又は組み合わせ並びに、少なくとも1種のQC(EC)阻害剤を含む医薬組成物は、QC活性の調節により治療することができる容態の治療に有用である。
3、11及び/又は22位にピログルタミン酸残基を伴うβ-アミロイドペプチドは、アミロイドβ-ペプチド1-40(42/43)よりも、より細胞傷害性があり、かつより疎水性であることが説明されている(Saido T.C.の文献(2000 Medical Hypotheses 54(3): 427-429))。
更にQYNADは、酵素グルタミニルシクラーゼ(QC, EC 2.3.2.5)の基質であり、これはまた哺乳動物の脳、特にヒト脳内にも存在する。グルタミニルシクラーゼは、pEYNADの前駆体QYNADからのpEYNADの形成を効果的に触媒する。
加えて、本発明のQC阻害剤の投与は、雄性不妊の抑制をもたらすことができる。
適切な実施態様において、本発明は、特にニューロン疾患、粥状硬化、及び多発性硬化症を治療するための、他の作用物質と併用する、QC(EC)活性の阻害剤の使用を提供する。
最も適切には、前記方法及び対応する使用は、治療的に活性のある量の少なくとも1種の式(I)の化合物を、哺乳動物、適切にはヒトに投与することを含む、軽度認知障害、アルツハイマー病、家族性英国型認知症、家族性デンマーク型認知症、ダウン症候群における神経変性、パーキンソン病、及びハンチントン舞踏病からなる群から選択される疾患の治療のためである。
特定の実施態様において、本発明は、少なくとも1種のQC阻害剤を、抗認知症薬、神経保護薬、抗パーキンソン病薬、アミロイドタンパク質沈着阻害薬、βアミロイド合成阻害薬、抗うつ薬、抗不安薬、抗精神病薬、及び抗多発性硬化症薬からなる群から選択される少なくとも1種の他の作用物質と任意に組み合わせて含む、組成物、適切には医薬組成物を提供する。
最も適切には、前記QC阻害剤は、本発明の式(I)の化合物である。
(a)ベンゾジアゼピン、例えば、アルプラゾラム、クロルジアゼポキシド、クロバザム、クロナゼパム、クロラゼプ酸、ジアゼパム、フルジアゼパム、ロフラゼプ酸、ロラゼパム、メタカロン、オキサゼパム、プラゼパム、トランゼン、
(b)選択的セロトニン再取り込み阻害剤(SSRI)、例えば、シタロプラム、フルオキセチン、フルボキサミン、エスシタロプラム、セルトラリン、パロキセチン、
(c)三環系抗うつ薬、例えば、アミトリプチリン、クロミプラミン、デシプラミン、ドキセピン、イミプラミン、
(d)モノアミンオキシダーゼ(MAO)阻害剤、
(e)アザピロン系薬、例えば、ブスピロン、タンドプシロン(tandopsirone)、
(f)セロトニン-ノルエピネフリン再取り込み阻害剤(SNRI)、例えば、ベンラファキシン、デュロキセチン、
(g)ミルタザピン、
(h)ノルエピネフリン再取り込み阻害剤(NRI)、例えば、レボキセチン、
(i)ブプロピオン、
(j)ネファゾドン、
(k)β-遮断薬、
(l)NPY-受容体リガンド:NPYアゴニスト又はアンタゴニスト。
a)ジヒドロオロト酸デヒドロゲナーゼ阻害剤、例えば、SC-12267、テリフルノミド、MNA-715、HMR-1279(HMR-1715、MNA-279と同義)、
b)自己免疫抑制薬、例えば、ラキニモド、
c)パクリタキセル、
d)抗体、例えば、AGT-1、抗顆粒球−マクロファージコロニー刺激因子(GM-CSF)モノクローナル抗体、Nogo受容体モジュレーター、ABT-874、アレムツズマブ(CAMPATH)、抗-OX40抗体、CNTO-1275、DN-1921、ナタリズマブ(AN-100226、Antegren、VLA-4 Mabと同義)、ダクリツマブ(Zenepax、Ro-34-7375、SMART抗-Tacと同義)、J-695、プリリキシマブ(Centara、CEN-000029、cM-T412と同義)、MRA、Dantes、抗-IL-12-抗体、
e)ペプチド核酸(PNA)調製物、例えば、レチキュロース(reticulose)、
f)インターフェロンα、例えば、アルファフェロン(Alfaferone)、ヒトαインターフェロン(Omniferon、Alpha Leukoferonと同義)、
g)インターフェロンβ、例えば、Frone、インターフェロンβ-1a様アボネックス(Avonex)、べトロン(Betron)(レビフ)、インターフェロンβアナログ、インターフェロンβ-トランスフェリン縮合タンパク質、組換えインターフェロンβ-1b様ベタセロン、
h)インターフェロンτ、
i)ペプチド、例えば、AT-008、AnergiX.MS、イムノカイン(Immunokine)(α-イムノカイン-NNSO3)、環状ペプチド様ZD-7349、
j)治療的酵素、例えば、可溶性CD8(sCD8)、
k)多発性硬化症特異的自己抗原をコードするプラスミド及びサイトカインをコードするプラスミド、例えば、BHT-3009;
l)TNF-αの阻害剤、例えば、BLX-1002、サリドマイド、SH-636、
m)TNFアンタゴニスト、例えば、ソリマスタット、レネルセプト(RO-45-2081、Tenefuseと同義)、オネルセプト(sTNFR1)、CC-1069、
n)TNFα、例えば、エタネルセプト(エンブレル、TNR-001と同義)、
o)CD28アンタゴニスト、例えば、アバタセプト、
p)Lckチロシンキナーゼ阻害剤、
q)カテプシンK阻害剤、
r)ニューロンを標的とする膜輸送体タンパク質タウリンのアナログ及び植物由来のカルパイン阻害剤ロイペプチン、例えば、Neurodur、
s)ケモカイン受容体-1(CCR1)アンタゴニスト、例えば、BX-471、
t)CCR2アンタゴニスト、
u)AMPA受容体アンタゴニスト、例えば、ER-167288-01及びER-099487、E-2007、タランパネル、
v)カリウムチャネル遮断薬、例えば、ファムプリジン、
w)VLA-4A/VCAM相互作用のトシル-プロリン-フェニルアラニン低分子アンタゴニスト、例えば、TBC-3342、
x)細胞接着分子阻害剤、例えば、TBC-772、
y)アンチセンスオリゴヌクレオチド、例えば、EN-101、
z)マスト細胞受容体に結合する遊離免疫グロブリン軽鎖(IgLC)のアンタゴニスト、例えば、F-991、
aa)アポトーシス誘導性抗原、例えば、Apogen MS、
bb)アドレナリンα-2受容体アゴニスト、例えば、チザニジン(ザナフレックス、テルネリン、Sirdalvo、シルダルード、Mionidineと同義)、
cc)L-チロシン、L-リシン、L-グルタミン酸及びL-アラニンのコポリマー、例えば、酢酸ガラティラメル(コパクソン、COP-1、コポリマー-1と同義)、
dd)トポイソメラーゼIIモジュレーター、例えば、塩酸ミトキサントロン、
ee)アデノシンデアミナーゼ阻害剤、例えば、クラドリビン(ロイスタチン、Mylinax、RWJ-26251と同義)、
ff)インターロイキン-10、例えば、イロデカキン(テノビル、Sch-52000、CSIFと同義)、
gg)インターロイキン-12アンタゴニスト、例えば、リソフィリン(CT-1501 R、LSF、リソフィリンと同義)、
hh)エタナミナム、例えば、SRI-62-834(CRC-8605、NSC-614383と同義)、
ii)免疫調節物質、例えば、SAIK-MS、PNU-156804、α-フェトプロテインペプチド(AFP)、IPDS、
jj)レチノイド受容体アゴニスト、例えば、アダパレン(ディフェリン、CD-271と同義)、
kk)TGF-β、例えば、GDF-1(増殖及び分化因子1)、
ll)TGF-β-2、例えば、ベタカイン、
mm)MMP阻害剤、例えば、グリコメド(glycomed)、
nn)ホスホジエステラーゼ4(PDE4)阻害剤、例えば、RPR-122818、
oo)プリンヌクレオシドホスホリラーゼ阻害剤、例えば、9-(3-ピリジルメチル)-9-デアザグアニン、ペルデシン(BCX-34、TO-200と同義)、
pp)α-4/β-1インテグリンアンタゴニスト、例えば、ISIS-104278、
qq)アンチセンスα4インテグリン(CD49d)、例えば、ISIS-17044、ISIS-27104、
rr)サイトカイン-誘導性物質、例えば、ヌクレオシド、ICN-17261、
ss)サイトカイン阻害剤、
tt)熱ショックタンパク質ワクチン、例えば、HSPPC-96、
uu)ニューレグリン増殖因子、例えば、GGF-2(ニューレグリン、グリア増殖因子2と同義)、
vv)カテプシンS-阻害剤、
ww)ブロピリミンアナログ、例えば、PNU-56169、PNU-63693、
xx)単球走化性タンパク質-1阻害剤、例えば、ベンズイミダゾール様MCP-1阻害剤、LKS-1456、PD-064036、PD-064126、PD-084486、PD-172084、PD-172386。
これらの組み合わせは、特に有益な効果を提供する。それゆえ、このような組み合わせは、上記の疾患の治療に有効かつ有用であることが示されている。従って、本発明は、これらの容態を治療する方法を提供する。
同時投与には、少なくとも1種のQC阻害剤と少なくとも1種の他の作用物質とを含む製剤の投与、又は各作用物質の個別の製剤の本質的に同時の投与を含む。
(i)WO 1999/61431に開示されたジペプチド-様化合物、例えば、N-バリルプロリル、O-ベンゾイルヒドロキシルアミン、アラニルピロリジン、イソロイシルチアゾリジン様L-アロ-イソロイシルチアゾリジン、L-トレオ-イソロイシルピロリジン及びそれらの塩、特にフマル酸塩、並びにL-アロ-イソロイシルピロリジン及びそれらの塩;
(ii)WO 2003/002593に開示されたペプチド構造、例えばトリペプチド;
(iii)WO 2003/033524に開示されたペプチジルケトン;
(vi)WO 2003/040174に開示された置換アミノケトン;
(v)WO 2001/14318に開示された局所的活性DP IV-阻害剤;
(vi)WO 1999/67278及びWO 1999/67279に開示されたDP IV-阻害剤プロドラッグ;並びに
(v)WO 2003/072556及びWO 2004/099134に開示されたグルタミニルベースのDP IV-阻害剤。
本発明の特に適切な化合物は、NPY受容体のアンタゴニストである。
適切なNPY受容体のリガンド又はアンタゴニストは、WO 2000/68197に開示されたような、3a, 4,5,9b-テトラヒドロ-1h-ベンズ[e]インドール-2-イルアミン由来の化合物である。
本発明の目的に適したM1受容体アンタゴニストは、例えば、CDD-0102(Cognitive Pharmaceuticals社);セビメリン(Evoxac)(雪印乳業);NGX-267(TorreyPines Therapeutics社);サブコメリン(グラクソスミスクライン社);アルバメリン(H Lundbeck社);LY-593093(イーライリリー社);VRTX-3(Vertex Pharmaceuticals社);WAY-132983(ワイス社)、及びCI-1017/(PD-151832)(ファイザー社)である。
好ましいAT1-受容体アンタゴニストは、認可されかつ市販されている該アンタゴニストの作用物質であり、最も好ましいのは、バルサルタン又はその医薬として許容し得る塩である。
本発明の組み合わせにおいて使用される適切なACE阻害薬は、例えばアラセプリル、ベナゼプリル、ベナゼプリラット;カプトプリル、セロナプリル、シラザプリル、デラプリル、エナラプリル、エナプリラット、フォシノプリル、イミダプリル、リシノプリル、モベルトプリル、ペリンドプリル、キナプリル、ラミプリル、スピラプリル、テモカプリル及びトランドラプリルからなる群から選択された化合物又は、いずれの場合においても、それらの医薬として許容し得る塩である。
好ましいACE阻害薬は、市販されているそのような薬物であり、最も好ましいのは、ベナゼプリル及びエナラプリルである。
前述の組み合わせにおいて有用なCCBは、適切には、アムロジピン、フェロジピン、リオシジン、イスラジピン、ラシジピン、ニカルジピン、ニフェジピン、ニグルジピン、ニルジピン、ニモジピン、ニソルジピン、ニトレンジピン及びニバルジピンからなる群から選択される代表的DHPであり、並びに適切には、フルナリジン、プレニラミン、ジルチアゼム、フェンジリン、ガロパミル、ミベフラジル、アニパミル、チアパミル及びベラパミルからなる群から選択される代表的非DHPであり、いずれの場合においても、それらの医薬として許容し得る塩を含む。これらのCCB類は全て、例えば抗高血圧薬、抗狭心症薬又は抗不整脈薬として、治療的に使われる。
コレステロール吸収モジュレーターは、ZETIA(登録商標)(エゼチミブ)、及びKT6-971(Kotobuki Pharmaceutical社、日本)を含む。
好ましいHMG-CoAレダクターゼ阻害薬は、市販されている該阻害薬の薬剤であり、最も好ましいのは、アトルバスタチン、ピバスタチン又はシンバスタチン又はそれらの医薬として許容し得る塩である。
適切な抗増殖薬は、クラドリビン、ラパマイシン、ビンクリスチン及びタキソールである。
適切な細胞外マトリックス合成阻害薬は、ハロフギノンである。
適切なチロシンキナーゼ阻害薬は、チルホスチンである。
適切なレニン阻害薬は、例えばWO 2006/116435に開示されている。好ましいレニン阻害薬は、アリスキレン、適切にはそのヘミフマル酸塩の形である。
QC阻害剤とMCP-1アンタゴニストとの組み合わせは、アルツハイマー病の治療に好ましい。
PF-4360365、m266、バピネオズマブ、R-1450、Posiphen、(+)-フェンセリン、MK-0752、LY-450139、E-2012、(R)-フルルビプロフェン、AZD-103、AAB-001(バピネオズマブ)、トラミプロセート、EGb-761、TAK-070、ドキソフィリン、テオフィリン、シロミラスト、トフィミラスト、ロフルミラスト、テトミラスト、チペルカスト、イブジラスト、HT-0712、MEM-1414、オグレミラスト、リネゾリド、ブジピン、イソカルボキサジド、フェネルジン、トラニルシプロミン、インダンタドール、モクロベミド、ラサジリン、ラドスチギル、サフィナミド、ABT-239、ABT-834、GSK-189254A、シプロキシファン、JNJ-17216498、Fmoc-Ala-Pyrr-CN、Z-Phe-Pro-ベンゾチアゾール、Z-321、ONO-1603、JTP-4819、S-17092、BIBP3226;(R)-N2-(ジフェニルアセチル)-(R)-N-[1-(4-ヒドロキシフェニル)エチル]アルギニンアミド、セビメリン、サブコメリン、(PD-151832)、ドネペジル、リバスチグミン、(-)-フェンセリン、ラドスチギル、ガランタミン、タクリン、メトリホナート、メマンチン、トピラマート、AVP-923、EN-3231、ネラメキサン、バルサルタン、ベナゼプリル、エナラプリル、ヒドロクロロチアジド、アムロジピン、ジルチアゼム、イスラジピン、ニカルジピン、ニフェジピン、ニモジピン、ニソルジピン、ニトレンジピン、ベラパミル、アムロジピン、アセブトロール、アテノロール、ベタキソロール、ビソプロロール、カルテオロール、カルベジロール、エスモロール、ラベタロール、メトプロロール、ナドロール、オクスプレノロール、ペンブトロール、ピンドロール、プロプラノロール、ソタロール、チモロール、PLAVIX(登録商標)(クロピドグレル重硫酸塩)、PLETAL(登録商標)(シロスタゾール)、アスピリン、ZETIA(登録商標)(エゼチミブ)及びKT6-971、スタチン、アトルバスタチン、ピタバスタチン又はシムバスタチン;デキサメタゾン、クラドリビン、ラパマイシン、ビンクリスチン、タキソール、アリスキレン、C-243、ABN-912、SSR-150106、MLN-1202及びベタフェロン。
−粥状硬化の治療及び/又は予防のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、アトルバスタチンとの組み合わせ
−再狭窄の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、免疫抑制薬、適切にはラパマイシンとの組み合わせ
−再狭窄の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、免疫抑制薬、適切にはパクリタキセルとの組み合わせ
−アルツハイマー病の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、AChE阻害剤、適切にはドネペジルとの組み合わせ
−多発性硬化症の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、インターフェロン、適切にはアロネックス(Aronex)との組み合わせ
−多発性硬化症の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、インターフェロン、適切にはベタフェロンとの組み合わせ
−多発性硬化症の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、インターフェロン、適切にはレビフとの組み合わせ
−多発性硬化症の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、コパクソンとの組み合わせ
−再狭窄の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、デキサメタゾンとの組み合わせ
−粥状硬化の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、デキサメタゾンとの組み合わせ
−関節リウマチの予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、デキサメタゾンとの組み合わせ
−再狭窄の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、HMG-CoA-レダクターゼ阻害薬との組み合わせ、ここでHMG-CoA-レダクターゼ阻害薬は、アトルバスタチン、セリバスタチン、フラバスタチン、ロバスタチン、ピタバスタチン、プラバスタチン、ロスバスタチン及びシンバスタチンから選択される
−粥状硬化の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、HMG-CoA-レダクターゼ阻害薬との組み合わせ、ここでHMG-CoA-レダクターゼ阻害薬は、アトルバスタチン、セリバスタチン、フラバスタチン、ロバスタチン、ピタバスタチン、プラバスタチン、ロスバスタチン及びシンバスタチンから選択される
−関節リウマチの予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、HMG-CoA-レダクターゼ阻害薬との組み合わせ、ここでHMG-CoA-レダクターゼ阻害薬は、アトルバスタチン、セリバスタチン、フラバスタチン、ロバスタチン、ピタバスタチン、プラバスタチン、ロスバスタチン及びシンバスタチンから選択される
−軽度認知障害の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、アミロイド-β抗体との組み合わせ、ここでアミロイド-β抗体はAcl-24である
−アルツハイマー病の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、アミロイド-β抗体の組み合わせ、ここでアミロイド-β抗体はAcl-24である
−ダウン症候群における神経変性の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、アミロイド-β抗体との組み合わせ、ここでアミロイド-β抗体はAcl-24である
−軽度認知障害の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、βセクレターゼ阻害剤との組み合わせ、ここでβセクレターゼ阻害剤は、WY-25105、GW-840736X及びCTS-21166から選択される
−アルツハイマー病の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、βセクレターゼ阻害剤との組み合わせ、ここでβセクレターゼ阻害剤は、WY-25105、GW-840736X及びCTS-21166から選択される
−ダウン症候群における神経変性の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、βセクレターゼ阻害剤との組み合わせ、ここでβセクレターゼ阻害剤は、WY-25105、GW-840736X及びCTS-21166から選択される
−軽度認知障害の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、γ-セクレターゼ阻害剤との組み合わせ、ここでγ-セクレターゼ阻害剤は、LY-450139、LY-411575及びAN-37124から選択される
−アルツハイマー病の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、γ-セクレターゼ阻害剤との組み合わせ、ここでγ-セクレターゼ阻害剤は、LY-450139、LY-411575及びAN-37124から選択される
−ダウン症候群における神経変性の予防及び/又は治療のための、QC阻害剤、適切には、式(I)のQC阻害剤、より適切には、実施例1〜46のいずれかより選択される阻害剤と、γ-セクレターゼ阻害剤との組み合わせ、ここでγ-セクレターゼ阻害剤は、LY-450139、LY-411575及びAN-37124から選択される。
QC阻害剤と更なる化合物との具体的な組み合わせに関して、この点について、特に、引用により本明細書中に組み込まれているWO 2004/098625が引用される。
本発明の医薬組成物を製造するために、式(I)の少なくとも1種の化合物を、少なくとも1種のその他の上記の薬剤と任意に組み合わせて、活性成分(類)として使用することができる。この活性成分(類)は、従来の医薬配合技術に従い、医薬担体と密に混合され、該担体は、例えば経口投与又は筋肉内投与などの非経口投与に望ましい製造物の形に応じ多種多様な形をとることができる。経口剤形での組成物の製造において、通常の医薬媒体のいずれかを使用してよい。従って、例えば懸濁剤、エリキシル剤及び液剤などの液体経口製造物に関して、適切な担体及び添加物は、水、グリコール、油類、アルコール、調味料、保存料、着色料などを含み;例えば散剤、カプセル剤、ゲルキャップ剤、及び錠剤などの固形経口製造物に関しては、適切な担体及び添加物には、デンプン、糖類、希釈剤、造粒剤、潤滑剤、結合剤、崩壊剤などを含む。錠剤及びカプセル剤が、それらの投与の容易さのために、最も有利な経口単位剤形であり、この場合固形医薬担体が明らかに使用される。所望の場合、錠剤は、標準の技術により、糖衣されるか、又は腸溶性にコーティングされてよい。非経口製造物に関しては、該担体は通常、滅菌水を含むが、例えば溶解を補助するか又は保存のためなどの目的のために、他の成分を含んでよい。
本組成物は好ましくは、関連する1日用量に適した量の単位剤形である。
方法1(実施例1〜32):
その後、TFA(10%(v/v))の水溶液を、0.01モルの出発材料の場合150mL添加し、混合物を50〜60℃で一晩撹拌した。その後、EtOH及びTFAを蒸発させ、残余の水溶液を半分取HPLCに供した。
生成物の遊離塩基を水に懸濁し、1当量のNaOH(水溶液)を添加した。溶液を凍結させ、凍結乾燥に供した。
エチレングリコール(0.01モルの出発材料の場合25mL)を添加し、溶液を0〜5℃に冷却した後、対応するイソニトリル(1当量)、KSCN(1当量)、及び塩化プリリジニウム(pryridinium-chloride)(1当量)を添加した。混合物を0〜5℃で2.5時間、次に室温で一晩撹拌した。
その後、TFA(10%(v/v))の水溶液を、0.01molの出発材料の場合150mL添加し、混合物を50〜60℃で一晩撹拌した。その後、EtOH及びTFAを蒸発させ、残余の水溶液を分取HPLCに供した。
1当量の対応する4-メチルイミノ-イムダゾルジン-2-オンを1.25MのHCl含有メタノール(無水、0.25mmolの出発材料につき1mL)に溶解し、1当量の1.5当量の硫化ナトリウム含有溶液を密封したマイクロ波容器に加える。反応混合物をマイクロ波において140℃で20分間加熱する。
溶媒の蒸発後、粗反応生成物をH2O/EtOAcで抽出する。有機相をNa2SO4で乾燥させ、濾過し、除去する。結果として生じる反応生成物を半分取HPLCによって精製する。
尿素又はチオ尿素をHCl:AcOH(1:40(v/v))の混合物に溶解し、対応するグリオキサルを添加した。グリオキサルの量は、1当量の尿素の量に対応していた。混合物を還流下で4時間維持した。その後、溶媒を除去し、結果として生じる生成物を分取HPLCによって精製した。
その後、混合物を氷/アンモニア(4mmolの出発材料の場合、12mLの25%NH3溶液を含む。)に注いだ。水性層をCH2Cl2によって3回抽出し、有機相を組み合わせ、乾燥させ、濾過し、溶媒を除去した。残余物を濃HClに再度溶解し、40℃で一晩維持した。水を添加し、NaOHを添加することによって溶液を中和した。水性相をCH2Cl2によって3回抽出した後、有機層を組み合わせて乾燥させた。溶媒を除去し、残余の油を下記の代替法のうちの1つに供した:
a)生成物を無水CHCl3に取り、EtO(CO)Cl及びトリエチルアミンを添加した。混合物を還流下で12時間維持した。その後、溶媒を除去し、残余の油を無水EtOHに溶解し、NaOEtを添加した。還流下で溶液を10時間維持した;又は
b)生成物をトルエンに溶解し、カルボニルジイミダゾール及びトリエチルアミンを添加した。溶液を還流下で18時間維持した;又は
c)生成物をホルムアミドに取り、200℃で2時間維持した。
本システムは、Luna(登録商標)100-7 C18半分取用カラム(Phenomenex.長さ:250mm、直径:21mm)を装備したMerck-Hitachi社の装置(モデルLaChrom)から構成された。本化合物は、勾配を用いて流速6mL/分で精製し;これにより、溶離剤(A)はアセトニトリルであり、溶離剤(B)は水であり、両方とも0.1%(v/v)トリフルオロ酢酸を含有し、下記勾配を適用した:0分〜40分。40〜95%の(A)。
(実施例1:5-(ベンゾ[c][1,2,5]チアジアゾール-6-イル)-1-(1H-ベンゾ[d]イミダゾール-5-イル)イミダゾリジン-2,4-ジオン)
方法1において説明したとおり、5-アミノベンズイミダゾール5.32g(40mmol)、ベンゾ[c][1,2,5]チアジアゾール-6-イル-カルボアルデヒド6.56g(40mmol)、n-ブチルイソニトリル4.24mL(40mmol)、及びKOCN 3.28g(40mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール1.331g(10mmol)、ベンズアルデヒド1.02mL(10mmol)、ベンジルイソニトリル1.22mL(10mmol)、及びKOCN 0.84g(10mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.4g(3.0mmol)、2-ヒドロキシ-5-メチルフェニルカルボアルデヒド0.409g(3.0mmol)、n-ブチルイソニトリル0.316mL(3.0mmol)、及びKOCN 0.244g(0.2mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.213g(1.6mmol)、2-フルオロ-5-(トリフルオロメチル)フェニルカルボアルデヒド0.362mL(1.6mmol)、n-ブチルイソニトリル0.169mL(1.6mmol)、塩化ピリジニウム0.185g(1.6mmol)、及びKOCN 0.13g(1.6mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.213g(1.6mmol)、2-ブロモ-5-フルオロフェニルカルボアルデヒド0.325(1.6mmol)、n-ブチルイソニトリル0.169mL(1.6mmol)、塩化ピリジニウム0.185g(1.6mmol)、及びKOCN 0.13g(1.6mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.213g(1.6mmol)、4-プロポキシフェニルカルボアルデヒド0.253mL(1.6mmol)、n-ブチルイソニトリル0.169mL(1.6mmol)、塩化ピリジニウム0.185g(1.6mmol)、及びKOCN 0.13g(1.6mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.213g(1.6mmol)、4-クロロ-3-(トリフルオロメチル)フェニルカルボアルデヒド0.23mL(1.6mmol)、n-ブチルイソニトリル0.169mL(1.6mmol)、塩化ピリジニウム0.185g(1.6mmol)、及びKOCN 0.13g(1.6mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.133g(1mmol)、3-フルオロ-4-(トリフルオロメチル)フェニルカルボアルデヒド0.192g(1mmol)、n-ブチルイソニトリル0.083g(1mmol)、塩化ピリジニウム0.185g(1.6mmol)、及びKOCN 0.081g(1mmol)から出発して、本化合物を合成した。
収量:0.151g(40%);MS m/z 379.2 (M+H)+
方法1において説明したとおり、5-アミノベンズイミダゾール0.213g(1.6mmol)、3-ヒドロキシ-4-メトキシフェニルカルボアルデヒド0.244g(1.6mmol)、n-ブチルイソニトリルn-ブチルイソニトリル0.169mL(1.6mmol)、塩化ピリジニウム0.185g(1.6mmol)、及びKOCN 0.13g(1.6mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.133g(1mmol)、2-ヒドロキシ-3-メトキシフェニルカルボアルデヒド0.153g(1mmol)、n-ブチルイソニトリル0.106mL(1mmol)、及びKOCN 0.082g(1mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.133g(1mmol)、1,1'-ビフェニル-4-イルカルボアルデヒド0.183(1mmol)、n-ブチルイソニトリルn-ブチルイソニトリル0.106mL(1mmol)、及びKOCN 0.082g(1mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール2.13g(16mmol)、3-クロロベンズアルデヒド2.24g(16mmol)、n-ブチルイソニトリル1.69mL(16mmol)、KOCN 1.3g(16mmol)、及び塩化ピリジニウム1.85g(16mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.213g(1.6mmol)、4-クロロベンズアルデヒド0.224g(1.6mmol)、n-ブチルイソニトリル0.169mL(1.6mmol)、塩化ピリジニウム0.185g(1.6mmol)、及びKOCN 0.130g(1.6mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.213g(1.6mmol)、2-クロロベンズアルデヒド0.225mg(1.6mmol)、n-ブチルイソニトリル0.169mL(1.6mmol)、塩化ピリジニウム0.185g(1.6mmol)、及びKOCN 0.130g(1.6mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.134g(1mmol)、4-フルオロベンズアルデヒド0.125g(1mmol)、n-ブチルイソニトリル0.106mL(1mmol)、塩化ピリジニウム0.116g(1mmol)、及びKOCN 0.082g(1mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.134g(1mmol)、2,3-ジヒドロベンゾ[b][1,4]ジオキシン-7-イルカルボアルデヒド0.165g(1mmol)、n-ブチルイソニトリル0.106mL(1mmol)、塩化ピリジニウム0.116g(1mmol)、及びKOCN 0.082g(1mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(1H-イミダゾール-1-イル)プロピルアミン1.0g(7.98mmol)、ベンズアルデヒド0.807mL(7.98mmol)、ベンジルイソニトリル0.972mL(7.98mmol)、塩化ピリジニウム0.920、及びKOCN 0.648g(7.98mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(1H-イミダゾール-1-イル)プロピルアミン0.358mL(3mmol)、2-ブロモ4-フルオロベンズアルデヒド0.610g(3mmol)、ベンジルイソニトリル0.365mL(3mmol)、塩化ピリジニウム0.347g(3mmol)、及びKOCN 0.243g(3mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(1H-イミダゾール-1-イル)プロピルアミン0.358mL(3mmol)、4-プロポキシフェニルカルボアルデヒド0.492g(3mmol)、n-ブチルイソニトリル0.315mL(3mmol)、塩化ピリジニウム0.347g(3mmol)、及びKOCN 0.243g(3mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(1H-イミダゾール-1-イル)プロピルアミン0.358mL(3mmol)、3-フルオロ-4-(トリフルオロメチル)フェニルカルボアルデヒド0.576g(3mmol)、n-ブチルイソニトリル0.315mL(3mmol)、塩化ピリジニウム0.347g(3mmol)、及びKOCN 0.243g(3mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(1H-イミダゾール-1-イル)プロピルアミン0.358mL(3mmol)、4-フェニルベンズアルデヒド0.546g(3mmol)、n-ブチルイソニトリル0.315mL(3mmol)、塩化ピリジニウム0.347g(3mmol)、及びKOCN 0.243g(3mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(1H-イミダゾール-1-イル)プロピルアミン0.358mL(3mmol)、3-クロロフェニルカルボアルデヒド0.42g(3mmol)、n-ブチルイソニトリル0.315mL(3mmol)、塩化ピリジニウム0.347g(3mmol)、及びKOCN 0.243g(3mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(1H-イミダゾール-1-イ(y))プロピルアミン0.358mL(3mmol)、2-クロロベンズアルデヒド0.420g(3mmol)、n-ブチルイソニトリル0.315mL(3mmol)塩化ピリジニウム0.347g(3mmol)、及びKOCN 0.243g(3mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)アミン0.278g(2mmol)、ベンズアルデヒド0.202mL(2mmol)、ベンジルイソニトリル0.245mL(2mmol)塩化ピリジニウム0.231g(2mmol)、及びKOCN 0.165g(2mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)アミン0.278g(2mmol)、2-ブロモ-5-フルオロフェニルカルボアルデヒド0.406g(2mmol)、ベンジルイソニトリル0.245mL(2mmol)塩化ピリジニウム0.231g(2mmol)、及びKOCN 0.165g(2mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)アミン0.278g(2mmol)、4-プロポキシフェニルカルボアルデヒド0.316mL(2mmol)、ベンジルイソニトリル0.245mL(2mmol)、塩化ピリジニウム0.231g(2mmol)、及びKOCN 0.165g(2mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)アミン0.278g(2mmol)、4-フェニルベンズアルデヒド0.364g(2mmol)、ベンジルイソニトリル0.245mL(2mmol)塩化ピリジニウム0.231g(2mmol)、及びKOCN 0.165g(2mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)アミン0.278g(2mmol)、3-クロロフェニルカルボアルデヒド0.226mL(2mmol)、ベンジルイソニトリル0.245mL(2mmol)塩化ピリジニウム0.231g(2mmol)、及びKOCN 0.165g(2mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(4-メチル-1H-イミダゾール-1-イル)プロピルアミン0.250g(1.8mmol)、ベンズアルデヒド0.182mL(1.8mmol)、ベンジルイソニトリル0.220mL(1.8mmol)塩化ピリジニウム0.210g(1.8mmol)、及びKOCN 0.150g(1.8mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(4-メチル-1H-イミダゾール-1-イル)プロピルアミン0.250g(1.8mmol)、4-フェニル-ベンズアルデヒド0.220g(1.8mmol)、ベンジルイソニトリル0.220mL(1.8mmol)、塩化ピリジニウム0.210g(1.8mmol)、及びKOCN 0.150g(1.8mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、3-(4-メチル-1H-イミダゾール-1-イル)プロピルアミン0.250g(1.8mmol)、3-クロロフェニルカルボアルデヒド0.204mL(1.8mmol)、ベンジルイソニトリル0.220mL(1.8mmol)塩化ピリジニウム0.210g(1.8mmol)、及びKOCN 0.150g(1.8mmol)から出発して、本化合物を合成した。
方法1において説明したとおり、5-アミノベンズイミダゾール0.4g(3mmol)、インダン-2-オン0.4g(3mmol)、n-ブチルイソニトリル0.316mL(3mmol)、塩化ピリジニウム0.347g(3mmol)、及びKOCN 0.244g(3mmol)から出発して、本化合物を合成した。
方法2において説明したとおり、5-アミノベンズイミダゾール0.013g(0.1mmol)、ベンゾ[c][1,2,5]チアジアゾール-6-イルカルボアルデヒド0.016g(0.1mmol)、n-ブチルイソニトリル0.010mL(0.1mmol)、塩化ピリジニウム0.012g(0.1mmol)、及びKSCN 0.01g(0.1mmol)から出発して、本化合物を合成した。
収量:0.0045g(12%);MS m/z 367.2 (M+H)+;HPLC(λ=220nm, [B]):室温1.91分(94%)。
方法2において説明したとおり、5-アミノベンズイミダゾール0.013g(0.1mmol)ベンズアルデヒド0.01mL(0.1mmol)、n-ブチルイソニトリル0.010mL(0.1mmol)、塩化ピリジニウム0.012g(0.1mmol)、及びKSCN 0.01g(0.1mmol)から出発して、本化合物を合成した。
収量:0.0069g(22%);MS m/z 309.3 (M+H)+;HPLC(λ=220nm, [B]):室温1.52分(96%)
方法2において説明したとおり、5-アミノベンズイミダゾール0.013g(0.1mmol)、4-フェニルベンズアルデヒド0.018g(0.1mmol)、n-ブチルイソニトリル0.010mL(0.1mmol)、塩化ピリジニウム0.012g(0.1mmol)、及びKSCN 0.01g(0.1mmol)から出発して、本化合物を合成した。
収量:0.00346g(8.9%);MS m/z 385.5 (M+H)+;HPLC(λ=220nm, [B]):室温2.93分(96%)。
方法2において説明したとおり、5-アミノベンズイミダゾール0.013g(0.1mmol)、3-ヒドロキシ-4-メトキシフェニルカルボアルデヒド0.015g(0.1mmol)、n-ブチルイソニトリル0.010mL(0.1mmol)、塩化ピリジニウム0.012g(0.1mmol)、及びKSCN 0.01g(0.1mmol)から出発して、本化合物を合成した。
収量:0.00162g(3.5%);MS m/z 355.3 (M+H)+;HPLC(λ=220nm, [B]):室温0.81分(92%)。
方法3において説明したとおり、1-(1H-ベンゾ[d]イミダゾール-5-イル)-4-(メチルイミノ)-5-フェニルイミダゾリジン-2-オン0.076g(0.25mmol)、及びNa2S 0.029g(0.375mmol)から出発して、本化合物を合成した。
収量:0.0092g(12%);MS m/z 309.5 (M+H)+;HPLC(λ=220nm, [B]):室温2.61分(64%)。
方法3において説明したとおり、1-(1H-ベンゾ[d]イミダゾール-5-イル)-4-(メチルイミノ)-5-(1,1'-ビフェニル-4-イル)イミダゾリジン-2-オン0.095g(0.25mmol)Na2S 0.029g(0.375mmol)から出発して、本化合物を合成した。
収量:0.00036g(0.37%);MS m/z 385.4 (M+H)+;HPLC(λ=220nm, [B]):室温3.02分(97%)。
方法3において説明したとおり、3-(1H-ベンズイミダゾール-5-イル)-4-(メチルイミノ)-1',3'-ジヒドロ-2H-スピロ[イミダゾリジン-4,2'-インデン]-2-オン0.082g(0.25mmol)及びNa2S 0.029g(0.375mmol)から出発して、本化合物を合成した。
収量:0.0016g(1.9%);MS m/z 335.2 (M+H)+;HPLC(λ=220nm, [D]):室温2.81分(84%)。
方法3において説明したとおり、1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロフェニル)-4-(メチルイミノ)イミダゾリジン-2-オン0.084g(0.25mmol)及びNa2S 0.029g(0.375mmol)から出発して、本化合物を合成した。
収量:0.00088g(1.0%);MS m/z 343.8 (M+H)+;HPLC(λ=220nm, [D]);室温2.73分(99%)。
方法3において説明したとおり、1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3,4-トリフルオロフェニル)-4-(メチルイミノ)イミダゾリジン-2-オン0.090g(0.25mmol)及びNa2S 0.029g(0.375mmol)から出発して、本化合物を合成した。
収量:0.00613g(6.7%);MS m/z 363.2 (M+H)+;HPLC(λ=220nm, [D]):室温2.02分(97%)。
方法3において説明したとおり、1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-ブロモ-2-フルオロフェニル)-4-(メチルイミノ)イミダゾリジン-2-オン0.100g(0.25mmol)及びNa2S 0.029g(0.375mmol)から出発して、本化合物を合成した。
収量:0.00071g(0.6%);MS m/z 406.2 (M+H)+;HPLC(λ=220nm, [D]):室温2.94分(90%)。
方法3において説明したとおり、1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3-ジフルオロ-4-メチルフェニル)-4-(メチルイミノ)イミダゾリジン-2-オン0.088g(0.25mmol)及びNa2S 0.029g(0.375mmol)から出発して、本化合物を合成した。
収量:0.0055g(6.1%);MS m/z 359.2 (M+H)+;HPLC(λ=220nm, [D]):室温3.12分(97%)。
方法3において説明したとおり、1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロ-3-メチルフェニル)-4-(メチルイミノ)イミダゾリジン-2-オン0.088g(0.25mmol)及びNa2S 0.029g(0.375mmol)から出発して、本化合物を合成した。
収量:0.00221g(2.4%);MS m/z 357.2 (M+H)+;HPLC(λ=220nm, [D]):室温3.21分(80%)。
方法4に従って、5-アミノベンズイミダゾール0.266g(2mmol)、ジ-(1H-イミダゾール-1-イル)メタノン0.324g(2mmol)、塩酸メチルアミン0.135g(2mmol)TEA 0.255mL(2mmol)、及びフェニルグリオキサル水和物0.102g(0.67mmol)から出発して、本化合物を合成した。
方法4に従って、1-(H-イミダゾ[1,2-a]ピリジン-7-イル)尿素0.03g(0.170mmol)及びフェニルグリオキサル水和物0.028g(0.20mmol)から出発して、本化合物を合成した。
HPLC:
方法[A]:分析的HPLCシステムは、LUNA(登録商標)100 RP 18(5μm)、分析カラム(長さ:125mm、直径:4mm)、及び記録波長としてλ=214nmを有するダイオードアレイ検出器(DAD)を利用する、メルク-日立装置(モデルLaChrom(登録商標))から構成された。本化合物は、流速1mL/分の勾配を用いて分析し;これにより、溶離剤(A)はアセトニトリルであり、溶離剤(B)は水であり、両方とも0.1%(v/v)トリフルオロ酢酸を含有し、下記の勾配を適用した:方法[A]:0分〜5分→5%の(A)、5分〜17分→5〜15%の(A)、15分〜27分→15〜95%の(A)、27分〜30分→95%の(A)、方法[B]:0分〜15分→5〜60%の(A)、15分〜20分→60〜95%の(A)、20分〜23分→95%の(A)、方法[C]:0分〜20分→5〜60%の(A)、20分〜25分→60〜95%の(A)。25分〜30分→95%の(A)。
ESI-質量スペクトルは、SCIEX API 365分光器(Perkin Elmer社)で、正イオン化モードを利用して得た。
1H NMR-スペクトル(500MHz)をBRUKER AC 500で記録した。溶媒は、特に明記しない限り、DNSO-D6とした。化学シフトは、テトラメチルシランからの低周波側での百万分率(ppm)で表す。分裂パターンを次のように示した:s (一重線)、 d(二重線)、 dd(二重の二重線)、t(三重線)、m(多重線)及びbr (広範のシグナル)。
マトリックス支援レーザー脱離/イオン化質量分析を、線形時間の飛行解析装置を備えたHewlett-Packard社G2025 LD-TOFシステムを用いて行った。この装置は、337nm窒素レーザー、電位加速源(5kV)及び1.0m飛行管を装備した。検出器の操作は、正イオンモードであり、シグナルは、パーソナルコンピュータに接続されたLeCroy 9350Mデジタルストレージオシロスコープを用い、記録し、かつフィルタリングする。試料(5μl)は、等容積のマトリックス溶液と混合した。マトリックス溶液に関して、水を溶媒とする1mlアセトニトリル:0.1%TFA(1:1(v/v))中に、2',6'-ジヒドロキシアセトフェノン(Aldrich社)30mg及びクエン酸水素ジアンモニウム(Fluka社)44mgを溶解することにより製造した、DHAP/DAHCを使用した。少量(ほぼ1μl)のマトリックス被検体-混合物を、プローブチップに移し、直ちに真空チャンバー(Hewlett-Packard社G2024A試料製造付属品)内で蒸発させ、迅速かつ均質な試料の結晶化を確実にした。
(活性スクリーニング)
(蛍光アッセイ)
全ての測定は、マイクロプレート用BioAssay Reader HTS-7000Plus(Perkin Elmer社)により30℃で行った。QC活性は、H-Gln-βNAを用い、蛍光測定により評価した。試料は、最終容積250μl中における、20mM EDTA及び適宜希釈した一定分量のQCを含有する、0.2mM蛍光発生基質、0.25Uピログルタミルアミノぺプチダーゼ(Unizyme社、ホルショルム、デンマーク)含有0.2Mトリス/HCl(pH8.0)からなった。励起/発光波長は、320/410nmであった。該アッセイ反応は、グルタミニルシクラーゼの添加により開始した。QC活性は、アッセイ条件下でのβ-ナフチルアミンの標準曲線から決定した。1単位は、記載した条件下で、1分間にH-Gln-βNAから1μmolのpGlu-βNAの形成を触媒するQC量と定義されている。
この新規アッセイを用いて、ほとんどのQC基質の反応速度パラメータを決定した。QC活性は、補助的な酵素としてグルタミン酸デヒドロゲナーゼを利用する、既存の不連続アッセイ(Bateman, R. C. J.の文献(1989 J Neurosci Methods 30, 23-28))を適応させることにより導いた連続法を用い、分光光度的に分析した。試料は、最終容積250μl中における、各QC基質、0.3mM NADH、14mMα-ケトグルタル酸、及び30U/mlグルタミン酸デヒドロゲナーゼからなった。反応は、QCの添加により出発し、吸光度の低下を340nmで8〜15分間モニタリングすることにより追跡した。
阻害剤の試験に関して、試料組成物は、推定阻害化合物を添加したこと以外は、先に説明したものと同じであった。QC-阻害に関する迅速試験について、試料は、4mMの各阻害剤及び1KMの基質濃度を含有した。阻害の詳細な研究及びKi-値の決定については、阻害剤の補助的な酵素に対する影響を最初に調べた。あらゆる場合において、検出されたいずれの酵素についても影響はなく、従ってQC阻害の信頼できる決定が可能であった。阻害定数は、GraFitソフトウェアを用い、反応進行曲線のセットを、競合阻害に関する一般式にあてはめることにより評価した。
結果:
脳の化合物レベル及びlogBBについてのスクリーニングをマウスにおいて実施した。化合物を単回静脈内注射によって適用した。10%DMSO及び5%トゥイーン80を含有する10mg/mL用量含有PBSを各個体に適用した。1つの化合物につき少なくとも3個体を分析した。化合物の適用の1時間後に動物を屠殺し、血液を心穿刺によって集めた。血液から血清を製造した。動物をPBSで還流し、脳を集めた。血清及び脳における化合物レベルをHPLC-MS/MS分析によって決定した。logBBを下記の通り算出した:
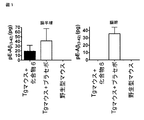
本発明の化合物のインビボでの有効性を立証するために、QCによってAβpE3-42に環化されるヒトAβQ3-42をニューロン特異的に過剰発現して、重度の神経変性表現型を発現するトランスジェニック(tg)マウスを、実施例化合物第6番(1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオン)で経口処置した。実施例化合物6を餌に入れ、トランスジェニック動物を経口処置した。該処置は以下の表に明記する。本試験において使用したマウスは、WO 2009/034158に記載されたとおり作出した。
ギ酸画分の脳均質液の分析を図1に示す。阻害剤による処置は、定量化限界を下回るpGlu-Aβ濃度の低下をもたらし、このように、本化合物の有意な処置効果を表した。それゆえ、該処置実験は下記を明確に示している:
1.導入遺伝子Aβがニューロンにおいてのみ発現し、脳組織のみを分析したので、QC阻害剤は、マウスにおける血液脳関門を通過する。
2. pGlu修飾したAβの濃度が有意に低下したので、QC阻害剤は、脳組織におけるQCの阻害によってpGlu-Aβ濃度を低下させる。
3. AβのpGlu修飾が細胞内プロセスであることが示されている(Cynis, H.らの文献((2008) Biochemistry 47, 7405-13))ので、QC阻害剤は、細胞内のQCを阻害する。
処置スキームは一般に、散発性アルツハイマー病及びダウン症候群における神経変性のモデルにおけるAβpE3-40及びAβpE3-42などのアミロイド形成的ペプチド、並びに家族性英国型又は家族性デンマーク型認知症のモデルにおける他のpGlu修飾したアミロイド形成的ペプチド、例えばADan又はABriの生成の低下に適用され得る。
本発明は、先に列挙した群の好ましい及びより好ましい群及び実施態様の全ての組み合わせを包含する。
Claims (39)
- 式(I)の化合物、又はそのすべての互変異性体及び立体異性体、又はそれらの医薬として許容し得る塩、溶媒和物、若しくは多形体:
ここで、上記のヘテロアリール基のいずれも、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、-C1-6チオアルキル、-SOC1-4アルキル、-SO2C1-4アルキル、C1-6アルコキシ-、-O-C3-8シクロアルキル、C3-8シクロアルキル、-SO2C3-8シクロアルキル、-SOC3-6シクロアルキル、C3-6アルケニルオキシ-、C3-6アルキニルオキシ-、-C(O)C1-6アルキル、-C(O)OC1-6アルキル、C1-6アルコキシ-C1-6アルキル-、ニトロ、ハロゲン、シアノ、ヒドロキシル、-C(O)OH、-NH2、-NHC1-4アルキル、-N(C1-4アルキル)(C1-4アルキル)、-C(O)N(C1-4アルキル)(C1-4アルキル)、-C(O)NH2、-C(O)NH(C1-4アルキル)、及び-C(O)NH(C3-10シクロアルキル)から選択される1つ以上の基によって任意に置換してもよく;
かつここで、上記のカルボシクリル基のいずれも、C1-4アルキル、オキソ、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
R2は、C1-8アルキル、アリール、ヘテロアリール、カルボシクリル、ヘテロシクリル、-C1-4アルキルアリール、-C1-4アルキルヘテロアリール、-C1-4アルキルカルボシクリル、又は-C1-4アルキルヘテロシクリルを表し;
ここで、上記のアリール基及びヘテロアリール基のいずれも、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、-C1-6チオアルキル、-SOC1-4アルキル、-SO2C1-4アルキル、C1-6アルコキシ-、-O-C3-8シクロアルキル、C3-8シクロアルキル、-SO2C3-8シクロアルキル、-SOC3-6シクロアルキル、C3-6アルケニルオキシ-、C3-6アルキニルオキシ-、-C(O)C1-6アルキル、-C(O)OC1-6アルキル、C1-6アルコキシ-C1-6アルキル-、ニトロ、ハロゲン、シアノ、ヒドロキシル、-C(O)OH、-NH2、-NHC1-4アルキル、-N(C1-4アルキル)(C1-4アルキル)、-C(O)N(C1-4アルキル)(C1-4アルキル)、-C(O)NH2、-C(O)NH(C1-4アルキル)、及び-C(O)NH(C3-10シクロアルキル)から選択される1つ以上の基によって任意に置換してもよく;
かつここで、上記のカルボシクリル基及びヘテロシクリル基のいずれも、C1-4アルキル、オキソ、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
或いはR2は、フェニルによって置換したフェニル、単環式ヘテロアリール基によって置換したフェニル、ベンジルオキシによって置換したフェニル、カルボシクリルに縮合したフェニル、ヘテロシクリルに縮合したフェニル、-C1-4アルキル(フェニルによって置換したフェニル)、-C1-4アルキル(単環式ヘテロアリール基によって置換したフェニル)、-C1-4アルキル(ベンジルオキシによって置換したフェニル)、-C1-4アルキル(任意に置換したカルボシクリルに縮合した任意に置換したフェニル)、又はC1-4アルキル(任意に置換したヘテロシクリルに縮合した任意に置換したフェニル)を表し;
ここで、上記のフェニル基、ベンジルオキシ基、及びヘテロアリール基のいずれも、C1-4アルキル、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく、かつここで、上記のカルボシクリル基及びヘテロシクリル基のいずれも、C1-4アルキル、オキソ、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
R3は、H、-C1-4アルキル、又はアリールを表し;
ここで、上記のアリールは、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、-C1-6チオアルキル、-SOC1-4アルキル、-SO2C1-4アルキル、C1-6アルコキシ-、-O-C3-8シクロアルキル、C3-8シクロアルキル、-SO2C3-8シクロアルキル、-SOC3-6シクロアルキル、C3-6アルケニルオキシ-、C3-6アルキニルオキシ-、-C(O)C1-6アルキル、-C(O)OC1-6アルキル、C1-6アルコキシ-C1-6アルキル-、ニトロ、ハロゲン、シアノ、ヒドロキシル、-C(O)OH、-NH2、-NHC1-4アルキル、-N(C1-4アルキル)(C1-4アルキル)、-C(O)N(C1-4アルキル)(C1-4アルキル)、-C(O)NH2、-C(O)NH(C1-4アルキル)、及び-C(O)NH(C3-10シクロアルキル)から選択される1つ以上の基によって任意に置換してもよく;
或いは、R2及びR3は、1つ以上のC1-2アルキル基によって任意に置換したカルボシクリル環を形成するよう結合し;
或いは、R2及びR3は、フェニルに縮合したカルボシクリル環を形成するよう結合し、ここで、上記のカルボシクリル及び/又はフェニルは、C1-4アルキル、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
或いは、R2及びR3は、単環式ヘテロアリールに縮合したカルボシクリル環を形成するよう結合し、ここで、上記のカルボシクリル及び/又はヘテロアリールは、C1-4アルキル、ハロゲン、及びC1-4アルコキシから選択される1つ以上の基によって任意に置換してもよく;
R4は、H、-C1-8アルキル、-C(O)C1-6アルキル、又はNH2を表し;
Xは、O又はSを表し;かつ
Yは、O又はSを表す。)。 - R1が二環式ヘテロアリール基を表す、請求項1記載の化合物。
- R1が、1個又は2個の窒素原子を含む5員環に縮合したベンゼン環又はピリジン環を表す、請求項2記載の化合物。
- 結合点が、ベンゼン環又はピリジン環を介している、請求項3記載の化合物。
- R1が-C1-6アルキルヘテロアリールを表す、請求項1記載の化合物。
- R1のヘテロアリール基が、C1-4アルキル、C1-4アルコキシ-、及びハロゲンから選択される1つ以上の置換基によって任意に置換した1〜3個の窒素原子を含む5員環である、請求項7記載の化合物。
- R2が、アリール、ヘテロアリール、フェニルによって置換したフェニル、ヘテロシクリルに縮合したフェニルを表し、又はR2及びR3が結合して、フェニルに縮合したカルボシクリル環を形成し;上記のアリール、ヘテロアリール、フェニル、ヘテロシクリル、及びカルボシクリルが任意に置換されている、請求項1〜12のいずれか一項記載の化合物。
- R2が、フェニルによって置換したフェニルを表し、上記のフェニル基が、同じでも又は異なってもよくかつハロ、OH、C1-3アルキル、C1-3ハロアルキル、C1-3アルコキシ、C1-3ハロアルコキシから選択される1つ以上の置換基によって任意に置換されている、請求項13記載の化合物。
- R2が-ビフェニル-4-イルである、請求項14記載の化合物。
- R2が、同じでも又は異なってもよくかつハロ、OH、C1-3アルキル、C1-3ハロアルキル、C1-3アルコキシ、C1-3ハロアルコキシから選択される1、2、又は3個の置換基によって任意に置換したフェニルを表す、請求項13記載の化合物。
- R2が、n-プロピルオキシによって置換したフェニルである、請求項16記載の化合物。
- R3がHを表す、請求項1〜17のいずれか一項記載の化合物。
- R2及びR3が結合して、フェニルに縮合したカルボシクリル環を形成する、請求項1〜13のいずれか一項記載の化合物。
- R4がHを表す、請求項1〜19のいずれか一項記載の化合物。
- XがOを表す、請求項1〜20のいずれか一項記載の化合物。
- YがOを表す、請求項1〜21のいずれか一項記載の化合物。
- 下記から選択される式(I)の化合物、又はそのすべての互変異性体及び立体異性体、又はそれらの医薬として許容し得る塩、溶媒和物、若しくは多形体:
5-(ベンゾ[c][1,2,5]チアジアゾール-6-イル)-1-(1H-ベンゾ[d]イミダゾール-5-イル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-フェニルイミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-ヒドロキシ-5-メチルフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-フルオロ-5-トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-ブロモ-5-フルオロフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロ-3-トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-フルオロ-4(トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-ヒドロキシ-4-メトキシフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-ヒドロキシ-3-メトキシフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンズイミダゾール-5-イル)-5-(1,1'-ビフェニル-4-イル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-クロロフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2-クロロフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-フルオロフェニル)イミダゾリジン-2,4-ジオン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3-ジヒドロベンゾ[b][1,4]ジオキシン-7-イル)イミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-フェニルイミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(2-ブロモ-4-フルオロフェニル)イミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(3-フルオロ-4-(トリフルオロメチル)フェニル)イミダゾリジン-2,4-ジオン;
1-[3-(1H-イミダゾール-1-イル)プロピル]-5-(4-ビフェニル)イミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(3-クロロフェニル)イミダゾリジン-2,4-ジオン;
1-(3-(1H-イミダゾール-1-イル)プロピル)-5-(2-クロロフェニル)イミダゾリジン-2,4-ジオン;
1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)-5-フェニルイミダゾリジン-2,4-ジオン;
5-(2-ブロモ-5-フルオロフェニル)-1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)イミダゾリジン-2,4-ジオン;
1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)-5-(4-プロポキシフェニル)イミダゾリジン-2,4-ジオン;
1-[3-(5-メチル-1H-イミダゾール-1-イル)プロピル]-5-(4-フェニルフェニル)イミダゾリジン-2,4-ジオン;
5-(3-クロロフェニル)-1-(3-(5-メチル-1H-イミダゾール-1-イル)プロピル)イミダゾリジン-2,4-ジオン;
1-(3-(4-メチル-1H-イミダゾール-1-イル)プロピル)-5-フェニルイミダゾリジン-2,4-ジオン;
1-[3-(4-メチル-1H-イミダゾール-1-イル)プロピル]-5-(4-ビフェニル)イミダゾリジン-2,4-ジオン;
5-(3-クロロフェニル)-1-(3-(4-メチル-1H-イミダゾール-1-イル)プロピル)イミダゾリジン-2,4-ジオン;
3-(1H-ベンズイミダゾール-5-イル)-1',3'-ジヒドロ-2H,5H-スピロ[イミダゾリジン-4,2'-インデン]-2,5-ジオン;
5-(ベンゾ[c][1,2,5]チアジアゾール-6-イル)-1-(1H-ベンゾ[d]イミダゾール-5-イル)-2-チオキソイミダゾリジン-4-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-フェニル-2-チオキソイミダゾリジン-4-オン;
1-(1H-ベンズイミダゾール-5-イル)-5-(1,1'-ビフェニル-4-イル)-2-チオキソイミダゾリジン-4-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(3-ヒドロキシ-4-メトキシフェニル)-2-チオキソイミダゾリジン-4-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-フェニル-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンズイミダゾール-5-イル)-5-(1,1'-ビフェニル-4-イル)-4-チオキソイミダゾリジン-2-オン;
3-(1H-ベンズイミダゾール-5-イル)-5-チオキソ-1',3'-ジヒドロ-2H-スピロ[イミダゾリジン-4,2'-インデン]-2-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロフェニル)-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3,4-トリフルオロフェニル)-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンゾ[d]イミダゾール-6-イル)-5-(4-ブロモ-2-フルオロフェニル)-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(2,3-ジフルオロ-4-メチルフェニル)-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-5-(4-クロロ-3-メチルフェニル)-4-チオキソイミダゾリジン-2-オン;
1-(1H-ベンゾ[d]イミダゾール-5-イル)-3-メチル-5-フェニルイミダゾリジン-2,4-ジオン;
1-(H-イミダゾ[1,2-a]ピリジン-7-イル)-5-フェニルイミダゾリジン-2,4-ジオン。 - 請求項1〜25のいずれか一項記載の式(I)の化合物の製造方法であって、下記のいずれかを含む、前記方法:
a)水性条件(例えば、水性トリフルオロ酢酸)下でイミンをカルボニルに変換することによって
式(II)の化合物
b)先に定義した式(II)の化合物を、硫化物イオン源(例えば、硫化ナトリウム)と反応させて、式(I)の化合物(式中、XはSであり、かつR4はHである。)を与えること;又は
c)式(VIII)の化合物
d)式(XIII)の化合物
e)式(I)の化合物(式中、R4はHを表す。)を亜硝酸イオン源(例えば、亜硝酸ナトリウム)と反応させ、その後還元(例えば、亜鉛粉を使用して)、式(I)の化合物(式中、R1、R2、R3、X、及びYは先に定義したとおりであり、かつR4は-NH2を表す。)を与えること。 - 薬剤として使用するための、請求項1〜25のいずれか一項記載の化合物。
- 1つ以上の医薬として許容し得る希釈剤又は担体との組み合わせで、請求項1〜25のいずれか一項記載の化合物を含む医薬組成物。
- 神経保護薬、抗パーキンソン病薬、アミロイドタンパク質沈着阻害薬、βアミロイド合成阻害薬、抗うつ薬、抗不安薬、抗精神病薬、及び抗多発性硬化症薬からなる群から選択される少なくとも1つの化合物を追加的に含む、請求項28記載の医薬組成物。
- PEP阻害剤、LiCl、DP IV又はDP IV様酵素の阻害剤の阻害剤、アセチルコリンエステラーゼ(ACE)阻害剤、PIMTエンハンサー、βセクレターゼの阻害剤、γセクレターゼの阻害剤、中性エンドペプチダーゼの阻害剤、ホスホジエステラーゼ-4(PDE-4)の阻害剤、TNFα阻害剤、ムスカリン性M1受容体アンタゴニスト、NMDA受容体アンタゴニスト、σ-1受容体阻害剤、ヒスタミンH3アンタゴニスト、免疫調節薬、免疫抑制薬、又はアンテグレン(ナタリズマブ)、Neurelan(ファムプリジン-SR)、カンパス(アレムツズマブ)、IR 208、NBI 5788/MSP771(チプリモチド)、パクリタキセル、Anergix.MS(AG 284)、SH636、ディフェリン(CD 271、アダパレン)、BAY 361677(インターロイキン-4)、マトリックス-メタロプロテイナーゼ-阻害剤、インターフェロン-τ(トロホブラスチン)、及びSAIK-MSからなる群から選択される作用物質からなる群から選択される少なくとも1つの化合物を追加的に含む、請求項28又は請求項29記載の医薬組成物。
- ケネディ病、ヘリコバクターピロリ感染を伴う又は伴わない十二指腸癌、結腸直腸癌、ゾリンジャー・エリソン症候群、ヘリコバクターピロリ感染を伴う又は伴わない胃癌、病原性精神病性容態、統合失調症、不妊、腫瘍、炎症性宿主応答、癌、悪性転移、メラノーマ、乾癬、液性及び細胞仲介性免疫応答障害、内皮内の白血球接着及び遊走プロセス、摂食障害、睡眠-覚醒障害、エネルギー代謝の恒常性調節障害、自律神経機能障害、ホルモン平衡障害又は体液の調節障害、多発性硬化症、ギラン・バレー症候群、及び慢性炎症性脱髄性多発性神経根症からなる群から選択される疾患の治療において使用するための、請求項1〜25のいずれか一項記載の化合物又は請求項28〜30のいずれか一項記載の医薬組成物。
- 軽度認知障害、アルツハイマー病、家族性英国型認知症、家族性デンマーク型認知症、ダウン症候群における神経変性、及びハンチントン病からなる群から選択される疾患の治療において使用するための、請求項1〜25のいずれか一項記載の化合物又は請求項28〜30のいずれか一項記載の医薬組成物。
- 関節リウマチ、粥状硬化、膵炎、及び再狭窄からなる群から選択される疾患の治療において使用するための、請求項1〜25のいずれか一項記載の化合物又は請求項28〜30のいずれか一項記載の医薬組成物。
- ケネディ病、ヘリコバクターピロリ感染を伴う又は伴わない十二指腸癌、結腸直腸癌、ゾリンジャー・エリソン症候群、ヘリコバクターピロリ感染を伴う又は伴わない胃癌、病原性精神病性容態、統合失調症、不妊、腫瘍、炎症性宿主応答、癌、悪性転移、メラノーマ、乾癬、液性及び細胞仲介性免疫応答障害、内皮内の白血球接着及び遊走プロセス、摂食障害、睡眠-覚醒障害、エネルギー代謝の恒常性調節障害、自律神経機能障害、ホルモン平衡障害又は体液の調節障害、多発性硬化症、ギラン・バレー症候群、及び慢性炎症性脱髄性多発性神経根症からなる群から選択される疾患を治療又は予防する方法であって、該治療を必要とする患者に、有効量の請求項1〜25のいずれか一項記載の化合物又は請求項28〜30のいずれか一項記載の医薬組成物を投与することを含む、前記方法。
- 軽度認知障害、アルツハイマー病、家族性英国型認知症、家族性デンマーク型認知症、ダウン症候群における神経変性、及びハンチントン病からなる群から選択される疾患を治療又は予防する方法であって、該治療を必要とする患者に、有効量の請求項1〜25のいずれか一項記載の化合物又は請求項28〜30のいずれか一項記載の医薬組成物を投与することを含む、前記方法。
- 関節リウマチ、粥状硬化、膵炎、及び再狭窄からなる群から選択される疾患を治療又は予防する方法であって、該治療を必要とする患者に、有効量の請求項1〜25のいずれか一項記載の化合物又は請求項28〜30のいずれか一項記載の医薬組成物を投与することを含む、前記方法。
- ケネディ病、ヘリコバクターピロリ感染を伴う又は伴わない十二指腸癌、結腸直腸癌、ゾリンジャー・エリソン症候群、ヘリコバクターピロリ感染を伴う又は伴わない胃癌、病原性精神病性容態、統合失調症、不妊、腫瘍、炎症性宿主応答、癌、悪性転移、メラノーマ、乾癬、液性及び細胞仲介性免疫応答障害、内皮内の白血球接着及び遊走プロセス、摂食障害、睡眠-覚醒障害、エネルギー代謝の恒常性調節障害、自律神経機能障害、ホルモン平衡障害又は体液の調節障害、多発性硬化症、ギラン・バレー症候群、及び慢性炎症性脱髄性多発性神経根症からなる群から選択される疾患の治療のための薬剤の製造における、請求項1〜25のいずれか一項記載の化合物又は請求項28〜30のいずれか一項記載の医薬組成物の使用。
- 軽度認知障害、アルツハイマー病、家族性英国型認知症、家族性デンマーク型認知症、ダウン症候群における神経変性、及びハンチントン病からなる群から選択される疾患の治療のための薬剤の製造における、請求項1〜25のいずれか一項記載の化合物又は請求項28〜30のいずれか一項記載の医薬組成物の使用。
- 関節リウマチ、粥状硬化、膵炎、及び再狭窄からなる群から選択される疾患の治療のための薬剤の製造における、請求項1〜25のいずれか一項記載の化合物又は請求項28〜30のいずれか一項記載の医薬組成物の使用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US9411808P | 2008-09-04 | 2008-09-04 | |
| US61/094,118 | 2008-09-04 | ||
| PCT/EP2009/061453 WO2010026212A1 (en) | 2008-09-04 | 2009-09-04 | Novel inhibitors |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2012502006A true JP2012502006A (ja) | 2012-01-26 |
| JP2012502006A5 JP2012502006A5 (ja) | 2012-10-18 |
| JP5707327B2 JP5707327B2 (ja) | 2015-04-30 |
Family
ID=41278686
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011525556A Active JP5707327B2 (ja) | 2008-09-04 | 2009-09-04 | 新規の阻害剤 |
Country Status (17)
| Country | Link |
|---|---|
| US (1) | US8962860B2 (ja) |
| EP (1) | EP2344157B1 (ja) |
| JP (1) | JP5707327B2 (ja) |
| KR (1) | KR101694556B1 (ja) |
| CN (1) | CN102186475B (ja) |
| AU (1) | AU2009289238B2 (ja) |
| BR (1) | BRPI0918564B1 (ja) |
| CA (1) | CA2735795C (ja) |
| DK (1) | DK2344157T3 (ja) |
| EA (1) | EA021150B1 (ja) |
| ES (1) | ES2599621T3 (ja) |
| IL (1) | IL211018A (ja) |
| MX (1) | MX2011002106A (ja) |
| NZ (1) | NZ591531A (ja) |
| SG (1) | SG193828A1 (ja) |
| WO (1) | WO2010026212A1 (ja) |
| ZA (1) | ZA201100898B (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012502005A (ja) * | 2008-09-04 | 2012-01-26 | プロビオドルグ エージー | イソqc阻害剤の使用 |
| JP2022542540A (ja) * | 2019-07-12 | 2022-10-05 | シーニック・イミュノロジー・ヴェンノーツハップ | isoQC及び/又はQC酵素の阻害剤としてのN-置換-3,4-(縮合5-環)-5-フェニル-ピロリジン-2-オン化合物 |
| JP2024523552A (ja) * | 2021-06-24 | 2024-06-28 | インシリコ メディシン アイピー リミテッド | 疾患の処置のためのベータ-ラクタム誘導体 |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5934645B2 (ja) | 2009-09-11 | 2016-06-15 | プロビオドルグ エージー | グルタミニルシクラーゼ阻害剤としてのヘテロ環式誘導体 |
| WO2011076854A1 (en) | 2009-12-22 | 2011-06-30 | Probiodrug Ag | CLEAVAGE OF β-AMYLOID PRECURSOR PROTEIN |
| EP2686313B1 (en) * | 2011-03-16 | 2016-02-03 | Probiodrug AG | Benzimidazole derivatives as inhibitors of glutaminyl cyclase |
| US8945510B2 (en) | 2011-05-27 | 2015-02-03 | Probiodrug Ag | Radiolabeled glutaminyl cyclase (QC) inhibitors and uses of same |
| US9512115B2 (en) * | 2013-03-15 | 2016-12-06 | Probiodrug Ag | Inhibitors |
| WO2016097305A1 (en) | 2014-12-19 | 2016-06-23 | Probiodrug Ag | Novel method for the detection of pglu-abeta peptides |
| CN108658869A (zh) * | 2017-03-29 | 2018-10-16 | 复旦大学 | 具有抗肿瘤活性的化合物及其制备方法和在制药中的用途 |
| GB201705263D0 (en) * | 2017-03-31 | 2017-05-17 | Probiodrug Ag | Novel inhibitors |
| RU2662559C1 (ru) * | 2017-10-27 | 2018-07-26 | Общество С Ограниченной Ответственностью "Фарминтерпрайсез" | Новый ингибитор глутаминилциклаз и его применение для лечения заболеваний легких и дыхательных путей |
| RU2665633C1 (ru) * | 2017-05-26 | 2018-09-03 | Общество С Ограниченной Ответственностью "Фарминтерпрайсез" | Новый ингибитор глутаминилциклаз и его применение |
| ES2812698T3 (es) | 2017-09-29 | 2021-03-18 | Probiodrug Ag | Inhibidores de glutaminil ciclasa |
| EP3521308B1 (en) | 2018-01-31 | 2024-03-13 | Vivoryon Therapeutics N.V. | Humanized and de-immunized antibodies |
| WO2019162458A1 (en) | 2018-02-23 | 2019-08-29 | Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. | Novel inhibitors of bacterial glutaminyl cyclases for use in the treatment of periodontal and related diseases |
| TWI715156B (zh) | 2018-08-31 | 2021-01-01 | 財團法人國家衛生研究院 | 苯并咪唑化合物及其用於治療阿茲海默症或亨丁頓氏症之用途 |
| CA3141720A1 (en) * | 2019-05-24 | 2020-12-03 | Emory University | Asparagine endopeptidase (aep) inhibitors, compositions, and uses related thereto |
| KR20260040085A (ko) * | 2023-07-21 | 2026-03-23 | 인실리코 메디신 아이피 리미티드 | 결정형 베타-락탐 유도체 및 이의 용도 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DD293584A5 (de) * | 1990-03-23 | 1991-09-05 | Adw,Zi Fuer Organische Chemie,De | Verfahren zur herstellung von neuen 3,5,5-trisubstituierten 1-(benzimidazol-2-yl)-imidazolidin-2,4-dionen bzw. -4-on-2-thionen |
| JPH0748369A (ja) * | 1993-06-21 | 1995-02-21 | Bayer Ag | 置換モノピリジルメチルおよびビピリジルメチル誘導体 |
| US20040006011A1 (en) * | 1996-07-12 | 2004-01-08 | Gour Barbara J. | Peptidomimetic modulators of cell adhesion |
| JP2007520520A (ja) * | 2004-02-05 | 2007-07-26 | プロビオドルグ エージー | グルタミニルシクラーゼの新規の阻害剤 |
| WO2008055947A1 (en) * | 2006-11-09 | 2008-05-15 | Probiodrug Ag | Novel inhibitors of glutaminyl cyclase |
| JP2012502005A (ja) * | 2008-09-04 | 2012-01-26 | プロビオドルグ エージー | イソqc阻害剤の使用 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| NZ501166A (en) | 1997-07-31 | 2001-12-21 | Abbott Lab | Reverse hydroxamate-containing compounds and their use as inhibitors of matrix metalloproteinases |
| US6235786B1 (en) * | 1997-08-06 | 2001-05-22 | Abbott Laboratories | Reverse hydroxamate inhibitors of matrix metalloproteinases |
| JP4806628B2 (ja) * | 2003-05-05 | 2011-11-02 | プロビオドルグ エージー | グルタミニルシクラーゼ阻害剤 |
| US7795287B2 (en) | 2006-09-01 | 2010-09-14 | Allergan, Inc. | Therapeutic substituted hydantoins and related compounds |
| BRPI0718507A2 (pt) * | 2006-09-21 | 2013-11-12 | Probiodrug Ag | Genes relacionados à glutaminil ciclase |
| TW200831080A (en) | 2006-12-15 | 2008-08-01 | Irm Llc | Compounds and compositions as inhibitors of cannabinoid receptor 1 activity |
| CN101519376B (zh) | 2008-02-27 | 2012-10-10 | 上海药明康德新药开发有限公司 | 一种芳香环双酰胺螺环类药物模板的合成方法 |
-
2009
- 2009-09-04 AU AU2009289238A patent/AU2009289238B2/en active Active
- 2009-09-04 SG SG2013064738A patent/SG193828A1/en unknown
- 2009-09-04 WO PCT/EP2009/061453 patent/WO2010026212A1/en not_active Ceased
- 2009-09-04 CN CN200980139148.0A patent/CN102186475B/zh active Active
- 2009-09-04 BR BRPI0918564-0A patent/BRPI0918564B1/pt active IP Right Grant
- 2009-09-04 ES ES09782605.1T patent/ES2599621T3/es active Active
- 2009-09-04 MX MX2011002106A patent/MX2011002106A/es active IP Right Grant
- 2009-09-04 JP JP2011525556A patent/JP5707327B2/ja active Active
- 2009-09-04 KR KR1020117007403A patent/KR101694556B1/ko active Active
- 2009-09-04 NZ NZ591531A patent/NZ591531A/en unknown
- 2009-09-04 CA CA2735795A patent/CA2735795C/en active Active
- 2009-09-04 US US12/554,611 patent/US8962860B2/en active Active
- 2009-09-04 DK DK09782605.1T patent/DK2344157T3/en active
- 2009-09-04 EP EP09782605.1A patent/EP2344157B1/en active Active
- 2009-09-04 EA EA201100424A patent/EA021150B1/ru not_active IP Right Cessation
-
2011
- 2011-02-02 IL IL211018A patent/IL211018A/en active IP Right Grant
- 2011-02-03 ZA ZA2011/00898A patent/ZA201100898B/en unknown
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DD293584A5 (de) * | 1990-03-23 | 1991-09-05 | Adw,Zi Fuer Organische Chemie,De | Verfahren zur herstellung von neuen 3,5,5-trisubstituierten 1-(benzimidazol-2-yl)-imidazolidin-2,4-dionen bzw. -4-on-2-thionen |
| JPH0748369A (ja) * | 1993-06-21 | 1995-02-21 | Bayer Ag | 置換モノピリジルメチルおよびビピリジルメチル誘導体 |
| US20040006011A1 (en) * | 1996-07-12 | 2004-01-08 | Gour Barbara J. | Peptidomimetic modulators of cell adhesion |
| JP2007520520A (ja) * | 2004-02-05 | 2007-07-26 | プロビオドルグ エージー | グルタミニルシクラーゼの新規の阻害剤 |
| WO2008055947A1 (en) * | 2006-11-09 | 2008-05-15 | Probiodrug Ag | Novel inhibitors of glutaminyl cyclase |
| JP2012502005A (ja) * | 2008-09-04 | 2012-01-26 | プロビオドルグ エージー | イソqc阻害剤の使用 |
Non-Patent Citations (7)
| Title |
|---|
| JPN5011013256; GRAUBAUM, H.: 'INTER- AND INTRAMOLECULAR ACYL TRANSFER IN 1(9)H-IMIDAZO[1,2-A]BENZIMIDAZOLEN' JOURNAL FUER PRAKTISCHE CHEMIE V332 N1, 1990, P83-92 * |
| JPN5011013257; Z. I. BERESNEVICIUS: 'REACTIONS OF AMINOQUINOLINES WITH UNSATURATED CARBOXYLIC ACIDS. 3. SYNTHESIS 以下備考' CHEMISTRY OF HETEROCYCLIC COMPOUNDS V36 N7, 20000701, P811-817 * |
| JPN5011013259; LAMOTHE MARIE: 'SOLID-PHASE PREPARATION OF HYDANTOINS THROUGH A NEW CYCLIZATION/CLEAVAGE STEP' JOURNAL OF COMBINATORIAL CHEMISTRY V4 N1, 200201, P73-78 * |
| JPN5011013262; SUNDARAM G S M: '1-(METHYLDITHIOCARBONYL)IMIDAZOLE AS THIOCARBONYL TRANSFER REAGENT: 以下備考' SYNLETT N2, 20070201, P251-254 * |
| JPN6014000709; WERBEL, Leslie M. et al.: 'Antischistosomal effects of 5-(2,4,5-trichlorophenyl)hydantoin and related compounds' Journal of Medicinal Chemistry Vol.20, No.12, 1977, pp.1569-1572 * |
| JPN6014000710; NAYANA, Munuganti Ravi Shashi et al.: '3D-QSAR CoMFA Study on human glutaminyl cyclase inhibitors' Internet Electronic Journal of Molecular Design Vol.6, No.10, 2007, pp.320-330 * |
| JPN7014000064; Database REGISTRY , 1999, RN 219618-29-8, 219618-28-7 * |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012502005A (ja) * | 2008-09-04 | 2012-01-26 | プロビオドルグ エージー | イソqc阻害剤の使用 |
| JP2022542540A (ja) * | 2019-07-12 | 2022-10-05 | シーニック・イミュノロジー・ヴェンノーツハップ | isoQC及び/又はQC酵素の阻害剤としてのN-置換-3,4-(縮合5-環)-5-フェニル-ピロリジン-2-オン化合物 |
| JP2024523552A (ja) * | 2021-06-24 | 2024-06-28 | インシリコ メディシン アイピー リミテッド | 疾患の処置のためのベータ-ラクタム誘導体 |
| JP7844513B2 (ja) | 2021-06-24 | 2026-04-13 | インシリコ メディシン アイピー リミテッド | 疾患の処置のためのベータ-ラクタム誘導体 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2344157A1 (en) | 2011-07-20 |
| KR20110074975A (ko) | 2011-07-05 |
| AU2009289238B2 (en) | 2014-09-04 |
| IL211018A0 (en) | 2011-04-28 |
| WO2010026212A1 (en) | 2010-03-11 |
| DK2344157T3 (en) | 2016-09-05 |
| ES2599621T3 (es) | 2017-02-02 |
| KR101694556B1 (ko) | 2017-01-09 |
| EA021150B1 (ru) | 2015-04-30 |
| CA2735795C (en) | 2018-02-20 |
| US20100119475A1 (en) | 2010-05-13 |
| EP2344157B1 (en) | 2016-05-25 |
| CA2735795A1 (en) | 2010-03-11 |
| BRPI0918564A2 (pt) | 2015-12-01 |
| IL211018A (en) | 2015-11-30 |
| NZ591531A (en) | 2012-03-30 |
| EA201100424A1 (ru) | 2011-10-31 |
| JP5707327B2 (ja) | 2015-04-30 |
| CN102186475B (zh) | 2016-08-03 |
| AU2009289238A1 (en) | 2010-03-11 |
| CN102186475A (zh) | 2011-09-14 |
| MX2011002106A (es) | 2011-04-07 |
| SG193828A1 (en) | 2013-10-30 |
| US8962860B2 (en) | 2015-02-24 |
| ZA201100898B (en) | 2012-02-29 |
| BRPI0918564B1 (pt) | 2023-11-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5707327B2 (ja) | 新規の阻害剤 | |
| JP5675340B2 (ja) | 新規阻害剤 | |
| JP5688745B2 (ja) | グルタミニルシクラーゼ(qc、ec2.3.2.5)の複素環阻害剤 | |
| JP5523107B2 (ja) | グルタミニルシクラーゼの新規阻害剤 | |
| JP5667440B2 (ja) | グルタミニルシクラーゼ阻害剤としてのチオ尿素誘導体 | |
| JP5612860B2 (ja) | グルタミニルシクラーゼ阻害剤としてのイミダゾ[1,5−a]ピリジン誘導体 | |
| JP5675343B2 (ja) | グルタミニルシクラーゼ阻害剤としての尿素誘導体 | |
| JP5798157B2 (ja) | 潰瘍、癌及び他の疾患の治療のためのグルタミニルシクラーゼの阻害薬としての3−ヒドロキシ−1,5−ジヒドロ−ピロール−2−オン誘導体 | |
| JP6026284B2 (ja) | グルタミニルシクラーゼの阻害剤 | |
| JP5676249B2 (ja) | グルタミニルシクラーゼ阻害剤としてのアミノピリジン誘導体 | |
| JP5934645B2 (ja) | グルタミニルシクラーゼ阻害剤としてのヘテロ環式誘導体 | |
| JP5675342B2 (ja) | グルタミニルシクラーゼ阻害剤としてのシアノグアニジン誘導体 | |
| JP5456479B2 (ja) | グルタミニルシクラーゼの新規阻害剤 | |
| JP5675344B2 (ja) | グルタミニルシクラーゼ阻害剤としてのニトロビニルジアミン誘導体 | |
| JP6050264B2 (ja) | グルタミニルシクラーゼの阻害剤としてのベンゾイミダゾール誘導体 | |
| JP2010509286A (ja) | グルタミニルシクラーゼの新規阻害剤 | |
| JP5945532B2 (ja) | グルタミニルシクラーゼの阻害剤としてのベンゾイミダゾール誘導体 | |
| HK1161540A (en) | Novel inhibitors |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120831 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120831 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140114 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140409 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140424 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140711 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140819 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20141117 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20141125 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20141201 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150113 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150119 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20150210 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20150302 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5707327 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |