JP2013200316A - イムノクロマト法を用いた標的物質の検出方法および検出装置セット - Google Patents
イムノクロマト法を用いた標的物質の検出方法および検出装置セット Download PDFInfo
- Publication number
- JP2013200316A JP2013200316A JP2013133073A JP2013133073A JP2013200316A JP 2013200316 A JP2013200316 A JP 2013200316A JP 2013133073 A JP2013133073 A JP 2013133073A JP 2013133073 A JP2013133073 A JP 2013133073A JP 2013200316 A JP2013200316 A JP 2013200316A
- Authority
- JP
- Japan
- Prior art keywords
- fluorescence
- dye
- target substance
- fluorescent
- wavelength
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Landscapes
- Investigating, Analyzing Materials By Fluorescence Or Luminescence (AREA)
- Investigating Or Analysing Materials By The Use Of Chemical Reactions (AREA)
Abstract
【解決手段】標識試薬として、蛍光粒子の母体の主成分がシリカである粒子中に、1種または2種以上の有機色素と、該有機色素よりも励起波長の長い有機蛍光色素とを共に含有し、共鳴エネルギー遷移現象によって励起波長と蛍光波長の差異を1種類の前記蛍光色素の場合よりも広げた蛍光粒子を用い、
高輝度LEDからの励起光を、励起光の長波長成分をカットする光フィルタを介して前記標的物質に結合した標識試薬を含む試料に照射し、共鳴エネルギー遷移現象による蛍光試薬の励起波長と蛍光検出波長のストークスシフトによる蛍光の励起光との色相変化を利用して試料からの蛍光を観察することを特徴とするイムノクロマト法を用いた標的物質の検出方法。
【選択図】図4
Description
〔1〕特定の抗体と結合する性質を有する標識試薬と、前記抗体を固定する抗体固定部位を有する親水性のメンブレンとを用いたイムノクロマト法による標的物質の検出方法であって、
前記標識試薬と結合された前記標的物質を含有する溶液が親水性のメンブレン中を移動し、該メンブレン内に作製した前記抗体固定部位に前記標識試薬を集積させ、集積した前記標識試薬を蛍光発色により可視化させるに当たり、
前記標識試薬として、蛍光粒子の母体の主成分がシリカである粒子中に、1種または2種以上の有機色素と、該有機色素よりも励起波長の長い有機蛍光色素とを共に含有し、共鳴エネルギー遷移現象によって励起波長と蛍光波長の差異を1種類の前記蛍光色素の場合よりも広げた蛍光粒子を用い、
高輝度LEDからの励起光を、励起光の長波長成分をカットする光フィルタを介して前記標的物質に結合した標識試薬を含む試料に照射し、蛍光試薬の共鳴エネルギー遷移現象によって生じる励起波長と蛍光検出波長のストークスシフトによる蛍光の励起光との色相変化を利用して試料からの蛍光を観察することを特徴とするイムノクロマト法を用いた標的物質の検出方法。
〔2〕特定の抗体と結合する性質を有する標識試薬と、前記抗体を固定する抗体固定部位を有する親水性のメンブレンとを用いたイムノクロマト法による標的物質の検出方法であって、
前記標識試薬と結合された前記標的物質を含有する溶液が親水性のメンブレン中を移動し、該メンブレン内に作製した前記抗体固定部位に前記標識試薬を集積させ、集積した前記標識試薬を蛍光発色により可視化させるに当たり、
前記標識試薬として、蛍光粒子の母体の主成分がシリカである粒子中に、1種または2種以上の有機色素と、該有機色素よりも励起波長の長い有機蛍光色素とを共に含有し、共鳴エネルギー遷移現象によって励起波長と蛍光波長の差異を1種類の前記蛍光色素の場合よりも広げた蛍光粒子を用い、
高輝度LEDからの励起光を、励起光を前記標的物質に結合した標識試薬を含む試料に照射し、蛍光試薬の共鳴エネルギー遷移現象によって生じる励起波長と蛍光検出波長のストークスシフトによる蛍光の励起光との色相変化を利用して、励起光をカットする蛍光側のフィルタを介して試料からの蛍光を観察することを特徴とするイムノクロマト法を用いた標的物質の検出方法。
〔3〕前記蛍光粒子としてフルオレセイン色素とローダミン6G色素を共に含有する水分散性のコロイド粒子であって、青緑色の励起光を吸収して緑色の蛍光を放つ蛍光粒子を用いることを特徴とする〔1〕または〔2〕に記載のイムノクロマト法を用いた標的物質の検出方法。
〔4〕前記蛍光粒子として、ローダミン6G色素と、テトラメチルローダミン色素、ローダミンB色素、およびX−ローダミン色素からなる群から選ばれる1種または2種以上の色素とを共に含有する水分散性のコロイド粒子であって、緑色の励起光を吸収して黄色もしくは赤色の蛍光を放つ蛍光粒子を用いることを特徴とする〔1〕または〔2〕に記載のイムノクロマト法を用いた標的物質の検出方法。
〔5〕前記蛍光粒子として、カルボキシローダミン6GとTAMRA色素とを共に含有するシリカコロイドの粒子を用いることを特徴とする〔1〕または〔2〕に記載のイムノクロマト法を用いた標的物質の検出方法。
〔6〕前記蛍光粒子として、カルボキシローダミン6GとBODIPY−FL色素とを共に含有するシリカコロイドの粒子を用いることを特徴とする〔1〕または〔2〕に記載のイムノクロマト法を用いた標的物質の検出方法。
〔7〕アミノ基と反応するNHS基を持つカルボキシ色素と3−アミノプロピルトリエトキシシラン(APS)を結合させ、それをシランカップリング剤と混合してシリカコロイドを合成し、シリカコロイド内部に色素を固定したことを特徴とする〔1〕〜〔6〕のいずれか1項に記載のイムノクロマト法を用いた標的物質の検出方法。
〔8〕前記蛍光粒子が、抗体、抗原、ペプチド、DNA、RNA、糖鎖、リガンド、受容体、また化学物質で表面修飾された〔1〕〜〔7〕のいずれか1項に記載のイムノクロマト法を用いた標的物質の検出方法。
〔9〕赤色LEDを照明光源として用いることを特徴とする〔1〕〜〔8〕のいずれか1項に記載のイムノクロマト法を用いた標的物質の検出方法。
〔10〕励起光の長波長成分をカットする光フィルタが緑色のフィルタである〔1〕及び〔3〕〜〔9〕のいずれか1項に記載のイムノクロマト法を用いた標的物質の検出方法。
〔11〕励起光をカットする光フィルタがオレンジ色のフィルタである〔2〕〜〔9〕のいずれか1項に記載のイムノクロマト法を用いた標的物質の検出方法。
〔12〕特定の抗体と結合する性質を有する標識試薬および前記抗体を固定する抗体固定部位を有する親水性のメンブレンと検出装置とを備えたイムノクロマト法による標的物質の検出装置セットであって、
前記検出装置は、高輝度LEDと、当該高輝度LEDからの励起光の長波長成分をカットする光フィルタを有し、 前記標識試薬として、蛍光粒子の母体の主成分がシリカである粒子中に、1種または2種以上の有機色素と、該有機色素よりも励起波長の長い有機蛍光色素とを共に含有し、共鳴エネルギー遷移現象によって励起波長と蛍光波長の差異を1種類の前記蛍光色素の場合よりも広げた蛍光粒子を用い、
前記標識試薬と結合された前記標的物質を含有する溶液が親水性のメンブレン中を移動し、該メンブレン内に作製した前記抗体固定部位に前記標識試薬を集積させ、集積した前記標識試薬を蛍光発色により可視化させるに当たり、
前記高輝度LEDからの励起光を、前記光フィルタを介して前記標的物質に結合した標識試薬を含む試料に照射し、共鳴エネルギー遷移現象による蛍光試薬の励起波長と蛍光検出波長のストークスシフトによる蛍光の励起光との色相変化を利用して試料からの蛍光を観察することを特徴とするイムノクロマト法を用いた標的物質の検出装置セット。
〔13〕特定の抗体と結合する性質を有する標識試薬および前記抗体を固定する抗体固定部位を有する親水性のメンブレンと検出装置とを備えたイムノクロマト法による標的物質の検出装置セットであって、
前記検出装置は、高輝度LEDと、当該高輝度LEDからの励起光をカットする蛍光を観察する側に配したフィルタを有し、前記標識試薬として、蛍光粒子の母体の主成分がシリカである粒子中に、1種または2種以上の有機色素と、該有機色素よりも励起波長の長い有機蛍光色素とを共に含有し、共鳴エネルギー遷移現象によって励起波長と蛍光波長の差異を1種類の前記蛍光色素の場合よりも広げた蛍光粒子を用い、
前記標識試薬と結合された前記標的物質を含有する溶液が親水性のメンブレン中を移動し、該メンブレン内に作製した前記抗体固定部位に前記標識試薬を集積させ、集積した前記標識試薬を蛍光発色により可視化させるに当たり、
前記高輝度LEDからの励起光を、励起光を前記標的物質に結合した標識試薬を含む試料に照射し、蛍光試薬の共鳴エネルギー遷移現象によって生じる励起波長と蛍光検出波長のストークスシフトによる蛍光の励起光との色相変化を利用して、前記フィルタを介して試料からの蛍光を観察することを特徴とするイムノクロマト法を用いた標的物質の検出装置セット。
本発明において、「高輝度LED」とは、光度が8000mcd以上、好ましくは14000mcd以上の発光ダイオードを意味する。
本実施態様において、フルオレセイン色素もしくはその誘導体の濃度は1.5〜4.5μmol/gが好ましく、2.5〜3.5μmol/gがさらに好ましい。ここでは濃度をシリカコロイドの乾燥重量に対して規定している。ローダミン6G色素の濃度についても同様である。これよりも色素濃度が高いと濃度消光によって蛍光強度が低下してしまい、逆に低いと色素の不足により蛍光強度が低下してしまう。このことは直接蛍光を放出する受容色素だけでなく光の吸収を担う供与色素についても言える。供与色素同士でのエネルギー遷移もまた非発光過程であるエネルギーの散逸につながり、濃度消光と同じような状況を引き起こすからである。
本実施態様において、ローダミン6G色素もしくはその誘導体の濃度は1.5〜4.5μmol/gが好ましく、2.5〜3.5μmol/gがさらに好ましい。前述したその他の色素群の濃度についても同様である。
前記蛍光粒子を表面修飾する前記標的生体分子を分子認識する物質としては、抗体、抗原、ペプチド、DNA、RNA、糖鎖、リガンド、受容体、化学物質等が挙げられる。
ここで、分子認識とは、(1)DNA分子間又はDNA−RNA分子間のハイブリダイゼーション、(2)抗原抗体反応、(3)酵素(受容体)−基質(リガンド)間の反応など、生体分子間の特異的相互作用をいう。
また化学物質とは天然有機化合物に限らず、人工的に合成された生理活性を有する化合物や環境ホルモン等を含む。
すなわち、前記シリカナノ粒子を表面修飾した標的生体分子を分子認識する物質は、それ自体が受容体部位となって、例えば抗原−抗体反応、ビオチン−アビジン反応、塩基配列の相補性を利用したハイブリダイゼーションなどの特異的な分子認識を利用して、標的生体分子に特異的に結合することができる。
蛍光粒子への前記生体分子による吸着等の表面修飾が、縮合剤ないしは架橋剤の存在下又は非存在下にて、前記積層構造のシリカナノ粒子のコロイドと前記生体分子の溶液とを混合することにより行われることが好ましい。
例えば、縮合剤等の非存在下、前記蛍光粒子分散溶液と前記生体分子の溶液とを混合することにより、前記生体分子を前記蛍光粒子の表面に吸着させることができる。
表面修飾に用いる前記縮合剤ないしは架橋剤の当量数、前記コロイドの分散媒、前記生体分子の溶液の溶媒の種類・容量、及び反応温度等の反応条件については表面修飾が進行する限り特に制限はない。
前記表面修飾した後、前記蛍光粒子と前記蛍光粒子に結合ないし吸着していない前記生体分子との分離は、遠心分離または限外ろ過によって可能である。
前記生体分子により前記蛍光粒子を表面修飾した後は、前述の非特異的吸着をさらに防止する観点から、PEG、BSAなどの任意のブロッキング剤でブロッキング処理を施してもよい。
前記生体分子の表面修飾が出来たかどうかの確認は、混合液から遠心分離または限外ろ過で粒子を除去した溶液に含まれる前記生体分子を一般的なタンパク質定量法(例えば、UV法、Lowry法、Bradford法)で定量し、減少した前記生体分子の量を定量することで行うことができる。
本発明の方法は、特定の抗体と結合する性質を有する前記蛍光標識試薬と結合された前記標的物質を含有する溶液が親水性のメンブレン中を移動し、該メンブレン内に作製した前記抗体固定部位に前記蛍光標識試薬を集積させ、蛍光発色させる標的物質の検出方法、特に、標的物質の検出に関して陽性又は陰性を判定するイムノクロマト法に好適に用いることができる。
図6に示す装置では、一つの側面にのぞき窓1を設けてある。以降、のぞき窓1を有する面を装置の「前面」と呼ぶことがある。のぞき窓1は、図示されるように前面の1部分に設けるものに限定されず、例えば、前面のみ透明なプラスチック製の外箱を作製することに設けられたものでもよい。
また、図示された装置では、上面と側面下部にそれぞれ穴2および穴3を開けた。側面下部の穴3は、蛍光試薬を含有するイムノクロマト検査用メンブレンなどの試料を挿入し、試料保持部材の試料保持台4に搭載するためのもので、外界の光が隙間から装置内部に入り込まないように穴3の大きさをぎりぎりまで小さくする、内部に中空形状のガイドを設けてその内壁で侵入してくる光を吸収させることが好ましい。検査する試料の大きさや形状が決まっているのであれば、試料のガイドや板バネなどの押さえ機構5を設けるとより使いやすく好ましい。穴3によって試料が十分に固定されるものであれば、穴3を試料保持部材として用いることができる。
また、のぞき窓1は透明プラスチック板の裏側に、オレンジ色の色フィルムを貼り付けてある。
LED8は外部の駆動装置(図示せず)で発光させるが、簡単な電子回路基板と乾電池を取り付ければLED8を一定電流で自家発光させることも可能である。
のぞき窓の大きさは試料が見える程度の大きさでよく、大きいほど外界から蛍光波長近傍の光が進入しやすくなる。のぞき窓の上部と下部に光を透過させない黒いシートを貼り付けてその面積を制限することが好ましい。
縦4cm、横8cm、高さ6cmで前面のみ透明なプラスチック製の箱を用意し、上面と側面下部に穴を開けた。側面下部の穴は蛍光試薬を含有するイムノクロマト検査用メンブレンなどの試料を挿入するためのものである。
上面の穴には箱の内側に透明なプラスチック製のカバーを取り付け、その先に緑色のプラスチックシート(有限会社マルシン;プラスチック板E−6)を貼り付けた。この穴の上から砲弾型の高輝度緑色LED(豊田合成;E1L51−3G)を箱の内部に差し込んで、蛍光観察用の励起光源とした。
また、箱の上面から赤色LED(OptoSupply社;OSHR5111A−TU)を箱の内部に差し込んで、照明用の光源とした。
本実施例の装置では、LEDは外部の駆動装置(Ship Electric Co., Ltd製)で発光させた。
のぞき窓である前面の透明プラスチック板の裏側に、オレンジ色の色フィルム(東京舞台照明;ポリカラーNo.31)を2枚重ねて貼り付けた。
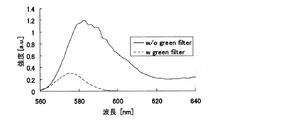
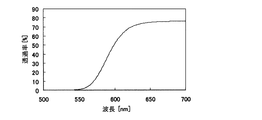
図1において蛍光試薬の蛍光波長として想定している580nm近傍の長波長成分が緑色プラスチックシートによって、図2に示されるように低減させられることが分かる。
しかしこの装置では励起光の長波長成分は前述の緑色プラスチックシートでカットされているため、のぞき窓から装置の外部に漏洩してくる励起光はごくわずかである。したがって、励起光に邪魔されることなく蛍光試薬からの蛍光のみを肉眼で認知することができる。
カルボキシTAMRA色素とカルボキシローダミン6G色素をシリカ粒子内部に共含有させ、前者を受容色素として、後者を供与色素として用いるFRET蛍光特性を持つシリカコロイドを合成した。
シリカ粒子内部に色素を含有させるには、まず色素分子のカルボキシル基をAPS分子のアミノ基と結合させ、APSをシリカの原料となるTEOSと共に合成溶液中に添加すればシロキサン結合によりシリカに取り込んだ。カルボキシル基の先にNHS基を持つ色素のスクシンイミドエステルをDMFまたはDMSOの溶媒中に分散させ、APSを混合して室温(25℃)で1時間撹拌し、APS結合色素分子を得た。前述2色素のスクシンイミドエステルは、Invitrogen社から購入した。
色素の添加量としては、色素濃度が濃くなりすぎると同一色素間でのFRETにより非発光過程で散逸するエネルギーの比率が増大してしまうので、それぞれの色素が単独で含有されているときに蛍光強度が最大となる濃度になるように、両APS結合色素の1.0mMに調整したDMF溶液を個別に用意し、対TEOSの体積比でカルボキシTAMRA色素溶液を30%分、カルボキシローダミン6G色素溶液を50%分添加した。合成は、50℃で4時間、その後室温(25℃)に冷まして20時間かけて行った。合成後の洗浄処理については、反応終了後、遠心分離(15000×g)を30分行い、粒子を沈降させた後、直ちに上清液を除去した。得られた沈殿物をエタノールに再分散させ、再度遠心分離(15000×g)を30分行い、粒子を沈降させた。同様のエタノール洗浄操作をさらに1回繰り返し、未反応のTEOS等を除去した。さらにエタノールの代わりに蒸留水を用いた以外は同様な洗浄操作を4回行い、遊離色素等を除去した。
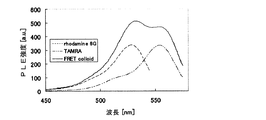
合成されたシリカコロイドのPLEスペクトル測定結果を図4に示す。ここでPLEスペクトルとは、励起波長を連続的に変化させたときに得られる固定された特定波長での蛍光強度である。逆に、固定された特定波長で励起したときに得られる蛍光強度の波長特性がPLスペクトルである。図4において、実線がカルボキシTAMRA色素とカルボキシローダミン6G色素を共に含有するFRET蛍光特性を持つシリカコロイドのPLEスペクトル、破線がカルボキシローダミン6G色素のスペクトルのみを含有するシリカコロイドのPLEスペクトル、二点鎖線がカルボキシTAMRA色素のみを含有するシリカコロイドのPLEスペクトルであり、横軸は波長(nm)、縦軸はPLE強度(a.u.)である。図4に示されるように、FRET蛍光特性を持つシリカコロイドのPLEスペクトルは、受容色素であるカルボキシTAMRA色素のみを含有させた場合に見られるスペクトルに供給色素であるカルボキシローダミン6G色素のスペクトルを足し合わせたような形となった。
カルボキシローダミン6GとBODIPY−FL色素をシリカ粒子内部に共含有させ、前者を受容色素として、後者を供与色素として用いるFRET蛍光特性を持つシリカコロイドを合成した。BODIPY−FL色素のスクシンイミドエステルをInvitrogen社から購入し、実施例2と同様の調製を行った。色素のシリカ粒子取り込み方法およびシリカコロイドの合成法も実施例2と同様に行った。
505nm近傍の波長で励起しても、このシリカコロイドの最適励起波長である530nmの光で励起した場合と遜色ない蛍光強度が得られることがわかる。この場合、蛍光強度は550nmで検出しているため、505nm(青緑LEDの発光ピーク波長)で励起した場合の実効的なストークス・シフトは45nmである。
遠沈管に50mMKH2PO4(pH7.5)を1mLと実施例2で作製したFRET蛍光特性を持つシリカコロイド粒子分散液(6.25mg/mL)8mLを加えて軽く撹拌した。遠沈管に抗hCG抗体(Anti−hCG clone codes/5008, Medix Biochemica社製)1mL(5mg/mL)を撹拌しながら加え、室温で1時間撹拌し、抗hCG抗体を前記シリカナノ粒子に吸着させた。
混合液を12000×gで15分間遠心分離し、上清を1mL程度残して取り除き、残した上清に沈殿を分散させた。この分散液に50mMKH2PO4(pH7.5)を20mL加え、再度遠心分離し上清を取り除き、これに50mMKH2PO4(pH7.5)を2mL加え、粒子を分散させた。
得られた抗体を吸着させてなるシリカナノ粒子分散液をGlass Fiber Conjugate Pad(GFCP、MILLIPORE社製)(8×150mm)1枚あたり、上記分散液0.8mLを均等に塗布した。デシケーター内で室温下、一夜減圧乾燥し、コンジュゲートパッドを作製した。
抗体固定化メンブレンの作製については、メンブレン(丈25mm、商品名Hi−Flow Plus120 メンブレン、MILLIPORE社製)の中央付近(端から約12mm)に幅約1mmのテストラインとして抗hCG抗体(alpha subunit of FSH(LH), clone code/6601、Medix Biochemica社製)が1mg/mL含まれる溶液((50mMKH2PO4,pH7.0)+5%スクロース)を0.75μL/cmの塗布量で塗布した。
続いて、幅約1mmのコントロールラインとして抗IgG抗体(Anti Mouse IgG、Dako社製)が1mg/mL含まれる溶液((50mMKH2PO4,pH7.0)シュガー・フリー)を0.75μL/cmの塗布量で塗布し、50℃で30分乾燥させた。
次に、ブロッキング処理として前記メンブレン全体をブロッキングバッファー中に室温で30分浸した。
前記得られたメンブレン、前記得られたコンジュゲートパッド、サンプルパッド(Glass Fiber Conjugate Pad(GFCP)、MILLIPORE社製)、吸収パッド(Cellulose Fiber Sample Pad(CFSP)(MILLIPORE社製)をバッキングシート(商品名AR9020,Adhesives Research社製)上で組み立て、5mm幅、長さ60mmのストリップ状に切断し、テストストリップを得た。
なお、各構成部材は、各々その両端を隣接する部材と2mm程度重ね合わせて貼付した(以下、同様である。)。
50IU/LのリコンビナントhCG(ロート製薬社製)を前記ストリップのサンプルパッド部分に100μL滴下し、五分間放置し実施例1で作製した装置で検出したところ、抗hCG抗体(alpha subunit of FSH(LH), clone code/6601、Medix Biochemica社製)を塗布したライン(テストライン)および、抗IgG抗体を塗布したライン(コントロールライン)の発光が肉眼で確認でき標的物質hCGの存在を確認した。
2,3 穴
4 試料保持台
5 押さえ機構
6 透明プラスチック製のカバー
7 緑色のプラスチックシート
8 高輝度緑色LED
9 赤色LED
Claims (13)
- 特定の抗体と結合する性質を有する標識試薬と、前記抗体を固定する抗体固定部位を有する親水性のメンブレンとを用いたイムノクロマト法による標的物質の検出方法であって、
前記標識試薬と結合された前記標的物質を含有する溶液が親水性のメンブレン中を移動し、該メンブレン内に作製した前記抗体固定部位に前記標識試薬を集積させ、集積した前記標識試薬を蛍光発色により可視化させるに当たり、
前記標識試薬として、蛍光粒子の母体の主成分がシリカである粒子中に、1種または2種以上の有機色素と、該有機色素よりも励起波長の長い有機蛍光色素とを共に含有し、共鳴エネルギー遷移現象によって励起波長と蛍光波長の差異を1種類の前記蛍光色素の場合よりも広げた蛍光粒子を用い、
高輝度LEDからの励起光を、励起光の長波長成分をカットする光フィルタを介して前記標的物質に結合した標識試薬を含む試料に照射し、蛍光試薬の共鳴エネルギー遷移現象によって生じる励起波長と蛍光検出波長のストークスシフトによる蛍光の励起光との色相変化を利用して試料からの蛍光を観察することを特徴とするイムノクロマト法を用いた標的物質の検出方法。 - 特定の抗体と結合する性質を有する標識試薬と、前記抗体を固定する抗体固定部位を有する親水性のメンブレンとを用いたイムノクロマト法による標的物質の検出方法であって、
前記標識試薬と結合された前記標的物質を含有する溶液が親水性のメンブレン中を移動し、該メンブレン内に作製した前記抗体固定部位に前記標識試薬を集積させ、集積した前記標識試薬を蛍光発色により可視化させるに当たり、
前記標識試薬として、蛍光粒子の母体の主成分がシリカである粒子中に、1種または2種以上の有機色素と、該有機色素よりも励起波長の長い有機蛍光色素とを共に含有し、共鳴エネルギー遷移現象によって励起波長と蛍光波長の差異を1種類の前記蛍光色素の場合よりも広げた蛍光粒子を用い、
高輝度LEDからの励起光を、励起光を前記標的物質に結合した標識試薬を含む試料に照射し、蛍光試薬の共鳴エネルギー遷移現象によって生じる励起波長と蛍光検出波長のストークスシフトによる蛍光の励起光との色相変化を利用して、励起光をカットする蛍光側のフィルタを介して試料からの蛍光を観察することを特徴とするイムノクロマト法を用いた標的物質の検出方法。 - 前記蛍光粒子としてフルオレセイン色素とローダミン6G色素を共に含有する水分散性のコロイド粒子であって、青緑色の励起光を吸収して緑色の蛍光を放つ蛍光粒子を用いることを特徴とする請求項1または2に記載のイムノクロマト法を用いた標的物質の検出方法。
- 前記蛍光粒子として、ローダミン6G色素と、テトラメチルローダミン色素、ローダミンB色素、およびX−ローダミン色素からなる群から選ばれる1種または2種以上の色素とを共に含有する水分散性のコロイド粒子であって、緑色の励起光を吸収して黄色もしくは赤色の蛍光を放つ蛍光粒子を用いることを特徴とする請求項1または2に記載のイムノクロマト法を用いた標的物質の検出方法。
- 前記蛍光粒子として、カルボキシローダミン6GとTAMRA色素とを共に含有するシリカコロイドの粒子を用いることを特徴とする請求項1または2に記載のイムノクロマト法を用いた標的物質の検出方法。
- 前記蛍光粒子として、カルボキシローダミン6GとBODIPY−FL色素とを共に含有するシリカコロイドの粒子を用いることを特徴とする請求項1または2に記載のイムノクロマト法を用いた標的物質の検出方法。
- アミノ基と反応するNHS基を持つカルボキシ色素と3−アミノプロピルトリエトキシシラン(APS)を結合させ、それをシランカップリング剤と混合してシリカコロイドを合成し、シリカコロイド内部に色素を固定したことを特徴とする請求項1〜6のいずれか1項に記載のイムノクロマト法を用いた標的物質の検出方法。
- 前記蛍光粒子が、抗体、抗原、ペプチド、DNA、RNA、糖鎖、リガンド、受容体、また化学物質で表面修飾された請求項1〜7のいずれか1項に記載のイムノクロマト法を用いた標的物質の検出方法。
- 赤色LEDを照明光源として用いることを特徴とする請求項1〜8のいずれか1項に記載のイムノクロマト法を用いた標的物質の検出方法。
- 励起光の長波長成分をカットする光フィルタが緑色のフィルタである請求項1及び3〜9のいずれか1項に記載のイムノクロマト法を用いた標的物質の検出方法。
- 励起光をカットする光フィルタがオレンジ色のフィルタである請求項2〜9のいずれか1項に記載のイムノクロマト法を用いた標的物質の検出方法。
- 特定の抗体と結合する性質を有する標識試薬および前記抗体を固定する抗体固定部位を有する親水性のメンブレンと検出装置とを備えたイムノクロマト法による標的物質の検出装置セットであって、
前記検出装置は、高輝度LEDと、当該高輝度LEDからの励起光の長波長成分をカットする光フィルタを有し、 前記標識試薬として、蛍光粒子の母体の主成分がシリカである粒子中に、1種または2種以上の有機色素と、該有機色素よりも励起波長の長い有機蛍光色素とを共に含有し、共鳴エネルギー遷移現象によって励起波長と蛍光波長の差異を1種類の前記蛍光色素の場合よりも広げた蛍光粒子を用い、
前記標識試薬と結合された前記標的物質を含有する溶液が親水性のメンブレン中を移動し、該メンブレン内に作製した前記抗体固定部位に前記標識試薬を集積させ、集積した前記標識試薬を蛍光発色により可視化させるに当たり、
前記高輝度LEDからの励起光を、前記光フィルタを介して前記標的物質に結合した標識試薬を含む試料に照射し、共鳴エネルギー遷移現象による蛍光試薬の励起波長と蛍光検出波長のストークスシフトによる蛍光の励起光との色相変化を利用して試料からの蛍光を観察することを特徴とするイムノクロマト法を用いた標的物質の検出装置セット。 - 特定の抗体と結合する性質を有する標識試薬および前記抗体を固定する抗体固定部位を有する親水性のメンブレンと検出装置とを備えたイムノクロマト法による標的物質の検出装置セットであって、
前記検出装置は、高輝度LEDと、当該高輝度LEDからの励起光をカットする蛍光を観察する側に配したフィルタを有し、前記標識試薬として、蛍光粒子の母体の主成分がシリカである粒子中に、1種または2種以上の有機色素と、該有機色素よりも励起波長の長い有機蛍光色素とを共に含有し、共鳴エネルギー遷移現象によって励起波長と蛍光波長の差異を1種類の前記蛍光色素の場合よりも広げた蛍光粒子を用い、
前記標識試薬と結合された前記標的物質を含有する溶液が親水性のメンブレン中を移動し、該メンブレン内に作製した前記抗体固定部位に前記標識試薬を集積させ、集積した前記標識試薬を蛍光発色により可視化させるに当たり、
前記高輝度LEDからの励起光を、励起光を前記標的物質に結合した標識試薬を含む試料に照射し、蛍光試薬の共鳴エネルギー遷移現象によって生じる励起波長と蛍光検出波長のストークスシフトによる蛍光の励起光との色相変化を利用して、前記フィルタを介して試料からの蛍光を観察することを特徴とするイムノクロマト法を用いた標的物質の検出装置セット。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013133073A JP5697059B2 (ja) | 2013-06-25 | 2013-06-25 | イムノクロマト法を用いた標的物質の検出方法および検出装置セット |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013133073A JP5697059B2 (ja) | 2013-06-25 | 2013-06-25 | イムノクロマト法を用いた標的物質の検出方法および検出装置セット |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008157182A Division JP5306714B2 (ja) | 2008-06-16 | 2008-06-16 | イムノクロマト法を用いた標的物質の検出方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2013200316A true JP2013200316A (ja) | 2013-10-03 |
| JP5697059B2 JP5697059B2 (ja) | 2015-04-08 |
Family
ID=49520644
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013133073A Expired - Fee Related JP5697059B2 (ja) | 2013-06-25 | 2013-06-25 | イムノクロマト法を用いた標的物質の検出方法および検出装置セット |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5697059B2 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3324174A4 (en) * | 2015-07-13 | 2019-03-06 | Sony Corporation | PROCESS FOR IMPROVING LIGHT EMISSION, METHOD FOR DETECTING SUBSTANCES, DEVICE FOR DETECTING SUBSTANCES AND LIGHT EMISSION AMPLIFIERS |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH05256763A (ja) * | 1992-03-12 | 1993-10-05 | Aisin Seiki Co Ltd | 蛍光物質検出用光照明装置 |
| JPH08503994A (ja) * | 1993-09-24 | 1996-04-30 | バイオサイト・ダイアグノスティックス・インコーポレイテッド | 新規化合物を用いた粒子内における蛍光エネルギー伝達および分子内エネルギー伝達 |
| JP2008505635A (ja) * | 2004-07-07 | 2008-02-28 | 独立行政法人農業生物資源研究所 | 核酸を配列特異的に標識する方法、およびそれを利用した新規核酸検出法 |
-
2013
- 2013-06-25 JP JP2013133073A patent/JP5697059B2/ja not_active Expired - Fee Related
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH05256763A (ja) * | 1992-03-12 | 1993-10-05 | Aisin Seiki Co Ltd | 蛍光物質検出用光照明装置 |
| JPH08503994A (ja) * | 1993-09-24 | 1996-04-30 | バイオサイト・ダイアグノスティックス・インコーポレイテッド | 新規化合物を用いた粒子内における蛍光エネルギー伝達および分子内エネルギー伝達 |
| JP2008505635A (ja) * | 2004-07-07 | 2008-02-28 | 独立行政法人農業生物資源研究所 | 核酸を配列特異的に標識する方法、およびそれを利用した新規核酸検出法 |
Non-Patent Citations (1)
| Title |
|---|
| JPN6012066290; 会澤英樹 等: '診断試薬用シリカナノ粒子の開発' 古河電工時報 No.121, 200803, 17-22 * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3324174A4 (en) * | 2015-07-13 | 2019-03-06 | Sony Corporation | PROCESS FOR IMPROVING LIGHT EMISSION, METHOD FOR DETECTING SUBSTANCES, DEVICE FOR DETECTING SUBSTANCES AND LIGHT EMISSION AMPLIFIERS |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5697059B2 (ja) | 2015-04-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5306714B2 (ja) | イムノクロマト法を用いた標的物質の検出方法 | |
| Gorris et al. | Perspectives and challenges of photon-upconversion nanoparticles-Part II: bioanalytical applications | |
| JP6128153B2 (ja) | 組織染色方法および生体物質検出方法 | |
| CN114761517B (zh) | 长余辉发光有机微球、其制备方法和应用 | |
| JP5812095B2 (ja) | 生体物質検出方法 | |
| US20140170674A1 (en) | Membraine-Based Assay Devices Utilizing Time-Resolved Up-Converting Luminescence | |
| JP6096779B2 (ja) | 光フィルタを有する分析デバイスおよび分析方法 | |
| US9726605B2 (en) | Fluorescence immuno-chromatography, kit and test strip for the same | |
| US20060245971A1 (en) | Photoluminescent silica-based sensors and methods of use | |
| CN114846329B (zh) | 长余辉发光的苯乙烯聚合物微球、其制备方法和应用 | |
| WO2012029752A1 (ja) | 生体物質検出方法 | |
| JP2022062284A (ja) | フェリチン検出用の検査キット及びフェリチンの検出方法 | |
| CN113125420B (zh) | 基于化学发光的多元分析光子晶体芯片及其制备方法和应用 | |
| JP5810195B1 (ja) | 紫外励起蛍光粒子、これを用いた検出方法、画像表示方法、画像表示スクリーンおよび画像表示装置 | |
| WO2011077838A1 (ja) | 蛍光物質内包シリカナノ粒子及び生体物質標識剤 | |
| US7842505B2 (en) | Fluorescent labeling reagent | |
| Schäferling et al. | Luminescent nanoparticles for chemical sensing and imaging | |
| JP5697059B2 (ja) | イムノクロマト法を用いた標的物質の検出方法および検出装置セット | |
| JP5540867B2 (ja) | 有機蛍光色素内包シリカナノ粒子、その製造方法、それを用いた生体物質標識剤 | |
| CN112924686A (zh) | 用于检测血清淀粉样蛋白a的免疫层析试纸条及其制备与检测方法 | |
| CN107421938B (zh) | 一种检测孔雀石绿的SiO2@ROX纳米粒子荧光探针阵列的制备方法 | |
| Diriwari | Resonance energy transfer within and to optical nanoparticles for bioimaging and biosensing applications | |
| Gupta | Towards the development of robust semiconducting polymer dots for applications in bioanalysis and imaging | |
| Tran | Development and evaluation of luminescent nanoparticles for immunolabeling and imaging via microscopy and smartphone-based devices |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20130701 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20130828 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20140430 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140507 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20140707 Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140707 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20150106 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20150203 |
|
| R151 | Written notification of patent or utility model registration |
Ref document number: 5697059 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R151 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| LAPS | Cancellation because of no payment of annual fees |