JP2014005247A - イリジウム錯体化合物、有機電界発光素子、有機el表示装置及び有機el照明 - Google Patents
イリジウム錯体化合物、有機電界発光素子、有機el表示装置及び有機el照明 Download PDFInfo
- Publication number
- JP2014005247A JP2014005247A JP2012143238A JP2012143238A JP2014005247A JP 2014005247 A JP2014005247 A JP 2014005247A JP 2012143238 A JP2012143238 A JP 2012143238A JP 2012143238 A JP2012143238 A JP 2012143238A JP 2014005247 A JP2014005247 A JP 2014005247A
- Authority
- JP
- Japan
- Prior art keywords
- group
- carbon atoms
- ring
- organic
- iridium complex
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Landscapes
- Electroluminescent Light Sources (AREA)
Abstract
【課題】イリジウム錯体化合物の構造と安定性の関係性を明らかとし、イリジウム錯体化合物の安定性向上ための分子設計指針を開発し、さらにその指針を用いて耐久性が高いイリジウム錯体化合物を提供する。また、耐久性が高い有機電界発光素子、並びに該有機電界素子を用いた有機EL表示装置及び有機EL照明を提供する。
【解決手段】アニオン電荷分布において、C2原子のスピン分布値(NBO population)が0.21より大きく、0.5未満であることを特徴とする、イリジウム錯体化合物。
{R1、R2は、水素原子、フッ素、塩素、臭素、炭素数1〜20のアルキル基、アルコキシ基、トリアルキルシリル基(但し、アルキルの炭素数は1〜20)、アルキルカルボニル基、アリールカルボニル基、アルキルアミノ基、アリールアミノ基、および炭素数6〜20のアリール基から選択される。Lは有機配位子であり、nは1から3。}
【選択図】なし
【解決手段】アニオン電荷分布において、C2原子のスピン分布値(NBO population)が0.21より大きく、0.5未満であることを特徴とする、イリジウム錯体化合物。
{R1、R2は、水素原子、フッ素、塩素、臭素、炭素数1〜20のアルキル基、アルコキシ基、トリアルキルシリル基(但し、アルキルの炭素数は1〜20)、アルキルカルボニル基、アリールカルボニル基、アルキルアミノ基、アリールアミノ基、および炭素数6〜20のアリール基から選択される。Lは有機配位子であり、nは1から3。}
【選択図】なし
Description
本発明はイリジウム錯体化合物に関し、特に、有機電界発光素子の発光層の材料として有用なイリジウム錯体化合物、該化合物を含有する有機電界発光素子、該有機電界発光素子を含む有機EL表示装置及び有機EL照明に関する。
近年、有機EL照明や有機ELディスプレイなど、有機電界発光素子(以下、「有機EL素子」と称す。)を利用する各種電子デバイスが実用化されつつある。有機EL素子は、印加電圧が低く消費電力が小さく、面発光であり、三原色発光も可能であることから、照明やディスプレイへの適用が盛んに検討されている。そのためにも発光効率の改善が求められる。発光効率の改善としては、例えば、有機EL素子の発光層に燐光発光材料を利用することが提案されている。燐光発光材料としては、例えば、ビス(2−フェニルピリジナト−N,C2’)イリジウムアセチルアセトナート(Irppy2(acac))や
、トリス(2−フェニルピリジナト−N,C2’)(Ir(ppy)3)イリジウムをはじめとしたオルソメタル化イリジウム錯体が広く知られている。
、トリス(2−フェニルピリジナト−N,C2’)(Ir(ppy)3)イリジウムをはじめとしたオルソメタル化イリジウム錯体が広く知られている。
このような燐光発光材料を使用して、有機EL素子が成膜し、層を形成することは可能である。さらに塗布成膜法を用いることで、容易に大型かつ安定した有機EL素子膜を作成できるため、有機EL素子材料がディスプレイや照明装置の量産化や大型デバイスへの適用が期待されている。
一方、耐久性において、有機EL素子材料が現在広く使われている液晶ディスプレイ材料や蛍光体照明装置に比べ、大きく劣っている。例えば、一般的に液晶ディスプレイ材料として要求される材料のHalf timeは初期輝度が1000cd/m2条件のときに60000〜100000hr
である。それに対して、塗布法により成膜した有機EL素子材料のhalf timeは、初期輝
度が1000cd/m2条件のときに約15000hr程度である(非特許文献1参照)。
一方、耐久性において、有機EL素子材料が現在広く使われている液晶ディスプレイ材料や蛍光体照明装置に比べ、大きく劣っている。例えば、一般的に液晶ディスプレイ材料として要求される材料のHalf timeは初期輝度が1000cd/m2条件のときに60000〜100000hr
である。それに対して、塗布法により成膜した有機EL素子材料のhalf timeは、初期輝
度が1000cd/m2条件のときに約15000hr程度である(非特許文献1参照)。
有機EL素子材料の耐久性を影響する原因として、各層で使用される材料に電荷(正孔と電子)がトラップする大きさが素子の劣化に大きな影響を与えているという報告がある(非特許文献2〜4)。その影響を小さくするために、各層材料のIP、Ea、移動度を調節することで、正孔と電子の移動をコントロールし、材料にトラップされる電荷量を小さくすることができると報告されている。また材料の電荷バランスを調節することによって、素子の耐久性を向上することができると報告されている。
また、非特許文献5及び6によれば、塗布型有機EL素子膜が通電された後、発光層に含まれるイリジウム錯体化合物が最も劣化することが分かっている。前記文献によれば、イリジウム錯体化合物のリガンド分子が錯体から外れることを示唆されているが、どのような分子構造によりイリジウム錯体化合物の安定性を向上できるかについては、記載も示唆もされていない。
以上、イリジウム錯体化合物に関し、分子自身の耐久性という点からは未だ検討が不十分であり、耐久性の高い有機電界発光素子を提供できる状況には至っていない。
以上、イリジウム錯体化合物に関し、分子自身の耐久性という点からは未だ検討が不十分であり、耐久性の高い有機電界発光素子を提供できる状況には至っていない。
インターネット<URL:<http://www.universaldisplay.com/default.asp?contentID=606>>
IEEE. 8(2)., 362-371 (2002)
J. Appl. Phys. 104., 084520 (2008)
Adv. Mater. 22., 3762-3777 (2010)
Org. Electron. 12., 341-347 (2011)
J. Appl. Phys. 104., 014510 (2008)
本発明は、上記課題を鑑みてなされたものであり、イリジウム錯体化合物の構造と安定性の関係性を明らかとし、イリジウム錯体化合物の安定性向上ための分子設計指針を開発し、さらにその指針を用いて耐久性が高いイリジウム錯体化合物を提供することを課題とする。また、本発明は耐久性が高い有機電界発光素子、並びに該有機電界素子を用いた有機EL表示装置及び有機EL照明を提供することを課題とする。
本発明者らは、上記課題に鑑み、イリジウム錯体化合物として、燐光性発光材料の分子構造と耐久性の関係性について検討した結果、イリジウム錯体化合物のピリジン環部分に属し、且つフェニル基と結合している炭素原子(以下、C2原子と称す)のアニオン状態での 電荷(NBO population)が、化合物の耐久性とよい相関を示していることを見出した
。また、そのような化学構造を有するイリジウム錯体化合物が、有機電界発光素子が通電されるときに、電荷輸送による受けたダメージに対して、強い耐久性をあることを見出した。さらにそれを用いて作成される有機EL素子の耐久性が高いことを見出し、本発明を完成した。
。また、そのような化学構造を有するイリジウム錯体化合物が、有機電界発光素子が通電されるときに、電荷輸送による受けたダメージに対して、強い耐久性をあることを見出した。さらにそれを用いて作成される有機EL素子の耐久性が高いことを見出し、本発明を完成した。
即ち、本発明は、下記式(1)又は(2)で表されることを含むイリジウム錯体化合物であって、アニオン電荷分布において、C2原子のスピン分布値(NBO population) が0.21
より大きく、0.5未満であることを特徴とする、イリジウム錯体化合物、該イリジウム錯
体化合物を含む有機電界発光素子、該有機電界発光素子を用いる有機EL表示装置及び有機EL照明、である。
より大きく、0.5未満であることを特徴とする、イリジウム錯体化合物、該イリジウム錯
体化合物を含む有機電界発光素子、該有機電界発光素子を用いる有機EL表示装置及び有機EL照明、である。
{式(1)において、R1、R2はそれぞれ同一または異なり、水素原子、フッ素、塩素、臭素、炭素数1〜20のアルキル基、炭素数1〜20のアルコキシ基、トリアルキルシリル基(但し、アルキルの炭素数は1〜20)、炭素数1〜20のアルキルカルボニル基、炭素数1〜20のアリールカルボニル基、炭素数1〜20のアルキルアミノ基、炭素数1〜20のアリールアミノ基、炭素数6〜20のアリール基から選択される。
Lは有機配位子であり、nは1〜3の整数を示す。}
Lは有機配位子であり、nは1〜3の整数を示す。}
{式(2)において、Ar1およびAr2は、炭素数4〜20の芳香族炭化水素基または
炭素数3〜20の芳香族複素環基を示す。
これらの基はさらに、フッ素、塩素、臭素、炭素数1〜20のアルキル基、炭素数1〜20のアルコキシ基、トリアルキルシリル基(但し、アルキルの炭素数は1〜20)、炭素数1〜20のアルキルカルボニル基、炭素数1〜20のアリールカルボニル基、炭素数1〜20のアルキルアミノ基、炭素数1〜20のアリールアミノ基、炭素数6〜20のアリール基で置換されていてもよい。Lは有機配位子であり、nは1から3の整数を示す。
Zは下記式(3)で表される。
炭素数3〜20の芳香族複素環基を示す。
これらの基はさらに、フッ素、塩素、臭素、炭素数1〜20のアルキル基、炭素数1〜20のアルコキシ基、トリアルキルシリル基(但し、アルキルの炭素数は1〜20)、炭素数1〜20のアルキルカルボニル基、炭素数1〜20のアリールカルボニル基、炭素数1〜20のアルキルアミノ基、炭素数1〜20のアリールアミノ基、炭素数6〜20のアリール基で置換されていてもよい。Lは有機配位子であり、nは1から3の整数を示す。
Zは下記式(3)で表される。
〔Rはそれぞれの場合で同一または異なり、水素原子、フッ素、塩素、臭素、炭素数1〜20のアルキル基、炭素数1〜20のアルコキシ基、炭素数3〜20のアリール基から選ばれる。rは1〜20の整数を示す。〕}
本発明のイリジウム錯体化合物は、有機電界発光素子が通電されるときに、電荷輸送による受けたダメージに対して、強い耐久性を有する。更に、それを用いて作成される素子の駆動電圧が低く、発光効率が高い。よって、有機電界発光素子用材料として有用であり、当該イリジウム錯体化合物を用いて得られた有機電界発光素子は、発光効率が高く、低い電圧で駆動可能であるとともに駆動安定性が高く、有機EL表示装置及び有機EL照明用として有用である。
以下に、本発明の実施の形態を詳細に説明するが、本発明は以下の実施の形態に限定されるものではなく、その要旨の範囲内で種々に変形して実施することができる。
<イリジウム錯体化合物>
本発明は、下記式(1)又は下記式(2)で表されるイリジウム錯体化合物であって、アニオン電荷分布において、C2原子のスピン分布値(NBO population) が0.21より大きく
、0.5未満であることを特徴とするイリジウム錯体化合物である。
<イリジウム錯体化合物>
本発明は、下記式(1)又は下記式(2)で表されるイリジウム錯体化合物であって、アニオン電荷分布において、C2原子のスピン分布値(NBO population) が0.21より大きく
、0.5未満であることを特徴とするイリジウム錯体化合物である。
{式(1)において、R1、R2はそれぞれ同一または異なり、水素原子、フッ素、塩素、臭素、炭素数1〜20のアルキル基、炭素数1〜20のアルコキシ基、トリアルキルシリル基(但し、アルキルの炭素数は1〜20)、炭素数1〜20のアルキルカルボニル基、炭素数1〜20のアリールカルボニル基、炭素数1〜20のアルキルアミノ基、炭素数1〜20のアリールアミノ基、炭素数6〜20のアリール基から選択される。
Lは有機配位子であり、nは1〜3の整数を示す。}
Lは有機配位子であり、nは1〜3の整数を示す。}
<R1及びR2>
R1及びR2はそれぞれ同一または異なり、水素原子、フッ素、塩素、臭素、炭素数1〜20のアルキル基、炭素数1〜20のアルコキシ基、トリアルキルシリル基(但し、アルキルの炭素数は1〜20)、炭素数1〜20のアルキルカルボニル基、炭素数1〜20のアリールカルボニル基、炭素数1〜20のアルキルアミノ基、炭素数1〜20のアリールアミノ基、炭素数6〜20のアリール基から選択される。
R1及びR2はそれぞれ同一または異なり、水素原子、フッ素、塩素、臭素、炭素数1〜20のアルキル基、炭素数1〜20のアルコキシ基、トリアルキルシリル基(但し、アルキルの炭素数は1〜20)、炭素数1〜20のアルキルカルボニル基、炭素数1〜20のアリールカルボニル基、炭素数1〜20のアルキルアミノ基、炭素数1〜20のアリールアミノ基、炭素数6〜20のアリール基から選択される。
炭素数1〜20のアルキル基の具体例としては、直鎖のアルキル基および分岐のアルキル基、環状のアルキル基などであり、より具体的には、n−プロピル基、n−ブチル基、n−ペンチル基、n−ヘキシル基、n−オクチル基、イソプロピル基、イソブチル基、シクロヘキシル基などが挙げられる。
炭素数1〜20のアルコキシ基の具体例としては、メトキシ基、エトキシ基、プロピルオキシ基、イソプロピルオキシ基、ヘキシルオキシ基、シクロヘキシルオキシ基、オクタデシルオキシ基等が挙げられる。
炭素数1〜20のアルコキシ基の具体例としては、メトキシ基、エトキシ基、プロピルオキシ基、イソプロピルオキシ基、ヘキシルオキシ基、シクロヘキシルオキシ基、オクタデシルオキシ基等が挙げられる。
アルキル基の炭素数1〜20であるトリアルキルシリル基の具体例としては、トリメチルシリル基、トリエチルシリル基、トリ(n−ブチル)シリル基、t−ブチルジメチルシリル基、トリオクチルシリル基等が挙げられる。
炭素数1〜20のアルキルカルボニル基の具体例としては、アセチル基、プロピオニル基、ピバロイル基、カプロイル基、デカノイル基、シクロヘキシルカルボニル基等が挙げられる。
炭素数1〜20のアルキルカルボニル基の具体例としては、アセチル基、プロピオニル基、ピバロイル基、カプロイル基、デカノイル基、シクロヘキシルカルボニル基等が挙げられる。
炭素数1〜20のアリールカルボニル基の具体例としては、ベンゾイル基、ナフトイル基、アントライル基等が挙げられる。
炭素数1〜20のアルキルアミノ基の例として、メチルアミノ基、ジメチルアミノ基、ジエチルアミノ基、エチルメチルアミノ基、ジヘキシルアミノ基、ジオクチルアミノ基、ジシクロヘキシルアミノ基等が挙げられる。
炭素数1〜20のアルキルアミノ基の例として、メチルアミノ基、ジメチルアミノ基、ジエチルアミノ基、エチルメチルアミノ基、ジヘキシルアミノ基、ジオクチルアミノ基、ジシクロヘキシルアミノ基等が挙げられる。
炭素数1〜20のアリールアミノ基の例として、フェニルアミノ基、ジフェニルアミノ基、ジトリルアミノ基、ジ(2,6−ジメチルフェニル)アミノ基等が挙げられる。
炭素数3〜20のアリール基とは、1個の遊離原子価を有する、芳香族炭化水素基およ
び芳香族複素環基の両方を意味し、その具体例としては、1個の遊離原子価を有する、ベ
ンゼン環、ナフタレン環、アントラセン環、フェナントレン環、ペリレン環、テトラセン環、ピレン環、ベンズピレン環、クリセン環、トリフェニレン環、フルオランテン環、フ
ラン環、ベンゾフラン環、チオフェン環、ベンゾチオフェン環、ピロール環、ピラゾール環、イミダゾール環、オキサジアゾール環、インドール環、カルバゾール環、ピロロイミダゾール環、ピロロピラゾール環、ピロロピロール環、チエノピロール環、チエノチオフェン環、フロピロール環、フロフラン環、チエノフラン環、ベンゾイソオキサゾール環、ベンゾイソチアゾール環、ベンゾイミダゾール環、ピリジン環、ピラジン環、ピリダジン環、ピリミジン環、トリアジン環、キノリン環、イソキノリン環、シノリン環、キノキサリン環、ベンゾイミダゾール環、ペリミジン環、キナゾリン環、キナゾリノン環、アズレン環等の基が挙げられる。
炭素数3〜20のアリール基とは、1個の遊離原子価を有する、芳香族炭化水素基およ
び芳香族複素環基の両方を意味し、その具体例としては、1個の遊離原子価を有する、ベ
ンゼン環、ナフタレン環、アントラセン環、フェナントレン環、ペリレン環、テトラセン環、ピレン環、ベンズピレン環、クリセン環、トリフェニレン環、フルオランテン環、フ
ラン環、ベンゾフラン環、チオフェン環、ベンゾチオフェン環、ピロール環、ピラゾール環、イミダゾール環、オキサジアゾール環、インドール環、カルバゾール環、ピロロイミダゾール環、ピロロピラゾール環、ピロロピロール環、チエノピロール環、チエノチオフェン環、フロピロール環、フロフラン環、チエノフラン環、ベンゾイソオキサゾール環、ベンゾイソチアゾール環、ベンゾイミダゾール環、ピリジン環、ピラジン環、ピリダジン環、ピリミジン環、トリアジン環、キノリン環、イソキノリン環、シノリン環、キノキサリン環、ベンゾイミダゾール環、ペリミジン環、キナゾリン環、キナゾリノン環、アズレン環等の基が挙げられる。
ここで、本発明において、遊離原子価とは、有機化学・生化学命名法(上)(改定第2版、南江堂、1992年発行)に記載のとおり、他の遊離原子価と結合を形成できるものを言う。すなわち、例えば、「1個の遊離原子価を有するベンゼン環」はフェニル基のこ
とを言い、「2個の遊離原子価を有するベンゼン環」はフェニレン基のことを言う。
また、R1及びR2はそれらが隣接する炭素数3〜12のアルケニレン基で結合して環を形成しても良い。
とを言い、「2個の遊離原子価を有するベンゼン環」はフェニレン基のことを言う。
また、R1及びR2はそれらが隣接する炭素数3〜12のアルケニレン基で結合して環を形成しても良い。
<補助配位子L>
本発明におけるイリジウム錯体化合物における補助配位子Lには特に制限は無いが、好ましくは1価の2座配位子であり、より好ましくは下記化学式の中から選ばれる。2つの補助配位子Lが存在する場合には、補助配位子Lは互いに異なる構造であっても良い。
本発明におけるイリジウム錯体化合物における補助配位子Lには特に制限は無いが、好ましくは1価の2座配位子であり、より好ましくは下記化学式の中から選ばれる。2つの補助配位子Lが存在する場合には、補助配位子Lは互いに異なる構造であっても良い。
R31からR40はそれぞれ独立に、水素原子、炭素数1〜20のフッ素で置換されていても良いアルキル基、炭素数1〜20のアルキル基で置換されていても良いフェニル基またはハロゲンを示す。より好ましくは、R31とR33がメチル基またはt−ブチル基であり、R32およびR34からR38は水素原子であり、R39およびR40は炭素数1〜10のアルキル基である。
次に式(2)について説明する。
次に式(2)について説明する。
{式(2)において、Ar1およびAr2は、炭素数4〜20の芳香族炭化水素基または
炭素数3〜20の芳香族複素環基を示す。これらの基はさらに、フッ素、塩素、臭素、炭素数1〜20のアルキル基、炭素数1〜20のアルコキシ基、トリアルキルシリル基(但し、アルキルの炭素数は1〜20)、炭素数1〜20のアルキルカルボニル基、炭素数1〜20のアリールカルボニル基、炭素数1〜20のアルキルアミノ基、炭素数1〜20のアリールアミノ基、炭素数6〜20のアリール基で置換されていてもよい。Lは有機配位子であり、nは1から3の整数を示す。
Zは下記式(3)で表される。
炭素数3〜20の芳香族複素環基を示す。これらの基はさらに、フッ素、塩素、臭素、炭素数1〜20のアルキル基、炭素数1〜20のアルコキシ基、トリアルキルシリル基(但し、アルキルの炭素数は1〜20)、炭素数1〜20のアルキルカルボニル基、炭素数1〜20のアリールカルボニル基、炭素数1〜20のアルキルアミノ基、炭素数1〜20のアリールアミノ基、炭素数6〜20のアリール基で置換されていてもよい。Lは有機配位子であり、nは1から3の整数を示す。
Zは下記式(3)で表される。
〔Rはそれぞれの場合で同一または異なり、水素原子、フッ素、塩素、臭素、炭素数1〜20のアルキル基、炭素数1〜20のアルコキシ基、炭素数3〜20のアリール基から選ばれる。rは1から20の整数を示す。〕}
<Ar1およびAr2>
Ar1およびAr2において、芳香族炭化水素基は、溶剤への溶解性の観点から、通常炭素数4〜20の基が用いられる。中でも結合手の数の遊離原子価を有する、6員環の単環、又は2〜5縮合環の芳香族炭化水素基が好ましい。例えば、結合手の数の遊離原子価を有する、ベンゼン環、ナフタレン環、アントラセン環、フェナントレン環、ペリレン環、テトラセン環、ピレン環、ベンズピレン環、クリセン環、トリフェニレン環、フルオランテン環などの芳香族炭化水素基が挙げられる。
Ar1およびAr2において、芳香族炭化水素基は、溶剤への溶解性の観点から、通常炭素数4〜20の基が用いられる。中でも結合手の数の遊離原子価を有する、6員環の単環、又は2〜5縮合環の芳香族炭化水素基が好ましい。例えば、結合手の数の遊離原子価を有する、ベンゼン環、ナフタレン環、アントラセン環、フェナントレン環、ペリレン環、テトラセン環、ピレン環、ベンズピレン環、クリセン環、トリフェニレン環、フルオランテン環などの芳香族炭化水素基が挙げられる。
芳香族複素環基は、通常炭素数3〜20の基が用いられる。好ましくは4以上、さらに好ましくは5以上、また好ましくは12以下、さらに好ましくは8以下である。上記範囲内であると、有機溶剤に対する溶解性が良好であり、また熱処理時に酸化劣化し難いため好ましい。
具体的には、結合手の数の遊離原子価を有する、フラン環、ベンゾフラン環、チオフェン環、ベンゾチオフェン環、ピロール環、ピラゾール環、イミダゾール環、オキサジアゾール環、インドール環、カルバゾール環、ピロロイミダゾール環、ピロロピラゾール環、ピロロピロール環、チエノピロール環、チエノチオフェン環、フロピロール環、フロフラン環、チエノフラン環、ベンゾイソオキサゾール環、ベンゾイソチアゾール環、ベンゾイミダゾール環、ピリジン環、ピラジン環、ピリダジン環、ピリミジン環、トリアジン環、キノリン環、イソキノリン環、シノリン環、キノキサリン環、ベンゾイミダゾール環、ペ
リミジン環、キナゾリン環、キナゾリノン環、アズレン環などの芳香族複素環基が挙げられる。
具体的には、結合手の数の遊離原子価を有する、フラン環、ベンゾフラン環、チオフェン環、ベンゾチオフェン環、ピロール環、ピラゾール環、イミダゾール環、オキサジアゾール環、インドール環、カルバゾール環、ピロロイミダゾール環、ピロロピラゾール環、ピロロピロール環、チエノピロール環、チエノチオフェン環、フロピロール環、フロフラン環、チエノフラン環、ベンゾイソオキサゾール環、ベンゾイソチアゾール環、ベンゾイミダゾール環、ピリジン環、ピラジン環、ピリダジン環、ピリミジン環、トリアジン環、キノリン環、イソキノリン環、シノリン環、キノキサリン環、ベンゾイミダゾール環、ペ
リミジン環、キナゾリン環、キナゾリノン環、アズレン環などの芳香族複素環基が挙げられる。
これらの芳香族炭化水素基および芳香族複素環基はさらに、フッ素、塩素、臭素、炭素数1〜20のアルキル基、炭素数1〜20のアルコキシ基、アルキル基の炭素数1〜20であるトリアルキルシリル基、炭素数1〜20のアルキルカルボニル基、炭素数1〜20のアリールカルボニル基、炭素数1〜20のアルキルアミノ基、炭素数1〜20のアリールアミノ基、炭素数3〜20のアリール基で置換されていてもよい。
炭素数1〜20のアルキル基の具体例としては、直鎖のアルキル基および分岐のアルキル基、環状のアルキル基などであり、より具体的には、n−プロピル基、n−ブチル基、n−ペンチル基、n−ヘキシル基、n−オクチル基、イソプロピル基、イソブチル基、シクロヘキシル基などが挙げられる。
炭素数1〜20のアルコキシ基の具体例としては、メトキシ基、エトキシ基、プロピルオキシ基、イソプロピルオキシ基、ヘキシルオキシ基、シクロヘキシルオキシ基、オクタデシルオキシ基等が挙げられる。
炭素数1〜20のアルコキシ基の具体例としては、メトキシ基、エトキシ基、プロピルオキシ基、イソプロピルオキシ基、ヘキシルオキシ基、シクロヘキシルオキシ基、オクタデシルオキシ基等が挙げられる。
アルキル基の炭素数1〜20であるトリアルキルシリル基の具体例としては、トリメチルシリル基、トリエチルシリル基、トリ(n−ブチル)シリル基、t−ブチルジメチルシリル基、トリオクチルシリル基等が挙げられる。
炭素数1〜20のアルキルカルボニル基の具体例としては、アセチル基、プロピオニル基、ピバロイル基、カプロイル基、デカノイル基、シクロヘキシルカルボニル基等が挙げられる。
炭素数1〜20のアルキルカルボニル基の具体例としては、アセチル基、プロピオニル基、ピバロイル基、カプロイル基、デカノイル基、シクロヘキシルカルボニル基等が挙げられる。
炭素数1〜20のアリールカルボニル基の具体例としては、ベンゾイル基、ナフトイル基、アントライル基等が挙げられる。
炭素数1〜20のアルキルアミノ基の例として、メチルアミノ基、ジメチルアミノ基、ジエチルアミノ基、エチルメチルアミノ基、ジヘキシルアミノ基、ジオクチルアミノ基、ジシクロヘキシルアミノ基等が挙げられる。
炭素数1〜20のアルキルアミノ基の例として、メチルアミノ基、ジメチルアミノ基、ジエチルアミノ基、エチルメチルアミノ基、ジヘキシルアミノ基、ジオクチルアミノ基、ジシクロヘキシルアミノ基等が挙げられる。
炭素数1〜20のアリールアミノ基の例として、フェニルアミノ基、ジフェニルアミノ基、ジトリルアミノ基、ジ(2,6−ジメチルフェニル)アミノ基等が挙げられる。
炭素数3〜20のアリール基とは、1個の遊離原子価を有する、芳香族炭化水素基およ
び芳香族複素環基の両方を意味し、その具体例としては、1個の遊離原子価を有する、ベ
ンゼン環、ナフタレン環、アントラセン環、フェナントレン環、ペリレン環、テトラセン環、ピレン環、ベンズピレン環、クリセン環、トリフェニレン環、フルオランテン環、フラン環、ベンゾフラン環、チオフェン環、ベンゾチオフェン環、ピロール環、ピラゾール環、イミダゾール環、オキサジアゾール環、インドール環、カルバゾール環、ピロロイミダゾール環、ピロロピラゾール環、ピロロピロール環、チエノピロール環、チエノチオフェン環、フロピロール環、フロフラン環、チエノフラン環、ベンゾイソオキサゾール環、ベンゾイソチアゾール環、ベンゾイミダゾール環、ピリジン環、ピラジン環、ピリダジン環、ピリミジン環、トリアジン環、キノリン環、イソキノリン環、シノリン環、キノキサリン環、ベンゾイミダゾール環、ペリミジン環、キナゾリン環、キナゾリノン環、アズレン環等の基が挙げられる。
炭素数3〜20のアリール基とは、1個の遊離原子価を有する、芳香族炭化水素基およ
び芳香族複素環基の両方を意味し、その具体例としては、1個の遊離原子価を有する、ベ
ンゼン環、ナフタレン環、アントラセン環、フェナントレン環、ペリレン環、テトラセン環、ピレン環、ベンズピレン環、クリセン環、トリフェニレン環、フルオランテン環、フラン環、ベンゾフラン環、チオフェン環、ベンゾチオフェン環、ピロール環、ピラゾール環、イミダゾール環、オキサジアゾール環、インドール環、カルバゾール環、ピロロイミダゾール環、ピロロピラゾール環、ピロロピロール環、チエノピロール環、チエノチオフェン環、フロピロール環、フロフラン環、チエノフラン環、ベンゾイソオキサゾール環、ベンゾイソチアゾール環、ベンゾイミダゾール環、ピリジン環、ピラジン環、ピリダジン環、ピリミジン環、トリアジン環、キノリン環、イソキノリン環、シノリン環、キノキサリン環、ベンゾイミダゾール環、ペリミジン環、キナゾリン環、キナゾリノン環、アズレン環等の基が挙げられる。
<R1>
R1については、式(1)と同義である。
<R>
Rはそれぞれの場合で同一または異なり、水素原子、フッ素、塩素、臭素、炭素数1〜20のアルキル基、炭素数1〜20のアルコキシ基、炭素数3〜20のアリール基から選
ばれる。これらの具体例は<Ar1およびAr2>で挙げたものと同義である。
R1については、式(1)と同義である。
<R>
Rはそれぞれの場合で同一または異なり、水素原子、フッ素、塩素、臭素、炭素数1〜20のアルキル基、炭素数1〜20のアルコキシ基、炭素数3〜20のアリール基から選
ばれる。これらの具体例は<Ar1およびAr2>で挙げたものと同義である。
<分子量>
本発明の上記式(1)または(2)で表されるイリジウム錯体化合物の分子量は、通常850以上、好ましくは900以上、通常3000以下、好ましくは2000以下である。上記範囲内であると、錯体の安定性が良好である。
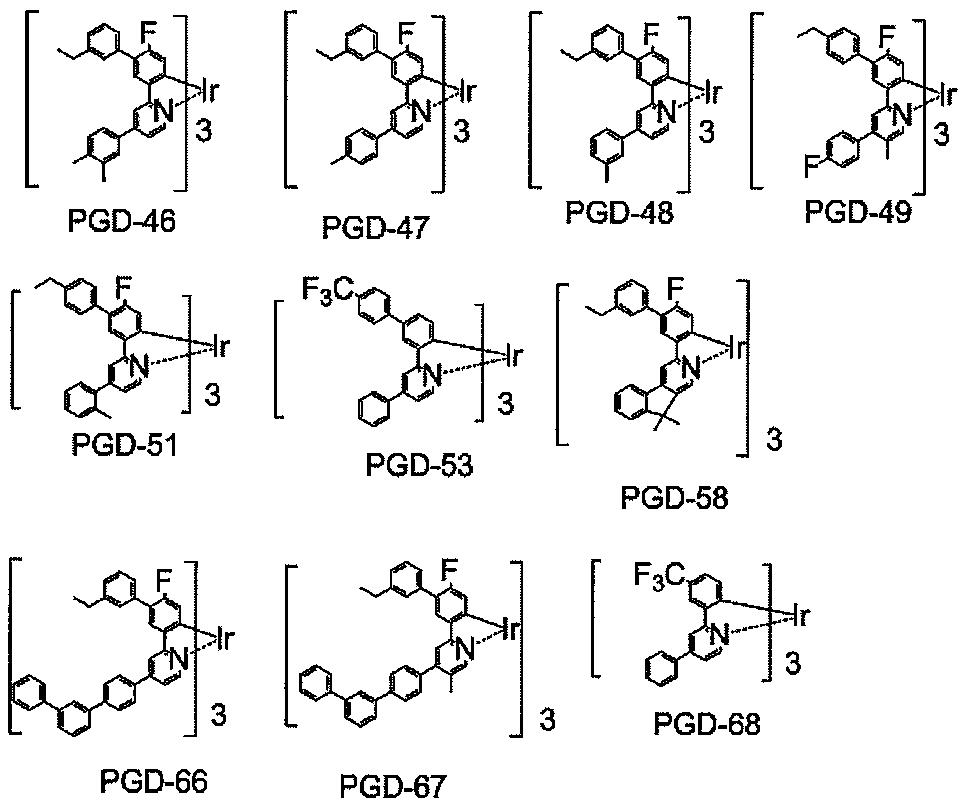
<具体例>
以下に、本発明のイリジウム錯体化合物の好ましい具体例を以下に示すが、本発明はこれらに限定されるものではない。
本発明の上記式(1)または(2)で表されるイリジウム錯体化合物の分子量は、通常850以上、好ましくは900以上、通常3000以下、好ましくは2000以下である。上記範囲内であると、錯体の安定性が良好である。
<具体例>
以下に、本発明のイリジウム錯体化合物の好ましい具体例を以下に示すが、本発明はこれらに限定されるものではない。
<構造上の特徴>
本発明は、前述のとおり、イリジウム錯体化合物を燐光性発光材料として使用する場合、前記化合物の分子構造と耐久性の関係性について検討した結果、イリジウム錯体化合物のピリジン環部分に属して、且つフェニル基と結合している炭素原子(C2原子と称す)がアニオン状態での 電荷(NBO population)が分子の耐久性とよい相関を示していること
を見出した。
本発明は、前述のとおり、イリジウム錯体化合物を燐光性発光材料として使用する場合、前記化合物の分子構造と耐久性の関係性について検討した結果、イリジウム錯体化合物のピリジン環部分に属して、且つフェニル基と結合している炭素原子(C2原子と称す)がアニオン状態での 電荷(NBO population)が分子の耐久性とよい相関を示していること
を見出した。
具体的にはアニオン状態のとき、C2原子上の電荷が0.21a.u.より大きい場合が、分子が高い耐久性を示していることである。これはイリジウム錯体化合物がアニオン状態のときに、C2原子上の電荷が大きくなることで、分子全体の共役構造が安定な中性状態と同じく容易に維持することができるため、高耐久性に繋がると考えられる。よって、アニオン状態のC2原子の電荷を大きくすることは、耐久性の高いイリジウム錯体化合物の開発に有用である。
フロンティア軌道理論によると、イリジウム錯体化合物の中性状態ではHOMO(最高被占軌道、Highest Occupied Molecular Orbital)が二つの対電子に占有されて、LUMO(最低空軌道、Lowest Unoccupied Molecular Orbital)が空軌道である。イリジウム錯体化合
物のリガンドであるフェニル基とピリジン環構造の芳香族性が高いため、それらの芳香環上のπ電子が非局在し、HOMOが高く共役分布している。言い換えるとHOMOの分布において、リガンドの芳香環上のπ電子のPz軌道の重なり(overlap)がとても大きい。その重な
りの寄与で、リガンドのフェニル基とピリジン環が同じ平面構造に保たれ、イリジウム錯体化合物が安定となる。
物のリガンドであるフェニル基とピリジン環構造の芳香族性が高いため、それらの芳香環上のπ電子が非局在し、HOMOが高く共役分布している。言い換えるとHOMOの分布において、リガンドの芳香環上のπ電子のPz軌道の重なり(overlap)がとても大きい。その重な
りの寄与で、リガンドのフェニル基とピリジン環が同じ平面構造に保たれ、イリジウム錯体化合物が安定となる。
一方で、アニオン状態では非結合性のLUMOが一つ不対電子に占有され、π電子の非局在化による分子の共役が弱くなって、Pz軌道の重なり(overlap)が小さくなる。これはア
ニオン状態において、フェニル基とピリジン環の同じ平面構造が容易に捻れ、イリジウム錯体化合物の構造が不安定となることを意味している。
よって、アニオン状態で平面構造を保つことができるどうかは、耐久性の高いイリジウム錯体化合物の開発に非常に重要である。そこで、構造の捻れと共役分布の関係を明らかにするために、分子が捻れるときに関わりがある原子上の電子分布について調査を行った。
ニオン状態において、フェニル基とピリジン環の同じ平面構造が容易に捻れ、イリジウム錯体化合物の構造が不安定となることを意味している。
よって、アニオン状態で平面構造を保つことができるどうかは、耐久性の高いイリジウム錯体化合物の開発に非常に重要である。そこで、構造の捻れと共役分布の関係を明らかにするために、分子が捻れるときに関わりがある原子上の電子分布について調査を行った。
その結果、C2原子上の電荷が大きいほど、原子上が不対電子に占有されにくい、Pz軌道の重なりが大きくなることが分かった。
それにより、アニオン状態でもフェニル基とピリジン環の同じ平面構造が保たれ、イ
リジウム錯体化合物が安定となる。このような理論を根拠とし、C2原子上の電荷と耐久性とを比較し、C2原子上の電荷が0.21a.u.より大きい場合はイリジウム錯体の耐久性が高いとの結論を見出した。さらに好ましくC2原子上の電荷は0.23a.u.以上である。特に好ましくC2原子上の電荷は0.25a.u.以上である。
それにより、アニオン状態でもフェニル基とピリジン環の同じ平面構造が保たれ、イ
リジウム錯体化合物が安定となる。このような理論を根拠とし、C2原子上の電荷と耐久性とを比較し、C2原子上の電荷が0.21a.u.より大きい場合はイリジウム錯体の耐久性が高いとの結論を見出した。さらに好ましくC2原子上の電荷は0.23a.u.以上である。特に好ましくC2原子上の電荷は0.25a.u.以上である。
<アニオン状態の電子構造及びC2原子電荷の計算方法>
以下に、本発明におけるアニオン状態の電子構造及びC2原子電荷の計算方法を示す。
[アニオン状態の電子構造の計算方法]
まずは量子化学計算で基底状態のドーパント分子の構造最適化を行う。
計算方法はハイブリッド型のB3LYP法(A.D. Becke, J.Chem.Phys. 98、5648(1993), C.Lee, W.Yang, and R.G. Parr, Phys.Rev.B 37、785(1988)及び B. Miehlich, A.Savin, H.Stoll, and H.Preuss, Chem.Phys.Lett. 157、200(1989)))を使用する。B3LYP法は高精
度で遷移金属化合物の物性値を予測する量子化学計算方法として知られている(S.Q. Niu, M.B. Hall, Chem.Rev. 100、353(2000), J. Baker, M. Muir, J. Andaelm, A. Scheiner, In Chemical Applications of Density-Functional Theory 629、342(1996))。
以下に、本発明におけるアニオン状態の電子構造及びC2原子電荷の計算方法を示す。
[アニオン状態の電子構造の計算方法]
まずは量子化学計算で基底状態のドーパント分子の構造最適化を行う。
計算方法はハイブリッド型のB3LYP法(A.D. Becke, J.Chem.Phys. 98、5648(1993), C.Lee, W.Yang, and R.G. Parr, Phys.Rev.B 37、785(1988)及び B. Miehlich, A.Savin, H.Stoll, and H.Preuss, Chem.Phys.Lett. 157、200(1989)))を使用する。B3LYP法は高精
度で遷移金属化合物の物性値を予測する量子化学計算方法として知られている(S.Q. Niu, M.B. Hall, Chem.Rev. 100、353(2000), J. Baker, M. Muir, J. Andaelm, A. Scheiner, In Chemical Applications of Density-Functional Theory 629、342(1996))。
算出の際に用いる基底関数系は、6−31Gに分極関数を加えた6−31G(d,p)を用いた(R. Ditchfield, W. J. Hehre, and J. A. Pople, J. Chem. Phys. 54, 724 (1971)、 W. J. Hehre, R. Ditchfield, and J. A. Pople, J. Chem. Phys. 56,2257 (1972)
、 P. C. Hariharan and J. A. Pople, Mol. Phys. 27, 209 (1974), M. S. Gordon, Chem. Phys. Lett. 76,163 (1980),、P. C. Hariharan and J. A. Pople, Theo. Chim. Acta
28、213、(1973)、 J.-P. Blaudeau, M. P. McGrath, L. A. Curtiss, and L. Radom, J. Chem. Phys. 107、5016(1997)、M. M. Francl, W. J. Pietro, W. J. Hehre, J. S. Binkley, D. J. DeFrees, J. A. Pople, and M. S. Gordon, J. Chem. Phys. 77、3654(1982)R. C. Binning Jr. and L. A. Curtiss, J. Comp. Chem. 11、1206(1990)、V. A. Rassolov, J. A. Pople, M. A. Ratner, and T. L. Windus, J. Chem. Phys. 109、1223(1998)、及びV. A. Rassolov, M. A. Ratner, J. A. Pople, P. C. Redfern, and L. A. Curtiss, J. Comp. Chem. 22、976(2001))。
、 P. C. Hariharan and J. A. Pople, Mol. Phys. 27, 209 (1974), M. S. Gordon, Chem. Phys. Lett. 76,163 (1980),、P. C. Hariharan and J. A. Pople, Theo. Chim. Acta
28、213、(1973)、 J.-P. Blaudeau, M. P. McGrath, L. A. Curtiss, and L. Radom, J. Chem. Phys. 107、5016(1997)、M. M. Francl, W. J. Pietro, W. J. Hehre, J. S. Binkley, D. J. DeFrees, J. A. Pople, and M. S. Gordon, J. Chem. Phys. 77、3654(1982)R. C. Binning Jr. and L. A. Curtiss, J. Comp. Chem. 11、1206(1990)、V. A. Rassolov, J. A. Pople, M. A. Ratner, and T. L. Windus, J. Chem. Phys. 109、1223(1998)、及びV. A. Rassolov, M. A. Ratner, J. A. Pople, P. C. Redfern, and L. A. Curtiss, J. Comp. Chem. 22、976(2001))。
また6−31G(g,p)の存在しないIr元素に関しては改良LANL2DZにdiffuse dおよびfを加えた既定関数を用いて計算を行う(K. Zhu, P. D. Achord, X. Zhang, K.Krogh-Jesperson, and A.S. Goldma, JACS. 126、13044(2004))。
計算で得た基底状態の最適化構造に対して、ドーパントのスピン数を一個増やし、アニオン状態を作成する。そのアニオン状態に対して、基底状態の計算と同じ手法(B3LYP)
で計算を行う。その計算で得られたドーパントの電子構造はアニオン状態の電子構造とする。
計算で得た基底状態の最適化構造に対して、ドーパントのスピン数を一個増やし、アニオン状態を作成する。そのアニオン状態に対して、基底状態の計算と同じ手法(B3LYP)
で計算を行う。その計算で得られたドーパントの電子構造はアニオン状態の電子構造とする。
[C2原子の電荷の計算方法]
上記で求めたドーパントのアニオン状態の電子構造を用いて、ドーパント分子に対してNatural Bond Orbital解析(J.P. Foster and F. Weinhold, JACS. 102、7211(1980)、A.E. Reed and F. Weinhold, J. Chem. Phys. 78、4066(1983)、A.E. Reed, R.B. Weinstock
and F. Weinhold, J. Chem. Phys. 83、735(1985)、A.E. Reed and F. Weinhold, J. Chem. Phys. 83、1736(1985)、J.E. Carpenter and F. Weinhold, J. Mol. Struct. 46、41(1988)、A.E. Reed, L.A. Curtiss and F. Weinhold, Chem. Rev. 88、899(1988)、F. Weinhold and J.E. Carpenter, in The Structure of Small Molecules and Ions, Ed. R. Namman and Z. Vager, 227、(Plenum,1988) )を行う。NBO解析は分子のπ共役、π−σ、σ−σ超共役、遷移金属のリガンド-metal電子相互作用を記述するのに有効な解析手法である(H.E. Zimmerman and F. Weinhold, JACS. 116、1579(1994)、C.R. Landis, Adv. Mol. Struct. Res. 2、129(1996))。
NBO解析で得られた電荷はドーパント分子各原子の電荷とする。そして三つのリガンド
上のC2原子(つまりドーパントのピリジン環部分に属してかつフェニル基と結合している炭素原子)の平均値をアニオン状態におけるC2原子の電荷とする。
上記で求めたドーパントのアニオン状態の電子構造を用いて、ドーパント分子に対してNatural Bond Orbital解析(J.P. Foster and F. Weinhold, JACS. 102、7211(1980)、A.E. Reed and F. Weinhold, J. Chem. Phys. 78、4066(1983)、A.E. Reed, R.B. Weinstock
and F. Weinhold, J. Chem. Phys. 83、735(1985)、A.E. Reed and F. Weinhold, J. Chem. Phys. 83、1736(1985)、J.E. Carpenter and F. Weinhold, J. Mol. Struct. 46、41(1988)、A.E. Reed, L.A. Curtiss and F. Weinhold, Chem. Rev. 88、899(1988)、F. Weinhold and J.E. Carpenter, in The Structure of Small Molecules and Ions, Ed. R. Namman and Z. Vager, 227、(Plenum,1988) )を行う。NBO解析は分子のπ共役、π−σ、σ−σ超共役、遷移金属のリガンド-metal電子相互作用を記述するのに有効な解析手法である(H.E. Zimmerman and F. Weinhold, JACS. 116、1579(1994)、C.R. Landis, Adv. Mol. Struct. Res. 2、129(1996))。
NBO解析で得られた電荷はドーパント分子各原子の電荷とする。そして三つのリガンド
上のC2原子(つまりドーパントのピリジン環部分に属してかつフェニル基と結合している炭素原子)の平均値をアニオン状態におけるC2原子の電荷とする。
<イリジウム錯体化合物の合成方法>
イリジウム錯体化合物の合成方法については、式1)一段階でトリス錯体を形成する方法、式2)Ir2核錯体のような中間体を形成させたのちにトリス体を形成させる方法等が例示できるが、これらに限定されるものではない。
例えば、式(A)で表される典型的な反応としては、配位子3当量とIr(acac)
3(イリジウムアセチルアセトナート錯体)1当量の反応により金属錯体を得る方法があげられる。
イリジウム錯体化合物の合成方法については、式1)一段階でトリス錯体を形成する方法、式2)Ir2核錯体のような中間体を形成させたのちにトリス体を形成させる方法等が例示できるが、これらに限定されるものではない。
例えば、式(A)で表される典型的な反応としては、配位子3当量とIr(acac)
3(イリジウムアセチルアセトナート錯体)1当量の反応により金属錯体を得る方法があげられる。
この際、配位子を過剰量もちいて反応を促進することもできるし、少量用いて選択性を高めても良い。また、配位子を複数種類用い、逐次的に添加し、混合配位子錯体を形成してもよい
また、式(B)で表される典型的な反応としては、例えば配位子2当量とIrCl3・
xH2O(イリジウムクロライド・x水和物)1当量の反応によりIr原子2個からなる2核金属錯体などの中間対を得たのち、さらに配位子をIrに対し1当量反応させて金属錯体を得る方法が挙げられる。
また、式(B)で表される典型的な反応としては、例えば配位子2当量とIrCl3・
xH2O(イリジウムクロライド・x水和物)1当量の反応によりIr原子2個からなる2核金属錯体などの中間対を得たのち、さらに配位子をIrに対し1当量反応させて金属錯体を得る方法が挙げられる。
式(A)と同様に反応の効率および選択性を考慮し、実際の配位子とIr化合物の仕込
み比は適当に調整することができる。式(B)の場合、最後に添加する配位子を最初の配
位子と異なるものを用いることにより、簡便に混合配位子錯体を形成できる。
Ir化合物としては上記のIr(acac)3錯体やIrCl3・xH2O錯体の他に、Irシクロオクタジエニル錯体など、適当なIr化合物を用いても良い。炭酸塩などの塩基化合物、Ag塩などのハロゲントラップ剤、などを併用して反応を促進させてもよい。反応温度は50℃〜400℃程度の温度が好ましく用いられる。一般的に150℃以上の高温が用いられる。反応は無溶剤で行っても良いし、既知の溶剤を用いてもよい。高温反応で行う場合、グリセリン等の高沸点溶剤が好ましい。
み比は適当に調整することができる。式(B)の場合、最後に添加する配位子を最初の配
位子と異なるものを用いることにより、簡便に混合配位子錯体を形成できる。
Ir化合物としては上記のIr(acac)3錯体やIrCl3・xH2O錯体の他に、Irシクロオクタジエニル錯体など、適当なIr化合物を用いても良い。炭酸塩などの塩基化合物、Ag塩などのハロゲントラップ剤、などを併用して反応を促進させてもよい。反応温度は50℃〜400℃程度の温度が好ましく用いられる。一般的に150℃以上の高温が用いられる。反応は無溶剤で行っても良いし、既知の溶剤を用いてもよい。高温反応で行う場合、グリセリン等の高沸点溶剤が好ましい。
<イリジウム錯体化合物の用途>
本発明のイリジウム錯体化合物は、有機電界発光素子に用いられる材料、すなわち有機電界発光素子材料として好適に使用可能であり、有機電界発光素子やその他の発光素子等の発光材料としても好適に使用可能である。
<イリジウム錯体化合物含有組成物>
本発明のイリジウム錯体化合物は、溶解性に優れることから、溶剤とともに使用されることが好ましい。以下、本発明のイリジウム錯体化合物と溶剤とを含有する組成物(イリジウム錯体化合物含有組成物)について説明する。
本発明のイリジウム錯体化合物は、有機電界発光素子に用いられる材料、すなわち有機電界発光素子材料として好適に使用可能であり、有機電界発光素子やその他の発光素子等の発光材料としても好適に使用可能である。
<イリジウム錯体化合物含有組成物>
本発明のイリジウム錯体化合物は、溶解性に優れることから、溶剤とともに使用されることが好ましい。以下、本発明のイリジウム錯体化合物と溶剤とを含有する組成物(イリジウム錯体化合物含有組成物)について説明する。
本発明のイリジウム錯体化合物含有組成物は、上述の本発明のイリジウム錯体化合物および溶剤を含有する。本発明のイリジウム錯体化合物含有組成物は通常湿式成膜法で層や膜を形成するために用いられ、特に有機電界発光素子の有機層を形成するために用いられることが好ましい。該有機層は、特に発光層であることが好ましい
つまり、イリジウム錯体化合物含有組成物は、有機電界発光素子用組成物であることが
好ましく、更に発光層形成用組成物として用いられることが特に好ましい
該イリジウム錯体化合物含有組成物における本発明のイリジウム錯体化合物の含有量は、通常0.1重量%以上、好ましくは1重量%以上、通常99.99重量%以下、好ましくは99.9重量%以下である。組成物のイリジウム錯体化合物の含有量をこの範囲とすることにより、隣接する層(例えば、正孔輸送層や正孔阻止層)から発光層へ効率よく、正孔や電子の注入が行われ、駆動電圧を低減することができる。尚、本発明のイリジウム錯体化合物はイリジウム錯体化合物含有組成物中に、1種のみ含まれていてもよく、2種以上が組み合わされて含まれていてもよい。
つまり、イリジウム錯体化合物含有組成物は、有機電界発光素子用組成物であることが
好ましく、更に発光層形成用組成物として用いられることが特に好ましい
該イリジウム錯体化合物含有組成物における本発明のイリジウム錯体化合物の含有量は、通常0.1重量%以上、好ましくは1重量%以上、通常99.99重量%以下、好ましくは99.9重量%以下である。組成物のイリジウム錯体化合物の含有量をこの範囲とすることにより、隣接する層(例えば、正孔輸送層や正孔阻止層)から発光層へ効率よく、正孔や電子の注入が行われ、駆動電圧を低減することができる。尚、本発明のイリジウム錯体化合物はイリジウム錯体化合物含有組成物中に、1種のみ含まれていてもよく、2種以上が組み合わされて含まれていてもよい。
本発明のイリジウム錯体化合物含有組成物を例えば有機電界発光素子用に用いる場合には、上述のイリジウム錯体化合物や溶剤の他、有機電界発光素子、特に発光層に用いられる電荷輸送性化合物を含有することができる。
本発明のイリジウム錯体化合物含有組成物を用いて、有機電界発光素子の発光層を形成する場合には、本発明のイリジウム錯体化合物をドーパント材料とし、他の電荷輸送性化合物をホスト材料として含むことが好ましい
本発明のイリジウム錯体化合物含有組成物に含有される溶剤は、湿式成膜によりイリジウム錯体化合物を含む層を形成するために用いる、揮発性を有する液体成分である。
本発明のイリジウム錯体化合物含有組成物を用いて、有機電界発光素子の発光層を形成する場合には、本発明のイリジウム錯体化合物をドーパント材料とし、他の電荷輸送性化合物をホスト材料として含むことが好ましい
本発明のイリジウム錯体化合物含有組成物に含有される溶剤は、湿式成膜によりイリジウム錯体化合物を含む層を形成するために用いる、揮発性を有する液体成分である。
該溶剤は、溶質である本発明のイリジウム錯体化合物が高い溶解性を有するために、むしろ後述の電荷輸送性化合物が良好に溶解する溶剤であれば特に限定されない。好ましい溶剤としては、例えば、n−デカン、シクロヘキサン、エチルシクロヘキサン、デカリン、ビシクロヘキサン等のアルカン類;トルエン、キシレン、メチシレン、フェニルシクロヘキサン、テトラリン等の芳香族炭化水素類;クロロベンゼン、ジクロロベンゼン、トリクロロベンゼン等のハロゲン化芳香族炭化水素類;1,2−ジメトキシベンゼン、1,3−ジメトキシベンゼン、アニソール、フェネトール、2−メトキシトルエン、3−メトキシトルエン、4−メトキシトルエン、2,3−ジメチルアニソール、2,4−ジメチルアニソール、ジフェニルエーテル等の芳香族エーテル類;酢酸フェニル、プロピオン酸フェニル、安息香酸メチル、安息香酸エチル、安息香酸エチル、安息香酸プロピル、安息香酸n−ブチル等の芳香族エステル類、シクロヘキサノン、シクロオクタノン、フェンコン等の脂環族ケトン類;シクロヘキサノール、シクロオクタノール等の脂環族アルコール類;メチルエチルケトン、ジブチルケトン等の脂肪族ケトン類;ブタノール、ヘキサノール等の脂肪族アルコール類;エチレングリコールジメチルエーテル、エチレングリコールジエチルエーテル、プロピレングリコール−1−モノメチルエーテルアセタート(PGMEA)等の脂肪族エーテル類;等が挙げられる。
中でも好ましくは、アルカン類や芳香族炭化水素類であり、特に、フェニルシクロヘキサンは湿式成膜プロセスにおいて好ましい粘度と沸点を有している。
これらの溶剤は1種類を単独で用いてもよく、また2種類以上を任意の組み合わせ、および比率で用いてもよい。
溶剤の沸点は、通常80℃以上、好ましくは100℃以上、より好ましくは150℃以上、特に好ましくは200℃以上である。通常沸点270℃以下、好ましくは250℃以下、より好ましくは230℃以下である。この範囲を下回ると、湿式成膜時において、組成物からの溶剤蒸発により、成膜安定性が低下する可能性がある。
これらの溶剤は1種類を単独で用いてもよく、また2種類以上を任意の組み合わせ、および比率で用いてもよい。
溶剤の沸点は、通常80℃以上、好ましくは100℃以上、より好ましくは150℃以上、特に好ましくは200℃以上である。通常沸点270℃以下、好ましくは250℃以下、より好ましくは230℃以下である。この範囲を下回ると、湿式成膜時において、組成物からの溶剤蒸発により、成膜安定性が低下する可能性がある。
溶剤の含有量は、組成物100重量部に対して、好ましくは10重量部以上、より好ましくは50重量部以上、特に好ましくは80重量部以上、また、好ましくは99.95重量部以下、より好ましくは99.9重量部以下、特に好ましくは99.8重量部以下である。通常発光層の厚みは3〜200nm程度であるが、溶剤の含有量がこの下限を下回ると、組成物の粘性が高くなりすぎ、成膜作業性が低下する可能性がある。一方、この上限を上回ると、成膜後、溶剤を除去して得られる膜の厚みが稼げなくなるため、成膜が困難
となる傾向がある。
となる傾向がある。
本発明のイリジウム錯体化合物含有組成物が含有し得る他の電荷輸送性化合物としては、従来有機電界発光素子用材料として用いられているものを使用することができる。例えば、ピリジン、カルバゾール、ナフタレン、ペリレン、ピレン、アントラセン、クリセン、ナフタセン、フェナントレン、コロネン、フルオランテン、ベンゾフェナントレン、フルオレン、アセトナフトフルオランテン、クマリン、p−ビス(2−フェニルエテニル)ベンゼンおよびそれらの誘導体、キナクリドン誘導体、DCM(4-(dicyanomethylene)-2-methyl-6-(p-dimethylaminostyryl)-4H-pyran)系化合物、ベンゾピラン誘導体、ローダミン誘導体、ベンゾチオキサンテン誘導体、アザベンゾチオキサンテン、アリールアミノ基が置換された縮合芳香族環化合物、アリールアミノ基が置換されたスチリル誘導体等が挙げられる。
これらは1種類を単独で用いてもよく、また2種類以上を任意の組み合わせ、および比率で用いてもよい。
本発明のイリジウム錯体化合物含有組成物中の他の電荷輸送性化合物の含有量は、該組成物を100重量部とすると、通常1重量部以上、また、通常50重量部以下、好ましくは30重量部以下である。
本発明のイリジウム錯体化合物含有組成物中の他の電荷輸送性化合物の含有量は、該組成物を100重量部とすると、通常1重量部以上、また、通常50重量部以下、好ましくは30重量部以下である。
また、イリジウム錯体化合物含有組成物中の他の電荷輸送性化合物の含有量は、イリジウム錯体化合物含有組成物中の本発明のイリジウム錯体化合物に対して、通常50重量%以下、特に30重量%以下で、通常0.01重量%以上、特に0.1重量%以上であることが好ましい。
本発明のイリジウム錯体化合物含有組成物には、必要に応じて、上記の化合物等の他に、更に他の化合物を含有していてもよい。例えば、上記の溶剤の他に、別の溶剤を含有していてもよい。そのような溶剤としては、例えば、N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド等のアミド類、ジメチルスルホキシド等が挙げられる。これらは1種類を単独で用いてもよく、また2種類以上を任意の組み合わせ、および比率で用いてもよい。
本発明のイリジウム錯体化合物含有組成物には、必要に応じて、上記の化合物等の他に、更に他の化合物を含有していてもよい。例えば、上記の溶剤の他に、別の溶剤を含有していてもよい。そのような溶剤としては、例えば、N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド等のアミド類、ジメチルスルホキシド等が挙げられる。これらは1種類を単独で用いてもよく、また2種類以上を任意の組み合わせ、および比率で用いてもよい。
<有機電界発光素子>
以下に、本発明の有機電界発光素子、有機電界発光照明装置及び有機電界発光表示装置の実施態様を詳細に説明するが、本発明はその要旨を超えない限り、これらの内容により限定されるものではない。
(基板)
基板は、有機電界発光素子の支持体となるものであり、通常、石英やガラスの板、金属板や金属箔、プラスチックフィルムやシート等が用いられる。これらのうち、ガラス板や、ポリエステル、ポリメタクリレート、ポリカーボネート、ポリスルホン等の透明な合成樹脂の板が好ましい。基板は、外気による有機電界発光素子の劣化が起こり難いことからガスバリア性の高い材質とするのが好ましい。このため、特に合成樹脂製の基板等のようにガスバリア性の低い材質を用いる場合は、基板の少なくとも片面に緻密なシリコン酸化膜等を設けてガスバリア性を上げるのが好ましい。
以下に、本発明の有機電界発光素子、有機電界発光照明装置及び有機電界発光表示装置の実施態様を詳細に説明するが、本発明はその要旨を超えない限り、これらの内容により限定されるものではない。
(基板)
基板は、有機電界発光素子の支持体となるものであり、通常、石英やガラスの板、金属板や金属箔、プラスチックフィルムやシート等が用いられる。これらのうち、ガラス板や、ポリエステル、ポリメタクリレート、ポリカーボネート、ポリスルホン等の透明な合成樹脂の板が好ましい。基板は、外気による有機電界発光素子の劣化が起こり難いことからガスバリア性の高い材質とするのが好ましい。このため、特に合成樹脂製の基板等のようにガスバリア性の低い材質を用いる場合は、基板の少なくとも片面に緻密なシリコン酸化膜等を設けてガスバリア性を上げるのが好ましい。
(陽極)
陽極は、発光層側の層に正孔を注入する機能を担う。陽極は、通常、アルミニウム、金、銀、ニッケル、パラジウム、白金等の金属;インジウム及び/又はスズの酸化物等の金属酸化物;ヨウ化銅等のハロゲン化金属;カーボンブラック及びポリ(3−メチルチオフェン)、ポリピロール、ポリアニリン等の導電性高分子等により構成される。陽極の形成は、通常、スパッタリング法、真空蒸着法等の乾式法により行われることが多い。また、銀等の金属微粒子、ヨウ化銅等の微粒子、カーボンブラック、導電性の金属酸化物微粒子
、導電性高分子微粉末等を用いて陽極を形成する場合には、適当なバインダー樹脂溶液に分散させて、基板上に塗布することにより形成することもできる。また、導電性高分子の場合は、電解重合により直接基板上に薄膜を形成したり、基板上に導電性高分子を塗布して陽極を形成することもできる(Appl.Phys.Lett.,60巻,2711頁,1992年)。
陽極は、発光層側の層に正孔を注入する機能を担う。陽極は、通常、アルミニウム、金、銀、ニッケル、パラジウム、白金等の金属;インジウム及び/又はスズの酸化物等の金属酸化物;ヨウ化銅等のハロゲン化金属;カーボンブラック及びポリ(3−メチルチオフェン)、ポリピロール、ポリアニリン等の導電性高分子等により構成される。陽極の形成は、通常、スパッタリング法、真空蒸着法等の乾式法により行われることが多い。また、銀等の金属微粒子、ヨウ化銅等の微粒子、カーボンブラック、導電性の金属酸化物微粒子
、導電性高分子微粉末等を用いて陽極を形成する場合には、適当なバインダー樹脂溶液に分散させて、基板上に塗布することにより形成することもできる。また、導電性高分子の場合は、電解重合により直接基板上に薄膜を形成したり、基板上に導電性高分子を塗布して陽極を形成することもできる(Appl.Phys.Lett.,60巻,2711頁,1992年)。
陽極は、通常、単層構造であるが、適宜、積層構造としてもよい。陽極が積層構造である場合、1層目の陽極上に異なる導電材料を積層してもよい。 陽極の厚みは、必要とされる透明性と材質等に応じて、決めればよい。特に高い透明性が必要とされる場合は、可視光の透過率が60%以上となる厚みが好ましく、80%以上となる厚みが更に好ましい。陽極の厚みは、通常5nm以上、好ましくは10nm以上であり、また、通常1000nm以下、好ましくは500nm以下とするのが好ましい。一方、透明性が不要な場合は、陽極の厚みは必要な強度等に応じて任意に厚みとすればよく、この場合、陽極は基板と同一の厚みでもよい。
陽極の表面に成膜を行う場合は、成膜前に、紫外線+オゾン、酸素プラズマ、アルゴンプラズマ等の処理を施すことにより、陽極上の不純物を除去すると共に、そのイオン化ポテンシャルを調整して正孔注入性を向上させておくのが好ましい。
(正孔注入層)
陽極側から発光層側に正孔を輸送する機能を担う層は、通常、正孔注入輸送層又は正孔輸送層と呼ばれる。そして、陽極側から発光層側に正孔を輸送する機能を担う層が2層以上ある場合に、より陽極側に近い方の層を正孔注入層と呼ぶことがある。正孔注入層は、陽極から発光層側に正孔を輸送する機能を強化する点で、用いることが好ましい。正孔注入層を用いる場合、通常、正孔注入層は、陽極上に形成される。
陽極側から発光層側に正孔を輸送する機能を担う層は、通常、正孔注入輸送層又は正孔輸送層と呼ばれる。そして、陽極側から発光層側に正孔を輸送する機能を担う層が2層以上ある場合に、より陽極側に近い方の層を正孔注入層と呼ぶことがある。正孔注入層は、陽極から発光層側に正孔を輸送する機能を強化する点で、用いることが好ましい。正孔注入層を用いる場合、通常、正孔注入層は、陽極上に形成される。
正孔注入層の膜厚は、通常1nm以上、好ましくは5nm以上、また、通常1000nm以下、好ましくは500nm以下である。
正孔注入層の形成方法は、真空蒸着法でも、湿式成膜法でもよい。成膜性が優れる点では、湿式成膜法により形成することが好ましい。
正孔注入層は、正孔輸送性化合物を含むことが好ましく、正孔輸送性化合物と電子受容性化合物とを含むことがより好ましい。更には、正孔注入層中にカチオンラジカル化合物を含むことが好ましく、カチオンラジカル化合物と正孔輸送性化合物とを含むことが特に好ましい。
正孔注入層の形成方法は、真空蒸着法でも、湿式成膜法でもよい。成膜性が優れる点では、湿式成膜法により形成することが好ましい。
正孔注入層は、正孔輸送性化合物を含むことが好ましく、正孔輸送性化合物と電子受容性化合物とを含むことがより好ましい。更には、正孔注入層中にカチオンラジカル化合物を含むことが好ましく、カチオンラジカル化合物と正孔輸送性化合物とを含むことが特に好ましい。
(正孔輸送性化合物)
正孔注入層形成用組成物は、通常、正孔注入層となる正孔輸送性化合物を含有する。また、湿式成膜法の場合は、通常、更に溶剤も含有する。正孔注入層形成用組成物は、正孔輸送性が高く、注入された正孔を効率よく輸送できるのが好ましい。このため、正孔移動度が大きく、トラップとなる不純物が製造時や使用時等に発生し難いのが好ましい。また、安定性に優れ、イオン化ポテンシャルが小さく、可視光に対する透明性が高いことが好ましい。特に、正孔注入層が発光層と接する場合は、発光層からの発光を消光しないものや発光層とエキサイプレックスを形成して、発光効率を低下させないものが好ましい。
正孔注入層形成用組成物は、通常、正孔注入層となる正孔輸送性化合物を含有する。また、湿式成膜法の場合は、通常、更に溶剤も含有する。正孔注入層形成用組成物は、正孔輸送性が高く、注入された正孔を効率よく輸送できるのが好ましい。このため、正孔移動度が大きく、トラップとなる不純物が製造時や使用時等に発生し難いのが好ましい。また、安定性に優れ、イオン化ポテンシャルが小さく、可視光に対する透明性が高いことが好ましい。特に、正孔注入層が発光層と接する場合は、発光層からの発光を消光しないものや発光層とエキサイプレックスを形成して、発光効率を低下させないものが好ましい。
正孔輸送性化合物としては、陽極から正孔注入層への電荷注入障壁の観点から、4.5eV〜6.0eVのイオン化ポテンシャルを有する化合物が好ましい。正孔輸送性化合物の例としては、芳香族アミン系化合物、フタロシアニン系化合物、ポルフィリン系化合物、オリゴチオフェン系化合物、ポリチオフェン系化合物、ベンジルフェニル系化合物、フルオレン基で3級アミンを連結した化合物、ヒドラゾン系化合物、シラザン系化合物系化合物、キナクリドン系化合物等が挙げられる。
上述の例示化合物のうち、非晶質性及び可視光透過性の点から、芳香族アミン化合物が好ましく、芳香族三級アミン化合物が特に好ましい。ここで、芳香族三級アミン化合物とは、芳香族三級アミン構造を有する化合物であって、芳香族三級アミン由来の基を有する化合物も含む。
芳香族三級アミン化合物の種類は、特に制限されないが、表面平滑化効果により均一な発光を得やすい点から、重量平均分子量が1000以上1000000以下の高分子化合物(繰り返し単位が連なる重合型化合物)を用いるのが好ましい。芳香族三級アミン高分子化合物の好ましい例としては、下記式(I)で表される繰り返し単位を有する高分子化合物等が挙げられる。
芳香族三級アミン化合物の種類は、特に制限されないが、表面平滑化効果により均一な発光を得やすい点から、重量平均分子量が1000以上1000000以下の高分子化合物(繰り返し単位が連なる重合型化合物)を用いるのが好ましい。芳香族三級アミン高分子化合物の好ましい例としては、下記式(I)で表される繰り返し単位を有する高分子化合物等が挙げられる。
(式(I)中、Ar1及びAr2は、それぞれ独立して、置換基を有していてもよい芳香族炭化水素基又は置換基を有していてもよい芳香族複素環基を表す。Ar3〜Ar5は、それぞれ独立して、置換基を有していてもよい芳香族炭化水素基又は置換基を有していてもよい芳香族複素環基を表す。Yは、下記の連結基群の中から選ばれる連結基を表す。また、Ar1〜Ar5のうち、同一のN原子に結合する二つの基は互いに結合して環を形成してもよい。
(上記各式中、Ar6〜Ar16は、それぞれ独立して、置換基を有していてもよい芳香族炭化水素基又は置換基を有していてもよい芳香族複素環基を表す。R1及びR2は、それぞれ独立して、水素原子又は任意の置換基を表す。) Ar1〜Ar16の芳香族炭化水素基及び芳香族複素環基としては、高分子化合物の溶解性、耐熱性、正孔注入輸送性の
点から、ベンゼン環、ナフタレン環、フェナントレン環、チオフェン環、ピリジン環由来の基が好ましく、ベンゼン環、ナフタレン環由来の基がさらに好ましい。
式(I)で表される繰り返し単位を有する芳香族三級アミン高分子化合物の具体例としては、国際公開第2005/089024号パンフレットに記載のもの等が挙げられる。
点から、ベンゼン環、ナフタレン環、フェナントレン環、チオフェン環、ピリジン環由来の基が好ましく、ベンゼン環、ナフタレン環由来の基がさらに好ましい。
式(I)で表される繰り返し単位を有する芳香族三級アミン高分子化合物の具体例としては、国際公開第2005/089024号パンフレットに記載のもの等が挙げられる。
(電子受容性化合物)
正孔注入層には、正孔輸送性化合物の酸化により、正孔注入層の導電率を向上させることができるため、電子受容性化合物を含有していることが好ましい。
電子受容性化合物としては、酸化力を有し、上述の正孔輸送性化合物から一電子受容する能力を有する化合物が好ましく、具体的には、電子親和力が4eV以上である化合物が好ましく、電子親和力が5eV以上である化合物が更に好ましい。
正孔注入層には、正孔輸送性化合物の酸化により、正孔注入層の導電率を向上させることができるため、電子受容性化合物を含有していることが好ましい。
電子受容性化合物としては、酸化力を有し、上述の正孔輸送性化合物から一電子受容する能力を有する化合物が好ましく、具体的には、電子親和力が4eV以上である化合物が好ましく、電子親和力が5eV以上である化合物が更に好ましい。
このような電子受容性化合物としては、例えば、トリアリールホウ素化合物、ハロゲン化金属、ルイス酸、有機酸、オニウム塩、アリールアミンとハロゲン化金属との塩、アリールアミンとルイス酸との塩よりなる群から選ばれる1種又は2種以上の化合物等が挙げられる。具体的には、4−イソプロピル−4’−メチルジフェニルヨードニウムテトラキス(ペンダフルオロフェニル)ボラート、トリフェニルスルホニウムテトラフルオロボラート等の有機基の置換したオニウム塩(国際公開2005/089024号パンフレット);塩化鉄(III)(特開平11−251067号公報)、ペルオキソ二硫酸アンモニウム等の高原子価の無機化合物;テトラシアノエチレン等のシアノ化合物;トリス(ペンダフルオロフェニル)ボラン(特開2003−31365号公報)等の芳香族ホウ素化合物;フラーレン誘導体及びヨウ素等が挙げられる。
(カチオンラジカル化合物)
カチオンラジカル化合物としては、正孔輸送性化合物から一電子取り除いた化学種であるカチオンラジカルと、対アニオンとからなるイオン化合物が好ましい。但し、カチオンラジカルが正孔輸送性の高分子化合物由来である場合、カチオンラジカルは高分子化合物の繰り返し単位から一電子取り除いた構造となる。
カチオンラジカル化合物としては、正孔輸送性化合物から一電子取り除いた化学種であるカチオンラジカルと、対アニオンとからなるイオン化合物が好ましい。但し、カチオンラジカルが正孔輸送性の高分子化合物由来である場合、カチオンラジカルは高分子化合物の繰り返し単位から一電子取り除いた構造となる。
カチオンラジカルとしては、正孔輸送性化合物として前述した化合物から一電子取り除いた化学種であることが好ましい。正孔輸送性化合物として好ましい化合物から一電子取り除いた化学種であることが、非晶質性、可視光の透過率、耐熱性、及び溶解性などの点から好適である。
ここで、カチオンラジカル化合物は、前述の正孔輸送性化合物と電子受容性化合物を混合することにより生成させることができる。即ち、前述の正孔輸送性化合物と電子受容性化合物とを混合することにより、正孔輸送性化合物から電子受容性化合物へと電子移動が起こり、正孔輸送性化合物のカチオンラジカルと対アニオンとからなるカチオンイオン化合物が生成する。
ここで、カチオンラジカル化合物は、前述の正孔輸送性化合物と電子受容性化合物を混合することにより生成させることができる。即ち、前述の正孔輸送性化合物と電子受容性化合物とを混合することにより、正孔輸送性化合物から電子受容性化合物へと電子移動が起こり、正孔輸送性化合物のカチオンラジカルと対アニオンとからなるカチオンイオン化合物が生成する。
PEDOT/PSS(Adv.Mater.,2000年,12巻,481頁)やエメラルジン塩酸塩(J.Phys.Chem.,1990年,94巻,7716頁)等の高分子化合物由来のカチオンラジカル化合物は、酸化重合(脱水素重合)することによっても生成する。
ここでいう酸化重合は、モノマーを酸性溶液中で、ペルオキソ二硫酸塩等を用いて化学的に、又は、電気化学的に酸化するものである。この酸化重合(脱水素重合)の場合、モノマーが酸化されることにより高分子化されるとともに、酸性溶液由来のアニオンを対アニオンとする、高分子の繰り返し単位から一電子取り除かれたカチオンラジカルが生成する。
ここでいう酸化重合は、モノマーを酸性溶液中で、ペルオキソ二硫酸塩等を用いて化学的に、又は、電気化学的に酸化するものである。この酸化重合(脱水素重合)の場合、モノマーが酸化されることにより高分子化されるとともに、酸性溶液由来のアニオンを対アニオンとする、高分子の繰り返し単位から一電子取り除かれたカチオンラジカルが生成する。
<湿式成膜法による正孔注入層の形成>
湿式成膜法により正孔注入層を形成する場合、通常、正孔注入層となる材料を可溶な溶剤(正孔注入層用溶剤)と混合して成膜用の組成物(正孔注入層形成用組成物)を調製し、この正孔注入層形成用組成物を正孔注入層の下層に該当する層(通常は、陽極)上に塗布して成膜し、乾燥させることにより形成させる。
湿式成膜法により正孔注入層を形成する場合、通常、正孔注入層となる材料を可溶な溶剤(正孔注入層用溶剤)と混合して成膜用の組成物(正孔注入層形成用組成物)を調製し、この正孔注入層形成用組成物を正孔注入層の下層に該当する層(通常は、陽極)上に塗布して成膜し、乾燥させることにより形成させる。
正孔注入層形成用組成物中における正孔輸送性化合物の濃度は、本発明の効果を著しく損なわない限り任意であるが、膜厚の均一性の点では、低い方が好ましく、また、一方、正孔注入層に欠陥が生じ難い点では、高い方が好ましい。具体的には、0.01重量%以上であるのが好ましく、0.1重量%以上であるのが更に好ましく、0.5重量%以上であるのが特に好ましく、また、一方、70重量%以下であるのが好ましく、60重量%以下であるのが更に好ましく、50重量%以下であるのが特に好ましい。
溶剤としては、例えば、エーテル系溶剤、エステル系溶剤、芳香族炭化水素系溶剤、アミド系溶剤などが挙げられる。
エーテル系溶剤としては、例えば、エチレングリコールジメチルエーテル、エチレングリコールジエチルエーテル、プロピレングリコール−1−モノメチルエーテルアセタート(PGMEA)等の脂肪族エーテル及び1,2−ジメトキシベンゼン、1,3−ジメトキシベンゼン、アニソール、フェネトール、2−メトキシトルエン、3−メトキシトルエン、4−メトキシトルエン、2,3−ジメチルアニソール、2,4−ジメチルアニソール等の芳香族エーテル等が挙げられる。
エーテル系溶剤としては、例えば、エチレングリコールジメチルエーテル、エチレングリコールジエチルエーテル、プロピレングリコール−1−モノメチルエーテルアセタート(PGMEA)等の脂肪族エーテル及び1,2−ジメトキシベンゼン、1,3−ジメトキシベンゼン、アニソール、フェネトール、2−メトキシトルエン、3−メトキシトルエン、4−メトキシトルエン、2,3−ジメチルアニソール、2,4−ジメチルアニソール等の芳香族エーテル等が挙げられる。
エステル系溶剤としては、例えば、酢酸フェニル、プロピオン酸フェニル、安息香酸メチル、安息香酸エチル、安息香酸プロピル、安息香酸n−ブチル等の芳香族エステル等が挙げられる。
芳香族炭化水素系溶剤としては、例えば、トルエン、キシレン、シクロヘキシルベンゼン、3−イソプロピルビフェニル、1,2,3,4−テトラメチルベンゼン、1,4−ジイソプロピルベンゼン、シクロヘキシルベンゼン、メチルナフタレン等が挙げられる。アミド系溶剤としては、例えば、N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド等が挙げられる。
芳香族炭化水素系溶剤としては、例えば、トルエン、キシレン、シクロヘキシルベンゼン、3−イソプロピルビフェニル、1,2,3,4−テトラメチルベンゼン、1,4−ジイソプロピルベンゼン、シクロヘキシルベンゼン、メチルナフタレン等が挙げられる。アミド系溶剤としては、例えば、N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド等が挙げられる。
これらの他、ジメチルスルホキシド等も用いることができる。
正孔注入層3の湿式成膜法による形成は、通常、正孔注入層形成用組成物を調製後に、これを、正孔注入層3の下層に該当する層(通常は、陽極2)上に塗布成膜し、乾燥することにより行われる。
正孔注入層3は、通常、成膜後に、加熱や減圧乾燥等により塗布膜を乾燥させる。
正孔注入層3の湿式成膜法による形成は、通常、正孔注入層形成用組成物を調製後に、これを、正孔注入層3の下層に該当する層(通常は、陽極2)上に塗布成膜し、乾燥することにより行われる。
正孔注入層3は、通常、成膜後に、加熱や減圧乾燥等により塗布膜を乾燥させる。
<真空蒸着法による正孔注入層の形成>
真空蒸着法により正孔注入層3を形成する場合には、通常、正孔注入層3の構成材料(前述の正孔輸送性化合物、電子受容性化合物等)の1種類又は2種類以上を真空容器内に設置された坩堝に入れ(2種類以上の材料を用いる場合は、通常各々を別々の坩堝に入れ)、真空容器内を真空ポンプで10−4Pa程度まで排気した後、坩堝を加熱して(2種類以上の材料を用いる場合は、通常各々の坩堝を加熱して)、坩堝内の材料の蒸発量を制御しながら蒸発させ(2種類以上の材料を用いる場合は、通常各々独立に蒸発量を制御しながら蒸発させ)、坩堝に向き合って置かれた基板上の陽極上に正孔注入層を形成させる。なお、2種類以上の材料を用いる場合は、それらの混合物を坩堝に入れ、加熱、蒸発させて正孔注入層を形成することもできる。
真空蒸着法により正孔注入層3を形成する場合には、通常、正孔注入層3の構成材料(前述の正孔輸送性化合物、電子受容性化合物等)の1種類又は2種類以上を真空容器内に設置された坩堝に入れ(2種類以上の材料を用いる場合は、通常各々を別々の坩堝に入れ)、真空容器内を真空ポンプで10−4Pa程度まで排気した後、坩堝を加熱して(2種類以上の材料を用いる場合は、通常各々の坩堝を加熱して)、坩堝内の材料の蒸発量を制御しながら蒸発させ(2種類以上の材料を用いる場合は、通常各々独立に蒸発量を制御しながら蒸発させ)、坩堝に向き合って置かれた基板上の陽極上に正孔注入層を形成させる。なお、2種類以上の材料を用いる場合は、それらの混合物を坩堝に入れ、加熱、蒸発させて正孔注入層を形成することもできる。
蒸着時の真空度は、本発明の効果を著しく損なわない限り限定されないが、通常0.1×10−6Torr(0.13×10−4Pa)以上、9.0×10−6Torr(12.0×10−4Pa)以下である。蒸着速度は、本発明の効果を著しく損なわない限り限
定されないが、通常0.1A/秒以上、5.0A/秒以下である。蒸着時の成膜温度は、本発明の効果を著しく損なわない限り限定されないが、好ましくは10℃以上、50℃以下で行われる。
定されないが、通常0.1A/秒以上、5.0A/秒以下である。蒸着時の成膜温度は、本発明の効果を著しく損なわない限り限定されないが、好ましくは10℃以上、50℃以下で行われる。
(正孔輸送層)
正孔輸送層は、陽極側から発光層側に正孔を輸送する機能を担う層である。正孔輸送層は、本発明の有機電界発光素子では、必須の層では無いが、陽極から発光層に正孔を輸送する機能を強化する点では、この層を用いるのが好ましい。正孔輸送層を用いる場合、通常、正孔輸送層は、陽極と発光層の間に形成される。また、上述の正孔注入層がある場合は、正孔注入層と発光層の間に形成される。
正孔輸送層の膜厚は、通常5nm以上、好ましくは10nm以上であり、また、一方、通常300nm以下、好ましくは100nm以下である。
正孔輸送層の形成方法は、真空蒸着法でも、湿式成膜法でもよい。成膜性が優れる点では、湿式成膜法により形成することが好ましい。
正孔輸送層は、陽極側から発光層側に正孔を輸送する機能を担う層である。正孔輸送層は、本発明の有機電界発光素子では、必須の層では無いが、陽極から発光層に正孔を輸送する機能を強化する点では、この層を用いるのが好ましい。正孔輸送層を用いる場合、通常、正孔輸送層は、陽極と発光層の間に形成される。また、上述の正孔注入層がある場合は、正孔注入層と発光層の間に形成される。
正孔輸送層の膜厚は、通常5nm以上、好ましくは10nm以上であり、また、一方、通常300nm以下、好ましくは100nm以下である。
正孔輸送層の形成方法は、真空蒸着法でも、湿式成膜法でもよい。成膜性が優れる点では、湿式成膜法により形成することが好ましい。
正孔輸送層は、通常、正孔輸送層となる正孔輸送性化合物を含有する。正孔輸送層に含まれる正孔輸送性化合物としては、特に、4,4’−ビス[N−(1−ナフチル)−N−フェニルアミノ]ビフェニルで代表される、2個以上の3級アミンを含み2個以上の縮合芳香族環が窒素原子に置換した芳香族ジアミン(特開平5−234681号公報)、4,4’,4’’−トリス(1−ナフチルフェニルアミノ)トリフェニルアミン等のスターバースト構造を有する芳香族アミン化合物(J.Lumin.,72−74巻、985頁、1997年)、トリフェニルアミンの四量体から成る芳香族アミン化合物(Chem.Commun.,2175頁、1996年)、2,2’,7,7’−テトラキス−(ジフェニルアミノ)−9,9’−スピロビフルオレン等のスピロ化合物(Synth.Metals,91巻、209頁、1997年)、4,4’−N,N’−ジカルバゾールビフェニルなどのカルバゾール誘導体などが挙げられる。また、例えばポリビニルカルバゾール、ポリビニルトリフェニルアミン(特開平7−53953号公報)、テトラフェニルベンジジンを含有するポリアリーレンエーテルサルホン(Polym.Adv.Tech.,7巻、33頁、1996年)等も好ましく使用できる。
<湿式成膜法による正孔輸送層の形成>
湿式成膜法で正孔輸送層を形成する場合は、通常、上述の正孔注入層を湿式成膜法で形成する場合と同様にして、正孔注入層形成用組成物の代わりに正孔輸送層形成用組成物を用いて形成させる。
湿式成膜法で正孔輸送層を形成する場合は、通常、正孔輸送層形成用組成物は、更に溶剤を含有する。正孔輸送層形成用組成物に用いる溶剤は、上述の正孔注入層形成用組成物で用いる溶剤と同様の溶剤を使用することができる。
湿式成膜法で正孔輸送層を形成する場合は、通常、上述の正孔注入層を湿式成膜法で形成する場合と同様にして、正孔注入層形成用組成物の代わりに正孔輸送層形成用組成物を用いて形成させる。
湿式成膜法で正孔輸送層を形成する場合は、通常、正孔輸送層形成用組成物は、更に溶剤を含有する。正孔輸送層形成用組成物に用いる溶剤は、上述の正孔注入層形成用組成物で用いる溶剤と同様の溶剤を使用することができる。
正孔輸送層形成用組成物中における正孔輸送性化合物の濃度は、正孔注入層形成用組成物中における正孔輸送性化合物の濃度と同様の範囲とすることができる。
正孔輸送層の湿式成膜法による形成は、前述の正孔注入層成膜法と同様に行うことができる。
正孔輸送層の湿式成膜法による形成は、前述の正孔注入層成膜法と同様に行うことができる。
<真空蒸着法による正孔輸送層の形成>
真空蒸着法で正孔輸送層を形成する場合についても、通常、上述の正孔注入層を真空蒸着法で形成する場合と同様にして、正孔注入層形成用組成物の代わりに正孔輸送層形成用組成物を用いて形成させることができる。蒸着時の真空度、蒸着速度及び温度などの成膜条件などは、前記正孔注入層の真空蒸着時と同様の条件で成膜することができる。
真空蒸着法で正孔輸送層を形成する場合についても、通常、上述の正孔注入層を真空蒸着法で形成する場合と同様にして、正孔注入層形成用組成物の代わりに正孔輸送層形成用組成物を用いて形成させることができる。蒸着時の真空度、蒸着速度及び温度などの成膜条件などは、前記正孔注入層の真空蒸着時と同様の条件で成膜することができる。
(発光層)
発光層は、一対の電極間に電界が与えられた時に、陽極から注入される正孔と陰極から注入される電子が再結合することにより励起され、発光する機能を担う層である。発光層は、陽極と陰極の間に形成される層であり、発光層は、陽極の上に正孔注入層がある場合は、正孔注入層と陰極の間に形成され、陽極の上に正孔輸送層がある場合は、正孔輸送層と陰極の間に形成される。
発光層は、一対の電極間に電界が与えられた時に、陽極から注入される正孔と陰極から注入される電子が再結合することにより励起され、発光する機能を担う層である。発光層は、陽極と陰極の間に形成される層であり、発光層は、陽極の上に正孔注入層がある場合は、正孔注入層と陰極の間に形成され、陽極の上に正孔輸送層がある場合は、正孔輸送層と陰極の間に形成される。
発光層の膜厚は、本発明の効果を著しく損なわない限り任意であるが、膜に欠陥が生じ難い点では厚い方が好ましく、また、一方、薄い方が低駆動電圧としやすい点で好ましい。このため、3nm以上であるのが好ましく、5nm以上であるのが更に好ましく、また、一方、通常200nm以下であるのが好ましく、100nm以下であるのが更に好ましい。
発光層は、少なくとも、発光の性質を有する材料(発光材料)を含有するとともに、好ましくは、電荷輸送性を有する材料(電荷輸送性材料)とを含有する。
発光層は、少なくとも、発光の性質を有する材料(発光材料)を含有するとともに、好ましくは、電荷輸送性を有する材料(電荷輸送性材料)とを含有する。
(発光材料)
発光材料は、所望の発光波長で発光し、本発明の効果を損なわない限り特に制限はなく、公知の発光材料を適用可能である。発光材料は、蛍光発光材料でも、燐光発光材料でもよいが、発光効率が良好である材料が好ましく、内部量子効率の観点から燐光発光材料が好ましい。燐光発光材料としては、本願発明のイリジウム錯体化合物を用いることが好ましい。
発光材料は、所望の発光波長で発光し、本発明の効果を損なわない限り特に制限はなく、公知の発光材料を適用可能である。発光材料は、蛍光発光材料でも、燐光発光材料でもよいが、発光効率が良好である材料が好ましく、内部量子効率の観点から燐光発光材料が好ましい。燐光発光材料としては、本願発明のイリジウム錯体化合物を用いることが好ましい。
蛍光発光材料としては、例えば、以下の材料が挙げられる。
青色発光を与える蛍光発光材料(青色蛍光発光材料)としては、例えば、ナフタレン、ペリレン、ピレン、アントラセン、クマリン、クリセン、p−ビス(2−フェニルエテニル)ベンゼン及びそれらの誘導体等が挙げられる。
緑色発光を与える蛍光発光材料(緑色蛍光発光材料)としては、例えば、キナクリドン誘導体、クマリン誘導体、Al(C9H6NO)3などのアルミニウム錯体等が挙げられる。
青色発光を与える蛍光発光材料(青色蛍光発光材料)としては、例えば、ナフタレン、ペリレン、ピレン、アントラセン、クマリン、クリセン、p−ビス(2−フェニルエテニル)ベンゼン及びそれらの誘導体等が挙げられる。
緑色発光を与える蛍光発光材料(緑色蛍光発光材料)としては、例えば、キナクリドン誘導体、クマリン誘導体、Al(C9H6NO)3などのアルミニウム錯体等が挙げられる。
黄色発光を与える蛍光発光材料(黄色蛍光発光材料)としては、例えば、ルブレン、ペリミドン誘導体等が挙げられる。
赤色発光を与える蛍光発光材料(赤色蛍光発光材料)としては、例えば、DCM(4−(dicyanomethylene)−2−methyl−6−(p−dimethylaminostyryl)−4H−pyran)系化合物、ベンゾピラン誘導体、ローダミン誘導体、ベンゾチオキサンテン誘導体、アザベンゾチオキサンテン等が挙げられる。
赤色発光を与える蛍光発光材料(赤色蛍光発光材料)としては、例えば、DCM(4−(dicyanomethylene)−2−methyl−6−(p−dimethylaminostyryl)−4H−pyran)系化合物、ベンゾピラン誘導体、ローダミン誘導体、ベンゾチオキサンテン誘導体、アザベンゾチオキサンテン等が挙げられる。
また、燐光発光材料としては、例えば、長周期型周期表(以下、特に断り書きの無い限り「周期表」という場合には、長周期型周期表を指すものとする。)の第7〜11族から選ばれる金属を含む有機金属錯体等が挙げられる。周期表の第7〜11族から選ばれる金属として、好ましくは、ルテニウム、ロジウム、パラジウム、銀、レニウム、オスミウム、イリジウム、白金、金等が挙げられる。
有機金属錯体の配位子としては、(ヘテロ)アリールピリジン配位子、(ヘテロ)アリールピラゾール配位子などの(ヘテロ)アリール基とピリジン、ピラゾール、フェナントロリンなどが連結した配位子が好ましく、特にフェニルピリジン配位子、フェニルピラゾール配位子が好ましい。ここで、(ヘテロ)アリールとは、アリール基またはヘテロアリール基を表す。
好ましい燐光発光材料として、具体的には、例えば、トリス(2−フェニルピリジン)
イリジウム、トリス(2−フェニルピリジン)ルテニウム、トリス(2−フェニルピリジン)パラジウム、ビス(2−フェニルピリジン)白金、トリス(2−フェニルピリジン)オスミウム、トリス(2−フェニルピリジン)レニウム等のフェニルピリジン錯体及びオクタエチル白金ポルフィリン、オクタフェニル白金ポルフィリン、オクタエチルパラジウムポルフィリン、オクタフェニルパラジウムポルフィリン等のポルフィリン錯体等が挙げられる。
イリジウム、トリス(2−フェニルピリジン)ルテニウム、トリス(2−フェニルピリジン)パラジウム、ビス(2−フェニルピリジン)白金、トリス(2−フェニルピリジン)オスミウム、トリス(2−フェニルピリジン)レニウム等のフェニルピリジン錯体及びオクタエチル白金ポルフィリン、オクタフェニル白金ポルフィリン、オクタエチルパラジウムポルフィリン、オクタフェニルパラジウムポルフィリン等のポルフィリン錯体等が挙げられる。
高分子系の発光材料としては、ポリ(9,9−ジオクチルフルオレン−2,7−ジイル)、ポリ[(9,9−ジオクチルフルオレン−2,7−ジイル)-co-(4,4’−(N
−(4−sec−ブチルフェニル))ジフェニルアミン)]、ポリ[(9,9−ジオクチルフルオレン−2,7−ジイル)-co-(1,4−ベンゾ−2{2,1’−3}−トリアゾール)]などのポリフルオレン系材料、ポリ[2−メトキシ−5−(2−ヘチルヘキシル
オキシ)−1,4−フェニレンビニレン]などのポリフェニレンビニレン系材料が挙げられる。
−(4−sec−ブチルフェニル))ジフェニルアミン)]、ポリ[(9,9−ジオクチルフルオレン−2,7−ジイル)-co-(1,4−ベンゾ−2{2,1’−3}−トリアゾール)]などのポリフルオレン系材料、ポリ[2−メトキシ−5−(2−ヘチルヘキシル
オキシ)−1,4−フェニレンビニレン]などのポリフェニレンビニレン系材料が挙げられる。
(電荷輸送性材料)
電荷輸送性材料は、正電荷(正孔)又は負電荷(電子)輸送性を有する材料であり、本発明の効果を損なわない限り、特に制限はなく、公知の発光材料を適用可能である。
電荷輸送性材料は、従来、有機電界発光素子の発光層に用いられている化合物等を用いることができ、特に、発光層のホスト材料として使用されている化合物が好ましい。
電荷輸送性材料は、正電荷(正孔)又は負電荷(電子)輸送性を有する材料であり、本発明の効果を損なわない限り、特に制限はなく、公知の発光材料を適用可能である。
電荷輸送性材料は、従来、有機電界発光素子の発光層に用いられている化合物等を用いることができ、特に、発光層のホスト材料として使用されている化合物が好ましい。
電荷輸送性材料としては、具体的には、芳香族アミン系化合物、フタロシアニン系化合物、ポルフィリン系化合物、オリゴチオフェン系化合物、ポリチオフェン系化合物、ベンジルフェニル系化合物、フルオレン基で3級アミンを連結した化合物、ヒドラゾン系化合物、シラザン系化合物、シラナミン系化合物、ホスファミン系化合物、キナクリドン系化合物等の正孔注入層の正孔輸送性化合物として例示した化合物等が挙げられる他、アントラセン系化合物、ピレン系化合物、カルバゾール系化合物、ピリジン系化合物、フェナントロリン系化合物、オキサジアゾール系化合物、シロール系化合物等の電子輸送性化合物等が挙げられる。
また、例えば、4,4'−ビス[N−(1−ナフチル)−N−フェニルアミノ]ビフェ
ニルで代表わされる2個以上の3級アミンを含み2個以上の縮合芳香族環が窒素原子に置換した芳香族ジアミン(特開平5−234681号公報)、4,4',4''−トリス(1
−ナフチルフェニルアミノ)トリフェニルアミン等のスターバースト構造を有する芳香族アミン系化合物(J.Lumin.,72−74巻、985頁、1997年)、トリフェニルアミンの四量体から成る芳香族アミン系化合物(Chem.Commun.,2175頁、1996年)、2,2',7,7'−テトラキス−(ジフェニルアミノ)−9,9'
−スピロビフルオレン等のフルオレン系化合物(Synth.Metals,91巻、209頁、1997年)、4,4'−N,N'−ジカルバゾールビフェニルなどのカルバゾール系化合物等の正孔輸送層の正孔輸送性化合物として例示した化合物等も好ましく用いることができる。また、この他、2−(4−ビフェニリル)−5−(p−ターシャルブチルフェニル)−1,3,4−オキサジアゾール(tBu−PBD)、2,5−ビス(1−ナフチル)−1,3,4−オキサジアゾール(BND)などのオキサジアゾール系化合物、2,5−ビス(6’−(2’,2”−ビピリジル))−1,1−ジメチル−3,4−ジフェニルシロール(PyPySPyPy)等のシロール系化合物、バソフェナントロリン(BPhen)、2,9−ジメチル−4,7−ジフェニル−1,10−フェナントロリン(BCP、バソクプロイン)などのフェナントロリン系化合物等も挙げられる。
ニルで代表わされる2個以上の3級アミンを含み2個以上の縮合芳香族環が窒素原子に置換した芳香族ジアミン(特開平5−234681号公報)、4,4',4''−トリス(1
−ナフチルフェニルアミノ)トリフェニルアミン等のスターバースト構造を有する芳香族アミン系化合物(J.Lumin.,72−74巻、985頁、1997年)、トリフェニルアミンの四量体から成る芳香族アミン系化合物(Chem.Commun.,2175頁、1996年)、2,2',7,7'−テトラキス−(ジフェニルアミノ)−9,9'
−スピロビフルオレン等のフルオレン系化合物(Synth.Metals,91巻、209頁、1997年)、4,4'−N,N'−ジカルバゾールビフェニルなどのカルバゾール系化合物等の正孔輸送層の正孔輸送性化合物として例示した化合物等も好ましく用いることができる。また、この他、2−(4−ビフェニリル)−5−(p−ターシャルブチルフェニル)−1,3,4−オキサジアゾール(tBu−PBD)、2,5−ビス(1−ナフチル)−1,3,4−オキサジアゾール(BND)などのオキサジアゾール系化合物、2,5−ビス(6’−(2’,2”−ビピリジル))−1,1−ジメチル−3,4−ジフェニルシロール(PyPySPyPy)等のシロール系化合物、バソフェナントロリン(BPhen)、2,9−ジメチル−4,7−ジフェニル−1,10−フェナントロリン(BCP、バソクプロイン)などのフェナントロリン系化合物等も挙げられる。
<湿式成膜法による発光層の形成>
発光層の形成方法は、真空蒸着法でも、湿式成膜法でもよいが、成膜性に優れることか
ら、湿式成膜法が好ましい。本発明において湿式成膜法とは、成膜方法、即ち、塗布方法として、例えば、スピンコート法、ディップコート法、ダイコート法、バーコート法、ブレードコート法、ロールコート法、スプレーコート法、キャピラリーコート法、インクジェット法、ノズルプリンティング法、スクリーン印刷法、グラビア印刷法、フレキソ印刷法等、湿式で成膜される方法を採用し、この塗布膜を乾燥して膜形成を行う方法をいう。湿式成膜法により発光層を形成する場合は、通常、上述の正孔注入層を湿式成膜法で形成する場合と同様にして、正孔注入層形成用組成物の代わりに、発光層となる材料を可溶な溶剤(発光層用溶剤)と混合して調製した発光層形成用組成物を用いて形成させる。
発光層の形成方法は、真空蒸着法でも、湿式成膜法でもよいが、成膜性に優れることか
ら、湿式成膜法が好ましい。本発明において湿式成膜法とは、成膜方法、即ち、塗布方法として、例えば、スピンコート法、ディップコート法、ダイコート法、バーコート法、ブレードコート法、ロールコート法、スプレーコート法、キャピラリーコート法、インクジェット法、ノズルプリンティング法、スクリーン印刷法、グラビア印刷法、フレキソ印刷法等、湿式で成膜される方法を採用し、この塗布膜を乾燥して膜形成を行う方法をいう。湿式成膜法により発光層を形成する場合は、通常、上述の正孔注入層を湿式成膜法で形成する場合と同様にして、正孔注入層形成用組成物の代わりに、発光層となる材料を可溶な溶剤(発光層用溶剤)と混合して調製した発光層形成用組成物を用いて形成させる。
溶剤としては、例えば、正孔注入層の形成について挙げたエーテル系溶剤、エステル系溶剤、芳香族炭化水素系溶剤、アミド系溶剤の他、アルカン系溶剤、ハロゲン化芳香族炭化水系溶剤、脂肪族アルコール系溶剤、脂環族アルコール系溶剤、脂肪族ケトン系溶剤及び脂環族ケトン系溶剤などが挙げられる。以下に溶媒の具体例を挙げるが、本発明の効果を損なわない限り、これらに限定されるものではない。
例えば、エチレングリコールジメチルエーテル、エチレングリコールジエチルエーテル、プロピレングリコール−1−モノメチルエーテルアセタート(PGMEA)等の脂肪族エーテル系溶剤;1,2−ジメトキシベンゼン、1,3−ジメトキシベンゼン、アニソール、フェネトール、2−メトキシトルエン、3−メトキシトルエン、4−メトキシトルエン、2,3−ジメチルアニソール、2,4−ジメチルアニソール、ジフェニルエーテル等の芳香族エーテル系溶剤;酢酸フェニル、プロピオン酸フェニル、安息香酸メチル、安息香酸エチル、安息香酸エチル、安息香酸プロピル、安息香酸n−ブチル等の芳香族エステル系溶剤;トルエン、キシレン、メチシレン、シクロヘキシルベンゼン、テトラリン、3−イロプロピルビフェニル、1,2,3,4−テトラメチルベンゼン、1,4−ジイソプロピルベンゼン、シクロヘキシルベンゼン、メチルナフタレン等の芳香族炭化水素系溶媒;N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド等のアミド系溶剤;n−デカン、シクロヘキサン、エチルシクロヘキサン、デカリン、ビシクロヘキサン等のアルカン系溶剤;クロロベンゼン、ジクロロベンゼン、トリクロロベンゼン等のハロゲン化芳香族炭化水素系溶剤;ブタノール、ヘキサノール等の脂肪族アルコール系溶剤;シクロヘキサノール、シクロオクタノール等の脂環族アルコール系溶剤;メチルエチルケトン、ジブチルケトン等の脂肪族ケトン系溶剤;シクロヘキサノン、シクロオクタノン、フェンコン等の脂環族ケトン系溶剤等が挙げられる。これらのうち、アルカン系溶剤及び芳香族炭化水素系溶剤が特に好ましい。
また、より均一な膜を得るためには、成膜直後の液膜から溶剤が適当な速度で蒸発することが好ましい。このため、溶剤の沸点は通常80℃以上、好ましくは100℃以上、より好ましくは120℃以上、また、通常270℃以下、好ましくは250℃以下、より好ましくは沸点230℃以下である。
溶媒の使用量は、本発明の効果を著しく損なわない限り任意であるが、発光層形成用組成物中の合計含有量は、低粘性なために成膜作業が行いやすい点で多い方が好ましく、また、一方、厚膜で成膜しやすい点で低い方が好ましい。具体的には、10重量%以上であるのが好ましく、50重量%以上であるのが更に好ましく、80重量%以上であるのが特に好ましく、また、一方、99.95重量%以下であるのが好ましく、99.90重量%以下であるのが更に好ましく、は99.80重量%以下であるのが特に好ましい。
溶媒の使用量は、本発明の効果を著しく損なわない限り任意であるが、発光層形成用組成物中の合計含有量は、低粘性なために成膜作業が行いやすい点で多い方が好ましく、また、一方、厚膜で成膜しやすい点で低い方が好ましい。具体的には、10重量%以上であるのが好ましく、50重量%以上であるのが更に好ましく、80重量%以上であるのが特に好ましく、また、一方、99.95重量%以下であるのが好ましく、99.90重量%以下であるのが更に好ましく、は99.80重量%以下であるのが特に好ましい。
発光層形成用組成物における発光材料、正孔輸送性化合物、電子輸送性化合物等の固形分濃度は、均一膜厚としやすい点では小さい方が好ましいが、一方で、膜に欠陥が生じ難い点では大きい方が好ましい。このため、0.01重量%以上70重量%以下であるのが好ましい。
溶媒除去方法としては、加熱または減圧を用いることができる。加熱方法において使用
する加熱手段としては、膜全体に均等に熱を与えることから、クリーンオーブン、ホットプレートが好ましい。
溶媒除去方法としては、加熱または減圧を用いることができる。加熱方法において使用
する加熱手段としては、膜全体に均等に熱を与えることから、クリーンオーブン、ホットプレートが好ましい。
加熱工程における加熱温度は、本発明の効果を著しく損なわない限り任意であるが、乾燥時間を短くする点では温度が高いほうが好ましく、材料へのダメージが少ない点では低い方が好ましい。上限は通常250℃以下であり、好ましくは200℃以下、さらに好ましくは150℃以下である。下限は通常30℃以上であり、好ましくは50℃以上であり、さらに好ましくは80℃以上である。上限以上の温度は、通常用いられる電荷輸送材料または燐光発光材料の耐熱性より高く、分解や結晶化する可能性があり好ましくない。下限以下では溶媒の除去に長時間を要するため、好ましくない。加熱工程における加熱時間は、発光層形成用組成物中の溶媒の沸点や蒸気圧、材料の耐熱性、および加熱条件によって適切に決定される。
<真空蒸着法による発光層の形成>
真空蒸着法により発光層を形成する場合には、通常、発光層の構成材料(前述の発光材料、電荷輸送性化合物等)の1種類又は2種類以上を真空容器内に設置された坩堝に入れ(2種類以上の材料を用いる場合は、通常各々を別々の坩堝に入れ)、真空容器内を真空ポンプで10−4Pa程度まで排気した後、坩堝を加熱して(2種類以上の材料を用いる場合は、通常各々の坩堝を加熱して)、坩堝内の材料の蒸発量を制御しながら蒸発させ(2種類以上の材料を用いる場合は、通常各々独立に蒸発量を制御しながら蒸発させ)、坩堝に向き合って置かれた正孔注入輸送層の上に発光層を形成させる。なお、2種類以上の材料を用いる場合は、それらの混合物を坩堝に入れ、加熱、蒸発させて発光層を形成することもできる。
真空蒸着法により発光層を形成する場合には、通常、発光層の構成材料(前述の発光材料、電荷輸送性化合物等)の1種類又は2種類以上を真空容器内に設置された坩堝に入れ(2種類以上の材料を用いる場合は、通常各々を別々の坩堝に入れ)、真空容器内を真空ポンプで10−4Pa程度まで排気した後、坩堝を加熱して(2種類以上の材料を用いる場合は、通常各々の坩堝を加熱して)、坩堝内の材料の蒸発量を制御しながら蒸発させ(2種類以上の材料を用いる場合は、通常各々独立に蒸発量を制御しながら蒸発させ)、坩堝に向き合って置かれた正孔注入輸送層の上に発光層を形成させる。なお、2種類以上の材料を用いる場合は、それらの混合物を坩堝に入れ、加熱、蒸発させて発光層を形成することもできる。
蒸着時の真空度は、本発明の効果を著しく損なわない限り限定されないが、通常0.1×10−6Torr(0.13×10−4Pa)以上、9.0×10−6Torr(12.0×10−4Pa)以下である。蒸着速度は、本発明の効果を著しく損なわない限り限定されないが、通常0.1Å/秒以上、5.0Å/秒以下である。蒸着時の成膜温度は、本発明の効果を著しく損なわない限り限定されないが、好ましくは10℃以上、50℃以下で行われる。
(正孔阻止層)
発光層と後述の電子注入層との間に、正孔阻止層を設けてもよい。正孔阻止層は、発光層の上に、発光層の陰極側の界面に接するように積層される層である。
この正孔阻止層は、陽極から移動してくる正孔を陰極に到達するのを阻止する役割と、陰極から注入された電子を効率よく発光層の方向に輸送する役割とを有する。正孔阻止層6を構成する材料に求められる物性としては、電子移動度が高く正孔移動度が低いこと、エネルギーギャップ(HOMO、LUMOの差)が大きいこと、励起三重項準位(T1)が高いことが挙げられる。
発光層と後述の電子注入層との間に、正孔阻止層を設けてもよい。正孔阻止層は、発光層の上に、発光層の陰極側の界面に接するように積層される層である。
この正孔阻止層は、陽極から移動してくる正孔を陰極に到達するのを阻止する役割と、陰極から注入された電子を効率よく発光層の方向に輸送する役割とを有する。正孔阻止層6を構成する材料に求められる物性としては、電子移動度が高く正孔移動度が低いこと、エネルギーギャップ(HOMO、LUMOの差)が大きいこと、励起三重項準位(T1)が高いことが挙げられる。
このような条件を満たす正孔阻止層の材料としては、例えば、ビス(2−メチル−8−キノリノラト)(フェノラト)アルミニウム、ビス(2−メチル−8−キノリノラト)(トリフェニルシラノラト)アルミニウム等の混合配位子錯体、ビス(2−メチル−8−キノラト)アルミニウム−μ−オキソ−ビス−(2−メチル−8−キノリラト)アルミニウム二核金属錯体等の金属錯体、ジスチリルビフェニル誘導体等のスチリル化合物(特開平11−242996号公報)、3−(4−ビフェニルイル)−4−フェニル−5(4−tert−ブチルフェニル)−1,2,4−トリアゾール等のトリアゾール誘導体(特開平7−41759号公報)、バソクプロイン等のフェナントロリン誘導体(特開平10−79297号公報)などが挙げられる。更に、国際公開第2005/022962号パンフレットに記載の2,4,6位が置換されたピリジン環を少なくとも1個有する化合物も、
正孔阻止層の材料として好ましい。
正孔阻止層の材料として好ましい。
正孔阻止層6の形成方法に制限はなく、前述の発光層の形成方法と同様にして形成することができる。
正孔阻止層の膜厚は、本発明の効果を著しく損なわない限り任意であるが、通常0.3nm以上、好ましくは0.5nm以上であり、また、通常100nm以下、好ましくは50nm以下である。
正孔阻止層の膜厚は、本発明の効果を著しく損なわない限り任意であるが、通常0.3nm以上、好ましくは0.5nm以上であり、また、通常100nm以下、好ましくは50nm以下である。
(電子輸送層)
電子輸送層は素子の電流効率をさらに向上させることを目的として、発光層と電子注入層との間に設けられる。
電子輸送層は、電界を与えられた電極間において陰極から注入された電子を効率よく発光層の方向に輸送することができる化合物より形成される。電子輸送層に用いられる電子輸送性化合物としては、陰極又は電子注入層からの電子注入効率が高く、かつ、高い電子移動度を有し注入された電子を効率よく輸送することができる化合物であることが必要である。
電子輸送層は素子の電流効率をさらに向上させることを目的として、発光層と電子注入層との間に設けられる。
電子輸送層は、電界を与えられた電極間において陰極から注入された電子を効率よく発光層の方向に輸送することができる化合物より形成される。電子輸送層に用いられる電子輸送性化合物としては、陰極又は電子注入層からの電子注入効率が高く、かつ、高い電子移動度を有し注入された電子を効率よく輸送することができる化合物であることが必要である。
電子輸送層に用いる電子輸送性化合物は、通常、陰極又は電子注入層からの電子注入効率が高く、注入された電子を効率よく輸送できる化合物が好ましい。電子輸送性化合物としては、具体的には、例えば、8−ヒドロキシキノリンのアルミニウム錯体などの金属錯体(特開昭59−194393号公報)、10−ヒドロキシベンゾ[h]キノリンの金属錯体、オキサジアゾール誘導体、ジスチリルビフェニル誘導体、シロール誘導体、3−ヒドロキシフラボン金属錯体、5−ヒドロキシフラボン金属錯体、ベンズオキサゾール金属錯体、ベンゾチアゾール金属錯体、トリスベンズイミダゾリルベンゼン(米国特許第5645948号明細書)、キノキサリン化合物(特開平6−207169号公報)、フェナントロリン誘導体(特開平5−331459号公報)、2−t−ブチル−9,10−N,N’−ジシアノアントラキノンジイミン、n型水素化非晶質炭化シリコン、n型硫化亜鉛、n型セレン化亜鉛などが挙げられる。
電子輸送層の膜厚は、通常1nm以上、好ましくは5nm以上であり、また、一方、通常300nm以下、好ましくは100nm以下である。
電子輸送層は、前記と同様にして湿式成膜法、或いは真空蒸着法により正孔阻止層上に積層することにより形成される。通常は、真空蒸着法が用いられる。
(電子注入層)
電子注入層は、陰極から注入された電子を効率よく、電子輸送層又は発光層へ注入する役割を果たす。
電子輸送層は、前記と同様にして湿式成膜法、或いは真空蒸着法により正孔阻止層上に積層することにより形成される。通常は、真空蒸着法が用いられる。
(電子注入層)
電子注入層は、陰極から注入された電子を効率よく、電子輸送層又は発光層へ注入する役割を果たす。
電子注入を効率よく行うには、電子注入層を形成する材料は、仕事関数の低い金属が好ましい。例としては、ナトリウムやセシウム等のアルカリ金属、バリウムやカルシウムなどのアルカリ土類金属等が用いられる。その膜厚は通常0.1nm以上、5nm以下が好ましい。
更に、バソフェナントロリン等の含窒素複素環化合物や8−ヒドロキシキノリンのアルミニウム錯体などの金属錯体に代表される有機電子輸送材料に、ナトリウム、カリウム、セシウム、リチウム、ルビジウム等のアルカリ金属をドープする(特開平10−270171号公報、特開2002−100478号公報、特開2002−100482号公報などに記載)ことも、電子注入・輸送性が向上し優れた膜質を両立させることが可能となるため好ましい。
更に、バソフェナントロリン等の含窒素複素環化合物や8−ヒドロキシキノリンのアルミニウム錯体などの金属錯体に代表される有機電子輸送材料に、ナトリウム、カリウム、セシウム、リチウム、ルビジウム等のアルカリ金属をドープする(特開平10−270171号公報、特開2002−100478号公報、特開2002−100482号公報などに記載)ことも、電子注入・輸送性が向上し優れた膜質を両立させることが可能となるため好ましい。
膜厚は通常、5nm以上、好ましくは10nm以上、また、通常200nm以下、好ましくは100nm以下の範囲である。
電子注入層は、湿式成膜法或いは真空蒸着法により、発光層又はその上の正孔阻止層上に積層することにより形成される。
湿式成膜法の場合の詳細は、前述の発光層の場合と同様である。
電子注入層は、湿式成膜法或いは真空蒸着法により、発光層又はその上の正孔阻止層上に積層することにより形成される。
湿式成膜法の場合の詳細は、前述の発光層の場合と同様である。
(陰極)
陰極は、発光層側の層(電子注入層又は発光層など)に電子を注入する役割を果たす。
陰極の材料としては、前記の陽極に使用される材料を用いることが可能であるが、効率良く電子注入を行なう上では、仕事関数の低い金属を用いることが好ましく、例えば、スズ、マグネシウム、インジウム、カルシウム、アルミニウム、銀等の金属又はそれらの合金などが用いられる。具体例としては、例えば、マグネシウム−銀合金、マグネシウム−インジウム合金、アルミニウム−リチウム合金等の低仕事関数の合金電極などが挙げられる。
陰極は、発光層側の層(電子注入層又は発光層など)に電子を注入する役割を果たす。
陰極の材料としては、前記の陽極に使用される材料を用いることが可能であるが、効率良く電子注入を行なう上では、仕事関数の低い金属を用いることが好ましく、例えば、スズ、マグネシウム、インジウム、カルシウム、アルミニウム、銀等の金属又はそれらの合金などが用いられる。具体例としては、例えば、マグネシウム−銀合金、マグネシウム−インジウム合金、アルミニウム−リチウム合金等の低仕事関数の合金電極などが挙げられる。
素子の安定性の点では、陰極の上に、仕事関数が高く、大気に対して安定な金属層を積層して、低仕事関数の金属からなる陰極を保護するのが好ましい。積層する金属としては、例えば、アルミニウム、銀、銅、ニッケル、クロム、金、白金等の金属が挙げられる。
陰極の膜厚は通常、陽極と同様である。
(その他の層)
本発明の有機電界発光素子は、本発明の効果を著しく損なわなければ、更に他の層を有していてもよい。すなわち、陽極と陰極との間に、上述の他の任意の層を有していてもよい。
陰極の膜厚は通常、陽極と同様である。
(その他の層)
本発明の有機電界発光素子は、本発明の効果を著しく損なわなければ、更に他の層を有していてもよい。すなわち、陽極と陰極との間に、上述の他の任意の層を有していてもよい。
<その他の素子構成>
なお、上述の説明とは逆の構造、即ち、基板上に陰極、電子注入層、発光層、正孔注入層、陽極の順に積層することも可能である。
<その他>
本発明の有機電界発光素子を有機電界発光装置に適用する場合は、単一の有機電界発光素子として用いても、複数の有機電界発光素子がアレイ状に配置された構成にして用いても、陽極と陰極がX−Yマトリックス状に配置された構成にして用いてもよい。
なお、上述の説明とは逆の構造、即ち、基板上に陰極、電子注入層、発光層、正孔注入層、陽極の順に積層することも可能である。
<その他>
本発明の有機電界発光素子を有機電界発光装置に適用する場合は、単一の有機電界発光素子として用いても、複数の有機電界発光素子がアレイ状に配置された構成にして用いても、陽極と陰極がX−Yマトリックス状に配置された構成にして用いてもよい。
<有機EL表示装置>
本発明の有機EL表示装置は、上述の本発明の有機電界発光素子を用いたものである。本発明の有機EL表示装置の型式や構造については特に制限はなく、本発明の有機電界発光素子を用いて常法に従って組み立てることができる。
例えば、「有機ELディスプレイ」(オーム社、平成16年8月20日発行、時任静士、安達千波矢、村田英幸著)に記載されているような方法で、本発明の有機EL表示装置を形成することができる。
本発明の有機EL表示装置は、上述の本発明の有機電界発光素子を用いたものである。本発明の有機EL表示装置の型式や構造については特に制限はなく、本発明の有機電界発光素子を用いて常法に従って組み立てることができる。
例えば、「有機ELディスプレイ」(オーム社、平成16年8月20日発行、時任静士、安達千波矢、村田英幸著)に記載されているような方法で、本発明の有機EL表示装置を形成することができる。
<有機EL照明>
本発明の有機EL照明は、上述の本発明の有機電界発光素子を用いたものである。本発明の有機EL照明の型式や構造については特に制限はなく、本発明の有機電界発光素子を用いて常法に従って組み立てることができる。
本発明の有機EL照明は、上述の本発明の有機電界発光素子を用いたものである。本発明の有機EL照明の型式や構造については特に制限はなく、本発明の有機電界発光素子を用いて常法に従って組み立てることができる。
本発明を実施例によって更に具体的に説明するが、本発明はその要旨を超えない限り、以下の実施例の記載に限定されるものではない。
(実施例1)
以下の手順で有機電界発光素子を作製した。
ガラス基板1上に、インジウム・スズ酸化物(ITO)透明導電膜をスパッタ成膜により堆積したものを、通常のフォトリソグラフィー技術と塩酸エッチングを用いて2mm幅
のストライプにパターニングして陽極2を形成した。パターン形成したITO基板を、界面活性剤水溶液による超音波洗浄、超純水による水洗、超純水による超音波洗浄、超純水による水洗の順で洗浄後、圧縮空気と接触させることにより乾燥させてから、紫外線オゾン洗浄を行った。
(実施例1)
以下の手順で有機電界発光素子を作製した。
ガラス基板1上に、インジウム・スズ酸化物(ITO)透明導電膜をスパッタ成膜により堆積したものを、通常のフォトリソグラフィー技術と塩酸エッチングを用いて2mm幅
のストライプにパターニングして陽極2を形成した。パターン形成したITO基板を、界面活性剤水溶液による超音波洗浄、超純水による水洗、超純水による超音波洗浄、超純水による水洗の順で洗浄後、圧縮空気と接触させることにより乾燥させてから、紫外線オゾン洗浄を行った。
次に、以下の構造式(HIT−1)に示すアリールアミンポリマー、構造式(A1)に示す4−イソプロピル−4’−メチルジフェニルヨードニウムテトラキス(ペンタフルオロフェニル)ボラートおよび安息香酸エチルを含有する正孔注入輸送層形成用塗布液を調製した。この塗布液を下記条件で陽極2上にスピンコート法により成膜し、膜厚41nmの正孔注入輸送層3を形成した。
<正孔注入輸送層形成用塗布液>
溶媒 安息香酸エチル
塗布液濃度 HIT−1:2.5重量%
A1:0.5重量%
<正孔注入輸送層3の成膜条件>
スピナ回転時間 2000rpm 30秒
加熱条件 230℃、1時間
引き続き、以下のHIT−2に示す構造式の化合物を含有する正孔注入輸送層形成用塗布液を調製し、これを以下の条件で正孔注入輸送層3上にスピンコート法により成膜し、加熱することにより重合させ、膜厚14nmの正孔注入輸送層4を形成した。
溶媒 安息香酸エチル
塗布液濃度 HIT−1:2.5重量%
A1:0.5重量%
<正孔注入輸送層3の成膜条件>
スピナ回転時間 2000rpm 30秒
加熱条件 230℃、1時間
引き続き、以下のHIT−2に示す構造式の化合物を含有する正孔注入輸送層形成用塗布液を調製し、これを以下の条件で正孔注入輸送層3上にスピンコート法により成膜し、加熱することにより重合させ、膜厚14nmの正孔注入輸送層4を形成した。
<正孔注入輸送層形成用塗布液>
溶媒 シクロヘキシルベンゼン
塗布液濃度 HIT−2:1.0重量
<正孔注入輸送層4の成膜条件>
スピナ回転時間 2000rpm×120秒
加熱条件 230℃、1時間
次に、以下の化合物(GH−1)、(GH−2) 及び(G1)の構造式の化合物を含
有する発光層形成用塗布液を調製し、以下の条件でスピンコート法によりこれを成膜し、加熱することにより、膜厚51nmの発光層5を正孔注入輸送層4上に形成した。
溶媒 シクロヘキシルベンゼン
塗布液濃度 HIT−2:1.0重量
<正孔注入輸送層4の成膜条件>
スピナ回転時間 2000rpm×120秒
加熱条件 230℃、1時間
次に、以下の化合物(GH−1)、(GH−2) 及び(G1)の構造式の化合物を含
有する発光層形成用塗布液を調製し、以下の条件でスピンコート法によりこれを成膜し、加熱することにより、膜厚51nmの発光層5を正孔注入輸送層4上に形成した。
<発光層形成用塗布液>
溶媒 シクロヘキシルベンゼン
塗布液濃度 GH−1:1.2重量%
GH−2:3.6重量%
G1:0.48重量%
<発光層5の成膜条件>
スピナ回転時間 1550rpm×120秒
加熱条件 120℃、20分
この発光層5まで成膜した基板を真空蒸着装置内に移し、装置内の真空度が2.0×10−4Pa以下になるまで排気した後、以下のHB−1に示す構造式の化合物を真空蒸着法にて、蒸着速度0.8〜1.2Å/秒で発光層5の上に積層させ、膜厚10nmの正孔阻止層6を得た。
溶媒 シクロヘキシルベンゼン
塗布液濃度 GH−1:1.2重量%
GH−2:3.6重量%
G1:0.48重量%
<発光層5の成膜条件>
スピナ回転時間 1550rpm×120秒
加熱条件 120℃、20分
この発光層5まで成膜した基板を真空蒸着装置内に移し、装置内の真空度が2.0×10−4Pa以下になるまで排気した後、以下のHB−1に示す構造式の化合物を真空蒸着法にて、蒸着速度0.8〜1.2Å/秒で発光層5の上に積層させ、膜厚10nmの正孔阻止層6を得た。
更に、以下に示す構造の有機化合物(E1)を真空蒸着法にて、蒸着速度0.8〜1.2Å/秒で、正孔阻止層6の上に積層させ、膜厚20nmの電子輸送層7を得た。
ここで、この電子輸送層7まで蒸着を行った基板上に陰極蒸着用のマスクとして2mm幅のストライプ状シャドーマスクを陽極2のITOストライプと直交するように電子輸送層7上に密着させ、真空蒸着装置内に移し、装置内の真空度が2.0×10−4Pa以下になるまで排気した。
電子注入層8として、先ずフッ化リチウム(LiF)を、モリブデンボートを用いて、
蒸着速度0.1〜0.4Å/秒で、0.5nmの膜厚で電子輸送層7の上に形成した。次に、陰極9として、アルミニウムを同様にモリブデンボートにより加熱して、蒸着速度0.7〜5.3Å/秒で、膜厚80nmのアルミニウム層を形成した。
電子注入層8として、先ずフッ化リチウム(LiF)を、モリブデンボートを用いて、
蒸着速度0.1〜0.4Å/秒で、0.5nmの膜厚で電子輸送層7の上に形成した。次に、陰極9として、アルミニウムを同様にモリブデンボートにより加熱して、蒸着速度0.7〜5.3Å/秒で、膜厚80nmのアルミニウム層を形成した。
引き続き、素子が保管中に大気中の水分等で劣化することを防ぐため、以下の方法で封止処理を行った。窒素グローブボックス中で、23mm×23mmサイズのガラス板の外周部に、1mmの幅で光硬化性樹脂(株式会社スリーボンド製30Y−437)を塗布し、中央部に水分ゲッターシート(ダイニック株式会社製)を設置した。この上に、陰極まで形成した基板を蒸着面が乾燥剤シートと対向するように貼り合わせた。その後、光硬化性樹脂が塗布された領域のみに紫外光を照射し、樹脂を硬化させた。
以上の様にして、2mm×2mmのサイズの発光面積部分を有する有機電界発光素子が得られた。この素子の特性を表に示す。
(参考例1)
発光層5として、化合物(G−1)の代わりに、化合物(G−2)を用いた以外は、実施例1と同様にして、有機電界発光素子を作製した。得られた素子の特性を下表に示す。
(参考例1)
発光層5として、化合物(G−1)の代わりに、化合物(G−2)を用いた以外は、実施例1と同様にして、有機電界発光素子を作製した。得られた素子の特性を下表に示す。
(比較例1)
発光層5として、化合物(G−1)の代わりに、化合物(G−3)を用いた以外は、実施例1と同様にして、有機電界発光素子を作製した。得られた素子の特性を下表に示す。
発光層5として、化合物(G−1)の代わりに、化合物(G−3)を用いた以外は、実施例1と同様にして、有機電界発光素子を作製した。得られた素子の特性を下表に示す。
(比較例2)
発光層5として、化合物(G−1)の代わりに、化合物(G−4)を用いた以外は、実施例1と同様にして、有機電界発光素子を作製した。得られた素子の特性を下表に示す。
発光層5として、化合物(G−1)の代わりに、化合物(G−4)を用いた以外は、実施例1と同様にして、有機電界発光素子を作製した。得られた素子の特性を下表に示す。
〈駆動寿命測定〉
駆動寿命の測定方法は、作成した有機EL素子に、試験時直流一定電流(20mA/cm2)の電流を通電したときの輝度変化をフォトダイオードにより、観察することにより行い、輝度値が試験開始時の80%となるまでの時間を求めた。このとき、比較例1の駆動寿命を1とした時の相対的な駆動寿命を記載した。この結果から、実施例は比較例と比べ、寿命が向上していることがわかる。
駆動寿命の測定方法は、作成した有機EL素子に、試験時直流一定電流(20mA/cm2)の電流を通電したときの輝度変化をフォトダイオードにより、観察することにより行い、輝度値が試験開始時の80%となるまでの時間を求めた。このとき、比較例1の駆動寿命を1とした時の相対的な駆動寿命を記載した。この結果から、実施例は比較例と比べ、寿命が向上していることがわかる。
Claims (5)
- 下記式(1)で示されるイリジウム錯体化合物であって、
アニオン電荷分布において、C2原子のスピン分布値(NBO population) が0.21より大き
く、0.5未満であることを特徴とする、
イリジウム錯体化合物。
位子であり、nは1から3の整数を示す。} - 下記式(2)で示されるイリジウム錯体化合物であって、
アニオン電荷分布において、C2原子のスピン分布値(NBO population) が0.21より大きく
、0.5未満であることを特徴とする、
イリジウム錯体化合物。
炭素数3〜20の芳香族複素環基を示す。これらの基はさらに、フッ素、塩素、臭素、炭素数1〜20のアルキル基、炭素数1〜20のアルコキシ基、トリアルキルシリル基(但し、アルキルの炭素数は1〜20)、炭素数1〜20のアルキルカルボニル基、炭素数1〜20のアリールカルボニル基、炭素数1〜20のアルキルアミノ基、炭素数1〜20のアリールアミノ基、炭素数6〜20のアリール基で置換されていてもよい。Lは有機配位子であり、nは1から3の整数を示す。
Zは下記式(3)で表される。
20のアルキル基、炭素数1〜20のアルコキシ基、炭素数3〜20のアリール基から選ばれる。rは1から20の整数を示す。〕} - 請求項1又は2に記載のイリジウム錯体化合物を含む、有機電界発光素子。
- 請求項3記載の有機電界発光素子を用いた有機EL表示装置。
- 請求項3記載の有機電界発光素子を用いた有機EL照明。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012143238A JP2014005247A (ja) | 2012-06-26 | 2012-06-26 | イリジウム錯体化合物、有機電界発光素子、有機el表示装置及び有機el照明 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012143238A JP2014005247A (ja) | 2012-06-26 | 2012-06-26 | イリジウム錯体化合物、有機電界発光素子、有機el表示装置及び有機el照明 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2014005247A true JP2014005247A (ja) | 2014-01-16 |
Family
ID=50103330
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012143238A Pending JP2014005247A (ja) | 2012-06-26 | 2012-06-26 | イリジウム錯体化合物、有機電界発光素子、有機el表示装置及び有機el照明 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2014005247A (ja) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN106279295A (zh) * | 2016-08-05 | 2017-01-04 | 昆明贵金属研究所 | 两种黄色铱磷光配合物及其制备方法 |
| JP2023029833A (ja) * | 2014-10-08 | 2023-03-07 | ユニバーサル ディスプレイ コーポレイション | 有機エレクトロルミネッセンス材料及びデバイス |
| US20230107413A1 (en) * | 2016-06-20 | 2023-04-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12082485B2 (en) | 2014-10-08 | 2024-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
-
2012
- 2012-06-26 JP JP2012143238A patent/JP2014005247A/ja active Pending
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2023029833A (ja) * | 2014-10-08 | 2023-03-07 | ユニバーサル ディスプレイ コーポレイション | 有機エレクトロルミネッセンス材料及びデバイス |
| US12082485B2 (en) | 2014-10-08 | 2024-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20230107413A1 (en) * | 2016-06-20 | 2023-04-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12552986B2 (en) * | 2016-06-20 | 2026-02-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| CN106279295A (zh) * | 2016-08-05 | 2017-01-04 | 昆明贵金属研究所 | 两种黄色铱磷光配合物及其制备方法 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5810417B2 (ja) | イリジウム錯体化合物、並びに該化合物を含む組成物、有機電界発光素子、表示装置及び照明装置 | |
| CN102106017B (zh) | 有机电致发光元件、有机电致发光显示装置以及有机电致发光光源 | |
| JP6879342B2 (ja) | 重合体、有機電界発光素子用組成物、有機電界発光素子、有機el表示装置及び有機el照明 | |
| JP6442977B2 (ja) | 重合体、有機電界発光素子用組成物、有機電界発光素子、有機el表示装置及び有機el照明 | |
| TWI894149B (zh) | 有機電場發光元件及顯示裝置 | |
| JP5668330B2 (ja) | 有機電界発光素子、有機el照明及び有機el表示装置 | |
| WO2016194784A1 (ja) | イリジウム錯体化合物、該化合物を含有する有機電界発光素子、表示装置及び照明装置 | |
| JP2018016641A (ja) | イリジウム錯体化合物、有機電界発光素子、表示装置ならびに照明装置 | |
| JP6119171B2 (ja) | イリジウム錯体化合物、該化合物及び溶剤を含有する組成物、該化合物を含有する有機電界発光素子、表示装置及び照明装置 | |
| JP5392438B1 (ja) | 重合体及び有機電界発光素子 | |
| JP6286872B2 (ja) | イリジウム錯体化合物、有機電界発光素子、表示装置および照明装置 | |
| JP7276059B2 (ja) | 有機電界発光素子用組成物、有機電界発光素子、表示装置及び照明装置 | |
| JP6593432B2 (ja) | 重合体、有機電界発光素子用組成物、有機電界発光素子、有機el表示装置及び有機el照明 | |
| JP2014005247A (ja) | イリジウム錯体化合物、有機電界発光素子、有機el表示装置及び有機el照明 | |
| JP2025128136A (ja) | 有機電界発光素子用組成物、有機電界発光素子、表示装置及び照明装置 | |
| WO2022149519A1 (ja) | 有機電界発光素子用組成物、有機電界発光素子、表示装置及び照明装置 | |
| JP2014058457A (ja) | イリジウム錯体化合物、有機電界発光素子、表示装置ならびに照明装置 | |
| JP2014033134A (ja) | 有機電界発光素子用組成物、有機膜、有機電界発光素子、有機el表示装置及び有機el照明 | |
| KR102941086B1 (ko) | 유기 전계 발광 소자용 조성물, 유기 전계 발광 소자와 그 제조 방법, 및 표시 장치 | |
| JP2010239127A (ja) | 有機電界発光素子、有機elディスプレイ及び有機el照明。 | |
| TW202309244A (zh) | 有機電場發光元件用組成物、有機電場發光元件及其製造方法、顯示裝置及照明裝置 | |
| JP2021127325A (ja) | 芳香族ジアミン誘導体 |