JP2017002045A - 口腔内崩壊錠 - Google Patents
口腔内崩壊錠 Download PDFInfo
- Publication number
- JP2017002045A JP2017002045A JP2016115792A JP2016115792A JP2017002045A JP 2017002045 A JP2017002045 A JP 2017002045A JP 2016115792 A JP2016115792 A JP 2016115792A JP 2016115792 A JP2016115792 A JP 2016115792A JP 2017002045 A JP2017002045 A JP 2017002045A
- Authority
- JP
- Japan
- Prior art keywords
- mannitol
- active ingredient
- granulated product
- mass
- orally disintegrating
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Landscapes
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
【解決手段】有効成分、マンニトール及び崩壊剤を含む湿式造粒物と、該造粒物とは別にマンニトール及び滑沢剤とを含有し、製剤中に有効成分を40〜80質量%含有することを特徴とする口腔内崩壊錠。
【選択図】なし
Description
従って、本発明の課題は、簡便な製造工程により、湿度条件下に保存しても硬度の低下や錠厚の変化、崩壊性の変化を生じない、有効成分高含有の口腔内崩壊錠を提供することにある。
〔2〕製剤中の有効成分の含有量が50〜70質量%である〔1〕記載の口腔内崩壊錠。
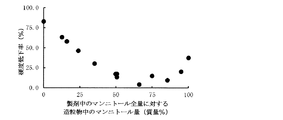
〔3〕製剤中のマンニトール全量に対する造粒物中のマンニトール量が12.5〜95質量%である〔1〕又は〔2〕記載の口腔内崩壊錠。
〔4〕製剤中のマンニトール全量に対する造粒物中のマンニトール量が23〜75質量%である〔1〕〜〔3〕のいずれかに記載の口腔内崩壊錠。
〔5〕造粒物内の崩壊剤がクロスポビドンである〔1〕〜〔4〕のいずれかに記載の口腔内崩壊錠。
〔6〕湿式造粒物が撹拌造粒法により得られる湿式造粒物である〔1〕〜〔5〕のいずれかに記載の口腔内崩壊錠。
〔7〕有効成分がポラプレジンク、アコチアミド塩酸塩水和物、イブプロフェン及びニザチジンから選ばれる成分である〔1〕〜〔6〕のいずれかに記載の口腔内崩壊錠。
〔8〕造粒物について乾式レーザー回折・散乱式測定法による粒度分布測定をするときD50が15〜75μmである〔1〕〜〔7〕のいずれかに記載の口腔内崩壊錠。
〔9〕自動分包機に適用可能である〔1〕〜〔8〕のいずれかに記載の口腔内崩壊錠。
〔10〕(1)有効成分、マンニトール及び崩壊剤を含有する組成物を湿式造粒する工程、及び(2)得られた湿式造粒物、マンニトール及び滑沢剤を含有する混合物を圧縮成形する工程、を有することを特徴とする、製剤中に有効成分を40〜80質量%含有する口腔内崩壊錠の製造法。
ここで、造粒物とは別のマンニトールの含有量は、良好な崩壊性、成形性の点から、処方全量に対して1質量%以上が好ましく、3質量%以上がより好ましく、5質量%以上がさらに好ましい。また、打錠障害防止、湿度条件下の硬度低下防止の点から、処方全量に対して25質量%以下が好ましく、20質量%以下がより好ましく、18質量%以下がさらに好ましい。具体的には、処方全量に対して1〜25質量%が好ましく、3〜20質量%がより好ましく、5〜18質量%がさらに好ましい。
滑沢剤の含有量は、例えば、ステアリン酸マグネシウムなら、製造性、打錠障害防止の点から、錠剤質量に対して0.5質量%以上が好ましく、0.6質量%以上がより好ましく、0.8質量%以上がさらに好ましい。また、良好な崩壊性、成形性の点から、処方全量に対して2.5質量%以下が好ましく、2.0質量%以下がより好ましく、1.5質量%以下がさらに好ましい。具体的には、処方全量に対して0.5〜2.5質量%が好ましく、0.6〜2.0質量%がより好ましく、0.8〜1.5質量%がさらに好ましい。
ポラプレジンク(有効成分)68.2%、D−マンニトール17.1%、ヒドロキシプロピルセルロース0.9%、クロスポビドン10.9%、軽質無水ケイ酸2.2%、粉末還元麦芽糖水アメ0.5%及びスクラロース微量を湿式攪拌造粒後、棚式乾燥機にて乾燥した。この造粒物84.6%に、D−マンニトール14.2%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物をロータリー打錠機で有効成分75mgを含む約130mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)67.6%、D−マンニトール14.7%、ヒドロキシプロピルセルロース0.9%、クロスポビドン10.8%、結晶セルロース5.9%及びスクラロース微量を湿式攪拌造粒後、棚式乾燥機にて乾燥した。この造粒物85.3%に、D−マンニトール12.7%、低置換度ヒドロキシプロピルセルロース0.8%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物をロータリー打錠機で有効成分75mgを含む約130mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)67.0%、D−マンニトール13.7%、クロスポビドン10.7%、結晶セルロース5.8%、軽質無水ケイ酸2.1%、粉末還元麦芽糖水アメ0.5%及びスクラロース微量を湿式攪拌造粒後、棚式乾燥機にて乾燥した。この造粒物86.1%に、D−マンニトール11.9%、低置換度ヒドロキシプロピルセルロース0.8%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物をロータリー打錠機で有効成分75mgを含む約130mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)74.0%、D−マンニトール3.7%、ヒドロキシプロピルセルロース1.0%、クロスポビドン11.8%、結晶セルロース6.4%、軽質無水ケイ酸2.4%、粉末還元麦芽糖水アメ0.6%及びスクラロース微量を湿式攪拌造粒後、棚式乾燥機にて乾燥した。この造粒物78.0%に、D−マンニトール20.1%、低置換度ヒドロキシプロピルセルロース0.8%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%と混合した。この混合物をロータリー打錠機で有効成分75mgを含む約130mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)73.1%、D−マンニトール4.8%、ヒドロキシプロピルセルロース1.0%、クロスポビドン11.7%、結晶セルロース6.3%、軽質無水ケイ酸2.3%、粉末還元麦芽糖水アメ0.6%及びスクラロース微量を湿式攪拌造粒後、棚式乾燥機にて乾燥した。この造粒物78.9%に、D−マンニトール19.9%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物を単発打錠機で有効成分75mgを含む約130mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)71.5%、D−マンニトール7.0%、ヒドロキシプロピルセルロース1.0%、クロスポビドン11.4%、結晶セルロース6.2%、軽質無水ケイ酸2.3%、粉末還元麦芽糖水アメ0.6%及びスクラロース微量を湿式攪拌造粒後、棚式乾燥機にて乾燥した。この造粒物80.7%に、D−マンニトール18.1%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物を単発打錠機で有効成分75mgを含む約130mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)69.2%、D−マンニトール10.0%、ヒドロキシプロピルセルロース0.9%、クロスポビドン11.1%、結晶セルロース6.0%、軽質無水ケイ酸2.2%、粉末還元麦芽糖水アメ0.6%及びスクラロース微量を湿式攪拌造粒後、棚式乾燥機にて乾燥した。この造粒物83.4%に、D−マンニトール15.4%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物をロータリー打錠機で有効成分75mgを含む約130mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)66.7%、D−マンニトール(D50:40μm)13.2%、ヒドロキシプロピルセルロース0.9%、クロスポビドン10.7%、結晶セルロース5.8%、軽質無水ケイ酸2.1%、粉末還元麦芽糖水アメ0.5%及びスクラロース微量を湿式攪拌造粒後、流動層乾燥機にて乾燥した。この造粒物86.5%に、D−マンニトール(D50:20μm)11.5%、低置換度ヒドロキシプロピルセルロース0.8%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物をロータリー打錠機で有効成分75mgを含む約130mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)68.2%、D−マンニトール(D50:40μm)17.1%、ヒドロキシプロピルセルロース0.9%、クロスポビドン10.9%、軽質無水ケイ酸2.2%、粉末還元麦芽糖水アメ0.5%及びスクラロース微量を湿式攪拌造粒後、流動層乾燥機にて乾燥した。この造粒物84.6%に、D−マンニトール(D50:40μm)14.2%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物を単発打錠機で有効成分75mgを含む約130mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)63.6%、D−マンニトール17.2%、ヒドロキシプロピルセルロース0.8%、クロスポビドン10.2%、結晶セルロース5.5%、軽質無水ケイ酸2.0%、粉末還元麦芽糖水アメ0.5%及びスクラロース微量を湿式攪拌造粒後、棚式乾燥機にて乾燥した。この造粒物90.7%に、D−マンニトール8.1%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物をロータリー打錠機で有効成分75mgを含む約130mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)62.5%、D−マンニトール18.6%、ヒドロキシプロピルセルロース0.8%、クロスポビドン10.0%、結晶セルロース5.4%、軽質無水ケイ酸2.0%、粉末還元麦芽糖水アメ0.5%及びスクラロース微量を湿式攪拌造粒後、棚式乾燥機にて乾燥した。この造粒物92.3%に、D−マンニトール5.8%、低置換度ヒドロキシプロピルセルロース0.8%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%と混合した。この混合物をロータリー打錠機で有効成分75mgを含む約130mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)60.5%、D−マンニトール21.3%、ヒドロキシプロピルセルロース0.8%、クロスポビドン9.7%、結晶セルロース5.2%、軽質無水ケイ酸1.9%、粉末還元麦芽糖水アメ0.5%及びスクラロース微量を湿式攪拌造粒後、棚式乾燥機にて乾燥した。この造粒物95.3%に、D−マンニトール3.5%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物をロータリー打錠機で有効成分75mgを含む約130mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)59.6%、D−マンニトール22.5%、ヒドロキシプロピルセルロース0.8%、クロスポビドン9.5%、結晶セルロース5.2%、軽質無水ケイ酸1.9%、粉末還元麦芽糖水アメ0.5%及びスクラロース微量を湿式攪拌造粒後、棚式乾燥機にて乾燥した。この造粒物97.6%に、D−マンニトール1.2%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物を単発打錠機で有効成分75mgを含む約129mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)66.7%、D−マンニトール13.2%、ヒドロキシプロピルセルロース0.9%、クロスポビドン10.7%、結晶セルロース5.8%、軽質無水ケイ酸2.1%、粉末還元麦芽糖水アメ0.5%及びスクラロース微量を湿式攪拌造粒後、流動層乾燥機にて乾燥した。この造粒物86.0%に、D−マンニトール11.5%、低置換度ヒドロキシプロピルセルロース0.8%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.5%を混合した。この混合物をロータリー打錠機で有効成分75mgを含む約131mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)66.7%、D−マンニトール13.2%、ヒドロキシプロピルセルロース0.9%、クロスポビドン10.7%、結晶セルロース5.8%、軽質無水ケイ酸2.1%、粉末還元麦芽糖水アメ0.5%及びスクラロース微量を湿式攪拌造粒後、流動層乾燥機にて乾燥した。この造粒物86.5%に、D−マンニトール11.5%、低置換度ヒドロキシプロピルセルロース0.8%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物をロータリー打錠機で有効成分75mgを含む約130mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)82.0%、D−マンニトール4.5%、ヒドロキシプロピルセルロース0.8%、クロスポビドン9.8%、結晶セルロース2.2%、粉末還元麦芽糖水アメ0.5%及びスクラロース微量を湿式攪拌造粒後、棚式乾燥機にて乾燥した。この造粒物93.8%に、D−マンニトール4.2%、低置換度ヒドロキシプロピルセルロース0.8%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物をロータリー打錠機で有効成分100mgを含む約130mgの錠剤に圧縮成形した。
アコチアミド塩酸塩水和物(有効成分)60.4%、D−マンニトール18.5%、ヒドロキシプロピルセルロース0.9%、クロスポビドン11.2%、結晶セルロース6.0%、軽質無水ケイ酸2.2%、粉末還元麦芽糖水アメ0.5%及びスクラロース微量を湿式攪拌造粒後、棚式乾燥機にて乾燥した。この造粒物82.8%に、D−マンニトール16.0%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物をロータリー打錠機で有効成分100mgを含む約200mgの錠剤に圧縮成形した。
イブプロフェン(有効成分)60.5%、D−マンニトール18.4%、ヒドロキシプロピルセルロース0.9%、クロスポビドン11.2%、結晶セルロース6.0%、軽質無水ケイ酸2.2%、粉末還元麦芽糖水アメ0.6%及びスクラロース0.2%を湿式攪拌造粒後、棚式乾燥機にて乾燥した。この造粒物82.6%に、D−マンニトール16.2%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物をロータリー打錠機で有効成分65mgを含む約130mgの錠剤に圧縮成形した。
ニザチジン(有効成分)60.1%、D−マンニトール18.3%、ヒドロキシプロピルセルロース1.0%、クロスポビドン11.1%、結晶セルロース6.0%、軽質無水ケイ酸2.2%、粉末還元麦芽糖水アメ1.1%及びスクラロース微量を湿式攪拌造粒後、棚式乾燥機にて乾燥した。この造粒物83.2%に、D−マンニトール15.5%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物をロータリー打錠機で有効成分75mgを含む約150mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)66.7%、D−マンニトール13.2%、ヒドロキシプロピルセルロース0.9%、クロスポビドン10.7%、結晶セルロース5.8%、軽質無水ケイ酸2.1%、粉末還元麦芽糖水アメ0.5%及びスクラロース微量を湿式攪拌造粒後、流動層乾燥機にて乾燥した。この造粒物86.5%に、D−マンニトール11.5%、低置換度ヒドロキシプロピルセルロース0.8%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物をロータリー打錠機で有効成分75mgを含む約130mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)59.0%、D−マンニトール29.2%、低置換度ヒドロキシプロピルセルロース11.4%、粉末還元麦芽糖水アメ0.3%及びスクラロース微量を湿式攪拌造粒後、棚式乾燥機にて乾燥した。この造粒物96.8%に、軽質無水ケイ酸1.0%、l−メントール微量、香料微量及びステアリン酸マグネシウム2.0%を混合した。この混合物をロータリー打錠機で有効成分75mgを含む約131mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)66.7%、D−マンニトール13.2%、ヒドロキシプロピルセルロース0.9%、クロスポビドン10.7%、結晶セルロース5.8%、メタケイ酸アルミン酸マグネシウム2.1%、粉末還元麦芽糖水アメ0.5%及びスクラロース微量を湿式攪拌造粒後、棚式乾燥機にて乾燥した。この造粒物86.5%に、D−マンニトール11.5%、低置換度ヒドロキシプロピルセルロース0.8%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物をロータリー打錠機で有効成分75mgを含む約130mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)93.8%、ポビドン6.3%を湿式攪拌造粒後、流動層乾燥機にて乾燥した。この造粒物61.5%に、D−マンニトール7.5%、合成ケイ酸アルミニウム・ヒドロキシプロピルスターチ・結晶セルロース20.4%、クロスポビドン7.7%、アスパルテーム0.8%、l−メントール微量、香料微量及びステアリン酸マグネシウム1.9%を混合した。この混合物をロータリー打錠機で有効成分75mgを含む約130mgの錠剤に圧縮成形した。
ポラプレジンク(有効成分)58.4%、D−マンニトール30.6%、ヒドロキシプロピルセルロース0.8%、クロスポビドン7.8%、軽質無水ケイ酸1.9%、粉末還元麦芽糖水アメ0.5%及びスクラロース微量を湿式攪拌造粒後、流動層乾燥機にて乾燥した。この造粒物98.8%に、l−メントール微量、香料微量及びステアリン酸マグネシウム1.0%を混合した。この混合物をロータリー打錠機で有効成分75mgを含む約130mgの錠剤に圧縮成形した。
硬度計、PHARMA TEST社製、PTB−502により測定した。
シックネスゲージ、テクロック製、SMD−540により錠剤の厚みを測定した。
2〜5人の健常成人の口腔内に錠剤1錠を入れ、唾液のみで完全に崩壊するまでの時間を測定し、その平均値を口腔内崩壊時間とした。
レーザー回折・散乱式粒子径分布測定装置、日機装製、マイクロトラックMS3200IIにより、造粒物及びマンニトールの粒度分布を測定し、D50を算出した。
Claims (10)
- 有効成分、マンニトール及び崩壊剤を含む湿式造粒物と、該造粒物とは別にマンニトール及び滑沢剤とを含有し、製剤中に有効成分を40〜80質量%含有することを特徴とする口腔内崩壊錠。
- 製剤中の有効成分の含有量が50〜70質量%である請求項1記載の口腔内崩壊錠。
- 製剤中のマンニトール全量に対する造粒物中のマンニトール量が12.5〜95質量%である請求項1又は2記載の口腔内崩壊錠。
- 製剤中のマンニトール全量に対する造粒物中のマンニトール量が23〜75質量%である請求項1〜3のいずれか1項記載の口腔内崩壊錠。
- 造粒物内の崩壊剤がクロスポビドンである請求項1〜4のいずれか1項記載の口腔内崩壊錠。
- 湿式造粒物が撹拌造粒法により得られる湿式造粒物である請求項1〜5のいずれか1項記載の口腔内崩壊錠。
- 有効成分がポラプレジンク、アコチアミド塩酸塩水和物、イブプロフェン及びニザチジンから選ばれる成分である請求項1〜6のいずれか1項記載の口腔内崩壊錠。
- 造粒物について乾式レーザー回折法による粒度分布測定をするときD50が15〜75μmである請求項1〜7のいずれか1項記載の口腔内崩壊錠。
- 自動分包機に適用可能である請求項1〜8のいずれか1項記載の口腔内崩壊錠。
- (1)有効成分、マンニトール及び崩壊剤を含有する組成物を湿式造粒する工程、及び(2)得られた湿式造粒物、マンニトール及び滑沢剤を含有する混合物を圧縮成形する工程、を有することを特徴とする、製剤中に有効成分を40〜80質量%含有する口腔内崩壊錠の製造法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015118826 | 2015-06-12 | ||
| JP2015118826 | 2015-06-12 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2017002045A true JP2017002045A (ja) | 2017-01-05 |
| JP6926404B2 JP6926404B2 (ja) | 2021-08-25 |
Family
ID=57751766
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016115792A Active JP6926404B2 (ja) | 2015-06-12 | 2016-06-10 | 口腔内崩壊錠 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6926404B2 (ja) |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017052755A (ja) * | 2015-09-10 | 2017-03-16 | 大正製薬株式会社 | 固形製剤 |
| JP2018177698A (ja) * | 2017-04-14 | 2018-11-15 | 大正製薬株式会社 | 固形組成物 |
| CN109999003A (zh) * | 2019-05-14 | 2019-07-12 | 湖南华纳大药厂股份有限公司 | 盐酸阿考替胺口崩片及其制备方法 |
| CN110384670A (zh) * | 2018-04-17 | 2019-10-29 | 北京泰德制药股份有限公司 | 一种含有盐酸阿考替胺的组合物及其制备方法 |
| JPWO2020246120A1 (ja) * | 2019-06-07 | 2020-12-10 | ||
| JP2023536341A (ja) * | 2020-08-06 | 2023-08-24 | エスケー バイオファーマスティカルズ カンパニー リミテッド | カルバメート化合物を含む経口用固形製剤及びその製造方法 |
| CN117398355A (zh) * | 2023-09-22 | 2024-01-16 | 南京海纳制药有限公司 | 一种盐酸阿考替胺片及其生产方法 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001058944A (ja) * | 1999-06-18 | 2001-03-06 | Takeda Chem Ind Ltd | 速崩壊性固形製剤 |
| WO2008120548A2 (ja) * | 2007-03-13 | 2008-10-09 | Dainippon Sumitomo Pharma Co., Ltd. | 口腔内崩壊錠 |
| JP2011012082A (ja) * | 2010-10-18 | 2011-01-20 | Asahi Kasei Pharma Kk | ナフトピジルを含有する医薬の製造方法 |
| JP2013147470A (ja) * | 2012-01-20 | 2013-08-01 | Nipro Corp | 口腔内崩壊錠 |
| WO2013125350A1 (ja) * | 2012-02-23 | 2013-08-29 | フロイント産業株式会社 | 口腔内崩壊錠用直打賦形剤及びその製造方法、並びに口腔内崩壊錠 |
| WO2014148520A1 (ja) * | 2013-03-21 | 2014-09-25 | 大正製薬株式会社 | 固形製剤 |
-
2016
- 2016-06-10 JP JP2016115792A patent/JP6926404B2/ja active Active
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001058944A (ja) * | 1999-06-18 | 2001-03-06 | Takeda Chem Ind Ltd | 速崩壊性固形製剤 |
| WO2008120548A2 (ja) * | 2007-03-13 | 2008-10-09 | Dainippon Sumitomo Pharma Co., Ltd. | 口腔内崩壊錠 |
| JP2011012082A (ja) * | 2010-10-18 | 2011-01-20 | Asahi Kasei Pharma Kk | ナフトピジルを含有する医薬の製造方法 |
| JP2013147470A (ja) * | 2012-01-20 | 2013-08-01 | Nipro Corp | 口腔内崩壊錠 |
| WO2013125350A1 (ja) * | 2012-02-23 | 2013-08-29 | フロイント産業株式会社 | 口腔内崩壊錠用直打賦形剤及びその製造方法、並びに口腔内崩壊錠 |
| WO2014148520A1 (ja) * | 2013-03-21 | 2014-09-25 | 大正製薬株式会社 | 固形製剤 |
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017052755A (ja) * | 2015-09-10 | 2017-03-16 | 大正製薬株式会社 | 固形製剤 |
| JP2018177698A (ja) * | 2017-04-14 | 2018-11-15 | 大正製薬株式会社 | 固形組成物 |
| CN110384670A (zh) * | 2018-04-17 | 2019-10-29 | 北京泰德制药股份有限公司 | 一种含有盐酸阿考替胺的组合物及其制备方法 |
| CN109999003A (zh) * | 2019-05-14 | 2019-07-12 | 湖南华纳大药厂股份有限公司 | 盐酸阿考替胺口崩片及其制备方法 |
| CN109999003B (zh) * | 2019-05-14 | 2022-03-25 | 湖南华纳大药厂股份有限公司 | 盐酸阿考替胺口崩片及其制备方法 |
| JPWO2020246120A1 (ja) * | 2019-06-07 | 2020-12-10 | ||
| JP7360460B2 (ja) | 2019-06-07 | 2023-10-12 | あゆみ製薬株式会社 | 口腔内崩壊錠及びその製造方法 |
| JP2023536341A (ja) * | 2020-08-06 | 2023-08-24 | エスケー バイオファーマスティカルズ カンパニー リミテッド | カルバメート化合物を含む経口用固形製剤及びその製造方法 |
| CN117398355A (zh) * | 2023-09-22 | 2024-01-16 | 南京海纳制药有限公司 | 一种盐酸阿考替胺片及其生产方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP6926404B2 (ja) | 2021-08-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6926404B2 (ja) | 口腔内崩壊錠 | |
| JP5409382B2 (ja) | 口腔内崩壊錠 | |
| JP5352474B2 (ja) | 口腔内崩壊錠およびその製造方法 | |
| JP5296456B2 (ja) | 溶出が良好なイルベサルタン含有医薬組成物および口腔内崩壊錠 | |
| JP5798642B2 (ja) | 経口用医薬組成物 | |
| KR20130076015A (ko) | 높은 경도를 갖는 속붕정 및 이의 제조 방법 | |
| RU2600831C2 (ru) | Перорально вводимая фармацевтическая композиция | |
| JP6496084B2 (ja) | 口腔内崩壊錠 | |
| JP2017141299A (ja) | 溶出が良好なイルベサルタン含有医薬組成物および口腔内崩壊錠 | |
| JP6836375B2 (ja) | 口腔内発泡製剤及びその製造法 | |
| KR101677775B1 (ko) | 붕괴성 및 용출성에 우수한 내복용 정제 | |
| JP5978335B2 (ja) | 溶出が良好なイルベサルタン含有医薬組成物および口腔内崩壊錠 | |
| JP5823592B2 (ja) | 安定性が改善された製剤 | |
| JP5575119B2 (ja) | 口腔内崩壊錠 | |
| JP2019116506A (ja) | 固形製剤 | |
| JP6114573B2 (ja) | ロキソプロフェンナトリウムと制酸剤を含有する固形製剤 | |
| JP4860486B2 (ja) | ポビドンヨードを含有する口腔内崩壊型の固形製剤 | |
| JP2018158903A (ja) | ガランタミン臭化水素酸塩含有口腔内崩壊錠 | |
| JP2021105057A (ja) | 固形製剤 | |
| JP5560104B2 (ja) | アスコルビン酸(塩)含有固形製剤 | |
| JP6151413B2 (ja) | 溶出が良好なイルベサルタン含有医薬組成物および口腔内崩壊錠 | |
| JP5714652B2 (ja) | 溶出が良好なイルベサルタン含有医薬組成物および口腔内崩壊錠 | |
| KR102259798B1 (ko) | 붕해가 개선된 레날리도마이드의 경구용 정제 조성물 | |
| JP7360460B2 (ja) | 口腔内崩壊錠及びその製造方法 | |
| JP2007332063A (ja) | ポビドンヨードを含有する口腔内崩壊型固形製剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190402 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200121 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20200117 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200304 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200804 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200928 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210105 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210215 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210706 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210719 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6926404 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |